News: https://ir.genfit.com/news-releases/news-release-details/ipsen-and-genfit-announce-positive-results-phase-iii-elativer
Zu erwartende Milestone Zahlungen aus dem Jahresbericht vom April 2023:
https://ir.genfit.com/static-files/2d379838-8e02-423d-a21e-7b2eafa7bd60
Ipsen $360m + 20% Lizenzgebühren bei einem Umsatzpotential von $500m für USA/Europa
Tern Pharma $193m (für China, Hongkong, Macau und Taiwan)
Genfit verfügt über $128m Cash
Interessant ist das die Aktien des Wettbewerbers Cymabay dessen Ergebnisse noch ausstehen gestern über 40% hochging und eine Mkap von über $1Mrd erreicht hat.
Alleine die anstehenden Milestone Zahlungen und der Cashbestand bei Genfit kommen auf über $680m ein BUYOUT von $1Mrd. würde den Käufer (Ipsen/Tern) eine Amortisation in 3-4 Jahren bescheren.
Hinzu kommt noch das Nash Medikament im Endstadium
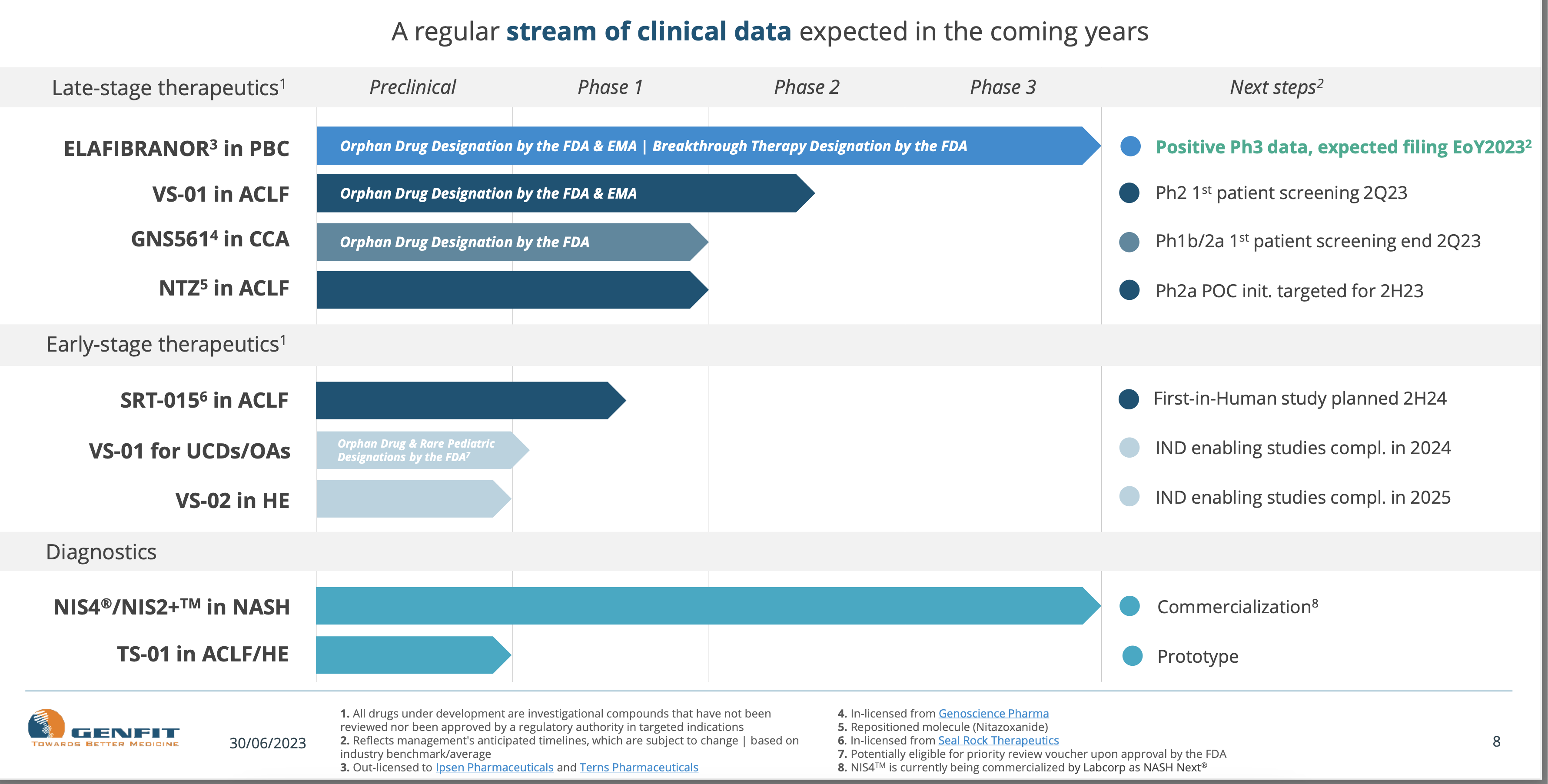
Genfit hat ab sofort keine Verantwortung mehr für die Zulassung weltweit, diese werden in Eigenregie von Ipsen uns Tern Pharma übernommen,
Übersetzung aus dem Jahresbericht:
Ipsen hat das Recht als erstes ein Kaufangebot abzugeben: Kooperations- und Lizenzvereinbarung mit Ipsen Pharma SAS
Am 16. Dezember 2021 haben wir eine exklusive Kooperations- und Lizenzvereinbarung mit Ipsen Pharma SAS oder Ipsen abgeschlossen, einem globalen, mittelständischen biopharmazeutischen Unternehmen, das sich auf transformative Medikamente in den Bereichen Onkologie, seltene Krankheiten und Neurowissenschaften sowie Produkte für die Verbrauchergesundheit konzentriert. Im Rahmen der Vereinbarung verfügt Ipsen über eine exklusive weltweite Lizenz (mit Ausnahme von Greater China, das an Terns lizenziert ist) zur Entwicklung, Herstellung und Vermarktung von Elafibranor, unserem firmeneigenen Prüfpräparat, für Menschen mit PBC und für alle anderen Indikationen.
Im Rahmen der Vereinbarung erhielten wir eine Vorauszahlung in Höhe von 120 Mio. € und haben
Anspruch auf behördliche, kommerzielle und umsatzbasierte Meilensteinzahlungen von bis zu 360 Mio. € sowie gestaffelte zweistellige Lizenzgebühren von bis zu 20 %.
Wir bleiben bis zum Abschluss der Doppelblindphase für die Phase-3-ELATIVE-Studie verantwortlich. Ipsen wird die Verantwortung für alle weiteren klinischen Entwicklungen übernehmen, einschließlich des Abschlusses der langfristigen Verlängerungsphase der ELATIVE-Studie und der weltweiten Kommerzialisierung (mit Ausnahme von Großchina, das an Terns lizenziert ist). Diese neu gegründete strategische Partnerschaft wird Ipsen durch das Recht auf erste Verhandlungen auch Zugang zu unseren Forschungskapazitäten und anderen klinischen Programmen verschaffen.
Darüber hinaus wurde Ipsen gemäß einer Investitionsvereinbarung, die am selben Tag wie die Kooperations- und Lizenzvereinbarung geschlossen wurde, durch den Kauf von 3.985.239 neu ausgegebenen Aktien, die nach der Ausgabe 8 % von GENFIT S.A. entsprechen, über eine Investition in Höhe von 28 Millionen Euro auch Aktionär von GENFIT . Die neuen Aktien unterliegen einer Sperrfrist, die entweder an dem Tag endet, an dem die EMA eine formelle Empfehlung an die Europäische Kommission für die Marktzulassung von Elafibranor in PBC abgibt, oder an dem Tag, an dem die US-amerikanische FDA die Zulassung erteilt Elafibranor bei PBC oder für den Fall, dass die ELATIVE-Studie ihren primären Endpunkt nicht erreicht. Nach der Zustimmung unserer Aktionäre auf der Aktionärsversammlung am 25. Mai 2022 wurde Ipsen Mitglied unseres Vorstands.
Die oben bereitgestellte Zusammenfassung erhebt keinen Anspruch auf Vollständigkeit und wird in ihrer Gesamtheit durch Verweis auf die vollständige Vereinbarung, die ein Anhang zu diesem Jahresbericht ist, eingeschränkt.
und dann hat Genfit noch die Kooperations- und Lizenzvereinbarung mit Terns Pharmaceuticals, Inc.
Am 24. Juni 2019 haben wir eine Kooperations- und Lizenzvereinbarung mit Terns Pharmaceuticals, Inc. oder Terns geschlossen, einem globalen biopharmazeutischen Unternehmen mit Sitz in den USA und China, dessen Schwerpunkt auf der Entwicklung neuartiger und Kombinationstherapien zur Behandlung von Lebererkrankungen liegt. Im Rahmen der Vereinbarung erhält Terns die Rechte zur Entwicklung und Vermarktung von Elafibranor, unserem firmeneigenen Prüfpräparat, auf dem chinesischen Festland, Hongkong, Macau und Taiwan (wir nennen es „Großchina“) für die Behandlung von NASH und PBC.
Gemäß den Bedingungen der Lizenzvereinbarung haben wir von Terns eine Vorauszahlung in Höhe von 35 Millionen US-Dollar erhalten
und sind berechtigt, bis zu 193 Millionen US-Dollar an potenziellen klinischen, regulatorischen und kommerziellen Meilensteinzahlungen zu erhalten. Terns erhält die exklusiven Rechte zur Entwicklung, Registrierung und Vermarktung von Elafibranor im Großraum China sowohl für NASH als auch für PBC. Nach der kommerziellen Markteinführung von Elafibranor zur Behandlung von NASH im Großraum China haben wir Anspruch auf Lizenzgebühren im mittleren Zehnprozentsatz von Terns, basierend auf den Verkäufen in diesem Gebiet.
Im Rahmen der Vereinbarung werden wir und Terns auch gemeinsame Forschungs- und Entwicklungsprojekte im Bereich Lebererkrankungen durchführen, einschließlich der Entwicklung von Elafibranor in Kombination mit den firmeneigenen Verbindungen von Terns.
Die oben bereitgestellte Zusammenfassung erhebt keinen Anspruch auf Vollständigkeit und wird in ihrer Gesamtheit durch Verweis auf die vollständige Vereinbarung, die ein Anhang zu diesem Jahresbericht ist, eingeschränkt.
Präsentation:
https://ir.genfit.com/static-files/069b79c6-6358-426c-8b59-06226784a333

 Frankreich
Frankreich








 Frankreich
Frankreich Frankreich
Frankreich