Ligand - Turnouround vor dem Herren? - 500 Beiträge pro Seite
eröffnet am 17.03.09 16:44:35 von
neuester Beitrag 31.01.21 11:22:21 von
neuester Beitrag 31.01.21 11:22:21 von
Beiträge: 273
ID: 1.149.070
ID: 1.149.070
Aufrufe heute: 1
Gesamt: 17.273
Gesamt: 17.273
Aktive User: 0
ISIN: US53220K5048 · WKN: A1C9RN · Symbol: LGDN
66,50
EUR
+1,53 %
+1,00 EUR
Letzter Kurs 24.04.24 Tradegate
Neuigkeiten
23.04.24 · Business Wire (engl.) |
08.04.24 · Business Wire (engl.) |
03.04.24 · Business Wire (engl.) |
05.03.24 · Business Wire (engl.) |
04.03.24 · Business Wire (engl.) |
Werte aus der Branche Pharmaindustrie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,3300 | +52,87 | |
| 6,0000 | +25,00 | |
| 9,2900 | +20,96 | |
| 111,75 | +18,87 | |
| 0,6400 | +18,52 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,8410 | -17,06 | |
| 9,7200 | -19,60 | |
| 2,7280 | -29,14 | |
| 14,510 | -32,32 | |
| 8,0000 | -36,76 |
Ich denke vielen ist der Name Ligand Pharmaceuticals noch bekannt und vermutlich in eher unangenehmer Erinnerung geblieben.
Ich halte Ligand zur Zeit aber als attraktistes Investment in dem Bereich und würde mich freuen, wenn andere Community-Mitglieder sich den Wert ansehen und ihre Meinung mitteilen.
Zur kurzen Übersicht einige Highligts:
Zulassung von Promacta im November erhalten (vertrieben durch GsK 5-10% Royalties))
Avinza am Markt (King macht damit ca. 150 Mio. Umsatz - z.Zt. 5% Royalties)
3 Medikamente in der Zulasung (Pfizer und Wyeth also Pfizer - nicht so wichtig, da nur 1-2% Royalties)
- nicht so wichtig, da nur 1-2% Royalties)
Im Dezember Verpartnerung von LGD-4665 an Glaxo zu 16% Royalties!)
Insgesamt sieht die Pipeline von Ligand so aus:
2 Medikamente am Markt bzw. zugelassen (King bzw. GlaxoSmithKline)
2 in Phase III (Pfizer, Wyeth)
5 in Phase II (Shering-Plough, Bristol-Myers Squibb, GlaxoSmithKline)
5 in Phase I (Celgene, Bristol-Myers-Squibb)
6 Präklinisch
Z.Zt potenzielle Meilensteinzahlungen von 500 Mio + Royalties
zuletzt gute Ergebnisse zu Dara gegen Bluthochdruck - Partner wird hier gesucht!
Marktkapitalisierung z.Zt. 320 Mio. Dollar
Kurze Rückblende:
Ligand ist ein \\\\\\\\\\\\\\\"alter Hase\\\\\\\\\\\\\\\" hatte bereits einige Medikamente auf den Markt gebracht - diese in eigener Regie vertrieben. Kam so aber so nicht wirklich auf einen grünen Zweig und verkaufte seine Onkologiemedikamente (3?).
Verpartnerte sein Schmerzmedikament an King. Hedgefonds stiegen ein und drängten auf eine Sonderdividende. Alles sehr unschön! Aktie wurde abgestraft. Pharmacopeia wurde gekauft - was der Markt auch nicht wirklich guthieß. Aber die neue Strategie wird langsam ersichtlich. Viele Medikamente, die nun nicht mehr in Eigenregie vertrieben werden sollen, sondern verpartnert sind.
Dann die Wende?
Die Zulassung von Promacta kann als Meilenstein angesehn werden. Es ist ein Medikament zur Vermehrung der Blutplättchen. Blut besteht bekanntlich aus rote und weißen Blutkörpern sowie Blutplättchen.
Neben Nplate von Amgen ist Promacta das einzig zugelassene Medikament. Nplate ist auch nur kurz davor zugelassen worden. Interessant ist langfristig, dass es mehrere Krankheitsblder gibt, bei denen eine Vermehrung der Blutplättchen von Vorteil sein könnte. Z.Zt ist es gegen ICP zugelassen. So hat Glaxo mehrere weitere Studien z.B zu Hepatitis C (III) (andere II) am laufen. Langfristig wird dem Medikamt Blockbuster Potenzial zugeschrieben. Die Chanchen sich gegen Nplate durchzusetzen sind nicht schlecht.
Als nächstes gutes Zeichen ist die Verpartnerung von LGD-4665 zu sehen - auch ein Blutplättchen-Vermehrer. Hier ist GSK schon zu 16% Royalties bereit.
Ein weiteres gutes Zeichen ist die unglaubliche relative Stärke. Wer mag sollte sich den Chart anschauen.
Grundsätzlich verfügt Ligand also über eine Menge Assets und hier ist vor allem die schon jetzt fast komplett verpartnerte Pipeline zu nennen. Und die ist nicht gerade an Laufkundschaft gegeangen:
GsK, Pfizer, Schering-Plough (Merck), Bristol Myers Squibb, Celgene...
Zum Schluss noch einige Links:
http://www.ligand.com/
http://www.fiercebiotech.com/tags/ligand-pharmaceuticals
http://finance.yahoo.com/q?s=LGND
Ich halte Ligand für absolut unterbewertet. Bis 2013 könnten 7 weitere Medikamente zugelassen werden. Im Gegenteil von vielen anderen Biotechs hat Ligand schon mehrmals bewiesen, dass auf Basis ihrer Technologie Medikamente entwickelt werden können, die es dann auch bis auf den Markt schaffen. Kurzfristig hängt die Entwicklung vor allem an Promacta und der Verpartnerung von DARA.
Meinungen?
Ich halte Ligand zur Zeit aber als attraktistes Investment in dem Bereich und würde mich freuen, wenn andere Community-Mitglieder sich den Wert ansehen und ihre Meinung mitteilen.
Zur kurzen Übersicht einige Highligts:
Zulassung von Promacta im November erhalten (vertrieben durch GsK 5-10% Royalties))
Avinza am Markt (King macht damit ca. 150 Mio. Umsatz - z.Zt. 5% Royalties)
3 Medikamente in der Zulasung (Pfizer und Wyeth also Pfizer
 - nicht so wichtig, da nur 1-2% Royalties)
- nicht so wichtig, da nur 1-2% Royalties)Im Dezember Verpartnerung von LGD-4665 an Glaxo zu 16% Royalties!)
Insgesamt sieht die Pipeline von Ligand so aus:
2 Medikamente am Markt bzw. zugelassen (King bzw. GlaxoSmithKline)
2 in Phase III (Pfizer, Wyeth)
5 in Phase II (Shering-Plough, Bristol-Myers Squibb, GlaxoSmithKline)
5 in Phase I (Celgene, Bristol-Myers-Squibb)
6 Präklinisch
Z.Zt potenzielle Meilensteinzahlungen von 500 Mio + Royalties
zuletzt gute Ergebnisse zu Dara gegen Bluthochdruck - Partner wird hier gesucht!
Marktkapitalisierung z.Zt. 320 Mio. Dollar
Kurze Rückblende:
Ligand ist ein \\\\\\\\\\\\\\\"alter Hase\\\\\\\\\\\\\\\" hatte bereits einige Medikamente auf den Markt gebracht - diese in eigener Regie vertrieben. Kam so aber so nicht wirklich auf einen grünen Zweig und verkaufte seine Onkologiemedikamente (3?).
Verpartnerte sein Schmerzmedikament an King. Hedgefonds stiegen ein und drängten auf eine Sonderdividende. Alles sehr unschön! Aktie wurde abgestraft. Pharmacopeia wurde gekauft - was der Markt auch nicht wirklich guthieß. Aber die neue Strategie wird langsam ersichtlich. Viele Medikamente, die nun nicht mehr in Eigenregie vertrieben werden sollen, sondern verpartnert sind.
Dann die Wende?
Die Zulassung von Promacta kann als Meilenstein angesehn werden. Es ist ein Medikament zur Vermehrung der Blutplättchen. Blut besteht bekanntlich aus rote und weißen Blutkörpern sowie Blutplättchen.
Neben Nplate von Amgen ist Promacta das einzig zugelassene Medikament. Nplate ist auch nur kurz davor zugelassen worden. Interessant ist langfristig, dass es mehrere Krankheitsblder gibt, bei denen eine Vermehrung der Blutplättchen von Vorteil sein könnte. Z.Zt ist es gegen ICP zugelassen. So hat Glaxo mehrere weitere Studien z.B zu Hepatitis C (III) (andere II) am laufen. Langfristig wird dem Medikamt Blockbuster Potenzial zugeschrieben. Die Chanchen sich gegen Nplate durchzusetzen sind nicht schlecht.
Als nächstes gutes Zeichen ist die Verpartnerung von LGD-4665 zu sehen - auch ein Blutplättchen-Vermehrer. Hier ist GSK schon zu 16% Royalties bereit.
Ein weiteres gutes Zeichen ist die unglaubliche relative Stärke. Wer mag sollte sich den Chart anschauen.
Grundsätzlich verfügt Ligand also über eine Menge Assets und hier ist vor allem die schon jetzt fast komplett verpartnerte Pipeline zu nennen. Und die ist nicht gerade an Laufkundschaft gegeangen:
GsK, Pfizer, Schering-Plough (Merck), Bristol Myers Squibb, Celgene...
Zum Schluss noch einige Links:
http://www.ligand.com/
http://www.fiercebiotech.com/tags/ligand-pharmaceuticals
http://finance.yahoo.com/q?s=LGND
Ich halte Ligand für absolut unterbewertet. Bis 2013 könnten 7 weitere Medikamente zugelassen werden. Im Gegenteil von vielen anderen Biotechs hat Ligand schon mehrmals bewiesen, dass auf Basis ihrer Technologie Medikamente entwickelt werden können, die es dann auch bis auf den Markt schaffen. Kurzfristig hängt die Entwicklung vor allem an Promacta und der Verpartnerung von DARA.
Meinungen?
Ligand paints an optimistic picture for 2009
Ligand Pharmaceuticals turned up at BIO's annual investor confab in New York this morning with some news to report.
The developer, which has inked a string of deals with some of the world's top pharma companies, earned a million-dollar milestone payment from Schering-Plough for the progress being made in an Alzheimer's program--an asset that was acquired with Ligand's recent buyout of Pharmacopeia.
But there's nothing new about making news at Ligand. Over the past 75 days Ligand reported an approval for Promacta (for thrombocytopenia); a full response letter was issued by the FDA for Fablyn, developed by Pfizer with technology from Ligand; there was a licensing deal with GlaxoSmithKline; positive mid-stage data came in on its hypertension therapy; a new screening deal was forged with Trevena and Ligand closed the deal to buy Pharmacopeia--which in turn helped generate some of the recent headlines.
"We have a company with great assets," says Ligand's upbeat CEO, John Higgins. And most of them have been partnered with companies like Glaxo, Pfizer, Schering-Plough, Wyeth, Bristol-Myers Squibb and King Pharmaceuticals. Out of 25 programs spelled out in its pipeline illustration, all but four are partnered.
Despite the tsunami of bad tidings that has swept over the biotech industry in recent months, Higgins is sticking with an optimistic forecast for 2009.
"We think this is going to be a momentous year for Ligand," says an enthusiastic Higgins. And in the years to come, he added, Ligand has established development timelines for a string of programs that could reach approval in or around 2013.
One of the reasons why Higgins can be optimistic is the steady stream of money the developer can rely on from its partners. In addition to a potential half billion dollars in prospective milestones, Ligand also has research deals with Schering-Plough and Wyeth that bring in millions of dollars in annual research income. Higgins is hopeful that Promacta will be a winner. And the CEO touted the company's discovery work for boosting platelet counts. One of its programs, LGD-4665, is in an ongoing Phase II trial and has turned in evidence of significantly boosting platelet counts.
"The anemia category is huge," says the CEO. "Platelets are at the forefront of hematologists' minds."
Higgins is equally upbeat about DARA, a dual-acting receptor antagonist that blocks the AT1 and ETa receptors. Ligand acquired DARA when it closed on Pharmacopeia at the end of last year.
Ligand recently released positive Phase IIb data on DARA that turned in some impressive numbers for treating hypertensive patients. While only nine percent of the placebo arm in the trial achieved the targeted blood pressure goal in the trial, 36 percent of the low-dose DARA group hit the mark and 61.5 percent of the high-dose group achieved the desired blood pressure goal.
Even better, from Ligand's perspective, is that the program is one of the few that the company doesn't have a partner for. That's something that Higgins and his team of executives plans to remedy as soon as possible. As Higgins noted this morning, Ligand is out to partner its assets at "the earliest inflection point possible."
To complete the deal for Pharmacopeia, Ligand issued about 18 million shares of Ligand common stock to Pharmacopeia stockholders along with $9.3 million in cash. Pharmacopeia shareholders also received a contingent value right that entitles them to an aggregate cash payment of $15 million under certain circumstances. And in a short period of time, Ligand has already managed to gin some revenue off of the deal.
If Higgins is right, there will be more such announcements in the years ahead.
Ligand Pharmaceuticals turned up at BIO's annual investor confab in New York this morning with some news to report.
The developer, which has inked a string of deals with some of the world's top pharma companies, earned a million-dollar milestone payment from Schering-Plough for the progress being made in an Alzheimer's program--an asset that was acquired with Ligand's recent buyout of Pharmacopeia.
But there's nothing new about making news at Ligand. Over the past 75 days Ligand reported an approval for Promacta (for thrombocytopenia); a full response letter was issued by the FDA for Fablyn, developed by Pfizer with technology from Ligand; there was a licensing deal with GlaxoSmithKline; positive mid-stage data came in on its hypertension therapy; a new screening deal was forged with Trevena and Ligand closed the deal to buy Pharmacopeia--which in turn helped generate some of the recent headlines.
"We have a company with great assets," says Ligand's upbeat CEO, John Higgins. And most of them have been partnered with companies like Glaxo, Pfizer, Schering-Plough, Wyeth, Bristol-Myers Squibb and King Pharmaceuticals. Out of 25 programs spelled out in its pipeline illustration, all but four are partnered.
Despite the tsunami of bad tidings that has swept over the biotech industry in recent months, Higgins is sticking with an optimistic forecast for 2009.
"We think this is going to be a momentous year for Ligand," says an enthusiastic Higgins. And in the years to come, he added, Ligand has established development timelines for a string of programs that could reach approval in or around 2013.
One of the reasons why Higgins can be optimistic is the steady stream of money the developer can rely on from its partners. In addition to a potential half billion dollars in prospective milestones, Ligand also has research deals with Schering-Plough and Wyeth that bring in millions of dollars in annual research income. Higgins is hopeful that Promacta will be a winner. And the CEO touted the company's discovery work for boosting platelet counts. One of its programs, LGD-4665, is in an ongoing Phase II trial and has turned in evidence of significantly boosting platelet counts.
"The anemia category is huge," says the CEO. "Platelets are at the forefront of hematologists' minds."
Higgins is equally upbeat about DARA, a dual-acting receptor antagonist that blocks the AT1 and ETa receptors. Ligand acquired DARA when it closed on Pharmacopeia at the end of last year.
Ligand recently released positive Phase IIb data on DARA that turned in some impressive numbers for treating hypertensive patients. While only nine percent of the placebo arm in the trial achieved the targeted blood pressure goal in the trial, 36 percent of the low-dose DARA group hit the mark and 61.5 percent of the high-dose group achieved the desired blood pressure goal.
Even better, from Ligand's perspective, is that the program is one of the few that the company doesn't have a partner for. That's something that Higgins and his team of executives plans to remedy as soon as possible. As Higgins noted this morning, Ligand is out to partner its assets at "the earliest inflection point possible."
To complete the deal for Pharmacopeia, Ligand issued about 18 million shares of Ligand common stock to Pharmacopeia stockholders along with $9.3 million in cash. Pharmacopeia shareholders also received a contingent value right that entitles them to an aggregate cash payment of $15 million under certain circumstances. And in a short period of time, Ligand has already managed to gin some revenue off of the deal.
If Higgins is right, there will be more such announcements in the years ahead.
Hab grad nochmal genauer rechechiert.
Fablyn (vermarktet von Pfizer) hat bereits die Empfehlung zu Zulassung bekommen - dem wird dann ja meistens entsprochen. Es werden dem Medikament Umsätze über 1 Milliarde zugetraut. Ligand bekommt 3% Royalties!!
Viviant/Aprela (vermarktet von Wyeth/Pfizer) ist in der Zulassung. Im Sommer wird darüber entschieden. Umsätze von über 2 Milliarden werden dem Medikament (Aprela ist eine Kombination aus Viviant und Östrogen) zugetraut.
Ab 1 Milliarde bekommt Ligand 2,5 % Royalties / 0,5 % unter 400 Mio/ 1,5 % zwischen 400 Mio und ! Milliarde.
Ligand hat somit 1 Blockbuster Medikament bereits zugelassen (Promacta/ GlaxoSmithkline/5-10 % Royalties).
2 weitere könnten 2009 folgen (Pfizer)!!!!
Im Gegensatz zu anderen hier heiß diskutierten Werten werden die Medikamente auch von potenten Partnern vertrieben. Denn was nützt ein zugelassenes Medikament, dass kaum Umsätze generiert?
Bei Interesse kann ich gerne eine aktuelle Präsentation von Ligand verlinken bzw. zusenden.
Fablyn (vermarktet von Pfizer) hat bereits die Empfehlung zu Zulassung bekommen - dem wird dann ja meistens entsprochen. Es werden dem Medikament Umsätze über 1 Milliarde zugetraut. Ligand bekommt 3% Royalties!!
Viviant/Aprela (vermarktet von Wyeth/Pfizer) ist in der Zulassung. Im Sommer wird darüber entschieden. Umsätze von über 2 Milliarden werden dem Medikament (Aprela ist eine Kombination aus Viviant und Östrogen) zugetraut.
Ab 1 Milliarde bekommt Ligand 2,5 % Royalties / 0,5 % unter 400 Mio/ 1,5 % zwischen 400 Mio und ! Milliarde.
Ligand hat somit 1 Blockbuster Medikament bereits zugelassen (Promacta/ GlaxoSmithkline/5-10 % Royalties).
2 weitere könnten 2009 folgen (Pfizer)!!!!
Im Gegensatz zu anderen hier heiß diskutierten Werten werden die Medikamente auch von potenten Partnern vertrieben. Denn was nützt ein zugelassenes Medikament, dass kaum Umsätze generiert?
Bei Interesse kann ich gerne eine aktuelle Präsentation von Ligand verlinken bzw. zusenden.
FABLYN(R) Approved in Europe for the Treatment of Osteoporosis
Ligand Earns Milestone Payment from Pfizer
SAN DIEGO, Mar 24, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced that its partner, Pfizer, Inc. (NYSE: PFE) has received approval from the European Commission(EC) for FABLYN(R) (lasofoxifene) Tablets, a selective estrogen receptor modulator (SERM) for the treatment of osteoporosis in post-menopausal women at increased risk of fracture. FABLYN was submitted for approval in Europe in January 2008. This is the first regulatory approval for FABLYN, a product that stems from a 1991 research collaboration with Ligand.
As a result of the first approval of FABLYN in a major market, Ligand has earned a $3 million milestone payment. Pursuant to the 1991 research agreement and 1996 settlement agreement with Pfizer, Pfizer has elected to pay the milestone payment by returning 323,338 shares of stock it owns in Ligand. The shares are valued as of the date of the settlement agreement adjusted for Ligand's 2007 return of capital paid to Ligand shareholders. After the payment of this milestone, Pfizer owns a remaining 674,230 shares in Ligand.
Pfizer is responsible for the registration and worldwide marketing of FABLYN. Ligand is entitled to receive royalty payments on net sales of the product. In January 2009, Pfizer received a complete response letter from the FDA requesting additional information for FABLYN. On September 8, 2008, the FDA's Advisory Committee for Reproductive Health Drugs voted 9-3 (with one abstention) that there is a population of postmenopausal women with osteoporosis in which the benefits of lasofoxifene likely outweigh the risks. FDA is not required to follow the advice of the panel.
"Today's announcement is an exciting development for Ligand as the European approval of FABLYN marks the fourth drug associated with Ligand's research platform that has been approved and the second to be approved in just the past six months. This milestone payment reduces Ligand's outstanding shares and paves the way for potential future royalty payments and cash flow following the launch of the product," said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. "We applaud Pfizer for its commitment and diligence in advancing the product to approval and developing an alternative treatment option for patients in Europe with osteoporosis."
Osteoporosis Prevalence
The International Osteoporosis Foundation (IOF) reports that more than 75 million people suffer from osteoporosis in Europe, Japan and the U.S. About 30% of all post-menopausal women have osteoporosis in Europe and in the U.S., and at least 40% of them will suffer osteoporotic fractures in their lifetime. In Europe alone, 3.78 million osteoporosis-related fractures were reported in 2000, with an estimated cost of 32 billion euros. In the U.S., the National Osteoporosis Foundation projects an estimated 10 million American women to have osteoporosis in 2010 and almost 26 million to have osteopenia (low-bone mass), placing them at increased risk of osteoporosis.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals. With nine pharmaceutical deals and more than twenty different molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Schon wieder gute News von Ligand! Wird sich auf jeden Fall positiv auf die Bilanz auswirken - auch wenn Ligand "nur" 3% Royalties bekommt. Verwundern tut mich gar nicht, dass Pfizer die Milestones in Aktien von Ligand zurückzahlt, da sie zum Wert von 1996 eingepreist werden und und da stand Ligand um einiges höher.
Trotzdem fantastische news - und eine Zulassung der fda wird dadurch auch nicht eben unwahrscheinlicher!
Somit sind schon 3 Medikamente zugelassen...
Ligand Earns Milestone Payment from Pfizer
SAN DIEGO, Mar 24, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced that its partner, Pfizer, Inc. (NYSE: PFE) has received approval from the European Commission(EC) for FABLYN(R) (lasofoxifene) Tablets, a selective estrogen receptor modulator (SERM) for the treatment of osteoporosis in post-menopausal women at increased risk of fracture. FABLYN was submitted for approval in Europe in January 2008. This is the first regulatory approval for FABLYN, a product that stems from a 1991 research collaboration with Ligand.
As a result of the first approval of FABLYN in a major market, Ligand has earned a $3 million milestone payment. Pursuant to the 1991 research agreement and 1996 settlement agreement with Pfizer, Pfizer has elected to pay the milestone payment by returning 323,338 shares of stock it owns in Ligand. The shares are valued as of the date of the settlement agreement adjusted for Ligand's 2007 return of capital paid to Ligand shareholders. After the payment of this milestone, Pfizer owns a remaining 674,230 shares in Ligand.
Pfizer is responsible for the registration and worldwide marketing of FABLYN. Ligand is entitled to receive royalty payments on net sales of the product. In January 2009, Pfizer received a complete response letter from the FDA requesting additional information for FABLYN. On September 8, 2008, the FDA's Advisory Committee for Reproductive Health Drugs voted 9-3 (with one abstention) that there is a population of postmenopausal women with osteoporosis in which the benefits of lasofoxifene likely outweigh the risks. FDA is not required to follow the advice of the panel.
"Today's announcement is an exciting development for Ligand as the European approval of FABLYN marks the fourth drug associated with Ligand's research platform that has been approved and the second to be approved in just the past six months. This milestone payment reduces Ligand's outstanding shares and paves the way for potential future royalty payments and cash flow following the launch of the product," said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. "We applaud Pfizer for its commitment and diligence in advancing the product to approval and developing an alternative treatment option for patients in Europe with osteoporosis."
Osteoporosis Prevalence
The International Osteoporosis Foundation (IOF) reports that more than 75 million people suffer from osteoporosis in Europe, Japan and the U.S. About 30% of all post-menopausal women have osteoporosis in Europe and in the U.S., and at least 40% of them will suffer osteoporotic fractures in their lifetime. In Europe alone, 3.78 million osteoporosis-related fractures were reported in 2000, with an estimated cost of 32 billion euros. In the U.S., the National Osteoporosis Foundation projects an estimated 10 million American women to have osteoporosis in 2010 and almost 26 million to have osteopenia (low-bone mass), placing them at increased risk of osteoporosis.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals. With nine pharmaceutical deals and more than twenty different molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Schon wieder gute News von Ligand! Wird sich auf jeden Fall positiv auf die Bilanz auswirken - auch wenn Ligand "nur" 3% Royalties bekommt. Verwundern tut mich gar nicht, dass Pfizer die Milestones in Aktien von Ligand zurückzahlt, da sie zum Wert von 1996 eingepreist werden und und da stand Ligand um einiges höher.
Trotzdem fantastische news - und eine Zulassung der fda wird dadurch auch nicht eben unwahrscheinlicher!
Somit sind schon 3 Medikamente zugelassen...
Eine gute Zusammenfassung zum aktuellen Stand der 3 bzw. 2 in der Zulassung befindlichen Medikamente:
The FDA Leaves Pfizer in the Waiting Room
Pfizer (NYSE: PFE) has nothing to be upset about with the European Union. Like clockwork, on Tuesday it approved Pfizer\'s and Ligand Pharmaceuticals\' (Nasdaq: LGND) osteoporosis drug, Fablyn, after the EU drug panel had given a positive opinion about the drug in December.
On the other hand, in the U.S., an advisory panel voted 9-3 (with one abstention) recommending approval of the drug, but the Food and Drug Administration sent Pfizer a response letter in January. Pfizer wasn\'t very forthcoming in its press release, so it\'s not clear exactly what it will need to do to get the drug approved.
The EU approval comes with a $3 million milestone payment for Ligand, but unfortunately for Ligand, it won\'t be in the form of cash. Pfizer is returning about a third of the shares of Ligand it owns as payment. But the deal works out well for Pfizer because the 323,000-plus shares it\'s using for that milestone payment are valued at roughly $9.27 each, more than three times Ligand\'s stock price, thanks to two agreements back in the 1990s.
However, the resulting lower number of shares outstanding will benefit Ligand\'s investors at least a small bit because they now own a slightly larger share of the pie. (The returned shares are about 0.28% of the total outstanding shares.) Unfortunately, the pie is still bleeding cash, and Ligand certainly could have used the cash. The company will get royalties on sales of Fablyn, so at least there\'s some green stuff headed its way.
Ironically, Ligand has a pair of deals with Wyeth (NYSE: WYE) to develop an osteoporosis treatment in the same class of drugs -- selective estrogen receptor modulator (SERM). The FDA also rejected one, Viviant, in its first attempt at approval. A filing for approval is expected for the other one -- Viviant plus Wyeth\'s Premarin -- in the second half of the year. However, once Pfizer completes its acquisition of Wyeth, it\'s not clear whether it\'ll need all three SERMs -- assuming they eventually get approved -- and that could affect potential royalties for Ligand.
Ligand\'s best hope is probably that the government makes Pfizer dispose of one or more of the SERMs, but I don\'t know how likely that is. Eli Lilly (NYSE: LLY) has a SERM, Evista, on the market to treat osteoporosis. And there\'s plenty of other osteoporosis drugs, like GlaxoSmithKline\'s (NYSE: GSK) Boniva and generic versions of Merck\'s (NYSE: MRK) Fosamax, as well as up-and-comers like Amgen\'s (Nasdaq: AMGN) denosumab.
The market for osteoporosis treatment is in flux -- no bones about it.
Quelle: http://www.fool.com/investing/general/2009/03/25/the-fda-lea…
The FDA Leaves Pfizer in the Waiting Room
Pfizer (NYSE: PFE) has nothing to be upset about with the European Union. Like clockwork, on Tuesday it approved Pfizer\'s and Ligand Pharmaceuticals\' (Nasdaq: LGND) osteoporosis drug, Fablyn, after the EU drug panel had given a positive opinion about the drug in December.
On the other hand, in the U.S., an advisory panel voted 9-3 (with one abstention) recommending approval of the drug, but the Food and Drug Administration sent Pfizer a response letter in January. Pfizer wasn\'t very forthcoming in its press release, so it\'s not clear exactly what it will need to do to get the drug approved.
The EU approval comes with a $3 million milestone payment for Ligand, but unfortunately for Ligand, it won\'t be in the form of cash. Pfizer is returning about a third of the shares of Ligand it owns as payment. But the deal works out well for Pfizer because the 323,000-plus shares it\'s using for that milestone payment are valued at roughly $9.27 each, more than three times Ligand\'s stock price, thanks to two agreements back in the 1990s.
However, the resulting lower number of shares outstanding will benefit Ligand\'s investors at least a small bit because they now own a slightly larger share of the pie. (The returned shares are about 0.28% of the total outstanding shares.) Unfortunately, the pie is still bleeding cash, and Ligand certainly could have used the cash. The company will get royalties on sales of Fablyn, so at least there\'s some green stuff headed its way.
Ironically, Ligand has a pair of deals with Wyeth (NYSE: WYE) to develop an osteoporosis treatment in the same class of drugs -- selective estrogen receptor modulator (SERM). The FDA also rejected one, Viviant, in its first attempt at approval. A filing for approval is expected for the other one -- Viviant plus Wyeth\'s Premarin -- in the second half of the year. However, once Pfizer completes its acquisition of Wyeth, it\'s not clear whether it\'ll need all three SERMs -- assuming they eventually get approved -- and that could affect potential royalties for Ligand.
Ligand\'s best hope is probably that the government makes Pfizer dispose of one or more of the SERMs, but I don\'t know how likely that is. Eli Lilly (NYSE: LLY) has a SERM, Evista, on the market to treat osteoporosis. And there\'s plenty of other osteoporosis drugs, like GlaxoSmithKline\'s (NYSE: GSK) Boniva and generic versions of Merck\'s (NYSE: MRK) Fosamax, as well as up-and-comers like Amgen\'s (Nasdaq: AMGN) denosumab.
The market for osteoporosis treatment is in flux -- no bones about it.
Quelle: http://www.fool.com/investing/general/2009/03/25/the-fda-lea…
Nun ist auch das zweite in Zulassung befindliche Medikament zumindest in Europa zugelassen. Wie oben beschrieben ist das nicht sooo wichtig, aber bestimmt kein Nachteil...
Das ist die 3.Zulassung innerhalb von 6 Monaten! Die Medikamente werden von GlaxoSmithkline, Pfizer und Wyeth (s.O.) vertrieben.
(s.O.) vertrieben.
SAN DIEGO--(BUSINESS WIRE)--Ligand Pharmaceuticals Incorporated today announced that its partner Wyeth has received approval from the European Commission (EC) for CONBRIZA™ (bazedoxifene), a selective estrogen receptor modulator (SERM) for the treatment of postmenopausal osteoporosis in women at increased risk of fracture.
CONBRIZA was submitted for approval in Europe in September 2007. This is the first regulatory approval for bazedoxifene, a product stemming from a 1994 research collaboration between Wyeth and Ligand. Wyeth is responsible for the registration and worldwide marketing of bazedoxifene, a synthetic drug specifically designed to reduce the risk of osteoporotic fractures while also protecting breast and uterine tissue.
As a result of the European approval of bazedoxifene, Ligand has earned a $550,000 milestone payment, and is entitled to receive royalty payments on net sales of the product. Wyeth intends to introduce CONBRIZA in Europe following receipt of necessary reimbursement authorizations.
“Today’s announcement is an exciting development for Ligand as the European approval of CONBRIZA marks the fifth drug associated with Ligand’s research platform that has been approved and the third to be approved in just the past six months,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. “We are very pleased with Wyeth's development progress and commitment to bringing a new osteoporosis treatment option to postmenopausal women in Europe.”
Wyeth is pursuing U.S. regulatory approval of bazedoxifene for the prevention and treatment of osteoporosis in postmenopausal women. In June 2006 Wyeth submitted a New Drug Application (NDA) for bazedoxifene to the U.S. Food and Drug Administration (FDA) for the prevention of postmenopausal osteoporosis, and in July 2007 submitted an NDA for bazedoxifene for the treatment of postmenopausal osteoporosis. Wyeth has indicated that it will file a complete response in 2009 and anticipates the FDA to convene an advisory committee to review the pending NDAs for both indications. Ligand is entitled to an $850,000 milestone payment upon approval of bazedoxifene in the U.S.
Wyeth is also studying bazedoxifene/conjugated estrogens, an investigational compound for the treatment of moderate to severe menopausal vasomotor symptoms such as hot flashes and night sweats and for the prevention of postmenopausal osteoporosis. Wyeth expects to file an NDA for this compound no earlier than the first half of 2010. Ligand is entitled to receive tiered royalties on bazedoxifene and bazedoxifene/CE.
Osteoporosis Prevalence
The International Osteoporosis Foundation reports that more than 75 million people suffer from osteoporosis in Europe, Japan and the U.S. In Europe, about 30% of all post-menopausal women have osteoporosis, and 3.78 million osteoporosis-related fractures were reported in 2000, at an estimated cost of 32 billion euros. In the U.S., the National Osteoporosis Foundation projects that 10 million American women will have osteoporosis in 2010 and that at least 40% of them will suffer osteoporotic fractures in their lifetime. Another 26 million are expected to have osteopenia (low bone mass), placing them at increased risk of osteoporosis.
Osteoporosis is characterized by low bone mass and structural deterioration of bone tissue, leading to bone fragility and an increased risk of fractures. Up to 20% of a woman's expected lifetime bone loss can occur in the years immediately following menopause. The treatment of postmenopausal osteoporosis could lead to significant improvement in the overall health for millions of women worldwide as well as reduce costs associated with postmenopausal osteoporosis-related fractures.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world’s largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals. With nine pharmaceutical deals and more than twenty different molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Das ist die 3.Zulassung innerhalb von 6 Monaten! Die Medikamente werden von GlaxoSmithkline, Pfizer und Wyeth
 (s.O.) vertrieben.
(s.O.) vertrieben. SAN DIEGO--(BUSINESS WIRE)--Ligand Pharmaceuticals Incorporated today announced that its partner Wyeth has received approval from the European Commission (EC) for CONBRIZA™ (bazedoxifene), a selective estrogen receptor modulator (SERM) for the treatment of postmenopausal osteoporosis in women at increased risk of fracture.
CONBRIZA was submitted for approval in Europe in September 2007. This is the first regulatory approval for bazedoxifene, a product stemming from a 1994 research collaboration between Wyeth and Ligand. Wyeth is responsible for the registration and worldwide marketing of bazedoxifene, a synthetic drug specifically designed to reduce the risk of osteoporotic fractures while also protecting breast and uterine tissue.
As a result of the European approval of bazedoxifene, Ligand has earned a $550,000 milestone payment, and is entitled to receive royalty payments on net sales of the product. Wyeth intends to introduce CONBRIZA in Europe following receipt of necessary reimbursement authorizations.
“Today’s announcement is an exciting development for Ligand as the European approval of CONBRIZA marks the fifth drug associated with Ligand’s research platform that has been approved and the third to be approved in just the past six months,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. “We are very pleased with Wyeth's development progress and commitment to bringing a new osteoporosis treatment option to postmenopausal women in Europe.”
Wyeth is pursuing U.S. regulatory approval of bazedoxifene for the prevention and treatment of osteoporosis in postmenopausal women. In June 2006 Wyeth submitted a New Drug Application (NDA) for bazedoxifene to the U.S. Food and Drug Administration (FDA) for the prevention of postmenopausal osteoporosis, and in July 2007 submitted an NDA for bazedoxifene for the treatment of postmenopausal osteoporosis. Wyeth has indicated that it will file a complete response in 2009 and anticipates the FDA to convene an advisory committee to review the pending NDAs for both indications. Ligand is entitled to an $850,000 milestone payment upon approval of bazedoxifene in the U.S.
Wyeth is also studying bazedoxifene/conjugated estrogens, an investigational compound for the treatment of moderate to severe menopausal vasomotor symptoms such as hot flashes and night sweats and for the prevention of postmenopausal osteoporosis. Wyeth expects to file an NDA for this compound no earlier than the first half of 2010. Ligand is entitled to receive tiered royalties on bazedoxifene and bazedoxifene/CE.
Osteoporosis Prevalence
The International Osteoporosis Foundation reports that more than 75 million people suffer from osteoporosis in Europe, Japan and the U.S. In Europe, about 30% of all post-menopausal women have osteoporosis, and 3.78 million osteoporosis-related fractures were reported in 2000, at an estimated cost of 32 billion euros. In the U.S., the National Osteoporosis Foundation projects that 10 million American women will have osteoporosis in 2010 and that at least 40% of them will suffer osteoporotic fractures in their lifetime. Another 26 million are expected to have osteopenia (low bone mass), placing them at increased risk of osteoporosis.
Osteoporosis is characterized by low bone mass and structural deterioration of bone tissue, leading to bone fragility and an increased risk of fractures. Up to 20% of a woman's expected lifetime bone loss can occur in the years immediately following menopause. The treatment of postmenopausal osteoporosis could lead to significant improvement in the overall health for millions of women worldwide as well as reduce costs associated with postmenopausal osteoporosis-related fractures.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world’s largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals. With nine pharmaceutical deals and more than twenty different molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
PROMACTA Awarded 2009 Prix Galien for Best Biotechnology Product
SAN DIEGO, Oct 05, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND) today announced that PROMACTA(R) (eltrombopag), a drug discovered in collaboration with GlaxoSmithKline (NYSE:GSK), was recognized as "Best Biotechnology Product" by the Prix Galien USA committee on October 1, 2009. The 2009 Prix Galien USA is the pharmaceutical industry's highest R&D accolade for treatments that could change the course of healthcare worldwide. The Prix Galien Award recognizes the technical, scientific and clinical research skills necessary to develop innovative medicines, and is considered the equivalent to the Nobel Prize.
"We are very proud to see PROMACTA recognized at the highest levels of our industry," said Ligand Chief Executive Officer John L. Higgins. "The Prix Galien is a testament to our drug discovery collaboration partnership with GlaxoSmithKline and Ligand's ability to discover and develop drugs that will benefit patients worldwide."
www.ligand.com
SAN DIEGO, Oct 05, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND) today announced that PROMACTA(R) (eltrombopag), a drug discovered in collaboration with GlaxoSmithKline (NYSE:GSK), was recognized as "Best Biotechnology Product" by the Prix Galien USA committee on October 1, 2009. The 2009 Prix Galien USA is the pharmaceutical industry's highest R&D accolade for treatments that could change the course of healthcare worldwide. The Prix Galien Award recognizes the technical, scientific and clinical research skills necessary to develop innovative medicines, and is considered the equivalent to the Nobel Prize.
"We are very proud to see PROMACTA recognized at the highest levels of our industry," said Ligand Chief Executive Officer John L. Higgins. "The Prix Galien is a testament to our drug discovery collaboration partnership with GlaxoSmithKline and Ligand's ability to discover and develop drugs that will benefit patients worldwide."
www.ligand.com
ligand wurde obwohl die aussichten mittel-langfristig recht gut zu scheinen seien, mächtig runtergeprügelt.
ich bin am freitag auch zu 1,39€ rein,dürfte wohl kein fehler gewesen sein.
asics
ich bin am freitag auch zu 1,39€ rein,dürfte wohl kein fehler gewesen sein.
asics
Antwort auf Beitrag Nr.: 38.248.051 von asics01 am 25.10.09 11:26:37Hallo asics01,
auch charttechnisch ein guter Einstiegspunkt!
Interessant wird es für Ligand aber erst wieder, wenn Daten zu neuen Indikationen für Promacta anstehen.
Endlich nicht mehr alleine ;-)
auch charttechnisch ein guter Einstiegspunkt!
Interessant wird es für Ligand aber erst wieder, wenn Daten zu neuen Indikationen für Promacta anstehen.
Endlich nicht mehr alleine ;-)
Antwort auf Beitrag Nr.: 38.249.102 von kmastra am 25.10.09 18:23:45seit wann bist du dabei???wenn man sich so den chart anschaut kann einem auch das grosse grausen kommen,aber deswegen bin ich rein weil ich auf den längst fälligen turnouround hoffe.
die pipline ist gut da geht noch was,ob der einstieg zu früh war????
den richtigen einstiegspunkt kriegt man eh nie.also hoffen wir mal auf bessere kurse und bessere zeiten.
asics
die pipline ist gut da geht noch was,ob der einstieg zu früh war????
den richtigen einstiegspunkt kriegt man eh nie.also hoffen wir mal auf bessere kurse und bessere zeiten.
asics
hallo kmastra
du bist doch sicher auf dem laufenden,was ist denn aktuell sache
mit VIVANT und FABLYN???
danke asics
du bist doch sicher auf dem laufenden,was ist denn aktuell sache
mit VIVANT und FABLYN???
danke asics
Antwort auf Beitrag Nr.: 38.254.266 von asics01 am 26.10.09 16:57:35Hallo asics01,
keine Sorge. Ich bin mittlerweile zwar leicht im Minus, aber Gott sei Dank nicht lange dabei.
Bzgl. Vivant und Fablyn:
Beide wurden in der EU zugelassen aber noch nicht vermarktet. In den USA steht die Entscheidung der FDA noch aus. Whyeth wird demnächst P III Daten veröffentlichen. Grundsätzlich sind die Medikamente aber nicht so wichtig, da Ligand nur eine geringe Umsatzbeteiligung bekommt. Andererseits werden beiden Medikamenten Umsätze im Milliardenbereich zugetraut.
Spannend ist natürlich auch, dass Pfizer Whyeth geschluckt hat. Das könnte für Ligand zum Nachteil werden, da evtl. nur ein Medikament auch tatsächlich auf den Markt kommt - aber auch ein Vorteil, weil Ligand dann evtl. die Rechte des anderen Medikaments zurückbekommen und neu verpartnern könnte. Man muss abwarten. Charttechnisch befindet sch Ligan gerade in einer starken Unterstützungsbereich. Hoffentlich hätst...
keine Sorge. Ich bin mittlerweile zwar leicht im Minus, aber Gott sei Dank nicht lange dabei.
Bzgl. Vivant und Fablyn:
Beide wurden in der EU zugelassen aber noch nicht vermarktet. In den USA steht die Entscheidung der FDA noch aus. Whyeth wird demnächst P III Daten veröffentlichen. Grundsätzlich sind die Medikamente aber nicht so wichtig, da Ligand nur eine geringe Umsatzbeteiligung bekommt. Andererseits werden beiden Medikamenten Umsätze im Milliardenbereich zugetraut.
Spannend ist natürlich auch, dass Pfizer Whyeth geschluckt hat. Das könnte für Ligand zum Nachteil werden, da evtl. nur ein Medikament auch tatsächlich auf den Markt kommt - aber auch ein Vorteil, weil Ligand dann evtl. die Rechte des anderen Medikaments zurückbekommen und neu verpartnern könnte. Man muss abwarten. Charttechnisch befindet sch Ligan gerade in einer starken Unterstützungsbereich. Hoffentlich hätst...
Antwort auf Beitrag Nr.: 38.263.249 von kmastra am 27.10.09 17:20:58hallo kmastra
danke für die info,eine frage hätte ich noch was ist mit der onkologie sparte bei ligand,nach dem die ja ihre onkologie präparate verklopft haben????
danke
asics
danke für die info,eine frage hätte ich noch was ist mit der onkologie sparte bei ligand,nach dem die ja ihre onkologie präparate verklopft haben????
danke
asics
Antwort auf Beitrag Nr.: 38.264.708 von asics01 am 27.10.09 19:54:50So. Diesmal auch mit Zeit.
Die Onkologiesparte wurde für Geld verkauft. Ligand erhält keinerlei Royalties. Ein Teil des Geldes wurde als Sonderdividende ausgeschüttet. Ist aber schon lange her.
Ansonsten sind wenig Medikamente gegen Krebs in der Pipeline.
Schau doch einfach selbst:
http://img522.imageshack.us/img522/6951/imgdbg.jpg
Die Onkologiesparte wurde für Geld verkauft. Ligand erhält keinerlei Royalties. Ein Teil des Geldes wurde als Sonderdividende ausgeschüttet. Ist aber schon lange her.
Ansonsten sind wenig Medikamente gegen Krebs in der Pipeline.
Schau doch einfach selbst:
http://img522.imageshack.us/img522/6951/imgdbg.jpg
Antwort auf Beitrag Nr.: 38.265.156 von kmastra am 27.10.09 20:47:45die frage war falsch formuliert.
hat sich ligand nach dem verkauf seiner oncologie produkte weitgehend aus dem bereich forschung und entwicklung von oncologie produkten zurüchgezogen???
asics
hat sich ligand nach dem verkauf seiner oncologie produkte weitgehend aus dem bereich forschung und entwicklung von oncologie produkten zurüchgezogen???
asics
Antwort auf Beitrag Nr.: 38.248.051 von asics01 am 25.10.09 11:26:37Hallo asics,
Ligand hat sich nicht zurückgezogen. In der Pipeline sehe ich 2 Programme gegen Krebs. Eins zusammen mit Shering-Plough und eins in Eigenregie.
Was sagst du denn zu den Bemühungen Ligands Metabasis zu übernehmen?
Ich fänds großartig, da fast für lau und dafür Beteiligung im Erfolgsfall. Ligand würde seine Pipeline erheblich erweitern und mit Roche und Merck weitere starke Partner gewinnen. Übrigens ist in der Pipeline von Metabasis auch ein Medikament gegen Leberkrebs ;-)
Ligand hat sich nicht zurückgezogen. In der Pipeline sehe ich 2 Programme gegen Krebs. Eins zusammen mit Shering-Plough und eins in Eigenregie.
Was sagst du denn zu den Bemühungen Ligands Metabasis zu übernehmen?
Ich fänds großartig, da fast für lau und dafür Beteiligung im Erfolgsfall. Ligand würde seine Pipeline erheblich erweitern und mit Roche und Merck weitere starke Partner gewinnen. Übrigens ist in der Pipeline von Metabasis auch ein Medikament gegen Leberkrebs ;-)
Antwort auf Beitrag Nr.: 38.275.975 von kmastra am 29.10.09 00:09:02hallo kmastra
klar haben die sich nicht komplett zurüchgezogen ich schrieb ja auch weitgehend.egal seis drum
ich habe zur zeit sehr wenig zeit um mich mal richtig mit ligand auseinander zusetzetn.
ob die sich mit dieser transaktion nicht verlupfen????,na ich weiss nicht???
erstens kostet sowas immer geld (und die kleinen bios haben sowieso nie geld übrig)
zweitens kenne ich die aktuellen studien für metabasis nierenkrebs medikament nicht, onyx mit nexavar und pfizer mit student
sind schon am markt ist metabasis mbo7133 besser???
und deren produkte sind auch noch meilenweit von einer möglichen zulassung entfernt.
mal sehen wie der markt diese transaktion aufnimmt???,die werden wohl ligand mal vorerst abstrafen oder ????????
asics
klar haben die sich nicht komplett zurüchgezogen ich schrieb ja auch weitgehend.egal seis drum
ich habe zur zeit sehr wenig zeit um mich mal richtig mit ligand auseinander zusetzetn.
ob die sich mit dieser transaktion nicht verlupfen????,na ich weiss nicht???
erstens kostet sowas immer geld (und die kleinen bios haben sowieso nie geld übrig)
zweitens kenne ich die aktuellen studien für metabasis nierenkrebs medikament nicht, onyx mit nexavar und pfizer mit student
sind schon am markt ist metabasis mbo7133 besser???
und deren produkte sind auch noch meilenweit von einer möglichen zulassung entfernt.
mal sehen wie der markt diese transaktion aufnimmt???,die werden wohl ligand mal vorerst abstrafen oder ????????
asics
Ligand to Acquire Metabasis for Cash and Contingent Value Rights
Ligand to Gain Fully Funded Partnership with Roche for Hepatitis and Promising Development-Stage Programs
SAN DIEGO, Oct 27, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) and Metabasis Therapeutics, Inc. (NASDAQ: MBRX) announced today they have entered into a definitive merger agreement under which Ligand will acquire all of the outstanding shares of Metabasis.
Under the transaction, Metabasis stockholders will receive a cash payment at the closing of the transaction of approximately $3.2 million, less Metabasis' estimated net liabilities at closing and an amount to be deposited in the stockholders' representative's fund (Metabasis currently estimates the closing payment to be approximately $1.8 million in cash). In addition, Metabasis stockholders will receive for each Metabasis share four tradable Contingent Value Rights ("CVRs") that will be registered on a Form S-4 registration statement to be filed by Ligand with the Securities and Exchange Commission. The CVRs will entitle Metabasis stockholders to cash payments as frequently as every six months as cash is received by Ligand from proceeds from the sale or partnering of any of the Metabasis drug development programs, among other triggering events. Ligand has committed to spend at least $8 million in new research and development funding on the Metabasis programs within 42 months following the closing of the transaction.
The Ligand and Metabasis Boards of Directors have unanimously voted in favor of the transaction. Stockholders of Metabasis representing approximately 29% of the outstanding shares of Metabasis have signed voting agreements in support of the transaction. Merriman Curhan Ford acted as financial advisor to Metabasis with respect to this transaction.
"This transaction utilizes a creative structure that we believe is potentially highly beneficial to the stockholders of both companies," said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. "Ligand obtains numerous high-quality partnered and development-stage programs that will increase our revenue potential and expand our pipeline of proprietary assets. In exchange, the non-partnered Metabasis programs will be advanced by a company with strong and proven research credentials, with the goal of generating cash proceeds payable directly to Metabasis stockholders. If any or all of the Metabasis programs are financially successful, stockholders at both companies will benefit meaningfully from their shared participation in the programs."
Mark D. Erion, Ph.D., President, Chief Executive Officer and Chief Scientific Officer of Metabasis, stated, "Metabasis has built a pipeline of product candidates and drug development programs that have the potential to one day yield new therapies for metabolic and chronic liver diseases, but due to our limited financial and operational resources, we are unable to independently realize their full potential value. Ligand's strong research and business development capabilities, coupled with its solid financial position and its commitment to additional research and development funding as part of this transaction, gives Metabasis' portfolio of programs the potential to deliver significant future value to Metabasis' stockholders."
Highlights of the Proposed Transaction
Under the terms of the agreement, Ligand will pay at the closing of the transaction approximately $3.2 million in cash, less Metabasis' estimated net liabilities at closing (currently estimated to then be over $1.3 million) and less an amount deposited in the stockholders' representative's fund. At this time, Metabasis estimates the net cash that will be available for distribution to stockholders of Metabasis at closing will be approximately $1.8 million.
In addition to cash, Metabasis stockholders will receive tradable Contingent Value Rights (one of each series of CVRs (or 4 in total), for each former Metabasis share) that may result in additional cash payments to the CVR holders including the following:
Approximately two-thirds of any milestone payments, royalties or saleback proceeds collected from Metabasis' partnership with Roche for the development of treatments for hepatitis;
50% of any net proceeds received for licensing or selling Metabasis' thyroid receptor B program for hyperlipidemia and/or glucagon program for diabetes for any transaction entered into in the six years following closing, 40% and 30%, respectively, of any proceeds from such a transaction entered into in the seventh and eighth years following closing, and 20% of any proceeds from such a transaction entered into in the ninth and tenth years following closing;
90% of any net proceeds received for licensing or selling Metabasis' MB07133 program for the treatment of hepatocellular carcinoma for any transaction entered into in the six months following closing, 30% of any proceeds from such a transaction entered into after the sixth month anniversary of closing and before the two year anniversary of closing, and 10% of any proceeds from such a transaction entered into in the third through tenth years following closing;
60% of any net proceeds from any disposition of Metabasis' equity interest in PeriCor Therapeutics, Inc., which in partnership with Schering-Plough Corporation is in Phase III development of a compound for the prevention of adverse cardiovascular and cerebrovascular outcomes in patients undergoing coronary artery bypass graft surgery;
50% of any net proceeds received for licensing or selling any of Metabasis' other drug development programs or certain platform technologies for any transaction occurring with respect to any such program before Ligand has made research and development investments in excess of a specified amount on such program, and 25% in the event Ligand's investments exceed such amount on such program; and
any shortfall in Ligand's commitment to spend at least $8 million in funding Metabasis programs over 42 months following the close of the transaction.
Aside from what is due to Metabasis' CVR holders and subject to certain obligations, Ligand will retain all rights and economic interests in the programs and have full control over the development decisions for the pipeline programs. Ligand has agreed to spend a minimum of $7 million on Metabasis programs over the 30 months following closing, unless both the glucagon and TRß programs have failed or a major licensing event has occurred for at least one of those two programs, and to spend a grand total of $8 million within the 42 months following closing.
A Metabasis stockholder representative will monitor compliance with Ligand's funding obligation and oversee the collection and disbursement of cash to the CVR holders. A rights agent will be retained to collect any cash payments due to the CVR holders and will disburse net proceeds, if any, every six months.
The transaction is expected to close in early 2010 and is subject to approval by Metabasis' stockholders and other customary closing conditions.
With the acquisition of Metabasis, Ligand does not anticipate any change to its year-end 2009 financial outlook. For 2010, the required cash payment of $3.2 million is projected to be largely offset by the potential receipt of a cash milestone from Roche for the advancement of its program for hepatitis, net of the portion of that payment to be allocated to CVR holders. The obligation for funding Metabasis' programs is not expected to materially change Ligand's overall spending over the next several years, as spending for R&D projects can be directed as needed to the highest priority programs.
Metabasis Contributes the Following to Ligand
Hepatitis Program -Metabasis entered into a fully funded collaboration and license agreement with Roche in 2008 to develop new treatments for hepatitis C viral infection utilizing the proprietary HepDirect(R) liver-targeting technology. The lead HepDirect Nucleoside, MB11362, was declared a clinical candidate in the second quarter of 2009. Advanced preclinical development studies are ongoing in preparation for a first-in-human clinical program. Under the terms of the license agreement, Roche will fund 100% of the program costs and will make milestone and royalty payments upon the achievement of certain development events and commercialization of MB11362 and/or other applicable HepDirect compounds covered under the agreement. Ligand will retain approximately one-third of any payments received.
Glucagon Receptor Antagonist Program - Metabasis has developed chemically novel, potent, orally bioavailable glucagon antagonists for treating type 2 diabetes. The lead compound, MB11262, has shown significant and consistent lowering of blood glucose when dosed orally in numerous diabetic animal models and is currently in advanced lead optimization stage. Ligand will retain 50% to 80% of the net proceeds of any transaction for this program.
Thyroid Receptor B Agonist Program - Thyroid receptor activation in the liver affects the expression of several genes, leading to reductions in LDL, triglycerides and LP(a) while its activation in extra-hepatic tissues result in dose-limiting side effects. Metabasis has developed a liver-targeted TRB agonist, MB07811, using HepDirect prodrug technology and other structural characteristics for the treatment of hyperlipidemia. Phase I single and multi-dose clinical trials of MB07811 have been completed. In addition, Metabasis has an advanced discovery program to identify second-generation TRß agonists with potential improvements in the therapeutic index for lowering cholesterol and other lipids associated with cardiovascular risks. Ligand will retain 50% to 80% of the net proceeds of any transaction for this program.
MB07133 Program - Metabasis has developed MB07133, a HepDirect prodrug of the intermediate form of a known oncolytic, which is designed to deliver high concentration of the active form of the drug for the treatment of hepatocellular carcinoma. Metabasis has completed a repeat cycle Phase I/II clinical trial of MB07133. Ligand will retain 10% to 90% of the net proceeds of any transaction for this program.
PeriCor Therapeutics - Metabasis has a common stock ownership position in PeriCor Therapeutics, Inc., a private, clinical-stage company focused on myocardial protection. PeriCor sublicensed rights from Metabasis to acadesine and three additional Adenosine Regulating Agents in 2005. PeriCor recently licensed acadesine to Schering-Plough and the compound is in a Phase III clinical trial for the prevention of adverse cardiovascular and cerebrovascular outcomes in patients undergoing coronary artery bypass graft surgery. Ligand will retain 40% of the net proceeds of any disposition of its PeriCor stock.
HepDirect Technology: HepDirect technology supplements Ligand's core drug discovery technology platform of ligand-dependent gene expression and ultra-high throughput combinatorial chemistry screening. HepDirect is a prodrug technology that targets delivery of certain drugs to the liver by using a proprietary chemical modification that renders a drug biologically inactive until cleaved by a liver-specific enzyme. HepDirect may improve efficacy and/or safety of certain drugs and can be applied to marketed or new drug products. Ligand will retain 50% to 75% of any net proceeds received for licensing or selling the HepDirect technology.
Other Product Candidates and R&D Programs - Metabasis has other product candidates, including MB07803 for diabetes and pradefovir for hepatitis B, and early stage R&D programs including glucokinase activators for diabetes and DGAT-1 inhibitors for obesity. Ligand will retain 50% to 75% of the net proceeds for any deal generated from these programs.
About Metabasis
Metabasis is a biopharmaceutical company that has discovered novel drugs for metabolic diseases using its proprietary technology and its knowledge of processes and pathways within the liver that are useful for liver-selective drug targeting and treatment of metabolic diseases. Metabasis has established a broad pipeline of product candidates and advanced discovery programs targeting large markets with significant unmet needs. Metabasis' product pipeline includes clinical-stage product candidates and advanced discovery programs for the treatment of metabolic diseases such as diabetes and hyperlipidemia, as well as product candidates and advanced discovery programs for the treatment of liver diseases such as hepatitis and primary liver cancer. All of Metabasis' product candidates were developed internally.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals. With more than 20 molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Forward-Looking Statements
This release contains forward-looking statements that involve risks and uncertainties. Ligand and Metabasis caution readers that any forward-looking information is not a guarantee of future performance and actual results could differ materially from those contained in the forward-looking information. Words such as "expect," "estimate," "project," "potential," and similar expressions are intended to identify such forward-looking statements. Such forward-looking statements include, but are not limited to, the expected timing of closing the merger, statements about the benefits of the transaction between Ligand and Metabasis, including future financial and operating results and revenue potential, the expected effect of the merger on Ligand's operating cash burn rate, the possibility of payments being made under the CVR agreements, the combined entity's plans, objectives, expectations and intentions and other statements that are not historical facts. Among the important factors that could cause actual results to differ materially from those in any forward-looking statements are the risks that payment events which would produce proceeds for the CVR holders may not occur soon, or ever; the CVRs may have an illiquid market; the anticipated synergies and benefits from the transaction may not be fully realized or may take longer to realize than expected; Metabasis' stockholders may fail to approve the merger; Ligand or Metabasis may be unable to satisfy the conditions to closing of the merger, or the merger may be otherwise delayed or ultimately not consummated; Metabasis' product candidates may have unexpected adverse side effects or inadequate therapeutic efficacy; and positive results in clinical trials may not be sufficient to obtain FDA approval. There can be no assurance that any product in Ligand's, Metabasis' or the projected combined company's product pipeline will be successfully developed or manufactured, that final results of clinical studies will be supportive of regulatory approvals required to market licensed products, or that any of the forward-looking information provided herein will be proven accurate. Additional important factors that may affect future results are detailed in Ligand's and Metabasis' filings with the SEC, including each company's recent filings on Forms 10-K and 10-Q, or in information disclosed in public conference calls, the date and time of which are released beforehand. Each of Ligand and Metabasis disclaims any intent or obligation to update these forward-looking statements beyond the date of this release.
Additional Information and Where to Find It
Ligand intends to file with the SEC a Registration Statement on Form S-4, which will include a proxy statement of Metabasis and other relevant materials in connection with the proposed transaction. The proxy statement, which will also constitute a Ligand prospectus, will be mailed to the stockholders of Metabasis. The proxy statement and the other relevant materials will, when they become available, contain important information about Ligand, Metabasis and the proposed transaction. The proxy statement and other relevant materials (when they become available), and any other documents filed by Ligand or Metabasis with the SEC, may be obtained free of charge at the SEC's web site at www.sec.gov. In addition, investors and security holders may obtain free copies of the documents filed with the SEC by Ligand by going to the Investor Relations page on Ligand's corporate website at www.ligand.com. Investors and security holders may obtain free copies of the documents filed with the SEC by Metabasis by going to the Investors page on Metabasis' corporate website at www.mbasis.com. Investors and security holders of Metabasis are urged to read the proxy statement and the other relevant materials when they become available before making any voting or investment decision with respect to the proposed transaction.
Ligand and its respective directors and executive officers may be deemed to be participants in the solicitation of proxies from the stockholders of Metabasis in favor of the proposed transaction. Information concerning Ligand's directors and executive officers is set forth in Ligand's proxy statement for its 2009 annual meeting of stockholders, which was filed with the SEC on April 29, 2009, and annual report on Form 10-K filed with the SEC on March 16, 2009.
Metabasis and its respective directors and executive officers may be deemed to be participants in the solicitation of proxies from the stockholders of Metabasis in favor of the proposed transaction. Information about Metabasis executive officers and directors and their ownership of Metabasis common stock is set forth in Metabasis' annual report on Form 10-K filed with the SEC on March 31, 2009, as amended on April 30, 2009. Investors and security holders may obtain more detailed information regarding the direct and indirect interests of Metabasis and its executive officers and directors in the acquisition by reading the proxy statement regarding the merger, which will be filed with the SEC.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Contacts:Ligand Pharmaceuticals IncorporatedJohn L. Higgins, President and CEOErika Luib, Investor Relations(858) 550-7896orLippert/Heilshorn & AssociatesDon Markleydmarkley@lhai.com(310) 691-7100orMetabasis Contacts:Metabasis Therapeutics, Inc.Mark D. Erion, Ph.D., President, CEO and CSOTran B. Nguyen, M.B.A., Vice President of Finance and CFO(858) 622-3909
Copyright Business Wire 2009
Close window | Back to top
Ligand to Gain Fully Funded Partnership with Roche for Hepatitis and Promising Development-Stage Programs
SAN DIEGO, Oct 27, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) and Metabasis Therapeutics, Inc. (NASDAQ: MBRX) announced today they have entered into a definitive merger agreement under which Ligand will acquire all of the outstanding shares of Metabasis.
Under the transaction, Metabasis stockholders will receive a cash payment at the closing of the transaction of approximately $3.2 million, less Metabasis' estimated net liabilities at closing and an amount to be deposited in the stockholders' representative's fund (Metabasis currently estimates the closing payment to be approximately $1.8 million in cash). In addition, Metabasis stockholders will receive for each Metabasis share four tradable Contingent Value Rights ("CVRs") that will be registered on a Form S-4 registration statement to be filed by Ligand with the Securities and Exchange Commission. The CVRs will entitle Metabasis stockholders to cash payments as frequently as every six months as cash is received by Ligand from proceeds from the sale or partnering of any of the Metabasis drug development programs, among other triggering events. Ligand has committed to spend at least $8 million in new research and development funding on the Metabasis programs within 42 months following the closing of the transaction.
The Ligand and Metabasis Boards of Directors have unanimously voted in favor of the transaction. Stockholders of Metabasis representing approximately 29% of the outstanding shares of Metabasis have signed voting agreements in support of the transaction. Merriman Curhan Ford acted as financial advisor to Metabasis with respect to this transaction.
"This transaction utilizes a creative structure that we believe is potentially highly beneficial to the stockholders of both companies," said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. "Ligand obtains numerous high-quality partnered and development-stage programs that will increase our revenue potential and expand our pipeline of proprietary assets. In exchange, the non-partnered Metabasis programs will be advanced by a company with strong and proven research credentials, with the goal of generating cash proceeds payable directly to Metabasis stockholders. If any or all of the Metabasis programs are financially successful, stockholders at both companies will benefit meaningfully from their shared participation in the programs."
Mark D. Erion, Ph.D., President, Chief Executive Officer and Chief Scientific Officer of Metabasis, stated, "Metabasis has built a pipeline of product candidates and drug development programs that have the potential to one day yield new therapies for metabolic and chronic liver diseases, but due to our limited financial and operational resources, we are unable to independently realize their full potential value. Ligand's strong research and business development capabilities, coupled with its solid financial position and its commitment to additional research and development funding as part of this transaction, gives Metabasis' portfolio of programs the potential to deliver significant future value to Metabasis' stockholders."
Highlights of the Proposed Transaction
Under the terms of the agreement, Ligand will pay at the closing of the transaction approximately $3.2 million in cash, less Metabasis' estimated net liabilities at closing (currently estimated to then be over $1.3 million) and less an amount deposited in the stockholders' representative's fund. At this time, Metabasis estimates the net cash that will be available for distribution to stockholders of Metabasis at closing will be approximately $1.8 million.
In addition to cash, Metabasis stockholders will receive tradable Contingent Value Rights (one of each series of CVRs (or 4 in total), for each former Metabasis share) that may result in additional cash payments to the CVR holders including the following:
Approximately two-thirds of any milestone payments, royalties or saleback proceeds collected from Metabasis' partnership with Roche for the development of treatments for hepatitis;
50% of any net proceeds received for licensing or selling Metabasis' thyroid receptor B program for hyperlipidemia and/or glucagon program for diabetes for any transaction entered into in the six years following closing, 40% and 30%, respectively, of any proceeds from such a transaction entered into in the seventh and eighth years following closing, and 20% of any proceeds from such a transaction entered into in the ninth and tenth years following closing;
90% of any net proceeds received for licensing or selling Metabasis' MB07133 program for the treatment of hepatocellular carcinoma for any transaction entered into in the six months following closing, 30% of any proceeds from such a transaction entered into after the sixth month anniversary of closing and before the two year anniversary of closing, and 10% of any proceeds from such a transaction entered into in the third through tenth years following closing;
60% of any net proceeds from any disposition of Metabasis' equity interest in PeriCor Therapeutics, Inc., which in partnership with Schering-Plough Corporation is in Phase III development of a compound for the prevention of adverse cardiovascular and cerebrovascular outcomes in patients undergoing coronary artery bypass graft surgery;
50% of any net proceeds received for licensing or selling any of Metabasis' other drug development programs or certain platform technologies for any transaction occurring with respect to any such program before Ligand has made research and development investments in excess of a specified amount on such program, and 25% in the event Ligand's investments exceed such amount on such program; and
any shortfall in Ligand's commitment to spend at least $8 million in funding Metabasis programs over 42 months following the close of the transaction.
Aside from what is due to Metabasis' CVR holders and subject to certain obligations, Ligand will retain all rights and economic interests in the programs and have full control over the development decisions for the pipeline programs. Ligand has agreed to spend a minimum of $7 million on Metabasis programs over the 30 months following closing, unless both the glucagon and TRß programs have failed or a major licensing event has occurred for at least one of those two programs, and to spend a grand total of $8 million within the 42 months following closing.
A Metabasis stockholder representative will monitor compliance with Ligand's funding obligation and oversee the collection and disbursement of cash to the CVR holders. A rights agent will be retained to collect any cash payments due to the CVR holders and will disburse net proceeds, if any, every six months.
The transaction is expected to close in early 2010 and is subject to approval by Metabasis' stockholders and other customary closing conditions.
With the acquisition of Metabasis, Ligand does not anticipate any change to its year-end 2009 financial outlook. For 2010, the required cash payment of $3.2 million is projected to be largely offset by the potential receipt of a cash milestone from Roche for the advancement of its program for hepatitis, net of the portion of that payment to be allocated to CVR holders. The obligation for funding Metabasis' programs is not expected to materially change Ligand's overall spending over the next several years, as spending for R&D projects can be directed as needed to the highest priority programs.
Metabasis Contributes the Following to Ligand
Hepatitis Program -Metabasis entered into a fully funded collaboration and license agreement with Roche in 2008 to develop new treatments for hepatitis C viral infection utilizing the proprietary HepDirect(R) liver-targeting technology. The lead HepDirect Nucleoside, MB11362, was declared a clinical candidate in the second quarter of 2009. Advanced preclinical development studies are ongoing in preparation for a first-in-human clinical program. Under the terms of the license agreement, Roche will fund 100% of the program costs and will make milestone and royalty payments upon the achievement of certain development events and commercialization of MB11362 and/or other applicable HepDirect compounds covered under the agreement. Ligand will retain approximately one-third of any payments received.
Glucagon Receptor Antagonist Program - Metabasis has developed chemically novel, potent, orally bioavailable glucagon antagonists for treating type 2 diabetes. The lead compound, MB11262, has shown significant and consistent lowering of blood glucose when dosed orally in numerous diabetic animal models and is currently in advanced lead optimization stage. Ligand will retain 50% to 80% of the net proceeds of any transaction for this program.
Thyroid Receptor B Agonist Program - Thyroid receptor activation in the liver affects the expression of several genes, leading to reductions in LDL, triglycerides and LP(a) while its activation in extra-hepatic tissues result in dose-limiting side effects. Metabasis has developed a liver-targeted TRB agonist, MB07811, using HepDirect prodrug technology and other structural characteristics for the treatment of hyperlipidemia. Phase I single and multi-dose clinical trials of MB07811 have been completed. In addition, Metabasis has an advanced discovery program to identify second-generation TRß agonists with potential improvements in the therapeutic index for lowering cholesterol and other lipids associated with cardiovascular risks. Ligand will retain 50% to 80% of the net proceeds of any transaction for this program.
MB07133 Program - Metabasis has developed MB07133, a HepDirect prodrug of the intermediate form of a known oncolytic, which is designed to deliver high concentration of the active form of the drug for the treatment of hepatocellular carcinoma. Metabasis has completed a repeat cycle Phase I/II clinical trial of MB07133. Ligand will retain 10% to 90% of the net proceeds of any transaction for this program.
PeriCor Therapeutics - Metabasis has a common stock ownership position in PeriCor Therapeutics, Inc., a private, clinical-stage company focused on myocardial protection. PeriCor sublicensed rights from Metabasis to acadesine and three additional Adenosine Regulating Agents in 2005. PeriCor recently licensed acadesine to Schering-Plough and the compound is in a Phase III clinical trial for the prevention of adverse cardiovascular and cerebrovascular outcomes in patients undergoing coronary artery bypass graft surgery. Ligand will retain 40% of the net proceeds of any disposition of its PeriCor stock.
HepDirect Technology: HepDirect technology supplements Ligand's core drug discovery technology platform of ligand-dependent gene expression and ultra-high throughput combinatorial chemistry screening. HepDirect is a prodrug technology that targets delivery of certain drugs to the liver by using a proprietary chemical modification that renders a drug biologically inactive until cleaved by a liver-specific enzyme. HepDirect may improve efficacy and/or safety of certain drugs and can be applied to marketed or new drug products. Ligand will retain 50% to 75% of any net proceeds received for licensing or selling the HepDirect technology.
Other Product Candidates and R&D Programs - Metabasis has other product candidates, including MB07803 for diabetes and pradefovir for hepatitis B, and early stage R&D programs including glucokinase activators for diabetes and DGAT-1 inhibitors for obesity. Ligand will retain 50% to 75% of the net proceeds for any deal generated from these programs.
About Metabasis
Metabasis is a biopharmaceutical company that has discovered novel drugs for metabolic diseases using its proprietary technology and its knowledge of processes and pathways within the liver that are useful for liver-selective drug targeting and treatment of metabolic diseases. Metabasis has established a broad pipeline of product candidates and advanced discovery programs targeting large markets with significant unmet needs. Metabasis' product pipeline includes clinical-stage product candidates and advanced discovery programs for the treatment of metabolic diseases such as diabetes and hyperlipidemia, as well as product candidates and advanced discovery programs for the treatment of liver diseases such as hepatitis and primary liver cancer. All of Metabasis' product candidates were developed internally.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals. With more than 20 molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Forward-Looking Statements
This release contains forward-looking statements that involve risks and uncertainties. Ligand and Metabasis caution readers that any forward-looking information is not a guarantee of future performance and actual results could differ materially from those contained in the forward-looking information. Words such as "expect," "estimate," "project," "potential," and similar expressions are intended to identify such forward-looking statements. Such forward-looking statements include, but are not limited to, the expected timing of closing the merger, statements about the benefits of the transaction between Ligand and Metabasis, including future financial and operating results and revenue potential, the expected effect of the merger on Ligand's operating cash burn rate, the possibility of payments being made under the CVR agreements, the combined entity's plans, objectives, expectations and intentions and other statements that are not historical facts. Among the important factors that could cause actual results to differ materially from those in any forward-looking statements are the risks that payment events which would produce proceeds for the CVR holders may not occur soon, or ever; the CVRs may have an illiquid market; the anticipated synergies and benefits from the transaction may not be fully realized or may take longer to realize than expected; Metabasis' stockholders may fail to approve the merger; Ligand or Metabasis may be unable to satisfy the conditions to closing of the merger, or the merger may be otherwise delayed or ultimately not consummated; Metabasis' product candidates may have unexpected adverse side effects or inadequate therapeutic efficacy; and positive results in clinical trials may not be sufficient to obtain FDA approval. There can be no assurance that any product in Ligand's, Metabasis' or the projected combined company's product pipeline will be successfully developed or manufactured, that final results of clinical studies will be supportive of regulatory approvals required to market licensed products, or that any of the forward-looking information provided herein will be proven accurate. Additional important factors that may affect future results are detailed in Ligand's and Metabasis' filings with the SEC, including each company's recent filings on Forms 10-K and 10-Q, or in information disclosed in public conference calls, the date and time of which are released beforehand. Each of Ligand and Metabasis disclaims any intent or obligation to update these forward-looking statements beyond the date of this release.
Additional Information and Where to Find It
Ligand intends to file with the SEC a Registration Statement on Form S-4, which will include a proxy statement of Metabasis and other relevant materials in connection with the proposed transaction. The proxy statement, which will also constitute a Ligand prospectus, will be mailed to the stockholders of Metabasis. The proxy statement and the other relevant materials will, when they become available, contain important information about Ligand, Metabasis and the proposed transaction. The proxy statement and other relevant materials (when they become available), and any other documents filed by Ligand or Metabasis with the SEC, may be obtained free of charge at the SEC's web site at www.sec.gov. In addition, investors and security holders may obtain free copies of the documents filed with the SEC by Ligand by going to the Investor Relations page on Ligand's corporate website at www.ligand.com. Investors and security holders may obtain free copies of the documents filed with the SEC by Metabasis by going to the Investors page on Metabasis' corporate website at www.mbasis.com. Investors and security holders of Metabasis are urged to read the proxy statement and the other relevant materials when they become available before making any voting or investment decision with respect to the proposed transaction.
Ligand and its respective directors and executive officers may be deemed to be participants in the solicitation of proxies from the stockholders of Metabasis in favor of the proposed transaction. Information concerning Ligand's directors and executive officers is set forth in Ligand's proxy statement for its 2009 annual meeting of stockholders, which was filed with the SEC on April 29, 2009, and annual report on Form 10-K filed with the SEC on March 16, 2009.
Metabasis and its respective directors and executive officers may be deemed to be participants in the solicitation of proxies from the stockholders of Metabasis in favor of the proposed transaction. Information about Metabasis executive officers and directors and their ownership of Metabasis common stock is set forth in Metabasis' annual report on Form 10-K filed with the SEC on March 31, 2009, as amended on April 30, 2009. Investors and security holders may obtain more detailed information regarding the direct and indirect interests of Metabasis and its executive officers and directors in the acquisition by reading the proxy statement regarding the merger, which will be filed with the SEC.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Contacts:Ligand Pharmaceuticals IncorporatedJohn L. Higgins, President and CEOErika Luib, Investor Relations(858) 550-7896orLippert/Heilshorn & AssociatesDon Markleydmarkley@lhai.com(310) 691-7100orMetabasis Contacts:Metabasis Therapeutics, Inc.Mark D. Erion, Ph.D., President, CEO and CSOTran B. Nguyen, M.B.A., Vice President of Finance and CFO(858) 622-3909
Copyright Business Wire 2009
Close window | Back to top
ligand momentan ein fass ohne boden,leider zu früh rein.
Antwort auf Beitrag Nr.: 38.278.992 von asics01 am 29.10.09 12:46:33onyxs nexavar und pfizers student werden auch gegen leberkrebs eingesetzt.
diese meldung müsste doch mal wieder für auftrieb sorgen
Ligand's JAK3 Research Collaboration Extended by Pfizer
SAN DIEGO, Nov 05, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) announced today that its research collaboration with Pfizer for JAK3 has been extended by one year. The Research and License Agreement entered into in December 2006 with Wyeth provided for an initial three year research term. Under this extension, Ligand will receive $3.1 million in research payments to continue conducting drug discovery and lead candidate optimization. Under the original agreement, Ligand is entitled to receive up to $175 million in milestone payments for the successful development and commercialization of multiple products. In addition, Ligand will receive royalties on product sales.
"We are very pleased to learn that Pfizer has elected to extend the JAK3 research collaboration with Ligand," said John L. Higgins, President and Chief Executive Officer of Ligand. "We view JAK3 inhibitors as a very promising market opportunity, and given Pfizer's clinical success with its own internal program we are convinced that they are highly committed to this category. Ligand has an exceptional record of drug discovery while serving major pharmaceutical companies in a number of research collaborations. We are pleased with the team's progress and look forward to continued success as we drive the program forward for Pfizer."
About JAK3
JAK3 is a tyrosine kinase that belongs to the Janus family of enzymes, and it is an important target for therapeutic interventions in the treatment of autoimmune disorders, inflammation, and organ transplant rejections. JAK3 expression seems to be limited to hematopoietic cells, and specific inhibitors of JAK3 could represent a new class of immunosuppressant drugs.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals (now Pfizer). With nine pharmaceutical agreements and more than 20 molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Caution Regarding Forward-Looking Statements
This news release contains forward-looking statements by Ligand that involve risks and uncertainties and reflect Ligand's judgment as of the date of this release. These statements include those regarding timing and results of clinical data for the JAK3 program, data analysis and evaluation of product candidates, the potential commercial market for JAK3 inhibitors, and plans for continued development of JAK3 inhibitors and related product candidates. Actual events or results may differ from Ligand's expectations. For example, there can be no assurance that trials or evaluations of any product candidates will be favorable, that we will receive any milestone payments or royalties in the future, that JAK3 inhibitors or related product candidates will provide utility or benefits to patients, or that commercial development of any product candidates will be initiated. The failure to meet expectations with respect to any of the foregoing matters may reduce Ligand's stock price. Additional information concerning risk factors affecting Ligand can be found in prior press releases available at www.ligand.com as well as in public periodic filings with the Securities and Exchange Commission, available via www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this press release. This caution is made under the safe harbor provisions of the Private Securities Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals IncorporatedJohn L. Higgins, President and CEO orErika Luib, Investor Relations858-550-7896orLippert/Heilshorn & AssociatesDon Markley310-691-7100dmarkley@lhai.com
Ligand's JAK3 Research Collaboration Extended by Pfizer
SAN DIEGO, Nov 05, 2009 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) announced today that its research collaboration with Pfizer for JAK3 has been extended by one year. The Research and License Agreement entered into in December 2006 with Wyeth provided for an initial three year research term. Under this extension, Ligand will receive $3.1 million in research payments to continue conducting drug discovery and lead candidate optimization. Under the original agreement, Ligand is entitled to receive up to $175 million in milestone payments for the successful development and commercialization of multiple products. In addition, Ligand will receive royalties on product sales.
"We are very pleased to learn that Pfizer has elected to extend the JAK3 research collaboration with Ligand," said John L. Higgins, President and Chief Executive Officer of Ligand. "We view JAK3 inhibitors as a very promising market opportunity, and given Pfizer's clinical success with its own internal program we are convinced that they are highly committed to this category. Ligand has an exceptional record of drug discovery while serving major pharmaceutical companies in a number of research collaborations. We are pleased with the team's progress and look forward to continued success as we drive the program forward for Pfizer."
About JAK3
JAK3 is a tyrosine kinase that belongs to the Janus family of enzymes, and it is an important target for therapeutic interventions in the treatment of autoimmune disorders, inflammation, and organ transplant rejections. JAK3 expression seems to be limited to hematopoietic cells, and specific inhibitors of JAK3 could represent a new class of immunosuppressant drugs.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Schering-Plough, Pfizer and Wyeth Pharmaceuticals (now Pfizer). With nine pharmaceutical agreements and more than 20 molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
Caution Regarding Forward-Looking Statements
This news release contains forward-looking statements by Ligand that involve risks and uncertainties and reflect Ligand's judgment as of the date of this release. These statements include those regarding timing and results of clinical data for the JAK3 program, data analysis and evaluation of product candidates, the potential commercial market for JAK3 inhibitors, and plans for continued development of JAK3 inhibitors and related product candidates. Actual events or results may differ from Ligand's expectations. For example, there can be no assurance that trials or evaluations of any product candidates will be favorable, that we will receive any milestone payments or royalties in the future, that JAK3 inhibitors or related product candidates will provide utility or benefits to patients, or that commercial development of any product candidates will be initiated. The failure to meet expectations with respect to any of the foregoing matters may reduce Ligand's stock price. Additional information concerning risk factors affecting Ligand can be found in prior press releases available at www.ligand.com as well as in public periodic filings with the Securities and Exchange Commission, available via www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this press release. This caution is made under the safe harbor provisions of the Private Securities Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals IncorporatedJohn L. Higgins, President and CEO orErika Luib, Investor Relations858-550-7896orLippert/Heilshorn & AssociatesDon Markley310-691-7100dmarkley@lhai.com
hallo kmastra
bist du noch dabei???ziemlich ruhig hier
bist du noch dabei???ziemlich ruhig hier
Antwort auf Beitrag Nr.: 38.397.772 von asics01 am 16.11.09 19:47:07Klar!
Bin allerdings langfristig investiert. Zur Zeit sind ja echt Kaufkurse.
Ligand hat mittlerweile alleine 33 verpartnerte Programme in den Phasen I II und III.
Kurzfristig belastet(e) der schwache Verkauf von Promacta.
Gruß kmastra
Bin allerdings langfristig investiert. Zur Zeit sind ja echt Kaufkurse.
Ligand hat mittlerweile alleine 33 verpartnerte Programme in den Phasen I II und III.
Kurzfristig belastet(e) der schwache Verkauf von Promacta.
Gruß kmastra
SAN DIEGO--(BUSINESS WIRE)--Ligand Pharmaceuticals Incorporated (NASDAQ: LGND - News) today announced that its partner GlaxoSmithKline (NYSE: GSK - News) has received a positive opinion for Revolade® (eltrombopag/Promacta®) from the European Medicines Agency’s Committee for Medicinal Products for Human Use (CHMP) for the oral treatment of thrombocytopenia (reduced platelet count) in adults with the blood disorder chronic immune (idiopathic) thrombocytopenic purpura (ITP).
The CHMP has recommended the marketing authorization of eltrombopag in the European Union for the treatment of ITP in adult patients who have had their spleen removed, and who do not respond to other treatments, such as corticosteroids and immunoglobulins therapies. Eltrombopag may also be considered as a second-line treatment for adult patients where surgery to remove their spleen is contraindicated.
“Approval in Europe presents an expanded market opportunity for eltrombopag and is an exciting development for Ligand as it continues to validate Ligand’s success in contributing to the discovery of novel and important commercial therapies,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. “Eltrombopag enjoys in excess of 10 years remaining patent life in both the U.S. and Europe, and the European approval of Revolade expands the commercial potential for the drug. We commend GSK for their clinical and regulatory successes and commitment to developing eltrombopag for other indications.”
ITP patients experience bruising and bleeding and, in some cases, serious hemorrhages, which can be fatal. ITP may also affect a patient’s quality of life, as it is often associated with fatigue and depression1 and a fear of bleeding may limit everyday activities.2 Traditional treatments with corticosteroids, immunoglobulins or splenectomy (removal of the spleen) all have potential drawbacks for chronic treatment of ITP patients.5, 6, 7
Eltrombopag significantly increases platelet counts
The positive opinion from CHMP is based on two Phase III randomized, double-blind, placebo-controlled clinical trials (TRA100773B8 and RAISE TRA1025379) and two open-label studies (REPEAT TRA10805710 and EXTEND TRA10532511) in adults who have previously received treatment for chronic ITP. The studies showed that the patients treated with eltrombopag (plus the standard of care) experienced significant increases in platelet counts, a reduction in the incidence of bleeding and an improvement in quality of life, compared with those receiving placebo (plus the standard of care) 8,9,11. Eltrombopag treatment has also allowed patients to reduce the dose of their concomitant medications, such as steroids.9
In clinical trials, eltrombopag was well-tolerated.8,12 In some cases, nausea and vomiting were recorded in the eltrombopag group and not in the placebo group.8 Elevation of liver enzymes was also seen, but these were mostly mild, reversible and not accompanied by any clinically significant symptoms that would indicate impaired liver function.8
Eltrombopag is the first oral platelet generator
Eltrombopag is an oral, non-peptide, thrombopoietin receptor agonist. It stimulates the proliferation and differentiation of megakaryoctes, resulting in an increase in platelet counts. Megakaryocytes are the bone marrow cells that give rise to blood platelets.13
About eltrombopag
Eltrombopag was given accelerated approval by the U.S. Food and Drug Administration (FDA) under the trade name Promacta® in November 2008, for the treatment of chronic ITP in adults who have had an insufficient response to corticosteroids, immunoglobulins or surgical removal of the spleen. Eltrombopag is also approved under the trade name Revolade® in Venezuela, Kuwait, Chile and Russia. In addition, orphan designation was granted by the European Commission for eltrombopag for the treatment of ITP on August 3, 2007.14 Eltrombopag was discovered as a result of a research collaboration between GSK and Ligand Pharmaceuticals, and developed by GSK.
About chronic ITP
Chronic ITP is a serious condition, where patients have low platelet levels in the blood. Platelets are essential to normal clotting, so patients with ITP are at increased risk of bleeding, and may develop bruises and experience nose or gum bleeds, have blood in the urine or feces, abnormally heavy menstrual bleeding, or other types of bleeding that is difficult to stop.14 Although very rare in occurrence, bleeding in the brain is potentially fatal.15 Quality of life is adversely affected in patients with chronic ITP, with a fear of bleeding limiting patients’ daily activities.2 Fatigue and depression are, also, often associated with the disease.1
Revolade® and Promacta® are registered trade marks of the GlaxoSmithKline group of companies. Information based on GSK’s press release.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Merck and Pfizer. With more than 20 molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
The CHMP has recommended the marketing authorization of eltrombopag in the European Union for the treatment of ITP in adult patients who have had their spleen removed, and who do not respond to other treatments, such as corticosteroids and immunoglobulins therapies. Eltrombopag may also be considered as a second-line treatment for adult patients where surgery to remove their spleen is contraindicated.
“Approval in Europe presents an expanded market opportunity for eltrombopag and is an exciting development for Ligand as it continues to validate Ligand’s success in contributing to the discovery of novel and important commercial therapies,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. “Eltrombopag enjoys in excess of 10 years remaining patent life in both the U.S. and Europe, and the European approval of Revolade expands the commercial potential for the drug. We commend GSK for their clinical and regulatory successes and commitment to developing eltrombopag for other indications.”
ITP patients experience bruising and bleeding and, in some cases, serious hemorrhages, which can be fatal. ITP may also affect a patient’s quality of life, as it is often associated with fatigue and depression1 and a fear of bleeding may limit everyday activities.2 Traditional treatments with corticosteroids, immunoglobulins or splenectomy (removal of the spleen) all have potential drawbacks for chronic treatment of ITP patients.5, 6, 7
Eltrombopag significantly increases platelet counts
The positive opinion from CHMP is based on two Phase III randomized, double-blind, placebo-controlled clinical trials (TRA100773B8 and RAISE TRA1025379) and two open-label studies (REPEAT TRA10805710 and EXTEND TRA10532511) in adults who have previously received treatment for chronic ITP. The studies showed that the patients treated with eltrombopag (plus the standard of care) experienced significant increases in platelet counts, a reduction in the incidence of bleeding and an improvement in quality of life, compared with those receiving placebo (plus the standard of care) 8,9,11. Eltrombopag treatment has also allowed patients to reduce the dose of their concomitant medications, such as steroids.9
In clinical trials, eltrombopag was well-tolerated.8,12 In some cases, nausea and vomiting were recorded in the eltrombopag group and not in the placebo group.8 Elevation of liver enzymes was also seen, but these were mostly mild, reversible and not accompanied by any clinically significant symptoms that would indicate impaired liver function.8
Eltrombopag is the first oral platelet generator
Eltrombopag is an oral, non-peptide, thrombopoietin receptor agonist. It stimulates the proliferation and differentiation of megakaryoctes, resulting in an increase in platelet counts. Megakaryocytes are the bone marrow cells that give rise to blood platelets.13
About eltrombopag
Eltrombopag was given accelerated approval by the U.S. Food and Drug Administration (FDA) under the trade name Promacta® in November 2008, for the treatment of chronic ITP in adults who have had an insufficient response to corticosteroids, immunoglobulins or surgical removal of the spleen. Eltrombopag is also approved under the trade name Revolade® in Venezuela, Kuwait, Chile and Russia. In addition, orphan designation was granted by the European Commission for eltrombopag for the treatment of ITP on August 3, 2007.14 Eltrombopag was discovered as a result of a research collaboration between GSK and Ligand Pharmaceuticals, and developed by GSK.
About chronic ITP
Chronic ITP is a serious condition, where patients have low platelet levels in the blood. Platelets are essential to normal clotting, so patients with ITP are at increased risk of bleeding, and may develop bruises and experience nose or gum bleeds, have blood in the urine or feces, abnormally heavy menstrual bleeding, or other types of bleeding that is difficult to stop.14 Although very rare in occurrence, bleeding in the brain is potentially fatal.15 Quality of life is adversely affected in patients with chronic ITP, with a fear of bleeding limiting patients’ daily activities.2 Fatigue and depression are, also, often associated with the disease.1
Revolade® and Promacta® are registered trade marks of the GlaxoSmithKline group of companies. Information based on GSK’s press release.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients with muscle wasting, frailty, hormone-related diseases, osteoporosis, inflammatory diseases, anemia, asthma, rheumatoid arthritis and psoriasis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including Bristol-Myers Squibb, Celgene, Cephalon, GlaxoSmithKline, Merck and Pfizer. With more than 20 molecules in various stages of development, Ligand utilizes proprietary technologies for identifying drugs with novel receptor and enzyme drug targets.
hallo kmastra
was sagst du zu dem aktuellem zahlenwerk,bzw den aussichten???
hört sich doch alles gut an,aber warum kommt ligand nicht in die gänge??
asics
was sagst du zu dem aktuellem zahlenwerk,bzw den aussichten???
hört sich doch alles gut an,aber warum kommt ligand nicht in die gänge??
asics
Antwort auf Beitrag Nr.: 38.920.586 von asics01 am 10.02.10 18:39:12Hallo asics,
ich bin überzeugter denn je. Zahlen sind gut, wobei Aussichten eher konservativ sind. Nicht zu vergessen auch, dass die Avinza Royalties immer in das letzte Quartal miteingehen.
Habe zwischenzeitlich nochmal nachgekauft.
Hast du die Präsentation gesehen?
http://investors.ligand.com/events.cfm
Insbesondere ist hervorzuheben, dass die jetzt scheinbar mehr Wert auf die PR legen. Neue Präsentation und Zahlen wurden auch in New York präsentiert und nicht mehr daheim.
Ich wundere mich auch darüber, dass die nicht in die Gänge kommen.
Aber vielleicht hilft ja die bessere PR?
Grundsätzlich ist der Markt wohl von den Verkaufszahlen von Promacta enttäuscht. Das war ja immerhin als potenzielles Blockbustermedikament angekündigt. Und jetzt wurden nur 20 Mio gemacht.Aber die Verkaufszahlen von Promacta werden m.E. völlig falsch bewertet. Denn zur Zeit ist es noch mit ganz strikten Auflagen zur Überwachung (black label) versehen und dann auch nur für eine kleine Indikation zugelassen. Interessant wird es, wenn das ausläuft und die Zulassung auch für Hepatitis C erfolgt.
GSK steckt da wohl auch ne Menge Kohle in die Studien. Sie scheinen sich also was davon zu versprechen...Ich meine Anfang 2011 kommen die P III Ergebnisse.
Wenn in der Präsenation von 33 \"fully funded programms\" die Rede ist: Versteh ich das richtig, dass heisst doch 33 Programme, die verpartnert sind und für die Ligand also nix in der Entwicklung zahlen muss!?
So long...kmastra
ich bin überzeugter denn je. Zahlen sind gut, wobei Aussichten eher konservativ sind. Nicht zu vergessen auch, dass die Avinza Royalties immer in das letzte Quartal miteingehen.
Habe zwischenzeitlich nochmal nachgekauft.
Hast du die Präsentation gesehen?
http://investors.ligand.com/events.cfm
Insbesondere ist hervorzuheben, dass die jetzt scheinbar mehr Wert auf die PR legen. Neue Präsentation und Zahlen wurden auch in New York präsentiert und nicht mehr daheim.
Ich wundere mich auch darüber, dass die nicht in die Gänge kommen.
Aber vielleicht hilft ja die bessere PR?
Grundsätzlich ist der Markt wohl von den Verkaufszahlen von Promacta enttäuscht. Das war ja immerhin als potenzielles Blockbustermedikament angekündigt. Und jetzt wurden nur 20 Mio gemacht.Aber die Verkaufszahlen von Promacta werden m.E. völlig falsch bewertet. Denn zur Zeit ist es noch mit ganz strikten Auflagen zur Überwachung (black label) versehen und dann auch nur für eine kleine Indikation zugelassen. Interessant wird es, wenn das ausläuft und die Zulassung auch für Hepatitis C erfolgt.
GSK steckt da wohl auch ne Menge Kohle in die Studien. Sie scheinen sich also was davon zu versprechen...Ich meine Anfang 2011 kommen die P III Ergebnisse.
Wenn in der Präsenation von 33 \"fully funded programms\" die Rede ist: Versteh ich das richtig, dass heisst doch 33 Programme, die verpartnert sind und für die Ligand also nix in der Entwicklung zahlen muss!?
So long...kmastra
Antwort auf Beitrag Nr.: 38.921.576 von kmastra am 10.02.10 20:56:26Moin asics,
was los?
Fänds nett, wenn du auch anwortest.
Bei Ligand ziehen die Umsätze seit Tagen merklich an - gutes Zeichen!
Sportlicher Gruß
kmallstar
was los?
Fänds nett, wenn du auch anwortest.
Bei Ligand ziehen die Umsätze seit Tagen merklich an - gutes Zeichen!
Sportlicher Gruß
kmallstar
Antwort auf Beitrag Nr.: 38.977.907 von kmastra am 19.02.10 22:37:07hallo kmastra
was soll ich sagen????ich harre der dinge die da kommen.freitag hab ich nochmal 1000 st geholt,gerade weil die umsätze seit ein paar tagen anziehen.
ob was dahinter steckt ???ich bin auf jeden fall dabei wenn was positives kommt,das gleiche gilt aber auch wenn was negatives kommt.
schönes wochenende und sportliche grüsse zurück,ich gehe jetzt 20km joggen.
asics
was soll ich sagen????ich harre der dinge die da kommen.freitag hab ich nochmal 1000 st geholt,gerade weil die umsätze seit ein paar tagen anziehen.
ob was dahinter steckt ???ich bin auf jeden fall dabei wenn was positives kommt,das gleiche gilt aber auch wenn was negatives kommt.
schönes wochenende und sportliche grüsse zurück,ich gehe jetzt 20km joggen.
asics
Antwort auf Beitrag Nr.: 38.978.583 von asics01 am 20.02.10 10:48:56Moin asics,
"bin auf jeden fall dabei wenn was positives kommt, aber auch wenn was negatives kommt" - finde ich mal ne geile Aussage - wirklich!
Wenn ich an manche user hier denke, die meinen die Weisheit mit Löffeln gefressen zu haben könnt ich echt kotzen. Deshalb Daumen hoch für diese sympathische Einschätzung! Bei Biotechs weiss man eben nie.
Mal sehen vielleicht steht der Umsatzanstieg ja wirklich mit der neuen PR im Zusammenhang. Ich fand die Präsentation extrem gelungen, zumal neben Promacta auch das Potenzial weiterer Programme deutlich wurde.
So sportlich wie du bin ich übrigens scheinbar nicht
Trotzdem sportlicher Gruß
kmallstar
"bin auf jeden fall dabei wenn was positives kommt, aber auch wenn was negatives kommt" - finde ich mal ne geile Aussage - wirklich!
Wenn ich an manche user hier denke, die meinen die Weisheit mit Löffeln gefressen zu haben könnt ich echt kotzen. Deshalb Daumen hoch für diese sympathische Einschätzung! Bei Biotechs weiss man eben nie.
Mal sehen vielleicht steht der Umsatzanstieg ja wirklich mit der neuen PR im Zusammenhang. Ich fand die Präsentation extrem gelungen, zumal neben Promacta auch das Potenzial weiterer Programme deutlich wurde.
So sportlich wie du bin ich übrigens scheinbar nicht

Trotzdem sportlicher Gruß
kmallstar
Antwort auf Beitrag Nr.: 38.980.437 von kmastra am 21.02.10 01:46:18hallo kmastra
ich habe mir mit bios schon einige mal die finger verbrannt,deshalb sicher ist nur das amen in der kirche.bin aber trotzdem von ligand überzeugt,wird zwar keine 1000% machen,aber 10-20% pro jahr ist auch nicht schlecht. potenzial ist auf jedenfall vorhanden.
asics
ich habe mir mit bios schon einige mal die finger verbrannt,deshalb sicher ist nur das amen in der kirche.bin aber trotzdem von ligand überzeugt,wird zwar keine 1000% machen,aber 10-20% pro jahr ist auch nicht schlecht. potenzial ist auf jedenfall vorhanden.
asics
Hallo kmastra,
da hast du dir aber ne Fleißarbeit ausgesucht. Von der Charttechnik würde ich allerdings jetzt nicht reingehen. Das sind ja drei Jahre nur Schmerzen.

Die Arbeit könnte sich irgendwann mal lohnen. Mir sind da zu viele Anwendungen, von denen ich absolut keine Ahnung habe. Deshalb halte ich mich hier mit meinen Kommentaren zurück. Das ist mir zu viel Arbeit, mich hier kundig zu machen.
Grüße und danke für dein Vertrauen
Erbse
da hast du dir aber ne Fleißarbeit ausgesucht. Von der Charttechnik würde ich allerdings jetzt nicht reingehen. Das sind ja drei Jahre nur Schmerzen.

Die Arbeit könnte sich irgendwann mal lohnen. Mir sind da zu viele Anwendungen, von denen ich absolut keine Ahnung habe. Deshalb halte ich mich hier mit meinen Kommentaren zurück. Das ist mir zu viel Arbeit, mich hier kundig zu machen.
Grüße und danke für dein Vertrauen
Erbse
Antwort auf Beitrag Nr.: 38.982.159 von Erbse1 am 21.02.10 20:23:22Moin Erbse,
Gott sei Dank bin ich ja nicht seit 3 oder gar 10 Jahren dabei
Bei Ligand habe ich natürlich aber trotzdem bisher Verlust gemacht.
Bin aber langfristig überzeugt, denn welcher Biotechwert hat schon 33 verpartnerte Programme zu bieten und das mit u.A. GSK, Pfizer, Merck, Roche, BMS, Celgene...bei einer Mkpt. von ca. 200 Mio US D.
Informativ ist das letzte webcast:
http://www.veracast.com/webcasts/bio/ceoinvestor2010/2520126…
SG kmastra
Gott sei Dank bin ich ja nicht seit 3 oder gar 10 Jahren dabei

Bei Ligand habe ich natürlich aber trotzdem bisher Verlust gemacht.
Bin aber langfristig überzeugt, denn welcher Biotechwert hat schon 33 verpartnerte Programme zu bieten und das mit u.A. GSK, Pfizer, Merck, Roche, BMS, Celgene...bei einer Mkpt. von ca. 200 Mio US D.
Informativ ist das letzte webcast:
http://www.veracast.com/webcasts/bio/ceoinvestor2010/2520126…
SG kmastra
komm kmastra hilf mal ein bischen schieben,weigstens mal über die 2$ marke 


asics



asics
Antwort auf Beitrag Nr.: 39.063.851 von asics01 am 04.03.10 21:26:01soll natürlich wenigstens heissen
Antwort auf Beitrag Nr.: 39.063.869 von asics01 am 04.03.10 21:27:38Yo,
hab grad anner Nasdaq 100K zu 2,01 geordert
Demnächst ist ja wieder Präsentation. Mal sehen, vielleicht gibt das ja Impulse. Im Yahoo forum wird zudem über die bevorstehende EU Zulassung von Promacta spekuliert...
Laut eines Users sind das die Umsatzschätzungen von UBS bezüglich Promacta:
2010 152
2011 355
2012 555
2013 1013
SG kmastra
hab grad anner Nasdaq 100K zu 2,01 geordert

Demnächst ist ja wieder Präsentation. Mal sehen, vielleicht gibt das ja Impulse. Im Yahoo forum wird zudem über die bevorstehende EU Zulassung von Promacta spekuliert...
Laut eines Users sind das die Umsatzschätzungen von UBS bezüglich Promacta:
2010 152
2011 355
2012 555
2013 1013
SG kmastra
Antwort auf Beitrag Nr.: 39.079.925 von kmastra am 07.03.10 20:00:30du warst zu schnell,hättest sie heute für 1,70$ bekommen


was war los heute minus 6%





was war los heute minus 6%



meine Englischkenntnisse sind doch immer wieder schnell am Ende.
Ich glaube verstanden zu haben, dass jede Menge Optionen bezahlt werden müssen, jedes Mal, wenn Milestonezahlungen erfolgen, da ein Großteil der Pipeline in Lizenz genommen wurde.
Jedenfalls würde das erklären, warum der Kurs vor sich hin dümpelt.
Andererseits gibt es eine gute Chance, dass ich etwas falsch verstanden habe
Ich glaube verstanden zu haben, dass jede Menge Optionen bezahlt werden müssen, jedes Mal, wenn Milestonezahlungen erfolgen, da ein Großteil der Pipeline in Lizenz genommen wurde.
Jedenfalls würde das erklären, warum der Kurs vor sich hin dümpelt.
Andererseits gibt es eine gute Chance, dass ich etwas falsch verstanden habe

wird wohl abtauchen auf 1,50$
Antwort auf Beitrag Nr.: 39.109.591 von dottore am 10.03.10 23:25:01Hallo dottore,
was genau meinst du mit den Lizenzen?
Davon weiß ich nichts.
Die Präsentation heute gab ein wenig neues. Laut Higgins wird Pfizer noch im ersten Halbjahr die NDA für Apprella einreichen. Ligand bekäme allerding nur 0,5 bis 2,5 % royalties. Von da her nicht so kursbewegend.
Interessant waren aber die ausführungen zu dem oral epo programm. Eine Verpartnerung hier dürfte möglich und lukrativ sein.
Der Kurs ist mir ein Rätsel. Aber da ligand noch über 50 Mio cash hat und mit 5 Mio Misen plant - bei steigenden Umsätzen - gehe ich davon aus, dass es Ligand auch in 10 Jahren noch gibt.
was genau meinst du mit den Lizenzen?
Davon weiß ich nichts.
Die Präsentation heute gab ein wenig neues. Laut Higgins wird Pfizer noch im ersten Halbjahr die NDA für Apprella einreichen. Ligand bekäme allerding nur 0,5 bis 2,5 % royalties. Von da her nicht so kursbewegend.
Interessant waren aber die ausführungen zu dem oral epo programm. Eine Verpartnerung hier dürfte möglich und lukrativ sein.
Der Kurs ist mir ein Rätsel. Aber da ligand noch über 50 Mio cash hat und mit 5 Mio Misen plant - bei steigenden Umsätzen - gehe ich davon aus, dass es Ligand auch in 10 Jahren noch gibt.
Antwort auf Beitrag Nr.: 39.119.779 von kmastra am 11.03.10 23:58:47wie kann mann auch solche verträge abschliessen,wo es nur 0,5-2,5%
roalties gibt???
und das ist bei ligand nicht nur 1x so.
asics
roalties gibt???
und das ist bei ligand nicht nur 1x so.
asics
Antwort auf Beitrag Nr.: 39.123.437 von asics01 am 12.03.10 12:52:47Hab ich mich auch gefragt.
Man muss aber sehen, dass Ligand diesen Vertrag Mitte der 90er mit Pfizer bzw. Wyeth abschloss. Damals waren die Biotechs noch nicht in einer so guten Verhandlungsposition.
Beim letzten abgeschlossenen Deal konnte Ligand GSK immerhin 14,5 % abringen.
Man muss aber sehen, dass Ligand diesen Vertrag Mitte der 90er mit Pfizer bzw. Wyeth abschloss. Damals waren die Biotechs noch nicht in einer so guten Verhandlungsposition.
Beim letzten abgeschlossenen Deal konnte Ligand GSK immerhin 14,5 % abringen.
So, Zulassung für Promacta in Europa ist da:
http://finance.yahoo.com/news/Ligand-Announces-Approval-for-…
SAN DIEGO--(BUSINESS WIRE)--Ligand Pharmaceuticals Incorporated today announced that GlaxoSmithKline was granted marketing authorization from the European Commission (EC) for Revolade® (eltrombopag) for the oral treatment of thrombocytopenia (reduced platelet count) in adults with the blood disorder chronic immune (idiopathic) thrombocytopenic purpura (ITP). Eltrombopag is indicated for adult chronic ITP splenectomized patients who have not responded (are refractory) to other treatments, such as corticosteroids and immunoglobulins. Eltrombopag may also be considered as second-line treatment for adult non-splenectomized patients where surgery is contraindicated.
Revolade was submitted for approval in Europe in December 2008, and received a positive opinion from the European Medicines Agency’s Committee for Medicinal Products for Human Use (CHMP) in December 2009. European Commission has granted orphan designation for eltrombopag for the treatment of ITP. Eltrombopag is the first oral platelet generator that stimulates the proliferation and differentiation of megakaryoctes, resulting in an increase in platelet counts. Megakaryocytes are the bone marrow cells that give rise to blood platelets.
“The marketing authorization from the EC of Revolade highlights Ligand’s success in entering pharmaceutical relationships that ultimately result in market approval. Revolade represents a significant treatment option available for ITP patients and the European approval expands the commercial potential for the drug,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals.
About Eltrombopag
Eltrombopag was given accelerated approval by the U.S. Food and Drug Administration (FDA) under the trade name Promacta® in November 2008, for the treatment of chronic ITP in adults who have had an insufficient response to corticosteroids, immunoglobulins or surgical removal of the spleen. Eltrombopag is also approved under the trade name Revolade in Venezuela, Kuwait, Chile and Russia. Eltrombopag was discovered as a result of a research collaboration between GSK and Ligand Pharmaceuticals, and developed by GSK.
Revolade® and Promacta® are registered trade marks of the GlaxoSmithKline group of companies.
http://finance.yahoo.com/news/Ligand-Announces-Approval-for-…
SAN DIEGO--(BUSINESS WIRE)--Ligand Pharmaceuticals Incorporated today announced that GlaxoSmithKline was granted marketing authorization from the European Commission (EC) for Revolade® (eltrombopag) for the oral treatment of thrombocytopenia (reduced platelet count) in adults with the blood disorder chronic immune (idiopathic) thrombocytopenic purpura (ITP). Eltrombopag is indicated for adult chronic ITP splenectomized patients who have not responded (are refractory) to other treatments, such as corticosteroids and immunoglobulins. Eltrombopag may also be considered as second-line treatment for adult non-splenectomized patients where surgery is contraindicated.
Revolade was submitted for approval in Europe in December 2008, and received a positive opinion from the European Medicines Agency’s Committee for Medicinal Products for Human Use (CHMP) in December 2009. European Commission has granted orphan designation for eltrombopag for the treatment of ITP. Eltrombopag is the first oral platelet generator that stimulates the proliferation and differentiation of megakaryoctes, resulting in an increase in platelet counts. Megakaryocytes are the bone marrow cells that give rise to blood platelets.
“The marketing authorization from the EC of Revolade highlights Ligand’s success in entering pharmaceutical relationships that ultimately result in market approval. Revolade represents a significant treatment option available for ITP patients and the European approval expands the commercial potential for the drug,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals.
About Eltrombopag
Eltrombopag was given accelerated approval by the U.S. Food and Drug Administration (FDA) under the trade name Promacta® in November 2008, for the treatment of chronic ITP in adults who have had an insufficient response to corticosteroids, immunoglobulins or surgical removal of the spleen. Eltrombopag is also approved under the trade name Revolade in Venezuela, Kuwait, Chile and Russia. Eltrombopag was discovered as a result of a research collaboration between GSK and Ligand Pharmaceuticals, and developed by GSK.
Revolade® and Promacta® are registered trade marks of the GlaxoSmithKline group of companies.
Antwort auf Beitrag Nr.: 39.128.912 von asics01 am 12.03.10 19:50:29so ist es schon besser,2$ wir kommen







Antwort auf Beitrag Nr.: 39.141.761 von asics01 am 15.03.10 16:25:57Die Zulassung in Europa hat zumindest für Vertrauen gesorgt. Stell dir mal vor was bei negativem Entscheid passiert wär!
Aber entscheidend werden eh die P III Daten zu Hepatitis C sein.
So lange haltge ich auf jeden Fall und kauf ggf. nochmal nach. Die Bewertung von Ligand ist echt ein Witz.
Aber entscheidend werden eh die P III Daten zu Hepatitis C sein.
So lange haltge ich auf jeden Fall und kauf ggf. nochmal nach. Die Bewertung von Ligand ist echt ein Witz.
Antwort auf Beitrag Nr.: 39.145.312 von kmastra am 15.03.10 23:02:47ich stimme dir voll zu was du da schreibst.
aber es wird schon wieder luft abgelassen,war wohl nur ein kurzes aufbäumen.
asics
aber es wird schon wieder luft abgelassen,war wohl nur ein kurzes aufbäumen.
asics
UBS research 3-4-10
http://messages.finance.yahoo.com/Business_%26_Finance/Inves…
Promacta: The real potential is in hepatitis C, not ITP
The opportunity: GSK’s Promacta, is the first once-a-day, oral, smallmolecule
TPO receptor agonist and was launched by GSK and its partner Ligand
Pharmaceuticals for chronic idiopathic thrombocytopenic purpura (ITP,
excessive platelet destruction) in patients with insufficient responses to steroids
in 2008 in the U.S., and launched in the EU in 4Q09. The conventional view is
that as chronic ITP is a small indication, Promacta is a small product. We note
an abundance of label-expanding clinical datasets are coming through 2012, and
the market is yet to show significant estimates. We view that much of
Promacta’s promise lies in other indications to follow, especially chronichepatitis-
C-related thrombocytopenia. Possible other indications include
myelodysplastic syndromes (tough indication), and chemotherapy-induced
thrombocytopenia (tougher still).
We view blue sky scenarios of £3bn sales in 2014. Consensus estimates of
£341m leave little room for downgrades.
http://messages.finance.yahoo.com/Business_%26_Finance/Inves…
Promacta: The real potential is in hepatitis C, not ITP
The opportunity: GSK’s Promacta, is the first once-a-day, oral, smallmolecule
TPO receptor agonist and was launched by GSK and its partner Ligand
Pharmaceuticals for chronic idiopathic thrombocytopenic purpura (ITP,
excessive platelet destruction) in patients with insufficient responses to steroids
in 2008 in the U.S., and launched in the EU in 4Q09. The conventional view is
that as chronic ITP is a small indication, Promacta is a small product. We note
an abundance of label-expanding clinical datasets are coming through 2012, and
the market is yet to show significant estimates. We view that much of
Promacta’s promise lies in other indications to follow, especially chronichepatitis-
C-related thrombocytopenia. Possible other indications include
myelodysplastic syndromes (tough indication), and chemotherapy-induced
thrombocytopenia (tougher still).
We view blue sky scenarios of £3bn sales in 2014. Consensus estimates of
£341m leave little room for downgrades.
Antwort auf Beitrag Nr.: 39.173.721 von kmastra am 19.03.10 00:31:50hallo kmastra
wenn das alles so kommt dann ist das natürlich ein pfund.aber wenn nicht????
wieso wird der kurs so manipuliert???
wieso schnappt sich GSK ligand nicht, bei diesem kurs und den aussichten???
asics
wenn das alles so kommt dann ist das natürlich ein pfund.aber wenn nicht????
wieso wird der kurs so manipuliert???
wieso schnappt sich GSK ligand nicht, bei diesem kurs und den aussichten???
asics
Antwort auf Beitrag Nr.: 39.176.809 von asics01 am 19.03.10 13:00:29Hallo asics,
die Studie von ubs ist natürlich sehr optimistisch. Ich denke aber, dass Umsätze von über 1 Milliarde drin sind - bei Hep C Zulassung.
Sollte die Studie oder die Zulassung scheitern weisst du ja was los ist.
In den USA muss man auch immer die Shorties bedenken. Oft wird der Kurs bei Ligand in den letzten Minuten gemacht. Das ist ärger lich. Das Gute ist aber, dass es recht schnell nach oben gehen kann, wenn die Shorties sich eindecken müssen.
Gruß kmastra
die Studie von ubs ist natürlich sehr optimistisch. Ich denke aber, dass Umsätze von über 1 Milliarde drin sind - bei Hep C Zulassung.
Sollte die Studie oder die Zulassung scheitern weisst du ja was los ist.
In den USA muss man auch immer die Shorties bedenken. Oft wird der Kurs bei Ligand in den letzten Minuten gemacht. Das ist ärger lich. Das Gute ist aber, dass es recht schnell nach oben gehen kann, wenn die Shorties sich eindecken müssen.
Gruß kmastra
Antwort auf Beitrag Nr.: 39.180.400 von kmastra am 19.03.10 18:59:13Ligand Pharmaceuticals Inc. $ 1.78
LGND -0.02
Short Interest (Shares Short) 4,909,500
Days To Cover (Short Interest Ratio) 8.6
Short Percent of Float 4.43 %
Short Interest - Prior 4,768,900
Short % Increase / Decrease 2.95 %
Short Squeeze Ranking™ -14
From 52-Wk High ($ 3.21 ) -80.34 %
From 52-Wk Low ($ 1.55 ) 12.92 %
From 200-Day MA ($ 2.28 ) -28.09 %
From 50-Day MA ($ 1.80 ) -1.12 %
Price % Change (52-Week) -36.40 %
Shares Float 110,718,046
Total Shares Outstanding 117,335,286
Owned by Insiders 2.00 %
Owned by Institutions 78.00 %
Market Cap. $ 208,856,809
Trading Volume - Today 520,492
Trading Volume - Average 572,200
Trading Volume - Today vs. Average 90.96 %
Earnings Per Share -0.02
PE Ratio
Record Date 2010-MarA
Sector Healthcare
Industry Biotechnology
Exchange NAS
LGND -0.02
Short Interest (Shares Short) 4,909,500
Days To Cover (Short Interest Ratio) 8.6
Short Percent of Float 4.43 %
Short Interest - Prior 4,768,900
Short % Increase / Decrease 2.95 %
Short Squeeze Ranking™ -14
From 52-Wk High ($ 3.21 ) -80.34 %
From 52-Wk Low ($ 1.55 ) 12.92 %
From 200-Day MA ($ 2.28 ) -28.09 %
From 50-Day MA ($ 1.80 ) -1.12 %
Price % Change (52-Week) -36.40 %
Shares Float 110,718,046
Total Shares Outstanding 117,335,286
Owned by Insiders 2.00 %
Owned by Institutions 78.00 %
Market Cap. $ 208,856,809
Trading Volume - Today 520,492
Trading Volume - Average 572,200
Trading Volume - Today vs. Average 90.96 %
Earnings Per Share -0.02
PE Ratio
Record Date 2010-MarA
Sector Healthcare
Industry Biotechnology
Exchange NAS
hallo kmastra
mühsam ernährt sich das eichhörnchen (ligand)

was gibt es neues???
asics
mühsam ernährt sich das eichhörnchen (ligand)


was gibt es neues???
asics
will nicht,kann nicht,darf nicht (steigen)





hi kmastra
ohne worte, oder wie siehst du das?????
asics
ohne worte, oder wie siehst du das?????
asics
Antwort auf Beitrag Nr.: 39.307.442 von asics01 am 10.04.10 10:22:38Moin.
Keine Ahnung warum der Kurs nicht steigt. Bin weiter long und erwarte einiges an newsflow.
Upcoming events:
1. LGD-4033 SARM data on tissue selectivity to be presented at the Endocrine Society Meeting june 19-22 San Diego.
2. Conbriza European launch in 1H'10. Partnered with PFE.
3. Promacta European launch underway. Partnered with GSK.
4. Beta-secretase PII trial in Alzheimer patients to be initiated; PI showed a 58% reduction in A-Beta Peptide in the cerebral/spinal fluid. Partnered with Merck.
5. Acadesine PIII trial w/ 7,500 patients for heart bypasss surgery to be completed in 4Q'10. Partnered with Pericor/MRK.
6. Aprela NDA submission in 2H'10. partnered with PFE.
7. Lead oral EPO candidate selection in Q3'10.
8. Promacta approval in Japan in 4Q'10.
9. HepDirect Nucleoside, MB11362, or hepatitis C viral infection utilizing the proprietary HepDirect® liver-targeting technology is progressing well and may produce some news. Partnered with Roche.
10. LGND working on additional license agreements that could produce additional revenue and cash infusion.
SG kmastra
Keine Ahnung warum der Kurs nicht steigt. Bin weiter long und erwarte einiges an newsflow.
Upcoming events:
1. LGD-4033 SARM data on tissue selectivity to be presented at the Endocrine Society Meeting june 19-22 San Diego.
2. Conbriza European launch in 1H'10. Partnered with PFE.
3. Promacta European launch underway. Partnered with GSK.
4. Beta-secretase PII trial in Alzheimer patients to be initiated; PI showed a 58% reduction in A-Beta Peptide in the cerebral/spinal fluid. Partnered with Merck.
5. Acadesine PIII trial w/ 7,500 patients for heart bypasss surgery to be completed in 4Q'10. Partnered with Pericor/MRK.
6. Aprela NDA submission in 2H'10. partnered with PFE.
7. Lead oral EPO candidate selection in Q3'10.
8. Promacta approval in Japan in 4Q'10.
9. HepDirect Nucleoside, MB11362, or hepatitis C viral infection utilizing the proprietary HepDirect® liver-targeting technology is progressing well and may produce some news. Partnered with Roche.
10. LGND working on additional license agreements that could produce additional revenue and cash infusion.
SG kmastra
Antwort auf Beitrag Nr.: 39.310.593 von kmastra am 11.04.10 16:50:39ob das was den kurs bewegt ?????und wenn ja dann nur ein kurzes aufbäumen,um dann wieder die luft abzulassen.







http://investors.ligand.com/releasedetail.cfm?ReleaseID=4613…
Ligand Earns $6.5 Million Milestone Payment from Roche
Roche Advances RG7348 into Clinical Development for Hepatitis C
SAN DIEGO, Apr 20, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced that it earned a $6.5 million payment from Roche (SWX: ROG.VX; RO.S, OTCQX: RHHBY) as a result of Roche progressing RG7348 into a Phase I clinical trial for the treatment of hepatitis C viral (HCV) infection. The milestone payment arises from a 2008 collaboration and license agreement between Roche and Metabasis Therapeutics, Inc. Ligand acquired Metabasis in January 2010. Ligand's net proceeds from the milestone payment will be approximately $2.3 million after paying $4.2 million to others including holders of the Ligand-issued "Roche" CVR.
"This is a great milestone for Ligand due to the cash revenue and because it validates the quality of assets we assumed through our recent acquisitions," said John L. Higgins, President and Chief Executive Officer of Ligand. "Recently we have acquired three public companies that have contributed a vast array of partnered and pipeline assets. We are very pleased with our partnership with Roche and are excited to see their program advance to human development for HCV."
Under the 2008 collaboration and license agreement, Metabasis contributed HepDirect(R) liver-targeting technology to help develop prodrugs of Roche's proprietary lead nucleosides against HCV infection. Ligand is eligible to receive additional payments from Roche upon the achievement of certain further development and regulatory milestones as well as royalties on potential sales of the drug, subject to obligations to share such payments with holders of the Ligand-issued Roche CVR.
The CVRs
Ligand issued a Roche contingent value right (CVR) to each former holder of a Metabasis common share as part of Ligand's acquisition of Metabasis. Each Roche CVR entitles holders to certain payments if and when Ligand receives certain payments in connection with the Roche-Metabasis collaboration and license agreement. Of the $6.5 million milestone payment, 65% is earmarked for the Roche CVR holders. After reduction for pre-existing contractual payment obligations, the Roche CVR holders will receive approximately $2.7 million in respect of this milestone payment.
Zur Erinnerung: http://investors.ligand.com/releasedetail.cfm?ReleaseID=4410…
Ligand Completes Acquisition of Metabasis
SAN DIEGO, Jan 28, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND) announced that it has completed the acquisition of Metabasis Therapeutics, Inc. (NASDAQ:MBRX), following approval of the transaction by Metabasis stockholders yesterday. As a result, Ligand gains a fully funded partnership with Roche, additional pipeline assets and drug discovery technologies and resources. The transaction was first announced on October 27, 2009.
"We are excited about this acquisition and the opportunities it presents for our shareholders," said John L. Higgins, President and Chief Executive Officer of Ligand. "The acquisition of Metabasis builds on our strategy to cultivate a robust pipeline with a broad array of royalty bearing assets and early stage pipeline programs."
In the acquisition, Ligand paid $1.6 million in cash or about $0.046 per Metabasis share to Metabasis' stockholders. In addition, Metabasis stockholders received four tradable Contingent Value Rights (CVRs), one CVR from each of four respective series of CVRs, for each Metabasis share. The CVRs will entitle Metabasis stockholders to cash payments as frequently as every six months as cash is received by Ligand from proceeds from Metabasis' partnership with Roche or the sale or partnering of any of the Metabasis drug development programs, among other triggering events.
Primary Acquired Assets
* Fully funded partnership with Roche to develop new treatments for hepatitis C viral infection utilizing the proprietary HepDirect(R) liver-targeting technology. The lead HepDirect nucleoside, MB11362, was declared a clinical candidate in the second quarter of 2009. Roche will fund 100% of program costs and will make milestone and royalty payments upon the achievement of certain development events and commercialization of MB11362 and/or other applicable HepDirect compounds covered under the agreement.
* Glucagon Receptor Antagonist Program - Metabasis has developed chemically novel, potent, orally bioavailable glucagon antagonists for treating type 2 diabetes. The lead compound, MB11262, has shown significant and consistent lowering of blood glucose when dosed orally in numerous diabetic animal models and is currently in pre-clinical development.
* Thyroid Receptor Beta Agonist Program - Metabasis has developed and evaluated in clinical trials a liver-targeted TR Beta agonist, MB07811, using HepDirect prodrug technology and other structural characteristics for the treatment of hyperlipidemia. In addition, there is an advanced discovery program to identify second-generation TR Beta agonists with potential improvements in the therapeutic index for lowering cholesterol and other lipids associated with cardiovascular risks.
* PeriCor Therapeutics - Metabasis has a common stock ownership position in privately-held PeriCor Therapeutics, Inc. PeriCor sublicensed rights from Metabasis to acadesine and three additional Adenosine Regulating Agents in 2005. PeriCor licensed acadesine to Schering-Plough Corporation (now Merck & Co.) and the compound is in a Phase III clinical trial for the prevention of adverse cardiovascular and cerebrovascular outcomes in patients undergoing coronary artery bypass graft surgery.
* HepDirect Technology - HepDirect technology supplements Ligand's core drug discovery technology platform of ligand-dependent gene expression and ultra-high throughput combinatorial chemistry screening. HepDirect is a prodrug technology that targets delivery of certain drugs to the liver by using a proprietary chemical modification that renders a drug biologically inactive until cleaved by a liver-specific enzyme.
* Other Product Candidates and R&D Programs - Metabasis has other product candidates, including MB07803 for diabetes and pradefovir for hepatitis B, which have been evaluated in clinical trials and early stage R&D programs including glucokinase activators for diabetes and DGAT-1 inhibitors for obesity.
Ligands Strategie im Sog der Finanzkrise kleiere Biotechs zu schlucken scheint sich auszuzahlen. Jetzt wird deutlich, dass sie Metabasis quasi geschenkt bekommen haben!
Helfen tuts dem Kurs nix. Mir egal. Ich bleib long!
Ligand Earns $6.5 Million Milestone Payment from Roche
Roche Advances RG7348 into Clinical Development for Hepatitis C
SAN DIEGO, Apr 20, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced that it earned a $6.5 million payment from Roche (SWX: ROG.VX; RO.S, OTCQX: RHHBY) as a result of Roche progressing RG7348 into a Phase I clinical trial for the treatment of hepatitis C viral (HCV) infection. The milestone payment arises from a 2008 collaboration and license agreement between Roche and Metabasis Therapeutics, Inc. Ligand acquired Metabasis in January 2010. Ligand's net proceeds from the milestone payment will be approximately $2.3 million after paying $4.2 million to others including holders of the Ligand-issued "Roche" CVR.
"This is a great milestone for Ligand due to the cash revenue and because it validates the quality of assets we assumed through our recent acquisitions," said John L. Higgins, President and Chief Executive Officer of Ligand. "Recently we have acquired three public companies that have contributed a vast array of partnered and pipeline assets. We are very pleased with our partnership with Roche and are excited to see their program advance to human development for HCV."
Under the 2008 collaboration and license agreement, Metabasis contributed HepDirect(R) liver-targeting technology to help develop prodrugs of Roche's proprietary lead nucleosides against HCV infection. Ligand is eligible to receive additional payments from Roche upon the achievement of certain further development and regulatory milestones as well as royalties on potential sales of the drug, subject to obligations to share such payments with holders of the Ligand-issued Roche CVR.
The CVRs
Ligand issued a Roche contingent value right (CVR) to each former holder of a Metabasis common share as part of Ligand's acquisition of Metabasis. Each Roche CVR entitles holders to certain payments if and when Ligand receives certain payments in connection with the Roche-Metabasis collaboration and license agreement. Of the $6.5 million milestone payment, 65% is earmarked for the Roche CVR holders. After reduction for pre-existing contractual payment obligations, the Roche CVR holders will receive approximately $2.7 million in respect of this milestone payment.
Zur Erinnerung: http://investors.ligand.com/releasedetail.cfm?ReleaseID=4410…
Ligand Completes Acquisition of Metabasis
SAN DIEGO, Jan 28, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND) announced that it has completed the acquisition of Metabasis Therapeutics, Inc. (NASDAQ:MBRX), following approval of the transaction by Metabasis stockholders yesterday. As a result, Ligand gains a fully funded partnership with Roche, additional pipeline assets and drug discovery technologies and resources. The transaction was first announced on October 27, 2009.
"We are excited about this acquisition and the opportunities it presents for our shareholders," said John L. Higgins, President and Chief Executive Officer of Ligand. "The acquisition of Metabasis builds on our strategy to cultivate a robust pipeline with a broad array of royalty bearing assets and early stage pipeline programs."
In the acquisition, Ligand paid $1.6 million in cash or about $0.046 per Metabasis share to Metabasis' stockholders. In addition, Metabasis stockholders received four tradable Contingent Value Rights (CVRs), one CVR from each of four respective series of CVRs, for each Metabasis share. The CVRs will entitle Metabasis stockholders to cash payments as frequently as every six months as cash is received by Ligand from proceeds from Metabasis' partnership with Roche or the sale or partnering of any of the Metabasis drug development programs, among other triggering events.
Primary Acquired Assets
* Fully funded partnership with Roche to develop new treatments for hepatitis C viral infection utilizing the proprietary HepDirect(R) liver-targeting technology. The lead HepDirect nucleoside, MB11362, was declared a clinical candidate in the second quarter of 2009. Roche will fund 100% of program costs and will make milestone and royalty payments upon the achievement of certain development events and commercialization of MB11362 and/or other applicable HepDirect compounds covered under the agreement.
* Glucagon Receptor Antagonist Program - Metabasis has developed chemically novel, potent, orally bioavailable glucagon antagonists for treating type 2 diabetes. The lead compound, MB11262, has shown significant and consistent lowering of blood glucose when dosed orally in numerous diabetic animal models and is currently in pre-clinical development.
* Thyroid Receptor Beta Agonist Program - Metabasis has developed and evaluated in clinical trials a liver-targeted TR Beta agonist, MB07811, using HepDirect prodrug technology and other structural characteristics for the treatment of hyperlipidemia. In addition, there is an advanced discovery program to identify second-generation TR Beta agonists with potential improvements in the therapeutic index for lowering cholesterol and other lipids associated with cardiovascular risks.
* PeriCor Therapeutics - Metabasis has a common stock ownership position in privately-held PeriCor Therapeutics, Inc. PeriCor sublicensed rights from Metabasis to acadesine and three additional Adenosine Regulating Agents in 2005. PeriCor licensed acadesine to Schering-Plough Corporation (now Merck & Co.) and the compound is in a Phase III clinical trial for the prevention of adverse cardiovascular and cerebrovascular outcomes in patients undergoing coronary artery bypass graft surgery.
* HepDirect Technology - HepDirect technology supplements Ligand's core drug discovery technology platform of ligand-dependent gene expression and ultra-high throughput combinatorial chemistry screening. HepDirect is a prodrug technology that targets delivery of certain drugs to the liver by using a proprietary chemical modification that renders a drug biologically inactive until cleaved by a liver-specific enzyme.
* Other Product Candidates and R&D Programs - Metabasis has other product candidates, including MB07803 for diabetes and pradefovir for hepatitis B, which have been evaluated in clinical trials and early stage R&D programs including glucokinase activators for diabetes and DGAT-1 inhibitors for obesity.
Ligands Strategie im Sog der Finanzkrise kleiere Biotechs zu schlucken scheint sich auszuzahlen. Jetzt wird deutlich, dass sie Metabasis quasi geschenkt bekommen haben!
Helfen tuts dem Kurs nix. Mir egal. Ich bleib long!
hallo kmastra
Ligand to Report First Quarter Results on May 5th,mal sehen was sie zu berichten haben.
asics
Ligand to Report First Quarter Results on May 5th,mal sehen was sie zu berichten haben.
asics
Antwort auf Beitrag Nr.: 39.402.108 von asics01 am 26.04.10 16:44:00Hallo asics.
Zahlen waren keine Überraschung. In der Präsentation wurde aber gesagt, dass Promacta nun auch in den ersten Märkten Europas erhältlich ist (Deutschland, GB...). Ich halte Europa für wichtiger als den US-markt. Von daher werden die nächsten Zahlen spannend!
Im Moment gehen bei Ligand komiche Dinge ab. Volumen zieht merklich an und Reuters bringt eine alte Nachricht aus dem Dezember erneut ans Tageslicht. Spekulationen dazu im Yahoo-Board...
Mit sportlichem Gruß
kmastra
Zahlen waren keine Überraschung. In der Präsentation wurde aber gesagt, dass Promacta nun auch in den ersten Märkten Europas erhältlich ist (Deutschland, GB...). Ich halte Europa für wichtiger als den US-markt. Von daher werden die nächsten Zahlen spannend!
Im Moment gehen bei Ligand komiche Dinge ab. Volumen zieht merklich an und Reuters bringt eine alte Nachricht aus dem Dezember erneut ans Tageslicht. Spekulationen dazu im Yahoo-Board...
Mit sportlichem Gruß
kmastra
Antwort auf Beitrag Nr.: 39.515.688 von kmastra am 13.05.10 17:06:51allo kmastra
ich war mal kurz draussen aus ligand,habe letzte woche bei 1,39€ aus frust verkauft (120€ gewinnn)bin aber vorgestern wieder in usa zu 1,62$ rein.
hier wird versucht die kleinen mürbe zu machen,anders kann ich mir das nicht erklären was hier abgeht.irgendwann kommt der weisse ritter......
sag mal kriegen die auch milestone zahlungen von pfizer wenn aprela auf den markt kommt????
asics
ich war mal kurz draussen aus ligand,habe letzte woche bei 1,39€ aus frust verkauft (120€ gewinnn)bin aber vorgestern wieder in usa zu 1,62$ rein.
hier wird versucht die kleinen mürbe zu machen,anders kann ich mir das nicht erklären was hier abgeht.irgendwann kommt der weisse ritter......
sag mal kriegen die auch milestone zahlungen von pfizer wenn aprela auf den markt kommt????
asics
Antwort auf Beitrag Nr.: 39.525.330 von asics01 am 15.05.10 08:10:35Moin asics.
Auch ich kann die Kursentwicklung von Ligand nicht nachvollziehen.
Zumal Ligand kurz vor der Gewinnzone ist.
Ich gehe mal davon aus, dass Ligand Milestones bei Zulassung von Aprela bekommt. Ist aber nur eine Vermutung. Die Roalties sind ja auch nur winzig.
Ich bleibe auf jeden Fall long.
Auch ich kann die Kursentwicklung von Ligand nicht nachvollziehen.
Zumal Ligand kurz vor der Gewinnzone ist.
Ich gehe mal davon aus, dass Ligand Milestones bei Zulassung von Aprela bekommt. Ist aber nur eine Vermutung. Die Roalties sind ja auch nur winzig.
Ich bleibe auf jeden Fall long.
Antwort auf Beitrag Nr.: 39.569.533 von kmastra am 22.05.10 13:16:04hab mir grstern abend noch mal bei 1,44$ ein paar gegönnt







Ligand Board Authorizes Reverse Stock Split and $10 Million Share Repurchase
Company Forecasts Operational Profitability and Positive Cash Flow from Operations for 2011
SAN DIEGO, Jun 15, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND) today announced that its Board of Directors has authorized a reverse stock split of the Company's common stock and a share repurchase program. Ligand also announced preliminary financial guidance for 2011 and updated financial guidance for 2010.
"Our revenue and financial performance outlook is positive over the foreseeable future," said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. "We have confidence in the business and believe this is an appropriate time to reduce our bloated share count through a reverse stock split as the company moves toward profitability. A higher share price and lower share count also may broaden Ligand's appeal to investors, and reduce per share transaction fees and certain administrative costs. As the Company does not require additional capital to fund operations, we believe it could be a good use of our cash to make selective repurchases of our stock from time to time."
Mr. Higgins continued, "Currently we are receiving royalties on two commercial products, AVINZA(R) and PROMACTA(R), and we look forward to the market launch of up to four additional royalty bearing products by our partners over the next three years. A total of ten potential products could be launched over the next eight years, coming from our existing portfolio of more than 30 milestone and royalty bearing partnered programs. Importantly, this growth outlook comes as we are substantially lowering spending compared with the past couple of years. We are excited about our business, and look forward to discussing today's announcement, our product portfolio and business strategies during our Investor and Analyst Meeting later this month."
Reverse Stock Split
The reverse stock split approved by the Ligand Board of Directors would effect a reverse stock split of the Company's outstanding common stock at a ratio in the range of 1-for-5 to 1-for-10. The reverse stock split is subject to stockholder approval. The Company will prepare and distribute a proxy statement for a special meeting of stockholders to consider and vote upon a proposal granting Ligand's Board of Directors the authority to amend the Certificate of Incorporation to effect a reverse stock split of the Company's outstanding common stock at a ratio in the range mentioned above, with the exact ratio to be determined at the discretion of the Company's Board of Directors. The timetable, location and other details regarding the special meeting will be communicated to stockholders at a later date. The Company currently expects the reverse stock split to be completed in the third quarter of 2010. As of March 31, 2010, Ligand had 117,579,148 shares of common stock outstanding.
Share Repurchase Program
Ligand's Board of Directors authorized the Company to repurchase up to $10 million of its common stock from time to time in privately negotiated and open market transactions for a period of up to two years, subject to the Company's evaluation of market conditions, applicable legal requirements and other factors. The Company is not obligated to acquire common stock under this program, and the program may be suspended at any time.
Financial Guidance
The Company is providing updated guidance for 2010. Ligand now expects total revenue to be approximately $25 million and total operating expenses to be approximately $30 million. Revenue and expenses are both lower than previously forecast due to the anticipated wind-down of certain early, pre-clinical research collaborations in the second half of 2010. Additionally, Ligand currently projects it will have more than $30 million of cash at the end of 2010.
Ligand is also announcing preliminary financial guidance for 2011. The Company expects operating expenses for 2011 to be in the range of $15 million to $18 million, which is approximately one-half of its expected operating expenses for 2010. The significant reduction in projected operating expenses is primarily due to eliminating non-recurring costs for terminated, early stage research collaborations and continued savings from the Company's restructuring initiated in 2007. Based on current projected royalty and milestone revenues and the reduced expense plan, Ligand expects to be profitable on an operating basis and to have positive cash flow from operations in 2011.
Investor and Analyst Meeting
Ligand's Investor and Analyst Meeting will take place from 4:15 p.m. Eastern time through 5:45 p.m. Eastern time on Thursday, June 24, 2010 at the Eventi hotel in New York City. A live webcast will be available in the Investor Relations section of www.ligand.com, and also will be available through July 23, 2010. To attend the event in person, please contact Erika Luib at (858) 550-7896.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients for a broad spectrum of diseases including hepatitis, muscle wasting, Alzheimer's, inflammatory diseases, anemia, COPD, asthma, rheumatoid arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including GlaxoSmithKline, Merck, Pfizer, Roche, Bristol-Myers Squibb, and Cephalon and more than 30 programs are in various stages of development by its partners.
Forward-Looking Statements
This news release contains certain forward-looking statements by Ligand that involve risks and uncertainties and reflect Ligand's judgment as of the date of this release. Actual events or results may differ from Ligand's expectations. For example, the reverse stock split may not be completed in accordance with the timing or terms contained in this press release, or at all, and the intended benefits of the reverse stock split, the share repurchase program and expense reductions may not be realized. Likewise, we may not receive expected royalties on AVINZA(R) from King Pharmaceuticals, PROMACTA(R) from GSK or any other partnered products or from research and development milestones and we may not be able to timely or successfully advance any product(s) in Ligand's pipeline. In addition, there can be no assurance that Ligand will achieve its guidance for 2010 or 2011, that Ligand will deliver strong cash flow over the long-term, that Ligand's 2010 or 2011 revenues will be driven by royalty payments related to AVINZA and PROMACTA sales, that results of any clinical study will be timely, favorable or confirmed by later studies, that products under development by Ligand or its partners will receive regulatory approval in 2010 or later, or that there will be a market for such product(s) if successfully developed and approved. Also, Ligand may experience delays in the commencement, enrollment, completion or analysis of clinical testing for its product candidates, or significant issues regarding the adequacy of its clinical trial designs or the execution of its clinical trials, which could result in increased costs and delays or limit Ligand's ability to obtain regulatory approval. Further, unexpected adverse side effects or inadequate therapeutic efficacy of Ligand's product(s) could delay or prevent regulatory approval or commercialization. Ligand may also have indemnification obligations to King Pharmaceuticals or Eisai in connection with the sales of the AVINZA and oncology product lines. In addition, Ligand may not be able to successfully implement its strategic growth plan or continue the development of its proprietary programs. The failure to meet expectations with respect to any of the foregoing matters may reduce Ligand's stock price. Additional information concerning these and other risk factors affecting Ligand's business can be found in prior press releases available via www.ligand.com as well as in Ligand's public periodic filings with the Securities and Exchange Commission at www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this release. This caution is made under the safe harbor provisions of the Private Securities Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Lippert/Heilshorn & Associates
Don Markley
310-691-7100
dmarkley@lhai.com
Copyright Business Wire 2010
Company Forecasts Operational Profitability and Positive Cash Flow from Operations for 2011
SAN DIEGO, Jun 15, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND) today announced that its Board of Directors has authorized a reverse stock split of the Company's common stock and a share repurchase program. Ligand also announced preliminary financial guidance for 2011 and updated financial guidance for 2010.
"Our revenue and financial performance outlook is positive over the foreseeable future," said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. "We have confidence in the business and believe this is an appropriate time to reduce our bloated share count through a reverse stock split as the company moves toward profitability. A higher share price and lower share count also may broaden Ligand's appeal to investors, and reduce per share transaction fees and certain administrative costs. As the Company does not require additional capital to fund operations, we believe it could be a good use of our cash to make selective repurchases of our stock from time to time."
Mr. Higgins continued, "Currently we are receiving royalties on two commercial products, AVINZA(R) and PROMACTA(R), and we look forward to the market launch of up to four additional royalty bearing products by our partners over the next three years. A total of ten potential products could be launched over the next eight years, coming from our existing portfolio of more than 30 milestone and royalty bearing partnered programs. Importantly, this growth outlook comes as we are substantially lowering spending compared with the past couple of years. We are excited about our business, and look forward to discussing today's announcement, our product portfolio and business strategies during our Investor and Analyst Meeting later this month."
Reverse Stock Split
The reverse stock split approved by the Ligand Board of Directors would effect a reverse stock split of the Company's outstanding common stock at a ratio in the range of 1-for-5 to 1-for-10. The reverse stock split is subject to stockholder approval. The Company will prepare and distribute a proxy statement for a special meeting of stockholders to consider and vote upon a proposal granting Ligand's Board of Directors the authority to amend the Certificate of Incorporation to effect a reverse stock split of the Company's outstanding common stock at a ratio in the range mentioned above, with the exact ratio to be determined at the discretion of the Company's Board of Directors. The timetable, location and other details regarding the special meeting will be communicated to stockholders at a later date. The Company currently expects the reverse stock split to be completed in the third quarter of 2010. As of March 31, 2010, Ligand had 117,579,148 shares of common stock outstanding.
Share Repurchase Program
Ligand's Board of Directors authorized the Company to repurchase up to $10 million of its common stock from time to time in privately negotiated and open market transactions for a period of up to two years, subject to the Company's evaluation of market conditions, applicable legal requirements and other factors. The Company is not obligated to acquire common stock under this program, and the program may be suspended at any time.
Financial Guidance
The Company is providing updated guidance for 2010. Ligand now expects total revenue to be approximately $25 million and total operating expenses to be approximately $30 million. Revenue and expenses are both lower than previously forecast due to the anticipated wind-down of certain early, pre-clinical research collaborations in the second half of 2010. Additionally, Ligand currently projects it will have more than $30 million of cash at the end of 2010.
Ligand is also announcing preliminary financial guidance for 2011. The Company expects operating expenses for 2011 to be in the range of $15 million to $18 million, which is approximately one-half of its expected operating expenses for 2010. The significant reduction in projected operating expenses is primarily due to eliminating non-recurring costs for terminated, early stage research collaborations and continued savings from the Company's restructuring initiated in 2007. Based on current projected royalty and milestone revenues and the reduced expense plan, Ligand expects to be profitable on an operating basis and to have positive cash flow from operations in 2011.
Investor and Analyst Meeting
Ligand's Investor and Analyst Meeting will take place from 4:15 p.m. Eastern time through 5:45 p.m. Eastern time on Thursday, June 24, 2010 at the Eventi hotel in New York City. A live webcast will be available in the Investor Relations section of www.ligand.com, and also will be available through July 23, 2010. To attend the event in person, please contact Erika Luib at (858) 550-7896.
About Ligand Pharmaceuticals
Ligand discovers and develops new drugs that address critical unmet medical needs of patients for a broad spectrum of diseases including hepatitis, muscle wasting, Alzheimer's, inflammatory diseases, anemia, COPD, asthma, rheumatoid arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based assays, gene-expression tools, ultra-high throughput screening and one of the world's largest combinatorial chemical libraries. Ligand has strategic alliances with major pharmaceutical and biotechnology companies, including GlaxoSmithKline, Merck, Pfizer, Roche, Bristol-Myers Squibb, and Cephalon and more than 30 programs are in various stages of development by its partners.
Forward-Looking Statements
This news release contains certain forward-looking statements by Ligand that involve risks and uncertainties and reflect Ligand's judgment as of the date of this release. Actual events or results may differ from Ligand's expectations. For example, the reverse stock split may not be completed in accordance with the timing or terms contained in this press release, or at all, and the intended benefits of the reverse stock split, the share repurchase program and expense reductions may not be realized. Likewise, we may not receive expected royalties on AVINZA(R) from King Pharmaceuticals, PROMACTA(R) from GSK or any other partnered products or from research and development milestones and we may not be able to timely or successfully advance any product(s) in Ligand's pipeline. In addition, there can be no assurance that Ligand will achieve its guidance for 2010 or 2011, that Ligand will deliver strong cash flow over the long-term, that Ligand's 2010 or 2011 revenues will be driven by royalty payments related to AVINZA and PROMACTA sales, that results of any clinical study will be timely, favorable or confirmed by later studies, that products under development by Ligand or its partners will receive regulatory approval in 2010 or later, or that there will be a market for such product(s) if successfully developed and approved. Also, Ligand may experience delays in the commencement, enrollment, completion or analysis of clinical testing for its product candidates, or significant issues regarding the adequacy of its clinical trial designs or the execution of its clinical trials, which could result in increased costs and delays or limit Ligand's ability to obtain regulatory approval. Further, unexpected adverse side effects or inadequate therapeutic efficacy of Ligand's product(s) could delay or prevent regulatory approval or commercialization. Ligand may also have indemnification obligations to King Pharmaceuticals or Eisai in connection with the sales of the AVINZA and oncology product lines. In addition, Ligand may not be able to successfully implement its strategic growth plan or continue the development of its proprietary programs. The failure to meet expectations with respect to any of the foregoing matters may reduce Ligand's stock price. Additional information concerning these and other risk factors affecting Ligand's business can be found in prior press releases available via www.ligand.com as well as in Ligand's public periodic filings with the Securities and Exchange Commission at www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this release. This caution is made under the safe harbor provisions of the Private Securities Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Lippert/Heilshorn & Associates
Don Markley
310-691-7100
dmarkley@lhai.com
Copyright Business Wire 2010
Antwort auf Beitrag Nr.: 39.689.116 von asics01 am 16.06.10 10:16:15Moin Asics,
tja einfach nur schlecht was da schon wieder von Seiten des Managements kommt. Vor allem alles auf einmal Reverssplit, Rückkaufprogram, Umsatzwarnung und Aussichten 2011) das sieht echt nach Panik aus. So nach dem Motto: Wie verkaufen wir die Umsatzwarung am besten?
Immerhin legen sie sich ja fest, im Jahr 2011 Gewinn machen zu wollen. Was das allerdings wert ist sieht man ja an den neuen Zahlen für 2010. Entäuschend!
SG kmastra
tja einfach nur schlecht was da schon wieder von Seiten des Managements kommt. Vor allem alles auf einmal Reverssplit, Rückkaufprogram, Umsatzwarnung und Aussichten 2011) das sieht echt nach Panik aus. So nach dem Motto: Wie verkaufen wir die Umsatzwarung am besten?
Immerhin legen sie sich ja fest, im Jahr 2011 Gewinn machen zu wollen. Was das allerdings wert ist sieht man ja an den neuen Zahlen für 2010. Entäuschend!
SG kmastra
Antwort auf Beitrag Nr.: 39.693.853 von kmastra am 16.06.10 20:44:17tja da wird in nächster zeit wohl nicht mehr viel passieren auser...?????man weiss ja nie
hallo kmastra
hast du nun den glauben an ligand verloren ???ich sehe den split und den aktienrückkauf positiv.
wen jetzt die zahlen noch gut sind dann gibt es einen ruck.
asics
hast du nun den glauben an ligand verloren ???ich sehe den split und den aktienrückkauf positiv.
wen jetzt die zahlen noch gut sind dann gibt es einen ruck.
asics
Antwort auf Beitrag Nr.: 39.721.684 von asics01 am 22.06.10 18:52:06Moin Asics,
ich habe den Glauben an Ligand natürlich nicht verloren. Finde den Kursverlauf allerdings enttäuschend. Grundsätzlich ist ein Aktienrückkaufprogram natürlich positiv. Aber dann noch die "Umsatzwarnung", Resplit und Zahlen für 2011 gleichzeitig mitzuteilen sieht einfach nur nach Panik aus.
Von den Zahlen würde ich zunächst nicht allzu viel erwarten.
Na ja ich bleib long...
SG kmastra
ich habe den Glauben an Ligand natürlich nicht verloren. Finde den Kursverlauf allerdings enttäuschend. Grundsätzlich ist ein Aktienrückkaufprogram natürlich positiv. Aber dann noch die "Umsatzwarnung", Resplit und Zahlen für 2011 gleichzeitig mitzuteilen sieht einfach nur nach Panik aus.
Von den Zahlen würde ich zunächst nicht allzu viel erwarten.
Na ja ich bleib long...
SG kmastra
Antwort auf Beitrag Nr.: 39.722.624 von kmastra am 22.06.10 21:41:15ich gehe mal in wartestellung,mal schaun wie weit sie ligand noch runterknüppeln?????
hallo kmastra
weisst du einen genauen termin wegen des rs ????3 quartal ist klar, wird wohl kurz nach den zahlen kommen oder ?????
hab heute noch mal bei 1,41$ nachgelegt,aber jetzt ist es genug
asics
weisst du einen genauen termin wegen des rs ????3 quartal ist klar, wird wohl kurz nach den zahlen kommen oder ?????
hab heute noch mal bei 1,41$ nachgelegt,aber jetzt ist es genug
asics
hallo kmastra
hast du die neue webseite von ligand gesehen ????gefällt mir gut,jetzt muss nur mal der kurs in die gänge kommen
asics
hast du die neue webseite von ligand gesehen ????gefällt mir gut,jetzt muss nur mal der kurs in die gänge kommen
asics
hallo kmastra
tröste mich und sag mir dass alles gut wird





tröste mich und sag mir dass alles gut wird






Antwort auf Beitrag Nr.: 40.098.123 von asics01 am 03.09.10 19:23:40Hallo asics01, ich bin bisweilen auch bedient.
Aber ich gebe die Hoffnung nicht auf. Zur Aufmunterung eine positive Perspektive: Vielleicht schreibt Ligand nächstes Jahr Gewinne!
Aber ich gebe die Hoffnung nicht auf. Zur Aufmunterung eine positive Perspektive: Vielleicht schreibt Ligand nächstes Jahr Gewinne!
Antwort auf Beitrag Nr.: 40.098.778 von kmastra am 03.09.10 20:59:35entweder sie dümppelt weiter so vor sich hin,oder es kommt eine hammermeldung und sie explodiert.meine meinung
dara ist wohl auch geschichte oder ???
asics
dara ist wohl auch geschichte oder ???
asics
Antwort auf Beitrag Nr.: 40.099.865 von asics01 am 04.09.10 06:57:55Ja Dara kannste vergessen. Hammermeldungen könnten nur durch eine Verpartnerung oder guten Studienergebnissen kommen...
Antwort auf Beitrag Nr.: 40.101.518 von kmastra am 04.09.10 21:13:04nach dem split wirds wohl auch einen schub geben ,gute studienergebnisse oder eine übernahme ???warum nicht
Antwort auf Beitrag Nr.: 40.102.112 von asics01 am 05.09.10 11:09:56Auf den Schub nach dem Respilt würde ich eher nicht setzen. Im Allgemeinen ist das eher negativ zu sehen. Aber schaun wir mal...
Antwort auf Beitrag Nr.: 40.107.853 von kmastra am 06.09.10 22:18:45hallo kmastra
irgendwas liegt in der luft (aber was ????),mein bauchgefühl sagt mir dass es demnächst kracht im gebälck



asics
irgendwas liegt in der luft (aber was ????),mein bauchgefühl sagt mir dass es demnächst kracht im gebälck




asics
Antwort auf Beitrag Nr.: 40.130.165 von asics01 am 10.09.10 08:05:07Mal sehen, ob auf dein Bauchgefühl verlass ist...ich hätte nichts dagegen

Antwort auf Beitrag Nr.: 40.132.368 von kmastra am 10.09.10 14:04:58die letzten 3 handelstage lassen mich darauf schliessen,dass etwas kommt aber ob positiv oder negativ ???glaube aber an ersteres, deswegen habe ich vorgestern nochmal bei 1,48$ nachgelegt.
asics
asics
hallo kmastra
die will mit aller gewalt nach oben,
ob der ausbruch dieses mal klappt???
asics
die will mit aller gewalt nach oben,
ob der ausbruch dieses mal klappt???
asics
Antwort auf Beitrag Nr.: 40.142.452 von asics01 am 13.09.10 16:52:32Moin asics,
ein Ausbruch über 1,70 $ könnte in der Tat als charttechnisches Kaufsignal gewertet werden.
Schaun mer mal.... Noch ist in US ja auch nicht schluss und meist wird der Kurs ja gegen Ende noch massiv beeinflust.
Welch Potenzial alleine im SARM Programm steckt wird in diesem Artikel deutlich:
http://www.stltoday.com/news/national/article_46a71328-b49b-…
Neben dem oral-epo Programm sicherlich das interessanteste Medikament in eigener Entwicklung.
SG kmastra
ein Ausbruch über 1,70 $ könnte in der Tat als charttechnisches Kaufsignal gewertet werden.
Schaun mer mal.... Noch ist in US ja auch nicht schluss und meist wird der Kurs ja gegen Ende noch massiv beeinflust.
Welch Potenzial alleine im SARM Programm steckt wird in diesem Artikel deutlich:
http://www.stltoday.com/news/national/article_46a71328-b49b-…
Neben dem oral-epo Programm sicherlich das interessanteste Medikament in eigener Entwicklung.
SG kmastra
Antwort auf Beitrag Nr.: 40.143.331 von kmastra am 13.09.10 19:10:46Ligand Pharma transfers CXCR4 target rights to Proximagen
Published: 20-Sep-2010
Ligand Pharmaceuticals has transferred exclusive license rights related to the CXCR4 target with application for a number of indications including those related to the central nervous system to Proximagen.
Ligand is expected to receive an upfront payment and continue to be entitled to receive potential future milestone and royalty payments.
Ligand Pharma president and CEO John Higgins said that the agreement with Proximagen partially monetises a program acquired in their 2008 acquisition of Pharmacopeia, and restarts another research collaboration with significant commercial potential in Ligand’s portfolio of fully funded and royalty-bearing programs.
Ligand said that the transfer of exclusive rights was made under a 2004 drug discovery alliance entered between Pharmacopeia and Swedish Orphan Biovitrum as per which Pharmacopeia's compound library was accessed to identify and optimise leads.
Published: 20-Sep-2010
Ligand Pharmaceuticals has transferred exclusive license rights related to the CXCR4 target with application for a number of indications including those related to the central nervous system to Proximagen.
Ligand is expected to receive an upfront payment and continue to be entitled to receive potential future milestone and royalty payments.
Ligand Pharma president and CEO John Higgins said that the agreement with Proximagen partially monetises a program acquired in their 2008 acquisition of Pharmacopeia, and restarts another research collaboration with significant commercial potential in Ligand’s portfolio of fully funded and royalty-bearing programs.
Ligand said that the transfer of exclusive rights was made under a 2004 drug discovery alliance entered between Pharmacopeia and Swedish Orphan Biovitrum as per which Pharmacopeia's compound library was accessed to identify and optimise leads.
1 schritt vor und 5 zurück, so wird das nix
hallo kmastra
nix mit ausbruch über 1.70$ das teil wird doch künstlich untengehalten oder haben die leichen im keller????
die allianz mit cephalon gibts wohl auch nicht mehr,wurde wohl stillschweigend beendet.
um was geht es hier genau,weisst du das ???
13.09.2010 23:25
BRIEF-Ligand Pharmaceuticals says GlaxoSmithkline to terminate agreement
Sept 13 (Reuters) - Ligand Pharmaceuticals Inc:
* Says received notice from GlaxoSmithkline that it was exercising its right to
terminate gsk agreement
* Says the termination becomes effective on October 7 - SEC filing
* Says it will not be required to refund payments already received relating
under the agreement
* Pharma-after termination, co will retain rights to current programs under gsk
agreement, may continue to develop programs
* Says gsk agreement relates to product development and commercialization
agreement for certain products
((Bangalore Equities Newsroom; +91 80 4135 5800; within U.S. +1 646 223 8780))
müsste der re split nicht noch dieses quartal über die bühne gehen????
weiterhin gute nerven und durchhaltevermögen
asics
nix mit ausbruch über 1.70$ das teil wird doch künstlich untengehalten oder haben die leichen im keller????
die allianz mit cephalon gibts wohl auch nicht mehr,wurde wohl stillschweigend beendet.
um was geht es hier genau,weisst du das ???
13.09.2010 23:25
BRIEF-Ligand Pharmaceuticals says GlaxoSmithkline to terminate agreement
Sept 13 (Reuters) - Ligand Pharmaceuticals Inc:
* Says received notice from GlaxoSmithkline that it was exercising its right to
terminate gsk agreement
* Says the termination becomes effective on October 7 - SEC filing
* Says it will not be required to refund payments already received relating
under the agreement
* Pharma-after termination, co will retain rights to current programs under gsk
agreement, may continue to develop programs
* Says gsk agreement relates to product development and commercialization
agreement for certain products
((Bangalore Equities Newsroom; +91 80 4135 5800; within U.S. +1 646 223 8780))
müsste der re split nicht noch dieses quartal über die bühne gehen????
weiterhin gute nerven und durchhaltevermögen
asics
Antwort auf Beitrag Nr.: 40.203.359 von asics01 am 24.09.10 09:52:22Moin asics,
das die aktie künstlich unten gehalten wird kann man so sagen. Tatsache ist zumindest, dass es seit einigen Jahren stetig bergab ging. Dazu muss man in die Geschichte von Ligand schauen. Ligand hatte 3 Medikamente zugelassen, die mittelmäßige Umsätze (ich meine so 300 Mio) brachten. Das reichte aber nicht, um den Vetrieb etc. wieder einzuspielen. Also wurden sie verkauft. Ein Teil des Gewinns wurde in einer Sonderdividende ausgschüttet. (ich meine das waren 2,5 $!). Für Shorts eine gute Situation, da es bis zur nächsten Zulassung noch lang hin war. Viele gingen also bei Ligand short. Und so fiel die Aktie auch entsprechend. Viele sind auch immer noch short. Es gibt also immer noch einige, die ein Interesse an einem niedrigen Kurs haben. Man sieht das auch daran, dass gegen Ende immer massive Umsätze stattfinden, um quasi auf den letzten Drücker den Kurs zu beeinflussen.
Andererseits wird Ligand auch zu 80 % von institutionellen Anlegern gehalten. Das bedeutet, das tatsächlich nur wenige Aktien auf dem Markt sind. Steigt der Kurs nun stark an (z.B. durch eine Zulassung, eine Verpartnerung etc.) müssen die Shorts sich eindecken. Dann steigt der Kurs also überproportional stark an. Ich glaube zumindest fest daran, dass es irgendwann so kommen wird. Prinzipiell hängt es aber primär davon ab, dass Newsflow kommt. Aber das schöne an Ligand ist ja gerade, dass sie nicht Pleite gehen können. Also m.E. alles eine Frage der Zeit und Geduld.
Sehr gut fasst es dieser user im yahoo-forum zusammen:
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
Zu dem GsK-deal: Das ist nicht schön war aber schon länger bekannt. Dementsprechend hat die Börse darauf ja auch nicht reagiert. Waren alles vorklinische Programme. Langfrsitig aber wie gesagt nicht gut für Ligand. Klar.
Zu Cephalon weiß ich nichts. Dort ist man über das vorklinische Stadium aber auch nicht hinaus. Also wenig werthaltig für Ligand.
das die aktie künstlich unten gehalten wird kann man so sagen. Tatsache ist zumindest, dass es seit einigen Jahren stetig bergab ging. Dazu muss man in die Geschichte von Ligand schauen. Ligand hatte 3 Medikamente zugelassen, die mittelmäßige Umsätze (ich meine so 300 Mio) brachten. Das reichte aber nicht, um den Vetrieb etc. wieder einzuspielen. Also wurden sie verkauft. Ein Teil des Gewinns wurde in einer Sonderdividende ausgschüttet. (ich meine das waren 2,5 $!). Für Shorts eine gute Situation, da es bis zur nächsten Zulassung noch lang hin war. Viele gingen also bei Ligand short. Und so fiel die Aktie auch entsprechend. Viele sind auch immer noch short. Es gibt also immer noch einige, die ein Interesse an einem niedrigen Kurs haben. Man sieht das auch daran, dass gegen Ende immer massive Umsätze stattfinden, um quasi auf den letzten Drücker den Kurs zu beeinflussen.
Andererseits wird Ligand auch zu 80 % von institutionellen Anlegern gehalten. Das bedeutet, das tatsächlich nur wenige Aktien auf dem Markt sind. Steigt der Kurs nun stark an (z.B. durch eine Zulassung, eine Verpartnerung etc.) müssen die Shorts sich eindecken. Dann steigt der Kurs also überproportional stark an. Ich glaube zumindest fest daran, dass es irgendwann so kommen wird. Prinzipiell hängt es aber primär davon ab, dass Newsflow kommt. Aber das schöne an Ligand ist ja gerade, dass sie nicht Pleite gehen können. Also m.E. alles eine Frage der Zeit und Geduld.
Sehr gut fasst es dieser user im yahoo-forum zusammen:
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
Zu dem GsK-deal: Das ist nicht schön war aber schon länger bekannt. Dementsprechend hat die Börse darauf ja auch nicht reagiert. Waren alles vorklinische Programme. Langfrsitig aber wie gesagt nicht gut für Ligand. Klar.
Zu Cephalon weiß ich nichts. Dort ist man über das vorklinische Stadium aber auch nicht hinaus. Also wenig werthaltig für Ligand.
hallo kmastra
die aktienstruktur von ligand ist mir bekannt,nur was mir nicht runter will es gab die letzten jahre eigentlich nur gute news aber seit jahren gehts nur bergab, kein aufbäumen nichts.
auch jetzt nach der kooperation mit proximagen es ging nicht hoch,nein es ging runter

aber wenn das stimmt das der junge 22000 st hält,ist das eine hausnummer.
ich habe ein paar weniger,aber dafür einen einstiegskurs im schnitt von 1,45$

ist dir was wegen des splittes bekannt der für das 3 quartal angeküdigt wurde ????
asics
die aktienstruktur von ligand ist mir bekannt,nur was mir nicht runter will es gab die letzten jahre eigentlich nur gute news aber seit jahren gehts nur bergab, kein aufbäumen nichts.
auch jetzt nach der kooperation mit proximagen es ging nicht hoch,nein es ging runter


aber wenn das stimmt das der junge 22000 st hält,ist das eine hausnummer.
ich habe ein paar weniger,aber dafür einen einstiegskurs im schnitt von 1,45$


ist dir was wegen des splittes bekannt der für das 3 quartal angeküdigt wurde ????
asics
hallo kmastra
mein bauchgefühl war doch nicht so gut,wahrscheinlich hat sich nur ein furz verirrt


wie geht es weiter???,das ist doch alles sehr traurig biotech index steigt und steigt,und wir schauen dumm hinterher
asics
mein bauchgefühl war doch nicht so gut,wahrscheinlich hat sich nur ein furz verirrt



wie geht es weiter???,das ist doch alles sehr traurig biotech index steigt und steigt,und wir schauen dumm hinterher
asics
stopp loss gesetzt bei 1,45€ wenns drunter geht bin ich raus und weg.
asics
asics
Antwort auf Beitrag Nr.: 40.260.718 von asics01 am 04.10.10 18:07:42muss natürlich 1,45$ heissen
hallo kmastra
heute gab es wieder eine news,nichts weltbewegendes aber kein schlechter schachzug seitens ligand.
geht wie immer nach news bestimmt wieder 3% abwärts heute
Ligand to Divest Combinatorial Compound Library and Screening Technology for $1.8
Million
SAN DIEGO, Oct 07, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced
that it has agreed to divest and sell its combinatorial chemical library and associated proprietary technology to Venenum
Biodesign, LLC, an affiliate of Medical Diagnostic Laboratories, LLC, members of Genesis Biotechnology Group (GBG), for
$1.8 million. Under the terms of the agreement, Ligand will receive $1 million at the close of the transaction, $800,000 over the
next two years and 10% of all revenues from third party collaborations for three years.
The combinatorial chemistry asset, which Ligand obtained in the acquisition of Pharmacopeia in December 2008, comprises an
encoded combinatorial library collection (ECLiPS) and an ultra-high throughput screening platform.
"While this screening technology was valuable in the discovery of multiple drug candidates for many of our existing
collaborations, it is no longer required in the service of those collaborations and going forward it is not a priority for our
research activities," said John L. Higgins, President and Chief Executive Officer of Ligand. "This transaction with Venenum
Biodesign reflects our ongoing strategy to focus resources on programs that will create the greatest long-term shareholder
value."
About Ligand Pharmaceuticals Incorporated
Ligand discovers and develops novel drugs that address critical unmet medical needs of patients for a broad spectrum of
diseases including hepatitis, muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid
arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based
assays, tissue-specific receptor ligand interactions and gene-expression tools. Among its peers, we believe Ligand has
assembled one of the largest portfolio of assets including commercial therapies developed in partnership with pharmaceutical
companies. Along with several internal programs, Ligand has established multiple alliances with the world's leading
pharmaceutical companies including GlaxoSmithKline (GSK), Merck, Pfizer, Roche, Bristol-Myers Squibb and AstraZeneca, and
more than 30 programs in various stages of development.
About Venenum Biodesign
Venenum Biodesign http://www.venenumbiodesign.com is a research center located in the "Einstein's Alley" research corridor
in Hamilton, New Jersey. Venenum Biodesign is dedicated to early stage drug discovery on novel targets and to providing ultrahigh-
throughput screens, assay development and compound optimization services to academic institutions, non-profit research
organizations and pharmaceutical companies in the US and internationally. Venenum Biodesign's scientific staff have years of
experience in assay development, high throughput screening, lead optimization, molecular biology and protein biochemistry.
Caution Regarding Forward-Looking Statements
This news release contains forward looking statements by Ligand that involve risks and uncertainties, including those related to
the creation of long-term shareholder value, and reflect Ligand's judgment as of the date of this release. Actual events or
results may differ from Ligand's expectations. Additional information concerning these and other risk factors affecting Ligand's
business can be found in prior press releases available via www.ligand.com as well as in Ligand's public periodic filings with the
Securities and Exchange Commission at www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking
statements beyond the date of this release. This caution is made under the safe harbor provisions of the Private Securities
Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
heute gab es wieder eine news,nichts weltbewegendes aber kein schlechter schachzug seitens ligand.
geht wie immer nach news bestimmt wieder 3% abwärts heute
Ligand to Divest Combinatorial Compound Library and Screening Technology for $1.8
Million
SAN DIEGO, Oct 07, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced
that it has agreed to divest and sell its combinatorial chemical library and associated proprietary technology to Venenum
Biodesign, LLC, an affiliate of Medical Diagnostic Laboratories, LLC, members of Genesis Biotechnology Group (GBG), for
$1.8 million. Under the terms of the agreement, Ligand will receive $1 million at the close of the transaction, $800,000 over the
next two years and 10% of all revenues from third party collaborations for three years.
The combinatorial chemistry asset, which Ligand obtained in the acquisition of Pharmacopeia in December 2008, comprises an
encoded combinatorial library collection (ECLiPS) and an ultra-high throughput screening platform.
"While this screening technology was valuable in the discovery of multiple drug candidates for many of our existing
collaborations, it is no longer required in the service of those collaborations and going forward it is not a priority for our
research activities," said John L. Higgins, President and Chief Executive Officer of Ligand. "This transaction with Venenum
Biodesign reflects our ongoing strategy to focus resources on programs that will create the greatest long-term shareholder
value."
About Ligand Pharmaceuticals Incorporated
Ligand discovers and develops novel drugs that address critical unmet medical needs of patients for a broad spectrum of
diseases including hepatitis, muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid
arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based
assays, tissue-specific receptor ligand interactions and gene-expression tools. Among its peers, we believe Ligand has
assembled one of the largest portfolio of assets including commercial therapies developed in partnership with pharmaceutical
companies. Along with several internal programs, Ligand has established multiple alliances with the world's leading
pharmaceutical companies including GlaxoSmithKline (GSK), Merck, Pfizer, Roche, Bristol-Myers Squibb and AstraZeneca, and
more than 30 programs in various stages of development.
About Venenum Biodesign
Venenum Biodesign http://www.venenumbiodesign.com is a research center located in the "Einstein's Alley" research corridor
in Hamilton, New Jersey. Venenum Biodesign is dedicated to early stage drug discovery on novel targets and to providing ultrahigh-
throughput screens, assay development and compound optimization services to academic institutions, non-profit research
organizations and pharmaceutical companies in the US and internationally. Venenum Biodesign's scientific staff have years of
experience in assay development, high throughput screening, lead optimization, molecular biology and protein biochemistry.
Caution Regarding Forward-Looking Statements
This news release contains forward looking statements by Ligand that involve risks and uncertainties, including those related to
the creation of long-term shareholder value, and reflect Ligand's judgment as of the date of this release. Actual events or
results may differ from Ligand's expectations. Additional information concerning these and other risk factors affecting Ligand's
business can be found in prior press releases available via www.ligand.com as well as in Ligand's public periodic filings with the
Securities and Exchange Commission at www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking
statements beyond the date of this release. This caution is made under the safe harbor provisions of the Private Securities
Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Antwort auf Beitrag Nr.: 40.290.052 von asics01 am 08.10.10 15:51:40da haben sie wohl wieder ein paar abgefischt
mal sehen wer zuerst kalte füsse bekommt,die shorties oder wir kleinaktionäre?????
Antwort auf Beitrag Nr.: 40.294.505 von asics01 am 09.10.10 20:37:01Ligand Appoints Sunil Patel to Board of Directors
SAN DIEGO, Oct 08, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced
the appointment of Sunil Patel to the Company's Board of Directors.
Mr. Patel, 39, has more than 17 years of senior management and R&D experience in the biotechnology industry and is
currently Senior Vice President of Corporate Development for OncoMed Pharmaceuticals, a development-stage company
focused on therapeutics targeting cancer stem cells. Mr. Patel has held senior management positions in corporate
development, marketing, and strategy with BiPar Sciences, Allos Therapeutics, Connetics, Abgenix and Gilead Sciences. Mr.
Patel also worked at McKinsey & Company serving biotech and pharmaceutical clients and has held scientific research
positions at ZymoGenetics and ProCyte.
"Given Ligand's unique biotech business model of conducting research, and acquiring and licensing assets, Sunil is an
excellent addition to Ligand's Board," said John L. Higgins, President and Chief Executive Officer of Ligand. "Sunil has played a
leadership role in numerous significant biotech licensing and M&A deals over the past several years. He has keen knowledge
of the small and mid-cap biotech universe, extensive licensing and deal execution experience, and good instincts for R&D and
pipeline priorities at big pharma. His ideas, knowledge and experience will be highly valuable as we work to continue to expand
our business."
Mr. Patel received his undergraduate degree in Chemistry at the University of California, Berkeley, and master's degree in
Molecular Bioengineering/Biotechnology at the University of Washington.
About Ligand Pharmaceuticals Incorporated
Ligand discovers and develops novel drugs that address critical unmet medical needs of patients for a broad spectrum of
diseases including hepatitis, muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid
arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based
assays, tissue-specific receptor ligand interactions and gene-expression tools. Among its peers, we believe Ligand has
assembled one of the largest portfolio of assets including commercial therapies developed in partnership with pharmaceutical
companies. Along with several internal programs, Ligand has established multiple alliances with the world's leading
pharmaceutical companies including GlaxoSmithKline (GSK), Merck, Pfizer, Roche, Bristol-Myers Squibb and AstraZeneca, and
more than 30 programs in various stages of development.
Caution Regarding Forward-Looking Statements
This news release contains forward looking statements by Ligand that involve risks and uncertainties and reflect Ligand's
judgment as of the date of this release. Actual events or results may differ from Ligand's expectations. Additional information
concerning these and other risk factors affecting Ligand's business can be found in prior press releases available via
www.ligand.com as well as in Ligand's public periodic filings with the Securities and Exchange Commission at www.sec.gov.
Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this release. This
caution is made under the safe harbor provisions of the Private Securities Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Lippert/Heilshorn & Associates
Don Markley, 310-691-7100
dmarkley@lhai.com
Copyright Business Wire 2010
SAN DIEGO, Oct 08, 2010 (BUSINESS WIRE) -- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced
the appointment of Sunil Patel to the Company's Board of Directors.
Mr. Patel, 39, has more than 17 years of senior management and R&D experience in the biotechnology industry and is
currently Senior Vice President of Corporate Development for OncoMed Pharmaceuticals, a development-stage company
focused on therapeutics targeting cancer stem cells. Mr. Patel has held senior management positions in corporate
development, marketing, and strategy with BiPar Sciences, Allos Therapeutics, Connetics, Abgenix and Gilead Sciences. Mr.
Patel also worked at McKinsey & Company serving biotech and pharmaceutical clients and has held scientific research
positions at ZymoGenetics and ProCyte.
"Given Ligand's unique biotech business model of conducting research, and acquiring and licensing assets, Sunil is an
excellent addition to Ligand's Board," said John L. Higgins, President and Chief Executive Officer of Ligand. "Sunil has played a
leadership role in numerous significant biotech licensing and M&A deals over the past several years. He has keen knowledge
of the small and mid-cap biotech universe, extensive licensing and deal execution experience, and good instincts for R&D and
pipeline priorities at big pharma. His ideas, knowledge and experience will be highly valuable as we work to continue to expand
our business."
Mr. Patel received his undergraduate degree in Chemistry at the University of California, Berkeley, and master's degree in
Molecular Bioengineering/Biotechnology at the University of Washington.
About Ligand Pharmaceuticals Incorporated
Ligand discovers and develops novel drugs that address critical unmet medical needs of patients for a broad spectrum of
diseases including hepatitis, muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid
arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based
assays, tissue-specific receptor ligand interactions and gene-expression tools. Among its peers, we believe Ligand has
assembled one of the largest portfolio of assets including commercial therapies developed in partnership with pharmaceutical
companies. Along with several internal programs, Ligand has established multiple alliances with the world's leading
pharmaceutical companies including GlaxoSmithKline (GSK), Merck, Pfizer, Roche, Bristol-Myers Squibb and AstraZeneca, and
more than 30 programs in various stages of development.
Caution Regarding Forward-Looking Statements
This news release contains forward looking statements by Ligand that involve risks and uncertainties and reflect Ligand's
judgment as of the date of this release. Actual events or results may differ from Ligand's expectations. Additional information
concerning these and other risk factors affecting Ligand's business can be found in prior press releases available via
www.ligand.com as well as in Ligand's public periodic filings with the Securities and Exchange Commission at www.sec.gov.
Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this release. This
caution is made under the safe harbor provisions of the Private Securities Litigation Reform Act of 1995.
SOURCE: Ligand Pharmaceuticals Incorporated
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Lippert/Heilshorn & Associates
Don Markley, 310-691-7100
dmarkley@lhai.com
Copyright Business Wire 2010
Antwort auf Beitrag Nr.: 40.294.959 von asics01 am 10.10.10 08:50:57Moin Asisc,
charttechnisch sieht es momentan ja nach Dreicksbildung aus. In letzter zeit kaum noch kursbewegungen. Demnächst also Entscheidung ob nach oben oder nach unten ausgebrochen wird.
Witzig finde ich Folgendes:
Pfizer schluckt gerade King - die vermarkten das z.zt. erfolgreichste medikament von ligand - avinza. Damit schmelzen die kooperationspartner von ligand erneut zusammen.
Pfizer hat ja schon whyeth geschluckt.
Merck hat schon Shering-Plough gekauft.
Nun kauft Pfizer also King...
Finde ich persönlich eher schlecht. Andereseits kann pfizer das medikament eventuell besser vermarkten...
SG kmastra
charttechnisch sieht es momentan ja nach Dreicksbildung aus. In letzter zeit kaum noch kursbewegungen. Demnächst also Entscheidung ob nach oben oder nach unten ausgebrochen wird.
Witzig finde ich Folgendes:
Pfizer schluckt gerade King - die vermarkten das z.zt. erfolgreichste medikament von ligand - avinza. Damit schmelzen die kooperationspartner von ligand erneut zusammen.
Pfizer hat ja schon whyeth geschluckt.
Merck hat schon Shering-Plough gekauft.
Nun kauft Pfizer also King...
Finde ich persönlich eher schlecht. Andereseits kann pfizer das medikament eventuell besser vermarkten...
SG kmastra
Keine Riesen-sache aber doch schön. Vielleicht hilft es ja über die 1,70$...
http://finance.yahoo.com/news/Ligand-Announces-Market-bw-181…
SAN DIEGO--(BUSINESS WIRE)-- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND - News) today announced that its partner Pfizer, Inc. (NYSE:PFE - News) launched Viviant® (Bazedoxifene) in Japan for the treatment of postmenopausal osteoporosis. Under the brand name Conbriza®, the drug is also marketed in Spain through a co-promotion with Almirall, an international pharmaceutical company based in Spain. Pfizer received manufacturing and marketing approval for the product in Japan in July 2010. Viviant was approved in April 2009 by the European Commission (under the trade name Conbriza®) for the treatment of postmenopausal osteoporosis in women at increased risk of fracture.
Viviant, a selective estrogen receptor modulator (SERM), is a result of the successful research collaboration between Wyeth (now Pfizer) and Ligand that began in 1994. Pfizer is responsible for the registration and worldwide marketing of bazedoxifene, a synthetic drug specifically designed to reduce the risk of osteoporotic fractures while also protecting uterine tissue. Ligand is entitled to receive tiered royalties on net sales of bazedoxifene.
“We are excited to see the progress of Viviant as it provides a new osteoporosis treatment option to postmenopausal women. This is now the third product that Ligand will earn royalties from out of a large portfolio of partnered, royalty bearing programs,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. “Viviant’s commercial introduction in Japan and Spain reflects the quality of Ligand’s collaborations and the expertise of its partners in business, product development and international regulatory affairs.”
http://finance.yahoo.com/news/Ligand-Announces-Market-bw-181…
SAN DIEGO--(BUSINESS WIRE)-- Ligand Pharmaceuticals Incorporated (NASDAQ:LGND - News) today announced that its partner Pfizer, Inc. (NYSE:PFE - News) launched Viviant® (Bazedoxifene) in Japan for the treatment of postmenopausal osteoporosis. Under the brand name Conbriza®, the drug is also marketed in Spain through a co-promotion with Almirall, an international pharmaceutical company based in Spain. Pfizer received manufacturing and marketing approval for the product in Japan in July 2010. Viviant was approved in April 2009 by the European Commission (under the trade name Conbriza®) for the treatment of postmenopausal osteoporosis in women at increased risk of fracture.
Viviant, a selective estrogen receptor modulator (SERM), is a result of the successful research collaboration between Wyeth (now Pfizer) and Ligand that began in 1994. Pfizer is responsible for the registration and worldwide marketing of bazedoxifene, a synthetic drug specifically designed to reduce the risk of osteoporotic fractures while also protecting uterine tissue. Ligand is entitled to receive tiered royalties on net sales of bazedoxifene.
“We are excited to see the progress of Viviant as it provides a new osteoporosis treatment option to postmenopausal women. This is now the third product that Ligand will earn royalties from out of a large portfolio of partnered, royalty bearing programs,” said John L. Higgins, President and Chief Executive Officer of Ligand Pharmaceuticals. “Viviant’s commercial introduction in Japan and Spain reflects the quality of Ligand’s collaborations and the expertise of its partners in business, product development and international regulatory affairs.”
Antwort auf Beitrag Nr.: 40.314.649 von kmastra am 13.10.10 17:20:03hallo kmastra
mühsam ernährt sich das eichhörnchen,aber noch glaube und hoffe ich dass demnächst die richtige meldung kommt und die shorties sich richtig die finger verbrennen.
die nachfolgende analyse ist zwar vom july aber noch top aktuell
Endingen (aktiencheck.de AG) - Nach den massiven Kursrückgängen der letzten Jahre dürfte die Talfahrt bei der Aktie von Ligand Pharmaceuticals (ISIN US53220K2078/ WKN 895777) nun ein Ende haben, so die Experten von "Global Biotech Investing".
Dafür würden gleich mehrere Gründe sprechen: Erstens erhalte die Firma jährliche Royaltyzahlungen für ihre bereits zugelassenen Wirkstoffe Avinza und Promacta. Zweitens erwarte das Management weitere Zulassungen in den kommenden Jahren. Drittens könnte auch der Newsflow in den nächsten zwei Quartalen positiv sein. Hier seien vor allem die Zulassung von Promacta in Japan sowie der NDA-Antrag für das Osteoporosemittel Aprela zu nennen. Viertens könnte Ligand Pharmaceuticals in 2011 das erste Mal in der Firmengeschichte einen operativen Gewinn sowie einen positiven Cashflow erwirtschaften. Fünftens wolle die Geschäftsführung im Herbst dieses Jahres einen Reverse-Split durchführen, was die Aktien optisch teurer und daher wertiger erscheinen lassen sollten.
Die Analysten von C.K. Cooper hätten kürzlich die Coverage für das Papier aufgenommen und ein Kursziel von 3,25 USD ausgegeben.
Nach Meinung der Experten sollen sich spekulative Anleger eine Miniposition der Ligand Pharmaceuticals-Aktie ins Depot holen und auf einen anstehenden Turnaround zocken. (Ausgabe 13 vom 05.07.2010) (05.07.2010/ac/a/a)
mühsam ernährt sich das eichhörnchen,aber noch glaube und hoffe ich dass demnächst die richtige meldung kommt und die shorties sich richtig die finger verbrennen.
die nachfolgende analyse ist zwar vom july aber noch top aktuell
Endingen (aktiencheck.de AG) - Nach den massiven Kursrückgängen der letzten Jahre dürfte die Talfahrt bei der Aktie von Ligand Pharmaceuticals (ISIN US53220K2078/ WKN 895777) nun ein Ende haben, so die Experten von "Global Biotech Investing".
Dafür würden gleich mehrere Gründe sprechen: Erstens erhalte die Firma jährliche Royaltyzahlungen für ihre bereits zugelassenen Wirkstoffe Avinza und Promacta. Zweitens erwarte das Management weitere Zulassungen in den kommenden Jahren. Drittens könnte auch der Newsflow in den nächsten zwei Quartalen positiv sein. Hier seien vor allem die Zulassung von Promacta in Japan sowie der NDA-Antrag für das Osteoporosemittel Aprela zu nennen. Viertens könnte Ligand Pharmaceuticals in 2011 das erste Mal in der Firmengeschichte einen operativen Gewinn sowie einen positiven Cashflow erwirtschaften. Fünftens wolle die Geschäftsführung im Herbst dieses Jahres einen Reverse-Split durchführen, was die Aktien optisch teurer und daher wertiger erscheinen lassen sollten.
Die Analysten von C.K. Cooper hätten kürzlich die Coverage für das Papier aufgenommen und ein Kursziel von 3,25 USD ausgegeben.
Nach Meinung der Experten sollen sich spekulative Anleger eine Miniposition der Ligand Pharmaceuticals-Aktie ins Depot holen und auf einen anstehenden Turnaround zocken. (Ausgabe 13 vom 05.07.2010) (05.07.2010/ac/a/a)
Antwort auf Beitrag Nr.: 40.314.649 von kmastra am 13.10.10 17:20:03wirst sehen wir schliessen heute wieder bei 1,62$,so eine meldung wird bei ligand schnell wieder abverkauft,dafür sorgen schon die richtigen leute.
 aber ist halt so
aber ist halt so
asics
 aber ist halt so
aber ist halt soasics
Antwort auf Beitrag Nr.: 40.316.181 von asics01 am 13.10.10 20:22:43Moin asics, deinen Pessimismus kann ich verstehen. Aber es hat gestern doch noch zu einem plus gereicht. Charttechnisch wie gesagt zur Zeit recht interessant. Ebenso, dass das Volumen gestern und heute merklich steigt. Ein Anstieg über 1,70 mit hohem volumen wäre doch mal was...
SG kmastra
SG kmastra
Antwort auf Beitrag Nr.: 40.322.826 von kmastra am 14.10.10 17:21:13ich traue dem braten noch nicht,aber da es heute keine technische gegenreakttion gab kann es durchaus sein dass es über 1,70 richtung 2,00$ geht.
vielleicht gibt es noch gute quartalszahlen,dann könnte was gehen.
asics
vielleicht gibt es noch gute quartalszahlen,dann könnte was gehen.
asics
Antwort auf Beitrag Nr.: 40.322.826 von kmastra am 14.10.10 17:21:13was muss passieren dass die mal über 1,70$ geht????ich vermute mal die taucht wieder ab auf 1,50$
Antwort auf Beitrag Nr.: 40.334.698 von asics01 am 16.10.10 11:52:18Bin auf jeden fall gespannt auf Montag. Mal sehen vielleicht wird es ja doch mal was mit den 1,70...
Antwort auf Beitrag Nr.: 40.337.683 von kmastra am 17.10.10 16:11:081,70$ packt die wohl so schnell nicht
Antwort auf Beitrag Nr.: 40.343.082 von asics01 am 18.10.10 17:44:53Sieht doch ganz gut aus! War heute der 4. Tag in Folge, an dem das Volumen ungefähr doppelt so hoch war wie im Schnitt. Morgen und die nächsten Tage wird definitiv spannend. Bin persönlich kurzfristig extrem bullish langfristig sowieso...
Antwort auf Beitrag Nr.: 40.345.381 von kmastra am 18.10.10 22:45:15sei froh wenn keine news kommen,die guten werden sowieso abverkauft. aber was passiert wenn die news mal schlecht sind ??,dann stehen wir bei 1,45$ wetten ????
asics
asics
hallo kmastra
ich habe heute den grössten teil meiner anteile die ich bei 1,42$ gekauft habe heute bei 1,69$ geschmissen.
ich trau dem braten nicht mehr,einfach nervig
asics
ich habe heute den grössten teil meiner anteile die ich bei 1,42$ gekauft habe heute bei 1,69$ geschmissen.
ich trau dem braten nicht mehr,einfach nervig
asics
Antwort auf Beitrag Nr.: 40.368.744 von asics01 am 21.10.10 19:29:58Klar. Is schon nervig. Andere Biotechs gehen hoch und Ligand kommt nicht vom Fleck...denke auch über einen Teilverkauf nach.
Heute hat GsK gemeldet, dass Promacta im Q3 nur 7 Mio gebracht hat. Von daher zumindest nicht die guten News, die endlich mal über 1,70 helfen...
SG Jan
Heute hat GsK gemeldet, dass Promacta im Q3 nur 7 Mio gebracht hat. Von daher zumindest nicht die guten News, die endlich mal über 1,70 helfen...
SG Jan
Antwort auf Beitrag Nr.: 40.369.094 von kmastra am 21.10.10 20:10:10Promacta/Revolade in Japan zugelassen worden (Samstag)!
Mal sehen, obs dem Kurs über die 1,70 hilft. In D tut sich noch nichts (Ligand hat auch noch keine Pressemeldung rausgehauen).Gelegenheit?
Mal sehen, obs dem Kurs über die 1,70 hilft. In D tut sich noch nichts (Ligand hat auch noch keine Pressemeldung rausgehauen).Gelegenheit?
Antwort auf Beitrag Nr.: 40.425.707 von bartflanders am 01.11.10 09:07:53ach ja:
http://www.gsk.com/media/pressreleases/2010/2010_pressreleas…" target="_blank" rel="nofollow ugc noopener">http://www.gsk.com/media/pressreleases/2010/2010_pressreleas…
http://www.gsk.com/media/pressreleases/2010/2010_pressreleas…" target="_blank" rel="nofollow ugc noopener">http://www.gsk.com/media/pressreleases/2010/2010_pressreleas…
Antwort auf Beitrag Nr.: 40.425.725 von bartflanders am 01.11.10 09:10:35Der link funktioniert irgendwie nicht. Sucht selbst auf der Glaxo-Homepage, schnell zu finden!
hallo kmastra
bist du noch an board ????bin heute wieder zu 1,55$ rein,mal sehen was geht
asics
bist du noch an board ????bin heute wieder zu 1,55$ rein,mal sehen was geht
asics
Antwort auf Beitrag Nr.: 40.539.874 von asics01 am 17.11.10 17:42:48Moin asics,
klar. Ich warte zumindest bis die Hep C Phantasie in den Kurs kommt.
Gestern war ja mördermäßiger Umsatz in den USA. Dann warst du das also;-)
SG kmastra
klar. Ich warte zumindest bis die Hep C Phantasie in den Kurs kommt.
Gestern war ja mördermäßiger Umsatz in den USA. Dann warst du das also;-)
SG kmastra
Antwort auf Beitrag Nr.: 40.549.250 von kmastra am 18.11.10 19:49:42Gestern war ja mördermäßiger Umsatz in den USA. Dann warst du das also;-)
 :laugh
:laugh hab nur 5000 st abgegriffen)
hab nur 5000 st abgegriffen)
ich bin immer noch der meinung dass sich nach dem re split was tut,und natürlich wie du schreibst die hep c daten,(da ist musik drin)
irgendwann muss die doch mal in die gänge kommen.
viel glück uns beiden,ich habe vorsichtshalber bei 1,50$ noch mal eine kauforder reigelegt falls da drüben jemand auf dumme gedanken kommen sollte.
asics

 :laugh
:laugh hab nur 5000 st abgegriffen)
hab nur 5000 st abgegriffen)ich bin immer noch der meinung dass sich nach dem re split was tut,und natürlich wie du schreibst die hep c daten,(da ist musik drin)
irgendwann muss die doch mal in die gänge kommen.
viel glück uns beiden,ich habe vorsichtshalber bei 1,50$ noch mal eine kauforder reigelegt falls da drüben jemand auf dumme gedanken kommen sollte.
asics
Ligand Reverse Stock Split Effective Today
SAN DIEGO--(BUSINESS WIRE)-- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced that its
previously disclosed 1-for-6 reverse stock split has become effective, and will be reflected in the share price beginning today.
The reverse stock split applies to all of Ligand's outstanding common stock, reducing current outstanding shares (excluding
treasury shares) from approximately 117.7 million to approximately 19.6 million. Shareholders will receive cash in lieu of
fractional shares. In connection with the reverse split, Ligand also proportionately reduced the number of its authorized shares
of common stock from 200.0 million to approximately 33.3 million shares.
Ligand's common stock will trade under the symbol "LGNDD" for a period of 20 trading days as a result of the reverse stock
split. Ligand's common stock will also trade under a new CUSIP number.
Ligand's shareholders of record will receive a letter of transmittal and instructions from Ligand's transfer agent, BNY Mellon
Shareowner Services, regarding the procedures for submitting their stock certificates in connection with the reverse stock split.
Shareholders are encouraged to surrender their stock certificates in connection with the reverse stock split. Those
shareholders holding Ligand common stock in "street name" will receive instructions from their broker if they need to take any
action in connection with the reverse stock split.
About Ligand Pharmaceuticals
Ligand discovers and develops novel drugs that address critical unmet medical needs of patients for a broad spectrum of
diseases including hepatitis, muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid
arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based
assays, tissue-specific receptor ligand interactions and gene-expression tools. Among our peers, we believe Ligand has
assembled one of the largest portfolios of assets including commercial therapies developed in partnership with pharmaceutical
companies. Ligand has established multiple alliances with the world's leading pharmaceutical companies including
GlaxoSmithKline, Merck, Pfizer, Roche, Bristol-Myers Squibb and AstraZeneca, and more than 30 programs in various stages
of development.
Caution Regarding Forward-Looking Statements
This news release contains forward looking statements by Ligand that involve risks and uncertainties, including with respect to
the reverse stock split, and reflect Ligand's judgment as of the date of this release. Actual events or results may differ from
Ligand's expectations. Additional information concerning these and other risk factors affecting Ligand's business can be found
in prior press releases available via www.ligand.com as well as in Ligand's public periodic filings with the Securities and
Exchange Commission at www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking statements
beyond the date of this release. This caution is made under the safe harbor provisions of the Private Securities Litigation
Reform Act of 1995.
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Lippert/Heilshorn & Associates
Don Markley
310-691-7100
dmarkley@lhai.com
Source: Ligand Pharmaceuticals Incorporated
News Provided by Acquire Media
SAN DIEGO--(BUSINESS WIRE)-- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced that its
previously disclosed 1-for-6 reverse stock split has become effective, and will be reflected in the share price beginning today.
The reverse stock split applies to all of Ligand's outstanding common stock, reducing current outstanding shares (excluding
treasury shares) from approximately 117.7 million to approximately 19.6 million. Shareholders will receive cash in lieu of
fractional shares. In connection with the reverse split, Ligand also proportionately reduced the number of its authorized shares
of common stock from 200.0 million to approximately 33.3 million shares.
Ligand's common stock will trade under the symbol "LGNDD" for a period of 20 trading days as a result of the reverse stock
split. Ligand's common stock will also trade under a new CUSIP number.
Ligand's shareholders of record will receive a letter of transmittal and instructions from Ligand's transfer agent, BNY Mellon
Shareowner Services, regarding the procedures for submitting their stock certificates in connection with the reverse stock split.
Shareholders are encouraged to surrender their stock certificates in connection with the reverse stock split. Those
shareholders holding Ligand common stock in "street name" will receive instructions from their broker if they need to take any
action in connection with the reverse stock split.
About Ligand Pharmaceuticals
Ligand discovers and develops novel drugs that address critical unmet medical needs of patients for a broad spectrum of
diseases including hepatitis, muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid
arthritis and osteoporosis. Ligand's proprietary drug discovery and development programs are based on advanced cell-based
assays, tissue-specific receptor ligand interactions and gene-expression tools. Among our peers, we believe Ligand has
assembled one of the largest portfolios of assets including commercial therapies developed in partnership with pharmaceutical
companies. Ligand has established multiple alliances with the world's leading pharmaceutical companies including
GlaxoSmithKline, Merck, Pfizer, Roche, Bristol-Myers Squibb and AstraZeneca, and more than 30 programs in various stages
of development.
Caution Regarding Forward-Looking Statements
This news release contains forward looking statements by Ligand that involve risks and uncertainties, including with respect to
the reverse stock split, and reflect Ligand's judgment as of the date of this release. Actual events or results may differ from
Ligand's expectations. Additional information concerning these and other risk factors affecting Ligand's business can be found
in prior press releases available via www.ligand.com as well as in Ligand's public periodic filings with the Securities and
Exchange Commission at www.sec.gov. Ligand disclaims any intent or obligation to update these forward-looking statements
beyond the date of this release. This caution is made under the safe harbor provisions of the Private Securities Litigation
Reform Act of 1995.
Ligand Pharmaceuticals Incorporated
John L. Higgins, President and CEO or
Erika Luib, Investor Relations
858-550-7896
or
Lippert/Heilshorn & Associates
Don Markley
310-691-7100
dmarkley@lhai.com
Source: Ligand Pharmaceuticals Incorporated
News Provided by Acquire Media
hallo kmastra
ist es richtig dass die hep daten januar 2011 vorliegen sollen????
danke
asics
ist es richtig dass die hep daten januar 2011 vorliegen sollen????
danke
asics
Antwort auf Beitrag Nr.: 40.561.179 von asics01 am 21.11.10 12:16:54hier gibts ja anscheinend nur eine richtung. ich verstehe nicht wieso. Pipeline ist gut gefüllt und mit namenswerten partner.
bin seit ein paar Tagen dabei; und schon gibts ärger....
bin seit ein paar Tagen dabei; und schon gibts ärger....
Antwort auf Beitrag Nr.: 40.570.361 von commodityleviathan am 22.11.10 22:41:26wo gibts ärger ??????
Antwort auf Beitrag Nr.: 40.570.976 von asics01 am 23.11.10 06:41:14Von Ärger ist mir auch nichts bekannt. Ärgerlich war allerdings der Abverkauf gestern: 8% Verlust ohne News und gegen den Trend. Das ist schon ärgerlich...
Zu deiner Frage:
Die Daten zu Promacta werden im 2 HJ 2011 erwartet. Zulassung in 2012.
SG kmastra
Zu deiner Frage:
Die Daten zu Promacta werden im 2 HJ 2011 erwartet. Zulassung in 2012.
SG kmastra
Antwort auf Beitrag Nr.: 40.578.218 von kmastra am 23.11.10 22:26:50ich dachte nach dem splitt gehts ein wenig gediegener zu,aber es geht gerade so weiter
drücken was das zeug hält.
ich ärgere mich schon wieder reingegengen zu sein,und nun hänge ich fest und kann nicht reagieren.
irgendwas ist da doch oberfaul,wo liegen die leichen begraben????
ich meine mal wo gelesen zuhaben,dass die daten im 1 quartal 2011 kommen.kann mich auch täuschen.na dann haben sie ja jetzt alle zeit der welt den kurs zu drücken,weil vorher wahrscheinlich nicht mehr viel an bewegenden news kommen wird.
asics
drücken was das zeug hält.
ich ärgere mich schon wieder reingegengen zu sein,und nun hänge ich fest und kann nicht reagieren.
irgendwas ist da doch oberfaul,wo liegen die leichen begraben????
ich meine mal wo gelesen zuhaben,dass die daten im 1 quartal 2011 kommen.kann mich auch täuschen.na dann haben sie ja jetzt alle zeit der welt den kurs zu drücken,weil vorher wahrscheinlich nicht mehr viel an bewegenden news kommen wird.
asics
Antwort auf Beitrag Nr.: 40.579.203 von asics01 am 24.11.10 08:40:53Das einzige worauf du kurzfristig setzen kannst ist, dass Ligand im nächsten Quartal wohl profitabel sein wird. Ansonsten kann natürlch jederzeit auch noch ein Deal mit den bisher unverpartnerten Medikamenten erfolgen...
Antwort auf Beitrag Nr.: 40.589.171 von kmastra am 25.11.10 12:04:22ligand wird ein spielball der spekulanten bleiben,die sind irgendwie zu brav, da fehlt das feuer.
asics
asics
Antwort auf Beitrag Nr.: 40.578.218 von kmastra am 23.11.10 22:26:50Gab schon News:
Roche-Partnerschaft wurde gecancelt (dieser Phase1 HepC-Wirkstoff ist auch schon aus der Pipeline genommen). Nicht toll, allerdings war der Hauptteil der Erlöse ohnehin bei den Metabasis-Alteignern gelegen.
Roche-Partnerschaft wurde gecancelt (dieser Phase1 HepC-Wirkstoff ist auch schon aus der Pipeline genommen). Nicht toll, allerdings war der Hauptteil der Erlöse ohnehin bei den Metabasis-Alteignern gelegen.
Antwort auf Beitrag Nr.: 40.601.567 von bartflanders am 27.11.10 08:41:42was da gerade alles passiert und schief läuft ist nicht im sinne des aktionärs.wird wohl weiter runtergehen in den bereich 7,50-8,00$
Antwort auf Beitrag Nr.: 40.602.322 von asics01 am 27.11.10 14:09:05Es gab einige positive Nachrichten wie die Zulassungen in Japan, die aber durch doch starke deckelnde Verkäufe den Kurs allenfalls stagnieren ließen. Dann gab es den reverse split, dessen Auswirkung zunächst auf jeden Fall Verunsicherung ist: Bei Unternehmen mit Verlusten gings meist schief, ist das nun bei einer Firma mit wohl operativ positivem Geschäft wirklich anders?
Dann diese Sache mir Roche, die man allerdings in der klinischen Entwicklung immer einkalkulieren muss. Wird durch die Breite der sonstigen Pipeline relativiert.
Hauptargumente pro Ligand für mich sind sowieso eher Promacta für die kommenden Indikationen (ist schon klasse, was der Vermarktungspartner hier in die Forschung investiert, ist ein Indiz für das Potenzial. Siehe clinicaltrials.gov.
Vor allem dann aber die Nachfolgesubstanz In P2, die deutlich wirksamer scheint und höhere Royalties mit sich bringt.
Auch der Wirkstoff gegen COPD in Phase 2b ist für mich interessant, in einem der letzten CCs wurde gesagt, eine mid-single-digit royalty wäre fällig und das Potenzial läge im Multimilliardenbereich.
Dann noch P38 mit den verschiedenen breiten Indikationen, die da getestet werden, das wäre schon echt was, wenn hier positiv weiterentwickelt wird. Royalties sind mir hier nicht bekannt.
Zum Abschluss SARM und die Möglichkeit, lukrativ zu verpartnern.
Für mich neben der finanziell relativ gesicherten Zukunft und den Erfolgen aus der Vergangenheit (bereits 5 eigene Wirkstoffe auf den Markt gebracht) einige Argumente, an denen ich momentan nicht vorbeikomme.
Ich baue darauf, dass die 8,14 $ nicht mehr maßgeblich und wenn dann nur kurzfristig, um die letzten unsicheren Aktionäre rauszuschütteln, unterschritten werden; wobei Shorts das sicher im Sinn haben. Auf das Rückkaufprogramm Ligands als Stütze kann man nicht so stark bauen, denn übermäßig Cash haben die auch nicht.
Dann diese Sache mir Roche, die man allerdings in der klinischen Entwicklung immer einkalkulieren muss. Wird durch die Breite der sonstigen Pipeline relativiert.
Hauptargumente pro Ligand für mich sind sowieso eher Promacta für die kommenden Indikationen (ist schon klasse, was der Vermarktungspartner hier in die Forschung investiert, ist ein Indiz für das Potenzial. Siehe clinicaltrials.gov.
Vor allem dann aber die Nachfolgesubstanz In P2, die deutlich wirksamer scheint und höhere Royalties mit sich bringt.
Auch der Wirkstoff gegen COPD in Phase 2b ist für mich interessant, in einem der letzten CCs wurde gesagt, eine mid-single-digit royalty wäre fällig und das Potenzial läge im Multimilliardenbereich.
Dann noch P38 mit den verschiedenen breiten Indikationen, die da getestet werden, das wäre schon echt was, wenn hier positiv weiterentwickelt wird. Royalties sind mir hier nicht bekannt.
Zum Abschluss SARM und die Möglichkeit, lukrativ zu verpartnern.
Für mich neben der finanziell relativ gesicherten Zukunft und den Erfolgen aus der Vergangenheit (bereits 5 eigene Wirkstoffe auf den Markt gebracht) einige Argumente, an denen ich momentan nicht vorbeikomme.
Ich baue darauf, dass die 8,14 $ nicht mehr maßgeblich und wenn dann nur kurzfristig, um die letzten unsicheren Aktionäre rauszuschütteln, unterschritten werden; wobei Shorts das sicher im Sinn haben. Auf das Rückkaufprogramm Ligands als Stütze kann man nicht so stark bauen, denn übermäßig Cash haben die auch nicht.
Antwort auf Beitrag Nr.: 40.603.780 von bartflanders am 28.11.10 08:27:11passt alles was du von dir gibst,nur der markt sieht die sache anders,trotz 5 zugelassenene wirkstoffen ist der kurs am boden (schau dir mal den chart an,da kriegste normal das grosse grausen)
und eine mk von 165.079.890$ spricht wohl auch für sich.
meine vermutung ist dass demnächst der gesamtmarkt in die knie geht und ligand mitgezogen wird.deswegen habe ich ein sl ganz in der nähe des aktuellen kurses gesetzt.
asics
und eine mk von 165.079.890$ spricht wohl auch für sich.
meine vermutung ist dass demnächst der gesamtmarkt in die knie geht und ligand mitgezogen wird.deswegen habe ich ein sl ganz in der nähe des aktuellen kurses gesetzt.
asics
Antwort auf Beitrag Nr.: 40.603.780 von bartflanders am 28.11.10 08:27:11Sehe bei Ligand insgesamt mehr Chancen als Risiken. Promacta ist sicher erstmal die Fantasie. Was mich aber am ehesten beruhigt ist, dass es viele "Shots on goal" gibt. Wenn ich da an andere Biotechs denke...
Was mich aber ebenso beunruhigt ist die Kursentwicklung. Kann mir das eigentlich kaum erklären. Erkläre mir das momentan am ehesten durch die fehlende Transparenz und Unsicherheit. Zwar weiß man dass es ca. 30 auslizensierte Projekte gibt. Aber was bleibt letzlich bei den einzelnen Projekten konkret bei Ligand hängen? Da sind die Aussagen auf der Homepage eher dürftig und zeigen auch ein Problem. Das schwankt zwichen 0,5 und 14,5 %
Warum steht das nicht zu allen Projekten da? Oder weiß man das im einzelnen noch gar nicht? Ich würde denken, dass das doch bekannt sein müsste und demensprechend auch kommuniziert werden sollte.
Eine weitere Unsicherheit liegt sicherlich in Promacta. Die Gefahr ist natürlich das Scheitern der Hep C Studien. Das könnte zum Beispiel durch die erhöhte Gefahr einer Trombose bei Promactagabe geschehen. Das ist sicherlich nicht von der Hand zu weisen. Zumindest ist Promacta kein Selbstgänger...und hat ja auch schon eine wechselhafte Vergangenheit.
Bin auf alle Fäle gespannt. Langweilig wirds im nächsten Jahr eher nicht;-)
Was mich aber ebenso beunruhigt ist die Kursentwicklung. Kann mir das eigentlich kaum erklären. Erkläre mir das momentan am ehesten durch die fehlende Transparenz und Unsicherheit. Zwar weiß man dass es ca. 30 auslizensierte Projekte gibt. Aber was bleibt letzlich bei den einzelnen Projekten konkret bei Ligand hängen? Da sind die Aussagen auf der Homepage eher dürftig und zeigen auch ein Problem. Das schwankt zwichen 0,5 und 14,5 %
Warum steht das nicht zu allen Projekten da? Oder weiß man das im einzelnen noch gar nicht? Ich würde denken, dass das doch bekannt sein müsste und demensprechend auch kommuniziert werden sollte.
Eine weitere Unsicherheit liegt sicherlich in Promacta. Die Gefahr ist natürlich das Scheitern der Hep C Studien. Das könnte zum Beispiel durch die erhöhte Gefahr einer Trombose bei Promactagabe geschehen. Das ist sicherlich nicht von der Hand zu weisen. Zumindest ist Promacta kein Selbstgänger...und hat ja auch schon eine wechselhafte Vergangenheit.
Bin auf alle Fäle gespannt. Langweilig wirds im nächsten Jahr eher nicht;-)
Antwort auf Beitrag Nr.: 40.605.855 von kmastra am 29.11.10 00:52:33Die Royalties sind in den Fällen, in denen nichts von Ligand veröffentlicht wurde, sicher bekannt. Nur wird da oft Vertraulichkeit zugesichert bzw. von den Lizenznehmern ausbedungen. Trotzdem wird teils eine Größenordnung genannt wie neulich für den COPD-Wirkstoff diese "mid-single-digits".
Letzlich ist das wie du (kmastra) schon sagtest ja bei allem Marktpotenzial die entscheidende Frage: Was bleibt unterm Strich bei Ligand hängen?
Bei Promacta und GSK 2285921 weiß mans zum Glück und bei SCH 527123 (Merck COPD) haben wir einen Anhaltspunkt. Bei Dinaciclib und P38 wüsste ich es gerne, vielleicht wird bei nem Conference Call mal was gesagt...
Die Kursentwicklung ist sicher miserabel. Der Reversesplit und der große Verkäufer der letzten Wochen hingen/hängen noch wie ein großer Schatten über der Aktie. Und vielleicht wird die Fülle der Pipeline misstrauisch beäugt: Man weiß noch nicht, ob sich wirkliche Werte in diesem teils zusammengekauften "Gemischtwarenladen" verbergen.
Wirklich helfen werden gute Daten und Profite. Vor allem die Hepatitis-Daten werden es zeigen, ob die Richtung stimmt.
Grüße,
bartflanders
Letzlich ist das wie du (kmastra) schon sagtest ja bei allem Marktpotenzial die entscheidende Frage: Was bleibt unterm Strich bei Ligand hängen?
Bei Promacta und GSK 2285921 weiß mans zum Glück und bei SCH 527123 (Merck COPD) haben wir einen Anhaltspunkt. Bei Dinaciclib und P38 wüsste ich es gerne, vielleicht wird bei nem Conference Call mal was gesagt...
Die Kursentwicklung ist sicher miserabel. Der Reversesplit und der große Verkäufer der letzten Wochen hingen/hängen noch wie ein großer Schatten über der Aktie. Und vielleicht wird die Fülle der Pipeline misstrauisch beäugt: Man weiß noch nicht, ob sich wirkliche Werte in diesem teils zusammengekauften "Gemischtwarenladen" verbergen.
Wirklich helfen werden gute Daten und Profite. Vor allem die Hepatitis-Daten werden es zeigen, ob die Richtung stimmt.
Grüße,
bartflanders
Weiß nicht ob ich das gut finden soll?
SAN DIEGO (AP) -- Ligand Pharmaceuticals Inc. said Thursday it licensed two liver disease drugs to drugmaker Chiva Pharmaceuticals Inc. as part of a deal that could be worth more than $100 million.
The deal gives Chiva the rights to develop and market the drugs in China. The partnership includes Pradefovir, a potential treatment for hepatitis B, and MB01733, which is being tested as a treatment for hepatocellular carcinoma, the most common type of liver cancer. Ligand said Chiva is also getting a non-exclusive license for newer drugs that could be used to treat hepatitis B and C and hepatocellular carcinoma.
Chiva is headquartered in Los Altos Hills, Calif., but Ligand said it is an affiliate of Hainan Kaihua Pharmaceutical Co., a drugmaker that focuses on the Chinese market.
The San Diego drugmaker said it could get more than $100 million in milestone payments and royalties on sales if the products are approved. It could receive up to $1 million in license payments in 2011. Ligand said it could also get a 10 percent equity stake in Chiva. If Chiva licenses the drugs to another company, Ligand will get a portion of that revenue.
Ligand acquired the drugs in January 2010 when it bought Metabasis Therapeutics Inc.
Shares of Ligand Pharmaceuticals slid 9 cents to $9.19 in morning trading.
http://finance.yahoo.com/news/Ligand-could-get-100M-in-apf-2101443884.html?x=0&.v=
SAN DIEGO (AP) -- Ligand Pharmaceuticals Inc. said Thursday it licensed two liver disease drugs to drugmaker Chiva Pharmaceuticals Inc. as part of a deal that could be worth more than $100 million.
The deal gives Chiva the rights to develop and market the drugs in China. The partnership includes Pradefovir, a potential treatment for hepatitis B, and MB01733, which is being tested as a treatment for hepatocellular carcinoma, the most common type of liver cancer. Ligand said Chiva is also getting a non-exclusive license for newer drugs that could be used to treat hepatitis B and C and hepatocellular carcinoma.
Chiva is headquartered in Los Altos Hills, Calif., but Ligand said it is an affiliate of Hainan Kaihua Pharmaceutical Co., a drugmaker that focuses on the Chinese market.
The San Diego drugmaker said it could get more than $100 million in milestone payments and royalties on sales if the products are approved. It could receive up to $1 million in license payments in 2011. Ligand said it could also get a 10 percent equity stake in Chiva. If Chiva licenses the drugs to another company, Ligand will get a portion of that revenue.
Ligand acquired the drugs in January 2010 when it bought Metabasis Therapeutics Inc.
Shares of Ligand Pharmaceuticals slid 9 cents to $9.19 in morning trading.
http://finance.yahoo.com/news/Ligand-could-get-100M-in-apf-2101443884.html?x=0&.v=
hallo kmastra
was sagst du zu dem cydex deal???die kaufen ein wie die grossen??
der chiva deal ist nicht gut....
Ligand Acquires CyDex Pharmaceuticals
Ligand Gains New Revenue Streams, Fully Funded Partnerships and Expanding Cash-Flow Positive Drug
Reformulation Business
Conference Call Scheduled for 5:00 p.m. Eastern Time Today
SAN DIEGO--(BUSINESS WIRE)-- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced it has acquired
privately held CyDex Pharmaceuticals, Inc. for a combination of cash and contingent payments. CyDex, based in Lenexa,
Kansas, had 2010 revenue of $16.3 million and EBITDA of $7.6 million, and will operate as a wholly-owned subsidiary of
Ligand.
CyDex shareholders will receive $31.2 million for the merger in upfront cash, a $4.3 million cash payment on the one year
anniversary of closing, and will be entitled to contingent cash payments related to certain transactions and pursuant to a
revenue share plan. In addition, Ligand paid approximately $800,000 at close for an adjustment for working capital.
"This transformational acquisition accelerates Ligand's financial growth and provides a unique and broad basket of new assets
to further expand our business and long-term potential," said John Higgins, President and Chief Executive Officer of Ligand.
"Ligand will now combine the royalties from seven marketed drugs, along with the substantial revenue from the selling of
Captisol®, to advance Ligand toward its goal of turning cash-flow positive with substantial future growth opportunities. This
growth will be largely fueled by what Ligand believes is an industry unprecedented portfolio of more than 50 fully-funded
partnered development programs, creating a myriad of new revenue stream possibilities."
"CyDex has created a very successful business around the Captisol drug reformulation technology over the last several years
and the company has significant growth potential," said Ted Odlaug, former President and Chief Executive Officer of CyDex
Pharmaceuticals. "We are very impressed with Ligand's business model, success in deal making and commitment to continue
driving the CyDex business to even greater success. We believe Ligand's broad licensing network and business acumen,
coupled with the opportunity to share in future upside in the business, created an attractive exit for CyDex shareholders."
Acquisition Rationale
The acquisition of CyDex' cash-flow positive business will accelerate Ligand's projected financial growth.
l Ligand's projected 2011 revenue is expected to more than double versus Ligand's stand-alone revenue as a result of
the transaction, not including any new licensing revenue (i.e. SARM) or accelerated growth in Promacta® royalties.
Ligand's asset portfolio (including development stage programs and marketed drugs) will greatly expand to more than 60
programs, significantly increasing the opportunity for new revenue streams over the next few years.
l The existing CyDex portfolio includes numerous high-quality license and royalty bearing agreements, including Onyx
Pharmaceuticals for carfilzomib and Prism for Nexterone®.
l Post-merger corporate portfolio is comprised of 7 marketed drugs and more than 50 fully funded partnered
collaborations.
CyDex diversifies Ligand's business by adding a proprietary and well-validated platform in the increasingly important drug
reformulation segment of the pharmaceutical industry.
l Ligand believes that drug reformulation has become an increasingly valuable solution to the issues related to market
erosion due to generic competition and continued clinical and regulatory uncertainty.
CyDex Brings the Following to Ligand:
Significant Annual Revenue —CyDex currently generates annual revenue from four marketed drugs, material sales from
the selling of Captisol, and license and milestone payments.
Onyx Collaboration—CyDex and Onyx Pharmaceuticals entered into a collaboration in 2005 (originally with Proteolix) to
develop the Captisol-enabled IV formulation of carfilzomib for refractory multiple myeloma. Onyx has recently reported positive
Phase II data for this program and plans to file an NDA in 2011 with the FDA. CyDex is eligible to receive milestones, royalties
and Captisol material sales revenue from this program.
Prism Collaboration—Prism Pharmaceuticals recently received marketing approval from the FDA for the Captisol-enabled IV
form of amiodarone, to be marketed as Nexterone. Prism plans to launch Nexterone in the near term. Nexterone was developed
by CyDex and licensed to Prism in 2007. CyDex is eligible to receive milestones, royalties, and Captisol material sales revenue
from this program.
Large Pharma Captisol-Supply Relationships —CyDex currently has multiple material sales collaborations with undisclosed
large pharmaceutical companies. These collaborations have Captisol-enabled drugs in clinical development and CyDex
anticipates selling Captisol to these partners in the coming years for clinical and commercial use.
Industry Recognized Captisol Technology Brand —Captisol is recognized in the pharmaceutical industry as a powerful
answer to the solubility challenges frequently faced by drug-development companies. CyDex' success is primarily based on
solving drug formulation problems, particularly in the area of IV and topical formulations. CyDex has also developed an
extensive Drug Master File (DMF) to which its partners can refer when filing with regulatory agencies around the world, adding
significant value to the Captisol brand.
Internal Pipeline of Captisol-Enabled Drugs —CyDex is currently developing four proprietary Captisol-enabled drugs for
future potential licensing:
l Clopidogrel IV in Phase I for thrombosis
l Melphalan IV in Phase II for stem cell conditioning
l Budesonide/Azelastine nasal in Phase II for seasonal rhinitis
l Topiramate IV in Phase I development for epilepsy
Acquisition Funding
The upfront acquisition payment to CyDex shareholders is comprised of $11.2 million of Ligand's internal cash and $20 million
borrowed on a 42-month secured term loan from Oxford Finance Corporation. Oxford is a specialty lender that has originated
loans ranging from $500,000 to $40 million to more than 200 companies. Ligand is also exploring additional financing options
for up to a further $10 million in borrowing, for a potential total borrowing of $30 million.
2011 Financial Outlook
For 2011, Ligand expects total revenues to be $22 million to $24 million. The guidance assumes approximately $13 million to
$14 million of revenue (partial year accounting) from the CyDex business, and approximately $9 million to $10 million of
revenue from the original Ligand business, before any revenue for new licensing agreements.
Ligand's 2011 operating expenses are expected to be $16 million to $18 million, with an average cost of goods as a
percentage of material sales to be approximately 35%. CyDex non-cash amortization expense estimates are expected to be
determined in the near-term. If Ligand borrows an additional $10 million during 2011, it anticipates ending 2011 with
approximately $20 million of cash. By the end of 2011, Ligand expects its operations to be profitable and cash-flow positive.
Conference Call
Ligand will host a conference call with accompanying slides to discuss the acquisition on Wednesday, January 26, 2011
beginning at 5:00 p.m. Eastern time (2:00 p.m. Pacific time). To participate via telephone please dial (877) 407-4019 from the
U.S. or (201) 689-8337 from outside the U.S., passcode is "Ligand." A replay of the call will be available until February 25,
2011 at 5:00 p.m. Eastern time by dialing (877) 660-6853 from the U.S. or (201) 612-7415 from outside the U.S., and entering
conference ID # 366148, Account # 361. The live and archived Webcast can be accessed through Ligand's Web site at
www.ligand.com.
Slides accompanying management's presentation will be available in the "Investor Relations" section of www.ligand.com.
About CyDex Pharmaceuticals, Inc.
CyDex Pharmaceuticals, Inc. is a specialty pharmaceutical company developing products and licensing its Captisol technology.
Captisol is currently incorporated in five FDA-approved medications and marketed by three of the company's licensees: Pfizer,
Bristol-Myers Squibb and Prism Pharmaceuticals. In addition, the company is supporting drug development efforts with more
than 40 other companies worldwide, including Onyx for carfilzomib. The company maintains patents in the U.S. and worldwide
for its Captisol technology, Captisol manufacturing and Captisol-enabled products, and comprehensive FDA Manufacturing and
Safety Drug Master Files. To learn more about the company, please visit www.cydexpharma.com.
About Ligand Pharmaceuticals
Ligand is a BioPharma company with a business model that is based upon the concept of developing or acquiring royalty
revenue generating assets and coupling them to an efficiently lean corporate cost structure. Ligand's goal is to produce a
bottom line that supports a sustainably profitable business. By diversifying the portfolio of assets across numerous technology
types, therapeutic areas, drug targets, and industry partners, we offer investors a de-risked opportunity to invest in the
increasingly complicated and unpredictable pharmaceutical industry. We believe Ligand has assembled one of the largest and
most diversified portfolio of current assets in the industry (now over 60 programs) with the potential to generate revenue in the
future. These therapies address the unmet medical needs of patients for a broad spectrum of diseases including hepatitis,
muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid arthritis and osteoporosis.
Ligand has established multiple alliances with the world's leading pharmaceutical companies including GlaxoSmithKline, Merck,
Pfizer, Bristol-Myers Squibb and AstraZeneca. For more information, please visit www.ligand.com.
Forward-Looking Statements
This release contains forward-looking statements that involve risks and uncertainties. Ligand cautions readers that any
forward-looking information is not a guarantee of future performance and actual results could differ materially from those
contained in the forward-looking information. Words such as "expect," "estimate," "project," "potential," and similar expressions
are intended to identify such forward-looking statements. Such forward-looking statements include, but are not limited to,
statements about the benefits of the transaction between Ligand and CyDex, including future financial and operating results
and revenue potential, the expected effect of the merger on Ligand's operating cash burn rate, the possibility of
future/contingent acquisition payments being made, the combined entity's plans, objectives, expectations and intentions and
other statements that are not historical facts. Among the important factors that could cause actual results to differ materially
from those in any forward-looking statements are the risks that payment events which would produce proceeds for the
contingent value rights may not occur soon, or ever; the anticipated synergies and benefits from the transaction may not be
fully realized or may take longer to realize than expected; CyDex' product candidates may have unexpected adverse side
effects or inadequate therapeutic efficacy; and positive results in clinical trials may not be sufficient to obtain FDA approval.
There can be no assurance that any product in Ligand's, CyDex' or the projected combined company's product pipeline will be
successfully developed or manufactured, that final results of clinical studies will be supportive of regulatory approvals required
to market licensed products, or that any of the forward-looking information provided herein will be proven accurate. Additional
important factors that may affect future results are detailed in Ligand's filings with the SEC, including the company's recent
filings on Forms 10-K and 10-Q, or in information disclosed in public conference calls, the date and time of which are released
beforehand. Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this
release.
Ligand Pharmaceuticals Incorporated
Rob McKay, Sr. Director Investor Relations
858-550-7760
rmckay@ligand.com
or
Lippert/Heilshorn & Associates
Don Markley
310-691-7100
dmarkley@lhai.com
Source: Ligand Pharmaceuticals Incorporated
News Provided by Acquire Media
was sagst du zu dem cydex deal???die kaufen ein wie die grossen??
der chiva deal ist nicht gut....
Ligand Acquires CyDex Pharmaceuticals
Ligand Gains New Revenue Streams, Fully Funded Partnerships and Expanding Cash-Flow Positive Drug
Reformulation Business
Conference Call Scheduled for 5:00 p.m. Eastern Time Today
SAN DIEGO--(BUSINESS WIRE)-- Ligand Pharmaceuticals Incorporated (NASDAQ: LGND) today announced it has acquired
privately held CyDex Pharmaceuticals, Inc. for a combination of cash and contingent payments. CyDex, based in Lenexa,
Kansas, had 2010 revenue of $16.3 million and EBITDA of $7.6 million, and will operate as a wholly-owned subsidiary of
Ligand.
CyDex shareholders will receive $31.2 million for the merger in upfront cash, a $4.3 million cash payment on the one year
anniversary of closing, and will be entitled to contingent cash payments related to certain transactions and pursuant to a
revenue share plan. In addition, Ligand paid approximately $800,000 at close for an adjustment for working capital.
"This transformational acquisition accelerates Ligand's financial growth and provides a unique and broad basket of new assets
to further expand our business and long-term potential," said John Higgins, President and Chief Executive Officer of Ligand.
"Ligand will now combine the royalties from seven marketed drugs, along with the substantial revenue from the selling of
Captisol®, to advance Ligand toward its goal of turning cash-flow positive with substantial future growth opportunities. This
growth will be largely fueled by what Ligand believes is an industry unprecedented portfolio of more than 50 fully-funded
partnered development programs, creating a myriad of new revenue stream possibilities."
"CyDex has created a very successful business around the Captisol drug reformulation technology over the last several years
and the company has significant growth potential," said Ted Odlaug, former President and Chief Executive Officer of CyDex
Pharmaceuticals. "We are very impressed with Ligand's business model, success in deal making and commitment to continue
driving the CyDex business to even greater success. We believe Ligand's broad licensing network and business acumen,
coupled with the opportunity to share in future upside in the business, created an attractive exit for CyDex shareholders."
Acquisition Rationale
The acquisition of CyDex' cash-flow positive business will accelerate Ligand's projected financial growth.
l Ligand's projected 2011 revenue is expected to more than double versus Ligand's stand-alone revenue as a result of
the transaction, not including any new licensing revenue (i.e. SARM) or accelerated growth in Promacta® royalties.
Ligand's asset portfolio (including development stage programs and marketed drugs) will greatly expand to more than 60
programs, significantly increasing the opportunity for new revenue streams over the next few years.
l The existing CyDex portfolio includes numerous high-quality license and royalty bearing agreements, including Onyx
Pharmaceuticals for carfilzomib and Prism for Nexterone®.
l Post-merger corporate portfolio is comprised of 7 marketed drugs and more than 50 fully funded partnered
collaborations.
CyDex diversifies Ligand's business by adding a proprietary and well-validated platform in the increasingly important drug
reformulation segment of the pharmaceutical industry.
l Ligand believes that drug reformulation has become an increasingly valuable solution to the issues related to market
erosion due to generic competition and continued clinical and regulatory uncertainty.
CyDex Brings the Following to Ligand:
Significant Annual Revenue —CyDex currently generates annual revenue from four marketed drugs, material sales from
the selling of Captisol, and license and milestone payments.
Onyx Collaboration—CyDex and Onyx Pharmaceuticals entered into a collaboration in 2005 (originally with Proteolix) to
develop the Captisol-enabled IV formulation of carfilzomib for refractory multiple myeloma. Onyx has recently reported positive
Phase II data for this program and plans to file an NDA in 2011 with the FDA. CyDex is eligible to receive milestones, royalties
and Captisol material sales revenue from this program.
Prism Collaboration—Prism Pharmaceuticals recently received marketing approval from the FDA for the Captisol-enabled IV
form of amiodarone, to be marketed as Nexterone. Prism plans to launch Nexterone in the near term. Nexterone was developed
by CyDex and licensed to Prism in 2007. CyDex is eligible to receive milestones, royalties, and Captisol material sales revenue
from this program.
Large Pharma Captisol-Supply Relationships —CyDex currently has multiple material sales collaborations with undisclosed
large pharmaceutical companies. These collaborations have Captisol-enabled drugs in clinical development and CyDex
anticipates selling Captisol to these partners in the coming years for clinical and commercial use.
Industry Recognized Captisol Technology Brand —Captisol is recognized in the pharmaceutical industry as a powerful
answer to the solubility challenges frequently faced by drug-development companies. CyDex' success is primarily based on
solving drug formulation problems, particularly in the area of IV and topical formulations. CyDex has also developed an
extensive Drug Master File (DMF) to which its partners can refer when filing with regulatory agencies around the world, adding
significant value to the Captisol brand.
Internal Pipeline of Captisol-Enabled Drugs —CyDex is currently developing four proprietary Captisol-enabled drugs for
future potential licensing:
l Clopidogrel IV in Phase I for thrombosis
l Melphalan IV in Phase II for stem cell conditioning
l Budesonide/Azelastine nasal in Phase II for seasonal rhinitis
l Topiramate IV in Phase I development for epilepsy
Acquisition Funding
The upfront acquisition payment to CyDex shareholders is comprised of $11.2 million of Ligand's internal cash and $20 million
borrowed on a 42-month secured term loan from Oxford Finance Corporation. Oxford is a specialty lender that has originated
loans ranging from $500,000 to $40 million to more than 200 companies. Ligand is also exploring additional financing options
for up to a further $10 million in borrowing, for a potential total borrowing of $30 million.
2011 Financial Outlook
For 2011, Ligand expects total revenues to be $22 million to $24 million. The guidance assumes approximately $13 million to
$14 million of revenue (partial year accounting) from the CyDex business, and approximately $9 million to $10 million of
revenue from the original Ligand business, before any revenue for new licensing agreements.
Ligand's 2011 operating expenses are expected to be $16 million to $18 million, with an average cost of goods as a
percentage of material sales to be approximately 35%. CyDex non-cash amortization expense estimates are expected to be
determined in the near-term. If Ligand borrows an additional $10 million during 2011, it anticipates ending 2011 with
approximately $20 million of cash. By the end of 2011, Ligand expects its operations to be profitable and cash-flow positive.
Conference Call
Ligand will host a conference call with accompanying slides to discuss the acquisition on Wednesday, January 26, 2011
beginning at 5:00 p.m. Eastern time (2:00 p.m. Pacific time). To participate via telephone please dial (877) 407-4019 from the
U.S. or (201) 689-8337 from outside the U.S., passcode is "Ligand." A replay of the call will be available until February 25,
2011 at 5:00 p.m. Eastern time by dialing (877) 660-6853 from the U.S. or (201) 612-7415 from outside the U.S., and entering
conference ID # 366148, Account # 361. The live and archived Webcast can be accessed through Ligand's Web site at
www.ligand.com.
Slides accompanying management's presentation will be available in the "Investor Relations" section of www.ligand.com.
About CyDex Pharmaceuticals, Inc.
CyDex Pharmaceuticals, Inc. is a specialty pharmaceutical company developing products and licensing its Captisol technology.
Captisol is currently incorporated in five FDA-approved medications and marketed by three of the company's licensees: Pfizer,
Bristol-Myers Squibb and Prism Pharmaceuticals. In addition, the company is supporting drug development efforts with more
than 40 other companies worldwide, including Onyx for carfilzomib. The company maintains patents in the U.S. and worldwide
for its Captisol technology, Captisol manufacturing and Captisol-enabled products, and comprehensive FDA Manufacturing and
Safety Drug Master Files. To learn more about the company, please visit www.cydexpharma.com.
About Ligand Pharmaceuticals
Ligand is a BioPharma company with a business model that is based upon the concept of developing or acquiring royalty
revenue generating assets and coupling them to an efficiently lean corporate cost structure. Ligand's goal is to produce a
bottom line that supports a sustainably profitable business. By diversifying the portfolio of assets across numerous technology
types, therapeutic areas, drug targets, and industry partners, we offer investors a de-risked opportunity to invest in the
increasingly complicated and unpredictable pharmaceutical industry. We believe Ligand has assembled one of the largest and
most diversified portfolio of current assets in the industry (now over 60 programs) with the potential to generate revenue in the
future. These therapies address the unmet medical needs of patients for a broad spectrum of diseases including hepatitis,
muscle wasting, Alzheimer's disease, dyslipidemia, diabetes, anemia, COPD, asthma, rheumatoid arthritis and osteoporosis.
Ligand has established multiple alliances with the world's leading pharmaceutical companies including GlaxoSmithKline, Merck,
Pfizer, Bristol-Myers Squibb and AstraZeneca. For more information, please visit www.ligand.com.
Forward-Looking Statements
This release contains forward-looking statements that involve risks and uncertainties. Ligand cautions readers that any
forward-looking information is not a guarantee of future performance and actual results could differ materially from those
contained in the forward-looking information. Words such as "expect," "estimate," "project," "potential," and similar expressions
are intended to identify such forward-looking statements. Such forward-looking statements include, but are not limited to,
statements about the benefits of the transaction between Ligand and CyDex, including future financial and operating results
and revenue potential, the expected effect of the merger on Ligand's operating cash burn rate, the possibility of
future/contingent acquisition payments being made, the combined entity's plans, objectives, expectations and intentions and
other statements that are not historical facts. Among the important factors that could cause actual results to differ materially
from those in any forward-looking statements are the risks that payment events which would produce proceeds for the
contingent value rights may not occur soon, or ever; the anticipated synergies and benefits from the transaction may not be
fully realized or may take longer to realize than expected; CyDex' product candidates may have unexpected adverse side
effects or inadequate therapeutic efficacy; and positive results in clinical trials may not be sufficient to obtain FDA approval.
There can be no assurance that any product in Ligand's, CyDex' or the projected combined company's product pipeline will be
successfully developed or manufactured, that final results of clinical studies will be supportive of regulatory approvals required
to market licensed products, or that any of the forward-looking information provided herein will be proven accurate. Additional
important factors that may affect future results are detailed in Ligand's filings with the SEC, including the company's recent
filings on Forms 10-K and 10-Q, or in information disclosed in public conference calls, the date and time of which are released
beforehand. Ligand disclaims any intent or obligation to update these forward-looking statements beyond the date of this
release.
Ligand Pharmaceuticals Incorporated
Rob McKay, Sr. Director Investor Relations
858-550-7760
rmckay@ligand.com
or
Lippert/Heilshorn & Associates
Don Markley
310-691-7100
dmarkley@lhai.com
Source: Ligand Pharmaceuticals Incorporated
News Provided by Acquire Media
Antwort auf Beitrag Nr.: 40.948.542 von asics01 am 29.01.11 16:44:48Moin asics,
bin mir nicht sicher wie ich den deal sehen soll.
Tatsache ist auf jeden Fall, dass eine satte Umsatzwarnung darin versteckt ist. Nur noch 9-10 Millionen Umsätze aus dem Ligand Geschäft! Dabei wollten sie 2011 Gewinne machen.
Nun scheint es mir so, dass Ligand durch einige Ereignisse (Roche, GSK) überrascht wurde und nun versucht dies zu kaschieren. Auch die Umsatzzahlen von Aviza waren in letzter Zeit rückläufig.
Tatsache ist aber auch, dass die nun 50 verpartnerte Programme haben. Das ist natürlich bei der Bewertung eine aberwitzige Zahl. Bei vielen weiß man aber auch nichts über die Qualität und die Royalties. Das ist einfach zu wenig transparent und unübersichtlich. Nur wenige Kooperationspartnet von Cydex sind bekannt und von den Royalties weiß man gar nichts. 1%, 5 % oder 10 % ist hier die Frage. Bei den auf dem Markt befindlichen Programmen von Cydex handelt es sich nicht um die Burner wie ich vermute. Ein Medikament ist sogar für Tiere.
Ligand ist für meinen Greschmack zu oft auf dem Grabbeltisch unterwegs. Das mag der Markt nicht. Sie schaffen es einfach nicht die zweifellos vorhandenen Qualitäten in den Vordergrund zu stellen. Die sollen mal lieber SARM für einen fetten Upfront verpartnern.
2011 bleibt aber auf jeden Fall spannend vor allem wegen der Hep C Daten von Promacta...
bin mir nicht sicher wie ich den deal sehen soll.
Tatsache ist auf jeden Fall, dass eine satte Umsatzwarnung darin versteckt ist. Nur noch 9-10 Millionen Umsätze aus dem Ligand Geschäft! Dabei wollten sie 2011 Gewinne machen.
Nun scheint es mir so, dass Ligand durch einige Ereignisse (Roche, GSK) überrascht wurde und nun versucht dies zu kaschieren. Auch die Umsatzzahlen von Aviza waren in letzter Zeit rückläufig.
Tatsache ist aber auch, dass die nun 50 verpartnerte Programme haben. Das ist natürlich bei der Bewertung eine aberwitzige Zahl. Bei vielen weiß man aber auch nichts über die Qualität und die Royalties. Das ist einfach zu wenig transparent und unübersichtlich. Nur wenige Kooperationspartnet von Cydex sind bekannt und von den Royalties weiß man gar nichts. 1%, 5 % oder 10 % ist hier die Frage. Bei den auf dem Markt befindlichen Programmen von Cydex handelt es sich nicht um die Burner wie ich vermute. Ein Medikament ist sogar für Tiere.
Ligand ist für meinen Greschmack zu oft auf dem Grabbeltisch unterwegs. Das mag der Markt nicht. Sie schaffen es einfach nicht die zweifellos vorhandenen Qualitäten in den Vordergrund zu stellen. Die sollen mal lieber SARM für einen fetten Upfront verpartnern.
2011 bleibt aber auf jeden Fall spannend vor allem wegen der Hep C Daten von Promacta...
alles sehr undurchsichtig in diesem laden,ich bin hier mit meinem latein am ende..............
Die Zahlen kommen scheinbar gut an - warum auch immer?:
http://finance.yahoo.com/news/Ligand-Pharma-posts-smaller-ap…" target="_blank" rel="nofollow ugc noopener">http://finance.yahoo.com/news/Ligand-Pharma-posts-smaller-ap…
SAN DIEGO (AP) -- Ligand Pharmaceuticals Inc. reported a smaller fourth-quarter profit on Tuesday compared to a year ago, when one-time payments boosted its revenue.
Ligand said its net income fell to $2.4 million, or 12 cents per share, in the three months ended Dec. 31 from $3 million, or 16 cents per share, a year earlier.
Its revenue fell 72 percent to $3.9 million from $14 million. Revenue from royalty payments edged up to $1.9 million from $1.8 million. The company said it received $2 million from collaboration agreements, down from $12.2 million a year ago.
In the fourth quarter of 2009, Ligand reported $9.2 million in revenue from collaborations between Pharmacopeia -- which it had acquired in December 2008 -- and other companies, including Pfizer Inc. and Bristol-Myers Squibb Co. The revenue included licensing payments and deferred revenue that was recorded because the collaborations were terminated.
Ligand's active collaborations include a partnership with GlaxoSmithKline PLC on a blood disorder drug that is marketed under the names Revolade and Promacta. The drug was approved in Europe and Japan in 2010; it reached the U.S. market in 2008. GlaxoSmithKline is studying the drug as a treatment for hepatitis C, and two late-stage trials should finish in the third quarter.
Promacta is a treatment for thrombocytopenia, or a lack of blood platelets.
Ligand is still collaborating with Pfizer on Viviant, a treatment for postmenopausal osteoporosis that is sold in Japan and Spain. Its other collaborations include a partnership with Onyx Pharmaceuticals on the blood cancer drug candidate carfilzomib. Ligand said Onyx expects to complete its filing for marketing approval of carfilzomib by the middle of the year.
For the full year, Ligand lost $12.5 million, or 64 cents per share. In 2009, it lost $1.9 million, or 10 cents per share. Revenue fell 40 percent, to $23.5 million from $38.9 million. The company said it expects $22 million to $24 million in revenue in 2011, and expects its operations to be profitable by the end of the year.
Ligand stock slipped a penny to $9.03 in afternoon trading.
http://finance.yahoo.com/news/Ligand-Pharma-posts-smaller-ap…" target="_blank" rel="nofollow ugc noopener">http://finance.yahoo.com/news/Ligand-Pharma-posts-smaller-ap…
SAN DIEGO (AP) -- Ligand Pharmaceuticals Inc. reported a smaller fourth-quarter profit on Tuesday compared to a year ago, when one-time payments boosted its revenue.
Ligand said its net income fell to $2.4 million, or 12 cents per share, in the three months ended Dec. 31 from $3 million, or 16 cents per share, a year earlier.
Its revenue fell 72 percent to $3.9 million from $14 million. Revenue from royalty payments edged up to $1.9 million from $1.8 million. The company said it received $2 million from collaboration agreements, down from $12.2 million a year ago.
In the fourth quarter of 2009, Ligand reported $9.2 million in revenue from collaborations between Pharmacopeia -- which it had acquired in December 2008 -- and other companies, including Pfizer Inc. and Bristol-Myers Squibb Co. The revenue included licensing payments and deferred revenue that was recorded because the collaborations were terminated.
Ligand's active collaborations include a partnership with GlaxoSmithKline PLC on a blood disorder drug that is marketed under the names Revolade and Promacta. The drug was approved in Europe and Japan in 2010; it reached the U.S. market in 2008. GlaxoSmithKline is studying the drug as a treatment for hepatitis C, and two late-stage trials should finish in the third quarter.
Promacta is a treatment for thrombocytopenia, or a lack of blood platelets.
Ligand is still collaborating with Pfizer on Viviant, a treatment for postmenopausal osteoporosis that is sold in Japan and Spain. Its other collaborations include a partnership with Onyx Pharmaceuticals on the blood cancer drug candidate carfilzomib. Ligand said Onyx expects to complete its filing for marketing approval of carfilzomib by the middle of the year.
For the full year, Ligand lost $12.5 million, or 64 cents per share. In 2009, it lost $1.9 million, or 10 cents per share. Revenue fell 40 percent, to $23.5 million from $38.9 million. The company said it expects $22 million to $24 million in revenue in 2011, and expects its operations to be profitable by the end of the year.
Ligand stock slipped a penny to $9.03 in afternoon trading.
Hat jemand eine Idee warumdie heute so abgegangen sind?
Die Zahlen waren ja nicht besonders...
Die Zahlen waren ja nicht besonders...
Antwort auf Beitrag Nr.: 41.054.652 von kmastra am 17.02.11 00:37:13Insiderkäufe haben eine Rolle gespielt. Ob die 10,20 nachhaltig genommen werden?
Antwort auf Beitrag Nr.: 41.082.250 von bartflanders am 22.02.11 10:20:53Vielleicht hilft das ja über die 10,20 
PHILADELPHIA, Feb. 25, 2011 /PRNewswire/ -- GlaxoSmithKline (NYSE:GSK - News) today announced that the United States Food and Drug Administration (FDA) granted full approval for PROMACTA® (eltrombopag), an oral tablet that can raise platelet counts in patients with the rare blood disorder chronic immune (idiopathic) thrombocytopenic purpura (ITP) who have had an insufficient response to corticosteroids, immunoglobulins or splenectomy.
PROMACTA initially received FDA orphan drug designation in May 2008 and accelerated approval in November 2008 for chronic ITP. The FDA Accelerated Approval program offers a pathway to gain provisional marketing approval for therapies that address unmet patient needs. Full approval of the therapy requires completion of post-marketing clinical trials and commitments that verify clinical benefit.
"Full approval of PROMACTA was based on clinical studies that provide physicians and patients with a broader understanding of its treatment effect and safety profile," said Steven Stein, MD, V.P. of Medicines Development, GlaxoSmithKline. "PROMACTA is a testament to how the FDA Accelerated Approval Program supports development of therapies that meet unmet patient needs. Patients with limited treatment options gained access to PROMACTA while GSK conducted clinical studies that yielded additional efficacy and safety data."
About Chronic ITP
Chronic ITP is a disorder marked by increased platelet destruction and/or inadequate platelet production in the blood, which causes an increased risk of bruising and bleeding. There are estimated to be approximately 60,000 individuals diagnosed with chronic ITP in the U.S. People with chronic ITP often bleed from small blood vessels causing bruises or nosebleeds.
Updated Prescribing Information (PI)
The major changes in the Prescribing Information of PROMACTA are to the Initial Dose Regimen and to the Thrombotic/Thromboembolic complications in the Warnings and Precautions section of the PI. The label also now includes efficacy and safety data from RAISE, a 6-month, randomized double-blind, placebo-controlled study in patients with ITP. The RAISE study which was published recently in the medical journal Lancet, showed that patients treated with PROMACTA were significantly more likely to achieve a platelet count between 50,000/microL and 400,000/microL during the entire 6-month treatment period compared to those patients treated with placebo.
The updated PI also incorporates two-year safety data from an open-label, single-arm extension study in patients with chronic ITP. This study showed that adverse reactions occurred in a pattern similar to those reported in the placebo-controlled studies.
Additional changes to the PI include updates on dose adjustments, risk of hepatotoxicity, bone marrow reticulin formation, thrombotic/thromboembolic complications, recurrence of thrombocytopenia, hematologic malignancies, cataracts, adverse event information, drug interactions, use in specific patient populations (hepatic and renal impairment) and to the pharmacokinetic section. For more information, please review the full Prescribing Information (Available by request: Contact Rob Perry at Robert.P.Perry@gsk.com).
BOXED WARNING and Important Safety Information
PROMACTA may cause hepatotoxicity. Increases in serum aminotransferase levels and bilirubin were observed. Liver chemistries must be measured before the initiation of treatment and regularly during treatment. See Full Prescribing Information for BOXED WARNING.
Because of the risk of hepatotoxicity, and other risks including bone marrow reticulin and risk for bone marrow fibrosis, thrombotic/thromboembolic complications, recurrence of thrombocytopenia and hemorrhage risk after PROMACTA cessation, hematologic malignancies and progression of malignancies, and cataracts, PROMACTA is available only through a restricted distribution program called PROMACTA CARES

PHILADELPHIA, Feb. 25, 2011 /PRNewswire/ -- GlaxoSmithKline (NYSE:GSK - News) today announced that the United States Food and Drug Administration (FDA) granted full approval for PROMACTA® (eltrombopag), an oral tablet that can raise platelet counts in patients with the rare blood disorder chronic immune (idiopathic) thrombocytopenic purpura (ITP) who have had an insufficient response to corticosteroids, immunoglobulins or splenectomy.
PROMACTA initially received FDA orphan drug designation in May 2008 and accelerated approval in November 2008 for chronic ITP. The FDA Accelerated Approval program offers a pathway to gain provisional marketing approval for therapies that address unmet patient needs. Full approval of the therapy requires completion of post-marketing clinical trials and commitments that verify clinical benefit.
"Full approval of PROMACTA was based on clinical studies that provide physicians and patients with a broader understanding of its treatment effect and safety profile," said Steven Stein, MD, V.P. of Medicines Development, GlaxoSmithKline. "PROMACTA is a testament to how the FDA Accelerated Approval Program supports development of therapies that meet unmet patient needs. Patients with limited treatment options gained access to PROMACTA while GSK conducted clinical studies that yielded additional efficacy and safety data."
About Chronic ITP
Chronic ITP is a disorder marked by increased platelet destruction and/or inadequate platelet production in the blood, which causes an increased risk of bruising and bleeding. There are estimated to be approximately 60,000 individuals diagnosed with chronic ITP in the U.S. People with chronic ITP often bleed from small blood vessels causing bruises or nosebleeds.
Updated Prescribing Information (PI)
The major changes in the Prescribing Information of PROMACTA are to the Initial Dose Regimen and to the Thrombotic/Thromboembolic complications in the Warnings and Precautions section of the PI. The label also now includes efficacy and safety data from RAISE, a 6-month, randomized double-blind, placebo-controlled study in patients with ITP. The RAISE study which was published recently in the medical journal Lancet, showed that patients treated with PROMACTA were significantly more likely to achieve a platelet count between 50,000/microL and 400,000/microL during the entire 6-month treatment period compared to those patients treated with placebo.
The updated PI also incorporates two-year safety data from an open-label, single-arm extension study in patients with chronic ITP. This study showed that adverse reactions occurred in a pattern similar to those reported in the placebo-controlled studies.
Additional changes to the PI include updates on dose adjustments, risk of hepatotoxicity, bone marrow reticulin formation, thrombotic/thromboembolic complications, recurrence of thrombocytopenia, hematologic malignancies, cataracts, adverse event information, drug interactions, use in specific patient populations (hepatic and renal impairment) and to the pharmacokinetic section. For more information, please review the full Prescribing Information (Available by request: Contact Rob Perry at Robert.P.Perry@gsk.com).
BOXED WARNING and Important Safety Information
PROMACTA may cause hepatotoxicity. Increases in serum aminotransferase levels and bilirubin were observed. Liver chemistries must be measured before the initiation of treatment and regularly during treatment. See Full Prescribing Information for BOXED WARNING.
Because of the risk of hepatotoxicity, and other risks including bone marrow reticulin and risk for bone marrow fibrosis, thrombotic/thromboembolic complications, recurrence of thrombocytopenia and hemorrhage risk after PROMACTA cessation, hematologic malignancies and progression of malignancies, and cataracts, PROMACTA is available only through a restricted distribution program called PROMACTA CARES
hallo kmastra
bist du noch immer überzeugt von ligand????
meinst du deren geschäftspolitik, mit den vielen übernahmen und verpartnerungen trägt einmal früchte????
wo ist das blockbuster medikament bei ligand????
asics
bist du noch immer überzeugt von ligand????
meinst du deren geschäftspolitik, mit den vielen übernahmen und verpartnerungen trägt einmal früchte????
wo ist das blockbuster medikament bei ligand????
asics
Antwort auf Beitrag Nr.: 41.235.371 von asics01 am 19.03.11 09:39:31Moin Asics,
hatt sich ja nichts geändert. Von daher bleib ich bei meiner Einschätzung.
Muss sich aber jeder seine eigene Meinung bilden. 2011 wird sicher ein wichtiges Jahr für Ligand. Ich bin gespannt....
SG kmastra
hatt sich ja nichts geändert. Von daher bleib ich bei meiner Einschätzung.
Muss sich aber jeder seine eigene Meinung bilden. 2011 wird sicher ein wichtiges Jahr für Ligand. Ich bin gespannt....
SG kmastra
In letzter Zeit gibt es dann auch mal einige Analysen zu Ligand:
http://sdbj.com/news/2011/apr/11/ligand-achieve-profitabilit…
http://www.xconomy.com/san-diego/2011/03/25/san-diegos-ligan…
http://www.investorplace.com/35521/insiders-like-ligand-phar…
http://sdbj.com/news/2011/apr/11/ligand-achieve-profitabilit…
http://www.xconomy.com/san-diego/2011/03/25/san-diegos-ligan…
http://www.investorplace.com/35521/insiders-like-ligand-phar…
2011 bleibt spannend:
Nächsten Monat Daten Ib zu SARM
Noch in diesem Jahr ist mit den Ergebnissen der P III Hepatitis C zu rechnen
In P II: 65% der Promactagruppe konnten ihre Therapie durchführen vs. 6 % in Placebo.
In der Indikation ICP könnte GsK dieses Jahr schon über die 100 Mio $ kommen (19 in Q1). Kommt die Zulassung für Hep C ist ein Umsatz im Blockbusterbereich möglich. Bin mal gespannt ob es da im Vorfeld der P III auch zu einem Runup kommt...
Nächsten Monat Daten Ib zu SARM
Noch in diesem Jahr ist mit den Ergebnissen der P III Hepatitis C zu rechnen
In P II: 65% der Promactagruppe konnten ihre Therapie durchführen vs. 6 % in Placebo.
In der Indikation ICP könnte GsK dieses Jahr schon über die 100 Mio $ kommen (19 in Q1). Kommt die Zulassung für Hep C ist ein Umsatz im Blockbusterbereich möglich. Bin mal gespannt ob es da im Vorfeld der P III auch zu einem Runup kommt...
Ist hier eigentlich noch jemand dabei?
GSK vermeldet Umsatzzahlen von Promacta:
2q2011 of $28m, up from $12m 2q2010 and $19m 1q2011
Damit wird Promacta wohl über 100 Mio in 2011 in der Nischenindikation ICP kommen.
Dazu geben sie grundsätzlich positive Studienergebnisse für Promacta bei Hep C bekannt.
http://finance.yahoo.com/news/Ligand-Partner-bw-3865638756.h…
Details sollen folgen. Es bleibt spannend...
2q2011 of $28m, up from $12m 2q2010 and $19m 1q2011
Damit wird Promacta wohl über 100 Mio in 2011 in der Nischenindikation ICP kommen.
Dazu geben sie grundsätzlich positive Studienergebnisse für Promacta bei Hep C bekannt.
http://finance.yahoo.com/news/Ligand-Partner-bw-3865638756.h…
Details sollen folgen. Es bleibt spannend...
CEO von GSK Andrew Witty im CC der Q2 Ergebnisse:
"Now you might be wondering why I haven't said anything about Promacta today. The reason we said something about Promacta today, even though we had 1 trial, it was so positive. It was so positive that we felt it would have been just completely wrong to delay sharing that information with you guys. There's no question, Promacta in Hepatitis C are allowing people to use interferer for longer. That's going to be an effective product. We've got one more trial, confirmatory trial to come. But the first trial was extraordinarily positive. Hopefully, the second will be the same. But based on the first, we'd be very surprised to not see that."
http://seekingalpha.com/article/281902-glaxosmithkline-plc-s…
Bin gespannt auf die genauen Ergebnisse.
"Now you might be wondering why I haven't said anything about Promacta today. The reason we said something about Promacta today, even though we had 1 trial, it was so positive. It was so positive that we felt it would have been just completely wrong to delay sharing that information with you guys. There's no question, Promacta in Hepatitis C are allowing people to use interferer for longer. That's going to be an effective product. We've got one more trial, confirmatory trial to come. But the first trial was extraordinarily positive. Hopefully, the second will be the same. But based on the first, we'd be very surprised to not see that."
http://seekingalpha.com/article/281902-glaxosmithkline-plc-s…
Bin gespannt auf die genauen Ergebnisse.

Insider nutzen die aktuelle Marktschwäche zum Kauf:
http://finance.yahoo.com/q/it?s=LGND+Insider+Transactions
Ich bin zwar kein Insider habe aber auch nochmal nachgekauft, da ich auf die endgültige Bekanntgabe der bereits als grundsätzlich positiv gemedeten Enable 1 und auch auf positive Daten von Enable 2 setze und somit auf den endgültigen Turnaround...vor dem Herren!
http://finance.yahoo.com/q/it?s=LGND+Insider+Transactions
Ich bin zwar kein Insider habe aber auch nochmal nachgekauft, da ich auf die endgültige Bekanntgabe der bereits als grundsätzlich positiv gemedeten Enable 1 und auch auf positive Daten von Enable 2 setze und somit auf den endgültigen Turnaround...vor dem Herren!
GSK hat in Q3 35 Mio US$ mit Promacta umgesetzt. Somit werden es in 2011 auf jeden Fall über 100 Mio (125?) werden (2010 39 Mio). Ich gehe davon aus, dass da schon der ein oder andere Patient in Sachen Hep C dabei ist. Dann bekommt der Patient halt vom Doc die Diagnose ITP und gut ist. Besser als: Sorry aber wir können sie momentan nicht weiterbehandeln, weil sie zu wenig Blutplättchen haben.
Am 7. 11 werden weitere Details in Sachen Hep C bekannt gegeben.
Ligand rechnet mit einer NDA für HepC im 2Q 12.
Am 7. 11 werden weitere Details in Sachen Hep C bekannt gegeben.
Ligand rechnet mit einer NDA für HepC im 2Q 12.
GSK presents phase III results for eltrombopag in hepatitis C virus related thrombocytopenia
Issued: Monday 07 November 2011, London UK
Full results from ENABLE 1 and initial data from ENABLE 2 presented at the 62nd Annual Meeting of the American Association for the Study of Liver Diseases
Findings from the ENABLE clinical trials, which evaluated the ability of eltrombopag to raise and maintain platelet levels in patients with chronic hepatitis C virus (HCV) infection and low platelet levels that would preclude initiation of interferon-based antiviral therapy, were presented today at the 62nd Annual Meeting of the American Association for the Study of Liver Diseases in San Francisco. Use of eltrombopag to treat thrombocytopenia in patients with chronic HCV infection is not approved anywhere in the world.
In ENABLE 1, patients who received eltrombopag along with Pegasys® (peginterferon alfa-2a) and ribavirin antiviral therapy achieved a statistically significant improvement in the primary endpoint of sustained virologic response (SVR), a clinically validated endpoint that means there is no detectable hepatitis C virus in a patient’s blood. 23% of patients in the eltrombopag group achieved SVR compared to 14% of patients receiving placebo (p=0.0064). Serious adverse events were reported in 20% of eltrombopag and 15% of placebo patients. During the entire study period death occurred in 2% of patients in the eltrombopag and 3% in the placebo group. Thromboembolic events were reported in 2% of eltrombopag patients and 2% of placebo patients. Elevations in liver enzymes were similar in both groups. Events consistent with worsening of liver function were reported in 13% of eltrombopag patients and 8% of placebo patients.
The ENABLE 1 trial enrolled 716 adults with HCV and platelet levels less than 75,000/µL into an open label eltrombopag treatment period. Those who achieved platelet levels greater than or equal to 90,000/µL were randomly assigned on a 2 to 1 basis to eltrombopag or placebo plus peginterferon alfa-2a and ribavirin.
Initial data from ENABLE 2, a randomised Phase III trial of eltrombopag plus PEG-Intron® (peginterferon alfa-2b) and ribavirin were also presented. The ENABLE 2 trial met its primary endpoint of improved SVR, with 19% of eltrombopag patients and 13% of placebo patients achieving SVR (p=0.0202). Serious adverse events were reported in 20% of eltrombopag and 15% of placebo patients. Death occurred in 4% of patients in the eltrombopag and 2% of placebo group. Thromboembolic events were reported in 4% of eltrombopag patients and less than 1% of placebo patients. Elevations in liver enzymes were similar in both groups. Events consistent with worsening of liver function were reported in 15% of eltrombopag patients and 8% placebo patients.
The ENABLE 2 trial enrolled 805 adults with HCV and platelet levels less than 75,000/µL into an open label eltrombopag treatment period and those who achieved platelet levels greater than or equal to 100,000/µL were randomly assigned on a 2 to 1 basis to eltrombopag or placebo plus peginterferon alfa-2b and ribavirin. Analyses are ongoing and full study results will be submitted for presentation at a future medical meeting.
“The ENABLE trials provide insight into a population that has generally been excluded from clinical trials because they are unable to initiate interferon therapy.” said Rafael Amado, Senior Vice President, Oncology Development “We will fully examine the efficacy and safety findings of both studies to evaluate the overall clinical benefit to these patients.”
http://www.gsk.com/media/pressreleases/2011/2011-pressreleas…
Das führte heute zu einem fetten Minus. Hintergrund scheint der, dass die FDA eine Studie - die Elevate Studie stoppte eben wegen der höheren Trombosefälle im Vergleich zur Plazebogruppe. Nun kommen natülich Zweifel auf, ob Promacta eine Zulassung bekommen kann für HEP C.
Was zusätzlich verunsichert ist die Tatsache, dass die Enable1 Studie eine ganz andere Sprache spricht nämlich eine gleiche anzahl an Trombosefällen in Promacta und Plazebogruppe. Sehr verwirrend.
Dann hat Ligand heute noch Zahlen bekannt gegeben nach Handelsschluss. Die waren für Q3 eher mau. Trotzdem wurde die guidance für das Gesamtjahr erhöht ...zumindest kommt keine Langeweile auf.
...zumindest kommt keine Langeweile auf.
http://finance.yahoo.com/news/Ligand-Pharmaceuticals-bw-4814…
Issued: Monday 07 November 2011, London UK
Full results from ENABLE 1 and initial data from ENABLE 2 presented at the 62nd Annual Meeting of the American Association for the Study of Liver Diseases
Findings from the ENABLE clinical trials, which evaluated the ability of eltrombopag to raise and maintain platelet levels in patients with chronic hepatitis C virus (HCV) infection and low platelet levels that would preclude initiation of interferon-based antiviral therapy, were presented today at the 62nd Annual Meeting of the American Association for the Study of Liver Diseases in San Francisco. Use of eltrombopag to treat thrombocytopenia in patients with chronic HCV infection is not approved anywhere in the world.
In ENABLE 1, patients who received eltrombopag along with Pegasys® (peginterferon alfa-2a) and ribavirin antiviral therapy achieved a statistically significant improvement in the primary endpoint of sustained virologic response (SVR), a clinically validated endpoint that means there is no detectable hepatitis C virus in a patient’s blood. 23% of patients in the eltrombopag group achieved SVR compared to 14% of patients receiving placebo (p=0.0064). Serious adverse events were reported in 20% of eltrombopag and 15% of placebo patients. During the entire study period death occurred in 2% of patients in the eltrombopag and 3% in the placebo group. Thromboembolic events were reported in 2% of eltrombopag patients and 2% of placebo patients. Elevations in liver enzymes were similar in both groups. Events consistent with worsening of liver function were reported in 13% of eltrombopag patients and 8% of placebo patients.
The ENABLE 1 trial enrolled 716 adults with HCV and platelet levels less than 75,000/µL into an open label eltrombopag treatment period. Those who achieved platelet levels greater than or equal to 90,000/µL were randomly assigned on a 2 to 1 basis to eltrombopag or placebo plus peginterferon alfa-2a and ribavirin.
Initial data from ENABLE 2, a randomised Phase III trial of eltrombopag plus PEG-Intron® (peginterferon alfa-2b) and ribavirin were also presented. The ENABLE 2 trial met its primary endpoint of improved SVR, with 19% of eltrombopag patients and 13% of placebo patients achieving SVR (p=0.0202). Serious adverse events were reported in 20% of eltrombopag and 15% of placebo patients. Death occurred in 4% of patients in the eltrombopag and 2% of placebo group. Thromboembolic events were reported in 4% of eltrombopag patients and less than 1% of placebo patients. Elevations in liver enzymes were similar in both groups. Events consistent with worsening of liver function were reported in 15% of eltrombopag patients and 8% placebo patients.
The ENABLE 2 trial enrolled 805 adults with HCV and platelet levels less than 75,000/µL into an open label eltrombopag treatment period and those who achieved platelet levels greater than or equal to 100,000/µL were randomly assigned on a 2 to 1 basis to eltrombopag or placebo plus peginterferon alfa-2b and ribavirin. Analyses are ongoing and full study results will be submitted for presentation at a future medical meeting.
“The ENABLE trials provide insight into a population that has generally been excluded from clinical trials because they are unable to initiate interferon therapy.” said Rafael Amado, Senior Vice President, Oncology Development “We will fully examine the efficacy and safety findings of both studies to evaluate the overall clinical benefit to these patients.”
http://www.gsk.com/media/pressreleases/2011/2011-pressreleas…
Das führte heute zu einem fetten Minus. Hintergrund scheint der, dass die FDA eine Studie - die Elevate Studie stoppte eben wegen der höheren Trombosefälle im Vergleich zur Plazebogruppe. Nun kommen natülich Zweifel auf, ob Promacta eine Zulassung bekommen kann für HEP C.
Was zusätzlich verunsichert ist die Tatsache, dass die Enable1 Studie eine ganz andere Sprache spricht nämlich eine gleiche anzahl an Trombosefällen in Promacta und Plazebogruppe. Sehr verwirrend.
Dann hat Ligand heute noch Zahlen bekannt gegeben nach Handelsschluss. Die waren für Q3 eher mau. Trotzdem wurde die guidance für das Gesamtjahr erhöht
 ...zumindest kommt keine Langeweile auf.
...zumindest kommt keine Langeweile auf.http://finance.yahoo.com/news/Ligand-Pharmaceuticals-bw-4814…
hallo kmastra
ligand wurde ja heftig verprügelt,das war dann wohl nix mit dem endgültigen Turnaround...vor dem Herren!
mir gab es die gelegenheit wieder einzusteigen,bin gestern abend noch mal rein.
ich bin wieder bei dir,auf ein neues und hoffentlich endgültigen Turnaround...vor dem Herren!
asics
ligand wurde ja heftig verprügelt,das war dann wohl nix mit dem endgültigen Turnaround...vor dem Herren!
mir gab es die gelegenheit wieder einzusteigen,bin gestern abend noch mal rein.
ich bin wieder bei dir,auf ein neues und hoffentlich endgültigen Turnaround...vor dem Herren!
asics
Hallo asics,
da hast du leider Recht. Die Spekulation auf die Enable2 Daten ging leider gründlich daneben. Schon bitter wie GSK das kommuniziert hat. Erst spricht der CEO von außergewöhnlich guten Ergebnissen und dass er überrascht wäre wenn enable2 floppe und dann hauen die völlig unkommentiert die (Fragen aufwerfenden) Fakten raus. Dabei hat promacta ja die Ziele der Studien erreicht. Problematisch sind die nebenwirkungen. Man muss dabei auch bedenken, dass die Probanden eine Gruppe darstellen über die bisher noch gar keine Daten vorlagen, weil sie schlicht nicht behandelt werden konnten.
Das jetzt Ligand so dermaßen abgestraft wurde liegt m.E. an der entstandenen Unsicherheit in Verbindung mit der allgemeinen Markterwartung. Es waren viele drin, die kurzfristig auf einen Schub durch die Daten gestzt hatten und gehen jetzt schnell raus.
Jetzt wird ja sogar angezweifelt, ob GSK überhaupt eine Zulassung beantragt.
Dazu kommt noch die neue Situation, da sich die Standardtherapie geändert hat und sich vermutlich demnächst noch mal ändern wird. Sowas kommt an der Börse bekanntlich gar nicht gut an. Bleibt nichts weiter als die kommenden Monate abzuwarten. Ligand selber hatte ja zur Diskussion bzgl. der Ergebnisse geladen. Falls es dich interessiert:
http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9N…
Zumindest haben Insider heute nochmal kleine Positionen zugekauft und vor allem nix verkauft. Dann wünsche ich uns nu aber den endgültigsten Turnaround vor dem Herren
da hast du leider Recht. Die Spekulation auf die Enable2 Daten ging leider gründlich daneben. Schon bitter wie GSK das kommuniziert hat. Erst spricht der CEO von außergewöhnlich guten Ergebnissen und dass er überrascht wäre wenn enable2 floppe und dann hauen die völlig unkommentiert die (Fragen aufwerfenden) Fakten raus. Dabei hat promacta ja die Ziele der Studien erreicht. Problematisch sind die nebenwirkungen. Man muss dabei auch bedenken, dass die Probanden eine Gruppe darstellen über die bisher noch gar keine Daten vorlagen, weil sie schlicht nicht behandelt werden konnten.
Das jetzt Ligand so dermaßen abgestraft wurde liegt m.E. an der entstandenen Unsicherheit in Verbindung mit der allgemeinen Markterwartung. Es waren viele drin, die kurzfristig auf einen Schub durch die Daten gestzt hatten und gehen jetzt schnell raus.
Jetzt wird ja sogar angezweifelt, ob GSK überhaupt eine Zulassung beantragt.
Dazu kommt noch die neue Situation, da sich die Standardtherapie geändert hat und sich vermutlich demnächst noch mal ändern wird. Sowas kommt an der Börse bekanntlich gar nicht gut an. Bleibt nichts weiter als die kommenden Monate abzuwarten. Ligand selber hatte ja zur Diskussion bzgl. der Ergebnisse geladen. Falls es dich interessiert:
http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9N…
Zumindest haben Insider heute nochmal kleine Positionen zugekauft und vor allem nix verkauft. Dann wünsche ich uns nu aber den endgültigsten Turnaround vor dem Herren

hallo kmastra
lgnd besteht ja nicht nur aus promacta,mal schauen was dieses jahr bei diesem marktumfeld noch geht.
heute auf jedenfall ein ordentliches plus,habe gestern bei 11,09$ ordentlich zugelagt.
asics
lgnd besteht ja nicht nur aus promacta,mal schauen was dieses jahr bei diesem marktumfeld noch geht.
heute auf jedenfall ein ordentliches plus,habe gestern bei 11,09$ ordentlich zugelagt.
asics
Antwort auf Beitrag Nr.: 42.339.224 von asics01 am 11.11.11 19:06:45Moin asics,
Ligand ist schon sehr breit aufgestellt. Die Zulassung für Promacta auf anderen Gebieten wäre aber extrem wichtig. Man kann sich ja ausrechnen welche Kurse dann zu erwarten wären.
Ich rechne mit einem ziemlich holprigen Verlauf in der nächsten Zeit.
Beruhigen könnte lediglich eine ausführliche und positive Präsentation der Enable2 Daten. Die soll ja noch kommen.
SG kmastra
Ligand ist schon sehr breit aufgestellt. Die Zulassung für Promacta auf anderen Gebieten wäre aber extrem wichtig. Man kann sich ja ausrechnen welche Kurse dann zu erwarten wären.
Ich rechne mit einem ziemlich holprigen Verlauf in der nächsten Zeit.
Beruhigen könnte lediglich eine ausführliche und positive Präsentation der Enable2 Daten. Die soll ja noch kommen.
SG kmastra
Unglaublich welche Dynamik zur Zeit im HEP C Markt ist. Mir scheint das auch eine direkte "Konkurrenz" zu Promacta zu sein.
http://www.fiercebiotech.com/story/gilead-sciences-bags-phar…
UPDATED: Gilead Sciences bags Pharmasset's hep C pipeline in $11B buyout
November 21, 2011 — 8:24am ET | By John Carroll
In a big gamble Gilead Sciences ($GILD) has struck a deal to buy Pharmasset, one of the hottest public biotech companies in the world, for $11 billion. Gilead will pay $137 per share for the company ($VRUS), which has seized wide attention for its work on new hepatitis C treatments that may do away with the need for interferon and create a new standard of care for the disease.
Remarkably, Pharmasset's investors are avoiding the hedging that often gets built into an acquisition of a clinical-stage development company. The news instantly triggered an 86% spike in the company's share price--which has been zooming up this year--as investors jumped on board for the ride up to the buyout price.
Angling for a potential approval in 2014, Pharmasset's unpartnered lead program--PSI-7977--has advanced into two late-stage studies involving genotype 2 and 3 patients. One study will compare the oral therapy combined with ribavirin against the standard-of-care: pegylated interferon/ribavirin in treatment-naive patients. The second study will compare PSI-7977 to a placebo in interferon-intolerant or ineligible patients. A third Phase III launches in the second half of 2012.
While Vertex ($VRTX) has been grabbing market share for the recently approved Incivek, a significant advance in the treatment of hepatitis C, a number of investors and analysts have picked Pharmasset as the biotech most likely to succeed at the near-term development of an interferon-free product. How much would that be worth?
Canaccord Genuity life sciences analyst George Farmer said this morning that an interferon-free competitor to Incivek would blast Vertex's revenue. "We model for a steep decline of Incivek sales from $3.7B in 2014 to ~$500M in 2015, as a consequence of the first interferon-free regimens expected to hit the market," he noted. "We anticipate significant threats to Incivek market share from competitive drugs under development in all-oral interferon-sparing regimens. Current innovation leaves Incivek well behind and without a role in future FDA approved all-oral regimens, in our view."
The acquisition marks a big step for Gilead, which has been adding new R&D space at its corporate headquarters. Gilead built its reputation developing treatments for HIV and intimately understands the work being done on hepatitis C.
Analysts quickly turned to a central question this morning: Is Pharmasset, which had a hefty market value of more than $5 billion on Friday, worth $11 billion to Gilead today? Some don't think so. "Pharmasset was an attractive company," noted the online site 24/7 Wall St, "but this one seems like Gilead is spending above and beyond a normal amount here to close this deal." A number of investors appeared to agree, driving down Gilead shares by 12% this morning.
Inevitably, the rich buyout immediately triggered an intense round of messaging on Twitter as some long-time industry observers began to wonder who else may have been sitting at the bargaining table, and whether other hepatitis C drug developers would be next in line. Something like that may be on the mind of Achillion CEO Michael Kishbauch, who was touting overtures from prospective buyers last Friday.
"The acquisition of Pharmasset represents an important and exciting opportunity to accelerate Gilead's effort to change the treatment paradigm for HCV-infected patients by developing all-oral regimens for the treatment of the disease regardless of viral genotype," said Gilead Sciences CEO John C. Martin. "Pharmasset presented compelling Phase 2 data earlier this month further characterizing the strong efficacy and safety profile of PSI-7977. The compound, together with Pharmasset's other pipeline candidates, represents a strong strategic fit with Gilead's vision, pipeline and capabilities. This transaction will serve to drive the long-term growth of our business, and we look forward to working closely with the Pharmasset team to advance a broad clinical program in HCV to address the unmet needs of patients and the medical community."
http://www.fiercebiotech.com/story/gilead-sciences-bags-phar…
UPDATED: Gilead Sciences bags Pharmasset's hep C pipeline in $11B buyout
November 21, 2011 — 8:24am ET | By John Carroll
In a big gamble Gilead Sciences ($GILD) has struck a deal to buy Pharmasset, one of the hottest public biotech companies in the world, for $11 billion. Gilead will pay $137 per share for the company ($VRUS), which has seized wide attention for its work on new hepatitis C treatments that may do away with the need for interferon and create a new standard of care for the disease.
Remarkably, Pharmasset's investors are avoiding the hedging that often gets built into an acquisition of a clinical-stage development company. The news instantly triggered an 86% spike in the company's share price--which has been zooming up this year--as investors jumped on board for the ride up to the buyout price.
Angling for a potential approval in 2014, Pharmasset's unpartnered lead program--PSI-7977--has advanced into two late-stage studies involving genotype 2 and 3 patients. One study will compare the oral therapy combined with ribavirin against the standard-of-care: pegylated interferon/ribavirin in treatment-naive patients. The second study will compare PSI-7977 to a placebo in interferon-intolerant or ineligible patients. A third Phase III launches in the second half of 2012.
While Vertex ($VRTX) has been grabbing market share for the recently approved Incivek, a significant advance in the treatment of hepatitis C, a number of investors and analysts have picked Pharmasset as the biotech most likely to succeed at the near-term development of an interferon-free product. How much would that be worth?
Canaccord Genuity life sciences analyst George Farmer said this morning that an interferon-free competitor to Incivek would blast Vertex's revenue. "We model for a steep decline of Incivek sales from $3.7B in 2014 to ~$500M in 2015, as a consequence of the first interferon-free regimens expected to hit the market," he noted. "We anticipate significant threats to Incivek market share from competitive drugs under development in all-oral interferon-sparing regimens. Current innovation leaves Incivek well behind and without a role in future FDA approved all-oral regimens, in our view."
The acquisition marks a big step for Gilead, which has been adding new R&D space at its corporate headquarters. Gilead built its reputation developing treatments for HIV and intimately understands the work being done on hepatitis C.
Analysts quickly turned to a central question this morning: Is Pharmasset, which had a hefty market value of more than $5 billion on Friday, worth $11 billion to Gilead today? Some don't think so. "Pharmasset was an attractive company," noted the online site 24/7 Wall St, "but this one seems like Gilead is spending above and beyond a normal amount here to close this deal." A number of investors appeared to agree, driving down Gilead shares by 12% this morning.
Inevitably, the rich buyout immediately triggered an intense round of messaging on Twitter as some long-time industry observers began to wonder who else may have been sitting at the bargaining table, and whether other hepatitis C drug developers would be next in line. Something like that may be on the mind of Achillion CEO Michael Kishbauch, who was touting overtures from prospective buyers last Friday.
"The acquisition of Pharmasset represents an important and exciting opportunity to accelerate Gilead's effort to change the treatment paradigm for HCV-infected patients by developing all-oral regimens for the treatment of the disease regardless of viral genotype," said Gilead Sciences CEO John C. Martin. "Pharmasset presented compelling Phase 2 data earlier this month further characterizing the strong efficacy and safety profile of PSI-7977. The compound, together with Pharmasset's other pipeline candidates, represents a strong strategic fit with Gilead's vision, pipeline and capabilities. This transaction will serve to drive the long-term growth of our business, and we look forward to working closely with the Pharmasset team to advance a broad clinical program in HCV to address the unmet needs of patients and the medical community."
Eine Nachricht, die das Vertrauen in Promacta und die Hoffnung auf eine Zulassung bei anderen Indikationen erhöhen dürfte.
http://www.prnewswire.com/news-releases/fda-announces-change…
Zusätzlich stehen Ergebnisse zu Promacta auf der ASH vom 10-13 Dezember und natürlich die Ergebnisse zur 2. HEP C Studie an:
http://ash.confex.com/ash/2011/webprogram/Paper41716.html
http://www.prnewswire.com/news-releases/fda-announces-change…
Zusätzlich stehen Ergebnisse zu Promacta auf der ASH vom 10-13 Dezember und natürlich die Ergebnisse zur 2. HEP C Studie an:
http://ash.confex.com/ash/2011/webprogram/Paper41716.html
Zurzeit charttechnisch nicht uninteressant:
http://chart.ly/vxhogv7
Ich denke in Erwartung der Q1 Daten von GSK zu Promacta und auch der Q1 Zahlen von Ligand am 7 bzw. 14. Februar stehen die Chancen auf den Ausbruch nicht schlecht.
Mittelfristig entscheidend dann vor allem die kompletten Daten zur Enable 2 wahrscheinlich auf der EASL in Barcelona im April.
http://chart.ly/vxhogv7
Ich denke in Erwartung der Q1 Daten von GSK zu Promacta und auch der Q1 Zahlen von Ligand am 7 bzw. 14. Februar stehen die Chancen auf den Ausbruch nicht schlecht.
Mittelfristig entscheidend dann vor allem die kompletten Daten zur Enable 2 wahrscheinlich auf der EASL in Barcelona im April.
Gsk gab heute Zahlen bekannt:
Promacta war 22 Mio. GBP also ca. 35 Mio US$ in Q4. Also robuste Zahlen
Aber weitaus wichtiger war die Ankündigung im CC die Zulassung für Hep C einzureichen:
"So regarding Promacta, as you know there is 2 ENABLE trials, 1 and 2. And observations were contrasted between the 2 studies and our overall assessment of the population on the 2 studies led us to conclude that the benefit risk intervention in chronic hepatitis C patients was positive and therefore, we will file and I'm sure, the observations made will be subjects of discussions during the review period. But we're confident to file and we are confident this is a beneficial medicine for patients."
http://seekingalpha.com/article/347681-glaxosmithkline-plc-s…
Bei Ligand ist dieses Jahr definitiv Musik drin: 3 FDA Entscheidungen:
Promacta Hep C (GsK)
Aprela (Pfizer)
Carfilzomib (Onyx)
Und gleich noch Zahlen von LGND selber. Angekündigt war ein ausgeglichenes Ergebnis. Wäre ja mal was wenn ein kleiner Gewinn übrig bliebe. Turnaround?
Promacta war 22 Mio. GBP also ca. 35 Mio US$ in Q4. Also robuste Zahlen
Aber weitaus wichtiger war die Ankündigung im CC die Zulassung für Hep C einzureichen:
"So regarding Promacta, as you know there is 2 ENABLE trials, 1 and 2. And observations were contrasted between the 2 studies and our overall assessment of the population on the 2 studies led us to conclude that the benefit risk intervention in chronic hepatitis C patients was positive and therefore, we will file and I'm sure, the observations made will be subjects of discussions during the review period. But we're confident to file and we are confident this is a beneficial medicine for patients."
http://seekingalpha.com/article/347681-glaxosmithkline-plc-s…
Bei Ligand ist dieses Jahr definitiv Musik drin: 3 FDA Entscheidungen:
Promacta Hep C (GsK)
Aprela (Pfizer)
Carfilzomib (Onyx)
Und gleich noch Zahlen von LGND selber. Angekündigt war ein ausgeglichenes Ergebnis. Wäre ja mal was wenn ein kleiner Gewinn übrig bliebe. Turnaround?
Zahlen haben mich eher positiv überrascht:
Fourth Quarter Results
Total revenues from continuing operations for the fourth quarter of 2011 were $12.9 million, compared with $3.9 million for the fourth quarter of 2010. The $9.0 million increase is primarily due to material sales of Captisol®, higher royalties and an increase in one-time license and milestone revenues.
Cost of goods sold was $2.1 million for the fourth quarter of 2011. Other operating costs and expenses from continuing operations for the fourth quarter of 2011 were $6.5 million; this compares with operating costs and expenses of $10.3 million for the fourth quarter of 2010 including a $2.8 million write-off of in-process research and development for a discontinued program. Research and development expenses were $2.6 million, a decline of $0.6 million compared with the fourth quarter of 2010, primarily due to lower spending related to internal research programs. General and administrative expenses were $3.7 million, an increase of $0.2 million compared with the fourth quarter of 2010.
Net income for the fourth quarter of 2011 was $4.8 million, or $0.24 per share, compared with net income for the fourth quarter of 2010 of $4.5 million, or $0.23 per share. Income from continuing operations for the fourth quarter of 2011 was $4.8 million, or $0.24 per share, compared with income from continuing operations for the fourth quarter of 2010 of $2.3 million, or $0.12 per share.
As of December 31, 2011, Ligand had cash, cash equivalents, short-term investments and restricted investments of $18.4 million and accounts receivable of $6.1 million.
Full-Year Results
Total revenues for 2011 were $30.0 million, compared with $23.5 million for 2010. Cost of goods sold was $4.9 million for 2011. Other operating costs and expenses for 2011 were $27.5 million, including a $2.3 million write-off of in-process research and development for discontinued programs; this compares with operating costs and expenses for 2010 of $54.5 million, including $16.9 million of lease exit and termination costs and a $2.8 million write-off of in-process research and development for a discontinued program.
Net income for 2011 was $10.2 million, or $0.52 per share, compared with a net loss for 2010 of $10.4 million, or $0.53 per share. Net income for 2011 includes a $13.1 million income tax benefit.
http://investor.ligand.com/phoenix.zhtml?c=102955&p=irol-new…
Fourth Quarter Results
Total revenues from continuing operations for the fourth quarter of 2011 were $12.9 million, compared with $3.9 million for the fourth quarter of 2010. The $9.0 million increase is primarily due to material sales of Captisol®, higher royalties and an increase in one-time license and milestone revenues.
Cost of goods sold was $2.1 million for the fourth quarter of 2011. Other operating costs and expenses from continuing operations for the fourth quarter of 2011 were $6.5 million; this compares with operating costs and expenses of $10.3 million for the fourth quarter of 2010 including a $2.8 million write-off of in-process research and development for a discontinued program. Research and development expenses were $2.6 million, a decline of $0.6 million compared with the fourth quarter of 2010, primarily due to lower spending related to internal research programs. General and administrative expenses were $3.7 million, an increase of $0.2 million compared with the fourth quarter of 2010.
Net income for the fourth quarter of 2011 was $4.8 million, or $0.24 per share, compared with net income for the fourth quarter of 2010 of $4.5 million, or $0.23 per share. Income from continuing operations for the fourth quarter of 2011 was $4.8 million, or $0.24 per share, compared with income from continuing operations for the fourth quarter of 2010 of $2.3 million, or $0.12 per share.
As of December 31, 2011, Ligand had cash, cash equivalents, short-term investments and restricted investments of $18.4 million and accounts receivable of $6.1 million.
Full-Year Results
Total revenues for 2011 were $30.0 million, compared with $23.5 million for 2010. Cost of goods sold was $4.9 million for 2011. Other operating costs and expenses for 2011 were $27.5 million, including a $2.3 million write-off of in-process research and development for discontinued programs; this compares with operating costs and expenses for 2010 of $54.5 million, including $16.9 million of lease exit and termination costs and a $2.8 million write-off of in-process research and development for a discontinued program.
Net income for 2011 was $10.2 million, or $0.52 per share, compared with a net loss for 2010 of $10.4 million, or $0.53 per share. Net income for 2011 includes a $13.1 million income tax benefit.
http://investor.ligand.com/phoenix.zhtml?c=102955&p=irol-new…
Im CC nannte es der CEO "12 in 2012" - 12 Programme sollen sich 2012 in P III befinden:
Promacta in HEP C - sNDA GsK
Promacta - P III oncology-related thrombocytopaenia GsK
Aprela - NDA Pfizer
Carfilzomib - FDA Entscheidung Onyx
Carbamazepine - P III Lundbeck
Dinaciclib - P III Merck
Delafloxacin - P III RibX
Melphalan - P III Ligand
Unbekannt- P III Merck
Unbekannt - P III Lily
Unbekannt - P III Hospira
Promacta in HEP C - sNDA GsK
Promacta - P III oncology-related thrombocytopaenia GsK
Aprela - NDA Pfizer
Carfilzomib - FDA Entscheidung Onyx
Carbamazepine - P III Lundbeck
Dinaciclib - P III Merck
Delafloxacin - P III RibX
Melphalan - P III Ligand
Unbekannt- P III Merck
Unbekannt - P III Lily
Unbekannt - P III Hospira
... und Clopidogrel von The Medicines Company P III
Freitag kam Volumen endlich rein. Bin gespannt wie es heute weitergeht.
Könnte mir vorstellen, dass in nächster Zeit der Widerstand bei 16 $ getestet wird.
Freitag kam Volumen endlich rein. Bin gespannt wie es heute weitergeht.
Könnte mir vorstellen, dass in nächster Zeit der Widerstand bei 16 $ getestet wird.
Mal sehen ob zeitnah die 16$ Marke überwunden wird. Auf jeden Fall bleibe ich extrem optimistisch, dass es dieses Jahr nochmal deutlich nach oben geht.
Vor allem der angekündigte Zulassungsantrag für Promacta in HEPC wird für Bewegung sorgen.
Diese Studie zeigt den Wert, den Promacta für Ligand haben könnte:
http://www.griffinsecurities.com/upload/reports/Griffin_LGND…
Projected Promacta Royalties
2012: $ 10,445
2013: $ 15,500
2014: $ 62,000
2015: $ 108,000
2016: $ 160,000
Ligand selber geht in einem positiven Szenario von Royalties von 150-200 Mio $ in 2015 aus.
http://investor.ligand.com/Theme/Ligand/files/doc_presentati…
Bei der derzeitigen Marktkapitalisierung entspräche das einem KGV von 2. Ligand könnte sich also - wenn es so käme - mindestens verzehnfachen bis 2015. Das wäre dann in der Tat ein Turnaround vor dem Herren...
Vor allem der angekündigte Zulassungsantrag für Promacta in HEPC wird für Bewegung sorgen.
Diese Studie zeigt den Wert, den Promacta für Ligand haben könnte:
http://www.griffinsecurities.com/upload/reports/Griffin_LGND…
Projected Promacta Royalties
2012: $ 10,445
2013: $ 15,500
2014: $ 62,000
2015: $ 108,000
2016: $ 160,000
Ligand selber geht in einem positiven Szenario von Royalties von 150-200 Mio $ in 2015 aus.
http://investor.ligand.com/Theme/Ligand/files/doc_presentati…
Bei der derzeitigen Marktkapitalisierung entspräche das einem KGV von 2. Ligand könnte sich also - wenn es so käme - mindestens verzehnfachen bis 2015. Das wäre dann in der Tat ein Turnaround vor dem Herren...
Charttechnisch sieht es nach Überwinden der 16 $ Marke nun sehr gut aus.
Kann natürlich auch ein Fehlsignal sein aber ich habe mir zusätzlich noch eine kleine Tradingposition gekauft und setze neben der charttechnik auch auf den zu erwartenden newsflow bis Ende des Jahres:
18-22 April Enable2 Daten zu Promacta in HEP C
27.7. Zulassungsentscheidung Carfilzomib
Herbst? Zulassungsantrag Promacta in HEP C
?? in 2012 NDA Aprela von Pfizer
?? Entscheid darüber wie es mit Promacta in anderen Indikationen z.B. Onkologie Related Thrombocytopenia weitergeht
??...
Kann natürlich auch ein Fehlsignal sein aber ich habe mir zusätzlich noch eine kleine Tradingposition gekauft und setze neben der charttechnik auch auf den zu erwartenden newsflow bis Ende des Jahres:
18-22 April Enable2 Daten zu Promacta in HEP C
27.7. Zulassungsentscheidung Carfilzomib
Herbst? Zulassungsantrag Promacta in HEP C
?? in 2012 NDA Aprela von Pfizer
?? Entscheid darüber wie es mit Promacta in anderen Indikationen z.B. Onkologie Related Thrombocytopenia weitergeht
??...
hallo kmastra
glückwunsch dass du so lange durchgehalten hast,mit so einem wert im depot kann man nachts auch ruhig schlafen.
die 20$ kriegst du dieses jahr noch.
asics
glückwunsch dass du so lange durchgehalten hast,mit so einem wert im depot kann man nachts auch ruhig schlafen.
die 20$ kriegst du dieses jahr noch.
asics
Antwort auf Beitrag Nr.: 42.897.594 von asics01 am 14.03.12 07:15:04Moin asics,
vielen Dank. Aber so dick sind die gewinne noch nicht...
Setze grundsätzlich eher auf biotechs mit breiter pipeline - auch dem bessern Schlaf wegen. Zur Zeit habe ich noch Array, Dyax, Astex im Depot.
SG kmastra
vielen Dank. Aber so dick sind die gewinne noch nicht...
Setze grundsätzlich eher auf biotechs mit breiter pipeline - auch dem bessern Schlaf wegen. Zur Zeit habe ich noch Array, Dyax, Astex im Depot.
SG kmastra
Heute der erwartete Anstieg unter hohem Volumen. Shorts müssen sich eindecken, und das ging heute bei 16,6 $ los. Ich finds gut!
Die letzten Tage ging es steil bergab. Neben der Nachricht einer Kapitalerhöhung wird auch ein negativer Beitrag auf fool.com seinen Anteil daran haben.
Sicherlich nicht ganz verkehrt was da steht aber doch sehr auf das Negative fokussiert. Vor allem sehr in die Vergangenheit gerichtet. Die positiven Aussichten von Promacta, 12 in 2012 usw. finden keine erwähnung...
Hätte man so auch vor einem halben Jahr schreiben können. das dies nun nach einem Anstieg erfolgt muss doch sehr verwundern. Die Shorts wird es aber freuen. Ein Schelm wer Böses dabei denkt!
http://biz.yahoo.com/e/120326/lgnd8-k.html
http://www.fool.com/investing/high-growth/2012/03/29/avoid-t…
I used to think that Ligand was a well-run and productive operation, successfully progressing drugs through early stages of development and then licensing or partnering them with large pharmaceutical companies. I looked past their weak quarterly revenues and the opacity of their partnership agreements, figuring that it would be only a matter of time before everything came together and they became cash flow positive.
In 2012, I've come to the conclusion that Ligand is more like a schizoaffective chimpanzee with a box of Godiva chocolates. They take a bite of one, and throw it on the floor. Take a bite of another, throw it at another chimpanzee. Take another one and mash it into their fur. The company seems to have an unending appetite for new pipeline projects, mostly picked up from other failed small pharmas, yet none ever translate into significant revenues. During the time I've been following the company, Ligand has taken over Metabasis, Neurogen, and Pharmacopeia with very little to show for it.
The latetst acquisition was of privately held Cydex and their Captisol drug formulation technology for 36M and contingent payments. Despite the cheap price, captisol compounds have now almost completely taken over Ligand's PR to the virtual exclusion of older projects such as Promacta and bazidoxifene. The final straw for me with Ligand came when the company proudly announced a partnership with Retrophin for DARA for 1M up front plus undisclosed milestones and royalties. There are so many things wrong with this deal, it's hard to list them with a straight face.
First of all, there's no objective evidence that Retrophin has any real operations. The CEO is Martin Shkreli, better known for running hedge fund MSMB Capital Management and penning tongue-in-cheek (and often painfully accurate) dissections of small biotech companies to support his fund's short positions. Shkreli's fund made a buyout bid for Amag Pharmaceuticals last year which was essentially disregarded. I've got nothing against Shkreli, but I suspect Retrophin is some form of sockpuppet he's created to hold biotech assets and possibly sell them a later date, without making any genuine effort to further their development himself. DARA was the main asset of the Ligand's Pharmacopeia acquisition in 2008. So Ligand paid 70M for DARA, and is now selling it for 1M. Good deal. Meanwhile, it seems unlikely any milestone and royalty payments will be coming from Retrophin.
I think I might buy Captisol for 1M up front and a trillion dollars in milestones and royalties, and then sit on it until I can sucker someone else into buying it for 5M. Anyone out there want to chip in?
Meanwhile, Ligand stock is rising rapidly with a market cap of 321M as of this writing. The company had 18M in cash, 30M in debt, and 2.6M in royalty revenue last quarter. Ligand makes more money selling Captisol to their partners for use in clinical trials than it does on royalties from their entire history of R&D. Hate to think what's going to happen if those trials don't end up in FDA approval of any Captisol products.
Sicherlich nicht ganz verkehrt was da steht aber doch sehr auf das Negative fokussiert. Vor allem sehr in die Vergangenheit gerichtet. Die positiven Aussichten von Promacta, 12 in 2012 usw. finden keine erwähnung...
Hätte man so auch vor einem halben Jahr schreiben können. das dies nun nach einem Anstieg erfolgt muss doch sehr verwundern. Die Shorts wird es aber freuen. Ein Schelm wer Böses dabei denkt!
http://biz.yahoo.com/e/120326/lgnd8-k.html
http://www.fool.com/investing/high-growth/2012/03/29/avoid-t…
I used to think that Ligand was a well-run and productive operation, successfully progressing drugs through early stages of development and then licensing or partnering them with large pharmaceutical companies. I looked past their weak quarterly revenues and the opacity of their partnership agreements, figuring that it would be only a matter of time before everything came together and they became cash flow positive.
In 2012, I've come to the conclusion that Ligand is more like a schizoaffective chimpanzee with a box of Godiva chocolates. They take a bite of one, and throw it on the floor. Take a bite of another, throw it at another chimpanzee. Take another one and mash it into their fur. The company seems to have an unending appetite for new pipeline projects, mostly picked up from other failed small pharmas, yet none ever translate into significant revenues. During the time I've been following the company, Ligand has taken over Metabasis, Neurogen, and Pharmacopeia with very little to show for it.
The latetst acquisition was of privately held Cydex and their Captisol drug formulation technology for 36M and contingent payments. Despite the cheap price, captisol compounds have now almost completely taken over Ligand's PR to the virtual exclusion of older projects such as Promacta and bazidoxifene. The final straw for me with Ligand came when the company proudly announced a partnership with Retrophin for DARA for 1M up front plus undisclosed milestones and royalties. There are so many things wrong with this deal, it's hard to list them with a straight face.
First of all, there's no objective evidence that Retrophin has any real operations. The CEO is Martin Shkreli, better known for running hedge fund MSMB Capital Management and penning tongue-in-cheek (and often painfully accurate) dissections of small biotech companies to support his fund's short positions. Shkreli's fund made a buyout bid for Amag Pharmaceuticals last year which was essentially disregarded. I've got nothing against Shkreli, but I suspect Retrophin is some form of sockpuppet he's created to hold biotech assets and possibly sell them a later date, without making any genuine effort to further their development himself. DARA was the main asset of the Ligand's Pharmacopeia acquisition in 2008. So Ligand paid 70M for DARA, and is now selling it for 1M. Good deal. Meanwhile, it seems unlikely any milestone and royalty payments will be coming from Retrophin.
I think I might buy Captisol for 1M up front and a trillion dollars in milestones and royalties, and then sit on it until I can sucker someone else into buying it for 5M. Anyone out there want to chip in?
Meanwhile, Ligand stock is rising rapidly with a market cap of 321M as of this writing. The company had 18M in cash, 30M in debt, and 2.6M in royalty revenue last quarter. Ligand makes more money selling Captisol to their partners for use in clinical trials than it does on royalties from their entire history of R&D. Hate to think what's going to happen if those trials don't end up in FDA approval of any Captisol products.
Nachdem der Kurs gestern auf der Unterstützung bei 16 $ abprallte wurde sie heute klar gebrochen. Grund war das abstract zur Enable2 Präsentation auf der EASL. Dort stand zwar nichts Neues drin aber somit auch nichts neues Gutes:
Background and aims: Thrombocytopenia limits the ability to initiate and maintain peginterferon alfa-2b [PEG-2b]+ribavirin therapy in patients with cirrhosis due to hepatitis C (HCV). PEG-2b is not recommended for patients with platelets < 100Gi /L. Eltrombopag is an oral thrombopoietin receptor agonist that improved sustained virologic response (SVR) in ENABLE 1 (PEG-2a/ribavirin). ENABLE 2 was a second study to evaluate the ability of eltrombopag to increase platelet counts, providing patients with pre-existing thrombocytopenia the opportunity to initiate PEG-2b and achieve SVR.
Methods: In Part 1, patients with HCV and platelets < 75Gi/L received eltrombopag 25mg, increased to 50, 75, or 100mg daily until platelets reached ≥100Gi/L to enter Part 2. In Part 2, patients eligible for PEG-2b (1.5µg/kg/week) and ribavirin (weight-based dosing) were randomized 2:1 to eltrombopag or placebo. Treatment was administered for 24 weeks or 48 weeks according to genotype. The primary endpoint was SVR.
Results: 805 patients were enrolled, 80% with bridging fibrosis or cirrhosis (FibroSURE™). Median platelets were 59Gi/L at enrollment and 93Gi/L by week 2 of eltrombopag treatment. 759 patients (94%) initiated HCV therapy (eltrombopag, 506; placebo, 253). In Part 2, median platelet counts in the eltrombopag and placebo arms were 136Gi/L vs 140Gi/L at randomization but 105Gi/L vs 51Gi/L at week 4, and > 50Gi/L throughout for 81% vs 23% of patients. Compared with placebo, eltrombopag was associated with improved SVR (19% vs 13%, p=0.0202), fewer antiviral dose reductions (54% vs 73%, p=0.0001), improved early virological response (EVR; 62% vs 41%, p< 0.0001), and end-of-treatment response (38% vs 23%, p< 0.0001). Adverse event (AE) rates were (eltrombopag, placebo): any AE (94%, 93%); serious AE (20%, 15%); events suggestive of decompensation (15%, 8%); thromboembolic events (4%, < 1%), and death (4%, 2%).
Conclusions: Eltrombopag increased and maintained platelet counts throughout PEG-2b/ribavirin treatment in patients who would otherwise be ineligible for antiviral therapy. Eltrombopag treatment was associated with clinically meaningful improvement in SVR, as previously reported with PEG-2a/ribavirin treatment in ENABLE 1. Unlike previously reported in ENABLE 1, there was an increased incidence of thromboembolic complications with eltrombopag treatment, which requires further analysis.
http://mobile.ilcapp.eu/EASL_161/poster_24296/program.aspx
Könnte mir vorstellen, dass jetzt erst mal wieder die Luft raus ist, da für die erhoffte Klarheit zumindest durch das abstract nicht gesorgt wurde.
Auf das Jahr gesehen bleibe ich aber bei meinem Optimismus, da GSK ja bereits angekündigt hat, dass sie die Zulassung beantragen werden.
Background and aims: Thrombocytopenia limits the ability to initiate and maintain peginterferon alfa-2b [PEG-2b]+ribavirin therapy in patients with cirrhosis due to hepatitis C (HCV). PEG-2b is not recommended for patients with platelets < 100Gi /L. Eltrombopag is an oral thrombopoietin receptor agonist that improved sustained virologic response (SVR) in ENABLE 1 (PEG-2a/ribavirin). ENABLE 2 was a second study to evaluate the ability of eltrombopag to increase platelet counts, providing patients with pre-existing thrombocytopenia the opportunity to initiate PEG-2b and achieve SVR.
Methods: In Part 1, patients with HCV and platelets < 75Gi/L received eltrombopag 25mg, increased to 50, 75, or 100mg daily until platelets reached ≥100Gi/L to enter Part 2. In Part 2, patients eligible for PEG-2b (1.5µg/kg/week) and ribavirin (weight-based dosing) were randomized 2:1 to eltrombopag or placebo. Treatment was administered for 24 weeks or 48 weeks according to genotype. The primary endpoint was SVR.
Results: 805 patients were enrolled, 80% with bridging fibrosis or cirrhosis (FibroSURE™). Median platelets were 59Gi/L at enrollment and 93Gi/L by week 2 of eltrombopag treatment. 759 patients (94%) initiated HCV therapy (eltrombopag, 506; placebo, 253). In Part 2, median platelet counts in the eltrombopag and placebo arms were 136Gi/L vs 140Gi/L at randomization but 105Gi/L vs 51Gi/L at week 4, and > 50Gi/L throughout for 81% vs 23% of patients. Compared with placebo, eltrombopag was associated with improved SVR (19% vs 13%, p=0.0202), fewer antiviral dose reductions (54% vs 73%, p=0.0001), improved early virological response (EVR; 62% vs 41%, p< 0.0001), and end-of-treatment response (38% vs 23%, p< 0.0001). Adverse event (AE) rates were (eltrombopag, placebo): any AE (94%, 93%); serious AE (20%, 15%); events suggestive of decompensation (15%, 8%); thromboembolic events (4%, < 1%), and death (4%, 2%).
Conclusions: Eltrombopag increased and maintained platelet counts throughout PEG-2b/ribavirin treatment in patients who would otherwise be ineligible for antiviral therapy. Eltrombopag treatment was associated with clinically meaningful improvement in SVR, as previously reported with PEG-2a/ribavirin treatment in ENABLE 1. Unlike previously reported in ENABLE 1, there was an increased incidence of thromboembolic complications with eltrombopag treatment, which requires further analysis.
http://mobile.ilcapp.eu/EASL_161/poster_24296/program.aspx
Könnte mir vorstellen, dass jetzt erst mal wieder die Luft raus ist, da für die erhoffte Klarheit zumindest durch das abstract nicht gesorgt wurde.
Auf das Jahr gesehen bleibe ich aber bei meinem Optimismus, da GSK ja bereits angekündigt hat, dass sie die Zulassung beantragen werden.
GSK gab heute Zahlen bekannt. Promacta: 44 Mio US $
Ist o.k. nach 39 in Q4 2011. Bei gleichem Wachstum sollten 200 Mio Umsatz in 2012 drin sein.
Ligand bekommt über 100 Mio 6,6 %, über 200 Mio dann 7,5 % Royalties.
In letzter Zeit war Ligand stark unter Druck. Wahrscheinlicher Grund - neben den Shorts beim Bruch der 16er Marke- sind die guten Daten der neueren HEPC Medikamente von z.B. Gilead. Da sie ohne Interferon etc. auskommen, stellen sie den nachhaltigen Nutzen von Promacta in HEP C in Zweifel. Jedoch sind diese Medikamente noch Jahre von einer Zulassung entfernt. Und ob diese dann Promacta gänzlich überflüssig machen glaube ich eher nicht. Zudem sind noch weitere Indikationen für Promacta in der Testung. Hier ist vor allem von Interesse, wie es mit ORT weitergeht...
Ist o.k. nach 39 in Q4 2011. Bei gleichem Wachstum sollten 200 Mio Umsatz in 2012 drin sein.
Ligand bekommt über 100 Mio 6,6 %, über 200 Mio dann 7,5 % Royalties.
In letzter Zeit war Ligand stark unter Druck. Wahrscheinlicher Grund - neben den Shorts beim Bruch der 16er Marke- sind die guten Daten der neueren HEPC Medikamente von z.B. Gilead. Da sie ohne Interferon etc. auskommen, stellen sie den nachhaltigen Nutzen von Promacta in HEP C in Zweifel. Jedoch sind diese Medikamente noch Jahre von einer Zulassung entfernt. Und ob diese dann Promacta gänzlich überflüssig machen glaube ich eher nicht. Zudem sind noch weitere Indikationen für Promacta in der Testung. Hier ist vor allem von Interesse, wie es mit ORT weitergeht...
Ligand gab gestern Zahlen bekannt:
http://finance.yahoo.com/news/ligand-pharmaceuticals-reports…
Was die Zahlen betrifft keine Überraschung - hätte mir aber mehr material sales erhofft. Trotzdem ein kleiner Gewinn - allerdings nicht operativ.
Überraschendes gab es trotzdem:
Positiv: Neue Captisol Programme von:
Merck-Serono (bzw. unkekannt vielleicht auch Auslizensierung)
Vertex (P I)
Und 2 Bigpharma - unbekannt wahrscheinlich Lily und/oder Merck (P I)
Negativ: GSK lässt Promacta in cronic liver disease fallen. Das ist vor allem deshalb bedenklich, weil GSK die Weiterführung von den Daten der HEP C P III abhängig machte. Erklärt auch den Kursverlauf der letzten Woche.
Die Vermutung liegt jetzt natürlich nahe, dass das Sicherheitsprofil (Thrombose) eine Zulassung in CLD unwahrscheinlich macht. Eine P II wurde ja genau deshalb in 2010 gestoppt. Abzuwarten bleit wie es mit der Indikation oncology related thrombocytopaenia weitergeht.
Mal sehen wie es heute weiter geht...
http://finance.yahoo.com/news/ligand-pharmaceuticals-reports…
Was die Zahlen betrifft keine Überraschung - hätte mir aber mehr material sales erhofft. Trotzdem ein kleiner Gewinn - allerdings nicht operativ.
Überraschendes gab es trotzdem:
Positiv: Neue Captisol Programme von:
Merck-Serono (bzw. unkekannt vielleicht auch Auslizensierung)
Vertex (P I)
Und 2 Bigpharma - unbekannt wahrscheinlich Lily und/oder Merck (P I)
Negativ: GSK lässt Promacta in cronic liver disease fallen. Das ist vor allem deshalb bedenklich, weil GSK die Weiterführung von den Daten der HEP C P III abhängig machte. Erklärt auch den Kursverlauf der letzten Woche.
Die Vermutung liegt jetzt natürlich nahe, dass das Sicherheitsprofil (Thrombose) eine Zulassung in CLD unwahrscheinlich macht. Eine P II wurde ja genau deshalb in 2010 gestoppt. Abzuwarten bleit wie es mit der Indikation oncology related thrombocytopaenia weitergeht.
Mal sehen wie es heute weiter geht...
GSK gab heute die SNDA für Promacta bekannt:
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Im Kurs lässt sich diese positive Nachricht nicht erkennen. Enttäuschend!
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Im Kurs lässt sich diese positive Nachricht nicht erkennen. Enttäuschend!
Gute Nachrichten eines Partners von Ligand:
http://www.fiercebiotech.com/story/onyx-clears-big-hurdle-hi…
Mal sehen wie es weitergeht. Ligand bekäme material sales und royalties. Ich denke die royalties sind aber eher gering.
http://www.fiercebiotech.com/story/onyx-clears-big-hurdle-hi…
Mal sehen wie es weitergeht. Ligand bekäme material sales und royalties. Ich denke die royalties sind aber eher gering.
Zulassung von Kyprolis ist da:
http://www.thestreet.com/story/11630615/1/onyxs-kyprolis-can…
Das Schlechte am Guten: Eigentlich sollte die Entscheidung erst nächste woche Freitag kommen. Warum heute schon ist mir schleierhaft. Dadurch könnte Ligand ein runup an die 20$ entgangen sein. Viele die darauf spekuliert haben könnten jetzt verkaufen, um auf den nächsten runup zu spekulieren. Mal sehen wie es weitergeht...
http://www.thestreet.com/story/11630615/1/onyxs-kyprolis-can…
Das Schlechte am Guten: Eigentlich sollte die Entscheidung erst nächste woche Freitag kommen. Warum heute schon ist mir schleierhaft. Dadurch könnte Ligand ein runup an die 20$ entgangen sein. Viele die darauf spekuliert haben könnten jetzt verkaufen, um auf den nächsten runup zu spekulieren. Mal sehen wie es weitergeht...
Ligand hat zur Zeit einen Lauf: GSK gab heute Zahlen bekannt. Umsatz von Promacta lag bei ca. 46 Mio $ im 2. Quartal.
Zudem gab GSK bekannt, dass Promacta priority review in sachen HEP C erhält.
http://www.theflyonthewall.com/permalinks/entry.php/LGND;GSK…
Zudem gab GSK bekannt, dass Promacta priority review in sachen HEP C erhält.
http://www.theflyonthewall.com/permalinks/entry.php/LGND;GSK…
Ligand gab zwischenzeitlich die Royatlies für Kyprolis bekannt:
bis 200 Mio 1,5 bis 250 2%, bis 300 2,5% ab 300 3% + material sales
Weitere Aussichten:
im Oktober/November Quartalszahlen von GSK, Onyx und Ligand
Und vor allem 30.11. Entscheidung der FDA zu Promacta in Hep C
http://www.thestreet.com/story/11668461/2/31-drugs-facing-fd…
bis 200 Mio 1,5 bis 250 2%, bis 300 2,5% ab 300 3% + material sales
Weitere Aussichten:
im Oktober/November Quartalszahlen von GSK, Onyx und Ligand
Und vor allem 30.11. Entscheidung der FDA zu Promacta in Hep C
http://www.thestreet.com/story/11668461/2/31-drugs-facing-fd…
Die SA Artikel sind qualitativ sehr schwankend. Aktuell einer zu Ligand.
Was der Verfasser jedoch verschweigt, ist dass am 30.11 die FDA Entscheidung zu Promacta ansteht. Da finde ich es fragwürdig auf den möglichen Runup zur EMA Entscheidung von Aprela in 2013 zu spekulieren. Trotzdem nicht uninteressant:
http://seekingalpha.com/article/842251-5-pharmaceutical-comp…
Mal sehen, wie sich der Kurs bis zu besagtem Termin entwickelt...
Was der Verfasser jedoch verschweigt, ist dass am 30.11 die FDA Entscheidung zu Promacta ansteht. Da finde ich es fragwürdig auf den möglichen Runup zur EMA Entscheidung von Aprela in 2013 zu spekulieren. Trotzdem nicht uninteressant:
http://seekingalpha.com/article/842251-5-pharmaceutical-comp…
Mal sehen, wie sich der Kurs bis zu besagtem Termin entwickelt...
Heute mal wieder eine Ligand typische Nachricht:
http://finance.yahoo.com/news/ligand-receive-2-million-miles…
Positiv ist natürlich das Fortschreiten von Dinaciclib und der Meilenstein von 2 Mio durch Merck. Darin verpackt aber eine Umstzwarnung für dieses Quartal, da die 2 Mio erst in Q4 verbucht werden können.
Charttechnisch haben die Unterstützungen nicht gehalten. Einzig die Tatsache, dass der Kurs noch über der 200 Tage Linie ist, gibt Anlass zu Optimismus.
Mittelfristig zählt eh vor allem der Termin Ende November...
http://finance.yahoo.com/news/ligand-receive-2-million-miles…
Positiv ist natürlich das Fortschreiten von Dinaciclib und der Meilenstein von 2 Mio durch Merck. Darin verpackt aber eine Umstzwarnung für dieses Quartal, da die 2 Mio erst in Q4 verbucht werden können.
Charttechnisch haben die Unterstützungen nicht gehalten. Einzig die Tatsache, dass der Kurs noch über der 200 Tage Linie ist, gibt Anlass zu Optimismus.
Mittelfristig zählt eh vor allem der Termin Ende November...
Heute wieder Zahlen von GSK: Promacta hat in Q3 55 Mio$ umgesetzt nach 46 in Q2.
Morgen Zahlen von Onyx zu Kyprolis. Dort kann man aber noch keine großen Umsätze erwarten.
Morgen Zahlen von Onyx zu Kyprolis. Dort kann man aber noch keine großen Umsätze erwarten.
Gestern kamen die Zahlen von Onyx: 18,6 Mio im ersten vermarkteten Quartal. Das ist weitaus mehr, als erwartet wurde.
http://www.thestreet.com/story/11755027/1/onyx-initial-kypro…
http://www.thestreet.com/story/11755027/1/onyx-initial-kypro…
Gestern dann die Zahlen von LGND:
http://seekingalpha.com/article/980341-ligand-pharmaceutical…
Die Bedeutung von Kyprolis für LGND wird noch unterschätzt, weil sie ihre Kosten einfach im Griff haben. Alles was jetzt noch an Royalties oben drauf kommt ist dann Gewinn.
Aber jetzt erst mal die Entscheidung der FDA...
http://seekingalpha.com/article/980341-ligand-pharmaceutical…
Die Bedeutung von Kyprolis für LGND wird noch unterschätzt, weil sie ihre Kosten einfach im Griff haben. Alles was jetzt noch an Royalties oben drauf kommt ist dann Gewinn.
Aber jetzt erst mal die Entscheidung der FDA...
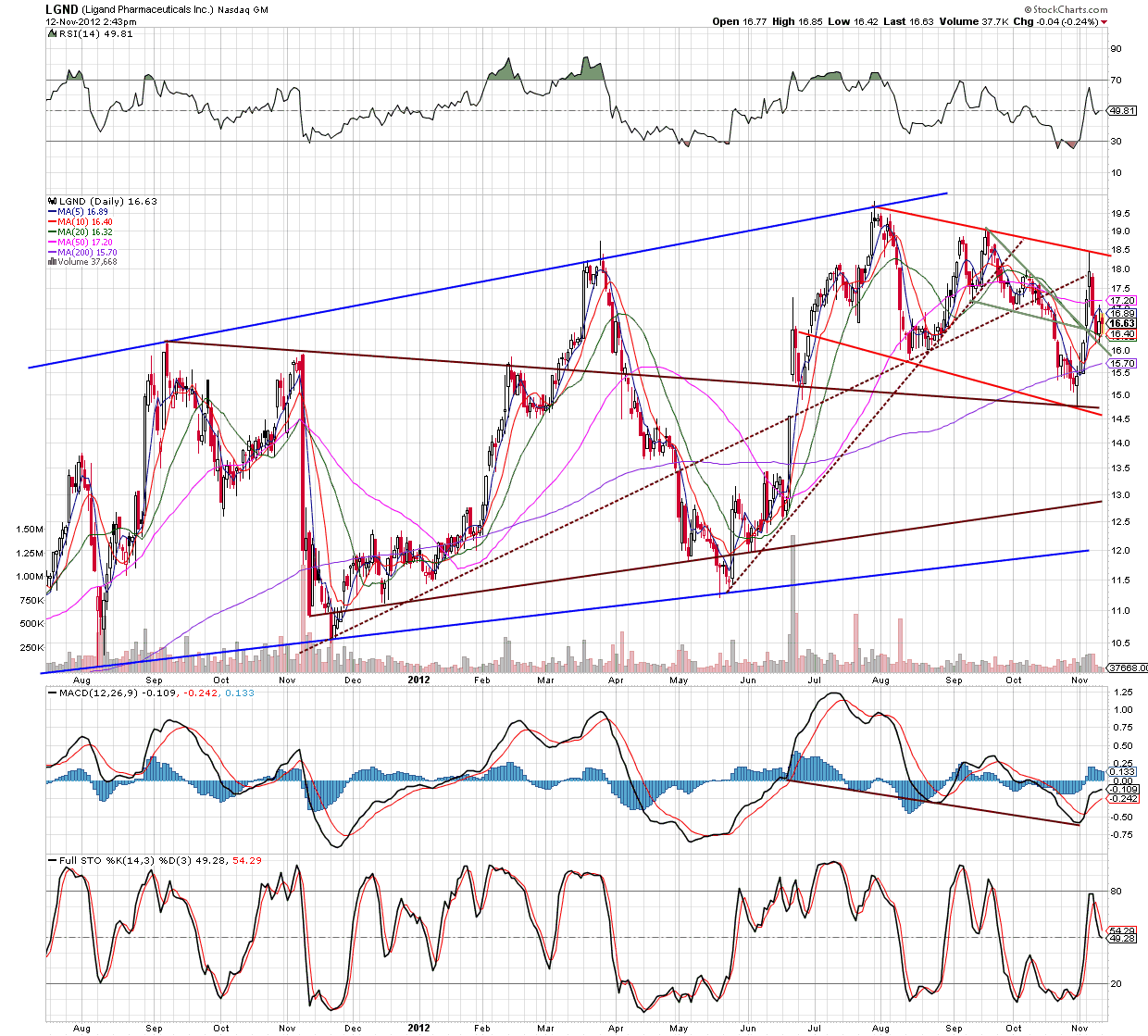
Die Zulassung ist da! 
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Zwar ist die Vermarktungsperspektive aufgrund der neueren entwicklungen im HEP C Bereich unsicher, jedoch darf man nicht vergessen, dass die Zulassung für die schwer erkrankten Patienten gedacht ist, nicht für die Masse. So traue ich Promacta durchaus Umsätze um die 500 Mio zu. Die weitere Entwicklung wird dann insbesondere von den Ergebnissen der zahlreichen Studien bei Krebs abhängen.

http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Zwar ist die Vermarktungsperspektive aufgrund der neueren entwicklungen im HEP C Bereich unsicher, jedoch darf man nicht vergessen, dass die Zulassung für die schwer erkrankten Patienten gedacht ist, nicht für die Masse. So traue ich Promacta durchaus Umsätze um die 500 Mio zu. Die weitere Entwicklung wird dann insbesondere von den Ergebnissen der zahlreichen Studien bei Krebs abhängen.
Habs mir fast gedacht. Anlässlich des heutigen investordays hat Ligand Umsatz und Gewinnziele für 2013 und 14 bekannt gegeben:
Ligand’s financial forecast includes the following:
Revenue in 2013 is projected to be between $41 million and $44 million, and is projected to grow to more than $60 million in 2014, representing a 40% compound annual growth rate from 2012 expected revenue of $30 million to $31 million.
Net income in 2013 is projected to be more than $0.35 per diluted share, and is projected to increase by 200% to more than $1.05 per diluted share in 2014.
Interessant auch, dass Ligand sich ausdrücklich zum Bace Programm von Merck bekennt. Das taucht in der aktuellen Pipeline nicht auf - hat aber absolutes Blockbuster Potenzial. Klar ist das Risiko des Scheiterns aber auch enorm hoch.
Ligand is entitled to royalties on Merck’s lead BACE inhibitor compound for Alzheimer’s disease. Merck has reported single doses are associated with up to a 92% mean reduction of beta amyloid levels from baseline. Merck announced the initiation of a Phase 2/3 clinical trial on December 3rd.
Mehr dazu auch:
http://finance.yahoo.com/news/ligand-present-growth-prospect…" target="_blank" rel="nofollow ugc noopener">http://finance.yahoo.com/news/ligand-present-growth-prospect…
http://www.fiercebiotech.com/story/merck-ignores-red-flags-a…
Ligand’s financial forecast includes the following:
Revenue in 2013 is projected to be between $41 million and $44 million, and is projected to grow to more than $60 million in 2014, representing a 40% compound annual growth rate from 2012 expected revenue of $30 million to $31 million.
Net income in 2013 is projected to be more than $0.35 per diluted share, and is projected to increase by 200% to more than $1.05 per diluted share in 2014.
Interessant auch, dass Ligand sich ausdrücklich zum Bace Programm von Merck bekennt. Das taucht in der aktuellen Pipeline nicht auf - hat aber absolutes Blockbuster Potenzial. Klar ist das Risiko des Scheiterns aber auch enorm hoch.
Ligand is entitled to royalties on Merck’s lead BACE inhibitor compound for Alzheimer’s disease. Merck has reported single doses are associated with up to a 92% mean reduction of beta amyloid levels from baseline. Merck announced the initiation of a Phase 2/3 clinical trial on December 3rd.
Mehr dazu auch:
http://finance.yahoo.com/news/ligand-present-growth-prospect…" target="_blank" rel="nofollow ugc noopener">http://finance.yahoo.com/news/ligand-present-growth-prospect…
http://www.fiercebiotech.com/story/merck-ignores-red-flags-a…
Antwort auf Beitrag Nr.: 43.889.625 von kmastra am 04.12.12 16:11:52(Ohne Fachmann zu sein) hab ich mir mal das letzte Financial Statement angeschaut, irgendwie sieht mir die finanzielle Situation nicht so rosig aus. Gibts dazu Meinungen?
Antwort auf Beitrag Nr.: 43.943.309 von me_2 am 19.12.12 10:48:45Ich nehme an, du meinst die niedrige Cashquote? Ich rechne nicht mit einer Verwässerung, weil Ligand im 4 Quartal definitiv Gewinn macht und von da an auch zumindest Gewinn prognostiziert. Ausschließen kann man natürlich nichts...halte das aber für sehr unwahrscheinlich!
Charttechnisch sieht es ganz gut aus:

Dazu beigetragen hat bestimmt, dass Pfizer dann doch noch die Zulassung für Aprela eingereicht hat. Ligand bekommt aber kaum Royalties, von daher ist das nicht so wichtig.
http://finance.yahoo.com/news/u-food-drug-administration-fda…
Zudem waren wieder einige Insiderkäufe zu beobachten:
http://investor.ligand.com/Investors/SEC-Filings/default.asp…
Dazu beigetragen hat bestimmt, dass Pfizer dann doch noch die Zulassung für Aprela eingereicht hat. Ligand bekommt aber kaum Royalties, von daher ist das nicht so wichtig.
http://finance.yahoo.com/news/u-food-drug-administration-fda…
Zudem waren wieder einige Insiderkäufe zu beobachten:
http://investor.ligand.com/Investors/SEC-Filings/default.asp…
Heute geht es gegen den Trend bergab. Grund ist eine Abstufung:
Cantor Fitzgerald downgraded Ligand Pharma (NASDAQ: LGND) from Buy to Hold with a price target of $23.00 (from $28.00).
The firm comments, "After attending a Hepatitis C lecture and speaking with physicians at the New York Society for Gastrointestinal Endoscopy on December 19 we are lowering our estimates on Promacta in the Hepatitis C (HCV) indication from $337M to $67.5M in 2017. Our reasons are as follows: (1) Physician awareness of Promacta in HCV is minimal a month after its approval and reimbursement is believed to be non-existent; (2) doctors indicated that low platelet levels are not a key reason for keeping very sick HCV patients off interferon treatments; (3) presenters indicated that effective non-interferon treatments are expected to be introduced in the next 2-3 years (which does not allow time for significant Promacta ramp, in our view); and (4) weekly prescription trends are not showing any significant pick-up since approval."
http://www.streetinsider.com/Analyst+PT+Change/Cantor+Fitzge…" target="_blank" rel="nofollow ugc noopener">http://www.streetinsider.com/Analyst+PT+Change/Cantor+Fitzge…
Habe hier einen Teil der Gewinne realisiert, weil es charttechnisch und fundamental momentan eher wackelig ist.
Cantor Fitzgerald downgraded Ligand Pharma (NASDAQ: LGND) from Buy to Hold with a price target of $23.00 (from $28.00).
The firm comments, "After attending a Hepatitis C lecture and speaking with physicians at the New York Society for Gastrointestinal Endoscopy on December 19 we are lowering our estimates on Promacta in the Hepatitis C (HCV) indication from $337M to $67.5M in 2017. Our reasons are as follows: (1) Physician awareness of Promacta in HCV is minimal a month after its approval and reimbursement is believed to be non-existent; (2) doctors indicated that low platelet levels are not a key reason for keeping very sick HCV patients off interferon treatments; (3) presenters indicated that effective non-interferon treatments are expected to be introduced in the next 2-3 years (which does not allow time for significant Promacta ramp, in our view); and (4) weekly prescription trends are not showing any significant pick-up since approval."
http://www.streetinsider.com/Analyst+PT+Change/Cantor+Fitzge…" target="_blank" rel="nofollow ugc noopener">http://www.streetinsider.com/Analyst+PT+Change/Cantor+Fitzge…
Habe hier einen Teil der Gewinne realisiert, weil es charttechnisch und fundamental momentan eher wackelig ist.
Onyx gab gestern sehr gute Zahlen zu Kyprolis bekannt - 43,4 Mio in Q4.
http://www.thestreet.com/story/11804993/1/onyx-pharma-kyprol…" target="_blank" rel="nofollow ugc noopener">http://www.thestreet.com/story/11804993/1/onyx-pharma-kyprol…
Ligand bekommt zwar nur wenig Royalties, jedoch sind die Aussichten sehr gut.
Zur Erinnerung:
First, could you please provide some details on your royalty agreement for carfilzomib with Ligand?
"We have, in connection with our purchase of Captisol from Ligand, Captisol is a component of the Kyprolis product, a royalty obligation to Ligand which is tied to global net sales of Kyprolis. Those royalty obligations range from 1.5%, which is the starting rate, up to a highest rate of 3% of global Kyprolis net sales. That top 3% royalty rate is triggered at sales levels over $750 million, and the royalty rate steps up between 1.5% and 3% with increasing levels of sales [note the intermediate thresholds are $250m and$500m, with royalties increasing by 0.5% each time]
http://www.thestreet.com/story/11804993/1/onyx-pharma-kyprol…" target="_blank" rel="nofollow ugc noopener">http://www.thestreet.com/story/11804993/1/onyx-pharma-kyprol…
Ligand bekommt zwar nur wenig Royalties, jedoch sind die Aussichten sehr gut.
Zur Erinnerung:
First, could you please provide some details on your royalty agreement for carfilzomib with Ligand?
"We have, in connection with our purchase of Captisol from Ligand, Captisol is a component of the Kyprolis product, a royalty obligation to Ligand which is tied to global net sales of Kyprolis. Those royalty obligations range from 1.5%, which is the starting rate, up to a highest rate of 3% of global Kyprolis net sales. That top 3% royalty rate is triggered at sales levels over $750 million, and the royalty rate steps up between 1.5% and 3% with increasing levels of sales [note the intermediate thresholds are $250m and$500m, with royalties increasing by 0.5% each time]
Heue Zahlen von GSK: Umsatz von 62 Mio US$ in Q4 für Promacta fürs Jahr über 200 Mio.
http://www.gsk.com/investors/quarterly-results.html
http://www.gsk.com/investors/quarterly-results.html
Gestern dann die Zahlen von LGND:
http://finance.yahoo.com/news/ligand-reports-fourth-quarter-…
Zahlen waren zwar gar nicht so gut aber ich denke die Prognose für 2013 kommt gut an.
http://finance.yahoo.com/news/ligand-reports-fourth-quarter-…
Zahlen waren zwar gar nicht so gut aber ich denke die Prognose für 2013 kommt gut an.
Eine aktuelle Studie sieht ein Kursziel von 30$:
http://www.griffinsecurities.com/upload/reports/Griffin_LGND…
http://www.griffinsecurities.com/upload/reports/Griffin_LGND…
Ligand hat Melphalan nun doch auslizensiert und zwar an Spectrum. Vor allem auch noch die Guidance für 2012 erhöht. Kommt natürlich gut so was:
http://finance.yahoo.com/news/ligand-signs-global-license-ag…
Positiv ist zu sehen, dass Spectrum bewiesen hat, dass sie vermarkten können.
Ebenso spart Ligand nun Geld, da die P III nun von Spectrum finanziert wird.
Mau finde ich die 3 Millionen Upfront, wobei leider die Höhe der Royalties nicht gemeldet wurde. Die sollten aber deutlich im zweistelligen Prozentbereich liegen.
http://finance.yahoo.com/news/ligand-signs-global-license-ag…
Positiv ist zu sehen, dass Spectrum bewiesen hat, dass sie vermarkten können.
Ebenso spart Ligand nun Geld, da die P III nun von Spectrum finanziert wird.
Mau finde ich die 3 Millionen Upfront, wobei leider die Höhe der Royalties nicht gemeldet wurde. Die sollten aber deutlich im zweistelligen Prozentbereich liegen.
Ein Programm das dieses Jahr noch sehr stark in den Fokus der Anleger rücken könnte ist das BACE Programm von Merck. Aufgrund der starken Ausbreitung und der limitierten Behandlungsoptionen scheint die FDA hier die "Ansprüche" gesenkt zu haben und insbesondere die Prävention fördern zu wollen.
http://www.nytimes.com/2013/03/14/health/fda-to-ease-alzheim…
Mercks Bace Programm hat genau hier seine Stärke und hat die P II/III bereits gestartet:
http://www.forbes.com/sites/edsilverman/2012/12/03/merck-mak…
Logischerweise hat jedes Programm in der Indikation absolutes Megablockbuster Potenzial. Die Chance des Scheiterns ist aber auch entsprechend hoch, auch wenn die PI vielversprechend war. Bin auf jeden Fall gespannt auf die PII Ergebnisse...
http://www.nytimes.com/2013/03/14/health/fda-to-ease-alzheim…
Mercks Bace Programm hat genau hier seine Stärke und hat die P II/III bereits gestartet:
http://www.forbes.com/sites/edsilverman/2012/12/03/merck-mak…
Logischerweise hat jedes Programm in der Indikation absolutes Megablockbuster Potenzial. Die Chance des Scheiterns ist aber auch entsprechend hoch, auch wenn die PI vielversprechend war. Bin auf jeden Fall gespannt auf die PII Ergebnisse...
Kyprolis hat sicherlich die besten Aussichten in Ligands Portfolio. Zwar reichen die Royalties nur von 1,5-3% jedoch ist Kyprolis sicher eines der heißesten Neuzulassungen der letzten Jahre. Die Einführung war auf jeden Fall über allen Erwartungen gut. Fantasie liegt nun letztlich in einer Erweiterung der Zulassung als Erst- oder Zweitlinien Option und natürlich der weltweiten Einführung. Es ist eigentlich Konsens, dass die Chancen auf Zulassung in Europa und auch eine Labelerweiterung ziemlich gut sind. Da laufen momentan einige Studien - auch ein direkter Vergleich zum Standardmedikament.
Sehr ausführlich und wie immer bei diesem Autor fundiert hier beschrieben:
http://www.orf-blog.com/onyx-a-must-own-biotech-for-2013/
Ebenso hier:
http://seekingalpha.com/article/1288831-onyx-pharmaceuticals…
Würde das bluskyszenario also Erstlinientherapie, weltweit zugelassen Realität, würden die Umsätze sicherlich im Blockbusterbereich ankommen.
Bei 2 Milliarden würden bei LGND so um die 50 Mio Royalties + Material Sales hängen bleiben. Da LGND - wie zuletzt durch den Spectrumdeal untermauert - seine Kosten konstant auf niedrigem Niveau halten will und die Gewinnzone durch Promacta erreicht hat, würden diese voll auf die Gewinnseite schlagen.
Sehr ausführlich und wie immer bei diesem Autor fundiert hier beschrieben:
http://www.orf-blog.com/onyx-a-must-own-biotech-for-2013/
Ebenso hier:
http://seekingalpha.com/article/1288831-onyx-pharmaceuticals…
Würde das bluskyszenario also Erstlinientherapie, weltweit zugelassen Realität, würden die Umsätze sicherlich im Blockbusterbereich ankommen.
Bei 2 Milliarden würden bei LGND so um die 50 Mio Royalties + Material Sales hängen bleiben. Da LGND - wie zuletzt durch den Spectrumdeal untermauert - seine Kosten konstant auf niedrigem Niveau halten will und die Gewinnzone durch Promacta erreicht hat, würden diese voll auf die Gewinnseite schlagen.
Charttechnisch ist der Ausbruch gelungen:

Liebes Tagebuch,
die nächsten Termine:
24.04. GSK Qartalsbericht
07.05. Onyx Quartalsbericht
Bald darauf Ligand Quartalsbericht
03.10. PDUFA Aprela - Pfizer
2-4 Q: Mehrere P II Ergebnisse von Promacta in diversen Krebsindikationen - GSK
3/4 Q: P III Ergebnisse von Kyprolis - Onyx
4 Q: PII Daten vom BACE Programm - Merck
4 Q: P III Daten von Melphalan - Spectrum
Dazu noch weitere mögliche Studienergebnisse und Zulassunganträge.
Eine Graphik aus der letzten Präsentation zeigt das langfristige Potenzial: http://investor.ligand.com/files/doc_presentations/LigandRot…

die nächsten Termine:
24.04. GSK Qartalsbericht
07.05. Onyx Quartalsbericht
Bald darauf Ligand Quartalsbericht
03.10. PDUFA Aprela - Pfizer
2-4 Q: Mehrere P II Ergebnisse von Promacta in diversen Krebsindikationen - GSK
3/4 Q: P III Ergebnisse von Kyprolis - Onyx
4 Q: PII Daten vom BACE Programm - Merck
4 Q: P III Daten von Melphalan - Spectrum
Dazu noch weitere mögliche Studienergebnisse und Zulassunganträge.
Eine Graphik aus der letzten Präsentation zeigt das langfristige Potenzial: http://investor.ligand.com/files/doc_presentations/LigandRot…

Grund für den gestrigen Kurssprung:
Analysts at Roth Capital upped their price target on shares of Ligand Pharmaceutica (NASDAQ: LGND) from $31.00 to $51.00 in a research report issued to clients and investors on Friday,
http://www.mideasttime.com/ligand-pharmaceutica-pt-raised-to…
Analysts at Roth Capital upped their price target on shares of Ligand Pharmaceutica (NASDAQ: LGND) from $31.00 to $51.00 in a research report issued to clients and investors on Friday,
http://www.mideasttime.com/ligand-pharmaceutica-pt-raised-to…
Heute die Zahlen von GSK: Promacta Umsatz sind 61 Mio - das sind zwar 45% mehr als im letzten Jahr aber kaum mehr als im letzten Quartal.
Dies ist das erste Quartal, in dem Promacta in den USA die Zulassung für HepC hatte - von daher ist das geringe Wachstum für mich enttäuschend.
http://www.gsk.com/content/dam/gsk/globals/documents/pdf/Inv…
Dies ist das erste Quartal, in dem Promacta in den USA die Zulassung für HepC hatte - von daher ist das geringe Wachstum für mich enttäuschend.
http://www.gsk.com/content/dam/gsk/globals/documents/pdf/Inv…
Ligand hat sein Portfolio heute erweitert. Unklar bleibt aber, wie aussichtsreich die Kandidaten sind. Bei dem Preis wird wohl kaum ein blockbuster dabei sein. Trotzdem: Ligand hat jetzt 85 voll von Partnern finanzierte Kandidaten in seiner Pipeline.
http://finance.yahoo.com/news/ligand-acquires-financial-righ…
http://finance.yahoo.com/news/ligand-acquires-financial-righ…
Erst die Zahlen von Kyprolis - 64 Mio:
http://finance.yahoo.com/news/ligand-reports-first-quarter-f…
Dann noch sehr solide Zahlen von Ligand:
11,7 Mio Umsatz mit 1,5 mio Gewinn. Die Royalties konnten um 100% zum Vorjahr zulegen. Dazu die Ankündigung eines Aktienrückkaufprogramms ( )
)
Interessant auch, dass SARM im CC auwieder rausgekramt wurde. Vielleicht gibt es ja vielversprechende Verhandlungen?
http://finance.yahoo.com/news/ligand-reports-first-quarter-f…
Negativ muss erwähnt werden, dass Onyx eine orale Version von Kyprolis in PII bringt. Ligand bekäme hier keinerlei Royalties.
http://finance.yahoo.com/news/ligand-reports-first-quarter-f…
Dann noch sehr solide Zahlen von Ligand:
11,7 Mio Umsatz mit 1,5 mio Gewinn. Die Royalties konnten um 100% zum Vorjahr zulegen. Dazu die Ankündigung eines Aktienrückkaufprogramms (
 )
)Interessant auch, dass SARM im CC auwieder rausgekramt wurde. Vielleicht gibt es ja vielversprechende Verhandlungen?
http://finance.yahoo.com/news/ligand-reports-first-quarter-f…
Negativ muss erwähnt werden, dass Onyx eine orale Version von Kyprolis in PII bringt. Ligand bekäme hier keinerlei Royalties.
Ligand hat anlässlich der Präsentation bei der Konferenz der Deutschen Bank am 29. seine Präsentation überarbeitet. Scheinbar kam die gut an.
http://www.ligand.com/~ligand/upload/File/v2%20Ligand%20DB%2…
Ligand stellt sein auf Royaltys basierendes Geschäftsmodell darin stark in den Vordergrund. Da die Kosten auf konstant niedrigem Niveau gehalten werden, und die derzeitigen Royalties alleine von Promacta ausreichen, um eine schwarze Null zu schreiben, geht von nun an alles darüber hinaus mehr oder weniger voll auf die Gewinnseite.
Neben den Wachstumsaussichten insbesondere bei Promacta und Kyprolis könnten theoretisch bis 2017 11 weitere voll durch Partner finanzierte Produkte auf den Markt kommen. In den von Ligand veröffentlichten Diagrammen (s. Vorposting) werden diese noch gar nicht berücksichtigt.
Natürlich haben nicht alle hohes Potenzial und auch nicht alle werden es durch die Zulasung schaffen.
Besonders gut gefällt mir der Spectrum Deal mit Melphalan. Da hier von significant double-digit Royalties die Rede ist, gehe ich mal von durchschnittlich 20% aus. Das wären bei 50 Mio Umsatz dann schon 10 Mio mehr an Royalties= 0,5 $ mehr Gewinn pro Aktie.
Spectrum selber hat auf der Konferenz auch präsentiert und sich auch zu den Vorteilen der Captisol Form gegenüber dem herkömlichen geäußert:
"Second key catalyst we'll have is Captisol-enabled melphalan. This is a product that we purchased from Ligand just a few months ago. The pivotal study's ongoing, and this is a very short pivotal study. It's only 60 patients. The study's enrolling very, very well. We expect that this study will be fully enrolled by the end of this year. And we'll file our second NDA for Captisol-enabled melphalan sometime next year."
"After the study is complete, if successful, it will be the first agent approved as a conditioning chemotherapy regimen for patients going under transplant for multiple myeloma. Today, the challenges the doctors have with myeloma is it's a very unstable molecule or product. Literally, once melphalan is mixed, it has to be given to the patient and infused within 30 minutes. Every minute after 30 minutes, it begins to degrade.
And so that does 2 things: One, it's logistically very difficult for accounts to administer melphalan because of that. Second, and big picture, much more important, is because of the limitation in infusion time, doctors could never explore the ability to give longer infusion durations of melphalan and potentially end up with a more effective drug. Couldn't do it with the existing formulations of melphalan. Captisol-enabled melphalan, once it's mixed, is actually stable for 24 hours. So it's easier for people to use it, and it dramatically extends the infusion time that doctors can look at.
The third benefit of Captisol-enabled melphalan is the fact that it does not contain propylene glycol. Propylene glycol is, in the current formulations of melphalan, it is known to increase the risk of both cardiac and renal toxicities. You do not have that fear with our version of melphalan.
This 60-patient study will be fully enrolled this year and we'll file it next year."
http://seekingalpha.com/article/1472461-spectrum-pharmaceuti…
http://www.ligand.com/~ligand/upload/File/v2%20Ligand%20DB%2…
Ligand stellt sein auf Royaltys basierendes Geschäftsmodell darin stark in den Vordergrund. Da die Kosten auf konstant niedrigem Niveau gehalten werden, und die derzeitigen Royalties alleine von Promacta ausreichen, um eine schwarze Null zu schreiben, geht von nun an alles darüber hinaus mehr oder weniger voll auf die Gewinnseite.
Neben den Wachstumsaussichten insbesondere bei Promacta und Kyprolis könnten theoretisch bis 2017 11 weitere voll durch Partner finanzierte Produkte auf den Markt kommen. In den von Ligand veröffentlichten Diagrammen (s. Vorposting) werden diese noch gar nicht berücksichtigt.
Natürlich haben nicht alle hohes Potenzial und auch nicht alle werden es durch die Zulasung schaffen.
Besonders gut gefällt mir der Spectrum Deal mit Melphalan. Da hier von significant double-digit Royalties die Rede ist, gehe ich mal von durchschnittlich 20% aus. Das wären bei 50 Mio Umsatz dann schon 10 Mio mehr an Royalties= 0,5 $ mehr Gewinn pro Aktie.
Spectrum selber hat auf der Konferenz auch präsentiert und sich auch zu den Vorteilen der Captisol Form gegenüber dem herkömlichen geäußert:
"Second key catalyst we'll have is Captisol-enabled melphalan. This is a product that we purchased from Ligand just a few months ago. The pivotal study's ongoing, and this is a very short pivotal study. It's only 60 patients. The study's enrolling very, very well. We expect that this study will be fully enrolled by the end of this year. And we'll file our second NDA for Captisol-enabled melphalan sometime next year."
"After the study is complete, if successful, it will be the first agent approved as a conditioning chemotherapy regimen for patients going under transplant for multiple myeloma. Today, the challenges the doctors have with myeloma is it's a very unstable molecule or product. Literally, once melphalan is mixed, it has to be given to the patient and infused within 30 minutes. Every minute after 30 minutes, it begins to degrade.
And so that does 2 things: One, it's logistically very difficult for accounts to administer melphalan because of that. Second, and big picture, much more important, is because of the limitation in infusion time, doctors could never explore the ability to give longer infusion durations of melphalan and potentially end up with a more effective drug. Couldn't do it with the existing formulations of melphalan. Captisol-enabled melphalan, once it's mixed, is actually stable for 24 hours. So it's easier for people to use it, and it dramatically extends the infusion time that doctors can look at.
The third benefit of Captisol-enabled melphalan is the fact that it does not contain propylene glycol. Propylene glycol is, in the current formulations of melphalan, it is known to increase the risk of both cardiac and renal toxicities. You do not have that fear with our version of melphalan.
This 60-patient study will be fully enrolled this year and we'll file it next year."
http://seekingalpha.com/article/1472461-spectrum-pharmaceuti…
Bei Ligand wurden die letzten tage massiv viele Aktien gehandelt. Heute z.B. fast 10x so viele wie normal.
Hier noch einige Folien aus der heutigen Präsentation:


http://wsw.com/webcast/jeff77/lgnd/
Hier noch einige Folien aus der heutigen Präsentation:
http://wsw.com/webcast/jeff77/lgnd/
Ein Konkurrenzprodukt von Mercks/Ligands BACE - Programm ist gescheitert- gut und schlecht zugleich für Ligand:
In yet another indication of the yawning gap between what drug developers know about Alzheimer's and how it could be treated, Eli Lilly ($LLY) today decided to scrap its Phase II study for a BACE inhibitor after gathering abnormal liver tests from patients.
"LLY and another company, Merck, have been racing to take their respective BACE inhibitors through development and have been neck-and-neck in terms of timelines," notes Bernstein's Tim Anderson today. "Both compounds have been working their way through brief phase 2 studies, with large and long phase 3 studies likely starting in the late 2013/early 2014 timeframe. LLY's is now out of the race, leaving MRK's compound as the survivor and investors will naturally wonder whether this new news heralds a problem with all BACE inhibitors or whether it was specific just to LLY's lead candidate. There had been some rumbling in the drug industry about LLY's compound potentially having a safety issue, which led to them choosing a lower dose of drug that could have explained the slightly weaker level of beta-amyloid lowering compared to Merck's compound. We asked LLY directly about this at one point, and they denied knowing of any safety issues."
http://www.fiercebiotech.com/story/eli-lilly-racks-another-a…
Wie gesagt ist hier das Riskio des Scheiterns wirklich ernorm groß. Neben den Problemen bei der Sicherheit bleibt natürlich noch die Frage nach der Wirksamkeit, an denen ja schon so manches Programm gescheitert ist.
Da Merck es ja bei moderaten Anzeichen von Alzheimer testet ist die Sicherheitsfrage nicht zu unterschätzen, da es ja über einen langen Zeitraum genommen worden werden soll.
Positiv ist zu vermerken, dass sich Merck selber auf dem letztzen CC sehr optimistisch über das BACE Programm geäußert hat:
"Our BACE inhibitor for Alzheimer's, which is in phase 2/3 and as you know, Alzheimer's is a disease that is going to have significant impact on our population. If you look in through the Alzheimer's Society, it costs the U.S. population about $200 billion right now. If we don’t have a disease modifying agent that number should go through $1 trillion in the year 2050. So its very important to have important therapeutic in that area."
Is there anything else? If you were to pick one or two other drugs in your Phase 2 or Phase 3 pipeline that you want to call special attention to that you think we will be generally excited about?
One that I am really excited about, although it is still very early days, is the BACE inhibitor for Alzheimer's. I think most people think that we are studying the most prominent, useful hypothesis around Alzheimer's development. We have a product that gets 90% receptor occupancy against the target. We are going to be able to test the data hypothesis in a robust way. It is one of these opportunities that really reflects why, at some point in this business, you have to be going for game changing therapies....
There is risk in this business, certainly. Everything can't be a swing for the fences opportunity. But sprinkled into your portfolio has to be some opportunity that can have a profound effect on health and therefore profound effect on Merck. BACE is one of those programs, frankly. So I would point to that as an example of the kind of thing that actually makes me very excited. The early data that we have produce on that really is very encouraging....
I think I wouldn’t go so far to say that we are all banking on it being the transformation of Merck. We are very cautiously data driven organization. We know that we are studying a compound and we are also trying to prove a fundamental hypothesis at the same time. So that makes you really try to be reserved a little bit. But I have got to tell you, behind all of those intellectual comments, is a very visceral excitement that this could be the kind of compound that changes the world...
We think we have a great compound. We think it is targeted at the right target. It has great, again, affinity for the target. I think it allows us to test whether or not that hypothesis is really the right basis for understanding what causes the disease progression. We are studying it now in mild to moderate, the intended study in prodromal or the pre-Alzheimer's population. I think this is the opportunity again for the fundamental transformation in the field.
I also want you to know that that’s the first of several programs that are aimed at Alzheimer's. We have earlier stage programs. It is just like the first hypertension drugs led in to an era of additional discovery for hypertension. I think we are on the verge of things. So in other words, we are out of time. That’s what really makes me excited about this business, Tim, is that you can go to a fallow period and then the science lines up to give you real great opportunities and application.
I think we are on the verge of that. I think the paths are hard in terms of things like Alzheimer's. I think that the tools are better and my job as CEO of Merck, is to make sure that Merck is positioned in terms of having access to the right program, the right tools, the right leadership and the right talent to be a company that can continue to succeed over the longer term as it has. If you look at 60 years past, you look at Merck has been a positive outlier when it comes to innovation. My job is to set it up to be that in the future...
Timeline?
We have safety analysis due this year for about 200 patients. So we are not talking about a filing next year but we are talking about a filing in the next few years if the data is there. So that’s a good thing."
http://www.biotechduediligence.com/1/post/2013/06/lgnd-recen…
Ein Erfolg würde mich hier eher überraschen. Merck wird nach den Daten zur Sicherheit entscheiden, ob eine P III zur Wirksamkeit Sinn macht.
Alles in allem zeigt sich hier aber die Stärke von LGNDs Geschäftsmodell. Ligand hat null Risko, keine Kosten und würde bei einem Erfolg signifikant profitieren. Dann wäre das hier wirlich der Turaround vor dem Herren...
In yet another indication of the yawning gap between what drug developers know about Alzheimer's and how it could be treated, Eli Lilly ($LLY) today decided to scrap its Phase II study for a BACE inhibitor after gathering abnormal liver tests from patients.
"LLY and another company, Merck, have been racing to take their respective BACE inhibitors through development and have been neck-and-neck in terms of timelines," notes Bernstein's Tim Anderson today. "Both compounds have been working their way through brief phase 2 studies, with large and long phase 3 studies likely starting in the late 2013/early 2014 timeframe. LLY's is now out of the race, leaving MRK's compound as the survivor and investors will naturally wonder whether this new news heralds a problem with all BACE inhibitors or whether it was specific just to LLY's lead candidate. There had been some rumbling in the drug industry about LLY's compound potentially having a safety issue, which led to them choosing a lower dose of drug that could have explained the slightly weaker level of beta-amyloid lowering compared to Merck's compound. We asked LLY directly about this at one point, and they denied knowing of any safety issues."
http://www.fiercebiotech.com/story/eli-lilly-racks-another-a…
Wie gesagt ist hier das Riskio des Scheiterns wirklich ernorm groß. Neben den Problemen bei der Sicherheit bleibt natürlich noch die Frage nach der Wirksamkeit, an denen ja schon so manches Programm gescheitert ist.
Da Merck es ja bei moderaten Anzeichen von Alzheimer testet ist die Sicherheitsfrage nicht zu unterschätzen, da es ja über einen langen Zeitraum genommen worden werden soll.
Positiv ist zu vermerken, dass sich Merck selber auf dem letztzen CC sehr optimistisch über das BACE Programm geäußert hat:
"Our BACE inhibitor for Alzheimer's, which is in phase 2/3 and as you know, Alzheimer's is a disease that is going to have significant impact on our population. If you look in through the Alzheimer's Society, it costs the U.S. population about $200 billion right now. If we don’t have a disease modifying agent that number should go through $1 trillion in the year 2050. So its very important to have important therapeutic in that area."
Is there anything else? If you were to pick one or two other drugs in your Phase 2 or Phase 3 pipeline that you want to call special attention to that you think we will be generally excited about?
One that I am really excited about, although it is still very early days, is the BACE inhibitor for Alzheimer's. I think most people think that we are studying the most prominent, useful hypothesis around Alzheimer's development. We have a product that gets 90% receptor occupancy against the target. We are going to be able to test the data hypothesis in a robust way. It is one of these opportunities that really reflects why, at some point in this business, you have to be going for game changing therapies....
There is risk in this business, certainly. Everything can't be a swing for the fences opportunity. But sprinkled into your portfolio has to be some opportunity that can have a profound effect on health and therefore profound effect on Merck. BACE is one of those programs, frankly. So I would point to that as an example of the kind of thing that actually makes me very excited. The early data that we have produce on that really is very encouraging....
I think I wouldn’t go so far to say that we are all banking on it being the transformation of Merck. We are very cautiously data driven organization. We know that we are studying a compound and we are also trying to prove a fundamental hypothesis at the same time. So that makes you really try to be reserved a little bit. But I have got to tell you, behind all of those intellectual comments, is a very visceral excitement that this could be the kind of compound that changes the world...
We think we have a great compound. We think it is targeted at the right target. It has great, again, affinity for the target. I think it allows us to test whether or not that hypothesis is really the right basis for understanding what causes the disease progression. We are studying it now in mild to moderate, the intended study in prodromal or the pre-Alzheimer's population. I think this is the opportunity again for the fundamental transformation in the field.
I also want you to know that that’s the first of several programs that are aimed at Alzheimer's. We have earlier stage programs. It is just like the first hypertension drugs led in to an era of additional discovery for hypertension. I think we are on the verge of things. So in other words, we are out of time. That’s what really makes me excited about this business, Tim, is that you can go to a fallow period and then the science lines up to give you real great opportunities and application.
I think we are on the verge of that. I think the paths are hard in terms of things like Alzheimer's. I think that the tools are better and my job as CEO of Merck, is to make sure that Merck is positioned in terms of having access to the right program, the right tools, the right leadership and the right talent to be a company that can continue to succeed over the longer term as it has. If you look at 60 years past, you look at Merck has been a positive outlier when it comes to innovation. My job is to set it up to be that in the future...
Timeline?
We have safety analysis due this year for about 200 patients. So we are not talking about a filing next year but we are talking about a filing in the next few years if the data is there. So that’s a good thing."
http://www.biotechduediligence.com/1/post/2013/06/lgnd-recen…
Ein Erfolg würde mich hier eher überraschen. Merck wird nach den Daten zur Sicherheit entscheiden, ob eine P III zur Wirksamkeit Sinn macht.
Alles in allem zeigt sich hier aber die Stärke von LGNDs Geschäftsmodell. Ligand hat null Risko, keine Kosten und würde bei einem Erfolg signifikant profitieren. Dann wäre das hier wirlich der Turaround vor dem Herren...
Dem kann ich nur zustimmen:
Be it efficacy or safety, Eli Lilly (NYSE: LLY ) just can't win with its Alzheimer's disease program .
The latest drug to bite the dust is LY2886721, a beta secretase, or BACE, inhibitor. Eli Lilly stopped a phase 2 trial after some patients had abnormal liver biochemical tests. Companies routinely run liver tests on clinical trial patients because it's one of the most common safety issues that affect drugs. The liver's job, after all, is to filter toxins out of the blood stream.
Lilly told the Wall Street Journal that it doesn't believe the liver toxicity has to do with the mechanism of inhibiting BACE and is most likely an off-target effect. That's good news for Merck (NYSE: MRK ) , which has its own BACE inhibitor, MK-8931. The company has already moved the drug into a phase 2/3 trial. If there is an issue, it'll likely be discovered in the phase 2 portion that's enrolling 200 patients.
Assuming there's no class effect, LY2886721's demise is good news for Merck as long as there's no class effect. Merck had a lead, but it wasn't enough to make a difference commercially. It's also good news for AstraZeneca (NYSE: AZN ) , which has a BACE inhibitor, AZD3293, licensed from Astex Pharmaceuticals (NASDAQ: ASTX ) , that entered a phase 1 trial last December .
Assuming, of course, that the drug works. It's not clear yet if targeting BACE will slow or reduce the symptoms of Alzheimer's disease. In a phase 1 trial, MK-8931 reduced the amount of beta-amyloid in cerebral spinal fluid by more than 90%, but it isn't known whether that will reduce the amyloid plaques seen in Alzheimer's patients' brains, and, even if it does reduce the plaque formation, whether that will have a clinical effect.
Failures abound
Rather than because of safety, most Alzheimer's disease drug failures -- and there have been a lot of them -- have fallen short because of lack of efficacy.
Eli Lilly's solanezumab failed a couple of trials last year. The company is retesting the drug in a different population. I wouldn't hold my breath.
And there was Pfizer, Johnson & Johnson, and Elan (NYSE: ELN ) that proved that having more companies developing a drug doesn't make it any more likely to succeed. The company's Alzheimer's disease drug bapineuzumab failed four different clinical trials last year.
And I could go on. But let's not. It's depressing.
Give up?
I doubt companies are going to throw in the towel. As hard as it's been to develop a successful Alzheimer's drug, the rewards are great enough to justify the failures. From a company's perspective, even drugs that have a low likelihood of succeeding, like solanezumab, are probably worth rolling the dice on.
Investors, on the other hand, would be best off not assigning any value to Alzheimer's disease pipeline drugs. If a company does finally figure out the magical formula, investors can benefit from the unexpected pop.
http://www.fool.com/investing/general/2013/06/15/another-alz…
Btw: Wer LGND mag sollte sich auch ASTX mal ansehen.
Be it efficacy or safety, Eli Lilly (NYSE: LLY ) just can't win with its Alzheimer's disease program .
The latest drug to bite the dust is LY2886721, a beta secretase, or BACE, inhibitor. Eli Lilly stopped a phase 2 trial after some patients had abnormal liver biochemical tests. Companies routinely run liver tests on clinical trial patients because it's one of the most common safety issues that affect drugs. The liver's job, after all, is to filter toxins out of the blood stream.
Lilly told the Wall Street Journal that it doesn't believe the liver toxicity has to do with the mechanism of inhibiting BACE and is most likely an off-target effect. That's good news for Merck (NYSE: MRK ) , which has its own BACE inhibitor, MK-8931. The company has already moved the drug into a phase 2/3 trial. If there is an issue, it'll likely be discovered in the phase 2 portion that's enrolling 200 patients.
Assuming there's no class effect, LY2886721's demise is good news for Merck as long as there's no class effect. Merck had a lead, but it wasn't enough to make a difference commercially. It's also good news for AstraZeneca (NYSE: AZN ) , which has a BACE inhibitor, AZD3293, licensed from Astex Pharmaceuticals (NASDAQ: ASTX ) , that entered a phase 1 trial last December .
Assuming, of course, that the drug works. It's not clear yet if targeting BACE will slow or reduce the symptoms of Alzheimer's disease. In a phase 1 trial, MK-8931 reduced the amount of beta-amyloid in cerebral spinal fluid by more than 90%, but it isn't known whether that will reduce the amyloid plaques seen in Alzheimer's patients' brains, and, even if it does reduce the plaque formation, whether that will have a clinical effect.
Failures abound
Rather than because of safety, most Alzheimer's disease drug failures -- and there have been a lot of them -- have fallen short because of lack of efficacy.
Eli Lilly's solanezumab failed a couple of trials last year. The company is retesting the drug in a different population. I wouldn't hold my breath.
And there was Pfizer, Johnson & Johnson, and Elan (NYSE: ELN ) that proved that having more companies developing a drug doesn't make it any more likely to succeed. The company's Alzheimer's disease drug bapineuzumab failed four different clinical trials last year.
And I could go on. But let's not. It's depressing.
Give up?
I doubt companies are going to throw in the towel. As hard as it's been to develop a successful Alzheimer's drug, the rewards are great enough to justify the failures. From a company's perspective, even drugs that have a low likelihood of succeeding, like solanezumab, are probably worth rolling the dice on.
Investors, on the other hand, would be best off not assigning any value to Alzheimer's disease pipeline drugs. If a company does finally figure out the magical formula, investors can benefit from the unexpected pop.
http://www.fool.com/investing/general/2013/06/15/another-alz…
Btw: Wer LGND mag sollte sich auch ASTX mal ansehen.
Unfassbar wie stark sich LGND momentan präsentiert. Heute geht es prozentual zweistellig nach Oben. Das liegt an 2 "Meldungen":
Ligand Pharmaceuticals Incorporated (LGND) announces that its Board of Directors has agreed to waive certain “poison pill” provisions to allow BVF Partners L.P., including its affiliates and associates (“BVF”), to increase its ownership of the Company from the previous limit of 19.99% of outstanding common stock to a new limit of 24.99%, subject to certain conditions. BVF has been Ligand’s largest shareholder since the second quarter of 2011 and currently owns 17.7% of the Company's outstanding stock.
BVF’s acquisition of stock, if any, is expected to be made in the open market or through direct purchases from other stockholders. Ligand has been diligent in setting the terms of the waiver for the potential benefit of all shareholders of Ligand. In summary, the conditions under which BVF will be permitted to exceed the current limit of 19.99% and own up to 24.99% of Ligand’s outstanding stock include the following:
BVF’s purchases must exceed the 19.99% threshold within nine months from the date of the agreement, or the waiver for the increased ownership limit automatically terminates.
At any time BVF holds a position in excess of 19.99% of Ligand’s outstanding stock, Ligand’s Board of Directors will have sole voting control over BVF-owned shares representing 15% of the company’s total outstanding shares (currently approximately 3 million shares).
BVF will not attempt to nominate any Director to the Ligand Board of Directors or undertake any other control initiative.
Any shares purchased in excess of 19.99% of the outstanding common stock must be held by BVF for a minimum of four years or until the stock reaches $100 per share.
http://finance.yahoo.com/news/ligand-raises-ownership-limit-…
Das sind wirklich tolle Bedingungen, die LGND denen aufgedrückt hat. LGND zeigt zudem, wie ernst sie shareholder value nehmen. Keine Kapitalerhöhung sondern über den Markt mit ganz klaren Bedingungen. Übt BVF das aus - wovon man ausgehen kann, ist das natürlich sehr positiv. Zudem werden diese starken Hände den Kurs ggf. auffangen. Auch eine Übernahme kann man nicht ausschließen. Hier hat ja Elan mit royalty pharma für Furore gesorgt.
Zusätzlich gab heute ein Analyst ein Kursziel von 60 $ aus:
Craig-Hallum initiated coverage on Ligand Pharma (NASDAQ: LGND) with a Buy rating and a price target of $60.00. Analysts thinks the stock allows investors to gain exposure to biotech without a great level of risk.
Revenue growth is seen growing at a sustainable 25% pace with 60% operating margins. This is based on the company's 5 current products. It could also earn royalties on 85 partner products still under development. Pfizer Inc.'s (NYSE: PFE) Aprela for postmenopausal symptoms is viewed as a meaningful potential royalty stream.
http://www.streetinsider.com/Hot+New+Coverage/UPDATE%3A+Crai…
Die Analyse an sich ist mir relativ wurscht. Jedoch zeigt sich, dass es immer mehr Profis gibt, die sich mit dem Wert beschäftigen. Er wird auch für Fonds zunehmend interessant. In diesem Fonds ist LGND schon mit Abstand die größte Position:
http://www.finanzen.net/fonds/FCP_OP_MEDICAL_BioHealth-Trend…
Ligand Pharmaceuticals Incorporated (LGND) announces that its Board of Directors has agreed to waive certain “poison pill” provisions to allow BVF Partners L.P., including its affiliates and associates (“BVF”), to increase its ownership of the Company from the previous limit of 19.99% of outstanding common stock to a new limit of 24.99%, subject to certain conditions. BVF has been Ligand’s largest shareholder since the second quarter of 2011 and currently owns 17.7% of the Company's outstanding stock.
BVF’s acquisition of stock, if any, is expected to be made in the open market or through direct purchases from other stockholders. Ligand has been diligent in setting the terms of the waiver for the potential benefit of all shareholders of Ligand. In summary, the conditions under which BVF will be permitted to exceed the current limit of 19.99% and own up to 24.99% of Ligand’s outstanding stock include the following:
BVF’s purchases must exceed the 19.99% threshold within nine months from the date of the agreement, or the waiver for the increased ownership limit automatically terminates.
At any time BVF holds a position in excess of 19.99% of Ligand’s outstanding stock, Ligand’s Board of Directors will have sole voting control over BVF-owned shares representing 15% of the company’s total outstanding shares (currently approximately 3 million shares).
BVF will not attempt to nominate any Director to the Ligand Board of Directors or undertake any other control initiative.
Any shares purchased in excess of 19.99% of the outstanding common stock must be held by BVF for a minimum of four years or until the stock reaches $100 per share.
http://finance.yahoo.com/news/ligand-raises-ownership-limit-…
Das sind wirklich tolle Bedingungen, die LGND denen aufgedrückt hat. LGND zeigt zudem, wie ernst sie shareholder value nehmen. Keine Kapitalerhöhung sondern über den Markt mit ganz klaren Bedingungen. Übt BVF das aus - wovon man ausgehen kann, ist das natürlich sehr positiv. Zudem werden diese starken Hände den Kurs ggf. auffangen. Auch eine Übernahme kann man nicht ausschließen. Hier hat ja Elan mit royalty pharma für Furore gesorgt.
Zusätzlich gab heute ein Analyst ein Kursziel von 60 $ aus:
Craig-Hallum initiated coverage on Ligand Pharma (NASDAQ: LGND) with a Buy rating and a price target of $60.00. Analysts thinks the stock allows investors to gain exposure to biotech without a great level of risk.
Revenue growth is seen growing at a sustainable 25% pace with 60% operating margins. This is based on the company's 5 current products. It could also earn royalties on 85 partner products still under development. Pfizer Inc.'s (NYSE: PFE) Aprela for postmenopausal symptoms is viewed as a meaningful potential royalty stream.
http://www.streetinsider.com/Hot+New+Coverage/UPDATE%3A+Crai…
Die Analyse an sich ist mir relativ wurscht. Jedoch zeigt sich, dass es immer mehr Profis gibt, die sich mit dem Wert beschäftigen. Er wird auch für Fonds zunehmend interessant. In diesem Fonds ist LGND schon mit Abstand die größte Position:
http://www.finanzen.net/fonds/FCP_OP_MEDICAL_BioHealth-Trend…
Erste Ergebnisse von Promacta bei Krebs sind da. Komischerweise war das scheinbar keine offizielle Meldung seitens Ligand wert. Versteh ich nicht, weil es zeigt, dass Promacta die Infusion von Blutplättchen bei vielen Patienten unnötig macht, schwere Blutungen verhindert und vor allem die Lebensdauer verdoppelt! Das ist vor allem deshalb von Bedeutung, weil es das wichtigste Kriterium zur Zulassung ist.
In Lower-Risk MDS
During the same oral presentation session, Dr. Esther Oliva from A.O. Bianchi-Melacrino-Morelli in Reggio Calabria, Italy, will discuss interim results from an ongoing Phase 2 trial that is investigating the efficacy and safety of Promacta (eltrombopag) versus placebo in lower-risk MDS patients (abstract). Promacta is an oral drug that stimulates platelet production. It is currently approved by the U.S. Food and Drug Administration for the treatment of patients who have a condition known as chronic immune (idiopathic) thrombocytopenia (ITP), and who have not responded to several common treatments for ITP.
So far, 36 patients with an average age of 66 years have been recruited to participate in the Phase 2 study. The results show that at a follow-up time of 12 weeks, 80 percent of patients receiving Promacta responded to treatment with increased platelet counts and achieved platelet transfusion independence, compared to none who received the placebo. In addition, the rate of immature stem cells (blasts) decreased in 20 percent of patients receiving Promacta. Overall, 27 percent of patients who were treated with Promacta experienced severe side effects, including infectious complications, arthritis, and heart disease.
In Higher-Risk MDS And AML
Dr. Uwe Platzbecker from the University Hospital in Dresden, Germany, will also present results from an ongoing Phase 1/2 study that is investigating the efficacy and safety of Promacta versus placebo in higher-risk MDS and AML patients (abstract). The study includes 98 patients who had received a median of one prior therapy. The results show that 38 percent of patients receiving Promacta achieved platelet transfusion independence for eight weeks or more, compared to 21 percent of patients receiving a placebo. In addition, fewer patients receiving Promacta experienced clinically relevant bleeding events (38 percent), compared to patients receiving a placebo (66 percent). Median overall survival was 27 weeks for patients receiving Promacta, compared to 15.7 weeks for patients receiving a placebo. The most common side effects observed in more than 20 percent of patients receiving Promacta included fever, nausea, diarrhea, fatigue, decreased appetite, and pneumonia.
For Patients Receiving Vidaza
During an oral presentation session on Saturday, Dr. Tobias Svensson from Uppsala University in Sweden will present findings from a Phase 1 study investigating the efficacy and safety of Promacta in MDS patients who are being treated with Vidaza (abstract). So far, 11 patients with a median age of 71 years have been recruited. The results show that platelet counts remained stable or improved in 82 percent of patients. According to the abstract, bleeding symptoms were uncommon, and no cases of MDS disease progression were reported. The most common side effects included bronchitis (9 percent), pneumonia (9 percent), and blood clots in the deep veins (9 percent).
http://www.mdsbeacon.com/news/2013/06/13/the-european-hemato…
Zudem steht die Zulassung von Promacta in GB an (:confused

http://www.pmlive.com/pharma_news/nice_u-turn_on_gsks_revola…
Schon erstaunlich, wieviel GsK in verschiedenste Studien investiert:
http://clinicaltrials.gov/ct2/results?term=Eltrombopag&recr=…
In Lower-Risk MDS
During the same oral presentation session, Dr. Esther Oliva from A.O. Bianchi-Melacrino-Morelli in Reggio Calabria, Italy, will discuss interim results from an ongoing Phase 2 trial that is investigating the efficacy and safety of Promacta (eltrombopag) versus placebo in lower-risk MDS patients (abstract). Promacta is an oral drug that stimulates platelet production. It is currently approved by the U.S. Food and Drug Administration for the treatment of patients who have a condition known as chronic immune (idiopathic) thrombocytopenia (ITP), and who have not responded to several common treatments for ITP.
So far, 36 patients with an average age of 66 years have been recruited to participate in the Phase 2 study. The results show that at a follow-up time of 12 weeks, 80 percent of patients receiving Promacta responded to treatment with increased platelet counts and achieved platelet transfusion independence, compared to none who received the placebo. In addition, the rate of immature stem cells (blasts) decreased in 20 percent of patients receiving Promacta. Overall, 27 percent of patients who were treated with Promacta experienced severe side effects, including infectious complications, arthritis, and heart disease.
In Higher-Risk MDS And AML
Dr. Uwe Platzbecker from the University Hospital in Dresden, Germany, will also present results from an ongoing Phase 1/2 study that is investigating the efficacy and safety of Promacta versus placebo in higher-risk MDS and AML patients (abstract). The study includes 98 patients who had received a median of one prior therapy. The results show that 38 percent of patients receiving Promacta achieved platelet transfusion independence for eight weeks or more, compared to 21 percent of patients receiving a placebo. In addition, fewer patients receiving Promacta experienced clinically relevant bleeding events (38 percent), compared to patients receiving a placebo (66 percent). Median overall survival was 27 weeks for patients receiving Promacta, compared to 15.7 weeks for patients receiving a placebo. The most common side effects observed in more than 20 percent of patients receiving Promacta included fever, nausea, diarrhea, fatigue, decreased appetite, and pneumonia.
For Patients Receiving Vidaza
During an oral presentation session on Saturday, Dr. Tobias Svensson from Uppsala University in Sweden will present findings from a Phase 1 study investigating the efficacy and safety of Promacta in MDS patients who are being treated with Vidaza (abstract). So far, 11 patients with a median age of 71 years have been recruited. The results show that platelet counts remained stable or improved in 82 percent of patients. According to the abstract, bleeding symptoms were uncommon, and no cases of MDS disease progression were reported. The most common side effects included bronchitis (9 percent), pneumonia (9 percent), and blood clots in the deep veins (9 percent).
http://www.mdsbeacon.com/news/2013/06/13/the-european-hemato…
Zudem steht die Zulassung von Promacta in GB an (:confused


http://www.pmlive.com/pharma_news/nice_u-turn_on_gsks_revola…
Schon erstaunlich, wieviel GsK in verschiedenste Studien investiert:
http://clinicaltrials.gov/ct2/results?term=Eltrombopag&recr=…
Ligand gewinnt heute wieder bisher prozetentual zweistellig. Grund dürfte auch sein, dass übers WE Gerüchte eines Übernahmeversuchs von Onyx durch Amgen bestätigt wurden. Der Markt antizipiert nun vielleicht, dass sich Kyprolis durch einen Big-Player besser in den Markt drücken ließe. Andereseits zeigt es auch, dass Amgen zumindest von einem Erfolg der PIII überzeugt ist.
Langsam kann man bei LGND nicht mehr davon sprechen, dass sie unterbewertet sind. Das bedeutet natürlich nicht, dass es nicht noch weiter nach Oben gehen kann. Werde trotzdem den Rest meiner Tradingposition schmeißen.
Mit der Longposition bleibe ich natürlich dabei...
Langsam kann man bei LGND nicht mehr davon sprechen, dass sie unterbewertet sind. Das bedeutet natürlich nicht, dass es nicht noch weiter nach Oben gehen kann. Werde trotzdem den Rest meiner Tradingposition schmeißen.
Mit der Longposition bleibe ich natürlich dabei...
Im Bereich vom 40$ könnte sich ein Widerstand bilden. Mal sehen, ob das so kommt. Ligand scheint momentan auch ein wenig überhitzt. Im gestrigen Handelsverlauf wurde der Kurs zumindest wieder unter den Widerstand gezogen.

Am Sonntag gab es weitere positive Daten vom BACE Programm (Merck)
Merck has pulled back the covers on its Phase Ib dose-escalating study for MK-8931, a BACE inhibitor for Alzheimer's which demonstrated a positive effect in reducing the level of toxic proteins flowing through patients.
The data secures Merck's ($MRK) leading position in the BACE-inhibition crowd, which includes AstraZeneca ($AZN), Eli Lilly ($LLY)--which recently had to scrap its top candidate--and others. The pharma giant has already begun a bigger, longer study for MK-8931, recruiting 200 patients for a Phase II leg which is designed to grow into a Phase III study--provided the efficacy and safety profiles stay in line with expectations.
The BACE-inhibition theory is simple. Investigators see this as a route to preventing the production of amyloid beta, a toxic protein found clustered in the brains of patients. The idea here is that if you can reduce the level of amyloid beta going into the brain, you can influence the course of the memory-destroying disease, which now afflicts millions of people around the world.
To determine if it's working, Merck checks on the flow of amyloid beta 40 and 42 in cerebral spinal fluid, key biomarkers for the study. Over the course of 7 days of treatment, investigators say they could see a noted, dose-dependent response in protein levels in the fluid. For the top 60 mg dose, investigators say they found an 84% drop in ab40, according to a spokesperson for Merck. There was an 81% drop for ab42.
Just as importantly, though, there were none of the adverse events that could destroy a drug early on, something that Lilly has just had to deal with. Lilly says that it believes the tox issues that blew up its program were related to the design of the drug, though, rather than a problem with the target itself.
Investigators in the field say that one of the chief concerns with BACE inhibition is that it raises the prospect of interfering with other functions, including myelination. Merck is also including patients with a moderate level of the disease along with patients suffering from mild, early forms of the disease, raising the prospect that they're including patients whose disease has progressed for years, causing significant and irreversible damage.
With a treasure trove waiting for any drug developer capable of developing a new drug worth approving, contenders in this field are pushing ahead as fast as possible.
"The amyloid β reduction observed with MK-8931 may offer an opportunity to further understand the role BACE1 inhibition plays in the underlying pathology of Alzheimer's disease," said Darryle Schoepp, Ph.D., vice president of Neuroscience Early Development and Discovery Sciences, Merck.
Alzheimer's has long reigned as the biggest disease target with the most consistent track record for failure. Dozens of drugs have failed in the clinic, most notably the Phase III trials for solanezumab and bapineuzumab, antibodies designed to remove the plaque from brains. Lilly, though, is going back into a third Phase III study of solanezumab after seeing a hint of efficacy in patients with mild disease.
http://www.fiercebiotech.com/story/merck-reports-positive-re…
Ist aber nur eine kleine Studie gewesen, jedoch anders als zuvor an Patienten durchgeführt. Zumindest macht dies einen Erfolg in der P II (gegen Ende des Jahres) und einen Start der PIII wahrscheinlicher.
Bei der PII kommt es vor allem auf die Sicherheitsdaten an, da ja Lilly grade deshalb sein BACE Programm einstampfen musste. Langfristig bleint die große Frage dann, ob es eben Auswirkungen auf die Gedächtnisleistung gibt oder nicht.
Weiterhin bleibt es schwer, den Wert für Ligand zu bewerten. Man weiß ja auch die Royalties nicht. Aber natürlich wäre der Markt für dieses Medimament gigantisch, wenn eine PIII zeigt, dass es präventiv Alzheimer verhindert und/oder die Symptome lindert.
Merck has pulled back the covers on its Phase Ib dose-escalating study for MK-8931, a BACE inhibitor for Alzheimer's which demonstrated a positive effect in reducing the level of toxic proteins flowing through patients.
The data secures Merck's ($MRK) leading position in the BACE-inhibition crowd, which includes AstraZeneca ($AZN), Eli Lilly ($LLY)--which recently had to scrap its top candidate--and others. The pharma giant has already begun a bigger, longer study for MK-8931, recruiting 200 patients for a Phase II leg which is designed to grow into a Phase III study--provided the efficacy and safety profiles stay in line with expectations.
The BACE-inhibition theory is simple. Investigators see this as a route to preventing the production of amyloid beta, a toxic protein found clustered in the brains of patients. The idea here is that if you can reduce the level of amyloid beta going into the brain, you can influence the course of the memory-destroying disease, which now afflicts millions of people around the world.
To determine if it's working, Merck checks on the flow of amyloid beta 40 and 42 in cerebral spinal fluid, key biomarkers for the study. Over the course of 7 days of treatment, investigators say they could see a noted, dose-dependent response in protein levels in the fluid. For the top 60 mg dose, investigators say they found an 84% drop in ab40, according to a spokesperson for Merck. There was an 81% drop for ab42.
Just as importantly, though, there were none of the adverse events that could destroy a drug early on, something that Lilly has just had to deal with. Lilly says that it believes the tox issues that blew up its program were related to the design of the drug, though, rather than a problem with the target itself.
Investigators in the field say that one of the chief concerns with BACE inhibition is that it raises the prospect of interfering with other functions, including myelination. Merck is also including patients with a moderate level of the disease along with patients suffering from mild, early forms of the disease, raising the prospect that they're including patients whose disease has progressed for years, causing significant and irreversible damage.
With a treasure trove waiting for any drug developer capable of developing a new drug worth approving, contenders in this field are pushing ahead as fast as possible.
"The amyloid β reduction observed with MK-8931 may offer an opportunity to further understand the role BACE1 inhibition plays in the underlying pathology of Alzheimer's disease," said Darryle Schoepp, Ph.D., vice president of Neuroscience Early Development and Discovery Sciences, Merck.
Alzheimer's has long reigned as the biggest disease target with the most consistent track record for failure. Dozens of drugs have failed in the clinic, most notably the Phase III trials for solanezumab and bapineuzumab, antibodies designed to remove the plaque from brains. Lilly, though, is going back into a third Phase III study of solanezumab after seeing a hint of efficacy in patients with mild disease.
http://www.fiercebiotech.com/story/merck-reports-positive-re…
Ist aber nur eine kleine Studie gewesen, jedoch anders als zuvor an Patienten durchgeführt. Zumindest macht dies einen Erfolg in der P II (gegen Ende des Jahres) und einen Start der PIII wahrscheinlicher.
Bei der PII kommt es vor allem auf die Sicherheitsdaten an, da ja Lilly grade deshalb sein BACE Programm einstampfen musste. Langfristig bleint die große Frage dann, ob es eben Auswirkungen auf die Gedächtnisleistung gibt oder nicht.
Weiterhin bleibt es schwer, den Wert für Ligand zu bewerten. Man weiß ja auch die Royalties nicht. Aber natürlich wäre der Markt für dieses Medimament gigantisch, wenn eine PIII zeigt, dass es präventiv Alzheimer verhindert und/oder die Symptome lindert.
In letzter Zeit geht bei LGND ja so Einiges. Ein Rücksetzer evtl. bis auf 40$ wäre vorstellbar. Es kann ja nicht nur in eine Richtung gehen. Demnächst kommen ja auch die Zahlen und da wird man sehen, wer die Oberhand behält.
Heute schon GSK mit 70 Mio Umsatz bei Promacta. Nach 62 in Q1 ein akzeptables Wachstum. Promacta könnte so an die 300 Mio in 2013 erlösen.
Bei Kyprolis dürfte sich das rasante Wachstum nicht so fortsetzen, da es ja nur 3rd Line zugelassen ist und das weitere Wachstumspotenzial sich in erster Linie aus den Studienergebnissen und den daraus folgenden Implikationen für 2t und 1st Linien Anwendung ergibt.
Ligand hat zudem sein Porttfolio erweitert. Ich gehe aber eher nicht davon aus, dass sich daraus viel Umsatz generieren lässt. Aber sicher keine schlechten news:
http://finance.yahoo.com/news/ligand-signs-license-agreement…
http://finance.yahoo.com/news/ligand-signs-global-license-ag…
Heute schon GSK mit 70 Mio Umsatz bei Promacta. Nach 62 in Q1 ein akzeptables Wachstum. Promacta könnte so an die 300 Mio in 2013 erlösen.
Bei Kyprolis dürfte sich das rasante Wachstum nicht so fortsetzen, da es ja nur 3rd Line zugelassen ist und das weitere Wachstumspotenzial sich in erster Linie aus den Studienergebnissen und den daraus folgenden Implikationen für 2t und 1st Linien Anwendung ergibt.
Ligand hat zudem sein Porttfolio erweitert. Ich gehe aber eher nicht davon aus, dass sich daraus viel Umsatz generieren lässt. Aber sicher keine schlechten news:
http://finance.yahoo.com/news/ligand-signs-license-agreement…
http://finance.yahoo.com/news/ligand-signs-global-license-ag…
Heute gleich zwei gute Nachrichten.
Promacta wurde in der EU bei HEP C zur Zulassung empfohlen:
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Captisol enabled Topiramate hat den orphan status bekommen. Hier wird jetzt ein Partner gesucht:
http://finance.yahoo.com/news/ligand-receives-orphan-designa…
Promacta wurde in der EU bei HEP C zur Zulassung empfohlen:
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Captisol enabled Topiramate hat den orphan status bekommen. Hier wird jetzt ein Partner gesucht:
http://finance.yahoo.com/news/ligand-receives-orphan-designa…
Heute Zahlen von Ligand:
http://finance.yahoo.com/news/ligand-reports-second-quarter-…
Royalty revenues were $4.9 million as compared with $3.0 million for the same period in 2012, primarily due to higher royalties from Promacta® and new royalties from Kyprolis®. Material sales increased to $4.0 million from $1.7 million for the same period in 2012, due to timing of customer purchases of Captisol.
Insegsamt kam so ein kleiner Gewinn zu Stande. Es wurden weitere Schulden abbezahlt. Wenn es so weiter läuft, rechne ich eigentlich damit, dass Ligand bald auch eine Dividende auszahlt.
http://finance.yahoo.com/news/ligand-reports-second-quarter-…
Royalty revenues were $4.9 million as compared with $3.0 million for the same period in 2012, primarily due to higher royalties from Promacta® and new royalties from Kyprolis®. Material sales increased to $4.0 million from $1.7 million for the same period in 2012, due to timing of customer purchases of Captisol.
Insegsamt kam so ein kleiner Gewinn zu Stande. Es wurden weitere Schulden abbezahlt. Wenn es so weiter läuft, rechne ich eigentlich damit, dass Ligand bald auch eine Dividende auszahlt.
Aufgrund der breiten Pipeline gibt es hier natürlich häufiger news - eine Zusammenfassung:
Onyx: Kyprolis Umsatz im letzten Q 61 Mio.
Lundbeck plant Zulasungsantrag noch in diesem jahr:
http://files.shareholder.com/downloads/AMDA-GGC00/2547763476…
Verpartnerung von IV Topiramate - leider kein Upfront und "nur" 6-7,5 % Royalties, aber keine Kosten mehr:
http://boardvote.com/symbol/LGND/communique/418008
Interessant auch, dass einige Analysten Kyprolis Umsatzziel schon bei 4 Milliarden sehen - das wären dann mehr als 100 Mio Royalties für Ligand:
http://blogs.barrons.com/stockstowatchtoday/2013/08/13/repor…
Ligand hat selber noch einige Fakten zum BACE Programm von Merck zusammengestellt:
http://investor.ligand.com/files/doc_presentations/MK-8931%2…
Ein bisher geheimes Captisol Programm von Merck wurde enthült. Es ist eine IV Version von Posaconazole - in P III:
http://www.abstractsonline.com/Plan/ViewAbstract.aspx?sKey=3…
Onyx: Kyprolis Umsatz im letzten Q 61 Mio.
Lundbeck plant Zulasungsantrag noch in diesem jahr:
http://files.shareholder.com/downloads/AMDA-GGC00/2547763476…
Verpartnerung von IV Topiramate - leider kein Upfront und "nur" 6-7,5 % Royalties, aber keine Kosten mehr:
http://boardvote.com/symbol/LGND/communique/418008
Interessant auch, dass einige Analysten Kyprolis Umsatzziel schon bei 4 Milliarden sehen - das wären dann mehr als 100 Mio Royalties für Ligand:
http://blogs.barrons.com/stockstowatchtoday/2013/08/13/repor…
Ligand hat selber noch einige Fakten zum BACE Programm von Merck zusammengestellt:
http://investor.ligand.com/files/doc_presentations/MK-8931%2…
Ein bisher geheimes Captisol Programm von Merck wurde enthült. Es ist eine IV Version von Posaconazole - in P III:
http://www.abstractsonline.com/Plan/ViewAbstract.aspx?sKey=3…
Aus Ligands Sicht ist das Hickhack um die Onyx Übernahme durch Amgen etc. spannend. Amgen scheint jetzt Einsicht in gewisse Daten der laufenden Studien bekommen zu haben. Sollte Amgen in der nächsten Zeit ein Angebot für Onyx abgeben würde das die Wahrscheinlichkeit guter Ergebnisse und somit einer Zulassung in Europa sowie der als 2t oder 1st Linientherapie weiter steigern.
Hier sollte man also ein Auge drauf haben. Kyprolis werden ja mittelfristig Umsätze zwischen 2-4 Milliarden zugetraut. Das wären für Ligand Royalties zwischen 50-110 Mio.
http://www.fiercebiotech.com/story/analyst-time-wrap-amgens-…
Hier sollte man also ein Auge drauf haben. Kyprolis werden ja mittelfristig Umsätze zwischen 2-4 Milliarden zugetraut. Das wären für Ligand Royalties zwischen 50-110 Mio.
http://www.fiercebiotech.com/story/analyst-time-wrap-amgens-…
Das Hickhack wird wohl noch eine Weile weiter gehen:
http://www.bloomberg.com/news/2013-08-22/amgen-said-to-push-…
http://www.bloomberg.com/news/2013-08-22/amgen-said-to-push-…
Die Onyx Übernahme ist durch:
http://wwwext.amgen.com/media/media_pr_detail.jsp?year=2013&…
Gut für LGND, da Amgen sicherlich Kyprolis noch besser verkaufen kann. Es stärkt auch das Vertrauen auf Zulassungserweiterungen.
http://wwwext.amgen.com/media/media_pr_detail.jsp?year=2013&…
Gut für LGND, da Amgen sicherlich Kyprolis noch besser verkaufen kann. Es stärkt auch das Vertrauen auf Zulassungserweiterungen.
Monday evening, Amgen announced that it was acquiring Onyx Pharmaceuticals for $10.4 billion at $125 per share (representing a 6.9% premium).
Amgen (ticker: AMGN) highlighted that they believe the early launch of Kyprolis [licensed from Ligand Pharmaceuticals (LGND) by Onyx (ONXX) for relapsed and refractory multiple myeloma] is attractive and will be putting added efforts to increasing global access to the drug.
Recall that Ligand receives tiered royalties off of Kyprolis sales (1.5% to $250 million, 2.0% to $500 million, 2.5% to 750 million and 3.0% above $750 million). Based on current Wall Street estimates, we believe that the 3.0% level will be reached in the next 24 months at the minimum.
With Onyx being acquired by Amgen, we remind investors that there is no change of control issue regarding the Kyprolis franchise. In fact, we believe it will benefit Ligand to have Kyprolis in Amgen's hands with their juggernaut sales and marketing efforts.
We have confirmed with Ligand management that there is no issue with the current Kyprolis arrangement should there be a change of control with Onyx. We believe that the Onyx acquisition is certainly beneficial to both Kyprolis and Ligand's future revenue streams. The drug's potential should be bolstered by Amgen's juggernaut sales and marketing efforts, in our belief.
From a macro standpoint, we believe the merger of Amgen and Onyx continues to bode well for the biotechnology arena, and we continue to expect continued mergers and acquisitions and partnering activity over the next year and beyond. Our thesis on Ligand remains unchanged.
We also believe the Street is not fully valuing the opportunity with Promacta, from both the new approved indication in treating thrombocytopenia associated with hepatitis C virus (HCV) and, importantly, the broad program by GlaxoSmithKline (GSK) in oncology settings.
We reiterate our Buy rating and $65 price target for Ligand and recommend steady accumulation of shares, as we anticipate that current revenue streams from partnered products and the broad "in development" portfolio are poised to drive significant growth both in the near and longer term.
http://online.barrons.com/article/SB500014240527487042878045…
Amgen selber hat sich auf dem CC sehr bullisch über die Zukunft von Kyprolis geäußert. Offiziell haben sie keinen Einblick in Daten der laufenden Studien bekommen:
Thanks, Michael. As I've said in my remarks and as we noted in the press release, we had the benefit of being able to spend considerable time with the Onyx team, coming to know and understand, in particular, Kyprolis very well through that process. So we feel excited about its prospects as a proteasome inhibitor with an attractive efficacy and safety profile. So we reviewed the data that are available to us, and our confidence is reflected in the price that we've moved forward the transaction with.
http://seekingalpha.com/article/1656942-amgens-ceo-hosts-ana…
Amgen (ticker: AMGN) highlighted that they believe the early launch of Kyprolis [licensed from Ligand Pharmaceuticals (LGND) by Onyx (ONXX) for relapsed and refractory multiple myeloma] is attractive and will be putting added efforts to increasing global access to the drug.
Recall that Ligand receives tiered royalties off of Kyprolis sales (1.5% to $250 million, 2.0% to $500 million, 2.5% to 750 million and 3.0% above $750 million). Based on current Wall Street estimates, we believe that the 3.0% level will be reached in the next 24 months at the minimum.
With Onyx being acquired by Amgen, we remind investors that there is no change of control issue regarding the Kyprolis franchise. In fact, we believe it will benefit Ligand to have Kyprolis in Amgen's hands with their juggernaut sales and marketing efforts.
We have confirmed with Ligand management that there is no issue with the current Kyprolis arrangement should there be a change of control with Onyx. We believe that the Onyx acquisition is certainly beneficial to both Kyprolis and Ligand's future revenue streams. The drug's potential should be bolstered by Amgen's juggernaut sales and marketing efforts, in our belief.
From a macro standpoint, we believe the merger of Amgen and Onyx continues to bode well for the biotechnology arena, and we continue to expect continued mergers and acquisitions and partnering activity over the next year and beyond. Our thesis on Ligand remains unchanged.
We also believe the Street is not fully valuing the opportunity with Promacta, from both the new approved indication in treating thrombocytopenia associated with hepatitis C virus (HCV) and, importantly, the broad program by GlaxoSmithKline (GSK) in oncology settings.
We reiterate our Buy rating and $65 price target for Ligand and recommend steady accumulation of shares, as we anticipate that current revenue streams from partnered products and the broad "in development" portfolio are poised to drive significant growth both in the near and longer term.
http://online.barrons.com/article/SB500014240527487042878045…
Amgen selber hat sich auf dem CC sehr bullisch über die Zukunft von Kyprolis geäußert. Offiziell haben sie keinen Einblick in Daten der laufenden Studien bekommen:
Thanks, Michael. As I've said in my remarks and as we noted in the press release, we had the benefit of being able to spend considerable time with the Onyx team, coming to know and understand, in particular, Kyprolis very well through that process. So we feel excited about its prospects as a proteasome inhibitor with an attractive efficacy and safety profile. So we reviewed the data that are available to us, and our confidence is reflected in the price that we've moved forward the transaction with.
http://seekingalpha.com/article/1656942-amgens-ceo-hosts-ana…
Die Zulassungserweiterung von Promacta in der EU ist da. Bei der derzeitigen Dynamik im Bereich HEP C ist es schwer zu sagen, wie sich das auswirkt.
http://finance.yahoo.com/news/ligand-partner-gsk-receives-ma…
http://finance.yahoo.com/news/ligand-partner-gsk-receives-ma…
Trotz Shutdown hat die FDA heute Duavee (Pfizer) zugelassen. Royalties sind aber gering (0,5-2,5%). Zum Marktpotenzial kann ich nicht viel sagen. Pfizer hat aber ziemlich viel Geld in die klinische Entwicklung gesteckt.
hat die FDA heute Duavee (Pfizer) zugelassen. Royalties sind aber gering (0,5-2,5%). Zum Marktpotenzial kann ich nicht viel sagen. Pfizer hat aber ziemlich viel Geld in die klinische Entwicklung gesteckt.
Insgesamt spricht es schon für Ligand, dass bisher alle Medikamente "von Ligand", die zur Zulassung standen, dann auch zugelassen wurden.
http://finance.yahoo.com/news/u-fda-approves-pfizer-drug-184…
 hat die FDA heute Duavee (Pfizer) zugelassen. Royalties sind aber gering (0,5-2,5%). Zum Marktpotenzial kann ich nicht viel sagen. Pfizer hat aber ziemlich viel Geld in die klinische Entwicklung gesteckt.
hat die FDA heute Duavee (Pfizer) zugelassen. Royalties sind aber gering (0,5-2,5%). Zum Marktpotenzial kann ich nicht viel sagen. Pfizer hat aber ziemlich viel Geld in die klinische Entwicklung gesteckt. Insgesamt spricht es schon für Ligand, dass bisher alle Medikamente "von Ligand", die zur Zulassung standen, dann auch zugelassen wurden.
http://finance.yahoo.com/news/u-fda-approves-pfizer-drug-184…
Ein etwas ausführlicherer Bericht zur Zulassung:
http://www.fiercepharma.com/story/pfizer-ligand-get-fda-nod-…
Bei einem Umsatz von 1 Milliarde bekäme LGND 11 Mio Royalties - das wären weitere 0,55 Cent Gewinn je Aktie mehr. In der guidance für 2013 und 2014 sind keinerlei Umsätze von Duavee berücksichtigt. Auch die Milestones von 425000$ nicht.
http://www.fiercepharma.com/story/pfizer-ligand-get-fda-nod-…
Bei einem Umsatz von 1 Milliarde bekäme LGND 11 Mio Royalties - das wären weitere 0,55 Cent Gewinn je Aktie mehr. In der guidance für 2013 und 2014 sind keinerlei Umsätze von Duavee berücksichtigt. Auch die Milestones von 425000$ nicht.
Ligand heute mit einem Ausbruch über die 50$ Marke. Es sind doch recht viele short gegangen und wurden zuerst bei der Zulassung und nun von dem charttechnischem Signal überrascht. Fundamental vielleicht noch interessant, dass Merck eine neue P III mit dem Bace Programm gestartet hat. Also scheint es nicht die Probleme mit der Sicherheit zu geben, wie beim Programm von Lilly. Andererseits fehlt bei dieser Studie die Höchstdosierung von 60mg. Es sollten eigentlich noch in diesem Jahr die Ergebnisse der PII kommen...

http://clinicaltrials.gov/show/NCT01953601
http://clinicaltrials.gov/show/NCT01953601
Gestern gab es Zahlen von Amgen: Kyprolis 65 Mio
Heute dann die Zahlen von Promacta: 76 Mio US$ (nach 70 in Q2)
Bei Kyprolis hängt jetzt alles weitere davon ab, wie die Ergebnisse der Studien ausfallen.
Bei Promacta wäre es toll, wenn das momentane Wachstum von ca. 10% von Quartal zu Quartal beibehalten bleiben könnte...
Heute dann die Zahlen von Promacta: 76 Mio US$ (nach 70 in Q2)
Bei Kyprolis hängt jetzt alles weitere davon ab, wie die Ergebnisse der Studien ausfallen.
Bei Promacta wäre es toll, wenn das momentane Wachstum von ca. 10% von Quartal zu Quartal beibehalten bleiben könnte...
Ligand kam heute nach den zahlen unter Druck, wobei die Zahlen eigentlich ganz gut waren:
Ligand Pharmaceuticals Incorporated (LGND) today reported financial results for the third quarter and nine months ended September 30, 2013, and provided an operating forecast and program updates.
Highlights for the third quarter of 2013 include:
Total revenues of $13.0 million
Non-GAAP net income from continuing operations of $2.5 million, or $0.12 per diluted share
Net income of $2.0 million, or $0.09 per diluted share
A description of the non-GAAP calculations and reconciliation to comparable GAAP financial measures is provided in the accompanying table titled “Non-GAAP Financial Measures.”
“Ligand continued to post significant revenue growth and to demonstrate the strength of its business model during the third quarter,” commented John Higgins, President and Chief Executive Officer of Ligand. “Recently, two significant partnered programs received regulatory approvals. Pfizer’s Duavee™ received FDA approval for the treatment of moderate-to-severe vasomotor symptoms associated with menopause and the prevention of postmenopausal osteoporosis. GlaxoSmithKline’s Revolade™ (Promacta®) received European Commission marketing approval to treat low platelet counts in patients with chronic hepatitis C infection. These are exciting developments, along with portfolio additions and other late-stage advancements that reinforce the long-term potential of Ligand's partnered portfolio.”
Third Quarter 2013 Financial Results
Total revenues for the third quarter of 2013 were $13.0 million, an increase of 104% compared with $6.4 million for the same period in 2012. Royalty revenues increased to $5.7 million from $3.2 million for the same period in 2012, primarily due to higher royalties from Promacta® and new royalties from Kyprolis®. Material sales increased to $6.7 million from $1.8 million for the same period in 2012 due to timing of customer purchases of Captisol.
Cost of goods sold was $2.5 million for the third quarter of 2013, compared with $0.7 million for the third quarter of 2012, with the increase primarily due to higher material sales. Other operating costs and expenses from continuing operations for the third quarter of 2013 were $7.4 million, compared with $7.1 million for the third quarter of 2012. Research and development expenses decreased $0.2 million, primarily due to lower spending on internal development programs, and general and administrative expenses increased $0.5 million, primarily due to higher non-cash stock-based compensation expense.
Net income for the third quarter of 2013 was $2.0 million, or $0.09 per diluted share, compared with a net loss for the third quarter of 2012 of $0.2 million, or $(0.01) per share. Non-GAAP net income for the third quarter of 2013 was $2.5 million, or $0.12 per diluted share, compared with a non-GAAP net loss for the third quarter of 2012 of $2.3 million, or $(0.11) per share.
As of September 30, 2013, Ligand had cash, cash equivalents, short-term investments and restricted investments of $8.2 million. During the first three quarters of 2013, Ligand has paid down $16.2 million in debt.
2013 Year-to-Date Results
Total revenues for the nine months ended September 30, 2013 increased 93% to $34.2 million compared with $17.8 million for the first nine months of 2012. Royalty revenues for the nine months ended September 30, 2013 increased to $16.5 million from $9.3 million for the same period in 2012, primarily due to higher royalties from Promacta and new royalties from Kyprolis. Material sales increased to $12.3 million from $4.2 million for the same period in 2012 due to timing of customer purchases of Captisol.
Cost of goods sold was $4.4 million for the first nine months of 2013, compared with $1.3 million for the first nine months of 2012. Other operating costs and expenses for the first nine months of 2013 were $21.3 million, compared with $20.6 million for the first nine months of 2012.
Net income for the first nine months of 2013 was $9.6 million, or $0.46 per diluted share, compared with a net loss for the first nine months of 2012 of $1.6 million, or $(0.08) per share. Non-GAAP net income for the first nine months of 2013 was $9.7 million, or $0.47 per diluted share, compared with a non-GAAP net loss for the first nine months of 2012 of $2.8 million, or $(0.14) per share.
2013 Financial Forecast
For its full-year 2013 financial forecast, the Company now expects total revenues to be between $45.0 million and $46.0 million and non-GAAP earnings from continuing operations per diluted share to be between $0.49 and $0.51, which is at the high end of its previous financial forecast. For the fourth quarter of 2013, Ligand expects total revenues to be between $11 million and $12 million and non-GAAP earnings per diluted share to be between $0.15 and $0.17. The non-GAAP earnings per diluted share guidance does not include the effects of any increase or decrease in contingent liabilities.
Third Quarter and Recent Business Highlights
Upcoming Events
Ligand is scheduled to host an Analyst Day in Chicago on Thursday, November 14, 2013 from 9:30 a.m. to 11:30 a.m. Central time. The event will feature presentations pertaining to the Company’s business and pipeline programs.
Partnered Program Updates
Ligand partner Spectrum Pharmaceuticals announced the completion of enrollment for the pivotal trial of Captisol-enabled®, propylene glycol-free (PG-free) high-dose melphalan as a conditioning treatment prior to autologous transplant for patients with multiple myeloma.
Ligand partner GlaxoSmithKline (GSK) announced that the European Medicines Agency's Committee for Medicinal Products for Human Use (CHMP) approved Revolade™ (eltrombopag) as a treatment for low platelet counts (thrombocytopenia) in adult patients with chronic hepatitis C infection, where the degree of thrombocytopenia is the main factor preventing the initiation or limiting the ability to maintain optimal interferon-based therapy. The FDA approved Promacta® (eltrombopag) for the treatment of thrombocytopenia in patients with chronic hepatitis C infection in November 2012. Promacta®/Revolade™ is currently approved in 95 markets for the treatment of idiopathic thrombocytopenia (ITP) and in more than 20 markets for the treatment of thrombocytopenia in patients with chronic hepatitis C infection.
Ligand partner Pfizer received approval from the U.S. Food and Drug Administration (FDA) for Duavee™ (conjugated estrogens/bazedoxifene) for the treatment of moderate-to-severe vasomotor symptoms associated with menopause and the prevention of postmenopausal osteoporosis. Under the terms of a license agreement with Pfizer, Ligand earned a $425,000 milestone payment upon the approval. Pfizer intends to launch Duavee™ in the first quarter of 2014 and expects it to be available for patients in February 2014. See www.Duavee.com for further information.
Ligand partner Merck presented positive Phase 3 data for its IV formulation of the antifungal agent posaconazole (Noxafil®) at the International Conference on Antimicrobial Agents and Chemotherapy (ICAAC) hosted by the American Society for Microbiology.
New Fully-Funded Shots-on-Goal
Ligand entered a global license agreement with CURx Pharmaceuticals, Inc. for the development and commercialization of Ligand's Captisol-enabled™ Topiramate Injection for the treatment of partial onset or primary generalized tonic-clonic seizures in hospitalized epilepsy patients who are unable to take oral topiramate. Under the terms of the agreement, Ligand will be eligible to receive approximately $20 million in potential net milestone payments and net royalties on future sales of 6.0% to 7.5%.
Internal Program Progress
The FDA accepted an Investigational New Drug (IND) application for Ligand's proprietary Glucagon receptor antagonist product candidate for the treatment of diabetes.
Ligand hat eigentlich die Guidance für dieses Jahr nach Oben angepasst, ursprünglich:
Revenue in 2013 is projected to be between $41 million and $44 million, and is projected to grow to more than $60 million in 2014, representing a 40% compound annual growth rate from 2012 expected revenue of $30 million to $31 million.
Net income in 2013 is projected to be more than $0.35 per diluted share, and is projected to increase by 200% to more than $1.05 per diluted share in 2014.
Was mir aber Sorge bereitet, ist der anvisierte Gewinnsprung im nächsten Jahr. Da frag ich mich schon, wo das herkommen soll. Bei Kyprolis haben sich die Aussichten momentan eher verschlechtert, weil ein Konkurenzprodukt von Celgene starke Konkurenz macht. Hier hängt nun alles von den Studien ab.
Insgesamt erscheint Ligand durchaus ambitioniert bewertet.
Ligand Pharmaceuticals Incorporated (LGND) today reported financial results for the third quarter and nine months ended September 30, 2013, and provided an operating forecast and program updates.
Highlights for the third quarter of 2013 include:
Total revenues of $13.0 million
Non-GAAP net income from continuing operations of $2.5 million, or $0.12 per diluted share
Net income of $2.0 million, or $0.09 per diluted share
A description of the non-GAAP calculations and reconciliation to comparable GAAP financial measures is provided in the accompanying table titled “Non-GAAP Financial Measures.”
“Ligand continued to post significant revenue growth and to demonstrate the strength of its business model during the third quarter,” commented John Higgins, President and Chief Executive Officer of Ligand. “Recently, two significant partnered programs received regulatory approvals. Pfizer’s Duavee™ received FDA approval for the treatment of moderate-to-severe vasomotor symptoms associated with menopause and the prevention of postmenopausal osteoporosis. GlaxoSmithKline’s Revolade™ (Promacta®) received European Commission marketing approval to treat low platelet counts in patients with chronic hepatitis C infection. These are exciting developments, along with portfolio additions and other late-stage advancements that reinforce the long-term potential of Ligand's partnered portfolio.”
Third Quarter 2013 Financial Results
Total revenues for the third quarter of 2013 were $13.0 million, an increase of 104% compared with $6.4 million for the same period in 2012. Royalty revenues increased to $5.7 million from $3.2 million for the same period in 2012, primarily due to higher royalties from Promacta® and new royalties from Kyprolis®. Material sales increased to $6.7 million from $1.8 million for the same period in 2012 due to timing of customer purchases of Captisol.
Cost of goods sold was $2.5 million for the third quarter of 2013, compared with $0.7 million for the third quarter of 2012, with the increase primarily due to higher material sales. Other operating costs and expenses from continuing operations for the third quarter of 2013 were $7.4 million, compared with $7.1 million for the third quarter of 2012. Research and development expenses decreased $0.2 million, primarily due to lower spending on internal development programs, and general and administrative expenses increased $0.5 million, primarily due to higher non-cash stock-based compensation expense.
Net income for the third quarter of 2013 was $2.0 million, or $0.09 per diluted share, compared with a net loss for the third quarter of 2012 of $0.2 million, or $(0.01) per share. Non-GAAP net income for the third quarter of 2013 was $2.5 million, or $0.12 per diluted share, compared with a non-GAAP net loss for the third quarter of 2012 of $2.3 million, or $(0.11) per share.
As of September 30, 2013, Ligand had cash, cash equivalents, short-term investments and restricted investments of $8.2 million. During the first three quarters of 2013, Ligand has paid down $16.2 million in debt.
2013 Year-to-Date Results
Total revenues for the nine months ended September 30, 2013 increased 93% to $34.2 million compared with $17.8 million for the first nine months of 2012. Royalty revenues for the nine months ended September 30, 2013 increased to $16.5 million from $9.3 million for the same period in 2012, primarily due to higher royalties from Promacta and new royalties from Kyprolis. Material sales increased to $12.3 million from $4.2 million for the same period in 2012 due to timing of customer purchases of Captisol.
Cost of goods sold was $4.4 million for the first nine months of 2013, compared with $1.3 million for the first nine months of 2012. Other operating costs and expenses for the first nine months of 2013 were $21.3 million, compared with $20.6 million for the first nine months of 2012.
Net income for the first nine months of 2013 was $9.6 million, or $0.46 per diluted share, compared with a net loss for the first nine months of 2012 of $1.6 million, or $(0.08) per share. Non-GAAP net income for the first nine months of 2013 was $9.7 million, or $0.47 per diluted share, compared with a non-GAAP net loss for the first nine months of 2012 of $2.8 million, or $(0.14) per share.
2013 Financial Forecast
For its full-year 2013 financial forecast, the Company now expects total revenues to be between $45.0 million and $46.0 million and non-GAAP earnings from continuing operations per diluted share to be between $0.49 and $0.51, which is at the high end of its previous financial forecast. For the fourth quarter of 2013, Ligand expects total revenues to be between $11 million and $12 million and non-GAAP earnings per diluted share to be between $0.15 and $0.17. The non-GAAP earnings per diluted share guidance does not include the effects of any increase or decrease in contingent liabilities.
Third Quarter and Recent Business Highlights
Upcoming Events
Ligand is scheduled to host an Analyst Day in Chicago on Thursday, November 14, 2013 from 9:30 a.m. to 11:30 a.m. Central time. The event will feature presentations pertaining to the Company’s business and pipeline programs.
Partnered Program Updates
Ligand partner Spectrum Pharmaceuticals announced the completion of enrollment for the pivotal trial of Captisol-enabled®, propylene glycol-free (PG-free) high-dose melphalan as a conditioning treatment prior to autologous transplant for patients with multiple myeloma.
Ligand partner GlaxoSmithKline (GSK) announced that the European Medicines Agency's Committee for Medicinal Products for Human Use (CHMP) approved Revolade™ (eltrombopag) as a treatment for low platelet counts (thrombocytopenia) in adult patients with chronic hepatitis C infection, where the degree of thrombocytopenia is the main factor preventing the initiation or limiting the ability to maintain optimal interferon-based therapy. The FDA approved Promacta® (eltrombopag) for the treatment of thrombocytopenia in patients with chronic hepatitis C infection in November 2012. Promacta®/Revolade™ is currently approved in 95 markets for the treatment of idiopathic thrombocytopenia (ITP) and in more than 20 markets for the treatment of thrombocytopenia in patients with chronic hepatitis C infection.
Ligand partner Pfizer received approval from the U.S. Food and Drug Administration (FDA) for Duavee™ (conjugated estrogens/bazedoxifene) for the treatment of moderate-to-severe vasomotor symptoms associated with menopause and the prevention of postmenopausal osteoporosis. Under the terms of a license agreement with Pfizer, Ligand earned a $425,000 milestone payment upon the approval. Pfizer intends to launch Duavee™ in the first quarter of 2014 and expects it to be available for patients in February 2014. See www.Duavee.com for further information.
Ligand partner Merck presented positive Phase 3 data for its IV formulation of the antifungal agent posaconazole (Noxafil®) at the International Conference on Antimicrobial Agents and Chemotherapy (ICAAC) hosted by the American Society for Microbiology.
New Fully-Funded Shots-on-Goal
Ligand entered a global license agreement with CURx Pharmaceuticals, Inc. for the development and commercialization of Ligand's Captisol-enabled™ Topiramate Injection for the treatment of partial onset or primary generalized tonic-clonic seizures in hospitalized epilepsy patients who are unable to take oral topiramate. Under the terms of the agreement, Ligand will be eligible to receive approximately $20 million in potential net milestone payments and net royalties on future sales of 6.0% to 7.5%.
Internal Program Progress
The FDA accepted an Investigational New Drug (IND) application for Ligand's proprietary Glucagon receptor antagonist product candidate for the treatment of diabetes.
Ligand hat eigentlich die Guidance für dieses Jahr nach Oben angepasst, ursprünglich:
Revenue in 2013 is projected to be between $41 million and $44 million, and is projected to grow to more than $60 million in 2014, representing a 40% compound annual growth rate from 2012 expected revenue of $30 million to $31 million.
Net income in 2013 is projected to be more than $0.35 per diluted share, and is projected to increase by 200% to more than $1.05 per diluted share in 2014.
Was mir aber Sorge bereitet, ist der anvisierte Gewinnsprung im nächsten Jahr. Da frag ich mich schon, wo das herkommen soll. Bei Kyprolis haben sich die Aussichten momentan eher verschlechtert, weil ein Konkurenzprodukt von Celgene starke Konkurenz macht. Hier hängt nun alles von den Studien ab.
Insgesamt erscheint Ligand durchaus ambitioniert bewertet.




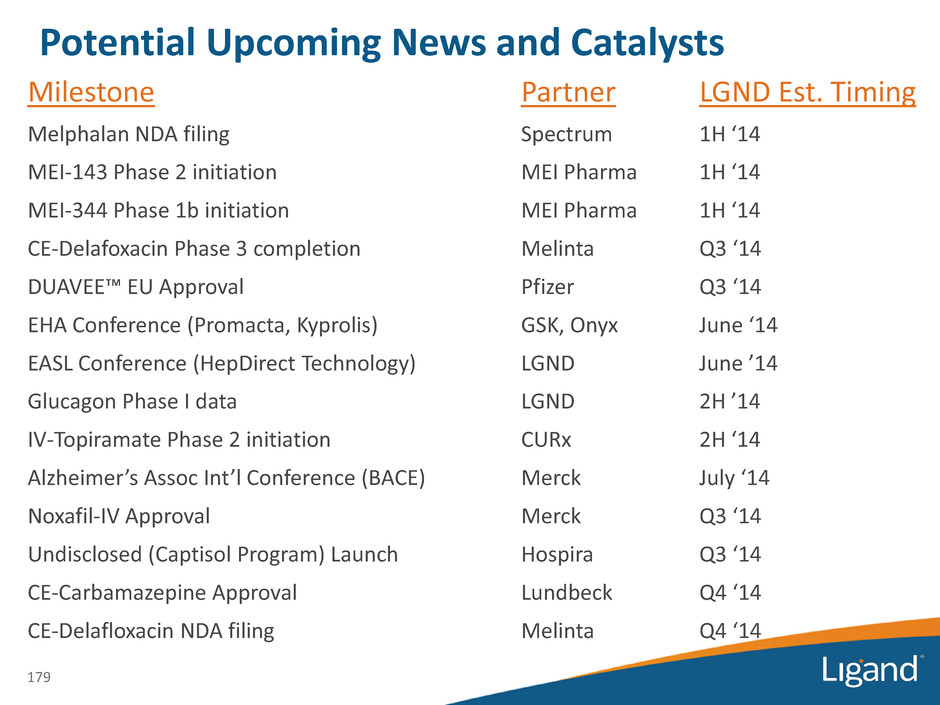
Ligand hatte gestern den Investorday mit einer ziemlich ausführlichen Präsentation. In diesem Rahmen wurde die Guidance für die nächsten Jahre gegeben.
Was mich am meisten begeistert, sind die Daten zu Promacta. Hier scheint es mir doch äußerst angenbracht, eine schnelle Zulassung zu beantragen, da eben viele Patienten verbluten und Promacta somit einen echten Überlebensvorteil mit sich bringt, zudem unabhängig von Bluttransfusion machen kann. Auf der ASH wird GSK Ergebnisse einer PII bei CLL präsentieren.
http://www.sec.gov/Archives/edgar/data/886163/00008861631300…
Ligand kommt grad stark unter Druck, weil es Zwiefel an der Sicherheit bei Kyprolis zu geben scheint. Das wäre natürlich extrem schlecht für die weiteren Aussichten. Wie ernst man das nehmen muss wird sich zeigen. So wie ich das sehe kommt das vom Konkurenten Celgene:


Antwort auf Beitrag Nr.: 45.890.024 von kmastra am 21.11.13 19:14:08Die Reaktion war zunächst wohl auch deshalb sehr heftig, weil sich einige an Ariad erinnert fühlten. Hier war ja auch die Zulassung nach einer PII erfolgt und in der anschließenden PIII gab es dann große Sicherheitsschwierigkeiten.
Aber Amgen hat sich dazu geäußert und gibt Entwarnung.

Aber Amgen hat sich dazu geäußert und gibt Entwarnung.

Heute eine positive Nachricht vom BACE Programm:
http://www.mercknewsroom.com/news-release/prescription-medic…
Das Merck da jetzt die P III (auch offiziell) durchzieht ist natürlich super. Vor allem, weil andere BACE Programme ja aus Sicherheitsgründen eingestellt werden mussten. Nun geht es also um die Effektivität. Ich persönlich rechne hier trotzdem eher mit einem Misserfolg, weil ein ähnlicher Ansatz schon mehrmals gescheitert ist. Anderseits wäre das Marktpotenzial definitiv gigantisch. Bisher gibt es ja quasi kein funktionierndes Medikament. Also eine explosive Mischung! Es ist momentan auch noch so, dass es wenig bekannt ist, dass Ligand Royalties bekäme. Heute auch keine Meldung seitens Ligand und auch kaum Kursbewegung. Das könnte sich natürlich noch ändern...
http://www.mercknewsroom.com/news-release/prescription-medic…
Das Merck da jetzt die P III (auch offiziell) durchzieht ist natürlich super. Vor allem, weil andere BACE Programme ja aus Sicherheitsgründen eingestellt werden mussten. Nun geht es also um die Effektivität. Ich persönlich rechne hier trotzdem eher mit einem Misserfolg, weil ein ähnlicher Ansatz schon mehrmals gescheitert ist. Anderseits wäre das Marktpotenzial definitiv gigantisch. Bisher gibt es ja quasi kein funktionierndes Medikament. Also eine explosive Mischung! Es ist momentan auch noch so, dass es wenig bekannt ist, dass Ligand Royalties bekäme. Heute auch keine Meldung seitens Ligand und auch kaum Kursbewegung. Das könnte sich natürlich noch ändern...
Amgen gab heute die Zahlen von Kxyprolis bekannt: 73 Mio in Q4
http://boerse.ard.de/aktien/amgen-der-riese-bleibt-am-boden1…
Alle Augen auf Kyprolis
Im laufenden Jahr wird sich die Aufmerksamkeit der Anleger mehr denn je auf das Blutkrebsmittel Kyprolis und die potenzielle Ausweitung seines Anwendungsgebietes fokussieren. Der Schlüssel zum Kursverlauf der Amgen-Aktie während der kommenden sechs Monate dürften neue Daten zu Kyprolis sein, unterstrich Mark Schoenebaum, Analyst des Researchhauses ISI Group.
Im vergangenen Quartal setzte Amgen mit dem 2012 von der FDA zugelassenen Medikament zwar lediglich 73 Millionen Dollar um nach 65 Millionen Dollar im Vorquartal. Doch Kyprolis gilt als "Blockbuster"-Favorit, Analysten trauen dem Mittel Umsätze von mehr als zwei Milliarden Dollar zu.
Erst Euphorie, dann Ernüchterung
Um sich die Rechte an dem viel versprechenden Medikament zu sichern, hatte Amgen den Bayer-Partner Onyx im August 2014 für 10,4 Milliarden Dollar geschluckt. Um die Verhältnisse deutlich zu machen: In der Biotech-Industrie steht Onyx für die fünftgrößte Transaktion überhaupt. Für Amgen war es nach der 16 Milliarden Dollar teuren Übernahme von Immunex der zweitgrößte Zukauf.
An der Börse wurde Amgen für den Deal zunächst gefeiert, doch mittlerweile ist Ernüchterung eingekehrt. Immer wieder verunsicherten skeptische Analystenstimmen zu Kyprolis die Anleger. Die Amgen-Aktie hinkte im vierten Quartal mit einem Plus von 1,9 Prozent dem S&P 500 (plus 9,9 Prozent) klar hinterher.
Die zunehmende Skepsis der Analysten wird in dieser Graphik deutlich:

Da Kyprolis natürlich auch für LGND wichtig bleibt ist das Ganze nicht ohne Risiko....
Alle Augen auf Kyprolis
Im laufenden Jahr wird sich die Aufmerksamkeit der Anleger mehr denn je auf das Blutkrebsmittel Kyprolis und die potenzielle Ausweitung seines Anwendungsgebietes fokussieren. Der Schlüssel zum Kursverlauf der Amgen-Aktie während der kommenden sechs Monate dürften neue Daten zu Kyprolis sein, unterstrich Mark Schoenebaum, Analyst des Researchhauses ISI Group.
Im vergangenen Quartal setzte Amgen mit dem 2012 von der FDA zugelassenen Medikament zwar lediglich 73 Millionen Dollar um nach 65 Millionen Dollar im Vorquartal. Doch Kyprolis gilt als "Blockbuster"-Favorit, Analysten trauen dem Mittel Umsätze von mehr als zwei Milliarden Dollar zu.
Erst Euphorie, dann Ernüchterung
Um sich die Rechte an dem viel versprechenden Medikament zu sichern, hatte Amgen den Bayer-Partner Onyx im August 2014 für 10,4 Milliarden Dollar geschluckt. Um die Verhältnisse deutlich zu machen: In der Biotech-Industrie steht Onyx für die fünftgrößte Transaktion überhaupt. Für Amgen war es nach der 16 Milliarden Dollar teuren Übernahme von Immunex der zweitgrößte Zukauf.
An der Börse wurde Amgen für den Deal zunächst gefeiert, doch mittlerweile ist Ernüchterung eingekehrt. Immer wieder verunsicherten skeptische Analystenstimmen zu Kyprolis die Anleger. Die Amgen-Aktie hinkte im vierten Quartal mit einem Plus von 1,9 Prozent dem S&P 500 (plus 9,9 Prozent) klar hinterher.
Die zunehmende Skepsis der Analysten wird in dieser Graphik deutlich:

Da Kyprolis natürlich auch für LGND wichtig bleibt ist das Ganze nicht ohne Risiko....
Bei LGND wurde eine Initiative gestartet, die ein Spinnoff der R&D Abteilung zum Ziel hat. Vorteil wäre wohl, dass diese dann genug Geld für eine weitere Finanzierung hätte, während der Rest die Royalties ohne die "Verluste" der Entwicklungsabteilung verbuchen könnte. Mir solls Wurscht sein.
http://www.spinoffligandrnd.com/the-blog.html
Ich habe meine doch recht große Position verkleinert, auch wenn es charttechnisch noch bis 75$ gehen könnte. Fundamental ist die Bewertung mir aber mittlerweile zu hoch. Das BACE Programm habe ich dabei allerdings ausgeklammert.
http://www.spinoffligandrnd.com/the-blog.html
Ich habe meine doch recht große Position verkleinert, auch wenn es charttechnisch noch bis 75$ gehen könnte. Fundamental ist die Bewertung mir aber mittlerweile zu hoch. Das BACE Programm habe ich dabei allerdings ausgeklammert.
Also was das Timing meiner Gewinnmitnahmen anbetrifft habe ich definitiv noch Luft nach Oben!!
LGND gab heute Breaktrough Designation für Promacta bekannt:
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Habe mich schon länger gewundert, dass GsK nicht aggressiver bei vielen Blutkrebsarten vorgeht. Für mich waren auch andere Ergebnisse schon exellent.
Das ist eine extrem gute Nachtricht, weil es die Wachstumsmöglichkeiten von Promacta unterstreicht!

LGND gab heute Breaktrough Designation für Promacta bekannt:
http://finance.yahoo.com/news/ligand-partner-glaxosmithkline…
Habe mich schon länger gewundert, dass GsK nicht aggressiver bei vielen Blutkrebsarten vorgeht. Für mich waren auch andere Ergebnisse schon exellent.
Das ist eine extrem gute Nachtricht, weil es die Wachstumsmöglichkeiten von Promacta unterstreicht!
GSK heute mit Zahlen:
Promacta 84 Mio UD$ in Q4
Es bleibt also ungefähr bei einem Wachtum von 10% von Q zu Q.
Promacta 84 Mio UD$ in Q4
Es bleibt also ungefähr bei einem Wachtum von 10% von Q zu Q.
Heute Ligand mit Zahlen, die scheinbar gut ankommen. Haben auf jeden Fall die eigene Guidance übertroffen: Umsatz 49 Mio statt 41, EPS 0,55 statt 0,35
http://www.wallstreet-online.de/nachricht/6561460-ligand-rep…
Im CC fand ich interessant und neu, dass PIII Ergebnisse von Promacta in peadiatric ITP (laut CC die Hälfte aller weltweiten Fälle) in diesem Jahr anstehen. Dazu noch die Breakthrough Designation bei AA. Hier sind die Zeichen also weiter auf Wachstum. Nächstes Jahr könnte schon die 400 Mio-Grenze erreicht werden. Das ist deshalb interessant, weil ab dann die Royalties bei 9,x % liegen.
Ansonsten wurde im CC mal wieder deutlich, wie viele Kandidaten LGND hat.
Vielleicht rücken auch die eigenen Kandidaten wieder mehr in den Vordergrund bzw. werden verpartnert.
http://www.wallstreet-online.de/nachricht/6561460-ligand-rep…
Im CC fand ich interessant und neu, dass PIII Ergebnisse von Promacta in peadiatric ITP (laut CC die Hälfte aller weltweiten Fälle) in diesem Jahr anstehen. Dazu noch die Breakthrough Designation bei AA. Hier sind die Zeichen also weiter auf Wachstum. Nächstes Jahr könnte schon die 400 Mio-Grenze erreicht werden. Das ist deshalb interessant, weil ab dann die Royalties bei 9,x % liegen.
Ansonsten wurde im CC mal wieder deutlich, wie viele Kandidaten LGND hat.
Vielleicht rücken auch die eigenen Kandidaten wieder mehr in den Vordergrund bzw. werden verpartnert.
Ligand ist nun charttechnisch im Bereich eines evtl. größeren Widerstandes angelangt, der allerdings aus den Jahren 2007 u. 2005 kommt.

Das ging jetzt schnell:
http://www.wallstreet-online.de/nachricht/6609165-ligand-par…
http://www.wallstreet-online.de/nachricht/6609165-ligand-par…
GsK gibt heute bekannt, dass sie u.A. die Onkologiesparte an Novartis verkaufen. Dies beinhaltet auch Promacta (so wie ich es versthe komplett). Schwer zu sagen, ob das gut oder schlecht für LGND ist. Bin auf die Marktreaktion heute gespannt.
Gerade im Bereich Onkologie hätte Promacta Imho noch beträchtliche Wachstumschancen. Mal sehen was Novartis plant...
Randnotiz:
Kyprolis: Amgen kauft Onyx
Promacta: Novartis kauft Rechte von GsK
BACE: Merck kauft Shering-Plough
Avinza: Pfizer kauft King
Duravee: Pfizer kauft Wyeth
...
http://www.cash.ch/news/alle/novartis_vollzieht_portfoliober…
Gerade im Bereich Onkologie hätte Promacta Imho noch beträchtliche Wachstumschancen. Mal sehen was Novartis plant...
Randnotiz:
Kyprolis: Amgen kauft Onyx
Promacta: Novartis kauft Rechte von GsK
BACE: Merck kauft Shering-Plough
Avinza: Pfizer kauft King
Duravee: Pfizer kauft Wyeth
...
http://www.cash.ch/news/alle/novartis_vollzieht_portfoliober…
Ligand hatte gestern einen Wert von fast 1,5 Milliarden US$. Ich halte die Bewertung schon länger - und jetzt erst recht - für sehr ambitioniert und habe heute meine letzten Stücke (abgeltungssteuerfrei ) verkauft.
) verkauft.
Amgen gab gestern die Zahlen für Kyprolis bekannt, die mit 68 Mio$ enttäuschten. Viel hängt da jetzt eben von den PIII Ergebnissen ab und das Risiko möchte ich vermeiden.
Wie sich der Novartis-GSK-Deal für Promacta auswirkt muss man erst noch sehen.
Ligand wird dieses Jahr m.E. evtl. eine Gewinnwarnung herausgeben müssen. Zumindest ist mir nicht so ganz klar, woher das Wachstum kommen soll?
Ich schaue mir das Ganze also erstmal von der Seitenlinie an und würde erst wieder einsteigen, wenn der Kurs zurückkommt oder absehbar ist, wie es mit Promacta (AML/MDS), Kyprolis (P III Ergebnisse) und/oder dem BACE Programm weitergeht.
 ) verkauft.
) verkauft. Amgen gab gestern die Zahlen für Kyprolis bekannt, die mit 68 Mio$ enttäuschten. Viel hängt da jetzt eben von den PIII Ergebnissen ab und das Risiko möchte ich vermeiden.
Wie sich der Novartis-GSK-Deal für Promacta auswirkt muss man erst noch sehen.
Ligand wird dieses Jahr m.E. evtl. eine Gewinnwarnung herausgeben müssen. Zumindest ist mir nicht so ganz klar, woher das Wachstum kommen soll?
Ich schaue mir das Ganze also erstmal von der Seitenlinie an und würde erst wieder einsteigen, wenn der Kurs zurückkommt oder absehbar ist, wie es mit Promacta (AML/MDS), Kyprolis (P III Ergebnisse) und/oder dem BACE Programm weitergeht.
Novartis - ganz großes Kino. Geben heute schon bekannt, wie es nach dem GSK-Deal weitergeht. Und siehe da: 2015 geplanter Antrag auf Zulassung von Promacta bei AML/MDS!! Das sind m.E. ganz hervorragende Nachrichten. Toll! Überlege gleich wieder einzusteigen, werde aber versuchen geduldig zu sein...


Ich finde es schon kriminell, was in den USA so möglich ist. Ein Hedgefonds (der short ist) gibt über SA den so ziemlich absurdesten Bericht, den ich je gelesen habe. Wer sich amüsieren möchte - ich sage nur Abwärtspotenzial 100%:
http://seekingalpha.com/article/2270903-ligand-pharmaceutica…
Hier der "Verfasser":
http://en.wikipedia.org/wiki/Emmanuel_Lemelson
Der Kurs gab zunächst tatsächlich um fast 10% nach. Unfassbar!
http://seekingalpha.com/article/2270903-ligand-pharmaceutica…
Hier der "Verfasser":
http://en.wikipedia.org/wiki/Emmanuel_Lemelson
Der Kurs gab zunächst tatsächlich um fast 10% nach. Unfassbar!
Es ist wirklich komisch, dass sich keiner für LGND interessiert. Dabei hat sich der Kurs phantastisch entwickelt. Selbt der jüngste Ausverkauf konnte LGND nicht viel anhaben. Um die Eingangsfrage zu beantworten. Ja das war ein Turnaround vor dem Herren 
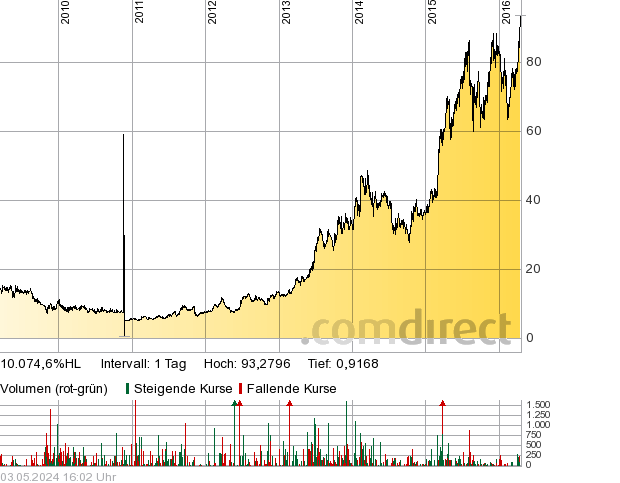
Leider seit einiger Zeit ohne mich. Aber ich will mich auch gar nicht groß beschweren...
Wer sich tatsächlich für Ligand interessiert sollte sich mal die aktualisierte Homepage ansehen. Die Pipeline ist extrem beeindruckend. Mittlerweile über 140 Medikamente. Das Geschäftsmodell ist einzigartig. Ligand verpartnert grundsätzlich und hat dadurch gleichbleibende Ausgaben bei steigenden Umsätzen. Steigende Royalties bei gleich bleibenden Kosten! Das ist ein unfassbar gutes Geschäftsmodell.
http://www.ligand.com/portfolio-summary/portfolio

Leider seit einiger Zeit ohne mich. Aber ich will mich auch gar nicht groß beschweren...
Wer sich tatsächlich für Ligand interessiert sollte sich mal die aktualisierte Homepage ansehen. Die Pipeline ist extrem beeindruckend. Mittlerweile über 140 Medikamente. Das Geschäftsmodell ist einzigartig. Ligand verpartnert grundsätzlich und hat dadurch gleichbleibende Ausgaben bei steigenden Umsätzen. Steigende Royalties bei gleich bleibenden Kosten! Das ist ein unfassbar gutes Geschäftsmodell.
http://www.ligand.com/portfolio-summary/portfolio
Antwort auf Beitrag Nr.: 52.201.453 von kmastra am 15.04.16 22:56:29Ich habe den Kursrückgang nach den etwas schwachen Zahlen dazu genutzt wieder eine keine Position einzugehen. Die Zahlen wurden m.E. auch falsch aufgenommen, da der Umsatzrückgang vor allem an den Captisol Umsätzen lag, die auch in der Vergangenheit schon unberechenbar schwankend waren. Die Royalties sind dagegen um ca. 50% gestiegen. Zudem gab es Abschreibungen auf die "Tochterfirma" Viking. Auch bei Viking VKTX bin ich eine kleine Position eingegangen. Hier hat man mehr oder weniger alle vielversprechenden Programme von Ligand zusammengefasst die man nicht auslizensieren konnte. Klingt nach Resterampe aber ich denke schon, dass dort auch Überraschungen möglich sind. Z.B. bin ich auf die Studie des SARM bei Hüftoperation gespannt.
Ganz aktuell gab Retrophin einen Erfolg einer P2 bekannt. Ligand bekäme bei Zulassung 9% Royalties. Umsatzschätzungen reichen von 500 Mio bis 1 Milliarde an Spitzenumsätzen! Selbst bei einem Umsatz von nur 250 Mio könnte der EPS von LGND um 1$ steigen.
http://amda-1pla2o.client.shareholder.com/releasedetail.cfm?…
SG kmastra
Ganz aktuell gab Retrophin einen Erfolg einer P2 bekannt. Ligand bekäme bei Zulassung 9% Royalties. Umsatzschätzungen reichen von 500 Mio bis 1 Milliarde an Spitzenumsätzen! Selbst bei einem Umsatz von nur 250 Mio könnte der EPS von LGND um 1$ steigen.
http://amda-1pla2o.client.shareholder.com/releasedetail.cfm?…
SG kmastra
Antwort auf Beitrag Nr.: 53.227.812 von kmastra am 07.09.16 16:31:35Hier eine aktuelle Analystenmeinung zu Retrophin:


Heute leider keine guten Nachrichten von Amgen bzgl. Kyprolis:
http://www.investors.com/news/technology/amgens-multiple-mye…
Natürlich ist Kyprolis jetzt nicht obsolet. Im Anbetracht der doch recht starken Konkurrenz würde ich aber von einem recht langsamen Wachstum ausgehen. Man muss einfach sehen, dass es bessere und bald auch günstigere Wirkstoffe gibt. Man muss aber auch sehen, dass MM ein stark wachsender Markt ist - besonders deshalb weil die Patienten jetzt länger leben. Ärzte haben hier mittlerweile mehrere Optionen. KPTI hat jetzt eine Studie am laufen, in denen Teilnehmer vorher Velcade, Kyprolis, Revlimid, Pomalist und Dazalex gesehen haben - penta refractory! Aber klar, dass heute ist erstmal nicht gut.
Der Hauptanteil der Royalties kommt von Promacta (ca. 45 Mio) und Kyprolis (ca. 9 Mio). Ligand hat in den Präsentationen Anaystenschätzungen zu den Umsätzen von beiden Wirkstoffen gezeigt. Dabei fällt auf, dass Kyprolis sich mit ca. 500 Mio Umsatz momentan etwa am unteren Ende der Analystenschätzungen bewegt, während Promacta sich mit 600 Mio Umsatz ziemlich genau am oberen Ende bewegt.

Besser als umgekehrt, denn alles Wachstum bei Promacta findet jetzt in der Royaltystufe 9,4% statt (ab 400 Mio), während Kyprolis zwischen 500 und 750 Mio nur 2,5% Umsatzbeteiligung bringt.
Von daher besteht die Hoffnung, dass die schwächeren Umsätze von Kyprolis sich durch bessere Umsätze bei Promacta ausgleichen lassen...
SG kmastra
http://www.investors.com/news/technology/amgens-multiple-mye…
Natürlich ist Kyprolis jetzt nicht obsolet. Im Anbetracht der doch recht starken Konkurrenz würde ich aber von einem recht langsamen Wachstum ausgehen. Man muss einfach sehen, dass es bessere und bald auch günstigere Wirkstoffe gibt. Man muss aber auch sehen, dass MM ein stark wachsender Markt ist - besonders deshalb weil die Patienten jetzt länger leben. Ärzte haben hier mittlerweile mehrere Optionen. KPTI hat jetzt eine Studie am laufen, in denen Teilnehmer vorher Velcade, Kyprolis, Revlimid, Pomalist und Dazalex gesehen haben - penta refractory! Aber klar, dass heute ist erstmal nicht gut.
Der Hauptanteil der Royalties kommt von Promacta (ca. 45 Mio) und Kyprolis (ca. 9 Mio). Ligand hat in den Präsentationen Anaystenschätzungen zu den Umsätzen von beiden Wirkstoffen gezeigt. Dabei fällt auf, dass Kyprolis sich mit ca. 500 Mio Umsatz momentan etwa am unteren Ende der Analystenschätzungen bewegt, während Promacta sich mit 600 Mio Umsatz ziemlich genau am oberen Ende bewegt.

Besser als umgekehrt, denn alles Wachstum bei Promacta findet jetzt in der Royaltystufe 9,4% statt (ab 400 Mio), während Kyprolis zwischen 500 und 750 Mio nur 2,5% Umsatzbeteiligung bringt.
Von daher besteht die Hoffnung, dass die schwächeren Umsätze von Kyprolis sich durch bessere Umsätze bei Promacta ausgleichen lassen...
SG kmastra
Zahlen, eine Zulassung und ein Zulassungsantrag
Novartis und Amgen mit Zahlen:
Promacta 168 Mio (158 in Q2)
Kyprolis 183 Mio (172 in Q2 aber kein Wachstum in US)
Lundbeck hat die Zulassung für eine IV Form von carbamazepine erhalten.
LGND bekommt 2,75% royalties und 1,25 Mio Meilensteinzahlung.
https://finance.yahoo.com/news/ligand-partner-lundbeck-recei…
Melinta hat die Zulassung von Baxdela beantragt.
LGND bekäme 2,5% royalties und 1,5 Mio Meilensteinzahlung bei Zulassung (bekamen schon 1,5 Mio für den Antrag).
https://finance.yahoo.com/news/ligand-partner-melinta-therap…
Am 3.11. dann die Zahlen von LGND selber. Ob gut oder schlecht hängt vor allem an den Captisol Verkäufen, die sehr schwankend und schwer berrechenbar sind...
SG kmastra
Novartis und Amgen mit Zahlen:
Promacta 168 Mio (158 in Q2)
Kyprolis 183 Mio (172 in Q2 aber kein Wachstum in US)
Lundbeck hat die Zulassung für eine IV Form von carbamazepine erhalten.
LGND bekommt 2,75% royalties und 1,25 Mio Meilensteinzahlung.
https://finance.yahoo.com/news/ligand-partner-lundbeck-recei…
Melinta hat die Zulassung von Baxdela beantragt.
LGND bekäme 2,5% royalties und 1,5 Mio Meilensteinzahlung bei Zulassung (bekamen schon 1,5 Mio für den Antrag).
https://finance.yahoo.com/news/ligand-partner-melinta-therap…
Am 3.11. dann die Zahlen von LGND selber. Ob gut oder schlecht hängt vor allem an den Captisol Verkäufen, die sehr schwankend und schwer berrechenbar sind...
SG kmastra
Antwort auf Beitrag Nr.: 53.569.911 von kmastra am 27.10.16 22:42:58"Umsatzwarnung", Rekorde, ein Ausrufezeichen, ein Fragezeichen und Nachschub
Die Zahlen waren aufgrund der Captisol Verkäufe nicht gut. LGND hat sogar die Ziele für das Jahr etwas zurückgeschraubt. Dafür sind neben den schwachen Captisol Umsätzen auch steuerliche Gründe verantwortlich. Ligand zahlt momentan einen recht geringen Steuersatz. So wie ich es verstehe werden vorherige Verluste geltend gemacht. Von steuerlichen Dingen habe ich aber 0,0 Ahnung, von daher...
Positiv an den Zahlen waren die Royalties. Und das ist das Wichtigste. Diese sind aufgrund der Umsätze von Promacta und Kyprolis auf Rekordniveau (15,7 vs. 9,8 Mio im Vorjahr). Aufgrund der mit zunehmenden Umsatz anstiegenden Royalties wachsen diese überproportional im Vergleich zu den Umsätzen der Medikamente selber. (60% vs. 45%). Dies wird in den nächsten beiden Quartalen so bleiben, da die Umsätze immer um ein Quartal verschoben verbucht werden. Also in Q1 am meisten, da dann die höchste Royaltystufe erreicht ist.
Zusätzlich gaben die Zahlen von SPPI Anlass zur Hoffnung. Im letzen Q hat Spectrum 5,9 Mio (vs. 0,9 im Vorquartal) durch Evomela umgesetzt. Klingt nicht viel. Ligand bekommt hier aber 20% Royalties! Wenn der Umsatz nicht auf Einmaleffekte zurückzuführen ist (Lagerbestände etc.) und der Umsatz sogar weiter gesteigert werden kann, könnte das die 3. Säule der Royaltyeinnahmen werden.
Gleichzeitig sorgte Spectrum aber auch für ein Fragezeichen. Sie wollen nochmal prüfen, wie sie die Umsätze von Evomela verbuchen. Laut LGND Management habe dies zwar keinen Einfluss auf LGND selber aber man muss hier sicher abwarten, ob das wirklich nur ein internes Problem ist?
Aldeyra Therapeutics startet gleich 2 PIII Studien für NS2. Es handelt sich um ein mit Captisol formuliertes Program. Die genauen Konditionen sind noch geheim. Von daher wird man abwarten müssen. Falls überhaupt gäbe es nur eine geringe prozentuale Umsatzbeteiligung zusätzlich zu den material sales.
http://finance.yahoo.com/news/ligand-reports-third-quarter-2…
SG kmastra
Die Zahlen waren aufgrund der Captisol Verkäufe nicht gut. LGND hat sogar die Ziele für das Jahr etwas zurückgeschraubt. Dafür sind neben den schwachen Captisol Umsätzen auch steuerliche Gründe verantwortlich. Ligand zahlt momentan einen recht geringen Steuersatz. So wie ich es verstehe werden vorherige Verluste geltend gemacht. Von steuerlichen Dingen habe ich aber 0,0 Ahnung, von daher...
Positiv an den Zahlen waren die Royalties. Und das ist das Wichtigste. Diese sind aufgrund der Umsätze von Promacta und Kyprolis auf Rekordniveau (15,7 vs. 9,8 Mio im Vorjahr). Aufgrund der mit zunehmenden Umsatz anstiegenden Royalties wachsen diese überproportional im Vergleich zu den Umsätzen der Medikamente selber. (60% vs. 45%). Dies wird in den nächsten beiden Quartalen so bleiben, da die Umsätze immer um ein Quartal verschoben verbucht werden. Also in Q1 am meisten, da dann die höchste Royaltystufe erreicht ist.
Zusätzlich gaben die Zahlen von SPPI Anlass zur Hoffnung. Im letzen Q hat Spectrum 5,9 Mio (vs. 0,9 im Vorquartal) durch Evomela umgesetzt. Klingt nicht viel. Ligand bekommt hier aber 20% Royalties! Wenn der Umsatz nicht auf Einmaleffekte zurückzuführen ist (Lagerbestände etc.) und der Umsatz sogar weiter gesteigert werden kann, könnte das die 3. Säule der Royaltyeinnahmen werden.
Gleichzeitig sorgte Spectrum aber auch für ein Fragezeichen. Sie wollen nochmal prüfen, wie sie die Umsätze von Evomela verbuchen. Laut LGND Management habe dies zwar keinen Einfluss auf LGND selber aber man muss hier sicher abwarten, ob das wirklich nur ein internes Problem ist?
Aldeyra Therapeutics startet gleich 2 PIII Studien für NS2. Es handelt sich um ein mit Captisol formuliertes Program. Die genauen Konditionen sind noch geheim. Von daher wird man abwarten müssen. Falls überhaupt gäbe es nur eine geringe prozentuale Umsatzbeteiligung zusätzlich zu den material sales.
http://finance.yahoo.com/news/ligand-reports-third-quarter-2…
SG kmastra
https://endpts.com/the-fda-just-signed-off-on-a-formula-1-pi…
Eine Zulassung in Post Partum Depression wird von SAGE nun doch für 547 angestrebt und nicht (gleich) für 217. Das ist deswegen relevant für LGND, weil sie für 547 3% Royalties bekommen (Captisol) und für 217 nichts. Gemeinhin ging man davon aus, dass SAGE sich in PPD gleich auf die Tablettenform konzentriert. Ich denke, dass die FDA klar signalisiert hat, dass dies die Zulassung verzögern könnte (547 hat auch die BTD in PPD). Langfrsitig könnte es so sein, dass die IV Version (547) für schwere Fälle und die orale Version für leichetere Fälle gedacht ist. 547 finde ich das beste Program aus den Big 6:

Zwar sind die Peak Revenues for LGND (rechte Spalte) recht optimistisch, aber es sind eben Royalties (100% Marge). Bedenken muss man auch, dass LGND ca. 21 Mio outstanding shares hat. Royalties von 21 Mio steigern also den Gewinn/Aktie vor Steuer um 1$. LGND zahlt zudem kaum Steuern. Vielleicht ändert sich das unter Trump aber noch, denn da kennt er sich ja scheinbar aus...
SG kmastra
Eine Zulassung in Post Partum Depression wird von SAGE nun doch für 547 angestrebt und nicht (gleich) für 217. Das ist deswegen relevant für LGND, weil sie für 547 3% Royalties bekommen (Captisol) und für 217 nichts. Gemeinhin ging man davon aus, dass SAGE sich in PPD gleich auf die Tablettenform konzentriert. Ich denke, dass die FDA klar signalisiert hat, dass dies die Zulassung verzögern könnte (547 hat auch die BTD in PPD). Langfrsitig könnte es so sein, dass die IV Version (547) für schwere Fälle und die orale Version für leichetere Fälle gedacht ist. 547 finde ich das beste Program aus den Big 6:

Zwar sind die Peak Revenues for LGND (rechte Spalte) recht optimistisch, aber es sind eben Royalties (100% Marge). Bedenken muss man auch, dass LGND ca. 21 Mio outstanding shares hat. Royalties von 21 Mio steigern also den Gewinn/Aktie vor Steuer um 1$. LGND zahlt zudem kaum Steuern. Vielleicht ändert sich das unter Trump aber noch, denn da kennt er sich ja scheinbar aus...
SG kmastra
Die nächste Short-Attacke von Emmanuel Lemelson:
Zur Einordnung. Der Herr hatte schon 2014 behauptet, dass LGND 0$ Wert sei. Scheinbar will er jetzt noch kurz vor Jahresende einige Positionen im Zuge des Tax Loss Sellings glatt stellen.
Die Argumentation ist selten dämlich. LGND wird hier z.B. in die Nähe von Shkreli, Valeant und Co gebracht (Exorbitante Preissteigerungen bei Generika). LGND hat aber mit Promacta und Kyprolis durchaus innovative, neue Medikamente entwickelt. Im Grunde sogar nur dabei geholfen. Vermarktet werden diese nun durch Novartis und Amgen. Es ist einfach nur offensichtlich, dass Lemelson versucht, LGND in ein schlechtes Licht zu rücken, um Profite zu machen.
Hier der Link...
https://de.scribd.com/document/334799493/Fr-Emmanuel-Lemelso…
Mit meiner Meinung bin ich nicht allein.

Erfreulich hingegen, dass mit Ono ein weiterer Partner gefunden wurde.
Interessant finde ich zudem, dass man mit Novartis eine Kooperation eingegangen ist. Dort will man für den MEK-Inhibitor trametinib eine "oral liquid formulation" mit Hilfe von Captisol entwickeln. Schön für LGND aber interessant auch für ARRY und EXEL, die auch einen MEK Inhibitor auf dem Markt bzw. fast auf dem Markt haben. Captisol wird gemeinhin eingestzt, um die Löslichkeit/Aufnahme zu erhöhen. Sieht Novartis da Probleme?
Vielleicht auch eine Reaktion auf die guten Ergebnisse von Binimetinib?
Zur Einordnung. Der Herr hatte schon 2014 behauptet, dass LGND 0$ Wert sei. Scheinbar will er jetzt noch kurz vor Jahresende einige Positionen im Zuge des Tax Loss Sellings glatt stellen.
Die Argumentation ist selten dämlich. LGND wird hier z.B. in die Nähe von Shkreli, Valeant und Co gebracht (Exorbitante Preissteigerungen bei Generika). LGND hat aber mit Promacta und Kyprolis durchaus innovative, neue Medikamente entwickelt. Im Grunde sogar nur dabei geholfen. Vermarktet werden diese nun durch Novartis und Amgen. Es ist einfach nur offensichtlich, dass Lemelson versucht, LGND in ein schlechtes Licht zu rücken, um Profite zu machen.
Hier der Link...
https://de.scribd.com/document/334799493/Fr-Emmanuel-Lemelso…
Mit meiner Meinung bin ich nicht allein.

Erfreulich hingegen, dass mit Ono ein weiterer Partner gefunden wurde.
Interessant finde ich zudem, dass man mit Novartis eine Kooperation eingegangen ist. Dort will man für den MEK-Inhibitor trametinib eine "oral liquid formulation" mit Hilfe von Captisol entwickeln. Schön für LGND aber interessant auch für ARRY und EXEL, die auch einen MEK Inhibitor auf dem Markt bzw. fast auf dem Markt haben. Captisol wird gemeinhin eingestzt, um die Löslichkeit/Aufnahme zu erhöhen. Sieht Novartis da Probleme?
Vielleicht auch eine Reaktion auf die guten Ergebnisse von Binimetinib?
Evomela:
Spectrums Partner hat die "Zulasung" in China eingereicht:
http://finance.yahoo.com/news/casi-pharmaceuticals-import-dr…
LGND bekäme wohl auch hier 20% der Netsales. Allerdings wird Melphalan in China momentan nicht benutzt.
Ab 40:00 zum Thema Evomela vs. Melphalan:
http://www.curetalks.com/event/rsvp/Post-Transplant-Outcomes…
Spectrums Partner hat die "Zulasung" in China eingereicht:
http://finance.yahoo.com/news/casi-pharmaceuticals-import-dr…
LGND bekäme wohl auch hier 20% der Netsales. Allerdings wird Melphalan in China momentan nicht benutzt.
Ab 40:00 zum Thema Evomela vs. Melphalan:
http://www.curetalks.com/event/rsvp/Post-Transplant-Outcomes…
Antwort auf Beitrag Nr.: 53.569.911 von kmastra am 27.10.16 22:42:58Es scheint so zu kommen wie vermutet:
Promacta wächst weiter (178 Mio$ Umsatz in Q4vs. 168 in Q3) und Kyprolis stagniert (183 Mio in Q4 vs. 183 in Q3).
Promacta wächst weiter (178 Mio$ Umsatz in Q4vs. 168 in Q3) und Kyprolis stagniert (183 Mio in Q4 vs. 183 in Q3).
Antwort auf Beitrag Nr.: 54.228.058 von kmastra am 02.02.17 22:38:58Kurzes Update:
LGND zwischenzeitlich mit Zahlen, die kurzfristig für Irritationen gesorgt haben. LGND hat mehr oder weniger einen genauen Ausblick verweigert. Das liegt aber nur an den Captisol Umsätzen, die scheinbar schwer zu planen sind. Ebenso ist wohl der genaue Steuersatz schwer planbar, solange von Trump keine Fakten kommen. Wichtiger ist aber, dass die Royalties wie geplant steigen. Und da sieht es gut aus. Besonders SPPI hat mit den Zahlen zu Evomela positiv überrascht (9,4 Mio). SPPI ist es doch recht schnell gelungen, gut 1/3 des Melphalanmarktes zu erobern. Somit ist Evomela auf Anhieb gleichzusetzen mit Kyprolis, da hier die Royalties bei 20% liegen. Man kann im nächsten Jahr wohl von 50 Mio Umsatz ausgehen = 10 Mio Royalties= +0,5 EPS vor Steuern. Folgerichtig spricht LGND jetzt in seinen Präsentationen von den big 3...
http://investor.ligand.com/press-releases/detail/315/ligand-…
Zudem gab es zur Abwechslung mal wieder gute Ergebnisse von Kyprolis:
http://wwwext.amgen.com/media/news-releases/2017/02/phase-3-…
SG kmastra
LGND zwischenzeitlich mit Zahlen, die kurzfristig für Irritationen gesorgt haben. LGND hat mehr oder weniger einen genauen Ausblick verweigert. Das liegt aber nur an den Captisol Umsätzen, die scheinbar schwer zu planen sind. Ebenso ist wohl der genaue Steuersatz schwer planbar, solange von Trump keine Fakten kommen. Wichtiger ist aber, dass die Royalties wie geplant steigen. Und da sieht es gut aus. Besonders SPPI hat mit den Zahlen zu Evomela positiv überrascht (9,4 Mio). SPPI ist es doch recht schnell gelungen, gut 1/3 des Melphalanmarktes zu erobern. Somit ist Evomela auf Anhieb gleichzusetzen mit Kyprolis, da hier die Royalties bei 20% liegen. Man kann im nächsten Jahr wohl von 50 Mio Umsatz ausgehen = 10 Mio Royalties= +0,5 EPS vor Steuern. Folgerichtig spricht LGND jetzt in seinen Präsentationen von den big 3...
http://investor.ligand.com/press-releases/detail/315/ligand-…
Zudem gab es zur Abwechslung mal wieder gute Ergebnisse von Kyprolis:
http://wwwext.amgen.com/media/news-releases/2017/02/phase-3-…
SG kmastra
Zwischenzeitlich Zahlen von Novartis, Amgen und Spectrum. Die Zeichen stehen auf Wachstum:
Promacta 210 Mio
Kyprolis 211 Mio
Evomela 10 Mio
Am 7.8. dann die Zahlen von LGND. Bei den Royalties läufts...
Promacta 210 Mio
Kyprolis 211 Mio
Evomela 10 Mio
Am 7.8. dann die Zahlen von LGND. Bei den Royalties läufts...
Antwort auf Beitrag Nr.: 55.462.554 von kmastra am 04.08.17 22:21:23Promacta in Q3 bei 227 Mio$.
Ich habe LGND aktuell nicht mehr im Depot, dafür aber mit RIGL einen last line bzw. Kombi Kandidaten bei ITP (in der Zulassung) und mit VKTX ein LGND Spin Off.
LGND ist aber einfach ein Top-Wert!
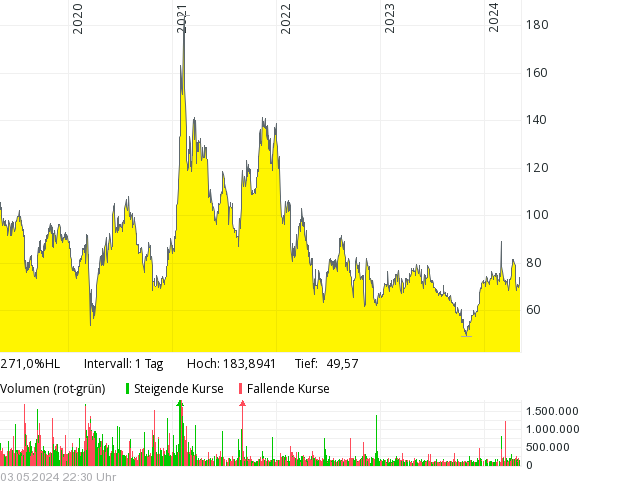
Ich habe LGND aktuell nicht mehr im Depot, dafür aber mit RIGL einen last line bzw. Kombi Kandidaten bei ITP (in der Zulassung) und mit VKTX ein LGND Spin Off.
LGND ist aber einfach ein Top-Wert!
Schöne Outperformance!
Antwort auf Beitrag Nr.: 47.160.932 von kmastra am 16.06.14 23:11:07
Den Typen haben sie jetzt verknackt!
Zitat von kmastra: Ich finde es schon kriminell, was in den USA so möglich ist. Ein Hedgefonds (der short ist) gibt über SA den so ziemlich absurdesten Bericht, den ich je gelesen habe. Wer sich amüsieren möchte - ich sage nur Abwärtspotenzial 100%:
http://seekingalpha.com/article/2270903-ligand-pharmaceutica…
Hier der "Verfasser":
http://en.wikipedia.org/wiki/Emmanuel_Lemelson
Der Kurs gab zunächst tatsächlich um fast 10% nach. Unfassbar!
Den Typen haben sie jetzt verknackt!
Die Zahlen sind doch super oder habe ich was übersehen. Warum fällt der Kurs so stark ?
Antwort auf Beitrag Nr.: 59.186.469 von HeiBay am 10.11.18 15:11:12Schwer zu sagen. Vielleicht war er vorher einfach ach zu stark gestiegen?
Wirkliche News gab es nicht. Zahlen waren besser als erwartet. Eventuell auch sell the news.
Langfristig muss man aber sehen, dass bei Promacta in ein paar Jahren der Patentschutz ausläuft.
Wirkliche News gab es nicht. Zahlen waren besser als erwartet. Eventuell auch sell the news.
Langfristig muss man aber sehen, dass bei Promacta in ein paar Jahren der Patentschutz ausläuft.
Aktuell die nächste Short Attacke diesmal von Citron. Kursziel ist 35$ was totaler Blödsinn ist!
Citron lag einmal ganz gut (Valeant) und seitdem mehrfach böse daneben. Gutes Beispiel ist SAGE. Da haben sie mit ihrer Short Attacke richtig daneben gelegen. Totale Totgeburt!
Für Unsicherheit und Panik reicht es aus! Nettes und recht simples Geschäftsmodell!
Citron lag einmal ganz gut (Valeant) und seitdem mehrfach böse daneben. Gutes Beispiel ist SAGE. Da haben sie mit ihrer Short Attacke richtig daneben gelegen. Totale Totgeburt!
Für Unsicherheit und Panik reicht es aus! Nettes und recht simples Geschäftsmodell!
mal sehen wie weit es runter geht. Könnte eine sehr gute Einstiegs Gelegebheit sein. Bist du wieder investiert?
Antwort auf Beitrag Nr.: 59.648.609 von Steel21x am 16.01.19 22:47:14Ja aber nur mit einer kleinen Position. Hab heute nochmal ein bisschen nachgekauft und würde erst bei Kursen weit unter 100 nochmal nachlegen.
Hier der Link zum Short:
https://citronresearch.com/wp-content/uploads/2019/01/The-Sm…
Meines Erachtens ist das eine Mischung aus Rosinenpickerei (das was passt wird aufgeführt und das was nicht passt wird verschwiegen) und unberechtigter Kritik (Es ist z.B. ganz normal, dass die genauen Royalties und Milestones nicht bekannt sind - s. Z.B. Morphosys; LGND ist da eher transparent)
Einige Argumente sind nachvollziehbar aber nix Neues (z.B. ist LGND sehr abhängig von Promacta und der Patentschutz läuft in ein paar Jahren aus auch das Projekt von SAGE wird nicht viel bringen)
Was verschwiegen wird:
-Es gibt über 170 voll verpartnerte Projekte - da wird schon was nachkommen.
-Bis zum Patentauslauf wird LGND noch mehrere 100 Mio $ Royalties nur durch Promacta bekommen.
-LGND besteht aus vielen Einzelteilen die man nicht so einfach miteinander vergleichen kann.
-Meilensteine spielen eine untergeordnete Rolle....
Hier der Link zum Short:
https://citronresearch.com/wp-content/uploads/2019/01/The-Sm…
Meines Erachtens ist das eine Mischung aus Rosinenpickerei (das was passt wird aufgeführt und das was nicht passt wird verschwiegen) und unberechtigter Kritik (Es ist z.B. ganz normal, dass die genauen Royalties und Milestones nicht bekannt sind - s. Z.B. Morphosys; LGND ist da eher transparent)
Einige Argumente sind nachvollziehbar aber nix Neues (z.B. ist LGND sehr abhängig von Promacta und der Patentschutz läuft in ein paar Jahren aus auch das Projekt von SAGE wird nicht viel bringen)
Was verschwiegen wird:
-Es gibt über 170 voll verpartnerte Projekte - da wird schon was nachkommen.
-Bis zum Patentauslauf wird LGND noch mehrere 100 Mio $ Royalties nur durch Promacta bekommen.
-LGND besteht aus vielen Einzelteilen die man nicht so einfach miteinander vergleichen kann.
-Meilensteine spielen eine untergeordnete Rolle....
Danke für die Einschätzung.Was mich hier anzieht ist die riesige Pipeline und die Vorhandene Profitabilität. Ich liege auf der Lauer.
Starke Zahlen von Promacta. Novartis hat im Q4 330 Mio umgesetzt. Zum Vergleich: Q4 2017 255 Mio und Q3 2018 295 Mio.
Zudem Amgen mit 250 Mio Umsatz für Kyprolis.
Zudem Amgen mit 250 Mio Umsatz für Kyprolis.
Surprise!
Ligand verkauft seine Royalty Rechte von Promacta an Royalty Pharm. Bekommt dafür immerhin 827 Mio und geht dem Patentrisiko aus dem Weg. (Patente laufen zwischen 2021 und 2018 aus) Da weiß man nicht, wie schnell es zu Generika kommt. Technisch wird das kaum ein Problem darstellen, da es ein small molecule ist. Die Frage ist wie sich die Gerichte positionieren und das ist immer so eine Sache. Von dem Geld her nicht schlecht; ich finde allerdings das Timing nicht so günstig, da momentan die Preise für neue Projekte nicht so günstig sein dürften. Der Aktienmarkt boomt. Im Privatsektor/VC lassen sich (so wie man hört) locker bei Finanzierungsrunden hohe Bewertungen durchdrücken. Ob LGND da einige Schnäppchen in der Mache hat?
Ligand verkauft seine Royalty Rechte von Promacta an Royalty Pharm. Bekommt dafür immerhin 827 Mio und geht dem Patentrisiko aus dem Weg. (Patente laufen zwischen 2021 und 2018 aus) Da weiß man nicht, wie schnell es zu Generika kommt. Technisch wird das kaum ein Problem darstellen, da es ein small molecule ist. Die Frage ist wie sich die Gerichte positionieren und das ist immer so eine Sache. Von dem Geld her nicht schlecht; ich finde allerdings das Timing nicht so günstig, da momentan die Preise für neue Projekte nicht so günstig sein dürften. Der Aktienmarkt boomt. Im Privatsektor/VC lassen sich (so wie man hört) locker bei Finanzierungsrunden hohe Bewertungen durchdrücken. Ob LGND da einige Schnäppchen in der Mache hat?
Antwort auf Beitrag Nr.: 60.028.811 von kmastra am 05.03.19 22:48:09LGND mit Zahlen und genau das ist jetzt das Problem. Man macht wieder Verluste. Auch wenn man das im Laufe des Jahres ausgleichen möchte:
https://investor.ligand.com/press-releases/detail/390/ligand…
https://investor.ligand.com/press-releases/detail/390/ligand…
Antwort auf Beitrag Nr.: 61.134.185 von kmastra am 30.07.19 14:31:46Der Markt in Panik! Die nackten Zahlen sehen im Vergleich auch bescheiden aus. Man muss aber bedenken, dass der Verlust auch durch die schlechte Performance von VKTX zustande kam. Zudem hat LGND 1,3 Milliarden Cash - bei einer Bewertung von 1,9 Milliarden und einem immer noch Gewinn bringenden Geschäftsmodell nicht zu vernachlässigen! Ich hab hier grad zugeschlagen!
Antwort auf Beitrag Nr.: 60.028.811 von kmastra am 05.03.19 22:48:09
Tja, so schnell kann das manchmal gehen! Jetzt steht LGND wieder sehr gut da mit dem Geschäftsmodell. LGND hat ca. 1 Milliarde Cash (600 Mio Schulden). Zudem hat man die Kosten im Griff. Eine Pleite droht definitiv nicht - jetzt kann LGND langfristig als einer der wenigen Biotechs sogar profitieren, weil man das Geld aus dem Promacta Verkauf plötzlich gut investieren kann.

Zitat von kmastra: Surprise!
Ligand verkauft seine Royalty Rechte von Promacta an Royalty Pharm. Bekommt dafür immerhin 827 Mio und geht dem Patentrisiko aus dem Weg. (Patente laufen zwischen 2021 und 2018 aus) Da weiß man nicht, wie schnell es zu Generika kommt. Technisch wird das kaum ein Problem darstellen, da es ein small molecule ist. Die Frage ist wie sich die Gerichte positionieren und das ist immer so eine Sache. Von dem Geld her nicht schlecht; ich finde allerdings das Timing nicht so günstig, da momentan die Preise für neue Projekte nicht so günstig sein dürften. Der Aktienmarkt boomt. Im Privatsektor/VC lassen sich (so wie man hört) locker bei Finanzierungsrunden hohe Bewertungen durchdrücken. Ob LGND da einige Schnäppchen in der Mache hat?
Tja, so schnell kann das manchmal gehen! Jetzt steht LGND wieder sehr gut da mit dem Geschäftsmodell. LGND hat ca. 1 Milliarde Cash (600 Mio Schulden). Zudem hat man die Kosten im Griff. Eine Pleite droht definitiv nicht - jetzt kann LGND langfristig als einer der wenigen Biotechs sogar profitieren, weil man das Geld aus dem Promacta Verkauf plötzlich gut investieren kann.
Ligand ist wirklich ein spannender Wert! Da ist immer was geboten.
Zunächst gute Zahlen, Erhöhung der Prognose etc. weil sie via Captisol an den Verkäufen von Remdesivir von GILD beteiligt sind. Die haben auch wirklich überall ihre Finger im Spiel ;-)
Jetzt ist LGND gestiegen, weil es sich einige zum Hobby gemacht haben in die Werte zu investieren, die besonders stark geshortet sind, um einen Short-Squeeze zu provozieren.
Zunächst gute Zahlen, Erhöhung der Prognose etc. weil sie via Captisol an den Verkäufen von Remdesivir von GILD beteiligt sind. Die haben auch wirklich überall ihre Finger im Spiel ;-)
Jetzt ist LGND gestiegen, weil es sich einige zum Hobby gemacht haben in die Werte zu investieren, die besonders stark geshortet sind, um einen Short-Squeeze zu provozieren.
Antwort auf Beitrag Nr.: 66.705.452 von kmastra am 29.01.21 19:22:38CEO hat kürzlich für 15,2 Mio. USD Aktien verkauft! Und das so kurz vor den Jahreszahlen. Ansonsten super Aufwärtstrend mit weiterem Short-Squeeze-Potential.
https://de.finance.yahoo.com/quote/LGND/insider-transactions…
https://de.finance.yahoo.com/quote/LGND/insider-transactions…
Antwort auf Beitrag Nr.: 66.708.161 von kartman am 29.01.21 21:14:14Das kann ich ihm nicht verdenken. Ich halte LGND momentan auch für fundamental überbewertet.
Wahrscheinlich richtet sich der CEO da auch eher nach fundamentalen Gesichtspunkten und nicht so sehr nach short squeeze Potenzial. LGND ist aber durchaus ein gutes Beispiel dafür, wie skrupellos Short Reporter teilweise vorgehen. Mit der Wahrheit nehmen die es da nicht so genau. Von daher geschieht es ihnen in diesem Fall recht! Kann man so aber auch über die Analysten sagen, die Kaufempfehlungen mit Kurszielen von mehreren 100% raushauen.
Die derzeitige Jagd auf geshortete Aktien ist nochmal ein anderes Thema, das ich extrem kritisch sehe!
Wahrscheinlich richtet sich der CEO da auch eher nach fundamentalen Gesichtspunkten und nicht so sehr nach short squeeze Potenzial. LGND ist aber durchaus ein gutes Beispiel dafür, wie skrupellos Short Reporter teilweise vorgehen. Mit der Wahrheit nehmen die es da nicht so genau. Von daher geschieht es ihnen in diesem Fall recht! Kann man so aber auch über die Analysten sagen, die Kaufempfehlungen mit Kurszielen von mehreren 100% raushauen.
Die derzeitige Jagd auf geshortete Aktien ist nochmal ein anderes Thema, das ich extrem kritisch sehe!
Ich sehe hier auch nur das Squeeze-Potentail. Aber das dafür doppelt und dreifach.Bin daher dabei mit einer Spekulationsposition
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -0,10 | |
| -1,23 | |
| -2,64 | |
| -3,45 | |
| +0,49 | |
| -0,21 | |
| -0,07 | |
| +0,57 | |
| +0,09 | |
| -1,73 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 228 | ||
| 96 | ||
| 90 | ||
| 76 | ||
| 53 | ||
| 49 | ||
| 48 | ||
| 44 | ||
| 42 | ||
| 33 |





















