Spark Therapeutics - 500 Beiträge pro Seite
eröffnet am 21.09.15 10:40:06 von
neuester Beitrag 25.02.19 10:28:18 von
neuester Beitrag 25.02.19 10:28:18 von
Beiträge: 113
ID: 1.218.786
ID: 1.218.786
Aufrufe heute: 0
Gesamt: 20.208
Gesamt: 20.208
Aktive User: 0
ISIN: US84652J1034 · WKN: A12HQS
102,55
EUR
+0,69 %
+0,70 EUR
Letzter Kurs 17.12.19 Tradegate
Neuigkeiten
Werte aus der Branche Pharmaindustrie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,8450 | +163,57 | |
| 0,5470 | +20,09 | |
| 384,00 | +20,00 | |
| 5,9050 | +17,86 | |
| 111,15 | +16,77 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 9,7200 | -19,60 | |
| 14,510 | -32,32 | |
| 71,33 | -33,92 | |
| 3,6400 | -38,62 | |
| 1.160,00 | -42,00 |
Hallo zusammen,
ich möchte einfach mal einen Thread eröffnen für eine
Biotechaktie aus den USA, die mittels Gentherapie bereits
jetzt in der Forschung (Entwicklung) große Erfolge aufzuweisen hat.
Durch einmalige Anwednung einer Gentherapie können Blinde,
zumindest teilweise ihr Augenlicht zurück erhalten.
Daneben gibt es weitere Forschungsprogramme.
Charttechnisch steht die Aktie kurz vor einem möglichen Ausbruch nach
oben.
Gruß
ich möchte einfach mal einen Thread eröffnen für eine
Biotechaktie aus den USA, die mittels Gentherapie bereits
jetzt in der Forschung (Entwicklung) große Erfolge aufzuweisen hat.
Durch einmalige Anwednung einer Gentherapie können Blinde,
zumindest teilweise ihr Augenlicht zurück erhalten.
Daneben gibt es weitere Forschungsprogramme.
Charttechnisch steht die Aktie kurz vor einem möglichen Ausbruch nach
oben.
Gruß
Antwort auf Beitrag Nr.: 50.668.869 von Solideinvestierenkomplex4you am 21.09.15 10:40:06Spark Therapeutics meldet soeben
den Durchbruch in Phase III.
Die Markteinführung einer Behandlung für eine
spezielle Form der Blindheit mittels einmaliger
Gentherapie kann/wird nun erfolgen.
Vorbörslich ist die Aktie bereits auf circa 65 US-$ geschossen.
Nun beginnen aber sicher Überlegungen,
was bei Spark langfristig möglich ist.
Denn neben weiteren Medikamenten gegen Augenerkrankungen
befinden sich auch Gentherapieansätze im Bereich der Haemophilie A und B
in der frühen Pipeline.
Doch jetzt, nach dem erfolgreichen Durchbruch der soeben beschriebenen Therapie,
könnte eventuell damit gerechnet werden, dass auch die Haemophilie A und B
nach einmaliger Gabe einer Gentherapie erfolgreich bekämpft werden kann.
Das könnte ein Riesending werden, wenngleich eine mögliche Markteinführung noch Jahre entfernt sein dürfte.
Und es gibt ein weiteres Produkt gegen eine Krankheit in der Pipeline dieser Firma,
dass der Öffentlichkeit, vermutlich aus Schutz vor Konkurrenz,
noch nicht mitgeteilt wurde.
Kurzfristig könnte der Kursanstieg bei Spark ausgereizt sein.
Aber langfristig werden sich nicht zuletzt auch die Blicke der großen Unternehmen
und der medizinischen Welt auf das meines Wissens erste Medikament richten,
dass überhaupt Gentherapie am Menschen erfolgreich anwenden darf.
Das dürfte Begehrlichkeiten unter den Großen der Branche wecken!?
Leider lässt sich die Firma im Wikifolio nicht kaufen.
Gruß
den Durchbruch in Phase III.
Die Markteinführung einer Behandlung für eine
spezielle Form der Blindheit mittels einmaliger
Gentherapie kann/wird nun erfolgen.
Vorbörslich ist die Aktie bereits auf circa 65 US-$ geschossen.
Nun beginnen aber sicher Überlegungen,
was bei Spark langfristig möglich ist.
Denn neben weiteren Medikamenten gegen Augenerkrankungen
befinden sich auch Gentherapieansätze im Bereich der Haemophilie A und B
in der frühen Pipeline.
Doch jetzt, nach dem erfolgreichen Durchbruch der soeben beschriebenen Therapie,
könnte eventuell damit gerechnet werden, dass auch die Haemophilie A und B
nach einmaliger Gabe einer Gentherapie erfolgreich bekämpft werden kann.
Das könnte ein Riesending werden, wenngleich eine mögliche Markteinführung noch Jahre entfernt sein dürfte.
Und es gibt ein weiteres Produkt gegen eine Krankheit in der Pipeline dieser Firma,
dass der Öffentlichkeit, vermutlich aus Schutz vor Konkurrenz,
noch nicht mitgeteilt wurde.
Kurzfristig könnte der Kursanstieg bei Spark ausgereizt sein.
Aber langfristig werden sich nicht zuletzt auch die Blicke der großen Unternehmen
und der medizinischen Welt auf das meines Wissens erste Medikament richten,
dass überhaupt Gentherapie am Menschen erfolgreich anwenden darf.
Das dürfte Begehrlichkeiten unter den Großen der Branche wecken!?
Leider lässt sich die Firma im Wikifolio nicht kaufen.
Gruß
Antwort auf Beitrag Nr.: 50.776.680 von Solideinvestierenkomplex4you am 05.10.15 13:19:22So, nach dem Verfall der Aktienkurse nach der Positivmeldung (sell on good news)
schickt sich die Aktie nach dem weiteren Anstieg am Freitag an,
eventuell wieder in den charttechnisch überkauften Bereich einzudringen!?
Das könnte evtl. bei erreichen und Überschreiten der charttechnischen Grenze
weitere schnelle und drastische Kursgewinne nach sich ziehen?
Ich habe meine Position in Spark T. inzwischen erhöht.
Alles nur meine persönliche Meinung!
Gruß
schickt sich die Aktie nach dem weiteren Anstieg am Freitag an,
eventuell wieder in den charttechnisch überkauften Bereich einzudringen!?
Das könnte evtl. bei erreichen und Überschreiten der charttechnischen Grenze
weitere schnelle und drastische Kursgewinne nach sich ziehen?
Ich habe meine Position in Spark T. inzwischen erhöht.
Alles nur meine persönliche Meinung!
Gruß
Nun ist Spark T. wieder im überkauften Bereich angekommen.
Ich halte selbst Aktien an dem Unternehmen.
Zwischenzeitlich gab es eine kurze Mißstimmung an der Börse,
als ein Wettbewerber berichtet hat, dass eine ältere Gentechnologie
nicht so funktioniert hat, wie es angedacht war.
Der Wettbewerber Bluebird Biotech hat aber ebenfalls bereits seine
Technologie verbessert und kann daher auch mit neueren Produkten aufwarten.
Der Vorfall aber zeigt, dass es nicht nur um die Idee geht,
diverse Krankheiten per Gentherapie zu bearbeiten,
was für sich genommen schon eine "Game Changing Idee" ist,
sondern auch darum, dass eine überaus ausgereifte Technologie
Grundlage für eine erfolgreiche Behandlung am Menschen darstellt.
Spark T. hat scheinbar beides.
Wenn der langfristig orientierte Anleger hier bei diesem Unternehmen
nicht so sehr auf die potentiellen Umsätze des ersten Produktes schielt,
sondern in Folge auf die potentiellen weiteren Therapiefelder,
insbesondere aber sich vergegenwärtigt, dass es sich mit diesem Unternehmen
um eine hoch effektive Technologieplattform handelt, die auch in anderen Therapiefeldern
eingesetz werden könnte, dann lässt sich eine "faire Bewertung" des Unternehmens
in der Zukunft nur erahnen.
Das Unternehmen gehört bislang immer noch von der Marktkapitalisierung
zu den Zwergen der Biotechnologieszene.
Warum sollte dies langfristig mit einer einzigartigen Technologieplattform,
die offenkundig funktioniert, immer so bleiben.
Große Risiken, riesige Chancen für einen Langfristinvestor,
so meine Meinung.
Ich halte selbst Aktien an dem Unternehmen.
Zwischenzeitlich gab es eine kurze Mißstimmung an der Börse,
als ein Wettbewerber berichtet hat, dass eine ältere Gentechnologie
nicht so funktioniert hat, wie es angedacht war.
Der Wettbewerber Bluebird Biotech hat aber ebenfalls bereits seine
Technologie verbessert und kann daher auch mit neueren Produkten aufwarten.
Der Vorfall aber zeigt, dass es nicht nur um die Idee geht,
diverse Krankheiten per Gentherapie zu bearbeiten,
was für sich genommen schon eine "Game Changing Idee" ist,
sondern auch darum, dass eine überaus ausgereifte Technologie
Grundlage für eine erfolgreiche Behandlung am Menschen darstellt.
Spark T. hat scheinbar beides.
Wenn der langfristig orientierte Anleger hier bei diesem Unternehmen
nicht so sehr auf die potentiellen Umsätze des ersten Produktes schielt,
sondern in Folge auf die potentiellen weiteren Therapiefelder,
insbesondere aber sich vergegenwärtigt, dass es sich mit diesem Unternehmen
um eine hoch effektive Technologieplattform handelt, die auch in anderen Therapiefeldern
eingesetz werden könnte, dann lässt sich eine "faire Bewertung" des Unternehmens
in der Zukunft nur erahnen.
Das Unternehmen gehört bislang immer noch von der Marktkapitalisierung
zu den Zwergen der Biotechnologieszene.
Warum sollte dies langfristig mit einer einzigartigen Technologieplattform,
die offenkundig funktioniert, immer so bleiben.
Große Risiken, riesige Chancen für einen Langfristinvestor,
so meine Meinung.
Ich bin grundsätzlich überrascht, wie viele stille Leser es hier täglich
im Durchschnitt gibt.
Daher schreibe ich hin und wieder über einige "Neuigkeiten"/Nachrichten über Spark
hier in diesem Thread.
Von der Homepage
http://www.sparktx.com/pipeline/neurodegenerative-diseases
lässt sich heraus lesen, dass noch in diesem Jahr im Feld "neurodegenerative Deseases"
mehr Informationen geliefert werden sollen.
Vielleicht ja, um welche Therapiefelder es sich handelt!?
Das könnte dann grundsätzlich noch mal zu einem Freudenhüpfer des Aktienkurses
kommen, wenn weitere Details bekannt werden.
Gruß
P.S: Ich halte aktuell Aktien in Spark Therapeutics
im Durchschnitt gibt.
Daher schreibe ich hin und wieder über einige "Neuigkeiten"/Nachrichten über Spark
hier in diesem Thread.
Von der Homepage
http://www.sparktx.com/pipeline/neurodegenerative-diseases
lässt sich heraus lesen, dass noch in diesem Jahr im Feld "neurodegenerative Deseases"
mehr Informationen geliefert werden sollen.
Vielleicht ja, um welche Therapiefelder es sich handelt!?
Das könnte dann grundsätzlich noch mal zu einem Freudenhüpfer des Aktienkurses
kommen, wenn weitere Details bekannt werden.
Gruß
P.S: Ich halte aktuell Aktien in Spark Therapeutics
noch ein paar Gedanken:
3500 Menschen leiden unter der speziellen Form von Augenerkrankung,
die Spark jetzt therapieren kann.
Eine Behandlung könnte rund 1 Million US-$ kosten.
Wenn rund 2000 Menschen in den USA und der EU die Therapiemöglichkeit wahr nehmen,
könnte Spark Einnahmen von rund 2 Milliarden US-$ generieren, von denen 50 % hängen bleiben sollten. Natürlich über die Jahre verteilt und natürlich nicht als Jahresüberschuss, denn es fallen ja auch weitere Kosten an für weitere
Forschungsprogramme.
Aber jetzt wurde durch die Zulassung bewiesen, dass das Konzept von Spark
funktioniert.
Wenn Spark jetzt die gleiche Technologie anwendet, aber den Fokus leicht dreht...
in Richtung von Krankheiten, die auch genetisch begründet werden können,
aber an denen viel mehr Menschen leiden....
Allein die Ankündigung einer Strategieerweiterung wäre vermutlich für den Kurs deutlich treibend.
Allerdings habe ich keine Ahnung, ob man sich bei Spark darüber Gedanken macht.
Trotzdem, wenn man alleine mal bedenkt, welche Unmengen an Krankheiten auch genetische Gründe
haben...darunter auch einige Formen von Krebs, bei denen ja eine erbliche Prädisposition unterstellt wird...
Ich glaube, dass dieser Bereich der Biotechnologie, dem Spark und wenige andere derzeit
nachgehen, einer der heißesten Eisen ist, die die Medizin derzeit im Fokus hat.
Vermutlich auch einer mit den größten Behandlungschancen, denn bei dieser Art von Medizin reden wir fast schon über eine Heilung der Krankheit.
Zumindest sollte eine einmalige Behandlung zu jahrelanger Ruhe vor der Krankheit führen können.
Alles wie immer nur meine eigenen Meinung und weder Kauf- noch Verkaufsempfehlung.
Gruß
3500 Menschen leiden unter der speziellen Form von Augenerkrankung,
die Spark jetzt therapieren kann.
Eine Behandlung könnte rund 1 Million US-$ kosten.
Wenn rund 2000 Menschen in den USA und der EU die Therapiemöglichkeit wahr nehmen,
könnte Spark Einnahmen von rund 2 Milliarden US-$ generieren, von denen 50 % hängen bleiben sollten. Natürlich über die Jahre verteilt und natürlich nicht als Jahresüberschuss, denn es fallen ja auch weitere Kosten an für weitere
Forschungsprogramme.
Aber jetzt wurde durch die Zulassung bewiesen, dass das Konzept von Spark
funktioniert.
Wenn Spark jetzt die gleiche Technologie anwendet, aber den Fokus leicht dreht...
in Richtung von Krankheiten, die auch genetisch begründet werden können,
aber an denen viel mehr Menschen leiden....
Allein die Ankündigung einer Strategieerweiterung wäre vermutlich für den Kurs deutlich treibend.
Allerdings habe ich keine Ahnung, ob man sich bei Spark darüber Gedanken macht.
Trotzdem, wenn man alleine mal bedenkt, welche Unmengen an Krankheiten auch genetische Gründe
haben...darunter auch einige Formen von Krebs, bei denen ja eine erbliche Prädisposition unterstellt wird...
Ich glaube, dass dieser Bereich der Biotechnologie, dem Spark und wenige andere derzeit
nachgehen, einer der heißesten Eisen ist, die die Medizin derzeit im Fokus hat.
Vermutlich auch einer mit den größten Behandlungschancen, denn bei dieser Art von Medizin reden wir fast schon über eine Heilung der Krankheit.
Zumindest sollte eine einmalige Behandlung zu jahrelanger Ruhe vor der Krankheit führen können.
Alles wie immer nur meine eigenen Meinung und weder Kauf- noch Verkaufsempfehlung.
Gruß
So, die Überhitzung im Aktienkurs hat
sich aktuell erst einmal wieder abgebaut, was letztlich auch Chancen
auf erneute Kursgewinne bedeuten kann, wenn die überkaufte Zone wieder näher rücken sollte.
Noch einige Überlegungen zu den Haemophilie Programmen.
Das am weitesten fortgeschrittene Programm ist Haemophilie B.
Auf der Homepage von Spark wird die Zahl 28.000 weltweit als betrofffene genannt.
Haemophilie A hingegen, haben scheinbar weltweit rund 400.000 Betroffene,, wie aus der jüngsten Meldung von Morphosys/Bayer hervor geht.
Haemophilie A ist zwar im Gegensatz zum Haemophilie B Programm in der präklinischen Phase,
aber die Anzahl der Betroffenen ist um mehr als den Faktor 10 größer.
P.S: Ich halte nach wie vor Aktien von Spark Therapeutics und hier abgegebene Kommentare sind
weder Kauf- noch Verkaufsempfehlungen.
Gruß
sich aktuell erst einmal wieder abgebaut, was letztlich auch Chancen
auf erneute Kursgewinne bedeuten kann, wenn die überkaufte Zone wieder näher rücken sollte.
Noch einige Überlegungen zu den Haemophilie Programmen.
Das am weitesten fortgeschrittene Programm ist Haemophilie B.
Auf der Homepage von Spark wird die Zahl 28.000 weltweit als betrofffene genannt.
Haemophilie A hingegen, haben scheinbar weltweit rund 400.000 Betroffene,, wie aus der jüngsten Meldung von Morphosys/Bayer hervor geht.
Haemophilie A ist zwar im Gegensatz zum Haemophilie B Programm in der präklinischen Phase,
aber die Anzahl der Betroffenen ist um mehr als den Faktor 10 größer.
P.S: Ich halte nach wie vor Aktien von Spark Therapeutics und hier abgegebene Kommentare sind
weder Kauf- noch Verkaufsempfehlungen.
Gruß
Antwort auf Beitrag Nr.: 50.966.631 von Solideinvestierenkomplex4you am 30.10.15 08:41:26ich halte nach wie vor Aktien an Spark T.
und dieser Kommentar ist rein informativer Natur.
Keine Kauf- oder Verkaufsempfehlung!
Rein charttechnisch gesehen ist Spark trotz des gestrigen Anstiegs
noch nicht in der überkauften Zone angelangt, sondern erst auf
dem Weg dahin.
Sollte der Bereich der überkauften Zone in Kürze betreten werden können,
erwarte ich signifikante Kursgewinne.
Gruß
und dieser Kommentar ist rein informativer Natur.
Keine Kauf- oder Verkaufsempfehlung!
Rein charttechnisch gesehen ist Spark trotz des gestrigen Anstiegs
noch nicht in der überkauften Zone angelangt, sondern erst auf
dem Weg dahin.
Sollte der Bereich der überkauften Zone in Kürze betreten werden können,
erwarte ich signifikante Kursgewinne.
Gruß
Antwort auf Beitrag Nr.: 51.010.050 von Solideinvestierenkomplex4you am 05.11.15 07:49:58Probleme eines Wettbewerbers von Spark mit seiner Technologieplattform
brachten in der vergangenen Woche auch die Aktien von Spark unter Druck.
Eingebettet übrigens in eine eher maue Woche für die Biotechnologie allgemein.
Angst machte sich breit, dass auch die Technologie von Spark nicht funktionieren könnte.
Trotzdem war der Abschlag moderat.
Schliesslich sollte daran erinnert werden, dass bereits 1 Produkt von Sparks Technologieplattform
alle klinischen Phasen durchlaufen hatund am Ende von der FDA grünes Licht erhalten hat.
Ergo, zumindest die Technologie von Spark funktioniert mindestens selektiv.
Im besten Fall ist die Technologie von Spark sehr viel ausgereifter als die einiger WEttbewerber.
brachten in der vergangenen Woche auch die Aktien von Spark unter Druck.
Eingebettet übrigens in eine eher maue Woche für die Biotechnologie allgemein.
Angst machte sich breit, dass auch die Technologie von Spark nicht funktionieren könnte.
Trotzdem war der Abschlag moderat.
Schliesslich sollte daran erinnert werden, dass bereits 1 Produkt von Sparks Technologieplattform
alle klinischen Phasen durchlaufen hatund am Ende von der FDA grünes Licht erhalten hat.
Ergo, zumindest die Technologie von Spark funktioniert mindestens selektiv.
Im besten Fall ist die Technologie von Spark sehr viel ausgereifter als die einiger WEttbewerber.
Antwort auf Beitrag Nr.: 51.036.594 von Solideinvestierenkomplex4you am 08.11.15 20:14:35das verdeckte Produkt im Bereich CNS wurde jetzt aufgedeckt.
Spark will sein erstes Produkt im Bereich CNS
auf die so genannte Batten Krankheit anwenden.
1 zu 30000 Betroffene steht unter Wikipedia.
In Deutschland also etwas mehr als 2.000 Personen betroffen.
In USA rund knapp 8.000 Personen.
Spark will sein erstes Produkt im Bereich CNS
auf die so genannte Batten Krankheit anwenden.
1 zu 30000 Betroffene steht unter Wikipedia.
In Deutschland also etwas mehr als 2.000 Personen betroffen.
In USA rund knapp 8.000 Personen.
Ich halte Aktien von Spark T.
Dies ist keine Kauf- oder Verkaufsempfehlung.
Nachdem nun die Batten Krankheit das Ziel von Spark im Bereich CNS ist,
gab es wohl eine Enttäuschung.
Auch ich hatte insgeheim gehofft, dass sie eine Krankheit adressieren,
unter der mehr Menschen leiden.
Nun denn, ein sehr großer Trost für die Betroffenen und es ist gut, dass Spark ihnen bald helfen kann.
Charttechnisch gab es Abverkäufe bis zur unteren Unterstützung bei 50,8 $.
Jetzt kann es wieder aufwärts gehen.
Dies ist keine Kauf- oder Verkaufsempfehlung.
Nachdem nun die Batten Krankheit das Ziel von Spark im Bereich CNS ist,
gab es wohl eine Enttäuschung.
Auch ich hatte insgeheim gehofft, dass sie eine Krankheit adressieren,
unter der mehr Menschen leiden.
Nun denn, ein sehr großer Trost für die Betroffenen und es ist gut, dass Spark ihnen bald helfen kann.
Charttechnisch gab es Abverkäufe bis zur unteren Unterstützung bei 50,8 $.
Jetzt kann es wieder aufwärts gehen.
nach wie vor halte ich Aktien von Spark T.
Dies ist weder Kauf- noch Verkaufsempfehlung.
Eine Kapitalerhöhung soll statt finden.
Daneben wurde bekannt, dass Spark Meilensteinzahlungen von bis zu 245 Millionen US-Dollar
von Pfizer erhalten kann plus Royalties für ein Haemophilie Produkt.
Ein weiterer Kandidat ist inzwischen in der Pipeline aufgetaucht, aber noch nicht veröffentlicht.
Es sieht so aus, als wollte man seine Pipeline ausbauen.
Ein logischer Schritt als Marktführer im Bereich der Gentherapie.
Gruß
Dies ist weder Kauf- noch Verkaufsempfehlung.
Eine Kapitalerhöhung soll statt finden.
Daneben wurde bekannt, dass Spark Meilensteinzahlungen von bis zu 245 Millionen US-Dollar
von Pfizer erhalten kann plus Royalties für ein Haemophilie Produkt.
Ein weiterer Kandidat ist inzwischen in der Pipeline aufgetaucht, aber noch nicht veröffentlicht.
Es sieht so aus, als wollte man seine Pipeline ausbauen.
Ein logischer Schritt als Marktführer im Bereich der Gentherapie.
Gruß
Antwort auf Beitrag Nr.: 51.311.523 von Solideinvestierenkomplex4you am 15.12.15 19:32:15nach wie vor halte ich Aktien von Spark T.
Dies ist weder Kauf- noch Verkaufsempfehlung.
Der Preis der neuen Aktien wird auf 47 US-Dollar festgezurrt. Eventuell
noch leichte Rabatte.
Cash hat Sparks eigentlich zunächst genug.
Doch ich denke, man will jetzt sehr schnell seine Pipeline
erweitern und sich die Rechte sichern.
Die Gendefekte bei seltenen Erbkrankheiten sind ja mehr oder
weniger bekannt.
Es geht also nur um ein Produkt und eine Technologie, dass (die) aus
diesen Gendefekten gesunde Gene machen kann.
Hier ist Spark die Nummer 1.
Gruß
Dies ist weder Kauf- noch Verkaufsempfehlung.
Der Preis der neuen Aktien wird auf 47 US-Dollar festgezurrt. Eventuell
noch leichte Rabatte.
Cash hat Sparks eigentlich zunächst genug.
Doch ich denke, man will jetzt sehr schnell seine Pipeline
erweitern und sich die Rechte sichern.
Die Gendefekte bei seltenen Erbkrankheiten sind ja mehr oder
weniger bekannt.
Es geht also nur um ein Produkt und eine Technologie, dass (die) aus
diesen Gendefekten gesunde Gene machen kann.
Hier ist Spark die Nummer 1.
Gruß
nach wie vor halte ich Aktien von Spark T.
Dies ist weder Kauf- noch Verkaufsempfehlung.
Die Zeit für die Aktienplatzierung endet wohl am 21. Dezember 2015.
Danach kann sich der Kurs rein theoretisch wieder frei bewegen.
Ich habe mal unter Erbkrankheiten gegoogelt.
Unglaublich viele Erbkrankheiten gibt es.
Auch solche, die erst im Leben entstehen und bei denen sich Probleme
auch aus dem Erbgut ergeben können (z.B. Autoimmunkrankheiten).
Wenn Sparks jetzt für einige der Erbkrankheiten, die teilweise nicht einmal
als seltene Erbkrankheiten gelten, aufgrund seiner Technologie Antworten geben kann,
dann wird dieses Unternehmen in 5 bis 10 Jahren ganz anders bewertet werden,
so meine höchst persönliche Meinung.
Wichtig an dieser Stelle ist meiner Meinung nach nur,
Geschwindigkeit aufzunehmen bezüglich der Patentierung und Etablierung
neuer Produkte und der zügigen Einbringung in die Klinischen Prüfungen.
Ich vermute, dass frische Geld ist eben dafür gedacht.
Gruß
Dies ist weder Kauf- noch Verkaufsempfehlung.
Die Zeit für die Aktienplatzierung endet wohl am 21. Dezember 2015.
Danach kann sich der Kurs rein theoretisch wieder frei bewegen.
Ich habe mal unter Erbkrankheiten gegoogelt.
Unglaublich viele Erbkrankheiten gibt es.
Auch solche, die erst im Leben entstehen und bei denen sich Probleme
auch aus dem Erbgut ergeben können (z.B. Autoimmunkrankheiten).
Wenn Sparks jetzt für einige der Erbkrankheiten, die teilweise nicht einmal
als seltene Erbkrankheiten gelten, aufgrund seiner Technologie Antworten geben kann,
dann wird dieses Unternehmen in 5 bis 10 Jahren ganz anders bewertet werden,
so meine höchst persönliche Meinung.
Wichtig an dieser Stelle ist meiner Meinung nach nur,
Geschwindigkeit aufzunehmen bezüglich der Patentierung und Etablierung
neuer Produkte und der zügigen Einbringung in die Klinischen Prüfungen.
Ich vermute, dass frische Geld ist eben dafür gedacht.
Gruß
Antwort auf Beitrag Nr.: 51.326.292 von Solideinvestierenkomplex4you am 17.12.15 14:58:55Nach wie vor halte ich Aktien von Spark.
Dies ist, wie immer, weder eine Kauf- noch Verlaufsempfehlung.
Wie bereits in meinem letzten Kommentar vermutet,
benötigt Spark das frische Geld zur klinischen Entwicklung der bestehenden
Pipeline und auch zur Entwicklung neuer Produkte.
Soeben wurde von Spark gemeldet,
dass in 2018 insgesamt 10 Produkte in Entwicklungspipeline
stecken werden, darunter auch (neu genannt)
die Erbkrankheit Huntington Disease,
an der zusammen (EU +USA) 60.000 Patienten leiden,
als auch eine Krankheit mit der Abkürzung LHON.
Obwohl die jüngste Kursentwicklung sehr enttäuschend verlief,
befindet sich Spark meiner Meinung nach weiterhin auf Kurs,
mehr und mehr Krankheiten durch seine Gentherapieplattform in
den Griff zu bekommen, was im Fall einer Gentherapie quasi gleichbedeutend
mindestens mit einer zeitlichen Heilung zu setzen ist.
Weiterhinwurde bekannt gegeben, dass die angesammelten finanziellen
Mittel aktuell ausreichen, um diese Zielsetzung umzusetzen,
also möglicherweise erst einmal keine weiteren Kapitalverwässerungen mehr!?
Gruß
Dies ist, wie immer, weder eine Kauf- noch Verlaufsempfehlung.
Wie bereits in meinem letzten Kommentar vermutet,
benötigt Spark das frische Geld zur klinischen Entwicklung der bestehenden
Pipeline und auch zur Entwicklung neuer Produkte.
Soeben wurde von Spark gemeldet,
dass in 2018 insgesamt 10 Produkte in Entwicklungspipeline
stecken werden, darunter auch (neu genannt)
die Erbkrankheit Huntington Disease,
an der zusammen (EU +USA) 60.000 Patienten leiden,
als auch eine Krankheit mit der Abkürzung LHON.
Obwohl die jüngste Kursentwicklung sehr enttäuschend verlief,
befindet sich Spark meiner Meinung nach weiterhin auf Kurs,
mehr und mehr Krankheiten durch seine Gentherapieplattform in
den Griff zu bekommen, was im Fall einer Gentherapie quasi gleichbedeutend
mindestens mit einer zeitlichen Heilung zu setzen ist.
Weiterhinwurde bekannt gegeben, dass die angesammelten finanziellen
Mittel aktuell ausreichen, um diese Zielsetzung umzusetzen,
also möglicherweise erst einmal keine weiteren Kapitalverwässerungen mehr!?
Gruß
Antwort auf Beitrag Nr.: 51.468.465 von Solideinvestierenkomplex4you am 12.01.16 06:54:39"als auch eine Krankheit mit der Abkürzung LHON."
Hi
Santhera Pharma hat letzten Herbst die Zulassung für Raxone bei LOHN erhalten, nachdem man in Frankreich dafür bereits seit 2 Jahren eine temporäre Zulassung hatte. Die Vermarktung startet diese Jahr, das Medi ist extrem teuer.
Gruß aaahhh
Hi
Santhera Pharma hat letzten Herbst die Zulassung für Raxone bei LOHN erhalten, nachdem man in Frankreich dafür bereits seit 2 Jahren eine temporäre Zulassung hatte. Die Vermarktung startet diese Jahr, das Medi ist extrem teuer.
Gruß aaahhh
Antwort auf Beitrag Nr.: 51.579.546 von aaahhh am 26.01.16 10:47:32Dazu:
Santhera unterzeichnet Vertriebs- und Liefervertrag für Raxone® mit Ewopharma für Osteuropa und das Baltikum
Nachrichtenquelle: GlobeNewswire
| 18.01.2016, 07:00 | 104 | 0
Santhera Pharmaceuticals Holding AG / Santhera unterzeichnet Vertriebs- und Liefervertrag für Raxone® mit Ewopharma für Osteuropa und das Baltikum . Verarbeitet und übermittelt durch NASDAQ OMX Corporate Solutions. Für den Inhalt der Mitteilung ist der Emittent verantwortlich. Source: Globenewswire
Santhera Pharmaceuticals (SIX: SANN) gibt die Unterzeichnung einer Vereinbarung mit Ewopharma für die Markteinführung von Raxone® zur Behandlung von Leber Hereditärer Optikusneuropathie (LHON) in einer Reihe von Ländern Osteuropas (Bulgarien, Kroatien, Polen, Rumänien, Slowakei, Slowenien, Tschechien und Ungarn) und dem Baltikum (Estland, Lettland und Litauen) bekannt. LHON ist eine seltene, vererbte, mitochondriale Erkrankung, die bei ansonsten gesunden Patienten rasch zu ausgeprägter und permanenter Erblindung führt. Raxone ist die erste Therapieoption für LHON und die erste zugelassene Behandlung für eine mitochondriale Erkrankung.
"Die Vereinbarung mit Ewopharma ist ein bedeutender Erfolg für Santhera und unterstreicht unser Bestreben, Raxone für Patienten in allen EU-Ländern verfügbar zu machen", sagte Giovanni Stropoli, Santheras Chief Commercial Officer für Europa. "Wir sind überzeugt, dass Ewopharmas Fachwissen auf dem Gebiet seltener Krankheiten und Marktverständnis in dieser Region von grossem Nutzen für Patienten mit dieser schwerwiegenden Krankheit sein werden."
"Als traditionell in Osteuropa und dem Baltikum verankertes Unternehmen und mit einem spezifischen Fokus auf Nischenindikationen und Krankheiten mit einem hohen medizinischen Bedarf sind wir begeistert von dieser Zusammenarbeit mit Santhera, um LHON-Patienten erstmals eine Behandlung zugänglich zu machen", sagte Alain Staub, CEO und Verwaltungsratspräsident von Ewopharma. "Wir werden alles daran setzen um Raxone in diesen Ländern möglichst rasch einzuführen."
Über Leber Hereditäre Optikusneuropathie und den therapeutischen Nutzen von Raxone
LHON ist eine genetisch vererbte Augenerkrankung, die zur Erblindung führt. Die Krankheit betrifft primär junge, ansonsten gesunde, männliche Erwachsene, welche einen schnell fortschreitenden, schmerzfreien Verlust der zentralen Sehschärfe erleiden und innert weniger Monate nach Auftreten der Symptome erblinden. Etwa 95% der Patienten weisen eine von drei möglichen Punktmutationen im mitochondrialen Gencode auf. Diese Mutationen bedingen eine Störung im Komplex I der mitochondrialen Atmungskette. Dadurch wird die zelluläre Energieproduktion reduziert und gleichzeitig der oxidative Stress erhöht, was zur Fehlfunktion der retinalen Ganglionzellen im Auge und damit zu einem rasch fortschreitenden Sehverlust und zur Erblindung führt.
Raxone (idebenone), ein synthetisches Benzoquinone und Kofaktor für das zelluläre Enzym NAD(P)H:quinone oxidoreductase (NQO1), umgeht die Störung im Komplex I, vermindert den oxidativen Stress, erhöht die Energieproduktion in den retinalen Ganglionzellen und fördert die Wiederherstellung des Sehvermögens der Patienten.
Raxone ist ein oral verabreichtes Medikament in einer zugelassenen Tagesdosis von 900 mg (Einnahme von zwei Tabletten dreimal täglich mit dem Essen) zur Behandlung von Sehbeeinträchtigungen bei jugendlichen und erwachsenen Patienten mit LHON. Die Behandlung sollte von einem Arzt mit Erfahrung bei LHON initiiert und überwacht werden. Die Wirksamkeitsdaten stützen sich auf Santheras randomisierte, Plazebo-kontrollierte RHODOS Studie und das Expanded Access Programm und haben insgesamt gezeigt, dass der Sehverlust bei mit Raxone behandelten Patienten gemildert oder rückgängig gemacht werden kann.
Dazu:http://www.elisana.de/shop/raxone-150-mg-filmtabletten/?id=3…
Gruß aaahhh
Santhera unterzeichnet Vertriebs- und Liefervertrag für Raxone® mit Ewopharma für Osteuropa und das Baltikum
Nachrichtenquelle: GlobeNewswire
| 18.01.2016, 07:00 | 104 | 0
Santhera Pharmaceuticals Holding AG / Santhera unterzeichnet Vertriebs- und Liefervertrag für Raxone® mit Ewopharma für Osteuropa und das Baltikum . Verarbeitet und übermittelt durch NASDAQ OMX Corporate Solutions. Für den Inhalt der Mitteilung ist der Emittent verantwortlich. Source: Globenewswire
Santhera Pharmaceuticals (SIX: SANN) gibt die Unterzeichnung einer Vereinbarung mit Ewopharma für die Markteinführung von Raxone® zur Behandlung von Leber Hereditärer Optikusneuropathie (LHON) in einer Reihe von Ländern Osteuropas (Bulgarien, Kroatien, Polen, Rumänien, Slowakei, Slowenien, Tschechien und Ungarn) und dem Baltikum (Estland, Lettland und Litauen) bekannt. LHON ist eine seltene, vererbte, mitochondriale Erkrankung, die bei ansonsten gesunden Patienten rasch zu ausgeprägter und permanenter Erblindung führt. Raxone ist die erste Therapieoption für LHON und die erste zugelassene Behandlung für eine mitochondriale Erkrankung.
"Die Vereinbarung mit Ewopharma ist ein bedeutender Erfolg für Santhera und unterstreicht unser Bestreben, Raxone für Patienten in allen EU-Ländern verfügbar zu machen", sagte Giovanni Stropoli, Santheras Chief Commercial Officer für Europa. "Wir sind überzeugt, dass Ewopharmas Fachwissen auf dem Gebiet seltener Krankheiten und Marktverständnis in dieser Region von grossem Nutzen für Patienten mit dieser schwerwiegenden Krankheit sein werden."
"Als traditionell in Osteuropa und dem Baltikum verankertes Unternehmen und mit einem spezifischen Fokus auf Nischenindikationen und Krankheiten mit einem hohen medizinischen Bedarf sind wir begeistert von dieser Zusammenarbeit mit Santhera, um LHON-Patienten erstmals eine Behandlung zugänglich zu machen", sagte Alain Staub, CEO und Verwaltungsratspräsident von Ewopharma. "Wir werden alles daran setzen um Raxone in diesen Ländern möglichst rasch einzuführen."
Über Leber Hereditäre Optikusneuropathie und den therapeutischen Nutzen von Raxone
LHON ist eine genetisch vererbte Augenerkrankung, die zur Erblindung führt. Die Krankheit betrifft primär junge, ansonsten gesunde, männliche Erwachsene, welche einen schnell fortschreitenden, schmerzfreien Verlust der zentralen Sehschärfe erleiden und innert weniger Monate nach Auftreten der Symptome erblinden. Etwa 95% der Patienten weisen eine von drei möglichen Punktmutationen im mitochondrialen Gencode auf. Diese Mutationen bedingen eine Störung im Komplex I der mitochondrialen Atmungskette. Dadurch wird die zelluläre Energieproduktion reduziert und gleichzeitig der oxidative Stress erhöht, was zur Fehlfunktion der retinalen Ganglionzellen im Auge und damit zu einem rasch fortschreitenden Sehverlust und zur Erblindung führt.
Raxone (idebenone), ein synthetisches Benzoquinone und Kofaktor für das zelluläre Enzym NAD(P)H:quinone oxidoreductase (NQO1), umgeht die Störung im Komplex I, vermindert den oxidativen Stress, erhöht die Energieproduktion in den retinalen Ganglionzellen und fördert die Wiederherstellung des Sehvermögens der Patienten.
Raxone ist ein oral verabreichtes Medikament in einer zugelassenen Tagesdosis von 900 mg (Einnahme von zwei Tabletten dreimal täglich mit dem Essen) zur Behandlung von Sehbeeinträchtigungen bei jugendlichen und erwachsenen Patienten mit LHON. Die Behandlung sollte von einem Arzt mit Erfahrung bei LHON initiiert und überwacht werden. Die Wirksamkeitsdaten stützen sich auf Santheras randomisierte, Plazebo-kontrollierte RHODOS Studie und das Expanded Access Programm und haben insgesamt gezeigt, dass der Sehverlust bei mit Raxone behandelten Patienten gemildert oder rückgängig gemacht werden kann.
Dazu:http://www.elisana.de/shop/raxone-150-mg-filmtabletten/?id=3…
Gruß aaahhh
Antwort auf Beitrag Nr.: 51.579.690 von aaahhh am 26.01.16 11:03:22Hallo,
danke für den Hinweis!
Die Form der Applikation (oral) ist natürlich sehr patientenfreundlich.
Im Fall von Spark ist die Applikation für das bereits von der FDA
durchgewunkene Medikament meines Wissens nach eine operative Methode,
bei der dann während der OP das Produkt direkt im Gewebe verabreicht wird.
Nun denn, wenn es nur diese Behandlungsmethode gibt, bleibt Patienten
nichts anderes übrig.
Bei Alternativen aber schon.
Wie ist denn Deiner Meinung nach der Heilungseffekt
bei Santhera Pharma im Bereich LHON?
Es wird ja auf der HP von Santhera über
"Raxone can mitigate further vision loss in acutely affected patients and can promote clinically relevant recovery of vision in patients with established disease." geschrieben.
Ist Raxone also eher ein kleiner Schritt in die richtige Richtung oder ein großer Wurf?
Gruß
danke für den Hinweis!
Die Form der Applikation (oral) ist natürlich sehr patientenfreundlich.
Im Fall von Spark ist die Applikation für das bereits von der FDA
durchgewunkene Medikament meines Wissens nach eine operative Methode,
bei der dann während der OP das Produkt direkt im Gewebe verabreicht wird.
Nun denn, wenn es nur diese Behandlungsmethode gibt, bleibt Patienten
nichts anderes übrig.
Bei Alternativen aber schon.
Wie ist denn Deiner Meinung nach der Heilungseffekt
bei Santhera Pharma im Bereich LHON?
Es wird ja auf der HP von Santhera über
"Raxone can mitigate further vision loss in acutely affected patients and can promote clinically relevant recovery of vision in patients with established disease." geschrieben.
Ist Raxone also eher ein kleiner Schritt in die richtige Richtung oder ein großer Wurf?
Gruß
Antwort auf Beitrag Nr.: 51.580.782 von Solideinvestierenkomplex4you am 26.01.16 12:56:06Das Research von RBC und Life Sci Capital ist dazu ganz interessant, findest du unter Investors/ Analyst Reports auf der HP von Santhera. Die Behandlungskosten mit Raxone belaufen sich auf über 100K€ pro Jahr und Patient, nicht ganz billig, zumal der Wirkstoff in den USA auch frei verkäuflich und billiger erhältlich ist. Aber welcher Arzt verschreibt schon so was und welcher Patient bezahlt es selber, wenn er es anders herum über das Rezept bezahlt bekommt.
Gruß aaahhh
Gruß aaahhh
Von den wenigen Biotech-Aktien, die man langfristig empfehlen kann, ist Spark Therapeutics.
Gute Technologie im Berech Gentherapie.
Bei Rücksetzern kann man sie kaufen.
Cashbestand um 8-9$ herum.
Gute Technologie im Berech Gentherapie.
Bei Rücksetzern kann man sie kaufen.
Cashbestand um 8-9$ herum.
Antwort auf Beitrag Nr.: 51.587.829 von jhackel am 27.01.16 08:50:45Hallo,
schön, dass hier auch mehr und mehr ehemals stille Leser
Beiträge posten.
Einverstanden bin ich mit Deinem ersten Statement, dass Spark langfristig
chancenreich erscheint.
In Deinem Statement steckt aber ein bischen weniger offensichtlich
eine eher negative Bewertung anderer Biotech-Aktien auf lange Sicht.
Wenn ich das richtig verstanden habe???, vielleicht kannst Du etwas mehr
dazu schreiben, warum Du diese Einschätzung hast.
Woher siehst Du langfristig möglichen Gegenwind für viele Biotechs?
Gruß
schön, dass hier auch mehr und mehr ehemals stille Leser
Beiträge posten.
Einverstanden bin ich mit Deinem ersten Statement, dass Spark langfristig
chancenreich erscheint.
In Deinem Statement steckt aber ein bischen weniger offensichtlich
eine eher negative Bewertung anderer Biotech-Aktien auf lange Sicht.
Wenn ich das richtig verstanden habe???, vielleicht kannst Du etwas mehr
dazu schreiben, warum Du diese Einschätzung hast.
Woher siehst Du langfristig möglichen Gegenwind für viele Biotechs?
Gruß
Antwort auf Beitrag Nr.: 51.592.020 von Solideinvestierenkomplex4you am 27.01.16 15:19:18Also, bei Spark ist übrigens noch keine Zulassung vorhanden. Es ist auch nicht sicher, ob die Zulassung kommt. Hier haben zwei Vorgänge den Pessimismus der Anleger erhöht, deswegen geht der Kurs auch runter.
Negativ:
- Es heißt, dass die Therapie keine Langzeitwirkung hat. Nach 1-2 Jahren würde die Wirkung nachlassen.
- Was viele Anleger sehr verstimmte ist, dass Spark mit der FDA besprochen hat, wie man die Daten der Phase 3 Studie, ich sags mal in meinen Worten, "aufhübschen" kann.
- Was auch auffällig ist, dass die im November eine Präsentation mit ihren Studiendaten hatten und seitdem geht der Kurs konsequent runter. Nun weiß man natürlich nicht, ob das mit den Studiendaten zusammenhängt, da auch andere Biotechs in der Zeit Federn lassen mussten. Ist aber auffällig.
- Es könnte durchaus passieren, dass die FDA weitere Studien verlangt. Weil, es wäre in den USA die erste Zulassung im Bereich Gentherapie überhaupt. Es gibt meines Wissens nur ein weiteres Produkt, das in der EU zugelassen wurde. Kynamro (oder ähnlich) heißt es glaub ich.
Daher, die Zulassung ist keineswegs sicher.
Positiv:
- Die Therapie hat eindeutig eine positive Wirkung gezeigt. Das primäre Ziel wurde erreicht und 2 von 3 sekundären Zielen wurde auch erreicht. Das was statistisch nicht signifikant war, dass die Teilnehmer an Lesetafeln die Buchstaben erkennen konnten. Hier konnte man zwar Verbesserungen auch erkennen, es war halt nicht statistisch signifikant. Außerdem hat die Therapie sowieso das Hauptaugenmerk für das Sehvermögen bei Dunkelheit und hier konnte man klare Unterschiede erkennen.
Also es gibt hier Pro und Cons.
Was Spark generell von vielen anderen Biotechs abhebt ist, dass sie genügend Liquidität haben. Die meisten Biotechs haben kaum Kapital, hangeln sich zum Teil von Jahr zu Jahr und haben Altlasten rumzuschleppen, weshalb auch die Kurse fallen ohne Ende. Es hat also weniger mit der Branche zu tun, sondern mit den beteiligten Unternehmen und da muss man einfach erkennen, dass die meisten Biotechs Schrott sind. Auf meiner Blacklist sind 500 Biotechs, die man nicht langfristig kaufen sollte (Zocks bleiben Ausnahme) und wenn man bei all den Unternehmen die langfristige Entwicklung anschaut, die Charts gehen in über 90% von oben links nach unten rechts, also abwärts.
Ich habe auch gemerkt, dass wenn man in dem Bereich erfolgreich sein möchte, man Zeit für Recherche benötigt, die habe ich und gehe da systematisch vor, um die Spreu vom Weizen zu trennen. Und Spark gehört schon mal zu den besseren Unternehmen, auch wenn hier ebenfalls Unsicherheiten da sind.
Negativ:
- Es heißt, dass die Therapie keine Langzeitwirkung hat. Nach 1-2 Jahren würde die Wirkung nachlassen.
- Was viele Anleger sehr verstimmte ist, dass Spark mit der FDA besprochen hat, wie man die Daten der Phase 3 Studie, ich sags mal in meinen Worten, "aufhübschen" kann.
- Was auch auffällig ist, dass die im November eine Präsentation mit ihren Studiendaten hatten und seitdem geht der Kurs konsequent runter. Nun weiß man natürlich nicht, ob das mit den Studiendaten zusammenhängt, da auch andere Biotechs in der Zeit Federn lassen mussten. Ist aber auffällig.
- Es könnte durchaus passieren, dass die FDA weitere Studien verlangt. Weil, es wäre in den USA die erste Zulassung im Bereich Gentherapie überhaupt. Es gibt meines Wissens nur ein weiteres Produkt, das in der EU zugelassen wurde. Kynamro (oder ähnlich) heißt es glaub ich.
Daher, die Zulassung ist keineswegs sicher.
Positiv:
- Die Therapie hat eindeutig eine positive Wirkung gezeigt. Das primäre Ziel wurde erreicht und 2 von 3 sekundären Zielen wurde auch erreicht. Das was statistisch nicht signifikant war, dass die Teilnehmer an Lesetafeln die Buchstaben erkennen konnten. Hier konnte man zwar Verbesserungen auch erkennen, es war halt nicht statistisch signifikant. Außerdem hat die Therapie sowieso das Hauptaugenmerk für das Sehvermögen bei Dunkelheit und hier konnte man klare Unterschiede erkennen.
Also es gibt hier Pro und Cons.
Was Spark generell von vielen anderen Biotechs abhebt ist, dass sie genügend Liquidität haben. Die meisten Biotechs haben kaum Kapital, hangeln sich zum Teil von Jahr zu Jahr und haben Altlasten rumzuschleppen, weshalb auch die Kurse fallen ohne Ende. Es hat also weniger mit der Branche zu tun, sondern mit den beteiligten Unternehmen und da muss man einfach erkennen, dass die meisten Biotechs Schrott sind. Auf meiner Blacklist sind 500 Biotechs, die man nicht langfristig kaufen sollte (Zocks bleiben Ausnahme) und wenn man bei all den Unternehmen die langfristige Entwicklung anschaut, die Charts gehen in über 90% von oben links nach unten rechts, also abwärts.
Ich habe auch gemerkt, dass wenn man in dem Bereich erfolgreich sein möchte, man Zeit für Recherche benötigt, die habe ich und gehe da systematisch vor, um die Spreu vom Weizen zu trennen. Und Spark gehört schon mal zu den besseren Unternehmen, auch wenn hier ebenfalls Unsicherheiten da sind.

Hallo,
ich halte Aktien von Spark und dies ist weder Kauf- noch Verkaufsempfehlung.
NAch einem dramatischen Verfall des Aktienkurses von Spark in der Vergangenheit
hat sich dieser fast ebenso dramatisch wieder Aufwärts bewegt.
Bis vor einigen Tagen die Ankündigung heraus kam, dass man abermals
3,5 Millionen Aktien am Markt verkaufen will.
Heute wurde der Verkaufspreis mit 45 US-$ festgelegt.
Dem Unternehmen erwachsen dadurch, bei erfolgreicher Veräusserung aller
geplanten Aktien, abermals über 150 Millionen US-$ an zusätzlicher Liquidität.
Eigentlich sollte die Liquidität nach der leztzten Aktienplatzierung ausreichen,
um die Kosten der Entwicklung neuer Medikamente auf Jahre hinaus zu finanzieren.
Interessant wird also sein, wofür das Geld eingesetzt werden soll!?
Abgesehen davon gibt es positive Nachrichten zu frühen Erfolgen im Kampf gegen
eine Form der Haemophilie.
Damit verfestigt sich die Annahme der Investoren und des Unternehmens etwas mehr,
dass die Methodik der Gentechnik aus dem Hause Spark scheinbar auch bei
anderen Krankheiten (ausser am Auge) wirksam sein kann.
Mit diesem Wissen baut sich natürlich sehr langfristig gedacht eine neue Macht auf,
die viele Erbkrankheiten vollständig heilen kann.
Neben den Fortschritten in der Krebsmedizin ist dieser Ansatz der Gentherapie für mich
scheinbar eines der heissesten und effektivsten Eisen im Kampf gegen
diverse Krankheiten.
Spark dürfte eine große Zukunft haben, vorausgesetzt man hat die Nerven,
jetzt oder in ein paar Wochen/Monaten ein paar Stücke einzusammeln und diese
für die nächsten 10 Jahre liegen zu lassen.
An der Börse ist nichts sicher. Auch nicht der Weg von Spark.
Aber sollte die Grundsatzidee hier langfristig aufgehen, können geringe
Summen von vielleicht 10.000 Euro ausreichend sein,
um in 10 oder 15 Jahren mit dieser Investitionssumme als Millionär wieder aus dem
Aktienengagement heraus zu gehen.
Und selbst "nur" ein 10-Bagger macht auch viel Freude.
Alles nur meine aktuelle Meinung und keine Aufforderung zum Erwerb dieser Aktie!!!
Gruß
ich halte Aktien von Spark und dies ist weder Kauf- noch Verkaufsempfehlung.
NAch einem dramatischen Verfall des Aktienkurses von Spark in der Vergangenheit
hat sich dieser fast ebenso dramatisch wieder Aufwärts bewegt.
Bis vor einigen Tagen die Ankündigung heraus kam, dass man abermals
3,5 Millionen Aktien am Markt verkaufen will.
Heute wurde der Verkaufspreis mit 45 US-$ festgelegt.
Dem Unternehmen erwachsen dadurch, bei erfolgreicher Veräusserung aller
geplanten Aktien, abermals über 150 Millionen US-$ an zusätzlicher Liquidität.
Eigentlich sollte die Liquidität nach der leztzten Aktienplatzierung ausreichen,
um die Kosten der Entwicklung neuer Medikamente auf Jahre hinaus zu finanzieren.
Interessant wird also sein, wofür das Geld eingesetzt werden soll!?
Abgesehen davon gibt es positive Nachrichten zu frühen Erfolgen im Kampf gegen
eine Form der Haemophilie.
Damit verfestigt sich die Annahme der Investoren und des Unternehmens etwas mehr,
dass die Methodik der Gentechnik aus dem Hause Spark scheinbar auch bei
anderen Krankheiten (ausser am Auge) wirksam sein kann.
Mit diesem Wissen baut sich natürlich sehr langfristig gedacht eine neue Macht auf,
die viele Erbkrankheiten vollständig heilen kann.
Neben den Fortschritten in der Krebsmedizin ist dieser Ansatz der Gentherapie für mich
scheinbar eines der heissesten und effektivsten Eisen im Kampf gegen
diverse Krankheiten.
Spark dürfte eine große Zukunft haben, vorausgesetzt man hat die Nerven,
jetzt oder in ein paar Wochen/Monaten ein paar Stücke einzusammeln und diese
für die nächsten 10 Jahre liegen zu lassen.
An der Börse ist nichts sicher. Auch nicht der Weg von Spark.
Aber sollte die Grundsatzidee hier langfristig aufgehen, können geringe
Summen von vielleicht 10.000 Euro ausreichend sein,
um in 10 oder 15 Jahren mit dieser Investitionssumme als Millionär wieder aus dem
Aktienengagement heraus zu gehen.
Und selbst "nur" ein 10-Bagger macht auch viel Freude.
Alles nur meine aktuelle Meinung und keine Aufforderung zum Erwerb dieser Aktie!!!
Gruß
Hallo,
ich halte Aktien von Spark und dies ist weder Kauf- noch Verkaufsempfehlung.
Soeben vermeldet Spark, dass die geplante Kapitalerhöhung, also das Andienen
weiterer 3,5 Millionen Aktien an Investoren bereits abgeschlossen ist.
Somit lastet dieser Fakt nicht mehr weiter über dem Aktienkurs von Spark.
Rein charttechnisch, und damit eher kurzfristig gesehen, läuft Spark parallel zum Index für
Biotechnologieaktien (IBB) und hat gute Chancen, heute oder in den nächsten Tagen den überverkauften Bereich hinter sich zu lassen.
Gruß
ich halte Aktien von Spark und dies ist weder Kauf- noch Verkaufsempfehlung.
Soeben vermeldet Spark, dass die geplante Kapitalerhöhung, also das Andienen
weiterer 3,5 Millionen Aktien an Investoren bereits abgeschlossen ist.
Somit lastet dieser Fakt nicht mehr weiter über dem Aktienkurs von Spark.
Rein charttechnisch, und damit eher kurzfristig gesehen, läuft Spark parallel zum Index für
Biotechnologieaktien (IBB) und hat gute Chancen, heute oder in den nächsten Tagen den überverkauften Bereich hinter sich zu lassen.
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und aktuell noch ein paar wenige Stücke in einem meiner Wikifolios.
Und das ist auch schon die erste Neuerung für alle Wikifoliorunner:
Spark kann endlich und glücklicherweise nun auch in Wikifolios aufgenommen werden!!!
Noch ein Hinweis:
Heute bzw bereits gestern Abend gab es Meldungen, dass es zu mehreren Todesfällen
gekommen ist im Zusammenhang mit Immuntherapien gegen Krebs.
Das bislang heisseste und effektivste Eisen im Kampf gegen verschiedenen Krebsarten.
Ich hätte damit nicht gerechnet.
In diesem Zusammenhang kann man davon ausgehen, dass dies bei Spark Therapeutics
eigentlich nicht passieren kann. Also gravierende Nebenwirkungen.
Naja, man hat ja schon öfters Pferde kotzen gesehen, aber eigentlich müsste das relativ sicher sein!?
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und aktuell noch ein paar wenige Stücke in einem meiner Wikifolios.
Und das ist auch schon die erste Neuerung für alle Wikifoliorunner:
Spark kann endlich und glücklicherweise nun auch in Wikifolios aufgenommen werden!!!
Noch ein Hinweis:
Heute bzw bereits gestern Abend gab es Meldungen, dass es zu mehreren Todesfällen
gekommen ist im Zusammenhang mit Immuntherapien gegen Krebs.
Das bislang heisseste und effektivste Eisen im Kampf gegen verschiedenen Krebsarten.
Ich hätte damit nicht gerechnet.
In diesem Zusammenhang kann man davon ausgehen, dass dies bei Spark Therapeutics
eigentlich nicht passieren kann. Also gravierende Nebenwirkungen.
Naja, man hat ja schon öfters Pferde kotzen gesehen, aber eigentlich müsste das relativ sicher sein!?
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und in einigen meiner Wikifolios.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient
der reinen Information.
Gestern gab es von offizieller Seite (FDA) das 2. Mal
den Status "Breakthrough Therapy Designation"
Jetzt für die Behandlung von Haemophilie B.
Also ein weiterer Ritterschlag, dass die Behandlungen
von Spark das Potential haben, Krankheitsbilder
meist durch einmalige Behandlungen
gravierend zu verbessern oder gar zu heilen.
Daher bleibe ich bei meiner Meinung,
dass dieses Unternehmen das Zeug hat,
im Lauf von vielen Jahren ein
ganz großes zu werden.
Eigentlich unglaublich, aber wir reden
bei dieser Technologie in vermutlich vielen Fällen
über Heilung, nicht über Linderung oder Verbesserung.
Das Potential ist gewaltig.
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und in einigen meiner Wikifolios.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient
der reinen Information.
Gestern gab es von offizieller Seite (FDA) das 2. Mal
den Status "Breakthrough Therapy Designation"
Jetzt für die Behandlung von Haemophilie B.
Also ein weiterer Ritterschlag, dass die Behandlungen
von Spark das Potential haben, Krankheitsbilder
meist durch einmalige Behandlungen
gravierend zu verbessern oder gar zu heilen.
Daher bleibe ich bei meiner Meinung,
dass dieses Unternehmen das Zeug hat,
im Lauf von vielen Jahren ein
ganz großes zu werden.
Eigentlich unglaublich, aber wir reden
bei dieser Technologie in vermutlich vielen Fällen
über Heilung, nicht über Linderung oder Verbesserung.
Das Potential ist gewaltig.
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und in einigen meiner Wikifolios.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient
der reinen Information.
Unter http://ir.sparktx.com gibt es eine Corporate Präsentation vom 14. Juni 2016,
in der dargelegt wird, dass es bis zu diesem Datum keine negativen Nebenwirkungen
und keine schädlichen Immunantworten des Körpers gibt.
Ich weiß zwar nicht, ob sich diese Technologie auf alle Erbkrankheiten
übertragen lässt, aber selbst wenn es nur auf einige übertragbar sein sollte,
klingt dass, was Spark hier betreibt, für mich wie der heilige Gral in der Medizin.
Einmalige Darreichung, vollständige Heilung über mindestens 3 Jahre
bei nicht vorhandenen Nebenwirkungen und Immunantworten.
Unglaublich und faszinierend zugleich.
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und in einigen meiner Wikifolios.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient
der reinen Information.
Unter http://ir.sparktx.com gibt es eine Corporate Präsentation vom 14. Juni 2016,
in der dargelegt wird, dass es bis zu diesem Datum keine negativen Nebenwirkungen
und keine schädlichen Immunantworten des Körpers gibt.
Ich weiß zwar nicht, ob sich diese Technologie auf alle Erbkrankheiten
übertragen lässt, aber selbst wenn es nur auf einige übertragbar sein sollte,
klingt dass, was Spark hier betreibt, für mich wie der heilige Gral in der Medizin.
Einmalige Darreichung, vollständige Heilung über mindestens 3 Jahre
bei nicht vorhandenen Nebenwirkungen und Immunantworten.
Unglaublich und faszinierend zugleich.
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und in einigen meiner Wikifolios.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient
der reinen Information.
Heute werden Quartalszahlen gemeldet.
Zwar kann die Börse daraufhin in die eine oder
andere Richtung reagieren.
Dennoch halte ich die Zahlen, egal wie sie ausfallen,
eher für unbedeutend.
Denn Geld hat Spark derzeit genug, um seine Pipeline
voran zu treiben und/oder eventuell neue Produkte
zu entdecken.
Wichtiger ist der medizinische Fortschritt,
und der ist aktuell, wie kürzlich auch wieder bei der Haemophilie B
gemeldet, beeindruckend.
Allerdings könnten positive Zahlen zum Quartal
meiner Meinung nach noch einmal einen weiteren Freudenschubauslösen!?
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots
und in einigen meiner Wikifolios.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient
der reinen Information.
Heute werden Quartalszahlen gemeldet.
Zwar kann die Börse daraufhin in die eine oder
andere Richtung reagieren.
Dennoch halte ich die Zahlen, egal wie sie ausfallen,
eher für unbedeutend.
Denn Geld hat Spark derzeit genug, um seine Pipeline
voran zu treiben und/oder eventuell neue Produkte
zu entdecken.
Wichtiger ist der medizinische Fortschritt,
und der ist aktuell, wie kürzlich auch wieder bei der Haemophilie B
gemeldet, beeindruckend.
Allerdings könnten positive Zahlen zum Quartal
meiner Meinung nach noch einmal einen weiteren Freudenschubauslösen!?
Gruß
Hallo zusammen, ich halte Aktien von Spark Therapeutics in meinen Privatdepots und in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der reinen Information.
Nachdem die Aktie in den vergangenen Tagen heiss gelaufen war,
geht es heute einen weiteren Tag in Folge herunter.
Vielleicht eine Gelegenheit, denn negative Meldungen sind mir bis dato nicht bekannt???
Gruß
Nachdem die Aktie in den vergangenen Tagen heiss gelaufen war,
geht es heute einen weiteren Tag in Folge herunter.
Vielleicht eine Gelegenheit, denn negative Meldungen sind mir bis dato nicht bekannt???
Gruß
Moin S.
Zum Thema Gentherapie (und Spark) hat Ohad Hammer kürzlich 2 Beiträge geschrieben. Er ist recht bullisch, wobei auch er nicht hellsehen kann und von daher für einen Basket an mehreren Gentherapiewerten plädiert.
http://www.orf-blog.com/
SG kmastra
Zum Thema Gentherapie (und Spark) hat Ohad Hammer kürzlich 2 Beiträge geschrieben. Er ist recht bullisch, wobei auch er nicht hellsehen kann und von daher für einen Basket an mehreren Gentherapiewerten plädiert.
http://www.orf-blog.com/
SG kmastra
Antwort auf Beitrag Nr.: 53.335.410 von kmastra am 23.09.16 13:23:52Hallo,
ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Herzlichen Dank für Dein gestriges Posting,
dass zunächst einmal eine Fülle von neuen Namen in
diesem Feld liefert, die ich bislang nicht auf dem Radarschirm hatte.
Aber der Link trägt aus meiner Sicht noch eine weitere fantastische Nachricht
in sich, nämlich die, dass andere Versuche mit der Gentherapie
zu ähnlich überzeugenden Ergebnissen gekommen sind wie auch Spark
und, dass die Gentherapie in der Lage ist, auch ganz andere Angriffspunkte
zu setzen, wie "nur" die Leber, das Auge und neurodegenerative Krankheiten.
Sogar die Blood-Brain-Schranke (Blut-Gehirn Schranke) konnte scheinbar überwunden werden...,
so dass die Hilfe für Alzheimer, Parkinson und andere Krankheiten
langfristig wohl von der Gentherapie ausgeht.
Im Übrigen ist scheinbar nicht nur der Erfolg ähnlich gut wie bei Spark,
sondern es reicht auch eine einmalige Behandlung aus, um gute Erfolge zu erzielen.
Wäre ich ein großer Pharmakonzern, würde ich am Montag damit beginnen,
all diese Gentherapie Unternehmen aufzukaufen.
Wäre ich Fussballfan und würde von der Gentherapie auf andere Biotechs schauen,
würde ich mit dem Lied "Ihr könnt nach Hause gehen...." beginnen...
ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Herzlichen Dank für Dein gestriges Posting,
dass zunächst einmal eine Fülle von neuen Namen in
diesem Feld liefert, die ich bislang nicht auf dem Radarschirm hatte.
Aber der Link trägt aus meiner Sicht noch eine weitere fantastische Nachricht
in sich, nämlich die, dass andere Versuche mit der Gentherapie
zu ähnlich überzeugenden Ergebnissen gekommen sind wie auch Spark
und, dass die Gentherapie in der Lage ist, auch ganz andere Angriffspunkte
zu setzen, wie "nur" die Leber, das Auge und neurodegenerative Krankheiten.
Sogar die Blood-Brain-Schranke (Blut-Gehirn Schranke) konnte scheinbar überwunden werden...,
so dass die Hilfe für Alzheimer, Parkinson und andere Krankheiten
langfristig wohl von der Gentherapie ausgeht.
Im Übrigen ist scheinbar nicht nur der Erfolg ähnlich gut wie bei Spark,
sondern es reicht auch eine einmalige Behandlung aus, um gute Erfolge zu erzielen.
Wäre ich ein großer Pharmakonzern, würde ich am Montag damit beginnen,
all diese Gentherapie Unternehmen aufzukaufen.
Wäre ich Fussballfan und würde von der Gentherapie auf andere Biotechs schauen,
würde ich mit dem Lied "Ihr könnt nach Hause gehen...." beginnen...

Antwort auf Beitrag Nr.: 53.339.862 von Solideinvestierenkomplex4you am 24.09.16 08:07:07Hallo zusammen,
nachdem ich mich nun ein wenig mehr mit dem
Link und dem Artikel dahinter beschäftigt habe,
fasse ich mal kurz die Erkenntnisse des Schreibers,
hoffentlich einigermassen richtig, zusammen.
Die Gentherapie mit dem Angriffspunkt
an der Leber hat in einigen Fällen zur Erhöhung
eines Enzyms geführt, dass allgemein bei
diversen Lebererkrakungen im Blut nachweisbar ist und
den Normlevel übersteigt.
Man kann diesen erhöhten ALT Wert aber wohl mit
anderen Medikamenten kontrollieren.
Unklar ist wohl bei diversen Gentherapien, welche Spätfolgen
wohl entstehen könnten und wie lange die Gentherapie wirkt.
Dazu werden jetzt wohl aus mehreren Studien Daten gesammelt,
um hier bezüglich der Langzeitwirkung mehr Klarheit zu erhalten.
Müsste die einmalige Gentherapie nach einigen Jahren wiederholt werden,
würde das für die Gentherapieunternehmen nicht das Aus bedeuten,
sondern im Gegenteil, noch größere Umsätze.
Kritischer ist wohl die Fragestellung, welche Veränderungen
langfristig durch die eingebrachten Gene auftreten.
Egal, was bei der ein oder anderen Gentherapie an
Nebenwirkungen eventuell auftritt, man kann die einmalige Gabe
der neuen DNA-Abschnitte für den Körper nicht mehr
rückgängig machen.
Auftretende Nebenwirkungen müssen daher wohl
mit anderen Medikamenten und Methoden in den Griff zu bekommen sein.
Bei gravierenden genetischen Krankheiten, die schwerste
Lebenseinschnitte bis hin zum Tod als Folge haben, dürfte die Gentherapie
wohl, selbst bei gewissen Nebenwirkungen alternativlos sein.
Von allen genannten Genthechnikunternehmen hat Spark wohl die
größte Marktkapitalisierung, zumal verschiedene Programme
wohl am weitesten fortgeschritten sind.
So dürfte Spark auch das UNternehmen sein, dass zum ersten Mal mit
Erlaubnis der FDA die Gentherapie an Patienten ausliefert, die nicht Probanden
sind.
Gruß
nachdem ich mich nun ein wenig mehr mit dem
Link und dem Artikel dahinter beschäftigt habe,
fasse ich mal kurz die Erkenntnisse des Schreibers,
hoffentlich einigermassen richtig, zusammen.
Die Gentherapie mit dem Angriffspunkt
an der Leber hat in einigen Fällen zur Erhöhung
eines Enzyms geführt, dass allgemein bei
diversen Lebererkrakungen im Blut nachweisbar ist und
den Normlevel übersteigt.
Man kann diesen erhöhten ALT Wert aber wohl mit
anderen Medikamenten kontrollieren.
Unklar ist wohl bei diversen Gentherapien, welche Spätfolgen
wohl entstehen könnten und wie lange die Gentherapie wirkt.
Dazu werden jetzt wohl aus mehreren Studien Daten gesammelt,
um hier bezüglich der Langzeitwirkung mehr Klarheit zu erhalten.
Müsste die einmalige Gentherapie nach einigen Jahren wiederholt werden,
würde das für die Gentherapieunternehmen nicht das Aus bedeuten,
sondern im Gegenteil, noch größere Umsätze.
Kritischer ist wohl die Fragestellung, welche Veränderungen
langfristig durch die eingebrachten Gene auftreten.
Egal, was bei der ein oder anderen Gentherapie an
Nebenwirkungen eventuell auftritt, man kann die einmalige Gabe
der neuen DNA-Abschnitte für den Körper nicht mehr
rückgängig machen.
Auftretende Nebenwirkungen müssen daher wohl
mit anderen Medikamenten und Methoden in den Griff zu bekommen sein.
Bei gravierenden genetischen Krankheiten, die schwerste
Lebenseinschnitte bis hin zum Tod als Folge haben, dürfte die Gentherapie
wohl, selbst bei gewissen Nebenwirkungen alternativlos sein.
Von allen genannten Genthechnikunternehmen hat Spark wohl die
größte Marktkapitalisierung, zumal verschiedene Programme
wohl am weitesten fortgeschritten sind.
So dürfte Spark auch das UNternehmen sein, dass zum ersten Mal mit
Erlaubnis der FDA die Gentherapie an Patienten ausliefert, die nicht Probanden
sind.
Gruß
Antwort auf Beitrag Nr.: 53.341.764 von Solideinvestierenkomplex4you am 24.09.16 18:49:31...ein weiteres Unternehmen sticht wohl in Bezug
auf die Marktkapitalisierung versus der
Anzahl der Therapiebereiche positiv heraus, namentlich
AveXis.
Warum das so ist, obwohl das Unternehmen lediglich einen
Teil der Spinalen Muskelatrophie mit seinem Produktkandidaten adressiert,
ist wohl der Hoffnung geschuldet, dass dieses Unternehmen
das Thema Nerven/Nervenbahnen erfolgreich adressiert,
und man sich aus dem Ansatz eine Übertragung auf größere
Anwendungsgebiete wie zum Beispiel Parkinson erhofft.
auf die Marktkapitalisierung versus der
Anzahl der Therapiebereiche positiv heraus, namentlich
AveXis.
Warum das so ist, obwohl das Unternehmen lediglich einen
Teil der Spinalen Muskelatrophie mit seinem Produktkandidaten adressiert,
ist wohl der Hoffnung geschuldet, dass dieses Unternehmen
das Thema Nerven/Nervenbahnen erfolgreich adressiert,
und man sich aus dem Ansatz eine Übertragung auf größere
Anwendungsgebiete wie zum Beispiel Parkinson erhofft.
Antwort auf Beitrag Nr.: 53.341.782 von Solideinvestierenkomplex4you am 24.09.16 18:55:27Hallo zusammen,
ich halte Aktien von Spark Therapeutics direkt und indirekt (über meine Wikifolios)
und Aktien von UniQure in einem Wikifolio mit sehr geringer Gewichtung.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen
Information.
Meiner Meinung nach lässt sich bei näherem Nachdenken wohl allgemein
zu Gentherapie konstatieren, dass das Wirkprofil enorm zu sein scheint.
Und das in verschiedenen Indikationen.
Die Risiken sind bislang wohl überschaubar und gegebenenfalls
bislang mit zusätzlichen Medikamenten beherrschbar.
Es bleibt jedoch die Restunsicherheit, dass eine langfristige
Veränderung durch Anwendung der Gentherapie unkontrollierbar werden könnte.
Obwohl es ja die gesunden (also richtigen) Gene sind, die dem Patienten eingespritzt werden.
Spark ist aktuell meines Wissens der klare Marktführer in diesem sich schnell
entwickelnden Bereich.
Meine lange Erfahrung an der Börse hat gezeigt, dass es in vielen "Zukunftsbranchen"
irgendwann zu gewaltigen Kurssprüngen in den jeweiligen Aktienkursen gekommen ist.
Manchmal berechtigt, manchmal auch nicht, aber Kurssprünge (so Pi mal Daumen innerhalb eines Jahres ungefähr eine Verzehnfachung)
gab es oft.
So zum Beispiel in der Solarindustrie, in der 3D-Druck Industrie,
verschiedene frühere Wellen innerhalb der Biotechindustrie usw.
Ich erinnere mich noch recht gut an ein Unternehmen, Human Genome Sciences,
welches 1997 in einem amerikanischen Börsenmagazin genannt wurde und
in 1998/1999 eine Kursexplosion vollzogen hat.
Das Unternehmen hat das menschliche Erbgut erforscht, aber kein einziges Produkt
durch seine Forschung konkret auf dem Tisch gehabt.
Dieses Unternehmen gibt es übrigens heute nicht mehr.
Wie dem auch sei:
Was mir auffällt, ist dass es innerhalb der noch jungen Branche der Gentherapie
die zuvor angeschriebenen Kurssprünge (noch) nicht gegeben hat.
Das wiederum könnte heißen, dass diese Kurssprünge irgendwann noch bevor stehen.
Irgendwann bewegt sich die Wall-Street vielleicht und schaut sich diesen Sektor an
und dann wollen eventuell wieder alle gleichzeitig durch diese eine Tür!!!???
Vom Timing her erinnert mich derzeit einiges an das Beispiel von 1997.
Die Unternehmen haben es bereits seit einiger Zeit in die mediale Landschaft der Börsenliteratur gebracht.
Seitdem ist ungefähr 1 Jahr vergangen. Vielleicht könnte also Ende 2016 oder das Jahr 2017
den Startschuss für eine Rally in den Gentherapieaktien bringen?
Vielleicht...
Alles nur meine Meinung!
Gruß
ich halte Aktien von Spark Therapeutics direkt und indirekt (über meine Wikifolios)
und Aktien von UniQure in einem Wikifolio mit sehr geringer Gewichtung.
Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen
Information.
Meiner Meinung nach lässt sich bei näherem Nachdenken wohl allgemein
zu Gentherapie konstatieren, dass das Wirkprofil enorm zu sein scheint.
Und das in verschiedenen Indikationen.
Die Risiken sind bislang wohl überschaubar und gegebenenfalls
bislang mit zusätzlichen Medikamenten beherrschbar.
Es bleibt jedoch die Restunsicherheit, dass eine langfristige
Veränderung durch Anwendung der Gentherapie unkontrollierbar werden könnte.
Obwohl es ja die gesunden (also richtigen) Gene sind, die dem Patienten eingespritzt werden.
Spark ist aktuell meines Wissens der klare Marktführer in diesem sich schnell
entwickelnden Bereich.
Meine lange Erfahrung an der Börse hat gezeigt, dass es in vielen "Zukunftsbranchen"
irgendwann zu gewaltigen Kurssprüngen in den jeweiligen Aktienkursen gekommen ist.
Manchmal berechtigt, manchmal auch nicht, aber Kurssprünge (so Pi mal Daumen innerhalb eines Jahres ungefähr eine Verzehnfachung)
gab es oft.
So zum Beispiel in der Solarindustrie, in der 3D-Druck Industrie,
verschiedene frühere Wellen innerhalb der Biotechindustrie usw.
Ich erinnere mich noch recht gut an ein Unternehmen, Human Genome Sciences,
welches 1997 in einem amerikanischen Börsenmagazin genannt wurde und
in 1998/1999 eine Kursexplosion vollzogen hat.
Das Unternehmen hat das menschliche Erbgut erforscht, aber kein einziges Produkt
durch seine Forschung konkret auf dem Tisch gehabt.
Dieses Unternehmen gibt es übrigens heute nicht mehr.
Wie dem auch sei:
Was mir auffällt, ist dass es innerhalb der noch jungen Branche der Gentherapie
die zuvor angeschriebenen Kurssprünge (noch) nicht gegeben hat.
Das wiederum könnte heißen, dass diese Kurssprünge irgendwann noch bevor stehen.
Irgendwann bewegt sich die Wall-Street vielleicht und schaut sich diesen Sektor an
und dann wollen eventuell wieder alle gleichzeitig durch diese eine Tür!!!???
Vom Timing her erinnert mich derzeit einiges an das Beispiel von 1997.
Die Unternehmen haben es bereits seit einiger Zeit in die mediale Landschaft der Börsenliteratur gebracht.
Seitdem ist ungefähr 1 Jahr vergangen. Vielleicht könnte also Ende 2016 oder das Jahr 2017
den Startschuss für eine Rally in den Gentherapieaktien bringen?
Vielleicht...
Alles nur meine Meinung!
Gruß
Hallo zusammen, ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen
meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information.
Heute nur etwas technisches:
Spark ist jetzt charttechnisch gesehen an der Grenze zum überkauften Bereich.
Sollte der Gesamtmarkt einigermaßen stabil sein, könnte Spark eventuell in den nächsten Tagen
einen Sprung nach oben machen, zumal Spark auch im Vergleich
zum Biotechindex (IBB) aktuell deutlich besser performt.
Könnte...muss aber nicht...
Gruß
meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information.
Heute nur etwas technisches:
Spark ist jetzt charttechnisch gesehen an der Grenze zum überkauften Bereich.
Sollte der Gesamtmarkt einigermaßen stabil sein, könnte Spark eventuell in den nächsten Tagen
einen Sprung nach oben machen, zumal Spark auch im Vergleich
zum Biotechindex (IBB) aktuell deutlich besser performt.
Könnte...muss aber nicht...
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information.
So viel zum rechtlichen Teil meines Kommentars.
Soeben wurde eine Kooperation zwischen Spark und einem Segment der Uni Massachusetts bekannt, in dem bestehende Transportwege für die Gentherapie verbessert werden sollen. Diese Information kann eine Interpretation zur Folge haben, von der ich aber nicht weiß, ob diese Interpretation nun richtig oder falsch ist.
Aber mir erscheint der Gedankengang zunächst logisch.
Ich habe mich in der Vergangenheit gefragt, warum sich viele Unternehmen in diesem Bereich auf gleiche oder ähnliche Ziele konzentrieren, obwohl es unzählig viele Krankheiten gibt, die sich auf genetische Ursachen zurück führen lassen und obwohl bei einer Vielzahl dieser Krankheiten die defekten Gene bekannt sind???
Die Kooperation jetzt könnte diesen Umstand tatsächlich damit erklären, dass die virale Übertragung
von Genabschnitten in den Körper nicht überall funktioniert und scheinbar, wenn ich es richtig verstehe, nicht einmal innerhalb eines Organs oder eines Zielpunktes, alle Genabschnitte übertragen
werden können.
Dies ist vielleicht dann der aktuelle Stand.
Natürlich arbeiten die Wissenschaftler weiter und werden wohl, früher oder später, diese
Problematiken überkommen können.
Spark hat hier wohl als bereits rennommiertes Unternehmen in diesem jungen Bereich (schliesslich wird die erste Gentherapie für Patienten aus dem Hause Spark kommen),
beste Chancen, die sehr guten Deals einzugehen.
Vor dem Hintergrund der vorhergehenden Überlegungen muss der Schritt heute wohl als Schritt in
die richtige Richtung gewertet werden.
Ich bin gespannt, wie sich Spark heute, vor dem Hintergrund dieser Meldung,
entwickelt.
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information.
So viel zum rechtlichen Teil meines Kommentars.
Soeben wurde eine Kooperation zwischen Spark und einem Segment der Uni Massachusetts bekannt, in dem bestehende Transportwege für die Gentherapie verbessert werden sollen. Diese Information kann eine Interpretation zur Folge haben, von der ich aber nicht weiß, ob diese Interpretation nun richtig oder falsch ist.
Aber mir erscheint der Gedankengang zunächst logisch.
Ich habe mich in der Vergangenheit gefragt, warum sich viele Unternehmen in diesem Bereich auf gleiche oder ähnliche Ziele konzentrieren, obwohl es unzählig viele Krankheiten gibt, die sich auf genetische Ursachen zurück führen lassen und obwohl bei einer Vielzahl dieser Krankheiten die defekten Gene bekannt sind???
Die Kooperation jetzt könnte diesen Umstand tatsächlich damit erklären, dass die virale Übertragung
von Genabschnitten in den Körper nicht überall funktioniert und scheinbar, wenn ich es richtig verstehe, nicht einmal innerhalb eines Organs oder eines Zielpunktes, alle Genabschnitte übertragen
werden können.
Dies ist vielleicht dann der aktuelle Stand.
Natürlich arbeiten die Wissenschaftler weiter und werden wohl, früher oder später, diese
Problematiken überkommen können.
Spark hat hier wohl als bereits rennommiertes Unternehmen in diesem jungen Bereich (schliesslich wird die erste Gentherapie für Patienten aus dem Hause Spark kommen),
beste Chancen, die sehr guten Deals einzugehen.
Vor dem Hintergrund der vorhergehenden Überlegungen muss der Schritt heute wohl als Schritt in
die richtige Richtung gewertet werden.
Ich bin gespannt, wie sich Spark heute, vor dem Hintergrund dieser Meldung,
entwickelt.
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information. So viel zum rechtlichen Teil meines Kommentars.
Hat irgendjemand eine Ahnung, warum Spark heute rund 20 % im Minus notiert???
Ausser den Quartalszahlen gab es noch Studienupdates zu einem Haemophilie Produkt, die
meiner Meinung doch ganz passabel ausgefallen sind.
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information. So viel zum rechtlichen Teil meines Kommentars.
Hat irgendjemand eine Ahnung, warum Spark heute rund 20 % im Minus notiert???
Ausser den Quartalszahlen gab es noch Studienupdates zu einem Haemophilie Produkt, die
meiner Meinung doch ganz passabel ausgefallen sind.
Gruß
Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information. So viel zum rechtlichen Teil meines Kommentars.
Ich möchte hier meinem vorletzten Beitrag eine für mich neue Information hinzu fügen,
die ich aus einer schriftlichen Anfrage an ein Unternehmen der Gentherapiebranche gestellt habe.
Ich habe in meinem vorletztem Kommentar gemutmasst, dass die entsprechenden Gene
möglicherweise nicht alle Zielpunkte erreichen können und es daher sein kann,
dass aus diesem Grunde nicht bereits deutliche mehr Krankheiten geheilt werden können.
Aus meiner Anfrage erfuhr ich jedoch, dass der so genannte AAV-Vektor, der zum Transport der
"reparierten Gene" in den menschlichen Körper dient,
wohl ein begrenztes Fassungsvermögen besitzt und daher als Transportmittel nur
für bestimmte Gene zur Verfügung stehen kann.
Meine eigene Interpretation wäre dann, dass je länger die "richtigen Genabschnitte" werden,
die an den Körper übermittelt werden müssen, umso unwahrscheinlicher ist es aus heutiger Sicht,
dass diese Genabschnitte überhaupt übertragen werden können.
Auch unter diesem Gesichtspunkt ist wohl die Verbesserung der Transportwege (hier hat Spark ja
kürzlich eine Kooperation bekannt gegeben)
ein Schlüssel zur Verbreitung der Gentherapie auf andere Krankheiten.
Inwieweit jedoch der AAV-Vektor hier moduliert werden muss oder ob eventuell strukturell
komplett neue Transportwege gefunden werden müssen, keine Ahnung.
Wer hier mehr weiss, kann dies gerne hier posten. Würde mich sehr freuen.
Gruß
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information. So viel zum rechtlichen Teil meines Kommentars.
Ich möchte hier meinem vorletzten Beitrag eine für mich neue Information hinzu fügen,
die ich aus einer schriftlichen Anfrage an ein Unternehmen der Gentherapiebranche gestellt habe.
Ich habe in meinem vorletztem Kommentar gemutmasst, dass die entsprechenden Gene
möglicherweise nicht alle Zielpunkte erreichen können und es daher sein kann,
dass aus diesem Grunde nicht bereits deutliche mehr Krankheiten geheilt werden können.
Aus meiner Anfrage erfuhr ich jedoch, dass der so genannte AAV-Vektor, der zum Transport der
"reparierten Gene" in den menschlichen Körper dient,
wohl ein begrenztes Fassungsvermögen besitzt und daher als Transportmittel nur
für bestimmte Gene zur Verfügung stehen kann.
Meine eigene Interpretation wäre dann, dass je länger die "richtigen Genabschnitte" werden,
die an den Körper übermittelt werden müssen, umso unwahrscheinlicher ist es aus heutiger Sicht,
dass diese Genabschnitte überhaupt übertragen werden können.
Auch unter diesem Gesichtspunkt ist wohl die Verbesserung der Transportwege (hier hat Spark ja
kürzlich eine Kooperation bekannt gegeben)
ein Schlüssel zur Verbreitung der Gentherapie auf andere Krankheiten.
Inwieweit jedoch der AAV-Vektor hier moduliert werden muss oder ob eventuell strukturell
komplett neue Transportwege gefunden werden müssen, keine Ahnung.
Wer hier mehr weiss, kann dies gerne hier posten. Würde mich sehr freuen.
Gruß
Antwort auf Beitrag Nr.: 53.783.052 von Solideinvestierenkomplex4you am 28.11.16 10:35:11Hallo zusammen,
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information. So viel zum rechtlichen Teil meines Kommentars.
Und wieder eine neue Lizenzvereinbarung mit der Selecta Biosciences, an der sich Spark
auch finanziell (über Aktienkäufe) beteiligt.
Zielpunkte sind, wenn ich es richtig verstehe, die abermalige Verbesserung des
großen Themas Gentransport.
Mit Hilfe von Selectas auf Nanopartikeln basierender Technologie,
soll wohl die Immunabwehr (auf das Capsid - also die AAV-Vektoren)
des Körpers vermindert werden.
Ausserdem kann damit eine Nachdosierung und eine abermalige Gentherapie in
einem kurzen Zeitfenster durchgeführt werden, so die Hoffnung von Spark.
Wie bereits in meinem Kommentar vom 20.10.2016 vermutet,
arbeitet Spark wohl daran, die Transportwege der Gentherapie
stetig zu verbessern, wohl auch, um das Anwendungsspektrum zu erweitern.
Der Transportmechanismus scheint derzeit noch die Achillesferse
der Gentherapie zu sein.
Eine Frage drängt sich an dieser Stelle für mich aber wieder einmal auf:
Wenn die neue CRISPR Technologie beliebig Genabschnitte austauschen kann,
warum geht dann Spark keine Kooperation mit diesen Unternehmen ein?
Sind das eventuell 2 völlig verschiedene Schuhe?
Wer weiss hier mehr?
Gruß
P.S: Noch etwas zur Charttechnik:
Wir scheinen hier aktuell kurz vor der überverkauften Zone zu sein.
Ein Auskotzen des AKtienkurses wäre also in den nächsten Tagen denkbar, wenn auch nicht
gewünscht. Egal,
sollte es so kommen wäre das vielleicht eine gute Gelegenheit zum Nachkauf!?
ich halte Aktien von Spark Therapeutics in meinen Privatdepots als auch in einigen meiner Wikifolios. Dies ist weder Kauf- noch Verkaufsempfehlung, sondern dient der allgemeinen Information. So viel zum rechtlichen Teil meines Kommentars.
Und wieder eine neue Lizenzvereinbarung mit der Selecta Biosciences, an der sich Spark
auch finanziell (über Aktienkäufe) beteiligt.
Zielpunkte sind, wenn ich es richtig verstehe, die abermalige Verbesserung des
großen Themas Gentransport.
Mit Hilfe von Selectas auf Nanopartikeln basierender Technologie,
soll wohl die Immunabwehr (auf das Capsid - also die AAV-Vektoren)
des Körpers vermindert werden.
Ausserdem kann damit eine Nachdosierung und eine abermalige Gentherapie in
einem kurzen Zeitfenster durchgeführt werden, so die Hoffnung von Spark.
Wie bereits in meinem Kommentar vom 20.10.2016 vermutet,
arbeitet Spark wohl daran, die Transportwege der Gentherapie
stetig zu verbessern, wohl auch, um das Anwendungsspektrum zu erweitern.
Der Transportmechanismus scheint derzeit noch die Achillesferse
der Gentherapie zu sein.
Eine Frage drängt sich an dieser Stelle für mich aber wieder einmal auf:
Wenn die neue CRISPR Technologie beliebig Genabschnitte austauschen kann,
warum geht dann Spark keine Kooperation mit diesen Unternehmen ein?
Sind das eventuell 2 völlig verschiedene Schuhe?
Wer weiss hier mehr?
Gruß
P.S: Noch etwas zur Charttechnik:
Wir scheinen hier aktuell kurz vor der überverkauften Zone zu sein.
Ein Auskotzen des AKtienkurses wäre also in den nächsten Tagen denkbar, wenn auch nicht
gewünscht. Egal,
sollte es so kommen wäre das vielleicht eine gute Gelegenheit zum Nachkauf!?
charttechnisch überverkaufter Zustand in einem generellen Aufwärtstrend
bei Spark aktuell.
Vielleicht ist der Boden nahe und vielleicht eine gute Möglichkeit,
ein paar Stücke einzusammenl?
Gruß und schönes WE
bei Spark aktuell.
Vielleicht ist der Boden nahe und vielleicht eine gute Möglichkeit,
ein paar Stücke einzusammenl?
Gruß und schönes WE
Hallo,
ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Wie ich durch einen User hier in einem anderen
Thread erfahren habe,
beruhen verschiedene Krankheiten und Erbkrankheiten
auf teils mehreren Gendefekten.
Dies verkompliziert eine mögliche Heilung durch Gentherapie.
Bisherige Therapien zielen wohl zunächst einmal auf
Erbkrankheiten mit nur einem Gendefekt.
Zusätzlich erschwerend kommt hinzu,
dass bei einigen Erbkrankheiten und KRankheiten
noch gar nicht klar ist, welche Gene in ihrer
Gesamtheit die Krankheit verursachen und
eventuell gibt es sogar bei gleichem Krankheitsbild
partiell unterschiedliche Gene, die dieses Krankheitsbild
auslösen.
Wenngleich durch die CRISPR/CAS9 Technologie
zunächst eine gute Möglichkeit gefunden wurde,
das Genom an bestimmten Stellen zu schneiden
und zu reparieren, scheint das nicht alles zu sein,
was zu einer Heilung von Krankheiten nötig ist.
Insofern haben alle Gentherapieunternehmen
prinzipiell die Chance, auf den nächsten großen Erkenntnissprung
mit samt Produkt(en).
Da Spark hier in den USA kurz vor Marktzulassung
des ersten Medikaments auf Basis der Gentherapie
steht, dürfte dieses Unternehmen bislang
auch als der Marktführer in diesem Bereich angesehen
werden, der zudem bereits jetzt die meisten Daten
und die meiste Erfahrung in diesem Bereich sammeln kann.
Dies sieht auch die Börse so, denn kein anderes Unternehmen
kommt derzeit auf eine so hohe Börsenbewertung wie Spark Therapeutics.
Gruß
ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Wie ich durch einen User hier in einem anderen
Thread erfahren habe,
beruhen verschiedene Krankheiten und Erbkrankheiten
auf teils mehreren Gendefekten.
Dies verkompliziert eine mögliche Heilung durch Gentherapie.
Bisherige Therapien zielen wohl zunächst einmal auf
Erbkrankheiten mit nur einem Gendefekt.
Zusätzlich erschwerend kommt hinzu,
dass bei einigen Erbkrankheiten und KRankheiten
noch gar nicht klar ist, welche Gene in ihrer
Gesamtheit die Krankheit verursachen und
eventuell gibt es sogar bei gleichem Krankheitsbild
partiell unterschiedliche Gene, die dieses Krankheitsbild
auslösen.
Wenngleich durch die CRISPR/CAS9 Technologie
zunächst eine gute Möglichkeit gefunden wurde,
das Genom an bestimmten Stellen zu schneiden
und zu reparieren, scheint das nicht alles zu sein,
was zu einer Heilung von Krankheiten nötig ist.
Insofern haben alle Gentherapieunternehmen
prinzipiell die Chance, auf den nächsten großen Erkenntnissprung
mit samt Produkt(en).
Da Spark hier in den USA kurz vor Marktzulassung
des ersten Medikaments auf Basis der Gentherapie
steht, dürfte dieses Unternehmen bislang
auch als der Marktführer in diesem Bereich angesehen
werden, der zudem bereits jetzt die meisten Daten
und die meiste Erfahrung in diesem Bereich sammeln kann.
Dies sieht auch die Börse so, denn kein anderes Unternehmen
kommt derzeit auf eine so hohe Börsenbewertung wie Spark Therapeutics.
Gruß
Hallo,
ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Wie gestern aus einer Unternehmensmeldung zu erfahren war,
ist die Zulasssung des ersten Medikaments von Spark
scheinbar nochmals einen deutlichen Schritt näher gerückt.
Charttechnisch gesehen wird es bei Spark derzeit sehr interessant.
Mit großem Schwung nach oben zeigt sich Spark seit rund 1 Monat.
Ganz im Gegensatz zum Sektor (zum Beispiel beim Vergleich mit dem IBB).
Nun steht Spark unmittelbar vor dem überkauftem Bereich.
Sollte Spark hier eintreten, könnte es kurzfristig zu einem
regelrechtem Kursfeuerwerk kommen!?
Gruß
ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Wie gestern aus einer Unternehmensmeldung zu erfahren war,
ist die Zulasssung des ersten Medikaments von Spark
scheinbar nochmals einen deutlichen Schritt näher gerückt.
Charttechnisch gesehen wird es bei Spark derzeit sehr interessant.
Mit großem Schwung nach oben zeigt sich Spark seit rund 1 Monat.
Ganz im Gegensatz zum Sektor (zum Beispiel beim Vergleich mit dem IBB).
Nun steht Spark unmittelbar vor dem überkauftem Bereich.
Sollte Spark hier eintreten, könnte es kurzfristig zu einem
regelrechtem Kursfeuerwerk kommen!?
Gruß
Antwort auf Beitrag Nr.: 54.908.840 von Solideinvestierenkomplex4you am 10.05.17 12:23:11Hallo,
Spark könnte meiner Meinung einer der Hauptprofiteure
bezüglich der jüngst bekannt gewordenen
unerwünschten "Fehlprogrammierung" der CRISPR/CAS9
Technologie sein bzw. werden.
P.S: Ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
Spark könnte meiner Meinung einer der Hauptprofiteure
bezüglich der jüngst bekannt gewordenen
unerwünschten "Fehlprogrammierung" der CRISPR/CAS9
Technologie sein bzw. werden.
P.S: Ich halte mittelbar und unmittelbar Aktien von Spark Th.
und dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der reinen Information.
am Donnerstag wird es interessant:
die FDA hat eine Expertenrunde eingeladen, um über die Zulassung von Sparks experimentelle Gen-Therapie zu beraten. Bei Zulassung wäre dies die erste "wahre" Gen-Therapie, welche zur Behandlung einer seltenen Form von Erblindung bei Kindern vorgesehen ist.
Die erste "wahre" Gen-Therapie, weil der Gendefekt durch das Ersetzen des defekten Gens behoben werden soll.
Ich rechne damit, dass Luxturna zur Zulassung empfohlen wird. Gespannt darf man sein, welcher Preis für Luxturna von Spark Therapeutics erhoben wird. Einige Akteure an der WallStreet rechnen mit einem Therapiepreis von 1 Mio USD!!
die FDA hat eine Expertenrunde eingeladen, um über die Zulassung von Sparks experimentelle Gen-Therapie zu beraten. Bei Zulassung wäre dies die erste "wahre" Gen-Therapie, welche zur Behandlung einer seltenen Form von Erblindung bei Kindern vorgesehen ist.
Die erste "wahre" Gen-Therapie, weil der Gendefekt durch das Ersetzen des defekten Gens behoben werden soll.
Ich rechne damit, dass Luxturna zur Zulassung empfohlen wird. Gespannt darf man sein, welcher Preis für Luxturna von Spark Therapeutics erhoben wird. Einige Akteure an der WallStreet rechnen mit einem Therapiepreis von 1 Mio USD!!
Antwort auf Beitrag Nr.: 55.913.507 von Cyberhexe am 09.10.17 17:56:57...bin mit 500 Stück zu USD 84.26 vor dem AC am Donnerstag eingestiegen - hoffe kurzfristig nach positiver Empfehlung auf dreistellige Kurse.
Die FDA wird die Preisvorstellungen des Unternehmens selbstverständlich nicht berücksichtigen, so dass einzig und allein dessen Risk/Benefit-Verhältnis zur Diskussion steht.
Hyperlink zur FDA:
https://www.fda.gov/AdvisoryCommittees/Calendar/ucm576950.ht…
Die FDA wird die Preisvorstellungen des Unternehmens selbstverständlich nicht berücksichtigen, so dass einzig und allein dessen Risk/Benefit-Verhältnis zur Diskussion steht.
Hyperlink zur FDA:
https://www.fda.gov/AdvisoryCommittees/Calendar/ucm576950.ht…
Antwort auf Beitrag Nr.: 55.915.895 von Cyberhexe am 10.10.17 00:06:39sorry, habe aus Versehen den falschen Hyperlink gewählt; anbei der Richtige:
https://www.fda.gov/AdvisoryCommittees/Calendar/ucm574394.ht…
Agenda
On October 12, 2017, the Cellular, Tissue and Gene Therapies Advisory Committee (CTGTAC) will meet in an open session to discuss and make recommendations on the safety and effectiveness of Biologics License Application (BLA) 125610, voretigene neparvovec, submitted by Spark Therapeutics, Inc. The proposed indication (use) for this product is treatment of patients with vision loss due to confirmed biallelic RPE65 mutation-associated retinal dystrophy.
https://www.fda.gov/AdvisoryCommittees/Calendar/ucm574394.ht…
Agenda
On October 12, 2017, the Cellular, Tissue and Gene Therapies Advisory Committee (CTGTAC) will meet in an open session to discuss and make recommendations on the safety and effectiveness of Biologics License Application (BLA) 125610, voretigene neparvovec, submitted by Spark Therapeutics, Inc. The proposed indication (use) for this product is treatment of patients with vision loss due to confirmed biallelic RPE65 mutation-associated retinal dystrophy.
Antwort auf Beitrag Nr.: 55.915.931 von Cyberhexe am 10.10.17 00:24:49anbei der HL zu den "Briefing Documents" zum Advisory Committee am Donnerstag:
https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesM…
Also auf den ersten Blick wird die Zulassung nicht in Frage gestellt. Die Fragen zielen vor allem auf eine Altersbeschränkung bzw. ab welchem Alter eine Therapie gut geheissen wird:
The FDA seeks the opinion of the Committee regarding the following issues:
1. The clinical meaningfulness of a 2-light level improvement in the multi-luminance mobility
testing (MLMT) in “patients with vision loss due to confirmed biallelic RPE65 mutationassociated
retinal dystrophy”
2. The optimal disease stage to treat patients with bilallelic RPE65 mutation-associated retinal
dystrophy, especially:
a. At what stage of clinical presentation do the benefits of therapy outweigh the risks?
b. How can the data from subjects with significant vision loss be extrapolated to patients
with earlier stages of disease with or without measurable vision loss prior to
treatment?
c. Considering the adverse events associated with the subretinal injection of voretigene
neparvovec and the concomitant use of oral prednisone, what are your concerns for
treating pediatric patients at a young age?
d. What is the reasonable minimal age, if any, that you would recommend for treatment?
3. The potential benefits and risks of repeat administration of voretigene neparvovec into one
eye, and what, if any, additional data is required to support such repeat administration
https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesM…
Also auf den ersten Blick wird die Zulassung nicht in Frage gestellt. Die Fragen zielen vor allem auf eine Altersbeschränkung bzw. ab welchem Alter eine Therapie gut geheissen wird:
The FDA seeks the opinion of the Committee regarding the following issues:
1. The clinical meaningfulness of a 2-light level improvement in the multi-luminance mobility
testing (MLMT) in “patients with vision loss due to confirmed biallelic RPE65 mutationassociated
retinal dystrophy”
2. The optimal disease stage to treat patients with bilallelic RPE65 mutation-associated retinal
dystrophy, especially:
a. At what stage of clinical presentation do the benefits of therapy outweigh the risks?
b. How can the data from subjects with significant vision loss be extrapolated to patients
with earlier stages of disease with or without measurable vision loss prior to
treatment?
c. Considering the adverse events associated with the subretinal injection of voretigene
neparvovec and the concomitant use of oral prednisone, what are your concerns for
treating pediatric patients at a young age?
d. What is the reasonable minimal age, if any, that you would recommend for treatment?
3. The potential benefits and risks of repeat administration of voretigene neparvovec into one
eye, and what, if any, additional data is required to support such repeat administration
Antwort auf Beitrag Nr.: 55.918.460 von Cyberhexe am 10.10.17 11:54:33...das intensive Studium der Unterlagen lässt dann doch noch einige Zweifel aufkommen und zwar wird neben dem bereits thematisierten Mindestalter die Dauer des Therapieerfolges in Frage gestellt.
Obschon ich mit einer Zulassungsempfehlung rechne, ist diese alles andere als gewiss, weshalb im Nachgang des AC mit einer Kursreaktion zu rechnen ist. Wäre das AC eine sicherer Angelegenheit, wäre die Zulassung bereits volsständig im Kurs eingepreist.
Obschon ich mit einer Zulassungsempfehlung rechne, ist diese alles andere als gewiss, weshalb im Nachgang des AC mit einer Kursreaktion zu rechnen ist. Wäre das AC eine sicherer Angelegenheit, wäre die Zulassung bereits volsständig im Kurs eingepreist.
Antwort auf Beitrag Nr.: 55.921.469 von Cyberhexe am 10.10.17 16:58:20
Spark Therapeutics faces a grilling as FDA ponders a pioneering OK for gene therapy
by john carroll — on October 10, 2017 07:14 AM EDT
Updated: 09:59 AM
With one of the most closely-watched FDA panel reviews of the year coming up for Spark Therapeutics’ $ONCE lead gene therapy, internal reviewers at the FDA have raised some serious questions for the experts to consider.
At the top of the heap of considerations the panel experts will field on Thursday are questions about the durability of this eye therapy, the possibility that patients will need multiple treatments in order to preserve vision gains, the right age to use it and the use of a completely novel endpoint for the primary goal when standard visual acuity achievements fell far short of the goal on statistical significance.
The reviewers readily agree that the gene therapy — angling to become the first such treatment approved in the US — met the main criteria for success. But the drug, voretigene neparvovec (or Luxturna), also was no once-and-done panacea.
Investors were upbeat but possibly a little ambivalent about the next step, with Spark’s stock up 1% in pre-market trading.
In the key study, investigators treated 21 patients with retinal dystrophy triggered by biallelic RPE65 mutations; 10 were recruited for the placebo group. Eleven of the 21 had a significant, two point or more improvement in light levels in both eyes, with 15 scoring a significant MLMT (multi-luminance mobility testing) gain in the first treated eye. That easily beat the response in the control arm.
Checking visual acuity, though, shows that the patients failed to demonstrate a significant improvement for the designated secondary, leaving Spark to seek a pioneering approval using an endpoint that’s never been used before in this way.
The FDA is asking the experts to consider the significance of the endpoint, the impact such improvements have on patients’ daily activities, as well as the consequences if patients need multiple treatments, given the fact that there’s no data on just how durable the treatment effect can be.
Notes the review:
(T)here is no available long term follow up data to address whether the effect decays over time. Therefore, the duration of AAV2- mediated transgene expression leading to sustained clinical benefits beyond one year is unclear.
The review also notes that Spark ignored a key piece of advice, avoiding a co-primary endpoint on evaluating how the first-treated eye was affected compared to both eyes, with reviewers concerned that a patient response could be judged a success even if vision in one eye deteriorated and only one eye improved.
This concern led FDA to recommend co-primary efficacy endpoints, i.e., MLMT score change using both eyes and MLMT score change using the first eye. However, Study 301 was designed with a single primary endpoint, an MLMT score change using both eyes.
None of that marks a kiss of death for this application. The reviewers are careful to avoid any harsh judgments or endorsements, staying neutral on the key questions regarding efficacy and safety. But it’s also not exactly the kind of discussion any gene therapy company wants to have just before a potential market launch like this.
While analysts have given Spark high marks for this therapy, with good odds of success, major questions remain on how these treatments will be covered by skeptical payers who may be asked to foot the bill on a million-dollar procedure. Will the payments be spread over time? And what happens if the gene therapy doesn’t work as billed, or fades over time?
RBC’s Matthew Eckler counted himself among the analysts who saw today’s review, with no big surprises, as a plus for Spark. He noted:
On first read, we see no major surprises in FDA briefing documents released this morning ahead of Thursday’s AdCom meeting for Luxturna. Focus of the FDA review is on efficacy (younger vs older patients, novel Phase III endpoint), safety (subretinal injection, immunogenicity), and duration of response; while the single voting question sets up a straight up/down vote. As outlined in our recent initiation (link), we anticipate a positive panel and approval by the 1/12/18 PDUFA. Separately, we see discussion and outcome Thursday as having read-through to the gene therapy space broadly, particularly FDA and panel members’ focus/comfort around safety and duration of response.
So far, two gene therapies have been approved in Europe, but the first one flat failed to gain traction and was dumped while the second is only rarely employed. With this first application in the US, Spark is initiating a discussion that will be closely followed throughout the industry.
The outcome is not assured.
https://endpts.com/spark-therapeutics-faces-a-grilling-as-fd…
Zitat von Cyberhexe: ...das intensive Studium der Unterlagen lässt dann doch noch einige Zweifel aufkommen und zwar wird neben dem bereits thematisierten Mindestalter die Dauer des Therapieerfolges in Frage gestellt.
Obschon ich mit einer Zulassungsempfehlung rechne, ist diese alles andere als gewiss, weshalb im Nachgang des AC mit einer Kursreaktion zu rechnen ist. Wäre das AC eine sicherer Angelegenheit, wäre die Zulassung bereits volsständig im Kurs eingepreist.
Spark Therapeutics faces a grilling as FDA ponders a pioneering OK for gene therapy
by john carroll — on October 10, 2017 07:14 AM EDT
Updated: 09:59 AM
With one of the most closely-watched FDA panel reviews of the year coming up for Spark Therapeutics’ $ONCE lead gene therapy, internal reviewers at the FDA have raised some serious questions for the experts to consider.
At the top of the heap of considerations the panel experts will field on Thursday are questions about the durability of this eye therapy, the possibility that patients will need multiple treatments in order to preserve vision gains, the right age to use it and the use of a completely novel endpoint for the primary goal when standard visual acuity achievements fell far short of the goal on statistical significance.
The reviewers readily agree that the gene therapy — angling to become the first such treatment approved in the US — met the main criteria for success. But the drug, voretigene neparvovec (or Luxturna), also was no once-and-done panacea.
Investors were upbeat but possibly a little ambivalent about the next step, with Spark’s stock up 1% in pre-market trading.
In the key study, investigators treated 21 patients with retinal dystrophy triggered by biallelic RPE65 mutations; 10 were recruited for the placebo group. Eleven of the 21 had a significant, two point or more improvement in light levels in both eyes, with 15 scoring a significant MLMT (multi-luminance mobility testing) gain in the first treated eye. That easily beat the response in the control arm.
Checking visual acuity, though, shows that the patients failed to demonstrate a significant improvement for the designated secondary, leaving Spark to seek a pioneering approval using an endpoint that’s never been used before in this way.
The FDA is asking the experts to consider the significance of the endpoint, the impact such improvements have on patients’ daily activities, as well as the consequences if patients need multiple treatments, given the fact that there’s no data on just how durable the treatment effect can be.
Notes the review:
(T)here is no available long term follow up data to address whether the effect decays over time. Therefore, the duration of AAV2- mediated transgene expression leading to sustained clinical benefits beyond one year is unclear.
The review also notes that Spark ignored a key piece of advice, avoiding a co-primary endpoint on evaluating how the first-treated eye was affected compared to both eyes, with reviewers concerned that a patient response could be judged a success even if vision in one eye deteriorated and only one eye improved.
This concern led FDA to recommend co-primary efficacy endpoints, i.e., MLMT score change using both eyes and MLMT score change using the first eye. However, Study 301 was designed with a single primary endpoint, an MLMT score change using both eyes.
None of that marks a kiss of death for this application. The reviewers are careful to avoid any harsh judgments or endorsements, staying neutral on the key questions regarding efficacy and safety. But it’s also not exactly the kind of discussion any gene therapy company wants to have just before a potential market launch like this.
While analysts have given Spark high marks for this therapy, with good odds of success, major questions remain on how these treatments will be covered by skeptical payers who may be asked to foot the bill on a million-dollar procedure. Will the payments be spread over time? And what happens if the gene therapy doesn’t work as billed, or fades over time?
RBC’s Matthew Eckler counted himself among the analysts who saw today’s review, with no big surprises, as a plus for Spark. He noted:
On first read, we see no major surprises in FDA briefing documents released this morning ahead of Thursday’s AdCom meeting for Luxturna. Focus of the FDA review is on efficacy (younger vs older patients, novel Phase III endpoint), safety (subretinal injection, immunogenicity), and duration of response; while the single voting question sets up a straight up/down vote. As outlined in our recent initiation (link), we anticipate a positive panel and approval by the 1/12/18 PDUFA. Separately, we see discussion and outcome Thursday as having read-through to the gene therapy space broadly, particularly FDA and panel members’ focus/comfort around safety and duration of response.
So far, two gene therapies have been approved in Europe, but the first one flat failed to gain traction and was dumped while the second is only rarely employed. With this first application in the US, Spark is initiating a discussion that will be closely followed throughout the industry.
The outcome is not assured.
https://endpts.com/spark-therapeutics-faces-a-grilling-as-fd…
Antwort auf Beitrag Nr.: 55.922.417 von bernie55 am 10.10.17 18:40:42...ich gehe dennoch von einer Zulassungsempfehlung aus und habe deswegen 10´000 PGNX in ONCE "eingetauscht" - ich denke, dass relativ kurzfristig dreistellige Kurse möglich sind.
Zitat von Cyberhexe: ...ich gehe dennoch von einer Zulassungsempfehlung aus und habe deswegen 10´000 PGNX in ONCE "eingetauscht" - ich denke, dass relativ kurzfristig dreistellige Kurse möglich sind.
Es wird auf jeden Fall spannend........
Ich habe mir heute beim bottomfishing
 auch mal eine kleine Posi zugelegt - zu 83,75 USD
auch mal eine kleine Posi zugelegt - zu 83,75 USD
Antwort auf Beitrag Nr.: 55.922.636 von bernie55 am 10.10.17 19:05:26
Kompliment, super "Timing" - hat bei mir nicht ganz so gut gepasst!
Zitat von bernie55:Zitat von Cyberhexe: ...ich gehe dennoch von einer Zulassungsempfehlung aus und habe deswegen 10´000 PGNX in ONCE "eingetauscht" - ich denke, dass relativ kurzfristig dreistellige Kurse möglich sind.
Es wird auf jeden Fall spannend........
Ich habe mir heute beim bottomfishingauch mal eine kleine Posi zugelegt - zu 83,75 USD
Kompliment, super "Timing" - hat bei mir nicht ganz so gut gepasst!
Antwort auf Beitrag Nr.: 55.922.741 von Cyberhexe am 10.10.17 19:17:17
Heute findet das AC statt:
https://www.fda.gov/AdvisoryCommittees/Calendar/ucm574394.ht…
Ich rechne mit einer positiven Zulassungsempfehlung und im Anschluss mit Kursen jenseits USD 90.
Werde die Teile dann möglichst rasch wieder abstossen und hoffe auf einen Gewinn von > 10%.
Heute findet das AC statt:
https://www.fda.gov/AdvisoryCommittees/Calendar/ucm574394.ht…
Ich rechne mit einer positiven Zulassungsempfehlung und im Anschluss mit Kursen jenseits USD 90.
Werde die Teile dann möglichst rasch wieder abstossen und hoffe auf einen Gewinn von > 10%.
Antwort auf Beitrag Nr.: 55.935.605 von Cyberhexe am 12.10.17 10:24:46anbei die Agenda für die heutige Sitzung der Expertenrunde:
https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesM…
https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesM…
Antwort auf Beitrag Nr.: 55.938.527 von Cyberhexe am 12.10.17 15:25:57October 12, 2017
Spark Therapeutics shares halted as FDA committee reviews gene therapy treatment for eye disease
Spark Therapeutics shares halted as FDA committee reviews gene therapy treatment for eye disease
Antwort auf Beitrag Nr.: 55.938.572 von Cyberhexe am 12.10.17 15:29:49Vom AC:
“This is exactly the type of disease that we hoped that gene therapy would someday treat,” sagte Dr. Wilson Bryan, Director of the FDA’s office of Tissues and Advanced Therapies.
Allerdings fügte er hinzu, dass die FDA unsicher sei, ob der neue Mobilitätetest hinsichtlich Sehvermögen von Spark genügt, um die Wirkung von Luxturna zu beweisen. Die FDA erwartet diesbezüglich Unterstützung und Führung von der aufgebotenen Expertenrunde.
“This is exactly the type of disease that we hoped that gene therapy would someday treat,” sagte Dr. Wilson Bryan, Director of the FDA’s office of Tissues and Advanced Therapies.
Allerdings fügte er hinzu, dass die FDA unsicher sei, ob der neue Mobilitätetest hinsichtlich Sehvermögen von Spark genügt, um die Wirkung von Luxturna zu beweisen. Die FDA erwartet diesbezüglich Unterstützung und Führung von der aufgebotenen Expertenrunde.
Antwort auf Beitrag Nr.: 55.938.911 von Cyberhexe am 12.10.17 16:06:43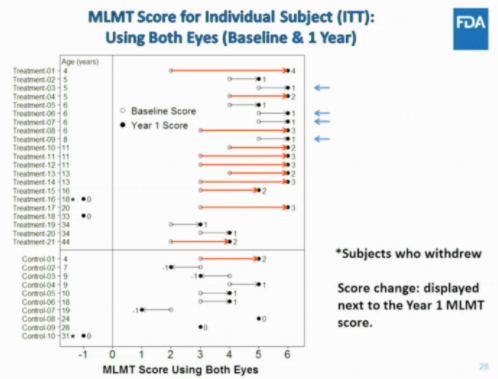

Antwort auf Beitrag Nr.: 55.938.944 von Cyberhexe am 12.10.17 16:07:55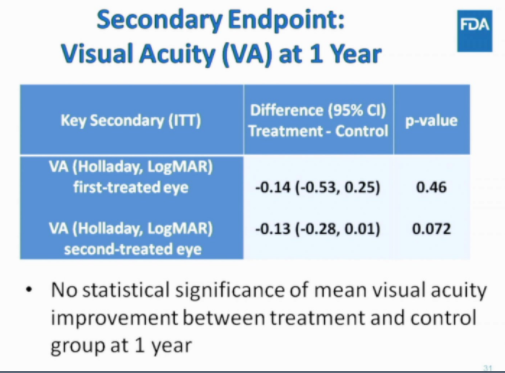

Antwort auf Beitrag Nr.: 55.939.085 von Cyberhexe am 12.10.17 16:17:36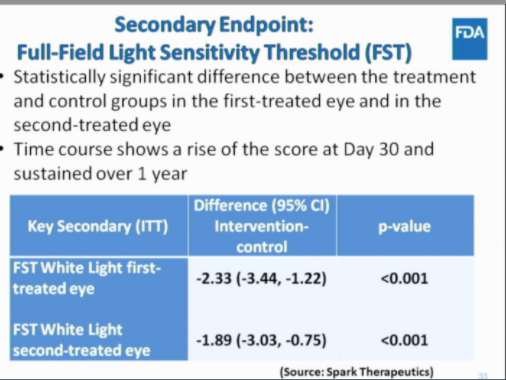

Antwort auf Beitrag Nr.: 55.939.211 von Cyberhexe am 12.10.17 16:26:09
Anmerkung von Dr. Albert Maguire ...a retinal disease specialist at Children’s Hospital of Philadelphia and the principal investigator of the Luxturna clinical trials.
“Rarely did I see a cane after treatment.”
“If my child or myself had this condition i would not hesitate for a moment getting treatment with [Luxturna.]”
Anmerkung von Dr. Albert Maguire ...a retinal disease specialist at Children’s Hospital of Philadelphia and the principal investigator of the Luxturna clinical trials.
“Rarely did I see a cane after treatment.”
“If my child or myself had this condition i would not hesitate for a moment getting treatment with [Luxturna.]”
Antwort auf Beitrag Nr.: 55.939.355 von Cyberhexe am 12.10.17 16:41:02
weisst du ob der kurs ausgesetzt ist ?
Zitat von Cyberhexe: Anmerkung von Dr. Albert Maguire ...a retinal disease specialist at Children’s Hospital of Philadelphia and the principal investigator of the Luxturna clinical trials.
“Rarely did I see a cane after treatment.”
“If my child or myself had this condition i would not hesitate for a moment getting treatment with [Luxturna.]”
weisst du ob der kurs ausgesetzt ist ?
Antwort auf Beitrag Nr.: 55.939.427 von peltram am 12.10.17 16:49:59ja, die Aktie wird aktuell nicht gehandelt, wobei der Kurs von anderen Firmen, die sich mit Gentherapie auseinandersetzen, positiv zu reagieren scheint --> Voyager Therapeutics (VYGR) um 6% sowie Regenxbio (RGNX) um 3%
....auch das beim AC gezeigte Video wird sicherlich Eindruck hinterlassen:
"Maguire also showed a video of a patient under his care. Before treatment, the six-year-old girl couldn’t navigate the mobility maze without bumping into objects or veering off course. Four years after Luxturna, the girl, now 10, speeds through the maze in seconds without missteps."
....auch das beim AC gezeigte Video wird sicherlich Eindruck hinterlassen:
"Maguire also showed a video of a patient under his care. Before treatment, the six-year-old girl couldn’t navigate the mobility maze without bumping into objects or veering off course. Four years after Luxturna, the girl, now 10, speeds through the maze in seconds without missteps."
Antwort auf Beitrag Nr.: 55.939.508 von Cyberhexe am 12.10.17 16:56:12
ok danke dir
Zitat von Cyberhexe: ja, die Aktie wird aktuell nicht gehandelt, wobei der Kurs von anderen Firmen, die sich mit Gentherapie auseinandersetzen, positiv zu reagieren scheint --> Voyager Therapeutics (VYGR) um 6% sowie Regenxbio (RGNX) um 3%
....auch das beim AC gezeigte Video wird sicherlich Eindruck hinterlassen:
"Maguire also showed a video of a patient under his care. Before treatment, the six-year-old girl couldn’t navigate the mobility maze without bumping into objects or veering off course. Four years after Luxturna, the girl, now 10, speeds through the maze in seconds without missteps."
ok danke dir
Antwort auf Beitrag Nr.: 55.939.544 von peltram am 12.10.17 16:58:27hinsichtlich der Beständigkeit der Wirkung hat SPARK angeboten, 4-Jahresdaten zu präsentieren, die nicht Bestandteil der Zulassungsunterlagen sind. FDA hat das erlaubt, weshalb folgende Info präsentiert wurde - verstehe das auf Anhieb zwar nicht!
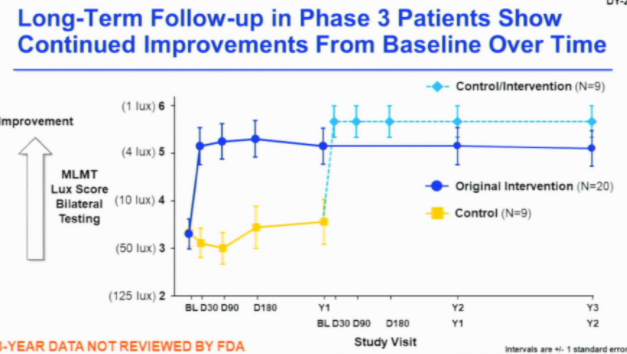
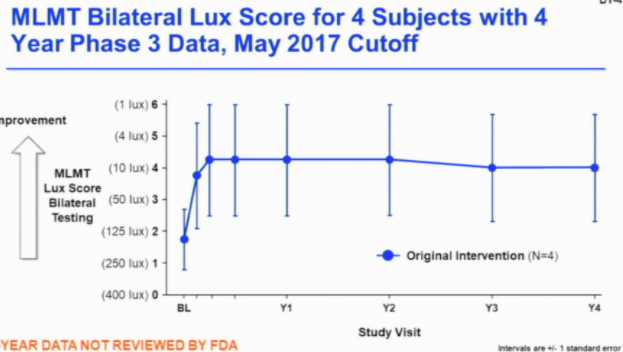


Antwort auf Beitrag Nr.: 55.939.718 von Cyberhexe am 12.10.17 17:14:37nun 14 Sprecher in der "Open Public Hearing Session" - das geht ja zügig vorwärts!
Antwort auf Beitrag Nr.: 55.939.787 von Cyberhexe am 12.10.17 17:22:03...also bis jetzt sehe ich keinen Grund, gegen eine Zulassung zu votieren! Falls da nichts Ungewöhnliches mehr kommt, dürfte die Abstimmung eine sehr einseitige Angelegenheit werden.
Bin gespannt, ob die USD90 heute noch übersprungen werden....oder, ob aufgrund fehlender Zweifel eine doch eher bescheidene Reaktion zu beobachten ist.
Bin gespannt, ob die USD90 heute noch übersprungen werden....oder, ob aufgrund fehlender Zweifel eine doch eher bescheidene Reaktion zu beobachten ist.
Antwort auf Beitrag Nr.: 55.939.862 von Cyberhexe am 12.10.17 17:29:25...ein Professor der University of California, San Francisco (UCSF) nennt die Ergebnisse “extremely impressive.”
Director of the Genetics Clinic at @ChildrensPhila beschreibt "impressive results". Sagt, dass man heute die Gelegenheit hätte, Geschichte zu schreiben. Starke Worte!
Antwort auf Beitrag Nr.: 55.940.189 von Cyberhexe am 12.10.17 18:05:48Chairman of Dep of Ophthalmology at UPenn sagt, er sah blinde Kinder, die ihre Sehkraft wieder gewonnen hätten... "Transforms lives!"
Antwort auf Beitrag Nr.: 55.940.204 von Cyberhexe am 12.10.17 18:07:18Eine Studienteilnehmerin beschreibt ihr Empfinden vor der Behandlung: "It was like sunglasses over your eyes while looking through a little tunnel,"
Antwort auf Beitrag Nr.: 55.940.249 von Cyberhexe am 12.10.17 18:11:04...nun ist Pause bis 1:15 US EDT.
Die Spannung ist etwas draussen, das dürfte nämlich eine klare Angelegenheit werden.
Die Spannung ist etwas draussen, das dürfte nämlich eine klare Angelegenheit werden.
bei l&s kann man handeln
Antwort auf Beitrag Nr.: 55.940.441 von Cyberhexe am 12.10.17 18:31:36Ich habe schon etliche solcher Expertenrunden der FDA beobachtet, aber ein derartig überwältigendes Zeugnis von Betroffenen habe ich noch selten erlebt. Ich weiss wirklich nicht, welche Argumente gegen eine Zulassung sprechen sollten.
Antwort auf Beitrag Nr.: 55.940.525 von peltram am 12.10.17 18:40:11...ich werde jetzt nicht mehr zukaufen, da ich mich zuvor reichlich eingedeckt habe.
Da ich nun eine Vedrpflichtung habe, bin ich bis ca. 22h "off line". Bin gespannt, ob heute noch gehandelt wird.
Da ich nun eine Vedrpflichtung habe, bin ich bis ca. 22h "off line". Bin gespannt, ob heute noch gehandelt wird.
FDA Advisory Committee Unanimously  Recommends Approval
Recommends Approval  of Investigational LUXTURNA™ (voretigene neparvovec) for Patients with Biallelic RPE65-mediated Inherited Retinal Disease[/u]
of Investigational LUXTURNA™ (voretigene neparvovec) for Patients with Biallelic RPE65-mediated Inherited Retinal Disease[/u]
GlobeNewswire•October 12, 2017
Investigational LUXTURNA has the potential to be both the first pharmacologic treatment for an inherited retinal disease (IRD) and the first gene therapy for a genetic disease in the United States
First adeno-associated viral (AAV) vector investigational candidate to reach this stage of FDA review
Investigational LUXTURNA clinical program includes up to four years of efficacy data, with observation ongoing
PHILADELPHIA, Oct. 12, 2017 (GLOBE NEWSWIRE) -- Spark Therapeutics (ONCE), a fully integrated gene therapy company dedicated to challenging the inevitability of genetic disease, announced today that the U.S. Food and Drug Administration’s (FDA) Cellular, Tissue and Gene Therapies Advisory Committee has unanimously recommended
 (16-0)
(16-0)
 approval of LUXTURNA™ (voretigene neparvovec), an investigational, potential one-time gene therapy, for the treatment of patients with vision loss due to confirmed biallelic RPE65-mediated inherited retinal disease (IRD).
approval of LUXTURNA™ (voretigene neparvovec), an investigational, potential one-time gene therapy, for the treatment of patients with vision loss due to confirmed biallelic RPE65-mediated inherited retinal disease (IRD).
“Today’s unanimous advisory committee vote recommending the approval of LUXTURNA moves us closer to bringing this investigational adeno-associated viral (AAV) vector gene therapy to patients with vision loss due to confirmed biallelic RPE65-mediated IRD,” said Katherine A. High, M.D., president and head of Research and Development, Spark Therapeutics. “The clinical program for LUXTURNA includes patient data that show efficacy for up to four years on endpoints including bilateral multi-luminance mobility test (MLMT) score change and full-field light sensitivity threshold (FST) testing, with observation ongoing. We look forward to continuing to work with FDA as it completes its review of LUXTURNA.”
The advisory committee’s recommendation is based on LUXTURNA’s clinical development program, which includes the first completed randomized, controlled Phase 3 gene therapy clinical trial ever conducted for a genetic disease. In the original Phase 3 intervention group, participants aged four to 44 years on average maintained the functional vision and visual function improvements demonstrated 30 days after LUXTURNA administration through their last annual follow-up visit, as measured by bilateral multi-luminance mobility test (MLMT) score change and full-field light sensitivity threshold (FST) testing. Data from a cohort of the Phase 1 clinical trial, in which investigational LUXTURNA was administered to the contralateral, or second previously uninjected eye, showed similarly maintained mean improvements. As part of the Biologics License Application (BLA) to FDA, Spark also submitted the results of two Phase 1 clinical trials, a natural history study and a MLMT validation study. Today’s advisory committee vote is non-binding, but FDA will take its recommendation into consideration when reviewing the BLA for LUXTURNA.
“There currently are no pharmacologic treatment options for people living with RPE65-mediated IRD, who in most cases progress to complete blindness,” said Principal Investigator Albert M. Maguire, M.D., professor of ophthalmology at the Scheie Eye Institute at the University of Pennsylvania’s Perelman School of Medicine and attending physician in the Division of Pediatric Ophthalmology at Children's Hospital of Philadelphia. “As a practicing physician who often speaks with patients and families living with IRDs, these conversations have been, up to now, frustrating in that there has been nothing to offer. Today’s advisory committee vote is an important step closer to the day that discussion can include potentially treating the blindness caused by their IRD.”
No serious adverse events (SAEs) associated with LUXTURNA or deleterious immune responses have been observed. Two ocular SAEs were reported in the clinical program, one in Phase 1 and one in Phase 3. The SAE in Phase 3 was related to the surgical procedure, and resulted in foveal thinning and a sustained reduction in visual acuity (VA) in one participant. The most common adverse reactions related to LUXTURNA reported in 10 percent or greater of the combined Phase 1 and Phase 3 trial participants included conjunctival hyperemia, cataract, increased intraocular pressure and retinal tear.
LUXTURNA is under Priority Review with FDA, with an assigned Prescription Drug User Fee Act (PDUFA) date of Jan. 12, 2018. LUXTURNA has received orphan drug, breakthrough therapy and rare pediatric disease designations from FDA. In August 2017, Spark Therapeutics’ Marketing Authorization Application (MAA) for LUXTURNA was validated by European Medicines Agency (EMA). LUXTURNA also has received orphan product designations from EMA.
https://finance.yahoo.com/news/fda-advisory-committee-unanim…
 Recommends Approval
Recommends Approval  of Investigational LUXTURNA™ (voretigene neparvovec) for Patients with Biallelic RPE65-mediated Inherited Retinal Disease[/u]
of Investigational LUXTURNA™ (voretigene neparvovec) for Patients with Biallelic RPE65-mediated Inherited Retinal Disease[/u]GlobeNewswire•October 12, 2017
Investigational LUXTURNA has the potential to be both the first pharmacologic treatment for an inherited retinal disease (IRD) and the first gene therapy for a genetic disease in the United States
First adeno-associated viral (AAV) vector investigational candidate to reach this stage of FDA review
Investigational LUXTURNA clinical program includes up to four years of efficacy data, with observation ongoing
PHILADELPHIA, Oct. 12, 2017 (GLOBE NEWSWIRE) -- Spark Therapeutics (ONCE), a fully integrated gene therapy company dedicated to challenging the inevitability of genetic disease, announced today that the U.S. Food and Drug Administration’s (FDA) Cellular, Tissue and Gene Therapies Advisory Committee has unanimously recommended

 (16-0)
(16-0)
 approval of LUXTURNA™ (voretigene neparvovec), an investigational, potential one-time gene therapy, for the treatment of patients with vision loss due to confirmed biallelic RPE65-mediated inherited retinal disease (IRD).
approval of LUXTURNA™ (voretigene neparvovec), an investigational, potential one-time gene therapy, for the treatment of patients with vision loss due to confirmed biallelic RPE65-mediated inherited retinal disease (IRD).“Today’s unanimous advisory committee vote recommending the approval of LUXTURNA moves us closer to bringing this investigational adeno-associated viral (AAV) vector gene therapy to patients with vision loss due to confirmed biallelic RPE65-mediated IRD,” said Katherine A. High, M.D., president and head of Research and Development, Spark Therapeutics. “The clinical program for LUXTURNA includes patient data that show efficacy for up to four years on endpoints including bilateral multi-luminance mobility test (MLMT) score change and full-field light sensitivity threshold (FST) testing, with observation ongoing. We look forward to continuing to work with FDA as it completes its review of LUXTURNA.”
The advisory committee’s recommendation is based on LUXTURNA’s clinical development program, which includes the first completed randomized, controlled Phase 3 gene therapy clinical trial ever conducted for a genetic disease. In the original Phase 3 intervention group, participants aged four to 44 years on average maintained the functional vision and visual function improvements demonstrated 30 days after LUXTURNA administration through their last annual follow-up visit, as measured by bilateral multi-luminance mobility test (MLMT) score change and full-field light sensitivity threshold (FST) testing. Data from a cohort of the Phase 1 clinical trial, in which investigational LUXTURNA was administered to the contralateral, or second previously uninjected eye, showed similarly maintained mean improvements. As part of the Biologics License Application (BLA) to FDA, Spark also submitted the results of two Phase 1 clinical trials, a natural history study and a MLMT validation study. Today’s advisory committee vote is non-binding, but FDA will take its recommendation into consideration when reviewing the BLA for LUXTURNA.
“There currently are no pharmacologic treatment options for people living with RPE65-mediated IRD, who in most cases progress to complete blindness,” said Principal Investigator Albert M. Maguire, M.D., professor of ophthalmology at the Scheie Eye Institute at the University of Pennsylvania’s Perelman School of Medicine and attending physician in the Division of Pediatric Ophthalmology at Children's Hospital of Philadelphia. “As a practicing physician who often speaks with patients and families living with IRDs, these conversations have been, up to now, frustrating in that there has been nothing to offer. Today’s advisory committee vote is an important step closer to the day that discussion can include potentially treating the blindness caused by their IRD.”
No serious adverse events (SAEs) associated with LUXTURNA or deleterious immune responses have been observed. Two ocular SAEs were reported in the clinical program, one in Phase 1 and one in Phase 3. The SAE in Phase 3 was related to the surgical procedure, and resulted in foveal thinning and a sustained reduction in visual acuity (VA) in one participant. The most common adverse reactions related to LUXTURNA reported in 10 percent or greater of the combined Phase 1 and Phase 3 trial participants included conjunctival hyperemia, cataract, increased intraocular pressure and retinal tear.
LUXTURNA is under Priority Review with FDA, with an assigned Prescription Drug User Fee Act (PDUFA) date of Jan. 12, 2018. LUXTURNA has received orphan drug, breakthrough therapy and rare pediatric disease designations from FDA. In August 2017, Spark Therapeutics’ Marketing Authorization Application (MAA) for LUXTURNA was validated by European Medicines Agency (EMA). LUXTURNA also has received orphan product designations from EMA.
https://finance.yahoo.com/news/fda-advisory-committee-unanim…
Antwort auf Beitrag Nr.: 55.943.138 von bernie55 am 13.10.17 00:46:4216:0 für eine Zulassung - eindeutiges Votum, welches sich im Laufe des AC abgezeichnet hat.
PDUFA ist der 12.1.2018. Bis dorthin hat das Unternehmen Zeit, sich über die Preisgestaltung Gedanken zu machen. Spekulationen reichen von $400.000 bis $1.000.000 (beide Augen).
Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem die Arznei $475,000 kostet sofern die Therapie anschlägt oder 0$, falls nicht.
Es bleibt auf alle Fälle spannend und die Aktie scheint nach unten nun bestens abgesichert zu sein.
Mein Kursziel jenseits $90 sollte ohne weiteres heute noch realisiert werden, allerdings scheinen nun auch dreistellige Kurse relativ rasch möglich sein.
PDUFA ist der 12.1.2018. Bis dorthin hat das Unternehmen Zeit, sich über die Preisgestaltung Gedanken zu machen. Spekulationen reichen von $400.000 bis $1.000.000 (beide Augen).
Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem die Arznei $475,000 kostet sofern die Therapie anschlägt oder 0$, falls nicht.
Es bleibt auf alle Fälle spannend und die Aktie scheint nach unten nun bestens abgesichert zu sein.
Mein Kursziel jenseits $90 sollte ohne weiteres heute noch realisiert werden, allerdings scheinen nun auch dreistellige Kurse relativ rasch möglich sein.
schon wieder unter 90$ ... da ist aber mehr drin
der kurs ist wohl ein witz
Antwort auf Beitrag Nr.: 55.949.951 von peltram am 13.10.17 19:22:48die Aktie ist jetzt nach unten sehr gut abgesichert; durch Gewährung von Priority Review der FDA ist eine Zulassungsentscheidung zum 12. Januar 2018 fällig, die, und da bin ich mir ziemlich sicher, positiv ausfallen wird:
Spannend wird die Preisfrage. Für Luxturna werden sehr hohe Preise erwartet, die sich neuerdings in einer Spanne von $400.000 bis $1.000.000 (beide Augen) bewegen. Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem für die Arznei $475,000 in Rechnung gestellt werden, sofern die Therapie anschlägt - falls nicht, wird der Verkaufspreis zurückerstattet.
Bei der jährlichen Umsatzspitze sind die Schätzungen sehr weit gestreut, da vor allem die Preisgestaltung und die Reaktion der Versicherer hierzu nur vage Schätzungen zulässt. Aufgrund der überschaubaren Populatuion erscheint jedoch eine rasche Penetration des Marktes möglich, so dass nach Zulassung ein schnelles Umsatzwachstum beobachtet werden sollte. Dreistellige Kurs dürften in naher Zukunft realisiert werden.
One seeking alpha author gives a peak sales estimate for LUXTURNA at $350 to $900 million. With approximately 3,500 individuals with RPE65-related IRDs in the United States and Europe, and an estimated price tag of more than $100,000 per treatment, the estimates may add up.
Habe gestern nochmals 100 Stück günstig nachgekauft!

Spannend wird die Preisfrage. Für Luxturna werden sehr hohe Preise erwartet, die sich neuerdings in einer Spanne von $400.000 bis $1.000.000 (beide Augen) bewegen. Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem für die Arznei $475,000 in Rechnung gestellt werden, sofern die Therapie anschlägt - falls nicht, wird der Verkaufspreis zurückerstattet.
Bei der jährlichen Umsatzspitze sind die Schätzungen sehr weit gestreut, da vor allem die Preisgestaltung und die Reaktion der Versicherer hierzu nur vage Schätzungen zulässt. Aufgrund der überschaubaren Populatuion erscheint jedoch eine rasche Penetration des Marktes möglich, so dass nach Zulassung ein schnelles Umsatzwachstum beobachtet werden sollte. Dreistellige Kurs dürften in naher Zukunft realisiert werden.
One seeking alpha author gives a peak sales estimate for LUXTURNA at $350 to $900 million. With approximately 3,500 individuals with RPE65-related IRDs in the United States and Europe, and an estimated price tag of more than $100,000 per treatment, the estimates may add up.
Habe gestern nochmals 100 Stück günstig nachgekauft!
Antwort auf Beitrag Nr.: 55.964.799 von Cyberhexe am 17.10.17 12:21:41@ cyberhexe
Du hast Dir ja schon einige Gedanken zu ONCE gemacht u.a. auch zum Thema >> Mögliche Finanzierung <<
Ich denke auch, dass die größte Unsicherheit bei einem Investment seitens von Aktionären in folgenden Fragen liegt.
Wie teuer wird eine möglichen Behandlung mit diesem revolutionären Therapieansatz sein ?
Wie werden Versicherungen damit umgehen ?
Zu diesem Punkt auch ein Artikel :l
Spark Therapeutics Ignites Excitement Over Unanimous Adcom Panel Vote
Oct.17.17 | About: Spark Therapeutics (ONCE)
Terry Chrisomalis
SUMMARY:
Advisory panel recommends unanimously with a 16 -0 vote that Luxturna should be approved by the FDA.
The positive vote from the panel came about because of a successful phase 3 study where patients treated with Luxturna improved over a control group after a one-year followup period.
Financials are sound until 2019, although upon approval there is a small chance the company may need to raise cash for commercial launch.
A big risk would be that insurance payers may not want to pay $1 million per patient for this treatment should its long-term efficacy not remain intact.
A potential catalyst would be potential European approval of Luxturna in the coming year.
https://seekingalpha.com/article/4113899-spark-therapeutics-…" target="_blank" rel="nofollow ugc noopener">
https://seekingalpha.com/article/4113899-spark-therapeutics-…
Du hast Dir ja schon einige Gedanken zu ONCE gemacht u.a. auch zum Thema >> Mögliche Finanzierung <<
Ich denke auch, dass die größte Unsicherheit bei einem Investment seitens von Aktionären in folgenden Fragen liegt.
Wie teuer wird eine möglichen Behandlung mit diesem revolutionären Therapieansatz sein ?
Wie werden Versicherungen damit umgehen ?
Zu diesem Punkt auch ein Artikel :l
Spark Therapeutics Ignites Excitement Over Unanimous Adcom Panel Vote
Oct.17.17 | About: Spark Therapeutics (ONCE)
Terry Chrisomalis
SUMMARY:
Advisory panel recommends unanimously with a 16 -0 vote that Luxturna should be approved by the FDA.
The positive vote from the panel came about because of a successful phase 3 study where patients treated with Luxturna improved over a control group after a one-year followup period.
Financials are sound until 2019, although upon approval there is a small chance the company may need to raise cash for commercial launch.
A big risk would be that insurance payers may not want to pay $1 million per patient for this treatment should its long-term efficacy not remain intact.
A potential catalyst would be potential European approval of Luxturna in the coming year.
https://seekingalpha.com/article/4113899-spark-therapeutics-…" target="_blank" rel="nofollow ugc noopener">
https://seekingalpha.com/article/4113899-spark-therapeutics-…
Guten Abend zusammen,
was ich nicht ganz verstehe an Spark Therapeutics
bzw. den Gewinnschätzungen.
Mit dem jetzt zugelassenen Produkt, vorausgesetzt,
man visiert tatsächlich 1 Million US-$ pro Behandlungseinheit an,
wieso sehendie durchschnittlichen Analystenprognosen
für das kommende Geschäftsjahr immer noch einen deutlichen
Verlust von rund 5 $ pro Aktie vor???
1.000 Patienten sollten meiner Meinung nach schnell
zusammen kommen (mindestens).
Das macht brutto 1 Milliarde US-$ Umsatz.
Da sollte schon so einiges hängen bleiben!!!???
Gruß
P.S: Ich halte Aktien von Spark in diversen Social Trading Aktivitäten und
in meinem Privatdepot.
Dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der allgemeinen Information.
was ich nicht ganz verstehe an Spark Therapeutics
bzw. den Gewinnschätzungen.
Mit dem jetzt zugelassenen Produkt, vorausgesetzt,
man visiert tatsächlich 1 Million US-$ pro Behandlungseinheit an,
wieso sehendie durchschnittlichen Analystenprognosen
für das kommende Geschäftsjahr immer noch einen deutlichen
Verlust von rund 5 $ pro Aktie vor???
1.000 Patienten sollten meiner Meinung nach schnell
zusammen kommen (mindestens).
Das macht brutto 1 Milliarde US-$ Umsatz.
Da sollte schon so einiges hängen bleiben!!!???
Gruß
P.S: Ich halte Aktien von Spark in diversen Social Trading Aktivitäten und
in meinem Privatdepot.
Dies ist weder Kauf- noch Verkaufsempfehlung,
sondern dient der allgemeinen Information.
Antwort auf Beitrag Nr.: 56.101.025 von Solideinvestierenkomplex4you am 04.11.17 19:24:36GUTEN Abend
also ich weiss nicht Wie sehr Du Dich mit Entwicklern/Technologieentwicklern usf auskennst??
fallbezogen weiss ich Das absolut nicht
-da vielleicht mal Die CyberHexe etc. fragen-,
aber ich habe so ein bisschen den Eiiiiindruck dass Du den Prozess des "roll outs" -ziemlich übel massiv-unterschcätzt???
also ich habe da bei Diversen (vor Allem Technik)Anderen mittlerweile doch schon Ganze Reihe Erfahrung gesammelt, und Wenn DU denkst "jetzt ist Die Tinte, unter Der Genehmigung trocken; (ab)next quartal earnings"
dann dürftest Du m.E. eher noch Einige, Einige Überraschungen nvor Dir haben.
da würde ich mir vielleicht auch schon versuchen mal Ein paar "Prozesse", Vorgänge zu visualisieren;
mal vorstellen Wie Sowas vielleicht praktisch abläuft.
also Der Ganze Aufbau Infrastruktur, Warenketten, Logistik, und EIniges Mehr.....................
(Deins)greift m.E. -i.D.R.-vollkommen zu kurz.
was haltet Ihr denn eigentlich vom "value-based payment model"??
also ich weiss nicht Wie sehr Du Dich mit Entwicklern/Technologieentwicklern usf auskennst??
fallbezogen weiss ich Das absolut nicht
-da vielleicht mal Die CyberHexe etc. fragen-,
aber ich habe so ein bisschen den Eiiiiindruck dass Du den Prozess des "roll outs" -ziemlich übel massiv-unterschcätzt???
also ich habe da bei Diversen (vor Allem Technik)Anderen mittlerweile doch schon Ganze Reihe Erfahrung gesammelt, und Wenn DU denkst "jetzt ist Die Tinte, unter Der Genehmigung trocken; (ab)next quartal earnings"
dann dürftest Du m.E. eher noch Einige, Einige Überraschungen nvor Dir haben.
da würde ich mir vielleicht auch schon versuchen mal Ein paar "Prozesse", Vorgänge zu visualisieren;
mal vorstellen Wie Sowas vielleicht praktisch abläuft.
also Der Ganze Aufbau Infrastruktur, Warenketten, Logistik, und EIniges Mehr.....................
(Deins)greift m.E. -i.D.R.-vollkommen zu kurz.
was haltet Ihr denn eigentlich vom "value-based payment model"??
Antwort auf Beitrag Nr.: 56.115.191 von Popeye82 am 06.11.17 21:28:28Hallo Popeye,
danke für Deine Antwort!
Vor vielen Monate hat Spark Th.
erklärt, dass sie sich bereits auf den Prozess
der "Serienproduktion" massiv vorbereiten.
Neue Anlagen, neue Strukturen etc.
Demnach gehe ich doch davon aus,
dass die ersten "Medikamente" so langsam
aber sicher mal ausgegeben werden können!!!???
Ich denke, in 9 Monaten müsste eine Produktion
hoch zu ziehen sein!!??
Falls ich hier falsch liege, bitte schreibe mir
doch einfach mal aus Deiner Sicht, wann es
denn final losgehen kann mit einer
ersten "Serienproduktion" bei Spark,
also mit dem ersten Verkauf???
Viele Grüße
danke für Deine Antwort!
Vor vielen Monate hat Spark Th.
erklärt, dass sie sich bereits auf den Prozess
der "Serienproduktion" massiv vorbereiten.
Neue Anlagen, neue Strukturen etc.
Demnach gehe ich doch davon aus,
dass die ersten "Medikamente" so langsam
aber sicher mal ausgegeben werden können!!!???
Ich denke, in 9 Monaten müsste eine Produktion
hoch zu ziehen sein!!??
Falls ich hier falsch liege, bitte schreibe mir
doch einfach mal aus Deiner Sicht, wann es
denn final losgehen kann mit einer
ersten "Serienproduktion" bei Spark,
also mit dem ersten Verkauf???
Viele Grüße
Zahlen sind da...glaubt man den Marktberichten einen
Tick schlechter als erwartet....
aber letztlich für mich persönlich völlig uninteressant,
da aktuell genügend Cash vorhanden ist und sich die
Zahlen in den Folgejahren schnell verändern dürften.
Gruß
P.S: Ich halte Aktien von Spark, sowohl privat wie auch in Social Trading
Aktivitäten und dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
Tick schlechter als erwartet....
aber letztlich für mich persönlich völlig uninteressant,
da aktuell genügend Cash vorhanden ist und sich die
Zahlen in den Folgejahren schnell verändern dürften.
Gruß
P.S: Ich halte Aktien von Spark, sowohl privat wie auch in Social Trading
Aktivitäten und dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
Antwort auf Beitrag Nr.: 55.964.799 von Cyberhexe am 17.10.17 12:21:41
ein hervorragendes Ergebnis einer Phase 1/2-Studie zur Behandlung von Hemophilia B wurde gestern im New England Journal of Medicine veröffentlicht: nach einer einzigen Infusion von Sparks gentherapeutischem Wirkstoff SPK-9001 ist die Faktor-IX-Aktivität von 1% auf 34% angestiegen, weshalb die Blutungsneigung bei den Probanden von durchschnittlich 11 Blutungen auf 0.4 Blutungen/Jahr zurück gegangen ist.
http://www.nejm.org/doi/full/10.1056/NEJMoa1708538
Zitat von Cyberhexe: die Aktie ist jetzt nach unten sehr gut abgesichert; durch Gewährung von Priority Review der FDA ist eine Zulassungsentscheidung zum 12. Januar 2018 fällig, die, und da bin ich mir ziemlich sicher, positiv ausfallen wird:
Spannend wird die Preisfrage. Für Luxturna werden sehr hohe Preise erwartet, die sich neuerdings in einer Spanne von $400.000 bis $1.000.000 (beide Augen) bewegen. Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem für die Arznei $475,000 in Rechnung gestellt werden, sofern die Therapie anschlägt - falls nicht, wird der Verkaufspreis zurückerstattet.
Bei der jährlichen Umsatzspitze sind die Schätzungen sehr weit gestreut, da vor allem die Preisgestaltung und die Reaktion der Versicherer hierzu nur vage Schätzungen zulässt. Aufgrund der überschaubaren Populatuion erscheint jedoch eine rasche Penetration des Marktes möglich, so dass nach Zulassung ein schnelles Umsatzwachstum beobachtet werden sollte. Dreistellige Kurs dürften in naher Zukunft realisiert werden.
One seeking alpha author gives a peak sales estimate for LUXTURNA at $350 to $900 million. With approximately 3,500 individuals with RPE65-related IRDs in the United States and Europe, and an estimated price tag of more than $100,000 per treatment, the estimates may add up.
Habe gestern nochmals 100 Stück günstig nachgekauft!
ein hervorragendes Ergebnis einer Phase 1/2-Studie zur Behandlung von Hemophilia B wurde gestern im New England Journal of Medicine veröffentlicht: nach einer einzigen Infusion von Sparks gentherapeutischem Wirkstoff SPK-9001 ist die Faktor-IX-Aktivität von 1% auf 34% angestiegen, weshalb die Blutungsneigung bei den Probanden von durchschnittlich 11 Blutungen auf 0.4 Blutungen/Jahr zurück gegangen ist.
http://www.nejm.org/doi/full/10.1056/NEJMoa1708538
Antwort auf Beitrag Nr.: 56.384.854 von Cyberhexe am 07.12.17 08:22:17die Ergebnisse haben sich ja in etwa
auch schon durch die letzten Meldungen
über die Haemophilie B Versuche angedeutet.
Und wurden heute noch mal zementiert.
Für mich ist die Zulassung der Haemophilie Produkte (A und B)
durch Spark eigentlich nur noch eine "Formsache".
Alles andere wäre eine große, negative Überraschung.
So weit mir bekannt, hat Spark bei Haemophilie B wohl die Nase vorn,
also First Mover Effekt.
Bei Haemophilie A weiss ich nicht, wer schneller sein wird,
Spark oder UniQure (oder ein Dritter???).
Vermutlich also noch ein offenes Rennen....!!!???
Die Aktie von Spark hat jetzt einen Bodenbildungsprozess durchlaufen,
und wäre so langsam mal wieder reif für neue All Time Highs (nur meine
Meinung).
Gruß
P.S: Ich halte Aktien von Spark Therapeutics in meinem Privatdepot und
in mehreren Wikifolios. Dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
auch schon durch die letzten Meldungen
über die Haemophilie B Versuche angedeutet.
Und wurden heute noch mal zementiert.
Für mich ist die Zulassung der Haemophilie Produkte (A und B)
durch Spark eigentlich nur noch eine "Formsache".
Alles andere wäre eine große, negative Überraschung.
So weit mir bekannt, hat Spark bei Haemophilie B wohl die Nase vorn,
also First Mover Effekt.
Bei Haemophilie A weiss ich nicht, wer schneller sein wird,
Spark oder UniQure (oder ein Dritter???).
Vermutlich also noch ein offenes Rennen....!!!???
Die Aktie von Spark hat jetzt einen Bodenbildungsprozess durchlaufen,
und wäre so langsam mal wieder reif für neue All Time Highs (nur meine
Meinung).
Gruß
P.S: Ich halte Aktien von Spark Therapeutics in meinem Privatdepot und
in mehreren Wikifolios. Dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
Antwort auf Beitrag Nr.: 56.391.451 von Solideinvestierenkomplex4you am 07.12.17 15:31:49
....ein Dritter: https://www.roche.com/media/store/releases/med-cor-2017-12-0…
Zitat von Solideinvestierenkomplex4you: Für mich ist die Zulassung der Haemophilie Produkte (A und B)
durch Spark eigentlich nur noch eine "Formsache".
Alles andere wäre eine große, negative Überraschung.
So weit mir bekannt, hat Spark bei Haemophilie B wohl die Nase vorn,
also First Mover Effekt.
Bei Haemophilie A weiss ich nicht, wer schneller sein wird,
Spark oder UniQure (oder ein Dritter???).
Vermutlich also noch ein offenes Rennen....!!!???
Die Aktie von Spark hat jetzt einen Bodenbildungsprozess durchlaufen,
und wäre so langsam mal wieder reif für neue All Time Highs (nur meine
Meinung).
Gruß
P.S: Ich halte Aktien von Spark Therapeutics in meinem Privatdepot und
in mehreren Wikifolios. Dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
....ein Dritter: https://www.roche.com/media/store/releases/med-cor-2017-12-0…
Antwort auf Beitrag Nr.: 56.394.505 von Cyberhexe am 07.12.17 18:15:22Danke für die Info.
Aber das ist so weit ich gelesen habe,
keine Gentechnik, also sind
fortwährende Behandlungen nötig.
Ich meinte allerdings, dass Spark der erste sein könnte,
der rein auf Gentechnik setzt in diesem Bereich.
Viele Grüße
Aber das ist so weit ich gelesen habe,
keine Gentechnik, also sind
fortwährende Behandlungen nötig.
Ich meinte allerdings, dass Spark der erste sein könnte,
der rein auf Gentechnik setzt in diesem Bereich.
Viele Grüße
Antwort auf Beitrag Nr.: 56.384.854 von Cyberhexe am 07.12.17 08:22:17
tolles Video, weil sehr anschaulich zusammengefasst, von NEJM zum Studienergebnis von SPK-9001:
http://www.nejm.org/do/10.1056/NEJMdo005231/full/
Zitat von Cyberhexe:Zitat von Cyberhexe: die Aktie ist jetzt nach unten sehr gut abgesichert; durch Gewährung von Priority Review der FDA ist eine Zulassungsentscheidung zum 12. Januar 2018 fällig, die, und da bin ich mir ziemlich sicher, positiv ausfallen wird:
Spannend wird die Preisfrage. Für Luxturna werden sehr hohe Preise erwartet, die sich neuerdings in einer Spanne von $400.000 bis $1.000.000 (beide Augen) bewegen. Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem für die Arznei $475,000 in Rechnung gestellt werden, sofern die Therapie anschlägt - falls nicht, wird der Verkaufspreis zurückerstattet.
Bei der jährlichen Umsatzspitze sind die Schätzungen sehr weit gestreut, da vor allem die Preisgestaltung und die Reaktion der Versicherer hierzu nur vage Schätzungen zulässt. Aufgrund der überschaubaren Populatuion erscheint jedoch eine rasche Penetration des Marktes möglich, so dass nach Zulassung ein schnelles Umsatzwachstum beobachtet werden sollte. Dreistellige Kurs dürften in naher Zukunft realisiert werden.
One seeking alpha author gives a peak sales estimate for LUXTURNA at $350 to $900 million. With approximately 3,500 individuals with RPE65-related IRDs in the United States and Europe, and an estimated price tag of more than $100,000 per treatment, the estimates may add up.
Habe gestern nochmals 100 Stück günstig nachgekauft!
ein hervorragendes Ergebnis einer Phase 1/2-Studie zur Behandlung von Hemophilia B wurde gestern im New England Journal of Medicine veröffentlicht: nach einer einzigen Infusion von Sparks gentherapeutischem Wirkstoff SPK-9001 ist die Faktor-IX-Aktivität von 1% auf 34% angestiegen, weshalb die Blutungsneigung bei den Probanden von durchschnittlich 11 Blutungen auf 0.4 Blutungen/Jahr zurück gegangen ist.
http://www.nejm.org/doi/full/10.1056/NEJMoa1708538
tolles Video, weil sehr anschaulich zusammengefasst, von NEJM zum Studienergebnis von SPK-9001:
http://www.nejm.org/do/10.1056/NEJMdo005231/full/
ein netter Bericht zum Thema Haemophilie:
https://finance.yahoo.com/news/game-changing-breakthrough-co…
Mir war zwar bewusst, dass Haemophilie A + B nur eine geringe Patientenanzahl weltweit
umfasst.
Warum aber die Großen in diesem Bereich sind, wie Roche (von Cyberhexe genannt)
oder auch Bayer war mir da nicht klar.
Der BEricht erläutert diesen Umstand und begründet es damit,
dass Haemophilie exorbitant hohe und ständige Behandlungskosten
nach sich zieht.
Es wird hier keine Zahl genannt, aber wenn Spark diese Produkte durchbringt,
wovon auszugehen ist, dürften diese Produkte wesentlich mehr als 1 Million pro Anwendung kosten...
und wären damit immer noch ein Schnäppchenim Vergleich zu den Behandlungskosten.
Kommen diese Produkte durch, wovon derzeit auszugehen ist, könnte Spark in deutlich
zweistellige Milliardengebiete bei der Marktkapitalisierung vordringen, so meine Meinung.
Gruß
https://finance.yahoo.com/news/game-changing-breakthrough-co…
Mir war zwar bewusst, dass Haemophilie A + B nur eine geringe Patientenanzahl weltweit
umfasst.
Warum aber die Großen in diesem Bereich sind, wie Roche (von Cyberhexe genannt)
oder auch Bayer war mir da nicht klar.
Der BEricht erläutert diesen Umstand und begründet es damit,
dass Haemophilie exorbitant hohe und ständige Behandlungskosten
nach sich zieht.
Es wird hier keine Zahl genannt, aber wenn Spark diese Produkte durchbringt,
wovon auszugehen ist, dürften diese Produkte wesentlich mehr als 1 Million pro Anwendung kosten...
und wären damit immer noch ein Schnäppchenim Vergleich zu den Behandlungskosten.
Kommen diese Produkte durch, wovon derzeit auszugehen ist, könnte Spark in deutlich
zweistellige Milliardengebiete bei der Marktkapitalisierung vordringen, so meine Meinung.
Gruß
Antwort auf Beitrag Nr.: 56.394.589 von Solideinvestierenkomplex4you am 07.12.17 18:22:54
"Aber das ist so weit ich gelesen habe,
keine Gentechnik, also sind
fortwährende Behandlungen nötig."
...das ist vollständig richtig - bei Roches Emicizumab (brand: HEMLIBRA) handelt es sich nicht um eine gentechnische Innovation sondern um einen intravenös zu applizierenden Antikörper, der ständig erneuert werden muss. Unter Hemlibra übernehmen andere blutgerinnende Faktoren die Funktion des fehlenden Faktor-VIII-Proteins. Das Ergebnis kann sich durchaus sehen lassen --> bei 95% der jugendlichen Studienteilnehmer ging die Blutungsrate während der Studiendauer auf 0 zurück.
Zukünftig wird Roche jedoch mit BMN270 starke Konkurrenz bekommen. Wie am Samstag auf der Jahrestagung der American Society of Hematology in Atlanta von Biomarin berichtet wurde (59th ASH Annual Meeting & Exposition) ist BMN270 wohl in der Lage HemophilaA dauerhaft zu heilen. Ein inaktivierter Virus liefert hierbei den Zellen von Hemophilie A-Patienten die genetische Anweisung, das fehlende Faktor-VIII-Protein zu produzieren. In einer ph1/2-Studie wurden 13 Hemophilia A-Patienten mit einer einzigen Infusion von BMN270 behandelt. Von den mit der höchsten Dosis behandelten 7 Patienten hatten nach 20 Wochen alle Teilnehmer eine normale Faktor-VIII-Konzentration im Blut und, das eigentlich sensationelle, bei nachhaltigem Erfolg auch nach 19 monatiger Beobachtungszeit - wow!
Nach Behandlung mit BMN270 waren bei allen Studienteilnehmern keine Faktor-VIII-Infusionen mehr erforderlich. Eine ph3-Studie soll noch in diesem jahr gestartet werden.
http://investors.biomarin.com/2017-12-09-BioMarin-Provides-1…
Biomarin ein perfektes Übernahmeziel, vielleicht auch von ROCHE.
Zitat von Solideinvestierenkomplex4you: Danke für die Info.
Aber das ist so weit ich gelesen habe,
keine Gentechnik, also sind
fortwährende Behandlungen nötig.
Ich meinte allerdings, dass Spark der erste sein könnte,
der rein auf Gentechnik setzt in diesem Bereich.
Viele Grüße
"Aber das ist so weit ich gelesen habe,
keine Gentechnik, also sind
fortwährende Behandlungen nötig."
...das ist vollständig richtig - bei Roches Emicizumab (brand: HEMLIBRA) handelt es sich nicht um eine gentechnische Innovation sondern um einen intravenös zu applizierenden Antikörper, der ständig erneuert werden muss. Unter Hemlibra übernehmen andere blutgerinnende Faktoren die Funktion des fehlenden Faktor-VIII-Proteins. Das Ergebnis kann sich durchaus sehen lassen --> bei 95% der jugendlichen Studienteilnehmer ging die Blutungsrate während der Studiendauer auf 0 zurück.
Zukünftig wird Roche jedoch mit BMN270 starke Konkurrenz bekommen. Wie am Samstag auf der Jahrestagung der American Society of Hematology in Atlanta von Biomarin berichtet wurde (59th ASH Annual Meeting & Exposition) ist BMN270 wohl in der Lage HemophilaA dauerhaft zu heilen. Ein inaktivierter Virus liefert hierbei den Zellen von Hemophilie A-Patienten die genetische Anweisung, das fehlende Faktor-VIII-Protein zu produzieren. In einer ph1/2-Studie wurden 13 Hemophilia A-Patienten mit einer einzigen Infusion von BMN270 behandelt. Von den mit der höchsten Dosis behandelten 7 Patienten hatten nach 20 Wochen alle Teilnehmer eine normale Faktor-VIII-Konzentration im Blut und, das eigentlich sensationelle, bei nachhaltigem Erfolg auch nach 19 monatiger Beobachtungszeit - wow!
Nach Behandlung mit BMN270 waren bei allen Studienteilnehmern keine Faktor-VIII-Infusionen mehr erforderlich. Eine ph3-Studie soll noch in diesem jahr gestartet werden.
http://investors.biomarin.com/2017-12-09-BioMarin-Provides-1…
Biomarin ein perfektes Übernahmeziel, vielleicht auch von ROCHE.
Antwort auf Beitrag Nr.: 56.419.587 von Cyberhexe am 11.12.17 04:21:13Von den mit der höchsten Dosis behandelten 7 Patienten hatten nach 20 Wochen alle Teilnehmer eine normale Faktor-VIII-Konzentration im Blut und, das eigentlich sensationelle, bei nachhaltigem Erfolg auch nach 19 monatiger Beobachtungszeit
___________________________________________________________________________
kann man dann Vermutungen anstellen Wie lange die "normale" Konzentration "mutmasslich"/vielleicht anhält?
___________________________________________________________________________
kann man dann Vermutungen anstellen Wie lange die "normale" Konzentration "mutmasslich"/vielleicht anhält?
Antwort auf Beitrag Nr.: 56.419.590 von Popeye82 am 11.12.17 04:40:18Ich denke, dass ist grundsätzlich eher Neuland in der Medizin.
Entsprechende Daten gibt es über einen so langen Zeitraum beim Menschen noch nicht.
Wenn ich richtig informiert bin.
Allerdings lässt sich aus den Daten des Medikaments
von Spark gegen eine spezielle Form der Blindheit ersehen,
dass die Hoffnung besteht, dass eine Dosis eventuell
für immer ausreicht.
Zumindest, wenn ich da bislang noch richtig informiert bin!!??
Die Hoffnung ist also, dass es auch in anderen Bereichen
so sein könnte.
Mal sehen...
Viele Grüße
Entsprechende Daten gibt es über einen so langen Zeitraum beim Menschen noch nicht.
Wenn ich richtig informiert bin.
Allerdings lässt sich aus den Daten des Medikaments
von Spark gegen eine spezielle Form der Blindheit ersehen,
dass die Hoffnung besteht, dass eine Dosis eventuell
für immer ausreicht.
Zumindest, wenn ich da bislang noch richtig informiert bin!!??
Die Hoffnung ist also, dass es auch in anderen Bereichen
so sein könnte.
Mal sehen...
Viele Grüße
 Oh Mann,
Oh Mann,reicht mir mal den Übelkübel, sonst wirds mir
ohne Kübel übel!



Naja, 40 % runter wegen einem Produkt, dass
schlechter wirkt als ein anderes...
Scheint mir doch etwas übertrieben.
Habe ein paar Stück nachgekauft...
Hoffnung!
P.S: Ich halte Aktien von Spark in meinem Privatdepot und
in diversen Social Media Aktivitäten
und dies ist weder Kauf- noch Verkaufsempfehlung,
sonderndient derallgemeinen Info.
der abverkauf scheint mir auch deutlich übertrieben, bin gestern auch rein
Antwort auf Beitrag Nr.: 56.429.519 von paul81 am 12.12.17 10:41:26Luxturna in den USA zugelassen.
Bezüglich Haemophilie A wäre ich nicht so pessimistisch.
Wie der Chef von Spark in einem Interview sagte,
versuchen sie wohl sehr vorsichtig die richtige Konzentration
zu finden, um zu hohe Konzentrationen
an Faktor VIII zu vermeiden...die dann eventuell
auch zu Komplikationen führen könnten.
Vielleicht ein Fingerzeig auf die Konkurrenz!?
Wenn da nämlich nur ein Patient in Komplikationen
gerät, verändert sich schlagartig wieder die Positionierung
im Rennen um die erste Zulassung.
Gruß und frohe Weihnachten
P.S: Ich halte AKtien von Spark, sowohl in meinem Privatdepot
als auch in diversen Social Trading Aktivitäten.
Bezüglich Haemophilie A wäre ich nicht so pessimistisch.
Wie der Chef von Spark in einem Interview sagte,
versuchen sie wohl sehr vorsichtig die richtige Konzentration
zu finden, um zu hohe Konzentrationen
an Faktor VIII zu vermeiden...die dann eventuell
auch zu Komplikationen führen könnten.
Vielleicht ein Fingerzeig auf die Konkurrenz!?
Wenn da nämlich nur ein Patient in Komplikationen
gerät, verändert sich schlagartig wieder die Positionierung
im Rennen um die erste Zulassung.
Gruß und frohe Weihnachten
P.S: Ich halte AKtien von Spark, sowohl in meinem Privatdepot
als auch in diversen Social Trading Aktivitäten.
Antwort auf Beitrag Nr.: 56.495.141 von Solideinvestierenkomplex4you am 19.12.17 19:40:18etwas neues ist in der Pipeline
von Spark aufgezeigt,
nämlich Morbus Pompe, einlizensiert von Genethon in 2017.
Scheinbar eine ähnlich "häufige" (seltene) Krankheit wie die, für die gerade
Luxturna zugelassen wurde, allerdings aus Patientensicht ohne Wahlmöglichkeit.
Einmal diagnostiziert, folgt der Tod des Patienten wohl in wenigen Monaten, wenn diese sehr jung sind.
Von daher dringender Handlungsbedarf.
Später, in fortgeschrittenem Alter diagnostiziert sind die Auswirkungen ähnlich verheerend,
aber zeitlich länger gestreckt.
Gruß
P.S: Ich halte Spark Th. in meinen Privatdepots und darüber hinaus in
Sacial Trading Aktivitäten.
Dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
von Spark aufgezeigt,
nämlich Morbus Pompe, einlizensiert von Genethon in 2017.
Scheinbar eine ähnlich "häufige" (seltene) Krankheit wie die, für die gerade
Luxturna zugelassen wurde, allerdings aus Patientensicht ohne Wahlmöglichkeit.
Einmal diagnostiziert, folgt der Tod des Patienten wohl in wenigen Monaten, wenn diese sehr jung sind.
Von daher dringender Handlungsbedarf.
Später, in fortgeschrittenem Alter diagnostiziert sind die Auswirkungen ähnlich verheerend,
aber zeitlich länger gestreckt.
Gruß
P.S: Ich halte Spark Th. in meinen Privatdepots und darüber hinaus in
Sacial Trading Aktivitäten.
Dieser Kommentar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
Antwort auf Beitrag Nr.: 56.115.191 von Popeye82 am 06.11.17 21:28:28ein kleiner Nachtrag zu der Frage der Vergangenheit,
wie schnell Spark Luxturna am Markt anbieten kann.
http://ir.sparktx.com/static-files/b8d67432-f735-4f92-bffe-d…
Aus dem Link ist zu ersehen, dass Ende Q1 2018 Luxturna
dem Markt zur Verfügung gestellt werden kann.
Gruß
P.S: Ich halte Aktien von Spark Th. in meinen Privatdepots und
in diversen Social Media Aktivitäten und dieser Kommentar ist
weder Kauf- noch Verkaufsempfehlung, sondern dient allein
der allgemeinen Information.
wie schnell Spark Luxturna am Markt anbieten kann.
http://ir.sparktx.com/static-files/b8d67432-f735-4f92-bffe-d…
Aus dem Link ist zu ersehen, dass Ende Q1 2018 Luxturna
dem Markt zur Verfügung gestellt werden kann.
Gruß
P.S: Ich halte Aktien von Spark Th. in meinen Privatdepots und
in diversen Social Media Aktivitäten und dieser Kommentar ist
weder Kauf- noch Verkaufsempfehlung, sondern dient allein
der allgemeinen Information.
Antwort auf Beitrag Nr.: 56.689.052 von Solideinvestierenkomplex4you am 11.01.18 18:17:42Hallo Solid,
hab hier jetzt auch mal einen Fuß in die Türe gestellt und werde bei Kurs-Rückgang
nochmals nachkaufen.
nachdem Clegene/Juno Gerücht??/Deal??
Wer weiß wo die TrumpTAx Dollars noch alle per M&A landen
Gruss S.
P.S. bei EDIT bin ich noch voll bei der Sache.
hab hier jetzt auch mal einen Fuß in die Türe gestellt und werde bei Kurs-Rückgang
nochmals nachkaufen.
nachdem Clegene/Juno Gerücht??/Deal??
Wer weiß wo die TrumpTAx Dollars noch alle per M&A landen

Gruss S.
P.S. bei EDIT bin ich noch voll bei der Sache.
Antwort auf Beitrag Nr.: 56.778.345 von Schaeffi am 20.01.18 19:55:34Hallo Schaefii,
immer wieder schön, etwas von Dir zu lesen.
Dir und uns allen wünsche ich viel Glück mit Spark.
Es scheint wohl so zu sein,
als ob Spark ein innovatives und führendes
Unternehmen im Bereich Gentherapie
ist, dass aber anscheinend nicht an die Grenze
des Machbaren heran geht, sondern,
gut für die Patienten, sich der Grenze des Machbaren
von unten nähert.
Andere Unternehmen steigen da scheinbar (Haemophilie A)
bedeutend höher in der Dosierung ein, was ihnen wohl Vorteile
gebracht hat. Ich gebe nur zu bedenken,
wenn auch nur bei einem einzigen Patienten aufgrund
der aggressiven Vorgehensweise eine Komplikation
entsteht, wird sich der Vorteil wieder in Richtung Spark
verlagern.
Viele Grüße und schönen Sonntag allerseits!
immer wieder schön, etwas von Dir zu lesen.

Dir und uns allen wünsche ich viel Glück mit Spark.
Es scheint wohl so zu sein,
als ob Spark ein innovatives und führendes
Unternehmen im Bereich Gentherapie
ist, dass aber anscheinend nicht an die Grenze
des Machbaren heran geht, sondern,
gut für die Patienten, sich der Grenze des Machbaren
von unten nähert.
Andere Unternehmen steigen da scheinbar (Haemophilie A)
bedeutend höher in der Dosierung ein, was ihnen wohl Vorteile
gebracht hat. Ich gebe nur zu bedenken,
wenn auch nur bei einem einzigen Patienten aufgrund
der aggressiven Vorgehensweise eine Komplikation
entsteht, wird sich der Vorteil wieder in Richtung Spark
verlagern.
Viele Grüße und schönen Sonntag allerseits!
Antwort auf Beitrag Nr.: 56.778.345 von Schaeffi am 20.01.18 19:55:34noch was vergessen:
Zu den Genscheren:
Wie schätzt Du denn den Bericht ein,
dass die Genscheren auf CRISPR-Basis
toxisch für den Menschen sein könnten,
und damit so niemals zum Ziel führen werden???
"Advantage Spark!!!???"
Gruß
P.S: Ich halte Aktien von Spark Therapeutics in
mehreren Wikifolios und auch in meinen Privatdepots.
Dieser Kommetar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
Zu den Genscheren:
Wie schätzt Du denn den Bericht ein,
dass die Genscheren auf CRISPR-Basis
toxisch für den Menschen sein könnten,
und damit so niemals zum Ziel führen werden???
"Advantage Spark!!!???"
Gruß
P.S: Ich halte Aktien von Spark Therapeutics in
mehreren Wikifolios und auch in meinen Privatdepots.
Dieser Kommetar ist weder Kauf- noch Verkaufsempfehlung,
sondern dient allein der allgemeinen Information.
Antwort auf Beitrag Nr.: 56.780.493 von Solideinvestierenkomplex4you am 21.01.18 10:55:57du meinst das hier, denk ich:
https://www.fool.de/2018/01/10/stehen-crispr-therapeutics-ed…
Neue Einsichten zur Anwendung im Menschen
Bisher wurde noch keine klinische Studie im Menschen begonnen, doch bereiten sich Unternehmen wie die Schweizer CRISPR Therapeutics (WKN:A2AT0Z) sowie die beiden amerikanischen Editas Medicine (WKN:A2AC4K) und Intellia Therapeutics (WKN:A2AG6H) genau darauf vor.
Das verwendete Cas9-Protein stammt aus Bakterien der Gattungen Staphylococcus und Streptococcus, die beide typische Kommensale und häufig auch Krankheitserreger beim Menschen sind. Deshalb liegt die Vermutung nahe, dass auch viele Menschen Antikörper gegen diese Bakterien gebildet haben. Genau das wurde von Forschern der renommierten Stanford University untersucht und am 05.01.2018 online publiziert.
Heraus kam, dass 65–79 % aller getesteten Personen tatsächlich Antikörper gegen das Cas9-Protein hatten. Knapp 50 % zeigten zudem Antigen-spezifische T-Zellen. Was heißt das nun für die Anwendung der Genschere im Menschen? Grundsätzlich muss man hier zwischen zwei unterschiedlichen Ansätzen unterscheiden:
In vivo bedeutet, dass genetisches Material mit der Information für das Cas9-Protein sowie die RNA der Zielsequenz über Nanopartikel oder Viren in den Patienten gebracht werden. Dort wird die genetische Information abgelesen und damit das Cas9-Protein sowie die zugehörige RNA gebildet.
Ex vivo bedeutet, dass dem Patienten Zellen entnommen werden, in die man außerhalb des Körpers durch elektrische Pulse genetisches Material mit der Information für das Cas9-Protein sowie die RNA der Zielsequenz überträgt.
******************************************
-das sollte man im Auge behalten
- Kursmäßig ist aber nicht viel passiert, also die großen sind nicht scharenweise davongelaufen
aus den Crispr Buden
d.h. entweder ist es nicht sehr relevant und es war wieder nur eine Art Marktmanipulation
oder keiner schätzt das richtig ein - derzeit noch?!
Edit hat das hauseigene Cpf1 Protein:
Cpf1 is a CRISPR effector protein that has greater specificity than Streptococcus pyogenes Cas9 (SpCas9) in genome-editing applications. Here we show that Lachnospiraceae bacterium (Lb) and Acidaminococus sp. (As) Cpf1 orthologs have RNase activities that can excise multiple CRISPR RNAs (crRNAs) from a single RNA polymerase II–driven RNA transcript expressed in mammalian cells. This property simplifies modification of multiple genomic targets and can be used to increase the efficiency of Cpf1-mediated editing.
Ist die Frage, was das in dem Zusammenhang, auch noch an Wert erlangen könnte.
Mal sehen, bleibt spannend.
auf gute Entscheidungen.
S.
https://www.fool.de/2018/01/10/stehen-crispr-therapeutics-ed…
Neue Einsichten zur Anwendung im Menschen
Bisher wurde noch keine klinische Studie im Menschen begonnen, doch bereiten sich Unternehmen wie die Schweizer CRISPR Therapeutics (WKN:A2AT0Z) sowie die beiden amerikanischen Editas Medicine (WKN:A2AC4K) und Intellia Therapeutics (WKN:A2AG6H) genau darauf vor.
Das verwendete Cas9-Protein stammt aus Bakterien der Gattungen Staphylococcus und Streptococcus, die beide typische Kommensale und häufig auch Krankheitserreger beim Menschen sind. Deshalb liegt die Vermutung nahe, dass auch viele Menschen Antikörper gegen diese Bakterien gebildet haben. Genau das wurde von Forschern der renommierten Stanford University untersucht und am 05.01.2018 online publiziert.
Heraus kam, dass 65–79 % aller getesteten Personen tatsächlich Antikörper gegen das Cas9-Protein hatten. Knapp 50 % zeigten zudem Antigen-spezifische T-Zellen. Was heißt das nun für die Anwendung der Genschere im Menschen? Grundsätzlich muss man hier zwischen zwei unterschiedlichen Ansätzen unterscheiden:
In vivo bedeutet, dass genetisches Material mit der Information für das Cas9-Protein sowie die RNA der Zielsequenz über Nanopartikel oder Viren in den Patienten gebracht werden. Dort wird die genetische Information abgelesen und damit das Cas9-Protein sowie die zugehörige RNA gebildet.
Ex vivo bedeutet, dass dem Patienten Zellen entnommen werden, in die man außerhalb des Körpers durch elektrische Pulse genetisches Material mit der Information für das Cas9-Protein sowie die RNA der Zielsequenz überträgt.
******************************************
-das sollte man im Auge behalten
- Kursmäßig ist aber nicht viel passiert, also die großen sind nicht scharenweise davongelaufen
aus den Crispr Buden
d.h. entweder ist es nicht sehr relevant und es war wieder nur eine Art Marktmanipulation
oder keiner schätzt das richtig ein - derzeit noch?!
Edit hat das hauseigene Cpf1 Protein:
Cpf1 is a CRISPR effector protein that has greater specificity than Streptococcus pyogenes Cas9 (SpCas9) in genome-editing applications. Here we show that Lachnospiraceae bacterium (Lb) and Acidaminococus sp. (As) Cpf1 orthologs have RNase activities that can excise multiple CRISPR RNAs (crRNAs) from a single RNA polymerase II–driven RNA transcript expressed in mammalian cells. This property simplifies modification of multiple genomic targets and can be used to increase the efficiency of Cpf1-mediated editing.
Ist die Frage, was das in dem Zusammenhang, auch noch an Wert erlangen könnte.
Mal sehen, bleibt spannend.
auf gute Entscheidungen.
S.
Antwort auf Beitrag Nr.: 56.781.715 von Schaeffi am 21.01.18 15:05:57Ja genau den Bericht meinte ich.
Danke für Deine Ausführungen!
Im Aktionär wird aktuell ein Unternehmen
vorgestellt (Sangamo Therapeutics),
dass sich durchaus auch sehr respektabel
liest.
Viele Grüße
Danke für Deine Ausführungen!
Im Aktionär wird aktuell ein Unternehmen
vorgestellt (Sangamo Therapeutics),
dass sich durchaus auch sehr respektabel
liest.
Viele Grüße
Antwort auf Beitrag Nr.: 56.787.079 von Solideinvestierenkomplex4you am 22.01.18 11:14:03Yep SGMO hatte ich auch mal.
bin dann leider vor dem großen Anstieg raus
Die haben den Zinkfinger (ZFN) die ältere, umständlichere teurere GenSchere.
Aber in letzter Zeit hatten sie viele Erfolge damit. Partnerschaften ….
Da sie schon länger Forschen haben sie auch einen gewissen Vorsprung gegen über z.B. Edit,
aber ich halte CRSPR für die bessere Technik.
Wobei wenn man die Thematik des SA Artikels oben im Hinterkopf behält könnte
sich auch ZFN behaupten.
Mal sehen - bleibt spannend.
S.
bin dann leider vor dem großen Anstieg raus
Die haben den Zinkfinger (ZFN) die ältere, umständlichere teurere GenSchere.
Aber in letzter Zeit hatten sie viele Erfolge damit. Partnerschaften ….
Da sie schon länger Forschen haben sie auch einen gewissen Vorsprung gegen über z.B. Edit,
aber ich halte CRSPR für die bessere Technik.
Wobei wenn man die Thematik des SA Artikels oben im Hinterkopf behält könnte
sich auch ZFN behaupten.
Mal sehen - bleibt spannend.
S.
top deal mit novartis für ex-us rechte an LUXTURNA
Spark Therapeutics to receive $105 million as an upfront fee and is eligible to receive up to $65 million in milestone payments, as well as receive a royalty on net sales outside the U.S.http://ir.sparktx.com/news-releases/news-release-details/spa…
Antwort auf Beitrag Nr.: 56.820.484 von paul81 am 25.01.18 07:34:33sieht für mich schon nach Überreaktion aus....
oder nach Kaufgelegenheit!?
Gruß
oder nach Kaufgelegenheit!?

Gruß
Roche!
Klappt das?
Klappt das?
Antwort auf Beitrag Nr.: 59.951.938 von Chancen1904 am 24.02.19 22:16:45Ja!
http://ir.sparktx.com/news-releases/news-release-details/spa…
Glückwunsch!!
http://ir.sparktx.com/news-releases/news-release-details/spa…
Glückwunsch!!
Antwort auf Beitrag Nr.: 55.964.799 von Cyberhexe am 17.10.17 12:21:41
...obwohl ich nur eine kleine Position aufgebaut habe, freut man sich über die Kursverdoppelung.
Zitat von Cyberhexe: die Aktie ist jetzt nach unten sehr gut abgesichert; durch Gewährung von Priority Review der FDA ist eine Zulassungsentscheidung zum 12. Januar 2018 fällig, die, und da bin ich mir ziemlich sicher, positiv ausfallen wird:
Spannend wird die Preisfrage. Für Luxturna werden sehr hohe Preise erwartet, die sich neuerdings in einer Spanne von $400.000 bis $1.000.000 (beide Augen) bewegen. Möglicherweise kommt auch ein "value-based payment model" wie bei Novartis' CAR-T -Medi Kymriah zur Anwendung, bei welchem für die Arznei $475,000 in Rechnung gestellt werden, sofern die Therapie anschlägt - falls nicht, wird der Verkaufspreis zurückerstattet.
Bei der jährlichen Umsatzspitze sind die Schätzungen sehr weit gestreut, da vor allem die Preisgestaltung und die Reaktion der Versicherer hierzu nur vage Schätzungen zulässt. Aufgrund der überschaubaren Populatuion erscheint jedoch eine rasche Penetration des Marktes möglich, so dass nach Zulassung ein schnelles Umsatzwachstum beobachtet werden sollte. Dreistellige Kurs dürften in naher Zukunft realisiert werden.
One seeking alpha author gives a peak sales estimate for LUXTURNA at $350 to $900 million. With approximately 3,500 individuals with RPE65-related IRDs in the United States and Europe, and an estimated price tag of more than $100,000 per treatment, the estimates may add up.
Habe gestern nochmals 100 Stück günstig nachgekauft!
...obwohl ich nur eine kleine Position aufgebaut habe, freut man sich über die Kursverdoppelung.
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -0,55 | |
| +0,89 | |
| -0,09 | |
| +0,59 | |
| +0,92 | |
| -0,54 | |
| -0,51 | |
| +0,40 | |
| -0,43 | |
| +0,41 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 221 | ||
| 201 | ||
| 153 | ||
| 41 | ||
| 41 | ||
| 39 | ||
| 33 | ||
| 31 | ||
| 30 | ||
| 28 |


























