ONCOLYTICS BIO INC. ► ► Neues Patent für neue Performens - 500 Beiträge pro Seite
eröffnet am 30.05.07 12:49:30 von
neuester Beitrag 29.11.07 22:59:23 von
neuester Beitrag 29.11.07 22:59:23 von
Beiträge: 6
ID: 1.128.041
ID: 1.128.041
Aufrufe heute: 0
Gesamt: 1.517
Gesamt: 1.517
Aktive User: 0
ISIN: CA6823108759 · WKN: A2JMW5 · Symbol: ONC
1,4400
CAD
-2,04 %
-0,0300 CAD
Letzter Kurs 17.04.24 Toronto
Neuigkeiten
14.02.24 · PR Newswire (engl.) |
03.11.23 · PR Newswire (engl.) |
23.10.23 · PR Newswire (engl.) |
23.10.23 · PR Newswire (engl.) |
16.10.23 · PR Newswire (engl.) |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 3.000,00 | +74.900,00 | |
| 0,9300 | +54,46 | |
| 2,3300 | +35,61 | |
| 2,4700 | +33,51 | |
| 1,9100 | +29,93 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,3000 | -20,96 | |
| 2,5000 | -21,88 | |
| 1,4300 | -24,34 | |
| 2,2000 | -31,25 | |
| 2,0900 | -40,52 |

ONCOLYTICS BIO INC. ► ► Neues Patent für neue Performens
http://www.oncolyticsbiotech.com/

Tages-Chart TSX Toronto Canada
Jahres-Chart Toronto Canada
Jahres-Chart USA Nasdaq-CM
Jahres-Chart Frankfurt-Deutschland
Oncolytics Biotech Inc. gibt die Erteilung des 21. US-Patents bekannt.
Calgary, Kanada (ots/PRNewswire) - Oncolytics Biotech Inc. (TSX:
ONC, NASDAQ: ONCY) (\"Oncolytics\") wurde das US-Patent Nr. 7.223.585
unter der Bezeichnung \"Viral Purification Methods\" erteilt. Die
Patentansprüche umfassen die Herstellung und Reinigung von Viren
einschliesslich des Reovirus.
\"Dieses Patent vergrössert unser Portfolio an geistigen
Eigentumsrechten weit über die Eigentumsrechte am Reovirus hinaus,\"
sagte Dr. Matt Coffey, Chief Scientific Officer bei Oncolytics.
\"Zusätzlich zu den verschiedenen Geschäftsgeheimnissen bezüglich der
Herstellung unseres Wirkstoffs haben wir uns mittlerweile sechs
US-Patente gesichert, welche die Herstellung oder Reinigung von Viren
beinhalten.\"

Informationen zu Oncolytics Biotech Inc.
Oncolytics ist ein Biotechnologieunternehmen mit Sitz in Calgary,
das sich auf die Entwicklung onkolytischer Viren als potentielle
Krebstherapeutika konzentriert. Das klinische Programm von Oncolytics
umfasst eine Vielzahl von Tests der Phasen I und II am Patienten mit
REOLYSIN(R), der proprietären Formel des menschlichen Reovirus, und
zwar allein und in Kombination mit Bestrahlungen oder Chemotherapie.
Für weitere Informationen über Oncolytics besuchen Sie bitte die
Webseite unter www.oncolyticsbiotech.com.
Diese Pressemitteilung enthält zukunftsweisende Aussagen im Sinne
des Artikels 21E des Securities Exchange Act von 1934 in seiner
gültigen Fassung. Zukunftsweisende Aussagen einschliesslich u.a. der
Überzeugung des Unternehmens hinsichtlich der Bedeutung dieser
Patenterteilung, der Sicherheit und Wirksamkeit des Reovirus, der
Erwartungen des Unternehmens in Bezug auf die möglichen Anwendungen
der patentierten Technik sowie anderer Erklärungen hinsichtlich
voraussichtlicher Entwicklungen des Geschäfts und der Techniken des
Unternehmens sind mit bekannten und unbekannten Risiken und
Unwägbarkeiten verbunden, die dazu führen können, dass die
tatsächlichen Ergebnisse des Unternehmens von den in den
zukunftsweisenden Aussagen gemachten Angaben erheblich abweichen. Zu
diesen Risiken und Unwägbarkeiten gehören u.a. die Wirksamkeit von
REOLYSIN(R) als Krebsmedikament, der Erfolg und der rechtzeitige
Abschluss klinischer Studien und Versuche, Unwägbarkeiten
hinsichtlich der Erforschung und Entwicklung von Arzneimitteln sowie
Unsicherheiten hinsichtlich des aufsichtsrechtlichen Prozesses.
Investoren sollten die den kanadischen und US-amerikanischen
Börsenaufsichtsbehörden pro Quartal und Jahr eingereichten Unterlagen
des Unternehmens hinsichtlich zusätzlicher Informationen über Risiken
und Unwägbarkeiten einsehen, die sich auf die zukunftsweisenden
Aussagen beziehen. Investoren werden davor gewarnt, sich auf
zukunftsweisende Aussagen übermässig zu verlassen. Das Unternehmen
ist nicht verpflichtet, diese zukunftsweisenden Aussagen zu
aktualisieren.
Originaltext: Oncolytics Biotech Inc
Digitale Pressemappe: http://presseportal.de/story.htx?firmaid=57146
Pressemappe via RSS : feed://presseportal.de/rss/pm_57146.rss2
Pressekontakt:
Für weitere Informationen wenden Sie sich bitte an folgende
Kontaktpersonen: Oncolytics Biotech Inc.: Cathy Ward, 210, 1167
Kensington Cr NW, Calgary, Alberta T2N 1X7, Tel: +1-403-670-7377,
Fax: +1-403-283-0858, E-Mail: cathy.ward@oncolytics.ca; The Equicom
Group: Nick Hurst, 333, 300 5th Ave SW, Calgary, Alberta T2P 3C4,
Tel: +1-403-538-4845, Fax: +1-403-237-6916, E-Mail:
nhurst@equicomgroup.com; The Investor Relations Group: Erika Moran,
11 Stone St, 3rd Floor, New York, NY 10004, Tel: +1-212-825-3210,
Fax: +1-212-825-3229, E-Mail: emoran@investorrelationsgroup.com
TOP Investment mit geringem Risiko
Y M
.

Wissenschaftler von Oncolytics Biotech präsentieren auf der ASCO-Konferenz
klinische Studienergebnisse mit REOLYSIN(R)
Calgary, Kanada (ots/PRNewswire) - Wissenschaftler von Oncolytics
Biotech Inc. ("Oncolytics") (TSX ONC, NASDAQ ONCY) werden auf der vom
1. bis zum 5. Juni in Chicago stattfindenden ASCO-Jahreskonferenz
(American Society of Clinical Oncology) eine Posterpräsentation zu
klinischen Ergebnissen mit REOLYSIN(R) veranstalten. Die Vorstellung
bezieht sich auf die endgültigen Ergebnisse der britischen Studie der
Phase I von Oncolytics zur systemischen Verabreichung.
Dr. James Spicer vom Royal Marsden Hospital und vom Institute of
Cancer Research, Grossbritannien, wird das Poster mit dem Titel
"Final Results of a Phase I Study of Wild-Type Oncolytic Reovirus
Administered Intravenously to Patients with Advanced Cancer" am
Sonntag, den 3. Juni 2007, vorstellen.
Das Poster steht am Montag, den 4. Juni 2007 auf der Webseite von
Oncolytics unter www.oncolyticsbiotech.com zur Verfügung.
Informationen zu Oncolytics Biotech Inc.
Oncolytics ist ein in Calgary ansässiges
Biotechnologie-Unternehmen, das sich auf die Entwicklung
onkolytischer Viren spezialisiert hat, die potenziell zur
Krebstherapie eingesetzt werden können.
Das klinische Programm von
Oncolytics umfasst verschiedene Phase I- und Phase II-Studien bei
denen REOLYSIN(R), die firmeneigene chemische Formulierung des
menschlichen Reovirus, allein oder in Kombination mit
Strahlentherapie bzw. Chemotherapie eingesetzt wird. Für
weitergehende Informationen zu Oncolytics besuchen Sie bitte die
Webseite unter www.oncolyticsbiotech.com
Diese Pressemitteilung enthält zukunftsweisende Aussagen im Sinne
des Abschnitts 21E der aktuellen Fassung des US-amerikanischen
Securities Exchange Act von 1934. Zukunftsweisende Aussagen,
inklusive die Schlussfolgerungen, die aus den auf dieser Konferenz
vorzustellenden Unterlagen gezogen werden können, die Erwartungen des
Unternehmens zu den Ergebnissen der klinischen Untersuchung zur
Verabreichung von REOLYSIN(R) und die Annahmen des Unternehmens zum
Potenzial von REOLYSIN(R) als Krebsmittel, unterliegen bekannten und
unbekannten Risiken und Unsicherheiten, die dazu führen können, dass
die tatsächlich eintretenden Ergebnisse des Unternehmens wesentlich
von den in den zukunftsweisenden Aussagen ausgedrückten, abweichen.
Zu diesen Risiken und Unsicherheiten gehören u.a.: Die Verfügbarkeit
der notwendigen Finanzmittel und Ressourcen, um Forschungs- und
Entwicklungsprojekte weiterzuführen, die Wirksamkeit von REOLYSIN(R)
als Krebsmittel, der erfolgreiche und rechtzeitige Abschluss
klinischer Studien und Tests, die Fähigkeit des Unternehmens,
REOLYSIN(R) erfolgreich zu vermarkten, Unsicherheiten im Zusammenhang
mit Forschung und Entwicklung von Pharmazeutika und Ungewissheiten im
Zusammenhang mit dem Zulassungsprozess. Investoren sollten die bei
den kanadischen und amerikanischen Börsenaufsichtsbehörden
eingereichten Quartals- und Jahresberichte hinsichtlich zusätzlicher
Informationen zu Risiken und Ungewissheiten in Bezug auf
zukunftsweisende Aussagen einsehen. Investoren werden davor gewarnt,
sich übermässig auf zukunftsweisende Aussagen zu verlassen. Das
Unternehmen hat nicht die Absicht, zukunftsweisende Aussagen zu
aktualisieren.
Originaltext: Oncolytics Biotech Inc
Digitale Pressemappe: http://presseportal.de/story.htx?firmaid=57146
Pressemappe via RSS : feed://presseportal.de/rss/pm_57146.rss2
Pressekontakt:
Weitergehende Informationen: Oncolytics Biotech Inc., Cathy Ward,
210, 1167 Kensington Cr NW, Calgary, Alberta, T2N 1X7, Tel.:
+1-403-670-7377, Fax: +1-403-283-0858, E-Mail:
cathy.ward@oncolytics.ca; The Equicom Group, Nick Hurst, 325, 300,
5th Ave. SW, Calgary, Alberta, T2P 3C4, Tel.: +1-403-538-4845, Fax:
+1-403-237-6916, E-Mail: nhurst@equicomgroup.com; The Investor
Relations Group, Erika Moran, 11 Stone St, 3rd Floor, New York, NY,
10004, Tel.: +1-212-825-3210, Fax: +1-212-825-3229, E-Mail:
emoran@investorrelationsgroup.com
.
.

Oncolytics Biotech Inc. meldet positive klinische Daten von Phase-I-US-Studie zu
REOLYSIN(R)
Calgary, Kanada (ots/PRNewswire) - Oncolytics Biotech Inc. ("
Oncolytics ") (TSX ONC, NASDAQ ONCY) gab heute positive Ergebnisse
von seiner in den USA durchgeführten klinischen Studie der Phase I
zur Prüfung der systemischen Gabe von REOLYSIN(R) bei Patienten mit
fortgeschrittenen Krebserkrankungen bekannt. Die Ergebnisse weisen
darauf hin, dass REOLYSIN(R) Patienten mit fortgeschrittenem oder
metastasiertem Krebs systemisch verabreicht werden kann und eine
gegen Tumoren gerichtete Wirkung aufweist.
"Die Verabreichung von REOLYSIN(R) in Form einer einstündigen
Infusion in monatlichen Abständen ist sicher und wird auch bei
mehreren Dosen gut vertragen ", so der Principal Investigator Dr.
Sanjay Goel vom Montefiore Medical Center und Albert Einstein College
of Medicine, New York. " Diese vorläufigen Ergebnisse legen nahe,
dass die alleinige Gabe von REOLYSIN(R) eine gegen Tumoren gerichtete
Wirkung aufweist, so dass die Durchführung weiterer Studien, entweder
als Monotherapie oder in Kombination mit einer zytotoxischen
Chemotherapie, gerechtfertigt ist. Solche Studien werden zurzeit
geplant. "
Insgesamt wurden 18 Patienten in der Studie, in der eine
eskalierende Dosierung bis zu einer maximalen Tagesdosis von 3x10(10)
TCID(50) in Form einer einstündigen Infusion zur Anwendung kam,
behandelt. Bei acht der 18 behandelten Patienten blieb die Erkrankung
stabil, wobei die Messung mittels RECIST (Response Evaluation
Criteria in Solid Tumours) erfolgte. Darunter war eine Patientin mit
progredientem Brustkrebs, bei der eine Tumorverkleinerung um 28.5%
beobachtet wurde. Das ursprüngliche Studiendesign sah den Nachweis
der Sicherheit einer einmaligen, einstündigen Infusion von
REOLYSIN(R) vor. Während der Behandlung der 4. Patientenkohorte
stellte Oncolytics jedoch den Antrag auf Genehmigung der Durchführung
von wiederholten monatlichen Behandlungen mit REOLYSIN(R) bei den
nachfolgenden Patienten. Diesem Antrag wurde stattgegeben. Drei der
zur Wiederholungsbehandlung zugelassenen Patienten erhielten zwei bis
sieben einstündige REOLYSIN(R)-Infusionen.
Die toxischen Wirkungen, die möglicherweise mit der REOLYSIN(R
)-Behandlung in Rahmen dieser Studie zusammenhingen, waren in der
Regel leichter Art (Grad 1 oder 2) und schlossen Schüttelfrost,
Fieber und Müdigkeit mit ein.
Das primäre Ziel der US-amerikanischen Phase-I-Studie besteht in
der Bestimmung der maximal tolerierten Dosis (MTD), der
dosislimitierenden Toxizität (DLT) und des Sicherheitsprofils von
REOLYSIN(R) bei systemischer Verabreichung. Ein sekundäres Ziel
besteht in der Untersuchung von allen Hinweisen auf eine
Antitumoraktivität. Zu den zur Studienteilnahme berechtigten
Patienten gehörten Probanden, bei denen die Diagnose eines
fortgeschrittenen oder metastasierten soliden Tumors gestellt wurde,
der Refraktärität (kein Ansprechen) auf Standardtherapie zeigt bzw.
für den keine kurative Standardtherapie existiert.
Informationen zu Oncolytics Biotech Inc.
Oncolytics ist ein in Calgary ansässiges
Biotechnologie-Unternehmen, das sich auf die Entwicklung
onkolytischer Viren spezialisiert hat, die potenziell zur
Krebstherapie eingesetzt werden können.
Das klinische Programm von Oncolytics umfasst verschiedene Phase
I- und Phase II-Studien, bei denen REOLYSIN(R), die firmeneigene Form
des menschlichen Reovirus allein oder in Kombination mit
Strahlentherapie bzw. Chemotherapie eingesetzt wird. Für
weitergehende Informationen zu Oncolytics besuchen Sie bitte die
Webseite unter www.oncolyticsbiotech.com.
Diese Pressemitteilung enthält zukunftsweisende Aussagen im Sinne
des Abschnitts 21E der aktuellen Fassung des US-amerikanischen
Securities Exchange Act von 1934.
Zukunftsweisende Aussagen einschliesslich der Erwartungen des
Unternehmens hinsichtlich der Ergebnisse der US-amerikanischen
klinischen Studie der Phase I zur systemischen Verabreichung von
REOLYSIN(R) zur Behandlung von fortgeschrittenen Krebserkrankungen
und der Überzeugungen des Unternehmens hinsichtlich des Potenzials
von REOLYSIN(R) als ein Medikament zur Krebstherapie sind mit
bekannten und unbekannten Risiken und Unwägbarkeiten verbunden, die
dazu führen können, dass die tatsächlichen Ergebnisse des
Unternehmens von den in den zukunftsweisenden Aussagen gemachten
Angaben erheblich abweichen. Zu diesen Risiken und Unwägbarkeiten
gehören u.a. die Verfügbarkeit von Finanzmitteln und Ressourcen zur
Durchführung von Forschungs- und Entwicklungsprojekten, die
Wirksamkeit von REOLYSIN(R) als Krebsbehandlung, der Erfolg und der
rechtzeitige Abschluss klinischer Studien und Prüfungen, die
tatsächliche Verträglichkeit beim Patienten, die erfolgreiche
Vermarktung von REOLYSIN(R) durch das Unternehmen, Unwägbarkeiten
hinsichtlich der Erforschung und Entwicklung von Arzneimitteln sowie
Unsicherheiten hinsichtlich des aufsichtsrechtlichen Prozesses.
Investoren sollten die bei den kanadischen und amerikanischen
Börsenaufsichtsbehörden eingereichten Quartals- und Jahresberichte
hinsichtlich zusätzlicher Informationen zu Risiken und Ungewissheiten
in Bezug auf zukunftsweisende Aussagen einsehen. Investoren werden
davor gewarnt, sich allzu sehr auf zukunftsweisende Aussagen zu
verlassen. Das Unternehmen hat nicht die Absicht, zukunftsweisende
Aussagen zu aktualisieren.
Originaltext: Oncolytics Biotech Inc
Digitale Pressemappe: http://presseportal.de/story.htx?firmaid=57146
Pressemappe via RSS : feed://presseportal.de/rss/pm_57146.rss2
Pressekontakt:
Weitere Informationen erhalten Sie von: Oncolytics Biotech Inc.,
Cathy Ward, 210, 1167 Kensington Cr NW, Calgary, Alberta, T2N 1X7,
Tel: +1-403-670-7377, Fax: +1-403-283-0858, cathy.ward@oncolytics.ca;
The Equicom Group, Nick Hurst, 325, 300 5th Ave. SW, Calgary,
Alberta, T2P 3C4, Tel: +1-403-538-4845, Fax: +1-403-237-6916,
nhurst@equicomgroup.com; The Investor Relations Group, Erika Moran,
11 Stone St, 3rd Floor, New York, NY, 10004, Tel: +1-212-825-3210,
Fax: +1-212-825-3229, emoran@investorrelationsgroup.com
.

Oncolytics Biotech Inc. meldet positive klinische Daten von Phase-I-US-Studie zu
REOLYSIN(R)
Calgary, Kanada (ots/PRNewswire) - Oncolytics Biotech Inc. ("
Oncolytics ") (TSX ONC, NASDAQ ONCY) gab heute positive Ergebnisse
von seiner in den USA durchgeführten klinischen Studie der Phase I
zur Prüfung der systemischen Gabe von REOLYSIN(R) bei Patienten mit
fortgeschrittenen Krebserkrankungen bekannt. Die Ergebnisse weisen
darauf hin, dass REOLYSIN(R) Patienten mit fortgeschrittenem oder
metastasiertem Krebs systemisch verabreicht werden kann und eine
gegen Tumoren gerichtete Wirkung aufweist.
"Die Verabreichung von REOLYSIN(R) in Form einer einstündigen
Infusion in monatlichen Abständen ist sicher und wird auch bei
mehreren Dosen gut vertragen ", so der Principal Investigator Dr.
Sanjay Goel vom Montefiore Medical Center und Albert Einstein College
of Medicine, New York. " Diese vorläufigen Ergebnisse legen nahe,
dass die alleinige Gabe von REOLYSIN(R) eine gegen Tumoren gerichtete
Wirkung aufweist, so dass die Durchführung weiterer Studien, entweder
als Monotherapie oder in Kombination mit einer zytotoxischen
Chemotherapie, gerechtfertigt ist. Solche Studien werden zurzeit
geplant. "
Insgesamt wurden 18 Patienten in der Studie, in der eine
eskalierende Dosierung bis zu einer maximalen Tagesdosis von 3x10(10)
TCID(50) in Form einer einstündigen Infusion zur Anwendung kam,
behandelt. Bei acht der 18 behandelten Patienten blieb die Erkrankung
stabil, wobei die Messung mittels RECIST (Response Evaluation
Criteria in Solid Tumours) erfolgte. Darunter war eine Patientin mit
progredientem Brustkrebs, bei der eine Tumorverkleinerung um 28.5%
beobachtet wurde. Das ursprüngliche Studiendesign sah den Nachweis
der Sicherheit einer einmaligen, einstündigen Infusion von
REOLYSIN(R) vor. Während der Behandlung der 4. Patientenkohorte
stellte Oncolytics jedoch den Antrag auf Genehmigung der Durchführung
von wiederholten monatlichen Behandlungen mit REOLYSIN(R) bei den
nachfolgenden Patienten. Diesem Antrag wurde stattgegeben. Drei der
zur Wiederholungsbehandlung zugelassenen Patienten erhielten zwei bis
sieben einstündige REOLYSIN(R)-Infusionen.
Die toxischen Wirkungen, die möglicherweise mit der REOLYSIN(R
)-Behandlung in Rahmen dieser Studie zusammenhingen, waren in der
Regel leichter Art (Grad 1 oder 2) und schlossen Schüttelfrost,
Fieber und Müdigkeit mit ein.
Das primäre Ziel der US-amerikanischen Phase-I-Studie besteht in
der Bestimmung der maximal tolerierten Dosis (MTD), der
dosislimitierenden Toxizität (DLT) und des Sicherheitsprofils von
REOLYSIN(R) bei systemischer Verabreichung. Ein sekundäres Ziel
besteht in der Untersuchung von allen Hinweisen auf eine
Antitumoraktivität. Zu den zur Studienteilnahme berechtigten
Patienten gehörten Probanden, bei denen die Diagnose eines
fortgeschrittenen oder metastasierten soliden Tumors gestellt wurde,
der Refraktärität (kein Ansprechen) auf Standardtherapie zeigt bzw.
für den keine kurative Standardtherapie existiert.
Informationen zu Oncolytics Biotech Inc.
Oncolytics ist ein in Calgary ansässiges
Biotechnologie-Unternehmen, das sich auf die Entwicklung
onkolytischer Viren spezialisiert hat, die potenziell zur
Krebstherapie eingesetzt werden können.
Das klinische Programm von Oncolytics umfasst verschiedene Phase
I- und Phase II-Studien, bei denen REOLYSIN(R), die firmeneigene Form
des menschlichen Reovirus allein oder in Kombination mit
Strahlentherapie bzw. Chemotherapie eingesetzt wird. Für
weitergehende Informationen zu Oncolytics besuchen Sie bitte die
Webseite unter www.oncolyticsbiotech.com.
Diese Pressemitteilung enthält zukunftsweisende Aussagen im Sinne
des Abschnitts 21E der aktuellen Fassung des US-amerikanischen
Securities Exchange Act von 1934.
Zukunftsweisende Aussagen einschliesslich der Erwartungen des
Unternehmens hinsichtlich der Ergebnisse der US-amerikanischen
klinischen Studie der Phase I zur systemischen Verabreichung von
REOLYSIN(R) zur Behandlung von fortgeschrittenen Krebserkrankungen
und der Überzeugungen des Unternehmens hinsichtlich des Potenzials
von REOLYSIN(R) als ein Medikament zur Krebstherapie sind mit
bekannten und unbekannten Risiken und Unwägbarkeiten verbunden, die
dazu führen können, dass die tatsächlichen Ergebnisse des
Unternehmens von den in den zukunftsweisenden Aussagen gemachten
Angaben erheblich abweichen. Zu diesen Risiken und Unwägbarkeiten
gehören u.a. die Verfügbarkeit von Finanzmitteln und Ressourcen zur
Durchführung von Forschungs- und Entwicklungsprojekten, die
Wirksamkeit von REOLYSIN(R) als Krebsbehandlung, der Erfolg und der
rechtzeitige Abschluss klinischer Studien und Prüfungen, die
tatsächliche Verträglichkeit beim Patienten, die erfolgreiche
Vermarktung von REOLYSIN(R) durch das Unternehmen, Unwägbarkeiten
hinsichtlich der Erforschung und Entwicklung von Arzneimitteln sowie
Unsicherheiten hinsichtlich des aufsichtsrechtlichen Prozesses.
Investoren sollten die bei den kanadischen und amerikanischen
Börsenaufsichtsbehörden eingereichten Quartals- und Jahresberichte
hinsichtlich zusätzlicher Informationen zu Risiken und Ungewissheiten
in Bezug auf zukunftsweisende Aussagen einsehen. Investoren werden
davor gewarnt, sich allzu sehr auf zukunftsweisende Aussagen zu
verlassen. Das Unternehmen hat nicht die Absicht, zukunftsweisende
Aussagen zu aktualisieren.
Originaltext: Oncolytics Biotech Inc
Digitale Pressemappe: http://presseportal.de/story.htx?firmaid=57146
Pressemappe via RSS : feed://presseportal.de/rss/pm_57146.rss2
Pressekontakt:
Weitere Informationen erhalten Sie von: Oncolytics Biotech Inc.,
Cathy Ward, 210, 1167 Kensington Cr NW, Calgary, Alberta, T2N 1X7,
Tel: +1-403-670-7377, Fax: +1-403-283-0858, cathy.ward@oncolytics.ca;
The Equicom Group, Nick Hurst, 325, 300 5th Ave. SW, Calgary,
Alberta, T2P 3C4, Tel: +1-403-538-4845, Fax: +1-403-237-6916,
nhurst@equicomgroup.com; The Investor Relations Group, Erika Moran,
11 Stone St, 3rd Floor, New York, NY, 10004, Tel: +1-212-825-3210,
Fax: +1-212-825-3229, emoran@investorrelationsgroup.com
.
.

Cosmic ist dabei seit 1,50 Can Doll (1,05 €)
TSX Toronto
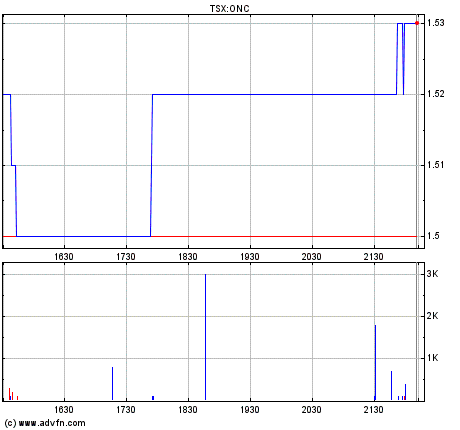
Nasdaq USA
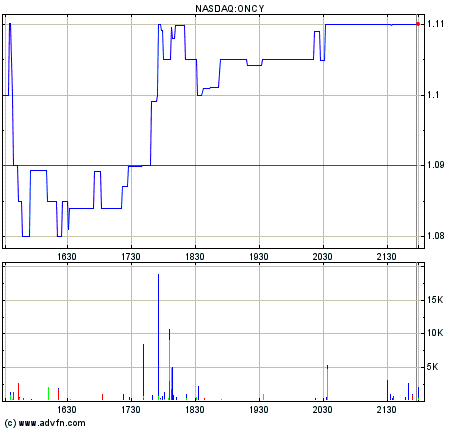
Oncolytics Biotech Inc. Reports Positive Interim Results of U.K. Phase Ia/Ib Combination REOLYSIN(R) and Radiation Clinical Trial
14:35 EDT Toronto Time Friday, September 28, 2007
CALGARY, Sept. 28 /PRNewswire-FirstCall/ - Oncolytics Biotech Inc. (\\\"Oncolytics\\\") (TSX ONC, NASDA ONCY) today announced that an oral presentation covering interim results from a U.K. Phase Ia/Ib combination REOLYSIN(R) and radiation clinical trial for patients with advanced or metastatic cancers is scheduled to be presented at the National Cancer Research Institute (NCRI) conference on October 2, 2007 in Birmingham, U.K. The presentation, entitled \\\"Biological Approaches to Radiosensitisation: Viruses, Gene Therapy and Novel Radiosensitisers\\\" will be presented by Dr. Kevin Harrington of The Institute of Cancer Research, London and one of the principal investigators for the trial. The conference runs from September 30 through October 3, 2007 in Birmingham, U.K.
\\\"We are very pleased with the results of this trial to date,\\\" said Dr. Brad Thompson, President and CEO of Oncolytics. \\\"We continue to evaluate the data and look forward to announcing final results.\\\"
To date, 22 patients have been treated with 15 having completed the study. Five patients withdrew from the study, and two patients are still on study.
A total of 11 patients in the Ia portion of the trial received two intratumoural treatments of REOLYSIN(R) at dosages of 1x10(8), 1x10(9), or 1x10(10) TCID(50) with a constant localized radiation dose of 20 Gy given in five fractions. Of these 11 patients, three patients (oesophageal, squamous skin carcinoma and squamous cell scalp) experienced significant partial responses.
One month following treatment, the oesophageal patient experienced a 28.5% reduction in the target tumour, with stable disease noted in four, non-treated tumours. At two and three months, the target tumour had shrunk 64%, with stable disease continuing in the four non-treated tumours, including a 15% volume reduction in non-treated mediastinal disease that was maintained for more than six months. The squamous skin cancer patient experienced a 50% reduction in the target tumour, as well as stable disease in two, non-treated tumours at one, two and three months post treatment. The squamous cell scalp patient experienced stable disease in the target tumour for two months which then became a partial response at three months. This patient also experienced stable disease in one non-treated tumour measured at three months post-treatment.
Patients in the Ib portion received either two, four or six intratumoural doses of REOLYSIN(R) at 1x10(10) TCID(50) with a constant localized radiation dose of 36 Gy given in 12 fractions. Of the six patients who have completed the study to date, three patients (colorectal, melanoma and lung cancer) experienced tumour regression in the target tumour, as well as stable disease in non-treated tumours.
The colorectal patient experienced a partial response with a more than 50% regression in the target tumour as well as stable disease in four, non-treated tumours measured at one month following treatment. A melanoma patient experienced minor regression in the target tumour as well as stable disease in two, non-treated tumours at one and two months following treatment. A lung cancer patient experienced minor regression in the target tumour, as well as stable disease in three, non-treated tumours at two months following treatment.
The treatment has been well tolerated, with mostly Grade 1 or 2 toxicities noted including fatigue, lymphopenia, fever, and neutropenia. Grade 3 toxicities including cellulitis, dysphasia and diarrhoea were related to disease progression and not to the combination treatment. Viral replication was unaffected by cellular irradiation.
The primary objective of the Phase Ia/Ib trial is to determine the maximum tolerated dose (MTD), dose limiting toxicity (DLT), and safety profile of REOLYSIN(R) when administered intratumourally to patients receiving radiation treatment. A secondary objective is to examine any evidence of anti-tumour activity. Eligible patients include those who have been diagnosed with advanced or metastatic solid tumours that are refractory (have not responded) to standard therapy or for which no curative standard therapy exists.
The principal investigators for the trial are Dr. Kevin Harrington of the Targeted Therapy Laboratory, The Institute of Cancer Research, Cancer Research UK Centre for Cell and Molecular Biology and Honorary Consultant in Clinical Oncology at The Royal Marsden NHS Foundation Trust, London, UK, and Dr. Alan Melcher of the Cancer Research U.K. Clinical Centre at St. James\\\'s University Hospital in Leeds. The trial is enrolling patients at the Royal Marsden and St. James\\\'s Hospitals in the U.K.
Further results of the combination REOLYSIN(R) and radiation trial are scheduled to be presented at the AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics in San Francisco October 22-26, 2007.
About Oncolytics Biotech Inc.
Oncolytics is a Calgary-based biotechnology company focused on the development of oncolytic viruses as potential cancer therapeutics. Oncolytics\\\' clinical program includes a variety of Phase I and Phase II human trials using REOLYSIN(R), its proprietary formulation of the human reovirus, alone and in combination with radiation or chemotherapy. For further information about Oncolytics, please visit www.oncolyticsbiotech.com
About The Institute of Cancer Research
The Institute of Cancer Research is Europe\\\'s leading cancer research centre with expert scientists working on cutting edge research. It was founded in 1909 to carry out research into the causes of cancer and to develop new strategies for its prevention, diagnosis, treatment and care. Website at: www.icr.ac.uk
The Institute works in a unique partnership with The Royal Marsden NHS Foundation Trust, forming the largest comprehensive cancer centre in Europe. This relationship enables close daily contact between research scientists and those on the frontline in the fight against cancer - the clinicians, the carers and most importantly, the patients.
This press release contains forward-looking statements, within the meaning of Section 21E of the Securities Exchange Act of 1934, as amended. Forward-looking statements, including the Company\\\'s expectations related to the Phase Ia/Ib U.K. combination REOLYSIN(R) and radiation clinical trial, and the Company\\\'s belief as to the potential of REOLYSIN(R) as a cancer therapeutic, involve known and unknown risks and uncertainties, which could cause the Company\\\'s actual results to differ materially from those in the forward-looking statements. Such risks and uncertainties include, among others, the availability of funds and resources to pursue research and development projects, the efficacy of REOLYSIN(R) as a cancer treatment, the success and timely completion of clinical studies and trials, the Company\\\'s ability to successfully commercialize REOLYSIN(R), uncertainties related to the research and development of pharmaceuticals and uncertainties related to the regulatory process. Investors should consult the Company\\\'s quarterly and annual filings with the Canadian and U.S. securities commissions for additional information on risks and uncertainties relating to the forward-looking statements. Investors are cautioned against placing undue reliance on forward-looking statements. The Company does not undertake to update these forward-looking statements.
SOURCE Oncolytics Biotech Inc.
For further information: Oncolytics Biotech Inc., Cathy Ward, 210, 1167 Kensington Cr NW, Calgary, Alberta, T2N 1X7, Tel: (403) 670-7377, Fax: (403) 283-0858, cathy.ward@oncolytics.ca; The Equicom Group, Nick Hurst, 325, 300 5th Ave. SW, Calgary, Alberta, T2P 3C4, Tel: (403) 538-4845, Fax: (403) 237-6916, nhurst@equicomgroup.com; The Investor Relations Group, Erika Moran, 11 Stone St, 3rd Floor, New York, NY, 10004, Tel: (212) 825-3210, Fax: (212) 825-3229, emoran@investorrelationsgroup.com
.

Cosmic ist dabei seit 1,50 Can Doll (1,05 €)
TSX Toronto
Nasdaq USA
Oncolytics Biotech Inc. Reports Positive Interim Results of U.K. Phase Ia/Ib Combination REOLYSIN(R) and Radiation Clinical Trial
14:35 EDT Toronto Time Friday, September 28, 2007
CALGARY, Sept. 28 /PRNewswire-FirstCall/ - Oncolytics Biotech Inc. (\\\"Oncolytics\\\") (TSX ONC, NASDA ONCY) today announced that an oral presentation covering interim results from a U.K. Phase Ia/Ib combination REOLYSIN(R) and radiation clinical trial for patients with advanced or metastatic cancers is scheduled to be presented at the National Cancer Research Institute (NCRI) conference on October 2, 2007 in Birmingham, U.K. The presentation, entitled \\\"Biological Approaches to Radiosensitisation: Viruses, Gene Therapy and Novel Radiosensitisers\\\" will be presented by Dr. Kevin Harrington of The Institute of Cancer Research, London and one of the principal investigators for the trial. The conference runs from September 30 through October 3, 2007 in Birmingham, U.K.
\\\"We are very pleased with the results of this trial to date,\\\" said Dr. Brad Thompson, President and CEO of Oncolytics. \\\"We continue to evaluate the data and look forward to announcing final results.\\\"
To date, 22 patients have been treated with 15 having completed the study. Five patients withdrew from the study, and two patients are still on study.
A total of 11 patients in the Ia portion of the trial received two intratumoural treatments of REOLYSIN(R) at dosages of 1x10(8), 1x10(9), or 1x10(10) TCID(50) with a constant localized radiation dose of 20 Gy given in five fractions. Of these 11 patients, three patients (oesophageal, squamous skin carcinoma and squamous cell scalp) experienced significant partial responses.
One month following treatment, the oesophageal patient experienced a 28.5% reduction in the target tumour, with stable disease noted in four, non-treated tumours. At two and three months, the target tumour had shrunk 64%, with stable disease continuing in the four non-treated tumours, including a 15% volume reduction in non-treated mediastinal disease that was maintained for more than six months. The squamous skin cancer patient experienced a 50% reduction in the target tumour, as well as stable disease in two, non-treated tumours at one, two and three months post treatment. The squamous cell scalp patient experienced stable disease in the target tumour for two months which then became a partial response at three months. This patient also experienced stable disease in one non-treated tumour measured at three months post-treatment.
Patients in the Ib portion received either two, four or six intratumoural doses of REOLYSIN(R) at 1x10(10) TCID(50) with a constant localized radiation dose of 36 Gy given in 12 fractions. Of the six patients who have completed the study to date, three patients (colorectal, melanoma and lung cancer) experienced tumour regression in the target tumour, as well as stable disease in non-treated tumours.
The colorectal patient experienced a partial response with a more than 50% regression in the target tumour as well as stable disease in four, non-treated tumours measured at one month following treatment. A melanoma patient experienced minor regression in the target tumour as well as stable disease in two, non-treated tumours at one and two months following treatment. A lung cancer patient experienced minor regression in the target tumour, as well as stable disease in three, non-treated tumours at two months following treatment.
The treatment has been well tolerated, with mostly Grade 1 or 2 toxicities noted including fatigue, lymphopenia, fever, and neutropenia. Grade 3 toxicities including cellulitis, dysphasia and diarrhoea were related to disease progression and not to the combination treatment. Viral replication was unaffected by cellular irradiation.
The primary objective of the Phase Ia/Ib trial is to determine the maximum tolerated dose (MTD), dose limiting toxicity (DLT), and safety profile of REOLYSIN(R) when administered intratumourally to patients receiving radiation treatment. A secondary objective is to examine any evidence of anti-tumour activity. Eligible patients include those who have been diagnosed with advanced or metastatic solid tumours that are refractory (have not responded) to standard therapy or for which no curative standard therapy exists.
The principal investigators for the trial are Dr. Kevin Harrington of the Targeted Therapy Laboratory, The Institute of Cancer Research, Cancer Research UK Centre for Cell and Molecular Biology and Honorary Consultant in Clinical Oncology at The Royal Marsden NHS Foundation Trust, London, UK, and Dr. Alan Melcher of the Cancer Research U.K. Clinical Centre at St. James\\\'s University Hospital in Leeds. The trial is enrolling patients at the Royal Marsden and St. James\\\'s Hospitals in the U.K.
Further results of the combination REOLYSIN(R) and radiation trial are scheduled to be presented at the AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics in San Francisco October 22-26, 2007.
About Oncolytics Biotech Inc.
Oncolytics is a Calgary-based biotechnology company focused on the development of oncolytic viruses as potential cancer therapeutics. Oncolytics\\\' clinical program includes a variety of Phase I and Phase II human trials using REOLYSIN(R), its proprietary formulation of the human reovirus, alone and in combination with radiation or chemotherapy. For further information about Oncolytics, please visit www.oncolyticsbiotech.com
About The Institute of Cancer Research
The Institute of Cancer Research is Europe\\\'s leading cancer research centre with expert scientists working on cutting edge research. It was founded in 1909 to carry out research into the causes of cancer and to develop new strategies for its prevention, diagnosis, treatment and care. Website at: www.icr.ac.uk
The Institute works in a unique partnership with The Royal Marsden NHS Foundation Trust, forming the largest comprehensive cancer centre in Europe. This relationship enables close daily contact between research scientists and those on the frontline in the fight against cancer - the clinicians, the carers and most importantly, the patients.
This press release contains forward-looking statements, within the meaning of Section 21E of the Securities Exchange Act of 1934, as amended. Forward-looking statements, including the Company\\\'s expectations related to the Phase Ia/Ib U.K. combination REOLYSIN(R) and radiation clinical trial, and the Company\\\'s belief as to the potential of REOLYSIN(R) as a cancer therapeutic, involve known and unknown risks and uncertainties, which could cause the Company\\\'s actual results to differ materially from those in the forward-looking statements. Such risks and uncertainties include, among others, the availability of funds and resources to pursue research and development projects, the efficacy of REOLYSIN(R) as a cancer treatment, the success and timely completion of clinical studies and trials, the Company\\\'s ability to successfully commercialize REOLYSIN(R), uncertainties related to the research and development of pharmaceuticals and uncertainties related to the regulatory process. Investors should consult the Company\\\'s quarterly and annual filings with the Canadian and U.S. securities commissions for additional information on risks and uncertainties relating to the forward-looking statements. Investors are cautioned against placing undue reliance on forward-looking statements. The Company does not undertake to update these forward-looking statements.
SOURCE Oncolytics Biotech Inc.
For further information: Oncolytics Biotech Inc., Cathy Ward, 210, 1167 Kensington Cr NW, Calgary, Alberta, T2N 1X7, Tel: (403) 670-7377, Fax: (403) 283-0858, cathy.ward@oncolytics.ca; The Equicom Group, Nick Hurst, 325, 300 5th Ave. SW, Calgary, Alberta, T2P 3C4, Tel: (403) 538-4845, Fax: (403) 237-6916, nhurst@equicomgroup.com; The Investor Relations Group, Erika Moran, 11 Stone St, 3rd Floor, New York, NY, 10004, Tel: (212) 825-3210, Fax: (212) 825-3229, emoran@investorrelationsgroup.com
.
Antwort auf Beitrag Nr.: 31.783.962 von CosmicTrade am 29.09.07 01:06:38Hallo Cosmictrade  !
!
Herzlichen glückwunsch zum exaxt getimeten einstieg!
War vor Jahren auch in oncy drin,aber jetzt nach dem Scheitern von GPC Biotech und sovieler anderer,die ebenfalls gescheitert sind,ist mir das alles zu unsicher geworden !
!
Wie lange willst du denn halten,und wieviel Cash hat Oncy noch,ich bekomme keine Informationen mehr
MFG
Chalifmann
 !
!Herzlichen glückwunsch zum exaxt getimeten einstieg!
War vor Jahren auch in oncy drin,aber jetzt nach dem Scheitern von GPC Biotech und sovieler anderer,die ebenfalls gescheitert sind,ist mir das alles zu unsicher geworden
 !
!Wie lange willst du denn halten,und wieviel Cash hat Oncy noch,ich bekomme keine Informationen mehr

MFG
Chalifmann

Antwort auf Beitrag Nr.: 32.254.251 von DrBlckburne123 am 02.11.07 13:26:37.
Cosmic hält weiter...denke wir sehen die 3 Can. Dollar
bis Jahresende...
wenn man bedenkt wieviel Bio-Schrottwerte in Deutschland
gekauft werden, ist man hier auf der sicheren Seite.
.
Cosmic hält weiter...denke wir sehen die 3 Can. Dollar
bis Jahresende...
wenn man bedenkt wieviel Bio-Schrottwerte in Deutschland
gekauft werden, ist man hier auf der sicheren Seite.
.
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -1,53 | |
| -1,48 | |
| -0,27 | |
| -1,70 | |
| +8,86 | |
| +1,60 | |
| -2,52 | |
| -3,92 | |
| +1,02 | |
| +10,76 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 212 | ||
| 116 | ||
| 101 | ||
| 85 | ||
| 77 | ||
| 46 | ||
| 44 | ||
| 41 | ||
| 32 | ||
| 30 |





















