DNL.L (Mkap €25 M) Attraktive Medikamente vor der Zulassung (Seite 55)
eröffnet am 15.07.19 22:09:04 von
neuester Beitrag 15.11.22 13:24:57 von
neuester Beitrag 15.11.22 13:24:57 von
Beiträge: 969
ID: 1.307.455
ID: 1.307.455
Aufrufe heute: 0
Gesamt: 134.188
Gesamt: 134.188
Aktive User: 0
ISIN: GB00BDB6Q760 · WKN: A2ACSA
0,2820
EUR
0,00 %
0,0000 EUR
Letzter Kurs 01.11.22 Frankfurt
Werte aus der Branche Dienstleistungen
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,1000 | +40,00 | |
| 0,8200 | +22,39 | |
| 1,5200 | +18,75 | |
| 0,8000 | +17,65 | |
| 35,18 | +15,72 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,0700 | -14,74 | |
| 41,65 | -14,88 | |
| 2,3800 | -17,93 | |
| 0,6300 | -30,00 | |
| 0,5200 | -48,52 |
Beitrag zu dieser Diskussion schreiben
Antwort auf Beitrag Nr.: 62.876.514 von Saaartlesip am 04.03.20 11:28:23Handel in London findet aber offenbar statt. Trading Status ist: "Periodic Call".
Ist die Aktie delisted vor kurzem??
Ich kann meine Aktien immer noch nicht verkaufen. Nicht mal marketorder geht. Bin ich der einzige bei dem das so ist?
Bei welchem Broker hat das denn bei euch funktioniert?
Bei welchem Broker hat das denn bei euch funktioniert?
Antwort auf Beitrag Nr.: 62.826.734 von urpferdchen am 28.02.20 16:27:42falsches Forum - der Beitrag gehört zum - Antisense -
auf www.finanznachrichten.de - ist heute der Finanzbericht zum 31.12. und wietere Infos - leider geht der link nicht.
der erste Teil - automatisch übersetzt -
----------------
Finanzielle Zusammenfassung Das Unternehmen meldete für das am 31. Dezember 2019 endende Halbjahr einen Verlust von 4.326.273 USD (einschließlich einer nicht zahlungswirksamen, vollständig amortisierten Optionsemission „Share Based Payment“ von 2.420.086 USD). Zum 31. Dezember 2019 verfügte das Unternehmen über Barreserven in Höhe von 5.128.667 USD, bevor es im Januar nach Abwicklung des Zeichnens der börsennotierten Optionen weitere 1,864 Mio. USD (vor Kosten) erhielt. Operations Summary ATL1102 für DMD Das Unternehmen führt die klinische Entwicklung von ATL1102 bei Patienten mit Duchenne-Muskeldystrophie (DMD) durch. Am 17. Dezember 2019 teilte das Unternehmen mit, dass die Daten aller neun Teilnehmer, die ihre 24-wöchige Dosierung in der klinischen Phase-II-Studie zur immunmodulatorischen Therapie von Antisense Therapeutics, ATL1102 für DMD, abgeschlossen haben, das hervorragende Sicherheitsprofil des Arzneimittels und die positiven Arzneimittelwirkungen auf Krankheiten bestätigt haben Progressionsendpunkte bei der getesteten niedrigen Dosis. Das Unternehmen stellte fest, dass die Ergebnisse die Pläne des Unternehmens, ATL1102 in eine potenziell entscheidende klinische Phase-IIb-Studie zu überführen, weiterhin stark unterstützten. Der endgültige Studienbericht ist nach der erwarteten Sperre der Versuchsdatenbank im ersten Quartal 20 zu erstellen.
Es fanden wissenschaftliche Beratungstreffen mit drei europäischen Regulierungsbehörden statt, die sich auf das Studiendesign der Phase IIb, Dosiserhöhungspläne, die Anwendbarkeit der Studienendpunkte und die Studiendauer konzentrierten. Das Unternehmen betonte, dass die Agenturen bei den Sitzungen die vorgeschlagenen Endpunkte für die Wirksamkeit der Studie (PUL2.0, Myoset), den Sicherheitsüberwachungsplan, die Dosierungsdauer (12 Monate) und die Verwendung höherer Dosen allgemein akzeptierten. Die Agenturen haben ermutigend klargestellt, dass dies ein Weg zu einer frühzeitigen behördlichen Genehmigung positiver Ergebnisse der Phase IIb sein könnte. Der nächste Schritt besteht darin, den Entwicklungsplan mit der Europäischen Arzneimittel-Agentur zu verfolgen und nach Abschluss der Ergebnisse der aktuellen Phase-II-Studie mit der Food and Drug Administration über Entwicklungspläne für die USA zu sprechen. ATL1103 für Akromegalie ATL1103 befindet sich in der klinischen Entwicklung zur Behandlung von Akromegalie. Das Unternehmen führte eine erfolgreiche Phase-II-Studie mit ATL1103 durch, wobei die Studie ihren primären Wirksamkeitsendpunkt erreicht hatte, indem sie eine statistisch signifikante durchschnittliche Verringerung der sIGF-1-Spiegel zeigte. Der aktuelle Entwicklungsschwerpunkt des Unternehmens ist auf die klinische Entwicklung von ATL1102 bei DMD gerichtet. Das Unternehmen ist jedoch der Ansicht, dass sich in Zukunft Umstände ergeben könnten, unter denen das Unternehmen über die Kapazität und Rechtfertigung verfügt, weiterhin in die weitere klinische Entwicklung von ATL1103 zu investieren, einschließlich der Aktivierung eines Early Access-Programms (EAP). Bis zu diesem Zeitpunkt wird das Unternehmen keine weiteren Ressourcen für den EAP-Prozess einsetzen und seinen Fokus und seine Mittel weiterhin auf das ATL1102 für DMD-Programm richten. Nur für den persönlichen Gebrauch
usw.
der erste Teil - automatisch übersetzt -
----------------
Finanzielle Zusammenfassung Das Unternehmen meldete für das am 31. Dezember 2019 endende Halbjahr einen Verlust von 4.326.273 USD (einschließlich einer nicht zahlungswirksamen, vollständig amortisierten Optionsemission „Share Based Payment“ von 2.420.086 USD). Zum 31. Dezember 2019 verfügte das Unternehmen über Barreserven in Höhe von 5.128.667 USD, bevor es im Januar nach Abwicklung des Zeichnens der börsennotierten Optionen weitere 1,864 Mio. USD (vor Kosten) erhielt. Operations Summary ATL1102 für DMD Das Unternehmen führt die klinische Entwicklung von ATL1102 bei Patienten mit Duchenne-Muskeldystrophie (DMD) durch. Am 17. Dezember 2019 teilte das Unternehmen mit, dass die Daten aller neun Teilnehmer, die ihre 24-wöchige Dosierung in der klinischen Phase-II-Studie zur immunmodulatorischen Therapie von Antisense Therapeutics, ATL1102 für DMD, abgeschlossen haben, das hervorragende Sicherheitsprofil des Arzneimittels und die positiven Arzneimittelwirkungen auf Krankheiten bestätigt haben Progressionsendpunkte bei der getesteten niedrigen Dosis. Das Unternehmen stellte fest, dass die Ergebnisse die Pläne des Unternehmens, ATL1102 in eine potenziell entscheidende klinische Phase-IIb-Studie zu überführen, weiterhin stark unterstützten. Der endgültige Studienbericht ist nach der erwarteten Sperre der Versuchsdatenbank im ersten Quartal 20 zu erstellen.
Es fanden wissenschaftliche Beratungstreffen mit drei europäischen Regulierungsbehörden statt, die sich auf das Studiendesign der Phase IIb, Dosiserhöhungspläne, die Anwendbarkeit der Studienendpunkte und die Studiendauer konzentrierten. Das Unternehmen betonte, dass die Agenturen bei den Sitzungen die vorgeschlagenen Endpunkte für die Wirksamkeit der Studie (PUL2.0, Myoset), den Sicherheitsüberwachungsplan, die Dosierungsdauer (12 Monate) und die Verwendung höherer Dosen allgemein akzeptierten. Die Agenturen haben ermutigend klargestellt, dass dies ein Weg zu einer frühzeitigen behördlichen Genehmigung positiver Ergebnisse der Phase IIb sein könnte. Der nächste Schritt besteht darin, den Entwicklungsplan mit der Europäischen Arzneimittel-Agentur zu verfolgen und nach Abschluss der Ergebnisse der aktuellen Phase-II-Studie mit der Food and Drug Administration über Entwicklungspläne für die USA zu sprechen. ATL1103 für Akromegalie ATL1103 befindet sich in der klinischen Entwicklung zur Behandlung von Akromegalie. Das Unternehmen führte eine erfolgreiche Phase-II-Studie mit ATL1103 durch, wobei die Studie ihren primären Wirksamkeitsendpunkt erreicht hatte, indem sie eine statistisch signifikante durchschnittliche Verringerung der sIGF-1-Spiegel zeigte. Der aktuelle Entwicklungsschwerpunkt des Unternehmens ist auf die klinische Entwicklung von ATL1102 bei DMD gerichtet. Das Unternehmen ist jedoch der Ansicht, dass sich in Zukunft Umstände ergeben könnten, unter denen das Unternehmen über die Kapazität und Rechtfertigung verfügt, weiterhin in die weitere klinische Entwicklung von ATL1103 zu investieren, einschließlich der Aktivierung eines Early Access-Programms (EAP). Bis zu diesem Zeitpunkt wird das Unternehmen keine weiteren Ressourcen für den EAP-Prozess einsetzen und seinen Fokus und seine Mittel weiterhin auf das ATL1102 für DMD-Programm richten. Nur für den persönlichen Gebrauch
usw.
Sehr schön, mit Relay Medical zusammen der einzige grüne Lichtblick heute in meinem Depot 👌
kurz vor 12 Uhr - Diurnal testete heute schon den Widerstand bei 37 penc -
wenn es darüber geht wären die 46 Penc der nächste Widerstand - darüber die 75 Penc
Mal sehen wie hoch es mit der nächsten Meldung in den nächsten Wochen erst mal steigt.
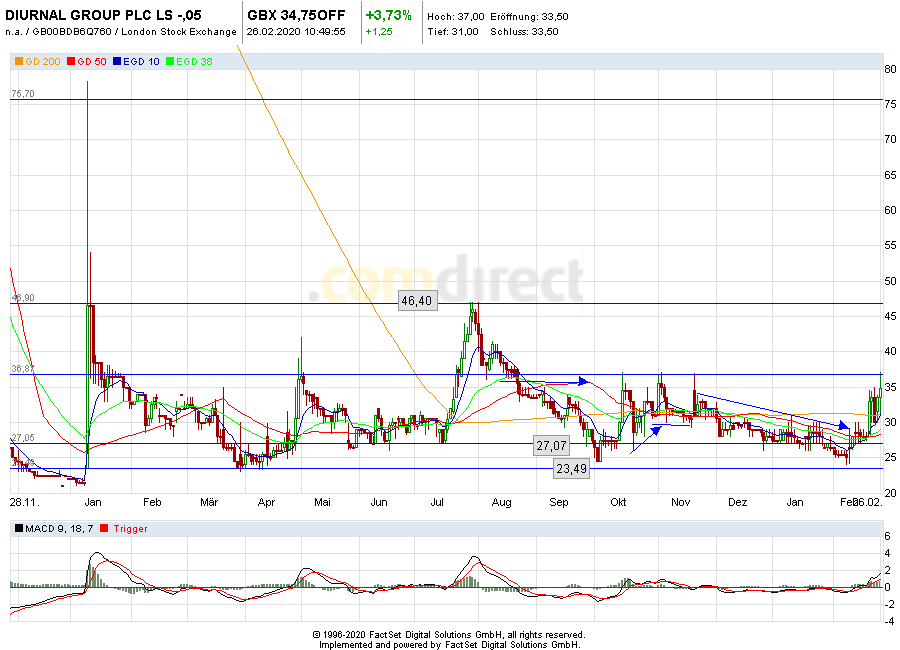
wenn es darüber geht wären die 46 Penc der nächste Widerstand - darüber die 75 Penc
Mal sehen wie hoch es mit der nächsten Meldung in den nächsten Wochen erst mal steigt.

Antwort auf Beitrag Nr.: 62.783.816 von Biohero am 25.02.20 17:24:55Diurnal scheint noch völlig unter dem Radar zu fliegen.
Ein weiterer großer Investor von DNL der seine Position um rund 340k Aktien erhöht .. Denke da wird was positives in naher Zukunft kommen
https://www.lse.co.uk/rns/DNL/holdings-in-company-6d8ghc8sea…
https://www.lse.co.uk/rns/DNL/holdings-in-company-6d8ghc8sea…
Kurz mal zur 30 Pence- Marke abgetaucht, sofort dort wieder gedreht und es wurde wieder beherzt zugegriffen. Gutes Zeichen 👌



















