Evotec 566480 - Fakten, Fakten, Fakten ... - 500 Beiträge pro Seite
eröffnet am 03.06.08 18:58:41 von
neuester Beitrag 18.02.09 17:45:59 von
neuester Beitrag 18.02.09 17:45:59 von
Beiträge: 89
ID: 1.141.759
ID: 1.141.759
Aufrufe heute: 0
Gesamt: 27.838
Gesamt: 27.838
Aktive User: 0
ISIN: DE0005664809 · WKN: 566480
9,6900
EUR
-33,06 %
-4,7850 EUR
Letzter Kurs 22:57:01 Lang & Schwarz
Neuigkeiten
11:36 Uhr · wallstreetONLINE Redaktion |
| Evotec Aktien ab 5,80 Euro handeln - Ohne versteckte Kosten!Anzeige |
19:03 Uhr · Shareribs Anzeige |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 52,00 | +92,59 | |
| 1,9000 | +59,66 | |
| 2,1600 | +29,34 | |
| 1,9200 | +23,87 | |
| 5,4500 | +19,00 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,8150 | -15,21 | |
| 2,2900 | -17,63 | |
| 2,6700 | -28,03 | |
| 9,6900 | -33,06 | |
| 5,1800 | -33,59 |
EVOTEC www.evotec.com - Portrait
Alles Wissenswerte in aller Kürze
1993 als Evotec BioSystems in Hamburg gegründet, begann die Firma Verfahren für die Biotechnologie zu entwickeln. Mitbegründer und -entwickler war der Nobelpreisträger Manfred Eigen vom Göttinger Max-Planck-Institut. In Zusammenarbeit mit dem Institut entstanden die ersten Apparaturen zur maschinellen Analyse chemischer und biologischer Substanzen - im Grunde nichts anderes als die Arbeit eines Laboranten mit der Pipette, nur in unvergleichlich größerem Maßstab.
Im Jahr 2000 schloss sich Evotec mit der englischen Oxford Asymmetry International (OAI) zusammen. 500 Millionen Euro in Aktien legten die Hamburger dafür auf den Tisch. Das Interesse galt in erster Linie der gigantischen Bibliothek mit 150.000 Testsubstanzen. Für Evotec waren diese eine entscheidende Voraussetzung, über die reine Anwendungsentwicklung hinaus eigenständig Wirkstoffe entwickeln zu können.
Die Biotech-Firma aus Hamburg feierte im November 1999 ihr Börsendebüt am Neuen Markt und machte sich einen Namen als Dienstleister, der im Auftrag von Pharma- und Biotechfirmen mit der hauseigenen Screening-Technologie Wirkstoffkandidaten für die pharmazeutische Forschung identifiziert.
http://www.evotec.com/en/partners/index.aspx
Mit diesem Geschäftsmodell schaffte Evotec nicht den Sprung in die schwarzen Zahlen, der Aktienkurs kam auch während des neuen Börsenaufschwung seit 2003 nicht in Fahrt. Die Folge: Seit 2005 befindet sich eine eigene klinische Forschungspipeline im Aufbau.
http://www.evotec.com/en/our_pipeline/index.aspx
Als aussichtsreichster Kandidat gilt ein Wirkstoff gegen Schlafstörungen, dem Experten ein Umsatzpotenzial im Milliardenbereich einräumen. Komplett wurde der Wandel zum Medikamentenentwickler im Dezember 2006, als die Gerätesparte für 23 Millionen Euro an die britische Firma ParkinElmer verkauft wurde.
Vorstandschef Jörn Aldag in einem Interview mit Börse Online:
http://www.boerse-online.de/aktien/interviews/487261.html?p=…
......
Unser festes Ziel ist es, dass unsere Forschungspipeline zum künftigen Wert-Generator wird.
Alles Wissenswerte in aller Kürze
1993 als Evotec BioSystems in Hamburg gegründet, begann die Firma Verfahren für die Biotechnologie zu entwickeln. Mitbegründer und -entwickler war der Nobelpreisträger Manfred Eigen vom Göttinger Max-Planck-Institut. In Zusammenarbeit mit dem Institut entstanden die ersten Apparaturen zur maschinellen Analyse chemischer und biologischer Substanzen - im Grunde nichts anderes als die Arbeit eines Laboranten mit der Pipette, nur in unvergleichlich größerem Maßstab.
Im Jahr 2000 schloss sich Evotec mit der englischen Oxford Asymmetry International (OAI) zusammen. 500 Millionen Euro in Aktien legten die Hamburger dafür auf den Tisch. Das Interesse galt in erster Linie der gigantischen Bibliothek mit 150.000 Testsubstanzen. Für Evotec waren diese eine entscheidende Voraussetzung, über die reine Anwendungsentwicklung hinaus eigenständig Wirkstoffe entwickeln zu können.
Die Biotech-Firma aus Hamburg feierte im November 1999 ihr Börsendebüt am Neuen Markt und machte sich einen Namen als Dienstleister, der im Auftrag von Pharma- und Biotechfirmen mit der hauseigenen Screening-Technologie Wirkstoffkandidaten für die pharmazeutische Forschung identifiziert.
http://www.evotec.com/en/partners/index.aspx
Mit diesem Geschäftsmodell schaffte Evotec nicht den Sprung in die schwarzen Zahlen, der Aktienkurs kam auch während des neuen Börsenaufschwung seit 2003 nicht in Fahrt. Die Folge: Seit 2005 befindet sich eine eigene klinische Forschungspipeline im Aufbau.
http://www.evotec.com/en/our_pipeline/index.aspx
Als aussichtsreichster Kandidat gilt ein Wirkstoff gegen Schlafstörungen, dem Experten ein Umsatzpotenzial im Milliardenbereich einräumen. Komplett wurde der Wandel zum Medikamentenentwickler im Dezember 2006, als die Gerätesparte für 23 Millionen Euro an die britische Firma ParkinElmer verkauft wurde.
Vorstandschef Jörn Aldag in einem Interview mit Börse Online:
http://www.boerse-online.de/aktien/interviews/487261.html?p=…
......
Unser festes Ziel ist es, dass unsere Forschungspipeline zum künftigen Wert-Generator wird.
http://www.welt.de/hamburg/article1154794/Hamburg_wird_zur_S…
3. September 2007
Pharmaforschung
Hamburg wird zur Spitzenadresse Europas
Unter dem Namen European Screening Port Hamburg hat jetzt ein Zentrum für die moderne Wirkstoffforschung. Sein Ziel ist es, Wirtschaft und Wissenschaft enger zu vernetzen. Der Fördertopf des Bundes ist 800 Millionen Euro schwer.
Die im Juli dieses Jahres von Bundesforschungsministerin Annette Schavan gestartete Initiative soll die Pharma-Forschung stärken.
Mit Unterstützung des Bundesministerium für Bildung und Forschung, der Stadt Hamburg, der Evotec AG und der norddeutschen Life Science Agentur Norgenta GmbH entsteht am Standort der Firma Evotec ein hochmodernes Dienstleistungszentrum für die Suche nach neuen Medikamentenwirkstoffen. Das Investitionsvolumen beträgt in der Aufbauphase bereits rund 7,4 Millionen Euro.
Hintergrund des Projekts ist die Tatsache, dass die Entwicklung eines Medikaments beispielsweise in den USA zwölf Jahre dauert und 800 Millionen Dollar oder mehr kostet. Eine der Ursachen: Nur eines von zehn Projekten auf dem Forschungssektor führt zum Erfolg. Und der Weg aus dem Labor zum Patienten ist wissenschaftlich, wirtschaftlich und bürokratisch langwierig und schwierig, sagte Evotec-Vorstandsvorsitzender Jörn Aldag.
Der in öffentlich-privater Partnerschaft betriebene European Screening Port soll nun effizient und systematisch aussichtsreiche Wirkstoffe für zukünftige Medikamente identifizieren und ihre Weiterentwicklung vorantreiben. Die Einrichtung wird Bindeglied sein zwischen Forschung und pharmazeutischer Industrie, der Screening Port ist Dienstleister und Marktplatz zugleich.
Zwei Projekte starten schon dieses Jahr
Für die Industrie bedeutet der mögliche Zugang zu den Ergebnissen eine Ergänzung zu ihrer eigenen Medikamentenforschung. Zwei Projekte starten schon dieses Jahr, bei voller Betriebskraft sollen von 2009 an pro Jahr 15 Projekte laufen.
Das Unternehmen Screening Port beschränkt sich dabei nicht nur auf deutsche Hochschulen. Zu den renommierten internationalen Partnern zählen die Eidgenössische Technische Hochschule Zürich, das Pasteur-Institut in Paris und das Karolinska Institut in Stockholm.
Initiiert wurde das Projekt von der Evotec AG, einem führenden Unternehmen der Wirkstoffforschung und -entwicklung, das seine Expertise in den Screening Port einfließen lassen wird. Die Realisierung lag bei der Norgenta, die als Clustermanager von Hamburg und Schleswig-Holstein die strukturelle Entwicklung der norddeutschen Life Science Region verantwortet.
Weitere Partner haben Interesse angemeldet. So wird sich die auf High Performance Lösungen für das Datenmanagement in den Lebenswissenschaften spezialisierte Carus IT AG beim Screening Port engagieren.
Rund 30 Arbeitsplätze entstehen mit dem Zentrum, weitere 25 im Umfeld. Doch sie werden weitere qualifizierte Arbeitsplätze in der Pharma-Branche nach sich ziehen, sagte Wirtschaftssenator Gunnar Uldall. „Mit der Errichtung des Screening Port hat Hamburg die Chance, zu einem der führenden europäischen Standorte für die moderne Wirkstoffforschung zu werden.“
Wissenschaftssenator Jörg Dräger sieht das Projekt als Meilenstein für den Ausbau des Wirtschaftszweigs Lebenswissenschaften in Norddeutschland. „Wenn hier in Zukunft Forscher die Wirkstoffe für die Medikamente von morgen entwickeln können, dann ist dies ein großer Erfolg für den Wissenschaftsstandort.“
Kathrin Adlkofer, Geschäftsführerin der Agentur unterstrich: „Unser Ziel ist vor allem, die vorhandenen Exzellenzen in Wissenschaft und Wirtschaft effektiv zusammenzuführen.“
keywordsDer Parlamentarische Staatssekretär im Bundesministerium für Bildung und Forschung, Thomas Rachel, versprach, das Ministerium werde den Aufbau dieses Dienstleistungszentrums und erste Pilotprojekte zur Wirkstoff-Untersuchung unterstützen. Rachel: „Der Screening Port ist ein wichtiges Element der Pharma-Initiative für Deutschland.“
3. September 2007
Pharmaforschung
Hamburg wird zur Spitzenadresse Europas
Unter dem Namen European Screening Port Hamburg hat jetzt ein Zentrum für die moderne Wirkstoffforschung. Sein Ziel ist es, Wirtschaft und Wissenschaft enger zu vernetzen. Der Fördertopf des Bundes ist 800 Millionen Euro schwer.
Die im Juli dieses Jahres von Bundesforschungsministerin Annette Schavan gestartete Initiative soll die Pharma-Forschung stärken.
Mit Unterstützung des Bundesministerium für Bildung und Forschung, der Stadt Hamburg, der Evotec AG und der norddeutschen Life Science Agentur Norgenta GmbH entsteht am Standort der Firma Evotec ein hochmodernes Dienstleistungszentrum für die Suche nach neuen Medikamentenwirkstoffen. Das Investitionsvolumen beträgt in der Aufbauphase bereits rund 7,4 Millionen Euro.
Hintergrund des Projekts ist die Tatsache, dass die Entwicklung eines Medikaments beispielsweise in den USA zwölf Jahre dauert und 800 Millionen Dollar oder mehr kostet. Eine der Ursachen: Nur eines von zehn Projekten auf dem Forschungssektor führt zum Erfolg. Und der Weg aus dem Labor zum Patienten ist wissenschaftlich, wirtschaftlich und bürokratisch langwierig und schwierig, sagte Evotec-Vorstandsvorsitzender Jörn Aldag.
Der in öffentlich-privater Partnerschaft betriebene European Screening Port soll nun effizient und systematisch aussichtsreiche Wirkstoffe für zukünftige Medikamente identifizieren und ihre Weiterentwicklung vorantreiben. Die Einrichtung wird Bindeglied sein zwischen Forschung und pharmazeutischer Industrie, der Screening Port ist Dienstleister und Marktplatz zugleich.
Zwei Projekte starten schon dieses Jahr
Für die Industrie bedeutet der mögliche Zugang zu den Ergebnissen eine Ergänzung zu ihrer eigenen Medikamentenforschung. Zwei Projekte starten schon dieses Jahr, bei voller Betriebskraft sollen von 2009 an pro Jahr 15 Projekte laufen.
Das Unternehmen Screening Port beschränkt sich dabei nicht nur auf deutsche Hochschulen. Zu den renommierten internationalen Partnern zählen die Eidgenössische Technische Hochschule Zürich, das Pasteur-Institut in Paris und das Karolinska Institut in Stockholm.
Initiiert wurde das Projekt von der Evotec AG, einem führenden Unternehmen der Wirkstoffforschung und -entwicklung, das seine Expertise in den Screening Port einfließen lassen wird. Die Realisierung lag bei der Norgenta, die als Clustermanager von Hamburg und Schleswig-Holstein die strukturelle Entwicklung der norddeutschen Life Science Region verantwortet.
Weitere Partner haben Interesse angemeldet. So wird sich die auf High Performance Lösungen für das Datenmanagement in den Lebenswissenschaften spezialisierte Carus IT AG beim Screening Port engagieren.
Rund 30 Arbeitsplätze entstehen mit dem Zentrum, weitere 25 im Umfeld. Doch sie werden weitere qualifizierte Arbeitsplätze in der Pharma-Branche nach sich ziehen, sagte Wirtschaftssenator Gunnar Uldall. „Mit der Errichtung des Screening Port hat Hamburg die Chance, zu einem der führenden europäischen Standorte für die moderne Wirkstoffforschung zu werden.“
Wissenschaftssenator Jörg Dräger sieht das Projekt als Meilenstein für den Ausbau des Wirtschaftszweigs Lebenswissenschaften in Norddeutschland. „Wenn hier in Zukunft Forscher die Wirkstoffe für die Medikamente von morgen entwickeln können, dann ist dies ein großer Erfolg für den Wissenschaftsstandort.“
Kathrin Adlkofer, Geschäftsführerin der Agentur unterstrich: „Unser Ziel ist vor allem, die vorhandenen Exzellenzen in Wissenschaft und Wirtschaft effektiv zusammenzuführen.“
keywordsDer Parlamentarische Staatssekretär im Bundesministerium für Bildung und Forschung, Thomas Rachel, versprach, das Ministerium werde den Aufbau dieses Dienstleistungszentrums und erste Pilotprojekte zur Wirkstoff-Untersuchung unterstützen. Rachel: „Der Screening Port ist ein wichtiges Element der Pharma-Initiative für Deutschland.“
http://www.welt.de/hamburg/article1205504/Evotec_konzentrier…
Evotec konzentriert sich auf neues Medikament
Es ist ein Wettlauf mit der Zeit, den Evotec gewinnen muss. Denn Geld hat die Hamburger Biotech-Firma bislang noch nicht verdient. Das könnte sich ändern. Derzeit testen die Hamburger ein neues Schlafmittel – mit großem Erfolg.
Bangen bei Evotec: Das neue Schlafmittel kann auch noch in der Phase III zurückgezogen werden. Dann wären alle bis dahin getätigten Investitionen umsonst gewesen
Mehr als 40 Millionen Euro investiert das Hamburger Biotech-Unternehmen jährlich in die Erforschung eigener Wirkstoffe, die zu neuen Medikamenten führen sollen. Noch sind die Einnahmen gering, die Ausgaben aber enorm hoch. Wie lange das Kapital vorhält, bleibt die entscheidende Frage.
„Wir sind sehr optimistisch für unsere Wirkstoffe“, sagt Evotec-Vorstand Jörn Aldag. Größte Hoffnung setzt der Firmenchef auf das Schlafmittel EVT 201. Das Medikament habe in einer klinischen Studie der sogenannten Phase II, in der es erstmals am Patienten erprobt wurde, „sehr robuste“ Ergebnisse bei der Einschlaf- und Durchschlafzeit gezeigt. Von den befragten Testpersonen hätten 80 Prozent am nächsten Morgen ein subjektiv „sehr gutes Schlafgefühl“ verspürt.
Auch auffällige Nachwirkungen seien bislang nicht festgestellt worden. „Es ist sehr wichtig, dass Patienten ihr Medikament mögen“, sagt Aldag. Das Durchschlafverhalten der Probanden sei nach Einnahme von EVT 201 gegenüber Vergleichsprodukten wesentlich besser. „Unser neuer Stoff ist über die ganze Nacht hochwirksam“, so Aldag. Die Konkurrenz schaffe nur vier bis fünf Stunden.
Entscheidende Testgruppe
Im Oktober erwartet Aldag die Daten einer weiteren Studie, diesmal mit Patienten, die älter als 65 Jahre sind und unter chronischen Schlafstörungen leiden. Gerade für diese Altersgruppe sei der Bedarf nach besseren Alternativen besonders groß. „Daher haben wir uns für diese Tests entschieden“, sagt der Evotec-Chef. Sein Unternehmen prüfe außerdem, ob möglicherweise für alle Altersgruppen das Medikament in der gleichen Dosierung verabreicht werden könne. Das sei untypisch, da sich bei älteren Menschen der Stoffwechsel verlangsame. Für den Arzt sei eine identische Dosierung aber sehr praktisch, sagt Aldag. „Unser Mittel soll auch vom Allgemeinmediziner verschrieben werden.“
Vor allem auf dem US-Markt will Evotec mit dem Schlafmittel punkten. Dort werden derartige Arzneien jährlich für mehr als 3,5 Milliarden Dollar verkauft. „In den USA dürfen Medikamente direkt in die Werbung gehen“, sagt Aldag. In Deutschland sei dies nicht möglich. Analysten schätzen das Verkaufsvolumen für das Evotec-Medikament auf 500 Millionen bis über eine Milliarde US-Dollar pro Jahr.
Um dieses Volumen ausschöpfen zu können, ist ein starker Vertrieb nötig. Diesen habe Evotec in Amerika nicht, sagt Aldag. „Wir benötigen die Marketingpower und das weltweite Vertriebsnetz eines großen Konzerns.“ Daher führt Evotec Verhandlungen mit verschiedenen Unternehmen, darunter auch einigen Pharma-Riesen, über den Verkauf der Wirkstoff-Lizenz. Ziel sei es, möglichst vielen Firmen die Substanz vorzustellen. In einer Art Auktion soll dann der Meistbietende den Zuschlag erhalten.
Evotec will US-Markt erobern
Da trifft es sich gut, dass die Hamburger auf dem US-Markt Flagge zeigen. Vor wenigen Tagen hatte Evotec angekündigt, das amerikanische Pharmaunternehmen Renovis per Aktientausch im Wert von rund 150 Millionen Dollar zu übernehmen. „Der Biotech-Markt spielt zu 70 Prozent in den USA“, sagt Aldag. Evotec sei jetzt dort präsent, wo auch die großen Investoren sitzen. Außerdem soll die Hamburger Firma künftig auch an der Technologiebörse Nasdaq notiert werden.
Durch den Zusammenschluss mit Renovis will Evotec aber vor allem seine Forschung stärken. „Im Gegensatz zu anderen Firmen setzen wir nicht nur auf ein Medikament“, sagt Aldag. Die Hamburger gewinnen mehrere Wirkstoffkandidaten zur Behandlung von Schmerzen und Entzündungskrankheiten hinzu. Bereits Ende 2008 sollen mindestens fünf Medikamentenprogramme in der klinischen Entwicklung sein.
„Zudem bringt Renovis einen ordentlichen Cashbetrag ein, sodass wir die Projekte gut durchfinanzieren können“, sagt Aldag. Im August hatten die Kalifornier ein Barvermögen von 87 Millionen Dollar. Zusammen kämen beide Firmen auf Finanzmittel von 175 Millionen Dollar. Weitere 60 Millionen Dollar erwartet Evotec durch den kürzlich angekündigten Verkauf seiner chemischen Entwicklung.
Langer Atem
Da das kombinierte Unternehmen zunächst noch nicht profitabel arbeiten werde, sei es für die nächsten Jahre „sehr gut finanziert“, betont Aldag. „Durch unsere sichere Cash-Decke haben wir eine gute Position in den Preisverhandlungen mit einem künftigen Partner.“
Derzeit bereitet Evotec den Hoffnungsträger EVT 201 für die eine Studie der Phase III vor. In diesem Stadium wird die Langzeitwirkung am Menschen geprüft. Neue Medikamente müssen drei klinische Phasen am Menschen vor einem Zulassungsantrag bestehen. Kosten von 100 Millionen Euro sind im dritten Stadium nicht ungewöhnlich. Solche Mittel hat Evotec aber nicht. Auch deswegen müssen die Hamburger einen Partner finden. Im kommenden Jahr sollen die weltweiten Rechte an einen Pharmakonzern gehen.
Zu den Vertragsbedingungen machte Aldag keine Angaben. Er sagte aber, dass in der Regel bei solchen Vereinbarungen deutlich zweistellige Millionenbeträge als Voraus- und Meilensteinzahlungen zu erwarten seien. Am lukrativsten könnten sich die prozentual zweistelligen Umsatzbeteiligungen herausstellen, wenn das Medikament sich zu einem Erfolg entwickelt.
Bei geschätzten 500 Millionen Euro Jahresumsatz könnten dann 50 Millionen Euro in die Evotec-Kasse fließen – pro Jahr. „Damit allein könnten wir unsere jährlichen Forschungsaufwendungen bestreiten“, sagt Aldag. Aber so weit sei es noch nicht. „Ich rechne mit einer Marktreife nicht vor 2011.“ Das hänge auch davon ab, mit welchem Tempo der künftige Lizenznehmer die Phase III betreibe. Käme das Medikament 2011 auf den Markt, würde es bis mindestens 2020 unter Patentschutz stehen.
Evotec konzentriert sich auf neues Medikament
Es ist ein Wettlauf mit der Zeit, den Evotec gewinnen muss. Denn Geld hat die Hamburger Biotech-Firma bislang noch nicht verdient. Das könnte sich ändern. Derzeit testen die Hamburger ein neues Schlafmittel – mit großem Erfolg.
Bangen bei Evotec: Das neue Schlafmittel kann auch noch in der Phase III zurückgezogen werden. Dann wären alle bis dahin getätigten Investitionen umsonst gewesen
Mehr als 40 Millionen Euro investiert das Hamburger Biotech-Unternehmen jährlich in die Erforschung eigener Wirkstoffe, die zu neuen Medikamenten führen sollen. Noch sind die Einnahmen gering, die Ausgaben aber enorm hoch. Wie lange das Kapital vorhält, bleibt die entscheidende Frage.
„Wir sind sehr optimistisch für unsere Wirkstoffe“, sagt Evotec-Vorstand Jörn Aldag. Größte Hoffnung setzt der Firmenchef auf das Schlafmittel EVT 201. Das Medikament habe in einer klinischen Studie der sogenannten Phase II, in der es erstmals am Patienten erprobt wurde, „sehr robuste“ Ergebnisse bei der Einschlaf- und Durchschlafzeit gezeigt. Von den befragten Testpersonen hätten 80 Prozent am nächsten Morgen ein subjektiv „sehr gutes Schlafgefühl“ verspürt.
Auch auffällige Nachwirkungen seien bislang nicht festgestellt worden. „Es ist sehr wichtig, dass Patienten ihr Medikament mögen“, sagt Aldag. Das Durchschlafverhalten der Probanden sei nach Einnahme von EVT 201 gegenüber Vergleichsprodukten wesentlich besser. „Unser neuer Stoff ist über die ganze Nacht hochwirksam“, so Aldag. Die Konkurrenz schaffe nur vier bis fünf Stunden.
Entscheidende Testgruppe
Im Oktober erwartet Aldag die Daten einer weiteren Studie, diesmal mit Patienten, die älter als 65 Jahre sind und unter chronischen Schlafstörungen leiden. Gerade für diese Altersgruppe sei der Bedarf nach besseren Alternativen besonders groß. „Daher haben wir uns für diese Tests entschieden“, sagt der Evotec-Chef. Sein Unternehmen prüfe außerdem, ob möglicherweise für alle Altersgruppen das Medikament in der gleichen Dosierung verabreicht werden könne. Das sei untypisch, da sich bei älteren Menschen der Stoffwechsel verlangsame. Für den Arzt sei eine identische Dosierung aber sehr praktisch, sagt Aldag. „Unser Mittel soll auch vom Allgemeinmediziner verschrieben werden.“
Vor allem auf dem US-Markt will Evotec mit dem Schlafmittel punkten. Dort werden derartige Arzneien jährlich für mehr als 3,5 Milliarden Dollar verkauft. „In den USA dürfen Medikamente direkt in die Werbung gehen“, sagt Aldag. In Deutschland sei dies nicht möglich. Analysten schätzen das Verkaufsvolumen für das Evotec-Medikament auf 500 Millionen bis über eine Milliarde US-Dollar pro Jahr.
Um dieses Volumen ausschöpfen zu können, ist ein starker Vertrieb nötig. Diesen habe Evotec in Amerika nicht, sagt Aldag. „Wir benötigen die Marketingpower und das weltweite Vertriebsnetz eines großen Konzerns.“ Daher führt Evotec Verhandlungen mit verschiedenen Unternehmen, darunter auch einigen Pharma-Riesen, über den Verkauf der Wirkstoff-Lizenz. Ziel sei es, möglichst vielen Firmen die Substanz vorzustellen. In einer Art Auktion soll dann der Meistbietende den Zuschlag erhalten.
Evotec will US-Markt erobern
Da trifft es sich gut, dass die Hamburger auf dem US-Markt Flagge zeigen. Vor wenigen Tagen hatte Evotec angekündigt, das amerikanische Pharmaunternehmen Renovis per Aktientausch im Wert von rund 150 Millionen Dollar zu übernehmen. „Der Biotech-Markt spielt zu 70 Prozent in den USA“, sagt Aldag. Evotec sei jetzt dort präsent, wo auch die großen Investoren sitzen. Außerdem soll die Hamburger Firma künftig auch an der Technologiebörse Nasdaq notiert werden.
Durch den Zusammenschluss mit Renovis will Evotec aber vor allem seine Forschung stärken. „Im Gegensatz zu anderen Firmen setzen wir nicht nur auf ein Medikament“, sagt Aldag. Die Hamburger gewinnen mehrere Wirkstoffkandidaten zur Behandlung von Schmerzen und Entzündungskrankheiten hinzu. Bereits Ende 2008 sollen mindestens fünf Medikamentenprogramme in der klinischen Entwicklung sein.
„Zudem bringt Renovis einen ordentlichen Cashbetrag ein, sodass wir die Projekte gut durchfinanzieren können“, sagt Aldag. Im August hatten die Kalifornier ein Barvermögen von 87 Millionen Dollar. Zusammen kämen beide Firmen auf Finanzmittel von 175 Millionen Dollar. Weitere 60 Millionen Dollar erwartet Evotec durch den kürzlich angekündigten Verkauf seiner chemischen Entwicklung.
Langer Atem
Da das kombinierte Unternehmen zunächst noch nicht profitabel arbeiten werde, sei es für die nächsten Jahre „sehr gut finanziert“, betont Aldag. „Durch unsere sichere Cash-Decke haben wir eine gute Position in den Preisverhandlungen mit einem künftigen Partner.“
Derzeit bereitet Evotec den Hoffnungsträger EVT 201 für die eine Studie der Phase III vor. In diesem Stadium wird die Langzeitwirkung am Menschen geprüft. Neue Medikamente müssen drei klinische Phasen am Menschen vor einem Zulassungsantrag bestehen. Kosten von 100 Millionen Euro sind im dritten Stadium nicht ungewöhnlich. Solche Mittel hat Evotec aber nicht. Auch deswegen müssen die Hamburger einen Partner finden. Im kommenden Jahr sollen die weltweiten Rechte an einen Pharmakonzern gehen.
Zu den Vertragsbedingungen machte Aldag keine Angaben. Er sagte aber, dass in der Regel bei solchen Vereinbarungen deutlich zweistellige Millionenbeträge als Voraus- und Meilensteinzahlungen zu erwarten seien. Am lukrativsten könnten sich die prozentual zweistelligen Umsatzbeteiligungen herausstellen, wenn das Medikament sich zu einem Erfolg entwickelt.
Bei geschätzten 500 Millionen Euro Jahresumsatz könnten dann 50 Millionen Euro in die Evotec-Kasse fließen – pro Jahr. „Damit allein könnten wir unsere jährlichen Forschungsaufwendungen bestreiten“, sagt Aldag. Aber so weit sei es noch nicht. „Ich rechne mit einer Marktreife nicht vor 2011.“ Das hänge auch davon ab, mit welchem Tempo der künftige Lizenznehmer die Phase III betreibe. Käme das Medikament 2011 auf den Markt, würde es bis mindestens 2020 unter Patentschutz stehen.
http://www.focus.de/finanzen/boerse/evotec-code-evt201_aid_2…
26.03.08
Die Biotech-Firma verhandelt mit den Größen der Pharma-Branche. Ein Millionendeal ist greifbar
Von FOCUS-Money-Redakteur Clemens Schömann-Finck
Die Zukunft trägt den Namen EVT201 – zumindest bei Evotec. Auf diesen sechs Zeichen ruht die Hoffnung des Managements, um sie dreht sich die Fantasie der Investoren. Von dieser Kombination sagt Evotec-Chef Jörn Aldag, sie sei nahe am Optimum.
Die Phase II. Ein Schlafmittel verbirgt sich hinter dem Kürzel EVT201. Im Herbst vergangenen Jahres schloss die Biotech-Firma für das Medikament die sogenannte Phase II ab. In dieser Entwicklungsstufe testen Wissenschaftler die Wirksamkeit eines neuen Präparats an einer kleinen Patientengruppe. Ergebnis: sehr gute Verträglichkeit, sehr gutes Einschlafen und sehr gutes Durchschlafen der Probanden. „In allen wichtigen Aspekten überzeugt EVT201“, urteilt Sal.-Oppenheim-Analyst Christian Peter. „EVT201 hat das Potenzial, einen neuen Maßstab zu setzen.“ Peter prognostiziert für das Medikament Spitzenumsätze von 900 Millionen Euro. Sein Kursziel: 3,80 Euro, mehr als doppelt so viel wie der aktuelle Wert der Aktie.
Evotec-Chef Aldag sucht noch nach ei-nem Partner für das Schlafmittel. Pharma-Konzerne zahlen meist hohe Millionenbeträge für die Rechte an aussichtsreichen Medikamentenentwicklungen und billigen Umsatzbeteiligungen im zweistelligen Prozentbereich zu. Auch wenn Aldag keine näheren Angaben machen will, erwarten einige Beobachter den Vertragsabschluss bis zum Sommer dieses Jahres. „Gelingt die Verpartnerung, wäre das ein Meilenstein in der Entwicklung von Evotec“, sagt Hanns Frohnmeyer, Analyst bei der Landesbank Baden-Württemberg.
Ähnliche Partnerschaften strebt Aldag auch für andere Wirkstoffe der Evotec-Pipeline an. Am weitesten fortgeschritten sind EVT101, das gegen Schmerzen und Alzheimer getestet wird (Phase I), und EVT302, ein Mittel zur Raucherentwöhnung (Phase II). Bis zum Zulassungsantrag muss ein neu entwickeltes Medikament insgesamt drei Teststadien durchlaufen. In der Phase I stehen mögliche Nebenwirkungen im Vordergrund, in den Phasen II und III Wirksamkeit und Dosierung. Mit jeder neuen Entwicklungsstufe sinkt das Risiko eines Fehlschlags. „Bei EVT302 werden wir dieses Jahr die Phase II beenden und dann einen Partner suchen“, sagt Aldag zu FOCUS-MONEY. „Für EVT101 gibt es schon ein großes Interesse in der Pharma-Industrie.“
Reichlich Reserven. Unter Druck steht Evotec bei der Partnersuche nicht. Die Firma ist solide finanziert und nicht auf schnelle Finanzspritzen angewiesen. Auch ohne Arznei auf dem Markt verdient das Unternehmen Geld: Zweites Geschäftsfeld ist neben der Medikamentenentwicklung das Service-Segment. Für andere Pharma-Unternehmen übernimmt Evotec Aufgaben wie das Prüfen und Herstellen von Proben. Außerdem schlummerten zwischen 93 und 98 Millionen Euro am Jahresende in der Kasse. Die Zahlen für 2007 veröffentlicht Evotec am 28. März.
Lukrative Zusammenarbeit. Klappt die im September vergangenen Jahres angekündigte Übernahme von Renovis, kämen noch weitere 87 Millionen Dollar (55 Millionen Euro) aus der Kasse des amerikanischen Biotech-Unternehmens hinzu. Außerdem bringt Renovis vier Wirkstoffkandidaten im frühen Entwicklungsstadium mit. Bei zweien davon will Aldag in diesem Jahr mit der Phase I beginnen. An einem der beiden Moleküle, dem Schmerzmittel VR1, ist bereits der US-Pharma-Riese Pfizer beteiligt. Bis zu 170 Millionen Dollar an Prämien kann Evotec im Erfolgsfall diese Partnerschaft einbringen.
Im Mai werden die Aktionäre von Renovis voraussichtlich über die Übernahme entscheiden. Evotec will diese über einen Aktientausch im Wert von 151 Millionen Dollar finanzieren. Eine Zustimmung gilt als wahrscheinlich. Das neue Unternehmen hätte 108 Millionen Aktien, rund 45 Prozent mehr als Evotec bisher. Ihr Handel soll auf beiden Seiten des Atlantik möglich sein. Aldag hat für seine Firma bei der amerikanischen Börsenaufsicht ein Listing an der Technologiebörse Nasdaq beantragt. Für Ende März oder Anfang April rechnet er mit der Zulassung. „Wir wollen uns als globales Unternehmen positionieren und dem amerikanischen Markt näher sein“, begründet Aldag den Schritt. „Der Biotech-Markt spielt zu 70 Prozent in den USA, dort sitzen die großen Investoren.“ Hohe zusätzliche Kosten erwartet er nicht, da Evotec schon jetzt die US-Auflagen erfülle.
Zurück in den TecDax. Das neue Unternehmen hätte bei dem momentanen Evotec-Aktienkurs eine Marktkapitalisierung von rund 180 Millionen Euro. Aldag sieht seine Firma damit wieder als Anwärter für den TecDax. Im März 2007 hatte Evotec seinen Platz in dem Index verloren. „Wir sind ein ernst zu nehmender Kandidat“, gibt er sich selbstbewusst.
EVT201 – Gut geregelter Schlaf
Wie ein Regler oder Lichtdimmer funktionieren Schlafmittel. Der Mechanismus nennt sich allosterische Modulation. Dabei wird mit Hilfe eines Moleküls ein Signal verstärkt oder abgeschwächt. Schlafmittel potenzieren die Wirkung der „Schlafbotenstoffe“ und sorgen so dafür, dass der Körper trotz Lärm oder Stress doch noch in den Ruhemodus wechselt. Das Besondere an EVT201 ist, dass es sich dabei um einen partiellen allosterischen Modulator handelt. Er wirkt schon in geringer Menge und ist bei einem bestimmten Niveau „abgeriegelt“. So wird eine falsche Dosierung verhindert. Zusätzlich ist die Halbwertszeit von EVT201 fast doppelt so hoch wie die anderer Medikamente. Der Wirkstoff blieb in den Tests länger im Körper und ließ die Probanden die ganze Nacht durchschlafen.
DIE AKTIE – Boden gefunden
Der Rutsch, der der Evotec-Aktie seit Herbst vergangenen Jahres einen Verlust von fast 50 Prozent gebracht hat, scheint gestoppt. Mittlerweile hat sich der Wert des Papiers bei etwa 1,70 Euro stabilisiert. Den Abwärtstrend brechen konnte es bisher aber nicht.
Gelingt die Verpartnerung von EVT201, dürfte das einen deutlichen Aufwärtsimpuls für die Aktie bedeuten. Im Bewertungsmodell von Sal. Oppenheim ist das Schlafmittel mit einem Wert von einem Euro je Aktie das wichtigste Produkt aus der Pipeline. Große Bedeutung für das Kursziel von 3,80 Euro hat auch das Molekül EVT101, das Evotec für verschiedene Indikationen testet. Mit insgesamt 70 Cent je Aktie fließt es in die Berechnung des fairen Wertes mit ein. Das Service-Geschäft bekommt 1,90 Euro pro Anteilschein in dem Modell zugeschrieben.
Bemerkenswert sind bei Evotec die Liquiditätsreserven von geschätzten 93 bis 98 Millionen Euro zum Jahresende 2007. Pro Aktie liegen sie zwischen 1,25 und 1,32 Euro. Nach der Fusion mit Renovis wird sich der Kassenbestand noch weiter verbessern. Die 55 Millionen Euro der US-Firma mitgerechnet, liegt sein Wert bei dann 108 Millionen Aktien zwischen 1,37 Euro und 1,41 Euro je Papier.
26.03.08
Die Biotech-Firma verhandelt mit den Größen der Pharma-Branche. Ein Millionendeal ist greifbar
Von FOCUS-Money-Redakteur Clemens Schömann-Finck
Die Zukunft trägt den Namen EVT201 – zumindest bei Evotec. Auf diesen sechs Zeichen ruht die Hoffnung des Managements, um sie dreht sich die Fantasie der Investoren. Von dieser Kombination sagt Evotec-Chef Jörn Aldag, sie sei nahe am Optimum.
Die Phase II. Ein Schlafmittel verbirgt sich hinter dem Kürzel EVT201. Im Herbst vergangenen Jahres schloss die Biotech-Firma für das Medikament die sogenannte Phase II ab. In dieser Entwicklungsstufe testen Wissenschaftler die Wirksamkeit eines neuen Präparats an einer kleinen Patientengruppe. Ergebnis: sehr gute Verträglichkeit, sehr gutes Einschlafen und sehr gutes Durchschlafen der Probanden. „In allen wichtigen Aspekten überzeugt EVT201“, urteilt Sal.-Oppenheim-Analyst Christian Peter. „EVT201 hat das Potenzial, einen neuen Maßstab zu setzen.“ Peter prognostiziert für das Medikament Spitzenumsätze von 900 Millionen Euro. Sein Kursziel: 3,80 Euro, mehr als doppelt so viel wie der aktuelle Wert der Aktie.
Evotec-Chef Aldag sucht noch nach ei-nem Partner für das Schlafmittel. Pharma-Konzerne zahlen meist hohe Millionenbeträge für die Rechte an aussichtsreichen Medikamentenentwicklungen und billigen Umsatzbeteiligungen im zweistelligen Prozentbereich zu. Auch wenn Aldag keine näheren Angaben machen will, erwarten einige Beobachter den Vertragsabschluss bis zum Sommer dieses Jahres. „Gelingt die Verpartnerung, wäre das ein Meilenstein in der Entwicklung von Evotec“, sagt Hanns Frohnmeyer, Analyst bei der Landesbank Baden-Württemberg.
Ähnliche Partnerschaften strebt Aldag auch für andere Wirkstoffe der Evotec-Pipeline an. Am weitesten fortgeschritten sind EVT101, das gegen Schmerzen und Alzheimer getestet wird (Phase I), und EVT302, ein Mittel zur Raucherentwöhnung (Phase II). Bis zum Zulassungsantrag muss ein neu entwickeltes Medikament insgesamt drei Teststadien durchlaufen. In der Phase I stehen mögliche Nebenwirkungen im Vordergrund, in den Phasen II und III Wirksamkeit und Dosierung. Mit jeder neuen Entwicklungsstufe sinkt das Risiko eines Fehlschlags. „Bei EVT302 werden wir dieses Jahr die Phase II beenden und dann einen Partner suchen“, sagt Aldag zu FOCUS-MONEY. „Für EVT101 gibt es schon ein großes Interesse in der Pharma-Industrie.“
Reichlich Reserven. Unter Druck steht Evotec bei der Partnersuche nicht. Die Firma ist solide finanziert und nicht auf schnelle Finanzspritzen angewiesen. Auch ohne Arznei auf dem Markt verdient das Unternehmen Geld: Zweites Geschäftsfeld ist neben der Medikamentenentwicklung das Service-Segment. Für andere Pharma-Unternehmen übernimmt Evotec Aufgaben wie das Prüfen und Herstellen von Proben. Außerdem schlummerten zwischen 93 und 98 Millionen Euro am Jahresende in der Kasse. Die Zahlen für 2007 veröffentlicht Evotec am 28. März.
Lukrative Zusammenarbeit. Klappt die im September vergangenen Jahres angekündigte Übernahme von Renovis, kämen noch weitere 87 Millionen Dollar (55 Millionen Euro) aus der Kasse des amerikanischen Biotech-Unternehmens hinzu. Außerdem bringt Renovis vier Wirkstoffkandidaten im frühen Entwicklungsstadium mit. Bei zweien davon will Aldag in diesem Jahr mit der Phase I beginnen. An einem der beiden Moleküle, dem Schmerzmittel VR1, ist bereits der US-Pharma-Riese Pfizer beteiligt. Bis zu 170 Millionen Dollar an Prämien kann Evotec im Erfolgsfall diese Partnerschaft einbringen.
Im Mai werden die Aktionäre von Renovis voraussichtlich über die Übernahme entscheiden. Evotec will diese über einen Aktientausch im Wert von 151 Millionen Dollar finanzieren. Eine Zustimmung gilt als wahrscheinlich. Das neue Unternehmen hätte 108 Millionen Aktien, rund 45 Prozent mehr als Evotec bisher. Ihr Handel soll auf beiden Seiten des Atlantik möglich sein. Aldag hat für seine Firma bei der amerikanischen Börsenaufsicht ein Listing an der Technologiebörse Nasdaq beantragt. Für Ende März oder Anfang April rechnet er mit der Zulassung. „Wir wollen uns als globales Unternehmen positionieren und dem amerikanischen Markt näher sein“, begründet Aldag den Schritt. „Der Biotech-Markt spielt zu 70 Prozent in den USA, dort sitzen die großen Investoren.“ Hohe zusätzliche Kosten erwartet er nicht, da Evotec schon jetzt die US-Auflagen erfülle.
Zurück in den TecDax. Das neue Unternehmen hätte bei dem momentanen Evotec-Aktienkurs eine Marktkapitalisierung von rund 180 Millionen Euro. Aldag sieht seine Firma damit wieder als Anwärter für den TecDax. Im März 2007 hatte Evotec seinen Platz in dem Index verloren. „Wir sind ein ernst zu nehmender Kandidat“, gibt er sich selbstbewusst.
EVT201 – Gut geregelter Schlaf
Wie ein Regler oder Lichtdimmer funktionieren Schlafmittel. Der Mechanismus nennt sich allosterische Modulation. Dabei wird mit Hilfe eines Moleküls ein Signal verstärkt oder abgeschwächt. Schlafmittel potenzieren die Wirkung der „Schlafbotenstoffe“ und sorgen so dafür, dass der Körper trotz Lärm oder Stress doch noch in den Ruhemodus wechselt. Das Besondere an EVT201 ist, dass es sich dabei um einen partiellen allosterischen Modulator handelt. Er wirkt schon in geringer Menge und ist bei einem bestimmten Niveau „abgeriegelt“. So wird eine falsche Dosierung verhindert. Zusätzlich ist die Halbwertszeit von EVT201 fast doppelt so hoch wie die anderer Medikamente. Der Wirkstoff blieb in den Tests länger im Körper und ließ die Probanden die ganze Nacht durchschlafen.
DIE AKTIE – Boden gefunden
Der Rutsch, der der Evotec-Aktie seit Herbst vergangenen Jahres einen Verlust von fast 50 Prozent gebracht hat, scheint gestoppt. Mittlerweile hat sich der Wert des Papiers bei etwa 1,70 Euro stabilisiert. Den Abwärtstrend brechen konnte es bisher aber nicht.
Gelingt die Verpartnerung von EVT201, dürfte das einen deutlichen Aufwärtsimpuls für die Aktie bedeuten. Im Bewertungsmodell von Sal. Oppenheim ist das Schlafmittel mit einem Wert von einem Euro je Aktie das wichtigste Produkt aus der Pipeline. Große Bedeutung für das Kursziel von 3,80 Euro hat auch das Molekül EVT101, das Evotec für verschiedene Indikationen testet. Mit insgesamt 70 Cent je Aktie fließt es in die Berechnung des fairen Wertes mit ein. Das Service-Geschäft bekommt 1,90 Euro pro Anteilschein in dem Modell zugeschrieben.
Bemerkenswert sind bei Evotec die Liquiditätsreserven von geschätzten 93 bis 98 Millionen Euro zum Jahresende 2007. Pro Aktie liegen sie zwischen 1,25 und 1,32 Euro. Nach der Fusion mit Renovis wird sich der Kassenbestand noch weiter verbessern. Die 55 Millionen Euro der US-Firma mitgerechnet, liegt sein Wert bei dann 108 Millionen Aktien zwischen 1,37 Euro und 1,41 Euro je Papier.
http://www.ad-hoc-news.de/CorporateNews/de/16089462/Evotecs+…
28. März 2008
Evotecs EVT 101 gelangt ins menschliche Gehirn und moduliert die Hirnaktivität während der Durchführung kognitiver Aufgaben
Corporate news- Mitteilung verarbeitet und übermittelt durch Hugin. Für den Inhalt der Mitteilung ist der Emittent verantwortlich.
Corporate news- Mitteilung verarbeitet und übermittelt durch Hugin.Für den Inhalt der Mitteilung ist der Emittent verantwortlich. - Vorläufige Ergebnisse der Einzeldosis-fMRI-Studie an gesundenProbanden -- Dosierungsphase der vierwöchigen Studie mit höherer Mehrfachdosisabgeschlossen -Hamburg, Deutschland | Oxford, England - Evotec AG (Deutsche Börse:EVT) gab heute bekannt, dass vorläufige Ergebnisse einer doppeltverblindeten, dreiarmigen Crossover-Studie mit einer Einzeldosis vonEVT 101, ihres oral verfügbaren, für den NR2B-Subtyp desNMDA-Rezeptors selektiven Antagonisten vorliegen. Die Studie wurde an19 jungen und gesunden Probanden im Centre for Neuroimaging Sciencesdes Institute of Psychiatry am King's College in London durchgeführt.Dabei wurden bildgebende Verfahren der funktionellenMagnetresonanztomographie (fMRI) eingesetzt, um Kurzzeiteffekte vonzwei Dosen EVT 101 bzw.
Placebo zu untersuchen. Dabei wurden dieAuswirkungen des Wirkstoffs auf bestimmte kognitive Leistungen,Veränderungen der lokalen zerebralen Durchblutung, die dieAktivierung bzw. Deaktivierung von Neuronen während der Durchführungkognitiver Aufgaben anzeigen sowie die basale Durchblutung inverschiedenen Hirnregionen ermittelt.Alle Behandlungen wurden gut vertragen und bestätigen frühereErfahrungen mit gesunden Versuchspersonen.Während es keine Hinweise für eine akute Verbesserung von kognitivenFunktionen gab - kein unerwarteter Befund bei jungen, gesundenProbanden, die zumeist ohnehin optimale Leistungen erbringen - wurdebeobachtet, dass bestimmte Hirnareale, die eine Rolle für das Abrufenvon Gedächtnisinhalten spielen, durch EVT 101 selektive Veränderungender zerebralen Durchblutung zeigten, während bestimmte kognitiveAufgaben durchgeführt wurden.Zudem zeigte eine Analyse der Veränderungen der basalen lokalenHirndurchblutung einen selektiven Anstieg der Durchblutung in einerbestimmten Region der Hirnrinde, die reich an NMDA-Rezeptoren ist undzur Behandlung von Erkrankungen wie z. B. neuropathische Schmerzenund Depressionen für wichtig erachtet wird. Die basale Durchblutunganderer Hirnregionen blieb unverändert.Diese Ergebnisse belegen zum ersten Mal eine Wirkung von EVT 101 aufdas menschliche Gehirn; noch dazu in Dosierungen, die gut verträglichsind und als klinisch relevant erachtet werden.Darüber hinaus hat Evotec die Dosierungsphase seiner vierwöchigenStudie mit wiederholter, höherer Dosierung erfolgreich abgeschlossen.Diese Studie wird in Frankreich durchgeführt. Erfreulicherweisezeigten erste vorläufige Ergebnisse hinsichtlich der Verfügbarkeitvon EVT 101 in der Zerebrospinalflüssigkeit, dass EVT 101 dortKonzentrationen erreicht, von denen angenommen wird, dass sieNMDA-Rezeptoren vom Typ NR2B in signifikant höherem Ausmaß blockierenals Memantin in der für die Alzheimer'sche Erkrankung üblichentherapeutischen Dosierung. Dies ergab die Auswertung einerUntergruppe, die EVT 101 erhalten hatte."Diese Daten sind sehr erfreulich. Sie zeigen, dass EVT 101 inDosierungen, die vom Menschen gut vertragen und als klinisch relevanterachtet werden, Aktivität in Hirnregionen aufzeigt, die für dieSchmerzbekämpfung als relevant erachtet werden", kommentierte Dr. TimTasker, Executive Vice President Clinical Development der Evotec AG."Vor allem sehen wir dabei auch einen Einfluss auf die Aktivitätspezifischer Hirnregionen während der Durchführung kognitiverAufgaben, die bei der Alzheimer'schen Erkrankung eine Rolle spielen."Dr. Mitul Mehta, akademischer Forschungsleiter für dieses Projekt amCentre for Neuroimaging Sciences des Institute of Psychiatry amKing's College London, fügte hinzu: "Wir haben in unseren Studiensowohl einen direkten dosisabhängigen Effekt von EVT 101 auf dasGehirn als auch ein Zusammenspiel der Substanz mit der Durchführungvon Test auf Funktionen, die bei der Alzheimer'schen Erkrankunggestört sind, visualisiert. Diese hoch interessanten neuen Daten sindviel versprechend für zukünftige Studien in mehreren Indikationenneurologischer und psychiatrischer Erkrankungen.
28. März 2008
Evotecs EVT 101 gelangt ins menschliche Gehirn und moduliert die Hirnaktivität während der Durchführung kognitiver Aufgaben
Corporate news- Mitteilung verarbeitet und übermittelt durch Hugin. Für den Inhalt der Mitteilung ist der Emittent verantwortlich.
Corporate news- Mitteilung verarbeitet und übermittelt durch Hugin.Für den Inhalt der Mitteilung ist der Emittent verantwortlich. - Vorläufige Ergebnisse der Einzeldosis-fMRI-Studie an gesundenProbanden -- Dosierungsphase der vierwöchigen Studie mit höherer Mehrfachdosisabgeschlossen -Hamburg, Deutschland | Oxford, England - Evotec AG (Deutsche Börse:EVT) gab heute bekannt, dass vorläufige Ergebnisse einer doppeltverblindeten, dreiarmigen Crossover-Studie mit einer Einzeldosis vonEVT 101, ihres oral verfügbaren, für den NR2B-Subtyp desNMDA-Rezeptors selektiven Antagonisten vorliegen. Die Studie wurde an19 jungen und gesunden Probanden im Centre for Neuroimaging Sciencesdes Institute of Psychiatry am King's College in London durchgeführt.Dabei wurden bildgebende Verfahren der funktionellenMagnetresonanztomographie (fMRI) eingesetzt, um Kurzzeiteffekte vonzwei Dosen EVT 101 bzw.
Placebo zu untersuchen. Dabei wurden dieAuswirkungen des Wirkstoffs auf bestimmte kognitive Leistungen,Veränderungen der lokalen zerebralen Durchblutung, die dieAktivierung bzw. Deaktivierung von Neuronen während der Durchführungkognitiver Aufgaben anzeigen sowie die basale Durchblutung inverschiedenen Hirnregionen ermittelt.Alle Behandlungen wurden gut vertragen und bestätigen frühereErfahrungen mit gesunden Versuchspersonen.Während es keine Hinweise für eine akute Verbesserung von kognitivenFunktionen gab - kein unerwarteter Befund bei jungen, gesundenProbanden, die zumeist ohnehin optimale Leistungen erbringen - wurdebeobachtet, dass bestimmte Hirnareale, die eine Rolle für das Abrufenvon Gedächtnisinhalten spielen, durch EVT 101 selektive Veränderungender zerebralen Durchblutung zeigten, während bestimmte kognitiveAufgaben durchgeführt wurden.Zudem zeigte eine Analyse der Veränderungen der basalen lokalenHirndurchblutung einen selektiven Anstieg der Durchblutung in einerbestimmten Region der Hirnrinde, die reich an NMDA-Rezeptoren ist undzur Behandlung von Erkrankungen wie z. B. neuropathische Schmerzenund Depressionen für wichtig erachtet wird. Die basale Durchblutunganderer Hirnregionen blieb unverändert.Diese Ergebnisse belegen zum ersten Mal eine Wirkung von EVT 101 aufdas menschliche Gehirn; noch dazu in Dosierungen, die gut verträglichsind und als klinisch relevant erachtet werden.Darüber hinaus hat Evotec die Dosierungsphase seiner vierwöchigenStudie mit wiederholter, höherer Dosierung erfolgreich abgeschlossen.Diese Studie wird in Frankreich durchgeführt. Erfreulicherweisezeigten erste vorläufige Ergebnisse hinsichtlich der Verfügbarkeitvon EVT 101 in der Zerebrospinalflüssigkeit, dass EVT 101 dortKonzentrationen erreicht, von denen angenommen wird, dass sieNMDA-Rezeptoren vom Typ NR2B in signifikant höherem Ausmaß blockierenals Memantin in der für die Alzheimer'sche Erkrankung üblichentherapeutischen Dosierung. Dies ergab die Auswertung einerUntergruppe, die EVT 101 erhalten hatte."Diese Daten sind sehr erfreulich. Sie zeigen, dass EVT 101 inDosierungen, die vom Menschen gut vertragen und als klinisch relevanterachtet werden, Aktivität in Hirnregionen aufzeigt, die für dieSchmerzbekämpfung als relevant erachtet werden", kommentierte Dr. TimTasker, Executive Vice President Clinical Development der Evotec AG."Vor allem sehen wir dabei auch einen Einfluss auf die Aktivitätspezifischer Hirnregionen während der Durchführung kognitiverAufgaben, die bei der Alzheimer'schen Erkrankung eine Rolle spielen."Dr. Mitul Mehta, akademischer Forschungsleiter für dieses Projekt amCentre for Neuroimaging Sciences des Institute of Psychiatry amKing's College London, fügte hinzu: "Wir haben in unseren Studiensowohl einen direkten dosisabhängigen Effekt von EVT 101 auf dasGehirn als auch ein Zusammenspiel der Substanz mit der Durchführungvon Test auf Funktionen, die bei der Alzheimer'schen Erkrankunggestört sind, visualisiert. Diese hoch interessanten neuen Daten sindviel versprechend für zukünftige Studien in mehreren Indikationenneurologischer und psychiatrischer Erkrankungen.
http://www.evotec.com/de/news_events/news_article.aspx?news_…
08 May 2008
Evotec berichtet Geschäftszahlen für das erste Quartal 2008
Hamburg, Deutschland - Evotec AG (Börse Frankfurt: EVT; NASDAQ: EVTC) berichtete die Geschäftszahlen zum ersten Quartal 2008.
Evotecs Umsatz belief sich im ersten Quartal 2008 auf 7,3 Mio. Euro und lag damit um 16 % unter dem Vorjahresniveau (2007: 8,7 Mio. Euro). Dies ist im Wesentlichen das Ergebnis zweier Effekte:
(i) Fehlende Umsätze aus der Synthese von Substanzbibliotheken infolge der strategischen Entscheidung, dieses gesamte Geschäft mit Wirkung per Oktober 2007 in ein Joint Venture mit der indischen RSIL auszugliedern. Im ersten Quartal 2007 belief sich der Umsatz dieses Geschäftsbereichs auf 0,6 Mio. Euro.
(ii) Der erneut schwächere Wechselkurs des US-Dollars gegenüber Evotecs Berichtswährung Euro. Bei gegenüber 2007 unveränderten Wechselkursen (britisches Pfund und US-Dollar) hätte der Umsatz im ersten Quartal 2008 um 0,7 Mio. Euro höher bei 8,0 Mio. Euro gelegen.
Nach Wechselkurs-Anpassung des Umsatzes 2008 und ohne Berücksichtigung 2007 ausgegliederter Aktivitäten hätten sich die Einnahmen in etwa auf Vorjahresniveau (2007 bereinigt: 8,1 Mio. Euro) bewegt.
Der operative Verlust der Gruppe lag im ersten Quartal 2008 bei 14,4 Mio. Euro (2007: 9,8 Mio. Euro). Dieser Anstieg ist das Ergebnis hoher Investitionen in die Forschung und Entwicklung (F+E). Die F+E-Aufwendungen betrugen im ersten Quartal 2008 12,8 Mio. Euro. Das ist ein Anstieg um 73% gegenüber den 7,4 Mio. Euro im ersten Quartal 2007. Die Höhe dieser Aufwendungen resultierte z. T. aus einer Meilensteinzahlung an Roche für den Beginn der klinischen Phase-II-Studien mit EVT 302. Dieser Meilenstein wird in Form von Aktien vergütet, die im zweiten Quartal 2008 an Roche ausgegeben werden. Zum anderen rührt dieser Anstieg von Evotecs umfangreichem klinischen Entwicklungsprogramm für EVT 302 und EVT 101. Die anderen operativen Ausgaben nahmen um 22% auf 3,7 Mio. Euro ab (erstes Quartal 2007: 4,8 Mio. Euro). Der Nettoverlust betrug 13,8 Mio. Euro nach 9,0 Mio. Euro im Vorjahr.
Der Bestand an liquiden Mitteln einschließlich Bargeld und Wertpapiere betrug Ende März 2008 73,1 Mio. Euro (Ende Dezember 2007: 93,7 Mio. Euro). Auf Proforma-Basis, d.h. inkl. Renovis, hätte die Liquidität des zusammengeschlossenen Unternehmens einschließlich "auction rated securities" (8,6 Mio. Euro) zum 31. März 2008 119,0 Mio. Euro betragen.
Die hier gezeigten Ergebnisse und Erläuterungen beziehen sich auf die fortgeführten Geschäftsbereiche in 2007. Am 11. September 2007 hat Evotec mit Wirkung zum 30. November 2007 einen bedeutenden Geschäftsbereich, die chemische Entwicklungssparte, an Aptuit verkauft. Ab dem 1. Dezember 2007 wurde dieses Geschäft nicht mehr im Abschluss der Evotec-Gruppe konsolidiert und Erträge und Aufwendungen für dieses Geschäft wurden in der Gewinn- und Verlust-Rechnung rückwirkend als aufzugebende Geschäftsbereiche ausgewiesen.
Jörn Aldag, Vorstandsvorsitzender der Evotec AG, kommentierte dazu: "Der Beginn des Jahres 2008 war geprägt von zahlreichen Aktivitäten hinsichtlich der Übernahme von Renovis. Wir freuen uns sehr, diesen wichtigen Meilenstein erreicht zu haben, und begrüßen, dass die überzeugende Mehrheit der Renovis-Aktionäre für den Zusammenschluss der Unternehmen gestimmt hat. Wir sind davon überzeugt, dass wir nun über eine der stärksten ZNS-Pipelines in unserem Sektor verfügen mit drei klinischen Wirkstoffkandidaten, einer starken fortgeschrittenen präklinischen Pipeline mit Schwerpunkt auf neurologischen und entzündlichen Erkrankungen sowie über umfangreiche liquide Mittel, um diese Programme weiter entwickeln zu können. Im ersten Quartal haben unsere klinischen Entwicklungsprogramme weiterhin gute Fortschritte gemacht. Wir haben eine Phase-I-Studie zur Sicherheit und Verträglichkeit von EVT 302 in gesunden Probanden erfolgreich abgeschlossen. Darüber hinaus haben wir positive erste Daten für unsere Phase-Ib-Studie mit EVT 101 berichtet. Diese zeigten, dass der Wirkstoff gut in das zentrale Nervensystem eindringt und lassen erste Schlüsse auf die Wirkung im menschlichen Gehirn zu. Außerdem gehen die Diskussionen für die Lizenzpartnerschaften zu unserem am weitesten fortgeschrittenen Wirkstoff EVT 201 weiter. Es ist eines unserer wichtigsten Ziele für 2008, eine Partnerschaftsvereinbarung zur weiteren Entwicklung dieser Substanz abzuschließen."
Das erste Quartal 2008 und aktuelle Highlights
- Weitere Fortschritte in der klinischen Pipeline
* Erfolgreicher Abschluss einer Phase-I-Studie zur Sicherheit und Verträglichkeit einer mehrfachen Gabe von EVT 302 (in der Entwicklung zur Raucherentwöhnung). Der Wirkstoff wurde von jüngeren und älteren gesunden Probanden bis zur höchsten eingesetzten Dosisstufe gut vertragen. Eine Phase-II-Entzugsstudie wurde im Februar 2008 begonnen, während der Start einer Phase-II-Studie zur Ermittlung der Erfolgsrate bei der Raucherentwöhnung für die Jahresmitte vorgesehen ist.
* Die im März 2008 abgeschlossene Phase-Ib-Studie für EVT 101 mit bildgebenden Verfahren am Gehirn von gesunden Probanden zeigte erste Hinweise auf positive Effekte in den entscheidenden Hirnregionen. Sie ergab ermutigende Signale potenzieller Aktivität bei der Alzheimer'schen Erkrankung wie auch bei der Schmerzbehandlung. Die Ergebnisse einer zweiten Phase-Ib-Studie mit mehrfacher Gabe höherer Dosen von EVT 101 werden für das zweite Quartal 2008 erwartet.
- Wichtige neue oder erweiterte Partnerschaften wurden mit CHDI, der US-amerikanischen Huntington Disease Foundation, und der japanischen Firma Ono Pharmaceutical unterzeichnet.
- Die Finanzdaten liegen im Rahmen der von Evotec erwarteten Spanne für das Gesamtjahr.
* Niedrigerer Gesamtumsatz aufgrund der Veräußerung von Randaktivitäten gegen Cash.
* Auf Pro-forma-Basis einschließlich Renovis belief sich der Bestand an liquiden Mitteln und "auction rated securities" zum 31. März 2008 auf 119,0 Millionen Euro.
* Liquidität ist voraussichtlich bis 2010 gesichert.
- Nach Abschluss der Berichtsperiode: Akquisition der US-Firma Renovis am 2. Mai 2008 erfolgreich abgeschlossen.
* Aus der Fusion geht ein global aufgestelltes Unternehmen mit drei klinischen Kandidaten hervor, das nun durch eine starke Pipeline im späten präklinischen Stadium mit Fokus auf neurologischen und entzündlichen Erkrankungen gestützt wird.
* Bei drei Projekten von Renovis wird für 2008/09 der Start der klinischen Phase I erwartet.
* Evotec ADSs sind jetzt am NASDAQ Global Market gelistet.
Finanzziele für 2008 bestätigt
Die in diesem Abschnitt dargestellten Finanzziele beziehen sich auf die neue Evotec-Gruppe mit Renovis ab dem 1. Mai 2008.
Im Geschäftsjahr 2008 sollen die Umsätze ohne Einnahmen aus möglichen Auslizenzierungen 34-36 Mio. Euro betragen. Diese Annahmen beruhen auf dem derzeitigen Auftragsbuch, erwarteten Neuverträgen sowie Vertragsverlängerungen und, zu einem geringeren Ausmaß, dem Erreichen bestimmter Meilensteine. Abhängig von zusätzlichen Einnahmen aus Auslizenzierungen und weiteren Meilensteinzahlungen könnten die Umsätze auch deutlich höher ausfallen.
Das operative Ergebnis ohne Berücksichtigung von Einnahmen durch Auslizenzierungen und ohne Wertberichtigungen im Jahr 2008 soll ungefähr auf dem Niveau von 2007 liegen. Im Fall einer erfolgreichen Auslizenzierung könnte es das Geschäftsergebnis von 2007 deutlich übertreffen. Evotec investiert weiterhin in Forschung und Entwicklung (F+E). Das Unternehmen geht davon aus, dass sich die F+E-Aufwendungen im Geschäftsjahr 2008 auf 46-51 Mio. Euro belaufen werden. Hinzu kämen Aufwendungen für Aktienoptionsprogramme für Mitarbeiter, die den Forschungs- und
-entwicklungsaufwendungen 2008 zugeordnet werden. Der Anstieg liegt überwiegend an dem Fortschritt der klinischen Pipeline sowie der Übernahme von Renovis.
Die liquiden Mittel und "auction rated securities" zum Ende des Geschäftsjahres 2008 sollen sich nach der Übernahme von Renovis und ohne Berücksichtigung von Einnahmen durch Auslizenzierungen auf über 85 Mio. Euro belaufen. Unter der Annahme, dass sich das Portfolio des Unternehmens wie beabsichtigt weiterentwickelt und selbst wenn keine wichtigen Auslizenzierungen zustande kommen, sollen die liquiden Mittel ausreichen, um Evotecs Entwicklungsprogramme bis zum Ende 2010 zu finanzieren.
Q1/2008 - PDF / Seite 9

Diese Erhöhung der Akteinanzahl und nicht die angeblichen Aktienverkäufe sorgen dafür, dass Dr. Oetker unter 10 % sank. Dr. Oetker hat keine meldepflichtigen Verkäufe getätigt.
08 May 2008
Evotec berichtet Geschäftszahlen für das erste Quartal 2008
Hamburg, Deutschland - Evotec AG (Börse Frankfurt: EVT; NASDAQ: EVTC) berichtete die Geschäftszahlen zum ersten Quartal 2008.
Evotecs Umsatz belief sich im ersten Quartal 2008 auf 7,3 Mio. Euro und lag damit um 16 % unter dem Vorjahresniveau (2007: 8,7 Mio. Euro). Dies ist im Wesentlichen das Ergebnis zweier Effekte:
(i) Fehlende Umsätze aus der Synthese von Substanzbibliotheken infolge der strategischen Entscheidung, dieses gesamte Geschäft mit Wirkung per Oktober 2007 in ein Joint Venture mit der indischen RSIL auszugliedern. Im ersten Quartal 2007 belief sich der Umsatz dieses Geschäftsbereichs auf 0,6 Mio. Euro.
(ii) Der erneut schwächere Wechselkurs des US-Dollars gegenüber Evotecs Berichtswährung Euro. Bei gegenüber 2007 unveränderten Wechselkursen (britisches Pfund und US-Dollar) hätte der Umsatz im ersten Quartal 2008 um 0,7 Mio. Euro höher bei 8,0 Mio. Euro gelegen.
Nach Wechselkurs-Anpassung des Umsatzes 2008 und ohne Berücksichtigung 2007 ausgegliederter Aktivitäten hätten sich die Einnahmen in etwa auf Vorjahresniveau (2007 bereinigt: 8,1 Mio. Euro) bewegt.
Der operative Verlust der Gruppe lag im ersten Quartal 2008 bei 14,4 Mio. Euro (2007: 9,8 Mio. Euro). Dieser Anstieg ist das Ergebnis hoher Investitionen in die Forschung und Entwicklung (F+E). Die F+E-Aufwendungen betrugen im ersten Quartal 2008 12,8 Mio. Euro. Das ist ein Anstieg um 73% gegenüber den 7,4 Mio. Euro im ersten Quartal 2007. Die Höhe dieser Aufwendungen resultierte z. T. aus einer Meilensteinzahlung an Roche für den Beginn der klinischen Phase-II-Studien mit EVT 302. Dieser Meilenstein wird in Form von Aktien vergütet, die im zweiten Quartal 2008 an Roche ausgegeben werden. Zum anderen rührt dieser Anstieg von Evotecs umfangreichem klinischen Entwicklungsprogramm für EVT 302 und EVT 101. Die anderen operativen Ausgaben nahmen um 22% auf 3,7 Mio. Euro ab (erstes Quartal 2007: 4,8 Mio. Euro). Der Nettoverlust betrug 13,8 Mio. Euro nach 9,0 Mio. Euro im Vorjahr.
Der Bestand an liquiden Mitteln einschließlich Bargeld und Wertpapiere betrug Ende März 2008 73,1 Mio. Euro (Ende Dezember 2007: 93,7 Mio. Euro). Auf Proforma-Basis, d.h. inkl. Renovis, hätte die Liquidität des zusammengeschlossenen Unternehmens einschließlich "auction rated securities" (8,6 Mio. Euro) zum 31. März 2008 119,0 Mio. Euro betragen.
Die hier gezeigten Ergebnisse und Erläuterungen beziehen sich auf die fortgeführten Geschäftsbereiche in 2007. Am 11. September 2007 hat Evotec mit Wirkung zum 30. November 2007 einen bedeutenden Geschäftsbereich, die chemische Entwicklungssparte, an Aptuit verkauft. Ab dem 1. Dezember 2007 wurde dieses Geschäft nicht mehr im Abschluss der Evotec-Gruppe konsolidiert und Erträge und Aufwendungen für dieses Geschäft wurden in der Gewinn- und Verlust-Rechnung rückwirkend als aufzugebende Geschäftsbereiche ausgewiesen.
Jörn Aldag, Vorstandsvorsitzender der Evotec AG, kommentierte dazu: "Der Beginn des Jahres 2008 war geprägt von zahlreichen Aktivitäten hinsichtlich der Übernahme von Renovis. Wir freuen uns sehr, diesen wichtigen Meilenstein erreicht zu haben, und begrüßen, dass die überzeugende Mehrheit der Renovis-Aktionäre für den Zusammenschluss der Unternehmen gestimmt hat. Wir sind davon überzeugt, dass wir nun über eine der stärksten ZNS-Pipelines in unserem Sektor verfügen mit drei klinischen Wirkstoffkandidaten, einer starken fortgeschrittenen präklinischen Pipeline mit Schwerpunkt auf neurologischen und entzündlichen Erkrankungen sowie über umfangreiche liquide Mittel, um diese Programme weiter entwickeln zu können. Im ersten Quartal haben unsere klinischen Entwicklungsprogramme weiterhin gute Fortschritte gemacht. Wir haben eine Phase-I-Studie zur Sicherheit und Verträglichkeit von EVT 302 in gesunden Probanden erfolgreich abgeschlossen. Darüber hinaus haben wir positive erste Daten für unsere Phase-Ib-Studie mit EVT 101 berichtet. Diese zeigten, dass der Wirkstoff gut in das zentrale Nervensystem eindringt und lassen erste Schlüsse auf die Wirkung im menschlichen Gehirn zu. Außerdem gehen die Diskussionen für die Lizenzpartnerschaften zu unserem am weitesten fortgeschrittenen Wirkstoff EVT 201 weiter. Es ist eines unserer wichtigsten Ziele für 2008, eine Partnerschaftsvereinbarung zur weiteren Entwicklung dieser Substanz abzuschließen."
Das erste Quartal 2008 und aktuelle Highlights
- Weitere Fortschritte in der klinischen Pipeline
* Erfolgreicher Abschluss einer Phase-I-Studie zur Sicherheit und Verträglichkeit einer mehrfachen Gabe von EVT 302 (in der Entwicklung zur Raucherentwöhnung). Der Wirkstoff wurde von jüngeren und älteren gesunden Probanden bis zur höchsten eingesetzten Dosisstufe gut vertragen. Eine Phase-II-Entzugsstudie wurde im Februar 2008 begonnen, während der Start einer Phase-II-Studie zur Ermittlung der Erfolgsrate bei der Raucherentwöhnung für die Jahresmitte vorgesehen ist.
* Die im März 2008 abgeschlossene Phase-Ib-Studie für EVT 101 mit bildgebenden Verfahren am Gehirn von gesunden Probanden zeigte erste Hinweise auf positive Effekte in den entscheidenden Hirnregionen. Sie ergab ermutigende Signale potenzieller Aktivität bei der Alzheimer'schen Erkrankung wie auch bei der Schmerzbehandlung. Die Ergebnisse einer zweiten Phase-Ib-Studie mit mehrfacher Gabe höherer Dosen von EVT 101 werden für das zweite Quartal 2008 erwartet.
- Wichtige neue oder erweiterte Partnerschaften wurden mit CHDI, der US-amerikanischen Huntington Disease Foundation, und der japanischen Firma Ono Pharmaceutical unterzeichnet.
- Die Finanzdaten liegen im Rahmen der von Evotec erwarteten Spanne für das Gesamtjahr.
* Niedrigerer Gesamtumsatz aufgrund der Veräußerung von Randaktivitäten gegen Cash.
* Auf Pro-forma-Basis einschließlich Renovis belief sich der Bestand an liquiden Mitteln und "auction rated securities" zum 31. März 2008 auf 119,0 Millionen Euro.
* Liquidität ist voraussichtlich bis 2010 gesichert.
- Nach Abschluss der Berichtsperiode: Akquisition der US-Firma Renovis am 2. Mai 2008 erfolgreich abgeschlossen.
* Aus der Fusion geht ein global aufgestelltes Unternehmen mit drei klinischen Kandidaten hervor, das nun durch eine starke Pipeline im späten präklinischen Stadium mit Fokus auf neurologischen und entzündlichen Erkrankungen gestützt wird.
* Bei drei Projekten von Renovis wird für 2008/09 der Start der klinischen Phase I erwartet.
* Evotec ADSs sind jetzt am NASDAQ Global Market gelistet.
Finanzziele für 2008 bestätigt
Die in diesem Abschnitt dargestellten Finanzziele beziehen sich auf die neue Evotec-Gruppe mit Renovis ab dem 1. Mai 2008.
Im Geschäftsjahr 2008 sollen die Umsätze ohne Einnahmen aus möglichen Auslizenzierungen 34-36 Mio. Euro betragen. Diese Annahmen beruhen auf dem derzeitigen Auftragsbuch, erwarteten Neuverträgen sowie Vertragsverlängerungen und, zu einem geringeren Ausmaß, dem Erreichen bestimmter Meilensteine. Abhängig von zusätzlichen Einnahmen aus Auslizenzierungen und weiteren Meilensteinzahlungen könnten die Umsätze auch deutlich höher ausfallen.
Das operative Ergebnis ohne Berücksichtigung von Einnahmen durch Auslizenzierungen und ohne Wertberichtigungen im Jahr 2008 soll ungefähr auf dem Niveau von 2007 liegen. Im Fall einer erfolgreichen Auslizenzierung könnte es das Geschäftsergebnis von 2007 deutlich übertreffen. Evotec investiert weiterhin in Forschung und Entwicklung (F+E). Das Unternehmen geht davon aus, dass sich die F+E-Aufwendungen im Geschäftsjahr 2008 auf 46-51 Mio. Euro belaufen werden. Hinzu kämen Aufwendungen für Aktienoptionsprogramme für Mitarbeiter, die den Forschungs- und
-entwicklungsaufwendungen 2008 zugeordnet werden. Der Anstieg liegt überwiegend an dem Fortschritt der klinischen Pipeline sowie der Übernahme von Renovis.
Die liquiden Mittel und "auction rated securities" zum Ende des Geschäftsjahres 2008 sollen sich nach der Übernahme von Renovis und ohne Berücksichtigung von Einnahmen durch Auslizenzierungen auf über 85 Mio. Euro belaufen. Unter der Annahme, dass sich das Portfolio des Unternehmens wie beabsichtigt weiterentwickelt und selbst wenn keine wichtigen Auslizenzierungen zustande kommen, sollen die liquiden Mittel ausreichen, um Evotecs Entwicklungsprogramme bis zum Ende 2010 zu finanzieren.
Q1/2008 - PDF / Seite 9

Diese Erhöhung der Akteinanzahl und nicht die angeblichen Aktienverkäufe sorgen dafür, dass Dr. Oetker unter 10 % sank. Dr. Oetker hat keine meldepflichtigen Verkäufe getätigt.
Danke für deine Arbeit bolero.
Das Fettgedruckte wusste ich noch gar nicht:
Außerdem bringt Renovis vier Wirkstoffkandidaten im frühen Entwicklungsstadium mit. Bei zweien davon will Aldag in diesem Jahr mit der Phase I beginnen. An einem der beiden Moleküle, dem Schmerzmittel VR1, ist bereits der US-Pharma-Riese Pfizer beteiligt. Bis zu 170 Millionen Dollar an Prämien kann Evotec im Erfolgsfall diese Partnerschaft einbringen.
Das Fettgedruckte wusste ich noch gar nicht:
Außerdem bringt Renovis vier Wirkstoffkandidaten im frühen Entwicklungsstadium mit. Bei zweien davon will Aldag in diesem Jahr mit der Phase I beginnen. An einem der beiden Moleküle, dem Schmerzmittel VR1, ist bereits der US-Pharma-Riese Pfizer beteiligt. Bis zu 170 Millionen Dollar an Prämien kann Evotec im Erfolgsfall diese Partnerschaft einbringen.
Charttechnisch kommt der Wert von ca. EUR 100,00 (Anfang 2000) auf ca. EUR 1,00 (Ende 2002) runter. Krass! 
Nach einer Gegenraktion die bis ca. EUR 7,00 (Ende 2003) lief, hat sich der Wert jetzt wieder bei ca. EUR 1,20 eingefunden.
Die große Frage ist: Ist Evotec einfach nur Schrott und dümpelt weiter vor sich hin, oder prallt der Wert wieder bei ca. EUR 1,00 nach oben ab. Dann wären die Wiederstände nach oben 7,00 (Hoch Ende 2003) und 11,00 (Ausgabekurs) auf dem Weg zu neuen Höhen. Wenn der Kurs über 12 EUR steigt, wäre das ein Kaufsignal - bis dahin ist alles nur Gezocke.


Nach einer Gegenraktion die bis ca. EUR 7,00 (Ende 2003) lief, hat sich der Wert jetzt wieder bei ca. EUR 1,20 eingefunden.
Die große Frage ist: Ist Evotec einfach nur Schrott und dümpelt weiter vor sich hin, oder prallt der Wert wieder bei ca. EUR 1,00 nach oben ab. Dann wären die Wiederstände nach oben 7,00 (Hoch Ende 2003) und 11,00 (Ausgabekurs) auf dem Weg zu neuen Höhen. Wenn der Kurs über 12 EUR steigt, wäre das ein Kaufsignal - bis dahin ist alles nur Gezocke.

...also bei einer MK von 1,3mrd !! siehst Du bei dem Laden ein Kaufsignal 



!
Dieser Beitrag wurde moderiert. !
Dieser Beitrag wurde moderiert.
Antwort auf Beitrag Nr.: 34.232.124 von pardon am 04.06.08 01:45:32Die große Frage ist: Ist Evotec einfach nur Schrott und dümpelt weiter vor sich hin, oder prallt der Wert wieder bei ca. EUR 1,00 nach oben ab.
Genau, das ist die Frage!
Evotec ist äußerst ambitioniert bewertet mit ca. 135 Mio EURO MK.
Zum Vergleich: Der DAX-Wert Merck bringt es gerade mal auf etwas mehr als die Hälfte der Aktienzahl!!! Evotec ist ein typisches Beispiel für das Wachsen der Aktienzahl ins Unermeßliche. Wenn wir die Milliarde erreichen, womit ich fest rechne, wird das Teil zum Pennystock, das ist typisch für solche Aktien. Insofern ist der Gang an die US-Börse nur konsequent, dort gibt es zahllose socher Buden.
Genau, das ist die Frage!
Evotec ist äußerst ambitioniert bewertet mit ca. 135 Mio EURO MK.
Zum Vergleich: Der DAX-Wert Merck bringt es gerade mal auf etwas mehr als die Hälfte der Aktienzahl!!! Evotec ist ein typisches Beispiel für das Wachsen der Aktienzahl ins Unermeßliche. Wenn wir die Milliarde erreichen, womit ich fest rechne, wird das Teil zum Pennystock, das ist typisch für solche Aktien. Insofern ist der Gang an die US-Börse nur konsequent, dort gibt es zahllose socher Buden.

!
Dieser Beitrag wurde moderiert.
Antwort auf Beitrag Nr.: 34.232.663 von MrBean07 am 04.06.08 08:51:28Hilfe!!!
Bayer hat auch fast 800 Mio. Aktien!


Wenn wir die Milliarde erreichen, womit ich fest rechne, wird das Teil zum Pennystock,
Gut, dass ich da noch rechtzeitig rausgekommen bin!
Der Chemie- und Pharmakonzern Bayer wird seine Notierung an der New York Stock Exchange Ende September einstellen. Der Konzern will damit 15 Millionen Euro jährlich einsparen.
Diese Meldung ist dann wohl nur ein Joke?
In Wahrheit wollte man dem unvermeidlichen Weg zum Pennystock einen Haken schlagen!
Bayer hat auch fast 800 Mio. Aktien!



Wenn wir die Milliarde erreichen, womit ich fest rechne, wird das Teil zum Pennystock,
Gut, dass ich da noch rechtzeitig rausgekommen bin!
Der Chemie- und Pharmakonzern Bayer wird seine Notierung an der New York Stock Exchange Ende September einstellen. Der Konzern will damit 15 Millionen Euro jährlich einsparen.
Diese Meldung ist dann wohl nur ein Joke?
In Wahrheit wollte man dem unvermeidlichen Weg zum Pennystock einen Haken schlagen!
also
FAKT ist
EVO hat nach 7 MONATEN (!!!!!) immer noch keinen pharma gefunden, welcher EVT201 für phaseIII übernommen hat
bis heute wird lt. aussage EVO über den wirkstoff diskutiert
EVO selbst schliesst nicht aus
dass weitere phasenII notwendig sein könnten
meine meinung
der wirkstoff ist nicht gerade begehrt
ergo
EVO macht viel wind um EVT201
es folgen aber keine ergebnisse
7 monate nach abschluss phaseII noch KEINE weiterentwicklung in sicht


FAKT ist
EVO hat nach 7 MONATEN (!!!!!) immer noch keinen pharma gefunden, welcher EVT201 für phaseIII übernommen hat
bis heute wird lt. aussage EVO über den wirkstoff diskutiert
EVO selbst schliesst nicht aus
dass weitere phasenII notwendig sein könnten
meine meinung
der wirkstoff ist nicht gerade begehrt
ergo
EVO macht viel wind um EVT201
es folgen aber keine ergebnisse
7 monate nach abschluss phaseII noch KEINE weiterentwicklung in sicht



weiterhin ist fakt
es liegt ein intakter year-downtrend vor, in welchem die obere begrenzung vor einigen wochen mehrtägig getestet und NICHT überwunden werden konnte
es liegt ein intakter year-downtrend vor, in welchem die obere begrenzung vor einigen wochen mehrtägig getestet und NICHT überwunden werden konnte
weiterhin ist fakt
dass nach JEDEM test der oberen begrenzung
in diesem downtrend
ERST die untere begrenzung getestet wurde
BEVOR ein erneuter test der oberen begrenzung stattfand
die untere begrenzung verläuft DERZEIT bei rd 70 cent !!!!!
dass nach JEDEM test der oberen begrenzung
in diesem downtrend
ERST die untere begrenzung getestet wurde
BEVOR ein erneuter test der oberen begrenzung stattfand
die untere begrenzung verläuft DERZEIT bei rd 70 cent !!!!!
!
Dieser Beitrag wurde moderiert.
die FUSION mit RENOVIS hat vor allem eines bewirkt:
aus 2 cashburner mach 1 super-cashburner
aus 2 cashburner mach 1 super-cashburner

!
Dieser Beitrag wurde moderiert.
seit über 7 MONATEN diskutiert EVO mit anderen firmen über EVT201
DAS schaun wir uns mal näher an
also, mal rechnen (nachfolgend ca.-werte)
anfrage nach interesse und daten versenden 7 tage
interessent daten lesen 1 tag
daten intern diskutieren 5 tage
mit EVOTEC über daten diskutieren 5 tage
leerlauf 12 tage
macht zusammen 1 MONAT
WAS haebn die bislang in den anderen 6 MONATEN vollbracht ?
der hammer kommt noch
EVO braucht evtl NOCHMAL 6 monate für die auspartnerung von EVT201
nein, noch besser
EVO sagt man will VERSUCHEN bis ende 2008 einen partner zu finden
d.h.
es könnte auch noch LÄNGER dauern
sacht mal, liebe EVO-freunde
merkt ihr überhaupt ETWAS ?
DAS schaun wir uns mal näher an

also, mal rechnen (nachfolgend ca.-werte)
anfrage nach interesse und daten versenden 7 tage
interessent daten lesen 1 tag
daten intern diskutieren 5 tage
mit EVOTEC über daten diskutieren 5 tage
leerlauf 12 tage
macht zusammen 1 MONAT
WAS haebn die bislang in den anderen 6 MONATEN vollbracht ?

der hammer kommt noch
EVO braucht evtl NOCHMAL 6 monate für die auspartnerung von EVT201
nein, noch besser
EVO sagt man will VERSUCHEN bis ende 2008 einen partner zu finden
d.h.
es könnte auch noch LÄNGER dauern

sacht mal, liebe EVO-freunde
merkt ihr überhaupt ETWAS ?

derweil hat der BIG-seller wieder 80000 aktien an euch kleinanleger verkauft 
30 187 1,21 1,23 33 514
40 149 1,20 1,24 20 864
23 000 1,16 1,25 8 162
21 439 1,15 1,26 6 800
3 500 1,13 1,27 38 419

30 187 1,21 1,23 33 514
40 149 1,20 1,24 20 864
23 000 1,16 1,25 8 162
21 439 1,15 1,26 6 800
3 500 1,13 1,27 38 419
auch wollen wir was wesentliches NICHT vergessen
selbst der derzeitig kurs von 1,22 €
erscheint den INSIDERN nicht gerade günstig
ich sage, wenn auf diesem NIVEAU selbst die INSIDER die finger von der aktie lassen, wieso bitteschön, sollten WIR sie dann kaufen ?
selbst der derzeitig kurs von 1,22 €
erscheint den INSIDERN nicht gerade günstig
ich sage, wenn auf diesem NIVEAU selbst die INSIDER die finger von der aktie lassen, wieso bitteschön, sollten WIR sie dann kaufen ?

!
Dieser Beitrag wurde moderiert. !
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. !
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt
Regt euch nicht auf. Der Typ ist allen ernstes der meinung, ein Unternehmen mit einem Kurs von 3,90e ist zwangsläufig höher bewertet als ein Unternehmen mit einem Kurs von 3,20e. Das sagt doch alles. 

ist euch schon mal in den sinn gekommen,
das ein möglicher partner an der seriösität der pase II ergebnisse herumnörgelt, ist wießt ja wie die big pharmas das machen oder die fda,
da können die finanzschwachen firmen wie evo dann nicht mithalten,
so kann man sich leidige konkurrenz vom halse halten,
um dann das produkt für appel und nen ei bekommen




das ein möglicher partner an der seriösität der pase II ergebnisse herumnörgelt, ist wießt ja wie die big pharmas das machen oder die fda,
da können die finanzschwachen firmen wie evo dann nicht mithalten,
so kann man sich leidige konkurrenz vom halse halten,
um dann das produkt für appel und nen ei bekommen





Antwort auf Beitrag Nr.: 34.233.385 von zenman am 04.06.08 10:08:04
Nr.19
die FUSION mit RENOVIS hat vor allem eines bewirkt:
aus 2 cashburner mach 1 super-cashburner

Nr.20
heut ist wieder mal "reinlock-tag" verrückt
fettes BID
kleines ASK
WAS soll das ???
FAKTEN !!! FAKTEN !
könnte vll. hier ein Mod. einschreiten und einige Beiträge löschen ??
"DER TYP" kann doch nur provozieren. DAS kann er aber im anderem Thread machen.
Warum antwortet man ihm noch ??

Nr.19
die FUSION mit RENOVIS hat vor allem eines bewirkt:
aus 2 cashburner mach 1 super-cashburner

Nr.20
heut ist wieder mal "reinlock-tag" verrückt
fettes BID
kleines ASK
WAS soll das ???
FAKTEN !!! FAKTEN !
könnte vll. hier ein Mod. einschreiten und einige Beiträge löschen ??
"DER TYP" kann doch nur provozieren. DAS kann er aber im anderem Thread machen.
Warum antwortet man ihm noch ??
!
Dieser Beitrag wurde moderiert. !
Dieser Beitrag wurde moderiert. !
Dieser Beitrag wurde moderiert.
#43 hätte er in anderem Thread schreiben können.
seine kritische betrachtungsweise gehört nicht hierhin.
Ich habe ihn drauf hingewisen, dass es hier um FAKTEN geht.
Liebe Mitglieder der Community,
willkommen in der Wallstreet:Online Community. Wir bitten darum, diesen Text sorgfältig zu lesen, da er die wichtigsten Grundlagen unserer Gemeinschaft enthält.
Der Sinn und Zweck dieses Forums ist, börseninteressierten Menschen einen Austausch zu ermöglichen. An diesem Ort ist ein Zusammentreffen der unterschiedlichsten Menschen mit den unterschiedlichsten Interessen gewährleistet, die Ihre Erfahrungen zum eigenen und zum Wohle der Allgemeinheit austauschen.
Schwerpunktthema ist dabei natürlich der Kapitalmarkt. Allerdings ist das Forum mehr als nur ein "Marktplatz der Informationen". Im Zuge der steigenden Popularität der Anlageform "Aktie" soll hier auch eine Anlagekultur entwickelt und gepflegt werden und den vielen Börseneinsteigern geholfen werden. Dazu stehen diverse Foren zur Verfügung.
Diese sind untergliedert in reservierte und offene Foren. Beide Forenarten unterscheiden sich nur in der Schreibberechtigung, jeder Nutzer von wallstreet:online kann in allen Foren lesen. In den offenen Foren kann sich auch jeder registrierte wallstreet:online Nutzer frei an Diskussionen beteiligen. Die reservierten Foren sind für jeden Nutzer lesbar. Um darin einen Beitrag zu verfassen, benötigen sie eine spezielle Freischaltung. Grundlage dafür ist, daß Sie sich mit Namen und Adresse bei wallstreet:online anmelden.
Durch die dann nicht mehr gegebene Anonymität erwarten wir ein weitaus angenehmeres Diskussionsklima. Wir werden die Daten selbstverständlich nicht weitergeben und sie sind auch nicht öffentlich einsehbar. Für alle Nutzer, die dennoch Bedenken hegen, stehen die freien Foren wie bisher zur Verfügung. Bei den reservierten Foren handelt es sich um ein Zusatzangebot. Alle Nutzer, die bereits für Realtimekurse freigeschaltet wurden, haben automatisch die Berechtigung an den reservierten Foren aktiv teilzunehmen.
Umgangsformen:
1. Man sollte auch im Internet auf rechtliche Bestimmungen achten. Das Verbreiten von Falschmeldungen etc. ist auch im Internet strafbar und wird ggf. entsprechend geahndet.
2. Behandle andere Boardteilnehmer so, wie Du selbst behandelt werden möchtest. Auch wenn es sich hierbei nur um virtuelle Persönlichkeiten handelt, so sollte man nie vergessen, dass sich dahinter reale Menschen verbergen.
3. Beleidigungen, sexuelle Anspielungen gegenüber Frauen etc. sind zu unterlassen.
4. Gerade im Internet ist das Recht auf Meinungsfreiheit von großer Bedeutung. Versuche deshalb niemand Deine Meinung aufzuzwingen. Jeder hat das Recht der eigenen Meinung und kann diese hier offen äußern.
5. Neue Boardteilnehmer sollten unterstützt werden, damit sie sich möglichst einfach in die Boardcommunity integrieren können. User, die sich nicht an die Boardrichtlinien halten, sollten von den anderen Teilnehmer höflich darauf hingewiesen werden.
1. Der Missbrauch des Brokerboards als Werbefläche für Webseiten oder Diensten ist nicht gestattet, da dieses als Austauschplattform für Diskussionen gedacht ist. Vereinzelte, dezente Werbungen werden jedoch zum Großteil toleriert. wallstreet:online behält sich jedoch vor, Werbungen ohne Vorwarnung zu entfernen und ggf. bei weiterem Missbrauch die User-ID zu sperren.
2. Grobe Verstöße gegen die Richtlinien (Umgangsformen / Werbung) sind bitte umgehend an das Feedback-Team zu melden und können zur Löschung des Threads bzw. zur Sperrung der User-ID führen.
Richtlinien zur Sperrung von Threads, Postings oder User:
1. Krasse Ausdrücke von Rassismus, Hasspropaganda oder Beleidigung
2. Das Fördern oder Anbieten von anleitenden Informationen über illegale Aktivitäten, wie die Anleitung zum Waffenbau, das Fördern von Spam Emails, Computerviren oder Material welches das intellektuelle Eigentumsrecht Dritter verletzt.
3. Das Aufrufen zur Gewalt oder die Androhung von Gewalt sowie das Fördern von physischem Schaden oder Verletzung gegen jede Gruppe von Individuen.
4. Frontale Nacktheit oder Ansichten von Genitalien, Sex, Pornographie, obszönes Material, Grafiken gegen den guten Geschmack. Das beinhaltet gleichzeitig jegliche Form von Material, das Kinder und Jugendliche in obszönen oder quasi obszönen Szenen oder Posen darstellt.
5. Jedes Material, das andere Personen oder Unternehmen beleidigt, entwürdigt oder diskriminiert.
6. Beiträge deren Thema thematisch nicht zu dem sonstigen Inhalt des Forums passen, in das sie eingestellt wurden werden in ein Forum verschoben, dessen Inhalt dem Thema des Beitrages am nächsten kommt.
Community-Moderatoren
Die Einhaltung der Boardregeln wird - ausser von wallstreet:online Mitarbeitern - auch von bestimmten Community Mitgliedern überwacht. Diese Mitglieder haben gewisse Administrationsrechte und können Nutzer sperren, die gegen die Boardregeln verstossen und können Threads laut Boardrichtlinie 6. verschieben.
wallstreet:online behält sich vor, diese Aufstellung bei Bedarf zu ergänzen.
seine kritische betrachtungsweise gehört nicht hierhin.
Ich habe ihn drauf hingewisen, dass es hier um FAKTEN geht.
Liebe Mitglieder der Community,
willkommen in der Wallstreet:Online Community. Wir bitten darum, diesen Text sorgfältig zu lesen, da er die wichtigsten Grundlagen unserer Gemeinschaft enthält.
Der Sinn und Zweck dieses Forums ist, börseninteressierten Menschen einen Austausch zu ermöglichen. An diesem Ort ist ein Zusammentreffen der unterschiedlichsten Menschen mit den unterschiedlichsten Interessen gewährleistet, die Ihre Erfahrungen zum eigenen und zum Wohle der Allgemeinheit austauschen.
Schwerpunktthema ist dabei natürlich der Kapitalmarkt. Allerdings ist das Forum mehr als nur ein "Marktplatz der Informationen". Im Zuge der steigenden Popularität der Anlageform "Aktie" soll hier auch eine Anlagekultur entwickelt und gepflegt werden und den vielen Börseneinsteigern geholfen werden. Dazu stehen diverse Foren zur Verfügung.
Diese sind untergliedert in reservierte und offene Foren. Beide Forenarten unterscheiden sich nur in der Schreibberechtigung, jeder Nutzer von wallstreet:online kann in allen Foren lesen. In den offenen Foren kann sich auch jeder registrierte wallstreet:online Nutzer frei an Diskussionen beteiligen. Die reservierten Foren sind für jeden Nutzer lesbar. Um darin einen Beitrag zu verfassen, benötigen sie eine spezielle Freischaltung. Grundlage dafür ist, daß Sie sich mit Namen und Adresse bei wallstreet:online anmelden.
Durch die dann nicht mehr gegebene Anonymität erwarten wir ein weitaus angenehmeres Diskussionsklima. Wir werden die Daten selbstverständlich nicht weitergeben und sie sind auch nicht öffentlich einsehbar. Für alle Nutzer, die dennoch Bedenken hegen, stehen die freien Foren wie bisher zur Verfügung. Bei den reservierten Foren handelt es sich um ein Zusatzangebot. Alle Nutzer, die bereits für Realtimekurse freigeschaltet wurden, haben automatisch die Berechtigung an den reservierten Foren aktiv teilzunehmen.
Umgangsformen:
1. Man sollte auch im Internet auf rechtliche Bestimmungen achten. Das Verbreiten von Falschmeldungen etc. ist auch im Internet strafbar und wird ggf. entsprechend geahndet.
2. Behandle andere Boardteilnehmer so, wie Du selbst behandelt werden möchtest. Auch wenn es sich hierbei nur um virtuelle Persönlichkeiten handelt, so sollte man nie vergessen, dass sich dahinter reale Menschen verbergen.
3. Beleidigungen, sexuelle Anspielungen gegenüber Frauen etc. sind zu unterlassen.
4. Gerade im Internet ist das Recht auf Meinungsfreiheit von großer Bedeutung. Versuche deshalb niemand Deine Meinung aufzuzwingen. Jeder hat das Recht der eigenen Meinung und kann diese hier offen äußern.
5. Neue Boardteilnehmer sollten unterstützt werden, damit sie sich möglichst einfach in die Boardcommunity integrieren können. User, die sich nicht an die Boardrichtlinien halten, sollten von den anderen Teilnehmer höflich darauf hingewiesen werden.
1. Der Missbrauch des Brokerboards als Werbefläche für Webseiten oder Diensten ist nicht gestattet, da dieses als Austauschplattform für Diskussionen gedacht ist. Vereinzelte, dezente Werbungen werden jedoch zum Großteil toleriert. wallstreet:online behält sich jedoch vor, Werbungen ohne Vorwarnung zu entfernen und ggf. bei weiterem Missbrauch die User-ID zu sperren.
2. Grobe Verstöße gegen die Richtlinien (Umgangsformen / Werbung) sind bitte umgehend an das Feedback-Team zu melden und können zur Löschung des Threads bzw. zur Sperrung der User-ID führen.
Richtlinien zur Sperrung von Threads, Postings oder User:
1. Krasse Ausdrücke von Rassismus, Hasspropaganda oder Beleidigung
2. Das Fördern oder Anbieten von anleitenden Informationen über illegale Aktivitäten, wie die Anleitung zum Waffenbau, das Fördern von Spam Emails, Computerviren oder Material welches das intellektuelle Eigentumsrecht Dritter verletzt.
3. Das Aufrufen zur Gewalt oder die Androhung von Gewalt sowie das Fördern von physischem Schaden oder Verletzung gegen jede Gruppe von Individuen.
4. Frontale Nacktheit oder Ansichten von Genitalien, Sex, Pornographie, obszönes Material, Grafiken gegen den guten Geschmack. Das beinhaltet gleichzeitig jegliche Form von Material, das Kinder und Jugendliche in obszönen oder quasi obszönen Szenen oder Posen darstellt.
5. Jedes Material, das andere Personen oder Unternehmen beleidigt, entwürdigt oder diskriminiert.
6. Beiträge deren Thema thematisch nicht zu dem sonstigen Inhalt des Forums passen, in das sie eingestellt wurden werden in ein Forum verschoben, dessen Inhalt dem Thema des Beitrages am nächsten kommt.
Community-Moderatoren
Die Einhaltung der Boardregeln wird - ausser von wallstreet:online Mitarbeitern - auch von bestimmten Community Mitgliedern überwacht. Diese Mitglieder haben gewisse Administrationsrechte und können Nutzer sperren, die gegen die Boardregeln verstossen und können Threads laut Boardrichtlinie 6. verschieben.
wallstreet:online behält sich vor, diese Aufstellung bei Bedarf zu ergänzen.
!
Dieser Beitrag wurde moderiert.
Antwort auf Beitrag Nr.: 34.229.548 von bolero6 am 03.06.08 19:13:51Es ist ein Wettlauf mit der Zeit, den Evotec gewinnen muss.
umso verwunderlicher ist es
dass EVO sich bis zu 15 Monaten für die auslizensierung einräumt.
ein wirkstoff, der 15 monate in der schublade ruht.
aus SOWAS soll ein blockbuster werden ?
umso verwunderlicher ist es
dass EVO sich bis zu 15 Monaten für die auslizensierung einräumt.
ein wirkstoff, der 15 monate in der schublade ruht.
aus SOWAS soll ein blockbuster werden ?

Antwort auf Beitrag Nr.: 34.239.219 von zenman am 04.06.08 19:34:44MEINE kritische betrachtungsweise von EVOTEC hat wenigstens hand und fuss Cool
IHR schreibt nur ab und labert nach
was EVO bzw analos euch vorschreiben
IHR hinterfragt gar nix lachen
IHR seid blauäugig und naiv erstaunt
Wie war das gleich noch mit den 3,90e KZ bei EVT und den 3,20e bei NBIX und der Bewertung?
IHR schreibt nur ab und labert nach
was EVO bzw analos euch vorschreiben
IHR hinterfragt gar nix lachen
IHR seid blauäugig und naiv erstaunt
Wie war das gleich noch mit den 3,90e KZ bei EVT und den 3,20e bei NBIX und der Bewertung?

!
Dieser Beitrag wurde moderiert.
Also meiner Meinung nach befindet sich EVOTEC langfristig im Abwärtstrend... hat aber kurzfirstig gute Chance 10-20% zu steigen. Auch die Bodenbildung bei 1,20€ halte ich nicht für ausgeschlossen.
Mein Tip - erstmal kanns nach oben bis etwa 1,50-1,60€
Die 70cent wie vorher mal angedeutet sehe ich in den nächsten Monaten nun wirklich nicht (außer der Markt crasht richtig).
Das ist meine betrachtung des Charts - um Fundamentaldaten kümmere ich mich nur wenig!
Mein Tip - erstmal kanns nach oben bis etwa 1,50-1,60€
Die 70cent wie vorher mal angedeutet sehe ich in den nächsten Monaten nun wirklich nicht (außer der Markt crasht richtig).
Das ist meine betrachtung des Charts - um Fundamentaldaten kümmere ich mich nur wenig!
Antwort auf Beitrag Nr.: 34.239.086 von bolero6 am 04.06.08 19:19:26Also man sollte hier keine Zensur gegen kritische Geister fordern sondern diesen Leuten danken, daß sie sich auch mal wirklich fundierte Gedanken um diesen Wert machen.
Zenman sagt doch nur:
WIESO ist das nicht passiert ?
WIESO wird jetzt VERSUCHT bis ENDE 2008 einen partner zu finden ?
WIESO versprechen die nicht , dass ein partner gwefunden wird ?
WIESO sagen die ihren aktionären nicht, WARUM die partnerfindung noch nicht erledigt ist ?
WIESO stehen die BIG-pharmas nicht schlange und prügeln sich um den ach so tollen wirkstoff ?
wiesowiesowieso ?
die antworten HIERRAUF erklären den kursverlauf
Das ist Fakt und alles richtig, ihr Lieben! Wacht auf! Jeder kann sich mal verzocken!
Ich erinnere bloß an GPC, an Paion, an Cybio, an November, an Genescan, an MWG, an ...., da wurden die wenigen Kritischen Geister auch niedergeprügelt, aber was passierte dann?


Also immer fair bleiben. Bin nach wie vor der Ansicht,daß ein Einstieg über 50 Cents nicht lohnen wird. Es wird auch keine Übernahme geben. Falls Evotec in den nächsten 6 Monaten keinen Schlafmittelpartner findet, wird Ende 2009 der Stecker gezogen.
Zenman sagt doch nur:
WIESO ist das nicht passiert ?
WIESO wird jetzt VERSUCHT bis ENDE 2008 einen partner zu finden ?
WIESO versprechen die nicht , dass ein partner gwefunden wird ?
WIESO sagen die ihren aktionären nicht, WARUM die partnerfindung noch nicht erledigt ist ?
WIESO stehen die BIG-pharmas nicht schlange und prügeln sich um den ach so tollen wirkstoff ?
wiesowiesowieso ?
die antworten HIERRAUF erklären den kursverlauf
Das ist Fakt und alles richtig, ihr Lieben! Wacht auf! Jeder kann sich mal verzocken!
Ich erinnere bloß an GPC, an Paion, an Cybio, an November, an Genescan, an MWG, an ...., da wurden die wenigen Kritischen Geister auch niedergeprügelt, aber was passierte dann?



Also immer fair bleiben. Bin nach wie vor der Ansicht,daß ein Einstieg über 50 Cents nicht lohnen wird. Es wird auch keine Übernahme geben. Falls Evotec in den nächsten 6 Monaten keinen Schlafmittelpartner findet, wird Ende 2009 der Stecker gezogen.

!
Dieser Beitrag wurde moderiert. !
Dieser Beitrag wurde moderiert.
Vielleicht auch daher der seltsame Kursverlauf der letzten Monate:
Bericht von 2002:
Roland Oetker im Visier der Staatsanwaltschaft
Gegen den Präsidenten der Aktionärsschützer wird ermittelt. Verdacht auf Insiderhandel.
Gegen Roland Oetker, Präsident der Deutschen Schutzvereinigung für Wertpapierbesitz (DSW), ermittelt die Staatsanwaltschaft
Hamburg - Gegen den Präsidenten der Deutschen Schutzvereinigung für Wertpapierbesitz (DSW), Roland Oetker, wird wegen des Verdachts auf Insiderhandel ermittelt. Er könnte nach Erkenntnissen der Ermittler sein frühzeitiges Wissen über zwei bevorstehende Fusionen ausgenutzt und dadurch Geld mit Aktienkäufen verdient haben. Oberstaatsanwalt Johannes Mocken von der Düsseldorfer Staatsanwaltschaft bestätigte am Samstag entsprechende Medienberichte.
"Ob aus dem Anfangsverdacht, der zweifellos auf Grund einer Reihe von Indizien feststeht, ein hinreichender Tatverdacht wird, steht noch nicht fest", sagte Mocken. Dies hänge von der weiteren Auswertung der Unterlagen ab. Die zu untersuchenden Aktien-Transaktionen bewegten sich insgesamt "im Millionenbereich". Oetker weise die Vorwürfe zurück, schrieb die "Welt" am Samstag.
In einem der Fälle - der Übernahme des Anlagenbauers Gea AG durch die damalige Metallgesellschaft - werden auch weitere Personen verdächtigt. Die Gea-Übernahme war am 8. Februar 1999 bekannt gegeben worden. Nach Erkenntnissen der Staatsanwaltschaft habe Oetker mit drei Kaufaufträgen zwischen dem 22. Januar 1999 und dem 3. Februar 1999 35.000 Aktien der Metallgesellschaft erworben, schrieb die "Welt".
Für seinen Bruder Ernst-August Oetker habe er außerdem über dessen Depotkonto 10.000 MG-Aktien gekauft. Als Geschäftsführender Gesellschafter der ROI Verwaltungsgesellschaft habe Roland Oetker auch über deren Wertpapierkonto weitere 26.000 Aktien und 60.000 Kaufoptionen auf MG-Aktien erworben.
Im zweiten Fall werde Oetker verdächtigt, von seinem Insiderwissen bei der Übernahme des Textilunternehmens Verseidag AG durch die Gamma Holding 1998 Gebrauch gemacht zu haben, schreibt das Nachrichtenmagazin "Focus" in seiner jüngsten Ausgabe. Unter den Verdächtigten im Fall MG/Gea sei auch ein PR-Berater des MG Technologies-Chefs Kajo Neukirchen, Lutz Dreesbach.
"Das dicke Ende kommt erst noch"
Die Deutsche Schutzvereinigung für Wertpapierbesitz (DSW) hat die größten Börsen-Flops ermittelt. Traurige Spitzenplätze erreichten Brokat und Intershop. Aber auch unter renommierten Standardwerten tummeln sich Kapitalvernichter. ...mehr
Dreesbach soll den Angaben zufolge am 1. und 2. Februar insgesamt 3000 Aktien der MG erworben haben, schrieb die "Welt". Auch er weist den Vorwurf, Insidergeschäfte gemacht zu haben, zurück. Er habe bereits in den Vormonaten MG-Aktien gekauft. Erst am 3. Februar habe er von Neukirchen von der geplanten Übernahme erfahren und dann keine Aktien mehr erworben.
Bisher sei noch keiner der Beschuldigten vernommen worden, hieß es. Beamte des Bundesaufsichtsamtes für den Wertpapierhandel und der Staatsanwaltschaft Düsseldorf hätten bereits am 21. März dieses Jahres die Büros der MG Technologies und der Gea durchsucht, um weitere Hinweise zu finden.
Oetker wolle nun kooperativ mit der Düsseldorfer Staatsanwaltschaft zusammenarbeiten und den Fall aufklären, hieß es. Die Sache sei für ihn in höchstem Maße unangenehm, wurde er von der "Welt" zitiert. Die DSW setzt sich für die Interessen privater Anleger ein.
Bericht von 2002:
Roland Oetker im Visier der Staatsanwaltschaft
Gegen den Präsidenten der Aktionärsschützer wird ermittelt. Verdacht auf Insiderhandel.
Gegen Roland Oetker, Präsident der Deutschen Schutzvereinigung für Wertpapierbesitz (DSW), ermittelt die Staatsanwaltschaft
Hamburg - Gegen den Präsidenten der Deutschen Schutzvereinigung für Wertpapierbesitz (DSW), Roland Oetker, wird wegen des Verdachts auf Insiderhandel ermittelt. Er könnte nach Erkenntnissen der Ermittler sein frühzeitiges Wissen über zwei bevorstehende Fusionen ausgenutzt und dadurch Geld mit Aktienkäufen verdient haben. Oberstaatsanwalt Johannes Mocken von der Düsseldorfer Staatsanwaltschaft bestätigte am Samstag entsprechende Medienberichte.
"Ob aus dem Anfangsverdacht, der zweifellos auf Grund einer Reihe von Indizien feststeht, ein hinreichender Tatverdacht wird, steht noch nicht fest", sagte Mocken. Dies hänge von der weiteren Auswertung der Unterlagen ab. Die zu untersuchenden Aktien-Transaktionen bewegten sich insgesamt "im Millionenbereich". Oetker weise die Vorwürfe zurück, schrieb die "Welt" am Samstag.
In einem der Fälle - der Übernahme des Anlagenbauers Gea AG durch die damalige Metallgesellschaft - werden auch weitere Personen verdächtigt. Die Gea-Übernahme war am 8. Februar 1999 bekannt gegeben worden. Nach Erkenntnissen der Staatsanwaltschaft habe Oetker mit drei Kaufaufträgen zwischen dem 22. Januar 1999 und dem 3. Februar 1999 35.000 Aktien der Metallgesellschaft erworben, schrieb die "Welt".
Für seinen Bruder Ernst-August Oetker habe er außerdem über dessen Depotkonto 10.000 MG-Aktien gekauft. Als Geschäftsführender Gesellschafter der ROI Verwaltungsgesellschaft habe Roland Oetker auch über deren Wertpapierkonto weitere 26.000 Aktien und 60.000 Kaufoptionen auf MG-Aktien erworben.
Im zweiten Fall werde Oetker verdächtigt, von seinem Insiderwissen bei der Übernahme des Textilunternehmens Verseidag AG durch die Gamma Holding 1998 Gebrauch gemacht zu haben, schreibt das Nachrichtenmagazin "Focus" in seiner jüngsten Ausgabe. Unter den Verdächtigten im Fall MG/Gea sei auch ein PR-Berater des MG Technologies-Chefs Kajo Neukirchen, Lutz Dreesbach.
"Das dicke Ende kommt erst noch"
Die Deutsche Schutzvereinigung für Wertpapierbesitz (DSW) hat die größten Börsen-Flops ermittelt. Traurige Spitzenplätze erreichten Brokat und Intershop. Aber auch unter renommierten Standardwerten tummeln sich Kapitalvernichter. ...mehr
Dreesbach soll den Angaben zufolge am 1. und 2. Februar insgesamt 3000 Aktien der MG erworben haben, schrieb die "Welt". Auch er weist den Vorwurf, Insidergeschäfte gemacht zu haben, zurück. Er habe bereits in den Vormonaten MG-Aktien gekauft. Erst am 3. Februar habe er von Neukirchen von der geplanten Übernahme erfahren und dann keine Aktien mehr erworben.
Bisher sei noch keiner der Beschuldigten vernommen worden, hieß es. Beamte des Bundesaufsichtsamtes für den Wertpapierhandel und der Staatsanwaltschaft Düsseldorf hätten bereits am 21. März dieses Jahres die Büros der MG Technologies und der Gea durchsucht, um weitere Hinweise zu finden.
Oetker wolle nun kooperativ mit der Düsseldorfer Staatsanwaltschaft zusammenarbeiten und den Fall aufklären, hieß es. Die Sache sei für ihn in höchstem Maße unangenehm, wurde er von der "Welt" zitiert. Die DSW setzt sich für die Interessen privater Anleger ein.
Ich finde, das ist es wert, in diesem Thread zu stehen.
Ein bisschen was zum Nachdenken!
zenman erspare mir deine Antwort in diesem Thread, auch wenn es dir in den Fingern juckt!
Encysive Pharmaceuticals


Coley Pharmaceutical


31.05.2005 17:47
Renovis: Lukrativer Pfizer-Deal


Renovis hat heute bekannt gegeben, eine Forschungs- und Lizenzierungs-Kooperation mit dem Pharmariesen Pfizer (News/Aktienkurs) abgeschlossen zu haben. Dabei gehe es um die Erforschung des Vanilloid-Rezeptors (VR1), einem Protein, das im Nervensystem Schmerzempfindungen auslöst. Man erhoffe sich durch die gewonnenen Aufschlüsse Fortschritte bei Entwicklung von Medikamenten gegen Schmerzen, Inkontinenz und andere Störungen.
Im Idealfall, so das auf neurologische Präparate spezialisierte Unternehmen, könne das Abkommen Erlöse von bis zu 170 Millionen Dollar abwerfen. Pfizer werde zunächst Lizenzgebühren in Höhe von 10 Millionen Dollar und Beiträge zu den Forschungskosten von bis zu 7 Millionen Dollar pro Jahr beisteuern. Der Jahresumsatz aus dem Lizenzabkommen selbst werde bei 6,5 bis 7 Millionen Dollar jährlich liegen. Im Erfolgsfall seien weitere Umsatzbeteiligungen geplant.
Pfizer steckt mehr Geld in Biotechfirma
Renovis und sorgt für Kurssprung
Der Pharmariese Pfizer und das US-Biotechunternehmen
Renovis haben ihre Zusammenarbeit ausgebaut.
Der weltgrößte Arzneimittelhersteller unterstützt Renovis
mit zusätzlichen Forschungsgeldern bis Ende Juni
2008, was der Aktie des Biotechunternehmens einen
Kursschub versetzte. Renovis-Aktien stiegen am Dienstag
an der Wall Street um mehr als 17 Prozent auf 4,66
Dollar. Renovis und Pfizer entwickeln im Rahmen der im
Jahr 2005 vereinbarten Zusammenarbeit kleine Moleküle,
die den sogenannten Vanilloid Rezeptor VR1
angreifen. Dieser nimmt eine wichtige Rolle bei der
Wahrnehmung von Schmerzen ein. Das Programm befindet
sich noch in der präklinischen Entwicklung. Ursprünglich
hätte Pfizer Renovis bis Ende Juni 2007
finanziell unter die Arme gegriffen. Für das laufende
Jahr erwartet die Biotechfirma nun Erlöse aus bestehenden
Vereinbarungen von 5,3 bis 9,8 Mio. Dollar.
Zuvor waren 4,3 bis 8,8 Mio. Dollar in Aussicht gestellt
worden.Quelle: Die Welt


 Was kommt danach???
Was kommt danach???
Die mit dem Pharmakonzern Pfizer laufenden Renovis-Projekte würden weiter geführt. Renovis erwarte, dass zwei der vier Pfizer-Projekte 2008 in die klinische Entwicklung kommen, wodurch Zahlungen von Pfizer fällig würden.
Quelle: Finanzen/süddeutsche
Die Kernelemente von Evotecs Geschäft umfassen: Drei klinische Programme, drei fortgeschrittene präklinische Programme und Partnerschaften
EVT 201: ein partiell-positiver allosterischer Modulator (pPAM) von GABAA-Rezeptoren zur Behandlung von Schlafstörungen. EVT 201 hat 2007 in zwei Phase-II-Wirksamkeitsstudien an erwachsenen Patienten als auch an älteren Patienten über 65 Jahren mit primärer Schlaflosigkeit starke Effekte auf das Einschlaf- und das Durchschlafverhalten gezeigt. Die Studienergebnisse haben uns viel versprechende Hinweise darauf gegeben, dass EVT 201 das Potenzial hat, viele der Schwächen von derzeit verfügbaren verschreibungspflichtigen Schlafmitteln zu überwinden. Evotec beabsichtigt, EVT 201 im Jahr 2008 zu verpartnern.
EVT 101: einer von wenigen oral verfügbaren, selektiven Antagonisten für den NR2B-Subtyp des NMDA-Rezeptors, die sich in der klinischen Entwicklung befinden. Die Selektivität von EVT 101 kann zu klinischen Vorteilen gegenüber bestehenden Alzheimer-Therapeutika führen. Zudem schreibt Evotec EVT 101 großes Potenzial in verschiedenen Schmerz-Indikationen zu. EVT 101 erwies sich in Phase-I-Studien als gut verträglich. Wir haben vor kurzem erste Daten von Phase-Ib-Studien veröffentlicht. Diese bestätigen unseren starken Glauben an das Potenzial der Substanz, das menschliche Gehirn zu erreichen und zu Aktivität in den Regionen des Gehirns zu führen, die hinsichtlich kognitiver Fähigkeiten und Schmerz eine Rolle spielen. Weitere Daten aus diesen Studien werden voraussichtlich noch in diesem Quartal veröffentlicht.
EVT 302: ein oral verfügbarer, hochselektiver und reversibler MAO-B-Inhibitor, der sich in der Entwicklung für die Raucherentwöhnung befindet. Die Substanz eignet sich möglicherweise als Ergänzung zu Nikotin-basierten Therapien und hat Potenzial für eine einmal wöchentliche Verabreichung sowie ein überlegenes Nebenwirkungsprofil. Seit Ankündigung der Transaktion wurden erfreuliche Ergebnisse von Phase-I-Studien mit PET-(Positronen-Emissions-Tomografie)-Bildanalyse und zur Sicherheit und Unbedenklichkeit bekannt gegeben und eine Grundlage für den Beginn der Phase-II-Wirksamkeitsstudien geschaffen. Eine Phase-II-Entzugsstudie hat im Februar 2008 begonnen und eine Phase-II-Studie zur Ermittlung der Erfolgsrate bei der Entwöhnung wird voraussichtlich Mitte des Jahres beginnen. Studienergebnisse werden im dritten Quartal 2008 bzw. in der ersten Jahreshälfte 2009 vorliegen.
. Innovative präklinische Pipeline
Die präklinische Pipeline des zusammengeschlossenen Unternehmens ist eine ideale Ergänzung zu Evotecs klinischem Portfolio und beinhaltet Kandidaten, die 2008 in die klinische Entwicklung überführt werden sollen:
VR1-Antagonisten: Für dieses präklinische Programm besteht eine Kooperation mit Pfizer Inc., in der Evotec Anspruch hat auf Meilensteinzahlungen von mehr als 170 Mio. US-Dollar sowie prozentuale Umsatzbeteiligungen in zweistelliger Höhe an den weltweiten Netto-Umsätzen für jedes Produkt, das im Rahmen dieser Zusammenarbeit erfolgreich entwickelt und vermarktet wird. Potenzielle Produkte beinhalten breit anwendbare Schmerzmittel mit einem möglicherweise differenzierten Profil für verschiedene akute und chronische Schmerzzustände sowie für Harninkontinenz und Asthma. Erste klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2008 begonnen.
P2X7-Antagonisten: Produkte umfassen potenzielle neue Wirkstoffe zur Behandlung von Gelenkrheumatismus, Reizdarmsyndrom sowie chronisch obstruktiver Lungenerkrankung. Klinische Studien werden voraussichtlich 2008 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
P2X3-Antagonisten: Potenzielle Produkte umfassen neue, in ihrer Form bisher einzigartige Wirkstoffkandidaten zur Behandlung von Entzündungen und neuropathischen Schmerzen sowie Harnerkrankungen. Klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2009 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
Quelle: mastertraders
Ein bisschen was zum Nachdenken!
zenman erspare mir deine Antwort in diesem Thread, auch wenn es dir in den Fingern juckt!
Encysive Pharmaceuticals



Coley Pharmaceutical



31.05.2005 17:47
Renovis: Lukrativer Pfizer-Deal



Renovis hat heute bekannt gegeben, eine Forschungs- und Lizenzierungs-Kooperation mit dem Pharmariesen Pfizer (News/Aktienkurs) abgeschlossen zu haben. Dabei gehe es um die Erforschung des Vanilloid-Rezeptors (VR1), einem Protein, das im Nervensystem Schmerzempfindungen auslöst. Man erhoffe sich durch die gewonnenen Aufschlüsse Fortschritte bei Entwicklung von Medikamenten gegen Schmerzen, Inkontinenz und andere Störungen.
Im Idealfall, so das auf neurologische Präparate spezialisierte Unternehmen, könne das Abkommen Erlöse von bis zu 170 Millionen Dollar abwerfen. Pfizer werde zunächst Lizenzgebühren in Höhe von 10 Millionen Dollar und Beiträge zu den Forschungskosten von bis zu 7 Millionen Dollar pro Jahr beisteuern. Der Jahresumsatz aus dem Lizenzabkommen selbst werde bei 6,5 bis 7 Millionen Dollar jährlich liegen. Im Erfolgsfall seien weitere Umsatzbeteiligungen geplant.
Pfizer steckt mehr Geld in Biotechfirma
Renovis und sorgt für Kurssprung
Der Pharmariese Pfizer und das US-Biotechunternehmen
Renovis haben ihre Zusammenarbeit ausgebaut.
Der weltgrößte Arzneimittelhersteller unterstützt Renovis
mit zusätzlichen Forschungsgeldern bis Ende Juni
2008, was der Aktie des Biotechunternehmens einen
Kursschub versetzte. Renovis-Aktien stiegen am Dienstag
an der Wall Street um mehr als 17 Prozent auf 4,66
Dollar. Renovis und Pfizer entwickeln im Rahmen der im
Jahr 2005 vereinbarten Zusammenarbeit kleine Moleküle,
die den sogenannten Vanilloid Rezeptor VR1
angreifen. Dieser nimmt eine wichtige Rolle bei der
Wahrnehmung von Schmerzen ein. Das Programm befindet
sich noch in der präklinischen Entwicklung. Ursprünglich
hätte Pfizer Renovis bis Ende Juni 2007
finanziell unter die Arme gegriffen. Für das laufende
Jahr erwartet die Biotechfirma nun Erlöse aus bestehenden
Vereinbarungen von 5,3 bis 9,8 Mio. Dollar.
Zuvor waren 4,3 bis 8,8 Mio. Dollar in Aussicht gestellt
worden.Quelle: Die Welt


 Was kommt danach???
Was kommt danach???Die mit dem Pharmakonzern Pfizer laufenden Renovis-Projekte würden weiter geführt. Renovis erwarte, dass zwei der vier Pfizer-Projekte 2008 in die klinische Entwicklung kommen, wodurch Zahlungen von Pfizer fällig würden.
Quelle: Finanzen/süddeutsche
Die Kernelemente von Evotecs Geschäft umfassen: Drei klinische Programme, drei fortgeschrittene präklinische Programme und Partnerschaften
EVT 201: ein partiell-positiver allosterischer Modulator (pPAM) von GABAA-Rezeptoren zur Behandlung von Schlafstörungen. EVT 201 hat 2007 in zwei Phase-II-Wirksamkeitsstudien an erwachsenen Patienten als auch an älteren Patienten über 65 Jahren mit primärer Schlaflosigkeit starke Effekte auf das Einschlaf- und das Durchschlafverhalten gezeigt. Die Studienergebnisse haben uns viel versprechende Hinweise darauf gegeben, dass EVT 201 das Potenzial hat, viele der Schwächen von derzeit verfügbaren verschreibungspflichtigen Schlafmitteln zu überwinden. Evotec beabsichtigt, EVT 201 im Jahr 2008 zu verpartnern.
EVT 101: einer von wenigen oral verfügbaren, selektiven Antagonisten für den NR2B-Subtyp des NMDA-Rezeptors, die sich in der klinischen Entwicklung befinden. Die Selektivität von EVT 101 kann zu klinischen Vorteilen gegenüber bestehenden Alzheimer-Therapeutika führen. Zudem schreibt Evotec EVT 101 großes Potenzial in verschiedenen Schmerz-Indikationen zu. EVT 101 erwies sich in Phase-I-Studien als gut verträglich. Wir haben vor kurzem erste Daten von Phase-Ib-Studien veröffentlicht. Diese bestätigen unseren starken Glauben an das Potenzial der Substanz, das menschliche Gehirn zu erreichen und zu Aktivität in den Regionen des Gehirns zu führen, die hinsichtlich kognitiver Fähigkeiten und Schmerz eine Rolle spielen. Weitere Daten aus diesen Studien werden voraussichtlich noch in diesem Quartal veröffentlicht.
EVT 302: ein oral verfügbarer, hochselektiver und reversibler MAO-B-Inhibitor, der sich in der Entwicklung für die Raucherentwöhnung befindet. Die Substanz eignet sich möglicherweise als Ergänzung zu Nikotin-basierten Therapien und hat Potenzial für eine einmal wöchentliche Verabreichung sowie ein überlegenes Nebenwirkungsprofil. Seit Ankündigung der Transaktion wurden erfreuliche Ergebnisse von Phase-I-Studien mit PET-(Positronen-Emissions-Tomografie)-Bildanalyse und zur Sicherheit und Unbedenklichkeit bekannt gegeben und eine Grundlage für den Beginn der Phase-II-Wirksamkeitsstudien geschaffen. Eine Phase-II-Entzugsstudie hat im Februar 2008 begonnen und eine Phase-II-Studie zur Ermittlung der Erfolgsrate bei der Entwöhnung wird voraussichtlich Mitte des Jahres beginnen. Studienergebnisse werden im dritten Quartal 2008 bzw. in der ersten Jahreshälfte 2009 vorliegen.
. Innovative präklinische Pipeline
Die präklinische Pipeline des zusammengeschlossenen Unternehmens ist eine ideale Ergänzung zu Evotecs klinischem Portfolio und beinhaltet Kandidaten, die 2008 in die klinische Entwicklung überführt werden sollen:
VR1-Antagonisten: Für dieses präklinische Programm besteht eine Kooperation mit Pfizer Inc., in der Evotec Anspruch hat auf Meilensteinzahlungen von mehr als 170 Mio. US-Dollar sowie prozentuale Umsatzbeteiligungen in zweistelliger Höhe an den weltweiten Netto-Umsätzen für jedes Produkt, das im Rahmen dieser Zusammenarbeit erfolgreich entwickelt und vermarktet wird. Potenzielle Produkte beinhalten breit anwendbare Schmerzmittel mit einem möglicherweise differenzierten Profil für verschiedene akute und chronische Schmerzzustände sowie für Harninkontinenz und Asthma. Erste klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2008 begonnen.
P2X7-Antagonisten: Produkte umfassen potenzielle neue Wirkstoffe zur Behandlung von Gelenkrheumatismus, Reizdarmsyndrom sowie chronisch obstruktiver Lungenerkrankung. Klinische Studien werden voraussichtlich 2008 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
P2X3-Antagonisten: Potenzielle Produkte umfassen neue, in ihrer Form bisher einzigartige Wirkstoffkandidaten zur Behandlung von Entzündungen und neuropathischen Schmerzen sowie Harnerkrankungen. Klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2009 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
Quelle: mastertraders
Aufgrund dieser und schon lange bekannten Trümpfe,
werde ich mich für einige tage naach Norwegen verabschieden,
zum Saunieren und.... und... ohne Wein und BMW 5....
zum rechtzeitigen Umschichten bin ich wieder zurück bzw. mein
Laptop wird mich begleiten....
mfg
skat
werde ich mich für einige tage naach Norwegen verabschieden,
zum Saunieren und.... und... ohne Wein und BMW 5....
zum rechtzeitigen Umschichten bin ich wieder zurück bzw. mein
Laptop wird mich begleiten....
mfg
skat
Antwort auf Beitrag Nr.: 34.318.778 von skat am 17.06.08 18:48:19Nimmst du Frau Hennecke mit ?
Antwort auf Beitrag Nr.: 34.320.939 von spero am 18.06.08 04:19:13die kommt in Kurzzeitpflege in Pflegeheim
wegen verdacht auf ALZHEIMER....




der nächste wird A.... sein...

skat
wegen verdacht auf ALZHEIMER....





der nächste wird A.... sein...


skat
Antwort auf Beitrag Nr.: 34.322.918 von skat am 18.06.08 11:43:13Kurs-steig-Pflege find ich für Frau Hennecke gut. Dir viel Spass in Norwegen. Nimm dir bloß genug Roten mit ! Du wirst uns fehlen.































Die Kernelemente von Evotecs Geschäft umfassen: Drei klinische Programme, drei fortgeschrittene präklinische Programme und Partnerschaften
EVT 201: ein partiell-positiver allosterischer Modulator (pPAM) von GABAA-Rezeptoren zur Behandlung von Schlafstörungen. EVT 201 hat 2007 in zwei Phase-II-Wirksamkeitsstudien an erwachsenen Patienten als auch an älteren Patienten über 65 Jahren mit primärer Schlaflosigkeit starke Effekte auf das Einschlaf- und das Durchschlafverhalten gezeigt. Die Studienergebnisse haben uns viel versprechende Hinweise darauf gegeben, dass EVT 201 das Potenzial hat, viele der Schwächen von derzeit verfügbaren verschreibungspflichtigen Schlafmitteln zu überwinden. Evotec beabsichtigt, EVT 201 im Jahr 2008 zu verpartnern.
EVT 101: einer von wenigen oral verfügbaren, selektiven Antagonisten für den NR2B-Subtyp des NMDA-Rezeptors, die sich in der klinischen Entwicklung befinden. Die Selektivität von EVT 101 kann zu klinischen Vorteilen gegenüber bestehenden Alzheimer-Therapeutika führen. Zudem schreibt Evotec EVT 101 großes Potenzial in verschiedenen Schmerz-Indikationen zu. EVT 101 erwies sich in Phase-I-Studien als gut verträglich. Wir haben vor kurzem erste Daten von Phase-Ib-Studien veröffentlicht. Diese bestätigen unseren starken Glauben an das Potenzial der Substanz, das menschliche Gehirn zu erreichen und zu Aktivität in den Regionen des Gehirns zu führen, die hinsichtlich kognitiver Fähigkeiten und Schmerz eine Rolle spielen. Weitere Daten aus diesen Studien werden voraussichtlich noch in diesem Quartal veröffentlicht.
EVT 302: ein oral verfügbarer, hochselektiver und reversibler MAO-B-Inhibitor, der sich in der Entwicklung für die Raucherentwöhnung befindet. Die Substanz eignet sich möglicherweise als Ergänzung zu Nikotin-basierten Therapien und hat Potenzial für eine einmal wöchentliche Verabreichung sowie ein überlegenes Nebenwirkungsprofil. Seit Ankündigung der Transaktion wurden erfreuliche Ergebnisse von Phase-I-Studien mit PET-(Positronen-Emissions-Tomografie)-Bildanalyse und zur Sicherheit und Unbedenklichkeit bekannt gegeben und eine Grundlage für den Beginn der Phase-II-Wirksamkeitsstudien geschaffen. Eine Phase-II-Entzugsstudie hat im Februar 2008 begonnen und eine Phase-II-Studie zur Ermittlung der Erfolgsrate bei der Entwöhnung wird voraussichtlich Mitte des Jahres beginnen. Studienergebnisse werden im dritten Quartal 2008 bzw. in der ersten Jahreshälfte 2009 vorliegen.
. Innovative präklinische Pipeline
Die präklinische Pipeline des zusammengeschlossenen Unternehmens ist eine ideale Ergänzung zu Evotecs klinischem Portfolio und beinhaltet Kandidaten, die 2008 in die klinische Entwicklung überführt werden sollen:
VR1-Antagonisten: Für dieses präklinische Programm besteht eine Kooperation mit Pfizer Inc., in der Evotec Anspruch hat auf Meilensteinzahlungen von mehr als 170 Mio. US-Dollar sowie prozentuale Umsatzbeteiligungen in zweistelliger Höhe an den weltweiten Netto-Umsätzen für jedes Produkt, das im Rahmen dieser Zusammenarbeit erfolgreich entwickelt und vermarktet wird. Potenzielle Produkte beinhalten breit anwendbare Schmerzmittel mit einem möglicherweise differenzierten Profil für verschiedene akute und chronische Schmerzzustände sowie für Harninkontinenz und Asthma. Erste klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2008 begonnen.
P2X7-Antagonisten: Produkte umfassen potenzielle neue Wirkstoffe zur Behandlung von Gelenkrheumatismus, Reizdarmsyndrom sowie chronisch obstruktiver Lungenerkrankung. Klinische Studien werden voraussichtlich 2008 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
P2X3-Antagonisten: Potenzielle Produkte umfassen neue, in ihrer Form bisher einzigartige Wirkstoffkandidaten zur Behandlung von Entzündungen und neuropathischen Schmerzen sowie Harnerkrankungen. Klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2009 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
PLANUNG für 2008

EVT 201: ein partiell-positiver allosterischer Modulator (pPAM) von GABAA-Rezeptoren zur Behandlung von Schlafstörungen. EVT 201 hat 2007 in zwei Phase-II-Wirksamkeitsstudien an erwachsenen Patienten als auch an älteren Patienten über 65 Jahren mit primärer Schlaflosigkeit starke Effekte auf das Einschlaf- und das Durchschlafverhalten gezeigt. Die Studienergebnisse haben uns viel versprechende Hinweise darauf gegeben, dass EVT 201 das Potenzial hat, viele der Schwächen von derzeit verfügbaren verschreibungspflichtigen Schlafmitteln zu überwinden. Evotec beabsichtigt, EVT 201 im Jahr 2008 zu verpartnern.
EVT 101: einer von wenigen oral verfügbaren, selektiven Antagonisten für den NR2B-Subtyp des NMDA-Rezeptors, die sich in der klinischen Entwicklung befinden. Die Selektivität von EVT 101 kann zu klinischen Vorteilen gegenüber bestehenden Alzheimer-Therapeutika führen. Zudem schreibt Evotec EVT 101 großes Potenzial in verschiedenen Schmerz-Indikationen zu. EVT 101 erwies sich in Phase-I-Studien als gut verträglich. Wir haben vor kurzem erste Daten von Phase-Ib-Studien veröffentlicht. Diese bestätigen unseren starken Glauben an das Potenzial der Substanz, das menschliche Gehirn zu erreichen und zu Aktivität in den Regionen des Gehirns zu führen, die hinsichtlich kognitiver Fähigkeiten und Schmerz eine Rolle spielen. Weitere Daten aus diesen Studien werden voraussichtlich noch in diesem Quartal veröffentlicht.
EVT 302: ein oral verfügbarer, hochselektiver und reversibler MAO-B-Inhibitor, der sich in der Entwicklung für die Raucherentwöhnung befindet. Die Substanz eignet sich möglicherweise als Ergänzung zu Nikotin-basierten Therapien und hat Potenzial für eine einmal wöchentliche Verabreichung sowie ein überlegenes Nebenwirkungsprofil. Seit Ankündigung der Transaktion wurden erfreuliche Ergebnisse von Phase-I-Studien mit PET-(Positronen-Emissions-Tomografie)-Bildanalyse und zur Sicherheit und Unbedenklichkeit bekannt gegeben und eine Grundlage für den Beginn der Phase-II-Wirksamkeitsstudien geschaffen. Eine Phase-II-Entzugsstudie hat im Februar 2008 begonnen und eine Phase-II-Studie zur Ermittlung der Erfolgsrate bei der Entwöhnung wird voraussichtlich Mitte des Jahres beginnen. Studienergebnisse werden im dritten Quartal 2008 bzw. in der ersten Jahreshälfte 2009 vorliegen.
. Innovative präklinische Pipeline
Die präklinische Pipeline des zusammengeschlossenen Unternehmens ist eine ideale Ergänzung zu Evotecs klinischem Portfolio und beinhaltet Kandidaten, die 2008 in die klinische Entwicklung überführt werden sollen:
VR1-Antagonisten: Für dieses präklinische Programm besteht eine Kooperation mit Pfizer Inc., in der Evotec Anspruch hat auf Meilensteinzahlungen von mehr als 170 Mio. US-Dollar sowie prozentuale Umsatzbeteiligungen in zweistelliger Höhe an den weltweiten Netto-Umsätzen für jedes Produkt, das im Rahmen dieser Zusammenarbeit erfolgreich entwickelt und vermarktet wird. Potenzielle Produkte beinhalten breit anwendbare Schmerzmittel mit einem möglicherweise differenzierten Profil für verschiedene akute und chronische Schmerzzustände sowie für Harninkontinenz und Asthma. Erste klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2008 begonnen.
P2X7-Antagonisten: Produkte umfassen potenzielle neue Wirkstoffe zur Behandlung von Gelenkrheumatismus, Reizdarmsyndrom sowie chronisch obstruktiver Lungenerkrankung. Klinische Studien werden voraussichtlich 2008 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
P2X3-Antagonisten: Potenzielle Produkte umfassen neue, in ihrer Form bisher einzigartige Wirkstoffkandidaten zur Behandlung von Entzündungen und neuropathischen Schmerzen sowie Harnerkrankungen. Klinische Studien werden voraussichtlich in der ersten Jahreshälfte 2009 begonnen. Das Programm ist nicht verpartnert. Folglich hält Evotec die weltweiten Entwicklungsrechte.
PLANUNG für 2008

05 Sep 2007
Evotec berichtet Details ihrer positiven Phase-II-Wirksamkeitsstudie mit EVT 201 gegen Schlafstörungen
Sehr robuste Ergebnisse hinsichtlich der Hauptprobleme von Patienten mit Schlafstörungen, d.h. Einschlaf- und Durchschlafzeit
- Evotec wird die Details in einer Telefonkonferenz heute um 11.00 Uhr deutscher Zeit direkt vom worldsleep07 Kongress in Australien vorstellen
Hamburg, Deutschland | Oxford, England - Evotec AG (Deutsche Börse: EVT) gab heute auf dem worldsleep07 Kongress in Cairns, Australien, die Details zu den Ergebnissen ihrer ersten klinischen Phase-II-Studie mit EVT 201 an Patienten, die unter primären Schlafstörungen leiden, bekannt. EVT 201 ist ein partiell-positiver allosterischer Modulator (pPAM) von GABAA-Rezeptoren. Die Doppelblind-Studie im Cross-Over-Design wurde mittels polysomnographischer Untersuchungen mit zwei Dosierungen von EVT 201 (1,5 mg und 2,5 mg) und Placebo an 67 Patienten in Schlafzentren in den USA durchgeführt. Nach Veröffentlichung der Ergebnisse zu den wesentlichen Endpunkten der Studie in einer Pressemitteilung am 4. Juni 2007 gibt Evotec hiermit die detaillierten Ergebnisse der Studie bekannt.
Die detaillierte Analyse hat gezeigt, dass die Studie hinsichtlich aller Endpunkte sogar ein noch höheres statistisches Signifikanzniveau erreichte als zunächst angedeutet. Die zuvor spezifizierte "Intention-to-treat-Analyse" hat gezeigt, dass die beiden co-primären Endpunkte Gesamtschlafdauer ("Total Sleep Time", TST) und Wachzeit nach dem ersten Einschlafen ("Wake After Sleep Onset", WASO) in beiden Dosierungsstufen mit einer statistischen Signifikanz von p<0,0001 gegenüber Placebo erreicht wurden.
Statistisch hoch signifikante und klinisch bedeutsame Effekte wurden auch hinsichtlich der Dauer bis zum Einsetzen eines anhaltenden Schlafs ("Latency to Persistent Sleep", LPS) und der Gesamtschlafdauer (TST) in der zweiten Nachthälfte erzielt. Dies deutet darauf hin, dass EVT 201 eine starke Wirkung sowohl auf das Einschlaf- als auch auf das Durchschlafverhalten hat. Zusätzlich zu diesen objektiven Messdaten aus polysomnographischen Untersuchungen fanden sich bei beiden Dosierungsstufen hoch signifikante Verbesserungen der subjektiv empfundenen Schlafqualität.
Am folgenden Morgen ist kein subjektives Empfinden von dämpfenden Nachwirkungen berichtet worden. Der so genannte Digital Symbol Substitution Test (DSST) zeigte eine kleine, aber klinisch nicht bedeutsame Veränderung am Folgetag (9 Stunden nach Einnahme).
Die Polysomnographie-Analyse zeigte darüber hinaus, dass EVT 201 anders als viele Benzodiazepin-Vollagonisten keinen negativen Einfluss auf die Schlafarchitektur hatte.
Wie in allen vorigen klinischen Studien erwies sich EVT 201 in beiden Dosierungsstufen als sicher und gut verträglich. Es gab keine Berichte über schwer wiegende oder unerwartete Nebenwirkungen.

Der große Effekt auf die Gesamtwachzeit ("Total Wake Time", TWT) in der zweiten Nachthälfte zeigt, dass EVT 201 sehr wirksam darin ist, den Schlaf über die gesamte Nacht aufrecht zu erhalten. Diese Beobachtung wird gestützt durch die stündliche Analyse der Gesamtwachzeit. Obwohl die Studie für eine solche Analyse nicht ausgelegt war, zeigt die durch EVT 201 hervorgerufene Reduktion der Gesamtwachzeit für alle Stunden der Nacht statistische Signifikanz mit Ausnahme für die 7. Stunde, die jedoch statistischer Signifikanz sehr nahe kam (p= 0,058).
Dr. John Kemp, Chief Research & Development Officer, Evotec AG, kommentierte die Ergebnisse: "Ich bin von den Ergebnissen dieser Phase-II-Wirksamkeitsstudie sehr begeistert. Die Größe des Effekts auf die Durchschlafzeit erscheint robuster als mit anderen Wirkstoffen in ähnlichen Cross-Over-Studien. Insbesondere sind uns keine ähnlichen Studien bekannt, die mit einer derartigen statistischen Signifikanz Effekte auf die Gesamtwachzeit in der zweiten Nachthälfte und die Gesamtwachzeit bezogen auf jede Nachtstunde erzielt haben."
Jörn Aldag, Vorstandsvorsitzender der Evotec AG, sagte: "Obwohl vorhandene Schlafmittel bestimmte Aspekte der Schlaflosigkeit behandeln, gibt es noch kein Medikament, das alle Bedürfnisse von Patienten mit Schlafstörungen befriedigt. In unserer Studie hat sich EVT 201 hinsichtlich aller Hauptprobleme von schlaflosen Menschen mit extrem beeindruckenden Ergebnissen bewährt. Dazu zählen insbesondere die Einschlaf- und Durchschlafdauer. Bemerkenswert ist auch, dass die Patienten gleichzeitig am nächsten Morgen subjektiv keine Nachwirkungen, so genannte Hang-over-Effekte, empfinden. Wir glauben, dass EVT 201 damit ein sehr vorteilhaftes Wirkungsprofil gegenüber derzeit verfügbaren Schlafmitteln besitzt, einschließlich solcher, die sich zurzeit in der Spätphase der klinischen Entwicklung befinden."
Hauptprüfarzt Dr. James Walsh, Executive Director des Sleep Medici-ne and Research Center, St. John's Mercy Medical Center, Chester-field, Missouri, USA, sagte: "Mit seinem Wirkmechanismus als partiell-positiver allosterischer Modulator von GABAA-Rezeptoren eröffnet EVT 201 einen neuen Weg zur Behandlung der Schlaflosigkeit. Da das GABAA-System sehr gut verstanden ist, ist das Risiko unerwarteter Nebenwirkungen deutlich geringer als bei vollständig neuen Wirkmechanismen. Dies in Kombination mit den robusten Ergebnissen dieser Studie, besonders im Hinblick auf das Durchschlafverhalten, lässt das Medikament als sehr viel versprechend für Patienten mit Schlafstörungen erscheinen.
Evotec führt derzeit eine zweite klinische Phase-II-Studie zur weiteren Differenzierung von EVT 201 in älteren Patienten durch, die unter primären Schlafstörungen leiden. Die Eckdaten zu den wesentlichen Endpunkten dieser Studie werden voraussichtlich im Oktober 2007 bekannt gegeben.
Evotec berichtet Details ihrer positiven Phase-II-Wirksamkeitsstudie mit EVT 201 gegen Schlafstörungen
Sehr robuste Ergebnisse hinsichtlich der Hauptprobleme von Patienten mit Schlafstörungen, d.h. Einschlaf- und Durchschlafzeit
- Evotec wird die Details in einer Telefonkonferenz heute um 11.00 Uhr deutscher Zeit direkt vom worldsleep07 Kongress in Australien vorstellen
Hamburg, Deutschland | Oxford, England - Evotec AG (Deutsche Börse: EVT) gab heute auf dem worldsleep07 Kongress in Cairns, Australien, die Details zu den Ergebnissen ihrer ersten klinischen Phase-II-Studie mit EVT 201 an Patienten, die unter primären Schlafstörungen leiden, bekannt. EVT 201 ist ein partiell-positiver allosterischer Modulator (pPAM) von GABAA-Rezeptoren. Die Doppelblind-Studie im Cross-Over-Design wurde mittels polysomnographischer Untersuchungen mit zwei Dosierungen von EVT 201 (1,5 mg und 2,5 mg) und Placebo an 67 Patienten in Schlafzentren in den USA durchgeführt. Nach Veröffentlichung der Ergebnisse zu den wesentlichen Endpunkten der Studie in einer Pressemitteilung am 4. Juni 2007 gibt Evotec hiermit die detaillierten Ergebnisse der Studie bekannt.
Die detaillierte Analyse hat gezeigt, dass die Studie hinsichtlich aller Endpunkte sogar ein noch höheres statistisches Signifikanzniveau erreichte als zunächst angedeutet. Die zuvor spezifizierte "Intention-to-treat-Analyse" hat gezeigt, dass die beiden co-primären Endpunkte Gesamtschlafdauer ("Total Sleep Time", TST) und Wachzeit nach dem ersten Einschlafen ("Wake After Sleep Onset", WASO) in beiden Dosierungsstufen mit einer statistischen Signifikanz von p<0,0001 gegenüber Placebo erreicht wurden.
Statistisch hoch signifikante und klinisch bedeutsame Effekte wurden auch hinsichtlich der Dauer bis zum Einsetzen eines anhaltenden Schlafs ("Latency to Persistent Sleep", LPS) und der Gesamtschlafdauer (TST) in der zweiten Nachthälfte erzielt. Dies deutet darauf hin, dass EVT 201 eine starke Wirkung sowohl auf das Einschlaf- als auch auf das Durchschlafverhalten hat. Zusätzlich zu diesen objektiven Messdaten aus polysomnographischen Untersuchungen fanden sich bei beiden Dosierungsstufen hoch signifikante Verbesserungen der subjektiv empfundenen Schlafqualität.
Am folgenden Morgen ist kein subjektives Empfinden von dämpfenden Nachwirkungen berichtet worden. Der so genannte Digital Symbol Substitution Test (DSST) zeigte eine kleine, aber klinisch nicht bedeutsame Veränderung am Folgetag (9 Stunden nach Einnahme).
Die Polysomnographie-Analyse zeigte darüber hinaus, dass EVT 201 anders als viele Benzodiazepin-Vollagonisten keinen negativen Einfluss auf die Schlafarchitektur hatte.
Wie in allen vorigen klinischen Studien erwies sich EVT 201 in beiden Dosierungsstufen als sicher und gut verträglich. Es gab keine Berichte über schwer wiegende oder unerwartete Nebenwirkungen.

Der große Effekt auf die Gesamtwachzeit ("Total Wake Time", TWT) in der zweiten Nachthälfte zeigt, dass EVT 201 sehr wirksam darin ist, den Schlaf über die gesamte Nacht aufrecht zu erhalten. Diese Beobachtung wird gestützt durch die stündliche Analyse der Gesamtwachzeit. Obwohl die Studie für eine solche Analyse nicht ausgelegt war, zeigt die durch EVT 201 hervorgerufene Reduktion der Gesamtwachzeit für alle Stunden der Nacht statistische Signifikanz mit Ausnahme für die 7. Stunde, die jedoch statistischer Signifikanz sehr nahe kam (p= 0,058).
Dr. John Kemp, Chief Research & Development Officer, Evotec AG, kommentierte die Ergebnisse: "Ich bin von den Ergebnissen dieser Phase-II-Wirksamkeitsstudie sehr begeistert. Die Größe des Effekts auf die Durchschlafzeit erscheint robuster als mit anderen Wirkstoffen in ähnlichen Cross-Over-Studien. Insbesondere sind uns keine ähnlichen Studien bekannt, die mit einer derartigen statistischen Signifikanz Effekte auf die Gesamtwachzeit in der zweiten Nachthälfte und die Gesamtwachzeit bezogen auf jede Nachtstunde erzielt haben."
Jörn Aldag, Vorstandsvorsitzender der Evotec AG, sagte: "Obwohl vorhandene Schlafmittel bestimmte Aspekte der Schlaflosigkeit behandeln, gibt es noch kein Medikament, das alle Bedürfnisse von Patienten mit Schlafstörungen befriedigt. In unserer Studie hat sich EVT 201 hinsichtlich aller Hauptprobleme von schlaflosen Menschen mit extrem beeindruckenden Ergebnissen bewährt. Dazu zählen insbesondere die Einschlaf- und Durchschlafdauer. Bemerkenswert ist auch, dass die Patienten gleichzeitig am nächsten Morgen subjektiv keine Nachwirkungen, so genannte Hang-over-Effekte, empfinden. Wir glauben, dass EVT 201 damit ein sehr vorteilhaftes Wirkungsprofil gegenüber derzeit verfügbaren Schlafmitteln besitzt, einschließlich solcher, die sich zurzeit in der Spätphase der klinischen Entwicklung befinden."
Hauptprüfarzt Dr. James Walsh, Executive Director des Sleep Medici-ne and Research Center, St. John's Mercy Medical Center, Chester-field, Missouri, USA, sagte: "Mit seinem Wirkmechanismus als partiell-positiver allosterischer Modulator von GABAA-Rezeptoren eröffnet EVT 201 einen neuen Weg zur Behandlung der Schlaflosigkeit. Da das GABAA-System sehr gut verstanden ist, ist das Risiko unerwarteter Nebenwirkungen deutlich geringer als bei vollständig neuen Wirkmechanismen. Dies in Kombination mit den robusten Ergebnissen dieser Studie, besonders im Hinblick auf das Durchschlafverhalten, lässt das Medikament als sehr viel versprechend für Patienten mit Schlafstörungen erscheinen.
Evotec führt derzeit eine zweite klinische Phase-II-Studie zur weiteren Differenzierung von EVT 201 in älteren Patienten durch, die unter primären Schlafstörungen leiden. Die Eckdaten zu den wesentlichen Endpunkten dieser Studie werden voraussichtlich im Oktober 2007 bekannt gegeben.
16 Oct 2007
Evotec berichtet positive Ergebnisse zu den wesentlichen Endpunkten ihrer Phase-II-Studie mit EVT 201 an älteren Patienten mit Schlafstörungen und Schläfrigkeit am Tag
- Statistische Signifikanz für primäre und wichtige sekundäre Endpunkte in beiden Dosierungsstufen
- Daten bestätigen robuste Ergebnisse der ersten Phase-II-Studie an Erwachsenen hinsichtlich Einschlafzeit und Durchschlafdauer
Hamburg, Deutschland | Oxford, England - Evotec AG (Deutsche Börse: EVT) gab heute positive Ergebnisse zu den wesentlichen Endpunkten (Top-Line-Ergebnisse) ihrer zweiten klinischen Phase-II-Studie mit EVT 201 bekannt. Die Studie wurde an älteren Patienten durchgeführt, die primär an Schlaflosigkeit sowie an Schläfrigkeit am Tag litten. Die Ergebnisse basieren auf der zuvor spezifizierten "Intention-to-treat-Analyse" aller 149 in die Studie aufgenommenen Patienten.
Die Studie zeigte für beide Dosierungen von EVT 201 statistisch hoch signifikante Verbesserungen gegenüber Placebo hinsichtlich des primären Endpunkts, der mittels polysomnographischer (PSG) Untersuchungen bestimmten Gesamtschlafdauer ("Total Sleep Time", TST). Im Vergleich zu Placebo stieg die Gesamtschlafdauer im Mittel um 30,9 Min. (9%) nach Gabe von 1,5 mg EVT 201 und um 56,4 Min. (17%) nach Gabe von 2,5 mg EVT 201 (p=0,0001 bzw. p=<0,0001).
Signifikante Verbesserungen wurden auch für wichtige, ebenfalls mit PSG bestimmte sekundäre Endpunkte beobachtet, darunter die Wachzeit nach dem ersten Einschlafen ("Wake After Sleep Onset", WASO) und die Dauer bis zum Einsetzen eines anhaltenden Schlafs ("Latency to Persistent Sleep", LPS). Obwohl die Studie nicht dafür ausgelegt war, zeigte die 2,5 mg Dosierung darüber hinaus einen signifikanten Effekt auf die gesamte Wachzeit ("Total Wake Time", TWT) während der zweiten Nachthälfte. Das lässt darauf schließen, dass EVT 201 sehr wirksam darin ist, den Schlaf über die gesamte Nacht aufrecht zu erhalten. Diese Schlussfolgerung wird gestützt durch die stündliche Analyse der Gesamtwachzeit. Die Behandlung mit EVT 201 führte zu einer statistisch signifikanten Reduktion der Gesamt-Wachzeit für alle Stunden der Nacht mit Ausnahme der Stunde 7.
Bei der Studie handelt es sich um eine Placebo-kontrollierte Doppelblindstudie im Parallelgruppen-Design zur Bestimmung der Wirksamkeit von EVT 201 in den Dosierungen 1,5 mg und 2,5 mg an sieben aufeinander folgenden Nächten. Die Studie wurde unter Verwendung objektiver und subjektiver Kriterien in 20 Schlaflabors in den USA durchgeführt. PSG-Daten wurden in den Nächten 1, 6 und 7 erhoben; die Ergebnisse stellen den Mittelwert der Daten aus diesen drei Nächten dar.


Darüber hinaus ergab die PSG-Analyse, dass EVT 201 die Schlafarchitektur grundsätzlich erhalten hat.
Diese PSG-Ergebnisse wurden gestützt durch die von den Patienten berichteten subjektiven Werte für Gesamtschlafdauer ("subjective Total Sleep Time", sTST), für die Zeit bis zum Einschlafen ("subjective Sleep Onset Latency", sSOL) sowie für die Wachzeit nach dem ersten Einschlafen ("subjective Wake after Sleep Onset", sWASO).
Die Patienten berichteten in jeder Nacht über eine verbesserte Schlafqualität und 30 Minuten nach Erwachen (etwa 9 Stunden nach Dosierung) über keine Nachwirkungen.
Ein weiteres Element des Studiendesigns war die Ermittlung der Leistungsfähigkeit am Tag 8. Dazu gehörte der Multiple Schlaflatenz-Test ("Multiple Sleep Latency Test", MSLT), ein objektiver Test zur Ermittlung der Schläfrigkeit am Tag. Erste Analysen zeigten, dass EVT 201 über den gesamten Tagesverlauf in beiden Dosierungen gegenüber Placebo zu einer statistisch signifikanten Verbesserung im MSLT führte - ein Hinweis darauf, dass Patienten nach der Behandlung mit EVT 201 tagsüber weniger schläfrig waren.
Die Leistungsfähigkeit am Tag wurde darüber hinaus anhand weiterer objektiver Tests ermittelt, und zwar durch den "Rey Auditory Verbal Learning Test" (RAVLT), einen Test zur Ermittlung des verbalen Kurzzeitgedächnisses, und den Psychomotorischen Vigilanz-Test ("Psychomotor Vigilance Task", PVT), einen Test zur Ermittlung der anhaltenden Aufmerksamkeit und Reaktionszeit. Zusätzlich wurde die Leistungsfähigkeit am Tag subjektiv mit Hilfe der Karolinska Schläfrigkeitsskala ("Karolinska Sleepiness Scale", KSS) bestimmt. Erste Analysen zeigten, dass es zwischen den mit EVT 201 und Placebo behandelten Probanden insgesamt keinen signifikanten Unterschied gab. Diese Endpunkte werden noch detaillierter analysiert.
Die Ergebnisse dieser Studie bestätigen die Wirkung von EVT 201 auf Einschlafzeit und Durchschlafdauer, die bereits an Erwachsenen in der Studie 2004 beobachtet wurde. Sie zeigen ebenfalls, dass die gleichen Dosierungen (1,5 mg bzw. 2,5 mg EVT 201) auch bei älteren Patienten wirken und keine signifikanten Nachwirkungen am Folgetag hervorrufen.
Die weitere Analyse der verbleibenden sekundären und exploratorischen Endpunkte ist noch nicht abgeschlossen.
"Wir freuen uns sehr, dass diese Ergebnisse bei älteren Patienten, die unter Schlafstörungen leiden, erneut das exzellente Profil von EVT 201 als potenzielles Schlafmittel bestätigen, das Patienten hilft schnell einzuschlafen, die Nacht über gut durchzuschlafen und am nächsten Morgen aufzuwachen, ohne Nachwirkungen zu verspüren und mit dem Gefühl wirklich gut geschlafen zu haben," sagte Dr. John Kemp, Chief Research & Development Officer, Evotec AG. "Mit seinem Wirkmechanismus als partiell-positiver allosterischer Modulator von GABAA-Rezeptoren eröffnet EVT 201 einen neuen Weg zur Behandlung der Schlaflosigkeit. Da das GABAA-System sehr gut verstanden ist, ist das Risiko unerwarteter Nebenwirkungen deutlich geringer als bei vollständig neuen Wirkmechanismen."
Jörn Aldag, Vorstandsvorsitzender der Evotec AG, kommentierte: "Die positiven Ergebnisse dieser zweiten klinischen Phase-II-Studie mit EVT 201 sind um so erfreulicher, als es diesmal um ältere Patienten ging, die mit heute verfügbaren Schlafmitteln oft nur unzureichend behandelt werden können. Die Bestätigung der Ergebnisse unserer früheren Phase-II-Studie an Erwachsenen belegt eindeutig, dass EVT 201 sich zur Behandlung von Schlafstörungen erwachsener und älterer Patienten eignet. Wir glauben, dass EVT 201 auf Basis dieser Daten jetzt sehr attraktiv für potenzielle Partner ist."
"Wir verfügen jetzt über zwei Datenpakete, die sehr eindeutig zeigen, dass EVT 201 bei erwachsenen und bei älteren Patienten das gleiche Profil besitzt - deutliche Effekte auf die Einschlafzeit und Durchschlafdauer mit nur minimalen Nachwirkungen am Folgetag. Das ist für einen Arzneimittelkandidaten in diesem Entwicklungsstadium außergewöhnlich gut", fügte Dr. Tim Tasker, Executive Vice President Clinical Development der Evotec AG hinzu. "Die Ergebnisse zeigen zudem, dass ältere Patienten, die unter Schlaflosigkeit während der Nacht und Schläfrigkeit am Tag leiden, gemessen mit dem objektiven MSLT-Test nach sieben Tagen Behandlung tagsüber deutlich weniger schläfrig waren. Die Größe dieses Effekts war klinisch signifikant und wurde bisher in keiner der neueren Studien mit Schlafmittelkandidaten gezeigt. Dieses viel versprechende Top-line-Ergebnis wird nun im Rahmen der weiteren Analyse der 2005-Daten im Detail untersucht."
Hauptprüfarzt Dr. James Walsh, Executive Director des Sleep Medicine and Research Center, St. John's Mercy Medical Center, Chesterfield, Missouri, USA sagte: "In dieser zweiten Phase II-Studie mit EVT 201 konnten wir bei älteren Patienten mit der gleichen Dosierung die gleiche deutliche Wirksamkeit erzielen wie zuvor in der ersten Phase II-Studie bei Erwachsenen. Es ist hoch interessant, dass die Schlaf fördernden Effekte, die wir während der gesamten Nacht beobachten, und das nachweisbare Ausbleiben signifikanter Nachwirkungen am Folgetag dazu führen, dass die Verbesserung des Schlafs mit einer deutlich verbesserten Wachheit während des Tages einhergeht. Diese Kombination verleiht EVT 201 ein sehr attraktives Profil als Schlafmittel, das die Symptome der Schlaflosigkeit bei älteren Patienten sowohl bei Nacht als auch bei Tag reduziert."
Evotec berichtet positive Ergebnisse zu den wesentlichen Endpunkten ihrer Phase-II-Studie mit EVT 201 an älteren Patienten mit Schlafstörungen und Schläfrigkeit am Tag
- Statistische Signifikanz für primäre und wichtige sekundäre Endpunkte in beiden Dosierungsstufen
- Daten bestätigen robuste Ergebnisse der ersten Phase-II-Studie an Erwachsenen hinsichtlich Einschlafzeit und Durchschlafdauer
Hamburg, Deutschland | Oxford, England - Evotec AG (Deutsche Börse: EVT) gab heute positive Ergebnisse zu den wesentlichen Endpunkten (Top-Line-Ergebnisse) ihrer zweiten klinischen Phase-II-Studie mit EVT 201 bekannt. Die Studie wurde an älteren Patienten durchgeführt, die primär an Schlaflosigkeit sowie an Schläfrigkeit am Tag litten. Die Ergebnisse basieren auf der zuvor spezifizierten "Intention-to-treat-Analyse" aller 149 in die Studie aufgenommenen Patienten.
Die Studie zeigte für beide Dosierungen von EVT 201 statistisch hoch signifikante Verbesserungen gegenüber Placebo hinsichtlich des primären Endpunkts, der mittels polysomnographischer (PSG) Untersuchungen bestimmten Gesamtschlafdauer ("Total Sleep Time", TST). Im Vergleich zu Placebo stieg die Gesamtschlafdauer im Mittel um 30,9 Min. (9%) nach Gabe von 1,5 mg EVT 201 und um 56,4 Min. (17%) nach Gabe von 2,5 mg EVT 201 (p=0,0001 bzw. p=<0,0001).
Signifikante Verbesserungen wurden auch für wichtige, ebenfalls mit PSG bestimmte sekundäre Endpunkte beobachtet, darunter die Wachzeit nach dem ersten Einschlafen ("Wake After Sleep Onset", WASO) und die Dauer bis zum Einsetzen eines anhaltenden Schlafs ("Latency to Persistent Sleep", LPS). Obwohl die Studie nicht dafür ausgelegt war, zeigte die 2,5 mg Dosierung darüber hinaus einen signifikanten Effekt auf die gesamte Wachzeit ("Total Wake Time", TWT) während der zweiten Nachthälfte. Das lässt darauf schließen, dass EVT 201 sehr wirksam darin ist, den Schlaf über die gesamte Nacht aufrecht zu erhalten. Diese Schlussfolgerung wird gestützt durch die stündliche Analyse der Gesamtwachzeit. Die Behandlung mit EVT 201 führte zu einer statistisch signifikanten Reduktion der Gesamt-Wachzeit für alle Stunden der Nacht mit Ausnahme der Stunde 7.
Bei der Studie handelt es sich um eine Placebo-kontrollierte Doppelblindstudie im Parallelgruppen-Design zur Bestimmung der Wirksamkeit von EVT 201 in den Dosierungen 1,5 mg und 2,5 mg an sieben aufeinander folgenden Nächten. Die Studie wurde unter Verwendung objektiver und subjektiver Kriterien in 20 Schlaflabors in den USA durchgeführt. PSG-Daten wurden in den Nächten 1, 6 und 7 erhoben; die Ergebnisse stellen den Mittelwert der Daten aus diesen drei Nächten dar.


Darüber hinaus ergab die PSG-Analyse, dass EVT 201 die Schlafarchitektur grundsätzlich erhalten hat.
Diese PSG-Ergebnisse wurden gestützt durch die von den Patienten berichteten subjektiven Werte für Gesamtschlafdauer ("subjective Total Sleep Time", sTST), für die Zeit bis zum Einschlafen ("subjective Sleep Onset Latency", sSOL) sowie für die Wachzeit nach dem ersten Einschlafen ("subjective Wake after Sleep Onset", sWASO).
Die Patienten berichteten in jeder Nacht über eine verbesserte Schlafqualität und 30 Minuten nach Erwachen (etwa 9 Stunden nach Dosierung) über keine Nachwirkungen.
Ein weiteres Element des Studiendesigns war die Ermittlung der Leistungsfähigkeit am Tag 8. Dazu gehörte der Multiple Schlaflatenz-Test ("Multiple Sleep Latency Test", MSLT), ein objektiver Test zur Ermittlung der Schläfrigkeit am Tag. Erste Analysen zeigten, dass EVT 201 über den gesamten Tagesverlauf in beiden Dosierungen gegenüber Placebo zu einer statistisch signifikanten Verbesserung im MSLT führte - ein Hinweis darauf, dass Patienten nach der Behandlung mit EVT 201 tagsüber weniger schläfrig waren.
Die Leistungsfähigkeit am Tag wurde darüber hinaus anhand weiterer objektiver Tests ermittelt, und zwar durch den "Rey Auditory Verbal Learning Test" (RAVLT), einen Test zur Ermittlung des verbalen Kurzzeitgedächnisses, und den Psychomotorischen Vigilanz-Test ("Psychomotor Vigilance Task", PVT), einen Test zur Ermittlung der anhaltenden Aufmerksamkeit und Reaktionszeit. Zusätzlich wurde die Leistungsfähigkeit am Tag subjektiv mit Hilfe der Karolinska Schläfrigkeitsskala ("Karolinska Sleepiness Scale", KSS) bestimmt. Erste Analysen zeigten, dass es zwischen den mit EVT 201 und Placebo behandelten Probanden insgesamt keinen signifikanten Unterschied gab. Diese Endpunkte werden noch detaillierter analysiert.
Die Ergebnisse dieser Studie bestätigen die Wirkung von EVT 201 auf Einschlafzeit und Durchschlafdauer, die bereits an Erwachsenen in der Studie 2004 beobachtet wurde. Sie zeigen ebenfalls, dass die gleichen Dosierungen (1,5 mg bzw. 2,5 mg EVT 201) auch bei älteren Patienten wirken und keine signifikanten Nachwirkungen am Folgetag hervorrufen.
Die weitere Analyse der verbleibenden sekundären und exploratorischen Endpunkte ist noch nicht abgeschlossen.
"Wir freuen uns sehr, dass diese Ergebnisse bei älteren Patienten, die unter Schlafstörungen leiden, erneut das exzellente Profil von EVT 201 als potenzielles Schlafmittel bestätigen, das Patienten hilft schnell einzuschlafen, die Nacht über gut durchzuschlafen und am nächsten Morgen aufzuwachen, ohne Nachwirkungen zu verspüren und mit dem Gefühl wirklich gut geschlafen zu haben," sagte Dr. John Kemp, Chief Research & Development Officer, Evotec AG. "Mit seinem Wirkmechanismus als partiell-positiver allosterischer Modulator von GABAA-Rezeptoren eröffnet EVT 201 einen neuen Weg zur Behandlung der Schlaflosigkeit. Da das GABAA-System sehr gut verstanden ist, ist das Risiko unerwarteter Nebenwirkungen deutlich geringer als bei vollständig neuen Wirkmechanismen."
Jörn Aldag, Vorstandsvorsitzender der Evotec AG, kommentierte: "Die positiven Ergebnisse dieser zweiten klinischen Phase-II-Studie mit EVT 201 sind um so erfreulicher, als es diesmal um ältere Patienten ging, die mit heute verfügbaren Schlafmitteln oft nur unzureichend behandelt werden können. Die Bestätigung der Ergebnisse unserer früheren Phase-II-Studie an Erwachsenen belegt eindeutig, dass EVT 201 sich zur Behandlung von Schlafstörungen erwachsener und älterer Patienten eignet. Wir glauben, dass EVT 201 auf Basis dieser Daten jetzt sehr attraktiv für potenzielle Partner ist."
"Wir verfügen jetzt über zwei Datenpakete, die sehr eindeutig zeigen, dass EVT 201 bei erwachsenen und bei älteren Patienten das gleiche Profil besitzt - deutliche Effekte auf die Einschlafzeit und Durchschlafdauer mit nur minimalen Nachwirkungen am Folgetag. Das ist für einen Arzneimittelkandidaten in diesem Entwicklungsstadium außergewöhnlich gut", fügte Dr. Tim Tasker, Executive Vice President Clinical Development der Evotec AG hinzu. "Die Ergebnisse zeigen zudem, dass ältere Patienten, die unter Schlaflosigkeit während der Nacht und Schläfrigkeit am Tag leiden, gemessen mit dem objektiven MSLT-Test nach sieben Tagen Behandlung tagsüber deutlich weniger schläfrig waren. Die Größe dieses Effekts war klinisch signifikant und wurde bisher in keiner der neueren Studien mit Schlafmittelkandidaten gezeigt. Dieses viel versprechende Top-line-Ergebnis wird nun im Rahmen der weiteren Analyse der 2005-Daten im Detail untersucht."
Hauptprüfarzt Dr. James Walsh, Executive Director des Sleep Medicine and Research Center, St. John's Mercy Medical Center, Chesterfield, Missouri, USA sagte: "In dieser zweiten Phase II-Studie mit EVT 201 konnten wir bei älteren Patienten mit der gleichen Dosierung die gleiche deutliche Wirksamkeit erzielen wie zuvor in der ersten Phase II-Studie bei Erwachsenen. Es ist hoch interessant, dass die Schlaf fördernden Effekte, die wir während der gesamten Nacht beobachten, und das nachweisbare Ausbleiben signifikanter Nachwirkungen am Folgetag dazu führen, dass die Verbesserung des Schlafs mit einer deutlich verbesserten Wachheit während des Tages einhergeht. Diese Kombination verleiht EVT 201 ein sehr attraktives Profil als Schlafmittel, das die Symptome der Schlaflosigkeit bei älteren Patienten sowohl bei Nacht als auch bei Tag reduziert."




2 Jahre gute Arbeit, nur die Aktionärsaugen glänzen nicht vor Freude
(22.06.2006) Evotec und Roche bilden globale Allianz zur Entdeckung neuartiger Wirkstoffe
(19.07.2006) Evotec schließt Forschungskooperation mit italienischem Biotechunternehmen DAC
(10.08.2006) Evotec schließt klinische Phase I mit EVT101 erfolgreich ab
(14.08.2006) CHDI wählt Evotec zum strategischen Forschungspartner bei der Suche nach Wirkstoffen zur Behandlung der Huntington-Krankheit
(25.09.2006) Evotec startet klinische Phase II-Studie mit EVT 201 zur Behandlung von Schlafstörungen
(17.10.2006) Daiichi Pharmaceutical wählt Evotec zum Wirkstoff-Forschungspartner
(21.11.2006) Evotec startet zweite klinische Phase II-Studie mit Schlafmittel-Wirkstoff EVT 201
(01.12.2006) PerkinElmer übernimmt Evotec Technologies
(24.01.2007) Solvay Pharmaceuticals wählt Evotec als Partner in der fragmentbasierten Wirkstoffforschung
(01.03.2007) Evotec und Interprotein unterzeichnen Vereinbarung über die Entwicklung von Inhibitoren von Interleukin 6
(21.03.2007) Evotec und Boehringer Ingelheim vereinbaren Zusammenarbeit zur Identifizierung neuer Alzheimer-Targets
(26.03.2007) Evotec beginnt ihre erste klinische Phase-I-Studie mit Raucherentwöhnungsmedikament EVT 302
(30.03.2007) Evotec übernimmt Neuro3d
(11.05.2007) Panacos verlängert Vertrag mit Evotec in der medizinischen Chemie ins vierte Jahr
(06.06.2007) Evotec berichtet positive Wirksamkeitsdaten für Schlafmittelkandidat EVT 201
(15.06.2007) Evotec erweitert seine fragmentbasierte Wirkstoffforschung durch den Kauf von NMR-Screening-Technologien von Combinature
(12.07.2007) Evotec und Research Support International Limited gründen Joint Venture zur Herstellung und Vermarktung von Substanzbibliotheken
(18.07.2007) Evotec erweitert seine Kapazitäten zur Sterilproduktion von Medikamenten nach GMP-Standards
(05.09.2007) Europäisches Zentrum für die moderne Wirkstoffforschung in Hamburg gegründet
(07.09.2007) Evotec berichtet Details ihrer positiven Phase-II-Wirksamkeitsstudie mit EVT 201 gegen Schlafstörungen
(12.09.2007) Evotec verkauft chemische Entwicklungssparte für 31,5 Mio. Britische Pfund (ca. 46,4 Mio. Euro) an Aptuit
(18.10.2007) Evotec berichtet positive Ergebnisse zu Endpunkten ihrer Phase-II-Studie mit EVT 201 an älteren Patienten mit Schlafstörungen
(09.01.2008) Evotec Phase I Unbedenklichkeits- und Verträglichkeitsstudie mit EVT 302 erfolgreich abgeschlossen
(18.02.2008) Evotec und CHDI erweitern Zusammenarbeit im Umfang von bis zu 37 Mio. US-Dollar
(03.03.2008) Evotec startet Phase II mit EVT 302 für die Raucherentwöhnung
(07.03.2008) Stärkung des Life-Science-Standortes Norddeutschland
(07.03.2008) Evotec erweitert Kooperation mit InterMune
(14.03.2008) Spermatech wählt Evotec zum Partner für Hochdurchsatz-Screening und Wirkstoffsuche
(31.03.2008) Evotecs EVT 101 gelangt ins menschliche Gehirn und moduliert die Hirnaktivität während der Durchführung kognitiver Aufgaben
(01.04.2008) Ono schließt neuen Vertrag zur fragment-basierten Wirkstoffforschung mit Evotec
(06.05.2008) Evotec schließt Akquisition von Renovis ab
(29.06.08) Evotec steht nahe am Allzeittief
Ticktack......ticktack.......ticktack!!!!
(22.06.2006) Evotec und Roche bilden globale Allianz zur Entdeckung neuartiger Wirkstoffe
(19.07.2006) Evotec schließt Forschungskooperation mit italienischem Biotechunternehmen DAC
(10.08.2006) Evotec schließt klinische Phase I mit EVT101 erfolgreich ab
(14.08.2006) CHDI wählt Evotec zum strategischen Forschungspartner bei der Suche nach Wirkstoffen zur Behandlung der Huntington-Krankheit
(25.09.2006) Evotec startet klinische Phase II-Studie mit EVT 201 zur Behandlung von Schlafstörungen
(17.10.2006) Daiichi Pharmaceutical wählt Evotec zum Wirkstoff-Forschungspartner
(21.11.2006) Evotec startet zweite klinische Phase II-Studie mit Schlafmittel-Wirkstoff EVT 201
(01.12.2006) PerkinElmer übernimmt Evotec Technologies
(24.01.2007) Solvay Pharmaceuticals wählt Evotec als Partner in der fragmentbasierten Wirkstoffforschung
(01.03.2007) Evotec und Interprotein unterzeichnen Vereinbarung über die Entwicklung von Inhibitoren von Interleukin 6
(21.03.2007) Evotec und Boehringer Ingelheim vereinbaren Zusammenarbeit zur Identifizierung neuer Alzheimer-Targets
(26.03.2007) Evotec beginnt ihre erste klinische Phase-I-Studie mit Raucherentwöhnungsmedikament EVT 302
(30.03.2007) Evotec übernimmt Neuro3d
(11.05.2007) Panacos verlängert Vertrag mit Evotec in der medizinischen Chemie ins vierte Jahr
(06.06.2007) Evotec berichtet positive Wirksamkeitsdaten für Schlafmittelkandidat EVT 201
(15.06.2007) Evotec erweitert seine fragmentbasierte Wirkstoffforschung durch den Kauf von NMR-Screening-Technologien von Combinature
(12.07.2007) Evotec und Research Support International Limited gründen Joint Venture zur Herstellung und Vermarktung von Substanzbibliotheken
(18.07.2007) Evotec erweitert seine Kapazitäten zur Sterilproduktion von Medikamenten nach GMP-Standards
(05.09.2007) Europäisches Zentrum für die moderne Wirkstoffforschung in Hamburg gegründet
(07.09.2007) Evotec berichtet Details ihrer positiven Phase-II-Wirksamkeitsstudie mit EVT 201 gegen Schlafstörungen
(12.09.2007) Evotec verkauft chemische Entwicklungssparte für 31,5 Mio. Britische Pfund (ca. 46,4 Mio. Euro) an Aptuit
(18.10.2007) Evotec berichtet positive Ergebnisse zu Endpunkten ihrer Phase-II-Studie mit EVT 201 an älteren Patienten mit Schlafstörungen
(09.01.2008) Evotec Phase I Unbedenklichkeits- und Verträglichkeitsstudie mit EVT 302 erfolgreich abgeschlossen
(18.02.2008) Evotec und CHDI erweitern Zusammenarbeit im Umfang von bis zu 37 Mio. US-Dollar
(03.03.2008) Evotec startet Phase II mit EVT 302 für die Raucherentwöhnung
(07.03.2008) Stärkung des Life-Science-Standortes Norddeutschland
(07.03.2008) Evotec erweitert Kooperation mit InterMune
(14.03.2008) Spermatech wählt Evotec zum Partner für Hochdurchsatz-Screening und Wirkstoffsuche
(31.03.2008) Evotecs EVT 101 gelangt ins menschliche Gehirn und moduliert die Hirnaktivität während der Durchführung kognitiver Aufgaben
(01.04.2008) Ono schließt neuen Vertrag zur fragment-basierten Wirkstoffforschung mit Evotec
(06.05.2008) Evotec schließt Akquisition von Renovis ab
(29.06.08) Evotec steht nahe am Allzeittief
Ticktack......ticktack.......ticktack!!!!
Juli 2007










Antwort auf Beitrag Nr.: 34.446.218 von bolero6 am 06.07.08 13:55:57


eine 0815 company scheint das wohl nicht zu sein
was meint denn unser meister zenman dazu ?






eine 0815 company scheint das wohl nicht zu sein
was meint denn unser meister zenman dazu ?



Antwort auf Beitrag Nr.: 34.446.218 von bolero6 am 06.07.08 13:55:57am Rande zu der VR1-Kooperation mit Pfizer
Es scheint so zu sein, dass die Entwicklung von AMG-517 eingestellt wurde. Wie beschrieben, richtet sich AMG-517 gegen den Capsaicin-Rezeptor. Dies ist der Rezeptor, bei dem es auch in Evotec's VR1-Kooperation mit Pfizer geht. VR1 bzw. TRPV1 soll u.a auch die Körpertemperatur regulieren... bei AMG-517 konnte es passieren, dass sich der Körper überhitzte. Ich weiß nicht, ob das ein Problem für diese Kooperation darstellt. Unten stehen zwei Abstrakts: eins kommt zu dem Schluss, dass sich VR1 nicht nutzen lässt (was das Ende der Kooperation mit Pfizer bedeuten würde), das andere spätere meint, dass es Möglichkeiten gibt, das Schmerzempfinden zu beeinflussen, ohne dass die Körpertemperatur dadurch negativ beeinflusst wird.
Capsaicin ist der Stoff im roten Chili, der die Schärfe erzeugt, indem er auf den VR1-Rezeptor einwirkt... also ein Brennen wie bei Hitze. Schmerz- und Hitzeempfinden können also über Stoffe, die auf VR1 einwirken, beeinflusst werden.
*********
http://www.evotec.com/en/our_pipeline/vr1.aspx
Expanded Partnership with Pfizer, Planned Phase I in 2008
Certain ion channels are known to be key mediators of pain signaling. A specific family of ion channels known as transient receptor potential (TRP) ion channels, are attractive targets for drug discovery. TRPV1 (VR1 - vanilloid receptor 1) is one specific member that has compelling preclinical validation as a target for the treatment of a number of different pain states. Evotec's VR1 program is partnered with Pfizer.
In this global alliance, Evotec's and Pfizer's combined research and development teams are working together to design drugs that block VR1 and prevent it from signaling the sensation of pain. If successful, Evotec expect to have an effective, non-narcotic, non-addictive and non-steroidal analgesic to treat chronic pain, with minimal side effects.
Evotec have demonstrated oral analgesic efficacy in multiple preclinical models of pain. In addition, given VR1's role in inflammatory disease pathologies, it may also be possible to develop treatments for non-neurological conditions, such as urinary incontinence, irritable bowel syndrome and asthma.
With Pfizer's extension of the program in 2007, Evotec expects one of these compounds to advance into human clinical trials in 2008. Although the joint research phase officially ends in June 2008, Evotec are eligible to receive total milestone payments of more than $170 million and double-digit royalties on worldwide net sales per product successfully developed and commercialized under this collaboration.
********
http://www.amgen.com/science/pipe_AMG517.html
AMG 517
A new target for inflammatory pain known as vanilloid receptor 1 (TRPV1) is being investigated. Clues about this novel target have been identified by the activity of capsaicin, an irritant found in hot chili peppers. Capsaicin selectively activates TRPV1, a receptor found in pain-sensing nerves. Loss of TRPV1 responsive nerves or loss of TRPV1 expression causes decreased pain sensitivity during inflammation. Phase 1 clinical studies with the TRPV1 antagonist AMG 517 were initiated in 2004.
*********
http://www.ncbi.nlm.nih.gov/pubmed/18337008
Pain. 2008 May;136(1-2):202-10. Epub 2008 Mar 11.
Pharmacological blockade of the vanilloid receptor TRPV1 elicits marked hyperthermia in humans.
The vanilloid receptor TRPV1 has been identified as a molecular target for the treatment of pain associated with inflammatory diseases and cancer. Hence, TRPV1 antagonists have been considered for therapeutic evaluation in such diseases. During Phase I clinical trials with AMG 517, a highly selective TRPV1 antagonist, we found that TRPV1 blockade elicited marked, but reversible, and generally plasma concentration-dependent hyperthermia. Similar to what was observed in rats, dogs, and monkeys, hyperthermia was attenuated after repeated dosing of AMG 517 (at the highest dose tested) in humans during a second Phase I trial. However, AMG 517 administered after molar extraction (a surgical cause of acute pain) elicited long-lasting hyperthermia with maximal body temperature surpassing 40 degrees C, suggesting that TRPV1 blockade elicits undesirable hyperthermia in susceptible individuals. Mechanisms of AMG 517-induced hyperthermia were then studied in rats. AMG 517 caused hyperthermia by inducing tail skin vasoconstriction and increasing thermogenesis, which suggests that TRPV1 regulates vasomotor tone and metabolic heat production. In conclusion, these results demonstrate that: (a) TRPV1-selective antagonists like AMG 517 cannot be developed for systemic use as stand alone agents for treatment of pain and other diseases, (b) individual susceptibility influences magnitude of hyperthermia observed after TRPV1 blockade, and (c) TRPV1 plays a pivotal role as a molecular regulator for body temperature in humans.
*********
http://lib.bioinfo.pl/auth:Magal,E
J Pharmacol Exp Ther. 2008 Apr 17; : 18420600 (P,S,E,B,D) Antihyperalgesic effects of AMG8562, a novel vanilloid receptor TRPV1 modulator that does not cause hyperthermia in rats.
Amgen Inc.
Antagonists of the vanilloid receptor TRPV1 have been reported to produce anti-hyperalgesic effects in animal models of pain. These antagonists, however, also caused concomitant hyperthermia in rodents, dogs, monkeys and humans. Antagonist-induced hyperthermia was not observed in TRPV1 knockout mice, suggesting that the hyperthermic effect is exclusively mediated through TRPV1. Since antagonist-induced hyperthermia is considered a hurdle for developing TRPV1 antagonists as therapeutics, we investigated the possibility of eliminating hyperthermia while maintaining anti-hyperalgesia. Here, we report four potent and selective TRPV1 modulators with unique in vitro pharmacology profiles (Profiles A through D) and their respective effects on body temperature. We found that Profile C modulator, AMG8562, blocks capsaicin activation of TRPV1, does not affect heat activation of TRPV1, potentiates pH 5 activation of TRPV1 in vitro and does not cause hyperthermia in vivo in rats. We further profiled AMG8562 in an in vivo biochemical (agonist) challenge model, rodent pain models and tested for its side effects. We show that AMG8562 significantly blocks capsaicin-induced flinching behavior, produces statistically significant efficacy in CFA- and skin incision-induced thermal hyperalgesia, and acetic acid-induced writhing models, with no profound effects on locomotor activity. Based on the data shown here, we conclude that it is feasible to modulate TRPV1 in a manner that does not cause hyperthermia while maintaining efficacy in rodent pain models.
mfg ipollit
Es scheint so zu sein, dass die Entwicklung von AMG-517 eingestellt wurde. Wie beschrieben, richtet sich AMG-517 gegen den Capsaicin-Rezeptor. Dies ist der Rezeptor, bei dem es auch in Evotec's VR1-Kooperation mit Pfizer geht. VR1 bzw. TRPV1 soll u.a auch die Körpertemperatur regulieren... bei AMG-517 konnte es passieren, dass sich der Körper überhitzte. Ich weiß nicht, ob das ein Problem für diese Kooperation darstellt. Unten stehen zwei Abstrakts: eins kommt zu dem Schluss, dass sich VR1 nicht nutzen lässt (was das Ende der Kooperation mit Pfizer bedeuten würde), das andere spätere meint, dass es Möglichkeiten gibt, das Schmerzempfinden zu beeinflussen, ohne dass die Körpertemperatur dadurch negativ beeinflusst wird.
Capsaicin ist der Stoff im roten Chili, der die Schärfe erzeugt, indem er auf den VR1-Rezeptor einwirkt... also ein Brennen wie bei Hitze. Schmerz- und Hitzeempfinden können also über Stoffe, die auf VR1 einwirken, beeinflusst werden.
*********
http://www.evotec.com/en/our_pipeline/vr1.aspx
Expanded Partnership with Pfizer, Planned Phase I in 2008
Certain ion channels are known to be key mediators of pain signaling. A specific family of ion channels known as transient receptor potential (TRP) ion channels, are attractive targets for drug discovery. TRPV1 (VR1 - vanilloid receptor 1) is one specific member that has compelling preclinical validation as a target for the treatment of a number of different pain states. Evotec's VR1 program is partnered with Pfizer.
In this global alliance, Evotec's and Pfizer's combined research and development teams are working together to design drugs that block VR1 and prevent it from signaling the sensation of pain. If successful, Evotec expect to have an effective, non-narcotic, non-addictive and non-steroidal analgesic to treat chronic pain, with minimal side effects.
Evotec have demonstrated oral analgesic efficacy in multiple preclinical models of pain. In addition, given VR1's role in inflammatory disease pathologies, it may also be possible to develop treatments for non-neurological conditions, such as urinary incontinence, irritable bowel syndrome and asthma.
With Pfizer's extension of the program in 2007, Evotec expects one of these compounds to advance into human clinical trials in 2008. Although the joint research phase officially ends in June 2008, Evotec are eligible to receive total milestone payments of more than $170 million and double-digit royalties on worldwide net sales per product successfully developed and commercialized under this collaboration.
********
http://www.amgen.com/science/pipe_AMG517.html
AMG 517
A new target for inflammatory pain known as vanilloid receptor 1 (TRPV1) is being investigated. Clues about this novel target have been identified by the activity of capsaicin, an irritant found in hot chili peppers. Capsaicin selectively activates TRPV1, a receptor found in pain-sensing nerves. Loss of TRPV1 responsive nerves or loss of TRPV1 expression causes decreased pain sensitivity during inflammation. Phase 1 clinical studies with the TRPV1 antagonist AMG 517 were initiated in 2004.
*********
http://www.ncbi.nlm.nih.gov/pubmed/18337008
Pain. 2008 May;136(1-2):202-10. Epub 2008 Mar 11.
Pharmacological blockade of the vanilloid receptor TRPV1 elicits marked hyperthermia in humans.
The vanilloid receptor TRPV1 has been identified as a molecular target for the treatment of pain associated with inflammatory diseases and cancer. Hence, TRPV1 antagonists have been considered for therapeutic evaluation in such diseases. During Phase I clinical trials with AMG 517, a highly selective TRPV1 antagonist, we found that TRPV1 blockade elicited marked, but reversible, and generally plasma concentration-dependent hyperthermia. Similar to what was observed in rats, dogs, and monkeys, hyperthermia was attenuated after repeated dosing of AMG 517 (at the highest dose tested) in humans during a second Phase I trial. However, AMG 517 administered after molar extraction (a surgical cause of acute pain) elicited long-lasting hyperthermia with maximal body temperature surpassing 40 degrees C, suggesting that TRPV1 blockade elicits undesirable hyperthermia in susceptible individuals. Mechanisms of AMG 517-induced hyperthermia were then studied in rats. AMG 517 caused hyperthermia by inducing tail skin vasoconstriction and increasing thermogenesis, which suggests that TRPV1 regulates vasomotor tone and metabolic heat production. In conclusion, these results demonstrate that: (a) TRPV1-selective antagonists like AMG 517 cannot be developed for systemic use as stand alone agents for treatment of pain and other diseases, (b) individual susceptibility influences magnitude of hyperthermia observed after TRPV1 blockade, and (c) TRPV1 plays a pivotal role as a molecular regulator for body temperature in humans.
*********
http://lib.bioinfo.pl/auth:Magal,E
J Pharmacol Exp Ther. 2008 Apr 17; : 18420600 (P,S,E,B,D) Antihyperalgesic effects of AMG8562, a novel vanilloid receptor TRPV1 modulator that does not cause hyperthermia in rats.
Amgen Inc.
Antagonists of the vanilloid receptor TRPV1 have been reported to produce anti-hyperalgesic effects in animal models of pain. These antagonists, however, also caused concomitant hyperthermia in rodents, dogs, monkeys and humans. Antagonist-induced hyperthermia was not observed in TRPV1 knockout mice, suggesting that the hyperthermic effect is exclusively mediated through TRPV1. Since antagonist-induced hyperthermia is considered a hurdle for developing TRPV1 antagonists as therapeutics, we investigated the possibility of eliminating hyperthermia while maintaining anti-hyperalgesia. Here, we report four potent and selective TRPV1 modulators with unique in vitro pharmacology profiles (Profiles A through D) and their respective effects on body temperature. We found that Profile C modulator, AMG8562, blocks capsaicin activation of TRPV1, does not affect heat activation of TRPV1, potentiates pH 5 activation of TRPV1 in vitro and does not cause hyperthermia in vivo in rats. We further profiled AMG8562 in an in vivo biochemical (agonist) challenge model, rodent pain models and tested for its side effects. We show that AMG8562 significantly blocks capsaicin-induced flinching behavior, produces statistically significant efficacy in CFA- and skin incision-induced thermal hyperalgesia, and acetic acid-induced writhing models, with no profound effects on locomotor activity. Based on the data shown here, we conclude that it is feasible to modulate TRPV1 in a manner that does not cause hyperthermia while maintaining efficacy in rodent pain models.
mfg ipollit
Antwort auf Beitrag Nr.: 34.447.157 von ipollit am 06.07.08 19:59:08der Vollständigkeit halber: von bolero...
Frau Hennecke hat geantwortet
Einige Fragen zur "Direvo" Meldung hatte ich:
Wie ist die Meldung ins Deutsche zu übersetzen? (im Forum ist man sich auch nicht einig)
Wurden Zahlungen geleistet?
Warum wurde Ihrerseits nichts gemeldet, auch wenn`s nicht meldepflichtig ist?
weterhin zu AMG-517:
Es scheint so zu sein, dass die Entwicklung von AMG-517 eingestellt wurde. AMG-517 richtet sich gegen den Capsaicin-Rezeptor. Dies ist der Rezeptor, bei dem es auch in Evotec's VR1-Kooperation mit Pfizer geht. VR1 bzw. TRPV1 soll u.a auch die Körpertemperatur regulieren... bei AMG-517 konnte es passieren, dass sich der Körper überhitzte. Ich weiß nicht, ob das ein Problem für diese Kooperation darstellt. Unten stehen zwei Abstrakts: eins kommt zu dem Schluss, dass sich VR1 nicht nutzen lässt (was das Ende der Kooperation mit Pfizer bedeuten würde), das andere spätere meint, dass es Möglichkeiten gibt, das Schmerzempfinden zu beeinflussen, ohne dass die Körpertemperatur dadurch negativ beeinflusst wird.
Wie sieht man das Problem (?) bei Ihnen in Hamburg?
Ist jetzt schon aus Ihrem Labor irgendwas bekannt?
********
Sehr geehrter Herr ...,
1. Wir haben Patente aus dem Arbeitsgebiet der so genannten "Directed Evolution - Biomoleküloptimierung" an Direvo transferiert, die Direvo zuvor von Evotec lizenziert hatte. Diese Patente sind für unseren heutigen Tätigkeitsbereich völlig irrelevant, für Direvo jedoch wichtig. Im Gegenzug haben wir von Direvo eine Zahlung erhalten und weitere erfolgsabhängige Zahlungen vereinbart, deren Umfang jedoch nicht so groß ist, dass es eine Pressemitteilung rechtfertigen würde.
2. Ja, ich glaube es ist richtig, dass Amgen ihr VR1-Programm beendet hat. Andere Pharmaunternehmen - Merck, AstraZeneca, GSK, Lilly und natürlich Evotec/Pfizer - arbeiten jedoch weiter an der klinischen Entwicklung ihrer VR1-Programme.
Wir wissen natürlich um den Temperatureffekt und den Inhalt dieser Abstracts und beobachten diesen Effekt in unseren Studien sehr sorgfältig. Während Amgen diesen Temperatureffekt als "Problem" und Grund für das Einstellen der Studie gemeldet hat, hat GSK scheinbar klar kommuniziert, dass sie keinen vergleichbaren Effekt in ihren Studien beobachtet haben.
Man muss insgesamt auch bedenken, dass ein möglicher Temperaturanstieg einen Einfluss auf die Entwicklung von VR1-Antagonisten als Schmerzmittel haben KÖNNTE - was wir erst im Laufe der Zeit über weitere Studien wissen werden - aber VR1-Antagonisten auch Potenzial in vielen anderen großen Indikationsgebieten haben, in denen dieser potentielle Nebeneffekt eine geringere oder keine Rolle spielen würde. Und, es mag Möglichkeiten geben, den Effekt auf Schmerz einerseits und die Temperatur andererseits zu separieren.
Sie sehen, es ist wie sie oft mit einem neuen Wirkmechanismus. Es gibt noch einiges zu klären und auch Hürden zu nehmen. Wenn jedoch ein solches Projekt erfolgreich sein sollte, hätte es sicher ein großes kommerzielles Potenzial.
Vielen Dank für Ihre Frage
Anne Hennecke
***********************
dass Evotec nicht alles meldet, finde ich nicht sonderlich tragisch. Vielleicht sind die Patente recht unbedeutend für Evotec und die Zahlungen von Direvo nicht weiter relevent.
es stimmt, VR1 ist bei mehreren Pharmas eine Zielstruktur, was grundsätzlich positiv zu bewerten ist, da dies die Bedeutung zeigt. So weit ich das verstanden habe, hat Pfizer (die ja auch nicht gerade klein sind) ihre komplette VR1-Entwicklung mit Evotec zusammen gelegt. Dass Amgen sein VR1-Programm beendet haben soll, kann ich nicht erkennen... AMG-517 ist gescheitert, das ja, aber die Abstracts zeigen doch, dass z.B. mit AMG-8562 entsprechende Nachfolger in der Pipeline stecken, die bis jetzt nicht diese Nebenwirkungen zeigen.
mfg ipollit
Frau Hennecke hat geantwortet
Einige Fragen zur "Direvo" Meldung hatte ich:
Wie ist die Meldung ins Deutsche zu übersetzen? (im Forum ist man sich auch nicht einig)
Wurden Zahlungen geleistet?
Warum wurde Ihrerseits nichts gemeldet, auch wenn`s nicht meldepflichtig ist?
weterhin zu AMG-517:
Es scheint so zu sein, dass die Entwicklung von AMG-517 eingestellt wurde. AMG-517 richtet sich gegen den Capsaicin-Rezeptor. Dies ist der Rezeptor, bei dem es auch in Evotec's VR1-Kooperation mit Pfizer geht. VR1 bzw. TRPV1 soll u.a auch die Körpertemperatur regulieren... bei AMG-517 konnte es passieren, dass sich der Körper überhitzte. Ich weiß nicht, ob das ein Problem für diese Kooperation darstellt. Unten stehen zwei Abstrakts: eins kommt zu dem Schluss, dass sich VR1 nicht nutzen lässt (was das Ende der Kooperation mit Pfizer bedeuten würde), das andere spätere meint, dass es Möglichkeiten gibt, das Schmerzempfinden zu beeinflussen, ohne dass die Körpertemperatur dadurch negativ beeinflusst wird.
Wie sieht man das Problem (?) bei Ihnen in Hamburg?
Ist jetzt schon aus Ihrem Labor irgendwas bekannt?
********
Sehr geehrter Herr ...,
1. Wir haben Patente aus dem Arbeitsgebiet der so genannten "Directed Evolution - Biomoleküloptimierung" an Direvo transferiert, die Direvo zuvor von Evotec lizenziert hatte. Diese Patente sind für unseren heutigen Tätigkeitsbereich völlig irrelevant, für Direvo jedoch wichtig. Im Gegenzug haben wir von Direvo eine Zahlung erhalten und weitere erfolgsabhängige Zahlungen vereinbart, deren Umfang jedoch nicht so groß ist, dass es eine Pressemitteilung rechtfertigen würde.
2. Ja, ich glaube es ist richtig, dass Amgen ihr VR1-Programm beendet hat. Andere Pharmaunternehmen - Merck, AstraZeneca, GSK, Lilly und natürlich Evotec/Pfizer - arbeiten jedoch weiter an der klinischen Entwicklung ihrer VR1-Programme.
Wir wissen natürlich um den Temperatureffekt und den Inhalt dieser Abstracts und beobachten diesen Effekt in unseren Studien sehr sorgfältig. Während Amgen diesen Temperatureffekt als "Problem" und Grund für das Einstellen der Studie gemeldet hat, hat GSK scheinbar klar kommuniziert, dass sie keinen vergleichbaren Effekt in ihren Studien beobachtet haben.
Man muss insgesamt auch bedenken, dass ein möglicher Temperaturanstieg einen Einfluss auf die Entwicklung von VR1-Antagonisten als Schmerzmittel haben KÖNNTE - was wir erst im Laufe der Zeit über weitere Studien wissen werden - aber VR1-Antagonisten auch Potenzial in vielen anderen großen Indikationsgebieten haben, in denen dieser potentielle Nebeneffekt eine geringere oder keine Rolle spielen würde. Und, es mag Möglichkeiten geben, den Effekt auf Schmerz einerseits und die Temperatur andererseits zu separieren.
Sie sehen, es ist wie sie oft mit einem neuen Wirkmechanismus. Es gibt noch einiges zu klären und auch Hürden zu nehmen. Wenn jedoch ein solches Projekt erfolgreich sein sollte, hätte es sicher ein großes kommerzielles Potenzial.
Vielen Dank für Ihre Frage
Anne Hennecke
***********************
dass Evotec nicht alles meldet, finde ich nicht sonderlich tragisch. Vielleicht sind die Patente recht unbedeutend für Evotec und die Zahlungen von Direvo nicht weiter relevent.
es stimmt, VR1 ist bei mehreren Pharmas eine Zielstruktur, was grundsätzlich positiv zu bewerten ist, da dies die Bedeutung zeigt. So weit ich das verstanden habe, hat Pfizer (die ja auch nicht gerade klein sind) ihre komplette VR1-Entwicklung mit Evotec zusammen gelegt. Dass Amgen sein VR1-Programm beendet haben soll, kann ich nicht erkennen... AMG-517 ist gescheitert, das ja, aber die Abstracts zeigen doch, dass z.B. mit AMG-8562 entsprechende Nachfolger in der Pipeline stecken, die bis jetzt nicht diese Nebenwirkungen zeigen.
mfg ipollit
hier nochmal ein aktueller Überblick über die EVT-201 Konkurrenten
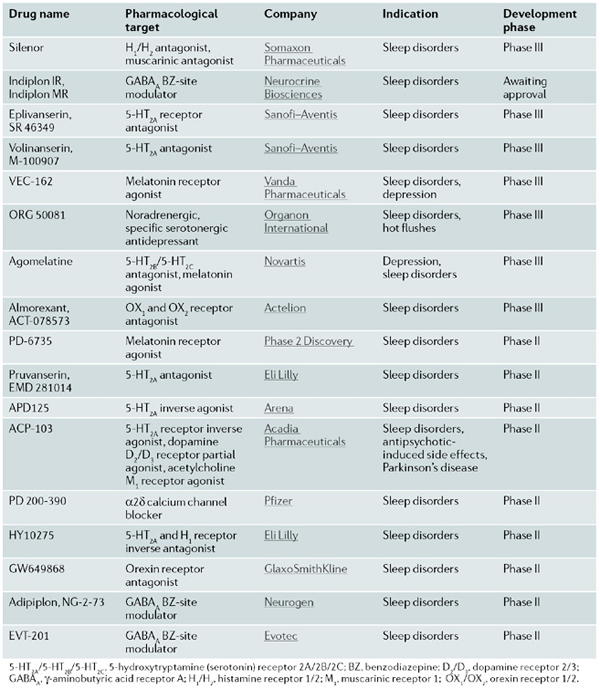
Der klassiche Ansatz für Schlafmittel ist heute GABA. Zu dieser Klasse gehören die Marktführer Ambien und Lunesta.
Neuere Ansätze sind u.a. die Einwirkung auf den Melatonin-Rezeptor (z.B. Rozerem... bis jetzt mit geringem kommerziellen Erfolg, weil die Wirkung noch zu schwach ist), als sehr aussichtsreich werden aktuell Mittel gesehen, die auf den Orexin-Rezeptor abzielen (z.B. Almorexant... hier sind eigentlich nur Actelion/GSK in der fortgeschrittenen Entwicklung). Eine breitere Entwicklung gibt es im Bereich der Serotonin-Rezeptoren (5-HT 2a/2c).
In der obrigen Tabelle scheinen mindestens folgende Projekte mit mehr oder weniger großen Problemem behaftet zu sein, die u.U. zu Einschränkungen und dem Projektende führen können: Silenor, Indiplon, VEC-162, GW649868, Adipiplon (mehr habe ich mir noch nicht angesehen)
mfg ipollit
Der klassiche Ansatz für Schlafmittel ist heute GABA. Zu dieser Klasse gehören die Marktführer Ambien und Lunesta.
Neuere Ansätze sind u.a. die Einwirkung auf den Melatonin-Rezeptor (z.B. Rozerem... bis jetzt mit geringem kommerziellen Erfolg, weil die Wirkung noch zu schwach ist), als sehr aussichtsreich werden aktuell Mittel gesehen, die auf den Orexin-Rezeptor abzielen (z.B. Almorexant... hier sind eigentlich nur Actelion/GSK in der fortgeschrittenen Entwicklung). Eine breitere Entwicklung gibt es im Bereich der Serotonin-Rezeptoren (5-HT 2a/2c).
In der obrigen Tabelle scheinen mindestens folgende Projekte mit mehr oder weniger großen Problemem behaftet zu sein, die u.U. zu Einschränkungen und dem Projektende führen können: Silenor, Indiplon, VEC-162, GW649868, Adipiplon (mehr habe ich mir noch nicht angesehen)
mfg ipollit
Antwort auf Beitrag Nr.: 34.527.255 von ipollit am 17.07.08 11:06:20EVT-201 wirkt wie der Blockbuster (inzwischen generisch) Ambien, Lunesta, Indiplon oder Adipiplon über GABA.
********
Allgemeines über Neurotransmitter
Neurotransmitter sind chemische Substanzen, die die Signalübertragung zwischen den Nervenzellen vermitteln. Man unterscheidet dämpfende und erregende Neurotransmitter. Sie werden als Antagonisten bezeichnet und sollten in einem ausgewogenen Verhältnis vorhanden sein. Diese Botenstoffe bestimmen maßgeblich unsere Stimmung und Leistungsfähigkeit. Das biochemische Zusammenspiel der Neurotransmitter entscheidet darüber, ob wir uns depressiv, ängstlich oder gestresst fühlen oder ob wir gut gelaunt und hoch belastbar sind. Aber auch die Gedächtnisleistung, das Konzentrationsvermögen, das Durchhaltevermögen und die Kreativität sind von den Botenstoffen abhängig.
Eine Substanz wird als Neurotransmitter bezeichnet, wenn sie folgende Kriterien erfüllt: Sie muss in der Nervenzelle gebildet und von dieser freigesetzt werden, biochemisch identifizierbar sein sowie bei Reizung der Nervenzelle ausgeschüttet werden und die Zielzelle beeinflussen. Die Transmitterwirkung muss durch Gegenspieler dosisabhängig gehemmt werden können. Die Transmittersubstanz muss nach Verabreichung die gleichen Effekte an den Zielnervenzellen auslösen wie diejenigen, die nach der Nervenreizung beobachtbar sind.
Zu den „klassischen“ Neurotransmittern zählt man die biogenen Amine Acetylcholin und Noradrenalin, Dopamin, GABA, Serotonin, Histamin und Adrenalin, sowie die Aminosäuren Glutaminsäure, Glycin und Asparaginsäure.
Auch die so genannten Neuropeptide werden mittlerweile zu den Neurotransmittern gerechnet.
Neben den Neurotransmittern gibt es eine Vielzahl von Substanzen, die man als Neuromodulatoren bezeichnet. Diese Stoffe können die Erregungsübertragung verstärken oder vermindern, sind aber nicht unmittelbar an der Erregungsübertragung beteiligt.
*********
GABA
Ein Neurotransmitter, der beruhigt
GABA im Gehirn
Gamma-Amino-Buttersäure (GABA) wird aus Glutaminsäure gebildet und ist der wichtigste inhibitorische (dämpfende) Neurotransmitter im Zentralnervensystem. Schätzungsweise 30 – 40 % aller Neuronen des ZNS schütten GABA aus. Man unterscheidet verschiedene GABA-Rezeptoren; einer der bedeutendsten ist der GABA(a)-Rezeptor. GABA-Neurotransmitter, die an diesen Rezeptor binden, modulieren den Chlorideinstrom in die Zelle und bewirken so eine dämpfende Zellerregung.Pharmaka wie z.B. Tranquillizer, oder auch Alkohol binden ebenfalls an den GABA(a)-Rezeptor und entfalten dadurch eine beruhigende Wirkung. Im gesamten limbischen System finden sich zahlreiche GABAerge Synapsen, auch in dem Hirnarial, das für die Angstentstehung ausschlaggebend ist – der Amygdala. Es ist nachvollziehbar, dass GABA hier durch Hemmung anderer Neuronen angstlösend wirkt.
Bei Stressreaktionen hat GABA einen beruhigenden Effekt, indem es der Aktivität der Hypothalamus-Hypophysen-Nebennieren-Achse entgegenwirkt. Auch im Hippocampus, dem Bereich der für die Gedächtnisbildung maßgeblich ist, befinden sich viele GABAerge Synapsen. Eine Unterdrückung der GABA-Funktion kann Störungen der Gedächtnisprozesse hervorrufen - dies wurde im Zusammenhang mit Benzodiazepinen beobachtet.
************
Zolpidem, ein Imidazopyridin-Derivat, ist ein Wirkstoff, der in modernen Schlafmitteln eingesetzt wird und eine andere chemische Struktur besitzt als Benzodiazepine, jedoch ähnlich wirkt. Es hat eine sehr kurze Halbwertszeit (2–3 Stunden) und bildet keine pharmakologisch wirksamen Metaboliten. Es ist momentan das in den USA (unter dem Markennamen Ambien®) und in Deutschland (Stilnox® oder seltener Bikalm®, sowie als Generikum) meistverordnete Schlafmittel.
Zolpidem gehört zur Gruppe der sogenannten GABA-Agonisten. Es wirkt auf die gleichen Rezeptoren, die sonst durch den inhibitorischen Neurotransmitter GABA aktiviert werden.
Zolpidem hat eine schwach sedierende, anxiolytische, muskelrelaxierende und antikonvulsive Wirkung. Es erleichtert das Einschlafen, die Dauer des Schlafes wird verlängert. Im Tierversuch geprüft, ließen sich Zolpidem-Effekte durch den Benzodiazepin-Antagonisten Flumazenil (Anexate®) aufheben. Die Schlafarchitektur scheint durch Zolpidem bei niedriger Dosierung nicht nennenswert beeinflusst zu werden. Bei höheren Dosen treten Schlafveränderungen vergleichbar den durch Benzodiazepine hervorgerufenen auf.
Durch die Verwandtschaft mit der Benzodiazepin-Gruppe sind trotz der geringen Plasmahalbwertszeit Rebound-Phänomene, Entzugssymptome sowie physische und psychische Abhängigkeiten möglich. In Kombination mit Alkohol oder anderen sedierend wirkenden Substanzen (insbesondere Benzodiazepinen) ist mit einer Verstärkung der Wirkung zu rechnen. Es wird empfohlen, die Tageshöchstdosis von 10 mg (Erwachsene) und 5 mg (ältere und geschwächte Patienten) nicht zu überschreiten.
mfg ipollit
********
Allgemeines über Neurotransmitter
Neurotransmitter sind chemische Substanzen, die die Signalübertragung zwischen den Nervenzellen vermitteln. Man unterscheidet dämpfende und erregende Neurotransmitter. Sie werden als Antagonisten bezeichnet und sollten in einem ausgewogenen Verhältnis vorhanden sein. Diese Botenstoffe bestimmen maßgeblich unsere Stimmung und Leistungsfähigkeit. Das biochemische Zusammenspiel der Neurotransmitter entscheidet darüber, ob wir uns depressiv, ängstlich oder gestresst fühlen oder ob wir gut gelaunt und hoch belastbar sind. Aber auch die Gedächtnisleistung, das Konzentrationsvermögen, das Durchhaltevermögen und die Kreativität sind von den Botenstoffen abhängig.
Eine Substanz wird als Neurotransmitter bezeichnet, wenn sie folgende Kriterien erfüllt: Sie muss in der Nervenzelle gebildet und von dieser freigesetzt werden, biochemisch identifizierbar sein sowie bei Reizung der Nervenzelle ausgeschüttet werden und die Zielzelle beeinflussen. Die Transmitterwirkung muss durch Gegenspieler dosisabhängig gehemmt werden können. Die Transmittersubstanz muss nach Verabreichung die gleichen Effekte an den Zielnervenzellen auslösen wie diejenigen, die nach der Nervenreizung beobachtbar sind.
Zu den „klassischen“ Neurotransmittern zählt man die biogenen Amine Acetylcholin und Noradrenalin, Dopamin, GABA, Serotonin, Histamin und Adrenalin, sowie die Aminosäuren Glutaminsäure, Glycin und Asparaginsäure.
Auch die so genannten Neuropeptide werden mittlerweile zu den Neurotransmittern gerechnet.
Neben den Neurotransmittern gibt es eine Vielzahl von Substanzen, die man als Neuromodulatoren bezeichnet. Diese Stoffe können die Erregungsübertragung verstärken oder vermindern, sind aber nicht unmittelbar an der Erregungsübertragung beteiligt.
*********
GABA
Ein Neurotransmitter, der beruhigt
GABA im Gehirn
Gamma-Amino-Buttersäure (GABA) wird aus Glutaminsäure gebildet und ist der wichtigste inhibitorische (dämpfende) Neurotransmitter im Zentralnervensystem. Schätzungsweise 30 – 40 % aller Neuronen des ZNS schütten GABA aus. Man unterscheidet verschiedene GABA-Rezeptoren; einer der bedeutendsten ist der GABA(a)-Rezeptor. GABA-Neurotransmitter, die an diesen Rezeptor binden, modulieren den Chlorideinstrom in die Zelle und bewirken so eine dämpfende Zellerregung.Pharmaka wie z.B. Tranquillizer, oder auch Alkohol binden ebenfalls an den GABA(a)-Rezeptor und entfalten dadurch eine beruhigende Wirkung. Im gesamten limbischen System finden sich zahlreiche GABAerge Synapsen, auch in dem Hirnarial, das für die Angstentstehung ausschlaggebend ist – der Amygdala. Es ist nachvollziehbar, dass GABA hier durch Hemmung anderer Neuronen angstlösend wirkt.
Bei Stressreaktionen hat GABA einen beruhigenden Effekt, indem es der Aktivität der Hypothalamus-Hypophysen-Nebennieren-Achse entgegenwirkt. Auch im Hippocampus, dem Bereich der für die Gedächtnisbildung maßgeblich ist, befinden sich viele GABAerge Synapsen. Eine Unterdrückung der GABA-Funktion kann Störungen der Gedächtnisprozesse hervorrufen - dies wurde im Zusammenhang mit Benzodiazepinen beobachtet.
************
Zolpidem, ein Imidazopyridin-Derivat, ist ein Wirkstoff, der in modernen Schlafmitteln eingesetzt wird und eine andere chemische Struktur besitzt als Benzodiazepine, jedoch ähnlich wirkt. Es hat eine sehr kurze Halbwertszeit (2–3 Stunden) und bildet keine pharmakologisch wirksamen Metaboliten. Es ist momentan das in den USA (unter dem Markennamen Ambien®) und in Deutschland (Stilnox® oder seltener Bikalm®, sowie als Generikum) meistverordnete Schlafmittel.
Zolpidem gehört zur Gruppe der sogenannten GABA-Agonisten. Es wirkt auf die gleichen Rezeptoren, die sonst durch den inhibitorischen Neurotransmitter GABA aktiviert werden.
Zolpidem hat eine schwach sedierende, anxiolytische, muskelrelaxierende und antikonvulsive Wirkung. Es erleichtert das Einschlafen, die Dauer des Schlafes wird verlängert. Im Tierversuch geprüft, ließen sich Zolpidem-Effekte durch den Benzodiazepin-Antagonisten Flumazenil (Anexate®) aufheben. Die Schlafarchitektur scheint durch Zolpidem bei niedriger Dosierung nicht nennenswert beeinflusst zu werden. Bei höheren Dosen treten Schlafveränderungen vergleichbar den durch Benzodiazepine hervorgerufenen auf.
Durch die Verwandtschaft mit der Benzodiazepin-Gruppe sind trotz der geringen Plasmahalbwertszeit Rebound-Phänomene, Entzugssymptome sowie physische und psychische Abhängigkeiten möglich. In Kombination mit Alkohol oder anderen sedierend wirkenden Substanzen (insbesondere Benzodiazepinen) ist mit einer Verstärkung der Wirkung zu rechnen. Es wird empfohlen, die Tageshöchstdosis von 10 mg (Erwachsene) und 5 mg (ältere und geschwächte Patienten) nicht zu überschreiten.
mfg ipollit
Ein paar deutsche Kunden für EVT 201
Baldrian und Co.
Gibt es harmlose Schlafmittel?
Tiefer, erholsamer Schlaf ist nicht jedem vergönnt."Der Schlaf ist wie eine Taube: streckt man die Hand ruhig nach ihr aus, setzt sie sich drauf; greift man nach ihr, fliegt sie weg." Diese Beschreibung eines Schweizer Psychologen trifft auf Millionen Deutschen zu: Müde gehen sie ins Bett, und kaum liegen sie, ist an Schlaf nicht mehr zu denken. Viele greifen dann zur Schlaftablette.
Das Ambien doch noch relativ unsicher ist betreffs Nebenwirkungen, zeigt folgender Artikel:
Über Schlafstörungen klagt jeder dritte Bundesbürger, Mittel dagegen kannten aber schon unsere Vorfahren vor fast 10.000 Jahren. Sie verordneten den Schlaflosen Tees aus Baldrian, Hopfen, Melisse und Passionsblumenkraut. Doch bei der Wirkung so genannter Schlaftees ist der Arzneimittelexperte Professor Walter Müller von der Universität Frankfurt skeptisch:
"Normalerweise ist eine Tasse Tee in der Dosierung der Wirkstoffe nicht ausreichend, um eine verlässliche Wirkung zu erreichen. Bei Baldrian müsste man mindestens 7-10 Gramm Baldrianwurzel aufbrühen. Das schmeckt so scheußlich, dass man das mit Sicherheit nicht trinken kann."
Und eine schlaffördernde Wirkung ist bei den pflanzlichen Schlafmitteln sowieso nur für Baldrian nachgewiesen:
"Wichtig zu wissen ist bei den pflanzlichen Präparaten auf Baldrianbasis, dass die Wirkung erst langsam kommt. Das heißt, hier sollte man das Präparat über mehrere Wochen nehmen, weil die Verbesserung des Schlafes oft erst in der zweiten oder dritten Woche deutlich wird."
Und erst die richtige Dosis bringt den Schlaf: Etwa 600 Milligramm Baldrianauszug sollten es allabendlich sein, bei einer niedrigeren Dosierung wälzt man sich sonst weiter schlaflos in den Kissen.
Ebenfalls rezeptfrei gibt es in der Apotheke eine bestimmte Gruppe von Schlafmitteln, die ursprünglich mal als Mittel gegen Allergien dienten. Als Nebenwirkung machen sie müde, deshalb verwendet man sie nun als Schlafmittel.
"Sie bewirken letztlich eine Verbesserung der Schlafzeit und auch des Einschlafens. Aber der große Nachteil ist, dass die Wirkung sehr schnell nachlässt. Das heißt, nach einigen Nächten sind die Substanzen einfach nicht mehr so wirksam. Man soll in keinem Fall dann weiter therapieren, zum Beispiel die Dosis verdoppeln - weil dann doch erhebliche Probleme auftreten können."
Helfen die rezeptfreien Schlafmittel nicht, sollte man zum Arzt gehen. Er klärt, ob es eine organische Ursache für die Schlafstörung gibt, beispielsweise eine Herz- oder Atemwegserkrankung. Zudem sind Schlafstörungen ein häufiges Symptom von Depressionen, die unbedingt behandelt werden müssen.
Sind organische Ursachen ausgeschlossen, wird der Arzt vielleicht für ein/zwei Wochen Medikamente aus der Gruppe der Benzodiazepine verordnen. "Valium" beispielsweise ist da wohl das bekannteste Medikament. "Benzodiazepine sind im Prinzip sehr gut verträglich und haben relativ wenig Nebenwirkungen, so lange man sie zeitlich begrenzt und den Dosierungsempfehlungen entsprechend hin anwendet."
Wird dagegen die Dosis gesteigert oder werden diese Schlafmittel über Wochen oder gar Monate regelmäßig eingenommen, kommt es zu einer Medikamentenabhängigkeit. Außerdem haben diese Mittel oft eine lange Wirkdauer, man fühlt sich dann auch tagsüber müde und nicht leistungsfähig. Grundsätzlich gilt: rezeptpflichtige Schlafmittel höchstens vier Wochen einnehmen. Und dauern die Schlafstörungen länger als drei Monate, sollte man auf jeden Fall zum Arzt gehen.
(nachlesen kann man auf hr-online.de)
15. März 2007, 18:09 UhrÜBERRASCHENDE NEBENWIRKUNGEN
Spritztour auf Schlaftablette
Von Stefan Schmitt
Die meistgeschluckte Schlaftablette Deutschlands und der USA hat seltene, verblüffende, geradezu exotische Nebenwirkungen. Die Pille könnte Menschen zum Autofahren im Schlaf bringen - und Komatöse wieder zu Bewusstsein.
Er sei Kongressabgeordneter, der dringend wählen müsse, hatte Patrick J. Kennedy den Polizisten gesagt. Jedenfalls geht das aus dem Protokoll der Beamten hervor. Der Neffe des früheren US-Präsidenten John F. Kennedy selbst konnte sich an den frühen Freitagmorgen des 5. Mai 2006 nicht mehr erinnern - obwohl er nächtens in seinen Wagen gestiegen war und damit einen Unfall gebaut hatte. "Ich hatte vorher keinen Alkohol getrunken", sagte Kennedy nach Angaben der "New York Times" am nächsten Morgen. Dafür hatte er etwas anderes intus: Ambien, die beliebteste Schlaftablette der US-Amerikaner.
Spätestens seitdem stehen die sogenannten sedativ-hypnotischen Schlafmittel im Verdacht, in - ebenso seltenen wie exotischen - Einzellfällen seltsame Nebenwirkungen hervorzurufen. Vor "komplexem Verhalten im Schlaf" warnt nun die US-Arzneiaufsichtbehörde FDA (US Food and Drug Administration). "Dazu könnte auch Fahren im Schlaf gehören", teilte die FDA mit. Auf den Beipackzetteln von 13 verschreibungspflichtigen Medikamenten soll in den USA künftig davor gewarnt werden.
Besonders im Rampenlicht steht das marktbeherrschende Ambien. Unter diesem Markennamen vertreibt der Hersteller Sanofi-Aventis in den USA den Wirkstoff Zolpidem als Schlaftablette. Eine Sprecherin von Sanofi-Aventis in den USA sagte der Nachrichtenagentur Reuters, nur weniger als jede tausendste Versuchsperson habe in Studien von Schlafwandeln berichtet. Der Hersteller teilte mit, er sehe "keine signifikanten Veränderungen im Sicherheitsprofil" des Schlafmittels.
Schlafwandeln, Futtern, Autofahren
Ambien zählt in den USA zu den zwanzig meistverkauften Medikamenten. Wie häufig die künftig aufgeführten Nebenwirkungen auftreten, dazu machte die FDA keine Angaben. Allerdings gab es in Medien und Fachkreisen in den letzten Jahren Berichte über seltene, exotische Einzelfälle:
Im Fachmagazin "Neurologic Clinics" berichtete Mark Mahowald von der University of Minnesota im Mai 2006 von Einzelfällen, in denen solche Schlaftabletten zum Schlafwandeln geführt hatten.
Bereits im Jahr 2002 hatte Michael Silber von der Mayo Clinic in Rochester (ebenfalls Minnesota) im Fachmagazin "Sleep Medicine" von Patienten berichtet, die unter Einfluss von Zolpidem zum Kühlschrank schlafwandelten - und aßen, ohne sich am nächsten Morgen daran erinnern zu können.
Die "New York Times" berichtete im März 2006, dass in den US-Bundesstaaten Wisconsin und Washington die Zahl aus dem Verkehr gezogener Autofahrer gestiegen sei, in deren Blut die Polizei Zolpidem fand. "In einigen toxikologischen Labors ist Ambien bereits auf der Top-10-Liste von Wirkstoffen im Blut beeinträchtigter Verkehrsteilnehmer", schrieb die Zeitung.
Auch von nächtlichen Telefonaten und gar von Geschlechtsverkehr wurde berichtet, an die sich die Patienten am nächsten Morgen partout nicht mehr erinnern konnten. FDA-Experte Katz hält es für möglich, dass einige solcher Ereignisse nicht von Ärzten und Konstumenten berichtet worden seien - kein abwegiger Gedanke.
"Spekatulär, aber selten"
"Hängen Sie Glöckchen an Ihre Schlafzimmertür. Wenn Sie schlafwandeln, könnte das Geläut sie aufwecken", riet die "New York Times" ihren Lesern im März vergangenen Jahres. In Deutschland wird der Wirkstoff Zolpidem unter dem Markennamen Stilnox vertrieben. "Wir weisen in diesem Zusammenhang darauf hin, dass Schlafwandeln zwar während der Behandlung mit Stilnox auftreten kann, aber deswegen nicht unbedingt durch Stilnox verursacht sein muss", sagte Judith Kramer, Sprecherin von Sanofi-Aventis in Deutschland.
"Zolpidem ist heute die Nummer eins der verordneten Schlafmittel", sagt Walter Müller, Pharmakologe von der Universität Frankfurt am Main, zu SPIEGEL ONLINE. Er hatte im Jahr 2003 in der Fachzeitschrift "Addiction" festgestellt: Im Vergleich zu den bislang gegen Schlafstörungen verabreichten Barbituraten und Benzodiazepinen ist die Suchtgefahr viel geringer, und auch für Selbstmörder ist der Wirkstoff unattraktiv.
In Anbetracht der höchst seltenen Nebenwirkungen rät Müller zur Gelassenheit: Millionen von Menschen würden weltweit erfolgreich mit dieser Wirkstoffklasse behandelt, ohne eigenwillig schlafzuwandeln. Müller sagt: "Das kling spektakulär, ist aber sehr selten."
Also alles nur viel Lärm um wenig? Tatsächlich, darauf verweisen Experten, führt das US-Haftungsrecht und die dort üblichen immensen Schadensersatzforderungen vor Gericht tendenziell dazu, dass Unternehmen sich gegen alle Eventualitäten absichern. So kontaktierte die FDA die 13 Hersteller sedativ-hypnotischer Medikamente in Sachen Schlafwandeln.
FDA-Neurologe Russell Katz sagte, bis auf eine namentlich nicht genannte Pharmafirma hätten sich alle kooperativ gezeigt. Die FDA sagte auch, kein Patient solle das Medikament ohne ärztliche Konsultation absetzen. Ernst genug, um die Präparate vom Markt zu nehmen, seien die Bedenken jedenfalls nicht.
Schlaftablette weckt Dahindämmernde auf
Dass aber noch nicht jedes Detail der Wirkweise solcher Medikamente bekannt ist, zeigt sich auch an ganz unerwarteter Stelle. Tatsächlich werden dem Wirkstoff des Schlafhelfers Ambien noch ganz andere - heilende - Nebenwirkungen zugeschrieben:
Eine Französin, die sich in einem Koma-ähnlichen Dämmerzustand befand, ist 20 Minuten nach der Einnahme von Zolpidem plötzlich zeitweilig aufgewacht. Sie habe sich drei Stunden lang mit Angehörigen und Pflegepersonal verständigen können, habe gegessen und sich bewegt. Das berichten Ärzte um Christine Brefel-Courbon von der Universität Toulouse in der März-Ausgabe des Fachmagazins "Annals of Neurology"
Bei drei weiteren Patienten im vegetativen Zustand hat Ralf Clauss vom Royal Surrey Country Hospital im südenglischen Guildford diesen Effekt beobachtet. "Zolpidem scheint ein effektives Medikament zu sein, um die Gehirnfunktionen mancher Patienten in vegetativen Zustand wiederherzustellen", schrieb er vor einem Jahr in der Fachzeitschrift "Neurorehabilitation".
"Wiedergeboren" titelte die Londoner Zeitung "Guardian" im vergangenen September angesichts dieser Veröffentlichungen. Clauss und sein Co-Forscher, der Südafrikaner Wally Nel, hätten schon 150 hirngeschädigte Patienten entsprechend behandelt - und bei 60 Prozent eine Verbesserung feststellen können. "Etwas Seltsames und Wunderbares passiert hier", sagte Nel der Zeitung, "und wir müssen dem auf den Grund gehen."
Dies gilt möglicherweise für mehr als eine unerwartete Wirkung von sedativ-hypnotischen Medikamenten. Die FDA jedenfalls hat die Hersteller zu weiterführenden Studien zu Häufigkeit und Art der überraschenden Effekte aufgefordert. Nach Angaben von Russell Katz hat aber bislang keiner der 13 angesprochenen dies zugesagt.
In Deutschland wird jedenfalls der Beipackzettel von Stilnox gerade verändert, wie Sanofi-Aventis-Sprecherin Kramer zu SPIEGEL ONLINE sagte, "auf unsere eigene Initiative hin".
mit Material von Reuters
Ein weiterer Artikel über Ambien unterstützt vorigen Beitrag:
Nebenwirkung
Halluzinationen durch Schlafmittel
Ein gängiges Schlafmedikament hat in Einzelfällen Halluzinationen und Gedächtnisstörungen ausgelöst und Patienten schlafwandeln lassen.
Zolpidem kann offenbar zu Schlafwandeln führenEin kürzlich veröffentlichter Report der australischen Gesundheitsbehörde berichtet im Zusammenhang mit Zolpidem von verschiedenen seltsamen Vorfällen. So klagten 104 Patienten über Halluzinationen, 62 litten unter einem zeitweiligen Gedächtnisverlust, in und 16 Fällen hatten die Patienten im Schlaf bizarre Verhaltensweisen gezeigt.
Eine Frau erwachte beispielsweise mit dem Pinsel in der Hand vor ihrer Haustür, die sie im Schlaf gestrichen hatte. Eine andere nahm 23 Kilo zu, weil sie nachts unwissentlich den Kühlschrank leer futterte.
Randale an Bord
Auch britische Behörden berichten über 68 ähnliche Vorfälle, die zwischen 2001 und 2005 aufgetreten waren. Besonders besorgniserregend waren Berichte von Personen, die unter Medikamenteneinfluss schlafwandelnd Auto gefahren waren. In einem Fall musste ein Transatlantikflug umgeleitet werden, nachdem ein Passagier unter Zolpidem-Einfluss an Bord randalierte.
Der Wirkstoff, der auch in Deutschland häufig zur Behandlung von Schlafstörungen verschrieben wird, gilt als wirksam und dabei weniger suchtgefährdend als beispielsweise Diazepam (Valium). Ähnlich wie dieses verbessert es den Tiefschlaf, indem er bestimmte Rezeptoren im Gehirn belegt. Während unter Zolpidem Teile des Gehirns im Schlaf weniger aktiv sind, kann sich der Köper weiterhin bewegen, was Schlafwandeln möglich macht.
Auf der Suche nach den Ursachen
Obwohl Millionen Menschen das Medikament problemlos vertragen, gäben Einzelfälle Anlass, sie genauer zu untersuchen. „Wir müssen herausfinden, ob es sich um echte Nebenwirkungen handelt“, erklärt Schlafforscher Kenneth Wright von der University of Colorado. Einige Vorfälle ließen sich jedoch durch eine falsche Einnahme erklären, beispielsweise, wenn die Schlaftabletten nicht unmittelbar vor dem Zubettgehen geschluckt worden seien.
Der Pharmahersteller Sanofi-Aventis, der Schlafmittel auf Zolpidembasis produziert, gibt zu bedenken, dass die Vorfälle nicht unbedingt durch das Medikament ausgelöst worden sein müssten. Sprecherin Melissa Feltman weist darauf hin, dass die Sicherheit des Medikaments wissenschaftlich gut belegt sei. Möglicherweise seien die bizarren Verhaltensweisen eher auf eine verborgene psychische Störung zurückzuführen.
Ich bin guter Dinge, daß der GABA-Agonist EVT-201 genug Potential für einen Blockbuster-Effekt haben wird.
Es gibt genug Potential für einen besseren GABA-Agonisten, sieht man die aufgetretenen Nebeneffekte bei Ambien.
Ich gehe von einer überzeugenderen Zusammensetzung bei EVT 201 aus, obwohl Zolpidem in Form von Ambien sicher schon viele Risiken ausschließt gegenüber den herkömmlichen anderen Verschreibungspflichtigen ausschließt.
Was sagt ipollit zu meiner Meinung?
Ostdi
Baldrian und Co.
Gibt es harmlose Schlafmittel?
Tiefer, erholsamer Schlaf ist nicht jedem vergönnt."Der Schlaf ist wie eine Taube: streckt man die Hand ruhig nach ihr aus, setzt sie sich drauf; greift man nach ihr, fliegt sie weg." Diese Beschreibung eines Schweizer Psychologen trifft auf Millionen Deutschen zu: Müde gehen sie ins Bett, und kaum liegen sie, ist an Schlaf nicht mehr zu denken. Viele greifen dann zur Schlaftablette.
Das Ambien doch noch relativ unsicher ist betreffs Nebenwirkungen, zeigt folgender Artikel:
Über Schlafstörungen klagt jeder dritte Bundesbürger, Mittel dagegen kannten aber schon unsere Vorfahren vor fast 10.000 Jahren. Sie verordneten den Schlaflosen Tees aus Baldrian, Hopfen, Melisse und Passionsblumenkraut. Doch bei der Wirkung so genannter Schlaftees ist der Arzneimittelexperte Professor Walter Müller von der Universität Frankfurt skeptisch:
"Normalerweise ist eine Tasse Tee in der Dosierung der Wirkstoffe nicht ausreichend, um eine verlässliche Wirkung zu erreichen. Bei Baldrian müsste man mindestens 7-10 Gramm Baldrianwurzel aufbrühen. Das schmeckt so scheußlich, dass man das mit Sicherheit nicht trinken kann."
Und eine schlaffördernde Wirkung ist bei den pflanzlichen Schlafmitteln sowieso nur für Baldrian nachgewiesen:
"Wichtig zu wissen ist bei den pflanzlichen Präparaten auf Baldrianbasis, dass die Wirkung erst langsam kommt. Das heißt, hier sollte man das Präparat über mehrere Wochen nehmen, weil die Verbesserung des Schlafes oft erst in der zweiten oder dritten Woche deutlich wird."
Und erst die richtige Dosis bringt den Schlaf: Etwa 600 Milligramm Baldrianauszug sollten es allabendlich sein, bei einer niedrigeren Dosierung wälzt man sich sonst weiter schlaflos in den Kissen.
Ebenfalls rezeptfrei gibt es in der Apotheke eine bestimmte Gruppe von Schlafmitteln, die ursprünglich mal als Mittel gegen Allergien dienten. Als Nebenwirkung machen sie müde, deshalb verwendet man sie nun als Schlafmittel.
"Sie bewirken letztlich eine Verbesserung der Schlafzeit und auch des Einschlafens. Aber der große Nachteil ist, dass die Wirkung sehr schnell nachlässt. Das heißt, nach einigen Nächten sind die Substanzen einfach nicht mehr so wirksam. Man soll in keinem Fall dann weiter therapieren, zum Beispiel die Dosis verdoppeln - weil dann doch erhebliche Probleme auftreten können."
Helfen die rezeptfreien Schlafmittel nicht, sollte man zum Arzt gehen. Er klärt, ob es eine organische Ursache für die Schlafstörung gibt, beispielsweise eine Herz- oder Atemwegserkrankung. Zudem sind Schlafstörungen ein häufiges Symptom von Depressionen, die unbedingt behandelt werden müssen.
Sind organische Ursachen ausgeschlossen, wird der Arzt vielleicht für ein/zwei Wochen Medikamente aus der Gruppe der Benzodiazepine verordnen. "Valium" beispielsweise ist da wohl das bekannteste Medikament. "Benzodiazepine sind im Prinzip sehr gut verträglich und haben relativ wenig Nebenwirkungen, so lange man sie zeitlich begrenzt und den Dosierungsempfehlungen entsprechend hin anwendet."
Wird dagegen die Dosis gesteigert oder werden diese Schlafmittel über Wochen oder gar Monate regelmäßig eingenommen, kommt es zu einer Medikamentenabhängigkeit. Außerdem haben diese Mittel oft eine lange Wirkdauer, man fühlt sich dann auch tagsüber müde und nicht leistungsfähig. Grundsätzlich gilt: rezeptpflichtige Schlafmittel höchstens vier Wochen einnehmen. Und dauern die Schlafstörungen länger als drei Monate, sollte man auf jeden Fall zum Arzt gehen.
(nachlesen kann man auf hr-online.de)
15. März 2007, 18:09 UhrÜBERRASCHENDE NEBENWIRKUNGEN
Spritztour auf Schlaftablette
Von Stefan Schmitt
Die meistgeschluckte Schlaftablette Deutschlands und der USA hat seltene, verblüffende, geradezu exotische Nebenwirkungen. Die Pille könnte Menschen zum Autofahren im Schlaf bringen - und Komatöse wieder zu Bewusstsein.
Er sei Kongressabgeordneter, der dringend wählen müsse, hatte Patrick J. Kennedy den Polizisten gesagt. Jedenfalls geht das aus dem Protokoll der Beamten hervor. Der Neffe des früheren US-Präsidenten John F. Kennedy selbst konnte sich an den frühen Freitagmorgen des 5. Mai 2006 nicht mehr erinnern - obwohl er nächtens in seinen Wagen gestiegen war und damit einen Unfall gebaut hatte. "Ich hatte vorher keinen Alkohol getrunken", sagte Kennedy nach Angaben der "New York Times" am nächsten Morgen. Dafür hatte er etwas anderes intus: Ambien, die beliebteste Schlaftablette der US-Amerikaner.
Spätestens seitdem stehen die sogenannten sedativ-hypnotischen Schlafmittel im Verdacht, in - ebenso seltenen wie exotischen - Einzellfällen seltsame Nebenwirkungen hervorzurufen. Vor "komplexem Verhalten im Schlaf" warnt nun die US-Arzneiaufsichtbehörde FDA (US Food and Drug Administration). "Dazu könnte auch Fahren im Schlaf gehören", teilte die FDA mit. Auf den Beipackzetteln von 13 verschreibungspflichtigen Medikamenten soll in den USA künftig davor gewarnt werden.
Besonders im Rampenlicht steht das marktbeherrschende Ambien. Unter diesem Markennamen vertreibt der Hersteller Sanofi-Aventis in den USA den Wirkstoff Zolpidem als Schlaftablette. Eine Sprecherin von Sanofi-Aventis in den USA sagte der Nachrichtenagentur Reuters, nur weniger als jede tausendste Versuchsperson habe in Studien von Schlafwandeln berichtet. Der Hersteller teilte mit, er sehe "keine signifikanten Veränderungen im Sicherheitsprofil" des Schlafmittels.
Schlafwandeln, Futtern, Autofahren
Ambien zählt in den USA zu den zwanzig meistverkauften Medikamenten. Wie häufig die künftig aufgeführten Nebenwirkungen auftreten, dazu machte die FDA keine Angaben. Allerdings gab es in Medien und Fachkreisen in den letzten Jahren Berichte über seltene, exotische Einzelfälle:
Im Fachmagazin "Neurologic Clinics" berichtete Mark Mahowald von der University of Minnesota im Mai 2006 von Einzelfällen, in denen solche Schlaftabletten zum Schlafwandeln geführt hatten.
Bereits im Jahr 2002 hatte Michael Silber von der Mayo Clinic in Rochester (ebenfalls Minnesota) im Fachmagazin "Sleep Medicine" von Patienten berichtet, die unter Einfluss von Zolpidem zum Kühlschrank schlafwandelten - und aßen, ohne sich am nächsten Morgen daran erinnern zu können.
Die "New York Times" berichtete im März 2006, dass in den US-Bundesstaaten Wisconsin und Washington die Zahl aus dem Verkehr gezogener Autofahrer gestiegen sei, in deren Blut die Polizei Zolpidem fand. "In einigen toxikologischen Labors ist Ambien bereits auf der Top-10-Liste von Wirkstoffen im Blut beeinträchtigter Verkehrsteilnehmer", schrieb die Zeitung.
Auch von nächtlichen Telefonaten und gar von Geschlechtsverkehr wurde berichtet, an die sich die Patienten am nächsten Morgen partout nicht mehr erinnern konnten. FDA-Experte Katz hält es für möglich, dass einige solcher Ereignisse nicht von Ärzten und Konstumenten berichtet worden seien - kein abwegiger Gedanke.
"Spekatulär, aber selten"
"Hängen Sie Glöckchen an Ihre Schlafzimmertür. Wenn Sie schlafwandeln, könnte das Geläut sie aufwecken", riet die "New York Times" ihren Lesern im März vergangenen Jahres. In Deutschland wird der Wirkstoff Zolpidem unter dem Markennamen Stilnox vertrieben. "Wir weisen in diesem Zusammenhang darauf hin, dass Schlafwandeln zwar während der Behandlung mit Stilnox auftreten kann, aber deswegen nicht unbedingt durch Stilnox verursacht sein muss", sagte Judith Kramer, Sprecherin von Sanofi-Aventis in Deutschland.
"Zolpidem ist heute die Nummer eins der verordneten Schlafmittel", sagt Walter Müller, Pharmakologe von der Universität Frankfurt am Main, zu SPIEGEL ONLINE. Er hatte im Jahr 2003 in der Fachzeitschrift "Addiction" festgestellt: Im Vergleich zu den bislang gegen Schlafstörungen verabreichten Barbituraten und Benzodiazepinen ist die Suchtgefahr viel geringer, und auch für Selbstmörder ist der Wirkstoff unattraktiv.
In Anbetracht der höchst seltenen Nebenwirkungen rät Müller zur Gelassenheit: Millionen von Menschen würden weltweit erfolgreich mit dieser Wirkstoffklasse behandelt, ohne eigenwillig schlafzuwandeln. Müller sagt: "Das kling spektakulär, ist aber sehr selten."
Also alles nur viel Lärm um wenig? Tatsächlich, darauf verweisen Experten, führt das US-Haftungsrecht und die dort üblichen immensen Schadensersatzforderungen vor Gericht tendenziell dazu, dass Unternehmen sich gegen alle Eventualitäten absichern. So kontaktierte die FDA die 13 Hersteller sedativ-hypnotischer Medikamente in Sachen Schlafwandeln.
FDA-Neurologe Russell Katz sagte, bis auf eine namentlich nicht genannte Pharmafirma hätten sich alle kooperativ gezeigt. Die FDA sagte auch, kein Patient solle das Medikament ohne ärztliche Konsultation absetzen. Ernst genug, um die Präparate vom Markt zu nehmen, seien die Bedenken jedenfalls nicht.
Schlaftablette weckt Dahindämmernde auf
Dass aber noch nicht jedes Detail der Wirkweise solcher Medikamente bekannt ist, zeigt sich auch an ganz unerwarteter Stelle. Tatsächlich werden dem Wirkstoff des Schlafhelfers Ambien noch ganz andere - heilende - Nebenwirkungen zugeschrieben:
Eine Französin, die sich in einem Koma-ähnlichen Dämmerzustand befand, ist 20 Minuten nach der Einnahme von Zolpidem plötzlich zeitweilig aufgewacht. Sie habe sich drei Stunden lang mit Angehörigen und Pflegepersonal verständigen können, habe gegessen und sich bewegt. Das berichten Ärzte um Christine Brefel-Courbon von der Universität Toulouse in der März-Ausgabe des Fachmagazins "Annals of Neurology"
Bei drei weiteren Patienten im vegetativen Zustand hat Ralf Clauss vom Royal Surrey Country Hospital im südenglischen Guildford diesen Effekt beobachtet. "Zolpidem scheint ein effektives Medikament zu sein, um die Gehirnfunktionen mancher Patienten in vegetativen Zustand wiederherzustellen", schrieb er vor einem Jahr in der Fachzeitschrift "Neurorehabilitation".
"Wiedergeboren" titelte die Londoner Zeitung "Guardian" im vergangenen September angesichts dieser Veröffentlichungen. Clauss und sein Co-Forscher, der Südafrikaner Wally Nel, hätten schon 150 hirngeschädigte Patienten entsprechend behandelt - und bei 60 Prozent eine Verbesserung feststellen können. "Etwas Seltsames und Wunderbares passiert hier", sagte Nel der Zeitung, "und wir müssen dem auf den Grund gehen."
Dies gilt möglicherweise für mehr als eine unerwartete Wirkung von sedativ-hypnotischen Medikamenten. Die FDA jedenfalls hat die Hersteller zu weiterführenden Studien zu Häufigkeit und Art der überraschenden Effekte aufgefordert. Nach Angaben von Russell Katz hat aber bislang keiner der 13 angesprochenen dies zugesagt.
In Deutschland wird jedenfalls der Beipackzettel von Stilnox gerade verändert, wie Sanofi-Aventis-Sprecherin Kramer zu SPIEGEL ONLINE sagte, "auf unsere eigene Initiative hin".
mit Material von Reuters
Ein weiterer Artikel über Ambien unterstützt vorigen Beitrag:
Nebenwirkung
Halluzinationen durch Schlafmittel
Ein gängiges Schlafmedikament hat in Einzelfällen Halluzinationen und Gedächtnisstörungen ausgelöst und Patienten schlafwandeln lassen.
Zolpidem kann offenbar zu Schlafwandeln führenEin kürzlich veröffentlichter Report der australischen Gesundheitsbehörde berichtet im Zusammenhang mit Zolpidem von verschiedenen seltsamen Vorfällen. So klagten 104 Patienten über Halluzinationen, 62 litten unter einem zeitweiligen Gedächtnisverlust, in und 16 Fällen hatten die Patienten im Schlaf bizarre Verhaltensweisen gezeigt.
Eine Frau erwachte beispielsweise mit dem Pinsel in der Hand vor ihrer Haustür, die sie im Schlaf gestrichen hatte. Eine andere nahm 23 Kilo zu, weil sie nachts unwissentlich den Kühlschrank leer futterte.
Randale an Bord
Auch britische Behörden berichten über 68 ähnliche Vorfälle, die zwischen 2001 und 2005 aufgetreten waren. Besonders besorgniserregend waren Berichte von Personen, die unter Medikamenteneinfluss schlafwandelnd Auto gefahren waren. In einem Fall musste ein Transatlantikflug umgeleitet werden, nachdem ein Passagier unter Zolpidem-Einfluss an Bord randalierte.
Der Wirkstoff, der auch in Deutschland häufig zur Behandlung von Schlafstörungen verschrieben wird, gilt als wirksam und dabei weniger suchtgefährdend als beispielsweise Diazepam (Valium). Ähnlich wie dieses verbessert es den Tiefschlaf, indem er bestimmte Rezeptoren im Gehirn belegt. Während unter Zolpidem Teile des Gehirns im Schlaf weniger aktiv sind, kann sich der Köper weiterhin bewegen, was Schlafwandeln möglich macht.
Auf der Suche nach den Ursachen
Obwohl Millionen Menschen das Medikament problemlos vertragen, gäben Einzelfälle Anlass, sie genauer zu untersuchen. „Wir müssen herausfinden, ob es sich um echte Nebenwirkungen handelt“, erklärt Schlafforscher Kenneth Wright von der University of Colorado. Einige Vorfälle ließen sich jedoch durch eine falsche Einnahme erklären, beispielsweise, wenn die Schlaftabletten nicht unmittelbar vor dem Zubettgehen geschluckt worden seien.
Der Pharmahersteller Sanofi-Aventis, der Schlafmittel auf Zolpidembasis produziert, gibt zu bedenken, dass die Vorfälle nicht unbedingt durch das Medikament ausgelöst worden sein müssten. Sprecherin Melissa Feltman weist darauf hin, dass die Sicherheit des Medikaments wissenschaftlich gut belegt sei. Möglicherweise seien die bizarren Verhaltensweisen eher auf eine verborgene psychische Störung zurückzuführen.
Ich bin guter Dinge, daß der GABA-Agonist EVT-201 genug Potential für einen Blockbuster-Effekt haben wird.
Es gibt genug Potential für einen besseren GABA-Agonisten, sieht man die aufgetretenen Nebeneffekte bei Ambien.
Ich gehe von einer überzeugenderen Zusammensetzung bei EVT 201 aus, obwohl Zolpidem in Form von Ambien sicher schon viele Risiken ausschließt gegenüber den herkömmlichen anderen Verschreibungspflichtigen ausschließt.
Was sagt ipollit zu meiner Meinung?
Ostdi
Eins möchte ich bitte noch zum vorigen Beitrag zu bedenken geben:
Fakt Nr.1:
Die bekannt gewordenen Fälle spiegeln nur verschleiert die Wirklichkeit wieder.
Viele werden aus ihrem Fall kein Aufsehens machen.
Die Pharmaindustrie ist schon allein deshalb, daß der Umsatz und der Ruf nicht gefährtet werden, äußerst bemüht, die Fehler von sich zu weisen.
Es wird mit Sicherheit eine Menge Geld in die Verschleierung der Tatsachen investiert. Wenn die Sprecher von Sanofi-Aventis in ihren Erklärungen deutlich machen, daß andere Schuld haben an den eindeutig auftretenden Nebeneffekten, dann haben sie aber die Beweise nicht mitgeliefert (ganz einfach, weil sie keine haben) , zu 100% steht aber fest, in welcher Form GABA beeinflußt werden kann.
Fakt Nr.2:
"Der GABA(a)-Rezeptor ist sehr weit im Gehirn und Rückenmark verbreitet und der wichtigste inhibitorische Rezeptor im zentralen Nervensystem (ZNS). 30 % der Transmittermenge im ZNS
entfallen auf GABA. Besondere Funktion hat er in den Basalganglien und dem Kleinhirn, wo er an der motorischen Kontrolle beteiligt ist. Die Purkinje-Zelle des Kleinhirns ist z. B. GABAerg. Im
Thalamus wirkt GABA an der Einleitung und Aufrechterhaltung des Schlafs.
Hier ist auch der Hauptangriffsort der pharmakologischen Beeinflussung durch Benzodiazepine und Barbiturate.
Im Rückenmark befinden sich GABA-Rezeptoren auf Motorneuronen, und sie sind an der Reflex-Verschaltung ebenso wie der Koordination von Bewegungsabläufen beteiligt (siehe: Renshaw-Zellen).
Einige funktionelle Unterschiede stehen in Verbindung mit den verschiedenen a-Untereinheiten:
- a-Untereinheiten sind mit der anxiolytischen (angstlösenden) Funktion des Rezeptors in Verbindung zu setzen, und
- a3-Untereinheiten kommen in Rezeptoren vor, die vornehmlich eine muskelrelaxierende Wirkung besitzen.", so die Funktionsbeschreibung."
Betrachtet man die Wirkung der Schlafmittel, so kann man feststellen, daß sie wie ein Klecks Farbe, der über alles breit läuft, auch auf den Gaba-Rezeptor komplex wirken:
Auch Zolpidem leitet also nicht nur den Schlaf ein, sondern fördert auch all die negativen Nettigkeiten, die damit zusammenhängen.
Schlicht und einfach ist eine punktuelle Wirkung bisher nicht möglich, auch nicht mit Zolpidem trotz geringerer Plasmahalbwertszeiten.
Bewiesen ist, daß Zolpidem als sedativ hypnotisches Schlafmittel sowie sein Blockbuster Ambien und andere Varianten davon ähnlich wie Benzodiazepine wirken, folglich auch Nebenwirkungen haben.
Eine Abriegelung der Wirkung gibt es auch hier nicht.
Die Vorfälle in den USA mit Ambien haben die amerikanische Aufsichtsbehörde FDA aufgerüttelt und aufmerksam gemacht.
Jetzt wird man (und hat sicherlich bei den letzten Zulassungsversuchen) viel genauer hinzuschauen und erneute Zulassungen verstärkt unter diesen und den schon bis dahin wichtigen Gesichtspunkten beim Zulassungsverfahren prüfen und bei ähnlichen Gebilden wie sicherlich Indiplon, etc. die Zulassung ablehnen.
Durch die Abriegelung in der Substanz bei EVT-201 sehe ich daher von dieser Seite gute Chancen trotz schwierigem Umfeld für den Erfolg.
Was EVT-201 sonst noch alles kann, ist im Details auch noch geheim.
Glaubt man den Aussagen von Aldag, so sieht es gut aus betreffs eines finanzkräftigen Partners.
Ostdi
Fakt Nr.1:
Die bekannt gewordenen Fälle spiegeln nur verschleiert die Wirklichkeit wieder.
Viele werden aus ihrem Fall kein Aufsehens machen.
Die Pharmaindustrie ist schon allein deshalb, daß der Umsatz und der Ruf nicht gefährtet werden, äußerst bemüht, die Fehler von sich zu weisen.
Es wird mit Sicherheit eine Menge Geld in die Verschleierung der Tatsachen investiert. Wenn die Sprecher von Sanofi-Aventis in ihren Erklärungen deutlich machen, daß andere Schuld haben an den eindeutig auftretenden Nebeneffekten, dann haben sie aber die Beweise nicht mitgeliefert (ganz einfach, weil sie keine haben) , zu 100% steht aber fest, in welcher Form GABA beeinflußt werden kann.
Fakt Nr.2:
"Der GABA(a)-Rezeptor ist sehr weit im Gehirn und Rückenmark verbreitet und der wichtigste inhibitorische Rezeptor im zentralen Nervensystem (ZNS). 30 % der Transmittermenge im ZNS
entfallen auf GABA. Besondere Funktion hat er in den Basalganglien und dem Kleinhirn, wo er an der motorischen Kontrolle beteiligt ist. Die Purkinje-Zelle des Kleinhirns ist z. B. GABAerg. Im
Thalamus wirkt GABA an der Einleitung und Aufrechterhaltung des Schlafs.
Hier ist auch der Hauptangriffsort der pharmakologischen Beeinflussung durch Benzodiazepine und Barbiturate.
Im Rückenmark befinden sich GABA-Rezeptoren auf Motorneuronen, und sie sind an der Reflex-Verschaltung ebenso wie der Koordination von Bewegungsabläufen beteiligt (siehe: Renshaw-Zellen).
Einige funktionelle Unterschiede stehen in Verbindung mit den verschiedenen a-Untereinheiten:
- a-Untereinheiten sind mit der anxiolytischen (angstlösenden) Funktion des Rezeptors in Verbindung zu setzen, und
- a3-Untereinheiten kommen in Rezeptoren vor, die vornehmlich eine muskelrelaxierende Wirkung besitzen.", so die Funktionsbeschreibung."
Betrachtet man die Wirkung der Schlafmittel, so kann man feststellen, daß sie wie ein Klecks Farbe, der über alles breit läuft, auch auf den Gaba-Rezeptor komplex wirken:
Auch Zolpidem leitet also nicht nur den Schlaf ein, sondern fördert auch all die negativen Nettigkeiten, die damit zusammenhängen.
Schlicht und einfach ist eine punktuelle Wirkung bisher nicht möglich, auch nicht mit Zolpidem trotz geringerer Plasmahalbwertszeiten.
Bewiesen ist, daß Zolpidem als sedativ hypnotisches Schlafmittel sowie sein Blockbuster Ambien und andere Varianten davon ähnlich wie Benzodiazepine wirken, folglich auch Nebenwirkungen haben.
Eine Abriegelung der Wirkung gibt es auch hier nicht.
Die Vorfälle in den USA mit Ambien haben die amerikanische Aufsichtsbehörde FDA aufgerüttelt und aufmerksam gemacht.
Jetzt wird man (und hat sicherlich bei den letzten Zulassungsversuchen) viel genauer hinzuschauen und erneute Zulassungen verstärkt unter diesen und den schon bis dahin wichtigen Gesichtspunkten beim Zulassungsverfahren prüfen und bei ähnlichen Gebilden wie sicherlich Indiplon, etc. die Zulassung ablehnen.
Durch die Abriegelung in der Substanz bei EVT-201 sehe ich daher von dieser Seite gute Chancen trotz schwierigem Umfeld für den Erfolg.
Was EVT-201 sonst noch alles kann, ist im Details auch noch geheim.
Glaubt man den Aussagen von Aldag, so sieht es gut aus betreffs eines finanzkräftigen Partners.
Ostdi
Warum sollte man den Aussagen Aldags eigentlich nicht vertrauen?!
Bis jetzt hat doch alles gestimmt, was er vorher geplant hatte...
Ostdi
Bis jetzt hat doch alles gestimmt, was er vorher geplant hatte...
Ostdi
Gelesen im Quartalsbericht 2008, II.Quartal
* Evotec wird die Ergebnisse der ersten Phase-II-Studie mit EVT 302, einem hoch selektiven und reversiblen
MAO-B-Inhibitor zur Unterstützung der Raucherentwöhnung, im dritten Quartal 2008 bekannt geben. Für die
relevante Wirksamkeitsstudie, die untersucht, in welchem Ausmaß starke Raucher unter dem Einfluss von EVT 302 das
Rauchen aufgeben, haben wir die Genehmigung der Ethikkommission erhalten und erwarten die endgültige Zulassung in
Kürze.
Die Bekanntgabe der ersten Ergebnisse ist also bis 30. September (Quartalsende) zu melden und durch.
M.f.G. Ostdi
* Evotec wird die Ergebnisse der ersten Phase-II-Studie mit EVT 302, einem hoch selektiven und reversiblen
MAO-B-Inhibitor zur Unterstützung der Raucherentwöhnung, im dritten Quartal 2008 bekannt geben. Für die
relevante Wirksamkeitsstudie, die untersucht, in welchem Ausmaß starke Raucher unter dem Einfluss von EVT 302 das
Rauchen aufgeben, haben wir die Genehmigung der Ethikkommission erhalten und erwarten die endgültige Zulassung in
Kürze.
Die Bekanntgabe der ersten Ergebnisse ist also bis 30. September (Quartalsende) zu melden und durch.
M.f.G. Ostdi
Hallo Freunde,
EVT 101 ist ein Wirkstoff, der auf einen der NMDA-Rezeptoren wirkt.
Dazu nochmals au dem HJ-Bericht 2008:
\"...Am 3. Juli 2008 gaben wir die Ergebnisse zu den wesentlichen Endpunkten einer doppelt verblindeten, vierwöchigen Phase-Ib-Studie mit EVT 101 bekannt. Bei diesem Wirkstoff handelt es sich um einen oral verfügbaren, für den NR2B-Subtyp des NMDA-Rezeptors selektiven Antagonisten mit Potenzial für die Behandlung der Alzheimer’schen Erkrankung, neuropathischer Schmerzen sowie anderer Erkrankungen. ....
Wir haben Dosierungen gefunden, die im Gehirn einen hohen Blockadegrad für den NR2B-Rezeptor erzielen. Diese Dosierungen rufen eine spezifische Modulation von relevanten Hirnregionen hervor ...\"
Was sind NMDA-Rezeptoren:
\"NMDA-Rezeptoren gehören zu den ionotropen Glutamatrezeptoren.
Das sind Ionenkanäle in der Zellmembran, die durch die Bindung ihres Liganden Glutamat aktiviert werden. Der Name „NMDA-Rezeptor“ rührt daher, dass diese Rezeptoren durch die Bindung des für sie spezifischen Agonisten N-Methyl-D-Aspartat (NMDA) aktiviert werden können. Dieser Stoff kommt im Körper normalerweise nicht vor, führt aber im Experiment zur Öffnung der Ionenkanal-Untereinheit des sog. Rezeptors.
In der postsynaptischen Membran lokalisiert, steuern sie den
Ionenfluss an der nachgeschalteten Nervenzelle der Synapse, und
zwar selektiv nach Art der Ionen.
Man nimmt also Einfluß auf den Ionenfluß, Ionenaustausch.
....
Man nimmt heute an, dass die Leitfähigkeitserhöhung
des NMDA-Rezeptors eins der wesentlichen Elemente für die Induktion synaptischer Plastizität ist
und damit einen molekularen Mechanismus für Lernen und Gedächtnis darstellt.
Das Modell besagt, dass NMDA-Rezeptoren bestimmter synaptischer Bahnen, die sehr häufig
benutzt werden, durch die ständige Depolarisation der postsynaptischen Membran deblockiert werden und somit diese Bahnen besser leitfähig werden als alternative Verschaltungsmuster. Somit
werden bestimmte „Wege“ gebahnt, ein wesentlicher Prozess des Lernens.\"
Sie sind also mit verantwortlich für normales Denken, sich erinnern, auch für funktionale Dinge wie:
ich muß essen, ich muß trinken, ich muß ´mal \"Pipi\", etc.
Folglich wirkt EVT 101 u.a. darauf, wenn denn der Ligant Glutamat nicht gebunden werden kann, EVT-101 als Ersatz gebunden werden kann, oder über EVT-101 Glutamat wieder angebunden werden kann...
Das ist aber nur eben die Bekämpfung der Symptome, die Linderung oder Verzögerung des Niedergangs in der Krankheit Alzheimer, eine Ersatzleistung für Unwiderbringliches bei dieser Krankheit.
Dazu unter Wikipedia:
\"Memantin ist Derivat des Amantadin und wird als Arzneistoff aus der Gruppe der Antidementiva in der Behandlung von moderater bis schwerer Demenz vom Alzheimer-Typ eingesetzt (Handelsnamen
AXURA® von MERZ; NAMENDA® von FOREST; EBIXA® von LUNDBECK).
Es ist der einzige Vertreter der Klasse der NMDA-Rezeptor-Antagonisten (NMDA = N-Methyl-D-Aspartat) bei den Antialzheimer-Medikamenten. Die Wirksamkeit wird kontrovers diskutiert.\"
und weiter:
Memantin ist ein moderat-affiner nichtkompetitiver Antagonist des NMDA-Rezeptors, und greift somit ins glutamaterge System ein. Glutamat ist ein erregender Neurotransmitter im zentralen
Nervensystem und Störungen im glutamatergen Neurotransmitter-System spielen eine bedeutende Rolle in der Pathophysiologie primärer Demenzen.
Aufgrund seines spezifischen Bindungsverhaltens am NMDA-Rezeptor blockiert Memantin schädliche Glutamat-Wirkungen, die zu Funktionseinschränkungen und schließlich zum Absterben
von Nervenzellen führen. Memantin gibt den mit dem Rezeptor verbundenen Ionenkanal wieder frei, sobald ein physiologisches Signal eintrifft, wie z. B. bei kognitiven Prozessen. Der Lern- und Gedächtnisvorgang kann weiter ablaufen. ...
Unerwünschte Wirkungen (Nebenwirkungen)
Nebenwirkungen sind motorische Unruhe, Kopfschmerzen, Müdigkeit, Verwirrtheit, Halluzinationen, Verstopfung, anormaler Gang, Schwindel, Übelkeit, Erbrechen, erhöhte
Krampfbereitschaft.
Geschichtliches
Memantin wurde von Merz entwickelt und ist seit 2002 zur Behandlung der Alzheimerschen
Krankheit zugelassen. Von Forest wurde Memantin für die USA und von Lundbeck für einige
europäische und internationale Märkte lizenziert. Zuvor wurde Memantin unter der BezeichnungAkatinol für die Behandlung spastischer Leiden, des hirnorganischen Psychosyndroms, Parkinson-
Krankheit bzw. leichter und mittelschwerer Hirnleistungsstörungen eingesetzt. Die Umbenennung und Indikationserweiterung ging mit einer drastischen Preiserhöhung einher.
Studien
In verschiedenen Untersuchungen konnte gezeigt werden, dass das cholinerge Defizit nicht alleinverantwortlich für die Demenz-Pathologie ist, sondern Störungen im glutamatergen
Neurotransmitter-System entscheidend an der Pathologie der Demenzen beteiligt sind. Deshalb ist
die Modulation der Glutamat-Wirkung im Gehirn, die vorwiegend über NMDA-Rezeptoren erfolgt, ein neuer Behandlungsansatz.
Die Memantin-Therapie führt bei mittelschwerer bis schwerer Alzheimersymptomatik bei den drei Kerndomänen (Kognition, Alltagskompetenz, klinischer Gesamteindruck) nach sechs Monaten zu
signifikanten, insgesamt jedoch geringen Besserungen bzw. Verzögerungen der Symptomatik verglichen mit einer Placebobehandlung. Weiterhin kann die Behandlung mit diesem
Antidementivum laut einer Auswertung von zwei randomisierten Studien unter Beteiligung des Herstellers Merz dazu beitragen, demenzbedingte Verhaltensstörungen zu vermindern .\"
Schauen wir auf den Ausblick bei Alzheimer-Behandlung:
Ausblick
Eine Vielzahl von Ansätzen zur Behandlung der Alzheimer-Krankheit befinden sich derzeit in der klinischen Prüfung. In Studien der Phase-II und Phase-III werden Patienten zwischen 12 und 18 Monaten
mit dem zu testenden Wirkstoff behandelt - hinzu kommen noch einige Monate, um geeignete Patienten in die Studie aufzunehmen und die Ergebnisse auszuwerten. Unter optimalen Bedingungen und bei
gegebener Wirksamkeit und Sicherheit benötigt ein Wirkstoff vom Beginn der Tests am Menschen bis zu seiner Marktzulassung mindestens vier Jahre.
Der Gamma-Secretase Modulator Tarenflurbil (MPC-7869,
früher R-flubiprofen), auch als selektiver A-Gamma-42 senkendes Medikament bezeichnet, soll die Entstehung von A-Gamma verringern und wird bereits in einer Phase-III Studie getestet .
Durch die Einnahme des Statins Simvastatin konnte die Entstehung von Alzheimer und Parkinson um bis zu 50 Prozent gesenkt werden. .
Eine Pilotstudie mit dem Wirkstoff Etanercept aus dem Jahr 2006 zeigte geringe aber dennoch statistisch
signifikante Verbesserungen in verschiedenen kognitiven Bewertungsskalen . In einer weiteren Studie
mit nur einem Patienten konnte durch spinale Infusion eine rasche und deutliche Besserung der
Symptome erzielt werden .
Die Entstehung des neurotoxischen A42-Peptids beruht nach Erkenntnissen von Wissenschaftlern
der Freien Universität Berlin auf der Dimerisierung des APP über sogenannte GxxxG-Motive und
einer damit verbundenen geänderten Prozessierung von APP durch die gamma-Sekretase. Das
GxxxG-Proteinmotiv wurde bisher nicht in APP oder A funktional beschrieben.
Das amerikanische Pharmaunternehmen Myriad wird voraussichtlich 2007 den neuen A-42
senkenden Wirkstoff Tarenflurbil unter dem Handelsnamen Flurizan auf den Markt bringen.
Momentan befindet er sich in Phase-III der klinischen Prüfung.
Möglicherweise geht die Alzheimersche Krankheit mit einem Mangel an Kupfer einher. Versuche
mit transgenen Mäusen haben ergeben, dass bei Mäusen mit amyloiden Plaques der Kupferspiegel
gegenüber gesunden Tieren stark absank. Testergebnisse legen den Schluss nahe, dass der
Stoffwechsel des essentiellen Metallions Kupfer bei Alzheimer-Patienten gestört ist. Bei In-Vitro-
Studien konnte gezeigt werden, dass ein erhöhter APP (Amyloid-Vorläuferprotein) und A-
Spiegel zum Absinken des Kupferspiegels führt.
Durch den verstärkten Abtransport von Kupfer aus den Zellen entsteht ein Mangel im Gewebe, der in den Zellen eine verminderte Aktivität des Enzyms Superoxid-Dismutase bewirkt.
Gerd Multhaup und Thomas Bayer von der Freien Universität Berlin verabreichten ihren Probanden bioaktives Kupfer über die Nahrung und fanden ihren Verdacht in sogenannten ADAS-cog-Tests bestätigt. Derzeit wird an der Universität des Saarlands in der Klinik für Psychiatrie unter der Leitung von Frank Pajonk und Thomas Bayer eine Phase-II Doppel-blind Studie mit Kupfergaben durchgeführt.
Seit 2002 wird in der wissenschaftlichen Literatur der Einfluss von fehlgefalteten oder biologisch inaktiven Metalloproteinen (z. B. Kupferchaperon für Superoxiddismutase) im Zusammenhang mit
Demenzerkrankungen diskutiert. In einem aktuellen Artikel wird dargelegt, mit welchen analytischen Methoden (z. B. der
quantitativen präparativen nativen kontinuierlichen Polyacrylamid- Gelelektrophorese = QPNC-PAGE und NMR-Spektroskopie) Struktur-
Funktionsbeziehungen von nativen und denaturierten Metalloproteinen in biologischen Flüssigkeiten aufgeklärt werden können.
In „Nature Precedings“ wird über eine Möglichkeit zur
ursächlichen Behandlung von Morbus, Alzheimer und anderen Proteinfehlfaltungskrankheiten berichtet. Die Studie zeigt, dass mit Hilfe von Chaperon-Proteinen, die aus Pflanzen gewonnen werden können (sog. \"Metallo-Phytochaperone\"), die Möglichkeit besteht, menschliche ungefaltete Superoxiddismutase zu aktivieren und unkomplexierte Metallionen (z.B. Kupfer, Zink, Eisen) im menschlichen Organismus zu binden, was zur Reduktion von oxidativem Stress in der Zelle führen kann.
Aus Langzeitstudien ist bekannt, dass Diabetes mellitus Typs II das Risiko, an einer sporadischen Alzheimer-Demenz zu erkranken, etwas erhöht. Die Forscher der Rotterdam-Studie schätzen, dass
fast neun Prozent aller Alzheimer-Fälle auf Diabetes zurückgehen.
Diskutiert wird auch ein Ansatz, nach dem Alzheimer durch eine Insulinresistenz der Zellen im Gehirn ausgelöst würde. Sie wäre demnach ein Subtyp von Diabetes. Diese Insulinresistenz würde
durch einen von Amyloid-Beta abgeleiteten, diffusionsfähigen Liganden verursacht.
Die beta-Amyloid-Immuntherapie, umgangsspachlich auch als Alzheimer-Impfung bezeichnet, stellt einen experimentellen Therapieansatz dar, bei dem durch eine passive Immunisierung mit dem Protein beta-Amyloid, das Fortschreiten der Erkrankung verlangsamt werden soll.
In einer Studie wurde über ein Jahr an 120 Alzheimer Patienten antihistamin Dimebon getestet. Dabei wurde gegenüber Placebo eine signifikante Steigerung der kognitiven Fähigkeiten erzielt.
Ein Impfstoff gegen Amyloid-Plaques, der in einer klinischen Studie an der Universität Southampton in England untersucht wurde, konnte erfolgreich die Plaques im Gehirn der Betroffenen entfernen, wie Post-Mortem analysen des Gewebes zeigten. Allerdings war damit nicht wie erhofft auch eine Linderung bzw. ein Rückgang der bereits entstandenen Symptome verbunden. Jetzt soll untersucht werden, ob der Impfstoff, wenn er in einer sehr frühen Phase der Erkrankung gegeben wird, das Voranschreiten verhindern oder verlangsamen kann .
Ermutigende Resultate brachte eine 50-wöchige Phase-II Studie mit dem Arzneistoff Methylblau (Rember) an 321 Patienten mit leicht bis moderat fortgeschrittener Erkrankung. Der Wirkstoff löst
Tau Protein Verbindungen auf und verhindt so die Bildung von Tau Protein Fasern in den Nervenzellen. Der beste Effekt konnte durch die Gabe von 60mg des Wirkstoffes erzielt werden.
Insgesamt wurde eine um 81 % geringere Verschlechterung der kognitiven Leistungsfähigkeit gegenüber Placebo festgestellt. Größere Phase-III Studien, welche 2009 starten sollen, sind
notwendig um das Resultat zu bestätigen. Wenn die weitere Prüfung des Medikaments reibungslos verläuft, könnte es im Jahr 2012 zugelassen werden .\"
Literatur: Wikipedia\"Alzheimer\"
Die entscheidenden Arzneistoffe scheinen schon für Alzheimer unterwegs zu sein. Letzteres Präparat wird wahrscheinlich 2012 zugelassen. Das sind, so glaube ich schlechte Chancen für Pfizer auf diesem Gebiet, denn dann wären spätestens dann Symptom-Präparate nicht mehr absetzbar.
EVT 101 ist ein Wirkstoff, der auf einen der NMDA-Rezeptoren wirkt.
Dazu nochmals au dem HJ-Bericht 2008:
\"...Am 3. Juli 2008 gaben wir die Ergebnisse zu den wesentlichen Endpunkten einer doppelt verblindeten, vierwöchigen Phase-Ib-Studie mit EVT 101 bekannt. Bei diesem Wirkstoff handelt es sich um einen oral verfügbaren, für den NR2B-Subtyp des NMDA-Rezeptors selektiven Antagonisten mit Potenzial für die Behandlung der Alzheimer’schen Erkrankung, neuropathischer Schmerzen sowie anderer Erkrankungen. ....
Wir haben Dosierungen gefunden, die im Gehirn einen hohen Blockadegrad für den NR2B-Rezeptor erzielen. Diese Dosierungen rufen eine spezifische Modulation von relevanten Hirnregionen hervor ...\"
Was sind NMDA-Rezeptoren:
\"NMDA-Rezeptoren gehören zu den ionotropen Glutamatrezeptoren.
Das sind Ionenkanäle in der Zellmembran, die durch die Bindung ihres Liganden Glutamat aktiviert werden. Der Name „NMDA-Rezeptor“ rührt daher, dass diese Rezeptoren durch die Bindung des für sie spezifischen Agonisten N-Methyl-D-Aspartat (NMDA) aktiviert werden können. Dieser Stoff kommt im Körper normalerweise nicht vor, führt aber im Experiment zur Öffnung der Ionenkanal-Untereinheit des sog. Rezeptors.
In der postsynaptischen Membran lokalisiert, steuern sie den
Ionenfluss an der nachgeschalteten Nervenzelle der Synapse, und
zwar selektiv nach Art der Ionen.
Man nimmt also Einfluß auf den Ionenfluß, Ionenaustausch.
....
Man nimmt heute an, dass die Leitfähigkeitserhöhung
des NMDA-Rezeptors eins der wesentlichen Elemente für die Induktion synaptischer Plastizität ist
und damit einen molekularen Mechanismus für Lernen und Gedächtnis darstellt.
Das Modell besagt, dass NMDA-Rezeptoren bestimmter synaptischer Bahnen, die sehr häufig
benutzt werden, durch die ständige Depolarisation der postsynaptischen Membran deblockiert werden und somit diese Bahnen besser leitfähig werden als alternative Verschaltungsmuster. Somit
werden bestimmte „Wege“ gebahnt, ein wesentlicher Prozess des Lernens.\"
Sie sind also mit verantwortlich für normales Denken, sich erinnern, auch für funktionale Dinge wie:
ich muß essen, ich muß trinken, ich muß ´mal \"Pipi\", etc.
Folglich wirkt EVT 101 u.a. darauf, wenn denn der Ligant Glutamat nicht gebunden werden kann, EVT-101 als Ersatz gebunden werden kann, oder über EVT-101 Glutamat wieder angebunden werden kann...
Das ist aber nur eben die Bekämpfung der Symptome, die Linderung oder Verzögerung des Niedergangs in der Krankheit Alzheimer, eine Ersatzleistung für Unwiderbringliches bei dieser Krankheit.
Dazu unter Wikipedia:
\"Memantin ist Derivat des Amantadin und wird als Arzneistoff aus der Gruppe der Antidementiva in der Behandlung von moderater bis schwerer Demenz vom Alzheimer-Typ eingesetzt (Handelsnamen
AXURA® von MERZ; NAMENDA® von FOREST; EBIXA® von LUNDBECK).
Es ist der einzige Vertreter der Klasse der NMDA-Rezeptor-Antagonisten (NMDA = N-Methyl-D-Aspartat) bei den Antialzheimer-Medikamenten. Die Wirksamkeit wird kontrovers diskutiert.\"
und weiter:
Memantin ist ein moderat-affiner nichtkompetitiver Antagonist des NMDA-Rezeptors, und greift somit ins glutamaterge System ein. Glutamat ist ein erregender Neurotransmitter im zentralen
Nervensystem und Störungen im glutamatergen Neurotransmitter-System spielen eine bedeutende Rolle in der Pathophysiologie primärer Demenzen.
Aufgrund seines spezifischen Bindungsverhaltens am NMDA-Rezeptor blockiert Memantin schädliche Glutamat-Wirkungen, die zu Funktionseinschränkungen und schließlich zum Absterben
von Nervenzellen führen. Memantin gibt den mit dem Rezeptor verbundenen Ionenkanal wieder frei, sobald ein physiologisches Signal eintrifft, wie z. B. bei kognitiven Prozessen. Der Lern- und Gedächtnisvorgang kann weiter ablaufen. ...
Unerwünschte Wirkungen (Nebenwirkungen)
Nebenwirkungen sind motorische Unruhe, Kopfschmerzen, Müdigkeit, Verwirrtheit, Halluzinationen, Verstopfung, anormaler Gang, Schwindel, Übelkeit, Erbrechen, erhöhte
Krampfbereitschaft.
Geschichtliches
Memantin wurde von Merz entwickelt und ist seit 2002 zur Behandlung der Alzheimerschen
Krankheit zugelassen. Von Forest wurde Memantin für die USA und von Lundbeck für einige
europäische und internationale Märkte lizenziert. Zuvor wurde Memantin unter der BezeichnungAkatinol für die Behandlung spastischer Leiden, des hirnorganischen Psychosyndroms, Parkinson-
Krankheit bzw. leichter und mittelschwerer Hirnleistungsstörungen eingesetzt. Die Umbenennung und Indikationserweiterung ging mit einer drastischen Preiserhöhung einher.
Studien
In verschiedenen Untersuchungen konnte gezeigt werden, dass das cholinerge Defizit nicht alleinverantwortlich für die Demenz-Pathologie ist, sondern Störungen im glutamatergen
Neurotransmitter-System entscheidend an der Pathologie der Demenzen beteiligt sind. Deshalb ist
die Modulation der Glutamat-Wirkung im Gehirn, die vorwiegend über NMDA-Rezeptoren erfolgt, ein neuer Behandlungsansatz.
Die Memantin-Therapie führt bei mittelschwerer bis schwerer Alzheimersymptomatik bei den drei Kerndomänen (Kognition, Alltagskompetenz, klinischer Gesamteindruck) nach sechs Monaten zu
signifikanten, insgesamt jedoch geringen Besserungen bzw. Verzögerungen der Symptomatik verglichen mit einer Placebobehandlung. Weiterhin kann die Behandlung mit diesem
Antidementivum laut einer Auswertung von zwei randomisierten Studien unter Beteiligung des Herstellers Merz dazu beitragen, demenzbedingte Verhaltensstörungen zu vermindern .\"
Schauen wir auf den Ausblick bei Alzheimer-Behandlung:
Ausblick
Eine Vielzahl von Ansätzen zur Behandlung der Alzheimer-Krankheit befinden sich derzeit in der klinischen Prüfung. In Studien der Phase-II und Phase-III werden Patienten zwischen 12 und 18 Monaten
mit dem zu testenden Wirkstoff behandelt - hinzu kommen noch einige Monate, um geeignete Patienten in die Studie aufzunehmen und die Ergebnisse auszuwerten. Unter optimalen Bedingungen und bei
gegebener Wirksamkeit und Sicherheit benötigt ein Wirkstoff vom Beginn der Tests am Menschen bis zu seiner Marktzulassung mindestens vier Jahre.
Der Gamma-Secretase Modulator Tarenflurbil (MPC-7869,
früher R-flubiprofen), auch als selektiver A-Gamma-42 senkendes Medikament bezeichnet, soll die Entstehung von A-Gamma verringern und wird bereits in einer Phase-III Studie getestet .
Durch die Einnahme des Statins Simvastatin konnte die Entstehung von Alzheimer und Parkinson um bis zu 50 Prozent gesenkt werden. .
Eine Pilotstudie mit dem Wirkstoff Etanercept aus dem Jahr 2006 zeigte geringe aber dennoch statistisch
signifikante Verbesserungen in verschiedenen kognitiven Bewertungsskalen . In einer weiteren Studie
mit nur einem Patienten konnte durch spinale Infusion eine rasche und deutliche Besserung der
Symptome erzielt werden .
Die Entstehung des neurotoxischen A42-Peptids beruht nach Erkenntnissen von Wissenschaftlern
der Freien Universität Berlin auf der Dimerisierung des APP über sogenannte GxxxG-Motive und
einer damit verbundenen geänderten Prozessierung von APP durch die gamma-Sekretase. Das
GxxxG-Proteinmotiv wurde bisher nicht in APP oder A funktional beschrieben.
Das amerikanische Pharmaunternehmen Myriad wird voraussichtlich 2007 den neuen A-42
senkenden Wirkstoff Tarenflurbil unter dem Handelsnamen Flurizan auf den Markt bringen.
Momentan befindet er sich in Phase-III der klinischen Prüfung.
Möglicherweise geht die Alzheimersche Krankheit mit einem Mangel an Kupfer einher. Versuche
mit transgenen Mäusen haben ergeben, dass bei Mäusen mit amyloiden Plaques der Kupferspiegel
gegenüber gesunden Tieren stark absank. Testergebnisse legen den Schluss nahe, dass der
Stoffwechsel des essentiellen Metallions Kupfer bei Alzheimer-Patienten gestört ist. Bei In-Vitro-
Studien konnte gezeigt werden, dass ein erhöhter APP (Amyloid-Vorläuferprotein) und A-
Spiegel zum Absinken des Kupferspiegels führt.
Durch den verstärkten Abtransport von Kupfer aus den Zellen entsteht ein Mangel im Gewebe, der in den Zellen eine verminderte Aktivität des Enzyms Superoxid-Dismutase bewirkt.
Gerd Multhaup und Thomas Bayer von der Freien Universität Berlin verabreichten ihren Probanden bioaktives Kupfer über die Nahrung und fanden ihren Verdacht in sogenannten ADAS-cog-Tests bestätigt. Derzeit wird an der Universität des Saarlands in der Klinik für Psychiatrie unter der Leitung von Frank Pajonk und Thomas Bayer eine Phase-II Doppel-blind Studie mit Kupfergaben durchgeführt.
Seit 2002 wird in der wissenschaftlichen Literatur der Einfluss von fehlgefalteten oder biologisch inaktiven Metalloproteinen (z. B. Kupferchaperon für Superoxiddismutase) im Zusammenhang mit
Demenzerkrankungen diskutiert. In einem aktuellen Artikel wird dargelegt, mit welchen analytischen Methoden (z. B. der
quantitativen präparativen nativen kontinuierlichen Polyacrylamid- Gelelektrophorese = QPNC-PAGE und NMR-Spektroskopie) Struktur-
Funktionsbeziehungen von nativen und denaturierten Metalloproteinen in biologischen Flüssigkeiten aufgeklärt werden können.
In „Nature Precedings“ wird über eine Möglichkeit zur
ursächlichen Behandlung von Morbus, Alzheimer und anderen Proteinfehlfaltungskrankheiten berichtet. Die Studie zeigt, dass mit Hilfe von Chaperon-Proteinen, die aus Pflanzen gewonnen werden können (sog. \"Metallo-Phytochaperone\"), die Möglichkeit besteht, menschliche ungefaltete Superoxiddismutase zu aktivieren und unkomplexierte Metallionen (z.B. Kupfer, Zink, Eisen) im menschlichen Organismus zu binden, was zur Reduktion von oxidativem Stress in der Zelle führen kann.
Aus Langzeitstudien ist bekannt, dass Diabetes mellitus Typs II das Risiko, an einer sporadischen Alzheimer-Demenz zu erkranken, etwas erhöht. Die Forscher der Rotterdam-Studie schätzen, dass
fast neun Prozent aller Alzheimer-Fälle auf Diabetes zurückgehen.
Diskutiert wird auch ein Ansatz, nach dem Alzheimer durch eine Insulinresistenz der Zellen im Gehirn ausgelöst würde. Sie wäre demnach ein Subtyp von Diabetes. Diese Insulinresistenz würde
durch einen von Amyloid-Beta abgeleiteten, diffusionsfähigen Liganden verursacht.
Die beta-Amyloid-Immuntherapie, umgangsspachlich auch als Alzheimer-Impfung bezeichnet, stellt einen experimentellen Therapieansatz dar, bei dem durch eine passive Immunisierung mit dem Protein beta-Amyloid, das Fortschreiten der Erkrankung verlangsamt werden soll.
In einer Studie wurde über ein Jahr an 120 Alzheimer Patienten antihistamin Dimebon getestet. Dabei wurde gegenüber Placebo eine signifikante Steigerung der kognitiven Fähigkeiten erzielt.
Ein Impfstoff gegen Amyloid-Plaques, der in einer klinischen Studie an der Universität Southampton in England untersucht wurde, konnte erfolgreich die Plaques im Gehirn der Betroffenen entfernen, wie Post-Mortem analysen des Gewebes zeigten. Allerdings war damit nicht wie erhofft auch eine Linderung bzw. ein Rückgang der bereits entstandenen Symptome verbunden. Jetzt soll untersucht werden, ob der Impfstoff, wenn er in einer sehr frühen Phase der Erkrankung gegeben wird, das Voranschreiten verhindern oder verlangsamen kann .
Ermutigende Resultate brachte eine 50-wöchige Phase-II Studie mit dem Arzneistoff Methylblau (Rember) an 321 Patienten mit leicht bis moderat fortgeschrittener Erkrankung. Der Wirkstoff löst
Tau Protein Verbindungen auf und verhindt so die Bildung von Tau Protein Fasern in den Nervenzellen. Der beste Effekt konnte durch die Gabe von 60mg des Wirkstoffes erzielt werden.
Insgesamt wurde eine um 81 % geringere Verschlechterung der kognitiven Leistungsfähigkeit gegenüber Placebo festgestellt. Größere Phase-III Studien, welche 2009 starten sollen, sind
notwendig um das Resultat zu bestätigen. Wenn die weitere Prüfung des Medikaments reibungslos verläuft, könnte es im Jahr 2012 zugelassen werden .\"
Literatur: Wikipedia\"Alzheimer\"
Die entscheidenden Arzneistoffe scheinen schon für Alzheimer unterwegs zu sein. Letzteres Präparat wird wahrscheinlich 2012 zugelassen. Das sind, so glaube ich schlechte Chancen für Pfizer auf diesem Gebiet, denn dann wären spätestens dann Symptom-Präparate nicht mehr absetzbar.
Hallo Freunde, hier Literatur zum Thema Kupfermangel
dabei hoffe ich, daß der Text sichtbar wird.
nsonsten werde ich noch eine andere Kopie versuchen.


Ich habe Kontakt zur Uni Saarland aufgenommen und teile Euch demnächst weitere Neuigkeiten mit.
Eure Schlüsse könnt Ihr selbst ziehen.
Gruß
Ostdi
dabei hoffe ich, daß der Text sichtbar wird.
nsonsten werde ich noch eine andere Kopie versuchen.
Ich habe Kontakt zur Uni Saarland aufgenommen und teile Euch demnächst weitere Neuigkeiten mit.
Eure Schlüsse könnt Ihr selbst ziehen.
Gruß
Ostdi
Ach, hat leider so nicht geklappt:
neues Angebot:
http://www.uni-protokolle.de/nachrichten/id/28533/
und
http://www.g-o.de/wissen-aktuell-3270-2005-08-03.html
nun trotzdem den Text versucht zu kopieren:
Kupfermangel führt zu Alzheimer
Studien erhärten bisherige These
Das Metall Kupfer spielt möglicherweise eine entscheidende Rolle bei der Entwicklung der Alzheimer-Krankheit. Neue Studien erhärten die These, dass ein Kupfermangel das Entstehen von Plaques-Ablagerungen im Gehirn begünstigt und so die Demenz vorantreibt.
Bei Alzheimer-Patienten fällt der Kupferspiegel im Hirngewebe weitaus niedriger aus als bei gesunden Personen. Wissenschaftler vermuten deshalb: Ist der Kupferspiegel im menschlichen Gehirn zu niedrig, kann APP, das so genannte Amyloid-Vorläuferprotein, das das Gleichgewicht des zellulären Kupferstoffwechsels beeinflusst, keine Bindungen eingehen. APP bildet dann die schädlichen Amyloid-Aß-Proteine, also die Plaques-Ablagerungen, die die Hirnzellen zerstören.
Die Annahme liegt nahe, dass eine Besserung des Gesundheitszustandes durch eine verstärkte Kupfersalzaufnahme erreicht werden kann. Das Kupfer ist zudem bioverfügbar, das heißt, es gelangt ganz einfach über die Nahrung bis in den Hirnstoffwechsel und soll dort zu einer Normalisierung des Kupferspiegels führen.
Den aussichtsreichen Therapieansatz mit Kupfer hat eine Arbeitsgruppe um den Biochemiker Gerd Multhaup von der Freien Universität Berlin gemeinsam mit dem Neurobiologen Thomas Bayer von der Universität des Saarlandes entdeckt. Erste Erfolge können die Forscher jetzt anhand einer Studie belegen, deren Ergebnisse in der September-Ausgabe des "Journal of Alzheimer's Disease" veröffentlicht werden.
Die Alzheimer Krankheit ist durch den Verfall der geistigen Leistungsfähigkeit gekennzeichnet, die im Verlauf zunimmt und zum Totalverlust der Urteilsfähigkeit und der Persönlichkeit führen kann. Ein charakteristisches neuropathologisches Merkmal ist die Entwicklung von so genannten amyloiden Plaques, die aus dem Aß-Peptid aufgebaut sind.
Es gibt vermehrt Hinweise darauf, dass der Stoffwechsel des essentiellen Metallions Kupfer bei der Alzheimer-Krankheit beeinträchtigt ist. Ergebnisse aus in vitro-Studien und aus Studien mit transgenen Mäusen, die das menschliche Amyloid Vorläuferprotein (AßPP) exprimieren, zeigen, dass erhöhte AßPP und Aß-Spiegel zu einer Absenkung des Kupfers in den Zellen führen. Kupfer wird aus den Zellen hinaustransportiert und führt so zu einem Mangel im Gewebe, der in den Zellen eine verminderte Aktivität des Enzyms Superoxid-Dismutase nach sich zieht.
Gerd Multhaup und Thomas Bayer haben im Rahmen einer Studie 32 Patienten mit milder bis moderater Demenz untersucht. Sie haben den Kupfergehalt des Bluts und mit Hilfe des ADAS-cog-Tests die kognitiven Leistungsmerkmale der an Alzheimer Erkrankten analysiert. Eine erste statistische Auswertung hat eine negative Korrelation zwischen Kupfergehalt des Plasmas und kognitiver Leistung ergeben.
Patienten mit niedrigem Kupferspiegel zeigten signifikant höhere ADAS- cog-Werte (mehr Fehler im Test) als Patienten mit durchschnittlichen Kupferwerten. "Das Ergebnis stützt die Hypothese, dass die meisten Alzheimer-Patienten unter Kupfermangel leiden", schlussfolgert Gerd Multhaup und glaubt, dass eine vermehrte Aufnahme von Kupfer über die Nahrung therapeutisch von Nutzen sein könnte.
Ob das zutrifft, wird die derzeit durchgeführte Doppelblind-Studie zeigen, die sich in der klinischen Phase II befindet und an der Universität des Saarlands unter der Leitung von Frank Pajonk und Thomas Bayer in der Klinik für Psychiatrie durchgeführt wird.
(NPO,Freie Universität Berlin,03.08.2005)
Hat geklappt.
Hoffentlich konnte ich damit noch offene Fragen besänftigend beantworten.
Wäre noch folgender Gesichtspunkt bei EVT 101 interessant:
- der Einsatz als Schmerzmittel,
damit habe ich mich aber im Moment noch nicht auseinandergesetzt.
Fakt ist, daß da ein riesiges Potential ist, aber es gibt jede Menge Kandidaten, die den Bereich schon voll abdecken.
Bekanntestes und erfolgreichstes Mittelchen zur Zeit:
Ibuprofen
Adios camerados
Ostdi
neues Angebot:
http://www.uni-protokolle.de/nachrichten/id/28533/
und
http://www.g-o.de/wissen-aktuell-3270-2005-08-03.html
nun trotzdem den Text versucht zu kopieren:
Kupfermangel führt zu Alzheimer
Studien erhärten bisherige These
Das Metall Kupfer spielt möglicherweise eine entscheidende Rolle bei der Entwicklung der Alzheimer-Krankheit. Neue Studien erhärten die These, dass ein Kupfermangel das Entstehen von Plaques-Ablagerungen im Gehirn begünstigt und so die Demenz vorantreibt.
Bei Alzheimer-Patienten fällt der Kupferspiegel im Hirngewebe weitaus niedriger aus als bei gesunden Personen. Wissenschaftler vermuten deshalb: Ist der Kupferspiegel im menschlichen Gehirn zu niedrig, kann APP, das so genannte Amyloid-Vorläuferprotein, das das Gleichgewicht des zellulären Kupferstoffwechsels beeinflusst, keine Bindungen eingehen. APP bildet dann die schädlichen Amyloid-Aß-Proteine, also die Plaques-Ablagerungen, die die Hirnzellen zerstören.
Die Annahme liegt nahe, dass eine Besserung des Gesundheitszustandes durch eine verstärkte Kupfersalzaufnahme erreicht werden kann. Das Kupfer ist zudem bioverfügbar, das heißt, es gelangt ganz einfach über die Nahrung bis in den Hirnstoffwechsel und soll dort zu einer Normalisierung des Kupferspiegels führen.
Den aussichtsreichen Therapieansatz mit Kupfer hat eine Arbeitsgruppe um den Biochemiker Gerd Multhaup von der Freien Universität Berlin gemeinsam mit dem Neurobiologen Thomas Bayer von der Universität des Saarlandes entdeckt. Erste Erfolge können die Forscher jetzt anhand einer Studie belegen, deren Ergebnisse in der September-Ausgabe des "Journal of Alzheimer's Disease" veröffentlicht werden.
Die Alzheimer Krankheit ist durch den Verfall der geistigen Leistungsfähigkeit gekennzeichnet, die im Verlauf zunimmt und zum Totalverlust der Urteilsfähigkeit und der Persönlichkeit führen kann. Ein charakteristisches neuropathologisches Merkmal ist die Entwicklung von so genannten amyloiden Plaques, die aus dem Aß-Peptid aufgebaut sind.
Es gibt vermehrt Hinweise darauf, dass der Stoffwechsel des essentiellen Metallions Kupfer bei der Alzheimer-Krankheit beeinträchtigt ist. Ergebnisse aus in vitro-Studien und aus Studien mit transgenen Mäusen, die das menschliche Amyloid Vorläuferprotein (AßPP) exprimieren, zeigen, dass erhöhte AßPP und Aß-Spiegel zu einer Absenkung des Kupfers in den Zellen führen. Kupfer wird aus den Zellen hinaustransportiert und führt so zu einem Mangel im Gewebe, der in den Zellen eine verminderte Aktivität des Enzyms Superoxid-Dismutase nach sich zieht.
Gerd Multhaup und Thomas Bayer haben im Rahmen einer Studie 32 Patienten mit milder bis moderater Demenz untersucht. Sie haben den Kupfergehalt des Bluts und mit Hilfe des ADAS-cog-Tests die kognitiven Leistungsmerkmale der an Alzheimer Erkrankten analysiert. Eine erste statistische Auswertung hat eine negative Korrelation zwischen Kupfergehalt des Plasmas und kognitiver Leistung ergeben.
Patienten mit niedrigem Kupferspiegel zeigten signifikant höhere ADAS- cog-Werte (mehr Fehler im Test) als Patienten mit durchschnittlichen Kupferwerten. "Das Ergebnis stützt die Hypothese, dass die meisten Alzheimer-Patienten unter Kupfermangel leiden", schlussfolgert Gerd Multhaup und glaubt, dass eine vermehrte Aufnahme von Kupfer über die Nahrung therapeutisch von Nutzen sein könnte.
Ob das zutrifft, wird die derzeit durchgeführte Doppelblind-Studie zeigen, die sich in der klinischen Phase II befindet und an der Universität des Saarlands unter der Leitung von Frank Pajonk und Thomas Bayer in der Klinik für Psychiatrie durchgeführt wird.
(NPO,Freie Universität Berlin,03.08.2005)
Hat geklappt.
Hoffentlich konnte ich damit noch offene Fragen besänftigend beantworten.
Wäre noch folgender Gesichtspunkt bei EVT 101 interessant:
- der Einsatz als Schmerzmittel,
damit habe ich mich aber im Moment noch nicht auseinandergesetzt.
Fakt ist, daß da ein riesiges Potential ist, aber es gibt jede Menge Kandidaten, die den Bereich schon voll abdecken.
Bekanntestes und erfolgreichstes Mittelchen zur Zeit:
Ibuprofen
Adios camerados
Ostdi
Antwort auf Beitrag Nr.: 34.998.082 von Ostdi am 05.09.08 15:47:36Hochinteressant.............

Ich habe an der UNI-Freiburg eine Studie in Auftrag
gegeben betreff Rotweine die sich positiv auf
Herzkranzgefäße sowie Alzheimer auswirken.
Da ich ab dem 13.09.2008 in das Land des BAROLO gehe, werde ich
auch dort versuchen an INFO zu kommen....

Bei positven Ergebnisse werde ich sie selbstverständlich
an " Henne " C Evotec ) weiterleiten!!!!


Prosit auf gute Kurse...
skat


Ich habe an der UNI-Freiburg eine Studie in Auftrag
gegeben betreff Rotweine die sich positiv auf
Herzkranzgefäße sowie Alzheimer auswirken.
Da ich ab dem 13.09.2008 in das Land des BAROLO gehe, werde ich
auch dort versuchen an INFO zu kommen....


Bei positven Ergebnisse werde ich sie selbstverständlich
an " Henne " C Evotec ) weiterleiten!!!!



Prosit auf gute Kurse...
skat
Antwort auf Beitrag Nr.: 35.058.988 von skat am 11.09.08 09:31:27Superidee
Antwort auf Beitrag Nr.: 35.058.563 von Ostdi am 11.09.08 08:39:24Hi Ostdi,
das mit dem Kupfer finde ich, wie schon erwähnt, nicht zuletzt wegen meines Engagements bei der Norddeutschen Affinerie, höchst interessant.
Ich zitiere einen Satz aus deinem Posting, an dem sich meine Frage aufhängt: "Es gibt vermehrt Hinweise darauf, dass der Stoffwechsel des essentiellen Metallions Kupfer bei der Alzheimer-Krankheit beeinträchtigt ist."
Ist der Kupfermangel nun ursächlich für die Alzheimersche Erkrankung oder ist er eine Folge?
Wäre er ursächlich, müssten alle ab einem gewissem Alter Kupfer futtern (für meine Aktien würde ich diesen Fall bevorzugen), wird der Kupermangel aber erst durch die Krankheit hervorgerufen, müssten nur die Alzheimer-Patienten damit gefüttert werden. Die im Saarland werden es schon herausfinden.
Skats Barolo-Ansatz ist aber auch nicht schlecht, würde mich bei ihm glatt als Doppelblind-Testperson zur Verfügung stellen. orfmen macht auch mit und kommt in die Plazebo-Gruppe.
Gruß spero
das mit dem Kupfer finde ich, wie schon erwähnt, nicht zuletzt wegen meines Engagements bei der Norddeutschen Affinerie, höchst interessant.
Ich zitiere einen Satz aus deinem Posting, an dem sich meine Frage aufhängt: "Es gibt vermehrt Hinweise darauf, dass der Stoffwechsel des essentiellen Metallions Kupfer bei der Alzheimer-Krankheit beeinträchtigt ist."
Ist der Kupfermangel nun ursächlich für die Alzheimersche Erkrankung oder ist er eine Folge?
Wäre er ursächlich, müssten alle ab einem gewissem Alter Kupfer futtern (für meine Aktien würde ich diesen Fall bevorzugen), wird der Kupermangel aber erst durch die Krankheit hervorgerufen, müssten nur die Alzheimer-Patienten damit gefüttert werden. Die im Saarland werden es schon herausfinden.
Skats Barolo-Ansatz ist aber auch nicht schlecht, würde mich bei ihm glatt als Doppelblind-Testperson zur Verfügung stellen. orfmen macht auch mit und kommt in die Plazebo-Gruppe.
Gruß spero
Antwort auf Beitrag Nr.: 35.062.577 von spero am 11.09.08 15:24:09Ich weiß, ich weiß, in diesem Thread soll nicht gescherzt werden. Hier geht es super korrekt zu. Deshalb muss es auch Placebo-Gruppe heißen.
Und das mir!
Und das mir!
Antwort auf Beitrag Nr.: 35.062.577 von spero am 11.09.08 15:24:09@spero
Ist beides richtig!
APP beeinflußt das Gleichgewicht des zellulären Stoffwechsels mit Kupferionen. Das passiert aber erst in dem Moment, wenn der Kupferspiegel im Hirngewebe weitaus niedriger ist als bei gesunden Personen. Anders ausgedrückt:
Als erstes fällt der Kupferspiegel im Hirngewebe, Ursache ist das Altern z.B., die Kupferzufuhr ist nicht mehr so intakt, ...
Zweitens APP (Amyloid-Vorläuferprotein fünktioniert dadurch nicht mehr, "spielt verrückt" und beeinflußt den Kupferstoffwechsel im Neuron im Gehirn negativ,
Da zu wenig Kupferionen vorhanden sind, kommt es zur Veränderung bei der normalen Aufspaltung von APP. Unter normalen Umständen wird APP durch alpha-Sekretasen in wasserlösliche Proteine gespalten, die neuroprotektive Eigenschaften besitzen (Lerneigenschaften z.B.).
Durch den herabgesetzten Kupferspiegel reagiert das APP plötzlich mit anderen Enzymen (abnorm), ß-Sekretase und Gamma-Sekretase zerschneiden APP völlig anders, am Ende entsteht ein neurotoxisches Bruchstück, (nicht wasserlöslich!!!)
ß-Amyloid genannt. Diese Bruchstücke (Peptide) bilden Plaques im Gehirn, die zusammen mit den Neurofibrillen, die sich in den Neuronen bilden und zum Absterben der Synapsen führen, das pathologische Kennzeichen der Krankheit darstellen.
Ich hoffe, daß Du es jetzt besser verstehst.
Ist beides richtig!
APP beeinflußt das Gleichgewicht des zellulären Stoffwechsels mit Kupferionen. Das passiert aber erst in dem Moment, wenn der Kupferspiegel im Hirngewebe weitaus niedriger ist als bei gesunden Personen. Anders ausgedrückt:
Als erstes fällt der Kupferspiegel im Hirngewebe, Ursache ist das Altern z.B., die Kupferzufuhr ist nicht mehr so intakt, ...
Zweitens APP (Amyloid-Vorläuferprotein fünktioniert dadurch nicht mehr, "spielt verrückt" und beeinflußt den Kupferstoffwechsel im Neuron im Gehirn negativ,
Da zu wenig Kupferionen vorhanden sind, kommt es zur Veränderung bei der normalen Aufspaltung von APP. Unter normalen Umständen wird APP durch alpha-Sekretasen in wasserlösliche Proteine gespalten, die neuroprotektive Eigenschaften besitzen (Lerneigenschaften z.B.).
Durch den herabgesetzten Kupferspiegel reagiert das APP plötzlich mit anderen Enzymen (abnorm), ß-Sekretase und Gamma-Sekretase zerschneiden APP völlig anders, am Ende entsteht ein neurotoxisches Bruchstück, (nicht wasserlöslich!!!)
ß-Amyloid genannt. Diese Bruchstücke (Peptide) bilden Plaques im Gehirn, die zusammen mit den Neurofibrillen, die sich in den Neuronen bilden und zum Absterben der Synapsen führen, das pathologische Kennzeichen der Krankheit darstellen.
Ich hoffe, daß Du es jetzt besser verstehst.
Antwort auf Beitrag Nr.: 35.062.577 von spero am 11.09.08 15:24:09Der von Dir hervorgehobene Satz ist übrigens nicht von mir, sondern aus diesem Text.
Was meinst Du, wieviel Leute Kupfermangel haben,
Kupfermangel ist z.B. bei Bluthochdruck, Herzrhytmusstörungen, Pigmentstörungen, Blutanämie, Osteoporose, natürlich Störungen des Zentralen Nervensystems, und, und, und...
Hier eine Seite zum Nachlesen, hochinteressant:
http://www.trace-elements.de/Service/Zink_und_Kupfer/Zink-un…
Übrigens, wie individuell auch Alzheimer ausgelöst werden kann, erfährst Du gleich in den ersten Zeilen dieser Seite.
Gut ist auch diese Seite:
http://www.novamex.de/nnb/vitaminspur/Spurenelemente/spurkup…
Der Weinproband wäre auch für mich interessant.



Beste Grüße an alle Interessenten
Ostdi
Was meinst Du, wieviel Leute Kupfermangel haben,
Kupfermangel ist z.B. bei Bluthochdruck, Herzrhytmusstörungen, Pigmentstörungen, Blutanämie, Osteoporose, natürlich Störungen des Zentralen Nervensystems, und, und, und...
Hier eine Seite zum Nachlesen, hochinteressant:
http://www.trace-elements.de/Service/Zink_und_Kupfer/Zink-un…
Übrigens, wie individuell auch Alzheimer ausgelöst werden kann, erfährst Du gleich in den ersten Zeilen dieser Seite.
Gut ist auch diese Seite:
http://www.novamex.de/nnb/vitaminspur/Spurenelemente/spurkup…
Der Weinproband wäre auch für mich interessant.



Beste Grüße an alle Interessenten
Ostdi
Antwort auf Beitrag Nr.: 35.065.211 von Ostdi am 11.09.08 18:52:10Das war es wohl mit dem Rebound!
Wochenschlusskurs unter 1,35 EURO und die Party ist gelaufen
Wochenschlusskurs unter 1,35 EURO und die Party ist gelaufen

Antwort auf Beitrag Nr.: 35.065.335 von altf4 am 11.09.08 19:03:46Kannst Du das nicht woanders ´reinschreiben?!
Liebe Freunde,
nun meine vorrübergehend abschließende Betrachtung betreffs EVT101:
Wie ich Euch versprochen hatte, wollte ich bei den Aktuellen Phase II Ergebnissen betreffs Alzheimer / Parkinson dran bleiben.
Meine Recherchen haben nun folgende Ergebnisse gebracht, die man mit einer schlechten und einer guten Nachricht zusammenfassen kann.
Ich versuche den Kern zu treffen unter dem Vorbehalt, daß ich gegenwärtig in argen Zeitproblemen stecke.
1. Ich bin trotzdem sehr traurig darüber, daß die relativ einfache Verhinderung des Ausbruchs der neurodegenerativen Arkrankung Morbus Alzheimer durch zusätzliche Kupfer-Zink-Gaben nicht möglich ist, und daß alle anderen, an der Substanz der Krankheit ansetzenden Behandlungsansätze gescheitert sind.
Ihr erinnert Euch:
\"Bei Alzheimer-Patienten fällt der Kupferspiegel im Hirngewebe weitaus niedriger aus als bei gesunden Personen. Wissenschaftler vermuten deshalb: Ist der Kupferspiegel im menschlichen Gehirn zu niedrig, kann APP, das so genannte Amyloid-Vorläuferprotein, das das Gleichgewicht des zellulären Kupferstoffwechsels beeinflusst, keine Bindungen eingehen. APP bildet dann die schädlichen Amyloid-Aß-Proteine, also die Plaques-Ablagerungen, die die Hirnzellen zerstören.
Die Annahme liegt nahe, dass eine Besserung des Gesundheitszustandes durch eine verstärkte Kupfersalzaufnahme erreicht werden kann. Das Kupfer ist zudem bioverfügbar, das heißt, es gelangt ganz einfach über die Nahrung bis in den Hirnstoffwechsel und soll dort zu einer Normalisierung des Kupferspiegels führen.
Die dann durchgeführte Doppelblind-Studie zeigen, die sich in der klinischen Phase II befand und an der Universität des Saarlands unter der Leitung von Frank Pajonk und Thomas Bayer in der Klinik für Psychiatrie durchgeführt wurde, erfüllte in keiner Weise die verfolgten Ziele direkt im menschlichen Gehirn im Gegensatz zu den zuvor erbrachten Ergebnissen bei den gleichen Tests an Mäusen.
Es wird also weitergehen mit dem lngsamen Dahinsiechen unter Verlust seines Verstandes bis hin zum Tod, dem Traurigsten auf Erden, zumindest für die Masse an Patienten, die nicht über das nötige Kleingeld verfügen...
Trotzdem will man an der Freien Universität weitere Ansätze prüfen, denn die oben beschriebene Lage des Kupfermangels ist nachgewiesen. Es wird aber neben den vielen anderen Forschungsansätzen aber nochmals schätzungsweise ca. 10 Jahre dauern, bis man die Ursachen dieser heimtückischen Krankheit vielleicht bekämpfen kann.
Dennoch, eine Geschichte läuft tatsächlich erfolgreich ab:
\"Ermutigende Resultate brachte eine 50-wöchige Phase-II Studie mit dem Arzneistoff Methylblau (Rember) an 321 Patienten mit leicht bis moderat fortgeschrittener Erkrankung. Der Wirkstoff löst
Tau Protein Verbindungen auf und verhindert so die Bildung von Tau Protein Fasern in den Nervenzellen. Der beste Effekt konnte durch die Gabe von 60mg des Wirkstoffes erzielt werden.
Insgesamt wurde eine um 81 % geringere Verschlechterung der kognitiven Leistungsfähigkeit gegenüber Placebo festgestellt. Größere Phase-III Studien, welche 2009 starten sollen, sind
notwendig um das Resultat zu bestätigen. Wenn die weitere Prüfung des Medikaments reibungslos verläuft, könnte es im Jahr 2012 zugelassen werden .\\\"
Der Arzneistoff wird in Form einer Pille namens \"Rember\" getestet.
Methylenblau als Wirkstoff findet als Antiseptikum bereits bei z.B. Malaria sowie anderer Infektionskrankheiten und als Antirheumatikum Verwendung. Das Ziel ist die Aufhaltung des Krankheitsfortschreitens, was zunächst bewiesen ist.
Vielleicht macht unter diesen Umständen eine symptomatische Behandlung als zusätzliche Maßnahme Sinn...
Das wäre zumindest ein Hoffnungsschimmer für EVT-101.
\"In verschiedenen Untersuchungen konnte gezeigt werden, dass das cholinerge Defizit nicht alleinverantwortlich für die Demenz-Pathologie ist, sondern Störungen im glutamatergen
Neurotransmitter-System entscheidend an der Pathologie der Demenzen beteiligt sind.
Deshalb ist die Modulation der Glutamat-Wirkung im Gehirn, die vorwiegend über NMDA-Rezeptoren erfolgt, ein neuer Behandlungsansatz.
Die Memantin-Therapie führt bei mittelschwerer bis schwerer Alzheimersymptomatik bei den drei Kerndomänen (Kognition, Alltagskompetenz, klinischer Gesamteindruck) nach sechs Monaten zu
signifikanten, insgesamt jedoch geringen Besserungen bzw. Verzögerungen der Symptomatik verglichen mit einer Placebobehandlung. Weiterhin kann die Behandlung mit diesem
Antidementivum laut einer Auswertung von zwei randomisierten Studien unter Beteiligung des Herstellers Merz dazu beitragen, demenzbedingte Verhaltensstörungen zu vermindern .\\\"
Bei den fortgeschrittenen Demenzfällen wird symptomatische Behandlung über die NMDA-Rezeptoren trotzdem Sinn machen.
nun meine vorrübergehend abschließende Betrachtung betreffs EVT101:
Wie ich Euch versprochen hatte, wollte ich bei den Aktuellen Phase II Ergebnissen betreffs Alzheimer / Parkinson dran bleiben.
Meine Recherchen haben nun folgende Ergebnisse gebracht, die man mit einer schlechten und einer guten Nachricht zusammenfassen kann.
Ich versuche den Kern zu treffen unter dem Vorbehalt, daß ich gegenwärtig in argen Zeitproblemen stecke.
1. Ich bin trotzdem sehr traurig darüber, daß die relativ einfache Verhinderung des Ausbruchs der neurodegenerativen Arkrankung Morbus Alzheimer durch zusätzliche Kupfer-Zink-Gaben nicht möglich ist, und daß alle anderen, an der Substanz der Krankheit ansetzenden Behandlungsansätze gescheitert sind.
Ihr erinnert Euch:
\"Bei Alzheimer-Patienten fällt der Kupferspiegel im Hirngewebe weitaus niedriger aus als bei gesunden Personen. Wissenschaftler vermuten deshalb: Ist der Kupferspiegel im menschlichen Gehirn zu niedrig, kann APP, das so genannte Amyloid-Vorläuferprotein, das das Gleichgewicht des zellulären Kupferstoffwechsels beeinflusst, keine Bindungen eingehen. APP bildet dann die schädlichen Amyloid-Aß-Proteine, also die Plaques-Ablagerungen, die die Hirnzellen zerstören.
Die Annahme liegt nahe, dass eine Besserung des Gesundheitszustandes durch eine verstärkte Kupfersalzaufnahme erreicht werden kann. Das Kupfer ist zudem bioverfügbar, das heißt, es gelangt ganz einfach über die Nahrung bis in den Hirnstoffwechsel und soll dort zu einer Normalisierung des Kupferspiegels führen.
Die dann durchgeführte Doppelblind-Studie zeigen, die sich in der klinischen Phase II befand und an der Universität des Saarlands unter der Leitung von Frank Pajonk und Thomas Bayer in der Klinik für Psychiatrie durchgeführt wurde, erfüllte in keiner Weise die verfolgten Ziele direkt im menschlichen Gehirn im Gegensatz zu den zuvor erbrachten Ergebnissen bei den gleichen Tests an Mäusen.
Es wird also weitergehen mit dem lngsamen Dahinsiechen unter Verlust seines Verstandes bis hin zum Tod, dem Traurigsten auf Erden, zumindest für die Masse an Patienten, die nicht über das nötige Kleingeld verfügen...
Trotzdem will man an der Freien Universität weitere Ansätze prüfen, denn die oben beschriebene Lage des Kupfermangels ist nachgewiesen. Es wird aber neben den vielen anderen Forschungsansätzen aber nochmals schätzungsweise ca. 10 Jahre dauern, bis man die Ursachen dieser heimtückischen Krankheit vielleicht bekämpfen kann.
Dennoch, eine Geschichte läuft tatsächlich erfolgreich ab:
\"Ermutigende Resultate brachte eine 50-wöchige Phase-II Studie mit dem Arzneistoff Methylblau (Rember) an 321 Patienten mit leicht bis moderat fortgeschrittener Erkrankung. Der Wirkstoff löst
Tau Protein Verbindungen auf und verhindert so die Bildung von Tau Protein Fasern in den Nervenzellen. Der beste Effekt konnte durch die Gabe von 60mg des Wirkstoffes erzielt werden.
Insgesamt wurde eine um 81 % geringere Verschlechterung der kognitiven Leistungsfähigkeit gegenüber Placebo festgestellt. Größere Phase-III Studien, welche 2009 starten sollen, sind
notwendig um das Resultat zu bestätigen. Wenn die weitere Prüfung des Medikaments reibungslos verläuft, könnte es im Jahr 2012 zugelassen werden .\\\"
Der Arzneistoff wird in Form einer Pille namens \"Rember\" getestet.
Methylenblau als Wirkstoff findet als Antiseptikum bereits bei z.B. Malaria sowie anderer Infektionskrankheiten und als Antirheumatikum Verwendung. Das Ziel ist die Aufhaltung des Krankheitsfortschreitens, was zunächst bewiesen ist.
Vielleicht macht unter diesen Umständen eine symptomatische Behandlung als zusätzliche Maßnahme Sinn...
Das wäre zumindest ein Hoffnungsschimmer für EVT-101.
\"In verschiedenen Untersuchungen konnte gezeigt werden, dass das cholinerge Defizit nicht alleinverantwortlich für die Demenz-Pathologie ist, sondern Störungen im glutamatergen
Neurotransmitter-System entscheidend an der Pathologie der Demenzen beteiligt sind.
Deshalb ist die Modulation der Glutamat-Wirkung im Gehirn, die vorwiegend über NMDA-Rezeptoren erfolgt, ein neuer Behandlungsansatz.
Die Memantin-Therapie führt bei mittelschwerer bis schwerer Alzheimersymptomatik bei den drei Kerndomänen (Kognition, Alltagskompetenz, klinischer Gesamteindruck) nach sechs Monaten zu
signifikanten, insgesamt jedoch geringen Besserungen bzw. Verzögerungen der Symptomatik verglichen mit einer Placebobehandlung. Weiterhin kann die Behandlung mit diesem
Antidementivum laut einer Auswertung von zwei randomisierten Studien unter Beteiligung des Herstellers Merz dazu beitragen, demenzbedingte Verhaltensstörungen zu vermindern .\\\"
Bei den fortgeschrittenen Demenzfällen wird symptomatische Behandlung über die NMDA-Rezeptoren trotzdem Sinn machen.
Antwort auf Beitrag Nr.: 35.214.500 von Ostdi am 22.09.08 11:14:17Evotec berichtet starkes drittes Quartal und hebt Prognose für das Geschäftsjahr 2008 an
Corporate news- Mitteilung verarbeitet und übermittelt durch Hugin. Für den Inhalt der Mitteilung ist der Emittent verantwortlich. -------------------------------------------------------------------- -- --------------
Hamburg, Deutschland - Evotec AG (News/Aktienkurs) (Deutsche Börse: EVT; NASDAQ: EVTC) berichtet heute über die Finanzergebnisse des dritten Quartals und der ersten neun Monate 2008.
Infolge eines starken dritten Quartals betrug Evotecs Umsatz in den ersten neun Monaten 2008 25,2 Mio. Euro und lag damit 9% höher als im Vorjahr (2007: 23,2 Mio. Euro). Bei konstanten 2007 Wechselkursen wäre der Umsatz im Vergleich zum Vorjahr um 18% auf 27,3 Mio. Euro gewachsen. Der Umsatz im dritten Quartal stieg 44% auf 10,7 Mio. Euro (2007: 7,4 Mio. Euro). Der Anstieg resultiert im Wesentlichen aus einer Meilensteinzahlung von Boehringer Ingelheim im dritten Quartal.
Der operative Verlust für die ersten neun Monate 2008 betrug 35,2 Mio. Euro (2007: 36,7 Mio. Euro). Der Rückgang gegenüber Vorjahr, trotz höherer diesjähriger Investitionen in Forschung und Entwicklung, ist auf den Umsatzanstieg sowie den Rückgang der Herstellkosten und der Abschreibungen auf immaterielle Vermögenswerte zurückzuführen.
Der Jahresfehlbetrag betrug 29,0 Mio. Euro (2007: 33,2 Mio. Euro). Der Rückgang des Jahresfehlbetrages resultiert vorwiegend aus dem Ertrag aus Finanzanlagen aus der Bewertung von Direvo-Wandelschuldver-schreibungen in Zusammenhang mit dem Verkauf von Direvo Biotech an Bayer HealthCare.
Der Bestand an liquiden Mitteln einschließlich "Auction Rate Securities" betrug Ende September 2008 97,6 Mio. Euro (Ende Dezember 2007: 93,7 Mio. Euro).
Wesentliche Ereignisse im Berichtszeitraum:
* Am 1. August 2008 haben wir bekannt gegeben, dass Pfizer eine klinische Phase-I-Studie mit einem niedermolekularen VR1 (Vanilloid-Rezeptor-1)-Antagonisten zur Behandlung von Schmerzen im Rahmen der Kooperation mit Evotec begonnen hat. Am 9. Oktober 2008 (nach Ende der Berichtsperiode) berichteten wir, dass wir mit dem Start der klinischen Phase-I-Studien mit unserem niedermolekularen P2X7-Rezeptor-Antagonisten für die Behandlung von Rheumatoider Arthritis sowie anderen Entzündungskrankheiten auch einen zweiten wichtigen klinischen Meilenstein in diesem Jahr in unserer amerikanischen Niederlassung erreicht haben. * Am 2. September 2008 berichteten wir das Erreichen des dritten Meilensteins in unserer Kooperation mit Boehringer Ingelheim. Am 30. Oktober 2008 (nach Ende der Berichtsperiode), kündigten wir an, dass zwei weitere Forschungsmeilensteine in dieser Kooperation erzielt worden sind. Damit bringen uns Meilensteine aus dieser Kooperation 2008 insgesamt Zahlungen in Höhe von 8,5 Mio. Euro. * Am 11. September 2008 gaben wir den Start einer Phase-II-Wirksamkeitsstudie mit EVT 302 bekannt. Diese Studie misst die Erfolgsrate bei Patienten, die mit dem Rauchen aufhören wollen, und soll den entscheidenden Wirksamkeitsnachweis für unseren Wirkstoff bei der Raucherentwöhnung erbringen. * Am 16. September 2008 meldeten wir, dass Evotec infolge des Verkaufs von Direvo Biotech an Bayer HealthCare etwa 5 Mio. Euro über den Verkauf von Direvo Wandelschuldverschreibungen einnehmen würde. Diese Wandelschuldverschreibungen hatten wir im Mai 2007 als Vergütungsbestandteil für den Verkauf unserer Beteilung an Direvo erhalten.
"Wir sind sehr zufrieden mit dem, was wir in diesem Quartal erreicht haben. Wir haben mit unserem klinischen und präklinischen ZNS-Portfolio weiter gute Fortschritte gemacht. Nachdem wir zwei neue Phase-I-Programme gestartet haben, verfügen wir aktuell über fünf Substanzen in der klinischen Entwicklung. Mit EVT 302 haben wir mit den entscheidenden Phase-II-Studien zum Nachweis der Wirksamkeit der Substanz bei der Raucherentwöhnung begonnen und bereiten jetzt für Anfang 2009 den Beginn entsprechender Phase-II-Wirksamkeitsstudien für EVT 101 im Bereich neuropathischer Schmerzen und in anderen Indikationen vor. Die Gespräche über die Verpartnerung unseres am weitesten fortgeschrittenen Wirkstoffkandidaten EVT 201 zur Behandlung von Schlafstörungen wurden im abgelaufenen Quartal fortgesetzt und fokussiert. Wir haben große Hoffnung, dass daraus Anfang 2009 ein Vertragsabschluss hervorgehen kann. Wir glauben an die Attraktivität unseres Wirkstoffkandidaten, der viele der Probleme herkömmlicher Schlafmittel adressiert, wenn auch das Marktumfeld für die Verpartnerung eines jeden Schlafmittels derzeit sicher schwierig ist. Auch für andere klinische und präklinische Programme sehen wir ein wachsendes Interesse seitens potenzieller Partner," sagte Jörn Aldag, Vorstandsvorsitzender der Evotec AG. "Wir sind zudem stolz auf ein außerordentlich starkes drittes Quartal 2008. Wir haben in unserem Kooperationsgeschäft zahlreiche Meilensteine erreicht, die uns zusammen mit dem Verkauf der Direvo-Wandelschuldverschreibungen und einem starken US-Dollar-Wechselkurs zu einer Anhebung unserer Finanzprognose für das laufende Jahr veranlasst haben. Trotz weltweiter Unsicherheit im Finanzsektor ist Evotec solide finanziert mit einem Liquiditätspolster von 98 Mio. Euro, das es uns erlauben wird, unsere Programme auch in diesem schwierigen Marktumfeld in der Entwicklung weiter voranzubringen."
Finanzprognose 2008 Die starke Entwicklung des Kooperationsgeschäfts sowie der Zufluss an liquiden Mitteln aus dem Verkauf von Finanzanlagen im Zusammenhang mit dem Verkauf von Direvo Biotech an Bayer HealthCare veranlassten uns zu einer Anhebung unserer Finanzziele für das Jahr 2008. Aufgrund höher als erwarteter Meilensteinzahlungen aus der Kooperation mit Boehringer Ingelheim und einer insgesamt soliden Entwicklung unseres Kooperationsgeschäfts erwarten wir nun einen Umsatz für das Geschäftsjahr 2008 in der Größenordnung von 38 bis 40 Mio. Euro (zuvor: 34 bis 36 Mio. Euro). Wie erwartet, werden die Forschungs- und Entwicklungsaufwendungen aufgrund des Fortschritts unserer klinischen Pipeline sowie der Einbeziehung von Renovis höher liegen als im Jahr 2007. Aufgrund reduzierter Aufwendungen für frühe Forschungsprojekte, der Verschiebung einer klinischen Meilensteinzahlung an Roche auf Anfang 2009 sowie allgemeiner Kosteneinsparung erwarten wir jedoch, dass die F+E-Aufwendungen im Geschäftsjahr 2008 niedriger als ursprünglich erwartet ausfallen und im Bereich von 40 bis 45 Mio. Euro liegen werden (zuvor: 46 bis 51 Mio. Euro). Auf der Basis und ohne Berücksichtigung von nicht liquiditätswirksamen Wertberichtigungen in beiden Jahren würde sich das operative Ergebnis gegenüber 2007 verbessern. Infolge der oben erwähnten Ereignisse und einem günstigen US-Dollar-Wechselkurs haben wir unsere Liquiditätsprognose inkl. Wertpapiere und "Auction Rate Securities" auf 90 bis 95 Mio. Euro zum Jahresende (Basis: Wechselkurse vom 30. September 2008) erhöht. Unsere im Halbjahresbericht 2008 veröffentlichte Prognose für die Liquidität zum Jahresende betrug auf Basis konstanter Wechselkurse über 80 Mio. Euro. Unter der Annahme, dass sich das Portfolio des Unternehmens wie geplant weiterentwickelt und selbst wenn keine wichtigen Auslizenzierungen abgeschlossen werden, sollten die liquiden Mittel ausreichen, um Evotecs Entwicklungsprogramme bis Ende 2010 zu finanzieren.
Alle in dieser Pressemitteilung ausgewiesenen Ergebnisse und Erläuterungen für das Jahr 2008 werden mit den fortgeführten Geschäftsbereichen im Jahr 2007 verglichen. Am 30. November 2007 hat Evotec einen größeren Geschäftsbereich, die chemische Entwicklungssparte, an die US-Firma Aptuit verkauft. Ab dem 1. Dezember 2007 wurde dieses Geschäft nicht mehr im Abschluss der Evotec-Gruppe konsolidiert. Erträge und Aufwendungen für dieses Geschäft wurden in der Gewinn- und Verlust-Rechnung rückwirkend als aufzugebende Geschäftsbereiche ausgewiesen. Darüber hinaus hat Evotec am 2. Mai 2008 die Akquisition von Renovis, Inc. abgeschlossen. Die operativen Ergebnisse von Renovis sind daher für den Zeitraum vom 2. Mai 2008 bis 30. September 2008 in den konsolidierten Zwischen-Gewinn- und Verlustrechnungen für die ersten neun Monate 2008 berücksichtigt sowie das Vermögen und die Verbindlichkeiten von Renovis per 30. September 2008 in der konsolidierten Zwischenbilanz enthalten. Daher sind die Ergebnisse der Jahre 2007 und 2008 nicht vollständig vergleichbar.
Telefonkonferenz Evotec wird heute um 14.00 Uhr deutscher Zeit eine Telefonkonferenz in englischer Sprache durchführen. Jörn Aldag, Vorstandsvorsitzender, Dr. Klaus Maleck, Finanzvorstand, und Dr. John Kemp, Chief Research&Development Officer, werden Ihnen die wesentlichen Ergebnisse und Schwerpunkte aus dem Berichtszeitraum näher erläutern.
Details der Telefonkonferenz: Datum: Freitag, 14. November 2008 Uhrzeit: 14.00 Uhr (deutsche Zeit)
Einwahlnummern: Europa: +49.(0)69.5007 1308 (Deutschland) +44.(0)20.7806 1955 (UK) USA: +1.718.354 1389 Passcode: 4668760 Webcast: www.evotec.com
Eine Aufnahme der Telefonkonferenz wird für 48 Stunden unter den Telefonnummern +49.(0)69.22222 0418 (Deutschland), +44.(0)20.7806 1970 (UK) und +1.718.354 1112 (USA), Passcode: 4668760#, verfügbar sein. Zusätzlich wird der Webcast auf unserer Website unter: www.evotec.com - Investors - Finanzberichte archiviert.
Kontakt: Anne Hennecke, Senior Vice President, Investor Relations&Corporate Communications, Evotec AG, Tel.: +49.(0)40.56081-286, anne.hennecke@evotec.com
Zukunftsbezogene Aussagen Diese Mitteilung enthält bestimmte vorausschauende Angaben, die Risiken und Unsicherheiten beinhalten. Derartige vorausschauende Aussagen beinhalten u. a., aber nicht ausschließlich, Aussagen über unsere Erwartungen und Vorstellungen hinsichtlich unserer regulatorischen, klinischen oder geschäftlichen Strategie, des Fortschreitens unserer klinischen Entwicklungsprogramme und der Zeitvorstellungen bis zum Vorliegen der Ergebnisse unserer klinischen Studien, hinsichtlich strategischer Kooperationen sowie Pläne, Ziele und Strategien des Managements. Diese Stellungnahmen stellen weder Versprechen noch Garantien dar, sondern sind abhängig von zahlreichen Risiken und Unsicherheiten, von denen sich viele unserer Kontrolle entziehen, und die dazu führen können, dass die tatsächlichen Ergebnisse erheblich von denen abweichen, die in diesen zukunftsbezogenen Aussagen in Erwägung gezogen werden. Diese Risiken und Unsicherheiten betreffen u. a.: Das Risiko, dass Produktkandidaten in klinischen Studien versagen oder nicht erfolgreich vermarktet bzw. hergestellt werden können; Risiken hinsichtlich unserer Fähigkeiten, die Entwicklung der Produktkandidaten, die sich in unserer Pipeline bzw. in klinischen Studien befinden, voranzutreiben; Erfolglosigkeit bei der Identifizierung, Entwicklung und erfolgreichen Kommerzialisierung neuer Produkte und Technologien; größerer Erfolg von Konkurrenzprodukten; Erfolglosigkeit bei dem Bemühen, potenzielle Partner für unsere Technologien und Produkte zu interessieren; Unvermögen, kommerziellen Erfolg für unsere Produkte und Technologien zu erreichen; Erfolglosigkeit beim Schutz unseres geistigen Eigentums sowie die Kosten, unsere Schutzrechte durchzusetzen oder zu verteidigen; Erfolglosigkeit bei der Einhaltung von gesetzlichen Vorschriften, einschließlich Anforderungen der FDA, hinsichtlich unserer Produkte und Produktkandidaten; das Risiko, dass die FDA die Ergebnisse unserer Studien anders interpretiert als wir; das Risiko, dass unsere klinischen Studien nicht zu marktfähigen Produkten führen; das Risiko, dass es uns nicht gelingt, die Zulassung unserer Wirkstoffkandidaten zu erlangen oder ihre Vermarktung zu erreichen; sowie das Risiko neuer, veränderter und kompetitiver Technologien und Vorschriften, sowohl in den USA als auch weltweit.
Die vorstehend aufgeführte Liste von Risiken erhebt keinen Anspruch auf Vollständigkeit. Im Jahresbericht, den Evotec bei der Securities and Exchange Commission eingereicht hat (Form 20-F), sowie anderen bei der Securities and Exchange Commission eingereichten bzw. hinterlegten Dokumenten werden zusätzliche Faktoren aufgeführt, die unsere Geschäftstätigkeit und finanzielle Leistungsfähigkeit beeinflussen können. Wir übernehmen ausdrücklich keine Verpflichtung, vorausschauende Aussagen hinsichtlich geänderter Erwartungen der Parteien oder hinsichtlich neuer Ereignisse, Bedingungen oder Umstände, auf denen diese Aussagen beruhen, öffentlich zu aktualisieren oder zu revidieren.
Eckdaten der konsolidierten Zwischen-Gewinn- und Verlustrechnungen Evotec AG und Tochtergesellschaften
+------------------------------------------------------------------- ----------- ----------
Corporate news- Mitteilung verarbeitet und übermittelt durch Hugin. Für den Inhalt der Mitteilung ist der Emittent verantwortlich. -------------------------------------------------------------------- -- --------------
Hamburg, Deutschland - Evotec AG (News/Aktienkurs) (Deutsche Börse: EVT; NASDAQ: EVTC) berichtet heute über die Finanzergebnisse des dritten Quartals und der ersten neun Monate 2008.
Infolge eines starken dritten Quartals betrug Evotecs Umsatz in den ersten neun Monaten 2008 25,2 Mio. Euro und lag damit 9% höher als im Vorjahr (2007: 23,2 Mio. Euro). Bei konstanten 2007 Wechselkursen wäre der Umsatz im Vergleich zum Vorjahr um 18% auf 27,3 Mio. Euro gewachsen. Der Umsatz im dritten Quartal stieg 44% auf 10,7 Mio. Euro (2007: 7,4 Mio. Euro). Der Anstieg resultiert im Wesentlichen aus einer Meilensteinzahlung von Boehringer Ingelheim im dritten Quartal.
Der operative Verlust für die ersten neun Monate 2008 betrug 35,2 Mio. Euro (2007: 36,7 Mio. Euro). Der Rückgang gegenüber Vorjahr, trotz höherer diesjähriger Investitionen in Forschung und Entwicklung, ist auf den Umsatzanstieg sowie den Rückgang der Herstellkosten und der Abschreibungen auf immaterielle Vermögenswerte zurückzuführen.
Der Jahresfehlbetrag betrug 29,0 Mio. Euro (2007: 33,2 Mio. Euro). Der Rückgang des Jahresfehlbetrages resultiert vorwiegend aus dem Ertrag aus Finanzanlagen aus der Bewertung von Direvo-Wandelschuldver-schreibungen in Zusammenhang mit dem Verkauf von Direvo Biotech an Bayer HealthCare.
Der Bestand an liquiden Mitteln einschließlich "Auction Rate Securities" betrug Ende September 2008 97,6 Mio. Euro (Ende Dezember 2007: 93,7 Mio. Euro).
Wesentliche Ereignisse im Berichtszeitraum:
* Am 1. August 2008 haben wir bekannt gegeben, dass Pfizer eine klinische Phase-I-Studie mit einem niedermolekularen VR1 (Vanilloid-Rezeptor-1)-Antagonisten zur Behandlung von Schmerzen im Rahmen der Kooperation mit Evotec begonnen hat. Am 9. Oktober 2008 (nach Ende der Berichtsperiode) berichteten wir, dass wir mit dem Start der klinischen Phase-I-Studien mit unserem niedermolekularen P2X7-Rezeptor-Antagonisten für die Behandlung von Rheumatoider Arthritis sowie anderen Entzündungskrankheiten auch einen zweiten wichtigen klinischen Meilenstein in diesem Jahr in unserer amerikanischen Niederlassung erreicht haben. * Am 2. September 2008 berichteten wir das Erreichen des dritten Meilensteins in unserer Kooperation mit Boehringer Ingelheim. Am 30. Oktober 2008 (nach Ende der Berichtsperiode), kündigten wir an, dass zwei weitere Forschungsmeilensteine in dieser Kooperation erzielt worden sind. Damit bringen uns Meilensteine aus dieser Kooperation 2008 insgesamt Zahlungen in Höhe von 8,5 Mio. Euro. * Am 11. September 2008 gaben wir den Start einer Phase-II-Wirksamkeitsstudie mit EVT 302 bekannt. Diese Studie misst die Erfolgsrate bei Patienten, die mit dem Rauchen aufhören wollen, und soll den entscheidenden Wirksamkeitsnachweis für unseren Wirkstoff bei der Raucherentwöhnung erbringen. * Am 16. September 2008 meldeten wir, dass Evotec infolge des Verkaufs von Direvo Biotech an Bayer HealthCare etwa 5 Mio. Euro über den Verkauf von Direvo Wandelschuldverschreibungen einnehmen würde. Diese Wandelschuldverschreibungen hatten wir im Mai 2007 als Vergütungsbestandteil für den Verkauf unserer Beteilung an Direvo erhalten.
"Wir sind sehr zufrieden mit dem, was wir in diesem Quartal erreicht haben. Wir haben mit unserem klinischen und präklinischen ZNS-Portfolio weiter gute Fortschritte gemacht. Nachdem wir zwei neue Phase-I-Programme gestartet haben, verfügen wir aktuell über fünf Substanzen in der klinischen Entwicklung. Mit EVT 302 haben wir mit den entscheidenden Phase-II-Studien zum Nachweis der Wirksamkeit der Substanz bei der Raucherentwöhnung begonnen und bereiten jetzt für Anfang 2009 den Beginn entsprechender Phase-II-Wirksamkeitsstudien für EVT 101 im Bereich neuropathischer Schmerzen und in anderen Indikationen vor. Die Gespräche über die Verpartnerung unseres am weitesten fortgeschrittenen Wirkstoffkandidaten EVT 201 zur Behandlung von Schlafstörungen wurden im abgelaufenen Quartal fortgesetzt und fokussiert. Wir haben große Hoffnung, dass daraus Anfang 2009 ein Vertragsabschluss hervorgehen kann. Wir glauben an die Attraktivität unseres Wirkstoffkandidaten, der viele der Probleme herkömmlicher Schlafmittel adressiert, wenn auch das Marktumfeld für die Verpartnerung eines jeden Schlafmittels derzeit sicher schwierig ist. Auch für andere klinische und präklinische Programme sehen wir ein wachsendes Interesse seitens potenzieller Partner," sagte Jörn Aldag, Vorstandsvorsitzender der Evotec AG. "Wir sind zudem stolz auf ein außerordentlich starkes drittes Quartal 2008. Wir haben in unserem Kooperationsgeschäft zahlreiche Meilensteine erreicht, die uns zusammen mit dem Verkauf der Direvo-Wandelschuldverschreibungen und einem starken US-Dollar-Wechselkurs zu einer Anhebung unserer Finanzprognose für das laufende Jahr veranlasst haben. Trotz weltweiter Unsicherheit im Finanzsektor ist Evotec solide finanziert mit einem Liquiditätspolster von 98 Mio. Euro, das es uns erlauben wird, unsere Programme auch in diesem schwierigen Marktumfeld in der Entwicklung weiter voranzubringen."
Finanzprognose 2008 Die starke Entwicklung des Kooperationsgeschäfts sowie der Zufluss an liquiden Mitteln aus dem Verkauf von Finanzanlagen im Zusammenhang mit dem Verkauf von Direvo Biotech an Bayer HealthCare veranlassten uns zu einer Anhebung unserer Finanzziele für das Jahr 2008. Aufgrund höher als erwarteter Meilensteinzahlungen aus der Kooperation mit Boehringer Ingelheim und einer insgesamt soliden Entwicklung unseres Kooperationsgeschäfts erwarten wir nun einen Umsatz für das Geschäftsjahr 2008 in der Größenordnung von 38 bis 40 Mio. Euro (zuvor: 34 bis 36 Mio. Euro). Wie erwartet, werden die Forschungs- und Entwicklungsaufwendungen aufgrund des Fortschritts unserer klinischen Pipeline sowie der Einbeziehung von Renovis höher liegen als im Jahr 2007. Aufgrund reduzierter Aufwendungen für frühe Forschungsprojekte, der Verschiebung einer klinischen Meilensteinzahlung an Roche auf Anfang 2009 sowie allgemeiner Kosteneinsparung erwarten wir jedoch, dass die F+E-Aufwendungen im Geschäftsjahr 2008 niedriger als ursprünglich erwartet ausfallen und im Bereich von 40 bis 45 Mio. Euro liegen werden (zuvor: 46 bis 51 Mio. Euro). Auf der Basis und ohne Berücksichtigung von nicht liquiditätswirksamen Wertberichtigungen in beiden Jahren würde sich das operative Ergebnis gegenüber 2007 verbessern. Infolge der oben erwähnten Ereignisse und einem günstigen US-Dollar-Wechselkurs haben wir unsere Liquiditätsprognose inkl. Wertpapiere und "Auction Rate Securities" auf 90 bis 95 Mio. Euro zum Jahresende (Basis: Wechselkurse vom 30. September 2008) erhöht. Unsere im Halbjahresbericht 2008 veröffentlichte Prognose für die Liquidität zum Jahresende betrug auf Basis konstanter Wechselkurse über 80 Mio. Euro. Unter der Annahme, dass sich das Portfolio des Unternehmens wie geplant weiterentwickelt und selbst wenn keine wichtigen Auslizenzierungen abgeschlossen werden, sollten die liquiden Mittel ausreichen, um Evotecs Entwicklungsprogramme bis Ende 2010 zu finanzieren.
Alle in dieser Pressemitteilung ausgewiesenen Ergebnisse und Erläuterungen für das Jahr 2008 werden mit den fortgeführten Geschäftsbereichen im Jahr 2007 verglichen. Am 30. November 2007 hat Evotec einen größeren Geschäftsbereich, die chemische Entwicklungssparte, an die US-Firma Aptuit verkauft. Ab dem 1. Dezember 2007 wurde dieses Geschäft nicht mehr im Abschluss der Evotec-Gruppe konsolidiert. Erträge und Aufwendungen für dieses Geschäft wurden in der Gewinn- und Verlust-Rechnung rückwirkend als aufzugebende Geschäftsbereiche ausgewiesen. Darüber hinaus hat Evotec am 2. Mai 2008 die Akquisition von Renovis, Inc. abgeschlossen. Die operativen Ergebnisse von Renovis sind daher für den Zeitraum vom 2. Mai 2008 bis 30. September 2008 in den konsolidierten Zwischen-Gewinn- und Verlustrechnungen für die ersten neun Monate 2008 berücksichtigt sowie das Vermögen und die Verbindlichkeiten von Renovis per 30. September 2008 in der konsolidierten Zwischenbilanz enthalten. Daher sind die Ergebnisse der Jahre 2007 und 2008 nicht vollständig vergleichbar.
Telefonkonferenz Evotec wird heute um 14.00 Uhr deutscher Zeit eine Telefonkonferenz in englischer Sprache durchführen. Jörn Aldag, Vorstandsvorsitzender, Dr. Klaus Maleck, Finanzvorstand, und Dr. John Kemp, Chief Research&Development Officer, werden Ihnen die wesentlichen Ergebnisse und Schwerpunkte aus dem Berichtszeitraum näher erläutern.
Details der Telefonkonferenz: Datum: Freitag, 14. November 2008 Uhrzeit: 14.00 Uhr (deutsche Zeit)
Einwahlnummern: Europa: +49.(0)69.5007 1308 (Deutschland) +44.(0)20.7806 1955 (UK) USA: +1.718.354 1389 Passcode: 4668760 Webcast: www.evotec.com
Eine Aufnahme der Telefonkonferenz wird für 48 Stunden unter den Telefonnummern +49.(0)69.22222 0418 (Deutschland), +44.(0)20.7806 1970 (UK) und +1.718.354 1112 (USA), Passcode: 4668760#, verfügbar sein. Zusätzlich wird der Webcast auf unserer Website unter: www.evotec.com - Investors - Finanzberichte archiviert.
Kontakt: Anne Hennecke, Senior Vice President, Investor Relations&Corporate Communications, Evotec AG, Tel.: +49.(0)40.56081-286, anne.hennecke@evotec.com
Zukunftsbezogene Aussagen Diese Mitteilung enthält bestimmte vorausschauende Angaben, die Risiken und Unsicherheiten beinhalten. Derartige vorausschauende Aussagen beinhalten u. a., aber nicht ausschließlich, Aussagen über unsere Erwartungen und Vorstellungen hinsichtlich unserer regulatorischen, klinischen oder geschäftlichen Strategie, des Fortschreitens unserer klinischen Entwicklungsprogramme und der Zeitvorstellungen bis zum Vorliegen der Ergebnisse unserer klinischen Studien, hinsichtlich strategischer Kooperationen sowie Pläne, Ziele und Strategien des Managements. Diese Stellungnahmen stellen weder Versprechen noch Garantien dar, sondern sind abhängig von zahlreichen Risiken und Unsicherheiten, von denen sich viele unserer Kontrolle entziehen, und die dazu führen können, dass die tatsächlichen Ergebnisse erheblich von denen abweichen, die in diesen zukunftsbezogenen Aussagen in Erwägung gezogen werden. Diese Risiken und Unsicherheiten betreffen u. a.: Das Risiko, dass Produktkandidaten in klinischen Studien versagen oder nicht erfolgreich vermarktet bzw. hergestellt werden können; Risiken hinsichtlich unserer Fähigkeiten, die Entwicklung der Produktkandidaten, die sich in unserer Pipeline bzw. in klinischen Studien befinden, voranzutreiben; Erfolglosigkeit bei der Identifizierung, Entwicklung und erfolgreichen Kommerzialisierung neuer Produkte und Technologien; größerer Erfolg von Konkurrenzprodukten; Erfolglosigkeit bei dem Bemühen, potenzielle Partner für unsere Technologien und Produkte zu interessieren; Unvermögen, kommerziellen Erfolg für unsere Produkte und Technologien zu erreichen; Erfolglosigkeit beim Schutz unseres geistigen Eigentums sowie die Kosten, unsere Schutzrechte durchzusetzen oder zu verteidigen; Erfolglosigkeit bei der Einhaltung von gesetzlichen Vorschriften, einschließlich Anforderungen der FDA, hinsichtlich unserer Produkte und Produktkandidaten; das Risiko, dass die FDA die Ergebnisse unserer Studien anders interpretiert als wir; das Risiko, dass unsere klinischen Studien nicht zu marktfähigen Produkten führen; das Risiko, dass es uns nicht gelingt, die Zulassung unserer Wirkstoffkandidaten zu erlangen oder ihre Vermarktung zu erreichen; sowie das Risiko neuer, veränderter und kompetitiver Technologien und Vorschriften, sowohl in den USA als auch weltweit.
Die vorstehend aufgeführte Liste von Risiken erhebt keinen Anspruch auf Vollständigkeit. Im Jahresbericht, den Evotec bei der Securities and Exchange Commission eingereicht hat (Form 20-F), sowie anderen bei der Securities and Exchange Commission eingereichten bzw. hinterlegten Dokumenten werden zusätzliche Faktoren aufgeführt, die unsere Geschäftstätigkeit und finanzielle Leistungsfähigkeit beeinflussen können. Wir übernehmen ausdrücklich keine Verpflichtung, vorausschauende Aussagen hinsichtlich geänderter Erwartungen der Parteien oder hinsichtlich neuer Ereignisse, Bedingungen oder Umstände, auf denen diese Aussagen beruhen, öffentlich zu aktualisieren oder zu revidieren.
Eckdaten der konsolidierten Zwischen-Gewinn- und Verlustrechnungen Evotec AG und Tochtergesellschaften
+------------------------------------------------------------------- ----------- ----------
Mit welchem Unternehmen könnte Evotec fusionieren?
Antwort auf Beitrag Nr.: 36.604.019 von altf4 am 18.02.09 16:11:44Optimaler Partner wäre die Müllabfuhr. Die verbrennen alles, dort stinkt es und die sind nur 200 m entfernt.
Antwort auf Beitrag Nr.: 36.604.491 von altonaer am 18.02.09 16:53:13und die sind nur 200 m entfernt.
Stimmt nicht ganz. 300 Meter sind es.
Grüße aus Bahrenfeld. ...könnte dort fast hinspucken.
Stimmt nicht ganz. 300 Meter sind es.
Grüße aus Bahrenfeld. ...könnte dort fast hinspucken.

Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -1,81 | |
| -1,36 | |
| -0,21 | |
| -0,40 | |
| -0,23 | |
| +3,79 | |
| -0,11 | |
| -0,36 | |
| -0,29 | |
| -1,10 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 212 | ||
| 207 | ||
| 188 | ||
| 68 | ||
| 32 | ||
| 29 | ||
| 28 | ||
| 28 | ||
| 26 | ||
| 25 |
19:03 Uhr · Shareribs · AmgenAnzeige |
17:50 Uhr · wO Newsflash · Carl Zeiss Meditec |
17:11 Uhr · dpa-AFX · Evotec |
16:00 Uhr · wO Chartvergleich · Caci International Registered (A) |
15:19 Uhr · dpa-AFX · Air Liquide |
14:58 Uhr · dpa-AFX · Deutsche Boerse |
11:58 Uhr · dpa-AFX · Deutsche Boerse |
11:50 Uhr · dpa-AFX · Evotec |
11:36 Uhr · wallstreetONLINE Redaktion · Evotec |
11:07 Uhr · dpa-AFX · Evotec |
| Zeit | Titel |
|---|---|
| 22:54 Uhr | |
| 18:21 Uhr | |
| 13.02.24 | |
| 22.01.24 | |
| 17.01.24 | |
| 08.01.24 | |
| 15.05.23 |





















