Geron mit Hammernews!! - 500 Beiträge pro Seite (Seite 5)
eröffnet am 18.03.03 18:26:10 von
neuester Beitrag 21.03.24 13:47:21 von
neuester Beitrag 21.03.24 13:47:21 von
Beiträge: 3.090
ID: 709.348
ID: 709.348
Aufrufe heute: 0
Gesamt: 213.056
Gesamt: 213.056
Aktive User: 0
ISIN: US3741631036 · WKN: 902213 · Symbol: GERN
3,6900
USD
-1,07 %
-0,0400 USD
Letzter Kurs 02:00:00 Nasdaq
Neuigkeiten
18.04.24 · Business Wire (engl.) |
03.04.24 · Business Wire (engl.) |
19.03.24 · Business Wire (engl.) |
14.03.24 · Business Wire (engl.) |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 3.000,00 | +74.900,00 | |
| 1,1060 | +30,10 | |
| 1,5400 | +25,71 | |
| 12,400 | +23,26 | |
| 7,0700 | +16,86 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,7255 | -15,15 | |
| 1,3500 | -15,63 | |
| 0,8700 | -20,18 | |
| 4,6600 | -28,75 | |
| 0,6021 | -35,26 |
Ach was solls, ich hol mir jetzt das runde Posting, so viele Tage der Versuchung, der ich jetzt nachgebe.
2000 Postings, Glückwunsch meislo! Toller Thread! Da hat Geron einiges gut zu machen...
Gruß, greenhorn
2000 Postings, Glückwunsch meislo! Toller Thread! Da hat Geron einiges gut zu machen...

Gruß, greenhorn
Antwort auf Beitrag Nr.: 23.467.089 von greenhorn1998 am 16.08.06 13:35:40greenhorn1998 
7:31AM Geron announced the presentation of new data supporting the development of TAT0002; data confirm and extend earlier findings (GERN) 6.35 : Co announced today the presentation of new data supporting the development of TAT0002, a small molecule telomerase activator for the treatment of HIV/AIDS, at the XVI International AIDS Conference. The data, which were presented by Calvin Harley, Ph.D., Geron's chief scientific officer, and co-authored by collaborating scientists at the Geffen School of Medicine at UCLA, confirm and extend earlier findings that TAT0002 enhances the function of key immune cells from HIV/AIDS donors. The results show that TAT0002 stimulates RANTES, MIP1-alpha and MIP1-beta, molecules that attract other immune cells to assist in the anti-viral response.

7:31AM Geron announced the presentation of new data supporting the development of TAT0002; data confirm and extend earlier findings (GERN) 6.35 : Co announced today the presentation of new data supporting the development of TAT0002, a small molecule telomerase activator for the treatment of HIV/AIDS, at the XVI International AIDS Conference. The data, which were presented by Calvin Harley, Ph.D., Geron's chief scientific officer, and co-authored by collaborating scientists at the Geffen School of Medicine at UCLA, confirm and extend earlier findings that TAT0002 enhances the function of key immune cells from HIV/AIDS donors. The results show that TAT0002 stimulates RANTES, MIP1-alpha and MIP1-beta, molecules that attract other immune cells to assist in the anti-viral response.
Untersuchungen
Stammzellen gewonnen - Embryo lebt

Das Team der US-Biotech-Firma Advanced Cell Technology schürt die Hoffnung, dass die Gewinnung von embryonalen Stammzellen nicht die Zerstörung eines Embryos bedeuten muss. In Deutschland ist Stammzellenforschung weiterhin strikt reglementiert.
Von Sonja Kastilan
Foto: AP Worcester - Warum sollte, was bereits bei Mäusen gezeigt wurde, nicht auch bei Menschen gelingen? Nicht immer lässt sich ein Studienergebnis einfach übertragen, vor allem wenn es sich um den Bereich der Stammzellenforschung handelt. Doch das Team um Robert Lanza von der US-Biotech-Firma Advanced Cell Technology (ACT) schürt jetzt im Fachmagazin "Nature" die Hoffnung, dass die Gewinnung von embryonalen Stammzellen (ESZ) in Zukunft nicht - wie bisher - die Zerstörung eines Embryos bedeuten muss.
Seine Methode beruht darauf, einem Embryo in sehr frühem Acht- oder Zehn-Zell-Stadium eine der potenten Zellen "behutsam" zu entnehmen. Ähnlich wie es zum Beispiel weltweit in Fortpflanzungskliniken bei der Präimplantationsdignostik (PID) geschieht, wenn man künstlich erzeugte Embryonen auf bestimmte Krankheiten hin untersuchen will. Anschließend können diese unbeschadet in den Mutterleib eingesetzt werden. Laut Studien beeinflusst eine PID weder Einpflanzung, Schwangerschaftsrate noch Entwicklung eines Embryos im Vergleich mit normalen Blastocysten.
ACT-Forscher Young Chung konnte mit diesem Verfahren schon bei Mäusen Erfolge erzielen und ESZ gewinnen, ohne den ursprünglichen Embryo zu zerstören. Und obwohl zuvor andere Forschergruppen mit dem gleichen Ansatz scheiterten, ist das dem Team aus Worcester nun auch bei menschlichen Embryonen gelungen. Indem eine Einzel-Blastomere entsprechend weiterbehandelt wurde, entstanden auf diese Weise erstmals 19 sogenannte ESZ-artige Auswüchse und zwei stabile Stammzelllinien. Letztere lassen sich seit mehr als acht Monaten undifferenziert vermehren. Außerdem weisen sie spezifische Signale der Pluripotenz auf, die eine - für die Therapie wichtige - gewünschte Wandlungsfähigkeit verspricht.
Tatsächlich zeigten erste Labortests, dass sich aus diesen Linien verschiedene Zelltypen aller drei Untergruppen entwickeln können. Sollte also eine vorsichtige Biopsie - mit Einverständnis der betroffenen Eltern - die Lösung aller ethischen Probleme der Stammzellentherapie sein? Schließlich entstehen alljährlich Tausende Babys in der Retorte, die auf diese Weise passende embryonale Stammzellen für sich selbst oder die Behandlung kranker Geschwister bieten könnten. Für die Forschung sind derartige ESZ ebenso von großem Interesse, insbesondere wenn sie Funktionsfähigkeit unter Beweis stellen.
Politische Debatte in Deutschland
Das Bundesforschungsministerium reagierte zurückhaltend auf Meldungen über neue Methoden in der Stammzellenforschung. „Die Ergebnisse nehmen wir zur Kenntnis. Die deutsche Stichtagsregelung für die Forschung mit embryonalen Stammzellen hat weiterhin Bestand“, sagte ein Sprecher.
In Deutschland ist nur Forschungsarbeit mit solchen embryonalen Stammzellen erlaubt, die vor dem 1. Januar 2002 im Ausland gewonnen worden sind.
Experten in deutschen Wissenschaftsorganisationen, die seit Jahren für eine Liberalisierung der in der Bundesrepublik gültigen Stichtagsregelung eintreten, warnten vor voreiligen Schlüssen. Zunächst müsse sich die Wiederholbarkeit der Forschungsarbeit erweisen.
Im Bundestag tritt bisher allein die FDP für einen Verzicht auf die strengen deutschen Auflagen ein. In der Union und SPD gibt es Gegner wie Befürworter der Stichtagsregelung. Die Grünen haben sich bisher strikt gegen Änderungen ausgesprochen.
Artikel erschienen am Do, 24. August 2006
Stammzellen gewonnen - Embryo lebt


Das Team der US-Biotech-Firma Advanced Cell Technology schürt die Hoffnung, dass die Gewinnung von embryonalen Stammzellen nicht die Zerstörung eines Embryos bedeuten muss. In Deutschland ist Stammzellenforschung weiterhin strikt reglementiert.
Von Sonja Kastilan
Foto: AP Worcester - Warum sollte, was bereits bei Mäusen gezeigt wurde, nicht auch bei Menschen gelingen? Nicht immer lässt sich ein Studienergebnis einfach übertragen, vor allem wenn es sich um den Bereich der Stammzellenforschung handelt. Doch das Team um Robert Lanza von der US-Biotech-Firma Advanced Cell Technology (ACT) schürt jetzt im Fachmagazin "Nature" die Hoffnung, dass die Gewinnung von embryonalen Stammzellen (ESZ) in Zukunft nicht - wie bisher - die Zerstörung eines Embryos bedeuten muss.
Seine Methode beruht darauf, einem Embryo in sehr frühem Acht- oder Zehn-Zell-Stadium eine der potenten Zellen "behutsam" zu entnehmen. Ähnlich wie es zum Beispiel weltweit in Fortpflanzungskliniken bei der Präimplantationsdignostik (PID) geschieht, wenn man künstlich erzeugte Embryonen auf bestimmte Krankheiten hin untersuchen will. Anschließend können diese unbeschadet in den Mutterleib eingesetzt werden. Laut Studien beeinflusst eine PID weder Einpflanzung, Schwangerschaftsrate noch Entwicklung eines Embryos im Vergleich mit normalen Blastocysten.
ACT-Forscher Young Chung konnte mit diesem Verfahren schon bei Mäusen Erfolge erzielen und ESZ gewinnen, ohne den ursprünglichen Embryo zu zerstören. Und obwohl zuvor andere Forschergruppen mit dem gleichen Ansatz scheiterten, ist das dem Team aus Worcester nun auch bei menschlichen Embryonen gelungen. Indem eine Einzel-Blastomere entsprechend weiterbehandelt wurde, entstanden auf diese Weise erstmals 19 sogenannte ESZ-artige Auswüchse und zwei stabile Stammzelllinien. Letztere lassen sich seit mehr als acht Monaten undifferenziert vermehren. Außerdem weisen sie spezifische Signale der Pluripotenz auf, die eine - für die Therapie wichtige - gewünschte Wandlungsfähigkeit verspricht.
Tatsächlich zeigten erste Labortests, dass sich aus diesen Linien verschiedene Zelltypen aller drei Untergruppen entwickeln können. Sollte also eine vorsichtige Biopsie - mit Einverständnis der betroffenen Eltern - die Lösung aller ethischen Probleme der Stammzellentherapie sein? Schließlich entstehen alljährlich Tausende Babys in der Retorte, die auf diese Weise passende embryonale Stammzellen für sich selbst oder die Behandlung kranker Geschwister bieten könnten. Für die Forschung sind derartige ESZ ebenso von großem Interesse, insbesondere wenn sie Funktionsfähigkeit unter Beweis stellen.
Politische Debatte in Deutschland
Das Bundesforschungsministerium reagierte zurückhaltend auf Meldungen über neue Methoden in der Stammzellenforschung. „Die Ergebnisse nehmen wir zur Kenntnis. Die deutsche Stichtagsregelung für die Forschung mit embryonalen Stammzellen hat weiterhin Bestand“, sagte ein Sprecher.
In Deutschland ist nur Forschungsarbeit mit solchen embryonalen Stammzellen erlaubt, die vor dem 1. Januar 2002 im Ausland gewonnen worden sind.
Experten in deutschen Wissenschaftsorganisationen, die seit Jahren für eine Liberalisierung der in der Bundesrepublik gültigen Stichtagsregelung eintreten, warnten vor voreiligen Schlüssen. Zunächst müsse sich die Wiederholbarkeit der Forschungsarbeit erweisen.
Im Bundestag tritt bisher allein die FDP für einen Verzicht auf die strengen deutschen Auflagen ein. In der Union und SPD gibt es Gegner wie Befürworter der Stichtagsregelung. Die Grünen haben sich bisher strikt gegen Änderungen ausgesprochen.
Artikel erschienen am Do, 24. August 2006
Ethisch unbedenkliche Stammzell-Linie geschaffen
Embryos sollen voll lebensfähig bleiben
Alameda (pte/24.08.2006/09:15) - Das Biotechnologieunternehmen Advanced Cell Technology (ACT) http://www.advancedcell.com hat menschliche embryonale Stammzellen geschaffen ohne Embryos zu zerstören. Die Zell-Linien wurden durch die Entfernung einzelner Zellen aus Embryos geschaffen. Ein Vorgang, der die Embryos, laut der in Nature http://www.nature.com veröffentlichten Studie, nicht beschädigt hat. Derzeit führt die Herstellung von dieser Art von Stammzellen zur Zerstörung des Embryos. Die Wissenschaftler hoffen, dass ihre Forschungsergebnisse helfen, einige ethische Barrieren in diesem Bereich zu überwinden und eine Möglichkeit zu bieten, einige der derzeit bestehenden gesetzlichen Beschränkungen in Amerika zu umgehen.
2001 erklärte Präsident Bush, dass eine staatliche Förderung nur für Forschungen zur Verfügung gestellt würde, die die bestehenden 61 Zell-Linien nutzt. Das bedeutete keine Förderung für die Schaffung neuer Zell-Linien, egal ob aus bestehenden Embryos oder aus geklonten Embryos. BBC Korrespondent James Westhead berichtet aus Washington, dass es derzeit nicht klar ist, ob das neue Verfahren die bestehenden Finanzierungseinschränkungen umgehen kann. Fragen hinsichtlich der Effektivität und ob es sich wirklich um einen ethischeren Ansatz handelt, bleiben derzeit noch ungeklärt.
Der leitenden Wissenschaftler Robert Lanza erklärte, dass man zum ersten Mal gezeigt habe, dass man menschliche embryonale Stammzellen schaffen kann ohne den Embryo zu zerstören und daher auch ohne eine Beeinträchtigung seines Lebenspotenzials. Bei überschüssigen Embryos aus künstlichen Befruchtungen entfernten die Forscher einzelne Zellen und wandten dafür ein Verfahren an, das auch bei der Präimplantationsdiagnostik zum Einsatz kommt. Dieser Eingriff hinterlässt einen intakten Embryo, der weiterwachsen und sich zu einem gesunden Fötus entwickeln kann. Aus den 16 eingesetzten Embryos schuf das Team zwei langfristige Linien von Stammzellen, die laut Lanza genetisch normal sind und alle Arten von Zellen hervorbringen können. Wird dieser Ansatz von anderen Wissenschaftlern erfolgreich wiederholt, könnte das zur Entstehung von mehr Linien von Stammzellen führen und möglicherweise auch zu maßgeschneiderten Linien für mit Hilfe von Präimplantationsdiagnostik geborenen Kindern. (Ende
Embryos sollen voll lebensfähig bleiben
Alameda (pte/24.08.2006/09:15) - Das Biotechnologieunternehmen Advanced Cell Technology (ACT) http://www.advancedcell.com hat menschliche embryonale Stammzellen geschaffen ohne Embryos zu zerstören. Die Zell-Linien wurden durch die Entfernung einzelner Zellen aus Embryos geschaffen. Ein Vorgang, der die Embryos, laut der in Nature http://www.nature.com veröffentlichten Studie, nicht beschädigt hat. Derzeit führt die Herstellung von dieser Art von Stammzellen zur Zerstörung des Embryos. Die Wissenschaftler hoffen, dass ihre Forschungsergebnisse helfen, einige ethische Barrieren in diesem Bereich zu überwinden und eine Möglichkeit zu bieten, einige der derzeit bestehenden gesetzlichen Beschränkungen in Amerika zu umgehen.
2001 erklärte Präsident Bush, dass eine staatliche Förderung nur für Forschungen zur Verfügung gestellt würde, die die bestehenden 61 Zell-Linien nutzt. Das bedeutete keine Förderung für die Schaffung neuer Zell-Linien, egal ob aus bestehenden Embryos oder aus geklonten Embryos. BBC Korrespondent James Westhead berichtet aus Washington, dass es derzeit nicht klar ist, ob das neue Verfahren die bestehenden Finanzierungseinschränkungen umgehen kann. Fragen hinsichtlich der Effektivität und ob es sich wirklich um einen ethischeren Ansatz handelt, bleiben derzeit noch ungeklärt.
Der leitenden Wissenschaftler Robert Lanza erklärte, dass man zum ersten Mal gezeigt habe, dass man menschliche embryonale Stammzellen schaffen kann ohne den Embryo zu zerstören und daher auch ohne eine Beeinträchtigung seines Lebenspotenzials. Bei überschüssigen Embryos aus künstlichen Befruchtungen entfernten die Forscher einzelne Zellen und wandten dafür ein Verfahren an, das auch bei der Präimplantationsdiagnostik zum Einsatz kommt. Dieser Eingriff hinterlässt einen intakten Embryo, der weiterwachsen und sich zu einem gesunden Fötus entwickeln kann. Aus den 16 eingesetzten Embryos schuf das Team zwei langfristige Linien von Stammzellen, die laut Lanza genetisch normal sind und alle Arten von Zellen hervorbringen können. Wird dieser Ansatz von anderen Wissenschaftlern erfolgreich wiederholt, könnte das zur Entstehung von mehr Linien von Stammzellen führen und möglicherweise auch zu maßgeschneiderten Linien für mit Hilfe von Präimplantationsdiagnostik geborenen Kindern. (Ende
aufwärts im stealth mode.
die obere begrenzung des abwärtstrendkanals liegt bei ca. 7 usd. ich glaube, dass der kurs dort abprallt. er wird dann zwar nicht mehr auf 5 usd oder sogar etwas weniger runter knallen (untere begrenzung des kanals), aber am ende wird alles von nachrichten abhängen.
vielleicht haben wir deshalb auch beim jüngsten tief von 5,75 usd das letzte mal geron so billig gesehen. in 6 monaten werden wir schlauer sein, über grn163l und seine potenz sowie den weiteren kursverlauf.
es ist spannend so etwas miterleben zu können.
grüße
luckycat.
die obere begrenzung des abwärtstrendkanals liegt bei ca. 7 usd. ich glaube, dass der kurs dort abprallt. er wird dann zwar nicht mehr auf 5 usd oder sogar etwas weniger runter knallen (untere begrenzung des kanals), aber am ende wird alles von nachrichten abhängen.
vielleicht haben wir deshalb auch beim jüngsten tief von 5,75 usd das letzte mal geron so billig gesehen. in 6 monaten werden wir schlauer sein, über grn163l und seine potenz sowie den weiteren kursverlauf.
es ist spannend so etwas miterleben zu können.
grüße
luckycat.
mit rasanz exakt bis an die obere begrenzung des einjährigen abwärtstrendkanals...
short squeeze vom feinsten!
das volumen steigt, der momentum-druck ebenso. die jüngste dynamik entstand ohne wirklich wichtige nachrichten - scheinbar aus sich selbst heraus. da kann mehr drin sein, denn am markt ist sehr vieles psychologie. keiner weiß, was genau hinter dem kursanstieg aus dem nichts steckt. das verunsichert vor allem die shorties.
weiteres potenzial zum trendbruch und einem großen reversal? abwarten.
short squeeze vom feinsten!
das volumen steigt, der momentum-druck ebenso. die jüngste dynamik entstand ohne wirklich wichtige nachrichten - scheinbar aus sich selbst heraus. da kann mehr drin sein, denn am markt ist sehr vieles psychologie. keiner weiß, was genau hinter dem kursanstieg aus dem nichts steckt. das verunsichert vor allem die shorties.
weiteres potenzial zum trendbruch und einem großen reversal? abwarten.
wie erwartet hat die obere begrenzung des abwärtstrendkanals gehalten. leider. bei 7,30 usd war das kaufinteresse gedeckelt, jetzt sehen wir wieder einen kurs, der gut 1 dollar tiefer liegt.
die untere begrenzung des kanals liegt bei ca. 5,20 usd. es ist also noch 1 dollar luft nach unten, der jetztige kurs liegt also in der mitte des kanals.
in kürze sind 3/4 des jahres 2006 vorbei und nach meiner analyse haben wir - was geron betrifft - ein recht nachrichtenarmes jahr erlebt. dem kurs blieb nichts anderes als abzurutschen, weil außer den (schwachen) fundamentaldaten gerons wie verluststeigerung, persistenter kapitalbedarf etc. nichts wirklich kurspositives in die kursbildung einfloss.
ich hoffe, dass ich das in spätestens 6 monaten ändert.
die untere begrenzung des kanals liegt bei ca. 5,20 usd. es ist also noch 1 dollar luft nach unten, der jetztige kurs liegt also in der mitte des kanals.
in kürze sind 3/4 des jahres 2006 vorbei und nach meiner analyse haben wir - was geron betrifft - ein recht nachrichtenarmes jahr erlebt. dem kurs blieb nichts anderes als abzurutschen, weil außer den (schwachen) fundamentaldaten gerons wie verluststeigerung, persistenter kapitalbedarf etc. nichts wirklich kurspositives in die kursbildung einfloss.
ich hoffe, dass ich das in spätestens 6 monaten ändert.
Antwort auf Beitrag Nr.: 24.216.762 von LuckyCat am 26.09.06 20:19:4127. September 2006, Neue Zürcher Zeitung
Neue Schritte auf dem Weg zu Stammzell-Therapien
Möglicherweise bald erste Therapieversuche mit embryonalen Stammzellen
Bereits im kommenden Jahr sollen menschliche embryonale Stammzellen an Menschen getestet werden. An einer Konferenz in Lausanne haben Experten jedoch darauf hingewiesen, dass man das Verhalten solcher Zellen im Organismus noch zu wenig kenne.
Während man in Fachwelt wie Öffentlichkeit noch diskutiert, ob es ethisch vertretbar ist, menschliche embryonale Stammzellen, für deren Gewinnung Embryonen zerstört werden, medizinisch einzusetzen, charakterisieren Grundlagenforscher weltweit die umstrittenen Zellen im Detail und etablieren standardisierte Protokolle für deren Haltung und Weiterentwicklung in der Zellkultur. Zudem sind bereits Experimente mit aus menschlichen embryonalen Stammzellen gewonnenen Zellen an Affen - und offenbar sogar erste klinische Versuche an Menschen - in Vorbereitung. Adulte Stammzellen sind bereits an Menschen eingesetzt worden. An der internationalen Konferenz «Advances in Stem Cell Research» in Lausanne haben Experten kürzlich Fortschritte und neue Erkenntnisse zu Therapien mit beiden Sorten Stammzellen vorgestellt und diskutiert.
Neue Nervenzellen fürs Gehirn
Eine der Krankheiten, bei denen man Therapien aus embryonalen Stammzellen einsetzen will, ist die Chorea Huntington, eine Erkrankung des Nervensystems. Hier will eine Forschergruppe aus Frankreich in den nächsten Monaten als weltweit erste Gruppe nicht mehr nur an Ratten, sondern an Affen eine Therapie mit aus menschlichen embryonalen Stammzellen entwickelten Zellen testen. Wie Marc Peschanski vom Institut national de la santé et de la recherche an dem Kongress berichtete, sei es seinem Team gelungen, spezielle Nervenzellen herzustellen, die in der bei Chorea Huntington zerstörten Gehirnregion, dem sogenannten Striatum, vorkommen. Diese Zellen habe man Ratten, deren Striatum zuvor zerstört worden war, implantiert. Noch lägen allerdings keine konkreten Ergebnisse vor.
Seine Hoffnung, dass bei Chorea Huntington ein Zellimplantat helfen könnte, stützt Peschanski ausser auf internationale Erfahrungen mit solchen Versuchen bei Ratten vor allem auf seit Ende der 1990er Jahre bei Menschen durchgeführte Implantationen von fötalem Hirngewebe. Dieses sei einigen wenigen Chorea-Huntington-Patienten direkt in die zerstörte Gehirnregion eingesetzt worden. Bei fast allen Behandelten hätten sich die Symptome deutlich klinisch gebessert und die kognitiven Leistungen stabilisiert. Die Besserung hielt laut Peschanski allerdings nur einige Jahre an. Er ist überzeugt, dass dies an den zu kleinen Mengen und der zu kurzen Lebensdauer der implantierten Zellen lag. Genau diese Probleme, so erklärt der Forscher, bekomme man mit den nahezu ewig lebenden und in ausreichenden Mengen herstellbaren Striatum- Nervenzellen aus embryonalen Stammzellen in den Griff. Deshalb glaubt Peschanski, dass er in absehbarer Zeit Menschen mit solchen Zellen behandeln kann.
Genau dies plant die amerikanische Biotechfirma Geron laut Pressemeldungen spätestens zu Beginn des nächsten Jahres. Sie will zum ersten Mal weltweit klinische Versuche mit einer solchen Therapie bei Menschen unternehmen. Man habe aus menschlichen embryonalen Stammzellen Vorläufer sogenannter Oligodendrozyten produziert. Diese spezialisierten Zellen sind dafür zuständig, dass die Nervenzellen ihre schützende Myelinhülle erhalten, ohne die sie keine Reize weiterleiten können. Gemäss den Mitteilungen sollen nun bei querschnittgelähmten Patienten genau an der Stelle der Rückenmarkszerstörung die im Reagenzglas entwickelten Oligodendrozyten implantiert werden. Tierversuche hätten nämlich ergeben, dass dadurch «nackte» Nervenfasern wieder myelinisiert würden. Zudem schütteten die implantierten Zellen auch - noch nicht vollständig identifizierte - Wachstumsfaktoren aus, so dass sich neue Nervenfasern in der zerstörten Region bildeten, heisst es weiter.
Offenbar wird dadurch zumindest ein Teil der fehlenden Nervenverbindung im Rückenmark überbrückt, denn laut Geron war die motorische Aktivität so behandelter Ratten auch noch neun Monate nach der Zellimplantation deutlich verbessert. Versuche mit Zellkulturen hätten zudem ergeben, dass die hergestellten Oligodendrozyten-Vorläufer nur sehr wenige das Immunsystems des Menschen aktivierende Proteine auf ihrer Oberfläche trügen. Es sei also keine gravierende Abstossungsreaktion zu erwarten.
Nach wie vor viele offene Fragen
Doch viele Forscher haben Bedenken, bereits zum jetzigen Zeitpunkt derartige Zellen tatsächlich in Menschen zu implantieren. Man müsse zum Beispiel vor einer Therapie sicher sein können, dass für ein solches Implantat ausschliesslich die spezialisierten Zellen verwendet würden, mahnten viele in Lausanne anwesende Forscher. Schliesslich könnten aus embryonalen Stammzellen auch Tumore entstehen. Noch sei unbekannt, welche Einflüsse während der Zellkultur oder der Behandlung dazu führten, dass sich diese auch Teratoma genannten bösartigen Zellwucherungen bildeten. Peschanski erklärte, dass er in der Zellkultur festgestellt habe, dass aus den von ihm für Implantate vorgesehenen Nervenzellen keine Teratoma entstünden. Allerdings weiss momentan niemand ganz genau, was in einen menschlichen Organismus implantierte, nicht spezialisierte embryonale Stammzellen bewirken.
Zudem gab Oliver Brüstle, Stammzellforscher aus Bonn, zu bedenken, dass man trotz jahrelangen Tierversuchen immer noch keine Ahnung habe, was die in die Gehirne von Versuchstieren injizierten spezialisierten Zellen dort tatsächlich machten. Auch er implantiere in seinem Labor aus menschlichen embryonalen Stammzellen hergestellte spezielle Nervenzellen in Ratten mit Chorea Huntington, erläuterte er. Doch ob sich diese Zellen dort vollständig oder nur teilweise in das bestehende neuronale Netzwerk einbauten, ob sie voll funktionsfähige Kontakte mit den umgebenden Nervenzellen eingingen und tatsächlich so kommunizierten wie körpereigenen Nervenzellen, das sei alles noch unklar.
Yves-Alain Barde von der Universität Basel, der selbst gerade begonnen hat, aus menschlichen embryonalen Stammzellen Nervenzellen herzustellen und dies seit Jahren mit Mauszellen tut, ist davon überzeugt, dass man noch nicht einmal eindeutig sagen könne, was eine gute, intakte menschliche embryonale Stammzelle charakterisiere. Viele der Erfolgsmeldungen aus Tierversuchen seien eher anekdotisch als wissenschaftlich genau dokumentiert - und verstanden. Allerdings entgegnen die Befürworter einer baldigen Therapie, dass man gar nicht genau wissen müsse, was jede implantierte Zelle vor Ort tatsächlich tue. Wichtig sei vielmehr, dass die Zellimplantate sicher seien und positive medizinische Effekte bei unheilbaren Krankheiten erzielten.
Medizinisch und wissenschaftlich deutlich weiter ist man bei den adulten Stammzellen. Dies sind schon etwas spezialisierte Stammzellen, die in den verschiedenen Geweben vorkommen. Seit Jahrzehnten werden patienteneigene oder auch fremde, aber immunologisch ähnliche Blutstammzellen zum Beispiel im Rahmen von Krebstherapien eingesetzt, um das Blutsystem nach einer Chemotherapie oder einer Bestrahlung wieder aufzubauen. Adulte Stammzellen sind ethisch unbedenklich, da sie aus einem erwachsenen Organismus entnommen werden können. Zudem kann man heute bereits einigen Patienten mit aus ihren eigenen adulten Stammzellen hergestelltem Ersatzgewebe helfen. So werden etwa aus Hautstammzellen Zellrasen gezüchtet und transplantiert. Doch da es sich bei dieser gezüchteten Haut nicht um eine echte Haut handelt, fehlen Schweissdrüsen oder Haare. Vor allem bei grossflächigen Transplantationen sei dies für die Betroffenen problematisch, hiess es in Lausanne.
Bis vor kurzem dachten weltweit viele Experten sogar, dass adulte Stammzellen dereinst Therapien mit embryonalen Stammzellen überflüssig machen könnten. Eine Vielzahl von Experimenten schien zu bestätigen, dass man mit den entsprechenden Tricks - etwa Behandlungen mit ausgeklügelten Cocktails aus Wachstumsfaktoren - eine adulte Stammzelle reprogrammieren und so quasi in einen embryonalen Zustand zurückversetzen könne. Sie sollte dann auch andere Zellen als die ihres eigentlichen Gewebes herstellen. Doch diese Hoffnung sei nun vom Tisch, betonte Andreas Trumpp vom Schweizerischen Institut für experimentelle Krebsforschung am Kongress.
Zu verstärkter Aktivität anregen
Statt völlig andere Typen von Zellen hervorzubringen, produzieren implantierte adulte Stammzellen diverse therapeutisch wirksame Proteine, meint heute der Grossteil der Stammzellforscher. Vermutlich milderten oder stoppten diese Proteine dann die Entzündungen im defekten Gewebe und regten die dort vorhandenen adulten Stammzellen zur Bildung neuer Gewebezellen an. Daher steht heute im Mittelpunkt der Forschung an adulten Stammzellen, wie man diese vermutlich in allen Geweben des Körpers vorhandenen Zellen bei einer Gewebezerstörung zu verstärkter Aktivität anregen kann. Es werden auch adulte Stammzellen getestet, bei denen durch den Einbau einer intakten Kopie eines defekten Gens ein Gendefekt repariert wurde. Dies wird ganz vereinzelt zwar auch bei menschlichen embryonalen Stammzellen durchgeführt, doch diese Versuche befinden sich noch im Anfangsstadium. Hingegen sind solche mit adulten Stammzellen derart fortgeschritten, dass bereits Tiere behandelt werden. So versucht man etwa bei Hunden mit einer degenerativen Muskelerkrankung die fortschreitenden Zerstörungen im Muskelgewebe aufzuhalten. Doch noch wisse man nicht genau, wann im Verlauf der Krankheit man mit den Zellinjektionen beginnen oder wie man die Zellen behandeln müsse, damit sie sich auch tatsächlich im ganzen Muskel verteilten, erläuterte Giulio Cossu vom Stem Cell Research Institute in Mailand in Lausanne.
Hoffen auf Kombinationstherapien
Momentan gehen die Experten davon aus, dass es Therapien sowohl mit adulten als auch embryonalen Stammzellen geben wird, wobei voraussichtlich jeder Zelltyp für andere Fragestellungen und Anwendungen verwendet werden wird. Und vielleicht werden in Zukunft sogar einmal Kombinationstherapien mit beiden Sorten von Stammzellen existieren. Wie Jan Cornelissen von der Erasmus-Universität in Rotterdam am Kongress erläuterte, bilden sich nach einer Injektion von Blutstammzellen im Rahmen einer Krebstherapie zwar viele Zelltypen des Immunsystems sehr schnell. Doch da das Thymusgewebe durch die in manchen Therapien eingesetzten Bestrahlungen in der Regel schwer angegriffen sei, können sich die vom Thymus abhängigen T-Zellen oftmals erst nach ein bis zwei Jahren wieder bilden. Erste Studien mit Tieren hätten nun gezeigt, dass eine gleichzeitige Implantation von Thymusgewebe und Blutstammzellen die Regeneration des Immunsystems deutlich verbessere.
Doch da im Spital in der Regel kein passendes Thymusgewebe verfügbar sei, plädiert Cornelissen dafür, solches aus embryonalen Stammzellen herzustellen. Ihm sei gelungen, so Vorläuferzellen von Thymusgewebe zu produzieren, berichtete er. Diese habe man dann in Mäuse implantiert. Dort hätten sie sich offenbar zu Thymuszellen entwickelt und seien sogar in der Lage gewesen, die Bildung neuer T-Zellen aus implantierten Blutstammzellen zu unterstützen. Doch alle Mäuse hätten Teratoma entwickelt. Man stehe also noch ganz am Anfang dieser Art von Kombinationstherapie.
Stephanie Lahrtz
Neue Schritte auf dem Weg zu Stammzell-Therapien
Möglicherweise bald erste Therapieversuche mit embryonalen Stammzellen
Bereits im kommenden Jahr sollen menschliche embryonale Stammzellen an Menschen getestet werden. An einer Konferenz in Lausanne haben Experten jedoch darauf hingewiesen, dass man das Verhalten solcher Zellen im Organismus noch zu wenig kenne.
Während man in Fachwelt wie Öffentlichkeit noch diskutiert, ob es ethisch vertretbar ist, menschliche embryonale Stammzellen, für deren Gewinnung Embryonen zerstört werden, medizinisch einzusetzen, charakterisieren Grundlagenforscher weltweit die umstrittenen Zellen im Detail und etablieren standardisierte Protokolle für deren Haltung und Weiterentwicklung in der Zellkultur. Zudem sind bereits Experimente mit aus menschlichen embryonalen Stammzellen gewonnenen Zellen an Affen - und offenbar sogar erste klinische Versuche an Menschen - in Vorbereitung. Adulte Stammzellen sind bereits an Menschen eingesetzt worden. An der internationalen Konferenz «Advances in Stem Cell Research» in Lausanne haben Experten kürzlich Fortschritte und neue Erkenntnisse zu Therapien mit beiden Sorten Stammzellen vorgestellt und diskutiert.
Neue Nervenzellen fürs Gehirn
Eine der Krankheiten, bei denen man Therapien aus embryonalen Stammzellen einsetzen will, ist die Chorea Huntington, eine Erkrankung des Nervensystems. Hier will eine Forschergruppe aus Frankreich in den nächsten Monaten als weltweit erste Gruppe nicht mehr nur an Ratten, sondern an Affen eine Therapie mit aus menschlichen embryonalen Stammzellen entwickelten Zellen testen. Wie Marc Peschanski vom Institut national de la santé et de la recherche an dem Kongress berichtete, sei es seinem Team gelungen, spezielle Nervenzellen herzustellen, die in der bei Chorea Huntington zerstörten Gehirnregion, dem sogenannten Striatum, vorkommen. Diese Zellen habe man Ratten, deren Striatum zuvor zerstört worden war, implantiert. Noch lägen allerdings keine konkreten Ergebnisse vor.
Seine Hoffnung, dass bei Chorea Huntington ein Zellimplantat helfen könnte, stützt Peschanski ausser auf internationale Erfahrungen mit solchen Versuchen bei Ratten vor allem auf seit Ende der 1990er Jahre bei Menschen durchgeführte Implantationen von fötalem Hirngewebe. Dieses sei einigen wenigen Chorea-Huntington-Patienten direkt in die zerstörte Gehirnregion eingesetzt worden. Bei fast allen Behandelten hätten sich die Symptome deutlich klinisch gebessert und die kognitiven Leistungen stabilisiert. Die Besserung hielt laut Peschanski allerdings nur einige Jahre an. Er ist überzeugt, dass dies an den zu kleinen Mengen und der zu kurzen Lebensdauer der implantierten Zellen lag. Genau diese Probleme, so erklärt der Forscher, bekomme man mit den nahezu ewig lebenden und in ausreichenden Mengen herstellbaren Striatum- Nervenzellen aus embryonalen Stammzellen in den Griff. Deshalb glaubt Peschanski, dass er in absehbarer Zeit Menschen mit solchen Zellen behandeln kann.
Genau dies plant die amerikanische Biotechfirma Geron laut Pressemeldungen spätestens zu Beginn des nächsten Jahres. Sie will zum ersten Mal weltweit klinische Versuche mit einer solchen Therapie bei Menschen unternehmen. Man habe aus menschlichen embryonalen Stammzellen Vorläufer sogenannter Oligodendrozyten produziert. Diese spezialisierten Zellen sind dafür zuständig, dass die Nervenzellen ihre schützende Myelinhülle erhalten, ohne die sie keine Reize weiterleiten können. Gemäss den Mitteilungen sollen nun bei querschnittgelähmten Patienten genau an der Stelle der Rückenmarkszerstörung die im Reagenzglas entwickelten Oligodendrozyten implantiert werden. Tierversuche hätten nämlich ergeben, dass dadurch «nackte» Nervenfasern wieder myelinisiert würden. Zudem schütteten die implantierten Zellen auch - noch nicht vollständig identifizierte - Wachstumsfaktoren aus, so dass sich neue Nervenfasern in der zerstörten Region bildeten, heisst es weiter.
Offenbar wird dadurch zumindest ein Teil der fehlenden Nervenverbindung im Rückenmark überbrückt, denn laut Geron war die motorische Aktivität so behandelter Ratten auch noch neun Monate nach der Zellimplantation deutlich verbessert. Versuche mit Zellkulturen hätten zudem ergeben, dass die hergestellten Oligodendrozyten-Vorläufer nur sehr wenige das Immunsystems des Menschen aktivierende Proteine auf ihrer Oberfläche trügen. Es sei also keine gravierende Abstossungsreaktion zu erwarten.
Nach wie vor viele offene Fragen
Doch viele Forscher haben Bedenken, bereits zum jetzigen Zeitpunkt derartige Zellen tatsächlich in Menschen zu implantieren. Man müsse zum Beispiel vor einer Therapie sicher sein können, dass für ein solches Implantat ausschliesslich die spezialisierten Zellen verwendet würden, mahnten viele in Lausanne anwesende Forscher. Schliesslich könnten aus embryonalen Stammzellen auch Tumore entstehen. Noch sei unbekannt, welche Einflüsse während der Zellkultur oder der Behandlung dazu führten, dass sich diese auch Teratoma genannten bösartigen Zellwucherungen bildeten. Peschanski erklärte, dass er in der Zellkultur festgestellt habe, dass aus den von ihm für Implantate vorgesehenen Nervenzellen keine Teratoma entstünden. Allerdings weiss momentan niemand ganz genau, was in einen menschlichen Organismus implantierte, nicht spezialisierte embryonale Stammzellen bewirken.
Zudem gab Oliver Brüstle, Stammzellforscher aus Bonn, zu bedenken, dass man trotz jahrelangen Tierversuchen immer noch keine Ahnung habe, was die in die Gehirne von Versuchstieren injizierten spezialisierten Zellen dort tatsächlich machten. Auch er implantiere in seinem Labor aus menschlichen embryonalen Stammzellen hergestellte spezielle Nervenzellen in Ratten mit Chorea Huntington, erläuterte er. Doch ob sich diese Zellen dort vollständig oder nur teilweise in das bestehende neuronale Netzwerk einbauten, ob sie voll funktionsfähige Kontakte mit den umgebenden Nervenzellen eingingen und tatsächlich so kommunizierten wie körpereigenen Nervenzellen, das sei alles noch unklar.
Yves-Alain Barde von der Universität Basel, der selbst gerade begonnen hat, aus menschlichen embryonalen Stammzellen Nervenzellen herzustellen und dies seit Jahren mit Mauszellen tut, ist davon überzeugt, dass man noch nicht einmal eindeutig sagen könne, was eine gute, intakte menschliche embryonale Stammzelle charakterisiere. Viele der Erfolgsmeldungen aus Tierversuchen seien eher anekdotisch als wissenschaftlich genau dokumentiert - und verstanden. Allerdings entgegnen die Befürworter einer baldigen Therapie, dass man gar nicht genau wissen müsse, was jede implantierte Zelle vor Ort tatsächlich tue. Wichtig sei vielmehr, dass die Zellimplantate sicher seien und positive medizinische Effekte bei unheilbaren Krankheiten erzielten.
Medizinisch und wissenschaftlich deutlich weiter ist man bei den adulten Stammzellen. Dies sind schon etwas spezialisierte Stammzellen, die in den verschiedenen Geweben vorkommen. Seit Jahrzehnten werden patienteneigene oder auch fremde, aber immunologisch ähnliche Blutstammzellen zum Beispiel im Rahmen von Krebstherapien eingesetzt, um das Blutsystem nach einer Chemotherapie oder einer Bestrahlung wieder aufzubauen. Adulte Stammzellen sind ethisch unbedenklich, da sie aus einem erwachsenen Organismus entnommen werden können. Zudem kann man heute bereits einigen Patienten mit aus ihren eigenen adulten Stammzellen hergestelltem Ersatzgewebe helfen. So werden etwa aus Hautstammzellen Zellrasen gezüchtet und transplantiert. Doch da es sich bei dieser gezüchteten Haut nicht um eine echte Haut handelt, fehlen Schweissdrüsen oder Haare. Vor allem bei grossflächigen Transplantationen sei dies für die Betroffenen problematisch, hiess es in Lausanne.
Bis vor kurzem dachten weltweit viele Experten sogar, dass adulte Stammzellen dereinst Therapien mit embryonalen Stammzellen überflüssig machen könnten. Eine Vielzahl von Experimenten schien zu bestätigen, dass man mit den entsprechenden Tricks - etwa Behandlungen mit ausgeklügelten Cocktails aus Wachstumsfaktoren - eine adulte Stammzelle reprogrammieren und so quasi in einen embryonalen Zustand zurückversetzen könne. Sie sollte dann auch andere Zellen als die ihres eigentlichen Gewebes herstellen. Doch diese Hoffnung sei nun vom Tisch, betonte Andreas Trumpp vom Schweizerischen Institut für experimentelle Krebsforschung am Kongress.
Zu verstärkter Aktivität anregen
Statt völlig andere Typen von Zellen hervorzubringen, produzieren implantierte adulte Stammzellen diverse therapeutisch wirksame Proteine, meint heute der Grossteil der Stammzellforscher. Vermutlich milderten oder stoppten diese Proteine dann die Entzündungen im defekten Gewebe und regten die dort vorhandenen adulten Stammzellen zur Bildung neuer Gewebezellen an. Daher steht heute im Mittelpunkt der Forschung an adulten Stammzellen, wie man diese vermutlich in allen Geweben des Körpers vorhandenen Zellen bei einer Gewebezerstörung zu verstärkter Aktivität anregen kann. Es werden auch adulte Stammzellen getestet, bei denen durch den Einbau einer intakten Kopie eines defekten Gens ein Gendefekt repariert wurde. Dies wird ganz vereinzelt zwar auch bei menschlichen embryonalen Stammzellen durchgeführt, doch diese Versuche befinden sich noch im Anfangsstadium. Hingegen sind solche mit adulten Stammzellen derart fortgeschritten, dass bereits Tiere behandelt werden. So versucht man etwa bei Hunden mit einer degenerativen Muskelerkrankung die fortschreitenden Zerstörungen im Muskelgewebe aufzuhalten. Doch noch wisse man nicht genau, wann im Verlauf der Krankheit man mit den Zellinjektionen beginnen oder wie man die Zellen behandeln müsse, damit sie sich auch tatsächlich im ganzen Muskel verteilten, erläuterte Giulio Cossu vom Stem Cell Research Institute in Mailand in Lausanne.
Hoffen auf Kombinationstherapien
Momentan gehen die Experten davon aus, dass es Therapien sowohl mit adulten als auch embryonalen Stammzellen geben wird, wobei voraussichtlich jeder Zelltyp für andere Fragestellungen und Anwendungen verwendet werden wird. Und vielleicht werden in Zukunft sogar einmal Kombinationstherapien mit beiden Sorten von Stammzellen existieren. Wie Jan Cornelissen von der Erasmus-Universität in Rotterdam am Kongress erläuterte, bilden sich nach einer Injektion von Blutstammzellen im Rahmen einer Krebstherapie zwar viele Zelltypen des Immunsystems sehr schnell. Doch da das Thymusgewebe durch die in manchen Therapien eingesetzten Bestrahlungen in der Regel schwer angegriffen sei, können sich die vom Thymus abhängigen T-Zellen oftmals erst nach ein bis zwei Jahren wieder bilden. Erste Studien mit Tieren hätten nun gezeigt, dass eine gleichzeitige Implantation von Thymusgewebe und Blutstammzellen die Regeneration des Immunsystems deutlich verbessere.
Doch da im Spital in der Regel kein passendes Thymusgewebe verfügbar sei, plädiert Cornelissen dafür, solches aus embryonalen Stammzellen herzustellen. Ihm sei gelungen, so Vorläuferzellen von Thymusgewebe zu produzieren, berichtete er. Diese habe man dann in Mäuse implantiert. Dort hätten sie sich offenbar zu Thymuszellen entwickelt und seien sogar in der Lage gewesen, die Bildung neuer T-Zellen aus implantierten Blutstammzellen zu unterstützen. Doch alle Mäuse hätten Teratoma entwickelt. Man stehe also noch ganz am Anfang dieser Art von Kombinationstherapie.
Stephanie Lahrtz
diese meldung hat gerons kurs gestern nicht gerade gut getan. geron hat für bestimmte exklusiv-lizenzen zu stammzellpatenten der university of wisconsin in vergangenheit viel geld ausgegeben. nun könnte es sein, dass diese patente nicht patentierbar waren.
das hat 2 folgen:
geron könnte die exklusive nutzung dieser patente verlieren - jedermann könnte kostenlos daran partizipieren.
geron hat geld zum fenster rausgeworfen, falls rückzahlansprüche ausgeschlossen sind (weiß ich nicht).
Agency Agrees to Review Human Stem Cell Patents
Sign In to E-Mail This Print Reprints Save
By ANDREW POLLACK
Published: October 4, 2006
The United States Patent and Trademark Office has agreed to re-examine the validity of fundamental patents on human embryonic stem cells granted to a scientist at the University of Wisconsin.
The decision, disclosed on the agency’s Web site, could lead to a narrowing or even a rescission of the three patents, which some scientists and consumer groups say are hindering research into a fledgling field that holds great medical promise.
The request for re-examination was filed in July by the Foundation for Taxpayer and Consumer Rights, a California consumer group, and the Public Patent Foundation, a New York organization advocating patent reform.
The patents are based on work by a University of Wisconsin scientist, James A. Thomson, who was the first to isolate human embryonic stem cells. The stem cells have the potential to turn into any type of tissue in the body and could one day lead to treatments for numerous diseases.
In their request for a re-examination, the consumer group and the Public Patent Foundation said Dr. Thomson’s work did not deserve patents because three scientific papers by others and one previous patent had already laid out how to derive embryonic stem cells in various animals including mice, pigs and sheep.
The patent office said the references cited in the petition raised substantial new questions about the patentability of the Wisconsin work.
Re-examinations brought about by a third party, as this one was, result in all the patent claims being canceled 12 percent of the time, said Brigid Quinn, a spokeswoman for the patent office. In another 59 percent of cases, smaller changes are made. Ms. Quinn said the patent office receives 400 to 500 requests for re-examinations each year and grants 90 percent of them.
The Wisconsin Alumni Research Foundation, or WARF, a patent licensing organization affiliated with the university, provides academic researchers with free licenses and charges them $500 for cells. Companies are charged $75,000 to $400,000, depending on their size and the terms of the license. One company, the Geron Corporation, has exclusive commercial rights to heart, nerve and pancreatic cells derived from the embryonic stem cells.
The California consumer group and some scientists say these conditions have slowed research and caused some of it to be moved offshore, since the patents apply only in the United States.
Last week, Gov. James E. Doyle of Wisconsin announced an agreement with WARF under which companies sponsoring stem cell research at academic or nonprofit research institutes in Wisconsin would get free licenses to the patents for such work. His office said that would give Wisconsin “a significant competitive advantage” over other states.
Elizabeth L. R. Donley, special counsel to WARF, said in a statement yesterday that the patents do not impede research and that the foundation had given free licenses and cells to 324 research groups. She said she was confident the validity of the patents would be affirmed.
“We believe this is a politically and financially motivated challenge, to which we will respond in the appropriate legal forum, which is the United States Patent and Trademark Office,” she said.
It could take years, however, for the patent office to finish its re-examination.
Daniel B. Ravicher, executive director of the Public Patent Foundation, said the fact that the patents are undergoing re-examination will make it harder for WARF to charge high fees. “Now WARF has lost a lot of the credibility and leverage that these patents give them,” he said.
das hat 2 folgen:
geron könnte die exklusive nutzung dieser patente verlieren - jedermann könnte kostenlos daran partizipieren.
geron hat geld zum fenster rausgeworfen, falls rückzahlansprüche ausgeschlossen sind (weiß ich nicht).
Agency Agrees to Review Human Stem Cell Patents
Sign In to E-Mail This Print Reprints Save
By ANDREW POLLACK
Published: October 4, 2006
The United States Patent and Trademark Office has agreed to re-examine the validity of fundamental patents on human embryonic stem cells granted to a scientist at the University of Wisconsin.
The decision, disclosed on the agency’s Web site, could lead to a narrowing or even a rescission of the three patents, which some scientists and consumer groups say are hindering research into a fledgling field that holds great medical promise.
The request for re-examination was filed in July by the Foundation for Taxpayer and Consumer Rights, a California consumer group, and the Public Patent Foundation, a New York organization advocating patent reform.
The patents are based on work by a University of Wisconsin scientist, James A. Thomson, who was the first to isolate human embryonic stem cells. The stem cells have the potential to turn into any type of tissue in the body and could one day lead to treatments for numerous diseases.
In their request for a re-examination, the consumer group and the Public Patent Foundation said Dr. Thomson’s work did not deserve patents because three scientific papers by others and one previous patent had already laid out how to derive embryonic stem cells in various animals including mice, pigs and sheep.
The patent office said the references cited in the petition raised substantial new questions about the patentability of the Wisconsin work.
Re-examinations brought about by a third party, as this one was, result in all the patent claims being canceled 12 percent of the time, said Brigid Quinn, a spokeswoman for the patent office. In another 59 percent of cases, smaller changes are made. Ms. Quinn said the patent office receives 400 to 500 requests for re-examinations each year and grants 90 percent of them.
The Wisconsin Alumni Research Foundation, or WARF, a patent licensing organization affiliated with the university, provides academic researchers with free licenses and charges them $500 for cells. Companies are charged $75,000 to $400,000, depending on their size and the terms of the license. One company, the Geron Corporation, has exclusive commercial rights to heart, nerve and pancreatic cells derived from the embryonic stem cells.
The California consumer group and some scientists say these conditions have slowed research and caused some of it to be moved offshore, since the patents apply only in the United States.
Last week, Gov. James E. Doyle of Wisconsin announced an agreement with WARF under which companies sponsoring stem cell research at academic or nonprofit research institutes in Wisconsin would get free licenses to the patents for such work. His office said that would give Wisconsin “a significant competitive advantage” over other states.
Elizabeth L. R. Donley, special counsel to WARF, said in a statement yesterday that the patents do not impede research and that the foundation had given free licenses and cells to 324 research groups. She said she was confident the validity of the patents would be affirmed.
“We believe this is a politically and financially motivated challenge, to which we will respond in the appropriate legal forum, which is the United States Patent and Trademark Office,” she said.
It could take years, however, for the patent office to finish its re-examination.
Daniel B. Ravicher, executive director of the Public Patent Foundation, said the fact that the patents are undergoing re-examination will make it harder for WARF to charge high fees. “Now WARF has lost a lot of the credibility and leverage that these patents give them,” he said.
Die Schweizer Stammzellenforscher legen los
In Genf werden gerade die ersten Stammzellen aus überzähligen Embryonen gewonnen. Während anderswo die Vorbereitungen für erste Tests am Menschen beginnen.
Von Anke Fossgreen, Genf
«Noch ist die Schweiz nicht in einer leitenden Position bei der Stammzellenforschung, aber sie wird es sein», sagte Ariel Ruiz Altaba von der Universität Genf selbstbewusst letzte Woche auf einer Tagung in Genf. Altaba sprach als Vertreter des neu gegründeten Schweizer Stammzellennetzwerks. «Wir brauchen eine kritische Masse an Forschern, die mit Stammzellen arbeiten», fügte Marisa Jaconi von der Universität Genf an. Eine Zusammenarbeit sei nötig. Dabei müsse ein Dialog zwischen den beteiligten Wissenschaftlern aber auch interdisziplinär stattfinden.
Seit wenigen Wochen laufen in Genf die ersten Versuche, Stammzellen aus überzähligen Embryonen herzustellen. Seit Juli dieses Jahres hat Jaconi zusammen mit ihrem Kollegen Anis Feki die Erlaubnis vom Bundesamt für Gesundheit und das Geld vom Nationalfonds, um die ersten Stammzelllinien in der Schweiz aus überzähligen Embryonen herzustellen. Und die Zeit drängt für die Forscher, denn es ist gesetzlich vorgeschrieben, dass die Embryonen, die vor 2001 bei einer künstlichen Befruchtung übrig geblieben sind, entweder für die Forschung benutzt werden können – wenn sie von den Eltern gespendet werden – oder bis 2008 zerstört werden müssen. Seit fünf Jahren dürfen keine Embryonen mehr eingefroren werden, lediglich Vorstadien.
Jaconi und Feki stehen jetzt etwa 100 Embryonen zur Verfügung, doch daraus Stammzellen zu gewinnen, ist kompliziert. «Die Herausforderung ist zurzeit, die Zellen so wachsen zu lassen, dass sie nicht mit tierischen Zellen oder tierischen Substanzen in Berührung kommen», erklärte Feki, der die Versuche zusammen mit einer Assistentin in einem speziell eingerichteten Labor am Universitätsspital Genf durchführt. Bisher wachsen die meisten Stammzelllinien auf einem Rasen aus Mäusezellen, die den Stammzellen noch unbekannte Stoffe zum Gedeihen liefern.
Outi Hovatta vom Karolinska-Institut in Stockholm hat den Weg bereitet, um Stammzellen ohne tierische Zellen zu kultivieren. Von ihr hat Feki die Technik erlernt. Hovatta hat in Schweden mit ihrem Team in den letzten vier Jahren 25 Stammzelllinien aus überzähligen Embryonen gewinnen können. Der Erfolg der Methode hänge aber von der Qualität der Embryonen ab, stellte die Forscherin fest.
Zellrasen kann Viren beherbergen
Und es gibt noch andere Schwierigkeiten: Die Zellen sollen nicht auf Mäusezellen wachsen, da sie bei späteren Therapien tierische Viren übertragen oder unerwünschte Immunreaktionen auslösen könnten. Doch auch ein Zellrasen aus menschlichen Zellen könnte gefährliche Viren beherbergen. Inzwischen ist es möglich, Stammzellen ganz ohne diese Helfer zu züchten. Dabei entwickeln aber manche von ihnen Schäden am Erbgut, den Chromosomen, haben die schwedischen Wissenschaftler entdeckt.
Für Therapien am Menschen muss jedoch sichergestellt sein, dass die Zellen einwandfrei sind. Eine EU-Richtlinie von 2003 regelt zusätzlich, unter welchen Bedingungen menschliche Zellen gezüchtet werden müssen, die transplantiert werden sollen. Die Richtlinien entsprechen der so genannten «good manufacturing practice» (GMP), die auch für die Herstellung von Arzneimitteln gilt. Am Karolinska-Institut besteht bereits ein spezielles GMP-Labor. Das ist ein Reinlabor, dessen Personal speziell geschult ist und strikt vorgegebene Arbeitsschritte einhalten muss, sodass Verunreinigungen oder Verwechslungen der Zellen vermieden werden.
Hovatta plant zusammen mit Kollegen bereits im nächsten Jahr erste klinische Versuche am Menschen: «Wir wollen zunächst etwa sechs Patienten mit einer Wirbelsäulenverletzung Nervenzellen spritzen, die wir zuvor im Labor aus den Stammzellen entwickelt haben», sagte Hovatta. Ähnliche Versuche plant auch die amerikanische Biotech-Firma Geron, die ebenfalls 2007 beginnen will, Querschnittsgelähmte zu behandeln.
Diese ersten Versuche von Therapien mit Stammzellen müssten die Forscher klar von «der dunklen Seite der Stammzelltherapien» abgrenzen, sagte Carlos Simón, Stammzellenexperte an der Universität von Valencia. Er fand im Internet zahlreiche unseriöse Angebote, die versprachen, schwere Krankheiten mit embryonalen Stammzellen zu heilen – für teures Geld.
In Genf werden gerade die ersten Stammzellen aus überzähligen Embryonen gewonnen. Während anderswo die Vorbereitungen für erste Tests am Menschen beginnen.
Von Anke Fossgreen, Genf
«Noch ist die Schweiz nicht in einer leitenden Position bei der Stammzellenforschung, aber sie wird es sein», sagte Ariel Ruiz Altaba von der Universität Genf selbstbewusst letzte Woche auf einer Tagung in Genf. Altaba sprach als Vertreter des neu gegründeten Schweizer Stammzellennetzwerks. «Wir brauchen eine kritische Masse an Forschern, die mit Stammzellen arbeiten», fügte Marisa Jaconi von der Universität Genf an. Eine Zusammenarbeit sei nötig. Dabei müsse ein Dialog zwischen den beteiligten Wissenschaftlern aber auch interdisziplinär stattfinden.
Seit wenigen Wochen laufen in Genf die ersten Versuche, Stammzellen aus überzähligen Embryonen herzustellen. Seit Juli dieses Jahres hat Jaconi zusammen mit ihrem Kollegen Anis Feki die Erlaubnis vom Bundesamt für Gesundheit und das Geld vom Nationalfonds, um die ersten Stammzelllinien in der Schweiz aus überzähligen Embryonen herzustellen. Und die Zeit drängt für die Forscher, denn es ist gesetzlich vorgeschrieben, dass die Embryonen, die vor 2001 bei einer künstlichen Befruchtung übrig geblieben sind, entweder für die Forschung benutzt werden können – wenn sie von den Eltern gespendet werden – oder bis 2008 zerstört werden müssen. Seit fünf Jahren dürfen keine Embryonen mehr eingefroren werden, lediglich Vorstadien.
Jaconi und Feki stehen jetzt etwa 100 Embryonen zur Verfügung, doch daraus Stammzellen zu gewinnen, ist kompliziert. «Die Herausforderung ist zurzeit, die Zellen so wachsen zu lassen, dass sie nicht mit tierischen Zellen oder tierischen Substanzen in Berührung kommen», erklärte Feki, der die Versuche zusammen mit einer Assistentin in einem speziell eingerichteten Labor am Universitätsspital Genf durchführt. Bisher wachsen die meisten Stammzelllinien auf einem Rasen aus Mäusezellen, die den Stammzellen noch unbekannte Stoffe zum Gedeihen liefern.
Outi Hovatta vom Karolinska-Institut in Stockholm hat den Weg bereitet, um Stammzellen ohne tierische Zellen zu kultivieren. Von ihr hat Feki die Technik erlernt. Hovatta hat in Schweden mit ihrem Team in den letzten vier Jahren 25 Stammzelllinien aus überzähligen Embryonen gewinnen können. Der Erfolg der Methode hänge aber von der Qualität der Embryonen ab, stellte die Forscherin fest.
Zellrasen kann Viren beherbergen
Und es gibt noch andere Schwierigkeiten: Die Zellen sollen nicht auf Mäusezellen wachsen, da sie bei späteren Therapien tierische Viren übertragen oder unerwünschte Immunreaktionen auslösen könnten. Doch auch ein Zellrasen aus menschlichen Zellen könnte gefährliche Viren beherbergen. Inzwischen ist es möglich, Stammzellen ganz ohne diese Helfer zu züchten. Dabei entwickeln aber manche von ihnen Schäden am Erbgut, den Chromosomen, haben die schwedischen Wissenschaftler entdeckt.
Für Therapien am Menschen muss jedoch sichergestellt sein, dass die Zellen einwandfrei sind. Eine EU-Richtlinie von 2003 regelt zusätzlich, unter welchen Bedingungen menschliche Zellen gezüchtet werden müssen, die transplantiert werden sollen. Die Richtlinien entsprechen der so genannten «good manufacturing practice» (GMP), die auch für die Herstellung von Arzneimitteln gilt. Am Karolinska-Institut besteht bereits ein spezielles GMP-Labor. Das ist ein Reinlabor, dessen Personal speziell geschult ist und strikt vorgegebene Arbeitsschritte einhalten muss, sodass Verunreinigungen oder Verwechslungen der Zellen vermieden werden.
Hovatta plant zusammen mit Kollegen bereits im nächsten Jahr erste klinische Versuche am Menschen: «Wir wollen zunächst etwa sechs Patienten mit einer Wirbelsäulenverletzung Nervenzellen spritzen, die wir zuvor im Labor aus den Stammzellen entwickelt haben», sagte Hovatta. Ähnliche Versuche plant auch die amerikanische Biotech-Firma Geron, die ebenfalls 2007 beginnen will, Querschnittsgelähmte zu behandeln.
Diese ersten Versuche von Therapien mit Stammzellen müssten die Forscher klar von «der dunklen Seite der Stammzelltherapien» abgrenzen, sagte Carlos Simón, Stammzellenexperte an der Universität von Valencia. Er fand im Internet zahlreiche unseriöse Angebote, die versprachen, schwere Krankheiten mit embryonalen Stammzellen zu heilen – für teures Geld.
hmmm. tolle outperformance zum wochenschluss
mich hat die action von heute und gestern doch etwas überrascht. es sieht ganz danach aus, als dass der kurs in das letzte kapitel einer größeren w-formation einschwenkt, wobei sich aktuell der zweite aufstrich ausbilden könnte. dann könnte der 2. dip, der vor 2 tagen intraday formiert wurde, höher sein als der 1., der vor einiger zeit das absolute jahrestief markierte. dieser höhere 2. dip würde gut zu einem turn around ins bild passen.
mal sehen. geron müssten mittlerweile die ersten starken indizien vorliegen, ob grn163l wirkt und sicher ist. das zweitere ist wahrscheinlich der fall, was man aus der tatsache ablesen kann, dass geron den test bislang nicht abbrechen musste (was meldepflichtig gewesen wäre).
können wir hoffen, dass sich allles weiter positiv entwickelt...
nice weekend
luckycat.
mich hat die action von heute und gestern doch etwas überrascht. es sieht ganz danach aus, als dass der kurs in das letzte kapitel einer größeren w-formation einschwenkt, wobei sich aktuell der zweite aufstrich ausbilden könnte. dann könnte der 2. dip, der vor 2 tagen intraday formiert wurde, höher sein als der 1., der vor einiger zeit das absolute jahrestief markierte. dieser höhere 2. dip würde gut zu einem turn around ins bild passen.
mal sehen. geron müssten mittlerweile die ersten starken indizien vorliegen, ob grn163l wirkt und sicher ist. das zweitere ist wahrscheinlich der fall, was man aus der tatsache ablesen kann, dass geron den test bislang nicht abbrechen musste (was meldepflichtig gewesen wäre).
können wir hoffen, dass sich allles weiter positiv entwickelt...
nice weekend
luckycat.
Dunkle Wolken über restlicher Amtszeit KTM 950 08.10.06 15:54
Bush
Dunkle Wolken über restlicher Amtszeit
Sex-Skandal im Kongress könnte Republikaner die Mehrheit kosten - Führung unter Druck
Washington - Über den letzten beiden Jahren der Amtszeit von US-Präsident George W. Bush liegen dunkle Wolken. Denn die Stimmung im Land wendet sich immer mehr gegen die Regierung. Da ist vor allem der Irak-Krieg, der immer unpopulärer wird, und dann erschüttert jetzt auch noch ein Sex-Skandal die Republikaner, was der Partei von Bush bei den Wahlen am 7. November möglicherweise die Mehrheit in beiden Häusern des Kongresses kosten könnte.
Viele Republikaner sind unzufrieden damit, wie Parlamentspräsident David Hastert und andere Politiker in dieser Krise reagierten - einige äußern dies schon öffentlich, die meisten aber nur privat. Die Strategen der Republikaner befürchten nun, dass die Demokraten, die 1994 die Mehrheit im Kongress verloren, die Regierung in den nächsten beiden Jahren mit Untersuchungsausschüssen, Vorladungen und Ähnlichem ständig unter Druck setzen. "Das würde ihnen großen Spaß machen und es würde sehr stark ablenken", sagt Charles Black, ein langjähriger republikanischer Stratege mit guten Beziehungen ins Weiße Haus.
Text zur Anzeige gekürzt. Gesamtes Posting anzeigen...
"Die Kontrolle über das Repräsentantenhaus stand schon vorher auf dem Spiel, bevor das mit Foley passierte", räumt Black ein. Der republikanische Abgeordnete Mark Foley legte in der vergangenen Woche sein Amt nieder, nachdem bekannt geworden war, das er sexuell anstößige E-Mails an einige jugendliche Helfer im Kongress geschickt hatte. "Wenn die Demokraten das Repräsentantenhaus erobern, dann wird es die Regierung weit schwerer haben, ihre Vorstellung durchzubringen", sagt Black.
Bei der Wahl werden alle 435 Abgeordneten des Repräsentantenhauses, 33 der 100 Senatoren sowie 38 der 50 Gouverneure der US-Staaten gewählt. Dabei konnte sich Bush in der Vergangenheit sogar mehr auf die Mehrheit im Repräsentantenhaus verlassen, wo Hastert die Fäden fest in der Hand hielt, als auf die Senatoren seiner Partei, von denen sich einige öfters auch gegen ihn stellten. Trotzdem tat das Weiße Haus in jüngster Zeit auffällig wenig, um Hastert zu stützen, von einigen öffentlichen Erklärungen Bushs und seines Vizes Dick Cheney einmal abgesehen.
Der Skandal im Kongress könnte sich nach Einschätzung der republikanischen Strategen auch negativ auf die Beteiligung an der Wahl auswirken, besonders was die konservative weiße Basis der Partei betrifft. "Wir verstehen, dass die Menschen deswegen besorgt sind", sagt Tony Snow, der Sprecher des Weißen Hauses. "Natürlich sind sie besorgt, das ist doch abscheulich."
Der Skandal kommt für die Republikaner, zu einem denkbar schlechten Zeitpunkt. Der Widerstand gegen den Irak-Krieg wächst und auch sonst schwindet, das Vertrauen in die politische Führung durch die Republikaner. Einige üben sich aber auch in Galgenhumor und verweisen darauf, dass dadurch wenigstens das neue Buch von Starreporter Bob Woodward von den Titelseiten der Zeitungen verschwunden ist. Es porträtiert Bush als völlig unbeweglich in der Verteidigung des Kriegs im Irak und seine Berater als völlig zerstritten.
Der republikanische Berater Rich Galen sieht die Wahl aber noch keineswegs entschieden. Er verweist dabei auf 1998 und Skandal um Präsident Bill Clinton und die Praktikantin Monica Lewinsky im Weißen Haus. "Wir haben uns schon die Hände gerieben, als die Demokraten jeden Tag über Monica und Bill redeten", sagt Galen. "Und, was passierte? Wir mussten bei den Wahlen Verluste hinnehmen. Es ist immer schwierig, die Zukunft aus gegenwärtigen Ereignissen vorherzusagen", sagt Galen. "Wenn etwas so heiß brennt, wie das jetzt, dann kann es auch ganz schnell vorbei sein."
AP
Bush
Dunkle Wolken über restlicher Amtszeit
Sex-Skandal im Kongress könnte Republikaner die Mehrheit kosten - Führung unter Druck
Washington - Über den letzten beiden Jahren der Amtszeit von US-Präsident George W. Bush liegen dunkle Wolken. Denn die Stimmung im Land wendet sich immer mehr gegen die Regierung. Da ist vor allem der Irak-Krieg, der immer unpopulärer wird, und dann erschüttert jetzt auch noch ein Sex-Skandal die Republikaner, was der Partei von Bush bei den Wahlen am 7. November möglicherweise die Mehrheit in beiden Häusern des Kongresses kosten könnte.
Viele Republikaner sind unzufrieden damit, wie Parlamentspräsident David Hastert und andere Politiker in dieser Krise reagierten - einige äußern dies schon öffentlich, die meisten aber nur privat. Die Strategen der Republikaner befürchten nun, dass die Demokraten, die 1994 die Mehrheit im Kongress verloren, die Regierung in den nächsten beiden Jahren mit Untersuchungsausschüssen, Vorladungen und Ähnlichem ständig unter Druck setzen. "Das würde ihnen großen Spaß machen und es würde sehr stark ablenken", sagt Charles Black, ein langjähriger republikanischer Stratege mit guten Beziehungen ins Weiße Haus.
Text zur Anzeige gekürzt. Gesamtes Posting anzeigen...
"Die Kontrolle über das Repräsentantenhaus stand schon vorher auf dem Spiel, bevor das mit Foley passierte", räumt Black ein. Der republikanische Abgeordnete Mark Foley legte in der vergangenen Woche sein Amt nieder, nachdem bekannt geworden war, das er sexuell anstößige E-Mails an einige jugendliche Helfer im Kongress geschickt hatte. "Wenn die Demokraten das Repräsentantenhaus erobern, dann wird es die Regierung weit schwerer haben, ihre Vorstellung durchzubringen", sagt Black.
Bei der Wahl werden alle 435 Abgeordneten des Repräsentantenhauses, 33 der 100 Senatoren sowie 38 der 50 Gouverneure der US-Staaten gewählt. Dabei konnte sich Bush in der Vergangenheit sogar mehr auf die Mehrheit im Repräsentantenhaus verlassen, wo Hastert die Fäden fest in der Hand hielt, als auf die Senatoren seiner Partei, von denen sich einige öfters auch gegen ihn stellten. Trotzdem tat das Weiße Haus in jüngster Zeit auffällig wenig, um Hastert zu stützen, von einigen öffentlichen Erklärungen Bushs und seines Vizes Dick Cheney einmal abgesehen.
Der Skandal im Kongress könnte sich nach Einschätzung der republikanischen Strategen auch negativ auf die Beteiligung an der Wahl auswirken, besonders was die konservative weiße Basis der Partei betrifft. "Wir verstehen, dass die Menschen deswegen besorgt sind", sagt Tony Snow, der Sprecher des Weißen Hauses. "Natürlich sind sie besorgt, das ist doch abscheulich."
Der Skandal kommt für die Republikaner, zu einem denkbar schlechten Zeitpunkt. Der Widerstand gegen den Irak-Krieg wächst und auch sonst schwindet, das Vertrauen in die politische Führung durch die Republikaner. Einige üben sich aber auch in Galgenhumor und verweisen darauf, dass dadurch wenigstens das neue Buch von Starreporter Bob Woodward von den Titelseiten der Zeitungen verschwunden ist. Es porträtiert Bush als völlig unbeweglich in der Verteidigung des Kriegs im Irak und seine Berater als völlig zerstritten.
Der republikanische Berater Rich Galen sieht die Wahl aber noch keineswegs entschieden. Er verweist dabei auf 1998 und Skandal um Präsident Bill Clinton und die Praktikantin Monica Lewinsky im Weißen Haus. "Wir haben uns schon die Hände gerieben, als die Demokraten jeden Tag über Monica und Bill redeten", sagt Galen. "Und, was passierte? Wir mussten bei den Wahlen Verluste hinnehmen. Es ist immer schwierig, die Zukunft aus gegenwärtigen Ereignissen vorherzusagen", sagt Galen. "Wenn etwas so heiß brennt, wie das jetzt, dann kann es auch ganz schnell vorbei sein."
AP
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10Langfristige Trendwende ist da
 plus 6,65%
plus 6,65%

 plus 6,65%
plus 6,65%
Antwort auf Beitrag Nr.: 24.661.096 von meislo am 16.10.06 16:54:29Sehe ich auch so, werde nochmals nachkaufen

Antwort auf Beitrag Nr.: 24.664.002 von cyberhai am 16.10.06 18:49:23GRN163L bringt's!!!
warum würden denn sonst eine ehemalige amgen-kapazität zu geron wechseln??? der weiß doch mehr!! nämlich, dass das produkt und demnach er groß rauskommen wird - nicht nur finanziell.
Geron Appoints Alan Colowick as President, Oncology
MENLO PARK, Calif., Oct 16, 2006 (BUSINESS WIRE) -- Geron Corporation
Last: 7.59+0.60+8.58%
2:42pm 10/16/2006
GERN (7.59, +0.60, +8.6%) announced today the appointment of Alan B. Colowick, M.D., M.P.H., as president, oncology.
In this newly created position, Dr. Colowick, 44, will manage the operational and strategic activities of the company's oncology programs. He will report to Dr. Thomas Okarma, Geron's president and CEO.
"Alan has a proven track record in bringing oncology products to the market successfully," said Dr. Okarma. "We've launched an ambitious program to advance our telomerase inhibitor drug, GRN163L, and our telomerase cancer vaccine, GRNVAC1, through the clinic. Alan's experience and expertise in all facets of oncology product development will enhance our strategic decision-making and accelerate our progress."
Dr. Colowick commented, "I am delighted with the opportunity to help develop Geron's exciting cancer product portfolio. Telomerase is an important, validated cancer target that is expressed across a wide variety of cancer types. Geron's inhibitor drug and dendritic cell vaccine elegantly target telomerase in complementary ways, enhancing the likelihood of clinical success. I look forward to working with the Geron team."
Prior to joining Geron, Dr. Colowick was the chief medical officer of Threshold Pharmaceuticals Inc., where he was responsible for all aspects of non-clinical and clinical development and manufacturing.
Before this, he held a wide range of positions with Amgen Inc. Most recently, he served as vice president of European Medical Affairs, where he was responsible for all products in multiple therapeutic areas, including hematology/oncology, nephrology and internal medicine. Earlier in his career with Amgen, Dr. Colowick directed the team responsible for leading the company's successful registration and launch of the drug, Aranesp(R), in the United States, European Union and Australia.
Dr. Colowick was a clinical and research fellow in hematology-oncology at Harvard University and the Dana Farber Cancer Institute. He earned his M.P.H. at the Harvard School of Public Health and his M.D. at Stanford University School of Medicine.
heute doppelter trendbruch ohne gap!!
durchbruch der 200 tage linie nach oben
massiver durchbruch des abwärtstrendkanals nach oben.
der weg nach oben ist frei, die guten nachrichten werden kommen.
evtl. abwarten, bis der kurs die seit gestern gemachten +13% zur hälfte wieder korrigiert.
luckycat.
warum würden denn sonst eine ehemalige amgen-kapazität zu geron wechseln??? der weiß doch mehr!! nämlich, dass das produkt und demnach er groß rauskommen wird - nicht nur finanziell.
Geron Appoints Alan Colowick as President, Oncology
MENLO PARK, Calif., Oct 16, 2006 (BUSINESS WIRE) -- Geron Corporation
Last: 7.59+0.60+8.58%
2:42pm 10/16/2006
GERN (7.59, +0.60, +8.6%) announced today the appointment of Alan B. Colowick, M.D., M.P.H., as president, oncology.
In this newly created position, Dr. Colowick, 44, will manage the operational and strategic activities of the company's oncology programs. He will report to Dr. Thomas Okarma, Geron's president and CEO.
"Alan has a proven track record in bringing oncology products to the market successfully," said Dr. Okarma. "We've launched an ambitious program to advance our telomerase inhibitor drug, GRN163L, and our telomerase cancer vaccine, GRNVAC1, through the clinic. Alan's experience and expertise in all facets of oncology product development will enhance our strategic decision-making and accelerate our progress."
Dr. Colowick commented, "I am delighted with the opportunity to help develop Geron's exciting cancer product portfolio. Telomerase is an important, validated cancer target that is expressed across a wide variety of cancer types. Geron's inhibitor drug and dendritic cell vaccine elegantly target telomerase in complementary ways, enhancing the likelihood of clinical success. I look forward to working with the Geron team."
Prior to joining Geron, Dr. Colowick was the chief medical officer of Threshold Pharmaceuticals Inc., where he was responsible for all aspects of non-clinical and clinical development and manufacturing.
Before this, he held a wide range of positions with Amgen Inc. Most recently, he served as vice president of European Medical Affairs, where he was responsible for all products in multiple therapeutic areas, including hematology/oncology, nephrology and internal medicine. Earlier in his career with Amgen, Dr. Colowick directed the team responsible for leading the company's successful registration and launch of the drug, Aranesp(R), in the United States, European Union and Australia.
Dr. Colowick was a clinical and research fellow in hematology-oncology at Harvard University and the Dana Farber Cancer Institute. He earned his M.P.H. at the Harvard School of Public Health and his M.D. at Stanford University School of Medicine.
heute doppelter trendbruch ohne gap!!
durchbruch der 200 tage linie nach oben
massiver durchbruch des abwärtstrendkanals nach oben.
der weg nach oben ist frei, die guten nachrichten werden kommen.
evtl. abwarten, bis der kurs die seit gestern gemachten +13% zur hälfte wieder korrigiert.
luckycat.
warum würden denn sonst eine ehemalige amgen-kapazität zu geron wechseln???
Weil der erst 44 ist und richtig karriere machen will

stochastics schon sehr weit oben.
korrektur steht an
Weil der erst 44 ist und richtig karriere machen will


stochastics schon sehr weit oben.
korrektur steht an
Antwort auf Beitrag Nr.: 24.667.317 von meislo am 16.10.06 21:16:49Wenn bush die Kongresswahlen verliert und vieles sieht danach aus
werden stammzellenfirmen ein comeback erleben.
werden stammzellenfirmen ein comeback erleben.

bush go home.
das wars, die reps werden die kongresswahlen verlieren - der anfang vom ende von bush präsidentschaft.
gute stammzellaussichten
das wars, die reps werden die kongresswahlen verlieren - der anfang vom ende von bush präsidentschaft.
gute stammzellaussichten

Geron Announces Conference Call to Discuss Financial Results for the 2006 Third Quarter
Friday October 27, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq: GERN - News) will announce its financial results for the three and nine months ended September 30, 2006, on Monday, October 30, 2006, prior to the opening of the equity market. Thomas B. Okarma, Ph.D., M.D., Geron's chief executive officer, and David L. Greenwood, Geron's chief financial officer, will host a conference call for analysts and investors following the announcement at 8 a.m. PST/11 a.m. EST.
ADVERTISEMENT
Participants can access the conference call live via telephone by dialing 866-831-6267 (U.S.) or 617-213-8857 (international). The passcode is 12545730. A live audio-only Webcast is also available through a link that is posted on the Conferences page in the Investor Relations section of Geron's Website at http://www.geron.com. The audio web broadcast of the conference call will be available for replay through November 30, 2006.
Geron is a Menlo Park, Calif.-based biopharmaceutical company that is developing and intends to commercialize first-in-class therapeutic products for the treatment of cancer and degenerative diseases, including spinal cord injury, heart failure, diabetes and HIV/AIDS. The products are based on Geron's core expertise in telomerase and human embryonic stem cells. For more information, visit www.geron.com.
Friday October 27, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq: GERN - News) will announce its financial results for the three and nine months ended September 30, 2006, on Monday, October 30, 2006, prior to the opening of the equity market. Thomas B. Okarma, Ph.D., M.D., Geron's chief executive officer, and David L. Greenwood, Geron's chief financial officer, will host a conference call for analysts and investors following the announcement at 8 a.m. PST/11 a.m. EST.
ADVERTISEMENT
Participants can access the conference call live via telephone by dialing 866-831-6267 (U.S.) or 617-213-8857 (international). The passcode is 12545730. A live audio-only Webcast is also available through a link that is posted on the Conferences page in the Investor Relations section of Geron's Website at http://www.geron.com. The audio web broadcast of the conference call will be available for replay through November 30, 2006.
Geron is a Menlo Park, Calif.-based biopharmaceutical company that is developing and intends to commercialize first-in-class therapeutic products for the treatment of cancer and degenerative diseases, including spinal cord injury, heart failure, diabetes and HIV/AIDS. The products are based on Geron's core expertise in telomerase and human embryonic stem cells. For more information, visit www.geron.com.
Wahlkämpfer setzen auf schmutzige Tricks
Je näher der Wahltermin rückt, umso heimtückischer wird der Kampf um die Stimmen: Die Kandidaten für den US-Kongress lassen alle Anstandsregeln fallen. Politiker sehen sich plötzlich als Kunden von Prostituierten und Sex-Hotlines dargestellt - oder als Freunde von Massenmördern.
Washington - "Ron Kind bezahlt für Sex" - dieser Slogan schmückt nach einem Bericht der "Washington Post" seit kurzem Wahlplakate im US-Staat Wisconsin. Kleben lassen hat sie der Republikaner Paul R. Nelson, Kandidat der Republikaner für einen Sitz im Kongress. Er ließ dem Konterfei seines demokratischen Kontrahenten Ron Kind zudem ein Schriftzug mit den Buchstaben "XXX" übers Gesicht drucken - dem Kürzel für nicht jugendfreie Inhalte.
AP
Kapitol in Washington: Kampf mit harten Bandagen
Der Hintergrund der Schmutzkampagne: Der Demokrat Kind widersetzt sich Forderungen, dem nationalen Gesundheitsinstitut in Zukunft kein Geld mehr für die Erforschung des sexuellen Verhaltens der Amerikaner zu geben. Die freche Folgerung von Nelson - Kind bezahlt für Sex.
Nelson schreibt seinem Kontrahenten außerdem noch zu, dieser wolle "illegalen Ausländern erlauben, die amerikanische Flagge zu verbrennen" und "zulassen, dass verurteilte Kinderschänder ins Land kommen". Nach seiner eigenen Ansicht wahrt der Republikaner trotz solcher Zuschreibungen die Grenzen des guten Geschmacks: "Negative Wahlwerbung heißt, auf üble Weise persönlich zu attackieren. Das hier ist überhaupt nicht persönlich gemeint."
Niveau sinkt ins Bodenlose
Kurz vor der Entscheidung, so die Analyse der "Washington Post", sinkt das Niveau des Wahlkampfes ins Bodenlose. Verzweifelte Kandidaten versuchen alles, um die Konkurrenten zu beschädigen. Sie unterstellen ihnen beispielsweise moralisches Fehlverhalten und sexuelle Perversion. Blogs und Websites helfen, den Schmutz in alle Winkel des Landes zu tragen. Die Kandidaten halten sich dabei meist von der eigentlichen Drecksarbeit fern: Diese erledigen Unterstützergruppen.
Shanto Iyengar, Politik-Professor in Stanford, sagt der "Washington Post": "Je negativer die Wahlwerbung ist, desto wahrscheinlicher berichten Medien darüber. Also ist der Anreiz groß, in die Extreme zu gehen."
Insbesondere die Republikaner, so die "Washington Post", sind nicht zimperlich, wenn es darum geht, das derzeit für die eigene Partei negative Meinungsklima zu beeinflussen: Die Wahlkampf-Zentrale der Republikaner gebe derzeit 90 Prozent des Werbebudgets für negative Wahlwerbung aus.
In New York unterstellten die Republikaner beispielsweise dem demokratischen Kandidaten Michael A. Arcuri, er verschwende Steuergelder für Telefonsex. Hintergrund der Attacke: Ein Mitarbeiter Arcuris hatte sich verwählt, als er eine offizielle Stelle anrufen wollten und war bei einer Sex-Hotline gelandet, die eine fast identische Nummer hatte. Kosten des Zahlendrehers für den Steuerzahler: 1 Dollar und 25 Cent.
Hauptargument der Demokraten: der Irak-Krieg
In Ohio wollten die Republikaner die Wähler glauben machen, der demokratische Kandidat sei nicht bereit, Sex mit Kindern zu verurteilen. In Wisconsin rückte man den Kandidaten in die Nähe eines verurteilten Massenmörders. In Tennessee wurde dem Demokraten Harold E. Ford Jr. vorgehalten, er habe eine vom "Playboy" gesponserte Super-Bowl-Party besucht - und er wolle außerdem Abtreibungspillen an Schüler verteilen.
Auch die Demokraten kämpfen mit harten Bandagen, konzentrieren sich jedoch vor allem auf Präsident Bush und dessen unpopulären Krieg im Irak. Eine erfolgversprechende Strategie, denn zwei Drittel der Wähler sind inzwischen der Meinung, dass die derzeitige Irak-Politik falsch ist. Der dauernde Hinweis auf die Probleme im Irak, so die Hoffnung der Demokraten, soll republikanische Wähler davon abhalten, am 7. November zur Urne zu gehen.
Der demokratische Senator von Wisconsin, Ron Kind, sagt zu der Schmutzkampagne: "Es ist ein verrücktes System, und es wird jedes Jahr schlimmer. Wir reißen einander in Stücke, und dann sollen wir alle nach Washington zurückkommen und dort zusammenarbeiten. Das ist ein höllischer Weg, Volksvertreter auszuwählen."
Je näher der Wahltermin rückt, umso heimtückischer wird der Kampf um die Stimmen: Die Kandidaten für den US-Kongress lassen alle Anstandsregeln fallen. Politiker sehen sich plötzlich als Kunden von Prostituierten und Sex-Hotlines dargestellt - oder als Freunde von Massenmördern.
Washington - "Ron Kind bezahlt für Sex" - dieser Slogan schmückt nach einem Bericht der "Washington Post" seit kurzem Wahlplakate im US-Staat Wisconsin. Kleben lassen hat sie der Republikaner Paul R. Nelson, Kandidat der Republikaner für einen Sitz im Kongress. Er ließ dem Konterfei seines demokratischen Kontrahenten Ron Kind zudem ein Schriftzug mit den Buchstaben "XXX" übers Gesicht drucken - dem Kürzel für nicht jugendfreie Inhalte.
AP
Kapitol in Washington: Kampf mit harten Bandagen
Der Hintergrund der Schmutzkampagne: Der Demokrat Kind widersetzt sich Forderungen, dem nationalen Gesundheitsinstitut in Zukunft kein Geld mehr für die Erforschung des sexuellen Verhaltens der Amerikaner zu geben. Die freche Folgerung von Nelson - Kind bezahlt für Sex.
Nelson schreibt seinem Kontrahenten außerdem noch zu, dieser wolle "illegalen Ausländern erlauben, die amerikanische Flagge zu verbrennen" und "zulassen, dass verurteilte Kinderschänder ins Land kommen". Nach seiner eigenen Ansicht wahrt der Republikaner trotz solcher Zuschreibungen die Grenzen des guten Geschmacks: "Negative Wahlwerbung heißt, auf üble Weise persönlich zu attackieren. Das hier ist überhaupt nicht persönlich gemeint."
Niveau sinkt ins Bodenlose
Kurz vor der Entscheidung, so die Analyse der "Washington Post", sinkt das Niveau des Wahlkampfes ins Bodenlose. Verzweifelte Kandidaten versuchen alles, um die Konkurrenten zu beschädigen. Sie unterstellen ihnen beispielsweise moralisches Fehlverhalten und sexuelle Perversion. Blogs und Websites helfen, den Schmutz in alle Winkel des Landes zu tragen. Die Kandidaten halten sich dabei meist von der eigentlichen Drecksarbeit fern: Diese erledigen Unterstützergruppen.
Shanto Iyengar, Politik-Professor in Stanford, sagt der "Washington Post": "Je negativer die Wahlwerbung ist, desto wahrscheinlicher berichten Medien darüber. Also ist der Anreiz groß, in die Extreme zu gehen."
Insbesondere die Republikaner, so die "Washington Post", sind nicht zimperlich, wenn es darum geht, das derzeit für die eigene Partei negative Meinungsklima zu beeinflussen: Die Wahlkampf-Zentrale der Republikaner gebe derzeit 90 Prozent des Werbebudgets für negative Wahlwerbung aus.
In New York unterstellten die Republikaner beispielsweise dem demokratischen Kandidaten Michael A. Arcuri, er verschwende Steuergelder für Telefonsex. Hintergrund der Attacke: Ein Mitarbeiter Arcuris hatte sich verwählt, als er eine offizielle Stelle anrufen wollten und war bei einer Sex-Hotline gelandet, die eine fast identische Nummer hatte. Kosten des Zahlendrehers für den Steuerzahler: 1 Dollar und 25 Cent.
Hauptargument der Demokraten: der Irak-Krieg
In Ohio wollten die Republikaner die Wähler glauben machen, der demokratische Kandidat sei nicht bereit, Sex mit Kindern zu verurteilen. In Wisconsin rückte man den Kandidaten in die Nähe eines verurteilten Massenmörders. In Tennessee wurde dem Demokraten Harold E. Ford Jr. vorgehalten, er habe eine vom "Playboy" gesponserte Super-Bowl-Party besucht - und er wolle außerdem Abtreibungspillen an Schüler verteilen.
Auch die Demokraten kämpfen mit harten Bandagen, konzentrieren sich jedoch vor allem auf Präsident Bush und dessen unpopulären Krieg im Irak. Eine erfolgversprechende Strategie, denn zwei Drittel der Wähler sind inzwischen der Meinung, dass die derzeitige Irak-Politik falsch ist. Der dauernde Hinweis auf die Probleme im Irak, so die Hoffnung der Demokraten, soll republikanische Wähler davon abhalten, am 7. November zur Urne zu gehen.
Der demokratische Senator von Wisconsin, Ron Kind, sagt zu der Schmutzkampagne: "Es ist ein verrücktes System, und es wird jedes Jahr schlimmer. Wir reißen einander in Stücke, und dann sollen wir alle nach Washington zurückkommen und dort zusammenarbeiten. Das ist ein höllischer Weg, Volksvertreter auszuwählen."
Geron Corporation Reports 2006 Third Quarter Financial Results and Events
Monday October 30, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq: GERN - News) today reported financial results for the three and nine months ended September 30, 2006.
ADVERTISEMENT
For the third quarter of 2006, the company reported a net loss of $9.8 million or $(0.15) per share compared to $11.9 million or $(0.21) per share for the same period in 2005. Net loss for the first nine months of 2006 was $28.1 million or $(0.43) per share compared to $24.6 million or $(0.44) per share for the same period in 2005.
Revenues for the third quarter of 2006 were $723,000 compared to $673,000 for the comparable period in 2005. Revenues for the first nine months of 2006 were $2.1 million compared to $5.4 million for the comparable period in 2005. The Company receives royalty and license fee revenue from various license agreements with companies involved with oncology, diagnostics, research tools and agriculture and revenues from collaborative agreements, including joint ventures. Revenues for the first nine months of 2005 were higher than 2006 reflecting the receipt of an upfront payment of $4.0 million in conjunction with the transfer of intellectual property rights related to nuclear transfer for use in animal cloning to the Company's joint venture, Start Licensing, Inc.
Operating expenses for the third quarter of 2006 were $12.8 million compared to $13.6 million for the comparable period in 2005. Research and development expenses for the third quarter of 2006 were $10.7 million compared to $12.2 million for the comparable 2005 period. Net expense for research and development decreased due to reduced raw materials purchases for the manufacture of Geron's telomerase inhibitor drug, GRN163L, offset by higher personnel-related costs, including the recognition of compensation expense related to stock option grants. General and administrative expenses for the third quarter of 2006 were $2.1 million compared to $1.4 million for the comparable 2005 period. The increase in general and administrative expenses in the third quarter of 2006 was primarily due to the recognition of compensation expense related to stock option grants.
Operating expenses for the first nine months of 2006 were $36.5 million compared to $32.6 million for the comparable period in 2005. Research and development expenses for the first nine months of 2006 were $29.4 million compared to $25.5 million for the comparable 2005 period. Overall research and development expenses increased in 2006 as a result of higher personnel-related costs, including the recognition of compensation expense related to stock option grants, and increased manufacturing costs related to the telomerase cancer vaccine, GRNVAC1, offset by reduced raw materials purchases for the manufacture of GRN163L. General and administrative expenses for the first nine months of 2006 and 2005 were each $7.1 million due to recognition of compensation expense related to stock option grants, offset by reduced consulting expense.
Third Quarter 2006 Highlights:
Clinical Development
Geron scientists and collaborators presented new data at the International Society for Stem Cell Research's (ISSCR) annual meeting pertaining to four products in development: (1) GRNOPC1, Oligodendroglial Progenitor Cells for acute spinal cord injury; (2) GRNIC1, Islet Clusters for diabetes; (3) GRNCM1, Cardiomyocytes for myocardial infarction and (4) osteoprogenitor cells for bone fractures and osteoporosis. In addition, several presentations at the meeting described advances in human embryonic stem cell (hESC) culture and derivation techniques and further characterization of hESC-derived hepatocytes for liver failure and drug metabolism testing.
An article describing novel chemical methods that reduce the number of chemical steps and cost of synthesizing the monomer building blocks of Geron's patented N3'-P5' thiophosphoramidate oligonucleotide compounds, including its lead anti-cancer drug, GRN163L, was published in Tetrahedron Letters.
Preclinical studies published in Regenerative Medicine support the safety and utility of GRNOPC1, Geron's lead hESC-based therapeutic product for the treatment of spinal cord injury. The studies demonstrated that when GRNOPC1 is injected into the lesion site of rats that received either very mild or moderate spinal cord contusion injuries, GRNOPC1 survived in both mild and moderate lesion sites, with broader distribution of transplanted cells and robust remyelination in the more severe injuries, replicating previous studies.
New data supporting the development of TAT0002, a small molecule telomerase activator for the treatment of HIV/AIDS, was presented at the XVI International AIDS Conference. The data confirm and extend earlier findings that TAT0002 enhances the function of key immune cells from HIV/AIDS donors.
Intellectual Property
The U.S. District Court for the District of Columbia dismissed appeals of two patent interference decisions pending before them regarding patents covering nuclear transfer (cloning) technology. Geron acquired rights to this technology from the Roslin Institute in 1999 and subsequently initiated patent interferences with conflicting patents held by the University of Massachusetts. The Board of Patent Appeals and Interferences of the U.S. Patent Office ruled in favor of Geron on all counts in both interference proceedings, and the University of Massachusetts and its licensee, Advanced Cell Technology (ACT), filed appeals. Both of those appeals by the University of Massachusetts and ACT have now been dismissed with prejudice.
Business Development
Geron and the University of Edinburgh entered into a collaboration to conduct preclinical safety and efficacy studies with three cell types derived from hESCs. The cell types are hepatocytes for the treatment of liver failure, and osteoblasts and chondrocytes for the treatment of musculoskeletal disorders, including osteoarthritis, bone fractures and osteoporosis.
Conference Call
Today at 8:00 a.m. PST / 11:00 a.m. EST, Thomas B. Okarma, Ph.D., M.D., Geron's chief executive officer, and David L. Greenwood, Geron's chief financial officer, will host a conference call to discuss the Company's third quarter and year to date results.
Participants can access the conference call live via telephone by dialing 866-831-6267 (U.S.) or 617-213-8857 (international). The passcode is 12545730. A live audio-only webcast is also available through a link that is posted on the Conferences page in the Investor Relations section of Geron's Website at http://www.geron.com. The audio web broadcast of the conference call will be available for replay through November 30, 2006.
Monday October 30, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq: GERN - News) today reported financial results for the three and nine months ended September 30, 2006.
ADVERTISEMENT
For the third quarter of 2006, the company reported a net loss of $9.8 million or $(0.15) per share compared to $11.9 million or $(0.21) per share for the same period in 2005. Net loss for the first nine months of 2006 was $28.1 million or $(0.43) per share compared to $24.6 million or $(0.44) per share for the same period in 2005.
Revenues for the third quarter of 2006 were $723,000 compared to $673,000 for the comparable period in 2005. Revenues for the first nine months of 2006 were $2.1 million compared to $5.4 million for the comparable period in 2005. The Company receives royalty and license fee revenue from various license agreements with companies involved with oncology, diagnostics, research tools and agriculture and revenues from collaborative agreements, including joint ventures. Revenues for the first nine months of 2005 were higher than 2006 reflecting the receipt of an upfront payment of $4.0 million in conjunction with the transfer of intellectual property rights related to nuclear transfer for use in animal cloning to the Company's joint venture, Start Licensing, Inc.
Operating expenses for the third quarter of 2006 were $12.8 million compared to $13.6 million for the comparable period in 2005. Research and development expenses for the third quarter of 2006 were $10.7 million compared to $12.2 million for the comparable 2005 period. Net expense for research and development decreased due to reduced raw materials purchases for the manufacture of Geron's telomerase inhibitor drug, GRN163L, offset by higher personnel-related costs, including the recognition of compensation expense related to stock option grants. General and administrative expenses for the third quarter of 2006 were $2.1 million compared to $1.4 million for the comparable 2005 period. The increase in general and administrative expenses in the third quarter of 2006 was primarily due to the recognition of compensation expense related to stock option grants.
Operating expenses for the first nine months of 2006 were $36.5 million compared to $32.6 million for the comparable period in 2005. Research and development expenses for the first nine months of 2006 were $29.4 million compared to $25.5 million for the comparable 2005 period. Overall research and development expenses increased in 2006 as a result of higher personnel-related costs, including the recognition of compensation expense related to stock option grants, and increased manufacturing costs related to the telomerase cancer vaccine, GRNVAC1, offset by reduced raw materials purchases for the manufacture of GRN163L. General and administrative expenses for the first nine months of 2006 and 2005 were each $7.1 million due to recognition of compensation expense related to stock option grants, offset by reduced consulting expense.
Third Quarter 2006 Highlights:
Clinical Development
Geron scientists and collaborators presented new data at the International Society for Stem Cell Research's (ISSCR) annual meeting pertaining to four products in development: (1) GRNOPC1, Oligodendroglial Progenitor Cells for acute spinal cord injury; (2) GRNIC1, Islet Clusters for diabetes; (3) GRNCM1, Cardiomyocytes for myocardial infarction and (4) osteoprogenitor cells for bone fractures and osteoporosis. In addition, several presentations at the meeting described advances in human embryonic stem cell (hESC) culture and derivation techniques and further characterization of hESC-derived hepatocytes for liver failure and drug metabolism testing.
An article describing novel chemical methods that reduce the number of chemical steps and cost of synthesizing the monomer building blocks of Geron's patented N3'-P5' thiophosphoramidate oligonucleotide compounds, including its lead anti-cancer drug, GRN163L, was published in Tetrahedron Letters.
Preclinical studies published in Regenerative Medicine support the safety and utility of GRNOPC1, Geron's lead hESC-based therapeutic product for the treatment of spinal cord injury. The studies demonstrated that when GRNOPC1 is injected into the lesion site of rats that received either very mild or moderate spinal cord contusion injuries, GRNOPC1 survived in both mild and moderate lesion sites, with broader distribution of transplanted cells and robust remyelination in the more severe injuries, replicating previous studies.
New data supporting the development of TAT0002, a small molecule telomerase activator for the treatment of HIV/AIDS, was presented at the XVI International AIDS Conference. The data confirm and extend earlier findings that TAT0002 enhances the function of key immune cells from HIV/AIDS donors.
Intellectual Property
The U.S. District Court for the District of Columbia dismissed appeals of two patent interference decisions pending before them regarding patents covering nuclear transfer (cloning) technology. Geron acquired rights to this technology from the Roslin Institute in 1999 and subsequently initiated patent interferences with conflicting patents held by the University of Massachusetts. The Board of Patent Appeals and Interferences of the U.S. Patent Office ruled in favor of Geron on all counts in both interference proceedings, and the University of Massachusetts and its licensee, Advanced Cell Technology (ACT), filed appeals. Both of those appeals by the University of Massachusetts and ACT have now been dismissed with prejudice.
Business Development
Geron and the University of Edinburgh entered into a collaboration to conduct preclinical safety and efficacy studies with three cell types derived from hESCs. The cell types are hepatocytes for the treatment of liver failure, and osteoblasts and chondrocytes for the treatment of musculoskeletal disorders, including osteoarthritis, bone fractures and osteoporosis.
Conference Call
Today at 8:00 a.m. PST / 11:00 a.m. EST, Thomas B. Okarma, Ph.D., M.D., Geron's chief executive officer, and David L. Greenwood, Geron's chief financial officer, will host a conference call to discuss the Company's third quarter and year to date results.
Participants can access the conference call live via telephone by dialing 866-831-6267 (U.S.) or 617-213-8857 (international). The passcode is 12545730. A live audio-only webcast is also available through a link that is posted on the Conferences page in the Investor Relations section of Geron's Website at http://www.geron.com. The audio web broadcast of the conference call will be available for replay through November 30, 2006.
stammzellen sind wieder in

!
Dieser Beitrag wurde vom System automatisch gesperrt. Bei Fragen wenden Sie sich bitte an feedback@wallstreet-online.deMarket betting on stem-cell stocks
Commentary: Election gains for research bakers could boost shares
By Michael Kahn
Last Update: 12:01 AM ET Nov 1, 2006
http://www.marketwatch.com/News/Story/Story.aspx?guid=%7B065…
Geron Licenses Antigen Targeting Patents for Cancer Vaccine Program from Immunomic Therapeutics
Monday November 6, 7:30 am ET
MENLO PARK, Calif., & GAITHERSBURG, Md.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) and Immunomic Therapeutics Inc. (ITI) announced today a patent license agreement under which Geron will receive exclusive rights to the LAMP antigen targeting sequence for use in cancer vaccines.
ADVERTISEMENT
Geron's therapeutic cancer vaccine, GRNVAC1, triggers an immune response against the universal cancer antigen, telomerase, and uses the LAMP sequence to enhance that immune response. The LAMP technology was invented at Johns Hopkins University and recently licensed to ITI for all applications.
Under the ITI-Geron license, Geron receives worldwide exclusive rights to the Johns Hopkins LAMP patents for cancer vaccines directed to telomerase as well as two additional antigen targets to be selected by Geron at a later date. Financial terms of the agreement were not disclosed.
"GRNVAC1 has demonstrated tolerability and immunogenicity in a Phase I/II clinical trial in metastatic prostate cancer," said Thomas B. Okarma, Ph.D., M.D., Geron's president and CEO. "In addition, results from this trial suggest that the use of the LAMP signal sequence may help to enhance the already potent immune responses seen with telomerase alone. We are pleased to secure rights for the use of the LAMP sequence in GRNVAC1 and future cancer vaccine products."
The LAMP sequence causes an antigen to which it is attached to be taken up by the lysosomal subcellular compartment of the cell. This has been shown to increase presentation on MHC class II molecules, which in turn, can produce greater CD4+ T-cell responses against the antigen and a more potent and longer lasting overall immune response. A Phase I/II clinical trial of Geron's GRNVAC1 telomerase cancer vaccine conducted at Duke University has previously shown that addition of the LAMP sequence to the telomerase antigen increased patient CD4+ T-cell responses and improved cytotoxic T-lymphocyte (CTL) mediated killing of cancer cells.
GRNVAC1 is comprised of autologous dendritic cells loaded with telomerase mRNA linked to a LAMP targeting sequence. In March 2005, results of the first completed Phase I/II clinical trial of GRNVAC1 in metastatic prostate cancer patients were published in the Journal of Immunology (JI, 2005, 174:3798-38097).
Monday November 6, 7:30 am ET
MENLO PARK, Calif., & GAITHERSBURG, Md.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) and Immunomic Therapeutics Inc. (ITI) announced today a patent license agreement under which Geron will receive exclusive rights to the LAMP antigen targeting sequence for use in cancer vaccines.
ADVERTISEMENT
Geron's therapeutic cancer vaccine, GRNVAC1, triggers an immune response against the universal cancer antigen, telomerase, and uses the LAMP sequence to enhance that immune response. The LAMP technology was invented at Johns Hopkins University and recently licensed to ITI for all applications.
Under the ITI-Geron license, Geron receives worldwide exclusive rights to the Johns Hopkins LAMP patents for cancer vaccines directed to telomerase as well as two additional antigen targets to be selected by Geron at a later date. Financial terms of the agreement were not disclosed.
"GRNVAC1 has demonstrated tolerability and immunogenicity in a Phase I/II clinical trial in metastatic prostate cancer," said Thomas B. Okarma, Ph.D., M.D., Geron's president and CEO. "In addition, results from this trial suggest that the use of the LAMP signal sequence may help to enhance the already potent immune responses seen with telomerase alone. We are pleased to secure rights for the use of the LAMP sequence in GRNVAC1 and future cancer vaccine products."
The LAMP sequence causes an antigen to which it is attached to be taken up by the lysosomal subcellular compartment of the cell. This has been shown to increase presentation on MHC class II molecules, which in turn, can produce greater CD4+ T-cell responses against the antigen and a more potent and longer lasting overall immune response. A Phase I/II clinical trial of Geron's GRNVAC1 telomerase cancer vaccine conducted at Duke University has previously shown that addition of the LAMP sequence to the telomerase antigen increased patient CD4+ T-cell responses and improved cytotoxic T-lymphocyte (CTL) mediated killing of cancer cells.
GRNVAC1 is comprised of autologous dendritic cells loaded with telomerase mRNA linked to a LAMP targeting sequence. In March 2005, results of the first completed Phase I/II clinical trial of GRNVAC1 in metastatic prostate cancer patients were published in the Journal of Immunology (JI, 2005, 174:3798-38097).
Geron to Present at Rodman & Renshaw 8th Annual Healthcare Conference
Tuesday November 7, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) will present an update of the company's product development programs at 8:30 a.m. EST on Wednesday, Nov. 8, 2006, at the Rodman & Renshaw 8th Annual Healthcare Conference in New York City.
ADVERTISEMENT
The update of Geron's portfolio of telomerase-based anti-cancer therapies will include information about GRN163L and GRNVAC1. The presentation will also include reviews of the company's human embryonic stem cell programs in spinal cord injury (GRNOPC1), heart disease (GRNCM1), and diabetes (GRNIPC1). Thomas B. Okarma, Ph.D., M.D., Geron's president and chief executive officer, will deliver the presentation.
The audio and slide presentation will be available at the following Web site address: http://www.wsw.com/webcast/rrshq10/gern/. The replay will be available until Dec. 8, 2006
Tuesday November 7, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) will present an update of the company's product development programs at 8:30 a.m. EST on Wednesday, Nov. 8, 2006, at the Rodman & Renshaw 8th Annual Healthcare Conference in New York City.
ADVERTISEMENT
The update of Geron's portfolio of telomerase-based anti-cancer therapies will include information about GRN163L and GRNVAC1. The presentation will also include reviews of the company's human embryonic stem cell programs in spinal cord injury (GRNOPC1), heart disease (GRNCM1), and diabetes (GRNIPC1). Thomas B. Okarma, Ph.D., M.D., Geron's president and chief executive officer, will deliver the presentation.
The audio and slide presentation will be available at the following Web site address: http://www.wsw.com/webcast/rrshq10/gern/. The replay will be available until Dec. 8, 2006
die demokraten - danke!
stammzellen sind wieder sexy. geron tuts gut. aber da ist doch noch was anderes, von dem ich noch wesentlich mehr erwarte:
leider gabs heute bei der analystenkonferenz keine daten zur klinischen phase i/ii von gern163l.
aber: beim nächsten ash meeting kommts... so auf slide 9 der prasi.
http://www.hematology.org/meetings/2006
am 9.12. ist es soweit!
stammzellen sind wieder sexy. geron tuts gut. aber da ist doch noch was anderes, von dem ich noch wesentlich mehr erwarte:
leider gabs heute bei der analystenkonferenz keine daten zur klinischen phase i/ii von gern163l.
aber: beim nächsten ash meeting kommts... so auf slide 9 der prasi.
http://www.hematology.org/meetings/2006
am 9.12. ist es soweit!
tja, oder die daten kommen schon bis übermorgen auf der nci eortc, was auch auf slide 9 der präsi niedergelgt war:
http://www.aacr.org/home/scientists/meetings--workshops/mole…
http://www.aacr.org/home/scientists/meetings--workshops/mole…
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10Angriff aufs Monopol
von Elke Binder (Pittsburgh)
Forscher der Universität Wisconsin halten die Patente auf alle Verfahren mit embryonalen Stammzellen des Menschen. Jetzt wehren sich Unternehmen und Interessenverbände.
Arbeit unter dem Mikroskop an der embryonalen Stammzelle einer MausIn den USA tobt derzeit ein heftiger Streit um drei Patente. Forscher um James Thomson, der 1998 an der Universität von Wisconsin in Madison die erste menschliche embryonale Stammzelllinie isolierte, halten nicht nur die Rechte an dem Verfahren, sondern auch an den Zellen selbst - und zwar an ausnahmslos allen embryonalen Stammzellkulturen des Menschen, die derzeit in den Staaten bestehen, eingeführt oder zukünftig neu isoliert werden. Dieses Monopol ist vielen Wissenschaftlern ein Dorn im Auge. Zwei Interessengruppen haben jetzt erreicht, dass es vom US Patent and Trademark Office auf seine Rechtmäßigkeit geprüft wird.
Mediziner hoffen, dass sich mit embryonalen Stammzellen eines Tages Diabetes, Alzheimer oder Parkinson heilen lassen. "Wir halten die Patente aber für eine enorme Behinderung bei der Suche nach neuen Therapien", sagt die Stammzellforscherin Jeanne Loring vom Burnham Institute in Kalifornien. Gemeinsam mit der Public Patent Foundation in New York und der Foundation for Taxpayer and Consumer Rights in Kalifornien hat sie den den Vorstoß zur Aufhebung der Patente initiiert. Bisher werden alle von der Wisconsin Alumni Research Foundation (WARF) der Universität in Madison verwaltet.
"Für uns ist das derzeit die größte Hürde"
ZUM THEMA
Embryofreundliche Stammzellen (http://www.ftd.de/forschung/107126.html)
(€) Stammzellen vom Fließband (http://www.ftd.de/forschung/7457.html)
(€) Herz in der Petrischale (http://www.ftd.de/forschung/54764.html)
Diesen Artikel jetzt anhören Aufgrund eines Erlasses von Präsident Bush von 2001 darf in den USA mit öffentlichen Geldern nur an den Stammzelllinien geforscht werden, die schon zu dem Zeitpunkt bestanden. Interessierte Wissenschaftler müssen diese Zellen nach den Bedingungen der WARF erwerben. Die National Institutes of Health haben daher mit der WARF jüngst ein Abkommen geschlossen, nach dem diese von akademischen Institutionen nur 500 $ Lizenzgebühr nehmen darf. Unternehmen zahlen allerdings 150.000 $ plus weitere 40.000 $ jährlich. "Für uns ist das derzeit die größte Hürde", sagt Jonathan Auerbach, der im Sommer dieses Jahres das Start-up Globalstem in Rockville, Maryland, gegründet hat. Er will Nährmedien für embryonale Stammzellen herstellen. Noch müssen sich seine Forscher mit denen der Maus zufriedengeben.
Die Lizenzgebühr ist aber bei Weitem nicht das einzige Problem: Das kalifornische Biotechunternehmen Geron hatte 1998 die erstmalige Isolierung der menschlichen embryonalen Stammzellen an der Universität von Wisconsin finanziert und hält daher heute die exklusive Lizenz an jeglichem therapeutischen Nutzen der Zellen. Das heißt, dass Wissenschaftler Geron an jedem potenziellen Gewinn aus neuen Entwicklungen mit embryonalen Stammzellen beteiligen müssen. "Nur wenige große Unternehmen forschen deshalb an den Zellen", so Loring. Bekannt seien ihr nur zwei. "Ohne die Patente wären das deutlich mehr", ist sich die Expertin sicher. Das Biotechunternehmen Invitrogen Corporation etwa würde derzeit außerhalb der USA an den umstrittenen Zellen arbeiten.
Streit mit internationaler Bedeutung
Damit nicht genug: Die Patente gelten auch für neue Zellen. Der Biologe Douglas Melton hat kürzlich an der Harvard-Universität in Cambridge, Massachusetts, mit privaten Geldern mehrere neue embryonale Stammzelllinien des Menschen gewonnen. Interessierte Forscher können diese von ihm kostenlos erhalten - müssen aber dennoch mit der WARF einen Lizenzvertrag unterzeichnen. Für Melton ist dies eine "lästige, restriktive und unkooperative" Praxis, wie er im Juli gegenüber dem Fachmagazin "Science" sagte.
Dass die WARF überhaupt diese weitreichenden Patente in den Jahren 1998, 2001 und 2006 erhalten konnte, liegt an einer Besonderheit des US-amerikanischen Patentrechts. Zwar dürfen auf in der Natur vorkommende Materien keine Patente erteilt werden, wohl aber auf isolierte Substanzen. Den Gegnern der Stammzellpatente bleibt deshalb nur die Möglichkeit, die Originalität der Arbeiten anzufechten. "Das Verfahren zur Isolierung von embryonalen Stammzellen wurde schon 1981 an Mäusen entwickelt", sagt Loring. "Thomson hat das exakt so auf den Menschen übertragen."
Der Streit hat auch internationale Bedeutung. Die Patente gelten zwar nur auf dem Gebiet der USA. Doch das WARF-Monopol wirkt sich auch auf die europäische Forschung aus. "Uns sind sehr enge Restriktionen auferlegt worden", sagt Jürgen Hescheler von der Universität Köln. Er hat menschliche embryonale Stammzellen aus Wisconsin bezogen, da deren Gewinnung hierzulande verboten ist.
"Sollten wir tatsächlich eine neue Therapie entwickeln, dann liegen alle kommerziellen Rechte in den USA", sagt Hescheler. Aus dem Dilemma würde nur helfen, wenn die Politik in Deutschland es erlauben würde, eigene Stammzelllinien zu gewinnen, so Hescheler. So könnte der Patentstreit weitreichende, ethische Konsequenzen haben.
von Elke Binder (Pittsburgh)
Forscher der Universität Wisconsin halten die Patente auf alle Verfahren mit embryonalen Stammzellen des Menschen. Jetzt wehren sich Unternehmen und Interessenverbände.
Arbeit unter dem Mikroskop an der embryonalen Stammzelle einer MausIn den USA tobt derzeit ein heftiger Streit um drei Patente. Forscher um James Thomson, der 1998 an der Universität von Wisconsin in Madison die erste menschliche embryonale Stammzelllinie isolierte, halten nicht nur die Rechte an dem Verfahren, sondern auch an den Zellen selbst - und zwar an ausnahmslos allen embryonalen Stammzellkulturen des Menschen, die derzeit in den Staaten bestehen, eingeführt oder zukünftig neu isoliert werden. Dieses Monopol ist vielen Wissenschaftlern ein Dorn im Auge. Zwei Interessengruppen haben jetzt erreicht, dass es vom US Patent and Trademark Office auf seine Rechtmäßigkeit geprüft wird.
Mediziner hoffen, dass sich mit embryonalen Stammzellen eines Tages Diabetes, Alzheimer oder Parkinson heilen lassen. "Wir halten die Patente aber für eine enorme Behinderung bei der Suche nach neuen Therapien", sagt die Stammzellforscherin Jeanne Loring vom Burnham Institute in Kalifornien. Gemeinsam mit der Public Patent Foundation in New York und der Foundation for Taxpayer and Consumer Rights in Kalifornien hat sie den den Vorstoß zur Aufhebung der Patente initiiert. Bisher werden alle von der Wisconsin Alumni Research Foundation (WARF) der Universität in Madison verwaltet.
"Für uns ist das derzeit die größte Hürde"
ZUM THEMA
Embryofreundliche Stammzellen (http://www.ftd.de/forschung/107126.html)
(€) Stammzellen vom Fließband (http://www.ftd.de/forschung/7457.html)
(€) Herz in der Petrischale (http://www.ftd.de/forschung/54764.html)
Diesen Artikel jetzt anhören Aufgrund eines Erlasses von Präsident Bush von 2001 darf in den USA mit öffentlichen Geldern nur an den Stammzelllinien geforscht werden, die schon zu dem Zeitpunkt bestanden. Interessierte Wissenschaftler müssen diese Zellen nach den Bedingungen der WARF erwerben. Die National Institutes of Health haben daher mit der WARF jüngst ein Abkommen geschlossen, nach dem diese von akademischen Institutionen nur 500 $ Lizenzgebühr nehmen darf. Unternehmen zahlen allerdings 150.000 $ plus weitere 40.000 $ jährlich. "Für uns ist das derzeit die größte Hürde", sagt Jonathan Auerbach, der im Sommer dieses Jahres das Start-up Globalstem in Rockville, Maryland, gegründet hat. Er will Nährmedien für embryonale Stammzellen herstellen. Noch müssen sich seine Forscher mit denen der Maus zufriedengeben.
Die Lizenzgebühr ist aber bei Weitem nicht das einzige Problem: Das kalifornische Biotechunternehmen Geron hatte 1998 die erstmalige Isolierung der menschlichen embryonalen Stammzellen an der Universität von Wisconsin finanziert und hält daher heute die exklusive Lizenz an jeglichem therapeutischen Nutzen der Zellen. Das heißt, dass Wissenschaftler Geron an jedem potenziellen Gewinn aus neuen Entwicklungen mit embryonalen Stammzellen beteiligen müssen. "Nur wenige große Unternehmen forschen deshalb an den Zellen", so Loring. Bekannt seien ihr nur zwei. "Ohne die Patente wären das deutlich mehr", ist sich die Expertin sicher. Das Biotechunternehmen Invitrogen Corporation etwa würde derzeit außerhalb der USA an den umstrittenen Zellen arbeiten.
Streit mit internationaler Bedeutung
Damit nicht genug: Die Patente gelten auch für neue Zellen. Der Biologe Douglas Melton hat kürzlich an der Harvard-Universität in Cambridge, Massachusetts, mit privaten Geldern mehrere neue embryonale Stammzelllinien des Menschen gewonnen. Interessierte Forscher können diese von ihm kostenlos erhalten - müssen aber dennoch mit der WARF einen Lizenzvertrag unterzeichnen. Für Melton ist dies eine "lästige, restriktive und unkooperative" Praxis, wie er im Juli gegenüber dem Fachmagazin "Science" sagte.
Dass die WARF überhaupt diese weitreichenden Patente in den Jahren 1998, 2001 und 2006 erhalten konnte, liegt an einer Besonderheit des US-amerikanischen Patentrechts. Zwar dürfen auf in der Natur vorkommende Materien keine Patente erteilt werden, wohl aber auf isolierte Substanzen. Den Gegnern der Stammzellpatente bleibt deshalb nur die Möglichkeit, die Originalität der Arbeiten anzufechten. "Das Verfahren zur Isolierung von embryonalen Stammzellen wurde schon 1981 an Mäusen entwickelt", sagt Loring. "Thomson hat das exakt so auf den Menschen übertragen."
Der Streit hat auch internationale Bedeutung. Die Patente gelten zwar nur auf dem Gebiet der USA. Doch das WARF-Monopol wirkt sich auch auf die europäische Forschung aus. "Uns sind sehr enge Restriktionen auferlegt worden", sagt Jürgen Hescheler von der Universität Köln. Er hat menschliche embryonale Stammzellen aus Wisconsin bezogen, da deren Gewinnung hierzulande verboten ist.
"Sollten wir tatsächlich eine neue Therapie entwickeln, dann liegen alle kommerziellen Rechte in den USA", sagt Hescheler. Aus dem Dilemma würde nur helfen, wenn die Politik in Deutschland es erlauben würde, eigene Stammzelllinien zu gewinnen, so Hescheler. So könnte der Patentstreit weitreichende, ethische Konsequenzen haben.
Unsicherheiten für US-Unternehmen
In den USA haben die Demokraten erstmals seit zwölf Jahren im Kongress wieder das Sagen. Das bedeutet für viele US-Unternehmen und Branchen neue Unsicherheiten - aber auch die Chance auf Hilfe aus Washington.
New York Die US-Konzerne hatten in den vergangenen sechs Jahren dank der wirtschaftsfreundlichen Einheitsfront des republikanischen Präsidenten George W. Bush und des von den Republikanern kontrollierten Parlaments weit gehend freie Hand. Zu den grössten Verlierern nach dem Wahlsieg der Demokraten könnte künftig die Pharmabranche gehören. Die Demokraten verlangen, dass die staatliche Krankenversicherung der Rentner als Grossabnehmer von Medikamenten die Möglichkeit erhält, direkt mit den Pharmakonzernen über Discountpreise zu verhandeln. Die Amerikaner zahlen mit die höchsten Arzneimittelpreise der Welt. Sie sind die Hauptgewinnquelle der dort tätigen Pharmaunternehmen. Die Aktien der amerikanischen Merck-Gruppe waren am Mittwoch um 3 Prozent und die des weltgrössten Pharmakonzerns Pfizer um 2,5 Prozent gefallen.
Krankenversicherungen wie Aetna und Krankenhauskonzerne wie Humana standen ebenfalls unter Druck. Die Kostenexplosion bei der Krankenversorgung hat Millionen Amerikaner schwer getroffen. Die Demokraten wollen eine weit reichende Krankenversicherungsreform.
Rüstungskonzerne unter Druck
Rüstungsunternehmen wie Lockheed Martin und Northrop Grumman standen ebenfalls unter Druck. Der Grund: Die Wall Street befürchtet zukünftig mehr Zurückhaltung bei Rüstungsaufträgen Washingtons. Zigarettenhersteller wie Altria könnten sich ebenfalls stärkerer Aufmerksamkeit von Seiten des demokratisch kontrollierten Kongresses ausgesetzt sehen. Es sind noch immer Raucherklagen hängig. Die Ölkonzerne haben sich angesichts der hohen Öl- und Energiepreise und der beispiellosen Rekordgewinne bei ExxonMobil, Chevron und ConocoPhillip und anderen Energiefirmen den Zorn der demokratischen Politiker und der Wähler zugezogen. Jetzt wollen die Demokraten zahlreiche Steuerhilfen für die Ölkonzerne abschaffen. Eine Gewinnabschöpfungssteuer für die Ölkonzerne scheint allerdings kaum Chancen zu haben.
Bush-Initiativen wie die Öffnung von Naturschutzgebieten in Alaska und küstennahen Off-Shore-Gebieten für die Öl- und Erdgasexploration lehnen die Demokraten ab. Dagegen schossen die Aktien von alternativen Energiefirmen wie Ballard Power, FuelCell und Pacific Ethanol in die Höhe, weil die Demokraten stärker auf alternative Energiequellen setzen wollen. Biotechfirmen wie Geron und StemCell können ebenfalls hoffen, da die Demokraten dem viel versprechenden Stammzellen-Forschungsbereich aufgeschlossen gegenüberstehen, während Bush ihn torpediert hatte.
Die Autometropole Detroit sieht mit gemischten Gefühlen nach Washington. Die im heimischen Markt schwer angeschlagenen Autoriesen General Motors und Ford sowie die zu DaimlerChrysler gehörende Chrysler Group könnten aus Washington möglicherweise Hilfestellung an der Handelsfront erhalten und von einer Reform der Krankenversicherung profitieren. Dagegen wehren sie sich gegen die von den Demokraten geforderten härteren staatlichen Auflagen zur rascheren Einführung benzinsparender und abgasarmer Autos. Die Demokraten wollen angesichts der Abwanderung und des Verlusts von drei Millionen industriellen Arbeitsplätzen unter Bush an der Handelsfront mit harten Bandagen kämpfen. (dpa)
In den USA haben die Demokraten erstmals seit zwölf Jahren im Kongress wieder das Sagen. Das bedeutet für viele US-Unternehmen und Branchen neue Unsicherheiten - aber auch die Chance auf Hilfe aus Washington.
New York Die US-Konzerne hatten in den vergangenen sechs Jahren dank der wirtschaftsfreundlichen Einheitsfront des republikanischen Präsidenten George W. Bush und des von den Republikanern kontrollierten Parlaments weit gehend freie Hand. Zu den grössten Verlierern nach dem Wahlsieg der Demokraten könnte künftig die Pharmabranche gehören. Die Demokraten verlangen, dass die staatliche Krankenversicherung der Rentner als Grossabnehmer von Medikamenten die Möglichkeit erhält, direkt mit den Pharmakonzernen über Discountpreise zu verhandeln. Die Amerikaner zahlen mit die höchsten Arzneimittelpreise der Welt. Sie sind die Hauptgewinnquelle der dort tätigen Pharmaunternehmen. Die Aktien der amerikanischen Merck-Gruppe waren am Mittwoch um 3 Prozent und die des weltgrössten Pharmakonzerns Pfizer um 2,5 Prozent gefallen.
Krankenversicherungen wie Aetna und Krankenhauskonzerne wie Humana standen ebenfalls unter Druck. Die Kostenexplosion bei der Krankenversorgung hat Millionen Amerikaner schwer getroffen. Die Demokraten wollen eine weit reichende Krankenversicherungsreform.
Rüstungskonzerne unter Druck
Rüstungsunternehmen wie Lockheed Martin und Northrop Grumman standen ebenfalls unter Druck. Der Grund: Die Wall Street befürchtet zukünftig mehr Zurückhaltung bei Rüstungsaufträgen Washingtons. Zigarettenhersteller wie Altria könnten sich ebenfalls stärkerer Aufmerksamkeit von Seiten des demokratisch kontrollierten Kongresses ausgesetzt sehen. Es sind noch immer Raucherklagen hängig. Die Ölkonzerne haben sich angesichts der hohen Öl- und Energiepreise und der beispiellosen Rekordgewinne bei ExxonMobil, Chevron und ConocoPhillip und anderen Energiefirmen den Zorn der demokratischen Politiker und der Wähler zugezogen. Jetzt wollen die Demokraten zahlreiche Steuerhilfen für die Ölkonzerne abschaffen. Eine Gewinnabschöpfungssteuer für die Ölkonzerne scheint allerdings kaum Chancen zu haben.
Bush-Initiativen wie die Öffnung von Naturschutzgebieten in Alaska und küstennahen Off-Shore-Gebieten für die Öl- und Erdgasexploration lehnen die Demokraten ab. Dagegen schossen die Aktien von alternativen Energiefirmen wie Ballard Power, FuelCell und Pacific Ethanol in die Höhe, weil die Demokraten stärker auf alternative Energiequellen setzen wollen. Biotechfirmen wie Geron und StemCell können ebenfalls hoffen, da die Demokraten dem viel versprechenden Stammzellen-Forschungsbereich aufgeschlossen gegenüberstehen, während Bush ihn torpediert hatte.
Die Autometropole Detroit sieht mit gemischten Gefühlen nach Washington. Die im heimischen Markt schwer angeschlagenen Autoriesen General Motors und Ford sowie die zu DaimlerChrysler gehörende Chrysler Group könnten aus Washington möglicherweise Hilfestellung an der Handelsfront erhalten und von einer Reform der Krankenversicherung profitieren. Dagegen wehren sie sich gegen die von den Demokraten geforderten härteren staatlichen Auflagen zur rascheren Einführung benzinsparender und abgasarmer Autos. Die Demokraten wollen angesichts der Abwanderung und des Verlusts von drei Millionen industriellen Arbeitsplätzen unter Bush an der Handelsfront mit harten Bandagen kämpfen. (dpa)
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10:30AM Geron presents early clinical data for its cancer drug (GERN) 8.39 : Co announces the presentation of the first clinical trial data for its telomerase inhibitor cancer drug, GRN163L. The data demonstrate the safety, tolerability and predicted pharmacokinetics in low-dose cohorts from a Phase I/II trial in patients with chronic lymphocytic leukemia (CLL) and a Phase I trial in patients with solid tumors. "The early clinical data are very encouraging... This is the first time telomerase inhibition has been tested in cancer patients. The excellent tolerability and pharmacokinetics observed so far enable us to advance to the therapeutic dose cohorts, where we hope to demonstrate safe, sustained telomerase inhibition in the targeted tumor cells."
Antwort auf Beitrag Nr.: 25.260.237 von meislo am 10.11.06 15:01:04dieser thread trägt den titel: geron mit hammernews!!
leute, A U F W A C H E N !!!
der erste teil dieser hammernews ist gestern veröffentlicht worden! grn163l erweist sich nach ersten erkenntnissen als sicher! das zeug wird von menschen vertragen, es wurden keine gravierenden sideeffects beobachtet.
weitere daten zur wiksamkeit werden in wenigen monaten folgen. wenn auch die wirksamkeit so ausfällt wie es bzgl. der sicherheit bei den tierversuchen der fall war, dann hat die forschung bei der onkologie einen weiteren meilenstein erreicht.
dass grn163l auch wirkt wie erhofft, lässt sich m. e. auch aus dem beitritt von a. colowick als gerons chefonkologe ableiten.
A U F W A C H E N !!!
leute, A U F W A C H E N !!!
der erste teil dieser hammernews ist gestern veröffentlicht worden! grn163l erweist sich nach ersten erkenntnissen als sicher! das zeug wird von menschen vertragen, es wurden keine gravierenden sideeffects beobachtet.
weitere daten zur wiksamkeit werden in wenigen monaten folgen. wenn auch die wirksamkeit so ausfällt wie es bzgl. der sicherheit bei den tierversuchen der fall war, dann hat die forschung bei der onkologie einen weiteren meilenstein erreicht.
dass grn163l auch wirkt wie erhofft, lässt sich m. e. auch aus dem beitritt von a. colowick als gerons chefonkologe ableiten.
A U F W A C H E N !!!
ein weiterer beweis für die sinnhaftigkeit der telomeraseinhibition:
UCSF study shows suppression of telomerase enzyme can inhibit spread of melanoma
July 11, 2006 - UCSF researchers have found that the spread of melanoma can be inhibited by suppressing telomerase, the enzyme active in cancer cell growth.
Findings reported in the July 5 Proceedings of the National Academy of Sciences show for the first time a link between telomerase and glycolysis, the metabolic pathway used to consume glucose and produce lactic acid within the body.
"Identification of this relationship has great significance in understanding the role of telomerase and glycolysis together," said Mohammed Kashani-Sabet, MD, UCSF associate professor of dermatology and lead author of the study. "These results support the rationale for blocking telomerase in cancer therapy."
In the study, researchers found through gene expression profiling in mice that eight genes involved in glucose metabolism were lowered when telomerase was suppressed in skin cancer cells. The result was a return of pigmentation, frequently absent in advanced melanomas, and of cancer cells losing their metastatic potential.
"We introduced a telomerase inhibitor into melanoma cells and found that by suppressing telomerase, melanoma cells start to change," said Kashani-Sabet. "In some melanomas, pigmentation is lost. We found that when we are able to shut down telomerase, the cells regain functions previously lost, such as the ability to make pigment."
"As the cells become too acidic from the buildup of lactic acid, the proteins that control pigment production can be turned off, suggesting that glucose metabolism plays a key role when combined with telomerase in metastasis."
The ribonucleoprotein enzyme, telomerase, was discovered by study co-investigator Elizabeth Blackburn, PhD, Morris Herzstein Professor of Biology and Physiology in the UCSF Department of Biochemistry and Biophysics. Telomerase is well-documented as an instigator of cancer cell proliferation, but according to the researchers, its impact on tumor invasion and metastasis has been less studied.
In normal cells, the telomere is a strand of DNA that exists at the end of each chromosome and shortens with each cell division until it stops dividing, signaling the end of the cell life. Telomerase is activated in abnormal cells such as cancer cells, restoring the telomeres, and allowing them to divide and grow. As such, telomerase has been found to be over-expressed in 90 percent of human cancers.
Researchers were also able to ascertain for the first time how the use of a glucose compound injected into the body for positron emission topography (PET) scans was effective in diagnosing cancer. Use of the PET scan is now a regularly used method to diagnose and effectively pinpoint the source of cancer in an individual by utilizing radiation emitted from a patient to develop images. A radioactive substance is made up of glucose, a naturally occurring sugar, combined with a radioactive fluoride atom. The metabolism of glucose can be seen through gamma radiation produced from the positron-emitting fluoride that is detected by the PET scanner.
"Now for the first time, we understand why melanomas have high glucose uptake," Kashani-Sabet said. "We knew that use of PET scanning was effective in detecting melanoma metastasis, but we really didn't know why. Through this study, we found that telomerase is responsible for activation of glycolysis in melanoma cells."
Connecting telomerase and glucose metabolism together has implications for further therapeutic study. "By manipulating telomerase in cancer cells and suppressing glycolysis, it is possible to inhibit both melanoma invasion and metastasis."
University of California San Francisco
http://www.brightsurf.com/news/headlines/25326/UCSF_study_sh…
UCSF study shows suppression of telomerase enzyme can inhibit spread of melanoma
July 11, 2006 - UCSF researchers have found that the spread of melanoma can be inhibited by suppressing telomerase, the enzyme active in cancer cell growth.
Findings reported in the July 5 Proceedings of the National Academy of Sciences show for the first time a link between telomerase and glycolysis, the metabolic pathway used to consume glucose and produce lactic acid within the body.
"Identification of this relationship has great significance in understanding the role of telomerase and glycolysis together," said Mohammed Kashani-Sabet, MD, UCSF associate professor of dermatology and lead author of the study. "These results support the rationale for blocking telomerase in cancer therapy."
In the study, researchers found through gene expression profiling in mice that eight genes involved in glucose metabolism were lowered when telomerase was suppressed in skin cancer cells. The result was a return of pigmentation, frequently absent in advanced melanomas, and of cancer cells losing their metastatic potential.
"We introduced a telomerase inhibitor into melanoma cells and found that by suppressing telomerase, melanoma cells start to change," said Kashani-Sabet. "In some melanomas, pigmentation is lost. We found that when we are able to shut down telomerase, the cells regain functions previously lost, such as the ability to make pigment."
"As the cells become too acidic from the buildup of lactic acid, the proteins that control pigment production can be turned off, suggesting that glucose metabolism plays a key role when combined with telomerase in metastasis."
The ribonucleoprotein enzyme, telomerase, was discovered by study co-investigator Elizabeth Blackburn, PhD, Morris Herzstein Professor of Biology and Physiology in the UCSF Department of Biochemistry and Biophysics. Telomerase is well-documented as an instigator of cancer cell proliferation, but according to the researchers, its impact on tumor invasion and metastasis has been less studied.
In normal cells, the telomere is a strand of DNA that exists at the end of each chromosome and shortens with each cell division until it stops dividing, signaling the end of the cell life. Telomerase is activated in abnormal cells such as cancer cells, restoring the telomeres, and allowing them to divide and grow. As such, telomerase has been found to be over-expressed in 90 percent of human cancers.
Researchers were also able to ascertain for the first time how the use of a glucose compound injected into the body for positron emission topography (PET) scans was effective in diagnosing cancer. Use of the PET scan is now a regularly used method to diagnose and effectively pinpoint the source of cancer in an individual by utilizing radiation emitted from a patient to develop images. A radioactive substance is made up of glucose, a naturally occurring sugar, combined with a radioactive fluoride atom. The metabolism of glucose can be seen through gamma radiation produced from the positron-emitting fluoride that is detected by the PET scanner.
"Now for the first time, we understand why melanomas have high glucose uptake," Kashani-Sabet said. "We knew that use of PET scanning was effective in detecting melanoma metastasis, but we really didn't know why. Through this study, we found that telomerase is responsible for activation of glycolysis in melanoma cells."
Connecting telomerase and glucose metabolism together has implications for further therapeutic study. "By manipulating telomerase in cancer cells and suppressing glycolysis, it is possible to inhibit both melanoma invasion and metastasis."
University of California San Francisco
http://www.brightsurf.com/news/headlines/25326/UCSF_study_sh…
Ist ja hier eine sehr überschaubare Investorengemeinde . Bin auch noch in Geron investiert
. Bin auch noch in Geron investiert
Die Phase I dürfte bei Geron kein Problem sein, Pharmexa hat bereits Telomerase in Phase III , siehe http://www.pharmexa.com/site.asp?p=81
, siehe http://www.pharmexa.com/site.asp?p=81
 . Bin auch noch in Geron investiert
. Bin auch noch in Geron investiert
Die Phase I dürfte bei Geron kein Problem sein, Pharmexa hat bereits Telomerase in Phase III
 , siehe http://www.pharmexa.com/site.asp?p=81
, siehe http://www.pharmexa.com/site.asp?p=81
Antwort auf Beitrag Nr.: 25.373.295 von cyberhai am 13.11.06 23:09:54alter hut
das telomeraseintellekt, also die meisten rechte (patente) daran besitzt géron
das telomeraseintellekt, also die meisten rechte (patente) daran besitzt géron
Antwort auf Beitrag Nr.: 25.373.295 von cyberhai am 13.11.06 23:09:54pharmexas versuche sagen nichts darüber aus, ob telomeraseinhibiton sicher ist, schon eher, ob telomerasevakzination verträgich ist. das hat grnvac1 aber bereits belegt.
lg
luckcat
lg
luckcat

7,03 4 wuro und stemcells noch steiler vorbörslich

7,04 und stem noch steiler vorbörslich

short interest (anzahl short verkaufter aktien) dramatisch rückläufig:
Nov. 15, 2006 4,861,099
Oct. 13, 2006 6,322,246
grüße
lc
Nov. 15, 2006 4,861,099
Oct. 13, 2006 6,322,246
grüße
lc
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10Weiss zwar auch nicht woran es liegt
aber im moment geht die post ab
aber im moment geht die post ab

Sieht sehr gut aus, hohes Volumen, da ist wohl was im Busch :
:

 :
:
Antwort auf Beitrag Nr.: 25.938.344 von meislo am 04.12.06 20:52:02Vor allem das hohe Volumen ist der Hammer...über 1 mio gehandelte Aktien.
Gibt es irgendwelche News???
Gibt es irgendwelche News???
Antwort auf Beitrag Nr.: 25.938.807 von harryzunder am 04.12.06 21:07:09Pfizer debakel mit cholesterinsenker bringt den kurs auf trab?

Antwort auf Beitrag Nr.: 25.938.903 von meislo am 04.12.06 21:09:55Habe sonst auch keine erklärung
28 Milliarden Dollar an Börse vernichtet
Das Scheitern eines viel versprechenden Cholesterin-Medikaments hat die Aktien des weltgrößten Pharmakonzerns Pfizer einbrechen lassen. An der New Yorker Börse rauschte der Kurs um 13 Prozent nach unten - das entspricht einem Verlust von 28 Milliarden Dollar.
New York - Am Wochenende hatte Pfizer "aus Sicherheitsgründen" die Entwicklung des Medikaments "Torcetrapib" und alle damit verbundenen klinischen Studien gestoppt. Die Pfizer-Aktien verloren damit seit dem Vorwochenschluss fast 28 Milliarden Dollar (21 Milliarden Euro) an Wert. Der Börsenwert der Pfizer- Aktien betrug heute nur noch rund 172 Milliarden Dollar.
"Torcetrapib" erhöht die Werte des "guten" HDL-Cholesterins erheblich und war für Pfizer nach Ansicht von Pharmaexperten das mit Abstand vielversprechendste Medikament. Es sollte Umsatzeinbußen in Milliardenhöhe ausgleichen, die durch das Auslaufen des Patentschutzes für wichtige Pfizer-Medikamente in den kommenden Jahren drohen.
Pfizer war mit dem Stopp einer Empfehlung eines unabhängigen Aufsichtsgremiums gefolgt, das die umfangreichen Patientenstudien überwachte. Es hatte eine erhöhte Zahl von Todesfällen während der klinischen Studien festgestellt. Die US-Arzneimittelbehörde FDA hatte erklärt, sie unterstütze die Pfizer-Entscheidung voll.
Lipitor ist umsatzstärkstes Medikament der Welt
Das unabhängige Aufsichtsgremium DSMB (Data Safety Monitoring Board) empfahl die Beendigung der so genannten "Illuminate"-Studie für das Medikament wegen "eines Ungleichgewichts von Sterblichkeits- und Herzkreislauf-Vorfällen", erklärte Pfizer am Wochenende.
Der Pfizer-Blutfett-Senker "Lipitor" war in der Studie als Vergleich für die Sicherheit und Wirksamkeit von "Torcetrapib" verwendet worden. "Lipitor" ist mit rund 13 Milliarden Dollar (9,8 Milliarden Euro) Jahresumsatz das umsatzstärkste Medikament der Welt. Der Lipitor-Patentschutz in den USA läuft 2010 oder 2011 aus. Pfizer verliert auch bei einigen anderen wichtigen Medikamenten in den kommenden Jahren Patentschutz.
An der "Torcetrapib"-Studie nahmen 15.000 Patienten teil. Es waren 82 Patienten gestorben, die eine Kombination von "Torcetrapib" und "Lipitor" eingenommen hatten gegenüber 51 Todesfällen von Patienten, denen nur "Lipitor" verabreicht worden war. Pfizer-Konzernchef Jeffrey B. Kindler hatte die DSMB- Informationen gestern "überraschend und enttäuschend" genannt.
Pfizer verstehe, was dies für das Geschäft bedeute und werde "rasch und aggressiv reagieren". Wall-Street-Analysten erwarten einen massiven Stellenabbau beim globalen Pharma-Branchenführer. Kindler geht weiterhin davon aus, dass der Umsatz 2007 und 2008 auf dem Niveau dieses Jahres bleiben wird. 2009 werde es dann wieder einen steigenden Umsatz geben. Pfizer will nach seinen Angaben jetzt beschleunigt die eigene Produktpalette erweitern, Produkte zukaufen und Kosten sparen. Pfizer setzte in den ersten neun Monaten dieses Jahres 35,8 (Vorjahresvergleichszeit: 34,9) Milliarden Dollar um und verdiente 9,9 (5,3) Milliarden Dollar.
Die haben nichts in der palette
28 Milliarden Dollar an Börse vernichtet
Das Scheitern eines viel versprechenden Cholesterin-Medikaments hat die Aktien des weltgrößten Pharmakonzerns Pfizer einbrechen lassen. An der New Yorker Börse rauschte der Kurs um 13 Prozent nach unten - das entspricht einem Verlust von 28 Milliarden Dollar.
New York - Am Wochenende hatte Pfizer "aus Sicherheitsgründen" die Entwicklung des Medikaments "Torcetrapib" und alle damit verbundenen klinischen Studien gestoppt. Die Pfizer-Aktien verloren damit seit dem Vorwochenschluss fast 28 Milliarden Dollar (21 Milliarden Euro) an Wert. Der Börsenwert der Pfizer- Aktien betrug heute nur noch rund 172 Milliarden Dollar.
"Torcetrapib" erhöht die Werte des "guten" HDL-Cholesterins erheblich und war für Pfizer nach Ansicht von Pharmaexperten das mit Abstand vielversprechendste Medikament. Es sollte Umsatzeinbußen in Milliardenhöhe ausgleichen, die durch das Auslaufen des Patentschutzes für wichtige Pfizer-Medikamente in den kommenden Jahren drohen.
Pfizer war mit dem Stopp einer Empfehlung eines unabhängigen Aufsichtsgremiums gefolgt, das die umfangreichen Patientenstudien überwachte. Es hatte eine erhöhte Zahl von Todesfällen während der klinischen Studien festgestellt. Die US-Arzneimittelbehörde FDA hatte erklärt, sie unterstütze die Pfizer-Entscheidung voll.
Lipitor ist umsatzstärkstes Medikament der Welt
Das unabhängige Aufsichtsgremium DSMB (Data Safety Monitoring Board) empfahl die Beendigung der so genannten "Illuminate"-Studie für das Medikament wegen "eines Ungleichgewichts von Sterblichkeits- und Herzkreislauf-Vorfällen", erklärte Pfizer am Wochenende.
Der Pfizer-Blutfett-Senker "Lipitor" war in der Studie als Vergleich für die Sicherheit und Wirksamkeit von "Torcetrapib" verwendet worden. "Lipitor" ist mit rund 13 Milliarden Dollar (9,8 Milliarden Euro) Jahresumsatz das umsatzstärkste Medikament der Welt. Der Lipitor-Patentschutz in den USA läuft 2010 oder 2011 aus. Pfizer verliert auch bei einigen anderen wichtigen Medikamenten in den kommenden Jahren Patentschutz.
An der "Torcetrapib"-Studie nahmen 15.000 Patienten teil. Es waren 82 Patienten gestorben, die eine Kombination von "Torcetrapib" und "Lipitor" eingenommen hatten gegenüber 51 Todesfällen von Patienten, denen nur "Lipitor" verabreicht worden war. Pfizer-Konzernchef Jeffrey B. Kindler hatte die DSMB- Informationen gestern "überraschend und enttäuschend" genannt.
Pfizer verstehe, was dies für das Geschäft bedeute und werde "rasch und aggressiv reagieren". Wall-Street-Analysten erwarten einen massiven Stellenabbau beim globalen Pharma-Branchenführer. Kindler geht weiterhin davon aus, dass der Umsatz 2007 und 2008 auf dem Niveau dieses Jahres bleiben wird. 2009 werde es dann wieder einen steigenden Umsatz geben. Pfizer will nach seinen Angaben jetzt beschleunigt die eigene Produktpalette erweitern, Produkte zukaufen und Kosten sparen. Pfizer setzte in den ersten neun Monaten dieses Jahres 35,8 (Vorjahresvergleichszeit: 34,9) Milliarden Dollar um und verdiente 9,9 (5,3) Milliarden Dollar.
Die haben nichts in der palette
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:108,80 und kein ende
es wird immer weiter gekauft
es wird immer weiter gekauft
Im Biotechsektor wird es noch eine gewaltige Übernahmewelle geben, in den letzten Wochen wurde fast jede Woche ein größeres Unternehmen übernommen. SIRNA vor kurzem für ca. 1 Milliarde Dollar. Ab dieser Größenordnung könnte es auch bei Geron passieren... Pfizer hatte sich von dem gescheiterten Medikament einen jährlich 2-stelligen Milliarenumsatz erhofft und sucht nun "Umsatzersatz" für die Zeit nach 2010, wo das Patent für den Hauptumsatzbringer Lipitor (12 Milliarden pro Jahr, damals wurde dieses Medikament ebenfalls aquiriert und kam nicht aus der eigenen Pipeline) ausläuft.
Antwort auf Beitrag Nr.: 25.939.077 von meislo am 04.12.06 21:15:27Vielleicht auch das der Auslöser
Die Neokonservativen sind wohl definitiv am Ende in den USA
Immerhin galten diese kreise auch Falken genannt als erbitterte Stammzellengegner
Dieser Artikel hat nichts mit Stammzellen am Sinn ist aber wohl eins zu eins übertragbar
Bye-bye, Betonköpfe
Von Gerhard Spörl
John Bolton als US-Botschafter bei der Uno - das war ein Treppenwitz. Endlich ist es vorbei. Die Neokonservativen in den USA sind am Ende. Man wüsste zu gerne, wie Bolton, Wolfowitz und Rumsfeld heute darüber denken, was sie im Nahen Osten angerichtet haben.
Erinnern Sie sich noch an Paul Wolfowitz? Das ist dieser kluge kleine Mann mit der sanften, leicht monotonen Stimme, der daran glaubte, dass die Iraker die US-Soldaten als ihre Befreier begrüßen würden. Er war die Nummer zwei im Pentagon, Stellvertreter des damaligen Verteidigungsministers Donald Rumsfeld, und ist heute Chef der Weltbank.
Wolfowitz ist das Schulbuchbeispiel für das Nebeneinander von Klugheit und Dummheit, oder um es netter auszudrücken: für die Koexistenz von Intellektualität und Naivität in einem Menschen.
Er war der Idealist, der sich darüber empörte, dass Amerika Diktaturen in Südkorea oder auf den Philippinen hinnahm, und er half dabei, daraus Demokratien zu machen. Ihn empörte gleichermaßen die Doppelmoral der amerikanischen Weltmacht im Nahen Osten: das Hinnehmen von Tyrannen oder Autokraten, wenn sie denn auf Öl saßen. Ihm schwebte eine Grand Strategy vor, und Irak sollte der Anfang sein. Demokratie auf Gottes Erdboden, überall: So sollte es sein, so will es die Geschichte.
Die US-Neokonservativen: Gescheiterte Ideologen
Fotostrecke starten: Klicken Sie auf ein Bild (8 Bilder)
Das ist ein schöner Traum, und dass er ihn geträumt hat, kann man ihm nicht vorwerfen. Man muß ihm aber vorwerfen, mit welcher Leichtfertigkeit Paul Wolfowitz Figuren wie Achmed Chalabi auf den Leim ging, wie begierig er dessen Behauptungen zu seinen eigenen machte und wie wenig Argwohn er, ein Intellektueller, seinen eigenen Prämissen schenkte.
Neue Ideen ausgerechnet zwei Tage vor dem Rücktritt
Wolfowitz ging als erster von denjenigen, die man halb zurecht, halb zu unrecht Neocons nannte. Er war wirklich ein Neocon, tief durchdrungen von der Aversion gegenüber lauer Liberalität, die sich mit dem Status quo abfindet, tief durchdrungen auch vom amerikanischen Idealismus, der gerne vieles falsch macht, aber am Ende doch das Richtige tut. So ähnlich hat Churchill seine Erfahrungen mit Amerika in ein Bonmot gefasst.
Foto: REUTERS
Video: ReutersDonald Rumsfeld ist kein Neocon, kein Idealist wie Wolfowitz. Er ist ein amerikanischer Nationalist, der Krieg gegen Saddam führen wollte, weil das gut für Amerika war, wie er meinte. Er wollte den Krieg gewinnen, mit wenigen Truppen und wenig Aufwand. Von Nation Building hielt er anders als die Neocons ziemlich wenig.
Die Neocons, die den Nahen Osten aufrollen wollten, hätten eigentlich mit einer großen Invasionsarmee die Sache regeln müssen. Die Nationalisten à la Rumsfeld oder Cheney wollten Vergeltung für den 11. September und hielten Saddam für gefährlicher als diese komischen Taliban in Afghanistan.
Zu den Treppenwitzen des Abenteuers gehört, dass Rumsfeld zwei Tage vor seinem Rücktritt Änderungen für den Irak einfielen. Zwei Tage vor dem Rücktritt. Als hätte er keine Zeit gehabt, vorher.
Bolton, Typ Betonkopf, Typ America First - als Uno-Diplomat
John Bolton gehörte zu den dienstbaren Geistern, zu den Hausknechten, die sich immer um starke Figuren wie Rumsfeld scharen. Douglas Feith war auch so einer. Erinnert sich noch einer an ihn? Er durfte Geheimdienstleute kujonieren, die sich erfrechten, anderer Meinung über die Massenvernichtungswaffen zu sein, als es das Pentagon und das Büro von Vizepräsident Cheney wollten. Bolton landete als Botschafter der Vereinigten Staaten von Amerika bei den Vereinten Nationen. Noch ein Treppenwitz: Bolton, Typ Betonkopf, Typ America First, bei der Uno. Als Diplomat. Er ist jetzt zurückgetreten. Endlich.
Man wüsste natürlich gerne, wie Wolfowitz, Rumsfeld und Bolton heute darüber denken, was sie im Irak angerichtet haben, im Irak und im Gefolge im ganzen Nahen Osten. Ärgern sie sich die Krätze über sich selber? Ergehen sich sich in What-Ifs: Was wäre gewesen, wenn wir's anders gemacht hätten? Trinken sie sich einen an, wenn sie länger darüber nachdenken, was da passiert ist? Treibt sie die Diskrepanz zwischen Idee und Durchführung in den Wahnsinn?
Die Neocons und Irak, das ist der Stoff, aus dem Antiamerikanismus entstanden ist, als könne es gar nicht anders sein. Die Idee aber, die dem Neokonservativismus zugrunde liegt, nämlich dass der Status quo nicht alles sein kann, jedenfalls nicht dann, wenn die Verhältnisse so trostlos und so ungerecht sind wie im Nahen Osten, lag damals und liegt immer noch ziemlich auf der Hand.
Welche Ironie der Geschichte, dass man diese Idee heute gegen beide verteidigen muß: gegen die Neocons und deren Verächter
Vielleicht sind das pfizerdebakel und das politdebakel auch als summe für den kursanstieg mitverantwortlich
Die Neokonservativen sind wohl definitiv am Ende in den USA
Immerhin galten diese kreise auch Falken genannt als erbitterte Stammzellengegner
Dieser Artikel hat nichts mit Stammzellen am Sinn ist aber wohl eins zu eins übertragbar
Bye-bye, Betonköpfe
Von Gerhard Spörl
John Bolton als US-Botschafter bei der Uno - das war ein Treppenwitz. Endlich ist es vorbei. Die Neokonservativen in den USA sind am Ende. Man wüsste zu gerne, wie Bolton, Wolfowitz und Rumsfeld heute darüber denken, was sie im Nahen Osten angerichtet haben.
Erinnern Sie sich noch an Paul Wolfowitz? Das ist dieser kluge kleine Mann mit der sanften, leicht monotonen Stimme, der daran glaubte, dass die Iraker die US-Soldaten als ihre Befreier begrüßen würden. Er war die Nummer zwei im Pentagon, Stellvertreter des damaligen Verteidigungsministers Donald Rumsfeld, und ist heute Chef der Weltbank.
Wolfowitz ist das Schulbuchbeispiel für das Nebeneinander von Klugheit und Dummheit, oder um es netter auszudrücken: für die Koexistenz von Intellektualität und Naivität in einem Menschen.
Er war der Idealist, der sich darüber empörte, dass Amerika Diktaturen in Südkorea oder auf den Philippinen hinnahm, und er half dabei, daraus Demokratien zu machen. Ihn empörte gleichermaßen die Doppelmoral der amerikanischen Weltmacht im Nahen Osten: das Hinnehmen von Tyrannen oder Autokraten, wenn sie denn auf Öl saßen. Ihm schwebte eine Grand Strategy vor, und Irak sollte der Anfang sein. Demokratie auf Gottes Erdboden, überall: So sollte es sein, so will es die Geschichte.
Die US-Neokonservativen: Gescheiterte Ideologen
Fotostrecke starten: Klicken Sie auf ein Bild (8 Bilder)
Das ist ein schöner Traum, und dass er ihn geträumt hat, kann man ihm nicht vorwerfen. Man muß ihm aber vorwerfen, mit welcher Leichtfertigkeit Paul Wolfowitz Figuren wie Achmed Chalabi auf den Leim ging, wie begierig er dessen Behauptungen zu seinen eigenen machte und wie wenig Argwohn er, ein Intellektueller, seinen eigenen Prämissen schenkte.
Neue Ideen ausgerechnet zwei Tage vor dem Rücktritt
Wolfowitz ging als erster von denjenigen, die man halb zurecht, halb zu unrecht Neocons nannte. Er war wirklich ein Neocon, tief durchdrungen von der Aversion gegenüber lauer Liberalität, die sich mit dem Status quo abfindet, tief durchdrungen auch vom amerikanischen Idealismus, der gerne vieles falsch macht, aber am Ende doch das Richtige tut. So ähnlich hat Churchill seine Erfahrungen mit Amerika in ein Bonmot gefasst.
Foto: REUTERS
Video: ReutersDonald Rumsfeld ist kein Neocon, kein Idealist wie Wolfowitz. Er ist ein amerikanischer Nationalist, der Krieg gegen Saddam führen wollte, weil das gut für Amerika war, wie er meinte. Er wollte den Krieg gewinnen, mit wenigen Truppen und wenig Aufwand. Von Nation Building hielt er anders als die Neocons ziemlich wenig.
Die Neocons, die den Nahen Osten aufrollen wollten, hätten eigentlich mit einer großen Invasionsarmee die Sache regeln müssen. Die Nationalisten à la Rumsfeld oder Cheney wollten Vergeltung für den 11. September und hielten Saddam für gefährlicher als diese komischen Taliban in Afghanistan.
Zu den Treppenwitzen des Abenteuers gehört, dass Rumsfeld zwei Tage vor seinem Rücktritt Änderungen für den Irak einfielen. Zwei Tage vor dem Rücktritt. Als hätte er keine Zeit gehabt, vorher.
Bolton, Typ Betonkopf, Typ America First - als Uno-Diplomat
John Bolton gehörte zu den dienstbaren Geistern, zu den Hausknechten, die sich immer um starke Figuren wie Rumsfeld scharen. Douglas Feith war auch so einer. Erinnert sich noch einer an ihn? Er durfte Geheimdienstleute kujonieren, die sich erfrechten, anderer Meinung über die Massenvernichtungswaffen zu sein, als es das Pentagon und das Büro von Vizepräsident Cheney wollten. Bolton landete als Botschafter der Vereinigten Staaten von Amerika bei den Vereinten Nationen. Noch ein Treppenwitz: Bolton, Typ Betonkopf, Typ America First, bei der Uno. Als Diplomat. Er ist jetzt zurückgetreten. Endlich.
Man wüsste natürlich gerne, wie Wolfowitz, Rumsfeld und Bolton heute darüber denken, was sie im Irak angerichtet haben, im Irak und im Gefolge im ganzen Nahen Osten. Ärgern sie sich die Krätze über sich selber? Ergehen sich sich in What-Ifs: Was wäre gewesen, wenn wir's anders gemacht hätten? Trinken sie sich einen an, wenn sie länger darüber nachdenken, was da passiert ist? Treibt sie die Diskrepanz zwischen Idee und Durchführung in den Wahnsinn?
Die Neocons und Irak, das ist der Stoff, aus dem Antiamerikanismus entstanden ist, als könne es gar nicht anders sein. Die Idee aber, die dem Neokonservativismus zugrunde liegt, nämlich dass der Status quo nicht alles sein kann, jedenfalls nicht dann, wenn die Verhältnisse so trostlos und so ungerecht sind wie im Nahen Osten, lag damals und liegt immer noch ziemlich auf der Hand.
Welche Ironie der Geschichte, dass man diese Idee heute gegen beide verteidigen muß: gegen die Neocons und deren Verächter
Vielleicht sind das pfizerdebakel und das politdebakel auch als summe für den kursanstieg mitverantwortlich

Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10mal sehn wann die 10 dollar fallen

Antwort auf Beitrag Nr.: 26.005.522 von meislo am 07.12.06 19:47:59Wenn es so weitergeht, heute oder spätestens morgen...
Last Trade: 9.42
Trade Time: 2:10PM ET
Change: Up 0.55 (6.20%)
Prev Close: 8.87
Open: 9.09
Bid: 9.41 x 300
Ask: 9.42 x 500

Last Trade: 9.42
Trade Time: 2:10PM ET
Change: Up 0.55 (6.20%)
Prev Close: 8.87
Open: 9.09
Bid: 9.41 x 300
Ask: 9.42 x 500
Antwort auf Beitrag Nr.: 26.006.126 von cyberhai am 07.12.06 20:11:05das hört sich doch gut an...
http://www.finanznachrichten.de/nachrichten-2006-12/artikel-…
Wenn wir über 9,90 USD gehen ist der Weg bis 70 USD frei

Naja, die Fundamentaldaten sollten schon mitspielen
aber ich warte auch dreistellige Kurse ab
http://www.finanznachrichten.de/nachrichten-2006-12/artikel-…
Wenn wir über 9,90 USD gehen ist der Weg bis 70 USD frei


Naja, die Fundamentaldaten sollten schon mitspielen

aber ich warte auch dreistellige Kurse ab

Data Show Geron's Telomerase Inhibitor Cancer Drug is Active Against Cancer Stem Cells From Multiple Myeloma Patients
Monday December 11, 7:30 am ET
Other Presentation at ASH Annual Meeting Demonstrates Drug's Excellent Tolerability and Predictable Pharmacokinetics in Ongoing Clinical Trials
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) today announced that its telomerase inhibitor cancer drug, GRN163L, is active against cancer stem cells from multiple myeloma patients, according to data presented at the American Society of Hematology 48th Annual Meeting in Orlando, Fla.
ADVERTISEMENT
Resulting from a collaboration between Geron and investigators with the department of oncology at the Johns Hopkins University School of Medicine, the data demonstrated activity in a model derived from multiple cell lines as well as cells from fresh specimens taken from the bone marrow of multiple myeloma patients. Cancer stem cells, which are often resistant to standard treatments, are believed to be critically important to cancer's ability to replicate and spread throughout the body. Johns Hopkins' William Matusi, M.D., was the lead author of the study, which Richard J. Jones, M.D., presented.
"I believe the activity of GRN163L against cancer stem cells in multiple myeloma is very intriguing," said Dr. Jones, who is the director of the bone marrow transplant program and co-director of hematologic malignancies at Johns Hopkins' Sidney Kimmel Comprehensive Cancer Center. "Our data suggest that cancer stem cells, which are resistant to most agents currently in use in multiple myeloma, are the cause of disease relapse in many patients. Therefore, the ability to target cancer stem cells holds considerable clinical promise."
Specifically, the data demonstrated that GRN163L inhibited telomerase activity and eliminated the colony forming potential of cancer stem cells from three independent multiple myeloma cell lines. GRN163L also inhibited the clonogenic potential of more mature myeloma cells. In separate experiments using primary clinical samples, cancer stem cells isolated from the bone marrow of three patients with multiple myeloma and then exposed to GRN163L also had a marked reduction in clonogenic growth. Previous data using these models for agents commonly used in the treatment of multiple myeloma did not demonstrate similar effects on myeloma cancer stem cells.
In another presentation (Tressler, et al., Abstract #2595), Geron showed that GRN163L continues to demonstrate excellent tolerability and predictable pharmacokinetics in a Phase I/II trial in patients with chronic lymphocytic leukemia (CLL) and a Phase I trial in patients with solid tumors.
Subjects with CLL received increasing doses of GRN163L intravenously over six hours, while subjects in the solid tumor trial were administered similar doses over two hours. To date, all infusions in the first three dose cohorts of both trials were well tolerated with no dose-limiting toxicities (DLTs). Pharmacokinetic analysis demonstrated dose-proportionality over the range of doses tested. Peak plasma concentrations achieved were 3 mcg/ml and 10 mcg/ml in these initial cohorts of the CLL and solid tumor studies, respectively. Pre-clinically, telomerase activity within cancer cells can typically be inhibited by concentrations of 5 to 10 mcg/ml. These data support escalation to higher doses which are predicted to result in sustained exposure levels that fall within the therapeutic range.
"The early clinical data continue to be encouraging," said Alan Colowick, M.D., Geron's president, oncology. "The excellent tolerability and pharmacokinetics observed in the early cohorts enable us to advance to the therapeutic dose cohorts. Additionally, based upon the data generated from our collaboration with the group from Johns Hopkins demonstrating important effects of GRN163L against myeloma cancer stem cells, we plan to initiate a clinical trial in patients with multiple myeloma in the first half of 2007."
Background
Telomerase is a broadly applicable and critical tumor target. It is expressed in a broad array of malignant tumors, essential for malignant cell growth and absent or expressed transiently, typically at low levels, in most normal adult tissues.
GRN163L is a short chain oligonucleotide that has high resistance to nuclease digestion in blood and tissues and very high affinity and specificity for telomerase. The molecule has superior cellular and tissue penetration properties due to its proprietary chemistry and its 5' lipid chain. The drug is a specific inhibitor of telomerase enzymatic activity. The mechanism of action involves direct binding to the template region of telomerase and is distinct from that of other oligonucleotide drugs with "antisense" activity.
GRN163L has been demonstrated to have anti-tumor effects in a wide range of hematological and solid tumor models and appears to be unique in its observed effects on tumor stem cells: the rare, chemotherapy-resistant cancer cells that cause cancer recurrence.
Monday December 11, 7:30 am ET
Other Presentation at ASH Annual Meeting Demonstrates Drug's Excellent Tolerability and Predictable Pharmacokinetics in Ongoing Clinical Trials
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) today announced that its telomerase inhibitor cancer drug, GRN163L, is active against cancer stem cells from multiple myeloma patients, according to data presented at the American Society of Hematology 48th Annual Meeting in Orlando, Fla.
ADVERTISEMENT
Resulting from a collaboration between Geron and investigators with the department of oncology at the Johns Hopkins University School of Medicine, the data demonstrated activity in a model derived from multiple cell lines as well as cells from fresh specimens taken from the bone marrow of multiple myeloma patients. Cancer stem cells, which are often resistant to standard treatments, are believed to be critically important to cancer's ability to replicate and spread throughout the body. Johns Hopkins' William Matusi, M.D., was the lead author of the study, which Richard J. Jones, M.D., presented.
"I believe the activity of GRN163L against cancer stem cells in multiple myeloma is very intriguing," said Dr. Jones, who is the director of the bone marrow transplant program and co-director of hematologic malignancies at Johns Hopkins' Sidney Kimmel Comprehensive Cancer Center. "Our data suggest that cancer stem cells, which are resistant to most agents currently in use in multiple myeloma, are the cause of disease relapse in many patients. Therefore, the ability to target cancer stem cells holds considerable clinical promise."
Specifically, the data demonstrated that GRN163L inhibited telomerase activity and eliminated the colony forming potential of cancer stem cells from three independent multiple myeloma cell lines. GRN163L also inhibited the clonogenic potential of more mature myeloma cells. In separate experiments using primary clinical samples, cancer stem cells isolated from the bone marrow of three patients with multiple myeloma and then exposed to GRN163L also had a marked reduction in clonogenic growth. Previous data using these models for agents commonly used in the treatment of multiple myeloma did not demonstrate similar effects on myeloma cancer stem cells.
In another presentation (Tressler, et al., Abstract #2595), Geron showed that GRN163L continues to demonstrate excellent tolerability and predictable pharmacokinetics in a Phase I/II trial in patients with chronic lymphocytic leukemia (CLL) and a Phase I trial in patients with solid tumors.
Subjects with CLL received increasing doses of GRN163L intravenously over six hours, while subjects in the solid tumor trial were administered similar doses over two hours. To date, all infusions in the first three dose cohorts of both trials were well tolerated with no dose-limiting toxicities (DLTs). Pharmacokinetic analysis demonstrated dose-proportionality over the range of doses tested. Peak plasma concentrations achieved were 3 mcg/ml and 10 mcg/ml in these initial cohorts of the CLL and solid tumor studies, respectively. Pre-clinically, telomerase activity within cancer cells can typically be inhibited by concentrations of 5 to 10 mcg/ml. These data support escalation to higher doses which are predicted to result in sustained exposure levels that fall within the therapeutic range.
"The early clinical data continue to be encouraging," said Alan Colowick, M.D., Geron's president, oncology. "The excellent tolerability and pharmacokinetics observed in the early cohorts enable us to advance to the therapeutic dose cohorts. Additionally, based upon the data generated from our collaboration with the group from Johns Hopkins demonstrating important effects of GRN163L against myeloma cancer stem cells, we plan to initiate a clinical trial in patients with multiple myeloma in the first half of 2007."
Background
Telomerase is a broadly applicable and critical tumor target. It is expressed in a broad array of malignant tumors, essential for malignant cell growth and absent or expressed transiently, typically at low levels, in most normal adult tissues.
GRN163L is a short chain oligonucleotide that has high resistance to nuclease digestion in blood and tissues and very high affinity and specificity for telomerase. The molecule has superior cellular and tissue penetration properties due to its proprietary chemistry and its 5' lipid chain. The drug is a specific inhibitor of telomerase enzymatic activity. The mechanism of action involves direct binding to the template region of telomerase and is distinct from that of other oligonucleotide drugs with "antisense" activity.
GRN163L has been demonstrated to have anti-tumor effects in a wide range of hematological and solid tumor models and appears to be unique in its observed effects on tumor stem cells: the rare, chemotherapy-resistant cancer cells that cause cancer recurrence.
Data Show Geron's Telomerase Inhibitor Cancer Drug is Active Against Cancer Stem Cells From Multiple Myeloma Patients
Monday December 11, 7:30 am ET
Other Presentation at ASH Annual Meeting Demonstrates Drug's Excellent Tolerability and Predictable Pharmacokinetics in Ongoing Clinical Trials
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) today announced that its telomerase inhibitor cancer drug, GRN163L, is active against cancer stem cells from multiple myeloma patients, according to data presented at the American Society of Hematology 48th Annual Meeting in Orlando, Fla.
ADVERTISEMENT
Resulting from a collaboration between Geron and investigators with the department of oncology at the Johns Hopkins University School of Medicine, the data demonstrated activity in a model derived from multiple cell lines as well as cells from fresh specimens taken from the bone marrow of multiple myeloma patients. Cancer stem cells, which are often resistant to standard treatments, are believed to be critically important to cancer's ability to replicate and spread throughout the body. Johns Hopkins' William Matusi, M.D., was the lead author of the study, which Richard J. Jones, M.D., presented.
"I believe the activity of GRN163L against cancer stem cells in multiple myeloma is very intriguing," said Dr. Jones, who is the director of the bone marrow transplant program and co-director of hematologic malignancies at Johns Hopkins' Sidney Kimmel Comprehensive Cancer Center. "Our data suggest that cancer stem cells, which are resistant to most agents currently in use in multiple myeloma, are the cause of disease relapse in many patients. Therefore, the ability to target cancer stem cells holds considerable clinical promise."
Specifically, the data demonstrated that GRN163L inhibited telomerase activity and eliminated the colony forming potential of cancer stem cells from three independent multiple myeloma cell lines. GRN163L also inhibited the clonogenic potential of more mature myeloma cells. In separate experiments using primary clinical samples, cancer stem cells isolated from the bone marrow of three patients with multiple myeloma and then exposed to GRN163L also had a marked reduction in clonogenic growth. Previous data using these models for agents commonly used in the treatment of multiple myeloma did not demonstrate similar effects on myeloma cancer stem cells.
In another presentation (Tressler, et al., Abstract #2595), Geron showed that GRN163L continues to demonstrate excellent tolerability and predictable pharmacokinetics in a Phase I/II trial in patients with chronic lymphocytic leukemia (CLL) and a Phase I trial in patients with solid tumors.
Subjects with CLL received increasing doses of GRN163L intravenously over six hours, while subjects in the solid tumor trial were administered similar doses over two hours. To date, all infusions in the first three dose cohorts of both trials were well tolerated with no dose-limiting toxicities (DLTs). Pharmacokinetic analysis demonstrated dose-proportionality over the range of doses tested. Peak plasma concentrations achieved were 3 mcg/ml and 10 mcg/ml in these initial cohorts of the CLL and solid tumor studies, respectively. Pre-clinically, telomerase activity within cancer cells can typically be inhibited by concentrations of 5 to 10 mcg/ml. These data support escalation to higher doses which are predicted to result in sustained exposure levels that fall within the therapeutic range.
"The early clinical data continue to be encouraging," said Alan Colowick, M.D., Geron's president, oncology. "The excellent tolerability and pharmacokinetics observed in the early cohorts enable us to advance to the therapeutic dose cohorts. Additionally, based upon the data generated from our collaboration with the group from Johns Hopkins demonstrating important effects of GRN163L against myeloma cancer stem cells, we plan to initiate a clinical trial in patients with multiple myeloma in the first half of 2007."
Background
Telomerase is a broadly applicable and critical tumor target. It is expressed in a broad array of malignant tumors, essential for malignant cell growth and absent or expressed transiently, typically at low levels, in most normal adult tissues.
GRN163L is a short chain oligonucleotide that has high resistance to nuclease digestion in blood and tissues and very high affinity and specificity for telomerase. The molecule has superior cellular and tissue penetration properties due to its proprietary chemistry and its 5' lipid chain. The drug is a specific inhibitor of telomerase enzymatic activity. The mechanism of action involves direct binding to the template region of telomerase and is distinct from that of other oligonucleotide drugs with "antisense" activity.
GRN163L has been demonstrated to have anti-tumor effects in a wide range of hematological and solid tumor models and appears to be unique in its observed effects on tumor stem cells: the rare, chemotherapy-resistant cancer cells that cause cancer recurrence.
Monday December 11, 7:30 am ET
Other Presentation at ASH Annual Meeting Demonstrates Drug's Excellent Tolerability and Predictable Pharmacokinetics in Ongoing Clinical Trials
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) today announced that its telomerase inhibitor cancer drug, GRN163L, is active against cancer stem cells from multiple myeloma patients, according to data presented at the American Society of Hematology 48th Annual Meeting in Orlando, Fla.
ADVERTISEMENT
Resulting from a collaboration between Geron and investigators with the department of oncology at the Johns Hopkins University School of Medicine, the data demonstrated activity in a model derived from multiple cell lines as well as cells from fresh specimens taken from the bone marrow of multiple myeloma patients. Cancer stem cells, which are often resistant to standard treatments, are believed to be critically important to cancer's ability to replicate and spread throughout the body. Johns Hopkins' William Matusi, M.D., was the lead author of the study, which Richard J. Jones, M.D., presented.
"I believe the activity of GRN163L against cancer stem cells in multiple myeloma is very intriguing," said Dr. Jones, who is the director of the bone marrow transplant program and co-director of hematologic malignancies at Johns Hopkins' Sidney Kimmel Comprehensive Cancer Center. "Our data suggest that cancer stem cells, which are resistant to most agents currently in use in multiple myeloma, are the cause of disease relapse in many patients. Therefore, the ability to target cancer stem cells holds considerable clinical promise."
Specifically, the data demonstrated that GRN163L inhibited telomerase activity and eliminated the colony forming potential of cancer stem cells from three independent multiple myeloma cell lines. GRN163L also inhibited the clonogenic potential of more mature myeloma cells. In separate experiments using primary clinical samples, cancer stem cells isolated from the bone marrow of three patients with multiple myeloma and then exposed to GRN163L also had a marked reduction in clonogenic growth. Previous data using these models for agents commonly used in the treatment of multiple myeloma did not demonstrate similar effects on myeloma cancer stem cells.
In another presentation (Tressler, et al., Abstract #2595), Geron showed that GRN163L continues to demonstrate excellent tolerability and predictable pharmacokinetics in a Phase I/II trial in patients with chronic lymphocytic leukemia (CLL) and a Phase I trial in patients with solid tumors.
Subjects with CLL received increasing doses of GRN163L intravenously over six hours, while subjects in the solid tumor trial were administered similar doses over two hours. To date, all infusions in the first three dose cohorts of both trials were well tolerated with no dose-limiting toxicities (DLTs). Pharmacokinetic analysis demonstrated dose-proportionality over the range of doses tested. Peak plasma concentrations achieved were 3 mcg/ml and 10 mcg/ml in these initial cohorts of the CLL and solid tumor studies, respectively. Pre-clinically, telomerase activity within cancer cells can typically be inhibited by concentrations of 5 to 10 mcg/ml. These data support escalation to higher doses which are predicted to result in sustained exposure levels that fall within the therapeutic range.
"The early clinical data continue to be encouraging," said Alan Colowick, M.D., Geron's president, oncology. "The excellent tolerability and pharmacokinetics observed in the early cohorts enable us to advance to the therapeutic dose cohorts. Additionally, based upon the data generated from our collaboration with the group from Johns Hopkins demonstrating important effects of GRN163L against myeloma cancer stem cells, we plan to initiate a clinical trial in patients with multiple myeloma in the first half of 2007."
Background
Telomerase is a broadly applicable and critical tumor target. It is expressed in a broad array of malignant tumors, essential for malignant cell growth and absent or expressed transiently, typically at low levels, in most normal adult tissues.
GRN163L is a short chain oligonucleotide that has high resistance to nuclease digestion in blood and tissues and very high affinity and specificity for telomerase. The molecule has superior cellular and tissue penetration properties due to its proprietary chemistry and its 5' lipid chain. The drug is a specific inhibitor of telomerase enzymatic activity. The mechanism of action involves direct binding to the template region of telomerase and is distinct from that of other oligonucleotide drugs with "antisense" activity.
GRN163L has been demonstrated to have anti-tumor effects in a wide range of hematological and solid tumor models and appears to be unique in its observed effects on tumor stem cells: the rare, chemotherapy-resistant cancer cells that cause cancer recurrence.
Geron Plans to Start Human Cancer Study
Monday December 11, 8:57 am ET
Geron Plans to Begin Clinical Trials on Cancer Drug Candidate in 1st Half of 2007
MENLO PARK, Calif. (AP) -- Biotech drug developer Geron Corp. said Monday it plans to start human clinical trials on an experimental cancer treatment that attacks the stem cells thought responsible for relapses.
Shares of Geron rose 50 cents, or 5.4 percent, to $9.85 in premarket activity on the INET electronic exchange, after closing Friday at $9.35 on the Nasdaq. Shares have traded between $5.66 and $9.90 over the past 52 weeks.
Lab tests suggest that the company's GRN163L drug candidate acts against multiple myeloma, or cancer of the plasma cells that produce antibodies for the immune system. The company plans to begin a clinical trial on the drug in the first half of 2007.
Data suggests that the compound interferes with replication of cancer stem cells from three independent multiple myeloma cell lines.
Monday December 11, 8:57 am ET
Geron Plans to Begin Clinical Trials on Cancer Drug Candidate in 1st Half of 2007
MENLO PARK, Calif. (AP) -- Biotech drug developer Geron Corp. said Monday it plans to start human clinical trials on an experimental cancer treatment that attacks the stem cells thought responsible for relapses.
Shares of Geron rose 50 cents, or 5.4 percent, to $9.85 in premarket activity on the INET electronic exchange, after closing Friday at $9.35 on the Nasdaq. Shares have traded between $5.66 and $9.90 over the past 52 weeks.
Lab tests suggest that the company's GRN163L drug candidate acts against multiple myeloma, or cancer of the plasma cells that produce antibodies for the immune system. The company plans to begin a clinical trial on the drug in the first half of 2007.
Data suggests that the compound interferes with replication of cancer stem cells from three independent multiple myeloma cell lines.
Antwort auf Beitrag Nr.: 26.103.806 von meislo am 11.12.06 15:28:00Krebs - eine Stammzell-Krankheit
Gewandeltes Verständnis der Tumorentstehung
Ein Tumor gilt nicht mehr als Haufen entarteter Zellen, sondern als «Organ», das aus Krebsstammzellen und den daraus hervorgegangenen spezialisierten Tumorzellen besteht. Ob diese neue Sichtweise - wie erhofft - auch die Möglichkeiten der Krebstherapie verbessern wird, ist noch hypothetisch.
slz. Ein Tumor, das ist ein Haufen entarteter Zellen, die sich unaufhörlich teilen und so das umliegende Gewebe zerstören - so die bisherige Lehrmeinung. Doch offenbar ist dies nicht nur eine stark vereinfachte, sondern auch eine falsche Sicht der Dinge. Denn die Resultate einer Vielzahl von Experimenten, die während der letzten Monate insbesondere in den USA und in Kanada durchgeführt worden sind, stützen eine schon vor Jahrzehnten aufgestellte Hypothese, wonach Krebs als Stammzell-Krankheit anzusehen ist. Diese neue Definition hat nicht nur Bedeutung für das Verständnis von Tumorerkrankungen, sondern könnte auch neue Wege in der Bekämpfung von Krebsleiden eröffnen.
Ein Tumor gleicht einem Organ
Heute beschreiben Experten einen Tumor als ein «Organ», das - wie andere Organe auch - aus Zellen unterschiedlicher Funktionen besteht. Denn offenbar existieren in Krebsgeschwülsten eine Vielzahl von zwar entarteten, aber doch spezialisierten Zellen, die sich ständig teilen und so die Masse des Tumors bilden. Inmitten dieser «Arbeiterinnen» sitzen einige wenige «Königinnen», die sogenannten Krebsstammzellen. Nur diese Stammzellen sind in der Lage, den Tumor am Leben zu erhalten. Denn nur aus ihnen können sich bei der Zellteilung sowohl die spezialisierteren, mit normalen Gewebezellen vergleichbaren Tumorzellen mit einer definierten und endlichen Lebensdauer bilden als auch neue unsterbliche oder nahezu ewig lebende Stammzellen. Diese letztgenannte Fähigkeit einer Zelle nennt man auch Selbsterneuerungspotenzial.
Dieser Eigenschaft verdankt die Krebsstammzelle ihre Entdeckung. Als nämlich John Dick und seine Kollegen an der Universität von Toronto 1997 bei Patienten mit einer besonders aggressiven Form der Leukämie (akute myeloische Leukämie) Krebszellen entnahmen und sie in Mäuse injizierten, erkrankten nur sehr wenige der Tiere an diesem Blutkrebs. Somit schien klar, dass nicht alle, sondern nur eine kleine Minderheit der Leukämiezellen in der Lage waren, einen Tumor in einem neuen Organismus zu bilden. Dick postulierte damals, dass bei einer Leukämie im Blut eine Vielzahl von entarteten Blutzellen, aber nur wenige Krebsstammzellen vorhanden sind. Es gelang ihm sogar, solche Stammzellen zu isolieren und teilweise zu charakterisieren, so dass man heute spezifische Oberflächenproteine kennt, anhand deren man bei einer Leukämie die Krebsstammzellen aufspüren kann.
Der fundamentale Unterschied zwischen einer Krebsstammzelle und einer normalen Gewebestammzelle (zum Beispiel einer Blut-, Hirn- oder Hautstammzelle) ist, dass erstere einige fatale genetische Veränderungen angesammelt hat. Dies erläuterte John Dick kürzlich auf der vom Boehringer-Ingelheim-Fonds organisierten internationalen Titisee-Konferenz in Deutschland. Diese Mutationen führen dazu, dass die äusserst strikte Kontrolle, der eine Gewebestammzelle normalerweise unterliegt, teilweise oder ganz aufgehoben ist. Deswegen kann sich eine Krebsstammzelle ungehindert teilen. Und sie gibt diese Mutationen an alle ihre Tochterzellen weiter, so dass auch diese sich unkontrolliert teilen und schliesslich einen Tumor bilden. Im Verlauf der Zeit können die Krebszellen selber weitere Mutationen ansammeln, die das Wachstum der Geschwulst noch beschleunigen können.
Der Ursprungszelle auf der Spur
Noch ist allerdings nicht bewiesen, aus welcher Zelle sich die Krebsstammzelle bildet. Laut Dick hat man aber eine Reihe von Hinweisen dafür, dass eine normale Gewebestammzelle durch verschiedene Mutationen - diese können genetisch bedingt oder durch Umwelteinflüsse wie Chemikalien oder UV-Licht verursacht sein - zur Krebsstammzelle werden kann. Darauf deute die Expression verschiedener Proteine in der Krebsstammzelle, die sonst nur in gesunden Gewebestammzellen hergestellt würden. Zudem habe man bei Leukämiepatienten beobachtet, dass aus der Krebsstammzelle eine ganze Serie von spezialisierten, ebenfalls entarteten Blutzellen entstünden, die genau dieselben Mutationen wie die Krebsstammzelle aufwiesen; und nur aus einer Zelle, die wie die Gewebestammzelle weit oben in der Zellhierarchie stehe, könnten überhaupt verschiedenartig spezialisierte Zellen entstehen.
Dick erachtet es zudem als wahrscheinlicher, dass eine Zelle wie die Gewebestammzelle, die bereits das Potenzial zur Selbsterneuerung besitze, zur Krebsstammzelle entarte, und nicht eine differenzierte Zelle. Aber es sei, so betonten manche Experten in Titisee, nicht auszuschliessen, dass bei gewissen Krebsarten auch eine bereits teilweise spezialisierte Gewebezelle jene Mutationen erfahre, die sie wieder in den Zustand einer Stammzelle mit Selbsterneuerungspotenzial zurückversetzten. Wie das allerdings genau funktionieren soll, sei noch unklar. - In den letzten Monaten sind Hinweise dafür vorgelegt worden, dass Krebsstammzellen nicht nur bei Leukämien vorkommen. Michael Clarke und sein Team von der University of Michigan konnten die Existenz einer solchen Krebsstammzelle bei Brustkrebs zeigen, auch wenn es noch nicht gelang, eine einzelne solche Zelle zu isolieren. Peter Dirks und seine Kollegen vom Kinderspital in Toronto haben Hinweise gefunden, dass auch bei Gehirntumoren Krebsstammzellen existieren. Diese sind dadurch charakterisiert, dass sie ein für Stammzellen des Blutes oder des Gehirns typisches Protein (CD133) auf ihrer Oberfläche tragen. Nur solche Zellen aus einem Gehirntumor seien in der Lage, in Mäusen identische Krebsgeschwülste zu bilden, berichtete Dirks in Titisee. Kürzlich wurde auch beim Prostatakarzinom eine Population von Tumorzellen mit den typischen Eigenschaften von Stammzellen gefunden.
Hoffnung auf gezieltere Behandlung
Noch weiss man allerdings sehr wenig über die verschiedenen Krebsstammzellen. So kennt man beispielsweise von keiner ein für sie charakteristisches genetisches Profil. Experten gehen davon aus, dass viele, wenn nicht sogar alle Tumorerkrankungen letztlich auf eine entartete Stammzelle zurückgehen. Allerdings schwankt die Anzahl solcher Krebsstammzellen in einer Geschwulst offenbar beträchtlich. Während bei einer Leukämie laut Dick schätzungsweise nur 1 von 100 000 entarteten Blutzellen eine solche Stammzelle ist, können es bei einem speziellen Gehirntumor, dem Glioblastom, bis zu 20 Prozent der Krebszellen sein. Dick vermutet, dass die Aggressivität eines Tumors mit der Anzahl Krebsstammzellen korreliert: Je mehr dieser bösartigen Stammzellen vorhanden sind, desto schneller wächst der Tumor und desto früher beginnt er zu metastasieren.
Trotz den noch vielen offenen Fragen sind die neuen Erkenntnisse nicht nur die Bestätigung einer jahrzehntealten Theorie, wonach Krebs als Stammzell-Krankheit zu verstehen ist, sondern sie bergen auch interessante Möglichkeiten für die Behandlung von Tumorleiden. Denn wie Dick erläuterte, sind bisher die meisten Antitumor-Substanzen danach ausgesucht worden, dass sie die grosse Masse der sich teilenden Tumorzellen zerstörten. Doch mit solchen Mitteln würden die Krebsstammzellen, die andere Eigenschaften als normale Tumorzellen besässen und bei denen andere Gene aktiv seien, nicht erwischt.
Wirkungsnachweis an den Stammzellen
So wirkt etwa auch Imatinib (Glivec), ein neueres Medikament gegen eine Form der Leukämie, nur gegen die sich schnell und oft teilenden normalen Tumorzellen, wie Dick betonte, nicht aber gegen die Krebsstammzellen, die sich weniger oft teilen. Die Wahrscheinlichkeit für einen erneuten Ausbruch der Leukämie sei deshalb unter der Therapie mit diesem Medikament recht hoch. Und wie die Erfahrung in der Klinik zeige, erlitten auch viele Patienten mit anderen Tumorerkrankungen oft Jahre nach der ersten Therapie einen Rückfall. Für Dick sind die dafür verantwortlichen Zellen nicht irgendwelche Tumorzellen, die aus unbekannten Gründen die Attacke der Chemotherapie überleben. An dem Aufflammen der Erkrankung Monate oder Jahre später seien höchstwahrscheinlich immer Krebsstammzellen schuld, denen die gängigen Therapeutika nichts anhaben könnten.
Doch um gezielt auf die Krebsstammzellen abgestimmte Arzneimittel entwickeln zu können, müsse man diese Zellen erst noch genauer charakterisieren, waren sich in Titisee alle Experten einig. Denn nur wenn man wisse, welche Gene in den Tumorstammzellen aktiv seien und - damit verbunden - welche Proteine hergestellt würden, sei es möglich, spezifische Angriffsziele für die Therapie zu definieren. Zudem sollten die Testverfahren zur Evaluation von neuen Chemotherapeutika verändert werden, forderten die Wissenschafter. So müsse der Wirkungsnachweis künftig an isolierten Krebsstammzellen durchgeführt werden, um zu überprüfen, ob ein Medikamentenkandidat diese wichtige Zellart vernichten könne, ohne gleichzeitig die normalen Gewebestammzellen zu zerstören.
Weiterführende Literatur: Übersichtsartikel in Oncogene 23 (2004) und in Nature Reviews Cancer 5 (2005).
Krebsstammzellen nachweisen
slz. Um als Krebsstammzelle zu gelten, muss eine Tumorzelle derzeit folgenden Test bestehen. Zuerst werden die Tumorzellen eines Patienten aus dem Blut oder Gewebe isoliert und dann in einer passenden Nährlösung so weit verdünnt, dass nur noch wenige Zellen pro Milliliter, im Idealfall nur noch eine Zelle, vorhanden sind. Dann werden diese vereinzelten Zellen in Mäuse injiziert, die genetisch derart verändert sind, dass sie menschliche Zellen nicht abstossen. Bildet sich nun in diesem Tier ein Tumor, der mit demjenigen des Patienten identisch ist, so werden erneut diese Tumorzellen isoliert, verdünnt und in neue Mäuse injiziert. Bildet sich nun erneut ein Tumor, der demjenigen des Patienten gleicht, kann man laut John Dick von der Universität von Toronto, Kanada, davon ausgehen, dass es sich bei den isolierten Tumorzellen tatsächlich um Krebsstammzellen handelt. Denn wenn eine Tumorzelle diese Testserie bestanden habe, so sei klar, dass sie eigenständig in der Lage sei, in einem neuen Organismus einen Tumor mit den Eigenschaften des menschlichen Tumors auszubilden.
Gewandeltes Verständnis der Tumorentstehung
Ein Tumor gilt nicht mehr als Haufen entarteter Zellen, sondern als «Organ», das aus Krebsstammzellen und den daraus hervorgegangenen spezialisierten Tumorzellen besteht. Ob diese neue Sichtweise - wie erhofft - auch die Möglichkeiten der Krebstherapie verbessern wird, ist noch hypothetisch.
slz. Ein Tumor, das ist ein Haufen entarteter Zellen, die sich unaufhörlich teilen und so das umliegende Gewebe zerstören - so die bisherige Lehrmeinung. Doch offenbar ist dies nicht nur eine stark vereinfachte, sondern auch eine falsche Sicht der Dinge. Denn die Resultate einer Vielzahl von Experimenten, die während der letzten Monate insbesondere in den USA und in Kanada durchgeführt worden sind, stützen eine schon vor Jahrzehnten aufgestellte Hypothese, wonach Krebs als Stammzell-Krankheit anzusehen ist. Diese neue Definition hat nicht nur Bedeutung für das Verständnis von Tumorerkrankungen, sondern könnte auch neue Wege in der Bekämpfung von Krebsleiden eröffnen.
Ein Tumor gleicht einem Organ
Heute beschreiben Experten einen Tumor als ein «Organ», das - wie andere Organe auch - aus Zellen unterschiedlicher Funktionen besteht. Denn offenbar existieren in Krebsgeschwülsten eine Vielzahl von zwar entarteten, aber doch spezialisierten Zellen, die sich ständig teilen und so die Masse des Tumors bilden. Inmitten dieser «Arbeiterinnen» sitzen einige wenige «Königinnen», die sogenannten Krebsstammzellen. Nur diese Stammzellen sind in der Lage, den Tumor am Leben zu erhalten. Denn nur aus ihnen können sich bei der Zellteilung sowohl die spezialisierteren, mit normalen Gewebezellen vergleichbaren Tumorzellen mit einer definierten und endlichen Lebensdauer bilden als auch neue unsterbliche oder nahezu ewig lebende Stammzellen. Diese letztgenannte Fähigkeit einer Zelle nennt man auch Selbsterneuerungspotenzial.
Dieser Eigenschaft verdankt die Krebsstammzelle ihre Entdeckung. Als nämlich John Dick und seine Kollegen an der Universität von Toronto 1997 bei Patienten mit einer besonders aggressiven Form der Leukämie (akute myeloische Leukämie) Krebszellen entnahmen und sie in Mäuse injizierten, erkrankten nur sehr wenige der Tiere an diesem Blutkrebs. Somit schien klar, dass nicht alle, sondern nur eine kleine Minderheit der Leukämiezellen in der Lage waren, einen Tumor in einem neuen Organismus zu bilden. Dick postulierte damals, dass bei einer Leukämie im Blut eine Vielzahl von entarteten Blutzellen, aber nur wenige Krebsstammzellen vorhanden sind. Es gelang ihm sogar, solche Stammzellen zu isolieren und teilweise zu charakterisieren, so dass man heute spezifische Oberflächenproteine kennt, anhand deren man bei einer Leukämie die Krebsstammzellen aufspüren kann.
Der fundamentale Unterschied zwischen einer Krebsstammzelle und einer normalen Gewebestammzelle (zum Beispiel einer Blut-, Hirn- oder Hautstammzelle) ist, dass erstere einige fatale genetische Veränderungen angesammelt hat. Dies erläuterte John Dick kürzlich auf der vom Boehringer-Ingelheim-Fonds organisierten internationalen Titisee-Konferenz in Deutschland. Diese Mutationen führen dazu, dass die äusserst strikte Kontrolle, der eine Gewebestammzelle normalerweise unterliegt, teilweise oder ganz aufgehoben ist. Deswegen kann sich eine Krebsstammzelle ungehindert teilen. Und sie gibt diese Mutationen an alle ihre Tochterzellen weiter, so dass auch diese sich unkontrolliert teilen und schliesslich einen Tumor bilden. Im Verlauf der Zeit können die Krebszellen selber weitere Mutationen ansammeln, die das Wachstum der Geschwulst noch beschleunigen können.
Der Ursprungszelle auf der Spur
Noch ist allerdings nicht bewiesen, aus welcher Zelle sich die Krebsstammzelle bildet. Laut Dick hat man aber eine Reihe von Hinweisen dafür, dass eine normale Gewebestammzelle durch verschiedene Mutationen - diese können genetisch bedingt oder durch Umwelteinflüsse wie Chemikalien oder UV-Licht verursacht sein - zur Krebsstammzelle werden kann. Darauf deute die Expression verschiedener Proteine in der Krebsstammzelle, die sonst nur in gesunden Gewebestammzellen hergestellt würden. Zudem habe man bei Leukämiepatienten beobachtet, dass aus der Krebsstammzelle eine ganze Serie von spezialisierten, ebenfalls entarteten Blutzellen entstünden, die genau dieselben Mutationen wie die Krebsstammzelle aufwiesen; und nur aus einer Zelle, die wie die Gewebestammzelle weit oben in der Zellhierarchie stehe, könnten überhaupt verschiedenartig spezialisierte Zellen entstehen.
Dick erachtet es zudem als wahrscheinlicher, dass eine Zelle wie die Gewebestammzelle, die bereits das Potenzial zur Selbsterneuerung besitze, zur Krebsstammzelle entarte, und nicht eine differenzierte Zelle. Aber es sei, so betonten manche Experten in Titisee, nicht auszuschliessen, dass bei gewissen Krebsarten auch eine bereits teilweise spezialisierte Gewebezelle jene Mutationen erfahre, die sie wieder in den Zustand einer Stammzelle mit Selbsterneuerungspotenzial zurückversetzten. Wie das allerdings genau funktionieren soll, sei noch unklar. - In den letzten Monaten sind Hinweise dafür vorgelegt worden, dass Krebsstammzellen nicht nur bei Leukämien vorkommen. Michael Clarke und sein Team von der University of Michigan konnten die Existenz einer solchen Krebsstammzelle bei Brustkrebs zeigen, auch wenn es noch nicht gelang, eine einzelne solche Zelle zu isolieren. Peter Dirks und seine Kollegen vom Kinderspital in Toronto haben Hinweise gefunden, dass auch bei Gehirntumoren Krebsstammzellen existieren. Diese sind dadurch charakterisiert, dass sie ein für Stammzellen des Blutes oder des Gehirns typisches Protein (CD133) auf ihrer Oberfläche tragen. Nur solche Zellen aus einem Gehirntumor seien in der Lage, in Mäusen identische Krebsgeschwülste zu bilden, berichtete Dirks in Titisee. Kürzlich wurde auch beim Prostatakarzinom eine Population von Tumorzellen mit den typischen Eigenschaften von Stammzellen gefunden.
Hoffnung auf gezieltere Behandlung
Noch weiss man allerdings sehr wenig über die verschiedenen Krebsstammzellen. So kennt man beispielsweise von keiner ein für sie charakteristisches genetisches Profil. Experten gehen davon aus, dass viele, wenn nicht sogar alle Tumorerkrankungen letztlich auf eine entartete Stammzelle zurückgehen. Allerdings schwankt die Anzahl solcher Krebsstammzellen in einer Geschwulst offenbar beträchtlich. Während bei einer Leukämie laut Dick schätzungsweise nur 1 von 100 000 entarteten Blutzellen eine solche Stammzelle ist, können es bei einem speziellen Gehirntumor, dem Glioblastom, bis zu 20 Prozent der Krebszellen sein. Dick vermutet, dass die Aggressivität eines Tumors mit der Anzahl Krebsstammzellen korreliert: Je mehr dieser bösartigen Stammzellen vorhanden sind, desto schneller wächst der Tumor und desto früher beginnt er zu metastasieren.
Trotz den noch vielen offenen Fragen sind die neuen Erkenntnisse nicht nur die Bestätigung einer jahrzehntealten Theorie, wonach Krebs als Stammzell-Krankheit zu verstehen ist, sondern sie bergen auch interessante Möglichkeiten für die Behandlung von Tumorleiden. Denn wie Dick erläuterte, sind bisher die meisten Antitumor-Substanzen danach ausgesucht worden, dass sie die grosse Masse der sich teilenden Tumorzellen zerstörten. Doch mit solchen Mitteln würden die Krebsstammzellen, die andere Eigenschaften als normale Tumorzellen besässen und bei denen andere Gene aktiv seien, nicht erwischt.
Wirkungsnachweis an den Stammzellen
So wirkt etwa auch Imatinib (Glivec), ein neueres Medikament gegen eine Form der Leukämie, nur gegen die sich schnell und oft teilenden normalen Tumorzellen, wie Dick betonte, nicht aber gegen die Krebsstammzellen, die sich weniger oft teilen. Die Wahrscheinlichkeit für einen erneuten Ausbruch der Leukämie sei deshalb unter der Therapie mit diesem Medikament recht hoch. Und wie die Erfahrung in der Klinik zeige, erlitten auch viele Patienten mit anderen Tumorerkrankungen oft Jahre nach der ersten Therapie einen Rückfall. Für Dick sind die dafür verantwortlichen Zellen nicht irgendwelche Tumorzellen, die aus unbekannten Gründen die Attacke der Chemotherapie überleben. An dem Aufflammen der Erkrankung Monate oder Jahre später seien höchstwahrscheinlich immer Krebsstammzellen schuld, denen die gängigen Therapeutika nichts anhaben könnten.
Doch um gezielt auf die Krebsstammzellen abgestimmte Arzneimittel entwickeln zu können, müsse man diese Zellen erst noch genauer charakterisieren, waren sich in Titisee alle Experten einig. Denn nur wenn man wisse, welche Gene in den Tumorstammzellen aktiv seien und - damit verbunden - welche Proteine hergestellt würden, sei es möglich, spezifische Angriffsziele für die Therapie zu definieren. Zudem sollten die Testverfahren zur Evaluation von neuen Chemotherapeutika verändert werden, forderten die Wissenschafter. So müsse der Wirkungsnachweis künftig an isolierten Krebsstammzellen durchgeführt werden, um zu überprüfen, ob ein Medikamentenkandidat diese wichtige Zellart vernichten könne, ohne gleichzeitig die normalen Gewebestammzellen zu zerstören.
Weiterführende Literatur: Übersichtsartikel in Oncogene 23 (2004) und in Nature Reviews Cancer 5 (2005).
Krebsstammzellen nachweisen
slz. Um als Krebsstammzelle zu gelten, muss eine Tumorzelle derzeit folgenden Test bestehen. Zuerst werden die Tumorzellen eines Patienten aus dem Blut oder Gewebe isoliert und dann in einer passenden Nährlösung so weit verdünnt, dass nur noch wenige Zellen pro Milliliter, im Idealfall nur noch eine Zelle, vorhanden sind. Dann werden diese vereinzelten Zellen in Mäuse injiziert, die genetisch derart verändert sind, dass sie menschliche Zellen nicht abstossen. Bildet sich nun in diesem Tier ein Tumor, der mit demjenigen des Patienten identisch ist, so werden erneut diese Tumorzellen isoliert, verdünnt und in neue Mäuse injiziert. Bildet sich nun erneut ein Tumor, der demjenigen des Patienten gleicht, kann man laut John Dick von der Universität von Toronto, Kanada, davon ausgehen, dass es sich bei den isolierten Tumorzellen tatsächlich um Krebsstammzellen handelt. Denn wenn eine Tumorzelle diese Testserie bestanden habe, so sei klar, dass sie eigenständig in der Lage sei, in einem neuen Organismus einen Tumor mit den Eigenschaften des menschlichen Tumors auszubilden.
Antwort auf Beitrag Nr.: 26.109.025 von meislo am 11.12.06 19:07:51höchstinteressanter beitrag - danke meislo!
wenn an der krebsstammzelltheorie etwas oder mehr dran ist, dann sitzt geron mit grn163l auf einer platinader ungeahnten ausmaßes.
im moment hat geron eine market cap von um die 600 mio. usd. bei jetzigen stand der produkte sicher sehr stolz. bei realisierung einer neuen krebsstammzelltherapie aber ein witz. 50 mrd. market cap könnte das einmal wert sein - oder mehr.
geron zu halten ist nicht wie ein long drink, nein, sondern wie ein long joint...
grüße
wenn an der krebsstammzelltheorie etwas oder mehr dran ist, dann sitzt geron mit grn163l auf einer platinader ungeahnten ausmaßes.
im moment hat geron eine market cap von um die 600 mio. usd. bei jetzigen stand der produkte sicher sehr stolz. bei realisierung einer neuen krebsstammzelltherapie aber ein witz. 50 mrd. market cap könnte das einmal wert sein - oder mehr.
geron zu halten ist nicht wie ein long drink, nein, sondern wie ein long joint...

grüße
da die entdeckung von krebsstammzellen gerade erst beginnt und die forschung hier in anfängen begreift, worum es sich handelt, gibt es natürlich gegen diesen zelltyp derzeit kein therapeutikum. jedenfalls wirken die aktuellen chemotherapeutika nur gegen normale krebszellen.
wie wir wissen gibt es bei grn163l aber handfeste hinweise zur wirksamkeit auch gegen krebsstammzellen. aufgrund des eingriffs von grn163l in die telomerase-biologie der zelle (ob gesund oder cancerogen) ist das auch nicht weiter überraschend und passt ins system.
aber: geron hat damit - ohne es bisher zu wissen - einen enormen know-how-fortschritt gegenüber big pharma.
leute!!!
wir können nur hoffen, dass eben gerade big pharma nicht bald auf den gedanken kommt, geron zu schlucken!!! die gefahr ist immens, da die pfizers dieser welt dringend ihre pipelines füllen müssen.
geron für 1 mrd. usd (ca 50 % premium auf den akt. kurs) hergeben zu müssen, wäre wirklich tragisch...
wie wir wissen gibt es bei grn163l aber handfeste hinweise zur wirksamkeit auch gegen krebsstammzellen. aufgrund des eingriffs von grn163l in die telomerase-biologie der zelle (ob gesund oder cancerogen) ist das auch nicht weiter überraschend und passt ins system.
aber: geron hat damit - ohne es bisher zu wissen - einen enormen know-how-fortschritt gegenüber big pharma.
leute!!!
wir können nur hoffen, dass eben gerade big pharma nicht bald auf den gedanken kommt, geron zu schlucken!!! die gefahr ist immens, da die pfizers dieser welt dringend ihre pipelines füllen müssen.
geron für 1 mrd. usd (ca 50 % premium auf den akt. kurs) hergeben zu müssen, wäre wirklich tragisch...
Geron sammelt 40 Mio Dollar ein und plaziert die aktien zu 8 dollar
deshalb auch der kurs unter druck
7:32AM Geron announced it has entered into an agreement to sell common stock to institutional investors at $8.00 per share (GERN) 9.34 : Co announces it has entered into a definitive agreement to sell common stock to institutional investors at $8.00 per share, for gross proceeds of $40.0 mln. In connection with the sale, the co will issue warrants with a 75-day exercise period to purchase an additional $15.0 mln of common stock at the same price per share, and longer term warrants, exercisable after 180 days, to purchase 3.0 mln shares at a premium. The shares were offered through a prospectus supplement to the co's effective universal shelf registration statement. The co arranged the financing directly with the investors.
deshalb auch der kurs unter druck
7:32AM Geron announced it has entered into an agreement to sell common stock to institutional investors at $8.00 per share (GERN) 9.34 : Co announces it has entered into a definitive agreement to sell common stock to institutional investors at $8.00 per share, for gross proceeds of $40.0 mln. In connection with the sale, the co will issue warrants with a 75-day exercise period to purchase an additional $15.0 mln of common stock at the same price per share, and longer term warrants, exercisable after 180 days, to purchase 3.0 mln shares at a premium. The shares were offered through a prospectus supplement to the co's effective universal shelf registration statement. The co arranged the financing directly with the investors.
ich verstehe es nicht.
geron hat ca. 170 mio. usd cash, keine schulden. die burn-rate liegt bei ca. 50/60 mio. pro jahr, wenn die klinischen test ausgeweitet werden. also sollte geron für mind. 3 jahre finanziert sein...
ok, geld muss irgendwann wieder rein, aber muss es denn gerade jetzt sein? in 1-2 jahren wäre das doch auch gegangen - zu dann hoffentlich weit höheren kursen und damit geringerer verwässerung als heute.
tssss?! bescheuert.
eines aber ist gut daran: 5 mio. aktien konnten offensichtlich easy plaziert werden. evtl. deshalb, weil geron den investoren signalisierte, dass demnächst gute nachrichten den kurs befeuern werden.
blöder tag heute.
grüße
geron hat ca. 170 mio. usd cash, keine schulden. die burn-rate liegt bei ca. 50/60 mio. pro jahr, wenn die klinischen test ausgeweitet werden. also sollte geron für mind. 3 jahre finanziert sein...
ok, geld muss irgendwann wieder rein, aber muss es denn gerade jetzt sein? in 1-2 jahren wäre das doch auch gegangen - zu dann hoffentlich weit höheren kursen und damit geringerer verwässerung als heute.
tssss?! bescheuert.
eines aber ist gut daran: 5 mio. aktien konnten offensichtlich easy plaziert werden. evtl. deshalb, weil geron den investoren signalisierte, dass demnächst gute nachrichten den kurs befeuern werden.
blöder tag heute.
grüße
Antwort auf Beitrag Nr.: 26.185.222 von LuckyCat am 14.12.06 20:20:27bin selber auch über den finanzhunger überreascht und teile deine meinung
14.12.2006 15:23
Geron verschafft sich $40 Mio aus Aktienverkauf
Die im Bereich Biopharmazie tätige Geron Corp. will aus dem Verkauf von Stammaktien an institutionelle Investoren Mehreinnahmen von 40 Millionen Dollar generieren. Der Verkauf der Papiere soll zu jeweils 8 Dollar erfolgen. Am Mittwoch schloss der Wert bei 9,34 Dollar. Der Deal beinhaltet eine Mehrzuteilungsoption zum selben Preisniveau von 15 Millionen Dollar sowie eine längerfristige Ermächtigung zum Kauf von 3 Millionen Anteilen zu einem nicht genannten Prämienbetrag.
Wie Geron am Donnerstag weiter mitteilte, sollen die Mehreinnahmen der Verwendung von klinischen Versuchen und Behördenangelegenheiten dienen. Für 2007 steht ein klnischer Versuch für einen Krebsimpfstoff auf dem Plan. Zudem werde ein klinischer Versuch für TAT0002 zur Aktivierung von Telomerase für Patienten mit HIV/AIDS in Gang gesetzt. Zudem stehe die Anmeldung für eine erforschte neue Anwendung für die von menschlichen embryonalen Stammzellen abgezweigten therapeutischen Zellen zur Behandlung von Rückenmarksverletzungen bevor. Die neuen Mittel sollen ebenso zur Finanzierung von meheren Versuchen zu dem Telomerase-Präparat GRN163L herangezogen werden.

14.12.2006 15:23
Geron verschafft sich $40 Mio aus Aktienverkauf
Die im Bereich Biopharmazie tätige Geron Corp. will aus dem Verkauf von Stammaktien an institutionelle Investoren Mehreinnahmen von 40 Millionen Dollar generieren. Der Verkauf der Papiere soll zu jeweils 8 Dollar erfolgen. Am Mittwoch schloss der Wert bei 9,34 Dollar. Der Deal beinhaltet eine Mehrzuteilungsoption zum selben Preisniveau von 15 Millionen Dollar sowie eine längerfristige Ermächtigung zum Kauf von 3 Millionen Anteilen zu einem nicht genannten Prämienbetrag.
Wie Geron am Donnerstag weiter mitteilte, sollen die Mehreinnahmen der Verwendung von klinischen Versuchen und Behördenangelegenheiten dienen. Für 2007 steht ein klnischer Versuch für einen Krebsimpfstoff auf dem Plan. Zudem werde ein klinischer Versuch für TAT0002 zur Aktivierung von Telomerase für Patienten mit HIV/AIDS in Gang gesetzt. Zudem stehe die Anmeldung für eine erforschte neue Anwendung für die von menschlichen embryonalen Stammzellen abgezweigten therapeutischen Zellen zur Behandlung von Rückenmarksverletzungen bevor. Die neuen Mittel sollen ebenso zur Finanzierung von meheren Versuchen zu dem Telomerase-Präparat GRN163L herangezogen werden.
Antwort auf Beitrag Nr.: 26.185.222 von LuckyCat am 14.12.06 20:20:27Großer Mist ist das, aber gut. Was will man machen. An Gerons Potenzial ändert das nichts, ich hoffe auch nicht, dass es am Potenzial der Aktie etwas ändert.
Wann rechnet ihr denn wieder mit News zu gern163l? Die uns wirklich weiterbringen könnten, meine ich? 1. Halbjahr 07?
Gruß, greenhorn
Wann rechnet ihr denn wieder mit News zu gern163l? Die uns wirklich weiterbringen könnten, meine ich? 1. Halbjahr 07?
Gruß, greenhorn
Geron says it's Telomerase inhibitor drug may benefit breast cancer patients receiving radiation therapy (GERN) 8.84 : Co says that its telomerase inhibitor drug, GRN163L, may benefit breast cancer patients receiving radiation therapy, according to the results of a study published online in the International Journal of Radiation Oncology, Biology and Physics. Co says the paper documents a substantial synergistic effect of GRN163L and radiation on breast cancer cells in vitro and in mice bearing human breast cancer. The study is the first to demonstrate the utility of GRN163L as a radiation sensitizer in cancer
heute gute umsätze und die 9 dollarmarke erklommen

Hat nicht ganz gereicht
Nur 64% stimmten für de förderung der embryobalen Stammzellenforschung 66,7% hätten es sein müssen
AP
Ahead of the Bell: Stem-Cell Researchers
Friday January 12, 9:24 am ET
Stem-Cell Researchers Still Face Uncertainty Over Government Funding After House Vote
NEW YORK (AP) -- Stem cell researchers still face uncertainty over their eligibilty for government funding, a day after lawmakers failed to garner enough votes to skirt an expected veto from President Bush on a bill promoting embryonic stem cell research.
ADVERTISEMENT
The Democratic-controlled House of Representatives passed the bill with a 253-174 vote -- short of the two-thirds margin needed to overturn a presidential veto.
Bush vetoed identical legislation last summer, and the White House on Thursday promised he would veto it again.
Advocates say embryonic stem cell research shows promise for numerous medical cures, but it typically involves the destruction of frozen embryos created for in vitro fertilization -- a step that stirs fierce opposition among anti-abortion lawmakers and like-minded constituents.
Shares of stem cell researchers rallied in the days before the widely publicized vote, but in Friday premarket trading, StemCells Inc. fell 18 cents, or 5.4 percent to $3.17, and Geron Corp. dropped 20 cents or 2.3 percent to $8.70.
Nur 64% stimmten für de förderung der embryobalen Stammzellenforschung 66,7% hätten es sein müssen
AP
Ahead of the Bell: Stem-Cell Researchers
Friday January 12, 9:24 am ET
Stem-Cell Researchers Still Face Uncertainty Over Government Funding After House Vote
NEW YORK (AP) -- Stem cell researchers still face uncertainty over their eligibilty for government funding, a day after lawmakers failed to garner enough votes to skirt an expected veto from President Bush on a bill promoting embryonic stem cell research.
ADVERTISEMENT
The Democratic-controlled House of Representatives passed the bill with a 253-174 vote -- short of the two-thirds margin needed to overturn a presidential veto.
Bush vetoed identical legislation last summer, and the White House on Thursday promised he would veto it again.
Advocates say embryonic stem cell research shows promise for numerous medical cures, but it typically involves the destruction of frozen embryos created for in vitro fertilization -- a step that stirs fierce opposition among anti-abortion lawmakers and like-minded constituents.
Shares of stem cell researchers rallied in the days before the widely publicized vote, but in Friday premarket trading, StemCells Inc. fell 18 cents, or 5.4 percent to $3.17, and Geron Corp. dropped 20 cents or 2.3 percent to $8.70.
Das Biotechnologieunternehmen Geron Corp. weist in Sudien auf die Produktion von Nervenzellenwachstum mit Hilfe embryonaler Stammzellen hin. Zudem stimuliere ein Protein das Überleben und die Regeneration der von Unfällen geschädigten Nervenzellen im Bereich der Wirbelsäule. Die veröffentlichten Studien beschreiben zudem eine neue Wirkung von Gerons GRNOPC1-Therapie, die in Tierversuchen bei Verletzungen der Wirbelsäule und der Nervenstränge angewendet worden ist.
Geron legen vorbörslich um 4,5% auf 9,04 Dollar zu
(HC)
Geron legen vorbörslich um 4,5% auf 9,04 Dollar zu
(HC)
GERON springt vorbörslich nach oben - Jetzt Rallye?
Geron (Nachrichten) (GERN / ISIN: US3741631036) : 9,00 $ (+4,05%)
Aktueller Tageschart (log) seit März 2006 (1 Kerze = 1 Tag)
Rückblick: Die GERON Aktie erreichte im Dezember den zentralen Kreuzwiderstand bei 9,75 - 9,90 $ und prallte daran nach unten hin ab. In den vergangenen Wochen korrigierte die Aktie moderat bis an den EMA50. Heute springt sie nach einer Meldung vorbörslich deutlich nach oben und wird zur Handelseröffnung im Preisbereich um 9,00 $ erwartet. Damit könnte die Zwischenkorrektur nun beendet werden.
Charttechnischer Ausblick: Steigt die Aktie jetzt per Tagesschluss über die letzten Zwischenhochs bei 9,24 $ an, sollte der zentralen Kreuzwiderstand bei 9,70 - 9,75 $ wieder erreicht werden. Ein Anstieg per Tages- und Wochenschluss über 9,75 $ per Wochenschluss generiert ein mittelfristiges Kaufsignal mit Zielen bei ca. 12,00 und 16,80 $. Fällt sie hingegen per Tagesschluss unter den EMA50 bei 8,55 $ zurück, wird eine Ausdehnung der Zwischenkorrektur bis 7,75 - 7,80 und ggf. 7,20 - 7,33 $ wahrscheinlich.
Meldung: Geron erreicht Fortschritte mit Stamzellen bei verletzten Nerven
Das Biotechnologieunternehmen Geron Corp. weist in Sudien auf die Produktion von Nervenzellenwachstum mit Hilfe embryonaler Stammzellen hin. Zudem stimuliere ein Protein das Überleben und die Regeneration der von Unfällen geschädigten Nervenzellen im Bereich der Wirbelsäule. Die veröffentlichten Studien beschreiben zudem eine neue Wirkung von Gerons GRNOPC1-Therapie, die in Tierversuchen bei Verletzungen der Wirbelsäule und der Nervenstränge angewendet worden ist.

Geron (Nachrichten) (GERN / ISIN: US3741631036) : 9,00 $ (+4,05%)
Aktueller Tageschart (log) seit März 2006 (1 Kerze = 1 Tag)
Rückblick: Die GERON Aktie erreichte im Dezember den zentralen Kreuzwiderstand bei 9,75 - 9,90 $ und prallte daran nach unten hin ab. In den vergangenen Wochen korrigierte die Aktie moderat bis an den EMA50. Heute springt sie nach einer Meldung vorbörslich deutlich nach oben und wird zur Handelseröffnung im Preisbereich um 9,00 $ erwartet. Damit könnte die Zwischenkorrektur nun beendet werden.
Charttechnischer Ausblick: Steigt die Aktie jetzt per Tagesschluss über die letzten Zwischenhochs bei 9,24 $ an, sollte der zentralen Kreuzwiderstand bei 9,70 - 9,75 $ wieder erreicht werden. Ein Anstieg per Tages- und Wochenschluss über 9,75 $ per Wochenschluss generiert ein mittelfristiges Kaufsignal mit Zielen bei ca. 12,00 und 16,80 $. Fällt sie hingegen per Tagesschluss unter den EMA50 bei 8,55 $ zurück, wird eine Ausdehnung der Zwischenkorrektur bis 7,75 - 7,80 und ggf. 7,20 - 7,33 $ wahrscheinlich.
Meldung: Geron erreicht Fortschritte mit Stamzellen bei verletzten Nerven
Das Biotechnologieunternehmen Geron Corp. weist in Sudien auf die Produktion von Nervenzellenwachstum mit Hilfe embryonaler Stammzellen hin. Zudem stimuliere ein Protein das Überleben und die Regeneration der von Unfällen geschädigten Nervenzellen im Bereich der Wirbelsäule. Die veröffentlichten Studien beschreiben zudem eine neue Wirkung von Gerons GRNOPC1-Therapie, die in Tierversuchen bei Verletzungen der Wirbelsäule und der Nervenstränge angewendet worden ist.

@ alle, die noch in gern investiert sind:
wir stehen am vorabend einer biotech-revolution und es ist ruhig, sehr ruhig geworden um geron - zumindest hier im board, und vielleicht auch sonst irgendwie. von intensiver diskussion und medieninteresse keine spur! das war schon einige male ganz anders.
2007 wird das jahr, das wichtigste jahr für geron seit unternehmensgründung.
aber es ist ruhig... nenneswertes interesse ist fast nicht auszumachen.
der klassische kontraindikator?
ich gehe auf jeden fall davon aus. wirkliche perlen sind nur die, die gerade nicht in der sonne glänzen, sondern diejenigen, die in ihr glänzen werden.
A U F W A C H E N
wir stehen am vorabend einer biotech-revolution und es ist ruhig, sehr ruhig geworden um geron - zumindest hier im board, und vielleicht auch sonst irgendwie. von intensiver diskussion und medieninteresse keine spur! das war schon einige male ganz anders.
2007 wird das jahr, das wichtigste jahr für geron seit unternehmensgründung.
aber es ist ruhig... nenneswertes interesse ist fast nicht auszumachen.
der klassische kontraindikator?
ich gehe auf jeden fall davon aus. wirkliche perlen sind nur die, die gerade nicht in der sonne glänzen, sondern diejenigen, die in ihr glänzen werden.
A U F W A C H E N
Ärzte Zeitung, 02.02.2007
Forscher entdecken Krebsstammzelle
ANN ARBOR (ple). In Gewebeproben von zehn Patienten mit Pankreas-Ca haben US-Forscher jene Stammzellen identifiziert, aus denen die Tumoren hervorgingen (Februar-Ausgabe von "Cancer Research").
Charakteristikum dieser seltenen Zellen ist die Kombination der Marker CD44, CD24 plus das Antigen ESA. Die Entdeckung gibt der These Auftrieb, dass nur Stammzellen Ausgangspunkt für Tumoren sind.
siehe dazu beitrag #2056
Forscher entdecken Krebsstammzelle
ANN ARBOR (ple). In Gewebeproben von zehn Patienten mit Pankreas-Ca haben US-Forscher jene Stammzellen identifiziert, aus denen die Tumoren hervorgingen (Februar-Ausgabe von "Cancer Research").
Charakteristikum dieser seltenen Zellen ist die Kombination der Marker CD44, CD24 plus das Antigen ESA. Die Entdeckung gibt der These Auftrieb, dass nur Stammzellen Ausgangspunkt für Tumoren sind.
siehe dazu beitrag #2056
Habe Geron schon seit über 2 Jahren auf der Watchlist und denke, man könnte nun vielleicht mal eine erste spekulative Position eingehen. Allerdings bin ich mir auch über die erheblichen Risiken dieses Investments im Klaren, wobei sich unterdessen m.E. allerdings hinreichend konkretisiert hat, dass Geron binnen der nächsten 6 - 7 Jahre den Durchbruch zu einem profitablen Unternehmen gelingen kann. Vor diesem Hintergrund relativiert sich die noch immer ambitionierte Bewertung von Geron.
Bei einem Kurs um die 6 € werde ich also mal zugreifen.
Meine Meinung.
Bei einem Kurs um die 6 € werde ich also mal zugreifen.
Meine Meinung.
und wieder eine konferenz und nichts wirklich neues zu grn163l.
bei geron muss man ewig warten - geduld für invetoren...
bei geron muss man ewig warten - geduld für invetoren...
:31AM Geron says unique structure of it's telomerase inhibitor drug promotes anti-tumor, anti-metastatic activity in lung cancer cells (GERN) 7.97 : Co announces the publication of preclinical data that show specific structural elements of GRN163L contribute to its unique anti-tumor and anti-metastatic activity. The studies demonstrated that GRN163L induces altered tumor cell adhesion in animal models of lung cancer and that it may have additional benefit in the prevention of metastasis. "These data contribute to the growing body of evidence regarding the anti-tumor effects of GRN163L... Based on these and other data, Geron intends to initiate a clinical trial this year in patients with lung cancer to determine if these results translate into clinically important anti-tumor activity."
Hier mehr
http://biz.yahoo.com/bw/070215/20070215005196.html?.v=1
Hier mehr
http://biz.yahoo.com/bw/070215/20070215005196.html?.v=1
Aus dem Labor in das Rückenmark
Embryonale Stammzellen sollen erstmals therapeutisch eingesetzt werden
Von Michael Lange
Medizin. - Embryonale Stammzellen gelten als Heilsbringer, geht es um bislang unheilbare Leiden wie Parkinson, Alzheimer oder Querschnittlähmungen. Jetzt will ein US-Biotech-Unternehmen Stammzellen direkt an Patienten einsetzen.
Embryonale Stammzellen des Menschen gelten als Hoffnungsträger Nummer eins für die Medizin der Zukunft. Wenn es um die Einsatzmöglichkeiten geht, ist immer wieder von der Parkinson-Krankheit, der Alzheimerschen Erkrankung und von Rückenmark-Verletzungen die Rede. Nun sollen die embryonalen Stammzellen erstmals am Menschen getestet werden, und zwar bei Rückenmarkverletzten. Das hat die US-amerikanische Firma Geron jetzt angekündigt. Dazu der Geschäftsführer des Unternehmens Thomas Okarma.
Bei unserem Produkt handelt es sich um lebende Zellen, die wir aus menschlichen embryonalen Stammzellen hergestellt haben. Es sind die gleichen Zellen, mit denen wir Rückenmarkverletzungen bei Tieren behandelt haben. Im nächsten Jahr werden wir sie zur Behandlung von querschnittgelähmten Patienten einsetzen.
Ursprünglich war der erste klinische Einsatz der Zellen bereits für dieses Jahr geplant. Nun heißt es bei Geron: Im ersten Quartal 2008 geht es los. Das Risiko von Nebenwirkungen wie Tumoren oder Abstoßungsreaktionen durch das körpereigene Immunsystem seien gering, betont Thomas Okarma. Denn es würden nicht embryonale Stammzellen direkt in die Patienten gespritzt, sondern Zellen, die aus embryonalen Stammzellen hervor gegangen sind: So genannte Gliazellen. Sie umhüllen die Nervenzellen, schützen und ernähren sie. Und sie isolieren die Nervenfasern.
Bei Rückenmarkverletzungen sind die Nerven in der Regel nicht durchschnitten. Aber die Gliazellen sterben ab. Die Nerven verlieren ihre Isolierung und können die Nervensignale nicht mehr übertragen. Deshalb sind die Betroffenen von ihrer Verletzung abwärts gelähmt. Die Zellen, die wir herstellen, werden direkt in die Verletzungsstelle hineingespritzt. Dort leben sie weiter und stellen die zerstörte Isolierung der Nerven wieder her.
Vielen Stammzellenforschern geht das zu schnell. Sie würden gerne weitere Laborexperimente abwarten, bevor der Schritt in die Praxis gewagt wird. Oliver Brüstle vom Institut für rekonstruktive Neurobiologie der Universität Bonn:
Ich halte das für früh, für zu riskant. Wenn hier auch nur in wenigen Fällen Schwierigkeiten auftreten, könnte das nachteilige Auswirkungen für die Patienten haben, gleichzeitig aber auch nachteilige Auswirkungen für das Forschungsfeld, wenn eine Technologie zu früh in die Anwendung gepresst wird, bevor alle Zwischenschritte systematisch durchlaufen worden sind.
Dazu gehören Experimente an Affen, die eher mit dem Menschen vergleichbar sind als die bisher als Versuchstiere dienenden Ratten. Thomas Okarma betont hingegen: Alle Probleme seien gelöst. Die Tierversuche an Ratten hätten eindeutig gezeigt, dass die verwendeten Zellen keine embryonalen Tumore, so genannte Teratome, bilden. Auch Abstoßungsreaktionen des Immunsystems der Patienten gegen die fremden Zellen erwartet er nicht.
Im Tierversuch haben wir keine Immunreaktion gegen die menschlichen Gliazellen beobachtet. Die ursprüngliche Idee war ja, dass man für jeden Patienten individuelle Stammzellen herstellen muss: Durch Zellkerntransfer, das so genannte "Therapeutische Klonen". Diese Annahme hat sich als falsch erwiesen, wegen der besonderen Eigenschaften der embryonalen Stammzellen. Das gilt auch für alle Zellen, die aus ihnen hervorgegangen sind. Sie werden vom menschlichen Immunsystem nicht als fremd erkannt. Der Kerntransfer ist deshalb für diese Therapie völlig unnötig.
Thomas Okarma ist sich sicher: alle Voraussetzungen für den Schritt zum Menschen sind gegeben. Das letzte Wort hat freilich nicht die Firma Geron, sondern die amerikanische Zulassungsbehörde, die Food and Drug Administration, FDA. Ende des Jahres wird sie über den Antrag von Geron entscheiden.
Embryonale Stammzellen sollen erstmals therapeutisch eingesetzt werden
Von Michael Lange
Medizin. - Embryonale Stammzellen gelten als Heilsbringer, geht es um bislang unheilbare Leiden wie Parkinson, Alzheimer oder Querschnittlähmungen. Jetzt will ein US-Biotech-Unternehmen Stammzellen direkt an Patienten einsetzen.
Embryonale Stammzellen des Menschen gelten als Hoffnungsträger Nummer eins für die Medizin der Zukunft. Wenn es um die Einsatzmöglichkeiten geht, ist immer wieder von der Parkinson-Krankheit, der Alzheimerschen Erkrankung und von Rückenmark-Verletzungen die Rede. Nun sollen die embryonalen Stammzellen erstmals am Menschen getestet werden, und zwar bei Rückenmarkverletzten. Das hat die US-amerikanische Firma Geron jetzt angekündigt. Dazu der Geschäftsführer des Unternehmens Thomas Okarma.
Bei unserem Produkt handelt es sich um lebende Zellen, die wir aus menschlichen embryonalen Stammzellen hergestellt haben. Es sind die gleichen Zellen, mit denen wir Rückenmarkverletzungen bei Tieren behandelt haben. Im nächsten Jahr werden wir sie zur Behandlung von querschnittgelähmten Patienten einsetzen.
Ursprünglich war der erste klinische Einsatz der Zellen bereits für dieses Jahr geplant. Nun heißt es bei Geron: Im ersten Quartal 2008 geht es los. Das Risiko von Nebenwirkungen wie Tumoren oder Abstoßungsreaktionen durch das körpereigene Immunsystem seien gering, betont Thomas Okarma. Denn es würden nicht embryonale Stammzellen direkt in die Patienten gespritzt, sondern Zellen, die aus embryonalen Stammzellen hervor gegangen sind: So genannte Gliazellen. Sie umhüllen die Nervenzellen, schützen und ernähren sie. Und sie isolieren die Nervenfasern.
Bei Rückenmarkverletzungen sind die Nerven in der Regel nicht durchschnitten. Aber die Gliazellen sterben ab. Die Nerven verlieren ihre Isolierung und können die Nervensignale nicht mehr übertragen. Deshalb sind die Betroffenen von ihrer Verletzung abwärts gelähmt. Die Zellen, die wir herstellen, werden direkt in die Verletzungsstelle hineingespritzt. Dort leben sie weiter und stellen die zerstörte Isolierung der Nerven wieder her.
Vielen Stammzellenforschern geht das zu schnell. Sie würden gerne weitere Laborexperimente abwarten, bevor der Schritt in die Praxis gewagt wird. Oliver Brüstle vom Institut für rekonstruktive Neurobiologie der Universität Bonn:
Ich halte das für früh, für zu riskant. Wenn hier auch nur in wenigen Fällen Schwierigkeiten auftreten, könnte das nachteilige Auswirkungen für die Patienten haben, gleichzeitig aber auch nachteilige Auswirkungen für das Forschungsfeld, wenn eine Technologie zu früh in die Anwendung gepresst wird, bevor alle Zwischenschritte systematisch durchlaufen worden sind.
Dazu gehören Experimente an Affen, die eher mit dem Menschen vergleichbar sind als die bisher als Versuchstiere dienenden Ratten. Thomas Okarma betont hingegen: Alle Probleme seien gelöst. Die Tierversuche an Ratten hätten eindeutig gezeigt, dass die verwendeten Zellen keine embryonalen Tumore, so genannte Teratome, bilden. Auch Abstoßungsreaktionen des Immunsystems der Patienten gegen die fremden Zellen erwartet er nicht.
Im Tierversuch haben wir keine Immunreaktion gegen die menschlichen Gliazellen beobachtet. Die ursprüngliche Idee war ja, dass man für jeden Patienten individuelle Stammzellen herstellen muss: Durch Zellkerntransfer, das so genannte "Therapeutische Klonen". Diese Annahme hat sich als falsch erwiesen, wegen der besonderen Eigenschaften der embryonalen Stammzellen. Das gilt auch für alle Zellen, die aus ihnen hervorgegangen sind. Sie werden vom menschlichen Immunsystem nicht als fremd erkannt. Der Kerntransfer ist deshalb für diese Therapie völlig unnötig.
Thomas Okarma ist sich sicher: alle Voraussetzungen für den Schritt zum Menschen sind gegeben. Das letzte Wort hat freilich nicht die Firma Geron, sondern die amerikanische Zulassungsbehörde, die Food and Drug Administration, FDA. Ende des Jahres wird sie über den Antrag von Geron entscheiden.
Servus!
Hatten wir glaube ich noch nicht.
Geron Corp. sells license to company for anti-aging treatments
Monday March 12, 1:36 pm ET
Geron Corp. said Monday it licensed its technology to Asia Biotech Corp. for use by a subsidiary in cosmetic and non-therapeutic treatments that, according to the subsidiary's web site, will make customers' cells "young again."
Menlo Park-based Geron (NASDAQ: GERN - News) didn't give any details about the license deal. Telomerase Activation Sciences, a wholly owned subsidiary of Asia Biotech based in New York, will used Geron's technology, which affects the telomerases at the end of chromosomes, in its cosmetic treatments and dietary supplements.
On its web site, Telomease Activation says in a tiny footnote that by "young again," it means the telomeres inside its customers' cells will be elongated, as they are in young people's cells.
Telomeres play a role in cell division and get shorter with age. Geron hopes to use its technology to shut off cell replication and division in order to stop cancer, which is runaway cell division and growth.
The Food and Drug Administration has not evaluated the claims made by Telomerase Activation Sciences on its web site.
Published March 12, 2007 by San Francisco Business Times
Gruß, greenhorn
Hatten wir glaube ich noch nicht.
Geron Corp. sells license to company for anti-aging treatments
Monday March 12, 1:36 pm ET
Geron Corp. said Monday it licensed its technology to Asia Biotech Corp. for use by a subsidiary in cosmetic and non-therapeutic treatments that, according to the subsidiary's web site, will make customers' cells "young again."
Menlo Park-based Geron (NASDAQ: GERN - News) didn't give any details about the license deal. Telomerase Activation Sciences, a wholly owned subsidiary of Asia Biotech based in New York, will used Geron's technology, which affects the telomerases at the end of chromosomes, in its cosmetic treatments and dietary supplements.
On its web site, Telomease Activation says in a tiny footnote that by "young again," it means the telomeres inside its customers' cells will be elongated, as they are in young people's cells.
Telomeres play a role in cell division and get shorter with age. Geron hopes to use its technology to shut off cell replication and division in order to stop cancer, which is runaway cell division and growth.
The Food and Drug Administration has not evaluated the claims made by Telomerase Activation Sciences on its web site.
Published March 12, 2007 by San Francisco Business Times
Gruß, greenhorn
was ist denn da wieder los...
erst die verschiebung der klinischen tests mit stammzellen auf 2008 und bisher immer noch keine aussagen zum telomerasehemmer.
und der kurs im free fall.
es nervt mal wieder. geron ist ankündigungsweltmeister - vielleicht gibts 2007 auch gar keine news zu grn163l, wer weiß. so langsam traue ich okarma alles zu.
auch die ausübung der putoption am 28.2. zu 8 usd lässt so manche frage offen. wenn nämlich damit gerechnet würde, dass grn163l den kurs bald pusht, dann hätte man getröst warten können.
alles sehr unerfreulich. ich bin mir unsicherer denn je, ob geron nur ansatzweise das hält, was es seit 15 jahren verspricht.
lg
luck
erst die verschiebung der klinischen tests mit stammzellen auf 2008 und bisher immer noch keine aussagen zum telomerasehemmer.
und der kurs im free fall.
es nervt mal wieder. geron ist ankündigungsweltmeister - vielleicht gibts 2007 auch gar keine news zu grn163l, wer weiß. so langsam traue ich okarma alles zu.
auch die ausübung der putoption am 28.2. zu 8 usd lässt so manche frage offen. wenn nämlich damit gerechnet würde, dass grn163l den kurs bald pusht, dann hätte man getröst warten können.
alles sehr unerfreulich. ich bin mir unsicherer denn je, ob geron nur ansatzweise das hält, was es seit 15 jahren verspricht.
lg
luck
Bin ich hier die Einzige die noch Aktien von Geron hält.
Meislo könntest Du mal bitte wieder ein Statement abgeben - wie Du die Lage derzeit siehst?
Wäre sehr schade, wenn das Medikament nicht zur Anwendung käme. Natürlich auch für den Aktienkurs - aber besonders für die vielen Patienten.
Viele Grüße
Antea
Meislo könntest Du mal bitte wieder ein Statement abgeben - wie Du die Lage derzeit siehst?
Wäre sehr schade, wenn das Medikament nicht zur Anwendung käme. Natürlich auch für den Aktienkurs - aber besonders für die vielen Patienten.
Viele Grüße
Antea
ja, in der tat.
es ist mega-still um geron geworden. ich denke, ein hochinteressanter kontraindikator. die ruhe vor dem perfekten sturm.
entweder sensationsnews mit raketenantrieb im kurs oder ein weiterer reinfall im segment biotech-investment mit einem in einem krater versinkenden kurswert...
ich halte ein für meine verhältnisse extrem hohes geron exposure. ich habe vor kurzem nochmals deutlich zugekauft, dachte allerdings, dass der kurs nicht mehr auf den level von 7 usd runterkommt. irrtum. high risk paper hat in der jüngsten korrektur leider extrem was auf die mütze bekommen. geron hat nichts substanzielles publiziert, was dazu führte, dass der kurs keine stütze hatte.
-- das wird sich ändern.
wait and see. dabei bleiben.
lg
es ist mega-still um geron geworden. ich denke, ein hochinteressanter kontraindikator. die ruhe vor dem perfekten sturm.
entweder sensationsnews mit raketenantrieb im kurs oder ein weiterer reinfall im segment biotech-investment mit einem in einem krater versinkenden kurswert...
ich halte ein für meine verhältnisse extrem hohes geron exposure. ich habe vor kurzem nochmals deutlich zugekauft, dachte allerdings, dass der kurs nicht mehr auf den level von 7 usd runterkommt. irrtum. high risk paper hat in der jüngsten korrektur leider extrem was auf die mütze bekommen. geron hat nichts substanzielles publiziert, was dazu führte, dass der kurs keine stütze hatte.
-- das wird sich ändern.
wait and see. dabei bleiben.
lg
Antwort auf Beitrag Nr.: 28.570.419 von LuckyCat am 29.03.07 20:13:40ja ist schon möglch das die 7 dollargrenze nicht hält und es dann schnell richtung 6 geht,es sei denn es kommt endlich mal was positives.hatte vor kurzem eine analysteneinstufung im amiland gelesen...hold...
Antwort auf Beitrag Nr.: 28.570.419 von LuckyCat am 29.03.07 20:13:40hallo lucky cat
bin auch investiert und auch ziemlich verunsichert ,hoffe auf mehr informationen hier..
bin auch investiert und auch ziemlich verunsichert ,hoffe auf mehr informationen hier..
So sieht es aus wenn etwas einschlägt
Dendreon + 238%!!!http://biz.yahoo.com/ap/070330/dendreon_ahead_of_the_bell.ht…
Gerons Telomerasehemmer(TVAX) ist bei weitem besser als Dendreons Provenge
Geron ist nicht tot.
die aktie schläft halt bis es Daten zu GNR 163 L oder der Krebsvaccance TVAX gibt.
Was passieren kann seht ihr am kurs von Dendreon. deren prostatakrebsvaccance aktiviert das immunsystem gegen die Tumore.
Nichts anderes macht TVAX . Es aktiviert das immunsystem gegenüber das enzym Telomerase was eben in fast allen krebszellen vorkommt.
die statistische verlängerungsrate beträgt bei provenge 4,5 Monate. Also weit weg von einer Heilung. Dieser wert gibt an um wieviele Monate ein Mensch länger leben kann als normal wenn er mit provenge medikamentiert wird.
Dendreon + 238%!!!http://biz.yahoo.com/ap/070330/dendreon_ahead_of_the_bell.ht…
Gerons Telomerasehemmer(TVAX) ist bei weitem besser als Dendreons Provenge
Geron ist nicht tot.
die aktie schläft halt bis es Daten zu GNR 163 L oder der Krebsvaccance TVAX gibt.
Was passieren kann seht ihr am kurs von Dendreon. deren prostatakrebsvaccance aktiviert das immunsystem gegen die Tumore.
Nichts anderes macht TVAX . Es aktiviert das immunsystem gegenüber das enzym Telomerase was eben in fast allen krebszellen vorkommt.
die statistische verlängerungsrate beträgt bei provenge 4,5 Monate. Also weit weg von einer Heilung. Dieser wert gibt an um wieviele Monate ein Mensch länger leben kann als normal wenn er mit provenge medikamentiert wird.
Antwort auf Beitrag Nr.: 28.584.965 von meislo am 30.03.07 15:11:37Hallo
das<wurde aber zeit,dachte schon jetzt geht es massiv richtung süden.kann mir jemand einen tip geben,wo man realtime von geron bekommt?
das<wurde aber zeit,dachte schon jetzt geht es massiv richtung süden.kann mir jemand einen tip geben,wo man realtime von geron bekommt?
Antwort auf Beitrag Nr.: 28.592.888 von optschraub am 30.03.07 20:39:52http://datasvr.tradearca.com/arcadataserver/JArcaBook.php?Sy…
Gruß Cyberhai
Gruß Cyberhai
Antwort auf Beitrag Nr.: 28.593.458 von cyberhai am 30.03.07 20:59:50hallo cyberhai
vielen dank...musste dann leider live erleben wie wir uns mit geron auf die 7 bewegen,hoffentlich bleiben wir heute drüber.
vielen dank...musste dann leider live erleben wie wir uns mit geron auf die 7 bewegen,hoffentlich bleiben wir heute drüber.
gibt es was neues?Kurs steigt ja heute mal stabil
Hier ist ja alles ziemlich still geworden.
Schöne ostern allerseits
Sprigt von Ast zu Ast und ist rot......?????
Ein Affe mit ner Radische im Arsch.
Schöne ostern allerseits
Sprigt von Ast zu Ast und ist rot......?????
Ein Affe mit ner Radische im Arsch.
Antwort auf Beitrag Nr.: 28.685.464 von optschraub am 05.04.07 23:54:23 um geron bleibt es weiterhin still.im herbst 2007 sind die wahlen in den usa.der größte feind gerons ist der konserative bush.wird bush abbgelöst bzw. die republikaner wird geron steigen.
um geron bleibt es weiterhin still.im herbst 2007 sind die wahlen in den usa.der größte feind gerons ist der konserative bush.wird bush abbgelöst bzw. die republikaner wird geron steigen.
geron wartet auf ein regierungswechsel um sein programm durchziehen zu können.der kurs wird noch einmal kräftig fallen.im jahre 2008 geht es los.
 um geron bleibt es weiterhin still.im herbst 2007 sind die wahlen in den usa.der größte feind gerons ist der konserative bush.wird bush abbgelöst bzw. die republikaner wird geron steigen.
um geron bleibt es weiterhin still.im herbst 2007 sind die wahlen in den usa.der größte feind gerons ist der konserative bush.wird bush abbgelöst bzw. die republikaner wird geron steigen.geron wartet auf ein regierungswechsel um sein programm durchziehen zu können.der kurs wird noch einmal kräftig fallen.im jahre 2008 geht es los.
diskussionswürdige aussagen von pedestrian.
mit einem möglichen regierungswechsel wird sich auch für geron einiges ändern, jedoch nicht besonders viel. private stammzellforschung (mit privatem kapital) ist auch heute schon in den usa erlaubt. sicherlich, der bann (nur bestimmte stammzelllinien verwenden zu dürfen), den bush verordnete, wird wahrsch. aufgehoben. zum glück für die gesamte 'stammzellindustrie'.
"der kurs wird noch einmal kräfig fallen". diese aussage ist interessant, impliziert sie doch ein scheitern von grn163l. die testergebnisse werden auf jeden fall in 2007 publiziert. scheitert grn163l, dann wird die stammzellschiene geron nicht aus der patsche helfen, denn neue finanzierungsrunde haben sich in vergangenheit v.a. auf den telomerasehemmer konzentriert. die anwendung von stammzelltherapien ist noch viel zu weit entfernt, als dass sie nennnenswert den unternehmenswert steigern könnte.
seien wir gespannt.
lg
mit einem möglichen regierungswechsel wird sich auch für geron einiges ändern, jedoch nicht besonders viel. private stammzellforschung (mit privatem kapital) ist auch heute schon in den usa erlaubt. sicherlich, der bann (nur bestimmte stammzelllinien verwenden zu dürfen), den bush verordnete, wird wahrsch. aufgehoben. zum glück für die gesamte 'stammzellindustrie'.
"der kurs wird noch einmal kräfig fallen". diese aussage ist interessant, impliziert sie doch ein scheitern von grn163l. die testergebnisse werden auf jeden fall in 2007 publiziert. scheitert grn163l, dann wird die stammzellschiene geron nicht aus der patsche helfen, denn neue finanzierungsrunde haben sich in vergangenheit v.a. auf den telomerasehemmer konzentriert. die anwendung von stammzelltherapien ist noch viel zu weit entfernt, als dass sie nennnenswert den unternehmenswert steigern könnte.
seien wir gespannt.
lg
Antwort auf Beitrag Nr.: 28.736.758 von LuckyCat am 10.04.07 11:23:39still.im herbst 2007
Wahlen sind erst im herbst 2008
Bush Would Veto Stem Cell Research Bill
http://biz.yahoo.com/ap/070410/congress_stem_cells.html?.v=1
Bald ist dieser Arsch weg
er, der mit seinem verückten vater der menschheit nur übel zugefügt hat!
hat dann ausgespielt
Seine Vetos die er nur noch einsetzt um regieren zu können sind dann rauch von gestern.
Wahlen sind erst im herbst 2008
Bush Would Veto Stem Cell Research Bill
http://biz.yahoo.com/ap/070410/congress_stem_cells.html?.v=1
Bald ist dieser Arsch weg
er, der mit seinem verückten vater der menschheit nur übel zugefügt hat!
hat dann ausgespielt

Seine Vetos die er nur noch einsetzt um regieren zu können sind dann rauch von gestern.
Antwort auf Beitrag Nr.: 28.735.061 von pedestrian am 10.04.07 09:18:57 @luckyCat,ich denke GRN163L wird ein erfolg.nur die spekulanten werden den kurs nochmal drücken um reichlich zu verdienen.das hat man auch bei dendreon gesehen der kurs ist vor der explosion stark gefallen.
@luckyCat,ich denke GRN163L wird ein erfolg.nur die spekulanten werden den kurs nochmal drücken um reichlich zu verdienen.das hat man auch bei dendreon gesehen der kurs ist vor der explosion stark gefallen.
 @luckyCat,ich denke GRN163L wird ein erfolg.nur die spekulanten werden den kurs nochmal drücken um reichlich zu verdienen.das hat man auch bei dendreon gesehen der kurs ist vor der explosion stark gefallen.
@luckyCat,ich denke GRN163L wird ein erfolg.nur die spekulanten werden den kurs nochmal drücken um reichlich zu verdienen.das hat man auch bei dendreon gesehen der kurs ist vor der explosion stark gefallen.
kaum sagt jim kramer in einer 2 min. randnotiz auf thestreet.com, dass in dieser woche über die förderung von embryonic stem cell research (= geron) entschieden wird, geht der kurs ab nach norden.
welch irrsinn.
welch irrsinn.
hier noch der link zu cramers gebrabbel, ich hoffe, er funktioniert (werbung von american airlines abspielen lassen, dann kommt der größe börsen-macker...)
http://videoplayer.thestreet.com/?clipId=1373_10349383&chann…
http://videoplayer.thestreet.com/?clipId=1373_10349383&chann…
der senat hat entschieden - wieder einmal. und bush wird sein veto einlegen.
okarma wird zitiert:
Senate stem cell vote may boost public perception
Industry trying to see silver lining in latest funding struggle
Last Update: 12:36 PM ET Apr 13, 2007
WASHINGTON (MarketWatch) -- Despite the promise of a presidential veto, this week's passage of a bill authorizing more federal funding for embryonic stem cell research might provide some good news for stem cell companies, at least in the eyes of investors, said industry officials.
"Investor psychology is very important," said Richard Garr, CEO of Maryland-based Neuralstem, Inc. (NRLS : neuralstem inc com
News , chart , profile , more
Last: 3.50+0.01+0.29%
"Anything that contributes to stem cells not being viewed as an outlaw industry is important for that."
"Anything that contributes to stem cells not being viewed as an outlaw industry is important."
— Richard Garr, CEO of Neuralstem, Inc.
NeuralStem doesn't work with embryonic stem cells, but with fetal stem cells. But nonembryonic players like Garr and George Dunbar, CEO of adult stem cell company Aastrom Biosciences (ASTM : Aastrom Biosciences Inc
News , chart , profile , more
Last: 1.47-0.02-1.34%
said good news for one type of stem cell research is good news for all.
"All of the stem cell-related public companies tend to rise and fall together," Dunbar said. "If a stem cell company produces good clinical data about one kind of cell, everybody benefits."
Any benefit from Wednesday's vote will likely be in public perception alone. Though the Senate did pass the bill 63-43, supporters didn't create the supermajority necessary to override the veto President Bush has promised, meaning that federal funds won't actually be authorized for the embryonic stem cell research outlined in the bill. But a lack of federal funding is not new for embryonic researchers.
"Since the Bush pronouncement about embryonic stem cells in 2001, only $130 million federal dollars have been spent total," said Tom Okarma, CEO of Geron Corp. (GERN : Geron Corporation
News , chart , profile , more
Last: 7.38-0.07-0.94%
a California embryonic stem cell research company. "(Geron) will have invested more than that by the end of 2007."
Most funding for embryonic research has come from companies like Geron, Okarma said. Though certain states have pledged funds, as in California, where $3 billion was earmarked for research over the next decade via referendum, Okarma said most of those dollars have been tied up in litigation.
"We have given up on actively trying to change the politics," he said. "We have our heads down trying to do the science."
Geron's embryonic research may be ready for clinical trials by year's end. If that happens, Okarma worries that federal funding for other medical advancements may come under fire.
"The way it worked in the past, it took 20 years of National Institute of Health-funded academic research before industry even thought to invest in creating a product," he said. "If Geron is successful and we put one or two or three cell pipes into the commercial realm, then the question arises if we really need the N.I.H."
The answer, he said, is yes. A cutoff of federal funding "would have a horrible, chilling effect on academia and molecular medicine," he said. "We're talking about a $30 billion per year taxpayer-funded program."
Even if there is a regime change that supports the research, Okarma said advancements already have been delayed by the lack of funding. But an influx of federal funds-or the release of promised funds from California and other states-could cause growth in investment in the industry.
"When the money becomes available to academia, new cells will be found and there might be a half-dozen startup Gerons," he said. "That's what the investment community wants to invest in. And these companies will have real, issued patents (developed by Geron) to start from. That's a good thing for an investor."
grüße
okarma wird zitiert:
Senate stem cell vote may boost public perception
Industry trying to see silver lining in latest funding struggle
Last Update: 12:36 PM ET Apr 13, 2007
WASHINGTON (MarketWatch) -- Despite the promise of a presidential veto, this week's passage of a bill authorizing more federal funding for embryonic stem cell research might provide some good news for stem cell companies, at least in the eyes of investors, said industry officials.
"Investor psychology is very important," said Richard Garr, CEO of Maryland-based Neuralstem, Inc. (NRLS : neuralstem inc com
News , chart , profile , more
Last: 3.50+0.01+0.29%
"Anything that contributes to stem cells not being viewed as an outlaw industry is important for that."
"Anything that contributes to stem cells not being viewed as an outlaw industry is important."
— Richard Garr, CEO of Neuralstem, Inc.
NeuralStem doesn't work with embryonic stem cells, but with fetal stem cells. But nonembryonic players like Garr and George Dunbar, CEO of adult stem cell company Aastrom Biosciences (ASTM : Aastrom Biosciences Inc
News , chart , profile , more
Last: 1.47-0.02-1.34%
said good news for one type of stem cell research is good news for all.
"All of the stem cell-related public companies tend to rise and fall together," Dunbar said. "If a stem cell company produces good clinical data about one kind of cell, everybody benefits."
Any benefit from Wednesday's vote will likely be in public perception alone. Though the Senate did pass the bill 63-43, supporters didn't create the supermajority necessary to override the veto President Bush has promised, meaning that federal funds won't actually be authorized for the embryonic stem cell research outlined in the bill. But a lack of federal funding is not new for embryonic researchers.
"Since the Bush pronouncement about embryonic stem cells in 2001, only $130 million federal dollars have been spent total," said Tom Okarma, CEO of Geron Corp. (GERN : Geron Corporation
News , chart , profile , more
Last: 7.38-0.07-0.94%
a California embryonic stem cell research company. "(Geron) will have invested more than that by the end of 2007."
Most funding for embryonic research has come from companies like Geron, Okarma said. Though certain states have pledged funds, as in California, where $3 billion was earmarked for research over the next decade via referendum, Okarma said most of those dollars have been tied up in litigation.
"We have given up on actively trying to change the politics," he said. "We have our heads down trying to do the science."
Geron's embryonic research may be ready for clinical trials by year's end. If that happens, Okarma worries that federal funding for other medical advancements may come under fire.
"The way it worked in the past, it took 20 years of National Institute of Health-funded academic research before industry even thought to invest in creating a product," he said. "If Geron is successful and we put one or two or three cell pipes into the commercial realm, then the question arises if we really need the N.I.H."
The answer, he said, is yes. A cutoff of federal funding "would have a horrible, chilling effect on academia and molecular medicine," he said. "We're talking about a $30 billion per year taxpayer-funded program."
Even if there is a regime change that supports the research, Okarma said advancements already have been delayed by the lack of funding. But an influx of federal funds-or the release of promised funds from California and other states-could cause growth in investment in the industry.
"When the money becomes available to academia, new cells will be found and there might be a half-dozen startup Gerons," he said. "That's what the investment community wants to invest in. And these companies will have real, issued patents (developed by Geron) to start from. That's a good thing for an investor."
grüße
Antwort auf Beitrag Nr.: 28.847.318 von LuckyCat am 16.04.07 22:39:14 hoffentlich vergisst der bush seine vetos nicht,wenn er mal krank wird und stammzellen benötigt.
hoffentlich vergisst der bush seine vetos nicht,wenn er mal krank wird und stammzellen benötigt.
 hoffentlich vergisst der bush seine vetos nicht,wenn er mal krank wird und stammzellen benötigt.
hoffentlich vergisst der bush seine vetos nicht,wenn er mal krank wird und stammzellen benötigt.
Geron Corporation to Present at UBS Global Generic & Specialty Pharmaceuticals Conference
Monday May 7, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) will be presenting an update of the company's product development programs on Tuesday, May 8, 2007, at the UBS Global Generic & Specialty Pharmaceuticals Conference at 9:00 a.m. Eastern Time in New York City.
ADVERTISEMENT
The presentation will include an update of Geron's portfolio of telomerase-based anti-cancer therapies, including GRN163L and GRNVAC1. Alan B. Colowick, M.D., M.P.H., Geron's president, oncology, will be giving the presentation.
The audio only webcast will be available at the following website address: www.ibb.ubs.com. To access the webcast, click the Conferences icon in the center right of the page and follow the link for Webcast located next to the Global Specialty Pharmaceuticals Conference heading. The replay will be available three hours after the live presentation and will be archived for 30 days.
Monday May 7, 7:30 am ET
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) will be presenting an update of the company's product development programs on Tuesday, May 8, 2007, at the UBS Global Generic & Specialty Pharmaceuticals Conference at 9:00 a.m. Eastern Time in New York City.
ADVERTISEMENT
The presentation will include an update of Geron's portfolio of telomerase-based anti-cancer therapies, including GRN163L and GRNVAC1. Alan B. Colowick, M.D., M.P.H., Geron's president, oncology, will be giving the presentation.
The audio only webcast will be available at the following website address: www.ibb.ubs.com. To access the webcast, click the Conferences icon in the center right of the page and follow the link for Webcast located next to the Global Specialty Pharmaceuticals Conference heading. The replay will be available three hours after the live presentation and will be archived for 30 days.
Sector Snap: Stem Cell Developers
Monday May 7, 2:20 pm ET
Stem Cell Developers' Shares Rise Following a Marketplace Overview From Barron's
NEW YORK (AP) -- Shares of biotechnology companies developing stem cell-based treatments jumped Monday following a report in Barron's on the technology's possibilities.
Shares of StemCells Inc. rose 12 cents, or 4.8 percent, to $2.63 in midday trading. Shares of Osiris Therapeutics Inc. rose 11 cents to $15.05, while shares of Geron Corp. rose 21 cents, or 2.8 percent, to $7.64 and shares of Cytori Therapeutics Inc. rose 38 cents, or 6.9 percent, to $5.88 on the Nasdaq Stock Market.
Thermogenesis Corp. saw shares rise 15 cents, or 4.6 percent, to $3.45.
Many companies in the field are developing stem cells for therapies to treat diseases such as Alzheimer's and Parkinson's. The research is also a lightning rod for debate. President Bush has vetoed a bill that would subsidize research using human embryos that are later destroyed.
Meanwhile, individual states have gone their own way, with California, Massachusetts, New York, and New Jersey all providing funding. Missouri voters narrowly passed a constitutional amendment last year to fund research.
StemCells is conducting an early stage trial for a Batten's disease treatment, a rare neurodegenerative disease that affects infants and young children.
Osiris has been given orphan drug status in Europe for its developing stem cell treatment Prochymal. That drug is being tested as a possible treatment to help prevent rejection of transplanted bone marrow and for Crohn's disease.
Monday May 7, 2:20 pm ET
Stem Cell Developers' Shares Rise Following a Marketplace Overview From Barron's
NEW YORK (AP) -- Shares of biotechnology companies developing stem cell-based treatments jumped Monday following a report in Barron's on the technology's possibilities.
Shares of StemCells Inc. rose 12 cents, or 4.8 percent, to $2.63 in midday trading. Shares of Osiris Therapeutics Inc. rose 11 cents to $15.05, while shares of Geron Corp. rose 21 cents, or 2.8 percent, to $7.64 and shares of Cytori Therapeutics Inc. rose 38 cents, or 6.9 percent, to $5.88 on the Nasdaq Stock Market.
Thermogenesis Corp. saw shares rise 15 cents, or 4.6 percent, to $3.45.
Many companies in the field are developing stem cells for therapies to treat diseases such as Alzheimer's and Parkinson's. The research is also a lightning rod for debate. President Bush has vetoed a bill that would subsidize research using human embryos that are later destroyed.
Meanwhile, individual states have gone their own way, with California, Massachusetts, New York, and New Jersey all providing funding. Missouri voters narrowly passed a constitutional amendment last year to fund research.
StemCells is conducting an early stage trial for a Batten's disease treatment, a rare neurodegenerative disease that affects infants and young children.
Osiris has been given orphan drug status in Europe for its developing stem cell treatment Prochymal. That drug is being tested as a possible treatment to help prevent rejection of transplanted bone marrow and for Crohn's disease.
Embryonic stem cells trial on track to start
Wednesday May 9, 8:00 am ET
By Clive Cookson in Boston
The first clinical trial of embryonic stem cells is on track to start early next year on patients with spinal cord injury. Geron (NASDAQ:GERN), the California-based biotechnology company, will carry out the study on accident victims in six trauma centres across the US.
ADVERTISEMENT
"The world's spotlight will be on this trial," Tom Okarma, Geron's chief executive, told the Bio conference in Boston. To get it right, the company has carried out several years of preparatory work in collaboration with its academic partners at the University of California, Irvine.
Geron's product will have been tested in 2,000 animals before it goes into its first patient, Mr Okarma said. It consists of immature oligodendrocytes - specialised nerve cells - grown from human embryonic stem cells. The animal tests show that these can repair spinal cord injuries in rats, by growing new nerves with the myelin sheaths they need to work properly. Paralysed rats can walk again.
Mr Okarma said the product was designed to repair recent spinal damage and would need to be injected into patients within two weeks of the accident. It could not help people with long-term paralysis such as the late actor Christopher Reeve who did so much to champion stem cell research for spinal injury.
Because the first application for a human embryonic stem cell trial is bound to receive extraordinary scrutiny from the US Food and Drug Administration, Geron is working closely with FDA officials to smooth the path in advance of the submission. The embryonic stem cells are already qualified for human therapeutic use, after exhaustive tests showed that the cell cultures contain no contamination with animal proteins or viruses.
Mr Okarma pointed out that human embryonic stem cell research was less than 10 years old; the first such cells were produced at the University of Wisconsin in 1998. "With breakthrough therapies such as antibodies and genetic engineering there is usually a 10 to 20 year period of government funding academic research that improves upon the basic invention before industry can put its toes in," he said.
That has not happened with stem cells because of the Bush Administration's federal funding restrictions. As a result, Mr Okarma said, "we have to pay the bill for every academic collaboration - and that is not sustainable."
Hans Kierstead, head of the embryonic stem cell team at UC Irvine, was worried about the high level of public expectation. "I find it unfair that people demand so much from such a young field," he said. "Just look at the strides we have already made."
Bob Klein, architect of California's Proposition 71 authorising the state to spend at least $3bn over 10 years on stem cell research, also told the Bio conference of his concern about excessive expectations. "In clinical trials there will inevitably be failures as well as successes," he said.
"The ideological right is not asleep," said Mr Klein, who chairs California Institute of Regenerative Medicine's governing board. "They will be prepared to spin [any problems] to promote their opposition to embryonic stem cell research, and we'll need a sophisticated fast-response messaging team to put across our message."
Wednesday May 9, 8:00 am ET
By Clive Cookson in Boston
The first clinical trial of embryonic stem cells is on track to start early next year on patients with spinal cord injury. Geron (NASDAQ:GERN), the California-based biotechnology company, will carry out the study on accident victims in six trauma centres across the US.
ADVERTISEMENT
"The world's spotlight will be on this trial," Tom Okarma, Geron's chief executive, told the Bio conference in Boston. To get it right, the company has carried out several years of preparatory work in collaboration with its academic partners at the University of California, Irvine.
Geron's product will have been tested in 2,000 animals before it goes into its first patient, Mr Okarma said. It consists of immature oligodendrocytes - specialised nerve cells - grown from human embryonic stem cells. The animal tests show that these can repair spinal cord injuries in rats, by growing new nerves with the myelin sheaths they need to work properly. Paralysed rats can walk again.
Mr Okarma said the product was designed to repair recent spinal damage and would need to be injected into patients within two weeks of the accident. It could not help people with long-term paralysis such as the late actor Christopher Reeve who did so much to champion stem cell research for spinal injury.
Because the first application for a human embryonic stem cell trial is bound to receive extraordinary scrutiny from the US Food and Drug Administration, Geron is working closely with FDA officials to smooth the path in advance of the submission. The embryonic stem cells are already qualified for human therapeutic use, after exhaustive tests showed that the cell cultures contain no contamination with animal proteins or viruses.
Mr Okarma pointed out that human embryonic stem cell research was less than 10 years old; the first such cells were produced at the University of Wisconsin in 1998. "With breakthrough therapies such as antibodies and genetic engineering there is usually a 10 to 20 year period of government funding academic research that improves upon the basic invention before industry can put its toes in," he said.
That has not happened with stem cells because of the Bush Administration's federal funding restrictions. As a result, Mr Okarma said, "we have to pay the bill for every academic collaboration - and that is not sustainable."
Hans Kierstead, head of the embryonic stem cell team at UC Irvine, was worried about the high level of public expectation. "I find it unfair that people demand so much from such a young field," he said. "Just look at the strides we have already made."
Bob Klein, architect of California's Proposition 71 authorising the state to spend at least $3bn over 10 years on stem cell research, also told the Bio conference of his concern about excessive expectations. "In clinical trials there will inevitably be failures as well as successes," he said.
"The ideological right is not asleep," said Mr Klein, who chairs California Institute of Regenerative Medicine's governing board. "They will be prepared to spin [any problems] to promote their opposition to embryonic stem cell research, and we'll need a sophisticated fast-response messaging team to put across our message."
09. Mai 2007
Zum ersten Mal seit der Verabschiedung des Stammzellgesetzes vor fünf Jahren wird man sich am heutigen Mittwoch auf einer Anhörung des Forschungsausschusses wieder im Bundestag mit einer Frage beschäftigen, die fast alle maßgeblichen Forschungsinstitutionen des Landes im Grunde seit ebenjenem Beschluss umtreibt: der Frage nach einer Lockerung der Regeln im Umgang mit den ethisch umstrittenen embryonalen Stammzellen des Menschen.
Die Deutsche Akademie der Naturforscher Leopoldina brachte das kürzlich auf die Kurzformel: Zulassung des Imports neuer Stammzell-Linien und damit Abschaffung des Stichtags, Forschung auch jenseits der Grundlagenforschung und Abschaffung der Strafvorschriften für Wissenschaftler, die im Ausland mit hierzulande verbotenen Stammzell-Linien arbeiten oder an solchen internationalen Projekten beteiligt sind.
Blutbildende Vorläuferzellen
Es geht dabei um Arbeiten mit Zellen, wie sie etwa in der Online-Ausgabe der Zeitschrift "Nature Methods" (doi:10.1038/NMETH1041) vom Montag gepriesen werden. Robert Lanza von der amerikanischen Firma ACT beschreibt darin mit Forschern des Memorial Sloan-Kettering Cancer Center in New York die Herstellung von funktionstüchtigen blutbildenden Vorläuferzellen und von Endothelzellen, die für die Gefäßbildung etwa nach einem Herzinfarkt entscheidend sind. Ihre in der Petrischale aus embryonalen Stammzellen des Menschen erzeugten Hämangioblasten - die embryonalen Urzellen des Blutkreislaufs - erwiesen sich als ideale Vorläuferzellen.
In kranke Mäuse transplantiert, übernahmen sie die gewünschte Funktion bei der Gefäßreparatur. Als ebenso funktionstüchtig, wenn auch vorerst ausschließlich in der Petrischale, erwiesen sich die in einem etwas komplizierteren Herstellungsverfahren aus embryonalen Stammzellen gewonnenen Leberzellen, über die David Hay von der kalifornischen Firma Geron kürzlich in der Zeitschrift "Cloning and Stem Cells" (Bd. 9, S. 51) berichtete.
Stichtag auf Prüfstand
In beiden Fällen, bei den Gefäßvorläufern wie bei den künstlichen Leberzellen, ließe sich die schon vor fünf Jahren immer wieder vorgebrachte Frage stellen, weshalb man sich nicht auf die ethisch unbedenklichen Reservoire des Körpers - die adulten Stammzellen - konzentriert. Was die Infarkttherapie angeht, könnte man sogar auf zahlreiche klinische Experimente mit nun schon weit mehr als tausend Patienten verweisen, in denen Knochenmark-Stammzellen verwendet wurden. Tatsächlich lassen die amerikanischen Wissenschaftler auch solche Fortschritte nicht unerwähnt. Immer wieder jedoch und mit wachsender Begeisterung kommt man in dem Forschungsgebiet offenbar auf die embryonalen Stammzellen zurück - ausgenommen in Deutschland.
Peter Löser vom Robert-Koch-Institut in Berlin hat zusammen mit Anna Wobus vom IPK Gatersleben in der "Naturwissenschaftlichen Rundschau" (Bd. 60, S. 229) mit beeindruckendem Zahlenmaterial aus der ganzen Welt deutlich gemacht, dass die deutsche Forschung mit erst 11 von 500 Publikationen auf diesem Gebiet längst im Abseits steht. Von den vorwiegend in den vergangenen beiden Jahren erzeugten weltweit mindestens 507 embryonalen Stammzell-Linien können deutsche Forscher nicht einmal zwei Dutzend nutzen. Alle anderen sind nach dem Stichtag 1. Januar 2002 hergestellt worden. Darunter vor allem auch jene im vorigen Jahr erst bekanntgewordenen Zell-Linien, die ohne jegliche tierischen Anteile im Nährmedium kultiviert werden und deshalb als Meilenstein für die medizinische Forschung angesehen werden. Ob die deutschen Stammzellforscher noch auf diesen Zug aufspringen dürfen, ist fraglich. Anhalten wird er für sie nicht, er nimmt gerade richtig Fahrt auf.
Text: jom / F.A.Z., 09.05.2007
Bildmaterial: dpa
Zum ersten Mal seit der Verabschiedung des Stammzellgesetzes vor fünf Jahren wird man sich am heutigen Mittwoch auf einer Anhörung des Forschungsausschusses wieder im Bundestag mit einer Frage beschäftigen, die fast alle maßgeblichen Forschungsinstitutionen des Landes im Grunde seit ebenjenem Beschluss umtreibt: der Frage nach einer Lockerung der Regeln im Umgang mit den ethisch umstrittenen embryonalen Stammzellen des Menschen.
Die Deutsche Akademie der Naturforscher Leopoldina brachte das kürzlich auf die Kurzformel: Zulassung des Imports neuer Stammzell-Linien und damit Abschaffung des Stichtags, Forschung auch jenseits der Grundlagenforschung und Abschaffung der Strafvorschriften für Wissenschaftler, die im Ausland mit hierzulande verbotenen Stammzell-Linien arbeiten oder an solchen internationalen Projekten beteiligt sind.
Blutbildende Vorläuferzellen
Es geht dabei um Arbeiten mit Zellen, wie sie etwa in der Online-Ausgabe der Zeitschrift "Nature Methods" (doi:10.1038/NMETH1041) vom Montag gepriesen werden. Robert Lanza von der amerikanischen Firma ACT beschreibt darin mit Forschern des Memorial Sloan-Kettering Cancer Center in New York die Herstellung von funktionstüchtigen blutbildenden Vorläuferzellen und von Endothelzellen, die für die Gefäßbildung etwa nach einem Herzinfarkt entscheidend sind. Ihre in der Petrischale aus embryonalen Stammzellen des Menschen erzeugten Hämangioblasten - die embryonalen Urzellen des Blutkreislaufs - erwiesen sich als ideale Vorläuferzellen.
In kranke Mäuse transplantiert, übernahmen sie die gewünschte Funktion bei der Gefäßreparatur. Als ebenso funktionstüchtig, wenn auch vorerst ausschließlich in der Petrischale, erwiesen sich die in einem etwas komplizierteren Herstellungsverfahren aus embryonalen Stammzellen gewonnenen Leberzellen, über die David Hay von der kalifornischen Firma Geron kürzlich in der Zeitschrift "Cloning and Stem Cells" (Bd. 9, S. 51) berichtete.
Stichtag auf Prüfstand
In beiden Fällen, bei den Gefäßvorläufern wie bei den künstlichen Leberzellen, ließe sich die schon vor fünf Jahren immer wieder vorgebrachte Frage stellen, weshalb man sich nicht auf die ethisch unbedenklichen Reservoire des Körpers - die adulten Stammzellen - konzentriert. Was die Infarkttherapie angeht, könnte man sogar auf zahlreiche klinische Experimente mit nun schon weit mehr als tausend Patienten verweisen, in denen Knochenmark-Stammzellen verwendet wurden. Tatsächlich lassen die amerikanischen Wissenschaftler auch solche Fortschritte nicht unerwähnt. Immer wieder jedoch und mit wachsender Begeisterung kommt man in dem Forschungsgebiet offenbar auf die embryonalen Stammzellen zurück - ausgenommen in Deutschland.
Peter Löser vom Robert-Koch-Institut in Berlin hat zusammen mit Anna Wobus vom IPK Gatersleben in der "Naturwissenschaftlichen Rundschau" (Bd. 60, S. 229) mit beeindruckendem Zahlenmaterial aus der ganzen Welt deutlich gemacht, dass die deutsche Forschung mit erst 11 von 500 Publikationen auf diesem Gebiet längst im Abseits steht. Von den vorwiegend in den vergangenen beiden Jahren erzeugten weltweit mindestens 507 embryonalen Stammzell-Linien können deutsche Forscher nicht einmal zwei Dutzend nutzen. Alle anderen sind nach dem Stichtag 1. Januar 2002 hergestellt worden. Darunter vor allem auch jene im vorigen Jahr erst bekanntgewordenen Zell-Linien, die ohne jegliche tierischen Anteile im Nährmedium kultiviert werden und deshalb als Meilenstein für die medizinische Forschung angesehen werden. Ob die deutschen Stammzellforscher noch auf diesen Zug aufspringen dürfen, ist fraglich. Anhalten wird er für sie nicht, er nimmt gerade richtig Fahrt auf.
Text: jom / F.A.Z., 09.05.2007
Bildmaterial: dpa
10. Mai 2007
War das also schon die sanfte biopolitische Wende? Erstaunlich gelöst jedenfalls hat man sie diesmal erlebt, die Stammzellforscher, Ethiker, Juristen, Forschungsmanager und die Biopolitiker des Bundestages, als sie am späten Mittwochnachmittag den Anhörungssaal im Marie-Elisabeth-Lüders-Haus des Bundestages verließen.
Nicht, dass sie sich in allem einig gewesen wären. Aber die erste Sachverständigenanhörung zum Stammzellgesetz im Forschungsausschuss fünf Jahre nach einem Debattenmarathon und Verabschiedung desselben brachte endgültig die Gewissheit, dass die seinerzeit beschlossene Wiedervorlage und Überprüfung des Gesetzes ganz und gar berechtigt war.
Pragmatismus war gefragt
Natürlich war es wieder ein rhetorisches Ringen der Beschleuniger gegen die Bremser. Die Naturwissenschaftler mit dem Vizepräsidenten der Deutschen Forschungsgemeinschaft, Jörg Hinrich Hacker, an der Spitze versuchten die Abgeordneten von der Abschaffung oder wenigstens der Neufestsetzung des Stichtages 1. Januar 2002 für die Verwendung importierter embryonaler Stammzellen zu überzeugen. Und die prinzipientreuen Lebensschützer unter den Bioethikern und Juristen trugen Überzeugungen vor, mit denen sie genau dieses zu verhindern suchten.
Dass es am Ende dann doch nicht auf die alten und seinerzeit erbittert geführten Konflikte um Statusfragen des Embryos oder um die Ethik des Heilens hinauslief, war Sachverständigen wie dem evangelischen Theologen Klaus Tanner aus Halle-Wittenberg zu verdanken, der diesen „endgültig wohl nie zu klärenden“ Streit mit einem Appell für einen „dann eben angemessenen Umgang mit dem Dissens“ zu lösen trachtete.
Pragmatismus war also gefragt. Und der kam nicht von ungefähr. Bischof Wolfgang Huber, der Ratsvorsitzende der Evangelischen Kirche, saß zwar nicht am Tisch, aber sein Einlenken in der Sache zugunsten der Forschung und der Festsetzung eines neuen Stichtages im Vorfeld hatte die Richtung vorgegeben. Das kirchliche Lager war damit gespalten. Und wie sich auf der Anhörung abzeichnete, galt diese Neuorientierung auch für einige andere Protagonisten des vor fünf Jahren als Kompromiss, als „biopolitischer Friedensvertrag“ gefeierten Gesetzestextes.
Strafbewehrung beim Arbeiten mit neuen Zell-Linien
Die Berliner Juristin und ehemalige Staatssekretärin Ulrike Riedel etwa, eine der treibenden Kräfte des damaligen Kompromisses, gab sich nach den wissenschaftlichen und ethischen Einlassungen überraschend konziliant: Was eine Verschiebung des Stichtages und damit die Möglichkeit der Nutzung neuer embryonaler Stammzell-Linien aus dem Ausland betreffe, gebe es keine Bedenken, „wenn es zwingende Gründe dafür gibt“. Gar dringenden Änderungsbedarf in dieser Hinsicht leiteten der Bonner Staatsrechtler Matthias Herdegen, der Hamburger Rechtsphilosoph Reinhard Merkel und der Heidelberger Medizinjurist Jochen Taupitz schon aus „verfassungsrechtlichen Bedenken“ ab, die sich durch die mit dem Stichtag verbundene Beschränkung der Forschungsfreiheit ergebe.
Änderungswünsche also allenthalben, auch wenn Richter Rainer Beckmann in einer Stichtagsverschiebung „zumindest eine Schwächung“ des Gesetzes in dessen Charakter als Verbotsgesetz sehen würde. Weniger eine Charakterfrage als eine Art Fehlerkorrektur sehen die Fachleute - und zwar mit großer Geschlossenheit - in der von allen maßgeblichen Institutionen und vielen Politikern monierten Strafandrohung im Gesetz. Wer heute als deutscher Forscher mit neuen Stammzell-Linien im Ausland arbeitet, muss mit Gefängnis rechnen. Zumindest müsse die Strafbewehrung beim Arbeiten mit neuen, nicht zugelassenen Zell-Linien auf das Inland eingegrenzt werden, war die einhellige Ansicht.
Verunreinigte Stammzellen „taugen nichts mehr“
Das ist den Wissenschaftlern freilich nicht genug. Denn die „zwingenden Gründe“ für eine Verschiebung oder gar Aufhebung des Stichtages sind längst aktenkundig - in einschlägigen Veröffentlichungen und nun vor allem in den schriftlichen Stellungnahmen. Darin wird deutlich, dass sich in den zurückliegenden fünf Jahren das Bild, das man sich damals von den Möglichkeiten der embryonalen Stammzellen und ihrer moralisch weniger umstrittenen Alternativen gemacht hat, grundlegend gewandelt hat.
Von den siebzig vor dem 1. Januar 2002 hergestellten embryonalen und registrierten Zell-Linien, die man seinerzeit als ausreichend für die Grundlagenforschung betrachtete, sind 21 übriggeblieben, die allerdings wegen gravierender genetischer Instabilitäten, Verunreinigungen und fehlerbehafteter Kulturbedingungen „wissenschaftlich nichts mehr taugen“, so Hans Schöler vom Max-Planck-Institut für Biomedizin.
Nicht einmal mehr für die Grundlagenforschung. Und schon gar nicht für vorklinische Experimente oder als Zellmaterial für die womöglich viel schneller realisierbaren Wirkstofftests in der Pharmazie und für Prüfungen der Embryotoxizität, wie sie etwa im neuen Chemikalienrecht genutzt werden könnten. Neue - inzwischen sind es weltweit 38 - Zellkulturen mit krankheitsspezifischen embryonalen Stammzellen, an denen genetische Krankheiten gezielt erforscht und mögliche Therapien geprüft werden könnten, sind tabu.
„Wir können nicht mehr verzichten“
Deutsche Spitzenforscher sind also vielfach isoliert, der Nachwuchs kehrt ihnen den Rücken, und in internationalen Projekten kommen sie kaum zum Zug. Und die adulten Stammzellen? Warum sich nicht auf diese ethisch unumstrittenen körpereigenen Zellen kaprizieren und diese Richtung ausbauen, wie mit dem Stammzellgesetz ja durchaus auch beabsichtigt? Der Heidelberger Stammzellforscher Anthony Ho, der sich ausschließlich mit Körperstammzellen beschäftigt, sprach die unangenehme Wahrheit ungeschminkt aus: „Wir haben gelernt, dass die adulten Stammzellen doch nicht die gewünschten pluripotenten Eigenschaften aufweisen.“
Mit Wolfgang Franz vom Klinikum der Universität München und Oliver Brüstle aus Bonn, zwei Anwälten der embryonalen Zellen, stimmte Gustav Steinhoff, Protagonist der adulten Stammzellen, den wissenschaftlichen Konsens an: „Wir können aus Sicht der Forschung und der Klinik nicht mehr auf embryonale Stammzellen verzichten.“
Text: F.A.Z.
Bildmaterial: AP
War das also schon die sanfte biopolitische Wende? Erstaunlich gelöst jedenfalls hat man sie diesmal erlebt, die Stammzellforscher, Ethiker, Juristen, Forschungsmanager und die Biopolitiker des Bundestages, als sie am späten Mittwochnachmittag den Anhörungssaal im Marie-Elisabeth-Lüders-Haus des Bundestages verließen.
Nicht, dass sie sich in allem einig gewesen wären. Aber die erste Sachverständigenanhörung zum Stammzellgesetz im Forschungsausschuss fünf Jahre nach einem Debattenmarathon und Verabschiedung desselben brachte endgültig die Gewissheit, dass die seinerzeit beschlossene Wiedervorlage und Überprüfung des Gesetzes ganz und gar berechtigt war.
Pragmatismus war gefragt
Natürlich war es wieder ein rhetorisches Ringen der Beschleuniger gegen die Bremser. Die Naturwissenschaftler mit dem Vizepräsidenten der Deutschen Forschungsgemeinschaft, Jörg Hinrich Hacker, an der Spitze versuchten die Abgeordneten von der Abschaffung oder wenigstens der Neufestsetzung des Stichtages 1. Januar 2002 für die Verwendung importierter embryonaler Stammzellen zu überzeugen. Und die prinzipientreuen Lebensschützer unter den Bioethikern und Juristen trugen Überzeugungen vor, mit denen sie genau dieses zu verhindern suchten.
Dass es am Ende dann doch nicht auf die alten und seinerzeit erbittert geführten Konflikte um Statusfragen des Embryos oder um die Ethik des Heilens hinauslief, war Sachverständigen wie dem evangelischen Theologen Klaus Tanner aus Halle-Wittenberg zu verdanken, der diesen „endgültig wohl nie zu klärenden“ Streit mit einem Appell für einen „dann eben angemessenen Umgang mit dem Dissens“ zu lösen trachtete.
Pragmatismus war also gefragt. Und der kam nicht von ungefähr. Bischof Wolfgang Huber, der Ratsvorsitzende der Evangelischen Kirche, saß zwar nicht am Tisch, aber sein Einlenken in der Sache zugunsten der Forschung und der Festsetzung eines neuen Stichtages im Vorfeld hatte die Richtung vorgegeben. Das kirchliche Lager war damit gespalten. Und wie sich auf der Anhörung abzeichnete, galt diese Neuorientierung auch für einige andere Protagonisten des vor fünf Jahren als Kompromiss, als „biopolitischer Friedensvertrag“ gefeierten Gesetzestextes.
Strafbewehrung beim Arbeiten mit neuen Zell-Linien
Die Berliner Juristin und ehemalige Staatssekretärin Ulrike Riedel etwa, eine der treibenden Kräfte des damaligen Kompromisses, gab sich nach den wissenschaftlichen und ethischen Einlassungen überraschend konziliant: Was eine Verschiebung des Stichtages und damit die Möglichkeit der Nutzung neuer embryonaler Stammzell-Linien aus dem Ausland betreffe, gebe es keine Bedenken, „wenn es zwingende Gründe dafür gibt“. Gar dringenden Änderungsbedarf in dieser Hinsicht leiteten der Bonner Staatsrechtler Matthias Herdegen, der Hamburger Rechtsphilosoph Reinhard Merkel und der Heidelberger Medizinjurist Jochen Taupitz schon aus „verfassungsrechtlichen Bedenken“ ab, die sich durch die mit dem Stichtag verbundene Beschränkung der Forschungsfreiheit ergebe.
Änderungswünsche also allenthalben, auch wenn Richter Rainer Beckmann in einer Stichtagsverschiebung „zumindest eine Schwächung“ des Gesetzes in dessen Charakter als Verbotsgesetz sehen würde. Weniger eine Charakterfrage als eine Art Fehlerkorrektur sehen die Fachleute - und zwar mit großer Geschlossenheit - in der von allen maßgeblichen Institutionen und vielen Politikern monierten Strafandrohung im Gesetz. Wer heute als deutscher Forscher mit neuen Stammzell-Linien im Ausland arbeitet, muss mit Gefängnis rechnen. Zumindest müsse die Strafbewehrung beim Arbeiten mit neuen, nicht zugelassenen Zell-Linien auf das Inland eingegrenzt werden, war die einhellige Ansicht.
Verunreinigte Stammzellen „taugen nichts mehr“
Das ist den Wissenschaftlern freilich nicht genug. Denn die „zwingenden Gründe“ für eine Verschiebung oder gar Aufhebung des Stichtages sind längst aktenkundig - in einschlägigen Veröffentlichungen und nun vor allem in den schriftlichen Stellungnahmen. Darin wird deutlich, dass sich in den zurückliegenden fünf Jahren das Bild, das man sich damals von den Möglichkeiten der embryonalen Stammzellen und ihrer moralisch weniger umstrittenen Alternativen gemacht hat, grundlegend gewandelt hat.
Von den siebzig vor dem 1. Januar 2002 hergestellten embryonalen und registrierten Zell-Linien, die man seinerzeit als ausreichend für die Grundlagenforschung betrachtete, sind 21 übriggeblieben, die allerdings wegen gravierender genetischer Instabilitäten, Verunreinigungen und fehlerbehafteter Kulturbedingungen „wissenschaftlich nichts mehr taugen“, so Hans Schöler vom Max-Planck-Institut für Biomedizin.
Nicht einmal mehr für die Grundlagenforschung. Und schon gar nicht für vorklinische Experimente oder als Zellmaterial für die womöglich viel schneller realisierbaren Wirkstofftests in der Pharmazie und für Prüfungen der Embryotoxizität, wie sie etwa im neuen Chemikalienrecht genutzt werden könnten. Neue - inzwischen sind es weltweit 38 - Zellkulturen mit krankheitsspezifischen embryonalen Stammzellen, an denen genetische Krankheiten gezielt erforscht und mögliche Therapien geprüft werden könnten, sind tabu.
„Wir können nicht mehr verzichten“
Deutsche Spitzenforscher sind also vielfach isoliert, der Nachwuchs kehrt ihnen den Rücken, und in internationalen Projekten kommen sie kaum zum Zug. Und die adulten Stammzellen? Warum sich nicht auf diese ethisch unumstrittenen körpereigenen Zellen kaprizieren und diese Richtung ausbauen, wie mit dem Stammzellgesetz ja durchaus auch beabsichtigt? Der Heidelberger Stammzellforscher Anthony Ho, der sich ausschließlich mit Körperstammzellen beschäftigt, sprach die unangenehme Wahrheit ungeschminkt aus: „Wir haben gelernt, dass die adulten Stammzellen doch nicht die gewünschten pluripotenten Eigenschaften aufweisen.“
Mit Wolfgang Franz vom Klinikum der Universität München und Oliver Brüstle aus Bonn, zwei Anwälten der embryonalen Zellen, stimmte Gustav Steinhoff, Protagonist der adulten Stammzellen, den wissenschaftlichen Konsens an: „Wir können aus Sicht der Forschung und der Klinik nicht mehr auf embryonale Stammzellen verzichten.“
Text: F.A.Z.
Bildmaterial: AP
6. Profite aus der Stammzellenforschung
Wie können Investoren von der Stammzellenforschung profitieren?
Die Stammzellenforschung hat bereits die Aufmerksamkeit der großen Investoren und der Pharmazieunternehmen geweckt. Unternehmen wie Genzyme (GENZ) machen kein Geheimnis daraus, dass sie nach kleinen, vielversprechenden Unternehmen suchen, um diese dann zu kaufen: Merck (MRK) finanziert schon Geron (GERN). GE (GE) kaufte die Rechte von ThermoGenesis für eine neue Methode, um Stammzellen zu extrahieren und zu lagern. Und Boston Scientific ist mit einem privaten Entwickler, der Herzerkrankungen behandelt, ein Joint Venture eingegangen. Investoren durchkämmen den Sektor, um vielversprechende Unternehmen zu finden, welche relativ knapp finanziert sind; sie wollen dann einsteigen und die Finanzierung sichern. Einige vielversprechende Namen in diesem Sektor sind:
StemCells (STEM) hat die erste Genehmigung der FDA bekommen, menschliche Nervenstammzellen zu erforschen. Damit können sie ein Medikament zur Behandlung der seltenen Batten-Krankheit - auch neuronale Zeroidlipofuszinose genannt – in die erste Testphase bringen. Unter dieser Krankheit leiden nur vier von einer Millionen Menschen. Deshalb hat das Medikament kein Massenmarktpotenzial; aber das Unternehmen sagt, dass es einen erheblichen Einfluss auf andere Forschungsbereiche haben könnte. Bei 2,50 US$ ist die Gefahr von Kursrückschlägen recht begrenzt; Resultate werden jedoch nicht vor Ende 2008 erwartet.
Die Knochenregenerationsmethode von Osiris Therapeutics (OSIR) generierte bereits 8,3 Mio. US$ an Einnahmen im Jahr 2006, aber hohe Kosten für Tests führten dazu, dass sie immer noch Verluste machen. Ihre Behandlungsmethoden für Herzerkrankungen und die Chrohn-Krankheit haben erste vielversprechende Testresultate geliefert. Ein Analyst sagt, dass die Aktien zwischen 19 und 22 US$ kosten müssten, wenn man die Gewinne im Jahr 2011 als Basis nimmt, da Herzbehandlungen über großes Potenzial verfügen. Bei Kursen um 15 US$ sind davon jedoch schon einige Dinge im Aktienpreis enthalten.
Geron sponsert vielversprechende Forschungen: Sie könnten auch die erste Genehmigung der FDA bekommen, um Tests an menschlichen embryonalen Stammzellen durchzuführen. Das Unternehmen ist aber bereits ambitioniert bepreist.
Unternehmen, welche die Stammzellenforschung unterstützen, sind vielleicht mit weniger Risiken behaftet. Ein solches Unternehmen ist KOOL, das wahrscheinlich letztlich von GE oder Biomet (BMET) aufgekauft werden wird. Cytori Therapeutics (CYTX) möchte in den USA die Zulassung für eine Maschine bekommen, welche Stammzellen aus Fett gewinnen kann.
Wie können Investoren von der Stammzellenforschung profitieren?
Die Stammzellenforschung hat bereits die Aufmerksamkeit der großen Investoren und der Pharmazieunternehmen geweckt. Unternehmen wie Genzyme (GENZ) machen kein Geheimnis daraus, dass sie nach kleinen, vielversprechenden Unternehmen suchen, um diese dann zu kaufen: Merck (MRK) finanziert schon Geron (GERN). GE (GE) kaufte die Rechte von ThermoGenesis für eine neue Methode, um Stammzellen zu extrahieren und zu lagern. Und Boston Scientific ist mit einem privaten Entwickler, der Herzerkrankungen behandelt, ein Joint Venture eingegangen. Investoren durchkämmen den Sektor, um vielversprechende Unternehmen zu finden, welche relativ knapp finanziert sind; sie wollen dann einsteigen und die Finanzierung sichern. Einige vielversprechende Namen in diesem Sektor sind:
StemCells (STEM) hat die erste Genehmigung der FDA bekommen, menschliche Nervenstammzellen zu erforschen. Damit können sie ein Medikament zur Behandlung der seltenen Batten-Krankheit - auch neuronale Zeroidlipofuszinose genannt – in die erste Testphase bringen. Unter dieser Krankheit leiden nur vier von einer Millionen Menschen. Deshalb hat das Medikament kein Massenmarktpotenzial; aber das Unternehmen sagt, dass es einen erheblichen Einfluss auf andere Forschungsbereiche haben könnte. Bei 2,50 US$ ist die Gefahr von Kursrückschlägen recht begrenzt; Resultate werden jedoch nicht vor Ende 2008 erwartet.
Die Knochenregenerationsmethode von Osiris Therapeutics (OSIR) generierte bereits 8,3 Mio. US$ an Einnahmen im Jahr 2006, aber hohe Kosten für Tests führten dazu, dass sie immer noch Verluste machen. Ihre Behandlungsmethoden für Herzerkrankungen und die Chrohn-Krankheit haben erste vielversprechende Testresultate geliefert. Ein Analyst sagt, dass die Aktien zwischen 19 und 22 US$ kosten müssten, wenn man die Gewinne im Jahr 2011 als Basis nimmt, da Herzbehandlungen über großes Potenzial verfügen. Bei Kursen um 15 US$ sind davon jedoch schon einige Dinge im Aktienpreis enthalten.
Geron sponsert vielversprechende Forschungen: Sie könnten auch die erste Genehmigung der FDA bekommen, um Tests an menschlichen embryonalen Stammzellen durchzuführen. Das Unternehmen ist aber bereits ambitioniert bepreist.
Unternehmen, welche die Stammzellenforschung unterstützen, sind vielleicht mit weniger Risiken behaftet. Ein solches Unternehmen ist KOOL, das wahrscheinlich letztlich von GE oder Biomet (BMET) aufgekauft werden wird. Cytori Therapeutics (CYTX) möchte in den USA die Zulassung für eine Maschine bekommen, welche Stammzellen aus Fett gewinnen kann.
Hohes vorbörsliches Volumen und Kurs steigt stark an
Geron Looks Born to Run
By Melissa Davis
Senior Writer
5/14/2007 7:04 AM EDT
Click here for more stories by Melissa Davis
http://www.thestreet.com/_yahoo/newsanalysis/businessnews/10…
Geron Looks Born to Run
By Melissa Davis
Senior Writer
5/14/2007 7:04 AM EDT
Click here for more stories by Melissa Davis
http://www.thestreet.com/_yahoo/newsanalysis/businessnews/10…
Das ist wohl die Trendwende



Jetzt gibt sie aber gas


On The Move For Monday, May 14
Jennifer Lee, 05.14.07, 1:07 PM ET
The U.S. Food and Drug Administration continues to move the markets. Shares of Critical Therapeutics are soaring--up more than 50% on the news the FDA will approve its respiratory treatment, Perforomist. The treatment alleviates chronic obstructive pulmonary disease--a condition that 12 million Americans have been diagnosed with and another 12 million don't even know they have.
Dendreon (nasdaq: DNDN - news - people ) continues to slowly recover ground after its huge sell-off last week. The FDA declined to approve its prostate cancer treatment--and the stock shed more than 60% on the news. Shares are now trading about 4% higher.
Also cleaning up in the biotechs is Geron (nasdaq: GERN - news - people ). The company develops stem-cell treatments. Rumors that Geron is doing extremely well are pushing the stock to double-digit gains.
Bald gibt es Ergebnisse zu GNR 163 L und die sollen toll!! sein
Jennifer Lee, 05.14.07, 1:07 PM ET
The U.S. Food and Drug Administration continues to move the markets. Shares of Critical Therapeutics are soaring--up more than 50% on the news the FDA will approve its respiratory treatment, Perforomist. The treatment alleviates chronic obstructive pulmonary disease--a condition that 12 million Americans have been diagnosed with and another 12 million don't even know they have.
Dendreon (nasdaq: DNDN - news - people ) continues to slowly recover ground after its huge sell-off last week. The FDA declined to approve its prostate cancer treatment--and the stock shed more than 60% on the news. Shares are now trading about 4% higher.
Also cleaning up in the biotechs is Geron (nasdaq: GERN - news - people ). The company develops stem-cell treatments. Rumors that Geron is doing extremely well are pushing the stock to double-digit gains.
Bald gibt es Ergebnisse zu GNR 163 L und die sollen toll!! sein


Antwort auf Beitrag Nr.: 29.323.551 von meislo am 15.05.07 13:08:42For its part, Geron recently gave investors some reason for hope.
"I can tell you that we are proceeding well," Geron CEO Thomas Okarma assured during the company's first-quarter conference call. But "the real interesting activity or information about the drug ... we are going to reserve for the presentation in June -- which will be an important milestone in the development of this drug."
At that conference, Geron will offer widely anticipated updates on GRN163L -- an agent thought to attack the enzyme needed for cancer stem cells to thrive -- for the treatment of leukemia and solid tumors. By now, the company has discovered evidence of the drug's safety and its ability to shrink myeloma stem cells already.
"GRN163L may have the potential to cure (multiple myeloma) by targeting the cancer stem cells," Rodman & Renshaw analyst Ren Benjamin explained earlier this month. Thus, "encouraged by the potential of eliminating cancer stem cells, the company plans to initiate two GRN163L phase II trials in 2Q/3Q07" to expand tests on myeloma and treat a common type of lung cancer.
Around that same timeframe, Geron plans to launch clinical trials of a new cancer vaccine. The company's vaccine program, which has led to a partnership with heavyweight drug-maker Merck (MRK - Cramer's Take - Stockpickr - Rating), has offered some hope for the prevention of prostate cancer already.
Geron now wishes to replicate the success seen in its early prostate cancer studies, targeting myeloma this time around.
"What we have demonstrated in the prostate cancer trials is really robust and reproducible cellular immune responses to the vaccine that generate killer T-cells that kill the patient's tumor," Okarma stated during the company's latest conference call. "This occurs reproducibly throughout the patient population; it is not anecdotal, and it is not one out of 10 patients.
"This is completely different from the vast majority of the more advanced cancer vaccine programs" currently underway.
Experts look for some preliminary results on Geron's myeloma vaccine, as well as fuller results on GRN163L, by the end of the year.
After that, in a groundbreaking study, Geron plans to use embryonic stem cells for the treatment of damaged spinal cords. Already, the company's technique has scored banner headlines -- and attention by 60 Minutes -- because it enabled partially paralyzed rats to start walking again.
Lawton views those looming human trials as perhaps "the sexiest aspect" of the entire Geron story. In a cover story published last week, Barron's took some notice of that coming study -- and the dashing scientist behind it -- as well.
"If there's a face from stem-cell research that's made for primetime, it's the one belonging to Hans Keirstead," Barron's reported, noting that a Calvin Klein-clad Keirstead has already been hailed as something of a miracle worker in a publication of Men's Vogue. "Based on his research, Geron is applying to the FDA [Food and Drug Administration] to begin ... potentially the first government-approved test using human embryonic stem cells.
"That would be a key milestone" for the company.
But at the same time, Barron's noted, investors have assigned Geron a handsome value already. Geron boasts a market capitalization of half-a-billion dollars, despite its faraway cures, although more than one-third of that does appear on its balance sheet as cash. Yet Geron's other assets could be worth far more. Notably, thanks to a prescient move about a decade ago, the company holds valuable -- if hotly contested -- patents that give it vast control over embryonic stem cell treatments in the U.S.
Still, Benjamin sees no reason for investors to make their move right now.
"We are maintaining our market-perform/speculative-risk rating on Geron based on the company's current valuation," wrote Benjamin, whose firm makes a market in the company's securities. "While we acknowledge that Geron is developing new modalities of treatment that address large areas of unmet clinical need -- and, therefore, may deserve to trade at a premium to its peers -- we await additional clinical data and peer-reviewed publications, as well as additional clarity regarding the timing of the company's clinical programs, before re-evaluating our rating of the company."
Meanwhile, however, some investors have decided to pounce on the stock already. During the fourth quarter, when Geron issued a big block of warrants, Rock Hill Investment Management bought so much stock in Geron that it emerged as the company's second-largest shareholder. Indeed, a Nasdaq filing indicates, Rock Hill owns far more common stock in Geron than it does in all other companies combined.
Lawton believes there is a reason why Rock Hill has placed that huge bet on Geron. He points to Dendreon (DNDN - Cramer's Take - Stockpickr - Rating), which briefly soared despite questions about the effectiveness of its own prostate cancer vaccine, for comparison. Dendreon, hit by a devastating regulatory ruling last week, has since crashed.
But Lawton feels that Geron is, by far, the better play.
"All Dendreon did is discover a drug that might extend lives for four months," Lawton says. "If Geron has discovered a cancer-fighting agent that works -- and really prolongs life -- then, in my opinion, it's a $50 stock."
"I can tell you that we are proceeding well," Geron CEO Thomas Okarma assured during the company's first-quarter conference call. But "the real interesting activity or information about the drug ... we are going to reserve for the presentation in June -- which will be an important milestone in the development of this drug."
At that conference, Geron will offer widely anticipated updates on GRN163L -- an agent thought to attack the enzyme needed for cancer stem cells to thrive -- for the treatment of leukemia and solid tumors. By now, the company has discovered evidence of the drug's safety and its ability to shrink myeloma stem cells already.
"GRN163L may have the potential to cure (multiple myeloma) by targeting the cancer stem cells," Rodman & Renshaw analyst Ren Benjamin explained earlier this month. Thus, "encouraged by the potential of eliminating cancer stem cells, the company plans to initiate two GRN163L phase II trials in 2Q/3Q07" to expand tests on myeloma and treat a common type of lung cancer.
Around that same timeframe, Geron plans to launch clinical trials of a new cancer vaccine. The company's vaccine program, which has led to a partnership with heavyweight drug-maker Merck (MRK - Cramer's Take - Stockpickr - Rating), has offered some hope for the prevention of prostate cancer already.
Geron now wishes to replicate the success seen in its early prostate cancer studies, targeting myeloma this time around.
"What we have demonstrated in the prostate cancer trials is really robust and reproducible cellular immune responses to the vaccine that generate killer T-cells that kill the patient's tumor," Okarma stated during the company's latest conference call. "This occurs reproducibly throughout the patient population; it is not anecdotal, and it is not one out of 10 patients.
"This is completely different from the vast majority of the more advanced cancer vaccine programs" currently underway.
Experts look for some preliminary results on Geron's myeloma vaccine, as well as fuller results on GRN163L, by the end of the year.
After that, in a groundbreaking study, Geron plans to use embryonic stem cells for the treatment of damaged spinal cords. Already, the company's technique has scored banner headlines -- and attention by 60 Minutes -- because it enabled partially paralyzed rats to start walking again.
Lawton views those looming human trials as perhaps "the sexiest aspect" of the entire Geron story. In a cover story published last week, Barron's took some notice of that coming study -- and the dashing scientist behind it -- as well.
"If there's a face from stem-cell research that's made for primetime, it's the one belonging to Hans Keirstead," Barron's reported, noting that a Calvin Klein-clad Keirstead has already been hailed as something of a miracle worker in a publication of Men's Vogue. "Based on his research, Geron is applying to the FDA [Food and Drug Administration] to begin ... potentially the first government-approved test using human embryonic stem cells.
"That would be a key milestone" for the company.
But at the same time, Barron's noted, investors have assigned Geron a handsome value already. Geron boasts a market capitalization of half-a-billion dollars, despite its faraway cures, although more than one-third of that does appear on its balance sheet as cash. Yet Geron's other assets could be worth far more. Notably, thanks to a prescient move about a decade ago, the company holds valuable -- if hotly contested -- patents that give it vast control over embryonic stem cell treatments in the U.S.
Still, Benjamin sees no reason for investors to make their move right now.
"We are maintaining our market-perform/speculative-risk rating on Geron based on the company's current valuation," wrote Benjamin, whose firm makes a market in the company's securities. "While we acknowledge that Geron is developing new modalities of treatment that address large areas of unmet clinical need -- and, therefore, may deserve to trade at a premium to its peers -- we await additional clinical data and peer-reviewed publications, as well as additional clarity regarding the timing of the company's clinical programs, before re-evaluating our rating of the company."
Meanwhile, however, some investors have decided to pounce on the stock already. During the fourth quarter, when Geron issued a big block of warrants, Rock Hill Investment Management bought so much stock in Geron that it emerged as the company's second-largest shareholder. Indeed, a Nasdaq filing indicates, Rock Hill owns far more common stock in Geron than it does in all other companies combined.
Lawton believes there is a reason why Rock Hill has placed that huge bet on Geron. He points to Dendreon (DNDN - Cramer's Take - Stockpickr - Rating), which briefly soared despite questions about the effectiveness of its own prostate cancer vaccine, for comparison. Dendreon, hit by a devastating regulatory ruling last week, has since crashed.
But Lawton feels that Geron is, by far, the better play.
"All Dendreon did is discover a drug that might extend lives for four months," Lawton says. "If Geron has discovered a cancer-fighting agent that works -- and really prolongs life -- then, in my opinion, it's a $50 stock."
Antwort auf Beitrag Nr.: 29.323.924 von meislo am 15.05.07 13:29:15
Hallo meislo,
ich war mit gemischtem erfolg bei Dndn dabei.
Was mich hier interessiert sind 2 dinge:
- bist du sicher, dass geron einen besseren impfstoff finden wird als Dndn?
- von anderen aktien weiß ich, dass investoren sich die rosinen aus dem kuchen picken; ist auf Rockhill Investment verlass??
Viele Grüße Ede
Hallo meislo,
ich war mit gemischtem erfolg bei Dndn dabei.
Was mich hier interessiert sind 2 dinge:
- bist du sicher, dass geron einen besseren impfstoff finden wird als Dndn?
- von anderen aktien weiß ich, dass investoren sich die rosinen aus dem kuchen picken; ist auf Rockhill Investment verlass??
Viele Grüße Ede
Antwort auf Beitrag Nr.: 29.331.376 von edelupolino am 15.05.07 19:29:14- bist du sicher, dass geron einen besseren impfstoff finden wird als Dndn?
provenge hat in allen ergebnissen bisher nicht überzeugt. Es war für mich nie eine wirkliche alternative. die überlebungsraten von ein paar wochen mehr als ohne sind kein argument.
der impfstoff gerons ist zwar weiter gediehen als der telomerasehemmer gnr 163 l, dieser jedoch, ist auch weit effektiver!!!
der juni könnte für geron spannend werden!
Dendreon habe ich nie als konkurenz empfunden, lediglich als first mover! das produkt ist einfach zu schlecht.
provenge hat in allen ergebnissen bisher nicht überzeugt. Es war für mich nie eine wirkliche alternative. die überlebungsraten von ein paar wochen mehr als ohne sind kein argument.
der impfstoff gerons ist zwar weiter gediehen als der telomerasehemmer gnr 163 l, dieser jedoch, ist auch weit effektiver!!!
der juni könnte für geron spannend werden!
Dendreon habe ich nie als konkurenz empfunden, lediglich als first mover! das produkt ist einfach zu schlecht.
Keine adulten Stammzellen im Pankreas
PHILADELPHIA (wsa). US-Forscher haben herausgefunden, dass es offenbar im Pankreas doch nicht wie vermutet adulte Stammzellen gibt. Indem sie einzelne Zellen mit Farbstoffen markierten, konnten sie zeigen, dass Betazellen selbst teilungsfähig sind. Deren geringe Teilungsrate zu erhöhen, könnte eine Möglichkeit sein, den Insulinmangel von Diabetespatienten zu beheben (Developmental Cell 12, 2007, 817).
"Wir müssen lernen, besser zu verstehen, was das Wachstum von Betazellen reguliert, anstatt nach adulten Stammzellen zu suchen, aus denen sie entstehen", so Dr. Jake Kushner vom Children’s Hospital of Philadelphia. Um Typ-1-Diabetikern dauerhaft zu helfen, versucht man unter anderem, adulte Stammzellen der Bauchspeicheldrüse dazu anzuregen, sich in Betazellen umzuwandeln.
Bei der Teilung der Betazellen legen diese zwischen zwei Teilungen eine ungewöhnlich lange Ruhephase ein. Damit vermehrt Betazellen entstehen, müsste man den Teilungszyklus beschleunigen. Davon würden, so Kushner, nicht nur Typ-1Diabetiker
PHILADELPHIA (wsa). US-Forscher haben herausgefunden, dass es offenbar im Pankreas doch nicht wie vermutet adulte Stammzellen gibt. Indem sie einzelne Zellen mit Farbstoffen markierten, konnten sie zeigen, dass Betazellen selbst teilungsfähig sind. Deren geringe Teilungsrate zu erhöhen, könnte eine Möglichkeit sein, den Insulinmangel von Diabetespatienten zu beheben (Developmental Cell 12, 2007, 817).
"Wir müssen lernen, besser zu verstehen, was das Wachstum von Betazellen reguliert, anstatt nach adulten Stammzellen zu suchen, aus denen sie entstehen", so Dr. Jake Kushner vom Children’s Hospital of Philadelphia. Um Typ-1-Diabetikern dauerhaft zu helfen, versucht man unter anderem, adulte Stammzellen der Bauchspeicheldrüse dazu anzuregen, sich in Betazellen umzuwandeln.
Bei der Teilung der Betazellen legen diese zwischen zwei Teilungen eine ungewöhnlich lange Ruhephase ein. Damit vermehrt Betazellen entstehen, müsste man den Teilungszyklus beschleunigen. Davon würden, so Kushner, nicht nur Typ-1Diabetiker
Antwort auf Beitrag Nr.: 29.332.890 von meislo am 15.05.07 20:40:21danke für die antwort!
Ede
Ede
http://biz.yahoo.com/bw/070517/20070517005178.html?.v=1
Geron Scientists and Collaborators Differentiate Human Embryonic Stem Cells Into Insulin-Producing Islet-Like Clusters
Thursday May 17, 7:30 am ET
Studies Demonstrate Feasibility of Producing Therapeutic Cells From hESCs for Treatment of Diabetes
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) today reported that its scientists and collaborators at the University of Alberta have differentiated human embryonic stem cells (hESCs) into islet-like clusters (ILCs) that secrete insulin in response to elevated glucose levels. The studies demonstrate the feasibility of producing therapeutic cell types from hESCs for the treatment of diabetes.
To be published in the August issue of Stem Cells, which is available now for online viewing in Stem Cells Express at http://stemcells.alphamedpress.org/papbyrecent.dtl, the paper describes studies showing how the researchers differentiated hESCs into cell clusters containing the main cellular components of the islets of Langerhans. The islets of Langerhans are structures in the pancreas that are responsible for regulating and producing insulin in response to changing glucose concentrations and are targets for autoimmune destruction or dysfunction in Type I Diabetes.
"These studies show that the islet-like clusters contain the major cellular components of islets and are sensitive to glucose, the key sugar to which they must respond to be therapeutically beneficial," stated Anish Majumdar, Ph.D., the senior author of the paper. "Our major goal moving forward is to improve the purity, yield and maturational status of these cells to induce normoglycemia in animal models of diabetes."
Geron Corporation was granted U.S. Patent No. 7,033,831 in April 2006 covering the production of insulin-secreting cells from hESCs as well as two U.K. patents covering similar production methods. Geron also has a worldwide exclusive commercial license covering hESC-derived islets from the Wisconsin Alumni Research Foundation.
Geron's scientists and collaborators produced ILCs containing individual cells types that express insulin, glucagon and somatostatin, three of the major hormones produced by islet beta, alpha and delta cells, respectively. Further analysis of the insulin-producing cells indicates they also produce c-peptide, a peptide cleaved upon secretion of the precursor of insulin, indicating that insulin was actually produced, and not absorbed, by the cells. Approximately 2%-8% of the differentiated cells contain insulin and c-peptide and their insulin content was higher than that of fetal islets.
The ILCs functioned to secrete insulin in response to elevated glucose levels. Cells within the ILCs contained secretory granules characteristic of those seen in islet beta cells. In cell culture, the ILCs produced c-peptide and insulin when exposed to higher concentrations of glucose with the kinetics of an immature islet.
The protocol to produce the ILCs drives hESCs through a series of cell culture steps that mimic the progressive differentiation stages during development of the pancreas in humans. Other pancreatic cell types resembling those of the exocrine pancreas were also observed during the differentiation process. The protocol does not utilize serum or feeder cells of any kind, underscoring the scalability of the process.
Originally developed at the University of Alberta, the Edmonton Protocol provides the proof of concept that transplantation of purified cadaveric islets can significantly reduce the need for insulin in patients with advanced Type 1 Diabetes. Problems limiting the accessibility of transplantation therapy for diabetes patients are the poor availability of organs from cadavers and the eventual failure of the grafts, which often require replacement and chronic immunosuppression.
"The Edmonton Protocol provides significant evidence that transplantation of primary islets can be used to successfully reduce the need for insulin in patients with Type 1 Diabetes," said Thomas B. Okarma, Ph.D., M.D., Geron's president and chief executive officer. "It is the work published today that demonstrates the potential of human embryonic stem cells to enable the ready availability of uniform, functional islet cells for therapeutic administration."
Geron Scientists and Collaborators Differentiate Human Embryonic Stem Cells Into Insulin-Producing Islet-Like Clusters
Thursday May 17, 7:30 am ET
Studies Demonstrate Feasibility of Producing Therapeutic Cells From hESCs for Treatment of Diabetes
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) today reported that its scientists and collaborators at the University of Alberta have differentiated human embryonic stem cells (hESCs) into islet-like clusters (ILCs) that secrete insulin in response to elevated glucose levels. The studies demonstrate the feasibility of producing therapeutic cell types from hESCs for the treatment of diabetes.
To be published in the August issue of Stem Cells, which is available now for online viewing in Stem Cells Express at http://stemcells.alphamedpress.org/papbyrecent.dtl, the paper describes studies showing how the researchers differentiated hESCs into cell clusters containing the main cellular components of the islets of Langerhans. The islets of Langerhans are structures in the pancreas that are responsible for regulating and producing insulin in response to changing glucose concentrations and are targets for autoimmune destruction or dysfunction in Type I Diabetes.
"These studies show that the islet-like clusters contain the major cellular components of islets and are sensitive to glucose, the key sugar to which they must respond to be therapeutically beneficial," stated Anish Majumdar, Ph.D., the senior author of the paper. "Our major goal moving forward is to improve the purity, yield and maturational status of these cells to induce normoglycemia in animal models of diabetes."
Geron Corporation was granted U.S. Patent No. 7,033,831 in April 2006 covering the production of insulin-secreting cells from hESCs as well as two U.K. patents covering similar production methods. Geron also has a worldwide exclusive commercial license covering hESC-derived islets from the Wisconsin Alumni Research Foundation.
Geron's scientists and collaborators produced ILCs containing individual cells types that express insulin, glucagon and somatostatin, three of the major hormones produced by islet beta, alpha and delta cells, respectively. Further analysis of the insulin-producing cells indicates they also produce c-peptide, a peptide cleaved upon secretion of the precursor of insulin, indicating that insulin was actually produced, and not absorbed, by the cells. Approximately 2%-8% of the differentiated cells contain insulin and c-peptide and their insulin content was higher than that of fetal islets.
The ILCs functioned to secrete insulin in response to elevated glucose levels. Cells within the ILCs contained secretory granules characteristic of those seen in islet beta cells. In cell culture, the ILCs produced c-peptide and insulin when exposed to higher concentrations of glucose with the kinetics of an immature islet.
The protocol to produce the ILCs drives hESCs through a series of cell culture steps that mimic the progressive differentiation stages during development of the pancreas in humans. Other pancreatic cell types resembling those of the exocrine pancreas were also observed during the differentiation process. The protocol does not utilize serum or feeder cells of any kind, underscoring the scalability of the process.
Originally developed at the University of Alberta, the Edmonton Protocol provides the proof of concept that transplantation of purified cadaveric islets can significantly reduce the need for insulin in patients with advanced Type 1 Diabetes. Problems limiting the accessibility of transplantation therapy for diabetes patients are the poor availability of organs from cadavers and the eventual failure of the grafts, which often require replacement and chronic immunosuppression.
"The Edmonton Protocol provides significant evidence that transplantation of primary islets can be used to successfully reduce the need for insulin in patients with Type 1 Diabetes," said Thomas B. Okarma, Ph.D., M.D., Geron's president and chief executive officer. "It is the work published today that demonstrates the potential of human embryonic stem cells to enable the ready availability of uniform, functional islet cells for therapeutic administration."
Mal wieder hoges vorbörsliches Volumen mit kräftigem Kursanstieg :
:
 :
:
Antwort auf Beitrag Nr.: 29.357.610 von meislo am 17.05.07 15:03:48Schwenken wir ein auf eine Art Zielgerade?  Habe mich lange nicht mehr geäußert hier in diesem Board, ich hatte Geron schon fast verdrängt. Aber es scheint ganz langsam was zu werden.
Habe mich lange nicht mehr geäußert hier in diesem Board, ich hatte Geron schon fast verdrängt. Aber es scheint ganz langsam was zu werden.
 Habe mich lange nicht mehr geäußert hier in diesem Board, ich hatte Geron schon fast verdrängt. Aber es scheint ganz langsam was zu werden.
Habe mich lange nicht mehr geäußert hier in diesem Board, ich hatte Geron schon fast verdrängt. Aber es scheint ganz langsam was zu werden.
Antwort auf Beitrag Nr.: 29.357.686 von greenhorn1998 am 17.05.07 15:11:03Denke der Knoten ist geplatzt
Geron Study Published in Stem Cells
Thursday May 17, 9:05 am ET
Geron Laboratory Study Shows Possible Future Stem Cell-Based Diabetes Treatment
NEW YORK (AP) -- Shares of Geron Corp. jumped Thursday after its scientists, in collaboration with the University of Alberta colleagues, saw positive results from a laboratory study on human embryonic stem cell treatments for diabetes.
The study, being published in the August issue of Stem Cells, shows scientists were able to differentiate human embryonic stem cells into clusters that produce an insulin response to elevated glucose levels. The results, the company said, show it may be possible to produce these therapeutic stem cells as a diabetes treatment.
The hope is that a stem-cell based treatment could reduce the need for insulin patients with Type 1 diabetes.
Shares jumped 48 cents,or 5.8 percent, to $8.72.
Anmerkung von mir
Typ 1 diabetiker sind der seltenere Fall (schätze das nur 5-10% an diesem Typ erkranken) Der häufigste Fall Typ 2 auch Alterszucker (90% leiden an diesem Typ) kann hierdurch nicht geheilt werden.

Geron Study Published in Stem Cells
Thursday May 17, 9:05 am ET
Geron Laboratory Study Shows Possible Future Stem Cell-Based Diabetes Treatment
NEW YORK (AP) -- Shares of Geron Corp. jumped Thursday after its scientists, in collaboration with the University of Alberta colleagues, saw positive results from a laboratory study on human embryonic stem cell treatments for diabetes.
The study, being published in the August issue of Stem Cells, shows scientists were able to differentiate human embryonic stem cells into clusters that produce an insulin response to elevated glucose levels. The results, the company said, show it may be possible to produce these therapeutic stem cells as a diabetes treatment.
The hope is that a stem-cell based treatment could reduce the need for insulin patients with Type 1 diabetes.
Shares jumped 48 cents,or 5.8 percent, to $8.72.
Anmerkung von mir
Typ 1 diabetiker sind der seltenere Fall (schätze das nur 5-10% an diesem Typ erkranken) Der häufigste Fall Typ 2 auch Alterszucker (90% leiden an diesem Typ) kann hierdurch nicht geheilt werden.
Die 9 Dollar sind gerade unter hohen Umsätzen gefallen

Antwort auf Beitrag Nr.: 29.357.785 von meislo am 17.05.07 15:19:12Geron\\\'s (GERN - Cramer\\\'s Take - Stockpickr) vital signs keep getting stronger.
The biotechnology company, which enjoyed a muscular rally following coverage by TheStreet.com earlier this week, extended its gains after reporting a new medical breakthrough on Thursday. In a preview of an article due out by Stem Cells in August, the company unveiled fresh progress on a stem cell-related treatment for diabetes.
Specifically, Geron said that it has differentiated embryonic stem cells into clusters that \\\"secrete insulin in response to elevated glucose levels.\\\" The advance could offer hope for huge crowds of people who suffer from Type 1 diabetes.
Geron shareholders sure feel optimistic. They saw the company\\\'s stock - which was stuck around $7 just two months ago - rocket 9.6% to $9.03 on the news.
Robert Lawton, managing partner of New York\\\'s Catoosa Fund, feels that Geron shareholders have finally started seeing the type of payoff that they deserve.
\\\"If Geron had published a press release like this a month ago - or even a week ago - it wouldn\\\'t have budged the stock,\\\" says Lawton, whose firm has a long position in the company itself. \\\"The stock could have even ended up red for the day.
\\\"But it\\\'s on the radar screen now.\\\"
Lawton feels that Geron\\\'s latest run has been fueled by a \\\"coalescence\\\" of favorable events, starting with TheStreet.com\\\'s big story on Monday. He says that new investors - including technical experts, momentum players and \\\"lazy brokers looking for new ideas\\\" - seem to be piling into the stock quite heavily this week.
Geron\\\'s stock has broken through several technical averages, on extremely heavy volume, during the recent rally.
\\\"There really hasn\\\'t been a lot of big institutional interest in the stock until this week,\\\" Lawton says. \\\"But you\\\'ve seen the market: It\\\'s looking for something to chase. (And) this is a very sexy story.\\\"
The biotechnology company, which enjoyed a muscular rally following coverage by TheStreet.com earlier this week, extended its gains after reporting a new medical breakthrough on Thursday. In a preview of an article due out by Stem Cells in August, the company unveiled fresh progress on a stem cell-related treatment for diabetes.
Specifically, Geron said that it has differentiated embryonic stem cells into clusters that \\\"secrete insulin in response to elevated glucose levels.\\\" The advance could offer hope for huge crowds of people who suffer from Type 1 diabetes.
Geron shareholders sure feel optimistic. They saw the company\\\'s stock - which was stuck around $7 just two months ago - rocket 9.6% to $9.03 on the news.
Robert Lawton, managing partner of New York\\\'s Catoosa Fund, feels that Geron shareholders have finally started seeing the type of payoff that they deserve.
\\\"If Geron had published a press release like this a month ago - or even a week ago - it wouldn\\\'t have budged the stock,\\\" says Lawton, whose firm has a long position in the company itself. \\\"The stock could have even ended up red for the day.
\\\"But it\\\'s on the radar screen now.\\\"
Lawton feels that Geron\\\'s latest run has been fueled by a \\\"coalescence\\\" of favorable events, starting with TheStreet.com\\\'s big story on Monday. He says that new investors - including technical experts, momentum players and \\\"lazy brokers looking for new ideas\\\" - seem to be piling into the stock quite heavily this week.
Geron\\\'s stock has broken through several technical averages, on extremely heavy volume, during the recent rally.
\\\"There really hasn\\\'t been a lot of big institutional interest in the stock until this week,\\\" Lawton says. \\\"But you\\\'ve seen the market: It\\\'s looking for something to chase. (And) this is a very sexy story.\\\"
Antwort auf Beitrag Nr.: 29.362.436 von nocherts am 17.05.07 19:39:13
9,37



Ich lege mich fest
das ist die trendwende




Ich lege mich fest
das ist die trendwende

Das wurde langsam Zeit. Die Aufmerksamkeit in nun wieder erwacht, Geron ist unter den Price % Gainers: http://finance.yahoo.com/gainers?e=us
Ein shortie gibt sich nicht geschlagen
http://www.youtube.com/watch?v=Tca-AkF2_6w&mode=related&sear…
Von denen gibt es ca. sechs millionen

http://www.youtube.com/watch?v=Tca-AkF2_6w&mode=related&sear…
Von denen gibt es ca. sechs millionen

Thursday's Health Winners & Losers
By Robert Holmes
TheStreet.com Staff Reporter (Die mögen Geton auf einmal!!!, da kann ich mich aber noch an ganz andere Zeiten erinnern)
5/17/2007 2:08 PM EDT
Click here for more stories by Robert Holmes
Charles Schwab
E*TRADE FINANCIAL
Bank of America
Zecco.com
The Trading Institute
TD AMERITRADE
Geron (GERN - Cramer's Take - Stockpickr) was the best health care performer of Thursday's sluggish session, following positive news out of a recently study.
Shares jumped 11% after Geron said that its scientists have seen progress in using embryonic stem cells as an effective treatment for type 1 diabetes. Recently, Geron was adding 91 cents to $9.15.
By Robert Holmes
TheStreet.com Staff Reporter (Die mögen Geton auf einmal!!!, da kann ich mich aber noch an ganz andere Zeiten erinnern)
5/17/2007 2:08 PM EDT
Click here for more stories by Robert Holmes
Charles Schwab
E*TRADE FINANCIAL
Bank of America
Zecco.com
The Trading Institute
TD AMERITRADE
Geron (GERN - Cramer's Take - Stockpickr) was the best health care performer of Thursday's sluggish session, following positive news out of a recently study.
Shares jumped 11% after Geron said that its scientists have seen progress in using embryonic stem cells as an effective treatment for type 1 diabetes. Recently, Geron was adding 91 cents to $9.15.
Antwort auf Beitrag Nr.: 29.363.062 von meislo am 17.05.07 20:23:519,47

Antwort auf Beitrag Nr.: 29.363.009 von meislo am 17.05.07 20:19:28
ich hasse shorts; wird zeit, dass die SEC oder wer auch immer denen bei ihren stinkigen spielen (bs "naked shorts" = illegal aber laufende praxis) auf die gierigen finger sieht.
mal beobachten, wie der heutige anstieg von denen gekontert wird...
ich hasse shorts; wird zeit, dass die SEC oder wer auch immer denen bei ihren stinkigen spielen (bs "naked shorts" = illegal aber laufende praxis) auf die gierigen finger sieht.
mal beobachten, wie der heutige anstieg von denen gekontert wird...
Antwort auf Beitrag Nr.: 29.363.115 von meislo am 17.05.07 20:29:16
klasse, sogar noch etwas gestiegen...
klasse, sogar noch etwas gestiegen...
Heute gehts über 10 dollar

Antwort auf Beitrag Nr.: 29.372.227 von meislo am 18.05.07 14:32:23 geron könnte in einen agressiven buy-trigger geraten.dann sehen wir kurse um 70 euro
geron könnte in einen agressiven buy-trigger geraten.dann sehen wir kurse um 70 euro
 geron könnte in einen agressiven buy-trigger geraten.dann sehen wir kurse um 70 euro
geron könnte in einen agressiven buy-trigger geraten.dann sehen wir kurse um 70 euro
Antwort auf Beitrag Nr.: 29.432.938 von pedestrian am 23.05.07 12:36:54
welche chartformation sagt dir das?
Gruß Ede
welche chartformation sagt dir das?
Gruß Ede
Antwort auf Beitrag Nr.: 29.443.481 von edelupolino am 23.05.07 22:20:09 @ede,schau bei finanznachrichten.de nach.der chart von godmode trader vom 07.12.2006.
@ede,schau bei finanznachrichten.de nach.der chart von godmode trader vom 07.12.2006.
mfg
pedestrian
 @ede,schau bei finanznachrichten.de nach.der chart von godmode trader vom 07.12.2006.
@ede,schau bei finanznachrichten.de nach.der chart von godmode trader vom 07.12.2006.mfg
pedestrian
!
Dieser Beitrag wurde vom System automatisch gesperrt. Bei Fragen wenden Sie sich bitte an feedback@wallstreet-online.de
Stem cell breakthrough a bust on Wall Street
Biotechs mixed after reports of major development in stem cell research; potential treatments far, far away
http://money.cnn.com/2007/06/07/news/companies/stemcell/inde…
Biotechs mixed after reports of major development in stem cell research; potential treatments far, far away
http://money.cnn.com/2007/06/07/news/companies/stemcell/inde…
http://biz.yahoo.com/bw/070611/20070611005188.html?.v=1
Geron says reserch indicates its embryonic stem cell-based therapeutic for spinal cord injury evades direct attack by the human immune system (GERN) 8.67 : Co announces the presentation of research studies indicating that GRNOPC1, the co's human embryonic stem cell (hESC)-based therapeutic for the treatment of spinal cord injury, evades a direct attack by the human immune system. Presented by GERN scientist Ross Okamura at the Federation of Clinical Immunology Societies meeting, the findings could mean that patients treated with GRNOPC1 would require significantly lower doses and/or shorter courses of immunosuppression than what are required for patients who undergo solid organ transplants. "The results imply that our cell-based therapeutic, unlike traditional solid organ transplants, is minimally recognized by the human immune system," said Thomas Okarma, Ph.D, M.D., GERN's president and CEO. "Because GRNOPC1 cells are allogenic, it was expected that they would be recognized and destroyed by multiple immune rejection modulators. This isn't the case. The benefit to patients is that a reduction in the requirement for immunosuppression decreases the potential for untoward side effects that are common with those types of drugs." The data indicate that GRNOPC1 cells have low susceptibility to both direct cell and antibody-mediated immune responses. The data also show that GRNOPC1 cells do not widely express non-human antigens, such as Neu5GC, that might have originated from mouse feeder cells to which the original hESC cell line was exposed in its initial derivation.
Geron says reserch indicates its embryonic stem cell-based therapeutic for spinal cord injury evades direct attack by the human immune system (GERN) 8.67 : Co announces the presentation of research studies indicating that GRNOPC1, the co's human embryonic stem cell (hESC)-based therapeutic for the treatment of spinal cord injury, evades a direct attack by the human immune system. Presented by GERN scientist Ross Okamura at the Federation of Clinical Immunology Societies meeting, the findings could mean that patients treated with GRNOPC1 would require significantly lower doses and/or shorter courses of immunosuppression than what are required for patients who undergo solid organ transplants. "The results imply that our cell-based therapeutic, unlike traditional solid organ transplants, is minimally recognized by the human immune system," said Thomas Okarma, Ph.D, M.D., GERN's president and CEO. "Because GRNOPC1 cells are allogenic, it was expected that they would be recognized and destroyed by multiple immune rejection modulators. This isn't the case. The benefit to patients is that a reduction in the requirement for immunosuppression decreases the potential for untoward side effects that are common with those types of drugs." The data indicate that GRNOPC1 cells have low susceptibility to both direct cell and antibody-mediated immune responses. The data also show that GRNOPC1 cells do not widely express non-human antigens, such as Neu5GC, that might have originated from mouse feeder cells to which the original hESC cell line was exposed in its initial derivation.
Geron announces its telomerase inhibitor cancer drug demonstrates 'good' pharmacokinetics and tolerability in Phase I/II trial (GERN) 8.73 : Co announces its telomerase inhibitor cancer drug, GRN163L, has demonstrated good pharmacokinetics and tolerability in its ongoing Phase I/II trial involving patients with chronic lymphocytic leukemia, according to data presented today by Alan Colowick, M.D., M.P.H., the co's president, oncology, at the Pan Pacific Lymphoma Conference in Maui, Hawaii. "Based on preclinical data demonstrating the effects of GRN163L on both mature and cancer stem cells in multiple myeloma, Geron will initiate a clinical trial involving multiple myeloma patients... In addition, the company will begin a fourth trial of GRN163L in combination with carboplatin and paclitaxel in patients with non-small cell lung cancer. The basis for this trial is the result of promising preclinical animal data demonstrating the drug's activity in this tumor type as well. Geron expects to initiate both trials in the coming months."
http://biz.yahoo.com/bw/070612/20070612005141.html?.v=1
http://biz.yahoo.com/bw/070612/20070612005141.html?.v=1
Unfassbar
Die Amis strafen Geron ab. Die spinnen die Amis und verstehen nichts!!!!
Nach den Ergebnissen Geron unbedingt einsammeln!!
Es ging soch nur um siccherheitsrelevante Tests und immerhin ist bei einer Person bei einer nur zweiwöchigen Verabreichung geringer Mengen von dem Telomerasehemmer die Zahl der gefährlichen Krebszellen um 48% gesunken.
Einsammeln!!!
Die Amis strafen Geron ab. Die spinnen die Amis und verstehen nichts!!!!
Nach den Ergebnissen Geron unbedingt einsammeln!!
Es ging soch nur um siccherheitsrelevante Tests und immerhin ist bei einer Person bei einer nur zweiwöchigen Verabreichung geringer Mengen von dem Telomerasehemmer die Zahl der gefährlichen Krebszellen um 48% gesunken.
Einsammeln!!!
Einige sehen das wohl auch so wie ich
No Knockout for Geron
By Melissa Davis
Senior Writer
6/12/2007 12:02 PM EDT
Click here for more stories by Melissa Davis
Fisher Investments
CyberTrader
Scottrade
TD AMERITRADE
Fidelity Investments
Charles Schwab
Geron (GERN - Cramer's Take - Stockpickr - Rating) is testing some investors' patience.
The California-based biotechnology company failed to deliver blockbuster news on its novel GRN163L cancer treatment during this week's Pan Pacific Lymphoma Conference in Hawaii. Instead, the company simply reported that GRN163L has "demonstrated good pharmacokinetics and tolerability" in patients tested during phase I/II studies so far.
GRN163L seeks to targets an enzyme, known as telomerase, that enables cancer cells to multiply and survive. At the modest doses tested thus far, however, GRN163L has failed to significantly alter telomerase activity or shorten the chromosome ends -- called telomeres -- that are involved in the cancer-development process.
Some investors seemed to be banking on an outright miracle instead. After pushing Geron toward $10 a share last month in anticipation of big news, they pounded the stock down 8.3% to $8.01 on Tuesday's modest development.
"Candidly, people don't know what to expect with Geron; that's the problem," says WBB Securities analyst Stephen Brozak. "Certainly, day traders want instant news that they can easily interpret. But this is not that simple.
"These are unique strategies that are difficult to understand and deal with."
Brozak, for one, feels that Geron continues to make steady and important progress. He has personally researched Geron for more than a decade and now sees a viable company -- with real commercial potential -- in the making. But he admits that newcomers could fail to recognize the same.
Brozak blames a potential overload of complex information for the confusion.
"It isn't like there's a shortage of news; it's like there is too much news for most investors to understand," he says. "But in fairness to the company, it's not like they're piling on with a lot of extraneous stuff. Everything they talk about has significance."
Brozak likes what he hears. He has a strong buy recommendation on Geron's stock. His firm has no position in Geron itself and has provided no investment banking services to the company over the past two years.
Meanwhile, Geron did witness some positive developments during its recent GRN163L study. For starters, the company said that one GRN163L recipient is experiencing "stable disease" patterns following two rounds of cancer treatment. Moreover, the company said that a second patient has experienced a rapid destruction in malignant cells -- with the "absolute lymphocyte count" dropping by 48% -- during a posttreatment period that has persisted for two weeks.
Geron stopped short of crediting GRN163L for progress in that patient, however, due to "the lack of measured telomerase inhibition" observed. Indeed, Geron indicated that patients should probably be exposed to GRN163L for longer periods of time in order for the treatment's telomerase-inhibiting powers to take effect.
Brozak, at least, feels more than willing to wait.
"They're starting to get some preliminary indication of how things are going," he explains. "This is one of the necessary steps in the progress that Geron is making in going from a research enterprise to a full-blown commercial operation."

No Knockout for Geron
By Melissa Davis
Senior Writer
6/12/2007 12:02 PM EDT
Click here for more stories by Melissa Davis
Fisher Investments
CyberTrader
Scottrade
TD AMERITRADE
Fidelity Investments
Charles Schwab
Geron (GERN - Cramer's Take - Stockpickr - Rating) is testing some investors' patience.
The California-based biotechnology company failed to deliver blockbuster news on its novel GRN163L cancer treatment during this week's Pan Pacific Lymphoma Conference in Hawaii. Instead, the company simply reported that GRN163L has "demonstrated good pharmacokinetics and tolerability" in patients tested during phase I/II studies so far.
GRN163L seeks to targets an enzyme, known as telomerase, that enables cancer cells to multiply and survive. At the modest doses tested thus far, however, GRN163L has failed to significantly alter telomerase activity or shorten the chromosome ends -- called telomeres -- that are involved in the cancer-development process.
Some investors seemed to be banking on an outright miracle instead. After pushing Geron toward $10 a share last month in anticipation of big news, they pounded the stock down 8.3% to $8.01 on Tuesday's modest development.
"Candidly, people don't know what to expect with Geron; that's the problem," says WBB Securities analyst Stephen Brozak. "Certainly, day traders want instant news that they can easily interpret. But this is not that simple.
"These are unique strategies that are difficult to understand and deal with."
Brozak, for one, feels that Geron continues to make steady and important progress. He has personally researched Geron for more than a decade and now sees a viable company -- with real commercial potential -- in the making. But he admits that newcomers could fail to recognize the same.
Brozak blames a potential overload of complex information for the confusion.
"It isn't like there's a shortage of news; it's like there is too much news for most investors to understand," he says. "But in fairness to the company, it's not like they're piling on with a lot of extraneous stuff. Everything they talk about has significance."
Brozak likes what he hears. He has a strong buy recommendation on Geron's stock. His firm has no position in Geron itself and has provided no investment banking services to the company over the past two years.
Meanwhile, Geron did witness some positive developments during its recent GRN163L study. For starters, the company said that one GRN163L recipient is experiencing "stable disease" patterns following two rounds of cancer treatment. Moreover, the company said that a second patient has experienced a rapid destruction in malignant cells -- with the "absolute lymphocyte count" dropping by 48% -- during a posttreatment period that has persisted for two weeks.
Geron stopped short of crediting GRN163L for progress in that patient, however, due to "the lack of measured telomerase inhibition" observed. Indeed, Geron indicated that patients should probably be exposed to GRN163L for longer periods of time in order for the treatment's telomerase-inhibiting powers to take effect.
Brozak, at least, feels more than willing to wait.
"They're starting to get some preliminary indication of how things are going," he explains. "This is one of the necessary steps in the progress that Geron is making in going from a research enterprise to a full-blown commercial operation."
Ist nur eine Meinung aus dem Yahoo-Board!
Warum auch nicht?!!
GERN - first TRILLION dollar company?
12-Jun-07 12:59 pm Looks like Geron (GERN) has a cure for cancer with no side effects.
I have not heard Geron's Okarma use the term cancer "cure" until last month. It is clear that Geron's focus of cancer research has shifted from attacking just any cancer cell to focusing on the cancer stem cell as a means of defining cancer "cure."How long will it take for the media to take the lead and announce that fact. When that happens, and I am confident that it will, all hell will break loose.
Geron's drug"163L knocks down the cancer stem cell by 50% in just 3 days " Geron's Dr. Okarma said.
Geron's president Dr.Okama said he was going to make Geron the next Amgen.
If he is successful 800 shares of Geron will be worth one million dollars $$$$.
It looks like Dr.Okarma is going to far exceed his goal!!!
"If there is a company whose suite of research projects better typifies where biotechnology is headed, it isn't publicly traded."----BARRON'S 4-27-06.
Geron "It's the most valuable patent estate in all of biotechnology", says Lissa Morgenthaler.
Michael Murphy said that Geron could be the worlds first trillion $$$ company.
Warum auch nicht?!!

GERN - first TRILLION dollar company?
12-Jun-07 12:59 pm Looks like Geron (GERN) has a cure for cancer with no side effects.
I have not heard Geron's Okarma use the term cancer "cure" until last month. It is clear that Geron's focus of cancer research has shifted from attacking just any cancer cell to focusing on the cancer stem cell as a means of defining cancer "cure."How long will it take for the media to take the lead and announce that fact. When that happens, and I am confident that it will, all hell will break loose.
Geron's drug"163L knocks down the cancer stem cell by 50% in just 3 days " Geron's Dr. Okarma said.
Geron's president Dr.Okama said he was going to make Geron the next Amgen.
If he is successful 800 shares of Geron will be worth one million dollars $$$$.
It looks like Dr.Okarma is going to far exceed his goal!!!
"If there is a company whose suite of research projects better typifies where biotechnology is headed, it isn't publicly traded."----BARRON'S 4-27-06.
Geron "It's the most valuable patent estate in all of biotechnology", says Lissa Morgenthaler.
Michael Murphy said that Geron could be the worlds first trillion $$$ company.
geron hätte gut daran getan, solche pressemitteilungen zu unterlassen. der vorher generierte hype war sträflich, da dadurch zuviele shortterm longs angezogen wurden, die nun ihr material auf die straße kippen, wo bereits das blut in den rinnen läuft.
wenn vorläufiges verwirrt bzw. verwirren kann, dann sollte geron bitte enggültiges abwarten und dann berichten.
das was wir gestern erlebt haben, ist eine echte pr-pleite und recht unprofessionell.
jetzt haben wir aber genau das, was wir gar nicht wollen: UNSICHERHEIT.
zuerst die aussage 'good pharmacokinetics' -- früher hieß das im tierversuch immer 'excellent'. Was heißt denn nun good im vergleich zu excellent?
und dann noch das: 'Up to the current dose levels, no significant changes in telomerase activity or telomere length in the bulk circulating CLL cells of treated patients have been observed.'
So eine Aussage ist der reine Alptraum!!
es bedeutet zum einen: grn163l wirkt derzeit grundsätzlich nicht
zum anderen: es ist noch zu beweisen, ob es bei höheren dosen wirkt.
und zuletzt noch das problem, dass grn163l bei einem patienten wohl zu stark gewirkt hat. wie furchtbar! denn diese tatsache steht im krassen widerspruch zu der aussage, dass grn163l erst bei höhern dosen wirkt.
ich habe gestern lange nachgedacht, ob ich mich von meinem bestand trennen soll. noch bin ich leicht im plus.
ich warte nochmal ab, bin aber alles andere als amused.
uns steht eine harte zeit bevor, freunde!
wenn vorläufiges verwirrt bzw. verwirren kann, dann sollte geron bitte enggültiges abwarten und dann berichten.
das was wir gestern erlebt haben, ist eine echte pr-pleite und recht unprofessionell.
jetzt haben wir aber genau das, was wir gar nicht wollen: UNSICHERHEIT.
zuerst die aussage 'good pharmacokinetics' -- früher hieß das im tierversuch immer 'excellent'. Was heißt denn nun good im vergleich zu excellent?
und dann noch das: 'Up to the current dose levels, no significant changes in telomerase activity or telomere length in the bulk circulating CLL cells of treated patients have been observed.'
So eine Aussage ist der reine Alptraum!!
es bedeutet zum einen: grn163l wirkt derzeit grundsätzlich nicht
zum anderen: es ist noch zu beweisen, ob es bei höheren dosen wirkt.
und zuletzt noch das problem, dass grn163l bei einem patienten wohl zu stark gewirkt hat. wie furchtbar! denn diese tatsache steht im krassen widerspruch zu der aussage, dass grn163l erst bei höhern dosen wirkt.
ich habe gestern lange nachgedacht, ob ich mich von meinem bestand trennen soll. noch bin ich leicht im plus.
ich warte nochmal ab, bin aber alles andere als amused.
uns steht eine harte zeit bevor, freunde!
Hallo zusammen!
Ich muss auch ehrlich zugeben, dass mich die Mitteilung alles andere als aus den Socken gehauen hat. Eher im Gegenteil. Es fing quasi mit der Überschrift an: Was heißt "good"?
LuckyCat hat das ja schon alles ausgeführt. Die 10 Prozent Minus gestern haben mich nicht verwundert. Naja, so lange dabei, entweder es wird - oder eben nicht. Immerhin, sie sind nach wie vor "encouraged"...
Gruß, greenhorn
Ich muss auch ehrlich zugeben, dass mich die Mitteilung alles andere als aus den Socken gehauen hat. Eher im Gegenteil. Es fing quasi mit der Überschrift an: Was heißt "good"?
LuckyCat hat das ja schon alles ausgeführt. Die 10 Prozent Minus gestern haben mich nicht verwundert. Naja, so lange dabei, entweder es wird - oder eben nicht. Immerhin, sie sind nach wie vor "encouraged"...

Gruß, greenhorn
http://stockcharts.com/h-sc/ui?c=gern,uu[m,a]daclyyay[dd][pb…
Gap geschlossen, Stochastics abgekühlt und in der kehrtposition
Seit ihr da nicht auf einem Holzweg?!
die Ergebnisse waren gut und gerade vor dem Hintergrund da Geron als Stammzellenunternehmen in Sachen Risiko nicht allzuviel riskieren kann. Die Verabreichungsdosen sind eben deshalb auch extrem schwach gewählt.
Wait and see
Gap geschlossen, Stochastics abgekühlt und in der kehrtposition
Seit ihr da nicht auf einem Holzweg?!
die Ergebnisse waren gut und gerade vor dem Hintergrund da Geron als Stammzellenunternehmen in Sachen Risiko nicht allzuviel riskieren kann. Die Verabreichungsdosen sind eben deshalb auch extrem schwach gewählt.
Wait and see

18.06.2007
Vier Gene helfen bei der verblüffenden Verjüngung erwachsener Hautzellen zu vielseitigen Stammzellen. (Bild: AP) Jungbrunnen für Hautzellen
Neues Verfahren könnte Stammzell-Dilemma lösen
Medizin. - Menschliche embryonale Stammzellen gelten als Hoffnungsträger bei der Heilung schwerer Krankheiten, doch sie sind auch ethisch höchst umstritten. Viel eleganter wäre ein Weg, der erst vor kurzem offenbar gelang: die Verjüngung von Körperzellen in den Stammzellzustand. Doch seit den Skandalen auf diesem Forschungsgebiet gibt sich die Wissenschaftsgemeinde skeptisch, so auch auf einem Treffen der Stammzellspezialisten im australischen Cairns. Der Wissenschaftsjournalist Volkart Wildermuth erläutert den Stand im Gespräch mit Gerd Pasch.
Gerd Pasch: Volkart Wildermuth, wie ist die neue Methode denn aufgenommen worden?
Volkart Wildermuth: Mit einem gewissen Maß an Erleichterung muss man sagen. Seit Korea mit dem Klonen von menschlichen embryonalen Stammzellen für Furore gesorgt hat und sich das alles später als Ente herausstellte, sind die Forscher vorsichtiger. Aber dieser Ansatz, künstlich vier Gene in eine Hautzelle einzubringen und damit ohne den Verbrauch von Eizellen und ohne die Erzeugung eines Embryos den Zeiger ihrer Lebensuhr quasi wieder auf Null zu stellen, der wurde ja vor einem Jahr zum ersten Mal vorgestellt. Jetzt konnten gleich mehrere Arbeitsgruppen das Ergebnis bestätigen und damit scheint festzustehen, das geht tatsächlich, daher die Erleichterung.
Pasch: Welche Bedeutung könnte das Verfahren denn jetzt bekommen?
Wildermuth: In der Forschung wird es sicher sehr wichtig werden und das aus ganz praktischen Gründen. Viele Forscher wollen Zellen von Patienten klonen, um ihre Krankheiten untersuchen zu können. Die Harvard Universität hatte dafür zum Beispiel eine Genehmigung. Allein die Experimente konnten nicht beginnen. Für das Forschungsklonen werden viele menschliche Eizellen benötigt. Es fanden sich aber keine Frauen dazu bereit, ihre Eizellen für die Wissenschaft zu spenden. Es sind also nicht nur ethische, sondern auch ganz praktische Gründe, die Forscher dazu bewegen, sich nach Alternativen umzusehen. Die Genmanipulation bietet nun die Möglichkeit, Patientenzellen ohne die Hilfe von Eizellen zu verjüngen. Kein Wunder, dass in Cairns viele Forscher genaueres über diese Thema erfahren wollten.
Pasch: Das war jetzt das Feld der Forschung. Kann man diese ethisch unbedenklichen embryonalen Stammzellen denn theoretisch auch in der Therapie einsetzen?
Wildermuth: Was therapeutische Ansätze betrifft, wurde da in Cairns erst einmal zur Vorsicht gemahnt. Eines der vier Jungbrunnen-Gene ist ein Krebs-Gen, mit ihm zu spielen ist also gefährlich, und tatsächlich haben einige der ersten Mäuse, die aus diesen embryonalen Stammzellen entstanden, inzwischen Tumoren entwickelt. Entscheidend ist aber, dass die Forscher jetzt Faktoren für diese Zellverjüngung in der Hand haben und untersuchen können. Sie hoffen, die bisweilen magisch anmutenden Rezepturen der Zellumwandlung durch klare chemische Regeln zu ersetzen. Und mit denen lassen sich dann vielleicht in Zukunft auch ohne Gentransfer ethisch unbedenkliche embryonale Stammzellen erzeugen.
Pasch: Wie sieht es überhaupt aus, bewegt sich die embryonale Stammzellforschung langsam in Richtung praktischer Anwendungen?
Wildermuth: Bislang wird das Feld der embryonalen Stammzellen von Versprechungen dominiert. So kündigt die Firma Geron schon lange Studien an Patienten mit Rückenmarkverletzungen an. In Cairns berichteten australischen Patienten, dass Geron sie gefragt hat, ob sie an eine Studie zur Querschnittslähmung Studie teilnehmen würden. Es sieht also so aus, als ob dieses Projekt endlich aus den Starlöchern käme. Das ist auch bitter nötig, denn es hat sich quasi ein Stammzelltourismus entwickelt. Wenn die Wissenschaft und Medizin der ersten Welt diese Therapien zwar hochjubelt, sie aber nicht anbieten, dann machen sich verzweifelte Patienten auf den Weg nach China oder Indien, und begeben sich in die Hände von eher zweifelhaften Ärzten, die sie angeblich mit embryonalen Stammzellen behandeln.
Pasch: Spielte die Ethik denn in Cairns eine Rolle?
Wildermuth: Es gab eine eigene Sitzung, auf der Ethiker und Juristen aus unterschiedlichen Nationen den Stand der jeweiligen Diskussion zusammenfassten. In Australien ist seit wenigen Tagen das Forschungsklonen erlaubt. In Großbritannien wird wohl schon bald ein Parlamentsausschuss die Erzeugung von Chimären ermöglichen. Dabei sollen für das Forschungsklonen statt der knappen Eizellen von Frauen solche von Hasen oder Kühen verwendet werden. In den USA wollen Senat und Repräsentantenhaus die Forschung an embryonalen Stammzellen erleichtern, allerdings wird wohl Präsident George Bush sein Veto einlegen. Insgesamt geht der Trend also zu liberaleren Regelungen. Für die Forscher allerdings wird es langsam schwer, abzuschätzen, welche Stammzellline nun welchen Ansprüchen genügt. Hier soll in Zukunft eine internationale Datenbank für Klarheit sorgen. Für deutsche Forscher sind die Gesetze aber ebenso restriktiv wie klar. Solange sich die Gesetze nicht ändern, werden sie mit den meisten neuen Linien nicht arbeiten können.
http://www.dradio.de/dlf/sendungen/forschak/636949/
Vier Gene helfen bei der verblüffenden Verjüngung erwachsener Hautzellen zu vielseitigen Stammzellen. (Bild: AP) Jungbrunnen für Hautzellen
Neues Verfahren könnte Stammzell-Dilemma lösen
Medizin. - Menschliche embryonale Stammzellen gelten als Hoffnungsträger bei der Heilung schwerer Krankheiten, doch sie sind auch ethisch höchst umstritten. Viel eleganter wäre ein Weg, der erst vor kurzem offenbar gelang: die Verjüngung von Körperzellen in den Stammzellzustand. Doch seit den Skandalen auf diesem Forschungsgebiet gibt sich die Wissenschaftsgemeinde skeptisch, so auch auf einem Treffen der Stammzellspezialisten im australischen Cairns. Der Wissenschaftsjournalist Volkart Wildermuth erläutert den Stand im Gespräch mit Gerd Pasch.
Gerd Pasch: Volkart Wildermuth, wie ist die neue Methode denn aufgenommen worden?
Volkart Wildermuth: Mit einem gewissen Maß an Erleichterung muss man sagen. Seit Korea mit dem Klonen von menschlichen embryonalen Stammzellen für Furore gesorgt hat und sich das alles später als Ente herausstellte, sind die Forscher vorsichtiger. Aber dieser Ansatz, künstlich vier Gene in eine Hautzelle einzubringen und damit ohne den Verbrauch von Eizellen und ohne die Erzeugung eines Embryos den Zeiger ihrer Lebensuhr quasi wieder auf Null zu stellen, der wurde ja vor einem Jahr zum ersten Mal vorgestellt. Jetzt konnten gleich mehrere Arbeitsgruppen das Ergebnis bestätigen und damit scheint festzustehen, das geht tatsächlich, daher die Erleichterung.
Pasch: Welche Bedeutung könnte das Verfahren denn jetzt bekommen?
Wildermuth: In der Forschung wird es sicher sehr wichtig werden und das aus ganz praktischen Gründen. Viele Forscher wollen Zellen von Patienten klonen, um ihre Krankheiten untersuchen zu können. Die Harvard Universität hatte dafür zum Beispiel eine Genehmigung. Allein die Experimente konnten nicht beginnen. Für das Forschungsklonen werden viele menschliche Eizellen benötigt. Es fanden sich aber keine Frauen dazu bereit, ihre Eizellen für die Wissenschaft zu spenden. Es sind also nicht nur ethische, sondern auch ganz praktische Gründe, die Forscher dazu bewegen, sich nach Alternativen umzusehen. Die Genmanipulation bietet nun die Möglichkeit, Patientenzellen ohne die Hilfe von Eizellen zu verjüngen. Kein Wunder, dass in Cairns viele Forscher genaueres über diese Thema erfahren wollten.
Pasch: Das war jetzt das Feld der Forschung. Kann man diese ethisch unbedenklichen embryonalen Stammzellen denn theoretisch auch in der Therapie einsetzen?
Wildermuth: Was therapeutische Ansätze betrifft, wurde da in Cairns erst einmal zur Vorsicht gemahnt. Eines der vier Jungbrunnen-Gene ist ein Krebs-Gen, mit ihm zu spielen ist also gefährlich, und tatsächlich haben einige der ersten Mäuse, die aus diesen embryonalen Stammzellen entstanden, inzwischen Tumoren entwickelt. Entscheidend ist aber, dass die Forscher jetzt Faktoren für diese Zellverjüngung in der Hand haben und untersuchen können. Sie hoffen, die bisweilen magisch anmutenden Rezepturen der Zellumwandlung durch klare chemische Regeln zu ersetzen. Und mit denen lassen sich dann vielleicht in Zukunft auch ohne Gentransfer ethisch unbedenkliche embryonale Stammzellen erzeugen.
Pasch: Wie sieht es überhaupt aus, bewegt sich die embryonale Stammzellforschung langsam in Richtung praktischer Anwendungen?
Wildermuth: Bislang wird das Feld der embryonalen Stammzellen von Versprechungen dominiert. So kündigt die Firma Geron schon lange Studien an Patienten mit Rückenmarkverletzungen an. In Cairns berichteten australischen Patienten, dass Geron sie gefragt hat, ob sie an eine Studie zur Querschnittslähmung Studie teilnehmen würden. Es sieht also so aus, als ob dieses Projekt endlich aus den Starlöchern käme. Das ist auch bitter nötig, denn es hat sich quasi ein Stammzelltourismus entwickelt. Wenn die Wissenschaft und Medizin der ersten Welt diese Therapien zwar hochjubelt, sie aber nicht anbieten, dann machen sich verzweifelte Patienten auf den Weg nach China oder Indien, und begeben sich in die Hände von eher zweifelhaften Ärzten, die sie angeblich mit embryonalen Stammzellen behandeln.
Pasch: Spielte die Ethik denn in Cairns eine Rolle?
Wildermuth: Es gab eine eigene Sitzung, auf der Ethiker und Juristen aus unterschiedlichen Nationen den Stand der jeweiligen Diskussion zusammenfassten. In Australien ist seit wenigen Tagen das Forschungsklonen erlaubt. In Großbritannien wird wohl schon bald ein Parlamentsausschuss die Erzeugung von Chimären ermöglichen. Dabei sollen für das Forschungsklonen statt der knappen Eizellen von Frauen solche von Hasen oder Kühen verwendet werden. In den USA wollen Senat und Repräsentantenhaus die Forschung an embryonalen Stammzellen erleichtern, allerdings wird wohl Präsident George Bush sein Veto einlegen. Insgesamt geht der Trend also zu liberaleren Regelungen. Für die Forscher allerdings wird es langsam schwer, abzuschätzen, welche Stammzellline nun welchen Ansprüchen genügt. Hier soll in Zukunft eine internationale Datenbank für Klarheit sorgen. Für deutsche Forscher sind die Gesetze aber ebenso restriktiv wie klar. Solange sich die Gesetze nicht ändern, werden sie mit den meisten neuen Linien nicht arbeiten können.
http://www.dradio.de/dlf/sendungen/forschak/636949/
20. Juni 2007 | 09:47 Uhr Kommentieren | Artikel drucken | Artikel versendenGeron investiert bleiben
Börsenticker aus Kulmbach (aktiencheck.de AG) - Die Experten vom Anlegermagazin "Der Aktionär" raten langfristig orientierten Anlegern der Geron-Aktie (ISIN US3741631036/ WKN 902213) weiter die Treue zu halten.
In der vergangenen Woche habe der Kurs der Geron-Aktie deutlich an Wert verloren. Grund: Das US-Biotechnologie-Unternehmen habe bei einer Konferenz auf Hawaii keine - wie von vielen Anlegern erwartet - neuen Studiendaten seines Krebsmittels GRN163L präsentiert. Darauf hätten einige Investoren enttäuscht reagiert und sich von der Aktie getrennt.
Die Experten hätten die Geron-Aktie im August vergangenen Jahres zu einem Kurs von 4,66 Euro empfohlen. Bis heute habe sich das Papier um 29,4 Prozent auf aktuell 6,03 Euro verbessern können. Das Kursziel sehe man bei 9 Euro.
Langfristig orientierten Anlegern empfehlen die Experten von "Der Aktionär" der Geron-Aktie nach wie vor die Treue zu halten. Zur Absicherung sollte ein Stoppkurs bei 5,10 Euro platziert werden. (Ausgabe 26) (20.06.2007/ac/a/a)
Börsenticker aus Kulmbach (aktiencheck.de AG) - Die Experten vom Anlegermagazin "Der Aktionär" raten langfristig orientierten Anlegern der Geron-Aktie (ISIN US3741631036/ WKN 902213) weiter die Treue zu halten.
In der vergangenen Woche habe der Kurs der Geron-Aktie deutlich an Wert verloren. Grund: Das US-Biotechnologie-Unternehmen habe bei einer Konferenz auf Hawaii keine - wie von vielen Anlegern erwartet - neuen Studiendaten seines Krebsmittels GRN163L präsentiert. Darauf hätten einige Investoren enttäuscht reagiert und sich von der Aktie getrennt.
Die Experten hätten die Geron-Aktie im August vergangenen Jahres zu einem Kurs von 4,66 Euro empfohlen. Bis heute habe sich das Papier um 29,4 Prozent auf aktuell 6,03 Euro verbessern können. Das Kursziel sehe man bei 9 Euro.
Langfristig orientierten Anlegern empfehlen die Experten von "Der Aktionär" der Geron-Aktie nach wie vor die Treue zu halten. Zur Absicherung sollte ein Stoppkurs bei 5,10 Euro platziert werden. (Ausgabe 26) (20.06.2007/ac/a/a)
geron - it\'s a stock pumper\'s dream.
das schreibt adam feuerstein (von the street.com). wie recht er hat. wie oft hat geron daten zu grn163l im klinischen einsatz angekündigt und vorher mit positiven studien im tierversuch investoreninteresse geweckt? geron ist mit der lieferung der daten letzte woche komplett gescheitert. was gemeldet wurde war reine mist (sorry für den ausdruck, aber es ist halt so).
das vertrauen in das management ist stark erschüttert. so langsam muss es auch mir als einem der letzten dämmern, dass geron ein jahrelanger ankündigungsweltmeister ist, aber kaum mehr.
was haben wir den mit geron? ein bio-high-tech relativ kleiner nummer mit einigen interessanten patenten und einem ceo als blender bzw. hervoragendem präsentierer! mehr? gewinne? produkte?
da enorm viel vertrauen zerstört wurde, wird der aktuell noch bestehende aufwärtstrend im kursverlauf brechen. die shortzahlen werden das belegen. die 200-tage-linie ist bereits deutlich unterschritten, mehr wird folgen. wir sehen den kurs in 2007 noch mal bei 5-6 usd. grund: es wird keine wirklich harten fakten mehr geben, die das bild wieder ändern könnten.
was für ein fehlinvestment! eigentlich hätte ich und viele andere es besser wissen können!?!
das schreibt adam feuerstein (von the street.com). wie recht er hat. wie oft hat geron daten zu grn163l im klinischen einsatz angekündigt und vorher mit positiven studien im tierversuch investoreninteresse geweckt? geron ist mit der lieferung der daten letzte woche komplett gescheitert. was gemeldet wurde war reine mist (sorry für den ausdruck, aber es ist halt so).
das vertrauen in das management ist stark erschüttert. so langsam muss es auch mir als einem der letzten dämmern, dass geron ein jahrelanger ankündigungsweltmeister ist, aber kaum mehr.
was haben wir den mit geron? ein bio-high-tech relativ kleiner nummer mit einigen interessanten patenten und einem ceo als blender bzw. hervoragendem präsentierer! mehr? gewinne? produkte?
da enorm viel vertrauen zerstört wurde, wird der aktuell noch bestehende aufwärtstrend im kursverlauf brechen. die shortzahlen werden das belegen. die 200-tage-linie ist bereits deutlich unterschritten, mehr wird folgen. wir sehen den kurs in 2007 noch mal bei 5-6 usd. grund: es wird keine wirklich harten fakten mehr geben, die das bild wieder ändern könnten.
was für ein fehlinvestment! eigentlich hätte ich und viele andere es besser wissen können!?!
insoweit sollten wir den thread "geron mit hammernews!!" so langsam schließen... und einen neuen eröffnen mit dem titel "geron mit katastrophennews"














































































ALLGEMEINE INFOS zur Zulassung neuer Arzneien
22.06.2007 - 09:28 Uhr
FTD: Das kann ja heiter werden
Die Zulassung neuer Arzneien ist für die Pharmabranche längst keine Kleinigkeit mehr. Regelmäßig lassen die Behörden Hoffnungsträger durchfallen und Börsenträume platzen. Künftig kommt es noch dicker.
Sanofi-Aventis ist fassungslos über die Ablehnung seiner Diätpille Acomplia bei der US-Behörde FDA. Begründung: psychische Nebenwirkungen.
GlaxoSmithKline fürchtet das Aus für das umsatzstarke Diabetesmittel Avandia. Risiko: Herzinfarkt.
Das neue Krebsmittel Vectibix vom weltgrößten Biotechkonzern Amgen findet nicht den Zuspruch der Kontrolleure bei der EU-Behörde Emea. Erklärung: Wirksamkeit zweifelhaft.
Drei Beispiele aus der jüngsten Vergangenheit - eine gemeinsame Wirkung: Aufruhr an der Börse. Die Aktienkurse der betreffenden Konzerne sackten nacheinander auf ein Zweijahrestief. Allen Beteiligten, den Managern, Analysten und Kontrolleuren steckt noch der Skandal um das Schmerzmittel Vioxx in den Knochen. Die Folge für den Hersteller Merck & Co. sowie die Branche waren Tausende Schadensersatzklagen, Imagekrisen und Milliardenverluste. Das mahnte zur Vorsicht. Im Jahr drei nach Vioxx zieht die Politik auf beiden Seiten des Atlantiks die Zügel nun noch fester an.
So feilten am Donnerstag in Washington US-Senatoren an letzten Details für ein Gesetz, das der FDA mehr Einfluss und Geld für zusätzliche Sicherheitskontrollen von Medikamenten gibt. Dazu zahlt die Industrie an die FDA Gebühren von rund 400 Mio. $ jährlich, weitere 225 Mio. $ bringt sie in den kommenden fünf Jahren für die FDA-Observierung von Neueinführungen auf. "Die Nation hat aus den Sicherheitsproblemen mit dem Diabetesmedikament Avandia gelernt", sagte der Vorsitzende des Kongressausschusses, John Dingell, vor wenigen Tagen. Zudem können Verstöße gegen Marketing- und Sicherheitsauflagen mit bis zu 100 Mio. $
Strafe geahndet werden.
Und auch die Emea kann nun härter durchgreifen. Die EU-Kommission hat am 15. Juni eine Verordnung in Kraft gesetzt die Verstöße gegen Emea-Regeln mit hohen Geldbußen ahndet - etwa, wenn Firmen Vorgaben ihrer Arzneimittelzulassungen nicht einhalten, Informationen zur Risikobewertung ihrer Produkte zurückhalten oder deren Nebenwirkungen gar nicht oder erst sehr spät melden.
"Sehr harte Sanktionen"
Die Höchstgrenze der Geldbußen liegt bei fünf Prozent des Jahresumsatzes des betroffenen Zulassungsinhabers. Zulassungsinhaber kann auch eine Konzerntochter sein. "Das dürfte zu ungerechten Bestrafungen führen", sagte Unternehmensanwalt Uwe Fröhlich vom Pharmakonzern Baxter. "Zufälligerweise oder sogar absichtlich kann ein besonders umsatzstarker oder umsatzschwacher Teil eines Konzerns Inhaber der Zulassung sein. Ein Schlupfloch könnten auch Vermarktungspartnerschaften unabhängiger Unternehmen bieten, von denen nur eines die Zulassung hält." Gerechter sei es, die Buße am EU-weiten Umsatz der Arznei festzumachen. "Das sind alles in allem sehr harte Sanktionen", sagt Anwalt Jörg Schickert von der Kanzlei Lovells in München. Er findet manches an der Verordnung unausgereift. "Es gibt noch Schwachstellen, darunter die Frage, wie die Abgrenzung zwischen einzelstaatlichen Strafmaßnahmen und EU-weiten Sanktionen geregelt werden soll."
Das für Zulassungen zuständige Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) habe in der jüngeren Vergangenheit einige Straf- und Bußgeldverfahren eingeleitet, mit unterschiedlichem Ausgang entsprechend der Beweislage, heißt es auf Anfrage. "Ob es in Zukunft wichtiger sein wird, derartige Instrumentarien zur Verfügung zu haben, lässt sich nur schwer einschätzen", so das BfArM. Die im Arzneimittelgesetz für Ordnungswidrigkeiten vorgesehenen Bußgelder von maximal 25.000 Euro seien vergleichsweise gering.
Die Verordnung (EG) 658/2007 zur Auferlegung von Geldbußen durch die Kommission ist ein neuartiges Sanktionsmittel, das es für von der Emea zugelassene Arzneimittel bislang noch nicht gab. "Die Industrie sollte schnellstmöglich alle Schwachstellen abklopfen und Verfahren aufsetzen, die zukünftig Verstöße vermeiden. Dies sollte auch dokumentiert werden", sagte der Anwalt Schickert.
Emea-Chef Thomas Lönngren zumindest will nie mehr einen Tag wie den 30. September 2004 erleben: Weder der Vioxx-Hersteller Merck & Co. noch die FDA-Kollegen hatten ihn frühzeitig über den geplanten Rückruf der Schmerzpille informiert. Die Börse wusste früher Bescheid als er. "Wir wollen von Konzernen so schnell wie möglich informiert werden", sagte er.
Autor/Autoren: Peter Kuchenbuch
http://www.finanztreff.de/ftreff/news.htm?sektion=topthemen&…
22.06.2007 - 09:28 Uhr
FTD: Das kann ja heiter werden
Die Zulassung neuer Arzneien ist für die Pharmabranche längst keine Kleinigkeit mehr. Regelmäßig lassen die Behörden Hoffnungsträger durchfallen und Börsenträume platzen. Künftig kommt es noch dicker.
Sanofi-Aventis ist fassungslos über die Ablehnung seiner Diätpille Acomplia bei der US-Behörde FDA. Begründung: psychische Nebenwirkungen.
GlaxoSmithKline fürchtet das Aus für das umsatzstarke Diabetesmittel Avandia. Risiko: Herzinfarkt.
Das neue Krebsmittel Vectibix vom weltgrößten Biotechkonzern Amgen findet nicht den Zuspruch der Kontrolleure bei der EU-Behörde Emea. Erklärung: Wirksamkeit zweifelhaft.
Drei Beispiele aus der jüngsten Vergangenheit - eine gemeinsame Wirkung: Aufruhr an der Börse. Die Aktienkurse der betreffenden Konzerne sackten nacheinander auf ein Zweijahrestief. Allen Beteiligten, den Managern, Analysten und Kontrolleuren steckt noch der Skandal um das Schmerzmittel Vioxx in den Knochen. Die Folge für den Hersteller Merck & Co. sowie die Branche waren Tausende Schadensersatzklagen, Imagekrisen und Milliardenverluste. Das mahnte zur Vorsicht. Im Jahr drei nach Vioxx zieht die Politik auf beiden Seiten des Atlantiks die Zügel nun noch fester an.
So feilten am Donnerstag in Washington US-Senatoren an letzten Details für ein Gesetz, das der FDA mehr Einfluss und Geld für zusätzliche Sicherheitskontrollen von Medikamenten gibt. Dazu zahlt die Industrie an die FDA Gebühren von rund 400 Mio. $ jährlich, weitere 225 Mio. $ bringt sie in den kommenden fünf Jahren für die FDA-Observierung von Neueinführungen auf. "Die Nation hat aus den Sicherheitsproblemen mit dem Diabetesmedikament Avandia gelernt", sagte der Vorsitzende des Kongressausschusses, John Dingell, vor wenigen Tagen. Zudem können Verstöße gegen Marketing- und Sicherheitsauflagen mit bis zu 100 Mio. $
Strafe geahndet werden.
Und auch die Emea kann nun härter durchgreifen. Die EU-Kommission hat am 15. Juni eine Verordnung in Kraft gesetzt die Verstöße gegen Emea-Regeln mit hohen Geldbußen ahndet - etwa, wenn Firmen Vorgaben ihrer Arzneimittelzulassungen nicht einhalten, Informationen zur Risikobewertung ihrer Produkte zurückhalten oder deren Nebenwirkungen gar nicht oder erst sehr spät melden.
"Sehr harte Sanktionen"
Die Höchstgrenze der Geldbußen liegt bei fünf Prozent des Jahresumsatzes des betroffenen Zulassungsinhabers. Zulassungsinhaber kann auch eine Konzerntochter sein. "Das dürfte zu ungerechten Bestrafungen führen", sagte Unternehmensanwalt Uwe Fröhlich vom Pharmakonzern Baxter. "Zufälligerweise oder sogar absichtlich kann ein besonders umsatzstarker oder umsatzschwacher Teil eines Konzerns Inhaber der Zulassung sein. Ein Schlupfloch könnten auch Vermarktungspartnerschaften unabhängiger Unternehmen bieten, von denen nur eines die Zulassung hält." Gerechter sei es, die Buße am EU-weiten Umsatz der Arznei festzumachen. "Das sind alles in allem sehr harte Sanktionen", sagt Anwalt Jörg Schickert von der Kanzlei Lovells in München. Er findet manches an der Verordnung unausgereift. "Es gibt noch Schwachstellen, darunter die Frage, wie die Abgrenzung zwischen einzelstaatlichen Strafmaßnahmen und EU-weiten Sanktionen geregelt werden soll."
Das für Zulassungen zuständige Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) habe in der jüngeren Vergangenheit einige Straf- und Bußgeldverfahren eingeleitet, mit unterschiedlichem Ausgang entsprechend der Beweislage, heißt es auf Anfrage. "Ob es in Zukunft wichtiger sein wird, derartige Instrumentarien zur Verfügung zu haben, lässt sich nur schwer einschätzen", so das BfArM. Die im Arzneimittelgesetz für Ordnungswidrigkeiten vorgesehenen Bußgelder von maximal 25.000 Euro seien vergleichsweise gering.
Die Verordnung (EG) 658/2007 zur Auferlegung von Geldbußen durch die Kommission ist ein neuartiges Sanktionsmittel, das es für von der Emea zugelassene Arzneimittel bislang noch nicht gab. "Die Industrie sollte schnellstmöglich alle Schwachstellen abklopfen und Verfahren aufsetzen, die zukünftig Verstöße vermeiden. Dies sollte auch dokumentiert werden", sagte der Anwalt Schickert.
Emea-Chef Thomas Lönngren zumindest will nie mehr einen Tag wie den 30. September 2004 erleben: Weder der Vioxx-Hersteller Merck & Co. noch die FDA-Kollegen hatten ihn frühzeitig über den geplanten Rückruf der Schmerzpille informiert. Die Börse wusste früher Bescheid als er. "Wir wollen von Konzernen so schnell wie möglich informiert werden", sagte er.
Autor/Autoren: Peter Kuchenbuch
http://www.finanztreff.de/ftreff/news.htm?sektion=topthemen&…
wie weit gehts noch runter?
der chart hängt total. alle chancen auf regionen von 10 usd und mehr sind für längere zeit weg. im gegenteil. die "chance", nochmal 6 usd oder etwas weniger zu sehen steigen momentam jeden tag.
traurig...
der chart hängt total. alle chancen auf regionen von 10 usd und mehr sind für längere zeit weg. im gegenteil. die "chance", nochmal 6 usd oder etwas weniger zu sehen steigen momentam jeden tag.
traurig...
wie vermutet, freunde!
gerons short-zahlen sind - absolut gesehen - am rekordhoch! 8,9 mio. aktien waren per 15.6. short verkauft, ein zuwachs von mehr als 2 mio. gegenüber mai! +25%!
am 12.6. kam es nach der pr-pleite um grn163l zu einem starken kursververfall. wie wir jetzt wissen, sind viele shorties auf geron aufgesprungen, das handelvolumen lag bei 5 mio. stück.
wie gehts weiter? ähnlich dendreon? da sind von den ausstehenden 81 mio. stück sage und schreibe 40 mio. stück short verkauft.
passiert das bei geron, dann ist der kurs wieder bei 1 usd...
luckycat
gerons short-zahlen sind - absolut gesehen - am rekordhoch! 8,9 mio. aktien waren per 15.6. short verkauft, ein zuwachs von mehr als 2 mio. gegenüber mai! +25%!
am 12.6. kam es nach der pr-pleite um grn163l zu einem starken kursververfall. wie wir jetzt wissen, sind viele shorties auf geron aufgesprungen, das handelvolumen lag bei 5 mio. stück.
wie gehts weiter? ähnlich dendreon? da sind von den ausstehenden 81 mio. stück sage und schreibe 40 mio. stück short verkauft.
passiert das bei geron, dann ist der kurs wieder bei 1 usd...
luckycat
Kulmbach (aktiencheck.de AG) - Die Experten vom Anlegermagazin "Der Aktionär" raten langfristig orientierten Anlegern der Geron-Aktie (ISIN US3741631036/ WKN 902213) weiter die Treue zu halten. In der vergangenen Woche habe der Kurs der Geron-Aktie deutlich an Wert verloren. Grund: Das US-Biotechnologie-Unternehmen habe bei einer Konferenz auf Hawaii keine - wie von vielen Anlegern erwartet - neuen Studiendaten seines Krebsmittels GRN163L präsentiert. Darauf hätten einige Investoren enttäuscht reagiert und sich von der Aktie getrennt. Die Experten hätten die Geron-Aktie im August vergangenen Jahres zu einem Kurs von 4,66 Euro empfohlen. Bis heute habe sich das Papier um 29,4 Prozent auf aktuell 6,03 Euro verbessern können. Das Kursziel sehe man bei 9 Euro. Langfristig orientierten Anlegern empfehlen die Experten von "Der Aktionär" der Geron-Aktie nach wie vor die Treue zu halten. Zur Absicherung sollte ein Stoppkurs bei 5,10 Euro platziert werden. (Ausgabe 26) (20.06.2007/ac/a/a)
LuckyCat siehe posting #2143
War schon mal eingestellt

Diese News treibt den Kurs heute gegen Norden
Geron Initiates Clinical Trial of Telomerase Inhibitor Drug in Combination With Paclitaxel and Carboplatin in Patients With Non-Small Cell Lung Cancer
Monday July 9, 7:30 am ET
Third Clinical Trial Program for 163L -- First Clinical Use in Combination Chemotherapy
Ongoing Studies in CLL and Solid Tumors Continue to Accrue Patients
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) announced today the initiation of a clinical trial of its telomerase inhibitor drug, GRN163L, in patients with advanced non-small cell lung cancer (NSCLC).
ADVERTISEMENT
The primary objective of the Phase I/II study is to determine the safety and maximum tolerated dose of GRN163L when administered intravenously in combination with a standard paclitaxel/carboplatin regimen. This is the first time GRN163L is being clinically tested in combination with standard chemotherapy.
"We are excited to study GRN163L in lung cancer," said Joan Schiller, M.D., chief of the Division of Hematology and Oncology and deputy director of Simmons Comprehensive Cancer Center at the University of Texas Southwestern, who is the study's lead investigator. "There is a striking unmet need to improve survival in NSCLC. Telomerase is highly expressed in lung cancer, and preclinical data suggest activity of the drug as a single agent in preventing disease progression in animals bearing human lung cancer cells."
Alan Colowick, M.D., Geron's president, oncology, said, "This is an important milestone in the clinical development of GRN163L. The favorable tolerability and pharmacokinetics demonstrated so far in our solid tumor and CLL trials enable us to test our drug in combination with standard chemotherapy in patients for the first time. Moreover, the safety data generated in our other ongoing trials enable us to start dosing GRN163L in this trial at levels comparable to doses given in cohort 4 of the solid tumor and CLL trials. Once we have established the safety and dosing parameters of GRN163L in combination with paclitaxel and carboplatin in NSCLC, we can study the same combination in other tumor settings."
Geron's two ongoing clinical trials are sequential cohort, dose escalation studies designed to determine the safety and tolerability of GRN163L administered intravenously on a weekly basis as monotherapy to patients with refractory or relapsed CLL and patients with advanced solid tumors. Patients interested in enrollment into either of these ongoing trials should visit the Patient Information page of Geron's website at www.geron.com.
Lung cancer is the leading cause of cancer death worldwide, with an estimated incidence of more than 210,000 new cases in 2007. Non-small cell lung cancer represents more than 85% of these cases, and only 15% of patients with NCSLC survive five years.
About Telomerase and GRN163L
Telomerase is a broadly applicable and critical tumor target. It is expressed in a broad array of malignant tumors, essential for malignant cell growth and absent or expressed transiently at low levels in most normal adult tissues.
GRN163L, Geron's telomerase inhibitor drug, is a short chain oligonucleotide that is unique in its resistance to nuclease digestion in blood and tissues and its very high affinity and specificity for telomerase. The molecule has superior cellular and tissue penetration properties due to its proprietary manufacturing chemistry and its 5' lipid chain.
GRN163L has been demonstrated to have anti-tumor effects in a wide range of hematological and solid tumor models and appears to be unique in its observed effects on tumor stem cells -- the rare, chemotherapy-resistant cancer cells that cause cancer recurrence.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure, diabetes and HIV/AIDS. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
War schon mal eingestellt

Diese News treibt den Kurs heute gegen Norden
Geron Initiates Clinical Trial of Telomerase Inhibitor Drug in Combination With Paclitaxel and Carboplatin in Patients With Non-Small Cell Lung Cancer
Monday July 9, 7:30 am ET
Third Clinical Trial Program for 163L -- First Clinical Use in Combination Chemotherapy
Ongoing Studies in CLL and Solid Tumors Continue to Accrue Patients
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) announced today the initiation of a clinical trial of its telomerase inhibitor drug, GRN163L, in patients with advanced non-small cell lung cancer (NSCLC).
ADVERTISEMENT
The primary objective of the Phase I/II study is to determine the safety and maximum tolerated dose of GRN163L when administered intravenously in combination with a standard paclitaxel/carboplatin regimen. This is the first time GRN163L is being clinically tested in combination with standard chemotherapy.
"We are excited to study GRN163L in lung cancer," said Joan Schiller, M.D., chief of the Division of Hematology and Oncology and deputy director of Simmons Comprehensive Cancer Center at the University of Texas Southwestern, who is the study's lead investigator. "There is a striking unmet need to improve survival in NSCLC. Telomerase is highly expressed in lung cancer, and preclinical data suggest activity of the drug as a single agent in preventing disease progression in animals bearing human lung cancer cells."
Alan Colowick, M.D., Geron's president, oncology, said, "This is an important milestone in the clinical development of GRN163L. The favorable tolerability and pharmacokinetics demonstrated so far in our solid tumor and CLL trials enable us to test our drug in combination with standard chemotherapy in patients for the first time. Moreover, the safety data generated in our other ongoing trials enable us to start dosing GRN163L in this trial at levels comparable to doses given in cohort 4 of the solid tumor and CLL trials. Once we have established the safety and dosing parameters of GRN163L in combination with paclitaxel and carboplatin in NSCLC, we can study the same combination in other tumor settings."
Geron's two ongoing clinical trials are sequential cohort, dose escalation studies designed to determine the safety and tolerability of GRN163L administered intravenously on a weekly basis as monotherapy to patients with refractory or relapsed CLL and patients with advanced solid tumors. Patients interested in enrollment into either of these ongoing trials should visit the Patient Information page of Geron's website at www.geron.com.
Lung cancer is the leading cause of cancer death worldwide, with an estimated incidence of more than 210,000 new cases in 2007. Non-small cell lung cancer represents more than 85% of these cases, and only 15% of patients with NCSLC survive five years.
About Telomerase and GRN163L
Telomerase is a broadly applicable and critical tumor target. It is expressed in a broad array of malignant tumors, essential for malignant cell growth and absent or expressed transiently at low levels in most normal adult tissues.
GRN163L, Geron's telomerase inhibitor drug, is a short chain oligonucleotide that is unique in its resistance to nuclease digestion in blood and tissues and its very high affinity and specificity for telomerase. The molecule has superior cellular and tissue penetration properties due to its proprietary manufacturing chemistry and its 5' lipid chain.
GRN163L has been demonstrated to have anti-tumor effects in a wide range of hematological and solid tumor models and appears to be unique in its observed effects on tumor stem cells -- the rare, chemotherapy-resistant cancer cells that cause cancer recurrence.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure, diabetes and HIV/AIDS. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
Geron Initiates Clinical Trial of Telomerase Cancer Vaccine in Patients with Acute Myelogenous Leukemia
Wednesday July 11, 7:30 am ET
Study Builds on Positive Data Previously Generated in Metastatic Prostate Cancer Patients
Protocol Under Geron's IND is First to Employ Prime-Boost Regimen to Extend Duration of Telomerase Immunity
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) announced today the initiation of a clinical trial of its telomerase cancer vaccine, GRNVAC1, in patients with acute myelogenous leukemia (AML) in complete remission.
ADVERTISEMENT
The vaccine is produced from a patient's blood using a unique process that generates highly activated dendritic cells (DC) that contain RNA coding for the protein component of telomerase. This new approach to cancer immunotherapy has been clinically shown to safely generate high levels of cytotoxic lymphocytes that kill telomerase positive cancer cells after as few as six weekly injections into the skin.
The primary objective of this new Phase I/II study is to evaluate the safety and feasibility of a prime-boost vaccination regimen that extends the duration of telomerase immunity. Secondary objectives are to evaluate the immune response to GRNVAC1 and to explore the effects of vaccination on minimal residual disease and relapse rates. A total of six sites in the United States are planned to participate in this multi-center trial.
"AML is an appropriate indication for investigating a cancer immunotherapy that targets telomerase because of high telomerase expression in AML cells, the great unmet clinical need, especially in older patients who frequently relapse after chemotherapy, and the low tumor burden after consolidation chemotherapy," said John DiPersio, M.D., Ph.D., chief of the Division of Oncology and deputy director of the Siteman Cancer Center at Washington University School of Medicine, St. Louis, who is the study's lead investigator. "Patients at high risk of relapse are in need of additional therapies that are well tolerated. This study is an important step in understanding the role that immunotherapy directed against telomerase might play in cancer treatment."
Alan Colowick, M.D., Geron's president, oncology, said, "We are excited to begin this multi-center study in AML patients who have a high risk for relapse. A great deal of work has enabled us to apply and extend the initial clinical findings for GRNVAC1 in prostate cancer to AML patients. We have scaled and modified the manufacturing of the vaccine to enable a multi-site design with central manufacturing. In addition, we have optimized the prime-boost regimen to enhance the duration of immunity to telomerase in previous clinical studies, and we have demonstrated successful ex vivo DC activation and loading with telomerase antigen in samples taken from patients with AML. We look forward to investigating the tolerability and potential clinical utility of GRNVAC1 in patients with AML."
AML is the most common form of acute leukemia in adults. Although present in all age groups, AML is most often diagnosed in adults over the age of 60. The American Cancer Society estimates that there were more than 11,900 new cases of AML in 2006 in the United States. With current standard chemotherapy regimens, estimates of five-year survival are 25% to 30% for adults younger than 60. Fewer than 10% of older patients with AML attain long-term survival.
GRNVAC1 is an immunotherapeutic product made from autologous dendritic cells transfected with mRNA encoding telomerase protein and the lysosomal targeting signal, lysosome-associated membrane protein (LAMP). This autologous product is designed to induce cellular immune responses to telomerase, an antigen highly expressed in the nucleus of cancer cells and found on their surface but not expressed in most normal cells. Unlike other tumor targets, hTERT, the protein component of telomerase, is essential for maintaining the proliferative capacity and survival of the majority of tumor cell types.
Researchers at Duke University, in collaboration with Geron, have conducted both preclinical and clinical studies using a vaccine product comparable to GRNVAC1.
In Vitro Studies
In vitro studies have demonstrated that autologous dendritic cells transfected with hTERT mRNA stimulate hTERT-specific cytotoxic T-cells (CTL) from the peripheral blood of patients with cancer. These studies have also shown that DC transfected with hTERT mRNA containing the sequence for LAMP may further enhance the efficacy of this approach by optimally stimulating CD8+ and CD4+ T-cell responses (Nair et al, Nat. Med. 2000;6(9):1011-1017) (Su et al, Cancer Res. 2002;62(17):5041-5048).
Clinical Studies
The results of the first study testing hTERT-LAMP mRNA-transfected DC in metastatic prostate cancer patients were published in the Journal of Immunology (Su et al, J. Immunol. 2005;174(6):3798-807). In this study, 20 patients were enrolled and randomized to receive either hTERT mRNA-transfected DC (11 patients) or hTERT-LAMP mRNA-transfected DC (9 patients). Treatment was well tolerated. In 19 of 20 patients, expansion of hTERT-specific T-cells in the peripheral blood of patients was measured after vaccination, with 0.9% to 1.8% of circulating T-cells exhibiting anti-telomerase activity. Patients immunized with the chimeric hTERT-LAMP vaccine exhibited slightly stronger T-cell, and particularly CD4+ T-cell, immune responses to telomerase compared to patients immunized with the unmodified hTERT mRNA-transfected DC vaccine. Moreover, hTERT-specific T-cell killing was enhanced in subjects receiving hTERT-LAMP, suggesting that the improved CD4+ response can augment a CTL response.
Three other Phase I optimization studies of hTERT-LAMP mRNA-transfected DC were conducted at Duke University in patients with metastatic prostate cancer, renal cell carcinoma and hematologic malignancies. Approximately 45 cancer subjects have been treated to date under the Duke protocols. Vaccine-related toxicities were primarily Grade 1-2. Overall, the adverse event pattern in these studies included non-specific, disease-related effects and skin reactions consistent with delayed type hypersensitivity (DTH).
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure, diabetes and HIV/AIDS. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
Wednesday July 11, 7:30 am ET
Study Builds on Positive Data Previously Generated in Metastatic Prostate Cancer Patients
Protocol Under Geron's IND is First to Employ Prime-Boost Regimen to Extend Duration of Telomerase Immunity
MENLO PARK, Calif.--(BUSINESS WIRE)--Geron Corporation (Nasdaq:GERN - News) announced today the initiation of a clinical trial of its telomerase cancer vaccine, GRNVAC1, in patients with acute myelogenous leukemia (AML) in complete remission.
ADVERTISEMENT
The vaccine is produced from a patient's blood using a unique process that generates highly activated dendritic cells (DC) that contain RNA coding for the protein component of telomerase. This new approach to cancer immunotherapy has been clinically shown to safely generate high levels of cytotoxic lymphocytes that kill telomerase positive cancer cells after as few as six weekly injections into the skin.
The primary objective of this new Phase I/II study is to evaluate the safety and feasibility of a prime-boost vaccination regimen that extends the duration of telomerase immunity. Secondary objectives are to evaluate the immune response to GRNVAC1 and to explore the effects of vaccination on minimal residual disease and relapse rates. A total of six sites in the United States are planned to participate in this multi-center trial.
"AML is an appropriate indication for investigating a cancer immunotherapy that targets telomerase because of high telomerase expression in AML cells, the great unmet clinical need, especially in older patients who frequently relapse after chemotherapy, and the low tumor burden after consolidation chemotherapy," said John DiPersio, M.D., Ph.D., chief of the Division of Oncology and deputy director of the Siteman Cancer Center at Washington University School of Medicine, St. Louis, who is the study's lead investigator. "Patients at high risk of relapse are in need of additional therapies that are well tolerated. This study is an important step in understanding the role that immunotherapy directed against telomerase might play in cancer treatment."
Alan Colowick, M.D., Geron's president, oncology, said, "We are excited to begin this multi-center study in AML patients who have a high risk for relapse. A great deal of work has enabled us to apply and extend the initial clinical findings for GRNVAC1 in prostate cancer to AML patients. We have scaled and modified the manufacturing of the vaccine to enable a multi-site design with central manufacturing. In addition, we have optimized the prime-boost regimen to enhance the duration of immunity to telomerase in previous clinical studies, and we have demonstrated successful ex vivo DC activation and loading with telomerase antigen in samples taken from patients with AML. We look forward to investigating the tolerability and potential clinical utility of GRNVAC1 in patients with AML."
AML is the most common form of acute leukemia in adults. Although present in all age groups, AML is most often diagnosed in adults over the age of 60. The American Cancer Society estimates that there were more than 11,900 new cases of AML in 2006 in the United States. With current standard chemotherapy regimens, estimates of five-year survival are 25% to 30% for adults younger than 60. Fewer than 10% of older patients with AML attain long-term survival.
GRNVAC1 is an immunotherapeutic product made from autologous dendritic cells transfected with mRNA encoding telomerase protein and the lysosomal targeting signal, lysosome-associated membrane protein (LAMP). This autologous product is designed to induce cellular immune responses to telomerase, an antigen highly expressed in the nucleus of cancer cells and found on their surface but not expressed in most normal cells. Unlike other tumor targets, hTERT, the protein component of telomerase, is essential for maintaining the proliferative capacity and survival of the majority of tumor cell types.
Researchers at Duke University, in collaboration with Geron, have conducted both preclinical and clinical studies using a vaccine product comparable to GRNVAC1.
In Vitro Studies
In vitro studies have demonstrated that autologous dendritic cells transfected with hTERT mRNA stimulate hTERT-specific cytotoxic T-cells (CTL) from the peripheral blood of patients with cancer. These studies have also shown that DC transfected with hTERT mRNA containing the sequence for LAMP may further enhance the efficacy of this approach by optimally stimulating CD8+ and CD4+ T-cell responses (Nair et al, Nat. Med. 2000;6(9):1011-1017) (Su et al, Cancer Res. 2002;62(17):5041-5048).
Clinical Studies
The results of the first study testing hTERT-LAMP mRNA-transfected DC in metastatic prostate cancer patients were published in the Journal of Immunology (Su et al, J. Immunol. 2005;174(6):3798-807). In this study, 20 patients were enrolled and randomized to receive either hTERT mRNA-transfected DC (11 patients) or hTERT-LAMP mRNA-transfected DC (9 patients). Treatment was well tolerated. In 19 of 20 patients, expansion of hTERT-specific T-cells in the peripheral blood of patients was measured after vaccination, with 0.9% to 1.8% of circulating T-cells exhibiting anti-telomerase activity. Patients immunized with the chimeric hTERT-LAMP vaccine exhibited slightly stronger T-cell, and particularly CD4+ T-cell, immune responses to telomerase compared to patients immunized with the unmodified hTERT mRNA-transfected DC vaccine. Moreover, hTERT-specific T-cell killing was enhanced in subjects receiving hTERT-LAMP, suggesting that the improved CD4+ response can augment a CTL response.
Three other Phase I optimization studies of hTERT-LAMP mRNA-transfected DC were conducted at Duke University in patients with metastatic prostate cancer, renal cell carcinoma and hematologic malignancies. Approximately 45 cancer subjects have been treated to date under the Duke protocols. Vaccine-related toxicities were primarily Grade 1-2. Overall, the adverse event pattern in these studies included non-specific, disease-related effects and skin reactions consistent with delayed type hypersensitivity (DTH).
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure, diabetes and HIV/AIDS. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
So Hammer kann das hier alles gar nicht sein, zumindest nicht wenn ich mir den Chart so ansehe.

http://www.worldofinvestment.com/wkn/902213/
Oder meint ihr das sich das nochmal im positiven Sinne entwickelt? Seit Jahren das Gleiche Bild, hoch und wieder runter, keine richtige Performance in den Norden wie es das Anlegerherz wünscht.
http://www.worldofinvestment.com/wkn/902213/
Oder meint ihr das sich das nochmal im positiven Sinne entwickelt? Seit Jahren das Gleiche Bild, hoch und wieder runter, keine richtige Performance in den Norden wie es das Anlegerherz wünscht.
Antwort auf Beitrag Nr.: 30.808.887 von ShareAnalyst am 23.07.07 10:18:27Geron ist nicht ein Investment für 5-7 Jahre!! Geron musst du bereits haben wenns richtig abgeht!
Ich bin dabei und werde 25-30 Jahre daran festhalten und bei Kursen zwischen 2-5€ nachkaufen...
Das Teil explodiert irgendwann!
Ich bin dabei und werde 25-30 Jahre daran festhalten und bei Kursen zwischen 2-5€ nachkaufen...
Das Teil explodiert irgendwann!
short interest im juli erneut auf neuem rekordhoch: ca. 9,5 mio. aktien - ein plus von etwas über einer halben mio.
werde bei kursen um die 6 usd wieder zukaufen.
werde bei kursen um die 6 usd wieder zukaufen.
da haben die shorts wohl einen satten dollar verdient (oder sogar mehr).
was ist los - sind hier im board alle erstarrt vor lauter kursbedingter paralyse?
was wir sehen ist ein großer, großer ausverkauf. der macd ist auf ein 3-jahrestief gefallen!! es sieht absolut bitter aus!
um die 5 dollar ist ein gewisser boden aus der vergangenheit, aber ob der hält -- i don't know.
was macht ihr? kaufen - halten -verkaufen? meinungen?
vg - lc
was ist los - sind hier im board alle erstarrt vor lauter kursbedingter paralyse?
was wir sehen ist ein großer, großer ausverkauf. der macd ist auf ein 3-jahrestief gefallen!! es sieht absolut bitter aus!
um die 5 dollar ist ein gewisser boden aus der vergangenheit, aber ob der hält -- i don't know.
was macht ihr? kaufen - halten -verkaufen? meinungen?
vg - lc
Antwort auf Beitrag Nr.: 31.059.972 von LuckyCat am 07.08.07 09:32:51Tja- ich lese ziemlich viel was läuft im Sektor und hatte mir auch ein Portion GERN zugelegt als Spekulation auf einen möglichen Merck-Deal wegen GRNVAC wo der Deadline am 15 Juli war. Am 17 Juli wurde dann beim Pressekonferenz in NY bekannt gemacht,dass das Optionszeitraum ein halbes Jahr verlängert worden ist.
Habe dann sofort wieder verkauft- natürlich mit Verlust.
Im Sektor scheint es ganz schwierig Versprechungen einzuhalten- ich kenne das von meinem eigenen Wert Cytori. Aber Geron sprich Okarma sind da absolute Meistern- also lass ich GERN erst mal ein paar Jahr in Ruhe arbeiten bevor man auf neu einsteigen kann.
Beispiele gefällig?
February 22, 2004: "The company believes it will be
cleared to start the first stem-cell therapy in human
tests next year, possibly for spinal-cord injury."
December 1, 2004: "According to Geron CEO Thomas
Okarma [right], the company is aiming to file an
investigational new drug application with the U.S.
Food and Drug Administration (FDA) requesting
permission to begin clinical trials using glial cells
derived from embryonic stem cells to repair damaged
spinal cords in 2005 or early 2006."
February 25, 2005: "Next year [Hans Keirstead] and his
corporate partner, Geron, plan to try treating people
who have recent spinal cord injuries, in what would
almost certainly be the first human trial of any
therapy derived from such cells.
April 19, 2005: Okarma "said he believes the clinical
trial could begin in mid-2006."
September 9, 2005: "Geron plans to begin clinical
trials on acute spinal cord injury treatment in early
2006, according to chief executive officer Tom
Okarma."
November 7, 2005: "[R]esearchers at Geron of Menlo
Park want to take the next step -- in people. They
hope to get federal permission to inject those cells
into damaged spinal cords. The procedure -- which
Geron intends to do next year -- would be the first
human tests of a treatment derived from human
embryonic stem cells, the highly versatile body cells
that can be coaxed into becoming almost any tissue in
the body."
June 17, 2006: "'I'm confident that we will be in the
clinic next year with the first human ESC-derived
product,' said Tom Okarma, chief executive of Geron."
August 4, 2006: "One company, in particular, Menlo
Park, CA-based Geron, is taking the lead in developing
experimental embryonic stem cell therapies and hopes
to begin human trials next year."
May 9, 2007: "The first clinical trial of embryonic
stem cells is on track to start early next year on
patients with spinal cord injury. Geron, the
California-based biotechnology company, will carry out
the study on accident victims in six trauma centres
across the US."
Ohne Kommentar.


Habe dann sofort wieder verkauft- natürlich mit Verlust.
Im Sektor scheint es ganz schwierig Versprechungen einzuhalten- ich kenne das von meinem eigenen Wert Cytori. Aber Geron sprich Okarma sind da absolute Meistern- also lass ich GERN erst mal ein paar Jahr in Ruhe arbeiten bevor man auf neu einsteigen kann.
Beispiele gefällig?
February 22, 2004: "The company believes it will be
cleared to start the first stem-cell therapy in human
tests next year, possibly for spinal-cord injury."
December 1, 2004: "According to Geron CEO Thomas
Okarma [right], the company is aiming to file an
investigational new drug application with the U.S.
Food and Drug Administration (FDA) requesting
permission to begin clinical trials using glial cells
derived from embryonic stem cells to repair damaged
spinal cords in 2005 or early 2006."
February 25, 2005: "Next year [Hans Keirstead] and his
corporate partner, Geron, plan to try treating people
who have recent spinal cord injuries, in what would
almost certainly be the first human trial of any
therapy derived from such cells.
April 19, 2005: Okarma "said he believes the clinical
trial could begin in mid-2006."
September 9, 2005: "Geron plans to begin clinical
trials on acute spinal cord injury treatment in early
2006, according to chief executive officer Tom
Okarma."
November 7, 2005: "[R]esearchers at Geron of Menlo
Park want to take the next step -- in people. They
hope to get federal permission to inject those cells
into damaged spinal cords. The procedure -- which
Geron intends to do next year -- would be the first
human tests of a treatment derived from human
embryonic stem cells, the highly versatile body cells
that can be coaxed into becoming almost any tissue in
the body."
June 17, 2006: "'I'm confident that we will be in the
clinic next year with the first human ESC-derived
product,' said Tom Okarma, chief executive of Geron."
August 4, 2006: "One company, in particular, Menlo
Park, CA-based Geron, is taking the lead in developing
experimental embryonic stem cell therapies and hopes
to begin human trials next year."
May 9, 2007: "The first clinical trial of embryonic
stem cells is on track to start early next year on
patients with spinal cord injury. Geron, the
California-based biotechnology company, will carry out
the study on accident victims in six trauma centres
across the US."
Ohne Kommentar.


das ärgert mich auch jedes mal. geron, der ankündigungsweltmeister. wenn es um\'s liefern von ergebnissen geht: blank, fehlanzeige.
Stammzellenforschung kehrt an die Universität zurück
In Singapur stellt privates Unternehmen seine Tätigkeit ein - "Dolly"-Erfinder Alan Colman bekommt neuen Job
Singapur - Die Hoffnungen auf einen schnellen Geschäftserfolg haben sich in Luft aufgelöst, die vor sieben Jahren mit großem Tamtam gegründete private Gesellschaft ES Cell International (ESI) wirft das Handtuch. In der noch vor kurzer Zeit als sichere Boombranche bezeichneten Forschungssparte lautet die Devise nun offenbar neuerdings wieder: Zurück zur Universität. Einer der prominentesten Mitarbeiter von ESI war Klonschaf-"Dolly"-Co-Erfinder Alan Colman.
Bei ESI hätten die Investoren ihr Interesse verloren, weil "die Wahrscheinlichkeit einer kurzfristigen Marktreife für Produkte zur klinischen Anwendung verschwindend gering war", wurde Colman - somit Ex-Geschäftsführer der Gesellschaft von Venture-Kapitalisten - vor kurzem in der US-Wissenschaftszeitschrift "Science" zitiert.
War vor zwei, drei Jahren noch die Rede davon, dass man über embryonale Stammzellen bald "Reparaturmaterial" zur Behandlung von neurologischen Erkrankungen, von Herzleiden etc. schaffen könnte, so sind diese Ziele mittlerweile in weite Ferne gerückt. Die Wahrscheinlichkeit, dass man mit einer solchen oder ähnlichen Zelltherapie wirklich medizinisch messbare Erfolge verbuchen kann, ist derzeit noch minimal.
Auch der in Fachkreisen weltbekannte Stammzellforscher Robert Lanza von Advanced Cell Technologty in Worcester (US-Bundesstaat Massachusetts) sieht das so: "Dieses ganze Forschungsfeld benötigt dringend ein oder zwei Erfolge."
"Extrem kompliziert"
Gerade die stehen aber aus. ESI hatte versucht, embryonale Stammzellen in Beta-Zellen der Bauchspeicheldrüse zur Behandlung von Diabetikern zu verwandeln und entsprechend zu züchten. Ähnliches versuchte man in der Züchtung von Herzzellen als "Ersatz" für geschädigten Herzmuskel. Laut Colman war das erste Projekt "extrem kompliziert". Auch die potenzielle Herztherapie erwies sich als mit den derzeit zur Verfügung stehenden Methoden als undurchführbar. Erstens ist offenbar die Kultivierung von embryonalen Stammzellen und deren Ausdifferenzierung zu spezialisierten Zellen sehr diffizil. Zweitens kann die "Reinheit" der gewonnen Zellen nur mit sehr teuren Verfahren sichergestellt werden.
Doch wenn nicht zumindest mittelfristig Erfolgsaussichten auf ein Geschäft bestehen, ziehen sich die privaten Geldgeber in der Stammzellforschung wieder zurück. US-Experte Iriving Weissman, der an der Stanford University in Kalifornien derartige Projekte betreibt: "Forschung zu den embryonalen Stammzellen ist zum größten Teil noch eine rein wissenschaftliche Angelegenheit." Von verwertbaren Ergebnissen ist aber noch weit und breit keine Spur.
Colman jedenfalls bleibt in Singapur: Er wurde zum Chef des sogenannten Singapur Stammzell-Konsortiums gemacht. Es wird von der staatlichen Agentur für Forschung und Technologie finanziert. In den USA allerdings will ein Unternehmen (Geron Corporation/Kalifornien) kommendes Jahr zumindest mit der Erprobung einer Stammzelltherapie nach Rückenmarkverletzungen beginnen. Lanza hingegen möchte kommendes Jahr damit die fortschreitende Netzhautdegeneration in einer Testphase zu behandeln beginnen. (APA)
In Singapur stellt privates Unternehmen seine Tätigkeit ein - "Dolly"-Erfinder Alan Colman bekommt neuen Job
Singapur - Die Hoffnungen auf einen schnellen Geschäftserfolg haben sich in Luft aufgelöst, die vor sieben Jahren mit großem Tamtam gegründete private Gesellschaft ES Cell International (ESI) wirft das Handtuch. In der noch vor kurzer Zeit als sichere Boombranche bezeichneten Forschungssparte lautet die Devise nun offenbar neuerdings wieder: Zurück zur Universität. Einer der prominentesten Mitarbeiter von ESI war Klonschaf-"Dolly"-Co-Erfinder Alan Colman.
Bei ESI hätten die Investoren ihr Interesse verloren, weil "die Wahrscheinlichkeit einer kurzfristigen Marktreife für Produkte zur klinischen Anwendung verschwindend gering war", wurde Colman - somit Ex-Geschäftsführer der Gesellschaft von Venture-Kapitalisten - vor kurzem in der US-Wissenschaftszeitschrift "Science" zitiert.
War vor zwei, drei Jahren noch die Rede davon, dass man über embryonale Stammzellen bald "Reparaturmaterial" zur Behandlung von neurologischen Erkrankungen, von Herzleiden etc. schaffen könnte, so sind diese Ziele mittlerweile in weite Ferne gerückt. Die Wahrscheinlichkeit, dass man mit einer solchen oder ähnlichen Zelltherapie wirklich medizinisch messbare Erfolge verbuchen kann, ist derzeit noch minimal.
Auch der in Fachkreisen weltbekannte Stammzellforscher Robert Lanza von Advanced Cell Technologty in Worcester (US-Bundesstaat Massachusetts) sieht das so: "Dieses ganze Forschungsfeld benötigt dringend ein oder zwei Erfolge."
"Extrem kompliziert"
Gerade die stehen aber aus. ESI hatte versucht, embryonale Stammzellen in Beta-Zellen der Bauchspeicheldrüse zur Behandlung von Diabetikern zu verwandeln und entsprechend zu züchten. Ähnliches versuchte man in der Züchtung von Herzzellen als "Ersatz" für geschädigten Herzmuskel. Laut Colman war das erste Projekt "extrem kompliziert". Auch die potenzielle Herztherapie erwies sich als mit den derzeit zur Verfügung stehenden Methoden als undurchführbar. Erstens ist offenbar die Kultivierung von embryonalen Stammzellen und deren Ausdifferenzierung zu spezialisierten Zellen sehr diffizil. Zweitens kann die "Reinheit" der gewonnen Zellen nur mit sehr teuren Verfahren sichergestellt werden.
Doch wenn nicht zumindest mittelfristig Erfolgsaussichten auf ein Geschäft bestehen, ziehen sich die privaten Geldgeber in der Stammzellforschung wieder zurück. US-Experte Iriving Weissman, der an der Stanford University in Kalifornien derartige Projekte betreibt: "Forschung zu den embryonalen Stammzellen ist zum größten Teil noch eine rein wissenschaftliche Angelegenheit." Von verwertbaren Ergebnissen ist aber noch weit und breit keine Spur.
Colman jedenfalls bleibt in Singapur: Er wurde zum Chef des sogenannten Singapur Stammzell-Konsortiums gemacht. Es wird von der staatlichen Agentur für Forschung und Technologie finanziert. In den USA allerdings will ein Unternehmen (Geron Corporation/Kalifornien) kommendes Jahr zumindest mit der Erprobung einer Stammzelltherapie nach Rückenmarkverletzungen beginnen. Lanza hingegen möchte kommendes Jahr damit die fortschreitende Netzhautdegeneration in einer Testphase zu behandeln beginnen. (APA)
kommt nun biotech?
alles andere ist ausgelutscht!
alles andere ist ausgelutscht!
Antwort auf Beitrag Nr.: 31.104.883 von meislo am 09.08.07 22:10:27wer von euch glaubt eigentlich noch, dass ein geron-investment ein investment ist, das irgendwann einmal nennenswerte returns abwirft?
ich bin aktuell wieder schön im minus... mein glaube schwindet von tag zu tag. wenn ich mir den chart ansehe, dann schwindet meine zuversicht noch schneller. der weg nach unten richtung 1 usd bzw. all-time-low ist mit dem tag, an dem der kurs bei 5,70 usd war, wieder 'frei'.
schöne sch.....
ich bin aktuell wieder schön im minus... mein glaube schwindet von tag zu tag. wenn ich mir den chart ansehe, dann schwindet meine zuversicht noch schneller. der weg nach unten richtung 1 usd bzw. all-time-low ist mit dem tag, an dem der kurs bei 5,70 usd war, wieder 'frei'.
schöne sch.....
wie wahr, aus dem yahoo board:
Even fast track would not be enough to break the stock manipulation now. Okarma and crowd have let it go too long. The only thing I can think of now that will break the $10 barrier for more than a week or two is solid Phase 3 data an FDA approval. That has to be at least another two years away.
Geron has allowed its reputation with investors be obliterated by manipulative trading and not fought back in the slightest. They've floated two secondaries on price spikes engineered by the investment banking houses on run of the mill news. The fact that this can and has been done demonstrates how potent Geron's story, IP and product status are. But nothing has been done to maintain this investment pressure by management. Rather they have taken the money and left investors twisting in the wind. It's a rather despicable approach IMO. And it diminishes the potential for the company and targets it as a roadblock for the most efficient development of its vast IP, which in turn invites potential bad news. When Dr. Okarma or David Greenwood actually do something that shows they have the ability to develop Geron to its highest and best potential rather than just riding the coattails of its fabulous promise, then maybe I'll give them credit for having paved the way. Otherwise they are looking a lot like Dr. West's carpetbaggers these days.
Read this post carefully. I'm not saying they won't get the results they need to succeed. I'm saying they are leaving the company open and vulnerable and have not come close to pushing its true potential.
Even fast track would not be enough to break the stock manipulation now. Okarma and crowd have let it go too long. The only thing I can think of now that will break the $10 barrier for more than a week or two is solid Phase 3 data an FDA approval. That has to be at least another two years away.
Geron has allowed its reputation with investors be obliterated by manipulative trading and not fought back in the slightest. They've floated two secondaries on price spikes engineered by the investment banking houses on run of the mill news. The fact that this can and has been done demonstrates how potent Geron's story, IP and product status are. But nothing has been done to maintain this investment pressure by management. Rather they have taken the money and left investors twisting in the wind. It's a rather despicable approach IMO. And it diminishes the potential for the company and targets it as a roadblock for the most efficient development of its vast IP, which in turn invites potential bad news. When Dr. Okarma or David Greenwood actually do something that shows they have the ability to develop Geron to its highest and best potential rather than just riding the coattails of its fabulous promise, then maybe I'll give them credit for having paved the way. Otherwise they are looking a lot like Dr. West's carpetbaggers these days.
Read this post carefully. I'm not saying they won't get the results they need to succeed. I'm saying they are leaving the company open and vulnerable and have not come close to pushing its true potential.
short interest auf neuem rekordhoch: 10,165 mio. aktien waren per 15. august leerverkauft (ca. 1/7 aller ausstehenden aktien).
das potenzial für einen short squeeze ist da, es fehlt nur noch der auslöser.
auf den warten wir nun schon seit jahren...
lg - luckycat
das potenzial für einen short squeeze ist da, es fehlt nur noch der auslöser.
auf den warten wir nun schon seit jahren...
lg - luckycat
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10http://www.br-online.de/wissen-bildung/artikel/0709/18-stamm…
das protokoll von okarmas letztem auftritt:
UBS Global Life Sciences Conference
Tuesday, September 25, 2007
COORDINATOR: The next presenter is Thomas Okarma, President and CEO of Geron Corporation, and just a reminder that there is a breakout session after the presentation in the Carnegie Room.
DR. OKARMA: Thank you and good morning. Thanks for coming to our presentation this morning. I'll be making forward looking statements today, and of course we refer you to our various SEC filings for our risk factors.
Well, those of you that know the company are familiar with this first slide. We are the world leader in embryonic stem cell and telomerase technologies, with two broad spectrum cancer products currently in the clinic and the world's first embryonic stem cell product scheduled for clinical introduction early next year.
Our intellectual property position is of course quite dominant. We have a strong balance sheet. We ended the second quarter this year with $217 million in cash without debt and have a very experienced management team which I'll turn to next.
So the original core group has been at Geron now for 10 years. During the last year we added some significant experience in clinical oncology led by Alan Colowick and Fabio Benedetti. And in the aggregate, our entire oncology team at Geron now has in their experience portfolio 27 successful cancer INDs and 17–or 16 successful cancer NDA or BLA applications. So we have the horsepower now to develop our oncology portfolio.
So today I'm going to focus on that cancer portfolio: our two programs in the clinic – 163L our telomerase inhibitor drug and VAC1, our telomerase vaccine, and I'll also focus on our most advanced embryonic stem cell product for acute spinal cord injury.
Now the take home message for today's status of 163L which is a homegrown, proprietary oligonucleotide that's lipidated and made with Geron-owned chemistry, is that we're now recruiting for four trials in 15 centers in the United States, the multiple myeloma program to begin imminently. This is a drug that targets telomerase, an extremely broad and important cancer target, and therefore has the opportunity to be useful in most of the major cancer types. It's quite potent and specific. Thus far it's safety profile is quite good, with excellent PK and biodistribution properties, even though it is in fact a short chain oligonucleotide. And I'll emphasize a very novel mechanism of action in terms of myeloma stem cells a little bit later.
Now the breadth of the activity of the drug is of course underpinned by a series – now all of which have now been published – of animal experiments demonstrating the activity of the drug as both a single agent - in myeloma, in non small cell lung , ovarian and other tumors - as well as in combination with standard of care in a similarly growing list of tumor types. Now these observations plus a few others that I'll mention cancer type by cancer type underpin the pretty aggressive program for the clinical development of this drug. Now in July we had an analyst day here in New York and we spent 3 hours going through this program, so I'll only at this moment give you the highlights. So, we are currently enrolling in two Phase I trials, one in CLL and one in solid tumors, and the outcome of those studies by end of this year will determine our single agent Phase II dose. We have recently introduced the first combination study of 163L with standard of care carboplatinum-Taxol in non small cell lung cancer. Once we have optimized the dose and dosing interval in that combination study, that triggers two events: a randomized Phase II non small cell lung cancer of–in combination, as well as a randomized Phase II in ovarian cancer with the same combination, and both of those randomized Phase II are scheduled to occur at the end of ‘08, assuming success in this trial. The most important part of this schema, though, is the potential registration pathway for the drug in multiple myeloma.
So imminently we will initiate a Phase I/II single agent trial in myeloma and if that is successful, that should lead to a pivotal trial in ‘08 of a single agent 163L in myeloma. It will also trigger a combination study that will occur in next year in the same disease indication. So, a very aggressive program, the most rapid pathway to registration we think today will be in multiple myeloma for reasons that I'll explain in a moment.
Let's look at a little more detail in those four programs. So the two Phase I trials – CLL and solid tumors – have a little bit, are different from one another in terms of the infusion duration, 6 hours in CLL and 2 hours in solid tumors. We are learning from the kinetic analysis of these data that the two hour infusion is a much better way to deliver this drug, and we will ultimately convert all of our trials to that 2 hour infusion. We're now enrolling in the 5th dose cohort, which is roughly 5 mgs per kilo, in both of these studies.
So in the CLL study, that's a standard three plus three per cohort, Phase I design. There are now five centers recruiting for this study and we expect to finish this program early next year, and as I mentioned, are currently enrolling in the 5th cohort. We presented in the summer some interim results from the first four cohorts. We had one subject with stable disease and another subject that had tumor lysis syndrome; we weren't able to document significant telomerase inhibition, so the etiology of these possible responses is unclear, but most importantly was the PK data that is dose proportional and that led us to conclude we could continue to dose escalate, which, as I mentioned, is now happening in the Cohort Number 5.
Solid tumor study was added onto this, to really, to look at the toxicity profile in a solid tumor as opposed to a hematologic malignancy like CLL. We have now two centers recruiting patients here and we're also in Cohort 5, roughly 5 mgs per kilo, once a week by intravenous infusion and when we get to the maximal tolerated dose, we'll elucidate PK-PD relationships in an extended cohort.
The new study we've begun recently is in non small cell lung cancer. Why? First, there is well established, published evidence that the higher the telomerase activity in the tumor cell in non small cell lung, the worse is your overall survival or event free survival -- there are multiple studies that show this. And there are plenty of tumors that have this same sort of rationale. So the more telomerase you have in your tumor, the worse is your prognosis.
Secondly, there's pretty profound animal model evidence of 163L in an animal model of non small cell lung as a single agent. The fluorescence here indicates tumor burden, and there is a dose response effect in this animal model, actually resulting in some animals that have no evidence of disease after a single course of this drug.
So the combination study is a Phase I trial of 163L in combination with standard dose, standard of care of non small cell lung carboplatinum and paclitaxel. We give the standard of care every 3 weeks: three weeks on, one week off and currently a 2 hour infusion every week of 163L. We're starting at a dose of the–of our drug equivalent to that of the 4th cohort in the previously described solid tumor trial. These are patients that are sort of early in their treatment, and we're able to do that because of the combination here with standard of care and the endpoints are of course, most importantly, establishing dose and dosing interval in a combination with standard of care.
Now the important program for us in terms of registration is multiple myeloma. Same sort of rationale. Again, your outcome is inversely proportional to the amount of telomerase in your tumor: the more tumor the worse is your overall survival or likelihood of relapse. We've also demonstrated in an animal model additivity between 163L and Velcade, shown here on the bottom line, in a long term study of an animal model of disseminated myeloma. Perhaps most importantly is the evidence that this drug, and this drug alone, impacts not only the mature myeloma cell, but also the myeloma stem cell. And on the left are data from myeloma lines; on the right are data from myeloma human patients that show a profound activity at low doses, very early in incubation, of our drug on the myeloma stem cell. And this will be actually presented at a public oncology meeting later this year. So, for those reasons, we plan a important study of single agent 163L in refractile and advanced myeloma patients who've had more than two prior therapies. And again it's a standard design, three plus three. We will also begin at the 4th cohort dose of our two Phase Is, so we don't have to repeat all of the low dose work and there are four centers that will be recruiting to this study, all of which are major referral centers for this disease. And as I mentioned, this is about to initiate, imminently.
So that's our oncology program in the telomerase inhibitor drug arena.
I want to segue now to our vaccine, which is also based upon telomerase and therefore in theory has the same upside potential in terms of broad utility in most major cancers, all of which express telomerase – in this case, on the surface of the tumor cell. So, we have completed as you know, a Phase I trial in prostate cancer which led to our agreement with Merck which I will talk about in a moment, and unlike all other dendritic cell cancer immunotherapies, our immune responses are robust and consistent across groups, and I'll show you that data, and we have now initiated a second Phase I/II in AML with disease endpoints. You've seen this data before. It's been published in JI. It's the results of our first trial with the vaccine in prostate cancer and it illustrates a few fundamental points. After 6 prime injections in the skin once a week we generate in all of the subjects very high titred CD8 and CD4 telomerase restricted T cells that kill tumors, and this occurs in all of the subjects. This is about 1 to 2 percent of the total T cell pool in these subjects which is therefore an extraordinarily high degree of anti tumor immunity generated in the context of hormone refractory, metastatic prostate cancer. In addition to demonstrating that these cells cleared tumor cells circulating in the bloodstream, we had a highly significant prolongation of PSA doubling time, a surrogate marker for disease progression, but certainly not an approvable endpoint. What we did subsequent to those studies was optimize a prime and boost strategy using the same cell administered over a longer period of time and we demonstrated an anamnestic response in the boost. In other words, in–even after 9 months of no therapy, the first injection of the boost immediately gave a peak of CD8 and CD4 cells after the first boost injection, confirming what we had published here, that in the prime we are generating memory, central memory T cells. So this is real immunology.
We've moving now into a Phase I/II trial in acute myelogenous leukemia, and these are subjects at intermediate or high risk for relapse. And the protocol is following standard consolidation chemotherapy we prepare the cells and give them 6 weekly intradermal injections for the prime, just as we had done in prostate cancer. There's then a month's rest and then we give 6 or more boost injections every other week. And depending upon the efficiency of the harvest, we will have enough boost injections probably for more than 6. Therefore we are able to we think sustain high level anti telomerase T cell immunity. There'll be five sites recrutiting to this trial and in addition to the obvious safety and immunological endpoints, we're really looking hard now on residual disease burden and clinical endpoints like remission, duration of remission and event free survival. So one of our hopes is that some of these subjects, particularly in the elderly high risk group, will have positive PCR signals in their bone marrow of residual AML cells post consolidation chemotherapy and those subjects we'll look at very carefully to see if vaccination takes them to PCR negativity, which is of course an approvable endpoint.
Now the prostate cancer data and the boost data that I talked to you about led us to an agreement with our vaccine collaborator, Merck, and there's been a lot of news and progress that I want to announce today in this relationship. So, first, under our license to Merck for the telomerase target for their platform, they have now decided to file their IND under our license in the fourth quarter of this year, not in ‘08 as we had said in the July, August–July analyst meeting. So that's an important milestone. It's a milestone payment to Geron and it indicates seriousness of purpose and good progress on our partner's part.
Now there's also a combination–excuse me, a collaboration arrangement in this existing agreement which has made substantial progress. So under Merck's guidance we have been combining our platform with theirs in an animal model, and we have shown pretty dramatic synergy between dendritic cells and their platform which is adenovirus and plasmid. So both companies are now motivated to look seriously at extending their option to our VAC1 program. That option formally expired in July of this year; we have granted them a 6 month extension til end of year while we negotiate a renewal of that option.
Also important in that context is progress we've made at Geron on the second generation vaccine, which is dendritic cells that are made from human embryonic stem cells. We've now shown that these ES DCs have all the bells and whistles of the dendritic cells we harvest from peripheral blood with the obvious advantage of multi dose production lots, greatly reduced cost of goods and absence of variability of the DC's activity from patient to patient. So we are hopeful that this renegotiation will include an option to the second generation, so-called VAC2 based on human embryonic stem cells.
I won't say much about TAT2, our telomerase activator drug, other than to remind you that we changed the relationship of the joint venture - it's now 75/25 in favor of Geron, so we are in control of this relationship in Hong Kong and we're in the final stages of our preclinical ADME tox with this compound, and we'll have more to say about that a little bit later in the year.
So in the remaining time let me talk mostly about the spinal cord injury program and a little bit about heart failure and diabetes and I'll close with our milestones for the coming two years.
UBS Global Life Sciences Conference
Tuesday, September 25, 2007
COORDINATOR: The next presenter is Thomas Okarma, President and CEO of Geron Corporation, and just a reminder that there is a breakout session after the presentation in the Carnegie Room.
DR. OKARMA: Thank you and good morning. Thanks for coming to our presentation this morning. I'll be making forward looking statements today, and of course we refer you to our various SEC filings for our risk factors.
Well, those of you that know the company are familiar with this first slide. We are the world leader in embryonic stem cell and telomerase technologies, with two broad spectrum cancer products currently in the clinic and the world's first embryonic stem cell product scheduled for clinical introduction early next year.
Our intellectual property position is of course quite dominant. We have a strong balance sheet. We ended the second quarter this year with $217 million in cash without debt and have a very experienced management team which I'll turn to next.
So the original core group has been at Geron now for 10 years. During the last year we added some significant experience in clinical oncology led by Alan Colowick and Fabio Benedetti. And in the aggregate, our entire oncology team at Geron now has in their experience portfolio 27 successful cancer INDs and 17–or 16 successful cancer NDA or BLA applications. So we have the horsepower now to develop our oncology portfolio.
So today I'm going to focus on that cancer portfolio: our two programs in the clinic – 163L our telomerase inhibitor drug and VAC1, our telomerase vaccine, and I'll also focus on our most advanced embryonic stem cell product for acute spinal cord injury.
Now the take home message for today's status of 163L which is a homegrown, proprietary oligonucleotide that's lipidated and made with Geron-owned chemistry, is that we're now recruiting for four trials in 15 centers in the United States, the multiple myeloma program to begin imminently. This is a drug that targets telomerase, an extremely broad and important cancer target, and therefore has the opportunity to be useful in most of the major cancer types. It's quite potent and specific. Thus far it's safety profile is quite good, with excellent PK and biodistribution properties, even though it is in fact a short chain oligonucleotide. And I'll emphasize a very novel mechanism of action in terms of myeloma stem cells a little bit later.
Now the breadth of the activity of the drug is of course underpinned by a series – now all of which have now been published – of animal experiments demonstrating the activity of the drug as both a single agent - in myeloma, in non small cell lung , ovarian and other tumors - as well as in combination with standard of care in a similarly growing list of tumor types. Now these observations plus a few others that I'll mention cancer type by cancer type underpin the pretty aggressive program for the clinical development of this drug. Now in July we had an analyst day here in New York and we spent 3 hours going through this program, so I'll only at this moment give you the highlights. So, we are currently enrolling in two Phase I trials, one in CLL and one in solid tumors, and the outcome of those studies by end of this year will determine our single agent Phase II dose. We have recently introduced the first combination study of 163L with standard of care carboplatinum-Taxol in non small cell lung cancer. Once we have optimized the dose and dosing interval in that combination study, that triggers two events: a randomized Phase II non small cell lung cancer of–in combination, as well as a randomized Phase II in ovarian cancer with the same combination, and both of those randomized Phase II are scheduled to occur at the end of ‘08, assuming success in this trial. The most important part of this schema, though, is the potential registration pathway for the drug in multiple myeloma.
So imminently we will initiate a Phase I/II single agent trial in myeloma and if that is successful, that should lead to a pivotal trial in ‘08 of a single agent 163L in myeloma. It will also trigger a combination study that will occur in next year in the same disease indication. So, a very aggressive program, the most rapid pathway to registration we think today will be in multiple myeloma for reasons that I'll explain in a moment.
Let's look at a little more detail in those four programs. So the two Phase I trials – CLL and solid tumors – have a little bit, are different from one another in terms of the infusion duration, 6 hours in CLL and 2 hours in solid tumors. We are learning from the kinetic analysis of these data that the two hour infusion is a much better way to deliver this drug, and we will ultimately convert all of our trials to that 2 hour infusion. We're now enrolling in the 5th dose cohort, which is roughly 5 mgs per kilo, in both of these studies.
So in the CLL study, that's a standard three plus three per cohort, Phase I design. There are now five centers recruiting for this study and we expect to finish this program early next year, and as I mentioned, are currently enrolling in the 5th cohort. We presented in the summer some interim results from the first four cohorts. We had one subject with stable disease and another subject that had tumor lysis syndrome; we weren't able to document significant telomerase inhibition, so the etiology of these possible responses is unclear, but most importantly was the PK data that is dose proportional and that led us to conclude we could continue to dose escalate, which, as I mentioned, is now happening in the Cohort Number 5.
Solid tumor study was added onto this, to really, to look at the toxicity profile in a solid tumor as opposed to a hematologic malignancy like CLL. We have now two centers recruiting patients here and we're also in Cohort 5, roughly 5 mgs per kilo, once a week by intravenous infusion and when we get to the maximal tolerated dose, we'll elucidate PK-PD relationships in an extended cohort.
The new study we've begun recently is in non small cell lung cancer. Why? First, there is well established, published evidence that the higher the telomerase activity in the tumor cell in non small cell lung, the worse is your overall survival or event free survival -- there are multiple studies that show this. And there are plenty of tumors that have this same sort of rationale. So the more telomerase you have in your tumor, the worse is your prognosis.
Secondly, there's pretty profound animal model evidence of 163L in an animal model of non small cell lung as a single agent. The fluorescence here indicates tumor burden, and there is a dose response effect in this animal model, actually resulting in some animals that have no evidence of disease after a single course of this drug.
So the combination study is a Phase I trial of 163L in combination with standard dose, standard of care of non small cell lung carboplatinum and paclitaxel. We give the standard of care every 3 weeks: three weeks on, one week off and currently a 2 hour infusion every week of 163L. We're starting at a dose of the–of our drug equivalent to that of the 4th cohort in the previously described solid tumor trial. These are patients that are sort of early in their treatment, and we're able to do that because of the combination here with standard of care and the endpoints are of course, most importantly, establishing dose and dosing interval in a combination with standard of care.
Now the important program for us in terms of registration is multiple myeloma. Same sort of rationale. Again, your outcome is inversely proportional to the amount of telomerase in your tumor: the more tumor the worse is your overall survival or likelihood of relapse. We've also demonstrated in an animal model additivity between 163L and Velcade, shown here on the bottom line, in a long term study of an animal model of disseminated myeloma. Perhaps most importantly is the evidence that this drug, and this drug alone, impacts not only the mature myeloma cell, but also the myeloma stem cell. And on the left are data from myeloma lines; on the right are data from myeloma human patients that show a profound activity at low doses, very early in incubation, of our drug on the myeloma stem cell. And this will be actually presented at a public oncology meeting later this year. So, for those reasons, we plan a important study of single agent 163L in refractile and advanced myeloma patients who've had more than two prior therapies. And again it's a standard design, three plus three. We will also begin at the 4th cohort dose of our two Phase Is, so we don't have to repeat all of the low dose work and there are four centers that will be recruiting to this study, all of which are major referral centers for this disease. And as I mentioned, this is about to initiate, imminently.
So that's our oncology program in the telomerase inhibitor drug arena.
I want to segue now to our vaccine, which is also based upon telomerase and therefore in theory has the same upside potential in terms of broad utility in most major cancers, all of which express telomerase – in this case, on the surface of the tumor cell. So, we have completed as you know, a Phase I trial in prostate cancer which led to our agreement with Merck which I will talk about in a moment, and unlike all other dendritic cell cancer immunotherapies, our immune responses are robust and consistent across groups, and I'll show you that data, and we have now initiated a second Phase I/II in AML with disease endpoints. You've seen this data before. It's been published in JI. It's the results of our first trial with the vaccine in prostate cancer and it illustrates a few fundamental points. After 6 prime injections in the skin once a week we generate in all of the subjects very high titred CD8 and CD4 telomerase restricted T cells that kill tumors, and this occurs in all of the subjects. This is about 1 to 2 percent of the total T cell pool in these subjects which is therefore an extraordinarily high degree of anti tumor immunity generated in the context of hormone refractory, metastatic prostate cancer. In addition to demonstrating that these cells cleared tumor cells circulating in the bloodstream, we had a highly significant prolongation of PSA doubling time, a surrogate marker for disease progression, but certainly not an approvable endpoint. What we did subsequent to those studies was optimize a prime and boost strategy using the same cell administered over a longer period of time and we demonstrated an anamnestic response in the boost. In other words, in–even after 9 months of no therapy, the first injection of the boost immediately gave a peak of CD8 and CD4 cells after the first boost injection, confirming what we had published here, that in the prime we are generating memory, central memory T cells. So this is real immunology.
We've moving now into a Phase I/II trial in acute myelogenous leukemia, and these are subjects at intermediate or high risk for relapse. And the protocol is following standard consolidation chemotherapy we prepare the cells and give them 6 weekly intradermal injections for the prime, just as we had done in prostate cancer. There's then a month's rest and then we give 6 or more boost injections every other week. And depending upon the efficiency of the harvest, we will have enough boost injections probably for more than 6. Therefore we are able to we think sustain high level anti telomerase T cell immunity. There'll be five sites recrutiting to this trial and in addition to the obvious safety and immunological endpoints, we're really looking hard now on residual disease burden and clinical endpoints like remission, duration of remission and event free survival. So one of our hopes is that some of these subjects, particularly in the elderly high risk group, will have positive PCR signals in their bone marrow of residual AML cells post consolidation chemotherapy and those subjects we'll look at very carefully to see if vaccination takes them to PCR negativity, which is of course an approvable endpoint.
Now the prostate cancer data and the boost data that I talked to you about led us to an agreement with our vaccine collaborator, Merck, and there's been a lot of news and progress that I want to announce today in this relationship. So, first, under our license to Merck for the telomerase target for their platform, they have now decided to file their IND under our license in the fourth quarter of this year, not in ‘08 as we had said in the July, August–July analyst meeting. So that's an important milestone. It's a milestone payment to Geron and it indicates seriousness of purpose and good progress on our partner's part.
Now there's also a combination–excuse me, a collaboration arrangement in this existing agreement which has made substantial progress. So under Merck's guidance we have been combining our platform with theirs in an animal model, and we have shown pretty dramatic synergy between dendritic cells and their platform which is adenovirus and plasmid. So both companies are now motivated to look seriously at extending their option to our VAC1 program. That option formally expired in July of this year; we have granted them a 6 month extension til end of year while we negotiate a renewal of that option.
Also important in that context is progress we've made at Geron on the second generation vaccine, which is dendritic cells that are made from human embryonic stem cells. We've now shown that these ES DCs have all the bells and whistles of the dendritic cells we harvest from peripheral blood with the obvious advantage of multi dose production lots, greatly reduced cost of goods and absence of variability of the DC's activity from patient to patient. So we are hopeful that this renegotiation will include an option to the second generation, so-called VAC2 based on human embryonic stem cells.
I won't say much about TAT2, our telomerase activator drug, other than to remind you that we changed the relationship of the joint venture - it's now 75/25 in favor of Geron, so we are in control of this relationship in Hong Kong and we're in the final stages of our preclinical ADME tox with this compound, and we'll have more to say about that a little bit later in the year.
So in the remaining time let me talk mostly about the spinal cord injury program and a little bit about heart failure and diabetes and I'll close with our milestones for the coming two years.
starker rückgang der short-positionen: von 10,16 mio auf 8,41 mio., also ca. 15%.
das erklärt die kurserholung, die wir nach dem sell-off bis 5,70 usd gesehen haben. geron hat seit dem tiefpunkt wieder 30% gut gemacht.
ich hab damals trotz extremen muffensausens zugekauft und bin recht glücklich damit.
wie gehts nun weiter?
geron betritt im augenblick die phase der therapeutischen dosen bei den grn163l-test. testergebnisse werden gegen jahresende erwartet (bei CLL sowie solid tumor).
dass grn163l wirkt, steht fest; offen ist aber, wie bzw. wie schnell und stark es wirkt.
let`s see
das erklärt die kurserholung, die wir nach dem sell-off bis 5,70 usd gesehen haben. geron hat seit dem tiefpunkt wieder 30% gut gemacht.
ich hab damals trotz extremen muffensausens zugekauft und bin recht glücklich damit.
wie gehts nun weiter?
geron betritt im augenblick die phase der therapeutischen dosen bei den grn163l-test. testergebnisse werden gegen jahresende erwartet (bei CLL sowie solid tumor).
dass grn163l wirkt, steht fest; offen ist aber, wie bzw. wie schnell und stark es wirkt.
let`s see
Geron's drug"163L knocks down the cancer stem cell by 50% in just 3 days " Geron's Dr. Okarma said. "The important news is that our drug shuts down tumor stem cells."
"GRN163L may have the potential to cure (multiple myeloma) by targeting the cancer stem cells," Rodman & Renshaw analyst Ren Benjamin explained earlier this month.
Geron's President Dr. Okarma also said,
"The new information has to do with the--its activity against cancer stem cells, which is sort of the new thing in cancer biology. So cancer stem cells are quiescent, resistant to chemotherapy and are responsible for clinical relapse. The important news is that our drug shuts down tumor stem cells."
"WBB analyst Brozak says Geron might one day cure cancer and paralysis."
Geron "strong buy," target price raised
Monday, August 27, 2007 9:19:12 AM ET
WBB Securities
NEW YORK, August 7 (newratings.com) - Analysts at WBB Securities maintain their "strong buy" rating on Geron Corporation Inc (GERN.NAS). The 12-month target price has been raised to $16.50.
In a research note published this morning, the analysts mention that the company and its scientific collaborators have announced success in a lab test, which is likely to result in the development of a hESC product for repairing human hearts damaged by myocardial infarction. Geron is now going to test the mixture of proteins and stem cells in larger animals and the results are expected by mid-2008, the analysts say. Geron�s share price does not reflect an acquisition premium, although the company could become a target due to its unique position in both hESC and Telomerase, WBB Securities adds.
"GRN163L may have the potential to cure (multiple myeloma) by targeting the cancer stem cells," Rodman & Renshaw analyst Ren Benjamin explained earlier this month.
Geron's President Dr. Okarma also said,
"The new information has to do with the--its activity against cancer stem cells, which is sort of the new thing in cancer biology. So cancer stem cells are quiescent, resistant to chemotherapy and are responsible for clinical relapse. The important news is that our drug shuts down tumor stem cells."
"WBB analyst Brozak says Geron might one day cure cancer and paralysis."
Geron "strong buy," target price raised
Monday, August 27, 2007 9:19:12 AM ET
WBB Securities
NEW YORK, August 7 (newratings.com) - Analysts at WBB Securities maintain their "strong buy" rating on Geron Corporation Inc (GERN.NAS). The 12-month target price has been raised to $16.50.
In a research note published this morning, the analysts mention that the company and its scientific collaborators have announced success in a lab test, which is likely to result in the development of a hESC product for repairing human hearts damaged by myocardial infarction. Geron is now going to test the mixture of proteins and stem cells in larger animals and the results are expected by mid-2008, the analysts say. Geron�s share price does not reflect an acquisition premium, although the company could become a target due to its unique position in both hESC and Telomerase, WBB Securities adds.
teil 2 des vortrags auf der ubs-konferenz:
Now it's important to understand that all of these embryonic stem cell based therapies are scalable and we have a very standard manufacturing schema based upon master and working cell banks which have been in use in the biotech industry for 20 years for, for example, monoclonal antibodies, that enables us to produce differentiated, functional therapeutic cells in a biological commodity fashion. So to illustrate that, our current master cell bank, if we were to convert every cell in that existing master cell bank to glial cells, the first cell type, for acute spinal cord injury, we would have enough doses to treat the entire US acute spinal cord injury market for 22 years. So this is like manufacturing a drug with the appropriate economics, low cost of goods, that are enjoyed in any product based business model in biotech and pharma. So the first therapy that we expect to begin human clinical trials in the beginning of next year are oligodendral glial progenitors for acute spinal cord injury. We've published now the proof of concept and mechanism of action in the Journal of Neurosciences in a spinal cord injured rat model these cells injected within two weeks of the injury remyelinate the injured nerves and secrete neurotrophins that enable a reconnection of the damaged axons. It's profound and it's durable. In our IND enabling studies -- which are nearly complete now -- we've followed some of these animals for as long as 9 months and the cells are still there and quite viable. So the scope and content of our IND has been agreed upon and is now finalized. Most of the in-life studies to enable this IND are done. We're now just waiting for the last few reports to come in. So we're in the process now of writing this IND, and so we're on track to submit by end of year as previously noted. Now we'll be only announcing the milestone here connected with clinical trial initiation; I need to tell you that this is an enormous application. It's both an IND and an IDE because we had to invent a delivery device that's computer controlled to allow precise placement of the needle to inject these cells in the OR into the spinal cord as the patients get standard stabilization therapy after their injury. This will be an IND that has over two thousand animal studies – there are animals in various studies – as well as over twenty thousand pages of information. So it'll be a major review task for the agency. So you've seen this slide before; it demonstrates that the control group are animals that are permanently paralytic, they cannot place their hind paws, they drag their tail on the bottom of the cage and many of them are incontinent; in contrast, animals that get the cells have almost normal weight bearing and paw placement and carry their tail above the cage floor.
So the clinical protocol is now virtually complete in collaboration with our clinical advisory panel, and it's really driven by a very conservative risk/benefit calculus. So the initial patients that will receive these cells are complete thoracic injuries. These are patients with no sensation or mobility below the thoracic lesion. Now these are rare today because of automobile airbags. The most common complete lesions are cervical. But the reason we're starting at the thoracic level is for safety. If there is a problem with these cells and you go from a, say a T4 to a T3 lesion, there's really no significant impact on the patient's longterm care. But if we started at the cervical region and went from a C3 to a C2, we could compromise respiratory drive. So we'll be starting with thoracic completes, then once safety's demonstrated, move to cervical completes, and then move lastly to incompletes, which is of course the full spectrum of acute spinal cord injured patients.
We've made a lot of progress on our second cell type, cardiomyocytes for heart failure and there is a landmark study that just was published in the September issue of Nature Biotechnology that I really refer you to. And this is the first time that anyone has demonstrated mature cardiomyocytes generated from any stem cell, in this case embryonic, that are surviving in an infarct zone. That was not an easy accomplishment to achieve and it required our development of a pro survival cocktail that enables these cells to survive longterm in the hostile environment of a myocardial scar. In addition to the improvement in structure and function that I'll show you in the next slide, a very striking finding documented in the paper is that the cells induce host angiogenesis. So we're not adding angiogenic cells of human origin, but the stimulus of these human cardiomyocytes turns the animals' response on to generate new blood vessels that infiltrate the tumor which in fact is part of the therapeutic response. So these are the data taken from the Nature Biotech paper. This shows the human cells surviving for at least four weeks in the body of the transmural left ventricular infarct. This is a major insult of both ischemia and reprofusion and the cells are injected 4 days after the infarction. And the significant results are a significant improvement in the ejection fraction in animals that receive cells, and no impact on animals that receive only the factors alone and highly significant improvements in contractile function and systolic thickening that you can easily visually see on the MRIs that all the animals receive. So this is a highly important validation of our second cell type. We are now in large animal studies, so we have scaled the production. These are now in sheep studies which will be taking place in two centers in the United States. And the purpose of the large animal study is to validate the notion that we are not creating arrhythmias in an animal whose heart rate is slow enough to be able to measure that. Obviously these animals have a heart rate of about 300 beats per minute so you can't be sure that we're not generating arrhythmias, and also, because these are human cells which can only beat at 180 beats per minute, the impact on function is minimized. So, every other animal heart beat is aided by the human cells in the ventricle. So we're very excited by these data.
And lastly the islet cells for diabetes. We really think we have the cell. It's taken us a long time to get there, but we now have cells that produce and secrete insulin in a glucose responsive fashion, as well as glucagon and somatostatin, the typical hormones of the pancreas. We have a scalable production method - as we do for all of our cell types - and we have early animal proof of concept in a diabetic animal. So this is actually the immunocytic chemistry to show that our ES derived islets make insulin - this is a precusor of insulin. Glucagon. Somatostatin. And that all of those hormone producing cells are in each of our produced islets in the merged image. This shows that the secretion of insulin is in fact glucose responsive, as it should be, and we have all the right secretory vessels in the cells. All of this has been published this year. We extend dramatically the survival of the diabetic animal, and can in fact pick up human insulin in the bloodstream of the animal that receives cells.
So to support this, we obviously have a very robust intellectual property platform. Geron is the fundamental adventurer and developer of both disruptive technologies - embryonic stem cells and the whole telomerase story in cancer and normal cells - so we have a broad portfolio of pioneering IP, as well as an expanding issue of impending portfolio on both sides of the house that cover specific product formulations that emanate from these disruptive technologies. And we are constantly operating and engaging in the world's patent literature to maintain our freedom to operate.
So the last slide in the last few seconds are our driving–value driving milestones. So, the two Phase I studies in 163L will come to a conclusion early next year and they will determine together the single agent dose for our Phase II programs. The non small cell lung program has initiated in combination and we expect to have results from that at the end of 2008. We are about to initiate our single agent Phase I/II in myeloma and we will later in next year initiate a combination Phase I/II that hopefully will lead to our pivotal study.
Under VAC1, we're–we have initiated the AML study and, not on this slide, is of course the Merck milestones of IND filing and by end of year hopefully the renewal of our–their option agreement.
Embryonic stem cells. Now the important milestone to focus on is the initiation of the spinal cord trial early next year and we do hope to have some interim safety data by end of year, again depending on enrollment kinetics and when this actually begins. We hope to have large animal proof of concept for cardiomyocytes from our large animal trials by end of the year, and that triggers the generation of our master cell bank and the IND filing which could occur in 2009. And final proof of concept for the islet cell in the middle of next year in terms of stably reducing hypoglycemia in diabetic animals.
So thanks very much. That's our program, maturing product portfolio in oncology, an emerging product portfolio in embryonic stem cells based upon Geron owned and developed disruptive technologies in telomerase and embryonic stem cells. Thank you very much.
Now it's important to understand that all of these embryonic stem cell based therapies are scalable and we have a very standard manufacturing schema based upon master and working cell banks which have been in use in the biotech industry for 20 years for, for example, monoclonal antibodies, that enables us to produce differentiated, functional therapeutic cells in a biological commodity fashion. So to illustrate that, our current master cell bank, if we were to convert every cell in that existing master cell bank to glial cells, the first cell type, for acute spinal cord injury, we would have enough doses to treat the entire US acute spinal cord injury market for 22 years. So this is like manufacturing a drug with the appropriate economics, low cost of goods, that are enjoyed in any product based business model in biotech and pharma. So the first therapy that we expect to begin human clinical trials in the beginning of next year are oligodendral glial progenitors for acute spinal cord injury. We've published now the proof of concept and mechanism of action in the Journal of Neurosciences in a spinal cord injured rat model these cells injected within two weeks of the injury remyelinate the injured nerves and secrete neurotrophins that enable a reconnection of the damaged axons. It's profound and it's durable. In our IND enabling studies -- which are nearly complete now -- we've followed some of these animals for as long as 9 months and the cells are still there and quite viable. So the scope and content of our IND has been agreed upon and is now finalized. Most of the in-life studies to enable this IND are done. We're now just waiting for the last few reports to come in. So we're in the process now of writing this IND, and so we're on track to submit by end of year as previously noted. Now we'll be only announcing the milestone here connected with clinical trial initiation; I need to tell you that this is an enormous application. It's both an IND and an IDE because we had to invent a delivery device that's computer controlled to allow precise placement of the needle to inject these cells in the OR into the spinal cord as the patients get standard stabilization therapy after their injury. This will be an IND that has over two thousand animal studies – there are animals in various studies – as well as over twenty thousand pages of information. So it'll be a major review task for the agency. So you've seen this slide before; it demonstrates that the control group are animals that are permanently paralytic, they cannot place their hind paws, they drag their tail on the bottom of the cage and many of them are incontinent; in contrast, animals that get the cells have almost normal weight bearing and paw placement and carry their tail above the cage floor.
So the clinical protocol is now virtually complete in collaboration with our clinical advisory panel, and it's really driven by a very conservative risk/benefit calculus. So the initial patients that will receive these cells are complete thoracic injuries. These are patients with no sensation or mobility below the thoracic lesion. Now these are rare today because of automobile airbags. The most common complete lesions are cervical. But the reason we're starting at the thoracic level is for safety. If there is a problem with these cells and you go from a, say a T4 to a T3 lesion, there's really no significant impact on the patient's longterm care. But if we started at the cervical region and went from a C3 to a C2, we could compromise respiratory drive. So we'll be starting with thoracic completes, then once safety's demonstrated, move to cervical completes, and then move lastly to incompletes, which is of course the full spectrum of acute spinal cord injured patients.
We've made a lot of progress on our second cell type, cardiomyocytes for heart failure and there is a landmark study that just was published in the September issue of Nature Biotechnology that I really refer you to. And this is the first time that anyone has demonstrated mature cardiomyocytes generated from any stem cell, in this case embryonic, that are surviving in an infarct zone. That was not an easy accomplishment to achieve and it required our development of a pro survival cocktail that enables these cells to survive longterm in the hostile environment of a myocardial scar. In addition to the improvement in structure and function that I'll show you in the next slide, a very striking finding documented in the paper is that the cells induce host angiogenesis. So we're not adding angiogenic cells of human origin, but the stimulus of these human cardiomyocytes turns the animals' response on to generate new blood vessels that infiltrate the tumor which in fact is part of the therapeutic response. So these are the data taken from the Nature Biotech paper. This shows the human cells surviving for at least four weeks in the body of the transmural left ventricular infarct. This is a major insult of both ischemia and reprofusion and the cells are injected 4 days after the infarction. And the significant results are a significant improvement in the ejection fraction in animals that receive cells, and no impact on animals that receive only the factors alone and highly significant improvements in contractile function and systolic thickening that you can easily visually see on the MRIs that all the animals receive. So this is a highly important validation of our second cell type. We are now in large animal studies, so we have scaled the production. These are now in sheep studies which will be taking place in two centers in the United States. And the purpose of the large animal study is to validate the notion that we are not creating arrhythmias in an animal whose heart rate is slow enough to be able to measure that. Obviously these animals have a heart rate of about 300 beats per minute so you can't be sure that we're not generating arrhythmias, and also, because these are human cells which can only beat at 180 beats per minute, the impact on function is minimized. So, every other animal heart beat is aided by the human cells in the ventricle. So we're very excited by these data.
And lastly the islet cells for diabetes. We really think we have the cell. It's taken us a long time to get there, but we now have cells that produce and secrete insulin in a glucose responsive fashion, as well as glucagon and somatostatin, the typical hormones of the pancreas. We have a scalable production method - as we do for all of our cell types - and we have early animal proof of concept in a diabetic animal. So this is actually the immunocytic chemistry to show that our ES derived islets make insulin - this is a precusor of insulin. Glucagon. Somatostatin. And that all of those hormone producing cells are in each of our produced islets in the merged image. This shows that the secretion of insulin is in fact glucose responsive, as it should be, and we have all the right secretory vessels in the cells. All of this has been published this year. We extend dramatically the survival of the diabetic animal, and can in fact pick up human insulin in the bloodstream of the animal that receives cells.
So to support this, we obviously have a very robust intellectual property platform. Geron is the fundamental adventurer and developer of both disruptive technologies - embryonic stem cells and the whole telomerase story in cancer and normal cells - so we have a broad portfolio of pioneering IP, as well as an expanding issue of impending portfolio on both sides of the house that cover specific product formulations that emanate from these disruptive technologies. And we are constantly operating and engaging in the world's patent literature to maintain our freedom to operate.
So the last slide in the last few seconds are our driving–value driving milestones. So, the two Phase I studies in 163L will come to a conclusion early next year and they will determine together the single agent dose for our Phase II programs. The non small cell lung program has initiated in combination and we expect to have results from that at the end of 2008. We are about to initiate our single agent Phase I/II in myeloma and we will later in next year initiate a combination Phase I/II that hopefully will lead to our pivotal study.
Under VAC1, we're–we have initiated the AML study and, not on this slide, is of course the Merck milestones of IND filing and by end of year hopefully the renewal of our–their option agreement.
Embryonic stem cells. Now the important milestone to focus on is the initiation of the spinal cord trial early next year and we do hope to have some interim safety data by end of year, again depending on enrollment kinetics and when this actually begins. We hope to have large animal proof of concept for cardiomyocytes from our large animal trials by end of the year, and that triggers the generation of our master cell bank and the IND filing which could occur in 2009. And final proof of concept for the islet cell in the middle of next year in terms of stably reducing hypoglycemia in diabetic animals.
So thanks very much. That's our program, maturing product portfolio in oncology, an emerging product portfolio in embryonic stem cells based upon Geron owned and developed disruptive technologies in telomerase and embryonic stem cells. Thank you very much.
big pharma entert stammzellen:
Human stem cell consortium unveiled
By Clive Cookson, Science Editor
Published: October 3 2007 02:18 | Last updated: October 3 2007 02:18
The pharmaceutical industry on Tuesday announced its first direct involvement in research using human embryonic stem cells.
Three companies have set up a consortium with the government to develop stem cells for safety testing of new drugs through a public-private partnership. The launch of Stem Cells for Safer Medicines, or SC4SM, is significant because �big pharma� has been reluctant to engage in embryonic stem cell research.
Companies fear the reaction in markets such as the US, where the use of human embryos is controversial, and they have left the field to universities and biotechnology businesses.
GlaxoSmithKline, AstraZeneca and Roche are inaugurating SC4SM in collaboration with several government departments.
More companies are expected to join, according to Philip Wright, science director at the Association of the British Pharmaceutical Industry, who will also serve as chief executive of SC4SM.
SC4SM is the international industry�s first public-private partnership on human embryonic stem cells, following a recommendation by Sir John Pattison�s 2005 report on the future of stem cell research in Britain.
Dr Wright said: �It has taken a long time to set up because of the sensitivities. We have an ethical framework that says we should only use existing embryonic stem cell lines [in the UK stem cell bank] and next year we will have an independent ethics advisory board to provide further advice.�
The �1m first phase of a five-year, �10m programme will focus on producing liver cells. Ian Cotgreave, head of molecular toxicity for AstraZeneca, said: �The liver is a key organ for toxicity. It is the dustbin of the body, which neutralises and destroys drugs and toxins.�
Unexpected liver toxicity is the biggest single reason why medicines fail during trials. AstraZeneca�s Exanta, a blood-thinning drug, was a recent casualty.
Animal tests had given no clue to this problem, said Prof Cotgreave. �The predictability for liver toxicity from pre-clinical regulatory testing is almost as good as tossing a coin.�
SC4SM plans to fund five projects over the next year, aimed at converting human embryonic stem cells into hepatocytes (liver cells). These should be a more reliable guide to a new drug�s effect on the human liver.
Two biotech companies with research labs in Dundee � CXR Biosciences and Cellartis � are working on hepatocytes for toxicity and are likely to be involved.
The consortium�s long term strategy will include the conversion of stem cells into other cell types. The second target will be cardiomyocytes (heart cells).
SC4SM will not investigate the therapeutic use of stem cells directly to treat disease, though it will collaborate with researchers who are doing so.
Human stem cell consortium unveiled
By Clive Cookson, Science Editor
Published: October 3 2007 02:18 | Last updated: October 3 2007 02:18
The pharmaceutical industry on Tuesday announced its first direct involvement in research using human embryonic stem cells.
Three companies have set up a consortium with the government to develop stem cells for safety testing of new drugs through a public-private partnership. The launch of Stem Cells for Safer Medicines, or SC4SM, is significant because �big pharma� has been reluctant to engage in embryonic stem cell research.
Companies fear the reaction in markets such as the US, where the use of human embryos is controversial, and they have left the field to universities and biotechnology businesses.
GlaxoSmithKline, AstraZeneca and Roche are inaugurating SC4SM in collaboration with several government departments.
More companies are expected to join, according to Philip Wright, science director at the Association of the British Pharmaceutical Industry, who will also serve as chief executive of SC4SM.
SC4SM is the international industry�s first public-private partnership on human embryonic stem cells, following a recommendation by Sir John Pattison�s 2005 report on the future of stem cell research in Britain.
Dr Wright said: �It has taken a long time to set up because of the sensitivities. We have an ethical framework that says we should only use existing embryonic stem cell lines [in the UK stem cell bank] and next year we will have an independent ethics advisory board to provide further advice.�
The �1m first phase of a five-year, �10m programme will focus on producing liver cells. Ian Cotgreave, head of molecular toxicity for AstraZeneca, said: �The liver is a key organ for toxicity. It is the dustbin of the body, which neutralises and destroys drugs and toxins.�
Unexpected liver toxicity is the biggest single reason why medicines fail during trials. AstraZeneca�s Exanta, a blood-thinning drug, was a recent casualty.
Animal tests had given no clue to this problem, said Prof Cotgreave. �The predictability for liver toxicity from pre-clinical regulatory testing is almost as good as tossing a coin.�
SC4SM plans to fund five projects over the next year, aimed at converting human embryonic stem cells into hepatocytes (liver cells). These should be a more reliable guide to a new drug�s effect on the human liver.
Two biotech companies with research labs in Dundee � CXR Biosciences and Cellartis � are working on hepatocytes for toxicity and are likely to be involved.
The consortium�s long term strategy will include the conversion of stem cells into other cell types. The second target will be cardiomyocytes (heart cells).
SC4SM will not investigate the therapeutic use of stem cells directly to treat disease, though it will collaborate with researchers who are doing so.
Stem-cell bond sales take off in California
Scientists confident research will yield treatments, cures for many diseases
By Kristen Gerencher, MarketWatch
SAN FRANCISCO (MarketWatch) -- California's stem cell research initiative got off to a strong start this week, nearly three years after state voters approved funding it with $3 billion in general obligation bonds.
Demand for the bonds exceeded expectations Wednesday, when retail investors bought $68.6 million, or more than 27%, of the $250 million issued in the sale. State Treasurer Bill Lockyer extended the purchase period for individual investors, who are required to invest a minimum of $5,000, through Thursday morning.
"We're extremely pleased with [Wednesday's] results, and happy to expand the opportunity for individuals to buy these historic bonds," Lockyer said in a statement.
"This $250 million sale will provide the nation's largest-ever investment in human embryonic stem cell research, and an unprecedented investment in the development of intellectual capital."
Scientists believe stem cells, which have the potential to become any kind of cell in the body, may hold the keys for treating or even curing a number of diseases such as diabetes, cancer, Alzheimer's and Parkinson's. Many say stem cells derived from embryos offer the greatest benefit because they are the most malleable or "pluripotent."
The pursuit of embryonic-stem-cell research has been a political flashpoint in recent years. Some religious groups object to it, saying it destroys human life. Many medical experts say those embryos would otherwise be discarded by couples who decide to donate their extra embryos after they have successful in vitro fertilization.
President Bush twice vetoed legislation that would have allowed the use of federal funds for embryonic-stem-cell research. As a result, researchers have been restricted to using adult stem cells and a small number of existing embryonic-stem-cell lines, which many say has put them at an educational and competitive disadvantage.
Setting a precedent
Californians approved the stem-cell measure, Proposition 71, with 59% of the vote in 2004.
After several years of legal challenges, the state now can begin raising $3 billion over 10 years, said Dale Carlson, spokesman for the California Institute for Regenerative Medicine (CIRM), the state agency that was created from the ballot initiative.
Other states such as Connecticut, Maryland and Illinois have put public money into similar research, but California's approach remains unparalleled, he said.
"Nobody else has ever floated general obligation bonds for scientific research in a state before," Carlson said, noting general obligation bonds typically pay for infrastructure projects such as roads and bridges. "You use debt financing to fund projects that have an extended life. Biomedical research is going to have an extended life, with the potential for an enormous payoff."
Stem cells have the potential to treat about 70 diseases, he said, noting that more than 50 well-known scientists have moved to California to participate in research since voters approved the measure.
"The world is looking at California to provide the global strategic leadership necessary to turn stem cells into therapies and cures."
CIRM has approved 136 grants with a total value of $208.5 million so far for training, research and facilities, Carlson said. Since 2005 the agency has been supported by a loan from the state and financing known as bond anticipation notes.
Researchers' understanding of the biology of both adult stem cells and embryonic ones is still in the very early stages, said Dr. Arnold Kriegstein, director of University of California-San Francisco's Institute for Regeneration Medicine.
But what's already clear is that embryonic stem cells offer a unique flexibility, he said. "They can become heart tissue or nerve tissue or skin tissue...These embryonic stem cells can really be the building blocks for regenerating a variety of different organs in the body."
Shot in the arm
UCSF is one of the biggest recipients of grants from CIRM. Its program, which has been privately funded for many years and has partnered with Geron Corp. (GERN:Geron Corporation
GERN 7.83, -0.06, -0.8%) , already has received 17 CIRM grants based on the use of human embryonic stem cells, Kriegstein said. "Seventeen labs here, most of whom, have not worked with human cells before, will now have the opportunity to do that."
"Instead of using animal cells we'll be using human cells," he said. "That will mean any treatment that works in that model is much more likely to work in a patient than if it demonstrated first in a mouse."
The tricky part of working with such stem cell lines is keeping them from mingling with activities supported either directly or indirectly by grants from the National Institutes of Health (NIH), which is how scientists traditionally have funded research, he said.
California's bond issue marks a turning point, Kriegstein said. "It's a dramatic new paradigm of the funding of biomedical research in this country."
"Research in this field is moving quickly, and much of it spurred on by the California initiative," he said. "You'll see other states just won't be able to do the work that California is going to be able to do in the next 10 to 12 years."
Despite the controversy, most Americans support stem cell research -- even Sen. Orrin Hatch, a Republican from Utah, and former first lady Nancy Reagan have endorsed it, said Alan Wolfe, a political science professor at Boston College.
"This is a popular issue," he said. "People generally support it. There's no automatic opposition to this from conservatives."
"The Republican party is divided between moral conservatives who don't like stem-cell research and entrepreneurs," he said. "Entrepreneurs are like 'Hey, if China and Israel are doing this, we should be doing this.'"
Stem-cell research has become more visible with the rise of celebrity advocates such as Michael J. Fox, who has Parkinson's disease and stands to benefit personally from any therapies that are developed. Actor Christopher Reeve, who was paralyzed in an accident in 1995, also called for government-sponsored funding before his death in 2004.
The next president, whether Democrat or Republican, likely will seek to loosen the federal ban on embryonic-stem-cell research, Wolfe said. "I think eventually we will be doing this research and doing it with federal support."
Kristen Gerencher is a reporter for MarketWatch in San Francisco.
Scientists confident research will yield treatments, cures for many diseases
By Kristen Gerencher, MarketWatch
SAN FRANCISCO (MarketWatch) -- California's stem cell research initiative got off to a strong start this week, nearly three years after state voters approved funding it with $3 billion in general obligation bonds.
Demand for the bonds exceeded expectations Wednesday, when retail investors bought $68.6 million, or more than 27%, of the $250 million issued in the sale. State Treasurer Bill Lockyer extended the purchase period for individual investors, who are required to invest a minimum of $5,000, through Thursday morning.
"We're extremely pleased with [Wednesday's] results, and happy to expand the opportunity for individuals to buy these historic bonds," Lockyer said in a statement.
"This $250 million sale will provide the nation's largest-ever investment in human embryonic stem cell research, and an unprecedented investment in the development of intellectual capital."
Scientists believe stem cells, which have the potential to become any kind of cell in the body, may hold the keys for treating or even curing a number of diseases such as diabetes, cancer, Alzheimer's and Parkinson's. Many say stem cells derived from embryos offer the greatest benefit because they are the most malleable or "pluripotent."
The pursuit of embryonic-stem-cell research has been a political flashpoint in recent years. Some religious groups object to it, saying it destroys human life. Many medical experts say those embryos would otherwise be discarded by couples who decide to donate their extra embryos after they have successful in vitro fertilization.
President Bush twice vetoed legislation that would have allowed the use of federal funds for embryonic-stem-cell research. As a result, researchers have been restricted to using adult stem cells and a small number of existing embryonic-stem-cell lines, which many say has put them at an educational and competitive disadvantage.
Setting a precedent
Californians approved the stem-cell measure, Proposition 71, with 59% of the vote in 2004.
After several years of legal challenges, the state now can begin raising $3 billion over 10 years, said Dale Carlson, spokesman for the California Institute for Regenerative Medicine (CIRM), the state agency that was created from the ballot initiative.
Other states such as Connecticut, Maryland and Illinois have put public money into similar research, but California's approach remains unparalleled, he said.
"Nobody else has ever floated general obligation bonds for scientific research in a state before," Carlson said, noting general obligation bonds typically pay for infrastructure projects such as roads and bridges. "You use debt financing to fund projects that have an extended life. Biomedical research is going to have an extended life, with the potential for an enormous payoff."
Stem cells have the potential to treat about 70 diseases, he said, noting that more than 50 well-known scientists have moved to California to participate in research since voters approved the measure.
"The world is looking at California to provide the global strategic leadership necessary to turn stem cells into therapies and cures."
CIRM has approved 136 grants with a total value of $208.5 million so far for training, research and facilities, Carlson said. Since 2005 the agency has been supported by a loan from the state and financing known as bond anticipation notes.
Researchers' understanding of the biology of both adult stem cells and embryonic ones is still in the very early stages, said Dr. Arnold Kriegstein, director of University of California-San Francisco's Institute for Regeneration Medicine.
But what's already clear is that embryonic stem cells offer a unique flexibility, he said. "They can become heart tissue or nerve tissue or skin tissue...These embryonic stem cells can really be the building blocks for regenerating a variety of different organs in the body."
Shot in the arm
UCSF is one of the biggest recipients of grants from CIRM. Its program, which has been privately funded for many years and has partnered with Geron Corp. (GERN:Geron Corporation
GERN 7.83, -0.06, -0.8%) , already has received 17 CIRM grants based on the use of human embryonic stem cells, Kriegstein said. "Seventeen labs here, most of whom, have not worked with human cells before, will now have the opportunity to do that."
"Instead of using animal cells we'll be using human cells," he said. "That will mean any treatment that works in that model is much more likely to work in a patient than if it demonstrated first in a mouse."
The tricky part of working with such stem cell lines is keeping them from mingling with activities supported either directly or indirectly by grants from the National Institutes of Health (NIH), which is how scientists traditionally have funded research, he said.
California's bond issue marks a turning point, Kriegstein said. "It's a dramatic new paradigm of the funding of biomedical research in this country."
"Research in this field is moving quickly, and much of it spurred on by the California initiative," he said. "You'll see other states just won't be able to do the work that California is going to be able to do in the next 10 to 12 years."
Despite the controversy, most Americans support stem cell research -- even Sen. Orrin Hatch, a Republican from Utah, and former first lady Nancy Reagan have endorsed it, said Alan Wolfe, a political science professor at Boston College.
"This is a popular issue," he said. "People generally support it. There's no automatic opposition to this from conservatives."
"The Republican party is divided between moral conservatives who don't like stem-cell research and entrepreneurs," he said. "Entrepreneurs are like 'Hey, if China and Israel are doing this, we should be doing this.'"
Stem-cell research has become more visible with the rise of celebrity advocates such as Michael J. Fox, who has Parkinson's disease and stands to benefit personally from any therapies that are developed. Actor Christopher Reeve, who was paralyzed in an accident in 1995, also called for government-sponsored funding before his death in 2004.
The next president, whether Democrat or Republican, likely will seek to loosen the federal ban on embryonic-stem-cell research, Wolfe said. "I think eventually we will be doing this research and doing it with federal support."
Kristen Gerencher is a reporter for MarketWatch in San Francisco.
telomeraseaktivierung gegen alzheimer? neue forschungsergebnisse:
October 6, 2007
A role for microglial senescence in Alzheimer’s?
Posted by ouroboros under Alzheimer's , Neurodegeneration , Senescence , Telomeres
Why do amyloid plaques cause Alzheimer’s disease? While it would seem to be self-evident that neurons would prefer not to be surrounded by tangled forest of malfolded, insoluble protein deposits, the mechanism by which these plaques cause neuronal death remains an active subject of inquiry.
Cell-autonomous mechanisms (i.e., those in which the plaques act directly on the neurons that will ultimately die, which are the same cells that produced the Aß and tau protein that make up the plaques) are likely to be most important, but some scholars have begun to consider the cell-non-autonomous possibilities. What if the primary action of amyloid plaques is on another type of cell entirely — such as the ubiquitous, essential, yet still poorly understood neuronal support cell, the microglia? Flanary et al. argue that the presence of amyloid plaques accelerates the process of microglial senescence:
Advanced age and presence of intracerebral amyloid deposits are known to be major risk factors for development of neurodegeneration in Alzheimer’s disease (AD), and both have been associated with microglial activation. However, the specific role of activated microglia in AD pathogenesis remains unresolved. Here we report that microglial cells exhibit significant telomere shortening and reduction of telomerase activity with normal aging in rats, and that in humans there is a tendency toward telomere shortening with presence of dementia. Human brains containing high amyloid loads demonstrate a significantly higher degree of microglial dystrophy than nondemented, amyloid-free control subjects. Collectively, these findings show that microglial cell senescence associated with telomere shortening and normal aging is exacerbated by the presence of amyloid. They suggest that degeneration of microglia is a factor in the pathogenesis of AD.
To summarize: Long-term activation of microglia exposed to amyloid results in telomere shortening (presumably the cells undergo more divisions than when they’re not activated), which ultimately leads to cellular senescence when telomeres become critically short. Consistent with this, senescent cells can be observed in amyloid brains, at higher levels than one would expect as a result of chronological age alone.
The authors do not demonstrate a direct connection to Alzheimer’s pathology, but it’s easy to build a model in which senescent microglia contribute to cell death. Evidence from our lab and others has shown that senescent cells, which accumulate throughout the body as a function of age and genotoxic damage, secrete high levels of dangerous signaling molecules, e.g., inflammatory cytokines, growth factors, and matrix metalloproteases. While the post-mitotic cells in the vicinity of senescent microglia are unlikely to respond to growth factors, the inflammatory factors and protease activity could easily conspire to make life quite unpleasant for the delicate neurons — especially if the amyloid plaques are also causing direct damage to these cells.
Several labs are already considering ways to therapeutically eliminate senescent cells, either exploiting the body’s natural methods (immunologically) or using gene therapy. A firm connection between senescence and a scourge like Alzheimer’s (which, unlike aging as such, is already recognized by funding agencies as a pathology) could go a long way toward energizing such efforts.
October 6, 2007
A role for microglial senescence in Alzheimer’s?
Posted by ouroboros under Alzheimer's , Neurodegeneration , Senescence , Telomeres
Why do amyloid plaques cause Alzheimer’s disease? While it would seem to be self-evident that neurons would prefer not to be surrounded by tangled forest of malfolded, insoluble protein deposits, the mechanism by which these plaques cause neuronal death remains an active subject of inquiry.
Cell-autonomous mechanisms (i.e., those in which the plaques act directly on the neurons that will ultimately die, which are the same cells that produced the Aß and tau protein that make up the plaques) are likely to be most important, but some scholars have begun to consider the cell-non-autonomous possibilities. What if the primary action of amyloid plaques is on another type of cell entirely — such as the ubiquitous, essential, yet still poorly understood neuronal support cell, the microglia? Flanary et al. argue that the presence of amyloid plaques accelerates the process of microglial senescence:
Advanced age and presence of intracerebral amyloid deposits are known to be major risk factors for development of neurodegeneration in Alzheimer’s disease (AD), and both have been associated with microglial activation. However, the specific role of activated microglia in AD pathogenesis remains unresolved. Here we report that microglial cells exhibit significant telomere shortening and reduction of telomerase activity with normal aging in rats, and that in humans there is a tendency toward telomere shortening with presence of dementia. Human brains containing high amyloid loads demonstrate a significantly higher degree of microglial dystrophy than nondemented, amyloid-free control subjects. Collectively, these findings show that microglial cell senescence associated with telomere shortening and normal aging is exacerbated by the presence of amyloid. They suggest that degeneration of microglia is a factor in the pathogenesis of AD.
To summarize: Long-term activation of microglia exposed to amyloid results in telomere shortening (presumably the cells undergo more divisions than when they’re not activated), which ultimately leads to cellular senescence when telomeres become critically short. Consistent with this, senescent cells can be observed in amyloid brains, at higher levels than one would expect as a result of chronological age alone.
The authors do not demonstrate a direct connection to Alzheimer’s pathology, but it’s easy to build a model in which senescent microglia contribute to cell death. Evidence from our lab and others has shown that senescent cells, which accumulate throughout the body as a function of age and genotoxic damage, secrete high levels of dangerous signaling molecules, e.g., inflammatory cytokines, growth factors, and matrix metalloproteases. While the post-mitotic cells in the vicinity of senescent microglia are unlikely to respond to growth factors, the inflammatory factors and protease activity could easily conspire to make life quite unpleasant for the delicate neurons — especially if the amyloid plaques are also causing direct damage to these cells.
Several labs are already considering ways to therapeutically eliminate senescent cells, either exploiting the body’s natural methods (immunologically) or using gene therapy. A firm connection between senescence and a scourge like Alzheimer’s (which, unlike aging as such, is already recognized by funding agencies as a pathology) could go a long way toward energizing such efforts.
Source: Ecole Polytechnique F�d�rale de Lausanne
Date: October 4, 2007
New Telomere Discovery Could Help Explain Why Cancer Cells Never Stop Dividing
Science Daily � A group working at the Swiss Institute for Experimental Cancer Research (ISREC) in collaboration with the University of Pavia has discovered that telomeres, the repeated DNA-protein complexes at the end of chromosomes that progressively shorten every time a cell divides, also contain RNA.
A human metaphase stained for telomeric repeats. DAPI stained chromosomes are false-colored in red, telomeres are in green. (Credit: Claus Azzalin, ISREC)Ads by Google This discovery, published in Science Express, calls into question our understanding of how telomeres function, and may provide a new avenue of attack for stopping telomere renewal in cancer cells.
Inside the cell nucleus, all our genetic information is located on twisted, double stranded molecules of DNA which are packaged into chromosomes. At the end of these chromosomes are telomeres, zones of repeated chains of DNA that are often compared to the plastic tips on shoelaces because they prevent chromosomes from fraying, and thus genetic information from getting scrambled when cells divide.
The telomere is like a cellular clock, because every time a cell divides, the telomere shortens. After a cell has grown and divided a few dozen times, the telomeres turn on an alarm system that prevents further division. If this clock doesn't function right, cells either end up with damaged chromosomes or they become "immortal" and continue dividing endlessly -- either way it's bad news and leads to cancer or disease. Understanding how telomeres function, and how this function can potentially be manipulated, is thus extremely important.
The DNA in the chromosome acts like a sort of instruction manual for the cell. Genetic information is transcribed into segments of RNA that then go out into the cell and carry out a variety of tasks such as making proteins, catalyzing chemical reactions, or fulfilling structural roles. It was thought that telomeres were "silent" -- that their DNA was not transcribed into strands of RNA. The researchers have turned this theory on its head by discovering telomeric RNA and showing that this RNA is transcribed from DNA on the telomere.
Why is this important" In embryonic cells (and some stem cells), an enzyme called telomerase rebuilds the telomere so that the cells can keep dividing. Over time, this telomerase dwindles and eventually the telomere shortens and the cell becomes inactive. In cancer cells, the telomerase enzyme keeps rebuilding telomeres long past the cell's normal lifetime. The cells become "immortal", endlessly dividing, resulting in a tumor. Researchers estimate that telomere maintenance activity occurs in about 90% of human cancers. But the mechanism by which this maintenance takes place is not well understood. The researchers discovered that the RNA in the telomere is regulated by a protein in the telomerase enzyme. Their discovery may thus uncover key elements of telomere function.
"It's too early to give yet a definitive answer," to whether this could lead to new cancer therapies, notes Joachim Lingner, senior author on the paper. "But the experiments published in the paper suggest that telomeric RNA may provide a new target to attack telomere function in cancer cells to stop their growth."
Joachim Lingner is an Associate Professor at the EPFL (Ecole Polytechnique F�d�rale de Lausanne). Funding for this research was provided in part by the Swiss National Science Foundation NCCR "Frontiers in Genetics".
Article: "Telomeric Repeat Containing RNA and RNA Surveillance Factors at Mammalian Chromosome Ends"
Note: This story has been adapted from material provided by Ecole Polytechnique F�d�rale de Lausanne.
Date: October 4, 2007
New Telomere Discovery Could Help Explain Why Cancer Cells Never Stop Dividing
Science Daily � A group working at the Swiss Institute for Experimental Cancer Research (ISREC) in collaboration with the University of Pavia has discovered that telomeres, the repeated DNA-protein complexes at the end of chromosomes that progressively shorten every time a cell divides, also contain RNA.
A human metaphase stained for telomeric repeats. DAPI stained chromosomes are false-colored in red, telomeres are in green. (Credit: Claus Azzalin, ISREC)Ads by Google This discovery, published in Science Express, calls into question our understanding of how telomeres function, and may provide a new avenue of attack for stopping telomere renewal in cancer cells.
Inside the cell nucleus, all our genetic information is located on twisted, double stranded molecules of DNA which are packaged into chromosomes. At the end of these chromosomes are telomeres, zones of repeated chains of DNA that are often compared to the plastic tips on shoelaces because they prevent chromosomes from fraying, and thus genetic information from getting scrambled when cells divide.
The telomere is like a cellular clock, because every time a cell divides, the telomere shortens. After a cell has grown and divided a few dozen times, the telomeres turn on an alarm system that prevents further division. If this clock doesn't function right, cells either end up with damaged chromosomes or they become "immortal" and continue dividing endlessly -- either way it's bad news and leads to cancer or disease. Understanding how telomeres function, and how this function can potentially be manipulated, is thus extremely important.
The DNA in the chromosome acts like a sort of instruction manual for the cell. Genetic information is transcribed into segments of RNA that then go out into the cell and carry out a variety of tasks such as making proteins, catalyzing chemical reactions, or fulfilling structural roles. It was thought that telomeres were "silent" -- that their DNA was not transcribed into strands of RNA. The researchers have turned this theory on its head by discovering telomeric RNA and showing that this RNA is transcribed from DNA on the telomere.
Why is this important" In embryonic cells (and some stem cells), an enzyme called telomerase rebuilds the telomere so that the cells can keep dividing. Over time, this telomerase dwindles and eventually the telomere shortens and the cell becomes inactive. In cancer cells, the telomerase enzyme keeps rebuilding telomeres long past the cell's normal lifetime. The cells become "immortal", endlessly dividing, resulting in a tumor. Researchers estimate that telomere maintenance activity occurs in about 90% of human cancers. But the mechanism by which this maintenance takes place is not well understood. The researchers discovered that the RNA in the telomere is regulated by a protein in the telomerase enzyme. Their discovery may thus uncover key elements of telomere function.
"It's too early to give yet a definitive answer," to whether this could lead to new cancer therapies, notes Joachim Lingner, senior author on the paper. "But the experiments published in the paper suggest that telomeric RNA may provide a new target to attack telomere function in cancer cells to stop their growth."
Joachim Lingner is an Associate Professor at the EPFL (Ecole Polytechnique F�d�rale de Lausanne). Funding for this research was provided in part by the Swiss National Science Foundation NCCR "Frontiers in Genetics".
Article: "Telomeric Repeat Containing RNA and RNA Surveillance Factors at Mammalian Chromosome Ends"
Note: This story has been adapted from material provided by Ecole Polytechnique F�d�rale de Lausanne.
Old hat to Geronphiles, but the last line is what caught my eye...
Lingner suspects this RNA may interact with telomerase. If so, disabling the RNA with a drug might block this process and prevent cells turning cancerous.
--------------------------------------------------------------------------------
Chromosome caps may explain cell immortality
17 October 2007
NewScientist.com news service
Telomeres, the supposedly "dead" sections of DNA that cap the ends of chromosomes, are showing definite signs of life.
Telomeres shorten every time a cell divides until they reach a critical length - at which point the cell dies through a process called apoptosis. Cancers sometimes develop when the telomerase enzyme gets switched on and rebuilds the telomeres, making the cells immortal.
Telomeres had been assumed to contain inactive DNA. Now Joachim Lingner of the Swiss Federal Institute of Technology in Lausanne and his colleagues have found that they behave like genes in that they make RNA copies of themselves (Science, DOI: 10.1126/science.1147182).
Lingner suspects this RNA may interact with telomerase. If so, disabling the RNA with a drug might block this process and prevent cells turning cancerous.
Lingner suspects this RNA may interact with telomerase. If so, disabling the RNA with a drug might block this process and prevent cells turning cancerous.
--------------------------------------------------------------------------------
Chromosome caps may explain cell immortality
17 October 2007
NewScientist.com news service
Telomeres, the supposedly "dead" sections of DNA that cap the ends of chromosomes, are showing definite signs of life.
Telomeres shorten every time a cell divides until they reach a critical length - at which point the cell dies through a process called apoptosis. Cancers sometimes develop when the telomerase enzyme gets switched on and rebuilds the telomeres, making the cells immortal.
Telomeres had been assumed to contain inactive DNA. Now Joachim Lingner of the Swiss Federal Institute of Technology in Lausanne and his colleagues have found that they behave like genes in that they make RNA copies of themselves (Science, DOI: 10.1126/science.1147182).
Lingner suspects this RNA may interact with telomerase. If so, disabling the RNA with a drug might block this process and prevent cells turning cancerous.
AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics.(Oct 22-26,2007)
Geron Abstract:
A97: The novel telomerase inhibitor GRN163L targets drug resistant cancer stem cells in multiple myeloma.
William H. Matsui1,Qiuju Wang1, Sarah Brennan1, Alan Meeker2, Robert Tressler2, CalvinHarley2, Carol Ann Huff1, B. Douglas Smith1, Richard J. Jones1. 1JohnsHopkins University School of Medicine, Baltimore, MD; 2Geron Corporation, Menlo Park, CA.
The majority of chronic hematologic malignancies are responsive to initial treatment using standard agents, but most patients relapse and experience progressive disease. The factors responsible for disease relapse are poorly defined, but increasing evidence in a wide range of human cancers suggests that all tumor cells are not functionally equivalent. In these models, tumor cells are organized in a hierarchical fashion reminiscent of normal tissue systems in which rare populations of less mature, self-renewing cancer stem cells (CSC) give rise to differentiated progeny that constitute the bulk of the tumor and lack long-term replicative potential. The typical clinical pattern of relapse following treatment suggests that mature tumor cells are inhibited, but that CSC are spared and capable of tumor regrowth.
We previously demonstrated that CSC in multiple myeloma (MM) do not express the characteristic plasma cell surface antigen CD138, but rather lack this antigen and phenotypically resemble B cells.We treated CD138+ plasma cells or CD138neg cells isolated by FACS from the human MM cell lines RPMI 8226 and NCI-H929 with the clinically utilized anti-MM agents dexamethasone (0.1�M), bortezomib (10nM), and lenalidomide (1�M) then evaluated their clonogenic growth. Similar to their clinical effects, each agent inhibited CD138+ plasma cells. In contrast, none of the agents significantly limited the clonogenic recovery of CD138neg MM precursors.
We hypothesized that cellular processes involved in the self-renewal of normal stem cells are aberrantly regulated in CSC and could serve as effective targets. Telomerase activity (TA) is required by normal stem cells to slow the progressive shortening of telomeres during cellular replication that would ultimately result in cellular senescence and/or apoptosis.We examined TA in CD138+ and CD138neg cells from the RPMI 8225, NCI-H929, and U266 cell lines and found that both cellular compartments contained elevated TA compared to normal B cells using a PCR-based assay. GRN163L is a novel lipid-conjugated 13 nucleotide thio-phosphoramidate oligonucleotide that acts as a potent and specific active site inhibitor of telomerase. GRN163L (0.1-5�M) markedly reduced TA in both CD138+ and CD138neg cells. In order to examine the effects of TA inhibition on clonogenic MM growth, we treated CD138+ and CD138neg RPMI 8226 and NCI-H929 cells continuously with GRN163L (1�M) for up to 6 weeks. Clonogenic growth potential was assessed each week by plating cells in methylcellulose. GRN163L was active against both CD138+ and CD138neg cells from each cell line and eliminated the colony forming potential by 5 weeks. Similarly, GRN163L progressively inhibited CD138neg CSC isolated from primary clinical MM bone marrow specimens during long-term culture.
These data demonstrate that MM CSC are relatively resistant to standard anti-MM therapies, but susceptible to TA inhibition, and clinical trials with GRN163L in MM patients are planned. In conclusion, active and specific telomerase inhibitors, such as GRN163L, may represent a novel therapeutic strategy with the potential to limit disease relapse in maligancies in which CSC play a critical pathogenic role.
Geron Abstract:
A97: The novel telomerase inhibitor GRN163L targets drug resistant cancer stem cells in multiple myeloma.
William H. Matsui1,Qiuju Wang1, Sarah Brennan1, Alan Meeker2, Robert Tressler2, CalvinHarley2, Carol Ann Huff1, B. Douglas Smith1, Richard J. Jones1. 1JohnsHopkins University School of Medicine, Baltimore, MD; 2Geron Corporation, Menlo Park, CA.
The majority of chronic hematologic malignancies are responsive to initial treatment using standard agents, but most patients relapse and experience progressive disease. The factors responsible for disease relapse are poorly defined, but increasing evidence in a wide range of human cancers suggests that all tumor cells are not functionally equivalent. In these models, tumor cells are organized in a hierarchical fashion reminiscent of normal tissue systems in which rare populations of less mature, self-renewing cancer stem cells (CSC) give rise to differentiated progeny that constitute the bulk of the tumor and lack long-term replicative potential. The typical clinical pattern of relapse following treatment suggests that mature tumor cells are inhibited, but that CSC are spared and capable of tumor regrowth.
We previously demonstrated that CSC in multiple myeloma (MM) do not express the characteristic plasma cell surface antigen CD138, but rather lack this antigen and phenotypically resemble B cells.We treated CD138+ plasma cells or CD138neg cells isolated by FACS from the human MM cell lines RPMI 8226 and NCI-H929 with the clinically utilized anti-MM agents dexamethasone (0.1�M), bortezomib (10nM), and lenalidomide (1�M) then evaluated their clonogenic growth. Similar to their clinical effects, each agent inhibited CD138+ plasma cells. In contrast, none of the agents significantly limited the clonogenic recovery of CD138neg MM precursors.
We hypothesized that cellular processes involved in the self-renewal of normal stem cells are aberrantly regulated in CSC and could serve as effective targets. Telomerase activity (TA) is required by normal stem cells to slow the progressive shortening of telomeres during cellular replication that would ultimately result in cellular senescence and/or apoptosis.We examined TA in CD138+ and CD138neg cells from the RPMI 8225, NCI-H929, and U266 cell lines and found that both cellular compartments contained elevated TA compared to normal B cells using a PCR-based assay. GRN163L is a novel lipid-conjugated 13 nucleotide thio-phosphoramidate oligonucleotide that acts as a potent and specific active site inhibitor of telomerase. GRN163L (0.1-5�M) markedly reduced TA in both CD138+ and CD138neg cells. In order to examine the effects of TA inhibition on clonogenic MM growth, we treated CD138+ and CD138neg RPMI 8226 and NCI-H929 cells continuously with GRN163L (1�M) for up to 6 weeks. Clonogenic growth potential was assessed each week by plating cells in methylcellulose. GRN163L was active against both CD138+ and CD138neg cells from each cell line and eliminated the colony forming potential by 5 weeks. Similarly, GRN163L progressively inhibited CD138neg CSC isolated from primary clinical MM bone marrow specimens during long-term culture.
These data demonstrate that MM CSC are relatively resistant to standard anti-MM therapies, but susceptible to TA inhibition, and clinical trials with GRN163L in MM patients are planned. In conclusion, active and specific telomerase inhibitors, such as GRN163L, may represent a novel therapeutic strategy with the potential to limit disease relapse in maligancies in which CSC play a critical pathogenic role.
am freitag, den 7.12. wirds spannend (siehe ganz unten) auf der der tagung der american association for cancer research (aacr)
AACR Special Conference (Dec.6-9,2007):
"The Role of Telomeres & Telomerase in Cancer Research"
Program:
THURSDAY, DECEMBER 6
SESSION 1: MAMMALIAN MODELS OF TELOMERE DYSFUNCTION
6:00 p.m.-7:45 p.m.
Dyskeratosis Congenita: A Disorder of Telomerase Dysfunction
Inderjeet S. Dokal, Queen Mary's School of Medicine and Dentistry, London, England
Tankyrase 1 Function at Telomeres
Susan Smith, Skirball Institute of Biomolecular Medicine, New York, NY
Short talk from proffered paper
Mouse Models of Telomere and Telomerase Regulation
Richard J. Hodes, National Institute on Aging, Bethesda, MD
Short talk from proffered paper
OPENING RECEPTION
7:45 p.m.-9:30 p.m.
--------------------------------------------------------------------------------
FRIDAY, DECEMBER 7
KEYNOTE ADDRESS
8:15 a.m.-9:00 a.m.
Title to be announced
Carol W. Greider, Johns Hopkins University School of Medicine, Baltimore, MD
SESSION 2: TELOMERE BIOLOGY IN STEM CELLS AND CANCER STEM CELLS
9:00 a.m.-10:30 a.m.
Title to be announced
Steven E. Artandi, Stanford University School of Medicine, Stanford, CA
Role of Telomerase in Normal and Cancer Cells
Jerry W. Shay, UT Southwestern Medical Center, Dallas, TX
Short talk from proffered paper
Title to be announced
María A. Blasco, Spanish National Cancer Center, Madrid, Spain
SESSION 3: TELOMERES AND GENOMIC INSTABILITY
10:50 a.m.-12:35 p.m.
Probing the DNA Damage Response
Stephen J. Elledge, Harvard Medical School, Boston, MA
Shelterin
Titia de Lange, Rockefeller University, New York, NY
Short talk from proffered paper
Sumoylation of RecQ Helicase Controls the Fate of Dysfunctional Telomeres
Julie Cooper, Cancer Research UK, London, England
Short talk from proffered paper
POSTER SESSION A (WITH LIGHT LUNCH)
12:35 p.m.-3:00 p.m.
SESSION 4: BIOLOGY OF TELOMERES AND TELOMERASE IN MODEL ORGANISMS
3:00 p.m.-4:45 p.m.
Mechanisms of Telomere Length Regulation in Budding Yeast
David Shore, University of Geneva, Geneva, Switzerland
Title to be announced
Victoria Lundblad, The Salk Institute for Biological Studies, La Jolla, CA
Short talk from proffered paper
Title to be announced
Virginia A. Zakian, Princeton University, Princeton, NJ
Short talk from proffered paper
SESSION 5: THERAPEUTIC APPROACHES BASED ON TELOMERES AND TELOMERASE
5:00 p.m.-6:20 p.m.
Title to be announced
Gustav Gaudermack, Norwegian Radium Hospital, Oslo, Norway
Short talk from proffered paper
Update on Clinical Trials with GRN163L: A Specific Telomerase Inhibitor
Alan B. Colowick , Geron Corporation, Menlo Park, CA
Short talk from proffered paper
AACR Special Conference (Dec.6-9,2007):
"The Role of Telomeres & Telomerase in Cancer Research"
Program:
THURSDAY, DECEMBER 6
SESSION 1: MAMMALIAN MODELS OF TELOMERE DYSFUNCTION
6:00 p.m.-7:45 p.m.
Dyskeratosis Congenita: A Disorder of Telomerase Dysfunction
Inderjeet S. Dokal, Queen Mary's School of Medicine and Dentistry, London, England
Tankyrase 1 Function at Telomeres
Susan Smith, Skirball Institute of Biomolecular Medicine, New York, NY
Short talk from proffered paper
Mouse Models of Telomere and Telomerase Regulation
Richard J. Hodes, National Institute on Aging, Bethesda, MD
Short talk from proffered paper
OPENING RECEPTION
7:45 p.m.-9:30 p.m.
--------------------------------------------------------------------------------
FRIDAY, DECEMBER 7
KEYNOTE ADDRESS
8:15 a.m.-9:00 a.m.
Title to be announced
Carol W. Greider, Johns Hopkins University School of Medicine, Baltimore, MD
SESSION 2: TELOMERE BIOLOGY IN STEM CELLS AND CANCER STEM CELLS
9:00 a.m.-10:30 a.m.
Title to be announced
Steven E. Artandi, Stanford University School of Medicine, Stanford, CA
Role of Telomerase in Normal and Cancer Cells
Jerry W. Shay, UT Southwestern Medical Center, Dallas, TX
Short talk from proffered paper
Title to be announced
María A. Blasco, Spanish National Cancer Center, Madrid, Spain
SESSION 3: TELOMERES AND GENOMIC INSTABILITY
10:50 a.m.-12:35 p.m.
Probing the DNA Damage Response
Stephen J. Elledge, Harvard Medical School, Boston, MA
Shelterin
Titia de Lange, Rockefeller University, New York, NY
Short talk from proffered paper
Sumoylation of RecQ Helicase Controls the Fate of Dysfunctional Telomeres
Julie Cooper, Cancer Research UK, London, England
Short talk from proffered paper
POSTER SESSION A (WITH LIGHT LUNCH)
12:35 p.m.-3:00 p.m.
SESSION 4: BIOLOGY OF TELOMERES AND TELOMERASE IN MODEL ORGANISMS
3:00 p.m.-4:45 p.m.
Mechanisms of Telomere Length Regulation in Budding Yeast
David Shore, University of Geneva, Geneva, Switzerland
Title to be announced
Victoria Lundblad, The Salk Institute for Biological Studies, La Jolla, CA
Short talk from proffered paper
Title to be announced
Virginia A. Zakian, Princeton University, Princeton, NJ
Short talk from proffered paper
SESSION 5: THERAPEUTIC APPROACHES BASED ON TELOMERES AND TELOMERASE
5:00 p.m.-6:20 p.m.
Title to be announced
Gustav Gaudermack, Norwegian Radium Hospital, Oslo, Norway
Short talk from proffered paper
Update on Clinical Trials with GRN163L: A Specific Telomerase Inhibitor
Alan B. Colowick , Geron Corporation, Menlo Park, CA
Short talk from proffered paper
Reiche fordert mehr Freiheiten für Stammzellforscher
Soll die Stammzellforschung in Deutschland erleichtert werden? Die stellvertretende Fraktionsvorsitzende der Union, Katherina Reiche, sagt Ja, Kanzlerin Angela Merkel sagt Nein. Die Chancen für eine Änderung des Stammzellengesetzes stehen dennoch gut.
http://www.spiegel.de/wissenschaft/mensch/0,1518,514025,00.h…
Soll die Stammzellforschung in Deutschland erleichtert werden? Die stellvertretende Fraktionsvorsitzende der Union, Katherina Reiche, sagt Ja, Kanzlerin Angela Merkel sagt Nein. Die Chancen für eine Änderung des Stammzellengesetzes stehen dennoch gut.
http://www.spiegel.de/wissenschaft/mensch/0,1518,514025,00.h…
Entschuldigt bitte die Störung,
aber habt ihr euch schon angemeldet für die schicke Advent Party von WO?
Schaut mal unter http://www.wallstreet-online.de/dyn/community/thread.html?th…

Ich freue mich auf jeden Gast, lasst knacken!
 Päpstin
Päpstin
aber habt ihr euch schon angemeldet für die schicke Advent Party von WO?
Schaut mal unter http://www.wallstreet-online.de/dyn/community/thread.html?th…

Ich freue mich auf jeden Gast, lasst knacken!
 Päpstin
Päpstin
liebe geronfans,
unsere adventsparty kommt am 6.12. - wenn mister colowick mal was substanzielles zu gern163l rauslässt. was wir im verg. juli gesehen haben, war ja bekanntlich der geronwitz des jahres. ich hoffe ein halbes jahr später auf wirklich interessante neuigkeiten.
anbei ein wieder mal bullisher kommentar (gab recht wenige in letzter zeit):
Biotech Heats Up in the Fall Thursday, October 25, 2007
Michael Murphy, editor of New World Radar Report, says biotech stocks post big gains at this time of year�and he finds one stock he thinks could benefit.
With the equinox just behind us, this is a timely update because fall is the best time of year for biotech stocks. Over the last 20 years, the AMEX Biotech Index (BTK) has compounded at 16% per year, and 80% of the gains come in the fall. Nineteen out of 20 years, the BTK rose in the last half of the year. The numbers are similar for the NASDAQ Biotech Index (NBI), which was up five of the last six years for the September to November three-month period, averaging a 9% gain.
Why do biotech stocks go up about now? There are so many annual medical society meetings and biotech brokerage firm conferences between now and January that it sometimes seems like companies time their clinical trials to conclude in time to have data ready for the fourth quarter. We'll also see filings [with the Food & Drug Administration] before year-end, so companies have something to brag about in their shareholder letters.
But with only a couple of exceptions, we don't need the FDA to do anything other than keep their special protocol agreements. What we are looking for is clinical trial or marketplace results.
Geron (NASDAQ: GERN) has been in a $6 to $9 range for a year, perhaps showing the impact of Federal policy on embryonic stem cell research. However, no matter which party wins the 2008 election, the bans are likely to be loosened or eliminated. Companies like Geron need independent validation of their work by academics, who in turn are funded by National Institutes of Health grants.
Today, these academics write grant applications for non-embryonic stem cell research, even though many of them don't believe their research will be useful. As Tom Okarma, CEO of Geron, says: "An enormous amount of scientific damage has been done. I assume whoever is elected will change the policy."
I don't assume anything, since President Clinton signed this ban into law. But I expect that the candidates will have to take a stand, and if it is Giuliani against Clinton, both will tend to lean towards reviewing or changing the policy.
In the meantime, Geron is spending millions of dollars of its own money on stem cell research, and announced in August that animal studies showed transplanted human embryonic stem cells improved heart function after a heart attack. Their showcase program is an embryonic stem cell drug to repair spinal cord damage for the 11,000 people a year that suffer these injuries�the same one that killed Superman. They need FDA approval to start a Phase I trial.
GERN is a buy up to $9 for a run to my $18 target after the next major news story. (The stock closed below $7.50 Wednesday�Editor.)
unsere adventsparty kommt am 6.12. - wenn mister colowick mal was substanzielles zu gern163l rauslässt. was wir im verg. juli gesehen haben, war ja bekanntlich der geronwitz des jahres. ich hoffe ein halbes jahr später auf wirklich interessante neuigkeiten.
anbei ein wieder mal bullisher kommentar (gab recht wenige in letzter zeit):
Biotech Heats Up in the Fall Thursday, October 25, 2007
Michael Murphy, editor of New World Radar Report, says biotech stocks post big gains at this time of year�and he finds one stock he thinks could benefit.
With the equinox just behind us, this is a timely update because fall is the best time of year for biotech stocks. Over the last 20 years, the AMEX Biotech Index (BTK) has compounded at 16% per year, and 80% of the gains come in the fall. Nineteen out of 20 years, the BTK rose in the last half of the year. The numbers are similar for the NASDAQ Biotech Index (NBI), which was up five of the last six years for the September to November three-month period, averaging a 9% gain.
Why do biotech stocks go up about now? There are so many annual medical society meetings and biotech brokerage firm conferences between now and January that it sometimes seems like companies time their clinical trials to conclude in time to have data ready for the fourth quarter. We'll also see filings [with the Food & Drug Administration] before year-end, so companies have something to brag about in their shareholder letters.
But with only a couple of exceptions, we don't need the FDA to do anything other than keep their special protocol agreements. What we are looking for is clinical trial or marketplace results.
Geron (NASDAQ: GERN) has been in a $6 to $9 range for a year, perhaps showing the impact of Federal policy on embryonic stem cell research. However, no matter which party wins the 2008 election, the bans are likely to be loosened or eliminated. Companies like Geron need independent validation of their work by academics, who in turn are funded by National Institutes of Health grants.
Today, these academics write grant applications for non-embryonic stem cell research, even though many of them don't believe their research will be useful. As Tom Okarma, CEO of Geron, says: "An enormous amount of scientific damage has been done. I assume whoever is elected will change the policy."
I don't assume anything, since President Clinton signed this ban into law. But I expect that the candidates will have to take a stand, and if it is Giuliani against Clinton, both will tend to lean towards reviewing or changing the policy.
In the meantime, Geron is spending millions of dollars of its own money on stem cell research, and announced in August that animal studies showed transplanted human embryonic stem cells improved heart function after a heart attack. Their showcase program is an embryonic stem cell drug to repair spinal cord damage for the 11,000 people a year that suffer these injuries�the same one that killed Superman. They need FDA approval to start a Phase I trial.
GERN is a buy up to $9 for a run to my $18 target after the next major news story. (The stock closed below $7.50 Wednesday�Editor.)
hätt ich beinahe vergessen:
short interest wieder rückläufig - was den kurs gestützt bzw. wieder auf über 8 usd getrieben hatte.
per 15. okt. 7,7 mio. aktien short, von der spitze im august 2,5 mio. weniger. alles wieder normal, keine anzeichen, dass shorties besser wüssten, wie es um grn163l bestellt ist.
good nite.
short interest wieder rückläufig - was den kurs gestützt bzw. wieder auf über 8 usd getrieben hatte.
per 15. okt. 7,7 mio. aktien short, von der spitze im august 2,5 mio. weniger. alles wieder normal, keine anzeichen, dass shorties besser wüssten, wie es um grn163l bestellt ist.
good nite.
2. nachtrag für heute abend:
geron hat mittlerweile 4 klinische test aktiv, 3 zu gern163l (telomerasehemmer), 1 zu grnvac1 (impfung auf telomeraseantigen), nachdem es schon bei prostatakrebs klinisch getestet wurde.
look here:
http://www.cancer.gov/search/ResultsClinicalTrialsAdvanced.a…
geron hat mittlerweile 4 klinische test aktiv, 3 zu gern163l (telomerasehemmer), 1 zu grnvac1 (impfung auf telomeraseantigen), nachdem es schon bei prostatakrebs klinisch getestet wurde.
look here:
http://www.cancer.gov/search/ResultsClinicalTrialsAdvanced.a…
Antwort auf Beitrag Nr.: 32.182.237 von LuckyCat am 28.10.07 22:13:51Hallo
Bin wieder vorsichtig eigestiegen ,bei dieser Achterbahnfahrt dieses Jahr kann mann ja nicht long bleiben.Nächstes Jahr sind ja Wahlen und so wird der Kurs glaub ich nächstes Jahr rein spekulativ steigen im Glauben die Demokraten gewinnen,na mal sehn.Verfolge hier immer alles,verstehe leider nicht alles,bin nicht vom Fach.
Bin wieder vorsichtig eigestiegen ,bei dieser Achterbahnfahrt dieses Jahr kann mann ja nicht long bleiben.Nächstes Jahr sind ja Wahlen und so wird der Kurs glaub ich nächstes Jahr rein spekulativ steigen im Glauben die Demokraten gewinnen,na mal sehn.Verfolge hier immer alles,verstehe leider nicht alles,bin nicht vom Fach.
Geron 2007 3rd Quarter Conference Call: Dr.Okarma
DR. OKARMA: Thank you, David, and good morning everyone. Thank you for calling in this morning. I'll first summarize our presentations in the quarter. We announced my presentation at UBS and Alan Colowick stood in for me at the Bio Investor Forum, and next week I'll be presenting at the Rodman conference on the 5th in New York City.
We also participate in quite a few scientific conferences which we routinely do not press release so I thought I would just quickly summarize some of those. These are important for the company to, you know, maintain our scientific, the scientific contacts and to also keep our ear to the ground on what's going on out there at the abstract level–at the presentation level before work gets published. So we did two talks on our diabetes embryonic stem cell islet program at the International Pancreas and Islet Transplantation Association and another one in Europe. We did two talks speaking to the manufacturability and the scalability of our master/working cell bank systems at the ISCT annual Somatic Cell Therapy symposium and at the American Association for Blood Banks. We gave two talks on 163L, both by our collaborator, Bill Matsui, at Johns Hopkins, describing his work of 163 impacting the biology of multiple myeloma stem cells both from stem cell lines as well as primary samples from patients with multiple myeloma. Those were at the ISEH meeting in late September and the AACR/NCI/EORTC meeting in San Francisco in October. And we gave one talk on our embryonic stem cell cardiomyocytes at the NIH symposium on cardiovascular regenerative medicine.
There were four major press releases of moment during the quarter. The first one in July, we announced the initiation of the first combination trial of 163L in patients with non small cell lung cancer combined with a standard paclitaxel-carboplatinum regimen. This, as I said, is the first time that we are using 163L in a combination setting. We chose the disease and that particular combination to reflect first of all the biology of 163L in non small cell lung cancer models, as well as the common paclitaxel-carboplatinum combination which sets us up to begin thinking about using this drug with that combination in other disease settings. Joan Schiller at UT Southwest is the lead investigator and as you may remember, we started our dose in this trial at a dose that's equivalent to that in the 4th cohort of the two solid tumor and CLL trials.
Later that month, in July, we announced the initiation of our telomerase vaccine clinical trial in patients with AML. This is led by at John DiPersio, Washington University, St. Louis; there'll be five other sites coming on board. This is an important study for us in that it's the first to document what we hope to show in terms of immune responses in the prime/boost regimen. We have talked about work done under an investigator IND at Duke where in prostate cancer and in some hematologic malignancies we demonstrated that the prime, the six weekly injections, actually prepares the patient's immune system to respond in an anamnestic manner. In other words, a recall response when the patient once again is boosted many months after the prime regimen. This is important because it enables us to maintain a very high anti-telomerase T cell response virtually indefinitely. So we now have the opportunity to look at the impact of disease related endpoints in AML given our expectation that the immune response will be durable and long lasting.
A major paper came out in the September issue of Nature Biotech which was published online at the very end of August on our embryonic stem cell derived cardiomyocytes, and this is really the second proof of concept in an animal model of disease that these cells derived from embryonic stem cells survive and function in the context of a disease. This is actually the first study ever to show survival of cells in an infarct zone in an animal. Not only did the cells survive in the infarct zone, but they showed statistically improved heart function as measured by decrease in n systolic and n diastolic diameters of the treated animals, improved fractional shortening, and improved left ventricular ejection fraction, and those variables were determined by both MRI and ECHO, as well as extensive histology of the animals after sacrifice. We also in that paper documented the scalable production of these cells � they are made with the same kind of efficiency and direct differentiation process as that which is characterized by our OPC1 product for spinal cord injury. We also in that paper disclosed a pro survival cocktail which is a fairly comlex combination of reagents, each individually determined to be important for the survival of these cells in the hostile environment of a myocardial scar. We also showed in the paper, frankly to our surprise, that the injection of these cells induces host angiogenesis - new blood vessel formation - that is of rat origin, not of human origin. There are no angiogenic cells to our knowledge in the cardiomyocyte prep, and clearly the improved vascularity in combination with the durable survival of human functioning cardiomyocytes combined to produce the hoped for significant effects in function,
And, lastly, in early September we announced a victory in the European Patent Office. Pharmexa lost their appeal to obtain broad claims to telomerase-based cancer vaccines. So this decision affirmed a prior decision made in 2003 by the European Patent Office to revoke the claims of Pharmexa's patent that purported to claim broadly telomerase-based cancer vaccines. At the, this particular decision, the patent office also rejected the claims of 16 alternative claim sets that Pharmexa had submitted along with this appeal. So their patent estate is now limited to 5 specific small peptides. Pharmexa has therefore failed to obtain broad claims to telomerase cancer vaccines. They are not licensed by us. And we have prevailed in protecting our own technology as well as that which is licensed to Merck.
And with that I think we'll open up to questions.
DR. OKARMA: Thank you, David, and good morning everyone. Thank you for calling in this morning. I'll first summarize our presentations in the quarter. We announced my presentation at UBS and Alan Colowick stood in for me at the Bio Investor Forum, and next week I'll be presenting at the Rodman conference on the 5th in New York City.
We also participate in quite a few scientific conferences which we routinely do not press release so I thought I would just quickly summarize some of those. These are important for the company to, you know, maintain our scientific, the scientific contacts and to also keep our ear to the ground on what's going on out there at the abstract level–at the presentation level before work gets published. So we did two talks on our diabetes embryonic stem cell islet program at the International Pancreas and Islet Transplantation Association and another one in Europe. We did two talks speaking to the manufacturability and the scalability of our master/working cell bank systems at the ISCT annual Somatic Cell Therapy symposium and at the American Association for Blood Banks. We gave two talks on 163L, both by our collaborator, Bill Matsui, at Johns Hopkins, describing his work of 163 impacting the biology of multiple myeloma stem cells both from stem cell lines as well as primary samples from patients with multiple myeloma. Those were at the ISEH meeting in late September and the AACR/NCI/EORTC meeting in San Francisco in October. And we gave one talk on our embryonic stem cell cardiomyocytes at the NIH symposium on cardiovascular regenerative medicine.
There were four major press releases of moment during the quarter. The first one in July, we announced the initiation of the first combination trial of 163L in patients with non small cell lung cancer combined with a standard paclitaxel-carboplatinum regimen. This, as I said, is the first time that we are using 163L in a combination setting. We chose the disease and that particular combination to reflect first of all the biology of 163L in non small cell lung cancer models, as well as the common paclitaxel-carboplatinum combination which sets us up to begin thinking about using this drug with that combination in other disease settings. Joan Schiller at UT Southwest is the lead investigator and as you may remember, we started our dose in this trial at a dose that's equivalent to that in the 4th cohort of the two solid tumor and CLL trials.
Later that month, in July, we announced the initiation of our telomerase vaccine clinical trial in patients with AML. This is led by at John DiPersio, Washington University, St. Louis; there'll be five other sites coming on board. This is an important study for us in that it's the first to document what we hope to show in terms of immune responses in the prime/boost regimen. We have talked about work done under an investigator IND at Duke where in prostate cancer and in some hematologic malignancies we demonstrated that the prime, the six weekly injections, actually prepares the patient's immune system to respond in an anamnestic manner. In other words, a recall response when the patient once again is boosted many months after the prime regimen. This is important because it enables us to maintain a very high anti-telomerase T cell response virtually indefinitely. So we now have the opportunity to look at the impact of disease related endpoints in AML given our expectation that the immune response will be durable and long lasting.
A major paper came out in the September issue of Nature Biotech which was published online at the very end of August on our embryonic stem cell derived cardiomyocytes, and this is really the second proof of concept in an animal model of disease that these cells derived from embryonic stem cells survive and function in the context of a disease. This is actually the first study ever to show survival of cells in an infarct zone in an animal. Not only did the cells survive in the infarct zone, but they showed statistically improved heart function as measured by decrease in n systolic and n diastolic diameters of the treated animals, improved fractional shortening, and improved left ventricular ejection fraction, and those variables were determined by both MRI and ECHO, as well as extensive histology of the animals after sacrifice. We also in that paper documented the scalable production of these cells � they are made with the same kind of efficiency and direct differentiation process as that which is characterized by our OPC1 product for spinal cord injury. We also in that paper disclosed a pro survival cocktail which is a fairly comlex combination of reagents, each individually determined to be important for the survival of these cells in the hostile environment of a myocardial scar. We also showed in the paper, frankly to our surprise, that the injection of these cells induces host angiogenesis - new blood vessel formation - that is of rat origin, not of human origin. There are no angiogenic cells to our knowledge in the cardiomyocyte prep, and clearly the improved vascularity in combination with the durable survival of human functioning cardiomyocytes combined to produce the hoped for significant effects in function,
And, lastly, in early September we announced a victory in the European Patent Office. Pharmexa lost their appeal to obtain broad claims to telomerase-based cancer vaccines. So this decision affirmed a prior decision made in 2003 by the European Patent Office to revoke the claims of Pharmexa's patent that purported to claim broadly telomerase-based cancer vaccines. At the, this particular decision, the patent office also rejected the claims of 16 alternative claim sets that Pharmexa had submitted along with this appeal. So their patent estate is now limited to 5 specific small peptides. Pharmexa has therefore failed to obtain broad claims to telomerase cancer vaccines. They are not licensed by us. And we have prevailed in protecting our own technology as well as that which is licensed to Merck.
And with that I think we'll open up to questions.
pharmexa, der große patent-looser. geron hat vor kurzem gegen pharmexa vor dem europäischen berufungsgericht in patentstreitigkeiten einen klaren sieg davon getragen. bis auf einige wenige kleine peptide. um die geht es wohl im folgenden statement:
Published: 14:24 02.11.2007 GMT+1 /HUGIN /Source: Pharmexa A/S /CSE: PHARMX /ISIN: DK0015966592
New clinical results support telomerase vaccination in breast cancer
Summary: US scientists have published promising clinical data on vaccination with a telomerase peptide in breast cancer. The peptide is claimed in Pharmexa's granted European patent.
A group of prominent scientists from the Abramson Cancer Center and the University of Pennsylvania School of Medicine has published new clinical data on vaccination with the telomerase peptide I540 in 19 metastatic breast cancer patients. The results were published in the recent edition of the scientific journal Cancer Research (Cancer Research; 67: (21). November 1, 2007).
The results show that vaccination with the I540 telomerase peptide led to changes in the tumor microenvironment, infiltration of T-cells and widespread tumor necrosis (tumor death). Furthermore, an exploratory analysis revealed that the median overall survival was significantly longer in those patients who achieved an immune response to the I540 peptide compared to patients who did not. Immune responses to a control peptide did not correlate with survival.
The I540 telomerase peptide and its use in cancer immunotherapy is claimed in Pharmexa's granted European patent. This and other claims on a number of telomerase peptides including GV1001 were recently upheld by the Appeal Board of the European Patent Office.
Jakob Schmidt, CEO of Pharmexa says: "Evidence of the importance of telomerase as a target for immunotherapy against a wide range of cancers continues to mount. This supports our ongoing efforts with GV1001 in pancreatic, liver and lung cancer. Whereas the I540 peptide is restricted to use in a selected group of patients with the correct genetic background (HLA-A2), GV1001 is designed to work in all patients".
H�rsholm, November 2, 2007
Jakob Schmidt
Chief Executive Officer
Published: 14:24 02.11.2007 GMT+1 /HUGIN /Source: Pharmexa A/S /CSE: PHARMX /ISIN: DK0015966592
New clinical results support telomerase vaccination in breast cancer
Summary: US scientists have published promising clinical data on vaccination with a telomerase peptide in breast cancer. The peptide is claimed in Pharmexa's granted European patent.
A group of prominent scientists from the Abramson Cancer Center and the University of Pennsylvania School of Medicine has published new clinical data on vaccination with the telomerase peptide I540 in 19 metastatic breast cancer patients. The results were published in the recent edition of the scientific journal Cancer Research (Cancer Research; 67: (21). November 1, 2007).
The results show that vaccination with the I540 telomerase peptide led to changes in the tumor microenvironment, infiltration of T-cells and widespread tumor necrosis (tumor death). Furthermore, an exploratory analysis revealed that the median overall survival was significantly longer in those patients who achieved an immune response to the I540 peptide compared to patients who did not. Immune responses to a control peptide did not correlate with survival.
The I540 telomerase peptide and its use in cancer immunotherapy is claimed in Pharmexa's granted European patent. This and other claims on a number of telomerase peptides including GV1001 were recently upheld by the Appeal Board of the European Patent Office.
Jakob Schmidt, CEO of Pharmexa says: "Evidence of the importance of telomerase as a target for immunotherapy against a wide range of cancers continues to mount. This supports our ongoing efforts with GV1001 in pancreatic, liver and lung cancer. Whereas the I540 peptide is restricted to use in a selected group of patients with the correct genetic background (HLA-A2), GV1001 is designed to work in all patients".
H�rsholm, November 2, 2007
Jakob Schmidt
Chief Executive Officer
viele von uns haben geron als ankündigungsweltmeister betitelt. ich auch - und ich stehe dazu. so oft wurden leere versprechungen gemacht, die meilensteine aber dann doch nicht geliefert.
beim letzten conference call (fragerunde) gab es zu den massiven verzögerungen des hesc-programms spinal cord injury (reparatur mit oligodendriten) folgende interessante aussage von ceo okarma:
Q Hi. A couple of questions. One is I heard talk regarding stem cell therapy in human spinal cords. When are such tests expected to begin?
DR. OKARMA: Well, we've, we've discussed this many, many times, John. So, the, the IND is in final stages of preparation. We are advising folks that the clinical trial would begin some time between the first and second quarter of next year, assuming FDA concurrence with the IND application and approval by each site's institutional review board, scientific review committee and escrow committee and the consummation of the financial contract with each of the institutions; those are the specific gating items.
Q In, in terms of that, because I know it was in early ‘04 that it was stated that it would have begun in ‘05, and so I'm just wondering what has been holding it up over the last three to four years.
DR. OKARMA: Well, first, you're exaggerating the period of time over which it's, in your words, held up. The reality of this is that the bar imposed upon us by the FDA is extraordinarily high, and that comes from a number of reasons.
First and uniquely, when the sponsor, in this case, Geron, of an IND is the only entity on the planet publishing in peer reviewed literature the characteristics of the product being submitted, the FDA has no external benchmarks with which to compare our claims to. So that means that the amount of animal data – not only in terms of the number of animals, but the length of time that the animals must be maintained alive carrying these cells becomes extraordinarily difficult and costly and time consuming. So, for example, we have many hundreds of rats that are spinal cord injured, completely immune compromised, who have to carry these cells in their spinal cords for 9 to 12 months. That means that people in reverse isolation – because these animals have no immune system – have to manually express the urine of these animals 3 times a day, just to keep them alive. For every animal that we want to survive for 9 months, we have to injure and inject three to four because the mortality rate in this animal model is so high; these are not normal animals. They're spinal cord injured and are immune compromised. So the length of the animal studies, the number of animals in each study is huge. And as we've said many times, the size of this application will be precedent setting for the agency.
In addition to the data supporting the safety of the cells, we have a whole other application that is an IDE that characterizes the utility of the injection device that we had to invent, develop and validate in order to inject these cells safety in the operating room.
So this is a combined IND/IDE.
So the simple, bottom line answer to your question is we are functioning in a country that has a federal policy that has been crafted to slow this work down for religious and political reasons. And we have suffered through that set of restrictions and it has cost us time. It has cost us money. But it has not cost us precision in demonstrating to ourselves, the agency and our investor community that we know what we're doing here, and this application and this clinical trial is going to be groundbreaking in terms of what specifically we're able to do in spinal cord injury, and more generally, what this platform is going to do for other chronic diseases that cannot be attacked by traditional drugs.
beim letzten conference call (fragerunde) gab es zu den massiven verzögerungen des hesc-programms spinal cord injury (reparatur mit oligodendriten) folgende interessante aussage von ceo okarma:
Q Hi. A couple of questions. One is I heard talk regarding stem cell therapy in human spinal cords. When are such tests expected to begin?
DR. OKARMA: Well, we've, we've discussed this many, many times, John. So, the, the IND is in final stages of preparation. We are advising folks that the clinical trial would begin some time between the first and second quarter of next year, assuming FDA concurrence with the IND application and approval by each site's institutional review board, scientific review committee and escrow committee and the consummation of the financial contract with each of the institutions; those are the specific gating items.
Q In, in terms of that, because I know it was in early ‘04 that it was stated that it would have begun in ‘05, and so I'm just wondering what has been holding it up over the last three to four years.
DR. OKARMA: Well, first, you're exaggerating the period of time over which it's, in your words, held up. The reality of this is that the bar imposed upon us by the FDA is extraordinarily high, and that comes from a number of reasons.
First and uniquely, when the sponsor, in this case, Geron, of an IND is the only entity on the planet publishing in peer reviewed literature the characteristics of the product being submitted, the FDA has no external benchmarks with which to compare our claims to. So that means that the amount of animal data – not only in terms of the number of animals, but the length of time that the animals must be maintained alive carrying these cells becomes extraordinarily difficult and costly and time consuming. So, for example, we have many hundreds of rats that are spinal cord injured, completely immune compromised, who have to carry these cells in their spinal cords for 9 to 12 months. That means that people in reverse isolation – because these animals have no immune system – have to manually express the urine of these animals 3 times a day, just to keep them alive. For every animal that we want to survive for 9 months, we have to injure and inject three to four because the mortality rate in this animal model is so high; these are not normal animals. They're spinal cord injured and are immune compromised. So the length of the animal studies, the number of animals in each study is huge. And as we've said many times, the size of this application will be precedent setting for the agency.
In addition to the data supporting the safety of the cells, we have a whole other application that is an IDE that characterizes the utility of the injection device that we had to invent, develop and validate in order to inject these cells safety in the operating room.
So this is a combined IND/IDE.
So the simple, bottom line answer to your question is we are functioning in a country that has a federal policy that has been crafted to slow this work down for religious and political reasons. And we have suffered through that set of restrictions and it has cost us time. It has cost us money. But it has not cost us precision in demonstrating to ourselves, the agency and our investor community that we know what we're doing here, and this application and this clinical trial is going to be groundbreaking in terms of what specifically we're able to do in spinal cord injury, and more generally, what this platform is going to do for other chronic diseases that cannot be attacked by traditional drugs.
Geron says data show its cell-based therapeutic for spinal cord injury survives and exhibits remyelination for at least nine months following injection (GERN) 7.12 : Co announces that data show GRNOPC1, the co's human embryonic stem cell (hESC)-based therapeutic for spinal cord injury, survives and exhibits durable and robust human remyelination in spinal cord-injured rats for at least nine months following a single injection. The data also demonstrate that GRNOPC1 does not amplify neuropathic pain or the reaction to painful stimuli. This finding is in contrast to research that shows many other cell types, when injected into the spinal cord, amplify neuropathic pain, a common long-term complication of spinal cord injury in man. Thomas Okarma, GERN's president and CEO, stated "A comparison of the GRNOPC1-treated rats at nine months after injection against untreated control rats shows dramatic evidence of durable remyelination of intact rat axons traversing the lesion. These results show that a single injection of GRNOPC1 cells produces significant and persistent remyelination of the damaged spinal cord."
Antwort auf Beitrag Nr.: 32.328.618 von meislo am 07.11.07 17:45:01November 7, 2007 - 7:34 AM EST
Data Show Geron's Cell-Based Therapeutic for Spinal Cord Injury Survives and Exhibits Remyelination for at Least Nine Months Following Injection
Study Also Shows GRNOPC1 Does Not Amplify Neuropathic Pain Like Other Neural Progenitor Cells Injected Into Spinal Cord
Geron Corporation (Nasdaq:GERN) today announced that data show GRNOPC1, the company’s human embryonic stem cell (hESC)-based therapeutic for spinal cord injury, survives and exhibits durable and robust human remyelination in spinal cord-injured rats for at least nine months following a single injection.
Presented by Geron’s Arjun Natesan, Ph.D., at the Society for Neurosciences Annual Meeting in San Diego, the data also demonstrate that GRNOPC1 does not amplify neuropathic pain or the reaction to painful stimuli. This finding is in contrast to research that shows many other cell types, when injected into the spinal cord, amplify neuropathic pain, a common long-term complication of spinal cord injury in man.
“These important results speak to both the long-term safety and duration of effectiveness of GRNOPC1,” said Thomas B. Okarma, Ph.D., M.D., Geron’s president and CEO. “A comparison of the GRNOPC1-treated rats at nine months after injection against untreated control rats shows dramatic evidence of durable remyelination of intact rat axons traversing the lesion. These results show that a single injection of GRNOPC1 cells produces significant and persistent remyelination of the damaged spinal cord.”
Allodynia, a painful response to a stimulus that normally does not elicit pain, was assessed on large numbers of GRNOPC1-treated and untreated spinal cord-injured rats at three, six, and nine months post-injury. Both mechanical and cold stimuli were repeatedly applied at the injury site and on the paws by observers blinded to the animals’ treatment. Measurements included vocalization, attendance to the stimulus site, and avoidance behaviors. GRNOPC1-treated animals exhibited no increase in allodynia or neuropathic pain compared to untreated spinal cord-injured animals at any time.
GRNOPC1 is an allogeneic population of cells containing oligodendroglial progenitors that is intended for transplantation into the lesion site of patients with spinal cord injury to induce tissue repair. Geron’s development plan for the product calls for the filing of an Investigational New Drug (IND) Application with the U.S. Food and Drug Administration and, pending the agency’s review, initiation of human clinical trials in 2008.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
This news release may contain forward-looking statements made pursuant to the “safe harbor” provisions of the Private Securities Litigation Reform Act of 1995. Investors are cautioned that statements in this press release regarding potential applications of Geron’s human embryonic stem cell technology constitute forward-looking statements that involve risks and uncertainties, including, without limitation, risks inherent in the development and commercialization of potential products, uncertainty of clinical trial results or regulatory approvals or clearances, need for future capital, dependence upon collaborators and maintenance of our intellectual property rights. Actual results may differ materially from the results anticipated in these forward-looking statements. Additional information on potential factors that could affect our results and other risks and uncertainties are detailed from time to time in Geron’s periodic reports, including the quarterly report on Form 10-Q for the quarter ended September 30, 2007.
Geron
David L. Greenwood, Chief Financial Officer, 650-473-7765
info@geron.com
or
Media and Investors:
Russo Partners LLC
David Schull, 858-717-2310
david.schull@russopartnersllc.com
Tracey Milani, 619-814-3511
tracey.milani@russopartnersllc.com
http://www.investorvillage.com/smbd.asp?mb=1200&pt=qn
Data Show Geron's Cell-Based Therapeutic for Spinal Cord Injury Survives and Exhibits Remyelination for at Least Nine Months Following Injection
Study Also Shows GRNOPC1 Does Not Amplify Neuropathic Pain Like Other Neural Progenitor Cells Injected Into Spinal Cord
Geron Corporation (Nasdaq:GERN) today announced that data show GRNOPC1, the company’s human embryonic stem cell (hESC)-based therapeutic for spinal cord injury, survives and exhibits durable and robust human remyelination in spinal cord-injured rats for at least nine months following a single injection.
Presented by Geron’s Arjun Natesan, Ph.D., at the Society for Neurosciences Annual Meeting in San Diego, the data also demonstrate that GRNOPC1 does not amplify neuropathic pain or the reaction to painful stimuli. This finding is in contrast to research that shows many other cell types, when injected into the spinal cord, amplify neuropathic pain, a common long-term complication of spinal cord injury in man.
“These important results speak to both the long-term safety and duration of effectiveness of GRNOPC1,” said Thomas B. Okarma, Ph.D., M.D., Geron’s president and CEO. “A comparison of the GRNOPC1-treated rats at nine months after injection against untreated control rats shows dramatic evidence of durable remyelination of intact rat axons traversing the lesion. These results show that a single injection of GRNOPC1 cells produces significant and persistent remyelination of the damaged spinal cord.”
Allodynia, a painful response to a stimulus that normally does not elicit pain, was assessed on large numbers of GRNOPC1-treated and untreated spinal cord-injured rats at three, six, and nine months post-injury. Both mechanical and cold stimuli were repeatedly applied at the injury site and on the paws by observers blinded to the animals’ treatment. Measurements included vocalization, attendance to the stimulus site, and avoidance behaviors. GRNOPC1-treated animals exhibited no increase in allodynia or neuropathic pain compared to untreated spinal cord-injured animals at any time.
GRNOPC1 is an allogeneic population of cells containing oligodendroglial progenitors that is intended for transplantation into the lesion site of patients with spinal cord injury to induce tissue repair. Geron’s development plan for the product calls for the filing of an Investigational New Drug (IND) Application with the U.S. Food and Drug Administration and, pending the agency’s review, initiation of human clinical trials in 2008.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
This news release may contain forward-looking statements made pursuant to the “safe harbor” provisions of the Private Securities Litigation Reform Act of 1995. Investors are cautioned that statements in this press release regarding potential applications of Geron’s human embryonic stem cell technology constitute forward-looking statements that involve risks and uncertainties, including, without limitation, risks inherent in the development and commercialization of potential products, uncertainty of clinical trial results or regulatory approvals or clearances, need for future capital, dependence upon collaborators and maintenance of our intellectual property rights. Actual results may differ materially from the results anticipated in these forward-looking statements. Additional information on potential factors that could affect our results and other risks and uncertainties are detailed from time to time in Geron’s periodic reports, including the quarterly report on Form 10-Q for the quarter ended September 30, 2007.
Geron
David L. Greenwood, Chief Financial Officer, 650-473-7765
info@geron.com
or
Media and Investors:
Russo Partners LLC
David Schull, 858-717-2310
david.schull@russopartnersllc.com
Tracey Milani, 619-814-3511
tracey.milani@russopartnersllc.com
http://www.investorvillage.com/smbd.asp?mb=1200&pt=qn
Forscher erzielen Durchbruch beim Klonen von Primaten
Kritiker befürchten Anwendung des Verfahrens beim Menschen
Primaten erstmals geklont (Foto: pixelio.de)
Beaverton (pte/14.11.2007/13:56) - Wissenschaftlern am Oregon National Primate Research Center (ONPRC) http://onprc.ohsu.edu ist es nach eigenen Angaben gelungen, dutzende Embryos von erwachsenen Primaten zu klonen. Wie der britische Independent berichtet, kostete der Erfolg mehr als 100 Versuche, bei denen es nicht geglückt war, lebensfähige Primaten-Embryos zu erzeugen. Obwohl die Forschungsergebnisse noch nicht offiziell bestätigt sind, sprechen Befürworter bereits von einem großen Fortschritt für die Forschung. Kritiker hingegen warnen davor, dass damit der erste Schritt zum Klonen von Menschen getan sei, hatte man doch bisher angenommen, dass das Klonen von Primaten - und so auch vom Menschen - prinzipiell nicht möglich sei.
"Die Effizienz beim Klonen von Tieren liegt derzeit bei zehn Prozent", erläutert Franco Laccone vom Department für Medizinische Genetik der Medizinischen Universität Wien http://www.meduniwien.ac.at/humangenetik gegenüber pressetext. Klonforscher hätten bislang vor allem mit technischen Problemen zu kämpfen. Ein Team von Wissenschaftlern unter Shoukhrat Mitalipov am Assisted Reproductive Technologies and Embryonic Stem Cell Core Laboratory des ONPRC hat es nun geschafft, mit Hilfe einer neu entwickelten Methode zahlreiche geklonte Rhesus-Affen-Embryos zu erzeugen, die sich in die Gebärmutter verpflanzen ließen. Embryonale Stammzellen, die diesen entnommen wurden, habe man laut den Forschern zum Züchten von Herzzellen und Neuronen verwenden können. Bis sich schlussendlich der Erfolg einstellte, haben die Wissenschaftler angeblich über 100 geklonte Embryos mittels des so genannten "reproduktiven Klonens" in die Gebärmutter von 50 Rhesus-Affen-Weibchen eingesetzt. Keine dieser Aktionen habe jedoch zu einer Vollzeitschwangerschaft geführt. Wie einer der Forscher erklärte, habe man aufgrund der geringen Erfolgsrate beim Klonen wahrscheinlich nur zu wenige Embryos verwendet und folglich Pech gehabt.
Neben der Problematik im technischen Bereich sind es aber vor allem Fragen zum grundrechtlichen und bioethischen Status von auf diese Weise erzeugten Klonen, die immer wieder heiße Diskussionen auslösen. "Das Problem ist, dass die Forschung in diesem Bereich viel schneller fortschreitet als die Gesetzgebung", so Laccone. Dennoch sei jetzt der richtige Zeitpunkt, um wichtige Fragen zu diskutieren und sich gesetzliche Regelungen zu überlegen. Besonders der Status des Embryos in vitro vor der Einnistung in den Mutterleib gilt als heftig umstritten. Nach Meinung vieler Experten sei mit der Verschmelzung der Vorkerne von Ei- und Samenzelle zum Hauptkern der Zygote die Schaffung menschlichen Lebens bereits vollzogen. Deshalb sei ein derartiges Leben auch unter den Schutz der Menschenwürde zu stellen. Wie eine Expertengruppe des Institute for Advanced Studies http://www.ias.unu.edu in einem Bericht an die UNO feststellt, sei man sich über das Verbot des Klonens von Menschen und der Forschung in diesem Bereich weitestgehend uneinig. Ein Versuch, das therapeutische und das reproduktive Klonen weltweit zu regeln, ist vor zwei Jahren gescheitert.
In der Vergangenheit gab es bereits einige, auch auf viel Geld spekulierende Ankündigungen, Menschen klonen zu wollen. Zumeist handelte es sich dabei allerdings nur um große Worte mit wenig faktischem Hintergrund. Auch der südkoreanische Wissenschaftler Woo Sook Hwang, der 2004 für sich in Anspruch nahm, den ersten Menschen erfolgreich geklont zu haben, entpuppte sich als Fälscher. Das erste geklonte Säugetier der Welt war das im Jahr 1996 zur Welt gekommene Schaf Dolly. Es lebte nur sechs Jahre, nur halb so lang wie ein gewöhnliches Schaf, und litt an Alterskrankheiten. (Ende)
Kritiker befürchten Anwendung des Verfahrens beim Menschen
Primaten erstmals geklont (Foto: pixelio.de)
Beaverton (pte/14.11.2007/13:56) - Wissenschaftlern am Oregon National Primate Research Center (ONPRC) http://onprc.ohsu.edu ist es nach eigenen Angaben gelungen, dutzende Embryos von erwachsenen Primaten zu klonen. Wie der britische Independent berichtet, kostete der Erfolg mehr als 100 Versuche, bei denen es nicht geglückt war, lebensfähige Primaten-Embryos zu erzeugen. Obwohl die Forschungsergebnisse noch nicht offiziell bestätigt sind, sprechen Befürworter bereits von einem großen Fortschritt für die Forschung. Kritiker hingegen warnen davor, dass damit der erste Schritt zum Klonen von Menschen getan sei, hatte man doch bisher angenommen, dass das Klonen von Primaten - und so auch vom Menschen - prinzipiell nicht möglich sei.
"Die Effizienz beim Klonen von Tieren liegt derzeit bei zehn Prozent", erläutert Franco Laccone vom Department für Medizinische Genetik der Medizinischen Universität Wien http://www.meduniwien.ac.at/humangenetik gegenüber pressetext. Klonforscher hätten bislang vor allem mit technischen Problemen zu kämpfen. Ein Team von Wissenschaftlern unter Shoukhrat Mitalipov am Assisted Reproductive Technologies and Embryonic Stem Cell Core Laboratory des ONPRC hat es nun geschafft, mit Hilfe einer neu entwickelten Methode zahlreiche geklonte Rhesus-Affen-Embryos zu erzeugen, die sich in die Gebärmutter verpflanzen ließen. Embryonale Stammzellen, die diesen entnommen wurden, habe man laut den Forschern zum Züchten von Herzzellen und Neuronen verwenden können. Bis sich schlussendlich der Erfolg einstellte, haben die Wissenschaftler angeblich über 100 geklonte Embryos mittels des so genannten "reproduktiven Klonens" in die Gebärmutter von 50 Rhesus-Affen-Weibchen eingesetzt. Keine dieser Aktionen habe jedoch zu einer Vollzeitschwangerschaft geführt. Wie einer der Forscher erklärte, habe man aufgrund der geringen Erfolgsrate beim Klonen wahrscheinlich nur zu wenige Embryos verwendet und folglich Pech gehabt.
Neben der Problematik im technischen Bereich sind es aber vor allem Fragen zum grundrechtlichen und bioethischen Status von auf diese Weise erzeugten Klonen, die immer wieder heiße Diskussionen auslösen. "Das Problem ist, dass die Forschung in diesem Bereich viel schneller fortschreitet als die Gesetzgebung", so Laccone. Dennoch sei jetzt der richtige Zeitpunkt, um wichtige Fragen zu diskutieren und sich gesetzliche Regelungen zu überlegen. Besonders der Status des Embryos in vitro vor der Einnistung in den Mutterleib gilt als heftig umstritten. Nach Meinung vieler Experten sei mit der Verschmelzung der Vorkerne von Ei- und Samenzelle zum Hauptkern der Zygote die Schaffung menschlichen Lebens bereits vollzogen. Deshalb sei ein derartiges Leben auch unter den Schutz der Menschenwürde zu stellen. Wie eine Expertengruppe des Institute for Advanced Studies http://www.ias.unu.edu in einem Bericht an die UNO feststellt, sei man sich über das Verbot des Klonens von Menschen und der Forschung in diesem Bereich weitestgehend uneinig. Ein Versuch, das therapeutische und das reproduktive Klonen weltweit zu regeln, ist vor zwei Jahren gescheitert.
In der Vergangenheit gab es bereits einige, auch auf viel Geld spekulierende Ankündigungen, Menschen klonen zu wollen. Zumeist handelte es sich dabei allerdings nur um große Worte mit wenig faktischem Hintergrund. Auch der südkoreanische Wissenschaftler Woo Sook Hwang, der 2004 für sich in Anspruch nahm, den ersten Menschen erfolgreich geklont zu haben, entpuppte sich als Fälscher. Das erste geklonte Säugetier der Welt war das im Jahr 1996 zur Welt gekommene Schaf Dolly. Es lebte nur sechs Jahre, nur halb so lang wie ein gewöhnliches Schaf, und litt an Alterskrankheiten. (Ende)
sollte geron eingentlich schon geleistet haben... hmm, wer weiß mehr dazu?
Telomerase Enzyme Structure Provides Significant New Target For Anti-cancer Therapies
ScienceDaily (Nov. 14, 2007) — Inappropriate activation of a single enzyme, telomerase, is associated with the uncontrollable proliferation of cells seen in as many as 90 percent of all of human cancers. Since the mid-1990s, when telomerase was first identified in human tumors, scientists have eyed the enzyme as an ideal target for developing broadly effective anti-cancer drugs.
Now, researchers working at The Wistar Institute have brought this goal closer by deciphering the three-dimensional structure of a domain, or region, of the telomerase molecule essential for the activity of the enzyme. The findings, published November 13 in the journal Structure, may help scientists develop strategies to design the first direct inhibitors of telomerase.
Telomerase also has been shown to play a central role in normal aging, and the new study may shed light on that vital life process as well. The potential for creating new cancer treatments, however, is the most important immediate implication of the study.
"Knowing the physical structure of this complex will give pharmaceutical companies a direct target for designing drugs that disrupt a mechanism that telomerase uses to assemble itself," says Emmanuel Skordalakes, Ph.D., an assistant professor in the Gene Expression and Regulation Program at Wistar and senior author on the study. "Such drugs could well have significant anti-cancer activity."
Telomerase is essential for normal cell division and survival, and has been associated with aging and cancer. In humans, the usual role of telomerase is to add multiple repeats of a short length of DNA to the ends of chromosomes, known as telomeres, thus preventing damage and the loss of genetic information during DNA replication. It performs this critical service in developing embryos and in a few specialized cell lines, including stem cells.
In normal adult cells, however, telomerase is switched off almost entirely to prevent the dangers of runaway cell proliferation. This lack of telomerase activity is also associated with normal aging and underlies a seminal observation known as the Hayflick limit. At Wistar in the 1960s, Leonard Hayflick, Ph.D., noted that cells in culture divide only about 50 times before dying. Later, scientists tied this effect to the shortening of telomeres with each cell division when telomerase is no longer active in the cell.
Cancer cells, however, often regain the ability to produce telomerase, permitting them to replicate indefinitely. Though scientists have sought ways to inhibit this enzyme, a lack of detailed information on the enzyme's structure has hindered progress.
Prior studies have shown that telomerase is made up of multiple protein components and a stretch of RNA that is used as a template to create the short DNA repeats that are added to the ends of chromosomes. In order for telomerase to function, the RNA and protein components of telomerase must interact to form a stable complex capable of DNA replication. This interaction occurs mainly on the so-called TRBD domain, which plays an essential role in complex formation and full assembly of the enzyme.
"Studies show if you delete the TRBD domain from telomerase, the enzyme is inactive because it can no longer assemble with RNA," Skordalakes says. "Without the RNA, the enzyme can no longer replicate telomeres."
To get a clear view of this interaction, Skordalakes and co-workers obtained the three-dimensional structure of TRBD using X-ray crystallography, a technique that analyzes the diffraction patterns of X-rays beamed at crystals of a molecule to determine the molecule's atomic structure.
Their studies reveal that the TRBD domain is shaped like a boomerang, with a structural organization that leads to the formation of a narrow well-defined pocket on the surface of the protein that enables the enzyme to bind the single-stranded RNA used as a template for the DNA repeats.
A second RNA-binding site is formed by a large cavity that serves as an extension of the single-strandedRNA-binding pocket. The extent of these RNA interactions indicates the important role of this domain in stabilizing the complex, Skordalakes says.
The research was supported in part by the Commonwealth Universal Research Enhancement Program of the Pennsylvania Department of Health.
Adapted from materials provided by The Wistar Institute.
Telomerase Enzyme Structure Provides Significant New Target For Anti-cancer Therapies
ScienceDaily (Nov. 14, 2007) — Inappropriate activation of a single enzyme, telomerase, is associated with the uncontrollable proliferation of cells seen in as many as 90 percent of all of human cancers. Since the mid-1990s, when telomerase was first identified in human tumors, scientists have eyed the enzyme as an ideal target for developing broadly effective anti-cancer drugs.
Now, researchers working at The Wistar Institute have brought this goal closer by deciphering the three-dimensional structure of a domain, or region, of the telomerase molecule essential for the activity of the enzyme. The findings, published November 13 in the journal Structure, may help scientists develop strategies to design the first direct inhibitors of telomerase.
Telomerase also has been shown to play a central role in normal aging, and the new study may shed light on that vital life process as well. The potential for creating new cancer treatments, however, is the most important immediate implication of the study.
"Knowing the physical structure of this complex will give pharmaceutical companies a direct target for designing drugs that disrupt a mechanism that telomerase uses to assemble itself," says Emmanuel Skordalakes, Ph.D., an assistant professor in the Gene Expression and Regulation Program at Wistar and senior author on the study. "Such drugs could well have significant anti-cancer activity."
Telomerase is essential for normal cell division and survival, and has been associated with aging and cancer. In humans, the usual role of telomerase is to add multiple repeats of a short length of DNA to the ends of chromosomes, known as telomeres, thus preventing damage and the loss of genetic information during DNA replication. It performs this critical service in developing embryos and in a few specialized cell lines, including stem cells.
In normal adult cells, however, telomerase is switched off almost entirely to prevent the dangers of runaway cell proliferation. This lack of telomerase activity is also associated with normal aging and underlies a seminal observation known as the Hayflick limit. At Wistar in the 1960s, Leonard Hayflick, Ph.D., noted that cells in culture divide only about 50 times before dying. Later, scientists tied this effect to the shortening of telomeres with each cell division when telomerase is no longer active in the cell.
Cancer cells, however, often regain the ability to produce telomerase, permitting them to replicate indefinitely. Though scientists have sought ways to inhibit this enzyme, a lack of detailed information on the enzyme's structure has hindered progress.
Prior studies have shown that telomerase is made up of multiple protein components and a stretch of RNA that is used as a template to create the short DNA repeats that are added to the ends of chromosomes. In order for telomerase to function, the RNA and protein components of telomerase must interact to form a stable complex capable of DNA replication. This interaction occurs mainly on the so-called TRBD domain, which plays an essential role in complex formation and full assembly of the enzyme.
"Studies show if you delete the TRBD domain from telomerase, the enzyme is inactive because it can no longer assemble with RNA," Skordalakes says. "Without the RNA, the enzyme can no longer replicate telomeres."
To get a clear view of this interaction, Skordalakes and co-workers obtained the three-dimensional structure of TRBD using X-ray crystallography, a technique that analyzes the diffraction patterns of X-rays beamed at crystals of a molecule to determine the molecule's atomic structure.
Their studies reveal that the TRBD domain is shaped like a boomerang, with a structural organization that leads to the formation of a narrow well-defined pocket on the surface of the protein that enables the enzyme to bind the single-stranded RNA used as a template for the DNA repeats.
A second RNA-binding site is formed by a large cavity that serves as an extension of the single-strandedRNA-binding pocket. The extent of these RNA interactions indicates the important role of this domain in stabilizing the complex, Skordalakes says.
The research was supported in part by the Commonwealth Universal Research Enhancement Program of the Pennsylvania Department of Health.
Adapted from materials provided by The Wistar Institute.
Der Krebsstammzelle auf der Spur
von Sascha Karberg
Chemotherapie und Bestrahlung zerstören möglicherweise nicht die Wachstumsmaschinen der tödlichen Krankheit. Forscher hoffen, ihnen langsam näher zu kommen.
Krebspatienten sind erleichtert, wenn Chemotherapie und Bestrahlung einen Tumor weitgehend zerstört haben. Allzu oft stellt sich aber heraus, dass die Reste wieder zu wachsen beginnen.
Offenbar kommt es nicht darauf an, wie viele Krebszellen abgetötet werden, sondern welche. Denn seit ein paar Jahren verdichten sich Hinweise, dass Krebszellen nicht gleich Krebszellen sind. "Wahrscheinlich entsteht die Mehrzahl aller Krebserkrankungen aus Körperstammzellen, die aufgrund von Genmutationen zu sogenannten Krebsstammzellen entartet sind", sagt Otmar Wiestler, Chef des Krebsforschungszentrums Heidelberg. Diese Krebsstammzellen machen nur ein bis zwei Prozent eines Tumors aus, scheinen aber für Entstehung, Wachstum und Streuung der Geschwulst von entscheidender Bedeutung zu sein. Damit sind sie in den Mittelpunkt des Interesses von Biotech- und Pharmafirmen gerückt.
"Erstaunliche Ähnlichkeiten"
Wie Krebsstammzellen zerstörte Tumoren wieder aufbauenAuf die Spur der Krebsstammzellen kam der kanadische Forscher John Dick 1997 als er menschliche Tumorzellen in Mäuse ohne Immunsystem transferierte. Eigentlich hatte Dick erwartet, dass die meisten transplantierten Zellen zu Tumoren auswachsen würden. Doch nur wenige Zellen waren dazu in der Lage. Seitdem nehmen Krebsforscher diese zur Krebsbildung fähigen Zellen unter die Lupe und entdecken "erstaunliche Ähnlichkeiten" zu normalen Stammzellen, sagt Wiestler. So werden Krebsstammzellen von ganz ähnlichen Signalstoffen gesteuert und besiedeln auch die gleichen Orte im Gewebe, wo sie optimal ernährt werden können, sogenannte Stammzellnischen.
"Es gibt kaum eine an Krebs forschende Pharma- oder Biotechfirma, die sich nicht für Krebsstammzellen interessieren würde", sagt Wiestler, denn offenbar sind es die Krebsstammzellen, die den bisherigen Behandlungsmethoden entgehen. So greifen herkömmliche Medikamente Zellen an, die sich schnell teilen - eine typische Eigenschaft von Krebsgewebe. Gerade die Krebsstammzellen aber teilen sich relativ langsam.
"Wenn unsere Vermutung stimmt, dass besonders die Krebsstammzellen resistent gegen die bisherigen Therapien sind, dann müssen sich neue Therapien daran messen lassen, ob sie auch Krebsstammzellen erreichen", sagt Wiestler. Eine weitere Herausforderung: Die Therapien dürfen nur die Krebsstammzellen angreifen, nicht aber die gesunden Stammzellen.
Keine Wunderwaffe gegen Krebs
"Nur weil man jetzt Krebsstammzellen kennt, hat man nicht automatisch eine Wunderwaffe gegen den Krebs in der Hand", sagt Harald Fricke, Forschungschef der Biotechfirma Apogenix, eine Ausgründung des Deutschen Krebsforschungszentrums (DKFZ). Man wisse noch zu wenig über Krebsstammzellen, um sie gezielt angreifen zu können. Apogenix arbeitet deswegen an Therapien, die auf normale Krebszellen ebenso wirken wie auf Krebsstammzellen.
So wies Giorgio Stassi von der Universität Palermo jetzt nach, dass sich beide Zellarten mit dem gleichen Mechanismus gegen die Chemotherapie schützen: Sie produzieren ständig Interleukin-4. Dieser Botenstoff blockiert das Selbstmordprogramm, das in allen Körperzellen angelegt ist, die sogenannte Apoptose.
Als Stassis Team die Wirkung von Interleukin-4 blockierte, wurden die Zellen wieder empfänglich für Medikamente. Das Apoptoseprogramm wurde aktiviert, und die Tumorzellen konnten getötet werden.
Eine Reihe von Hemmstoffen
In Zusammenarbeit mit Apogenix testen die Forscher jetzt eine Reihe von Hemmstoffen gegen Interleukin-4. "Wir können die Apoptosesensitivität von Krebszellen und Krebsstammzellen wieder herstellen", ist Harald Fricke überzeugt.
Andreas Strasser vom Royal Melbourne Hospital warnt davor, die Rolle der Krebsstammzellen überzubewerten. Von einem regelrechten "Hype" spricht der Schweizer Krebsforscher. Die bisher vorliegenden Erkenntnisse beruhten meist auf Experimenten, bei denen menschliche Zellen in Mäuse transplantiert wurden. Ob sie sich im menschlichen Körper genauso verhielten, sei ungewiss.
Strasser glaubt zwar, dass mutierte Stammzellen Tumoren auslösen können. Ihr Anteil am Gewebe sei aber zu gering, um allein das Wachstum der Geschwulste voranzutreiben. Außerdem sei offen, ob nur Krebsstammzellen Tochtergeschwülste bilden können. "Es ist Zufall, welche Tumorzelle erfolgreich eine Krebskolonie in einem anderen Organ startet", sagt Strasser. Solange diese Fragen ungeklärt sind, sei es besser "Medikamente zu entwickeln, die alle Tumorzellen angreifen".
von Sascha Karberg
Chemotherapie und Bestrahlung zerstören möglicherweise nicht die Wachstumsmaschinen der tödlichen Krankheit. Forscher hoffen, ihnen langsam näher zu kommen.
Krebspatienten sind erleichtert, wenn Chemotherapie und Bestrahlung einen Tumor weitgehend zerstört haben. Allzu oft stellt sich aber heraus, dass die Reste wieder zu wachsen beginnen.
Offenbar kommt es nicht darauf an, wie viele Krebszellen abgetötet werden, sondern welche. Denn seit ein paar Jahren verdichten sich Hinweise, dass Krebszellen nicht gleich Krebszellen sind. "Wahrscheinlich entsteht die Mehrzahl aller Krebserkrankungen aus Körperstammzellen, die aufgrund von Genmutationen zu sogenannten Krebsstammzellen entartet sind", sagt Otmar Wiestler, Chef des Krebsforschungszentrums Heidelberg. Diese Krebsstammzellen machen nur ein bis zwei Prozent eines Tumors aus, scheinen aber für Entstehung, Wachstum und Streuung der Geschwulst von entscheidender Bedeutung zu sein. Damit sind sie in den Mittelpunkt des Interesses von Biotech- und Pharmafirmen gerückt.
"Erstaunliche Ähnlichkeiten"
Wie Krebsstammzellen zerstörte Tumoren wieder aufbauenAuf die Spur der Krebsstammzellen kam der kanadische Forscher John Dick 1997 als er menschliche Tumorzellen in Mäuse ohne Immunsystem transferierte. Eigentlich hatte Dick erwartet, dass die meisten transplantierten Zellen zu Tumoren auswachsen würden. Doch nur wenige Zellen waren dazu in der Lage. Seitdem nehmen Krebsforscher diese zur Krebsbildung fähigen Zellen unter die Lupe und entdecken "erstaunliche Ähnlichkeiten" zu normalen Stammzellen, sagt Wiestler. So werden Krebsstammzellen von ganz ähnlichen Signalstoffen gesteuert und besiedeln auch die gleichen Orte im Gewebe, wo sie optimal ernährt werden können, sogenannte Stammzellnischen.
"Es gibt kaum eine an Krebs forschende Pharma- oder Biotechfirma, die sich nicht für Krebsstammzellen interessieren würde", sagt Wiestler, denn offenbar sind es die Krebsstammzellen, die den bisherigen Behandlungsmethoden entgehen. So greifen herkömmliche Medikamente Zellen an, die sich schnell teilen - eine typische Eigenschaft von Krebsgewebe. Gerade die Krebsstammzellen aber teilen sich relativ langsam.
"Wenn unsere Vermutung stimmt, dass besonders die Krebsstammzellen resistent gegen die bisherigen Therapien sind, dann müssen sich neue Therapien daran messen lassen, ob sie auch Krebsstammzellen erreichen", sagt Wiestler. Eine weitere Herausforderung: Die Therapien dürfen nur die Krebsstammzellen angreifen, nicht aber die gesunden Stammzellen.
Keine Wunderwaffe gegen Krebs
"Nur weil man jetzt Krebsstammzellen kennt, hat man nicht automatisch eine Wunderwaffe gegen den Krebs in der Hand", sagt Harald Fricke, Forschungschef der Biotechfirma Apogenix, eine Ausgründung des Deutschen Krebsforschungszentrums (DKFZ). Man wisse noch zu wenig über Krebsstammzellen, um sie gezielt angreifen zu können. Apogenix arbeitet deswegen an Therapien, die auf normale Krebszellen ebenso wirken wie auf Krebsstammzellen.
So wies Giorgio Stassi von der Universität Palermo jetzt nach, dass sich beide Zellarten mit dem gleichen Mechanismus gegen die Chemotherapie schützen: Sie produzieren ständig Interleukin-4. Dieser Botenstoff blockiert das Selbstmordprogramm, das in allen Körperzellen angelegt ist, die sogenannte Apoptose.
Als Stassis Team die Wirkung von Interleukin-4 blockierte, wurden die Zellen wieder empfänglich für Medikamente. Das Apoptoseprogramm wurde aktiviert, und die Tumorzellen konnten getötet werden.
Eine Reihe von Hemmstoffen
In Zusammenarbeit mit Apogenix testen die Forscher jetzt eine Reihe von Hemmstoffen gegen Interleukin-4. "Wir können die Apoptosesensitivität von Krebszellen und Krebsstammzellen wieder herstellen", ist Harald Fricke überzeugt.
Andreas Strasser vom Royal Melbourne Hospital warnt davor, die Rolle der Krebsstammzellen überzubewerten. Von einem regelrechten "Hype" spricht der Schweizer Krebsforscher. Die bisher vorliegenden Erkenntnisse beruhten meist auf Experimenten, bei denen menschliche Zellen in Mäuse transplantiert wurden. Ob sie sich im menschlichen Körper genauso verhielten, sei ungewiss.
Strasser glaubt zwar, dass mutierte Stammzellen Tumoren auslösen können. Ihr Anteil am Gewebe sei aber zu gering, um allein das Wachstum der Geschwulste voranzutreiben. Außerdem sei offen, ob nur Krebsstammzellen Tochtergeschwülste bilden können. "Es ist Zufall, welche Tumorzelle erfolgreich eine Krebskolonie in einem anderen Organ startet", sagt Strasser. Solange diese Fragen ungeklärt sind, sei es besser "Medikamente zu entwickeln, die alle Tumorzellen angreifen".
Forscher programmieren Haut- zu Stammzellen um
Wichtiger Durchbruch bei der Erzeugung maßgeschneiderter Stammzellen: Forschern aus Japan und den USA ist es gelungen, menschliche Haut- und Bindegewebszellen umzuprogrammieren. Wird die ethisch umstrittene Nutzung von Embyros überflüssig?
Sie gelten als mögliche Wunderwaffe im Kampf gegen Parkinson, Diabetes oder Herzkrankheiten: embryonale Stammzellen. Bisher können sie nur aus Embryonen gewonnen werden, die bei der Entnahme zerstört werden. Ein ethisch äußerst umstrittenes Verfahren (mehr...). Deshalb suchen Forscher schon seit längerem nach Alternativen. Jetzt berichten ein japanisches und ein US-Wissenschaftlerteam über entscheidende Erfolge, die unabhängig voneinander geglückt sind.
http://www.spiegel.de/wissenschaft/mensch/0,1518,518531,00.h…
Wichtiger Durchbruch bei der Erzeugung maßgeschneiderter Stammzellen: Forschern aus Japan und den USA ist es gelungen, menschliche Haut- und Bindegewebszellen umzuprogrammieren. Wird die ethisch umstrittene Nutzung von Embyros überflüssig?
Sie gelten als mögliche Wunderwaffe im Kampf gegen Parkinson, Diabetes oder Herzkrankheiten: embryonale Stammzellen. Bisher können sie nur aus Embryonen gewonnen werden, die bei der Entnahme zerstört werden. Ein ethisch äußerst umstrittenes Verfahren (mehr...). Deshalb suchen Forscher schon seit längerem nach Alternativen. Jetzt berichten ein japanisches und ein US-Wissenschaftlerteam über entscheidende Erfolge, die unabhängig voneinander geglückt sind.
http://www.spiegel.de/wissenschaft/mensch/0,1518,518531,00.h…
Antwort auf Beitrag Nr.: 32.499.001 von meislo am 20.11.07 18:46:15http://money.cnn.com/2007/11/20/news/companies/stem_cell/ind…
Antwort auf Beitrag Nr.: 32.499.412 von meislo am 20.11.07 19:18:53http://www.sueddeutsche.de/,tt7m1/wissen/artikel/197/143874/
okarma sieht den jüngsten 'durchbruch' gelassen:
Drug Firms Cool to Stem Cell Findings
By MARCUS WOHLSEN �
SAN FRANCISCO (AP) � Despite excitement among some scientists � and at the White House � about an embryo-free technique for creating human stem cells, reaction from companies that might turn the research into treatments was muted.
In two papers published Tuesday, researchers reported successfully programming ordinary human skin cells to behave like embryonic stem cells, which can theoretically be transformed into a variety of human tissues.
Biotech executives said the announcement is scientifically interesting. But they said the new technique of creating stem cells is even less likely to yield meaningful results soon than is the method using embryonic cells � which requires destroying embryos.
One executive, whose company's stem-cell treatments may soon enter human clinical trials, noted that the U.S. Food and Drug Administration is unlikely to quickly approve a regimen that requires a separate treatment be developed for each patient.
At South San Francisco-based Genentech Inc., one of the country's oldest and largest biotech companies, researchers did not seem poised to change course and leap on the new findings.
"We don't use stem cells, not because we're for them or against them, just because the way we make therapeutics doesn't require their use," said Robin Snyder, a Genentech spokeswoman.
The technique isn't likely "to bear any fruit," said Tom Okarma, president and chief executive of Geron Corp., a California biotech drug developer that has spent $100 million on human embryonic stem cell research.
"Most of the people who are doing this work and make the claim that this is going to change the therapeutic field really know nothing about cell therapy," Okarma said.
The scientists who pioneered the new approach have said that reprogramming an individual's own cells to mimic stem cells provides a way to create individually tailored transplant tissue unlikely to be rejected by that person's immune system.
But the process of getting the FDA to approve personalized treatments for medical use would ultimately prove far more expensive than using tissue grown from embryonic cells, Okarma said.
Menlo Park-based Geron hopes to start clinical trials next year for its long-promised stem cell treatment for spinal cord injuries. The company's stock fell six percent Tuesday following the research announcement.
At Advanced Cell Technology, Geron's chief rival in the race to create medical therapies using stem cells, the head of research hailed the new technique as revolutionary, though he advised calm.
Dr. Robert Lanza, chief science officer at Advanced Cell Technology, called the breakthrough the biological equivalent of the Wright Brothers' first airplane.
Still, he said any medical uses of stem cells developed using the new technique were many years away.
"I can't overemphasize the use of caution here," Lanza said. "These are not ready for prime time."
Large drug companies appeared far from ready to embrace the new stem cells.
Stem cells generally may have "high potential" for creating more effective medicines, said Laura Woodin, a spokeswoman for AstraZeneca PLC, known for its blockbuster anti-cholesterol drug Crestor and its anti-psychotic Seroquel. She too advised caution.
"It is too early to say how the studies announced today might affect any research we pursue in this area," Woodin said.
Drug Firms Cool to Stem Cell Findings
By MARCUS WOHLSEN �
SAN FRANCISCO (AP) � Despite excitement among some scientists � and at the White House � about an embryo-free technique for creating human stem cells, reaction from companies that might turn the research into treatments was muted.
In two papers published Tuesday, researchers reported successfully programming ordinary human skin cells to behave like embryonic stem cells, which can theoretically be transformed into a variety of human tissues.
Biotech executives said the announcement is scientifically interesting. But they said the new technique of creating stem cells is even less likely to yield meaningful results soon than is the method using embryonic cells � which requires destroying embryos.
One executive, whose company's stem-cell treatments may soon enter human clinical trials, noted that the U.S. Food and Drug Administration is unlikely to quickly approve a regimen that requires a separate treatment be developed for each patient.
At South San Francisco-based Genentech Inc., one of the country's oldest and largest biotech companies, researchers did not seem poised to change course and leap on the new findings.
"We don't use stem cells, not because we're for them or against them, just because the way we make therapeutics doesn't require their use," said Robin Snyder, a Genentech spokeswoman.
The technique isn't likely "to bear any fruit," said Tom Okarma, president and chief executive of Geron Corp., a California biotech drug developer that has spent $100 million on human embryonic stem cell research.
"Most of the people who are doing this work and make the claim that this is going to change the therapeutic field really know nothing about cell therapy," Okarma said.
The scientists who pioneered the new approach have said that reprogramming an individual's own cells to mimic stem cells provides a way to create individually tailored transplant tissue unlikely to be rejected by that person's immune system.
But the process of getting the FDA to approve personalized treatments for medical use would ultimately prove far more expensive than using tissue grown from embryonic cells, Okarma said.
Menlo Park-based Geron hopes to start clinical trials next year for its long-promised stem cell treatment for spinal cord injuries. The company's stock fell six percent Tuesday following the research announcement.
At Advanced Cell Technology, Geron's chief rival in the race to create medical therapies using stem cells, the head of research hailed the new technique as revolutionary, though he advised calm.
Dr. Robert Lanza, chief science officer at Advanced Cell Technology, called the breakthrough the biological equivalent of the Wright Brothers' first airplane.
Still, he said any medical uses of stem cells developed using the new technique were many years away.
"I can't overemphasize the use of caution here," Lanza said. "These are not ready for prime time."
Large drug companies appeared far from ready to embrace the new stem cells.
Stem cells generally may have "high potential" for creating more effective medicines, said Laura Woodin, a spokeswoman for AstraZeneca PLC, known for its blockbuster anti-cholesterol drug Crestor and its anti-psychotic Seroquel. She too advised caution.
"It is too early to say how the studies announced today might affect any research we pursue in this area," Woodin said.
November 27, 2007 - 7:31 AM EST
Geron Corporation to Present at Lazard Capital Markets Healthcare Conference
Geron Corporation (Nasdaq:GERN) today announced that Thomas B. Okarma, Ph.D., M.D., president and chief executive officer, will present an update of the company’s product development programs at 2:00 p.m. EST on Wednesday, Nov. 28, 2007, at the Lazard Capital Markets 4th Annual Healthcare Conference in New York City.
The update will include information about Geron’s portfolio of anti-cancer therapies, including its telomerase inhibitor drug (GRN163L) and telomerase therapeutic vaccine (GRNVAC1). The presentation will also include a review of the company’s human embryonic stem cell (hESC) development programs for spinal cord injury (GRNOPC1), heart disease (GRNCM1) and diabetes (GRNIC1).
An audio and slide Webcast of the presentation will be available at the following Website address: http://www.wsw.com/webcast/lz4/gern/.
A replay will be available at this address within 24 hours of the presentation and for a period of 30 days.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
http://www.investorvillage.com/smbd.asp?mb=1200&pt=qn
Geron Corporation to Present at Lazard Capital Markets Healthcare Conference
Geron Corporation (Nasdaq:GERN) today announced that Thomas B. Okarma, Ph.D., M.D., president and chief executive officer, will present an update of the company’s product development programs at 2:00 p.m. EST on Wednesday, Nov. 28, 2007, at the Lazard Capital Markets 4th Annual Healthcare Conference in New York City.
The update will include information about Geron’s portfolio of anti-cancer therapies, including its telomerase inhibitor drug (GRN163L) and telomerase therapeutic vaccine (GRNVAC1). The presentation will also include a review of the company’s human embryonic stem cell (hESC) development programs for spinal cord injury (GRNOPC1), heart disease (GRNCM1) and diabetes (GRNIC1).
An audio and slide Webcast of the presentation will be available at the following Website address: http://www.wsw.com/webcast/lz4/gern/.
A replay will be available at this address within 24 hours of the presentation and for a period of 30 days.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
http://www.investorvillage.com/smbd.asp?mb=1200&pt=qn
Motley Fool article on Stem cells
Stem Your Expectations of Stem-Cell Discoveries
Brian Orelli
November 28, 2007
After last week's fanfare about scientists turning skin cells into cells that resemble embryonic stem cells, you'd think that scientists had invented an immortality potion or something. Alas, I'm here to tell you that we're no closer to having stem-cell therapeutics than we were before the announcement.
That's not because I don't think stem cells have promise -- I certainly do. It's just that the recent discovery has a long way to go before it can catch up to the research currently being done with stem cells.
While the creation of pluripotent cells -- those that can become any of the hundreds of human cell types -- from a source other than an embryo certainly skirts around the ethical dilemma, they're far from being ready to go into humans.
The pluripotent cells were created by using a retrovirus to inject certain genes into the cells' DNA. Unfortunately, this could cause mutations as the injected DNA gets incorporated into the cells' chromosomes. Those mutations could cause the cells to grow uncontrollably, potentially leading to the formation of a tumor. An earlier study where this technique was used with mouse cells resulted in tumors in about 20% of the mice derived from the mouse pluripotent cells. Needless to say, a treatment that will cure a spinal injury while causing the patient to develop cancer isn't going to fly with the FDA.
Scientists will need to find another way to activate the pluripotent abilities that apparently lie within cells. Until then, companies such as Geron (Nasdaq: GERN), which is developing embryonic stem cell therapies, and StemCells (Nasdaq: STEM) or Cytori Therapeutics (Nasdaq: CYTX), which are using other types of stem cells, will have a head start and likely will be filing marketing applications with the FDA before any therapy arises from using pluripotent-modified skin cells.
The real winners
While the new discovery shouldn't hurt the near-term prospects for stem-cell companies, there's potential for the method to actually help pharmaceutical companies such as Merck (NYSE: MRK) or GlaxoSmithKline (NYSE: GSK). While the cells can't be used as therapies in humans yet, they could be used in laboratory research. A virtually endless supply of stem cells will almost certainly help advance drug discovery.
The stem-cell nirvana for scientists gets even better because they can theoretically create stem cells from any patient. That means scientists from Elan (NYSE: ELN), for example, could take cells from a patient with Alzheimer's disease, make them pluripotent, and then differentiate them into nerve cells (something that's already been done) to try to figure out more about the disease. While most of the scientific discoveries about diseases will probably be made in basic-science laboratories at universities, pharmaceutical companies -- big and small -- will surely use the published results to develop new disease-fighting drugs.
The other major advantage for drug developers is that they can use the cells to learn about toxicity of drugs before they hit the clinic. Having an endless supply of cells that could be made into liver or heart cells -- the two most common places for toxicity -- might have saved Pfizer (NYSE: PFE) hundreds of millions of dollars in developing Bextra.
Currently, there are no good models for determining whether a drug will be toxic in humans. Companies on both sides of the Atlantic have set up consortiums to try and develop better toxicity models, and these new cells could give them a head start in developing systems for detecting toxicity of drugs before they're tested in humans.
Final Foolish thoughts
While the discovery is certainly newsworthy and maybe even Nobel-worthy, it's not something that should cause investors to jump on or off the stem-cell bus. Any drug discoveries -- stem cell-based or not -- from this newly discovered technique are still many years away. Even for the most long-term investor, that's a long time to wait for a payoff.
Legal Information. ©1995-2006 The Motley Fool. All rights reserved.
http://www.fool.com/investing/high-growth/2007/11/28/stem-yo…
Stem Your Expectations of Stem-Cell Discoveries
Brian Orelli
November 28, 2007
After last week's fanfare about scientists turning skin cells into cells that resemble embryonic stem cells, you'd think that scientists had invented an immortality potion or something. Alas, I'm here to tell you that we're no closer to having stem-cell therapeutics than we were before the announcement.
That's not because I don't think stem cells have promise -- I certainly do. It's just that the recent discovery has a long way to go before it can catch up to the research currently being done with stem cells.
While the creation of pluripotent cells -- those that can become any of the hundreds of human cell types -- from a source other than an embryo certainly skirts around the ethical dilemma, they're far from being ready to go into humans.
The pluripotent cells were created by using a retrovirus to inject certain genes into the cells' DNA. Unfortunately, this could cause mutations as the injected DNA gets incorporated into the cells' chromosomes. Those mutations could cause the cells to grow uncontrollably, potentially leading to the formation of a tumor. An earlier study where this technique was used with mouse cells resulted in tumors in about 20% of the mice derived from the mouse pluripotent cells. Needless to say, a treatment that will cure a spinal injury while causing the patient to develop cancer isn't going to fly with the FDA.
Scientists will need to find another way to activate the pluripotent abilities that apparently lie within cells. Until then, companies such as Geron (Nasdaq: GERN), which is developing embryonic stem cell therapies, and StemCells (Nasdaq: STEM) or Cytori Therapeutics (Nasdaq: CYTX), which are using other types of stem cells, will have a head start and likely will be filing marketing applications with the FDA before any therapy arises from using pluripotent-modified skin cells.
The real winners
While the new discovery shouldn't hurt the near-term prospects for stem-cell companies, there's potential for the method to actually help pharmaceutical companies such as Merck (NYSE: MRK) or GlaxoSmithKline (NYSE: GSK). While the cells can't be used as therapies in humans yet, they could be used in laboratory research. A virtually endless supply of stem cells will almost certainly help advance drug discovery.
The stem-cell nirvana for scientists gets even better because they can theoretically create stem cells from any patient. That means scientists from Elan (NYSE: ELN), for example, could take cells from a patient with Alzheimer's disease, make them pluripotent, and then differentiate them into nerve cells (something that's already been done) to try to figure out more about the disease. While most of the scientific discoveries about diseases will probably be made in basic-science laboratories at universities, pharmaceutical companies -- big and small -- will surely use the published results to develop new disease-fighting drugs.
The other major advantage for drug developers is that they can use the cells to learn about toxicity of drugs before they hit the clinic. Having an endless supply of cells that could be made into liver or heart cells -- the two most common places for toxicity -- might have saved Pfizer (NYSE: PFE) hundreds of millions of dollars in developing Bextra.
Currently, there are no good models for determining whether a drug will be toxic in humans. Companies on both sides of the Atlantic have set up consortiums to try and develop better toxicity models, and these new cells could give them a head start in developing systems for detecting toxicity of drugs before they're tested in humans.
Final Foolish thoughts
While the discovery is certainly newsworthy and maybe even Nobel-worthy, it's not something that should cause investors to jump on or off the stem-cell bus. Any drug discoveries -- stem cell-based or not -- from this newly discovered technique are still many years away. Even for the most long-term investor, that's a long time to wait for a payoff.
Legal Information. ©1995-2006 The Motley Fool. All rights reserved.
http://www.fool.com/investing/high-growth/2007/11/28/stem-yo…
22:00:10 - $ 7,16 - 297
22:00:04 - $ 7,16 - 563344
21:59:59 - $ 7,16 - 300
After Hours
Last: $ 7.21
After Hours
High: $ 7.22
After Hours
Volume: 49,300
After Hours
Low: $ 6.9304
22:00:04 - $ 7,16 - 563344

21:59:59 - $ 7,16 - 300
After Hours
Last: $ 7.21
After Hours
High: $ 7.22
After Hours
Volume: 49,300
After Hours
Low: $ 6.9304
...da wollen wir doch hin, oder ????


aacr: keine neuen ergebnisse, eher die bestätigung der letzten zu grn163l aus dem cll trial vom juni, welche bekanntlich sehr durchwachsen waren.
eher bad news...
entnommen www.gerntalk.com
GRN163L 6 months later ...
The good news: No new cases of Grade 4 thrombocytopenia since the one CLL case in cohort 4. Thrombocytopenia can be mitigated by increasing the infusion time as needed. While PTT and reduction in red blood cells have been the biggest toxicity issues, it may be possible to go beyond cohort 5 before hitting the MTD.
The bad news: Still no evidence of telomerase inhibition or 163L-induced efficacy. Geron trying out new more sensitive and less invasive methods to look for telomerase inhibition - with the most promising one looking at normal hair follicle stem cells.
Telomerase activation/over-expression (from the Blasco group) ...
The good news: Mice with telomerase activation/over-expression from birth are 'more fit' at a given age, and those with telomerase activation/over-expression from birth AND an added tumor suppressor gene live significantly longer.
The bad news: If not given an added tumor suppressor gene, the mice get more cancers and have about the same average lifespan due to competing effects. It is felt that it would be extremely risky for an adult human to take a telomerase activitor drug, expecially prior to careful and long-term preclinical and clinical trials. [An adult human would presumably start out with many more pre-malignant cells than a human or mouse at birth and therefore cancer would be even more of a concern.] Privately one researcher used the word "irresponsible" to describe what TA Sciences is doing.
eher bad news...
entnommen www.gerntalk.com
GRN163L 6 months later ...
The good news: No new cases of Grade 4 thrombocytopenia since the one CLL case in cohort 4. Thrombocytopenia can be mitigated by increasing the infusion time as needed. While PTT and reduction in red blood cells have been the biggest toxicity issues, it may be possible to go beyond cohort 5 before hitting the MTD.
The bad news: Still no evidence of telomerase inhibition or 163L-induced efficacy. Geron trying out new more sensitive and less invasive methods to look for telomerase inhibition - with the most promising one looking at normal hair follicle stem cells.
Telomerase activation/over-expression (from the Blasco group) ...
The good news: Mice with telomerase activation/over-expression from birth are 'more fit' at a given age, and those with telomerase activation/over-expression from birth AND an added tumor suppressor gene live significantly longer.
The bad news: If not given an added tumor suppressor gene, the mice get more cancers and have about the same average lifespan due to competing effects. It is felt that it would be extremely risky for an adult human to take a telomerase activitor drug, expecially prior to careful and long-term preclinical and clinical trials. [An adult human would presumably start out with many more pre-malignant cells than a human or mouse at birth and therefore cancer would be even more of a concern.] Privately one researcher used the word "irresponsible" to describe what TA Sciences is doing.
Antwort auf Beitrag Nr.: 32.706.294 von LuckyCat am 08.12.07 21:43:28eher bad news...
..tja, das sehe ich mittlerweile leider auch so...
Pharmexa soll auf dem selben meeting sehr beeindruckende Daten präsentiert haben....
Ich habe mich nach langem Hin und Her dafür entschieden zu verkaufen.....
Allen GERON-Investierten wünsche ich " good luck "
Grüße bernie55
..tja, das sehe ich mittlerweile leider auch so...
Pharmexa soll auf dem selben meeting sehr beeindruckende Daten präsentiert haben....
Ich habe mich nach langem Hin und Her dafür entschieden zu verkaufen.....
Allen GERON-Investierten wünsche ich " good luck "
Grüße bernie55
bin heute zu börsenöffnung mit 70% raus.
ich seh momentan definitv mehr risiken als chancen.
geron, mein liebling. scheint, dass sich die liebe neu definieren muss...
ich seh momentan definitv mehr risiken als chancen.
geron, mein liebling. scheint, dass sich die liebe neu definieren muss...
Antwort auf Beitrag Nr.: 32.716.564 von LuckyCat am 10.12.07 17:06:31Ich habe vor ein paar Monaten erste Positionen abgebaut und werde wohl jetzt weiter veräußern. Meine Hoffnung ruhte vor allem auf gern163L, aber es tat sich einfach nichts und mittlerweile muss man wirklich bedenken haben.
greenhorn
greenhorn
gerons chart siecht dahin. selbst das 4 mio. $ milestone payment von merck & co. vor zwei tagen hat den kurs nicht beflügeln können.
geron spricht i.ü. von alternativen molekülen, die es im falle des scheiterns von 163l in der hinterhand hätte. kein trost, die entwicklung dauert dann wieder jahre, verschlingt 100 mio, $.
so hart es ist, geron ist in der riege der geldvernichter wieder einiges nach oben gerutscht. ob daran die stammzellversuche am menschen in 2008 etwas verändern werden??? don't bet on it.
geron spricht i.ü. von alternativen molekülen, die es im falle des scheiterns von 163l in der hinterhand hätte. kein trost, die entwicklung dauert dann wieder jahre, verschlingt 100 mio, $.
so hart es ist, geron ist in der riege der geldvernichter wieder einiges nach oben gerutscht. ob daran die stammzellversuche am menschen in 2008 etwas verändern werden??? don't bet on it.
REGENERATIVE MEDICINE | December 03, 2007
Eye on the Prize
The Company Who Cried Clinical Trial,” blazoned a headline on Wired magazine’s blog network this summer, with the blogger calling attention to how often Geron has said it was on the verge of a first-of-its-kind clinical trial that entails transplanting a type of neural cell into spinal cord-injured patients.
Even so, and with Geron researchers now saying the trial will begin in 2008, no one is tuning them out. Anticipation remains strong, not only because of what the test could portend for spinal cord repair, but because success would represent, according to Menlo Park, California-based Geron, the first time a product derived from embryonic stem cells (ES cells) has proved safe and effective for humans. This would be a boon for those who want to ease restrictions on federal funding for ES cell research. Should the trial fail, however, it could be a major setback for ES cells and the many labs hoping to channel them into countless therapies.
Such a product doesn’t come cheap. The investigational new drug application (IND) that Geron expects to file by year’s end will be some 20- to 30-thousand pages long. “Granted, this IND is larger than most,” notes Anthony Davies, Geron’s vice president of product development, “but that’s where the bar is, in terms of getting products into the clinic,” especially a product meant for the tricky confines of the spinal cord.
The research is part of Geron’s much larger, multiyear, human embryonic stem cell program, into which the company has sunk more than $100 million. Notes Davies, “This is biology; the raw materials are complex and expensive. This is the first time we”—or possibly anyone—“has tried to manufacture human embryonic stem cells under GMP [Good Manufacturing Practice Regulations] to meet FDA requirements.”
Geron has no products for patients yet, and the only return on investment to date comes from marketing its assay kits and selling cell lines through licensees. Still, Reni Benjamin, a research analyst at New York-based Rodman and Renshaw, remains optimistic about several prototypes inching through Geron’s pipeline. They include six different cell types that are slated for transplant therapies, respectively, for cardiovascular, central nervous system, pancreas, liver, and bone and joint disorders. Each cell type is derived from embryonic stem cells.
“Geron is master of its domain,” observes Benjamin. “It’s been a leader in the stem cell space for quite some time, has been slowly making headway, and has been able to successfully raise money from investors repeatedly, such that now it has a cash hoard of about $217 million.” Benjamin projects that, on the heels of a net loss of around $31 million last year, Geron this year will burn through another $42 million. The company needs to spend money, he allows, if it’s to attain its goal of becoming a commercial drug company that manufactures off-the-shelf cell therapies for entire patient populations—no small undertaking when you consider that, in the area of spinal cord injury alone, there are as many as 50,000 new cases worldwide.
China by itself is fueling demand for spinal cord intervention, notes Wise Young, the director of the W.M. Keck Center for Collaborative Neuroscience at Rutgers University. In 1995, a study of spinal cord injuries in Beijing, its rural surroundings, and Shanghai recorded only five cases per million people in a year in comparison to the United States’ 35 cases per million. Ten years later, a survey in the same regions in China counted a 10-fold increase in spinal cord injuries, to 65 cases per million. “I think China’s incidence in 1995 was much lower because people probably died before reaching tertiary care centers,” says Young, “and also because there was so little travel by motor vehicle.”
Motivated by the need for effective therapies, Young, in conjunction with the China Spinal Cord Injury Network, also has plans in 2008 to test a cell therapy in spinal cord-injured humans. Their approach will attempt to regenerate severed neurons by means of injecting umbilical cord blood stem cells and lithium, a drug known to stimulate the proliferation of cord cells.
Geron’s approach does not try to repair the spine’s severed nerve cells. Instead, it attempts to restore the benefit of myelin, the fat-like material that wraps around and insulates nerve cells’ axons, the long fibers that connect the cord to different parts of the body. Injury to the cord is accompanied by a significant loss of the myelin sheaths, rendering axons incapable of conducting signals between brain and muscles. The body’s oligodendrocyte cells, a type of neural cell, produce myelin, and so Geron’s plan is to remyelinate denuded axons by putting oligodendrocyte progenitor cells (OPCs) into the site and letting them do their thing, a strategy that might restore at least a modicum of spinal function. (OPCs are simply immature precursors of mature oligodendrocytes.)
When Geron was founded in the early 1990s, hardly anyone imagined mending an injured spinal cord. The company’s early mission—one conceived by Geron’s then-CEO Michael West—was to outsmart human aging. Toward that end, Geron’s scientists went in search of telomerase, the protein responsible for making a cell’s telomeres, the ends of chromosomes that appear to play a role in a cell’s aging process. Put telomerase into cells and it might lengthen telomeres as well as a person’s life. Inhibit telomerase, and you possibly might slow the reckless division of cancer cells.
Geron today has two telomerase drugs undergoing clinical trials—a vaccine and an inhibitor both aimed at cancer cells—and is researching how drugs that activate telomerase might counter the effects of aging and associated degenerative conditions.
Mouse ES cells had been isolated in the 1980s, and West came to realize that he might achieve his goal using those cells, if only they could be harvested from human embryos. In 1995 Geron began funding Jamie Thomson at the University of Wisconsin for that work and three years later, in May 1998, Geron received a call from Thomson saying he had succeeded. By that time, West had left the company, later taking up the reins at Advanced Cell Technology on the opposite coast. Thomas Okarma has headed Geron ever since.
Over the next two years, Geron’s gene therapy program, aimed at placing telomerase into cells, lost momentum. “The blush of gene therapy eroded away due to numerous problems,” says Jane Lebkowski, Geron’s senior vice president of regenerative medicine. Gene therapy everywhere slowed to a crawl when an 18-year-old patient named Jesse Gelsinger died after receiving gene therapy for a rare liver disorder at the University of Pennsylvania. During the same period, Geron’s stem cell program got stronger and stronger.
“I would have predicted Parkinson’s disease was going to be our first goal,” Lebkowski says today. The protocol seemed straightforward enough: Grow ES cells; steer them to yield dopamine-producing cells, the brain cells ravaged by Parkinson’s; and then transplant those cells into the appropriate brain regions. Researchers transplanting stem cells into Parkinson’s animal models weren’t demonstrating “terribly good results,” however, Lebkowski recounts. That’s when a new partnership emerged, along with a new direction in research.
Hans Keirstead at UC Irvine’s Reeve-Irvine Research Center was getting positive results when he implanted OPCs into the spinal cords of rats. Keirstead, a neurobiologist who did his postdoctoral training at Cambridge University, is one of the scientists who originally demonstrated that injury to the spinal cord is accompanied by a significant loss of the myelin that sheathes axons. He realized that no matter how many neurons had been severed at the injury site, axons off to the side sometimes escaped injury, although they were missing their myelin and couldn’t function. Hence Keirstead’s goal of re-sheathing them. It wasn’t long before Geron formed a working relationship with Keirstead, whose lab ended up the glad recipient of funds from both Geron and the University of California’s grant-matching BioSTAR program.
Results from testing their OPCs on lab rats with paralyzed hind limbs “are big enough to spur you on to humans,” says Lebkowski. Before treatment, they drag their hind legs. When injected with human OPCs seven days after the injury, they can plant their hind legs and support themselves as they move about. Scans of the animals validate that axons denuded of myelin have indeed been re-sheathed, says Gabriel Nistor, a postdoctoral researcher in Keirstead’s group. Remyelination isn’t the only factor that appears to benefit the rodents. The transplanted cells, Nistor says, also “secrete growth factors that can rescue some neurons from dying.”
Previous work on “shiver mice”—mice in which a deficiency of myelin causes a shivering-like tremor—gives credence to this approach, as well. When human oligodendrocytes are injected into these animals, their missing myelin is replaced with human myelin and the mice stop shaking.
Geron’s expectations for its human trials are fairly modest. “What we’re looking for isn’t necessarily that everyone is going to get up and walk,” notes Lebkowski. “But if you could improve even just one level of spinal function, especially in someone with a cervical [neck] injury, it could make a big difference.” Reducing a patient’s impairment by just one spinal column segment might re-establish some small hand or arm movement, restore a bit of bladder control, or improve some portion of heart or lung function. It’s been said about Christopher Reeve, for instance, who sustained his injury high in the cervical region, that had he regained one level of function, he might have been able to dispense with his ventilator.
To convert ES cells into OPCs, the scientists follow a 42-day protocol. The ES cells they start with come from Jamie Thomson’s very first cell line. The concern that these early cell lines might be contaminated because they were made with mouse feeder cells, Lebkowski says, is unwarranted. “As soon as Jamie’s cells arrived, we tested them for any pathogens that could have come from mouse feeder cells and any other agents they might have been exposed to,” she recounts. “We asked ourselves, ‘Are these cells suitable for human use? Are we going to pour millions of dollars into developing these cell lines for clinical use?’” The cells passed all their tests, and Geron subsequently developed a method that enables embryonic cells to be grown in the company of human, not mouse, feeder cells, thus avoiding any suspicion of pathogen contamination.
Up to 30 patients will participate in Geron’s Phase 1 trial, each one a “complete” patient, meaning someone with total paralysis. “The idea is to start conservative, with the worst patients who have the most to gain and the least to lose,” says Lebkowski. A transplant’s timing will be tremendously important, the researchers believe, since their animal studies indicate that cells need to be inserted into the spinal cord between seven to 14 days after an injury occurs. If they are implanted any earlier, the notorious inflammation that occurs immediately following a spinal injury might destroy the cells; any later, and scarring might impede their ability to reach those axons that need rewrapping.
Patients initially will be injected with 1 million cells, and if no toxic effect occurs, the doses will be increased up to 20 million cells. Geron has evidence that its OPCs do not trigger a recipient’s immune response. Still, to be on the safe side, the researchers will administer immunosuppressive drugs to their patients. For the purpose of injecting the cells, Geron has designed a special syringe and syringe holder that will allow a surgeon to release cells into the spinal cord at a defined depth for a set period of time without the cells squirting back out. These devices will require the U.S. Food and Drug Administration’s signoff, as well.
Geron’s pre-clinical animal studies have dragged on, says CEO Tom Okarma, primarily because of the large number of animals—some 2,000—in which Geron has had to test its OPCs. “What surprised us the first time we had a conversation with the agency,” says Okarma, “was how high the bar was going to be, in terms of numbers of animals and the length of time we had to keep the animals alive.”
“There are a number of unique things about this IND,” notes Okarma. “First of all, it’s almost unprecedented when the sponsor of an IND, in this case Geron, is the only producer of peer-reviewed literature that speaks to the technology being regulated. All the publications on glial cells in spinal cord injury made from human ES cells are Geron’s. The publications in the literature from non-Geron scientists are contaminated from bad results, because no one knows how to grow these cells the way we do.” When other researchers transplant their cells into animals, they report a high frequency of tumor formation, says Okarma, which the FDA “must obligatorily examine when they look at our application. So because of all that noise in the literature, the bar is higher.”
The fact that no clinical studies have ever been done with derivatives of embryonic cells makes ruling out a whole host of safety issues—from whether the cells will spawn tumors or migrate to the wrong places in the spinal column—all the more necessary, says Anthony Davies, especially since these cells could serve as the foundation of an entire new template for pharmaceutical products.
“These are the very early days,” says Susan Howley, director of research for the Christopher and Dana Reeve Foundation, which allocates only about 10 percent of its funds to stem cell-related projects. “It’s not that we don’t believe in stem cells, but simply because, from the perspective of our individual grants program, many of the projects we have seen have lacked scientific rigor, or they’ve been good, substantial science, but have been so basic and so removed from spinal cord application that they are more appropriately funded at the NIH level.” Howley admits, however, that someone has to go first.
“We don’t know if cell therapies will restore function to patients,” notes Wise Young, “but what we do know is that we need to set up the infrastructure to be able to test different kinds of cells.”
Ann Parson is the author of The Proteus Effect: Stem Cells and Their Promise for Medicine, which was chosen by Library Journal for its yearly list of best science books for general readers
Eye on the Prize
The Company Who Cried Clinical Trial,” blazoned a headline on Wired magazine’s blog network this summer, with the blogger calling attention to how often Geron has said it was on the verge of a first-of-its-kind clinical trial that entails transplanting a type of neural cell into spinal cord-injured patients.
Even so, and with Geron researchers now saying the trial will begin in 2008, no one is tuning them out. Anticipation remains strong, not only because of what the test could portend for spinal cord repair, but because success would represent, according to Menlo Park, California-based Geron, the first time a product derived from embryonic stem cells (ES cells) has proved safe and effective for humans. This would be a boon for those who want to ease restrictions on federal funding for ES cell research. Should the trial fail, however, it could be a major setback for ES cells and the many labs hoping to channel them into countless therapies.
Such a product doesn’t come cheap. The investigational new drug application (IND) that Geron expects to file by year’s end will be some 20- to 30-thousand pages long. “Granted, this IND is larger than most,” notes Anthony Davies, Geron’s vice president of product development, “but that’s where the bar is, in terms of getting products into the clinic,” especially a product meant for the tricky confines of the spinal cord.
The research is part of Geron’s much larger, multiyear, human embryonic stem cell program, into which the company has sunk more than $100 million. Notes Davies, “This is biology; the raw materials are complex and expensive. This is the first time we”—or possibly anyone—“has tried to manufacture human embryonic stem cells under GMP [Good Manufacturing Practice Regulations] to meet FDA requirements.”
Geron has no products for patients yet, and the only return on investment to date comes from marketing its assay kits and selling cell lines through licensees. Still, Reni Benjamin, a research analyst at New York-based Rodman and Renshaw, remains optimistic about several prototypes inching through Geron’s pipeline. They include six different cell types that are slated for transplant therapies, respectively, for cardiovascular, central nervous system, pancreas, liver, and bone and joint disorders. Each cell type is derived from embryonic stem cells.
“Geron is master of its domain,” observes Benjamin. “It’s been a leader in the stem cell space for quite some time, has been slowly making headway, and has been able to successfully raise money from investors repeatedly, such that now it has a cash hoard of about $217 million.” Benjamin projects that, on the heels of a net loss of around $31 million last year, Geron this year will burn through another $42 million. The company needs to spend money, he allows, if it’s to attain its goal of becoming a commercial drug company that manufactures off-the-shelf cell therapies for entire patient populations—no small undertaking when you consider that, in the area of spinal cord injury alone, there are as many as 50,000 new cases worldwide.
China by itself is fueling demand for spinal cord intervention, notes Wise Young, the director of the W.M. Keck Center for Collaborative Neuroscience at Rutgers University. In 1995, a study of spinal cord injuries in Beijing, its rural surroundings, and Shanghai recorded only five cases per million people in a year in comparison to the United States’ 35 cases per million. Ten years later, a survey in the same regions in China counted a 10-fold increase in spinal cord injuries, to 65 cases per million. “I think China’s incidence in 1995 was much lower because people probably died before reaching tertiary care centers,” says Young, “and also because there was so little travel by motor vehicle.”
Motivated by the need for effective therapies, Young, in conjunction with the China Spinal Cord Injury Network, also has plans in 2008 to test a cell therapy in spinal cord-injured humans. Their approach will attempt to regenerate severed neurons by means of injecting umbilical cord blood stem cells and lithium, a drug known to stimulate the proliferation of cord cells.
Geron’s approach does not try to repair the spine’s severed nerve cells. Instead, it attempts to restore the benefit of myelin, the fat-like material that wraps around and insulates nerve cells’ axons, the long fibers that connect the cord to different parts of the body. Injury to the cord is accompanied by a significant loss of the myelin sheaths, rendering axons incapable of conducting signals between brain and muscles. The body’s oligodendrocyte cells, a type of neural cell, produce myelin, and so Geron’s plan is to remyelinate denuded axons by putting oligodendrocyte progenitor cells (OPCs) into the site and letting them do their thing, a strategy that might restore at least a modicum of spinal function. (OPCs are simply immature precursors of mature oligodendrocytes.)
When Geron was founded in the early 1990s, hardly anyone imagined mending an injured spinal cord. The company’s early mission—one conceived by Geron’s then-CEO Michael West—was to outsmart human aging. Toward that end, Geron’s scientists went in search of telomerase, the protein responsible for making a cell’s telomeres, the ends of chromosomes that appear to play a role in a cell’s aging process. Put telomerase into cells and it might lengthen telomeres as well as a person’s life. Inhibit telomerase, and you possibly might slow the reckless division of cancer cells.
Geron today has two telomerase drugs undergoing clinical trials—a vaccine and an inhibitor both aimed at cancer cells—and is researching how drugs that activate telomerase might counter the effects of aging and associated degenerative conditions.
Mouse ES cells had been isolated in the 1980s, and West came to realize that he might achieve his goal using those cells, if only they could be harvested from human embryos. In 1995 Geron began funding Jamie Thomson at the University of Wisconsin for that work and three years later, in May 1998, Geron received a call from Thomson saying he had succeeded. By that time, West had left the company, later taking up the reins at Advanced Cell Technology on the opposite coast. Thomas Okarma has headed Geron ever since.
Over the next two years, Geron’s gene therapy program, aimed at placing telomerase into cells, lost momentum. “The blush of gene therapy eroded away due to numerous problems,” says Jane Lebkowski, Geron’s senior vice president of regenerative medicine. Gene therapy everywhere slowed to a crawl when an 18-year-old patient named Jesse Gelsinger died after receiving gene therapy for a rare liver disorder at the University of Pennsylvania. During the same period, Geron’s stem cell program got stronger and stronger.
“I would have predicted Parkinson’s disease was going to be our first goal,” Lebkowski says today. The protocol seemed straightforward enough: Grow ES cells; steer them to yield dopamine-producing cells, the brain cells ravaged by Parkinson’s; and then transplant those cells into the appropriate brain regions. Researchers transplanting stem cells into Parkinson’s animal models weren’t demonstrating “terribly good results,” however, Lebkowski recounts. That’s when a new partnership emerged, along with a new direction in research.
Hans Keirstead at UC Irvine’s Reeve-Irvine Research Center was getting positive results when he implanted OPCs into the spinal cords of rats. Keirstead, a neurobiologist who did his postdoctoral training at Cambridge University, is one of the scientists who originally demonstrated that injury to the spinal cord is accompanied by a significant loss of the myelin that sheathes axons. He realized that no matter how many neurons had been severed at the injury site, axons off to the side sometimes escaped injury, although they were missing their myelin and couldn’t function. Hence Keirstead’s goal of re-sheathing them. It wasn’t long before Geron formed a working relationship with Keirstead, whose lab ended up the glad recipient of funds from both Geron and the University of California’s grant-matching BioSTAR program.
Results from testing their OPCs on lab rats with paralyzed hind limbs “are big enough to spur you on to humans,” says Lebkowski. Before treatment, they drag their hind legs. When injected with human OPCs seven days after the injury, they can plant their hind legs and support themselves as they move about. Scans of the animals validate that axons denuded of myelin have indeed been re-sheathed, says Gabriel Nistor, a postdoctoral researcher in Keirstead’s group. Remyelination isn’t the only factor that appears to benefit the rodents. The transplanted cells, Nistor says, also “secrete growth factors that can rescue some neurons from dying.”
Previous work on “shiver mice”—mice in which a deficiency of myelin causes a shivering-like tremor—gives credence to this approach, as well. When human oligodendrocytes are injected into these animals, their missing myelin is replaced with human myelin and the mice stop shaking.
Geron’s expectations for its human trials are fairly modest. “What we’re looking for isn’t necessarily that everyone is going to get up and walk,” notes Lebkowski. “But if you could improve even just one level of spinal function, especially in someone with a cervical [neck] injury, it could make a big difference.” Reducing a patient’s impairment by just one spinal column segment might re-establish some small hand or arm movement, restore a bit of bladder control, or improve some portion of heart or lung function. It’s been said about Christopher Reeve, for instance, who sustained his injury high in the cervical region, that had he regained one level of function, he might have been able to dispense with his ventilator.
To convert ES cells into OPCs, the scientists follow a 42-day protocol. The ES cells they start with come from Jamie Thomson’s very first cell line. The concern that these early cell lines might be contaminated because they were made with mouse feeder cells, Lebkowski says, is unwarranted. “As soon as Jamie’s cells arrived, we tested them for any pathogens that could have come from mouse feeder cells and any other agents they might have been exposed to,” she recounts. “We asked ourselves, ‘Are these cells suitable for human use? Are we going to pour millions of dollars into developing these cell lines for clinical use?’” The cells passed all their tests, and Geron subsequently developed a method that enables embryonic cells to be grown in the company of human, not mouse, feeder cells, thus avoiding any suspicion of pathogen contamination.
Up to 30 patients will participate in Geron’s Phase 1 trial, each one a “complete” patient, meaning someone with total paralysis. “The idea is to start conservative, with the worst patients who have the most to gain and the least to lose,” says Lebkowski. A transplant’s timing will be tremendously important, the researchers believe, since their animal studies indicate that cells need to be inserted into the spinal cord between seven to 14 days after an injury occurs. If they are implanted any earlier, the notorious inflammation that occurs immediately following a spinal injury might destroy the cells; any later, and scarring might impede their ability to reach those axons that need rewrapping.
Patients initially will be injected with 1 million cells, and if no toxic effect occurs, the doses will be increased up to 20 million cells. Geron has evidence that its OPCs do not trigger a recipient’s immune response. Still, to be on the safe side, the researchers will administer immunosuppressive drugs to their patients. For the purpose of injecting the cells, Geron has designed a special syringe and syringe holder that will allow a surgeon to release cells into the spinal cord at a defined depth for a set period of time without the cells squirting back out. These devices will require the U.S. Food and Drug Administration’s signoff, as well.
Geron’s pre-clinical animal studies have dragged on, says CEO Tom Okarma, primarily because of the large number of animals—some 2,000—in which Geron has had to test its OPCs. “What surprised us the first time we had a conversation with the agency,” says Okarma, “was how high the bar was going to be, in terms of numbers of animals and the length of time we had to keep the animals alive.”
“There are a number of unique things about this IND,” notes Okarma. “First of all, it’s almost unprecedented when the sponsor of an IND, in this case Geron, is the only producer of peer-reviewed literature that speaks to the technology being regulated. All the publications on glial cells in spinal cord injury made from human ES cells are Geron’s. The publications in the literature from non-Geron scientists are contaminated from bad results, because no one knows how to grow these cells the way we do.” When other researchers transplant their cells into animals, they report a high frequency of tumor formation, says Okarma, which the FDA “must obligatorily examine when they look at our application. So because of all that noise in the literature, the bar is higher.”
The fact that no clinical studies have ever been done with derivatives of embryonic cells makes ruling out a whole host of safety issues—from whether the cells will spawn tumors or migrate to the wrong places in the spinal column—all the more necessary, says Anthony Davies, especially since these cells could serve as the foundation of an entire new template for pharmaceutical products.
“These are the very early days,” says Susan Howley, director of research for the Christopher and Dana Reeve Foundation, which allocates only about 10 percent of its funds to stem cell-related projects. “It’s not that we don’t believe in stem cells, but simply because, from the perspective of our individual grants program, many of the projects we have seen have lacked scientific rigor, or they’ve been good, substantial science, but have been so basic and so removed from spinal cord application that they are more appropriately funded at the NIH level.” Howley admits, however, that someone has to go first.
“We don’t know if cell therapies will restore function to patients,” notes Wise Young, “but what we do know is that we need to set up the infrastructure to be able to test different kinds of cells.”
Ann Parson is the author of The Proteus Effect: Stem Cells and Their Promise for Medicine, which was chosen by Library Journal for its yearly list of best science books for general readers
das geron board scheint tot zu sehen, ganz ähnlich dem aktienkurs... nicht mal meislo lässt sich zu einem kleinen beitrag mehr hinreißen.
short interest bei geron zu jahresende auf einem tiefstand. heisst, die shorties haben sich eingedeckt. der kurs könnte ebenso einen boden gefunden haben.
wer kauft jetzt noch?
lg
short interest bei geron zu jahresende auf einem tiefstand. heisst, die shorties haben sich eingedeckt. der kurs könnte ebenso einen boden gefunden haben.
wer kauft jetzt noch?
lg
KREBSFORSCHUNG
Den dunklen Stammzellen auf der Spur
Von Jens Lubbadeh
Stammzellen sind bei Medizinern begehrt, sie haben aber auch dunkle Brüder: Krebsstammzellen, die Tumore wachsen lassen. Wissenschaftler haben bei Hautkrebs diese Zellen nun identifizieren und gezielt ausschalten können.
Krebsforscher sind bestimmten, sehr zerstörerischen Zellen auf der Spur: Krebsstammzellen. Diese stehen unter Verdacht, bei der Entstehung eines Tumors und der Bildung von Metastasen eine Schlüsselrolle zu spielen. Wissenschaftler vermuten, dass es im Tumorgewebe ein kleines Reservoir dieser Übeltäter gibt, die den Tumor ständig nachfüttern.
AP
Hautkrebs: Für das Tumorwachstum entscheidend sind die Krebsstammzellen
Forschern um Tobias Schatton von der Harvard Medical School in Boston im US-Bundesstaat Massachusetts ist es nun gelungen, diese Krebsstammzellen zu identifizieren und mit Antikörpern gezielt auszuschalten. Ihre Ergebnisse haben sie im Fachmagazin "Nature" veröffentlicht.
Schatton und seine Kollegen untersuchten Zellen von Hautkrebs-Patienten. Hautkrebs ist eine besonders aggressive Krebsvariante. Um die Stammzellen im Hautkrebsgewebe zu finden, nutzten die Wissenschaftler aus, dass diese ein ganz bestimmtes Protein, ABCB5 genannt, auf ihrer Zelloberfläche tragen. Die Wissenschaftler verwendeten dann spezifische Antikörper gegen dieses Protein, mit dem sie die Krebsstammzellen sowohl von den normalen Hautkrebszellen unterscheiden und auch ausschalten konnten.
Um nun nachzuweisen, dass es die Krebsstammzellen waren, die das Wachstum des Hautkrebses forcierten, machten sie verschiedene Experimente. Sie konnten das Tumorwachstum unterdrücken, wenn sie die Krebsstammzellen mit den Antikörpern ausschalteten. Und auch bei Verpflanzung der Hautkrebszellen in Mäuse zeigte sich unterschiedlich starke Krebsentstehung: Die Krebsstammzellen lösten eine stärkere Tumorbildung aus als die normalen Tumorzellen. Auch in der Kultivierung der Zellen zeigten sich Unterschiede: Krebsstammzellen konnten sowohl Krebsstammzellen als auch gewöhnliche Hautkrebszellen hervorbringen. Normale Hautkrebszellen jedoch nicht - die konnten nur ihresgleichen herstellen, nicht aber die potenteren Krebsstammzellen.
Sie widerstehen Chemotherapie und Bestrahlung
Die Ergebnisse Schattons und seiner Kollegen bestätigen frühere Experimente an Krebsstammzellen (mehr...). Diese sind - genauso wie die nützlichen Stammzellen - praktisch unsterblich. Und sie können, was auch die aktuelle Arbeit Schattons bestätigt, zu unterschiedlichen Zelltypen heranreifen: Eine Krebsstammzelle kann sämtliche Zellen entstehen lassen, die sich in einem Tumor finden.
DER SPIEGELAuch bei Dickdarmtumoren konnten Wissenschaftler die zerstörerische Kraft dieser Krebsstammzellen zeigen. Wie Schatton bei den Hautkrebszellen trennten sie die Dickdarmkrebsstammzellen anhand ihrer Oberflächenproteine von gewöhnlichen Tumorzellen. Als sie nur wenige dieser Zellen in Mäuse spritzten, wucherten in den Versuchstieren die Krebsherde. Diese bestanden ihrerseits aus vielen ausgereiften Krebszellen und einigen wenigen Krebsstammzellen. Bei der Injektion viel größerer Mengen gewöhnlicher Krebszellen wuchsen den Mäusen keine Tumoren.
Fatale bei den Krebsstammzellen: Mit herkömmlichen Krebstherapien - Bestrahlung und Chemotherapie - ist ihnen nicht beizukommen. Sie zerstören zwar einen Großteil des Tumorgewebes, nicht aber die Krebsstammzellen. Wissenschaftler vermuten darin den Grund, warum nach einer gelungenen Chemotherapie für den Patienten jederzeit die Gefahr besteht, dass sich neue Tumoren und Metastasen bilden können.
Es gibt Vermutungen, warum Krebsstammzellen Chemotherapie und Bestrahlung widerstehen: Zytostatika zerstören generell Zellen, die sich vermehren. Krebsstammzellen teilen sich aber eher selten. Außerdem stellen sie Transportproteine her, die chemotherapeutische Gifte regelrecht aus der Zelle pumpen.
Auch radioaktive Bestrahlung halten sie aus - für Zellen normalerweise das sichere Todesurteil. Wissenschaftler glauben, dass diese Strahlenresistenz auf einen gestörten Kontrollmechanismus bei den Krebsstammzellen zurückzuführen ist. Im Unterschied zu normalen Zellen haben sie offenbar die wichtige Fähigkeit verloren Selbstmord zu begehen, wenn ihr Erbgut allzu sehr beschädigt wird. Dieser Freitod der nicht mehr funktionstüchtigen Zelle geschieht normalerweise zum Wohl des Gesamtorganismus.
Den dunklen Stammzellen auf der Spur
Von Jens Lubbadeh
Stammzellen sind bei Medizinern begehrt, sie haben aber auch dunkle Brüder: Krebsstammzellen, die Tumore wachsen lassen. Wissenschaftler haben bei Hautkrebs diese Zellen nun identifizieren und gezielt ausschalten können.
Krebsforscher sind bestimmten, sehr zerstörerischen Zellen auf der Spur: Krebsstammzellen. Diese stehen unter Verdacht, bei der Entstehung eines Tumors und der Bildung von Metastasen eine Schlüsselrolle zu spielen. Wissenschaftler vermuten, dass es im Tumorgewebe ein kleines Reservoir dieser Übeltäter gibt, die den Tumor ständig nachfüttern.
AP
Hautkrebs: Für das Tumorwachstum entscheidend sind die Krebsstammzellen
Forschern um Tobias Schatton von der Harvard Medical School in Boston im US-Bundesstaat Massachusetts ist es nun gelungen, diese Krebsstammzellen zu identifizieren und mit Antikörpern gezielt auszuschalten. Ihre Ergebnisse haben sie im Fachmagazin "Nature" veröffentlicht.
Schatton und seine Kollegen untersuchten Zellen von Hautkrebs-Patienten. Hautkrebs ist eine besonders aggressive Krebsvariante. Um die Stammzellen im Hautkrebsgewebe zu finden, nutzten die Wissenschaftler aus, dass diese ein ganz bestimmtes Protein, ABCB5 genannt, auf ihrer Zelloberfläche tragen. Die Wissenschaftler verwendeten dann spezifische Antikörper gegen dieses Protein, mit dem sie die Krebsstammzellen sowohl von den normalen Hautkrebszellen unterscheiden und auch ausschalten konnten.
Um nun nachzuweisen, dass es die Krebsstammzellen waren, die das Wachstum des Hautkrebses forcierten, machten sie verschiedene Experimente. Sie konnten das Tumorwachstum unterdrücken, wenn sie die Krebsstammzellen mit den Antikörpern ausschalteten. Und auch bei Verpflanzung der Hautkrebszellen in Mäuse zeigte sich unterschiedlich starke Krebsentstehung: Die Krebsstammzellen lösten eine stärkere Tumorbildung aus als die normalen Tumorzellen. Auch in der Kultivierung der Zellen zeigten sich Unterschiede: Krebsstammzellen konnten sowohl Krebsstammzellen als auch gewöhnliche Hautkrebszellen hervorbringen. Normale Hautkrebszellen jedoch nicht - die konnten nur ihresgleichen herstellen, nicht aber die potenteren Krebsstammzellen.
Sie widerstehen Chemotherapie und Bestrahlung
Die Ergebnisse Schattons und seiner Kollegen bestätigen frühere Experimente an Krebsstammzellen (mehr...). Diese sind - genauso wie die nützlichen Stammzellen - praktisch unsterblich. Und sie können, was auch die aktuelle Arbeit Schattons bestätigt, zu unterschiedlichen Zelltypen heranreifen: Eine Krebsstammzelle kann sämtliche Zellen entstehen lassen, die sich in einem Tumor finden.
DER SPIEGELAuch bei Dickdarmtumoren konnten Wissenschaftler die zerstörerische Kraft dieser Krebsstammzellen zeigen. Wie Schatton bei den Hautkrebszellen trennten sie die Dickdarmkrebsstammzellen anhand ihrer Oberflächenproteine von gewöhnlichen Tumorzellen. Als sie nur wenige dieser Zellen in Mäuse spritzten, wucherten in den Versuchstieren die Krebsherde. Diese bestanden ihrerseits aus vielen ausgereiften Krebszellen und einigen wenigen Krebsstammzellen. Bei der Injektion viel größerer Mengen gewöhnlicher Krebszellen wuchsen den Mäusen keine Tumoren.
Fatale bei den Krebsstammzellen: Mit herkömmlichen Krebstherapien - Bestrahlung und Chemotherapie - ist ihnen nicht beizukommen. Sie zerstören zwar einen Großteil des Tumorgewebes, nicht aber die Krebsstammzellen. Wissenschaftler vermuten darin den Grund, warum nach einer gelungenen Chemotherapie für den Patienten jederzeit die Gefahr besteht, dass sich neue Tumoren und Metastasen bilden können.
Es gibt Vermutungen, warum Krebsstammzellen Chemotherapie und Bestrahlung widerstehen: Zytostatika zerstören generell Zellen, die sich vermehren. Krebsstammzellen teilen sich aber eher selten. Außerdem stellen sie Transportproteine her, die chemotherapeutische Gifte regelrecht aus der Zelle pumpen.
Auch radioaktive Bestrahlung halten sie aus - für Zellen normalerweise das sichere Todesurteil. Wissenschaftler glauben, dass diese Strahlenresistenz auf einen gestörten Kontrollmechanismus bei den Krebsstammzellen zurückzuführen ist. Im Unterschied zu normalen Zellen haben sie offenbar die wichtige Fähigkeit verloren Selbstmord zu begehen, wenn ihr Erbgut allzu sehr beschädigt wird. Dieser Freitod der nicht mehr funktionstüchtigen Zelle geschieht normalerweise zum Wohl des Gesamtorganismus.
STAMMZELLENFORSCHUNG
Wissenschaftler klonen menschlichen Embryo aus Hautzelle
Von Jens Lubbadeh
Spektakulärer Durchbruch in der medizinischen Forschung: US-Wissenschaftlern ist es erstmals gelungen, einen menschlichen Embryo aus einer Hautzelle zu klonen. Es ist ein Etappensieg auf dem Weg zur Herstellung maßgeschneiderter embryonaler Stammzellen.
Es ist vollbracht. Andrew French von der Stemagen Corporation in La Jolla, im US-Bundesstaat Kalifornien und seinen Kollegen ist nun das gelungen, was der südkoreanische Klonforscher Woo Suk Hwang bereits im Jahr 2004 behauptet hatte, erreicht zu haben: einen menschlichen Embryo aus einer Körperzelle zu klonen. Der Unterschied: Hwang entpuppte sich als Fälscher, French und seine Kollegen hingegen haben es tatsächlich geschafft. Ihren Durchbruch haben die Wissenschaftler im Fachmagazin "Stem Cells" veröffentlicht.
http://www.spiegel.de/wissenschaft/mensch/0,1518,528999,00.h…
Wissenschaftler klonen menschlichen Embryo aus Hautzelle
Von Jens Lubbadeh
Spektakulärer Durchbruch in der medizinischen Forschung: US-Wissenschaftlern ist es erstmals gelungen, einen menschlichen Embryo aus einer Hautzelle zu klonen. Es ist ein Etappensieg auf dem Weg zur Herstellung maßgeschneiderter embryonaler Stammzellen.
Es ist vollbracht. Andrew French von der Stemagen Corporation in La Jolla, im US-Bundesstaat Kalifornien und seinen Kollegen ist nun das gelungen, was der südkoreanische Klonforscher Woo Suk Hwang bereits im Jahr 2004 behauptet hatte, erreicht zu haben: einen menschlichen Embryo aus einer Körperzelle zu klonen. Der Unterschied: Hwang entpuppte sich als Fälscher, French und seine Kollegen hingegen haben es tatsächlich geschafft. Ihren Durchbruch haben die Wissenschaftler im Fachmagazin "Stem Cells" veröffentlicht.
http://www.spiegel.de/wissenschaft/mensch/0,1518,528999,00.h…
Antwort auf Beitrag Nr.: 33.083.978 von meislo am 17.01.08 16:44:17das scheint von der Börse noch nicht honoriert zu werden. jetzt schnell spekulativ rein???
Zellbiologie
Entstehung und Ende des Lebens nah beieinander
Krebs- und Stammzellen sind derzeit zwei der brisantesten Forschungsbereiche. Eine Parallele zwischen der Entstehung von Embryonen und neuem Leben auf der einen Seite sowie dem Außer-Kontrolle-Geraten von Zellen auf der anderen könnte die Forschung in den kommenden Jahren revolutionieren.
Foto: dpaDie künstliche Zeugung eines solchen Wonneproppen ist bemerkenswert eng mit der überbordenden Zellteilung bei Krebs verbunden
Einzelne medizinische Forschungsgebiete lösen in der Öffentlichkeit vor allem Schaudern aus – teils aus Respekt vor unbeherrschbaren Krankheiten, teils aus ethischen Beweggründen. Dies gilt insbesondere für zwei der dynamischsten Forschungsfelder überhaupt, die Onkologie, die Krebs in all seinen Spielarten untersucht, und die Stammzellenforschung. Dass ausgerechnet diese beiden brisanten Felder viel mehr gemeinsam haben als bislang angenommen, ist ein erstaunlicher Befunde. Stamm- und Krebszellen sind, bildlich gesprochen, die zwei Seiten einer Medaille. Weiterführende links
Auf der einen Seite forschen Onkologen, die die Ursachen und Behandlungsmöglichkeiten von mehr als 100 Krankheiten untersuchen, die unter dem Sammelbegriff „Krebs“ bekannt sind. Die Wissenschaftler haben in den vergangenen Jahren spektakuläre Erfolge erzielt, vor allem dank neuer und neuartiger Wirkstoffe. Insbesondere das stetig anwachsende Arsenal therapeutischer Antikörper gibt Patienten und Ärzten gleichermaßen Hoffnung. Medikamente wie Avastin, Herceptin oder Rituxan haben Hunderttausenden Menschen das Leben gerettet oder nennenswert verlängert.
Aus einer Stammzelle kann alles werden
Ähnlich vielversprechend – und für viele religiös verankerte Menschen zugleich entsetzlich – ist eine zweite wissenschaftliche Front, die Forschung mit embryonalen Stammzellen. Jede einzelne dieser embryonalen Stammzellen verfügt über eine wunderbare Fähigkeit: Sie ist pluripotent, „für mehrere Zwecke gebräuchlich“ also, und kann sich in jede einzelne Zellart im Körper wandeln – zum Beispiel in eine Knochen-, Muskel- oder Nervenzelle. Doch sie hat noch eine weitere Gabe. Eine embryonale Stammzelle kann sich im Prinzip immer und immer wieder teilen, unendlich oft. In diesem Sinne ist sie unsterblich. Ausgerechnet diese Eigenschaft hat sie mit tödlichen Tumorzellen gemeinsam. Diese kranken, „entarteten“ Zellen vermehren sich im Körper unkontrolliert, während gesunde Zellen – wie im genetischen Bauplan vorgesehen – altern und nach einer bestimmten Anzahl von Teilungen den Dienst quittieren. Irgendwann gewinnen die Krebszellen schließlich die Oberhand; der Körper stirbt. Diese bemerkenswerte Parallele zwischen der Entstehung von Embryonen und neuem Leben auf der einen Seite sowie dem Außer-Kontrolle-Geraten von Zellen auf der anderen könnte die Forschung in den kommenden Jahren revolutionieren.
Metastasen sind tödlich
Erst seit wenigen Jahren ist bekannt, dass es nicht nur „gute“ Stammzellen im Organismus gibt, sondern auch höchst gefährliche Krebs-Stammzellen. Mehr noch: Forscher vermuten, dass Tumore durch einige wenige Krebs-Stammzellen überhaupt erst tödlich werden. Denn Patienten sterben in der Regel nicht an einem Primärtumor, der ein einzelnes Organ oder Gewebe befällt, sondern an Metastasen. Diese Streugeschwüre können sich mit der Zeit in einem anderen Organ bilden, etwa in Lunge, Knochen oder Leber, und tödlich verlaufen. Sie bilden sich, so mutmaßen Onkologen, genau dann, wenn Krebs-Stammzellen durch den Körper wandern, sich irgendwo niederlassen und zu wuchern beginnen. Verantwortlich für die frappierende Parallele zwischen embryonaler und Krebs-Stammzelle ist ein ungewöhnliches Enzym: die 1985 von Elizabeth Blackburn und ihrer Studentin Carol Greider (siehe Kasten) identifizierte Telomerase. Dieses Enzym ist sowohl in Tumoren also auch in embryonalen Stammzellen besonders aktiv, nicht aber in normalem, gesundem Gewebe. Sie ist verantwortlich für den Mechanismus in Zellen, der über das Altern entscheidet – und damit über Leben und Tod.
Regulation der Endstücke
Bei jeder Teilung einer gesunden Zelle werden die Spitzen der Chromosomen, die so genannten Telomere – griechisch für „Endteile“ – um ein winziges Stück gekürzt. Diese Telomere sitzen wie ein Plastikring am Ende eines Schnürsenkels auf den Kappen der Chromosomen, halten das Knäuel in Form und schützen es vor einer gefährlichen „Zerfledderung“ an den Enden. Sind die Telomere nach einer bestimmten Zahl von Teilungen aufgebraucht, stirbt eine normale Zelle. Geschieht dies im Körper milliardenfach, altert der Mensch. Haare werden mit der Zeit grau, Knochen brüchig, die Haut bildet Falten, der Körper schrumpft. Der Telomerase kommt dabei eine Schlüsselrolle zu. Sie reguliert die Telomere und kann die Verkürzung von Telomeren unterbinden. Sie ist gewissermaßen die Uhr, die über die Lebensspanne von Zellen wacht. Telomerase kommt ausgerechnet in fast allen Krebszellen besonders reichlich vor und ermöglicht Tumoren damit erst das lebensgefährliche, unkontrollierte Wachstum. In gesunden, ausgeformten Zellen des Körpers ist sie dagegen kaum präsent und wenn doch – wie beispielsweise in sich besonders schnell teilenden Zellen der Schleimhaut oder in Keimzellen – dann nur für kurze Zeit. Anders gesagt: Wo im Körper besonders viel Telomerase ist, handelt es sich mit großer Wahrscheinlichkeit um eine Krebszelle. „Krebszellen scheinen gewissermaßen süchtig nach einer sehr hohen Telomerase-Konzentration zu sein“, so Elizabeth Blackburn. Sie geben rasch auf, wenn ihnen die Telomerase genommen wird.
Enzym als Jungbrunnen
Wie genau der Telomerase-Mechanismus funktioniert, wird heute noch erforscht. Sicher ist aber schon jetzt, dass das Enzym eine Vielzahl von Genen, die bei der Entstehung von Krebs eine Rolle spielen, beeinflusst. Blackburn selbst spricht vom „Dr.Jekyll-und-Mr.Hyde-Gesicht der Telomerase“. Das Enzym ist zum einen eine Art „Jungbrunnen“, indem es Zellen unsterblich machen kann, zum anderen aber auch eine „Massenvernichtungswaffe“, indem es Krebszellen außer Kontrolle geraten lässt. Es ist naheliegend, dass Telomerase „einen sehr attraktiven Weg für eine Intervention“ weisen könnte, glaubt Blackburn – also für einen Therapieansatz. Wer dieses Enzym in bösartigen Zellen gezielt blockieren könnte, hätte möglicherweise eine völlig neue Waffengattung im Kampf gegen den Krebs in der Hand. Es handelt sich um „einen wichtigen Forschungsbereich, der jetzt in die klinischen Studien geht“, sagt Professor Petra Boukamp, Telomerase-Expertin beim Deutschen Krebsforschungszentrum der Universität Heidelberg. Es sei „ein interessantes Enzym“, das möglicherweise die Chance für einen Angriff auf Tumorzellen biete.
Impfstoff in der Zulassung
Diesen Gedanken der Telomerase-Hemmung verfolgen mehrere akademische Institute, aber auch Forscher des kalifornischen Unternehmens Geron, das in den vergangenen Jahren die weltweit umfangreichste Patentsammlung sowohl in der Forschung mit Telomerase als auch mit embryonalen Stammzellen aufgebaut hat. Ähnlichen Ideen gehen die dänische Biotechnologie-Firma Pharmexa sowie – in Kooperation mit Geron – Merck & Co nach. Erst im vergangenen Monat hat der amerikanische Pharmakonzern bei der amerikanischen Gesundheitsbehörde FDA einen neuartigen therapeutischen Krebsimpfstoff angemeldet, der eines Tages gezielt Telomerase in Tumoren hemmen soll. Recht optimistisch sieht Boukamp den Ansatz der Enzym-Hemmung. „Man geht davon aus, dass das in Kombination mit anderen Wirkstoffen mindestens so gut sein könnte wie Angiogenese-Hemmer - ob sich das halten wird, wird man sehen.“ Ein Satz, der Hoffnung macht: Angiogenese-Hemmer – in diese Wirkstoffgruppe zählt beispielsweise das außerordentlich erfolgreiche Krebsmittel Avastin von Roche – zielen darauf ab, die Blutversorgung eines Tumors ganz gezielt zu unterbrechen, ihn gewissermaßen von Nährstoffen abzuschneiden und damit „auszuhungern“. Schlagworte
Entym Stammzellen Krebs Jungbrunnen Telomerase Doch nicht nur das Blockieren der Telomerase könnte bei der Krebstherapie eines Tages Wunder wirken, sondern auch die gezielte Aktivierung von Telomerase. Denn wer die Kürzung der Telomere gesunder Zellen – und damit den genetisch programmierten Zelltod (Apoptose) – bremsen oder ganz verhindern könnte, hätte eine Art zellulären Jungbrunnen zur Hand. Genau dieses Ziel verfolgen die Telomerase-Forscher bei Geron ebenfalls. Sie wollen als erstes die geschwächten Immunzellen von Aids-Kranken gezielt mit Hilfe von Telomerase-Aktivierung „verjüngen“ und dadurch das Immunsystem der Patienten stärken
Entstehung und Ende des Lebens nah beieinander
Krebs- und Stammzellen sind derzeit zwei der brisantesten Forschungsbereiche. Eine Parallele zwischen der Entstehung von Embryonen und neuem Leben auf der einen Seite sowie dem Außer-Kontrolle-Geraten von Zellen auf der anderen könnte die Forschung in den kommenden Jahren revolutionieren.
Foto: dpaDie künstliche Zeugung eines solchen Wonneproppen ist bemerkenswert eng mit der überbordenden Zellteilung bei Krebs verbunden
Einzelne medizinische Forschungsgebiete lösen in der Öffentlichkeit vor allem Schaudern aus – teils aus Respekt vor unbeherrschbaren Krankheiten, teils aus ethischen Beweggründen. Dies gilt insbesondere für zwei der dynamischsten Forschungsfelder überhaupt, die Onkologie, die Krebs in all seinen Spielarten untersucht, und die Stammzellenforschung. Dass ausgerechnet diese beiden brisanten Felder viel mehr gemeinsam haben als bislang angenommen, ist ein erstaunlicher Befunde. Stamm- und Krebszellen sind, bildlich gesprochen, die zwei Seiten einer Medaille. Weiterführende links
Auf der einen Seite forschen Onkologen, die die Ursachen und Behandlungsmöglichkeiten von mehr als 100 Krankheiten untersuchen, die unter dem Sammelbegriff „Krebs“ bekannt sind. Die Wissenschaftler haben in den vergangenen Jahren spektakuläre Erfolge erzielt, vor allem dank neuer und neuartiger Wirkstoffe. Insbesondere das stetig anwachsende Arsenal therapeutischer Antikörper gibt Patienten und Ärzten gleichermaßen Hoffnung. Medikamente wie Avastin, Herceptin oder Rituxan haben Hunderttausenden Menschen das Leben gerettet oder nennenswert verlängert.
Aus einer Stammzelle kann alles werden
Ähnlich vielversprechend – und für viele religiös verankerte Menschen zugleich entsetzlich – ist eine zweite wissenschaftliche Front, die Forschung mit embryonalen Stammzellen. Jede einzelne dieser embryonalen Stammzellen verfügt über eine wunderbare Fähigkeit: Sie ist pluripotent, „für mehrere Zwecke gebräuchlich“ also, und kann sich in jede einzelne Zellart im Körper wandeln – zum Beispiel in eine Knochen-, Muskel- oder Nervenzelle. Doch sie hat noch eine weitere Gabe. Eine embryonale Stammzelle kann sich im Prinzip immer und immer wieder teilen, unendlich oft. In diesem Sinne ist sie unsterblich. Ausgerechnet diese Eigenschaft hat sie mit tödlichen Tumorzellen gemeinsam. Diese kranken, „entarteten“ Zellen vermehren sich im Körper unkontrolliert, während gesunde Zellen – wie im genetischen Bauplan vorgesehen – altern und nach einer bestimmten Anzahl von Teilungen den Dienst quittieren. Irgendwann gewinnen die Krebszellen schließlich die Oberhand; der Körper stirbt. Diese bemerkenswerte Parallele zwischen der Entstehung von Embryonen und neuem Leben auf der einen Seite sowie dem Außer-Kontrolle-Geraten von Zellen auf der anderen könnte die Forschung in den kommenden Jahren revolutionieren.
Metastasen sind tödlich
Erst seit wenigen Jahren ist bekannt, dass es nicht nur „gute“ Stammzellen im Organismus gibt, sondern auch höchst gefährliche Krebs-Stammzellen. Mehr noch: Forscher vermuten, dass Tumore durch einige wenige Krebs-Stammzellen überhaupt erst tödlich werden. Denn Patienten sterben in der Regel nicht an einem Primärtumor, der ein einzelnes Organ oder Gewebe befällt, sondern an Metastasen. Diese Streugeschwüre können sich mit der Zeit in einem anderen Organ bilden, etwa in Lunge, Knochen oder Leber, und tödlich verlaufen. Sie bilden sich, so mutmaßen Onkologen, genau dann, wenn Krebs-Stammzellen durch den Körper wandern, sich irgendwo niederlassen und zu wuchern beginnen. Verantwortlich für die frappierende Parallele zwischen embryonaler und Krebs-Stammzelle ist ein ungewöhnliches Enzym: die 1985 von Elizabeth Blackburn und ihrer Studentin Carol Greider (siehe Kasten) identifizierte Telomerase. Dieses Enzym ist sowohl in Tumoren also auch in embryonalen Stammzellen besonders aktiv, nicht aber in normalem, gesundem Gewebe. Sie ist verantwortlich für den Mechanismus in Zellen, der über das Altern entscheidet – und damit über Leben und Tod.
Regulation der Endstücke
Bei jeder Teilung einer gesunden Zelle werden die Spitzen der Chromosomen, die so genannten Telomere – griechisch für „Endteile“ – um ein winziges Stück gekürzt. Diese Telomere sitzen wie ein Plastikring am Ende eines Schnürsenkels auf den Kappen der Chromosomen, halten das Knäuel in Form und schützen es vor einer gefährlichen „Zerfledderung“ an den Enden. Sind die Telomere nach einer bestimmten Zahl von Teilungen aufgebraucht, stirbt eine normale Zelle. Geschieht dies im Körper milliardenfach, altert der Mensch. Haare werden mit der Zeit grau, Knochen brüchig, die Haut bildet Falten, der Körper schrumpft. Der Telomerase kommt dabei eine Schlüsselrolle zu. Sie reguliert die Telomere und kann die Verkürzung von Telomeren unterbinden. Sie ist gewissermaßen die Uhr, die über die Lebensspanne von Zellen wacht. Telomerase kommt ausgerechnet in fast allen Krebszellen besonders reichlich vor und ermöglicht Tumoren damit erst das lebensgefährliche, unkontrollierte Wachstum. In gesunden, ausgeformten Zellen des Körpers ist sie dagegen kaum präsent und wenn doch – wie beispielsweise in sich besonders schnell teilenden Zellen der Schleimhaut oder in Keimzellen – dann nur für kurze Zeit. Anders gesagt: Wo im Körper besonders viel Telomerase ist, handelt es sich mit großer Wahrscheinlichkeit um eine Krebszelle. „Krebszellen scheinen gewissermaßen süchtig nach einer sehr hohen Telomerase-Konzentration zu sein“, so Elizabeth Blackburn. Sie geben rasch auf, wenn ihnen die Telomerase genommen wird.
Enzym als Jungbrunnen
Wie genau der Telomerase-Mechanismus funktioniert, wird heute noch erforscht. Sicher ist aber schon jetzt, dass das Enzym eine Vielzahl von Genen, die bei der Entstehung von Krebs eine Rolle spielen, beeinflusst. Blackburn selbst spricht vom „Dr.Jekyll-und-Mr.Hyde-Gesicht der Telomerase“. Das Enzym ist zum einen eine Art „Jungbrunnen“, indem es Zellen unsterblich machen kann, zum anderen aber auch eine „Massenvernichtungswaffe“, indem es Krebszellen außer Kontrolle geraten lässt. Es ist naheliegend, dass Telomerase „einen sehr attraktiven Weg für eine Intervention“ weisen könnte, glaubt Blackburn – also für einen Therapieansatz. Wer dieses Enzym in bösartigen Zellen gezielt blockieren könnte, hätte möglicherweise eine völlig neue Waffengattung im Kampf gegen den Krebs in der Hand. Es handelt sich um „einen wichtigen Forschungsbereich, der jetzt in die klinischen Studien geht“, sagt Professor Petra Boukamp, Telomerase-Expertin beim Deutschen Krebsforschungszentrum der Universität Heidelberg. Es sei „ein interessantes Enzym“, das möglicherweise die Chance für einen Angriff auf Tumorzellen biete.
Impfstoff in der Zulassung
Diesen Gedanken der Telomerase-Hemmung verfolgen mehrere akademische Institute, aber auch Forscher des kalifornischen Unternehmens Geron, das in den vergangenen Jahren die weltweit umfangreichste Patentsammlung sowohl in der Forschung mit Telomerase als auch mit embryonalen Stammzellen aufgebaut hat. Ähnlichen Ideen gehen die dänische Biotechnologie-Firma Pharmexa sowie – in Kooperation mit Geron – Merck & Co nach. Erst im vergangenen Monat hat der amerikanische Pharmakonzern bei der amerikanischen Gesundheitsbehörde FDA einen neuartigen therapeutischen Krebsimpfstoff angemeldet, der eines Tages gezielt Telomerase in Tumoren hemmen soll. Recht optimistisch sieht Boukamp den Ansatz der Enzym-Hemmung. „Man geht davon aus, dass das in Kombination mit anderen Wirkstoffen mindestens so gut sein könnte wie Angiogenese-Hemmer - ob sich das halten wird, wird man sehen.“ Ein Satz, der Hoffnung macht: Angiogenese-Hemmer – in diese Wirkstoffgruppe zählt beispielsweise das außerordentlich erfolgreiche Krebsmittel Avastin von Roche – zielen darauf ab, die Blutversorgung eines Tumors ganz gezielt zu unterbrechen, ihn gewissermaßen von Nährstoffen abzuschneiden und damit „auszuhungern“. Schlagworte
Entym Stammzellen Krebs Jungbrunnen Telomerase Doch nicht nur das Blockieren der Telomerase könnte bei der Krebstherapie eines Tages Wunder wirken, sondern auch die gezielte Aktivierung von Telomerase. Denn wer die Kürzung der Telomere gesunder Zellen – und damit den genetisch programmierten Zelltod (Apoptose) – bremsen oder ganz verhindern könnte, hätte eine Art zellulären Jungbrunnen zur Hand. Genau dieses Ziel verfolgen die Telomerase-Forscher bei Geron ebenfalls. Sie wollen als erstes die geschwächten Immunzellen von Aids-Kranken gezielt mit Hilfe von Telomerase-Aktivierung „verjüngen“ und dadurch das Immunsystem der Patienten stärken
Haben ne ganze Menge vor bezügl. ihres Oligonucleotid-WS GERN163L (http://www.clinicaltrial.gov/ct2/results?term=Geron), der im Zuge der Stammtellendiskussion etwas untergeht. Es handelt sich auch dabei um einen Telomerase Inhibitor, der übrigens von der dt. Girindus AG in Cincinnati hergestellt wird (vergl. SEC-Filings).
Gut für GERN gut für GIR. Zahlen die immer mit Aktien?
Girindus hat derbe 320,000 Stk ´07 bekommen.
Mal sehen, wann es erste Indikationen bezügl. GERN163 gibt. Vielleicht ist GERN ne Investition wert.
Gut für GERN gut für GIR. Zahlen die immer mit Aktien?

Girindus hat derbe 320,000 Stk ´07 bekommen.
Mal sehen, wann es erste Indikationen bezügl. GERN163 gibt. Vielleicht ist GERN ne Investition wert.
Sector Snap: Biotechnology
Tuesday January 29, 1:26 pm ET
Biotech Stocks Get Boost From UBS Recommendations, Citing Key Drugs and Drug Candidates
NEW YORK (AP) -- Shares of biotechnology companies Geron Corp. and ArQule Inc. rose Tuesday after an analyst upgraded the stocks, citing the potential of their respective stem cell and cancer treatment development programs.
ADVERTISEMENT
UBS Investment Research analyst Graig Suvannavejh upgraded Menlo Park, Calif.-based Geron and Woburn, Mass.-based ArQule to "Buy" from "Neutral." Several other biotechnology companies also benefited from UBS recommendations Tuesday.
Geron shares rose 46 cents, or 9.9 percent, to $5.10, while ArQule rose 14 cents, or 3 percent, to $4.88 in afternoon trading.
The stocks led sector gains. The American Stock Exchange's biotechnology index, which tracks several bellwether stocks, fell less than 1 percent, while the Nasdaq's biotechnology index rose 2.6 points to 803.10.
Stem cell research and funding will likely benefit from a change in the White House, painting a better long-term outlook for Geron, Suvannavejh said. The company's next catalyst may come from Food and Drug Administration approval to start clinical trials on a stem cell treatment for spinal cord injuries.
He lowered his price target to $6 from $8, and said the stock is cheap, coming off a 35 percent since the end of October.
Suvannavejh said the long-term risk-reward prospects for ArQule are attractive. ArQule is developing ARQ 197 as a cancer treatment and early stage study data has so far been impressive, he added.
"While we don't see many near-term catalysts for the shares, we nonetheless recommend being constructive given a longer-term outlook," he said.
He lowered his price target to $6 from $7, and noted the company's shares are down 20 percent year-to-date.
Meanwhile, coverage initiations by UBS analyst Jeff Elliott lifted shares of Cheshire, Conn.-based Alexion Pharmaceuticals Inc. and Princeton, N.J.-based Medarex Inc.
Elliott gave Alexion a "Buy" rating with an $82 price target, citing the company's blood disorder drug Soliris. The disorder the drug treats is rare, but the drug costs about $389,000 per year.
Sales in the European Union will likely be more significant in the near term, with U.S. sales underpinning longer term growth, he said.
Alexion shares rose $1.33, or 2.1 percent, to $64.79.
Medarex shares rose 18 cents to $9.77 after Elliott started coverage with a "Buy" and a $14 price target.
The company's cancer drug candidate Ipilimumab is in late-stage development and has shown it can maintain a durable response in patients with metastatic melanoma, a cancer that ordinarily is difficult to treat. But, he said, there is still risk to the drug's approval.
The remainder of the company's pipeline has potential as it matures, he said, and Medarex could be viewed as a viable buyout candidate.
Elliott also initiated coverage of Seattle-based ZymoGenetics Inc. with a "Buy" rating and $16 price target, and Novato, Calif.-based BioMarin Pharmaceutical Inc. at "Neutral" with a $38 price target.
Shares of ZymoGenetics fell 17 cents to $10.52 and shares of BioMarin fell 11 cents to $36.40.
Tuesday January 29, 1:26 pm ET
Biotech Stocks Get Boost From UBS Recommendations, Citing Key Drugs and Drug Candidates
NEW YORK (AP) -- Shares of biotechnology companies Geron Corp. and ArQule Inc. rose Tuesday after an analyst upgraded the stocks, citing the potential of their respective stem cell and cancer treatment development programs.
ADVERTISEMENT
UBS Investment Research analyst Graig Suvannavejh upgraded Menlo Park, Calif.-based Geron and Woburn, Mass.-based ArQule to "Buy" from "Neutral." Several other biotechnology companies also benefited from UBS recommendations Tuesday.
Geron shares rose 46 cents, or 9.9 percent, to $5.10, while ArQule rose 14 cents, or 3 percent, to $4.88 in afternoon trading.
The stocks led sector gains. The American Stock Exchange's biotechnology index, which tracks several bellwether stocks, fell less than 1 percent, while the Nasdaq's biotechnology index rose 2.6 points to 803.10.
Stem cell research and funding will likely benefit from a change in the White House, painting a better long-term outlook for Geron, Suvannavejh said. The company's next catalyst may come from Food and Drug Administration approval to start clinical trials on a stem cell treatment for spinal cord injuries.

He lowered his price target to $6 from $8, and said the stock is cheap, coming off a 35 percent since the end of October.
Suvannavejh said the long-term risk-reward prospects for ArQule are attractive. ArQule is developing ARQ 197 as a cancer treatment and early stage study data has so far been impressive, he added.
"While we don't see many near-term catalysts for the shares, we nonetheless recommend being constructive given a longer-term outlook," he said.
He lowered his price target to $6 from $7, and noted the company's shares are down 20 percent year-to-date.
Meanwhile, coverage initiations by UBS analyst Jeff Elliott lifted shares of Cheshire, Conn.-based Alexion Pharmaceuticals Inc. and Princeton, N.J.-based Medarex Inc.
Elliott gave Alexion a "Buy" rating with an $82 price target, citing the company's blood disorder drug Soliris. The disorder the drug treats is rare, but the drug costs about $389,000 per year.
Sales in the European Union will likely be more significant in the near term, with U.S. sales underpinning longer term growth, he said.
Alexion shares rose $1.33, or 2.1 percent, to $64.79.
Medarex shares rose 18 cents to $9.77 after Elliott started coverage with a "Buy" and a $14 price target.
The company's cancer drug candidate Ipilimumab is in late-stage development and has shown it can maintain a durable response in patients with metastatic melanoma, a cancer that ordinarily is difficult to treat. But, he said, there is still risk to the drug's approval.
The remainder of the company's pipeline has potential as it matures, he said, and Medarex could be viewed as a viable buyout candidate.
Elliott also initiated coverage of Seattle-based ZymoGenetics Inc. with a "Buy" rating and $16 price target, and Novato, Calif.-based BioMarin Pharmaceutical Inc. at "Neutral" with a $38 price target.
Shares of ZymoGenetics fell 17 cents to $10.52 and shares of BioMarin fell 11 cents to $36.40.
[url08.02.2008 - Änderung des Stammzellengesetzes steht an ]http://www.wiwo.de/politik/aenderung-des-stammzellengesetzes-steht-an-265172/[/url]
Nach sechs Jahren Stillstand zeichnet sich erstmals eine Verbesserung der Arbeitsbedingungen für deutsche Zellforscher ab. Vier Gesetzesentwürfe und ein Antrag, alles zu lassen, wie es ist, bilden am kommenden Donnerstag die Grundlage für eine dreistündige Debatte im Bundestag über eine Änderung des Stammzellgesetzes.
Wie die WirtschaftsWoche berichtet, konnten die Abgeordneten René Röspel (SPD) und Ilse Aigner (CSU) die meisten Unterschriften (185) unter ihren Entwurf sammeln. Sie wollen den Stichtag verschieben, der besagt, dass Forscher nur Zelllinien verwenden dürfen, die vor dem 1. Januar 2002 im Ausland hergestellt wurden. Neuer Stichtag soll der 1. Mai 2007 sein.
Zudem sollen Rechtsunsicherheiten beseitigt werden, denen deutsche Forscher ausgesetzt sind, die etwa im Ausland mit neueren Stammzelllinien forschen oder sich an EU-Projekten beteiligen. Prominenteste Unterstützer des Entwurfs sind Bundesforschungsministerin Annette Schavan (CDU), Gesundheitsministerin Ulla Schmidt (SPD), Verbraucherminister Horst Seehofer (CSU), Wirtschaftsminister Michel Glos (CSU) und der SPD-Fraktionsvorsitzende Peter Struck. Bundeskanzlerin Angela Merkel hat zwar nicht unterschrieben, sich aber ebenfalls für die Stichtagsverschiebung ausgesprochen.
Fast ebenso groß (149 Stimmen) ist die Gruppe um die Grünen-Abgeordnete Priska Hinz, die alles beim alten Recht belassen will. Zu den Unterstützern gehören Unions-Fraktionschef Volker Kauder sowie die Staatsministerinnen Maria Böhmer und Hildegard Müller (beide CDU), aber auch Renate Künast, Claudia Roth und Fritz Kuhn von den Grünen. Ein Teil der Gruppe will per Gesetzentwurf (67 Unterschriften) für deutsche Forscher im Ausland – ähnlich wie beim Aigner/Röspel-Antrag – mehr Rechtssicherheit erreichen. 94 Anhänger hat ein Antrag der FDP-Gentechnikexpertin Ulrike Flach, die – gestützt von der Mehrheit der FDP-Fraktion – die Stichtagsregelung kippen will.
Die extreme Gegenposition dazu vertritt eine Gruppe rund um den Unions-Mann Hubert Hüppe, der von 52 Parlamentariern unterstützt wird. Sie fordern ein generelles Verbot der embryonalen Stammzellforschung. Prominenteste Unterzeichner sind der stellvertretende CDU/CSU-Fraktionsvorsitzende Wolfgang Bosbach, der Rechtsexperte der Grünen, Volker Beck, und der Vorsitzende der Jungen Union, Philipp Mißfelder.
Die gesammelten Unterschriften lagen am Mittwoch, 6. Februar, 14 Uhr vor (Abgabefrist für die Anträge im Bundestag). Welcher Gesetzentwurf sich durchsetzt, ist ungewiss. Als wahrscheinlich gilt, dass viele Anhänger des chancenlosen Flach-Entwurfs für die Stichtagsverschiebung votieren werden und das Hüppe-Lager zum Teil für den Hinz-Antrag stimmt. Da sich jedoch rund 150 Abgeordnete noch nicht festgelegt haben, bleibt das Rennen offen.
Habe Geron noch immer auf der Watchlist. Könnte aber bald Zeit zum Einstieg sein (binnen 6 - 9 Monaten).
Nach sechs Jahren Stillstand zeichnet sich erstmals eine Verbesserung der Arbeitsbedingungen für deutsche Zellforscher ab. Vier Gesetzesentwürfe und ein Antrag, alles zu lassen, wie es ist, bilden am kommenden Donnerstag die Grundlage für eine dreistündige Debatte im Bundestag über eine Änderung des Stammzellgesetzes.
Wie die WirtschaftsWoche berichtet, konnten die Abgeordneten René Röspel (SPD) und Ilse Aigner (CSU) die meisten Unterschriften (185) unter ihren Entwurf sammeln. Sie wollen den Stichtag verschieben, der besagt, dass Forscher nur Zelllinien verwenden dürfen, die vor dem 1. Januar 2002 im Ausland hergestellt wurden. Neuer Stichtag soll der 1. Mai 2007 sein.
Zudem sollen Rechtsunsicherheiten beseitigt werden, denen deutsche Forscher ausgesetzt sind, die etwa im Ausland mit neueren Stammzelllinien forschen oder sich an EU-Projekten beteiligen. Prominenteste Unterstützer des Entwurfs sind Bundesforschungsministerin Annette Schavan (CDU), Gesundheitsministerin Ulla Schmidt (SPD), Verbraucherminister Horst Seehofer (CSU), Wirtschaftsminister Michel Glos (CSU) und der SPD-Fraktionsvorsitzende Peter Struck. Bundeskanzlerin Angela Merkel hat zwar nicht unterschrieben, sich aber ebenfalls für die Stichtagsverschiebung ausgesprochen.
Fast ebenso groß (149 Stimmen) ist die Gruppe um die Grünen-Abgeordnete Priska Hinz, die alles beim alten Recht belassen will. Zu den Unterstützern gehören Unions-Fraktionschef Volker Kauder sowie die Staatsministerinnen Maria Böhmer und Hildegard Müller (beide CDU), aber auch Renate Künast, Claudia Roth und Fritz Kuhn von den Grünen. Ein Teil der Gruppe will per Gesetzentwurf (67 Unterschriften) für deutsche Forscher im Ausland – ähnlich wie beim Aigner/Röspel-Antrag – mehr Rechtssicherheit erreichen. 94 Anhänger hat ein Antrag der FDP-Gentechnikexpertin Ulrike Flach, die – gestützt von der Mehrheit der FDP-Fraktion – die Stichtagsregelung kippen will.
Die extreme Gegenposition dazu vertritt eine Gruppe rund um den Unions-Mann Hubert Hüppe, der von 52 Parlamentariern unterstützt wird. Sie fordern ein generelles Verbot der embryonalen Stammzellforschung. Prominenteste Unterzeichner sind der stellvertretende CDU/CSU-Fraktionsvorsitzende Wolfgang Bosbach, der Rechtsexperte der Grünen, Volker Beck, und der Vorsitzende der Jungen Union, Philipp Mißfelder.
Die gesammelten Unterschriften lagen am Mittwoch, 6. Februar, 14 Uhr vor (Abgabefrist für die Anträge im Bundestag). Welcher Gesetzentwurf sich durchsetzt, ist ungewiss. Als wahrscheinlich gilt, dass viele Anhänger des chancenlosen Flach-Entwurfs für die Stichtagsverschiebung votieren werden und das Hüppe-Lager zum Teil für den Hinz-Antrag stimmt. Da sich jedoch rund 150 Abgeordnete noch nicht festgelegt haben, bleibt das Rennen offen.
Habe Geron noch immer auf der Watchlist. Könnte aber bald Zeit zum Einstieg sein (binnen 6 - 9 Monaten).

Mäuse mit Diabetes konnten mit Stammzellen erfolgreich behandelt werden.
Mittwoch, 20. Februar 2008
Mit Stammzellentherapie
Hilfe für Mäuse mit Diabetes
Mit menschlichen embryonalen Stammzellen haben US-Forscher erfolgreich zuckerkranke Mäuse behandelt. Diese Ergebnisse seien ein wichtiger Schritt auf dem Weg zu einer Zelltherapie für Diabetiker, betonen die Autoren im Fachjournal "Nature Biotechnology". Emmanuel Baetge und seine Arbeitsgruppe vom Biotechnologie-Unternehmen Novocell in San Diego (US-Staat Kalifornien) zeigen mit ihrer Studie, dass sich menschliche embryonale Stammzellen zu insulinproduzierenden Zellen entwickeln können, die in Abhängigkeit vom Blutzuckerspiegel das benötigte Hormon ausschütten.
Aus den embryonalen Stammzellen hatten die Forscher zunächst im Labor Bauchspeicheldrüsengewebe gezüchtet, das dem Gewebe eines sechs bis neun Wochen alten Embryos entspricht. Dieses Gewebe wurde Mäusen eingepflanzt, die zuvor künstlich zuckerkrank gemacht worden waren. Dazu hatten die Forscher die Beta-Zellen der Versuchstiere chemisch zerstört. Beta-Zellen sind üblicherweise für die Blutzuckerregulierung zuständig. Rund einen Monat nach der Einpflanzung beobachteten die Forscher neue insulinproduzierende Zellen, die sich aus dem menschlichen Gewebe entwickelt hatten.
Drei Monate nach der Zellimplantation erreichten diese neuen Beta- Zellen ihre maximale Insulinausschüttung. Ein Großteil der Mäuse produzierte genügend Insulin, um vollständig gegen die künstliche Zuckerkrankheit gewappnet zu sein. Auch die C-Peptid-Werte, ein Maß für die Insulineigenproduktion des Körpers, stiegen auf ein bisher in keinem Experiment erreichtes Niveau, berichten die Forscher. Menschliche embryonale Stammzellen könnten sich als Quelle für nachwachsende Beta-Zellen für Diabetiker erweisen, meinen die Mediziner. Gemäß den Statuten des Fachjournals erklären die Forscher wirtschaftliche Interessen an den Resultaten.
Bis zu einer möglichen Anwendung beim Menschen ist es allerdings noch ein langer Weg - bislang gibt es weltweit für keine Krankheit eine etablierte Therapie mit menschlichen embryonalen Stammzellen. Diabetiker kommen bisher nur durch eine Transplantation der Bauchspeicheldrüse oder eine Infusion mit sogenannten Langerhansschen Inseln, die Beta-Zellen enthalten, zu insulinproduzierenden Zellen. Keines dieser Verfahren ist für die breite Masse der Diabetiker geeignet, unter anderem mangelt es an Spenderorganen.
In Deutschland sind mehr als fünf Millionen Menschen an Diabetes mellitus erkrankt. Davon leiden etwa 250.000 Patienten am Typ 1 Diabetes, für die eine Stammzelltherapie besonders geeignet wäre. Insgesamt starben im Jahr 2006 mehr als 22.000 Deutsche an den Folgen von Diabetes. Die Zahl der Erkrankungen und Todesfälle steigt langfristig an, was vor allem dadurch zu erklären ist, dass zunehmend mehr Menschen sich falsch ernähren, sich zu wenig bewegen und übergewichtig sind.
Mittwoch, 20. Februar 2008
Mit Stammzellentherapie
Hilfe für Mäuse mit Diabetes
Mit menschlichen embryonalen Stammzellen haben US-Forscher erfolgreich zuckerkranke Mäuse behandelt. Diese Ergebnisse seien ein wichtiger Schritt auf dem Weg zu einer Zelltherapie für Diabetiker, betonen die Autoren im Fachjournal "Nature Biotechnology". Emmanuel Baetge und seine Arbeitsgruppe vom Biotechnologie-Unternehmen Novocell in San Diego (US-Staat Kalifornien) zeigen mit ihrer Studie, dass sich menschliche embryonale Stammzellen zu insulinproduzierenden Zellen entwickeln können, die in Abhängigkeit vom Blutzuckerspiegel das benötigte Hormon ausschütten.
Aus den embryonalen Stammzellen hatten die Forscher zunächst im Labor Bauchspeicheldrüsengewebe gezüchtet, das dem Gewebe eines sechs bis neun Wochen alten Embryos entspricht. Dieses Gewebe wurde Mäusen eingepflanzt, die zuvor künstlich zuckerkrank gemacht worden waren. Dazu hatten die Forscher die Beta-Zellen der Versuchstiere chemisch zerstört. Beta-Zellen sind üblicherweise für die Blutzuckerregulierung zuständig. Rund einen Monat nach der Einpflanzung beobachteten die Forscher neue insulinproduzierende Zellen, die sich aus dem menschlichen Gewebe entwickelt hatten.
Drei Monate nach der Zellimplantation erreichten diese neuen Beta- Zellen ihre maximale Insulinausschüttung. Ein Großteil der Mäuse produzierte genügend Insulin, um vollständig gegen die künstliche Zuckerkrankheit gewappnet zu sein. Auch die C-Peptid-Werte, ein Maß für die Insulineigenproduktion des Körpers, stiegen auf ein bisher in keinem Experiment erreichtes Niveau, berichten die Forscher. Menschliche embryonale Stammzellen könnten sich als Quelle für nachwachsende Beta-Zellen für Diabetiker erweisen, meinen die Mediziner. Gemäß den Statuten des Fachjournals erklären die Forscher wirtschaftliche Interessen an den Resultaten.
Bis zu einer möglichen Anwendung beim Menschen ist es allerdings noch ein langer Weg - bislang gibt es weltweit für keine Krankheit eine etablierte Therapie mit menschlichen embryonalen Stammzellen. Diabetiker kommen bisher nur durch eine Transplantation der Bauchspeicheldrüse oder eine Infusion mit sogenannten Langerhansschen Inseln, die Beta-Zellen enthalten, zu insulinproduzierenden Zellen. Keines dieser Verfahren ist für die breite Masse der Diabetiker geeignet, unter anderem mangelt es an Spenderorganen.
In Deutschland sind mehr als fünf Millionen Menschen an Diabetes mellitus erkrankt. Davon leiden etwa 250.000 Patienten am Typ 1 Diabetes, für die eine Stammzelltherapie besonders geeignet wäre. Insgesamt starben im Jahr 2006 mehr als 22.000 Deutsche an den Folgen von Diabetes. Die Zahl der Erkrankungen und Todesfälle steigt langfristig an, was vor allem dadurch zu erklären ist, dass zunehmend mehr Menschen sich falsch ernähren, sich zu wenig bewegen und übergewichtig sind.
Herzmuskelzellen aus der Stammzellenforschung
Wissenschaftler feiern Entdeckung als Meilenstein in der Forschung
Entschlüsselung der Herzentwicklung auf molekularer Ebene (Foto: pixelio.de)
München (pte/29.02.2008/06:05) - Nichts scheidet die Geister so sehr wie die Forschung an embryonalen Stammzellen. Zwar ist sie seit Jahren heftig umstritten, doch für die Wissenschaft stellt sie eines der zukunftsträchtigsten Felder dar. Diabetes mellitus, Herzinfarkte oder Unfälle haben eine Zerstörung von Gewebe oder ganzer Organe zur Folge. Engpässe bei Spenderorganen lassen die Hoffnung auf regenerative Medizin durch Stammzellen wachsen. Forschern der Medizinischen Klinik und Poliklinik I der Universität München http://med1.klinikum.uni-muenchen.de/ ist es erstmalig gelungen, grundlegende Prozesse der Herzentwicklung auf molekularer Ebene zu entschlüsseln. Dadurch ist eine vermehrte Bildung von schlagenden Herzmuskelzellen aus embryonalen Stammzellen möglich.
Um die Prozesse der Herzentwicklung auf molekularer Ebene entschlüsseln zu können, programmierten die Forscher pluripotente Stammzellen mit einem herzspezifischen Protein. Pluripotente Stammzellen sind "zu allem fähig" und befinden sich im so genannten Blastozysten-Stadium der Embryonenentwicklung. Spätestens nach drei Tagen spezialisieren sich diese Zellen sehr stark. Ihre Besonderheit liegt darin, dass zwar alle Zellarten wie beispielsweise Muskelgewebe oder Nerven entwickelt werden können, die Entwicklung eines vollständigen Organismus aber nicht mehr möglich ist. Dieser letzte Aspekt stellt eine wichtige Komponente in der Diskussion zu embryonalen Stammzellen dar.
Dieses Forschungsergebnis der Arbeitsgruppe um den Münchener Professor Wolfgang-Michael Franz stellt einen Meilenstein für das Verständnis der Programmierung von Stammzellen zu Herzmuskelzellen dar. " Unsere Forschung bezieht sich nur auf Stammzellen, die nach einem bestimmten clinical grade, dem GMP (Good Manufacturing Practice) hergestellt wurden. Damit in Zukunft auch Patienten von dieser bedeutenden Entwicklung profitieren können, müssen diese Ergebnisse eben auf diese Stammzellen übertragen werden. Diese können aber nur aus dem Ausland bezogen werden", erklärt Wolfgang-Michael Franz, Stammzellenforscher an der Medizinischen Klinik und Poliklinik I der Universität München auf Anfrage von pressetext. Auf die Frage, ob Tierversuche geplant sind meint Franz: "Bis dato kommen Tierversuche für uns noch nicht in Frage. Etabliert sich unsere Forschung, können wir uns am Mausmodell zum Beispiel Transplantationen vorstellen", sagt Franz.
Laut Franz können solche Zellen auch für die Erprobung von Medikamenten eingesetzt werden. „Vorausgesetzt ist eine Liberalisierung der Stichtagsregelung des deutschen Stammzellengesetzes“, sagt Franz. Die sogenannte deutsche Stichtagsregelung erlaubt den Import von humanen embryonalen Stammzellen, die vor dem 1. Januar 2002 etabliert wurden. Dadurch bleibt den deutschen Wissenschaftlern die Arbeit mit neueren embryonalen Stammzelllinien verwährt. Der Bundestag entscheidet voraussichtlich im April 2008 über eine mögliche Änderung des Stammzellgesetzes. (Ende)
Wissenschaftler feiern Entdeckung als Meilenstein in der Forschung
Entschlüsselung der Herzentwicklung auf molekularer Ebene (Foto: pixelio.de)
München (pte/29.02.2008/06:05) - Nichts scheidet die Geister so sehr wie die Forschung an embryonalen Stammzellen. Zwar ist sie seit Jahren heftig umstritten, doch für die Wissenschaft stellt sie eines der zukunftsträchtigsten Felder dar. Diabetes mellitus, Herzinfarkte oder Unfälle haben eine Zerstörung von Gewebe oder ganzer Organe zur Folge. Engpässe bei Spenderorganen lassen die Hoffnung auf regenerative Medizin durch Stammzellen wachsen. Forschern der Medizinischen Klinik und Poliklinik I der Universität München http://med1.klinikum.uni-muenchen.de/ ist es erstmalig gelungen, grundlegende Prozesse der Herzentwicklung auf molekularer Ebene zu entschlüsseln. Dadurch ist eine vermehrte Bildung von schlagenden Herzmuskelzellen aus embryonalen Stammzellen möglich.
Um die Prozesse der Herzentwicklung auf molekularer Ebene entschlüsseln zu können, programmierten die Forscher pluripotente Stammzellen mit einem herzspezifischen Protein. Pluripotente Stammzellen sind "zu allem fähig" und befinden sich im so genannten Blastozysten-Stadium der Embryonenentwicklung. Spätestens nach drei Tagen spezialisieren sich diese Zellen sehr stark. Ihre Besonderheit liegt darin, dass zwar alle Zellarten wie beispielsweise Muskelgewebe oder Nerven entwickelt werden können, die Entwicklung eines vollständigen Organismus aber nicht mehr möglich ist. Dieser letzte Aspekt stellt eine wichtige Komponente in der Diskussion zu embryonalen Stammzellen dar.
Dieses Forschungsergebnis der Arbeitsgruppe um den Münchener Professor Wolfgang-Michael Franz stellt einen Meilenstein für das Verständnis der Programmierung von Stammzellen zu Herzmuskelzellen dar. " Unsere Forschung bezieht sich nur auf Stammzellen, die nach einem bestimmten clinical grade, dem GMP (Good Manufacturing Practice) hergestellt wurden. Damit in Zukunft auch Patienten von dieser bedeutenden Entwicklung profitieren können, müssen diese Ergebnisse eben auf diese Stammzellen übertragen werden. Diese können aber nur aus dem Ausland bezogen werden", erklärt Wolfgang-Michael Franz, Stammzellenforscher an der Medizinischen Klinik und Poliklinik I der Universität München auf Anfrage von pressetext. Auf die Frage, ob Tierversuche geplant sind meint Franz: "Bis dato kommen Tierversuche für uns noch nicht in Frage. Etabliert sich unsere Forschung, können wir uns am Mausmodell zum Beispiel Transplantationen vorstellen", sagt Franz.
Laut Franz können solche Zellen auch für die Erprobung von Medikamenten eingesetzt werden. „Vorausgesetzt ist eine Liberalisierung der Stichtagsregelung des deutschen Stammzellengesetzes“, sagt Franz. Die sogenannte deutsche Stichtagsregelung erlaubt den Import von humanen embryonalen Stammzellen, die vor dem 1. Januar 2002 etabliert wurden. Dadurch bleibt den deutschen Wissenschaftlern die Arbeit mit neueren embryonalen Stammzelllinien verwährt. Der Bundestag entscheidet voraussichtlich im April 2008 über eine mögliche Änderung des Stammzellgesetzes. (Ende)
http://biz.yahoo.com/e/080331/gern8-k.html
Die schonen echt ihre Barreserven und bezahlen scheinabr alles mit Aktien. Auch Girindus (588 040) bekommt nen ordentlichen Batzen Scheine. Girindus auf dem Weg zum Oligo-Monopol.
Die schonen echt ihre Barreserven und bezahlen scheinabr alles mit Aktien. Auch Girindus (588 040) bekommt nen ordentlichen Batzen Scheine. Girindus auf dem Weg zum Oligo-Monopol.
Vielleicht schafft Geron heute die 5$.
5$*375,926=1,879,630$
immerhin...
5$*375,926=1,879,630$
immerhin...
Antwort auf Beitrag Nr.: 33.770.989 von Salem- am 31.03.08 21:08:28Willst wohl deine Grindus in den Himmel loben!
Embryonale Stammmzellem sind scheinbar tot!
Wildere doch irgendwo ansers.


Embryonale Stammmzellem sind scheinbar tot!
Wildere doch irgendwo ansers.



Stammzellen brauchen noch mindestens 5.000, wenn nicht sogar 1 Milliarden Jahre, aber bei GRN163L gehts wenigstens mit mehreren Studien los.
Kick mal bei http://www.clinicaltrial.gov/! Kannste ja mal die Nüstern reinhalten und nach Geron suchen. Stammzellen sind noch offiziell Teufelswerk und der Papst hat sicher das letzte Wort.
Und wer bei Oligos deutsche Wertarbeit haben will, geht nunmal zu Girindus.
Ich wünsche trotzdem Erfolg!
Kick mal bei http://www.clinicaltrial.gov/! Kannste ja mal die Nüstern reinhalten und nach Geron suchen. Stammzellen sind noch offiziell Teufelswerk und der Papst hat sicher das letzte Wort.

Und wer bei Oligos deutsche Wertarbeit haben will, geht nunmal zu Girindus.
Ich wünsche trotzdem Erfolg!

Antwort auf Beitrag Nr.: 33.771.253 von Salem- am 31.03.08 21:31:02Benutzername: Salem88 (gesperrt)
Registriert seit: 21.10.2004 [ seit 1.257 Tagen ]
Benutzer ist momentan: Offline seit dem 28.10.2007 um 20:40
Erstellte Themen: 10 [ 291 - Verhältnis Postings zu Threads ]
Alle Threads anzeigen
Erstellte Antworten: 2911 [ Durchschnittlich 2,3157 Beiträge/Tag ]
Postings der letzten 30 Tage anzeigen
Bist nicht zufälligerweise DU!!



Registriert seit: 21.10.2004 [ seit 1.257 Tagen ]
Benutzer ist momentan: Offline seit dem 28.10.2007 um 20:40
Erstellte Themen: 10 [ 291 - Verhältnis Postings zu Threads ]
Alle Threads anzeigen
Erstellte Antworten: 2911 [ Durchschnittlich 2,3157 Beiträge/Tag ]
Postings der letzten 30 Tage anzeigen
Bist nicht zufälligerweise DU!!




Ja der war ich. Aber diesmal bin ich friedlich und ohne "88er Ideologie". Es ging damals um die "88" in meinem Nick. Als GIR Aktionär bekomme ich es numal mit, wenn sich Unternehmen die Dienste von Girindus sichern. Das hat auch seine Gründe. Hat schon Solvay erkannt. Und es ist ja nicht nur Geron Kunde von GIR. Ich wäre wie Du heilfroh, wenn die Oligos/Antisense/mRNA u.s.w., sich als Thearpie durchsetzen. Aber es wird noch ein langer, steiniger Weg zu gehen sein.
Hat schon Solvay erkannt. Und es ist ja nicht nur Geron Kunde von GIR. Ich wäre wie Du heilfroh, wenn die Oligos/Antisense/mRNA u.s.w., sich als Thearpie durchsetzen. Aber es wird noch ein langer, steiniger Weg zu gehen sein.
 Hat schon Solvay erkannt. Und es ist ja nicht nur Geron Kunde von GIR. Ich wäre wie Du heilfroh, wenn die Oligos/Antisense/mRNA u.s.w., sich als Thearpie durchsetzen. Aber es wird noch ein langer, steiniger Weg zu gehen sein.
Hat schon Solvay erkannt. Und es ist ja nicht nur Geron Kunde von GIR. Ich wäre wie Du heilfroh, wenn die Oligos/Antisense/mRNA u.s.w., sich als Thearpie durchsetzen. Aber es wird noch ein langer, steiniger Weg zu gehen sein.
FDA to take key stem-cell step
Government advisors meet this week to discuss designs for embryonic stem cell testing in humans.
EMAIL | PRINT | DIGG | RSS Subscribe to Companies
feed://rss.cnn.com/rss/money_news_companies.rss
Paste this link into your favorite RSS desktop reader
See all CNNMoney.com RSS FEEDS (close) By Aaron Smith, CNNMoney.com staff writer
April 9, 2008: 3:31 PM EDT
Gator blood a super drug?
More Videos
NEW YORK (CNNMoney.com) -- The Food and Drug Administration looks like it's bowing to the inevitable this week and drawing the blueprint for the first-ever human experiments with human embryonic stem cells.
FDA advisors meet Thursday and Friday to begin to design how these embryonic stem cell tests will be conducted. It's an important regulatory step that could lead to human testing as early as this year. So far, biotechs have tested their spinal-cord drugs in animals, not people.
"[The FDA meeting] is the first step towards clinical trials," said Laurie Zoloth, professor of medical humanities and bioethics at Northwestern University. "It's an important moment. And it's only the very beginning."
Human embryos are prized by medical researchers because of their fast and malleable regenerative properties. In theory, they could be used to heal severed spines, as well as damaged or diseased brains, hearts and other organs.
But their use is one of the most controversial issues in medical research, a controversy that centers on whether embryonic cell groupings, called blastocysts, are considered human life.
Dave Prentice, senior fellow for life sciences at the Christian organization Family Research Council, opposes the use of human embryos in research. "You shouldn't be destroying human embryos at the earlier stage of human life to harvest cells," said Prentice, who has a PhD. in biochemistry from the University of Kansas.
Other stem cell options are available, he said, such as harvesting them from umbilical cord blood or adult tissue, or "reprogramming" adult cells to behave like stem cells, as demonstrated in recently-released but early-stage studies.
Zoloth said she supports stem cell research because "the human embryo does not have the moral status of a dying child." Like other supporters, she pointed to the vast potential - though still unproven - of this science in healing traumatic injuries and degenerative diseases.
"I strongly support learning as much as we possibly can about human embryonic stem cells, as well as learning about other types of regenerative medicines," she said. "The fact that science could develop ways of healing very tragic human fates is an extraordinary capacity that we have been given by God. For people who aren't religious, you might say that we stand in a remarkable moment in human history."
Safety over ethics for the FDAThe FDA seems to be more concerned with the stem cells' possible side effect of producing tumors. Because of the "potential risks" of human embryonic stem cell products, data showing a drug's effectiveness "may need to be particularly strong," the document said.
An administration spokesman would not comment further than the released document.
"The FDA needs to feel comfortable that the cells we use for our cell products will not cause teratomas," said Alan Lewis, chief executive of privately-held biotech Novocell, which hopes to begin human stem cell testing within three years for a possible diabetes treatment.
Lewis described the teratomas as non-malignant but unwanted pieces of muscle, hair or other matter that form as an offshoot of embryonic stem cells, which replicate quickly and can morph into different types of tissues, such as the liver or pancreas.
The biotechs line up
Geron (GERN) could be the first company to conduct experiments in humans with drugs made from human embryonic stem cells. The biotech is developing a treatment to repair spinal cord injuries. Geron has already filed an application to the FDA to begin human testing, according to analysts. But the biotech refused to confirm this and would not discuss the upcoming meeting.
So far, Geron's animal experiments have been tumor-free, said UBS analyst Graig Suvannavejh, who doesn't expect the company to run into problems with the FDA.
"For Geron, the best possible outcome overall is for [the] FDA to be peachy with everything they've done so far," said Suvannavejh in an email to CNNMoney.com. He believes Geron could begin human testing by mid-2008.
Steve Brozak, analyst for WBB Securities, emphasized that tumor-safety is imperative, and there is little room for failure in the current environment.
"It is one of the things that can be a problem if the science is not understood completely," he said. Geron needs "to make sure that the critics of the field don't have room to assail them with."
Advanced Cell is using embryonic stem cells to develop a treatment for vision loss. Chief scientific officer Robert Lanza said his company plans to file an application for human testing to the FDA within months. He said the company has found a way to "differentiate" stem cells to reduce the possibility of tumor formation.
Neuralstem (CUR) works with stem cells derived from a donated human fetus, rather than embryonic stem cells. CEO Richard Garr said his company is developing a treatment for Lou Gehrig's disease, which degrades spinal cord nerve cells. He intends to file an application for human testing to the FDA in September or October.
Garr said that his company's pig tests have been tumor-free, and he hopes the FDA panelists focus on the science of stem cells, not the controversy, in designing requirements for clinical trials.
"What we hope to come out of this meeting is rationality," said Garr. "[We] hope that this isn't just something that a stem cell-unfriendly administration is trying put in place before they leave."
Nursing: the recession-proof job market
Government advisors meet this week to discuss designs for embryonic stem cell testing in humans.
EMAIL | PRINT | DIGG | RSS Subscribe to Companies
feed://rss.cnn.com/rss/money_news_companies.rss
Paste this link into your favorite RSS desktop reader
See all CNNMoney.com RSS FEEDS (close) By Aaron Smith, CNNMoney.com staff writer
April 9, 2008: 3:31 PM EDT
Gator blood a super drug?
More Videos
NEW YORK (CNNMoney.com) -- The Food and Drug Administration looks like it's bowing to the inevitable this week and drawing the blueprint for the first-ever human experiments with human embryonic stem cells.
FDA advisors meet Thursday and Friday to begin to design how these embryonic stem cell tests will be conducted. It's an important regulatory step that could lead to human testing as early as this year. So far, biotechs have tested their spinal-cord drugs in animals, not people.
"[The FDA meeting] is the first step towards clinical trials," said Laurie Zoloth, professor of medical humanities and bioethics at Northwestern University. "It's an important moment. And it's only the very beginning."
Human embryos are prized by medical researchers because of their fast and malleable regenerative properties. In theory, they could be used to heal severed spines, as well as damaged or diseased brains, hearts and other organs.
But their use is one of the most controversial issues in medical research, a controversy that centers on whether embryonic cell groupings, called blastocysts, are considered human life.
Dave Prentice, senior fellow for life sciences at the Christian organization Family Research Council, opposes the use of human embryos in research. "You shouldn't be destroying human embryos at the earlier stage of human life to harvest cells," said Prentice, who has a PhD. in biochemistry from the University of Kansas.
Other stem cell options are available, he said, such as harvesting them from umbilical cord blood or adult tissue, or "reprogramming" adult cells to behave like stem cells, as demonstrated in recently-released but early-stage studies.
Zoloth said she supports stem cell research because "the human embryo does not have the moral status of a dying child." Like other supporters, she pointed to the vast potential - though still unproven - of this science in healing traumatic injuries and degenerative diseases.
"I strongly support learning as much as we possibly can about human embryonic stem cells, as well as learning about other types of regenerative medicines," she said. "The fact that science could develop ways of healing very tragic human fates is an extraordinary capacity that we have been given by God. For people who aren't religious, you might say that we stand in a remarkable moment in human history."
Safety over ethics for the FDAThe FDA seems to be more concerned with the stem cells' possible side effect of producing tumors. Because of the "potential risks" of human embryonic stem cell products, data showing a drug's effectiveness "may need to be particularly strong," the document said.
An administration spokesman would not comment further than the released document.
"The FDA needs to feel comfortable that the cells we use for our cell products will not cause teratomas," said Alan Lewis, chief executive of privately-held biotech Novocell, which hopes to begin human stem cell testing within three years for a possible diabetes treatment.
Lewis described the teratomas as non-malignant but unwanted pieces of muscle, hair or other matter that form as an offshoot of embryonic stem cells, which replicate quickly and can morph into different types of tissues, such as the liver or pancreas.
The biotechs line up
Geron (GERN) could be the first company to conduct experiments in humans with drugs made from human embryonic stem cells. The biotech is developing a treatment to repair spinal cord injuries. Geron has already filed an application to the FDA to begin human testing, according to analysts. But the biotech refused to confirm this and would not discuss the upcoming meeting.
So far, Geron's animal experiments have been tumor-free, said UBS analyst Graig Suvannavejh, who doesn't expect the company to run into problems with the FDA.
"For Geron, the best possible outcome overall is for [the] FDA to be peachy with everything they've done so far," said Suvannavejh in an email to CNNMoney.com. He believes Geron could begin human testing by mid-2008.
Steve Brozak, analyst for WBB Securities, emphasized that tumor-safety is imperative, and there is little room for failure in the current environment.
"It is one of the things that can be a problem if the science is not understood completely," he said. Geron needs "to make sure that the critics of the field don't have room to assail them with."
Advanced Cell is using embryonic stem cells to develop a treatment for vision loss. Chief scientific officer Robert Lanza said his company plans to file an application for human testing to the FDA within months. He said the company has found a way to "differentiate" stem cells to reduce the possibility of tumor formation.
Neuralstem (CUR) works with stem cells derived from a donated human fetus, rather than embryonic stem cells. CEO Richard Garr said his company is developing a treatment for Lou Gehrig's disease, which degrades spinal cord nerve cells. He intends to file an application for human testing to the FDA in September or October.
Garr said that his company's pig tests have been tumor-free, and he hopes the FDA panelists focus on the science of stem cells, not the controversy, in designing requirements for clinical trials.
"What we hope to come out of this meeting is rationality," said Garr. "[We] hope that this isn't just something that a stem cell-unfriendly administration is trying put in place before they leave."
Nursing: the recession-proof job market
In Deutschland fällt heute die politische Entscheidung über die Regelung des Feldes; in den USA bereiten sich Behörden auf technische Details der Zulassung vor.
Diesen Sommer sollen in den USA erste Tests von embryonalen Stammzellen (ES) bzw. daraus gewonnenen Zellen an Menschen beginnen: Die Firma Geron plant, Querschnittsgelähmten mit Nervenzellen zu helfen (www.geron.com). Andere wollen folgen, die Firma Neuralstem zielt auch mit Nervenzellen auf ALS – eine fortschreitende Lähmung, auch Lou Gehrig's Disease genannt –, Advanced Cell will mit Sehpigmentzellen bestimmte Formen der Erblindung bekämpfen. Deshalb hat die zuständige Behörde – Food and Drug Administration, FDA – für Donnerstag/Freitag eine Tagung angesetzt, auf der die technischen Probleme der Anwendung dieser Zellen präzisiert werden.
Umstrittene Stichtagsregelung
Um die ethischen Probleme der Forschung an den Zellen geht es hingegen in Deutschland: Heute, Freitag, entscheidet der Bundestag darüber, wie es bei ES weitergeht. Mit der bisherigen Regelung – in Deutschland dürfen keine ES hergestellt werden, aber bestimmte Zelllinien dürfen zu Forschungszwecken importiert werden, es gilt eine Stichtagsregelung, die Zelllinien müssen vor dem 1.1.2002 hergestellt worden sein – ist niemand zufrieden. Die Forschung will jüngere Zellen (importieren, die Herstellung in Deutschland fordert niemand), die Kirchen wollen überhaupt keine Forschung an ES (weil bei deren Herstellung Embryos zerstört werden). Das Parlament muss entscheiden, die Parteien sind ineinander gespalten, vier Gruppen haben sich zusammengefunden: Die eine will ein Verbot, die zweite eine Freigabe (Import ohne Stichtagsregelung), die dritte empfiehlt eine einmalige Stichtagsverschiebung (auf 1.5.2007), die vierte will alles beim Alten lassen.
Bundeskanzlerin Merkel und Forschungsministerin Schavan sind die prominentesten Vertreterinnen der dritten Gruppe, diese hat im Vorfeld die meisten Unterstützer gefunden, 182 unterschrieben dafür. Allerdings gibt es viele Unentschiedene, und es ist unklar, wie sich die jüngsten Entwicklungen auf deren Abstimmungsverhalten auswirken werden, vor allem die in England, wo gerade erstmals ein Mischwesen aus Mensch und Kuh gebaut wurde, um ES zu gewinnen. Damit will man die ethischen Probleme umgehen – das Mischwesen ist kein menschlicher Embryo –, stieß aber auf breite Empörung, in England ziehen christliche Gruppen laut BBC (9.4.) gegen das Experiment bzw. die Regulierungsbehörde vor Gericht.
In Bewegung kommen wird die Lage auch in den USA, derzeit ist sie höchst verwirrend: Öffentlich geförderte Forschung – also vor allem die an Universitäten – darf ähnlich wie in Deutschland nur mit Zellen arbeiten, die vor einem gewissen Stichtag gewonnen wurden; private Forschung hingegen – also vor allem die der Pharmaindustrie – darf alles, sie agiert in einem gesetzesfreien Raum. Ob sich Letzteres nach der Präsidentenwahl ändern wird, ist unbekannt, die Lage der öffentlichen Forschung hingegen wird sich ändern, alle drei verbliebenen Kandidaten – McCain, Clinton, Obama – haben sich für eine Liberalisierung ausgesprochen, Stammzellen sind diesmal kein großes Wahlkampfthema.
Gefahr: Krebs
Stattdessen wächst der Regelungsbedarf bei der Anwendung, die Zeit für die FDA wird knapp, der Druck von Industrie – und Patienten – steigt, deshalb die derzeitige Tagung. Klären soll sie vor allem, wie sicher – vor der Nebenfolge Krebs – Stammzelltherapien sind: ES wachsen, sofern sie in Körpergewebe injiziert werden, zu besonderen Tumoren heran, zu Teratomen (das ist nachgerade das äußerliche Erkennungszeichen von ES, innerlich sind sie durch Genaktivitäten charakterisiert). Nun will niemand ES injizieren, man will aus ES die differenzierten Zellen ziehen, die man als Transplantate braucht, Nervenzellen etwa. Aber zum Transplantieren braucht man Millionen Zellen, darunter darf keine einzige ES sein.
Im Vorfeld der FDA-Tagung ließen die Firmen wissen, sie hätten das Problem gelöst und in letzten Vorversuchen – an Schweinen – keine Tumore gesehen, die Zellen hätten sich auch alle entwickelt wie vorgesehen. Das ist die zweite Sorge: Niemand will, dass man etwa Hirnzellen implantiert – und Knochenzellen daraus werden.
Beide Sorgen gibt es auch bei den Zellen, die ethisch keine Probleme machen, aber in ihrer Nützlichkeit umstritten sind: adulten Stammzellen, etwa aus Knochenmark oder Nabelschnurblut. Auch sie können sich zu Tumoren entwickeln, das ist eines der Themen auf dem dritten derzeitigen Großtreffen des Feldes, die britischen Spezialisten tagen in Edinburgh (www.bbsrc.ac.uk).
STAMMZELLEN: Vielfalt
ES, embryonale Stammzellen: Aus ihnen kann sich jeder Zelltyp entwickeln. Bei der Herstellung werden Embryos zerstört.
iPS, induzierte pluripotente Stammzellen: Auch aus ihnen kann sich jeder Zelltyp entwickeln. Zur Gewinnung werden Zellen verjüngt, man hat noch wenig Erfahrung.
Adulte: Auch sie haben keine ethischen Probleme – sie stammen etwa aus Knochenmark –, aber ihr Nutzen ist umstritten.
("Die Presse", Print-Ausgabe, 11.04.2008)
Diesen Sommer sollen in den USA erste Tests von embryonalen Stammzellen (ES) bzw. daraus gewonnenen Zellen an Menschen beginnen: Die Firma Geron plant, Querschnittsgelähmten mit Nervenzellen zu helfen (www.geron.com). Andere wollen folgen, die Firma Neuralstem zielt auch mit Nervenzellen auf ALS – eine fortschreitende Lähmung, auch Lou Gehrig's Disease genannt –, Advanced Cell will mit Sehpigmentzellen bestimmte Formen der Erblindung bekämpfen. Deshalb hat die zuständige Behörde – Food and Drug Administration, FDA – für Donnerstag/Freitag eine Tagung angesetzt, auf der die technischen Probleme der Anwendung dieser Zellen präzisiert werden.
Umstrittene Stichtagsregelung
Um die ethischen Probleme der Forschung an den Zellen geht es hingegen in Deutschland: Heute, Freitag, entscheidet der Bundestag darüber, wie es bei ES weitergeht. Mit der bisherigen Regelung – in Deutschland dürfen keine ES hergestellt werden, aber bestimmte Zelllinien dürfen zu Forschungszwecken importiert werden, es gilt eine Stichtagsregelung, die Zelllinien müssen vor dem 1.1.2002 hergestellt worden sein – ist niemand zufrieden. Die Forschung will jüngere Zellen (importieren, die Herstellung in Deutschland fordert niemand), die Kirchen wollen überhaupt keine Forschung an ES (weil bei deren Herstellung Embryos zerstört werden). Das Parlament muss entscheiden, die Parteien sind ineinander gespalten, vier Gruppen haben sich zusammengefunden: Die eine will ein Verbot, die zweite eine Freigabe (Import ohne Stichtagsregelung), die dritte empfiehlt eine einmalige Stichtagsverschiebung (auf 1.5.2007), die vierte will alles beim Alten lassen.
Bundeskanzlerin Merkel und Forschungsministerin Schavan sind die prominentesten Vertreterinnen der dritten Gruppe, diese hat im Vorfeld die meisten Unterstützer gefunden, 182 unterschrieben dafür. Allerdings gibt es viele Unentschiedene, und es ist unklar, wie sich die jüngsten Entwicklungen auf deren Abstimmungsverhalten auswirken werden, vor allem die in England, wo gerade erstmals ein Mischwesen aus Mensch und Kuh gebaut wurde, um ES zu gewinnen. Damit will man die ethischen Probleme umgehen – das Mischwesen ist kein menschlicher Embryo –, stieß aber auf breite Empörung, in England ziehen christliche Gruppen laut BBC (9.4.) gegen das Experiment bzw. die Regulierungsbehörde vor Gericht.
In Bewegung kommen wird die Lage auch in den USA, derzeit ist sie höchst verwirrend: Öffentlich geförderte Forschung – also vor allem die an Universitäten – darf ähnlich wie in Deutschland nur mit Zellen arbeiten, die vor einem gewissen Stichtag gewonnen wurden; private Forschung hingegen – also vor allem die der Pharmaindustrie – darf alles, sie agiert in einem gesetzesfreien Raum. Ob sich Letzteres nach der Präsidentenwahl ändern wird, ist unbekannt, die Lage der öffentlichen Forschung hingegen wird sich ändern, alle drei verbliebenen Kandidaten – McCain, Clinton, Obama – haben sich für eine Liberalisierung ausgesprochen, Stammzellen sind diesmal kein großes Wahlkampfthema.
Gefahr: Krebs
Stattdessen wächst der Regelungsbedarf bei der Anwendung, die Zeit für die FDA wird knapp, der Druck von Industrie – und Patienten – steigt, deshalb die derzeitige Tagung. Klären soll sie vor allem, wie sicher – vor der Nebenfolge Krebs – Stammzelltherapien sind: ES wachsen, sofern sie in Körpergewebe injiziert werden, zu besonderen Tumoren heran, zu Teratomen (das ist nachgerade das äußerliche Erkennungszeichen von ES, innerlich sind sie durch Genaktivitäten charakterisiert). Nun will niemand ES injizieren, man will aus ES die differenzierten Zellen ziehen, die man als Transplantate braucht, Nervenzellen etwa. Aber zum Transplantieren braucht man Millionen Zellen, darunter darf keine einzige ES sein.
Im Vorfeld der FDA-Tagung ließen die Firmen wissen, sie hätten das Problem gelöst und in letzten Vorversuchen – an Schweinen – keine Tumore gesehen, die Zellen hätten sich auch alle entwickelt wie vorgesehen. Das ist die zweite Sorge: Niemand will, dass man etwa Hirnzellen implantiert – und Knochenzellen daraus werden.
Beide Sorgen gibt es auch bei den Zellen, die ethisch keine Probleme machen, aber in ihrer Nützlichkeit umstritten sind: adulten Stammzellen, etwa aus Knochenmark oder Nabelschnurblut. Auch sie können sich zu Tumoren entwickeln, das ist eines der Themen auf dem dritten derzeitigen Großtreffen des Feldes, die britischen Spezialisten tagen in Edinburgh (www.bbsrc.ac.uk).
STAMMZELLEN: Vielfalt
ES, embryonale Stammzellen: Aus ihnen kann sich jeder Zelltyp entwickeln. Bei der Herstellung werden Embryos zerstört.
iPS, induzierte pluripotente Stammzellen: Auch aus ihnen kann sich jeder Zelltyp entwickeln. Zur Gewinnung werden Zellen verjüngt, man hat noch wenig Erfahrung.
Adulte: Auch sie haben keine ethischen Probleme – sie stammen etwa aus Knochenmark –, aber ihr Nutzen ist umstritten.
("Die Presse", Print-Ausgabe, 11.04.2008)
Poppen für neues Genmaterial zur Heilung der Kloppies dieser Welt. Ab heute auch in Germany möglich.
Na mal sehen was Geron heute macht. Hat Geron denn in Germany Forschung?

Na mal sehen was Geron heute macht. Hat Geron denn in Germany Forschung?
Antwort auf Beitrag Nr.: 33.865.001 von Salem- am 11.04.08 11:50:06Bin mal mit 2000 Stk. dabei. Mal sehen was geht.

Antwort auf Beitrag Nr.: 33.865.720 von Kambyses am 11.04.08 13:02:12Zahlreiche Studienergebnisse in den laufenden Wochen erwartet. GERN163L, Geron´s Telomerase Inhibitor.
http://biz.yahoo.com/bw/080416/20080416005314.html?.v=1
7:34AM Geron announces new data on activity of GRN163L in breast cancer cells (GERN) 5.07 : Co announces five presentations of its anti-cancer drug, GRN163L, given at this year's American Association for Cancer Research meeting. Co is currently testing GRN163L in four clinical trials with 15 U.S. medical centers recruiting patients with solid tumors, chronic lymphoproliferative disease, multiple myeloma and non-small cell lung cancer. New combination trials in breast cancer and multiple myeloma at additional trial sites are scheduled to initiate in the coming months. Co is also conducting a multi-center Phase II trial of GRNVAC1, a telomerase therapeutic vaccine, in high risk acute myelogenous leukemia patients. Co expects Merck (MRK), under license from Geron, to initiate a therapeutic vaccine trial targeting telomerase in patients with non-small cell lung and prostate cancers.
http://finance.yahoo.com/marketupdate/inplay
http://biz.yahoo.com/bw/080416/20080416005314.html?.v=1
7:34AM Geron announces new data on activity of GRN163L in breast cancer cells (GERN) 5.07 : Co announces five presentations of its anti-cancer drug, GRN163L, given at this year's American Association for Cancer Research meeting. Co is currently testing GRN163L in four clinical trials with 15 U.S. medical centers recruiting patients with solid tumors, chronic lymphoproliferative disease, multiple myeloma and non-small cell lung cancer. New combination trials in breast cancer and multiple myeloma at additional trial sites are scheduled to initiate in the coming months. Co is also conducting a multi-center Phase II trial of GRNVAC1, a telomerase therapeutic vaccine, in high risk acute myelogenous leukemia patients. Co expects Merck (MRK), under license from Geron, to initiate a therapeutic vaccine trial targeting telomerase in patients with non-small cell lung and prostate cancers.
http://finance.yahoo.com/marketupdate/inplay
Die jetzt laufenden Studien mit GRN163L sowie die zu erwartenden Ergebnisse, werden die Weichen stellen, ob und für welchen Anwendungsbereich GRN163L letztendlich ne Marktchance hat. Auch wichtig für zukünfige Vermarktungspartner.
Hoffentlich klappt alles!
Hoffentlich klappt alles!
Antwort auf Beitrag Nr.: 33.899.585 von Salem- am 16.04.08 16:18:59Das hoffe ich auch. Bin etwas zu früh eingestigen. Hätte erst auf die kleine Korrektur oder die Gewinnmitnahmen warten sollen. Wenn bei GRN163L Erfolg versprechende Ansätze vorhanden sein sollten, müßte das den Kurs etwas beflügeln.
Antwort auf Beitrag Nr.: 33.907.512 von Kambyses am 17.04.08 13:02:19Das wirst Du in den nächsten Wochen gaaaaaaannnnnz sicher mitbekommen. Was die Veröffentlichung von Studienergebnisse anbetrifft, sind die Amis äußerst sensibel. Was mich von einem Engagement noch abhält ist die Tatsache, dass sowohl die Oligos (GRN163L), GRNVAC1 und die Stammzellen noch zu wenig verwertbare Infos liefern.
Was die Veröffentlichung von Studienergebnisse anbetrifft, sind die Amis äußerst sensibel. Was mich von einem Engagement noch abhält ist die Tatsache, dass sowohl die Oligos (GRN163L), GRNVAC1 und die Stammzellen noch zu wenig verwertbare Infos liefern.
Und die andere Sache ist die Dilution mit Aktien, um Verträge wie zuletzt mit Lonza und Girindus zu bezahlen. Grundsätzlich nicht falsch, aber naja.
 Was die Veröffentlichung von Studienergebnisse anbetrifft, sind die Amis äußerst sensibel. Was mich von einem Engagement noch abhält ist die Tatsache, dass sowohl die Oligos (GRN163L), GRNVAC1 und die Stammzellen noch zu wenig verwertbare Infos liefern.
Was die Veröffentlichung von Studienergebnisse anbetrifft, sind die Amis äußerst sensibel. Was mich von einem Engagement noch abhält ist die Tatsache, dass sowohl die Oligos (GRN163L), GRNVAC1 und die Stammzellen noch zu wenig verwertbare Infos liefern. Und die andere Sache ist die Dilution mit Aktien, um Verträge wie zuletzt mit Lonza und Girindus zu bezahlen. Grundsätzlich nicht falsch, aber naja.

Gewebe auf Bestellung
Von Emily Singer
5421 Zeichen
Druck | Leserbrief | Weitermailen | Heft bestellen | Forum
Michael West, ein prominenter amerikanischer Wissenschaftler und Unternehmer im Bereich der Stammzellenforschung, will mit seiner kalifornischen Biotechnologiefirma BioTime künftig zum verlässlichen Lieferanten von Stammzellprodukten für die Forschung werden. Die daraus gewonnenen Zellen gelten als enorm viel versprechend in der Medizin – sei es nun als potenziellen "Ersatzteillager" für geschädigte Organe oder als Versuchsobjekt zur genauen Untersuchung von Krankheitsabläufen und zum Testen neuer Medikationen.
Damit das alles Realität wird, muss die Forschung herausfinden, wie sich solche Zellprodukte im industriellen Maßstab herstellen lassen. "Es ist klar, dass wir eine wesentlich bessere Strategie brauchen, um verlässlich und reproduzierbar große Mengen gewünschter Zelltypen zu schaffen", meint Arnold R. Kriegstein, Direktor des Instituts für regenerative Medizin an der University of California in San Francisco. Die meisten Studien hätten sich noch nicht in dieses Gebiet vorgewagt.
Das, was Stammzellen so begehrenswert macht – ihre Fähigkeit, sich selbst zu replizieren und in die verschiedensten Zellvarianten zu entwickeln -, macht es gleichzeitig schwer, sie zu kontrollieren. Beispielsweise verhalten sich zwei Zelllinien, die auf die gleiche Art produziert wurden, aber aus verschiedenen Ausgangsquellen stammen, nicht immer gleich. Doch genau das wäre für stammzellbasierte Therapien und genaue wissenschaftliche Studien so wichtig.
Anzeige
West, Gründer der Firma und ihrer Tochter Embryome Sciences, will nun Zelllinien verkaufen, die er "menschliche embryonale Vorläufer" nennt – Zellen, die einen Teil des Weges von der Embryonalzelle zur ausdifferenzierten (adulten) Variante bereits zurückgelegt haben. West und sein Team publizierten dazu eine Studie, die ihre Anstrengungen, Zellen zu generieren, die stets den gleichen Zelltypnachwuchs produzierten, beschrieb. So soll sich ein besser definiertes Endprodukt ergeben.
In den frühen Neunzigerjahren war West Mitbegründer von Geron, einer Biotech-Firma im kalifornischen Menlo Park, die ursprünglich auf die Entwicklung von Behandlungsmethoden gegen Alterserkrankungen spezialisiert war und nun Therapien mit embryonalen Stammzellen für Rückenmarksverletzungen und andere Leiden entwickelt. (Geron unterstützte die frühe Forschung zum Thema an der University of Wisconsin, wo erstmals menschliche embryonale Stammzellen isoliert wurden. Sie lizenzierte wichtige Patente der Hochschule.) Vor BioTeam leitete West dann Advanced Cell Technologies, eine Firma aus Los Angeles, die ebenfalls an neuen Therapieformen mit embryonalen Stammzellen arbeitet und Methoden erforscht, sie leichter zu erzeugen.
Wests späte Karriere, eine Firma zu leiten, die Werkzeuge für sein Forschungsgebiet entwickelt, anstatt selbst an Therapieformen zu arbeiten, zeigt, wie weit der Bereich der Stammzellmedizin inzwischen gekommen ist. Immer mehr Wissenschaftler interessieren sich für sie, obwohl ihr Fachwissen eher in anderen Bereichen liegt – sei es nun Neurologie oder Kardiologie.. "Das ist ein interessantes Geschäftsmodell", meint Evan Snyder, Direktor des Stammzellforschungszentrums am Burnham Institute in La Jolla. "Ich sehe hier eine solide Kundengruppe in der Wissenschaft – besonders Forscher, die Stammzellen nur als eine Methode sehen, viele Zellen für ihre Zwecke zu erhalten." Arbeite jemand beispielsweise an einem neuen Medikament gegen Parkinson, sei es ideal, wenn eine große Anzahl von Dopamin-Neuronen vorliegen – dem Zelltyp, den die Krankheit besonders angreift.
Derzeit bewegen Wissenschaftler Stammzellen zur Ausdifferenzierung in bestimmte Zelltypen, in dem sie den gleichen chemischen Stoffen ausgesetzt werden, die sie auch in der normalen Entwicklung vorfinden würden. Dieser Prozess ist jedoch oft ineffizient und es ergibt sich nur eine kleine Anzahl der gewünschten Zellen, die dann auch noch gereinigt werden müssen, um keine Fehlbildungen mitzunehmen.
In ihrer Studie zeigen West und seine Kollegen, wie sie embryonale Stammzellen unter verschiedenen Bedingungen heranzüchteten und dann Stammzelllinien isolierten, die sich nur in Form von Klonen vermehrten. (Embryonale Stammzellen entwickeln sich hingegen zu Clustern von Nerven und anderen Gewebearten, wenn man sie sich frei entwickeln lässt.) Über molekulare Marker ließen sich mehr als 140 einzigartige Zelllinien identifizieren. "Dieser Ansatz ist sehr ungewöhnlich", sagt Jeanne Loring, Direktorin am Zentrum für regenerative Medizin am Scripps Research Institute in La Jolla. "Ich denke nicht, dass das jemand anderes auf diese Art bislang gemacht hat."
BioTime bereitet sich bereits auf die kommerzielle Herstellung vor. Die ersten Zellen will man in sechs bis 12 Monaten ausliefern können. Es muss jedoch noch viel Arbeit geleistet werden, um die Eigenschaften des Endprodukts besser zu beschreiben. Es ist unklar, wie sehr diese Zellen den üblichen Vorläuferzellen im Körper ähneln, die sich normal entwickeln. Folgestudien müssen durchgeführt werden, die das volle Ausdifferenzierungspotenzial bestimmen – den Zelltyp, in den sich die Zelllinie schließlich entwickeln soll. Und dann wäre da noch die Frage, ob die Produktion wirklich so verlässlich läuft, wie BioTime dies hofft. Nur das wollen die Kunden.
Von Emily Singer
5421 Zeichen
Druck | Leserbrief | Weitermailen | Heft bestellen | Forum
Michael West, ein prominenter amerikanischer Wissenschaftler und Unternehmer im Bereich der Stammzellenforschung, will mit seiner kalifornischen Biotechnologiefirma BioTime künftig zum verlässlichen Lieferanten von Stammzellprodukten für die Forschung werden. Die daraus gewonnenen Zellen gelten als enorm viel versprechend in der Medizin – sei es nun als potenziellen "Ersatzteillager" für geschädigte Organe oder als Versuchsobjekt zur genauen Untersuchung von Krankheitsabläufen und zum Testen neuer Medikationen.
Damit das alles Realität wird, muss die Forschung herausfinden, wie sich solche Zellprodukte im industriellen Maßstab herstellen lassen. "Es ist klar, dass wir eine wesentlich bessere Strategie brauchen, um verlässlich und reproduzierbar große Mengen gewünschter Zelltypen zu schaffen", meint Arnold R. Kriegstein, Direktor des Instituts für regenerative Medizin an der University of California in San Francisco. Die meisten Studien hätten sich noch nicht in dieses Gebiet vorgewagt.
Das, was Stammzellen so begehrenswert macht – ihre Fähigkeit, sich selbst zu replizieren und in die verschiedensten Zellvarianten zu entwickeln -, macht es gleichzeitig schwer, sie zu kontrollieren. Beispielsweise verhalten sich zwei Zelllinien, die auf die gleiche Art produziert wurden, aber aus verschiedenen Ausgangsquellen stammen, nicht immer gleich. Doch genau das wäre für stammzellbasierte Therapien und genaue wissenschaftliche Studien so wichtig.
Anzeige
West, Gründer der Firma und ihrer Tochter Embryome Sciences, will nun Zelllinien verkaufen, die er "menschliche embryonale Vorläufer" nennt – Zellen, die einen Teil des Weges von der Embryonalzelle zur ausdifferenzierten (adulten) Variante bereits zurückgelegt haben. West und sein Team publizierten dazu eine Studie, die ihre Anstrengungen, Zellen zu generieren, die stets den gleichen Zelltypnachwuchs produzierten, beschrieb. So soll sich ein besser definiertes Endprodukt ergeben.
In den frühen Neunzigerjahren war West Mitbegründer von Geron, einer Biotech-Firma im kalifornischen Menlo Park, die ursprünglich auf die Entwicklung von Behandlungsmethoden gegen Alterserkrankungen spezialisiert war und nun Therapien mit embryonalen Stammzellen für Rückenmarksverletzungen und andere Leiden entwickelt. (Geron unterstützte die frühe Forschung zum Thema an der University of Wisconsin, wo erstmals menschliche embryonale Stammzellen isoliert wurden. Sie lizenzierte wichtige Patente der Hochschule.) Vor BioTeam leitete West dann Advanced Cell Technologies, eine Firma aus Los Angeles, die ebenfalls an neuen Therapieformen mit embryonalen Stammzellen arbeitet und Methoden erforscht, sie leichter zu erzeugen.
Wests späte Karriere, eine Firma zu leiten, die Werkzeuge für sein Forschungsgebiet entwickelt, anstatt selbst an Therapieformen zu arbeiten, zeigt, wie weit der Bereich der Stammzellmedizin inzwischen gekommen ist. Immer mehr Wissenschaftler interessieren sich für sie, obwohl ihr Fachwissen eher in anderen Bereichen liegt – sei es nun Neurologie oder Kardiologie.. "Das ist ein interessantes Geschäftsmodell", meint Evan Snyder, Direktor des Stammzellforschungszentrums am Burnham Institute in La Jolla. "Ich sehe hier eine solide Kundengruppe in der Wissenschaft – besonders Forscher, die Stammzellen nur als eine Methode sehen, viele Zellen für ihre Zwecke zu erhalten." Arbeite jemand beispielsweise an einem neuen Medikament gegen Parkinson, sei es ideal, wenn eine große Anzahl von Dopamin-Neuronen vorliegen – dem Zelltyp, den die Krankheit besonders angreift.
Derzeit bewegen Wissenschaftler Stammzellen zur Ausdifferenzierung in bestimmte Zelltypen, in dem sie den gleichen chemischen Stoffen ausgesetzt werden, die sie auch in der normalen Entwicklung vorfinden würden. Dieser Prozess ist jedoch oft ineffizient und es ergibt sich nur eine kleine Anzahl der gewünschten Zellen, die dann auch noch gereinigt werden müssen, um keine Fehlbildungen mitzunehmen.
In ihrer Studie zeigen West und seine Kollegen, wie sie embryonale Stammzellen unter verschiedenen Bedingungen heranzüchteten und dann Stammzelllinien isolierten, die sich nur in Form von Klonen vermehrten. (Embryonale Stammzellen entwickeln sich hingegen zu Clustern von Nerven und anderen Gewebearten, wenn man sie sich frei entwickeln lässt.) Über molekulare Marker ließen sich mehr als 140 einzigartige Zelllinien identifizieren. "Dieser Ansatz ist sehr ungewöhnlich", sagt Jeanne Loring, Direktorin am Zentrum für regenerative Medizin am Scripps Research Institute in La Jolla. "Ich denke nicht, dass das jemand anderes auf diese Art bislang gemacht hat."
BioTime bereitet sich bereits auf die kommerzielle Herstellung vor. Die ersten Zellen will man in sechs bis 12 Monaten ausliefern können. Es muss jedoch noch viel Arbeit geleistet werden, um die Eigenschaften des Endprodukts besser zu beschreiben. Es ist unklar, wie sehr diese Zellen den üblichen Vorläuferzellen im Körper ähneln, die sich normal entwickeln. Folgestudien müssen durchgeführt werden, die das volle Ausdifferenzierungspotenzial bestimmen – den Zelltyp, in den sich die Zelllinie schließlich entwickeln soll. Und dann wäre da noch die Frage, ob die Produktion wirklich so verlässlich läuft, wie BioTime dies hofft. Nur das wollen die Kunden.
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10Genickschuss
UPDATE 1-Geron says FDA puts cell therapy drug on clinical hold
Wed May 14, 2008 3:29pm EDT Email | Print | Share| Reprints | Single Page| Recommend (0) [-] Text [+]
May 14 (Reuters) - Geron Corp (GERN.O: Quote, Profile, Research) said U.S. health regulators placed a clinical hold on its investigational new drug submission for GRNOPC1, a cell therapy for spinal cord injury, sending its shares down 22 percent to their lowest in more than four years.
"We have not yet received a letter from the FDA explaining the decision to place the submission on hold, so we are unable to comment specifically," Chief Executive Thomas Okarma said in a statement.
The biopharmaceutical company said it had received a verbal notice from the U.S. Food and Drug Administration about the clinical hold.
A clinical hold is an order that the FDA issues to delay a proposed trial or to suspend an ongoing investigation.
Shares of the company, which is working to develop therapeutics based on human embryonic stem cells, fell $1.08 to $3.82 in late trade on Nasdaq. (Reporting by Aradhana Aravindan in Bangalore; Editing by Himani Sarkar)
UPDATE 1-Geron says FDA puts cell therapy drug on clinical hold
Wed May 14, 2008 3:29pm EDT Email | Print | Share| Reprints | Single Page| Recommend (0) [-] Text [+]
May 14 (Reuters) - Geron Corp (GERN.O: Quote, Profile, Research) said U.S. health regulators placed a clinical hold on its investigational new drug submission for GRNOPC1, a cell therapy for spinal cord injury, sending its shares down 22 percent to their lowest in more than four years.
"We have not yet received a letter from the FDA explaining the decision to place the submission on hold, so we are unable to comment specifically," Chief Executive Thomas Okarma said in a statement.
The biopharmaceutical company said it had received a verbal notice from the U.S. Food and Drug Administration about the clinical hold.
A clinical hold is an order that the FDA issues to delay a proposed trial or to suspend an ongoing investigation.
Shares of the company, which is working to develop therapeutics based on human embryonic stem cells, fell $1.08 to $3.82 in late trade on Nasdaq. (Reporting by Aradhana Aravindan in Bangalore; Editing by Himani Sarkar)
Antwort auf Beitrag Nr.: 34.095.511 von meislo am 14.05.08 21:54:19So ein DRECK! Bin letzte Woche rein...
Vorerst keine Therapie mit embryonalen Stammzellen in den USA
Behörde lässt klinische Studie zur Heilung von Querschnittsgelähmten nicht zu - Experten vermuten politische GründeWashington -
Die Food and Drug Administration (FDA) hat der klinischen Forschung mit embryonalen Stammzellen vorerst eine Abfuhr erteilt. Die amerikanische Gesundheitsbehörde hat jetzt den ersten geplanten Patienten-Einsatz dieser Stammzellengattung ausgebremst. Sie versah einen Studienantrag der kalifornischen Biotech-Firma Geron mit dem Vermerk "clinical hold" - einem vorläufigen Stopp.
Das in Menlo Park bei San Francisco beheimatete Unternehmen hatte zuvor beantragt, mithilfe des Stammzell-Produkts GRNOPC1 Querschnittsgelähmte im Rahmen einer klinischen Studie behandeln zu dürfen. Die Buchstaben "OPC" des Produktkürzels stehen für sogenannte oligodendrogliale Progenitor-Zellen. Dabei handelt es sich um spezialisierte, aus embryonalen Stammzellen gewonnene Zellen, die nach Einschätzung von Geron-Chef Thomas Okarma das Potenzial haben, Schädigungen des Rückenmarks rückgängig zu machen oder gar zu heilen. Ziel dieses Ansatzes ist die teilweise oder vollständige Wiederherstellung von Körperfunktion und -kontrolle bei Querschnittsgelähmten.
Dem Studienantrag vorausgegangen waren nach Okarmas Angaben mehr als vierjährige Forschungen in direkter Abstimmung mit der FDA. So hat Geron unter anderem mehr als 2000 gelähmte Ratten mit GRNOPC1 behandelt, um herauszufinden, ob das Produkt Nebenwirkungen verursachen könnte. Diese Studien gelten unter Experten als ausgesprochen kompliziert und arbeitsintensiv, da sie mit immungeschwächten, gezielt gelähmten Ratten durchgeführt wurden. So mussten Geron-Forscher den Nagetieren mehrmals täglich per Hand die Blase entleeren. Mit einem Umfang von "gut 21 000 Seiten", so Okarma, ist der GRNOPC1-Antrag bei der FDA einer der umfangreichsten aller Zeiten.
Mit dem FDA-Entscheid dürften sich die ersten klinischen Studien mit embryonalen Stammzellen in den USA deutlich verzögern. Neben Geron stehen zwei weitere Unternehmen, Advanced Cell Technologies in Los Angeles und Novocell in San Diego, in den Startlöchern, um Produkte auf Basis embryonaler Stammzellen in der Klinik zu testen. Diese ethisch umstrittenen Zellen sind pluripotent, das heißt, sie können sich in jede der gut 200 verschiedenen Zellarten des menschlichen Körpers wandeln, also beispielsweise in Muskel- oder Nervenzellen. Sie werden aus Blastozysten gewonnen, die bei der künstlichen Befruchtung entstehen und überzählig sind.
Die Hintergründe der FDA-Entscheidung sind bislang offen. Die Bundesbehörde ist nun verpflichtet, sich bis spätestens übermorgen schriftlich gegenüber Geron zu erklären. Indes kursieren Gerüchte, wonach es sich um eine politisch motivierte Entscheidung der FDA handeln könnte. US-Präsident George W. Bush, in dessen präsidiale Befugnisse es fällt, den FDA-Chef zu ernennen, gilt als vehementer Gegner der Forschung mit embryonalen Stammzellen. Die drei amerikanischen Präsidentschaftskandidaten John McCain (Republikaner) sowie Hillary Clinton und Barack Obama (beide Demokraten) nehmen gegenüber der Stammzellenforschung hingegen eine deutlich liberalere Haltung ein. Pikanterweise hatte David Greenwood, Finanzvorstand bei Geron, nur einen Tag vor der FDA-Entscheidung erklärt, sein Unternehmen könne den Stand der GRNOPC1-Studie nicht kommentieren, um diese Forschung nicht zu einem "politischen Fußball" zu machen. Während der klinische Einsatz von embryonalen Stammzellen damit in den USA weiter offen ist, setzen indische Mediziner bereits seit Jahren auf diese neue Therapieform.
So habe die Ärztin Geeta Shroff in Neu-Delhi nach Agenturberichten bislang mehr als 300 Patienten erfolgreich mit embryonalen Stammzellen behandelt, darunter 50 mit Verletzungen des Rückenmarks. Die gesundheitsbehördlichen Auflagen in Indien sind indes nicht mit denen in Nordamerika oder Westeuropa vergleichbar.
Behörde lässt klinische Studie zur Heilung von Querschnittsgelähmten nicht zu - Experten vermuten politische GründeWashington -
Die Food and Drug Administration (FDA) hat der klinischen Forschung mit embryonalen Stammzellen vorerst eine Abfuhr erteilt. Die amerikanische Gesundheitsbehörde hat jetzt den ersten geplanten Patienten-Einsatz dieser Stammzellengattung ausgebremst. Sie versah einen Studienantrag der kalifornischen Biotech-Firma Geron mit dem Vermerk "clinical hold" - einem vorläufigen Stopp.
Das in Menlo Park bei San Francisco beheimatete Unternehmen hatte zuvor beantragt, mithilfe des Stammzell-Produkts GRNOPC1 Querschnittsgelähmte im Rahmen einer klinischen Studie behandeln zu dürfen. Die Buchstaben "OPC" des Produktkürzels stehen für sogenannte oligodendrogliale Progenitor-Zellen. Dabei handelt es sich um spezialisierte, aus embryonalen Stammzellen gewonnene Zellen, die nach Einschätzung von Geron-Chef Thomas Okarma das Potenzial haben, Schädigungen des Rückenmarks rückgängig zu machen oder gar zu heilen. Ziel dieses Ansatzes ist die teilweise oder vollständige Wiederherstellung von Körperfunktion und -kontrolle bei Querschnittsgelähmten.
Dem Studienantrag vorausgegangen waren nach Okarmas Angaben mehr als vierjährige Forschungen in direkter Abstimmung mit der FDA. So hat Geron unter anderem mehr als 2000 gelähmte Ratten mit GRNOPC1 behandelt, um herauszufinden, ob das Produkt Nebenwirkungen verursachen könnte. Diese Studien gelten unter Experten als ausgesprochen kompliziert und arbeitsintensiv, da sie mit immungeschwächten, gezielt gelähmten Ratten durchgeführt wurden. So mussten Geron-Forscher den Nagetieren mehrmals täglich per Hand die Blase entleeren. Mit einem Umfang von "gut 21 000 Seiten", so Okarma, ist der GRNOPC1-Antrag bei der FDA einer der umfangreichsten aller Zeiten.
Mit dem FDA-Entscheid dürften sich die ersten klinischen Studien mit embryonalen Stammzellen in den USA deutlich verzögern. Neben Geron stehen zwei weitere Unternehmen, Advanced Cell Technologies in Los Angeles und Novocell in San Diego, in den Startlöchern, um Produkte auf Basis embryonaler Stammzellen in der Klinik zu testen. Diese ethisch umstrittenen Zellen sind pluripotent, das heißt, sie können sich in jede der gut 200 verschiedenen Zellarten des menschlichen Körpers wandeln, also beispielsweise in Muskel- oder Nervenzellen. Sie werden aus Blastozysten gewonnen, die bei der künstlichen Befruchtung entstehen und überzählig sind.
Die Hintergründe der FDA-Entscheidung sind bislang offen. Die Bundesbehörde ist nun verpflichtet, sich bis spätestens übermorgen schriftlich gegenüber Geron zu erklären. Indes kursieren Gerüchte, wonach es sich um eine politisch motivierte Entscheidung der FDA handeln könnte. US-Präsident George W. Bush, in dessen präsidiale Befugnisse es fällt, den FDA-Chef zu ernennen, gilt als vehementer Gegner der Forschung mit embryonalen Stammzellen. Die drei amerikanischen Präsidentschaftskandidaten John McCain (Republikaner) sowie Hillary Clinton und Barack Obama (beide Demokraten) nehmen gegenüber der Stammzellenforschung hingegen eine deutlich liberalere Haltung ein. Pikanterweise hatte David Greenwood, Finanzvorstand bei Geron, nur einen Tag vor der FDA-Entscheidung erklärt, sein Unternehmen könne den Stand der GRNOPC1-Studie nicht kommentieren, um diese Forschung nicht zu einem "politischen Fußball" zu machen. Während der klinische Einsatz von embryonalen Stammzellen damit in den USA weiter offen ist, setzen indische Mediziner bereits seit Jahren auf diese neue Therapieform.
So habe die Ärztin Geeta Shroff in Neu-Delhi nach Agenturberichten bislang mehr als 300 Patienten erfolgreich mit embryonalen Stammzellen behandelt, darunter 50 mit Verletzungen des Rückenmarks. Die gesundheitsbehördlichen Auflagen in Indien sind indes nicht mit denen in Nordamerika oder Westeuropa vergleichbar.
denke auch, dass wir nach der US-Präsidentschaftswahl einen neuen Anlauf nehmen werden!
Ich bleibe langfristig dabei, schon allein wegen der Spekusteuer
Ich bleibe langfristig dabei, schon allein wegen der Spekusteuer

Antwort auf Beitrag Nr.: 34.127.960 von Sugar2000 am 19.05.08 20:02:59Ein Rep gewinnt wegen des Golfktieges und auch der wirtschaftlichen Situationm eh nicht die Wahl!! und die Demokraten haben gerade in Sachen Stammzellen Bush stark attakiert.
und die Demokraten haben gerade in Sachen Stammzellen Bush stark attakiert.
Ein Mc Cain liegt nach Wählerumfragen noch deutlich hinter den anderen beiden (Obama und Clinton).
Mit der Wahl könnte da wirklich was passieren.
 und die Demokraten haben gerade in Sachen Stammzellen Bush stark attakiert.
und die Demokraten haben gerade in Sachen Stammzellen Bush stark attakiert.Ein Mc Cain liegt nach Wählerumfragen noch deutlich hinter den anderen beiden (Obama und Clinton).
Mit der Wahl könnte da wirklich was passieren.

21.5.2008 11:03 Uhr
Die ersten potenziellen klinischen Tests einer Therapie mit embryonalen Stammzellen sind von der US Food and Drug Administration (FDA) auf Eis gelegt worden. Wissenschaftler sind der Meinung, dies reflektiere die immer noch unbekannten Risiken einer solchen Therapie bei Menschen.
Die Biotech-Firma Geron in Menlo Park, Kalifornien, hatte seit über vier Jahren mit der FDA über ihr Vorhaben, Patienten mit Rückenmarksverletzungen mit Injektionen oligodendroglialer Progenitorzellen, die aus embryonalen Stammzellen gewonnen wurden, zu behandeln, gesprochen. Das Unternehmen verlautbarte letzte Woche, dass bevorstehende Tests gestoppt wurden, die FDA ihre Gründe aber bislang nicht offengelegt habe.
Wissenschaftler sind sich unsicher, ob das Vorgehen der FDA auf spezifischen Problemen mit Gerons Testreihe beruht oder generelle Bedenken hinsichtlich der Sicherheit von Stammzelltherapien den Ausschlag gaben, im letzteren Fall könnten sich auch weitere anstehende klinische Tests verzögern. Um klinische Tests aufnehmen zu können, müssen Unternehmen überzeugende Daten vorlegen, dass die transplantierten Zellen sicher sind, insbesondere, dass sie keine Tumoren oder andere Schäden verursachen, erklärt Ole Isacson, Neurowissenschaftler an der Harvard Medical School.
Es gibt hierfür jedoch bislang keine Kriterien. "Ich denke, die FDA macht sich selbst noch schlau und niemand kennt das Risiko embryonaler Stammzellen", fügt er hinzu.
Zulassung erwartet
Der Stopp kommt einen Monat nach dem ersten Advisory-Meeting der FDA zur Frage, wie sich Stammzellprodukte am besten evaluieren lassen. Der Industrieanalyst Steven Brozak von WBB Securities in San Diego, Kalifornien, befürchtet, dass die Entscheidung von politischen Überlegungen motiviert ist, Forscher auf diesem Gebiet schätzen diese Möglichkeit allerdings gering ein und gehen davon aus, dass die FDA grundsätzlich unsicher ist, wie Sicherheit zu gewährleisten sei.
Während ihres Meetings im April deutete die FDA an, sie könnte sich leichter damit tun, Tests mit todkranken Patienten zuzulassen, für die es keine anderen Therapieoptionen gibt, Gerons Produkt und diejenigen, deren Entwicklung am weisteten fortgeschritten ist, fallen nicht unter diese Kategorie. Außer Geron hofft Advanced Cell Technology in Los Angeles, embryonale Stammzellen in der Therapie der Makuladegeneration einsetzen zu können und Novocell in San Diego arbeitet an Stammzellen für die Diabetes-Therapie.
Offene Fragen
In der Vergangenheit hat die FDA Stopps über mehrere andere klinische Testreihen für Zelltherapien verhängt, die schließlich fortgesetzt wurden, als die Unternehmen auf die Bedenken der FDA eingingen, sagt Curt Freed, Leiter der Neurotransplantation an der University of Colorado School of Medicine in Denver. Er fügt jedoch hinzu, dass zusätzliche von der FDA geforderte Experimente manchmal eine unüberwindbare Hürde darstellen, in die klinische Phase einzutreten.
Evan Snyder, Stammzellbiologe am Burnham Institute for Medical Research in La Jolla, Kalifornien, und Berater der FDA für Stammzelltherapien, glaubt, dass die Testreihe letztlich fortgeführt werden wird. Er sagt, die extreme Vorsicht der FDA reflektiert den Wunsch der Forscher, jede schädliche Reaktion zu vermeiden, die das gesamte Forschungsfeld zurückwerfen könnte.
Dieser Artikel wurde erstmals am 19.5.2008 bei news@nature.com veröffentlicht. doi: 10.1038/news.2008.842. Übersetzung: Sonja Hinte. © 2007, Macmillan Publishers Ltd
Die ersten potenziellen klinischen Tests einer Therapie mit embryonalen Stammzellen sind von der US Food and Drug Administration (FDA) auf Eis gelegt worden. Wissenschaftler sind der Meinung, dies reflektiere die immer noch unbekannten Risiken einer solchen Therapie bei Menschen.
Die Biotech-Firma Geron in Menlo Park, Kalifornien, hatte seit über vier Jahren mit der FDA über ihr Vorhaben, Patienten mit Rückenmarksverletzungen mit Injektionen oligodendroglialer Progenitorzellen, die aus embryonalen Stammzellen gewonnen wurden, zu behandeln, gesprochen. Das Unternehmen verlautbarte letzte Woche, dass bevorstehende Tests gestoppt wurden, die FDA ihre Gründe aber bislang nicht offengelegt habe.
Wissenschaftler sind sich unsicher, ob das Vorgehen der FDA auf spezifischen Problemen mit Gerons Testreihe beruht oder generelle Bedenken hinsichtlich der Sicherheit von Stammzelltherapien den Ausschlag gaben, im letzteren Fall könnten sich auch weitere anstehende klinische Tests verzögern. Um klinische Tests aufnehmen zu können, müssen Unternehmen überzeugende Daten vorlegen, dass die transplantierten Zellen sicher sind, insbesondere, dass sie keine Tumoren oder andere Schäden verursachen, erklärt Ole Isacson, Neurowissenschaftler an der Harvard Medical School.
Es gibt hierfür jedoch bislang keine Kriterien. "Ich denke, die FDA macht sich selbst noch schlau und niemand kennt das Risiko embryonaler Stammzellen", fügt er hinzu.
Zulassung erwartet
Der Stopp kommt einen Monat nach dem ersten Advisory-Meeting der FDA zur Frage, wie sich Stammzellprodukte am besten evaluieren lassen. Der Industrieanalyst Steven Brozak von WBB Securities in San Diego, Kalifornien, befürchtet, dass die Entscheidung von politischen Überlegungen motiviert ist, Forscher auf diesem Gebiet schätzen diese Möglichkeit allerdings gering ein und gehen davon aus, dass die FDA grundsätzlich unsicher ist, wie Sicherheit zu gewährleisten sei.
Während ihres Meetings im April deutete die FDA an, sie könnte sich leichter damit tun, Tests mit todkranken Patienten zuzulassen, für die es keine anderen Therapieoptionen gibt, Gerons Produkt und diejenigen, deren Entwicklung am weisteten fortgeschritten ist, fallen nicht unter diese Kategorie. Außer Geron hofft Advanced Cell Technology in Los Angeles, embryonale Stammzellen in der Therapie der Makuladegeneration einsetzen zu können und Novocell in San Diego arbeitet an Stammzellen für die Diabetes-Therapie.
Offene Fragen
In der Vergangenheit hat die FDA Stopps über mehrere andere klinische Testreihen für Zelltherapien verhängt, die schließlich fortgesetzt wurden, als die Unternehmen auf die Bedenken der FDA eingingen, sagt Curt Freed, Leiter der Neurotransplantation an der University of Colorado School of Medicine in Denver. Er fügt jedoch hinzu, dass zusätzliche von der FDA geforderte Experimente manchmal eine unüberwindbare Hürde darstellen, in die klinische Phase einzutreten.
Evan Snyder, Stammzellbiologe am Burnham Institute for Medical Research in La Jolla, Kalifornien, und Berater der FDA für Stammzelltherapien, glaubt, dass die Testreihe letztlich fortgeführt werden wird. Er sagt, die extreme Vorsicht der FDA reflektiert den Wunsch der Forscher, jede schädliche Reaktion zu vermeiden, die das gesamte Forschungsfeld zurückwerfen könnte.
Dieser Artikel wurde erstmals am 19.5.2008 bei news@nature.com veröffentlicht. doi: 10.1038/news.2008.842. Übersetzung: Sonja Hinte. © 2007, Macmillan Publishers Ltd

June 12, 2008 - 7:36 AM EDT
GERN 3.90 -0.09
Today 5d 1m 3m 1y 5y 10y
Geron Presents Data at ISSCR Showing That Its Embryonic Stem Cell Therapeutic for Heart Failure Evades Direct Attack by the Human Immune System
Three Additional Presentations Document Continued Progress in Development of hESC-based Therapeutics for Liver Disease and Orthopedic Indications
Geron Corporation (Nasdaq:GERN) today announced the presentation of research studies indicating that GRNCM1, the company’s human embryonic stem cell (hESC)-based therapeutic for the treatment of heart failure, evades direct attack by the human immune system in vitro.
The data presented at the International Society for Stem Cell Research (ISSCR) Annual Meeting indicate that, unlike whole organ transplants, cell therapies derived from hESCs may provoke only minimal immune reactions suggesting that rejection may be controlled or prevented by short courses of low-dose immunosuppressive drugs. The work also suggests that patient-specific hESC lines may not be needed to prevent immune rejection.
“We published evidence in 2007 demonstrating the immune-privileged properties of GRNOPC1, our hESC-derived oligodendroglial progenitor cell therapeutic for acute spinal cord injury,” said Thomas B Okarma, Ph.D., M.D., Geron’s president and chief executive officer. “We now have evidence that a second hESC-derived therapeutic cell type, cardiomyocytes for the treatment of heart failure, displays the same properties in vitro. These results suggest that patients treated with GRNCM1 may only require a short course of low-dose immunosuppression which decreases the possibility of unwanted side effects commonly associated with those types of drugs.”
The data presented show that GRNCM1 expresses HLA class I antigen on their surface, but not HLA class II, or other surface markers required for T-cell activation, even after stimulation by inflammatory cytokines. In these studies, GRNCM1 cells were tested for susceptibility to immune effector cells and sera from several allogeneic normal healthy individuals. GRNCM1 cells did not stimulate the proliferation of T cells in vitro, a standard measure of immune recognition of foreign transplanted tissue. Even when GRNCM1 cells were exposed to proinflammatory cytokines, such as γ-interferon or TNF-alpha, allogeneic T cell proliferation was not induced. In addition, GRNCM1 cells were largely resistant to killing by sera of normal healthy individuals.
Additional presentations by Geron collaborators from the University of Edinburgh, Scotland, demonstrated 1) successful engraftment of hESC-derived hepatocytes in mice, 2) engraftment of hESC-derived osteogenic cells in rat calvarial defects and 3) repair of rodent knee cartilage defects by hESC-derived cartilage progenitor cells.
“We are pleased with the progress of our collaborators at the University of Edinburgh who have advanced three additional hESC-derived therapeutic cell types into early animal feasibility studies,” continued Dr. Okarma. “This work is supported by a recently awarded $7.2 million grant to the University of Edinburgh from the UK Stem Cell Foundation.”
Presentations on hESC-Derived Hepatocytes
Geron collaborators at the University of Edinburgh led by Dr. John Iredale presented studies that demonstrated survival of hESC-derived hepatocytes injected into the livers and spleens of immune-compromised mice for up to 31 days. The surviving cells produced human albumin, which was also detectable in the serum of the transplanted mice. These studies provide early evidence that hESC-derived hepatocytes may have application for the treatment of liver failure.
Presentations on hESC-Derived Chondrocytes
Geron collaborators at the University of Edinburgh led by Dr. Brendon Noble presented studies examining the engraftment of hESC-derived chondrogenic and osteogenic progenitor cells in rodents with cartilage or bone defects. hESC-derived chondroprogenitor cells that expressed type II collagen were implanted into an articular chondral defect in the knees of rats. Human cells were detected within the regenerating cartilage at 21 days, and histological analysis indicated a significantly improved overall grading of the repair compared to untreated controls or animals implanted with progenitors derived from human bone marrow stromal cells. These early results suggest that hESC-derived cartilage progenitors may have application in cartilage repair.
Presentations on hESC-Derived Osteoblasts
In separate studies, hESC-derived osteogenic progenitors were implanted into rat calvarial lesions. Human cells were detected at 14 days and there was a significant increase in newly mineralized tissue compared to controls, demonstrating bone regeneration by these cells.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem cell-based therapeutics, with its spinal cord injury treatment anticipated to be the first product to enter clinical development. For more information, visit www.geron.com.
This news release may contain forward-looking statements made pursuant to the “safe harbor” provisions of the Private Securities Litigation Reform Act of 1995. Investors are cautioned that statements in this press release regarding potential applications of Geron’s human embryonic stem cell technology constitute forward-looking statements that involve risks and uncertainties, including, without limitation, risks inherent in the development and commercialization of potential products, uncertainty of clinical trial results or regulatory approvals or clearances, need for future capital, dependence upon collaborators and maintenance of our intellectual property rights. Actual results may differ materially from the results anticipated in these forward-looking statements. Additional information on potential factors that could affect our results and other risks and uncertainties are detailed from time to time in Geron’s periodic reports, including the quarterly report on Form 10-Q for the quarter ended March 31, 2008.
Russo Partners, LLC
David Schull, 858-717-2310
Media and Investors
david.schull@russopartnersllc.com
or
Geron
Anna Krassowska, 650-473-7765
Investor and Media Relations
info@geron.com
Source: Business Wire (June 12, 2008 - 7:36 AM EDT)
News by QuoteMedia
June 19, 2008 - 8:12 AM EDT

Start Licensing, Inc. Reaffirms Control of Key Cloning Patents
Firm responds to South Korean company’s recent actions
Today Start Licensing, Inc. (Start) reaffirmed that it controls key patents in Korea and elsewhere that cover animal cloning technology, including the technology used to clone dogs. RNL Bio Ltd (RNL) previously announced on February 12, 2008 that it was launching a dog cloning service and had signed its first client. More recently it has been reported that RNL is offering cloned cancer-sniffing dogs for commercial sale. RNL is not licensed under Start’s patents to engage in these commercial activities.
The patents Start controls include Korean Patent Nos. 10-0533476, 10-0533477, 10-0743006, and 10-0793220 as well as numerous foreign counterparts in the U.S., Europe, Japan and elsewhere. These patents are part of a portfolio of patents and patent applications directed to foundational somatic cell nuclear transfer (SCNT) cloning technology. Start recently granted a sole, worldwide license under these patents to BioArts International Ltd. for cloning dogs and cats.
"Start will pursue available legal remedies as necessary to protect and preserve its patent rights," said Jonathan Thatcher, President of Start Licensing, "including the remedy of blocking importation of products produced under the patented methods into jurisdictions where such rights are available.”
About Start Licensing
Start is a joint venture of Geron Corporation (Nasdaq: GERN) and Exeter Life Sciences, Inc. Start manages and licenses a broad portfolio of intellectual property rights related to animal reproductive technologies, including foundational nuclear transfer cloning technology developed at the Roslin Institute for the cloning of Dolly the sheep. Start's licensees are on the cutting edge of research and product development in food production, medical applications and many other fields.
Start Licensing, Inc.
Ben Carlson, 202-466-9633
ben@turnerstrategies.com
Source: Business Wire (June 19, 2008 - 8:12 AM EDT)
News by QuoteMedia

Start Licensing, Inc. Reaffirms Control of Key Cloning Patents
Firm responds to South Korean company’s recent actions
Today Start Licensing, Inc. (Start) reaffirmed that it controls key patents in Korea and elsewhere that cover animal cloning technology, including the technology used to clone dogs. RNL Bio Ltd (RNL) previously announced on February 12, 2008 that it was launching a dog cloning service and had signed its first client. More recently it has been reported that RNL is offering cloned cancer-sniffing dogs for commercial sale. RNL is not licensed under Start’s patents to engage in these commercial activities.
The patents Start controls include Korean Patent Nos. 10-0533476, 10-0533477, 10-0743006, and 10-0793220 as well as numerous foreign counterparts in the U.S., Europe, Japan and elsewhere. These patents are part of a portfolio of patents and patent applications directed to foundational somatic cell nuclear transfer (SCNT) cloning technology. Start recently granted a sole, worldwide license under these patents to BioArts International Ltd. for cloning dogs and cats.
"Start will pursue available legal remedies as necessary to protect and preserve its patent rights," said Jonathan Thatcher, President of Start Licensing, "including the remedy of blocking importation of products produced under the patented methods into jurisdictions where such rights are available.”
About Start Licensing
Start is a joint venture of Geron Corporation (Nasdaq: GERN) and Exeter Life Sciences, Inc. Start manages and licenses a broad portfolio of intellectual property rights related to animal reproductive technologies, including foundational nuclear transfer cloning technology developed at the Roslin Institute for the cloning of Dolly the sheep. Start's licensees are on the cutting edge of research and product development in food production, medical applications and many other fields.
Start Licensing, Inc.
Ben Carlson, 202-466-9633
ben@turnerstrategies.com
Source: Business Wire (June 19, 2008 - 8:12 AM EDT)
News by QuoteMedia
Antwort auf Beitrag Nr.: 34.333.280 von gled77 am 19.06.08 14:49:10Hallo allerseits
Habe mal rein spekulativ ein paar Stücke gekauft ,die Wahlen sind ja nicht mehr fern und beide Kandidaten wollen ja Lockerungen auf dem Gebiet.
Habe mal rein spekulativ ein paar Stücke gekauft ,die Wahlen sind ja nicht mehr fern und beide Kandidaten wollen ja Lockerungen auf dem Gebiet.
Hallo! Melde mich auch mal wieder:
http://www.fool.com/investing/high-growth/2008/07/16/5-stock…
Ist zwar schon eine Woche alt, aber trotzdem schön zu lesen!
5 Stocks That Swayed the Skeptics
By Rich Duprey July 16, 2008 Comments (1)
2
Recommendations
It pays to be skeptical when you invest. In addition to doubting what the analysts tell you, you often have to discount what the companies tell you, too. On Wall Street, going against the grain can reap huge rewards. Like baseball's greatest place hitter, "Wee Willie" Keeler, great contrarian investors such as Benjamin Graham, Warren Buffett, and John Neff "hit 'em where they ain't."
Today's new breed of contrarian investor can be found at Motley Fool CAPS, where these savvy Fools are willing to see both the upside and the downside of a stock. While their often negative opinions peg them as "skeptics," their top player ratings mean they're right far more often than not. And when they find a stock they actually believe will outperform, perhaps we should take notice.
Here are some recent picks from our list of Foolish CAPS skeptics:
Company
CAPS Rating (5 Max)
Skeptic
Player Rating
Chubb (NYSE: CB)
****
nicvo
100.00
Yingli Green Energy (NYSE: YGE)
****
DemonDoug
99.98
Geron (Nasdaq: GERN)
***
MakeItSeven
99.98
Indevus Pharmaceuticals (Nasdaq: IDEV)
****
luvb2b
99.98
Wachovia (NYSE: WB)
*
d1david
99.97
Just as a list of their worst stocks would not be a list of stocks to short, this list of the skeptics' favorites isn't one of automatic buys. But they do offer an excellent starting place for your own research.
Skeptically skeptical
The potential to regenerate body parts and organs may sound like the stuff of science fiction, but stem-cell research holds just such promise. Stem cells are what allow our bodies to grow and heal. However, the field has been steeped in controversy because the use of embryonic stem cells -- those taken from fetuses -- has raised ethical questions.
Adult stem cells, on the other hand, don't hold such concerns, but they also don't hold the same regenerative powers that embryonic stem cells do. You can turn embryonic stem cells, but not adult stem cells, into virtually any cell type you want: That's why they hold such potential. However, it seems to be possible to reprogram adult stem cells to do the same trick. If that turns out to be true, it would eliminate the ethical dilemma. But this science is still in its infancy. Pfizer (NYSE: PFE) is investigating adult stem cell therapies for diabetes-induced retinal damage, while Cytori Therapeutics (Nasdaq: CYTX) is studying the potential of stem cells found in the body's own fat tissue.
Geron, though, has been a leader in embryonic stem cell research and recently reported that a heart-failure therapy has passed a very early-stage test. It's also exploring treatments for cancer and diabetes. Investors hold a lot of hope for Geron and other stem-cell research companies because both candidates for president support expanded stem-cell research. That's why some investors like CAPS member zheindel believe the company is on the path to profitability.
With a new president being elected this stock will get a huge boost of government money, regardless of who the elected president [is]. With this research the stem cell company will make great strides in curing Diabetes and other [diseases,] making the stock profitable.
One lump or two?
Indevus Pharmaceuticals is one pharmaceutical that has borne the brunt of what seems to be capricious regulatory interference. The Food and Drug Administration set back its hypogonadism therapy Nebido because of a single instance of a U.S. patient coughing when the treatment was administered, along with a few similar incidents in Europe. Nebido is already approved in Europe and carries a warning label noting that such rare side effects may occur.
The FDA subsequently gave Indevus recommendations to put the experimental testosterone drug back on track to regulatory approval. The guidelines the company received make it optimistic that Nebido will be approved here in the States.
CAPS members like fojaha find that even with the Nebido hurdles, Indevus remains an attractive investment because it's more than just a one-drug company.
Indevus was bid down as a result of FDA conditions for new drug nebido. Traders have ignored the fact that the company has other products on the market. Sanctura & sanctura xr, Vantas, supprelin, and delastestryl... Seven more drugs in development. Valstar, a bladder cancer drug is most advanced. No huge sellers, but combined it makes a pretty good revenue stream.
Seeing past the obvious
Skeptics know that just beyond the storm clouds lies a shimmering morning. Conversely, the sun can't shine forever, whatever the crowds may think. What's your forecast? Drop by CAPS and tell us which stocks are your favorite contrarian picks.
Get the best of the Fool delivered to your inbox every Friday
Pfizer is both a Motley Fool Income Investor and an Inside Value recommendation. Try any of our Foolish newsletters today, free for 30 days.
Fool contributor Rich Duprey does not have a financial position in any of the stocks mentioned in this article. You can see his holdings. The Motley Fool has a disclosure policy.
http://www.fool.com/investing/high-growth/2008/07/16/5-stock…
Ist zwar schon eine Woche alt, aber trotzdem schön zu lesen!
5 Stocks That Swayed the Skeptics
By Rich Duprey July 16, 2008 Comments (1)
2
Recommendations
It pays to be skeptical when you invest. In addition to doubting what the analysts tell you, you often have to discount what the companies tell you, too. On Wall Street, going against the grain can reap huge rewards. Like baseball's greatest place hitter, "Wee Willie" Keeler, great contrarian investors such as Benjamin Graham, Warren Buffett, and John Neff "hit 'em where they ain't."
Today's new breed of contrarian investor can be found at Motley Fool CAPS, where these savvy Fools are willing to see both the upside and the downside of a stock. While their often negative opinions peg them as "skeptics," their top player ratings mean they're right far more often than not. And when they find a stock they actually believe will outperform, perhaps we should take notice.
Here are some recent picks from our list of Foolish CAPS skeptics:
Company
CAPS Rating (5 Max)
Skeptic
Player Rating
Chubb (NYSE: CB)
****
nicvo
100.00
Yingli Green Energy (NYSE: YGE)
****
DemonDoug
99.98
Geron (Nasdaq: GERN)
***
MakeItSeven
99.98
Indevus Pharmaceuticals (Nasdaq: IDEV)
****
luvb2b
99.98
Wachovia (NYSE: WB)
*
d1david
99.97
Just as a list of their worst stocks would not be a list of stocks to short, this list of the skeptics' favorites isn't one of automatic buys. But they do offer an excellent starting place for your own research.
Skeptically skeptical
The potential to regenerate body parts and organs may sound like the stuff of science fiction, but stem-cell research holds just such promise. Stem cells are what allow our bodies to grow and heal. However, the field has been steeped in controversy because the use of embryonic stem cells -- those taken from fetuses -- has raised ethical questions.
Adult stem cells, on the other hand, don't hold such concerns, but they also don't hold the same regenerative powers that embryonic stem cells do. You can turn embryonic stem cells, but not adult stem cells, into virtually any cell type you want: That's why they hold such potential. However, it seems to be possible to reprogram adult stem cells to do the same trick. If that turns out to be true, it would eliminate the ethical dilemma. But this science is still in its infancy. Pfizer (NYSE: PFE) is investigating adult stem cell therapies for diabetes-induced retinal damage, while Cytori Therapeutics (Nasdaq: CYTX) is studying the potential of stem cells found in the body's own fat tissue.
Geron, though, has been a leader in embryonic stem cell research and recently reported that a heart-failure therapy has passed a very early-stage test. It's also exploring treatments for cancer and diabetes. Investors hold a lot of hope for Geron and other stem-cell research companies because both candidates for president support expanded stem-cell research. That's why some investors like CAPS member zheindel believe the company is on the path to profitability.
With a new president being elected this stock will get a huge boost of government money, regardless of who the elected president [is]. With this research the stem cell company will make great strides in curing Diabetes and other [diseases,] making the stock profitable.
One lump or two?
Indevus Pharmaceuticals is one pharmaceutical that has borne the brunt of what seems to be capricious regulatory interference. The Food and Drug Administration set back its hypogonadism therapy Nebido because of a single instance of a U.S. patient coughing when the treatment was administered, along with a few similar incidents in Europe. Nebido is already approved in Europe and carries a warning label noting that such rare side effects may occur.
The FDA subsequently gave Indevus recommendations to put the experimental testosterone drug back on track to regulatory approval. The guidelines the company received make it optimistic that Nebido will be approved here in the States.
CAPS members like fojaha find that even with the Nebido hurdles, Indevus remains an attractive investment because it's more than just a one-drug company.
Indevus was bid down as a result of FDA conditions for new drug nebido. Traders have ignored the fact that the company has other products on the market. Sanctura & sanctura xr, Vantas, supprelin, and delastestryl... Seven more drugs in development. Valstar, a bladder cancer drug is most advanced. No huge sellers, but combined it makes a pretty good revenue stream.
Seeing past the obvious
Skeptics know that just beyond the storm clouds lies a shimmering morning. Conversely, the sun can't shine forever, whatever the crowds may think. What's your forecast? Drop by CAPS and tell us which stocks are your favorite contrarian picks.
Get the best of the Fool delivered to your inbox every Friday
Pfizer is both a Motley Fool Income Investor and an Inside Value recommendation. Try any of our Foolish newsletters today, free for 30 days.
Fool contributor Rich Duprey does not have a financial position in any of the stocks mentioned in this article. You can see his holdings. The Motley Fool has a disclosure policy.
Kommen bei Geron nicht bald die ersten Studiendaten zu GRN163L, ihrem Oligo Wirkstoff, einem Telomerase Inhibitor.
http://www.clinicaltrials.gov/ct2/results?term=GRN163l
CLL z.B.
Das ist mE z.Z. heißer als die Stammzellen. Der gesamte Markt der Oligos wird regelrecht geflutet mit Partnerschaften und Millionen(GSK 900 Mios$+Santaris, Novartis 700 Mios$+Alnylam, Roche ist auch sehr aktiv, Solvay+Girindus). Tja, und vielleicht könnte auch bei Geron bald was anstehen. Geld sitzt jedenfalls locker für Partnerschaften.
http://www.clinicaltrials.gov/ct2/results?term=GRN163l
CLL z.B.
Das ist mE z.Z. heißer als die Stammzellen. Der gesamte Markt der Oligos wird regelrecht geflutet mit Partnerschaften und Millionen(GSK 900 Mios$+Santaris, Novartis 700 Mios$+Alnylam, Roche ist auch sehr aktiv, Solvay+Girindus). Tja, und vielleicht könnte auch bei Geron bald was anstehen. Geld sitzt jedenfalls locker für Partnerschaften.

guten morgen
wie steht das in verbindung
http://de.news.yahoo.com/ap/20080805/twl-sdkoreanische-firma…
Seoul (AP) Booger ist wieder da. Die Amerikanerin Bernann McKinney hat am Dienstag fünf Welpen bekommen, die aus dem Erbgut ihres verstorbenen Pitbulls geklont wurden. Da sie die erste Kundin der südkoreanischen Firma RNL Bio ist, bekam sie die Tiere zum Preis von 50.000 Dollar (32.000 Euro). Danach berechnet das Unternehmen das Klonen eines Hundes mit 150.000 Dollar (96.000 Euro). Die Klon-Hunde kamen in der vergangenen Woche zur Welt.
Anzeige
«Es ist ein Wunder!» rief McKinney immer wieder am Dienstag, als sie die Klone von Booger in einem Labor der Universität von Seoul zum ersten Mal sah. «Ja, ich kenne Euch! Ihr kennt mich auch», sagte McKinney und herzte die Welpen, die bei einer ihrer beiden Leih-Hundemütter schliefen.
Das Team der für RNL Bio arbeitenden Wissenschaftler wird von Lee Byeong Chun geleitet, einem früheren Kollegen des Forschers Hwang Woo Suk, der wegen gefälschter Forschungsergebnisse in Misskredit geraten ist. Das Klonen von Hunden wurde aber 2005 auch von unabhängiger Seite bestätigt. Lees Team hat seitdem rund 20 Hunde geklont. RNL Bio erklärte, das sei jetzt aber das erste Mal gewesen, dass ein Hund kommerziell geklont worden sei. «Booger war unser erster erfolgreicher Klon», erklärte das Unternehmen.
McKinney nahm mit Lee Kontakt auf, nachdem Booger im April 2006 an Krebs gestorben war. Die südkoreanischen Forscher brachten im März gefrorene Zellen des Hundes nach Seoul. Der Chef von RNL Bio, Ra Jeong Chan, erklärte, seine Firma wolle rund 300 Hunde im Jahr klonen, für Kunden im Nahen Osten könnten vielleicht auch Kamele geklont werden.
http://rnl.co.kr/eng/main.asp
wie steht das in verbindung

http://de.news.yahoo.com/ap/20080805/twl-sdkoreanische-firma…
Seoul (AP) Booger ist wieder da. Die Amerikanerin Bernann McKinney hat am Dienstag fünf Welpen bekommen, die aus dem Erbgut ihres verstorbenen Pitbulls geklont wurden. Da sie die erste Kundin der südkoreanischen Firma RNL Bio ist, bekam sie die Tiere zum Preis von 50.000 Dollar (32.000 Euro). Danach berechnet das Unternehmen das Klonen eines Hundes mit 150.000 Dollar (96.000 Euro). Die Klon-Hunde kamen in der vergangenen Woche zur Welt.
Anzeige
«Es ist ein Wunder!» rief McKinney immer wieder am Dienstag, als sie die Klone von Booger in einem Labor der Universität von Seoul zum ersten Mal sah. «Ja, ich kenne Euch! Ihr kennt mich auch», sagte McKinney und herzte die Welpen, die bei einer ihrer beiden Leih-Hundemütter schliefen.
Das Team der für RNL Bio arbeitenden Wissenschaftler wird von Lee Byeong Chun geleitet, einem früheren Kollegen des Forschers Hwang Woo Suk, der wegen gefälschter Forschungsergebnisse in Misskredit geraten ist. Das Klonen von Hunden wurde aber 2005 auch von unabhängiger Seite bestätigt. Lees Team hat seitdem rund 20 Hunde geklont. RNL Bio erklärte, das sei jetzt aber das erste Mal gewesen, dass ein Hund kommerziell geklont worden sei. «Booger war unser erster erfolgreicher Klon», erklärte das Unternehmen.
McKinney nahm mit Lee Kontakt auf, nachdem Booger im April 2006 an Krebs gestorben war. Die südkoreanischen Forscher brachten im März gefrorene Zellen des Hundes nach Seoul. Der Chef von RNL Bio, Ra Jeong Chan, erklärte, seine Firma wolle rund 300 Hunde im Jahr klonen, für Kunden im Nahen Osten könnten vielleicht auch Kamele geklont werden.
http://rnl.co.kr/eng/main.asp
Antwort auf Beitrag Nr.: 8.919.753 von meislo am 18.03.03 18:26:10Heilung von Diabetes rückt näher
Proteine lassen Zellen Insulin produzieren
Ständiges Insulinspritzen soll bald der Vergangenheit angehören (Foto ixelio.de/Gerd Altmann)
ixelio.de/Gerd Altmann)
Cambridge (pte/28.08.2008/15:00) - Forscher der US-Universität Harvard http://www.harvard.edu könnten einen großen Schritt in Richtung Heilung von Diabetes gemacht haben. Im Mausversuch ist es ihnen gelungen, aus einfachen Pankreaszellen, die im Darm für die Zerlegung von Nahrung verantwortlich sind, Insulin produzierende Zellen zu züchten. Dazu injizierten sie den Mäusen einen Protein-Cocktail, der dazu führte, dass ein Trio von normalerweise schlafenden Genen in den Zellen erwachte und dort mit einer Umprogrammierung begann. "Das ist, als ob jemand ein Programm auf seinen Computer herunterlädt und plötzlich wird aus dem PC ein Mac", erläutern die Wissenschaftler ihr Vorgehen.
Bereits nach drei Tagen begannen die so umgewandelten Zellen mit der Produktion kleiner Insulinmengen. Eine Woche später hatten sich bereits mehr als 20 Prozent in sogenannte Beta-Zellen umgewandelt. "Deren Insulinproduktion war mit der echter Beta-Zellen identisch", erklärt Doug Melton, Studienleiter und stellvertretender Leiter des Harvard Stammzellen-Instituts. Die Forschungsergebnisse könnten seiner Meinung nach aber nicht nur ein großer Fortschritt in der Diabetesbehandlung sein, sondern auch zur Regeneration von Herzmuskelzellen bei Herzinfarktpatienten oder zur Erneuerung von anderen beschädigten Zellen eingesetzt werden. "Es sollte möglich sein, einen jeden Zelltyp, der im Körper fehlt, aus einer anderen Zelle herzustellen", fährt Melton fort.
Das von den Forschern als "direct reprogramming" bezeichnete Verfahren, basiert auf dem Fakt, dass jede Zelle die komplette Bibliothek von Genen ihrer DNA beinhaltet. Die externe Zufuhr der Proteine führte in den Zellen durch einen noch unbekannten Prozess dazu, dass sich neue Zelltypen, Muskelfäden und Neuronen bildeten. Im Versuch stellten die Diabetes-Experten zudem fest, dass durch ihre Behandlungsmethode gewonnene Beta-Zellen nicht nur schneller, sondern auch stärker den Blutzuckerspiegel senkten als Beta-Zellen, die aus Stammzellen gewonnen waren. "Die Transformation scheint sicherer zu sein als Methoden, bei denen unreife Stammzellen eingesetzt werden und die dazu tendieren zu Tumoren auszuwachsen", meint Konrad Hochedlinger, Wissenschaftler am Harvard Stammzellen-Institut.
Für die Motivation der Heilung von Diabetes ein Stück näher zu kommen, sorgte bei Melton ein ganz persönlicher Umstand: "Meine beiden Kinder Emma und Sam haben beide selber Diabetes Typ I und ich wache jeden Tag auf und frage mich, wie kann ich Beta-Zellen herstellen kann", berichtet der Forscher im Gespräch mit der New York Times. Jedoch warnt der Harvard-Professor vor verfrühten Hoffnungen. Denn bisher befinde man sich noch im Tierversuch und es könne zwei bis fünf Jahre dauern, bis Testergebnisse für den Menschen vorliegen. "Sollten sich die Ergebnisse bestätigen, wäre es ein tatsächlicher Durchbruch", sagte ein deutscher Diabetes-Experte auf pressetext-Nachfrage. Denn damit würde man nicht nur der Heilung zahlreicher Krankheiten näher kommen, sondern könnte auch die umstrittene embryonale Stammzellenforschung zurückfahren. (Ende)
Proteine lassen Zellen Insulin produzieren
Ständiges Insulinspritzen soll bald der Vergangenheit angehören (Foto
 ixelio.de/Gerd Altmann)
ixelio.de/Gerd Altmann) Cambridge (pte/28.08.2008/15:00) - Forscher der US-Universität Harvard http://www.harvard.edu könnten einen großen Schritt in Richtung Heilung von Diabetes gemacht haben. Im Mausversuch ist es ihnen gelungen, aus einfachen Pankreaszellen, die im Darm für die Zerlegung von Nahrung verantwortlich sind, Insulin produzierende Zellen zu züchten. Dazu injizierten sie den Mäusen einen Protein-Cocktail, der dazu führte, dass ein Trio von normalerweise schlafenden Genen in den Zellen erwachte und dort mit einer Umprogrammierung begann. "Das ist, als ob jemand ein Programm auf seinen Computer herunterlädt und plötzlich wird aus dem PC ein Mac", erläutern die Wissenschaftler ihr Vorgehen.
Bereits nach drei Tagen begannen die so umgewandelten Zellen mit der Produktion kleiner Insulinmengen. Eine Woche später hatten sich bereits mehr als 20 Prozent in sogenannte Beta-Zellen umgewandelt. "Deren Insulinproduktion war mit der echter Beta-Zellen identisch", erklärt Doug Melton, Studienleiter und stellvertretender Leiter des Harvard Stammzellen-Instituts. Die Forschungsergebnisse könnten seiner Meinung nach aber nicht nur ein großer Fortschritt in der Diabetesbehandlung sein, sondern auch zur Regeneration von Herzmuskelzellen bei Herzinfarktpatienten oder zur Erneuerung von anderen beschädigten Zellen eingesetzt werden. "Es sollte möglich sein, einen jeden Zelltyp, der im Körper fehlt, aus einer anderen Zelle herzustellen", fährt Melton fort.
Das von den Forschern als "direct reprogramming" bezeichnete Verfahren, basiert auf dem Fakt, dass jede Zelle die komplette Bibliothek von Genen ihrer DNA beinhaltet. Die externe Zufuhr der Proteine führte in den Zellen durch einen noch unbekannten Prozess dazu, dass sich neue Zelltypen, Muskelfäden und Neuronen bildeten. Im Versuch stellten die Diabetes-Experten zudem fest, dass durch ihre Behandlungsmethode gewonnene Beta-Zellen nicht nur schneller, sondern auch stärker den Blutzuckerspiegel senkten als Beta-Zellen, die aus Stammzellen gewonnen waren. "Die Transformation scheint sicherer zu sein als Methoden, bei denen unreife Stammzellen eingesetzt werden und die dazu tendieren zu Tumoren auszuwachsen", meint Konrad Hochedlinger, Wissenschaftler am Harvard Stammzellen-Institut.
Für die Motivation der Heilung von Diabetes ein Stück näher zu kommen, sorgte bei Melton ein ganz persönlicher Umstand: "Meine beiden Kinder Emma und Sam haben beide selber Diabetes Typ I und ich wache jeden Tag auf und frage mich, wie kann ich Beta-Zellen herstellen kann", berichtet der Forscher im Gespräch mit der New York Times. Jedoch warnt der Harvard-Professor vor verfrühten Hoffnungen. Denn bisher befinde man sich noch im Tierversuch und es könne zwei bis fünf Jahre dauern, bis Testergebnisse für den Menschen vorliegen. "Sollten sich die Ergebnisse bestätigen, wäre es ein tatsächlicher Durchbruch", sagte ein deutscher Diabetes-Experte auf pressetext-Nachfrage. Denn damit würde man nicht nur der Heilung zahlreicher Krankheiten näher kommen, sondern könnte auch die umstrittene embryonale Stammzellenforschung zurückfahren. (Ende)
Hab doch gesagt, dass GRN163L erstmal das interessantere ist.
http://biz.yahoo.com/bw/081015/20081015005789.html?.v=1
http://biz.yahoo.com/bw/081015/20081015005789.html?.v=1


16.10.2008 • 16:35 Uhr
„Gutes Gefühl, dass wir im kommenden Jahr beginnen“
Stammzelltherapie wird erstmals an Menschen getestet werden
Von Arndt Reuning
Medizin. - Bislang gelten embryonale Stammzellen vornehmlich als Hoffnungsträger für die Forschung, noch weit entfernt von der klinischen Anwendung. Doch ein US-Biotechnologieunternehmen will bald mit den ersten Therapietests am Menschen beginnen. 22.000 Seiten umfasst der Genehmigungsantrag, der der US-Aufsichtsbehörde vorliegt.
Ein Berg von Papier, der kaum auf eine Schreibtischplatte passt. Das ist der Antrag, den die kalifornische Firma Geron Corporation [http://geron.com/] aus Menlo Park bei der FDA eingereicht hat, bei der amerikanischen Behörde für Lebensmittel- und Arzneisicherheit. Die Botschaft ist klar: die Geschäftsleute wollen kein Risiko eingehen. Deshalb haben sie die neuartige Stammzell-Therapie auf alle möglichen Gefahren hin abgeklopft. Ein Misserfolg könnte in der öffentlichen Wahrnehmung auf das gesamte Forschungsgebiet zurückfallen und den potentiellen Markt ersticken, bevor er überhaupt Gelegenheit gehabt hat, sich zu entwickeln. Und was sich die Forscher des Biotechnologie-Unternehmens vorgenommen haben, ist keine geringe Herausforderung. Sie wollen Patienten mit Querschnittslähmung und anderen Rückenmarksverletzungen heilen, sagt der Geron-Geschäftsführer, Thomas Okarma.
"Wir haben herausgefunden, wie man aus Stammzellen jene Art von Zellen züchten kann, die bei einer Rückenmarksverletzung beschädigt werden -sie gehören zu den so genannten Glia-Zellen. Die isolieren die Nervenfasern und versorgen sie mit Wachstums-Stoffen, so dass sie sich nach einer Verletzung wieder erholen können. Im Tierversuch mit gelähmten Ratten haben wir gezeigt, dass unsere Zellen tatsächlich die Nervenfasern wieder umschließen. Und das bleibt so selbst neun Monate, nachdem wir sie den Tieren gespritzt hatten. Den Ratten geht es nach einer einzigen Injektion deutlich besser - und zwar auf Dauer."
Der Erfolg bei den Nagern bedeutet allerdings nicht unbedingt, dass die Therapie bei Menschen genauso gut anschlägt. Am meisten Sorgen machen sich die Entwickler darum, dass das Immunsystem der Patienten die unbekannten Zellen bekämpft - Entzündungen wären die Folge. Schließlich wurden die Gliazellen nicht aus körpereigenen Stammzellen der Patienten gewonnen, sondern aus Stammzellen von fremden Embryonen. Deshalb wollen die Kalifornier in den ersten Wochen die Immunabwehr der Patienten leicht unterdrücken. Aber auf lange Sicht könnte ein anderes Problem ihnen einen Strich durch die Rechnung machen. Die Zellen könnten anfangen, unkontrolliert zu wuchern. Okama:
"Es geht dabei nicht um Krebs, sondern um so genannte Teratome. Das sind gutartige Wucherungen, die man aber im Rückenmark natürlich trotzdem nicht haben will. Wir haben das zwölf Monate lang untersucht und kein einziges Teratom in den Tieren gefunden."
Für ein Rattenleben mag das eine lange Zeit sein, aber ob zwölf Monate ausreichen, um das Risiko beim Menschen abzuschätzen, das bleibt fraglich. Zunächst einmal wollen die Forscher der Firma Geron daher nur solche Patienten behandeln, die unter einer kompletten Querschnittslähmung leiden. Unterhalb der Taille können sie sich nicht bewegen und nichts fühlen. Bei solchen Patienten kann die Stammzell-Therapie die Symptome aber höchstens lindern, nicht ganz zum Verschwinden bringen. Okama:
"Ganz sicher: An den ersten Patienten werden wir prüfen, ob die Methode sicher ist. Aus diesem Grund beginnen wir mit den kompletten Lähmungen. Sollte es Nebenwirkungen geben und sich der Zustand der Betroffenen verschlechtern, dann wird das für die Langzeitversorgung der Patienten wenige Auswirkungen haben. Aber würden wir mit den teilweisen Lähmungen anfangen, die deutlich häufiger vorkommen, dann könnte ein Fehler ganz katastrophale Folgen haben, zum Beispiel für die Atmung des Patienten."
Vier Jahre haben die Geron-Wissenschaftler für die Genehmigung der klinischen Studie geforscht. Im vergangenen Mai hat die FDA das Zulassungsverfahren aber erst einmal auf Eis gelegt. Trotzdem ist Tom Okarma optimistisch, dass die erste Studie mit Gewebe, das aus embryonalen Stammzellen gezüchtet worden ist, demnächst beginnen kann.
"Eigentlich hoffen wir, dass es im nächsten Jahr los geht. Aber noch gibt es da ein paar Probleme mit der Behörde zu klären. Wir müssen noch ein paar ergänzende Analysen einreichen. Aber wir haben ein gutes Gefühl, dass wir im kommenden Jahr diese Studie beginnen."
© 2008 Deutschlandradio
Die Stammenzellen dauern bestimmt noch 10-15 Jahre oder länger und mehrere Millionen $. In der Zeit werden noch viele Päpste sterben und US Präsidenten gewählt. Das ist "kurzfristig" kein Grund GERN zu keufen. Im Prinzip gibt es selten einen Grund Biotechs kurzfr. zu kaufen, es sei denn, sie haben den langen Weg hinter sich, oder stehen unmittelbar vor der Zulassung. Trotzdem gehört GERN nicht zuletzt durch die Stammzellen, zu den interessanteren Werten bei den Biotechs. Und vielleicht ist es eines kühlen Tages im Jahr 2030 so weit. Oder früher... Was fehlt sind hochkarätige Partner bei GRN163L. Aber wenn se so weiter machen.
Wichtig, auch heute wieder ne Meldung zu GRN163L. Macht druuuk!
http://biz.yahoo.com/bw/081020/20081020005447.html?.v=1

Wichtig, auch heute wieder ne Meldung zu GRN163L. Macht druuuk!
http://biz.yahoo.com/bw/081020/20081020005447.html?.v=1
Schnell, aber sicher bitte ...
Patienten warten auf Stammzelltherapien
Von Arndt Reuning
Eine Leberzelle ist eine Leberzelle, eine Herzzelle eine Herzzelle. Ganz anders ist das bei embryonalen Stammzellen - sie gelten als Alleskönner. Eine Behandlung mit Stammzellen aber gibt es bis heute nicht. Eine US-amerikanische Initiative in New York will das ändern und den Stammzellen Starthilfe geben.
Der Mediziner Thomas Okarma ist zuversichtlich, dass seine Firma die erste sein wird, die eine Stammzelltherapie an Menschen erproben wird. Die Geron Corporation hat aus humanen embryonalen Stammzellen ein Präparat hergestellt, das komplett querschnittgelähmten Menschen dabei helfen soll, sich wieder bewegen zu können.
Indem wir diesen Patienten unsere Zellen injizieren, hoffen wir, dass sich ihr Zustand bessern wird. Von einem Leben im Rollstuhl hin zu einem Leben, wie es teilgelähmte Menschen führen - so dass sie einer Physiotherapie zugänglich sind. Das ist unser Behandlungsziel.
Im Tierversuch mit Ratten funktioniert das tadellos. Allerdings ist der Beginn der Studie mit menschlichen Patienten immer wieder verschoben worden. Zuletzt im vergangenen Mai, als die amerikanische Zulassungsbehörde FDA weitere Informationen über die Risiken solch einer Behandlung gefordert hat. Jetzt glaubt der Geron-Geschäftsführer Okarma allerdings, dass die Klinische Studie anfangs 2009 beginnen kann. Dass das Biotechnologie-Unternehmen dafür genug Freiwillige finden wird, daran zweifelt niemand. Ähnlich wie in den 80er Jahren, als die ersten AIDS-Medikamente ihre Wirksamkeit im Tierversuch bewiesen hatten, fordern auch heute viele Betroffene, die neuen Therapien endlich an Menschen zu erproben. Von den Betroffenen unter Druck gesetzt fühlt sich Thomas Okarma allerdings nicht.
Die Patientenvertreter seien ausgesprochen hilfsbereit und verständnisvoll. Keiner wolle, dass hier irgendwelche Fehler gemacht werden, sagt Okarma. Viele Experten befürchten, dass sich das wiederholen könnte, was zuvor schon die Gentherapie in Verruf gebracht hat: dass ein geringer Behandlungserfolg oder unvorhergesehene Nebenwirkungen dem gesamte Arbeitsgebiet schaden könnte - und es somit um Jahre zurück werfen. So sieht es auch Susan Solomon, die Geschäftsführerin der New York Stem Cell Foundation, welche die Konferenz organisiert hat.
Vor allem muss die Forschung sehr sorgfältig durchgeführt werden. Wir brauchen einwandfreie Risikostudien. Natürlich, es gibt sehr ergreifende Geschichten von verzweifelten Patienten, die ihr Glück mit einer Behandlung im Ausland versuchen. Stammzelltourismus hat das einer unserer Referenten genannt. Denn es gibt immer genug skrupellose Menschen, welche die hoffnungslose Lage der Betroffenen ausnutzen und ihnen alles mögliche versprechen. Das ist wirklich eine traurige Geschichte. Ich denke schon, es ist wichtig, dass wir uns vor Augen führen, wie dringlich die Situation ist. Aber die Dringlichkeit besteht darin, eine Therapie zu finden, die wirklich etwas bewirkt und sicher ist.
Susan Solomon glaubt, dass Therapien noch auf sich warten lassen werden, bei denen embryonale Stammzellen oder daraus gezüchtetes Gewebe die kranken Zellen ersetzen. Mittlerweile ist es aber vielen Wissenschaftlern gelungen, Körperzellen von Patienten so umzuprogrammieren, dass sie embryonalen Stammzellen ähneln. An solchen Kulturen könnten die Forscher in der Petrischale die Krankheit genau studieren - um sie besser zu verstehen und Möglichkeiten zu finden, wie die Mediziner frühzeitig eine Diagnose stellen könnten.
Oft fragen mich die Leute: 'Wann wird es ein Heilmittel geben?' Dann ist meine Antwort: Wenn man eine schwere Krankheit erkennen kann, noch bevor sie ausgebrochen ist und daraufhin vorbeugend eingreift, dann ist das für mich ein Heilmittel.

Patienten warten auf Stammzelltherapien
Von Arndt Reuning
Eine Leberzelle ist eine Leberzelle, eine Herzzelle eine Herzzelle. Ganz anders ist das bei embryonalen Stammzellen - sie gelten als Alleskönner. Eine Behandlung mit Stammzellen aber gibt es bis heute nicht. Eine US-amerikanische Initiative in New York will das ändern und den Stammzellen Starthilfe geben.
Der Mediziner Thomas Okarma ist zuversichtlich, dass seine Firma die erste sein wird, die eine Stammzelltherapie an Menschen erproben wird. Die Geron Corporation hat aus humanen embryonalen Stammzellen ein Präparat hergestellt, das komplett querschnittgelähmten Menschen dabei helfen soll, sich wieder bewegen zu können.
Indem wir diesen Patienten unsere Zellen injizieren, hoffen wir, dass sich ihr Zustand bessern wird. Von einem Leben im Rollstuhl hin zu einem Leben, wie es teilgelähmte Menschen führen - so dass sie einer Physiotherapie zugänglich sind. Das ist unser Behandlungsziel.
Im Tierversuch mit Ratten funktioniert das tadellos. Allerdings ist der Beginn der Studie mit menschlichen Patienten immer wieder verschoben worden. Zuletzt im vergangenen Mai, als die amerikanische Zulassungsbehörde FDA weitere Informationen über die Risiken solch einer Behandlung gefordert hat. Jetzt glaubt der Geron-Geschäftsführer Okarma allerdings, dass die Klinische Studie anfangs 2009 beginnen kann. Dass das Biotechnologie-Unternehmen dafür genug Freiwillige finden wird, daran zweifelt niemand. Ähnlich wie in den 80er Jahren, als die ersten AIDS-Medikamente ihre Wirksamkeit im Tierversuch bewiesen hatten, fordern auch heute viele Betroffene, die neuen Therapien endlich an Menschen zu erproben. Von den Betroffenen unter Druck gesetzt fühlt sich Thomas Okarma allerdings nicht.
Die Patientenvertreter seien ausgesprochen hilfsbereit und verständnisvoll. Keiner wolle, dass hier irgendwelche Fehler gemacht werden, sagt Okarma. Viele Experten befürchten, dass sich das wiederholen könnte, was zuvor schon die Gentherapie in Verruf gebracht hat: dass ein geringer Behandlungserfolg oder unvorhergesehene Nebenwirkungen dem gesamte Arbeitsgebiet schaden könnte - und es somit um Jahre zurück werfen. So sieht es auch Susan Solomon, die Geschäftsführerin der New York Stem Cell Foundation, welche die Konferenz organisiert hat.
Vor allem muss die Forschung sehr sorgfältig durchgeführt werden. Wir brauchen einwandfreie Risikostudien. Natürlich, es gibt sehr ergreifende Geschichten von verzweifelten Patienten, die ihr Glück mit einer Behandlung im Ausland versuchen. Stammzelltourismus hat das einer unserer Referenten genannt. Denn es gibt immer genug skrupellose Menschen, welche die hoffnungslose Lage der Betroffenen ausnutzen und ihnen alles mögliche versprechen. Das ist wirklich eine traurige Geschichte. Ich denke schon, es ist wichtig, dass wir uns vor Augen führen, wie dringlich die Situation ist. Aber die Dringlichkeit besteht darin, eine Therapie zu finden, die wirklich etwas bewirkt und sicher ist.
Susan Solomon glaubt, dass Therapien noch auf sich warten lassen werden, bei denen embryonale Stammzellen oder daraus gezüchtetes Gewebe die kranken Zellen ersetzen. Mittlerweile ist es aber vielen Wissenschaftlern gelungen, Körperzellen von Patienten so umzuprogrammieren, dass sie embryonalen Stammzellen ähneln. An solchen Kulturen könnten die Forscher in der Petrischale die Krankheit genau studieren - um sie besser zu verstehen und Möglichkeiten zu finden, wie die Mediziner frühzeitig eine Diagnose stellen könnten.
Oft fragen mich die Leute: 'Wann wird es ein Heilmittel geben?' Dann ist meine Antwort: Wenn man eine schwere Krankheit erkennen kann, noch bevor sie ausgebrochen ist und daraufhin vorbeugend eingreift, dann ist das für mich ein Heilmittel.
Da der DOW ja heute endlich mal (hoffentlich) während der kompletten Handelszeit im positiven sein wird, wird sicher die Geron auch davon profitieren 

Umgang mit embryonalen Stammzellen im Ausbildungslabor des WiCell Research Institutes (Bild: Michael Lange) Stammzell-Pioniere
Zehn Jahre Forschung mit embryonalen Stammzellen des Menschen
Von Michael Lange
Was vor 10 Jahren in Madison, Wisconsin, westlich der Großen Seen gelang, könnte die Medizin revolutionieren. Hier in den Labors von WiCell wurden zum ersten mal embryonale Stammzellen des Menschen gezüchtet. Irgendwann einmal sollen sie zerstörtes Gewebe ersetzen, bei Alzheimer, Parkinson, Herzinfarkt oder Rückenmarksverletzungen. Doch wie weit sind die Arbeiten tatsächlich gediehen? Der Wissenschaftsreporter Michael Lange reist von Wisconsin nach Kalifornien, um nachzuprüfen, was aus den hochfliegenden Plänen geworden ist.
Manchmal gibt es einen Mann.
Das ist genau der richtige Mann am richtigen Ort.
Und wenn dieser Ort in Kalifornien liegt,
dann ist dieser Mann so etwas wie ein Held.
"Bob is like ... he is bigger than life. You know.... "
"Bob ist überlebensgroß. Was immer getan werden muss, Bob tut es."
"... he is an amazing person."
"Er ist ein erstaunlicher Mensch."
"Bob is the kind of guy, who knows how to get things done .…"
"Bob ist der Typ, der weiß, wie man etwas anpackt. Er hat Träume und vage Ideen Wirklichkeit werden lassen."
".... his energy, his organisational skills made it all possible."
"Seine Energie, sein Organisationstalent haben all das möglich gemacht."
Kalifornier lieben die Show, und sie lieben ihre Helden. Die Macher. Die Pioniere. Aber in dieser Geschichte geht es nicht in erster Linie um Helden, auch nicht um Kalifornien. Es geht um Biotechnologie. Insbesondere um Stammzellen. Und zwar um die umstrittenen embryonalen Stammzellen.
Aber wenn einer nach Kalifornien reist, ob nun wegen der Stammzellen oder wegen der Sonne, dann kommen die Helden irgendwann von selbst.
"Es ist wunderbar, all diese großartigen Dinge hier in Kalifornien zu sehen. "
"California is not only the biotech capitol of America. It is the biotech capitol of the world."
Kalifornien ist nicht nur die Biotechnologie-Hauptstadt Amerikas, es ist die Biotech-Hauptstadt der Welt. Diese Geschichte endet in Kalifornien, so wie einst der Treck nach Westen, aber sie beginnt viel weiter im Osten.
Ich bin nach Madison gereist. Dorthin, wo alles angefangen hat. Hier wurden die ersten embryonalen Stammzellen des Menschen gezüchtet.
Madison - das ist eine Universitätsstadt in Wisconsin. 100 Meilen westlich von Chicago. Hier beginnt der Mittlere Westen. Das heißt: viel Land, viel Mais, viele Kühe, viel Patriotismus, viel Religion - und ein wenig Wissenschaft.
James Thomson und sein Team von der Universität von Wisconsin verkündeten am 6. November 1998 einen Durchbruch für die Biotechnologie und für die Medizin. Sie hatten als erste embryonale Stammzellen des Menschen gezüchtet. Ein Traum war geboren: Menschliche Zellen, die sich im Labor immer weiter vermehrten. Zellen, die sich auf Kommando verwandeln ließen: in Muskelzellen, in Drüsenzellen, ja sogar in Nervenzellen. Die Möglichkeiten schienen unbegrenzt. Herzinfarkt, Diabetes, Parkinson, Alzheimer. Alles bald heilbar - mit Zellen aus der Retorte. Nur noch eine Frage der Zeit. Das Wort, das alle im Munde führten, lautete: Hoffnung.
Five-O-Five Rosa Road. Hier - in einem Industriegebiet am Stadtrand von Madison - habe ich das WiCell Research Institute gefunden. Von außen ein zweistöckiges unscheinbares Gebäude. Darin soll sich die nationale Stammzellenbank der USA befinden und das weltweit größte Versandhaus für Stammzellen.
Der Traum hatte von Anfang an eine dunkle Seite. Wer neue embryonale Stammzellen schaffen wollte, musste dazu einen Embryo töten. Einen frühen Menschen - sagen die einen. Eine nur unter dem Mikroskop sichtbare Zellkugel - sagen die anderen.
Ich darf sogar in den Lagerraum mit den wertvollen Zellen. Ein kleiner Raum im hinteren Teil des Gebäudes. Kein Tresor, kein Panzerglas, keine Zahlenkombination. Einige Tanks mit flüssigem Stickstoff stehen an der Wand. Und vier Gefrier-Truhen. Darin die kostbaren Zellkulturen. Tausende kleine Plastikdöschen. Tiefgefroren bei minus 196 Grad. Wenn ein Labor irgendwo auf der Welt eine Zellkultur anfordert, wird die Truhe geöffnet, ein Döschen herausgenommen und in spezielle Transportbehälter gepackt.
Der Leiter der Stammzellenbank Erik Forsberg nimmt einen der Behälter aus dem Regal. Nicht viel größer als ein Plastikeimer, aber deutlich schwerer.
"Der Behälter mit dem flüssigen Stickstoff befindet sich hier in dieser Transportkiste aus Kunststoff. Ich kann Ihnen das einmal demonstrieren. Dort in dieser kleinen Kapsel sind die Zellen."
Damit ich die Zellen in voller Pracht anschauen kann, gehen wir in das Ausbildungslabor. Monat für Monat kommen Wissenschaftler aus aller Welt hierher zum Üben.
Die Wissenschaftlerin Rupa Shevde holt ein Plastik-Schälchen aus einem Brutschrank. Dort lagern und wachsen embryonale Stammzellen bei 37 Grad Celsius. Sie schwimmen in einer rosaroten Flüssigkeit. Mit bloßem Auge erkenne ich nur diffuse weiße Wölkchen. Jetzt legt sie ein Schälchen unter das Mikroskop.
"Die Zellen sind winzig klein. Sie liegen dicht beieinander und bilden eine Kolonie. Zu einer Stammzellenkolonie gehören jeweils Hunderte oder Tausende Zellen. Diese Zellen hier wurden vor zehn Jahren in Madison erzeugt und wachsen immer noch weiter. Sie gehören zu den Zellen, die wir hier in der Staatlichen Stammzellenbank verwalten. Am Rand der Kolonie sehen Sie dünne, längliche Zellen. Das sind embryonale Gewebezellen von Mäusen. Sie ernähren die menschlichen Stammzellen. Sie füttern sie gewissermaßen. "
Wie ich erfahre, gibt es bei WiCell zwei Stammzellenbanken: Eine staatliche mit staatlich geförderten Stammzellen - und eine private mit neuen Stammzellen. "Präsidiale" und "Nicht-Präsidiale Zellen," sagen die Forscher. Beide darf ich mir unter dem Mikroskop anschauen. Die Unterschiede sind wohl nur für Profis zu erkennen.
Auch bei Stammzellen gibt es in Amerika die Guten und die Bösen. Staatliches Geld gibt es nur für gute "präsidiale" Zellen. Sie wurden vor dem 1. August 2001 aus Embryonen hergestellt. Auf einer Liste der staatlichen Gesundheitsbehörde sind sie aufgezählt. Alles, was später kam, sind "nicht-präsidiale" Zellen. Böse Zellen. Für sie gibt es natürlich kein staatliches Geld. Das ist die Einteilung, wie sie die Regierung in Washington vorgibt. - In der Sonne Kaliforniens sieht man das anders.
Über 3000 Kilometer bin ich nach Westen gereist - nach San Diego. Bis zum Pazifik ist es nicht mehr weit. Überall, wo man hinsieht: Forschungsinstitute. Und hinter den Mauern und Glasfassaden forschen mehr Stammzellenforscher als sonstwo auf der Welt. Dahinter steckt eine "Pro-Stammzellen-Bürgerinitiative" und der Gouverneur Arnold Schwarzenegger. Letztlich entschieden aber haben die Wähler. Sie stimmten zu über 60 Prozent dafür, drei Milliarden Dollar staatliches Geld auszugeben für Forschung mit embryonalen Stammzellen. So wurde Kalifornien zum Stammzellen-Paradies. Geklagt wird über die da in Washington.
"Die staatlichen Richtlinien und Beschränkungen waren nervend und sinnlos."
Ich spreche zunächst mit Larry Goldstein von der Universität von Kalifornien in San Diego.
"Das Ziel der Bush-Regierung war doch, dass weniger Embryonen zerstört werden sollten. Das haben sie nicht erreicht. Nur eines haben sie geschafft: Die Forschung wurde gebremst und unsere Arbeit unnötig komplizierter gemacht. Dass die Regierung nur bestimmte Stammzellen fördert, hat doch nur zur Folge, dass die besten und talentiertesten Wissenschaftler nicht mit dem besten Material arbeiten können. Und dort, wo genug privates Geld fließt, um auch die 'nicht präsidialen' Stammzellen zu erforschen, da hat die Politik die Kosten in die Höhe getrieben. Denn alles, jeder Labortisch und jede Pipette, muss ja doppelt vorhanden sein, damit auch garantiert kein staatliches Geld für Forschung mit 'nicht-präsidialen Zellen' ausgegeben wird. Das alles bringt doch überhaupt nichts. Das ist dumm und sinnlos."
Stammzellenähnliche menschliche Zellen lassen sich seit einem Jahr auch ohne Embryonen herstellen - aus Körperzellen. Hautzellen zum Beispiel werden mit Gentechnik so manipuliert, dass sie sich wie embryonale Stammzellen teilen und umwandeln können. Werden diese so genannten IPS-Zellen die embryonalen Stammzellen demnächst ablösen, frage ich Larry Goldstein. Die Antwort fällt eindeutig aus.
"Nein, die IPS-Zellen können embryonale Stammzellen nicht ersetzen. Sie sind nicht identisch, und deshalb brauchen wir beide. Das ist, wie mit einem Werkzeugkasten. Ein Handwerker mit nur einem Werkzeug kann nicht viel machen. Er braucht mehrere Werkzeuge und gutes Werkzeug. Und so ist das auch, wenn man Krankheiten verstehen und heilen will."
Wer lässt sich schon gerne in seine Arbeit hineinreden. Und dann auch noch von Politikern, die von Wissenschaft nichts verstehen. Aber als Forscher braucht man sie nunmal: die Politik. Zumindest als Geldgeber.
Ich treffe die Stammzellenforscherin Jeanne Loring im Scripps-Institut in La Jolla, nördlich von San Diego. Während wir uns über ihre Forschung unterhalten, fliegt ein Düsenjet nach dem anderen über das Scripps-Institut.
"Wenn ich das Geld hätte, das so ein Jet kostet, könnte ich so manche Krankheit heilen."
Nicht nur die Politiker im fernen Washington machen Stammzellenforschern wie Jeanne Loring das Leben schwer. Die Patente, die sich zum Beispiel die Forscherkollegen aus Wisconsin gesichert haben, verhindern ihrer Ansicht nach, dass Pharma-Firmen sich in der Stammzellenforschung engagieren. Loring:
"Embryonale Stammzellen sind patentiert. Das bedeutet: Jeder in den USA, der diese Zellen benutzt oder erforscht, muss eine Lizenz besitzen. Die muss man in Wisconsin beantragen. Und sobald man irgendetwas kommerzielles mit den Stammzellen macht und Geld verdient, wollen die Patentinhaber ihren Anteil."
Die Pharma-Industrie steigt deshalb nicht in die Stammzellenforschung ein, weil sie im Falle von späteren Gewinnen zu viel abgeben müsste, erklärt Jeanne Loring. Da investiert man doch lieber in klassische Wirkstoffe, die man in der Apotheke verkaufen kann, als in lebende Zellen. Und sollten Stammzellen irgendwann tatsächlich Menschen heilen, dann ist immer noch nicht klar, wie ein Unternehmen damit Geld verdienen kann. Stammzellenforscher sind also angewiesen - auf staatliches oder privates Geld.
Einer war bereits ein Held, bevor er sich mit Stammzellen und Biotechnologie beschäftigte: Er war Mister Universum und Hollywoodstar: Arnold Schwarzenegger. Als Gouverneur von Kalifornien kam er in die Forscherhochburg La Jolla und eroberte die Wissenschaftler-Herzen im Sturm. Jeanne Loring:
"Ich setzte ihn vor das Mikroskop und zeigte ihm einige Herzmuskelzellen, die wir aus embryonalen Stammzellen gezüchtet hatten. Er war sofort fasziniert und rief: Sie bewegen sich! Und es stellte sich heraus: Er wußte fast alles über Muskelzellen. Wir haben Arnold Schwarzenegger sehr viel zu verdanken. Er und Bob Klein sind beide furchtlos."
Bob Klein, der Held der Stammzellenforscher. Da ist er wieder. In einem Atemzug genannt mit dem Superstar und Gouverneur Arnold Schwarzenegger. Bob Klein ist Jurist, gelernter Anwalt, Familienvater und Immobilien-Investor. Eigentlich nicht die besten Voraussetzungen, um zum Helden zu werden. Doch 2004 gründete Bob Klein eine Bürgerinitiative und machte sich zu ihrem Anführer. Er setzte sich für die Stammzellenforschung in Kalifornien ein und erreichte eine Volksabstimmung über "Embryonale Stammzellen".
Schwarzenegger:
"Almost sixty per cent of the people said yes to proposition 71. They said yes to three billion dollar for stem cell research."
Jeanne Loring:
"Das hat mich sehr beeindruckt. Die Wähler von Kalifornien haben sich zu über 60 Prozent dafür entschieden, die Stammzellenforschung über zehn Jahre hinweg mit drei Milliarden Dollar zusätzlich zu fördern. Das hat uns immens geholfen. Ich kann alle Stammzellen erforschen, die ich brauche, und bin nicht gebunden an irgendwelche Vorgaben aus Washington. Alles, was Sie hier in diesem Labor sehen, wurde vom Staat Kalifornien bezahlt."
Schwarzenegger:
"Biotechnologie. Das sind nicht nur Leute in weißen Kitteln, die ihre Forschung betreiben. Biotechnologie ist ein Geschäft. Und sie wird das Leben von Milliarden Menschen verbessern. Das ist ein großartiger Kurs. Es ist mein Kurs. Und Kalifornien wird diesen Kurs unterstützen. Immer zu 100 Prozent."
Kalifornien ist das Land des Goldrauschs. Hier kann jeder sein Glück machen. Auf die da oben hat man hier noch nie gewartet. Auf eigene Faust loslegen. Das ist Kalifornien. Kein Wunder, dass nirgends sonst so viele Biotechnologie-Firmen aus dem Boden schießen wie zwischen San Diego und San Francisco.
Die ersten Biotechnologie-Unternehmen entwickeln mittlerweile praxisreife Therapien - mit embryonalen Stammzellen. Geron in San Francisco will seine Zellen an Rückenmarksverletzten erproben. Aber die Zulassungsbehörde zögert noch. Ein Misserfolg wäre fatal für das ganze Forschungsfeld. Ein anderes Unternehmen ist ebenfalls auf dem Weg in Richtung Praxis: Die Firma Novocell in San Diego. Hier will man eine Diabetes-Therapie entwickeln.
"Der ganze Hype und all die Hoffnungen, die sich von Anfang an um die embryonalen Stammzellen gerankt haben, werden jetzt nach und nach Realität."
Emmanuel Baetge ist Forschungschef bei Novocell. Aus embryonalen Stammzellen will er Pankreaszellen machen. Zellen der Bauchspeicheldrüse sollen im Labor heranwachsen - zur Behandlung von Diabetes-Patienten.
Wir gehen durch einen Gang in eines der Labors. Eine Mitarbeiterin sitzt vor einem Mikroskop. Baetge:
"A little baby pancreas made of embryonic stem cells. Look under the microscope!"
Die Mitarbeiterin entfernt noch etwas Fettgewebe und legt den Blick frei auf die winzige Bauchspeicheldrüse - gezüchtet aus embryonalen Stammzellen. Sie wird in eine Maus transplantiert werden und dort Insulin produzieren. Noch ist nicht klar, ob die Stammzellen Diabetespatienten wirklich heilen können. Wahrscheinlich müssten selbst bei einem Erfolg immer wieder neue Zellen gespritzt werden. Baetge
"Wir glauben, dass wir mittlerweile ein fertiges Konzept für ein Produkt zusammenhaben. Nun müssen wir es weiterentwickeln, so dass die Zellen stets in gleicher Qualität mit vergleichbarem Erfolg verpflanzt werden können. Und zwar ohne Risiko. Ich schätze: In zwei bis drei Jahren können wir uns an die Zulassungsbehörde wenden, um die ersten klinischen Versuche zu starten."
Das wäre die erste Therapie mit embryonalen Stammzellen gegen Diabetes.
Pioniere sind besondere Menschen - insbesondere in den USA. Dorthin zu gehen, wo noch nie ein Mensch zuvor gewesen ist, wer würde das nicht gerne. Aber jeder Schritt in unbekanntem Land ist riskant. Da braucht es Pioniere.
Als ich Novocell verlassen möchte, fällt mein Blick auf eine Tafel im Gang. In großen Buchstaben steht dort geschrieben: "Ein neuer Tag, eine neue Entdeckung." Unterschrieben mit "Captain Stem Cell". Aber wer ist "Captain Stammzelle"?
"Oh, Captain Stem Cell. Why he became known als Captain Stem Cell?"
Emmanuel Baetge weist auf seinen Mitarbeiter Evert Kroon, der gerade vorbeikommt. Doch der wehrt ab.
".... he is an unknown entity. He is like a hidden superhero."
Captain Stem Cell - ein unbekanntes Wesen? Ein Superheld im Verborgenen? Baetge:
"I show you a picture!"
Emmanuel Baetge lüftet das Geheimnis. Ein Zeitungsausschnitt an der Pinnwand. Mit einem Diaprojektor hat der Fotograf aus dem Wissenschaftler Kroon einen futuristisch aussehenden Superhelden gezaubert: Captain Stem Cell eben.
Die Stammzellenforschung hat viele Pioniere hervorgebracht. Wissenschaftler, die Neuland erkunden. Viele von ihnen Querdenker: Mavericks. Einer von ihnen sticht hervor: Der große alte Herr der kalifornischen Stammzellenforschung. Man könnte auch sagen: der Pate. Amerikanisch klingt das noch besser: "Godfather of Stem Cells".
Ich finde Irving Weissman in seinem kleinen vollgepackten Büro an der Stanford-Universität. Seine Assistentin im Vorzimmer ist etwa genau so alt wie er. Eigentlich müssten beide längst pensioniert sein. Noch ein wichtiger Anruf. Dann hat Irving Weissman Zeit für mich.
" Bob Klein? Hi Bob!"
Bob Klein ist am Apparat.
"Terrific. Terrific. Good. Oh, that's wonderful. I have to talk to"
Irving Weissman ist ganz aus dem Häuschen. Anscheinend sprechen die beiden über Forschungsförderung und eine neue Idee. Es hat irgendwas mit der Umsetzung von Laborergebnissen in die klinische Praxis zu tun.
"Good! Have a good day!"
Wir suchen einen Raum, um uns in Ruhe zu unterhalten. Irving Weissman ist immer noch ganz aufgekratzt.
"Normalerweise machen wir an der Universität zwar die wichtigen Entdeckungen, aber dann sind die Unternehmen an der Reihe. Sie bringen das Produkt auf den Markt oder die Heilmethode in die Klinik. Wir haben dann nichts mehr damit zu tun. Das wollen wir ändern. Wir bilden jetzt Teams, die nach neuen Behandlungsmethoden für bestimmte Krankheiten suchen. Denn die Firmen und die Investoren verstehen einfach nichts von Stammzellen-Forschung."
"Knock knock knocking on heaven's door, knock knock knocking..…"
Ein Straßenmusikant in der Innenstadt von San Francisco.
"I feel good. I know that I should."
Die Touristen haben Zeit. Sie stehen Schlange, um einen Platz in der berühmten Cable Car zu bekommen.
" .....so good. So good. I feel nice .…"
Einige Minuten Fussweg. Dann - zwischen einem Buchladen und einer Pizzeria - finde ich einen Eingang. Die Aufschrift über der Tür verrät: Kalifornisches Institut für Regenerative Medizin.
Wer Träume in Wirklichkeit verwandeln will - oder auch nur Entdeckungen in Produkte - braucht vor allem eines: Geld. Viel Geld. Seit Anfang des Jahres fließt das Geld für die kalifornischen Stammzellenforscher. Und der Hüter des Schatzes ist das CIRM. Oder auch: Cirm.
Im zweiten Stock stehe ich plötzlich in einem Parkhaus. Aber im dritten bin ich richtig. Ein Flur mit Büros. Einige werden gerade erst eingerichtet. Vor etwa einem Jahr hat das Cirm seine Arbeit begonnen. Hier wird entschieden, wer Geld aus dem 3-Milliarden-Topf der kalifornischen Regierung erhält. Der Pressesprecher Don Gibbons begrüßt mich.
Bob Klein ist noch beschäftigt. Aber ich kann vorher mit Alan Trounson sprechen. Arnold Schwarzenegger:
"Superstar Alan Trounson. The new President of Cirm. An amazing scientist, who is one of the true pioneers of in-vitro-fertilisation."
Noch ein Superstar - noch ein Pionier. Der australische Reproduktionsbiologe Alan Trounson ist Anfang des Jahres als neuer Präsident ans Cirm gekommen. Schwarzenegger:
"…. for what he calls the best stem cell job in the world. Right here in California."
"We recognised that Jamie Thomson …."
Reporter:
Ruhig ist es nicht im Büro des Cirm-Präsidenten Alan Trounson. Er hat eine beeindruckende Karriere als Wissenschaftler hinter sich. Fast hätte sein Team in Australien vor zehn Jahren die ersten embryonalen Stammzellen des Menschen gezüchtet. Aber es fehlten einige Daten, und die Konkurrenz in Wisconsin war schneller. Nun hat der australische Wissenschaftler eine neue Aufgabe übernommen. Trounson:
"Bob Klein kam auf mich zu und fragte, ob ich das machen wolle. Und ich dachte mir: Das ist möglicherweise der beste Stammzellen-Job der Welt. Uns stehen 300 Millionen Dollar im Jahr zur Verfügung. Hier haben wir die Möglichkeit, eine Revolution in der Medizin auszulösen. Ich dachte: Das ist phantastisch. Eine Herausforderung, die ich annehmen will."
"When we talk about building teams. It's about …."
Während ich mit Alan Trounson spreche, kommt ein Mann ganz leise in den Raum. Konservativ gekleidet: Dunkler Anzug mit Krawatte. Alles sitzt korrekt. Der Mann - um die 60 - setzt sich zu uns an den Tisch und scheint aufmerksam zuzuhören. Nach ein paar Minuten beginnt er mitzudiskutieren.
"Wir suchen nach Wegen, um schneller von einer Entdeckung in die Klinik zu gelangen. Unter Einhaltung aller Richtlinien. Es ist wichtig für alle Patienten und deren Angehörige, dass wir schneller mit Studien am Patienten beginnen."
Das also ist Bob Klein. Der Vorsitzende des Cirm-Bürgerkommittees. Jurist, Immobilien-Investor - inzwischen aber auch Fachmann für Stammzellen.
"Ich bin ein engagierter Student in diesen Fragen. Dr. Trounson ist der Experte. Ich habe einen jungen Sohn mit Diabetes 1. Die erbliche Form der Krankheit, bei der das eigene Immunsystem die insulinbildenden Zellen zerstört. Das kann zu Nierenschäden, Erblindung oder anderen schweren Leiden führen. Als Vater habe ich mich in einem Patientenverband engagiert und mich in Washington beim Senat für verstärkte Diabetes-Forschung eingesetzt. Aber die Leute von der staatlichen Gesundheitsbehörde sagten mir ganz klar: Diese Krankheit ist auf absehbare Zeit nicht heilbar. Das größte Potential liegt in den neuen embryonalen Stammzellen. Aber da werden wir von der Regierung Bush ausgebremst. Das dürfen wir nicht fördern."
"Chronic disease is tragic. It is a tragic and devastating experience."
So begann Bob Kleins Kampf. Nicht für die Stammzellenforschung. Das betont er immer wieder. Für die chronisch Kranken.
"To meet the challenge of chronic disease."
Bob Klein ist ein Jedermann. Freundlich, souverän, aber keinesfalls charismatisch. Ein wenig bin ich enttäuscht. Er könnte auch der Filialleiter meiner Sparkasse sein oder Versicherungsvertreter.
Zwei Dinge braucht es. Dann wird aus einem Normalbürger vielleicht so etwas wie ein Held: Eine gute Sache. Oder zumindest eine Sache, an die man glaubt. Und einen starken Gegner. Bob Klein glaubt an neue Heilmethoden für seinen Sohn und alle chronisch Kranken. Und auch den starken Gegner gibt es: den Präsidenten der Vereinigten Staaten. Klein:
"Acht Jahre lang wurden viele Anstrengungen behindert durch eine religiöse Ideologie des Präsidenten, die er dem Land aufgedrückt hat. Das ist unverantwortlich."
Bald wird der Präsident nicht mehr Bush heißen. Die US-Biotechnologie erwarten auf jeden Fall "bessere Zeiten". Obama oder McCain? Beide gelten als forschungsfreundlich. Das Paradies für Stammzellenforscher jedoch dürfte Kalifornien bleiben. Schwarzenegger:
"I just want to take a moment and say: thank you very much to Bob Klein."
Krankheiten sind besiegbar, im Prinzip.
Glück ist machbar. Manchmal.
Das ist der kalifornische Traum.
"So, thank you very much to Bob Klein."
"Thank you very much for listening and thank you for being here today. Thank you!"
Den 2. Teil der Reihe hören Sie in einer Woche: Die Klon-Cowboys. Dollys Erben im "Wilden Westen" der USA. In Wissenschaft im Brennpunkt, am nächsten Sonntag um 16 Uhr 30.
Hinweis: Den zweiten Teil von Michael Langes Reisereportage über die Klon-Cowboys aus den USA können Sie am Sonntag, 9. November, 16:30 Uhr, in "Wissenschaft im Brennpunkt" im Deutschlandfunk hören.
aus den USA können Sie am Sonntag, 9. November, 16:30 Uhr, in "Wissenschaft im Brennpunkt" im Deutschlandfunk hören.
Lesen Sie auch das Reisetagebuch unseres Reporters.
Zehn Jahre Forschung mit embryonalen Stammzellen des Menschen
Von Michael Lange
Was vor 10 Jahren in Madison, Wisconsin, westlich der Großen Seen gelang, könnte die Medizin revolutionieren. Hier in den Labors von WiCell wurden zum ersten mal embryonale Stammzellen des Menschen gezüchtet. Irgendwann einmal sollen sie zerstörtes Gewebe ersetzen, bei Alzheimer, Parkinson, Herzinfarkt oder Rückenmarksverletzungen. Doch wie weit sind die Arbeiten tatsächlich gediehen? Der Wissenschaftsreporter Michael Lange reist von Wisconsin nach Kalifornien, um nachzuprüfen, was aus den hochfliegenden Plänen geworden ist.
Manchmal gibt es einen Mann.
Das ist genau der richtige Mann am richtigen Ort.
Und wenn dieser Ort in Kalifornien liegt,
dann ist dieser Mann so etwas wie ein Held.
"Bob is like ... he is bigger than life. You know.... "
"Bob ist überlebensgroß. Was immer getan werden muss, Bob tut es."
"... he is an amazing person."
"Er ist ein erstaunlicher Mensch."
"Bob is the kind of guy, who knows how to get things done .…"
"Bob ist der Typ, der weiß, wie man etwas anpackt. Er hat Träume und vage Ideen Wirklichkeit werden lassen."
".... his energy, his organisational skills made it all possible."
"Seine Energie, sein Organisationstalent haben all das möglich gemacht."
Kalifornier lieben die Show, und sie lieben ihre Helden. Die Macher. Die Pioniere. Aber in dieser Geschichte geht es nicht in erster Linie um Helden, auch nicht um Kalifornien. Es geht um Biotechnologie. Insbesondere um Stammzellen. Und zwar um die umstrittenen embryonalen Stammzellen.
Aber wenn einer nach Kalifornien reist, ob nun wegen der Stammzellen oder wegen der Sonne, dann kommen die Helden irgendwann von selbst.
"Es ist wunderbar, all diese großartigen Dinge hier in Kalifornien zu sehen. "
"California is not only the biotech capitol of America. It is the biotech capitol of the world."
Kalifornien ist nicht nur die Biotechnologie-Hauptstadt Amerikas, es ist die Biotech-Hauptstadt der Welt. Diese Geschichte endet in Kalifornien, so wie einst der Treck nach Westen, aber sie beginnt viel weiter im Osten.
Ich bin nach Madison gereist. Dorthin, wo alles angefangen hat. Hier wurden die ersten embryonalen Stammzellen des Menschen gezüchtet.
Madison - das ist eine Universitätsstadt in Wisconsin. 100 Meilen westlich von Chicago. Hier beginnt der Mittlere Westen. Das heißt: viel Land, viel Mais, viele Kühe, viel Patriotismus, viel Religion - und ein wenig Wissenschaft.
James Thomson und sein Team von der Universität von Wisconsin verkündeten am 6. November 1998 einen Durchbruch für die Biotechnologie und für die Medizin. Sie hatten als erste embryonale Stammzellen des Menschen gezüchtet. Ein Traum war geboren: Menschliche Zellen, die sich im Labor immer weiter vermehrten. Zellen, die sich auf Kommando verwandeln ließen: in Muskelzellen, in Drüsenzellen, ja sogar in Nervenzellen. Die Möglichkeiten schienen unbegrenzt. Herzinfarkt, Diabetes, Parkinson, Alzheimer. Alles bald heilbar - mit Zellen aus der Retorte. Nur noch eine Frage der Zeit. Das Wort, das alle im Munde führten, lautete: Hoffnung.
Five-O-Five Rosa Road. Hier - in einem Industriegebiet am Stadtrand von Madison - habe ich das WiCell Research Institute gefunden. Von außen ein zweistöckiges unscheinbares Gebäude. Darin soll sich die nationale Stammzellenbank der USA befinden und das weltweit größte Versandhaus für Stammzellen.
Der Traum hatte von Anfang an eine dunkle Seite. Wer neue embryonale Stammzellen schaffen wollte, musste dazu einen Embryo töten. Einen frühen Menschen - sagen die einen. Eine nur unter dem Mikroskop sichtbare Zellkugel - sagen die anderen.
Ich darf sogar in den Lagerraum mit den wertvollen Zellen. Ein kleiner Raum im hinteren Teil des Gebäudes. Kein Tresor, kein Panzerglas, keine Zahlenkombination. Einige Tanks mit flüssigem Stickstoff stehen an der Wand. Und vier Gefrier-Truhen. Darin die kostbaren Zellkulturen. Tausende kleine Plastikdöschen. Tiefgefroren bei minus 196 Grad. Wenn ein Labor irgendwo auf der Welt eine Zellkultur anfordert, wird die Truhe geöffnet, ein Döschen herausgenommen und in spezielle Transportbehälter gepackt.
Der Leiter der Stammzellenbank Erik Forsberg nimmt einen der Behälter aus dem Regal. Nicht viel größer als ein Plastikeimer, aber deutlich schwerer.
"Der Behälter mit dem flüssigen Stickstoff befindet sich hier in dieser Transportkiste aus Kunststoff. Ich kann Ihnen das einmal demonstrieren. Dort in dieser kleinen Kapsel sind die Zellen."
Damit ich die Zellen in voller Pracht anschauen kann, gehen wir in das Ausbildungslabor. Monat für Monat kommen Wissenschaftler aus aller Welt hierher zum Üben.
Die Wissenschaftlerin Rupa Shevde holt ein Plastik-Schälchen aus einem Brutschrank. Dort lagern und wachsen embryonale Stammzellen bei 37 Grad Celsius. Sie schwimmen in einer rosaroten Flüssigkeit. Mit bloßem Auge erkenne ich nur diffuse weiße Wölkchen. Jetzt legt sie ein Schälchen unter das Mikroskop.
"Die Zellen sind winzig klein. Sie liegen dicht beieinander und bilden eine Kolonie. Zu einer Stammzellenkolonie gehören jeweils Hunderte oder Tausende Zellen. Diese Zellen hier wurden vor zehn Jahren in Madison erzeugt und wachsen immer noch weiter. Sie gehören zu den Zellen, die wir hier in der Staatlichen Stammzellenbank verwalten. Am Rand der Kolonie sehen Sie dünne, längliche Zellen. Das sind embryonale Gewebezellen von Mäusen. Sie ernähren die menschlichen Stammzellen. Sie füttern sie gewissermaßen. "
Wie ich erfahre, gibt es bei WiCell zwei Stammzellenbanken: Eine staatliche mit staatlich geförderten Stammzellen - und eine private mit neuen Stammzellen. "Präsidiale" und "Nicht-Präsidiale Zellen," sagen die Forscher. Beide darf ich mir unter dem Mikroskop anschauen. Die Unterschiede sind wohl nur für Profis zu erkennen.
Auch bei Stammzellen gibt es in Amerika die Guten und die Bösen. Staatliches Geld gibt es nur für gute "präsidiale" Zellen. Sie wurden vor dem 1. August 2001 aus Embryonen hergestellt. Auf einer Liste der staatlichen Gesundheitsbehörde sind sie aufgezählt. Alles, was später kam, sind "nicht-präsidiale" Zellen. Böse Zellen. Für sie gibt es natürlich kein staatliches Geld. Das ist die Einteilung, wie sie die Regierung in Washington vorgibt. - In der Sonne Kaliforniens sieht man das anders.
Über 3000 Kilometer bin ich nach Westen gereist - nach San Diego. Bis zum Pazifik ist es nicht mehr weit. Überall, wo man hinsieht: Forschungsinstitute. Und hinter den Mauern und Glasfassaden forschen mehr Stammzellenforscher als sonstwo auf der Welt. Dahinter steckt eine "Pro-Stammzellen-Bürgerinitiative" und der Gouverneur Arnold Schwarzenegger. Letztlich entschieden aber haben die Wähler. Sie stimmten zu über 60 Prozent dafür, drei Milliarden Dollar staatliches Geld auszugeben für Forschung mit embryonalen Stammzellen. So wurde Kalifornien zum Stammzellen-Paradies. Geklagt wird über die da in Washington.
"Die staatlichen Richtlinien und Beschränkungen waren nervend und sinnlos."
Ich spreche zunächst mit Larry Goldstein von der Universität von Kalifornien in San Diego.
"Das Ziel der Bush-Regierung war doch, dass weniger Embryonen zerstört werden sollten. Das haben sie nicht erreicht. Nur eines haben sie geschafft: Die Forschung wurde gebremst und unsere Arbeit unnötig komplizierter gemacht. Dass die Regierung nur bestimmte Stammzellen fördert, hat doch nur zur Folge, dass die besten und talentiertesten Wissenschaftler nicht mit dem besten Material arbeiten können. Und dort, wo genug privates Geld fließt, um auch die 'nicht präsidialen' Stammzellen zu erforschen, da hat die Politik die Kosten in die Höhe getrieben. Denn alles, jeder Labortisch und jede Pipette, muss ja doppelt vorhanden sein, damit auch garantiert kein staatliches Geld für Forschung mit 'nicht-präsidialen Zellen' ausgegeben wird. Das alles bringt doch überhaupt nichts. Das ist dumm und sinnlos."
Stammzellenähnliche menschliche Zellen lassen sich seit einem Jahr auch ohne Embryonen herstellen - aus Körperzellen. Hautzellen zum Beispiel werden mit Gentechnik so manipuliert, dass sie sich wie embryonale Stammzellen teilen und umwandeln können. Werden diese so genannten IPS-Zellen die embryonalen Stammzellen demnächst ablösen, frage ich Larry Goldstein. Die Antwort fällt eindeutig aus.
"Nein, die IPS-Zellen können embryonale Stammzellen nicht ersetzen. Sie sind nicht identisch, und deshalb brauchen wir beide. Das ist, wie mit einem Werkzeugkasten. Ein Handwerker mit nur einem Werkzeug kann nicht viel machen. Er braucht mehrere Werkzeuge und gutes Werkzeug. Und so ist das auch, wenn man Krankheiten verstehen und heilen will."
Wer lässt sich schon gerne in seine Arbeit hineinreden. Und dann auch noch von Politikern, die von Wissenschaft nichts verstehen. Aber als Forscher braucht man sie nunmal: die Politik. Zumindest als Geldgeber.
Ich treffe die Stammzellenforscherin Jeanne Loring im Scripps-Institut in La Jolla, nördlich von San Diego. Während wir uns über ihre Forschung unterhalten, fliegt ein Düsenjet nach dem anderen über das Scripps-Institut.
"Wenn ich das Geld hätte, das so ein Jet kostet, könnte ich so manche Krankheit heilen."
Nicht nur die Politiker im fernen Washington machen Stammzellenforschern wie Jeanne Loring das Leben schwer. Die Patente, die sich zum Beispiel die Forscherkollegen aus Wisconsin gesichert haben, verhindern ihrer Ansicht nach, dass Pharma-Firmen sich in der Stammzellenforschung engagieren. Loring:
"Embryonale Stammzellen sind patentiert. Das bedeutet: Jeder in den USA, der diese Zellen benutzt oder erforscht, muss eine Lizenz besitzen. Die muss man in Wisconsin beantragen. Und sobald man irgendetwas kommerzielles mit den Stammzellen macht und Geld verdient, wollen die Patentinhaber ihren Anteil."
Die Pharma-Industrie steigt deshalb nicht in die Stammzellenforschung ein, weil sie im Falle von späteren Gewinnen zu viel abgeben müsste, erklärt Jeanne Loring. Da investiert man doch lieber in klassische Wirkstoffe, die man in der Apotheke verkaufen kann, als in lebende Zellen. Und sollten Stammzellen irgendwann tatsächlich Menschen heilen, dann ist immer noch nicht klar, wie ein Unternehmen damit Geld verdienen kann. Stammzellenforscher sind also angewiesen - auf staatliches oder privates Geld.
Einer war bereits ein Held, bevor er sich mit Stammzellen und Biotechnologie beschäftigte: Er war Mister Universum und Hollywoodstar: Arnold Schwarzenegger. Als Gouverneur von Kalifornien kam er in die Forscherhochburg La Jolla und eroberte die Wissenschaftler-Herzen im Sturm. Jeanne Loring:
"Ich setzte ihn vor das Mikroskop und zeigte ihm einige Herzmuskelzellen, die wir aus embryonalen Stammzellen gezüchtet hatten. Er war sofort fasziniert und rief: Sie bewegen sich! Und es stellte sich heraus: Er wußte fast alles über Muskelzellen. Wir haben Arnold Schwarzenegger sehr viel zu verdanken. Er und Bob Klein sind beide furchtlos."
Bob Klein, der Held der Stammzellenforscher. Da ist er wieder. In einem Atemzug genannt mit dem Superstar und Gouverneur Arnold Schwarzenegger. Bob Klein ist Jurist, gelernter Anwalt, Familienvater und Immobilien-Investor. Eigentlich nicht die besten Voraussetzungen, um zum Helden zu werden. Doch 2004 gründete Bob Klein eine Bürgerinitiative und machte sich zu ihrem Anführer. Er setzte sich für die Stammzellenforschung in Kalifornien ein und erreichte eine Volksabstimmung über "Embryonale Stammzellen".
Schwarzenegger:
"Almost sixty per cent of the people said yes to proposition 71. They said yes to three billion dollar for stem cell research."
Jeanne Loring:
"Das hat mich sehr beeindruckt. Die Wähler von Kalifornien haben sich zu über 60 Prozent dafür entschieden, die Stammzellenforschung über zehn Jahre hinweg mit drei Milliarden Dollar zusätzlich zu fördern. Das hat uns immens geholfen. Ich kann alle Stammzellen erforschen, die ich brauche, und bin nicht gebunden an irgendwelche Vorgaben aus Washington. Alles, was Sie hier in diesem Labor sehen, wurde vom Staat Kalifornien bezahlt."
Schwarzenegger:
"Biotechnologie. Das sind nicht nur Leute in weißen Kitteln, die ihre Forschung betreiben. Biotechnologie ist ein Geschäft. Und sie wird das Leben von Milliarden Menschen verbessern. Das ist ein großartiger Kurs. Es ist mein Kurs. Und Kalifornien wird diesen Kurs unterstützen. Immer zu 100 Prozent."
Kalifornien ist das Land des Goldrauschs. Hier kann jeder sein Glück machen. Auf die da oben hat man hier noch nie gewartet. Auf eigene Faust loslegen. Das ist Kalifornien. Kein Wunder, dass nirgends sonst so viele Biotechnologie-Firmen aus dem Boden schießen wie zwischen San Diego und San Francisco.
Die ersten Biotechnologie-Unternehmen entwickeln mittlerweile praxisreife Therapien - mit embryonalen Stammzellen. Geron in San Francisco will seine Zellen an Rückenmarksverletzten erproben. Aber die Zulassungsbehörde zögert noch. Ein Misserfolg wäre fatal für das ganze Forschungsfeld. Ein anderes Unternehmen ist ebenfalls auf dem Weg in Richtung Praxis: Die Firma Novocell in San Diego. Hier will man eine Diabetes-Therapie entwickeln.
"Der ganze Hype und all die Hoffnungen, die sich von Anfang an um die embryonalen Stammzellen gerankt haben, werden jetzt nach und nach Realität."
Emmanuel Baetge ist Forschungschef bei Novocell. Aus embryonalen Stammzellen will er Pankreaszellen machen. Zellen der Bauchspeicheldrüse sollen im Labor heranwachsen - zur Behandlung von Diabetes-Patienten.
Wir gehen durch einen Gang in eines der Labors. Eine Mitarbeiterin sitzt vor einem Mikroskop. Baetge:
"A little baby pancreas made of embryonic stem cells. Look under the microscope!"
Die Mitarbeiterin entfernt noch etwas Fettgewebe und legt den Blick frei auf die winzige Bauchspeicheldrüse - gezüchtet aus embryonalen Stammzellen. Sie wird in eine Maus transplantiert werden und dort Insulin produzieren. Noch ist nicht klar, ob die Stammzellen Diabetespatienten wirklich heilen können. Wahrscheinlich müssten selbst bei einem Erfolg immer wieder neue Zellen gespritzt werden. Baetge
"Wir glauben, dass wir mittlerweile ein fertiges Konzept für ein Produkt zusammenhaben. Nun müssen wir es weiterentwickeln, so dass die Zellen stets in gleicher Qualität mit vergleichbarem Erfolg verpflanzt werden können. Und zwar ohne Risiko. Ich schätze: In zwei bis drei Jahren können wir uns an die Zulassungsbehörde wenden, um die ersten klinischen Versuche zu starten."
Das wäre die erste Therapie mit embryonalen Stammzellen gegen Diabetes.
Pioniere sind besondere Menschen - insbesondere in den USA. Dorthin zu gehen, wo noch nie ein Mensch zuvor gewesen ist, wer würde das nicht gerne. Aber jeder Schritt in unbekanntem Land ist riskant. Da braucht es Pioniere.
Als ich Novocell verlassen möchte, fällt mein Blick auf eine Tafel im Gang. In großen Buchstaben steht dort geschrieben: "Ein neuer Tag, eine neue Entdeckung." Unterschrieben mit "Captain Stem Cell". Aber wer ist "Captain Stammzelle"?
"Oh, Captain Stem Cell. Why he became known als Captain Stem Cell?"
Emmanuel Baetge weist auf seinen Mitarbeiter Evert Kroon, der gerade vorbeikommt. Doch der wehrt ab.
".... he is an unknown entity. He is like a hidden superhero."
Captain Stem Cell - ein unbekanntes Wesen? Ein Superheld im Verborgenen? Baetge:
"I show you a picture!"
Emmanuel Baetge lüftet das Geheimnis. Ein Zeitungsausschnitt an der Pinnwand. Mit einem Diaprojektor hat der Fotograf aus dem Wissenschaftler Kroon einen futuristisch aussehenden Superhelden gezaubert: Captain Stem Cell eben.
Die Stammzellenforschung hat viele Pioniere hervorgebracht. Wissenschaftler, die Neuland erkunden. Viele von ihnen Querdenker: Mavericks. Einer von ihnen sticht hervor: Der große alte Herr der kalifornischen Stammzellenforschung. Man könnte auch sagen: der Pate. Amerikanisch klingt das noch besser: "Godfather of Stem Cells".
Ich finde Irving Weissman in seinem kleinen vollgepackten Büro an der Stanford-Universität. Seine Assistentin im Vorzimmer ist etwa genau so alt wie er. Eigentlich müssten beide längst pensioniert sein. Noch ein wichtiger Anruf. Dann hat Irving Weissman Zeit für mich.
" Bob Klein? Hi Bob!"
Bob Klein ist am Apparat.
"Terrific. Terrific. Good. Oh, that's wonderful. I have to talk to"
Irving Weissman ist ganz aus dem Häuschen. Anscheinend sprechen die beiden über Forschungsförderung und eine neue Idee. Es hat irgendwas mit der Umsetzung von Laborergebnissen in die klinische Praxis zu tun.
"Good! Have a good day!"
Wir suchen einen Raum, um uns in Ruhe zu unterhalten. Irving Weissman ist immer noch ganz aufgekratzt.
"Normalerweise machen wir an der Universität zwar die wichtigen Entdeckungen, aber dann sind die Unternehmen an der Reihe. Sie bringen das Produkt auf den Markt oder die Heilmethode in die Klinik. Wir haben dann nichts mehr damit zu tun. Das wollen wir ändern. Wir bilden jetzt Teams, die nach neuen Behandlungsmethoden für bestimmte Krankheiten suchen. Denn die Firmen und die Investoren verstehen einfach nichts von Stammzellen-Forschung."
"Knock knock knocking on heaven's door, knock knock knocking..…"
Ein Straßenmusikant in der Innenstadt von San Francisco.
"I feel good. I know that I should."
Die Touristen haben Zeit. Sie stehen Schlange, um einen Platz in der berühmten Cable Car zu bekommen.
" .....so good. So good. I feel nice .…"
Einige Minuten Fussweg. Dann - zwischen einem Buchladen und einer Pizzeria - finde ich einen Eingang. Die Aufschrift über der Tür verrät: Kalifornisches Institut für Regenerative Medizin.
Wer Träume in Wirklichkeit verwandeln will - oder auch nur Entdeckungen in Produkte - braucht vor allem eines: Geld. Viel Geld. Seit Anfang des Jahres fließt das Geld für die kalifornischen Stammzellenforscher. Und der Hüter des Schatzes ist das CIRM. Oder auch: Cirm.
Im zweiten Stock stehe ich plötzlich in einem Parkhaus. Aber im dritten bin ich richtig. Ein Flur mit Büros. Einige werden gerade erst eingerichtet. Vor etwa einem Jahr hat das Cirm seine Arbeit begonnen. Hier wird entschieden, wer Geld aus dem 3-Milliarden-Topf der kalifornischen Regierung erhält. Der Pressesprecher Don Gibbons begrüßt mich.
Bob Klein ist noch beschäftigt. Aber ich kann vorher mit Alan Trounson sprechen. Arnold Schwarzenegger:
"Superstar Alan Trounson. The new President of Cirm. An amazing scientist, who is one of the true pioneers of in-vitro-fertilisation."
Noch ein Superstar - noch ein Pionier. Der australische Reproduktionsbiologe Alan Trounson ist Anfang des Jahres als neuer Präsident ans Cirm gekommen. Schwarzenegger:
"…. for what he calls the best stem cell job in the world. Right here in California."
"We recognised that Jamie Thomson …."
Reporter:
Ruhig ist es nicht im Büro des Cirm-Präsidenten Alan Trounson. Er hat eine beeindruckende Karriere als Wissenschaftler hinter sich. Fast hätte sein Team in Australien vor zehn Jahren die ersten embryonalen Stammzellen des Menschen gezüchtet. Aber es fehlten einige Daten, und die Konkurrenz in Wisconsin war schneller. Nun hat der australische Wissenschaftler eine neue Aufgabe übernommen. Trounson:
"Bob Klein kam auf mich zu und fragte, ob ich das machen wolle. Und ich dachte mir: Das ist möglicherweise der beste Stammzellen-Job der Welt. Uns stehen 300 Millionen Dollar im Jahr zur Verfügung. Hier haben wir die Möglichkeit, eine Revolution in der Medizin auszulösen. Ich dachte: Das ist phantastisch. Eine Herausforderung, die ich annehmen will."
"When we talk about building teams. It's about …."
Während ich mit Alan Trounson spreche, kommt ein Mann ganz leise in den Raum. Konservativ gekleidet: Dunkler Anzug mit Krawatte. Alles sitzt korrekt. Der Mann - um die 60 - setzt sich zu uns an den Tisch und scheint aufmerksam zuzuhören. Nach ein paar Minuten beginnt er mitzudiskutieren.
"Wir suchen nach Wegen, um schneller von einer Entdeckung in die Klinik zu gelangen. Unter Einhaltung aller Richtlinien. Es ist wichtig für alle Patienten und deren Angehörige, dass wir schneller mit Studien am Patienten beginnen."
Das also ist Bob Klein. Der Vorsitzende des Cirm-Bürgerkommittees. Jurist, Immobilien-Investor - inzwischen aber auch Fachmann für Stammzellen.
"Ich bin ein engagierter Student in diesen Fragen. Dr. Trounson ist der Experte. Ich habe einen jungen Sohn mit Diabetes 1. Die erbliche Form der Krankheit, bei der das eigene Immunsystem die insulinbildenden Zellen zerstört. Das kann zu Nierenschäden, Erblindung oder anderen schweren Leiden führen. Als Vater habe ich mich in einem Patientenverband engagiert und mich in Washington beim Senat für verstärkte Diabetes-Forschung eingesetzt. Aber die Leute von der staatlichen Gesundheitsbehörde sagten mir ganz klar: Diese Krankheit ist auf absehbare Zeit nicht heilbar. Das größte Potential liegt in den neuen embryonalen Stammzellen. Aber da werden wir von der Regierung Bush ausgebremst. Das dürfen wir nicht fördern."
"Chronic disease is tragic. It is a tragic and devastating experience."
So begann Bob Kleins Kampf. Nicht für die Stammzellenforschung. Das betont er immer wieder. Für die chronisch Kranken.
"To meet the challenge of chronic disease."
Bob Klein ist ein Jedermann. Freundlich, souverän, aber keinesfalls charismatisch. Ein wenig bin ich enttäuscht. Er könnte auch der Filialleiter meiner Sparkasse sein oder Versicherungsvertreter.
Zwei Dinge braucht es. Dann wird aus einem Normalbürger vielleicht so etwas wie ein Held: Eine gute Sache. Oder zumindest eine Sache, an die man glaubt. Und einen starken Gegner. Bob Klein glaubt an neue Heilmethoden für seinen Sohn und alle chronisch Kranken. Und auch den starken Gegner gibt es: den Präsidenten der Vereinigten Staaten. Klein:
"Acht Jahre lang wurden viele Anstrengungen behindert durch eine religiöse Ideologie des Präsidenten, die er dem Land aufgedrückt hat. Das ist unverantwortlich."
Bald wird der Präsident nicht mehr Bush heißen. Die US-Biotechnologie erwarten auf jeden Fall "bessere Zeiten". Obama oder McCain? Beide gelten als forschungsfreundlich. Das Paradies für Stammzellenforscher jedoch dürfte Kalifornien bleiben. Schwarzenegger:
"I just want to take a moment and say: thank you very much to Bob Klein."
Krankheiten sind besiegbar, im Prinzip.
Glück ist machbar. Manchmal.
Das ist der kalifornische Traum.
"So, thank you very much to Bob Klein."
"Thank you very much for listening and thank you for being here today. Thank you!"
Den 2. Teil der Reihe hören Sie in einer Woche: Die Klon-Cowboys. Dollys Erben im "Wilden Westen" der USA. In Wissenschaft im Brennpunkt, am nächsten Sonntag um 16 Uhr 30.
Hinweis: Den zweiten Teil von Michael Langes Reisereportage über die Klon-Cowboys
 aus den USA können Sie am Sonntag, 9. November, 16:30 Uhr, in "Wissenschaft im Brennpunkt" im Deutschlandfunk hören.
aus den USA können Sie am Sonntag, 9. November, 16:30 Uhr, in "Wissenschaft im Brennpunkt" im Deutschlandfunk hören.Lesen Sie auch das Reisetagebuch unseres Reporters.
der Deutschlandfunk beschätigt sich ziemlich intensiv mit dem Thema


Das hätte ich vor ein paar Tagen nicht geglaubt, das Geron gleich so durchstartet 
Glück für diejenigen, welche jetzt erst einsteigen.
Die neue Regierung wird der Stammzellenforschung auf jeden Fall positiver gesinnt sein und dementsprechend auch unterstützen.
(Bush Regierung wirkte als Bremse)

Glück für diejenigen, welche jetzt erst einsteigen.
Die neue Regierung wird der Stammzellenforschung auf jeden Fall positiver gesinnt sein und dementsprechend auch unterstützen.
(Bush Regierung wirkte als Bremse)
Osiris: Milliardendeal mit Genzyme
Bastian Galuschka
Die Stammzellen-Firma Osiris Therapeutics hat eine Kooperation mit dem Biotech-Konzern Genzyme geschlossen. Bis zu 1,38 Milliarden Dollar könnten so in die Kasse des Unternehmens fließen.
Beim Stichwort Stammzellen-Aktien werden die meisten Anleger sofort an bekannte Namen wie Stemcells, Geron oder Aastrom Biosciences denken. Gestern machte jedoch eine ganz andere Firma in den USA Schlagzeilen: Osiris Therapeutics.
Ritterschlag durch Genzyme
Osiris, das sich auf die Entwicklung von Therapien auf Basis adulter Stammzellen spezialisiert hat, gelang es, mit Genzyme einen der ganz Großen in der Biotech-Branche als Partner zu gewinnen. Im Zuge der Kooperation wird Genzyme an Osiris bis zu 1,38 Milliarden Dollar überweisen. Davon fließen 130 Millionen Dollar sofort, weitere 1,25 Milliarden Dollar werden fällig, sollte Osiris bestimmte Meilensteine wie beispielsweise den erfolgreichen Abschluss klinischer Studien oder eine Marktzulassung eines Produkts erreichen.
Projekte weit fortgeschritten
Genzymes Interesse haben vor allem zwei Kandidaten in der Medikamentenpipeline von Osiris geweckt, die zum Teil bereits die entscheidenden Testreihen vor einer möglichen Marktzulassung durchlaufen. Prochymal wird neben der Behandlung diverser Immunstörungen auch bei Morbus Crohn, einer chronischen Entzündung des Magen-Darm-Trakts, getestet. Chondrogen dagegen zielt auf die Behandlung von Arthritis im Knie ab. Der Vertrag sieht vor, dass Osiris die Vermarktungsrechte für beide Produkte in den USA und Kanada behalten, diese in den anderen Ländern aber nun an Genzyme abtreten wird.
Erste Stammzellentherapie vor Zulassung
Mit dem Geld wird Osiris alle laufenden Studien finanzieren, an den Kosten für weitere Testreihen wird sich Genzyme mit 40 Prozent beteiligen. Für eine Zulassung entscheidende Daten von Prochymal werden im nächsten Jahr erwartet. Sollten diese positiv ausfallen, stehen die Chancen gut, dass Prochymal die erste von der amerikanischen Gesundheitsbehörde FDA zugelassene Therapie auf Basis adulter Stammzellen wird. Ohne Frage würde das dem gesamten Sektor einen gehörigen Schub verleihen.
Für jeden Anlegertyp etwas
Nachdem die Osiris-Aktie kurz nach der Meldung noch die Gewinnerliste im Nasdaq Biotech Index (NBI) deutlich anführte, gab sie bis zum Handelsende fast das gesamte Plus wieder ab. Nichtsdestotrotz hat sich der Titel in den vergangenen Wochen gut geschlagen. Anleger, die im Stammzellen-Sektor investieren wollen und somit ein gewisses Risiko nicht scheuen, sollten sich das Unternehmen auf die Watchlist nehmen und bei Kursrücksetzern zuschlagen. Eher risikoscheue Naturen investieren dagegen in Genzyme, die Biotech-Empfehlung des Aktionärs in Ausgabe 45/08.
Bastian Galuschka
Die Stammzellen-Firma Osiris Therapeutics hat eine Kooperation mit dem Biotech-Konzern Genzyme geschlossen. Bis zu 1,38 Milliarden Dollar könnten so in die Kasse des Unternehmens fließen.
Beim Stichwort Stammzellen-Aktien werden die meisten Anleger sofort an bekannte Namen wie Stemcells, Geron oder Aastrom Biosciences denken. Gestern machte jedoch eine ganz andere Firma in den USA Schlagzeilen: Osiris Therapeutics.
Ritterschlag durch Genzyme
Osiris, das sich auf die Entwicklung von Therapien auf Basis adulter Stammzellen spezialisiert hat, gelang es, mit Genzyme einen der ganz Großen in der Biotech-Branche als Partner zu gewinnen. Im Zuge der Kooperation wird Genzyme an Osiris bis zu 1,38 Milliarden Dollar überweisen. Davon fließen 130 Millionen Dollar sofort, weitere 1,25 Milliarden Dollar werden fällig, sollte Osiris bestimmte Meilensteine wie beispielsweise den erfolgreichen Abschluss klinischer Studien oder eine Marktzulassung eines Produkts erreichen.
Projekte weit fortgeschritten
Genzymes Interesse haben vor allem zwei Kandidaten in der Medikamentenpipeline von Osiris geweckt, die zum Teil bereits die entscheidenden Testreihen vor einer möglichen Marktzulassung durchlaufen. Prochymal wird neben der Behandlung diverser Immunstörungen auch bei Morbus Crohn, einer chronischen Entzündung des Magen-Darm-Trakts, getestet. Chondrogen dagegen zielt auf die Behandlung von Arthritis im Knie ab. Der Vertrag sieht vor, dass Osiris die Vermarktungsrechte für beide Produkte in den USA und Kanada behalten, diese in den anderen Ländern aber nun an Genzyme abtreten wird.
Erste Stammzellentherapie vor Zulassung
Mit dem Geld wird Osiris alle laufenden Studien finanzieren, an den Kosten für weitere Testreihen wird sich Genzyme mit 40 Prozent beteiligen. Für eine Zulassung entscheidende Daten von Prochymal werden im nächsten Jahr erwartet. Sollten diese positiv ausfallen, stehen die Chancen gut, dass Prochymal die erste von der amerikanischen Gesundheitsbehörde FDA zugelassene Therapie auf Basis adulter Stammzellen wird. Ohne Frage würde das dem gesamten Sektor einen gehörigen Schub verleihen.
Für jeden Anlegertyp etwas
Nachdem die Osiris-Aktie kurz nach der Meldung noch die Gewinnerliste im Nasdaq Biotech Index (NBI) deutlich anführte, gab sie bis zum Handelsende fast das gesamte Plus wieder ab. Nichtsdestotrotz hat sich der Titel in den vergangenen Wochen gut geschlagen. Anleger, die im Stammzellen-Sektor investieren wollen und somit ein gewisses Risiko nicht scheuen, sollten sich das Unternehmen auf die Watchlist nehmen und bei Kursrücksetzern zuschlagen. Eher risikoscheue Naturen investieren dagegen in Genzyme, die Biotech-Empfehlung des Aktionärs in Ausgabe 45/08.
Ich hatte vor ein paar Tagen alle Shares verkauft, mal schaun ob ich heute wieder einsteige.
Geron war die letzten beiden Wochen gut zu traden
Geron war die letzten beiden Wochen gut zu traden

Obama will Bush-Politik zurücknehmen
Der gewählte Präsident Obama plant Zeitungsberichten zufolge, nach Amtsantritt mehr als 200 Verordnungen der Bush-Regierung rückgängig zu machen.
Der gewählte Präsident Barack Obama will die Bush-Politik rückgängig machen.
Der gewählte US-Präsident Barack Obama will offenbar mehr als 200 Regierungshandlungen und Durchführungsverordnungen der Bush-Regierung zurücknehmen.
Laut der Zeitung The Washington Post will Obama die Politik von Präsident George W. Bush zum Klimawandel, zur Stammzellenforschung und anderen Themen sobald wie möglich nach seinem Amtsantritt im Januar rückgängig machen.
Obamas Beraterstab arbeite schon....
Hier ganzer artikel
http://www.sueddeutsche.de/,tt5m1/politik/305/317181/text/
Der gewählte Präsident Obama plant Zeitungsberichten zufolge, nach Amtsantritt mehr als 200 Verordnungen der Bush-Regierung rückgängig zu machen.
Der gewählte Präsident Barack Obama will die Bush-Politik rückgängig machen.
Der gewählte US-Präsident Barack Obama will offenbar mehr als 200 Regierungshandlungen und Durchführungsverordnungen der Bush-Regierung zurücknehmen.
Laut der Zeitung The Washington Post will Obama die Politik von Präsident George W. Bush zum Klimawandel, zur Stammzellenforschung und anderen Themen sobald wie möglich nach seinem Amtsantritt im Januar rückgängig machen.
Obamas Beraterstab arbeite schon....
Hier ganzer artikel
http://www.sueddeutsche.de/,tt5m1/politik/305/317181/text/
Obama will Hunderte Bush-Verordnungen kassieren
In Windeseile will Barack Obama die gröbsten Spuren seines Vorgängers beseitigen: Einem Zeitungsbericht zufolge hat der designierte US-Präsident schon vor Monaten eine Liste mit Verfügungen Bushs in Auftrag gegeben, die er jetzt per Federstrich rückgängig machen kann.
Washington - Barack Obama steht erst seit wenigen Tagen als nächster Präsident der USA fest, doch offenbar hat er von langer Hand einen blitzschnellen Politikwechsel geplant. Wie die "Washington Post" berichtet, hat Obama vor Monaten ein rund 50-köpfiges Beraterteam beauftragt, Verordnungen der Regierung Bush zusammenzutragen, die sich ohne größeren Aufwand rückgängig machen lassen.
Designierter Präsident Obama (Mitte) mit Michigans Gouverneurin Jennifer Granholm, dem künftigen Vizepräsidenten Joe Biden und Ex-Notenbankchef Paul Volcker: Mammutprogramm zur Machtübernahme
Herausgekommen ist eine Liste von rund 200 Gesetzesinitiativen und Verordnungen von Noch-Präsident George W. Bush und seinem Kabinett, berichtet die Zeitung unter Berufung auf ein ranghohes Mitglied von Obamas Team. Um welche Regelungen es sich dabei im Einzelnen handelt, blieb offen. Es gehe aber insbesondere um politisch brisante Themen wie den Klimaschutz, die Stammzellforschung, die Energieversorgung und die Abtreibungsfrage.
Obamas Mannschaft berate sich derzeit mit liberalen Lobbygruppen, Parlamentsmitgliedern und potentiellen Behördenchefs darüber, welche Entscheidungen der Bush-Regierung die folgenschwersten und am stärksten parteipolitisch motiviert seien, damit diese zuerst beseitigt werden. In den nächsten Tagen könnte die Liste durchaus noch länger werden, spekuliert die Zeitung - denn Bush und seine Mitstreiter versuchen derzeit, mit einer Flut von Last-Minute-Verordnungen ihr politisches Erbe zu zementieren.
Nach Angaben von Obamas Sprecherin Stephanie Cutter ist noch nicht entschieden, welche Verordnungen verändert oder rückgängig gemacht werden. Dies werde der designierte Präsident zunächst mit seinen künftigen Kabinettsmitgliedern, den Führungspersonen des Kongresses und Interessengruppen besprechen.
Doch die bisherigen Signale aus Obamas Team, das den Machtwechsel organisieren soll, lassen auf eines schließen: Aller politischen Versöhnungsrhetorik zum Trotz dürfte Obama auf einigen Gebieten schnell und entschlossen handeln - auch auf die Gefahr hin, bisher einflussreiche Gruppen wie die Öl-Lobby und die religiöse Rechte gegen sich aufzubringen.
Letztere hat George W. Bush erfreut, indem er sich jahrelang beharrlich einer Lockerung der Einschränkungen in der Stammzellforschung verweigert hat. Bush hat jeden Gesetzentwurf, der eine staatliche Förderung der Arbeit mit embryonalen Stammzellen erlaubt hätte, mit seinem Veto blockiert - obwohl im Kongress große Mehrheiten dafür gestimmt hatten. Er wolle verhindern, dass "Steuerzahler die mutwillige Zerstörung menschlicher Embryos unterstützen", argumentierte Bush.
"Mit einer einfachen Verfügung rückgängig machen"
Nicht nur Demokraten, sondern auch zahlreiche Republikaner hatten sich für die Stammzellforschung stark gemacht - darunter Prominente wie Nancy Reagan, die Witwe von Ex-Präsident Ronald Reagan. Der von Republikanern geradezu ikonenhaft verehrte Politiker war 2004 an der Alzheimerschen Krankheit gestorben - einem jener Leiden, das Mediziner mit Hilfe von Stammzellen behandeln wollen.
Die derzeit gültigen Beschränkungen sind jedoch nie formell als Gesetz beschlossen worden, sagte die Demokraten-Abgeordnete Diana DeGette der "Washington Post". "Deshalb könnte Obama sie mit einer einfachen Verfügung rückgängig machen." Sie habe den designierten Präsidenten kürzlich an diese Tatsache erinnert, "und er war davon sehr angetan". Die Gegner der Beschränkungen sollen bereits eine solche Verfügung vorbereitet haben, die Obama nur noch unterschreiben müsse.
Auch im Klimaschutz könnte Obama schon bald das Ruder herumreißen. So hat er selbst betont, dass er die im Dezember von Bush gefällte Entscheidung, der Regierung Kaliforniens die Regulierung des Kohlendioxid-Ausstoßes von Autos zu verbieten, schnell beseitigen würde. "Die effektive Bekämpfung der globalen Erwärmung verlangt nach mutigen und innovativen Lösungen", sagte Obama im Januar. Da die Bush-Regierung nicht handele, "sollte Kalifornien erlaubt werden, voranzugehen".
Nächste Woche wird der Center for American Progress, ein liberaler Thinktank, ein Buch mit dem Titel "Change for America" herausgeben. Die Autoren empfehlen Obama laut "Washington Post" die Schaffung eines Nationalen Energierats, der alle politischen Entscheidungen bezüglich des Klimawandels bündeln soll. Es handelt sich dabei nicht um irgendein Buch: Der Center for American Progress wurde von John Podesta gegründet - einem der drei Leiter von Obamas Machtwechsel-Team. Er gilt derzeit als eine der einflussreichsten Figuren in der US-Politik.
Halst sich Obama zu viel auf?
Allerdings ist da auch noch eine Wirtschafts- und Finanzkrise, die Obama bekämpfen muss - und die genießt nach seinen Angaben derzeit die höchste Priorität. Doch die Berater des künftigen Präsidenten betonen, dass dies den Wechsel auf anderen wichtigen sozialen und politischen Feldern nicht verlangsamen werde - zumal einige, wie etwa der Klimaschutz, eng mit der Wirtschaft und der Energieversorgung verwoben seien.
US- Wahl Regierungswechsel Barack Obama Energie Klimaschutz Stammzellforschung
zu SPIEGEL WISSEN In der "New York Times" klingt dagegen alles ein wenig vorsichtiger. Dort ist davon die Rede, dass Obamas Berater durchaus unsicher seien, ob der künftige Präsident Großthemen wie den Klimaschutz, die dringend notwendige Reform des Gesundheitswesens, die Energiefrage und die Wirtschaftskrise zugleich angehen kann - und sollte.
Derzeit, so berichtet die Zeitung, gebe es in Obamas Lager eine Kontroverse darüber, ob man den Frontalangriff an mehreren Fronten wagt oder besser ein Problem nach dem anderen angeht. "Jeder Präsident wird in Versuchung geführt, zu viel zu versuchen", zitiert das Blatt einen Obama-Berater. Andererseits nannte er Franklin D. Roosevelt, der während der Weltwirtschaftskrise der dreißiger Jahre an die Macht kam, und Vietnam-Präsident Lyndon B. Johnson als Beispiele dafür, "dass ein außerordentlicher Präsident verdammt viel schaffen kann". Die Frage sei: "Ist es für den Präsidenten zu riskant, ehrgeizig zu sein?"
mbe
In Windeseile will Barack Obama die gröbsten Spuren seines Vorgängers beseitigen: Einem Zeitungsbericht zufolge hat der designierte US-Präsident schon vor Monaten eine Liste mit Verfügungen Bushs in Auftrag gegeben, die er jetzt per Federstrich rückgängig machen kann.
Washington - Barack Obama steht erst seit wenigen Tagen als nächster Präsident der USA fest, doch offenbar hat er von langer Hand einen blitzschnellen Politikwechsel geplant. Wie die "Washington Post" berichtet, hat Obama vor Monaten ein rund 50-köpfiges Beraterteam beauftragt, Verordnungen der Regierung Bush zusammenzutragen, die sich ohne größeren Aufwand rückgängig machen lassen.
Designierter Präsident Obama (Mitte) mit Michigans Gouverneurin Jennifer Granholm, dem künftigen Vizepräsidenten Joe Biden und Ex-Notenbankchef Paul Volcker: Mammutprogramm zur Machtübernahme
Herausgekommen ist eine Liste von rund 200 Gesetzesinitiativen und Verordnungen von Noch-Präsident George W. Bush und seinem Kabinett, berichtet die Zeitung unter Berufung auf ein ranghohes Mitglied von Obamas Team. Um welche Regelungen es sich dabei im Einzelnen handelt, blieb offen. Es gehe aber insbesondere um politisch brisante Themen wie den Klimaschutz, die Stammzellforschung, die Energieversorgung und die Abtreibungsfrage.
Obamas Mannschaft berate sich derzeit mit liberalen Lobbygruppen, Parlamentsmitgliedern und potentiellen Behördenchefs darüber, welche Entscheidungen der Bush-Regierung die folgenschwersten und am stärksten parteipolitisch motiviert seien, damit diese zuerst beseitigt werden. In den nächsten Tagen könnte die Liste durchaus noch länger werden, spekuliert die Zeitung - denn Bush und seine Mitstreiter versuchen derzeit, mit einer Flut von Last-Minute-Verordnungen ihr politisches Erbe zu zementieren.
Nach Angaben von Obamas Sprecherin Stephanie Cutter ist noch nicht entschieden, welche Verordnungen verändert oder rückgängig gemacht werden. Dies werde der designierte Präsident zunächst mit seinen künftigen Kabinettsmitgliedern, den Führungspersonen des Kongresses und Interessengruppen besprechen.
Doch die bisherigen Signale aus Obamas Team, das den Machtwechsel organisieren soll, lassen auf eines schließen: Aller politischen Versöhnungsrhetorik zum Trotz dürfte Obama auf einigen Gebieten schnell und entschlossen handeln - auch auf die Gefahr hin, bisher einflussreiche Gruppen wie die Öl-Lobby und die religiöse Rechte gegen sich aufzubringen.
Letztere hat George W. Bush erfreut, indem er sich jahrelang beharrlich einer Lockerung der Einschränkungen in der Stammzellforschung verweigert hat. Bush hat jeden Gesetzentwurf, der eine staatliche Förderung der Arbeit mit embryonalen Stammzellen erlaubt hätte, mit seinem Veto blockiert - obwohl im Kongress große Mehrheiten dafür gestimmt hatten. Er wolle verhindern, dass "Steuerzahler die mutwillige Zerstörung menschlicher Embryos unterstützen", argumentierte Bush.
"Mit einer einfachen Verfügung rückgängig machen"
Nicht nur Demokraten, sondern auch zahlreiche Republikaner hatten sich für die Stammzellforschung stark gemacht - darunter Prominente wie Nancy Reagan, die Witwe von Ex-Präsident Ronald Reagan. Der von Republikanern geradezu ikonenhaft verehrte Politiker war 2004 an der Alzheimerschen Krankheit gestorben - einem jener Leiden, das Mediziner mit Hilfe von Stammzellen behandeln wollen.
Die derzeit gültigen Beschränkungen sind jedoch nie formell als Gesetz beschlossen worden, sagte die Demokraten-Abgeordnete Diana DeGette der "Washington Post". "Deshalb könnte Obama sie mit einer einfachen Verfügung rückgängig machen." Sie habe den designierten Präsidenten kürzlich an diese Tatsache erinnert, "und er war davon sehr angetan". Die Gegner der Beschränkungen sollen bereits eine solche Verfügung vorbereitet haben, die Obama nur noch unterschreiben müsse.
Auch im Klimaschutz könnte Obama schon bald das Ruder herumreißen. So hat er selbst betont, dass er die im Dezember von Bush gefällte Entscheidung, der Regierung Kaliforniens die Regulierung des Kohlendioxid-Ausstoßes von Autos zu verbieten, schnell beseitigen würde. "Die effektive Bekämpfung der globalen Erwärmung verlangt nach mutigen und innovativen Lösungen", sagte Obama im Januar. Da die Bush-Regierung nicht handele, "sollte Kalifornien erlaubt werden, voranzugehen".
Nächste Woche wird der Center for American Progress, ein liberaler Thinktank, ein Buch mit dem Titel "Change for America" herausgeben. Die Autoren empfehlen Obama laut "Washington Post" die Schaffung eines Nationalen Energierats, der alle politischen Entscheidungen bezüglich des Klimawandels bündeln soll. Es handelt sich dabei nicht um irgendein Buch: Der Center for American Progress wurde von John Podesta gegründet - einem der drei Leiter von Obamas Machtwechsel-Team. Er gilt derzeit als eine der einflussreichsten Figuren in der US-Politik.
Halst sich Obama zu viel auf?
Allerdings ist da auch noch eine Wirtschafts- und Finanzkrise, die Obama bekämpfen muss - und die genießt nach seinen Angaben derzeit die höchste Priorität. Doch die Berater des künftigen Präsidenten betonen, dass dies den Wechsel auf anderen wichtigen sozialen und politischen Feldern nicht verlangsamen werde - zumal einige, wie etwa der Klimaschutz, eng mit der Wirtschaft und der Energieversorgung verwoben seien.
US- Wahl Regierungswechsel Barack Obama Energie Klimaschutz Stammzellforschung
zu SPIEGEL WISSEN In der "New York Times" klingt dagegen alles ein wenig vorsichtiger. Dort ist davon die Rede, dass Obamas Berater durchaus unsicher seien, ob der künftige Präsident Großthemen wie den Klimaschutz, die dringend notwendige Reform des Gesundheitswesens, die Energiefrage und die Wirtschaftskrise zugleich angehen kann - und sollte.
Derzeit, so berichtet die Zeitung, gebe es in Obamas Lager eine Kontroverse darüber, ob man den Frontalangriff an mehreren Fronten wagt oder besser ein Problem nach dem anderen angeht. "Jeder Präsident wird in Versuchung geführt, zu viel zu versuchen", zitiert das Blatt einen Obama-Berater. Andererseits nannte er Franklin D. Roosevelt, der während der Weltwirtschaftskrise der dreißiger Jahre an die Macht kam, und Vietnam-Präsident Lyndon B. Johnson als Beispiele dafür, "dass ein außerordentlicher Präsident verdammt viel schaffen kann". Die Frage sei: "Ist es für den Präsidenten zu riskant, ehrgeizig zu sein?"
mbe
Antwort auf Beitrag Nr.: 35.894.416 von meislo am 09.11.08 20:23:31Hallo Meislo,
Ist es dir gelungen,zu schnäppchenkursen um 2 dollar geron aufzustocken ? Ich denke die 2 dollar werden wir so schnell nicht wiedersehen ... Aber was meinst du,wird das clinical hold,was derzeit über der spinal cord injury therapy von Geron schwebt,bald aufgehoben
? Ich denke die 2 dollar werden wir so schnell nicht wiedersehen ... Aber was meinst du,wird das clinical hold,was derzeit über der spinal cord injury therapy von Geron schwebt,bald aufgehoben  ???
???
MFG
Chali
Ist es dir gelungen,zu schnäppchenkursen um 2 dollar geron aufzustocken
 ? Ich denke die 2 dollar werden wir so schnell nicht wiedersehen ... Aber was meinst du,wird das clinical hold,was derzeit über der spinal cord injury therapy von Geron schwebt,bald aufgehoben
? Ich denke die 2 dollar werden wir so schnell nicht wiedersehen ... Aber was meinst du,wird das clinical hold,was derzeit über der spinal cord injury therapy von Geron schwebt,bald aufgehoben  ???
???MFG
Chali

Nein
Habe leider nicht weiter aufgestockt.
Schwer zu sagen. Vielleicht muss bei der FDA auch noch ausgekehrt werden.
Bush hat da ja auch dort durch die Besetzung wichtiger Posten die Zügel angezogen.
Obama wirds schon richten.
Habe leider nicht weiter aufgestockt.
Schwer zu sagen. Vielleicht muss bei der FDA auch noch ausgekehrt werden.

Bush hat da ja auch dort durch die Besetzung wichtiger Posten die Zügel angezogen.
Obama wirds schon richten.

warum zieht Geron "nur" 15% rauf? Während Stemcells und Aastrom gut 30-40% machen?
@sugar
das würde ich auch gerne wissen...!
worin unterscheidet sich geron von den anderen beiden???
wir sind doch auch gerade an nen widerstand....
dann wäre doch der weg frei nach oben, oder nicht?!
bitte um weitere meinungen...
das würde ich auch gerne wissen...!

worin unterscheidet sich geron von den anderen beiden???
wir sind doch auch gerade an nen widerstand....
dann wäre doch der weg frei nach oben, oder nicht?!
bitte um weitere meinungen...

Antwort auf Beitrag Nr.: 35.905.549 von bandit7 am 10.11.08 18:44:49Der Unterschied
embryonale und adulte Stammzellen

embryonale und adulte Stammzellen


trotzdem sollten doch alle gleichermaßen
von Obama profitieren, oder nicht?!
von Obama profitieren, oder nicht?!

Antwort auf Beitrag Nr.: 35.905.846 von bandit7 am 10.11.08 19:16:45gleichermaßen profitieren. wie soll das denn funktionieren ??
Fakt ist doch, das Geron seit ein paar Wochen super läuft.
Geron wird quasi wiederentdeckt, sehr schön zu sehen am ständig steigenden Handelsvolumen.
Ich sage jetzt schon mal Dank an Obama
Fakt ist doch, das Geron seit ein paar Wochen super läuft.
Geron wird quasi wiederentdeckt, sehr schön zu sehen am ständig steigenden Handelsvolumen.
Ich sage jetzt schon mal Dank an Obama

Antwort auf Beitrag Nr.: 35.894.416 von meislo am 09.11.08 20:23:31Danke fürs reinstellen 

@larry
mit gleichermaßen meine ich, daß die stammzellen stocks ja erstmal alle gleich reagieren sollten...
die profitieren ja alle am anfang von obama´s aufmerksamkeit
aber wenn man sich zumindest die beiden (kleineren!) Konkurrenten anschaut, klafft schon noch ne ziemlich große Lücke...
(stem und aa laufen ja ziemlich gleich)
wundert mich nur... deshalb wollt ich mal paar meinungen hören...
was meinst du, wie es die nächsten tage hier laufen wird?
holen wir den unterschied auf???
mit gleichermaßen meine ich, daß die stammzellen stocks ja erstmal alle gleich reagieren sollten...
die profitieren ja alle am anfang von obama´s aufmerksamkeit
aber wenn man sich zumindest die beiden (kleineren!) Konkurrenten anschaut, klafft schon noch ne ziemlich große Lücke...

(stem und aa laufen ja ziemlich gleich)
wundert mich nur... deshalb wollt ich mal paar meinungen hören...
was meinst du, wie es die nächsten tage hier laufen wird?
holen wir den unterschied auf???
Antwort auf Beitrag Nr.: 35.906.200 von Larry_1 am 10.11.08 19:54:55Ja, Geron läuft derzeit gut... aber STEM und ASTM laufen besser 
Ich will mich mal nicht beschweren Ich halte GERN für ein besseres Investment, u.a. wegen der embryonalen Stammzellenforschung und wegen des vorhandenen Cashs!
Ich halte GERN für ein besseres Investment, u.a. wegen der embryonalen Stammzellenforschung und wegen des vorhandenen Cashs!

Ich will mich mal nicht beschweren
 Ich halte GERN für ein besseres Investment, u.a. wegen der embryonalen Stammzellenforschung und wegen des vorhandenen Cashs!
Ich halte GERN für ein besseres Investment, u.a. wegen der embryonalen Stammzellenforschung und wegen des vorhandenen Cashs!
Antwort auf Beitrag Nr.: 35.906.713 von Sugar2000 am 10.11.08 21:03:13Ist doch wohl logisch! erstmal laufen die politisch einfacher handelbaren und das sind nun mal die adulten.
Mal sehen wer am Ende die Nase vorne hat.
Dieser Prozess dauert aber noch Jahre an.
Mal sehen wer am Ende die Nase vorne hat.
Dieser Prozess dauert aber noch Jahre an.

Nach dieser Korrektur, heute schon aufstocken, oder noch warten?
Schwierige Entscheidung

Schwierige Entscheidung


Da bin ich ja mal froh, auf GERN gesetzt zu haben! STEM wirft Aktien auf den Markt um sich zu finanzieren...
Antwort auf Beitrag Nr.: 35.935.994 von Sugar2000 am 13.11.08 10:14:16Das Problem
Sollten die Stammzellen nun auch un den USA durch die Bundesregierung gefördert werden haben private Firmen wie Geron oder Stemcells ein Problem.
Die Institute des öffentlichen Bereichs werden wohl stärker davon profitieren.
Ich hatte ja schon mal geschrieben das der Bush-bang, Geron auch einen Wettbewerbsvorteil ermöglicht.
Dieser ist wäre dann egalisiert.
Sollten die Stammzellen nun auch un den USA durch die Bundesregierung gefördert werden haben private Firmen wie Geron oder Stemcells ein Problem.
Die Institute des öffentlichen Bereichs werden wohl stärker davon profitieren.
Ich hatte ja schon mal geschrieben das der Bush-bang, Geron auch einen Wettbewerbsvorteil ermöglicht.
Dieser ist wäre dann egalisiert.
Antwort auf Beitrag Nr.: 35.951.156 von meislo am 14.11.08 20:53:57auf der anderen seite würde GERN wieder in den Fokus der Anleger geraten...
Antwort auf Beitrag Nr.: 34.591.020 von -Salem- am 26.07.08 03:29:06Seht, ick hatte recht... Wir Berliner sind eh die schlausten. Nicht so blöd wie der Rest der deutschen Nation.(auch eine im Suff getroffene Aussage stimmt)
Wir Berliner sind eh die schlausten. Nicht so blöd wie der Rest der deutschen Nation.(auch eine im Suff getroffene Aussage stimmt)
Siehe heutige Veröffentlichung. GRN163L (L wie Legastheniker) dürfte Geron´s Top Story werden. Die Stammzellen sind ne Sache für die nächsten 20-45.500 Jahre. GRN163L kommt früher und ischt heißer.
GRN163L kommt übrigens von einem deutschen Unternehmen (WKN 588040).
http://biz.yahoo.com/bw/081208/20081208005642.html?.v=1
 Wir Berliner sind eh die schlausten. Nicht so blöd wie der Rest der deutschen Nation.(auch eine im Suff getroffene Aussage stimmt)
Wir Berliner sind eh die schlausten. Nicht so blöd wie der Rest der deutschen Nation.(auch eine im Suff getroffene Aussage stimmt)Siehe heutige Veröffentlichung. GRN163L (L wie Legastheniker) dürfte Geron´s Top Story werden. Die Stammzellen sind ne Sache für die nächsten 20-45.500 Jahre. GRN163L kommt früher und ischt heißer.

GRN163L kommt übrigens von einem deutschen Unternehmen (WKN 588040).
http://biz.yahoo.com/bw/081208/20081208005642.html?.v=1
Chronologie der Stammzellforschung
1981 In Embryonen von Mäusen werden Stammzellen entdeckt. Sie haben das Potential, sich in jedes Gewebe eines Mauskörpers zu verwandeln.
1996 Das Schaf Dolly kommt zur Welt. Es ist der erste Klon eines Säugetiers, geschaffen aus einer Euterzelle eines erwachsenen Schafs. Erst im Frühjahr 1997 wird das Experiment bekannt.
1998 Im November gelingt es James Thomson erstmals, menschliche embryonale Stammzellen (hES-Zellen) zu züchten. Dafür hat er etwa zehn Tage alte Embryonen zerstört. Die ethische Kontroverse um die Stammzellforschung beginnt, denn die Zellen könnten auch einmal dazu dienen, krankes Gewebe zu ersetzen und defekte Organe zu reparieren.
2002 Ein Team um Rudolf Jaenisch zeigt, dass das "therapeutische Klonen" bei Mäusen funktioniert: Die Forscher klonten dazu eine Maus mit Gen-Defekt, stellten aus dem Klon-Embryo Stammzellen her, reparierten deren Gen-Defekt mittels Gentherapie und pflanzten die gesunden Zellen kranken Mäusen ein.
2004 Der südkoreanische Tierarzt Hwang Woo-Suk wird weltberühmt, weil es ihm angeblich gelungen ist, einen menschlichen Embryo zu klonen und daraus Stammzellen zu gewinnen. Zum Jahreswechsel 2005/2006 wird Hwang jedoch der Fälschung überführt.
2006 Im Frühjahr veröffentlicht der japanische Arzt Shinya Yamanaka ein Rezept, mit dem sich Zellen ausgewachsener Mäuse biochemisch in den Embryonalzustand zurückversetzen lassen. Erstmals lassen sich hES-ähnliche Zellen herstellen, ohne dass dafür ein Embryo zerstört werden muss.
2007 Zehn Monate nach Yamanakas erstaunlichem Bericht kann er sein Rezept verbessern. Viren schleusen dabei vier Gene in die Zellen, die normalerweise nur in embryoähnlichen Zellen aktiv sind. Durch den technisch einfachen Eingriff wird die biologische Uhr der erwachsenen Zellen auf Null zurückgestellt. Die verwendeten Viren und zwei der Gene können jedoch die Entstehung von Krebs begünstigen.
Im November demonstrieren zwei Arbeitsgruppen unabhängig voneinander, dass das Rezept auch mit menschlichen Zellen funktioniert. Wieder ist Yamanaka beteiligt. Die entstehenden iPS-Zellen haben die Fähigkeit, sich in alle Gewebe des menschlichen Körpers zu verwandeln - das können sonst nur embryonale Stammzellen.
2008 Gleich nach dem Jahreswechsel verkündet die kalifornische Firma Stemagen, sie habe einen Menschenklon für einige Tage im Labor wachsen lassen. Stammzellen wurden nicht isoliert.
Im April berichten britische Forscher, dass sie einem Herzpatienten Zellen entnommen und mit dem Yamanaka-Rezept in iPS-Zellen verwandelt haben. Sie tragen dieselben genetischen Informationen wie der Patient und sollen die Krankheit im Kleinmaßstab nachbilden, um sie besser erforschen zu können. Dies könne der Entwicklung neuer Medikament dienen, so die Hoffnung. Bis Ende des Jahren liegen weltweit etwa 20 iPS-Zelllinien für verschiedene Krankheiten vor.
Im Verlauf des Jahres gibt es Berichte über vereinfachte Rezepte zur iPS-Herstellung. Manche verzichten auf die Krebs-Gene, andere auf die Viren.
2009 Die Bemühungen, die Rückverwandlung erwachsener Zellen in einen embryonalen Zustand einfacher und sicherer zu machen, werden weitergehen. Eine der wichtigsten Fragen ist zudem, ob die iPS-Zellen die embryonalen wirklich ersetzen können. Das Biotech-Unternehmen Geron hofft auf eine Genehmigung für Versuche mit umgewandelten embryonalen Stammzellen. Es geht darum, Verletzungen im Rückenmark zu heilen. Die über 20 000 Seiten mit Vorstudien und Anträgen liegen seit fast einem Jahr bei der zuständigen Behörde.hach
1981 In Embryonen von Mäusen werden Stammzellen entdeckt. Sie haben das Potential, sich in jedes Gewebe eines Mauskörpers zu verwandeln.
1996 Das Schaf Dolly kommt zur Welt. Es ist der erste Klon eines Säugetiers, geschaffen aus einer Euterzelle eines erwachsenen Schafs. Erst im Frühjahr 1997 wird das Experiment bekannt.
1998 Im November gelingt es James Thomson erstmals, menschliche embryonale Stammzellen (hES-Zellen) zu züchten. Dafür hat er etwa zehn Tage alte Embryonen zerstört. Die ethische Kontroverse um die Stammzellforschung beginnt, denn die Zellen könnten auch einmal dazu dienen, krankes Gewebe zu ersetzen und defekte Organe zu reparieren.
2002 Ein Team um Rudolf Jaenisch zeigt, dass das "therapeutische Klonen" bei Mäusen funktioniert: Die Forscher klonten dazu eine Maus mit Gen-Defekt, stellten aus dem Klon-Embryo Stammzellen her, reparierten deren Gen-Defekt mittels Gentherapie und pflanzten die gesunden Zellen kranken Mäusen ein.
2004 Der südkoreanische Tierarzt Hwang Woo-Suk wird weltberühmt, weil es ihm angeblich gelungen ist, einen menschlichen Embryo zu klonen und daraus Stammzellen zu gewinnen. Zum Jahreswechsel 2005/2006 wird Hwang jedoch der Fälschung überführt.
2006 Im Frühjahr veröffentlicht der japanische Arzt Shinya Yamanaka ein Rezept, mit dem sich Zellen ausgewachsener Mäuse biochemisch in den Embryonalzustand zurückversetzen lassen. Erstmals lassen sich hES-ähnliche Zellen herstellen, ohne dass dafür ein Embryo zerstört werden muss.
2007 Zehn Monate nach Yamanakas erstaunlichem Bericht kann er sein Rezept verbessern. Viren schleusen dabei vier Gene in die Zellen, die normalerweise nur in embryoähnlichen Zellen aktiv sind. Durch den technisch einfachen Eingriff wird die biologische Uhr der erwachsenen Zellen auf Null zurückgestellt. Die verwendeten Viren und zwei der Gene können jedoch die Entstehung von Krebs begünstigen.
Im November demonstrieren zwei Arbeitsgruppen unabhängig voneinander, dass das Rezept auch mit menschlichen Zellen funktioniert. Wieder ist Yamanaka beteiligt. Die entstehenden iPS-Zellen haben die Fähigkeit, sich in alle Gewebe des menschlichen Körpers zu verwandeln - das können sonst nur embryonale Stammzellen.
2008 Gleich nach dem Jahreswechsel verkündet die kalifornische Firma Stemagen, sie habe einen Menschenklon für einige Tage im Labor wachsen lassen. Stammzellen wurden nicht isoliert.
Im April berichten britische Forscher, dass sie einem Herzpatienten Zellen entnommen und mit dem Yamanaka-Rezept in iPS-Zellen verwandelt haben. Sie tragen dieselben genetischen Informationen wie der Patient und sollen die Krankheit im Kleinmaßstab nachbilden, um sie besser erforschen zu können. Dies könne der Entwicklung neuer Medikament dienen, so die Hoffnung. Bis Ende des Jahren liegen weltweit etwa 20 iPS-Zelllinien für verschiedene Krankheiten vor.
Im Verlauf des Jahres gibt es Berichte über vereinfachte Rezepte zur iPS-Herstellung. Manche verzichten auf die Krebs-Gene, andere auf die Viren.
2009 Die Bemühungen, die Rückverwandlung erwachsener Zellen in einen embryonalen Zustand einfacher und sicherer zu machen, werden weitergehen. Eine der wichtigsten Fragen ist zudem, ob die iPS-Zellen die embryonalen wirklich ersetzen können. Das Biotech-Unternehmen Geron hofft auf eine Genehmigung für Versuche mit umgewandelten embryonalen Stammzellen. Es geht darum, Verletzungen im Rückenmark zu heilen. Die über 20 000 Seiten mit Vorstudien und Anträgen liegen seit fast einem Jahr bei der zuständigen Behörde.hach
Aufwärtstrend weiter in takt


Nicht lange her, dass Geron Neuigkeiten zum MM-Versuch von GRN163L sowie die Probleme mit der Toxizität (Thombozytenschwund) publizierte: Hier ein paar Fachkommentare:
My take on today's news ...
First a summary of the main result. In one of six ongoing studies, the monotherapy MM study, two patients exhibited bulk tumor telomerase inhibition of 78% and 48%, and 33% and 63% inhibition in the "myeloma stem cell-containing fraction of their bone marrow".
Both of these patients were treated at 4.8 mg/kg, probably with a weekly dosing.
We don't know how many other patients exhibited less TI or no TI and were not reported in Geron's PR. It may be that only a small subset of the MM patients got pre and post treatment bone marrow biopsies, or it may be that all of them did. But it is likely that these two patients had the best TI results from among those tested. We do know that data from 13 of the MM patients was presented at ASH.
According to the ASH MM abstract, "The MTD for continuous weekly dosing of GRN163L in this heavily pretreated, relapsed and refractory MM population appears to be ≥ 4.8 and < 7.2 mg/kg."
So (assuming we can trust the assay) we can say that TI has been seen in at least two 163L-treated patients at or below the MTD.
That is PD. That is molecular activity. That is first base. That is excellent news.
Now ... is it sufficient TI to give rise to clinical efficacy? Any TI has the potential to slow down the cancer growth. From other studies, one needs a rather high amount of TI to actually cause the cancer to regress rather than simply grow more slowly. (Something like 75% for many weeks, if memory serves.) Clearly clinical efficacy has not been close to demonstrated at this point. But let me wax optimistic for a moment.
While there are many unanswered questions, I think we are beginning to get some evidence that there may be a *potential* therapeutic window. To remove the word "potential" it is necessary to show that TI can be converted into some sort of clinical efficacy in humans, such as an increase in the TTP. The therapeutic window may be small, due to the serious AEs seen at and below 7.2 mg/kg and the fact that the MTD is less than 50% above the dose where TI was seen. But there is a very real potential that that the therapeutic window can be widened by playing the dosing games that Geron has been working on for some time.
My initial reaction is that the probability that GRN163L may someday result in commercial sales has been increased from ~10-15% to ~20-25% with this news.
Other views would be most appreciated.
micro
**************************************************************
My quick take on this is that Telomerase Inhibition is not directly causing the thromocytopenia, however since thromocytopenia results from prolonged weekly dosing of GRN163l at levels approaching 7.2mg/kg that is a side effect of GRN163L.
Dr OKarma describes a dosing schedule that includes a skipped week every third week that at least at 4.8mg/kg demonstrated that the progression to thromocytopenia is controlled. He showed graphs of thromocytopenia development in two cohorts, with the alternate dosing showing the platelet count staying above the 50. Thromocytopenia begins at 10. He stated that the alternating dosing schedule should allow dosing beyond the 7.2mg/kg but did no show trial results that demonstrated it.
Although I would like to think that the heavy pretreatment of the patients predisposed the patients to thromocytopenia when dosed with 163 the graph of platelets showed values at initiation that were in the normal range.
However the patients that demonstrated the worse thromocytopenia apparently had previously received bone marrow transplants. This may indicate that the rebuilt blood producing hemeopoetic system is fundamentally weak and more suseptible to the impact of 163.
I find it interesting the LPC is one of the patients that demonstrated Telomerase inhibition of 78% in the bulk cells, but at this time it is unclear whether there has been a beneficial effect. However he was being dosed only at 4.8mg/kg. If we can really get closer to 7.2 mg/kg with alternate dosing, and still get a long enough period of inhibition then the amount of Telomerase inhibition may become very significant.
RX7171
Grüße
LuckCat
My take on today's news ...
First a summary of the main result. In one of six ongoing studies, the monotherapy MM study, two patients exhibited bulk tumor telomerase inhibition of 78% and 48%, and 33% and 63% inhibition in the "myeloma stem cell-containing fraction of their bone marrow".
Both of these patients were treated at 4.8 mg/kg, probably with a weekly dosing.
We don't know how many other patients exhibited less TI or no TI and were not reported in Geron's PR. It may be that only a small subset of the MM patients got pre and post treatment bone marrow biopsies, or it may be that all of them did. But it is likely that these two patients had the best TI results from among those tested. We do know that data from 13 of the MM patients was presented at ASH.
According to the ASH MM abstract, "The MTD for continuous weekly dosing of GRN163L in this heavily pretreated, relapsed and refractory MM population appears to be ≥ 4.8 and < 7.2 mg/kg."
So (assuming we can trust the assay) we can say that TI has been seen in at least two 163L-treated patients at or below the MTD.
That is PD. That is molecular activity. That is first base. That is excellent news.
Now ... is it sufficient TI to give rise to clinical efficacy? Any TI has the potential to slow down the cancer growth. From other studies, one needs a rather high amount of TI to actually cause the cancer to regress rather than simply grow more slowly. (Something like 75% for many weeks, if memory serves.) Clearly clinical efficacy has not been close to demonstrated at this point. But let me wax optimistic for a moment.
While there are many unanswered questions, I think we are beginning to get some evidence that there may be a *potential* therapeutic window. To remove the word "potential" it is necessary to show that TI can be converted into some sort of clinical efficacy in humans, such as an increase in the TTP. The therapeutic window may be small, due to the serious AEs seen at and below 7.2 mg/kg and the fact that the MTD is less than 50% above the dose where TI was seen. But there is a very real potential that that the therapeutic window can be widened by playing the dosing games that Geron has been working on for some time.
My initial reaction is that the probability that GRN163L may someday result in commercial sales has been increased from ~10-15% to ~20-25% with this news.
Other views would be most appreciated.
micro
**************************************************************
My quick take on this is that Telomerase Inhibition is not directly causing the thromocytopenia, however since thromocytopenia results from prolonged weekly dosing of GRN163l at levels approaching 7.2mg/kg that is a side effect of GRN163L.
Dr OKarma describes a dosing schedule that includes a skipped week every third week that at least at 4.8mg/kg demonstrated that the progression to thromocytopenia is controlled. He showed graphs of thromocytopenia development in two cohorts, with the alternate dosing showing the platelet count staying above the 50. Thromocytopenia begins at 10. He stated that the alternating dosing schedule should allow dosing beyond the 7.2mg/kg but did no show trial results that demonstrated it.
Although I would like to think that the heavy pretreatment of the patients predisposed the patients to thromocytopenia when dosed with 163 the graph of platelets showed values at initiation that were in the normal range.
However the patients that demonstrated the worse thromocytopenia apparently had previously received bone marrow transplants. This may indicate that the rebuilt blood producing hemeopoetic system is fundamentally weak and more suseptible to the impact of 163.
I find it interesting the LPC is one of the patients that demonstrated Telomerase inhibition of 78% in the bulk cells, but at this time it is unclear whether there has been a beneficial effect. However he was being dosed only at 4.8mg/kg. If we can really get closer to 7.2 mg/kg with alternate dosing, and still get a long enough period of inhibition then the amount of Telomerase inhibition may become very significant.
RX7171
Grüße
LuckCat
Video-Interview mit CEO Tom Okarma zu Embryonalen Stammzellen:
http://news.bbc.co.uk/2/hi/health/7828800.stm
.
http://news.bbc.co.uk/2/hi/health/7828800.stm
.
Geron hat sich extremst gut entwickelt nach dem Low bei 1,9$. Und ich muss ehrlich sagen, bis auf die guten Studiendaten zu GRN163L, gibt es eigentlich nüschts wesentlich Neues. Die Umsätze wieder weit über Average und nicht nur heute rel. stabil. Aber GERN braucht unbedingt Erfolge und Partnerschften, denn Stammzellen+Oligonucleotide sind elendig teure Forschungsgebiete. Und 174 Mios Cash sind zwar solide, werden aber sicher nicht über die volle Distanz reichen.
Übrigens ist Geron zu Gast bei dem Girindus Oligonucleotid Symposium ende März.
Übrigens ist Geron zu Gast bei dem Girindus Oligonucleotid Symposium ende März.

Wahnsinn... ein weiterer Meilenstein...
http://www.finanznachrichten.de/nachrichten-2009-01/12914393…23.01.2009 06:02
Geron Receives FDA Clearance to Begin World’s First Human Clinical Trial of Embryonic Stem Cell-Based Therapy
Geron to Study GRNOPC1 in Patients With Acute Spinal Cord Injury
Conference Call and Video Webcast Set for 6:00 a.m. PST/9:00 a.m. EST
Geron Corporation (News) (Nasdaq:GERN) announced today that the U.S. Food and Drug Administration (FDA) has granted clearance of the company’s Investigational New Drug (IND) application for the clinical trial of GRNOPC1 in patients with acute spinal cord injury.
The clearance enables Geron to move forward with the world’s first study of a human embryonic stem cell (hESC)-based therapy in man. Geron plans to initiate a Phase I multi-center trial that is designed to establish the safety of GRNOPC1 in patients with ”complete” American Spinal Injury Association (ASIA) grade A subacute thoracic spinal cord injuries.
”The FDA’s clearance of our GRNOPC1 IND is one of Geron’s most significant accomplishments to date,” said Thomas B. Okarma, Ph.D., M.D., Geron’s president and CEO. ”This marks the beginning of what is potentially a new chapter in medical therapeutics - one that reaches beyond pills to a new level of healing: the restoration of organ and tissue function achieved by the injection of healthy replacement cells. The ultimate goal for the use of GRNOPC1 is to achieve restoration of spinal cord function by the injection of hESC-derived oligodendrocyte progenitor cells directly into the lesion site of the patient’s injured spinal cord.”
GRNOPC1, Geron’s lead hESC-based therapeutic candidate, contains hESC-derived oligodendrocyte progenitor cells that have demonstrated remyelinating and nerve growth stimulating properties leading to restoration of function in animal models of acute spinal cord injury (Journal of Neuroscience, Vol. 25, 2005).
”The neurosurgical community is very excited by this new approach to treating devastating spinal cord injury,” said Richard Fessler, M.D., Ph.D., professor of neurological surgery at the Feinberg School of Medicine at Northwestern University. ”Demyelination is central to the pathology of the injury, and its reversal by means of injecting oligodendrocyte progenitor cells would be revolutionary for the field. If safe and effective, the therapy would provide a viable treatment option for thousands of patients who suffer severe spinal cord injuries each year.”
The GRNOPC1 Clinical Program
Patients eligible for the Phase I trial must have documented evidence of functionally complete spinal cord injury with a neurological level of T3 to T10 spinal segments and agree to have GRNOPC1 injected into the lesion sites between seven and 14 days after injury. Geron has selected up to seven U.S. medical centers as candidates to participate in this study and in planned protocol extensions. The sites will be identified as they come online and are ready to enroll subjects into the study.
Although the primary endpoint of the trial is safety, the protocol includes secondary endpoints to assess efficacy, such as improved neuromuscular control or sensation in the trunk or lower extremities. Once safety in this patient population has been established and the FDA reviews clinical data in conjunction with additional data from ongoing animal studies, Geron plans to seek FDA approval to extend the study to increase the dose of GRNOPC1, enroll subjects with complete cervical injuries and expand the trial to include patients with severe incomplete (ASIA grade B or C) injuries to enable access to the therapy for as broad a population of severe spinal cord-injured patients as is medically appropriate.
Preclinical Evidence of Safety, Tolerability and Efficacy
Geron submitted evidence of the safety, tolerability and efficacy of GRNOPC1 to the FDA in a 21,000-page IND application that described 24 separate animal studies requiring the production of more than five billion GRNOPC1 cells. Included in the safety package were studies that showed no evidence of teratoma formation 12 months after injection of clinical grade GRNOPC1 into the injured spinal cord of rats and mice. Other studies documented the absence of significant migration of the injected cells outside the spinal cord, allodynia induction (increased neuropathic pain due to the injected cells), systemic toxicity or increased mortality in animals receiving GRNOPC1.
In vitro studies have shown that GRNOPC1 is minimally recognized by the human immune system. GRNOPC1 is not recognized in vitro by allogeneic sera, NK cells or T cells (Journal of Neuroimmunology, Vol. 192, 2007). These immune-privileged characteristics of the hESC-derived cells allow a clinical trial design that incorporates a limited course of low-dose immunosuppression and provide the rationale for an off-the-shelf, allogeneic cell therapy.
Also included in the IND application were published studies supporting the utility of GRNOPC1 for the treatment of spinal cord injury. Those studies showed that administration of GRNOPC1 significantly improved locomotor activity and kinematic scores of animals with spinal cord injuries when injected seven days after the injury (Journal of Neuroscience, Vol. 25, 2005). Histological examination of the injured spinal cords treated with GRNOPC1 showed improved axon survival and extensive remyelination surrounding the rat axons. These effects of GRNOPC1 were present nine months after a single injection of cells. In these nine-month studies, the cells were shown to migrate and fill the lesion cavity, with bundles of myelinated axons crossing the injury site.
Production and Qualification of GRNOPC1
GRNOPC1 is produced using current Good Manufacturing Practices (cGMP) in Geron’s manufacturing facilities. Geron’s GRNOPC1 production process and clean-room suites have been inspected and licensed by the state of California. The cells are derived from the H1 human embryonic stem cell line, which was created before August 9, 2001. Studies using this line qualify for U.S. federal research funding, although no federal funding was received for the development of the product or to support the clinical trial.
Geron’s H1 hESC master cell bank is fully qualified for human use and was shown to be karyotypically normal and free of measurable contaminants of human or animal origin. Production of GRNOPC1 from undifferentiated hESCs in the master cell bank uses qualified reagents and a standardized protocol developed at Geron over the past three years. Each manufacturing run of GRNOPC1 is subjected to standardized quality control testing to ensure viability, sterility and appropriate cellular composition before release for clinical use. GRNOPC1 product that has passed all such specifications and has been released is available for the approved clinical trial. The current production scale can supply product needs through pivotal clinical trials. The existing master cell bank could potentially supply sufficient starting material for GRNOPC1 to commercially supply the U.S. acute spinal cord injury market for more than 20 years.
Intellectual Property
The production and commercialization of GRNOPC1 is protected by a portfolio of patent rights owned by or exclusively licensed to Geron. Patent rights owned by Geron protect key technologies developed at Geron for the scalable manufacturing of hESCs, as well as the production of neural cells by differentiation of hESCs. The fundamental patents covering hESCs are exclusively licensed to Geron from the Wisconsin Alumni Research Foundation (WARF) for the production of neural cells, cardiomyocytes and pancreatic islets for therapeutic applications. The validity of these patents was recently confirmed by the U.S. Patent and Trademark Office in a re-examination proceeding. Geron funded the original research at the University of Wisconsin-Madison that led to the first isolation of hESCs. The production of oligodendrocytes from hESCs is covered by patent rights exclusively licensed to Geron from the University of California. These patent rights cover technology developed in a research collaboration between Geron and University of California scientists.
Conference Call and Video Webcast
Thomas B. Okarma, Ph.D., M.D., will host a conference call and video Webcast presentation for investors and the media at 6:00 a.m. PST/9:00 a.m. EST today. Participants can access the conference call via telephone by dialing 866-783-2145 (U.S.) or 857-350-1604 (international). The passcode is 89631672. The video Webcast presentation is available at http://phx.corporate-ir.net/phoenix.zhtml?p=irol-eventDetail… All participants are encouraged to view Dr. Okarma’s presentation on the Internet. The video Webcast will also be accessible through a link that is posted on the home page of Geron’s Web site at http://www.geron.com. Participants are encouraged to log on at least 15 minutes prior to the beginning of the presentation in order to download any necessary software. The video Webcast will be available for replay through February 23, 2009.
Background information about human embryonic stem cells, GRNOPC1 and the spinal cord injury clinical trial can be found at http://eon.businesswire.com/news/eon/20090122006356/en.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem (hESC) cell-based therapeutics. The company has received FDA clearance to begin the world’s first human clinical trial of a hESC-based therapy: GRNOPC1 for acute spinal cord injury. For more information, visit www.geron.com.
This news release may contain forward-looking statements made pursuant to the ”safe harbor” provisions of the Private Securities Litigation Reform Act of 1995. Investors are cautioned that statements in this press release regarding potential applications of Geron’s human embryonic stem cell technology constitute forward-looking statements that involve risks and uncertainties, including, without limitation, risks inherent in the development and commercialization of potential products, uncertainty of clinical trial results or regulatory approvals or clearances, need for future capital, dependence upon collaborators and maintenance of our intellectual property rights. Actual results may differ materially from the results anticipated in these forward-looking statements. Additional information on potential factors that could affect our results and other risks and uncertainties are detailed from time to time in Geron’s periodic reports, including the quarterly report on Form 10-Q for the quarter ended September 30, 2008.
Contacts:
Russo Partners, LLC
David Schull, 858-717-2310 (Media)
david.schull@russopartnersllc.com
or
Geron
Anna Krassowska, 650-473-7765
Investor and Media Relations
info@geron.com
http://www.finanznachrichten.de/nachrichten-2009-01/12914393…23.01.2009 06:02
Geron Receives FDA Clearance to Begin World’s First Human Clinical Trial of Embryonic Stem Cell-Based Therapy
Geron to Study GRNOPC1 in Patients With Acute Spinal Cord Injury
Conference Call and Video Webcast Set for 6:00 a.m. PST/9:00 a.m. EST
Geron Corporation (News) (Nasdaq:GERN) announced today that the U.S. Food and Drug Administration (FDA) has granted clearance of the company’s Investigational New Drug (IND) application for the clinical trial of GRNOPC1 in patients with acute spinal cord injury.
The clearance enables Geron to move forward with the world’s first study of a human embryonic stem cell (hESC)-based therapy in man. Geron plans to initiate a Phase I multi-center trial that is designed to establish the safety of GRNOPC1 in patients with ”complete” American Spinal Injury Association (ASIA) grade A subacute thoracic spinal cord injuries.
”The FDA’s clearance of our GRNOPC1 IND is one of Geron’s most significant accomplishments to date,” said Thomas B. Okarma, Ph.D., M.D., Geron’s president and CEO. ”This marks the beginning of what is potentially a new chapter in medical therapeutics - one that reaches beyond pills to a new level of healing: the restoration of organ and tissue function achieved by the injection of healthy replacement cells. The ultimate goal for the use of GRNOPC1 is to achieve restoration of spinal cord function by the injection of hESC-derived oligodendrocyte progenitor cells directly into the lesion site of the patient’s injured spinal cord.”
GRNOPC1, Geron’s lead hESC-based therapeutic candidate, contains hESC-derived oligodendrocyte progenitor cells that have demonstrated remyelinating and nerve growth stimulating properties leading to restoration of function in animal models of acute spinal cord injury (Journal of Neuroscience, Vol. 25, 2005).
”The neurosurgical community is very excited by this new approach to treating devastating spinal cord injury,” said Richard Fessler, M.D., Ph.D., professor of neurological surgery at the Feinberg School of Medicine at Northwestern University. ”Demyelination is central to the pathology of the injury, and its reversal by means of injecting oligodendrocyte progenitor cells would be revolutionary for the field. If safe and effective, the therapy would provide a viable treatment option for thousands of patients who suffer severe spinal cord injuries each year.”
The GRNOPC1 Clinical Program
Patients eligible for the Phase I trial must have documented evidence of functionally complete spinal cord injury with a neurological level of T3 to T10 spinal segments and agree to have GRNOPC1 injected into the lesion sites between seven and 14 days after injury. Geron has selected up to seven U.S. medical centers as candidates to participate in this study and in planned protocol extensions. The sites will be identified as they come online and are ready to enroll subjects into the study.
Although the primary endpoint of the trial is safety, the protocol includes secondary endpoints to assess efficacy, such as improved neuromuscular control or sensation in the trunk or lower extremities. Once safety in this patient population has been established and the FDA reviews clinical data in conjunction with additional data from ongoing animal studies, Geron plans to seek FDA approval to extend the study to increase the dose of GRNOPC1, enroll subjects with complete cervical injuries and expand the trial to include patients with severe incomplete (ASIA grade B or C) injuries to enable access to the therapy for as broad a population of severe spinal cord-injured patients as is medically appropriate.
Preclinical Evidence of Safety, Tolerability and Efficacy
Geron submitted evidence of the safety, tolerability and efficacy of GRNOPC1 to the FDA in a 21,000-page IND application that described 24 separate animal studies requiring the production of more than five billion GRNOPC1 cells. Included in the safety package were studies that showed no evidence of teratoma formation 12 months after injection of clinical grade GRNOPC1 into the injured spinal cord of rats and mice. Other studies documented the absence of significant migration of the injected cells outside the spinal cord, allodynia induction (increased neuropathic pain due to the injected cells), systemic toxicity or increased mortality in animals receiving GRNOPC1.
In vitro studies have shown that GRNOPC1 is minimally recognized by the human immune system. GRNOPC1 is not recognized in vitro by allogeneic sera, NK cells or T cells (Journal of Neuroimmunology, Vol. 192, 2007). These immune-privileged characteristics of the hESC-derived cells allow a clinical trial design that incorporates a limited course of low-dose immunosuppression and provide the rationale for an off-the-shelf, allogeneic cell therapy.
Also included in the IND application were published studies supporting the utility of GRNOPC1 for the treatment of spinal cord injury. Those studies showed that administration of GRNOPC1 significantly improved locomotor activity and kinematic scores of animals with spinal cord injuries when injected seven days after the injury (Journal of Neuroscience, Vol. 25, 2005). Histological examination of the injured spinal cords treated with GRNOPC1 showed improved axon survival and extensive remyelination surrounding the rat axons. These effects of GRNOPC1 were present nine months after a single injection of cells. In these nine-month studies, the cells were shown to migrate and fill the lesion cavity, with bundles of myelinated axons crossing the injury site.
Production and Qualification of GRNOPC1
GRNOPC1 is produced using current Good Manufacturing Practices (cGMP) in Geron’s manufacturing facilities. Geron’s GRNOPC1 production process and clean-room suites have been inspected and licensed by the state of California. The cells are derived from the H1 human embryonic stem cell line, which was created before August 9, 2001. Studies using this line qualify for U.S. federal research funding, although no federal funding was received for the development of the product or to support the clinical trial.
Geron’s H1 hESC master cell bank is fully qualified for human use and was shown to be karyotypically normal and free of measurable contaminants of human or animal origin. Production of GRNOPC1 from undifferentiated hESCs in the master cell bank uses qualified reagents and a standardized protocol developed at Geron over the past three years. Each manufacturing run of GRNOPC1 is subjected to standardized quality control testing to ensure viability, sterility and appropriate cellular composition before release for clinical use. GRNOPC1 product that has passed all such specifications and has been released is available for the approved clinical trial. The current production scale can supply product needs through pivotal clinical trials. The existing master cell bank could potentially supply sufficient starting material for GRNOPC1 to commercially supply the U.S. acute spinal cord injury market for more than 20 years.
Intellectual Property
The production and commercialization of GRNOPC1 is protected by a portfolio of patent rights owned by or exclusively licensed to Geron. Patent rights owned by Geron protect key technologies developed at Geron for the scalable manufacturing of hESCs, as well as the production of neural cells by differentiation of hESCs. The fundamental patents covering hESCs are exclusively licensed to Geron from the Wisconsin Alumni Research Foundation (WARF) for the production of neural cells, cardiomyocytes and pancreatic islets for therapeutic applications. The validity of these patents was recently confirmed by the U.S. Patent and Trademark Office in a re-examination proceeding. Geron funded the original research at the University of Wisconsin-Madison that led to the first isolation of hESCs. The production of oligodendrocytes from hESCs is covered by patent rights exclusively licensed to Geron from the University of California. These patent rights cover technology developed in a research collaboration between Geron and University of California scientists.
Conference Call and Video Webcast
Thomas B. Okarma, Ph.D., M.D., will host a conference call and video Webcast presentation for investors and the media at 6:00 a.m. PST/9:00 a.m. EST today. Participants can access the conference call via telephone by dialing 866-783-2145 (U.S.) or 857-350-1604 (international). The passcode is 89631672. The video Webcast presentation is available at http://phx.corporate-ir.net/phoenix.zhtml?p=irol-eventDetail… All participants are encouraged to view Dr. Okarma’s presentation on the Internet. The video Webcast will also be accessible through a link that is posted on the home page of Geron’s Web site at http://www.geron.com. Participants are encouraged to log on at least 15 minutes prior to the beginning of the presentation in order to download any necessary software. The video Webcast will be available for replay through February 23, 2009.
Background information about human embryonic stem cells, GRNOPC1 and the spinal cord injury clinical trial can be found at http://eon.businesswire.com/news/eon/20090122006356/en.
Geron is developing first-in-class biopharmaceuticals for the treatment of cancer and chronic degenerative diseases, including spinal cord injury, heart failure and diabetes. The company is advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials. Geron is also the world leader in the development of human embryonic stem (hESC) cell-based therapeutics. The company has received FDA clearance to begin the world’s first human clinical trial of a hESC-based therapy: GRNOPC1 for acute spinal cord injury. For more information, visit www.geron.com.
This news release may contain forward-looking statements made pursuant to the ”safe harbor” provisions of the Private Securities Litigation Reform Act of 1995. Investors are cautioned that statements in this press release regarding potential applications of Geron’s human embryonic stem cell technology constitute forward-looking statements that involve risks and uncertainties, including, without limitation, risks inherent in the development and commercialization of potential products, uncertainty of clinical trial results or regulatory approvals or clearances, need for future capital, dependence upon collaborators and maintenance of our intellectual property rights. Actual results may differ materially from the results anticipated in these forward-looking statements. Additional information on potential factors that could affect our results and other risks and uncertainties are detailed from time to time in Geron’s periodic reports, including the quarterly report on Form 10-Q for the quarter ended September 30, 2008.
Contacts:
Russo Partners, LLC
David Schull, 858-717-2310 (Media)
david.schull@russopartnersllc.com
or
Geron
Anna Krassowska, 650-473-7765
Investor and Media Relations
info@geron.com
FDA Greenlights Testing of Geron's Stem Cell Treatment
Just four days into the new administration a small biotechnology company is taking a giant step forward in the field of stem cell research.
Geron is announcing that it has received U.S. Food and Drug Administration clearance to do the first-ever test of an embryonic stem cell treatment in people.
The injection will be given to a small number of patients with a specific type of new spinal cord injury to make sure it is safe and to begin to measure how well it works.
In a press release, Geron CEO Dr. Thomas Okarma is quoted as saying, "This marks the beginning of what is potentially a new chapter in medical therapeutics -- one that reaches beyond pills to a new level of healing: the restoration of organ and tissue function achieved by the injection of healthy replacement cells."
Dr. Okarma will appear in a "First on CNBC" live interview on "Squawk on the Street" at approximately 10:40 a.m. ET Friday.
President George W. Bush prohibited federal funding of embryonic stem cell research. President Obama supports it.
Shares of Geron [GERN 5.21 -0.08 (-1.51%) ] closed eight cents lower on Thursday after hitting a new 52-week high of $5.64 intra-day on heavier-than-normal trading volume.
http://www.cnbc.com//id/28804364?__source=yahoo%7Cheadline%7…
Just four days into the new administration a small biotechnology company is taking a giant step forward in the field of stem cell research.
Geron is announcing that it has received U.S. Food and Drug Administration clearance to do the first-ever test of an embryonic stem cell treatment in people.
The injection will be given to a small number of patients with a specific type of new spinal cord injury to make sure it is safe and to begin to measure how well it works.
In a press release, Geron CEO Dr. Thomas Okarma is quoted as saying, "This marks the beginning of what is potentially a new chapter in medical therapeutics -- one that reaches beyond pills to a new level of healing: the restoration of organ and tissue function achieved by the injection of healthy replacement cells."
Dr. Okarma will appear in a "First on CNBC" live interview on "Squawk on the Street" at approximately 10:40 a.m. ET Friday.
President George W. Bush prohibited federal funding of embryonic stem cell research. President Obama supports it.
Shares of Geron [GERN 5.21 -0.08 (-1.51%) ] closed eight cents lower on Thursday after hitting a new 52-week high of $5.64 intra-day on heavier-than-normal trading volume.
http://www.cnbc.com//id/28804364?__source=yahoo%7Cheadline%7…
Wahnsinn! Überall "DAS" Thema in den USA!
Finacial Times:
http://www.ft.com/cms/s/0/8c9243f6-e924-11dd-9535-0000779fd2…
US allows use of embryonic stem cells
By Andrew Jack in London
Published: January 23 2009 08:13 | Last updated: January 23 2009 08:13
US regulators have approved the first use of embryonic stem cells in humans.
The move raises the prospect of a groundbreaking approach to medical treatment that had been blocked since 2001 by George W. Bush as president. Just two days after the inauguration of President Barack Obama, who opposed his predecessor’s ban on federal funding for embryonic stem-cell research, the Food & Drug Administration authorised Geron, a US biotech company, to begin clinical trials for patients with severe spinal cord injuries.
While commercial and academic researchers have begun to use adult stem cells to treat patients, Geron, based in Menlo Park, California, has moved furthest and fastest in the field of embryonic stem cells, which scientists believe have far greater potential in treatment because they can evolve into any cell in the body.
The FDA decision paves the way for Geron to start trials in patients to test the safety of its product, called GRNOPC1, after which it will need fresh regulatory approvals to show efficacy before potential commercialisation within as little as three years.
Thomas Okarma, president and chief executive of Geron said: “This is the dawn of a new era. This goes beyond pills and scalpels to achieve a new level of healing.” He said there could be setbacks. Geron would need to recruit at least eight patients, and follow their progress for at least a year but “if we can turn a quadriplegic into someone who can walk with a cane, this will go fast-track like lightning”.
Mr Okarma said there were considerable challenges for regulators in ensuring safety in the fledgling field of embryonic stem-cell treatment. The chief executive was not aware of any political interference in the decision of the FDA, which had respected a series of deadlines since the company first sought approval in March.
But he criticised the “crazy” period following President Bush’s ban on federal funding, which he said left Geron isolated in supporting embryonic stem-cell research while many other researchers had followed financial support to study less promising uses of adult stems. “This is a triumph of private innovation over public inertia,” he said, stressing that Geron had invested $200m since 1995 in the field, and that the new administration needed to draw up more ambitious plans than simply permitting federal funding.
Mr Okarma said Geron could achieve important economies of scale designed to ensure that the price of the new treatment would be “reasonable”. The chief executive said he was keen to license its technology to other developers of stem cells to treat a variety of different treatments.
Copyright The Financial Times Limited 2009
Wall Street Journal: http://online.wsj.com/article/SB123268485825709415.html?mod=…
JANUARY 23, 2009, 3:29 A.M. ET First Embryonic Stem-Cell Trial Gets Approval From the FDA Article
Comments
more in Politics »By RON WINSLOW and ALICIA MUNDY
In a watershed moment for one of the most contentious areas of science and American politics, the U.S. Food and Drug Administration cleared the way for the first-ever human trial of a medical treatment derived from embryonic stem cells.
Geron Corp., a Menlo Park, Calif., biotechnology company, is expected to announce Friday that it received a green light from the agency to mount a study of its stem-cell treatment for spinal cord injuries in up to 10 patients. The announcement caps more than a decade of advances in the company's labs and comes on the cusp of a widely expected shift in U.S. policy toward support of embryonic stem-cell research after years of official opposition.
"This is the dawn of a new era in medical therapeutics," said Thomas B. Okarma, Geron's president and chief executive officer. The hope that stem-cell therapy will repair and regenerate diseased organs and tissue "goes beyond what pills and scalpels can ever do."
Limits on stem-cell research, which prevented federal funding and were imposed by Congress and former President George W. Bush for ethical and religious reasons, have had a chilling effect on both academic and corporate research involving such cells. Proponents of stem-cell research say restrictions have delayed development of promising new treatments, while critics contend that harvesting stem cells from embryos destroys human life.
President Barack Obama said during his campaign that overturning research limits would be a top priority in his administration.
Both Geron and the FDA said the timing of the decision to approve the study was coincidental. "The FDA looks to the science on these types of issues, and we approve [such applications] based on a showing of safety," said Karen Riley, an FDA spokeswoman. "Political considerations have no role in this process."
Approval of the study is far from a guarantee that stem-cell treatments will work or make it to the market, but it is likely to be seen as an indication that opportunities for stem-cell research are poised to open and will fuel enthusiasm among academic and corporate researchers.
Mr. Obama's plans for acting on the current research restrictions haven't been finalized. Shortly after the election, Obama advisers thrilled biotech companies and investors when they suggested that the new president could use his executive authority to undo the Bush administration ban. But in a Jan. 18 interview on CNN, Mr. Obama said he might let Congress take the lead. "I like the idea of the American people's representatives expressing their views on an issue like this," he said.
Regulating stem-cell therapy is new turf for both industry and the FDA, a major reason why it took the agency nearly a year to review Geron's 21,000-page application for the trial, which it filed last March. Approval came in a phone call Wednesday afternoon, Dr. Okarma said.
The study will focus on the safety of the treatment. At an FDA hearing in April, several firms' executives and researchers complained that they were at a loss about what the FDA wanted in terms of clinical trials involving stem cells because the FDA itself wasn't sure.
Embryonic stem cells are the building-block cells that help drive prenatal development. Geron has developed banks of embryonic stem cells and found a way to coax them into differentiating as they do in nature into progenitors of specific cells that make spinal-cord tissue, heart muscle, cartilage and other organs and tissues.
Spinal-cord injury is one of medicine's most debilitating conditions, typically causing paralysis and other issues for which there are few, if any, effective treatments. The Geron study will enroll paralyzed patients who can be treated within 14 days of their injury. Patients will be evaluated for at least one year, after which, if the treatment proves safe, the company hopes to increase the dose and expand the potential candidates for the therapy.
In addition to safety, researchers will look for signs that the treatment is effective.
Write to Ron Winslow at ron.winslow@wsj.com and Alicia Mundy at alicia.mundy@wsj.com
Printed in The Wall Street Journal, page A12
Finacial Times:
http://www.ft.com/cms/s/0/8c9243f6-e924-11dd-9535-0000779fd2…
US allows use of embryonic stem cells
By Andrew Jack in London
Published: January 23 2009 08:13 | Last updated: January 23 2009 08:13
US regulators have approved the first use of embryonic stem cells in humans.
The move raises the prospect of a groundbreaking approach to medical treatment that had been blocked since 2001 by George W. Bush as president. Just two days after the inauguration of President Barack Obama, who opposed his predecessor’s ban on federal funding for embryonic stem-cell research, the Food & Drug Administration authorised Geron, a US biotech company, to begin clinical trials for patients with severe spinal cord injuries.
While commercial and academic researchers have begun to use adult stem cells to treat patients, Geron, based in Menlo Park, California, has moved furthest and fastest in the field of embryonic stem cells, which scientists believe have far greater potential in treatment because they can evolve into any cell in the body.
The FDA decision paves the way for Geron to start trials in patients to test the safety of its product, called GRNOPC1, after which it will need fresh regulatory approvals to show efficacy before potential commercialisation within as little as three years.
Thomas Okarma, president and chief executive of Geron said: “This is the dawn of a new era. This goes beyond pills and scalpels to achieve a new level of healing.” He said there could be setbacks. Geron would need to recruit at least eight patients, and follow their progress for at least a year but “if we can turn a quadriplegic into someone who can walk with a cane, this will go fast-track like lightning”.
Mr Okarma said there were considerable challenges for regulators in ensuring safety in the fledgling field of embryonic stem-cell treatment. The chief executive was not aware of any political interference in the decision of the FDA, which had respected a series of deadlines since the company first sought approval in March.
But he criticised the “crazy” period following President Bush’s ban on federal funding, which he said left Geron isolated in supporting embryonic stem-cell research while many other researchers had followed financial support to study less promising uses of adult stems. “This is a triumph of private innovation over public inertia,” he said, stressing that Geron had invested $200m since 1995 in the field, and that the new administration needed to draw up more ambitious plans than simply permitting federal funding.
Mr Okarma said Geron could achieve important economies of scale designed to ensure that the price of the new treatment would be “reasonable”. The chief executive said he was keen to license its technology to other developers of stem cells to treat a variety of different treatments.
Copyright The Financial Times Limited 2009
Wall Street Journal: http://online.wsj.com/article/SB123268485825709415.html?mod=…
JANUARY 23, 2009, 3:29 A.M. ET First Embryonic Stem-Cell Trial Gets Approval From the FDA Article
Comments
more in Politics »By RON WINSLOW and ALICIA MUNDY
In a watershed moment for one of the most contentious areas of science and American politics, the U.S. Food and Drug Administration cleared the way for the first-ever human trial of a medical treatment derived from embryonic stem cells.
Geron Corp., a Menlo Park, Calif., biotechnology company, is expected to announce Friday that it received a green light from the agency to mount a study of its stem-cell treatment for spinal cord injuries in up to 10 patients. The announcement caps more than a decade of advances in the company's labs and comes on the cusp of a widely expected shift in U.S. policy toward support of embryonic stem-cell research after years of official opposition.
"This is the dawn of a new era in medical therapeutics," said Thomas B. Okarma, Geron's president and chief executive officer. The hope that stem-cell therapy will repair and regenerate diseased organs and tissue "goes beyond what pills and scalpels can ever do."
Limits on stem-cell research, which prevented federal funding and were imposed by Congress and former President George W. Bush for ethical and religious reasons, have had a chilling effect on both academic and corporate research involving such cells. Proponents of stem-cell research say restrictions have delayed development of promising new treatments, while critics contend that harvesting stem cells from embryos destroys human life.
President Barack Obama said during his campaign that overturning research limits would be a top priority in his administration.
Both Geron and the FDA said the timing of the decision to approve the study was coincidental. "The FDA looks to the science on these types of issues, and we approve [such applications] based on a showing of safety," said Karen Riley, an FDA spokeswoman. "Political considerations have no role in this process."
Approval of the study is far from a guarantee that stem-cell treatments will work or make it to the market, but it is likely to be seen as an indication that opportunities for stem-cell research are poised to open and will fuel enthusiasm among academic and corporate researchers.
Mr. Obama's plans for acting on the current research restrictions haven't been finalized. Shortly after the election, Obama advisers thrilled biotech companies and investors when they suggested that the new president could use his executive authority to undo the Bush administration ban. But in a Jan. 18 interview on CNN, Mr. Obama said he might let Congress take the lead. "I like the idea of the American people's representatives expressing their views on an issue like this," he said.
Regulating stem-cell therapy is new turf for both industry and the FDA, a major reason why it took the agency nearly a year to review Geron's 21,000-page application for the trial, which it filed last March. Approval came in a phone call Wednesday afternoon, Dr. Okarma said.
The study will focus on the safety of the treatment. At an FDA hearing in April, several firms' executives and researchers complained that they were at a loss about what the FDA wanted in terms of clinical trials involving stem cells because the FDA itself wasn't sure.
Embryonic stem cells are the building-block cells that help drive prenatal development. Geron has developed banks of embryonic stem cells and found a way to coax them into differentiating as they do in nature into progenitors of specific cells that make spinal-cord tissue, heart muscle, cartilage and other organs and tissues.
Spinal-cord injury is one of medicine's most debilitating conditions, typically causing paralysis and other issues for which there are few, if any, effective treatments. The Geron study will enroll paralyzed patients who can be treated within 14 days of their injury. Patients will be evaluated for at least one year, after which, if the treatment proves safe, the company hopes to increase the dose and expand the potential candidates for the therapy.
In addition to safety, researchers will look for signs that the treatment is effective.
Write to Ron Winslow at ron.winslow@wsj.com and Alicia Mundy at alicia.mundy@wsj.com
Printed in The Wall Street Journal, page A12
aus der Times UK:
http://www.timesonline.co.uk/tol/life_and_style/health/artic…" target="_blank" rel="nofollow ugc noopener">
http://www.timesonline.co.uk/tol/life_and_style/health/artic…
From The Times January 23, 2009
Geron: the world leader working on a shoestring budget
Mike Harvey in San Francisco
Geron is a leading biotech company based in Menlo Park in the heart of Silicon Valley, south of San Francisco. It is acknowledged as a world leader in the development of human embryonic stem cell-based therapeutics and its spinal cord injury treatment is expected to be its first product to enter clinical development.
The company, which has more than 125 employees, was set up in 1990 and went public in 1996. It is quoted on the Nasdaq stock exchange in New York. Geron has a wholly owned subsidiary, Geron Bio-Med Ltd, that is based in Edinburgh.
As well as spinal cord injuries, Geron is looking at developing treatments for cancer and chronic degenerative diseases, including heart failure and diabetes. The company says it is “advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials”.
Geron, which has been operating at a loss, has been waiting for a change in leadership at the White House. Its shares shot up 10 per cent after Barack Obama was elected as President in November.
David Greenwood, the company’s chief financial officer, said in November that a reversal in stem-cell research policy should result in a surge of funding and interest. “We at this company have spent probably $170 million on embryonic stem cells,” he said. “I think our $170 million probably is equal to what all other stem cell companies have managed to raise, and that’s not a large sum to do industrial science.”
Dr Tom Okarma, Geron chief executive, has said that he would like to see a presidential commission on stem cell policy. He told the BBC: “The impact of eight years under the previous administration for stem cell research has really been devastating. We want the new administration to do more than the merely political - of reversing the prior administration’s ban.
“Twenty or thirty years from now, hopefully I’ll be full of embryonic stem cell products that will keep me healthy into my 90s and beyond.”
http://www.timesonline.co.uk/tol/life_and_style/health/artic…" target="_blank" rel="nofollow ugc noopener">
http://www.timesonline.co.uk/tol/life_and_style/health/artic…
From The Times January 23, 2009
Geron: the world leader working on a shoestring budget
Mike Harvey in San Francisco
Geron is a leading biotech company based in Menlo Park in the heart of Silicon Valley, south of San Francisco. It is acknowledged as a world leader in the development of human embryonic stem cell-based therapeutics and its spinal cord injury treatment is expected to be its first product to enter clinical development.
The company, which has more than 125 employees, was set up in 1990 and went public in 1996. It is quoted on the Nasdaq stock exchange in New York. Geron has a wholly owned subsidiary, Geron Bio-Med Ltd, that is based in Edinburgh.
As well as spinal cord injuries, Geron is looking at developing treatments for cancer and chronic degenerative diseases, including heart failure and diabetes. The company says it is “advancing an anti-cancer drug and a cancer vaccine that target the enzyme telomerase through multiple clinical trials”.
Geron, which has been operating at a loss, has been waiting for a change in leadership at the White House. Its shares shot up 10 per cent after Barack Obama was elected as President in November.
David Greenwood, the company’s chief financial officer, said in November that a reversal in stem-cell research policy should result in a surge of funding and interest. “We at this company have spent probably $170 million on embryonic stem cells,” he said. “I think our $170 million probably is equal to what all other stem cell companies have managed to raise, and that’s not a large sum to do industrial science.”
Dr Tom Okarma, Geron chief executive, has said that he would like to see a presidential commission on stem cell policy. He told the BBC: “The impact of eight years under the previous administration for stem cell research has really been devastating. We want the new administration to do more than the merely political - of reversing the prior administration’s ban.
“Twenty or thirty years from now, hopefully I’ll be full of embryonic stem cell products that will keep me healthy into my 90s and beyond.”
was glaubt ihr, wie entwickelt sich der Kurs heute?
!
Dieser Beitrag wurde vom System automatisch gesperrt. Bei Fragen wenden Sie sich bitte an feedback@wallstreet-online.de
Geron - FDA genehmigt Versuche mit Stammzellen, Aktie vorb. +24%
New York (BoerseGo.de) - Das Biotechnologieunternehmen Geron Corp. (News) hat von der US-Gesundheitsbehörde FDA grünes Licht für den Beginn von Versuchen mit menschlichen embryonalen Stammzellen erhalten. Damit würden für diesen Bereich weltweit erste Studien über einen entsprechenden Therapieeinsatz bei Menschen durchgeführt. Die Phase I diene zur Etablierung eines mit “GRNOPC1” bezeichneten Sicherheitsstandards bei Behandlung von Patienten mit akuten Brustlymphgängen und Rückenmarksschädigungen.
Geron schießen vorbörslich um 24,76% auf 6,5 Dollar nach oben
New York (BoerseGo.de) - Das Biotechnologieunternehmen Geron Corp. (News) hat von der US-Gesundheitsbehörde FDA grünes Licht für den Beginn von Versuchen mit menschlichen embryonalen Stammzellen erhalten. Damit würden für diesen Bereich weltweit erste Studien über einen entsprechenden Therapieeinsatz bei Menschen durchgeführt. Die Phase I diene zur Etablierung eines mit “GRNOPC1” bezeichneten Sicherheitsstandards bei Behandlung von Patienten mit akuten Brustlymphgängen und Rückenmarksschädigungen.
Geron schießen vorbörslich um 24,76% auf 6,5 Dollar nach oben
Erste Therapie mit embryonalen Stammzellen genehmigt
Von Jens Lubbadeh
Ist es der Beginn einer neuen Ära der Medizin? In den USA werden im Sommer dieses Jahres zum ersten Mal embryonale Stammzellen an Querschnittsgelähmten erprobt. Die Hoffnungen sind groß, die Wissenschaftler wollen zunächst einmal Risiken ausschließen.
"Change" hat in den USA auch in der Stammzellforschung Einzug gehalten. Während die Regierung George W. Bushs aus ideologischen Gründen die Gelder für die Forschung an embryonalen Stammzellen blockierte, will der neue Präsident Obama hier eine Trendwende einleiten.
Querschnittsgelähmter Rollstuhlfahrer: "Es geht nicht darum, dass wir jemanden von heute auf morgen wieder zum Gehen und Tanzen bekommen möchten"
Im Sommer dieses Jahres wird die allererste Studie mit embryonalen Stammzellen am Menschen stattfinden. Die US-amerikanische Arzneimittelbehörde Food and Drug Administration (FDA) hat Wissenschaftlern des Biotech-Unternehmens Geron nun genehmigt, zehn querschnittsgelähmten Patienten aus embryonalen Stammzellen gezüchtete Rückenmarkszellen zu injizieren. Der Antrag Gerons lag der Behörde schon seit längerem vor. Der Präsident des Unternehmens Thomas Okarma erklärte, die nun erteilte FDA-Genehmigung stehe nicht in Zusammenhang mit dem Amtswechsel im Weißen Haus.
Die Studie solle erst einmal dazu dienen, Sicherheitsrisiken einer Therapie mit humanen embryonalen Stammzellen auszuschließen. Die Patienten werden eine einmalige Injektion in die beschädigte Stelle des Rückenmarks erhalten. Dennoch hoffen die Wissenschaftler, dass die Zellen die beschädigten Nerven der Patienten wieder zum Wachsen anregen, sodass das Gefühlsempfinden wieder hergestellt wird und womöglich sogar das Gehvermögen. Tierversuche haben gezeigt, dass die injizierten Zellen am Verletzungsort ausreifen und Wachstumsfaktoren produzieren, die das beschädigte Gewebe in der Umgebung wieder zum Wachsen stimulieren könnten.
STAMMZELLEN - DIE ZELLULÄREN MULTITALENTEEmbryonale Stammzellen (ES)
DPASie gelten als die zellulären Alleskönner: Reift eine befruchtete Eizelle zu einer Blastozyste, einem kleinen Zellklumpen, heran, entsteht in deren Inneren eine Masse aus embryonalen Stammzellen. Die noch nicht differenzierten Stammzellen können sich zu jeder Zellart des menschlichen Körpers entwickeln. In Tierversuchen haben sich die Stammzellen bereits in Nerven-, Blut-, Leber- oder Herzmuskelzellen verwandeln lassen. Voraussetzung ist, dass sie zuvor mit geeigneten Wachstumsfaktoren behandelt werden.
Induzierte pluripotente Stammzellen (iPS)
Körperzellen einfach in Stammzellen umprogrammieren - das gelang Forschern nun, indem sie vier bestimmte Steuerungsgene in die Zelle einschleusten. Aus den dabei entstandenen maßgeschneiderten Stammzellen züchteten sie erfolgreich Nerven- und Muskelzellen. Diese Methode wäre nicht nur elegant, sondern auch ethisch unbedenklich, da dabei kein Embryo hergestellt und verbraucht wird. Allerdings ist noch unklar, ob die induzierten Stammzellen wirklich so potent sind wie embryonale Stammzellen.
Adulte Stammzellen
Nicht nur Embryonen sind eine Quelle der Zellen, aus denen sich verschiedene Arten menschlichen Gewebes entwickeln können. In etwa 20 Organen inklusive der Muskeln, der Knochen, der Haut, der Plazenta und des Nervensystems haben Forscher adulte Stammzellen aufgespürt. Sie besitzen zwar weniger verlockende Eigenschaften als die embryonalen Stammzellen, bereiten aber in der Herstellung auch keine ethischen Probleme. Dem Körper eines Erwachsenen werden Stammzellen entnommen und in Zellkulturen durch Zugabe entsprechender Wachstumsfaktoren so umprogrammiert, dass sie zu den gewünschten Gewebearten heranreifen.
Ethik und Recht
Die Stammzellforschung birgt ethische Konflikte. Embryonale Stammzellen werden aus Embryonen gewonnen, die entweder eigens hergestellt werden oder bei künstlichen Befruchtungen übriggeblieben sind. Die Argumentation der Befürworter: Sie würden ohnehin vernichtet. Kritiker sprechen dagegen von der Tötung ungeborenen Lebens.
In Deutschland ist das Herstellen menschlicher Embryonen zur Gewinnung von Stammzellen verboten. In Ausnahmefällen erlaubt das Gesetz aber den Import von Stammzellen, die vor dem 1. Mai 2007 hergestellt wurden. In Großbritannien und Südkorea ist das therapeutische Klonen ausdrücklich erlaubt, ebenso in den USA, wo das Klonen von Embryonen aber nicht mit staatlichen Mitteln gefördert werden darf.
Überzogene Erwartungen dämpfte Okarma allerdings: "Es geht nicht darum, dass wir jemanden von heute auf morgen wieder zum Gehen und Tanzen bekommen möchten." Man wolle eine Verbesserung der Bewegungsfähigkeit erzielen, die mit Physiotherapie ausgebaut werden könne. Allerdings kommen für die Studie nur Patienten infrage, die erst seit einer oder zwei Wochen gelähmt sind. Langzeitgelähmte seien nicht geeignet. "Bei chronisch Verletzten wirkt die Stammzelltherapie nicht, weil sich schon Narbengewebe gebildet hat", sagt Miodrag Stojkovic, Stammzellforscher am Prinz Felipe Forschungszentrum im spanischen Valencia im Gespräch mit SPIEGEL ONLINE. Die Patienten müssten zudem für mindestens einen Monat Immunsuppressiva erhalten und würden ein Jahr lang beobachtet.
Stojkovic beurteilt die kommende Studie als wichtigen Schritt: "Das ist eine wunderbare Sache und der erste Versuch, differenzierte humane embryonale Stammzellen für therapeutische Zwecke zu nutzen." Die Studie sei seriös, die Wissenschaftler erfahren. Stojkovic: "Dahinter steckt jahrelange Arbeit."
Vielversprechende Ergebnisse aus Tierversuchen
Embryonale Stammzellen sind ethisch umstritten, weil für ihre Herstellung menschliche Embryonen zerstört werden müssen. Mediziner setzten aber große Hoffnungen in die Zellen, weil sie sich in jedes Körpergewebe ausdifferenzieren können. Mit ihnen wollen sie eines Tages Krankheiten wie Parkinson, Diabetes und Querschnittslähmung heilen. Allerdings wird auch an Alternativen geforscht: Manche Wissenschaftler hoffe, die gleichen Erfolge mit adulten Stammzellen oder iPS-Stammzellen zu erzielen, die ethisch unbedenklich sind.
Verschiedene Kliniken weltweit behaupten schon, humane embryonale Stammzellen einzusetzen. Erst kürzlich kritisierten Wissenschaftler im Fachmagazin "Cell Stem Cell" die fragwürdigen Stammzell-Therapien diverser Kliniken, die diese für meist teures Geld anbieten. "Zahlreiche Kliniken weltweit beuten die Hoffnungen von Patienten aus, indem sie behaupten, Schwerkranke mit neuen und effektiven Stammzelltherapien behandeln zu können", heißt es in den Richtlinien, die die Internationale Gesellschaft für Stammzellforschung ISSCR daher für die klinische Anwendung von Stammzellen erlassen hat. "Es gibt leider selbsternannte Ärzte, die undifferenzierte Stammzellen einsetzen - und das ohne jegliche wissenschaftliche Grundlage", so Stojkovic.
Therapien mit embryonalen Stammzellen wurden bisher nur an Tieren erprobt. Die Ergebnisse allerdings sind vielversprechend: So gelang es Forschern, das Bewegungsvermögen gelähmter Ratten mit Hilfe von Stammzellen zu verbessern. Und auch Parkinsonsymptome konnten sie lindern.
MEHR ÜBER...
Embryonale Stammzellen Querschnittslähmung Parkinson Diabetes Geron Stammzellforschung
zu SPIEGEL WISSEN Stammzellforscher verweisen immer wieder darauf, dass noch viele Fragen und Risiken bei dem Einsatz von Stammzellen ungeklärt sind. "Es ist nicht ausgeschlossen, dass die Stammzellen Krebs hervorrufen", warnte Jürgen Hescheler, Präsident der Deutschen Gesellschaft für Stammzellforschung, im Gespräch mit SPIEGEL ONLINE. Es sei auch möglich, dass sich die Zellen am Einsatzort zu einem unerwünschten Gewebetyp entwickelten. Und auch Stojkovic bestätigt: "Die Stammzellen könnten nicht komplett differenziert sein, es könnten sich Tumoren entwickeln." Adulte Stammzellen hingegen werden schon am Menschen eingesetzt, beispielsweise bei der Behandlung von Blut- und Herzerkrankungen.
"Es ist ein Meilenstein und ein Durchbruch für die Stammzellforschung", kommentierte Ed Baetge die Genehmigung. Baetge ist Leiter der Forschungsabteilung der US-Biotech-Firma Novocell, die eine Stammzell-Studie an Diabetes-Patienten plant. Die Firma gilt weltweit als führender Hersteller embryonaler Stammzell-Linien

Von Jens Lubbadeh
Ist es der Beginn einer neuen Ära der Medizin? In den USA werden im Sommer dieses Jahres zum ersten Mal embryonale Stammzellen an Querschnittsgelähmten erprobt. Die Hoffnungen sind groß, die Wissenschaftler wollen zunächst einmal Risiken ausschließen.
"Change" hat in den USA auch in der Stammzellforschung Einzug gehalten. Während die Regierung George W. Bushs aus ideologischen Gründen die Gelder für die Forschung an embryonalen Stammzellen blockierte, will der neue Präsident Obama hier eine Trendwende einleiten.
Querschnittsgelähmter Rollstuhlfahrer: "Es geht nicht darum, dass wir jemanden von heute auf morgen wieder zum Gehen und Tanzen bekommen möchten"
Im Sommer dieses Jahres wird die allererste Studie mit embryonalen Stammzellen am Menschen stattfinden. Die US-amerikanische Arzneimittelbehörde Food and Drug Administration (FDA) hat Wissenschaftlern des Biotech-Unternehmens Geron nun genehmigt, zehn querschnittsgelähmten Patienten aus embryonalen Stammzellen gezüchtete Rückenmarkszellen zu injizieren. Der Antrag Gerons lag der Behörde schon seit längerem vor. Der Präsident des Unternehmens Thomas Okarma erklärte, die nun erteilte FDA-Genehmigung stehe nicht in Zusammenhang mit dem Amtswechsel im Weißen Haus.
Die Studie solle erst einmal dazu dienen, Sicherheitsrisiken einer Therapie mit humanen embryonalen Stammzellen auszuschließen. Die Patienten werden eine einmalige Injektion in die beschädigte Stelle des Rückenmarks erhalten. Dennoch hoffen die Wissenschaftler, dass die Zellen die beschädigten Nerven der Patienten wieder zum Wachsen anregen, sodass das Gefühlsempfinden wieder hergestellt wird und womöglich sogar das Gehvermögen. Tierversuche haben gezeigt, dass die injizierten Zellen am Verletzungsort ausreifen und Wachstumsfaktoren produzieren, die das beschädigte Gewebe in der Umgebung wieder zum Wachsen stimulieren könnten.
STAMMZELLEN - DIE ZELLULÄREN MULTITALENTEEmbryonale Stammzellen (ES)
DPASie gelten als die zellulären Alleskönner: Reift eine befruchtete Eizelle zu einer Blastozyste, einem kleinen Zellklumpen, heran, entsteht in deren Inneren eine Masse aus embryonalen Stammzellen. Die noch nicht differenzierten Stammzellen können sich zu jeder Zellart des menschlichen Körpers entwickeln. In Tierversuchen haben sich die Stammzellen bereits in Nerven-, Blut-, Leber- oder Herzmuskelzellen verwandeln lassen. Voraussetzung ist, dass sie zuvor mit geeigneten Wachstumsfaktoren behandelt werden.
Induzierte pluripotente Stammzellen (iPS)
Körperzellen einfach in Stammzellen umprogrammieren - das gelang Forschern nun, indem sie vier bestimmte Steuerungsgene in die Zelle einschleusten. Aus den dabei entstandenen maßgeschneiderten Stammzellen züchteten sie erfolgreich Nerven- und Muskelzellen. Diese Methode wäre nicht nur elegant, sondern auch ethisch unbedenklich, da dabei kein Embryo hergestellt und verbraucht wird. Allerdings ist noch unklar, ob die induzierten Stammzellen wirklich so potent sind wie embryonale Stammzellen.
Adulte Stammzellen
Nicht nur Embryonen sind eine Quelle der Zellen, aus denen sich verschiedene Arten menschlichen Gewebes entwickeln können. In etwa 20 Organen inklusive der Muskeln, der Knochen, der Haut, der Plazenta und des Nervensystems haben Forscher adulte Stammzellen aufgespürt. Sie besitzen zwar weniger verlockende Eigenschaften als die embryonalen Stammzellen, bereiten aber in der Herstellung auch keine ethischen Probleme. Dem Körper eines Erwachsenen werden Stammzellen entnommen und in Zellkulturen durch Zugabe entsprechender Wachstumsfaktoren so umprogrammiert, dass sie zu den gewünschten Gewebearten heranreifen.
Ethik und Recht
Die Stammzellforschung birgt ethische Konflikte. Embryonale Stammzellen werden aus Embryonen gewonnen, die entweder eigens hergestellt werden oder bei künstlichen Befruchtungen übriggeblieben sind. Die Argumentation der Befürworter: Sie würden ohnehin vernichtet. Kritiker sprechen dagegen von der Tötung ungeborenen Lebens.
In Deutschland ist das Herstellen menschlicher Embryonen zur Gewinnung von Stammzellen verboten. In Ausnahmefällen erlaubt das Gesetz aber den Import von Stammzellen, die vor dem 1. Mai 2007 hergestellt wurden. In Großbritannien und Südkorea ist das therapeutische Klonen ausdrücklich erlaubt, ebenso in den USA, wo das Klonen von Embryonen aber nicht mit staatlichen Mitteln gefördert werden darf.
Überzogene Erwartungen dämpfte Okarma allerdings: "Es geht nicht darum, dass wir jemanden von heute auf morgen wieder zum Gehen und Tanzen bekommen möchten." Man wolle eine Verbesserung der Bewegungsfähigkeit erzielen, die mit Physiotherapie ausgebaut werden könne. Allerdings kommen für die Studie nur Patienten infrage, die erst seit einer oder zwei Wochen gelähmt sind. Langzeitgelähmte seien nicht geeignet. "Bei chronisch Verletzten wirkt die Stammzelltherapie nicht, weil sich schon Narbengewebe gebildet hat", sagt Miodrag Stojkovic, Stammzellforscher am Prinz Felipe Forschungszentrum im spanischen Valencia im Gespräch mit SPIEGEL ONLINE. Die Patienten müssten zudem für mindestens einen Monat Immunsuppressiva erhalten und würden ein Jahr lang beobachtet.
Stojkovic beurteilt die kommende Studie als wichtigen Schritt: "Das ist eine wunderbare Sache und der erste Versuch, differenzierte humane embryonale Stammzellen für therapeutische Zwecke zu nutzen." Die Studie sei seriös, die Wissenschaftler erfahren. Stojkovic: "Dahinter steckt jahrelange Arbeit."
Vielversprechende Ergebnisse aus Tierversuchen
Embryonale Stammzellen sind ethisch umstritten, weil für ihre Herstellung menschliche Embryonen zerstört werden müssen. Mediziner setzten aber große Hoffnungen in die Zellen, weil sie sich in jedes Körpergewebe ausdifferenzieren können. Mit ihnen wollen sie eines Tages Krankheiten wie Parkinson, Diabetes und Querschnittslähmung heilen. Allerdings wird auch an Alternativen geforscht: Manche Wissenschaftler hoffe, die gleichen Erfolge mit adulten Stammzellen oder iPS-Stammzellen zu erzielen, die ethisch unbedenklich sind.
Verschiedene Kliniken weltweit behaupten schon, humane embryonale Stammzellen einzusetzen. Erst kürzlich kritisierten Wissenschaftler im Fachmagazin "Cell Stem Cell" die fragwürdigen Stammzell-Therapien diverser Kliniken, die diese für meist teures Geld anbieten. "Zahlreiche Kliniken weltweit beuten die Hoffnungen von Patienten aus, indem sie behaupten, Schwerkranke mit neuen und effektiven Stammzelltherapien behandeln zu können", heißt es in den Richtlinien, die die Internationale Gesellschaft für Stammzellforschung ISSCR daher für die klinische Anwendung von Stammzellen erlassen hat. "Es gibt leider selbsternannte Ärzte, die undifferenzierte Stammzellen einsetzen - und das ohne jegliche wissenschaftliche Grundlage", so Stojkovic.
Therapien mit embryonalen Stammzellen wurden bisher nur an Tieren erprobt. Die Ergebnisse allerdings sind vielversprechend: So gelang es Forschern, das Bewegungsvermögen gelähmter Ratten mit Hilfe von Stammzellen zu verbessern. Und auch Parkinsonsymptome konnten sie lindern.
MEHR ÜBER...
Embryonale Stammzellen Querschnittslähmung Parkinson Diabetes Geron Stammzellforschung
zu SPIEGEL WISSEN Stammzellforscher verweisen immer wieder darauf, dass noch viele Fragen und Risiken bei dem Einsatz von Stammzellen ungeklärt sind. "Es ist nicht ausgeschlossen, dass die Stammzellen Krebs hervorrufen", warnte Jürgen Hescheler, Präsident der Deutschen Gesellschaft für Stammzellforschung, im Gespräch mit SPIEGEL ONLINE. Es sei auch möglich, dass sich die Zellen am Einsatzort zu einem unerwünschten Gewebetyp entwickelten. Und auch Stojkovic bestätigt: "Die Stammzellen könnten nicht komplett differenziert sein, es könnten sich Tumoren entwickeln." Adulte Stammzellen hingegen werden schon am Menschen eingesetzt, beispielsweise bei der Behandlung von Blut- und Herzerkrankungen.
"Es ist ein Meilenstein und ein Durchbruch für die Stammzellforschung", kommentierte Ed Baetge die Genehmigung. Baetge ist Leiter der Forschungsabteilung der US-Biotech-Firma Novocell, die eine Stammzell-Studie an Diabetes-Patienten plant. Die Firma gilt weltweit als führender Hersteller embryonaler Stammzell-Linien
7 Dollar bei hohem Volumen

Antwort auf Beitrag Nr.: 36.436.901 von meislo am 23.01.09 16:13:58Super!
Charttechnisch auch ausgebrochen! neues 52 Wochen Hoch!
auch im Weekly interessant!
Da wird sich einiges machen! Leider ist meine Kauforder heute Mittag nicht mehr bedient worden!
Hatte das Limit zu knapp gesetzt 4,37... naja, was solls...
Charttechnisch auch ausgebrochen! neues 52 Wochen Hoch!
auch im Weekly interessant!
Da wird sich einiges machen! Leider ist meine Kauforder heute Mittag nicht mehr bedient worden!

Hatte das Limit zu knapp gesetzt 4,37... naja, was solls...
Hallo allerseits,
ich melde mich nach langer Zeit hier mal wieder auf dem Board zurück.
Seit einem halben Jahr bin ich an Geron investiert, und seit dem totalen Ausbruch der Finanzkrise sind Geron und Aastrom meine einzigen Werte im Depot, da ich keinen anderen Unternehmen ähnliche positive Zukunftsaussichten zugestehe.
Aber das heute sollte nur der Anfang sein, immerhin entsteht hier eine der IT Industrie vergleichbare Branche.
Wo steht wohl erst der Kurs der Geron-Aktie, wenn die Injektionen von Stammzellen ähnliche Ergebnisse wie an Mäusen zeigen?
Ich war noch nie in Kalifornien, ob es hinbekomme das Arnie
mir mal die Hand bricht ?
?
Bei Dr. O. und seinen Mäusen würde ich natürlich auch mal vorbeischauen.
Grüsse, an alle anderen Geron Fans,
Golden_Star
ich melde mich nach langer Zeit hier mal wieder auf dem Board zurück.
Seit einem halben Jahr bin ich an Geron investiert, und seit dem totalen Ausbruch der Finanzkrise sind Geron und Aastrom meine einzigen Werte im Depot, da ich keinen anderen Unternehmen ähnliche positive Zukunftsaussichten zugestehe.
Aber das heute sollte nur der Anfang sein, immerhin entsteht hier eine der IT Industrie vergleichbare Branche.
Wo steht wohl erst der Kurs der Geron-Aktie, wenn die Injektionen von Stammzellen ähnliche Ergebnisse wie an Mäusen zeigen?
Ich war noch nie in Kalifornien, ob es hinbekomme das Arnie
mir mal die Hand bricht
 ?
?Bei Dr. O. und seinen Mäusen würde ich natürlich auch mal vorbeischauen.
Grüsse, an alle anderen Geron Fans,
Golden_Star
der Aktionär:
Geron: Kursfeuerwerk bei Stammzellen-Aktien
Frank Phillipps
Geron darf erstmals Therapien auf Basis embryonaler Stammzellen am Menschen testen. Mediziner träumen von revolutionären Therapien, Aktionäre von exorbitanten Kurssprüngen. Zumindest Letztere kommen schon kurzfristig auf ihre Kosten.
Kurz nach Börseneröffnung in den USA notiert die Aktie von Geron über 30 Prozent im Plus. Und das aus gutem Grund: Die US-Gesundheitsbehörde FDA hat dem US-Unternehmen erlaubt, ein Medikament, das auf Basis embryonaler Stammzellen entwickelt wurde, erstmals am Menschen zu testen. Im Sommer dieses Jahres sollen die Tests starten. Dann werden zehn querschnittsgelähmte Patienten mit Rückenmarkszellen behandelt, die aus embryonalen Stammzellen gezüchtet wurden. In der ersten Phase der Studien geht es darum, die Sicherheit der Arznei zu belegen und eine gesundheitliche Gefährdung der Patienten auszuschließen.
Auf den Marktführer setzen
Vom Geron-Erfolg profitierten auch die Papiere anderer Stammzellenforscher. So notiert etwa die ohnehin in den letzten Wochen sehr gut gelaufene Aktie von Stemcells ebenso deutlich im Plus wie der Anteilschein von Aastrom Biosciences. Favorit von DER AKTIONÄR ist eindeutig die Aktie von Geron. Das Unternehmen, das über ein weiteres Standbein in der Onkologie verfügt, ist unangefochtener Marktführer im Bereich der embryonalen Stammzellen und Stand bereits auf der Top-Empfehlungsliste des AKTIONÄRS für 2008. Da die Erlaubnis für die Tests am Menschen nun etwas später kam als gedacht und das Papier in den Strudel der Finanzkrise geriet, wurde die Aktie zwischenzeitlich ausgestoppt.
Geduld und Mut gefragt
Wer in Geron investiert, sollte jedoch bedenken, dass die Therapien auf Stammzellen-Basis noch in den Kinderschuhen stecken und noch Jahre von einer möglichen Zulassung entfernt sind. Zudem haben sich die Aktien aus diesem Bereich in den letzten Jahren als extrem volatil erwiesen. Anleger, die sich bei Geron engagieren sollten dementsprechend über einen langfristigen Investitionshorizont verfügen und gute Nerven mitbringen.
Geron: Kursfeuerwerk bei Stammzellen-Aktien
Frank Phillipps
Geron darf erstmals Therapien auf Basis embryonaler Stammzellen am Menschen testen. Mediziner träumen von revolutionären Therapien, Aktionäre von exorbitanten Kurssprüngen. Zumindest Letztere kommen schon kurzfristig auf ihre Kosten.
Kurz nach Börseneröffnung in den USA notiert die Aktie von Geron über 30 Prozent im Plus. Und das aus gutem Grund: Die US-Gesundheitsbehörde FDA hat dem US-Unternehmen erlaubt, ein Medikament, das auf Basis embryonaler Stammzellen entwickelt wurde, erstmals am Menschen zu testen. Im Sommer dieses Jahres sollen die Tests starten. Dann werden zehn querschnittsgelähmte Patienten mit Rückenmarkszellen behandelt, die aus embryonalen Stammzellen gezüchtet wurden. In der ersten Phase der Studien geht es darum, die Sicherheit der Arznei zu belegen und eine gesundheitliche Gefährdung der Patienten auszuschließen.
Auf den Marktführer setzen
Vom Geron-Erfolg profitierten auch die Papiere anderer Stammzellenforscher. So notiert etwa die ohnehin in den letzten Wochen sehr gut gelaufene Aktie von Stemcells ebenso deutlich im Plus wie der Anteilschein von Aastrom Biosciences. Favorit von DER AKTIONÄR ist eindeutig die Aktie von Geron. Das Unternehmen, das über ein weiteres Standbein in der Onkologie verfügt, ist unangefochtener Marktführer im Bereich der embryonalen Stammzellen und Stand bereits auf der Top-Empfehlungsliste des AKTIONÄRS für 2008. Da die Erlaubnis für die Tests am Menschen nun etwas später kam als gedacht und das Papier in den Strudel der Finanzkrise geriet, wurde die Aktie zwischenzeitlich ausgestoppt.
Geduld und Mut gefragt
Wer in Geron investiert, sollte jedoch bedenken, dass die Therapien auf Stammzellen-Basis noch in den Kinderschuhen stecken und noch Jahre von einer möglichen Zulassung entfernt sind. Zudem haben sich die Aktien aus diesem Bereich in den letzten Jahren als extrem volatil erwiesen. Anleger, die sich bei Geron engagieren sollten dementsprechend über einen langfristigen Investitionshorizont verfügen und gute Nerven mitbringen.
7,30 +40%

Antwort auf Beitrag Nr.: 36.437.373 von meislo am 23.01.09 16:49:54RT 7,86 USD
Ask ist leergekauft...
Ask ist leergekauft...
Antwort auf Beitrag Nr.: 36.437.446 von Sugar2000 am 23.01.09 16:55:598,08 USD
Antwort auf Beitrag Nr.: 36.437.472 von Sugar2000 am 23.01.09 16:57:56Wenn Sie über 8 schliesst ist das ja nicht schlecht
fürs erste
fürs erste

Kann hier einer mal nen Live-Chart rein stellen. Denke wir gehen heute noch locker über 10,00 Dollar.
Antwort auf Beitrag Nr.: 36.437.607 von Trader28 am 23.01.09 17:08:44dann muss aber der Gesamtmarkt mitspielen...
in den ersten 90 Handelsminuten liegt das Volumen 25-fach über dem Durchschnitt!
Hier siehst du die Liveanzeige
aber nicht als chart
http://finance.yahoo.com/q?s=GERN
Mehr als 20 Mio Aktien gehandelt.
Da stört das Gap nicht
aber nicht als chart
http://finance.yahoo.com/q?s=GERN
Mehr als 20 Mio Aktien gehandelt.
Da stört das Gap nicht

Interview mit Okarma
http://www.cnbc.com/id/15840232?video=1010671493
http://www.cnbc.com/id/15840232?video=1010671493
8 Mio Aktien sind noch short und müssten gecovert werden...
Antwort auf Beitrag Nr.: 36.438.099 von Sugar2000 am 23.01.09 17:45:00Denen brennt der Arsch heute

Es wird immer mehr darüber berichtet
Hoffnung für Gelähmte
USA genehmigt Stammzelltherapie am Menschen
Wenige Stunden nach Barack Obamas Amtseid dürfen zehn Querschnittsgelähmte in den USA erstmals mit embryonalen Stammzellen behandelt werden: Damit soll die Frage geklärt werden, ob die von Embryonen gewonnenen Zellen tatsächlich Lähmungen rückgängig machen können.
Der ehemalige "Superman"-Darsteller Christopher Reeve (r.) hatte nach einem Reitunfall lange auf eine Stammzellentherapie gehofft und dafür Spenden gesammelt. Im Jahr 2004 starb der querschnittsgelähmte Hollywoodstar (l.) im Alter von 52 Jahren, ohne dass sein Traum in Erfüllung ging
Der praktizierende Christ George W. Bush hatte in seiner Präsidentschaftszeit die Forschung an menschlichen embryonalen Stammzellen, die der Grundbaustein für die mehr als 200 Zellarten im menschlichen Körper sind – streng reglementiert. Denn bei der Gewinnung der Stammzellen werden schließlich Embryonen zerstört, aus denen sich ein menschliches Lebewesen hätte entwickeln können. Auch in Deutschland ist die Forschung mit embryonalen Stammzellen ethisch umstritten. Hierzulande erlaubt die Stichtagsregelung, dass nur mit ganz bestimmten, im Ausland vor einem bestimmten Stichtag gewonnene Stammzellen gearbeitet werden darf. In den USA hatte der frühere Präsident George W. Bush die staatliche Förderung dieser Forschung schlicht per Dekret ausgehebelt.
Forschung mit Stammzellen aus der Haut noch einfacher Es ist jetzt ein Akt von großer Symbolik, dass die amerikanische Gesundheitsbehörde FDA just einen Tag nach dem Amtsantritt von Präsident Barack Obama grünes Licht für die klinische Anwendung einer umstrittenen Stammzelltherapie gegeben. Sie erlaubte der Biotechfirma Geron in Menlo Park bei San Francisco, erstmals in der Medizingeschichte ein Zellprodukt an Patienten zu testen, das aus menschlichen embryonalen Stammzellen gewonnen wird. Es handelt sich um sogenannte oligodendrogliale Progenitorzellen (GRNOPC1), die gelähmte Patienten mit Verletzungen des Rückenmarks heilen sollen.
Obgleich diese Entscheidung der FDA lediglich der Auftakt zur ersten klinischen Studienphase ist, kommt sie einem Signal für den wissenschaftlichen und politischen Aufbruch in den USA gleich. Geron hatte nach jahrelanger Grundlagenforschung bereits im März 2008 den Zulassungsantrag bei der FDA eingereicht, der mit 21000 Seiten der umfangreichste in der Geschichte der Behörde sein dürfte. Teil dieses Antrags waren 24 Studien mit Tausenden Labortieren, bei denen insgesamt mehr als fünf Milliarden GRNOPC1-Zellen zum Einsatz gekommen waren.
Im Mai 2008 hatte die FDA diesen Antrag mit dem Vermerk „clinical hold“ versehen, ihn also vorerst ausgebremst. Da das Weiße Haus die Behörde politisch beeinflusst, war in der Amtszeit von GeorgeW. Bush die Forschung mit embryonalen Stammzellen immer wieder blockiert worden. Zu den Kritikern der Stammzell-Politik Bushs gehörten und gehören seit Jahren zahlreiche Wissenschaftler und nicht wenige Nobelpreisträger – und auch der im Jahr 2004 verstorbene US-Schauspieler Christopher Reeve, der durch seine Rolle im Film „Superman“ berühmt gewordenist. Reeve war nach einem Reitunfall 1995 querschnittsgelähmt und hatte sich bis zu seinem Tod vehement für die Erforschung und Nutzung embryonaler Stammzellen eingesetzt.
Vor diesem Hintergrund ist die Entscheidung der FDA, die fast auf den Tag genau mit dem Ende der Bush-Ära korrespondiert, von enormer politischer Tragweite. Obama selbst hat in den vergangenen Monaten immer wieder betont, die US-Stammzellforschung von ihrem staatlichen Korsett befreien und finanziell fördern zu wollen.
Die Stammzellen, die Geron zur Erzeugung von GRNOPC1 einsetzt, stammen aus einer Linie, die vor dem 9. August 2001 angelegt wurde.
Die wissenschaftliche Seite des FDA-Votums ist ebenso komplex wie revolutionär. Bei GRNOPC1 handelt es sich um sogenannte Gliazellen, die die Nervenzellen im Rückenmark gewissermaßen isolieren und damit erst – analog zur Gummiisolierung eines Kupferkabels – die Signalübermittlung ermöglichen. Sterben diese Gliazellen nach einer Verletzung ab, ist die Übertragung von Nervensignalen unterbrochen. Die Folgen sind unter anderem eine Lähmung der Gliedmaßen und ein Kontrollverlust der Blasenfunktion. Gerons „Ersatzzellen“ sollen Patienten in „bis zu sieben“ Kliniken in den USA ein bis zwei Wochen nach einer Verletzung direkt ins Rückenmark injiziert werden.
Ein Risiko besteht darin, dass die Verabreichung von GRNOPC1 zu unerwünschten Wucherungen, sogenannten Teratomen, führen könnte. Bislang ist dies jedoch bei keinem Versuchstier beobachtet worden. Es gibt auch keine Hinweise darauf, dass die Injektion des Stammzell-Produkts zu anderen gefährlichen Nebenwirkungen führt oder die Sterblichkeit erhöht. Alle Studien deuten darauf hin, dass das Immunsystem die injizierten Stammzellen nicht als „fremd“ erkennt. Medikamente, die eine Abstoßung verhindern, werden daher voraussichtlich nur in geringen Dosen zum Einsatz kommen.
Im Tierversuch überbrückten die injizierten GRNOPC1-Zellen die Verletzung im Rückenmark und sorgten dafür, dass nach und nach wieder Nervensignale übertragen werden. Die Geron-Forscher gelang ist, rund 2000 gelähmte Ratten mit Hilfe embryonaler Stammzellen wieder laufen zu lassen.
Die FDA-Entscheidung „markiert den Anfang eines möglicherweise neuen Kapitels in der therapeutischen Medizin“, sagte Okarma – eines Kapitels, „das über Pillen hinausgeht hin zu einem neuen Heilungsansatz: der Wiederherstellung von Organ- und Gewebefunktion durch die Injizierung von gesunden Ersatzzellen“.
Neben GRNOPC1 entwickelt Geron weitere Stammzellprodukte, die in einigen Jahren zur Behandlung von Diabetes, Herzmuskelschwäche sowie Knochenerkrankungen zum Einsatz kommen sollen. Darüber hinaus ist es in der Telomerase-Forschung führend. Telomerase ist ein Zellenzym, das sowohl bei der Alterung gesunder Zellen als auch bei der Entstehung von Tumoren und Tochtergeschwülsten (Metastasen) eine wichtige – möglicherweise sogar eine entscheidende – Rolle spielt. Der Aktienkurs von Geron stieg gestern um 50 Prozent.
Hoffnung für Gelähmte
USA genehmigt Stammzelltherapie am Menschen
Wenige Stunden nach Barack Obamas Amtseid dürfen zehn Querschnittsgelähmte in den USA erstmals mit embryonalen Stammzellen behandelt werden: Damit soll die Frage geklärt werden, ob die von Embryonen gewonnenen Zellen tatsächlich Lähmungen rückgängig machen können.
Der ehemalige "Superman"-Darsteller Christopher Reeve (r.) hatte nach einem Reitunfall lange auf eine Stammzellentherapie gehofft und dafür Spenden gesammelt. Im Jahr 2004 starb der querschnittsgelähmte Hollywoodstar (l.) im Alter von 52 Jahren, ohne dass sein Traum in Erfüllung ging
Der praktizierende Christ George W. Bush hatte in seiner Präsidentschaftszeit die Forschung an menschlichen embryonalen Stammzellen, die der Grundbaustein für die mehr als 200 Zellarten im menschlichen Körper sind – streng reglementiert. Denn bei der Gewinnung der Stammzellen werden schließlich Embryonen zerstört, aus denen sich ein menschliches Lebewesen hätte entwickeln können. Auch in Deutschland ist die Forschung mit embryonalen Stammzellen ethisch umstritten. Hierzulande erlaubt die Stichtagsregelung, dass nur mit ganz bestimmten, im Ausland vor einem bestimmten Stichtag gewonnene Stammzellen gearbeitet werden darf. In den USA hatte der frühere Präsident George W. Bush die staatliche Förderung dieser Forschung schlicht per Dekret ausgehebelt.
Forschung mit Stammzellen aus der Haut noch einfacher Es ist jetzt ein Akt von großer Symbolik, dass die amerikanische Gesundheitsbehörde FDA just einen Tag nach dem Amtsantritt von Präsident Barack Obama grünes Licht für die klinische Anwendung einer umstrittenen Stammzelltherapie gegeben. Sie erlaubte der Biotechfirma Geron in Menlo Park bei San Francisco, erstmals in der Medizingeschichte ein Zellprodukt an Patienten zu testen, das aus menschlichen embryonalen Stammzellen gewonnen wird. Es handelt sich um sogenannte oligodendrogliale Progenitorzellen (GRNOPC1), die gelähmte Patienten mit Verletzungen des Rückenmarks heilen sollen.
Obgleich diese Entscheidung der FDA lediglich der Auftakt zur ersten klinischen Studienphase ist, kommt sie einem Signal für den wissenschaftlichen und politischen Aufbruch in den USA gleich. Geron hatte nach jahrelanger Grundlagenforschung bereits im März 2008 den Zulassungsantrag bei der FDA eingereicht, der mit 21000 Seiten der umfangreichste in der Geschichte der Behörde sein dürfte. Teil dieses Antrags waren 24 Studien mit Tausenden Labortieren, bei denen insgesamt mehr als fünf Milliarden GRNOPC1-Zellen zum Einsatz gekommen waren.
Im Mai 2008 hatte die FDA diesen Antrag mit dem Vermerk „clinical hold“ versehen, ihn also vorerst ausgebremst. Da das Weiße Haus die Behörde politisch beeinflusst, war in der Amtszeit von GeorgeW. Bush die Forschung mit embryonalen Stammzellen immer wieder blockiert worden. Zu den Kritikern der Stammzell-Politik Bushs gehörten und gehören seit Jahren zahlreiche Wissenschaftler und nicht wenige Nobelpreisträger – und auch der im Jahr 2004 verstorbene US-Schauspieler Christopher Reeve, der durch seine Rolle im Film „Superman“ berühmt gewordenist. Reeve war nach einem Reitunfall 1995 querschnittsgelähmt und hatte sich bis zu seinem Tod vehement für die Erforschung und Nutzung embryonaler Stammzellen eingesetzt.
Vor diesem Hintergrund ist die Entscheidung der FDA, die fast auf den Tag genau mit dem Ende der Bush-Ära korrespondiert, von enormer politischer Tragweite. Obama selbst hat in den vergangenen Monaten immer wieder betont, die US-Stammzellforschung von ihrem staatlichen Korsett befreien und finanziell fördern zu wollen.
Die Stammzellen, die Geron zur Erzeugung von GRNOPC1 einsetzt, stammen aus einer Linie, die vor dem 9. August 2001 angelegt wurde.
Die wissenschaftliche Seite des FDA-Votums ist ebenso komplex wie revolutionär. Bei GRNOPC1 handelt es sich um sogenannte Gliazellen, die die Nervenzellen im Rückenmark gewissermaßen isolieren und damit erst – analog zur Gummiisolierung eines Kupferkabels – die Signalübermittlung ermöglichen. Sterben diese Gliazellen nach einer Verletzung ab, ist die Übertragung von Nervensignalen unterbrochen. Die Folgen sind unter anderem eine Lähmung der Gliedmaßen und ein Kontrollverlust der Blasenfunktion. Gerons „Ersatzzellen“ sollen Patienten in „bis zu sieben“ Kliniken in den USA ein bis zwei Wochen nach einer Verletzung direkt ins Rückenmark injiziert werden.
Ein Risiko besteht darin, dass die Verabreichung von GRNOPC1 zu unerwünschten Wucherungen, sogenannten Teratomen, führen könnte. Bislang ist dies jedoch bei keinem Versuchstier beobachtet worden. Es gibt auch keine Hinweise darauf, dass die Injektion des Stammzell-Produkts zu anderen gefährlichen Nebenwirkungen führt oder die Sterblichkeit erhöht. Alle Studien deuten darauf hin, dass das Immunsystem die injizierten Stammzellen nicht als „fremd“ erkennt. Medikamente, die eine Abstoßung verhindern, werden daher voraussichtlich nur in geringen Dosen zum Einsatz kommen.
Im Tierversuch überbrückten die injizierten GRNOPC1-Zellen die Verletzung im Rückenmark und sorgten dafür, dass nach und nach wieder Nervensignale übertragen werden. Die Geron-Forscher gelang ist, rund 2000 gelähmte Ratten mit Hilfe embryonaler Stammzellen wieder laufen zu lassen.
Die FDA-Entscheidung „markiert den Anfang eines möglicherweise neuen Kapitels in der therapeutischen Medizin“, sagte Okarma – eines Kapitels, „das über Pillen hinausgeht hin zu einem neuen Heilungsansatz: der Wiederherstellung von Organ- und Gewebefunktion durch die Injizierung von gesunden Ersatzzellen“.
Neben GRNOPC1 entwickelt Geron weitere Stammzellprodukte, die in einigen Jahren zur Behandlung von Diabetes, Herzmuskelschwäche sowie Knochenerkrankungen zum Einsatz kommen sollen. Darüber hinaus ist es in der Telomerase-Forschung führend. Telomerase ist ein Zellenzym, das sowohl bei der Alterung gesunder Zellen als auch bei der Entstehung von Tumoren und Tochtergeschwülsten (Metastasen) eine wichtige – möglicherweise sogar eine entscheidende – Rolle spielt. Der Aktienkurs von Geron stieg gestern um 50 Prozent.
von reuters...
UPDATE 2-US FDA allows first test of human stem cell therapy
Fri Jan 23, 2009 8:30am EST
(Adds reaction, analyst comment)
WASHINGTON, Jan 23 (Reuters) - The U.S. Food and Drug Administration has cleared the way for the world's first study of human embryonic stem cell therapy, Geron Corp (GERN.O: Quote, Profile, Research, Stock Buzz) said on Friday.
The California biotechnology company plans to start a clinical trial to try to use the stem cells to regrow nerve tissue in patients with acute spinal cord injury.
"This marks the beginning of what is potentially a new chapter in medical therapeutics -- one that reaches beyond pills to a new level of healing: the restoration of organ and tissue function achieved by the injection of healthy replacement cells," Geron Chief Executive Thomas Okarma said in a statement.
Shares of Geron rose nearly 30 percent to $6.75 in premarket electronic trading on Nasdaq.
The FDA rejected his company's first request to conduct the trial of GRNOPC1, Oligodendroglial Progenitor Cells. It put the trial on hold in May.
"If GRNOPC1 eventually does become the first human Embryonic Stem Cell drug to receive an approved Biologic License Application it could be as important to drug therapy as the discovery of Salvarsan or penicillin," drug analysts Stephen Brozak and Daniel Mallin of WBB Securities LLC said in a statement.
Salvarssan was the first modern drug, used to treat syphilis early in the last century.
Joel Sendek of Lazard Capital Markets was cautious, saying he was recommending a hold in Geron shares. "Cellular-based therapies carry substantially more regulatory risk than do traditional small-molecule drugs or protein therapeutics," he said.
AT ODDS
Former President George W. Bush had been at odds with Congress, researchers and advocates for years over the issue and by executive order restricted federal funding of work involving human embryonic stem cells.
President Barack Obama, who succeeded Bush on Tuesday, had been widely expected to rescind that directive. Although the FDA says it does not make decisions based on politics, the company made the decision public just days after Obama was sworn into office.
Stem cells are the body's master cells, giving rise to all the tissues, organs and blood. Embryonic stem cells are considered the most powerful kinds of stem cells, as they have the potential to give rise to any type of tissue.
But they are difficult to make, requiring the use of an embryo or cloning technology. Geron and some other companies have been pursuing the goal without the use of federal funds.
Advocates say stem cell-related research could lead to a whole new field of regenerative medicine, in which patients could get transplants and treatments for Parkinson's, juvenile diabetes, cancer, injuries and a range of other ills.
"If safe and effective, the therapy would provide a viable treatment option for thousands of patients who suffer severe spinal cord injuries each year," Richard Fessler, professor of neurological surgery at the Feinberg School of Medicine at Northwestern University said in a statement.
"There has been so much speculative and unsubstantiated information about the use of stem cells in spinal cord injury; it is important to study these cells in a rigorously designed clinical trial that is monitored by the FDA," said Peter Wilderotter, president and CEO of the Christopher & Dana Reeve Foundation.
Actor Christopher Reeve died in 2004 after having broken his spine years earlier in a horseback riding accident and was a vocal advocate of embryonic stem cell research.
(Writing by Doina Chiacu and Maggie Fox; Additional reporting by Toni Clarke in Boston; Editing by Vicki Allen)
© Thomson Reuters 2008. All rights reserved. Users may download and print extracts of content from this website for their own personal and non-commercial use only. Republication or redistribution of Thomson Reuters content, including by framing or similar means, is expressly prohibited without the prior written consent of Thomson Reuters. Thomson Reuters and its logo are registered trademarks or trademarks of the Thomson Reuters group of companies around the world.
UPDATE 2-US FDA allows first test of human stem cell therapy
Fri Jan 23, 2009 8:30am EST
(Adds reaction, analyst comment)
WASHINGTON, Jan 23 (Reuters) - The U.S. Food and Drug Administration has cleared the way for the world's first study of human embryonic stem cell therapy, Geron Corp (GERN.O: Quote, Profile, Research, Stock Buzz) said on Friday.
The California biotechnology company plans to start a clinical trial to try to use the stem cells to regrow nerve tissue in patients with acute spinal cord injury.
"This marks the beginning of what is potentially a new chapter in medical therapeutics -- one that reaches beyond pills to a new level of healing: the restoration of organ and tissue function achieved by the injection of healthy replacement cells," Geron Chief Executive Thomas Okarma said in a statement.
Shares of Geron rose nearly 30 percent to $6.75 in premarket electronic trading on Nasdaq.
The FDA rejected his company's first request to conduct the trial of GRNOPC1, Oligodendroglial Progenitor Cells. It put the trial on hold in May.
"If GRNOPC1 eventually does become the first human Embryonic Stem Cell drug to receive an approved Biologic License Application it could be as important to drug therapy as the discovery of Salvarsan or penicillin," drug analysts Stephen Brozak and Daniel Mallin of WBB Securities LLC said in a statement.
Salvarssan was the first modern drug, used to treat syphilis early in the last century.
Joel Sendek of Lazard Capital Markets was cautious, saying he was recommending a hold in Geron shares. "Cellular-based therapies carry substantially more regulatory risk than do traditional small-molecule drugs or protein therapeutics," he said.
AT ODDS
Former President George W. Bush had been at odds with Congress, researchers and advocates for years over the issue and by executive order restricted federal funding of work involving human embryonic stem cells.
President Barack Obama, who succeeded Bush on Tuesday, had been widely expected to rescind that directive. Although the FDA says it does not make decisions based on politics, the company made the decision public just days after Obama was sworn into office.
Stem cells are the body's master cells, giving rise to all the tissues, organs and blood. Embryonic stem cells are considered the most powerful kinds of stem cells, as they have the potential to give rise to any type of tissue.
But they are difficult to make, requiring the use of an embryo or cloning technology. Geron and some other companies have been pursuing the goal without the use of federal funds.
Advocates say stem cell-related research could lead to a whole new field of regenerative medicine, in which patients could get transplants and treatments for Parkinson's, juvenile diabetes, cancer, injuries and a range of other ills.
"If safe and effective, the therapy would provide a viable treatment option for thousands of patients who suffer severe spinal cord injuries each year," Richard Fessler, professor of neurological surgery at the Feinberg School of Medicine at Northwestern University said in a statement.
"There has been so much speculative and unsubstantiated information about the use of stem cells in spinal cord injury; it is important to study these cells in a rigorously designed clinical trial that is monitored by the FDA," said Peter Wilderotter, president and CEO of the Christopher & Dana Reeve Foundation.
Actor Christopher Reeve died in 2004 after having broken his spine years earlier in a horseback riding accident and was a vocal advocate of embryonic stem cell research.
(Writing by Doina Chiacu and Maggie Fox; Additional reporting by Toni Clarke in Boston; Editing by Vicki Allen)
© Thomson Reuters 2008. All rights reserved. Users may download and print extracts of content from this website for their own personal and non-commercial use only. Republication or redistribution of Thomson Reuters content, including by framing or similar means, is expressly prohibited without the prior written consent of Thomson Reuters. Thomson Reuters and its logo are registered trademarks or trademarks of the Thomson Reuters group of companies around the world.
Stammzelltherapien
Stammzellen für Gelähmte
Von Joachim Müller-Jung
DruckenVersendenSpeichernVorherige Seite
Entnahme einer einzelnen Zelle aus einem Embryo im Frühstadium
23. Januar 2009 Möglicherweise ist es gar nicht der weltweit erste Behandlungsversuch mit embryonalen Stammzellen an Menschen, sehr wahrscheinlich sogar hat es in weniger reglementierten Ländern wie China schon Experimente an schwer kranken Patienten gegeben. Unbestritten aber ist die klinische Studie der kalifornischen Firma Geron, die jetzt offensichtlich von der amerikanischen Zulassungsbehörde FDA genehmigt worden ist, der erste offizielle und von vielen lange erwartete Therapieversuch.
Die Mitteilung über die Zulassung durch die Pressestelle der kalifornischen Firma jedenfalls ist gezeichnet von der Erleichterung, endlich eine der biopolitisch umstrittensten medizinischen Techniken in die Klinik zu bringen. Genehmigt worden ist der Versuch, an wenigen Patienten mit schweren Rückenmarkverletzungen - die Rede ist von acht bis zehn - die Sicherheit der aus embryonalen Stammzellen hergestellten Nervenersatzzellen zu testen. Dabei handelt es sich um rückenmarksgeschädigte, aber nicht vollständig querschnittgelähmten Patienten. Solche Patienten sollen erst in späteren klinischen Studien mit den Zellen behandelt werden. In dieser ersten Phase geht es zunächst nicht um einen Heilversuch. Aber die Auswahl der von den Wissenschaftlern gewählten klinischen Endpunkte zeigt, dass man sich einen möglicherweise sogar raschen therapeutischen Effekt verspricht.
Erprobung an Unfallopfern
Durchgeführt werden die Therapieversuche an einem halben Dutzend Kliniken im Land. In Frage kommen dabei erst einmal nur freiwillige Unfallopfer, die schwere Verletzungen der mittleren Brust- und Rückenwirbel (T3-T10) erlitten haben. Von acht bis zehn Versuchspersonen ist die Rede. Ihnen werden nach Einwilligung ein bis zwei Wochen nach der Rückenmarksverletzung Vorläufer von spezialisierten Nervenzellen, sogenannten Oligodendrozyten, ins Rückenmark injiziert. Diese Vorläufer hat man in den Labors von Geron aus einer Stammzelllinie H1 gewonnen, die bereits vor acht Jahren erzeugt und unter der restriktiven Stammzellpolitik der Bush-Regierung auch offiziell genehmigt und registriert worden war. Die Stammzellen waren als Ressource für zahlreiche Tierexperimente in den vergangenen Jahren schon genutzt worden. Unter anderem hat Geron nach eigenen Angaben daraus fünf Milliarden Nervenzellvorläufer erzeugt, die für die 24 vorklinischen Tierversuche genutzt wurden.
Diese Ergebnisse waren Grundlage für die Zulassungsentscheidung der FDA. In dem 21.000-seitigen Antrag wurde etwa gezeigt, dass die injizierten Stammzellabkömmlinge an der verletzten Stelle des Rückenmarks das Überleben der Nervenzellverbindungen verbesserte und die zur Heilung notwendige Isolierung der Nervenzellausläufer - zur Erneuerung der Myelinscheiden - ermöglichte. Das Loch im Rückenmark, das sich nach der Verletzung gebildet hatte, wurde durch die einwandernden Oligodendrozyten-Vorläufer gefüllt. Zwischen den durchtrennten Enden bildeten sich schon nach einem Dreivierteljahr neue Nervenverbindungen.
Nach Bush
Wie gesagt: Alles bisher nur im Tierversuch, und niemand kann sagen, ob dieser Ansatz beim Menschen den gleichen Effekt hat. Jedenfalls waren die so behandelten akut querschnittgelähmten Ratten etwa wieder in der Lage, anschließend auch ihre Hinterbeine wieder einzusetzen - wenn auch keineswegs wieder völlig störungsfrei. Im Jahr 2007 waren die entscheidenden Tierstudien von Wissenschaftlern der Firma in der Zeitschrift „Journal of Neuroscience“ veröffentlicht worden. Kurze Zeit später wurden die Zulassungsanträge für Transplantationsversuche mit der Oligodendrozyten-Kultur Nr. GRNOPC1 gestellt. Präsident Bush allerdings hatte stets klar gemacht, dass er Menschenversuche mit embryonalen Stammzellen nicht dulden wolle.
Weil diese Stammzellen aus bis zu zwei Wochen alten und einhundert bis zweihundert Zellen großen Embryonen gewonnen wurden, die aus Reproduktionskliniken stammten, hatte Bush stets religiöse und ethische Bedenken angemeldet und eine restriktive Stammzellpolitik im Land durchgesetzt. Die galt allerdings nur für die Finanzierung von Projekten an staatlichen Instituten. Die freie Wirtschaft war viel freier, konnte aber auf die für solche Studien nötige finanzielle und personelle Unterstützung an den großen Kliniken kaum rechnen.
Eine angekündigte Wende in der Stammzellpolitik
Dass die Zulassung für Geron nun ausgerechnet wenige Tage nach dem Ende der Bush-Ära eintrifft, halten viele Beobachter für keinen Zufall. Das Geron-Management streitet zwar ab, dass man behindert worden oder der Genehmigungsprozess verschleppt worden sei. Sicher aber ist, dass der neue Präsident Obama schon während des Wahlkampfes eine Änderung der Stammzellpolitik angekündigt und den Befürwortern der embryonalen Stammzellforschung seine Unterstützung zugesagt hatte.
Geron selbst war in der Bush-Ära durchaus schon in finanzielle Schwierigkeiten geraten und drohte gelegentlich, die aufwändige Forschung zu verlassen. Nun rüstet sich offenbar Thomas Okarma, der Vorstandschef der Biotechnik-Firma Geron in Menlo Park, für eine möglicherweise neue Ära der regenerativen Medizin: „Unsere Stammzellbank könnte genügend Material für die kommerzielle Herstellung von GRNOPC1 liefern, um damit den gesamten amerikanischen Markt für Querschnittverletzungen zu decken.“
Ob Geron allerdings überhaupt in diese günstige Lage kommt, müssen erst die Patientenversuche zeigen. Es wäre nicht das erste Mal - speziell bei biologisch hergestellten Medikamenten und Zellpräparaten -, dass man in Versuchen an Patienten andere oder jedenfalls nicht dieselben erwünschten Therapiewirkungen wie bei Versuchstieren feststellt. Schließlich gilt es als Erstes auch zu klären, wie es um das Risiko steht, dass die transplantierten Nervenzell-Vorläufer entarten und möglicherweise Tumore bilden. In den Experimenten mit Nagern hat man zwar nach einem Jahr keinerlei Geschwülste entdeckt. Aber auch hier gilt: Ratte ist Ratte, Mensch ist Mensch.
Text: FAZ.NET
Bildmaterial: dpa
Stammzellen für Gelähmte
Von Joachim Müller-Jung
DruckenVersendenSpeichernVorherige Seite
Entnahme einer einzelnen Zelle aus einem Embryo im Frühstadium
23. Januar 2009 Möglicherweise ist es gar nicht der weltweit erste Behandlungsversuch mit embryonalen Stammzellen an Menschen, sehr wahrscheinlich sogar hat es in weniger reglementierten Ländern wie China schon Experimente an schwer kranken Patienten gegeben. Unbestritten aber ist die klinische Studie der kalifornischen Firma Geron, die jetzt offensichtlich von der amerikanischen Zulassungsbehörde FDA genehmigt worden ist, der erste offizielle und von vielen lange erwartete Therapieversuch.
Die Mitteilung über die Zulassung durch die Pressestelle der kalifornischen Firma jedenfalls ist gezeichnet von der Erleichterung, endlich eine der biopolitisch umstrittensten medizinischen Techniken in die Klinik zu bringen. Genehmigt worden ist der Versuch, an wenigen Patienten mit schweren Rückenmarkverletzungen - die Rede ist von acht bis zehn - die Sicherheit der aus embryonalen Stammzellen hergestellten Nervenersatzzellen zu testen. Dabei handelt es sich um rückenmarksgeschädigte, aber nicht vollständig querschnittgelähmten Patienten. Solche Patienten sollen erst in späteren klinischen Studien mit den Zellen behandelt werden. In dieser ersten Phase geht es zunächst nicht um einen Heilversuch. Aber die Auswahl der von den Wissenschaftlern gewählten klinischen Endpunkte zeigt, dass man sich einen möglicherweise sogar raschen therapeutischen Effekt verspricht.
Erprobung an Unfallopfern
Durchgeführt werden die Therapieversuche an einem halben Dutzend Kliniken im Land. In Frage kommen dabei erst einmal nur freiwillige Unfallopfer, die schwere Verletzungen der mittleren Brust- und Rückenwirbel (T3-T10) erlitten haben. Von acht bis zehn Versuchspersonen ist die Rede. Ihnen werden nach Einwilligung ein bis zwei Wochen nach der Rückenmarksverletzung Vorläufer von spezialisierten Nervenzellen, sogenannten Oligodendrozyten, ins Rückenmark injiziert. Diese Vorläufer hat man in den Labors von Geron aus einer Stammzelllinie H1 gewonnen, die bereits vor acht Jahren erzeugt und unter der restriktiven Stammzellpolitik der Bush-Regierung auch offiziell genehmigt und registriert worden war. Die Stammzellen waren als Ressource für zahlreiche Tierexperimente in den vergangenen Jahren schon genutzt worden. Unter anderem hat Geron nach eigenen Angaben daraus fünf Milliarden Nervenzellvorläufer erzeugt, die für die 24 vorklinischen Tierversuche genutzt wurden.
Diese Ergebnisse waren Grundlage für die Zulassungsentscheidung der FDA. In dem 21.000-seitigen Antrag wurde etwa gezeigt, dass die injizierten Stammzellabkömmlinge an der verletzten Stelle des Rückenmarks das Überleben der Nervenzellverbindungen verbesserte und die zur Heilung notwendige Isolierung der Nervenzellausläufer - zur Erneuerung der Myelinscheiden - ermöglichte. Das Loch im Rückenmark, das sich nach der Verletzung gebildet hatte, wurde durch die einwandernden Oligodendrozyten-Vorläufer gefüllt. Zwischen den durchtrennten Enden bildeten sich schon nach einem Dreivierteljahr neue Nervenverbindungen.
Nach Bush
Wie gesagt: Alles bisher nur im Tierversuch, und niemand kann sagen, ob dieser Ansatz beim Menschen den gleichen Effekt hat. Jedenfalls waren die so behandelten akut querschnittgelähmten Ratten etwa wieder in der Lage, anschließend auch ihre Hinterbeine wieder einzusetzen - wenn auch keineswegs wieder völlig störungsfrei. Im Jahr 2007 waren die entscheidenden Tierstudien von Wissenschaftlern der Firma in der Zeitschrift „Journal of Neuroscience“ veröffentlicht worden. Kurze Zeit später wurden die Zulassungsanträge für Transplantationsversuche mit der Oligodendrozyten-Kultur Nr. GRNOPC1 gestellt. Präsident Bush allerdings hatte stets klar gemacht, dass er Menschenversuche mit embryonalen Stammzellen nicht dulden wolle.
Weil diese Stammzellen aus bis zu zwei Wochen alten und einhundert bis zweihundert Zellen großen Embryonen gewonnen wurden, die aus Reproduktionskliniken stammten, hatte Bush stets religiöse und ethische Bedenken angemeldet und eine restriktive Stammzellpolitik im Land durchgesetzt. Die galt allerdings nur für die Finanzierung von Projekten an staatlichen Instituten. Die freie Wirtschaft war viel freier, konnte aber auf die für solche Studien nötige finanzielle und personelle Unterstützung an den großen Kliniken kaum rechnen.
Eine angekündigte Wende in der Stammzellpolitik
Dass die Zulassung für Geron nun ausgerechnet wenige Tage nach dem Ende der Bush-Ära eintrifft, halten viele Beobachter für keinen Zufall. Das Geron-Management streitet zwar ab, dass man behindert worden oder der Genehmigungsprozess verschleppt worden sei. Sicher aber ist, dass der neue Präsident Obama schon während des Wahlkampfes eine Änderung der Stammzellpolitik angekündigt und den Befürwortern der embryonalen Stammzellforschung seine Unterstützung zugesagt hatte.
Geron selbst war in der Bush-Ära durchaus schon in finanzielle Schwierigkeiten geraten und drohte gelegentlich, die aufwändige Forschung zu verlassen. Nun rüstet sich offenbar Thomas Okarma, der Vorstandschef der Biotechnik-Firma Geron in Menlo Park, für eine möglicherweise neue Ära der regenerativen Medizin: „Unsere Stammzellbank könnte genügend Material für die kommerzielle Herstellung von GRNOPC1 liefern, um damit den gesamten amerikanischen Markt für Querschnittverletzungen zu decken.“
Ob Geron allerdings überhaupt in diese günstige Lage kommt, müssen erst die Patientenversuche zeigen. Es wäre nicht das erste Mal - speziell bei biologisch hergestellten Medikamenten und Zellpräparaten -, dass man in Versuchen an Patienten andere oder jedenfalls nicht dieselben erwünschten Therapiewirkungen wie bei Versuchstieren feststellt. Schließlich gilt es als Erstes auch zu klären, wie es um das Risiko steht, dass die transplantierten Nervenzell-Vorläufer entarten und möglicherweise Tumore bilden. In den Experimenten mit Nagern hat man zwar nach einem Jahr keinerlei Geschwülste entdeckt. Aber auch hier gilt: Ratte ist Ratte, Mensch ist Mensch.
Text: FAZ.NET
Bildmaterial: dpa
Eins dürfte klar sein
Es ist bestimmt kein Zufall dass die Genehmigung nur drei Tage nach der Ära Bush erteilt wurde. Die FDA wollte ein Zeichen setzten. Die wissenschaftliche Forschung und dazu zählen Stammzellen, insbesondere embryonale, haben nun auch in Amerika nach der Ära Bush wieder Zukunft. Dies kann auch als ein politisches Zeichen gewertet werden. Die Bushadministration galt als äusserst wissenschaftbehindernd und hat die wissenschaftliche Forschung massiv bekämpft. Nicht nur bei den Stammzellen.

Es ist bestimmt kein Zufall dass die Genehmigung nur drei Tage nach der Ära Bush erteilt wurde. Die FDA wollte ein Zeichen setzten. Die wissenschaftliche Forschung und dazu zählen Stammzellen, insbesondere embryonale, haben nun auch in Amerika nach der Ära Bush wieder Zukunft. Dies kann auch als ein politisches Zeichen gewertet werden. Die Bushadministration galt als äusserst wissenschaftbehindernd und hat die wissenschaftliche Forschung massiv bekämpft. Nicht nur bei den Stammzellen.

Antwort auf Beitrag Nr.: 36.438.806 von meislo am 23.01.09 18:53:36USA erlauben Stammzelltest an MenschenIn den Vereinigen Staaten ist eine Behandlung genehmigt worden, die auf menschlichen embryonalen Stammzellen basiert. Die weltweit erste Therapie dieser Art soll Querschnittslähmungen heilen. Hat der Machtwechsel in Washington die Genehmigung ermöglicht?
Anzeige
Von Hartmut Wewetzer
24.1.2009 0:00 Uhr Von Hartmut Wewetzer
24.1.2009 0:00 Uhr
Berlin - In den USA ist weltweit zum ersten Mal eine Behandlung genehmigt worden, die auf menschlichen embryo nalen Stammzellen basiert. Die Arzneimittelbehörde FDA erlaubte es der Biotechnik-Firma Geron, die Zelltherapie bei freiwilligen Versuchspersonen mit Querschnittslähmung einzusetzen. Das teilte das im kalifornischen Menlo ansässige Unternehmen am Freitag mit.
Embryonale Stammzellen gelten als „Alleskönner“. Sie können sich unter geeigneten Bedingungen in jedes beliebige Gewebe verwandeln. Mediziner hoffen, dass mit ihrer Hilfe eines Tages erkranktes oder zerstörtes Gewebe ersetzt werden kann, zum Beispiel bei der Zuckerkrankheit (Diabetes) oder der Schüttellähmung (Parkinson).
Weil die Stammzellen aus wenige Tage alten Embryonen gewonnen werden, ist die Therapie jedoch umstritten. In den USA hatte Präsident George W. Bush die Forschungsförderung aus Bundesmitteln blockiert. Dass nun kurz nach dem Amtswechsel die Behandlung erlaubt wurde, werten Beobachter als Zeichen dafür, dass die Aufsichtsbehörde unter politischem Druck der Bush-Regierung stand und deshalb die Genehmigung bisher nicht erteilen konnte.
Bei der Untersuchung, die im Sommer beginnen soll, handelt es sich um eine Phase-1-Studie. In diesem frühen Stadium geht es darum, zu prüfen, ob die Behandlung grundsätzlich sicher ist. Es ist vorgesehen, acht bis zehn Patienten mit einer Querschnittslähmung in Höhe des Brustkorbs zu behandeln. Die Verletzung darf nur sieben bis 14 Tage zurückliegen. Ist schon mehr Zeit verstrichen, ist die Zelltherapie möglicherweise nicht mehr wirksam. Die Patienten sollen Hüllzellen des Nervensystems bekommen, die aus embryonalen Stammzellen gezüchtet wurden. Diese Hüllzellen, Oligodendrozyten genannt, werden dorthin gespritzt, wo das aus Nervenfasern bestehende Rückenmark durchtrennt wurde. An Ort und Stelle sollen die Zellen das durchtrennte Nervenkabel reparieren, es wieder „zusammenschweißen“ und einhüllen. Im Tierversuch gelang es, Lähmungen zumindest teilweise rückgängig zu machen.
Embryonale Stammzellen haben ein erhebliches Wachstumspotenzial. Deshalb neigen sie dazu, Tumoren zu bilden. Diese sind zwar nicht so gefährlich wie herkömmliche Krebstumoren, stellen aber trotzdem ein erhebliches Risiko dar. Nach Angaben von Geron ist jedoch sichergestellt, dass die injizierten Zellen kein Tumorrisiko mehr besitzen. Außerdem müssen die Patienten Medikamente nehmen, um Abstoßungsreaktionen gegen die fremden Zellen zu unterdrücken.
Die Reaktionen der US-Wissenschaftler schwanken zwischen Hoffnung und Skepsis. So wird kritisiert, dass die Therapie möglicherweise noch nicht ausgereift sei und bei einem Fehlschlag die ganze Forschung in Misskredit bringen werde. „Das wäre ein Desaster, ein Albtraum“, sagte der Stammzellforscher John Kessler von der Northwestern University. In den vergangenen Jahren wurde zudem erfolgreich gezeigt, dass sich auch patienteneigenes Gewebe gentechnisch so umprogrammieren lässt, dass es embryonalen Stammzellen ähnelt.
Anzeige
Von Hartmut Wewetzer
24.1.2009 0:00 Uhr Von Hartmut Wewetzer
24.1.2009 0:00 Uhr
Berlin - In den USA ist weltweit zum ersten Mal eine Behandlung genehmigt worden, die auf menschlichen embryo nalen Stammzellen basiert. Die Arzneimittelbehörde FDA erlaubte es der Biotechnik-Firma Geron, die Zelltherapie bei freiwilligen Versuchspersonen mit Querschnittslähmung einzusetzen. Das teilte das im kalifornischen Menlo ansässige Unternehmen am Freitag mit.
Embryonale Stammzellen gelten als „Alleskönner“. Sie können sich unter geeigneten Bedingungen in jedes beliebige Gewebe verwandeln. Mediziner hoffen, dass mit ihrer Hilfe eines Tages erkranktes oder zerstörtes Gewebe ersetzt werden kann, zum Beispiel bei der Zuckerkrankheit (Diabetes) oder der Schüttellähmung (Parkinson).
Weil die Stammzellen aus wenige Tage alten Embryonen gewonnen werden, ist die Therapie jedoch umstritten. In den USA hatte Präsident George W. Bush die Forschungsförderung aus Bundesmitteln blockiert. Dass nun kurz nach dem Amtswechsel die Behandlung erlaubt wurde, werten Beobachter als Zeichen dafür, dass die Aufsichtsbehörde unter politischem Druck der Bush-Regierung stand und deshalb die Genehmigung bisher nicht erteilen konnte.
Bei der Untersuchung, die im Sommer beginnen soll, handelt es sich um eine Phase-1-Studie. In diesem frühen Stadium geht es darum, zu prüfen, ob die Behandlung grundsätzlich sicher ist. Es ist vorgesehen, acht bis zehn Patienten mit einer Querschnittslähmung in Höhe des Brustkorbs zu behandeln. Die Verletzung darf nur sieben bis 14 Tage zurückliegen. Ist schon mehr Zeit verstrichen, ist die Zelltherapie möglicherweise nicht mehr wirksam. Die Patienten sollen Hüllzellen des Nervensystems bekommen, die aus embryonalen Stammzellen gezüchtet wurden. Diese Hüllzellen, Oligodendrozyten genannt, werden dorthin gespritzt, wo das aus Nervenfasern bestehende Rückenmark durchtrennt wurde. An Ort und Stelle sollen die Zellen das durchtrennte Nervenkabel reparieren, es wieder „zusammenschweißen“ und einhüllen. Im Tierversuch gelang es, Lähmungen zumindest teilweise rückgängig zu machen.
Embryonale Stammzellen haben ein erhebliches Wachstumspotenzial. Deshalb neigen sie dazu, Tumoren zu bilden. Diese sind zwar nicht so gefährlich wie herkömmliche Krebstumoren, stellen aber trotzdem ein erhebliches Risiko dar. Nach Angaben von Geron ist jedoch sichergestellt, dass die injizierten Zellen kein Tumorrisiko mehr besitzen. Außerdem müssen die Patienten Medikamente nehmen, um Abstoßungsreaktionen gegen die fremden Zellen zu unterdrücken.
Die Reaktionen der US-Wissenschaftler schwanken zwischen Hoffnung und Skepsis. So wird kritisiert, dass die Therapie möglicherweise noch nicht ausgereift sei und bei einem Fehlschlag die ganze Forschung in Misskredit bringen werde. „Das wäre ein Desaster, ein Albtraum“, sagte der Stammzellforscher John Kessler von der Northwestern University. In den vergangenen Jahren wurde zudem erfolgreich gezeigt, dass sich auch patienteneigenes Gewebe gentechnisch so umprogrammieren lässt, dass es embryonalen Stammzellen ähnelt.
Antwort auf Beitrag Nr.: 36.438.806 von meislo am 23.01.09 18:53:36Dieser Kommentar kommt meinem sehr nahe. Und natürlich muss ich auch sagen. Es ist noch ein weiter Weg und keiner weiss wo er endet. Die Risiken sind natürlich nicht zu übersehen. Aber der Weg wird erst einmal begangen und das ist doch das positive.
The Politics And Science Of Geron
A few days into his term, President Obama appears to have begun to undo another Bush-era policy.
He hasn't yet formally lifted the Bush-imposed ban on federal funding of new embryonic stem cell research, but Obama's Food and Drug Administration has already set the stage for it.
The FDA, which doesn't even have a new, permanent commissioner, is allowing Geron [GERN 7.20 1.99 (+38.2%) ] to do the first test on people of an embryonic stem cell treatment. GERN shares are soaring on very heavy volume and a handful of other little stocks that play in the stem cell space are rallying as well.
In a "First on CNBC" live interview this morning, the CEO of Geron, Dr. Tom Okarma, said, "There's no question that the Bush administration was very instrumental in slowing down the progress in a number of ways. But we have really no direct evidence that that actually influenced the FDA's review. So, we really have no view that there was a political overhang at the FDA."
I think Dr. Okarma is being polite and diplomatic.
I and at least a couple of analyst think the timing of this announcement is more than a coincidence. Joe Pantginis at Merriman Curhan Ford boldly titled his research note to clients today, "Bye Bye Bush; Hello New Era for Embryonic Stem Cells; Reiterate Buy." MCF makes a market in GERN. And Steve Brozak at the boutique WBB Securities writes, "The FDA decision to allow a clinical trial...is a reversal of policy. We predicted that a newly inaugurated president would reverse the clinical trial hold...." Brozak is a Democrat who ran for Congress several years ago.
Whether the FDA's decision is driven by science, politics or maybe both, this is still a significant milestone. When a company moves a drug from the lab to the clinic it rarely, if ever, gets much media attention. Of course, the circumstances here are different and worthy of an exception. But the rules and the odds remain the same: the overwhelming majority of drugs that go into this first stage of testing on people doesn't ever get to market.
I'm not saying that's the fate Geron's experimental spinal cord treatment will meet. I'm only saying that despite all of the excitement and promise surrounding embryonic stem cells today, there's still a long, challenging road ahead.
The Politics And Science Of Geron
A few days into his term, President Obama appears to have begun to undo another Bush-era policy.
He hasn't yet formally lifted the Bush-imposed ban on federal funding of new embryonic stem cell research, but Obama's Food and Drug Administration has already set the stage for it.
The FDA, which doesn't even have a new, permanent commissioner, is allowing Geron [GERN 7.20 1.99 (+38.2%) ] to do the first test on people of an embryonic stem cell treatment. GERN shares are soaring on very heavy volume and a handful of other little stocks that play in the stem cell space are rallying as well.
In a "First on CNBC" live interview this morning, the CEO of Geron, Dr. Tom Okarma, said, "There's no question that the Bush administration was very instrumental in slowing down the progress in a number of ways. But we have really no direct evidence that that actually influenced the FDA's review. So, we really have no view that there was a political overhang at the FDA."
I think Dr. Okarma is being polite and diplomatic.
I and at least a couple of analyst think the timing of this announcement is more than a coincidence. Joe Pantginis at Merriman Curhan Ford boldly titled his research note to clients today, "Bye Bye Bush; Hello New Era for Embryonic Stem Cells; Reiterate Buy." MCF makes a market in GERN. And Steve Brozak at the boutique WBB Securities writes, "The FDA decision to allow a clinical trial...is a reversal of policy. We predicted that a newly inaugurated president would reverse the clinical trial hold...." Brozak is a Democrat who ran for Congress several years ago.
Whether the FDA's decision is driven by science, politics or maybe both, this is still a significant milestone. When a company moves a drug from the lab to the clinic it rarely, if ever, gets much media attention. Of course, the circumstances here are different and worthy of an exception. But the rules and the odds remain the same: the overwhelming majority of drugs that go into this first stage of testing on people doesn't ever get to market.
I'm not saying that's the fate Geron's experimental spinal cord treatment will meet. I'm only saying that despite all of the excitement and promise surrounding embryonic stem cells today, there's still a long, challenging road ahead.
mehr als 50 millionen Aktien wurden gehandelt
Schlusskurs 7,09 Dollar
Schlusskurs 7,09 Dollar

Antwort auf Beitrag Nr.: 36.438.449 von meislo am 23.01.09 18:17:13Wahnsinn! 

Antwort auf Beitrag Nr.: 36.438.449 von meislo am 23.01.09 18:17:13im positiven Sinne.
Antwort auf Beitrag Nr.: 36.440.522 von [KERN]Codex am 23.01.09 22:50:14Bist noch investiert??

Antwort auf Beitrag Nr.: 36.440.585 von meislo am 23.01.09 23:04:04Nein aber ich werde wieder reingehen, Geron ist ein potentieller Tenbagger, wenn die Therapie funktioniert, ABER ich werde nur 1000 EUR investieren, das kann ich verschmerzen falls es unerwünschte Nebenwirkungen gibt. Hast du deine alte Position noch?
Denke mal das ganze Thema wird in den nächsten Wochen und Monaten politisch strapaziert werden.
In wieweit der Kurs davon profitieren wird ist noch nicht absehbar. Es kann sein, dass die Welle noch einige Zeit trägt. Jedem sollte aber klar sein, dass noch mindestens ein Jahr (eher zwei Jahre) vergehen müssen, bis erste Ergebnisse die Evidenz aber auch vor allem die Sicherheit einer kontrollierten Behandlung aufgezeigt werden können.
Ich persönlich rechne nicht mit Kursen, die in den Himmel steigen! Man sollte die Entwicklung nun verfolgen um eventuell nichts zu verpassen.
In wieweit der Kurs davon profitieren wird ist noch nicht absehbar. Es kann sein, dass die Welle noch einige Zeit trägt. Jedem sollte aber klar sein, dass noch mindestens ein Jahr (eher zwei Jahre) vergehen müssen, bis erste Ergebnisse die Evidenz aber auch vor allem die Sicherheit einer kontrollierten Behandlung aufgezeigt werden können.
Ich persönlich rechne nicht mit Kursen, die in den Himmel steigen! Man sollte die Entwicklung nun verfolgen um eventuell nichts zu verpassen.
Genau man sollte auf jeden Fall ZEIT mitbringen, so ist das mit den Biotechs 

Antwort auf Beitrag Nr.: 36.440.637 von [KERN]Codex am 23.01.09 23:18:23Habe zwischenzeitlich verkauft aber auch wieder zugekauft. Leider nicht bei weitem im Tief.
Habe aber ungefähr meine alte Position.
Mit der von Geron genannten Entscheidung seitens der FDA (Die FDA hat ja noch nicht bestätigt, aber da habe ich keine Zweifel)wird seitens der Pharmabrache einiges losgetreten. Geron ist der Leader. Die Aktie hat, wenn alles fluppt enormes Potential. Keine andere Aktie kann das in diesem Segment bieten. Bei aller Überschwänglichkeit muss amn trotzdem betonen, die Aktie betritt FDA-Neuland. Da ist noch bei weitem nichts in trockenen Tüchern.

Habe aber ungefähr meine alte Position.
Mit der von Geron genannten Entscheidung seitens der FDA (Die FDA hat ja noch nicht bestätigt, aber da habe ich keine Zweifel)wird seitens der Pharmabrache einiges losgetreten. Geron ist der Leader. Die Aktie hat, wenn alles fluppt enormes Potential. Keine andere Aktie kann das in diesem Segment bieten. Bei aller Überschwänglichkeit muss amn trotzdem betonen, die Aktie betritt FDA-Neuland. Da ist noch bei weitem nichts in trockenen Tüchern.

Aus dem Ärzteblatt
Querschnittslähmung: Grünes Licht für Phase-1-Studie mit embryonalen Stammzellen
Freitag, 23. Januar 2009
Washington – Drei Tage nach dem Regierungswechsel in den USA hat eine Firma von der Arzneimittelbehörde FDA die Erlaubnis erhalten, in einer Studie paraplegische Patienten durch Injektion von Zellen zu behandeln, die aus embryonalen Stammzellen gewonnen wurden.
Die weltweit erste Studie dieser Art wird als Zeichen des forschungspolitischen Wandels in den USA gewertet. Rechtlich wäre sie aber schon unter der Bush-Administration möglich gewesen.
An der Phase-1-Studie sollen acht bis zehn Patienten teilnehmen, deren Rückenmarksverletzung in Höhe von Th3 bis Th10 (also in der unteren Brustwirbelsäule) nicht länger als 14 Tage zurück liegt. Der Plan sieht vor, dass die Patienten Injektionen direkt in die Läsionen erhalten.
Die Injektionen enthalten Vorläuferzellen von Oligodendrozyten. Diese Zellen werden zuvor aus embryonalen Stammzellen hergestellt. Im Rückenmark sollen sich die Vorläuferzellen zu reifen Oligodendrozyten ausdifferenzieren, dann die Myelinscheiden erneuern und das Wachstum von Nervenzellen stimulieren.
Über die von den Oligodendrozyten geschaffenen neuen Myelinscheiden sollen sich dann die durchtrennten Nervenzellen regenerieren und die Verbindung zu den Motoneuronen wieder herstellen, was die Lähmung im Idealfall beseitigen würde.
Zu hoch sollten die Erwartungen jedoch nicht sein. Hans Keirstead von der Universität von Irvine/Kalifornien konnte zwar 2005 an Ratten zeigen, dass die Stammzelltherapie der Paraplegie im Prinzip möglich ist (Journal of Neuroscience 2005; 25: 4694-4705). Die zuvor an den Hinterläufen gelähmten Ratten konnten sich danach wieder besser fortbewegen. Eine vollständige Heilung wurde jedoch nicht erzielt.
Die Firma begründet ihren Antrag auf Zulassung einer klinischen Studie auf 21.000 Seiten mit den Ergebnissen von 24 tierexperimentellen Studien. Für die Phase-I-Studie musste die Firma vor allem nachweisen, dass die Therapie den Patienten nicht schadet.
Die Bedenken gehen dahin, dass die eine oder andere der etwa 5 Millionen Zellen, die in das Rückenmark injiziert werden, zum Ausgangspunkt eines Tumorwachstums (zum Beispiel Teratom) werden kann.
Die Firma meint, dies anhand der experimentellen Daten ausschließen zu können. Die Zellen würden auch keine Migrationstendenz zeigen, keine Allodynie induzieren, heißt es in der Pressemitteilung. Es gebe keine Hinweise auf eine systemische Toxizität oder eine erhöhte Sterblichkeit der Versuchstiere. Auch allergische Reaktionen sind nach Auskunft von Geron Corp. nicht zu erwarten.
In-vitro-Studien hätten gezeigt, dass die Zellen vom Immunsystem nicht als fremd erkannt werden und deshalb kein Angriff von natürlichen Killerzellen oder T-Zellen auf das frisch reparierte Rückenmark zu befürchten sei, was einen Anfangserfolg schnell wieder zunichte machen könnte.
Dass seit der Publikation der tierexperimentellen Studie noch zweieinhalb Jahr vergingen, bis die FDA ihre Zustimmung erteilte, mag mit der obstruktiven Haltung der Bush-Adminstration zusammenhängen. Auch wenn die verwendeten embryonalen Stammzellen vor dem August 2001 gewonnen wurden, und somit nicht unter das Verbot der öffentlichen Förderung dieser Therapie fielen.
Der Staat Kalifornien stand dem Forschungsvorhaben ohnehin positiver gegenüber als die Bundesregierung. Seit 2004 gibt es dort ein mit 3 Milliarden US-Dollar gefördertes öffentliches Forschungsprojekt.
Die neue Administration steht der Stammzellforschung positiver gegenüber, waeshalb die Erlaubnis unmittelbar nach der Amtseinführung von Barack Obama als Zeichen einer Wende gewertet werden.
Sieben Zentren haben ihre Beteiligung an der Phase-I-Studie zugesagt, die in diesem Sommer beginnen soll. Gegenstand ist die Sicherheit der Therapie, doch das Interesse wird sich darauf konzentrieren, ob sich die Beweglichkeit in den Beinen der paraplegischen Patienten verbessert.
Das wäre dann sicherlich ein Durchbruch in der Behandlung dieser Erkrankung und Grundlage für den wirtschaftlichen Erfolg der Firma Geron (1990 übrigens als Anti-Aging-Firma gegründet, daher der Name), die laut Presseberichten weit mehr als 100 Millionen US-Dollar in die Stammzellforschung gesteckt hat.
Die Pressemitteilung betont, dass die Therapie durch Patente geschützt ist. Der Leiter der Firma versicherte jedoch, dass eine Behandlung weit weniger als 500.000 US-Dollar kosten werde und deshalb erschwinglich sei. Vielleicht sollte aber zunächst einmal abgewartet werden, ob sie auch wirkt. © rme/aerzteblatt.de
Links zum Thema
» Aktuelle Pressemitteilung von Geron Corpht…
» PDF der Studie Keirstead et al http…
Querschnittslähmung: Grünes Licht für Phase-1-Studie mit embryonalen Stammzellen
Freitag, 23. Januar 2009
Washington – Drei Tage nach dem Regierungswechsel in den USA hat eine Firma von der Arzneimittelbehörde FDA die Erlaubnis erhalten, in einer Studie paraplegische Patienten durch Injektion von Zellen zu behandeln, die aus embryonalen Stammzellen gewonnen wurden.
Die weltweit erste Studie dieser Art wird als Zeichen des forschungspolitischen Wandels in den USA gewertet. Rechtlich wäre sie aber schon unter der Bush-Administration möglich gewesen.
An der Phase-1-Studie sollen acht bis zehn Patienten teilnehmen, deren Rückenmarksverletzung in Höhe von Th3 bis Th10 (also in der unteren Brustwirbelsäule) nicht länger als 14 Tage zurück liegt. Der Plan sieht vor, dass die Patienten Injektionen direkt in die Läsionen erhalten.
Die Injektionen enthalten Vorläuferzellen von Oligodendrozyten. Diese Zellen werden zuvor aus embryonalen Stammzellen hergestellt. Im Rückenmark sollen sich die Vorläuferzellen zu reifen Oligodendrozyten ausdifferenzieren, dann die Myelinscheiden erneuern und das Wachstum von Nervenzellen stimulieren.
Über die von den Oligodendrozyten geschaffenen neuen Myelinscheiden sollen sich dann die durchtrennten Nervenzellen regenerieren und die Verbindung zu den Motoneuronen wieder herstellen, was die Lähmung im Idealfall beseitigen würde.
Zu hoch sollten die Erwartungen jedoch nicht sein. Hans Keirstead von der Universität von Irvine/Kalifornien konnte zwar 2005 an Ratten zeigen, dass die Stammzelltherapie der Paraplegie im Prinzip möglich ist (Journal of Neuroscience 2005; 25: 4694-4705). Die zuvor an den Hinterläufen gelähmten Ratten konnten sich danach wieder besser fortbewegen. Eine vollständige Heilung wurde jedoch nicht erzielt.
Die Firma begründet ihren Antrag auf Zulassung einer klinischen Studie auf 21.000 Seiten mit den Ergebnissen von 24 tierexperimentellen Studien. Für die Phase-I-Studie musste die Firma vor allem nachweisen, dass die Therapie den Patienten nicht schadet.
Die Bedenken gehen dahin, dass die eine oder andere der etwa 5 Millionen Zellen, die in das Rückenmark injiziert werden, zum Ausgangspunkt eines Tumorwachstums (zum Beispiel Teratom) werden kann.
Die Firma meint, dies anhand der experimentellen Daten ausschließen zu können. Die Zellen würden auch keine Migrationstendenz zeigen, keine Allodynie induzieren, heißt es in der Pressemitteilung. Es gebe keine Hinweise auf eine systemische Toxizität oder eine erhöhte Sterblichkeit der Versuchstiere. Auch allergische Reaktionen sind nach Auskunft von Geron Corp. nicht zu erwarten.
In-vitro-Studien hätten gezeigt, dass die Zellen vom Immunsystem nicht als fremd erkannt werden und deshalb kein Angriff von natürlichen Killerzellen oder T-Zellen auf das frisch reparierte Rückenmark zu befürchten sei, was einen Anfangserfolg schnell wieder zunichte machen könnte.
Dass seit der Publikation der tierexperimentellen Studie noch zweieinhalb Jahr vergingen, bis die FDA ihre Zustimmung erteilte, mag mit der obstruktiven Haltung der Bush-Adminstration zusammenhängen. Auch wenn die verwendeten embryonalen Stammzellen vor dem August 2001 gewonnen wurden, und somit nicht unter das Verbot der öffentlichen Förderung dieser Therapie fielen.
Der Staat Kalifornien stand dem Forschungsvorhaben ohnehin positiver gegenüber als die Bundesregierung. Seit 2004 gibt es dort ein mit 3 Milliarden US-Dollar gefördertes öffentliches Forschungsprojekt.
Die neue Administration steht der Stammzellforschung positiver gegenüber, waeshalb die Erlaubnis unmittelbar nach der Amtseinführung von Barack Obama als Zeichen einer Wende gewertet werden.
Sieben Zentren haben ihre Beteiligung an der Phase-I-Studie zugesagt, die in diesem Sommer beginnen soll. Gegenstand ist die Sicherheit der Therapie, doch das Interesse wird sich darauf konzentrieren, ob sich die Beweglichkeit in den Beinen der paraplegischen Patienten verbessert.
Das wäre dann sicherlich ein Durchbruch in der Behandlung dieser Erkrankung und Grundlage für den wirtschaftlichen Erfolg der Firma Geron (1990 übrigens als Anti-Aging-Firma gegründet, daher der Name), die laut Presseberichten weit mehr als 100 Millionen US-Dollar in die Stammzellforschung gesteckt hat.
Die Pressemitteilung betont, dass die Therapie durch Patente geschützt ist. Der Leiter der Firma versicherte jedoch, dass eine Behandlung weit weniger als 500.000 US-Dollar kosten werde und deshalb erschwinglich sei. Vielleicht sollte aber zunächst einmal abgewartet werden, ob sie auch wirkt. © rme/aerzteblatt.de
Links zum Thema
» Aktuelle Pressemitteilung von Geron Corpht…
» PDF der Studie Keirstead et al http…
interview mit dr. hans keirstead (university of irvine, cal.), welcher das klinische stammzellen-programm gerons leitet:
http://www.cirm.ca.gov/about/videos/Keristead_neuron.asp
tolle nachrichten gestern. kam überraschend für mich.
lg
http://www.cirm.ca.gov/about/videos/Keristead_neuron.asp
tolle nachrichten gestern. kam überraschend für mich.
lg
Hier noch passend dazu eine Video Illustration und zusätzliche Infos
http://www.geron.com/grnopc1clearance/
http://www.geron.com/grnopc1clearance/
Biotechfirma will Therapie mit embryonalen Stammzellen ausweiten
Samstag, 24. Januar 2009, 20:23 Uhr Diesen Artikel drucken[-] Text [+]
Washington, 24. Jan (Reuters) - Das US-Biotech-Unternehmen Geron(GERN.O: Kurs) will Therapien mit embryonalen Stammzellen ausbauen. Eine entsprechende Behandlung sei für die Masse zu einem vergleichsweise billigen Preis möglich, sagte Geron-Chef Thomas Okarma. Am Freitag hatte die US-Arzneimittelbehörde FDA der Firma die Genehmigung für eine Pilotstudie mit zehn querschnittsgelähmten Menschen erteilt. Mediziner werden den Patienten Stammzellen injizieren und hoffen, dass diese die beschädigten Nerven der Probanden wieder zum Wachsen anregen.
"Für uns ist es der Beginn eines neuen Ära medizinischer Therapien", sagte Okarma. "Es ist eine neue Form des Heilens ohne Pillen und Skalpell." Auch Krankheiten wie Multiple Sklerose könnten auf diese Weise möglicherweise geheilt werden. Analysten waren begeistert über die ethisch und medizinisch umstrittene Entscheidung der FDA. Das Projekt könne so wichtig sein wie die Erfindung des Penizillin, erklärten die Analysten Stephen Brozak und Daniel Mallin von WBB Securities.
 Der Kurs der Geron-Aktie schoss am Freitag um 36 Prozent nach oben. (Reporter: Maggie Fox; bearbeitet von Andreas Kröner)
Der Kurs der Geron-Aktie schoss am Freitag um 36 Prozent nach oben. (Reporter: Maggie Fox; bearbeitet von Andreas Kröner)
© Thomson Reuters 2009 Alle Rechte vorbehalten.
Samstag, 24. Januar 2009, 20:23 Uhr Diesen Artikel drucken[-] Text [+]
Washington, 24. Jan (Reuters) - Das US-Biotech-Unternehmen Geron(GERN.O: Kurs) will Therapien mit embryonalen Stammzellen ausbauen. Eine entsprechende Behandlung sei für die Masse zu einem vergleichsweise billigen Preis möglich, sagte Geron-Chef Thomas Okarma. Am Freitag hatte die US-Arzneimittelbehörde FDA der Firma die Genehmigung für eine Pilotstudie mit zehn querschnittsgelähmten Menschen erteilt. Mediziner werden den Patienten Stammzellen injizieren und hoffen, dass diese die beschädigten Nerven der Probanden wieder zum Wachsen anregen.
"Für uns ist es der Beginn eines neuen Ära medizinischer Therapien", sagte Okarma. "Es ist eine neue Form des Heilens ohne Pillen und Skalpell." Auch Krankheiten wie Multiple Sklerose könnten auf diese Weise möglicherweise geheilt werden. Analysten waren begeistert über die ethisch und medizinisch umstrittene Entscheidung der FDA. Das Projekt könne so wichtig sein wie die Erfindung des Penizillin, erklärten die Analysten Stephen Brozak und Daniel Mallin von WBB Securities.

 Der Kurs der Geron-Aktie schoss am Freitag um 36 Prozent nach oben. (Reporter: Maggie Fox; bearbeitet von Andreas Kröner)
Der Kurs der Geron-Aktie schoss am Freitag um 36 Prozent nach oben. (Reporter: Maggie Fox; bearbeitet von Andreas Kröner) © Thomson Reuters 2009 Alle Rechte vorbehalten.
Antwort auf Beitrag Nr.: 36.443.448 von meislo am 24.01.09 23:14:55http://de.reuters.com/article/deEuroRpt/idDELO59614620090124

25.01.2009 06:22
Geron erhält FDA-Genehmigung, um mit der weltweit größten klinischen Studie über eine auf embryonalen Stammzellen basierende Therapie zu beginnen
Geron betreibt Studie über GRNOPC1 bei Patienten mit akuten Verletzungen des Rückenmarks
Konferenzgespräch und Video-Webcast vorgesehen für 6:00 Uhr PST/ 9:00 Uhr EST (15.00 Uhr MEZ)
Geron Corporation (News) (Nasdaq:GERN) gab heute bekannt, dass die amerikanische Arzneimittelzulassungsbehörde (FDA, Food and Drug Administration) die Genehmigung des Antrags in Bezug auf ein Investigational New Drug (IND) des Unternehmens für die klinische Studie von GRNOPC1 bei Patienten mit einer akuten Verletzung des Rückenmarks erteilt hat.
Die Genehmigung ermöglicht es Geron, mit der weltweit ersten Studie über eine Therapie bei Menschen auf der Grundlage einer menschlichen embryonalen Stammzelle (hESC) voranzukommen. Geron plant die Einführung einer Phase I-Multicenter-Studie, die darauf ausgelegt ist, die Sicherheit von GRNOPC1 bei Patienten mit „vollständigen” subakuten thorakalen Verletzungen des Rückenmarks Grad A laut der US-amerikanische Vereinigung für Verletzungen des Rückenmarks (ASIA, American Spinal Injury Association) aufzubauen.
„Die Genehmigung unseres GRNOPC1 IND durch FDA stellt derzeit eine der wichtigsten Leistungen von Geron dar”, so Thomas B. Okarma, Ph.D., M.D., President und CEO von Geron. „Dies ist der Anfang eines möglichen neuen Kapitels in medizinischer Therapeutik - ein Kapitel, welches über Pillen hinausgeht und ein neues Heilniveau erreicht: Die Wiederherstellung der Funktion von Organen und Geweben, welche durch die Injektion gesunder Ersatzzellen erzielt wird. Das letztendliche Ziel für die Verwendung von GRNOPC1 ist es, die Wiederherstellung der Rückenmarksfunktion durch die direkte Injektion von hESC-abgeleiteten Oligodendrozyten-Progenitorzellen in die Läsionsstelle des verletzten Rückenmarks des Patienten zu erreichen.”
GRNOPC1, der führende hESC-basierte therapeutische Kandidat von Geron, enthält hESC-abgeleitete Oligodendrozyten-Progenitorzellen, die Eigenschaften aufgezeigt haben, welche eine remyelisierende Wirkung aufweisen und das Nervenwachstum anregen und somit zur Wiederherstellung der Funktion im Falle von akuten Verletzungen des Rückenmarks bei Tieren führen (Journal of Neuroscience, Ausgabe 25, 2005).
„Die neurochirurgische Gemeinschaft zeigt große Begeisterung für diesen neuen Ansatz zur Behandlung vernichtender Verletzungen des Rückenmarks”, so Richard Fessler, M.D., Ph.D., Professor für neurologische Chirurgie an der Feinberg School of Medicine an der Northwestern University. „Demyelinisierung ist wesentlich für die Pathologie der Verletzung, und deren Umkehr durch die Injektion von Oligodendrozyten-Progenitorzellen wäre eine Revolution für diesen Bereich. Wenn die Therapie sicher und wirksam wäre, würde sie eine praktikable Behandlungsoption für tausende von Patienten darstellen, die jedes Jahr an ernsthaften Verletzungen des Rückenmarks erkranken.”
Das Klinische Programm GRNOPC1
Patienten, die für die Phase I-Studie in Frage kommen, müssen einen dokumentierten Nachweis über eine vollständige funktionale Verletzung des Rückenmarks mit einer neurologischen Stufe von T3 bis T10 spinalen Segmenten vorlegen können und damit einverstanden sein, dass ihnen GRNOPC1 innerhalb von sieben bis 14 Tagen nach der Verletzung in die Läsionsstellen injiziert wird. Geron hat bis zu sieben medizinische Zentren in den USA als Kandidaten ausgewählt, die an dieser Studie und den geplanten Erweiterungen des Protokolls teilnehmen sollen. Die Standorte werden identifiziert, sobald sie online veröffentlicht werden und eine Eintragung von Versuchspersonen für die Studie möglich ist.
Obwohl Sicherheit der primäre Endpunkt der Untersuchung ist, schließt das Protokoll sekundäre Endpunkte zur Beurteilung der Wirksamkeit, wie zum Beispiel eine verbesserte neuromuskuläre Kontrolle oder Empfindung im Rumpf oder in den unteren Extremitäten mit ein. Sobald Sicherheit bei dieser Patientenpopulation aufgebaut wurde und die FDA die klinischen Daten in Verbindung mit zusätzlichen Daten aus aktuellen Tierstudien überarbeitet, plant Geron, sich eine Zustimmung der FDA zur Erweiterung der Studie einzuholen, damit die Dosis an GRNOPC1 erhöht werden kann, Versuchspersonen mit kompletten Verletzungen des Gehirns eingeschrieben werden können und die Studie dahingehend ausgeweitet werden kann, dass Patienten mit ernsthaften unvollständigen (ASIA Grad B- oder C-) Verletzungen ebenfalls eingeschlossen werden können, so dass eine umfassende Population von Patienten mit ernsthaften Verletzungen des Rückenmarks einen angemessenen medizinischen Zugang zu der Therapie hat.
Vorklinische Beweise für Sicherheit, Verträglichkeit und Wirksamkeit
Geron legte der FDA in einem 21.000-seitigen IND-Antrag Beweise für die Sicherheit, Verträglichkeit und Wirksamkeit von GRNOPC1 vor; darin wurden 24 einzelne Tierstudien beschrieben, bei denen die Produktion von mehr als fünf Milliarden GRNOPC1-Zellen erforderlich war. Das Sicherheitspaket enthielt auch Studien, die 12 Monate nach der Injektion von GRNOPC1 klinischen Grades in das verletzte Rückenmark von Ratten und Mäusen keine Anzeichen von teratoiden Geschwülsten aufweisen. Andere Studien dokumentierten das Nichtvorhandensein von einer bedeutenden Migration der injizierten Zellen außerhalb des Rückenmarks, von Allodynieinduktion (erhöhter neuropathischer Schmerz aufgrund von injizierten Zellen), von systemischer Toxizität oder erhöhter Mortalität bei Tieren, welchen GRNOPC1 verabreicht wurde.
In vitro-Studien haben gezeigt, dass GRNOPC1 vom menschlichen Immunsystem minimal erkannt wird. GRNOPC1 wird in vitro nicht von allogenen Sera, NK-Zellen oder T-Zellen erkannt (Journal of Neuroimmunology, Ausgabe 192, 2007). Diese immunpriviligierten Eigenschaften der hESC-abgeleiteten Zellen ermöglichen eine Gestaltung der klinischen Studie, welche einen eingeschränkten Verlauf von Immunosuppression mit einer niedrigen Dosis integrieren und die Begründung für eine standardmäßige allogene Zelltherapie liefern.
Der IND-Antrag enthielt auch veröffentlichte Studien, welche die Nützlichkeit von GRNOPC1 für die Behandlung von Verletzungen des Rückenmarks unterstützten. Diese Studien zeigten, dass die Verabreichung von GRNOPC1 die Aktivität des Bewegungsapparats und die kinematischen Wertungen von Tieren mit Verletzungen des Rückenmarks bedeutend verbesserte, wenn es innerhalb von sieben Tagen nach der Verletzung injiziert wurde (Journal of Neuroscience, Ausgabe 25, 2005). Histologische Untersuchungen des verletzten Rückenmarks, welches mit GRNOPC1 behandelt wurde, zeigten eine verbesserte Überlebensdauer des Axons und eine ausgebreitete Remyelinisierung in der Umgebung der Axone von Ratten. Diese Wirkungen von GRNOPC1 zeigten sich neun Monate nach einer einzigen Injektion von Zellen. In diesen neunmonatigen Studien wurde aufgezeigt, dass diese Zellen wanderten und den Hohlraum der Läsion mit Bündeln aus markhaltigen Axonen auffüllten, die quer über die Stelle der Verletzung verliefen.
Produktion und Qualifizierung von GRNOPC1
GRNOPC1 wird unter Anwendung der current Good Manufacturing Practices (cGMP) in den Produktionsanlagen von Geron hergestellt. Der Herstellungsprozess für GRNOPC1 von Geron und die Reinraum-Suites wurden vom Bundesstaat Kalifornien untersucht und lizenziert. Die Zellen stammen von der menschlichen embryonalen Stammzelllinie H1, welche vor dem 9. August 2001 geschaffen wurde. Studien, welche diese Linie verwenden, qualifizieren sich für die US-amerikanische bundesstaatliche Forschungsfinanzierung, obwohl für die Entwicklung des Produktes oder für die Unterstützung der klinischen Studie keine bundesstaatlichen Finanzierungen erhalten wurden.
Die H1 hESC-Stammzellbank von Geron ist für die Verwendung bei Menschen vollständig qualifiziert und zeigte einen normalen Karyotyp und keine Anzeichen von messbaren Kontaminaten menschlichen oder tierischen Ursprungs. Die Produktion von GRNOPC1 aus undifferenzierten hESC in der Stammzellenbank verwendet qualifizierte Reagenzien und ein standardisiertes Protokoll, welches bei Geron im Laufe der letzen drei Jahre entwickelt wurde. Jeder Herstellungsdurchlauf von GRNOPC1 unterliegt einer standardisierten Überprüfung der Qualitätskontrolle, um Lebensfähigkeit, Sterilität und eine angemessene zelluläre Zusammensetzung sicherzustellen, bevor das Produkt für die klinische Verwendung freigegeben wird. Das GRNOPC1 Produkt, welches alle derartigen Spezifizierungen bestanden hat und freigegeben wurde, ist für die genehmigte klinische Studie erhältlich. Das aktuelle Produktionssortiment kann die Produktbedürfnisse durch grundlegende klinische Studien liefern. Die bestehende Stammzellbank liefert möglicherweise genügend Ausgangsmaterial, damit GRNOPC1 den US-amerikanischen Markt für akute Verletzungen des Rückenmarks mehr als 20 Jahre lang beliefern könnte.
Geistiges Eigentum
Die Produktion und Vermarktung von GRNOPC1 wird durch ein Portfolio von Patentrechten geschützt, welches sich im Besitz von Geron befindet oder ausschließlich für Geron lizenziert ist. Patentrechte, die sich im Besitz von Geron befinden, schützen Schlüsseltechnologien, die bei Geron für die skalierbare Herstellung von hESC sowie für die Produktion von neuralen Zellen durch die Differenzierung von hESC entwickelt wurden. Die grundlegenden Patente, welche hESC abdecken, wurden von der Wisconsin Alumni Research Foundation (WARF) ausschließlich für Geron für die Produktion von neuralen Zellen, Kardiomyozyten und pankreatischen Inselzellen für therapeutische Anwendungen lizenziert. Die Gültigkeit dieser Patente wurde kürzlich vom US-amerikanischen Patent- und Markenamt in einem Ablauf zur Nachprüfung bestätigt. Geron finanzierte die Original-Forschung bei der University of Wisconsin-Madison, die zur ersten Isolierung von hESC führte. Die Produktion von Oligodendrozyten von hESC wird von Patentrechten abgedeckt, die Geron ausschließlich von der University of California lizenziert wurden. Diese Patentrechte decken die Technologie ab, die in einer Forschungszusammenarbeit zwischen Wissenschaftlern von Geron und der University of California entwickelt wurde.
Konferenzschaltung und Video-Webcast
Thomas B. Okarma, Ph.D., M.D., richtet heute um 6:00 Uhr PST/9:00 Uhr EST (15.00 Uhr MEZ) eine Konferenzschaltung sowie eine Video-Webcast-Präsentation für Investoren und die Medien aus. Teilnehmer können der Konferenzschaltung per Telefon beiwohnen, indem sie die Nummer 866-783-2145 (USA) oder +1-857-350-1604 (international) wählen. Der Passcode lautet 89631672. Die Video-Webcast-Präsentation ist verfügbar unter http://phx.corporate-ir.net/phoenix.zhtml?p=irol-eventDetail…. Alle Teilnehmer werden aufgerufen, die Präsentation von Dr. Okarma im Internet zu verfolgen. Zugriff auf den Video-Webcast ist auch über einen Link möglich, der auf der Homepage der Webseite von Geron unter http://www.geron.com angeklickt werden kann. Die Teilnehmer werden angeregt, sich mindestens 15 Minuten vor Beginn der Präsentation einzuloggen, um sich die notwendige Software herunterzuladen. Eine Wiederholung des Video-Webcast ist bis einschließlich 23. Februar 2009 verfügbar.
Hintergrundinformationen über menschliche embryonale Stammzellen, GRNOPC1 und die klinische Studie über Verletzungen des Rückenmarks finden Sie unter http://eon.businesswire.com/news/eon/20090122006356/en.
Geron entwickelt erstklassige Arzneimittel für die Behandlung von Krebs und chronisch degenerativen Krankheiten, einschließlich Verletzungen des Rückenmarks, Herzstörungen und Diabetes. Das Unternehmen fördert ein Anti-Krebs-Arzneimittel und einen Impfstoff gegen Krebs, die durch verschiedene klinische Studien auf das Enzym Telomerase abzielen. Geron ist ebenfalls weltweit führend in der Entwicklung von Therapeutika auf der Grundlage von menschlichen embryonalen Stammzellen (hESC). Das Unternehmen hat die Genehmigung von der FDA erhalten, die weltweit erste klinische Studie einer hESC-basierten Therapie zu beginnen: GRNOPC1 für akute Verletzungen des Rückenmarks. Für weitere Informationen besuchen Sie bitte www.geron.com.
Diese Pressemitteilung kann zukunftsweisende Aussagen enthalten, die aufgrund der „Safe Harbor”-Vorschriften des Private Securities Litigation Reform Act aus dem Jahre 1995 gemacht wurden. Investoren werden davor gewarnt, dass Aussagen in dieser Pressemitteilung in Bezug auf mögliche Anwendungen der menschlichen embryonalen Stammzelltechnologie von Geron zukunftsweisende Aussagen darstellen, welche Risiken und Unsicherheiten mit sich bringen, u.a. Risiken bei der Entwicklung und Kommerzialisierung von potentiellen Produkten, die Unsicherheit von Ergebnissen klinischer Studien oder regulatorischer Bewilligungen oder Genehmigungen, den Bedarf an zukünftigem Kapital, die Abhängigkeit von Mitarbeitern und die Aufrechterhaltung unserer Rechte an geistigem Eigentum. Die eigentlichen Ergebnisse können erheblich von den Ergebnissen abweichen, die in diesen zukunftsweisenden Aussagen vorhergesehen wurden. Zusätzliche Informationen über mögliche Faktoren, die sich auf unsere Ergebnisse und andere Risiken auswirken könnten, werden von Zeit zu Zeit in den regelmäßigen Berichten von Geron genau beschrieben, einschließlich des vierteljährlichen Berichts auf Formular 10-Q für das Quartal, welches am 30. September 2008 endete.
Die Ausgangssprache, in der der Originaltext veröffentlicht wird, ist die offizielle und autorisierte Version. Übersetzungen werden zur besseren Verständigung mitgeliefert. Nur die Sprachversion, die im Original veröffentlicht wurde, ist rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen Sprachversion der Veröffentlichung ab.
Contacts:
Russo Partners, LLC
David Schull, +1-858-717-2310 (Medien)
david.schull@russopartnersllc.com
oder
Geron
Anna Krassowska, +1-650-473-7765
Investorenbeziehungen und Medienarbeit
info@geron.com
Klicken Sie hier, um weitere aktuelle Nachrichten zum Unternehmen zu finden:
http://www.finanznachrichten.de/nachrichten-aktien/geron-cor…" target="_blank" rel="nofollow ugc noopener">GERON CORPORATION
http://www.finanznachrichten.de/nachrichten-aktien/geron-cor…
Geron erhält FDA-Genehmigung, um mit der weltweit größten klinischen Studie über eine auf embryonalen Stammzellen basierende Therapie zu beginnen
Geron betreibt Studie über GRNOPC1 bei Patienten mit akuten Verletzungen des Rückenmarks
Konferenzgespräch und Video-Webcast vorgesehen für 6:00 Uhr PST/ 9:00 Uhr EST (15.00 Uhr MEZ)
Geron Corporation (News) (Nasdaq:GERN) gab heute bekannt, dass die amerikanische Arzneimittelzulassungsbehörde (FDA, Food and Drug Administration) die Genehmigung des Antrags in Bezug auf ein Investigational New Drug (IND) des Unternehmens für die klinische Studie von GRNOPC1 bei Patienten mit einer akuten Verletzung des Rückenmarks erteilt hat.
Die Genehmigung ermöglicht es Geron, mit der weltweit ersten Studie über eine Therapie bei Menschen auf der Grundlage einer menschlichen embryonalen Stammzelle (hESC) voranzukommen. Geron plant die Einführung einer Phase I-Multicenter-Studie, die darauf ausgelegt ist, die Sicherheit von GRNOPC1 bei Patienten mit „vollständigen” subakuten thorakalen Verletzungen des Rückenmarks Grad A laut der US-amerikanische Vereinigung für Verletzungen des Rückenmarks (ASIA, American Spinal Injury Association) aufzubauen.
„Die Genehmigung unseres GRNOPC1 IND durch FDA stellt derzeit eine der wichtigsten Leistungen von Geron dar”, so Thomas B. Okarma, Ph.D., M.D., President und CEO von Geron. „Dies ist der Anfang eines möglichen neuen Kapitels in medizinischer Therapeutik - ein Kapitel, welches über Pillen hinausgeht und ein neues Heilniveau erreicht: Die Wiederherstellung der Funktion von Organen und Geweben, welche durch die Injektion gesunder Ersatzzellen erzielt wird. Das letztendliche Ziel für die Verwendung von GRNOPC1 ist es, die Wiederherstellung der Rückenmarksfunktion durch die direkte Injektion von hESC-abgeleiteten Oligodendrozyten-Progenitorzellen in die Läsionsstelle des verletzten Rückenmarks des Patienten zu erreichen.”
GRNOPC1, der führende hESC-basierte therapeutische Kandidat von Geron, enthält hESC-abgeleitete Oligodendrozyten-Progenitorzellen, die Eigenschaften aufgezeigt haben, welche eine remyelisierende Wirkung aufweisen und das Nervenwachstum anregen und somit zur Wiederherstellung der Funktion im Falle von akuten Verletzungen des Rückenmarks bei Tieren führen (Journal of Neuroscience, Ausgabe 25, 2005).
„Die neurochirurgische Gemeinschaft zeigt große Begeisterung für diesen neuen Ansatz zur Behandlung vernichtender Verletzungen des Rückenmarks”, so Richard Fessler, M.D., Ph.D., Professor für neurologische Chirurgie an der Feinberg School of Medicine an der Northwestern University. „Demyelinisierung ist wesentlich für die Pathologie der Verletzung, und deren Umkehr durch die Injektion von Oligodendrozyten-Progenitorzellen wäre eine Revolution für diesen Bereich. Wenn die Therapie sicher und wirksam wäre, würde sie eine praktikable Behandlungsoption für tausende von Patienten darstellen, die jedes Jahr an ernsthaften Verletzungen des Rückenmarks erkranken.”
Das Klinische Programm GRNOPC1
Patienten, die für die Phase I-Studie in Frage kommen, müssen einen dokumentierten Nachweis über eine vollständige funktionale Verletzung des Rückenmarks mit einer neurologischen Stufe von T3 bis T10 spinalen Segmenten vorlegen können und damit einverstanden sein, dass ihnen GRNOPC1 innerhalb von sieben bis 14 Tagen nach der Verletzung in die Läsionsstellen injiziert wird. Geron hat bis zu sieben medizinische Zentren in den USA als Kandidaten ausgewählt, die an dieser Studie und den geplanten Erweiterungen des Protokolls teilnehmen sollen. Die Standorte werden identifiziert, sobald sie online veröffentlicht werden und eine Eintragung von Versuchspersonen für die Studie möglich ist.
Obwohl Sicherheit der primäre Endpunkt der Untersuchung ist, schließt das Protokoll sekundäre Endpunkte zur Beurteilung der Wirksamkeit, wie zum Beispiel eine verbesserte neuromuskuläre Kontrolle oder Empfindung im Rumpf oder in den unteren Extremitäten mit ein. Sobald Sicherheit bei dieser Patientenpopulation aufgebaut wurde und die FDA die klinischen Daten in Verbindung mit zusätzlichen Daten aus aktuellen Tierstudien überarbeitet, plant Geron, sich eine Zustimmung der FDA zur Erweiterung der Studie einzuholen, damit die Dosis an GRNOPC1 erhöht werden kann, Versuchspersonen mit kompletten Verletzungen des Gehirns eingeschrieben werden können und die Studie dahingehend ausgeweitet werden kann, dass Patienten mit ernsthaften unvollständigen (ASIA Grad B- oder C-) Verletzungen ebenfalls eingeschlossen werden können, so dass eine umfassende Population von Patienten mit ernsthaften Verletzungen des Rückenmarks einen angemessenen medizinischen Zugang zu der Therapie hat.
Vorklinische Beweise für Sicherheit, Verträglichkeit und Wirksamkeit
Geron legte der FDA in einem 21.000-seitigen IND-Antrag Beweise für die Sicherheit, Verträglichkeit und Wirksamkeit von GRNOPC1 vor; darin wurden 24 einzelne Tierstudien beschrieben, bei denen die Produktion von mehr als fünf Milliarden GRNOPC1-Zellen erforderlich war. Das Sicherheitspaket enthielt auch Studien, die 12 Monate nach der Injektion von GRNOPC1 klinischen Grades in das verletzte Rückenmark von Ratten und Mäusen keine Anzeichen von teratoiden Geschwülsten aufweisen. Andere Studien dokumentierten das Nichtvorhandensein von einer bedeutenden Migration der injizierten Zellen außerhalb des Rückenmarks, von Allodynieinduktion (erhöhter neuropathischer Schmerz aufgrund von injizierten Zellen), von systemischer Toxizität oder erhöhter Mortalität bei Tieren, welchen GRNOPC1 verabreicht wurde.
In vitro-Studien haben gezeigt, dass GRNOPC1 vom menschlichen Immunsystem minimal erkannt wird. GRNOPC1 wird in vitro nicht von allogenen Sera, NK-Zellen oder T-Zellen erkannt (Journal of Neuroimmunology, Ausgabe 192, 2007). Diese immunpriviligierten Eigenschaften der hESC-abgeleiteten Zellen ermöglichen eine Gestaltung der klinischen Studie, welche einen eingeschränkten Verlauf von Immunosuppression mit einer niedrigen Dosis integrieren und die Begründung für eine standardmäßige allogene Zelltherapie liefern.
Der IND-Antrag enthielt auch veröffentlichte Studien, welche die Nützlichkeit von GRNOPC1 für die Behandlung von Verletzungen des Rückenmarks unterstützten. Diese Studien zeigten, dass die Verabreichung von GRNOPC1 die Aktivität des Bewegungsapparats und die kinematischen Wertungen von Tieren mit Verletzungen des Rückenmarks bedeutend verbesserte, wenn es innerhalb von sieben Tagen nach der Verletzung injiziert wurde (Journal of Neuroscience, Ausgabe 25, 2005). Histologische Untersuchungen des verletzten Rückenmarks, welches mit GRNOPC1 behandelt wurde, zeigten eine verbesserte Überlebensdauer des Axons und eine ausgebreitete Remyelinisierung in der Umgebung der Axone von Ratten. Diese Wirkungen von GRNOPC1 zeigten sich neun Monate nach einer einzigen Injektion von Zellen. In diesen neunmonatigen Studien wurde aufgezeigt, dass diese Zellen wanderten und den Hohlraum der Läsion mit Bündeln aus markhaltigen Axonen auffüllten, die quer über die Stelle der Verletzung verliefen.
Produktion und Qualifizierung von GRNOPC1
GRNOPC1 wird unter Anwendung der current Good Manufacturing Practices (cGMP) in den Produktionsanlagen von Geron hergestellt. Der Herstellungsprozess für GRNOPC1 von Geron und die Reinraum-Suites wurden vom Bundesstaat Kalifornien untersucht und lizenziert. Die Zellen stammen von der menschlichen embryonalen Stammzelllinie H1, welche vor dem 9. August 2001 geschaffen wurde. Studien, welche diese Linie verwenden, qualifizieren sich für die US-amerikanische bundesstaatliche Forschungsfinanzierung, obwohl für die Entwicklung des Produktes oder für die Unterstützung der klinischen Studie keine bundesstaatlichen Finanzierungen erhalten wurden.
Die H1 hESC-Stammzellbank von Geron ist für die Verwendung bei Menschen vollständig qualifiziert und zeigte einen normalen Karyotyp und keine Anzeichen von messbaren Kontaminaten menschlichen oder tierischen Ursprungs. Die Produktion von GRNOPC1 aus undifferenzierten hESC in der Stammzellenbank verwendet qualifizierte Reagenzien und ein standardisiertes Protokoll, welches bei Geron im Laufe der letzen drei Jahre entwickelt wurde. Jeder Herstellungsdurchlauf von GRNOPC1 unterliegt einer standardisierten Überprüfung der Qualitätskontrolle, um Lebensfähigkeit, Sterilität und eine angemessene zelluläre Zusammensetzung sicherzustellen, bevor das Produkt für die klinische Verwendung freigegeben wird. Das GRNOPC1 Produkt, welches alle derartigen Spezifizierungen bestanden hat und freigegeben wurde, ist für die genehmigte klinische Studie erhältlich. Das aktuelle Produktionssortiment kann die Produktbedürfnisse durch grundlegende klinische Studien liefern. Die bestehende Stammzellbank liefert möglicherweise genügend Ausgangsmaterial, damit GRNOPC1 den US-amerikanischen Markt für akute Verletzungen des Rückenmarks mehr als 20 Jahre lang beliefern könnte.
Geistiges Eigentum
Die Produktion und Vermarktung von GRNOPC1 wird durch ein Portfolio von Patentrechten geschützt, welches sich im Besitz von Geron befindet oder ausschließlich für Geron lizenziert ist. Patentrechte, die sich im Besitz von Geron befinden, schützen Schlüsseltechnologien, die bei Geron für die skalierbare Herstellung von hESC sowie für die Produktion von neuralen Zellen durch die Differenzierung von hESC entwickelt wurden. Die grundlegenden Patente, welche hESC abdecken, wurden von der Wisconsin Alumni Research Foundation (WARF) ausschließlich für Geron für die Produktion von neuralen Zellen, Kardiomyozyten und pankreatischen Inselzellen für therapeutische Anwendungen lizenziert. Die Gültigkeit dieser Patente wurde kürzlich vom US-amerikanischen Patent- und Markenamt in einem Ablauf zur Nachprüfung bestätigt. Geron finanzierte die Original-Forschung bei der University of Wisconsin-Madison, die zur ersten Isolierung von hESC führte. Die Produktion von Oligodendrozyten von hESC wird von Patentrechten abgedeckt, die Geron ausschließlich von der University of California lizenziert wurden. Diese Patentrechte decken die Technologie ab, die in einer Forschungszusammenarbeit zwischen Wissenschaftlern von Geron und der University of California entwickelt wurde.
Konferenzschaltung und Video-Webcast
Thomas B. Okarma, Ph.D., M.D., richtet heute um 6:00 Uhr PST/9:00 Uhr EST (15.00 Uhr MEZ) eine Konferenzschaltung sowie eine Video-Webcast-Präsentation für Investoren und die Medien aus. Teilnehmer können der Konferenzschaltung per Telefon beiwohnen, indem sie die Nummer 866-783-2145 (USA) oder +1-857-350-1604 (international) wählen. Der Passcode lautet 89631672. Die Video-Webcast-Präsentation ist verfügbar unter http://phx.corporate-ir.net/phoenix.zhtml?p=irol-eventDetail…. Alle Teilnehmer werden aufgerufen, die Präsentation von Dr. Okarma im Internet zu verfolgen. Zugriff auf den Video-Webcast ist auch über einen Link möglich, der auf der Homepage der Webseite von Geron unter http://www.geron.com angeklickt werden kann. Die Teilnehmer werden angeregt, sich mindestens 15 Minuten vor Beginn der Präsentation einzuloggen, um sich die notwendige Software herunterzuladen. Eine Wiederholung des Video-Webcast ist bis einschließlich 23. Februar 2009 verfügbar.
Hintergrundinformationen über menschliche embryonale Stammzellen, GRNOPC1 und die klinische Studie über Verletzungen des Rückenmarks finden Sie unter http://eon.businesswire.com/news/eon/20090122006356/en.
Geron entwickelt erstklassige Arzneimittel für die Behandlung von Krebs und chronisch degenerativen Krankheiten, einschließlich Verletzungen des Rückenmarks, Herzstörungen und Diabetes. Das Unternehmen fördert ein Anti-Krebs-Arzneimittel und einen Impfstoff gegen Krebs, die durch verschiedene klinische Studien auf das Enzym Telomerase abzielen. Geron ist ebenfalls weltweit führend in der Entwicklung von Therapeutika auf der Grundlage von menschlichen embryonalen Stammzellen (hESC). Das Unternehmen hat die Genehmigung von der FDA erhalten, die weltweit erste klinische Studie einer hESC-basierten Therapie zu beginnen: GRNOPC1 für akute Verletzungen des Rückenmarks. Für weitere Informationen besuchen Sie bitte www.geron.com.
Diese Pressemitteilung kann zukunftsweisende Aussagen enthalten, die aufgrund der „Safe Harbor”-Vorschriften des Private Securities Litigation Reform Act aus dem Jahre 1995 gemacht wurden. Investoren werden davor gewarnt, dass Aussagen in dieser Pressemitteilung in Bezug auf mögliche Anwendungen der menschlichen embryonalen Stammzelltechnologie von Geron zukunftsweisende Aussagen darstellen, welche Risiken und Unsicherheiten mit sich bringen, u.a. Risiken bei der Entwicklung und Kommerzialisierung von potentiellen Produkten, die Unsicherheit von Ergebnissen klinischer Studien oder regulatorischer Bewilligungen oder Genehmigungen, den Bedarf an zukünftigem Kapital, die Abhängigkeit von Mitarbeitern und die Aufrechterhaltung unserer Rechte an geistigem Eigentum. Die eigentlichen Ergebnisse können erheblich von den Ergebnissen abweichen, die in diesen zukunftsweisenden Aussagen vorhergesehen wurden. Zusätzliche Informationen über mögliche Faktoren, die sich auf unsere Ergebnisse und andere Risiken auswirken könnten, werden von Zeit zu Zeit in den regelmäßigen Berichten von Geron genau beschrieben, einschließlich des vierteljährlichen Berichts auf Formular 10-Q für das Quartal, welches am 30. September 2008 endete.
Die Ausgangssprache, in der der Originaltext veröffentlicht wird, ist die offizielle und autorisierte Version. Übersetzungen werden zur besseren Verständigung mitgeliefert. Nur die Sprachversion, die im Original veröffentlicht wurde, ist rechtsgültig. Gleichen Sie deshalb Übersetzungen mit der originalen Sprachversion der Veröffentlichung ab.
Contacts:
Russo Partners, LLC
David Schull, +1-858-717-2310 (Medien)
david.schull@russopartnersllc.com
oder
Geron
Anna Krassowska, +1-650-473-7765
Investorenbeziehungen und Medienarbeit
info@geron.com
Klicken Sie hier, um weitere aktuelle Nachrichten zum Unternehmen zu finden:
http://www.finanznachrichten.de/nachrichten-aktien/geron-cor…" target="_blank" rel="nofollow ugc noopener">GERON CORPORATION
http://www.finanznachrichten.de/nachrichten-aktien/geron-cor…
Antwort auf Beitrag Nr.: 36.444.340 von meislo am 25.01.09 12:28:0214:57:57 5,60 2000 
14:51:39 5,90 360
14:35:57 5,81 20
14:14:18 5,80 2000
14:02:45 5,75 2000
13:38:21 5,75 4000
13:33:11 5,95 73
13:01:13 6,00 135
12:50:19 5,90 1000
12:32:32 6,00 450
12:13:08 6,10 50
11:34:25 6,10 1700
Anscheint jetzt schon "verblasst" hier in good old Germany...

14:51:39 5,90 360
14:35:57 5,81 20
14:14:18 5,80 2000
14:02:45 5,75 2000
13:38:21 5,75 4000
13:33:11 5,95 73
13:01:13 6,00 135
12:50:19 5,90 1000
12:32:32 6,00 450
12:13:08 6,10 50
11:34:25 6,10 1700
Anscheint jetzt schon "verblasst" hier in good old Germany...

Antwort auf Beitrag Nr.: 36.449.850 von Uptick08 am 26.01.09 15:20:57aber nicht in Amiland!
7,71 USD
7,71 USD
Hescheler: Erste klinische Versuche sehr vorsichtig machen
Stammzellenforscher über die Risiken und Chancen der Versuche am Menschen
Jürgen Hescheler im Gespräch mit Dirk Müller
Die erste Genehmigung für Forschungstests mit embryonalen Stammzellen am Menschen in den USA hat der Kölner Stammzellenforscher Professor Jürgen Hescheler grundsätzlich als Meilenstein begrüßt. Gleichzeitig warnte er vor ähnlichen Fehlern wie bei der Gentherapie, bei der ohne ausreichende Grundlagenforschung klinische Tests durchgeführt wurden. Unerwartete Nebenwirkungen beim Menschen könnten zum Tod des Patienten führen, warnte Hescheler.
Dirk Müller: Als Supermann flog er für die gute Sache über die Kinoleinwände, der amerikanische Schauspieler Christopher Reeve. Nach einem Reitunfall war Reeve querschnittsgelähmt. Seitdem hoffte er auch ganz persönlich auf eine Stammzellentherapie, sammelte Millionenspenden für die Forschung. Christopher Reeve starb im Jahr 2004 im Alter von 52, ohne dass sein Traum in Erfüllung ging. Vielleicht könnte aber dieser Traum jetzt für andere Patienten in Erfüllung gehen, denn erstmals hat die kalifornische Firma Geron die Erlaubnis bekommen, embryonale Stammzellen im Versuch an Menschen einzusetzen - eine sehr umstrittene Entscheidung, weltweit.
Bei uns im Studio hier im Deutschlandfunk ist nun der Kölner Stammzellenforscher Professor Jürgen Hescheler von der Universität in Köln. Guten Morgen!
Jürgen Hescheler: Guten Morgen!
Müller: Herr Hescheler, die Entscheidung jetzt, ist das ein Meilenstein für die Forschung?
Hescheler: Ja. Es ist sicherlich sehr wichtig, dass die embryonale Stammzellforschung jetzt auch in die klinische Anwendung kommt. Allerdings muss man da doch einige Probleme auch sehen. Ich bin der Meinung, dass man da doch vielleicht noch mehr Grundlagenforschung hätte machen sollen. Ich hoffe nur, dass die ersten Versuche von Geron positiv sind, weil wir wollen alle nicht das haben, was ja mit der Gentherapie auch passiert ist, dass da viel zu früh klinische Anwendungen gemacht worden sind, und dann sind Patienten daran gestorben. Das bringt das Gebiet wirklich dann sehr schnell zurück und das wollen wir auf jeden Fall vermeiden.
Müller: Wenn ich Sie richtig verstanden habe, ist die Forschung noch gar nicht so weit, mit Stammzellen am Menschen zu experimentieren?
Hescheler: Na ja, es gibt sehr viele Tierversuche und die Tierversuche sind sicherlich auch sehr positiv gewesen. Aber man muss natürlich sehen, dass das ein sehr komplexes Gebilde ist. Das gilt übrigens auch für die adulten Stammzellen. Die Knochenmarkszellen sind keineswegs so harmlos, wie man das immer darstellt. Man hat ein komplexes Gewebe, in dem Fall das Rückenmark, was ja sehr viele Bahnen hat, wo schon viele Informationen verarbeitet werden, und da jetzt eine fremde Zelle einzuschleusen, das ist auf der zellulären Ebene extrem komplex. Da genau alle Dinge zu beherrschen, das ist recht kompliziert und da hätte ich mir schon gewünscht, dass noch mehr Tierversuche vorher gemacht worden wären.
Müller: Wie groß sind die Risiken denn für den Patienten?
Hescheler: Es gibt verschiedene Möglichkeiten. Entweder, wenn zunächst mal keine negativen Dinge passieren, dann kann es eventuell auch sein, dass nichts Positives passiert, dass also keine Verbesserung da ist. Aber die negative Seite könnte zum Beispiel sein, dass eine Fehldifferenzierung stattfindet, dass die Zellen sich in ein anderes Gewebe entwickeln, etwa Muskelzellen oder so und nicht in Nervenzellgewebe, oder auch dass Tumore entstehen. Auch das muss wirklich sehr gut vorher getestet werden.
Müller: Wenn wir dabei, Herr Hescheler, noch einmal konkret bleiben. Wir haben über die Risiken gesprochen, Sie haben das gerade skizziert. Was heißt das denn konkret für den betroffenen Patienten? Was kann da passieren?
Hescheler: Wenn ein Tumor zum Beispiel entsteht, dann hat man die ganzen Probleme, die der Tumor verursachen könnte, dass die Krankheit noch schlimmer wird und dass der Patient letzten Endes sterben würde. Man hat wirklich, wie erwähnt, bei der Gentherapie auch verfrüht Dinge gemacht, die im Tierversuch funktioniert haben, und hat dann beim Menschen unerwartete Nebenwirkungen entdeckt. Das hat dann letzten Endes zum Tod von einigen Patienten geführt, und das ist auf jeden Fall zu vermeiden.
Müller: Um noch einmal auf den Ausgangspunkt zurückzukommen: das heißt aus Ihrer Sicht ganz klar etwas zu früh?
Hescheler: Ich denke, es ist wie gesagt richtig, dass man auch in Richtung Klinik geht, dass die Vorbereitungen sind. Es heißt ja hier nur, dass die FDA denen grünes Licht gegeben hat, um hier in Richtung klinischer Therapie zu gehen, was sicherlich sehr begrüßenswert ist. Man kann jetzt nur hoffen, dass Geron die hohe Verantwortung sieht und die ersten klinischen Versuche wirklich so vorsichtig macht, die Risiken sehr gut abschätzt, um hier keine Gefährdung vom Patienten darzustellen.
Müller: Die Stammzellenforschung, Professor Hescheler, war ja nun auch in den Vereinigten Staaten unter George Bush unter bestimmten Restriktionen auch gelegt. Die Amerikaner sind in vielen Bereichen nicht viel weiter gekommen, hat man jedenfalls nachlesen können, weil es eben nicht ging. Warum sind es jetzt ausgerechnet die Amerikaner, die diesen Schritt nach vorne tun können?
Hescheler: Die wichtige Änderung ist ja sicherlich der Wechsel des Präsidenten. Obama hat ja schon im Wahlkampf klar gesagt, dass er die Stammzellforschung, die embryonale Stammzellforschung sehr stark unterstützen möchte, und das wird jetzt umgesetzt. Ich denke, es ist natürlich auch sehr wichtig, dass wir uns hier in Deutschland, in Europa die Dinge sehr genau anschauen. Ich denke, wir müssen schauen, dass wir da noch mit dabei bleiben, nicht dass die Amerikaner wirklich jetzt die ganzen Entwicklungen alleine vorantreiben, weil wenn letzten Endes, wenn es wirklich dann zu einer klinischen Anwendung kommt, die erfolgreich ist, dann ist da natürlich auch eine sehr große wirtschaftliche positive Entwicklung für das Land, was die ersten Schritte gemacht hat, vorhanden. Da sollten wir uns sicherlich nicht abhängen lassen.
Müller: Es geht in der Diskussion ja auch oft um den Standortfaktor, das heißt wer kann wo wie weit gehen in der Forschung, was kann er ausprobieren, was kann er experimentieren. Wer ist denn in der Stammzellenforschung derzeit an erster Stelle?
Hescheler: Hier in Europa sind wir sicherlich in England am weitesten. Auch Schweden macht sehr große Fortschritte in der embryonalen Stammzellforschung. In Deutschland hat man ja eher auf die adulten Stammzellen gesetzt, was meiner Ansicht nach der falsche Weg war. Es gibt jetzt aber noch einen dritten Weg, die IPS-Zellen, die Induzierten Pluripotenten Zellen, ein Weg, der aus Japan aufgezeigt worden ist, den wir hier in Deutschland jetzt sehr stark beschreiten wollen. Auch damit kommt man zu pluripotenten Zellen, die sehr ähnlich sind wie die embryonalen Stammzellen. Ich hoffe, dass das mal der Königsweg sein wird, der dann auch beim Patienten definitiv verhindert, dass diese Zellen abgestoßen werden. Das muss man ja auch noch sehen bei den Versuchen von Geron. Da ist ja eine sehr hohe Imunsupression notwendig, um das überhaupt anwenden zu können.
Müller: Sind Sie, Herr Hescheler, als Wissenschaftler hier vor Ort, also in Köln, eingeschränkt in Ihrer Tätigkeit, in dem, was Sie wagen dürfen?
Hescheler: Wir sind da sicherlich doch eingeschränkt durch die Gesetze, die hier in Deutschland herrschen. Bezüglich der embryonalen Stammzellen muss jedes einzelne Experiment vorher beim Robert-Koch-Institut angemeldet werden. Das sind also hohe Hürden. Auch die Förderung, die Drittmittelförderung, von der wir ja alle abhängen, ist sehr stark eingeschränkt für die embryonalen Stammzellen, so dass wir hier nicht mit demselben Maß vorangehen können, wie die Amerikaner das gemacht haben. Auch fehlt bei uns die Kultur, wie Biotechfirmen gefördert werden, auf eigene Beine gestellt werden und dann durch die privaten Gelder, die ja wirklich sehr extrem bei Geron eingeflossen sind, die Förderung oder die Forschung voranzubringen.
Müller: Also in Deutschland zu forschen bei den Stammzellen, ist ein Standortnachteil?
Hescheler: Ja, das würde ich schon so sagen. Einmal durch die gesetzlichen Bestimmungen, durch die Diskussion, die wir haben, durch die eingeschränkten finanziellen Mittel, durch die gesamte universitäre Situation. Alles das ist in Amerika besser und es ist ja auch Tatsache, dass wirklich viele junge deutsche Wissenschaftler nach Amerika gehen, weil sie dort einfach bessere Chancen sehen.
Müller: Kritiker und Ethiker sagen ja, es ist ein hoch riskanter Eingriff in das Leben des Menschen, in die Natur des Menschen. Können Sie das nicht nachvollziehen?
Hescheler: Doch, das sehe ich genauso. Deshalb sage ich ja, die Grundlagenforschung ist sehr wichtig. Ich würde mir wünschen, dass wir in Deutschland intensiv auf die Grundlagenforschung zunächst setzen würden, dass wir die einzelnen Punkte, die bei der Therapie passieren, wirklich gut verstehen. Wenn wir das verstehen, dann kann man allerdings zur klinischen Anwendung kommen. Dann sehe ich die Risiken also nicht so groß.
Müller: Sagen Sie uns noch etwas aus der Praxis. Wenn wir das richtig recherchiert haben, gibt es auch Vorwürfe gegen Sie vom Robert-Koch-Institut. Da geht es um Genehmigungsverfahren, inwieweit Sie geforscht haben, was noch nicht ganz genehmigt war. Worum geht es da genau?
Hescheler: Wir haben Experimente durchgeführt, wo wir der Auffassung sind, dass wir hier die Genehmigung haben. Das Robert-Koch-Institut hat im Nachhinein gesagt, dass sie das anders sehen. Da hat es eine Diskussion mit dem Robert-Koch-Institut gegeben, die hoffentlich bald abgeschlossen sein wird. Für die Zukunft wissen wir, wie wir das dann besser handhaben sollten, dass wir früher das Robert-Koch-Institut informieren sollten. Ich denke, das ist wichtig, dass man da gegenseitig mehr dann miteinander spricht und die Informationen austauscht, so dass das in Zukunft doch klarer wird.
Müller: Es gibt ja einen politischen Prozess, auch im Bundestag immer wieder die Auseinandersetzung um diesen ominösen Stichtag. Es geht darum: Wann kann man Stammzellen benutzen und wann nicht. Kann man mit dieser Regelung, die im Moment aktuell ist, eigentlich inzwischen ganz gut leben?
Hescheler: Im Frühjahr letzten Jahres ist ja der Stichtag noch mal verschoben worden auf 2007. Das heißt, wir können jetzt auch neuere Stammzell-Linien einführen.
Müller: Und neuere sind immer besser?
Hescheler: Ja. Das Problem war, dass die alten Linien, mit denen wir im Moment auch noch arbeiten, wahrscheinlich genetische Veränderungen haben, dass die nicht mehr so gut sind. Deshalb ist es da immer wichtig, viele Kontrollversuche auch zu machen. Die neueren Linien sollen angeblich besser sein. Das sind wir im Moment am prüfen und wir versuchen, auch dann neuere Linien zu importieren, und an denen kann man dann hoffentlich noch bessere, noch relevantere Forschungen machen, weil wenn die Zellen nicht mehr so gut sind, dann weiß man nicht, ob die Ergebnisse entsprechend auch das Abbild darstellen, was sie sein sollten.
Müller: Bei uns im Deutschlandfunk-Studio hier in Köln der Kölner Stammzellenforscher Professor Jürgen Hescheler von der Universität in der Domstadt. Vielen Dank für das Gespräch.
Hescheler: Danke schön.
Stammzellenforscher über die Risiken und Chancen der Versuche am Menschen
Jürgen Hescheler im Gespräch mit Dirk Müller
Die erste Genehmigung für Forschungstests mit embryonalen Stammzellen am Menschen in den USA hat der Kölner Stammzellenforscher Professor Jürgen Hescheler grundsätzlich als Meilenstein begrüßt. Gleichzeitig warnte er vor ähnlichen Fehlern wie bei der Gentherapie, bei der ohne ausreichende Grundlagenforschung klinische Tests durchgeführt wurden. Unerwartete Nebenwirkungen beim Menschen könnten zum Tod des Patienten führen, warnte Hescheler.
Dirk Müller: Als Supermann flog er für die gute Sache über die Kinoleinwände, der amerikanische Schauspieler Christopher Reeve. Nach einem Reitunfall war Reeve querschnittsgelähmt. Seitdem hoffte er auch ganz persönlich auf eine Stammzellentherapie, sammelte Millionenspenden für die Forschung. Christopher Reeve starb im Jahr 2004 im Alter von 52, ohne dass sein Traum in Erfüllung ging. Vielleicht könnte aber dieser Traum jetzt für andere Patienten in Erfüllung gehen, denn erstmals hat die kalifornische Firma Geron die Erlaubnis bekommen, embryonale Stammzellen im Versuch an Menschen einzusetzen - eine sehr umstrittene Entscheidung, weltweit.
Bei uns im Studio hier im Deutschlandfunk ist nun der Kölner Stammzellenforscher Professor Jürgen Hescheler von der Universität in Köln. Guten Morgen!
Jürgen Hescheler: Guten Morgen!
Müller: Herr Hescheler, die Entscheidung jetzt, ist das ein Meilenstein für die Forschung?
Hescheler: Ja. Es ist sicherlich sehr wichtig, dass die embryonale Stammzellforschung jetzt auch in die klinische Anwendung kommt. Allerdings muss man da doch einige Probleme auch sehen. Ich bin der Meinung, dass man da doch vielleicht noch mehr Grundlagenforschung hätte machen sollen. Ich hoffe nur, dass die ersten Versuche von Geron positiv sind, weil wir wollen alle nicht das haben, was ja mit der Gentherapie auch passiert ist, dass da viel zu früh klinische Anwendungen gemacht worden sind, und dann sind Patienten daran gestorben. Das bringt das Gebiet wirklich dann sehr schnell zurück und das wollen wir auf jeden Fall vermeiden.
Müller: Wenn ich Sie richtig verstanden habe, ist die Forschung noch gar nicht so weit, mit Stammzellen am Menschen zu experimentieren?
Hescheler: Na ja, es gibt sehr viele Tierversuche und die Tierversuche sind sicherlich auch sehr positiv gewesen. Aber man muss natürlich sehen, dass das ein sehr komplexes Gebilde ist. Das gilt übrigens auch für die adulten Stammzellen. Die Knochenmarkszellen sind keineswegs so harmlos, wie man das immer darstellt. Man hat ein komplexes Gewebe, in dem Fall das Rückenmark, was ja sehr viele Bahnen hat, wo schon viele Informationen verarbeitet werden, und da jetzt eine fremde Zelle einzuschleusen, das ist auf der zellulären Ebene extrem komplex. Da genau alle Dinge zu beherrschen, das ist recht kompliziert und da hätte ich mir schon gewünscht, dass noch mehr Tierversuche vorher gemacht worden wären.
Müller: Wie groß sind die Risiken denn für den Patienten?
Hescheler: Es gibt verschiedene Möglichkeiten. Entweder, wenn zunächst mal keine negativen Dinge passieren, dann kann es eventuell auch sein, dass nichts Positives passiert, dass also keine Verbesserung da ist. Aber die negative Seite könnte zum Beispiel sein, dass eine Fehldifferenzierung stattfindet, dass die Zellen sich in ein anderes Gewebe entwickeln, etwa Muskelzellen oder so und nicht in Nervenzellgewebe, oder auch dass Tumore entstehen. Auch das muss wirklich sehr gut vorher getestet werden.
Müller: Wenn wir dabei, Herr Hescheler, noch einmal konkret bleiben. Wir haben über die Risiken gesprochen, Sie haben das gerade skizziert. Was heißt das denn konkret für den betroffenen Patienten? Was kann da passieren?
Hescheler: Wenn ein Tumor zum Beispiel entsteht, dann hat man die ganzen Probleme, die der Tumor verursachen könnte, dass die Krankheit noch schlimmer wird und dass der Patient letzten Endes sterben würde. Man hat wirklich, wie erwähnt, bei der Gentherapie auch verfrüht Dinge gemacht, die im Tierversuch funktioniert haben, und hat dann beim Menschen unerwartete Nebenwirkungen entdeckt. Das hat dann letzten Endes zum Tod von einigen Patienten geführt, und das ist auf jeden Fall zu vermeiden.
Müller: Um noch einmal auf den Ausgangspunkt zurückzukommen: das heißt aus Ihrer Sicht ganz klar etwas zu früh?
Hescheler: Ich denke, es ist wie gesagt richtig, dass man auch in Richtung Klinik geht, dass die Vorbereitungen sind. Es heißt ja hier nur, dass die FDA denen grünes Licht gegeben hat, um hier in Richtung klinischer Therapie zu gehen, was sicherlich sehr begrüßenswert ist. Man kann jetzt nur hoffen, dass Geron die hohe Verantwortung sieht und die ersten klinischen Versuche wirklich so vorsichtig macht, die Risiken sehr gut abschätzt, um hier keine Gefährdung vom Patienten darzustellen.
Müller: Die Stammzellenforschung, Professor Hescheler, war ja nun auch in den Vereinigten Staaten unter George Bush unter bestimmten Restriktionen auch gelegt. Die Amerikaner sind in vielen Bereichen nicht viel weiter gekommen, hat man jedenfalls nachlesen können, weil es eben nicht ging. Warum sind es jetzt ausgerechnet die Amerikaner, die diesen Schritt nach vorne tun können?
Hescheler: Die wichtige Änderung ist ja sicherlich der Wechsel des Präsidenten. Obama hat ja schon im Wahlkampf klar gesagt, dass er die Stammzellforschung, die embryonale Stammzellforschung sehr stark unterstützen möchte, und das wird jetzt umgesetzt. Ich denke, es ist natürlich auch sehr wichtig, dass wir uns hier in Deutschland, in Europa die Dinge sehr genau anschauen. Ich denke, wir müssen schauen, dass wir da noch mit dabei bleiben, nicht dass die Amerikaner wirklich jetzt die ganzen Entwicklungen alleine vorantreiben, weil wenn letzten Endes, wenn es wirklich dann zu einer klinischen Anwendung kommt, die erfolgreich ist, dann ist da natürlich auch eine sehr große wirtschaftliche positive Entwicklung für das Land, was die ersten Schritte gemacht hat, vorhanden. Da sollten wir uns sicherlich nicht abhängen lassen.
Müller: Es geht in der Diskussion ja auch oft um den Standortfaktor, das heißt wer kann wo wie weit gehen in der Forschung, was kann er ausprobieren, was kann er experimentieren. Wer ist denn in der Stammzellenforschung derzeit an erster Stelle?
Hescheler: Hier in Europa sind wir sicherlich in England am weitesten. Auch Schweden macht sehr große Fortschritte in der embryonalen Stammzellforschung. In Deutschland hat man ja eher auf die adulten Stammzellen gesetzt, was meiner Ansicht nach der falsche Weg war. Es gibt jetzt aber noch einen dritten Weg, die IPS-Zellen, die Induzierten Pluripotenten Zellen, ein Weg, der aus Japan aufgezeigt worden ist, den wir hier in Deutschland jetzt sehr stark beschreiten wollen. Auch damit kommt man zu pluripotenten Zellen, die sehr ähnlich sind wie die embryonalen Stammzellen. Ich hoffe, dass das mal der Königsweg sein wird, der dann auch beim Patienten definitiv verhindert, dass diese Zellen abgestoßen werden. Das muss man ja auch noch sehen bei den Versuchen von Geron. Da ist ja eine sehr hohe Imunsupression notwendig, um das überhaupt anwenden zu können.
Müller: Sind Sie, Herr Hescheler, als Wissenschaftler hier vor Ort, also in Köln, eingeschränkt in Ihrer Tätigkeit, in dem, was Sie wagen dürfen?
Hescheler: Wir sind da sicherlich doch eingeschränkt durch die Gesetze, die hier in Deutschland herrschen. Bezüglich der embryonalen Stammzellen muss jedes einzelne Experiment vorher beim Robert-Koch-Institut angemeldet werden. Das sind also hohe Hürden. Auch die Förderung, die Drittmittelförderung, von der wir ja alle abhängen, ist sehr stark eingeschränkt für die embryonalen Stammzellen, so dass wir hier nicht mit demselben Maß vorangehen können, wie die Amerikaner das gemacht haben. Auch fehlt bei uns die Kultur, wie Biotechfirmen gefördert werden, auf eigene Beine gestellt werden und dann durch die privaten Gelder, die ja wirklich sehr extrem bei Geron eingeflossen sind, die Förderung oder die Forschung voranzubringen.
Müller: Also in Deutschland zu forschen bei den Stammzellen, ist ein Standortnachteil?
Hescheler: Ja, das würde ich schon so sagen. Einmal durch die gesetzlichen Bestimmungen, durch die Diskussion, die wir haben, durch die eingeschränkten finanziellen Mittel, durch die gesamte universitäre Situation. Alles das ist in Amerika besser und es ist ja auch Tatsache, dass wirklich viele junge deutsche Wissenschaftler nach Amerika gehen, weil sie dort einfach bessere Chancen sehen.
Müller: Kritiker und Ethiker sagen ja, es ist ein hoch riskanter Eingriff in das Leben des Menschen, in die Natur des Menschen. Können Sie das nicht nachvollziehen?
Hescheler: Doch, das sehe ich genauso. Deshalb sage ich ja, die Grundlagenforschung ist sehr wichtig. Ich würde mir wünschen, dass wir in Deutschland intensiv auf die Grundlagenforschung zunächst setzen würden, dass wir die einzelnen Punkte, die bei der Therapie passieren, wirklich gut verstehen. Wenn wir das verstehen, dann kann man allerdings zur klinischen Anwendung kommen. Dann sehe ich die Risiken also nicht so groß.
Müller: Sagen Sie uns noch etwas aus der Praxis. Wenn wir das richtig recherchiert haben, gibt es auch Vorwürfe gegen Sie vom Robert-Koch-Institut. Da geht es um Genehmigungsverfahren, inwieweit Sie geforscht haben, was noch nicht ganz genehmigt war. Worum geht es da genau?
Hescheler: Wir haben Experimente durchgeführt, wo wir der Auffassung sind, dass wir hier die Genehmigung haben. Das Robert-Koch-Institut hat im Nachhinein gesagt, dass sie das anders sehen. Da hat es eine Diskussion mit dem Robert-Koch-Institut gegeben, die hoffentlich bald abgeschlossen sein wird. Für die Zukunft wissen wir, wie wir das dann besser handhaben sollten, dass wir früher das Robert-Koch-Institut informieren sollten. Ich denke, das ist wichtig, dass man da gegenseitig mehr dann miteinander spricht und die Informationen austauscht, so dass das in Zukunft doch klarer wird.
Müller: Es gibt ja einen politischen Prozess, auch im Bundestag immer wieder die Auseinandersetzung um diesen ominösen Stichtag. Es geht darum: Wann kann man Stammzellen benutzen und wann nicht. Kann man mit dieser Regelung, die im Moment aktuell ist, eigentlich inzwischen ganz gut leben?
Hescheler: Im Frühjahr letzten Jahres ist ja der Stichtag noch mal verschoben worden auf 2007. Das heißt, wir können jetzt auch neuere Stammzell-Linien einführen.
Müller: Und neuere sind immer besser?
Hescheler: Ja. Das Problem war, dass die alten Linien, mit denen wir im Moment auch noch arbeiten, wahrscheinlich genetische Veränderungen haben, dass die nicht mehr so gut sind. Deshalb ist es da immer wichtig, viele Kontrollversuche auch zu machen. Die neueren Linien sollen angeblich besser sein. Das sind wir im Moment am prüfen und wir versuchen, auch dann neuere Linien zu importieren, und an denen kann man dann hoffentlich noch bessere, noch relevantere Forschungen machen, weil wenn die Zellen nicht mehr so gut sind, dann weiß man nicht, ob die Ergebnisse entsprechend auch das Abbild darstellen, was sie sein sollten.
Müller: Bei uns im Deutschlandfunk-Studio hier in Köln der Kölner Stammzellenforscher Professor Jürgen Hescheler von der Universität in der Domstadt. Vielen Dank für das Gespräch.
Hescheler: Danke schön.
Wieder gehen dank Stammzellen
Neuartige Therapie soll am Menschen erprobt werden
Von Arndt Reuning
Medizin. - Die amerikanische Arzneimittelbehörde FDA hat die weltweit erste Genehmigung für eine Therapie mit embryonalen Stammzellen am Menschen erteilt. Somit dürften erste klinische Tests an freiwilligen Patienten mit Querschnittslähmung durchgeführt werden.
Gelähmte könnten eines Tages wieder gehen. Diese Hoffnung steckt hinter der Stammzelltherapie, welche das kalifornische Biotechnologie-Unternehmen Geron Corporation nun an Menschen erproben möchte. Aus humanen embryonalen Stammzellen haben die Forscher ein Präparat entwickelt, das im Rückenmark der Patienten verletzte Nervenzellen teilweise wiederherstellen soll. Allzu große Erwartungen auf eine vollständige Heilung dämpft aber der Geron-Geschäftsführer, Thomas Okarma.
"Indem wir diesen Patienten unsere Zellen injizieren, hoffen wir, dass sich ihr Zustand bessern wird. Von einem Leben im Rollstuhl hin zu einem Leben, wie es teilgelähmte Menschen führen - so dass sie an einer Physiotherapie teilnehmen können. Das ist unser Behandlungsziel."
Im Tierversuch an gelähmten Ratten konnten die Wissenschaftler den Tieren einen Teil ihrer Bewegungsfähigkeit zurück geben. Die im Sommer anlaufende Studie an Menschen soll zunächst klären, ob die Behandlung keine Risiken für die Patienten birgt. Ihr körpereigenes Immunsystem könnte die fremden Zellen nämlich abstoßen. Entzündungen wären die Folge. Deshalb werden die Studienteilnehmer in den ersten Wochen Medikamente erhalten, die solche Immunreaktionen unterdrücken. Auf längere Sicht besteht die Gefahr, dass die Zellen anfangen, unkontrolliert zu wuchern.
"Es geht dabei nicht um Krebs, sondern um so genannte Teratome. Das sind gutartige Wucherungen, die man aber im Rückenmark natürlich trotzdem nicht haben will. Wir haben das bei den Ratten zwölf Monate lang untersucht und kein einziges Teratom in den Tieren gefunden."
Vier Jahre haben die Geron-Wissenschaftler für die Genehmigung der klinischen Studie geforscht, knapp 22.000 Seiten sind für den Antrag zusammen gekommen. Im vergangenen Mai hatte die Zulassungsbehörde FDA das Verfahren aber erst einmal auf Eis gelegt. Manche Beobachter hatten vermutet, dass die Behörde es lieber gesehen hätte, wenn die allererste Therapie mit embryonalen Stammzellen nicht an einem solch komplexen Gebilde wie dem Zentralen Nervensystem erprobt würde. Ein Fehlschlag könnte dem ganzen Arbeitsgebiet schaden und es um Jahre zurück werfen. Andererseits wächst der Druck von Seiten der Patientenvereinigungen, die fordern, dass die Therapien aus dem Labor nun endlich ihren Weg in die Klinik finden sollen.
Die Entscheidung der FDA kommt nun zu einem Zeitpunkt, der eine Wende in der Stammzellpolitik der US-Regierung einleiten könnte. Die Forschergemeinschaft erwartet, dass Präsident Obama das Verbot der Vorgänger-Regierung aufheben wird. George W. Bush hatte angeordnet, dass Fördergelder der Bundesregierung nur an solche Projekte fließen sollen, die mit Stammzelllinien arbeiten, die schon vor dem 9. August 2001 existiert haben. Viele Wissenschaftler sehen das als nicht praktikabel an, sagt Susan Solomon von der privaten Förderorganisation New York Stem Cell Foundation.
"Diese Zelllinien sind wirklich veraltet. Niemand, der etwas auf sich hält, möchte an ihnen forschen. Sie sind einfach überholt und sie verhalten sich nicht immer so, wie sie es sollten."
Interessanterweise hat die Geron Corporation aber genau auf jene alten Linien zurückgegriffen, die unter dem Bush-Erlass frei gegeben waren. Trotzdem hat das Biotechnologie-Unternehmen für das Projekt keine Fördermittel vom der amerikanische Bundesregierung beantragt.
Neuartige Therapie soll am Menschen erprobt werden
Von Arndt Reuning
Medizin. - Die amerikanische Arzneimittelbehörde FDA hat die weltweit erste Genehmigung für eine Therapie mit embryonalen Stammzellen am Menschen erteilt. Somit dürften erste klinische Tests an freiwilligen Patienten mit Querschnittslähmung durchgeführt werden.
Gelähmte könnten eines Tages wieder gehen. Diese Hoffnung steckt hinter der Stammzelltherapie, welche das kalifornische Biotechnologie-Unternehmen Geron Corporation nun an Menschen erproben möchte. Aus humanen embryonalen Stammzellen haben die Forscher ein Präparat entwickelt, das im Rückenmark der Patienten verletzte Nervenzellen teilweise wiederherstellen soll. Allzu große Erwartungen auf eine vollständige Heilung dämpft aber der Geron-Geschäftsführer, Thomas Okarma.
"Indem wir diesen Patienten unsere Zellen injizieren, hoffen wir, dass sich ihr Zustand bessern wird. Von einem Leben im Rollstuhl hin zu einem Leben, wie es teilgelähmte Menschen führen - so dass sie an einer Physiotherapie teilnehmen können. Das ist unser Behandlungsziel."
Im Tierversuch an gelähmten Ratten konnten die Wissenschaftler den Tieren einen Teil ihrer Bewegungsfähigkeit zurück geben. Die im Sommer anlaufende Studie an Menschen soll zunächst klären, ob die Behandlung keine Risiken für die Patienten birgt. Ihr körpereigenes Immunsystem könnte die fremden Zellen nämlich abstoßen. Entzündungen wären die Folge. Deshalb werden die Studienteilnehmer in den ersten Wochen Medikamente erhalten, die solche Immunreaktionen unterdrücken. Auf längere Sicht besteht die Gefahr, dass die Zellen anfangen, unkontrolliert zu wuchern.
"Es geht dabei nicht um Krebs, sondern um so genannte Teratome. Das sind gutartige Wucherungen, die man aber im Rückenmark natürlich trotzdem nicht haben will. Wir haben das bei den Ratten zwölf Monate lang untersucht und kein einziges Teratom in den Tieren gefunden."
Vier Jahre haben die Geron-Wissenschaftler für die Genehmigung der klinischen Studie geforscht, knapp 22.000 Seiten sind für den Antrag zusammen gekommen. Im vergangenen Mai hatte die Zulassungsbehörde FDA das Verfahren aber erst einmal auf Eis gelegt. Manche Beobachter hatten vermutet, dass die Behörde es lieber gesehen hätte, wenn die allererste Therapie mit embryonalen Stammzellen nicht an einem solch komplexen Gebilde wie dem Zentralen Nervensystem erprobt würde. Ein Fehlschlag könnte dem ganzen Arbeitsgebiet schaden und es um Jahre zurück werfen. Andererseits wächst der Druck von Seiten der Patientenvereinigungen, die fordern, dass die Therapien aus dem Labor nun endlich ihren Weg in die Klinik finden sollen.
Die Entscheidung der FDA kommt nun zu einem Zeitpunkt, der eine Wende in der Stammzellpolitik der US-Regierung einleiten könnte. Die Forschergemeinschaft erwartet, dass Präsident Obama das Verbot der Vorgänger-Regierung aufheben wird. George W. Bush hatte angeordnet, dass Fördergelder der Bundesregierung nur an solche Projekte fließen sollen, die mit Stammzelllinien arbeiten, die schon vor dem 9. August 2001 existiert haben. Viele Wissenschaftler sehen das als nicht praktikabel an, sagt Susan Solomon von der privaten Förderorganisation New York Stem Cell Foundation.
"Diese Zelllinien sind wirklich veraltet. Niemand, der etwas auf sich hält, möchte an ihnen forschen. Sie sind einfach überholt und sie verhalten sich nicht immer so, wie sie es sollten."
Interessanterweise hat die Geron Corporation aber genau auf jene alten Linien zurückgegriffen, die unter dem Bush-Erlass frei gegeben waren. Trotzdem hat das Biotechnologie-Unternehmen für das Projekt keine Fördermittel vom der amerikanische Bundesregierung beantragt.
Ärzte Zeitung online, 27.01.2009 12:01
Ja zu Stammzellentherapie in den USA: Zufall oder Omen für bessere Zeiten?
NEW YORK (dpa). So schnell hatte wohl niemand mit dem Wandel gerechnet. Der neue US-Präsident Barack Obama hatte kaum seinen Amtseid abgelegt, als in Amerika auch schon das Zeitalter der Stammzelltherapien anbrach: Dienstag vergangener Woche hat die US-amerikanische Gesundheitsbehörde FDA eine Studie mit embryonalen Stammzellen genehmigt (wir berichteten).
Die Vermutung lag nah, dass die Freigabe des ersten klinischen Versuchs mit embryonalen Stammzellen dem frischen Wind in der US-Politik zu verdanken war. Weit gefehlt, behauptet die Gesundheitsbehörde FDA (Food and Drug Administration). Dass ihre Zusage gleich nach dem Wechsel im Weißen Haus erfolgte, "war reiner Zufall", bekräftigte FDA-Sprecherin Karen Riley am Montag in Bethesda bei Washington.
Zufall oder nicht: Für die amerikanische Wissenschaft ist das "Ja" zur ethisch umstrittenen Stammzellentherapie wie ein Silberstreif am lange verhangenen Himmel. Unter der Regierung von George W. Bush war die Forschung mit den Zellen von Ungeborenen wegen der Auflagen aus Washington so gut wie zum Erliegen gekommen. Der Mangel an Forschungsgeldern ließ auch andere hochkarätige Wissenschaftler ins Ausland abwandern.
Der "Brain Drain" in den USA kam unter anderem Kanada zugute: Zwischen 2002 und 2007 stieg die Zahl amerikanischer Lehrer im nördlichen Nachbarland nach Angaben der kanadischen Einwanderbehörde um 15 Prozent, die der Professoren und Hochschulassistenten sogar um 17 Prozent.
"Das Schlimme war, dass Forschungslabore an renommierten Universitäten wie Stanford und Harvard plötzlich zumachen mussten, obwohl sie 20 und mehr Jahre (aus Washington) unterstützt worden waren", beschreibt Professor Guri Giaever von der Universität von Toronto den Wandel unter Bush. Die Genforscherin war 2006 mit ihrem Mann und Laborpartner Doktor Corey Nislow nach Kanada gegangen, weil es in San Francisco keine Mittel mehr gab.
In den Vereinigten Staaten blieb derweil der Nachschub aus. Einige Nachwuchsforscher aus Europa und Asien scheiterten an den neuen Visa-Beschränkungen der Bush-Administration, andere blieben wegen der knapper werdenden Angebote von Forschungsplätzen fern. Die Maßnahmen schlossen nach Einschätzung von Beobachtern "eine ganze Generation junger Wissenschaftler" aus den USA aus.
Derweil gewannen die Kreationisten mit ihrer Absage an Darwins Evolutionslehre in Amerikas sogenanntem "Bibel-Gürtel" zunehmend Oberwasser. Einige Bundesstaaten strichen den Aufklärungsunterricht an ihren Schulen. Washington bezweifelte die wissenschaftlich belegten Ursachen des Klimawandels. In Forscherkreisen wurden die Vereinigten Staaten wegen ihrer "Rückkehr ins Mittelalter" verspottet und bemitleidet.
Erst im Wahljahr 2008 kam wieder Hoffnung auf. Obama versprach, sich für Bildung, Umwelt, alternative Energien und das amerikanische Gesundheitswesen einsetzen. Selbst in seiner Antrittsrede vor dem Capitol am vergangenen Dienstag verhieß der neue Präsident seinen Landsleuten, "der Wissenschaft wieder den ihr gebührenden Rang einzuräumen". Kein Wunder also, dass auch der Durchbruch in der seit 2001 zum Teil kaltgestellten Stammzellenforschung ihm zugute gehalten wurde.
Dazu sagt die FDA, dass nicht der Regierungswechsel, sondern ein Treffen ihres Beraterausschusses im April vergangenen Jahres den Ausschlag gegeben habe. Damals seien im Prinzip die Würfel gefallen, sagte Riley der Deutschen Presse-Agentur dpa. Dass die Biotech-Firma Geron in Menlo Park (Kalifornien) erst jetzt Bescheid erhielt, lag ihren Angaben nach an der schleppenden Beantwortung von Fragen durch das Unternehmen sowie an einer vorgeschriebenen Wartefrist.
Ja zu Stammzellentherapie in den USA: Zufall oder Omen für bessere Zeiten?
NEW YORK (dpa). So schnell hatte wohl niemand mit dem Wandel gerechnet. Der neue US-Präsident Barack Obama hatte kaum seinen Amtseid abgelegt, als in Amerika auch schon das Zeitalter der Stammzelltherapien anbrach: Dienstag vergangener Woche hat die US-amerikanische Gesundheitsbehörde FDA eine Studie mit embryonalen Stammzellen genehmigt (wir berichteten).
Die Vermutung lag nah, dass die Freigabe des ersten klinischen Versuchs mit embryonalen Stammzellen dem frischen Wind in der US-Politik zu verdanken war. Weit gefehlt, behauptet die Gesundheitsbehörde FDA (Food and Drug Administration). Dass ihre Zusage gleich nach dem Wechsel im Weißen Haus erfolgte, "war reiner Zufall", bekräftigte FDA-Sprecherin Karen Riley am Montag in Bethesda bei Washington.
Zufall oder nicht: Für die amerikanische Wissenschaft ist das "Ja" zur ethisch umstrittenen Stammzellentherapie wie ein Silberstreif am lange verhangenen Himmel. Unter der Regierung von George W. Bush war die Forschung mit den Zellen von Ungeborenen wegen der Auflagen aus Washington so gut wie zum Erliegen gekommen. Der Mangel an Forschungsgeldern ließ auch andere hochkarätige Wissenschaftler ins Ausland abwandern.
Der "Brain Drain" in den USA kam unter anderem Kanada zugute: Zwischen 2002 und 2007 stieg die Zahl amerikanischer Lehrer im nördlichen Nachbarland nach Angaben der kanadischen Einwanderbehörde um 15 Prozent, die der Professoren und Hochschulassistenten sogar um 17 Prozent.
"Das Schlimme war, dass Forschungslabore an renommierten Universitäten wie Stanford und Harvard plötzlich zumachen mussten, obwohl sie 20 und mehr Jahre (aus Washington) unterstützt worden waren", beschreibt Professor Guri Giaever von der Universität von Toronto den Wandel unter Bush. Die Genforscherin war 2006 mit ihrem Mann und Laborpartner Doktor Corey Nislow nach Kanada gegangen, weil es in San Francisco keine Mittel mehr gab.
In den Vereinigten Staaten blieb derweil der Nachschub aus. Einige Nachwuchsforscher aus Europa und Asien scheiterten an den neuen Visa-Beschränkungen der Bush-Administration, andere blieben wegen der knapper werdenden Angebote von Forschungsplätzen fern. Die Maßnahmen schlossen nach Einschätzung von Beobachtern "eine ganze Generation junger Wissenschaftler" aus den USA aus.
Derweil gewannen die Kreationisten mit ihrer Absage an Darwins Evolutionslehre in Amerikas sogenanntem "Bibel-Gürtel" zunehmend Oberwasser. Einige Bundesstaaten strichen den Aufklärungsunterricht an ihren Schulen. Washington bezweifelte die wissenschaftlich belegten Ursachen des Klimawandels. In Forscherkreisen wurden die Vereinigten Staaten wegen ihrer "Rückkehr ins Mittelalter" verspottet und bemitleidet.
Erst im Wahljahr 2008 kam wieder Hoffnung auf. Obama versprach, sich für Bildung, Umwelt, alternative Energien und das amerikanische Gesundheitswesen einsetzen. Selbst in seiner Antrittsrede vor dem Capitol am vergangenen Dienstag verhieß der neue Präsident seinen Landsleuten, "der Wissenschaft wieder den ihr gebührenden Rang einzuräumen". Kein Wunder also, dass auch der Durchbruch in der seit 2001 zum Teil kaltgestellten Stammzellenforschung ihm zugute gehalten wurde.
Dazu sagt die FDA, dass nicht der Regierungswechsel, sondern ein Treffen ihres Beraterausschusses im April vergangenen Jahres den Ausschlag gegeben habe. Damals seien im Prinzip die Würfel gefallen, sagte Riley der Deutschen Presse-Agentur dpa. Dass die Biotech-Firma Geron in Menlo Park (Kalifornien) erst jetzt Bescheid erhielt, lag ihren Angaben nach an der schleppenden Beantwortung von Fragen durch das Unternehmen sowie an einer vorgeschriebenen Wartefrist.
http://finance.yahoo.com/news/Geron-Announces-John-Walker-bw…
Wieso geht er gerade jetzt?
(Bin aktuell nicht investiert, aber habe sie auf dem watchlist)
Wieso geht er gerade jetzt?

(Bin aktuell nicht investiert, aber habe sie auf dem watchlist)

gute Frage... ich denke, er muss wegen einiger rechtlichen Sachen zurücktreten... liegt am Merger von Novacea und Transcept!
Walker ist auch in vielen anderen Biotech Unternehmen im Board!!!
Im Text steht:
I have accepted a position to head another company, following the closing of the Novacea and Transcept merger, which shall be announced shortly, and must in that context resign as a Geron Director.
John P. Walker
Chief Executive Officer and Chairman of the Board
Mr. Walker is an experienced leader in the biotechnology industry and has served as Novacea's Chairman since August of 2006. Mr. Walker also currently is Chairman of the Board of Directors for Renovis, Inc.and serves on the Board of Directors for Affymax, Inc. and Geron Corporation. During his 35-year career, Mr. Walker has served as Chairman, CEO, or Interim CEO of a number of biotechnology and pharmaceutical companies, including KAI Pharmaceuticals and Guava Technologies. From 1993 to 2001, he was Chairman, CEO, and a Director of AXYS Pharmaceuticals Inc. and its predecessor company, Arris Pharmaceutical Corporation. Prior to Arris, Mr. Walker was Chairman and CEO of Vitaphore Corporation, a biomaterials company that was sold to Union Carbide Chemical and Plastics Company, Inc. Mr. Walker began his career with American Hospital Supply Corporation, where he held a variety of general management, sales, and operational positions. Mr. Walker also has served as President of American Medical Systems and The Hospital Company.
Walker ist auch in vielen anderen Biotech Unternehmen im Board!!!
Im Text steht:
I have accepted a position to head another company, following the closing of the Novacea and Transcept merger, which shall be announced shortly, and must in that context resign as a Geron Director.
John P. Walker
Chief Executive Officer and Chairman of the Board
Mr. Walker is an experienced leader in the biotechnology industry and has served as Novacea's Chairman since August of 2006. Mr. Walker also currently is Chairman of the Board of Directors for Renovis, Inc.and serves on the Board of Directors for Affymax, Inc. and Geron Corporation. During his 35-year career, Mr. Walker has served as Chairman, CEO, or Interim CEO of a number of biotechnology and pharmaceutical companies, including KAI Pharmaceuticals and Guava Technologies. From 1993 to 2001, he was Chairman, CEO, and a Director of AXYS Pharmaceuticals Inc. and its predecessor company, Arris Pharmaceutical Corporation. Prior to Arris, Mr. Walker was Chairman and CEO of Vitaphore Corporation, a biomaterials company that was sold to Union Carbide Chemical and Plastics Company, Inc. Mr. Walker began his career with American Hospital Supply Corporation, where he held a variety of general management, sales, and operational positions. Mr. Walker also has served as President of American Medical Systems and The Hospital Company.
Here we go!
http://www.whas11.com/medical/stories/012409whascwTopStemCel…
President Obama to reverse stem cell research funding restrictions
04:31 PM EST on Tuesday, January 27, 2009
Early next week, President Obama is planning on reversing the restrictions imposed by President Bush, which will allow federal funding of embryonic stem cell research.
This is major, new health news from the office of the president, for supporters of those asking for permission to use embryonic stem cells in clinical trials to treat human paralysis.
The first trial is already planned and will be small; only eight-to-ten people in a bio tech company in California. The patients will be paraplegics who can use their arms, but cannot walk. They will receive one injection within two weeks of their injury.
Dr. David Scadden, Harvard Stem Cell Institute, said “If we could have any evidence of activity, if they could now feel cold, or warm or touch, that would be a sign of success.”
This first test will show only if the cells are safe in humans. Animal research has been very successful. Scientists have helped paralyzed rats walk again by repairing damaged nerve endings in their spines.
Web story published by Chris Wright
http://www.whas11.com/medical/stories/012409whascwTopStemCel…
President Obama to reverse stem cell research funding restrictions
04:31 PM EST on Tuesday, January 27, 2009
Early next week, President Obama is planning on reversing the restrictions imposed by President Bush, which will allow federal funding of embryonic stem cell research.
This is major, new health news from the office of the president, for supporters of those asking for permission to use embryonic stem cells in clinical trials to treat human paralysis.
The first trial is already planned and will be small; only eight-to-ten people in a bio tech company in California. The patients will be paraplegics who can use their arms, but cannot walk. They will receive one injection within two weeks of their injury.
Dr. David Scadden, Harvard Stem Cell Institute, said “If we could have any evidence of activity, if they could now feel cold, or warm or touch, that would be a sign of success.”
This first test will show only if the cells are safe in humans. Animal research has been very successful. Scientists have helped paralyzed rats walk again by repairing damaged nerve endings in their spines.
Web story published by Chris Wright
January 29, 2009, 2:15 PM
Obama's Science Grade, A New Ice Age, And A Hint Of Google
Posted by Daniel Sieberg
Scientists across the country have heralded the Obama administration's approach to research and development. Already it’s a stark contrast to the Bush years. But what exactly will be done for areas like stem cells, global warming, and space exploration?
These are some of the questions that we try to answer in an upcoming story for the CBS Evening News with Katie Couric. It may be airing tomorrow (Friday) night. We spoke to a number of prominent people from all those fields about their expectations and hopes. We also talked to one woman who may be directly affected by any policy decisions; she puts a human face on all the scientific data and studies.
Also, before cozying up for commercials and football this weekend, I hope you'll tune in to CBS Sunday Morning. It's the 30th anniversary edition of the beloved program (OK, I'm a little biased), and I'm contributed a story about ice. Yes, ice. As in cubes. But not just any old frozen water. For those who enjoy imbibing a good cocktail it can be the unsung hero by adding a touch of class or esthetic. But at too many bars or (Super Bowl) parties the ice ends up melting in such a hurry that it ruins the work of your favorite mixologist. It's also a story about people who carve ice, eat ice (true), and generally believe that ice is now hot. You'll have to watch to find out more -- including the secrets to a bar in Las Vegas that's all made of ice, even the glasses.
Finally, a little teaser -- on Monday night's CBS Evening News with Katie Couric we're planning to have a story about a new Google tool. Can't say more than that right now but I hope you'll join us.
In the meantime, stay connected.
http://www.cbsnews.com/blogs/2009/01/29/eveningnews/techtalk…
Obama's Science Grade, A New Ice Age, And A Hint Of Google
Posted by Daniel Sieberg
Scientists across the country have heralded the Obama administration's approach to research and development. Already it’s a stark contrast to the Bush years. But what exactly will be done for areas like stem cells, global warming, and space exploration?
These are some of the questions that we try to answer in an upcoming story for the CBS Evening News with Katie Couric. It may be airing tomorrow (Friday) night. We spoke to a number of prominent people from all those fields about their expectations and hopes. We also talked to one woman who may be directly affected by any policy decisions; she puts a human face on all the scientific data and studies.
Also, before cozying up for commercials and football this weekend, I hope you'll tune in to CBS Sunday Morning. It's the 30th anniversary edition of the beloved program (OK, I'm a little biased), and I'm contributed a story about ice. Yes, ice. As in cubes. But not just any old frozen water. For those who enjoy imbibing a good cocktail it can be the unsung hero by adding a touch of class or esthetic. But at too many bars or (Super Bowl) parties the ice ends up melting in such a hurry that it ruins the work of your favorite mixologist. It's also a story about people who carve ice, eat ice (true), and generally believe that ice is now hot. You'll have to watch to find out more -- including the secrets to a bar in Las Vegas that's all made of ice, even the glasses.
Finally, a little teaser -- on Monday night's CBS Evening News with Katie Couric we're planning to have a story about a new Google tool. Can't say more than that right now but I hope you'll join us.
In the meantime, stay connected.
http://www.cbsnews.com/blogs/2009/01/29/eveningnews/techtalk…
meint ihr es lohnt sich noch drauf zuspringen? Wäre nur nen kleiner zock.. aber der sollte ja auch was bringen
lg
lg
Antwort auf Beitrag Nr.: 36.498.529 von revolt am 02.02.09 22:45:14Hallo!
Also wenn der erste Querschnittgelähmte wieder läuft ist der Einstieg zu spät warscheinlich...besser wenn es an den Zehen anfängt zu kribbeln...
Also wenn der erste Querschnittgelähmte wieder läuft ist der Einstieg zu spät warscheinlich...besser wenn es an den Zehen anfängt zu kribbeln...
Antwort auf Beitrag Nr.: 36.501.689 von optschraub am 03.02.09 13:54:58Ja, das ist klar... Wird wohl nen Zock bleiben, weil wenn der stirbt wars das mit der Aktie
Antwort auf Beitrag Nr.: 36.503.845 von revolt am 03.02.09 18:13:08Die ganze Börse ist zur Zeit ein Zock.Wird die Coba zB.komplett verstaatlicht und die Aktionäre enteignet steht sie bei 0,0.
Sie kann sich aber auch vervielfachen.So ist es auch bei Geron.
Ich hab mich für Geron entschieden.Die Banken haben fertig.
Sie kann sich aber auch vervielfachen.So ist es auch bei Geron.
Ich hab mich für Geron entschieden.Die Banken haben fertig.
in den nächsten Wochen wirds heiss hergehen... Schaut euch mal die Optionsumsätze an der ISE an...
hier ein Kommentar von Schaeffler Research:
http://www.schaeffersresearch.com/commentary/observations.as…
Analyzing Massive Call Volume on Geron Corporation, By the Numbers
Can this stem cell stock convince investors that its rally is for real?
by Elizabeth Harrow and Rocky White 2/5/2009 12:13 PM
As you may have noticed, we keep a close eye on unusual developments in the fast-paced and glamorous world of options trading. Thanks to this diligence, it has not escaped our notice that buy-to-open call volume has absolutely exploded on Geron Corporation ( GERN: View sentiment for GERNsentiment, chart, options) during the past couple of weeks. Yes, this surge in optimistic option activity is supported by a positive fundamental development -- but, with everyone piling onto the bullish bandwagon, how long can the stock extend its rally?
FDA decision sparks massive call volume
First things first -- let's explain why GERN is attracting so much enthusiasm from speculative investors. Back on Jan. 23, the stock spiked sharply higher after word hit the Street that the U.S. Food and Drug Administration (FDA) granted its approval for the world's first clinical trial of human embryonic stem cell therapy.
Previously, the agency had rejected Geron's request to conduct a trial of its GRNOPC1 drug. With this regulatory hurdle cleared, investors flocked to buy the stock's call options (apparently, tens of thousands of traders have absolutely no moral qualms about the often-controversial topic of embryonic stem cells).
Lest you think we're exaggerating, let's define what we mean when we refer to "massive" call volume. Year-to-date, about 47,500 calls have been bought to open on the International Securities Exchange (ISE), compared to about 3,700 puts. On Jan. 23 alone, there were about 17,000 calls bought to open and 750 puts bought to open.

Most of the recent call additions have been focused around the February options series, which expires in a couple of weeks. There are 12,189 call contracts in residence at the 7.50 strike, and 10,693 calls open at the 10 strike. The 7.50 call is also the most popular option in the March series, where there are 9,000 open contracts.
Thanks to the FDA-related boost, GERN has rocketed to a year-to-date gain of 62.7%. However, the shares' momentum stalled out near the 8 level, and they're now trading nearly flat with the closely watched 7.50 strike. With February expiration approaching the Friday after next, this region could exert some options-related resistance on the shares during the short term.

n fact, this unfavorable open interest configuration has us a little concerned about the short-term prospects for GERN. Is the equity's rally on its last legs?
Is there any room left on the bandwagon?
We decided to check out the rest of the stock's sentiment backdrop to see if any additional buyers are still lingering on the sidelines. GERN's Schaeffer's put/call open interest ratio (SOIR) has pulled back sharply of late, moving inversely to the equity's powerhouse rally. Now, the SOIR is docked at 0.23, with calls more than quadrupling puts among near-term options. This ratio ranks lower than 78% of other such readings taken during the past year, underscoring the recent upswing in option-player optimism.

While we would expect the SOIR to decline as the stock rises, it's troubling in the context of GERN's recent price action -- which has been primarily sideways. If this heavily bullish group grows discouraged, an unwinding of long positions could apply new selling pressure.
GERN short interestAs for short sellers, it seems that short interest on GERN has steadily declined since August 2008. Now, the number of shares sold short is near a 1-year low. However, it's all relative -- this apparently low number still accounts for a healthy 10.9% of the stock's available float, or 10.2 times its average daily volume. These bearish bets represent a potential source of buying pressure for GERN.
Additional attention from analysts could also serve as a positive catalyst, as Zacks reports just 1 "buy" and 1 "hold" rating. Any bullish initiations or upgrades could draw another wave of buyers to the stock.

The long and short of it
While we're encouraged by the respectable amount of short interest on GERN, we're still hung up on the 7.50 level... and, as contrarians, we can't help but be leery of the bandwagon mentality among option players. It seems that some investors have already priced in plenty of upside, which means the security has high expectations to meet.
Additionally, there's no denying that buying power has waned since the stock's initial pop higher. During the short term, traders should keep an eye on the 7.50 strike. If the shares fail to surmount this level during the next week or 2, it could prompt some frustrated bulls to hit the exits, and the equity may even be forced to fill in its bull gap.
On the other hand, a successful journey atop this region could convince the lingering skeptics of GERN's strength, resulting in additional gains. Overall, proceed with caution when it comes to this stem cell concern. The potential for further gains is there, but the stock will have to convince the remaining bears that its rally has legs to run higher.
As always, please contact us with any questions, comments, or suggestions for future columns. For more commentary on today's market-moving news, please visit our Schaeffer's Daily Market Blog section throughout the trading day.
hier ein Kommentar von Schaeffler Research:
http://www.schaeffersresearch.com/commentary/observations.as…
Analyzing Massive Call Volume on Geron Corporation, By the Numbers
Can this stem cell stock convince investors that its rally is for real?
by Elizabeth Harrow and Rocky White 2/5/2009 12:13 PM
As you may have noticed, we keep a close eye on unusual developments in the fast-paced and glamorous world of options trading. Thanks to this diligence, it has not escaped our notice that buy-to-open call volume has absolutely exploded on Geron Corporation ( GERN: View sentiment for GERNsentiment, chart, options) during the past couple of weeks. Yes, this surge in optimistic option activity is supported by a positive fundamental development -- but, with everyone piling onto the bullish bandwagon, how long can the stock extend its rally?
FDA decision sparks massive call volume
First things first -- let's explain why GERN is attracting so much enthusiasm from speculative investors. Back on Jan. 23, the stock spiked sharply higher after word hit the Street that the U.S. Food and Drug Administration (FDA) granted its approval for the world's first clinical trial of human embryonic stem cell therapy.
Previously, the agency had rejected Geron's request to conduct a trial of its GRNOPC1 drug. With this regulatory hurdle cleared, investors flocked to buy the stock's call options (apparently, tens of thousands of traders have absolutely no moral qualms about the often-controversial topic of embryonic stem cells).
Lest you think we're exaggerating, let's define what we mean when we refer to "massive" call volume. Year-to-date, about 47,500 calls have been bought to open on the International Securities Exchange (ISE), compared to about 3,700 puts. On Jan. 23 alone, there were about 17,000 calls bought to open and 750 puts bought to open.

Most of the recent call additions have been focused around the February options series, which expires in a couple of weeks. There are 12,189 call contracts in residence at the 7.50 strike, and 10,693 calls open at the 10 strike. The 7.50 call is also the most popular option in the March series, where there are 9,000 open contracts.
Thanks to the FDA-related boost, GERN has rocketed to a year-to-date gain of 62.7%. However, the shares' momentum stalled out near the 8 level, and they're now trading nearly flat with the closely watched 7.50 strike. With February expiration approaching the Friday after next, this region could exert some options-related resistance on the shares during the short term.

n fact, this unfavorable open interest configuration has us a little concerned about the short-term prospects for GERN. Is the equity's rally on its last legs?
Is there any room left on the bandwagon?
We decided to check out the rest of the stock's sentiment backdrop to see if any additional buyers are still lingering on the sidelines. GERN's Schaeffer's put/call open interest ratio (SOIR) has pulled back sharply of late, moving inversely to the equity's powerhouse rally. Now, the SOIR is docked at 0.23, with calls more than quadrupling puts among near-term options. This ratio ranks lower than 78% of other such readings taken during the past year, underscoring the recent upswing in option-player optimism.

While we would expect the SOIR to decline as the stock rises, it's troubling in the context of GERN's recent price action -- which has been primarily sideways. If this heavily bullish group grows discouraged, an unwinding of long positions could apply new selling pressure.
GERN short interestAs for short sellers, it seems that short interest on GERN has steadily declined since August 2008. Now, the number of shares sold short is near a 1-year low. However, it's all relative -- this apparently low number still accounts for a healthy 10.9% of the stock's available float, or 10.2 times its average daily volume. These bearish bets represent a potential source of buying pressure for GERN.
Additional attention from analysts could also serve as a positive catalyst, as Zacks reports just 1 "buy" and 1 "hold" rating. Any bullish initiations or upgrades could draw another wave of buyers to the stock.

The long and short of it
While we're encouraged by the respectable amount of short interest on GERN, we're still hung up on the 7.50 level... and, as contrarians, we can't help but be leery of the bandwagon mentality among option players. It seems that some investors have already priced in plenty of upside, which means the security has high expectations to meet.
Additionally, there's no denying that buying power has waned since the stock's initial pop higher. During the short term, traders should keep an eye on the 7.50 strike. If the shares fail to surmount this level during the next week or 2, it could prompt some frustrated bulls to hit the exits, and the equity may even be forced to fill in its bull gap.
On the other hand, a successful journey atop this region could convince the lingering skeptics of GERN's strength, resulting in additional gains. Overall, proceed with caution when it comes to this stem cell concern. The potential for further gains is there, but the stock will have to convince the remaining bears that its rally has legs to run higher.
As always, please contact us with any questions, comments, or suggestions for future columns. For more commentary on today's market-moving news, please visit our Schaeffer's Daily Market Blog section throughout the trading day.
es geht los!!!
U.S. Representative James Forbes submits new stem cell bill
http://www.govtrack.us/congress/bill.xpd?bill=h111-877
H.R. 877:
111st Congress
This is a bill in the U.S. Congress originating in the House of Representatives ("H.R."). A bill must be passed by both the House and Senate and then be signed by the President before it becomes law.
Bill numbers restart from 1 every two years. Each two-year cycle is called a session of Congress. This bill was created in the 111st Congress, in 2009-2010.
The titles of bills are written by the bill's sponsor and are a part of the legislation itself. GovTrack does not editorialize bill summaries.
2009-2010
To intensify stem cell research showing evidence of substantial clinical benefit to patients, and...
To intensify stem cell research showing evidence of substantial clinical benefit to patients, and for other purposes.
U.S. Representative James Forbes submits new stem cell bill
http://www.govtrack.us/congress/bill.xpd?bill=h111-877
H.R. 877:
111st Congress
This is a bill in the U.S. Congress originating in the House of Representatives ("H.R."). A bill must be passed by both the House and Senate and then be signed by the President before it becomes law.
Bill numbers restart from 1 every two years. Each two-year cycle is called a session of Congress. This bill was created in the 111st Congress, in 2009-2010.
The titles of bills are written by the bill's sponsor and are a part of the legislation itself. GovTrack does not editorialize bill summaries.
2009-2010
To intensify stem cell research showing evidence of substantial clinical benefit to patients, and...
To intensify stem cell research showing evidence of substantial clinical benefit to patients, and for other purposes.
Heilen mit Zellen
7. Februar 2009, 02:42 Uhr
In der Medizin bahnt sich eine Revolution an. Bislang noch unheilbare Krankheiten könnten schon bald therapierbar sein. Stammzellforscher haben wichtige Fortschritte erzielt
DIE Welt:
Das kalifornische Biotechunternehmen Geron hat von der amerikanischen Zulassungsbehörde FDA die Genehmigung erhalten, klinische Versuche mit Querschnittsgelähmten durchzuführen. Sie sollen mithilfe von menschlichen embryonalen Stammzellen geheilt werden. Sie arbeiten mit Geron zusammen?
Paul Fairchild:
Ja, wir arbeiten bei einem Projekt sehr eng zusammen. Dabei geht es um immunologische Fragen, wie man es erreichen kann, fremde embryonale Stammzellen zu implantieren, ohne dass diese vom Immunsystem abgestoßen werden. Dies ist bislang eines der größten Hindernisse auf dem Weg zu einer erfolgreichen Stammzelltherapie. Gemeinsam mit Geron-Wissenschaftlern versuche ich eine immunologische Toleranz zu erzeugen, sodass die zur Therapie genutzten Stammzellen vom Körper akzeptiert und nicht abgestoßen werden.
Das grüne Licht für die weltweit ersten klinischen Versuche mit menschlichen embryonalen Stammzellen dürfte Sie also ganz besonders erfreuen?
Fairchild:
Selbstverständlich. Wir haben jahrelang auf diesen Startschuss gewartet. Das ist ein sehr wichtiger Meilenstein in der Geschichte der regenerativen Medizin. Wir haben jetzt erstmals die Chance zu zeigen, dass mit differenzierten embryonalen Stammzellen tatsächlich Therapien möglich sind. Und wenn dies ohne Nebenwirkungen möglich sein sollte, wäre es der ganz große Durchbruch.
Die Entscheidung der FDA kam einen Tag, nachdem Barack Obama die amerikanische Präsidentschaft übernommen hatte. War das purer Zufall oder kommt hier die liberalere Grundeinstellung Obamas im Vergleich zum bisherigen Präsidenten George W. Bush zum Tragen?
Fairchild:
Nach allem, was mir dazu Insider erzählt haben, war es wirklich Zufall. Aber es ist ein glücklicher Zufall, der durchaus symbolisch verdeutlicht, dass die neue Administration in Washington ein neues, positiveres Verhältnis zur Stammzellforschung und zur regenerativen Medizin hat.
Präsident Bush hat die Stammzellforschung eher behindert?
Fairchild:
Ganz ohne Frage. George Bush hatte bei der Forschung mit menschlichen embryonalen Stammzellen sehr große ethische Bedenken. Unter dem neuen Präsidenten wird nun dieses Wissenschaftsgebiet in den USA ganz sicher aufblühen. Ich erwarte schon im Laufe der nächsten Jahre eine ganze Reihe von wichtigen neuen Erkenntnissen und wissenschaftlichen Durchbrüchen.
Das wird die Stammzellforschung auch weltweit stimulieren?
Fairchild:
Ja, davon bin ich überzeugt. Die amerikanischen Wissenschaftler werden jetzt aktiv Ausschau nach Kooperationspartnern halten - unter anderem auch in Europa. Es werden neue Allianzen entstehen, die die Stammzellforschung dynamisch voranbringen werden.
Welche weiteren Therapien mithilfe embryonaler Stammzellen stehen kurz vor einer klinischen Prüfung?
Fairchild:
Bei den klinischen Versuchen von Geron werden weltweit zum ersten Mal menschliche embryonale Stammzellen genutzt. Doch auch anderenorts gibt es ähnliche Projekte. Die britische Biotechfirma Reneuron entwickelt beispielsweise mithilfe menschlicher neuraler Stammzellen eine Therapie für Schlaganfallpatienten.
Wie groß ist die Chance, dass die Stammzelltherapien von Geron oder Reneuron tatsächlich Patienten helfen können?
Fairchild:
Ich bin da sehr optimistisch, denn die vorangegangenen Tierversuche haben wirklich beeindruckende Ergebnisse gezeigt. Den querschnittsgelähmten Ratten wurde nicht nur die Fähigkeit zu Sinnesempfindungen wiedergegeben, sie konnten nach der Therapie mit Stammzellen tatsächlich auch wieder laufen. Es ist durchaus wahrscheinlich, dass dies auch beim Menschen gelingen könnte.
Was ist das größte noch ungelöste Problem der Stammzelltherapie?
Fairchild:
Dass ist in der Tat die eingangs schon angesprochene Abwehrreaktion des Immunsystems. Ein Leben lang Medikamente einzunehmen, um die Immunabwehr des Körpers zu unterdrücken, ist sicher keine gute Lösung. Ziel muss es also sein, Zellen zu implantieren, die genetisch soweit identisch sind, dass diese vom Empfänger akzeptiert werden.
Ein anderes Problem ist doch aber auch das Risiko, dass durch die implantierten Zellen Tumore induziert werden könnten?
Fairchild:
Ja, das ist richtig. Genau wegen dieser Gefahr hat die FDA andere Anträge für klinische Studien mit embryonalen Stammzellen abgelehnt. Doch den Geron-Forschern ist offenbar ein Ansatz geglückt, bei dem dieses Risiko sehr viel geringer ist. Jedenfalls wurde bei keinem der behandelten Versuchstiere das Entstehen eines Tumors beobachtet. Ich denke, dies war eine Voraussetzung dafür, dass die FDA die klinischen Versuche erlaubt hat.Sie gewähren Geron eine Lizenz zur Nutzung eines Patents der Universität Oxford. Worum geht es in diesem Patent?
Fairchild:
Dabei geht es um die Gewinnung von sogenannten dendritische Zellen aus embryonalen Stammzellen. Dentritische Zellen sind von großer Bedeutung, weil sie der wichtigste Zelltyp im Immunsystem sind. Sie balancieren das sensible Verhältnis zwischen Immunabwehr und Immuntoleranz aus. Unsere Idee war nun, aus embryonalen Stammzellen sowohl die für die Therapie benötigten Zellen als auch dendritische Zellen zu erzeugen. Durch eine Injektion der dendritischen Zellen in die zu transplantierenden Zellen hoffen wir, das Immunsystem zu überlisten, sodass es die therapeutischen Zellen beziehungsweise das transplantierte Gewebe toleriert. Ich hoffe, dass wir dieses Konzept bald schon gemeinsam mit Geron-Wissenschaftlern in klinischen Versuchen testen dürfen.
Aus deutscher Sicht erscheint Großbritannien als ein Land, in dem es Stammzellforscher sehr viel einfacher haben. Ist dieser Eindruck richtig?
Fairchild:
Ich denke ja. Die britische Regierung unterstützt die Stammzellforschung statt sie zu behindern. Es gibt ausreichend viel Fördermittel. Unter dem Strich führen diese Bedingungen natürlich auch zu Erfolgen in der Forschung.
Welche anderen Länder fallen Ihnen denn zuallererst ein, wenn es um exzellente Stammzellforschung geht?
Fairchild:
Singapur, Israel, Australien und die USA, wo es die Wissenschaftler trotz aller Behinderungen auch bislang schon geschafft haben, Spitzenforschung auf diesem Gebiet zu leisten - besonders in Kalifornien.
Und wo sehen Sie die Position von Deutschland in der Stammzellforschung?
Fairchild:
Die Forschung mit menschlichen embryonalen Stammzellen kann in Deutschland aufgrund der gesetzlichen Beschränkungen nicht mit der Weltspitze mithalten. Andererseits hat die Forschung mit adulten Stammzellen in Deutschland allerhöchstes Niveau. Im Max-Planck-Institut für Molekulare Medizin in Münster ist es deutschen Wissenschaftlern um Professor Hans Schöler jetzt gelungen, adulte Zellen mithilfe nur eines einzigen Genfaktors so zu reprogrammieren, dass aus ihnen wieder pluripotente Zellen geworden sind. Aus diesen lassen sich dann wieder alle gewünschten Körperzellen herstellen. Dies ist ein ganz wichtiger Ansatz im Hinblick auf spätere Therapien. Insbesondere weil dabei das ethische Problem umschifft wird, embryonale Stammzellen, aus denen sich ja Menschen entwickeln könnten, zu therapeutischen Zwecken zu verbrauchen. Ich bin davon überzeugt, dass dieser vielversprechende Forschungsansatz in Deutschland intensiv weiterverfolgt werden wird.
Was die Geron-Forscher jetzt also mit embryonalen Stammzellen erreichen wollen, nämlich querschnittsgelähmte Menschen zu heilen, könnte also irgendwann mit pluripotenten Zellen funktionieren, die aus Körperzellen des Patienten gewonnen werden können?
Fairchild:
Ja, genau das ist die Hoffnung. Und das Problem der immunologischen Abstoßung wäre damit auch gelöst. Die implantierten Zellen wären ja nicht fremd, sondern gleichsam körpereigen.
Dann würde aber Ihr Patent wertlos, mit dem die Immunabwehr bei den embryonalen Stammzellen unterdrückt wird?
Fairchild:
Da bin ich mir nicht sicher. Das größte Problem bei der Nutzung pluripotenter Zellen zur Therapie von Patienten ist nämlich von ökonomischer Natur. Man müsste in diesem Fall nämlich für jeden Patienten eine eigene Zelllinie anlegen. Dieser Aufwand wäre sehr groß und ließe sich gewiss nicht für eine große Zahl von Patienten betreiben. Für die Therapie mit pluripotenten Stammzellen gibt es kein "business model". Keine Pharmafirma würde sich darauf einlassen. Aus wirtschaftlichen Gründen wird hier die wahrscheinlichste Entwicklung so aussehen, dass man eine Sammlung von induzierten pluripotenten Stammzellen anlegt. Aus dieser Zellbank wird man dann jeweils jene Zellen aussuchen, die am besten zu einem bestimmten Patienten passen. Doch diese wären eben nicht ganz identisch mit den Körperzellen des Patienten, sodass nach wie vor das Problem der immunologischen Abstoßung bestehen würde.
Gibt es einen Unterschied zwischen den beiden Ansätzen - also den embryonalen und den pluripotenten Stammzellen - im Hinblick auf das Risiko, dass bei einer Therapie Krebszellen entstehen können?
Fairchild:
Das wissen wir bislang einfach noch nicht. Dafür ist das Forschungsgebiet der pluripotenten Stammzellen, die aus adulten Zellen gewonnen wurden, noch viel zu jung. Es ist durchaus möglich, dass auch die pluripotenten Stammzellen Tumore induzieren können. Es gibt dazu aber noch keine Studien.
Gibt es Kooperationen zwischen Ihnen und deutschen Wissenschaftlern?
Fairchild:
Nein.
Was sind Ihre großen Visionen in der Stammzellforschung?
Fairchild:
In den entwickelten Ländern ist die Lebenserwartung stark angestiegen - unter anderem durch die Verfügbarkeit von Antibiotika und Impfstoffen. Es gibt daher immer mehr alte Menschen und damit auch eine wachsende Zahl von Patienten mit Alzheimer, Parkinson, Diabetes oder einer Makuladegeneration, um nur einige Beispiele zu nennen. Die Hoffnung ist nun, dass wir diese Erkrankungen mit Stammzelltherapien zurückdrängen können. In zehn bis 20 Jahren werden die Menschen also nicht nur länger leben können - sondern eben auch frei von diesen altersbedingten Leiden.
7. Februar 2009, 02:42 Uhr
In der Medizin bahnt sich eine Revolution an. Bislang noch unheilbare Krankheiten könnten schon bald therapierbar sein. Stammzellforscher haben wichtige Fortschritte erzielt
DIE Welt:
Das kalifornische Biotechunternehmen Geron hat von der amerikanischen Zulassungsbehörde FDA die Genehmigung erhalten, klinische Versuche mit Querschnittsgelähmten durchzuführen. Sie sollen mithilfe von menschlichen embryonalen Stammzellen geheilt werden. Sie arbeiten mit Geron zusammen?
Paul Fairchild:
Ja, wir arbeiten bei einem Projekt sehr eng zusammen. Dabei geht es um immunologische Fragen, wie man es erreichen kann, fremde embryonale Stammzellen zu implantieren, ohne dass diese vom Immunsystem abgestoßen werden. Dies ist bislang eines der größten Hindernisse auf dem Weg zu einer erfolgreichen Stammzelltherapie. Gemeinsam mit Geron-Wissenschaftlern versuche ich eine immunologische Toleranz zu erzeugen, sodass die zur Therapie genutzten Stammzellen vom Körper akzeptiert und nicht abgestoßen werden.
Das grüne Licht für die weltweit ersten klinischen Versuche mit menschlichen embryonalen Stammzellen dürfte Sie also ganz besonders erfreuen?
Fairchild:
Selbstverständlich. Wir haben jahrelang auf diesen Startschuss gewartet. Das ist ein sehr wichtiger Meilenstein in der Geschichte der regenerativen Medizin. Wir haben jetzt erstmals die Chance zu zeigen, dass mit differenzierten embryonalen Stammzellen tatsächlich Therapien möglich sind. Und wenn dies ohne Nebenwirkungen möglich sein sollte, wäre es der ganz große Durchbruch.
Die Entscheidung der FDA kam einen Tag, nachdem Barack Obama die amerikanische Präsidentschaft übernommen hatte. War das purer Zufall oder kommt hier die liberalere Grundeinstellung Obamas im Vergleich zum bisherigen Präsidenten George W. Bush zum Tragen?
Fairchild:
Nach allem, was mir dazu Insider erzählt haben, war es wirklich Zufall. Aber es ist ein glücklicher Zufall, der durchaus symbolisch verdeutlicht, dass die neue Administration in Washington ein neues, positiveres Verhältnis zur Stammzellforschung und zur regenerativen Medizin hat.
Präsident Bush hat die Stammzellforschung eher behindert?
Fairchild:
Ganz ohne Frage. George Bush hatte bei der Forschung mit menschlichen embryonalen Stammzellen sehr große ethische Bedenken. Unter dem neuen Präsidenten wird nun dieses Wissenschaftsgebiet in den USA ganz sicher aufblühen. Ich erwarte schon im Laufe der nächsten Jahre eine ganze Reihe von wichtigen neuen Erkenntnissen und wissenschaftlichen Durchbrüchen.
Das wird die Stammzellforschung auch weltweit stimulieren?
Fairchild:
Ja, davon bin ich überzeugt. Die amerikanischen Wissenschaftler werden jetzt aktiv Ausschau nach Kooperationspartnern halten - unter anderem auch in Europa. Es werden neue Allianzen entstehen, die die Stammzellforschung dynamisch voranbringen werden.
Welche weiteren Therapien mithilfe embryonaler Stammzellen stehen kurz vor einer klinischen Prüfung?
Fairchild:
Bei den klinischen Versuchen von Geron werden weltweit zum ersten Mal menschliche embryonale Stammzellen genutzt. Doch auch anderenorts gibt es ähnliche Projekte. Die britische Biotechfirma Reneuron entwickelt beispielsweise mithilfe menschlicher neuraler Stammzellen eine Therapie für Schlaganfallpatienten.
Wie groß ist die Chance, dass die Stammzelltherapien von Geron oder Reneuron tatsächlich Patienten helfen können?
Fairchild:
Ich bin da sehr optimistisch, denn die vorangegangenen Tierversuche haben wirklich beeindruckende Ergebnisse gezeigt. Den querschnittsgelähmten Ratten wurde nicht nur die Fähigkeit zu Sinnesempfindungen wiedergegeben, sie konnten nach der Therapie mit Stammzellen tatsächlich auch wieder laufen. Es ist durchaus wahrscheinlich, dass dies auch beim Menschen gelingen könnte.
Was ist das größte noch ungelöste Problem der Stammzelltherapie?
Fairchild:
Dass ist in der Tat die eingangs schon angesprochene Abwehrreaktion des Immunsystems. Ein Leben lang Medikamente einzunehmen, um die Immunabwehr des Körpers zu unterdrücken, ist sicher keine gute Lösung. Ziel muss es also sein, Zellen zu implantieren, die genetisch soweit identisch sind, dass diese vom Empfänger akzeptiert werden.
Ein anderes Problem ist doch aber auch das Risiko, dass durch die implantierten Zellen Tumore induziert werden könnten?
Fairchild:
Ja, das ist richtig. Genau wegen dieser Gefahr hat die FDA andere Anträge für klinische Studien mit embryonalen Stammzellen abgelehnt. Doch den Geron-Forschern ist offenbar ein Ansatz geglückt, bei dem dieses Risiko sehr viel geringer ist. Jedenfalls wurde bei keinem der behandelten Versuchstiere das Entstehen eines Tumors beobachtet. Ich denke, dies war eine Voraussetzung dafür, dass die FDA die klinischen Versuche erlaubt hat.Sie gewähren Geron eine Lizenz zur Nutzung eines Patents der Universität Oxford. Worum geht es in diesem Patent?
Fairchild:
Dabei geht es um die Gewinnung von sogenannten dendritische Zellen aus embryonalen Stammzellen. Dentritische Zellen sind von großer Bedeutung, weil sie der wichtigste Zelltyp im Immunsystem sind. Sie balancieren das sensible Verhältnis zwischen Immunabwehr und Immuntoleranz aus. Unsere Idee war nun, aus embryonalen Stammzellen sowohl die für die Therapie benötigten Zellen als auch dendritische Zellen zu erzeugen. Durch eine Injektion der dendritischen Zellen in die zu transplantierenden Zellen hoffen wir, das Immunsystem zu überlisten, sodass es die therapeutischen Zellen beziehungsweise das transplantierte Gewebe toleriert. Ich hoffe, dass wir dieses Konzept bald schon gemeinsam mit Geron-Wissenschaftlern in klinischen Versuchen testen dürfen.
Aus deutscher Sicht erscheint Großbritannien als ein Land, in dem es Stammzellforscher sehr viel einfacher haben. Ist dieser Eindruck richtig?
Fairchild:
Ich denke ja. Die britische Regierung unterstützt die Stammzellforschung statt sie zu behindern. Es gibt ausreichend viel Fördermittel. Unter dem Strich führen diese Bedingungen natürlich auch zu Erfolgen in der Forschung.
Welche anderen Länder fallen Ihnen denn zuallererst ein, wenn es um exzellente Stammzellforschung geht?
Fairchild:
Singapur, Israel, Australien und die USA, wo es die Wissenschaftler trotz aller Behinderungen auch bislang schon geschafft haben, Spitzenforschung auf diesem Gebiet zu leisten - besonders in Kalifornien.
Und wo sehen Sie die Position von Deutschland in der Stammzellforschung?
Fairchild:
Die Forschung mit menschlichen embryonalen Stammzellen kann in Deutschland aufgrund der gesetzlichen Beschränkungen nicht mit der Weltspitze mithalten. Andererseits hat die Forschung mit adulten Stammzellen in Deutschland allerhöchstes Niveau. Im Max-Planck-Institut für Molekulare Medizin in Münster ist es deutschen Wissenschaftlern um Professor Hans Schöler jetzt gelungen, adulte Zellen mithilfe nur eines einzigen Genfaktors so zu reprogrammieren, dass aus ihnen wieder pluripotente Zellen geworden sind. Aus diesen lassen sich dann wieder alle gewünschten Körperzellen herstellen. Dies ist ein ganz wichtiger Ansatz im Hinblick auf spätere Therapien. Insbesondere weil dabei das ethische Problem umschifft wird, embryonale Stammzellen, aus denen sich ja Menschen entwickeln könnten, zu therapeutischen Zwecken zu verbrauchen. Ich bin davon überzeugt, dass dieser vielversprechende Forschungsansatz in Deutschland intensiv weiterverfolgt werden wird.
Was die Geron-Forscher jetzt also mit embryonalen Stammzellen erreichen wollen, nämlich querschnittsgelähmte Menschen zu heilen, könnte also irgendwann mit pluripotenten Zellen funktionieren, die aus Körperzellen des Patienten gewonnen werden können?
Fairchild:
Ja, genau das ist die Hoffnung. Und das Problem der immunologischen Abstoßung wäre damit auch gelöst. Die implantierten Zellen wären ja nicht fremd, sondern gleichsam körpereigen.
Dann würde aber Ihr Patent wertlos, mit dem die Immunabwehr bei den embryonalen Stammzellen unterdrückt wird?
Fairchild:
Da bin ich mir nicht sicher. Das größte Problem bei der Nutzung pluripotenter Zellen zur Therapie von Patienten ist nämlich von ökonomischer Natur. Man müsste in diesem Fall nämlich für jeden Patienten eine eigene Zelllinie anlegen. Dieser Aufwand wäre sehr groß und ließe sich gewiss nicht für eine große Zahl von Patienten betreiben. Für die Therapie mit pluripotenten Stammzellen gibt es kein "business model". Keine Pharmafirma würde sich darauf einlassen. Aus wirtschaftlichen Gründen wird hier die wahrscheinlichste Entwicklung so aussehen, dass man eine Sammlung von induzierten pluripotenten Stammzellen anlegt. Aus dieser Zellbank wird man dann jeweils jene Zellen aussuchen, die am besten zu einem bestimmten Patienten passen. Doch diese wären eben nicht ganz identisch mit den Körperzellen des Patienten, sodass nach wie vor das Problem der immunologischen Abstoßung bestehen würde.
Gibt es einen Unterschied zwischen den beiden Ansätzen - also den embryonalen und den pluripotenten Stammzellen - im Hinblick auf das Risiko, dass bei einer Therapie Krebszellen entstehen können?
Fairchild:
Das wissen wir bislang einfach noch nicht. Dafür ist das Forschungsgebiet der pluripotenten Stammzellen, die aus adulten Zellen gewonnen wurden, noch viel zu jung. Es ist durchaus möglich, dass auch die pluripotenten Stammzellen Tumore induzieren können. Es gibt dazu aber noch keine Studien.
Gibt es Kooperationen zwischen Ihnen und deutschen Wissenschaftlern?
Fairchild:
Nein.
Was sind Ihre großen Visionen in der Stammzellforschung?
Fairchild:
In den entwickelten Ländern ist die Lebenserwartung stark angestiegen - unter anderem durch die Verfügbarkeit von Antibiotika und Impfstoffen. Es gibt daher immer mehr alte Menschen und damit auch eine wachsende Zahl von Patienten mit Alzheimer, Parkinson, Diabetes oder einer Makuladegeneration, um nur einige Beispiele zu nennen. Die Hoffnung ist nun, dass wir diese Erkrankungen mit Stammzelltherapien zurückdrängen können. In zehn bis 20 Jahren werden die Menschen also nicht nur länger leben können - sondern eben auch frei von diesen altersbedingten Leiden.
Endingen (aktiencheck.de AG) - Die Experten von "Global Biotech Investing" empfehlen, bei der Aktie von Geron (ISIN US3741631036/ WKN 902213) einen Teil der Gewinne zu sichern.
Seit ihrem Oktobertief bei 1,95 USD sei die Aktie in der Spitze um 330% auf 8,50 USD nach oben geschossen. Allein in den letzten zwei Wochen habe sich das Papier um gut 70% verteuert.
Die Kursavancen hätten mehrere Gründe. Die Obama-Regierung sorge mit der Aussicht auf eine Aufhebung des Verbotes zur Förderung von Stammzellenforschung für Kursfantasie. Vorvergangene Woche habe der Konzern zudem die Zulassung seitens der FDA zum Start der ersten Forschungstests mit embryonalen Stammzellen am Menschen in den USA erhalten. Der Konzern habe ein Präparat entwickelt, das im Rückenmark der Patienten verletzte Nervenzellen teilweise wiederherstellen solle. Hierdurch könnten gelähmte Personen möglicherweise eines Tages wieder gehen. Im Erfolgsfall würde dies die Aktie nach Ansicht der Experten in ungeahnte Höhen treiben. Allerdings sei das Unternehmen noch lange nicht soweit.
Die Experten von "Global Biotech Investing" empfehlen, bei der Aktie von Geron einen Teil der Gewinne zu sichern. Bei den restlichen Stücken sollte die Stoppmarke entsprechend nachgezogen werden. (Ausgabe 03 vom 09.02.2009)
(09.02.2009/ac/a/a)
Analyse-Datum: 09.02.2009
Seit ihrem Oktobertief bei 1,95 USD sei die Aktie in der Spitze um 330% auf 8,50 USD nach oben geschossen. Allein in den letzten zwei Wochen habe sich das Papier um gut 70% verteuert.
Die Kursavancen hätten mehrere Gründe. Die Obama-Regierung sorge mit der Aussicht auf eine Aufhebung des Verbotes zur Förderung von Stammzellenforschung für Kursfantasie. Vorvergangene Woche habe der Konzern zudem die Zulassung seitens der FDA zum Start der ersten Forschungstests mit embryonalen Stammzellen am Menschen in den USA erhalten. Der Konzern habe ein Präparat entwickelt, das im Rückenmark der Patienten verletzte Nervenzellen teilweise wiederherstellen solle. Hierdurch könnten gelähmte Personen möglicherweise eines Tages wieder gehen. Im Erfolgsfall würde dies die Aktie nach Ansicht der Experten in ungeahnte Höhen treiben. Allerdings sei das Unternehmen noch lange nicht soweit.
Die Experten von "Global Biotech Investing" empfehlen, bei der Aktie von Geron einen Teil der Gewinne zu sichern. Bei den restlichen Stücken sollte die Stoppmarke entsprechend nachgezogen werden. (Ausgabe 03 vom 09.02.2009)
(09.02.2009/ac/a/a)
Analyse-Datum: 09.02.2009
FACTBOX-Biggest changes in Nasdaq short interest
Tue Feb 10, 2009 4:16pm
- Short interest on the Nasdaq rose 1.1 percent
in late January, the exchange said on Tuesday, suggesting an increase in bearish sentiment in the stock market. For story please see [ID:nWNA6186]. Below are the five Nasdaq stocks that experienced the largest increases and decreases in their short positions from mid-January to late January, according to information released by the exchange. The five companies with the largest overall short positions are also listed. The latest date is as of Jan 30, while the previous period's data is as of
Jan 15.
COMPANY JAN 30 JAN 15 NET CHANGE PCT CHANGE
-----------------------------------------------------------------------------
FIVE BIGGEST INCREASES:
Sirius XM Radio (SIRI.O) 271,931,355 219,626,558 52,304,797 23.8
Geron Corp (GERN.O) 15,691,935 8,543,297 7,148,638 83.7Bed Bath & Beyond (BBBY.O) 29,388,487 23,472,514 5,915,973 25.2
Flextronics (FLEX.O) 24,123,279 18,333,022 5,790,257 31.6
JDS Uniphase (JDSU.O) 12,907,667 7,782,856 5,124,811 65.9
FIVE BIGGEST DECREASES:
Intel Corp (INTC.O) 94,599,665 109,807,015 -15,207,350 -13.9
Microsoft Corp (MSFT.O) 80,372,599 92,445,347 -12,072,748 -13.1
Comcast Corp (CMCSA.O) 51,439,903 60,429,706 -8,989,803 -14.9
Level 3 Comm (LVLT.O) 151,093,640 159,950,081 -8,856,441 -5.5
*Smurfit-Stone 3,380,960 10,897,724 -7,516,764 -69.0
FIVE BIGGEST POSITIONS:
Sirius XM Radio (SIRI.O) 271,931,355 219,626,558 52,304,797 23.8
Level 3 Comm (LVLT.O) 151,093,640 159,950,081 -8,856,441 -5.5
Intel Corp (INTC.O) 94,599,665 109,807,015 -15,207,350 -13.9
Microsoft Corp (MSFT.O) 80,372,599 92,445,347 -12,072,748 -13.1
E*TRADE Financial (ETFC.O) 75,776,287 77,665,801 -1,889,514 -2.4
*Smurfit-Stone Container Corp filed for bankruptcy protection on Jan. 26. It
now trades under the symbol (SSCCQ.PK) Source: Nasdaq data as of Jan 30, Reuters Estimates
(Compiled by Emily Chasan; Editing by Andre Grenon)
Tue Feb 10, 2009 4:16pm
- Short interest on the Nasdaq rose 1.1 percent
in late January, the exchange said on Tuesday, suggesting an increase in bearish sentiment in the stock market. For story please see [ID:nWNA6186]. Below are the five Nasdaq stocks that experienced the largest increases and decreases in their short positions from mid-January to late January, according to information released by the exchange. The five companies with the largest overall short positions are also listed. The latest date is as of Jan 30, while the previous period's data is as of
Jan 15.
COMPANY JAN 30 JAN 15 NET CHANGE PCT CHANGE
-----------------------------------------------------------------------------
FIVE BIGGEST INCREASES:
Sirius XM Radio (SIRI.O) 271,931,355 219,626,558 52,304,797 23.8
Geron Corp (GERN.O) 15,691,935 8,543,297 7,148,638 83.7Bed Bath & Beyond (BBBY.O) 29,388,487 23,472,514 5,915,973 25.2
Flextronics (FLEX.O) 24,123,279 18,333,022 5,790,257 31.6
JDS Uniphase (JDSU.O) 12,907,667 7,782,856 5,124,811 65.9
FIVE BIGGEST DECREASES:
Intel Corp (INTC.O) 94,599,665 109,807,015 -15,207,350 -13.9
Microsoft Corp (MSFT.O) 80,372,599 92,445,347 -12,072,748 -13.1
Comcast Corp (CMCSA.O) 51,439,903 60,429,706 -8,989,803 -14.9
Level 3 Comm (LVLT.O) 151,093,640 159,950,081 -8,856,441 -5.5
*Smurfit-Stone 3,380,960 10,897,724 -7,516,764 -69.0
FIVE BIGGEST POSITIONS:
Sirius XM Radio (SIRI.O) 271,931,355 219,626,558 52,304,797 23.8
Level 3 Comm (LVLT.O) 151,093,640 159,950,081 -8,856,441 -5.5
Intel Corp (INTC.O) 94,599,665 109,807,015 -15,207,350 -13.9
Microsoft Corp (MSFT.O) 80,372,599 92,445,347 -12,072,748 -13.1
E*TRADE Financial (ETFC.O) 75,776,287 77,665,801 -1,889,514 -2.4
*Smurfit-Stone Container Corp filed for bankruptcy protection on Jan. 26. It
now trades under the symbol (SSCCQ.PK) Source: Nasdaq data as of Jan 30, Reuters Estimates
(Compiled by Emily Chasan; Editing by Andre Grenon)
Was passiert gerade in Amiland??? Nachbörslich -15%!!!
Antwort auf Beitrag Nr.: 36.569.904 von Sugar2000 am 12.02.09 22:42:53Hier hast Du die Antwort.
Immer das gleiche Spiel. Immer wenn der Kurs stark angezogen war wurde eine KE flankiert
Geron announced today the pricing of an underwritten public offering of 7.25 million shares of its common stock. The offering is expected to close on February 19, 2009. On February 12, 2009, the last reported sales price of Geron common stock on the Nasdaq Global Market was $7.77.
Related Quotes
Symbol Price Change
GERN 7.77 0.00
{"s" : "gern","k" : "c10,l10,p20,t10","o" : "","j" : ""} UBS Investment Bank is acting as sole book-running manager for the offering. Lazard Capital Markets LLC is acting as co-manager for this offering. Geron intends to use the net proceeds from the offering for research and development, clinical trials and general corporate purposes.
A registration statement relating to the shares was filed with the Securities and Exchange Commission and declared effective on August 18, 2006. This offering is being made pursuant to a prospectus supplement to the registration statement. Copies of the prospectus supplement relating to this offering, when available, may be obtained from UBS Investment Bank, Attention: Prospectus Department, 299 Park Avenue, New York, NY 10171, or by calling (888) 827-7275.
This press release does not constitute an offer to sell or the solicitation of an offer to buy any of the securities described herein.
Immer das gleiche Spiel. Immer wenn der Kurs stark angezogen war wurde eine KE flankiert

Geron announced today the pricing of an underwritten public offering of 7.25 million shares of its common stock. The offering is expected to close on February 19, 2009. On February 12, 2009, the last reported sales price of Geron common stock on the Nasdaq Global Market was $7.77.
Related Quotes
Symbol Price Change
GERN 7.77 0.00
{"s" : "gern","k" : "c10,l10,p20,t10","o" : "","j" : ""} UBS Investment Bank is acting as sole book-running manager for the offering. Lazard Capital Markets LLC is acting as co-manager for this offering. Geron intends to use the net proceeds from the offering for research and development, clinical trials and general corporate purposes.
A registration statement relating to the shares was filed with the Securities and Exchange Commission and declared effective on August 18, 2006. This offering is being made pursuant to a prospectus supplement to the registration statement. Copies of the prospectus supplement relating to this offering, when available, may be obtained from UBS Investment Bank, Attention: Prospectus Department, 299 Park Avenue, New York, NY 10171, or by calling (888) 827-7275.
This press release does not constitute an offer to sell or the solicitation of an offer to buy any of the securities described herein.
Antwort auf Beitrag Nr.: 36.574.240 von meislo am 13.02.09 15:13:59Ja, das hatte ich gestern schon auf thestreet gelesen...
naja, ich bin ja 2008 rein, um Abgeltungssteuerfrei bei Dausend rauszugehen


naja, ich bin ja 2008 rein, um Abgeltungssteuerfrei bei Dausend rauszugehen



Geron zahlt alles mit Aktien. Die dilution bis der Notarzt kommt. Das kann nochmal nach hinten losgehen, falls es bei GRN163L oder den Stammzellentest zu Schwulitäten kommen sollte. Und wenn die nächste Runde von Aktienausschüttungen an Lonza und Girindus AG bezügl. GRN163L ansteht, werden bestimmt nochmals 1.000.000 Aktien zu 0,01$ kommen.
Yesterday 11:45pm
(US) President Obama is expected to soon issue an executive order lifting the 8 yr ban on embryonic stem cell research
- The report cites sr adviser David Axelrod on "Fox News Sunday"
- Note: On 2/6, President Obama guaranteed that he would sign an executive order for stem cell research.
(US) President Obama is expected to soon issue an executive order lifting the 8 yr ban on embryonic stem cell research
- The report cites sr adviser David Axelrod on "Fox News Sunday"
- Note: On 2/6, President Obama guaranteed that he would sign an executive order for stem cell research.
+10 Milliarden in die Stammzellenforschung aus dem Stimulus package
Gehirnstammzellen in Hülle und Fülle
Bonner Forscher haben eine nach ihren Worten "unerschöpfliche Quelle" für menschliche Gehirnstammzellen entdeckt. Ausgangspunkt waren embryonale Stammzellen. Die daraus gewonnenen Nervenzellen konnten die Mediziner erfolgreich in Hirnschaltkreise einbauen.
Deutsche Wissenschaftler haben aus menschlichen embryonalen Stammzellen funktionierende Nervenzellen hergestellt und sie in das Gehirn von Mäusen transplantiert. "Das ist der erste direkte Beweis, dass sich Nervenzellen aus menschlichen Stammzellen in die Schaltkreise eines Gehirns integrieren können", sagte Philipp Koch von der Universität Bonn, einer der Autoren der Studie. Nach Angaben der Universität sind unter den gewonnenen Nervenzellen auch solche, die bei der Parkinson-Krankheit ausfallen.
Die zunächst aus den embryonalen Stammzellen gewonnenen adulten Stammzellen lassen sich den Angaben zufolge nicht nur nahezu unbegrenzt in Kultur halten, sondern können sich auch in verschiedene Nervenzelltypen entwickeln. "Die Gehirnstammzellen funktionieren wie eine unerschöpfliche Quelle: Sie liefert über Monate und Jahre menschliche Nervenzellen", sagte Arbeitsgruppenleiter Oliver Brüstle. Die Ergebnisse sind im Fachblatt "Proceedings of the National Academy of Sciences" zu finden.
Mit den künstlich gewonnenen Nervenzellen führen die Wissenschaftler zwei Ansätze der Stammzellforschung zusammen. Sie entwickelten aus embryonalen Stammzellen eine Art adulte Stammzellen - die Gehirnstammzellen. Aus diesen konnten Sie dann verschiedene Nervenzelltypen gewinnen.
Der Bedarf an embryonalen Stammzellen als Ausgangsmaterial könne nun reduziert werden, sagte Brüstle. Die Gewinnung embryonaler Stammzellen ist ethisch umstritten, weil dabei Embryonen getötet werden müssen. In vielen Ländern, auch die Deutschland, ist die Arbeit damit gesetzlich eingeschränkt. In einem nächsten Schritt wollen die Forscher die Stammzellen in ein - beispielsweise an Parkinson - erkranktes Tier einbringen und prüfen, ob sie die Symptome lindern können.
Bonner Forscher haben eine nach ihren Worten "unerschöpfliche Quelle" für menschliche Gehirnstammzellen entdeckt. Ausgangspunkt waren embryonale Stammzellen. Die daraus gewonnenen Nervenzellen konnten die Mediziner erfolgreich in Hirnschaltkreise einbauen.
Deutsche Wissenschaftler haben aus menschlichen embryonalen Stammzellen funktionierende Nervenzellen hergestellt und sie in das Gehirn von Mäusen transplantiert. "Das ist der erste direkte Beweis, dass sich Nervenzellen aus menschlichen Stammzellen in die Schaltkreise eines Gehirns integrieren können", sagte Philipp Koch von der Universität Bonn, einer der Autoren der Studie. Nach Angaben der Universität sind unter den gewonnenen Nervenzellen auch solche, die bei der Parkinson-Krankheit ausfallen.
Die zunächst aus den embryonalen Stammzellen gewonnenen adulten Stammzellen lassen sich den Angaben zufolge nicht nur nahezu unbegrenzt in Kultur halten, sondern können sich auch in verschiedene Nervenzelltypen entwickeln. "Die Gehirnstammzellen funktionieren wie eine unerschöpfliche Quelle: Sie liefert über Monate und Jahre menschliche Nervenzellen", sagte Arbeitsgruppenleiter Oliver Brüstle. Die Ergebnisse sind im Fachblatt "Proceedings of the National Academy of Sciences" zu finden.
Mit den künstlich gewonnenen Nervenzellen führen die Wissenschaftler zwei Ansätze der Stammzellforschung zusammen. Sie entwickelten aus embryonalen Stammzellen eine Art adulte Stammzellen - die Gehirnstammzellen. Aus diesen konnten Sie dann verschiedene Nervenzelltypen gewinnen.
Der Bedarf an embryonalen Stammzellen als Ausgangsmaterial könne nun reduziert werden, sagte Brüstle. Die Gewinnung embryonaler Stammzellen ist ethisch umstritten, weil dabei Embryonen getötet werden müssen. In vielen Ländern, auch die Deutschland, ist die Arbeit damit gesetzlich eingeschränkt. In einem nächsten Schritt wollen die Forscher die Stammzellen in ein - beispielsweise an Parkinson - erkranktes Tier einbringen und prüfen, ob sie die Symptome lindern können.
der heutige Absturz liegt wohl an folgender Meldung:
http://www.msnbc.msn.com/id/29243132
Fetal stem cells trigger tumors in ill boy
Highly experimental injections led to growths in patient’s brain, spinal cord
Da ist wohl in Moskau ein russisches Kind mit Stammzellen behandelt worden und es hat sich ein Turmor gebildet...
Diese Meldung hat NICHTS mit Geron zu tun!!! und auch somit nichts mit GRNOPC1!
Auch Jim Cramer von thestreet.com äußerte sich heute:
http://www.thestreet.com/story/10464653/1/geron-short-closed…
"The reason for the dive in Geron's stock price Wednesday was the publication of a medical paper detailing the case of a boy with a fatal brain disease who was treated with an experimental concoction of fetal neural stem cells. These fetal stem cells caused benign tumors to grow on his brain and spinal column.
The case was reported last night in the medical journal PLoS Medicine and can be downloaded here. An MSNBC story on the boy can be found here.
This tragic case had nothing to do directly with Geron. The boy was apparently treated with neural stem cells at a clinic in Moscow. He was not enrolled in a clinical trial involving Geron or its stem-cell drug GRNOPC1."
http://www.msnbc.msn.com/id/29243132
Fetal stem cells trigger tumors in ill boy
Highly experimental injections led to growths in patient’s brain, spinal cord
Da ist wohl in Moskau ein russisches Kind mit Stammzellen behandelt worden und es hat sich ein Turmor gebildet...
Diese Meldung hat NICHTS mit Geron zu tun!!! und auch somit nichts mit GRNOPC1!
Auch Jim Cramer von thestreet.com äußerte sich heute:
http://www.thestreet.com/story/10464653/1/geron-short-closed…
"The reason for the dive in Geron's stock price Wednesday was the publication of a medical paper detailing the case of a boy with a fatal brain disease who was treated with an experimental concoction of fetal neural stem cells. These fetal stem cells caused benign tumors to grow on his brain and spinal column.
The case was reported last night in the medical journal PLoS Medicine and can be downloaded here. An MSNBC story on the boy can be found here.
This tragic case had nothing to do directly with Geron. The boy was apparently treated with neural stem cells at a clinic in Moscow. He was not enrolled in a clinical trial involving Geron or its stem-cell drug GRNOPC1."
Ja,wenn wie jeden Tag -10%,dann sind wir nächste Woche bei 0,0
Endweder es gibt Probleme oder die Shortprofis leisten ganze Arbeit.
Endweder es gibt Probleme oder die Shortprofis leisten ganze Arbeit.
Von der Euphorie in die Realität. Der Kursanstieg war für Trader sicher ne schöne Sache, aber sowas führt idR immer wieder zu heftigen Korrekturen. Das ist bei den Amis ein abolut typisches Bild und erlebe ich selbst in meinen Invests.
Geron plant zahlreiche P2 Studien mit dem Antisense GRN163L in nächster Zeit, was wieder ein bisschen Fanatsie in die Bude bringen könnte. Auch der muss sich erstmal beweisen.
Bei den Stammzellen werden jetzt sicher Studien ausgearbeitet, die auch erst von der FDA freigegeben werden müssen. Und sollte es wirklich eines Tgaes so sein, dass Blinde wieder laufen können und Querschnittsgelähmte wieder sehen, dann ist Geron am Ziel.
Geron plant zahlreiche P2 Studien mit dem Antisense GRN163L in nächster Zeit, was wieder ein bisschen Fanatsie in die Bude bringen könnte. Auch der muss sich erstmal beweisen.
Bei den Stammzellen werden jetzt sicher Studien ausgearbeitet, die auch erst von der FDA freigegeben werden müssen. Und sollte es wirklich eines Tgaes so sein, dass Blinde wieder laufen können und Querschnittsgelähmte wieder sehen, dann ist Geron am Ziel.
Hallo,
seit einiger Zeit bin ich nun ja auch in Geron investiert.
Aber irgendwie werde ich bei Geron´s Stammzellenforschung den Verdacht nicht los, das es sobald greifbare Ergebnisse der Phase 2 oder 3 Tests vorliegen keine Geron AG mehr geben wird.
Big Pharma wird sich die Butter nicht vom Brot nehmen lassen.http://www.aerztezeitung.de/suchen/default.aspx?query=La+Jol…
In Kalifornien ist sanofi-aventis nun schon, ob das Salk-Institut bald für seine Forschungen Lizenzgebühren an Geron zahlen wird? Zumindest wird man in Kalifornien Geron kennen.
Wachstumsstärkstes Produkt von sanofi ist das Insulin Lantus, Geron könnte hier mit Stammzellen(GRNIC1) die Bauchspeicheldrüse der Diabetes-Patienten wieder aufbauen und Insulin fast überflüssig machen.
Was macht sanofi-aventis dann, wenn Sie mit der Nase darauf gestoßen werden ?
Geron ist doch noch ein Zwerg, Big Pharma kauft beinahe monatlich konkurrierende Unternehmen auf.
Ich würde mich irgendwie ärgern, wenn ich zu früh meine Geron Aktien abgeben sollte, bevor GRN163L Ergebnisse bringt.
Grüsse, golden_star
seit einiger Zeit bin ich nun ja auch in Geron investiert.
Aber irgendwie werde ich bei Geron´s Stammzellenforschung den Verdacht nicht los, das es sobald greifbare Ergebnisse der Phase 2 oder 3 Tests vorliegen keine Geron AG mehr geben wird.
Big Pharma wird sich die Butter nicht vom Brot nehmen lassen.http://www.aerztezeitung.de/suchen/default.aspx?query=La+Jol…
In Kalifornien ist sanofi-aventis nun schon, ob das Salk-Institut bald für seine Forschungen Lizenzgebühren an Geron zahlen wird? Zumindest wird man in Kalifornien Geron kennen.
Wachstumsstärkstes Produkt von sanofi ist das Insulin Lantus, Geron könnte hier mit Stammzellen(GRNIC1) die Bauchspeicheldrüse der Diabetes-Patienten wieder aufbauen und Insulin fast überflüssig machen.
Was macht sanofi-aventis dann, wenn Sie mit der Nase darauf gestoßen werden ?
Geron ist doch noch ein Zwerg, Big Pharma kauft beinahe monatlich konkurrierende Unternehmen auf.
Ich würde mich irgendwie ärgern, wenn ich zu früh meine Geron Aktien abgeben sollte, bevor GRN163L Ergebnisse bringt.
Grüsse, golden_star
Antwort auf Beitrag Nr.: 36.707.501 von Golden_Star am 05.03.09 17:06:01geron gehört zum größenteil merck and co
Antwort auf Beitrag Nr.: 36.708.702 von pedestrian am 05.03.09 19:00:35das Biotechnologieunternehmen Geron Corp. traf mit Merck & Co. eine Übereinkunft mit dem Ziel der gemeinsamen Entwicklung eines Krebsimpfstoffes und der gleichzeitigen Erforschung des in Krebszellen aktiven Enzyms Telomerase.
Wie Geron am Montag weiter mitteilte, wird das Unternehmen eine Vorabzahlung in nicht bestimmter Höhe erhalten. Danach würden Meilensteinzahlungen für geplante Leistungen wie das Erreichen von Entwicklungsschritten, behördliche Genehmigungen und Lizenzeinnahmen gewährt. Darüberhinaus schließt die Kooperation die Wahrscheinlichkeit der Übernahme Geron`s durch Merck zu einem späteren Zeitpunkt ein.
Geron schießen dank der Meldung vorbörslich um rund 22% auf 10,46 USD nach oben.
Wie Geron am Montag weiter mitteilte, wird das Unternehmen eine Vorabzahlung in nicht bestimmter Höhe erhalten. Danach würden Meilensteinzahlungen für geplante Leistungen wie das Erreichen von Entwicklungsschritten, behördliche Genehmigungen und Lizenzeinnahmen gewährt. Darüberhinaus schließt die Kooperation die Wahrscheinlichkeit der Übernahme Geron`s durch Merck zu einem späteren Zeitpunkt ein.
Geron schießen dank der Meldung vorbörslich um rund 22% auf 10,46 USD nach oben.
Kickt mal After Hours!
Ne News seh ick keene. Aber schon seltsam.
Ne News seh ick keene. Aber schon seltsam.
Janz schön wat los. Aber warum?

Antwort auf Beitrag Nr.: 36.720.239 von -Salem- am 06.03.09 23:12:45Obama hat wohl vor, die strengen Gesetze von olle George uffzuheben.
Najut ist, dit is natürlich die Vorausetzung von allem was mit Stammzellen zu tun hat. Aber dit letzte Wort hat der Papst.
Aber dit letzte Wort hat der Papst.
Najut ist, dit is natürlich die Vorausetzung von allem was mit Stammzellen zu tun hat.
 Aber dit letzte Wort hat der Papst.
Aber dit letzte Wort hat der Papst.
Antwort auf Beitrag Nr.: 36.720.239 von -Salem- am 06.03.09 23:12:45http://www.marketwatch.com/news/story/geron-stemcells-jump-a…
AFTER HOURS
Geron surges after U.S. stem-cell research news
By Carla Mozee, MarketWatch
Last update: 6:38 p.m. EST March 6, 2009
Comments: 31
LOS ANGELES (MarketWatch) -- Geron Corp. was among the biotech stocks whose shares jumped Friday evening following reports that a ban on government funding of embryonic stem-cell research will come to an end next week.
Chart of GERN
Geron (GERN:
Geron Corporation
News , chart , profile , more
Last: 3.87+0.08+2.11%
4:00pm 03/06/2009
Delayed quote data
Add to portfolio
Analyst
Create alert
Insider
Discuss
Financials
Sponsored by:
GERN 3.87, +0.08, +2.1%) shares climbed 33% to $5.15 in heavy trading on news reports that President Barack Obama on Monday will sign an executive order overturning the ban that was put in place by President George W. Bush in 1991. The move would make good on a campaign pledge by Obama to lift the ban.
The new order would allow the National Institutes of Health to be able to consider requests from scientists who are seeking funds for stem-cell research, according to the Washington Post. Proponents of such research say it could lead to cures for numerous illnesses.
In late January, the Food and Drug Administration granted clearance to Geron to conduct the first human trial of an embryonic-stem cell treatment to treat spinal cord injuries.
Stock in StemCells Inc. (STEM:
STEM
News , chart , profile , more
Last:
Delayed quote data
Add to portfolio
Analyst
Create alert
Insider
Discuss
Financials
Sponsored by:
STEM, , ) climbed 46% to $2.02 and Aastrom Biosciences Inc. (ASTM:
ASTM
News , chart , profile , more
Last:
Delayed quote data
Add to portfolio
Analyst
Create alert
Insider
Discuss
Financials
Sponsored by:
ASTM, , ) leaped 60% to 53 cents.
AFTER HOURS
Geron surges after U.S. stem-cell research news
By Carla Mozee, MarketWatch
Last update: 6:38 p.m. EST March 6, 2009
Comments: 31
LOS ANGELES (MarketWatch) -- Geron Corp. was among the biotech stocks whose shares jumped Friday evening following reports that a ban on government funding of embryonic stem-cell research will come to an end next week.
Chart of GERN
Geron (GERN:
Geron Corporation
News , chart , profile , more
Last: 3.87+0.08+2.11%
4:00pm 03/06/2009
Delayed quote data
Add to portfolio
Analyst
Create alert
Insider
Discuss
Financials
Sponsored by:
GERN 3.87, +0.08, +2.1%) shares climbed 33% to $5.15 in heavy trading on news reports that President Barack Obama on Monday will sign an executive order overturning the ban that was put in place by President George W. Bush in 1991. The move would make good on a campaign pledge by Obama to lift the ban.
The new order would allow the National Institutes of Health to be able to consider requests from scientists who are seeking funds for stem-cell research, according to the Washington Post. Proponents of such research say it could lead to cures for numerous illnesses.
In late January, the Food and Drug Administration granted clearance to Geron to conduct the first human trial of an embryonic-stem cell treatment to treat spinal cord injuries.
Stock in StemCells Inc. (STEM:
STEM
News , chart , profile , more
Last:
Delayed quote data
Add to portfolio
Analyst
Create alert
Insider
Discuss
Financials
Sponsored by:
STEM, , ) climbed 46% to $2.02 and Aastrom Biosciences Inc. (ASTM:
ASTM
News , chart , profile , more
Last:
Delayed quote data
Add to portfolio
Analyst
Create alert
Insider
Discuss
Financials
Sponsored by:
ASTM, , ) leaped 60% to 53 cents.
Die Hürden fallen, die Mauern reißen.
Jetzt fehlen "nur" noch gute Studienergebnisse.
Jetzt fehlen "nur" noch gute Studienergebnisse.
KEHRTWENDE
Obama will Forschung mit embryonalen Stammzellen fördern
US-Präsident Barack Obama will das Verbot staatlicher Finanzierung embryonaler Stammzellenforschung aufheben. Er verspricht sich davon Fortschritte im Kampf gegen Krankheiten wie Alzheimer. Abtreibungsgegner haben die Pläne bereits scharf kritisiert.
http://www.spiegel.de/wissenschaft/mensch/0,1518,611911,00.h…
Obama will Forschung mit embryonalen Stammzellen fördern
US-Präsident Barack Obama will das Verbot staatlicher Finanzierung embryonaler Stammzellenforschung aufheben. Er verspricht sich davon Fortschritte im Kampf gegen Krankheiten wie Alzheimer. Abtreibungsgegner haben die Pläne bereits scharf kritisiert.
http://www.spiegel.de/wissenschaft/mensch/0,1518,611911,00.h…
Stammzellen
Den Nerv getroffenDer deutsche Forscher Rudolf Jaenisch hat erstmals aus den Hautzellen von Patienten Stammzellen gezüchtet, die keine Krebs erregenden Gene mehr enthalten. Wie wichtig ist dieser Durchbruch?
Die neue Methode von Rudolf Jaenisch, die an diesem Freitag veröffentlicht wird, ist doppelt wichtig: für eine eventuelle Therapie genauso wie für die Grundlagenforschung. Denn sie eröffnet neue Möglichkeiten auf dem Gebiet künstlich erzeugter Stammzellen. Dabei gibt es diese Stammzellen, kurz iPS genannt, seit nicht einmal drei Jahren. Ende 2006 hatten japanische Forscher berichtet, dass sie mit einem Virus vier Gene in die Hautzelle einer Maus schleusen und sie so in den Zustand einer Stammzelle zurückzwingen konnten. „Dass man Zellen mit so einer kleinen Manipulation komplett umprogrammieren kann, das hat wohl keiner erwartet“, sagt der Stammzellforscher Jürgen Hescheler von der Universität Köln. Aber es funktionierte, und im folgenden Jahr zeigte die japanische Gruppe, dass die Technik auch bei menschlichen Zellen wirkt.
Im Februar konnte der Münsteraner Forscher Hans Schöler nun beweisen, dass zumindest bei manchen Zellen des Menschen schon ein einziges Gen ausreicht, um sie wieder auf „Null“ zu setzen. Und Anfang dieser Woche gab ein Team von Wissenschaftlern aus Amerika und Großbritannien bekannt, dass es ihnen gelungen sei, iPS-Zellen herzustellen ohne dabei Viren als Genfähre zu benutzen. Für eine Therapie galt das bisher als großes Hindernis. Das Virus integriert die Gene zwar in das Erbgut der Zelle, doch wo es das tut, ist Zufall. So kann es passieren, dass ein wichtiges Gen gestört wird, das die Zellteilung reguliert. Die Zelle hört dann nicht mehr auf, sich zu vermehren, ein Tumor entsteht. Diese Gefahr besteht mit der neuen Methode kaum. Den Großteil ihrer Experimente machten die Forscher allerdings an Mauszellen, auch wenn die ersten Versuche an menschlichen Zellen darauf hindeuten, dass die Methode auch dort funktioniert.
Nun ist der deutsche Wissenschaftler Rudolf Jaenisch noch einen Schritt weiter gegangen und hat aus den Hautzellen von Parkinsonpatienten Stammzellen erzeugt. Dazu benutzte er zwar ein Virus, das er aber anschließend wieder aus dem Erbgut der Zelle entfernen konnte. Die iPS-Zellen verwandelte Jaenisch dann in genau die Gehirnzellen, die Parkinsonpatienten fehlen. „Das große Versprechen dieser Methode ist, dass wir Parkinson jetzt sozusagen in der Petrischale erforschen können“, sagt er.
Allerdings betont Jaenisch selbst, dass es noch ein sehr weiter Weg sei, bis iPS-Zellen am Menschen eingesetzt werden könnten. „Jede Krankheit hat ihre eigenen Hürden, die da noch überwunden werden müssen.“ Für ihn seien die Stammzellen vor allem interessant als Methode, um Krankheiten zu verstehen und so nach neuen Medikamenten zu suchen. Eine Therapie, die aus der Stammzellforschung komme, müsse nicht unbedingt eine Stammzelltherapie sein. „Das Gebiet der iPS-Zellen entwickelt sich allerdings rasend schnell“, gibt er zu.
Unstrittig ist, dass für eine Therapie mit iPS-Zellen noch wichtige Schritte fehlen. „Wir müssen erst einmal herausfinden, welche Zellen wir eigentlich wo genau hinspritzen müssen“, sagt Jaenisch. Ein entscheidendes Problem nennt auch Jürgen Hescheler: „Was passiert eigentlich, wenn ich diese Zellen in das Gewebe gebe? Integrieren die sich dann richtig?“ Doch er ist optimistisch. Wahrscheinlich werde eine Stammzellentherapie viel schneller kommen, als man denke, sagen beide Forscher. Hescheler spricht von „wenigen Jahren“. Seine Befürchtung sei eher, dass Versuche gemacht würden, bevor man die Stammzellen ausreichend verstehe. Ein unnötiger Fehlschlag könne dem ganzen Forschungsgebiet schaden.
Die Diskussion um embryonale Stammzellen hat sich damit allerdings längst nicht erledigt. Obwohl die ersten Politiker sich schon zu Wort melden und embryonale Stammzellen für überflüssig erklären, werden diese ethisch umstrittenen Zellen in der Forschung dringend benötigt. iPS-Zellen haben zwar den Vorteil, dass für ihre Herstellung keine Embryonen getötet werden müssen. Aber vieles deutet darauf hin, dass sie sich im Detail anders verhalten als ihre embryonalen Vorbilder. „Deswegen brauchen wir embryonale Stammzellen als Vergleich“, sagt Hescheler. Was die Wissenschaft über iPS-Zellen wisse, das habe sie vor allem durch die Forschung an den embryonalen Stammzellen herausgefunden.
„Ich denke, dass es ein Riesenfehler war, dass wir uns in Deutschland aus politischen Gründen so wenig mit embryonalen Stammzellen beschäftigt haben“, sagt Hescheler. Auch Jaenisch, der in Amerika forscht, meint, dass die Beschränkungen in Deutschland die Forschung massiv behindert haben. „Das war eine absurde Debatte, die typische Ideologisierung in der deutschen Politik.“
Inzwischen sind Therapieansätze mit embryonalen Stammzellen weiter fortgeschritten. Im Januar sorgte die Nachricht für Schlagzeilen, dass die amerikanische Regulierungsbehörde FDA einen ersten klinischen Test mit embryonalen Stammzellen genehmigt hat. Geron heißt das Biotechunternehmen, das ab dem Sommer Querschnittsgelähmten diese Zellen spritzen will und hofft, dass sie durchtrennte Nervenbahnen in der Wirbelsäule wieder zusammenbringen. Sollte das auch nur im Ansatz gelingen, würde die Stammzellforschung wohl ein Momentum entwickeln, dem Deutschland sich schwer entziehen könnte. Dann bliebe Kritikern nur zu hoffen, dass die iPS-Zellen möglichst schnell dasselbe Potenzial entfalten.
Den Nerv getroffenDer deutsche Forscher Rudolf Jaenisch hat erstmals aus den Hautzellen von Patienten Stammzellen gezüchtet, die keine Krebs erregenden Gene mehr enthalten. Wie wichtig ist dieser Durchbruch?
Die neue Methode von Rudolf Jaenisch, die an diesem Freitag veröffentlicht wird, ist doppelt wichtig: für eine eventuelle Therapie genauso wie für die Grundlagenforschung. Denn sie eröffnet neue Möglichkeiten auf dem Gebiet künstlich erzeugter Stammzellen. Dabei gibt es diese Stammzellen, kurz iPS genannt, seit nicht einmal drei Jahren. Ende 2006 hatten japanische Forscher berichtet, dass sie mit einem Virus vier Gene in die Hautzelle einer Maus schleusen und sie so in den Zustand einer Stammzelle zurückzwingen konnten. „Dass man Zellen mit so einer kleinen Manipulation komplett umprogrammieren kann, das hat wohl keiner erwartet“, sagt der Stammzellforscher Jürgen Hescheler von der Universität Köln. Aber es funktionierte, und im folgenden Jahr zeigte die japanische Gruppe, dass die Technik auch bei menschlichen Zellen wirkt.
Im Februar konnte der Münsteraner Forscher Hans Schöler nun beweisen, dass zumindest bei manchen Zellen des Menschen schon ein einziges Gen ausreicht, um sie wieder auf „Null“ zu setzen. Und Anfang dieser Woche gab ein Team von Wissenschaftlern aus Amerika und Großbritannien bekannt, dass es ihnen gelungen sei, iPS-Zellen herzustellen ohne dabei Viren als Genfähre zu benutzen. Für eine Therapie galt das bisher als großes Hindernis. Das Virus integriert die Gene zwar in das Erbgut der Zelle, doch wo es das tut, ist Zufall. So kann es passieren, dass ein wichtiges Gen gestört wird, das die Zellteilung reguliert. Die Zelle hört dann nicht mehr auf, sich zu vermehren, ein Tumor entsteht. Diese Gefahr besteht mit der neuen Methode kaum. Den Großteil ihrer Experimente machten die Forscher allerdings an Mauszellen, auch wenn die ersten Versuche an menschlichen Zellen darauf hindeuten, dass die Methode auch dort funktioniert.
Nun ist der deutsche Wissenschaftler Rudolf Jaenisch noch einen Schritt weiter gegangen und hat aus den Hautzellen von Parkinsonpatienten Stammzellen erzeugt. Dazu benutzte er zwar ein Virus, das er aber anschließend wieder aus dem Erbgut der Zelle entfernen konnte. Die iPS-Zellen verwandelte Jaenisch dann in genau die Gehirnzellen, die Parkinsonpatienten fehlen. „Das große Versprechen dieser Methode ist, dass wir Parkinson jetzt sozusagen in der Petrischale erforschen können“, sagt er.
Allerdings betont Jaenisch selbst, dass es noch ein sehr weiter Weg sei, bis iPS-Zellen am Menschen eingesetzt werden könnten. „Jede Krankheit hat ihre eigenen Hürden, die da noch überwunden werden müssen.“ Für ihn seien die Stammzellen vor allem interessant als Methode, um Krankheiten zu verstehen und so nach neuen Medikamenten zu suchen. Eine Therapie, die aus der Stammzellforschung komme, müsse nicht unbedingt eine Stammzelltherapie sein. „Das Gebiet der iPS-Zellen entwickelt sich allerdings rasend schnell“, gibt er zu.
Unstrittig ist, dass für eine Therapie mit iPS-Zellen noch wichtige Schritte fehlen. „Wir müssen erst einmal herausfinden, welche Zellen wir eigentlich wo genau hinspritzen müssen“, sagt Jaenisch. Ein entscheidendes Problem nennt auch Jürgen Hescheler: „Was passiert eigentlich, wenn ich diese Zellen in das Gewebe gebe? Integrieren die sich dann richtig?“ Doch er ist optimistisch. Wahrscheinlich werde eine Stammzellentherapie viel schneller kommen, als man denke, sagen beide Forscher. Hescheler spricht von „wenigen Jahren“. Seine Befürchtung sei eher, dass Versuche gemacht würden, bevor man die Stammzellen ausreichend verstehe. Ein unnötiger Fehlschlag könne dem ganzen Forschungsgebiet schaden.
Die Diskussion um embryonale Stammzellen hat sich damit allerdings längst nicht erledigt. Obwohl die ersten Politiker sich schon zu Wort melden und embryonale Stammzellen für überflüssig erklären, werden diese ethisch umstrittenen Zellen in der Forschung dringend benötigt. iPS-Zellen haben zwar den Vorteil, dass für ihre Herstellung keine Embryonen getötet werden müssen. Aber vieles deutet darauf hin, dass sie sich im Detail anders verhalten als ihre embryonalen Vorbilder. „Deswegen brauchen wir embryonale Stammzellen als Vergleich“, sagt Hescheler. Was die Wissenschaft über iPS-Zellen wisse, das habe sie vor allem durch die Forschung an den embryonalen Stammzellen herausgefunden.
„Ich denke, dass es ein Riesenfehler war, dass wir uns in Deutschland aus politischen Gründen so wenig mit embryonalen Stammzellen beschäftigt haben“, sagt Hescheler. Auch Jaenisch, der in Amerika forscht, meint, dass die Beschränkungen in Deutschland die Forschung massiv behindert haben. „Das war eine absurde Debatte, die typische Ideologisierung in der deutschen Politik.“
Inzwischen sind Therapieansätze mit embryonalen Stammzellen weiter fortgeschritten. Im Januar sorgte die Nachricht für Schlagzeilen, dass die amerikanische Regulierungsbehörde FDA einen ersten klinischen Test mit embryonalen Stammzellen genehmigt hat. Geron heißt das Biotechunternehmen, das ab dem Sommer Querschnittsgelähmten diese Zellen spritzen will und hofft, dass sie durchtrennte Nervenbahnen in der Wirbelsäule wieder zusammenbringen. Sollte das auch nur im Ansatz gelingen, würde die Stammzellforschung wohl ein Momentum entwickeln, dem Deutschland sich schwer entziehen könnte. Dann bliebe Kritikern nur zu hoffen, dass die iPS-Zellen möglichst schnell dasselbe Potenzial entfalten.


as expected...
[urlObama Overturns Bush Policy on Stem Cell Research Funding]http://online.wsj.com/article/SB123660715909671041.html?mod=yahoo_hs&ru=yahoo[/url]
Scientists who have eagerly anticipated the policy change say it will provide a crucial boost for basic stem-cell research, attract young scientists to the field and enable the nation to re-establish leadership in an area where Europe and Asia have made recent inroads.
[urlDer Neue und die Stammzellen - Obama wird Bushs Stammzell-Verbot außer Kraft setzen]http://podcast-mp3.dradio.de/podcast/2009/03/09/dlf_20090309_1636_435723f3.mp3[/url]

Antwort auf Beitrag Nr.: 36.742.023 von kevin.lomax am 10.03.09 23:30:54so bin dabei  mfg frank012
mfg frank012
 mfg frank012
mfg frank012
Antwort auf Beitrag Nr.: 36.746.011 von Frank012 am 11.03.09 15:20:09hier das orderbuch
und Symbol: GERN eingeben
http://www.level2stockquotes.com/level-ii-quotes.html
und Symbol: GERN eingeben

http://www.level2stockquotes.com/level-ii-quotes.html
Antwort auf Beitrag Nr.: 36.747.175 von Frank012 am 11.03.09 17:17:25guten morgen @all
http://data.cnbc.com/quotes/gern
http://data.cnbc.com/quotes/gern
bin seit heute auch mal mit 1000 Stück dabei...freue mich über einen regen gedankenaustausch mit euch!!

es scheint so das sich viele auf biotec aktien stürzen werden.
Einfach so mal 20 %

das nenn ich mal ein vorbörslich geniales Orderbuch :-)
Last Trade: N/A
Trade Time: N/A
Change: N/A
Bid: 6.23 x 100
Ask: 1000000.00 x 100
Last Trade: N/A
Trade Time: N/A
Change: N/A
Bid: 6.23 x 100
Ask: 1000000.00 x 100
Geron Corporation Up 14% Since SmarTrend's Buy Recommendation
49 minutes ago - Comtex Smartrend(r)
Related Companies
Symbol Last %Chg
GERN 6.92 1.16%
As of 11:11 AM ET 6/4/09SmarTrend, our automated pattern recognition system, called an Uptrend for Geron Corporation (NASDAQ:GERN) on 5/5/2009 at $6.20. Since then, Geron Corporation has returned 14% as of today's recent price of $7.07.
---------------------------------------------------------------------------------------------
SmarTrend scans over 5,000 stocks daily and alerts you when a change in trend is identified. Get a free trial of our trading calls at http://www.TradeTheTrend.com.
Get exclusive insight into how the market is expected to perform...before the market opens. Sign up for our free daily market analysis newsletter: http://www.TradeTheTrend.com/signup.html
SmarTrend is a registered trademark of Comtex News Network, Inc., a premier provider of relevant, licensed news and content to companies worldwide. Want licensed news on your website? Visit http://www.Comtex.com for a free trial.
49 minutes ago - Comtex Smartrend(r)
Related Companies
Symbol Last %Chg
GERN 6.92 1.16%
As of 11:11 AM ET 6/4/09SmarTrend, our automated pattern recognition system, called an Uptrend for Geron Corporation (NASDAQ:GERN) on 5/5/2009 at $6.20. Since then, Geron Corporation has returned 14% as of today's recent price of $7.07.
---------------------------------------------------------------------------------------------
SmarTrend scans over 5,000 stocks daily and alerts you when a change in trend is identified. Get a free trial of our trading calls at http://www.TradeTheTrend.com.
Get exclusive insight into how the market is expected to perform...before the market opens. Sign up for our free daily market analysis newsletter: http://www.TradeTheTrend.com/signup.html
SmarTrend is a registered trademark of Comtex News Network, Inc., a premier provider of relevant, licensed news and content to companies worldwide. Want licensed news on your website? Visit http://www.Comtex.com for a free trial.
auf zu neuen Höhen 
UPDATE: Geron, GE Unit Team Up In Stem-Cell Development Pact6-30-09 12:19 PM EDT | E-mail Article | Print Article
NEW YORK -(Dow Jones)- Geron Corp. (GERN) agreed to provide stem cells to General Electric Co.'s (GE) GE Healthcare for use in tools that test drug treatments for their toxic effects on the body, particularly the heart and liver.
Financial terms were not disclosed, but the news sent shares of biotech company Geron up $1.18, or 17.7%, to $7.88 Tuesday. Investors applauded the support of a deep-pocketed company like GE Healthcare, the possibility of Geron securing a royalty stream and the potential use for Geron's stem cell platform. GE's shares were down 6 cents to $11.70.
"We had an asset that we were not able to exploit fully," said David Earp, Geron's senior vice president for business development and chief patents counsel.
Konstantin Fiedler, GE Healthcare's cell-technologies general manager, said he expects the market for toxicity testing under the deal to be in the low hundreds of millions of dollars. Analysts expect Geron to begin receiving royalties as early as next year.
In January, Geron received clearance from the U.S. Food and Drug Administration for the first-ever human trial of a medical treatment derived from embryonic stem cells.
Tuesday, Geron said it is giving GE Healthcare an exclusive license regarding the growth and differentiation of the cells. Scientists from both companies will work on the project, with GE Healthcare funding research and development and being responsible for any manufacturing, sales and distribution of products developed under the deal.
Shares of other stem-cell companies rose. StemCells Inc. (STEM) added 2.4% to $1.72, Aastrom Biosciences Inc. (ASTM) rose 4% to 42 cents and Neostem Inc. ( NBS) gained 16% to $2.05.
Joe Pantginis, an analyst at Merriman Curham Ford, said Geron shares rose on the likelihood of near-term royalty payments plus on the research and development and manufacturing heft that GE provides. Needham analyst Mark Monane also pointed to the fact that the companies expect the first product by early 2010.
For GE, the announcement comes as the conglomerate aims to both reposition its health-care group as well as to align its business units to benefit from White House priorities.
About two months ago, GE unveiled a campaign focused on how GE is improving access and quality to health care globally while lowering costs, The Wall Street Journal reported. Most of GE Healthcare's revenue now comes from diagnostic and imaging equipment, but sales are under pressure as public and private insurers try to reduce health-care costs.
-By Brendan Conway, Dow Jones Newswires; 212-416-2670; brendan.conway@ dowjones.com
(Mike Barris contributed to this report.)
(END) Dow Jones Newswires
06-30-091219ET
Copyright (c) 2009 Dow Jones & Company, Inc.

UPDATE: Geron, GE Unit Team Up In Stem-Cell Development Pact6-30-09 12:19 PM EDT | E-mail Article | Print Article
NEW YORK -(Dow Jones)- Geron Corp. (GERN) agreed to provide stem cells to General Electric Co.'s (GE) GE Healthcare for use in tools that test drug treatments for their toxic effects on the body, particularly the heart and liver.
Financial terms were not disclosed, but the news sent shares of biotech company Geron up $1.18, or 17.7%, to $7.88 Tuesday. Investors applauded the support of a deep-pocketed company like GE Healthcare, the possibility of Geron securing a royalty stream and the potential use for Geron's stem cell platform. GE's shares were down 6 cents to $11.70.
"We had an asset that we were not able to exploit fully," said David Earp, Geron's senior vice president for business development and chief patents counsel.
Konstantin Fiedler, GE Healthcare's cell-technologies general manager, said he expects the market for toxicity testing under the deal to be in the low hundreds of millions of dollars. Analysts expect Geron to begin receiving royalties as early as next year.
In January, Geron received clearance from the U.S. Food and Drug Administration for the first-ever human trial of a medical treatment derived from embryonic stem cells.
Tuesday, Geron said it is giving GE Healthcare an exclusive license regarding the growth and differentiation of the cells. Scientists from both companies will work on the project, with GE Healthcare funding research and development and being responsible for any manufacturing, sales and distribution of products developed under the deal.
Shares of other stem-cell companies rose. StemCells Inc. (STEM) added 2.4% to $1.72, Aastrom Biosciences Inc. (ASTM) rose 4% to 42 cents and Neostem Inc. ( NBS) gained 16% to $2.05.
Joe Pantginis, an analyst at Merriman Curham Ford, said Geron shares rose on the likelihood of near-term royalty payments plus on the research and development and manufacturing heft that GE provides. Needham analyst Mark Monane also pointed to the fact that the companies expect the first product by early 2010.
For GE, the announcement comes as the conglomerate aims to both reposition its health-care group as well as to align its business units to benefit from White House priorities.
About two months ago, GE unveiled a campaign focused on how GE is improving access and quality to health care globally while lowering costs, The Wall Street Journal reported. Most of GE Healthcare's revenue now comes from diagnostic and imaging equipment, but sales are under pressure as public and private insurers try to reduce health-care costs.
-By Brendan Conway, Dow Jones Newswires; 212-416-2670; brendan.conway@ dowjones.com
(Mike Barris contributed to this report.)
(END) Dow Jones Newswires
06-30-091219ET
Copyright (c) 2009 Dow Jones & Company, Inc.
Schöner Aufwärtstrend
Kann man ein Lineal anlegen

[http://finance.yahoo.com/echarts?s=GERN#chart2:symbol=gern;r…
Kann man ein Lineal anlegen


[http://finance.yahoo.com/echarts?s=GERN#chart2:symbol=gern;r…
Stem Cell Stocks Up Big on Monday
The stem cell research sector is flying today, led by market-cap leader Geron (NASDAQ: GERN - News).
Geron is up by 11% today, sprinting ahead of the $8 resistance point from back in late-January and early February. Short sellers, which accounted for 17.5% of the float as of July 15, are scrambling to cover shares, accelerating the rally. Though no news has been released to support the trade, the volatile industry is often subject to moves based on technical indicators. Today, stem cell stocks are all in the green, many by more than 4%.
As a whole, the Stem Cell Stocks Index is ahead by 6.7% today. It is now lagging the S&P 500 by less than -1% over the last month.
StemCells (NASDAQ: STEM - News) may also be benefiting from technical indicators today, testing resistance at around $1.80. The stock has failed to break past the resistance since March, despite testing it twice in June. The stock is up by 9% today.
Aastrom Biosciences (NASDAQ: ASTM - News) is up by 8% in the stem cell rally. Unlike many of its peers, Aastrom had a short interest of less than 1% as of July 15. The stock is fighting to break above its 200-day moving average after slipping below it earlier in the month.
Pluristem Therapeutics (NASDAQ: PSTI - News) is up by 7% today. Meanwhile, Neuralstem (AMEX: CUR - News), Thermogenesis (NASDAQ: KOOL - News), and Opexa Therapeutics (NASDAQ: OPXA - News) are all up by more than 4%.
Osiris Therapeutics (NASDAQ: OSIR - News) is a laggard today, despite breaking into positive territory.
As of this writing, the Stem Cell Stocks Index is one of the top-10 performing tickerspy Indexes over the last five days, up by 11.6%.
Investors can follow the Stem Cell Stocks Index and view related performance charts and metrics at tickerspy.com.
Fun and informative, tickerspy.com is a free investing website where you can track multiple stock portfolios and compare against 250 proprietary Indexes tracking themes from nanotech to agriculture to precious metals. Best of all, tickerspy.com lets you spy on the portfolios of nearly 3,000 Wall Street institutions and hedge funds and see graphs of their performance. Try tickerspy.com today and find out how you stack up against investing legends like Warren Buffett!
http://finance.yahoo.com/news/Stem-Cell-Stocks-Up-Big-on-ind…
The stem cell research sector is flying today, led by market-cap leader Geron (NASDAQ: GERN - News).
Geron is up by 11% today, sprinting ahead of the $8 resistance point from back in late-January and early February. Short sellers, which accounted for 17.5% of the float as of July 15, are scrambling to cover shares, accelerating the rally. Though no news has been released to support the trade, the volatile industry is often subject to moves based on technical indicators. Today, stem cell stocks are all in the green, many by more than 4%.
As a whole, the Stem Cell Stocks Index is ahead by 6.7% today. It is now lagging the S&P 500 by less than -1% over the last month.
StemCells (NASDAQ: STEM - News) may also be benefiting from technical indicators today, testing resistance at around $1.80. The stock has failed to break past the resistance since March, despite testing it twice in June. The stock is up by 9% today.
Aastrom Biosciences (NASDAQ: ASTM - News) is up by 8% in the stem cell rally. Unlike many of its peers, Aastrom had a short interest of less than 1% as of July 15. The stock is fighting to break above its 200-day moving average after slipping below it earlier in the month.
Pluristem Therapeutics (NASDAQ: PSTI - News) is up by 7% today. Meanwhile, Neuralstem (AMEX: CUR - News), Thermogenesis (NASDAQ: KOOL - News), and Opexa Therapeutics (NASDAQ: OPXA - News) are all up by more than 4%.
Osiris Therapeutics (NASDAQ: OSIR - News) is a laggard today, despite breaking into positive territory.
As of this writing, the Stem Cell Stocks Index is one of the top-10 performing tickerspy Indexes over the last five days, up by 11.6%.
Investors can follow the Stem Cell Stocks Index and view related performance charts and metrics at tickerspy.com.
Fun and informative, tickerspy.com is a free investing website where you can track multiple stock portfolios and compare against 250 proprietary Indexes tracking themes from nanotech to agriculture to precious metals. Best of all, tickerspy.com lets you spy on the portfolios of nearly 3,000 Wall Street institutions and hedge funds and see graphs of their performance. Try tickerspy.com today and find out how you stack up against investing legends like Warren Buffett!
http://finance.yahoo.com/news/Stem-Cell-Stocks-Up-Big-on-ind…
Hat jemand eine Erklärung zum heutigen Kursverlauf?
7.94 - 9.19
7.94 - 9.19
Antwort auf Beitrag Nr.: 37.691.008 von jub2 am 31.07.09 22:35:30Q2 Zahlen?
Antwort auf Beitrag Nr.: 37.691.008 von jub2 am 31.07.09 22:35:30Geron meldete einen erneut höheren Quartalsverlust von ca. 20 Millionen $.
Bis Geron Geld verdienen kann, werden noch zahlreiche Jahre vergehen und die vorhandenen finanziellen Mittel sind spätestens in 2 Jahren aufgebraucht. - Also wird Geron immer mal wieder Geld am Kapitalmarkt beschaffen müssen, was zu Aktienausgaben (Verwässerung) führen wird.
Gestern belastete zunächst der angestiegene Quartalsverlust und als die später anlaufende Konferenz zwischenzeitlich missverstanden wurde, schnellte der Kurs ganz kurz auf 9,19 $.
Als sich die Missverständnisse (Geld von GE und bereits 18 Patienten für spinal-disease rekrutiert) klärten (es fehlen noch überwiegend die Zustimmungen der teilnehmenden Unikliniken und Geld von GE gibt es nur im Sinne von GE) rückte der Fokus wieder auf die hohe cash-burn-rate und der Kurs begann kontinuierlich zu fallen.
Persönlich erwarte ich, dass Geron bis spätestens Ende Oktober im Bereich 5 - 6 $ zu haben sein wird - vielleicht auch noch preiswerter.
Für ein Biotech-Unternehmen, welches bis zum Durchbruch wahrscheinlich noch 300 - 600 Millionen $ verbrauchen wird, ist eine Marktkapitalisierung von 700 Millionen $ m.E. deutlich übertrieben. Ob der Durchbruch gelingen wird, ist übrigens keines Falls absolut Gewiss.
Hinzu kommt, dass Mitbewerber zumindest von der Zeitschiene her deutlich die Nase vorn haben : Cellerix, Osiris, Cytori usw.
Und wie schnell man ganz unter gehen kann, zeigt Aastrom gut auf, obwohl deren medizinischer Weg gar erfolgreich sein kann / könnte.
Geron sprang von unter 2 $ auf über 9 $, nur weil sie in der Klinik starten dürfen. - Ist das gerechtfertigt ?
Cytori hat z.B. bereits 2 unterschiedliche Herzanwendungen, Brustaugmentation, Brustrekonstruktion, Gewebeaufbau im Gesicht von Aidspatienten, Leberbehandlung usw. in der Klinik und erzielt bereits erste und deutlich höhere Einnahmen als Geron. MK von Cytori allerdings nur ca. 130 Millionen $.
Bis Geron Geld verdienen kann, werden noch zahlreiche Jahre vergehen und die vorhandenen finanziellen Mittel sind spätestens in 2 Jahren aufgebraucht. - Also wird Geron immer mal wieder Geld am Kapitalmarkt beschaffen müssen, was zu Aktienausgaben (Verwässerung) führen wird.
Gestern belastete zunächst der angestiegene Quartalsverlust und als die später anlaufende Konferenz zwischenzeitlich missverstanden wurde, schnellte der Kurs ganz kurz auf 9,19 $.
Als sich die Missverständnisse (Geld von GE und bereits 18 Patienten für spinal-disease rekrutiert) klärten (es fehlen noch überwiegend die Zustimmungen der teilnehmenden Unikliniken und Geld von GE gibt es nur im Sinne von GE) rückte der Fokus wieder auf die hohe cash-burn-rate und der Kurs begann kontinuierlich zu fallen.
Persönlich erwarte ich, dass Geron bis spätestens Ende Oktober im Bereich 5 - 6 $ zu haben sein wird - vielleicht auch noch preiswerter.
Für ein Biotech-Unternehmen, welches bis zum Durchbruch wahrscheinlich noch 300 - 600 Millionen $ verbrauchen wird, ist eine Marktkapitalisierung von 700 Millionen $ m.E. deutlich übertrieben. Ob der Durchbruch gelingen wird, ist übrigens keines Falls absolut Gewiss.
Hinzu kommt, dass Mitbewerber zumindest von der Zeitschiene her deutlich die Nase vorn haben : Cellerix, Osiris, Cytori usw.
Und wie schnell man ganz unter gehen kann, zeigt Aastrom gut auf, obwohl deren medizinischer Weg gar erfolgreich sein kann / könnte.
Geron sprang von unter 2 $ auf über 9 $, nur weil sie in der Klinik starten dürfen. - Ist das gerechtfertigt ?
Cytori hat z.B. bereits 2 unterschiedliche Herzanwendungen, Brustaugmentation, Brustrekonstruktion, Gewebeaufbau im Gesicht von Aidspatienten, Leberbehandlung usw. in der Klinik und erzielt bereits erste und deutlich höhere Einnahmen als Geron. MK von Cytori allerdings nur ca. 130 Millionen $.
bin auf den Wert aufmerksam gemacht worden.Was gibt es hier zu wissen bei der company ?
danke
danke
Sie fanden ein Enzym, das die Alterung reguliert - und beim Entstehen von Krebs eine Schlüsselrolle spielt. Zwei US-Forscherinnen und ein Kollege wurden jetzt für ihre Entdeckung mit dem Nobelpreis geehrt. Pharma- und Anti-Aging-Industrie setzen große Hoffnung auf die Erforschung der Telomerase.
Als das "Time Magazine" vor zwei Jahren Elizabeth Blackburn in die Liste der 100 einflussreichsten Menschen der Welt aufnahm, vermied es die Wissenschaftlerin, einen Fehler der Redakteure korrigieren zu lassen. In dem Artikel wurde ihr Alter mit 44 angegeben. In Wahrheit war die Wissenschaftlerin schon 58.
ANZEIGE
Seither wurde der Fehler nicht korrigiert. Auch eine Art des Jungbrunnens.
Dabei ist Blackburn, die am Montag zusammen mit den US-Forschern Carol Greider und Jack Szostak mit dem Nobelpreis für Medizin ausgezeichnet worden ist, dem Geheimnis der ewigen Jugend dicht auf der Spur. Seit mehr als 30 Jahren untersucht die Wissenschaftlerin das Altern und dessen biochemische Prozesse in der Zelle. Den Nobelpreis teilt sie sich mit ihren Kollegen für die Entdeckung eines lebensnotwendigen Enzyms, dem beim Altern eine wichtige Funktion zugeschrieben wird: Telomerase.Schon zu Beginn der siebziger Jahre standen die Genetiker vor einem grundlegenden Problem: Eine Zelle muss vor jeder Teilung ihr Erbgut akkurat kopieren. Nur so erhält jede Tochterzelle das vollständige genetische Material, andernfalls drohen Fehlfunktionen oder gar der Untergang der Zelle. Doch schon James D. Watson, ebenfalls Nobelpreisträger und Mitentdecker der Doppelhelix-Struktur der DNA, wusste, dass es beim Kopieren der Erbsubstanz Stolpersteine gibt. Die Enzyme, die DNA herstellen können und die man bis dahin kannte, sind nicht in der Lage, die Enden der Chromosomen exakt und vollständig zu vervielfältigen. Somit müsste bei jeder Zellteilung ein Teil der Chromosomenenden, der sogenannten Telomere, unweigerlich schwinden und schließlich auch kritische Erbsubstanz verlorengehen. Dieses Problem nannten die Wissenschaftler das "Endreplikationsproblem".
Die Suche nach der Telomerase
Blackburn, die seinerzeit in Berkley an der University of California war, hatte gemeinsam mit dem Kollegen Jack Szostak von der Harvard University eine eigene Theorie für dieses Problem. Ihre Annahme war, es müsse einen Mechanismus geben, der diesem Verschwinden der Chromosomenenden entgegenarbeitet. Schon bald darauf fanden die Wissenschaftler heraus, dass die Telomere im Zuge von Zellteilungen tatsächlich schrumpfen. Doch durch Anhängen einzelner DNA-Bausteine werden sie auch wieder verlängert.
Für diesen Prozess musste es ein Enzym geben, dessen waren sich die Forscher einig. Und tatsächlich gelang es Blackburn, ihrer Doktorandin Carol Greider sowie Jack Szostak Anfang der achtziger Jahre dessen Existenz in einem Reagenzglastest zu belegen. "Das waren ganz entscheidende Experimente, die Szostak und Blackburn 1982 zusammen durchgeführt haben. Sie waren sehr originell, geradezu frech", begründet der schwedische Medizinprofessor Nils-Göran Larsson vom Karolinska-Institut in Stockholm, einer der Juroren zur Verleihung des Medizin-Nobelpreises, die Entscheidung für die Verleihung des Preises. In den darauffolgenden Jahren wiesen sie und andere Arbeitsgruppen die Telomerase erst in einzelligen Organismen, später auch in Hefepilzen, Fröschen und Mäusen nach. Bald sollte der Wissenschaft klar werden, dass praktisch alle Organismen, darunter auch der Mensch, die Zellen mit Kernen haben, Telomerase produzieren. Zwar unterscheidet sich das Enzym in Details von Art zu Art, im Grunde funktioniert es aber immer nach dem gleichen Prinzip.
Dank der grundlegenden Forschungen von Blackburn, Greider und Szostak weiß man heute, dass die Länge der Telomere und das Altern einer Zelle zusammenhängen. Wenn sich die Telomere verkürzen, altert die Zelle. Dieser Vorgang passiert in den meisten normalen ausgewachsenen menschlichen Zellen. Dort ist die Telomerase meistens nicht mehr oder nur kaum aktiv und die Zahl der Vermehrungszyklen dadurch beschränkt. Für viele Forscher begann mit dieser Erkenntnis die Jagd nach dem ewigen Jungbrunnen. Die Idee: Man müsste in den Zellen die Aktivität der Telomerase nur wieder einschalten und schon könnten sie sich wieder unbegrenzt teilen. Die Anti-Aging-Medizin sieht hier einen Ansatzpunkt zur Steigerung der Lebenserwartung.
Telomerase spielt eine entscheidende Rolle bei der Entstehung von Krebs
Doch dass Zellen ohne aktive Telomerase an Teilungsfähigkeit einbüßen, ist nicht zwangsläufig ein Makel. Vielmehr verhindert die Deaktivierung von Telomerase mitunter den Ausbruch vor Krebs. In den vergangenen Jahren wurden in einer Reihe von Untersuchungen gezeigt, dass Telomerase in vielen Krebszellen besonders aktiv ist. Krebszellen teilen sich unkontrolliert, weshalb es zu Wucherungen im Gewebe kommen kann. Deshalb ist eine Krebszelle besonders daran interessiert, sich unbegrenzt teilen zu können. Das geht nur mit stabilen Telomeren, die mit Hilfe von Telomerase ständig wieder aufgefüllt werden.
Diese Erkenntnis hat zu einer Reihe von Ansätzen für die Therapie von Krebs geführt. Forscher und Pharmaindustrie hoffen, mit neuen Wirkstoffen die Telomerase-Aktivität in Tumorzellen zu vermindern. Dann wäre der schützende Mechanismus außer Kraft gesetzt, die Krebszelle würde genau eine normale Körperzelle altern und nach einer bestimmten Anzahl an Zellteilungen sterben. Dieses Ziel verfolgt beispielsweise die kalifornische Firma Geron. Sie hat einen Telomerase-Inhibitor entwickelt, der derzeit in einer Reihe von klinischen Studien untersucht wird. Doch Ergebnisse, die eine Wirksamkeit solcher Substanzen bei Krebserkrankungen belegen würden, gibt es noch nicht.
Doch bis aus den Forschungsarbeiten der drei Nobelpreisträger nützliche Medikamente für Krebskranke entstanden sind, wird es noch eine Weile dauern. "Die Entdeckung wird sehr, sehr viele Konsequenzen für die Medizin haben. Aber wann, das kann man nicht sagen. Bei ähnlichen Nobelpreisen in der Vergangenheit dauerte es 30 Jahre", sagt der Juror Nils-Göran Larsson.
Als das "Time Magazine" vor zwei Jahren Elizabeth Blackburn in die Liste der 100 einflussreichsten Menschen der Welt aufnahm, vermied es die Wissenschaftlerin, einen Fehler der Redakteure korrigieren zu lassen. In dem Artikel wurde ihr Alter mit 44 angegeben. In Wahrheit war die Wissenschaftlerin schon 58.
ANZEIGE
Seither wurde der Fehler nicht korrigiert. Auch eine Art des Jungbrunnens.
Dabei ist Blackburn, die am Montag zusammen mit den US-Forschern Carol Greider und Jack Szostak mit dem Nobelpreis für Medizin ausgezeichnet worden ist, dem Geheimnis der ewigen Jugend dicht auf der Spur. Seit mehr als 30 Jahren untersucht die Wissenschaftlerin das Altern und dessen biochemische Prozesse in der Zelle. Den Nobelpreis teilt sie sich mit ihren Kollegen für die Entdeckung eines lebensnotwendigen Enzyms, dem beim Altern eine wichtige Funktion zugeschrieben wird: Telomerase.Schon zu Beginn der siebziger Jahre standen die Genetiker vor einem grundlegenden Problem: Eine Zelle muss vor jeder Teilung ihr Erbgut akkurat kopieren. Nur so erhält jede Tochterzelle das vollständige genetische Material, andernfalls drohen Fehlfunktionen oder gar der Untergang der Zelle. Doch schon James D. Watson, ebenfalls Nobelpreisträger und Mitentdecker der Doppelhelix-Struktur der DNA, wusste, dass es beim Kopieren der Erbsubstanz Stolpersteine gibt. Die Enzyme, die DNA herstellen können und die man bis dahin kannte, sind nicht in der Lage, die Enden der Chromosomen exakt und vollständig zu vervielfältigen. Somit müsste bei jeder Zellteilung ein Teil der Chromosomenenden, der sogenannten Telomere, unweigerlich schwinden und schließlich auch kritische Erbsubstanz verlorengehen. Dieses Problem nannten die Wissenschaftler das "Endreplikationsproblem".
Die Suche nach der Telomerase
Blackburn, die seinerzeit in Berkley an der University of California war, hatte gemeinsam mit dem Kollegen Jack Szostak von der Harvard University eine eigene Theorie für dieses Problem. Ihre Annahme war, es müsse einen Mechanismus geben, der diesem Verschwinden der Chromosomenenden entgegenarbeitet. Schon bald darauf fanden die Wissenschaftler heraus, dass die Telomere im Zuge von Zellteilungen tatsächlich schrumpfen. Doch durch Anhängen einzelner DNA-Bausteine werden sie auch wieder verlängert.
Für diesen Prozess musste es ein Enzym geben, dessen waren sich die Forscher einig. Und tatsächlich gelang es Blackburn, ihrer Doktorandin Carol Greider sowie Jack Szostak Anfang der achtziger Jahre dessen Existenz in einem Reagenzglastest zu belegen. "Das waren ganz entscheidende Experimente, die Szostak und Blackburn 1982 zusammen durchgeführt haben. Sie waren sehr originell, geradezu frech", begründet der schwedische Medizinprofessor Nils-Göran Larsson vom Karolinska-Institut in Stockholm, einer der Juroren zur Verleihung des Medizin-Nobelpreises, die Entscheidung für die Verleihung des Preises. In den darauffolgenden Jahren wiesen sie und andere Arbeitsgruppen die Telomerase erst in einzelligen Organismen, später auch in Hefepilzen, Fröschen und Mäusen nach. Bald sollte der Wissenschaft klar werden, dass praktisch alle Organismen, darunter auch der Mensch, die Zellen mit Kernen haben, Telomerase produzieren. Zwar unterscheidet sich das Enzym in Details von Art zu Art, im Grunde funktioniert es aber immer nach dem gleichen Prinzip.
Dank der grundlegenden Forschungen von Blackburn, Greider und Szostak weiß man heute, dass die Länge der Telomere und das Altern einer Zelle zusammenhängen. Wenn sich die Telomere verkürzen, altert die Zelle. Dieser Vorgang passiert in den meisten normalen ausgewachsenen menschlichen Zellen. Dort ist die Telomerase meistens nicht mehr oder nur kaum aktiv und die Zahl der Vermehrungszyklen dadurch beschränkt. Für viele Forscher begann mit dieser Erkenntnis die Jagd nach dem ewigen Jungbrunnen. Die Idee: Man müsste in den Zellen die Aktivität der Telomerase nur wieder einschalten und schon könnten sie sich wieder unbegrenzt teilen. Die Anti-Aging-Medizin sieht hier einen Ansatzpunkt zur Steigerung der Lebenserwartung.
Telomerase spielt eine entscheidende Rolle bei der Entstehung von Krebs
Doch dass Zellen ohne aktive Telomerase an Teilungsfähigkeit einbüßen, ist nicht zwangsläufig ein Makel. Vielmehr verhindert die Deaktivierung von Telomerase mitunter den Ausbruch vor Krebs. In den vergangenen Jahren wurden in einer Reihe von Untersuchungen gezeigt, dass Telomerase in vielen Krebszellen besonders aktiv ist. Krebszellen teilen sich unkontrolliert, weshalb es zu Wucherungen im Gewebe kommen kann. Deshalb ist eine Krebszelle besonders daran interessiert, sich unbegrenzt teilen zu können. Das geht nur mit stabilen Telomeren, die mit Hilfe von Telomerase ständig wieder aufgefüllt werden.
Diese Erkenntnis hat zu einer Reihe von Ansätzen für die Therapie von Krebs geführt. Forscher und Pharmaindustrie hoffen, mit neuen Wirkstoffen die Telomerase-Aktivität in Tumorzellen zu vermindern. Dann wäre der schützende Mechanismus außer Kraft gesetzt, die Krebszelle würde genau eine normale Körperzelle altern und nach einer bestimmten Anzahl an Zellteilungen sterben. Dieses Ziel verfolgt beispielsweise die kalifornische Firma Geron. Sie hat einen Telomerase-Inhibitor entwickelt, der derzeit in einer Reihe von klinischen Studien untersucht wird. Doch Ergebnisse, die eine Wirksamkeit solcher Substanzen bei Krebserkrankungen belegen würden, gibt es noch nicht.
Doch bis aus den Forschungsarbeiten der drei Nobelpreisträger nützliche Medikamente für Krebskranke entstanden sind, wird es noch eine Weile dauern. "Die Entdeckung wird sehr, sehr viele Konsequenzen für die Medizin haben. Aber wann, das kann man nicht sagen. Bei ähnlichen Nobelpreisen in der Vergangenheit dauerte es 30 Jahre", sagt der Juror Nils-Göran Larsson.
http://www.sciencedaily.com/releases/2010/01/100104041830.ht…
Experimental Drug Shows Promise Against Brain, Prostate Cancers
ScienceDaily (Jan. 4, 2010) — An experimental drug currently being tested against breast and lung cancer shows promise in fighting the brain cancer glioblastoma and prostate cancer, researchers at UT Southwestern Medical Center have found in two preclinical studies.
The drug's actions, observed in isolated human cells in one trial and in rodents in the other, are especially encouraging because they attacked not only the bulk of the tumor cells but also the rare cancer stem cells that are believed to be responsible for most of a cancer's growth, said Dr. Jerry Shay, professor of cell biology and a senior co-author of both papers. The glioblastoma study appears in the January issue of Clinical Cancer Research. The prostate cancer study is available online in the International Journal of Cancer.
In the glioblastoma study, performed in mice, the drug also crossed from the bloodstream into the brain, which is especially important because many drugs are not able to cross the blood-brain barrier.
"Because it attacks a mechanism that's active in most cancers, it might prove to be widely useful, especially when combined with other therapies," said Dr. Shay.
Dr. Shay and his colleagues study telomeres, bits of DNA that help control how many times a cell divides. Telomeres are protective "caps" of DNA on the ends of chromosomes, the structures that contain the body's genes. As long as telomeres are longer than a certain minimum length, a cell can keep dividing. But telomeres shorten with each cell division, so a cell stops dividing once the telomeres are whittled down to that minimum.
In cancer cells, however, an enzyme called telomerase keeps rebuilding the telomeres, so the cell never receives the cue to stop dividing. In essence, they become immortal, dividing endlessly.
The drug used in these studies (imetelstat or GRN163L) blocks telomerase. It is already in clinical trials as a potential treatment for breast and lung cancer, as well as for chronic lymphocytic leukemia.
Glioblastomas are the most common malignant brain tumors in adults, according to the American Cancer Society. They are difficult to treat with drugs because blood vessels in the brain have tightly constructed walls that allow only a few substances to pass through.
The researcher focused on cells called tumor-initiating cells. Some researchers believe that tumors contain a small subset of initiating cells -- or cancer stem cells -- that are able to initiate and drive tumors and that are often resistant to radiation therapy and chemotherapy.
In the glioblastoma study, Dr. Shay and his colleagues found that imetelstat blocked the action of telomerase in isolated tumor-initiating cells as well as the bulk of the tumor cells, eventually killing the cells. Combining imetelstat with radiation and a standard chemotherapy drug made imetelstat even more effective. When the researchers implanted human tumor-initiating cells into rodents, they found that imetelstat was able to enter brain tissue and inhibit telomerase activity.
In the prostate cancer study, the researchers isolated tumor-initiating cells from human prostate cancer cells. The cells showed significant telomerase activity. Imetelstat blocked the enzyme's activity, and telomeres shortened greatly.
Other UT Southwestern researchers involved in the glioblastoma study were lead author Dr. Calin Marian, postdoctoral researcher in cell biology; Dr. Steve Cho, postdoctoral researcher in neurology; graduate student Brian McEllin; Dr. Elizabeth Maher, associate professor of internal medicine; Dr. Kimmo Hatanpaa, assistant professor of pathology; Dr. Christopher Madden, associate professor of neurological surgery; Dr. Bruce Mickey, professor of neurological surgery; Dr. Woodring Wright, professor of cell biology; and co-senior author Dr. Robert Bachoo, assistant professor of neurology.
Other UT Southwestern researchers involved in the prostate cancer study were lead author Dr. Marian and Dr. Wright.
Geron Corporation, which manufactures GRN163L under the name imetelstat, provided the drug for both studies. The glioblastoma study was supported by the National Institutes of Health. The prostate cancer study was supported by a Department of Defense Prostate Cancer Training Award and the Southland Financial Corporation.
Experimental Drug Shows Promise Against Brain, Prostate Cancers
ScienceDaily (Jan. 4, 2010) — An experimental drug currently being tested against breast and lung cancer shows promise in fighting the brain cancer glioblastoma and prostate cancer, researchers at UT Southwestern Medical Center have found in two preclinical studies.
The drug's actions, observed in isolated human cells in one trial and in rodents in the other, are especially encouraging because they attacked not only the bulk of the tumor cells but also the rare cancer stem cells that are believed to be responsible for most of a cancer's growth, said Dr. Jerry Shay, professor of cell biology and a senior co-author of both papers. The glioblastoma study appears in the January issue of Clinical Cancer Research. The prostate cancer study is available online in the International Journal of Cancer.
In the glioblastoma study, performed in mice, the drug also crossed from the bloodstream into the brain, which is especially important because many drugs are not able to cross the blood-brain barrier.
"Because it attacks a mechanism that's active in most cancers, it might prove to be widely useful, especially when combined with other therapies," said Dr. Shay.
Dr. Shay and his colleagues study telomeres, bits of DNA that help control how many times a cell divides. Telomeres are protective "caps" of DNA on the ends of chromosomes, the structures that contain the body's genes. As long as telomeres are longer than a certain minimum length, a cell can keep dividing. But telomeres shorten with each cell division, so a cell stops dividing once the telomeres are whittled down to that minimum.
In cancer cells, however, an enzyme called telomerase keeps rebuilding the telomeres, so the cell never receives the cue to stop dividing. In essence, they become immortal, dividing endlessly.
The drug used in these studies (imetelstat or GRN163L) blocks telomerase. It is already in clinical trials as a potential treatment for breast and lung cancer, as well as for chronic lymphocytic leukemia.
Glioblastomas are the most common malignant brain tumors in adults, according to the American Cancer Society. They are difficult to treat with drugs because blood vessels in the brain have tightly constructed walls that allow only a few substances to pass through.
The researcher focused on cells called tumor-initiating cells. Some researchers believe that tumors contain a small subset of initiating cells -- or cancer stem cells -- that are able to initiate and drive tumors and that are often resistant to radiation therapy and chemotherapy.
In the glioblastoma study, Dr. Shay and his colleagues found that imetelstat blocked the action of telomerase in isolated tumor-initiating cells as well as the bulk of the tumor cells, eventually killing the cells. Combining imetelstat with radiation and a standard chemotherapy drug made imetelstat even more effective. When the researchers implanted human tumor-initiating cells into rodents, they found that imetelstat was able to enter brain tissue and inhibit telomerase activity.
In the prostate cancer study, the researchers isolated tumor-initiating cells from human prostate cancer cells. The cells showed significant telomerase activity. Imetelstat blocked the enzyme's activity, and telomeres shortened greatly.
Other UT Southwestern researchers involved in the glioblastoma study were lead author Dr. Calin Marian, postdoctoral researcher in cell biology; Dr. Steve Cho, postdoctoral researcher in neurology; graduate student Brian McEllin; Dr. Elizabeth Maher, associate professor of internal medicine; Dr. Kimmo Hatanpaa, assistant professor of pathology; Dr. Christopher Madden, associate professor of neurological surgery; Dr. Bruce Mickey, professor of neurological surgery; Dr. Woodring Wright, professor of cell biology; and co-senior author Dr. Robert Bachoo, assistant professor of neurology.
Other UT Southwestern researchers involved in the prostate cancer study were lead author Dr. Marian and Dr. Wright.
Geron Corporation, which manufactures GRN163L under the name imetelstat, provided the drug for both studies. The glioblastoma study was supported by the National Institutes of Health. The prostate cancer study was supported by a Department of Defense Prostate Cancer Training Award and the Southland Financial Corporation.
Antwort auf Beitrag Nr.: 38.119.077 von Lotschka am 05.10.09 21:42:02http://www.newkerala.com/news/fullnews-23890.html
Experimental lung cancer drug may help treat brain, prostate cancer
Washington, Jan 4 : A drug, currently undergoing trials for breast and lung cancer, has also been found effective in treating brain cancer glioblastoma and prostate cancer, say researchers.
According to Dr. Jerry Shay, professor of cell biology, the drug''s actions, observed in isolated human cells in one trial and in rodents in the other, are especially encouraging because they attacked not only the bulk of the tumour cells but also the rare cancer stem cells that are believed to be responsible for most of a cancer''s growth.
In the brain cancer study, the drug could successfully cross the bloodstream into the brain, which is especially important because many drugs are not able to cross the blood-brain barrier.
"Because it attacks a mechanism that''s active in most cancers, it might prove to be widely useful, especially when combined with other therapies," said Shay.
The researchers focussed their study on telomeres, bits of DNA that help control how many times a cell divides. Telomeres are protective "caps" of DNA on the ends of chromosomes, the structures that contain the body''s genes. As long as telomeres are longer than a certain minimum length, a cell can keep dividing.
But telomeres shorten with each cell division, so a cell stops dividing once the telomeres are whittled down to that minimum.
In cancer cells, however, an enzyme called telomerase keeps rebuilding the telomeres, so the cell never receives the cue to stop dividing. In essence, they become immortal, dividing endlessly.
The experimental drug called imetelstat or GRN163L was found to block telomerase.
It is already in clinical trials as a potential treatment for breast and lung cancer, as well as for chronic lymphocytic leukemia.
Glioblastomas are the most common malignant brain tumours in adults. In the glioblastoma study Shay and his colleagues found that imetelstat blocked the action of telomerase in isolated tumour-initiating cells as well as the bulk of the tumour cells, eventually killing the cells.
Combining imetelstat with radiation and a standard chemotherapy drug made imetelstat even more effective.
In the prostate cancer study, the researchers isolated tumour-initiating cells from human prostate cancer cells. The cells showed significant telomerase activity. Imetelstat blocked the enzyme''s activity, and telomeres shortened greatly.
The glioblastoma study appears in Clinical Cancer Research. The prostate cancer study appears in the International Journal of Cancer.
Experimental lung cancer drug may help treat brain, prostate cancer
Washington, Jan 4 : A drug, currently undergoing trials for breast and lung cancer, has also been found effective in treating brain cancer glioblastoma and prostate cancer, say researchers.
According to Dr. Jerry Shay, professor of cell biology, the drug''s actions, observed in isolated human cells in one trial and in rodents in the other, are especially encouraging because they attacked not only the bulk of the tumour cells but also the rare cancer stem cells that are believed to be responsible for most of a cancer''s growth.
In the brain cancer study, the drug could successfully cross the bloodstream into the brain, which is especially important because many drugs are not able to cross the blood-brain barrier.
"Because it attacks a mechanism that''s active in most cancers, it might prove to be widely useful, especially when combined with other therapies," said Shay.
The researchers focussed their study on telomeres, bits of DNA that help control how many times a cell divides. Telomeres are protective "caps" of DNA on the ends of chromosomes, the structures that contain the body''s genes. As long as telomeres are longer than a certain minimum length, a cell can keep dividing.
But telomeres shorten with each cell division, so a cell stops dividing once the telomeres are whittled down to that minimum.
In cancer cells, however, an enzyme called telomerase keeps rebuilding the telomeres, so the cell never receives the cue to stop dividing. In essence, they become immortal, dividing endlessly.
The experimental drug called imetelstat or GRN163L was found to block telomerase.
It is already in clinical trials as a potential treatment for breast and lung cancer, as well as for chronic lymphocytic leukemia.
Glioblastomas are the most common malignant brain tumours in adults. In the glioblastoma study Shay and his colleagues found that imetelstat blocked the action of telomerase in isolated tumour-initiating cells as well as the bulk of the tumour cells, eventually killing the cells.
Combining imetelstat with radiation and a standard chemotherapy drug made imetelstat even more effective.
In the prostate cancer study, the researchers isolated tumour-initiating cells from human prostate cancer cells. The cells showed significant telomerase activity. Imetelstat blocked the enzyme''s activity, and telomeres shortened greatly.
The glioblastoma study appears in Clinical Cancer Research. The prostate cancer study appears in the International Journal of Cancer.
Scheint so als hätte man Stammzellen wiederentdeckt. Geron jedenfalls ist unter hohen Umsätzen aus dem Abwärtstrend der vergangennen Jahre heute scheinbar ausgebrochen.
Hoffen wir mal das es dabei bleibt
Just like investors need to swing for the fences once in a while, pharmaceutical companies sometimes have to look for the next big thing even if it's a long shot.
Enter Pfizer's (NYSE: PFE) license of a stem cell product, MultiStem, from tiny Athersys. And by tiny, I mean really tiny, as in $19-million-market-cap small before the announcement. That's well below my radar, so kudos to Pfizer for not blowing it off like the rest of us investors.
Having a big pharma partner validate its technology has caused Athersys to more than quadruple, as I write, over the last two days.
MultiStem is being tested in several conditions, but Pfizer's license is specifically for the treatment of inflammatory bowel disease (IBD), a group of conditions that includes ulcerative colitis and Crohn's disease. The license is only costing Pfizer $6 million up front because the technology is still relatively unproven, having not entered clinical trials for IBD yet. Athersys can get milestones of up to $105 million and royalties as the drug passes through clinical trials and is commercialized.
Pfizer will pay for the phase 1 and 2 trials. Then, if it gets that far, Athersys will have the option of co-developing the drug -- sharing profits and losses -- or letting Pfizer proceed on its own and take the milestones and royalty payments.
Unlike traditional stem cell companies like Geron (Nasdaq: GERN) that are developing stem cells to regenerate tissue, MultiStem uses donated bone marrow cells to produce a product that promotes healing of the tissue through cell signaling. Essentially it has a more drug-like profile as the stem cells are cleared from the body.
Stem cells aren't particularly new to large pharma. GlaxoSmithKline (NYSE: GSK) has a partnership with Harvard Stem Cell Institute and many companies, including Pfizer, Johnson & Johnson (NYSE: JNJ), Abbott Labs (NYSE: ABT), and sanofi-aventis (NYSE: SNY), teamed up to develop stem cells to help predict side effects.
But Pfizer seems to have taken a particular liking to stem cells, having established a unit to study them last year. If you're going to follow Pfizer's lead and invest in stem cell companies, I'd suggest you also follow its lead and keep your investments in stem cell technology to a very small fraction of your portfolio.
Hoffen wir mal das es dabei bleibt

Just like investors need to swing for the fences once in a while, pharmaceutical companies sometimes have to look for the next big thing even if it's a long shot.
Enter Pfizer's (NYSE: PFE) license of a stem cell product, MultiStem, from tiny Athersys. And by tiny, I mean really tiny, as in $19-million-market-cap small before the announcement. That's well below my radar, so kudos to Pfizer for not blowing it off like the rest of us investors.
Having a big pharma partner validate its technology has caused Athersys to more than quadruple, as I write, over the last two days.
MultiStem is being tested in several conditions, but Pfizer's license is specifically for the treatment of inflammatory bowel disease (IBD), a group of conditions that includes ulcerative colitis and Crohn's disease. The license is only costing Pfizer $6 million up front because the technology is still relatively unproven, having not entered clinical trials for IBD yet. Athersys can get milestones of up to $105 million and royalties as the drug passes through clinical trials and is commercialized.
Pfizer will pay for the phase 1 and 2 trials. Then, if it gets that far, Athersys will have the option of co-developing the drug -- sharing profits and losses -- or letting Pfizer proceed on its own and take the milestones and royalty payments.
Unlike traditional stem cell companies like Geron (Nasdaq: GERN) that are developing stem cells to regenerate tissue, MultiStem uses donated bone marrow cells to produce a product that promotes healing of the tissue through cell signaling. Essentially it has a more drug-like profile as the stem cells are cleared from the body.
Stem cells aren't particularly new to large pharma. GlaxoSmithKline (NYSE: GSK) has a partnership with Harvard Stem Cell Institute and many companies, including Pfizer, Johnson & Johnson (NYSE: JNJ), Abbott Labs (NYSE: ABT), and sanofi-aventis (NYSE: SNY), teamed up to develop stem cells to help predict side effects.
But Pfizer seems to have taken a particular liking to stem cells, having established a unit to study them last year. If you're going to follow Pfizer's lead and invest in stem cell companies, I'd suggest you also follow its lead and keep your investments in stem cell technology to a very small fraction of your portfolio.
Geron Announces Publication of Data on Its Telomerase Inhibitor in Glioblastoma
http://finance.yahoo.com/news/Geron-Announces-Publication-bw…
Bei GRN163L o. imetelstat müsste sich doch so langsam mal ne Partnerschaft finden lassen Jetzt sind se mit anderen GRN163L Studien teilw. in P2 und da wirds doch mal Zeit. Jedes Dorfbiotech mit einem interessanten Oligo-Wirkstoff findet einen Partner, warum nicht auch Geron? 2010 gehts weiter mit Studien.
http://finance.yahoo.com/news/Geron-Announces-Publication-bw…
Bei GRN163L o. imetelstat müsste sich doch so langsam mal ne Partnerschaft finden lassen Jetzt sind se mit anderen GRN163L Studien teilw. in P2 und da wirds doch mal Zeit. Jedes Dorfbiotech mit einem interessanten Oligo-Wirkstoff findet einen Partner, warum nicht auch Geron? 2010 gehts weiter mit Studien.
hallo allerseits,nach dem sturz von 6.60 auf 5,39 schein es gestern einige shorteindeckungen gegeben zu haben,hatte zumindest keine news gefunden als ursache für den anstieg,oder weiß jemand mehr?hier waren doch sonst immer genug stammzellenkundige vertreten in der diskussion,ist aber ruhig geworden hier...
mal sehen wie morgen die zahlen ausfallen,ob der verlust verringert werden konnte...die verbrennen aber auch jeden monat mio $ das es nur so raucht.. bei verlustausweitung gibt es sicherlich den üblichen rutsch
Antwort auf Beitrag Nr.: 39.005.622 von optschraub am 24.02.10 20:04:58Um den Cashburn zu drosseln, bezahlen die Brüder ja auch sehr häufig mit Aktien. Hab ich so exzessiv bei noch keener anderen Aktie gesehen. Und Dilution wird mE weiter gehen. Spätestens bei neuen GRN163L Studien muss der Wirkstoff von Lonza und Girindus teuer sythetisiert werden. An beide wurde beim letzten Mal Aktien im Millionenbereich (Stück) ausgeschüttet.
Antwort auf Beitrag Nr.: 39.005.887 von Berliner_Landstreicher am 24.02.10 20:42:04na das hält sich ja in grenzen mit den verlusten...so schnell gewöhnen sich die investoren an das vierteljährliche debakel.
ich habe heute mal ein paar stücke ins depot gelegt.amiaktien sind bei mir angesagt...wenn die hedgefonds es schaffen den euro/dollar auf 1:1 zu bekommen verdient man dann mit...doppelt
ich habe heute mal ein paar stücke ins depot gelegt.amiaktien sind bei mir angesagt...wenn die hedgefonds es schaffen den euro/dollar auf 1:1 zu bekommen verdient man dann mit...doppelt
Antwort auf Beitrag Nr.: 39.022.581 von optschraub am 26.02.10 17:46:33Das ist aber alles soweit im Rahmen. Geron ist mit den Stammzellen und der Antisense (GRN163L) auf einem wirklich hochtechnologischen Gebiet innerhalb der Biotechnologie unterwegs. Und teuer ist es auch noch. Aber wenn alles klappt, dann rollt der Rubel. Gerade der Erfolg der Antisense bei zahlreichen Biotechs (besonders Isis, Alnylam, Prosensa, Santaris), sollte mE nicht spurlos an Geron´s GRN163L vorbei gehen. Geron braucht dringend große Konzerne als Geldgeber.
Antwort auf Beitrag Nr.: 39.022.581 von optschraub am 26.02.10 17:46:33tja ,geht der kurs über 6$ scheinen die firmen die mit aktien bezahlt wurden dann auch mal bare münze sehn zu wollen verständlich... man hat ja auch so seine kosten am laufen.
die stückzahlen nehmen auch jedes jahr zu dadurch.verfolge jetzt schon ein paar jahre die aktie und kann an einen entscheidenen durchbruch kaum noch glauben...falls es doch noch klappt hofft man natürlich vorher drin zu sein...wie ist denn so die prognose ? wieviele jahre gehen noch ins land ...
die stückzahlen nehmen auch jedes jahr zu dadurch.verfolge jetzt schon ein paar jahre die aktie und kann an einen entscheidenen durchbruch kaum noch glauben...falls es doch noch klappt hofft man natürlich vorher drin zu sein...wie ist denn so die prognose ? wieviele jahre gehen noch ins land ...
Antwort auf Beitrag Nr.: 39.005.887 von Berliner_Landstreicher am 24.02.10 20:42:04Um den Cashburn zu drosseln, bezahlen die Brüder ja auch sehr häufig mit Aktien. Hab ich so exzessiv bei noch keener anderen Aktie gesehen. Und Dilution wird mE weiter gehen. Spätestens bei neuen GRN163L Studien muss der Wirkstoff von Lonza und Girindus teuer sythetisiert werden. An beide wurde beim letzten Mal Aktien im Millionenbereich (Stück) ausgeschüttet.
This prospectus relates to the sale of up to 293,225 shares of our common stock by Girindus America, Inc., the sale of up to 259,965 shares of our common stock by ReSearch Pharmaceutical Services, Inc., the sale of up to 24,536 shares of our common stock by Prime Synthesis, Inc., and the sale of up to 93,258 shares of our common stock by Exponent, Inc. We will not receive any of the proceeds from the sale of these shares covered by this prospectus.
http://www.sec.gov/Archives/edgar/data/886744/00012067741000…
This prospectus relates to the sale of up to 293,225 shares of our common stock by Girindus America, Inc., the sale of up to 259,965 shares of our common stock by ReSearch Pharmaceutical Services, Inc., the sale of up to 24,536 shares of our common stock by Prime Synthesis, Inc., and the sale of up to 93,258 shares of our common stock by Exponent, Inc. We will not receive any of the proceeds from the sale of these shares covered by this prospectus.
http://www.sec.gov/Archives/edgar/data/886744/00012067741000…
.

.
.
RüCKENMARKVERLETZUNG
Erste Stammzelltherapie in den USA
Washington - In den USA haben Ärzte einen teilweise gelähmten Patienten mit embryonalen Stammzellen behandelt. Die Phase-I-Studie sei die weltweit erste dieser Art, teilte das Biotech-Unternehmen Geron mit. Einem Patienten mit Rückenmarkverletzung waren in einer Klinik im US-Staat Atlanta Millionen Stammzellen gespritzt worden.
Die verwendeten Zellen stammen von menschlichen Embryonen, die nach einer künstlichen Befruchtung übrig geblieben waren. Durch Veränderung wurden sie zu Vorläufern von Nervenzellen; sie sollen die geschädigten Zellen reparieren. Der Versuch diene zunächst dazu, die Sicherheit und Verträglichkeit der Methode zu prüfen, so Geron.
Die Stammzelltherapie könne innerhalb von 14 Tagen nach der Verletzung begonnen werden. Über den Ausgang der Studie wurde noch nichts bekannt. Als eine Gefahr beim Einsatz embryonaler Stammzellen sehen Experten die Entwicklung von Krebs.
dpa/APOTHEKE ADHOC, Dienstag, 12. Oktober 2010, 11:04 Uhr
Erste Stammzelltherapie in den USA
Washington - In den USA haben Ärzte einen teilweise gelähmten Patienten mit embryonalen Stammzellen behandelt. Die Phase-I-Studie sei die weltweit erste dieser Art, teilte das Biotech-Unternehmen Geron mit. Einem Patienten mit Rückenmarkverletzung waren in einer Klinik im US-Staat Atlanta Millionen Stammzellen gespritzt worden.
Die verwendeten Zellen stammen von menschlichen Embryonen, die nach einer künstlichen Befruchtung übrig geblieben waren. Durch Veränderung wurden sie zu Vorläufern von Nervenzellen; sie sollen die geschädigten Zellen reparieren. Der Versuch diene zunächst dazu, die Sicherheit und Verträglichkeit der Methode zu prüfen, so Geron.
Die Stammzelltherapie könne innerhalb von 14 Tagen nach der Verletzung begonnen werden. Über den Ausgang der Studie wurde noch nichts bekannt. Als eine Gefahr beim Einsatz embryonaler Stammzellen sehen Experten die Entwicklung von Krebs.
dpa/APOTHEKE ADHOC, Dienstag, 12. Oktober 2010, 11:04 Uhr
Noch jemand drin ?
Da soll die Tage irgendwas rauskommen von einem Patienten..
Da soll die Tage irgendwas rauskommen von einem Patienten..
bin noch dabei...
okay,
das mit dem Blog gesehen von der Dame mit TJ ?
das mit dem Blog gesehen von der Dame mit TJ ?
Antwort auf Beitrag Nr.: 41.320.702 von sven641 am 05.04.11 14:14:23???
http://mobile.washingtonpost.com/c.jsp?item=http%3a%2f%2fwww…
Jetzt sollte es mal losgehen.........ist bestätigt
Jetzt sollte es mal losgehen.........ist bestätigt
ist hier noch was los?....habe mir jetzt geron mal ins depot gelegt...
Was haltet ihr von den News? Geron will sich aus der Stammzellenforschung zurückziehen, sich von 66 Mitarbeitern trennen und sich auf die Onkologie konzentrieren?!
22:58 14Nov11 -UPDATE 1-Geron to shut down stem cell programs, shares fall
* Says to cut 66 jobs
* Says to take one-time charge of $8 mln
* Shares fall 20 percent
Nov 14 (Reuters) - Geron Corp <GERN.O> said it will stop development of its stem cell programs to focus more on its cancer drugs, sending its shares down as much as 20 percent in after-market trading.
The move will see Geron cut 66 full-time positions, or about 38 percent of its workforce and stop the development of the first U.S.-approved human embryonic stem cell trial.
The company expects to take a one-time charge of about $5 million in the fourth quarter and about $3 million in the first half of next year.
"In the current environment of capital scarcity and uncertain economic conditions, we intend to focus our resources on advancing our Phase 2 clinical trials of imetelstat and GRN1005," Chief Executive John Scarlett said.
"This would not be possible if we continue to fund the stem cell programs at the current levels."
Geron expects to end the year with cash and investments in excess of $150 million.
Shares of Menlo Park, California-based company were down 20 percent at $1.75 in extended trading. They had closed at $2.20 on Monday on Nasdaq.
* Says to cut 66 jobs
* Says to take one-time charge of $8 mln
* Shares fall 20 percent
Nov 14 (Reuters) - Geron Corp <GERN.O> said it will stop development of its stem cell programs to focus more on its cancer drugs, sending its shares down as much as 20 percent in after-market trading.
The move will see Geron cut 66 full-time positions, or about 38 percent of its workforce and stop the development of the first U.S.-approved human embryonic stem cell trial.
The company expects to take a one-time charge of about $5 million in the fourth quarter and about $3 million in the first half of next year.
"In the current environment of capital scarcity and uncertain economic conditions, we intend to focus our resources on advancing our Phase 2 clinical trials of imetelstat and GRN1005," Chief Executive John Scarlett said.
"This would not be possible if we continue to fund the stem cell programs at the current levels."
Geron expects to end the year with cash and investments in excess of $150 million.
Shares of Menlo Park, California-based company were down 20 percent at $1.75 in extended trading. They had closed at $2.20 on Monday on Nasdaq.
Antwort auf Beitrag Nr.: 42.351.241 von Sugar2000 am 15.11.11 09:20:32 sehr schade - was das bedeutet - aus den Infos kann man viel reininterpretieren. Für den Kurs heute runter...
sehr schade - was das bedeutet - aus den Infos kann man viel reininterpretieren. Für den Kurs heute runter...
Mittelfristige Chance - wenn ein Partner mit ins Boot kommt.
Positiv wirtschaftlich betrachtet - wenn die cancer drugs mehr Chancen haben, warum nicht Geld sparen und sich umorientieren. Für die Sharholder hätte man diesen Weg aber auch schöner verpacken können.
 sehr schade - was das bedeutet - aus den Infos kann man viel reininterpretieren. Für den Kurs heute runter...
sehr schade - was das bedeutet - aus den Infos kann man viel reininterpretieren. Für den Kurs heute runter... Mittelfristige Chance - wenn ein Partner mit ins Boot kommt.
Positiv wirtschaftlich betrachtet - wenn die cancer drugs mehr Chancen haben, warum nicht Geld sparen und sich umorientieren. Für die Sharholder hätte man diesen Weg aber auch schöner verpacken können.
Kurz vor Handelsschluß 1.6 Mio. Stücke gehandelt.
Tagensvolumen fast 7x höher als 3 Mnt. Durchschnitt.
Any idea why ?
 ##
##
Tagensvolumen fast 7x höher als 3 Mnt. Durchschnitt.
Any idea why ?
 ##
##
allgemeine empfehlung von biotecs in usa!!
 Bin nun nach etlichen Jahren wieder eingestiegen
Bin nun nach etlichen Jahren wieder eingestiegenDer chart sieht ja nicht schlecht aus
Könnte bis 5 Dollar gehem
Antwort auf Beitrag Nr.: 43.580.998 von Lotschka am 07.09.12 19:16:48erstaml mit 2500 Aktien heute eingestiegen
am 11.9 Rodman and Renshaw Global healthcare confrence
Geron Presents on September 11th at 9:35 am EST.
Vielleicht hilfts
am 11.9 Rodman and Renshaw Global healthcare confrence
Geron Presents on September 11th at 9:35 am EST.
Vielleicht hilfts

waren schon mit 10 000 Stück bei Kursen von über 3 Euro eingestiegen kaufen jetz noch dazu !!
Antwort auf Beitrag Nr.: 43.586.395 von Nicklaussohn am 10.09.12 14:30:58rummms.... -50% vorbörslich!
Phase 2 zurückgezogen!
Phase 2 zurückgezogen!
 Bin wieder raus ! Tolles timing mal eben 3000 Euro an nur einem Handelstag in den Klo gespült
Bin wieder raus ! Tolles timing mal eben 3000 Euro an nur einem Handelstag in den Klo gespült
Die kommt wieder, locker bleiben
Die Firma wird weiter arbeiten und früher oder später die Phase 2
erreichen, bleibt locker und nutzt die billigen EinkUfskurse
Börse kann so einfach in manchen Fällen sein
erreichen, bleibt locker und nutzt die billigen EinkUfskurse
Börse kann so einfach in manchen Fällen sein
Antwort auf Beitrag Nr.: 43.587.098 von Lotschka am 10.09.12 17:17:24Ja Mist - So schnell kanns gehen bei den Bios.
A Phase II casualty
There's a good reason why many biotech investors only focus on a company once its drugs have moved into Phase III clinical trials. The Phase II testing, which greatly expands the size of a drug trial from the smaller samples of Phase I, can really trip a company up. Often, a drug that looks promising in a small controlled Phase I setting shows much weaker results as the trial is expanded to a much bigger population of patients.
That was the hard lesson learned by investors in Geron today, which is seeing its shares lose more than half their value after Imetelstat, which targets the growth of telomerase, an enzyme found in many cancer cells, showed little promise in Phase II trials. The company will now focus its efforts solely on GRN1005, which is used for hard-to-treat brain tumors. Although Geron still has more than $100 million in the bank, that money will likely dwindle in coming quarters as GRN1005 progresses through Phase II trials. The only hope for a rebound hinges on GRN1005 showing great data and moving onto Phase III. For the rest of 2012, at least, this stock is likely dead money, and could drift lower still as cash levels dwindle.
Read more: http://www.investopedia.com/stock-analysis/StreetAuthority/B…
 ##
##
A Phase II casualty
There's a good reason why many biotech investors only focus on a company once its drugs have moved into Phase III clinical trials. The Phase II testing, which greatly expands the size of a drug trial from the smaller samples of Phase I, can really trip a company up. Often, a drug that looks promising in a small controlled Phase I setting shows much weaker results as the trial is expanded to a much bigger population of patients.
That was the hard lesson learned by investors in Geron today, which is seeing its shares lose more than half their value after Imetelstat, which targets the growth of telomerase, an enzyme found in many cancer cells, showed little promise in Phase II trials. The company will now focus its efforts solely on GRN1005, which is used for hard-to-treat brain tumors. Although Geron still has more than $100 million in the bank, that money will likely dwindle in coming quarters as GRN1005 progresses through Phase II trials. The only hope for a rebound hinges on GRN1005 showing great data and moving onto Phase III. For the rest of 2012, at least, this stock is likely dead money, and could drift lower still as cash levels dwindle.
Read more: http://www.investopedia.com/stock-analysis/StreetAuthority/B…
 ##
##
Antwort auf Beitrag Nr.: 43.588.003 von zwitscherton am 10.09.12 21:30:55Das heißt heute eben Ziel verfehlt und es wird weiter gearbeitet...
Kaufen wenn die Kanonen donnern, ich hoffe morgen gibt es welche unter dem €

Kaufen wenn die Kanonen donnern, ich hoffe morgen gibt es welche unter dem €

Ja das ist schon ein harter Schlag. Gleich die Hauptschlagader getroffen.
Wer vieeel Geduld hat soll jetzt rein.
Wer vieeel Geduld hat soll jetzt rein.
Antwort auf Beitrag Nr.: 43.588.073 von lunatics am 10.09.12 21:49:45Jetzt würde ich noch nicht rein, denn die Kapitalreserven werden
erstmal schmolzen und dann auch der Aktienkurs.....
Aber ich geb dir recht, es sind klare Kaufkurse im kommen,
allerdings nur wenn man an ein Überleben der Firma glaubt.
Aktuell ist das hier jetzt eine reine Zockeraktie, nicht mehr und
nicht weniger, leider....
erstmal schmolzen und dann auch der Aktienkurs.....
Aber ich geb dir recht, es sind klare Kaufkurse im kommen,
allerdings nur wenn man an ein Überleben der Firma glaubt.
Aktuell ist das hier jetzt eine reine Zockeraktie, nicht mehr und
nicht weniger, leider....
Antwort auf Beitrag Nr.: 43.588.017 von Wohnwunsch am 10.09.12 21:34:43Es bleibt nur noch GRN1005.
Die nächsten Ergebnisse hierzu werden Ende 2012 erwartet.
Bis dahin ist Geron is supposed to be Dead Money.
KA warum man jetzt noch so optimistisch sein kann.
 ##
##
Die nächsten Ergebnisse hierzu werden Ende 2012 erwartet.
Bis dahin ist Geron is supposed to be Dead Money.
KA warum man jetzt noch so optimistisch sein kann.
 ##
##
Antwort auf Beitrag Nr.: 43.588.134 von zwitscherton am 10.09.12 22:02:48Aus dem Ami-Board
I Smell A Rat
By mruyog . 4 hours ago . Permalink
The management decides to divest its hESC portfolio just last Fall giving us shareholders upbeat hopes for Imetelstat/GRN1005 and accelerating the Imetelstat trial while stopping the OPC1 trial, then they (deliberately?) loose the Viacyte case, then just 10 days ago (on Aug 30, 2012) none other than Stifel Nicolous comes out with a BUY recommendation (didn't they know the iffy nature of the Oncology trials?), and finally, if you look at carefully, just last Friday during the last 15 minutes or so of trading, the rapidly rising share price heading to cross $3.00 suddenly stalls on large-volume(sale?) trades dragging it down from $3.99 to below $3.90!! This is all now seems fishy to me and makes it worth investigated for fraud by the SEC.
http://finance.yahoo.com/mbview/threadview/?&bn=15bb63b2-892…
Wenn da nicht noch ne Klage hinterher kommt.
 ##
##
I Smell A Rat
By mruyog . 4 hours ago . Permalink
The management decides to divest its hESC portfolio just last Fall giving us shareholders upbeat hopes for Imetelstat/GRN1005 and accelerating the Imetelstat trial while stopping the OPC1 trial, then they (deliberately?) loose the Viacyte case, then just 10 days ago (on Aug 30, 2012) none other than Stifel Nicolous comes out with a BUY recommendation (didn't they know the iffy nature of the Oncology trials?), and finally, if you look at carefully, just last Friday during the last 15 minutes or so of trading, the rapidly rising share price heading to cross $3.00 suddenly stalls on large-volume(sale?) trades dragging it down from $3.99 to below $3.90!! This is all now seems fishy to me and makes it worth investigated for fraud by the SEC.
http://finance.yahoo.com/mbview/threadview/?&bn=15bb63b2-892…
Wenn da nicht noch ne Klage hinterher kommt.
 ##
##
Hi @all 
Geron ein Wert mit Zukunft ?
http://www.reuters.com/article/2013/11/07/geron-study-cancer…
http://www.finanznachrichten.de/nachrichten-aktien/geron-cor…


Geron ein Wert mit Zukunft ?
http://www.reuters.com/article/2013/11/07/geron-study-cancer…
http://www.finanznachrichten.de/nachrichten-aktien/geron-cor…
Antwort auf Beitrag Nr.: 45.787.208 von lunatics am 07.11.13 20:39:58
Jepp , die Nachrichten sprechen für sich...
Nach Börsenschluss...
Menlo Park, Calif., November 1, 2013 - Geron Corporation (Nasdaq: GERN) will announce its financial results for the third quarter ended September 30, 2013, on Thursday, November 7, 2013, after the market close. Geron's management will also host a conference call for analysts and investors on Thursday, November 7, 2013, at 4:30 p.m. Eastern Time to discuss the company's third quarter results and recent events.
http://de.advfn.com/p.php?pid=nmona&article=59845608
Jepp , die Nachrichten sprechen für sich...

Nach Börsenschluss...
Menlo Park, Calif., November 1, 2013 - Geron Corporation (Nasdaq: GERN) will announce its financial results for the third quarter ended September 30, 2013, on Thursday, November 7, 2013, after the market close. Geron's management will also host a conference call for analysts and investors on Thursday, November 7, 2013, at 4:30 p.m. Eastern Time to discuss the company's third quarter results and recent events.
http://de.advfn.com/p.php?pid=nmona&article=59845608
Auf so eine Nachricht musste man bei GERN lange warten. Ein steiniger Weg aber schlussendlich der richtige.
Oh ist noch jemand mit dabei... Aber so tief wie heute sind wir schon lange nicht mehr gefallen... ;-)
...und weil es soo schön ist:
Today's Dead Cat Bounce Stock Is Geron
http://www.thestreet.com/story/12099765/1/todays-dead-cat-bo…
Today's Dead Cat Bounce Stock Is Geron
http://www.thestreet.com/story/12099765/1/todays-dead-cat-bo…
Ich bin auch noch dabei...
Hi @all 
Late Thursday, MLV Equity raised its price target on GERN to $8 from $6.50 and backed its "buy" rating. However, the stock is down 13% at $4.53 today as traders respond to the latest quarterly earnings report from Geron Corporation (NASDAQ:GERN). Despite this steep drop, GERN continues to trade above the $4.50 level -- a region that had served as resistance in recent weeks, until some positive trial data sent the shares gapping above it on Thursday.
http://www.schaeffersresearch.com/commentary/content/blogs/a…
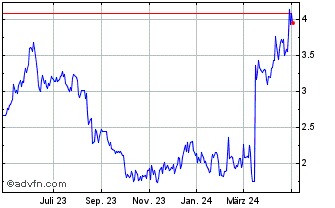
Hmmm , wenn man sich den Chart ab September 13 anguckt...
Fällt auf , nach jedem UP folgt ein kleiner Rücksetzer

Late Thursday, MLV Equity raised its price target on GERN to $8 from $6.50 and backed its "buy" rating. However, the stock is down 13% at $4.53 today as traders respond to the latest quarterly earnings report from Geron Corporation (NASDAQ:GERN). Despite this steep drop, GERN continues to trade above the $4.50 level -- a region that had served as resistance in recent weeks, until some positive trial data sent the shares gapping above it on Thursday.
http://www.schaeffersresearch.com/commentary/content/blogs/a…
Hmmm , wenn man sich den Chart ab September 13 anguckt...
Fällt auf , nach jedem UP folgt ein kleiner Rücksetzer

Schönen Sonntag @all 
Equities researchers at MLV Capital lifted their price objective on shares of Geron Corp. (NASDAQ:GERN) from $6.50 to $8.00 in a research report issued on Friday, StockRatingsNetwork reports. The firm currently has a “buy” rating on the stock. MLV Capital’s price target indicates a potential upside of 73.72% from the company’s current price.
http://www.i3investor.com/servlets/fdnews/164922.jsp

Equities researchers at MLV Capital lifted their price objective on shares of Geron Corp. (NASDAQ:GERN) from $6.50 to $8.00 in a research report issued on Friday, StockRatingsNetwork reports. The firm currently has a “buy” rating on the stock. MLV Capital’s price target indicates a potential upside of 73.72% from the company’s current price.
http://www.i3investor.com/servlets/fdnews/164922.jsp
Bis 9.12.13 ist warten angesagt...
Ist ja bald
Geron lost 12% of its value, although the move only gave back a portion of the stock's 45% jump yesterday. As Fool biotech expert Brian Orelli noted earlier today, investors had hoped to learn more about the study results about its imetelstat myelofibrosis treatment that led to yesterday's big gains, but CEO John Scarlett instead cited a nondisclosure embargo in advance of the conference next month at which the results will be presented. Investors will likely have to wait until the December 9 presentation to get all the details, and that apparently was too long to expect some traders to be with the highly volatile stock.
http://www.fool.com/investing/general/2013/11/08/why-rocket-…
Ist ja bald

Geron lost 12% of its value, although the move only gave back a portion of the stock's 45% jump yesterday. As Fool biotech expert Brian Orelli noted earlier today, investors had hoped to learn more about the study results about its imetelstat myelofibrosis treatment that led to yesterday's big gains, but CEO John Scarlett instead cited a nondisclosure embargo in advance of the conference next month at which the results will be presented. Investors will likely have to wait until the December 9 presentation to get all the details, and that apparently was too long to expect some traders to be with the highly volatile stock.
http://www.fool.com/investing/general/2013/11/08/why-rocket-…
GERN wird nun profitabel mit guten Produkten. Jetzt hat das Warten ein Ende
Guten Abend 
Jepp, GERN ein Wert mit Zukunft

Jepp, GERN ein Wert mit Zukunft

Guten Abend 
Zur Info...
Geron Corporation (NASDAQ:GERN) gained 1.12% recently, while trading on 838,550 shares at the price of $5.42. If we look at its trading history of the past 52 weeks, the share price suffered a low of $0.91 and was moved to its maximum level of $7.79.The stock changed hands in a range of $5.20 to $5.42, bringing its market capitalization at about $699.00 million. Geron Corporation (Geron) is a clinical-stage biopharmaceutical company developing a first-in-class telomerase inhibitor, imetelstat, in hematologic myeloid malignancies. Telomerase is an enzyme that enables cancer cells to maintain telomere length, which provides them with the capacity for limitless cellular replication. Imetelstat is a specific inhibitor of telomerase.
http://www.sbwire.com/press-releases/bullish-runners-geron-c…

Zur Info...
Geron Corporation (NASDAQ:GERN) gained 1.12% recently, while trading on 838,550 shares at the price of $5.42. If we look at its trading history of the past 52 weeks, the share price suffered a low of $0.91 and was moved to its maximum level of $7.79.The stock changed hands in a range of $5.20 to $5.42, bringing its market capitalization at about $699.00 million. Geron Corporation (Geron) is a clinical-stage biopharmaceutical company developing a first-in-class telomerase inhibitor, imetelstat, in hematologic myeloid malignancies. Telomerase is an enzyme that enables cancer cells to maintain telomere length, which provides them with the capacity for limitless cellular replication. Imetelstat is a specific inhibitor of telomerase.
http://www.sbwire.com/press-releases/bullish-runners-geron-c…
Hi @all 
Die nächsten Events...
Dec 9, 2013
American Society of Hematology (ASH) Annual Meeting - 5:45PM EST - Add to calendar
Dec 4, 2013
Geron at Piper Jaffray Healthcare Conference - 12:30PM EST - Add to calendar
http://www.google.com/finance?q=NASDAQ%3AGERN&ei=xUaWUqixB6z…

Die nächsten Events...
Dec 9, 2013
American Society of Hematology (ASH) Annual Meeting - 5:45PM EST - Add to calendar
Dec 4, 2013
Geron at Piper Jaffray Healthcare Conference - 12:30PM EST - Add to calendar
http://www.google.com/finance?q=NASDAQ%3AGERN&ei=xUaWUqixB6z…
Nur weiter so. Wird noch viel Spass machen.
Antwort auf Beitrag Nr.: 45.989.486 von lunatics am 05.12.13 19:40:15
Ja, das denke ich auch
Im Moment sind die 6 Dollar ,
noch eine harte Nuss !
Ja, das denke ich auch

Im Moment sind die 6 Dollar ,
noch eine harte Nuss !
Geron Corporation(NASDAQ:GERN) percentage change surged +4.74% to close at $5.74 with the total traded volume of 3.33 million shares, and average volume of 5.93 million. The 52 week range of the stock remained $0.91 - $7.79, while its day lowest price was $5.35 and it hit its day highest price at $5.78. Geron Corporation is a clinical stage biopharmaceutical company developing a first-in-class telomerase inhibitor, imetelstat, in hematologic myeloid malignancies. The company was founded in 1990 and is based in Menlo Park, California.
http://www.sbwire.com/press-releases/news-recap-newmont-mini…
http://www.sbwire.com/press-releases/news-recap-newmont-mini…
Geron Corporation (GERN) today announced that management will be hosting a live webcast of an analyst and investor meeting at 6:30 p.m. CT on December 9
was ist denn der Grund für die heutige Achterbahnfahrt?
Geron ist gerne volatil 
Vielleicht schließen die Amis auch das
Eröffnungsgap ?
Dann kann es ja wieder up gehen

Vielleicht schließen die Amis auch das
Eröffnungsgap ?
Dann kann es ja wieder up gehen

begrüsse spät aber doch hab mi was zu 5,98 ins depot gelegt!!!
Noch interessant:
Geron's Game-Changing Myelofibrosis Drug Story Has a Familiar Feel
http://www.thestreet.com/story/12148234/1/gerons-game-changi…
Geron's Game-Changing Myelofibrosis Drug Story Has a Familiar Feel
http://www.thestreet.com/story/12148234/1/gerons-game-changi…
Hmmm , mal wieder Achterbahn fahren !

Hi @all 
3 Reasons Behind Geron's Rebound
http://www.fool.com/investing/general/2013/12/12/3-reasons-b…

3 Reasons Behind Geron's Rebound
http://www.fool.com/investing/general/2013/12/12/3-reasons-b…
Geron wird ja mal wieder massiv ausgeschlachtet. Schade nach den letzten positiven Chartsignalen.
Hi @all 
Mit Geron kommt keine Langeweile auf

Mit Geron kommt keine Langeweile auf

Das Auf und Ab. es wird mir schlecht.
Bist du noch drinn?
Bist du noch drinn?
heute keine Kommentare ???
Kahn Swick & Foti, LLC Investigates Geron Corporation Following FDA Clinical Hold of Blood Medicine and Analyst Downgrade
Nachrichtenquelle: Business Wire (engl.)
| 13.03.2014, 03:00 | 202 Aufrufe | 0 | druckversion
Former Attorney General of Louisiana, Charles C. Foti, Jr., Esq., a partner at the law firm of Kahn Swick & Foti, LLC (“KSF”), announces that KSF has commenced an investigation into Geron Corporation (Nasdaq: GERN).
On March 12, 2014, Geron announced that the Company has received verbal notice from the U.S. Food and Drug Administration (“FDA”) that its investigational new drug application for its only experimental drug, imetelstat for blood disorders, has been placed on full clinical hold, affecting its mid-stage trials of imetelstat because of low-grade liver function test abnormalities. The FDA expressed concern about whether these LFT abnormalities are reversible.
On this news, Geron was downgraded by MLV & Co, and the price of its shares plummeted by over 61%.
KSF’s investigation is focusing on whether Geron and/or its officers and directors violated state or federal securities laws.
If you have information that would assist KSF in its investigation, or would like to discuss your legal rights, you may, without obligation or cost to you, e-mail or call KSF Managing Partner Lewis Kahn (lewis.kahn@ksfcounsel.com) or KSF Partner Melinda Nicholson (melinda.nicholson@ksfcounsel.com) toll free at 1-877-515-1850.
About Kahn Swick & Foti, LLC
KSF, whose partners include the Former Louisiana Attorney General Charles C. Foti, Jr., is a law firm focused on securities class action and shareholder derivative litigation with offices in New York and Louisiana. KSF's lawyers have significant experience litigating complex securities class actions nationwide on behalf of both institutional and individual shareholders.
To learn more about KSF, you may visit www.ksfcounsel.com.
Nachrichtenquelle: Business Wire (engl.)
| 13.03.2014, 03:00 | 202 Aufrufe | 0 | druckversion
Former Attorney General of Louisiana, Charles C. Foti, Jr., Esq., a partner at the law firm of Kahn Swick & Foti, LLC (“KSF”), announces that KSF has commenced an investigation into Geron Corporation (Nasdaq: GERN).
On March 12, 2014, Geron announced that the Company has received verbal notice from the U.S. Food and Drug Administration (“FDA”) that its investigational new drug application for its only experimental drug, imetelstat for blood disorders, has been placed on full clinical hold, affecting its mid-stage trials of imetelstat because of low-grade liver function test abnormalities. The FDA expressed concern about whether these LFT abnormalities are reversible.
On this news, Geron was downgraded by MLV & Co, and the price of its shares plummeted by over 61%.
KSF’s investigation is focusing on whether Geron and/or its officers and directors violated state or federal securities laws.
If you have information that would assist KSF in its investigation, or would like to discuss your legal rights, you may, without obligation or cost to you, e-mail or call KSF Managing Partner Lewis Kahn (lewis.kahn@ksfcounsel.com) or KSF Partner Melinda Nicholson (melinda.nicholson@ksfcounsel.com) toll free at 1-877-515-1850.
About Kahn Swick & Foti, LLC
KSF, whose partners include the Former Louisiana Attorney General Charles C. Foti, Jr., is a law firm focused on securities class action and shareholder derivative litigation with offices in New York and Louisiana. KSF's lawyers have significant experience litigating complex securities class actions nationwide on behalf of both institutional and individual shareholders.
To learn more about KSF, you may visit www.ksfcounsel.com.
Hier ist die Aussicht einer Entwicklung wie bei Ariad mit Wiederzulassung wohl nicht möglich. Ist ein Studienabbruch. Der Kurs wird in USA heute wohl noch einmal 30-50% nachgeben.
Ich würde hier nicht ins fallende Messer greifen wollen.
Allen Investierten wünsche ich, dass meine Einschätzung nicht zutrifft.
Ich würde hier nicht ins fallende Messer greifen wollen.
Allen Investierten wünsche ich, dass meine Einschätzung nicht zutrifft.
nicht ins fallende Messer greifen wollen, ne klar, und so den Anstieg um 30% verpassen, sch....
Antwort auf Beitrag Nr.: 46.653.157 von dottore am 18.03.14 18:05:3930 % ist zu wenig....
News... wer am 28.5 die Aktie hält erhält die Ausschüttung der Aktien von Asterias Biotherapeuthics
Antwort auf Beitrag Nr.: 46.954.418 von Schablonski am 09.05.14 18:21:14der Link dazu
http://finance.yahoo.com/news/geron-announces-record-date-di…


http://finance.yahoo.com/news/geron-announces-record-date-di…


Und was soll das Heissen ?? werden die übernommen und man bekommt von dem unternhemen aktien ??
Es kommt, wie es kommen musste: Heute +30% 

Antwort auf Beitrag Nr.: 46.954.424 von Schablonski am 09.05.14 18:22:22
Asterias Bio Aktien wurden bei mir heute eingebucht
Zitat von Schablonski: der Link dazu
http://finance.yahoo.com/news/geron-announces-record-date-di…
Asterias Bio Aktien wurden bei mir heute eingebucht
noch jemand dabei? 





GERON CORP UP 44.2 PCT IN PREMARKET; LICENSED CANCER COMPOUND TO JOHNSON & JOHNSON UNIT FOR UP TO $935 MLN GERN.O - RTRS
GERON SELLS LAST DRUG IN PIPELINE TO J&J UNIT GERN.O JNJ.N - RTRS
14-Nov-2014 00:27
Nov 13 (Reuters) - Geron Corp GERN.O licensed its cancer compound, the last in its pipeline, to a unit of Johnson & Johnson JNJ.N for up to $935 million, sending its shares up as much as 33 percent in extended trading.
The license deal comes as a welcome break to the company, which has seen its stock price drop from a high of $71.69 in 2000 to $2.31 on Thursday.
The drug developer will receive $35 million in upfront payment and the rest in milestone payments. (Full Story)
Under the deal, J&J's unit Janssen Biotech Inc, will be responsible for the development, regulatory approval and sales of the cancer compound, imetelstat, worldwide. Geron will receive royalties on net sales.
If successful, imetelstat would compete with Incyte Corp's INCY.O myelofibrosis drug, Jakafi, which generated sales of $235.4 million last year.
Some analysts have indicated that imetelstat's ability to evoke a disease-modifying effect - defined as partial or complete remission - suggests it would be superior to Jakafi.
Geron did not disclose plans for its pipeline. The company could not be reached immediately for additional comments.
The deal includes a clause for Janssen to terminate the agreement at any time due to a safety-related concern, according to a filing. (http://1.usa.gov/1zRPRsJ)
The Menlo Park, California-based company came under pressure in March after the U.S. Food and Drug Administration placed a hold on Geron's studies of the drug in blood cancers, citing possible liver damage. (Full Story)
Once heralded as a pioneer in stem-cell technology, Geron focused its research and development on imetelstat in blood cancers from December 2012 when it stopped development of its brain cancer drug and cut about 40 percent of its workforce.
The company had to abandon its research in human embryonic stem cells in November 2011 when political and general sentiment were against such testing, a move that left the company with two cancer compounds and a portfolio of stem cell therapies.
In October last year, the company completed the sale of its stem cell assets to BioTime.
Geron's shares have fallen 67 percent since it sold its stem cell assets.
14-Nov-2014 00:27
Nov 13 (Reuters) - Geron Corp GERN.O licensed its cancer compound, the last in its pipeline, to a unit of Johnson & Johnson JNJ.N for up to $935 million, sending its shares up as much as 33 percent in extended trading.
The license deal comes as a welcome break to the company, which has seen its stock price drop from a high of $71.69 in 2000 to $2.31 on Thursday.
The drug developer will receive $35 million in upfront payment and the rest in milestone payments. (Full Story)
Under the deal, J&J's unit Janssen Biotech Inc, will be responsible for the development, regulatory approval and sales of the cancer compound, imetelstat, worldwide. Geron will receive royalties on net sales.
If successful, imetelstat would compete with Incyte Corp's INCY.O myelofibrosis drug, Jakafi, which generated sales of $235.4 million last year.
Some analysts have indicated that imetelstat's ability to evoke a disease-modifying effect - defined as partial or complete remission - suggests it would be superior to Jakafi.
Geron did not disclose plans for its pipeline. The company could not be reached immediately for additional comments.
The deal includes a clause for Janssen to terminate the agreement at any time due to a safety-related concern, according to a filing. (http://1.usa.gov/1zRPRsJ)
The Menlo Park, California-based company came under pressure in March after the U.S. Food and Drug Administration placed a hold on Geron's studies of the drug in blood cancers, citing possible liver damage. (Full Story)
Once heralded as a pioneer in stem-cell technology, Geron focused its research and development on imetelstat in blood cancers from December 2012 when it stopped development of its brain cancer drug and cut about 40 percent of its workforce.
The company had to abandon its research in human embryonic stem cells in November 2011 when political and general sentiment were against such testing, a move that left the company with two cancer compounds and a portfolio of stem cell therapies.
In October last year, the company completed the sale of its stem cell assets to BioTime.
Geron's shares have fallen 67 percent since it sold its stem cell assets.
Nicht schlecht erstes Ziel 3,50 Dollar und dann wie damals, es sah noch nie so gut aus.
Das ging schnell mit den 3,50 hätte ich nicht gedacht, warum aber hier in Deutschland kaum einer zugreift verstehe ich nicht aber egal bei 4,51 Euro ist erst die nächste Hürde mal schauen.
Geiles Teil auf jeden
Geiles Teil auf jeden

Mal wieder eine Aktie die hier fast keiner kennt.
Wann bekommen die denn weitere Zahlungen von J&J und was haben die jetzt mit dem Geld vor wenns das letzte MED in der Pipeline war?
Und sie steigt und steigt. Seit 1,2 auf der Watchlist aber leider nicht reingegangen, war mir zu undurchsichtig.
Könnte was dran sein. Kenn mich leider ind iesem Segment nicht aus !! Aber ein paar hundert € könnte man durchaus riskieren.... hmmmh, mal sehn. Gruß B.
hmmh steht fast wieder da, wo sie vor einem Jahr stand !!! Einstieg, vor allem wegen Phase 2/3 Jonson.... ?? Gruß B.
Ja, weiter abwärts, vielleicht knallen sie sie auf unter 1 €, dann bin ich dabei ! Gruß B.
Lohnt ein Einstieg,Risiko und Chance bei Geron
Infos: Geron.com
http://imetelchat.imetelstat.eu/viewforum.php?f=1 gute infos
http://finance.yahoo.com/quote/GERN/community?ltr=1 natürlich viel Amimüll dabei...
immerhin wird imetelstat an einer Klinik in Leipzig getestet...unter Jansen.+.JNJ Ph 2
http://imetelchat.imetelstat.eu/viewforum.php?f=1 gute infos
http://finance.yahoo.com/quote/GERN/community?ltr=1 natürlich viel Amimüll dabei...
immerhin wird imetelstat an einer Klinik in Leipzig getestet...unter Jansen.+.JNJ Ph 2
Antwort auf Beitrag Nr.: 53.669.190 von optschraub am 10.11.16 22:29:47
Diese Frage kann man sich immer bei Aktien stellen?
Bei Biotechs besteht aber immer ein hohes Risiko sofern sie nicht zu den Big Playern gehören.
Sollte die nächste Studie mit niedrigere Dosierung positiv verlaufen, dann sehen wir recht schnell die 4-5 $. Im Umkehrschluss auch ein Absturz in Cent-Bereich, denn dann heißt es Game-over.
Der Vorstand von Geron ist aber optimistisch das die aktuelle Studie erfplgreich sein wird. Dann dürfte Geron ein Übernahmekandidat sein.
Zitat von optschraub: Lohnt ein Einstieg,Risiko und Chance bei Geron
Diese Frage kann man sich immer bei Aktien stellen?
Bei Biotechs besteht aber immer ein hohes Risiko sofern sie nicht zu den Big Playern gehören.
Sollte die nächste Studie mit niedrigere Dosierung positiv verlaufen, dann sehen wir recht schnell die 4-5 $. Im Umkehrschluss auch ein Absturz in Cent-Bereich, denn dann heißt es Game-over.
Der Vorstand von Geron ist aber optimistisch das die aktuelle Studie erfplgreich sein wird. Dann dürfte Geron ein Übernahmekandidat sein.
Antwort auf Beitrag Nr.: 54.028.867 von Eulenfoerster am 06.01.17 23:12:11wer sollte denn Geron übernehmen wollen?



Antwort auf Beitrag Nr.: 54.130.232 von sharepicker321 am 20.01.17 22:17:19wenn dann jnj warscheinlich,die wissen ja auch ob die Droge funktioniert...aber nicht vor Beginn P3
im Sommer..falls sie denn kommt.5-6$ wären drin.Haben gerade zu dem Zeitpunkt viele Shortseller
leerverkauft kann es auch höher gehen,aber die werden in den nächsten Monaten vorsichtiger werden.Blackrock hat dick aufgestockt heute auf 7.5%. Da könnte ja auch so manch Zocker mit Insiderinfos sitzen.Das Risiko mit Totalverlust ist ziemlich hoch bei Geron. Oder JnJ kaufen die würden wenig fallen falls die Tests eigestellt werden...haben ja noch mehr heiße Eisen in ihrer Pipeline.
im Sommer..falls sie denn kommt.5-6$ wären drin.Haben gerade zu dem Zeitpunkt viele Shortseller
leerverkauft kann es auch höher gehen,aber die werden in den nächsten Monaten vorsichtiger werden.Blackrock hat dick aufgestockt heute auf 7.5%. Da könnte ja auch so manch Zocker mit Insiderinfos sitzen.Das Risiko mit Totalverlust ist ziemlich hoch bei Geron. Oder JnJ kaufen die würden wenig fallen falls die Tests eigestellt werden...haben ja noch mehr heiße Eisen in ihrer Pipeline.
Antwort auf Beitrag Nr.: 54.130.232 von sharepicker321 am 20.01.17 22:17:19
Warum sollte Jansen 900 Mio. an Lizenzzahlungen an Geron abdrücken, wenn man sie für 700-800 Mio. kaufen könnte ?

Zitat von sharepicker321: wer sollte denn Geron übernehmen wollen?
Warum sollte Jansen 900 Mio. an Lizenzzahlungen an Geron abdrücken, wenn man sie für 700-800 Mio. kaufen könnte ?


Antwort auf Beitrag Nr.: 54.179.975 von Eulenfoerster am 27.01.17 13:23:10Neuer Player im Spiel... will seine Droge mi imet kombinieren.. AML ...schon kommt Phantasie auf...
Institute stocken weiter auf... mal sehen ob diese endlose Geschichte auch mal endet.
bin dabei
Institute stocken weiter auf... mal sehen ob diese endlose Geschichte auch mal endet.
bin dabei
Antwort auf Beitrag Nr.: 54.320.710 von optschraub am 14.02.17 21:30:12Bei Geron steckte schon immer Phantasie dahinter.
Jetzige Kurse waren immer Kaufkurse. Denke es kann sehr schnell Richtung 3€ gehen.
Wenn die neuen Studien Erfolg versprechen wie bereits angetönt, dann sind 6-7€ locker drin.
Jetzige Kurse waren immer Kaufkurse. Denke es kann sehr schnell Richtung 3€ gehen.
Wenn die neuen Studien Erfolg versprechen wie bereits angetönt, dann sind 6-7€ locker drin.
2. M&As (vor allem im Pharma-Sektor) und Partnerschaften Wir können davon ausgehen, dass Johnson & Johnson sich weiterhin auf Fusionen und Übernahmen (M&A) verlassen wird, um die Ausweitung seiner Pipeline und seines Produktportfolios voranzutreiben – insbesondere im schnell wachsenden Pharma-Sektor. Ende vergangenen Monats hat J&J verkündet, dass es den Schweizer Medikamentenhersteller Actelion (WKN:936767) für 30 Mrd. US-Dollar übernehmen wird, um sich die Rechte an Opsumit und Uptravi – zwei Medikamente zur Behandlung von pulmonal-arteriellem Lungenhochdruck – zu sichern. Beide Medikamente haben Schätzungen zufolge das Potenzial, jährlich bis zu 2 Mrd. US-Dollar umzusetzen. J&J hat mitgeteilt, dass der Deal die langfristige Wachstumsrate des Unternehmens um 1,5 – 2 % steigern soll. Zusätzlich erhält J&J eine Beteiligung von 16 % an Actelions Pipeline, die vor Abschluss des Deals in ein eigenes Unternehmen ausgegliedert wird. J&J ist eigentlich nicht dafür bekannt, große Übernahmen zu tätigen. In der Regel akquiriert es Early- und Mid-Stage-Beteiligungen und entwickelt diese dann weiter. Außerdem ist J&J gerade fleißig dabei, Partnerschaften abzuschließen. Seine Partnerschaft mit Geron (WKN:902213) zur Entwicklung von Imetelstat, einem Medikament zur Behandlung von myelodysplastischen Syndromen ist Teil der oben genannten 10 Blockbuster-Produkte, die J&J noch in diesem Jahrzehnt auf den Markt bringen möchte. In frühen Testphasen – noch bevor J&J eine Vorauszahlung von 30 Mrd. US-Dollar geleistet hat und zu welcher möglicherweise 900 Mio. US-Dollar als Meilensteinzahlungen hinzukommen – hat Geron verkündet, dass Imetelstat Myelofibrose-Patienten vollständig oder teilweise geheilt hat. Bisher hat dies noch kein anderes Medikament in klinischen Studien geschafft. In anderen Worten: J&J hat genug Optionen, seinen Cashflow zur Steigerung seiner Wachstumsraten einzusetzen.
Kein Scherz: Johnson & Johnson könnte im kommenden Jahrzehnt seinen Umsatz jährlich um mindestens 5 % steigern | wallstreet-online.de - Vollständiger Artikel unter:
http://www.wallstreet-online.de/nachricht/9329086-scherz-joh…

Kein Scherz: Johnson & Johnson könnte im kommenden Jahrzehnt seinen Umsatz jährlich um mindestens 5 % steigern | wallstreet-online.de - Vollständiger Artikel unter:
http://www.wallstreet-online.de/nachricht/9329086-scherz-joh…

Geron Announces Presentation at American Association for Cancer Research Annual Meeting
March 02, 2017 07:30 ET | Source: Geron Corporation
MENLO PARK, Calif., March 02, 2017 (GLOBE NEWSWIRE) -- Geron Corporation (Nasdaq:GERN) today announced an abstract submitted by Janssen Research & Development, LLC describing non-clinical data[/u] on imetelstat has been accepted for presentation as a poster at the 2017 American Association for Cancer Research (AACR) Annual Meeting to be held in Washington, D.C. from April 1-5, 2017.
The abstract is available on the AACR website at www.aacr.org.
Abstract Title:
Telomerase inhibitor imetelstat in combination with the BCL-2 inhibitor venetoclax enhances apoptosis in vitro and increases survival in vivo in acute myeloid leukemia (Abstract #1101)
AACR Session Title: Combination Therapy 1
Session Date: Monday, April 3, 2017
Session Time: 8:00 a.m. ET - 12:00 p.m. ET
In accordance with AACR policies, abstracts submitted to the AACR Annual Meeting are embargoed from the time of submission. To be eligible for presentation at the AACR Annual Meeting,information contained in the abstract,as well as additional data and information to be presented at the Annual Meeting, may not be made public before the abstract has been presented in connection with the AACR Annual Meeting.
March 02, 2017 07:30 ET | Source: Geron Corporation
MENLO PARK, Calif., March 02, 2017 (GLOBE NEWSWIRE) -- Geron Corporation (Nasdaq:GERN) today announced an abstract submitted by Janssen Research & Development, LLC describing non-clinical data[/u] on imetelstat has been accepted for presentation as a poster at the 2017 American Association for Cancer Research (AACR) Annual Meeting to be held in Washington, D.C. from April 1-5, 2017.
The abstract is available on the AACR website at www.aacr.org.
Abstract Title:
Telomerase inhibitor imetelstat in combination with the BCL-2 inhibitor venetoclax enhances apoptosis in vitro and increases survival in vivo in acute myeloid leukemia (Abstract #1101)
AACR Session Title: Combination Therapy 1
Session Date: Monday, April 3, 2017
Session Time: 8:00 a.m. ET - 12:00 p.m. ET
In accordance with AACR policies, abstracts submitted to the AACR Annual Meeting are embargoed from the time of submission. To be eligible for presentation at the AACR Annual Meeting,information contained in the abstract,as well as additional data and information to be presented at the Annual Meeting, may not be made public before the abstract has been presented in connection with the AACR Annual Meeting.
Beitrag zu dieser Diskussion schreiben
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| +2,35 | |
| -0,90 | |
| +0,13 | |
| +11,18 | |
| +0,91 | |
| +2,03 | |
| -0,15 | |
| -0,05 | |
| +0,20 | |
| -0,70 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 196 | ||
| 93 | ||
| 66 | ||
| 50 | ||
| 46 | ||
| 42 | ||
| 42 | ||
| 37 | ||
| 35 | ||
| 27 |





















