Medarex, oder wie kommt ein Esel von tiefen Süden in den hohen Norden - 500 Beiträge pro Seite (Seite 8)
eröffnet am 03.07.03 18:54:04 von
neuester Beitrag 13.09.09 21:31:37 von
neuester Beitrag 13.09.09 21:31:37 von
Beiträge: 3.951
ID: 749.702
ID: 749.702
Aufrufe heute: 1
Gesamt: 312.629
Gesamt: 312.629
Aktive User: 0
Top-Diskussionen
| Titel | letzter Beitrag | Aufrufe |
|---|---|---|
| heute 19:16 | 6508 | |
| vor 58 Minuten | 5751 | |
| vor 1 Stunde | 4545 | |
| vor 1 Stunde | 4169 | |
| vor 1 Stunde | 3146 | |
| heute 19:35 | 2567 | |
| vor 59 Minuten | 2126 | |
| vor 1 Stunde | 2005 |
Meistdiskutierte Wertpapiere
| Platz | vorher | Wertpapier | Kurs | Perf. % | Anzahl | ||
|---|---|---|---|---|---|---|---|
| 1. | 1. | 18.170,90 | +1,31 | 210 | |||
| 2. | 2. | 145,05 | +2,11 | 94 | |||
| 3. | 19. | 0,1950 | +7,14 | 82 | |||
| 4. | 3. | 2.322,13 | -0,22 | 62 | |||
| 5. | 9. | 44,00 | -2,65 | 53 | |||
| 6. | 43. | 0,0262 | +63,75 | 49 | |||
| 7. | 17. | 4,7540 | +3,48 | 41 | |||
| 8. | 5. | 767,62 | +7,06 | 34 |
Antwort auf Beitrag Nr.: 34.653.606 von Gruenfeld am 05.08.08 18:12:29Gruenfeld,
die MEDX machts nicht leicht.
Wahrscheinlich hast du recht: Die Anleger hatten Ängstlichkeit abgelegt, nach der schönen Rallye. Nach den Zahlen dafür der Abverkauf.

Mit Korrektur bis 8,75 oder eher bis 8,20 sollte man durchaus rechnen. Gute Studienergebnisse machen aber jeden versuchten limitabgriff zur Makulatur.
die MEDX machts nicht leicht.
Wahrscheinlich hast du recht: Die Anleger hatten Ängstlichkeit abgelegt, nach der schönen Rallye. Nach den Zahlen dafür der Abverkauf.
Mit Korrektur bis 8,75 oder eher bis 8,20 sollte man durchaus rechnen. Gute Studienergebnisse machen aber jeden versuchten limitabgriff zur Makulatur.
Antwort auf Beitrag Nr.: 34.657.621 von Ville7 am 06.08.08 09:53:26Korrektur zu meiner Zusammenfassung. Nicht Humax-CD4 sondern Humax-EGFR Phase III Daten (Interim Look) werden noch 2008 von Genmab erwartet.
"It looks to me like the whole world is waking up to them." [antibodies]
Lisa N. Drakeman, CEO Genmab
http://www.wsw.com/webcast/jeff26/gen.dc
Lisa N. Drakeman, CEO Genmab
http://www.wsw.com/webcast/jeff26/gen.dc
Pipeline ist derzeit recht wenig wert. Der Aufbau kostet Geld, parallel werden aber (mehr) Werte geschaffen.
Medarex-Pipe ca.:
Partnerprogramme:
2 BLA
2 P III
5 P II
12 P I
>10 Präklinik
Eigenentwicklung:
1 P III
3 P II
8 P I
>10 Präklinik
Equity Interest (AVANT und Genmab):
3 P III
6 P II
6 P I
>10 Präklinik
Anzahlen in Forschung jeweils unbekannt.
Finanzposition:
425 Mio USD Cash
80 Mio Equity-Stake in Avant
100 Mio Equity-Stake in Genmab
Weitere hohe Buchwerte wie komplette Production-Facility
Cashburn derzeit 12,4 Mio USD pro Monat
MK: 1150 Mio USD
Nur zur Info.
Medarex-Pipe ca.:
Partnerprogramme:
2 BLA
2 P III
5 P II
12 P I
>10 Präklinik
Eigenentwicklung:
1 P III
3 P II
8 P I
>10 Präklinik
Equity Interest (AVANT und Genmab):
3 P III
6 P II
6 P I
>10 Präklinik
Anzahlen in Forschung jeweils unbekannt.
Finanzposition:
425 Mio USD Cash
80 Mio Equity-Stake in Avant
100 Mio Equity-Stake in Genmab
Weitere hohe Buchwerte wie komplette Production-Facility
Cashburn derzeit 12,4 Mio USD pro Monat
MK: 1150 Mio USD
Nur zur Info.
Das ist ja alles schön und gut, aber eine große Pipeline hat MEDX ja nicht erst seit gestern. Was im Endeffekt zählt, ist, ob es die Medikamente auf den Markt schaffen. Und in dieser Hinsicht sieht es ja nicht sonderlich rosig aus.
Und bis ein Produkt auf dem Markt ist, glaube ich Pien&Schade kein Wort. Drakeman beschrieb MEDX60 und MDX-010 einst als Goldmine, na davon ist leider nicht viel zu sehen.
Und bis ein Produkt auf dem Markt ist, glaube ich Pien&Schade kein Wort. Drakeman beschrieb MEDX60 und MDX-010 einst als Goldmine, na davon ist leider nicht viel zu sehen.
Antwort auf Beitrag Nr.: 34.669.914 von Ennox am 07.08.08 14:10:29Für ihn war das eine Goldmine, der mußte auch nicht schürfen
Immerhin hat er damit Kurse auf die Reihe bekommen. Große Zukunft anpreisen und Kurse machten sich auf, damit kommt man in den Himmel auf Erden. Das ist ja nicht nur bei GPC so, die Originale kommen aus USA. Die kommunizieren künftige Märkte und Fristen, diese Ziele werden konsequent nicht erreicht und gleichzeitig wird in weiser Ahnung neues Kapital beschafft.
Das ist ja auch der primäre Geschäftszweck, Hoffnung stiften wie Fernsehprediger und Millionen an die Seite bringen. Dafür erzählt sich was von neuen Paradigmen hier und dort, muß ja auch für die ewig überforderten Investmentobermuffties mit Dr. eingängig sein.
Gleich in den fünften Gang und Vollgas selbst wenn das Auto fehlt
selbst wenn das Auto fehlt

Immerhin hat er damit Kurse auf die Reihe bekommen. Große Zukunft anpreisen und Kurse machten sich auf, damit kommt man in den Himmel auf Erden. Das ist ja nicht nur bei GPC so, die Originale kommen aus USA. Die kommunizieren künftige Märkte und Fristen, diese Ziele werden konsequent nicht erreicht und gleichzeitig wird in weiser Ahnung neues Kapital beschafft.
Das ist ja auch der primäre Geschäftszweck, Hoffnung stiften wie Fernsehprediger und Millionen an die Seite bringen. Dafür erzählt sich was von neuen Paradigmen hier und dort, muß ja auch für die ewig überforderten Investmentobermuffties mit Dr. eingängig sein.
Gleich in den fünften Gang und Vollgas
 selbst wenn das Auto fehlt
selbst wenn das Auto fehlt
Warum ging Medx heute eigentlich nochmal mit Gap runter?
Zahlennews waren gestern. Da ist das gap schon etwas seltsam....
Zahlennews waren gestern. Da ist das gap schon etwas seltsam....
Weil per BM nachgefragt wurde, was ich von dem CB216J noch halte. 
CB216J, Basis 8 USD und Laufzeit 17.9.08:

Seinerzeit viel zu früh von mir verkauft.
Wer dringeblieben ist, hat hoffentlich den Absprung hinbekommen.
 Bei der Laufzeit ist der Schein natürlich jetzt extrem giftig und mit Aussitzen ist fast gar nichts mehr drin. Sollte Medarex mit V-Form rebounden wäre das natürlich ein totaler Hit.
Bei der Laufzeit ist der Schein natürlich jetzt extrem giftig und mit Aussitzen ist fast gar nichts mehr drin. Sollte Medarex mit V-Form rebounden wäre das natürlich ein totaler Hit.
Deutlich sanfter ist der hier:
CB8WWV Basis 10USD bis 17.12.08 Allerdings ist auch hier im Moment die Vola mit 72% sehr teuer eingepreist....

Im Moment ein Griff ins fallende Messer. Ich rühre keine so Dinger an, bevor es nicht ein Zeichen auf Stabilisierung und Dreh gibt. Am besten mit Markt- und/oder newsunterstützung.

CB216J, Basis 8 USD und Laufzeit 17.9.08:
Seinerzeit viel zu früh von mir verkauft.

Wer dringeblieben ist, hat hoffentlich den Absprung hinbekommen.

 Bei der Laufzeit ist der Schein natürlich jetzt extrem giftig und mit Aussitzen ist fast gar nichts mehr drin. Sollte Medarex mit V-Form rebounden wäre das natürlich ein totaler Hit.
Bei der Laufzeit ist der Schein natürlich jetzt extrem giftig und mit Aussitzen ist fast gar nichts mehr drin. Sollte Medarex mit V-Form rebounden wäre das natürlich ein totaler Hit.Deutlich sanfter ist der hier:
CB8WWV Basis 10USD bis 17.12.08 Allerdings ist auch hier im Moment die Vola mit 72% sehr teuer eingepreist....
Im Moment ein Griff ins fallende Messer. Ich rühre keine so Dinger an, bevor es nicht ein Zeichen auf Stabilisierung und Dreh gibt. Am besten mit Markt- und/oder newsunterstützung.
Das ist wohl der Grund für die Kursverluste der letzten Tage;
Johnson & Johnson drug review delayed by 3 months
Friday August 8, 9:09 am ET
Johnson & Johnson says FDA will delay psoriasis drug candidate review by 3 months
NEW BRUNSWICK, N.J. (AP) -- Johnson & Johnson's Centocor unit said Friday the Food and Drug Administration will take an additional three months to review an application for the experimental psoriasis drug ustekinumab.
The company said the review could now run through December. Centocor is seeking approval of the drug for adult patients with chronic moderate to severe plaque psoriasis, a severe skin disease. The FDA extended the review period because of application amendments made over the last three months.
In June, an FDA advisory panel unanimously recommended approval. The regulatory agency normally follows the recommendations of its advisory panels, though it is not required to do so.
Shares of Johnson & Johnson closed at $70.65 Thursday.
Johnson & Johnson drug review delayed by 3 months
Friday August 8, 9:09 am ET
Johnson & Johnson says FDA will delay psoriasis drug candidate review by 3 months
NEW BRUNSWICK, N.J. (AP) -- Johnson & Johnson's Centocor unit said Friday the Food and Drug Administration will take an additional three months to review an application for the experimental psoriasis drug ustekinumab.
The company said the review could now run through December. Centocor is seeking approval of the drug for adult patients with chronic moderate to severe plaque psoriasis, a severe skin disease. The FDA extended the review period because of application amendments made over the last three months.
In June, an FDA advisory panel unanimously recommended approval. The regulatory agency normally follows the recommendations of its advisory panels, though it is not required to do so.
Shares of Johnson & Johnson closed at $70.65 Thursday.
Medarex ist einfach ne Drecksaktie, jetzt gehts schon
wieder nach unten, den x-ten Tag in Folge.
Die Aktie war und ist und bleibt eine Loseraktie!!!!
wieder nach unten, den x-ten Tag in Folge.
Die Aktie war und ist und bleibt eine Loseraktie!!!!
Glaube es geht bald wieder rauf. Hier musste wohl ein Fond seinen gesamten Bestand abbauen(übrigens auch in Microsoft)
LONG BEACH (Mffais.com) - Vanguard Group Inc sold -3,421,641 (-98.61 %) of their shares in Medarex Inc (MEDX), bringing their current holdings to 48,190 shares as shown by filings made public on 2008-08-06.
LONG BEACH (Mffais.com) - Vanguard Group Inc sold -3,421,641 (-98.61 %) of their shares in Medarex Inc (MEDX), bringing their current holdings to 48,190 shares as shown by filings made public on 2008-08-06.
Die mussten wohl erst einmal verdaut werden. kurs zieht jetzt +übrigens deutlich an!

Antwort auf Beitrag Nr.: 34.689.486 von Icanfly am 08.08.08 20:42:51Eine Feindliche Übernahme ist gänzlich nie auszuschließen.
www.n-tv.de/PharmaRiesen_suchen_Biotechs_im_Visier/200520081…
Eine gute Aktie kann man immer kaufen
PS.Der Verfasser ist in Medarex investiert.

www.n-tv.de/PharmaRiesen_suchen_Biotechs_im_Visier/200520081…
Eine gute Aktie kann man immer kaufen

PS.Der Verfasser ist in Medarex investiert.
Antwort auf Beitrag Nr.: 34.657.621 von Ville7 am 06.08.08 09:53:26da ich Genmab verfolge, hier auch noch mal ein paar potentielle Events... (Unibodys sind übrigens zur Stabilisierung der IgG4-AKs gedacht)
•Zalutumumab: Interim phase-III data for the head and neck cancer indication (expected in Q4 2008)
•Ofatumumab: Approval of the CLL indication (expected in Q4, 2008)
•Zalutumumab: Partnership agreement
•Unibody: Technology update
•Unibody: Partnership agreement
•Zanolimumab: Phase III data for the CTCL indication (expected in 2009, 2H)
*********************
und eine Analystenmeinung:
"Bullets Genmab: Spectacular Phase III data HuMax CD20 CLL, BUY maintained by SNS Securities
Yesterday, Genmab announced spectacular Phase III data of HuMax CD20 (ofatumumab) CLL in refractory patients. The overall response rate of the two patients group treated was 51% in patients refractory to fludarabine (chemotherapy) and Campath (competitive antibody against CLL), and 44% in patients to fludarabine alone. Market consensus was around 25% overall response rate.
Also compared to Phase III data of competitive antibodies like Rituxan (25% response rate in refractory CLL patients) and Campath (33% response rate), the data of Genmab are superior. In our view there should be no doubt that this product will be approved by the FDA. We expect Genmab/GSK to go for BLA filing very soon. The filing and the subsequent approval will trigger a milestone that we estimate to be USD 200m. Genmab has a fast track on HuMax CD20 CLL, so the FDA is likely to give approval between 2 and 6 months.
The strong Phase III data on refractory patients also makes a strong case for the off label use of the drug for other groups of patients (first line) and even for other indications like Non Hodgkin’s Lymphoma. It has always been Genmab’s strategy to go for off label use after getting the Phase III data on HuMax CD20 CLL in refractory patients. In the next few weeks, Genmab/GSK will likely start a large Phase III study with HuMax CD20 in first line patients. The first data on this study should coincide with the market launch of the drug in refractory patients. Positive data would support the launch of the product, which we expect to happen end 2009Q1.
The case of a strong and swift market introduction is backed by GSK, who seems to have made reservations on 40,000 liter capacity at Lonza for the production of HuMax CD20. Considering a yield of 3-5 grams per liter, this would mean USD 1.2-2bn.
Later this year, an interim analysis of HuMax EGFr refractory H&N Phase III is to be expected. In April 132 patients were included in the pivotal trial. The last few weeks patient inclusion is about 5-10 persons per week. Counted from April this would mean that now 192-252 patients are enrolled. Two third of patients are receiving the drug. An interim analysis is possible with the data of 116 patients. The longer it takes that we need to wait for the interim analysis, the better the data are expected to be (with higher survival rates, current treatment in refractory has survival rate of about 3-4 months). The recent bid on ImClone by BMS (USD 4.5bn, specifically on its drug Erbitux), also gives an indication what the potential value is for this program.
We believe that the strong data on HuMax CD20 CLL will pave the way for a move from GSK in taking over the company. The time frame seems to be between August and November (between CLL data and interim analysis EGFr). With positive data on CLL, GSK has the hard data in hand to validate a take over. Wating till the announcement of the interim analysis on HuMax EGFr H&N would only increase the price. Pressure to come with interim analysis on EGFr sooner rather than later will increase in the next few months. Good data on 116 patients should be enough to file for approval. For GSK the risks have decreased considerably with the hard data on HuMax CD20. Also bear in mind that for GSK the financial ratio to go for a take over scenario becomes more interesting, since the company still needs to pay milestones up to USD 1bn and royalties up to 50%.
A take over scenario is becoming also more likely considering the ongoing M&A activity in the sector. The biotech companies that have been taken over announced positive Phase III data and /or already have products on the market. Genmab now can also be put in this select group of candidates.
In all, we strongly maintain our Buy rating on the stock. We advice our clients to maintain current holdings or even increase stakes in the company. At the current share price we still see considerable upside potential of 60-100%."
mfg ipollit
•Zalutumumab: Interim phase-III data for the head and neck cancer indication (expected in Q4 2008)
•Ofatumumab: Approval of the CLL indication (expected in Q4, 2008)
•Zalutumumab: Partnership agreement
•Unibody: Technology update
•Unibody: Partnership agreement
•Zanolimumab: Phase III data for the CTCL indication (expected in 2009, 2H)
*********************
und eine Analystenmeinung:
"Bullets Genmab: Spectacular Phase III data HuMax CD20 CLL, BUY maintained by SNS Securities
Yesterday, Genmab announced spectacular Phase III data of HuMax CD20 (ofatumumab) CLL in refractory patients. The overall response rate of the two patients group treated was 51% in patients refractory to fludarabine (chemotherapy) and Campath (competitive antibody against CLL), and 44% in patients to fludarabine alone. Market consensus was around 25% overall response rate.
Also compared to Phase III data of competitive antibodies like Rituxan (25% response rate in refractory CLL patients) and Campath (33% response rate), the data of Genmab are superior. In our view there should be no doubt that this product will be approved by the FDA. We expect Genmab/GSK to go for BLA filing very soon. The filing and the subsequent approval will trigger a milestone that we estimate to be USD 200m. Genmab has a fast track on HuMax CD20 CLL, so the FDA is likely to give approval between 2 and 6 months.
The strong Phase III data on refractory patients also makes a strong case for the off label use of the drug for other groups of patients (first line) and even for other indications like Non Hodgkin’s Lymphoma. It has always been Genmab’s strategy to go for off label use after getting the Phase III data on HuMax CD20 CLL in refractory patients. In the next few weeks, Genmab/GSK will likely start a large Phase III study with HuMax CD20 in first line patients. The first data on this study should coincide with the market launch of the drug in refractory patients. Positive data would support the launch of the product, which we expect to happen end 2009Q1.
The case of a strong and swift market introduction is backed by GSK, who seems to have made reservations on 40,000 liter capacity at Lonza for the production of HuMax CD20. Considering a yield of 3-5 grams per liter, this would mean USD 1.2-2bn.
Later this year, an interim analysis of HuMax EGFr refractory H&N Phase III is to be expected. In April 132 patients were included in the pivotal trial. The last few weeks patient inclusion is about 5-10 persons per week. Counted from April this would mean that now 192-252 patients are enrolled. Two third of patients are receiving the drug. An interim analysis is possible with the data of 116 patients. The longer it takes that we need to wait for the interim analysis, the better the data are expected to be (with higher survival rates, current treatment in refractory has survival rate of about 3-4 months). The recent bid on ImClone by BMS (USD 4.5bn, specifically on its drug Erbitux), also gives an indication what the potential value is for this program.
We believe that the strong data on HuMax CD20 CLL will pave the way for a move from GSK in taking over the company. The time frame seems to be between August and November (between CLL data and interim analysis EGFr). With positive data on CLL, GSK has the hard data in hand to validate a take over. Wating till the announcement of the interim analysis on HuMax EGFr H&N would only increase the price. Pressure to come with interim analysis on EGFr sooner rather than later will increase in the next few months. Good data on 116 patients should be enough to file for approval. For GSK the risks have decreased considerably with the hard data on HuMax CD20. Also bear in mind that for GSK the financial ratio to go for a take over scenario becomes more interesting, since the company still needs to pay milestones up to USD 1bn and royalties up to 50%.
A take over scenario is becoming also more likely considering the ongoing M&A activity in the sector. The biotech companies that have been taken over announced positive Phase III data and /or already have products on the market. Genmab now can also be put in this select group of candidates.
In all, we strongly maintain our Buy rating on the stock. We advice our clients to maintain current holdings or even increase stakes in the company. At the current share price we still see considerable upside potential of 60-100%."
mfg ipollit
Short Interest zum 15.7. gestiegen, 20% des Aktienbestandes zu diesem Zeitpunkt short:
7/15/2008 25,860,272
7/15/2008 25,860,272
Es ist echt zum Kotzen, der Wert ist nur noch Schrott, ab und zu gehts mal Gerüchtemäßig nach oben aber ansonsten geht es strikt
nach unten seit 2000!
Was hat den Medarex die letzten 8 Jahre raus gebracht???
Nix, gar nichts!! In 8 ganzen Jahren wurde nur eld verbrannt!
nach unten seit 2000!
Was hat den Medarex die letzten 8 Jahre raus gebracht???
Nix, gar nichts!! In 8 ganzen Jahren wurde nur eld verbrannt!
Antwort auf Beitrag Nr.: 34.653.606 von Gruenfeld am 05.08.08 18:12:29MEDX 5-MinutenChart
Zeitraum: 10 Wochentage

PMedarex^.Close.At['22.08.2008 19:05:00']
Nach dem Verkaufssignal aus Beitrag #3485 steht 'Rotating Gruen' seit heute 19:05 Uhr wieder auf Kauf. Rein optisch gesehen wäre vielleicht der Bar um 16:30 Uhr besser geeignet. Ein Bug in Rotating Gruen??
Zeitraum: 10 Wochentage
PMedarex^.Close.At['22.08.2008 19:05:00']
Nach dem Verkaufssignal aus Beitrag #3485 steht 'Rotating Gruen' seit heute 19:05 Uhr wieder auf Kauf. Rein optisch gesehen wäre vielleicht der Bar um 16:30 Uhr besser geeignet. Ein Bug in Rotating Gruen??
Shorts abgebaut auf knapp 20 mios:
Medarex, Inc. - Common Stock
Settlement Date Short Interest Percent Change Average Daily Share Volume Days to Cover
08/15/2008 19,848,109 (15.23) 2,142,761 9.26
07/31/2008 23,414,203 (9.46) 1,989,171 11.77
07/15/2008 25,860,272 5.35 1,767,457 14.63
06/30/2008 24,547,914 (3.37) 1,737,619 14.13
06/13/2008 25,405,283 16.34 1,599,951 15.88
05/30/2008 21,837,573 10.95 1,571,104 13.90
05/15/2008 19,682,828 (9.13) 1,378,221 14.28
04/30/2008 21,660,590 2.88 1,429,506 15.15
04/15/2008 21,054,891 (4.73) 3,246,555 6.49
03/31/2008 22,099,908 (12.82) 1,860,757 11.88
03/14/2008 25,349,777 4.53 1,841,857 13.76
02/29/2008 24,252,089 (1.72) 1,768,877 13.71
02/15/2008 24,677,334 (12.96) 2,065,614 11.95
01/31/2008 28,351,360 (9.01) 2,130,559 13.31
01/15/2008 31,157,261 3.40 1,888,482 16.50
Antwort auf Beitrag Nr.: 34.816.981 von Gruenfeld am 22.08.08 19:38:44Und rotiert das grün mal wieder, besser mittelfristig bis 9 oder 10 USD?
Wer versucht sich an dieser Aktie bitte mal
Verklatschen die ihre restlichen Genmabs noch und schieben mal wieder eine KE ein oder bekommen die neben Dauerankündigungen ausnahmsweise mal was Richtung Zulassung
oder bekommen die neben Dauerankündigungen ausnahmsweise mal was Richtung Zulassung
Wie sieht das aus

Verklatschen die ihre restlichen Genmabs noch und schieben mal wieder eine KE ein
 oder bekommen die neben Dauerankündigungen ausnahmsweise mal was Richtung Zulassung
oder bekommen die neben Dauerankündigungen ausnahmsweise mal was Richtung Zulassung
Wie sieht das aus

Antwort auf Beitrag Nr.: 34.894.010 von eck64 am 28.08.08 16:33:22Der 5-MinutenChart ist über längere Zeiträume* nach wie vor positiv gekrümmt. Sehr ärgerlich, dass nach dem Signal aus #3513 keine Kursgewinne anfielen. Die Medarex- Aktie hat sich nur stabilisiert, eine Bodenbildung auf diesem Niveau wahrscheinlich. Trotzdem ist Vorsicht geboten, denn das Abwärtstempo der Korrektur seit dem zyklischen Hoch 01.08.2008 kann nur als extrem bezeichnet werden, ganz ähnlich der Abwärtsbewegung im Juni.
Mittelfristig sind höhere Kurse von $9 oder $10 sicherlich drin. Aber ich werde hier nichts vorwegnehmen, denn an dieser Stelle ist auch Gegenteiliges denkbar. Die ganze Kursentwicklung seit dem Gap vom 02.04.2008 ist aus meiner Sicht sehr ungewöhnlich (inverses symmetrisches Dreieck).
* von 400 bis zu 1500 Bars schätzungsweise
Mittelfristig sind höhere Kurse von $9 oder $10 sicherlich drin. Aber ich werde hier nichts vorwegnehmen, denn an dieser Stelle ist auch Gegenteiliges denkbar. Die ganze Kursentwicklung seit dem Gap vom 02.04.2008 ist aus meiner Sicht sehr ungewöhnlich (inverses symmetrisches Dreieck).
* von 400 bis zu 1500 Bars schätzungsweise
Hilf mir bitte auf die Sprünge


Antwort auf Beitrag Nr.: 34.895.882 von Friseuse am 28.08.08 18:22:38Würde ich gerne tun. Rotating Gruen ist aber nicht kompatibel mit konventioneller Charttechnik. Nur soviel: Im TagesChart waren die Bars vom 10.09.2007, 15.10.2007 und vom 11.12.2007 Verkaussignale 'Rotating Gruen' und haben den Medarex- Chart zerstört. Danach wurde jede kleine Erholung abverkauft und der Abwärtstrend der Aktie so stark, dass selbst die extrem starke Rallye im Juli nur ausreichte, die Abwärts- Dynamik erstmal zu stoppen. Momentan kann man von einer seitwärts gerichteten Tendenz im TagesChart ausgehen. Und zwar seit dem angesprochenen Gap vom 02.04.2008. In Form eines inversen symmetrischen Dreiecks. Es kann sich weiter zu einem Diamant ausbilden, aber wie schon gesagt man soll nichts vorwegnehmen.
Unterstützung einer oberen Umkehrformation
Abschwächelnder Hausbau im Chart
Kann man so sehen, ist aber eigentlich erst im Nachhinein so zu sehen und deklarierbar. Für Rotating Gruen war der MEDX- TagesChart bis zum 10.09.2007 voll intakt, das letzte Kaufsignal war vom 07.08.2007.
Öhm jetzt seh ich´s, Du hast die gelben Linien vom falschen Gap aus gezogen. Also das Gap vom 02.04.2008 als Startpunkt benutzen, um das inverse symmetrische Dreieck zu identifizieren.
Unterstützung einer oberen Umkehrformation
Abschwächelnder Hausbau im Chart
Kann man so sehen, ist aber eigentlich erst im Nachhinein so zu sehen und deklarierbar. Für Rotating Gruen war der MEDX- TagesChart bis zum 10.09.2007 voll intakt, das letzte Kaufsignal war vom 07.08.2007.
Öhm jetzt seh ich´s, Du hast die gelben Linien vom falschen Gap aus gezogen. Also das Gap vom 02.04.2008 als Startpunkt benutzen, um das inverse symmetrische Dreieck zu identifizieren.
Antwort auf Beitrag Nr.: 34.816.981 von Gruenfeld am 22.08.08 19:38:44Update Beitrag #3513
PMedarex^.Close.At['02.09.2008 20:50:00'] //Sell
PMedarex^.Close.At['03.09.2008 15:35:00'] //Sell
PMedarex^.Close.At['03.09.2008 20:25:00'] //Buy
Die Situation heute ist vergleichbar der vom 01.Juli 2008. Es kommt zu einer kleinen Panik- /VerkaufsAttacke mit Eröffnungsgap. Die ganze Inszenierung geht einher mit zwei Verkaufssignalen 'Rotating Gruen', die charttechnische Lage ist prekär. Aber Überraschung, der Kursverlust wird unmittelbar wieder aufgeholt. Ein zyklisches Tief etabliert. Unglaublich, dass Rotating Gruen schon wieder auf Kauf steht! Eigentlich sieht der Kursverlauf im Moment eher neutral, denn wirklich postiv gekrümmt aus. Stimmt hier etwas nicht?
MEDX 5-MinutenChart siehe Beitrag #3513
PMedarex^.Close.At['02.09.2008 20:50:00'] //Sell
PMedarex^.Close.At['03.09.2008 15:35:00'] //Sell
PMedarex^.Close.At['03.09.2008 20:25:00'] //Buy
Die Situation heute ist vergleichbar der vom 01.Juli 2008. Es kommt zu einer kleinen Panik- /VerkaufsAttacke mit Eröffnungsgap. Die ganze Inszenierung geht einher mit zwei Verkaufssignalen 'Rotating Gruen', die charttechnische Lage ist prekär. Aber Überraschung, der Kursverlust wird unmittelbar wieder aufgeholt. Ein zyklisches Tief etabliert. Unglaublich, dass Rotating Gruen schon wieder auf Kauf steht! Eigentlich sieht der Kursverlauf im Moment eher neutral, denn wirklich postiv gekrümmt aus. Stimmt hier etwas nicht?
MEDX 5-MinutenChart siehe Beitrag #3513
Hi,
@Gruenfeld.
wenn ich es richtig mitbekommen habe, ist Rotating Gruen eine von dir entwickelte Software??

Wenn ja, könntest du kurz zusammenfassen, wie das Teil funktioniert bzw. wie du danach handelst?
Welchen Input verwendest du? Wie ziehst du Schlüsse daraus.
Wenn es sich allerdings um ein Betriebsgeheimnis handelt, dann versteh ich das auch.
lg -Lycos
@Gruenfeld.
wenn ich es richtig mitbekommen habe, ist Rotating Gruen eine von dir entwickelte Software??


Wenn ja, könntest du kurz zusammenfassen, wie das Teil funktioniert bzw. wie du danach handelst?
Welchen Input verwendest du? Wie ziehst du Schlüsse daraus.
Wenn es sich allerdings um ein Betriebsgeheimnis handelt, dann versteh ich das auch.

lg -Lycos
Lycos2, ich hoffe nicht das Du Dich nach
so einem Hocuspokus beeinflussen lässt.
Die Kommentare über dieses Modell wehen
wie der Wind von einer falschen Prognose
zur nächsten. Ich beobachte schon lange
die Kommentare zu diesem Modell und das
Modell liegt mindestens zu 80% falsch!
Ich bekomme so ein Hals wenn zwielichtige
Modelle hier vorgestellt werden und andere
vielleicht nicht so erfahrene Trader
falsch beeinflusst werden!
Daher absolut die FINGER WEG von solchen
Modellen.
Ich bitte euch eure Modelle für euch zu behalten
und keine Kauf- oder Verkaufsempfehlungen zu geben!
so einem Hocuspokus beeinflussen lässt.
Die Kommentare über dieses Modell wehen
wie der Wind von einer falschen Prognose
zur nächsten. Ich beobachte schon lange
die Kommentare zu diesem Modell und das
Modell liegt mindestens zu 80% falsch!
Ich bekomme so ein Hals wenn zwielichtige
Modelle hier vorgestellt werden und andere
vielleicht nicht so erfahrene Trader
falsch beeinflusst werden!
Daher absolut die FINGER WEG von solchen
Modellen.
Ich bitte euch eure Modelle für euch zu behalten
und keine Kauf- oder Verkaufsempfehlungen zu geben!
@JamM
Danke für deinen Beitrag. Ich hab allerdings rein aus Interesse heraus gefragt, da Gruenfeld oft ihre Charts (5 Minuten Charts
 )postet, von irgendwelchen Kauf- und Verkaussignalen spricht und diese (mir eben nicht verständlich) interpretiert. Mich hätte rein das Modell dahinter, die verwendeten Daten und ihr handeln danach interessiert.
)postet, von irgendwelchen Kauf- und Verkaussignalen spricht und diese (mir eben nicht verständlich) interpretiert. Mich hätte rein das Modell dahinter, die verwendeten Daten und ihr handeln danach interessiert.
Bei MEDX bin ich aus ganz anderen Gründen dabei. (ob die letztendlich richtig sind/waren, wird sich zeigen

Danke für deinen Beitrag. Ich hab allerdings rein aus Interesse heraus gefragt, da Gruenfeld oft ihre Charts (5 Minuten Charts

 )postet, von irgendwelchen Kauf- und Verkaussignalen spricht und diese (mir eben nicht verständlich) interpretiert. Mich hätte rein das Modell dahinter, die verwendeten Daten und ihr handeln danach interessiert.
)postet, von irgendwelchen Kauf- und Verkaussignalen spricht und diese (mir eben nicht verständlich) interpretiert. Mich hätte rein das Modell dahinter, die verwendeten Daten und ihr handeln danach interessiert. Bei MEDX bin ich aus ganz anderen Gründen dabei. (ob die letztendlich richtig sind/waren, wird sich zeigen


Rotating icanfly sagt jedenfalls, dass wir ende des Jahres die 10$ überschritten haben!
sagt jedenfalls, dass wir ende des Jahres die 10$ überschritten haben!
 sagt jedenfalls, dass wir ende des Jahres die 10$ überschritten haben!
sagt jedenfalls, dass wir ende des Jahres die 10$ überschritten haben!
Antwort auf Beitrag Nr.: 34.968.803 von Gruenfeld am 03.09.08 20:58:49Update Beitrag #3520
Eine Zusammenstellung der geposteten Signale. Kann sich jeder selbst eine Meinung zu bilden.
PMedarex^.Close.At['17.04.2008 19:35:00'] //Buy (Beitrag #3382)
PMedarex^.Close.At['07.05.2008 16:35:00'] //Buy (Beitrag #3394)
PMedarex^.Close.At['09.05.2008 16:45:00'] //Buy (Beitrag #3397)
PMedarex^.Close.At['28.05.2008 15:30:00'] //Buy (Beitrag #3421)
PMedarex^.Close.At['04.06.2008 17:20:00'] //Buy (Beitrag #3423)
PMedarex^.Close.At['16.06.2008 21:10:00'] //Buy (Beitrag #3431)
PMedarex^.Close.At['19.06.2008 21:30:00'] //Buy (Beitrag #3441)
PMedarex^.Close.At['24.06.2008 15:45:00'] //Buy (Beitrag #3444)
PMedarex^.Close.At['26.06.2008 19:50:00'] //Buy (Beitrag #3446)
PMedarex^.Close.At['30.06.2008 21:10:00'] //Buy (Beitrag #3449)
PMedarex^.Close.At['01.07.2008 15:30:00'] //Sell (Beitrag #3450)
PMedarex^.Close.At['01.07.2008 16:00:00'] //Buy (Beitrag #3450)
PMedarex^.Close.At['22.07.2008 15:30:00'] //Sell (Beitrag #3471)
PMedarex^.Close.At['24.07.2008 16:45:00'] //Sell (Beitrag #3480)
PMedarex^.Close.At['05.08.2008 16:15:00'] //Sell (Beitrag #3485)
PMedarex^.Close.At['22.08.2008 19:05:00'] //Buy (Beitrag #3513)
PMedarex^.Close.At['02.09.2008 20:50:00'] //Sell (Beitrag #3520)
PMedarex^.Close.At['03.09.2008 15:35:00'] //Sell (Beitrag #3520)
PMedarex^.Close.At['03.09.2008 20:25:00'] //Buy (Beitrag #3520)
PMedarex^.Close.At['04.09.2008 15:30:00'] //Sell (Beitrag #3525)
PMedarex^.Close.At['05.09.2008 15:30:00'] //Sell (Beitrag #3525)
PMedarex^.Close.At['05.09.2008 21:35:00'] //Buy (Beitrag #3525)
Ich beobachte schon lange
die Kommentare zu diesem Modell und das
Modell liegt mindestens zu 80% falsch!
A good laugh. Von den 19 Signalen (die letzten 3 ausgeklammert), waren also mindestens 15 falsch. Aha.
Von den 19 Signalen (die letzten 3 ausgeklammert), waren also mindestens 15 falsch. Aha.
Die Kriterien für seine Klassifizierung in richtige und falsche Signale wird Benutzer 'JamM' freilich schuldig bleiben.
Bekommt einen Hals beim Lesen meiner Beiträge..... dazu fällt mir also nichts mehr ein!
Definitiv ein unverschämter Beitrag. Mein Modell für mich behalten? Genau das werde ich jetzt tun.
Eine Zusammenstellung der geposteten Signale. Kann sich jeder selbst eine Meinung zu bilden.
PMedarex^.Close.At['17.04.2008 19:35:00'] //Buy (Beitrag #3382)
PMedarex^.Close.At['07.05.2008 16:35:00'] //Buy (Beitrag #3394)
PMedarex^.Close.At['09.05.2008 16:45:00'] //Buy (Beitrag #3397)
PMedarex^.Close.At['28.05.2008 15:30:00'] //Buy (Beitrag #3421)
PMedarex^.Close.At['04.06.2008 17:20:00'] //Buy (Beitrag #3423)
PMedarex^.Close.At['16.06.2008 21:10:00'] //Buy (Beitrag #3431)
PMedarex^.Close.At['19.06.2008 21:30:00'] //Buy (Beitrag #3441)
PMedarex^.Close.At['24.06.2008 15:45:00'] //Buy (Beitrag #3444)
PMedarex^.Close.At['26.06.2008 19:50:00'] //Buy (Beitrag #3446)
PMedarex^.Close.At['30.06.2008 21:10:00'] //Buy (Beitrag #3449)
PMedarex^.Close.At['01.07.2008 15:30:00'] //Sell (Beitrag #3450)
PMedarex^.Close.At['01.07.2008 16:00:00'] //Buy (Beitrag #3450)
PMedarex^.Close.At['22.07.2008 15:30:00'] //Sell (Beitrag #3471)
PMedarex^.Close.At['24.07.2008 16:45:00'] //Sell (Beitrag #3480)
PMedarex^.Close.At['05.08.2008 16:15:00'] //Sell (Beitrag #3485)
PMedarex^.Close.At['22.08.2008 19:05:00'] //Buy (Beitrag #3513)
PMedarex^.Close.At['02.09.2008 20:50:00'] //Sell (Beitrag #3520)
PMedarex^.Close.At['03.09.2008 15:35:00'] //Sell (Beitrag #3520)
PMedarex^.Close.At['03.09.2008 20:25:00'] //Buy (Beitrag #3520)
PMedarex^.Close.At['04.09.2008 15:30:00'] //Sell (Beitrag #3525)
PMedarex^.Close.At['05.09.2008 15:30:00'] //Sell (Beitrag #3525)
PMedarex^.Close.At['05.09.2008 21:35:00'] //Buy (Beitrag #3525)
Ich beobachte schon lange
die Kommentare zu diesem Modell und das
Modell liegt mindestens zu 80% falsch!
A good laugh.
 Von den 19 Signalen (die letzten 3 ausgeklammert), waren also mindestens 15 falsch. Aha.
Von den 19 Signalen (die letzten 3 ausgeklammert), waren also mindestens 15 falsch. Aha.Die Kriterien für seine Klassifizierung in richtige und falsche Signale wird Benutzer 'JamM' freilich schuldig bleiben.
Bekommt einen Hals beim Lesen meiner Beiträge..... dazu fällt mir also nichts mehr ein!
Definitiv ein unverschämter Beitrag. Mein Modell für mich behalten? Genau das werde ich jetzt tun.
Ist nun endlich mal ein Boden gefunden???

Medarex gets milestone payment from Pfizer
Monday September 8, 12:21 pm ET
Medarex receives undisclosed payment from Pfizer for drug developed with UltiMAb technology
PRINCETON, N.J. (AP) -- Medarex Inc. said Monday it received a milestone payment after Pfizer Inc. planned to begin clinical trials of a product Pfizer developed using Madera's ultimo technology.
Madera did not disclose the size of the payment and the purpose of the drug candidate, but said it was an antibody developed using ultimo human antibody technology. The payment was triggered by the filing of an investigational new drug application by Pfizer, indicating it intends to start human clinical trials.
The company may receive farther milestone payments if the product advances through clinical development and receives Food and Drug Administration approval.
Shares of Madera rose 14 cents, or 2.1 percent, to $6.97 in afternoon trading. Pfizer stock advanced 52 cents, or 2.8 percent, to $19.03.

Medarex gets milestone payment from Pfizer
Monday September 8, 12:21 pm ET
Medarex receives undisclosed payment from Pfizer for drug developed with UltiMAb technology
PRINCETON, N.J. (AP) -- Medarex Inc. said Monday it received a milestone payment after Pfizer Inc. planned to begin clinical trials of a product Pfizer developed using Madera's ultimo technology.
Madera did not disclose the size of the payment and the purpose of the drug candidate, but said it was an antibody developed using ultimo human antibody technology. The payment was triggered by the filing of an investigational new drug application by Pfizer, indicating it intends to start human clinical trials.
The company may receive farther milestone payments if the product advances through clinical development and receives Food and Drug Administration approval.
Shares of Madera rose 14 cents, or 2.1 percent, to $6.97 in afternoon trading. Pfizer stock advanced 52 cents, or 2.8 percent, to $19.03.
Antwort auf Beitrag Nr.: 35.037.036 von Handbuch am 09.09.08 16:04:18Zur Info:
15.09.2008 09:20
Neu entstehende Therapien, darunter Ipilimumab von Bristol-Myers Squibb/Medarex, sorgen für Wachstum im Markt der medikamentösen Behandlung des malignen Melanoms
Waltham, Massachusetts (ots/PRNewswire) -
- Interviewte Experten mangelt es aufgrund von in jüngster Zeit veröffentlichten Daten an Vertrauen in Impfungen gegen malignes Melanom, so ein neuer Bericht von Decision Resources
Decision Resources, eines der weltweit führenden Forschungs- und Beratungsunternehmen für den Pharma- und Gesundheitssektor, kommt zu dem Ergebnis, dass der Markt der medikamentösen Behandlung des malignen Melanom bedingt durch die Einführung von neuen Wirkstoffen ein robustes jährliches Wachstum von 12 Prozent bis zum Jahr 2012 in den Vereinigten Staaten, Frankreich, Deutschland, Italien, Spanien, Grossbritannien und Japan aufweisen wird.
Der neue Pharmacor-Bericht trägt den Titel Malignes Melanom und kommt zu dem Schluss, dass es durch die Einführung von Bristol-Myers (News) Squibb/Medarexs Ipilimumab zu einer bedeutenden Vergrösserung des Marktes der medikamentösen Behandlung des malignen Melanoms kommen wird, da der Ipilimumab-Absatz von 2012 bis 2017 jährlich um 17 Prozent steigen wird. Auf Ipilimumab werden 2012 fast ein Viertel des Absatzes bei den Medikamenten zur Behandlung des malignen Melanoms entfallen und etwas mehr als ein Drittel des Absatzes im Jahr 2017.
Der Bericht stellt auch fest, dass aufgrund von in jüngster Zeit veröffentlichten Daten zu Impfungen gegen malignes Melanom Experten wenig Vertrauen in die Impfstoff-Medikamentenklasse setzen. Bei den Krebsimpfstoffen, die zuvor als vielversprechende neue Wirkstoffe angesehen wurden, stellte sich unlängst heraus, dass GM2-KLH21 von Progenics beim malignen Melanom im Frühstadium eine verheerende Wirkung zeigt.
"Die Inzidenz des malignen Melanoms steigt rasch an", so Marcus Hoyle, Analytiker bei Decision Resources. "Bei der Behandlung dieser Krebsart besteht weiterhin ein gewaltiger, nicht gedeckter Bedarf hinsichtlich der Entwicklung von Therapien, die eine Verlängerung der Gesamtüberlebenszeit in fortgeschrittenen Stadien herbeiführen können, denn die Prognose des fortgeschrittenen malignen Melanoms ist schlecht, die mediane Gesamtüberlebenszeit beträgt nur sechs bis neun Monate."
Informationen zur Decision Resources
Decision Resources (www.decisionresources.com) ist weltweit führend in den Bereichen Marktforschungspublikationen, Beratungsdienste und Consulting. So hilft das Unternehmen seinen Kunden bei der Strategiegestaltung, Zuweisung von Ressourcen und dem erfolgreichen Bestehen in den von ihnen gewählten Märkten. Decision Resources ist ein Decision Resources, Inc.-Unternehmen.
Hmmm,Boden gefunden wer weiss das schon?
15.09.2008 09:20
Neu entstehende Therapien, darunter Ipilimumab von Bristol-Myers Squibb/Medarex, sorgen für Wachstum im Markt der medikamentösen Behandlung des malignen Melanoms
Waltham, Massachusetts (ots/PRNewswire) -
- Interviewte Experten mangelt es aufgrund von in jüngster Zeit veröffentlichten Daten an Vertrauen in Impfungen gegen malignes Melanom, so ein neuer Bericht von Decision Resources
Decision Resources, eines der weltweit führenden Forschungs- und Beratungsunternehmen für den Pharma- und Gesundheitssektor, kommt zu dem Ergebnis, dass der Markt der medikamentösen Behandlung des malignen Melanom bedingt durch die Einführung von neuen Wirkstoffen ein robustes jährliches Wachstum von 12 Prozent bis zum Jahr 2012 in den Vereinigten Staaten, Frankreich, Deutschland, Italien, Spanien, Grossbritannien und Japan aufweisen wird.
Der neue Pharmacor-Bericht trägt den Titel Malignes Melanom und kommt zu dem Schluss, dass es durch die Einführung von Bristol-Myers (News) Squibb/Medarexs Ipilimumab zu einer bedeutenden Vergrösserung des Marktes der medikamentösen Behandlung des malignen Melanoms kommen wird, da der Ipilimumab-Absatz von 2012 bis 2017 jährlich um 17 Prozent steigen wird. Auf Ipilimumab werden 2012 fast ein Viertel des Absatzes bei den Medikamenten zur Behandlung des malignen Melanoms entfallen und etwas mehr als ein Drittel des Absatzes im Jahr 2017.
Der Bericht stellt auch fest, dass aufgrund von in jüngster Zeit veröffentlichten Daten zu Impfungen gegen malignes Melanom Experten wenig Vertrauen in die Impfstoff-Medikamentenklasse setzen. Bei den Krebsimpfstoffen, die zuvor als vielversprechende neue Wirkstoffe angesehen wurden, stellte sich unlängst heraus, dass GM2-KLH21 von Progenics beim malignen Melanom im Frühstadium eine verheerende Wirkung zeigt.
"Die Inzidenz des malignen Melanoms steigt rasch an", so Marcus Hoyle, Analytiker bei Decision Resources. "Bei der Behandlung dieser Krebsart besteht weiterhin ein gewaltiger, nicht gedeckter Bedarf hinsichtlich der Entwicklung von Therapien, die eine Verlängerung der Gesamtüberlebenszeit in fortgeschrittenen Stadien herbeiführen können, denn die Prognose des fortgeschrittenen malignen Melanoms ist schlecht, die mediane Gesamtüberlebenszeit beträgt nur sechs bis neun Monate."
Informationen zur Decision Resources
Decision Resources (www.decisionresources.com) ist weltweit führend in den Bereichen Marktforschungspublikationen, Beratungsdienste und Consulting. So hilft das Unternehmen seinen Kunden bei der Strategiegestaltung, Zuweisung von Ressourcen und dem erfolgreichen Bestehen in den von ihnen gewählten Märkten. Decision Resources ist ein Decision Resources, Inc.-Unternehmen.
Hmmm,Boden gefunden wer weiss das schon?

Trotzdem ein seltsamer Artikel.
Das Ding steigt also jährlich um 17% im Umsatz.
Heute ist allerdings der Umsatz noch bei 0. So kann ich da nicht so richtig was draus ziehen.....
Das Ding steigt also jährlich um 17% im Umsatz.
Heute ist allerdings der Umsatz noch bei 0. So kann ich da nicht so richtig was draus ziehen.....
Antwort auf Beitrag Nr.: 35.115.182 von eck64 am 15.09.08 16:39:57Updated Survival Data from Three Phase 2 Ipilimumab Studies Showed Almost Half of Previously Treated Metastatic Melanoma Patients Alive Beyond One Year
Bristol-Myers Squibb Company (NYSE: BMY) and Medarex, Inc. (NASDAQ: MEDX) today announced updated survival data from three Phase 2 studies of ipilimumab in patients with advanced metastatic melanoma (Stage III or IV) who had previously been treated. Study results show that approximately half of patients who received ipilimumab (10 mg/kg) remained alive beyond one year.
The results are based on follow-up of the patient population from studies 008, 022 and 007 treated with 10 mg/kg of ipilimumab (induction and maintenance) and show a consistent one-year survival rate between 47 and 51 percent. Specifically, the results show:
-- One-year survival rate of 47 percent in patients who had progressed while on or after receiving standard treatment (Study 008, Abstract #776PD);
-- One-year survival rate of 48 percent in patients who were previously treated, relapsed or failed to respond to experimental treatment or were unable to tolerate currently approved therapies (Study 022, Abstract #769O);
-- One-year survival rate of 51 percent in patients previously treated with therapy other than ipilimumab (Study 007, Abstract #778PD).
Follow-up for survival was up to 24.8, 21.88 and 26.32 months in studies 008, 022 and 007, respectively.
Recent medical literature based on a meta-analysis of 42 Phase 2 trials with 2,100 patients reported a one-year survival rate of approximately 25 percent for patients with Stage III or IV metastatic melanoma, the most advanced type of the disease(1).
"Currently, there are few treatment options available for patients with advanced melanoma," said Michele Maio, M.D., Ph.D. Director, Division of Medical Oncology and Immunotherapy, University Hospital of Siena. "As these data on ipilimumab continue to mature, we are encouraged by the durability of response and consistency of survival results observed across all three Phase 2 studies."
Safety results from the three studies were generally consistent with data from previously reported clinical trials of ipilimumab. The most common immune-related adverse events were rash, diarrhea and hepatitis. Grade 3 and 4 immune-related adverse event rates were approximately 20 to 28 percent and zero to 12 percent, respectively, in patients who received 10 mg/kg of ipilimumab. Adverse events were generally manageable and reversible within days or weeks with the use of supportive care and systemic steroids using established treatment guidelines in the majority of patients.
Additional data on efficacy and survival with an active control group will come from an ongoing Phase 3, randomized, double-blind study (024) assessing ipilimumab (10 mg/kg) in combination with dacarbazine (DTIC) versus DTIC alone in patients with untreated, unresectable Stage III or Stage IV metastatic melanoma. A Phase 3 study (029) of ipilimumab administered as adjuvant therapy in patients with high-risk Stage III metastatic melanoma is also currently being conducted.
"We are excited by the consistent one-year survival rates among the three Phase 2 studies," said Geoffrey M. Nichol, MBChB, Senior Vice President of Product Development at Medarex. "Medarex and Bristol-Myers Squibb remain fully committed to the registrational program, including advanced melanoma, adjuvant melanoma, lung and prostate cancer trials."
About Studies 008, 022 and 007
The three studies enrolled a total of 487 patients across North America, Europe, South America, Africa and Australia with Stage III or Stage IV metastatic melanoma treated with 0.3 mg/kg, 3.0 mg/kg or 10 mg/kg of ipilimumab therapy. Approximately half of the patients in each of the trials had stage M1c disease, which indicates that cancer has spread to internal organs. M1c disease can also be associated with an elevated level of serum cholesterol and lactate dehydrogenase (LDH) and is typically indicative of the worst prognosis. Additionally, 10 percent of patients in study 007 had brain metastases at baseline as determined by an Independent Review Committee (IRC). Specifically, the three Phase 2 monotherapy trials include:
-- A Phase 2 open-label, single-arm trial (008) evaluating overall response rate in 155 patients who progressed while on or after receiving standard treatment;
-- A Phase 2 randomized, double-blind trial (022) evaluating the efficacy of three dose levels of ipilimumab in 217 patients who were previously treated, relapsed or failed to respond to experimental treatment or were unable to tolerate currently approved therapies; and
-- A Phase 2 randomized, double-blind trial (007) evaluating the rate of Grade 2+ diarrhea in 115 patients receiving ipilimumab with or without prophylactic oral budesonide.
The primary endpoint of studies 008 and 022 was best overall response rate and the primary endpoint of study 007 was to compare the rate of Grade 2+ diarrhea in patients receiving ipilimumab with or without prophylactic oral budesonide. Overall survival, one-year survival rates, disease control rate, stable disease, and other measurements of anti-tumor activity and patterns of responses were secondary endpoints in studies 008, 022 and 007.
Bristol-Myers Squibb Company (NYSE: BMY) and Medarex, Inc. (NASDAQ: MEDX) today announced updated survival data from three Phase 2 studies of ipilimumab in patients with advanced metastatic melanoma (Stage III or IV) who had previously been treated. Study results show that approximately half of patients who received ipilimumab (10 mg/kg) remained alive beyond one year.
The results are based on follow-up of the patient population from studies 008, 022 and 007 treated with 10 mg/kg of ipilimumab (induction and maintenance) and show a consistent one-year survival rate between 47 and 51 percent. Specifically, the results show:
-- One-year survival rate of 47 percent in patients who had progressed while on or after receiving standard treatment (Study 008, Abstract #776PD);
-- One-year survival rate of 48 percent in patients who were previously treated, relapsed or failed to respond to experimental treatment or were unable to tolerate currently approved therapies (Study 022, Abstract #769O);
-- One-year survival rate of 51 percent in patients previously treated with therapy other than ipilimumab (Study 007, Abstract #778PD).
Follow-up for survival was up to 24.8, 21.88 and 26.32 months in studies 008, 022 and 007, respectively.
Recent medical literature based on a meta-analysis of 42 Phase 2 trials with 2,100 patients reported a one-year survival rate of approximately 25 percent for patients with Stage III or IV metastatic melanoma, the most advanced type of the disease(1).
"Currently, there are few treatment options available for patients with advanced melanoma," said Michele Maio, M.D., Ph.D. Director, Division of Medical Oncology and Immunotherapy, University Hospital of Siena. "As these data on ipilimumab continue to mature, we are encouraged by the durability of response and consistency of survival results observed across all three Phase 2 studies."
Safety results from the three studies were generally consistent with data from previously reported clinical trials of ipilimumab. The most common immune-related adverse events were rash, diarrhea and hepatitis. Grade 3 and 4 immune-related adverse event rates were approximately 20 to 28 percent and zero to 12 percent, respectively, in patients who received 10 mg/kg of ipilimumab. Adverse events were generally manageable and reversible within days or weeks with the use of supportive care and systemic steroids using established treatment guidelines in the majority of patients.
Additional data on efficacy and survival with an active control group will come from an ongoing Phase 3, randomized, double-blind study (024) assessing ipilimumab (10 mg/kg) in combination with dacarbazine (DTIC) versus DTIC alone in patients with untreated, unresectable Stage III or Stage IV metastatic melanoma. A Phase 3 study (029) of ipilimumab administered as adjuvant therapy in patients with high-risk Stage III metastatic melanoma is also currently being conducted.
"We are excited by the consistent one-year survival rates among the three Phase 2 studies," said Geoffrey M. Nichol, MBChB, Senior Vice President of Product Development at Medarex. "Medarex and Bristol-Myers Squibb remain fully committed to the registrational program, including advanced melanoma, adjuvant melanoma, lung and prostate cancer trials."
About Studies 008, 022 and 007
The three studies enrolled a total of 487 patients across North America, Europe, South America, Africa and Australia with Stage III or Stage IV metastatic melanoma treated with 0.3 mg/kg, 3.0 mg/kg or 10 mg/kg of ipilimumab therapy. Approximately half of the patients in each of the trials had stage M1c disease, which indicates that cancer has spread to internal organs. M1c disease can also be associated with an elevated level of serum cholesterol and lactate dehydrogenase (LDH) and is typically indicative of the worst prognosis. Additionally, 10 percent of patients in study 007 had brain metastases at baseline as determined by an Independent Review Committee (IRC). Specifically, the three Phase 2 monotherapy trials include:
-- A Phase 2 open-label, single-arm trial (008) evaluating overall response rate in 155 patients who progressed while on or after receiving standard treatment;
-- A Phase 2 randomized, double-blind trial (022) evaluating the efficacy of three dose levels of ipilimumab in 217 patients who were previously treated, relapsed or failed to respond to experimental treatment or were unable to tolerate currently approved therapies; and
-- A Phase 2 randomized, double-blind trial (007) evaluating the rate of Grade 2+ diarrhea in 115 patients receiving ipilimumab with or without prophylactic oral budesonide.
The primary endpoint of studies 008 and 022 was best overall response rate and the primary endpoint of study 007 was to compare the rate of Grade 2+ diarrhea in patients receiving ipilimumab with or without prophylactic oral budesonide. Overall survival, one-year survival rates, disease control rate, stable disease, and other measurements of anti-tumor activity and patterns of responses were secondary endpoints in studies 008, 022 and 007.
Also nächstes Jahr auch nicht profitabel

Seit Tagen immer das gleiche Spiel. Nach Börsenschluß wird Medarex immer wieder runtergezogen. Von der meist guten Intradayentwicklung bleibt nix übrig.


Hier ist ja nichts mehr los.
Habe mir gestern gegen Schluss noch ein paar zu 4,25€ gekauft.
Habe mir gestern gegen Schluss noch ein paar zu 4,25€ gekauft.

Antwort auf Beitrag Nr.: 35.410.343 von Icanfly am 04.10.08 16:15:00Wo willst Du die denn bekommen haben - für den Kurs?
Bist Du sicher, dass Du sie auch im Depot hast?
Als ich mir vorhin den Endkurs in Amiland ansah (Tiefstkurs von Juni durchbrochen), überlegte ich, ob das jetzt ein guter Zeitpunkt wäre. "Könnte" von der Unterkante des mittelfristigen Kanals (seit April08) abprallen (bei ca. 5,50$).
Ich warte lieber die nächsten paar Tage noch ab (muss ich nun ja auch).
Ist ca. auf dem Niveau von Dez 03. Und Fundamentales zählt im Moment sowie nicht. Schau Dir mal Porsche und VW an.

Gruß
Zock
Bist Du sicher, dass Du sie auch im Depot hast?

Als ich mir vorhin den Endkurs in Amiland ansah (Tiefstkurs von Juni durchbrochen), überlegte ich, ob das jetzt ein guter Zeitpunkt wäre. "Könnte" von der Unterkante des mittelfristigen Kanals (seit April08) abprallen (bei ca. 5,50$).
Ich warte lieber die nächsten paar Tage noch ab (muss ich nun ja auch).

Ist ca. auf dem Niveau von Dez 03. Und Fundamentales zählt im Moment sowie nicht. Schau Dir mal Porsche und VW an.


Gruß
Zock
Antwort auf Beitrag Nr.: 35.411.316 von Zock1000 am 04.10.08 17:59:44Gestern Abend über L%S
Sind auch in meinem Depot
Sind auch in meinem Depot

Antwort auf Beitrag Nr.: 35.411.316 von Zock1000 am 04.10.08 17:59:44Schau Dir mal Porsche und VW an
VW hatte ich mal 300 Stck zu 29€



VW hatte ich mal 300 Stck zu 29€




Für ein Unternehmen mit Nichtspitzenstellung von Pipeline bis Technologie immer noch eine satte Marktkapitalisierung
Immerhin gibts noch Kurse

Immerhin gibts noch Kurse

Und wenn du denkst es geht nich mehr tiefer, dann setzt Medx einen drauf....
Ist heute Weihnachten

Antwort auf Beitrag Nr.: 35.748.270 von Friseuse am 29.10.08 15:33:57Ich bin seit 3,50 drin
antwort sicher nicht
antwort sicher nicht
Endlich mal ein paar gute News von Medarex. Medarex zeigt in den Ergebnissen einer Phase II Studie, dass Antikörper auch Potential ausserhalb klassischer Indikationen wie krebs und Autoimmun haben. Hier geht es konkret um ein Bakterium, das Durchfall verursacht. Standardtherapie ist Antibiotikum. Allerdings ist die Rückfallquote hoch. Medarex zielt mit seinen zwei Antikörpern nicht gegen das Bakterium selbst gegen die Gifte d.h. Toxine der Bakterien und erreicht signifikant bessere Ergebnisse hinsichtlich der Rückfallquoten.
------------------------------------
Medarex and Massachusetts Biologic Laboratories Announce Primary Objective Achieved in Phase 2 Trial of Monoclonal Antibody Combination for the Treatment of Clostridium difficile Associated Diarrhea (CDAD)
Monday November 3, 7:00 am ET
Top-line data from randomized, double-blind, placebo controlled Phase 2 clinical trial indicate statistically significant reduction in recurrences of CDAD
PRINCETON, N.J. and JAMAICA PLAIN, Mass., Nov. 3 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) and The Massachusetts Biologic Laboratories (MBL) of the University of Massachusetts Medical School (UMMS) today announced that a Phase 2 trial of an anti-C. difficile antibody combination treatment in patients with C. difficile Associated Diarrhea (CDAD) successfully met its primary objective. The top-line results from the recently completed multi- center, randomized, double-blind, placebo-controlled Phase 2 trial indicated a statistically significant reduction in recurrences of CDAD when compared with placebo. In the study, 200 patients symptomatic with CDAD receiving standard of care antibiotics (metronidazole or vancomycin) were randomized to receive either intravenous placebo or intravenous administration of a combination of MDX-066 (CDA-1) and MDX-1388 (CDB-1), two fully human antibodies that neutralize C. difficile toxins A and B, respectively.
Consistent with the published literature, the recurrence rate in the placebo-treated group exceeded 20 percent for patients following successful treatment with standard of care antibiotics. In comparison with placebo, MDX- 066/MDX-1388 treatment reduced recurrence rates by approximately 70 percent (p=0.0004 on the intent-to-treat population). The antibody combination treatment was generally safe and well-tolerated. Full results from this Phase 2 trial are planned to be presented at a future scientific meeting.
The incidence and mortality associated with CDAD has been increasing(1), with estimates of over 500,000 cases in the United States, and approximately 15,000 deaths caused or contributed by C. difficile.(2) The emergence of a highly virulent epidemic strain that produces much higher levels of toxins A and B has also been associated with morbidity and mortality in younger, healthier, and non-hospitalized patients.(3)
"We are delighted with these dramatic results. CDAD is a growing and serious epidemic, with twenty to fifty percent of hospitalized patients relapsing after receiving antibiotic treatment," said Donna Ambrosino, MD, Executive Director of the MBL and Professor of Pediatrics at UMMS. "The demonstration of significant protection from relapse indicates that treatment with monoclonal antibodies against the toxins could reduce this significant and costly public health problem."
"These results highlight the exquisite specificity of monoclonal antibodies and their important role to save lives," said Howard H. Pien, President and CEO of Medarex. "We believe that the strength of our antibody technology platform for generating potentially important treatment options, such as the C. difficile program antibodies, will continue to shape the future of medicine. Furthermore, Medarex's strategy of proving the utility of potentially promising candidates for development by well-designed and well- executed studies is amply demonstrated."
------------------------------------
Medarex and Massachusetts Biologic Laboratories Announce Primary Objective Achieved in Phase 2 Trial of Monoclonal Antibody Combination for the Treatment of Clostridium difficile Associated Diarrhea (CDAD)
Monday November 3, 7:00 am ET
Top-line data from randomized, double-blind, placebo controlled Phase 2 clinical trial indicate statistically significant reduction in recurrences of CDAD
PRINCETON, N.J. and JAMAICA PLAIN, Mass., Nov. 3 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) and The Massachusetts Biologic Laboratories (MBL) of the University of Massachusetts Medical School (UMMS) today announced that a Phase 2 trial of an anti-C. difficile antibody combination treatment in patients with C. difficile Associated Diarrhea (CDAD) successfully met its primary objective. The top-line results from the recently completed multi- center, randomized, double-blind, placebo-controlled Phase 2 trial indicated a statistically significant reduction in recurrences of CDAD when compared with placebo. In the study, 200 patients symptomatic with CDAD receiving standard of care antibiotics (metronidazole or vancomycin) were randomized to receive either intravenous placebo or intravenous administration of a combination of MDX-066 (CDA-1) and MDX-1388 (CDB-1), two fully human antibodies that neutralize C. difficile toxins A and B, respectively.
Consistent with the published literature, the recurrence rate in the placebo-treated group exceeded 20 percent for patients following successful treatment with standard of care antibiotics. In comparison with placebo, MDX- 066/MDX-1388 treatment reduced recurrence rates by approximately 70 percent (p=0.0004 on the intent-to-treat population). The antibody combination treatment was generally safe and well-tolerated. Full results from this Phase 2 trial are planned to be presented at a future scientific meeting.
The incidence and mortality associated with CDAD has been increasing(1), with estimates of over 500,000 cases in the United States, and approximately 15,000 deaths caused or contributed by C. difficile.(2) The emergence of a highly virulent epidemic strain that produces much higher levels of toxins A and B has also been associated with morbidity and mortality in younger, healthier, and non-hospitalized patients.(3)
"We are delighted with these dramatic results. CDAD is a growing and serious epidemic, with twenty to fifty percent of hospitalized patients relapsing after receiving antibiotic treatment," said Donna Ambrosino, MD, Executive Director of the MBL and Professor of Pediatrics at UMMS. "The demonstration of significant protection from relapse indicates that treatment with monoclonal antibodies against the toxins could reduce this significant and costly public health problem."
"These results highlight the exquisite specificity of monoclonal antibodies and their important role to save lives," said Howard H. Pien, President and CEO of Medarex. "We believe that the strength of our antibody technology platform for generating potentially important treatment options, such as the C. difficile program antibodies, will continue to shape the future of medicine. Furthermore, Medarex's strategy of proving the utility of potentially promising candidates for development by well-designed and well- executed studies is amply demonstrated."
Golimumab und Ustekinumab werden ab 2009 den Revenuestream bei Medarex kräftig aufpeppen. 3 bis 5% auf zu erwartende Blockbuster-Sales könnten genug sein um an den Rande des Break Even zu gelangen.
http://www.aerztezeitung.de/medizin/krankheiten/skelett_und_…
http://www.aerztezeitung.de/medizin/?sid=513651
Richtig verdient werden soll dann aber mit den eigenen Produkten, die ab 2010/2011 den Markt erreichen könnten.
http://www.aerztezeitung.de/medizin/krankheiten/skelett_und_…
http://www.aerztezeitung.de/medizin/?sid=513651
Richtig verdient werden soll dann aber mit den eigenen Produkten, die ab 2010/2011 den Markt erreichen könnten.
CNTO-95 Phase II ist abgeschlossen. CNTO-95 sollte das nächste Projekt sein, das in Phase III geht. Die Pipeline wächst - trotz Rückschlägen!
---------------------------------
Medarex Receives Milestone Payment for Investigational Antibody Targeting Integrin Receptors
Wednesday November 5, 6:00 am ET
PRINCETON, N.J., Nov. 5 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) today announced that it has received a milestone payment of an undisclosed amount from its licensing partner, Centocor R&D Inc., for the completion of a Phase 2 trial of CNTO 95, a fully human antibody targeting the integrin receptors that are implicated in tumor-induced angiogenesis. The CNTO 95 human antibody was generated using Medarex's UltiMAb® technology. Medarex may receive future milestone payments and royalties should this product candidate progress to commercialization and achieve commercial sales.
"We are pleased with the progress of this program and the potential of technology licensing programs under our partnership with Centocor to contribute to future revenues," said Howard H. Pien, President and CEO of Medarex.
---------------------------------
Medarex Receives Milestone Payment for Investigational Antibody Targeting Integrin Receptors
Wednesday November 5, 6:00 am ET
PRINCETON, N.J., Nov. 5 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) today announced that it has received a milestone payment of an undisclosed amount from its licensing partner, Centocor R&D Inc., for the completion of a Phase 2 trial of CNTO 95, a fully human antibody targeting the integrin receptors that are implicated in tumor-induced angiogenesis. The CNTO 95 human antibody was generated using Medarex's UltiMAb® technology. Medarex may receive future milestone payments and royalties should this product candidate progress to commercialization and achieve commercial sales.
"We are pleased with the progress of this program and the potential of technology licensing programs under our partnership with Centocor to contribute to future revenues," said Howard H. Pien, President and CEO of Medarex.
Antwort auf Beitrag Nr.: 35.811.372 von Ville7 am 03.11.08 15:26:10Das hört sich ja erst einmal nicht schlecht an.
Die Informationen sind aber wahrscheinlich in der kürzlichen Erholung der Aktie auf 6€ schon eingepreist.
Die Informationen sind aber wahrscheinlich in der kürzlichen Erholung der Aktie auf 6€ schon eingepreist.
Antwort auf Beitrag Nr.: 35.840.710 von Pete the Rabbit am 05.11.08 15:33:58Die Informationen sind aber wahrscheinlich in der kürzlichen Erholung der Aktie auf 6€ schon eingepreist.
Bei den derzeitigen Bewertungsmasstäben in der Finanzmarktkrise gut möglich. Diese werden sich aber auch wieder ändern. Und schliesslich gibt es ja auch noch mehr Projekte in der Pipeline.
Z.b. die Eigenentwicklung MDX-1100 mit Target anti-IP10, Phase II Ergebnisse sollten in HJ1 2009 kommen. Von ipilimumab Phase III und weitere Phase II Studien nicht zu reden, Ergebnisse Ende 2009.
Pipeline:
http://www.medarex.com/Development/Pipeline.htm
Bei den derzeitigen Bewertungsmasstäben in der Finanzmarktkrise gut möglich. Diese werden sich aber auch wieder ändern. Und schliesslich gibt es ja auch noch mehr Projekte in der Pipeline.
Z.b. die Eigenentwicklung MDX-1100 mit Target anti-IP10, Phase II Ergebnisse sollten in HJ1 2009 kommen. Von ipilimumab Phase III und weitere Phase II Studien nicht zu reden, Ergebnisse Ende 2009.
Pipeline:
http://www.medarex.com/Development/Pipeline.htm
Nun vermeldet das 3. Partnerprodukt ACZ885 mit Target IL-1β (sehr) gute Phase III Ergebnisse. In 2010 könnten dann 3 Partnermedikamente von Medarex am Markt sein.
http://www.novartis.com/newsroom/media-releases/en/2008/1263…
http://www.novartis.com/newsroom/media-releases/en/2008/1263…
Antwort auf Beitrag Nr.: 35.841.095 von Ville7 am 05.11.08 15:58:38Alles eingepreist?
Bei den derzeitigen Bewertungsmasstäben in der Finanzmarktkrise gut möglich. Diese werden sich aber auch wieder ändern.

Im Herbst 07 stieg der Kurs noch bis 18 USD hoch.
Aktuell muss man wohl froh sein, dass der Kurs sich wieder von gut 4 auf gut 6 erholt hat.
Das ist aktuell eine Marktakpitalisierung von 845 mio USD.
Wenn man das mit der pipeline (eigene Projekte und mit Partnern) abgleicht ist es geradezu lächerlich, was der Finanzmarkt in Summe einpreist.
Die Übernahmepreise sind jedenfalls in anderen Größenordnungen. Teilweise werden Firmen mit Präklinik-Projekten für satt dreistellige Millionenbeträge übernommen.
Bei den derzeitigen Bewertungsmasstäben in der Finanzmarktkrise gut möglich. Diese werden sich aber auch wieder ändern.
Im Herbst 07 stieg der Kurs noch bis 18 USD hoch.
Aktuell muss man wohl froh sein, dass der Kurs sich wieder von gut 4 auf gut 6 erholt hat.
Das ist aktuell eine Marktakpitalisierung von 845 mio USD.
Wenn man das mit der pipeline (eigene Projekte und mit Partnern) abgleicht ist es geradezu lächerlich, was der Finanzmarkt in Summe einpreist.
Die Übernahmepreise sind jedenfalls in anderen Größenordnungen. Teilweise werden Firmen mit Präklinik-Projekten für satt dreistellige Millionenbeträge übernommen.

Antwort auf Beitrag Nr.: 35.881.953 von eck64 am 08.11.08 11:23:06In Zeiten in denen Biotechs mit fortgeschrittenen Pipelines unter Cash und ohne Schulden an der Börse gehandelt werden gelten eben andere Bewertungsmasstäbe.
Das steht in keinem Verhältnis zu so manchen Deals. Ich erwarte daher auch ein reichliches M&A Aufkommen sobald sich der Höhepunkt der Finanzkrise dem Ende neigt.
Das steht in keinem Verhältnis zu so manchen Deals. Ich erwarte daher auch ein reichliches M&A Aufkommen sobald sich der Höhepunkt der Finanzkrise dem Ende neigt.
Antwort auf Beitrag Nr.: 35.900.291 von Ville7 am 10.11.08 11:35:34Hier ist die Marktkapitalisierung weit über Cash und das bei einem chronischen Burnout. Selbst bei noch zu verklatschenden Beteiligungen ändert sich das nicht wirklich. Fies ist die Nennung von Celldex und Genmab i.d.Zshg schon.
Was macht eigentlich der Drakeman
Was macht eigentlich der Drakeman

Antwort auf Beitrag Nr.: 35.900.291 von Ville7 am 10.11.08 11:35:34Ist jemand mal zufällig über neuere Infos zu CNTO-1275 bzw CNTO 148 gestossen? Gibts Updates zu den Zulassungsverfahren? BLA für CNTO-1275 wurde 11/07 beantragt und es gibt immer noch keine Entscheidung.  Das wär doch mal ein Lebenszeichen
Das wär doch mal ein Lebenszeichen 
lG
Lycos
 Das wär doch mal ein Lebenszeichen
Das wär doch mal ein Lebenszeichen 
lG
Lycos
ustekinumab (aus dem Yahoo MSG-Board)
Beerse, Belgium, November 21 (ots/PRNewswire) - Janssen-Cilag announced today that ustekinumab, the first in a new class of biologics, has received a positive opinion for the treatment of moderate to severe plaque psoriasis from the European Committee for Medical Products for Human Use (CHMP).
**************
**************
News von Novartis (ich weiß, nicht mehr ganz neu - aber zur Info
Somit also bald der nächste Mab in der Zulassungsphase. Mal sehen..
ACZ885 (canakinumab) is a new treatment for a group of rare, but potentially life-threatening, auto-inflammatory diseases called Cryopyrin-Associated Periodic Syndromes (CAPS), which includes Muckle-Wells Syndrome. The first submissions were previously planned for 2009, but are being moved forward to the end of 2008 after data from two clinical studies showed adults and children achieved rapid and long-lasting clinical remission of these diseases. Orphan drug status has already been granted to ACZ885 in the European Union and US for treating CAPS, and also in the US and EU for Systemic Juvenile Idiopathic Arthritis (SJIA), the most severe form of arthritis in children. Phase III trials in SJIA are set to begin in 2009. Studies are also either underway or are planned to start in patients with gout (Phase II started in 2008), adult rheumatoid arthritis (Phase III start in 2010) and type 2 diabetes (Phase II start in 2009).
(www.novartis.com/newsroom/media-releases...
Beerse, Belgium, November 21 (ots/PRNewswire) - Janssen-Cilag announced today that ustekinumab, the first in a new class of biologics, has received a positive opinion for the treatment of moderate to severe plaque psoriasis from the European Committee for Medical Products for Human Use (CHMP).
**************
**************
News von Novartis (ich weiß, nicht mehr ganz neu - aber zur Info

Somit also bald der nächste Mab in der Zulassungsphase. Mal sehen..
ACZ885 (canakinumab) is a new treatment for a group of rare, but potentially life-threatening, auto-inflammatory diseases called Cryopyrin-Associated Periodic Syndromes (CAPS), which includes Muckle-Wells Syndrome. The first submissions were previously planned for 2009, but are being moved forward to the end of 2008 after data from two clinical studies showed adults and children achieved rapid and long-lasting clinical remission of these diseases. Orphan drug status has already been granted to ACZ885 in the European Union and US for treating CAPS, and also in the US and EU for Systemic Juvenile Idiopathic Arthritis (SJIA), the most severe form of arthritis in children. Phase III trials in SJIA are set to begin in 2009. Studies are also either underway or are planned to start in patients with gout (Phase II started in 2008), adult rheumatoid arthritis (Phase III start in 2010) and type 2 diabetes (Phase II start in 2009).
(www.novartis.com/newsroom/media-releases...
Scheinbar eine No News

Die Höchststrafe an Aktie ist Xoma, da kann Forschung sein wie auch immer und stets fehlts an wirtschaftlich angewendeten Grundrechenarten.

Kann der neue Medarexchef mal was auf den Teller bringen
Kann der neue Medarexchef mal was auf den Teller bringen

Lösen die sich auf oder hats die nicht gegeben

Wer weiß

Wer weiß

Antwort auf Beitrag Nr.: 35.979.372 von Friseuse am 17.11.08 17:05:07Ja das ist richtig, Medarex notierte nicht unter Cash. Hab ich auch nicht gesagt.
Medarex wird bald zwei Blockbuster-Partner-Medikamente am Markt haben und ca. 3% daran profitieren. Das dürfte mittelfrstig für den break even reichen.
ipilimumab. Wenn es ein Erfolg wird, dann kommt Gewinn zur bottom line. Wenn nicht, dann hört mit der Einstellung dann wenigstens der massive Cash burn auf. Das wäre dann aber alles andere als glücklich, hat man ja bereits mehrere 100 Millionen reininvestiert - der Kurs käme dann so schnell nicht mehr ans Laufen. Im Falle eines Erfolgs von ipilimumab wird Medarex recht schnell an BMS gehen.
Drakeman lebt sehr gut, schliesslich hat er die besten Assets seiner Frau zugeschustert und sich selbst fetteste Optionen gegönnt.
Medarex wird bald zwei Blockbuster-Partner-Medikamente am Markt haben und ca. 3% daran profitieren. Das dürfte mittelfrstig für den break even reichen.
ipilimumab. Wenn es ein Erfolg wird, dann kommt Gewinn zur bottom line. Wenn nicht, dann hört mit der Einstellung dann wenigstens der massive Cash burn auf. Das wäre dann aber alles andere als glücklich, hat man ja bereits mehrere 100 Millionen reininvestiert - der Kurs käme dann so schnell nicht mehr ans Laufen. Im Falle eines Erfolgs von ipilimumab wird Medarex recht schnell an BMS gehen.
Drakeman lebt sehr gut, schliesslich hat er die besten Assets seiner Frau zugeschustert und sich selbst fetteste Optionen gegönnt.
Antwort auf Beitrag Nr.: 36.080.594 von Friseuse am 26.11.08 20:44:51Xoma ist in spätestens zwei Quartalen pleite wenn sie so weiter machen. Sie haben nur noch 10Mio Cash bei 10 Mio Cashburn pro Quartal.
Medarex hat bei derzeitigem Cashburn noch zweieinhalb Jahre Cash, Einnahmen durch Ustekinumab und Golimumab nicht eingerechnet. Ein Pleitegehen schliesse ich hier mittelfristig aus.
Medarex hat bei derzeitigem Cashburn noch zweieinhalb Jahre Cash, Einnahmen durch Ustekinumab und Golimumab nicht eingerechnet. Ein Pleitegehen schliesse ich hier mittelfristig aus.
Hallo Ville,
Ich kenne deine Beiträge aus den Yahoo Board... schätze Sie sehr.

ich hab mich mal auch hier angemeldet. Weil das ja im deutschen Bereich das einzige Board ist, wo man sich zu Medarex austauschen kann.
Hast du oder jemand anderes eine Ahnung ob Medarex auch für die außer US Umsätze von dem neuen Psoriasis MAb royalties bekommt.
Das Ding wird ja groß werden... [arbeite im medizin. Bereich... und kann das ein wenig einschätzen]
... ich befürchte nur das wir nur was von den Umsätzen in der USA bekommen werden. Das wäre "mit Verlaub" Be... für uns Aktienbesitzer...
Ich bin gespannt nä. Jahr auf die results von der Phase II von MDX 1100...
dieser Mab ist sehr interessant...
So... noch etwas Off Topic... ist hier jemand auch in genmab investiert?! Du vielleich Ville!?
Würde mich interessieren...
Ich hab mein Risiko gestreut und bin auch voll in Genmab reingegangen.... zumal die Dänen ja die besten Stücke von Medarex bekommen haben...
und bin auch voll in Genmab reingegangen.... zumal die Dänen ja die besten Stücke von Medarex bekommen haben...
Thank you Donald!
Gruß where_is_the_beef
Ich kenne deine Beiträge aus den Yahoo Board... schätze Sie sehr.

ich hab mich mal auch hier angemeldet. Weil das ja im deutschen Bereich das einzige Board ist, wo man sich zu Medarex austauschen kann.
Hast du oder jemand anderes eine Ahnung ob Medarex auch für die außer US Umsätze von dem neuen Psoriasis MAb royalties bekommt.
Das Ding wird ja groß werden... [arbeite im medizin. Bereich... und kann das ein wenig einschätzen]
... ich befürchte nur das wir nur was von den Umsätzen in der USA bekommen werden. Das wäre "mit Verlaub" Be... für uns Aktienbesitzer...
Ich bin gespannt nä. Jahr auf die results von der Phase II von MDX 1100...
dieser Mab ist sehr interessant...
So... noch etwas Off Topic... ist hier jemand auch in genmab investiert?! Du vielleich Ville!?
Würde mich interessieren...
Ich hab mein Risiko gestreut
 und bin auch voll in Genmab reingegangen.... zumal die Dänen ja die besten Stücke von Medarex bekommen haben...
und bin auch voll in Genmab reingegangen.... zumal die Dänen ja die besten Stücke von Medarex bekommen haben...Thank you Donald!
Gruß where_is_the_beef
Antwort auf Beitrag Nr.: 36.119.674 von where_is_the_beef am 30.11.08 19:05:33Hallo were_is_the_beef,
Mein Stand ist, dass Medarex auf alle weltweiten Verkäufe von Ustekinumab und Golimumab Royalties bekommt - geht auch nichts anderes aus deren GB hervor. Zwischen 2-4%, die meisten Analysten nennen 'nur' 2,5%. Nicht viel, aber bei Medikamenten, die in ihren wenigen bisherigen Indikationen klar besser als mehrere derzeitige Multimilliarden-USD Blockbuster (gleichen Targets) sind summiert sich das auf, wenn mal das Potential abgerufen und in die Nähe der Peaksales gekommen wird.
Kannst du erläutern, was im Speziellen für dich den anti-IP-10 Antikörper so interessant macht? Weil du das Target aussichtsreich hälst oder weil es eben der nächste spannende potentielle Werttreiber bei Medarex ist?
Mein Genmab Engagement ist klein, aber vorhanden. Ich versuche den Antikörper-Zukunftsmarkt zum größten Teil über Morphosys und Medarex zu spielen. Im Falle von Medarex kurzfristig gesehen noch recht suboptimal. Aber was nicht ist wird hoffentlich noch.
Mein Stand ist, dass Medarex auf alle weltweiten Verkäufe von Ustekinumab und Golimumab Royalties bekommt - geht auch nichts anderes aus deren GB hervor. Zwischen 2-4%, die meisten Analysten nennen 'nur' 2,5%. Nicht viel, aber bei Medikamenten, die in ihren wenigen bisherigen Indikationen klar besser als mehrere derzeitige Multimilliarden-USD Blockbuster (gleichen Targets) sind summiert sich das auf, wenn mal das Potential abgerufen und in die Nähe der Peaksales gekommen wird.
Kannst du erläutern, was im Speziellen für dich den anti-IP-10 Antikörper so interessant macht? Weil du das Target aussichtsreich hälst oder weil es eben der nächste spannende potentielle Werttreiber bei Medarex ist?
Mein Genmab Engagement ist klein, aber vorhanden. Ich versuche den Antikörper-Zukunftsmarkt zum größten Teil über Morphosys und Medarex zu spielen. Im Falle von Medarex kurzfristig gesehen noch recht suboptimal. Aber was nicht ist wird hoffentlich noch.
PDUFA Date (spätestes Entscheidungsdatum der FDA über Zulassung) ist übrigens für
Ustekinumab: Ende Dezember 08
Golimumab: Ende März 09
Für ACZ885 will Novartis noch 2008 einen BLA stellen. Mit Fast Track bedeutet dies PDUFA Ende Juni 09.
Wir werden also möglicherweise die nächsten drei Quartale (beginnend mit diesem) je eine Zulassung eines Medarex Partner-AKs in USA erleben. So schlechte Aussichten sind das m.E. auch wieder nicht.
Parallel dann die Zulassungsentscheidungen in Europa.
Ustekinumab: Ende Dezember 08
Golimumab: Ende März 09
Für ACZ885 will Novartis noch 2008 einen BLA stellen. Mit Fast Track bedeutet dies PDUFA Ende Juni 09.
Wir werden also möglicherweise die nächsten drei Quartale (beginnend mit diesem) je eine Zulassung eines Medarex Partner-AKs in USA erleben. So schlechte Aussichten sind das m.E. auch wieder nicht.
Parallel dann die Zulassungsentscheidungen in Europa.
Antwort auf Beitrag Nr.: 36.120.668 von Ville7 am 01.12.08 03:47:08Morgen Ville...
Also fangen wir mal an.
Ich arbeite auf einer Rheumastation + angeschlossener Studienabteilung.
Da wir regelmäßig Rituximab off Label gegen alle mgl. seltsamen Rheuma Erkrankungen geben.
Da hab ich mir gedacht.. ich profitiere davon das Ofmatumab der potentielle nachfolger sein wird.
Ich glaube fest an den Erfolg. Ofmatumab ist voll human, die Dänen haben die Bindungsstruktur verbessert und scheinbar "was heutzutage" mit entscheidend ist
wohl vernünftige klinische Studien mit entsprechenden Pat.Anzahl gestartet.
Außerdem ist das halt auch Medarex Core Technology!
Rituximab ist 10 Jahre alt => Time for change! :-)
Gott.. wo würden wir stehen, wenn Old Donald nicht das alles ans sein Ehweib verschachert hätte!
Gott sei Dank bin ich investiert... Genmab halt mein Port. noch so etwas über Wasser! :-)
anti-IP-10 (CXCL10) ist deswegen interessant, da Medarex der Phase II Mittelbau in der Pipeline fehlt!
IPI ist unsicher, ob er funktioniert. Ich glaube dran.. ist aber halt ein völliger neuer Therapieansatz.
"Entfessel das Immunsystem...."
MDX-1100 ist der einzige interessante Phase II Mab. Soweit ich weiß einer er ersten der CXCL Fanmilie in klinischen Studien.
Die Phase II Studie ist einfach designed, aber wirkungsvoll.
2 Gruppen 106 Pat.
53 Pat. erhalten MDX-1100
53. Pat. bekommen ne NaCl Infusion
Am Ende ist der Efolg sehr gut sichtbar!
Du brauchst in pubmed nur mal CXCL10 eingeben un wirst sehen, wieviele Treffer du bekommst. 1527!
Enorm!
http://www.ncbi.nlm.nih.gov/sites/entrez?db=pubmed&cmd=Detai…
Soweit ich diesen Mab verstehe, ist das auch kein neuer Therapieansatz.
Es wird ein Öberflächenmolekül überexprimiert... Mederax hat dazu den fertigen human AK gebastelt ...
und fertig!.... (Ist jetzt sehr vereinfacht... ich weiss)
Ist aber halt nicht wie IPI... ein neues Behandlungsparadigma!
In Phase I ist Medarex wieder sehr stark... sehr viele hochinteressant Mab!
Aber wir wissen beide das diese noch 8 - 9 Jahre von der Zulassung weg sind.
Morphosys... ist eigentlich ein Muss als Deutscher, wenn man sich für MAb´s interessiert und investiert.
Nur nach dem Novartis Deal ist die Phantasie raus.
Die eigenen Mab sind noch in Phase I... und außerdem auf therapeutischen Gebiet mit starker Konkurrenz... Außerdem hab ich auch keen Geld mehr über!
Hätte eher mich investieren sollen... anyway..
Die Zukunft wird sowieso die Bahndlung von Erkrankungen mit meheren Mabs sein.
Einer gege CD20 + einer gegen CD20 + villeicht ein Immunboster/entfessler (IPI z.b)
oder was gegen Blutgefäße (Avsatin)....
das dauert aber bestimmt noch 10 Jahre bis das voll in der Klinik angekommen ist.
Außerdem ist das ne Kostenfrage.... kostet alles ein Schweinegeld!
Sowas wir hier:
http://clinicaltrials.gov/ct2/show/NCT00790010?term=mdx-010&…
Gruß
Also fangen wir mal an.
Ich arbeite auf einer Rheumastation + angeschlossener Studienabteilung.
Da wir regelmäßig Rituximab off Label gegen alle mgl. seltsamen Rheuma Erkrankungen geben.
Da hab ich mir gedacht.. ich profitiere davon das Ofmatumab der potentielle nachfolger sein wird.
Ich glaube fest an den Erfolg. Ofmatumab ist voll human, die Dänen haben die Bindungsstruktur verbessert und scheinbar "was heutzutage" mit entscheidend ist
wohl vernünftige klinische Studien mit entsprechenden Pat.Anzahl gestartet.
Außerdem ist das halt auch Medarex Core Technology!
Rituximab ist 10 Jahre alt => Time for change! :-)
Gott.. wo würden wir stehen, wenn Old Donald nicht das alles ans sein Ehweib verschachert hätte!
Gott sei Dank bin ich investiert... Genmab halt mein Port. noch so etwas über Wasser! :-)
anti-IP-10 (CXCL10) ist deswegen interessant, da Medarex der Phase II Mittelbau in der Pipeline fehlt!
IPI ist unsicher, ob er funktioniert. Ich glaube dran.. ist aber halt ein völliger neuer Therapieansatz.
"Entfessel das Immunsystem...."
MDX-1100 ist der einzige interessante Phase II Mab. Soweit ich weiß einer er ersten der CXCL Fanmilie in klinischen Studien.
Die Phase II Studie ist einfach designed, aber wirkungsvoll.
2 Gruppen 106 Pat.
53 Pat. erhalten MDX-1100
53. Pat. bekommen ne NaCl Infusion
Am Ende ist der Efolg sehr gut sichtbar!
Du brauchst in pubmed nur mal CXCL10 eingeben un wirst sehen, wieviele Treffer du bekommst. 1527!
Enorm!
http://www.ncbi.nlm.nih.gov/sites/entrez?db=pubmed&cmd=Detai…
Soweit ich diesen Mab verstehe, ist das auch kein neuer Therapieansatz.
Es wird ein Öberflächenmolekül überexprimiert... Mederax hat dazu den fertigen human AK gebastelt ...
und fertig!.... (Ist jetzt sehr vereinfacht... ich weiss)
Ist aber halt nicht wie IPI... ein neues Behandlungsparadigma!
In Phase I ist Medarex wieder sehr stark... sehr viele hochinteressant Mab!
Aber wir wissen beide das diese noch 8 - 9 Jahre von der Zulassung weg sind.
Morphosys... ist eigentlich ein Muss als Deutscher, wenn man sich für MAb´s interessiert und investiert.
Nur nach dem Novartis Deal ist die Phantasie raus.
Die eigenen Mab sind noch in Phase I... und außerdem auf therapeutischen Gebiet mit starker Konkurrenz... Außerdem hab ich auch keen Geld mehr über!
Hätte eher mich investieren sollen... anyway..
Die Zukunft wird sowieso die Bahndlung von Erkrankungen mit meheren Mabs sein.
Einer gege CD20 + einer gegen CD20 + villeicht ein Immunboster/entfessler (IPI z.b)
oder was gegen Blutgefäße (Avsatin)....
das dauert aber bestimmt noch 10 Jahre bis das voll in der Klinik angekommen ist.
Außerdem ist das ne Kostenfrage.... kostet alles ein Schweinegeld!
Sowas wir hier:
http://clinicaltrials.gov/ct2/show/NCT00790010?term=mdx-010&…
Gruß

Fehlen Genmab zur Übernahme die Talers

Medarex hat in Kursen doch gut abgetrottelt

Medarex hat in Kursen doch gut abgetrottelt

Antwort auf Beitrag Nr.: 36.120.668 von Ville7 am 01.12.08 03:47:08Ne kleine Korrektur: Golimumab PDUFA ist erst Ende April 2009. (Filing Ende Juni 2008 plus 10 Monate!)
Antwort auf Beitrag Nr.: 36.121.784 von where_is_the_beef am 01.12.08 10:52:15Danke für deine Einschätzung. Ich sehe auch die Antikörper als die am stärksten wachsende Medikamentenklasse an und habe hier im Biotech/Pharma Bereich den klaren Schwerpunkt gelegt.
2007 war der Antikörpermarkt bei $26 Milliarden. 2013 prognostiziert Datamonitor bereits 50Milliarden. Und all die Prognosen, die ich seit gut zwei Jahren verfolge werden regelmässig nach oben korrigiert, weil der Markt noch weit schneller wächst als zuvor prognostiziert. Und das obwohl die Zulassungsbehörden recht restriktiv geworden sind.
Datamonitor prognostiziert für 2013 sogar weiterhin starkes Wachstum für die bisherigen umstzstärksten mabs (Remicade, Rituxan, Herceptin, Humira, Avastin). Ich bin hier nicht so sicher, ich glaube die neuen Mabs gleichen Targets und verbesserter Funktion werden schneller Track gewinnen als von denen prognostiziert. Die alten anti-TNF-alphas (Remicade, Humira) werden Druck bekommen, ebenso Rituxan. Die neuen mabs sind unterwegs und sie sind besser. Du sprichst es an, Ofatumumab, Golimumab, Ustekinumab etc. Und dahinter eine massive Welle an AKs gegen alle Arten Zytokine, gegen unterschiedlichste Krebstargets in allen möglichen Indikationen. Da kommt ne Menge nach - einiges wird nicht klappen, aber vieles wird funktionieren.
CXL10 oder IPI10 - ich habe mich bisher nur ein klein wenig mit dem Target beschäftigt. Ich bin zwar nicht vom Fach und mehr oder weniger Autodidakt, aber den Ansatz finde auch ich verfolgenswert. Ich bin auch gespannt auf die Phase II Ergebnisse nächstes Jahr.
Ich finde übrigens auch den Ansatz therapeutische AKs gegen Infektionskrankheiten einzusetzen nicht unausichtsreich - um auf den zweiten AK in Phase II anzusprechen. Speziell, wenn nicht das Target selbst sondern beispielsweise Nebenprodukte wie die Bakterientoxine angegriffen werden und somit auch hier Kombinationstherapien entstehen können (z.b. Antibiotika und Antikörper). Antikörper sind wirklich breit einsetzbar.
Die Kombinationen von verschiedenen Antikörpern sind für mich auch der Schlüssel zum erweiterten Marktwachstum der Antikörper. Verschiedene AKs auf unterschiedliche Targets könnten (bin da vorsichtig) über lange Frist etablieterte Chemotherapien ablösen, da sie möglicherweise - selbst in Kombination- ein weit besseres Sicherheitsprofil haben. Oder im Bereich der Autoimmunerkrankungen bessere Ansprechraten erzeugen.
Bezüglich Morphosys: die haben in 2009 zwei bis drei Partner-AKs in der Phase II, dazu ein eigenes Programm MOR103 gegen GM-CSF. Die Pipeline wächst endlich mal los. Sie sind zudem noch hochprofitabel und abgesichert und bieten upside durch Partner- und eigene AKs. M.E. die mittel- bis langfristige und recht risikoarme Variante um den Markt zu spielen.
Was hälst du als "jemand vom Fach" vom anti-GM-CSF Ansatz. Morphosys These ist, dass GM-CSF die Vorstufe diverser Cytokine, inkl. anti-TNF-alpha und IL-x ist.
http://www.morphosys.com/de/therapeutische_antikoerper/firme…
Der Ansatz wurde von der Uni Melbourne entdeckt, hier ein paar Infos aus dem kürzlich erteilten Patent:
http://www.wallstreet-online.de/diskussion/1134050-neustebei…
2007 war der Antikörpermarkt bei $26 Milliarden. 2013 prognostiziert Datamonitor bereits 50Milliarden. Und all die Prognosen, die ich seit gut zwei Jahren verfolge werden regelmässig nach oben korrigiert, weil der Markt noch weit schneller wächst als zuvor prognostiziert. Und das obwohl die Zulassungsbehörden recht restriktiv geworden sind.
Datamonitor prognostiziert für 2013 sogar weiterhin starkes Wachstum für die bisherigen umstzstärksten mabs (Remicade, Rituxan, Herceptin, Humira, Avastin). Ich bin hier nicht so sicher, ich glaube die neuen Mabs gleichen Targets und verbesserter Funktion werden schneller Track gewinnen als von denen prognostiziert. Die alten anti-TNF-alphas (Remicade, Humira) werden Druck bekommen, ebenso Rituxan. Die neuen mabs sind unterwegs und sie sind besser. Du sprichst es an, Ofatumumab, Golimumab, Ustekinumab etc. Und dahinter eine massive Welle an AKs gegen alle Arten Zytokine, gegen unterschiedlichste Krebstargets in allen möglichen Indikationen. Da kommt ne Menge nach - einiges wird nicht klappen, aber vieles wird funktionieren.
CXL10 oder IPI10 - ich habe mich bisher nur ein klein wenig mit dem Target beschäftigt. Ich bin zwar nicht vom Fach und mehr oder weniger Autodidakt, aber den Ansatz finde auch ich verfolgenswert. Ich bin auch gespannt auf die Phase II Ergebnisse nächstes Jahr.
Ich finde übrigens auch den Ansatz therapeutische AKs gegen Infektionskrankheiten einzusetzen nicht unausichtsreich - um auf den zweiten AK in Phase II anzusprechen. Speziell, wenn nicht das Target selbst sondern beispielsweise Nebenprodukte wie die Bakterientoxine angegriffen werden und somit auch hier Kombinationstherapien entstehen können (z.b. Antibiotika und Antikörper). Antikörper sind wirklich breit einsetzbar.
Die Kombinationen von verschiedenen Antikörpern sind für mich auch der Schlüssel zum erweiterten Marktwachstum der Antikörper. Verschiedene AKs auf unterschiedliche Targets könnten (bin da vorsichtig) über lange Frist etablieterte Chemotherapien ablösen, da sie möglicherweise - selbst in Kombination- ein weit besseres Sicherheitsprofil haben. Oder im Bereich der Autoimmunerkrankungen bessere Ansprechraten erzeugen.
Bezüglich Morphosys: die haben in 2009 zwei bis drei Partner-AKs in der Phase II, dazu ein eigenes Programm MOR103 gegen GM-CSF. Die Pipeline wächst endlich mal los. Sie sind zudem noch hochprofitabel und abgesichert und bieten upside durch Partner- und eigene AKs. M.E. die mittel- bis langfristige und recht risikoarme Variante um den Markt zu spielen.
Was hälst du als "jemand vom Fach" vom anti-GM-CSF Ansatz. Morphosys These ist, dass GM-CSF die Vorstufe diverser Cytokine, inkl. anti-TNF-alpha und IL-x ist.
http://www.morphosys.com/de/therapeutische_antikoerper/firme…
Der Ansatz wurde von der Uni Melbourne entdeckt, hier ein paar Infos aus dem kürzlich erteilten Patent:
http://www.wallstreet-online.de/diskussion/1134050-neustebei…
Antwort auf Beitrag Nr.: 36.121.784 von where_is_the_beef am 01.12.08 10:52:15Hallo where is the beef,
freut mich, wenn hier weitere Fachkompetenz in den Thread reinkommt.
Ich arbeite auf einer Rheumastation + angeschlossener Studienabteilung.
Wenn man da ab und an von deinen Fachkenntnissen, aber auch den Verfahrensablaufkenntnissen profitieren könnte, wäre das schon toll.
Also zunächst einmal ein herzliches Willkommen.
freut mich, wenn hier weitere Fachkompetenz in den Thread reinkommt.
Ich arbeite auf einer Rheumastation + angeschlossener Studienabteilung.
Wenn man da ab und an von deinen Fachkenntnissen, aber auch den Verfahrensablaufkenntnissen profitieren könnte, wäre das schon toll.
Also zunächst einmal ein herzliches Willkommen.

Antwort auf Beitrag Nr.: 36.123.769 von eck64 am 01.12.08 15:11:22Hallo Alle zusammen,
ich möchte dann doch ein wenig zurückrudern!
Ich arbeite als Krankenpfleger, welcher sich aber seit 2000 (erste Medarex Aktien) gekauft mit dem Thema AK
beschäftigt!
Ergo... ähnlich wir ihr.. auch (teilweise) Audidakt.
Konkrekt bin in der Charite Berlin beschäftigt. Wenn mein Stationsarzt + seine beide OA (beide Profs. natürlich)
rheumatologisch nicht weiter wissen, dann hat man als Pat. ein echtes Problem.
Die stellen quasi das aktuelle, abrufbar Wissen rheumatologisch dar.
Ich habe schon echt ne Menge Mist gesehen, Lupus in Vollausprägung (insbesondere junge Frauen), Sklerodermie, Myosititis..
gibt echt ne Menge Sch...
Auf der selber Station ist auch die Studienabteilung und unsere Ärzte zapfen Unmengen Blut ab... was dann in die Studienabteilung geht. Bzw. wo Assistenzärzte scharf drauf sind, da sie an irgendwas
rumforschen! :-) Alles ganz spannend zum Teil.
Aber auch ganz schön harte Arbeit in meinem Bereich (Pflege).
Könnte mir glauben! :-)
Meine Aufgabe ist es z.B.: die Rituximabinfusion vorzubereiten + die Begleitinjektionen (1. Amp. Fenistil + 1 Amp Dexamethason 8 mg i.v., 1 g Paracetamol p.o) Öfter mal Blutdruck messen... wenn man schafft! :-)
Allen die mit AK arbeiten sollte aber immer bewußt sein, das die Zulassungsstudien ein eng umschriebenen Patientengut haben.
Funktionbiert die Niere nicht => nix Studie
Im harten klinischen Alltag sieht es dann schon wieder anders aus.
Ist ähnlich wie bei den Autoherstellern und dem Benzinverbrauch...
Das sind Verbrauchswerte die im alltäglichen Einsatz nicht so erreicht werden können.!
Trotzdem haben die AK die Therapie von Hogh-kin, Leukämie und Brustkrebs entscheidend zu Gusten der Patienten verbessert!
Und euch die hier regelmäßig posten, wie Ville, oder eck64 sprechen ebenfalls ein entsprechendes Wissen zu.
Ihr habt euch intensiv damit beschäftigt, ergo also auch Ahnung. (Tschuldigung, wenn ich jemanden vergessen habe)
Ich verfolge diesen Thread schon sehr lange... + den Medarex yahoo.com Thread...
Nun zu Morphosys... hab mich echt noch nicht damit intensiv beschäftigt.
Muss eingestehen. Bei MOR ist mir die eigene Pipeline zu schwachbrustig!
MOR202 => CD38 mab... da ist z.B. auch Genmab dran und entwickelt einen AK
MOR103... hmn.. wenn es funktioniert... klingt gut! Aber insbesondere in RA sehr starke Konkurrenz!
Welche schon jahrelang in der Praxis (klinischer Alltag) sind und es kommen auch immer wieder verbessert Ak wie (Golimumab)
eher in die Klinik. Ist noch ein sehr weiter Weg! Und es gehört auch eine riesen Menge Lobbyarbeit ... ähh :-) tschuldigung, Marketing-
aktivitäten neue Konzepte in der Klinik einzuführen! :-)
Nichtdestrotz Mor ist gut geführt, sie machen Gewinn und können den positiven Cashflow in ihre eigenen Projekte stecken.
Viele Biotechs... haben nie und werden die Gewinnschwelle erreichen! Sie haben die kritische Größe + einen etablierten Namen dazu!
Janz großes Plus für MOR...
Siehe meine heißgeliebte...gehaßte Medarex.
Die Vorreiter der AK Industrie. Bekommen vorraussichtlich nach 20 Jahre Forschung ihr erstes Produkt auf den Markt.
:-) Oh man... dieser Mab ist sehr gut... aber good old Medarex bekommt lausige 3 % royalties!
Aber so waren nunmal damals die Verträge...
Ja.. das fetzt... so hab ich mir das vorgestellt... hochinteressanter Thread hier.
Dank an Alle!
Gruß where_is_the_beef
ich möchte dann doch ein wenig zurückrudern!
Ich arbeite als Krankenpfleger, welcher sich aber seit 2000 (erste Medarex Aktien) gekauft mit dem Thema AK
beschäftigt!
Ergo... ähnlich wir ihr.. auch (teilweise) Audidakt.
Konkrekt bin in der Charite Berlin beschäftigt. Wenn mein Stationsarzt + seine beide OA (beide Profs. natürlich)
rheumatologisch nicht weiter wissen, dann hat man als Pat. ein echtes Problem.
Die stellen quasi das aktuelle, abrufbar Wissen rheumatologisch dar.
Ich habe schon echt ne Menge Mist gesehen, Lupus in Vollausprägung (insbesondere junge Frauen), Sklerodermie, Myosititis..
gibt echt ne Menge Sch...
Auf der selber Station ist auch die Studienabteilung und unsere Ärzte zapfen Unmengen Blut ab... was dann in die Studienabteilung geht. Bzw. wo Assistenzärzte scharf drauf sind, da sie an irgendwas
rumforschen! :-) Alles ganz spannend zum Teil.
Aber auch ganz schön harte Arbeit in meinem Bereich (Pflege).
Könnte mir glauben! :-)
Meine Aufgabe ist es z.B.: die Rituximabinfusion vorzubereiten + die Begleitinjektionen (1. Amp. Fenistil + 1 Amp Dexamethason 8 mg i.v., 1 g Paracetamol p.o) Öfter mal Blutdruck messen... wenn man schafft! :-)
Allen die mit AK arbeiten sollte aber immer bewußt sein, das die Zulassungsstudien ein eng umschriebenen Patientengut haben.
Funktionbiert die Niere nicht => nix Studie
Im harten klinischen Alltag sieht es dann schon wieder anders aus.
Ist ähnlich wie bei den Autoherstellern und dem Benzinverbrauch...
Das sind Verbrauchswerte die im alltäglichen Einsatz nicht so erreicht werden können.!
Trotzdem haben die AK die Therapie von Hogh-kin, Leukämie und Brustkrebs entscheidend zu Gusten der Patienten verbessert!
Und euch die hier regelmäßig posten, wie Ville, oder eck64 sprechen ebenfalls ein entsprechendes Wissen zu.
Ihr habt euch intensiv damit beschäftigt, ergo also auch Ahnung. (Tschuldigung, wenn ich jemanden vergessen habe)
Ich verfolge diesen Thread schon sehr lange... + den Medarex yahoo.com Thread...
Nun zu Morphosys... hab mich echt noch nicht damit intensiv beschäftigt.
Muss eingestehen. Bei MOR ist mir die eigene Pipeline zu schwachbrustig!
MOR202 => CD38 mab... da ist z.B. auch Genmab dran und entwickelt einen AK
MOR103... hmn.. wenn es funktioniert... klingt gut! Aber insbesondere in RA sehr starke Konkurrenz!
Welche schon jahrelang in der Praxis (klinischer Alltag) sind und es kommen auch immer wieder verbessert Ak wie (Golimumab)
eher in die Klinik. Ist noch ein sehr weiter Weg! Und es gehört auch eine riesen Menge Lobbyarbeit ... ähh :-) tschuldigung, Marketing-
aktivitäten neue Konzepte in der Klinik einzuführen! :-)
Nichtdestrotz Mor ist gut geführt, sie machen Gewinn und können den positiven Cashflow in ihre eigenen Projekte stecken.
Viele Biotechs... haben nie und werden die Gewinnschwelle erreichen! Sie haben die kritische Größe + einen etablierten Namen dazu!
Janz großes Plus für MOR...
Siehe meine heißgeliebte...gehaßte Medarex.
Die Vorreiter der AK Industrie. Bekommen vorraussichtlich nach 20 Jahre Forschung ihr erstes Produkt auf den Markt.
:-) Oh man... dieser Mab ist sehr gut... aber good old Medarex bekommt lausige 3 % royalties!
Aber so waren nunmal damals die Verträge...
Ja.. das fetzt... so hab ich mir das vorgestellt... hochinteressanter Thread hier.
Dank an Alle!
Gruß where_is_the_beef
Antwort auf Beitrag Nr.: 36.124.245 von where_is_the_beef am 01.12.08 16:02:07Hier einen Prüfarzt/Prof. anzutreffen wäre auch ein unglaublicher Glücksgriff.
Aber auch als Krnakenpfleger kriegst du garantiert einiges mit, was für viele Interessant ist.
Bereitest du auch Infusionen für die Studienabteilung vor?
Hat mich nämlich schon immer interessiert, wie das praktisch mit Medikamenten für Doppel-blindstudien läuft. Placebo und manchmal meherere Dosierungsarme.
Und das Klinikarbeit ganz schön hart sein kann weiß ich.
Alles Gute und viel Kraft.
Aber auch als Krnakenpfleger kriegst du garantiert einiges mit, was für viele Interessant ist.
Bereitest du auch Infusionen für die Studienabteilung vor?
Hat mich nämlich schon immer interessiert, wie das praktisch mit Medikamenten für Doppel-blindstudien läuft. Placebo und manchmal meherere Dosierungsarme.
Und das Klinikarbeit ganz schön hart sein kann weiß ich.
Alles Gute und viel Kraft.
Antwort auf Beitrag Nr.: 36.124.245 von where_is_the_beef am 01.12.08 16:02:07Hallo where_is_the_beef,
super, dass mit dir jemand hier ist, der täglich mit Patienten zu tun hat. ich kann nachvollziehen, was für ein herausfordernder beruf das ist. Wer schonmal fälle von schweren krankheiten in der familie hatte oder wer sie hat und diese begleitet (hat), kann dies nachvollziehen. Zudem sollte man, wenn man das Leid sieht das Finanzielle eher vergessen, denn eigentlich ist es teilweise auch ein schnutziges Geschäft was Pharma mit dem Leid der Patienten macht.
----
Klar, dass auf dem Feld viel probiert wird, auch Dinge die nachher nicht so gut wirken. Aber auch die Studien zeigen, dass oftmals nur weniger als die Hälfte der Patienten profitiert. Ich hoffe eben AK Therapien sind irgendwann so weit, dass bildlich gesprochen mit einem Cocktail an verschiedenen AKs der Benzinverbrauch so niedrig oder die Reichweite so hoch ist, dass es nicht ins Gewicht fällt, wenn der Verbrauch mal geringfügig höher ist oder die Reichweite kürzer. Ich hoffe, dass mit entsprechenden Therapien fast alle Betroffenen Hoffnung haben können und nicht befürchten müssen zu den x% oder xx% Nichtansprecher zu gehören. Bis dahin ist es aber bestimmt noch jahrzehnte entfernt und vielleicht gibt es bis dahin (hoffentlich) neue Medikamentenklassen, die noch besser sind, wie z.b. Stammzellentherapien etc.
----
Ich will dich nicht zu sehr mit Fragen bombardieren, aber einige Fragen interessieren mich und du bist du sicher auskunftsfähig. Also wenn du Lust zum Beantworten hast, super!
Du berichtest, dass du MabThera (Rituximab) Infusionen vorbereitest (verabreichen dürfen das in D ja nur die Ärzte, was ich nie verstanden habe, denn meistens kann das nicht-ärztliche Personal viel besser Blut abzapfen oder Infusionen legen und sie sind viel näher am Patienten und können besser auf sie eingehen).
Rituximab wird ja vorwiegend bei Non-Hodgkin verabreicht. Hodkin wird in D zumeist mit ABVD oder BEACOPP Chemotherapie behandelt. Hier gibt es die Studienprotokolle der Uni Köln nach der sehr viele Kliniken in Deutschland arbeiten.
Wird Rituximab bei Euch auch kombinativ in Hodgkin eingesetzt? Wenn ja mit welcher Chemotherapie und in welchen Stages? Als first, second oder third line?
Wenn du die Infusionen vorbereitest, bekommen die Patienten bei Euch einen Port gelegt oder gehen die Infusionen in den Arm?
Grüße
super, dass mit dir jemand hier ist, der täglich mit Patienten zu tun hat. ich kann nachvollziehen, was für ein herausfordernder beruf das ist. Wer schonmal fälle von schweren krankheiten in der familie hatte oder wer sie hat und diese begleitet (hat), kann dies nachvollziehen. Zudem sollte man, wenn man das Leid sieht das Finanzielle eher vergessen, denn eigentlich ist es teilweise auch ein schnutziges Geschäft was Pharma mit dem Leid der Patienten macht.
----
Klar, dass auf dem Feld viel probiert wird, auch Dinge die nachher nicht so gut wirken. Aber auch die Studien zeigen, dass oftmals nur weniger als die Hälfte der Patienten profitiert. Ich hoffe eben AK Therapien sind irgendwann so weit, dass bildlich gesprochen mit einem Cocktail an verschiedenen AKs der Benzinverbrauch so niedrig oder die Reichweite so hoch ist, dass es nicht ins Gewicht fällt, wenn der Verbrauch mal geringfügig höher ist oder die Reichweite kürzer. Ich hoffe, dass mit entsprechenden Therapien fast alle Betroffenen Hoffnung haben können und nicht befürchten müssen zu den x% oder xx% Nichtansprecher zu gehören. Bis dahin ist es aber bestimmt noch jahrzehnte entfernt und vielleicht gibt es bis dahin (hoffentlich) neue Medikamentenklassen, die noch besser sind, wie z.b. Stammzellentherapien etc.
----
Ich will dich nicht zu sehr mit Fragen bombardieren, aber einige Fragen interessieren mich und du bist du sicher auskunftsfähig. Also wenn du Lust zum Beantworten hast, super!
Du berichtest, dass du MabThera (Rituximab) Infusionen vorbereitest (verabreichen dürfen das in D ja nur die Ärzte, was ich nie verstanden habe, denn meistens kann das nicht-ärztliche Personal viel besser Blut abzapfen oder Infusionen legen und sie sind viel näher am Patienten und können besser auf sie eingehen).
Rituximab wird ja vorwiegend bei Non-Hodgkin verabreicht. Hodkin wird in D zumeist mit ABVD oder BEACOPP Chemotherapie behandelt. Hier gibt es die Studienprotokolle der Uni Köln nach der sehr viele Kliniken in Deutschland arbeiten.
Wird Rituximab bei Euch auch kombinativ in Hodgkin eingesetzt? Wenn ja mit welcher Chemotherapie und in welchen Stages? Als first, second oder third line?
Wenn du die Infusionen vorbereitest, bekommen die Patienten bei Euch einen Port gelegt oder gehen die Infusionen in den Arm?
Grüße
Antwort auf Beitrag Nr.: 36.128.124 von Ville7 am 02.12.08 07:03:25Ich hoffe, dass mit entsprechenden Therapien fast alle Betroffenen Hoffnung haben können und nicht befürchten müssen zu den x% oder xx% Nichtansprecher zu gehören.
Ich erwarte mir massive Fortschritte im nächsten Jahrzehnt durch bessere Diagnostik, auch Gendiagnostik.
Wenn du ein bestimmtes Gen hast oder eben nicht hast, dann kann man vor der Therapie wissen ob du ein non-responder auf ein bestimmtes Medikament bist oder nicht.
Das steigert die Wirksamkeitsraten von Medikamenten, weckt weniger überflüssige Hoffnungen und spart die damit verbundenen Kosten und grenzt auch für neue Studien die Patientengruppen mit dem vordringlichsten ungedeckten Bedarf ein.
Als Beispiel:
Die tnf-Blocker wären noch viel bessere Medikamente, wenn man vor der Behandlung wüsste, das man zu den Patienten gehört, bei denen es anspricht.....
Ich erwarte mir massive Fortschritte im nächsten Jahrzehnt durch bessere Diagnostik, auch Gendiagnostik.
Wenn du ein bestimmtes Gen hast oder eben nicht hast, dann kann man vor der Therapie wissen ob du ein non-responder auf ein bestimmtes Medikament bist oder nicht.
Das steigert die Wirksamkeitsraten von Medikamenten, weckt weniger überflüssige Hoffnungen und spart die damit verbundenen Kosten und grenzt auch für neue Studien die Patientengruppen mit dem vordringlichsten ungedeckten Bedarf ein.
Als Beispiel:
Die tnf-Blocker wären noch viel bessere Medikamente, wenn man vor der Behandlung wüsste, das man zu den Patienten gehört, bei denen es anspricht.....
Antwort auf Beitrag Nr.: 36.128.124 von Ville7 am 02.12.08 07:03:25Hi Ville,
so Frühdienst vorbei!
Also gleich vorne weg. Ich arbeite ja auf der Rheuma! Hoghkin ist was für die Hämo bzw. Onkologie.
Dann mal was ich weiß...
Hier erstmal ein guter Link: http://www.lymphome.de/
An die Studienprotokolle kommst du leider nicht ran. Ist aber ein ganz guter Überblick was Im Bereich Maligne Lymphome in Deutschland läuft!
Wenn nach der Histo bei Hodgkin CD20 überexprimiert wird, wird versucht der Hodgkin mit Mabthera zu beschiessen!
Soweit ich weiß aber immer in Kombo mit Chemo => R - CHOP... Nie Monotherapie!
R Rituximab CD-20-Antikörper (Immuntherapie)
C Cyclophosphamid Alkylanzien (Stickstofflost-Derivat)
H Hydroxy-Doxorubicin Topoisomerase-II-Hemmer (Anthracyclin)
O Vincristin Mitosespindelgift
P Prednisolon Glukokortikoid
+ Zofran 8 mg Injektionen gegen die Übelkeit davor. Ist Stand des medizischen Behandlung z.Z.
Nur zu Rheuma...
Ick bereite das Rituximab vor + Begleitinjektionen. Bastel Infusiomat zusammen... Doktor hängt es ran
z.B.: 2 x 500 mg Rituximab in 500 ml Nacl Infusionsflasche läuft mit 25 - 50 ml/ h...
Laufrate ist aber verschieden! Vor Infusion gabe von z.B.: 1 Ampulle Fenistil + 1 Amp mit 8 mg Dexamethason...
Behandlunsgschema sind aber individuell und von Station und Behandlungsgebiet abhängig
Rituximab läuft bei den meisten Pat. über die Flexule. Bei Krebspatienten wird oft nen Port gelegt... ergo geht es dann da rüber.
Da ich den Überblick in der Rheuma insbesondere als RA Rheumatoid arthritish habe, wo Morphosys mit ihrem AK punkten will.
Da gibt es schon sehr ausgefeilte Therapiekonzepte.
Die AK Therapie gibt es erst bei Therapieversagen der klassischen Konzepte...
Ergo grob ungfähr so
1. Therapie mit Basistherapeutikern
MTX (Methotrexat) Immunsuppressiver)
bei Unverträglichkeit: Ciclosporin (Sandimmun) usw....
2) bei Therapieversaegn
Infliximab (TNF Blocker)
3) bei Therapieversagen mit TNF Blocker + CD20 Aktivität
Rituximab
dazu die ganze Zeit Pred meist dazu...
Neuer Ansatz: "Hit hart and hit early..."
Da will sich MOR 101 mit reinsetzten.... wird hart werden!
Sie müssen ganz klare Vorteile haben. Sonst seh ich schwarz...
Die etablierte Konkurrenz wird dann auch die Preise senken... wenn es soweit ist...
Da sie schon jahrelang produzieren... ist das dann kein Problem für sie!
Und dann entscheidet der Preis!
Rituximab im Rheuma gibt es off label bei Lupus bzw. bei weiteren sehr exotischen und durchgeknallten Erkrankungen.
Ist ein großes Feld Rheuma... kurzum... CD20 Aktivität.... dann kann ne Uniklinik das Off Label einsetzen.
Das Problem ist ja das nicht alle "bösen Zellen" sich im gleichen Entwicklungsstadium befinden bzw. gleich viel CD20 an der Zellöberfläche exprimieren. Man nimmt sogar an das es die Cancer stem cells gar nichts exprimieren.
Deswegen erwischt halt auch Rituximab nicht alles!
Deshalb Combo mit Chemo.... in Zukunft vielleicht mit weiteren AK (einer gegen CD19, Avastin, ein Immunsbooster)
Mal gucken... seh ich ähnlich wie Eck.... man wird schon vorher wissen können, wo was anschlägt und wo nicht!
Gruß
so Frühdienst vorbei!
Also gleich vorne weg. Ich arbeite ja auf der Rheuma! Hoghkin ist was für die Hämo bzw. Onkologie.
Dann mal was ich weiß...
Hier erstmal ein guter Link: http://www.lymphome.de/
An die Studienprotokolle kommst du leider nicht ran. Ist aber ein ganz guter Überblick was Im Bereich Maligne Lymphome in Deutschland läuft!
Wenn nach der Histo bei Hodgkin CD20 überexprimiert wird, wird versucht der Hodgkin mit Mabthera zu beschiessen!
Soweit ich weiß aber immer in Kombo mit Chemo => R - CHOP... Nie Monotherapie!
R Rituximab CD-20-Antikörper (Immuntherapie)
C Cyclophosphamid Alkylanzien (Stickstofflost-Derivat)
H Hydroxy-Doxorubicin Topoisomerase-II-Hemmer (Anthracyclin)
O Vincristin Mitosespindelgift
P Prednisolon Glukokortikoid
+ Zofran 8 mg Injektionen gegen die Übelkeit davor. Ist Stand des medizischen Behandlung z.Z.
Nur zu Rheuma...
Ick bereite das Rituximab vor + Begleitinjektionen. Bastel Infusiomat zusammen... Doktor hängt es ran
z.B.: 2 x 500 mg Rituximab in 500 ml Nacl Infusionsflasche läuft mit 25 - 50 ml/ h...
Laufrate ist aber verschieden! Vor Infusion gabe von z.B.: 1 Ampulle Fenistil + 1 Amp mit 8 mg Dexamethason...
Behandlunsgschema sind aber individuell und von Station und Behandlungsgebiet abhängig
Rituximab läuft bei den meisten Pat. über die Flexule. Bei Krebspatienten wird oft nen Port gelegt... ergo geht es dann da rüber.
Da ich den Überblick in der Rheuma insbesondere als RA Rheumatoid arthritish habe, wo Morphosys mit ihrem AK punkten will.
Da gibt es schon sehr ausgefeilte Therapiekonzepte.
Die AK Therapie gibt es erst bei Therapieversagen der klassischen Konzepte...
Ergo grob ungfähr so
1. Therapie mit Basistherapeutikern
MTX (Methotrexat) Immunsuppressiver)
bei Unverträglichkeit: Ciclosporin (Sandimmun) usw....
2) bei Therapieversaegn
Infliximab (TNF Blocker)
3) bei Therapieversagen mit TNF Blocker + CD20 Aktivität
Rituximab
dazu die ganze Zeit Pred meist dazu...
Neuer Ansatz: "Hit hart and hit early..."
Da will sich MOR 101 mit reinsetzten.... wird hart werden!
Sie müssen ganz klare Vorteile haben. Sonst seh ich schwarz...
Die etablierte Konkurrenz wird dann auch die Preise senken... wenn es soweit ist...
Da sie schon jahrelang produzieren... ist das dann kein Problem für sie!
Und dann entscheidet der Preis!
Rituximab im Rheuma gibt es off label bei Lupus bzw. bei weiteren sehr exotischen und durchgeknallten Erkrankungen.
Ist ein großes Feld Rheuma... kurzum... CD20 Aktivität.... dann kann ne Uniklinik das Off Label einsetzen.
Das Problem ist ja das nicht alle "bösen Zellen" sich im gleichen Entwicklungsstadium befinden bzw. gleich viel CD20 an der Zellöberfläche exprimieren. Man nimmt sogar an das es die Cancer stem cells gar nichts exprimieren.
Deswegen erwischt halt auch Rituximab nicht alles!
Deshalb Combo mit Chemo.... in Zukunft vielleicht mit weiteren AK (einer gegen CD19, Avastin, ein Immunsbooster)
Mal gucken... seh ich ähnlich wie Eck.... man wird schon vorher wissen können, wo was anschlägt und wo nicht!
Gruß
Antwort auf Beitrag Nr.: 36.132.258 von where_is_the_beef am 02.12.08 16:52:25Die Welt (besonders der AK-Entwickler) ist klein. 
was mich in letzter zeit ein bischen zum Überlegen gebracht hat, bzgl langzeittherapie bzw investment, war eine Aussage eines befreundeten Arztes:
"Wir werden in letzter Zeit häufig bis oft ins Kliniksekretariat zitiert um Informationen zu Nebenwirkungen von versch. AK gegenzuzeichnen"
des weiteren hat er auch schon das auftreten von lymphomen beobachtet (aktuell anch 3jähriger AK-Therapie). Statistischer Zufall od nicht? Die Zeit wirds zeigen.
Also ganzs ungefährlich schätz ich, besonders die AK - Lanzeittherapien, zb bei RA od Psoriasis nicht ein! Mal schaun was da in den nächsten Monaten-Jahren so kommt, nachdem die AK jetzt dann einige Jahre im Einsatz sind u theoretisch in die onkologisch bedeutsame Zeitspanne kommen.
Kennt wer ähnliche Beobachtungen??

was mich in letzter zeit ein bischen zum Überlegen gebracht hat, bzgl langzeittherapie bzw investment, war eine Aussage eines befreundeten Arztes:
"Wir werden in letzter Zeit häufig bis oft ins Kliniksekretariat zitiert um Informationen zu Nebenwirkungen von versch. AK gegenzuzeichnen"
des weiteren hat er auch schon das auftreten von lymphomen beobachtet (aktuell anch 3jähriger AK-Therapie). Statistischer Zufall od nicht? Die Zeit wirds zeigen.
Also ganzs ungefährlich schätz ich, besonders die AK - Lanzeittherapien, zb bei RA od Psoriasis nicht ein! Mal schaun was da in den nächsten Monaten-Jahren so kommt, nachdem die AK jetzt dann einige Jahre im Einsatz sind u theoretisch in die onkologisch bedeutsame Zeitspanne kommen.
Kennt wer ähnliche Beobachtungen??
Antwort auf Beitrag Nr.: 36.134.452 von bestoff am 02.12.08 21:17:45N'Abend...
auf jeden Fall. Auch AK haben zum Teil gravierende NW.
Ohne Frage... Tysabri, der gegen MS wirkende AK, führt in seltenen Fällen zur einer irreversiblen Gehirnentzündung...
Ist ja durch die Presse gegangen und Biogen Idec (BIIB) und sein irischer Partner Elan wurden dafür abgestraft!
Avastin greift das Herz an (hab mal was dazu gelesen...glaub ich zu mindest...)
vor Gabe von TNF Blockern muss ein TBC Test gemacht werden! Nicht ohne Grund...
AK sind keine Aspirin. Die klassische Chemo ist jedoch . systemisches Gift im ganzen Körper.
AK versprechen hier und schaffen es z. Teil auch einen gezielteren Ansatz.
Die klassischen chemotherapeutischen Ansätze insbesondere in der Onko... sind zum Teil ausgereizt...
Da das Thema aber sehr komplex ist, wird eine AK Kombietherapie noch eine ganze Zeit dauern!
Und nicht zu verdenken... das ganze Ganze kostet richtig Knete!

auf jeden Fall. Auch AK haben zum Teil gravierende NW.
Ohne Frage... Tysabri, der gegen MS wirkende AK, führt in seltenen Fällen zur einer irreversiblen Gehirnentzündung...
Ist ja durch die Presse gegangen und Biogen Idec (BIIB) und sein irischer Partner Elan wurden dafür abgestraft!
Avastin greift das Herz an (hab mal was dazu gelesen...glaub ich zu mindest...)
vor Gabe von TNF Blockern muss ein TBC Test gemacht werden! Nicht ohne Grund...

AK sind keine Aspirin. Die klassische Chemo ist jedoch . systemisches Gift im ganzen Körper.
AK versprechen hier und schaffen es z. Teil auch einen gezielteren Ansatz.
Die klassischen chemotherapeutischen Ansätze insbesondere in der Onko... sind zum Teil ausgereizt...
Da das Thema aber sehr komplex ist, wird eine AK Kombietherapie noch eine ganze Zeit dauern!
Und nicht zu verdenken... das ganze Ganze kostet richtig Knete!

Antwort auf Beitrag Nr.: 36.134.452 von bestoff am 02.12.08 21:17:45"...Lanzeittherapien, zb bei RA od Psoriasis nicht ein! Mal schaun was da in den nächsten Monaten-Jahren so kommt, nachdem die AK jetzt dann einige Jahre im Einsatz sind u theoretisch in die onkologisch bedeutsame Zeitspanne kommen."
hmn.... von Psoriasis hab ich auch mal was gehört... bei RA wäre mir das neu....
Deswegen hat sich ja auch der AK von Medarex und Centocor, Inc. verzögert...
FDA will Safety-Daten darüber sehen...
werd mal meinen Stationchef auf Zahn fühlen...
[Hausaufgaben notiert... ]
]
hmn.... von Psoriasis hab ich auch mal was gehört... bei RA wäre mir das neu....
Deswegen hat sich ja auch der AK von Medarex und Centocor, Inc. verzögert...
FDA will Safety-Daten darüber sehen...
werd mal meinen Stationchef auf Zahn fühlen...

[Hausaufgaben notiert...
 ]
]
Macht mal Kurse anders und der Rest kann später kommen

Hat jemand Kenntnis, wieviel Partnerprojekte von Medarex je in der Discovery und in der Präklinik schlummern?
Interessant wäre auch die durchschnittliche Meilensteinhöhe je Projektfortschritt zu wissen.
Ich habe ein Simulationsmodell für die Partnerpipeline von Morphosys entwickelt (Meilensteine/Royalties). Mit entsprechender Parameterumstellung (z.b. 3% Royalties statt 5%, anderer Projektstand) kann das Modell auch für Medarex angeworfen werden.
Interessant wäre auch die durchschnittliche Meilensteinhöhe je Projektfortschritt zu wissen.
Ich habe ein Simulationsmodell für die Partnerpipeline von Morphosys entwickelt (Meilensteine/Royalties). Mit entsprechender Parameterumstellung (z.b. 3% Royalties statt 5%, anderer Projektstand) kann das Modell auch für Medarex angeworfen werden.
Antwort auf Beitrag Nr.: 36.184.446 von Ville7 am 11.12.08 06:28:36Amis wollen Events und daraus Kurse feiern. Der Rest ist egal.
Medarex's anti-PD1, ein Mittel gegen Aids? In Affen scheint es zu funktionieren.
Antibody treatment controls AIDS in monkeys
Keith Alcorn, Thursday, December 11, 2008
Blocking a receptor on immune cells that inhibits immune response to viral infections using a specially designed antibody resulted in control of SIV, prolonged survival and impressive anti-SIV immune responses in monkeys – all without antiretroviral therapy – researchers reported this week in Nature.
The receptor, PD-1, is a hallmark of `exhausted` T-cells, and is found most frequently on the virus-specific T-cells of people suffering chronic viral infections such as cytomegalovirus, hepatitis C and HIV, in the virus-specific T-cells are unable to control viral replication. But up until now it has been unclear whether the high levels of PD-1 expression had any bearing on HIV disease, and whether blocking the PD-1 receptors would have any impact on disease progression.
In a series of animal experiments researchers from Emory University, Atlanta, along with colleagues at Harvard Medical School, University of Pennsylvania Medical School and the Dana-Farber Cancer Institute have now shown that blocking the PD-1 receptor offers a potential new pathway both for treating HIV infection – and perhaps for its prevention too.
The investigators tested an antibody for human PD-1 in nine macaques that had been infected with SIV, the simian equivalent of HIV, for varying periods of time. Of the nine animals, five had been infected for three months and four for around 21 months at the time of antibody treatment.
The monkeys received four injections with the antibody over a ten-day period, while five further monkeys received a control vaccination with another antibody.
While four out of five control animals died of simian AIDS within four months, all nine animals that received the PD-1 antibody were still alive and healthy after seven months, and exhibited strong SIV-specific CD8 cell responses, a decline in SIV viral load and an expansion in the number of SIV-specific CD8 cells in both the blood and the gut (the major reservoir of SIV and HIV).
Sustained viral load declines lasting at least three months were seen in only two of the nine animals (both treated in early infection); in the remainder viral load returned to pre-antibody levels, or began to rebound within 43 days of antibody treatment.
The PD-1 antibody appeared safe during the short period of study, with no observable side-effects and no changes in markers such as liver enzymes, lipids or blood counts after administration. There has been concern that PD-1 antibody, however it is used, could cause autoimmune problems due to an over-stimulation of CD8 cell activity.
PD-1 blockade is being investigated as a treatment for cancer and for hepatitis C; Medarex has two candidates in early clinical trials. According to Nature News, another company hopes to win permission to begin trials of a PD-1 antibody in people with HIV in 2009.
The existing research consortium plans further work with anti-PD-1 in order to test its effects in combination with antiretroviral therapy, as well as the effects of prolonged dosing.
Reference
Vijayakumar V et al.Enhancing SIV-specific immunity in vivo by PD-1 blockade. Nature (online advance publication, Dec 10 2008). Doi:10.1038/nature07662
Antibody treatment controls AIDS in monkeys
Keith Alcorn, Thursday, December 11, 2008
Blocking a receptor on immune cells that inhibits immune response to viral infections using a specially designed antibody resulted in control of SIV, prolonged survival and impressive anti-SIV immune responses in monkeys – all without antiretroviral therapy – researchers reported this week in Nature.
The receptor, PD-1, is a hallmark of `exhausted` T-cells, and is found most frequently on the virus-specific T-cells of people suffering chronic viral infections such as cytomegalovirus, hepatitis C and HIV, in the virus-specific T-cells are unable to control viral replication. But up until now it has been unclear whether the high levels of PD-1 expression had any bearing on HIV disease, and whether blocking the PD-1 receptors would have any impact on disease progression.
In a series of animal experiments researchers from Emory University, Atlanta, along with colleagues at Harvard Medical School, University of Pennsylvania Medical School and the Dana-Farber Cancer Institute have now shown that blocking the PD-1 receptor offers a potential new pathway both for treating HIV infection – and perhaps for its prevention too.
The investigators tested an antibody for human PD-1 in nine macaques that had been infected with SIV, the simian equivalent of HIV, for varying periods of time. Of the nine animals, five had been infected for three months and four for around 21 months at the time of antibody treatment.
The monkeys received four injections with the antibody over a ten-day period, while five further monkeys received a control vaccination with another antibody.
While four out of five control animals died of simian AIDS within four months, all nine animals that received the PD-1 antibody were still alive and healthy after seven months, and exhibited strong SIV-specific CD8 cell responses, a decline in SIV viral load and an expansion in the number of SIV-specific CD8 cells in both the blood and the gut (the major reservoir of SIV and HIV).
Sustained viral load declines lasting at least three months were seen in only two of the nine animals (both treated in early infection); in the remainder viral load returned to pre-antibody levels, or began to rebound within 43 days of antibody treatment.
The PD-1 antibody appeared safe during the short period of study, with no observable side-effects and no changes in markers such as liver enzymes, lipids or blood counts after administration. There has been concern that PD-1 antibody, however it is used, could cause autoimmune problems due to an over-stimulation of CD8 cell activity.
PD-1 blockade is being investigated as a treatment for cancer and for hepatitis C; Medarex has two candidates in early clinical trials. According to Nature News, another company hopes to win permission to begin trials of a PD-1 antibody in people with HIV in 2009.
The existing research consortium plans further work with anti-PD-1 in order to test its effects in combination with antiretroviral therapy, as well as the effects of prolonged dosing.
Reference
Vijayakumar V et al.Enhancing SIV-specific immunity in vivo by PD-1 blockade. Nature (online advance publication, Dec 10 2008). Doi:10.1038/nature07662
Ustekinumab nun in Kanada zugelassen (Info aus Yahoo):
TORONTO, Dec. 15 /CNW/ - Canadians living with moderate to severe plaque
psoriasis, a chronic and often debilitating inflammatory disease, now have a
new treatment option with the approval of STELARA(TM) (ustekinumab). STELARA,
which is self-injected every 12 weeks following two starter doses at weeks 0
and 4, has demonstrated significant efficacy in clinical studies involving
more than 3,000 participants from around the world. In Canada, STELARA is
marketed by Janssen-Ortho Inc.
TORONTO, Dec. 15 /CNW/ - Canadians living with moderate to severe plaque
psoriasis, a chronic and often debilitating inflammatory disease, now have a
new treatment option with the approval of STELARA(TM) (ustekinumab). STELARA,
which is self-injected every 12 weeks following two starter doses at weeks 0
and 4, has demonstrated significant efficacy in clinical studies involving
more than 3,000 participants from around the world. In Canada, STELARA is
marketed by Janssen-Ortho Inc.
Hi Ville...
:-))
Let`s celebrate....
Krass nach mehr als 20 Jahren das erste Produkt im Markt!
Der Kurs dreht trotzdem nach Süden.... versteh jemand die Börse!
Egal... ich werde mir heute ein schönes Bierchen auf Ustekinumab genehmigen!

:-))
Let`s celebrate....
Krass nach mehr als 20 Jahren das erste Produkt im Markt!
Der Kurs dreht trotzdem nach Süden.... versteh jemand die Börse!
Egal... ich werde mir heute ein schönes Bierchen auf Ustekinumab genehmigen!

Hoffentlich eselt der Esel jetzt anders http://www.medarex.com/cgi-local/item.pl/20081215-1236218
Bisher bin ich noch der Meinung einen potentiellen Südpol schon erreicht zu haben.

Die Ausmährung vor einem Durchmarsch über die 6€ und folgende Trendkäufe von Mondkälbern kann ruhig einige Monate dauern. Wichtig ist jetzt der mögliche wirtschaftliche Sinn in dem Unternehmen Medarex.
Die Ausmährung vor einem Durchmarsch über die 6€ und folgende Trendkäufe von Mondkälbern kann ruhig einige Monate dauern. Wichtig ist jetzt der mögliche wirtschaftliche Sinn in dem Unternehmen Medarex.
Ist einem Shortie das Konto geplatzt, gabs News

Oder Mitleidskäufe von einem Pharma

Oder Mitleidskäufe von einem Pharma

Antwort auf Beitrag Nr.: 36.233.673 von Friseuse am 18.12.08 19:51:50Heute ja, die FDA versagt Ustekinumab erst mal die Zulassung und antwortet mit Complete Response Letter. Sie wollen ein Riskmanagement von JnJ sehen. Schaut nach Verzögerung aus, aber dieses Medikament nicht haben zu wollen wäre bescheuert. Aber was sind die Amis nicht alles...

Hallo Alle zusammen...
so hab mich mal schlau gemacht. Zwecks Studien, und wie das logistisch abläuft.
Also z.Z. laufen 32 Studien im Bereich Rheuma an der Charite. Das ist ganz ordentlich.
Bei placebokontrollierten Studien gibt es einen neutralen Dienstleister zwischen Studiengeber und teilnehmenden Kliniken, welcher gewährleisten soll, das die Studie ordnungsgemäß verblindet ist.
Dieser stellt dann auch die Medikamente. Infusion oder Medikamentenampulle, wo Pat.-Nr, StudieNr. + Gewicht draufsteht.
Mehr nicht. Keinerlei weiterer Anhaltspunkt, ob Placebo oder zutestenden Medikament.
Postkuriere bringen regelmäßig Medikament oder nehmen z.B. Blutproben mit.
Irgendwann, wenn die Studie komplett ist und nach einer gewissen Zeit, wird diese von dem neutralen Dienstleister entblindet.... => Tag der Wahrheit! :-)
Soweit mein grober Einblick... vielleicht nicht neu für einige hier... aber das ist was bisher mitbekommen habe...
:-)
Nun zu Medarex... die Verschiebung der Zulassung für Stelera ist ärgerlich, aber auf den 1 Monat kommt das Warten auch nicht an!
Die jetzige Marktkap. von Medarex ist ein einziger Scherz! Dieses Jahr wurde im Sommer Jerini ein kl. Biotechunternehmen aus Berlin mit einem zugelassenen Wirkstoff gegen HAE für 350 Mill. €verkauft.
HAE == 20.000 Betroffene eurapaweit... weitere Pipeline von Jerini... nun ja... vernachlässigbar!
Und nun schauen, wir uns mal Medarex an! Mit dieser Pipeline und der dahinterliegenden Technologie + Patente....
=> ein einziger schlechter Scherz!
Generell zu Medarex bleibt zu sagen, das ihr Ansatz eigene Targets zu verfolgen, auf denen keine Konkurrenz schon arbeitet... vielleicht auf lange Sicht der erfolgsversprechendere Ansatz ist!
PDL1, PD1, CTLA, CXC4... sind alles Targets, wo sich die Konkurrenz nicht drum kümmert... gut für Medarex!
Sicherlich würde Medarex im Kurs ziemlich weit nördlicher stehen, wenn wir Genmabs optimierten Mee-too CD20 AK in deren Phase jetzt im Angebot hätten! Ohne Frage...
Jedoch muss auch Ofmatumab erstmal durchsetzten... Rituximab wurde weltweit bis jetzt bei mehr als 1,5 Millionen Pat. angewendet. Die Ärzte haben einen breiten Erfahrungsschatz zu Rituximab, sei es bei NW... off label Anwendungen etc. pp. => deshalb muss der Genmab AK klar überlegen sein!
Ich zweifel nicht daran... (Ist ja Medarex Technologie) + die Dänen haben die Bindungsstruktur optimiert... aber der CD20 Markt ist halt schon gut besetzt!
Deshalb nochmals etwas H2O in den Morphosyswein.... der MOR103 AK ist noch weit von der Klink weg
Und wenn es hart wird... muss das Ding entscheidend besser sein + Vorteile anbieten, welche die breite Konkurrenz im rheumatischen Bereich nicht hat!
Guti... wünsch Allen hier einen guten Rutsch ins Neue Jahr...
und hoffe, das die Prognosen für 2009 nicht so schlecht ausfallen, wie jetzt schwarzgemalt wird!
Sonst können wir uns wohl nä. Jahr alle frisch machen! :-)
so hab mich mal schlau gemacht. Zwecks Studien, und wie das logistisch abläuft.
Also z.Z. laufen 32 Studien im Bereich Rheuma an der Charite. Das ist ganz ordentlich.
Bei placebokontrollierten Studien gibt es einen neutralen Dienstleister zwischen Studiengeber und teilnehmenden Kliniken, welcher gewährleisten soll, das die Studie ordnungsgemäß verblindet ist.
Dieser stellt dann auch die Medikamente. Infusion oder Medikamentenampulle, wo Pat.-Nr, StudieNr. + Gewicht draufsteht.
Mehr nicht. Keinerlei weiterer Anhaltspunkt, ob Placebo oder zutestenden Medikament.
Postkuriere bringen regelmäßig Medikament oder nehmen z.B. Blutproben mit.
Irgendwann, wenn die Studie komplett ist und nach einer gewissen Zeit, wird diese von dem neutralen Dienstleister entblindet.... => Tag der Wahrheit! :-)
Soweit mein grober Einblick... vielleicht nicht neu für einige hier... aber das ist was bisher mitbekommen habe...
:-)
Nun zu Medarex... die Verschiebung der Zulassung für Stelera ist ärgerlich, aber auf den 1 Monat kommt das Warten auch nicht an!
Die jetzige Marktkap. von Medarex ist ein einziger Scherz! Dieses Jahr wurde im Sommer Jerini ein kl. Biotechunternehmen aus Berlin mit einem zugelassenen Wirkstoff gegen HAE für 350 Mill. €verkauft.
HAE == 20.000 Betroffene eurapaweit... weitere Pipeline von Jerini... nun ja... vernachlässigbar!
Und nun schauen, wir uns mal Medarex an! Mit dieser Pipeline und der dahinterliegenden Technologie + Patente....
=> ein einziger schlechter Scherz!
Generell zu Medarex bleibt zu sagen, das ihr Ansatz eigene Targets zu verfolgen, auf denen keine Konkurrenz schon arbeitet... vielleicht auf lange Sicht der erfolgsversprechendere Ansatz ist!
PDL1, PD1, CTLA, CXC4... sind alles Targets, wo sich die Konkurrenz nicht drum kümmert... gut für Medarex!
Sicherlich würde Medarex im Kurs ziemlich weit nördlicher stehen, wenn wir Genmabs optimierten Mee-too CD20 AK in deren Phase jetzt im Angebot hätten! Ohne Frage...
Jedoch muss auch Ofmatumab erstmal durchsetzten... Rituximab wurde weltweit bis jetzt bei mehr als 1,5 Millionen Pat. angewendet. Die Ärzte haben einen breiten Erfahrungsschatz zu Rituximab, sei es bei NW... off label Anwendungen etc. pp. => deshalb muss der Genmab AK klar überlegen sein!
Ich zweifel nicht daran... (Ist ja Medarex Technologie) + die Dänen haben die Bindungsstruktur optimiert... aber der CD20 Markt ist halt schon gut besetzt!
Deshalb nochmals etwas H2O in den Morphosyswein.... der MOR103 AK ist noch weit von der Klink weg
Und wenn es hart wird... muss das Ding entscheidend besser sein + Vorteile anbieten, welche die breite Konkurrenz im rheumatischen Bereich nicht hat!
Guti... wünsch Allen hier einen guten Rutsch ins Neue Jahr...
und hoffe, das die Prognosen für 2009 nicht so schlecht ausfallen, wie jetzt schwarzgemalt wird!
Sonst können wir uns wohl nä. Jahr alle frisch machen! :-)
A Stage IV Malignant Melanoma Drug That Increases Overall Survival Would Earn a Higher Patient Share in the U.S. Than in Europe
Ipilimumab Will Earn Decision Resources' Clinical Gold Standard for Stage IV Malignant Melanoma in 2012, According to a New Report from Decision Resources
WALTHAM, Mass., Jan. 19 /PRNewswire/ -- Decision Resources, one of the world's leading research and advisory firms for pharmaceutical and healthcare issues, finds that a drug for treating stage IV malignant melanoma that can increase median overall survival when compared with standard of care dacarbazine (Bedford Laboratories' DTIC-Dome, generics) would earn a higher patient share in the U.S. (60 percent) than in Europe (40 percent), according to surveyed U.S. and European oncologists.
The new report entitled Malignant Melanoma (Stage IV): Emerging Therapies Must Increase Overall Survival over Dacarbazine to Attain High Patient Share finds that clinical data and the opinions of interviewed thought leaders indicate that Bristol-Myers Squibb/Medarex's ipilimumab has advantages over dacarbazine in the attribute of median overall survival. Following its approval in 2010 for the indication, ipilimumab will earn Decision Resources' proprietary clinical gold standard for stage IV malignant melanoma from 2012 to 2017.
"Ipilimumab has competitive advantages in efficacy and has been shown, in combination with dacarbazine, to almost double median overall survival when compared to Schering-Plough's Temodar, our clinical gold standard in 2008 for stage IV malignant melanoma," said Decision Resources Analyst Karen Pomeranz, Ph.D. "According to oncologists we surveyed, overall survival is the highest-weighted end point for stage IV malignant melanoma, which further stresses the significance of ipilimumab's achievement in increasing overall survival."
About the Report
Malignant Melanoma (Stage IV): Emerging Therapies Must Increase Overall Survival over Dacarbazine to Attain High Patient Share is a DecisionBase 2009 report. DecisionBase 2009 is a decision-support tool that provides in-depth analysis of unmet need, physician expectations of new therapies and commercial dynamics to help pharmaceutical companies optimize their investments in drug development.
The report can be purchased by contacting Decision Resources. Members of the media may request an interview with an analyst.
http://sev.prnewswire.com/null/20090119/NE5985619012009-1.ht…
Ipilimumab Will Earn Decision Resources' Clinical Gold Standard for Stage IV Malignant Melanoma in 2012, According to a New Report from Decision Resources
WALTHAM, Mass., Jan. 19 /PRNewswire/ -- Decision Resources, one of the world's leading research and advisory firms for pharmaceutical and healthcare issues, finds that a drug for treating stage IV malignant melanoma that can increase median overall survival when compared with standard of care dacarbazine (Bedford Laboratories' DTIC-Dome, generics) would earn a higher patient share in the U.S. (60 percent) than in Europe (40 percent), according to surveyed U.S. and European oncologists.
The new report entitled Malignant Melanoma (Stage IV): Emerging Therapies Must Increase Overall Survival over Dacarbazine to Attain High Patient Share finds that clinical data and the opinions of interviewed thought leaders indicate that Bristol-Myers Squibb/Medarex's ipilimumab has advantages over dacarbazine in the attribute of median overall survival. Following its approval in 2010 for the indication, ipilimumab will earn Decision Resources' proprietary clinical gold standard for stage IV malignant melanoma from 2012 to 2017.
"Ipilimumab has competitive advantages in efficacy and has been shown, in combination with dacarbazine, to almost double median overall survival when compared to Schering-Plough's Temodar, our clinical gold standard in 2008 for stage IV malignant melanoma," said Decision Resources Analyst Karen Pomeranz, Ph.D. "According to oncologists we surveyed, overall survival is the highest-weighted end point for stage IV malignant melanoma, which further stresses the significance of ipilimumab's achievement in increasing overall survival."
About the Report
Malignant Melanoma (Stage IV): Emerging Therapies Must Increase Overall Survival over Dacarbazine to Attain High Patient Share is a DecisionBase 2009 report. DecisionBase 2009 is a decision-support tool that provides in-depth analysis of unmet need, physician expectations of new therapies and commercial dynamics to help pharmaceutical companies optimize their investments in drug development.
The report can be purchased by contacting Decision Resources. Members of the media may request an interview with an analyst.
http://sev.prnewswire.com/null/20090119/NE5985619012009-1.ht…
Macht mal höhere Kurse, besser gestern als heute
Muß ja nicht wegen Zulassung von irgendwas sein, kann nicht eine Sofortübernahme durch Pfizer oder BMS bei Yahoo erfunden werden

Muß ja nicht wegen Zulassung von irgendwas sein, kann nicht eine Sofortübernahme durch Pfizer oder BMS bei Yahoo erfunden werden

Antwort auf Beitrag Nr.: 36.413.551 von Friseuse am 20.01.09 19:16:55Tja wirst wohl noch länger Kamm und Schere schwingen müssen, ob es gut ist sich die Haare von Dir schneiden zulassen bei fallenden Kursen ?

Antwort auf Beitrag Nr.: 36.415.115 von StaatsKnecht am 20.01.09 22:36:51Du wirst Medarex bald nicht mehr so günstig bekommen wie im Januar. Deine einzige Hoffnung muss dann der abstürzende Gesamtmarkt sein in dessen Strudel auch eine MEDX nochmal geraten könnte.
Zulassung von Ustekinumab und Golimumab steht ins Haus. Noch im ersten Halbjahr. Beides mit Multi-Blockbusterpotential.
Golimumab ist in klinischen Tests klar besser als Humira gewesen. Humira hat in 2008 4,5 Milliarden USD Umsatz gemacht. Sollte Golimumab dies 5 Jahre nach Zulassung auch schaffen ist der Cashburn von Medarex allein mit diesem einen Parterprodukt gestoppt.
Und ACZ885 wird 2010 die Partnerprodukte ergänzen, auch ein Produkt, das in seiner vollen Bandbreite dann Blockbusterstatus erreichen könnte (ein anti-IL1b AK gegen ale möglichen Autoimmunerkrankungen).
Richtiges Upside dann mit den eigenen Produkten und der massiven Pipe. Die Neinsager inklusive der Haarschneiderinnen werden es noch lernen.
Kleines Schmankerl am Rande: Bei der letzten JP Morgan Präsentation beim Webcast war das Micro schon etwas früher offen als geplant und man hörte wie Pien mit dem JPMorgan Analysten sprach (flüsterte). Dieser Analyst meinte dabei zu Pien, dass seine Firma in 2009 vorhabe einen signifikanten Anteil an Medarex zu erwerben.
Zulassung von Ustekinumab und Golimumab steht ins Haus. Noch im ersten Halbjahr. Beides mit Multi-Blockbusterpotential.
Golimumab ist in klinischen Tests klar besser als Humira gewesen. Humira hat in 2008 4,5 Milliarden USD Umsatz gemacht. Sollte Golimumab dies 5 Jahre nach Zulassung auch schaffen ist der Cashburn von Medarex allein mit diesem einen Parterprodukt gestoppt.
Und ACZ885 wird 2010 die Partnerprodukte ergänzen, auch ein Produkt, das in seiner vollen Bandbreite dann Blockbusterstatus erreichen könnte (ein anti-IL1b AK gegen ale möglichen Autoimmunerkrankungen).
Richtiges Upside dann mit den eigenen Produkten und der massiven Pipe. Die Neinsager inklusive der Haarschneiderinnen werden es noch lernen.
Kleines Schmankerl am Rande: Bei der letzten JP Morgan Präsentation beim Webcast war das Micro schon etwas früher offen als geplant und man hörte wie Pien mit dem JPMorgan Analysten sprach (flüsterte). Dieser Analyst meinte dabei zu Pien, dass seine Firma in 2009 vorhabe einen signifikanten Anteil an Medarex zu erwerben.
http://www.ots.at/presseaussendung.php?schluessel=OTE_200901…
New Biologic STELARA(TM) Receives Approval in Europe for Treatment of Moderate to Severe Plaque Psoriasis =
Beerse, Belgium (ots/PRNewswire) -
- First and Only Biologic Approved With Infrequent, Every
Twelve-Week Maintenance Dosing
BEERSE, Belgium, January 22 /PRNewswire/ --
Janssen-Cilag announced today that STELARA(TM) (ustekinumab), the
first in a new class of biologics, has been approved by the European
Commission for use across Europe. The approved indication of
ustekinumab is for the treatment of moderate to severe plaque
psoriasis in adults who failed to respond to, or who have a
contraindication to, or are intolerant to other systemic therapies
including ciclosporin, methotrexate and PUVA (psoralen plus
ultraviolet A light). With the approval by the European Commission,
ustekinumab is approved in 27 countries in the EU. Psoriasis, a
chronic skin disease that affects between two and three percent of
the European population,[1] is associated with substantial physical
and emotional burdens and potentially serious co-morbidities.[2,3]
In clinical studies, treatment with ustekinumab demonstrated
significant improvements in patients' psoriasis, and quality of life,
which were sustained with as few as four injections a year (every
twelve weeks) following two starter doses at weeks 0 and 4. The
approval of ustekinumab offers adults living with moderate-to-severe
plaque psoriasis a new therapy which has the potential to make a
considerable impact on their daily lives.
The approval is based on data from two large, pivotal Phase III,
multi-centre, randomised, double-blind, placebo controlled trials
(PHOENIX 1 & 2) involving nearly 2,000 patients in whom the efficacy
and safety of ustekinumab in the treatment of moderate-to-severe
plaque psoriasis were evaluated.[4,5] Two-thirds or more of patients
achieved the primary endpoint of each trial, at least 75%
improvement in psoriasis using the Psoriasis Area and Severity Index
(PASI 75) at week 12, after receiving just two doses of ustekinumab
45 mg or 90 mg, respectively, at weeks 0 and 4. At week 12, 66
percent to 76 percent of patients receiving ustekinumab 45 mg or 90
mg doses, respectively, achieved PASI 75 compared with 3 to 4 per
cent of patients receiving placebo (p<0.001). The majority of
responders receiving injections every 12 weeks maintained PASI 75
response through up to 18 months.
Rates of serious adverse events, including serious infections,
malignancies and cardiovascular events, were low and consistent with
the expected background rates. The most common adverse reactions in
Phase III clinical trials were arthralgia, cough, headache, injection
site erythema, nasopharyngitis and upper respiratory tract infection.
Most were considered to be mild and did not necessitate
discontinuation of therapy.
About Psoriasis
Psoriasis is a chronic, immune-mediated inflammatory disease,
which results from the over-production of skin cells resulting in
their accumulation on the surface of the skin, which causes red,
scaly plaques that may itch and bleed. It is estimated that between
two and three percent of the European population have psoriasis.[1]
Twenty to thirty percent of people with psoriasis have cases that
are considered severe.[6]
About STELARA (ustekinumab)
Ustekinumab is a new, human monoclonal antibody with a novel
mechanism of action that targets the p40 sub-unit of cytokines
interleukin-12 (IL-12) and interleukin-23 (IL-23), naturally
occurring proteins that are important in regulating immune responses
and that are thought to be associated with some immune-mediated
inflammatory disorders, including plaque psoriasis.
Centocor Ortho Biotech Inc. discovered STELARA and has exclusive
marketing rights to the product in the United States. Janssen-Cilag
companies have exclusive marketing rights in all countries outside of
the United States.
Important Safety Information
STELARA is a selective immunosuppressant and may have the
potential to increase the risk of infections and reactivate latent
infections. Serious infections have been observed in patients
receiving STELARA in clinical trials. Do not start STELARA during an
active infection. If a serious infection develops, monitor patients
carefully and stop STELARA until the infection resolves. Patients
should be evaluated for tuberculosis (TB) infection prior to
initiating treatment with STELARA.
STELARA is a selective immunosuppressant. Immunosuppressive
agents have the potential to increase the risk of malignancy.
Malignancies have been observed in patients receiving STELARA in
clinical trials. Caution should be exercised when considering the use
of STELARA in patients with a history of malignancy or when
considering continuing treatment in patients who develop a
malignancy.
Grüße cristrader
New Biologic STELARA(TM) Receives Approval in Europe for Treatment of Moderate to Severe Plaque Psoriasis =
Beerse, Belgium (ots/PRNewswire) -
- First and Only Biologic Approved With Infrequent, Every
Twelve-Week Maintenance Dosing
BEERSE, Belgium, January 22 /PRNewswire/ --
Janssen-Cilag announced today that STELARA(TM) (ustekinumab), the
first in a new class of biologics, has been approved by the European
Commission for use across Europe. The approved indication of
ustekinumab is for the treatment of moderate to severe plaque
psoriasis in adults who failed to respond to, or who have a
contraindication to, or are intolerant to other systemic therapies
including ciclosporin, methotrexate and PUVA (psoralen plus
ultraviolet A light). With the approval by the European Commission,
ustekinumab is approved in 27 countries in the EU. Psoriasis, a
chronic skin disease that affects between two and three percent of
the European population,[1] is associated with substantial physical
and emotional burdens and potentially serious co-morbidities.[2,3]
In clinical studies, treatment with ustekinumab demonstrated
significant improvements in patients' psoriasis, and quality of life,
which were sustained with as few as four injections a year (every
twelve weeks) following two starter doses at weeks 0 and 4. The
approval of ustekinumab offers adults living with moderate-to-severe
plaque psoriasis a new therapy which has the potential to make a
considerable impact on their daily lives.
The approval is based on data from two large, pivotal Phase III,
multi-centre, randomised, double-blind, placebo controlled trials
(PHOENIX 1 & 2) involving nearly 2,000 patients in whom the efficacy
and safety of ustekinumab in the treatment of moderate-to-severe
plaque psoriasis were evaluated.[4,5] Two-thirds or more of patients
achieved the primary endpoint of each trial, at least 75%
improvement in psoriasis using the Psoriasis Area and Severity Index
(PASI 75) at week 12, after receiving just two doses of ustekinumab
45 mg or 90 mg, respectively, at weeks 0 and 4. At week 12, 66
percent to 76 percent of patients receiving ustekinumab 45 mg or 90
mg doses, respectively, achieved PASI 75 compared with 3 to 4 per
cent of patients receiving placebo (p<0.001). The majority of
responders receiving injections every 12 weeks maintained PASI 75
response through up to 18 months.
Rates of serious adverse events, including serious infections,
malignancies and cardiovascular events, were low and consistent with
the expected background rates. The most common adverse reactions in
Phase III clinical trials were arthralgia, cough, headache, injection
site erythema, nasopharyngitis and upper respiratory tract infection.
Most were considered to be mild and did not necessitate
discontinuation of therapy.
About Psoriasis
Psoriasis is a chronic, immune-mediated inflammatory disease,
which results from the over-production of skin cells resulting in
their accumulation on the surface of the skin, which causes red,
scaly plaques that may itch and bleed. It is estimated that between
two and three percent of the European population have psoriasis.[1]
Twenty to thirty percent of people with psoriasis have cases that
are considered severe.[6]
About STELARA (ustekinumab)
Ustekinumab is a new, human monoclonal antibody with a novel
mechanism of action that targets the p40 sub-unit of cytokines
interleukin-12 (IL-12) and interleukin-23 (IL-23), naturally
occurring proteins that are important in regulating immune responses
and that are thought to be associated with some immune-mediated
inflammatory disorders, including plaque psoriasis.
Centocor Ortho Biotech Inc. discovered STELARA and has exclusive
marketing rights to the product in the United States. Janssen-Cilag
companies have exclusive marketing rights in all countries outside of
the United States.
Important Safety Information
STELARA is a selective immunosuppressant and may have the
potential to increase the risk of infections and reactivate latent
infections. Serious infections have been observed in patients
receiving STELARA in clinical trials. Do not start STELARA during an
active infection. If a serious infection develops, monitor patients
carefully and stop STELARA until the infection resolves. Patients
should be evaluated for tuberculosis (TB) infection prior to
initiating treatment with STELARA.
STELARA is a selective immunosuppressant. Immunosuppressive
agents have the potential to increase the risk of malignancy.
Malignancies have been observed in patients receiving STELARA in
clinical trials. Caution should be exercised when considering the use
of STELARA in patients with a history of malignancy or when
considering continuing treatment in patients who develop a
malignancy.
Grüße cristrader

Antwort auf Beitrag Nr.: 36.424.086 von cristrader am 22.01.09 08:53:25http://sev.prnewswire.com/health-care-hospitals/20090121/NE6…
An Oral Agent for the Treatment of Moderate to Severe Psoriasis Would Earn a Higher Patient Share in the United States than in Europe
Stelara Will Earn Decision Resources' Clinical Gold-Standard for Psoriasis in 2012, According to a New Report from Decision Resources
WALTHAM, Mass., Jan. 21 /PRNewswire/ -- Decision Resources, one of the world's leading research and advisory firms for pharmaceutical and healthcare issues, finds that an oral agent for the treatment of moderate to severe psoriasis that demonstrates improved efficacy and lasting remission when compared with Amgen/Wyeth/Takeda's Enbrel would earn a higher patient share in the United States (20 percent) than in Europe (10 percent), according to surveyed U.S. and European dermatologists. Although the parenteral route of administration has not handicapped the performance of biological agents in the psoriasis market, oral therapies are still preferred by dermatologists for their convenience and the assumption that they will be priced lower than biological agents.
The new report entitled Psoriasis: Physicians Identify Key Differentiating Product Features in Crowded Market for Moderate to Severe Psoriasis finds that surveyed dermatologists indicate that a therapy's effect on psoriatic plaques at 10 or 12 weeks is the attribute that most influences their prescribing decisions in moderate to severe psoriasis. Clinical data and the opinions of interviewed thought leaders indicate that emerging therapies, Centocor/Janssen-Cilag's Stelara, Abbott's ABT-874 and UCB/Otsuka's Cimzia, have advantages in this attribute over Enbrel, the psoriasis market sales leader. Following its likely approval in 2009 for moderate to severe psoriasis, Stelara will earn Decision Resources' proprietary clinical gold-standard for psoriasis from 2012 to 2017.
"Stelara's unique and most significant advantage among therapies for moderate to severe psoriasis is its effect on lasting remission," said Decision Resources Analyst Joanna Kim. "Interviewed experts believe that Stelara's notable efficacy, combined with its 12-week dosing interval, will position this agent to compete directly with agents in the TNF-alpha inhibitors drug class and will capture significant use as a first-line biologic in the psoriasis market."
About the Report
Psoriasis: Physicians Identify Key Differentiating Product Features in Crowded Market for Moderate to Severe Psoriasis is a DecisionBase 2009 report. DecisionBase 2009 is a decision-support tool that provides in-depth analysis of unmet need, physician expectations of new therapies and commercial dynamics to help pharmaceutical companies optimize their investments in drug development.
The report can be purchased by contacting Decision Resources. Members of the media may request an interview with an analyst.
About Decision Resources
Decision Resources (www.decisionresources.com) is a world leader in market research publications, advisory services and consulting designed to help clients shape strategy, allocate resources and master their chosen markets. Decision Resources is a Decision Resources, Inc. company.
About Decision Resources, Inc.
Decision Resources, Inc. is a cohesive portfolio of companies that offers best-in-class, high-value information and insights on important sectors of the healthcare industry. Clients rely on this analysis and data to make informed decisions. Please visit Decision Resources, Inc. at www.DecisionResourcesInc.com.
Grüße cristrader
An Oral Agent for the Treatment of Moderate to Severe Psoriasis Would Earn a Higher Patient Share in the United States than in Europe
Stelara Will Earn Decision Resources' Clinical Gold-Standard for Psoriasis in 2012, According to a New Report from Decision Resources
WALTHAM, Mass., Jan. 21 /PRNewswire/ -- Decision Resources, one of the world's leading research and advisory firms for pharmaceutical and healthcare issues, finds that an oral agent for the treatment of moderate to severe psoriasis that demonstrates improved efficacy and lasting remission when compared with Amgen/Wyeth/Takeda's Enbrel would earn a higher patient share in the United States (20 percent) than in Europe (10 percent), according to surveyed U.S. and European dermatologists. Although the parenteral route of administration has not handicapped the performance of biological agents in the psoriasis market, oral therapies are still preferred by dermatologists for their convenience and the assumption that they will be priced lower than biological agents.
The new report entitled Psoriasis: Physicians Identify Key Differentiating Product Features in Crowded Market for Moderate to Severe Psoriasis finds that surveyed dermatologists indicate that a therapy's effect on psoriatic plaques at 10 or 12 weeks is the attribute that most influences their prescribing decisions in moderate to severe psoriasis. Clinical data and the opinions of interviewed thought leaders indicate that emerging therapies, Centocor/Janssen-Cilag's Stelara, Abbott's ABT-874 and UCB/Otsuka's Cimzia, have advantages in this attribute over Enbrel, the psoriasis market sales leader. Following its likely approval in 2009 for moderate to severe psoriasis, Stelara will earn Decision Resources' proprietary clinical gold-standard for psoriasis from 2012 to 2017.
"Stelara's unique and most significant advantage among therapies for moderate to severe psoriasis is its effect on lasting remission," said Decision Resources Analyst Joanna Kim. "Interviewed experts believe that Stelara's notable efficacy, combined with its 12-week dosing interval, will position this agent to compete directly with agents in the TNF-alpha inhibitors drug class and will capture significant use as a first-line biologic in the psoriasis market."
About the Report
Psoriasis: Physicians Identify Key Differentiating Product Features in Crowded Market for Moderate to Severe Psoriasis is a DecisionBase 2009 report. DecisionBase 2009 is a decision-support tool that provides in-depth analysis of unmet need, physician expectations of new therapies and commercial dynamics to help pharmaceutical companies optimize their investments in drug development.
The report can be purchased by contacting Decision Resources. Members of the media may request an interview with an analyst.
About Decision Resources
Decision Resources (www.decisionresources.com) is a world leader in market research publications, advisory services and consulting designed to help clients shape strategy, allocate resources and master their chosen markets. Decision Resources is a Decision Resources, Inc. company.
About Decision Resources, Inc.
Decision Resources, Inc. is a cohesive portfolio of companies that offers best-in-class, high-value information and insights on important sectors of the healthcare industry. Clients rely on this analysis and data to make informed decisions. Please visit Decision Resources, Inc. at www.DecisionResourcesInc.com.
Grüße cristrader

Antwort auf Beitrag Nr.: 36.424.961 von cristrader am 22.01.09 10:41:11Na also. Super News für MEDX!
Antwort auf Beitrag Nr.: 36.415.115 von StaatsKnecht am 20.01.09 22:36:51Für den Anfang sieht das ordentlich aus. Kursanstieg bei den ersten nachhaltig positiven Nachrichten seit Börsengang. Die verlauste Substanzverschleuderung gegen Cash könnte auch ein Ende haben. Themen klopfen an weitere Zulassungen, Break Even, gute Gewinnzeiten, charttechnische Schmackos, Übernahme von BMS oder Pfizer bei deren Gefühl für eine Marktzulassung.
weitere Zulassungen, Break Even, gute Gewinnzeiten, charttechnische Schmackos, Übernahme von BMS oder Pfizer bei deren Gefühl für eine Marktzulassung.
Ich sehe mich hier nicht in einer Mehrjahresabhängepartie a la Morphosys, der Kurs bekommt Flügel auf Monatssicht und die Aufbaubewegung ist schon mal ordentlich.
Glück auf
 weitere Zulassungen, Break Even, gute Gewinnzeiten, charttechnische Schmackos, Übernahme von BMS oder Pfizer bei deren Gefühl für eine Marktzulassung.
weitere Zulassungen, Break Even, gute Gewinnzeiten, charttechnische Schmackos, Übernahme von BMS oder Pfizer bei deren Gefühl für eine Marktzulassung.Ich sehe mich hier nicht in einer Mehrjahresabhängepartie a la Morphosys, der Kurs bekommt Flügel auf Monatssicht und die Aufbaubewegung ist schon mal ordentlich.
Glück auf
Antwort auf Beitrag Nr.: 36.425.146 von Friseuse am 22.01.09 11:04:17Medarex ist langfristig gesehen ein gutes Investment ohne frage ,was mich aber stört ist der hohe Cashburn und die Schulden und in naher Zukunft wird sich daran auch nichts ändern deshalb hat mich Medarex nie sonderlich interessiert .
http://finance.yahoo.com/news/Medarex-Reviews-Recent-prnews-…
Medarex currently expects a cash burn rate per month of approximately $12.2 million, a decrease from previous guidance for a monthly 2008 cash burn rate of approximately $12.4 million. This guidance includes Medarex's continual investment in its pipeline and the net contributions to the ipilimumab program. Medarex expects its monthly cash burn rate per month for the full year of 2009 to remain largely consistent with full-year 2008 net cash burn.
http://finance.yahoo.com/news/Medarex-Reviews-Recent-prnews-…
Medarex currently expects a cash burn rate per month of approximately $12.2 million, a decrease from previous guidance for a monthly 2008 cash burn rate of approximately $12.4 million. This guidance includes Medarex's continual investment in its pipeline and the net contributions to the ipilimumab program. Medarex expects its monthly cash burn rate per month for the full year of 2009 to remain largely consistent with full-year 2008 net cash burn.
Antwort auf Beitrag Nr.: 36.425.444 von StaatsKnecht am 22.01.09 11:37:06Ob sich die Patienten Usbekistan spritzen lassen würden wenn sie das hier wüssten .....Ich jedenfalls nicht
spritzen lassen würden wenn sie das hier wüssten .....Ich jedenfalls nicht
http://www.medknowledge.de/neu/med/jahr/2008/II-2008-18-uste…
Da der Wirkstoff tief in das Immungeschehen eingreift, sind vermehrte Infektionen oder sogar ein Krebsrisiko (wie bei anderen “Biologicals” auch) zumindest vorstellbar. Es bleibt abzuwarten, welche Vorsichtsmaßnahmen die beiden Zulassungsbehörden hier ergreifen werden..."
 spritzen lassen würden wenn sie das hier wüssten .....Ich jedenfalls nicht
spritzen lassen würden wenn sie das hier wüssten .....Ich jedenfalls nicht http://www.medknowledge.de/neu/med/jahr/2008/II-2008-18-uste…
Da der Wirkstoff tief in das Immungeschehen eingreift, sind vermehrte Infektionen oder sogar ein Krebsrisiko (wie bei anderen “Biologicals” auch) zumindest vorstellbar. Es bleibt abzuwarten, welche Vorsichtsmaßnahmen die beiden Zulassungsbehörden hier ergreifen werden..."
YESSSS!
Medarex hat das erste Produkt auf dem europäischen Markt!
http://www.ots.at/presseaussendung.php?schluessel=OTE_200901…



Na 20 Jahren der Forschung...
Jetzt noch gute Nachricht von Novartis +
weitere Fortschritte der Pipeline... und wir sehen endlich einen besseren, gerechtfertigten Kurs!
Medarex hat das erste Produkt auf dem europäischen Markt!
http://www.ots.at/presseaussendung.php?schluessel=OTE_200901…



Na 20 Jahren der Forschung...
Jetzt noch gute Nachricht von Novartis +
weitere Fortschritte der Pipeline... und wir sehen endlich einen besseren, gerechtfertigten Kurs!
Antwort auf Beitrag Nr.: 36.425.444 von StaatsKnecht am 22.01.09 11:37:06Es treffen zwei eher seltene Geschichten zusammen
Aufkommende Sinnhaftigkeit des Unternehmens und die historisch wohl einmalige Horizontverkürzung der Finanzgemeinde entspannt sich.
Ein großer Teil der Downbewegung lag am allgemeinen Krebs in Börsianertaschen, die Leute sind klamm und Klammheit beherrschte Kurse akut und die Perspektivsicht der Dinge interessierte gegen null. Das macht mehr Kursbewegung als jeder abgeleitete Vernunftsansatz, es kommt eine Glaubenszeit an Zukunft auf und die Eisfachgefühle weichen. Die Maßstäbe verlagern sich, Glaube versetzt bekanntlich Berge und den will ich im Kurs sehen.
Den Berg
Das kann für Bildungsbürger auah machen, für Eindimensionalstatiker mit Buchhalterbackground eh. Die zweite Dimension bewegt sich mit, Bock auf Zock und so
Allgemein sind Aktien eine Launefrage, bei Biotechs mehr als bei Schuhfabriken. Der Kurs geht die großen Gesamtmarktbewegungen gehebelt.

Spitzen in 2000 und 2007, jetzt gut ein Jahr Subprimefeierlichkeiten

Für die Vernunftsfreunde unter und in uns wechseln die Glubscher von der Cashsicht auf die Gewinnsicht der Zukunft.
Diese aufkommende Zuversicht wird den Börsianern nach Armutsbezeugungen selbst der größten der Kapitalmarktgrößen wieder gangbar sein.
Wann hier die erste Analyse mit einem EPS von einem Dollar kommt Kurse von 20+ fabuliert werden
Kurse von 20+ fabuliert werden Charties aufspringen
Charties aufspringen wird man sehen
wird man sehen
Analysten sind so

Aufkommende Sinnhaftigkeit des Unternehmens und die historisch wohl einmalige Horizontverkürzung der Finanzgemeinde entspannt sich.
Ein großer Teil der Downbewegung lag am allgemeinen Krebs in Börsianertaschen, die Leute sind klamm und Klammheit beherrschte Kurse akut und die Perspektivsicht der Dinge interessierte gegen null. Das macht mehr Kursbewegung als jeder abgeleitete Vernunftsansatz, es kommt eine Glaubenszeit an Zukunft auf und die Eisfachgefühle weichen. Die Maßstäbe verlagern sich, Glaube versetzt bekanntlich Berge und den will ich im Kurs sehen.
Den Berg

Das kann für Bildungsbürger auah machen, für Eindimensionalstatiker mit Buchhalterbackground eh. Die zweite Dimension bewegt sich mit, Bock auf Zock und so

Allgemein sind Aktien eine Launefrage, bei Biotechs mehr als bei Schuhfabriken. Der Kurs geht die großen Gesamtmarktbewegungen gehebelt.
Spitzen in 2000 und 2007, jetzt gut ein Jahr Subprimefeierlichkeiten
Für die Vernunftsfreunde unter und in uns wechseln die Glubscher von der Cashsicht auf die Gewinnsicht der Zukunft.
Diese aufkommende Zuversicht wird den Börsianern nach Armutsbezeugungen selbst der größten der Kapitalmarktgrößen wieder gangbar sein.
Wann hier die erste Analyse mit einem EPS von einem Dollar kommt
 Kurse von 20+ fabuliert werden
Kurse von 20+ fabuliert werden Charties aufspringen
Charties aufspringen wird man sehen
wird man sehen
Analysten sind so

Antwort auf Beitrag Nr.: 36.425.621 von StaatsKnecht am 22.01.09 11:57:01Medikamente sind immer eine Abwägung zwischen Nutzen und Risiko...
Ich sehe das nicht so kritisch... dies betrifft sehr, sehr viele Medikamente!
Die modulieren (dämpfen) alle das Immunsystem...
Prednisolon, Urbason, Ciclosphorin haben zum Teil massive NW!
Eine Medaille hat nur einmal zwei Seiten!
Ich sehe das nicht so kritisch... dies betrifft sehr, sehr viele Medikamente!
Die modulieren (dämpfen) alle das Immunsystem...
Prednisolon, Urbason, Ciclosphorin haben zum Teil massive NW!
Eine Medaille hat nur einmal zwei Seiten!
Antwort auf Beitrag Nr.: 36.425.901 von Friseuse am 22.01.09 12:28:07Mir gefällt Dein Schreibstil....Friseuse
Aber den Berg wirst Du trotzdem nicht sehen
Aber den Berg wirst Du trotzdem nicht sehen

Das kann doch einen Ami nicht erschüttern....

ich mein so eine Europa dingsda... Wo in Afrika liegt das überhaupt?
ich mein so eine Europa dingsda... Wo in Afrika liegt das überhaupt?
Antwort auf Beitrag Nr.: 36.427.779 von eck64 am 22.01.09 16:00:15Interessant, erste europäische Zulassung von Medarex, aber es wird für nicht notwendig erachtet eine eigene Presseerklärung herauszugeben. Aber das ist ja ein bekanntes Problem, sonst wäre Medarex ja auch nicht so günstig bewertet.
Grüße cristrader
Grüße cristrader

Hat jetzt doch einer zum Einstieg geklingelt?
Antwort auf Beitrag Nr.: 36.425.864 von where_is_the_beef am 22.01.09 12:24:30Nächster zu erwartender signifikanter Newsflow binnen drei Monate:
* Einreichung Zulassungsantrag Azzera(Ofatumumab) Genmab/GSK (bis Ende Jan.)
* Zulassung Ustekinumab USA (jederzeit)
* Einreichung BLA ACZ885 Novartis (jederzeit)
* Zulassung Golimumab USA (bis Ende Apr.)
Newsmässig schauts sehr gut aus. Kursmässig noch nicht.
* Einreichung Zulassungsantrag Azzera(Ofatumumab) Genmab/GSK (bis Ende Jan.)
* Zulassung Ustekinumab USA (jederzeit)
* Einreichung BLA ACZ885 Novartis (jederzeit)
* Zulassung Golimumab USA (bis Ende Apr.)
Newsmässig schauts sehr gut aus. Kursmässig noch nicht.
Antwort auf Beitrag Nr.: 36.429.551 von eck64 am 22.01.09 18:42:51Meinste wegen dem Volumen oder wieso leitest du das aus einer Underperformance ab? Dem Einsteiger scheint eher auch ein Aussteiger gegenüber zu stehen.
Antwort auf Beitrag Nr.: 36.432.019 von Ville7 am 23.01.09 06:38:23Ich hatte da unmittelbar in den realtimechart geschaut. Um ca. 18:40 wurden über 100 000 Aktien gekauft, der Kurs sprang um fast 2% in Minutenfrist hoch.
Da habe ich dann gefragt:
Hat jetzt doch einer zum Einstieg geklingelt?
Der weitere Kursverlauf hats nicht bestätigt.
Da habe ich dann gefragt:
Hat jetzt doch einer zum Einstieg geklingelt?
Der weitere Kursverlauf hats nicht bestätigt.
Antwort auf Beitrag Nr.: 36.427.779 von eck64 am 22.01.09 16:00:15Situation wie 2002/2003

Biotechs als Zukunftsfreudenindikator, Unternehmensentwicklung ist collateral.
Medarex gibt den gehebelten Bankenindex BKX auf einer verdeckt positiven Basisentwicklung

Die Aktie war früher die Citigroup für Arme und wird die Citigroup für Reiche

Beschlossen habe ich das, jetzt muß es nur noch werden

Biotechs als Zukunftsfreudenindikator, Unternehmensentwicklung ist collateral.
Medarex gibt den gehebelten Bankenindex BKX auf einer verdeckt positiven Basisentwicklung
Die Aktie war früher die Citigroup für Arme und wird die Citigroup für Reiche
Beschlossen habe ich das, jetzt muß es nur noch werden

Antwort auf Beitrag Nr.: 36.435.279 von Friseuse am 23.01.09 13:26:37Hey Friseuse hast du was damit zu tun ? Er sagt die Person die Ihn bedient hat, hätte irgendwas von Medarex gemurmelt .
Er hat das für eine Spezielspülung gehalten .

Er hat das für eine Spezielspülung gehalten .

Moin,

vielleicht hilft das hier endlich etwas, nachdem die Zulassung von Ustek. in Europa und Kanada fast keinen Effekt auf den Kurs hatte...
Gruß q.
Press Release Source: Medarex, Inc.
Medarex Announces Allowance of Investigational New Drug Application for Company's First Antibody-Drug Conjugate, MDX-1203
Wednesday January 28, 2009, 8:00 am EST
Yahoo! Buzz Print Related:Medarex, Inc.
PRINCETON, N.J., Jan. 28 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) announced today the allowance of an investigational new drug (IND) application filed with the U.S. Food & Drug Administration (FDA) for MDX-1203, the Company's first Antibody-Drug Conjugate (ADC) candidate generated from its proprietary technology. MDX-1203 is comprised of a potent cytotoxic prodrug chemically linked with a fully human anti-CD70 antibody. CD70 is expressed in renal cell carcinoma (RCC), leukemias, lymphomas, and other cancers. The Phase 1 study will evaluate MDX-1203 for the treatment of advanced/recurrent RCC and relapsed/refractory B-cell non-Hodgkin's lymphoma (NHL).
Related Quotes
Symbol Price Change
MEDX 5.82 0.00
{"s" : "medx","k" : "c10,l10,p20,t10","o" : "","j" : ""} "Antibody-drug conjugates are another important and innovative therapeutic approach used to fight cancer by effectively and selectively killing tumor cells over-expressing specific tumor antigens, so we are extremely excited in achieving the IND filing for MDX-1203, the first candidate from our proprietary ADC technology platform," said Howard H. Pien, Chairman and CEO of Medarex. "We developed our ADC technology to have significant competitive advantages over existing technologies and the Phase 1 trial for MDX-1203 will be the first study to evaluate these potential benefits."
An open-label, multi-dose, dose-escalation Phase 1 clinical trial will be conducted in patients with RCC and NHL. This trial is designed to establish and evaluate the safety, tolerability and maximum tolerated dose, as well as preliminary distribution, metabolism and pharmacokinetics of MDX-1203.
About Medarex's Antibody-Drug Conjugate (ADC) Technology
Medarex has enhanced its core UltiMAb® antibody platform with a suite of technologies that optimize or augment the therapeutic activity of antibodies, and one important technology expansion is the company's proprietary Antibody-Drug Conjugate platform. Medarex's proprietary ADC technology uses a cytotoxic agent that is a potent, synthetically manufactured prodrug (a DNA minor-groove binding alkylating agent) which is attached to an antibody using a stable peptide-based linker. Medarex believes that its ADC technology overcomes many of the key development challenges of drug conjugates, including issues of linker stability, potency and multi-drug resistance while maintaining a wide therapeutic window with minimal toxicity.
Medarex has conducted multiple preclinical studies on several investigational antibody-drug conjugate candidates in development demonstrating enhanced anti-tumor activity in xenograft models, even with single doses as low as 0.005 micro mol/kg, when compared to the anti-cancer antibodies alone. Preclinical studies have also demonstrated that anti-tumor activity is maintained in drug-resistant cancer cells. Additionally, Medarex's activatable prodrug has been shown to accumulate in the targeted tumor cells but not in normal tissue cells, thereby minimizing the toxicity profile but not the anti-tumor activity in animal and primate models.
About Medarex
Medarex is a biopharmaceutical company focused on the discovery, development and potential commercialization of fully human antibody-based therapeutics to treat life-threatening and debilitating diseases, including cancer, inflammation, autoimmune disorders and infectious diseases. Medarex applies its UltiMAb® technology and product development and clinical manufacturing experience to generate, support and potentially commercialize a broad range of fully human antibody product candidates for itself and its partners. Over forty of these therapeutic product candidates derived from Medarex technology are in human clinical testing or have had INDs submitted for such trials, with the most advanced product candidates currently in Phase 3 clinical trials, the subject of regulatory applications for marketing authorization or approved in Canada and Europe. Medarex is committed to building value by developing a diverse pipeline of antibody products to address the world's unmet healthcare needs. For more information about Medarex, visit its website at www.medarex.com.
Statement on Cautionary Factors
Except for the historical information presented herein, matters discussed herein may constitute forward-looking statements, as defined in the Private Securities Litigation Reform Act of 1995, that are subject to certain risks and uncertainties that could cause actual results to differ materially from any future results, performance or achievements expressed or implied by such statements. Statements that are not historical facts, including statements preceded by, followed by, or that include the words "potential", "expect", "believe", or "may" or similar statements are forward-looking statements. Medarex disclaims, however, any intent or obligation to update these forward-looking statements. These risks and uncertainties include those detailed from time to time in Medarex's public disclosure filings with the U.S. Securities and Exchange Commission (SEC), including its Annual Report on Form 10-K for the fiscal year ended December 31, 2007 and its quarterly reports on Form 10-Q. There can be no assurance that MDX-1203 development efforts will succeed or that other developed products will receive required regulatory clearance or that, even if such regulatory clearance were received, such products would ultimately achieve commercial success. Copies of Medarex's public disclosure filings are available from its investor relations department.
Medarex®, the Medarex logo and UltiMAb® are registered trademarks of Medarex, Inc. All rights are reserved.

vielleicht hilft das hier endlich etwas, nachdem die Zulassung von Ustek. in Europa und Kanada fast keinen Effekt auf den Kurs hatte...
Gruß q.
Press Release Source: Medarex, Inc.
Medarex Announces Allowance of Investigational New Drug Application for Company's First Antibody-Drug Conjugate, MDX-1203
Wednesday January 28, 2009, 8:00 am EST
Yahoo! Buzz Print Related:Medarex, Inc.
PRINCETON, N.J., Jan. 28 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) announced today the allowance of an investigational new drug (IND) application filed with the U.S. Food & Drug Administration (FDA) for MDX-1203, the Company's first Antibody-Drug Conjugate (ADC) candidate generated from its proprietary technology. MDX-1203 is comprised of a potent cytotoxic prodrug chemically linked with a fully human anti-CD70 antibody. CD70 is expressed in renal cell carcinoma (RCC), leukemias, lymphomas, and other cancers. The Phase 1 study will evaluate MDX-1203 for the treatment of advanced/recurrent RCC and relapsed/refractory B-cell non-Hodgkin's lymphoma (NHL).
Related Quotes
Symbol Price Change
MEDX 5.82 0.00
{"s" : "medx","k" : "c10,l10,p20,t10","o" : "","j" : ""} "Antibody-drug conjugates are another important and innovative therapeutic approach used to fight cancer by effectively and selectively killing tumor cells over-expressing specific tumor antigens, so we are extremely excited in achieving the IND filing for MDX-1203, the first candidate from our proprietary ADC technology platform," said Howard H. Pien, Chairman and CEO of Medarex. "We developed our ADC technology to have significant competitive advantages over existing technologies and the Phase 1 trial for MDX-1203 will be the first study to evaluate these potential benefits."
An open-label, multi-dose, dose-escalation Phase 1 clinical trial will be conducted in patients with RCC and NHL. This trial is designed to establish and evaluate the safety, tolerability and maximum tolerated dose, as well as preliminary distribution, metabolism and pharmacokinetics of MDX-1203.
About Medarex's Antibody-Drug Conjugate (ADC) Technology
Medarex has enhanced its core UltiMAb® antibody platform with a suite of technologies that optimize or augment the therapeutic activity of antibodies, and one important technology expansion is the company's proprietary Antibody-Drug Conjugate platform. Medarex's proprietary ADC technology uses a cytotoxic agent that is a potent, synthetically manufactured prodrug (a DNA minor-groove binding alkylating agent) which is attached to an antibody using a stable peptide-based linker. Medarex believes that its ADC technology overcomes many of the key development challenges of drug conjugates, including issues of linker stability, potency and multi-drug resistance while maintaining a wide therapeutic window with minimal toxicity.
Medarex has conducted multiple preclinical studies on several investigational antibody-drug conjugate candidates in development demonstrating enhanced anti-tumor activity in xenograft models, even with single doses as low as 0.005 micro mol/kg, when compared to the anti-cancer antibodies alone. Preclinical studies have also demonstrated that anti-tumor activity is maintained in drug-resistant cancer cells. Additionally, Medarex's activatable prodrug has been shown to accumulate in the targeted tumor cells but not in normal tissue cells, thereby minimizing the toxicity profile but not the anti-tumor activity in animal and primate models.
About Medarex
Medarex is a biopharmaceutical company focused on the discovery, development and potential commercialization of fully human antibody-based therapeutics to treat life-threatening and debilitating diseases, including cancer, inflammation, autoimmune disorders and infectious diseases. Medarex applies its UltiMAb® technology and product development and clinical manufacturing experience to generate, support and potentially commercialize a broad range of fully human antibody product candidates for itself and its partners. Over forty of these therapeutic product candidates derived from Medarex technology are in human clinical testing or have had INDs submitted for such trials, with the most advanced product candidates currently in Phase 3 clinical trials, the subject of regulatory applications for marketing authorization or approved in Canada and Europe. Medarex is committed to building value by developing a diverse pipeline of antibody products to address the world's unmet healthcare needs. For more information about Medarex, visit its website at www.medarex.com.
Statement on Cautionary Factors
Except for the historical information presented herein, matters discussed herein may constitute forward-looking statements, as defined in the Private Securities Litigation Reform Act of 1995, that are subject to certain risks and uncertainties that could cause actual results to differ materially from any future results, performance or achievements expressed or implied by such statements. Statements that are not historical facts, including statements preceded by, followed by, or that include the words "potential", "expect", "believe", or "may" or similar statements are forward-looking statements. Medarex disclaims, however, any intent or obligation to update these forward-looking statements. These risks and uncertainties include those detailed from time to time in Medarex's public disclosure filings with the U.S. Securities and Exchange Commission (SEC), including its Annual Report on Form 10-K for the fiscal year ended December 31, 2007 and its quarterly reports on Form 10-Q. There can be no assurance that MDX-1203 development efforts will succeed or that other developed products will receive required regulatory clearance or that, even if such regulatory clearance were received, such products would ultimately achieve commercial success. Copies of Medarex's public disclosure filings are available from its investor relations department.
Medarex®, the Medarex logo and UltiMAb® are registered trademarks of Medarex, Inc. All rights are reserved.
Antwort auf Beitrag Nr.: 36.438.087 von StaatsKnecht am 23.01.09 17:44:15Vorn rasiert wie Medarex im Kurs
Da kann noch was wachsen

Da kann noch was wachsen

Aller Anfang ist schwer

Legt mal Kohlen unter

Legt mal Kohlen unter


Na also, geht doch!
Und da kommt noch mehr, die Wende war schon.
Volumen auch überdurchschnittlich.
Die Kombination von Antikörpern mit "Killermolekülen" finde ich sehr spannend, war mal mit ein Grund, in diese Technologien zu investieren.
Solche Stoffe könnten sehr effektiv sein, aber auch einige Nebenwirkungen haben ("Selbstmordattentäter!").
Gruß q.
(P.S.: Hoffentlich bekomme ich nun keine Schäuble-Trojaner wegen des Schlagwortes!)
Laut Novartis gestriger Präsentation haben sie Zulassungsanträge für ACZ885 in USA und Europa gestellt. Schaut S.38 an:
http://www.novartis.com/downloads/investors/sales-results/Q4…
D.h. das könnte dieses Jahr das dritte Partnerprodukt sein, das die Zulassung erhält. Sag mal einer noch, es gäbe keinen Output.
http://www.novartis.com/downloads/investors/sales-results/Q4…
D.h. das könnte dieses Jahr das dritte Partnerprodukt sein, das die Zulassung erhält. Sag mal einer noch, es gäbe keinen Output.
Antwort auf Beitrag Nr.: 36.469.940 von quepos am 28.01.09 22:19:34Die Toxizitäten waren bei den bisherigen Konjugatantikörpern nicht (viel) schlechter als bei normalen Antikörpern. Was aber in der Tat besser ist ist die Wirksamkeit, diese ist weit weit besser. Bexxar, Zevalin und Co. sind ihren nicht-Konjugatbeladenen Varianten, die auf das selbe Target gehen, weit überlegen. Zevalin z.b. verbessert die Complete Response Rate bei Non Hodgkin Lymphomen von 55% auf 83%. 77% der Partial Responder nach Chemo+Rituxan Schema werden zusätzlich Complete Responder wenn sie im Anschluss an die Therapie Zevalin erhalten. Rituxan ist ein CD19 AK, Zevalin ist ein CD19 AK mit radioaktivem Knjugat.
Das geile an der Sache mit den Konjugatantikörpern ist, dass du die toxischen Stoffe in einer Konzentration von weniger als 1/100 an die Krebszellen bekommst. Bei gleicher Wirkung wie in einer Chemo oder (wie bei Zevalin) mit Bestrahlung, weil der Antikörper eben hochspezifisch bindet. Was das für die Chemo- oder Bestrahlungsnebenwirkungen bedeutet, wenn nur ein winziger Bruchteil des giftigen Stoffes oder der Strahlung in den Körper gelangt und auch noch nur spezifisch an die Krebstargets bindet, kann sich jeder selbst ausmalen.
Ich kann nur jedem empfehlen den R&D Day 2008 nochmal anzusehen. Die präklinischen Daten der Konjugat-AKs sind sehr vielversprechend. Medarex Homepage, IR, Webcasts. Medarex hat zahlreiche weitere Konjugat-Aks in der Entwicklung, sie scheinen eine Menge darauf zu halten.
Hier noch eine Posterpräsentation zum heute gestarteten MDX-1203 AK:
http://www.oncodesign.fr/posters/2007/AACR2007_Medarex_OncoD…
Die bisherige Erfolglosigkeit der Konjugat-Aks am Markt hat übrigens nichts mit ihrer Wirksamkeit zu tun sondern vorwiegend mit unnötigen regulatorischen Hemmnissen und mangelden finanziellen Anreizen für die Ärzte die aufwendigere aber weit wirksamere Therapie durchzuführen.
Das geile an der Sache mit den Konjugatantikörpern ist, dass du die toxischen Stoffe in einer Konzentration von weniger als 1/100 an die Krebszellen bekommst. Bei gleicher Wirkung wie in einer Chemo oder (wie bei Zevalin) mit Bestrahlung, weil der Antikörper eben hochspezifisch bindet. Was das für die Chemo- oder Bestrahlungsnebenwirkungen bedeutet, wenn nur ein winziger Bruchteil des giftigen Stoffes oder der Strahlung in den Körper gelangt und auch noch nur spezifisch an die Krebstargets bindet, kann sich jeder selbst ausmalen.
Ich kann nur jedem empfehlen den R&D Day 2008 nochmal anzusehen. Die präklinischen Daten der Konjugat-AKs sind sehr vielversprechend. Medarex Homepage, IR, Webcasts. Medarex hat zahlreiche weitere Konjugat-Aks in der Entwicklung, sie scheinen eine Menge darauf zu halten.
Hier noch eine Posterpräsentation zum heute gestarteten MDX-1203 AK:
http://www.oncodesign.fr/posters/2007/AACR2007_Medarex_OncoD…
Die bisherige Erfolglosigkeit der Konjugat-Aks am Markt hat übrigens nichts mit ihrer Wirksamkeit zu tun sondern vorwiegend mit unnötigen regulatorischen Hemmnissen und mangelden finanziellen Anreizen für die Ärzte die aufwendigere aber weit wirksamere Therapie durchzuführen.
Antwort auf Beitrag Nr.: 36.470.633 von Ville7 am 29.01.09 02:46:21Kleine Korrektur: Rituxan und Zevalin binden natürlich beide an CD20 und nicht CD19. Freud'scher Vertippsler, weil ich den MDX-AK gegen CD19, der ein besseres Rituxan werden soll, auch sehr sehr vielversprechend finde.
Die Pipe ist voller vielversprechender Kandidaten.
Die Pipe ist voller vielversprechender Kandidaten.
Antwort auf Beitrag Nr.: 36.470.627 von Ville7 am 29.01.09 02:26:42PS: Heute oder morgen wird es (lt. Genmab Ankündigung) den Zulassungsantrag für den vierten Antikörper aus der Ultimab Technologie von Medarex geben (zur Erinnerung: 1. Ustekinumab, 2. Golimumab, 3. ACZ885). Allerdings ist Ofatumumab von Genmab, die sich seinerzeit eine Lizenz auf die Medarex Technologie gesichert haben. Immerhin hält Medarex noch 5% an Genmab und profitiert somit indirekt auch hiervon.
ACZ885 (Canakinumab) ist ein neues Medikament gegen eine Gruppe seltener, aber lebensbedrohlicher autoinflammatorischer Erkrankungen, die unter dem Begriff Cryopyrin-assoziierte periodische Syndrome (CAPS) zusammengefasst werden und zu denen auch das Muckle-Wells-Syndrom zählt. Die ersten Zulassungsanträge waren ursprünglich für 2009 geplant, wurden jedoch auf Dezember 2008 vorgezogen, nachdem Daten aus zwei klinischen Studien bei Erwachsenen und Kindern eine schnelle und lang anhaltende klinische Remission von Symptomen dieser Krankheiten belegten. In der EU, der Schweiz und den USA wurde ACZ885 in der Behandlung von CAPS als Orphan-Arzneimittel eingestuft - in den USA und der EU auch in der Behandlung systemischer juveniler idiopathischer Arthritis (SJIA), der schwersten Form von Arthritis bei Kindern. Gegenwärtig laufen Studien für die mögliche Anwendung von ACZ885 in anderen Therapiegebieten.
Scheint alles sehr gut zu laufen für Medarex!
Mir ist aber immer noch nicht klar, wieso Sie nicht die Zulassung
von Ustekinumab in Europa als Nachricht veröffentlich haben?!?!?
Also, so` Sch....
Nicht das wir nur in den USA milestones und royalties auf Umsätze bekommen!...
Als in Kanada die Zulassung erfolgte hatten wie prompt die nachricht darüber von Medarex!!! [sehr seltsam...]
Ustekinumab wird auf mittelfristige Sicht ein richtiger Blockbuster werden...
Etwas Problemmatisch ich sehe ich z.Zeit auch.... das viele neuen Medikamententrails Thread: Kosovo Spenden noch keine Patienten rekrutieren...
Medarex ist gerade an vielen Baustellen beschäftigt und scheinbar hängt da etwas...
Nichtdestrotz glaube ich fest daran, dass wir dieses Jahr endlich einen ordentlichen Schub bekommen werden...
Mir ist aber immer noch nicht klar, wieso Sie nicht die Zulassung
von Ustekinumab in Europa als Nachricht veröffentlich haben?!?!?

Also, so` Sch....

Nicht das wir nur in den USA milestones und royalties auf Umsätze bekommen!...
Als in Kanada die Zulassung erfolgte hatten wie prompt die nachricht darüber von Medarex!!! [sehr seltsam...]
Ustekinumab wird auf mittelfristige Sicht ein richtiger Blockbuster werden...
Etwas Problemmatisch ich sehe ich z.Zeit auch.... das viele neuen Medikamententrails Thread: Kosovo Spenden noch keine Patienten rekrutieren...
Medarex ist gerade an vielen Baustellen beschäftigt und scheinbar hängt da etwas...
Nichtdestrotz glaube ich fest daran, dass wir dieses Jahr endlich einen ordentlichen Schub bekommen werden...
Antwort auf Beitrag Nr.: 36.473.138 von where_is_the_beef am 29.01.09 12:56:54Wir kennen die Verträge und Meldungsbestimmungen zwischen JnJ und MEDx nicht. Es könnte sein, dass die erste Zulassung gemeldet werden darf, mehr aber nicht. Die erste Zulassung (hier Kanada) löst dann die vereinbarte Meilensteinzahlung aus.
Ähnlich bei Novartis, die ja offensichtlich noch in 2008 gefilt haben- sowohl MAA als auch BLA. Von der ACZ885 Submission hören wir vielleicht deswegen nichts, weil MEDX erst bei Annahme der Anträghe durch die Zulassugnsbehörden melden darf. Also keine Ahnung ob sie nicht wollen (dann sind sie doof) oder nicht dürfen (dann bleibt nichts anderes übrig).
Ähnlich bei Novartis, die ja offensichtlich noch in 2008 gefilt haben- sowohl MAA als auch BLA. Von der ACZ885 Submission hören wir vielleicht deswegen nichts, weil MEDX erst bei Annahme der Anträghe durch die Zulassugnsbehörden melden darf. Also keine Ahnung ob sie nicht wollen (dann sind sie doof) oder nicht dürfen (dann bleibt nichts anderes übrig).
Genmab hat heute den Zulassungs-Antrag für Ofatumumab gestellt. Good news auch für Medarex.
Sehr schön!
Läuft alles nach Plan für Medarex...
Trotzdem kapier ich es immer noch nicht...
die Geschichte mit dem Approval von Ustekinumab in Europa!
Genauso die Sache, falls das stimmt mit Novartis...
... welche beso..... CEO macht solche Verträge!
Egal....
Medarex steigt heute schön bei fallenden Märkten...
Läuft alles nach Plan für Medarex...
Trotzdem kapier ich es immer noch nicht...
die Geschichte mit dem Approval von Ustekinumab in Europa!
Genauso die Sache, falls das stimmt mit Novartis...
... welche beso..... CEO macht solche Verträge!
Egal....

Medarex steigt heute schön bei fallenden Märkten...
@Ville7
Hi... sach mal... im Yahoo.com Board ist so ein allwissenden Checker dabei, welcher behauptet das die BLA von Genmab für CLL sinnlos ist.
Begründung: Die Studie ist zu klein, nicht doppel-blind und randomisiert...
Da mag ja was dran sein, aber Genmab und GSK werden wohl kam eine BLA stellen, wenn sie nicht annehmen, das Sie Erfolg haben.
Außerdem denke ich, dass diese BLA noch mit weiteren Daten unterfüttert wird. Ähnlich wie J&J mit Golimumab, wo auch die BLA eher gestellt wurde und einige Studien zum Teil noch liefen!
Was denkst Du bzw. jemand anderes dazu...
Medarex hält sich heute noch ganz gut, wobei ich endlich mal einen ordentlich, dicken, grünen Anstieg gen Norden sehen will!
Hi... sach mal... im Yahoo.com Board ist so ein allwissenden Checker dabei, welcher behauptet das die BLA von Genmab für CLL sinnlos ist.
Begründung: Die Studie ist zu klein, nicht doppel-blind und randomisiert...
Da mag ja was dran sein, aber Genmab und GSK werden wohl kam eine BLA stellen, wenn sie nicht annehmen, das Sie Erfolg haben.
Außerdem denke ich, dass diese BLA noch mit weiteren Daten unterfüttert wird. Ähnlich wie J&J mit Golimumab, wo auch die BLA eher gestellt wurde und einige Studien zum Teil noch liefen!
Was denkst Du bzw. jemand anderes dazu...
Medarex hält sich heute noch ganz gut, wobei ich endlich mal einen ordentlich, dicken, grünen Anstieg gen Norden sehen will!

Antwort auf Beitrag Nr.: 36.484.687 von where_is_the_beef am 30.01.09 19:04:05Das Problem ist, dass big pharma meist die Bedinungen vorschrieben kann. Ihnen ist eben Geheimhaltung wichtiger. Bei Morphosys ist das genauso. Sie dürfen auch nur das melden was vorher explizit vertrgalich gestattet wurde oder das was der Partner auf Anfrage erlaubt. Und big pharma erlaubt wenig. Also ich würde das nicht als ungewöhnlich erachten.
Antwort auf Beitrag Nr.: 36.486.106 von where_is_the_beef am 30.01.09 22:22:18Ich muss gestehen, dass ich mich mit den kleinsten Ofatumumb Einzelheiten nicht beschäftigt habe, da mein Engagement in Genmab doch recht beschränkt ist.
Fakt ist doch: Ofatumumab ist das klar bessere Produkt im Vergleich zu Marktführer Rituxan. Es hat ein besseres Nebenwirkungsprofil (voll human) und es wirkt besser - zumindest bei den Indikationen in denen ich Ergebnisse las.
Ob die Zulassung nun schon mit diesem BLA erfolgt oder einer der anderen Indikationen ist nur eine zeitliche Verzögerung.
Bei der FDA weiß man derzeit nicht wie sie reagiert, auch bei guten Produkten, siehe Ustekinumab. Da kann es gut mal vorkommen, dass Schwächen im Trialdesign (wenig Patienten, nicht verblindet) trotz überragender Ergebnisse zu einem nur Approvable Letter führen können oder ein Complete Response Letter mit verzögernder Wirkung versendet wird. Motivation der FDA ist hier m.E. auch der finanzielle Aspekt. Möglichst lange neue und teure Mittel nicht an den Markt zu bringen, da sonst die Kosten im Gesundheitswesen zu schnell exploderen.
Also einfach Abwarten, Tee trinken. Ich denke die Zulassung von Ofatumumab ist recht sicher, ob schon in dieser Indikation wird sich aber zeigen.
Fakt ist doch: Ofatumumab ist das klar bessere Produkt im Vergleich zu Marktführer Rituxan. Es hat ein besseres Nebenwirkungsprofil (voll human) und es wirkt besser - zumindest bei den Indikationen in denen ich Ergebnisse las.
Ob die Zulassung nun schon mit diesem BLA erfolgt oder einer der anderen Indikationen ist nur eine zeitliche Verzögerung.
Bei der FDA weiß man derzeit nicht wie sie reagiert, auch bei guten Produkten, siehe Ustekinumab. Da kann es gut mal vorkommen, dass Schwächen im Trialdesign (wenig Patienten, nicht verblindet) trotz überragender Ergebnisse zu einem nur Approvable Letter führen können oder ein Complete Response Letter mit verzögernder Wirkung versendet wird. Motivation der FDA ist hier m.E. auch der finanzielle Aspekt. Möglichst lange neue und teure Mittel nicht an den Markt zu bringen, da sonst die Kosten im Gesundheitswesen zu schnell exploderen.
Also einfach Abwarten, Tee trinken. Ich denke die Zulassung von Ofatumumab ist recht sicher, ob schon in dieser Indikation wird sich aber zeigen.
Antwort auf Beitrag Nr.: 36.486.106 von where_is_the_beef am 30.01.09 22:22:18In der PIII ging es ja auch nicht darum, ob Ofatumumb besser als andere Therapeutika gegen CLL wirkt, sondern ob es nach allen verfügbaren Standardtherapien überhaupt irgendeine Wirkung zeigt. Die CLL-Patienten in dieser PIII sprechen weder auf Fludarabin noch auf Campath an... ist das der Fall, so gibt es keine weitere zugelassene Therapie.
In einem solchen Fall akzeptiert die FDA auch positive Ansprechraten (normalerweise sollte bei diesen Patienten nichts mehr ansprechen) für eine vorzeitige Zulassung.
http://www.jyskebank.dk/_jb/commoninc/bin.asp?id=226086&src=…
Despite the fact that the US health authorities, the FDA, do not recognise
objective response as a consistent survival indicator, the criterion is
frequently used for patients with a very short life expectancy and where no
effective drugs exist. The reason is that the FDA under these conditions
accepts objective response as an indicator of life expectancy and quality of life.
...
To obtain FDA approval of Ofatumumab in refractory B-cell chronic lymphatic
leukaemia, Genmab will, in our opinion, have to demonstrate objective
response similar to that of Alemtuzumab, i.e. a response rate of 30 per cent or
above. In phase III, Alemtuzumab showed an objective response rate of 30 per
cent, but its safety profile is inferior to that of Ofatumumab. Genmab has,
however, indicated that the company, together with GlaxoSmithKline, will
submit an application for approval provided that a response rate of 25 per cent
is achieved.
Die Ansprechraten lagen sogar deutlich über 30%... nämlich 47% und 58%, was bei diesen eigentlich austherapierten Patienten sehr gut ist.
http://www.journalonko.de/newsview.php?id=2997
Der Unterschied zwischen Ofatumumab und Rituxan liegt neben dem voll-humanen in einer leicht anderen Bindungsstelle an CD20, die näher an der Zelloberfläche liegt. Dadurch wirkt Ofatumumab bereits bei niedrigerer Dosierung und bei Krebsarten mit niedriger CD20-Expressionierung wie z.B. CLL. Rituxan wird meistens gegen NHL eingesetzt, ob Ofatumumab da Vorteile bietet, muss sich noch zeigen... aber bei CLL soll es zumindest theoretisch deutlich besser wirken als Rituxan.
mfg ipollit
In einem solchen Fall akzeptiert die FDA auch positive Ansprechraten (normalerweise sollte bei diesen Patienten nichts mehr ansprechen) für eine vorzeitige Zulassung.
http://www.jyskebank.dk/_jb/commoninc/bin.asp?id=226086&src=…
Despite the fact that the US health authorities, the FDA, do not recognise
objective response as a consistent survival indicator, the criterion is
frequently used for patients with a very short life expectancy and where no
effective drugs exist. The reason is that the FDA under these conditions
accepts objective response as an indicator of life expectancy and quality of life.
...
To obtain FDA approval of Ofatumumab in refractory B-cell chronic lymphatic
leukaemia, Genmab will, in our opinion, have to demonstrate objective
response similar to that of Alemtuzumab, i.e. a response rate of 30 per cent or
above. In phase III, Alemtuzumab showed an objective response rate of 30 per
cent, but its safety profile is inferior to that of Ofatumumab. Genmab has,
however, indicated that the company, together with GlaxoSmithKline, will
submit an application for approval provided that a response rate of 25 per cent
is achieved.
Die Ansprechraten lagen sogar deutlich über 30%... nämlich 47% und 58%, was bei diesen eigentlich austherapierten Patienten sehr gut ist.
http://www.journalonko.de/newsview.php?id=2997
Der Unterschied zwischen Ofatumumab und Rituxan liegt neben dem voll-humanen in einer leicht anderen Bindungsstelle an CD20, die näher an der Zelloberfläche liegt. Dadurch wirkt Ofatumumab bereits bei niedrigerer Dosierung und bei Krebsarten mit niedriger CD20-Expressionierung wie z.B. CLL. Rituxan wird meistens gegen NHL eingesetzt, ob Ofatumumab da Vorteile bietet, muss sich noch zeigen... aber bei CLL soll es zumindest theoretisch deutlich besser wirken als Rituxan.
mfg ipollit
Antwort auf Beitrag Nr.: 36.489.852 von ipollit am 01.02.09 13:29:20und was vielleicht auch noch wichtig ist... Ofatumumb wirkt auch nach einer vorherigen Therpaie mit Rituxan.
Strong safety and efficacy support approval in CLL
We attended the oral data presentation of Genmab’s ofatumumab phase III trial in relapsed/refractory CLL (a blood cancer) at the ASH clinical meeting. The data, described as "quite stunning" by a leading CLL clinician, showed impressive response rates across all patient subgroups, including patients previously exposed to Rituxan, another antibody commonly used to treat CLL. Clinicians also thought ofatumumab was safe and well tolerated. In our view the data strongly support approval of ofatumumab in relapsed/refractory CLL, for which Genmab and partner GSK plan to file in January 2009. We have increased our CLL peak sales forecasts from $350mn to $500mn and upgrade to Buy from Neutral.
High response rates across patient subgroups
Response rates were consistently high in all patient subgroup analyses performed (47-50+%), including prior exposure to the Rituxan. 54% of double refractory (DR) patients previously exposed to Rituxan achieved a response vs. 63% of those not exposed. The response rates in the Campath-ineligible (BFR) group were 44%
and 50%. It is not clear whether ofatumumab is effective in Rituxan refractory patients, however, as it is difficult to discern whether patients were refractory to the chemotherapy or to Rituxan itself.
Safety profile benign, impressive survival
Clinicians we spoke to had no concerns about ofatumumab's safety profile, and most thought it was comparable to Rituxan's. The 25% infection rate was not seen as an issue, as late-stage CLL patients are generally immunosuppressed and hence highly susceptible to infections regardless of therapy. Clinicians were both
surprised and impressed by the high response rates achieved. Historical analysis and their own data demonstrate that these patients do not respond to antibody therapy and survive for only 9-10 months (vs. 14-15 months in this study).
Duration of response slightly disappointing to some
Patients who responded to ofatumumab maintained their response for 6-7 months and experienced progression-free survival (PFS) of 5.7 (DR) and 5.9 (BFR) months. While this is well above the 3-4 months indicated by FDA for approval, some clinicians voiced disappointment, particularly given the strength of the response rates. However, it needs to be taken into account that the study enrolled
a very challenging patient population.
mfg ipollit
Strong safety and efficacy support approval in CLL
We attended the oral data presentation of Genmab’s ofatumumab phase III trial in relapsed/refractory CLL (a blood cancer) at the ASH clinical meeting. The data, described as "quite stunning" by a leading CLL clinician, showed impressive response rates across all patient subgroups, including patients previously exposed to Rituxan, another antibody commonly used to treat CLL. Clinicians also thought ofatumumab was safe and well tolerated. In our view the data strongly support approval of ofatumumab in relapsed/refractory CLL, for which Genmab and partner GSK plan to file in January 2009. We have increased our CLL peak sales forecasts from $350mn to $500mn and upgrade to Buy from Neutral.
High response rates across patient subgroups
Response rates were consistently high in all patient subgroup analyses performed (47-50+%), including prior exposure to the Rituxan. 54% of double refractory (DR) patients previously exposed to Rituxan achieved a response vs. 63% of those not exposed. The response rates in the Campath-ineligible (BFR) group were 44%
and 50%. It is not clear whether ofatumumab is effective in Rituxan refractory patients, however, as it is difficult to discern whether patients were refractory to the chemotherapy or to Rituxan itself.
Safety profile benign, impressive survival
Clinicians we spoke to had no concerns about ofatumumab's safety profile, and most thought it was comparable to Rituxan's. The 25% infection rate was not seen as an issue, as late-stage CLL patients are generally immunosuppressed and hence highly susceptible to infections regardless of therapy. Clinicians were both
surprised and impressed by the high response rates achieved. Historical analysis and their own data demonstrate that these patients do not respond to antibody therapy and survive for only 9-10 months (vs. 14-15 months in this study).
Duration of response slightly disappointing to some
Patients who responded to ofatumumab maintained their response for 6-7 months and experienced progression-free survival (PFS) of 5.7 (DR) and 5.9 (BFR) months. While this is well above the 3-4 months indicated by FDA for approval, some clinicians voiced disappointment, particularly given the strength of the response rates. However, it needs to be taken into account that the study enrolled
a very challenging patient population.
mfg ipollit
Hi Ville & ipollit...
sehr interessante Beiträge!!!
> Motivation der FDA ist hier m.E. auch der finanzielle Aspekt. Möglichst lange neue und teure Mittel nicht an den Markt zu bringen, da sonst die Kosten im Gesundheitswesen zu schnell exploderen.
Das denke ich auch! Da ich das ja tagtäglich sehe; was das alles kostet, glaube ich ebenfalls das die Zulassungsbehörden manche Dinge bewußt in die Länge ziehen... wegen der Kosten...
Genmab CD20 Mab ist besser! Basiert ja auf unserer geliebten vollhumanen Medarexmaus!
Das ist ja auch der Reiz an Medarex... ist halt kein one-trick-pony Firma ala Ex-oder-Hopp!...
sehr interessante Beiträge!!!

> Motivation der FDA ist hier m.E. auch der finanzielle Aspekt. Möglichst lange neue und teure Mittel nicht an den Markt zu bringen, da sonst die Kosten im Gesundheitswesen zu schnell exploderen.
Das denke ich auch! Da ich das ja tagtäglich sehe; was das alles kostet, glaube ich ebenfalls das die Zulassungsbehörden manche Dinge bewußt in die Länge ziehen... wegen der Kosten...
Genmab CD20 Mab ist besser! Basiert ja auf unserer geliebten vollhumanen Medarexmaus!

Das ist ja auch der Reiz an Medarex... ist halt kein one-trick-pony Firma ala Ex-oder-Hopp!...

1 Mio ist nicht viel, aber immerhin. Ein Beispiel auch für einen Vertrag bei dem MEDX sogar die Summe melden darf.
................................
Medarex to Receive Milestone Payment from MedImmune for Allowance of an Investigational New Drug Application for MEDI-546
* Monday February 2, 2009, 8:00 am EST
PRINCETON, N.J., Feb. 2 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) today announced that it will receive a milestone payment of $1 million from its partner, MedImmune, LLC for the allowance of an Investigational New Drug (IND) application for MEDI-546, a fully human antibody that targets a component of the type 1 interferon pathway. MEDI-546 will be studied in patients with scleroderma, a chronic autoimmune disease characterized by hardening and thickening of the skin and other organs.
"This IND application marks the second antibody targeting the interferon inflammatory pathway that MedImmune has supported for advancement into the clinic using our UltiMAb® technology," said Howard H. Pien, Chairman and CEO of Medarex.
In November 2004, MedImmune entered into collaboration with Medarex to focus on two specific antibodies, MDX-1103 (now known as MEDI-545) and MDX-1333 (now known as MEDI-546). Under the terms of the agreement, MedImmune is responsible for all ongoing clinical development activities. Prior to the beginning of pivotal studies, Medarex may elect to co-develop the products in return for the opportunity to co-promote and to receive a share of the commercial profits in the United States. In all other cases, Medarex will be entitled to receive milestone payments and royalties.
................................
Medarex to Receive Milestone Payment from MedImmune for Allowance of an Investigational New Drug Application for MEDI-546
* Monday February 2, 2009, 8:00 am EST
PRINCETON, N.J., Feb. 2 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) today announced that it will receive a milestone payment of $1 million from its partner, MedImmune, LLC for the allowance of an Investigational New Drug (IND) application for MEDI-546, a fully human antibody that targets a component of the type 1 interferon pathway. MEDI-546 will be studied in patients with scleroderma, a chronic autoimmune disease characterized by hardening and thickening of the skin and other organs.
"This IND application marks the second antibody targeting the interferon inflammatory pathway that MedImmune has supported for advancement into the clinic using our UltiMAb® technology," said Howard H. Pien, Chairman and CEO of Medarex.
In November 2004, MedImmune entered into collaboration with Medarex to focus on two specific antibodies, MDX-1103 (now known as MEDI-545) and MDX-1333 (now known as MEDI-546). Under the terms of the agreement, MedImmune is responsible for all ongoing clinical development activities. Prior to the beginning of pivotal studies, Medarex may elect to co-develop the products in return for the opportunity to co-promote and to receive a share of the commercial profits in the United States. In all other cases, Medarex will be entitled to receive milestone payments and royalties.
Antwort auf Beitrag Nr.: 36.494.664 von Ville7 am 02.02.09 14:10:34Höchstens 4 Jahre und 3 Monate ist auch ganz ok von Projektstart bis IND.
Antwort auf Beitrag Nr.: 36.494.945 von eck64 am 02.02.09 14:56:31Wo kannst du das da rauslesen?
Ich lese da nur raus, dass sie seit Nov.2004 zusammenarbeiten. Mir klingt das eher so als waren die AKs schon von MEDX selektiert (MDX-1103 und MDX-1333) und Medimmune ist in Nov.2004 draufgesprungen. Deswegen seit dem auch das neue Medimmune-Entwicklungskürzel.
Also nach meiner Interpretation weit mehr als 4 Jahre und drei Monate.
Ich lese da nur raus, dass sie seit Nov.2004 zusammenarbeiten. Mir klingt das eher so als waren die AKs schon von MEDX selektiert (MDX-1103 und MDX-1333) und Medimmune ist in Nov.2004 draufgesprungen. Deswegen seit dem auch das neue Medimmune-Entwicklungskürzel.
Also nach meiner Interpretation weit mehr als 4 Jahre und drei Monate.
Antwort auf Beitrag Nr.: 36.495.172 von Ville7 am 02.02.09 15:22:17Jetzt habe ichs im Original rausgesucht und du hast recht, der bzw. die tAKs ist/sind schon älter:
http://www.medimmune.com/press/fullstory.asp?reqid=646855&yr…
MedImmune and Medarex Announce Collaboration to Develop and Commercialize Fully Human Antibodies for Autoimmune Diseases
11/23/2004 8:01:00 AM
GAITHERSBURG, Md. and PRINCETON, N.J., Nov. 23 /PRNewswire-FirstCall/ -- MedImmune, Inc. (Nasdaq: MEDI) and Medarex, Inc. (Nasdaq: MEDX) today announced a collaboration to develop antibodies targeting interferon-alpha and the type I interferon receptor 1. The collaboration will initially focus on two antibodies, MDX-1103 and MDX-1333, that are currently in preclinical development by Medarex for the treatment of autoimmune diseases, such as systemic lupus erythematosus (SLE or lupus). The companies expect to file investigational new drug applications with the U.S. Food & Drug Administration within the next 18 months.
usw...
xxxxxxxxx
Die waren also 2004 bereits in anderer Indikation in Entwicklung und konnten also unmitelbar in die Präklinik starten.
18 Monate als Zeitziel bis IND ging aber gewaltig daneben.
http://www.medimmune.com/press/fullstory.asp?reqid=646855&yr…
MedImmune and Medarex Announce Collaboration to Develop and Commercialize Fully Human Antibodies for Autoimmune Diseases
11/23/2004 8:01:00 AM
GAITHERSBURG, Md. and PRINCETON, N.J., Nov. 23 /PRNewswire-FirstCall/ -- MedImmune, Inc. (Nasdaq: MEDI) and Medarex, Inc. (Nasdaq: MEDX) today announced a collaboration to develop antibodies targeting interferon-alpha and the type I interferon receptor 1. The collaboration will initially focus on two antibodies, MDX-1103 and MDX-1333, that are currently in preclinical development by Medarex for the treatment of autoimmune diseases, such as systemic lupus erythematosus (SLE or lupus). The companies expect to file investigational new drug applications with the U.S. Food & Drug Administration within the next 18 months.
usw...
xxxxxxxxx
Die waren also 2004 bereits in anderer Indikation in Entwicklung und konnten also unmitelbar in die Präklinik starten.
18 Monate als Zeitziel bis IND ging aber gewaltig daneben.

Antwort auf Beitrag Nr.: 36.495.308 von eck64 am 02.02.09 15:39:02Leider ist das die Realität, es dauert bei allen meist viel viel länger mit der Entwicklung als in der blanken Theorie möglich. Biogen Idecs Anti-Lingo IND ist auch so ein typisches Beispiel. 2007 noch für 2008 angekündigt. Anfang 2009 plötzlich auf Q4 2009 verschoben.
Antwort auf Beitrag Nr.: 36.495.763 von Ville7 am 02.02.09 16:26:52Tolle recherchen hier,ich bin begeistert.
Weiter so ,LG Bio

Weiter so ,LG Bio
Ab sofort wird nur mehr Stelara verschrieben statt Raptiva®(efalizumab,side effects).
Nicht nur Medarex wirds freun!
Nicht nur Medarex wirds freun!

Gestern nun auch der europäische Zulassungsantrag von GSk und Genmab zu Ofatumumab.
Wir sollten im Februar jetzt noch folgendes hören:
1. Annahme BLA ACZ885 in USA durch FDA
2. Annahme MAA ACZ885 in Europa durch EMEA
3. Zulassung Stelara in USA durch FDA
(Meine Einschätzung)
Wir sollten im Februar jetzt noch folgendes hören:
1. Annahme BLA ACZ885 in USA durch FDA
2. Annahme MAA ACZ885 in Europa durch EMEA
3. Zulassung Stelara in USA durch FDA
(Meine Einschätzung)
Ich halte auch MDX-1100 für sehr, sehr interessant!
(Hatte ich schon mal erzählt) Extrem breites Anwendungsgebiet!
CED, scheinbar Diabetes, "Schutz bei frischen Rückenmarkverletzungen..." kurzum => sehr interessant!
MDX-1100 Mab gegen CXCL10
Neue Erkenntnisse für Behandlung von Diabetes
09.02.2009 - Eine Entdeckung von Wissenschaftlern der Universität Bremen könnte dabei helfen, neue Therapien gegen die Volkskrankheit Diabetes zu entwickeln. Dr. Kathrin Mädler und ihr Forscherteam vom Inselzellforschungslabor am Centre for Biomolecular Interactions des Fachbereichs Biologie/Chemie haben bei Diabetespatienten den entzündlichen Faktor namens CXCL10 aufgedeckt, der an der Zerstörung der insulinproduzierenden Beta-Zellen entscheidend beteiligt ist.
"Wir haben einen entzündlichen Marker in beiden Typen der Zuckerkrankheit gefunden", sagt Mädler. "Wenn wir Zellen vor dem entzündlichen CXCL10 schützen könnten, wäre es möglich, die Zerstörung der Beta-Zellmasse zu verhindern, die zum Ausbruch der Zuckerkrankheit führt."
Bei Diabetes unterscheidet man zwischen Typ I und Typ II. Typ I entsteht durch eine Überschussreaktion des Immunsystems. Körpereigene Beta-Zellen werden durch hohe Konzentrationen von entzündlichen Signalen zerstört. Während Wissenschaftler viele Erkenntnisse über diese Autoimmunreaktion gewonnen haben, ist die Ursache des Beta-Zellverlust im Typ II Diabetes - bekannt auch als Altersdiabetes - eine vieldiskutierte Debatte. Das Forscherteam von Mädler vermutet, dass auch hier entzündliche Faktoren eine Schlüsselrolle spielen. Die neuen Erkenntnisse könnten dabei helfen, entsprechende Entzündungshemmer zu entwickeln, um die Beta-Zellen vor ihrer Zerstörung zu retten.
Dr. Kathrin Mädler und ihr Team arbeiten an der Universität Bremen an der Erforschung der Ursachen von Diabetesentstehung. Ziel ihrer Arbeit ist es, neue Ansätze für die Therapie des Diabetes zu finden.
Originalveröffentlichung: Cell Metabolism, Februar 2009
(Hatte ich schon mal erzählt) Extrem breites Anwendungsgebiet!
CED, scheinbar Diabetes, "Schutz bei frischen Rückenmarkverletzungen..." kurzum => sehr interessant!
MDX-1100 Mab gegen CXCL10
Neue Erkenntnisse für Behandlung von Diabetes
09.02.2009 - Eine Entdeckung von Wissenschaftlern der Universität Bremen könnte dabei helfen, neue Therapien gegen die Volkskrankheit Diabetes zu entwickeln. Dr. Kathrin Mädler und ihr Forscherteam vom Inselzellforschungslabor am Centre for Biomolecular Interactions des Fachbereichs Biologie/Chemie haben bei Diabetespatienten den entzündlichen Faktor namens CXCL10 aufgedeckt, der an der Zerstörung der insulinproduzierenden Beta-Zellen entscheidend beteiligt ist.
"Wir haben einen entzündlichen Marker in beiden Typen der Zuckerkrankheit gefunden", sagt Mädler. "Wenn wir Zellen vor dem entzündlichen CXCL10 schützen könnten, wäre es möglich, die Zerstörung der Beta-Zellmasse zu verhindern, die zum Ausbruch der Zuckerkrankheit führt."
Bei Diabetes unterscheidet man zwischen Typ I und Typ II. Typ I entsteht durch eine Überschussreaktion des Immunsystems. Körpereigene Beta-Zellen werden durch hohe Konzentrationen von entzündlichen Signalen zerstört. Während Wissenschaftler viele Erkenntnisse über diese Autoimmunreaktion gewonnen haben, ist die Ursache des Beta-Zellverlust im Typ II Diabetes - bekannt auch als Altersdiabetes - eine vieldiskutierte Debatte. Das Forscherteam von Mädler vermutet, dass auch hier entzündliche Faktoren eine Schlüsselrolle spielen. Die neuen Erkenntnisse könnten dabei helfen, entsprechende Entzündungshemmer zu entwickeln, um die Beta-Zellen vor ihrer Zerstörung zu retten.
Dr. Kathrin Mädler und ihr Team arbeiten an der Universität Bremen an der Erforschung der Ursachen von Diabetesentstehung. Ziel ihrer Arbeit ist es, neue Ansätze für die Therapie des Diabetes zu finden.
Originalveröffentlichung: Cell Metabolism, Februar 2009
Verkauf von Stelara im großen Markt Europa gestartet, d.h. ab diesem Monat auch erste Produkt-Umsätze für Medarex aus einem ihrer Antikörper.
http://www.pharmatimes.com/UKNews/article.aspx?id=15280
Stelara ist besser in der Wirksamkeit und vor allem in der Häufigkeit der Dosierung gegenüber seinen Konkurrenten. Während Enbrel und Co. teils wöchentlich gespritzt werden müssen reicht bei Stelara eine viermalige Dosis pro Jahr!
Professor Kristian Reich, Facharzt für Dermatologie und Partner am Dermatologikum in Hamburg, sagt: „Mit Ustekinumab haben wir einen völlig neuen und vielversprechenden Wirkstoff, der schon nach wenigen Wochen zu einer erheblichen Reduktion der Symptome führt. Mit nur vier Verabreichungen pro Jahr in der Erhaltungstherapie kann das Medikament zu einem anhaltenden Therapieerfolg führen und die Lebensqualität dieser Patienten deutlich steigern.“
http://www.psoriasis-netz.de/stelara_zulassung.html
Stelara dürfte also bal signifikante Umsätze erzielen und spätestens in ein paar Jahren den Blockbusterstatus erreichen (Verkäufe > 1Milliarde USD).
Fehlt jetzt noch Zulassung und Marktstart in USA.
http://www.pharmatimes.com/UKNews/article.aspx?id=15280
Stelara ist besser in der Wirksamkeit und vor allem in der Häufigkeit der Dosierung gegenüber seinen Konkurrenten. Während Enbrel und Co. teils wöchentlich gespritzt werden müssen reicht bei Stelara eine viermalige Dosis pro Jahr!
Professor Kristian Reich, Facharzt für Dermatologie und Partner am Dermatologikum in Hamburg, sagt: „Mit Ustekinumab haben wir einen völlig neuen und vielversprechenden Wirkstoff, der schon nach wenigen Wochen zu einer erheblichen Reduktion der Symptome führt. Mit nur vier Verabreichungen pro Jahr in der Erhaltungstherapie kann das Medikament zu einem anhaltenden Therapieerfolg führen und die Lebensqualität dieser Patienten deutlich steigern.“
http://www.psoriasis-netz.de/stelara_zulassung.html
Stelara dürfte also bal signifikante Umsätze erzielen und spätestens in ein paar Jahren den Blockbusterstatus erreichen (Verkäufe > 1Milliarde USD).
Fehlt jetzt noch Zulassung und Marktstart in USA.
Moin....
dazu passt => einfach mal im PS-Board zu lesen!
http://www.psoriasis-netz.net/forum/showthread.php?t=224145&…
5 x Spritzen von Stelara verteilt im Jahr und viele Betroffene können wieder normal leben!
Das Medi. wird sich schneller durchsetzen als prognostiziert!
So! => Jetzt will ich ne Erfolgsnews auf der Medarex HP sehen!!!
dazu passt => einfach mal im PS-Board zu lesen!
http://www.psoriasis-netz.net/forum/showthread.php?t=224145&…
5 x Spritzen von Stelara verteilt im Jahr und viele Betroffene können wieder normal leben!
Das Medi. wird sich schneller durchsetzen als prognostiziert!
So! => Jetzt will ich ne Erfolgsnews auf der Medarex HP sehen!!!

Nach einem langen Ringen mit mir selbst, bin ich gerade eben MEDX-Aktionär geworden (zu 5,97 Dollar). Ich finde den cashburn des Unternehmens wirklich gruselig und darum habe ich so lange gezweifelt. Ich hoffe, die Pipeline ist wirklich so werthaltig, wie ich es mir einbilde...
Antwort auf Beitrag Nr.: 36.567.409 von SLGramann am 12.02.09 17:24:50Überraschung wäre ein finanzkriselnder Cashberg. Eben ängstigte noch der Cashburn und ratzfatz gehts schneller.
Gibts keine Biotechs mit Subprimegedöhns
Gibts keine Biotechs mit Subprimegedöhns

Antwort auf Beitrag Nr.: 36.577.508 von Friseuse am 13.02.09 21:03:02
Ich weiß nicht, in welcher Form und bei wem MEDX Cash hält. Die größere Gefahr für den Cashhügel von MEDX sind aber aus meiner Sicht die hohen Ausgaben für R&D, nicht die Finanzkrise, obschon die gewiss weitere Risiken mit sich bringt - selbst für Anlagen in "cash".
Investiert habe ich jetzt aber, weil ich Villes Argumentation nachvollziehbar finde, dass durch eine Zulassung von Golimumab und Ustekinumab bei MEDX endlich ein stabiles Geschäftsmodell aufgebaut werden könnte, das meint ganz simpel, dass die Ausgaben- und die Einnahmeseite ins Gleichgewicht kommen - vielleicht mit leichtem Übergewicht bei den Einnahmen, statt wie bisher krassem Übergewicht bei den Ausgaben. Das scheint mir übrigens für jedes Unternhehmen ein verfolgenswertes Konzept zu sein...
Die Einstellung von Ipilimumab würde dieses nachhaltige Businessmodell sogar unterstützen. Natürlich wäre hier ein Erfolg sehr viel mehr zu wünschen, aber aus dem Bauch und völlig frei von medizinischer Kompetenz , fürchte ich nach der bisherigen Geschichte eben einfach, dass man hier versucht, ein totes Pferd zu reiten. Insofern würde ich sagen, dass sich der status quo bei Ipilimumab in einigermaßen absehbarer Zeit (bis 2010 oder 11) auf jeden Fall ändern wird und dass jede Änderung positiv ist, selbst die negative... auch wenn das jetzt etwas heftig dialektisch ist...
, fürchte ich nach der bisherigen Geschichte eben einfach, dass man hier versucht, ein totes Pferd zu reiten. Insofern würde ich sagen, dass sich der status quo bei Ipilimumab in einigermaßen absehbarer Zeit (bis 2010 oder 11) auf jeden Fall ändern wird und dass jede Änderung positiv ist, selbst die negative... auch wenn das jetzt etwas heftig dialektisch ist... 
Ich weiß nicht, in welcher Form und bei wem MEDX Cash hält. Die größere Gefahr für den Cashhügel von MEDX sind aber aus meiner Sicht die hohen Ausgaben für R&D, nicht die Finanzkrise, obschon die gewiss weitere Risiken mit sich bringt - selbst für Anlagen in "cash".
Investiert habe ich jetzt aber, weil ich Villes Argumentation nachvollziehbar finde, dass durch eine Zulassung von Golimumab und Ustekinumab bei MEDX endlich ein stabiles Geschäftsmodell aufgebaut werden könnte, das meint ganz simpel, dass die Ausgaben- und die Einnahmeseite ins Gleichgewicht kommen - vielleicht mit leichtem Übergewicht bei den Einnahmen, statt wie bisher krassem Übergewicht bei den Ausgaben. Das scheint mir übrigens für jedes Unternhehmen ein verfolgenswertes Konzept zu sein...
Die Einstellung von Ipilimumab würde dieses nachhaltige Businessmodell sogar unterstützen. Natürlich wäre hier ein Erfolg sehr viel mehr zu wünschen, aber aus dem Bauch und völlig frei von medizinischer Kompetenz
 , fürchte ich nach der bisherigen Geschichte eben einfach, dass man hier versucht, ein totes Pferd zu reiten. Insofern würde ich sagen, dass sich der status quo bei Ipilimumab in einigermaßen absehbarer Zeit (bis 2010 oder 11) auf jeden Fall ändern wird und dass jede Änderung positiv ist, selbst die negative... auch wenn das jetzt etwas heftig dialektisch ist...
, fürchte ich nach der bisherigen Geschichte eben einfach, dass man hier versucht, ein totes Pferd zu reiten. Insofern würde ich sagen, dass sich der status quo bei Ipilimumab in einigermaßen absehbarer Zeit (bis 2010 oder 11) auf jeden Fall ändern wird und dass jede Änderung positiv ist, selbst die negative... auch wenn das jetzt etwas heftig dialektisch ist... 
Antwort auf Beitrag Nr.: 36.579.854 von SLGramann am 14.02.09 14:17:12Investiert habe ich jetzt aber, weil ich Villes Argumentation nachvollziehbar finde, dass durch eine Zulassung von Golimumab und Ustekinumab bei MEDX endlich ein stabiles Geschäftsmodell aufgebaut werden könnte
Ich hoffe du weißt das MEDX nur je 3-5% an royalties für Goli und Uste bekommt ,das bedeutet die zwei Produkte müssen Blockbuster werden damit es sich für Medarex einigermaßen lohnt .
Immer mehr Investore verabschieden sich von MEDX ...
http://www.nasdaq.com/asp/holdings.asp?symbol=MEDX&symbol=SP…
Ich sehe nicht wirklich viel Spielraum nach oben ....
Ich hoffe du weißt das MEDX nur je 3-5% an royalties für Goli und Uste bekommt ,das bedeutet die zwei Produkte müssen Blockbuster werden damit es sich für Medarex einigermaßen lohnt .
Immer mehr Investore verabschieden sich von MEDX ...
http://www.nasdaq.com/asp/holdings.asp?symbol=MEDX&symbol=SP…
Ich sehe nicht wirklich viel Spielraum nach oben ....
Antwort auf Beitrag Nr.: 36.580.387 von BrauchGeld am 14.02.09 17:28:08Immer mehr Investoren haben sich von allen Werten, die ich kenne, verabschiedet. MEDX hat die Finanzkrise nicht erfunden. Interessanterweise springen bekannte Größen auf MEDX. Carl Icahn hat sich eine erste Position mit über 300.000 Aktien geholt.
Ich zweifle übrigens nicht, dass Golimumab (Achtung noch nicht zugelassen!) und Ustekinumab Blockbuster werden. Zwar nicht von heute auf morgen, aber in ihren Kernindikationen sind sie derzeit mit Abstand "best in class". Und ich sehe in den Entwicklungspipelines kein Produkt, dass dies in den nächsten Jahren angreifen könnte.
Wenn ich Golimumab mit Humira vergleiche, was durchaus ein valider Vergleich ist, denn Humira ging als "best in class" Produkt in den Markt, der bereits durch andere schlechtere Produkte mit Riesenumsätzen belegt war. Humira hat in 2008 4,5 Milliarden USD Umsatz gemacht und wächst weiter schnell. Sollte Golimumab dies 5 Jahre nach Zulassung auch schaffen ist der Cashburn von Medarex allein mit diesem einen Parterprodukt gestoppt.
Zur Einstellung von Ipilimumab: Das ist natürlich ganz und gar nicht positiv für Medarex, denn man hat hier bereits 100e Millionen Dollar versenkt. Ipilimumab sollte ein Erfolg werden, sonst kommt die Firma so schnell nicht wieder auf die Beine. Wenn ipilimumab auf den Markt kommt, dann erwarte ich hier auch gute Umsätze, denn ipilimumab hat das Potential Hoffnung: es heilt in geringer Anzahl auch dem Tod geweihte Krebspatienten. D.h. hohes Potential für off-label Einsatz, da im Falle einer Zulassung für Melanoma eine hohe Nachfrage enstehen würde. Schliesslich hat ipilimumab auch in anderen Krebsarten wundersame Compete Responses produziert. Und nicht nur da, sogar in Hunden wurden komlette Remissionen nachgewiesen. Nehmen wir nur solche Leute wie Steve Jobs, Apple Chef. Er hat Bauchspeicheldrüsenkrebs, unheilbar. Aber mit ipilimumab vielleicht eine 3-5%ige Chance auf eine komplette Remission und eine 30%ige Chance auf ein längeres Leben. Das will einer, der es sich leisten kann, auf jeden Fall haben. Ich hoffe er bekommt es auch jetzt schon auf anderen Wegen und wünsche ihm alles Gute und eine Wunderheilung - egal mit wlechem Mittel.
MEDX hat kurzfristig nur ein shot on goal für die Zulassung. Die Wirksamkeit muss jetzt aber in einem verblindeten Trial bewiesen werden. Die Chancen sind einigermassen gut, wenngleich der First Line Trial in Melanoma mit 500 Patienten etwas underpowered sein könnte. Schliesslich hat man von PFS auf OS umgeswitcht und dabei aber nicht nochmal nachrekrutiert - möglicherweise ein Fehler- falls man keine statistische Signifikanz erreicht. Dann heisst es weitere Jahre warten auf die Ergebnisse des Prostate Trials) oder Einstellung des Projekts. Ich würde aber vermuten, so wie BMS und MEDX bei ipilimumab Gas geben ist es eher Warten. Die sind m.E. sehr überzeugt von ipilimumab und den bisher (leider nur offen) gewonnenen Daten, welche z.b. im Melanomabereich eine einjährige Überlebenschance bei spätphasigen Patienten von ca. 50% im Vergleich zu bisherigen 25% gebracht hat. D.h. ca. 50% der Patienten mit ipilimumab Behandlung leben nach einem Jahr noch, wogegen historisch eigentlich nur 25% dies schaffen. Wenn das nur im Geringsten doppeltverblindet bestätigt werden kann wird der first line Trial in Kombi mit DTIC ein Erfolg. Aber man hat auch schon viele Pferde vor der Apotheke kotzen sehen-vor allem in der Medikamentenentwicklung.
Ich persönlich bin der Meinung, dass Antikörper die Medikamentenklasse der Zukunft sind und dass Medarex als ein führender Anbieter hier zum Erfolg verdammt ist. Cash reicht aus um zu Überleben und die Pipeline ist prall gefüllt.
Möglicherweise kann der Cash durch weitere Deals (z.b. MDX-1100 oder MDX-066) aufgehübscht werden. Wir werden sehen was passiert. Überlebensgefährdet halte ich Medarex auf jeden Fall nicht.
Ich zweifle übrigens nicht, dass Golimumab (Achtung noch nicht zugelassen!) und Ustekinumab Blockbuster werden. Zwar nicht von heute auf morgen, aber in ihren Kernindikationen sind sie derzeit mit Abstand "best in class". Und ich sehe in den Entwicklungspipelines kein Produkt, dass dies in den nächsten Jahren angreifen könnte.
Wenn ich Golimumab mit Humira vergleiche, was durchaus ein valider Vergleich ist, denn Humira ging als "best in class" Produkt in den Markt, der bereits durch andere schlechtere Produkte mit Riesenumsätzen belegt war. Humira hat in 2008 4,5 Milliarden USD Umsatz gemacht und wächst weiter schnell. Sollte Golimumab dies 5 Jahre nach Zulassung auch schaffen ist der Cashburn von Medarex allein mit diesem einen Parterprodukt gestoppt.
Zur Einstellung von Ipilimumab: Das ist natürlich ganz und gar nicht positiv für Medarex, denn man hat hier bereits 100e Millionen Dollar versenkt. Ipilimumab sollte ein Erfolg werden, sonst kommt die Firma so schnell nicht wieder auf die Beine. Wenn ipilimumab auf den Markt kommt, dann erwarte ich hier auch gute Umsätze, denn ipilimumab hat das Potential Hoffnung: es heilt in geringer Anzahl auch dem Tod geweihte Krebspatienten. D.h. hohes Potential für off-label Einsatz, da im Falle einer Zulassung für Melanoma eine hohe Nachfrage enstehen würde. Schliesslich hat ipilimumab auch in anderen Krebsarten wundersame Compete Responses produziert. Und nicht nur da, sogar in Hunden wurden komlette Remissionen nachgewiesen. Nehmen wir nur solche Leute wie Steve Jobs, Apple Chef. Er hat Bauchspeicheldrüsenkrebs, unheilbar. Aber mit ipilimumab vielleicht eine 3-5%ige Chance auf eine komplette Remission und eine 30%ige Chance auf ein längeres Leben. Das will einer, der es sich leisten kann, auf jeden Fall haben. Ich hoffe er bekommt es auch jetzt schon auf anderen Wegen und wünsche ihm alles Gute und eine Wunderheilung - egal mit wlechem Mittel.
MEDX hat kurzfristig nur ein shot on goal für die Zulassung. Die Wirksamkeit muss jetzt aber in einem verblindeten Trial bewiesen werden. Die Chancen sind einigermassen gut, wenngleich der First Line Trial in Melanoma mit 500 Patienten etwas underpowered sein könnte. Schliesslich hat man von PFS auf OS umgeswitcht und dabei aber nicht nochmal nachrekrutiert - möglicherweise ein Fehler- falls man keine statistische Signifikanz erreicht. Dann heisst es weitere Jahre warten auf die Ergebnisse des Prostate Trials) oder Einstellung des Projekts. Ich würde aber vermuten, so wie BMS und MEDX bei ipilimumab Gas geben ist es eher Warten. Die sind m.E. sehr überzeugt von ipilimumab und den bisher (leider nur offen) gewonnenen Daten, welche z.b. im Melanomabereich eine einjährige Überlebenschance bei spätphasigen Patienten von ca. 50% im Vergleich zu bisherigen 25% gebracht hat. D.h. ca. 50% der Patienten mit ipilimumab Behandlung leben nach einem Jahr noch, wogegen historisch eigentlich nur 25% dies schaffen. Wenn das nur im Geringsten doppeltverblindet bestätigt werden kann wird der first line Trial in Kombi mit DTIC ein Erfolg. Aber man hat auch schon viele Pferde vor der Apotheke kotzen sehen-vor allem in der Medikamentenentwicklung.
Ich persönlich bin der Meinung, dass Antikörper die Medikamentenklasse der Zukunft sind und dass Medarex als ein führender Anbieter hier zum Erfolg verdammt ist. Cash reicht aus um zu Überleben und die Pipeline ist prall gefüllt.
Möglicherweise kann der Cash durch weitere Deals (z.b. MDX-1100 oder MDX-066) aufgehübscht werden. Wir werden sehen was passiert. Überlebensgefährdet halte ich Medarex auf jeden Fall nicht.
Antwort auf Beitrag Nr.: 36.577.508 von Friseuse am 13.02.09 21:03:02Wieso sollte Medarex direkt in Subprime angelegt haben? Welch wunderbare Phantasie muss man haben? Wären sie von Lehmann oder Madoff betroffen gewesen hätten sie es bereits mitteilen müssen.
Die reale Bedrohung ist eher, ob Banken bei denen MEDX angelegt hat, hopps gehen und dadurch deren Geld futsch ist. Da ich aber davon ausgehe, dass keine Bank mehr a la Lehmann hopps gegangen gelassen werden wird, wird dies wohl nicht psassieren. Da gehen eher die Staaten, die die Banken retten und für sie garantieren, hopps.
Aber dann hast du Armageddon. Dann kannste die meisten Firmen begraben.
Die reale Bedrohung ist eher, ob Banken bei denen MEDX angelegt hat, hopps gehen und dadurch deren Geld futsch ist. Da ich aber davon ausgehe, dass keine Bank mehr a la Lehmann hopps gegangen gelassen werden wird, wird dies wohl nicht psassieren. Da gehen eher die Staaten, die die Banken retten und für sie garantieren, hopps.
Aber dann hast du Armageddon. Dann kannste die meisten Firmen begraben.
Antwort auf Beitrag Nr.: 36.581.260 von Ville7 am 15.02.09 06:46:20Interessanterweise springen bekannte Größen auf MEDX. Carl Icahn hat sich eine erste Position mit über 300.000 Aktien geholt.
Lol was sind schon 313tsd Aktien selbst für den Carl ist das ein Witz .
Sollte Golimumab dies 5 Jahre nach Zulassung auch schaffen ist der Cashburn von Medarex allein mit diesem einen Parterprodukt gestoppt
Das problem ist nur das MEDX nach aktuellem Stand max. für ca 2,5 Jahre cash hat .
Ipilimumab und die knapp 150 million US$ Schulden halte ich für weitere Risikofaktoren .
Medx habe ich schon immer gemieden und werde es auch weiterhin tun .
Lol was sind schon 313tsd Aktien selbst für den Carl ist das ein Witz .
Sollte Golimumab dies 5 Jahre nach Zulassung auch schaffen ist der Cashburn von Medarex allein mit diesem einen Parterprodukt gestoppt
Das problem ist nur das MEDX nach aktuellem Stand max. für ca 2,5 Jahre cash hat .
Ipilimumab und die knapp 150 million US$ Schulden halte ich für weitere Risikofaktoren .
Medx habe ich schon immer gemieden und werde es auch weiterhin tun .
Antwort auf Beitrag Nr.: 36.581.523 von BrauchGeld am 15.02.09 10:47:19Du hast bei deiner Rechnung vergessen, dass 1. der Cashburn mit den zugelassenen Produkten weniger werden wird, 2. den Equity interest zu berücksichtigen (5% Genmab, xx% Avant,..). Das 2. allein reicht nach deiner Rechnung für ein weiteres Jahr vollen Cashburns.
Keiner zwingt dich hier zu kaufen. Meide es ruhig weiter. Kein Problem damit.
Keiner zwingt dich hier zu kaufen. Meide es ruhig weiter. Kein Problem damit.
Antwort auf Beitrag Nr.: 36.581.523 von BrauchGeld am 15.02.09 10:47:19
Ich sehe dieses Problem und es ist ja evident, dass, vom status quo aus betrachtet, das Geschäftsmodell von Medarex unhaltbar ist.
Meine Spekulation ist nun aber, dass sich genau das in den nächsten drei Jahren ändern wird - also gerade noch rechtzeitig vor dem burnout. Ville hat hier ja mehrfach dargestellt, dass bei einer Zulassung von Golimumab und Ustekinumab royalties anfallen würden, die den cashburn signifikant verkleinern bzw. aufheben, im besten Falle sogar umdrehen. Auch ACZ885 kann auf diesem Weg helfen, wenn es gut geht. Indes muss sicher auch Medarex etwas tun und künftig mehr Ausgabendisziplin einkehren lassen.
Die These ist also, dass Medarex in den nächsten Jahren aus einem cashburner zu einem nachhaltig finanzierten Unternehmen werden könnte - das bedeutete eine völlig andere Qualität des Unternehmens. Aus dieser gesicherten Position heraus könnte dann die Pipeline in Ruhe ausgebaut werden, was langfristig - hoffe ich - sehr bedeutende Werte schaffen würde. Ich sehe das also als eine zweistufige Entwicklung. Zunächst muss das Unternehmen nachhaltig werden (break even) und (viel) später sind dann hoffentlich erhebliche Wertsteigerungen aufgrund von Pipelineprojekten möglich, die noch viele Jahre der Entwicklung vor sich haben (ich habe Zeit).
Natürlich setzt das zunächst die (vollständige) Zulassung von Golimumab und Ustekinumab voraus und insofern ist das schon ein ziemlich spekulatives Investment.
An Ville nochmals Dank für die Ausführungen heute zu Ipilimumab.
Ich sehe dieses Problem und es ist ja evident, dass, vom status quo aus betrachtet, das Geschäftsmodell von Medarex unhaltbar ist.
Meine Spekulation ist nun aber, dass sich genau das in den nächsten drei Jahren ändern wird - also gerade noch rechtzeitig vor dem burnout. Ville hat hier ja mehrfach dargestellt, dass bei einer Zulassung von Golimumab und Ustekinumab royalties anfallen würden, die den cashburn signifikant verkleinern bzw. aufheben, im besten Falle sogar umdrehen. Auch ACZ885 kann auf diesem Weg helfen, wenn es gut geht. Indes muss sicher auch Medarex etwas tun und künftig mehr Ausgabendisziplin einkehren lassen.
Die These ist also, dass Medarex in den nächsten Jahren aus einem cashburner zu einem nachhaltig finanzierten Unternehmen werden könnte - das bedeutete eine völlig andere Qualität des Unternehmens. Aus dieser gesicherten Position heraus könnte dann die Pipeline in Ruhe ausgebaut werden, was langfristig - hoffe ich - sehr bedeutende Werte schaffen würde. Ich sehe das also als eine zweistufige Entwicklung. Zunächst muss das Unternehmen nachhaltig werden (break even) und (viel) später sind dann hoffentlich erhebliche Wertsteigerungen aufgrund von Pipelineprojekten möglich, die noch viele Jahre der Entwicklung vor sich haben (ich habe Zeit).
Natürlich setzt das zunächst die (vollständige) Zulassung von Golimumab und Ustekinumab voraus und insofern ist das schon ein ziemlich spekulatives Investment.
An Ville nochmals Dank für die Ausführungen heute zu Ipilimumab.
So... Stelara ist erhältlich und erste Patienten bekommen es regulär (nicht in Studien) verschrieben!
Siehe hier:
http://www.psoriasis-netz.net/forum/showthread.php?t=227888
und
http://www.psoriasis-netz.net/forum/showthread.php?t=227635
das Medi. wird für sehr lange Zeit der Goldstandard werden!
Die Preise sind heftig...
http://www.mycare.de/home_2918653_STELARA%2B45MG%2BINJEKTION…
Ergo wird schon das ein oder andere brotkrummen abfallen für Medarex.
Ich hatte in einem Morphosys Thread gelesen, das MOR für ein Medi. auch 5 % royalties bekommt, wenn Sie nix weiter machen als den mab zu stellen und zu warten bis Roche durch alle Phasen durchgehechelt ist!
Ergo muß ich sagen, das Medarex somit im guten Rahmen liegt.
Der IL 12/23 Mab wurde ja von Medarex generiert und dann komplett an J&J abgegeben noch wohl vor Phase I. Und das ziemlich früh... bei einer späteren Einlizesierung hätte old dirty DD sicherlich damals mehr rausgeschunden...
Außerdem sind die Preis und die Bedeutung von Mab in den letzten Jahren gestiegen!
Beim nächsten Deal wird es eindeutig mehr % und milestones für Medarex geben!
Trotzdem... wo ist die PR über die Europazulassung auf der Homepage von Medarex....
Naja... die Zulassung in Amerika ist nur noch eine Frage der Zeit!
Siehe hier:
http://www.psoriasis-netz.net/forum/showthread.php?t=227888
und
http://www.psoriasis-netz.net/forum/showthread.php?t=227635
das Medi. wird für sehr lange Zeit der Goldstandard werden!
Die Preise sind heftig...
http://www.mycare.de/home_2918653_STELARA%2B45MG%2BINJEKTION…
Ergo wird schon das ein oder andere brotkrummen abfallen für Medarex.
Ich hatte in einem Morphosys Thread gelesen, das MOR für ein Medi. auch 5 % royalties bekommt, wenn Sie nix weiter machen als den mab zu stellen und zu warten bis Roche durch alle Phasen durchgehechelt ist!
Ergo muß ich sagen, das Medarex somit im guten Rahmen liegt.
Der IL 12/23 Mab wurde ja von Medarex generiert und dann komplett an J&J abgegeben noch wohl vor Phase I. Und das ziemlich früh... bei einer späteren Einlizesierung hätte old dirty DD sicherlich damals mehr rausgeschunden...
Außerdem sind die Preis und die Bedeutung von Mab in den letzten Jahren gestiegen!
Beim nächsten Deal wird es eindeutig mehr % und milestones für Medarex geben!
Trotzdem... wo ist die PR über die Europazulassung auf der Homepage von Medarex....

Naja... die Zulassung in Amerika ist nur noch eine Frage der Zeit!
Antwort auf Beitrag Nr.: 36.589.865 von where_is_the_beef am 16.02.09 20:40:29In der Regel werden die Cash&Carry Antikörper nach der Generierung und eventuellen Nachoptimierung an den Partner abgegeben. Dies erfolgt noch vor der Präklinik. Also weit weit vor der Klinik. Ab da entwickelt und zahlt nur noch der Partner. Nur dauert es i.d.R. um die 10 Jahre nach Abgabe des AKs bis das Produkt dann den Markt erreicht-wenn es ihn erreicht.
Morphosys nennt als normale Deal Terms 5% Royalties. Medarex 3-5%. Medarex ist also generell etwas "günstiger".
Morphosys nennt als normale Deal Terms 5% Royalties. Medarex 3-5%. Medarex ist also generell etwas "günstiger".
Antwort auf Beitrag Nr.: 36.589.865 von where_is_the_beef am 16.02.09 20:40:29Finde ich auch verwunderlich, hier so eine publizistische Zurückhaltung zu üben.
Da mag in den ersten Quartalen noch nicht die Riesensumme für Medarex herausspringen, aber es ist doch ein großer Meilenstein der Firmengeschichte, das erste zugelassene Medikament zu haben, dass auf der eigenen Technologie beruht und das man zum Tantiemeempfänger geworden ist.
Und letztlich: Kleinvieh macht auch Mist. Abgesehen davon, dass das Kleinvieh bis in 3 oder 4 Jahren ganz ordentlich wachsen und entsprechend mehr Mist machen könnte.
Abgesehen davon, dass das Kleinvieh bis in 3 oder 4 Jahren ganz ordentlich wachsen und entsprechend mehr Mist machen könnte.
Da mag in den ersten Quartalen noch nicht die Riesensumme für Medarex herausspringen, aber es ist doch ein großer Meilenstein der Firmengeschichte, das erste zugelassene Medikament zu haben, dass auf der eigenen Technologie beruht und das man zum Tantiemeempfänger geworden ist.
Und letztlich: Kleinvieh macht auch Mist.
 Abgesehen davon, dass das Kleinvieh bis in 3 oder 4 Jahren ganz ordentlich wachsen und entsprechend mehr Mist machen könnte.
Abgesehen davon, dass das Kleinvieh bis in 3 oder 4 Jahren ganz ordentlich wachsen und entsprechend mehr Mist machen könnte.
Antwort auf Beitrag Nr.: 36.591.365 von eck64 am 17.02.09 09:09:49Finde ich auch verwunderlich, hier so eine publizistische Zurückhaltung zu üben.
Wieso verwunderlich Ustekinumab wurde von Centocor entwickelt und haben es bis zur Zulassung geschafft ,Medarex hat hier lediglich die lizenz erteilt.
Ohne diese Partner wäre Medarex ziemlich arm dran.
Wieso verwunderlich Ustekinumab wurde von Centocor entwickelt und haben es bis zur Zulassung geschafft ,Medarex hat hier lediglich die lizenz erteilt.
Ohne diese Partner wäre Medarex ziemlich arm dran.
Antwort auf Beitrag Nr.: 36.591.844 von BrauchGeld am 17.02.09 10:09:37Erster "UltiMAb Human Antibody" zugelassen!
Ich halte das für meldenswert. Marktzugang USA wird Centocor wichtiger sein, ok. Aber der Meilenstein in der Firmenentwicklung Medarex ist das erstmals Patienten regulär behandelt werden und nicht im Rahmen von Studien.
Ich halte das für meldenswert. Marktzugang USA wird Centocor wichtiger sein, ok. Aber der Meilenstein in der Firmenentwicklung Medarex ist das erstmals Patienten regulär behandelt werden und nicht im Rahmen von Studien.
Antwort auf Beitrag Nr.: 36.591.844 von BrauchGeld am 17.02.09 10:09:37Ohne die Medarex Technologie wären sehr viele Partner sehr sehr arm dran, denn nicht jeder hat(te) eine so gute Technologie zur Generierung von humanen Antikörpern, die so früh verfügbar war.
Nur zur Erinnerung: 25% aller weltweiten Antikörper in klinischer Entwicklung enstammen der Medarex Technologie!!! Und der Anteil der vollhumanen AKs ist noch dramatisch größer, ich glaube mich an Zahlen von >80 oder 90% zu erinnern (habe hierfür nur keinen Slide)
Für die 25% Quelle siehe Slide 61, Seite 27:
http://www.medarex.com/Investor/documents/RD08Slides.pdf" target="_blank" rel="nofollow ugc noopener">
http://www.medarex.com/Investor/documents/RD08Slides.pdf
Nur zur Erinnerung: 25% aller weltweiten Antikörper in klinischer Entwicklung enstammen der Medarex Technologie!!! Und der Anteil der vollhumanen AKs ist noch dramatisch größer, ich glaube mich an Zahlen von >80 oder 90% zu erinnern (habe hierfür nur keinen Slide)
Für die 25% Quelle siehe Slide 61, Seite 27:
http://www.medarex.com/Investor/documents/RD08Slides.pdf" target="_blank" rel="nofollow ugc noopener">
http://www.medarex.com/Investor/documents/RD08Slides.pdf
Antwort auf Beitrag Nr.: 36.592.328 von Ville7 am 17.02.09 11:12:01Noch wären die Medx-Partner zwar nicht arm dran, aber bei gar manchem Partner hängen potentielle Milliardenumsätze am Erfolg der Medx-mABs.
Und deren pipeline würde tatsächlich massiv verarmen ohne MEDX.....
Und deren pipeline würde tatsächlich massiv verarmen ohne MEDX.....
Moin...
das sehe ich genauso Ville!
"Unsere Medarex ist die Mutter aller voll-humanen Mab!"
Die Medarex Maus hat eine überragende Bedeutung in dem Bereich...
Alle bedeutenden voll-humanen Blockbuster, welche jetzt kurz vorm Markteintritt sich befinden.... basieren auf "den vielen kleinen" menschlichen Medarex-Mäusen....
Ausnahmen + neue Technologieanbieter (wie MOR) natürlich abgesehen!
das sehe ich genauso Ville!
"Unsere Medarex ist die Mutter aller voll-humanen Mab!"

Die Medarex Maus hat eine überragende Bedeutung in dem Bereich...
Alle bedeutenden voll-humanen Blockbuster, welche jetzt kurz vorm Markteintritt sich befinden.... basieren auf "den vielen kleinen" menschlichen Medarex-Mäusen....
Ausnahmen + neue Technologieanbieter (wie MOR) natürlich abgesehen!
Antwort auf Beitrag Nr.: 36.592.328 von Ville7 am 17.02.09 11:12:01Ohne die Medarex Technologie wären sehr viele Partner sehr sehr arm dran,
Warte mal ich will einwenig Lachen "bawahahahaha" so genug gelacht war nämlich witzisch .
Medarex müsste die füsse von Johnson&Johnson küssen das die es geschafft haben die Platform so wertvoll zumachen ,Medx selbst ist doch mit Ipilimumab schon einmal kläglich gescheitert .
Medarex muss also sehr dankbar sein denn sie selbst haben es bisher nicht geschafft ein Produkt bis zur Zulassung zu bringen diese Loser .



Warte mal ich will einwenig Lachen "bawahahahaha" so genug gelacht war nämlich witzisch .
Medarex müsste die füsse von Johnson&Johnson küssen das die es geschafft haben die Platform so wertvoll zumachen ,Medx selbst ist doch mit Ipilimumab schon einmal kläglich gescheitert .
Medarex muss also sehr dankbar sein denn sie selbst haben es bisher nicht geschafft ein Produkt bis zur Zulassung zu bringen diese Loser .




Antwort auf Beitrag Nr.: 36.593.634 von BrauchGeld am 17.02.09 13:38:41Was willst du eigentlich hier? Rum-trollen?
Endlich hat dieses Board mit "BrauchGeld" auch einen allseits beliebten Forentroll bekommen! 
Da kann es mit der Medarex nur aufwärts gehen...

Da kann es mit der Medarex nur aufwärts gehen...

Antwort auf Beitrag Nr.: 36.593.857 von Ville7 am 17.02.09 14:08:10Was willst du eigentlich hier? Rum-trollen?
Ich bin hier um dinge richtig zustellen und wenn man dabei Spaß haben kann warum nicht ? Willst du mir etwa verbieten hier zuschreiben ?
@where_is_the_beef
Wen nennst du hier Forentroll ? Du Hofnarr
Damit es nochmal klar ist Ich sage nicht das Medx ein schlechtes Investment ist ,sondern das nur mittelfristig hier nicht viel zu erwarten ist .
Ich bin hier um dinge richtig zustellen und wenn man dabei Spaß haben kann warum nicht ? Willst du mir etwa verbieten hier zuschreiben ?

@where_is_the_beef
Wen nennst du hier Forentroll ? Du Hofnarr
Damit es nochmal klar ist Ich sage nicht das Medx ein schlechtes Investment ist ,sondern das nur mittelfristig hier nicht viel zu erwarten ist .
Trolle sind nicht nett. Eher einfach lästig. 

Und Medx kommt nicht vom Fleck, aber immerhin sind neue Tiefs noch weit weg.....

Und Medx kommt nicht vom Fleck, aber immerhin sind neue Tiefs noch weit weg.....
Antwort auf Beitrag Nr.: 36.596.180 von eck64 am 17.02.09 17:32:21Niveau sinkt mit dem Aktienkurs ....
Viel glück mit euer Medx..

Viel glück mit euer Medx..
Antwort auf Beitrag Nr.: 36.596.044 von BrauchGeld am 17.02.09 17:21:12"Richtigstellungen" sind mit sachlichen und nachvollziehbaren Argumenten verbunden, diese lese ich bei dir nicht, sondern vorwiegend Verhöhnungen und Provokationen.
Wahrscheinlich bist du hier, weil ich beim Spectrum Thread Vajo's oft falsche Statements sachlich und begründet entgegnet hatte und dir das nicht gepasst hat. Wenn es dir hier Spass macht mich zu ärgern, bitte. Ernst nehmen kann ich dich nur wenn du sachlich argumentierst.
Wahrscheinlich bist du hier, weil ich beim Spectrum Thread Vajo's oft falsche Statements sachlich und begründet entgegnet hatte und dir das nicht gepasst hat. Wenn es dir hier Spass macht mich zu ärgern, bitte. Ernst nehmen kann ich dich nur wenn du sachlich argumentierst.
Antwort auf Beitrag Nr.: 36.596.802 von Ville7 am 17.02.09 18:34:43Wahrscheinlich bist du hier, weil ich beim Spectrum Thread Vajo's oft falsche Statements sachlich und begründet entgegnet hatte und dir das nicht gepasst hat.
Hä Vajo ??? Was interessiert mich Vajo oder sonst wer ich bin hier um geld zu verdienen und sonst gar nichts .
Um sachlich über deren Produkte zu diskutieren musst du schon bei Medx arbeiten , das einzige was man kann ist spekulieren mehr auch nicht .
Wie gesagt viel glück mit Medx ,ich bin nicht investiert also werde ich auch nix mehr dazu sschreiben .
Hä Vajo ??? Was interessiert mich Vajo oder sonst wer ich bin hier um geld zu verdienen und sonst gar nichts .
Um sachlich über deren Produkte zu diskutieren musst du schon bei Medx arbeiten , das einzige was man kann ist spekulieren mehr auch nicht .
Wie gesagt viel glück mit Medx ,ich bin nicht investiert also werde ich auch nix mehr dazu sschreiben .
No broad-based anticancer antidotes have emerged from the immune system work yet. In trials to date, immune-boosting drugs have generally helped only a minority of patients, particularly those with melanoma. But when they do work, it can be spectacular.
By the odds, 27-year-old Sharon Belvin should no longer be alive. The North Carolina resident found out that she had melanoma in her lung a week before her wedding when she was only 22. That sort of tumor usually sprouts like a weed once it has migrated beyond the skin to internal organs, and it resists most chemotherapy. By the time she turned 24 the few standard treatments had failed, and she had tumors in both lungs.
But then Memorial's Wolchok put her on an experimental drug called ipilimumab that aims to trigger the immune system. Within four months her lung tumors started to shrivel. By late 2006 they were gone. Today Belvin remains free of cancer and off treatment. She spends her time caring for her husband and 1-year-old daughter, whom she calls "a miracle baby, after all we have been through." Her case is so unusual that during a recent appointment the radiologist called Wolchok in disbelief. "He said, 'What did you do for this patient? Am I reading the diagnosis correctly?'"
Seven years ago Los Angeles high school social studies teacher Joseph Rick spotted a purple pimple on the small of his back. Too late: The melanoma soon spread into his colon. Nine surgeries and 40 chemo rounds over two years failed to stop it. By fall 2004 dozens of tumors riddled his body. Doctors gave Rick, then 43, four months to live. Rick bought a grave site for himself and went home to his L.A. condo to die. By December his weight had plummeted to 90 pounds from 240. He could barely walk.
Then he heard about a new immune-system-boosting drug being tested at UCLA, similar to the one Belvin received. A week after his first infusion visible brown tumors on his neck and thigh began to fade and his appetite returned. By March his tumors had shrunk 25%, and by early 2006 they were gone. When he could go back to work, he broke into tears watching the sunrise. Says Rick: "I would have been dead [years ago] without this drug."
Comment On This Story
Belvin's drug, from Bristol-Myers Squibb and Medarex (nasdaq: MEDX - news - people ), shrank tumors in about 10% of melanoma patients in a 2007 trial--not enough to get approval without more study. A larger trial that could lead to approval will wrap up late this year. Rick's drug is being tested by Pfizer. In a recent final-stage trial it failed to beat chemotherapy, and Pfizer sent it back a grade; the drug will start over at an earlier stage of trials. Both drugs turn off a natural brake on immune system activity called CTLA4 (cytotoxic T-lymphocyte antigen 4). They are part of a new breed of drugs that hit specific molecular components of the immune system.
http://www.forbes.com/free_forbes/2009/0302/074_cancer_mirac…
By the odds, 27-year-old Sharon Belvin should no longer be alive. The North Carolina resident found out that she had melanoma in her lung a week before her wedding when she was only 22. That sort of tumor usually sprouts like a weed once it has migrated beyond the skin to internal organs, and it resists most chemotherapy. By the time she turned 24 the few standard treatments had failed, and she had tumors in both lungs.
But then Memorial's Wolchok put her on an experimental drug called ipilimumab that aims to trigger the immune system. Within four months her lung tumors started to shrivel. By late 2006 they were gone. Today Belvin remains free of cancer and off treatment. She spends her time caring for her husband and 1-year-old daughter, whom she calls "a miracle baby, after all we have been through." Her case is so unusual that during a recent appointment the radiologist called Wolchok in disbelief. "He said, 'What did you do for this patient? Am I reading the diagnosis correctly?'"
Seven years ago Los Angeles high school social studies teacher Joseph Rick spotted a purple pimple on the small of his back. Too late: The melanoma soon spread into his colon. Nine surgeries and 40 chemo rounds over two years failed to stop it. By fall 2004 dozens of tumors riddled his body. Doctors gave Rick, then 43, four months to live. Rick bought a grave site for himself and went home to his L.A. condo to die. By December his weight had plummeted to 90 pounds from 240. He could barely walk.
Then he heard about a new immune-system-boosting drug being tested at UCLA, similar to the one Belvin received. A week after his first infusion visible brown tumors on his neck and thigh began to fade and his appetite returned. By March his tumors had shrunk 25%, and by early 2006 they were gone. When he could go back to work, he broke into tears watching the sunrise. Says Rick: "I would have been dead [years ago] without this drug."
Comment On This Story
Belvin's drug, from Bristol-Myers Squibb and Medarex (nasdaq: MEDX - news - people ), shrank tumors in about 10% of melanoma patients in a 2007 trial--not enough to get approval without more study. A larger trial that could lead to approval will wrap up late this year. Rick's drug is being tested by Pfizer. In a recent final-stage trial it failed to beat chemotherapy, and Pfizer sent it back a grade; the drug will start over at an earlier stage of trials. Both drugs turn off a natural brake on immune system activity called CTLA4 (cytotoxic T-lymphocyte antigen 4). They are part of a new breed of drugs that hit specific molecular components of the immune system.
http://www.forbes.com/free_forbes/2009/0302/074_cancer_mirac…
Nur zur Info, falls es jemanden Interessiert:
Ich hatte im Laufe der Woche ein Telefongespräch mit Herrn Lanthaler, CFO von Intercell. Die arbeiten mit Merck zusammen an der klinischen Entwicklung eines Impfstoffes bezüglich s.aureus.
Im Gespräch erwähnte er, dass der präklinische mAB zur therapeutischen Behandlung von s.aureus auf Basis Medarex-technologie bzw. mit Medx-Maus generiert worden sei.
Im Laufe 2009 soll hier möglicherweise noch ein IND stattfinden.
Ich hatte im Laufe der Woche ein Telefongespräch mit Herrn Lanthaler, CFO von Intercell. Die arbeiten mit Merck zusammen an der klinischen Entwicklung eines Impfstoffes bezüglich s.aureus.
Im Gespräch erwähnte er, dass der präklinische mAB zur therapeutischen Behandlung von s.aureus auf Basis Medarex-technologie bzw. mit Medx-Maus generiert worden sei.
Im Laufe 2009 soll hier möglicherweise noch ein IND stattfinden.
"...
The future of Raptiva in psoriasis, as well as its chances for development in other indications, looks extremely bleak. Stelara (ustekinumab; Centocor, Johnson & Johnson, Janssen-Cilag), which was approved by the EMEA for psoriasis in January 2009, is hotly anticipated by dermatologists. Stelara is a MAb targeted towards interleukin (IL)-12 and IL-23, and is delivered subcutaneously every 12 weeks. Datamonitor's assessment of physician perception in auto-immune diseases, including psoriasis, indicates that dermatologists rate Stelara highly on attributes such as efficacy, with most respondents scoring it 40% above an average for all biologics in auto-immune disease in terms of predicted efficacy. The ACCEPT study demonstrated that Stelara was superior to Enbrel, a fact that will likely drive uptake of this brand.
..."
http://www.tradingmarkets.com/.site/news/Stock%20News/218930…
The future of Raptiva in psoriasis, as well as its chances for development in other indications, looks extremely bleak. Stelara (ustekinumab; Centocor, Johnson & Johnson, Janssen-Cilag), which was approved by the EMEA for psoriasis in January 2009, is hotly anticipated by dermatologists. Stelara is a MAb targeted towards interleukin (IL)-12 and IL-23, and is delivered subcutaneously every 12 weeks. Datamonitor's assessment of physician perception in auto-immune diseases, including psoriasis, indicates that dermatologists rate Stelara highly on attributes such as efficacy, with most respondents scoring it 40% above an average for all biologics in auto-immune disease in terms of predicted efficacy. The ACCEPT study demonstrated that Stelara was superior to Enbrel, a fact that will likely drive uptake of this brand.
..."
http://www.tradingmarkets.com/.site/news/Stock%20News/218930…
Medarex, Inc. Q4 2008 Earnings Call Transcript
http://seekingalpha.com/article/122740-medarex-inc-q4-2008-e…
http://seekingalpha.com/article/122740-medarex-inc-q4-2008-e…
Also, Medarex Konkurrent "Synta" musste seine Phase III trail stoppen! Sehr traurig und schlecht für Melanom Patienten... Neutral für Medarex...
Wenn wir Pech haben, wird dieses auch wieder gegen Medarex ausgelegt!
=> die Schlachtung der Aktie geht weiter...
Wenn mir ansehe, wie die Hedgefond, Shorties weiterhin mit Leerverkäufen Aktien zerstören... =>
Medarex hat nach 20 Jahren das 1. Produkt auf dem Markt (einen absoluten Blockbuster scheinbar)
...
einen starken Newsflow ist zu erwarten in der nächsten Zeit
...
trotzdem wird die Aktie förmlich geschlachtet!?!?
...
Weltwirtschaftskrise hin oder her... =>
...
[nachdenklich am Kopfkratzend...]
Wenn wir Pech haben, wird dieses auch wieder gegen Medarex ausgelegt!
=> die Schlachtung der Aktie geht weiter...
Wenn mir ansehe, wie die Hedgefond, Shorties weiterhin mit Leerverkäufen Aktien zerstören... =>

Medarex hat nach 20 Jahren das 1. Produkt auf dem Markt (einen absoluten Blockbuster scheinbar)
...
einen starken Newsflow ist zu erwarten in der nächsten Zeit
...
trotzdem wird die Aktie förmlich geschlachtet!?!?
...
Weltwirtschaftskrise hin oder her... =>

...
[nachdenklich am Kopfkratzend...]
Antwort auf Beitrag Nr.: 36.663.801 von where_is_the_beef am 27.02.09 08:12:13Der Grund fürs aktuelle Schlachtfest:
Obama fordert günstigeren Zugang für Biotech-Generikas, wie immer man das auch definiert.
Das wäre aber zunächst nur eine Gefahr für die Firmen mit Präparaten am Markt, die leichter unter Druck gesetzt werden können.
Wobei ich es für sehr schwierig halte einen Antikörper ganz exakt nachzubauen.
Im Prinzip wäre es besser aufs gleiche target einen neuen und besseren, voll humanen AK anzusetzen.
Aber das bedeutet das komplette Entwicklungsprogramm von vorne. Auch nicht gerade billig.....
Obama fordert günstigeren Zugang für Biotech-Generikas, wie immer man das auch definiert.
Das wäre aber zunächst nur eine Gefahr für die Firmen mit Präparaten am Markt, die leichter unter Druck gesetzt werden können.
Wobei ich es für sehr schwierig halte einen Antikörper ganz exakt nachzubauen.
Im Prinzip wäre es besser aufs gleiche target einen neuen und besseren, voll humanen AK anzusetzen.
Aber das bedeutet das komplette Entwicklungsprogramm von vorne. Auch nicht gerade billig.....
Antwort auf Beitrag Nr.: 36.663.801 von where_is_the_beef am 27.02.09 08:12:13Jetzt haben die ihren Bericht für 2008 vorgelegt, der ist schon grauenhaft. Es läuft auf einen Showdown zwischen Pipeline und Cashburn raus. Es verbleiben 2 Jahre voller Bastelfreude und nicht wirklich mehr, Umsatz mag fast auf Morphosysniveau sein. Was gänzlich nicht geht ist die muntere Verklatschung von Genmabaktien, die signalisiert eine zögerliche Cash Flow Perspektive und eine völlig versiffte Finanzakrobatie. Schlimm an Vorurteilen ist ihre permanente Bestätigung, hier die des schön erzählenden Amerikaners mit Selbstbedienungswirtschaft und einem anderen Gang in der Realität.
Die eine Frage ist die nach der wirtschaftlichen Zukunft aus der reifenden Pipeline, da muß was kommen und das nicht auf einer NPO-Basis. Sollte ja mal machbar sein, inklusive Break Even 2010.
Eine Medarex ist an der Börse gelistet, weniger an der Uni eingeschrieben. Vielleicht wirtschaften die nach langen Übungsjahren mal entsprechend.
Butter bei die Fische, Produkterfolg zu den an der Börse verkauften Heilungsversprechen ist gefragt. Vielleicht koppeln die von Medarex ihre Einkommen mal an den Forschungserfolg, eine Ankopplung vom Forschungserfolg an die Einkommen würde auch helfen.
Ich stell mir einen Autoschrauber mit 80E Stundensatz vor, wenn der dann nicht repariert und nur labert sind wir bei Medarex
Die eine Frage ist die nach der wirtschaftlichen Zukunft aus der reifenden Pipeline, da muß was kommen und das nicht auf einer NPO-Basis. Sollte ja mal machbar sein, inklusive Break Even 2010.
Eine Medarex ist an der Börse gelistet, weniger an der Uni eingeschrieben. Vielleicht wirtschaften die nach langen Übungsjahren mal entsprechend.
Butter bei die Fische, Produkterfolg zu den an der Börse verkauften Heilungsversprechen ist gefragt. Vielleicht koppeln die von Medarex ihre Einkommen mal an den Forschungserfolg, eine Ankopplung vom Forschungserfolg an die Einkommen würde auch helfen.
Ich stell mir einen Autoschrauber mit 80E Stundensatz vor, wenn der dann nicht repariert und nur labert sind wir bei Medarex

Antwort auf Beitrag Nr.: 36.665.280 von Friseuse am 27.02.09 10:58:49
Das trifft schon den Punkt. MEDX kann so nicht mehr weitermachen. Und das ist keine Rhetorik, sondern einfach nur Mathematik. Jeder kann sehen, dass das derzeitige überaggressive Geschäftsmodell nur noch eine kurze Zeit aufrechtzuerhalten ist, bevor die finanzielle Substanz ausgebrannt ist. Der Zugang zum Kapitalmarkt dürfte sowohl in Sachen Kapitalerhöhung wie auch über FK-Aufnahme weitgehend verbaut sein, zumindest, wenn es um relevante Summen geht.
Dass sich ziemlich bald etwas ändern muss, ist also ganz klar. Nur was und wie und wann genau es sich ändern wird, das weiß man nicht und so etwas hasst "der Markt" nunmal.
Ich bin aber dennoch ganz positiv gestimmt. Denn bevor man mutwillig in die Insolvenz geht, wird man ja wohl hoffentlich die Ausgaben an die Einnahmen anpassen und die Pipeline hat - hoffe ich - durchaus ihren Wert. Auf welchem Niveau dieses Gleichgewicht erreicht wird, also ob und wenn ja, wie extrem die Reduzierung der Forschung ausfallen muss, das hängt dann wieder ganz von den anstehenden Zulassungen ab.
- durchaus ihren Wert. Auf welchem Niveau dieses Gleichgewicht erreicht wird, also ob und wenn ja, wie extrem die Reduzierung der Forschung ausfallen muss, das hängt dann wieder ganz von den anstehenden Zulassungen ab.
Das trifft schon den Punkt. MEDX kann so nicht mehr weitermachen. Und das ist keine Rhetorik, sondern einfach nur Mathematik. Jeder kann sehen, dass das derzeitige überaggressive Geschäftsmodell nur noch eine kurze Zeit aufrechtzuerhalten ist, bevor die finanzielle Substanz ausgebrannt ist. Der Zugang zum Kapitalmarkt dürfte sowohl in Sachen Kapitalerhöhung wie auch über FK-Aufnahme weitgehend verbaut sein, zumindest, wenn es um relevante Summen geht.
Dass sich ziemlich bald etwas ändern muss, ist also ganz klar. Nur was und wie und wann genau es sich ändern wird, das weiß man nicht und so etwas hasst "der Markt" nunmal.
Ich bin aber dennoch ganz positiv gestimmt. Denn bevor man mutwillig in die Insolvenz geht, wird man ja wohl hoffentlich die Ausgaben an die Einnahmen anpassen und die Pipeline hat - hoffe ich
 - durchaus ihren Wert. Auf welchem Niveau dieses Gleichgewicht erreicht wird, also ob und wenn ja, wie extrem die Reduzierung der Forschung ausfallen muss, das hängt dann wieder ganz von den anstehenden Zulassungen ab.
- durchaus ihren Wert. Auf welchem Niveau dieses Gleichgewicht erreicht wird, also ob und wenn ja, wie extrem die Reduzierung der Forschung ausfallen muss, das hängt dann wieder ganz von den anstehenden Zulassungen ab.
Wie ist eigentlich die Strategie ausgerichtet bei den eigenen Pipelineprojekten?
Klamm am cash ist es noch nicht, aber eben auch nicht mehr allzulange hin. Soll hier ein Eigenvertrieb aufgebaut werden, oder geht es bei alle Projekten um weltweite Vertriebspartner?
Denn Auslizenzierungserlöse fortgeschrittener Projekte kippen natürlich schnell alle cashsorgen.
Statt eigenen Kosten gibts Geldzufluss und BE. Natürlich nur, wenn man sich hier um interessenten kümmert.
Klamm am cash ist es noch nicht, aber eben auch nicht mehr allzulange hin. Soll hier ein Eigenvertrieb aufgebaut werden, oder geht es bei alle Projekten um weltweite Vertriebspartner?
Denn Auslizenzierungserlöse fortgeschrittener Projekte kippen natürlich schnell alle cashsorgen.
Statt eigenen Kosten gibts Geldzufluss und BE. Natürlich nur, wenn man sich hier um interessenten kümmert.
Echt derb, die Entwicklung. 


Der Esel ist wieder tief im Süden. 


Antwort auf Beitrag Nr.: 36.686.346 von eck64 am 03.03.09 00:46:51Medarex notiert jetzt bei einer Marktkapitalisierung von 438Mio USD und somit unter Cash(350) + Equity-Wert(ca. 100) von gesamt ca. 450Mio USD.
Antwort auf Beitrag Nr.: 36.686.564 von Ville7 am 03.03.09 07:16:54Nicht nur die positiven dinge erwähnen bist ja schon wie dein bester kollege Vajo .
Total Debt (mrq): 145.43M << was ist hiermit ?
Cashburn : 12-14 million US$ monatlich << und damit ?
Was ist wenn Ipilimumab in PIII scheitert ? Melanoma ist nicht gerade einfach zu behandeln . << auch eine große gefahr für Medarex
Wer eine gute BioAktie mit weniger Risiko kaufen will der ist bei Celgene wesentlich besser aufgehoben und momentan sind die sehr günstig zuhaben .
Total Debt (mrq): 145.43M << was ist hiermit ?
Cashburn : 12-14 million US$ monatlich << und damit ?
Was ist wenn Ipilimumab in PIII scheitert ? Melanoma ist nicht gerade einfach zu behandeln . << auch eine große gefahr für Medarex
Wer eine gute BioAktie mit weniger Risiko kaufen will der ist bei Celgene wesentlich besser aufgehoben und momentan sind die sehr günstig zuhaben .
Antwort auf Beitrag Nr.: 36.687.182 von BrauchGeld am 03.03.09 09:35:58Amen.
Antwort auf Beitrag Nr.: 36.687.448 von Ville7 am 03.03.09 10:13:18Die wirtschaftlichen Daten sagen eine mutmaßliche Überlebenszeit von 2 Jahren an. Dagegen haben Forschungserfolge mit einem brauchbaren wirtschaftlichen Resultat zu stehen.
Eine positive Auflösung vertagt Medarex immer wieder.
Im Grunde lebt sich jetzt in Kursen Drakemans Börsenverarsche aus. Fette Zukunft versprechen und cashen, nichts halten.Von daher können Kurse als Nachverständnis und nicht als finaler Abgesang der Pipeline verstanden werden. Andererseits wäre es bei positiver Pipelineentwicklung der verdeckten Art wohl schon zu einem Übernahmeangebot gekommen.
Ziemlicher Nebel, macht mal klare Aussichten
Eine positive Auflösung vertagt Medarex immer wieder.
Im Grunde lebt sich jetzt in Kursen Drakemans Börsenverarsche aus. Fette Zukunft versprechen und cashen, nichts halten.Von daher können Kurse als Nachverständnis und nicht als finaler Abgesang der Pipeline verstanden werden. Andererseits wäre es bei positiver Pipelineentwicklung der verdeckten Art wohl schon zu einem Übernahmeangebot gekommen.
Ziemlicher Nebel, macht mal klare Aussichten

Antwort auf Beitrag Nr.: 36.669.741 von eck64 am 27.02.09 17:48:54Das ist dann die Xomalösung. Typisches Beispiel für einen nicht an der Produktfront gescheiterten Vollsinnlosbio.
Das Vorständen wirtschaftlicher Erfolg am Markt und für Aktionäre relativ egal ist kann ja sein. Aber Aktionären muß doch die Zurechenbarkeit von Erfolg wichtig sein.
kann ja sein. Aber Aktionären muß doch die Zurechenbarkeit von Erfolg wichtig sein.
Außerdem ist MDX10 vorverklatscht a la Satraplatin.
Das Vorständen wirtschaftlicher Erfolg am Markt und für Aktionäre relativ egal ist
 kann ja sein. Aber Aktionären muß doch die Zurechenbarkeit von Erfolg wichtig sein.
kann ja sein. Aber Aktionären muß doch die Zurechenbarkeit von Erfolg wichtig sein.Außerdem ist MDX10 vorverklatscht a la Satraplatin.
Medarex Announces Presentations at Annual Meeting of the American Association for Cancer Research
Tuesday March 17, 8:00 am ET
PRINCETON, N.J., March 17 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) announced today that the following clinical and preclinical abstracts are expected to be the subject of poster presentations at the Annual Meeting of the American Association for Cancer Research (AACR), being held April 18-22, 2009 in Colorado:
* "A Phase I, open-label, dose-escalation, multi-dose study of MDX-1401 (defucosylated human antiCD30 monoclonal antibody) in patients with CD30-positive refractory/relapsed Hodgkin's lymphoma" (Abstract #1227), R. Thertulien - Poster presentation from 1:00 to 5:00 p.m. local time on Sunday, April 19, 2009.
* "Efficacy of MDX-1110, an anti-Fucosyl-GM1 antibody in a SCLC tumor model" (Abstract #838), B. Chen - Poster presentation from 8:00 to 12:00 p.m. local time on Sunday, April 19, 2009.
* "The critical role of cleavable linkers for minor groove binding alkylating agent (MGBA) based antibody-drug conjugates" (Abstract #1722), S. Gangwar - Poster presentation from 1:00 to 5:00 p.m. local time on Sunday, April 19, 2009.
* "Development of anti-Glypican 3 therapeutic antibodies" (Abstract #1233), L. Lu - Poster presentation from 1:00 to 5:00 p.m. local time on Sunday, April 19, 2009.
* "Efficacy and Toxicity of anti-mesothelin antibody drug conjugate" (Abstract #3235), C. Rao - Poster presentation from 8:00 to 12:00 p.m. local time on Tuesday, April 21, 2009.
Tuesday March 17, 8:00 am ET
PRINCETON, N.J., March 17 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) announced today that the following clinical and preclinical abstracts are expected to be the subject of poster presentations at the Annual Meeting of the American Association for Cancer Research (AACR), being held April 18-22, 2009 in Colorado:
* "A Phase I, open-label, dose-escalation, multi-dose study of MDX-1401 (defucosylated human antiCD30 monoclonal antibody) in patients with CD30-positive refractory/relapsed Hodgkin's lymphoma" (Abstract #1227), R. Thertulien - Poster presentation from 1:00 to 5:00 p.m. local time on Sunday, April 19, 2009.
* "Efficacy of MDX-1110, an anti-Fucosyl-GM1 antibody in a SCLC tumor model" (Abstract #838), B. Chen - Poster presentation from 8:00 to 12:00 p.m. local time on Sunday, April 19, 2009.
* "The critical role of cleavable linkers for minor groove binding alkylating agent (MGBA) based antibody-drug conjugates" (Abstract #1722), S. Gangwar - Poster presentation from 1:00 to 5:00 p.m. local time on Sunday, April 19, 2009.
* "Development of anti-Glypican 3 therapeutic antibodies" (Abstract #1233), L. Lu - Poster presentation from 1:00 to 5:00 p.m. local time on Sunday, April 19, 2009.
* "Efficacy and Toxicity of anti-mesothelin antibody drug conjugate" (Abstract #3235), C. Rao - Poster presentation from 8:00 to 12:00 p.m. local time on Tuesday, April 21, 2009.
Ustekinumab (Stelara) ist (immer) noch nicht in USA zugelassen, da erscheint diesen Monat (Ende April) bereits der nächste MEDX-Partner-Antikörper auf der Ziellinie zur Zulassung in USA: Golimumab.
Wird die FDA wieder versuchen zu verzögern?
Wird die FDA wieder versuchen zu verzögern?
Hallöchen!
Ein sehr interessanter Artikel über die Entwicklung von Rituximab!

http://www.faz.net/s/Rub268AB64801534CF288DF93BB89F2D797/Doc…
Ein sehr interessanter Artikel über die Entwicklung von Rituximab!

http://www.faz.net/s/Rub268AB64801534CF288DF93BB89F2D797/Doc…
Aus Yahoo. Sepsis (Blutvergiftung), eine sehr interessante Indikation für PD-1 Blockade!
-----------
PD-1 Absract Courtesy Iceberg SI 1-Apr-09 09:06 pm
From: Icebrg 4/1/2009 8:00:07 AM
Read Replies (1) of 2135
PD-1 expression by macrophages plays a pathologic role in altering microbial clearance and the innate inflammatory response to sepsis.
Proc Natl Acad Sci U S A. 2009 Mar 30. [Epub ahead of print]
Huang X, Venet F, Wang YL, Lepape A, Yuan Z, Chen Y, Swan R, Kherouf H, Monneret G, Chung CS, Ayala A.
Division of Surgical Research, Department of Surgery, Brown University School of Medicine/Rhode Island Hospital, 593 Eddy Street, Providence, RI 02903.
Sepsis, a leading cause of death worldwide, involves concomitant expression of an overzealous inflammatory response and inefficient bacterial clearance. Macrophage function is pivotal to the development of these two aspects during sepsis; however, the mechanisms underlying these changes remain unclear. Here we report that the PD-1:PD-L pathway appears to be a determining factor of the outcome of sepsis, regulating the delicate balance between effectiveness and damage by the antimicrobial immune response. To this end we observed that PD-1(-/-) mice were markedly protected from the lethality of sepsis, accompanied by a decreased bacterial burden and suppressed inflammatory cytokine response. To the extent that this is a macrophage-specific aspect of the effects of PD-1, we found the following: first, peritoneal macrophages expressed significantly higher levels of PD-1 during sepsis, which was associated with their development of cellular dysfunction; second, when peritoneal macrophages were depleted (using clodronate liposomes) from PD-1(-/-) mice, the animals' bactericidal capacity was lowered, their inflammatory cytokine levels were elevated, and protection from septic lethality was diminished; and third, blood monocytes from both septic mice and patients with septic shock shared markedly increased PD-1 levels. Together, these data suggest that PD-1 may not only be a dysfunctional marker/effector of macrophages/monocytes, but may also be a potential therapeutic target for designing measures to modulate the innate immune response, thereby preventing the detrimental effects of sepsis.
-----------
PD-1 Absract Courtesy Iceberg SI 1-Apr-09 09:06 pm
From: Icebrg 4/1/2009 8:00:07 AM
Read Replies (1) of 2135
PD-1 expression by macrophages plays a pathologic role in altering microbial clearance and the innate inflammatory response to sepsis.
Proc Natl Acad Sci U S A. 2009 Mar 30. [Epub ahead of print]
Huang X, Venet F, Wang YL, Lepape A, Yuan Z, Chen Y, Swan R, Kherouf H, Monneret G, Chung CS, Ayala A.
Division of Surgical Research, Department of Surgery, Brown University School of Medicine/Rhode Island Hospital, 593 Eddy Street, Providence, RI 02903.
Sepsis, a leading cause of death worldwide, involves concomitant expression of an overzealous inflammatory response and inefficient bacterial clearance. Macrophage function is pivotal to the development of these two aspects during sepsis; however, the mechanisms underlying these changes remain unclear. Here we report that the PD-1:PD-L pathway appears to be a determining factor of the outcome of sepsis, regulating the delicate balance between effectiveness and damage by the antimicrobial immune response. To this end we observed that PD-1(-/-) mice were markedly protected from the lethality of sepsis, accompanied by a decreased bacterial burden and suppressed inflammatory cytokine response. To the extent that this is a macrophage-specific aspect of the effects of PD-1, we found the following: first, peritoneal macrophages expressed significantly higher levels of PD-1 during sepsis, which was associated with their development of cellular dysfunction; second, when peritoneal macrophages were depleted (using clodronate liposomes) from PD-1(-/-) mice, the animals' bactericidal capacity was lowered, their inflammatory cytokine levels were elevated, and protection from septic lethality was diminished; and third, blood monocytes from both septic mice and patients with septic shock shared markedly increased PD-1 levels. Together, these data suggest that PD-1 may not only be a dysfunctional marker/effector of macrophages/monocytes, but may also be a potential therapeutic target for designing measures to modulate the innate immune response, thereby preventing the detrimental effects of sepsis.
Quelle: Yahoo Msg-Board
**********************************
Golimumab Significantly Improves Active Psoriatic Arthritis, Nail Psoriasis
HOBOKEN, NJ -- April 7, 2009 -- Golimumab significantly improves active psoriatic arthritis and associated skin and nail psoriasis, according to a study published in the April issue of the journal of Arthritis & Rheumatism.
...The primary end point of the study was the proportion of patients who met the American College of Rheumatology 20% improvement criteria (ACR20 response) at week 14. This response included at least a 20% improvement in swollen and tender joint counts and other measures such as pain, disease activity, physical function, and C-reactive protein. ACR50 and ACR70 responses were defined by at least 50% and at least 70% improvement.
Golimumab was efficacious and generally well tolerated. An ACR20 response was achieved at week 14 by 51% of patients receiving golimumab 50mg and 45% of those receiving golimumab 100mg, compared with 9% of placebo-treated patients.
In addition, significantly more golimumab-treated patients than placebo-treated patients achieved ACR50 and ACR70 responses and those who initially showed little improvement and switched from placebo to golimumab or increased their dosage also showed improvement.
Patients treated with the drug had significant improvement in physical function and health-related quality of life, as well as significant improvement in enthesitis.
In addition to improving arthritic symptoms, golimumab also improved psoriasis symptoms with 40% of the 50 mg group and 58% of the 100 mg group having at least a 75% improvement in psoriasis symptoms, compared with 3% in the placebo group.
"The safety profile of golimumab in psoriatic arthritis was similar to other anti-TNF agents that have been studied in this disease," the authors wrote. "Subcutaneous administrations were well tolerated. Only a small number of patients had injection site reactions, which were mostly mild."
"This was also the first placebo-controlled study evaluating the effect of an anti-TNFalpha on nail psoriasis, which affected about 70% of the patients involved in the study," the continued. "Significant improvements in nail symptoms were seen in those treated with golimumab as early as week 14 and were maintained or improved through the end of the study period."
http://www.docguide.com/news/content.nsf...
**********************************
Golimumab Significantly Improves Active Psoriatic Arthritis, Nail Psoriasis
HOBOKEN, NJ -- April 7, 2009 -- Golimumab significantly improves active psoriatic arthritis and associated skin and nail psoriasis, according to a study published in the April issue of the journal of Arthritis & Rheumatism.
...The primary end point of the study was the proportion of patients who met the American College of Rheumatology 20% improvement criteria (ACR20 response) at week 14. This response included at least a 20% improvement in swollen and tender joint counts and other measures such as pain, disease activity, physical function, and C-reactive protein. ACR50 and ACR70 responses were defined by at least 50% and at least 70% improvement.
Golimumab was efficacious and generally well tolerated. An ACR20 response was achieved at week 14 by 51% of patients receiving golimumab 50mg and 45% of those receiving golimumab 100mg, compared with 9% of placebo-treated patients.
In addition, significantly more golimumab-treated patients than placebo-treated patients achieved ACR50 and ACR70 responses and those who initially showed little improvement and switched from placebo to golimumab or increased their dosage also showed improvement.
Patients treated with the drug had significant improvement in physical function and health-related quality of life, as well as significant improvement in enthesitis.
In addition to improving arthritic symptoms, golimumab also improved psoriasis symptoms with 40% of the 50 mg group and 58% of the 100 mg group having at least a 75% improvement in psoriasis symptoms, compared with 3% in the placebo group.
"The safety profile of golimumab in psoriatic arthritis was similar to other anti-TNF agents that have been studied in this disease," the authors wrote. "Subcutaneous administrations were well tolerated. Only a small number of patients had injection site reactions, which were mostly mild."
"This was also the first placebo-controlled study evaluating the effect of an anti-TNFalpha on nail psoriasis, which affected about 70% of the patients involved in the study," the continued. "Significant improvements in nail symptoms were seen in those treated with golimumab as early as week 14 and were maintained or improved through the end of the study period."
http://www.docguide.com/news/content.nsf...
Biotech Stock Mailbag: Medarex
Adam Feuerstein
04/10/09 - 07:59 AM EDT
Welcome back to the Biotech Mailbag. Let's get started with an email from Charles B.
"Adam: What do you think of Johnson & Johnson's(JNJ Quote) golimumab for first-pass FDA approval on April 29? Also, Stelara should be approved any day... I believe this may be a game changer for Medarex(MEDX Quote). These approvals should provide enough royalties to limit the need for additional funding and may spark a take-out by J&J or price war with Bristol-Myers Squibb(BMY Quote). With updated survival from ipilimumab at ASCO, I believe Bristol will move to buy Medarex this summer. They do not want to wind up in another ImClone situation."
Charles is a fervent Medarex bull with a persuasive argument for owning the stock now. I know because he and I had a lengthy email discussion about Medarex earlier this week.
Golimumab, for treating rheumatoid arthritis, and Stelara, for moderate to severe plaque psoriasis, each have the potential to be billion-dollar drugs for J&J. Both drugs were created using Medarex's humanized monoclonal antibody technology, which entitles the company to a low single-digit royalty on sales -- call it 3%.
If one or both of these J&J drugs achieves peak annual sales in the $3 billion to $4 billion range of market leaders Enbrel, sold by Amgen(AMGN Quote), or Abbott Lab's(ABT Quote) Humira, then the royalty revenue flowing back to Medarex is substantial.
Charles' estimate of Medarex's Stelara royalties alone tops $100 million a year.
His math pencils out OK, but I do worry that he overestimates the peak revenue potential for both Stelara and golimumab. Both seem like strong drugs, but so are Enbrel and Humira. It's not going to be easy to unseat well-entrenched drugs like Enbrel and Humira, especially since both drugs are considered very safe for patients. Stelara and golimumab may be as safe, but they lack the years of data to prove it.
This exact point was made by two rheumatologists speaking last month on a panel at a health care conference sponsored by Cowen & Co. Both doctors believed that drugs like golimumab (Stelara didn't come up specifically) would be fighting for second- or third-line treatment. Neither was enthusiastic at all about swapping out a new drug for either Humira or Enbrel any time soon.
Couple this conservatism on the part of doctors with a recession-fueled pullback in the use of all expensive biologic drugs to treat auto-immune diseases like rheumatoid arthritis (which I wrote about this week), and you've got plenty of reasons to be cautious about assuming huge royalty revenue flowing into Medarex's coffers.
I don't want to leave the impression that the approval of golimumab and/or Stelara isn't positive for Medarex. Both drugs will bring non-dilutive cash to the company which is definitely a plus in this market environment. Moreover, the approval of either drug will validate Medarex's antibody technology platform, another good thing.
But for Medarex to be truly successful, the company must become more than just the next PDL Biopharma(PDLI Quote) or Xoma(XOMA Quote). Both of these companies have been disappointments. They collect royalty revenues on other companies' successful drugs but have never been able to develop drugs successfully on their own.
Charles believes that ipilimumab, Medarex's melanoma drug (partnered with Bristol-Myers Squibb) may be that internally developed drug that gets Medarex really moving. I have my serious doubts about that, based on the uninspiring data released so far.
And let's not forget the lameness of Medarex's management team, which seems incapable of doing anything right. Honestly, CEO Howard Pien is like a black hole -- shareholder value goes in, but never comes out.
At around $5.50 a share (a $700 million market cap), Medarex is already getting credit for some of the anticipated royalties from golimumab and Stelara. As one analyst said to me this week, think of that royalty stream as a backstop on Medarex's current valuation and not so much as a future growth driver for the stock price.
That will come if Medarex can successfully develop its internal pipeline of drug candidates. And on that front, I'm definitely in wait-and-see mode.
Adam Feuerstein
04/10/09 - 07:59 AM EDT
Welcome back to the Biotech Mailbag. Let's get started with an email from Charles B.
"Adam: What do you think of Johnson & Johnson's(JNJ Quote) golimumab for first-pass FDA approval on April 29? Also, Stelara should be approved any day... I believe this may be a game changer for Medarex(MEDX Quote). These approvals should provide enough royalties to limit the need for additional funding and may spark a take-out by J&J or price war with Bristol-Myers Squibb(BMY Quote). With updated survival from ipilimumab at ASCO, I believe Bristol will move to buy Medarex this summer. They do not want to wind up in another ImClone situation."
Charles is a fervent Medarex bull with a persuasive argument for owning the stock now. I know because he and I had a lengthy email discussion about Medarex earlier this week.
Golimumab, for treating rheumatoid arthritis, and Stelara, for moderate to severe plaque psoriasis, each have the potential to be billion-dollar drugs for J&J. Both drugs were created using Medarex's humanized monoclonal antibody technology, which entitles the company to a low single-digit royalty on sales -- call it 3%.
If one or both of these J&J drugs achieves peak annual sales in the $3 billion to $4 billion range of market leaders Enbrel, sold by Amgen(AMGN Quote), or Abbott Lab's(ABT Quote) Humira, then the royalty revenue flowing back to Medarex is substantial.
Charles' estimate of Medarex's Stelara royalties alone tops $100 million a year.
His math pencils out OK, but I do worry that he overestimates the peak revenue potential for both Stelara and golimumab. Both seem like strong drugs, but so are Enbrel and Humira. It's not going to be easy to unseat well-entrenched drugs like Enbrel and Humira, especially since both drugs are considered very safe for patients. Stelara and golimumab may be as safe, but they lack the years of data to prove it.
This exact point was made by two rheumatologists speaking last month on a panel at a health care conference sponsored by Cowen & Co. Both doctors believed that drugs like golimumab (Stelara didn't come up specifically) would be fighting for second- or third-line treatment. Neither was enthusiastic at all about swapping out a new drug for either Humira or Enbrel any time soon.
Couple this conservatism on the part of doctors with a recession-fueled pullback in the use of all expensive biologic drugs to treat auto-immune diseases like rheumatoid arthritis (which I wrote about this week), and you've got plenty of reasons to be cautious about assuming huge royalty revenue flowing into Medarex's coffers.
I don't want to leave the impression that the approval of golimumab and/or Stelara isn't positive for Medarex. Both drugs will bring non-dilutive cash to the company which is definitely a plus in this market environment. Moreover, the approval of either drug will validate Medarex's antibody technology platform, another good thing.
But for Medarex to be truly successful, the company must become more than just the next PDL Biopharma(PDLI Quote) or Xoma(XOMA Quote). Both of these companies have been disappointments. They collect royalty revenues on other companies' successful drugs but have never been able to develop drugs successfully on their own.
Charles believes that ipilimumab, Medarex's melanoma drug (partnered with Bristol-Myers Squibb) may be that internally developed drug that gets Medarex really moving. I have my serious doubts about that, based on the uninspiring data released so far.
And let's not forget the lameness of Medarex's management team, which seems incapable of doing anything right. Honestly, CEO Howard Pien is like a black hole -- shareholder value goes in, but never comes out.
At around $5.50 a share (a $700 million market cap), Medarex is already getting credit for some of the anticipated royalties from golimumab and Stelara. As one analyst said to me this week, think of that royalty stream as a backstop on Medarex's current valuation and not so much as a future growth driver for the stock price.
That will come if Medarex can successfully develop its internal pipeline of drug candidates. And on that front, I'm definitely in wait-and-see mode.
Hi Ville
So! Ich hoffe, jetzt geht es los!!!
Haben wir uns verdient! Lets rock!!!
So! Ich hoffe, jetzt geht es los!!!

Haben wir uns verdient! Lets rock!!!
Antwort auf Beitrag Nr.: 36.964.447 von where_is_the_beef am 14.04.09 13:38:40Hi WITB, Dendreons Provenge hat seinen OS Endpunkt signifikant erreicht, wie vor 10min per PM von Dendreon herausgegeben wurde. Dies ist unglaublich wichtig auch für Medarex, validiert es doch den Ansatz "Immuntherapie gegen Krebs" und sollte etwas Zuvertrauen in Ipilimumab zurückbringen. Ich erinnere nur an das Jahr 2007, in dem Medarex mit der Odac Entscheidung für DNDN etwas mit nach oben gesprungen ist.
Antwort auf Beitrag Nr.: 36.962.169 von Ville7 am 14.04.09 07:35:20
PRINCETON, N.J., April 14 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) today announced that it will receive a milestone payment of an undisclosed amount from its licensing partner, Centocor Ortho Biotech Inc., in connection with the marketing approval from Health Canada's Biologics and Genetic Therapies Directorate, to market SIMPONI(TM) (golimumab, also known as CNTO 148) as a once-monthly subcutaneous treatment for adults with active forms of rheumatoid arthritis, psoriatic arthritis and ankylosing spondylitis.
SIMPONI is a new, human anti-tumor necrosis factor (TNF) monoclonal antibody that was generated by Medarex's UltiMAb® technology that targets and neutralizes both the soluble and membrane-bound forms of TNF-alpha. Regulatory applications seeking marketing authorization for SIMPONI have also been filed in the United States and Europe. Under the agreement with Centocor Ortho Biotech, Medarex will receive future sales-based royalty payments from the commercial sales of SIMPONI.
"SIMPONI is the second antibody generated from our UltiMAb® technology to receive regulatory approval, further demonstrating the potential of our antibody technology platform for generating therapeutics addressing underserved medical needs," said Howard H. Pien, Chairman and CEO of Medarex. "As antibodies continue to grow as a source of breakthrough medicines for many diseases, we believe that therapeutics from our core technology will continue to play a prominent role in expanding treatment options for patients."
Centocor Ortho Biotech Inc. first licensed Medarex's UltiMAb® technology for the generation of human antibodies in 1997. The agreement was expanded in 2000 and later extended in 2007 to provide Centocor Ortho Biotech Inc. with continued access to Medarex's UltiMAb® technology. Other antibodies generated from Medarex's UltiMAb® technology in development by Centocor Ortho Biotech Inc. or its partners include STELARA(TM) (ustekinumab), a human antibody approved in Canada and Europe for the treatment of moderate to severe plaque psoriasis; and CNTO 95, an anti-integrin human antibody in Phase 2 development for the treatment of cancer.
---------------
Jetzt haben also beide mabs (irgend)einen regierungsamtlichen "Stempel". So richtig glücklich bin ich aber erst, wenn das Okay der FDA da ist. Ob das noch in diesem Quartal für beide der Fall sein wird?
PRINCETON, N.J., April 14 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX - News) today announced that it will receive a milestone payment of an undisclosed amount from its licensing partner, Centocor Ortho Biotech Inc., in connection with the marketing approval from Health Canada's Biologics and Genetic Therapies Directorate, to market SIMPONI(TM) (golimumab, also known as CNTO 148) as a once-monthly subcutaneous treatment for adults with active forms of rheumatoid arthritis, psoriatic arthritis and ankylosing spondylitis.
SIMPONI is a new, human anti-tumor necrosis factor (TNF) monoclonal antibody that was generated by Medarex's UltiMAb® technology that targets and neutralizes both the soluble and membrane-bound forms of TNF-alpha. Regulatory applications seeking marketing authorization for SIMPONI have also been filed in the United States and Europe. Under the agreement with Centocor Ortho Biotech, Medarex will receive future sales-based royalty payments from the commercial sales of SIMPONI.
"SIMPONI is the second antibody generated from our UltiMAb® technology to receive regulatory approval, further demonstrating the potential of our antibody technology platform for generating therapeutics addressing underserved medical needs," said Howard H. Pien, Chairman and CEO of Medarex. "As antibodies continue to grow as a source of breakthrough medicines for many diseases, we believe that therapeutics from our core technology will continue to play a prominent role in expanding treatment options for patients."
Centocor Ortho Biotech Inc. first licensed Medarex's UltiMAb® technology for the generation of human antibodies in 1997. The agreement was expanded in 2000 and later extended in 2007 to provide Centocor Ortho Biotech Inc. with continued access to Medarex's UltiMAb® technology. Other antibodies generated from Medarex's UltiMAb® technology in development by Centocor Ortho Biotech Inc. or its partners include STELARA(TM) (ustekinumab), a human antibody approved in Canada and Europe for the treatment of moderate to severe plaque psoriasis; and CNTO 95, an anti-integrin human antibody in Phase 2 development for the treatment of cancer.
---------------
Jetzt haben also beide mabs (irgend)einen regierungsamtlichen "Stempel". So richtig glücklich bin ich aber erst, wenn das Okay der FDA da ist. Ob das noch in diesem Quartal für beide der Fall sein wird?
ein Beitrag aus dem Yahoo-Msg-Board. Mitgelauscht beim CC von JNJ
JNJ erwartet FDA-Zulassung für Stelara im Juli und für Simponi noch im April
lg - Lycos
*****************************************
Nice work kblumb. I listened to the call this evening, and the information was provided at minute 42 (Q&A), for those of you interested.
They anticipate Stelera now in July, and it does look like they received a Class 2 response, but did not report it -- not fair. Of course, it may come earlier with illegal importation issues with Stelera in Canada growing.
JNJ states that they have been active on both files, and anticiapte GOLI approval at the end of the month.
I'm a bit disappointed in the delay for Stelera, but at least we know that it is not an "unusual" delay, the timeframe communicated is now July 2009.
JNJ erwartet FDA-Zulassung für Stelara im Juli und für Simponi noch im April
lg - Lycos
*****************************************
Nice work kblumb. I listened to the call this evening, and the information was provided at minute 42 (Q&A), for those of you interested.
They anticipate Stelera now in July, and it does look like they received a Class 2 response, but did not report it -- not fair. Of course, it may come earlier with illegal importation issues with Stelera in Canada growing.
JNJ states that they have been active on both files, and anticiapte GOLI approval at the end of the month.
I'm a bit disappointed in the delay for Stelera, but at least we know that it is not an "unusual" delay, the timeframe communicated is now July 2009.
DAUSEND!!!!!!!!!!!! 
sonsst schreibt ja auch keiner was....
..............................................

sonsst schreibt ja auch keiner was....
..............................................
morgen 27 euro.............. oder nicht............. oder was?
Brüder Grimm - Tischchen deck dich, Goldesel und Knüppel aus dem Sack
Vor Zeiten war ein Schneider, der drei Söhne hatte und nur eine einzige Ziege. Aber die Ziege, weil sie alle zusammen mit ihrer Milch ernährte, mußte ihr gutes Futter haben und täglich hinaus auf die Weide geführt werden. Die Söhne taten das auch nach der Reihe. Einmal brachte sie der älteste auf den Kirchhof, wo die schönsten Kräuter standen, ließ sie da fressen und herumspringen. Abends, als es Zeit war heimzugehen, fragte er: "Ziege, bist du satt ?" Die Ziege antwortete:
"Ich bin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sprach der Junge, faßte sie am Strickchen, führte sie in den Stall und band sie fest. "Nun", sagte der alte Schneider, "hat die Ziege ihr gehöriges Futter ?" "Oh", antwortete der Sohn, "die ist so satt, sie mag kein Blatt." Der Vater aber wollte sich selbst überzeugen, ging hinab in den Stall streichelte das liebe Tier und fragte: "Ziege, bist du auch satt ?" Die Ziege antwortete:
"Wovon sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
"Was muß ich hören !" rief der Schneider, lief hinauf und sprach zu dem Jungen: "Ei, du Lügner, sagst die Ziege wäre satt und hast sie hungern lassen ?" Und in seinem Zorne nahm er die Elle von der Wand und jagte ihn mit Schlägen hinaus. Am andern Tag war die Reihe am zweiten Sohn, der suchte an der Gartenhecke einen Platz aus, wo lauter gute Kräuter standen, und die Ziege fraß sie rein ab. Abends, als er heim wollte, fragte er: "Ziege, bist du satt ?" Die Ziege antwortete:
"Ich bin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sprach der Junge, zog sie heim und band sie im Stall fest. "Nun", sagte der alte Schneider, "hat die Ziege ihr gehöriges Futter ?" "Oh", antwortete der Sohn, ,die ist so satt, sie mag kein Blatt. ' Der Schneider wollte sich darauf nicht verlassen, ging hinab in den Stall und fragte: "Ziege, bist du auch satt ?" Die Ziege antwortete:
Wovon sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
"Der gottlose Bösewicht !" schrie der Schneider, "so ein frommes Tier hungern zu lassen " Lief hinauf und schlug mit der Elle den Jungen zur Haustüre hinaus.
Die Reihe kam jetzt an den dritten Sohn, der wollte seine Sache gut machen, suchte Buschwerk mit dem schönsten Laube aus und ließ die Ziege daran fressen. Abends, als er heim wollte, fragte er: "Ziege, bist du auch satt ?" Die Ziege antwortete:
"Ich bin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sagte der Junge, führte sie in den Stall und band sie fest. "Nun", sagte der alte Schneider, "hat die Ziege ihr gehöriges Futter ?" "Oh", antwortete der Sohn, "die ist so satt, sie mag kein Blatt." Der Schneider traute nicht, ging hinab und fragte: "Ziege, bist du auch satt ?" Das boshafte Tier antwortete:
"Wovon sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
"Oh, die Lügenbrut !" rief der Schneider, "einer so gottlos und pflichtvergessen wie der andere ! Ihr sollt mich nicht länger zum Narren haben !" Und vor Zorn ganz außer sich sprang er hinauf und gerbte dem armen Jungen mit der Elle den Rücken so gewaltig, daß er zum Haus hinaussprang.
Der alte Schneider war nun mit seiner Ziege allein. Am andern Morgen ging er hinab in den Stall, liebkoste die Ziege und sprach: "Komm, mein liebes Tierlein, ich will dich selbst zur Weide führen." Er nahm sie am Strick und brachte sie zu grünen Hecken und unter Schafrippe und was sonst die Ziegen gerne fressen. "Da kannst du dich einmal nach Herzenslust sättigen", sprach er zu ihr und ließ sie weiden bis zum Abend. Da fragte er: "Ziege, bist du satt ?" Sie antwortete:
"Ich hin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sagte der Schneider, führte sie in den Stall und band sie fest. Als er wegging, kehrte er sich noch einmal um und sagte: "Nun bist du doch einmal satt !" Aber die Ziege machte es ihm nicht besser und rief:
"Wie sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
Als der Schneider das hörte, stutzte er und sah wohl, daß er seine drei Söhne ohne Ursache verstoßen hatte. "Wart", rief er, " Du undankbares Geschöpf, dich fortzujagen ist noch zu wenig, ich will dich zeichnen, daß du dich unter ehrbaren Schneidern nicht mehr darfst sehen lassen." In einer Hast sprang er hinauf, holte sein Bartmesser, seifte der Ziege den Kopf ein und schor sie so glatt wie seine flache Hand. Und weil die Elle zu ehrenvoll gewesen wäre, holte er die Peitsche und versetzte ihr solche Hiebe, daß sie in gewaltigen Sprüngen davonlief.
Der Schneider, als er so ganz einsam in seinem Hause saß, verfiel in große Traurigkeit und hätte seine Söhne gerne wieder gehabt, aber niemand wußte, wo sie hingeraten waren.
Der älteste war zu einem Schreiner in die Lehre gegangen, da lernte er fleißig und unverdrossen, und als seine Zeit herum war, daß er wandern sollte, schenkte ihm der Meister ein Tischchen, das gar kein besonderes Ansehen hatte und von gewöhnlichem Holz war; aber es hatte eine gute Eigenschaft. Wenn man es hinstellte und sprach: "Tischchen, deck dich !" so war das gute Tischchen auf einmal mit einem sauberen Tüchlein bedeckt und stand da ein Teller, und Messer und Gabel daneben und Schüsseln mit Gesottenem und Gebratenem und ein großes Glas mit rotem Wein leuchtete, daß einem das Herz lachte. Der junge Gesell dachte: Damit hast du genug für dein Lebtag, zog guter Dinge in der Welt umher und bekümmerte sich gar nicht darum, ob ein Wirtshaus gut oder schlecht und ob etwas darin zu finden war oder nicht. Wenn es ihm gefiel, so kehrte er gar nicht ein, sondern im Felde, im Wald, auf einer Wiese, wo er Lust hatte, nahm er sein Tischchen vom Rücken, stellte es vor sich und sprach: "Deck dich !" so war alles da, was sein Herz begehrte. Endlich kam es ihm in den Sinn, er wollte zu seinem Vater zurückkehren, sein Zorn würde sich gelegt haben, und mit dem "Tischchen deck dich" würde er ihn gerne wieder aufnehmen. Es trug sich zu, daß er auf dem Heimweg abends in ein Wirtshaus kam, das mit Gästen angefüllt war. Sie hießen ihn willkommen und luden ihn ein, sich zu ihnen zu setzen und mit ihnen zu essen, sonst würde er schwerlich noch etwas bekommen. "Nein", antwortete der Schreiner, "die paar Bissen will ich euch nicht von dem Munde nehmen, lieber sollt ihr meine Gäste sein." Sie lachten und meinten, er triebe seinen Spaß mit ihnen. Er aber stellte sein hölzernes Tischchen mitten in die Stube und sprach: "Tischchen, deck dich "' Augenblicklich war es mit Speisen besetzt, so gut, wie sie der Wirt nicht hätte herbeischaffen können und wovon der Geruch den Gästen lieblich in die Nase stieg. "Zugegriffen, liebe Freunde !" sprach der Schreiner, und die Gäste, als sie sahen, wie es gemeint war, ließen sich nicht zweimal bitten, rückten heran, zogen ihre Messer und griffen tapfer zu. Und was sie am meisten verwunderte, wenn eine Schüssel leer geworden war, so stellte sich gleich von selbst eine volle an ihren Platz. Der Wirt stand in einer Ecke und sah dem Dinge zu; er wußte gar nicht, was er sagen sollte, dachte aber: Einen solchen Koch könntest du in deiner Wirtschaft wohl brauchen. Der Schreiner und seine Gesellschaft waren lustig bis in die späte Nacht, endlich legten sie sich schlafen, und der junge Geselle ging auch zu Bett und stellte sein Wunschtischchen an die Wand. Dem Wirte aber ließen seine Gedanken keine Ruhe, es fiel ihm ein, daß in seiner Rumpelkammer ein altes Tischchen stände, das geradeso aussah; das holte er ganz sachte herbei und vertauschte es mit dem Wünschtischchen. Am andern Morgen zahlte der Schreiner sein Schlafgeld, packte sein Tischchen auf, dachte gar nicht daran, daß er ein falsches hätte, und ging seiner Wege. Zu Mittag kam er bei seinem Vater an, der ihn mit großer Freude empfing. "Nun, mein lieber Sohn, was hast du gelernt ?" sagte er zu ihm. "Vater, ich bin ein Schreiner geworden." "Ein gutes Handwerk", erwiderte der Alte, "aber was hast du von deiner Wanderschaft mitgebracht ?" "Vater, das beste, was ich mitgebracht habe, ist das Tischchen." Der Schneider betrachtete es von allen Seiten und sagte: "Daran hast du kein Meisterstück gemacht, das ist ein altes und schlechtes Tischchen." "Aber es ist ein ,Tischchen deck dich'", antwortete der Sohn, "wenn ich es hinstelle und sage ihm, es solle sich decken, so stehen gleich die schönsten Gerichte darauf und ein Wein dabei, der das Herz erfreut. Ladet nur alle Verwandte und Freunde ein, die sollen sich einmal laben und erquicken, denn das Tischchen macht sie alle satt." Als die Gesellschaft beisammen war, stellte er sein Tischchen mitten in die Stube und sprach: "Tischchen, deck dich !" Aber das Tischchen regte sich nicht und blieb so leer wie ein anderer Tisch, der die Sprache nicht versteht. Da merkte der arme Geselle, daß ihm das Tischchen vertauscht war, und schämte sich, daß er wie ein Lügner dastand. Die Verwandten aber lachten ihn aus und mußten ungetrunken und ungegessen wieder heimwandern. Der Vater holte seine Lappen wieder herbei und schneiderte fort, der Sohn aber ging bei einem Meister in die Arbeit.
Der zweite Sohn war zu einem Müller gekommen und bei ihm in die Lehre gegangen. Als er seine Jahre herum hatte, sprach der Meister: "Weil du dich so wohl gehalten hast, so schenke ich dir einen Esel von einer besonderen Art, er zieht nicht am Wagen und trägt auch keine Säcke." "Wozu ist er denn nütze ?" fragte der junge Geselle. "Er speit Gold", antwortete der Müller, "wenn du ihn auf ein Tuch stellst und sprichst: ,Bricklebrit !' so speit dir das gute Tier Goldstücke aus, hinten und vorn." "Das ist eine schöne Sache", sprach der Geselle, dankte dem Meister und zog in die Welt. Wenn er Gold nötig hatte, brauchte er nur zu seinem Esel "Bricklebrit !" zu sagen, so regnete es Goldstücke, und er hatte weiter keine Mühe, als sie von der Erde aufzuheben. Wo er hinkam, war ihm das Beste gut genug, und je teurer je lieber, denn er hatte immer einen vollen Beutel. Als er sich eine Zeitlang in der Welt umgesehen hatte, dachte er: Du mußt deinen Vater aufsuchen, wenn du mit dem Goldesel kommst, so wird er seinen Zorn vergessen und dich gut aufnehmen. Es trug sich zu, daß er in dasselbe Wirtshaus geriet, in welchem seinem Bruder das Tischchen vertauscht war. Er führte seinen Esel an der Hand, und der Wirt wollte ihm das Tier abnehmen und anbinden, der junge Geselle aber sprach: "Gebt Euch keine Mühe, meinen Grauschimmel führe ich selbst in den Stall und binde ihn auch selbst an, denn ich muß wissen, wo er steht." Dem Wirt kam das wunderlich vor, und er meinte, einer, der seinen Esel selbst besorgen müßte, hätte nicht viel zu verzehren; aber als der Fremde in die Tasche griff, zwei Goldstücke herausholte und sagte, er solle nur etwas Gutes für ihn einkaufen, so machte er große Augen, lief und suchte das Beste, das er auftreiben konnte. Nach der Mahlzeit fragte der Gast, was er schuldig wäre, der Wirt wollte die doppelte Kreide nicht sparen und sagte, noch ein paar Goldstücke müßte er zulegen. Der Geselle griff in die Tasche, aber sein Geld war eben zu Ende. "Wartet einen Augenblick, Herr Wirt", sprach er, "ich will nur gehen und Gold holen !" nahm aber das Tischtuch mit. Der Wirt wußte nicht, was das heißen sollte, war neugierig, schlich ihm nach, und da der Gast die Stalltüre zuriegelte, so guckte er durch ein Astloch. Der Fremde breitete unter dem Esel das Tuch aus, rief "Bricklebrit !" und augenblicklich fing das Tier an zu speien von hinten und von vorne, daß es ordentlich auf die Erde herabregnete. "Ei, der Tausend !" sagte der Wirt, "da sind die Dukaten bald geprägt ! So ein Geldbeutel ist nicht übel !" Der Gast bezahlte seine Zeche und legte sich schlafen, der Wirt aber schlich in der Nacht herab in den Stall, führte den Münzmeister weg und band einen andern Esel an seine Stelle. Den folgenden Morgen in der Frühe zog der Geselle mit seinem Esel ab und meinte, er hätte seinen "Goldesel". Mittags kam er bei seinem Vater an, der sich freute, als er ihn wiedersah, und ihn gerne aufnahm. "Was ist aus dir geworden, mein Sohn ?" fragte der Alte. "Ein Müller, lieber Vater", antwortete er. "Was hast du von deiner Wanderschaft mitgebracht ?" "Weiter nichts als einen Esel." "Esel gibt's hier genug", sagte der Vater, "da wäre mir doch eine gute Ziege lieber gewesen." "Ja", antwortete der Sohn, "aber es ist kein gemeiner Esel, sondern ein ,Goldesel'; wenn ich sage ,Bricklebrit !', so speit Euch das gute Tier ein ganzes Tuch voll Goldstücke. Laßt nur alle Verwandten herbeirufen, ich mache sie alle zu reichen Leuten." "Das laß ich mir gefallen", sagte der Schneider, "dann brauch ich mich mit der Nadel nicht weiter zu quälen", sprang selbst fort und rief die Verwandten herbei. Sobald sie beisammen waren, hieß sie der Müller Platz machen, breitete sein Tuch aus und brachte den Esel in die Stube. "Jetzt gebt acht !" sagte er und rief: "Bricklebrit !", aber es waren keine Goldstücke, was herabfiel, und es zeigte sich, daß das Tier nichts von der Kunst verstand, denn es bringt's nicht jeder Esel soweit. Da machte der arme Müller ein langes Gesicht, sah, daß er betrogen war, und bat die Verwandten um Verzeihung, die so arm heimgingen, als sie gekommen waren. Es blieb nichts übrig, der Alte mußte wieder nach der Nadel greifen und der Junge sich bei einem Müller verdingen.
Der dritte Bruder war zu einem Drechsler in die Lehre gegangen, und weil es ein kunstreiches Handwerk ist, mußte er am längsten lernen. Seine Brüder aber meldeten ihm in einem Briefe, wie schlimm es ihnen ergangen wäre und wie sie der Wirt noch am letzten Abend um ihre schönen Wünschdinge gebracht hätte. Als der Drechsler nun ausgelernt hatte und wandern sollte, so schenkte ihm sein Meister, weil er sich so wohl gehalten, einen Sack und sagte: "Es liegt ein Knüppel darin." "Den Sack kann ich umhängen, und er kann mir gute Dienste leisten, aber was soll der Knüppel darin ? Der macht ihn nur schwer." "Das will ich dir sagen", antwortete der Meister. "Hat dir jemand etwas zuleid getan, so sprich nur: ,Knüppel, aus dem Sack !', so springt dir der Knüppel heraus unter die Leute und tanzt ihnen so lustig auf dem Rücken herum, daß sie sich acht Tage lang nicht regen und bewegen können; und eher läßt er nicht ab, als bis du sagst: ,Knüppel, in den Sack !"' Der Gesell dankte ihm, hing den Sack um, und wenn ihm jemand zu nahe kam und auf den Leib wollte, so sprach er: "Knüppel, aus dem Sack !", alsbald sprang der Knüppel heraus und klopfte einem nach dem andern den Rock oder das Wams gleich auf dem Rücken aus und wartete nicht erst, bis er ihn ausgezogen hatte; und das ging so geschwind, daß, eh' sich's einer versah, die Reihe schon an ihm war. Der junge Drechsler langte zur Abendzeit in dem Wirtshaus an, wo seine Brüder betrogen worden waren. Er legte seinen Ranzen vor sich auf den Tisch und fing an zu erzählen, was er alles Merkwürdiges in der Welt gesehen habe. "Ja", sagte er, "man findet wohl ein ,Tischchen deck dich', einen ,Goldesel' und dergleichen, lauter gute Dinge, die ich nicht verachte, aber das ist alles nichts gegen den Schatz, den ich mir erworben habe und mit mir da in meinem Sack führe." Der Wirt spitzte die Ohren: Was in aller Welt mag das sein ? dachte er, der Sack ist wohl mit lauter Edelsteinen angefüllt den sollte ich billig auch noch haben, denn aller guten Dinge sind drei. Als Schlafenszeit war, streckte sich der Gast auf die Bank und legte seinen Sack als Kopfkissen unter. Der Wirt, als er meinte, der Gast läge in tiefem Schlaf, ging herbei, rückte und zog ganz sachte und vorsichtig an dem Sack, ob er ihn vielleicht wegziehen und einen andern unterlegen könnte. Der Drechsler aber hatte schon lange darauf gewartet; wie nun der Wirt eben einen herzhaften Ruck tun wollte, rief er: "Knüppel, aus dem Sack " Alsbald fuhr das Knüppelchen heraus, dem Wirt auf den Leib und rieb ihm die Nähte, daß es eine Art hatte. Der Wirt schrie zum Erbarmen, aber je lauter er schrie, desto kräftiger schlug der Knüppel ihm den Takt dazu auf den Rücken, bis er endlich erschöpft zur Erde fiel. Da sprach der Drechsler: "Wenn du das ,Tischchen deck dich' und den ,Goldesel' nicht wieder herausgibst, so soll der Tanz von neuem angehen !" "Ach nein", rief der Wirt ganz kleinlaut, ich gebe alles gerne wieder heraus, laßt nur den verwünschten Kobold wieder in den Sack kriechen." Da sprach der Geselle: "Ich will Gnade vor Recht ergehen lassen, aber hüte dich vor Schaden !" Dann rief er "Knüppel, in den Sack !" und ließ ihn ruhen.
Der Drechsler zog am andern Morgen mit dem "Tichchen deck dich" und dem "Goldesel" heim zu seinem Vater. Der Schneider freute, als er ihn wiedersah, und fragte auch ihn, was es in der Fremde gelernt hätte. "Lieber Vater", antwortete er "Ich bin ein Drechsler geworden." "Ein kunstreiches Handwerk", sagte der Vater, "was hast du von der Wanderschaft mitgebracht ?" "Ein kostbares Stück, lieber Vater", antwortete der Sohn, "einen Knüppel in dem Sack." "Was ?" rief der Vater, "einen Knüppel ! Das ist der Mühe wert ! Den kannst du dir von jedem Baume abhauen." "Aber einen solchen nicht lieber Vater. Sage ich: 'Knüppel aus dem Sack' so springt der Knüppel heraus und macht mit dem, der es nicht gut mit mir meint, einen schlimmen Tanz und läßt nicht eher nach, als bis er auf der Erde liegt und um gut Wetter bittet. Seht ihr mit diesem Knüppel habe ich das ,Tischlein deck dich' und den ,Goldesel' wieder herbeigeschafft, die der diebische Wirt meinen Brüdern abgenommen hatte. Jetzt laßt sie beide rufen und ladet alle Verwandten ein, ich will sie speisen und tränken und will ihnen die Taschen noch mit Gold füllen."
Der alte Schneider wollte nicht recht trauen, brachte aber doch die Verwandten zusammen. Da deckte der Drechsler ein Tuch in die Stube, führte den Goldesel herein und sagte zu seinem Bruder: "Nun, lieber Bruder, sprich mit ihm !" Der Müller sagte: "Bricklebrit !", und augenblicklich sprangen die Goldstücke auf das Tuch herab, als käme ein Platzregen, und der Esel hörte nicht eher auf, als bis alle so viel hatten, daß sie nicht mehr tragen konnten. (Ich sehe dir's an, du wärst auch gerne dabeigewesen !) Dann holte der Drechsler das Tischchen und sagte: "Lieber Bruder, nun sprich mit ihm !" Und kaum hatte der Schreiner "Tischchen, deck dich !" gesagt, so war es gedeckt und mit den schönsten Schüsseln reichlich besetzt. Da ward eine Mahlzeit gehalten, wie der gute Schneider noch keine in seinem Hause erlebt hatte, und die ganze Verwandtschaft blieb beisammen bis in die Nacht, und waren alle lustig und vergnügt. Der Schneider verschloß Nadel und Zwirn, Elle und Bügeleisen in einen Schrank und lebte mit seinen drei .Söhnen in Freude und Herrlichkeit.
Wo ist aber die Ziege hingekommen, die schuld war, daß der Schneider seine drei Söhne fortjagte ? Das will ich dir sagen. Sie schämte sich, daß sie einen kahlen Kopf hatte, lief in eine Fuchshöhle und verkroch sich hinein. Als der Fuchs nach Hause kam, funkelten ihm ein paar große Augen aus der Dunkelheit entgegen, daß er erschrak und wieder zurücklief. Der Bär begegnete ihm, und da der Fuchs ganz verstört aussah, so sprach er: "Was ist dir, Bruder Fuchs, was machst du für ein Gesicht ?" "Ach", antwortete der Rote, "ein grimmig Tier sitzt in meiner Höhle und hat mich mit feurigen Augen angeglotzt." "Das wollen wir bald austreiben", sprach der Bär, ging mit zu der Höhle und schaute hinein; als er aber die feurigen Augen erblickte, wandelte ihn ebenfalls Furcht an, er wollte mit dem grimmigen Tiere nichts zu tun haben und nahm Reißaus. Die Biene begegnete ihm, und da sie merkte, daß es ihm in seiner Haut nicht wohl zumute war, sprach sie: "Bär, du machst ja ein gewaltig verdrießlich Gesicht, wo ist deine Lustigkeit geblieben ?" "Du hast gut reden", antwortete der Bär, "es sitzt ein grimmiges Tier mit Glotzaugen in dem Hause des Roten, und wir können es nicht herausjagen." Die Biene sprach: "Du dauerst mich, Bär, ich bin ein armes, schwaches Geschöpf, das ihr im Wege nicht anguckt, aber ich glaube doch, daß ich euch helfen kann." Sie flog in die Fuchshöhle, setzte sich der Ziege auf den glatten, geschorenen Kopf und stach sie so gewaltig, daß sie aufsprang, "meh ! meh !" schrie und wie toll in die Welt hineinlief; und weiß niemand auf diese Stunde, wo sie hingelaufen ist.
Vor Zeiten war ein Schneider, der drei Söhne hatte und nur eine einzige Ziege. Aber die Ziege, weil sie alle zusammen mit ihrer Milch ernährte, mußte ihr gutes Futter haben und täglich hinaus auf die Weide geführt werden. Die Söhne taten das auch nach der Reihe. Einmal brachte sie der älteste auf den Kirchhof, wo die schönsten Kräuter standen, ließ sie da fressen und herumspringen. Abends, als es Zeit war heimzugehen, fragte er: "Ziege, bist du satt ?" Die Ziege antwortete:
"Ich bin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sprach der Junge, faßte sie am Strickchen, führte sie in den Stall und band sie fest. "Nun", sagte der alte Schneider, "hat die Ziege ihr gehöriges Futter ?" "Oh", antwortete der Sohn, "die ist so satt, sie mag kein Blatt." Der Vater aber wollte sich selbst überzeugen, ging hinab in den Stall streichelte das liebe Tier und fragte: "Ziege, bist du auch satt ?" Die Ziege antwortete:
"Wovon sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
"Was muß ich hören !" rief der Schneider, lief hinauf und sprach zu dem Jungen: "Ei, du Lügner, sagst die Ziege wäre satt und hast sie hungern lassen ?" Und in seinem Zorne nahm er die Elle von der Wand und jagte ihn mit Schlägen hinaus. Am andern Tag war die Reihe am zweiten Sohn, der suchte an der Gartenhecke einen Platz aus, wo lauter gute Kräuter standen, und die Ziege fraß sie rein ab. Abends, als er heim wollte, fragte er: "Ziege, bist du satt ?" Die Ziege antwortete:
"Ich bin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sprach der Junge, zog sie heim und band sie im Stall fest. "Nun", sagte der alte Schneider, "hat die Ziege ihr gehöriges Futter ?" "Oh", antwortete der Sohn, ,die ist so satt, sie mag kein Blatt. ' Der Schneider wollte sich darauf nicht verlassen, ging hinab in den Stall und fragte: "Ziege, bist du auch satt ?" Die Ziege antwortete:
Wovon sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
"Der gottlose Bösewicht !" schrie der Schneider, "so ein frommes Tier hungern zu lassen " Lief hinauf und schlug mit der Elle den Jungen zur Haustüre hinaus.
Die Reihe kam jetzt an den dritten Sohn, der wollte seine Sache gut machen, suchte Buschwerk mit dem schönsten Laube aus und ließ die Ziege daran fressen. Abends, als er heim wollte, fragte er: "Ziege, bist du auch satt ?" Die Ziege antwortete:
"Ich bin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sagte der Junge, führte sie in den Stall und band sie fest. "Nun", sagte der alte Schneider, "hat die Ziege ihr gehöriges Futter ?" "Oh", antwortete der Sohn, "die ist so satt, sie mag kein Blatt." Der Schneider traute nicht, ging hinab und fragte: "Ziege, bist du auch satt ?" Das boshafte Tier antwortete:
"Wovon sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
"Oh, die Lügenbrut !" rief der Schneider, "einer so gottlos und pflichtvergessen wie der andere ! Ihr sollt mich nicht länger zum Narren haben !" Und vor Zorn ganz außer sich sprang er hinauf und gerbte dem armen Jungen mit der Elle den Rücken so gewaltig, daß er zum Haus hinaussprang.
Der alte Schneider war nun mit seiner Ziege allein. Am andern Morgen ging er hinab in den Stall, liebkoste die Ziege und sprach: "Komm, mein liebes Tierlein, ich will dich selbst zur Weide führen." Er nahm sie am Strick und brachte sie zu grünen Hecken und unter Schafrippe und was sonst die Ziegen gerne fressen. "Da kannst du dich einmal nach Herzenslust sättigen", sprach er zu ihr und ließ sie weiden bis zum Abend. Da fragte er: "Ziege, bist du satt ?" Sie antwortete:
"Ich hin so satt,
Ich mag kein Blatt, meh ! meh !"
"So komm nach Haus", sagte der Schneider, führte sie in den Stall und band sie fest. Als er wegging, kehrte er sich noch einmal um und sagte: "Nun bist du doch einmal satt !" Aber die Ziege machte es ihm nicht besser und rief:
"Wie sollt' ich satt sein ?
Ich sprang nur über Gräbelein
Und fand kein einzig Blättelein, meh ! meh !"
Als der Schneider das hörte, stutzte er und sah wohl, daß er seine drei Söhne ohne Ursache verstoßen hatte. "Wart", rief er, " Du undankbares Geschöpf, dich fortzujagen ist noch zu wenig, ich will dich zeichnen, daß du dich unter ehrbaren Schneidern nicht mehr darfst sehen lassen." In einer Hast sprang er hinauf, holte sein Bartmesser, seifte der Ziege den Kopf ein und schor sie so glatt wie seine flache Hand. Und weil die Elle zu ehrenvoll gewesen wäre, holte er die Peitsche und versetzte ihr solche Hiebe, daß sie in gewaltigen Sprüngen davonlief.
Der Schneider, als er so ganz einsam in seinem Hause saß, verfiel in große Traurigkeit und hätte seine Söhne gerne wieder gehabt, aber niemand wußte, wo sie hingeraten waren.
Der älteste war zu einem Schreiner in die Lehre gegangen, da lernte er fleißig und unverdrossen, und als seine Zeit herum war, daß er wandern sollte, schenkte ihm der Meister ein Tischchen, das gar kein besonderes Ansehen hatte und von gewöhnlichem Holz war; aber es hatte eine gute Eigenschaft. Wenn man es hinstellte und sprach: "Tischchen, deck dich !" so war das gute Tischchen auf einmal mit einem sauberen Tüchlein bedeckt und stand da ein Teller, und Messer und Gabel daneben und Schüsseln mit Gesottenem und Gebratenem und ein großes Glas mit rotem Wein leuchtete, daß einem das Herz lachte. Der junge Gesell dachte: Damit hast du genug für dein Lebtag, zog guter Dinge in der Welt umher und bekümmerte sich gar nicht darum, ob ein Wirtshaus gut oder schlecht und ob etwas darin zu finden war oder nicht. Wenn es ihm gefiel, so kehrte er gar nicht ein, sondern im Felde, im Wald, auf einer Wiese, wo er Lust hatte, nahm er sein Tischchen vom Rücken, stellte es vor sich und sprach: "Deck dich !" so war alles da, was sein Herz begehrte. Endlich kam es ihm in den Sinn, er wollte zu seinem Vater zurückkehren, sein Zorn würde sich gelegt haben, und mit dem "Tischchen deck dich" würde er ihn gerne wieder aufnehmen. Es trug sich zu, daß er auf dem Heimweg abends in ein Wirtshaus kam, das mit Gästen angefüllt war. Sie hießen ihn willkommen und luden ihn ein, sich zu ihnen zu setzen und mit ihnen zu essen, sonst würde er schwerlich noch etwas bekommen. "Nein", antwortete der Schreiner, "die paar Bissen will ich euch nicht von dem Munde nehmen, lieber sollt ihr meine Gäste sein." Sie lachten und meinten, er triebe seinen Spaß mit ihnen. Er aber stellte sein hölzernes Tischchen mitten in die Stube und sprach: "Tischchen, deck dich "' Augenblicklich war es mit Speisen besetzt, so gut, wie sie der Wirt nicht hätte herbeischaffen können und wovon der Geruch den Gästen lieblich in die Nase stieg. "Zugegriffen, liebe Freunde !" sprach der Schreiner, und die Gäste, als sie sahen, wie es gemeint war, ließen sich nicht zweimal bitten, rückten heran, zogen ihre Messer und griffen tapfer zu. Und was sie am meisten verwunderte, wenn eine Schüssel leer geworden war, so stellte sich gleich von selbst eine volle an ihren Platz. Der Wirt stand in einer Ecke und sah dem Dinge zu; er wußte gar nicht, was er sagen sollte, dachte aber: Einen solchen Koch könntest du in deiner Wirtschaft wohl brauchen. Der Schreiner und seine Gesellschaft waren lustig bis in die späte Nacht, endlich legten sie sich schlafen, und der junge Geselle ging auch zu Bett und stellte sein Wunschtischchen an die Wand. Dem Wirte aber ließen seine Gedanken keine Ruhe, es fiel ihm ein, daß in seiner Rumpelkammer ein altes Tischchen stände, das geradeso aussah; das holte er ganz sachte herbei und vertauschte es mit dem Wünschtischchen. Am andern Morgen zahlte der Schreiner sein Schlafgeld, packte sein Tischchen auf, dachte gar nicht daran, daß er ein falsches hätte, und ging seiner Wege. Zu Mittag kam er bei seinem Vater an, der ihn mit großer Freude empfing. "Nun, mein lieber Sohn, was hast du gelernt ?" sagte er zu ihm. "Vater, ich bin ein Schreiner geworden." "Ein gutes Handwerk", erwiderte der Alte, "aber was hast du von deiner Wanderschaft mitgebracht ?" "Vater, das beste, was ich mitgebracht habe, ist das Tischchen." Der Schneider betrachtete es von allen Seiten und sagte: "Daran hast du kein Meisterstück gemacht, das ist ein altes und schlechtes Tischchen." "Aber es ist ein ,Tischchen deck dich'", antwortete der Sohn, "wenn ich es hinstelle und sage ihm, es solle sich decken, so stehen gleich die schönsten Gerichte darauf und ein Wein dabei, der das Herz erfreut. Ladet nur alle Verwandte und Freunde ein, die sollen sich einmal laben und erquicken, denn das Tischchen macht sie alle satt." Als die Gesellschaft beisammen war, stellte er sein Tischchen mitten in die Stube und sprach: "Tischchen, deck dich !" Aber das Tischchen regte sich nicht und blieb so leer wie ein anderer Tisch, der die Sprache nicht versteht. Da merkte der arme Geselle, daß ihm das Tischchen vertauscht war, und schämte sich, daß er wie ein Lügner dastand. Die Verwandten aber lachten ihn aus und mußten ungetrunken und ungegessen wieder heimwandern. Der Vater holte seine Lappen wieder herbei und schneiderte fort, der Sohn aber ging bei einem Meister in die Arbeit.
Der zweite Sohn war zu einem Müller gekommen und bei ihm in die Lehre gegangen. Als er seine Jahre herum hatte, sprach der Meister: "Weil du dich so wohl gehalten hast, so schenke ich dir einen Esel von einer besonderen Art, er zieht nicht am Wagen und trägt auch keine Säcke." "Wozu ist er denn nütze ?" fragte der junge Geselle. "Er speit Gold", antwortete der Müller, "wenn du ihn auf ein Tuch stellst und sprichst: ,Bricklebrit !' so speit dir das gute Tier Goldstücke aus, hinten und vorn." "Das ist eine schöne Sache", sprach der Geselle, dankte dem Meister und zog in die Welt. Wenn er Gold nötig hatte, brauchte er nur zu seinem Esel "Bricklebrit !" zu sagen, so regnete es Goldstücke, und er hatte weiter keine Mühe, als sie von der Erde aufzuheben. Wo er hinkam, war ihm das Beste gut genug, und je teurer je lieber, denn er hatte immer einen vollen Beutel. Als er sich eine Zeitlang in der Welt umgesehen hatte, dachte er: Du mußt deinen Vater aufsuchen, wenn du mit dem Goldesel kommst, so wird er seinen Zorn vergessen und dich gut aufnehmen. Es trug sich zu, daß er in dasselbe Wirtshaus geriet, in welchem seinem Bruder das Tischchen vertauscht war. Er führte seinen Esel an der Hand, und der Wirt wollte ihm das Tier abnehmen und anbinden, der junge Geselle aber sprach: "Gebt Euch keine Mühe, meinen Grauschimmel führe ich selbst in den Stall und binde ihn auch selbst an, denn ich muß wissen, wo er steht." Dem Wirt kam das wunderlich vor, und er meinte, einer, der seinen Esel selbst besorgen müßte, hätte nicht viel zu verzehren; aber als der Fremde in die Tasche griff, zwei Goldstücke herausholte und sagte, er solle nur etwas Gutes für ihn einkaufen, so machte er große Augen, lief und suchte das Beste, das er auftreiben konnte. Nach der Mahlzeit fragte der Gast, was er schuldig wäre, der Wirt wollte die doppelte Kreide nicht sparen und sagte, noch ein paar Goldstücke müßte er zulegen. Der Geselle griff in die Tasche, aber sein Geld war eben zu Ende. "Wartet einen Augenblick, Herr Wirt", sprach er, "ich will nur gehen und Gold holen !" nahm aber das Tischtuch mit. Der Wirt wußte nicht, was das heißen sollte, war neugierig, schlich ihm nach, und da der Gast die Stalltüre zuriegelte, so guckte er durch ein Astloch. Der Fremde breitete unter dem Esel das Tuch aus, rief "Bricklebrit !" und augenblicklich fing das Tier an zu speien von hinten und von vorne, daß es ordentlich auf die Erde herabregnete. "Ei, der Tausend !" sagte der Wirt, "da sind die Dukaten bald geprägt ! So ein Geldbeutel ist nicht übel !" Der Gast bezahlte seine Zeche und legte sich schlafen, der Wirt aber schlich in der Nacht herab in den Stall, führte den Münzmeister weg und band einen andern Esel an seine Stelle. Den folgenden Morgen in der Frühe zog der Geselle mit seinem Esel ab und meinte, er hätte seinen "Goldesel". Mittags kam er bei seinem Vater an, der sich freute, als er ihn wiedersah, und ihn gerne aufnahm. "Was ist aus dir geworden, mein Sohn ?" fragte der Alte. "Ein Müller, lieber Vater", antwortete er. "Was hast du von deiner Wanderschaft mitgebracht ?" "Weiter nichts als einen Esel." "Esel gibt's hier genug", sagte der Vater, "da wäre mir doch eine gute Ziege lieber gewesen." "Ja", antwortete der Sohn, "aber es ist kein gemeiner Esel, sondern ein ,Goldesel'; wenn ich sage ,Bricklebrit !', so speit Euch das gute Tier ein ganzes Tuch voll Goldstücke. Laßt nur alle Verwandten herbeirufen, ich mache sie alle zu reichen Leuten." "Das laß ich mir gefallen", sagte der Schneider, "dann brauch ich mich mit der Nadel nicht weiter zu quälen", sprang selbst fort und rief die Verwandten herbei. Sobald sie beisammen waren, hieß sie der Müller Platz machen, breitete sein Tuch aus und brachte den Esel in die Stube. "Jetzt gebt acht !" sagte er und rief: "Bricklebrit !", aber es waren keine Goldstücke, was herabfiel, und es zeigte sich, daß das Tier nichts von der Kunst verstand, denn es bringt's nicht jeder Esel soweit. Da machte der arme Müller ein langes Gesicht, sah, daß er betrogen war, und bat die Verwandten um Verzeihung, die so arm heimgingen, als sie gekommen waren. Es blieb nichts übrig, der Alte mußte wieder nach der Nadel greifen und der Junge sich bei einem Müller verdingen.
Der dritte Bruder war zu einem Drechsler in die Lehre gegangen, und weil es ein kunstreiches Handwerk ist, mußte er am längsten lernen. Seine Brüder aber meldeten ihm in einem Briefe, wie schlimm es ihnen ergangen wäre und wie sie der Wirt noch am letzten Abend um ihre schönen Wünschdinge gebracht hätte. Als der Drechsler nun ausgelernt hatte und wandern sollte, so schenkte ihm sein Meister, weil er sich so wohl gehalten, einen Sack und sagte: "Es liegt ein Knüppel darin." "Den Sack kann ich umhängen, und er kann mir gute Dienste leisten, aber was soll der Knüppel darin ? Der macht ihn nur schwer." "Das will ich dir sagen", antwortete der Meister. "Hat dir jemand etwas zuleid getan, so sprich nur: ,Knüppel, aus dem Sack !', so springt dir der Knüppel heraus unter die Leute und tanzt ihnen so lustig auf dem Rücken herum, daß sie sich acht Tage lang nicht regen und bewegen können; und eher läßt er nicht ab, als bis du sagst: ,Knüppel, in den Sack !"' Der Gesell dankte ihm, hing den Sack um, und wenn ihm jemand zu nahe kam und auf den Leib wollte, so sprach er: "Knüppel, aus dem Sack !", alsbald sprang der Knüppel heraus und klopfte einem nach dem andern den Rock oder das Wams gleich auf dem Rücken aus und wartete nicht erst, bis er ihn ausgezogen hatte; und das ging so geschwind, daß, eh' sich's einer versah, die Reihe schon an ihm war. Der junge Drechsler langte zur Abendzeit in dem Wirtshaus an, wo seine Brüder betrogen worden waren. Er legte seinen Ranzen vor sich auf den Tisch und fing an zu erzählen, was er alles Merkwürdiges in der Welt gesehen habe. "Ja", sagte er, "man findet wohl ein ,Tischchen deck dich', einen ,Goldesel' und dergleichen, lauter gute Dinge, die ich nicht verachte, aber das ist alles nichts gegen den Schatz, den ich mir erworben habe und mit mir da in meinem Sack führe." Der Wirt spitzte die Ohren: Was in aller Welt mag das sein ? dachte er, der Sack ist wohl mit lauter Edelsteinen angefüllt den sollte ich billig auch noch haben, denn aller guten Dinge sind drei. Als Schlafenszeit war, streckte sich der Gast auf die Bank und legte seinen Sack als Kopfkissen unter. Der Wirt, als er meinte, der Gast läge in tiefem Schlaf, ging herbei, rückte und zog ganz sachte und vorsichtig an dem Sack, ob er ihn vielleicht wegziehen und einen andern unterlegen könnte. Der Drechsler aber hatte schon lange darauf gewartet; wie nun der Wirt eben einen herzhaften Ruck tun wollte, rief er: "Knüppel, aus dem Sack " Alsbald fuhr das Knüppelchen heraus, dem Wirt auf den Leib und rieb ihm die Nähte, daß es eine Art hatte. Der Wirt schrie zum Erbarmen, aber je lauter er schrie, desto kräftiger schlug der Knüppel ihm den Takt dazu auf den Rücken, bis er endlich erschöpft zur Erde fiel. Da sprach der Drechsler: "Wenn du das ,Tischchen deck dich' und den ,Goldesel' nicht wieder herausgibst, so soll der Tanz von neuem angehen !" "Ach nein", rief der Wirt ganz kleinlaut, ich gebe alles gerne wieder heraus, laßt nur den verwünschten Kobold wieder in den Sack kriechen." Da sprach der Geselle: "Ich will Gnade vor Recht ergehen lassen, aber hüte dich vor Schaden !" Dann rief er "Knüppel, in den Sack !" und ließ ihn ruhen.
Der Drechsler zog am andern Morgen mit dem "Tichchen deck dich" und dem "Goldesel" heim zu seinem Vater. Der Schneider freute, als er ihn wiedersah, und fragte auch ihn, was es in der Fremde gelernt hätte. "Lieber Vater", antwortete er "Ich bin ein Drechsler geworden." "Ein kunstreiches Handwerk", sagte der Vater, "was hast du von der Wanderschaft mitgebracht ?" "Ein kostbares Stück, lieber Vater", antwortete der Sohn, "einen Knüppel in dem Sack." "Was ?" rief der Vater, "einen Knüppel ! Das ist der Mühe wert ! Den kannst du dir von jedem Baume abhauen." "Aber einen solchen nicht lieber Vater. Sage ich: 'Knüppel aus dem Sack' so springt der Knüppel heraus und macht mit dem, der es nicht gut mit mir meint, einen schlimmen Tanz und läßt nicht eher nach, als bis er auf der Erde liegt und um gut Wetter bittet. Seht ihr mit diesem Knüppel habe ich das ,Tischlein deck dich' und den ,Goldesel' wieder herbeigeschafft, die der diebische Wirt meinen Brüdern abgenommen hatte. Jetzt laßt sie beide rufen und ladet alle Verwandten ein, ich will sie speisen und tränken und will ihnen die Taschen noch mit Gold füllen."
Der alte Schneider wollte nicht recht trauen, brachte aber doch die Verwandten zusammen. Da deckte der Drechsler ein Tuch in die Stube, führte den Goldesel herein und sagte zu seinem Bruder: "Nun, lieber Bruder, sprich mit ihm !" Der Müller sagte: "Bricklebrit !", und augenblicklich sprangen die Goldstücke auf das Tuch herab, als käme ein Platzregen, und der Esel hörte nicht eher auf, als bis alle so viel hatten, daß sie nicht mehr tragen konnten. (Ich sehe dir's an, du wärst auch gerne dabeigewesen !) Dann holte der Drechsler das Tischchen und sagte: "Lieber Bruder, nun sprich mit ihm !" Und kaum hatte der Schreiner "Tischchen, deck dich !" gesagt, so war es gedeckt und mit den schönsten Schüsseln reichlich besetzt. Da ward eine Mahlzeit gehalten, wie der gute Schneider noch keine in seinem Hause erlebt hatte, und die ganze Verwandtschaft blieb beisammen bis in die Nacht, und waren alle lustig und vergnügt. Der Schneider verschloß Nadel und Zwirn, Elle und Bügeleisen in einen Schrank und lebte mit seinen drei .Söhnen in Freude und Herrlichkeit.
Wo ist aber die Ziege hingekommen, die schuld war, daß der Schneider seine drei Söhne fortjagte ? Das will ich dir sagen. Sie schämte sich, daß sie einen kahlen Kopf hatte, lief in eine Fuchshöhle und verkroch sich hinein. Als der Fuchs nach Hause kam, funkelten ihm ein paar große Augen aus der Dunkelheit entgegen, daß er erschrak und wieder zurücklief. Der Bär begegnete ihm, und da der Fuchs ganz verstört aussah, so sprach er: "Was ist dir, Bruder Fuchs, was machst du für ein Gesicht ?" "Ach", antwortete der Rote, "ein grimmig Tier sitzt in meiner Höhle und hat mich mit feurigen Augen angeglotzt." "Das wollen wir bald austreiben", sprach der Bär, ging mit zu der Höhle und schaute hinein; als er aber die feurigen Augen erblickte, wandelte ihn ebenfalls Furcht an, er wollte mit dem grimmigen Tiere nichts zu tun haben und nahm Reißaus. Die Biene begegnete ihm, und da sie merkte, daß es ihm in seiner Haut nicht wohl zumute war, sprach sie: "Bär, du machst ja ein gewaltig verdrießlich Gesicht, wo ist deine Lustigkeit geblieben ?" "Du hast gut reden", antwortete der Bär, "es sitzt ein grimmiges Tier mit Glotzaugen in dem Hause des Roten, und wir können es nicht herausjagen." Die Biene sprach: "Du dauerst mich, Bär, ich bin ein armes, schwaches Geschöpf, das ihr im Wege nicht anguckt, aber ich glaube doch, daß ich euch helfen kann." Sie flog in die Fuchshöhle, setzte sich der Ziege auf den glatten, geschorenen Kopf und stach sie so gewaltig, daß sie aufsprang, "meh ! meh !" schrie und wie toll in die Welt hineinlief; und weiß niemand auf diese Stunde, wo sie hingelaufen ist.
Nicht mal einer da, der Schreibfehler moniert?




Antwort auf Beitrag Nr.: 36.982.726 von Reinhardz am 16.04.09 19:08:05Jeder Thread braucht einen D*pp*n!
Herzlich willkommen!



Herzlich willkommen!




Gegen Ende des Jahres kommt die Entscheidung. Ist 1st line advanced Melanoma DTIC plus ipiliumumab 10mg besser als DTIC alleine?
Hier ein paar Overall Survival Daten aus zwei kleineren Phase II Studien in 2nd line advanced Melanoma
(Grafik unten plus von mir eingezeichnet) und historischem DTIC aus denen man schliessen könnte, dass
* DTIC plus ipilimumab 3mg möglicherweise besser wirkt als ipilimumab 3mg alleine (study MDX-10-08)
* ipilimumab 10mg besser wirkt als ipilimumab 0.3mg oder 3mg (study 022)
* alle ipilimumab Dosierungen besser wirken als DTIC historisch (diese Aussage allerdings sehr fraglich).
Daraus könnte man schliessen, dass auch DTIC plus ipilimumab 10mg besser als DTIC alleine wirken sollte, da ipilimumab 10mg klar den besten Effekt aufweisen konnte und auch keine gegenseitige Hemmung von DTIC und ipilimumab in study MDX-10-08 gefunden werden konnte - im Gegenteil. Trotzdem muss man ob der Ergebnisse der teils unverblindeten und in der Patientenauswahl unterschiedlichen Studien vorsichtig sein. Zudem geht es in der 1st line Studie darum statistische Signifikanz aufzeigen zu können, wofür die 1st line Studie mit nur 500 Patienten eventuell underpowered sein könnte.
Es bleibt spannend und leider hängt der Börsen-Erfolg von Medarex erst mal an dieser einen Studie. Showdown gegen Jahresende.

Hier ein paar Overall Survival Daten aus zwei kleineren Phase II Studien in 2nd line advanced Melanoma
(Grafik unten plus von mir eingezeichnet) und historischem DTIC aus denen man schliessen könnte, dass
* DTIC plus ipilimumab 3mg möglicherweise besser wirkt als ipilimumab 3mg alleine (study MDX-10-08)
* ipilimumab 10mg besser wirkt als ipilimumab 0.3mg oder 3mg (study 022)
* alle ipilimumab Dosierungen besser wirken als DTIC historisch (diese Aussage allerdings sehr fraglich).
Daraus könnte man schliessen, dass auch DTIC plus ipilimumab 10mg besser als DTIC alleine wirken sollte, da ipilimumab 10mg klar den besten Effekt aufweisen konnte und auch keine gegenseitige Hemmung von DTIC und ipilimumab in study MDX-10-08 gefunden werden konnte - im Gegenteil. Trotzdem muss man ob der Ergebnisse der teils unverblindeten und in der Patientenauswahl unterschiedlichen Studien vorsichtig sein. Zudem geht es in der 1st line Studie darum statistische Signifikanz aufzeigen zu können, wofür die 1st line Studie mit nur 500 Patienten eventuell underpowered sein könnte.
Es bleibt spannend und leider hängt der Börsen-Erfolg von Medarex erst mal an dieser einen Studie. Showdown gegen Jahresende.

Antwort auf Beitrag Nr.: 36.987.542 von Ville7 am 17.04.09 12:04:57(diese Aussage allerdings sehr fraglich)
Und diese Aussage hier liegt daran, dass in der study 022 ein Crossover der 0.3 und 3mg Dosierung nach 12Wochen auf die 10mg Dosierung durchgeführt wurde. Siomit dürfte der positive ipilimumab Effekt auch dieser Dosierungen gegenüber DTIC vorwiegend den höheren ipilimumab Dosierungen zuzuschreiben sein.
Und diese Aussage hier liegt daran, dass in der study 022 ein Crossover der 0.3 und 3mg Dosierung nach 12Wochen auf die 10mg Dosierung durchgeführt wurde. Siomit dürfte der positive ipilimumab Effekt auch dieser Dosierungen gegenüber DTIC vorwiegend den höheren ipilimumab Dosierungen zuzuschreiben sein.
Antwort auf Beitrag Nr.: 36.987.684 von Ville7 am 17.04.09 12:19:05
Ville, vielen Dank für diese interessanten Erklärungen des Sachverhalts.
Nehmen wir nun mal den negativen Fall an, nämlich dass ipilimumab in der Indikation Melanom scheitert.
Ich habe Dich in einem früheren Posting so verstanden, dass Du davon ausgehst, dass dann von BMS und Medarex in anderen Indikationen voll weiterentwickelt wird. Würde dann nicht mal der Cashburn bei Medarex reduziert werden?
Wenn das so wäre, wäre ipilimumab ja wirklich für Medarex fast ein "Leben oder Sterben"-Schicksal...
Die nächste ASCO bringt ja neue Überlebensdaten. Hältst Du die für relevant oder bringt nur noch die Auswertung der P 3 etwas wirklich neues?
Ville, vielen Dank für diese interessanten Erklärungen des Sachverhalts.
Nehmen wir nun mal den negativen Fall an, nämlich dass ipilimumab in der Indikation Melanom scheitert.
Ich habe Dich in einem früheren Posting so verstanden, dass Du davon ausgehst, dass dann von BMS und Medarex in anderen Indikationen voll weiterentwickelt wird. Würde dann nicht mal der Cashburn bei Medarex reduziert werden?
Wenn das so wäre, wäre ipilimumab ja wirklich für Medarex fast ein "Leben oder Sterben"-Schicksal...

Die nächste ASCO bringt ja neue Überlebensdaten. Hältst Du die für relevant oder bringt nur noch die Auswertung der P 3 etwas wirklich neues?
Antwort auf Beitrag Nr.: 36.987.839 von SLGramann am 17.04.09 12:35:06Ich gehe derzeit von voller Weiterentwicklung aus - hängt aber natürlich davon ab, wie die Studie scheitert. ist es nur die Signifikanz oder auch die Wirksamkeit überhauot in Frage gestellt.
Medarex hat auf der letzten Company Presentation angekündigt, dass bald auch eine Studie der Kombination von PD1 mit ipilimumab kommen wird. Nach POC (proof of concept) von PD1/PDL1. Möglicherweise noch Ende 2009.
Das Cash ausgehen wird die nächsten 2,5 Jahre nicht. Neben 350Mio USD haben sie auch noch über 100Mio USD Beteiligungen. Und der Kredit muss so schnell nicht zurückgezahlt werden. 2012 sollten sie es aber geschafft haben aus eigener Kraft zu (über-)leben.
Ich gehe zudem davon aus dass folgende Ereignisse den Cashburn signifikant reduzieren:
* Zulassung Golimumab hoffentlich noch im April, Marktstart USA baldigst danach, bald signifikante Royalties
* Zulassung Stelara hoffentlich bis Juli und signifikante Royalties hieraus
* Auslizensierung eigener Projekte (POC für anti-diff. haben sie bereits, POC für den anti-IP10 kommt noch in 2009. Weitere POC für anti-PD1, anti-PDL1, anti-IFNα, anti-CD30, anti-CD70 sollten ebenfalls binnen zwei /drei Jahren vorliegen und Auslizensierungserlöse ermöglichen)
Also ganz so extrem sehe ich das Thema nicht. Aber es wäre schon ein herber Schlag, wenn die Studie scheitern sollte. Sollten die Studienergebnisse aber wieder Markterwartungen gut und signifikant sein, so wird es einen heftigen Lift im Kurs geben - m.E. bis 15-20 USD und mit danach aufkommender Übernahmespekulation auch darüber!?
Den upgedateten Überlebensdaten messe ich nicht die Bedeutung bei. Sie werden einen weiter positiven Verlauf aufzeigen und allerhöchstens die Zuversicht in den Ansatz steigern. Kursmässig erwarte ich mir aber nichts davon - ausserhalb dessen, dass Biotechs allgemein zu ASCO steigen. Viel mehr erwarte ich allerdings von den anstehenden Proff of Concepts und möglichen Verpartnerungen mit Upfront.
Medarex hat auf der letzten Company Presentation angekündigt, dass bald auch eine Studie der Kombination von PD1 mit ipilimumab kommen wird. Nach POC (proof of concept) von PD1/PDL1. Möglicherweise noch Ende 2009.
Das Cash ausgehen wird die nächsten 2,5 Jahre nicht. Neben 350Mio USD haben sie auch noch über 100Mio USD Beteiligungen. Und der Kredit muss so schnell nicht zurückgezahlt werden. 2012 sollten sie es aber geschafft haben aus eigener Kraft zu (über-)leben.
Ich gehe zudem davon aus dass folgende Ereignisse den Cashburn signifikant reduzieren:
* Zulassung Golimumab hoffentlich noch im April, Marktstart USA baldigst danach, bald signifikante Royalties
* Zulassung Stelara hoffentlich bis Juli und signifikante Royalties hieraus
* Auslizensierung eigener Projekte (POC für anti-diff. haben sie bereits, POC für den anti-IP10 kommt noch in 2009. Weitere POC für anti-PD1, anti-PDL1, anti-IFNα, anti-CD30, anti-CD70 sollten ebenfalls binnen zwei /drei Jahren vorliegen und Auslizensierungserlöse ermöglichen)
Also ganz so extrem sehe ich das Thema nicht. Aber es wäre schon ein herber Schlag, wenn die Studie scheitern sollte. Sollten die Studienergebnisse aber wieder Markterwartungen gut und signifikant sein, so wird es einen heftigen Lift im Kurs geben - m.E. bis 15-20 USD und mit danach aufkommender Übernahmespekulation auch darüber!?
Den upgedateten Überlebensdaten messe ich nicht die Bedeutung bei. Sie werden einen weiter positiven Verlauf aufzeigen und allerhöchstens die Zuversicht in den Ansatz steigern. Kursmässig erwarte ich mir aber nichts davon - ausserhalb dessen, dass Biotechs allgemein zu ASCO steigen. Viel mehr erwarte ich allerdings von den anstehenden Proff of Concepts und möglichen Verpartnerungen mit Upfront.
Antwort auf Beitrag Nr.: 36.988.354 von Ville7 am 17.04.09 13:26:17Rechtschreibfehler bitte nach Fund behalten - war eine Schnelltippsermessage.
Geht doch: 
4,90 €
+0,65
+15,29 %
Gruß
Zock

4,90 €
+0,65
+15,29 %
Gruß
Zock
Antwort auf Beitrag Nr.: 36.989.399 von Zock1000 am 17.04.09 15:20:55Nun müssen nur noch die Amiländer die "maßgebliche" Börse in Fra beachten. 
Gruß
Zock

Gruß
Zock
Medarex Announces Clinical Data for MDX-1401 in Hodgkin's Lymphoma at Annual Meeting of the American Association for Cancer Research
PRINCETON, N.J., April 20 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX)
today announced preliminary data from an ongoing Phase 1 clinical trial of MDX-1401
in patients with relapsed or refractory Hodgkin's lymphoma (HL) that demonstrated both
clinical and immunological activity signals. MDX-1401 is a fully human,
non-fucosylated antibody that targets CD30, a marker for activated lymphocytes that is present on
malignant cells of HL as well as other CD30-expressing cancers. Results from the study
were presented in a poster session (Abstract #1227) at the Annual Meeting of the
American Association for Cancer Research (AACR), held April 18-22, 2009 in Colorado.
An ongoing multi-dose, dose-escalation Phase 1 trial of MDX-1401 in patients
with relapsed or refractory HL is being conducted to establish and evaluate the safety
profile and initial efficacy of MDX-1401. Preliminary data from the Phase 1 trial
demonstrate that multiple doses (ranging from 0.01 to 1.0 mg/kg) of MDX-1401 in patients
with HL were generally safe and well-tolerated. Two of the 8 patients with stable disease
had a reduction of 40 percent or more in tumor burden after two treatment cycles of
MDX-1401. In addition, flow cytometry indicated decreased circulating CD30 positive
cells in 83 percent of patients (10/12) after one cycle of four weekly intravenous
infusions.
"We find these preliminary safety and efficacy data for our second generation
anti-CD30 antibody encouraging," said Geoffrey M. Nichol, MBChB, Senior Vice President
of Product Development at Medarex. "We are currently enrolling additional patients at
higher dose levels and look forward to examining further results from the ongoing Phase
1 trial."
Information about the AACR and its Annual Meeting may be found at www.aacr.org.
About MDX-1401
MDX-1401 is a second-generation anti-CD30 antibody where fucose (a sugar
structure) is absent, thereby increasing the antibody's antibody-dependent cellular
cytotoxicity, or ADCC, activity (using the Potelligent(R) Technology of BioWa, Inc.). In
preclinical studies, MDX-1401 has shown improved antibody effector function over a first
generation anti-CD30 antibody. The ongoing Phase 1 trial of MDX-1401 continues to enroll
patients with relapsed or refractory Hodgkin lymphoma to further characterize the
clinical profile of the fully human, non-fucosylated antibody.
PRINCETON, N.J., April 20 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX)
today announced preliminary data from an ongoing Phase 1 clinical trial of MDX-1401
in patients with relapsed or refractory Hodgkin's lymphoma (HL) that demonstrated both
clinical and immunological activity signals. MDX-1401 is a fully human,
non-fucosylated antibody that targets CD30, a marker for activated lymphocytes that is present on
malignant cells of HL as well as other CD30-expressing cancers. Results from the study
were presented in a poster session (Abstract #1227) at the Annual Meeting of the
American Association for Cancer Research (AACR), held April 18-22, 2009 in Colorado.
An ongoing multi-dose, dose-escalation Phase 1 trial of MDX-1401 in patients
with relapsed or refractory HL is being conducted to establish and evaluate the safety
profile and initial efficacy of MDX-1401. Preliminary data from the Phase 1 trial
demonstrate that multiple doses (ranging from 0.01 to 1.0 mg/kg) of MDX-1401 in patients
with HL were generally safe and well-tolerated. Two of the 8 patients with stable disease
had a reduction of 40 percent or more in tumor burden after two treatment cycles of
MDX-1401. In addition, flow cytometry indicated decreased circulating CD30 positive
cells in 83 percent of patients (10/12) after one cycle of four weekly intravenous
infusions.
"We find these preliminary safety and efficacy data for our second generation
anti-CD30 antibody encouraging," said Geoffrey M. Nichol, MBChB, Senior Vice President
of Product Development at Medarex. "We are currently enrolling additional patients at
higher dose levels and look forward to examining further results from the ongoing Phase
1 trial."
Information about the AACR and its Annual Meeting may be found at www.aacr.org.
About MDX-1401
MDX-1401 is a second-generation anti-CD30 antibody where fucose (a sugar
structure) is absent, thereby increasing the antibody's antibody-dependent cellular
cytotoxicity, or ADCC, activity (using the Potelligent(R) Technology of BioWa, Inc.). In
preclinical studies, MDX-1401 has shown improved antibody effector function over a first
generation anti-CD30 antibody. The ongoing Phase 1 trial of MDX-1401 continues to enroll
patients with relapsed or refractory Hodgkin lymphoma to further characterize the
clinical profile of the fully human, non-fucosylated antibody.
Merck to license infection drug for up to $225 million
By Steve Goldstein
MEDX and the Massachusetts Biologic Laboratories of the University of Massachusetts Medical School to license investigational a fully human monoclonal antibody combination developed to target and neutralize Clostridium difficile toxins A and B, for the treatment of C. difficile infection. Terms call for Merck to pay $60 million and up to $165 million more depending on milestones to Medarex and the MBL. C. difficile infection is the primary cause of infectious diarrhea in hospitalized elderly patients in developed countries, Merck noted.
--------------------------
Na also, scheinbar 60Mio USD Upfront für C difficile - wohl halb für MEDX und halb für MBL. Oder Cash für ein viertel Jahr derzeitig hohe Entwicklungskosten.
Ich hoffe sie bekommen
By Steve Goldstein
MEDX and the Massachusetts Biologic Laboratories of the University of Massachusetts Medical School to license investigational a fully human monoclonal antibody combination developed to target and neutralize Clostridium difficile toxins A and B, for the treatment of C. difficile infection. Terms call for Merck to pay $60 million and up to $165 million more depending on milestones to Medarex and the MBL. C. difficile infection is the primary cause of infectious diarrhea in hospitalized elderly patients in developed countries, Merck noted.
--------------------------
Na also, scheinbar 60Mio USD Upfront für C difficile - wohl halb für MEDX und halb für MBL. Oder Cash für ein viertel Jahr derzeitig hohe Entwicklungskosten.
Ich hoffe sie bekommen
Merck & Co., Inc., Medarex, Inc. and Massachusetts Biologic Laboratories Sign Exclusive Licensing Agreement for Investigational Monoclonal Antibody Combination for Clostridium Difficile Infection
WHITEHOUSE STATION, N.J., PRINCETON, N.J. & JAMAICA PLAIN, Mass.--(BUSINESS WIRE)--Merck & Co., Inc., (through an affiliate), Medarex, Inc. (NASDAQ: MEDX - News) and Massachusetts Biologic Laboratories (MBL) of the University of Massachusetts Medical School (UMMS) today announced that they have signed an exclusive worldwide license agreement for CDA-1 and CDB-1 (also known as MDX-066/MDX-1388 and MBL-CDA1/MBL-CDB1), an investigational fully human monoclonal antibody combination developed to target and neutralize Clostridium difficile toxins A and B, for the treatment of C. difficile infection (CDI). CDA-1 and CDB-1 were co-developed by Medarex and MBL.
Under the terms of the agreement, Merck gains worldwide rights to develop and commercialize CDA-1 and CDB-1. Medarex and MBL will receive an upfront payment of $60 million and are potentially eligible to receive additional cash payments up to $165 million upon achievement of certain milestones associated with the development and approval of a drug candidate covered by this agreement. Upon commercialization, Medarex and MBL will also be eligible to receive double-digit royalties on product sales and milestones if certain sales targets are met. In accordance with the co-development agreement between Medarex and MBL, all payments will be divided equally.
The incidence of C. difficile infection (CDI) in the U.S. is rapidly increasing, with rates doubling from 2000 to 2005. The Centers for Disease Control and Prevention has projected that there will be as many as 750,000 cases of CDI per year by 20101.
\"C. difficile infection is the primary cause of infectious diarrhea in hospitalized elderly patients in developed countries,\" said Tony Ford-Hutchinson, Ph.D., senior vice president and franchise head, Infectious Diseases and Vaccines, Merck Research Laboratories. \"This agreement underscores Merck\'s ongoing commitment to infectious disease and our strategy of licensing promising candidates with the potential to address serious unmet medical needs.\"
“Discovering and developing an effective new treatment for a significant public health threat is the mission of MBL,” said Donna Ambrosino, M.D., executive director of MBL and professor of pediatrics at UMMS. “We are delighted that through this license agreement this candidate will advance towards final clinical studies and thus will potentially be available to patients in the shortest possible time.”
“This agreement exemplifies our ability to execute our corporate strategy combining creative science with an industry-leading platform to successfully enter into partnerships that are financially attractive and value-enhancing,” said Howard H. Pien, chairman and chief executive officer of Medarex. “We will continue to invest in our growing pipeline of innovative product candidates to address significant unmet medical needs, advance them to proof-of-concept and explore strategic options, either through partnership or by advancing the candidate ourselves, that would create long-term value for Medarex shareholders.”
Top-line results from a Phase II multicenter, randomized, double-blind, placebo-controlled trial evaluating CDA-1/CDB-1 provided evidence of a statistically significant reduction in the rate of recurrence of CDI compared with placebo. In the study, 200 patients symptomatic with an acute episode of CDI receiving standard of care antibiotics (metronidazole or vancomycin) were randomized to receive intravenous CDA-1/CDB-1 or intravenous placebo. An oral presentation of the Phase II data is scheduled at the upcoming Digestive Disease Week (DDW) in Chicago on June 2, 2009 at 2:15 p.m. local time.
About CDA-1 and CDB-1
CDA-1 and CDB-1 (also known as MDX-066/MDX-1388 and MBL-CDA1/MBL-CDB1) are novel, fully human antibodies that were developed by MBL and Medarex to target and neutralize the effects of toxin A and toxin B, respectively, the toxins produced by the bacterium C. difficile and which are associated with a serious and sometimes deadly form of diarrhea called C. difficile associated diarrhea. Published epidemiologic studies of hospitalized patients at risk for CDI have shown a positive correlation between detectable levels of antibodies in the blood to both toxins A and B and protection from disease or relapse.
About Clostridium difficile infection (CDI)
C. difficile is a spore-forming bacterium that is common in the environment and can colonize the gastrointestinal (GI) tract. It can be easily spread among hospitalized patients and residents of long-term care facilities, but also can be found in otherwise healthy individuals in the community. The disease most often develops in the presence of antibiotics administered for other infections, in which the complex microbial makeup of the GI tract is altered, and C. difficile spores may germinate, grow, and produce toxins A and B. The toxins cause damage to the GI tract lining in the colon, resulting in severe diarrhea, and may lead to perforation of the colon and/or death. Treatment of severe disease requires administration of additional antibiotics to kill the C. difficile bacteria, but because of the persistence of spores, as well as the difficulty for the intestinal flora to re-normalize in the setting of antibiotics, relapse/recurrence of CDI is common, and is estimated to occur in 20 percent of cases, with post-therapy recurrence rates as high as 60 percent. Recurrence can be difficult to manage and is a challenging complication of CDI; however, the use of non-antibiotic based approaches to neutralize C. difficile toxins may be important options to facilitate recovery of the GI flora.
More information on CDI can be found at: www.cdc.gov/ncidod/dhqp/id_Cdiff.html
About Merck
Merck & Co., Inc. is a global research-driven pharmaceutical company dedicated to putting patients first. Established in 1891, Merck discovers, develops, manufactures and markets vaccines and medicines to address unmet medical needs. The Company devotes extensive efforts to increase access to medicines through far-reaching programs that not only donate Merck medicines but help deliver them to the people who need them. Merck also publishes unbiased health information as a not-for-profit service. For more information, visit www.merck.com.
About Massachusetts Biologic Laboratories
The Massachusetts Biologic Laboratories is the only non-profit FDA- licensed manufacturer of vaccines and other biologic products in the United States. MBL produces 30 percent of the U.S. tetanus/diphtheria vaccine supply. In addition to the C. difficile program, MBL has discovered and developed human monoclonal antibodies for rabies and Hepatitis C, which are expected to enter clinical trials in 2009. The MBL was established in 1894 and since then the MBL\'s mission has been to improve public health through applied research, development and production of biologic products. MBL has been a part of the University of Massachusetts Medical School since 1997.
About The University of Massachusetts Medical School
The University of Massachusetts Medical School is one of the fastest growing academic health centers in the country and has built a reputation as a world-class research institution, consistently producing noteworthy advances in clinical and basic research. The Medical School attracts more than $200 million in extramural research funding annually. Visit www.umassmed.edu for additional information.
About Medarex
Medarex is a biopharmaceutical company focused on the discovery, development and potential commercialization of fully human antibody-based therapeutics to treat life-threatening and debilitating diseases, including cancer, inflammation, autoimmune disorders and infectious diseases. Medarex applies its UltiMAb® technology and product development and clinical manufacturing experience to generate, support and potentially commercialize a broad range of fully human antibody product candidates for itself and its partners. Over forty of these therapeutic product candidates derived from Medarex technology are in human clinical testing or have had INDs submitted for such trials, with the most advanced product candidates currently in Phase III clinical trials, the subject of regulatory applications for marketing authorization or approved in Canada and Europe. Medarex is committed to building value by developing a diverse pipeline of antibody products to address the world\'s unmet healthcare needs. For more information about Medarex, visit its website at www.medarex.com.
WHITEHOUSE STATION, N.J., PRINCETON, N.J. & JAMAICA PLAIN, Mass.--(BUSINESS WIRE)--Merck & Co., Inc., (through an affiliate), Medarex, Inc. (NASDAQ: MEDX - News) and Massachusetts Biologic Laboratories (MBL) of the University of Massachusetts Medical School (UMMS) today announced that they have signed an exclusive worldwide license agreement for CDA-1 and CDB-1 (also known as MDX-066/MDX-1388 and MBL-CDA1/MBL-CDB1), an investigational fully human monoclonal antibody combination developed to target and neutralize Clostridium difficile toxins A and B, for the treatment of C. difficile infection (CDI). CDA-1 and CDB-1 were co-developed by Medarex and MBL.
Under the terms of the agreement, Merck gains worldwide rights to develop and commercialize CDA-1 and CDB-1. Medarex and MBL will receive an upfront payment of $60 million and are potentially eligible to receive additional cash payments up to $165 million upon achievement of certain milestones associated with the development and approval of a drug candidate covered by this agreement. Upon commercialization, Medarex and MBL will also be eligible to receive double-digit royalties on product sales and milestones if certain sales targets are met. In accordance with the co-development agreement between Medarex and MBL, all payments will be divided equally.
The incidence of C. difficile infection (CDI) in the U.S. is rapidly increasing, with rates doubling from 2000 to 2005. The Centers for Disease Control and Prevention has projected that there will be as many as 750,000 cases of CDI per year by 20101.
\"C. difficile infection is the primary cause of infectious diarrhea in hospitalized elderly patients in developed countries,\" said Tony Ford-Hutchinson, Ph.D., senior vice president and franchise head, Infectious Diseases and Vaccines, Merck Research Laboratories. \"This agreement underscores Merck\'s ongoing commitment to infectious disease and our strategy of licensing promising candidates with the potential to address serious unmet medical needs.\"
“Discovering and developing an effective new treatment for a significant public health threat is the mission of MBL,” said Donna Ambrosino, M.D., executive director of MBL and professor of pediatrics at UMMS. “We are delighted that through this license agreement this candidate will advance towards final clinical studies and thus will potentially be available to patients in the shortest possible time.”
“This agreement exemplifies our ability to execute our corporate strategy combining creative science with an industry-leading platform to successfully enter into partnerships that are financially attractive and value-enhancing,” said Howard H. Pien, chairman and chief executive officer of Medarex. “We will continue to invest in our growing pipeline of innovative product candidates to address significant unmet medical needs, advance them to proof-of-concept and explore strategic options, either through partnership or by advancing the candidate ourselves, that would create long-term value for Medarex shareholders.”
Top-line results from a Phase II multicenter, randomized, double-blind, placebo-controlled trial evaluating CDA-1/CDB-1 provided evidence of a statistically significant reduction in the rate of recurrence of CDI compared with placebo. In the study, 200 patients symptomatic with an acute episode of CDI receiving standard of care antibiotics (metronidazole or vancomycin) were randomized to receive intravenous CDA-1/CDB-1 or intravenous placebo. An oral presentation of the Phase II data is scheduled at the upcoming Digestive Disease Week (DDW) in Chicago on June 2, 2009 at 2:15 p.m. local time.
About CDA-1 and CDB-1
CDA-1 and CDB-1 (also known as MDX-066/MDX-1388 and MBL-CDA1/MBL-CDB1) are novel, fully human antibodies that were developed by MBL and Medarex to target and neutralize the effects of toxin A and toxin B, respectively, the toxins produced by the bacterium C. difficile and which are associated with a serious and sometimes deadly form of diarrhea called C. difficile associated diarrhea. Published epidemiologic studies of hospitalized patients at risk for CDI have shown a positive correlation between detectable levels of antibodies in the blood to both toxins A and B and protection from disease or relapse.
About Clostridium difficile infection (CDI)
C. difficile is a spore-forming bacterium that is common in the environment and can colonize the gastrointestinal (GI) tract. It can be easily spread among hospitalized patients and residents of long-term care facilities, but also can be found in otherwise healthy individuals in the community. The disease most often develops in the presence of antibiotics administered for other infections, in which the complex microbial makeup of the GI tract is altered, and C. difficile spores may germinate, grow, and produce toxins A and B. The toxins cause damage to the GI tract lining in the colon, resulting in severe diarrhea, and may lead to perforation of the colon and/or death. Treatment of severe disease requires administration of additional antibiotics to kill the C. difficile bacteria, but because of the persistence of spores, as well as the difficulty for the intestinal flora to re-normalize in the setting of antibiotics, relapse/recurrence of CDI is common, and is estimated to occur in 20 percent of cases, with post-therapy recurrence rates as high as 60 percent. Recurrence can be difficult to manage and is a challenging complication of CDI; however, the use of non-antibiotic based approaches to neutralize C. difficile toxins may be important options to facilitate recovery of the GI flora.
More information on CDI can be found at: www.cdc.gov/ncidod/dhqp/id_Cdiff.html
About Merck
Merck & Co., Inc. is a global research-driven pharmaceutical company dedicated to putting patients first. Established in 1891, Merck discovers, develops, manufactures and markets vaccines and medicines to address unmet medical needs. The Company devotes extensive efforts to increase access to medicines through far-reaching programs that not only donate Merck medicines but help deliver them to the people who need them. Merck also publishes unbiased health information as a not-for-profit service. For more information, visit www.merck.com.
About Massachusetts Biologic Laboratories
The Massachusetts Biologic Laboratories is the only non-profit FDA- licensed manufacturer of vaccines and other biologic products in the United States. MBL produces 30 percent of the U.S. tetanus/diphtheria vaccine supply. In addition to the C. difficile program, MBL has discovered and developed human monoclonal antibodies for rabies and Hepatitis C, which are expected to enter clinical trials in 2009. The MBL was established in 1894 and since then the MBL\'s mission has been to improve public health through applied research, development and production of biologic products. MBL has been a part of the University of Massachusetts Medical School since 1997.
About The University of Massachusetts Medical School
The University of Massachusetts Medical School is one of the fastest growing academic health centers in the country and has built a reputation as a world-class research institution, consistently producing noteworthy advances in clinical and basic research. The Medical School attracts more than $200 million in extramural research funding annually. Visit www.umassmed.edu for additional information.
About Medarex
Medarex is a biopharmaceutical company focused on the discovery, development and potential commercialization of fully human antibody-based therapeutics to treat life-threatening and debilitating diseases, including cancer, inflammation, autoimmune disorders and infectious diseases. Medarex applies its UltiMAb® technology and product development and clinical manufacturing experience to generate, support and potentially commercialize a broad range of fully human antibody product candidates for itself and its partners. Over forty of these therapeutic product candidates derived from Medarex technology are in human clinical testing or have had INDs submitted for such trials, with the most advanced product candidates currently in Phase III clinical trials, the subject of regulatory applications for marketing authorization or approved in Canada and Europe. Medarex is committed to building value by developing a diverse pipeline of antibody products to address the world\'s unmet healthcare needs. For more information about Medarex, visit its website at www.medarex.com.
Antwort auf Beitrag Nr.: 37.009.215 von Ville7 am 21.04.09 13:48:07
Upon commercialization, Medarex and MBL will also be eligible to receive double-digit royalties on product sales and milestones if certain sales targets are met.
Das finde ich wirklich sehr schön.
Noch nicht klar ist mir dabei, ob Medarex jetzt auch von allen Entwicklungskosten freigestellt ist. Dann wäre es ein wirklich eleganter Deal... Oder ist das zu viel erwartet?
(Ich wünschte mir, dass man so ein Auslizensierungsmodell fahren könnte und wollte, falls ipilimumab zunächst scheitern sollte, aber BMS in anderen Indikationen unbedingt weitermachen will. Der cashburn bei Medarex macht mich nunmal krank.)
Upon commercialization, Medarex and MBL will also be eligible to receive double-digit royalties on product sales and milestones if certain sales targets are met.
Das finde ich wirklich sehr schön.
Noch nicht klar ist mir dabei, ob Medarex jetzt auch von allen Entwicklungskosten freigestellt ist. Dann wäre es ein wirklich eleganter Deal... Oder ist das zu viel erwartet?

(Ich wünschte mir, dass man so ein Auslizensierungsmodell fahren könnte und wollte, falls ipilimumab zunächst scheitern sollte, aber BMS in anderen Indikationen unbedingt weitermachen will. Der cashburn bei Medarex macht mich nunmal krank.)
Antwort auf Beitrag Nr.: 37.012.187 von SLGramann am 21.04.09 19:29:46Merck zahlt ab jetzt alles an Ent.kosten.
Royalties und Meilensteine werden zwischen Medarex und MBL geteilt.
Royalties und Meilensteine werden zwischen Medarex und MBL geteilt.
Antwort auf Beitrag Nr.: 37.012.657 von Ville7 am 21.04.09 20:29:27
Perfekt. Ein Geschäft, bei dem Medarex ab jetzt nichts mehr verlieren, aber dennoch einiges gewinnen kann. So etwas mag ich.
Perfekt. Ein Geschäft, bei dem Medarex ab jetzt nichts mehr verlieren, aber dennoch einiges gewinnen kann. So etwas mag ich.
Antwort auf Beitrag Nr.: 37.012.657 von Ville7 am 21.04.09 20:29:27 Royalties und Meilensteine werden zwischen Medarex und MBL geteilt.
Klingt sehr verlockend,das Risiko wird minimiert.
Danke für Deine immer aktuell und interessanten Recherchen.
Klingt sehr verlockend,das Risiko wird minimiert.
Danke für Deine immer aktuell und interessanten Recherchen.

Medarex kündigt Präklinische Daten aus mehreren Forschung Demonstration Anti-Tumor-Aktivität bei Krebs
und weitere Forschung auf dem Gebiet der Antikörper-Medikament
conjugates, gab heute bekannt, präklinische Wirksamkeit und Sicherheit von Daten aus verschiedenen Programmen,
April 18-22, 2009 April 18-22, 2009 , in , In Colorado Colorado . .
http://translate.google.de/translate?hl=de&sl=en&u=http://ww…
Bin sehr gespannt.
und weitere Forschung auf dem Gebiet der Antikörper-Medikament
conjugates, gab heute bekannt, präklinische Wirksamkeit und Sicherheit von Daten aus verschiedenen Programmen,
April 18-22, 2009 April 18-22, 2009 , in , In Colorado Colorado . .
http://translate.google.de/translate?hl=de&sl=en&u=http://ww…
Bin sehr gespannt.

Erster Medarex Antikörper in USA zugelassen
http://antibody-world.blogspot.com/2009/04/erster-medarex-an…
http://antibody-world.blogspot.com/2009/04/erster-medarex-an…
Antwort auf Beitrag Nr.: 37.039.531 von SLGramann am 25.04.09 07:14:09
Mal noch eine Frage zum Unterschied zu Stelara. Da hat die FDA doch mit einem Complete Response Letter weitere Daten zum Risikomanagement angefordert. War das jetzt bei Simponi nicht der Fall?
Wer hat Erfahrungen mit diesen Complete Response Letters? Wie "gefährlich" sind die? Gibt es Erfahrungen, wie sehr so etwas die Zulassung verzögert? Habe so etwas kürzlich auch bei Actelion gesehen. Ein Analyst hielt das eher für eine Formalie...
Mal noch eine Frage zum Unterschied zu Stelara. Da hat die FDA doch mit einem Complete Response Letter weitere Daten zum Risikomanagement angefordert. War das jetzt bei Simponi nicht der Fall?
Wer hat Erfahrungen mit diesen Complete Response Letters? Wie "gefährlich" sind die? Gibt es Erfahrungen, wie sehr so etwas die Zulassung verzögert? Habe so etwas kürzlich auch bei Actelion gesehen. Ein Analyst hielt das eher für eine Formalie...
Antwort auf Beitrag Nr.: 37.039.324 von Ville7 am 25.04.09 00:03:54tolle Nachricht. endlich 1. Zulassung für MEDX durch FDA (hoffentlich folgt Stelara bald 
FYI:
hier der Link zur PR von J&J http://www.jnj.com/connect/news/all/20090424_150000
bzw. direkt zu Simponi http://www.simponi.com/simponi/index.html
leider wird MEDX dabei nicht erwähnt eine PR sollte aber doch am spätestens Montag drinnen sein
eine PR sollte aber doch am spätestens Montag drinnen sein 
veröffentlich haben sie bis jetzt noch nichts
lg - Lycos
@ville: Super Blog. Gratuliere

FYI:
hier der Link zur PR von J&J http://www.jnj.com/connect/news/all/20090424_150000
bzw. direkt zu Simponi http://www.simponi.com/simponi/index.html
leider wird MEDX dabei nicht erwähnt
 eine PR sollte aber doch am spätestens Montag drinnen sein
eine PR sollte aber doch am spätestens Montag drinnen sein 
veröffentlich haben sie bis jetzt noch nichts
lg - Lycos
@ville: Super Blog. Gratuliere

Antwort auf Beitrag Nr.: 37.039.616 von Lycos2 am 25.04.09 08:30:12Ja Hallo mal wieder,

nach Vogel- nun Schweinegrippe. Könnte (leider) Thema des Jahres werden...
Auch MEDX schon dabei:
Grüße q.
Printer friendly version
SARS Antibody Sent to China for Preclinical Testing
Fully Human Antibody Developed by Medarex and the Massachusetts Biologic
Laboratories May be Part of China's Response to the Recent Outbreak of
SARS in Beijing
PRINCETON, N.J. and WORCESTER, Mass., April 26 /PRNewswire-FirstCall/ --
Responding to a request from a Chinese biotechnology company working closely
with officials in China, Medarex, Inc. (Nasdaq: MEDX) and the Massachusetts
Biologic Laboratories (MBL) of the University of Massachusetts Medical School
(UMMS) have shipped to Beijing a sample of the fully human antibody to SARS
developed by Medarex and MBL/UMMS.
The antibody was sent to Sinovac Biotech Co., Ltd.
(OTC Bulletin Board: SNVBF) for preclinical testing against SARS strains used
for their vaccine and the control strain from previous cases in China.
In response to the recent outbreak of SARS, and to assist with research on
potential therapies, Beijing-based Sinovac submitted this idea to the Chinese
State Food and Drug Administration and received support to test the
Medarex/MBL/UMMS antibody before any further action. Sinovac plans to conduct
preclinical tests to determine the antibody's effectiveness in neutralizing
the strains of the SARS virus.
"When faced with an outbreak of a deadly infectious disease like SARS,
those with a public health mission need to move fast," said Donna Ambrosino,
MD, Director of the MBL and a Professor of Pediatrics at UMass Medical School.
"When the request was made to us, we were able to ship the antibody within
hours."
Donald L. Drakeman, President and CEO of Medarex, Inc., agreed, saying
Medarex was ready to help. "We hope that our fully human antibody technology
can be useful in addressing this important public health issue," he said.
The antibody developed by scientists at MBL, Medarex and at UMass Medical
School's Worcester Campus, is the result of an accelerated research effort
funded by the National Institute of Allergy and Infectious Diseases (part of
the National Institutes of Health) that was launched in April of 2003
following the first global outbreak of SARS.
As previously announced, MBL/UMMS partnered with Medarex to use Medarex's
UltiMAb(TM) technology to generate fully human antibodies with the potential
to treat SARS. Under the terms of the agreement, Medarex and MBL expect to
share equally the full development costs of any antibody products as well as
any future revenues arising from these products.
SARS, a viral respiratory illness caused by a coronavirus, was first
reported in Asia in February 2003, and over the next few months, the illness
spread to more than two dozen countries in North America, South America,
Europe, and Asia. According to the World Health Organization, during the SARS
outbreak of 2003, a total of 8,098 people worldwide became sick with SARS; of
these, 774 died. The SARS global outbreak of 2003 was contained; however, it
is expected that the disease could re-emerge periodically in a cycle similar
to the common flu.
About Sinovac
Sinovac is one of the leading emerging biotechnology companies in China.
Working closely with Chinese public health officials, Sinovac focuses on
manufacturing and marketing human-use vaccines and related products, and
currently markets a vaccine for Hepatitis A. Sinovac is the first company in
China, as well as the world, granted permission by the Chinese government to
begin clinical trials for a vaccine to prevent SARS. The vaccine development
effort was funded by the Chinese government. The project began in April 2003.
About UMass Medical School
The University of Massachusetts Medical School is one of the fastest
growing academic health centers in the country and has built a reputation as a
world-class research institution, consistently producing noteworthy advances
in clinical and basic research. The Medical School attracts more than $153
million in extramural research funding annually, 80 percent of which comes
from federal funding sources. Research dollars enable UMMS scientists to
explore human disease from the molecular level to large-scale clinical trials.
Basic and clinical research leads to new approaches for diagnosis, treatment
and prevention of disease. Visit www.umassmed.edu for additional information.
About the Massachusetts Biologic Laboratories
The Massachusetts Biologic Laboratories is the only non-profit
FDA-licensed manufacturer of vaccines and other biologic products in the
United States. The laboratory was established in 1894; since then, the MBL's
mission has been to improve public health through applied research,
development and production of biologic products. MBL has been a part of the
UMass Medical School since 1997.
About Medarex
Medarex is a biopharmaceutical company focused on the discovery and
development of therapeutics to treat life-threatening and debilitating
diseases. Medarex's UltiMAb Human Antibody Development System(R) is a unique
combination of human antibody technologies that Medarex believes enables the
rapid creation and development of fully human antibodies to a wide range of
potential disease targets for therapeutic antibody products, including
products for the treatment of cancer, inflammation, autoimmune and infectious
diseases. Medarex's product pipeline is based on a variety of therapeutic
antibody products developed through the use of its UltiMAb(TM) technology.
Medarex creates and develops fully human antibodies for itself and others,
offering a full range of antibody related capabilities, including pre-clinical
and clinical development supported by cGMP manufacturing services. For more
information about Medarex, visit its website at www.medarex.com.
Except for the historical information presented herein, matters discussed
herein may constitute forward-looking statements that are subject to certain
risks and uncertainties that could cause actual results to differ materially
from any future results, performance or achievements expressed or implied by
such statements. Statements that are not historical facts, including
statements preceded by, followed by, or that include the words "potential,"
"believe," "anticipate," "intend," "plan," "expect," "estimate," "could,"
"may," or similar statements are forward-looking statements. Medarex
disclaims, however, any intent or obligation to update these forward-looking
statements. Risks and uncertainties include risks associated with product
discovery and development, uncertainties related to the outcome of preclinical
testing, unforeseen safety issues, uncertainties associated with the
collaborative process as well as risks detailed from time to time in Medarex's
public disclosure filings with the U.S. Securities and Exchange Commission
(SEC), including its Annual Report on Form 10-K for the fiscal year ended
December 31, 2003 and subsequent Quarterly Reports on Form 10-Q. There can be
no assurance that such development efforts will succeed, that such products
will receive required regulatory clearance or that, even if such regulatory
clearance were received, such products would ultimately achieve commercial
success. Copies of Medarex's public disclosure filings are available from its
investor relations department.
Medarex(R), the Medarex logo, and UltiMAb Human Antibody Development
System(R) are registered trademarks of Medarex, Inc. UltiMAb(TM) is a
trademark of Medarex, Inc. All rights are reserved.
SOURCE Medarex, Inc.; Massachusetts Biologic Laboratories
©2001-2009 Medarex, Inc. All rights reserved. - Legal Disclaimer - Trademarks - Privacy Policy

nach Vogel- nun Schweinegrippe. Könnte (leider) Thema des Jahres werden...
Auch MEDX schon dabei:
Grüße q.
Printer friendly version
SARS Antibody Sent to China for Preclinical Testing
Fully Human Antibody Developed by Medarex and the Massachusetts Biologic
Laboratories May be Part of China's Response to the Recent Outbreak of
SARS in Beijing
PRINCETON, N.J. and WORCESTER, Mass., April 26 /PRNewswire-FirstCall/ --
Responding to a request from a Chinese biotechnology company working closely
with officials in China, Medarex, Inc. (Nasdaq: MEDX) and the Massachusetts
Biologic Laboratories (MBL) of the University of Massachusetts Medical School
(UMMS) have shipped to Beijing a sample of the fully human antibody to SARS
developed by Medarex and MBL/UMMS.
The antibody was sent to Sinovac Biotech Co., Ltd.
(OTC Bulletin Board: SNVBF) for preclinical testing against SARS strains used
for their vaccine and the control strain from previous cases in China.
In response to the recent outbreak of SARS, and to assist with research on
potential therapies, Beijing-based Sinovac submitted this idea to the Chinese
State Food and Drug Administration and received support to test the
Medarex/MBL/UMMS antibody before any further action. Sinovac plans to conduct
preclinical tests to determine the antibody's effectiveness in neutralizing
the strains of the SARS virus.
"When faced with an outbreak of a deadly infectious disease like SARS,
those with a public health mission need to move fast," said Donna Ambrosino,
MD, Director of the MBL and a Professor of Pediatrics at UMass Medical School.
"When the request was made to us, we were able to ship the antibody within
hours."
Donald L. Drakeman, President and CEO of Medarex, Inc., agreed, saying
Medarex was ready to help. "We hope that our fully human antibody technology
can be useful in addressing this important public health issue," he said.
The antibody developed by scientists at MBL, Medarex and at UMass Medical
School's Worcester Campus, is the result of an accelerated research effort
funded by the National Institute of Allergy and Infectious Diseases (part of
the National Institutes of Health) that was launched in April of 2003
following the first global outbreak of SARS.
As previously announced, MBL/UMMS partnered with Medarex to use Medarex's
UltiMAb(TM) technology to generate fully human antibodies with the potential
to treat SARS. Under the terms of the agreement, Medarex and MBL expect to
share equally the full development costs of any antibody products as well as
any future revenues arising from these products.
SARS, a viral respiratory illness caused by a coronavirus, was first
reported in Asia in February 2003, and over the next few months, the illness
spread to more than two dozen countries in North America, South America,
Europe, and Asia. According to the World Health Organization, during the SARS
outbreak of 2003, a total of 8,098 people worldwide became sick with SARS; of
these, 774 died. The SARS global outbreak of 2003 was contained; however, it
is expected that the disease could re-emerge periodically in a cycle similar
to the common flu.
About Sinovac
Sinovac is one of the leading emerging biotechnology companies in China.
Working closely with Chinese public health officials, Sinovac focuses on
manufacturing and marketing human-use vaccines and related products, and
currently markets a vaccine for Hepatitis A. Sinovac is the first company in
China, as well as the world, granted permission by the Chinese government to
begin clinical trials for a vaccine to prevent SARS. The vaccine development
effort was funded by the Chinese government. The project began in April 2003.
About UMass Medical School
The University of Massachusetts Medical School is one of the fastest
growing academic health centers in the country and has built a reputation as a
world-class research institution, consistently producing noteworthy advances
in clinical and basic research. The Medical School attracts more than $153
million in extramural research funding annually, 80 percent of which comes
from federal funding sources. Research dollars enable UMMS scientists to
explore human disease from the molecular level to large-scale clinical trials.
Basic and clinical research leads to new approaches for diagnosis, treatment
and prevention of disease. Visit www.umassmed.edu for additional information.
About the Massachusetts Biologic Laboratories
The Massachusetts Biologic Laboratories is the only non-profit
FDA-licensed manufacturer of vaccines and other biologic products in the
United States. The laboratory was established in 1894; since then, the MBL's
mission has been to improve public health through applied research,
development and production of biologic products. MBL has been a part of the
UMass Medical School since 1997.
About Medarex
Medarex is a biopharmaceutical company focused on the discovery and
development of therapeutics to treat life-threatening and debilitating
diseases. Medarex's UltiMAb Human Antibody Development System(R) is a unique
combination of human antibody technologies that Medarex believes enables the
rapid creation and development of fully human antibodies to a wide range of
potential disease targets for therapeutic antibody products, including
products for the treatment of cancer, inflammation, autoimmune and infectious
diseases. Medarex's product pipeline is based on a variety of therapeutic
antibody products developed through the use of its UltiMAb(TM) technology.
Medarex creates and develops fully human antibodies for itself and others,
offering a full range of antibody related capabilities, including pre-clinical
and clinical development supported by cGMP manufacturing services. For more
information about Medarex, visit its website at www.medarex.com.
Except for the historical information presented herein, matters discussed
herein may constitute forward-looking statements that are subject to certain
risks and uncertainties that could cause actual results to differ materially
from any future results, performance or achievements expressed or implied by
such statements. Statements that are not historical facts, including
statements preceded by, followed by, or that include the words "potential,"
"believe," "anticipate," "intend," "plan," "expect," "estimate," "could,"
"may," or similar statements are forward-looking statements. Medarex
disclaims, however, any intent or obligation to update these forward-looking
statements. Risks and uncertainties include risks associated with product
discovery and development, uncertainties related to the outcome of preclinical
testing, unforeseen safety issues, uncertainties associated with the
collaborative process as well as risks detailed from time to time in Medarex's
public disclosure filings with the U.S. Securities and Exchange Commission
(SEC), including its Annual Report on Form 10-K for the fiscal year ended
December 31, 2003 and subsequent Quarterly Reports on Form 10-Q. There can be
no assurance that such development efforts will succeed, that such products
will receive required regulatory clearance or that, even if such regulatory
clearance were received, such products would ultimately achieve commercial
success. Copies of Medarex's public disclosure filings are available from its
investor relations department.
Medarex(R), the Medarex logo, and UltiMAb Human Antibody Development
System(R) are registered trademarks of Medarex, Inc. UltiMAb(TM) is a
trademark of Medarex, Inc. All rights are reserved.
SOURCE Medarex, Inc.; Massachusetts Biologic Laboratories
©2001-2009 Medarex, Inc. All rights reserved. - Legal Disclaimer - Trademarks - Privacy Policy
einige wichtige MEDX-Termine für Mai/Juni
lg - Lycos
May 12-14, 2009 (New York, NY)
Bank of America Merrill Lynch 2009 Health Care Conference
May 12-16 7th World Conference on Melanoma
May 21 Annual Meeting
May 29 - June 2 ASCO
June 10-11, 2009 (New York, NY)
8th Annual Needham Life Sciences Conference
June 17-18, 2009 (New York, NY)
Jefferies 3rd Annual Healthcare Conference
lg - Lycos
May 12-14, 2009 (New York, NY)
Bank of America Merrill Lynch 2009 Health Care Conference
May 12-16 7th World Conference on Melanoma
May 21 Annual Meeting
May 29 - June 2 ASCO
June 10-11, 2009 (New York, NY)
8th Annual Needham Life Sciences Conference
June 17-18, 2009 (New York, NY)
Jefferies 3rd Annual Healthcare Conference
Abott (Humira) klagt gegen JnJ (Simponi) wegen Patentverletzung. Ich hoffe das hemmt die Verkäufe von Simponi nicht.
Antwort auf Beitrag Nr.: 37.114.807 von Ville7 am 07.05.09 07:07:41Genau das aber verspricht sich Abott davon. Ihr Humira-Umsatz soll weiter wachsen und keine Anteile an Simoni verlieren. Und Unsicherheit hemmt immer.
Die Patentverletzung an sich kann ich überhaupt nicht beurteilen. Ob das mehr ist als heiße Luft und Gegenwind zur Zulassung?
Die Patentverletzung an sich kann ich überhaupt nicht beurteilen. Ob das mehr ist als heiße Luft und Gegenwind zur Zulassung?
Antwort auf Beitrag Nr.: 37.114.978 von eck64 am 07.05.09 08:07:43JnJ hat scheints zuvor auch Abott wegen Humira verklagt. Die werden sich einigen.
Die Verkäufe wird es nicht hemmen, solange es keine Injunction eines Gerichts gibt - und diese Mühlen mahlen langsam. Zudem hat Simponi eindeutigen Mehrwert gegenüber Humira, wie soll das von Abott gegenüber den Patienten verargumentiert werden?
Abott wird hier höchstens Cash + Royalties erwirken. An den Royalties für MEDX ändert das nichts.
Die Verkäufe wird es nicht hemmen, solange es keine Injunction eines Gerichts gibt - und diese Mühlen mahlen langsam. Zudem hat Simponi eindeutigen Mehrwert gegenüber Humira, wie soll das von Abott gegenüber den Patienten verargumentiert werden?
Abott wird hier höchstens Cash + Royalties erwirken. An den Royalties für MEDX ändert das nichts.
Zur Zeit findet der 7. Hautkrebs Weltkongress in Wien statt. Thema ist unter anderem auch Ipi. Hier der Link und ein Auszug aus dem Bericht.
lg Lycos
***********************
7. Hautkrebs-Weltkongress - 1.200 internationale Spezialisten tagen in Wien von 12. - 16. Mai
http://www.meduniwien.ac.at/homepage/news-und-topstories/de/…
.....
Neue Therapieansätze – Wiener Forschung spielt wichtige Rolle
Bei der Entwicklung neuer Therapiemöglichkeiten, mit denen sich diese Resistenzen umgehen lassen, ist die Universitätsklinik für Dermatologie Wien auch im internationalen Maßstab besonders aktiv. Erst kürzlich hat ein Team um Dr. K. Harmankaya eine große Studie (Phase II) mit dem neuartigen monoklonalen Antikörper Ipilimumab bei Menschen mit besonders fortgeschrittenem metastasierendem Melanom abgeschlossen. Die Substanz hat sich in einer Reihe von Fällen als vielversprechend erwiesen, was nicht nur einen Krankheitsstopp, sondern sogar eine Remission bestehender Metastasen betrifft. Die diesem Effekt zugrundeliegenden Mechanismen sind im Detail noch unklar. „Jetzt sind weitere Studien nötig, bevor an einen routinemäßigen klinischen Einsatz zu denken ist“, sagt Prof. Pehamberger.
.....
lg Lycos
***********************
7. Hautkrebs-Weltkongress - 1.200 internationale Spezialisten tagen in Wien von 12. - 16. Mai
http://www.meduniwien.ac.at/homepage/news-und-topstories/de/…
.....
Neue Therapieansätze – Wiener Forschung spielt wichtige Rolle
Bei der Entwicklung neuer Therapiemöglichkeiten, mit denen sich diese Resistenzen umgehen lassen, ist die Universitätsklinik für Dermatologie Wien auch im internationalen Maßstab besonders aktiv. Erst kürzlich hat ein Team um Dr. K. Harmankaya eine große Studie (Phase II) mit dem neuartigen monoklonalen Antikörper Ipilimumab bei Menschen mit besonders fortgeschrittenem metastasierendem Melanom abgeschlossen. Die Substanz hat sich in einer Reihe von Fällen als vielversprechend erwiesen, was nicht nur einen Krankheitsstopp, sondern sogar eine Remission bestehender Metastasen betrifft. Die diesem Effekt zugrundeliegenden Mechanismen sind im Detail noch unklar. „Jetzt sind weitere Studien nötig, bevor an einen routinemäßigen klinischen Einsatz zu denken ist“, sagt Prof. Pehamberger.
.....
Medarex erreicht Primary Endpoint bei MDX-1100
deutliche Verbesserung gegenüber Placebo.
lg - Lycos
*************************************
Medarex Announces Primary Endpoint Achieved in MDX-1100 Anti-IP-10 Antibody Phase 2 Trial for Rheumatoid Arthritis
Top-line data indicate statistically significant improvement in ACR20 responses
over placebo
PRINCETON, N.J., May 14 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX)
today announced that the MDX-1100 Phase 2 proof-of-concept trial in patients with
active rheumatoid arthritis (RA) receiving methotrexate successfully met its primary
endpoint. The top-line results from the recently completed 70-patient multi-center,
randomized, double-blind, placebo-controlled Phase 2 trial indicated that when compared to
placebo, three times the number of patients treated with 10 mg/kg of MDX-1100 every two
weeks achieved at least a 20% improvement in RA signs and symptoms at 12 weeks, the
primary endpoint of the study, as measured by the American College of Rheumatology (ACR)
20 measurement of response. These results were statistically significant when compared
with placebo (p=0.0024). The antibody combination with methotrexate was generally
safe and well-tolerated. Full results from this Phase 2 trial are planned to be presented
at a future scientific meeting.
"We are greatly encouraged by this demonstration of efficacy from a
well-designed and well-executed study," said Howard H. Pien, Chairman and CEO of Medarex. "These
results show that by targeting the chemokine IP-10 with our MDX-1100 antibody, we may
be able to offer a potentially important and novel treatment option for rheumatoid
arthritis and potentially other inflammatory indications."
"Based on these positive results with a novel pro-inflammatory target, we are
actively preparing for the next stage of clinical development for MDX-1100 in RA,
including the potential for subcutaneous dosing," said Geoffrey M. Nichol, M.B.Ch.B., Senior
Vice President of Product Development at Medarex. "We also look forward to exploring
the broader potential of MDX-1100 in a range of inflammatory diseases, including
ulcerative colitis in an ongoing companion Phase 2 study."
deutliche Verbesserung gegenüber Placebo.
lg - Lycos
*************************************
Medarex Announces Primary Endpoint Achieved in MDX-1100 Anti-IP-10 Antibody Phase 2 Trial for Rheumatoid Arthritis
Top-line data indicate statistically significant improvement in ACR20 responses
over placebo
PRINCETON, N.J., May 14 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX)
today announced that the MDX-1100 Phase 2 proof-of-concept trial in patients with
active rheumatoid arthritis (RA) receiving methotrexate successfully met its primary
endpoint. The top-line results from the recently completed 70-patient multi-center,
randomized, double-blind, placebo-controlled Phase 2 trial indicated that when compared to
placebo, three times the number of patients treated with 10 mg/kg of MDX-1100 every two
weeks achieved at least a 20% improvement in RA signs and symptoms at 12 weeks, the
primary endpoint of the study, as measured by the American College of Rheumatology (ACR)
20 measurement of response. These results were statistically significant when compared
with placebo (p=0.0024). The antibody combination with methotrexate was generally
safe and well-tolerated. Full results from this Phase 2 trial are planned to be presented
at a future scientific meeting.
"We are greatly encouraged by this demonstration of efficacy from a
well-designed and well-executed study," said Howard H. Pien, Chairman and CEO of Medarex. "These
results show that by targeting the chemokine IP-10 with our MDX-1100 antibody, we may
be able to offer a potentially important and novel treatment option for rheumatoid
arthritis and potentially other inflammatory indications."
"Based on these positive results with a novel pro-inflammatory target, we are
actively preparing for the next stage of clinical development for MDX-1100 in RA,
including the potential for subcutaneous dosing," said Geoffrey M. Nichol, M.B.Ch.B., Senior
Vice President of Product Development at Medarex. "We also look forward to exploring
the broader potential of MDX-1100 in a range of inflammatory diseases, including
ulcerative colitis in an ongoing companion Phase 2 study."
Moin,

die Anzeichen häuften sich ja ohnehin, aber die positiven Zeichen für Ipilimumab verdichten sich:

Hoffentlich hilfts irgendwann mal auch dem Kurs (und zwar nachhaltig)!
Gruß q.
Ipilimumab linked to melanoma survival: studies
Thu May 14, 2009 6:01pm EDT Email | Print | Share| Reprints | Single Page[-] Text [+]
Market News
Recovery hopes still alive, push up Asia stocks
Oil steadies below $59/bbl, eyes equities, dollar | Video
Nikkei rises 1.7 percent; Sony, Tokyo Electron jump
More Business & Investing News... Featured Broker sponsored link
LOS ANGELES, May 14 (Reuters) - More than a third of advanced melanoma patients treated with ipilimumab, an antibody being developed by Bristol-Myers Squibb Co (BMY.N) and Medarex Inc (MEDX.O), continued to survive after 18 months, according to data released on Thursday.
The 18-month survival rate for three Phase 2 trials ranged from 34.5 percent to 39.4 percent. Most trial participants had been previously treated with other therapies.
"The median survival in the past was only six months," said Renzo Canetta, head of oncology research at Bristol-Myers.
Two-year survival results are slated for presentation later this month at a meeting of the American Society of Clinical Oncology in Orlando.
Bristol-Myers and Medarex said last year that they would delay seeking approval of the experimental treatment after U.S. health regulators asked for additional overall survival data to further demonstrate the benefit of ipilimumab.
Canetta said Phase 3 data for ipilimumab in melanoma patients is expected to mature toward the end of this year or early 2010.
Ipilimumab is a fully human antibody that binds to a molecule on T-cells that plays a critical role in regulating natural immune responses to disease. The drug is also being studied in other tumor types, including lung cancer and prostate cancer.
© Thomson Reuters 2009 All rights reserved

die Anzeichen häuften sich ja ohnehin, aber die positiven Zeichen für Ipilimumab verdichten sich:

Hoffentlich hilfts irgendwann mal auch dem Kurs (und zwar nachhaltig)!
Gruß q.
Ipilimumab linked to melanoma survival: studies
Thu May 14, 2009 6:01pm EDT Email | Print | Share| Reprints | Single Page[-] Text [+]
Market News
Recovery hopes still alive, push up Asia stocks
Oil steadies below $59/bbl, eyes equities, dollar | Video
Nikkei rises 1.7 percent; Sony, Tokyo Electron jump
More Business & Investing News... Featured Broker sponsored link
LOS ANGELES, May 14 (Reuters) - More than a third of advanced melanoma patients treated with ipilimumab, an antibody being developed by Bristol-Myers Squibb Co (BMY.N) and Medarex Inc (MEDX.O), continued to survive after 18 months, according to data released on Thursday.
The 18-month survival rate for three Phase 2 trials ranged from 34.5 percent to 39.4 percent. Most trial participants had been previously treated with other therapies.
"The median survival in the past was only six months," said Renzo Canetta, head of oncology research at Bristol-Myers.
Two-year survival results are slated for presentation later this month at a meeting of the American Society of Clinical Oncology in Orlando.
Bristol-Myers and Medarex said last year that they would delay seeking approval of the experimental treatment after U.S. health regulators asked for additional overall survival data to further demonstrate the benefit of ipilimumab.
Canetta said Phase 3 data for ipilimumab in melanoma patients is expected to mature toward the end of this year or early 2010.
Ipilimumab is a fully human antibody that binds to a molecule on T-cells that plays a critical role in regulating natural immune responses to disease. The drug is also being studied in other tumor types, including lung cancer and prostate cancer.
© Thomson Reuters 2009 All rights reserved
Antwort auf Beitrag Nr.: 37.181.109 von quepos am 15.05.09 08:56:02Interessant die 2009er Asco Abstracts von Medarex:
http://www.abstract.asco.org/AbstView_65_34536.html
http://www.abstract.asco.org/AbstView_65_35657.html
http://www.abstract.asco.org/AbstView_65_32956.html
http://www.abstract.asco.org/AbstView_65_34399.html
ipi, wenn auch unkontrolliert und daher extrem mit Vorsicht zu geniessen, überzeugt hier mit seinen Daten.
PD-1 enttäuscht etwas.
http://www.abstract.asco.org/AbstView_65_34536.html
http://www.abstract.asco.org/AbstView_65_35657.html
http://www.abstract.asco.org/AbstView_65_32956.html
http://www.abstract.asco.org/AbstView_65_34399.html
ipi, wenn auch unkontrolliert und daher extrem mit Vorsicht zu geniessen, überzeugt hier mit seinen Daten.
PD-1 enttäuscht etwas.
Hier der wichtisgte Abstract, 18 monats Überlebensdaten ipi:
http://www.abstract.asco.org/AbstView_65_34626.html
Schauen echt gut aus.
http://www.abstract.asco.org/AbstView_65_34626.html
Schauen echt gut aus.
Antwort auf Beitrag Nr.: 37.183.603 von Ville7 am 15.05.09 12:54:15Study 12-month survival rate, %
[95% CI]
18-month survival rate, %
[95% CI]
Diese Daten sind wohl mehr als Ordentlich.
Wann wohl ein Ausbruch/oder eine Übernahme erfolgt?
Danke für Deine informativen Ausführungen.
PS.Der Verfasser ist in Medarex investiert.
[95% CI]

18-month survival rate, %
[95% CI]

Diese Daten sind wohl mehr als Ordentlich.

Wann wohl ein Ausbruch/oder eine Übernahme erfolgt?
Danke für Deine informativen Ausführungen.

PS.Der Verfasser ist in Medarex investiert.
Antwort auf Beitrag Nr.: 37.183.603 von Ville7 am 15.05.09 12:54:15Ja, das sind doch tolle Ergebnisse, vor allem im Vergleich mit den bisher verfügbaren Medikamenten.
Nebenwirkungen hin oder her - mangels Alternative müsste eigentlich die Zulassung allmählich mal drin sein, ist m.E. nur eine Frage der Zeit.
Bin nun wieder deutlich zuversichtlicher.
 Gruß q.
Gruß q.
Nebenwirkungen hin oder her - mangels Alternative müsste eigentlich die Zulassung allmählich mal drin sein, ist m.E. nur eine Frage der Zeit.
Bin nun wieder deutlich zuversichtlicher.
 Gruß q.
Gruß q.
hi
sieht doch vielversprechend aus der chart in us$ oder nicht ??
mein persöhnliches erstes kurziel lautet 8 us$ und dann 10 us$.
ist keine kaufempfehlung nur meine prognose
medarex75
sieht doch vielversprechend aus der chart in us$ oder nicht ??
mein persöhnliches erstes kurziel lautet 8 us$ und dann 10 us$.
ist keine kaufempfehlung nur meine prognose

medarex75
Da werden sicher die ASCO-Präsentationen zusammengefasst... oder ist mehr zu erwarten?
PRINCETON, N.J., May 26 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX) is scheduled to host a conference call and live webcast at 4:00 p.m. Eastern Time on Tuesday, June 2, 2009. Geoffrey M. Nichol, M.B.Ch.B., Senior Vice President of Product Development at Medarex will provide an update and recent highlights from Medarex's pipeline.
The webcast of the live event and archive can be accessed through the Investor Relations section of Medarex's website at www.medarex.com. To access the call live, please dial 1-877-874-1567 (U.S./Canada) or 1-719-325-4768 (international).
An archived telephonic replay of the conference call will be available until midnight Eastern Time on June 9, 2009. Access numbers for this replay are 1-888-203-1112 (U.S./Canada) or 1-719-457-0820 (international); the replay passcode is 4826956.
PRINCETON, N.J., May 26 /PRNewswire-FirstCall/ -- Medarex, Inc. (Nasdaq: MEDX) is scheduled to host a conference call and live webcast at 4:00 p.m. Eastern Time on Tuesday, June 2, 2009. Geoffrey M. Nichol, M.B.Ch.B., Senior Vice President of Product Development at Medarex will provide an update and recent highlights from Medarex's pipeline.
The webcast of the live event and archive can be accessed through the Investor Relations section of Medarex's website at www.medarex.com. To access the call live, please dial 1-877-874-1567 (U.S./Canada) or 1-719-325-4768 (international).
An archived telephonic replay of the conference call will be available until midnight Eastern Time on June 9, 2009. Access numbers for this replay are 1-888-203-1112 (U.S./Canada) or 1-719-457-0820 (international); the replay passcode is 4826956.
Antwort auf Beitrag Nr.: 37.258.211 von SLGramann am 26.05.09 22:30:44Ne, mehr erwarte ich mir auch nicht. Die 24Monats Überlebensdaten werden zu ASCO releast, die sind noch spannend und bisher nicht bekannt. Die restlichen Abstracts sind bereits raus.
Nach ASCO wird wohl bis Ende 2009/Anfang 2010 nachrichtenmäßig wieder saure Gurken-Zeit. Allerdings könnte ein drehendes Sentiment zu ipi den kurs wieder an die Zweistelligkeit heranführen.
Nach ASCO wird wohl bis Ende 2009/Anfang 2010 nachrichtenmäßig wieder saure Gurken-Zeit. Allerdings könnte ein drehendes Sentiment zu ipi den kurs wieder an die Zweistelligkeit heranführen.
Antwort auf Beitrag Nr.: 37.258.947 von Ville7 am 27.05.09 07:26:24Ganz so saure Gurken-Zeit wirds dann wohl doch nicht sein. Die Stelara Zulassung in US verzögert sich um weitere 3 Monate (bis zu) 
Wenn ich's richtig verstanden hab, hat es mit der Lagerfähigkeit von Stelara zu tun. Es werden keine zusätzlichen klinischen Studien gebraucht (also doch hoffentlich eine nicht allzu schlimme Verzögerung ) Trotzdem
) Trotzdem 
lg - Lycos
*********************************************
LOS ANGELES, May 26 (Reuters) - U.S. regulators have extended for a second time their review of Johnson & Johnson's (JNJ.N) experimental psoriasis drug, named Stelara, the company said on Tuesday.
J&J said the deadline for a decision by the Food and Drug Administration was extended by three months and the agency has requested no additional clinical trials.
An FDA advisory committee last June recommended that the drug, also known as ustekinumab, be approved, but the agency said in December that would hold off on making a decision on the marketing application until it received certain risk-mitigation information.
J&J said it responded to that request in January.
"We remain focused on collaboration with the FDA and providing the necessary information to support the review and approval of Stelara for the treatment of adults with moderate to severe plaque psoriasis," Jay Siegel, J&J's chief biotechnology officer, said in a statement.
Psoriasis, a condition in which itchy red plaques accumulate on the surface of the skin, is caused by an overproduction of skin cells. It affects an estimated 7.5 million patients in the United States, J&J said.
Ustekinumab, a monoclonal antibody which was highly effective in treating psoriasis in clinical trials, is given by infrequent injections and works by taming two immune system proteins called interleukin-12 (IL-12) and interleukin-23 (IL-23) that are linked to inflammation.
It was well tolerated in two large trials, with generally mild side effects that did not require adjustments in the medicine.
By contrast, current treatments -- including Wyeth's (WYE.N) leading injectable Enbrel, Abbott Laboratories' (ABT.N) injectable Humira and J&J's older Remicade medicine that is given by intravenous infusion -- can increase risk of infection and reactivate tuberculosis. (Reporting by Deena Beasley; Editing by Tim Dobbyn)

Wenn ich's richtig verstanden hab, hat es mit der Lagerfähigkeit von Stelara zu tun. Es werden keine zusätzlichen klinischen Studien gebraucht (also doch hoffentlich eine nicht allzu schlimme Verzögerung
 ) Trotzdem
) Trotzdem 
lg - Lycos
*********************************************
LOS ANGELES, May 26 (Reuters) - U.S. regulators have extended for a second time their review of Johnson & Johnson's (JNJ.N) experimental psoriasis drug, named Stelara, the company said on Tuesday.
J&J said the deadline for a decision by the Food and Drug Administration was extended by three months and the agency has requested no additional clinical trials.
An FDA advisory committee last June recommended that the drug, also known as ustekinumab, be approved, but the agency said in December that would hold off on making a decision on the marketing application until it received certain risk-mitigation information.
J&J said it responded to that request in January.
"We remain focused on collaboration with the FDA and providing the necessary information to support the review and approval of Stelara for the treatment of adults with moderate to severe plaque psoriasis," Jay Siegel, J&J's chief biotechnology officer, said in a statement.
Psoriasis, a condition in which itchy red plaques accumulate on the surface of the skin, is caused by an overproduction of skin cells. It affects an estimated 7.5 million patients in the United States, J&J said.
Ustekinumab, a monoclonal antibody which was highly effective in treating psoriasis in clinical trials, is given by infrequent injections and works by taming two immune system proteins called interleukin-12 (IL-12) and interleukin-23 (IL-23) that are linked to inflammation.
It was well tolerated in two large trials, with generally mild side effects that did not require adjustments in the medicine.
By contrast, current treatments -- including Wyeth's (WYE.N) leading injectable Enbrel, Abbott Laboratories' (ABT.N) injectable Humira and J&J's older Remicade medicine that is given by intravenous infusion -- can increase risk of infection and reactivate tuberculosis. (Reporting by Deena Beasley; Editing by Tim Dobbyn)
Antwort auf Beitrag Nr.: 37.259.035 von Lycos2 am 27.05.09 07:56:21
Schade. Es war ja mal von Ende August für eine Zulassungsentscheidung die Rede (wurde hier im Thread gepostet). Sind wir jetzt bei Ende November oder drei Monate ab jetzt? Dann wärs wieder oder noch August...
Schade. Es war ja mal von Ende August für eine Zulassungsentscheidung die Rede (wurde hier im Thread gepostet). Sind wir jetzt bei Ende November oder drei Monate ab jetzt? Dann wärs wieder oder noch August...
PRINCETON, N.J., May 27 /PRNewswire-FirstCall/ -- Medarex, Inc. (NASDAQ: MEDX) announced today the allowance of an investigational new drug application (IND) filed with the U.S. Food & Drug Administration (FDA) for MDX-1338, for the treatment of patients with acute myelogenous leukemia (AML). MDX-1338 is a fully human antibody that targets CXCR4, a chemokine receptor found on the surface of many cancer cells, including certain leukemias, lymphomas and other cancers. Preclinical laboratory experiments have shown that MDX-1338 can block the growth of, and even directly kill, selected human tumor cells.
The Phase 1, open-label, multicenter, dose-escalation study of MDX-1338 as a monotherapy and in combination with chemotherapy is expected to enroll up to 34 patients with relapsed/ refractory AML. This trial is designed to establish and evaluate the safety, tolerability and maximum tolerated dose, as well as preliminary pharmacodynamics and efficacy of MDX-1338.
"We are pleased that MDX-1338 has progressed into the clinic, representing our eighth development candidate in oncology and further enhancing our focus on oncology/immunology therapeutic indications," said Howard H. Pien, Chairman and CEO of Medarex. "We believe that MDX-1338 could have potential activity in multiple cancers. Our first Phase 1 study will be conducted in AML and future studies are expected to target a variety of other leukemias and solid tumors and may involve monotherapy and combination therapy."
The American Cancer Society estimates that in 2008, approximately 13,290 patients in the United States will be diagnosed with AML
The Phase 1, open-label, multicenter, dose-escalation study of MDX-1338 as a monotherapy and in combination with chemotherapy is expected to enroll up to 34 patients with relapsed/ refractory AML. This trial is designed to establish and evaluate the safety, tolerability and maximum tolerated dose, as well as preliminary pharmacodynamics and efficacy of MDX-1338.
"We are pleased that MDX-1338 has progressed into the clinic, representing our eighth development candidate in oncology and further enhancing our focus on oncology/immunology therapeutic indications," said Howard H. Pien, Chairman and CEO of Medarex. "We believe that MDX-1338 could have potential activity in multiple cancers. Our first Phase 1 study will be conducted in AML and future studies are expected to target a variety of other leukemias and solid tumors and may involve monotherapy and combination therapy."
The American Cancer Society estimates that in 2008, approximately 13,290 patients in the United States will be diagnosed with AML
Antwort auf Beitrag Nr.: 37.265.119 von SLGramann am 27.05.09 18:23:27
Bin mal gespannt, wie die Experten das Programm bewerten werden. Auf jeden Fall tut sich was in der Pipeline-Entwicklung.
Bin mal gespannt, wie die Experten das Programm bewerten werden. Auf jeden Fall tut sich was in der Pipeline-Entwicklung.
Antwort auf Beitrag Nr.: 37.265.216 von SLGramann am 27.05.09 18:31:10MEDX hat gestern zwischenzeitlich ordentlich zugelegt. Leider gegen Ende wieder den Großteil abgegeben 
Zu Stelara. Wenn ich mich recht erinnere, wurde mal vermutet dass die Zulassung im Juli hätten folgen sollen (nach Ablauf der 6 Monate für die erste Verzögerung). Jetzt kommen nochmal bis zu 3 Monate (vermutlich ab jetzt ???) dazu. Dann wären wir im August. Erhofft wurde die Zulassung bei Antrag für 12/08. Man merkt wie zäh diese Verfahren sein können
Find ich sehr erfreulich, dass die Pipline weiter wächst. Schön wär's natürlich, wenn das den Kurs mal nachhaltig antreibt

Zu Stelara. Wenn ich mich recht erinnere, wurde mal vermutet dass die Zulassung im Juli hätten folgen sollen (nach Ablauf der 6 Monate für die erste Verzögerung). Jetzt kommen nochmal bis zu 3 Monate (vermutlich ab jetzt ???) dazu. Dann wären wir im August. Erhofft wurde die Zulassung bei Antrag für 12/08. Man merkt wie zäh diese Verfahren sein können

Find ich sehr erfreulich, dass die Pipline weiter wächst. Schön wär's natürlich, wenn das den Kurs mal nachhaltig antreibt

Heute ODAC Meeting zu Ofatumumab von Medarex's ehemaligem "Spinoff" Genmab (woran sie nur noch 5% halten).
Im Vorfeld hatte sich die FDA kritisch zur BLA relevanten Ofatumumabstudie geäußert, daher vorgestern Kursabsturz bei Genmab, der sich gestern wieder etwas erholte.
Heute zählts dann was die ODAC-Experten sagen. Ich drücke die Daumen für Genmab (obwohl ich aktuell keine Aktien von der Firma besitze).
Im Vorfeld hatte sich die FDA kritisch zur BLA relevanten Ofatumumabstudie geäußert, daher vorgestern Kursabsturz bei Genmab, der sich gestern wieder etwas erholte.
Heute zählts dann was die ODAC-Experten sagen. Ich drücke die Daumen für Genmab (obwohl ich aktuell keine Aktien von der Firma besitze).
Antwort auf Beitrag Nr.: 37.268.551 von Lycos2 am 28.05.09 07:51:26Gibts einen Zusammenhang zwischen Pipeline und Kursen? 
Das ist heutzutage nur noch rudimentär korreliert.

EPS zählt oder Übernahme, der Rest ist den meisten zu kompliziert.

Das ist heutzutage nur noch rudimentär korreliert.


EPS zählt oder Übernahme, der Rest ist den meisten zu kompliziert.
Es gibt neue Daten zu Ipi...
http://finance.yahoo.com/news/Results-from-Three-Phase-2-bw-…
Ich denke, die Daten sind so vielversprechend, daß man noch heute Aktien kaufen sollte
http://finance.yahoo.com/news/Results-from-Three-Phase-2-bw-…
Ich denke, die Daten sind so vielversprechend, daß man noch heute Aktien kaufen sollte

Antwort auf Beitrag Nr.: 37.291.369 von Ennox am 31.05.09 17:57:14
Feuerstein siehts jetzt auch etwas optimistischer:
...Medarex has not yet successfully developed a drug on its own, and the biggest disappointment to date has been ipilimumab, a drug for skin cancer, which posted disappointing results from three pivotal trials in late 2007.
The failure of those three studies, coupled with the failure of a similar skin cancer drug being developed by Pfizer(PFE Quote), put ipilimumab in Wall Street's penalty box. Both Medarex and its partner Bristol-Myers Squibb(BMY Quote) insisted that ipilimumab wasn't done, but investors have been skeptical.
Perhaps perseverance is paying off. Medarex and Bristol-Myers continued to follow the patients treated with ipilimumab in those studies, and the results after two years show that between 30% and 42% of these skin cancer patients are still alive, according to data presented Sunday at the ASCO meeting.
Now, there were no control patients in any of these studies to make appropriate survival comparisons, but Medarex says that a search of the old melanoma studies covering about 2,000 patients shows that similar patients typically have about a 25% survival rate at one year.
For Medarex, this is encouraging news on ipilumumab and a big reason to look forward to later this year, when results are expected from another phase III study of ipilummab -- this one prospectively designed to assess the drug's ability to prolong survival in patients with newly treated melanoma.
http://www.thestreet.com/story/10507476/4/biotech-orphans-se…
Feuerstein siehts jetzt auch etwas optimistischer:
...Medarex has not yet successfully developed a drug on its own, and the biggest disappointment to date has been ipilimumab, a drug for skin cancer, which posted disappointing results from three pivotal trials in late 2007.
The failure of those three studies, coupled with the failure of a similar skin cancer drug being developed by Pfizer(PFE Quote), put ipilimumab in Wall Street's penalty box. Both Medarex and its partner Bristol-Myers Squibb(BMY Quote) insisted that ipilimumab wasn't done, but investors have been skeptical.
Perhaps perseverance is paying off. Medarex and Bristol-Myers continued to follow the patients treated with ipilimumab in those studies, and the results after two years show that between 30% and 42% of these skin cancer patients are still alive, according to data presented Sunday at the ASCO meeting.
Now, there were no control patients in any of these studies to make appropriate survival comparisons, but Medarex says that a search of the old melanoma studies covering about 2,000 patients shows that similar patients typically have about a 25% survival rate at one year.
For Medarex, this is encouraging news on ipilumumab and a big reason to look forward to later this year, when results are expected from another phase III study of ipilummab -- this one prospectively designed to assess the drug's ability to prolong survival in patients with newly treated melanoma.
http://www.thestreet.com/story/10507476/4/biotech-orphans-se…
Erstaunlicherweise bewegt sich der Kurs heute so gut wie gar nicht, vermutlich müssen die Amis erst aktiv werden, oder wir haben das übliche Szenario, daß MEDX bei guten News fällt.
Wenn ich das richtig sehe, dann beziehen sich die von Feuerstein zitierten 25% auf einen Zeitraum von 1 Jahr. Medarex hat Daten über 2 Jahre und wenn man die mit Dacarbazine über 2 Jahre vergleicht (8-12%), dann stellt man eine Verdopplung fest.
"Results from three separately published randomized Phase 3 studies using dacarbazine as the control arm reported that, at two years, approximately 8 to 12 percent of metastatic melanoma patients were alive."
"Results from three separately published randomized Phase 3 studies using dacarbazine as the control arm reported that, at two years, approximately 8 to 12 percent of metastatic melanoma patients were alive."
Antwort auf Beitrag Nr.: 37.293.753 von Ennox am 01.06.09 10:46:21
Das hängt sicher von den Erwartungswerten ab. Gute 2-Jahres-Daten waren wohl schon eingepreist.
Jedenfalls hat Ville hier im April zu diesem Thema folgendes geschrieben:
Den upgedateten Überlebensdaten messe ich nicht die Bedeutung bei. Sie werden einen weiter positiven Verlauf aufzeigen und allerhöchstens die Zuversicht in den Ansatz steigern. Kursmässig erwarte ich mir aber nichts davon - ausserhalb dessen, dass Biotechs allgemein zu ASCO steigen.
Das hängt sicher von den Erwartungswerten ab. Gute 2-Jahres-Daten waren wohl schon eingepreist.
Jedenfalls hat Ville hier im April zu diesem Thema folgendes geschrieben:
Den upgedateten Überlebensdaten messe ich nicht die Bedeutung bei. Sie werden einen weiter positiven Verlauf aufzeigen und allerhöchstens die Zuversicht in den Ansatz steigern. Kursmässig erwarte ich mir aber nichts davon - ausserhalb dessen, dass Biotechs allgemein zu ASCO steigen.
Antwort auf Beitrag Nr.: 37.294.511 von SLGramann am 01.06.09 12:25:0601.06.2009 14:10
Medarex Announces Efficacy Data in Cancer Patients Treated with Investigational Anti-PD-1 Antibody at American Society of Clinical Oncology Annual Meeting
-Phase 1 Single-Dose and Phase 1b Multi-Dose Data Presented-
Medarex, Inc. (NASDAQ: MEDX) today announced anti-tumor activity and efficacy data for MDX-1106 (also known as ONO-4538), a fully human anti-PD-1 antibody that Medarex is co-developing with Ono Pharmaceutical Co. Ltd. for the treatment of recurrent or treatment-refractory cancers, including malignant melanoma, renal cell carcinoma, colorectal carcinoma, non-small cell lung cancer, and castrate resistant prostate carcinoma. Results presented at the annual meeting of the American Society of Clinical Oncology (ASCO) showed:
•Durable anti-tumor activity in patients treated with intermittent 10 mg/kg dosing of MDX-1106 in the 21-patient expansion cohort from the Phase 1 trial, including one patient with renal cell cancer experiencing an ongoing objective partial response of over 9 months and one patient with melanoma experiencing ongoing stable disease with marked clinical improvement for over 19 months and 9 doses of MDX-1106. One patient with colorectal carcinoma treated with five doses at the earlier 3 mg/kg cohort has also maintained a partial response for over 20 months;
•All patients showing clinical benefit with MDX-1106 had previously progressed after prior chemotherapies;
•None of the patients treated at 10 mg/kg have developed any significant drug-related adverse events. MDX-1106 appeared to be well-tolerated at the 10 mg/kg dose, including those patients in the cohort eligible to receive between two and nine doses of 10mg/kg MDX-1106; and
•No dose-limiting toxicities have been reached.
These data focused on the experience of an expansion cohort of 21 patients dosed at 10 mg/kg of MDX-1106 from the single-dose Phase 1 trial and were presented by investigator Julie Brahmer, M.D., Assistant Professor of Oncology from the Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins University (Abstract #3018). The complete study was designed to examine the safety, tolerability and pharmacokinetic profile of single-dose MDX-1106 (0.3, 1, 3 or 10 mg/kg) in patients with recurrent or treatment-refractory cancers. However, per protocol, patients demonstrating clinical benefit could receive additional intermittent doses (up to nine doses of 10 mg/kg MDX-1106) until an objective response was obtained. In addition to the durable responses outlined above, lesional regressions were observed in two additional patients, including one with non-small cell lung cancer, and one with melanoma. Enrollment in the single-dose Phase 1 trial is complete with 39 patients.
Also presented were preliminary data from an ongoing multi-dose, dose escalating Phase 1b monotherapy study of MDX-1106. One patient with melanoma in the first treatment cohort of 4 patients has demonstrated marked tumor regression of liver and lung lesions after receiving four doses of 1 mg/kg of MDX-1106. The tumors have continued to shrink after additional cycles of four doses, and the patient continues to tolerate the treatment without adverse events. Additional anti-tumor activity has been observed with lung lesion regression in a patient with renal cell cancer. Subsequently observed in the second dose level cohort, one patient with non-small cell lung cancer has demonstrated regression of a solitary adrenal metastasis after the first 4 doses of 3 mg/kg of MDX-1106. The trial is designed to examine the safety and activity in patients treated with multiple doses of MDX-1106 (1, 3 and 10 mg/kg) administered every two weeks until a confirmed complete response, clear progression or serious adverse event emerges. This multi-center, open label study is expected to enroll up to 76 patients in the United States.
”We are encouraged by both the safety profile and the initial anti-tumor activity that included durable responses in several cancer indications for patients treated intermittently with MDX-1106 up to the 10 mg/kg dose. We are also pleased by our ongoing Phase 1b study of repeated doses of the antibody which has also shown early evidence of activity at a repeated dose of 1 or 3 mg/kg,” said Geoffrey M. Nichol, MBChB, Senior Vice President of Product Development at Medarex. ”While we are still in early stages of development, it is also exciting that these treatments continue to be generally well tolerated.”
About MDX-1106/ONO-4538
MDX-1106/ONO-4538 is a novel fully human antibody designed to target and inhibit the function of PD-1 (programmed cell death 1), a receptor expressed on the surface of activated lymphocytes (T-cells). The binding of PD-1 with one of two ligands (PD-L1 or PD-L2) is an important negative regulation pathway that suppresses or inhibits activated lymphocytes. Recent research has noted increased PD-1 expression levels on antigen specific T-cells in both the oncology and chronic infectious disease settings, as well as a strong correlation between increased PD-L1 expression on tumors and a negative survival prognosis in cancer patients. Preclinical studies indicate that antibodies targeting the PD-1 signaling pathway reinvigorate antigen-specific T-cell responses and promote an immune response to fight tumors and infectious diseases.
MDX-1106/ONO-4538 is being investigated in both the oncology and infectious disease settings. In addition to the Phase 1b study in cancer, a Phase 1 trial is ongoing for the treatment of hepatitis C. In September 2008, Ono initiated a single and multi-dose Phase 1 clinical study in patients with advanced solid malignancies in Japan. MDX-1106/ONO-4538 may also have the potential to be used synergistically in combination with other treatment modalities, including with anti-CTLA-4 blockade.
In May 2005, Ono entered into a collaboration agreement with Medarex to research and develop a fully human anti-PD-1 antibody for the treatment of cancer. The two companies plan to share the costs and responsibilities of research and product development up to the completion of a Phase 2 clinical study in each party’s territory. Thereafter, each company will be fully responsible for any continued development and any commercialization in its exclusive territory; Medarex’s exclusive territory is North America, and Ono’s exclusive territory is all areas outside of North America.
Medarex Announces Efficacy Data in Cancer Patients Treated with Investigational Anti-PD-1 Antibody at American Society of Clinical Oncology Annual Meeting
-Phase 1 Single-Dose and Phase 1b Multi-Dose Data Presented-
Medarex, Inc. (NASDAQ: MEDX) today announced anti-tumor activity and efficacy data for MDX-1106 (also known as ONO-4538), a fully human anti-PD-1 antibody that Medarex is co-developing with Ono Pharmaceutical Co. Ltd. for the treatment of recurrent or treatment-refractory cancers, including malignant melanoma, renal cell carcinoma, colorectal carcinoma, non-small cell lung cancer, and castrate resistant prostate carcinoma. Results presented at the annual meeting of the American Society of Clinical Oncology (ASCO) showed:
•Durable anti-tumor activity in patients treated with intermittent 10 mg/kg dosing of MDX-1106 in the 21-patient expansion cohort from the Phase 1 trial, including one patient with renal cell cancer experiencing an ongoing objective partial response of over 9 months and one patient with melanoma experiencing ongoing stable disease with marked clinical improvement for over 19 months and 9 doses of MDX-1106. One patient with colorectal carcinoma treated with five doses at the earlier 3 mg/kg cohort has also maintained a partial response for over 20 months;
•All patients showing clinical benefit with MDX-1106 had previously progressed after prior chemotherapies;
•None of the patients treated at 10 mg/kg have developed any significant drug-related adverse events. MDX-1106 appeared to be well-tolerated at the 10 mg/kg dose, including those patients in the cohort eligible to receive between two and nine doses of 10mg/kg MDX-1106; and
•No dose-limiting toxicities have been reached.
These data focused on the experience of an expansion cohort of 21 patients dosed at 10 mg/kg of MDX-1106 from the single-dose Phase 1 trial and were presented by investigator Julie Brahmer, M.D., Assistant Professor of Oncology from the Sidney Kimmel Comprehensive Cancer Center at Johns Hopkins University (Abstract #3018). The complete study was designed to examine the safety, tolerability and pharmacokinetic profile of single-dose MDX-1106 (0.3, 1, 3 or 10 mg/kg) in patients with recurrent or treatment-refractory cancers. However, per protocol, patients demonstrating clinical benefit could receive additional intermittent doses (up to nine doses of 10 mg/kg MDX-1106) until an objective response was obtained. In addition to the durable responses outlined above, lesional regressions were observed in two additional patients, including one with non-small cell lung cancer, and one with melanoma. Enrollment in the single-dose Phase 1 trial is complete with 39 patients.
Also presented were preliminary data from an ongoing multi-dose, dose escalating Phase 1b monotherapy study of MDX-1106. One patient with melanoma in the first treatment cohort of 4 patients has demonstrated marked tumor regression of liver and lung lesions after receiving four doses of 1 mg/kg of MDX-1106. The tumors have continued to shrink after additional cycles of four doses, and the patient continues to tolerate the treatment without adverse events. Additional anti-tumor activity has been observed with lung lesion regression in a patient with renal cell cancer. Subsequently observed in the second dose level cohort, one patient with non-small cell lung cancer has demonstrated regression of a solitary adrenal metastasis after the first 4 doses of 3 mg/kg of MDX-1106. The trial is designed to examine the safety and activity in patients treated with multiple doses of MDX-1106 (1, 3 and 10 mg/kg) administered every two weeks until a confirmed complete response, clear progression or serious adverse event emerges. This multi-center, open label study is expected to enroll up to 76 patients in the United States.
”We are encouraged by both the safety profile and the initial anti-tumor activity that included durable responses in several cancer indications for patients treated intermittently with MDX-1106 up to the 10 mg/kg dose. We are also pleased by our ongoing Phase 1b study of repeated doses of the antibody which has also shown early evidence of activity at a repeated dose of 1 or 3 mg/kg,” said Geoffrey M. Nichol, MBChB, Senior Vice President of Product Development at Medarex. ”While we are still in early stages of development, it is also exciting that these treatments continue to be generally well tolerated.”
About MDX-1106/ONO-4538
MDX-1106/ONO-4538 is a novel fully human antibody designed to target and inhibit the function of PD-1 (programmed cell death 1), a receptor expressed on the surface of activated lymphocytes (T-cells). The binding of PD-1 with one of two ligands (PD-L1 or PD-L2) is an important negative regulation pathway that suppresses or inhibits activated lymphocytes. Recent research has noted increased PD-1 expression levels on antigen specific T-cells in both the oncology and chronic infectious disease settings, as well as a strong correlation between increased PD-L1 expression on tumors and a negative survival prognosis in cancer patients. Preclinical studies indicate that antibodies targeting the PD-1 signaling pathway reinvigorate antigen-specific T-cell responses and promote an immune response to fight tumors and infectious diseases.
MDX-1106/ONO-4538 is being investigated in both the oncology and infectious disease settings. In addition to the Phase 1b study in cancer, a Phase 1 trial is ongoing for the treatment of hepatitis C. In September 2008, Ono initiated a single and multi-dose Phase 1 clinical study in patients with advanced solid malignancies in Japan. MDX-1106/ONO-4538 may also have the potential to be used synergistically in combination with other treatment modalities, including with anti-CTLA-4 blockade.
In May 2005, Ono entered into a collaboration agreement with Medarex to research and develop a fully human anti-PD-1 antibody for the treatment of cancer. The two companies plan to share the costs and responsibilities of research and product development up to the completion of a Phase 2 clinical study in each party’s territory. Thereafter, each company will be fully responsible for any continued development and any commercialization in its exclusive territory; Medarex’s exclusive territory is North America, and Ono’s exclusive territory is all areas outside of North America.
@Ville: Im Yahoo MSG Board hast du glaub ich was Positives zu ACZ885 berichtet. Wärst du so nett und könntest du das hier kurz zusammenfassen?
Was sagst du zu den auf der ASCO präsentierten Ipi Daten?
Nächste richtig positive News wird dann wohl (hoffentlich) die Zulassung von Stelara in US sein. Aber da heißts weiterhin etwas Geduld haben
lg - Lycos
Was sagst du zu den auf der ASCO präsentierten Ipi Daten?
Nächste richtig positive News wird dann wohl (hoffentlich) die Zulassung von Stelara in US sein. Aber da heißts weiterhin etwas Geduld haben

lg - Lycos
Antwort auf Beitrag Nr.: 37.321.851 von Lycos2 am 04.06.09 18:18:10Ich hatte einen Artikel aus dem WSJ gepostet. Novartis hat in einer sehr seltenen Indikation (CAPS) super Ergebnisse erzielt. Es wird dann das Ziel von Novartis angesprochen, den Antikörper ACZ885, Name Ilaris, in kommerziell aussichtsreiche Indikationen weiterzuentwicklen: z.b. Gicht, Rheumatoide Arthritis, Typ2 Diabetes. (Übrigens: Zulassungsentscheidung USA und Europa steht dieses Jahr noch an, allerspätestens Anfang nächstes Jahr).
------------------
Novartis Drug Ilaris Works In CAPS, Exploring Wider Use
ZURICH (Dow Jones)--Novartis AG (NVS) Wednesday said a new experimental drug to treat a rare auto-inflammatory disease helped to alleviate symptoms within hours of treatment, encouraging the Swiss drugmaker to investigate its potential in similar, more widely-spread diseases.
Novartis, based in Basel, said its new biological drug Ilaris produced rapid and sustained remission of symptoms in the majority of children and adults with a rare auto-inflammatory disease called cryopyrin-associated periodic syndrome, or CAPS. CAPS affects around 1 person in a million.
Novartis has filed the drug for regulatory approval in the U.S., the European Union, Switzerland and Australia.
The 48-weeks study involved 35 patients aged nine to 74 years old. Out of 31 patients who entered the third and last part of the trial, 28 completed it without suffering a relapse.
Symptoms of CAPS include debilitating fatigue, fever and chronic anemia from infancy. Complications of the disease range from hearing loss, visual and intellectual to renal failure.
"In the study, patients experienced a benefit within hours after receiving a single dose [of Ilaris] and only needed further treatment every two months to control their symptoms," said Helen Lachmann, author of the study and a medical doctor of the U.K. National Amyloidosis Centre at the Royal Free and University College Medical School in London. "They were essentially cured," she added in a telephone interview with Dow Jones Newswires.
Ilaris is a fully human monoclonal antibody, which neutralized a protein known as interleukin 1-beta that has a pivotal role in driving inflammation and tissue destruction.
To develop the drug as a treatment for more common auto-inflammatory disorders such as gout, rheumatoid arthritis or type 2 diabetes, scientists will first have to find out if they are caused by the same protein, Dr. Lachmann said.
Novartis intends to explore the drug's potential in treating similar diseases.
"We are extremely excited about the efficacy shown by Ilaris in patients with CAPS, and we hope to be able to extend these benefits to many more patients with other inflammatory diseases which are more widespread, and often equally debilitating," said Trevor Mundel, head of development at Novartis.
Detailed results of the study are being published Wednesday in The New England Journal of Medicine.
------------------
Novartis Drug Ilaris Works In CAPS, Exploring Wider Use
ZURICH (Dow Jones)--Novartis AG (NVS) Wednesday said a new experimental drug to treat a rare auto-inflammatory disease helped to alleviate symptoms within hours of treatment, encouraging the Swiss drugmaker to investigate its potential in similar, more widely-spread diseases.
Novartis, based in Basel, said its new biological drug Ilaris produced rapid and sustained remission of symptoms in the majority of children and adults with a rare auto-inflammatory disease called cryopyrin-associated periodic syndrome, or CAPS. CAPS affects around 1 person in a million.
Novartis has filed the drug for regulatory approval in the U.S., the European Union, Switzerland and Australia.
The 48-weeks study involved 35 patients aged nine to 74 years old. Out of 31 patients who entered the third and last part of the trial, 28 completed it without suffering a relapse.
Symptoms of CAPS include debilitating fatigue, fever and chronic anemia from infancy. Complications of the disease range from hearing loss, visual and intellectual to renal failure.
"In the study, patients experienced a benefit within hours after receiving a single dose [of Ilaris] and only needed further treatment every two months to control their symptoms," said Helen Lachmann, author of the study and a medical doctor of the U.K. National Amyloidosis Centre at the Royal Free and University College Medical School in London. "They were essentially cured," she added in a telephone interview with Dow Jones Newswires.
Ilaris is a fully human monoclonal antibody, which neutralized a protein known as interleukin 1-beta that has a pivotal role in driving inflammation and tissue destruction.
To develop the drug as a treatment for more common auto-inflammatory disorders such as gout, rheumatoid arthritis or type 2 diabetes, scientists will first have to find out if they are caused by the same protein, Dr. Lachmann said.
Novartis intends to explore the drug's potential in treating similar diseases.
"We are extremely excited about the efficacy shown by Ilaris in patients with CAPS, and we hope to be able to extend these benefits to many more patients with other inflammatory diseases which are more widespread, and often equally debilitating," said Trevor Mundel, head of development at Novartis.
Detailed results of the study are being published Wednesday in The New England Journal of Medicine.
Antwort auf Beitrag Nr.: 37.321.851 von Lycos2 am 04.06.09 18:18:10Auch die 24 Monats ipi Daten sind sehr gut.
Allerdings bitte bedenken, dass die Daten gegen historisches DTIC antreten und dieser Wert durch neue Behandlungsergänzungen inzwischen besser sein kann. Zudem, dass die Trials unkontrolliert waren und die Aussagekraft daher begrenzt ist. Ausserdem wurden Abbrecher nicht in der Statistik inkludiert - aber selbst wenn man diese als sofort gestorben reinrechnet sind die Werte noch weit besser als die fiktive Kontrollgruppe (historisches DTIC). Ändert an der grundsätzlich positiven Meldung aber wenig.
Einzig entscheidend werden die ipi/DTIC Daten in (wahrscheinlich) Q1 2010 sein.
Allerdings bitte bedenken, dass die Daten gegen historisches DTIC antreten und dieser Wert durch neue Behandlungsergänzungen inzwischen besser sein kann. Zudem, dass die Trials unkontrolliert waren und die Aussagekraft daher begrenzt ist. Ausserdem wurden Abbrecher nicht in der Statistik inkludiert - aber selbst wenn man diese als sofort gestorben reinrechnet sind die Werte noch weit besser als die fiktive Kontrollgruppe (historisches DTIC). Ändert an der grundsätzlich positiven Meldung aber wenig.
Einzig entscheidend werden die ipi/DTIC Daten in (wahrscheinlich) Q1 2010 sein.
Antwort auf Beitrag Nr.: 37.329.641 von Ville7 am 05.06.09 15:14:32vielen Dank für deine Erklärungen/Einschätzungen
lG Lycos
lG Lycos
FDA erteilt Zulassung für Ilaris® (canakinumab) Indikation Cryopyrin-associated periodic syndrome (CAPS)
http://www.novartis.com/newsroom/media-releases/en/2009/1323…
.....
Ilaris, previously known as ACZ885, is a fully human monoclonal antibody that rapidly and selectively blocks IL-1ß[1],[3],[4],[7]. The dosing schedule for Ilaris is once every eight weeks, which is less frequent than the current approved therapy[2],[8]. Also, more than 90% of patients studied did not experience any injection site reactions and those that did occur were of a mild-to-moderate nature[1],[2].....
...
Ok. Zugegeben, die Royalities von Novartis für Ilaris CAPS werden sich schwer in Grenzen halten (eine Meilensteinzahlung dürfte auch fällig sein). Aber trotzdem toller Erfolg und Bestätigung, dass MEDX auch neben IPI was Zustande bringt.
http://www.novartis.com/newsroom/media-releases/en/2009/1323…
.....
Ilaris, previously known as ACZ885, is a fully human monoclonal antibody that rapidly and selectively blocks IL-1ß[1],[3],[4],[7]. The dosing schedule for Ilaris is once every eight weeks, which is less frequent than the current approved therapy[2],[8]. Also, more than 90% of patients studied did not experience any injection site reactions and those that did occur were of a mild-to-moderate nature[1],[2].....
...
Ok. Zugegeben, die Royalities von Novartis für Ilaris CAPS werden sich schwer in Grenzen halten (eine Meilensteinzahlung dürfte auch fällig sein). Aber trotzdem toller Erfolg und Bestätigung, dass MEDX auch neben IPI was Zustande bringt.

So der Vollständigkeit halber - als Dokumentation.
Schöne Erfolgsgeschichte und wie ich finde tolle Nachricht (inkl. PR für MEDX).
************************************************
Link zum Artikel der Mayo Klinik
http://discoverysedge.mayo.edu/de09-2-kwonblute/
Link zum Artikel des Telegraph
http://www.telegraph.co.uk/health/men_shealth/5578222/Drug-c…
PR von Medarex
Mayo Clinic Researchers Highlight Prostate Cancer Study with Ipilimumab
The Mayo Clinic issued a press release today on a prostate cancer study with
ipilimumab, a fully human antibody that binds to CTLA-4 ( cytotoxic T lymphocyte-associated
antigen 4) , a molecule on T-cells that plays a critical role in regulating natural
immune responses. The associated press release entitled "Mayo Researchers: Dramatic
Outcomes in Prostate Cancer Study" reported on the following data:
Two Mayo Clinic patients whose prostate cancer had been considered inoperable have
no evidence of disease thanks in part to an experimental drug therapy that was used in
combination with standardized hormone treatment and radiation therapy. The men were
participating in an investigator sponsored clinical trial of ipilimumab. In these two
cases, physicians say the approach initiated the death of a majority of cancer cells and
caused extensive tumor shrinkage, allowing surgery. In both cases, the aggressive
tumors had grown well beyond the prostate into the abdominal areas.
The patients first received a type of hormone therapy called androgen ablation,
which removes testosterone and usually causes some initial reduction in tumor size.
Researchers then introduced a single dose of ipilimumab, an antibody, which builds on the
anti-tumor action of the hormone and causes a much larger immune response, resulting in
massive death of the tumor cells. Both men experienced consistent drops in their
prostate specific antigen (PSA) counts over the following weeks until both were deemed
eligible for surgery. Then, during surgery, extensive tumor shrinkage was observed. One
patient underwent radiation therapy after surgery; both have resumed their regular
lives.
The research was supported by the Department of Defense, The Richard M. Schulze
Family Foundation, the Mayo Clinic Cancer Center and the Mayo Clinic Center for
Translational Science Activities. Medarex, Inc. provided the study drug free of charge and
supported safety monitoring during the protocol.
Schöne Erfolgsgeschichte und wie ich finde tolle Nachricht (inkl. PR für MEDX).
************************************************
Link zum Artikel der Mayo Klinik
http://discoverysedge.mayo.edu/de09-2-kwonblute/
Link zum Artikel des Telegraph
http://www.telegraph.co.uk/health/men_shealth/5578222/Drug-c…
PR von Medarex
Mayo Clinic Researchers Highlight Prostate Cancer Study with Ipilimumab
The Mayo Clinic issued a press release today on a prostate cancer study with
ipilimumab, a fully human antibody that binds to CTLA-4 ( cytotoxic T lymphocyte-associated
antigen 4) , a molecule on T-cells that plays a critical role in regulating natural
immune responses. The associated press release entitled "Mayo Researchers: Dramatic
Outcomes in Prostate Cancer Study" reported on the following data:
Two Mayo Clinic patients whose prostate cancer had been considered inoperable have
no evidence of disease thanks in part to an experimental drug therapy that was used in
combination with standardized hormone treatment and radiation therapy. The men were
participating in an investigator sponsored clinical trial of ipilimumab. In these two
cases, physicians say the approach initiated the death of a majority of cancer cells and
caused extensive tumor shrinkage, allowing surgery. In both cases, the aggressive
tumors had grown well beyond the prostate into the abdominal areas.
The patients first received a type of hormone therapy called androgen ablation,
which removes testosterone and usually causes some initial reduction in tumor size.
Researchers then introduced a single dose of ipilimumab, an antibody, which builds on the
anti-tumor action of the hormone and causes a much larger immune response, resulting in
massive death of the tumor cells. Both men experienced consistent drops in their
prostate specific antigen (PSA) counts over the following weeks until both were deemed
eligible for surgery. Then, during surgery, extensive tumor shrinkage was observed. One
patient underwent radiation therapy after surgery; both have resumed their regular
lives.
The research was supported by the Department of Defense, The Richard M. Schulze
Family Foundation, the Mayo Clinic Cancer Center and the Mayo Clinic Center for
Translational Science Activities. Medarex, Inc. provided the study drug free of charge and
supported safety monitoring during the protocol.
Antwort auf Beitrag Nr.: 37.433.483 von Lycos2 am 20.06.09 17:01:21Moin,

die Mayo-Geschichte geht ja rum wie ein Lauffeuer - sogar schon im Wikipedia-Eintrag:
Man darf gespannt auf Montag sein!
Gruß q.
Ipilimumab
From Wikipedia, the free encyclopedia
Jump to: navigation, search
Ipilimumab?
Therapeutic monoclonal antibody
Source Human
Target CTLA-4
Identifiers
CAS number 477202-00-9
ATC code none
PubChem ?
Chemical data
Formula C6742H9972N1732O2004S40
Mol. mass 148634.914 g/mol
Pharmacokinetic data
Bioavailability ?
Metabolism ?
Half life ?
Excretion ?
Therapeutic considerations
Pregnancy cat. ?
Legal status
Routes ?
Ipilimumab (also known as MDX-010 or MDX-101) is a human monoclonal antibody being developed by Bristol-Myers Squibb and Medarex. It is intended to be used as a drug to activate the immune system. Ipilimumab is undergoing clinical trials for the treatment of melanoma.[1]
Ipilimumab is a fully human antibody that binds to CTLA-4 (cytotoxic T lymphocyte-associated antigen 4), a molecule on T-cells that is believed to play a critical role in regulating natural immune responses. The absence or presence of CTLA-4 can augment or suppress the immune system's T-cell response in fighting disease. Ipilimumab is designed to block the activity of CTLA-4, thereby sustaining an active immune response in its attack on cancer cells.
As of October 2007 there are two fully human anti CTLA-4 [1] monoclonal antibodies in advanced clinical trials. Ipilimumab, which is an IgG1 isotype, and Tremelimumab (from Pfizer) which is an IgG2 isotype.
On December 10, 2007, Bristol-Myers Squibb and Medarex released the results of three studies on ipilimumab. One of the three studies failed to meet its primary goal of shrinking tumors in at least 10.0% of the study's 155 patients. The three studies tested 487 patients with advanced skin cancer. Side effects are often considered acceptable risks for cancer drugs given the severity of the disease, and ipilimumab is no exception. The medication caused rashes, diarrhea and hepatitis in a number of the patients being tested. Despite the weaker-than-anticipated results, the companies are still planning to meet with regulatory agencies to discuss moving ahead with the medication. They hope to submit a filing to the U.S. Food and Drug Administration seeking approval in the first half of 2008. Since patients suffering from extremely serious diseases like melanoma have so few treatment options, the companies believe that even the marginal success rate will be appealing to some.
As of September 2008, Medarex is performing a Phase I/II dose escalation clinical trial of ipilimumab in metastatic hormone-refractory prostate cancer (HRPC). As of 2009, some of the patients with advanced prostate cancer had their tumors drastically shrank, promoting further trials. [2]
On 19 June 2009 the Mayo Clinic reported two prostate cancer patients who had been told their condition was inoperable are now cancer-free as the result of a Phase II study using MDX-010 therapy. The study is headed by Dr. Eugene Kwon. [3]
[edit] References
^ ClinicalTrials.gov NCT00094653

die Mayo-Geschichte geht ja rum wie ein Lauffeuer - sogar schon im Wikipedia-Eintrag:
Man darf gespannt auf Montag sein!
Gruß q.
Ipilimumab
From Wikipedia, the free encyclopedia
Jump to: navigation, search
Ipilimumab?
Therapeutic monoclonal antibody
Source Human
Target CTLA-4
Identifiers
CAS number 477202-00-9
ATC code none
PubChem ?
Chemical data
Formula C6742H9972N1732O2004S40
Mol. mass 148634.914 g/mol
Pharmacokinetic data
Bioavailability ?
Metabolism ?
Half life ?
Excretion ?
Therapeutic considerations
Pregnancy cat. ?
Legal status
Routes ?
Ipilimumab (also known as MDX-010 or MDX-101) is a human monoclonal antibody being developed by Bristol-Myers Squibb and Medarex. It is intended to be used as a drug to activate the immune system. Ipilimumab is undergoing clinical trials for the treatment of melanoma.[1]
Ipilimumab is a fully human antibody that binds to CTLA-4 (cytotoxic T lymphocyte-associated antigen 4), a molecule on T-cells that is believed to play a critical role in regulating natural immune responses. The absence or presence of CTLA-4 can augment or suppress the immune system's T-cell response in fighting disease. Ipilimumab is designed to block the activity of CTLA-4, thereby sustaining an active immune response in its attack on cancer cells.
As of October 2007 there are two fully human anti CTLA-4 [1] monoclonal antibodies in advanced clinical trials. Ipilimumab, which is an IgG1 isotype, and Tremelimumab (from Pfizer) which is an IgG2 isotype.
On December 10, 2007, Bristol-Myers Squibb and Medarex released the results of three studies on ipilimumab. One of the three studies failed to meet its primary goal of shrinking tumors in at least 10.0% of the study's 155 patients. The three studies tested 487 patients with advanced skin cancer. Side effects are often considered acceptable risks for cancer drugs given the severity of the disease, and ipilimumab is no exception. The medication caused rashes, diarrhea and hepatitis in a number of the patients being tested. Despite the weaker-than-anticipated results, the companies are still planning to meet with regulatory agencies to discuss moving ahead with the medication. They hope to submit a filing to the U.S. Food and Drug Administration seeking approval in the first half of 2008. Since patients suffering from extremely serious diseases like melanoma have so few treatment options, the companies believe that even the marginal success rate will be appealing to some.
As of September 2008, Medarex is performing a Phase I/II dose escalation clinical trial of ipilimumab in metastatic hormone-refractory prostate cancer (HRPC). As of 2009, some of the patients with advanced prostate cancer had their tumors drastically shrank, promoting further trials. [2]
On 19 June 2009 the Mayo Clinic reported two prostate cancer patients who had been told their condition was inoperable are now cancer-free as the result of a Phase II study using MDX-010 therapy. The study is headed by Dr. Eugene Kwon. [3]
[edit] References
^ ClinicalTrials.gov NCT00094653
Moin,

wird tatsächlich spannend heute, vorbörslich schon über 9$ bei ernsthaften Umsätzen...
Sehr schön an so einem ansonsten etwas rotgefärbten Börsentag!
Gruß q.

wird tatsächlich spannend heute, vorbörslich schon über 9$ bei ernsthaften Umsätzen...
Sehr schön an so einem ansonsten etwas rotgefärbten Börsentag!
Gruß q.
+20%
das ist wie Balsam auf die Wunde. Bin jetzt nur noch ca. 30% im Minus
das ist wie Balsam auf die Wunde. Bin jetzt nur noch ca. 30% im Minus

Was soll man denn inhaltlich von dieser Meldung halten?
Ist ein Ergebnis bei zwei Patienten überhaupt relevant? Und ist es üblich, dass ein Unternehmen wie Medarex so etwas zu einer Pressemitteilung verarbeitet? Wer boshaft sein will, kann hier ja auch hineininterpretieren, dass Medarex schon mal den nächsten "Horizont der Hoffnung" aufbauen will - statt Melanom wird es nun eben Prostata-Krebs werden...
(Das war jetzt bewusst etwas provozierend formuliert. Ich freue mich sehr wohl darüber, dass Ipilimumab hier Wirkung gezeigt hat. Indes sind die Fragen durchaus ernst gemeint.)
Ist ein Ergebnis bei zwei Patienten überhaupt relevant? Und ist es üblich, dass ein Unternehmen wie Medarex so etwas zu einer Pressemitteilung verarbeitet? Wer boshaft sein will, kann hier ja auch hineininterpretieren, dass Medarex schon mal den nächsten "Horizont der Hoffnung" aufbauen will - statt Melanom wird es nun eben Prostata-Krebs werden...
(Das war jetzt bewusst etwas provozierend formuliert. Ich freue mich sehr wohl darüber, dass Ipilimumab hier Wirkung gezeigt hat. Indes sind die Fragen durchaus ernst gemeint.)
Antwort auf Beitrag Nr.: 37.441.610 von SLGramann am 22.06.09 15:57:07Das war nicht Medarex, das die PR rausgab, sondern die Mayo Klinik. Medarex' PM hat nur die PM der Mayo Klinik zitiert.
Ich verstehe den Hype heute auch nicht, denn die PM der Mayo Klinik war schon am Freitag zu Handelsminuten draussen. Wieso erst jetzt der Kurssprung?
Schaut eher nach Pump and Dump einer größeren Addresse aus.
Ich verstehe den Hype heute auch nicht, denn die PM der Mayo Klinik war schon am Freitag zu Handelsminuten draussen. Wieso erst jetzt der Kurssprung?
Schaut eher nach Pump and Dump einer größeren Addresse aus.

Weil AP sich so schön (und berechtigt?!) wundert, poste ich mal deren Meldung zu Thema:
Shares of Medarex jump on premature report of results in just 2 prostate cancer patients
* By Linda A. Johnson, AP Business Writer
* On Monday June 22, 2009, 2:48 pm EDT
TRENTON, N.J. (AP) -- Shares of drug developer Medarex Inc. jumped Monday after an unusual report that two men in a study of its experimental prostate cancer drug had their tumors shrink dramatically. The report gave no information on how other men in the study fared.
Shares of Princeton, N.J.-based Medarex opened at $8.88, just over 20 percent above their close at $7.36 on Friday. By early afternoon, they were up $1.15, or 15.6 percent, at $8.51, while the broader markets were all down.
The jump followed a press release issued by the Mayo Clinic of Rochester, Minn., which is co-sponsoring a study of a genetically engineered, antibody-based Medarex drug, called ipilimumab, to treat prostate cancer.
The release states that two patients who had what was considered inoperable prostate cancer that had spread to other areas now "have no evidence of disease." The release credits the combination of ipilimumab with standard hormone treatment and radiation therapy.
The press release gave no information about how many people are participating in the trial, whether the other patients were improving or getting worse, how long they had survived or whether the study is an early, midstage or late-stage trial. Also, the two men still had to undergo surgery to remove the remaining tumors.
Results from just two patients must be interpreted very cautiously. Researchers normally do not release data until a study has been completed and all the data thoroughly analyzed and vetted for presentation in a medical journal or at a medical conference. In addition, studies typically compare patients getting a new treatment with a second group getting a standard treatment or a placebo, but the press release gave no information about this study's design.
Ipilimumab targets CTLA-4, short for cytotoxic T lymphocyte-associated antigen 4. CTLA-4 is a molecule on immune cells called T-cells that plays an important role in regulating the body's natural immune defenses.
Medarex, which is supporting the study, trumpeted the brief press release on its Web site Monday, but has posted no recent information on other test results of the drug for prostate cancer.
Sehr, sehr skeptisch... was ja vielleicht nachvollziehbar ist.
Lauf Google Finance sind heute knapp 25 Mio. Aktien gehandelt worden. Normal sind 1,7 Mio. Stück. Zumindest das ist beeindruckend.
Shares of Medarex jump on premature report of results in just 2 prostate cancer patients
* By Linda A. Johnson, AP Business Writer
* On Monday June 22, 2009, 2:48 pm EDT
TRENTON, N.J. (AP) -- Shares of drug developer Medarex Inc. jumped Monday after an unusual report that two men in a study of its experimental prostate cancer drug had their tumors shrink dramatically. The report gave no information on how other men in the study fared.
Shares of Princeton, N.J.-based Medarex opened at $8.88, just over 20 percent above their close at $7.36 on Friday. By early afternoon, they were up $1.15, or 15.6 percent, at $8.51, while the broader markets were all down.
The jump followed a press release issued by the Mayo Clinic of Rochester, Minn., which is co-sponsoring a study of a genetically engineered, antibody-based Medarex drug, called ipilimumab, to treat prostate cancer.
The release states that two patients who had what was considered inoperable prostate cancer that had spread to other areas now "have no evidence of disease." The release credits the combination of ipilimumab with standard hormone treatment and radiation therapy.
The press release gave no information about how many people are participating in the trial, whether the other patients were improving or getting worse, how long they had survived or whether the study is an early, midstage or late-stage trial. Also, the two men still had to undergo surgery to remove the remaining tumors.
Results from just two patients must be interpreted very cautiously. Researchers normally do not release data until a study has been completed and all the data thoroughly analyzed and vetted for presentation in a medical journal or at a medical conference. In addition, studies typically compare patients getting a new treatment with a second group getting a standard treatment or a placebo, but the press release gave no information about this study's design.
Ipilimumab targets CTLA-4, short for cytotoxic T lymphocyte-associated antigen 4. CTLA-4 is a molecule on immune cells called T-cells that plays an important role in regulating the body's natural immune defenses.
Medarex, which is supporting the study, trumpeted the brief press release on its Web site Monday, but has posted no recent information on other test results of the drug for prostate cancer.
Sehr, sehr skeptisch... was ja vielleicht nachvollziehbar ist.
Lauf Google Finance sind heute knapp 25 Mio. Aktien gehandelt worden. Normal sind 1,7 Mio. Stück. Zumindest das ist beeindruckend.

Weiterer Schritt zur Zulassung von Simponi in Europa
*************************
Simponi has been recommended for approval in Europe to treat moderate to severe rheumatoid arthritis.
http://www.reuters.com/article/marketsNews/idINLQ57923020090…
*************************
Simponi has been recommended for approval in Europe to treat moderate to severe rheumatoid arthritis.
http://www.reuters.com/article/marketsNews/idINLQ57923020090…
So, Ilaris (ACZ885) ist jetzt auch zugelassen und per Medarex PM vermeldet worden. Damit sind nun bereits drei Medarex Produkte zugelassen.
Antwort auf Beitrag Nr.: 37.493.235 von Ville7 am 30.06.09 14:44:00Wird dann zu Lebzeiten zum Break Even reichen und zur gar fürchterlichen KGV-Bewertung

Antwort auf Beitrag Nr.: 37.493.471 von Friseuse am 30.06.09 15:14:56Aus dem Morphosys-Thread rüberkopiert:
NEW YORK (Dow Jones)--Der US-Pharmakonzern Abbott Laboratories soll nach einer Gerichtsentscheidung seinem Wettbewerber Johnson & Johnson für eine Verletzung von Patentrechten 1,67 Mrd USD zahlen. Ein Schwurgericht im texanischen Marshall bestätigte am Montag nach einwöchiger Verhandlung das Patent von Johnson & Johnson für das Mittel "Remicade" gegen rheumatoide Arthritis. Dagegen habe Abbott mit seinem Medikament "Humira" verstoßen.
Abbott kündigte in einer ersten Stellungnahme an, die Entscheidung anfechten zu wollen. Der Pharmakonzern machte mit "Humira" im vergangenen Jahr 15% seines Umsatzes. Insgesamt summierten sich die Einnahmen allein mit dem Blockbuster auf 4,5 Mrd USD. Ein Abbott-Sprecher gab sich zuversichtlich, vor einem Einzelrichter eine günstigere Entscheidung zu bekommen.
Beim Pharmazie- und Konsumgüterhersteller Johnson & Johnson mit Sitz in New Brunswick wird das Patent auf den monoklonalen Antikörper Infliximab (Handelsname "Remicade") vom Biotech-Tochterunternehmen Centocor zusammen mit der Universität von New York gehalten.
Infliximab und der von Abbott entwickelte Wirkstoff Adalimumab (Handelsname "Humira") gehören zur Klasse der TNF-Blocker, die zur Behandlung von entzündlichen Erkrankungen eingesetzt werden.
Webseite: http://online.wsj.com/
Die Patentverletzung müsste dann eigentlich auch für Simponi gelten. Oder ist mir da was entgangen?
NEW YORK (Dow Jones)--Der US-Pharmakonzern Abbott Laboratories soll nach einer Gerichtsentscheidung seinem Wettbewerber Johnson & Johnson für eine Verletzung von Patentrechten 1,67 Mrd USD zahlen. Ein Schwurgericht im texanischen Marshall bestätigte am Montag nach einwöchiger Verhandlung das Patent von Johnson & Johnson für das Mittel "Remicade" gegen rheumatoide Arthritis. Dagegen habe Abbott mit seinem Medikament "Humira" verstoßen.
Abbott kündigte in einer ersten Stellungnahme an, die Entscheidung anfechten zu wollen. Der Pharmakonzern machte mit "Humira" im vergangenen Jahr 15% seines Umsatzes. Insgesamt summierten sich die Einnahmen allein mit dem Blockbuster auf 4,5 Mrd USD. Ein Abbott-Sprecher gab sich zuversichtlich, vor einem Einzelrichter eine günstigere Entscheidung zu bekommen.
Beim Pharmazie- und Konsumgüterhersteller Johnson & Johnson mit Sitz in New Brunswick wird das Patent auf den monoklonalen Antikörper Infliximab (Handelsname "Remicade") vom Biotech-Tochterunternehmen Centocor zusammen mit der Universität von New York gehalten.
Infliximab und der von Abbott entwickelte Wirkstoff Adalimumab (Handelsname "Humira") gehören zur Klasse der TNF-Blocker, die zur Behandlung von entzündlichen Erkrankungen eingesetzt werden.
Webseite: http://online.wsj.com/
Die Patentverletzung müsste dann eigentlich auch für Simponi gelten. Oder ist mir da was entgangen?
Medarex erhält Meilenstein-Zahlungen  für die Genehmigung des Ilaris für die Behandlung von Cryopyrin-assoziierte Periodische Syndrom , es wird eine Meilenstein-Zahlung von einem unbekannten Betrag von Novartis Pharma AG Novartis Pharma AG geben (
für die Genehmigung des Ilaris für die Behandlung von Cryopyrin-assoziierte Periodische Syndrom , es wird eine Meilenstein-Zahlung von einem unbekannten Betrag von Novartis Pharma AG Novartis Pharma AG geben (
www.medarex.com/cgi-local/item.pl/20090630-1303263
Ordentlich,schon die dritte Zulassung.
PS.Der Verfasser ist in Medarex investiert.
 für die Genehmigung des Ilaris für die Behandlung von Cryopyrin-assoziierte Periodische Syndrom , es wird eine Meilenstein-Zahlung von einem unbekannten Betrag von Novartis Pharma AG Novartis Pharma AG geben (
für die Genehmigung des Ilaris für die Behandlung von Cryopyrin-assoziierte Periodische Syndrom , es wird eine Meilenstein-Zahlung von einem unbekannten Betrag von Novartis Pharma AG Novartis Pharma AG geben (www.medarex.com/cgi-local/item.pl/20090630-1303263
Ordentlich,schon die dritte Zulassung.

PS.Der Verfasser ist in Medarex investiert.
Antwort auf Beitrag Nr.: 37.493.235 von Ville7 am 30.06.09 14:44:00Also irgendwie finde ich die Pipelinedarstellung bei Novartis nicht eben übersichtlich:
http://www.novartis.com/downloads/research/planned-filings.p…
Kann es sein, dass da ACZ 885 (Ilaris) in der jetzt zugelassenen Indikation überhaupt nicht auftaucht? (Aber scheinbar lief hier der Zulassungsprozess sowieso anders und viel schneller ab, als gewöhnlich. Vielleicht liegts daran.)
In der PM von Novartis wurden dann ja noch folgende Indikationen bestätigt:
- some forms (?) of gout -> in der Pipeline für 2010 mit "refractory gout" angegeben
- systemic juvenile idiopathic arthritis (SJIA) -> in der Pipeline für 2011 angegeben
- type 2 diabetes -> in der Pipeline für 2012 und später angegeben
- chronic obstructive pulmonary disorder (COPD) -> finde ich in der Pipeline nicht mit ACZ 885, sondern mit QVA 149 und QMF 149 (?)
- Further development in rheumatoid arthritis (RA) is not planned -> das ist in der Pipeline für 2012 und später noch drin, wurde aber offensichtlich nun abgebrochen.
Jedenfalls könnte 2010 ein BLA für "refractory gout" anstehen. Ich habe aber keine Ahnung, ob das eine wirtschaftlich bedeutende Indikation ist. Bei CAPS geht es wohl um "nur" ca. 300 Fälle in den USA. Aber vielleicht sollte man Ilaris einfach nicht finanziell, sondern symbolisch bewerten.
http://www.novartis.com/downloads/research/planned-filings.p…
Kann es sein, dass da ACZ 885 (Ilaris) in der jetzt zugelassenen Indikation überhaupt nicht auftaucht? (Aber scheinbar lief hier der Zulassungsprozess sowieso anders und viel schneller ab, als gewöhnlich. Vielleicht liegts daran.)
In der PM von Novartis wurden dann ja noch folgende Indikationen bestätigt:
- some forms (?) of gout -> in der Pipeline für 2010 mit "refractory gout" angegeben
- systemic juvenile idiopathic arthritis (SJIA) -> in der Pipeline für 2011 angegeben
- type 2 diabetes -> in der Pipeline für 2012 und später angegeben
- chronic obstructive pulmonary disorder (COPD) -> finde ich in der Pipeline nicht mit ACZ 885, sondern mit QVA 149 und QMF 149 (?)
- Further development in rheumatoid arthritis (RA) is not planned -> das ist in der Pipeline für 2012 und später noch drin, wurde aber offensichtlich nun abgebrochen.
Jedenfalls könnte 2010 ein BLA für "refractory gout" anstehen. Ich habe aber keine Ahnung, ob das eine wirtschaftlich bedeutende Indikation ist. Bei CAPS geht es wohl um "nur" ca. 300 Fälle in den USA. Aber vielleicht sollte man Ilaris einfach nicht finanziell, sondern symbolisch bewerten.
Antwort auf Beitrag Nr.: 37.497.894 von SLGramann am 01.07.09 08:55:55Betrachte die Zulassung von Ilaris in dieser Micro-Indikation als Geniestreich. Anti-IL1-beta gilt als sehr sehr interessantes Target, viele Firmen haben hier was im Köcher, nur eben erst in den früheren Phasen und Novartis hat schon ein zugelassenes Produkt und nicht mehr das Zulassungsrisiko. Erwarte mit positiven klinischen Studien in allen möglichen Autoimmunindikationen zunehmenden Offlabeleinsatz!
Gicht (gout) ist eine wirtschaflich recht bedeutende Indikation.
Gicht (gout) ist eine wirtschaflich recht bedeutende Indikation.
Antwort auf Beitrag Nr.: 37.504.603 von Ville7 am 02.07.09 04:55:24Ob Geniestreich oder nicht wird sich in einigen Jahren herausstellen.
Aber ville hat klar Recht:
Zulassung und günstiges Nebenwirkungsprofil,
das bietet Chancen auf off label vermarktung und Platzhirsch zu werden.
Aber ville hat klar Recht:
Zulassung und günstiges Nebenwirkungsprofil,
das bietet Chancen auf off label vermarktung und Platzhirsch zu werden.
Im Morphosys-Thread (#5492) hat caldo auf die BCG-Studie "Medizinische Biotechnologie in Deutschland 2009" hingewiesen, die im Auftrage des Verbandes der forschenden Pharma-Unternehmen Deutschlands erstellt wurde (ist dort verlinkt).
Auf Seite 33 der Studie heißt es:
Seit kurzem liegen aber erste vielversprechende Daten
für eine Therapie mit dem monoklonalen Antikörper Ipilimumab
vor. Dieser humane Antikörper bindet an das
Oberflächenprotein CTLA-4 auf den T-Helferzellen.30 Da
Tumore aus körpereigenen Zellen bestehen, werden sie
nur durch wenige T-Zellen als „entartet“ erkannt. Dies ist
für eine ausreichende Immunantwort zu wenig. Ipilimumab
verhindert durch die Bindung an CTLA-4, dass
diese T-Zellen inaktiviert werden, und ermöglicht somit,
dass sie die Tumorzellen erkennen und abtöten können.
Ipilimumab befindet sich als Monotherapie und in Kombination
mit Chemo- oder Immuntherapie in Phase II/III
der klinischen Entwicklung.30
Prinzipiell ist darüber hinaus denkbar, dass der Wirkmechanismus
von Ipilimumab auch bei weiteren Tumorarten
funktionieren kann („Multi-Tumor-Konzept“).31 So
wird der Antikörper derzeit für die Therapie weiterer
Krebsarten, wie z. B. Prostata-, Lungen- und Blasenkrebs,
klinisch getestet.
------------------------
Zwar ist die Studie sicher als "Werbeschrift" für die Biotechforschung und speziell die mabs gedacht, indes ist sie was einzelne Projekte angeht neutral. Die positive Bewertung von Ipilimumab fand ich daher erfreulich.
Auf Seite 33 der Studie heißt es:
Seit kurzem liegen aber erste vielversprechende Daten
für eine Therapie mit dem monoklonalen Antikörper Ipilimumab
vor. Dieser humane Antikörper bindet an das
Oberflächenprotein CTLA-4 auf den T-Helferzellen.30 Da
Tumore aus körpereigenen Zellen bestehen, werden sie
nur durch wenige T-Zellen als „entartet“ erkannt. Dies ist
für eine ausreichende Immunantwort zu wenig. Ipilimumab
verhindert durch die Bindung an CTLA-4, dass
diese T-Zellen inaktiviert werden, und ermöglicht somit,
dass sie die Tumorzellen erkennen und abtöten können.
Ipilimumab befindet sich als Monotherapie und in Kombination
mit Chemo- oder Immuntherapie in Phase II/III
der klinischen Entwicklung.30
Prinzipiell ist darüber hinaus denkbar, dass der Wirkmechanismus
von Ipilimumab auch bei weiteren Tumorarten
funktionieren kann („Multi-Tumor-Konzept“).31 So
wird der Antikörper derzeit für die Therapie weiterer
Krebsarten, wie z. B. Prostata-, Lungen- und Blasenkrebs,
klinisch getestet.
------------------------
Zwar ist die Studie sicher als "Werbeschrift" für die Biotechforschung und speziell die mabs gedacht, indes ist sie was einzelne Projekte angeht neutral. Die positive Bewertung von Ipilimumab fand ich daher erfreulich.
Medarex and Lonza Sign Collaboration Agreement for the Supply of Antibody-Based Products
Agreement Includes Manufacture of Antibodies and Antibody Drug Conjugates
PRINCETON, N.J. & BASEL, Switzerland--(BUSINESS WIRE)--Lonza and Medarex, Inc. (NASDAQ:MEDX) today announced that they have signed an agreement giving Medarex the option to work with Lonza as a collaboration partner to provide manufacturing services in support of the development and commercialization of Medarex’s pipeline of therapeutic proteins and antibody drug conjugates (ADCs). As part of the agreement, Lonza may provide process development services for certain Medarex programs and may reserve manufacturing capacity for Medarex antibody and antibody drug conjugate programs at Lonza’s biopharmaceutical facilities around the world. Further details of the agreement were not disclosed.
“We are pleased to be working with such a successful mid-size biotech company to advance and strengthen their robust portfolio of innovative therapies,” said Dr. Stephan Kutzer, Head of Lonza Biopharmaceuticals. “Supporting Medarex’s immediate and long-term needs with our expertise in mammalian cell culture and antibody drug conjugates is both exciting and rewarding.”
This collaboration agreement represents the continued extension of Lonza’s contract manufacturing business model, evolving from a short-term product-by-product development and manufacturing arrangement toward more strategic long-term collaboration on a pipeline of products. The Medarex agreement leverages Lonza’s expertise and asset base in biologics manufacturing and its new state-of-the-art facilities to produce antibody drug conjugates in milligram to multiple kilogram quantities for both clinical and commercial supply.
Medarex’s biologics portfolio is focused on treating oncology and immunology therapeutic indications with ten antibody programs in Phase 3 to Phase 1 clinical development. Medarex is a leader in therapeutic antibody development, and there are over forty therapeutic product candidates derived from its UltiMAb® technology in development or at the IND submission stage for clinical trials, either through its internal efforts or through partnerships. Under the terms of the agreement, Lonza may be supporting a portion of the Medarex product pipeline.
About Lonza
Lonza is one of the world's leading suppliers to the pharmaceutical, healthcare and life science industries. Its products and services span its customers’ needs from research to final product manufacture. Lonza is the global leader in the production and support of active pharmaceutical ingredients both chemically as well as biotechnologically. Biopharmaceuticals are one of the key growth drivers of the pharmaceutical and biotechnology industries. Lonza has strong capabilities in large and small molecules, peptides, amino acids and niche bioproducts which play an important role in the development of novel medicines and healthcare products. Lonza is a leader in cell-based research, endotoxin detection and cell therapy manufacturing. Lonza is also a leading provider of value chemical and biotech ingredients to the nutrition, hygiene, preservation, agro and personal care markets.
Lonza is headquartered in Basel, Switzerland and is listed on the SWX Swiss Exchange. In 2008, Lonza had sales of CHF 2.937 billion. Further information can be found at www.lonza.com.
Agreement Includes Manufacture of Antibodies and Antibody Drug Conjugates
PRINCETON, N.J. & BASEL, Switzerland--(BUSINESS WIRE)--Lonza and Medarex, Inc. (NASDAQ:MEDX) today announced that they have signed an agreement giving Medarex the option to work with Lonza as a collaboration partner to provide manufacturing services in support of the development and commercialization of Medarex’s pipeline of therapeutic proteins and antibody drug conjugates (ADCs). As part of the agreement, Lonza may provide process development services for certain Medarex programs and may reserve manufacturing capacity for Medarex antibody and antibody drug conjugate programs at Lonza’s biopharmaceutical facilities around the world. Further details of the agreement were not disclosed.
“We are pleased to be working with such a successful mid-size biotech company to advance and strengthen their robust portfolio of innovative therapies,” said Dr. Stephan Kutzer, Head of Lonza Biopharmaceuticals. “Supporting Medarex’s immediate and long-term needs with our expertise in mammalian cell culture and antibody drug conjugates is both exciting and rewarding.”
This collaboration agreement represents the continued extension of Lonza’s contract manufacturing business model, evolving from a short-term product-by-product development and manufacturing arrangement toward more strategic long-term collaboration on a pipeline of products. The Medarex agreement leverages Lonza’s expertise and asset base in biologics manufacturing and its new state-of-the-art facilities to produce antibody drug conjugates in milligram to multiple kilogram quantities for both clinical and commercial supply.
Medarex’s biologics portfolio is focused on treating oncology and immunology therapeutic indications with ten antibody programs in Phase 3 to Phase 1 clinical development. Medarex is a leader in therapeutic antibody development, and there are over forty therapeutic product candidates derived from its UltiMAb® technology in development or at the IND submission stage for clinical trials, either through its internal efforts or through partnerships. Under the terms of the agreement, Lonza may be supporting a portion of the Medarex product pipeline.
About Lonza
Lonza is one of the world's leading suppliers to the pharmaceutical, healthcare and life science industries. Its products and services span its customers’ needs from research to final product manufacture. Lonza is the global leader in the production and support of active pharmaceutical ingredients both chemically as well as biotechnologically. Biopharmaceuticals are one of the key growth drivers of the pharmaceutical and biotechnology industries. Lonza has strong capabilities in large and small molecules, peptides, amino acids and niche bioproducts which play an important role in the development of novel medicines and healthcare products. Lonza is a leader in cell-based research, endotoxin detection and cell therapy manufacturing. Lonza is also a leading provider of value chemical and biotech ingredients to the nutrition, hygiene, preservation, agro and personal care markets.
Lonza is headquartered in Basel, Switzerland and is listed on the SWX Swiss Exchange. In 2008, Lonza had sales of CHF 2.937 billion. Further information can be found at www.lonza.com.
Medarex to Receive Milestone Payment from FibroGen for the Initiation of a Phase 2 Study of FG-3019 in Patients with Diabetic Kidney Disease
PRINCETON, N.J.--(BUSINESS WIRE)--Medarex, Inc. (NASDAQ:MEDX) today announced it will receive a milestone payment of an undisclosed amount from its licensing partner, FibroGen, Inc., in connection with a recently initiated Phase 2 clinical trial of FG-3019 in patients with type 2 diabetes and advanced kidney disease as announced by FibroGen on June 15, 2009.
FG-3019 is a fully human monoclonal antibody generated using Medarex's UltiMAb® technology against connective tissue growth factor (CTGF). Under the agreement with FibroGen, Medarex could receive future milestone payments and sales-based royalty payments.
“We are pleased with the progress our licensing partners continue to make in the development of antibodies generated from our UltiMAb® technology,” said Howard H. Pien, Chairman and CEO of Medarex. “We believe the advancements of other antibody programs generated from Medarex’s UltiMAb® platform will continue to emphasize the therapeutic importance of our technology to address underserved medical needs.”
PRINCETON, N.J.--(BUSINESS WIRE)--Medarex, Inc. (NASDAQ:MEDX) today announced it will receive a milestone payment of an undisclosed amount from its licensing partner, FibroGen, Inc., in connection with a recently initiated Phase 2 clinical trial of FG-3019 in patients with type 2 diabetes and advanced kidney disease as announced by FibroGen on June 15, 2009.
FG-3019 is a fully human monoclonal antibody generated using Medarex's UltiMAb® technology against connective tissue growth factor (CTGF). Under the agreement with FibroGen, Medarex could receive future milestone payments and sales-based royalty payments.
“We are pleased with the progress our licensing partners continue to make in the development of antibodies generated from our UltiMAb® technology,” said Howard H. Pien, Chairman and CEO of Medarex. “We believe the advancements of other antibody programs generated from Medarex’s UltiMAb® platform will continue to emphasize the therapeutic importance of our technology to address underserved medical needs.”
Antwort auf Beitrag Nr.: 37.561.735 von SLGramann am 13.07.09 15:52:51
Wo gibte es eigentlich einen Überblick über die gesamte Pipeline samt aller Partnerprojekte von Medarex?
Das Projekt, das hier gemeldet wurde, ist unter "Pipeline" auf der Medarex-Website nicht zu entdecken...
Wo gibte es eigentlich einen Überblick über die gesamte Pipeline samt aller Partnerprojekte von Medarex?
Das Projekt, das hier gemeldet wurde, ist unter "Pipeline" auf der Medarex-Website nicht zu entdecken...
Antwort auf Beitrag Nr.: 37.561.773 von SLGramann am 13.07.09 15:57:30Lieber SLGramann,
hier die US Patente.
www.freepatentsonline.com/result.html?query_txt=Medarex&sort…
Im EPA finde ich nichts.
v3.espacenet.com/searchResults?locale=de_EP&AB=MEDAREX+inc.&…
PS.Der Verfasser ist in Medarex investiert.
hier die US Patente.
www.freepatentsonline.com/result.html?query_txt=Medarex&sort…
Im EPA finde ich nichts.
v3.espacenet.com/searchResults?locale=de_EP&AB=MEDAREX+inc.&…
PS.Der Verfasser ist in Medarex investiert.

Antwort auf Beitrag Nr.: 37.562.304 von Bioperle am 13.07.09 16:48:57Medarex = Jahrhundertchance!
Beim aktuellen Kurs wird Medarex (NASDAQ: MEDX) mit einer Market Cap. von rund 1 Mrd. US$ bewertet. Auf den ersten Blick nicht gerade günstig, denn zuletzt erzielte das Unternehmen gerade mal Umsätze von etwas mehr als 50 Mio. US$, ein stattliches KUV von 20 also. Und auch von Gewinnen ist die Company weit entfernt, denn das EBITDA lag bei rund -165 Mio. US$ und der Nettoverlust sogar bei -190 Mio. US$. Allerdings ist die Gesellschaft trotz allem aktuell bestens durchfinanziert, denn Schulden von rund 145 Mio. US$ steht Cash in Höhe von rund 323 Mio. US$ gegenüber, so dass das Geld noch problemlos für mehr als 1 Jahr reichen sollte. Und dennoch ist das sehr, sehr teuer, besonders im Vergleich zu MorphoSys, die bereits profitabel arbeiten und deutlich niedriger bewertet werden.
Und dennoch diese Kaufempfehlung als "Jahrhundertchance"? Genau, denn Medarex (NASDAQ: MEDX) hat zuletzt ein Medikament gegen Prostatakrebs entwickelt. Dieses wurde nun kürzlich erstmals an zwei Patienten ausprobiert, bei denen der Krebs weit fortgeschritten war und die daher "nichts mehr zu verlieren hatten". Die Hoffnung der behandelnden Ärzte war, dass man mit dem Medikament von Medarex wenigstens das Leben der Patienten einige Zeit verlängern könnte. Doch zur Überraschung aller wirkte das Medikament so gut, dass beide Patienten in der Zweischenzeit als "geheilt" entlassen werden konnten. Denn Medarex Medikament zerstörte den Krebs soweit, dass die Reste der Tumore schließlich in einer Operation entfernt werden konnten.
Euphorisiert von dieser Wirkung gingen die Ärzte mit dieser Nachricht dann kürzlich an die Öffentlichkeit, woraufhin der Aktienkurs von Medarex in der Spitze um mehr als 30% stieg. Heute sehen wir nun nach dieser "Euphorie" erste Gewinnmitnahmen. Und vor dem Hintergrund der Tatsache, dass die Ärzte Medarex bescheinigten "womöglich den "heiligen Gral" im Kampf gegen Prostatakrebs" gefunden haben zu können, dürfte hier bald noch viel mehr möglich sein. Daher nutze ich den heutigen schwachen Tag selbst zum Aufbau einer Position in Medarex (NASDAQ: MEDX) und rate spekulativ eingestellten Sharewise Mitgliedern dazu es mir gleich zu tun. Trotz der mit einem KUV von ca. 20 extrem hohen Bewertung...
Kursziel erstmal 10 €.
quelle:www.sharewise.com/aktien/US5839161016-medarex/analyse/200906…
PS.Eine gute Aktie kann man immer kaufen.

Beim aktuellen Kurs wird Medarex (NASDAQ: MEDX) mit einer Market Cap. von rund 1 Mrd. US$ bewertet. Auf den ersten Blick nicht gerade günstig, denn zuletzt erzielte das Unternehmen gerade mal Umsätze von etwas mehr als 50 Mio. US$, ein stattliches KUV von 20 also. Und auch von Gewinnen ist die Company weit entfernt, denn das EBITDA lag bei rund -165 Mio. US$ und der Nettoverlust sogar bei -190 Mio. US$. Allerdings ist die Gesellschaft trotz allem aktuell bestens durchfinanziert, denn Schulden von rund 145 Mio. US$ steht Cash in Höhe von rund 323 Mio. US$ gegenüber, so dass das Geld noch problemlos für mehr als 1 Jahr reichen sollte. Und dennoch ist das sehr, sehr teuer, besonders im Vergleich zu MorphoSys, die bereits profitabel arbeiten und deutlich niedriger bewertet werden.
Und dennoch diese Kaufempfehlung als "Jahrhundertchance"? Genau, denn Medarex (NASDAQ: MEDX) hat zuletzt ein Medikament gegen Prostatakrebs entwickelt. Dieses wurde nun kürzlich erstmals an zwei Patienten ausprobiert, bei denen der Krebs weit fortgeschritten war und die daher "nichts mehr zu verlieren hatten". Die Hoffnung der behandelnden Ärzte war, dass man mit dem Medikament von Medarex wenigstens das Leben der Patienten einige Zeit verlängern könnte. Doch zur Überraschung aller wirkte das Medikament so gut, dass beide Patienten in der Zweischenzeit als "geheilt" entlassen werden konnten. Denn Medarex Medikament zerstörte den Krebs soweit, dass die Reste der Tumore schließlich in einer Operation entfernt werden konnten.
Euphorisiert von dieser Wirkung gingen die Ärzte mit dieser Nachricht dann kürzlich an die Öffentlichkeit, woraufhin der Aktienkurs von Medarex in der Spitze um mehr als 30% stieg. Heute sehen wir nun nach dieser "Euphorie" erste Gewinnmitnahmen. Und vor dem Hintergrund der Tatsache, dass die Ärzte Medarex bescheinigten "womöglich den "heiligen Gral" im Kampf gegen Prostatakrebs" gefunden haben zu können, dürfte hier bald noch viel mehr möglich sein. Daher nutze ich den heutigen schwachen Tag selbst zum Aufbau einer Position in Medarex (NASDAQ: MEDX) und rate spekulativ eingestellten Sharewise Mitgliedern dazu es mir gleich zu tun. Trotz der mit einem KUV von ca. 20 extrem hohen Bewertung...
Kursziel erstmal 10 €.
quelle:www.sharewise.com/aktien/US5839161016-medarex/analyse/200906…
PS.Eine gute Aktie kann man immer kaufen.

Antwort auf Beitrag Nr.: 37.566.630 von Bioperle am 14.07.09 10:14:45
Hi Bioperle, danke für Deine Links. Leider bin ich fachlich nicht in der Lage, Patentanmeldungen inhaltlich zu bewerten.
Ich gehe davon aus, dass die Gesamtpipeline von Medarex für uns hier im Thread mehr oder weniger ein Geheimnis ist... Das lässt natürlich auch Hoffnungen zu.
Ansonsten gebe ich Dir bei der Bemerkung recht, dass man eine gute Aktie immer kaufen kann. Die "Analyse" von sharewise ist indes ein übles Machwerk imho.
Hi Bioperle, danke für Deine Links. Leider bin ich fachlich nicht in der Lage, Patentanmeldungen inhaltlich zu bewerten.

Ich gehe davon aus, dass die Gesamtpipeline von Medarex für uns hier im Thread mehr oder weniger ein Geheimnis ist... Das lässt natürlich auch Hoffnungen zu.

Ansonsten gebe ich Dir bei der Bemerkung recht, dass man eine gute Aktie immer kaufen kann. Die "Analyse" von sharewise ist indes ein übles Machwerk imho.
Antwort auf Beitrag Nr.: 37.567.798 von SLGramann am 14.07.09 12:19:34Lieber SLGramann,
ich bin davon überzeugt dass Medarex-Technologie sich durchsetzt.
Bei so vielen Projekten mit potentiellen großen Pharmaunternehmen,muss Qualität in der Pipeline sein.
Eine Übernahme ist gänzlich nie auszuschliessen.
Siehe dazu;mobile.wiwo.de/7val.fit/s_83e80fe62591edd863da5014d7b9d030/1…
14.7.2009 14:20
Johnson & Johnson kauft Cougar
Johnson & Johnson übernimmt für eine Milliarde Dollar das Biotechnologieunternehmen Cougar.
Pharmakonzerne sind derzeit auf der Suche nach Zukäufen in den Biotechbranche, um sich angesichts anstehender Patentausläufe bei etablierten Medikamenten Nachschub zu sichern. J&J stieg erst Anfang des Monats für eine Milliarde Dollar bei dem irischen Biotechunternehmen Elan ein.
J&J stieg erst Anfang des Monats für eine Milliarde Dollar bei dem irischen Biotechunternehmen Elan ein.
ich bin davon überzeugt dass Medarex-Technologie sich durchsetzt.
Bei so vielen Projekten mit potentiellen großen Pharmaunternehmen,muss Qualität in der Pipeline sein.

Eine Übernahme ist gänzlich nie auszuschliessen.
Siehe dazu;mobile.wiwo.de/7val.fit/s_83e80fe62591edd863da5014d7b9d030/1…
14.7.2009 14:20
Johnson & Johnson kauft Cougar
Johnson & Johnson übernimmt für eine Milliarde Dollar das Biotechnologieunternehmen Cougar.
Pharmakonzerne sind derzeit auf der Suche nach Zukäufen in den Biotechbranche, um sich angesichts anstehender Patentausläufe bei etablierten Medikamenten Nachschub zu sichern.
 J&J stieg erst Anfang des Monats für eine Milliarde Dollar bei dem irischen Biotechunternehmen Elan ein.
J&J stieg erst Anfang des Monats für eine Milliarde Dollar bei dem irischen Biotechunternehmen Elan ein.
Hallo,
@ Ville und/oder Andere, die sich etwas besser mit Charttechnik auskennen als ich.
Der Medarex-Chart sieht mMn so aus, als könnte er ein Doppeltop entwickeln. Soweit ich weiß, muss dazu der Tiefstkurs zwischen den beiden Spitzen unterboten werden. 1. Stimmt das? und 2. wo liegt dan das potentielle Kursziel?
Gruß
milestones
@ Ville und/oder Andere, die sich etwas besser mit Charttechnik auskennen als ich.
Der Medarex-Chart sieht mMn so aus, als könnte er ein Doppeltop entwickeln. Soweit ich weiß, muss dazu der Tiefstkurs zwischen den beiden Spitzen unterboten werden. 1. Stimmt das? und 2. wo liegt dan das potentielle Kursziel?
Gruß
milestones
Antwort auf Beitrag Nr.: 37.589.162 von Milestones am 16.07.09 22:11:10Zu einem Doppeltop:
Wenn der Kurs nach einem Anstieg zweimal auf einem sehr naheliegenden Niveau hängenbleibt und dann das zwischenliegende Tief unterschreitet, dann nennt man das ein Doppeltop (DT).
Also z.B. Doppeltop bei 12,5, Tief dazwischen bei 10.
Kursziel nach unten ist dann 8. Die breite der Range des DT wird nach unten abgetragen.
12,5/10=10/8
Zu Medarex:
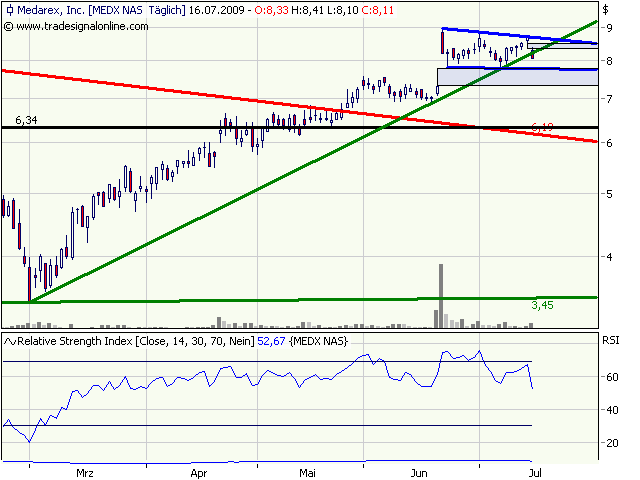
Da ist kein DT, aber trotzdem eine kritische Situation.
Der Aufwärtstrend wurde heute verletzt mit einem gap nach unten.
Gannz allgemein ist Medx natürlich die letzten Monate hervorragend gelaufen, so dass es viele geben wird, die lieber Gewinne sichern, als ordentliche Korrekturen mitzugehen.
Im Moment gibt es ein flach fallendes Dreieck mit einem Gap oben eingelagert, aber vor allem einem großen Gap nach unten.
Ist das Gap für die gepushte 2-Patienten-Geschichte? Es würde mich nicht wundern, wenn das Gap in einer Marktkorrektur wieder schliesst. Spätestens im Bereich zwischen 6 und 7 gibt es aber einiges an Unterstützung.
Wenn der Kurs nach einem Anstieg zweimal auf einem sehr naheliegenden Niveau hängenbleibt und dann das zwischenliegende Tief unterschreitet, dann nennt man das ein Doppeltop (DT).
Also z.B. Doppeltop bei 12,5, Tief dazwischen bei 10.
Kursziel nach unten ist dann 8. Die breite der Range des DT wird nach unten abgetragen.
12,5/10=10/8
Zu Medarex:
Da ist kein DT, aber trotzdem eine kritische Situation.
Der Aufwärtstrend wurde heute verletzt mit einem gap nach unten.
Gannz allgemein ist Medx natürlich die letzten Monate hervorragend gelaufen, so dass es viele geben wird, die lieber Gewinne sichern, als ordentliche Korrekturen mitzugehen.
Im Moment gibt es ein flach fallendes Dreieck mit einem Gap oben eingelagert, aber vor allem einem großen Gap nach unten.
Ist das Gap für die gepushte 2-Patienten-Geschichte? Es würde mich nicht wundern, wenn das Gap in einer Marktkorrektur wieder schliesst. Spätestens im Bereich zwischen 6 und 7 gibt es aber einiges an Unterstützung.
Was den Kurs in den nächsten 6 Monaten wirklich bewegen wird, wird die Entwicklung bei Ipilimumab sein. Sollten die Ergebnisse enttäuschen/erfreuen, dürfte es wohl massiv abwärts/aufwärts gehen.
Eine interessante Frage ist aus meiner Sicht, wie tief der Kurs fallen wird, falls die Ergebnisse enttäuschen. Sehen wir dann wieder die 4 Dollar? Man kann die Frage auch anders formulieren: Wieviel Ipilimumab steckt im gegenwärtigen Kurs drin?
Eine interessante Frage ist aus meiner Sicht, wie tief der Kurs fallen wird, falls die Ergebnisse enttäuschen. Sehen wir dann wieder die 4 Dollar? Man kann die Frage auch anders formulieren: Wieviel Ipilimumab steckt im gegenwärtigen Kurs drin?
Antwort auf Beitrag Nr.: 37.590.058 von SLGramann am 17.07.09 07:34:53Da hast Du vollkommen Recht. Aber kurzfristig denke ich, dass die Marktteilnehmer psychologisch motiviert handeln. Und damit kommt (in diesem Zusammenhang) die Charttechnik ins Spiel. Ich denke nicht, dass der Chart die Kursentwicklung nachhaltig bestimmt. Manche glauben ja sogar, am Chart die zukünftige Unternehmensentwicklung ablesen können... Das halte ich für Schwachsinn. Aber kurzfristig und in an Nachrichten armen Zeiten, kann der Chart schon die Kursentwicklung beeinflussen.
milestones
milestones
Antwort auf Beitrag Nr.: 37.590.058 von SLGramann am 17.07.09 07:34:53Börse macht positiv wie negativ immer wieder Kurse möglich, die man fundamental nicht erwartet hätte und wo es Schwierigkeiten macht diese sinnvoll zu begründen.

Extrembeispiel ist die Euphorie 99/2000.
Aber so weit muss man jetzt nicht zurückgehen. Nicht lange her, da war Medx noch bei 15 bis 20 USD zuhause. Durchaus im Vorgriff auf Nachrichten aus der fortgeschrittenen Pipeline.
Im Rahmen der aufkommenden Finanzkrise haben viele dann die Geduld verloren und trotz nahender Zulassungsnews den Kurs unter die 4 geprügelt.
Damit ist 4 bis 20 der aktuelle Kursbereich für den sich immer Analysten finden lassen werden, warum es gerade jetzt genau so sein muss.
Wieviel Ipilimumab steckt im gegenwärtigen Kurs drin?
Beantwortet sich damit von selbst. "Drin" ist das erst bei 20, denn soviel war auch schon vor 2 Jahren drin.
Extrembeispiel ist die Euphorie 99/2000.
Aber so weit muss man jetzt nicht zurückgehen. Nicht lange her, da war Medx noch bei 15 bis 20 USD zuhause. Durchaus im Vorgriff auf Nachrichten aus der fortgeschrittenen Pipeline.
Im Rahmen der aufkommenden Finanzkrise haben viele dann die Geduld verloren und trotz nahender Zulassungsnews den Kurs unter die 4 geprügelt.
Damit ist 4 bis 20 der aktuelle Kursbereich für den sich immer Analysten finden lassen werden, warum es gerade jetzt genau so sein muss.
Wieviel Ipilimumab steckt im gegenwärtigen Kurs drin?
Beantwortet sich damit von selbst. "Drin" ist das erst bei 20, denn soviel war auch schon vor 2 Jahren drin.
und wieder eine Biotech-Firma weniger:
http://www.marketwatch.com/story/bristol-myers-to-buy-medare…
http://www.marketwatch.com/story/bristol-myers-to-buy-medare…
Auf der langfristigen Nahtstelle wird Medarex übernommen, für Investoren nichts gerissen. Die Lehre ist die von der Leere der Aktionäre, dem langen Atem von Big Pharma
Alles hat ein Ende. Da kaufen Investoren jahrelang zu allen möglichen Preisen MEDX, in der Hoffnung an der Technologie partizipieren zu können und dann kommt ein inkompetentes Management, das nur an sich denkt und verscherbelt alles für einen Spotpreis.
Zumindest haben Pien&Co ja ausgesorgt.
Zumindest haben Pien&Co ja ausgesorgt.
Der gleiche Mist wie bei Medimmune. Verkauft für'n Apple und nen Ei 

Antwort auf Beitrag Nr.: 37.627.840 von VaJo am 23.07.09 06:47:08Auch ich bin recht enttäuscht vom Übernahmepreis und vor allem nach all den riesigen Ups und Downs und dem immensen Potential der Pipeline, dass dieses Unternehmen für diesen lächerlichen Preis weggeht.
Allerdings -und das ist mein lachendes Auge- habe ich mit meinem Engagement hier einen recht guten Schnitt gemacht und bin deswegen nicht traurig über die Übernahme.
Allerdings -und das ist mein lachendes Auge- habe ich mit meinem Engagement hier einen recht guten Schnitt gemacht und bin deswegen nicht traurig über die Übernahme.
Mit diesem Übernahmepreis wird nur das faktische jetzt bezahlt, aber nicht das enorme Potential der Pipeline. Vergleiche #3777.
War echt nicht mehr zu holen?

War echt nicht mehr zu holen?


Moin,



ja das lachende und das weinende Auge...
Bin einerseits auch froh, dass ich jetzt ein fettes Plus habe (steuerfrei natürlich).
Andererseits ist der Preis wirklich gering. Jetzt wo sich die Ipi-Zulassung recht deutlich abzeichnet mit allem, was noch an Folgeanwendungen möglich ist...
Ist noch gar nicht so lange her, da war der Aktienpreis auch ohne Übernahme schon bei 18$!
Na was solls.
Allen, die wie ich jahrelang mit dem doch oft extrem störrischen Esel gekämpft haben, hier wahlweise Gratulation/Beileid auf jeden Fall
herzliche Grüße
quepos
(P.S.: Werde wohl nicht sofort verkaufen, vielleicht gibt´s ja noch ein paar Bieterstreitgerüchte o.ä.)



ja das lachende und das weinende Auge...
Bin einerseits auch froh, dass ich jetzt ein fettes Plus habe (steuerfrei natürlich).
Andererseits ist der Preis wirklich gering. Jetzt wo sich die Ipi-Zulassung recht deutlich abzeichnet mit allem, was noch an Folgeanwendungen möglich ist...
Ist noch gar nicht so lange her, da war der Aktienpreis auch ohne Übernahme schon bei 18$!
Na was solls.
Allen, die wie ich jahrelang mit dem doch oft extrem störrischen Esel gekämpft haben, hier wahlweise Gratulation/Beileid auf jeden Fall
herzliche Grüße
quepos
(P.S.: Werde wohl nicht sofort verkaufen, vielleicht gibt´s ja noch ein paar Bieterstreitgerüchte o.ä.)
Ebenfalls Moin 
Naja, mir gehts da wohl genauso wie den meisten hier. Einerseits bin ich froh, dass das Investment einen netten Gewinn abwirft, andererseits waren die letzten Ergebnisse von IPI und der restlichen Pipe doch sehr vielversprechend und es hätte mehr rausschauen müssen. Bewahrheitet sich wohl doch. Pien macht damit wohl den besten Schnitt
Wir verhaltet ihr euch jetzt? Ich war noch nie in so einer Situation Wer könnte da noch Interesse an MEDX zeigen?
Wer könnte da noch Interesse an MEDX zeigen?
ok. Viel Erfolg allen weiterhin
lg
Lycos

Naja, mir gehts da wohl genauso wie den meisten hier. Einerseits bin ich froh, dass das Investment einen netten Gewinn abwirft, andererseits waren die letzten Ergebnisse von IPI und der restlichen Pipe doch sehr vielversprechend und es hätte mehr rausschauen müssen. Bewahrheitet sich wohl doch. Pien macht damit wohl den besten Schnitt

Wir verhaltet ihr euch jetzt? Ich war noch nie in so einer Situation
 Wer könnte da noch Interesse an MEDX zeigen?
Wer könnte da noch Interesse an MEDX zeigen?ok. Viel Erfolg allen weiterhin

lg
Lycos
Antwort auf Beitrag Nr.: 37.627.945 von Lycos2 am 23.07.09 07:44:14Ich glaube eigentlich, dass die Sache gelaufen ist. Es wird keine anderen Interessenten geben, da BMS ja bei Ipi mit im Boot sitzt. Aber Gerüchte und natürlich auch Widerstände gegen die Übernahme (auch wenn sie zwecklos sind) könnte ich mir gerade auch in USA schon vorstellen.
Unter den Angebotspreis fallen wird die Aktie jedenfalls kaum (es sei denn, BMS meldet überraschend Insolvenz an, was bei big pharma ziemlich unwahrscheinlich ist).
Vielleicht lohnt es sich etwas zu warten, wahrscheinlich wird sich aber nicht mehr sehr viel ändern.
Wenn man nichts tut, erreicht einen normalerweise irgendwann über die Bank ein förmliches Übernahmeangebot. Man kann aber ebensogut vorher über die Börse verkaufen.
Gruß q.
(
 :rolleyes
:rolleyes
Unter den Angebotspreis fallen wird die Aktie jedenfalls kaum (es sei denn, BMS meldet überraschend Insolvenz an, was bei big pharma ziemlich unwahrscheinlich ist).
Vielleicht lohnt es sich etwas zu warten, wahrscheinlich wird sich aber nicht mehr sehr viel ändern.
Wenn man nichts tut, erreicht einen normalerweise irgendwann über die Bank ein förmliches Übernahmeangebot. Man kann aber ebensogut vorher über die Börse verkaufen.
Gruß q.
(

 :rolleyes
:rolleyes
Antwort auf Beitrag Nr.: 37.628.025 von quepos am 23.07.09 08:06:23Manchmal passieren wundersame Dinge und ein anderer Pharma wirft schon lange einen Blick auf die Medarex Pipeline und Technologie. Wieso nicht JnJ? Wieso nicht Pfizer? Was Medarex im Köcher hat ist locker das Doppelte des Mergerpreises wert. Die Wahrscheinlichkeit, dass ein anderer Bieter kommt ist allerdings nicht sehr hoch - zugegeben, dazu sind die Rahmenbedingungen der Finanzkrise einfach nicht gut genug. Allerdings kann ich auch bis Ende August warten, bis die Angebotsfrist endet. Was ich verliere sind höchstens ein paar Krümel Zinsen (die es ja heutzutage kaum mehr gibt).
Antwort auf Beitrag Nr.: 37.628.074 von Ville7 am 23.07.09 08:17:44Totaler Bullshit
Hatte gehofft eines Tages wenigstens meinen Einstandskurs wieder zu bekommen, so bleibt nach vielen Jahren ein fetter Verlust.
Werde auf keinen Fall verkaufen, mal sehen was passiert.

Hatte gehofft eines Tages wenigstens meinen Einstandskurs wieder zu bekommen, so bleibt nach vielen Jahren ein fetter Verlust.
Werde auf keinen Fall verkaufen, mal sehen was passiert.
Antwort auf Beitrag Nr.: 37.627.840 von VaJo am 23.07.09 06:47:08richtig, hatte mich bei Medimmune und Millennium auch schwarz geärgert!
Jetzt hoffe ich mal das MOR nicht das gleiche Schiksal ereilt. Wobei wenn MOR für 1,5 Mrd EUR über den Tisch gehen würde hätte ich im Moment nichts dagegen.
Antwort auf Beitrag Nr.: 37.628.461 von VaJo am 23.07.09 09:06:17und dann noch Medigene und ich war bei allen Vieren dabei:
hgsi, medx, mor, mdg...
hgsi, medx, mor, mdg...

Antwort auf Beitrag Nr.: 37.627.840 von VaJo am 23.07.09 06:47:08Hallo Zusammen,
der Medarex-Kurs stand im März bei 3,50 USD.
Es kann nicht wahr sein, das sich hier einige über den Übernahmepreis von 16 USD beschweren.
Wer jetzt bei einem Interessenten, der 2,4 Mrd USD in die Übernahme investiert, sagt, die Pipeline wäre mehr wert, ist sehr, sehr undankbar.
Gruss
KJ
der Medarex-Kurs stand im März bei 3,50 USD.
Es kann nicht wahr sein, das sich hier einige über den Übernahmepreis von 16 USD beschweren.
Wer jetzt bei einem Interessenten, der 2,4 Mrd USD in die Übernahme investiert, sagt, die Pipeline wäre mehr wert, ist sehr, sehr undankbar.
Gruss
KJ
Weil ich ein echtes Genie bin, hatte ich am Montag meine Medarex-Posi auf die Hälfte reduziert. 
Na ja, jetzt schließe ich mich Ville an und warte mal den August ab. Dass da noch ein Bieterwettstreit ausbricht, ist zwar sehr unwahrscheinlich, aber wer weiß. Denn andererseits: Was gibts denn schon noch an mab-Schmieden zu angeln? Selbst Morphosys ist ja ziemlich ernsthaft verlobt. Also, vielleicht packt ja jetzt einen die Torschlusspanik.

Na ja, jetzt schließe ich mich Ville an und warte mal den August ab. Dass da noch ein Bieterwettstreit ausbricht, ist zwar sehr unwahrscheinlich, aber wer weiß. Denn andererseits: Was gibts denn schon noch an mab-Schmieden zu angeln? Selbst Morphosys ist ja ziemlich ernsthaft verlobt. Also, vielleicht packt ja jetzt einen die Torschlusspanik.

Antwort auf Beitrag Nr.: 37.628.882 von KillingJoke am 23.07.09 09:47:01Es kann nicht wahr sein, das sich hier einige über den Übernahmepreis von 16 USD beschweren.
Es kommt wie bei allen Aktien auf den Blickwinkel an.
Du kannst Dich jetzt als toller Investor fühlen.
Viele andere waren vom Konzept von Medarex überzeugt und sind viel früher eingestiegen.
Eine Aktie sollte doch als Gegenstand zur Unternehmensbeteiligung verstanden werden und nicht als Lottoschein.
Trotzdem Glückwunsch an Dich.
Es kommt wie bei allen Aktien auf den Blickwinkel an.
Du kannst Dich jetzt als toller Investor fühlen.
Viele andere waren vom Konzept von Medarex überzeugt und sind viel früher eingestiegen.
Eine Aktie sollte doch als Gegenstand zur Unternehmensbeteiligung verstanden werden und nicht als Lottoschein.
Trotzdem Glückwunsch an Dich.
MOR steigt jetzt vorsichtshalber, man weis ja nie 

Antwort auf Beitrag Nr.: 37.628.074 von Ville7 am 23.07.09 08:17:44Lieber Ville7,
-ist dieses Angebot von Medarex angenommen?
-Können wir noch auf ein verbessertes Angebot hoffen?
-Wieviel Prozent besitzt Bristol-Myers an Medarex?
Mein posting vom 14.7.09!!
Das ging aber schnell........
#3771 von Bioperle Benutzerinfo Nachricht an Benutzer Beiträge des Benutzers ausblenden 14.07.09 14:49:23 Beitrag Nr.: 37.569.083
Dieses Posting: versenden | melden Diskussion drucken
Folgende Antwort bezieht sich auf Beitrag Nr.: 37.567.798 im neuen Fenster öffnen von SLGramann am 14.07.09 12:19:34 Lieber SLGramann,
ich bin davon überzeugt dass Medarex-Technologie sich durchsetzt.
Bei so vielen Projekten mit potentiellen großen Pharmaunternehmen,muss Qualität in der Pipeline sein. Küsschen
Eine Übernahme ist gänzlich nie auszuschliessen.
Siehe dazu; mobile.wiwo.de/7val.fit/s_83e80fe62591edd863da5014d7b9d030/1…
14.7.2009 14:20
Johnson & Johnson kauft Cougar
.
Johnson & Johnson übernimmt für eine Milliarde Dollar das Biotechnologieunternehmen Cougar.
Pharmakonzerne sind derzeit auf der Suche nach Zukäufen in den Biotechbranche,
um sich angesichts anstehender Patentausläufe bei etablierten Medikamenten Nachschub zu sichern.
Schade,auch ich dachte da wäre mehr zu holen gewesen
- Welches Pharmaunternehmen könnte auch Interesse an einer Übernahme von Medarex haben?
Ich werde wohl weiter abwarten.
-ist dieses Angebot von Medarex angenommen?

-Können wir noch auf ein verbessertes Angebot hoffen?
-Wieviel Prozent besitzt Bristol-Myers an Medarex?
Mein posting vom 14.7.09!!
Das ging aber schnell........
#3771 von Bioperle Benutzerinfo Nachricht an Benutzer Beiträge des Benutzers ausblenden 14.07.09 14:49:23 Beitrag Nr.: 37.569.083
Dieses Posting: versenden | melden Diskussion drucken
Folgende Antwort bezieht sich auf Beitrag Nr.: 37.567.798 im neuen Fenster öffnen von SLGramann am 14.07.09 12:19:34 Lieber SLGramann,
ich bin davon überzeugt dass Medarex-Technologie sich durchsetzt.
Bei so vielen Projekten mit potentiellen großen Pharmaunternehmen,muss Qualität in der Pipeline sein. Küsschen
Eine Übernahme ist gänzlich nie auszuschliessen.
Siehe dazu; mobile.wiwo.de/7val.fit/s_83e80fe62591edd863da5014d7b9d030/1…
14.7.2009 14:20
Johnson & Johnson kauft Cougar
.
Johnson & Johnson übernimmt für eine Milliarde Dollar das Biotechnologieunternehmen Cougar.
Pharmakonzerne sind derzeit auf der Suche nach Zukäufen in den Biotechbranche,
um sich angesichts anstehender Patentausläufe bei etablierten Medikamenten Nachschub zu sichern.

Schade,auch ich dachte da wäre mehr zu holen gewesen
- Welches Pharmaunternehmen könnte auch Interesse an einer Übernahme von Medarex haben?
Ich werde wohl weiter abwarten.

Antwort auf Beitrag Nr.: 37.629.309 von Bioperle am 23.07.09 10:29:34Da wird es bei dem Preis bleiben, weil die Übernahme ja abgesprochen ist. Es wird sicher keine Bieter mit Torschlusspanik geben.
Antwort auf Beitrag Nr.: 37.629.309 von Bioperle am 23.07.09 10:29:34Das Medarex Management hat den Merger vor. Die Aktionäre müssen dazu aber an BMY verkaufen. Was sie wohl auch tun werden, es sei denn es kommt noch ein anderer Bieter und bietet einen höheren Preis.
Ich mache schon sehr lange auf die Möglichkeit einer Übernahme aufmerksam. Bei diesem Preis - so er bleibt- muss man sich aber dennoch beraubt fühlen, da die Pipeline und Firma weit mehr wert ist.
Ich mache schon sehr lange auf die Möglichkeit einer Übernahme aufmerksam. Bei diesem Preis - so er bleibt- muss man sich aber dennoch beraubt fühlen, da die Pipeline und Firma weit mehr wert ist.
Antwort auf Beitrag Nr.: 37.629.329 von VaJo am 23.07.09 10:31:49Es gab schon häufiger Bietergefechte, obwohl das Management mit den Gegenseiten jeweils schon einig war.
Antwort auf Beitrag Nr.: 37.629.457 von Ville7 am 23.07.09 10:44:44Ja eben, die Aktionäre müssen erst mal an Bristol-Myers verkaufen. Ab wann gibt es einen Squeeze-Out? 95 %.
Die Übernahme kann zwar abgesprochen sein, wenn jetzt aber rein theoretisch keiner bereit wäre seine Anteile zu verkaufen, dann hat BMS Pech.
Ich glaub, der einzige Kandidat der noch Interesse an einer Übernahme hätte, wäre JNJ. Aber da hats doch mal schon Gerüchte gegeben, dass sie selber an BMS interessiert sind. Ich glaub im Yahoo-Msg Board hat jemand mal spekuliert, dass BMS zunächst MEDX übernimmt und JNJ sich mit BMS zusammenschließt. Teil 1 ist somit erledigt
Schade jedenfalls, die FDA Zulassung von Stelara hätten sie schon noch im Kurs abwarten können Dann wär wohl die 20 gefallen.
Dann wär wohl die 20 gefallen.
Die Übernahme kann zwar abgesprochen sein, wenn jetzt aber rein theoretisch keiner bereit wäre seine Anteile zu verkaufen, dann hat BMS Pech.
Ich glaub, der einzige Kandidat der noch Interesse an einer Übernahme hätte, wäre JNJ. Aber da hats doch mal schon Gerüchte gegeben, dass sie selber an BMS interessiert sind. Ich glaub im Yahoo-Msg Board hat jemand mal spekuliert, dass BMS zunächst MEDX übernimmt und JNJ sich mit BMS zusammenschließt. Teil 1 ist somit erledigt

Schade jedenfalls, die FDA Zulassung von Stelara hätten sie schon noch im Kurs abwarten können
 Dann wär wohl die 20 gefallen.
Dann wär wohl die 20 gefallen.
hallo,
das Ding ist gelaufen. Lest Euch mal die Pressemeldung durch. Da verpflichtet sich MEDX kein weiteres Angebot einzuholen.
das Ding ist gelaufen. Lest Euch mal die Pressemeldung durch. Da verpflichtet sich MEDX kein weiteres Angebot einzuholen.
Antwort auf Beitrag Nr.: 37.629.918 von pharmapro am 23.07.09 11:31:09Und? Heisst das, dass andere big pharmas kein Angebot mehr abgeben dürfen? Nein, also ist es prinzipiell noch nicht endgültig gelaufen. Gelaufen ist es, wenn BMY die Mehrheit an MEDX erringen kann.
Antwort auf Beitrag Nr.: 37.630.304 von Ville7 am 23.07.09 12:08:31Gelaufen ist es, wenn BMY die Mehrheit an MEDX erringen kann.
Dann ist nur die Selbständigkeit weg. Wenn genügend den Verkauf verweigern, kann Medx noch weiter an der Börse bleiben und Aktionäre auf nachbesserung und squeeze out hoffen.
Dann ist nur die Selbständigkeit weg. Wenn genügend den Verkauf verweigern, kann Medx noch weiter an der Börse bleiben und Aktionäre auf nachbesserung und squeeze out hoffen.
Antwort auf Beitrag Nr.: 37.630.351 von eck64 am 23.07.09 12:12:46Lieber eck64,
also endgültig ist noch nichts vollzogen.Oder habe ich dass falsch verstanden?
dass die Unternehmen haben einen endgültigen Fusionsvertrag
für den Erwerb von Medarex Medarex by Von Bristol-Myers Squibb Bristol-Myers Squibb
Wie Endgültig ist diese Aussage?
-Wieviel % hält BMB an Medarex?
-Wie hoch muß der prozentuale Anteil sein,ab wann kann man mit einem squeeze out hoffen?
-Wie lange zählt dass Angebot,und kann BMB vorher dieses zurückziehen?
Viele Fragen,ich bitte um viele ernstgemeinte Antworten.
also endgültig ist noch nichts vollzogen.Oder habe ich dass falsch verstanden?
dass die Unternehmen haben einen endgültigen Fusionsvertrag
für den Erwerb von Medarex Medarex by Von Bristol-Myers Squibb Bristol-Myers Squibb
Wie Endgültig ist diese Aussage?
-Wieviel % hält BMB an Medarex?
-Wie hoch muß der prozentuale Anteil sein,ab wann kann man mit einem squeeze out hoffen?
-Wie lange zählt dass Angebot,und kann BMB vorher dieses zurückziehen?
Viele Fragen,ich bitte um viele ernstgemeinte Antworten.

-Wer weiss wie die Aktionärsstruktur beschaffen ist?
-Wer hält wieviel prozent an Anteilen?
-Welches Pharmaunternehmen hält Anteile(Wieviel)?
Sollten nicht genügend Aktionäre auf dieses Angebot eingehen,ist mit einer Nachbesserung zu rechnen(auch ohne Mitbieter).
PS.Der Verfasser ist bei Medarex investiert.
-Wer hält wieviel prozent an Anteilen?
-Welches Pharmaunternehmen hält Anteile(Wieviel)?
Sollten nicht genügend Aktionäre auf dieses Angebot eingehen,ist mit einer Nachbesserung zu rechnen(auch ohne Mitbieter).

PS.Der Verfasser ist bei Medarex investiert.
könnte heulen, erst human jetzt medarex. die ganzen bioperlen von damals...
gratulation allen investierten

gratulation allen investierten
Antwort auf Beitrag Nr.: 37.630.624 von Bioperle am 23.07.09 12:40:22Under the terms of the definitive merger agreement, Bristol-Myers Squibb will commence a cash tender offer on or about July 27, 2009 to purchase all of the outstanding shares of Medarex common stock for $16.00 per share in cash. The closing of the tender offer is subject to customary terms and conditions, including the tender of a number of shares that, together with the number of shares already owned by Bristol-Myers Squibb, constitutes at least a majority of Medarex's outstanding shares of common stock (on a fully diluted basis) and expiration or termination of the waiting period under the Hart Scott Rodino Antitrust Improvement Act. The agreement also provides for the parties to effect, subject to customary conditions, a merger to be completed following the completion of the tender offer which would result in all shares not tendered in the tender offer being converted into the right to received $16.00 per share in cash. The merger agreement contains a provision under which Medarex has agreed not to solicit any competing offers for the company. Bristol-Myers Squibb will finance the acquisition from its existing cash resources. The companies expect the tender offer to close in approximately thirty (30) days after commencement of the tender offer.
**************
Für mich der interessante Teil der PR
Frage an die Experten hier: Kennt sich jemand mit dem definitive merger agreement aus? Was bedeutet das nun genau?
....a merger to be completed following the completion of the tender offer which would result in all shares not tendered in the tender offer being converted into the right to received $16.00 per share in cash...
gleich bedeutend mit einem Squeeze-Out zu 16.00 $???
und MEDX hat sich verpflichtet keine weiteren Angebote aktiv einzuholen. --> heißt für mich aber sehr wohl, dass es zu weiteren "unfreiwilligen" Angeboten kommen könnte!?!
Alles in allem ist das trotzdem sehr verwirrend für mich. Auch im YahooMsg Board ist man sich nicht einig, was dieses Angebot nun wirklich bedeutet.
Vielleicht kann einer der Experten hier Licht ins Dunkel bringen. THX
lg
Lycos
**************
Für mich der interessante Teil der PR

Frage an die Experten hier: Kennt sich jemand mit dem definitive merger agreement aus? Was bedeutet das nun genau?
....a merger to be completed following the completion of the tender offer which would result in all shares not tendered in the tender offer being converted into the right to received $16.00 per share in cash...
gleich bedeutend mit einem Squeeze-Out zu 16.00 $???

und MEDX hat sich verpflichtet keine weiteren Angebote aktiv einzuholen. --> heißt für mich aber sehr wohl, dass es zu weiteren "unfreiwilligen" Angeboten kommen könnte!?!
Alles in allem ist das trotzdem sehr verwirrend für mich. Auch im YahooMsg Board ist man sich nicht einig, was dieses Angebot nun wirklich bedeutet.
Vielleicht kann einer der Experten hier Licht ins Dunkel bringen. THX
lg
Lycos
Hallo Leute.
Ja wer hier bei 3,50 Dollar ein ist hat nen guten Deal gemacht.Die die gestern eingestiegen sind finden es sicherlich zu wenig obwohl 50% innerhalb von 24 Stunden ist doch auch OK.
Bei MEDX ist denke ich jetzt Kurstechnisch alles gelaufen.So wie ich es verstanden habe will MEDX such kein anderes Angebot einholen also wird es zu dem Deal kommen.
Also Glückwunsch an alle die hier Gewinne erzielt haben.
Ich weiße euch aber auch auf eine eventuell andere Chance im Biotechbereich hin.
Soll keine Empfehlung sein aber für die Watch ist doch imemr gut Tips zu bekommen.Ob man einsteigt oder nciht muß jeder selber wissen.
Es handelt sich um Antigenics(AGEN)(US0370321095).
Anfang Juni gabs schon nen fetten Anstieg und gestern zog das Volumen ohne Grund wieder heftigst an.
Schauts Euch an dort könnte denke ich GSK vielelicht zuschlagen die schon mit AGEN in kooperation stehen.
Ja wer hier bei 3,50 Dollar ein ist hat nen guten Deal gemacht.Die die gestern eingestiegen sind finden es sicherlich zu wenig obwohl 50% innerhalb von 24 Stunden ist doch auch OK.
Bei MEDX ist denke ich jetzt Kurstechnisch alles gelaufen.So wie ich es verstanden habe will MEDX such kein anderes Angebot einholen also wird es zu dem Deal kommen.
Also Glückwunsch an alle die hier Gewinne erzielt haben.
Ich weiße euch aber auch auf eine eventuell andere Chance im Biotechbereich hin.
Soll keine Empfehlung sein aber für die Watch ist doch imemr gut Tips zu bekommen.Ob man einsteigt oder nciht muß jeder selber wissen.
Es handelt sich um Antigenics(AGEN)(US0370321095).
Anfang Juni gabs schon nen fetten Anstieg und gestern zog das Volumen ohne Grund wieder heftigst an.
Schauts Euch an dort könnte denke ich GSK vielelicht zuschlagen die schon mit AGEN in kooperation stehen.
Medarex komplett für 2,1 Milliarden Dollar
Insgesamt beläuft sich der Kaufpreis damit auf 2,4 Milliarden Dollar. Medarex bringt rund 300 Millionen Dollar an Cash mit in die Liaison.
Das ist das absolute Schnäppchen...


-Pfizer macht 68 Milliarden für Wyeth locker.
für Wyeth locker.
-Merck will für rund 41,1 Milliarden Dollar den kleineren US-Rivalen Schering-Plough übernehmen.
-Roche übernimmt Genentech ganz
Roche hat die seit längerem angestrebte Komplettübernahme seiner Biotechnologie-Tochter Genentech so gut wie abgeschlossen. Die Schweizer erhöhten ihr Angebot auf 95 $ je Aktie. Im Gegenzug gibt der Sonderausschuss des Genentech-Verwaltungsrates seine Blockadehaltung auf und empfiehlt den eigenen Aktionären, ihre Titel zu verkaufen. Das Angebot beläuft sich auf insgesamt rund 46,8 Mrd. $

Insgesamt beläuft sich der Kaufpreis damit auf 2,4 Milliarden Dollar. Medarex bringt rund 300 Millionen Dollar an Cash mit in die Liaison.
Das ist das absolute Schnäppchen...



-Pfizer macht 68 Milliarden
 für Wyeth locker.
für Wyeth locker.-Merck will für rund 41,1 Milliarden Dollar den kleineren US-Rivalen Schering-Plough übernehmen.
-Roche übernimmt Genentech ganz
Roche hat die seit längerem angestrebte Komplettübernahme seiner Biotechnologie-Tochter Genentech so gut wie abgeschlossen. Die Schweizer erhöhten ihr Angebot auf 95 $ je Aktie. Im Gegenzug gibt der Sonderausschuss des Genentech-Verwaltungsrates seine Blockadehaltung auf und empfiehlt den eigenen Aktionären, ihre Titel zu verkaufen. Das Angebot beläuft sich auf insgesamt rund 46,8 Mrd. $
Antwort auf Beitrag Nr.: 37.631.946 von Bioperle am 23.07.09 15:08:19Ja, der übernommene cash dient der Finanzierung.
Morphosys hat auf 370 mio Marktkap. zur Zeit wahrscheinlich deutlich über 140 mio€ cash.
Der Finanzmarkt macht Schnäppchen für Pharmas möglich.
Morphosys hat auf 370 mio Marktkap. zur Zeit wahrscheinlich deutlich über 140 mio€ cash.
Der Finanzmarkt macht Schnäppchen für Pharmas möglich.

Antwort auf Beitrag Nr.: 37.632.007 von eck64 am 23.07.09 15:14:22$16.00 per share in cash. The transaction, with an aggregate purchase
price of approximately$2.4 billion
www.medarex.com/cgi-local/item.pl/20090722-1310338
Laut Übereinkunft zahlt BMS 16 US-Dollar pro Aktie, insgesamt kostet die Akquisition damit rund 2,4 Milliarden US-Dollar.
www.apotheke-adhoc.de/Nachrichten/Markt/7072.html
Ist schon komisch,kann Medarex nicht rechnen oder wars ein Druckfehler (160 $) ?
?
Oder hab ich da etwas falsch verstanden?
price of approximately$2.4 billion

www.medarex.com/cgi-local/item.pl/20090722-1310338
Laut Übereinkunft zahlt BMS 16 US-Dollar pro Aktie, insgesamt kostet die Akquisition damit rund 2,4 Milliarden US-Dollar.
www.apotheke-adhoc.de/Nachrichten/Markt/7072.html
Ist schon komisch,kann Medarex nicht rechnen oder wars ein Druckfehler (160 $)
 ?
?Oder hab ich da etwas falsch verstanden?
hätte ich meine im August 2007 gekauften Aktien behalten hätte ich etwa 15 % Minus gemacht. Also einfaches Buy and Hold war auch hier nicht erfolgreich. Kann man nur hoffen, das alles bei Morphosys besser läuft.
Irgendwie kann man kaum glauben, das die Fa. dafür über den Tisch geht. Bescheuertes Management.
Irgendwie kann man kaum glauben, das die Fa. dafür über den Tisch geht. Bescheuertes Management.
Antwort auf Beitrag Nr.: 37.633.377 von riverstar_de am 23.07.09 17:02:39Hallo riverstar,



(bezieht sich auf den Übernahmepreis)
buy and hold alleine würde ich für Bios auch nicht empfehlen. Bei Firmen, die ich für gut halte und auch in größerem Umfang kaufe, habe ich auch immer wieder einen Teil der Aktien (fast immer erfolgreich) getradet, also zu Kursen, die mir niedrig vorkamen, gekauft und wenn sie mir hoch vorkamen verkauft. Die Vola ist ja oft hoch und ein Blick auf Langfristcharts oft hilfreich. Natürlich muß man vom Konzept überzeugt sein. Habe aber dann immer einen Teil behalten für die Fälle a) Erfolg/Zulassung b) Übernahme.

MEDX habe ich immer wieder gekauft und verkauft und dabei ordentlich Gewinn gemacht, so dass das Halten der "Core"-Position psychologisch leichter fiel. Wurde in diesem Falle mal belohnt (oder auch nicht, habe MEDX auch schon für 12€ verkauft vorletztes Jahr).
Gruß q.



(bezieht sich auf den Übernahmepreis)
buy and hold alleine würde ich für Bios auch nicht empfehlen. Bei Firmen, die ich für gut halte und auch in größerem Umfang kaufe, habe ich auch immer wieder einen Teil der Aktien (fast immer erfolgreich) getradet, also zu Kursen, die mir niedrig vorkamen, gekauft und wenn sie mir hoch vorkamen verkauft. Die Vola ist ja oft hoch und ein Blick auf Langfristcharts oft hilfreich. Natürlich muß man vom Konzept überzeugt sein. Habe aber dann immer einen Teil behalten für die Fälle a) Erfolg/Zulassung b) Übernahme.

MEDX habe ich immer wieder gekauft und verkauft und dabei ordentlich Gewinn gemacht, so dass das Halten der "Core"-Position psychologisch leichter fiel. Wurde in diesem Falle mal belohnt (oder auch nicht, habe MEDX auch schon für 12€ verkauft vorletztes Jahr).
Gruß q.
Ich könnte mir vorstellen, BMS ist schon großteils durch:

80 mio Stücke sind heute auch zu Kursen von fast 16 gekauft worden, bei einem Bestand von 120 mio Aktien. Ok, ein paar mio shorties, die müssen praktisch doppelt gekauft werden. Aber es würde mich sehr wundern, wenn BMS nicht morgen schon die Mehrheit hätte. Das heißt allerdings nicht, das es nicht trotzdem zu einem squeeze out in einigen Monaten kommen könnte. Denn 100% sammelt man nie an der Börse ein.
80 mio Stücke sind heute auch zu Kursen von fast 16 gekauft worden, bei einem Bestand von 120 mio Aktien. Ok, ein paar mio shorties, die müssen praktisch doppelt gekauft werden. Aber es würde mich sehr wundern, wenn BMS nicht morgen schon die Mehrheit hätte. Das heißt allerdings nicht, das es nicht trotzdem zu einem squeeze out in einigen Monaten kommen könnte. Denn 100% sammelt man nie an der Börse ein.
Antwort auf Beitrag Nr.: 37.633.354 von Bioperle am 23.07.09 17:00:49Deshalb http://de.wikipedia.org/wiki/Billion, oder

Antwort auf Beitrag Nr.: 37.627.788 von Friseuse am 23.07.09 04:47:58
Ich wiederhole nochmals Friseuses Post:
"Auf der langfristigen Nahtstelle wird Medarex übernommen, für Investoren nichts gerissen. Die Lehre ist die von der Leere der Aktionäre, dem langen Atem von Big Pharma"
Das ist die bittere Wahrheit für Langfristanleger! Über lange Jahre haben diese Eigentümer Geld und Zeit investiert und am Ende keinen Return erzielt. Dass man mit Traden oder einem glücklich-späten Einstieg durchaus etwas verdienen konnte, ist dabei absolut kein taugliches Gegenargument. 16 Dollar kostete die Aktie auch schon im Januar 2002. Die Früchte der operativen Fortschritte der letzten sieben Jahre gehen indes nun an andere.
Das gibt Anlass, über einige Dinge grundsätzlich nachzudenken... Zum Beispiel darüber, ob man mit Morphosys in 7 oder 10 Jahren eine ähnliches Ergebnis erzielen wird, wie man es mit Medarex zw. 2002 und 2009 erzielt hätte...
Ich wiederhole nochmals Friseuses Post:
"Auf der langfristigen Nahtstelle wird Medarex übernommen, für Investoren nichts gerissen. Die Lehre ist die von der Leere der Aktionäre, dem langen Atem von Big Pharma"
Das ist die bittere Wahrheit für Langfristanleger! Über lange Jahre haben diese Eigentümer Geld und Zeit investiert und am Ende keinen Return erzielt. Dass man mit Traden oder einem glücklich-späten Einstieg durchaus etwas verdienen konnte, ist dabei absolut kein taugliches Gegenargument. 16 Dollar kostete die Aktie auch schon im Januar 2002. Die Früchte der operativen Fortschritte der letzten sieben Jahre gehen indes nun an andere.
Das gibt Anlass, über einige Dinge grundsätzlich nachzudenken... Zum Beispiel darüber, ob man mit Morphosys in 7 oder 10 Jahren eine ähnliches Ergebnis erzielen wird, wie man es mit Medarex zw. 2002 und 2009 erzielt hätte...
Antwort auf Beitrag Nr.: 37.637.392 von SLGramann am 24.07.09 07:24:02genau das ist der Punkt und wenn es dem Management nicht gelingt Aufmerksamkeit und Vertrauen bei Anlegern zu gewinnen und dadurch zwischenzeitlich schon den Kurs entsprechend hochzubekommen, dann wird man eben billig abgefunden.
Ein bisschen Angst habe ich ja schon bei Morphosys, das das auch nicht viel besser wird. Aber mit 33 EUR steht man ja schon ganz gut da. Eine solche Rendite ist ja nicht so schlecht.
Ein bisschen Angst habe ich ja schon bei Morphosys, das das auch nicht viel besser wird. Aber mit 33 EUR steht man ja schon ganz gut da. Eine solche Rendite ist ja nicht so schlecht.
Antwort auf Beitrag Nr.: 37.639.187 von riverstar_de am 24.07.09 11:22:11
Ein bisschen Angst habe ich ja schon bei Morphosys, das das auch nicht viel besser wird. Aber mit 33 EUR steht man ja schon ganz gut da. Eine solche Rendite ist ja nicht so schlecht.
Nun ja, dabei ist aber zu bedenken, dass Medarex zu einem Zeitpunkt aufgekauft wird, wo erhebliche Tantiemen-Zahlungen sicher sind (Stelara und Simponi) und mit Ipilimumab eine Chance bestanden hätte, in eine ganz andere Dimension zu wachsen. Dass diese Chance vielleicht besser war, als ich zuletzt glauben wollte, dafür spricht die jetzige Übernahme durch BMY.
Bei Morphosys sind ähnliche Pipeline-Erfolge in absehbarer Zeit einfach nicht erkennbar. Eines Tages wird es soweit sein, aber ein "Morphosys-Simponi" ist mindestens 7 Jahre weit in der Zukunft - vielleicht aber auch 10 oder 20 Jahre...
Wenn dann zu 33 übernommen wird, ist die (Jahres)Rendite bescheiden.
-----------------
Zum Preis für Medarex:
Man kann sich ja mal fragen, was allein schon die abgezinsten Tantiemen für Stelara und Simponi wert sein könnten. Je nach Szenario kann man da natürlich sonst was ausrechnen, aber irgendwas zwischen 500 Mio. und 1,5 Mrd. Dollar könnte realistisch sein. Auch der Rest der Pipeline und der Tantiemen-Rechte von Medarex ist nicht nichts wert. Ich gehe deshalb davon aus, dass BMY de facto die Ipilimumab-Rechte so ziemlich für lau bekommen hat. Sollte der Wirkstoff am Ende erfolgreich sein, sind die Medarex-Aktionäre gerade um die ein oder andere Milliarde Marktkapitalisierung betrogen worden.
Ein bisschen Angst habe ich ja schon bei Morphosys, das das auch nicht viel besser wird. Aber mit 33 EUR steht man ja schon ganz gut da. Eine solche Rendite ist ja nicht so schlecht.
Nun ja, dabei ist aber zu bedenken, dass Medarex zu einem Zeitpunkt aufgekauft wird, wo erhebliche Tantiemen-Zahlungen sicher sind (Stelara und Simponi) und mit Ipilimumab eine Chance bestanden hätte, in eine ganz andere Dimension zu wachsen. Dass diese Chance vielleicht besser war, als ich zuletzt glauben wollte, dafür spricht die jetzige Übernahme durch BMY.
Bei Morphosys sind ähnliche Pipeline-Erfolge in absehbarer Zeit einfach nicht erkennbar. Eines Tages wird es soweit sein, aber ein "Morphosys-Simponi" ist mindestens 7 Jahre weit in der Zukunft - vielleicht aber auch 10 oder 20 Jahre...
Wenn dann zu 33 übernommen wird, ist die (Jahres)Rendite bescheiden.
-----------------
Zum Preis für Medarex:
Man kann sich ja mal fragen, was allein schon die abgezinsten Tantiemen für Stelara und Simponi wert sein könnten. Je nach Szenario kann man da natürlich sonst was ausrechnen, aber irgendwas zwischen 500 Mio. und 1,5 Mrd. Dollar könnte realistisch sein. Auch der Rest der Pipeline und der Tantiemen-Rechte von Medarex ist nicht nichts wert. Ich gehe deshalb davon aus, dass BMY de facto die Ipilimumab-Rechte so ziemlich für lau bekommen hat. Sollte der Wirkstoff am Ende erfolgreich sein, sind die Medarex-Aktionäre gerade um die ein oder andere Milliarde Marktkapitalisierung betrogen worden.
Antwort auf Beitrag Nr.: 37.640.171 von SLGramann am 24.07.09 13:17:10Sollte der Wirkstoff am Ende erfolgreich sein, sind die Medarex-Aktionäre gerade um die ein oder andere Milliarde Marktkapitalisierung betrogen worden.
Definitiv. Nicht nur die Pipe, die den Umfang dessen eines kleinen Pharmas hat, aber auch die führende Technologie sind m.E. mindestens 5Mrd USD wert. Dieser Merger ist ein Betrug an den Aktionären und die Verbrecher heissen Pien und Co.
Definitiv. Nicht nur die Pipe, die den Umfang dessen eines kleinen Pharmas hat, aber auch die führende Technologie sind m.E. mindestens 5Mrd USD wert. Dieser Merger ist ein Betrug an den Aktionären und die Verbrecher heissen Pien und Co.
Antwort auf Beitrag Nr.: 37.641.059 von Ville7 am 24.07.09 14:51:53Lieber Ville7,
was meinst Du?
Muss BMS Ihr Angebot an die Medarex Aktionäre erhöhen ,falls nicht die gewünschte prozentuale Anlegerscharr ,zu 16 Dollar verkauft??
was meinst Du?
Muss BMS Ihr Angebot an die Medarex Aktionäre erhöhen ,falls nicht die gewünschte prozentuale Anlegerscharr ,zu 16 Dollar verkauft??
Antwort auf Beitrag Nr.: 37.640.171 von SLGramann am 24.07.09 13:17:10Deine Preisüberschläge zu Medx kann ich nachvollziehen. Auch mir ist unverständlich, warum man sich bereits jetzt, zu diesem Preis und vor allem im Einverständnis übernehmen lässt. Immerhin hatte man cash genug um sorgenfrei die nächsten Schritte zu gehen, partielle Deals abzuschliessen. Wenn jetz gerade eine neue große KE angestanden hätte um sich am Leben zu erhalten, dann hätte man es vielleicht anders sehen können, aber so?
Die 5 mrd über villes Daumen wären auch meiner Meinung nach angemessener gewesen.
xxxxxxxxx
Was ich aber nicht ganz so sehe wie du:
Bei Morphosys sind ähnliche Pipeline-Erfolge in absehbarer Zeit einfach nicht erkennbar. Eines Tages wird es soweit sein, aber ein "Morphosys-Simponi" ist mindestens 7 Jahre weit in der Zukunft - vielleicht aber auch 10 oder 20 Jahre...
7, 10 oder 20 Jahre?
Wo bringst du solche Zeiträume her? Vor 20 Jahren gabs MEDX noch nicht, oder?
Aktuell sind 7 Projekte in der Klinik. Die sollten sich alle im Zeitraum der nächsten 7 Jahre entschieden haben, ob sie was taugen oder nicht. Und alles murks davon wäre eine selbst für Medikamentenentwickler extrem miese Quote.
Die 5 mrd über villes Daumen wären auch meiner Meinung nach angemessener gewesen.
xxxxxxxxx
Was ich aber nicht ganz so sehe wie du:
Bei Morphosys sind ähnliche Pipeline-Erfolge in absehbarer Zeit einfach nicht erkennbar. Eines Tages wird es soweit sein, aber ein "Morphosys-Simponi" ist mindestens 7 Jahre weit in der Zukunft - vielleicht aber auch 10 oder 20 Jahre...
7, 10 oder 20 Jahre?

Wo bringst du solche Zeiträume her? Vor 20 Jahren gabs MEDX noch nicht, oder?
Aktuell sind 7 Projekte in der Klinik. Die sollten sich alle im Zeitraum der nächsten 7 Jahre entschieden haben, ob sie was taugen oder nicht. Und alles murks davon wäre eine selbst für Medikamentenentwickler extrem miese Quote.
Antwort auf Beitrag Nr.: 37.641.293 von eck64 am 24.07.09 15:14:58 Bei Morphosys sind ähnliche Pipeline-Erfolge in absehbarer Zeit einfach nicht erkennbar. Eines Tages wird es soweit sein, aber ein "Morphosys-Simponi" ist mindestens 7 Jahre weit in der Zukunft - vielleicht aber auch 10 oder 20 Jahre...
Lieber eck64,
Diese Behauptung stammt nicht von mir.
LG Bio
Lieber eck64,
Diese Behauptung stammt nicht von mir.
LG Bio
Antwort auf Beitrag Nr.: 37.641.330 von Bioperle am 24.07.09 15:20:30Keine Panik,
ich habe mich direkt auf SLGrammans posting bezogen.
ich habe mich direkt auf SLGrammans posting bezogen.

Antwort auf Beitrag Nr.: 37.641.293 von eck64 am 24.07.09 15:14:58Wo bringst du solche Zeiträume her?

Erstens wollte ich provozieren.
Zweitens ist das Problem, dass nicht nur "was durchkommen muss", sondern dass es auch um eine fette Indikation + überlegenes Profil gehen muss, um so etwas wie Simponi zu haben (was Du ja alles selber weißt). Aber gut - vielleicht wird schon der erste Schuss ein Volltreffer (R1450). Das ist ja zumindest denkbar und dann wäre Morphosys schon in 5 Jahren(?) an dem Punkt, an dem Medarex jetzt ist.
Was Medarex angeht: Unter den gegebenen Umständen (bspw. die Haltung des Managements) ist es wohl leider eher unwahrscheinlich, dass sich in Aktionärskreisen ein wirksamer Widerstand formieren wird. Im US-Recht kenne ich mich nicht aus, weiß aber zumindest, dass es wesentlich auf Richterrecht basiert. Das gilt wohl auch für einen squeeze out bzw. freeze out. Mit 90% Eigentumsanteilen, kann BMY wahrscheinlich den "Rest" gegen Barabfindung rausdrängen.
Einiges dazu kann man hier lesen (ab Seite 59):
http://books.google.de/books?id=hiQYLoitEbkC&pg=PA59&lpg=PA5…

Erstens wollte ich provozieren.
Zweitens ist das Problem, dass nicht nur "was durchkommen muss", sondern dass es auch um eine fette Indikation + überlegenes Profil gehen muss, um so etwas wie Simponi zu haben (was Du ja alles selber weißt). Aber gut - vielleicht wird schon der erste Schuss ein Volltreffer (R1450). Das ist ja zumindest denkbar und dann wäre Morphosys schon in 5 Jahren(?) an dem Punkt, an dem Medarex jetzt ist.
Was Medarex angeht: Unter den gegebenen Umständen (bspw. die Haltung des Managements) ist es wohl leider eher unwahrscheinlich, dass sich in Aktionärskreisen ein wirksamer Widerstand formieren wird. Im US-Recht kenne ich mich nicht aus, weiß aber zumindest, dass es wesentlich auf Richterrecht basiert. Das gilt wohl auch für einen squeeze out bzw. freeze out. Mit 90% Eigentumsanteilen, kann BMY wahrscheinlich den "Rest" gegen Barabfindung rausdrängen.
Einiges dazu kann man hier lesen (ab Seite 59):
http://books.google.de/books?id=hiQYLoitEbkC&pg=PA59&lpg=PA5…
Antwort auf Beitrag Nr.: 37.642.224 von SLGramann am 24.07.09 16:47:49Morphosys-Pipelinepotentiale und -Zeithorizonte zu diskutieren im Medx-Thread ist eigentlich nicht der richtige Platz. 
Aber wenns bei Medx hauptsächlich nur noch um squeeze out oder nicht geht, ist vielleicht auch angrenzendes akzeptabel.
R1450 ist zwar als erster der laufenden Programme in die Klinik gekommen, aber der erste Kandidate für Zulassung wirds wohl eer nicht.
Ich denke, das selbst MOR103 R1450 abhängt, vom Zeitraum her.
Ordentlich Tempo macht Novartis, Centocor eher langwierig:
Novartis:
[urlA Study to Assess BHQ880 in Combination With Zoledronic Acid in Relapsed or Refractory Myeloma Patients]http://www.clinicaltrials.gov/ct2/show/NCT00741377?term=novartis+bhq&rank=1[/url]
Estimated Enrollment: 267
Study Start Date: January 2009
Estimated Primary Completion Date: November 2010 (Final data collection date for primary outcome measure)
Aktuell 7 Kliniken.
Centocor:
[urlA Study to Evaluate the Safety and Effectiveness of CNTO 888 Administered Intravenously (IV) in Subjects With Idiopathic Pulmonary Fibrosis (IPF)]http://clinicaltrials.gov/ct2/show/NCT00786201?term=cnto+888&rank=1[/url]
Estimated Enrollment: 120
Study Start Date: October 2008
Estimated Study Completion Date: June 2012
Estimated Primary Completion Date: February 2012 (Final data collection date for primary outcome measure)
2012, obwohl 30 Kliniken beteiligt sind!
Insofern könnte Morphosys mit MOR103 auch an CNTO888 vorbeiziehen. Die wollen möglichst 2010 noch die erste Studie mit 135 Patienten abschliessen.
Aber CNTO888 läuft ja auch seit August 2007 in einer Krebsstudie, wer weiß, was da für Zeiträume realistisch sind.
Ich hoffe doch sehr, das man vor 2016 was sieht.
Abgesehen davon: Medarex kommt zum 5 fachen Preis von MOR weg, und das halte ich für zu billig, das doppelte wäre eigentlich durchaus angemessen.
Also wenn sich MOR in den nächsten 5 bis 7 Jahren verzehnfacht, dann wäre es jedenfalls nicht so schlimm.

Aber wenns bei Medx hauptsächlich nur noch um squeeze out oder nicht geht, ist vielleicht auch angrenzendes akzeptabel.
R1450 ist zwar als erster der laufenden Programme in die Klinik gekommen, aber der erste Kandidate für Zulassung wirds wohl eer nicht.
Ich denke, das selbst MOR103 R1450 abhängt, vom Zeitraum her.
Ordentlich Tempo macht Novartis, Centocor eher langwierig:
Novartis:
[urlA Study to Assess BHQ880 in Combination With Zoledronic Acid in Relapsed or Refractory Myeloma Patients]http://www.clinicaltrials.gov/ct2/show/NCT00741377?term=novartis+bhq&rank=1[/url]
Estimated Enrollment: 267
Study Start Date: January 2009
Estimated Primary Completion Date: November 2010 (Final data collection date for primary outcome measure)
Aktuell 7 Kliniken.
Centocor:
[urlA Study to Evaluate the Safety and Effectiveness of CNTO 888 Administered Intravenously (IV) in Subjects With Idiopathic Pulmonary Fibrosis (IPF)]http://clinicaltrials.gov/ct2/show/NCT00786201?term=cnto+888&rank=1[/url]
Estimated Enrollment: 120
Study Start Date: October 2008
Estimated Study Completion Date: June 2012
Estimated Primary Completion Date: February 2012 (Final data collection date for primary outcome measure)
2012, obwohl 30 Kliniken beteiligt sind!
Insofern könnte Morphosys mit MOR103 auch an CNTO888 vorbeiziehen. Die wollen möglichst 2010 noch die erste Studie mit 135 Patienten abschliessen.
Aber CNTO888 läuft ja auch seit August 2007 in einer Krebsstudie, wer weiß, was da für Zeiträume realistisch sind.

Ich hoffe doch sehr, das man vor 2016 was sieht.

Abgesehen davon: Medarex kommt zum 5 fachen Preis von MOR weg, und das halte ich für zu billig, das doppelte wäre eigentlich durchaus angemessen.
Also wenn sich MOR in den nächsten 5 bis 7 Jahren verzehnfacht, dann wäre es jedenfalls nicht so schlimm.

Antwort auf Beitrag Nr.: 37.641.156 von Bioperle am 24.07.09 15:01:06Muss BMS Ihr Angebot an die Medarex Aktionäre erhöhen ,falls nicht die gewünschte prozentuale Anlegerscharr ,zu 16 Dollar verkauft
Diese Frage erübrigt sich. Das wird gar nicht das Thema sein. Ich rechne fest mit einem Konkurrenzangebot deutlich über 16 Dollar in den nächsten 1-3 Wochen. Kommen ja nur ganz wenige weitere Bieter aus dem Onkologiebereich infrage, die sich Medarex nicht von BMS (eigentlich selbst schon immer ein Übernahmekandidat) wegschnappen lassen werden.
Also schön die Aktien behalten.
Diese Frage erübrigt sich. Das wird gar nicht das Thema sein. Ich rechne fest mit einem Konkurrenzangebot deutlich über 16 Dollar in den nächsten 1-3 Wochen. Kommen ja nur ganz wenige weitere Bieter aus dem Onkologiebereich infrage, die sich Medarex nicht von BMS (eigentlich selbst schon immer ein Übernahmekandidat) wegschnappen lassen werden.

Also schön die Aktien behalten.
2,4 Mrd USD sind kein so schlechter Preis, finde ich...
ob Ipilimumab ein Erfolg wird, ist immer noch sehr unsicher und die bisherigen Royalties könnten niedriger ausfallen, als manche hoffen.
Die Royalties für Simponi und Stelara (Ilaris kann man bisher vernachlässigen) dürften zwischen 2-3% betragen. Simponi tritt hier u.a. gegen das etablierte Embrel an und Stelara gegen Humira. Bei z.B. 500 Mio USD für Simponi und 1 Mrd USD für Embrel peak sales wären das über 10 Jahre maximale Umsätze in Summe 15 Mrd USD, von denen Medarex 2-3% erhält... also 300 bis 450 Mio USD, die in diesem Fall diese beiden Produkte Medarex innerhalb der nächsten 15 Jahre einbringen würden. Im Vergleich zu den jetzt gezahlten 2,4 Mrd USD scheint das nicht der Hauptgrund für die Übernahme gewesen zu sein. PDLI hat mit Royalties von u.a. Avastin, Herceptin, Synagis, Lucentis, Tysabri dieses Jahr einen Umsatz von vielleicht 330 Mio USD bei einem aktuellen KGV10e von schwachen 6,5(!). Royalties alleine bringen es offensichtlich nicht... PDLI ist damit gerade mal 1 Mrd USD (MK) wert.
z.B. ein Kommentar von Ohad Hammer, der eigentlich kompentent erscheint... http://www.hammerstockblog.com/micromet-%e2%80%93-the-plot-t…
"I really want to be bullish on MEDX but I just don’t find enough reasons. Theoreticallly, they have many shots on goals but their pipeline is not too impressive. Of course this could change if even one antibody shows good results in clinical testing. The approval of Stelara is a positive development especially after Genentech withdrew Raptiva of the market. Golimumab is more tricky since there is a multitude of anti TNF agents out there."
oder http://www.thestreet.com/story/10484664/1/biotech-stock-mail…
"Adam: What do you think of Johnson & Johnson's(JNJ Quote) golimumab for first-pass FDA approval on April 29? Also, Stelara should be approved any day... I believe this may be a game changer for Medarex(MEDX Quote). These approvals should provide enough royalties to limit the need for additional funding and may spark a take-out by J&J or price war with Bristol-Myers Squibb(BMY Quote). With updated survival from ipilimumab at ASCO, I believe Bristol will move to buy Medarex this summer. They do not want to wind up in another ImClone situation." Charles is a fervent Medarex bull with a persuasive argument for owning the stock now. I know because he and I had a lengthy email discussion about Medarex earlier this week.
Golimumab, for treating rheumatoid arthritis, and Stelara, for moderate to severe plaque psoriasis, each have the potential to be billion-dollar drugs for J&J. Both drugs were created using Medarex's humanized monoclonal antibody technology, which entitles the company to a low single-digit royalty on sales -- call it 3%.
If one or both of these J&J drugs achieves peak annual sales in the $3 billion to $4 billion range of market leaders Enbrel, sold by Amgen(AMGN Quote), or Abbott Lab's(ABT Quote) Humira, then the royalty revenue flowing back to Medarex is substantial.
Charles' estimate of Medarex's Stelara royalties alone tops $100 million a year.
His math pencils out OK, but I do worry that he overestimates the peak revenue potential for both Stelara and golimumab. Both seem like strong drugs, but so are Enbrel and Humira. It's not going to be easy to unseat well-entrenched drugs like Enbrel and Humira, especially since both drugs are considered very safe for patients. Stelara and golimumab may be as safe, but they lack the years of data to prove it.
This exact point was made by two rheumatologists speaking last month on a panel at a health care conference sponsored by Cowen & Co. Both doctors believed that drugs like golimumab (Stelara didn't come up specifically) would be fighting for second- or third-line treatment. Neither was enthusiastic at all about swapping out a new drug for either Humira or Enbrel any time soon.
Couple this conservatism on the part of doctors with a recession-fueled pullback in the use of all expensive biologic drugs to treat auto-immune diseases like rheumatoid arthritis (which I wrote about this week), and you've got plenty of reasons to be cautious about assuming huge royalty revenue flowing into Medarex's coffers. I don't want to leave the impression that the approval of golimumab and/or Stelara isn't positive for Medarex. Both drugs will bring non-dilutive cash to the company which is definitely a plus in this market environment. Moreover, the approval of either drug will validate Medarex's antibody technology platform, another good thing.
But for Medarex to be truly successful, the company must become more than just the next PDL Biopharma(PDLI Quote) or Xoma(XOMA Quote). Both of these companies have been disappointments. They collect royalty revenues on other companies' successful drugs but have never been able to develop drugs successfully on their own.
Charles believes that ipilimumab, Medarex's melanoma drug (partnered with Bristol-Myers Squibb) may be that internally developed drug that gets Medarex really moving. I have my serious doubts about that, based on the uninspiring data released so far.
And let's not forget the lameness of Medarex's management team, which seems incapable of doing anything right. Honestly, CEO Howard Pien is like a black hole -- shareholder value goes in, but never comes out.
At around $5.50 a share (a $700 million market cap), Medarex is already getting credit for some of the anticipated royalties from golimumab and Stelara. As one analyst said to me this week, think of that royalty stream as a backstop on Medarex's current valuation and not so much as a future growth driver for the stock price. That will come if Medarex can successfully develop its internal pipeline of drug candidates. And on that front, I'm definitely in wait-and-see mode."
jetzt sind es nicht 5,5 USD sondern 16 USD geworden...
nach dieser Schätzung soll Humira 2014 9 Mrd USD Jahresumsatz haben und Embrel 6,5 Mrd USD:
http://www.fiercebiotech.com/pages/top-10-products-sales-201…
es ist nicht einfach gegen etablierte Produkte anzukommen.
********
und dann zu Ipilimumab... warum gibt es hier so große Zuversicht? Ich denke eher, dass hier BMS einiges riskiert, ein kompletter Fehlschlag ist nicht ausgeschlossen. Die folgenden Punkte sprechen eher nicht für Ipilimumab:
- Ipilimumab ist bereits in PIII-Studien bei fortgeschittenem Hautkrebs gescheitert
- die FDA hat auf Basis der bisherigen Daten Ipilimumab nicht zugelassen
- fortgeschittener Hautkrebs ist eine extrem schwer zu behandelnde Indikation, in der bereits viele Kandidaten, die in der PII erfolgreich aussahen, am Ende gescheitert sind (andererseits besteht daher auch ein großer Bedarf)
- Ipilimumab wirkt über das Immunsystem... die meisten ähnlichen Ansätze sind bisher gescheitert
- die PIII ist eine Kombi mit Chemo, die sich theoretisch negativ auf den Ansatz Stimulation des Immunsystems auswirkt (die Chemo unterdrückt das Immunsystem, so dass es schwerer stimuliert werden kann)
- bisher gibt es, soweit ich das sehe, nur PII Daten, die auf eine Verbesserung der Überlebenszeit hindeuten. PII-Daten sind aber sehr unzuverlässig.
insgesamt besteht also noch ein hohes Risiko für Ipilimumab... was wäre bei einem Scheitern der PIII Medarex ohne Ipilimumab wert?
http://www.forbes.com/2009/07/23/bristol-myers-medarex-busin…
Bristol's Cancer Bet
Robert Langreth, 07.23.09, 05:26 PM EDT
Cancer immunotherapy has mostly been a failure so far. With its $2.4B purchase of Medarex, the company wagers it has found a winner.
Attempts to spur the immune system to kill tumors have mostly failed in trials. Now Bristol-Myers Squibb is betting billions that it can make immune-targeting therapies finally work against cancer.
Its $2.4 billion cash acquisition of the biotech firm Medarex ( MEDX - news - people ), announced late Wednesday, represents a giant gamble that immunotherapy will become the next big thing in cancer treatment. Medarex's lead drug, ipilimumab, now in a final-stage trial for advanced melanoma, doesn't target tumors directly at all. Instead it works by removing the brakes on the immune system so it can attack and kill the tumor.
In recent years, evidence has built that the immune system can sometimes attack and kill cancer cells--sometimes--but that cancer finds ways to fight back and evade or blunt the attack. (See "Cancer Miracles") For some people with advanced cancer, ipilimumab may be just enough to trigger a full-fledged anti-tumor attack. Bristol-Myers Squibb ( BMY - news - people ) has been collaborating with Medarex for years but now will get full rights to the drug.
"We wouldn't be betting $2.4 billion in cash unless we were optimistic" it would work, said Bristol-Myers Chief Executive James Cornelius in a conference call. "This will not be a cure-all for all types of cancer" but it could be "complementary to therapies that are out there today." Medarex has other cancer immunotherapies in earlier stages of testing, as well as drugs targeting lupus, rheumatoid arthritis and inflammatory bowel disease.
Bristol's buy is a risky move because numerous treatments and vaccines that aim to stimulate the body against cancer have mostly failed. One of the few that has worked so far is an experimental prostate cancer vaccine from Dendreon ( DNDN - news - people ) that recently had good trial results. The immune system is one of the more complicated parts of the body and doctors are only beginning to understand its intricacies. Another immune-boosting therapy against cancer, the natural immune system protein interleukin-2, has been limited by severe side effects.
Most trials of ipilimumab to date have been in advanced melanoma, where a small percentage of patients have experienced spectacular long-lasting remissions, even as the drug appears to do relatively little for the majority. Why more patients don't respond is a subject of intense research at laboratories worldwide. Some patients get autoimmune side-effects.
A Pfizer ( PFE - news - people ) drug similar to ipilimumab failed to improve survival in a large final-stage trial in melanoma. Bristol hopes to get better results in its final-stage trial by combining ipilimumab with chemotherapy and using a more intensive dosing regimen. Bristol and Medarex also have ipilimumab trials ongoing in prostate and lung cancer.
Results from the melanoma trial are expected next year and nobody quite knows what will happen. "Only the results of the large phase III study will be able to tell what is the role of this combination. We all hope it works, but there are obvious reservations," says melanoma expert Antoni Ribas at UCLA, who helped test the Pfizer drug. One worry, he said, is that chemotherapy may counteract ipilimumab by killing the new immune cells it helps activate.
Other companies working on immune therapies against cancer include GlaxoSmithKline ( GSK - news - people ) and Sanofi Aventis.
One reason why Bristol did the deal: With prices for cancer drugs in the stratosphere, even a modest success in trials could lead to billions in sales. Getting in early could allow huge rewards if the approach pays off. Also, if it had waited for successful trial results, the price for Medarex would have gone up like crazy.
mfg ipollit
ob Ipilimumab ein Erfolg wird, ist immer noch sehr unsicher und die bisherigen Royalties könnten niedriger ausfallen, als manche hoffen.
Die Royalties für Simponi und Stelara (Ilaris kann man bisher vernachlässigen) dürften zwischen 2-3% betragen. Simponi tritt hier u.a. gegen das etablierte Embrel an und Stelara gegen Humira. Bei z.B. 500 Mio USD für Simponi und 1 Mrd USD für Embrel peak sales wären das über 10 Jahre maximale Umsätze in Summe 15 Mrd USD, von denen Medarex 2-3% erhält... also 300 bis 450 Mio USD, die in diesem Fall diese beiden Produkte Medarex innerhalb der nächsten 15 Jahre einbringen würden. Im Vergleich zu den jetzt gezahlten 2,4 Mrd USD scheint das nicht der Hauptgrund für die Übernahme gewesen zu sein. PDLI hat mit Royalties von u.a. Avastin, Herceptin, Synagis, Lucentis, Tysabri dieses Jahr einen Umsatz von vielleicht 330 Mio USD bei einem aktuellen KGV10e von schwachen 6,5(!). Royalties alleine bringen es offensichtlich nicht... PDLI ist damit gerade mal 1 Mrd USD (MK) wert.
z.B. ein Kommentar von Ohad Hammer, der eigentlich kompentent erscheint... http://www.hammerstockblog.com/micromet-%e2%80%93-the-plot-t…
"I really want to be bullish on MEDX but I just don’t find enough reasons. Theoreticallly, they have many shots on goals but their pipeline is not too impressive. Of course this could change if even one antibody shows good results in clinical testing. The approval of Stelara is a positive development especially after Genentech withdrew Raptiva of the market. Golimumab is more tricky since there is a multitude of anti TNF agents out there."
oder http://www.thestreet.com/story/10484664/1/biotech-stock-mail…
"Adam: What do you think of Johnson & Johnson's(JNJ Quote) golimumab for first-pass FDA approval on April 29? Also, Stelara should be approved any day... I believe this may be a game changer for Medarex(MEDX Quote). These approvals should provide enough royalties to limit the need for additional funding and may spark a take-out by J&J or price war with Bristol-Myers Squibb(BMY Quote). With updated survival from ipilimumab at ASCO, I believe Bristol will move to buy Medarex this summer. They do not want to wind up in another ImClone situation." Charles is a fervent Medarex bull with a persuasive argument for owning the stock now. I know because he and I had a lengthy email discussion about Medarex earlier this week.
Golimumab, for treating rheumatoid arthritis, and Stelara, for moderate to severe plaque psoriasis, each have the potential to be billion-dollar drugs for J&J. Both drugs were created using Medarex's humanized monoclonal antibody technology, which entitles the company to a low single-digit royalty on sales -- call it 3%.
If one or both of these J&J drugs achieves peak annual sales in the $3 billion to $4 billion range of market leaders Enbrel, sold by Amgen(AMGN Quote), or Abbott Lab's(ABT Quote) Humira, then the royalty revenue flowing back to Medarex is substantial.
Charles' estimate of Medarex's Stelara royalties alone tops $100 million a year.
His math pencils out OK, but I do worry that he overestimates the peak revenue potential for both Stelara and golimumab. Both seem like strong drugs, but so are Enbrel and Humira. It's not going to be easy to unseat well-entrenched drugs like Enbrel and Humira, especially since both drugs are considered very safe for patients. Stelara and golimumab may be as safe, but they lack the years of data to prove it.
This exact point was made by two rheumatologists speaking last month on a panel at a health care conference sponsored by Cowen & Co. Both doctors believed that drugs like golimumab (Stelara didn't come up specifically) would be fighting for second- or third-line treatment. Neither was enthusiastic at all about swapping out a new drug for either Humira or Enbrel any time soon.
Couple this conservatism on the part of doctors with a recession-fueled pullback in the use of all expensive biologic drugs to treat auto-immune diseases like rheumatoid arthritis (which I wrote about this week), and you've got plenty of reasons to be cautious about assuming huge royalty revenue flowing into Medarex's coffers. I don't want to leave the impression that the approval of golimumab and/or Stelara isn't positive for Medarex. Both drugs will bring non-dilutive cash to the company which is definitely a plus in this market environment. Moreover, the approval of either drug will validate Medarex's antibody technology platform, another good thing.
But for Medarex to be truly successful, the company must become more than just the next PDL Biopharma(PDLI Quote) or Xoma(XOMA Quote). Both of these companies have been disappointments. They collect royalty revenues on other companies' successful drugs but have never been able to develop drugs successfully on their own.
Charles believes that ipilimumab, Medarex's melanoma drug (partnered with Bristol-Myers Squibb) may be that internally developed drug that gets Medarex really moving. I have my serious doubts about that, based on the uninspiring data released so far.
And let's not forget the lameness of Medarex's management team, which seems incapable of doing anything right. Honestly, CEO Howard Pien is like a black hole -- shareholder value goes in, but never comes out.
At around $5.50 a share (a $700 million market cap), Medarex is already getting credit for some of the anticipated royalties from golimumab and Stelara. As one analyst said to me this week, think of that royalty stream as a backstop on Medarex's current valuation and not so much as a future growth driver for the stock price. That will come if Medarex can successfully develop its internal pipeline of drug candidates. And on that front, I'm definitely in wait-and-see mode."
jetzt sind es nicht 5,5 USD sondern 16 USD geworden...
nach dieser Schätzung soll Humira 2014 9 Mrd USD Jahresumsatz haben und Embrel 6,5 Mrd USD:
http://www.fiercebiotech.com/pages/top-10-products-sales-201…
es ist nicht einfach gegen etablierte Produkte anzukommen.
********
und dann zu Ipilimumab... warum gibt es hier so große Zuversicht? Ich denke eher, dass hier BMS einiges riskiert, ein kompletter Fehlschlag ist nicht ausgeschlossen. Die folgenden Punkte sprechen eher nicht für Ipilimumab:
- Ipilimumab ist bereits in PIII-Studien bei fortgeschittenem Hautkrebs gescheitert
- die FDA hat auf Basis der bisherigen Daten Ipilimumab nicht zugelassen
- fortgeschittener Hautkrebs ist eine extrem schwer zu behandelnde Indikation, in der bereits viele Kandidaten, die in der PII erfolgreich aussahen, am Ende gescheitert sind (andererseits besteht daher auch ein großer Bedarf)
- Ipilimumab wirkt über das Immunsystem... die meisten ähnlichen Ansätze sind bisher gescheitert
- die PIII ist eine Kombi mit Chemo, die sich theoretisch negativ auf den Ansatz Stimulation des Immunsystems auswirkt (die Chemo unterdrückt das Immunsystem, so dass es schwerer stimuliert werden kann)
- bisher gibt es, soweit ich das sehe, nur PII Daten, die auf eine Verbesserung der Überlebenszeit hindeuten. PII-Daten sind aber sehr unzuverlässig.
insgesamt besteht also noch ein hohes Risiko für Ipilimumab... was wäre bei einem Scheitern der PIII Medarex ohne Ipilimumab wert?
http://www.forbes.com/2009/07/23/bristol-myers-medarex-busin…
Bristol's Cancer Bet
Robert Langreth, 07.23.09, 05:26 PM EDT
Cancer immunotherapy has mostly been a failure so far. With its $2.4B purchase of Medarex, the company wagers it has found a winner.
Attempts to spur the immune system to kill tumors have mostly failed in trials. Now Bristol-Myers Squibb is betting billions that it can make immune-targeting therapies finally work against cancer.
Its $2.4 billion cash acquisition of the biotech firm Medarex ( MEDX - news - people ), announced late Wednesday, represents a giant gamble that immunotherapy will become the next big thing in cancer treatment. Medarex's lead drug, ipilimumab, now in a final-stage trial for advanced melanoma, doesn't target tumors directly at all. Instead it works by removing the brakes on the immune system so it can attack and kill the tumor.
In recent years, evidence has built that the immune system can sometimes attack and kill cancer cells--sometimes--but that cancer finds ways to fight back and evade or blunt the attack. (See "Cancer Miracles") For some people with advanced cancer, ipilimumab may be just enough to trigger a full-fledged anti-tumor attack. Bristol-Myers Squibb ( BMY - news - people ) has been collaborating with Medarex for years but now will get full rights to the drug.
"We wouldn't be betting $2.4 billion in cash unless we were optimistic" it would work, said Bristol-Myers Chief Executive James Cornelius in a conference call. "This will not be a cure-all for all types of cancer" but it could be "complementary to therapies that are out there today." Medarex has other cancer immunotherapies in earlier stages of testing, as well as drugs targeting lupus, rheumatoid arthritis and inflammatory bowel disease.
Bristol's buy is a risky move because numerous treatments and vaccines that aim to stimulate the body against cancer have mostly failed. One of the few that has worked so far is an experimental prostate cancer vaccine from Dendreon ( DNDN - news - people ) that recently had good trial results. The immune system is one of the more complicated parts of the body and doctors are only beginning to understand its intricacies. Another immune-boosting therapy against cancer, the natural immune system protein interleukin-2, has been limited by severe side effects.
Most trials of ipilimumab to date have been in advanced melanoma, where a small percentage of patients have experienced spectacular long-lasting remissions, even as the drug appears to do relatively little for the majority. Why more patients don't respond is a subject of intense research at laboratories worldwide. Some patients get autoimmune side-effects.
A Pfizer ( PFE - news - people ) drug similar to ipilimumab failed to improve survival in a large final-stage trial in melanoma. Bristol hopes to get better results in its final-stage trial by combining ipilimumab with chemotherapy and using a more intensive dosing regimen. Bristol and Medarex also have ipilimumab trials ongoing in prostate and lung cancer.
Results from the melanoma trial are expected next year and nobody quite knows what will happen. "Only the results of the large phase III study will be able to tell what is the role of this combination. We all hope it works, but there are obvious reservations," says melanoma expert Antoni Ribas at UCLA, who helped test the Pfizer drug. One worry, he said, is that chemotherapy may counteract ipilimumab by killing the new immune cells it helps activate.
Other companies working on immune therapies against cancer include GlaxoSmithKline ( GSK - news - people ) and Sanofi Aventis.
One reason why Bristol did the deal: With prices for cancer drugs in the stratosphere, even a modest success in trials could lead to billions in sales. Getting in early could allow huge rewards if the approach pays off. Also, if it had waited for successful trial results, the price for Medarex would have gone up like crazy.
mfg ipollit
Antwort auf Beitrag Nr.: 37.646.479 von ipollit am 25.07.09 18:39:29Deine Meinung:
Die Royalties für Simponi und Stelara (Ilaris kann man bisher vernachlässigen) ..... also 300 bis 450 Mio USD, die in diesem Fall diese beiden Produkte Medarex innerhalb der nächsten 15 Jahre einbringen würden.
Aus deinem posting:
Charles' estimate of Medarex's Stelara royalties alone tops $100 million a year.
Wenn du eins von 3 Produkten ganz weglässt und für die restlichen 2 nur Bruchstücke der Umsätze ansetzt wie andere, dann relativiert sich der faire Preis natürlich.
Die Royalties für Simponi und Stelara (Ilaris kann man bisher vernachlässigen) ..... also 300 bis 450 Mio USD, die in diesem Fall diese beiden Produkte Medarex innerhalb der nächsten 15 Jahre einbringen würden.
Aus deinem posting:
Charles' estimate of Medarex's Stelara royalties alone tops $100 million a year.
Wenn du eins von 3 Produkten ganz weglässt und für die restlichen 2 nur Bruchstücke der Umsätze ansetzt wie andere, dann relativiert sich der faire Preis natürlich.
Antwort auf Beitrag Nr.: 37.646.905 von eck64 am 25.07.09 21:44:00Dieser Charles ist ja kein Analyst, sondern einer wie jeder, der hier postet... während dieser Feuerstein (der mir eigentlich eher suspekt ist) Charles darauf entgegnet, dass er mit diesen 100 Mio USD wohl die Royalties überschätzt, da Enbrel und Humira genauso gut seien, aber als etablierte Mittel nur schwer zu verdrängen wären. Die dann zitierten Rheumatologen sahen das ähnlich.
Würde Simponi oder Stelara die Marktführer Embrel oder Humira komplett ersetzen, also ein 5 Mrd USD Produkt werden, dann wären natürlich 2-3% davon 100-150 Mio USD pro Jahr, die an Medarex fließen. Die Frage ist allerdings, warum die Etablierten, mit denen man vertraut ist, plötzlich verschwinden sollten. Und selbst wenn... PDLI bekommt heute mit 300 Mio USD bereits mehr als Medarex im optimistischsten Fall mit Simponi und Stelara erzielen könnte und ist mit 1 Mrd USD trotzdem nichtmal halb so hoch wie Medarex jetzt mit 2,4 Mrd USD bewertet. Diese eigentlich Mini-Royalties sind eher nur die Basis bei Medarex gewesen... interessant für BMS war wohl mehr die Pipeline und die Technologie.
Ilaris habe ich weg gelassen, da es gegen CAPS nichtmal 100 Mio Umsatz pro Jahr erreichen wird.
mfg ipollit
Würde Simponi oder Stelara die Marktführer Embrel oder Humira komplett ersetzen, also ein 5 Mrd USD Produkt werden, dann wären natürlich 2-3% davon 100-150 Mio USD pro Jahr, die an Medarex fließen. Die Frage ist allerdings, warum die Etablierten, mit denen man vertraut ist, plötzlich verschwinden sollten. Und selbst wenn... PDLI bekommt heute mit 300 Mio USD bereits mehr als Medarex im optimistischsten Fall mit Simponi und Stelara erzielen könnte und ist mit 1 Mrd USD trotzdem nichtmal halb so hoch wie Medarex jetzt mit 2,4 Mrd USD bewertet. Diese eigentlich Mini-Royalties sind eher nur die Basis bei Medarex gewesen... interessant für BMS war wohl mehr die Pipeline und die Technologie.
Ilaris habe ich weg gelassen, da es gegen CAPS nichtmal 100 Mio Umsatz pro Jahr erreichen wird.
mfg ipollit
Antwort auf Beitrag Nr.: 37.647.046 von ipollit am 25.07.09 22:54:13Ich finde nicht, dass der PDLI-Vergleich zieht, ausser in einer Hinsicht: Man sollte nicht in dem Moment verkaufen, wo der Markt faire Preise nicht zu zahlen bereit ist. Im speziellen Fall Medarex bestand kein Handlungszwang aufgrund von cashnot oder ähnlichem. Da hätte man einfach warten können. Und wenn BMS mit einem Übernahmeangebot wedelt, dann muss man das als Management nicht annehmen, sondern kann auch den Aktionären die nicht-Annahme empfehlen. Ich nehme an, der Kurs stünde dann trotzdem bei 16.....
Sollte das Management allerdings wissen, das es um Ipilimumab nicht gut steht, dann wäre es natürlich super gemacht, aber ich hätte dann Angst vor "der russischen Mafia".....
Sollte das Management allerdings wissen, das es um Ipilimumab nicht gut steht, dann wäre es natürlich super gemacht, aber ich hätte dann Angst vor "der russischen Mafia".....
Ipilimumab hat erst durch die BMS-Übernahme eine Erfolgsvisibilität bekommen. Medarex wird keinen Informationsvorsprung in einer 50:50 Kooperation haben. Ohne Ipi ist Medarex wirtschaftlich und technologisch Asche bleibend. Die renitente Kooperationsschwäche hält seit Jahren an und die Cashburneraufstellung darf auch nicht vergessen werden.
Es mag noch eine Chance auf ein Pfizerangebot geben. Sonst ist das Angebot schon in Ordnung, wirklich weh tut ein Abgang von diesem Selbstbedienungsladen nicht. Spekulativ ist ein Angebot von Pfizer für BMS. Und der finanzielle Sicherheitsabstand bedurfte auch einer Entscheidung. Die jahrelange Alimentierungspraxis vom Management findet hier ihre GPC-Entsprechung, vorher organisiert down, Optionen eingesackt und Fanta frei
Alles kein Zufall
Es mag noch eine Chance auf ein Pfizerangebot geben. Sonst ist das Angebot schon in Ordnung, wirklich weh tut ein Abgang von diesem Selbstbedienungsladen nicht. Spekulativ ist ein Angebot von Pfizer für BMS. Und der finanzielle Sicherheitsabstand bedurfte auch einer Entscheidung. Die jahrelange Alimentierungspraxis vom Management findet hier ihre GPC-Entsprechung, vorher organisiert down, Optionen eingesackt und Fanta frei

Alles kein Zufall
Antwort auf Beitrag Nr.: 37.646.479 von ipollit am 25.07.09 18:39:29ipollit, eigentlich schätze ich deine Beiträge, aber hier hast du nicht richtig hingeschaut und dich nur auf schnellen Research anderer gestützt. Ich verfolge Medarex seit drei Jahren intensivst (inklusive wissenschaftliche Artikel und Konferenzen).
Medarex hat mit ipilimumab ein Produkt, das in allen Krebsarten sehr gute Wirkung (hinsichtlich Goldstandard OS) zeigen kann und m.E. auch wird (ohne Sicherheitsbedenken) und selbst in schwierigsten late stage settings sogar mit Heilungen aufwarten kann. Das Ding wird nicht nur in Melanoma funktionieren sondern auch z.b. in Prostata und anderen Krebsarten.
Dass ipilimumab nicht verstanden wird und die Phase II Ergebnisse als Misserfolg dargestellt werden liegt am Wirkprinzip und an der falschen Messmethode der Zulassungsbehörden, die sich an Chemotherapien orientieren, bei denen die Wirkweise im Laufe der Zeit anders ist als bei Immunansätzen. Initial kann es bei immunbasierten Ansätzen wie ipi zu einer Progression kommen bis das Immunsystem aktiv wird und den Tumor in Schach hält, schrumpft oder teilweise sogar vollständig eliminiert. Letzteres hat nicht mal Provenge hinbekommen.
ipilimumab wird einfach vom Markt nicht verstanden und deswegen ist es für BMS so einfach diese Firma so billig übernehmen zu wollen. Erst OS Daten in PIII bei DTIC/ipi, die m.E. zu 99,9% sehr positv sein werden, hätten dem Markt die Augen geöffnet und der Aktienkurs wäre schlagartig explodiert. Denn dann würde ipi dort hin übertragen wo es hingehört, als universelle Krebstherapie und Booster des Immunsystems gegen Krebs. Desweiteren hat Medarex Produktionsanlagen für AKs, eine extrem viel versprechende ADC Technologie, einen Booster für ipilimumab (PD1), weitere vielversprechende Eigenentwicklungen, eine mehr als pralle Partnerpipe mit schon zugelassenen potentiellen Blockbustern und 1Milliarde tax loss, die der Übernehmer steuerlich nutzen kann. Zudem die Beteiligungen an Celldex und Genmab. Alles in allem ist 2,1Mrd Übernahmepreis ex cash ein Witz.
Ich gehe absolut von Betrug von Management und BOD aus, die sich zuvor massiv Optionen in Rekordhöhe zugeschustert haben und nun auscashen wollen, denen ist es egal ob sie 50USD oder 16USD bekommen, hauptsache schnell raus und sich nen schönen Ruhestand gönnen - so lange die alten Säcke noch leben. Es deutet für mich alles darauf hin, dass es mit unrechten Dingen bei dem Merger zugegangen ist. Es deutet für mich zudem alles darauf hin, dass Pien und das BOD die Verarschung der Aktionäre geplant haben. Beispiele: 1. Das Shareholdermeeting wurde trotz Sitz an der Ostküste plötzlich an der Westküste veranstaltet. Dadurch konnten kaum die vielen lästigen Retail Aktionäre teilnehmen. 2. Die Darstellung der immensen Pipeline auf der HP wurde auf die P III Kandidaten zusammengeschrumpft. Somit wurde die Sichtbarkeit der mehr als 25 PI und PII Kandidaten eliminiert.
Medarex hatte z.b. die weit bessere Technologie und Pipeline als Abgenix und geht zwei Jahre später für weniger über die Bühne. Und dann auch noch vor den entscheidenden Daten und vor dem entscheidenden potentiellen Wertzuwachs. Das ist nicht im Interesse der Aktionäre und ich hoffe ein zweiter Bieter erkennt das Potential und beginnt eine Bieterschlacht.
Medarex hat mit ipilimumab ein Produkt, das in allen Krebsarten sehr gute Wirkung (hinsichtlich Goldstandard OS) zeigen kann und m.E. auch wird (ohne Sicherheitsbedenken) und selbst in schwierigsten late stage settings sogar mit Heilungen aufwarten kann. Das Ding wird nicht nur in Melanoma funktionieren sondern auch z.b. in Prostata und anderen Krebsarten.
Dass ipilimumab nicht verstanden wird und die Phase II Ergebnisse als Misserfolg dargestellt werden liegt am Wirkprinzip und an der falschen Messmethode der Zulassungsbehörden, die sich an Chemotherapien orientieren, bei denen die Wirkweise im Laufe der Zeit anders ist als bei Immunansätzen. Initial kann es bei immunbasierten Ansätzen wie ipi zu einer Progression kommen bis das Immunsystem aktiv wird und den Tumor in Schach hält, schrumpft oder teilweise sogar vollständig eliminiert. Letzteres hat nicht mal Provenge hinbekommen.
ipilimumab wird einfach vom Markt nicht verstanden und deswegen ist es für BMS so einfach diese Firma so billig übernehmen zu wollen. Erst OS Daten in PIII bei DTIC/ipi, die m.E. zu 99,9% sehr positv sein werden, hätten dem Markt die Augen geöffnet und der Aktienkurs wäre schlagartig explodiert. Denn dann würde ipi dort hin übertragen wo es hingehört, als universelle Krebstherapie und Booster des Immunsystems gegen Krebs. Desweiteren hat Medarex Produktionsanlagen für AKs, eine extrem viel versprechende ADC Technologie, einen Booster für ipilimumab (PD1), weitere vielversprechende Eigenentwicklungen, eine mehr als pralle Partnerpipe mit schon zugelassenen potentiellen Blockbustern und 1Milliarde tax loss, die der Übernehmer steuerlich nutzen kann. Zudem die Beteiligungen an Celldex und Genmab. Alles in allem ist 2,1Mrd Übernahmepreis ex cash ein Witz.
Ich gehe absolut von Betrug von Management und BOD aus, die sich zuvor massiv Optionen in Rekordhöhe zugeschustert haben und nun auscashen wollen, denen ist es egal ob sie 50USD oder 16USD bekommen, hauptsache schnell raus und sich nen schönen Ruhestand gönnen - so lange die alten Säcke noch leben. Es deutet für mich alles darauf hin, dass es mit unrechten Dingen bei dem Merger zugegangen ist. Es deutet für mich zudem alles darauf hin, dass Pien und das BOD die Verarschung der Aktionäre geplant haben. Beispiele: 1. Das Shareholdermeeting wurde trotz Sitz an der Ostküste plötzlich an der Westküste veranstaltet. Dadurch konnten kaum die vielen lästigen Retail Aktionäre teilnehmen. 2. Die Darstellung der immensen Pipeline auf der HP wurde auf die P III Kandidaten zusammengeschrumpft. Somit wurde die Sichtbarkeit der mehr als 25 PI und PII Kandidaten eliminiert.
Medarex hatte z.b. die weit bessere Technologie und Pipeline als Abgenix und geht zwei Jahre später für weniger über die Bühne. Und dann auch noch vor den entscheidenden Daten und vor dem entscheidenden potentiellen Wertzuwachs. Das ist nicht im Interesse der Aktionäre und ich hoffe ein zweiter Bieter erkennt das Potential und beginnt eine Bieterschlacht.
Antwort auf Beitrag Nr.: 37.647.373 von Ville7 am 26.07.09 08:55:21Sorry aber die Übernahme ist sogut wie abgeschlossen hier wird nicht mehr viel passieren .
The merger agreement contains a provision under which Medarex has agreed not to solicit any competing offers for the company
It's a done deal at $16.00.
They've already SIGNED the agreement. It's not open to other offers at this point. And I'm sure that other offers were sought before taking the deal. All it needs now is the formality of stockholders approve and federal approval. And they would have gotten majority approval verbally from the major stockholders before signing the deal.
And it could die in federal approval, so take the $15.88 now. It's not worth waiting months for a gain of only pennies.
BMY-MEDX deal: With a 90% premium, all-cash terms, a no shop
clause, and no need for financing, this deal is a fait accompli. The
probability it doesn’t go through is roughly the probability that
HEB’s CEO, William Carter, wins the Nobel Prize in Medicine.
http://finance.yahoo.com/news/BristolMyers-Squibb-to-bw-5713…
›Bristol-Myers Squibb to Acquire Medarex
• Positions Bristol-Myers Squibb for Long-Term Leadership in Biologics
• Acquires Proven Antibody Discovery Technology
• Gains Full Rights to Promising Phase III Compound, Ipilimumab
• Significantly Expands Oncology and Immunology Pipeline
›Wednesday July 22, 2009, 7:16 pm EDT
NEW YORK & PRINCETON, N.J.--(BUSINESS WIRE)--Bristol-Myers Squibb Company (NYSE: BMY ) and Medarex, Inc. (NASDAQ: MEDX ) announced today that the companies have signed a definitive merger agreement providing for the acquisition of Medarex by Bristol-Myers Squibb, for $16.00 per share in cash. The transaction, with an aggregate purchase price of approximately $2.4 billion, has been unanimously approved by the boards of directors of both companies. Medarex’s projected $300 million in net cash and marketable securities at closing would be an asset acquired by Bristol-Myers Squibb resulting in an implied purchase price of approximately $2.1 billion.
“Medarex’s technology platform, people and pipeline provide a strong complement to our company’s biologics strategy, specifically in immuno-oncology,” said James M. Cornelius, chairman and chief executive officer, Bristol-Myers Squibb. “With its productive and proven antibody discovery capabilities, ability to generate interesting therapeutic programs and unique set of pre-clinical and clinical assets in development, Medarex represents what we’re looking for in terms of our String of Pearls strategy. This acquisition is another important step in our BioPharma transformation.”
“We believe that this combination with Bristol-Myers Squibb, a global leader in oncology, provides an excellent opportunity to realize the full potential of Medarex’s development portfolio and our UltiMAb® technology platform through a transaction which also provides an attractive valuation for our shareholders,” said Howard H. Pien, chairman and chief executive officer, Medarex. “Medarex has evolved significantly over the past two decades from a research platform to a development company. We believe that this transaction represents a great opportunity to place our clinical programs and technology assets in the hands of one of the world’s premier biopharmaceutical companies with the expertise, resources, motivation and dedication to bring innovative cancer treatment options to patients in need.”
Bristol-Myers Squibb gains the following as a result of the acquisition:
* Medarex’s UltiMAb Human Antibody Development System®, which produces high affinity, fully human antibodies for use in a broad range of therapeutic areas, including immunology and oncology. This validated technology platform has produced compounds which are now currently marketed therapies (SIMPONI™, STELARA™ and ILARIS®).
* Medarex’s next-generation Antibody-Drug Conjugate (ADC) technology, which is a novel and proprietary platform that could open new fields in oncology drug development.
* Rights to seven antibodies in clinical trials under Medarex’s sole sponsorship and three other antibodies being co-developed with other partners. Rights to pre-clinical assets in various stages of development by Medarex -- in particular, monoclonal antibodies focused in oncology and immunology.
* Full ownership and rights to ipilimumab, which, if approved, could be an important contributor to Bristol-Myers Squibb’s future growth. The companies have collaborated on the development of ipilimumab, a novel immunotherapy currently in Phase III development for the treatment of metastatic melanoma. The companies also have an ongoing Phase II study in lung cancer as well as Phase III studies in adjuvant melanoma and hormone-refractory prostate cancer.
* Royalties based on percentage of sales for SIMPONI™, STELARA™ and ILARIS®.
“We welcome the opportunity to further collaborate with the Medarex scientific leadership,” said Elliott Sigal, M.D., Ph.D., executive vice president and president, research and development at Bristol-Myers Squibb. “In addition to our Adnexus team, which has been expanded since it was acquired in 2007, Medarex scientists will help us create an industry-leading biologics capability. We believe Medarex’s antibody generation expertise, located in California and New Jersey, will complement our existing biologics efforts with a dedicated discovery and development capability in immuno-oncology.”
Under the terms of the definitive merger agreement, Bristol-Myers Squibb will commence a cash tender offer on or about July 27, 2009 to purchase all of the outstanding shares of Medarex common stock for $16.00 per share in cash. The closing of the tender offer is subject to customary terms and conditions, including the tender of a number of shares that, together with the number of shares already owned by Bristol-Myers Squibb, constitutes at least a majority of Medarex’s outstanding shares of common stock (on a fully diluted basis) and expiration or termination of the waiting period under the Hart Scott Rodino Antitrust Improvement Act. The agreement also provides for the parties to effect, subject to customary conditions, a merger to be completed following the completion of the tender offer which would result in all shares not tendered in the tender offer being converted into the right to received $16.00 per share in cash. The merger agreement contains a provision under which Medarex has agreed not to solicit any competing offers for the company. Bristol-Myers Squibb will finance the acquisition from its existing cash resources. The companies expect the tender offer to close in approximately thirty (30) days after commencement of the tender offer.
JPMorgan Securities, Inc. is serving as financial advisor to Bristol-Myers Squibb in connection with the acquisition, and Bristol-Myers Squibb is represented by Cravath, Swaine & Moore LLP, New York, New York. Goldman, Sachs & Co. is serving as financial advisor to Medarex in connection with the acquisition, and Medarex is represented by Covington & Burling LLP, New York, New York.‹
The merger agreement contains a provision under which Medarex has agreed not to solicit any competing offers for the company
It's a done deal at $16.00.
They've already SIGNED the agreement. It's not open to other offers at this point. And I'm sure that other offers were sought before taking the deal. All it needs now is the formality of stockholders approve and federal approval. And they would have gotten majority approval verbally from the major stockholders before signing the deal.
And it could die in federal approval, so take the $15.88 now. It's not worth waiting months for a gain of only pennies.
BMY-MEDX deal: With a 90% premium, all-cash terms, a no shop
clause, and no need for financing, this deal is a fait accompli. The
probability it doesn’t go through is roughly the probability that
HEB’s CEO, William Carter, wins the Nobel Prize in Medicine.
http://finance.yahoo.com/news/BristolMyers-Squibb-to-bw-5713…
›Bristol-Myers Squibb to Acquire Medarex
• Positions Bristol-Myers Squibb for Long-Term Leadership in Biologics
• Acquires Proven Antibody Discovery Technology
• Gains Full Rights to Promising Phase III Compound, Ipilimumab
• Significantly Expands Oncology and Immunology Pipeline
›Wednesday July 22, 2009, 7:16 pm EDT
NEW YORK & PRINCETON, N.J.--(BUSINESS WIRE)--Bristol-Myers Squibb Company (NYSE: BMY ) and Medarex, Inc. (NASDAQ: MEDX ) announced today that the companies have signed a definitive merger agreement providing for the acquisition of Medarex by Bristol-Myers Squibb, for $16.00 per share in cash. The transaction, with an aggregate purchase price of approximately $2.4 billion, has been unanimously approved by the boards of directors of both companies. Medarex’s projected $300 million in net cash and marketable securities at closing would be an asset acquired by Bristol-Myers Squibb resulting in an implied purchase price of approximately $2.1 billion.
“Medarex’s technology platform, people and pipeline provide a strong complement to our company’s biologics strategy, specifically in immuno-oncology,” said James M. Cornelius, chairman and chief executive officer, Bristol-Myers Squibb. “With its productive and proven antibody discovery capabilities, ability to generate interesting therapeutic programs and unique set of pre-clinical and clinical assets in development, Medarex represents what we’re looking for in terms of our String of Pearls strategy. This acquisition is another important step in our BioPharma transformation.”
“We believe that this combination with Bristol-Myers Squibb, a global leader in oncology, provides an excellent opportunity to realize the full potential of Medarex’s development portfolio and our UltiMAb® technology platform through a transaction which also provides an attractive valuation for our shareholders,” said Howard H. Pien, chairman and chief executive officer, Medarex. “Medarex has evolved significantly over the past two decades from a research platform to a development company. We believe that this transaction represents a great opportunity to place our clinical programs and technology assets in the hands of one of the world’s premier biopharmaceutical companies with the expertise, resources, motivation and dedication to bring innovative cancer treatment options to patients in need.”
Bristol-Myers Squibb gains the following as a result of the acquisition:
* Medarex’s UltiMAb Human Antibody Development System®, which produces high affinity, fully human antibodies for use in a broad range of therapeutic areas, including immunology and oncology. This validated technology platform has produced compounds which are now currently marketed therapies (SIMPONI™, STELARA™ and ILARIS®).
* Medarex’s next-generation Antibody-Drug Conjugate (ADC) technology, which is a novel and proprietary platform that could open new fields in oncology drug development.
* Rights to seven antibodies in clinical trials under Medarex’s sole sponsorship and three other antibodies being co-developed with other partners. Rights to pre-clinical assets in various stages of development by Medarex -- in particular, monoclonal antibodies focused in oncology and immunology.
* Full ownership and rights to ipilimumab, which, if approved, could be an important contributor to Bristol-Myers Squibb’s future growth. The companies have collaborated on the development of ipilimumab, a novel immunotherapy currently in Phase III development for the treatment of metastatic melanoma. The companies also have an ongoing Phase II study in lung cancer as well as Phase III studies in adjuvant melanoma and hormone-refractory prostate cancer.
* Royalties based on percentage of sales for SIMPONI™, STELARA™ and ILARIS®.
“We welcome the opportunity to further collaborate with the Medarex scientific leadership,” said Elliott Sigal, M.D., Ph.D., executive vice president and president, research and development at Bristol-Myers Squibb. “In addition to our Adnexus team, which has been expanded since it was acquired in 2007, Medarex scientists will help us create an industry-leading biologics capability. We believe Medarex’s antibody generation expertise, located in California and New Jersey, will complement our existing biologics efforts with a dedicated discovery and development capability in immuno-oncology.”
Under the terms of the definitive merger agreement, Bristol-Myers Squibb will commence a cash tender offer on or about July 27, 2009 to purchase all of the outstanding shares of Medarex common stock for $16.00 per share in cash. The closing of the tender offer is subject to customary terms and conditions, including the tender of a number of shares that, together with the number of shares already owned by Bristol-Myers Squibb, constitutes at least a majority of Medarex’s outstanding shares of common stock (on a fully diluted basis) and expiration or termination of the waiting period under the Hart Scott Rodino Antitrust Improvement Act. The agreement also provides for the parties to effect, subject to customary conditions, a merger to be completed following the completion of the tender offer which would result in all shares not tendered in the tender offer being converted into the right to received $16.00 per share in cash. The merger agreement contains a provision under which Medarex has agreed not to solicit any competing offers for the company. Bristol-Myers Squibb will finance the acquisition from its existing cash resources. The companies expect the tender offer to close in approximately thirty (30) days after commencement of the tender offer.
JPMorgan Securities, Inc. is serving as financial advisor to Bristol-Myers Squibb in connection with the acquisition, and Bristol-Myers Squibb is represented by Cravath, Swaine & Moore LLP, New York, New York. Goldman, Sachs & Co. is serving as financial advisor to Medarex in connection with the acquisition, and Medarex is represented by Covington & Burling LLP, New York, New York.‹
Antwort auf Beitrag Nr.: 37.647.373 von Ville7 am 26.07.09 08:55:21"Medarex hat mit ipilimumab ein Produkt, das in allen Krebsarten sehr gute Wirkung (hinsichtlich Goldstandard OS) zeigen kann"
... für "kann" gibt es aber keine Zulassung, es bleibt noch zu beweisen
"und selbst in schwierigsten late stage settings sogar mit Heilungen aufwarten kann"
... du meinst die zwei Prostatakrebs-Patienten, oder? Es war ein populistischer Zeitungsartikel und kein wissenschaftlicher Beleg, darauf sollte man sich nicht stützen.
"Erst OS Daten in PIII bei DTIC/ipi, die m.E. zu 99,9% sehr positv sein werden"
99,9%, da bist du dir aber sehr sicher. Gut, ich kenne mich wirklich nicht so genau mit Medarex oder Ipilimumab aus. Ich war mir auch mal 99% sicher, dass Satraplatin auf Basis der positiven PFS-Daten unter SPA zugelassen wird. Den Ausgang einer PIII und auch noch in metastasierten Hautkrebs kann wohl niemand prognostizieren... ein Erfolg wäre allerdings sehr schön, das stimmt.
Wenn die Aktivierung des Immunsystems so dramatische Erfolge erzielen würde, warum sind dann so viele Ansätze bisher gescheitert? Mag sein, dass es da Wege gibt, aber es sind wohl keine Selbstläufer mit 99%iger Erfolgsgarantie.
Wenn das Wirkprinzip hier entscheidend ist, wie erklärst du dir, dass Pfizers Tremelimumab, der analoge anti-CTLA4 AK zu Ipilimumab, in der PIII bezügl. OS gescheitert ist? Und wenn es nicht alleine entscheidend ist, woher weißt du mit Bestimmtheit, dass bei Ipilimumab im Gegensatz zu Tremelimumab alles passt? Ursprünglich wollte Medarex ja bereits die Zulassung für Ipilimumab beantragen... aber die bisherigen Ergebnisse reichten anscheinend für die FDA nicht aus. Mit der Übernahme muss Medarex jetzt das Risiko eines Fehlschlags nicht mehr tragen.
"2,1Mrd Übernahmepreis ex cash" ... die Zahlen auf yahoo sind zwar nicht immer aktuell, aber danach sind es 323 Mio USD Cash und 146 Mio USD Schulden... also netto-cash "nur" etwa 175 Mio USD. Naja... Kleinigkeiten, aber es sieht so aus, als ob du bei Medarex alles ein wenig optimistischer beurteilst, als es vielleicht in der Realität ist. Ob das Management wirklich mit der Übernahme einverstanden sein würde, wenn z.B. Ipilimumab eine sichere Sache wäre? Andererseits verstehe ich auch, dass man sich ärgert, wenn man MEDX über Jahre hält und am Ende einen Preis bekommt, den es vielleicht so auch schon früher gegeben hat. Trotzdem noch besser, als z.B. die 5 USD Anfang des Jahres...
mfg ipollit
... für "kann" gibt es aber keine Zulassung, es bleibt noch zu beweisen
"und selbst in schwierigsten late stage settings sogar mit Heilungen aufwarten kann"
... du meinst die zwei Prostatakrebs-Patienten, oder? Es war ein populistischer Zeitungsartikel und kein wissenschaftlicher Beleg, darauf sollte man sich nicht stützen.
"Erst OS Daten in PIII bei DTIC/ipi, die m.E. zu 99,9% sehr positv sein werden"
99,9%, da bist du dir aber sehr sicher. Gut, ich kenne mich wirklich nicht so genau mit Medarex oder Ipilimumab aus. Ich war mir auch mal 99% sicher, dass Satraplatin auf Basis der positiven PFS-Daten unter SPA zugelassen wird. Den Ausgang einer PIII und auch noch in metastasierten Hautkrebs kann wohl niemand prognostizieren... ein Erfolg wäre allerdings sehr schön, das stimmt.
Wenn die Aktivierung des Immunsystems so dramatische Erfolge erzielen würde, warum sind dann so viele Ansätze bisher gescheitert? Mag sein, dass es da Wege gibt, aber es sind wohl keine Selbstläufer mit 99%iger Erfolgsgarantie.
Wenn das Wirkprinzip hier entscheidend ist, wie erklärst du dir, dass Pfizers Tremelimumab, der analoge anti-CTLA4 AK zu Ipilimumab, in der PIII bezügl. OS gescheitert ist? Und wenn es nicht alleine entscheidend ist, woher weißt du mit Bestimmtheit, dass bei Ipilimumab im Gegensatz zu Tremelimumab alles passt? Ursprünglich wollte Medarex ja bereits die Zulassung für Ipilimumab beantragen... aber die bisherigen Ergebnisse reichten anscheinend für die FDA nicht aus. Mit der Übernahme muss Medarex jetzt das Risiko eines Fehlschlags nicht mehr tragen.
"2,1Mrd Übernahmepreis ex cash" ... die Zahlen auf yahoo sind zwar nicht immer aktuell, aber danach sind es 323 Mio USD Cash und 146 Mio USD Schulden... also netto-cash "nur" etwa 175 Mio USD. Naja... Kleinigkeiten, aber es sieht so aus, als ob du bei Medarex alles ein wenig optimistischer beurteilst, als es vielleicht in der Realität ist. Ob das Management wirklich mit der Übernahme einverstanden sein würde, wenn z.B. Ipilimumab eine sichere Sache wäre? Andererseits verstehe ich auch, dass man sich ärgert, wenn man MEDX über Jahre hält und am Ende einen Preis bekommt, den es vielleicht so auch schon früher gegeben hat. Trotzdem noch besser, als z.B. die 5 USD Anfang des Jahres...
mfg ipollit
In meinem nächsten Leben werde ich Analyst!
Zürich (aktiencheck.de AG) - Jeff Elliott, Analyst der UBS, stuft die Aktie von Medarex (ISIN US5839161016/ WKN 883040) unverändert mit "neutral" ein. Das Kursziel werde von 8,75 auf 16 USD angehoben. (27.07.2009/ac/a/u)
Analyse-Datum: 27.07.2009
16 USD? Wie er wohl darauf kommt?
Zürich (aktiencheck.de AG) - Jeff Elliott, Analyst der UBS, stuft die Aktie von Medarex (ISIN US5839161016/ WKN 883040) unverändert mit "neutral" ein. Das Kursziel werde von 8,75 auf 16 USD angehoben. (27.07.2009/ac/a/u)
Analyse-Datum: 27.07.2009
16 USD? Wie er wohl darauf kommt?

Antwort auf Beitrag Nr.: 37.649.672 von SLGramann am 27.07.09 08:31:08Ob er sich da nicht verrechnet hat? 



Antwort auf Beitrag Nr.: 37.650.634 von eck64 am 27.07.09 10:51:49Die Hoffnung stirbt zuletzt.....
24.07.09 15,88 15,90 15,86 15,90 12.674.100
23.07.09 15,87 15,89 15,83 15,89 77.239.800
89.913.900
Laut Ariva sind die letzten zwei tage ca.90 Mill.Aktien gekauft/verkauft worden.
Wie verlässlich ist diese Angabe?

24.07.09 15,88 15,90 15,86 15,90 12.674.100
23.07.09 15,87 15,89 15,83 15,89 77.239.800
89.913.900

Laut Ariva sind die letzten zwei tage ca.90 Mill.Aktien gekauft/verkauft worden.
Wie verlässlich ist diese Angabe?
Antwort auf Beitrag Nr.: 37.651.843 von Bioperle am 27.07.09 13:32:21Offizielle Anzahl von Aktien (Medarex)
Aktienanzahl 127,3 Mio. (Stand: 16.12.08)
Aktienanzahl 127,3 Mio. (Stand: 16.12.08)
So, die fällige Klage ist anhängig. Nutzen wird das freilich nichts.
http://www.pr-inside.com/medarex-inc-faces-investor-class-ac…
http://www.pr-inside.com/medarex-inc-faces-investor-class-ac…
Antwort auf Beitrag Nr.: 37.654.679 von SLGramann am 27.07.09 19:28:00So, die fällige Klage ist anhängig. Nutzen wird das freilich nichts.
Abwarten, hier ist das letzte Wort noch nicht gesprochen.
Die oben genannten Handelsvolumina im Vergleich zu den gesamten shares sagen übrigens rein gar nichts darüber aus, wieviel BMS davon bereits erworben haben könnte.
Abwarten, hier ist das letzte Wort noch nicht gesprochen.
Die oben genannten Handelsvolumina im Vergleich zu den gesamten shares sagen übrigens rein gar nichts darüber aus, wieviel BMS davon bereits erworben haben könnte.

Antwort auf Beitrag Nr.: 37.654.679 von SLGramann am 27.07.09 19:28:00Moin,

auch noch dieses hier, wird schon spannend
(interessant übrigens, dass der Kläger vielleicht wirklich identisch mit dem user "kblumb" vom yahoo-Messageboard ist). Hier der Text:
---------------------
By David Voreacos and Phil Milford
July 27 (Bloomberg) -- Medarex Inc. was sued by an investor who claims he would be shortchanged in a $2.4 billion takeover by drugmaker Bristol-Myers Squibb Co.
The companies announced the acquisition on July 22, saying Bristol-Myers would pay a 90 percent premium over the closing price of $8.40 a share for Medarex before the announcement. The deal would give Bristol-Myers full ownership of the skin-cancer drug ipilimumab, which it had been developing jointly with Princeton, New Jersey-based Medarex.
The price is “grossly inadequate” because of the “very real possibility that ipilimumab will be a major blockbuster cancer drug for years to come,” Medarex shareholder Kenneth Blumberg said July 23 in a complaint in federal court in Trenton, New Jersey.
New York-based Bristol-Myers is acquiring companies and forming partnerships to find new products to offset losses from Plavix, its top-selling medicine, when the anti-clotting drug faces generic competition in 2012. Bristol-Myers said it will pay for the Medarex acquisition with cash, and it had about $9 billion as of June 30.
Brian Henry, a Bristol-Myers spokesman, declined to comment on the complaint. A Medarex spokeswoman, Nichol Ochsner, didn’t immediately return a call seeking comment.
Blumberg’s complaint alleges breach of fiduciary duty by Bristol-Myers, Medarex and its directors, as well aiding and abetting such a breach. The shareholder, who seeks class-action, or group, status, asked a judge to void the deal.
The board at Medarex failed to negotiate a change-of- control premium that exceeded the close of $17.90 on Aug. 21, 2007, according to the complaint by Blumberg.
‘Financially Unfair’
The acquisition is “procedurally and financially unfair” and the “product of a flawed sales process” in which Medarex failed to explore “alternative opportunities for other strategic combinations, and then erected unreasonable deal protection devices,” according to the complaint.
Blumberg, who lives in Pikesville, Maryland, owns “tens of thousands” of Medarex shares, according to the complaint.
Bristol-Myers fell 16 cents to $21.24 at 1:09 p.m. in New York Stock Exchange composite trading. Medarex fell 2 cents to $15.88 in Nasdaq Stock Market trading.
The case is Blumberg v. Pien, 09-cv-3615, U.S. District Court, District of New Jersey (

auch noch dieses hier, wird schon spannend
(interessant übrigens, dass der Kläger vielleicht wirklich identisch mit dem user "kblumb" vom yahoo-Messageboard ist). Hier der Text:
---------------------
By David Voreacos and Phil Milford
July 27 (Bloomberg) -- Medarex Inc. was sued by an investor who claims he would be shortchanged in a $2.4 billion takeover by drugmaker Bristol-Myers Squibb Co.
The companies announced the acquisition on July 22, saying Bristol-Myers would pay a 90 percent premium over the closing price of $8.40 a share for Medarex before the announcement. The deal would give Bristol-Myers full ownership of the skin-cancer drug ipilimumab, which it had been developing jointly with Princeton, New Jersey-based Medarex.
The price is “grossly inadequate” because of the “very real possibility that ipilimumab will be a major blockbuster cancer drug for years to come,” Medarex shareholder Kenneth Blumberg said July 23 in a complaint in federal court in Trenton, New Jersey.
New York-based Bristol-Myers is acquiring companies and forming partnerships to find new products to offset losses from Plavix, its top-selling medicine, when the anti-clotting drug faces generic competition in 2012. Bristol-Myers said it will pay for the Medarex acquisition with cash, and it had about $9 billion as of June 30.
Brian Henry, a Bristol-Myers spokesman, declined to comment on the complaint. A Medarex spokeswoman, Nichol Ochsner, didn’t immediately return a call seeking comment.
Blumberg’s complaint alleges breach of fiduciary duty by Bristol-Myers, Medarex and its directors, as well aiding and abetting such a breach. The shareholder, who seeks class-action, or group, status, asked a judge to void the deal.
The board at Medarex failed to negotiate a change-of- control premium that exceeded the close of $17.90 on Aug. 21, 2007, according to the complaint by Blumberg.
‘Financially Unfair’
The acquisition is “procedurally and financially unfair” and the “product of a flawed sales process” in which Medarex failed to explore “alternative opportunities for other strategic combinations, and then erected unreasonable deal protection devices,” according to the complaint.
Blumberg, who lives in Pikesville, Maryland, owns “tens of thousands” of Medarex shares, according to the complaint.
Bristol-Myers fell 16 cents to $21.24 at 1:09 p.m. in New York Stock Exchange composite trading. Medarex fell 2 cents to $15.88 in Nasdaq Stock Market trading.
The case is Blumberg v. Pien, 09-cv-3615, U.S. District Court, District of New Jersey (
Antwort auf Beitrag Nr.: 37.655.366 von quepos am 27.07.09 20:56:38Hi,
hat bereits jemand oder hat jemand vor dieser Sammelklage beizutreten? Kennt sich da jemand aus. Welche Konsequenzen hat dies für den Einzelnen?
Die nächsten Wochen werden wohl wirklich interessant werden. Bin schon gespannt, wie sich das weiterentwickelt bei MEDX.
Wer hat schon Kasse gemacht? Wer bleibt dabei?
Naja, allen viel Erfolg
lg
Lycos
hat bereits jemand oder hat jemand vor dieser Sammelklage beizutreten? Kennt sich da jemand aus. Welche Konsequenzen hat dies für den Einzelnen?
Die nächsten Wochen werden wohl wirklich interessant werden. Bin schon gespannt, wie sich das weiterentwickelt bei MEDX.
Wer hat schon Kasse gemacht? Wer bleibt dabei?
Naja, allen viel Erfolg

lg
Lycos
Antwort auf Beitrag Nr.: 37.657.759 von Lycos2 am 28.07.09 09:55:42Lieber Lycos2,
ich habe keinerlei Ahnung wie man einer solchen Sammelklage beitritt.
Ich habe einen Teil meines Medarexanteils realisiert.
Jetzt besitze ich noch etwas über 3.300 Aktien von Medarex.
Ich schau mir die sache noch etwas an,vll.kommt ja noch ein Mitschreiter.
ich habe keinerlei Ahnung wie man einer solchen Sammelklage beitritt.

Ich habe einen Teil meines Medarexanteils realisiert.
Jetzt besitze ich noch etwas über 3.300 Aktien von Medarex.
Ich schau mir die sache noch etwas an,vll.kommt ja noch ein Mitschreiter.

Geld Geld-Brief Brief Brief-Stk. Spread Zeit
L&S RT 0 -11,19 € - 11,24 € -16:11:13
Der kurs steigt,das hat wohl nicht nur mit Währungsschwankungen zu tun.
PS.Abwarten,und bleiben.
bleiben.
L&S RT 0 -11,19 € - 11,24 € -16:11:13
Der kurs steigt,das hat wohl nicht nur mit Währungsschwankungen zu tun.

PS.Abwarten,und
 bleiben.
bleiben.
Antwort auf Beitrag Nr.: 37.661.757 von Bioperle am 28.07.09 16:14:55Wenn du meinst 
In USA kostet es 15,88 bis 15,90.....

In USA kostet es 15,88 bis 15,90.....
Antwort auf Beitrag Nr.: 37.661.777 von eck64 am 28.07.09 16:16:57Na ja der kurs in den USA scheint festgezurrt zu sein .
Schade...........
Schade...........
Antwort auf Beitrag Nr.: 37.647.942 von ipollit am 26.07.09 13:30:17ipollit, du bist auf dem falschen Dampfer. Leider bringt es keinem mehr was (weder dir noch mir), zu erklären, wo das von mir reklamierte Potential steckt und wieso es von der breiten Masse so massiv übersehen wurde. 3 Jahre intensivsten Research kann ich dir hier nicht in Kürze darlegen und dich mit wenigen Worten und Fakten überzeugen. Wie gesagt, auch egal, die Firma geht weg....
Antwort auf Beitrag Nr.: 37.655.364 von MrBean07 am 27.07.09 20:55:57Die oben genannten Handelsvolumina im Vergleich zu den gesamten shares sagen übrigens rein gar nichts darüber aus, wieviel BMS davon bereits erworben haben könnte.
Absolut korrekt.
Absolut korrekt.
Antwort auf Beitrag Nr.: 37.655.366 von quepos am 27.07.09 20:56:38Es ist kblumb,kann ich dir bestätigen.
Antwort auf Beitrag Nr.: 37.657.759 von Lycos2 am 28.07.09 09:55:42Ich bleibe bis kurz vor dem Ablauf der Frist bei meinen Aktien und entscheide dann. So einfach und schnell wird sie Brystol-Myers Sq..-Dingsbums nicht stehlen können. Ich hoffe noch viele Aktionäre werden so handeln, das könnte - auch ohne Gegenangebot BMY etwas unter Druck setzen.
Antwort auf Beitrag Nr.: 37.662.017 von Bioperle am 28.07.09 16:38:22Du siehst den Dollar leicht fallen heute, daher der kleine Anstieg. Ansonsten festgezurrt auf 15,88 bis 15,90 in USA.
July 28, 2009 05:00 AM Eastern Daylight Time
Bristol-Myers Squibb Begins Tender Offer to Acquire Medarex, Inc.
NEW YORK--(BUSINESS WIRE)--Bristol-Myers Squibb Company (NYSE:BMY) is commencing today, through its wholly owned subsidiary Puma Acquisition Corporation, a cash tender offer to purchase all outstanding shares of common stock of Medarex, Inc. (NASDAQ:MEDX). Bristol-Myers Squibb announced on Wednesday, July 22 its intent to acquire Medarex.
Upon the successful closing of the tender offer, shareholders of Medarex will receive $16.00 in cash for each share of Medarex common stock validly tendered and not validly withdrawn in the offer, without interest and less any required withholding taxes. Following the purchase of shares in the tender offer, Medarex will become a subsidiary of Bristol-Myers Squibb.
Bristol-Myers Squibb will file today with the Securities and Exchange Commission (SEC) a tender offer statement on Schedule TO that provides the terms of the tender offer. Medarex will file today with the SEC a solicitation/recommendation statement on Schedule 14D-9 that includes the recommendation of the Medarex board of directors that Medarex shareholders accept the tender offer and tender their shares to Bristol-Myers Squibb. As previously announced, Medarex's board of directors has unanimously concluded that the merger agreement and its related transactions (including the tender offer and the merger) are advisable, fair, and in the best interests of Medarex and its shareholders that are unaffiliated with Bristol-Myers Squibb.
The tender offer will expire at 12:00 midnight (New York City time) on Monday, August 24, 2009, unless extended in accordance with the merger agreement and the applicable rules and regulations of the SEC. The closing of the tender offer is subject to customary terms and conditions, including the tender of a number of shares that, together with the number of shares already owned by Bristol-Myers Squibb, constitutes at least a majority of Medarex’s outstanding shares of common stock (on a fully diluted basis) and expiration or termination of the waiting period under the Hart Scott Rodino Antitrust Improvement Act.
Georgeson Inc. is acting as information agent for Bristol-Myers Squibb. J.P. Morgan Securities Inc. is serving as financial advisor to Bristol-Myers Squibb in connection with the transactions and will be the dealer-manager for the tender offer. Cravath, Swaine & Moore LLP is acting as legal counsel to Bristol-Myers Squibb. Goldman, Sachs & Co. is serving as financial advisor to Medarex in connection with the transactions and Medarex is represented by Covington & Burling LLP.
Bristol-Myers Squibb Begins Tender Offer to Acquire Medarex, Inc.
NEW YORK--(BUSINESS WIRE)--Bristol-Myers Squibb Company (NYSE:BMY) is commencing today, through its wholly owned subsidiary Puma Acquisition Corporation, a cash tender offer to purchase all outstanding shares of common stock of Medarex, Inc. (NASDAQ:MEDX). Bristol-Myers Squibb announced on Wednesday, July 22 its intent to acquire Medarex.
Upon the successful closing of the tender offer, shareholders of Medarex will receive $16.00 in cash for each share of Medarex common stock validly tendered and not validly withdrawn in the offer, without interest and less any required withholding taxes. Following the purchase of shares in the tender offer, Medarex will become a subsidiary of Bristol-Myers Squibb.
Bristol-Myers Squibb will file today with the Securities and Exchange Commission (SEC) a tender offer statement on Schedule TO that provides the terms of the tender offer. Medarex will file today with the SEC a solicitation/recommendation statement on Schedule 14D-9 that includes the recommendation of the Medarex board of directors that Medarex shareholders accept the tender offer and tender their shares to Bristol-Myers Squibb. As previously announced, Medarex's board of directors has unanimously concluded that the merger agreement and its related transactions (including the tender offer and the merger) are advisable, fair, and in the best interests of Medarex and its shareholders that are unaffiliated with Bristol-Myers Squibb.
The tender offer will expire at 12:00 midnight (New York City time) on Monday, August 24, 2009, unless extended in accordance with the merger agreement and the applicable rules and regulations of the SEC. The closing of the tender offer is subject to customary terms and conditions, including the tender of a number of shares that, together with the number of shares already owned by Bristol-Myers Squibb, constitutes at least a majority of Medarex’s outstanding shares of common stock (on a fully diluted basis) and expiration or termination of the waiting period under the Hart Scott Rodino Antitrust Improvement Act.
Georgeson Inc. is acting as information agent for Bristol-Myers Squibb. J.P. Morgan Securities Inc. is serving as financial advisor to Bristol-Myers Squibb in connection with the transactions and will be the dealer-manager for the tender offer. Cravath, Swaine & Moore LLP is acting as legal counsel to Bristol-Myers Squibb. Goldman, Sachs & Co. is serving as financial advisor to Medarex in connection with the transactions and Medarex is represented by Covington & Burling LLP.
Antwort auf Beitrag Nr.: 37.663.689 von SLGramann am 28.07.09 19:38:22
Der Aufkauf hat nun also begonnen.
Hier das SEC-File mit den Details:
http://www.sec.gov/Archives/edgar/data/14272/000095012309026…
Der Aufkauf hat nun also begonnen.
Hier das SEC-File mit den Details:
http://www.sec.gov/Archives/edgar/data/14272/000095012309026…
Moin,

bzw.


aber ich werde auch langsam fatalistisch und konzentriere mich auf das lachende Auge.
sich einer Klage anzuschließen, macht m.E. keinerlei Sinn - für die Aufmerksamkeit der Anlegergemeinde ist so immerhin gesorgt (die Pharmas beobachten eh alles mit Argusaugen). Ob Pfizer, Sanofi-Aventis oder sonst wer ein höheres Angebot abgeben, kann man jedoch nicht völlig ausschließen.
Werde erstmal abwarten, was meine Bank mir zuschickt, bis zum Ende der Frist im August kann man ja auf jeden Fall halten (hier in D könnte es eine kürzere Frist geben, um die fristgerechte Rückmeldung nach USA zu gewährleisten). Wenn überhaupt, wird eine Gegenofferte wohl bald kommen, sonst macht es irgendwann keinen Sinn mehr. Es sei denn, sie bekommen die Mehrheit tatsächlich deutlich nicht hin, da würde aber wahrscheinlich irgendwas durchsickern und der Kurs über 16$ gehen (ist auch sehr unwahrscheinlich).
Über die Frist hinaus halten werde ich wohl nicht, der Handel würde auch bald extrem dünn oder sogar eingestellt werden, dann gibt´s auch Probleme.
Ein squeeze-out der letzten Aktien kann man versuchen, aber da weiß ich nicht so genau, wie das in USA geregelt ist, vielleicht kann man da ewig warten.
so long
q.

bzw.


aber ich werde auch langsam fatalistisch und konzentriere mich auf das lachende Auge.
sich einer Klage anzuschließen, macht m.E. keinerlei Sinn - für die Aufmerksamkeit der Anlegergemeinde ist so immerhin gesorgt (die Pharmas beobachten eh alles mit Argusaugen). Ob Pfizer, Sanofi-Aventis oder sonst wer ein höheres Angebot abgeben, kann man jedoch nicht völlig ausschließen.
Werde erstmal abwarten, was meine Bank mir zuschickt, bis zum Ende der Frist im August kann man ja auf jeden Fall halten (hier in D könnte es eine kürzere Frist geben, um die fristgerechte Rückmeldung nach USA zu gewährleisten). Wenn überhaupt, wird eine Gegenofferte wohl bald kommen, sonst macht es irgendwann keinen Sinn mehr. Es sei denn, sie bekommen die Mehrheit tatsächlich deutlich nicht hin, da würde aber wahrscheinlich irgendwas durchsickern und der Kurs über 16$ gehen (ist auch sehr unwahrscheinlich).
Über die Frist hinaus halten werde ich wohl nicht, der Handel würde auch bald extrem dünn oder sogar eingestellt werden, dann gibt´s auch Probleme.
Ein squeeze-out der letzten Aktien kann man versuchen, aber da weiß ich nicht so genau, wie das in USA geregelt ist, vielleicht kann man da ewig warten.
so long
q.
Antwort auf Beitrag Nr.: 37.664.803 von quepos am 28.07.09 21:33:45weil's hier her passt - beitrag von erniewerner ausm yahoo-board
Re: Tender Started 28-Jul-09 09:45 am
<<Also, how does the tender work?>>
If the tender succeeds, all shareholders, including those who did not tender, will get the full $16 per share.
If the tender is not succeeding, BMY will extend the offer period and negotiate with enough of the large 'swing votes' holding out to see what it will take to get them to tender. Whatever price they pay, will be the price everyone gets.
If a competing offer comes in that is superior to the BMY offer, the BMY $16 tender will fail. Shareholders have the right to withdraw their tendered shares at any time.
As a shareholder, at this time, it is in your best interest to not tender your shares. The only things that will get BMY to raise the offer are imminent failure of the tender or a competing bid.
<<Will the share (ask) price go up to 16 today or will we be contacted to tender our shares.>>
You will be contacted by your broker. The stock will continue to trade based on expectations. If the markets senses a sweetened offer, it may trade above $16.
Re: Tender Started 28-Jul-09 09:45 am
<<Also, how does the tender work?>>
If the tender succeeds, all shareholders, including those who did not tender, will get the full $16 per share.
If the tender is not succeeding, BMY will extend the offer period and negotiate with enough of the large 'swing votes' holding out to see what it will take to get them to tender. Whatever price they pay, will be the price everyone gets.
If a competing offer comes in that is superior to the BMY offer, the BMY $16 tender will fail. Shareholders have the right to withdraw their tendered shares at any time.
As a shareholder, at this time, it is in your best interest to not tender your shares. The only things that will get BMY to raise the offer are imminent failure of the tender or a competing bid.
<<Will the share (ask) price go up to 16 today or will we be contacted to tender our shares.>>
You will be contacted by your broker. The stock will continue to trade based on expectations. If the markets senses a sweetened offer, it may trade above $16.
Antwort auf Beitrag Nr.: 37.665.095 von PathFinder2 am 28.07.09 21:58:50The only things that will get BMY to raise the offer are imminent failure of the tender or a competing bid.
Habe meine Meinung aus gegebenem Anlaß geändert und zu 11,15 verkauft. Es hat auch schon Fälle gegeben, da wurde die Offerte zurückgenommen. Der Übernehmer könnte bei näherem Hinsehen oder durch neue Ergebnisse durchaus sein Angebot zuückziehen.
Pfizer wird erstmal nichts kaufen, Sanofi hat sich bereits bei MAbs eingedeckt mit Regeneron, kommen beide als Bieter nicht infrage.
Habe meine Meinung aus gegebenem Anlaß geändert und zu 11,15 verkauft. Es hat auch schon Fälle gegeben, da wurde die Offerte zurückgenommen. Der Übernehmer könnte bei näherem Hinsehen oder durch neue Ergebnisse durchaus sein Angebot zuückziehen.
Pfizer wird erstmal nichts kaufen, Sanofi hat sich bereits bei MAbs eingedeckt mit Regeneron, kommen beide als Bieter nicht infrage.
Das Material zu diesem Preis geht aus!
Und dann wird man sehen.
Bin heute auch zu 11,30 außerbörslich raus. Vielleicht kann ich damit in den nächsten Tagen noch mal günstig bei Morphosys nachlegen.


Antwort auf Beitrag Nr.: 37.663.405 von Ville7 am 28.07.09 19:00:21Ich bleibe bis kurz vor dem Ablauf der Frist bei meinen Aktien und entscheide dann.
Das ist auch meine grundsätzliche Überlegung.
Allerdings habe ich heute ein - schon steuerfreies - Viertel verkauft.
An Gewinnmitnahmen ist noch keiner gestorben. Und mit dem Steuerfreien wollte ich nix riskieren.
Gruß
Zock
Das ist auch meine grundsätzliche Überlegung.
Allerdings habe ich heute ein - schon steuerfreies - Viertel verkauft.
An Gewinnmitnahmen ist noch keiner gestorben. Und mit dem Steuerfreien wollte ich nix riskieren.
Gruß
Zock
Wie läuft das eigentlich ab wenn man das Übernahmeangebot annimmt:
-Wie hoch ist der Preis in Euro wo gezahlt würde (bei jetztigem Dollarkurs)???
-Wenn ich das Übernahmeangebot annehme spare ich mir die Ordergebühr oder?
-Wie hoch ist der Preis in Euro wo gezahlt würde (bei jetztigem Dollarkurs)???
-Wenn ich das Übernahmeangebot annehme spare ich mir die Ordergebühr oder?
Der störrische Esel hats vom tiefen Süden bis kaum zum Äquator zurück geschafft. Und nun ein aus für die freie Medx-Maus?
Hallo zusammen,
mal ne blöde Frage in die Runde.
Was passiert denn wenn ich bis zum 18.08.2009 (schreibt meine Bank) nichts unternehme und die Sache einfach "aussitze"? Bekomme ich bei einer Fusion mit BMS dann "deren" Aktien im Verhältnis wie auch immer? Oder sind meine MDX-Aktien dann "wertlos"?
Da ich ein solches Szenario noch nie hatte wäre ich für eine Antwort sehr dankbar.
Grüße
Gorko
mal ne blöde Frage in die Runde.
Was passiert denn wenn ich bis zum 18.08.2009 (schreibt meine Bank) nichts unternehme und die Sache einfach "aussitze"? Bekomme ich bei einer Fusion mit BMS dann "deren" Aktien im Verhältnis wie auch immer? Oder sind meine MDX-Aktien dann "wertlos"?
Da ich ein solches Szenario noch nie hatte wäre ich für eine Antwort sehr dankbar.
Grüße
Gorko
Antwort auf Beitrag Nr.: 37.708.933 von GorkoLuno am 04.08.09 17:22:20Ich hatte so ein Ding mit US-Aktien auch noch nie.
Wertlos ist nicht. Bis jetzt gibt es ein freundliches Übernahmeangebot, dass der MEDX-Vorstand befürwortet.
Also wahrscheinlich können die einen Großteil der Aktien einsammeln. Und wie es weitergeht hängt vor allem daran, wie viele nicht verkaufen und auf Nachbesserung hoffen.
Es gibt auch Firmen die Jahrelang mit Minifreefloat und Beherrschungsvertrag weitergführt werden wie z.B. die Audi AG.
Kommt drauf an, wie schnell BMS die 100% will und ob die Klagen gegen den vereinbarten Preis noch Erfolg haben.
Üblicherweise kannst du eher noch höhere Preise erwarten, aber sicher ist das nicht. Und erst recht nicht, dass BMS z.B. die Notierung in Deutschland weiter aufrecht erhält. Börse Frankfurt dürfte noch weit illiquider werden als sie es ist und auch L&S wird nicht ewig weitertaxen, wenns zu langweilig wird.
Wertlos ist nicht. Bis jetzt gibt es ein freundliches Übernahmeangebot, dass der MEDX-Vorstand befürwortet.
Also wahrscheinlich können die einen Großteil der Aktien einsammeln. Und wie es weitergeht hängt vor allem daran, wie viele nicht verkaufen und auf Nachbesserung hoffen.
Es gibt auch Firmen die Jahrelang mit Minifreefloat und Beherrschungsvertrag weitergführt werden wie z.B. die Audi AG.
Kommt drauf an, wie schnell BMS die 100% will und ob die Klagen gegen den vereinbarten Preis noch Erfolg haben.
Üblicherweise kannst du eher noch höhere Preise erwarten, aber sicher ist das nicht. Und erst recht nicht, dass BMS z.B. die Notierung in Deutschland weiter aufrecht erhält. Börse Frankfurt dürfte noch weit illiquider werden als sie es ist und auch L&S wird nicht ewig weitertaxen, wenns zu langweilig wird.
Antwort auf Beitrag Nr.: 37.709.018 von eck64 am 04.08.09 17:31:32Es ist ganz einfach. Es gibt einen Merger Agreement, dem Unternehmensführung und das Board of Directors unterschrieben haben. Sollte BMS es schaffen, 50% + 1 Aktie zu erringen, dann wird der Rest mit ebenfalls 16USD abgefunden. Es ist quasi ein Squeeze Out. Ich selbst bin ziemlich geschockt, dass in USA so etwas möglich ist. In Deutschland geht so ein Squeeze Out so einfach nicht, da braucht man schon 95% der Aktien oder muss anstelle Cash Aktientausch in die gemergte Company anbieten. Die Wut der Kleinaktionäre und die Class Action Lawsuits sind mehr als zu verstehen.
Antwort auf Beitrag Nr.: 37.710.270 von Ville7 am 04.08.09 20:14:06 Sollte BMS es schaffen, 50% + 1 Aktie zu erringen, dann wird der Rest mit ebenfalls 16USD abgefunden. Es ist quasi ein Squeeze Out. 

Ist mir neu, kannte ich so nicht und echt ein übles Ding.
Gebt dem Board zunder!


Ist mir neu, kannte ich so nicht und echt ein übles Ding.
Gebt dem Board zunder!
Das gleiche Spiel hatten wir m.E. z.B. auch schon bei Medimmune und bei Millennium. Aber wir haben ja noch ein paar Tage zu hoffen, daß der Weiße Ritter kommt....
ach ja, bei CV Therapeutics (durch Gilead) ging die Abfindung auch recht schnell
Antwort auf Beitrag Nr.: 37.710.270 von Ville7 am 04.08.09 20:14:06Heißt also das ich auf jedn Fall meine 16 US$ bekomme (vorausgesetzt die 50%+1 Aktien werden geschafft)... also mache ich am Besten gar nichts, hab ich keinen Ärger, keine Lauferei und freue mich dann einfach irgendwann das Geld auf meinen Konto zu sehen, richtig?
Oder hab ich jetzt irgendwas falsch verstanden?!?
Oder hab ich jetzt irgendwas falsch verstanden?!?

Antwort auf Beitrag Nr.: 37.713.002 von GorkoLuno am 05.08.09 09:52:01So einfach kann es dann wohl auch nicht sein.
Sonst würde es sich doch überhaupt nicht lohnen auf das Angebot einzugehen. Man wartet einfach ab und vielleicht springt noch mehr dabei heraus. Der einzige Haken den ich jetzt noch sehe ist ein steigender oder fallender Euro und damit Wertverlust bzw.-steigerung.
Bei mir steht im Schreiben:"Bei dieser Kapitalmaßnahme können ausländische Gebühren und Steuern in noch nicht bekannter Höhe anfallen." Was erwartet mich da noch?
Sonst würde es sich doch überhaupt nicht lohnen auf das Angebot einzugehen. Man wartet einfach ab und vielleicht springt noch mehr dabei heraus. Der einzige Haken den ich jetzt noch sehe ist ein steigender oder fallender Euro und damit Wertverlust bzw.-steigerung.
Bei mir steht im Schreiben:"Bei dieser Kapitalmaßnahme können ausländische Gebühren und Steuern in noch nicht bekannter Höhe anfallen." Was erwartet mich da noch?
Hallo,
sollten man das Angebot nun annehmen oder nicht!?
Was sagst Du dazu @ville!?
Bin hin und her gerissen...
Medarex ist eindeutig mehr wert, als die gebotenen 16 $...
Wie sieht ihr das!?
sollten man das Angebot nun annehmen oder nicht!?
Was sagst Du dazu @ville!?
Bin hin und her gerissen...
Medarex ist eindeutig mehr wert, als die gebotenen 16 $...
Wie sieht ihr das!?
Antwort auf Beitrag Nr.: 37.760.304 von where_is_the_beef am 12.08.09 09:38:48Hi,
mir gehts genauso. Bin auch hin und hergerissen. Das triffts ganz gut.
Irgendwie mag ich gar nicht mehr an ein Gegenangebot glauben. Aus welchem Grund auch immer. JNJ ist für viele der potentielle Kandidat. Aber vielleicht wollen die ja bewusst auch den Preis für MEDX niedrig halten. Spekulationen über einen Merger JNJ & BMS gabs ja schon häufiger.
Was kann sonst noch passieren?
BMS schafft es die geforderten Aktien zusammenzubringen. 16 USD und Ofen aus. (70%)
BMS schafft es nicht --> entweder sie erhöhen das Angebot um 2 - 3 USD (20%) oder sie sagen die Übernahme ab (10%).
Meine persönlichen Einschätzungen in % in ().
mir gehts genauso. Bin auch hin und hergerissen. Das triffts ganz gut.
Irgendwie mag ich gar nicht mehr an ein Gegenangebot glauben. Aus welchem Grund auch immer. JNJ ist für viele der potentielle Kandidat. Aber vielleicht wollen die ja bewusst auch den Preis für MEDX niedrig halten. Spekulationen über einen Merger JNJ & BMS gabs ja schon häufiger.
Was kann sonst noch passieren?
BMS schafft es die geforderten Aktien zusammenzubringen. 16 USD und Ofen aus. (70%)
BMS schafft es nicht --> entweder sie erhöhen das Angebot um 2 - 3 USD (20%) oder sie sagen die Übernahme ab (10%).
Meine persönlichen Einschätzungen in % in ().

Antwort auf Beitrag Nr.: 37.762.122 von Lycos2 am 12.08.09 12:50:07mir gehts genauso. Bin auch hin und hergerissen
Mir gehts genauso,
auch ich habe noch die hälfte meines Medarexdepots.
Wenn man die gehandelten Aktien an der Nasdaq sieht ,
sollten nicht mehr viele im freien Umlauf sein.
Siehe dazu:Stücke
11.08.09 3.399.800
10.08.09 1.675.100
07.08.09 4.075.400
06.08.09 5.741.500
05.08.09 8.856.000
04.08.09 2.480.900
03.08.09 9.048.100
31.07.09 7.102.100
30.07.09 7.003.100
29.07.09 5.763.000
28.07.09 9.602.000
27.07.09 7.028.700
24.07.09 12.674.100
23.07.09 77.239.800
--------------
161.689.600
Aktienanzahl 127,3 Mio. (Stand: 16.12.08)
www.ariva.de/medarex-aktie
PS.Ich warte noch ein paar tage ab.
Mir gehts genauso,
auch ich habe noch die hälfte meines Medarexdepots.

Wenn man die gehandelten Aktien an der Nasdaq sieht ,
sollten nicht mehr viele im freien Umlauf sein.
Siehe dazu:Stücke
11.08.09 3.399.800
10.08.09 1.675.100
07.08.09 4.075.400
06.08.09 5.741.500
05.08.09 8.856.000
04.08.09 2.480.900
03.08.09 9.048.100
31.07.09 7.102.100
30.07.09 7.003.100
29.07.09 5.763.000
28.07.09 9.602.000
27.07.09 7.028.700
24.07.09 12.674.100
23.07.09 77.239.800
--------------
161.689.600

Aktienanzahl 127,3 Mio. (Stand: 16.12.08)
www.ariva.de/medarex-aktie
PS.Ich warte noch ein paar tage ab.
Mir gehts wie euch. Ich halte mir die Entscheidung bis zur letzten Minute offen und entscheide dann ob ich tendere.
Ich bin übrigens nicht der Meinung, dass die meisten Stücke schon bei BMS sind. Möglicherweise hat jemand anderer die Stücke gesammelt um ebenfalls auf ein höheres Gebot zu setzen oder BMS dazu zu drängen.
Also folgende Möglichkeiten:
1. BMS kommt easy durch mit dem 16er Angebot und hat am Ende mehr als 50%, dann kann man anscheinend jederzeit seine Aktien zu 16USD umtauschen gemäß Merger Vertrag.
2. BMS kommt nicht durch, hat weniger als 50% und muss erhöhen um die Mehrheit zu erlengen. Dann bekommt man mehr als 16USD.
3. Ein weiterer Bieter steigt ein: Dann bekommt man viel mehr als 16USD, da man ein Bietergefecht erwarten kann.
Für mich ist die Untergrenze somit ca. 16USD. Ich verliere somit m.E. nichts, wenn ich erstmal zuwarte. Ich kann nur gewinnen, wenn ich Glück habe und BMS Pech.
Im Übrigen sind die Umsätze heute premarket recht hoch, schon 800TSD Stück nur premarket bisher. Zudem ist der Preis auf 15.95 angesprungen.
Ich bin übrigens nicht der Meinung, dass die meisten Stücke schon bei BMS sind. Möglicherweise hat jemand anderer die Stücke gesammelt um ebenfalls auf ein höheres Gebot zu setzen oder BMS dazu zu drängen.
Also folgende Möglichkeiten:
1. BMS kommt easy durch mit dem 16er Angebot und hat am Ende mehr als 50%, dann kann man anscheinend jederzeit seine Aktien zu 16USD umtauschen gemäß Merger Vertrag.
2. BMS kommt nicht durch, hat weniger als 50% und muss erhöhen um die Mehrheit zu erlengen. Dann bekommt man mehr als 16USD.
3. Ein weiterer Bieter steigt ein: Dann bekommt man viel mehr als 16USD, da man ein Bietergefecht erwarten kann.
Für mich ist die Untergrenze somit ca. 16USD. Ich verliere somit m.E. nichts, wenn ich erstmal zuwarte. Ich kann nur gewinnen, wenn ich Glück habe und BMS Pech.
Im Übrigen sind die Umsätze heute premarket recht hoch, schon 800TSD Stück nur premarket bisher. Zudem ist der Preis auf 15.95 angesprungen.
Associated Press
Bristol-Myers says Medarex deal cleared in review
Associated Press, 08.12.09, 10:29 AM EDT
NEW YORK -- Bristol-Myers Squibb Co. said Wednesday a regulatory review period for its acquisition of Medarex Inc. has expired, allowing the $2.1 billion deal to go forward.
The review of the deal was required under antitrust law. Plavix maker Bristol-Myers agreed to buy Medarex ( MEDX - news - people ), a biotechnology company, on July 28. The offer values Medarex shares at $16 each, and Medarex's board of directors has recommended shareholders support the deal.
http://www.forbes.com/feeds/ap/2009/08/12/ap6770587.html
Bristol-Myers says Medarex deal cleared in review
Associated Press, 08.12.09, 10:29 AM EDT
NEW YORK -- Bristol-Myers Squibb Co. said Wednesday a regulatory review period for its acquisition of Medarex Inc. has expired, allowing the $2.1 billion deal to go forward.
The review of the deal was required under antitrust law. Plavix maker Bristol-Myers agreed to buy Medarex ( MEDX - news - people ), a biotechnology company, on July 28. The offer values Medarex shares at $16 each, and Medarex's board of directors has recommended shareholders support the deal.
http://www.forbes.com/feeds/ap/2009/08/12/ap6770587.html
Moin,

habe noch alle Aktien. Die Nachricht besagt überhaupt nichts darüber, wieviele Aktien BMS haben. Es geht nur um kartellrechtliche (?) Formalien, die anscheinend erfüllt sind.
Das immerhin um 6-7 Cent Anziehen des Kurses kann verschieden gedeutet werden, ich versuchs daher garnicht.
Warte auch weiter ab.
Im Gegensatz zu anderen hier hat sich meine Bank noch nicht mal bei mir gemeldet, sollte das so bleinen, machen sie sich ja schon einer Unterlassung schuldig, soll mir nur recht sein (könnte man sie ja verklagen, wenn der Deal scheitert und der Kurs absackt).
Das halte ich aber für ein unwahrscheinliches Szenario.
Gruß q.

habe noch alle Aktien. Die Nachricht besagt überhaupt nichts darüber, wieviele Aktien BMS haben. Es geht nur um kartellrechtliche (?) Formalien, die anscheinend erfüllt sind.
Das immerhin um 6-7 Cent Anziehen des Kurses kann verschieden gedeutet werden, ich versuchs daher garnicht.
Warte auch weiter ab.
Im Gegensatz zu anderen hier hat sich meine Bank noch nicht mal bei mir gemeldet, sollte das so bleinen, machen sie sich ja schon einer Unterlassung schuldig, soll mir nur recht sein (könnte man sie ja verklagen, wenn der Deal scheitert und der Kurs absackt).
Das halte ich aber für ein unwahrscheinliches Szenario.
Gruß q.
Antwort auf Beitrag Nr.: 37.767.201 von quepos am 12.08.09 21:46:50wenn du comdirect hast, schau mal in deinen posteingang im depot. da kannst du online weisung machen. cortalconsors hat mir ein briefchen geschickt, da geht das per fax.
ansonsten ist die alleinige tatsache, dass BMY noch nicht gemeldet hat, dass sie 50%+ haben das indiz, dass sie es bisher nicht erreicht haben. denn eine 50%+ Meldung würde nahezu alle anderen zum tenderen bringen, da der rest der teilnehmer im mergerfalle auch 16usd erhält, aber ohne zinsen bei zuwarten.
die gestrige meldung von bmy ist erneut ein versuch die aktionäre in den tender zu bringen, marketing eben. aber ihr habt keine eile, wartet den letzten tag der frist ab und entscheidet an diesem tag. JMHO.
ansonsten ist die alleinige tatsache, dass BMY noch nicht gemeldet hat, dass sie 50%+ haben das indiz, dass sie es bisher nicht erreicht haben. denn eine 50%+ Meldung würde nahezu alle anderen zum tenderen bringen, da der rest der teilnehmer im mergerfalle auch 16usd erhält, aber ohne zinsen bei zuwarten.
die gestrige meldung von bmy ist erneut ein versuch die aktionäre in den tender zu bringen, marketing eben. aber ihr habt keine eile, wartet den letzten tag der frist ab und entscheidet an diesem tag. JMHO.
Ärgerlich, dass der Euro immer stärker wird und dadurch 16USD immer weniger wert werden.
Antwort auf Beitrag Nr.: 37.768.349 von Ville7 am 13.08.09 06:39:55Hallo,

nun habe ich immerhin eine E-mail bekommen, dass etwas in meiner postbox ist (bin zumindest bei MEDX bei onvista). Schade, hätte mich lieber blind und taub gestellt, E-mail ist wohl rechtlich so wie Brief.
Auch mir wurde ein Ultimatum von 19.08.09 (sogar mit Uhrzeit 12:00) mitgeteilt, obwohl der Stichtag doch der 24.08.08 (?) war.
Naja, eine E-mail in die USA kann natürlich schom mal 5 Tage dauern, muß ja schließlich alles auch durch CIA, FBI, NSA usw. überprüft werden.

So long, werden seh´n, was passiert!
q.

nun habe ich immerhin eine E-mail bekommen, dass etwas in meiner postbox ist (bin zumindest bei MEDX bei onvista). Schade, hätte mich lieber blind und taub gestellt, E-mail ist wohl rechtlich so wie Brief.
Auch mir wurde ein Ultimatum von 19.08.09 (sogar mit Uhrzeit 12:00) mitgeteilt, obwohl der Stichtag doch der 24.08.08 (?) war.
Naja, eine E-mail in die USA kann natürlich schom mal 5 Tage dauern, muß ja schließlich alles auch durch CIA, FBI, NSA usw. überprüft werden.

So long, werden seh´n, was passiert!
q.
Bristol-Myers Squibb gibt Hart-Scott-Rodino Überprüfungszeitraum für Medarex Übernahme abgelaufen
12. 12. August 2009 19:06 August 2009 19:06
Bristol-Myers Squibb Company (NYSE: BMY) gab heute bekannt, dass die Hart-Scott-Rodino (HSR) Überprüfungszeitraum für seine Angebot für Medarex, Inc. (NASDAQ: MedX) abgelaufen ist.
Bristol-Myers Squibb, die am 28. Juli 2009, durch seine hundertprozentige Tochtergesellschaft Puma Acquisition Corporation, einem Cash-Angebot zum Erwerb aller ausstehenden Aktien der Medarex für $ 16 je Aktie.
Der Ablauf der HSR Wartezeit erfüllt eine der Voraussetzungen für das Angebot bieten, die läuft um 12 Uhr (Ortszeit New York City) am Montag, 24. August 2009, es sei denn, im Einklang mit den Fusionsvertrag und die geltenden Regeln und Regelungen der SEC.
Die Schließung des Angebots nach wie vor unter den üblichen Bedingungen, einschließlich der Ausschreibung von einer Reihe von Aktien, die zusammen mit der Anzahl der Aktien, die bereits im Besitz von Bristol-Myers Squibb, mindestens der Mehrheit der Medarex der ausstehenden Aktien des Stammkapitals (auf vollständig verwässerter Basis).
JP Morgan Securities Inc. ist als finanzielle Berater für Bristol-Myers Squibb im Zusammenhang mit den Transaktionen und den Händler-Manager für das Angebot. Cravath, Swaine & Moore LLP is acting as legal counsel to Bristol-Myers Squibb. Cravath, Swaine & Moore LLP agiert als Rechtsberater für Bristol-Myers Squibb. Goldman, Sachs & Co. is serving as financial advisor to Medarex in connection with the transactions and Medarex is represented by Covington & Burling LLP. Goldman, Sachs & Co. ist als finanzielle Berater Medarex im Zusammenhang mit den Transaktionen und Medarex wird durch Covington & Burling LLP.
translate.google.de/translate?hl=de&sl=en&u=http://www.news-…

12. 12. August 2009 19:06 August 2009 19:06
Bristol-Myers Squibb Company (NYSE: BMY) gab heute bekannt, dass die Hart-Scott-Rodino (HSR) Überprüfungszeitraum für seine Angebot für Medarex, Inc. (NASDAQ: MedX) abgelaufen ist.
Bristol-Myers Squibb, die am 28. Juli 2009, durch seine hundertprozentige Tochtergesellschaft Puma Acquisition Corporation, einem Cash-Angebot zum Erwerb aller ausstehenden Aktien der Medarex für $ 16 je Aktie.
Der Ablauf der HSR Wartezeit erfüllt eine der Voraussetzungen für das Angebot bieten, die läuft um 12 Uhr (Ortszeit New York City) am Montag, 24. August 2009, es sei denn, im Einklang mit den Fusionsvertrag und die geltenden Regeln und Regelungen der SEC.
Die Schließung des Angebots nach wie vor unter den üblichen Bedingungen, einschließlich der Ausschreibung von einer Reihe von Aktien, die zusammen mit der Anzahl der Aktien, die bereits im Besitz von Bristol-Myers Squibb, mindestens der Mehrheit der Medarex der ausstehenden Aktien des Stammkapitals (auf vollständig verwässerter Basis).
JP Morgan Securities Inc. ist als finanzielle Berater für Bristol-Myers Squibb im Zusammenhang mit den Transaktionen und den Händler-Manager für das Angebot. Cravath, Swaine & Moore LLP is acting as legal counsel to Bristol-Myers Squibb. Cravath, Swaine & Moore LLP agiert als Rechtsberater für Bristol-Myers Squibb. Goldman, Sachs & Co. is serving as financial advisor to Medarex in connection with the transactions and Medarex is represented by Covington & Burling LLP. Goldman, Sachs & Co. ist als finanzielle Berater Medarex im Zusammenhang mit den Transaktionen und Medarex wird durch Covington & Burling LLP.
translate.google.de/translate?hl=de&sl=en&u=http://www.news-…

Vorsicht mit dem Tendern der Aktien!!
Möglicherweise unterliegen die Aktien trotz Kauf in Deutschland bei Annahme des Übernahmeangebots tatsächlich der US Quellensteuer, trotz Stuerfreiheit in Deutschland. Da lohnt sich dann kein Tendern für diejenigen, die in Deutschland gekauft haben. Ich versuche das rechtlich noch rechtzeitig bis 19.8. zu klären und gebe hier Bescheid, falls es mir zeitlich reicht.
Ich mache es jetzt so:
1. knapp 40% habe ich heute über die Börse verkauft, da der Dollarkurs recht günstig, zumindest günstiger als die Tage bzw. Woche zuvor stand.
2. 55% meiner ursprünglichen Aktienzahl werde ich bis nach der Tenderfrist halten und schauen ob BMS die Mehrheit erringt oder gar erhöht. Dieser Teil wird dann ebenfalls über die Börse verkauft, egal was passiert. Ich hoffe natürlich auf eine Erhöhung durch BMS.
3. 15% meiner Aktien sind erst Ende November steuerfrei. Diese versuche ich davor nicht herzugeben, falls es möglich ist um die Stuerfreiheit noch zu erringen, würde sich bei EK unter 4Euro sehr lohnen. Ansonsten verkaufe ich auch vorher über die Börse, falls BMS vor Ende November den Squeeze Out hinbekommt.
Möglicherweise unterliegen die Aktien trotz Kauf in Deutschland bei Annahme des Übernahmeangebots tatsächlich der US Quellensteuer, trotz Stuerfreiheit in Deutschland. Da lohnt sich dann kein Tendern für diejenigen, die in Deutschland gekauft haben. Ich versuche das rechtlich noch rechtzeitig bis 19.8. zu klären und gebe hier Bescheid, falls es mir zeitlich reicht.
Ich mache es jetzt so:
1. knapp 40% habe ich heute über die Börse verkauft, da der Dollarkurs recht günstig, zumindest günstiger als die Tage bzw. Woche zuvor stand.
2. 55% meiner ursprünglichen Aktienzahl werde ich bis nach der Tenderfrist halten und schauen ob BMS die Mehrheit erringt oder gar erhöht. Dieser Teil wird dann ebenfalls über die Börse verkauft, egal was passiert. Ich hoffe natürlich auf eine Erhöhung durch BMS.
3. 15% meiner Aktien sind erst Ende November steuerfrei. Diese versuche ich davor nicht herzugeben, falls es möglich ist um die Stuerfreiheit noch zu erringen, würde sich bei EK unter 4Euro sehr lohnen. Ansonsten verkaufe ich auch vorher über die Börse, falls BMS vor Ende November den Squeeze Out hinbekommt.
Antwort auf Beitrag Nr.: 37.797.497 von Ville7 am 17.08.09 20:25:06Lieber Ville7,
Danke für deinen Beitrag(wohl ein Fehlerteufel eingeschlichen).
40%
+55%
+15%
-----
110%
Bin ziemlich unschlüssig,habe mich aber auch von einem Anteil getrennt.
PS.Der Kurs steigt,warum auch immer.
Danke für deinen Beitrag(wohl ein Fehlerteufel eingeschlichen).
40%
+55%
+15%
-----
110%

Bin ziemlich unschlüssig,habe mich aber auch von einem Anteil getrennt.
PS.Der Kurs steigt,warum auch immer.

Antwort auf Beitrag Nr.: 37.798.400 von Bioperle am 17.08.09 22:39:23Danke für den Hinweis. Die 55% sollten 45% heissen.
Die Aktie ist übrigens deswegen gestiegen, weil der Dollar auf 1,405 zurückkam. Aktuell ist der Dollar bei 1,41. Sollten die Märkte weiter abtauchen und Rohstoffe wie Öl zurückkommen wäre dies gut für den Dollar und somit gut für den Kurs. Ich rechne aber mit einem letzten Move der Märkte und des Euros nach oben und dann erst im September/Oktober einem Absturz und einem stärkeren Dollar.
Die Aktie ist übrigens deswegen gestiegen, weil der Dollar auf 1,405 zurückkam. Aktuell ist der Dollar bei 1,41. Sollten die Märkte weiter abtauchen und Rohstoffe wie Öl zurückkommen wäre dies gut für den Dollar und somit gut für den Kurs. Ich rechne aber mit einem letzten Move der Märkte und des Euros nach oben und dann erst im September/Oktober einem Absturz und einem stärkeren Dollar.
Antwort auf Beitrag Nr.: 37.797.497 von Ville7 am 17.08.09 20:25:06Update: Leider konnte mir mein Broker keine rechtliche Klärung in der Quellensteuersache mitteilen. Vielleicht hat jemand anderer die Angelegenheit klären können, der möge hier bitte posten.
Soeben lief folgende Mitteilung über die Ticker: Bristol-Myers Squibb verlängert Annahmefrist für Medarax-Übernahme, siehe hier:
dpa-afx
Bristol-Myers Squibb verlängert Annahmefrist für Medarax-Übernahme
Donnerstag 20. August 2009, 23:28 Uhr
NEW YORK(dpa-AFX) - Der US-Pharmakonzern Bristol-Myers Squibb (BMS (NYSE: BMY - Nachrichten) ) gibt den Aktionären des Biotechnologie-Unternehmens Medarex zwei Tage mehr Zeit zur Annahme seines Übernahmeangebots. Die Barofferte in Höhe von 16,00 US-Dollar je Aktie sei mit Einwilligung von Medarex (MEDX - Nachrichten) zunächst bis Mittwoch, 26. August Mitternacht (New York City Zeit), verlängert worden, teilte BMS am Donnerstag nach US-Börsenschluss in New York mit. An den Bedingungen des Angebots sei nichts geändert worden. Bis 9.00 Uhr an diesem Tag seien BMS 11,6 Millionen Medarex-Aktien und damit rund 8,7 Prozent des ausstehenden Aktienkapitals offeriert worden. Insgesamt bietet BMS für Medarex 2,4 Milliarden US-Dollar (1,69 Mrd Euro). BMS hatte seine Offerte am 23. Juli bekanntgegeben, der Aufschlag auf den Medarex-Kurs betrug damals rund 90 Prozent./ck
Dies deutet darauf hin, dass nicht alles glatt läuft bei der Übernahme, wohl weil einigen Medarex Aktionären der Preis hier nicht hoch genug erscheint. Ich bin gespannt, wie es hier weitergehen wird, evtl. muss ja Bristol-Myers Squibb sogar nochmal nachlegen, um die Übernahme unter Dach und Fach zu bringen.
Mehr Infos zu Medarex finden Sie übrigens auch hier: http://www.sharewise.com/aktien/US5839161016-medarex/analyse…
LG Enzo
dpa-afx
Bristol-Myers Squibb verlängert Annahmefrist für Medarax-Übernahme
Donnerstag 20. August 2009, 23:28 Uhr
NEW YORK(dpa-AFX) - Der US-Pharmakonzern Bristol-Myers Squibb (BMS (NYSE: BMY - Nachrichten) ) gibt den Aktionären des Biotechnologie-Unternehmens Medarex zwei Tage mehr Zeit zur Annahme seines Übernahmeangebots. Die Barofferte in Höhe von 16,00 US-Dollar je Aktie sei mit Einwilligung von Medarex (MEDX - Nachrichten) zunächst bis Mittwoch, 26. August Mitternacht (New York City Zeit), verlängert worden, teilte BMS am Donnerstag nach US-Börsenschluss in New York mit. An den Bedingungen des Angebots sei nichts geändert worden. Bis 9.00 Uhr an diesem Tag seien BMS 11,6 Millionen Medarex-Aktien und damit rund 8,7 Prozent des ausstehenden Aktienkapitals offeriert worden. Insgesamt bietet BMS für Medarex 2,4 Milliarden US-Dollar (1,69 Mrd Euro). BMS hatte seine Offerte am 23. Juli bekanntgegeben, der Aufschlag auf den Medarex-Kurs betrug damals rund 90 Prozent./ck
Dies deutet darauf hin, dass nicht alles glatt läuft bei der Übernahme, wohl weil einigen Medarex Aktionären der Preis hier nicht hoch genug erscheint. Ich bin gespannt, wie es hier weitergehen wird, evtl. muss ja Bristol-Myers Squibb sogar nochmal nachlegen, um die Übernahme unter Dach und Fach zu bringen.
Mehr Infos zu Medarex finden Sie übrigens auch hier: http://www.sharewise.com/aktien/US5839161016-medarex/analyse…
LG Enzo
Eine äußerst erfreuliche Nachricht, danke.
Antwort auf Beitrag Nr.: 37.822.334 von enzofran am 20.08.09 23:39:12Sehr gut. Meiner Meinung nach wird es ohne Erhöhung nicht klappen für BMS. Die großen Institutionen werden aber für etwas mehr Dollar schon abgeben. 18USD? 20 USD? Alles Verhandlungssache. Zurücklehnen, zuschauen!! 

Antwort auf Beitrag Nr.: 37.822.334 von enzofran am 20.08.09 23:39:12Was bringen 2 tage bei der miesen Quote?
Allerdings: 8,7% der ausstehenden Aktien. Haben die auch schon Pakete über Instis sicher, die bei 8,7% nicht dabei sind?
Nachbösliche Kursreaktion null. Kur weiter knapp unter 16.
Übrigens: Wenn der deal platzt, dann fällt Medx nochmal auf 10 bis 12. Meine Meinung.
Allerdings: 8,7% der ausstehenden Aktien. Haben die auch schon Pakete über Instis sicher, die bei 8,7% nicht dabei sind?
Nachbösliche Kursreaktion null. Kur weiter knapp unter 16.
Übrigens: Wenn der deal platzt, dann fällt Medx nochmal auf 10 bis 12. Meine Meinung.
Sehr gut finde ich, dass sich nur so wenige mit diesem Witz-Kurs abspeisen lassen wollen. Medx-AKs sin in einer breiten pipline im kommen, bei vielen Partnern. Das ist viel zu wertvoll als dreingabe zur Pipelinespitze.
Antwort auf Beitrag Nr.: 37.823.181 von eck64 am 21.08.09 09:06:02Übrigens: Wenn der deal platzt, dann fällt Medx nochmal auf 10 bis 12. Meine Meinung.
Oder tiefer. Dann kauf ich meinen zur Sicherheit in diesem Falle verkauften Teil wieder zurück.
Ich gehe allerdings davon aus, dass BMS seine Offer erhöht. Es gibt Hinweise darauf, dass einige große (vom BMY unabhängige) Investoren massiv Aktien zu knapp unter 16 USD gekauft haben (von denen da: http://www.gabelli.com/ weiß ich, dass sie seit dem Übernahmeangebot im Wert von 100Mio USD Aktien gekauft haben) und das sicherlich nicht wegen ein paar Cent je Aktie Arbitragegeschäft. Zudem ist es dieses Mal m.M.n. nicht wie bei IMCL, als BMS nen Rückzieher machte. BMS kennt die Interna, vor allem die von ipilimumab, das wird wohl ein Multimilliardenblockbuster. MEDX ist viel viel mehr wert als 16 USD und BMY wird m.M.n. den Deal wenigstens ein bisschen versüssen.
Oder tiefer. Dann kauf ich meinen zur Sicherheit in diesem Falle verkauften Teil wieder zurück.
Ich gehe allerdings davon aus, dass BMS seine Offer erhöht. Es gibt Hinweise darauf, dass einige große (vom BMY unabhängige) Investoren massiv Aktien zu knapp unter 16 USD gekauft haben (von denen da: http://www.gabelli.com/ weiß ich, dass sie seit dem Übernahmeangebot im Wert von 100Mio USD Aktien gekauft haben) und das sicherlich nicht wegen ein paar Cent je Aktie Arbitragegeschäft. Zudem ist es dieses Mal m.M.n. nicht wie bei IMCL, als BMS nen Rückzieher machte. BMS kennt die Interna, vor allem die von ipilimumab, das wird wohl ein Multimilliardenblockbuster. MEDX ist viel viel mehr wert als 16 USD und BMY wird m.M.n. den Deal wenigstens ein bisschen versüssen.
Antwort auf Beitrag Nr.: 37.823.671 von Ville7 am 21.08.09 09:55:38Grundsätzlich und taktisch gesehen hat BMS ja auch nicht auf anhieb die Schmerzgrenze zur Übernahme geboten, nehme ich an. Also mal optisch schöne 90% Übernahmeprämie und noch Luft zum nachbessern.
Die werden kaufen bis zur beherrschenden Mehrheit. Vielleicht lassen sie danach MEDX auch leben, ähnlich wie Genentech und Roche über Jahre hinweg?
Die werden kaufen bis zur beherrschenden Mehrheit. Vielleicht lassen sie danach MEDX auch leben, ähnlich wie Genentech und Roche über Jahre hinweg?
Antwort auf Beitrag Nr.: 37.823.671 von Ville7 am 21.08.09 09:55:38Oder tiefer.
off topic:
Den Kursrückgang würde MOR dann aber sicher mit nachvollziehen, nachdem man den Kursanstieg aus Medx-deal schon lange wiedeer ausgepreist hat.....
off topic:
Den Kursrückgang würde MOR dann aber sicher mit nachvollziehen, nachdem man den Kursanstieg aus Medx-deal schon lange wiedeer ausgepreist hat.....
Antwort auf Beitrag Nr.: 37.823.752 von eck64 am 21.08.09 10:03:25Vielleicht lassen sie danach MEDX auch leben, ähnlich wie Genentech und Roche über Jahre hinweg?
Höchstgradig unwahrscheinlich, der Merger Vertrag sieht vor, bei Erreichen von 50,1%, die restlichen 49,9% mit dem Übernahmepreis abzufinden und rauszudrängen. Das geht in USA scheints easy mit allein der Mehrheit.
Höchstgradig unwahrscheinlich, der Merger Vertrag sieht vor, bei Erreichen von 50,1%, die restlichen 49,9% mit dem Übernahmepreis abzufinden und rauszudrängen. Das geht in USA scheints easy mit allein der Mehrheit.
Antwort auf Beitrag Nr.: 37.823.774 von eck64 am 21.08.09 10:05:17Was spielt das eine Rolle? Morphosys konnte auch nicht dauerhaft von der CAT, Abgenix, usw.- Übernahme profitieren. Daher wird der Effekt auch verschwinden.
Achtung, persönliche Einschätzung: Für Morphosys gehe ich davon aus, dass wir Anfang September vielleicht noch 19 sehen (aktuell wird sie ja wohl wegen dem kleinen Verfallstag auf 16 bis 16,3 festgepinnt) und danach mit dem Markt wieder abtauchen. Wie weit wird alleinig das Marktumfeld bestimmen. Und das kann nochmal richtig übel werden.
Achtung, persönliche Einschätzung: Für Morphosys gehe ich davon aus, dass wir Anfang September vielleicht noch 19 sehen (aktuell wird sie ja wohl wegen dem kleinen Verfallstag auf 16 bis 16,3 festgepinnt) und danach mit dem Markt wieder abtauchen. Wie weit wird alleinig das Marktumfeld bestimmen. Und das kann nochmal richtig übel werden.
Antwort auf Beitrag Nr.: 37.823.781 von Ville7 am 21.08.09 10:05:52Wenn das in USA so easy ist, warum hatte Roche dann so lange Schwierigkeiten die Genentech komplett zu kriegen?
Nur wegen dem zur Übernahme negativ eingestellten Management? Das würde noch mehr mieses Licht auf das MEdx-Management werfen.
Nur wegen dem zur Übernahme negativ eingestellten Management? Das würde noch mehr mieses Licht auf das MEdx-Management werfen.
Noch eine Überlegung von mir: ein konkurrierendes Angebot oder eine Erhöhung wird sicher nicht vor Ablauf des Verfallstages heute erfolgen, denn sonst würden heute ziemlich viele Optionen noch ins Geld laufen. Erwartet eine mögliches Konkurrenzangebot oder eine Erhöhung frühestens After hours oder am Wochenende.
Antwort auf Beitrag Nr.: 37.823.894 von eck64 am 21.08.09 10:16:10Wenn das in USA so easy ist, warum hatte Roche dann so lange Schwierigkeiten die Genentech komplett zu kriegen?
Nur wegen dem zur Übernahme negativ eingestellten Management? Das würde noch mehr mieses Licht auf das MEdx-Management werfen.
Du hast dir deine Frage selbst beantwortet. Management und BOD haben den Mergervertrag mit eben dieser Besonderheit unterzeichnet und somit ihr okay gegeben. Dann geht das. Bei Genentech gab es kein Okay vom BOD, dass es okay ist die restlichen Aktionäre im Falle einer Kontrollmehrheit auch rauszusqeeuzen.
Das MEDX Management und das MEDX BOD sind Verbrecher, die die Aktionäre verraten haben. Natürlich zu ihrem eigenen Vorteil, denn zuvor haben sie sich Rekordmenngen an billigsten Optionen zugeschustert. Die sind saniert und können nun früher in Rente denn je. Das ist der Anreiz eben nicht weitere ein-zwei Jahre zu arbeiten um aus eigener Kraft die Werte an der Börse zu heben. Eine riesen Sauerei, aber nicht umsonst gibt es eine Rekordflut an Aktionärsklagen zu diesem Deal. Es ist so offensichtlich, das das hier stinkt.
Alles JMHO!
Nur wegen dem zur Übernahme negativ eingestellten Management? Das würde noch mehr mieses Licht auf das MEdx-Management werfen.
Du hast dir deine Frage selbst beantwortet. Management und BOD haben den Mergervertrag mit eben dieser Besonderheit unterzeichnet und somit ihr okay gegeben. Dann geht das. Bei Genentech gab es kein Okay vom BOD, dass es okay ist die restlichen Aktionäre im Falle einer Kontrollmehrheit auch rauszusqeeuzen.
Das MEDX Management und das MEDX BOD sind Verbrecher, die die Aktionäre verraten haben. Natürlich zu ihrem eigenen Vorteil, denn zuvor haben sie sich Rekordmenngen an billigsten Optionen zugeschustert. Die sind saniert und können nun früher in Rente denn je. Das ist der Anreiz eben nicht weitere ein-zwei Jahre zu arbeiten um aus eigener Kraft die Werte an der Börse zu heben. Eine riesen Sauerei, aber nicht umsonst gibt es eine Rekordflut an Aktionärsklagen zu diesem Deal. Es ist so offensichtlich, das das hier stinkt.
Alles JMHO!
Das Bollingerband ist nun extrem zusammengezogen.

Die gestrige Meldung juckt den Kurs null.
Wenn viele 18, 20 oder gar mehr als Nachbesserungsziel für realistisch hielten, dann würde der Kurs die 16 übersteigen.
Die gestrige Meldung juckt den Kurs null.
Und warum wurde dass Kaufangebot um zwei tage Verlängert?
Da fehlen wohl noch einige Prozent,auch ohne Gegenangebot.
Und warum wurde dass Kaufangebot um zwei tage Verlängert?
Da fehlen wohl noch einige Prozent,auch ohne Gegenangebot.

Scheinbar verzichtet BMS auf ihre top-up Option im Mergervertrag, also dass sie bei 50,1% die anderen Aktionäre mit Cash aussqueezen können. Jetzt gehts angeblich nur noch bei 90% Mehrheit. So zumindest die Diskussion eines SEC Filings im Yahoo Board, das MEDX heute gefile't haben soll. Ich konnte es noch nicht verifizieren.
Antwort auf Beitrag Nr.: 37.829.548 von Ville7 am 21.08.09 20:09:15Lieber Ville7,
jetzt wird es richtig spannend.
Ein mögliches Gegenangebot erwarte ich nicht mehr,da ist wohl inzwischen zu viel zeit vergangen.
Ich denke dass einige Instis ihre Positionen festhalten,um einen höheren Verkaufspreis zu erlangen.
Ich pers. verkaufe kein einziges Stück mehr,sonst würde ich mir nachher in den Allerwertesten beissen,
wenn ich es könnte.
Selbst jetzt wird auf ein höheres Angebot spekuliert.
PS.Der Verfasser bleibt in Medarex investiert.
jetzt wird es richtig spannend.

Ein mögliches Gegenangebot erwarte ich nicht mehr,da ist wohl inzwischen zu viel zeit vergangen.
Ich denke dass einige Instis ihre Positionen festhalten,um einen höheren Verkaufspreis zu erlangen.
Ich pers. verkaufe kein einziges Stück mehr,sonst würde ich mir nachher in den Allerwertesten beissen,
wenn ich es könnte.

Selbst jetzt wird auf ein höheres Angebot spekuliert.
PS.Der Verfasser bleibt in Medarex investiert.
Medarex Inhaber Shrug auf BMS Buyout:
Ist das Glas 11% leer oder 190% voll ist?
By Jim Edwards | Aug 21, 2009 Mit Jim Edwards | 21 August 2009
Wenn Sie waren ratlos zu erfahren, dass Bristol-Myers Squibb hatte nur 8,7 Prozent bekommen von Medarex "-Anteile in ihrem Angebot zum Kauf der Aktien für $ 16 -
74.125.39.132/translate_c?hl=de&sl=en&u=http://industry.bnet…
Ist das Glas 11% leer oder 190% voll ist?
By Jim Edwards | Aug 21, 2009 Mit Jim Edwards | 21 August 2009
Wenn Sie waren ratlos zu erfahren, dass Bristol-Myers Squibb hatte nur 8,7 Prozent bekommen von Medarex "-Anteile in ihrem Angebot zum Kauf der Aktien für $ 16 -
74.125.39.132/translate_c?hl=de&sl=en&u=http://industry.bnet…
Ach noch etwas,
MEDAREX, INC
Lead Plaintiff Deadline: Sep 30, 2009 Lead Kläger Termin: Sep 30, 2009
Zusammenfassung der Falls.
Wertpapiere der Klasse A wurde gegen Medarex, Inc. (MedX) ( "Medarex" oder das "Unternehmen" genannt) im Namen einer Klasse öffentlichen Anteilseigner von Medarex auf Unterlassung ein selbst-Behandlung Angebot (das "Tender Offer") von die das Board of Directors von Medarex (die "Individuelle Beklagten") haben vereinbart, das Unternehmen zu verkaufen, um von Bristol-Myers Squibb ( "Bristol-Myers")
Die Beschwerde macht geltend, dass das Board of Directors von Medarex vereinbart, das Unternehmen zu verkaufen, um von Bristol-Myers, ohne sich ordnungsgemäß in einer Ausschreibung für den Verkauf und die während eines Zeitraums von ungewöhnlich, dass die Instabilität Markt hat die Preise von Medarex Lager für die makroökonomische Gründe nicht auf den Wert des Unternehmens. Wie sie hier, die Tender Offer ist verfahrenstechnisch und finanziell unfair.
Die Angebotsunterlage wird Medarex Aktionäre zahlen $ 16.00 in bar je Aktie, was einer fast 11% Rabatt auf Medarex den höchsten Schlusskurs von $ 17,90, die am 21. August 2007, vor der aktuellen Finanzkrise. Die Angebotsunterlage wird daher bestreiten, Kläger und die übrigen Mitglieder der Klasse die Möglichkeit, Nutzen aus der Gesellschaft, die langfristige Wachstumschancen und proportional in den zukünftigen Erfolg des Unternehmens. Die Angebotsunterlage ist das Ergebnis einer fehlerhaften Verkaufsprozess, bei dem der Einzelne Beklagten vereinbarten einen etwa $ 2,4 Milliarden verkaufen, ohne ausreichend um alternative Möglichkeiten für die anderen strategischen Kombinationen, und dann errichtet unangemessen viel Schutz Geräte zur Abwehr von konkurrierenden Bieter während der Empfehlung, dass die Aktionäre genehmigen Die Angebotsunterlage.
translate.google.de/translate?hl=de&sl=en&u=http://www.scott…
MEDAREX, INC
Lead Plaintiff Deadline: Sep 30, 2009 Lead Kläger Termin: Sep 30, 2009
Zusammenfassung der Falls.
Wertpapiere der Klasse A wurde gegen Medarex, Inc. (MedX) ( "Medarex" oder das "Unternehmen" genannt) im Namen einer Klasse öffentlichen Anteilseigner von Medarex auf Unterlassung ein selbst-Behandlung Angebot (das "Tender Offer") von die das Board of Directors von Medarex (die "Individuelle Beklagten") haben vereinbart, das Unternehmen zu verkaufen, um von Bristol-Myers Squibb ( "Bristol-Myers")
Die Beschwerde macht geltend, dass das Board of Directors von Medarex vereinbart, das Unternehmen zu verkaufen, um von Bristol-Myers, ohne sich ordnungsgemäß in einer Ausschreibung für den Verkauf und die während eines Zeitraums von ungewöhnlich, dass die Instabilität Markt hat die Preise von Medarex Lager für die makroökonomische Gründe nicht auf den Wert des Unternehmens. Wie sie hier, die Tender Offer ist verfahrenstechnisch und finanziell unfair.
Die Angebotsunterlage wird Medarex Aktionäre zahlen $ 16.00 in bar je Aktie, was einer fast 11% Rabatt auf Medarex den höchsten Schlusskurs von $ 17,90, die am 21. August 2007, vor der aktuellen Finanzkrise. Die Angebotsunterlage wird daher bestreiten, Kläger und die übrigen Mitglieder der Klasse die Möglichkeit, Nutzen aus der Gesellschaft, die langfristige Wachstumschancen und proportional in den zukünftigen Erfolg des Unternehmens. Die Angebotsunterlage ist das Ergebnis einer fehlerhaften Verkaufsprozess, bei dem der Einzelne Beklagten vereinbarten einen etwa $ 2,4 Milliarden verkaufen, ohne ausreichend um alternative Möglichkeiten für die anderen strategischen Kombinationen, und dann errichtet unangemessen viel Schutz Geräte zur Abwehr von konkurrierenden Bieter während der Empfehlung, dass die Aktionäre genehmigen Die Angebotsunterlage.
translate.google.de/translate?hl=de&sl=en&u=http://www.scott…
Gibt es für solche "Übersetzungen" keine Antikörper ?
Antwort auf Beitrag Nr.: 37.829.548 von Ville7 am 21.08.09 20:09:15nunja, unklar, was nun stimmt. Eine andere plausible Meinung ist, dass BMS nach Erreichen der 50,1% sofort ein Shareholdermeeting einberufen kann um zu beschliessen, dass die anderen Aktionäre mit eben den 16 USD abgefunden werden.
Ich hab keine Ahnung.
Übrigens: Kenneth Blumberg, einer der ersten, die geklagt haben, scheint mit größerer Wahrscheinlichkeit davon auszugehen, dass der Deal für 16USD durchgeht. Er begründet allerdings nicht wieso.
Ich hab keine Ahnung.
Übrigens: Kenneth Blumberg, einer der ersten, die geklagt haben, scheint mit größerer Wahrscheinlichkeit davon auszugehen, dass der Deal für 16USD durchgeht. Er begründet allerdings nicht wieso.
Hier das SEC Filing zur Verzögerung des Deals:
http://www.sec.gov/Archives/edgar/data/874255/00009501230903…
Der entscheidende Part des vorgeschlagenen Settlements, das keine Erhöhung des Angebots durch BMS vorsieht.
“On August 19, 2009, the Honorable Maria M. Sypek entered a written order memorializing the consolidation for all purposes of the Superior Court Complaints (the complaint filed on July 30, 2009, by Ralph Roelofsz (the “Roelofsz Complaint”) was inadvertently omitted from the court’s written order) under the caption Hersh, et al. v. Pien, et al. (the “Consolidated State Action”), Docket No. C-71-09, in the Superior Court of New Jersey. On August 20, 2009, the parties to the Consolidated State Action, the Roelofsz Complaint, the Blumberg Complaint, the Federal Halegoua Complaint and the Blevins Complaint (collectively, the “Actions”) entered into a Memorandum of Understanding (the “Memorandum”) pursuant to which the parties reached an agreement in principle to settle the Actions subject to certain conditions, including court approval and the completion of further definitive documentation. Pursuant to the agreements in the Memorandum, Medarex will make certain supplemental disclosures which are contained in Amendment 3 to the Schedule 14D-9. In addition, under the terms of the Memorandum, BMS agreed (1) to extend the Offer until 12:00 midnight, New York City time, on Wednesday, August 26, 2009 and (2) that neither BMS, nor any of its subsidiaries or affiliates, will exercise the Top-Up Option described in the fifth paragraph under “The Tender Offer — Section 11 — The Merger Agreement” of the Offer to Purchase. In addition, the parties agreed to present to the Superior Court of New Jersey a Stipulation of Settlement (the “Stipulation of Settlement”) and any other documentation as may be required in order to obtain approval by the court of the settlement and the dismissal of the Actions upon the terms set forth in the Memorandum. The Stipulation of Settlement will include a release of all claims against all defendants and their affiliates and agents held by the plaintiffs and class members. In the Memorandum, the defendants in the Actions acknowledge that plaintiffs’ counsel intends to seek reasonable attorney fees and expenses from such defendants in connection with the Actions. In the event that the settlement is not approved and such conditions are not satisfied, Medarex will continue to vigorously defend these Actions.”
Blieben die Klagen möglicherweise zahnlos? Kommt es jetzt auf die Institutionellen an. Machen die noch Stress beim Preis oder haben die nur bisher nicht getendert, weil die Klagen noch anhängig waren?
I don't know!!
http://www.sec.gov/Archives/edgar/data/874255/00009501230903…
Der entscheidende Part des vorgeschlagenen Settlements, das keine Erhöhung des Angebots durch BMS vorsieht.
“On August 19, 2009, the Honorable Maria M. Sypek entered a written order memorializing the consolidation for all purposes of the Superior Court Complaints (the complaint filed on July 30, 2009, by Ralph Roelofsz (the “Roelofsz Complaint”) was inadvertently omitted from the court’s written order) under the caption Hersh, et al. v. Pien, et al. (the “Consolidated State Action”), Docket No. C-71-09, in the Superior Court of New Jersey. On August 20, 2009, the parties to the Consolidated State Action, the Roelofsz Complaint, the Blumberg Complaint, the Federal Halegoua Complaint and the Blevins Complaint (collectively, the “Actions”) entered into a Memorandum of Understanding (the “Memorandum”) pursuant to which the parties reached an agreement in principle to settle the Actions subject to certain conditions, including court approval and the completion of further definitive documentation. Pursuant to the agreements in the Memorandum, Medarex will make certain supplemental disclosures which are contained in Amendment 3 to the Schedule 14D-9. In addition, under the terms of the Memorandum, BMS agreed (1) to extend the Offer until 12:00 midnight, New York City time, on Wednesday, August 26, 2009 and (2) that neither BMS, nor any of its subsidiaries or affiliates, will exercise the Top-Up Option described in the fifth paragraph under “The Tender Offer — Section 11 — The Merger Agreement” of the Offer to Purchase. In addition, the parties agreed to present to the Superior Court of New Jersey a Stipulation of Settlement (the “Stipulation of Settlement”) and any other documentation as may be required in order to obtain approval by the court of the settlement and the dismissal of the Actions upon the terms set forth in the Memorandum. The Stipulation of Settlement will include a release of all claims against all defendants and their affiliates and agents held by the plaintiffs and class members. In the Memorandum, the defendants in the Actions acknowledge that plaintiffs’ counsel intends to seek reasonable attorney fees and expenses from such defendants in connection with the Actions. In the event that the settlement is not approved and such conditions are not satisfied, Medarex will continue to vigorously defend these Actions.”
Blieben die Klagen möglicherweise zahnlos? Kommt es jetzt auf die Institutionellen an. Machen die noch Stress beim Preis oder haben die nur bisher nicht getendert, weil die Klagen noch anhängig waren?
I don't know!!
Ein an der Klage beteiligter Aktionär (rothco619) beschreibt im Yahoo MB, was gerade hinter den Kulissen in den Verhandlungen mit MEDX und BMY läuft:
Re: August 20, 2009 Amended SEC Filing by Medarex - must read 22-Aug-09 03:21 am
Not sure where your getting info. Personally I was against settlement as was our group, we were unanimous. We wanted to letigate, however, after reviewing what would happen,and due to laws in NJ that deal with valuations of a company which really are screwed up as they don't provide for future valuations the fight could not go in to those areas. Our best option was to raise the bar for BMY to get 90% approval as opposed to 51%. We felt with Gibelli, and Ichan, the institutions and individual shareholders it would be dififcult for BMY to get 90% . By having additional information released which was uncovered during the discovey phase revealed to share holders who had tendered or were considering, the new info ,the delay and raised bar of shares needed for approval gave us the best chance. Getting additional info also to possible suitors would give them time to look at information that they had not seen before. So the process has begun. Should we not be successful in changing anything, I have the right as does anyone else to object and to speak at a hearing. Everyone who holds Medarex shares should be getting all the info shortly and has the same rights. Hope the judge will allow personal appearances and not just written statements. If 90% of shareholders decide to tender shares then we are screwed, but 51% was much easier to attain. We know we were sold out by Medarex and they did not represent us well and I am convinced of that more then ever,but that was not the focus as that had to do with future valuations. I have probably said to much and will be scolded by my lawyers, but I can tell you how proud I am of Bart, Dani and two others in our group who fought with and continue to fight with me on this. When all is resolved, I will tell the whole story about exactly what happened. Don't tender your shares, recall them if you have and know that we never quit, are still fighting and have accepted nothing. It is in the hands of the system now and if shareholders want to be represented they can do it by voting with there shares as they matter more then you could ever know. Those who work for BMY,GS or have a routing interest the other way would love for you to believe we sold out. WE have not, will never,give up until all options are exhausted. For the piece of crap who insulted our intentions by suggesting we have gotten something monetary from this. Go straight to hell. Just because you lack ethics,don't believe that we do. Medarex mangement sold us out, and if they had our backbone and lived their lives as we live ours we would be looking at a differnt picture. I don't hear any fat lady singing, just thunder so god must really be pissed.
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
Re: August 20, 2009 Amended SEC Filing by Medarex - must read 22-Aug-09 03:21 am
Not sure where your getting info. Personally I was against settlement as was our group, we were unanimous. We wanted to letigate, however, after reviewing what would happen,and due to laws in NJ that deal with valuations of a company which really are screwed up as they don't provide for future valuations the fight could not go in to those areas. Our best option was to raise the bar for BMY to get 90% approval as opposed to 51%. We felt with Gibelli, and Ichan, the institutions and individual shareholders it would be dififcult for BMY to get 90% . By having additional information released which was uncovered during the discovey phase revealed to share holders who had tendered or were considering, the new info ,the delay and raised bar of shares needed for approval gave us the best chance. Getting additional info also to possible suitors would give them time to look at information that they had not seen before. So the process has begun. Should we not be successful in changing anything, I have the right as does anyone else to object and to speak at a hearing. Everyone who holds Medarex shares should be getting all the info shortly and has the same rights. Hope the judge will allow personal appearances and not just written statements. If 90% of shareholders decide to tender shares then we are screwed, but 51% was much easier to attain. We know we were sold out by Medarex and they did not represent us well and I am convinced of that more then ever,but that was not the focus as that had to do with future valuations. I have probably said to much and will be scolded by my lawyers, but I can tell you how proud I am of Bart, Dani and two others in our group who fought with and continue to fight with me on this. When all is resolved, I will tell the whole story about exactly what happened. Don't tender your shares, recall them if you have and know that we never quit, are still fighting and have accepted nothing. It is in the hands of the system now and if shareholders want to be represented they can do it by voting with there shares as they matter more then you could ever know. Those who work for BMY,GS or have a routing interest the other way would love for you to believe we sold out. WE have not, will never,give up until all options are exhausted. For the piece of crap who insulted our intentions by suggesting we have gotten something monetary from this. Go straight to hell. Just because you lack ethics,don't believe that we do. Medarex mangement sold us out, and if they had our backbone and lived their lives as we live ours we would be looking at a differnt picture. I don't hear any fat lady singing, just thunder so god must really be pissed.
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
kblumb
<<With the requirement for 90% tender, it's a new ballgame. If we can get 20% of investors not to tender, we can stop the TO, at least for some time, maybe enough time to get results on the Ipi trial. The reason we would need 20% would be to make it more difficult for one of the arbitrage buyers that own 6-8% from cutting a deal with Medarex to get them over the 90% hurdle. >>>>
Bob, 20% is not enough it will stop the Short Form Merger , but if thats stopped MEDX will call a stockholder meeting and have a merger vote and BMY will own all shares tendered to them and unless over 50% are not tendered they will have a majority and the merger will go through. So 20% will slow down the train but it will take over 50% to stop it. Kenny
<<With the requirement for 90% tender, it's a new ballgame. If we can get 20% of investors not to tender, we can stop the TO, at least for some time, maybe enough time to get results on the Ipi trial. The reason we would need 20% would be to make it more difficult for one of the arbitrage buyers that own 6-8% from cutting a deal with Medarex to get them over the 90% hurdle. >>>>
Bob, 20% is not enough it will stop the Short Form Merger , but if thats stopped MEDX will call a stockholder meeting and have a merger vote and BMY will own all shares tendered to them and unless over 50% are not tendered they will have a majority and the merger will go through. So 20% will slow down the train but it will take over 50% to stop it. Kenny
Das Angebot an die Aktionäre zu 16$ zu verkaufen wird um 2! Tage verlängert. Komisch, komisch.
Ist da etwas im Busch?
Ist da etwas im Busch?
Antwort auf Beitrag Nr.: 37.863.936 von Pete the Rabbit am 27.08.09 13:43:26Bristol-Myers Squibb verlängert Annahmefrist für Medarex-Übernahme
21.08.2009 - (dpa-AFX) Der US-Pharmakonzern Bristol-Myers Squibb (BMS) gibt den Aktionären des Biotechnologie-Unternehmens Medarex zwei Tage mehr Zeit zur Annahme seines Übernahmeangebots. Die Barofferte in Höhe von 16,00 US-Dollar je Aktie sei mit Einwilligung von Medarex zunächst bis Mittwoch, 26. August Mitternacht (New York City Zeit), verlängert worden, teilte BMS am Donnerstag nach US-Börsenschluss in New York mit. An den Bedingungen des Angebots sei nichts geändert worden. Bis 9.00 Uhr an diesem Tag seien BMS 11,6 Millionen Medarex-Aktien und damit rund 8,7 Prozent des ausstehenden Aktienkapitals offeriert worden. Insgesamt bietet BMS für Medarex 2,4 Milliarden US-Dollar (1,69 Mrd Euro). BMS hatte seine Offerte am 23. Juli bekanntgegeben, der Aufschlag auf den Medarex-Kurs betrug damals rund 90 Prozent
Da kommt noch eine Nachbesserung.
21.08.2009 - (dpa-AFX) Der US-Pharmakonzern Bristol-Myers Squibb (BMS) gibt den Aktionären des Biotechnologie-Unternehmens Medarex zwei Tage mehr Zeit zur Annahme seines Übernahmeangebots. Die Barofferte in Höhe von 16,00 US-Dollar je Aktie sei mit Einwilligung von Medarex zunächst bis Mittwoch, 26. August Mitternacht (New York City Zeit), verlängert worden, teilte BMS am Donnerstag nach US-Börsenschluss in New York mit. An den Bedingungen des Angebots sei nichts geändert worden. Bis 9.00 Uhr an diesem Tag seien BMS 11,6 Millionen Medarex-Aktien und damit rund 8,7 Prozent des ausstehenden Aktienkapitals offeriert worden. Insgesamt bietet BMS für Medarex 2,4 Milliarden US-Dollar (1,69 Mrd Euro). BMS hatte seine Offerte am 23. Juli bekanntgegeben, der Aufschlag auf den Medarex-Kurs betrug damals rund 90 Prozent
Da kommt noch eine Nachbesserung.

Antwort auf Beitrag Nr.: 37.864.188 von Bioperle am 27.08.09 14:11:3787,7%.
Meine Einschätzung: das ist gelaufen. Die restlichen 2,3% bekommen sie auch noch und dann haben sie 90% und können auch nach dem Lawsuit Settlement im Merger die restlichen Aktionäre zu 16 USD (ohne Zinsaufschlag) herausdrängen.
Meine Einschätzung: das ist gelaufen. Die restlichen 2,3% bekommen sie auch noch und dann haben sie 90% und können auch nach dem Lawsuit Settlement im Merger die restlichen Aktionäre zu 16 USD (ohne Zinsaufschlag) herausdrängen.
So, ich habe den Rest jetzt über die Börse geworfen bis auf den Teil, der noch nicht steuerfrei ist. Den behalte ich - vielleicht schaffe ich es ja bis nach der Steuerfreiheit - was ich zwar nicht glaube, denn bis Ende November müsste ich es schaffen nicht verkaufen zu müssen.
Ich verabschiede mich schon mal. War schön mit euch , war leider nichts mit dem großen Erfolg, der uns vergönnt gewesen wäre- nach all den Werten, die in der Pipeline schlummern, aber leider nicht bezahlt werden wollten. Den Erfolg hat uns jemand anderer weggeräubert (Management, BOD und Bristol Myers Squibb).
, war leider nichts mit dem großen Erfolg, der uns vergönnt gewesen wäre- nach all den Werten, die in der Pipeline schlummern, aber leider nicht bezahlt werden wollten. Den Erfolg hat uns jemand anderer weggeräubert (Management, BOD und Bristol Myers Squibb).
Cya bei Morphosys, Spectrum, www.rambus.info, Micromet, Medigene und meinen sonstigen Werten und Watchlist-Werten.
Ich verabschiede mich schon mal. War schön mit euch
 , war leider nichts mit dem großen Erfolg, der uns vergönnt gewesen wäre- nach all den Werten, die in der Pipeline schlummern, aber leider nicht bezahlt werden wollten. Den Erfolg hat uns jemand anderer weggeräubert (Management, BOD und Bristol Myers Squibb).
, war leider nichts mit dem großen Erfolg, der uns vergönnt gewesen wäre- nach all den Werten, die in der Pipeline schlummern, aber leider nicht bezahlt werden wollten. Den Erfolg hat uns jemand anderer weggeräubert (Management, BOD und Bristol Myers Squibb). Cya bei Morphosys, Spectrum, www.rambus.info, Micromet, Medigene und meinen sonstigen Werten und Watchlist-Werten.

Antwort auf Beitrag Nr.: 37.864.690 von Ville7 am 27.08.09 15:04:16Scheint so, als ob es tatsächlich schlecht aussieht... Aber findest Du es nicht komisch, dass BMS um 2 Tage verlängert, weil sie bis zum offiziellen Schluss nur ca. 8% hatten? Und dann erhalten sie innerhalb von 2 Tagen weitere 80%??? Jeder, der die 80% hielt, wusste, dass er nach dem Ende der Angebotsfrist eine erhebliche Chance auf deutlich mehr hat! Das sollen sich 80% der Shareholder anders überlegt haben? Kommt mir jedenfalls spanisch vor. Ich denke, da stimmt irgend etwas nicht.
milestones
milestones
Tja ciao,


schade zwar aber unterm Strich bleibt immer noch ein fettes Plus, das anderswo investiert sein will.
Warte trotzdem noch über das Wochenende ab, nun habe ich die shares so lange gehalten, dann kommt´s auf 2-3 Tage auch nicht mehr an.
Vielleicht steigt der $ ja noch ein wenig...
Gruß q.


schade zwar aber unterm Strich bleibt immer noch ein fettes Plus, das anderswo investiert sein will.
Warte trotzdem noch über das Wochenende ab, nun habe ich die shares so lange gehalten, dann kommt´s auf 2-3 Tage auch nicht mehr an.
Vielleicht steigt der $ ja noch ein wenig...
Gruß q.
Antwort auf Beitrag Nr.: 37.865.087 von Milestones am 27.08.09 15:44:48Es könnte daran gelegen haben, dass die Institutionellen bis zur letzten Sekunde gewartet haben und dies deren übliches Prozedere ist. Möglicherweise war es auch ein Deal von BMS mit den Institutionellen um den Lawsuit wegzubekommen und die klagenden Shareholders in der Hoffnung auf Erfolg ein derartiges Settlement (90% statt 50% für sofortigen Squeeze Out) unterzeichnen zu lassen.
Was da an sonstigen Schweinereien ablief weiß ich nicht, werd ich auch nie erfahren. Bin mir aber sicher, dass alles getan wurde, damit die anderen profitieren und nicht wir.
Was da an sonstigen Schweinereien ablief weiß ich nicht, werd ich auch nie erfahren. Bin mir aber sicher, dass alles getan wurde, damit die anderen profitieren und nicht wir.
Hallo...
scheinbar ist Medarex in Europa vom Handel ausgesetzt...
hab noch ein paar von ihnen... will Sie verkaufen.
Geht nicht?
Sind die jetzt wertlos, oder wie!?
Oder muss ich jetzt warten bis BM die Übernahme vollzogen hat?!
Versteh ich nicht?!
Bitte um dringende Aufklärung...
scheinbar ist Medarex in Europa vom Handel ausgesetzt...
hab noch ein paar von ihnen... will Sie verkaufen.
Geht nicht?
Sind die jetzt wertlos, oder wie!?
Oder muss ich jetzt warten bis BM die Übernahme vollzogen hat?!
Versteh ich nicht?!
Bitte um dringende Aufklärung...
Antwort auf Beitrag Nr.: 37.901.664 von where_is_the_beef am 02.09.09 13:25:09Hi where_is_the_beef,
ich habe nachdem ich die Meldung von BMS las, dass sie Medarex noch gestern von der NASDAQ nehmen wollen in einer Nachaktion noch meine restlichen Stücke über Tradegate und Lang und Schwarz verkauft, da ich nicht mehr die Chance sah sie in die Steuerfreiheit zu retten - zumindest gefiel mir nicht, nicht mehr über die Börse verkaufen zu können. Sehr fies das so kurzfristig durchzuführen.
Geht das heute nicht mehr (z.b. Livetrading bei Comdirect)? Auf L+S bekomme ich zumindest noch einen Kurs, aktuell 11,20 Euro im Bid.
Ansonsten setz dich mit deiner Depotbank in Verbindung, die sollen das klären. Laut Mergervertrag stehen die 16USD zur Abfindung je Stück zu. Die müssen dir auf jeden Fall gezahlt werden. Inwieweit du diesen Prozess zur Zahlung antriggern musst, weiss ich nicht.
Grüße
Ville
ich habe nachdem ich die Meldung von BMS las, dass sie Medarex noch gestern von der NASDAQ nehmen wollen in einer Nachaktion noch meine restlichen Stücke über Tradegate und Lang und Schwarz verkauft, da ich nicht mehr die Chance sah sie in die Steuerfreiheit zu retten - zumindest gefiel mir nicht, nicht mehr über die Börse verkaufen zu können. Sehr fies das so kurzfristig durchzuführen.
Geht das heute nicht mehr (z.b. Livetrading bei Comdirect)? Auf L+S bekomme ich zumindest noch einen Kurs, aktuell 11,20 Euro im Bid.
Ansonsten setz dich mit deiner Depotbank in Verbindung, die sollen das klären. Laut Mergervertrag stehen die 16USD zur Abfindung je Stück zu. Die müssen dir auf jeden Fall gezahlt werden. Inwieweit du diesen Prozess zur Zahlung antriggern musst, weiss ich nicht.
Grüße
Ville
Antwort auf Beitrag Nr.: 37.904.112 von Ville7 am 02.09.09 17:23:37Bristol-Myers Squibb schließt Übernahme von Medarex, Inc.
- Bristol-Myers Squibb Company (NYSE: BMY - News) gab heute bekannt, dass diese bereits abgeschlossen seiner zuvor angekündigten 2,4 Milliarden Dollar Erwerb von Medarex, Inc. (NASDAQ: MedX - News) ( \"Medarex\" ). Als Ergebnis der Transaktion hat Medarex zu einer hundertprozentigen Tochtergesellschaft von Bristol-Myers Squibb.
In Verbindung stehende Kurse
Symbol Symbol Price Preis Change Ändern
BMY BMY 21.75 21,75 +0.06 +0,06
Bristol-Myers Squibb leitete am 28. Juli 2009 ein öffentliches Barangebot für alle ausstehenden Aktien der Stammaktien von Medarex für $ 16,00 pro Aktie zu erwerben.
Das Übernahmeangebot abgelaufen um Mitternacht (Ortszeit New York) am 26. August 2009 und die anschließende Angebotsfrist für das Übernahmeangebot endete um Mitternacht (Ortszeit New York) am 31. August 2009, zu welchem Zeitpunkt die Aktionäre von Medarex ausgeschrieben hatte insgesamt ungefähr 120.417.467 Aktien von Medarex-Stammaktien, die zusammen mit der 2879223 Aktien von Medarex-Stammaktien im Besitz von Bristol-Myers Squibb seit Januar 2005, entfielen rund 90,7% der ausstehenden Aktien Medarex.
Heute, Bristol-Myers Squibb erworben alle restlichen ausstehenden Aktien von Medarex-Stammaktien mit einem \"short form merger\", in dem alle diese Aktien wurden in das Recht auf $ 16,00 je Aktie in bar erhalten und ohne Zinsen und abzüglich konvertiert alle Verrechnungssteuern.
Diese Pressemitteilung stellt weder ein Angebot zum Kauf noch eine Aufforderung zur Abgabe eines Angebots zum Aktien Aktien von Medarex.
finance.yahoo.com/news/BristolMyers-Squibb-Completes-bw-3598…
Sehr unverständlich....
- Bristol-Myers Squibb Company (NYSE: BMY - News) gab heute bekannt, dass diese bereits abgeschlossen seiner zuvor angekündigten 2,4 Milliarden Dollar Erwerb von Medarex, Inc. (NASDAQ: MedX - News) ( \"Medarex\" ). Als Ergebnis der Transaktion hat Medarex zu einer hundertprozentigen Tochtergesellschaft von Bristol-Myers Squibb.
In Verbindung stehende Kurse
Symbol Symbol Price Preis Change Ändern
BMY BMY 21.75 21,75 +0.06 +0,06
Bristol-Myers Squibb leitete am 28. Juli 2009 ein öffentliches Barangebot für alle ausstehenden Aktien der Stammaktien von Medarex für $ 16,00 pro Aktie zu erwerben.
Das Übernahmeangebot abgelaufen um Mitternacht (Ortszeit New York) am 26. August 2009 und die anschließende Angebotsfrist für das Übernahmeangebot endete um Mitternacht (Ortszeit New York) am 31. August 2009, zu welchem Zeitpunkt die Aktionäre von Medarex ausgeschrieben hatte insgesamt ungefähr 120.417.467 Aktien von Medarex-Stammaktien, die zusammen mit der 2879223 Aktien von Medarex-Stammaktien im Besitz von Bristol-Myers Squibb seit Januar 2005, entfielen rund 90,7% der ausstehenden Aktien Medarex.
Heute, Bristol-Myers Squibb erworben alle restlichen ausstehenden Aktien von Medarex-Stammaktien mit einem \"short form merger\", in dem alle diese Aktien wurden in das Recht auf $ 16,00 je Aktie in bar erhalten und ohne Zinsen und abzüglich konvertiert alle Verrechnungssteuern.
Diese Pressemitteilung stellt weder ein Angebot zum Kauf noch eine Aufforderung zur Abgabe eines Angebots zum Aktien Aktien von Medarex.
finance.yahoo.com/news/BristolMyers-Squibb-Completes-bw-3598…
Sehr unverständlich....

Tja also...
(stirnrunzel)
dass das nun so schnell geht, hätte ich auch nicht gedacht. Yahoo-Thread existiert schon nicht mehr, Aktie nicht gehandelt...
Habe auch bis zur letzten Sekunde (oder sagen wir mal dem letzten Tag) abgewartet, und auch gestern das Geld gutgeschrieben bekommen. 16$ ohne Abzüge und Kosten, allerdings zum aus heutiger Sicht lausigen $-Kurs von 1,4380.
An alle, die noch ein paar oder auch viele Aktien haben: Macht euch keine Sorgen, wird für alle 16$ gezahlt werden, fragt sich nur wann.
Mein letztes Posting hier, tatsächlich trauere ich der Sache ein wenig nach, man hatte ja immer die große Hoffnung, die viel größer war, als die Kurssteigerung durch die Übernahme. Immerhin habe ich ja auch selbst den letzten Verkauf von MEDX zu höheren Kursen getätigt (zu 12) als jetzt mit Übernahmeangebot...

Egal, ist alles gesagt worden.
Habe vorhin schon versucht, MOR zu Abstauberkursen zu kaufen, hat nicht geklappt...
MITI läuft gut heute...
Grüße q.
(stirnrunzel)
dass das nun so schnell geht, hätte ich auch nicht gedacht. Yahoo-Thread existiert schon nicht mehr, Aktie nicht gehandelt...
Habe auch bis zur letzten Sekunde (oder sagen wir mal dem letzten Tag) abgewartet, und auch gestern das Geld gutgeschrieben bekommen. 16$ ohne Abzüge und Kosten, allerdings zum aus heutiger Sicht lausigen $-Kurs von 1,4380.
An alle, die noch ein paar oder auch viele Aktien haben: Macht euch keine Sorgen, wird für alle 16$ gezahlt werden, fragt sich nur wann.
Mein letztes Posting hier, tatsächlich trauere ich der Sache ein wenig nach, man hatte ja immer die große Hoffnung, die viel größer war, als die Kurssteigerung durch die Übernahme. Immerhin habe ich ja auch selbst den letzten Verkauf von MEDX zu höheren Kursen getätigt (zu 12) als jetzt mit Übernahmeangebot...

Egal, ist alles gesagt worden.
Habe vorhin schon versucht, MOR zu Abstauberkursen zu kaufen, hat nicht geklappt...
MITI läuft gut heute...
Grüße q.
Antwort auf Beitrag Nr.: 37.906.530 von quepos am 02.09.09 22:42:14Die ultrakurzfristige Löschung von der NASDAQ passt doch ins Bild wie das ganze ablief. Kein Respekt von keiner Seite (Management, BOD, BMS) für die (ehemaligen) Eigentümer der Firma.
Ich habe meine Lektion gelernt, solche Firmen wie Medarex, die so ein Management haben (das sich ohne Ende bereichert und nur auf sich selbst schaut) werde ich trotz bester Technologie und mittel- bis langfristiger Aussichten nicht mehr anfassen. Bzw. maximal nur noch zum Traden.
re Auszahlung von BMS: Dann kann ich mich glücklich schätzen, dass ich unter 16USD verkauft habe, denn in Euro habe ich mehr bekommen als du, da der Dollar höher stand. Du müsstest nur 11,13 Euro bekommen haben. Ich hatte meine Tranchen für 11,29, 11,18 und 11,23 verkauft.
Der Dollarverfall kam ja noch hinzu bei einem Investment in Medarex und hat einem die letzten Jahre bestimmt 20% Performance genommen. Dumm gelaufen, alles.
Ja Mircomet läuft und läuft und läuft, aber keine Ahnung wieso. Ich bin seit $3,67 dabei und wundere mich, wer den Kurs hier so wie am Strich gezogen nach oben bringt, da keine Meldungen anstanden.
Ich habe meine Lektion gelernt, solche Firmen wie Medarex, die so ein Management haben (das sich ohne Ende bereichert und nur auf sich selbst schaut) werde ich trotz bester Technologie und mittel- bis langfristiger Aussichten nicht mehr anfassen. Bzw. maximal nur noch zum Traden.
re Auszahlung von BMS: Dann kann ich mich glücklich schätzen, dass ich unter 16USD verkauft habe, denn in Euro habe ich mehr bekommen als du, da der Dollar höher stand. Du müsstest nur 11,13 Euro bekommen haben. Ich hatte meine Tranchen für 11,29, 11,18 und 11,23 verkauft.
Der Dollarverfall kam ja noch hinzu bei einem Investment in Medarex und hat einem die letzten Jahre bestimmt 20% Performance genommen. Dumm gelaufen, alles.
Ja Mircomet läuft und läuft und läuft, aber keine Ahnung wieso. Ich bin seit $3,67 dabei und wundere mich, wer den Kurs hier so wie am Strich gezogen nach oben bringt, da keine Meldungen anstanden.
Antwort auf Beitrag Nr.: 37.904.112 von Ville7 am 02.09.09 17:23:37ich habe nachdem ich die Meldung von BMS las, dass sie Medarex noch gestern von der NASDAQ nehmen wollen in einer Nachaktion noch meine restlichen Stücke über Tradegate und Lang und Schwarz verkauft, da ich nicht mehr die Chance sah sie in die Steuerfreiheit zu retten - zumindest gefiel mir nicht, nicht mehr über die Börse verkaufen zu können.
Glückwunsch.
Ich war leider 4 Tage nicht da - und lese den Käse erst jetzt.
Soooon Hals habe ich! Und die Fäuste in der Tasche geballt. Aber nutzt nix.
Da werden die mir wohl 25% Ami-Steuern abknöpfen (außer der hier sowieso fälligen Speku-Steuer). Die wird man wohl wieder (langwierig) zurückholen können, aber ich weiß noch nicht, wie: Den Fall hatte ich noch nicht.
Man hat ja sonst nix zu tun.
Menno, bin ich froh, dass ich die steuerfreien Stücke schon rausgehauen hatte.
So eine Saubande. (Falls man das hier nicht schreiben darf: Ich meine es aber so.)
Gruß
Zock
Glückwunsch.
Ich war leider 4 Tage nicht da - und lese den Käse erst jetzt.
Soooon Hals habe ich! Und die Fäuste in der Tasche geballt. Aber nutzt nix.
Da werden die mir wohl 25% Ami-Steuern abknöpfen (außer der hier sowieso fälligen Speku-Steuer). Die wird man wohl wieder (langwierig) zurückholen können, aber ich weiß noch nicht, wie: Den Fall hatte ich noch nicht.
Man hat ja sonst nix zu tun.

Menno, bin ich froh, dass ich die steuerfreien Stücke schon rausgehauen hatte.
So eine Saubande. (Falls man das hier nicht schreiben darf: Ich meine es aber so.)

Gruß
Zock
Antwort auf Beitrag Nr.: 37.912.795 von Zock1000 am 03.09.09 17:33:48Nunja, so wie ich where_is_the_beef verstehe muss man erst mal klären, wie man überhaupt an seine 16USD je Aktie als deutscher Ex-Aktionär kommt. Der Aktienbesitz wurde ja in das Recht transferiert 16USD pro Aktie zu erhalten. Aber scheinbar sind die Broker und auch die Börse ahnungslos wie das jetzt geht.
Nicht sehr hilfreich ist dabei auch, dass das Yahoo Board komplett verschwunden ist und man die amerikanischen Anleger nicht mehr dazu fragen kann.
Hilft wohl nur der Weg sich direkt an Bristol Myers Squibb zu wenden.
Nicht sehr hilfreich ist dabei auch, dass das Yahoo Board komplett verschwunden ist und man die amerikanischen Anleger nicht mehr dazu fragen kann.
Hilft wohl nur der Weg sich direkt an Bristol Myers Squibb zu wenden.
Als Anleger must du gar nichts machen. Deine Depotführende Bank meldet die Aktien und bucht sie im Gegenzug zum Betrag aus.
Was soll daran so schwierig sein? War bei Medimmune nicht anders.
Was soll daran so schwierig sein? War bei Medimmune nicht anders.
Antwort auf Beitrag Nr.: 37.916.870 von VaJo am 04.09.09 09:20:37Vajo in seiner üblichen Selbstüberschätzung weiß wie immer mehr - diesmal mehr als die Depotbanken selbst, die keine Auskunft geben können. (kopfschüttel)
Antwort auf Beitrag Nr.: 37.916.870 von VaJo am 04.09.09 09:20:37Dein Wort in Gottes Ohr... VaJo!
Ein Rechtsnanspruch hat man wohl, die Frage ist halt nur die Umsetzung dieses Anspruches!?
Ein Rechtsnanspruch hat man wohl, die Frage ist halt nur die Umsetzung dieses Anspruches!?

Antwort auf Beitrag Nr.: 37.916.870 von VaJo am 04.09.09 09:20:37Zumindest für die Dresdner Bank kann ich diese Vorgehensweise bei Medimmune,Millennium + CV Therapeutics ohne Selbstüberschätzung bestätigen. Ich unterstelle mal,daß bei Medarex ebenso verfahren wird.
Antwort auf Beitrag Nr.: 37.920.654 von Ulf-Imat am 04.09.09 15:51:56Die waren aber bestimmmt noch handelbar zur der Zeit, oder?!
Die Schnelle Einziehung.. quasi eine Nacht-und-Nebelaktion macht mich stuzig!
Wer ist hier denn noch davon betroffen!??!?!?!?!?
Die Schnelle Einziehung.. quasi eine Nacht-und-Nebelaktion macht mich stuzig!
Wer ist hier denn noch davon betroffen!??!?!?!?!?
Die genannten Aktien wurden sicher nicht eingezogen, als sie noch handelbar waren. Früher oder später werden die Medarex-Aktien eingezogen und dafür 16$ gezahlt. Solch ein Squeeze Out geschieht in den USA aber viel schneller als das mit einer deutschen Aktie passieren würde. Sowas ist keine Nacht-und Nebelaktion, sondern Praxis und gängiges Recht. Abwarten und Tee trinken, das Geld wird schon kommen.
Die ganze Aktion war zum Kotzen für uns aktionäre.
Vorallem wird BMS vermutl noch heuer die Phase 3 Daten von ipilimumab zu melanoma veröffentlichen können u rechnet vermutl. fix mit zulassung spätestens 2011.
und dann noch Prostata!
Die 16$ werden immer mehr zu einer Riesenverarschung.Warum lassen sich institutionelle so simple über den tisch ziehen??
Vorallem wird BMS vermutl noch heuer die Phase 3 Daten von ipilimumab zu melanoma veröffentlichen können u rechnet vermutl. fix mit zulassung spätestens 2011.
und dann noch Prostata!
Die 16$ werden immer mehr zu einer Riesenverarschung.Warum lassen sich institutionelle so simple über den tisch ziehen??
Antwort auf Beitrag Nr.: 37.920.654 von Ulf-Imat am 04.09.09 15:51:56Es mag ja so sein, nur gibt es bei BMS-Medarex einen kleinen aber feinen Unterschied: es war ein Merger, keine Übernahme. Nach Vollendung des Mergers, der bereits geschehen ist, gibt es nur das Recht zum Erhalt von 16USD und zwar ohne Zinsen. Es gibt seitens der Exaktionäre keine Beteiligung mehr an der Firma. Wenn BMS also die Auszahlung auf St.Nimmerlein oder sehr lange verschiebt bekommen sie ein zinsloses Darlehen - ein Anreiz, genau das zu tun (verzögern). Bei einer Übernahme hast du auch als Minderheitsaktionär immer noch das Anteilsrecht an der Firma bis du eben ausgesqueezt bist und es liegt im Interesse der übernehmenden Firma dich so schnell wie möglich abzufinden. Deswegen gibt es hier sehr wohl einen feinen Unterschied und ich würde mich nicht einfach so darauf verlassen, dass ich mein Geld recht schnell sehe. Speziell dieser Punkt ist eine absolute Frechheit von Medarex Management und BOD gegenüber den Shareholdern und zeigt, dass sie deren Interesse in keinster Weise berücksichtigt haben.
Ansonsten kann ich bestoff nur zustimmen. Das alles hat sowas von gestunken. Aber die Erklärung für die hohe Institutionellen quote ist recht einfach: die Institutionen sehen nur das schnelle Geld und keiner hat mehr das Interesse in die Tiefe zu schauen oder gewisse Risiken einzugehen. Das erklärt den geringen und lächerlichen Übernahmepreis und die Willigkeit dieses Angebot anzunehmen. Und ich könnte mir auch vorstellen, dass bestimmte Institutionen noch mit illegalen Extra-Goodies zum Tendern gelockt wurden. Kriegt ja keiner mit und über die SEC lacht ja auch die ganze Welt (Stichwort: Madoff).
Ansonsten kann ich bestoff nur zustimmen. Das alles hat sowas von gestunken. Aber die Erklärung für die hohe Institutionellen quote ist recht einfach: die Institutionen sehen nur das schnelle Geld und keiner hat mehr das Interesse in die Tiefe zu schauen oder gewisse Risiken einzugehen. Das erklärt den geringen und lächerlichen Übernahmepreis und die Willigkeit dieses Angebot anzunehmen. Und ich könnte mir auch vorstellen, dass bestimmte Institutionen noch mit illegalen Extra-Goodies zum Tendern gelockt wurden. Kriegt ja keiner mit und über die SEC lacht ja auch die ganze Welt (Stichwort: Madoff).
Antwort auf Beitrag Nr.: 37.916.250 von Ville7 am 04.09.09 05:55:14Der Aktienbesitz wurde ja in das Recht transferiert 16USD pro Aktie zu erhalten. Aber scheinbar sind die Broker und auch die Börse ahnungslos wie das jetzt geht.
Tach alle,
mal ein Zwischenstand:
Heute bekam ich 2x Post von der Sparkasse (bei der ich auch in 2 voneinander unabhängigen Depots Medarex habe/hatte).
Man stellt klar, dass sie -als Depotverwalter- für mich die 16 USD Barabfindung pro Share "reinholen" (sich also drum kümmern) und mit mir abrechnen.
Man weist außerdem darauf hin, dass die Zahlung einer 30%igen Ami-Quellensteuer unterliegen kann. (gemäß IRC Section 302 - was immer das auch heißt).
Allerdings bin ich erstaunt, dass ich bisher nur von der SPK informiert wurde - und dann noch per Schneckenpost (was aber dort der übliche Weg ist).
Gruß
Zock
Tach alle,
mal ein Zwischenstand:
Heute bekam ich 2x Post von der Sparkasse (bei der ich auch in 2 voneinander unabhängigen Depots Medarex habe/hatte).
Man stellt klar, dass sie -als Depotverwalter- für mich die 16 USD Barabfindung pro Share "reinholen" (sich also drum kümmern) und mit mir abrechnen.
Man weist außerdem darauf hin, dass die Zahlung einer 30%igen Ami-Quellensteuer unterliegen kann. (gemäß IRC Section 302 - was immer das auch heißt).
Allerdings bin ich erstaunt, dass ich bisher nur von der SPK informiert wurde - und dann noch per Schneckenpost (was aber dort der übliche Weg ist).
Gruß
Zock
Antwort auf Beitrag Nr.: 37.926.304 von Zock1000 am 05.09.09 19:25:58Hi Zock...
welche Sparkasse bist du!?
welche Sparkasse bist du!?
Antwort auf Beitrag Nr.: 37.924.666 von Ville7 am 05.09.09 07:03:36Bei einem Merger gibt es in der Regel aber einen Aktientausch, keine Barzahlung (siehe z.B. Merger Idec/Biogen).
Antwort auf Beitrag Nr.: 37.926.744 von Ulf-Imat am 05.09.09 23:46:42@Ulf-Imat
Kannst Du auch sagen, wie ein solcher Aktientausch steuerlich behandelt wird - wenn die alten Aktien z.B. noch in 2008 gekauft wurden.
Läuft dann die "alte" Speku-Frist von 1 Jahr mit den neuen Aktien einfach weiter, oder erlischt diese dann. Sprich ist es dann so, als ob die neuen Aktien zu Stichtag des Tausches gekauft und die alten am gleichen Tag verkauft wurden.
Dann würden ja für die alten Aktien Steuern anfallen, und später beim Verkauf der neuen ebenfalls. (Sofern Gewinne gemacht wurden).
Oder läuft die Frist mit den neuen Aktien einfach weiter (wäre schön - glaub ich aber fast nicht, weil wir Aktionäre steuerlich fast immer über den Tisch gezogen werden).
Vielen Dank im Voraus.
ZT
Kannst Du auch sagen, wie ein solcher Aktientausch steuerlich behandelt wird - wenn die alten Aktien z.B. noch in 2008 gekauft wurden.
Läuft dann die "alte" Speku-Frist von 1 Jahr mit den neuen Aktien einfach weiter, oder erlischt diese dann. Sprich ist es dann so, als ob die neuen Aktien zu Stichtag des Tausches gekauft und die alten am gleichen Tag verkauft wurden.
Dann würden ja für die alten Aktien Steuern anfallen, und später beim Verkauf der neuen ebenfalls. (Sofern Gewinne gemacht wurden).
Oder läuft die Frist mit den neuen Aktien einfach weiter (wäre schön - glaub ich aber fast nicht, weil wir Aktionäre steuerlich fast immer über den Tisch gezogen werden).
Vielen Dank im Voraus.
ZT
für Medarex nicht relevant, da Barausschüttung, aber hier die Theorie:
http://www.ratgeber-steuer24.de/Besteuerung_von_Spekulations…
http://www.ratgeber-steuer24.de/Besteuerung_von_Spekulations…
Antwort auf Beitrag Nr.: 37.926.831 von Ulf-Imat am 06.09.09 01:42:00Klar, ist nicht relevant für MEDX - aber ggf. in anderem Zusammenhang interessant.
Trotzdem Danke für den Link. Schau morgen mal genauer rein.
ZT
Trotzdem Danke für den Link. Schau morgen mal genauer rein.
ZT
Antwort auf Beitrag Nr.: 37.926.744 von Ulf-Imat am 05.09.09 23:46:42Das besondere am Medarex-BMS Merger ist, dass kein Aktientausch stattfand. Es ist ein reiner Cashmerger und eine Seite der Aktionäre wird einfach gegen Barzahlung "enteignet". De facto heisst das hier: Die beiden Firmen gehen zusammen und der Rest der Medarexaktionäre werden barabgefunden oder out-ge-squeezed (rausgedrängt). Aber wie gesagt, wenn man (wie BMS) auf die Barabfindung nicht mal Zinsen zahlen muß, könnte ich mit vorstellen, dass man es nicht so eilig hat.
Antwort auf Beitrag Nr.: 37.926.716 von where_is_the_beef am 05.09.09 23:28:00welche Sparkasse bist du!?
Diese Infos habe ich von der Sparkasse Bochum.
Dat is da, wo der Pott kocht.
Gruß
Zock
Diese Infos habe ich von der Sparkasse Bochum.
Dat is da, wo der Pott kocht.

Gruß
Zock
Das Medarex Messageboard in Yahoo gibt es übrigens noch, auch wenn nicht mehr über die Aktie zu finden. Hier der Link:
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
Nur als Information für diejenigen, die ihre Anteile auch nicht mehr über die Börse verkauft haben: Meine Medarex-Anteile sind heute ausgebucht worden. Amerikanische Steueren sind offenbar nicht angefallen.
Antwort auf Beitrag Nr.: 37.921.457 von Ulf-Imat am 04.09.09 17:07:14Die Dresdner Bank hat mir heute 16$ pro Aktie gutgeschrieben.
Kann ich für Consors bestätigen. Für die Restposi dort sind 16 Dollar pro Aktie gutgeschrieben worden.
Damit verabschiede ich mich aus diesem Thread. Man liest sich anderswo.
Damit verabschiede ich mich aus diesem Thread. Man liest sich anderswo.
So wie ich es gesagt habe.
Wer gewartet hat und sich die Stücke hat ausbuchen lassen hat weder Gebühren gezahlt und sogar einen etwas höheren Kurs gesehen.

Wer gewartet hat und sich die Stücke hat ausbuchen lassen hat weder Gebühren gezahlt und sogar einen etwas höheren Kurs gesehen.

Antwort auf Beitrag Nr.: 37.945.852 von VaJo am 09.09.09 13:39:47Das war wieder ein typischer Vajo, einfach falsches Geschwätz ohne zu Recherchieren oder nachzudenken.
Wir sind hier alle europäische Investoren, daher interessiert uns die Währung Euro, nicht Dollar.
Wer gewartet hat, hat nicht automatisch mehr bekommen - im Gegenteil. Ich habe meine Teile zu 11,29, 11,18 und 11,23 Euro abgestossen und dabei vernachlässigbare Gebühren gezahlt, ein paar cent je Aktie.
Der Dollar hat allerdings stetig und nicht unerheblich an Wert verloren, daher waren 16 USD zum Tender-Auszahlungszeitpunkt weniger.
Bei Kurs 1,4380 (wie von quepos angegeben) sind das nur noch knapp 11,13 je Medarex-Aktie gewesen.
Wir sind hier alle europäische Investoren, daher interessiert uns die Währung Euro, nicht Dollar.
Wer gewartet hat, hat nicht automatisch mehr bekommen - im Gegenteil. Ich habe meine Teile zu 11,29, 11,18 und 11,23 Euro abgestossen und dabei vernachlässigbare Gebühren gezahlt, ein paar cent je Aktie.
Der Dollar hat allerdings stetig und nicht unerheblich an Wert verloren, daher waren 16 USD zum Tender-Auszahlungszeitpunkt weniger.
Bei Kurs 1,4380 (wie von quepos angegeben) sind das nur noch knapp 11,13 je Medarex-Aktie gewesen.
Antwort auf Beitrag Nr.: 37.951.964 von Ville7 am 10.09.09 09:44:35hab's auch noch recht gut erwischt, mit 11,22 / 11,31 / 11,18. hab die zweite hälfte von x.xxx shares bei ankündigung, dass bereits 87% getendered sind, auch eilig über die börse verscherbelt.
naja, ich kann mich nicht beklagen. für mich war MEDX von anfang an eine übernahme-spekulation. da ich das management nie wirklich gut fand, wollte ich hier nie langfristig kohle ablagern (so wie bei MOR); die pipeline war aber dann doch zu beeindruckend, um nichts vom den zeugs zu kaufen.
sicher, mehr kann es immer sein, aber ich danke trotzdem für die fetten prozente
in diesem sinne wünsche ich weiterhin allen gute investemententscheidungen!
lg
pf2
naja, ich kann mich nicht beklagen. für mich war MEDX von anfang an eine übernahme-spekulation. da ich das management nie wirklich gut fand, wollte ich hier nie langfristig kohle ablagern (so wie bei MOR); die pipeline war aber dann doch zu beeindruckend, um nichts vom den zeugs zu kaufen.
sicher, mehr kann es immer sein, aber ich danke trotzdem für die fetten prozente

in diesem sinne wünsche ich weiterhin allen gute investemententscheidungen!
lg
pf2
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 210 | ||
| 94 | ||
| 82 | ||
| 62 | ||
| 53 | ||
| 49 | ||
| 41 | ||
| 34 | ||
| 29 | ||
| 28 |
| Wertpapier | Beiträge | |
|---|---|---|
| 25 | ||
| 22 | ||
| 22 | ||
| 22 | ||
| 21 | ||
| 21 | ||
| 20 | ||
| 19 | ||
| 18 | ||
| 18 |



















