Sarepta Therapeutics - first-in-class RNA - 500 Beiträge pro Seite
eröffnet am 08.11.12 23:37:01 von
neuester Beitrag 04.11.16 16:16:22 von
neuester Beitrag 04.11.16 16:16:22 von
Beiträge: 352
ID: 1.177.703
ID: 1.177.703
Aufrufe heute: 0
Gesamt: 27.385
Gesamt: 27.385
Aktive User: 0
ISIN: US8036071004 · WKN: A1J1BH · Symbol: SRPT
127,39
USD
+2,53 %
+3,14 USD
Letzter Kurs 02:00:00 Nasdaq
Neuigkeiten
24.04.24 · Business Wire (engl.) |
29.03.24 · Business Wire (engl.) |
04.03.24 · Business Wire (engl.) |
01.03.24 · Business Wire (engl.) |
29.02.24 · Business Wire (engl.) |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,9000 | +59,66 | |
| 4,7450 | +35,57 | |
| 0,5250 | +19,08 | |
| 5,8900 | +17,80 | |
| 1,9700 | +15,20 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,7000 | -13,71 | |
| 3,0400 | -19,95 | |
| 1,9500 | -25,14 | |
| 1,6052 | -30,21 | |
| 0,5121 | -30,80 |
Bin beim durchforsten von RNA- Forschungsprojekten kürzlich auf die ehemals AVI und heute Sarepeta (SRPT) site gestossen. Etliche Programme am laufen, unter anderem auch die Prüfungsantrag auf orphan status von AVI-4658
Der Kurs hat sich auch dadurch binnen 2 Monaten ver 3-facht.
Die RNA-Interferenz-Technologie wird meiner Meinung nach die Biotech-Branche in Zukunft stark prägen.
Jemand investiert oder nähere Infos?
http://www.sareptatherapeutics.com/
http://www.sareptatherapeutics.com/our-programs/
Der Kurs hat sich auch dadurch binnen 2 Monaten ver 3-facht.
Die RNA-Interferenz-Technologie wird meiner Meinung nach die Biotech-Branche in Zukunft stark prägen.
Jemand investiert oder nähere Infos?
http://www.sareptatherapeutics.com/
http://www.sareptatherapeutics.com/our-programs/
Hier noch ein Monatschart Chart
Gute News aus London!
Sarepta Therapeutics' Shares Skyrocket on Success of Muscular Dystrophy Drug
http://www.minyanville.com/sectors/biotech-pharma/articles/s…" target="_blank" rel="nofollow ugc noopener">http://www.minyanville.com/sectors/biotech-pharma/articles/s…
Sarepta Therapeutics' Shares Skyrocket on Success of Muscular Dystrophy Drug
http://www.minyanville.com/sectors/biotech-pharma/articles/s…" target="_blank" rel="nofollow ugc noopener">http://www.minyanville.com/sectors/biotech-pharma/articles/s…
News am 24.
at the Piper Jaffray Healthcare Conference in New York
at the Piper Jaffray Healthcare Conference in New York
Antwort auf Beitrag Nr.: 43.804.510 von lunatics am 08.11.12 23:37:01Hallo lunatics,
"Die RNA-Interferenz-Technologie wird meiner Meinung nach die Biotech-Branche in Zukunft stark prägen."
Könntest Du in 1-2 Sätzen erklären, was man sich unter dieser Technologie vorzustellen hat?
Danke und Gruss,
s.
"Die RNA-Interferenz-Technologie wird meiner Meinung nach die Biotech-Branche in Zukunft stark prägen."
Könntest Du in 1-2 Sätzen erklären, was man sich unter dieser Technologie vorzustellen hat?
Danke und Gruss,
s.
Antwort auf Beitrag Nr.: 43.804.510 von lunatics am 08.11.12 23:37:01Eines noch,
Kennst/hast Du Dich mit der Firma Stemcells beschäftigt/hast Du eine Meinung?
Und grundsätzlich: Kennst Du einen Biotech-Börsenbrief, der empfehlenswert wäre?
Schönen Tag,
s.
Kennst/hast Du Dich mit der Firma Stemcells beschäftigt/hast Du eine Meinung?
Und grundsätzlich: Kennst Du einen Biotech-Börsenbrief, der empfehlenswert wäre?
Schönen Tag,
s.
SRPT wird momentan getrieben durch bullische comments from Piper Jaffray 

Zitat von sufenta: Hallo lunatics,
Könntest Du in 1-2 Sätzen erklären, was man sich unter dieser Technologie vorzustellen hat?
s.
Die RNA interferenz ist einfach gesagt ein Werkzeug zur Gensteuerung.
Hier primär zwei Ansatzpunkte:
1. Bei der Targetvalidierung mittels Genexpression, also bei der gezielten Suche nach Genen, die bei einer bestimmten Krankheit involviert sind, können diese mittels RNAi ausgeschaltet werden. Dabei hemmen kurze RNA-Moleküle die Bildung bestimmter Genprodukte. Mit den gewonnen Erkenntnissen der Wirkung von Signalwegen, können schneller und gezielter neue Therapieansätze und somit effizientere Wirkstoffe entwickelt werden.
2. Theoretisch lässt sich auch der Zellbauplan verändern. So dass beispielsweise Tumorzellen manipuliert werden können.
Forschungen setzen aber auch primär auf RNAi-gesteuerte Stammzellen. Somit wäre es möglich aus einer Stammzelle ein beliebiges Organ entwickeln zu lassen.
Zitat von sufenta: Eines noch,
Kennst/hast Du Dich mit der Firma Stemcells beschäftigt/hast Du eine Meinung?
Und grundsätzlich: Kennst Du einen Biotech-Börsenbrief, der empfehlenswert wäre?
s.
STEM ist sicher einer der am weitesten fortgeschrittenen in Sachen Entwicklung. Hat ein vielversprechendes CNS-Programm. Würde ich bei einem Einstieg favorisieren. Will man in eine andere Richtung, wären Pluristem, Opexa, Geron, Aastrom, NeuralStem zu prüfen.
Ich kenne keinen "empfehlenswerten" Biotech-Börsenbrief.
Hallo lunatics,
Hab' vielen Dank für die Erklärung einer komplexen Technologie in einfachen und sehr verständlichen Worten. Hätte mit diesem Wissen sogar vor Jahren (schon) investiert. So gibt es nach dem Rückgang der letzten Jahre, man siehe sich nur die entsprechenden Charts an (z.B. STEM), eigentlich keine bessere Investition und besseren Zeitpunkt, als jetzt einzusteigen.
Stammzellen und o.g. Technologie wird und MUSS kommen.
Hab' vielen Dank für die Erklärung einer komplexen Technologie in einfachen und sehr verständlichen Worten. Hätte mit diesem Wissen sogar vor Jahren (schon) investiert. So gibt es nach dem Rückgang der letzten Jahre, man siehe sich nur die entsprechenden Charts an (z.B. STEM), eigentlich keine bessere Investition und besseren Zeitpunkt, als jetzt einzusteigen.
Stammzellen und o.g. Technologie wird und MUSS kommen.
Antwort auf Beitrag Nr.: 43.849.956 von sufenta am 22.11.12 00:43:56Ja sie wird kommen aber es ist ein langer Weg mit möglichen Rückschlägen.
Aber der Zeitpunkt ist nicht schlecht.
Aber der Zeitpunkt ist nicht schlecht.
Multibagger Potential
http://www.fool.com/investing/general/2012/11/22/piper-jaffr…
http://www.fool.com/investing/general/2012/11/22/piper-jaffr…
Sarepta Therapeutics into collaboration for the development of additional exon-skipping product for
Duchenne muscular dystrophy with University College London's (UCL)
Duchenne muscular dystrophy with University College London's (UCL)
Eine Aktie mit Potential.
Hier sollte man früh genug dabei sein.
(Nur meine Meinung)
Danke für den Tip lunatics :-)
Hier sollte man früh genug dabei sein.
(Nur meine Meinung)
Danke für den Tip lunatics :-)
Rumors:
Vertex zeigt plötzlich Interesse an Sarepta's AVI-4658 (Eteplirsen), Indikation DMD...
Facts:
Piper Jaffray sieht für den SRPT-Stock 60-80 USD kurzzeitig sogar 160..
let's party ?!
Vertex zeigt plötzlich Interesse an Sarepta's AVI-4658 (Eteplirsen), Indikation DMD...
Facts:
Piper Jaffray sieht für den SRPT-Stock 60-80 USD kurzzeitig sogar 160..

let's party ?!

Antwort auf Beitrag Nr.: 43.876.038 von lunatics am 29.11.12 17:11:37Wow 
Das hört sich doch super an.
Wurde ein Zeitraum genannt?

Das hört sich doch super an.
Wurde ein Zeitraum genannt?
Antwort auf Beitrag Nr.: 43.876.265 von Go for it am 29.11.12 17:52:22nein.
aber wenn die so weiterpushen kann es ziemlich schnell gehen.
aber wenn die so weiterpushen kann es ziemlich schnell gehen.
Antwort auf Beitrag Nr.: 43.876.588 von lunatics am 29.11.12 19:08:35Darüber würde ich mich auch freuen 

Seeking Alpha meint:
...We agree with analysts who believe that this firm's drug eteplirsen for Duchenne muscular dystrophy. should be approved. The key word here is safety and the drug seems safe. We agree also that the FDA has its own rules and regulations regarding accelerated approvals of drugs. But we also believe there is substantial need for such a drug right now. Based on the proof of concept of Sarepta RNA-derived treatments, a novel difficult technology, and the drug's positive results on a disease as dangerous and crippling as Duchenne muscular dystrophy, we feel good about the drug and the firm.
Data, indeed, exist that the drug increases the level of dystrophin, which offers the proof of concept towards the fact that the molecules could bring hope to the hopeless children and their families.
So, the odds of an accelerated approval are favorable towards and, yes, with the condition of conducting a large trial then after more confirmatory results.
In any case, the firm's technology seems to offer safe and effective REN-derived therapeutics - a hard task that took years of the firm's time, effort and money.
...We agree with analysts who believe that this firm's drug eteplirsen for Duchenne muscular dystrophy. should be approved. The key word here is safety and the drug seems safe. We agree also that the FDA has its own rules and regulations regarding accelerated approvals of drugs. But we also believe there is substantial need for such a drug right now. Based on the proof of concept of Sarepta RNA-derived treatments, a novel difficult technology, and the drug's positive results on a disease as dangerous and crippling as Duchenne muscular dystrophy, we feel good about the drug and the firm.
Data, indeed, exist that the drug increases the level of dystrophin, which offers the proof of concept towards the fact that the molecules could bring hope to the hopeless children and their families.
So, the odds of an accelerated approval are favorable towards and, yes, with the condition of conducting a large trial then after more confirmatory results.
In any case, the firm's technology seems to offer safe and effective REN-derived therapeutics - a hard task that took years of the firm's time, effort and money.
Antwort auf Beitrag Nr.: 43.912.411 von lunatics am 10.12.12 21:58:28Sorry, weil falscher Thread (wird dann vielleicht mehr frequentiert), aber auch Multibagger-Potential: Uni-Pixel (heute >50%). Denke, dass kurzfristige KZ um 30-40$ absolut realistisch sein dürften bei aktueller MK. Langfristig bin ich gespannt, werd' unter 50 nicht verkaufen.
P.S. Wie würdest Du mit Stemcells "verfahren"? Ruduce/Hold/Sell? (will ja noch Sarepta )
)
Gruss,s.
P.S. Wie würdest Du mit Stemcells "verfahren"? Ruduce/Hold/Sell? (will ja noch Sarepta
 )
)Gruss,s.
Antwort auf Beitrag Nr.: 43.912.629 von sufenta am 10.12.12 22:54:38UNXL kenn ich ehrlich zuwenig...scheint aber Ende der Fahnenstange ? chartmässig könnte das Stück auf 6 runter...kenne aber diesen Markt nicht.
STEM: Was hast du für einen EP? Unter 5 würd ich halten. Braucht viel Zeit. Ich habe meiner Jüngsten unter anderem STEM ins Depot gelegt. In 30 Jahren will sie ernten à la Intel oder MSFT,..... wir werden sehen.
wir werden sehen.
SRPT, schwierig momentan. Viel ist schon im Kurs eingepreist. Ein Rücksetzer auf 15 liegt durchaus drinn. Sauber wäre jettzt nochmals ein Split. Nochmals 1:10...macht sie optisch nochmals günstiger und zieht die Fliegen an.
Bei weiterer Daten zu AVI-4658 kann die Aktie neue Höhen gewinnen. Momentan in der open-label Phase IIb safety-Studie in DMD.
STEM: Was hast du für einen EP? Unter 5 würd ich halten. Braucht viel Zeit. Ich habe meiner Jüngsten unter anderem STEM ins Depot gelegt. In 30 Jahren will sie ernten à la Intel oder MSFT,.....
 wir werden sehen.
wir werden sehen.SRPT, schwierig momentan. Viel ist schon im Kurs eingepreist. Ein Rücksetzer auf 15 liegt durchaus drinn. Sauber wäre jettzt nochmals ein Split. Nochmals 1:10...macht sie optisch nochmals günstiger und zieht die Fliegen an.
Bei weiterer Daten zu AVI-4658 kann die Aktie neue Höhen gewinnen. Momentan in der open-label Phase IIb safety-Studie in DMD.
Sarepta Therapeutics: No Problem With Cash 
http://seekingalpha.com/article/1067121-sarepta-therapeutics…

http://seekingalpha.com/article/1067121-sarepta-therapeutics…
am 09. Januar interessante News!
So, Sarepta verabschiedet sich mit +450% im 2012 
Interessant und witzig die Predictions für 2013
http://beta.fool.com/briannichols/2012/12/28/healthcare-outl…

Interessant und witzig die Predictions für 2013

http://beta.fool.com/briannichols/2012/12/28/healthcare-outl…
Am 09 Januar interssante NEWS?
Was genau ist am 9. Januar für ein Termin?
Was sind das für News?
Was genau ist am 9. Januar für ein Termin?
Was sind das für News?
Hallo lunatics,
wo kann ich nachlesen, dass es am 9. Januar News gibt?
Quelle?
Danke
wo kann ich nachlesen, dass es am 9. Januar News gibt?
Quelle?
Danke
Quelle Sarepta Homepage
Event Details
Title Sarepta Therapeutics Inc at JPMorgan Global Healthcare Conference
Date and Time Wednesday, January 9, 2013 4:30 p.m. PT
Location Westin St. Francis Hotel
San Francisco, CA
Event Details
Title Sarepta Therapeutics Inc at JPMorgan Global Healthcare Conference
Date and Time Wednesday, January 9, 2013 4:30 p.m. PT
Location Westin St. Francis Hotel
San Francisco, CA
Am besten via webcast live...so kann man notfalls reagieren 

Hallo Lunatics,
in Deutschland scheinen nicht sehr viele in Sarepta investiert zu sein.
Was wird am 09. Januar das Thema sein.
Wird die Aktie weiter steigen?
Gruß Go for it
in Deutschland scheinen nicht sehr viele in Sarepta investiert zu sein.

Was wird am 09. Januar das Thema sein.
Wird die Aktie weiter steigen?
Gruß Go for it
Huhu
noch jemand hier?
Gibts bald News o.ä.
noch jemand hier?
Gibts bald News o.ä.

Antwort auf Beitrag Nr.: 44.058.953 von Go for it am 24.01.13 13:58:04Ja SRPT steigt weiter.
zudem:
http://www.fool.com/investing/general/2013/01/10/jpmorgan-he…

zudem:
http://www.fool.com/investing/general/2013/01/10/jpmorgan-he…
unsere Sarepta ist sehr Volatil...
aber heute gehts ja fix rauf...
aber heute gehts ja fix rauf...
Ja, beachtlich heute wieder der Anstieg.
Die Vola kommt wohl auch von dem schnellen Anstieg im 2012. +400% müssen zuerst verdaut werden.
Die Vola kommt wohl auch von dem schnellen Anstieg im 2012. +400% müssen zuerst verdaut werden.
Na also die News von der JPM-konferenz sitzen!...wenn auch verspätet. Cowen hat als erster reagiert.
Cowen lit a fire under Sarepta today by initiating coverage on the company with a rating of "outperform." The move comes just two weeks after the JPMorgan Healthcare Conference where Sarepta laid out its next steps for readying commercial production for eteplirsen, its Duchenne muscular dystrophy drug that performed exceptionally in mid-stage trials.

Cowen lit a fire under Sarepta today by initiating coverage on the company with a rating of "outperform." The move comes just two weeks after the JPMorgan Healthcare Conference where Sarepta laid out its next steps for readying commercial production for eteplirsen, its Duchenne muscular dystrophy drug that performed exceptionally in mid-stage trials.
Weiteres Vorgehen:
(Artikel jetzt online bei MF und Sarepta)
Eteplirsen wird weiter stark vorangetrieben...Treffen mit FDA noch in diesem Quartal...das Marktpotential bei DMD scheint grösser zu sein als bisher angenommen.
http://www.sareptatherapeutics.com/
(Artikel jetzt online bei MF und Sarepta)
Eteplirsen wird weiter stark vorangetrieben...Treffen mit FDA noch in diesem Quartal...das Marktpotential bei DMD scheint grösser zu sein als bisher angenommen.

http://www.sareptatherapeutics.com/
bin gestern zu 27,50 $ mit einer ersten Position eingestiegen und versuche diese bei Kursen unter 25 $ weiter auszubauen. Ich bin sowohl von der RNA-Technologie überzeugt als auch vom ersten Medikamentenkandidaten eteplirsen.
Die MK von 650 Mio. $ halte ich für angemessen. Wird eteplirsen tatsächlich auf den Markt kommen halte ich mehrere Mrd. $ Unternehmenswert für möglich ( Grüßenordnung 3-5 Mrd. $).
Bin hier langfristig investiert und hoffe auf weitere Zukäufe, die momentane Volativität kümmert mich überhaupt nicht.
Zudem kann ich mir sehr gut vorstellen, dass wielunatics schon sagte diese Technologie noch einige Krankheiten mehr heilen/besiegen/lindern könnte. Daher gebe ich kein Stück mehr aus der Hand!
Die MK von 650 Mio. $ halte ich für angemessen. Wird eteplirsen tatsächlich auf den Markt kommen halte ich mehrere Mrd. $ Unternehmenswert für möglich ( Grüßenordnung 3-5 Mrd. $).
Bin hier langfristig investiert und hoffe auf weitere Zukäufe, die momentane Volativität kümmert mich überhaupt nicht.
Zudem kann ich mir sehr gut vorstellen, dass wielunatics schon sagte diese Technologie noch einige Krankheiten mehr heilen/besiegen/lindern könnte. Daher gebe ich kein Stück mehr aus der Hand!
hmmm...dunkle Wolken... The Street rechnet mit Verzögerung der Zulassung
...zur Sicherheit stoploss über Gewinnschwelle montiert.

...zur Sicherheit stoploss über Gewinnschwelle montiert.
Wo steht das?
Wer ist The Street?
Danke
Wer ist The Street?

Danke
Danke
Bin auch erstmal rausgegangen.
Bin auch erstmal rausgegangen.
Ich bleibe drinn.
...Habe mich aber abgesichert.
...Habe mich aber abgesichert.
Antwort auf Beitrag Nr.: 44.132.840 von Go for it am 12.02.13 19:45:35Hoffentlich bekomme ich den Zug bei 24, -24,50 $ wieder.

Antwort auf Beitrag Nr.: 44.132.770 von lunatics am 12.02.13 19:31:35von solchen Mußmaßungen und Spekulationen lasse ich mich nicht beeinflussen. Jeder der bei Sarepta investiert ist weiß um die Risiken, aber auch um die Chancen.
Und was die FDA macht und was nicht, dass weiß kein Analyst/Journalist dieser Welt!
Und was die FDA macht und was nicht, dass weiß kein Analyst/Journalist dieser Welt!
Da kann ich dir nur zustimmen
Zukauf zu 26,20 $. Höre mir heute Abend das webcast zur LeerinkSwann Global Healthcare-Konferenz an, bin mal gespannt wie sie sich heute präsentieren. Mein nächstes Kauflimit liegt bei 25,50 und 24,50 $.
war eine meiner Meinung nach gute Konferenz. Es sollen weitere exon-scipping-targets untersucht werden. Man möchte weitere Indikationen finden und ggf. selbst das Muskelwachstum anregen. Für mich bleibt die company ein klarer Kauf!
Antwort auf Beitrag Nr.: 44.147.050 von Stockfinder am 15.02.13 18:13:14Ein gutes Zeichen ..die 29$ sind wieder da

gebe hier definitiv kein Stück mehr aus der Hand zu unter 100 $ - kommt die Zulassung in 1-2 Jahren haben wir hier einen neuen Pharmaplayer mit 5 Mrd+x an Börsenwert!
bin auch schon mit der Hälfte zufrieden.

Nein, wäre nicht mit der Hälfte zufrieden wenn es zu einer Marktzulassung kommt, denn dann ist es ein Blockbuster-Medikament und die Technologie dürfte auch bei der Bekämpfung anderen Krankheiten durchaus Resultate erzeugen, wenn denn mal genug Cashflow/Gewinn aus Eteplirsen generiert und in diversen Indikationen geforscht werden kann.
unsere Sarepta
Nun schon über 30 $ "Ausbruch..."
Nun schon über 30 $ "Ausbruch..."

die Kurzfristige Entwicklung ist natürlich schön, spielt jedoch für mich keine Rolle. Aller Unkenrufe zum Trotz ( "the street" ) hat sich die Aktie binnen Tage wieder an die Höchstände der letzten Woche heran gearbeitet. Das sollte der Maßstab sein!
Jetzt wo auch noch der Georges Soros fund seine Finger drin hat kann's nur noch gut kommen.
@stockfinder: Nur nicht in Übermut verfallen. SRPT hat im letzten Jahr über 400% zugelegt...und wenn die Marktzulassung kommt muss der Kurs nicht unbedingt steigen. Die geilste Zeit ist hier und jetzt...einige Monate vor der Zulassung. Hier verdient man am meisten.
SRPT-Gruss Lunatics
....der gerade den Stoploss nachzieht.
@stockfinder: Nur nicht in Übermut verfallen. SRPT hat im letzten Jahr über 400% zugelegt...und wenn die Marktzulassung kommt muss der Kurs nicht unbedingt steigen. Die geilste Zeit ist hier und jetzt...einige Monate vor der Zulassung. Hier verdient man am meisten.
SRPT-Gruss Lunatics
....der gerade den Stoploss nachzieht.

Antwort auf Beitrag Nr.: 44.194.294 von lunatics am 27.02.13 19:29:14ich bleibe bei meiner Aussage: "Das Ziel sind 100$"
o.k. hab nichts dagegen 

>100$ ui das wäre nicht schlecht.
Schaun wir mal wie es gleich losgeht.
Schaun wir mal wie es gleich losgeht.

Gestern noch reingekommen:
Sarepta higher after report of hospitalizations related to GSK drug
Shares of Sarepta Therapeutics (SRPT) are up $2.86, or 9.85%, to $31.89 and the strength is being attributed to a report by TheStreet.com that said patients were hospitalized after being treated with GlaxoSmithKline's (GSK) experimental drug for Duchenne muscular dystrophy. The report adds that Sarepta is scheduled to meet with the FDA this quarter to discuss a possible accelerated approval filing of its own Duchenne muscular dystrophy treatment, eteplirsen.
Sarepta higher after report of hospitalizations related to GSK drug
Shares of Sarepta Therapeutics (SRPT) are up $2.86, or 9.85%, to $31.89 and the strength is being attributed to a report by TheStreet.com that said patients were hospitalized after being treated with GlaxoSmithKline's (GSK) experimental drug for Duchenne muscular dystrophy. The report adds that Sarepta is scheduled to meet with the FDA this quarter to discuss a possible accelerated approval filing of its own Duchenne muscular dystrophy treatment, eteplirsen.
Sarepta Therapeutics'AVI-7288 marburg drug shows high survival rates after intramuscular delivery in non-human primates
Antwort auf Beitrag Nr.: 44.212.601 von lunatics am 04.03.13 19:32:58Hört sich doch gut an. 
Pö a Pö geht`s voran

Pö a Pö geht`s voran
Jetzt sollten wir uns charttechnisch nur über der 30 $ halten, dann sieht es kurzfristig rosig aus. Habe noch zwei Kaufaufträge platziert zu 29,50 und 29 $, danach ist sarepta in meinem Biotech-Depot 33,33 % schwer.
wäre natürlich schön. EP $ 22.41 habe aber nur 1 Kauf bisher.
Hoffentlich hält die 30 $ Marke 

habe einen Mischkurs von knapp 27$ und versuche final zu den o.g. Kursen die Positionsgröße auszubauen. Die 30$ hat gehalten, Volumen wieder einmal sehr hoch!
Antwort auf Beitrag Nr.: 44.218.140 von Stockfinder am 05.03.13 22:32:43Ist Morgen 07.03.2013 ein wichtiger Termin?
Gibt es News?
Wann ist der nächste interessante Termin?
Gibt es News?
Wann ist der nächste interessante Termin?
ja, morgen werden die Zahlen für 2012 veröffentlicht und ein neuer company-overview......könnte durchaus spannend werden....
Antwort auf Beitrag Nr.: 44.222.895 von Stockfinder am 06.03.13 21:30:18Da bin ich gespannt... 

gibt es News .. wie waren die gestrigen Ergebnisse..?
Antwort auf Beitrag Nr.: 44.230.015 von Go for it am 08.03.13 13:27:49Verlust vergrössert, Ertrag gesunken.
Alles im normalen Rahmen. Kurs steigt weiter.
Alles im normalen Rahmen. Kurs steigt weiter.
RNA-Schmieden im 6-Monatsvergleich gegenüber NBI
Opko Healt OPK
Alnylam Pharmaceuticals ALNY
Sarepta Therapeutics SRPT

Opko Healt OPK
Alnylam Pharmaceuticals ALNY
Sarepta Therapeutics SRPT
Morgen treffen sich einige betroffene Familien mit Frau Dr. Hamburg von der FDA. Grundsätzlich gehe ich davon aus, dass sie die Betroffenen mit Sicherheit nicht eingeladen hat um ihnen zu verkünden, dass es keine Fast-Track-Studie geben wird, denn es wurde von der Durchenne-community gute Lobbyarbeit geleistet. Die heißen Tage brechen an.....es wird spannend
Antwort auf Beitrag Nr.: 44.237.356 von Stockfinder am 11.03.13 14:11:21Danke für die Info
Gerne. Die Wortführerin hat einen ihrer Söhne, den jüngeren der beiden, bereits an der PhaseII mit eteplirsen teilnehmen lassen. Der Junge kann mittlerweile sogar selbständig greifen und Flaschen sowie Gläser öffnen. Im Internet gibt es sogar ein Video das den Jungen beim Skilaufen zeigt. Der Ältere der beiden durfte/konnte an der Studie noch nicht teilnehmen, er soll nun im besten Fall bei der nächsten Studie dabei sein!
Gibt`s was zu berichten?
Wann ist der nächste spannende Termin?
Wann ist der nächste spannende Termin?
leider noch nicht wirklich....warte auch auf Nachrichten bzw. erste Stellungnahmen/Aussagen der Durchenne-D-community....
Zumindest steigt die Aktie gegen den Gesamtmarkt, dass werte ich als positives Zeichen.
Zumindest steigt die Aktie gegen den Gesamtmarkt, dass werte ich als positives Zeichen.
Kurs steigt jedenfalls. Ist doch gut so.
Bin auch mit einer kleinen Position dabei. Das mit MD hört sich gut an. Gibt es hier einen Breakthrough-Status? Orphan drug ja wohl bestimmt.
Die Kampfvirenforschung wird ja wohl vom Pentagon unterstützt...
Die Kampfvirenforschung wird ja wohl vom Pentagon unterstützt...
Habe leider immer noch nichts Neues erfahren können, jedoch ist das steigende Volumen und das deutliche Kursplus ein extrem gutes Zeichen. Vllt. wissen da schon einige mehr....
Schön wenn man dabei ist 

...jetzt sind wir schon über 34...SRPT explodiert.
Ich hätte gern auch nochmals nachgekauft...aber der Kurs geht momentan nur in eine Richtung ...kann nur noch stoploss nachziehen
...kann nur noch stoploss nachziehen

Ich hätte gern auch nochmals nachgekauft...aber der Kurs geht momentan nur in eine Richtung
 ...kann nur noch stoploss nachziehen
...kann nur noch stoploss nachziehen
Antwort auf Beitrag Nr.: 44.254.084 von lunatics am 14.03.13 19:50:59Kleine Konso heute
sieht so aus - bin hier ja sowieso langfristig mit einer buy an hold Strategie investiert. Spätestens in der 1. Aprilwoche wissen wir mehr.
Na dann drücken wir uns die Daumen 

Eröffnung über 34,50$  die Täglichen Eröffnungskurse sind der Brüller..
die Täglichen Eröffnungskurse sind der Brüller..
 die Täglichen Eröffnungskurse sind der Brüller..
die Täglichen Eröffnungskurse sind der Brüller..
Antwort auf Beitrag Nr.: 44.271.418 von Go for it am 19.03.13 14:42:31ich stelle das bei allen Biotechs an der Nasdaq fest: das erste Drittel der Sitzung kannst du ignrieren, das gibts wilde Ausschläge in alle Richtungen, erst danach stellt sich eine Art Trend ein.
Deutsche Bank neu mit rating: buy
Laut Analysten müsste die Rakete bald starten...
erster Halt bei 45-52 $
erster Halt bei 45-52 $

Deutsche Bank sieht 45$ 
Die Börse sieht 2 interessierte Käufer für SRPT und sein Wundermittel.

Die Börse sieht 2 interessierte Käufer für SRPT und sein Wundermittel.

Alles wartet auf die beschleunigte Zulassung... 

Antwort auf Beitrag Nr.: 44.296.329 von Go for it am 25.03.13 16:20:15... bzw. auf die Beantragung derselben durch SRPT.
Antwort auf Beitrag Nr.: 44.296.363 von me_2 am 25.03.13 16:22:40und wieder Anlauf auf die
34,50 $... ist eine harte Nuss...
34,50 $... ist eine harte Nuss...
Sarepta shares could hit $50 with accelerated approval, Barron's says


Antwort auf Beitrag Nr.: 44.298.339 von lunatics am 25.03.13 19:37:59Yeah, that's what Barron's said
Antwort auf Beitrag Nr.: 44.298.423 von me_2 am 25.03.13 19:51:08und wieder Anlauf auf die 34,50$
..langsam sollte SRPT über einen Split nachdenken damit der Kurs wieder günstiger aussieht...

Antwort auf Beitrag Nr.: 44.298.567 von lunatics am 25.03.13 20:09:13sehe ich auch als eine gute Idee 
Aber anscheinend sind nicht sehr viele deutsche Anleger investiert...

Aber anscheinend sind nicht sehr viele deutsche Anleger investiert...

Antwort auf Beitrag Nr.: 44.298.635 von Go for it am 25.03.13 20:19:12Ich gehe davon aus, dass wir (bzw. die AMIs) Morgen die 34,50$
nachhaltig knacken...
nachhaltig knacken...

Antwort auf Beitrag Nr.: 44.298.871 von Go for it am 25.03.13 20:51:30schon heute 

Wow 36,46 $ 

Antwort auf Beitrag Nr.: 44.305.217 von Go for it am 26.03.13 15:23:28Was meint Ihr...
Schaffen wir diese Woche die 40 $ ?
Schaffen wir diese Woche die 40 $ ?

Antwort auf Beitrag Nr.: 44.306.965 von Go for it am 26.03.13 18:06:53schon möglich, wenn der newsflow stimmt (FDA meeting). Als Neueinsteiger bin ich mit dem Kursverlauf der letzten Tage allerdings auch so schon recht happy.
Rock'n Roll today
Jetzt kommt der Nachbrenner. SRPT zieht jetzt Trader wie Fliegen an. Werden den Kurs auf 50 treiben.
Habe Stoploss nachgezogen und mache mir erste Gedanken über die Absprungshöhe.

Jetzt kommt der Nachbrenner. SRPT zieht jetzt Trader wie Fliegen an. Werden den Kurs auf 50 treiben.
Habe Stoploss nachgezogen und mache mir erste Gedanken über die Absprungshöhe.
Antwort auf Beitrag Nr.: 44.307.701 von lunatics am 26.03.13 19:28:54In Sareptas Research and Development Pipeline schlummern noch mehr schätzchen 

Antwort auf Beitrag Nr.: 44.308.225 von Go for it am 26.03.13 20:34:19http://www.sareptatherapeutics.com/our-programs/
Die grosse Kohle bringt aber eindeutig AVI-4658
750 Mio +
750 Mio +
Antwort auf Beitrag Nr.: 44.316.471 von lunatics am 27.03.13 17:44:34der März ist bald rum ...
Ich bin gespannt, wann es News gibt
Ich bin gespannt, wann es News gibt

Antwort auf Beitrag Nr.: 44.323.275 von Go for it am 28.03.13 13:20:26Kann immer noch was passieren, US haben ja weniger Osterfeiertage als wir.
Je länger es geht umso mehr steigt der Kurs.
Von mir aus kann sich SRPT Zeit lassen.
Von mir aus kann sich SRPT Zeit lassen.

Antwort auf Beitrag Nr.: 44.331.279 von lunatics am 29.03.13 17:59:39Kurze Zeit bei 35,30$ ging ganz schön runter...
War das eine Schüttelaktion... bevor...
War das eine Schüttelaktion... bevor...
Antwort auf Beitrag Nr.: 44.348.395 von lunatics am 02.04.13 19:25:32 Gut Analysiert
Gut Analysiert
 Gut Analysiert
Gut Analysiert
Heute deutlich nach unten. Gibts news?
Antwort auf Beitrag Nr.: 44.355.525 von me_2 am 03.04.13 17:07:36Ich habe nichts negatives gelesen, nur dass bis ende April eine Entscheidung
wegen der vorzeitigen Zulassung ansteht.. (Die Analysten sind eher positiv gestimmt)
Zulassung erst ende März nun doch erst ende April... mit ?
Sarepta war schon im Februar sehr volatil.. ich vermute, dass einige die Zeit biszur Entscheidung zum traden nutzen...
Im Februar, gab es teilweise über 3 $ Ausschläge "Schwankung" am Tag...
nur meine Meinung.
wegen der vorzeitigen Zulassung ansteht.. (Die Analysten sind eher positiv gestimmt)
Zulassung erst ende März nun doch erst ende April... mit ?
Sarepta war schon im Februar sehr volatil.. ich vermute, dass einige die Zeit biszur Entscheidung zum traden nutzen...
Im Februar, gab es teilweise über 3 $ Ausschläge "Schwankung" am Tag...
nur meine Meinung.

Hier gibt`s Infos zu Sarepta
http://finance.yahoo.com/q?s=SRPT&ql=0
Die Nerven behalten der Boden ist für heute gefunden ...
Die Volatilität bleibt in den nächsten 14 Tagen.
Nur meine Meinung
Sarepta ist eine Chance mit Risiken (Börse eben)
http://finance.yahoo.com/q?s=SRPT&ql=0
Die Nerven behalten der Boden ist für heute gefunden ...
Die Volatilität bleibt in den nächsten 14 Tagen.
Nur meine Meinung
Sarepta ist eine Chance mit Risiken (Börse eben)
Antwort auf Beitrag Nr.: 44.355.901 von Go for it am 03.04.13 17:45:37Das ist echt der Hammer heute 

Zulassung steht unmittelbar bevor..Kurs sinkt. Schon so oft erlebt.
Normal
Normal

Zukauf einer weiteren Position zu 33,25....auch diese Position wird eingemottet.
Die Biotechs insgesamt kommen heute deutlich unter die Räder zumal gerade diejenigen die in den vergangenen Wochen deutlich outperformt haben (RNA-Techs).....auch Isis heute 4% down.
Nutze bei beiden die Schwäche zum Nachkauf.
Die Biotechs insgesamt kommen heute deutlich unter die Räder zumal gerade diejenigen die in den vergangenen Wochen deutlich outperformt haben (RNA-Techs).....auch Isis heute 4% down.
Nutze bei beiden die Schwäche zum Nachkauf.
ich warte noch mit dem Nachkauf bis der Boden erreicht ist ... (aber wann ist das nur ???)
Robert W. Baird startet Sarepta Therapeutics mit Outperform. Kursziel $63.
Nachbörslich schon wieder bei 35 $. Ruhig bleiben und Schwächen zum Kaufen nutzen.
Nachbörslich schon wieder bei 35 $. Ruhig bleiben und Schwächen zum Kaufen nutzen.
Antwort auf Beitrag Nr.: 44.358.733 von Stockfinder am 03.04.13 23:05:19Das war wohl wieder eine Schüttelaktion um günstig reinzukommen..
Nachbörslich ging es ja wieder kräftig rauf...
Wichtig ist die Nerven zu behalten und auf die baldige Zulassung hoffen...
Es bleibt spannend
Nur meine Meinung
SL setzen... aber nicht zu weit oben
Nachbörslich ging es ja wieder kräftig rauf...

Wichtig ist die Nerven zu behalten und auf die baldige Zulassung hoffen...
Es bleibt spannend

Nur meine Meinung
SL setzen... aber nicht zu weit oben

Hallo Echo...
Noch jemand hier?
Noch jemand hier?

yesss...bin noch drin. 

Antwort auf Beitrag Nr.: 44.365.447 von Go for it am 04.04.13 19:14:02Ja klar. Hab nachgekauft
05.04.2013 | 14:32
Sarepta Therapeutics Announces Eteplirsen Demonstrates Sustained Benefit on Walking Test Through 74 Weeks in Phase IIb Study in Duchenne Muscular Dystrophy / Data to Be Presented at the Muscular Dystrophy Association Scientific Conference
CAMBRIDGE, MA -- (Marketwired) -- 04/05/13 -- Sarepta Therapeutics, Inc. (NASDAQ: SRPT), a developer of innovative RNA-based therapeutics, today announced updated data from Study 202, a Phase IIb open-label extension study of eteplirsen in patients with Duchenne muscular dystrophy (DMD). Results at 74 weeks showed a continued stabilization of walking ability in eteplirsen-treated patients evaluable on the 6-minute walk test (6MWT). As previously reported, Study 202 met its primary endpoint of increased novel dystrophin as assessed by muscle biopsy at week 48 and is now in the long-term extension phase in which patients continue to be followed for safety and clinical outcomes. Eteplirsen is Sarepta's lead exon-skipping compound in development for the treatment of patients with DMD who have a genotype amenable to skipping of exon 51.
After 74 weeks, patients in the 30 mg/kg and 50 mg/kg dose cohorts who were able to perform the 6MWT (modified Intent-to-Treat or mITT population; n=6) showed a statistically significant treatment benefit of 65.2 meters (p ≤ 0.004) when compared to the placebo/delayed-treatment cohort (n=4). The eteplirsen-treated patients in the mITT population demonstrated less than a 5 percent decline (13.4 meters) from baseline in walking ability. After experiencing a substantial decline earlier in the study, the placebo/delayed-treatment cohort also demonstrated stabilization in walking ability from week 36 through 74, the period in which meaningful levels of dystrophin were likely produced, with a less than 10 meter decline over this timeframe.
...
http://www.finanznachrichten.de/nachrichten-2013-04/26447685…
Sarepta Therapeutics Announces Eteplirsen Demonstrates Sustained Benefit on Walking Test Through 74 Weeks in Phase IIb Study in Duchenne Muscular Dystrophy / Data to Be Presented at the Muscular Dystrophy Association Scientific Conference
CAMBRIDGE, MA -- (Marketwired) -- 04/05/13 -- Sarepta Therapeutics, Inc. (NASDAQ: SRPT), a developer of innovative RNA-based therapeutics, today announced updated data from Study 202, a Phase IIb open-label extension study of eteplirsen in patients with Duchenne muscular dystrophy (DMD). Results at 74 weeks showed a continued stabilization of walking ability in eteplirsen-treated patients evaluable on the 6-minute walk test (6MWT). As previously reported, Study 202 met its primary endpoint of increased novel dystrophin as assessed by muscle biopsy at week 48 and is now in the long-term extension phase in which patients continue to be followed for safety and clinical outcomes. Eteplirsen is Sarepta's lead exon-skipping compound in development for the treatment of patients with DMD who have a genotype amenable to skipping of exon 51.
After 74 weeks, patients in the 30 mg/kg and 50 mg/kg dose cohorts who were able to perform the 6MWT (modified Intent-to-Treat or mITT population; n=6) showed a statistically significant treatment benefit of 65.2 meters (p ≤ 0.004) when compared to the placebo/delayed-treatment cohort (n=4). The eteplirsen-treated patients in the mITT population demonstrated less than a 5 percent decline (13.4 meters) from baseline in walking ability. After experiencing a substantial decline earlier in the study, the placebo/delayed-treatment cohort also demonstrated stabilization in walking ability from week 36 through 74, the period in which meaningful levels of dystrophin were likely produced, with a less than 10 meter decline over this timeframe.
...
http://www.finanznachrichten.de/nachrichten-2013-04/26447685…
Experten, was sagen euch diese Ergebnisse des 6MWT ??
Study 202 met its primary endpoint and is now in the long-term extension phase in which patients continue to be followed for safety and clinical outcomes.
Das sagt alles.
Das sagt alles.

SChon klar, aber ich wollte gerne wissen, wie die Experten, die sich schon länger mit SRPT befassen, die 65.2 m treatment benefit vs. Placebo bei 72w beurteilen, ist das ein erwartetes Resultat, oder besser, oder ... ???
oder hat sich niemenad mit diesen Details beschäftigt ?
... jedenfalls spricht der Markt heute eine deutliche Sprache.
... jedenfalls spricht der Markt heute eine deutliche Sprache.
Das Resultat entspricht den Erwartungen und bestätigt die Oktober-Ergebnisse. Von einer Überraschung kann nicht die Rede sein.
Sarepta's Eteplirsen Walks Closer to Success
http://www.fool.com/investing/general/2013/04/05/sareptas-et…
http://www.fool.com/investing/general/2013/04/05/sareptas-et…
Stoploss nachziehen Jungs 

Antwort auf Beitrag Nr.: 44.395.999 von lunatics am 09.04.13 18:51:10... aber nicht zu knapp !!
Antwort auf Beitrag Nr.: 44.396.743 von me_2 am 09.04.13 20:26:54was jetzt los?
..heute fallen die 40 !
..heute fallen die 40 !
...und schon geschehen...geht durch wie Butter..
...weit und breit keine Shorties...
...weit und breit keine Shorties...
Antwort auf Beitrag Nr.: 44.396.955 von lunatics am 09.04.13 20:53:42
Was gibt es neues, was den Kurs so getrieben hat?
Was gibt es neues, was den Kurs so getrieben hat?

ab 45 $ werde ich meinen Zukauf zu 33,25 auflösen und die Position in Astex und vorallem Galena vergrößern. Ich glaube langsam aber sicher das der Markt hier dabei ist eine Zulassung einzupreisen....
Sarepta ist und bleibt einer der Top-Picks im Biotechsektor zur Zeit, ab Mitte des Jahres vermute ich das ISIS die Position von Sarepta einnehmen kann/wird, deren Pipeline ist unglaublich gut besetzt!
stay long
Sarepta ist und bleibt einer der Top-Picks im Biotechsektor zur Zeit, ab Mitte des Jahres vermute ich das ISIS die Position von Sarepta einnehmen kann/wird, deren Pipeline ist unglaublich gut besetzt!
stay long
Antwort auf Beitrag Nr.: 44.398.325 von Stockfinder am 10.04.13 00:32:58wow ein sehr großes Volumen gestern. Aufmersamkeit steigt...
Wo seht Ihr Sarepta am Ende des Monats?
Gruß Go for it
Wo seht Ihr Sarepta am Ende des Monats?
Gruß Go for it
Antwort auf Beitrag Nr.: 44.401.437 von Go for it am 10.04.13 12:19:28Hängt ja wohl vom AA ab, in den höheren 40ern sicher.
das Allzeithoch dürfte wohl in den nächsten Tagen angegriffen werden, ab 45$ wird der Zukauf liquidiert...bin eindeutig überinvestiert.....fühl mich aber zur Zeit pudelwohl.
gleich geht`s weiter ...
Werde bei 44.- die Hälfte meines Bestandes veräussern. Somit könnte SRPT auf 0.00 fallen ohne dass es Schaden gibt. Mit der anderen Hälfte warte ich die Zulassung ab.
...und es geht weiter rauf.
Sarepta, University of Western Australia announce licensing agreement
http://finance.yahoo.com/news/sarepta-university-western-aus…
Sarepta, University of Western Australia announce licensing agreement
http://finance.yahoo.com/news/sarepta-university-western-aus…
Antwort auf Beitrag Nr.: 44.411.801 von lunatics am 11.04.13 17:22:50Der Kurs seit über 4 Stunden bei 39,9x wie festgeklebt...
Kommt gleich der Turbo... oder worauf wird gewaretet...
im Vergleich zur Volatilität in den letzten Tagen...
Kommt gleich der Turbo... oder worauf wird gewaretet...
im Vergleich zur Volatilität in den letzten Tagen...

...grosser Endspurt gestern...geschlossen über 40xx
Sarepta's breakthrough
Sarepta Therapeutics (NASDAQ: SRPT) announced good results for its phase two trial for Duchenne Muscular Dystrophy. This disease effects one out of every 3,500 boys worldwide, and does not have many treatment options. Sarepta was able to show patients in the study, who took Eteplirsen, were on average able to walk 89 meters more than those who just took the placebo drug instead after 48 weeks.
After these results were announced, it created a huge buzz, and Sarepta traded up to a high of $45 per share. It has since come down from its high, but investors who are patient will soon be rewarded, especially since Sarepta is about to find out whether it's drug Eteplirsen will receive accelerated approval from the FDA or not.
Sarepta's technology is called PMO. PMO is modeled after normal RNA structure, but is modified into different structures to target certain diseases. After a successful phase two trial of Eteplirsen, Sarepta seems to have found a way around the delivery method problem that has plagued RNA drug companies. Investors should keep an eye on this company as it may be a good long-term hold as its pipeline progresses.
Sarepta's breakthrough
Sarepta Therapeutics (NASDAQ: SRPT) announced good results for its phase two trial for Duchenne Muscular Dystrophy. This disease effects one out of every 3,500 boys worldwide, and does not have many treatment options. Sarepta was able to show patients in the study, who took Eteplirsen, were on average able to walk 89 meters more than those who just took the placebo drug instead after 48 weeks.
After these results were announced, it created a huge buzz, and Sarepta traded up to a high of $45 per share. It has since come down from its high, but investors who are patient will soon be rewarded, especially since Sarepta is about to find out whether it's drug Eteplirsen will receive accelerated approval from the FDA or not.
Sarepta's technology is called PMO. PMO is modeled after normal RNA structure, but is modified into different structures to target certain diseases. After a successful phase two trial of Eteplirsen, Sarepta seems to have found a way around the delivery method problem that has plagued RNA drug companies. Investors should keep an eye on this company as it may be a good long-term hold as its pipeline progresses.
Feuerstein zu den Glaxo-Drisapersen-Ergebnissen und deren Bedeutung für Eteplirsen, wie immer sehr kritisch und m.E. in etlichen Punkten so nicht haltbar:
http://www.thestreet.com/story/11894391/3/sarepta-fans-a-sin…
http://www.thestreet.com/story/11894391/3/sarepta-fans-a-sin…
News!!!!!
Sarepta Therapeutics Announces FDA Will Consider Accelerated Approval for Eteplirsen After Further Review of Data on Dystrophin and Clinical Outcomes
nachbörslich 43 $............
Sarepta Therapeutics Announces FDA Will Consider Accelerated Approval for Eteplirsen After Further Review of Data on Dystrophin and Clinical Outcomes
nachbörslich 43 $............
jetzt sackt sie nachbörslich deutlich ab - 35 $.....warten wir mal den conference-call ab....
Antwort auf Beitrag Nr.: 44.437.993 von Stockfinder am 15.04.13 22:56:29Irgendwie gerade Chaos bei den Info`S zur Zulassung...


Antwort auf Beitrag Nr.: 44.438.357 von Go for it am 15.04.13 23:48:24siehe dazu auch
http://www.thestreet.com/story/11896146/1/a-proactive-fda-is…
http://www.thestreet.com/story/11896146/1/a-proactive-fda-is…
Antwort auf Beitrag Nr.: 44.438.361 von Go for it am 15.04.13 23:50:03ich meine das sindeigtl. good news. die reaktion der aktie ist unverständlich. da haben einige vielleicht auf eine sofortige zulassung spekuliert (was sowieso unsinn ist, da es erstmal um eine vorläufige im rahmen des AA geht, die dann später, mit den P3 daten validiert werden muss) und waren im 1. moment enttäuscht. dass sich die fda so aktiv kümmert ist doch positiv, hoffe nur dass die dünne datenbasis erstmal für die AA entscheidung ausreicht.
zumindest scheinen sie sich gerade zu fangen - in Frankfurt ca. 28 €....für mich ist das ebenfalls nicht nachvollziehbar, die FDA hat Sarepta den roten Teppich ausgebreitet!
Falls wir heute wirklich nochmals die 34 $ testen, werde ich nochmals zukaufen und eine dritte Position aufbauen.
Falls wir heute wirklich nochmals die 34 $ testen, werde ich nochmals zukaufen und eine dritte Position aufbauen.
Antwort auf Beitrag Nr.: 44.439.807 von Stockfinder am 16.04.13 09:40:52-13%, völlig irrational das ganze
Antwort auf Beitrag Nr.: 44.442.911 von me_2 am 16.04.13 15:38:25Irgendwie fehlt hier "bei Sarepta" gerade eine klare Aussage...
möglichst mit Terminvorgabe...
Der Sachstand ist...
möglichst mit Terminvorgabe...

Der Sachstand ist...

Bin mal mit dabei!...

Antwort auf Beitrag Nr.: 44.442.985 von Go for it am 16.04.13 15:47:19Terminplan wirds keinen geben. andererseits kann es ja nicht ewig dauern sich die paar Daten anzuschauen, das geht wenn man sich a weng konzentriert in 1-2 Tagen. Die Dystrophindaten solltens halt auch parat haben.
Nur die Ruhe bewahren...
Die Zulassung wird kommen.
Die Zulassung wird kommen.
Antwort auf Beitrag Nr.: 44.445.201 von lunatics am 16.04.13 20:23:26nur wann? Diesen Monat oder dieses Jahr noch oder...

3. Position zu 33,60 - vermutlich kommt die Zulassung nicht vor dem dritten Quartal - nutze diese Kaufgelegenheit und bleibe cool. Eigentlich hat die FDA ja im Sinne von Sarepta entschieden, es war klar das es keine direkte Zulassung gibt, daß wäre völlig unmöglich gewesen, dazu bedarf es halt noch der weiteren Daten. Aber scheinbar schüttelt man hier nochmals eifrig nervöse Hände ab, die völlig falsch informiert waren und mit einer direkten Zulassung gerechnet haben.
Und sobald diese ausgewertet sind, geht es Richtung 60 $+ x.....wir werden sehen....
Und sobald diese ausgewertet sind, geht es Richtung 60 $+ x.....wir werden sehen....
...trotz gestrigem Downgrade...Kurs gibt Gegensteuer und fängt sich mit grosser Stärke.
Leerink Swann downgraded its rating on this company from Outperform to Market Perform and changed its price target to $419.00.

..scheint wohl ein Tippfehler zu sein...
Leerink Swann downgraded its rating on this company from Outperform to Market Perform and changed its price target to $419.00.


..scheint wohl ein Tippfehler zu sein...
Antwort auf Beitrag Nr.: 44.454.243 von lunatics am 17.04.13 20:31:17Bei 419 würde ich mir glatt überlegen zu verkaufen.
Sarepta Therapeutics to Present Company Overview at the Needham Annual Healthcare Conference on Tuesday, April 30, 2013 at 4:20 p.m.
...mal wieder ein Tageschart

Minus 5 % - keine News - was is los heut ??
Antwort auf Beitrag Nr.: 44.495.693 von me_2 am 23.04.13 17:33:34Hallo,
wie weit geht Sarepta noch runter?
Wann geht `s wieder nach oben?
Ich habe das Gefühl, dass die 30 $ nicht halten..
Verkaufen ist auch gefährlich, da jederzeit die News kommen könnten..
Was tun?
Langzeitinvest ---
wie weit geht Sarepta noch runter?
Wann geht `s wieder nach oben?
Ich habe das Gefühl, dass die 30 $ nicht halten..

Verkaufen ist auch gefährlich, da jederzeit die News kommen könnten..
Was tun?
Langzeitinvest ---
waren grad schon kurz unter 30.
ich bleib unverändert dran, irgendwann kommen die news.
nachkaufen is nich, dafür ist mein SRPT-Anteil im Biotechdepot schon zu groß...
ich bleib unverändert dran, irgendwann kommen die news.
nachkaufen is nich, dafür ist mein SRPT-Anteil im Biotechdepot schon zu groß...
Habe 1/2 meines Bestandes verkauft (Stoploss USD 30) +40% Gewinn.
Den Rest lass ich auch noch drinn. Zusätzlicher Kaufauftrag bei 22 gesetzt.
Den Rest lass ich auch noch drinn. Zusätzlicher Kaufauftrag bei 22 gesetzt.
..und the street äussert sich:
Sarepta: Staying Long and Strong
http://www.thestreet.com/story/11905515/1/sarepta-staying-lo…
Sarepta: Staying Long and Strong
http://www.thestreet.com/story/11905515/1/sarepta-staying-lo…
So, SRPT nimmt wieder Anlauf. Die Chaertprofis sprechen von einer günstigen Konstellation 

Gar nicht sooo schlecht
"Documents Requested by FDA for Accelerated Approval Consideration of Eteplirsen Will Be Submitted This Month; Clinical, Regulatory, and Manufacturing Activities Continue to Progress for Eteplirsen and Additional Duchenne Muscular Dystrophy Drug Candidates; Strong Cash Balance of $175 Million at Quarter-End"
http://www.nasdaq.com/article/sarepta-therapeutics-announces…
"Documents Requested by FDA for Accelerated Approval Consideration of Eteplirsen Will Be Submitted This Month; Clinical, Regulatory, and Manufacturing Activities Continue to Progress for Eteplirsen and Additional Duchenne Muscular Dystrophy Drug Candidates; Strong Cash Balance of $175 Million at Quarter-End"
http://www.nasdaq.com/article/sarepta-therapeutics-announces…
...tönt nicht schlecht...Piper Jaffray rechnet daher mit der Zulassung bis Ende dieses Jahres.
Nochmals Angriff auf die 40 in den nächsten Tagen MACD steht voll auf KAUFEN!
Wieder Angriff auf die 40. Diesmal klappt es vielleicht. Bin noch mit der Hälfte dabei. Bei 50 verkaufe ich die Kiste.
meine Zukäufe haben sich als richtig erwiesen. Bleibe weiterhin mittel- bis langfristig investiert - ab 45 $ werde ich erste Teilpositionen veräußern. Meine erste Position bleibt im Biotech-Grund-Depot.
Antwort auf Beitrag Nr.: 44.704.787 von Stockfinder am 24.05.13 00:21:13Bin noch mit Allem dabei. Ab 42 würde ich mir überlegen einen Teil zu versilbern. Die andere Hälfte bleibt bis ich die Kohle brauche ...
George Soros Has Been Buying Sarepta
...normalerweise lässt er die Finger von Biotechs..

...normalerweise lässt er die Finger von Biotechs..


Antwort auf Beitrag Nr.: 44.711.825 von lunatics am 24.05.13 20:26:50coool, da hat er doch noch die Chinesen überboten ...
Eteplirsen/SRPT vs. drisapersen/GSK, interessante Überlegungen von Feuerstein
http://www.thestreet.com/story/11934489/1/prosensa-ipo-filin…
Stay tuned!
http://www.thestreet.com/story/11934489/1/prosensa-ipo-filin…
Stay tuned!
Antwort auf Beitrag Nr.: 44.736.433 von me_2 am 29.05.13 08:55:50Komischer Verlauf knapp die 40$ erreicht Groß-Investoren steigen ein
und dann fällt Sarepta wie ein Stein auf 35,35$
Sehen wir nächste Woche wieder 29,x$ bevor Sarepta dann wieder
Richtung 40 läuft... oder kommen vorher News..
Habt Ihr eine Meinung dazu?
und dann fällt Sarepta wie ein Stein auf 35,35$
Sehen wir nächste Woche wieder 29,x$ bevor Sarepta dann wieder
Richtung 40 läuft... oder kommen vorher News..
Habt Ihr eine Meinung dazu?

Könnte daran liegen, dass der gesamte Einreichungs-/Approval-prozeß länger dauert als der Markt das erhofft hatte:
http://seekingalpha.com/article/1473831-for-the-long-term-in…
Die (für mich) Key-aussagen daraus:
"... Thursday's commentary that an NDA filing may still be months away...
... Garabedian at the Deutsche Bank dbAccess Health Care Conference said that the company had submitted the two papers that the FDA requested at their last Meeting...
...Sarepta is still hopeful that it will have communication about accelerated approval yet this summer, possibly in August...
...However ...it sounds like an NDA filing won't materialize until at least 1Q14, although in the interim the company may reveal whether it plans to file.
...we're expecting investor interest to wane in the back half of this year..."
http://seekingalpha.com/article/1473831-for-the-long-term-in…
Die (für mich) Key-aussagen daraus:
"... Thursday's commentary that an NDA filing may still be months away...
... Garabedian at the Deutsche Bank dbAccess Health Care Conference said that the company had submitted the two papers that the FDA requested at their last Meeting...
...Sarepta is still hopeful that it will have communication about accelerated approval yet this summer, possibly in August...
...However ...it sounds like an NDA filing won't materialize until at least 1Q14, although in the interim the company may reveal whether it plans to file.
...we're expecting investor interest to wane in the back half of this year..."
SRPT Target wird von Baird auf 63$ gesetzt. 

Hallo!
Als ISIS Investor bin ich natürlich auch an Sarepta interessiert. Zum einen da jede gute Meldung der wenigen Antisense/RNAi-Biotechs (ISIS, SRPT, ALNY, RXI, RGLS, Sangamo, Tekmira) auch positive Auswirkungen auf den ganzen Bereich hat und die verdiente Aufmerksamkeit bringt, zum anderen hat ISIS auch finanzielle Vereinbarungen mit SPRT.
isis's agreement with Sarepta
From Sarepta's 10-K FYE 12-31-2012:
(Link is in the article mdcelts referenced.)
>>..
Strategic Alliances
Isis—Ercole Agreement
In May 2003, Ercole Biotechnology, Inc., or Ercole, and Isis Pharmaceuticals, or Isis, entered into a collaboration and license agreement related to RNA splicing. In March 2008, we acquired all of the stock of Ercole in exchange for 5,811,721 shares of our common stock, which was valued at approximately $8.4 million, and the assumption of approximately $1.8 million in liabilities of Ercole. We also issued warrants to purchase our common stock (also classified as equity), which were valued at $437,000, in exchange for certain outstanding warrants issued by Ercole. In connection with the March 2008 acquisition, we assumed Ercole’s obligations under the Isis agreement. This agreement contains several cross-licenses between the parties granting each party certain exclusive and nonexclusive rights under a selected set of the other parties’ patents and patent applications for the research, development, and commercialization of antisense therapeutics using RNA splicing with respect to certain gene targets.
Subject to the satisfaction of certain milestones triggering the obligation to make any such payments, we may be obligated to make milestone payments to Isis of up to $23.4 million in the aggregate for each product developed under a licensed patent under this agreement.
As of December 31, 2012, we have not made, and are not under any current obligation to make, any such milestone payments, as the conditions triggering any such milestone payment obligations have not been satisfied. The range of percentage royalty payments required to be made by us under the terms of this agreement is from a fraction of a percent to mid single digits. We believe that our DMD, Ebola, Marburg and influenza programs will not fall under the scope of this agreement and therefore will not be subject to milestone or royalty obligations under its provisions.
Subject to the satisfaction of certain milestones triggering the obligation to make any such payments, Isis may be obligated to make milestone payments to us of up to $21.1 million in the aggregate for each product developed under a licensed patent under this agreement. As of December 31, 2012, Isis has not made any such milestone payments, as the conditions triggering any such milestone payment obligations have not been satisfied. The percentage royalty payments required to be made by Isis under the terms of this agreement is a fraction of a percent. As to any product commercialized under the agreement, the agreement will terminate on the expiration date of the last to expire licensed patent covering such product. Research collaboration activity defined in the agreement expired in 2006.
-13-
..<<
Als ISIS Investor bin ich natürlich auch an Sarepta interessiert. Zum einen da jede gute Meldung der wenigen Antisense/RNAi-Biotechs (ISIS, SRPT, ALNY, RXI, RGLS, Sangamo, Tekmira) auch positive Auswirkungen auf den ganzen Bereich hat und die verdiente Aufmerksamkeit bringt, zum anderen hat ISIS auch finanzielle Vereinbarungen mit SPRT.
isis's agreement with Sarepta
From Sarepta's 10-K FYE 12-31-2012:
(Link is in the article mdcelts referenced.)
>>..
Strategic Alliances
Isis—Ercole Agreement
In May 2003, Ercole Biotechnology, Inc., or Ercole, and Isis Pharmaceuticals, or Isis, entered into a collaboration and license agreement related to RNA splicing. In March 2008, we acquired all of the stock of Ercole in exchange for 5,811,721 shares of our common stock, which was valued at approximately $8.4 million, and the assumption of approximately $1.8 million in liabilities of Ercole. We also issued warrants to purchase our common stock (also classified as equity), which were valued at $437,000, in exchange for certain outstanding warrants issued by Ercole. In connection with the March 2008 acquisition, we assumed Ercole’s obligations under the Isis agreement. This agreement contains several cross-licenses between the parties granting each party certain exclusive and nonexclusive rights under a selected set of the other parties’ patents and patent applications for the research, development, and commercialization of antisense therapeutics using RNA splicing with respect to certain gene targets.
Subject to the satisfaction of certain milestones triggering the obligation to make any such payments, we may be obligated to make milestone payments to Isis of up to $23.4 million in the aggregate for each product developed under a licensed patent under this agreement.
As of December 31, 2012, we have not made, and are not under any current obligation to make, any such milestone payments, as the conditions triggering any such milestone payment obligations have not been satisfied. The range of percentage royalty payments required to be made by us under the terms of this agreement is from a fraction of a percent to mid single digits. We believe that our DMD, Ebola, Marburg and influenza programs will not fall under the scope of this agreement and therefore will not be subject to milestone or royalty obligations under its provisions.
Subject to the satisfaction of certain milestones triggering the obligation to make any such payments, Isis may be obligated to make milestone payments to us of up to $21.1 million in the aggregate for each product developed under a licensed patent under this agreement. As of December 31, 2012, Isis has not made any such milestone payments, as the conditions triggering any such milestone payment obligations have not been satisfied. The percentage royalty payments required to be made by Isis under the terms of this agreement is a fraction of a percent. As to any product commercialized under the agreement, the agreement will terminate on the expiration date of the last to expire licensed patent covering such product. Research collaboration activity defined in the agreement expired in 2006.
-13-
..<<
Antwort auf Beitrag Nr.: 44.811.825 von cristrader am 08.06.13 11:47:42++++NEWS+++
Quelle The Street.com
Sarepta's Eteplirsen Walk-A-Thon Now Stretches For 84 Weeks
BY Adam Feuerstein| 06/19/13 - 09:43 AM EDT
Stock quotes in this article: SRPT
.
Find out if (SRPT) is in Cramer's Portfolio.
CAMBRIDGE, Mass. (TheStreet) -- A handful of pre-teen boys suffering with Duchenne muscular dystrophy have now been treated with Sarepta Therapeutics'(SRPT) eteplirsen for 84 weeks. The boys are still walking, defying the debilitating and progressive nature of a disease that would be forcing them into wheelchairs without treatment.
As with previous updates from Sarepta's eteplirsen study, no significant safety problems were reported. No serious adverse events, no hospitalizations or treatment discontinuations.
Well, there was one disruption in the study but it was actually more evidence of eteplirsen's profound benefit for DMD patients. Here's how Sarepta describes it:
One boy in the placebo/delayed-treatment cohort was not able to perform the 6MWT at the Week 84 clinic visit due to a physical injury unrelated to treatment, and therefore had no 6MWT data captured at the Week 84 time point. The boy has recovered from the injury, continues to be ambulatory and is expected to be evaluated on the 6MWT at future clinic visits.
Sarepta doesn't say, but the injured boy suffered a broken leg, according to people familiar with his case. The leg healed and the boy is walking again normally. Boys with DMD who break a leg aren't supposed to recover and walk again normally, but in this case, he is.
After 84 weeks, DMD patients treated with eteplirsen are walking, on average, 9.2 meters less over six minutes than they were at the start of the study. When the same walk test was performed at 74 weeks, the decrease in walking distance was 2.2 meters, on average.
Another small group of DMD patients started the study on placebo and switched over to eteplirsen after 24 weeks. Initially, the walking ability of these boys declined while on placebo, but it's since stabilized following treatment with eteplirsen.
"We now have demonstrated stability of walking for over a year and a half in the original eteplirsen treatment cohort in boys who are now 11 years old on average, an age when many DMD boys have lost the ability to walk," said Sarepta CEO Chris Garabedian, in a statement. "In addition, the placebo/delayed-treatment cohort, which has now received eteplirsen for over a year, has demonstrated a stabilization in walking ability for 48 weeks compared with the precipitous decline observed earlier in the study before dystrophin was confirmed in these patients. Overall, we believe the data across all treatment cohorts are remarkably consistent and continue to support eteplirsen as a potential treatment option in DMD."
Sarepta continues to work work with the FDA to reach agreement on an accelerated approval filing strategy for eteplirsen.
Today's positive update from the eteplirsen study makes Sarepta's case even stronger.
Sarepta shares are up 5 percent to $40.10 in early Wednesday trading.
-- Reported by Adam Feuerstein in Boston.

Quelle The Street.com
Sarepta's Eteplirsen Walk-A-Thon Now Stretches For 84 Weeks
BY Adam Feuerstein| 06/19/13 - 09:43 AM EDT
Stock quotes in this article: SRPT
.
Find out if (SRPT) is in Cramer's Portfolio.
CAMBRIDGE, Mass. (TheStreet) -- A handful of pre-teen boys suffering with Duchenne muscular dystrophy have now been treated with Sarepta Therapeutics'(SRPT) eteplirsen for 84 weeks. The boys are still walking, defying the debilitating and progressive nature of a disease that would be forcing them into wheelchairs without treatment.
As with previous updates from Sarepta's eteplirsen study, no significant safety problems were reported. No serious adverse events, no hospitalizations or treatment discontinuations.
Well, there was one disruption in the study but it was actually more evidence of eteplirsen's profound benefit for DMD patients. Here's how Sarepta describes it:
One boy in the placebo/delayed-treatment cohort was not able to perform the 6MWT at the Week 84 clinic visit due to a physical injury unrelated to treatment, and therefore had no 6MWT data captured at the Week 84 time point. The boy has recovered from the injury, continues to be ambulatory and is expected to be evaluated on the 6MWT at future clinic visits.
Sarepta doesn't say, but the injured boy suffered a broken leg, according to people familiar with his case. The leg healed and the boy is walking again normally. Boys with DMD who break a leg aren't supposed to recover and walk again normally, but in this case, he is.
After 84 weeks, DMD patients treated with eteplirsen are walking, on average, 9.2 meters less over six minutes than they were at the start of the study. When the same walk test was performed at 74 weeks, the decrease in walking distance was 2.2 meters, on average.
Another small group of DMD patients started the study on placebo and switched over to eteplirsen after 24 weeks. Initially, the walking ability of these boys declined while on placebo, but it's since stabilized following treatment with eteplirsen.
"We now have demonstrated stability of walking for over a year and a half in the original eteplirsen treatment cohort in boys who are now 11 years old on average, an age when many DMD boys have lost the ability to walk," said Sarepta CEO Chris Garabedian, in a statement. "In addition, the placebo/delayed-treatment cohort, which has now received eteplirsen for over a year, has demonstrated a stabilization in walking ability for 48 weeks compared with the precipitous decline observed earlier in the study before dystrophin was confirmed in these patients. Overall, we believe the data across all treatment cohorts are remarkably consistent and continue to support eteplirsen as a potential treatment option in DMD."
Sarepta continues to work work with the FDA to reach agreement on an accelerated approval filing strategy for eteplirsen.
Today's positive update from the eteplirsen study makes Sarepta's case even stronger.
Sarepta shares are up 5 percent to $40.10 in early Wednesday trading.
-- Reported by Adam Feuerstein in Boston.
Antwort auf Beitrag Nr.: 44.794.087 von lunatics am 05.06.13 20:26:14auf geht`s
Nach den guten Nachrichten heute
Nach den guten Nachrichten heute
Antwort auf Beitrag Nr.: 44.878.945 von Go for it am 19.06.13 16:24:30Sarepta continues to work work with the FDA to reach agreement on an accelerated approval filing strategy for eteplirsen. 

Habe meine erste und zweite Position (27$+31$) zu 40,30 $ verkauft - und so meine dritte Position quasi gratis. Diese verbleibt ohne SL im Depot!
Sarepta Gains On Positive Muscular Dystrophy Drug Results




http://blogs.barrons.com/stockstowatchtoday/2013/06/19/sarep…




http://blogs.barrons.com/stockstowatchtoday/2013/06/19/sarep…
Die Zulassung wird kommen, spätestens am Jahresende. Nur an Gewinnmitnahmen ist noch niemand gestorben. Habe jeweils ISIS, Celldex und Array zu gleichen Teilen zugekauft.
Jetzt schon raus? 
Sarepta bekommt doch gerade richtig Rückenwind.
Grosse Investoren werden langsam aufmerksam...

Sarepta bekommt doch gerade richtig Rückenwind.
Grosse Investoren werden langsam aufmerksam...
Hier noch ein interessanter Artikel:
Top Buys by Directors: Chase's $385K Bet on SRPT
Top Buys by Directors: Chase's $385K Bet on SRPT
Antwort auf Beitrag Nr.: 44.884.063 von Go for it am 20.06.13 09:35:40ISIS ist jedoch breiter aufgestellt - sowohl was die Pipeline betrifft als auch die Partnerschaften, die Technologie ist ja de gleiche.
Bin von Sarepta weiterhin überzeugt, wollte mich mit der Umschichtung einfach breiter aufstellen, die Tecnnologie wird m.E. nach über Jahre dominieren.
Bin von Sarepta weiterhin überzeugt, wollte mich mit der Umschichtung einfach breiter aufstellen, die Tecnnologie wird m.E. nach über Jahre dominieren.
Ist natürlich auch viel Fantasie drinn. Die Technik ist noch nicht vollständig akzeptiert....aber solange alle drann glauben kann die bubble steigen.
Werde bei 45 wieder ein paar verkaufen.
Werde bei 45 wieder ein paar verkaufen.
Antwort auf Beitrag Nr.: 44.912.255 von lunatics am 24.06.13 20:37:35uiii
Da hat Glaxo seine Pferde schon im rennen...
Da hat Glaxo seine Pferde schon im rennen...

Sarepta Therapeutics announced today that it is scheduled to present at the JMP Securities Healthcare Conference in New York, on Wednesday, July 10, 2013 at 11:00 a.m.
Hi, ich war eine Weile Forum-abstinent. Bin aber bei SRPT noch dabei. Läuft doch gut ...
ja sogar sehr gut! bei 45 verkaufe ich das 1. Paket
Grüsse aus Miami Biscayne bay
Sarepta Traders Brace For Possible Accelerated Approval For Eteplirsen
http://seekingalpha.com/article/1542622-sarepta-traders-brac…
Grüsse aus Miami Biscayne bay
Sarepta Traders Brace For Possible Accelerated Approval For Eteplirsen
http://seekingalpha.com/article/1542622-sarepta-traders-brac…
Antwort auf Beitrag Nr.: 45.042.643 von lunatics am 14.07.13 18:53:02Mit 45 ist bei mir noch nicht Schluss. Grüße aus Veli Losinj. Aber Miami komm ich auch noch hin wenn SRPT so weitermacht 

Antwort auf Beitrag Nr.: 45.089.729 von me_2 am 22.07.13 11:41:53Bin inzwischen wieder zurück. Ich wünsche dir aber noch schöne Ferien. 
Bei mir ist 1/3 Sarepta heute weg. Nächster Verkaufspunkt 55. Den Rest lass ich einfach liegen.

Bei mir ist 1/3 Sarepta heute weg. Nächster Verkaufspunkt 55. Den Rest lass ich einfach liegen.
Antwort auf Beitrag Nr.: 45.092.975 von lunatics am 22.07.13 20:03:02Vorbörslich ist schon ganz schön was los bei Sarepta...
Seit 8.. AM
Es gibt Info`s vom Vorstand...
Seit 8.. AM
Es gibt Info`s vom Vorstand...
Antwort auf Beitrag Nr.: 45.105.483 von Go for it am 24.07.13 14:18:21vorbörslich 68 und jetzt wieder ins minus. schnelles AA wäre halt doch besser als späteres full NDA ...
Antwort auf Beitrag Nr.: 45.105.993 von me_2 am 24.07.13 15:24:15Habe das Gefühl dass das noch eine Nachkaufgelegenheit wird, was meint ihr?
Ist das nun ernshaft gemeint mit der Nachkaufgelegenheit?
Immo schwankt das Minus zwischen Ca. 6,5-8,00- US-$*,
Sind das Nachkauf-Kurse*?-
http://www.thestreet.com/_nasdaq/story/11987227/1/sarepta-to…
''Frage ist das sell on good news, oder war die news nicht gut genug?
Sarepta will submit the approval filing in the first half of 2014, the company said Wednesday.
Here's how Sarepta described the decision to file in its press release this morning:''
Immo schwankt das Minus zwischen Ca. 6,5-8,00- US-$*,
Sind das Nachkauf-Kurse*?-
http://www.thestreet.com/_nasdaq/story/11987227/1/sarepta-to…
''Frage ist das sell on good news, oder war die news nicht gut genug?
Sarepta will submit the approval filing in the first half of 2014, the company said Wednesday.
Here's how Sarepta described the decision to file in its press release this morning:''
So wie es ausschaut kann ich meinen Drittel heute wieder günstig kaufen...
Antwort auf Beitrag Nr.: 45.108.279 von lunatics am 24.07.13 19:52:05Hallo lunatics
was hat den massiven Kursrutsch ausgelöst?
Wie weit wird Sarepta noch fallen?
Wie ich rauslese soll erst 2014 die Zulassung geprüft werden...
oder passiert evtl. noch vorher was (vorzeitige Zulassung)?
was hat den massiven Kursrutsch ausgelöst?
Wie weit wird Sarepta noch fallen?
Wie ich rauslese soll erst 2014 die Zulassung geprüft werden...
oder passiert evtl. noch vorher was (vorzeitige Zulassung)?
sehe hier noch keine Nachkaufgelegenheit. Insgesamt sind die Bios zur Zeit sehr schwach, dies könnte noch ein paar Tage andauern. Würde Sarepta erst unter 35 $ wieder kaufen. Das Momentum dürfte die nächsten Tage negativ bleiben.
Meine Rest-Position bleibt trotzdem ungesichert im Depot, ab 33 $ kaufe ich nach.
Meine Rest-Position bleibt trotzdem ungesichert im Depot, ab 33 $ kaufe ich nach.
FDA macht Schwierigkeiten. SRPT will fast track für eteplirsen .. nun gibt es Verzögerung bis Mitte 2014. Mehr Daten werden gefordert. Analysten sehen den Hauptgrung in der Verzögerung, denn die Konkurrenz schläft nicht. Glaxo kommt auch nächstes Jahr.
...Doch eteplirsen works.
SRPT fällt bis sie konsolidiert. Dann kaufen und nochmals Geld verdienen.
...Doch eteplirsen works.
SRPT fällt bis sie konsolidiert. Dann kaufen und nochmals Geld verdienen.

Antwort auf Beitrag Nr.: 45.108.581 von lunatics am 24.07.13 20:45:48Vllt. geht`s Morgen wieder Bergauf.
Durch gute News...oder ad hoc...
Durch gute News...oder ad hoc...
Antwort auf Beitrag Nr.: 45.108.657 von Go for it am 24.07.13 20:54:16sonst geht`s wohl erstmal wieder an die 30 Dollargrenze...
da bis Mitte 2014 noch eine lange Zeit ist...

da bis Mitte 2014 noch eine lange Zeit ist...
''sehe hier noch keine Nachkaufgelegenheit. Insgesamt sind die Bios zur Zeit sehr schwach, dies könnte noch ein paar Tage andauern.''
Na ganz so schlimm ist es nun auch nicht ...*?-
Wüßte schon noch einen vllt. interesanten Wert, welcher in den nächsten Tgaen starten könnte*?-
Nur meine Meinung, keine Handelsempfehlung usw. *!
Aktueller Kurs + akt. Bid für SRPT*:
37.7301
-8.6999 -23.06%
Range: 37.50 - 46.36
Open: 45.00
Vol: 12,543,625
Bid: 37.75 Ask: 37.78 Size: 1 x 2
NASD 37.75 100
EDGX 37.73 100
BATS 37.73 100
ARCA 37.7 100
PHEX 37.7 1
BOST 37.63 9
EDGA 37.53 2
CINN 37.53 3
CBOE 37.47 400
Na ganz so schlimm ist es nun auch nicht ...*?-
Wüßte schon noch einen vllt. interesanten Wert, welcher in den nächsten Tgaen starten könnte*?-
Nur meine Meinung, keine Handelsempfehlung usw. *!
Aktueller Kurs + akt. Bid für SRPT*:
37.7301
-8.6999 -23.06%
Range: 37.50 - 46.36
Open: 45.00
Vol: 12,543,625
Bid: 37.75 Ask: 37.78 Size: 1 x 2
NASD 37.75 100
EDGX 37.73 100
BATS 37.73 100
ARCA 37.7 100
PHEX 37.7 1
BOST 37.63 9
EDGA 37.53 2
CINN 37.53 3
CBOE 37.47 400
Antwort auf Beitrag Nr.: 45.108.699 von where-is-the-insider am 24.07.13 20:58:59Sarepta news upside surprise to expectations, says Deutsche Bank
Deutsche Bank said today's news that Sarepta plans on filing for accelerated approval in the first half of 2014 is an upside surprise to investor expectations. However, Deutsche expects some of the cautious comments in the release could limit share upside. The firm notes the press release states that the FDA is requesting more methodology and verification of dystrophin quantification. Deutsche has a Buy rating on the stock.
..
Quelle
http://finance.yahoo.com/news/sarepta-news-upside-surprise-e…
Deutsche Bank said today's news that Sarepta plans on filing for accelerated approval in the first half of 2014 is an upside surprise to investor expectations. However, Deutsche expects some of the cautious comments in the release could limit share upside. The firm notes the press release states that the FDA is requesting more methodology and verification of dystrophin quantification. Deutsche has a Buy rating on the stock.
..
Quelle
http://finance.yahoo.com/news/sarepta-news-upside-surprise-e…
Der Dämpfer kam zur richtigen Zeit. SRPT braucht eine Abkühlung. Zu schnell gings bergauf. Bis zur Zulassung wird am meisten Geld verdient. Warum nicht ein halbes Jahr länger?
Die News wird nicht gerade vom Markt bejubelt, siehe Erscheinungszeitpunkt *?-
''Sarepta news upside surprise to expectations, says Deutsche Bank
Theflyonthewall.comTheflyonthewall.com'' – 6 hours ago
so schnell wie der Kurs manchmal nachgibt kann man immo garnicht aktualisieren?:
US: bid* Zahl mal Hundert versteht sich?
37.6201
-8.8099 -23.42%
Range: 37.06 - 46.36
Open: 45.00
Vol: 13,039,307
Bid: 37.55 Ask: 37.58 Size: 1 x 2
ARCA 37.55 1
NASD 37.55 1
EDGX 37.55 1
BYX 37.51 1
BOST 37.51 1
PHEX 37.5 1
BATS 37.5 2
CBOE 37.5 1
EDGA 37.22 3[/b]
''Sarepta news upside surprise to expectations, says Deutsche Bank
Theflyonthewall.comTheflyonthewall.com'' – 6 hours ago
so schnell wie der Kurs manchmal nachgibt kann man immo garnicht aktualisieren?:
US: bid* Zahl mal Hundert versteht sich?
37.6201
-8.8099 -23.42%
Range: 37.06 - 46.36
Open: 45.00
Vol: 13,039,307
Bid: 37.55 Ask: 37.58 Size: 1 x 2
ARCA 37.55 1
NASD 37.55 1
EDGX 37.55 1
BYX 37.51 1
BOST 37.51 1
PHEX 37.5 1
BATS 37.5 2
CBOE 37.5 1
EDGA 37.22 3[/b]
Volume SRPT*
37.58
-8.85 -23.55%
Range: 37.06 - 46.36
Open: 45.00
Vol: 13,861,393
Bid: 37.58 Ask: 37.65 Size: 1 x 4
Vllt. hat Jemand interesse an einem neuen Biotech-Wert*?-
seit 16.07.13 an der Nasdaq nur 2,3 Mio shares,
heutiger Kursverlauf von ca. 4% Minuns zum Schußk. 4,21% Plus *
check Biotech in m. Prof.(alle Infos im thread?-)* ...
lg where-
Nur Info keine Handelsempfehlung usw.
[/red]
37.58
-8.85 -23.55%
Range: 37.06 - 46.36
Open: 45.00
Vol: 13,861,393
Bid: 37.58 Ask: 37.65 Size: 1 x 4
Vllt. hat Jemand interesse an einem neuen Biotech-Wert*?-
seit 16.07.13 an der Nasdaq nur 2,3 Mio shares,
heutiger Kursverlauf von ca. 4% Minuns zum Schußk. 4,21% Plus *
check Biotech in m. Prof.(alle Infos im thread?-)* ...
lg where-
Nur Info keine Handelsempfehlung usw.
[/red]
Nun bin ich schon einige Jahre an der Nasdaq*
Jedoch konnte ich bis Heute nicht herausfinden, wie das mit dem canceln von schon ausgeführten trades funkioniert*?-
siehe SRPT* nachbörslich:
16:05 $ 37.58 100
16:03 $ 37.2032 5,000 - Cancelled Trade
16:03 $ 37.58 100
16:02 $ 37.2032 Low 5,000
meine Vermutung hierzu wäre,
das gerade bei Stocks welche extrem im tagesverlauf am Fallen waren, gerade nachbörslich sehr oft solche gecancelten trades auftretten ...*?-
NmM*
Jedoch konnte ich bis Heute nicht herausfinden, wie das mit dem canceln von schon ausgeführten trades funkioniert*?-
siehe SRPT* nachbörslich:
16:05 $ 37.58 100
16:03 $ 37.2032 5,000 - Cancelled Trade
16:03 $ 37.58 100
16:02 $ 37.2032 Low 5,000
meine Vermutung hierzu wäre,
das gerade bei Stocks welche extrem im tagesverlauf am Fallen waren, gerade nachbörslich sehr oft solche gecancelten trades auftretten ...*?-
NmM*
Ocera Therapeutics, ist nicht dein Ernst - oder?
Vllt. möchte jemand die US-Vorbörse von SRPT* gerne kennen?:
Sarepta Therapeutics, Inc. - Common Stock
36.80
-0.88 -2.39%
Range: 0.00 - 0.00
Open: 0.00
Vol: 43,762
Bid: 36.51 Ask: 36.63 Size: 1 x 1
Sarepta Therapeutics, Inc. - Common Stock
36.80
-0.88 -2.39%
Range: 0.00 - 0.00
Open: 0.00
Vol: 43,762
Bid: 36.51 Ask: 36.63 Size: 1 x 1
SRPT*
Short volume ratio ... July24*: 0,254
Short interests ratio July 24*: 6,24
freiwillige short Angaben ohne Gewähr Quelle FINRA
Short volume ratio ... July24*: 0,254
Short interests ratio July 24*: 6,24
freiwillige short Angaben ohne Gewähr Quelle FINRA
mal wieder Zeit für eine Chartübersicht 

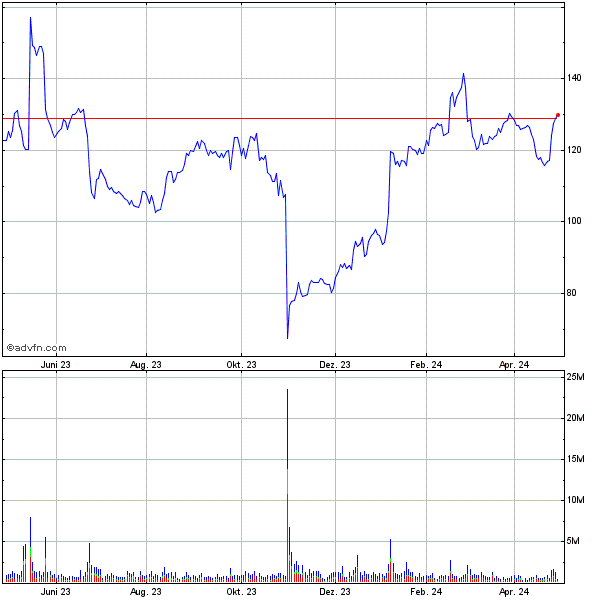


Heute guter Nachkaufkurs
Wurde die Marke von 35,76- US-Dollar schon getestet*?-
Wenn ja, dann bin ich der gleichen Meinung,
Wenn nein, würde ich persönlich noch einwenig abwarten ..........
NmM*
37.20
0.30 0.81%
Range: 36.54 - 37.77
Open: 36.76
Vol: 1,032,021
Bid: 37.20 Ask: 37.22 Size: 1 x 1
Mini Bid und mini Ask, keine Unterstützung erkennbar*?-
Wenn ja, dann bin ich der gleichen Meinung,
Wenn nein, würde ich persönlich noch einwenig abwarten ..........
NmM*
37.20
0.30 0.81%
Range: 36.54 - 37.77
Open: 36.76
Vol: 1,032,021
Bid: 37.20 Ask: 37.22 Size: 1 x 1
Mini Bid und mini Ask, keine Unterstützung erkennbar*?-
so habe wieder alten Bestand. ep 24.-
Wie ich sehe wurde Heute die von mir genannte Marke getestet und leider unterschritten,
das läßt leider keine guten Aussichten für den weiteren SRPT* Kursverlauf aufkommen ...*?-
Keine Handelsempfehlung nur meine Meinung usw. *!
lg where-
US-Kurs*
35.09-
-1.87 -5.33%
Range: 35.02 - 37.472
Open: 36.99
Vol: 1,724,786
Bid: 35.10 Ask: 35.15 Size: 8 x 8
das läßt leider keine guten Aussichten für den weiteren SRPT* Kursverlauf aufkommen ...*?-
Keine Handelsempfehlung nur meine Meinung usw. *!
lg where-
US-Kurs*
35.09-
-1.87 -5.33%
Range: 35.02 - 37.472
Open: 36.99
Vol: 1,724,786
Bid: 35.10 Ask: 35.15 Size: 8 x 8
Es geht wieder aufwärts mit

Sarepta Therapeutics to Present Company Overview at Upcoming Conferences
http://finance.yahoo.com/news/sarepta-therapeutics-present-c…

Sarepta Therapeutics to Present Company Overview at Upcoming Conferences
http://finance.yahoo.com/news/sarepta-therapeutics-present-c…
Antwort auf Beitrag Nr.: 45.146.433 von lunatics am 30.07.13 22:37:02Quelle Barron`s
Sarepta Therapeutics (SRPT) saw its director Anthony Chase buy 10,000 shares for $385,000. Sarepta saw a slight uptick in share price around this time after it announced positive results in a Phase 2b extension study involving the use of eteplirsen as a treatment for patients with Duchenne muscular dystrophy.
InsiderScore notes that in buying, Chase reversed sentiment, as he sold shares last year at a lower rate. “His move to buy shares here on strength in the stock shows strong conviction as the company once again reports positive data,” writes InsiderScore.

Sarepta Therapeutics (SRPT) saw its director Anthony Chase buy 10,000 shares for $385,000. Sarepta saw a slight uptick in share price around this time after it announced positive results in a Phase 2b extension study involving the use of eteplirsen as a treatment for patients with Duchenne muscular dystrophy.
InsiderScore notes that in buying, Chase reversed sentiment, as he sold shares last year at a lower rate. “His move to buy shares here on strength in the stock shows strong conviction as the company once again reports positive data,” writes InsiderScore.

Insiders Are Buying Sarepta Therapeutics
http://seekingalpha.com/article/1655942-insiders-are-buying-…
http://seekingalpha.com/article/1655942-insiders-are-buying-…
Ich sehe es ist noch jemand da ...
ich Depp hatte bei 39 nachgekauft als es runterging.
Aber es geht ja eh schon wieder aufi.
ich Depp hatte bei 39 nachgekauft als es runterging.
Aber es geht ja eh schon wieder aufi.
SRPT: Insiders vs. Shorts
http://www.forbes.com/sites/dividendchannel/2013/08/28/srpt-…
http://www.forbes.com/sites/dividendchannel/2013/08/28/srpt-…
DMD-Rennen gegen Glaxo läuft und nimmt an Spannung zu.
DIE Chance für SRPT.
Wäre schön, sie wären die ersten. Derzeit herrscht Stillschweigen über die Fortschritte.
Weitere Artikel:
http://www.fool.com/investing/general/2013/08/27/could-this-…
DIE Chance für SRPT.
Wäre schön, sie wären die ersten. Derzeit herrscht Stillschweigen über die Fortschritte.
Weitere Artikel:
http://www.fool.com/investing/general/2013/08/27/could-this-…
Stifel Initiated Buy!
Die 40 sind wieder in Reichweite.
Die 40 sind wieder in Reichweite.
Sarepta has scheduled a meeting with FDA in October to discuss the requirements for the CMC (chemistry, manufacturing and controls) section of the planned eteplirsen approval filing.
Frau Direktorin Behrens hat sich heute kurzerhand 6'500 Sarepta-Aktien unter den Nagel gerissen. Weiss sie mehr oder war es einfach der korrekten Loyalität gegenüber der Firma wegen?.

Prosensa -74 % Ergebnisse der Studie nicht positiev...
Quelle Yahoo Finance
Die Chance für Sarepta...
Quelle Yahoo Finance
Die Chance für Sarepta...

Antwort auf Beitrag Nr.: 45.489.275 von Go for it am 20.09.13 15:37:34Positiv da hat sich wohl ein e eingeschlichen.
Mal schaun wie es nun mit Sarepta weiter geht...

Mal schaun wie es nun mit Sarepta weiter geht...
Tja Glaxo hat den Kampf vorerst verloren.
Weg frei für

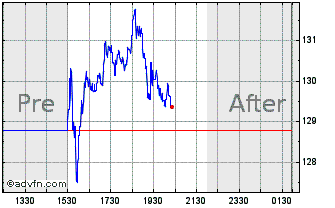
Weg frei für
Zitat von lunatics: Frau Direktorin Behrens hat sich heute kurzerhand 6'500 Sarepta-Aktien unter den Nagel gerissen. Weiss sie mehr oder war es einfach der korrekten Loyalität gegenüber der Firma wegen?.
Glaxo scheitert
Somit ist wohl klar warum Frau Direktorin nochmals nachlegte. Grenzt an Insiderhandel...

Sie scheint zumindest einen heissen Draht zur FDA oder zu Glaxo zu haben.
Ich rechne mal: 40'000 USD Gewinn...einfach mal so.
RW Baird believes that the elimination of Prosensa as a potential competitor to Sarepta Therapeutics offsets any increase in risk to its fundamental thesis.
The firm believes a drug failure will also open the door in Europe into other exons that previously would be blocked, increasing the potential upside for shareholders. The shares are Outperform rated with a $63 price target.
The firm believes a drug failure will also open the door in Europe into other exons that previously would be blocked, increasing the potential upside for shareholders. The shares are Outperform rated with a $63 price target.
Wenn DMD (DuchEnne Muscular Dystrophy ) so ein riesiger Markt ist warum dann nicht eine Santhera Pharma kaufen ? Die Marktkap liegt im unterschied zu SRPT ( $1.6 Milliarden) gerade mal bei lächerlichen $14 Million und auch die Pipeline ist um lichtjahre besser einzig kleiner Nachteil ist das Santhera in kürze eine kleine KE durchführen wird aber dafür haben die gerade mal nur um die 3,6 million ausstehende Aktien . Übrigens ist der größte Aktienhalter von Santhera der Milliadär Bertarelli also braucht man keine angst zuhaben was die KE angeht .
http://www.santhera.com/index.php?mid=19&vid=&lang=en
The ongoing pivotal Phase III DELOS study (DuchEnne Muscular Dystrophy Long-term IdebenOne Study) is a double-blind, randomized, placebo-controlled clinical trial evaluating the safety, tolerability and efficacy of 900 mg/day idebenone (Catena®) compared to placebo. Study centers in Europe and US have recruited patients aged 10 to 18 years for this 12-month clinical trial. The primary endpoint of the DELOS study is the change from baseline to week 52 in respiratory function measured by peak expiratory flow (PEF). Secondary endpoints relate to other respiratory parameters, muscle strength and motor function, as well as quality of life.
Recently, the DELOS study successfully passed a planned interim futility and safety analysis.

http://www.santhera.com/index.php?mid=19&vid=&lang=en
The ongoing pivotal Phase III DELOS study (DuchEnne Muscular Dystrophy Long-term IdebenOne Study) is a double-blind, randomized, placebo-controlled clinical trial evaluating the safety, tolerability and efficacy of 900 mg/day idebenone (Catena®) compared to placebo. Study centers in Europe and US have recruited patients aged 10 to 18 years for this 12-month clinical trial. The primary endpoint of the DELOS study is the change from baseline to week 52 in respiratory function measured by peak expiratory flow (PEF). Secondary endpoints relate to other respiratory parameters, muscle strength and motor function, as well as quality of life.
Recently, the DELOS study successfully passed a planned interim futility and safety analysis.

DMD ist kein riesiger Markt.
Sarepta aber die ersten.
Sarepta aber die ersten.
Sarepta Therapeutics announces eteplirsen demonstrates continued stability on walking test through 96 weeks in Phase IIb study in Duchenne muscular dystrophy (SRPT) 46.44 : Co announced data through Week 96 from Study 202, a Phase IIb open-label extension study of eteplirsen in patients with Duchenne muscular dystrophy. Results through nearly two years showed a continued stabilization of walking ability in eteplirsen-treated patients evaluable on the 6-minute walk test (6MWT). As previously reported, Study 202 met its primary endpoint of increased novel dystrophin as assessed by muscle biopsy at Week 48 and is now in the long-term extension phase in which patients continue to be followed for safety and clinical outcomes.
Wow unsere Sarepta geht gut ab...
So habe alles realisiert.
EP 24.-
VP 47.36
EP 24.-
VP 47.36
Alle Sarepta Anteile realisiert oder hast Du alles Börsennotierten Aktien realisiert? Cash?
-Warum hast Du alle Sarepta realisiert
-Warum hast Du alle Sarepta realisiert

ich habe nur Sarepta realisiert.
Ich bin der Meinung, dass sie weiter korrigieren werden. Zum einen weil der Sektor allgemein überhitzt ist und zum anderen weil SRPT in den letzten Tagen kursmässig schon sehr viel Zukunft vorweggenommen hat.
Wenn alles gut geht wird SRPT die Zulassung erreichen. Ich hoffe, dass ich nochmals tief einsteigen kann.
Ich bin der Meinung, dass sie weiter korrigieren werden. Zum einen weil der Sektor allgemein überhitzt ist und zum anderen weil SRPT in den letzten Tagen kursmässig schon sehr viel Zukunft vorweggenommen hat.
Wenn alles gut geht wird SRPT die Zulassung erreichen. Ich hoffe, dass ich nochmals tief einsteigen kann.
http://finance.yahoo.com/news/sarepta-therapeutics-announces…
Sarepta Therapeutics Announces FDA Considers NDA Filing for Eteplirsen Premature in Light of Recent Competitive Drug Failure and Recent DMD Natural History Data
FDA Questions Dystrophin as a Biomarker Due to Failed Studies of Other Investigational Drugs for DMD; FDA Questions 6-Minute Walk Test Results for Eteplirsen, Suggesting Study Population Should Be Stable Over Two-Year Timeframe Due to Recent Natural History Data; FDA Requests Further Discussion on Endpoints, Design of Confirmatory Clinical Study
CAMBRIDGE, MA--(Marketwired - Nov 12, 2013) - Sarepta Therapeutics, Inc. (NASDAQ: SRPT) today provided an update on its discussions with the U.S. Food and Drug Administration (FDA) regarding its planned New Drug Application (NDA) submission and confirmatory clinical study with eteplirsen for the treatment of Duchenne muscular dystrophy (DMD). Citing recent developments since Sarepta's last meeting with the agency, including a failed study with a competitive product and recent natural history data in DMD, the FDA indicated the new data raise "considerable doubt" about both the dystrophin biomarker and the supportive clinical efficacy assessed on the 6-minute walk test (6MWT) in the Phase IIb clinical study of eteplirsen. As a result of these recent data, the FDA stated that they "currently consider an NDA filing for eteplirsen as premature."
"We are very disappointed with the FDA's decision to reconsider their openness to a potential NDA filing based on our current data and the resultant impact this change may have on our efforts to achieve an earlier approval of eteplirsen," said Chris Garabedian, president and chief executive officer of Sarepta Therapeutics. "We strongly believe in the potential of eteplirsen to address a serious unmet medical need in DMD and we are committed to its development. Our team at Sarepta recognizes the urgency of families who are seeking new treatments, and we will continue to work with the FDA on an acceptable confirmatory study design and, in parallel, seek to address their concerns regarding a potential NDA filing based on our current dataset."
The FDA provided the feedback in pre-meeting comments and clarified them in a meeting with Sarepta that took place late last week to discuss the eteplirsen clinical program.
Excerpts from the FDA's pre-meeting comments on reconsidering an NDA filing included:
"Since our last meeting, a large phase 3 trial of drisapersen, a drug with a similar mechanism of action, was reported to be negative, despite increased expression of dystrophin. The disconnect between increased expression of dystrophin and clinical efficacy for drisapersen, combined with previous negative reports for PTC124, another drug thought to act by increasing dystrophin, raises considerable doubt about the biomarker, and consequentially, its ability to reasonably likely predict clinical benefit."
"...the quantity of dystrophin that might be necessary to be considered reasonably likely to predict clinical benefit is even less clear; small or perhaps even moderate increases are seemingly not enough, at least in the subpopulation of boys studied so far. An adequately validated quantitative assay for dystrophin now seems a prerequisite to further consideration of the biomarker as supportive of approval. Since our last meeting, our concern about the shortcomings of your current quantification methods has grown."
"Recent natural history data in DMD indicate that a baseline 6-Minute Walk Test (6MWT) ≥350 meters predicts continued general stability for such patients, not the 75- to 83-meter yearly decline you suggest in the meeting package. Thus, considerable doubt is also cast on the efficacy support provided by your ongoing open-label study (4658-us-202, 96-week data submitted), in which baseline 6MWT was >350 m for all patients."
"...the expected variability of 6MWT values appears sufficient to explain differences between arms on which the post-hoc analysis was based. Because of this, together with our lack of confidence in the capacity of your dystrophin biomarker to predict clinical benefit, we currently consider an NDA filing for eteplirsen as premature."
Additional excerpts from the FDA's pre-meeting comments on the eteplirsen confirmatory study design included:
"Recent trial failures in DMD suggest it may be productive to re-examine study enrollment criteria and endpoints."
"...it seems worthwhile to consider selection of other endpoints and/or populations for the next trial of eteplirsen. We stress that we would still accept 6MWT in an appropriately powered study; however, because 6MWT excludes both younger boys who cannot perform such a demanding test, and older boys who are no longer ambulatory, we are concerned that seemingly avoidable limitations on enrollment could undermine study feasibility. Many possible combinations of endpoints and subpopulations appear possible. Motor scales that measure a broader range of function and demand less sustained effort than 6MWT could be appropriate for a much wider range of boys, perhaps including non-ambulatory boys. To allow inclusion of a broader range of patients, a study could also be designed that mathematically combined findings from, for example, an ambulation endpoint in less advanced patients with findings from an upper-limb or respiratory endpoint in more advanced patients. We remain open to consideration of endpoints and populations you may suggest."
"...we believe that a placebo-controlled trial would be the most likely method for developing interpretable evidence of efficacy for eteplirsen, because efficacy endpoints in DMD are effort-dependent and susceptible to bias, and the natural history is highly variable and has recently improved with steroid use and advances in ancillary care. We would like to discuss the perceived barriers to conducting such a trial with you."
The FDA's request to discuss different clinical endpoints, combined endpoints, and different DMD subpopulations for a confirmatory clinical study, along with their questions about dystrophin as a biomarker and the need for a placebo-controlled study, will delay the initiation of dosing in the eteplirsen confirmatory study until at least the second quarter of 2014. A follow up meeting with FDA has been scheduled to take place this month to discuss the confirmatory study design.
Sarepta Therapeutics Announces FDA Considers NDA Filing for Eteplirsen Premature in Light of Recent Competitive Drug Failure and Recent DMD Natural History Data
FDA Questions Dystrophin as a Biomarker Due to Failed Studies of Other Investigational Drugs for DMD; FDA Questions 6-Minute Walk Test Results for Eteplirsen, Suggesting Study Population Should Be Stable Over Two-Year Timeframe Due to Recent Natural History Data; FDA Requests Further Discussion on Endpoints, Design of Confirmatory Clinical Study
CAMBRIDGE, MA--(Marketwired - Nov 12, 2013) - Sarepta Therapeutics, Inc. (NASDAQ: SRPT) today provided an update on its discussions with the U.S. Food and Drug Administration (FDA) regarding its planned New Drug Application (NDA) submission and confirmatory clinical study with eteplirsen for the treatment of Duchenne muscular dystrophy (DMD). Citing recent developments since Sarepta's last meeting with the agency, including a failed study with a competitive product and recent natural history data in DMD, the FDA indicated the new data raise "considerable doubt" about both the dystrophin biomarker and the supportive clinical efficacy assessed on the 6-minute walk test (6MWT) in the Phase IIb clinical study of eteplirsen. As a result of these recent data, the FDA stated that they "currently consider an NDA filing for eteplirsen as premature."
"We are very disappointed with the FDA's decision to reconsider their openness to a potential NDA filing based on our current data and the resultant impact this change may have on our efforts to achieve an earlier approval of eteplirsen," said Chris Garabedian, president and chief executive officer of Sarepta Therapeutics. "We strongly believe in the potential of eteplirsen to address a serious unmet medical need in DMD and we are committed to its development. Our team at Sarepta recognizes the urgency of families who are seeking new treatments, and we will continue to work with the FDA on an acceptable confirmatory study design and, in parallel, seek to address their concerns regarding a potential NDA filing based on our current dataset."
The FDA provided the feedback in pre-meeting comments and clarified them in a meeting with Sarepta that took place late last week to discuss the eteplirsen clinical program.
Excerpts from the FDA's pre-meeting comments on reconsidering an NDA filing included:
"Since our last meeting, a large phase 3 trial of drisapersen, a drug with a similar mechanism of action, was reported to be negative, despite increased expression of dystrophin. The disconnect between increased expression of dystrophin and clinical efficacy for drisapersen, combined with previous negative reports for PTC124, another drug thought to act by increasing dystrophin, raises considerable doubt about the biomarker, and consequentially, its ability to reasonably likely predict clinical benefit."
"...the quantity of dystrophin that might be necessary to be considered reasonably likely to predict clinical benefit is even less clear; small or perhaps even moderate increases are seemingly not enough, at least in the subpopulation of boys studied so far. An adequately validated quantitative assay for dystrophin now seems a prerequisite to further consideration of the biomarker as supportive of approval. Since our last meeting, our concern about the shortcomings of your current quantification methods has grown."
"Recent natural history data in DMD indicate that a baseline 6-Minute Walk Test (6MWT) ≥350 meters predicts continued general stability for such patients, not the 75- to 83-meter yearly decline you suggest in the meeting package. Thus, considerable doubt is also cast on the efficacy support provided by your ongoing open-label study (4658-us-202, 96-week data submitted), in which baseline 6MWT was >350 m for all patients."
"...the expected variability of 6MWT values appears sufficient to explain differences between arms on which the post-hoc analysis was based. Because of this, together with our lack of confidence in the capacity of your dystrophin biomarker to predict clinical benefit, we currently consider an NDA filing for eteplirsen as premature."
Additional excerpts from the FDA's pre-meeting comments on the eteplirsen confirmatory study design included:
"Recent trial failures in DMD suggest it may be productive to re-examine study enrollment criteria and endpoints."
"...it seems worthwhile to consider selection of other endpoints and/or populations for the next trial of eteplirsen. We stress that we would still accept 6MWT in an appropriately powered study; however, because 6MWT excludes both younger boys who cannot perform such a demanding test, and older boys who are no longer ambulatory, we are concerned that seemingly avoidable limitations on enrollment could undermine study feasibility. Many possible combinations of endpoints and subpopulations appear possible. Motor scales that measure a broader range of function and demand less sustained effort than 6MWT could be appropriate for a much wider range of boys, perhaps including non-ambulatory boys. To allow inclusion of a broader range of patients, a study could also be designed that mathematically combined findings from, for example, an ambulation endpoint in less advanced patients with findings from an upper-limb or respiratory endpoint in more advanced patients. We remain open to consideration of endpoints and populations you may suggest."
"...we believe that a placebo-controlled trial would be the most likely method for developing interpretable evidence of efficacy for eteplirsen, because efficacy endpoints in DMD are effort-dependent and susceptible to bias, and the natural history is highly variable and has recently improved with steroid use and advances in ancillary care. We would like to discuss the perceived barriers to conducting such a trial with you."
The FDA's request to discuss different clinical endpoints, combined endpoints, and different DMD subpopulations for a confirmatory clinical study, along with their questions about dystrophin as a biomarker and the need for a placebo-controlled study, will delay the initiation of dosing in the eteplirsen confirmatory study until at least the second quarter of 2014. A follow up meeting with FDA has been scheduled to take place this month to discuss the confirmatory study design.
und wat passiert nu?
Mal schauen. Vielleicht steige ich wieder ein. Hat aber noch keine Eile
So, bin seit gestern mit einem ersten Einkauf wieder beteiligt.
Leute, Kursziel Pennystock ! Keine Zukunft, keine Kohle !
Wenn es so weitergeht bin ich bald wieder am verkaufen 


26-Nov-13 WBB Securities kommt aus dem Busch und setzt Pionier SRPT auf Speculative Buy !
Banc of Lunatics mit Buy, sieht die 25 in bälde.
Banc of Lunatics mit Buy, sieht die 25 in bälde.

...und schwupps wieder auf 20xx.
die kommen wieder ganz gross !
die kommen wieder ganz gross !
erklärt vielleicht das up der letzten Tage:
FDA's Janet Woodcock may have made some comments supportive of eteplirsen's regulatory timelines.
FDA's Janet Woodcock may have made some comments supportive of eteplirsen's regulatory timelines.
Der Chef kauft immer noch dick ein:
11/14/2013 Anthony R. Chase Director 10,000 $13.95 $139,483.00
11/14/2013 Anthony R. Chase Director 10,000 $13.95 $139,483.00
Sarepta upgraded at Piper Jaffray
Eteplirsen's Competitive Advantage Is Setting Up Sarepta For 2014



http://seekingalpha.com/article/1915971-eteplirsens-competit…




http://seekingalpha.com/article/1915971-eteplirsens-competit…
Antwort auf Beitrag Nr.: 46.131.921 von lunatics am 30.12.13 18:41:20Hi @lunatics
Meine in Erinnerung zu haben, dass Du auch mal eine Meinung zu Catalyst Pharmac. hattest, hatte ich doch irgendwann mal dazu etwas von Dir gelesen. Bist Du noch drin?
Sind ja von > 3 deutlich < 2 gerutscht und aktuell seitwärts um die 2.
Könnten die nicht eine zweite Galena werden? Potential wäre bei der Pipeline ja durchaus vorhanden.Dürfte ich Deine Meinung dazu wissen?
Ansosnten: Sorry für die Frage im falschen Thread. Wünsch Euch aber weiterhin steigende Kurse. Bei mir hats mit dem Einstieg unter 20 leider nicht geklappt und so beobachte ich momentan nur (bin mit grosser Position in Cardiome Pharma drin, falls es jemanden interessiert).
Gruss
Meine in Erinnerung zu haben, dass Du auch mal eine Meinung zu Catalyst Pharmac. hattest, hatte ich doch irgendwann mal dazu etwas von Dir gelesen. Bist Du noch drin?
Sind ja von > 3 deutlich < 2 gerutscht und aktuell seitwärts um die 2.
Könnten die nicht eine zweite Galena werden? Potential wäre bei der Pipeline ja durchaus vorhanden.Dürfte ich Deine Meinung dazu wissen?
Ansosnten: Sorry für die Frage im falschen Thread. Wünsch Euch aber weiterhin steigende Kurse. Bei mir hats mit dem Einstieg unter 20 leider nicht geklappt und so beobachte ich momentan nur (bin mit grosser Position in Cardiome Pharma drin, falls es jemanden interessiert).
Gruss
Bei CPRX am 30.09. 100% verkauft
und seit 05.12. wieder long.
http://www.wallstreet-online.de/diskussion/1166173-61-70/cat…
und seit 05.12. wieder long.
http://www.wallstreet-online.de/diskussion/1166173-61-70/cat…
Citibank kommt heute mit einem sell. Aktie taucht.
....doch Feuersteins Brieflein von der FDA lässt aufhorchen:
The full text of Chew's letter is below:
Thank you for your message to the Food and Drug Administration (FDA) about eteplirsen, a new drug under investigation for the treatment of Duchenne muscular dystrophy.
We recognize the huge unmet medical need in Duchenne muscular dystrophy, the devastating nature of the disease for patients and their families, and the great urgency to make new treatments available.We understand that you feel that eteplirsen is highly effective, and may be confused by what you have read or heard about FDA's actions on eteplirsen. Unfortunately, the information reported in the press or discussed in blogs does not necessarily reflect FDA's position. FDA has reached no conclusions about the possibility of using accelerated approval for any new drug for the treatment of Duchenne muscular dystrophy, and for eteplirsen in particular.
FDA's analyses of eteplirsen and other drugs for the treatment of Duchenne muscular dystrophy have been based on thorough and extensive assessments and discussion of all available data and information by a large multi-disciplinary team of FDA scientists. Many assessments are ongoing. Some of this information, in particular, information about the dystrophin biomarker, the natural progression of the disease, and the results from clinical studies, are not available to the public. We are prevented by legal regulations from divulging this information, and this makes it difficult for you to understand FDA's evolving position on these drugs. We know this is very frustrating, and we think this may have caused some of the misunderstanding here.
FDA is fully committed to make safe and effective drugs available for patients with Duchenne muscular dystrophy as soon as possible, and is actively engaged with all drug companies developing new drugs for Duchenne muscular dystrophy, including Sarepta Therapeutics, the company developing eteplirsen.
As you may know, we recently participated in a policy forum with the Duchenne community, including patients, parents, experts, and other stakeholders. Please know that we understand your frustration, and fully understand the dire urgency of the situation. We will continue to work relentlessly with the community to make safe and effective treatments for Duchenne muscular dystrophy available to patients.
Thank you again for taking the time to write to us.
Sincerely,
Catherine Chew, PharmD
Acting Director, Division of Drug Information
Center for Drug Evaluation and Research
Food and Drug Administration
-- Reported by Adam Feuerstein in Boston.
....doch Feuersteins Brieflein von der FDA lässt aufhorchen:
The full text of Chew's letter is below:
Thank you for your message to the Food and Drug Administration (FDA) about eteplirsen, a new drug under investigation for the treatment of Duchenne muscular dystrophy.
We recognize the huge unmet medical need in Duchenne muscular dystrophy, the devastating nature of the disease for patients and their families, and the great urgency to make new treatments available.We understand that you feel that eteplirsen is highly effective, and may be confused by what you have read or heard about FDA's actions on eteplirsen. Unfortunately, the information reported in the press or discussed in blogs does not necessarily reflect FDA's position. FDA has reached no conclusions about the possibility of using accelerated approval for any new drug for the treatment of Duchenne muscular dystrophy, and for eteplirsen in particular.
FDA's analyses of eteplirsen and other drugs for the treatment of Duchenne muscular dystrophy have been based on thorough and extensive assessments and discussion of all available data and information by a large multi-disciplinary team of FDA scientists. Many assessments are ongoing. Some of this information, in particular, information about the dystrophin biomarker, the natural progression of the disease, and the results from clinical studies, are not available to the public. We are prevented by legal regulations from divulging this information, and this makes it difficult for you to understand FDA's evolving position on these drugs. We know this is very frustrating, and we think this may have caused some of the misunderstanding here.
FDA is fully committed to make safe and effective drugs available for patients with Duchenne muscular dystrophy as soon as possible, and is actively engaged with all drug companies developing new drugs for Duchenne muscular dystrophy, including Sarepta Therapeutics, the company developing eteplirsen.
As you may know, we recently participated in a policy forum with the Duchenne community, including patients, parents, experts, and other stakeholders. Please know that we understand your frustration, and fully understand the dire urgency of the situation. We will continue to work relentlessly with the community to make safe and effective treatments for Duchenne muscular dystrophy available to patients.
Thank you again for taking the time to write to us.
Sincerely,
Catherine Chew, PharmD
Acting Director, Division of Drug Information
Center for Drug Evaluation and Research
Food and Drug Administration
-- Reported by Adam Feuerstein in Boston.
Essplosione!

Wurde auch Zeit 



Es kommt bald noch besser
Antwort auf Beitrag Nr.: 46.243.823 von lunatics am 16.01.14 20:52:13Ich hoffe du hast recht, ich denke schon ans verkaufen.
Ich auch aber erst später!
Na mal sehen ob ich morgen ruhig bleiben kann ich versuch, die Handelseröffnung wird mir hoffentlich den richtigen Weg weisen. Also gute Nacht ......
Sarepta upgraded to Buy at Needham
Aktie explodiert
Sarepta Therapeutics announces eteplirsen demonstrates stability on pulmonary function tests through 120 weeks in phase IIb study in duchenne muscular dystrophy
SRPT announced new pulmonary function data through Week 120 from Study 202, a Phase IIb open-label extension study of eteplirsen in patients with Duchenne muscular dystrophy (DMD). Results through more than two years of treatment showed stable pulmonary function in the Intent-to-Treat (ITT) study population. These data are consistent with previously reported 120-week clinical data showing a general stabilization of walking ability in eteplirsen-treated patients evaluable on the 6-minute walk test (6MWT).

Sarepta Therapeutics announces eteplirsen demonstrates stability on pulmonary function tests through 120 weeks in phase IIb study in duchenne muscular dystrophy
SRPT announced new pulmonary function data through Week 120 from Study 202, a Phase IIb open-label extension study of eteplirsen in patients with Duchenne muscular dystrophy (DMD). Results through more than two years of treatment showed stable pulmonary function in the Intent-to-Treat (ITT) study population. These data are consistent with previously reported 120-week clinical data showing a general stabilization of walking ability in eteplirsen-treated patients evaluable on the 6-minute walk test (6MWT).
Advocates set to meet with Congress on Sarepta DMD drug
http://www.theflyonthewall.com/permalinks/entry.php/SRPTid19…
http://www.theflyonthewall.com/permalinks/entry.php/SRPTid19…
Sarepta Therapeutics Announces Positive Safety Results from Phase I Clinical Study of Marburg Drug Candidate
http://finance.yahoo.com/news/sarepta-therapeutics-announces…
http://finance.yahoo.com/news/sarepta-therapeutics-announces…
Schön wie sie wieder kommt..100% in 2 Monaten bei nachgebenden Index.
Ab 30 wird's kritisch! rechtzeitig aussteigen nicht vergessen.


Ab 30 wird's kritisch! rechtzeitig aussteigen nicht vergessen.
So, nochmals höhenflug über 30 angesagt 

Stifel said raised its price target on Sarepta to $34 from $21 citing reduced uncertainty for the confirmatory Eteplirsen trial as well as positive recent 120-week data. The firm maintains its Buy rating on the stock.
Morgen Zahltag ??

Sarepta jumps +50% on progress for muscle disorder drug

http://finance.yahoo.com/news/sarepta-jumps-progress-muscle-…

http://finance.yahoo.com/news/sarepta-jumps-progress-muscle-…
..und noch ein schöner Artikel aus Brron's
Few Fund Managers Saw This One Coming
http://blogs.barrons.com/focusonfunds/2014/04/21/sarepta-few…
Few Fund Managers Saw This One Coming
http://blogs.barrons.com/focusonfunds/2014/04/21/sarepta-few…
Sarepta upgraded to Buy from Hold at Canaccord Price target is $63.
Sarepta price target raised to $37 from $19 at Piper Jaffray
Sarepta price target raised to $37 from $19 at Piper Jaffray
SRPT-Party geht weiter !
Sarepta Therapeutics: Keep on Climbing
...meint Barron's @ http://blogs.barrons.com/stockstowatchtoday/2014/04/22/sarep…
Sarepta Therapeutics: Keep on Climbing
...meint Barron's @ http://blogs.barrons.com/stockstowatchtoday/2014/04/22/sarep…
SRPT announces proposed $100 mln public offering of common stock
Antwort auf Beitrag Nr.: 46.864.092 von lunatics am 23.04.14 20:18:46 Wird dadurch der Kurs verwässert ?
Wird dadurch der Kurs verwässert ?
 Wird dadurch der Kurs verwässert ?
Wird dadurch der Kurs verwässert ?
Sarepta Therapeutics is scheduled to present at the 39th Annual Deutsche Bank Healthcare Conference in Boston, MA on Wednesday, May 7, 2014 at 8:40 a.m. Eastern Time.
Antwort auf Beitrag Nr.: 46.896.288 von lunatics am 29.04.14 20:46:12Warum nicht ? Die bringen doch einige Aktien mehr unters Volk, oder verstehe ich das falsch?
Sarepta entered into a Purchase and Sale Agreement with Eisai Inc. pursuant to which Sarepta will acquire from Eisai certain real and personal property, including a manufacturing facility in Andover, Massachusetts for an aggregate purchase price of approximately $15 million, subject to adjustments and apportionments set forth in the Agreementof which approximately $10 million will be paid at closing and the remaining $5 million will be paid in two installments payable on or before July 15, 2015 and January 15, 2016.
warum wird dieser Thread nicht beschrieben?? die Aktie läuft doch richti8g gut
WBB Securities upgrade auf buy 

Credit Suisse geht auf outperform
FDA Comments on Talks With Sarepta on Muscular Dystrophy Drug
http://online.wsj.com/articles/fda-comments-on-talks-with-sa…
http://online.wsj.com/articles/fda-comments-on-talks-with-sa…
Sarepta Therapeutics tops 3Q profit forecasts
http://finance.yahoo.com/news/sarepta-therapeutics-tops-3q-p…
http://finance.yahoo.com/news/sarepta-therapeutics-tops-3q-p…
For the third quarter of 2014, Sarepta reported a non-GAAP net loss of $28.8 million, or $0.70 per share, compared to a non-GAAP net loss of $21.3 million for the third quarter of 2013, or $0.63 per share.
The incremental loss of $7.5 million was primarily the result of increased general and administrative expenses as a result of corporate growth as well as a decrease in revenue from the Company’s government contracts.
On a GAAP basis, the net loss for the third quarter of 2014 was $29.2 million, or $0.71 per share (including $4.6 million of stock-based compensation expenses), compared to a net loss of $42.0 million, or $1.24 per share (including $3.5 million of stock-based compensation and restructuring expenses) for the third quarter of 2013. The decrease in net loss is primarily due to a favorable change of $21.4 million in gain (loss) on change in warrant valuation offset by an increase of $5.6 million in operating expenses and a decrease of $3.1 million in contract revenue.
Revenue for the third quarter of 2014 was $1.1 million, down from $4.2 million for the third quarter of 2013. The $3.1 million decrease was primarily due to decreases in revenue from the Company’s government contracts. The government contract under which the Marburg drug
candidate was being developed expired in July 2014 and the Company is currently evaluating options to continue advancing its Marburg drug candidate and other infectious disease research and development efforts.
The incremental loss of $7.5 million was primarily the result of increased general and administrative expenses as a result of corporate growth as well as a decrease in revenue from the Company’s government contracts.
On a GAAP basis, the net loss for the third quarter of 2014 was $29.2 million, or $0.71 per share (including $4.6 million of stock-based compensation expenses), compared to a net loss of $42.0 million, or $1.24 per share (including $3.5 million of stock-based compensation and restructuring expenses) for the third quarter of 2013. The decrease in net loss is primarily due to a favorable change of $21.4 million in gain (loss) on change in warrant valuation offset by an increase of $5.6 million in operating expenses and a decrease of $3.1 million in contract revenue.
Revenue for the third quarter of 2014 was $1.1 million, down from $4.2 million for the third quarter of 2013. The $3.1 million decrease was primarily due to decreases in revenue from the Company’s government contracts. The government contract under which the Marburg drug
candidate was being developed expired in July 2014 and the Company is currently evaluating options to continue advancing its Marburg drug candidate and other infectious disease research and development efforts.
jetzt hat es geknallt, wird übernommen ubnd keiner hier
Sarepta Therapeutics, which, like Prosensa, is working on a treatment for Duchenne muscular dystrophy, surged 12% in a possible sympathy move.
Interessanter Artikel:
BioMarin CEO Angers Sarepta CEO With Slides Comparing Trial Data
http://blogs.wsj.com/pharmalot/2015/01/16/biomarin-ceo-anger…
BioMarin CEO Angers Sarepta CEO With Slides Comparing Trial Data
http://blogs.wsj.com/pharmalot/2015/01/16/biomarin-ceo-anger…
...interessanter Artikel
Analyst Sees Over 50% Upside in Sarepta
http://247wallst.com/healthcare-business/2015/02/17/why-one-…
Analyst Sees Over 50% Upside in Sarepta
http://247wallst.com/healthcare-business/2015/02/17/why-one-…
..und noch einer...
Why Muscular Dystrophy Is Biotech's Favorite Orphan
http://news.investors.com/021915-740034-bmrn-ptct-srpt-tackl…
Why Muscular Dystrophy Is Biotech's Favorite Orphan
http://news.investors.com/021915-740034-bmrn-ptct-srpt-tackl…
Garabedian geht...versichert jedoch dass Eteplirsen’s Zulassung nach wie vor
nicht gefährdet sei...("on track")
http://finance.yahoo.com/news/sarepta-ceo-exits-eteplirsen-r…
nicht gefährdet sei...("on track")

http://finance.yahoo.com/news/sarepta-ceo-exits-eteplirsen-r…
Why BioMarin’s New Drug Application is Good News for Sarepta Therapuetics
http://blogs.barrons.com/stockstowatchtoday/2015/05/06/why-b…
http://blogs.barrons.com/stockstowatchtoday/2015/05/06/why-b…
So, heute ist ein guter Tag.
ZAHLTAG !!
Sarepta Therapeutics (SRPT) Stock Soars Following Positive Meeting With FDA
http://www.thestreet.com/story/13158457/1/sarepta-therapeuti…
ZAHLTAG !!
Sarepta Therapeutics (SRPT) Stock Soars Following Positive Meeting With FDA
http://www.thestreet.com/story/13158457/1/sarepta-therapeuti…
Das wars.
Kohle nach Hause bringen und nicht auf die FDA warten. Bei pos. Entscheid sinkt der Kurs sowieso.

Kohle nach Hause bringen und nicht auf die FDA warten. Bei pos. Entscheid sinkt der Kurs sowieso.

Biotech stock set to double
http://finance.yahoo.com/video/biotech-stock-set-double-2124…
http://finance.yahoo.com/video/biotech-stock-set-double-2124…
SRPT erwartet NDA für Eteplirsen Ende nächsten Monat!
Kurs spricht deutlich an.
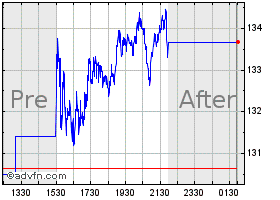
Kurs spricht deutlich an.
Oppenheimer increased its price target on the stock to $60 

FDA Still Negative on Sarepta's DMD Drug
Blutbad am Aktienmarkt.
Blutbad am Aktienmarkt.
FDA added a voting question to the agenda for the Monday meeting of the Peripheral and Central Nervous System Drugs Advisory Committee. Aktie wieder rauf um 35%
SRPT heute erneut stark !

Wohin geht der Kurs? Die Entwicklung der letzten Tage ist ja echt supi...
Der Kurs geht weiterhin nach oben
die Luft ist raus?!?!
halloho,
was macht Ihr ? kauft ihr nach weil es günstig ist oder wartet ihr auf die Entscheidung ob es nun doch zugelassen wird ?
was macht Ihr ? kauft ihr nach weil es günstig ist oder wartet ihr auf die Entscheidung ob es nun doch zugelassen wird ?
So der Tag der Entscheidung rückt näher Hero oder Zero...
Antwort auf Beitrag Nr.: 52.473.952 von sky2 am 25.05.16 13:40:39.. oder doch noch nicht:
http://www.bloomberg.com/news/articles/2016-05-25/desperate-…
http://www.bloomberg.com/news/articles/2016-05-25/desperate-…
Antwort auf Beitrag Nr.: 52.474.372 von linkshaender am 25.05.16 14:22:43
für mich ist die Wette (und nichts anderes ist das) das es doch klappen könnte zu hoch !
auch ist von der letzten Zulassung des Unternehmens die Rede (wenn ich den Artikel richtig verstanden habe), was ist das Unternehmen bei einem Flopp noch Wert ?
die Leute mit dem Blick hinter die Kulissen klären mich bitte mal auf... DANKE
würde bei bei um die 10 Euro wieder einsteigen ...
nicht zu verstehen
es ist hier von 10-20 Euro alles drin und was die schwanken, man oh manfür mich ist die Wette (und nichts anderes ist das) das es doch klappen könnte zu hoch !
auch ist von der letzten Zulassung des Unternehmens die Rede (wenn ich den Artikel richtig verstanden habe), was ist das Unternehmen bei einem Flopp noch Wert ?
die Leute mit dem Blick hinter die Kulissen klären mich bitte mal auf... DANKE
würde bei bei um die 10 Euro wieder einsteigen ...
Hier liegt mehr drinn.
Die Bude revolutioniert den RNA-Markt.
Die Bude revolutioniert den RNA-Markt.
jetzt geht es aber bergab
Antwort auf Beitrag Nr.: 52.477.498 von lunatics am 25.05.16 20:41:34und warum liegt hier mehr drin...
der Kurs ist mal wieder runter, nehme an wegen Infos der Zulassung...
was können die ?
der Kurs ist mal wieder runter, nehme an wegen Infos der Zulassung...
was können die ?
Antwort auf Beitrag Nr.: 52.533.236 von OliKo am 03.06.16 10:58:14Zuletzt gab es nach jeder schlechten Nachricht immer einen ordentlichen Rebound...die AKtie hat nach wie vor viel Phantasie 

Antwort auf Beitrag Nr.: 52.534.748 von Schablonski am 03.06.16 13:41:59das wiederkommen war auch nachzuvollziehen, weil eine Zulassung immer weiter verschoben wurde...
aber was, wenn es nun endgültig gestrichen wird...
aber was, wenn es nun endgültig gestrichen wird...
Sarepta looks to raise $38M in offering 
http://www.bizjournals.com/boston/blog/bioflash/2016/06/afte…

http://www.bizjournals.com/boston/blog/bioflash/2016/06/afte…
Schöner Artikel aus Barrons
Is There Hope for Sarepta?
http://finance.yahoo.com/m/98bbf979-891c-3f97-afeb-7c74b4ecc…
Is There Hope for Sarepta?
http://finance.yahoo.com/m/98bbf979-891c-3f97-afeb-7c74b4ecc…
So, habe heute Kasse gemacht.
jetzt kauf ich SANN
jetzt kauf ich SANN

Gut, dass ich gestern einen Call Schein mit Hebel 100 gekauft hatte. War der richtige Zeitpunkt.
Tja, im Ernst. Glückwunsch an alle investierten! Auf so einen Tag träumen viele. Und alle die leider nicht dabei sind, wie ich, schauen staunend aus der Ferne zu.
Tja, im Ernst. Glückwunsch an alle investierten! Auf so einen Tag träumen viele. Und alle die leider nicht dabei sind, wie ich, schauen staunend aus der Ferne zu.
Gratulation zurück. Hatte zwar keinen Hebel und nur die Aktie aber trotzdem 100%...Operation geglückt. Ich denke unter anderem auch dank SANN-Teilmisserfolg

Antwort auf Beitrag Nr.: 53.305.374 von lunatics am 19.09.16 17:07:10Wo kaufst Du Sann ??? Bei 12.50 !!!
Antwort auf Beitrag Nr.: 53.307.615 von F430Spyder am 19.09.16 22:12:15Ja, und erst dann ! ..und dies erst noch mit einem Bruchteil des SRPT-Gewinns
..und dies erst noch mit einem Bruchteil des SRPT-Gewinns
 ..und dies erst noch mit einem Bruchteil des SRPT-Gewinns
..und dies erst noch mit einem Bruchteil des SRPT-Gewinns
Leider seit ihr viel zu früh raus. Sofern ihr überhaupt drin wart.
Sofern ihr überhaupt drin wart. 
 Sofern ihr überhaupt drin wart.
Sofern ihr überhaupt drin wart. 
AUSBRUCH!!!!!!
Antwort auf Beitrag Nr.: 53.312.559 von harri11 am 20.09.16 16:21:52
Zitat von harri11: Leider seit ihr viel zu früh raus.Sofern ihr überhaupt drin wart.
Den richtigen Zeitpunkt trifft man nie.....aber ich arbeite drann
Hauptsache die gewonnene Kohle ist auf dem Konto....und die Erkenntnis, dass man mit der Aktie goldrichtig lag.

Hauptsache die gewonnene Kohle ist auf dem Konto....und die Erkenntnis, dass man mit der Aktie goldrichtig lag.
Ausbruch!!!!!!
 :laugh:
:laugh:







Ist das schön.

 :laugh:
:laugh:







Ist das schön.
sehr lesenswert:
How Sarepta Is Cashing In on Its FDA Homerun
http://247wallst.com/healthcare-business/2016/09/22/how-sare…
How Sarepta Is Cashing In on Its FDA Homerun
http://247wallst.com/healthcare-business/2016/09/22/how-sare…
RBC raised SRPT price target by more than double the current level to $108 
http://www.marketwatch.com/story/rbc-capital-markets-more-th…

http://www.marketwatch.com/story/rbc-capital-markets-more-th…
Catabasis Pharma and SRPT Announce a Joint Research Collaboration in Duchenne Muscular Dystrophy
http://investorrelations.sarepta.com/phoenix.zhtml?c=64231&p…
http://investorrelations.sarepta.com/phoenix.zhtml?c=64231&p…
!
Dieser Beitrag wurde von CloudMOD moderiert. Grund: ohne nachvollziehbare Quellenangabe, ggf überarbeitet neu einstellen
Antwort auf Beitrag Nr.: 53.392.653 von N424671 am 02.10.16 10:26:41ja das war vor eine Jahr....Inzwischen steht sie Über 60+
Sarepta Therapeutics Announces First Patient Dosed in Phase III Clinical Trial of SRP-4045 and SRP-4053 for the Treatment of Duchenne Muscular Dystrophy
https://finance.yahoo.com/news/sarepta-therapeutics-announce…
https://finance.yahoo.com/news/sarepta-therapeutics-announce…
Auch interessant: FDA's new drugs director slams Sarepta, says biotech’s approval ‘NOT a good model’ by Ben Adams | Oct 20, 2016 6:13am John Jenkins, who runs the FDA’s office for new meds, has not taken kindly to the regulator’s recent, and highly controversial, approval of Sarepta’s ($SRPT) Duchenne med Exondys 51 (eteplirsen) after hitting out at bad trials with questionable data. In a presentation given this week at the NORD summit in Arlington, called “Lessons learned from eteplirsen and other recent rare disease programs,” Jenkins spoke specifically of the biotech’s drug, saying: the “path taken by Sarepta NOT a good model for other development programs.” A month ago, the FDA approved Exondys 51 against all odds. The approval was considered unlikely because many of the data used to back a speedy approval were based largely on a small study of a dozen children with no placebo control, comparing eteplirsen’s results against historical data in the muscle-wasting disease. Back in April, an FDA panel of outside experts voted narrowly, 7 to 6, that Sarepta did not provide substantial evidence from “adequate and well-controlled” studies that the drug produced dystrophin at a level that was reasonably likely to produce a clinical benefit. On the big question--do the clinical results of the single study provide “substantial evidence” of eteplirsen’s efficacy--seven of the panel members voted no, with three voting yes and three abstaining. Five months down the line, however, it was approved, but as became apparent, this approval came at the cost of some major internal wrangling from within the agency. In documents posted by the FDA along with its approval last month, the high level of lobbying undertaken by Dr. Janet Woodcock, the CDER director, for the med to be given the green light became clear. It was, in the end, Dr. Woodcock who helped push the drug through to approval--despite internal protestations from Dr. Ellis Unger, a senior doc at the agency, among others, to FDA Commissioner Dr. Robert Califf. Dr. Unger had expressed concerns at the small study size and its lack of clear efficacy, but Dr. Woodcock said the FDA must be “prepared to be flexible with respect to a devastating illness with no treatment options.” Dr. Califf said he would “defer” to Dr. Woodcock in this case and allow the approval. A few weeks before this decision, another strange thing happened when Dr. Ron Farkas, a fierce critic of Sarepta’s DMD drug, left the FDA unexpectedly to take on a consulting role at CRO Parexel ($PRXL), with no word from any party until reports of the move surfaced in the press, and each were forced to concede that he had moved on. Reasons for his departure were not given. In his presentation, Jenkins set out his stall as to why the FDA on his watch isn't looking to lower standards--a concern many have voiced since the DMD approval. He reeled off the regulator's desired data list and what it wants, and doesn't want, to see: “In many cases, randomized controlled clinical trials represent the fastest way to determine if a drug is effective,” and that companies should “randomize as early as possible in development to avoid potentially misleading and uninterpretable findings from open-label trials.” On the issue of being more flexible, as per Dr. Woodcock’s philosophy, he said: “Flexibility in FDA regulations does not mean marketing approval prior to demonstration of substantial evidence of effectiveness.” He said that the FDA’s use of speedy reviews should be prospectively planned, “NOT as a ‘rescue’ for a failed program.” He also said that personal attacks on FDA reviewers “creates an atmosphere of distrust and isolation rather than collaboration,” and that “recruitment and retention of qualified review staff is very challenging in such an environment.” In short, be nicer to the FDA, and see Sarepta as an exception to the rule. http://www.fiercebiotech.com/biotech/fda-news-drugs-director…
Santhera (Mkap 11 M€) DMD P3 Data in early 2Q = ZOCK des Jahres 2014 | wallstreet-online.de - Vollständige Diskussion unter:
http://www.wallstreet-online.de/diskussion/1191124-9891-9900…
Santhera (Mkap 11 M€) DMD P3 Data in early 2Q = ZOCK des Jahres 2014 | wallstreet-online.de - Vollständige Diskussion unter:
http://www.wallstreet-online.de/diskussion/1191124-9891-9900…
die geht ja sehr gut ab, gibt es was neues? Santhera 



habe es schon gefunden
Ispta Therapeutics (NASDAQ: SRPT), ein kommerzieller Entwickler von innovativen RNA-zielgerichteten Therapeutika, gab heute bekannt, dass es auf der 25. jährlichen Gesundheitskonferenz der Credit Suisse in Phoenix, Arizona, am Montag, den 7. November 2016 um 5: 30 PM, östliche Zeit. Edward Kaye, Chief Executive Officer von Sarepta, wird der Moderator am Kaminchat sein. Die Präsentation wird live im Bereich Investor Relations auf der Sarepta Therapeutics-Website unter www.sarepta.com präsentiert und unter der Rubrik "Events und Präsentationen" nach der Präsentation für 90 Tage archiviert. Stellen Sie eine Verbindung zu Sarepta's Website einige Minuten vor dem Beginn der Übertragung, um angemessene Zeit für jeden möglichen Software-Download sicherzustellen, der notwendig sein kann. Über Sarepta Therapeutics Sarepta Therapeutics ist ein kommerzielles biopharmazeutisches Unternehmen, das sich auf die Entdeckung und Entwicklung von einzigartigen RNA-zielgerichteten Therapeutika für die Behandlung seltener neuromuskulärer Erkrankungen konzentriert. Das Unternehmen konzentriert sich hauptsächlich darauf, die Entwicklung seiner potenziell krankheitsmodifizierenden DMD-Arzneimittelkandidaten rasch voranzutreiben. Weitere Informationen finden Sie unter www.sarepta.com. Internet-Buchung von Informationen Wir informieren routinemäßig Informationen, die für Investoren im Bereich "Für Investoren" auf unserer Website unter www.sarepta.com wichtig sind. Wir ermutigen Investoren und potenzielle Investoren, unsere Website regelmäßig auf wichtige Informationen über uns zu konsultieren. Quell-Version auf businesswire.com anzeigen: http://www.businesswire.com/news/home/20161104005220/de/ Wertpapier: Sarepta Therapeutics
Sarepta Therapeutics präsentiert Unternehmensüberblick bei der Credit Suisse 25th Annual Healthcare Conference | Wallstreet-online.de - Vollständiger Artikel unter:
http://www.wallstreet-online.de/nachricht/9061968-sarepta-th…
Ispta Therapeutics (NASDAQ: SRPT), ein kommerzieller Entwickler von innovativen RNA-zielgerichteten Therapeutika, gab heute bekannt, dass es auf der 25. jährlichen Gesundheitskonferenz der Credit Suisse in Phoenix, Arizona, am Montag, den 7. November 2016 um 5: 30 PM, östliche Zeit. Edward Kaye, Chief Executive Officer von Sarepta, wird der Moderator am Kaminchat sein. Die Präsentation wird live im Bereich Investor Relations auf der Sarepta Therapeutics-Website unter www.sarepta.com präsentiert und unter der Rubrik "Events und Präsentationen" nach der Präsentation für 90 Tage archiviert. Stellen Sie eine Verbindung zu Sarepta's Website einige Minuten vor dem Beginn der Übertragung, um angemessene Zeit für jeden möglichen Software-Download sicherzustellen, der notwendig sein kann. Über Sarepta Therapeutics Sarepta Therapeutics ist ein kommerzielles biopharmazeutisches Unternehmen, das sich auf die Entdeckung und Entwicklung von einzigartigen RNA-zielgerichteten Therapeutika für die Behandlung seltener neuromuskulärer Erkrankungen konzentriert. Das Unternehmen konzentriert sich hauptsächlich darauf, die Entwicklung seiner potenziell krankheitsmodifizierenden DMD-Arzneimittelkandidaten rasch voranzutreiben. Weitere Informationen finden Sie unter www.sarepta.com. Internet-Buchung von Informationen Wir informieren routinemäßig Informationen, die für Investoren im Bereich "Für Investoren" auf unserer Website unter www.sarepta.com wichtig sind. Wir ermutigen Investoren und potenzielle Investoren, unsere Website regelmäßig auf wichtige Informationen über uns zu konsultieren. Quell-Version auf businesswire.com anzeigen: http://www.businesswire.com/news/home/20161104005220/de/ Wertpapier: Sarepta Therapeutics
Sarepta Therapeutics präsentiert Unternehmensüberblick bei der Credit Suisse 25th Annual Healthcare Conference | Wallstreet-online.de - Vollständiger Artikel unter:
http://www.wallstreet-online.de/nachricht/9061968-sarepta-th…
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -7,04 | |
| -2,70 | |
| -1,08 | |
| +0,23 | |
| -1,48 | |
| +0,48 | |
| -0,76 | |
| -0,30 | |
| -3,44 | |
| -1,57 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 240 | ||
| 98 | ||
| 81 | ||
| 78 | ||
| 75 | ||
| 53 | ||
| 41 | ||
| 38 | ||
| 36 | ||
| 33 |
Sarepta Therapeutics - first-in-class RNA






















