BRAINSTORM CELL Therapeutics Inc - Stammzelltherapien zur Linderung neurodegenerativer Störungen
eröffnet am 06.12.20 23:01:26 von
neuester Beitrag 02.04.24 11:03:24 von
neuester Beitrag 02.04.24 11:03:24 von
Beiträge: 24
ID: 1.335.659
ID: 1.335.659
Aufrufe heute: 0
Gesamt: 3.256
Gesamt: 3.256
Aktive User: 0
ISIN: US10501E2019 · WKN: A12BXW · Symbol: GHDN
0,5050
EUR
+1,71 %
+0,0085 EUR
Letzter Kurs 29.04.24 Tradegate
Neuigkeiten
31.12.23 · Business Wire (engl.) |
28.12.23 · Business Wire (engl.) |
20.11.23 · Business Wire (engl.) |
14.11.23 · Business Wire (engl.) |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,2000 | +65,41 | |
| 4,7450 | +35,57 | |
| 5,0200 | +26,13 | |
| 1,2200 | +18,45 | |
| 56,08 | +18,34 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,6050 | -18,24 | |
| 1,9850 | -18,65 | |
| 6,5500 | -19,14 | |
| 3,9900 | -21,30 | |
| 2,3100 | -25,00 |
Beitrag zu dieser Diskussion schreiben
Brainstorm Cell Therapeutics
Brainstorm Cell Therapeutics Aktie > 0,7060 EUR -- +34,48 % / +0,1810 EU .. ist weiterhin gut im Kurs ....
Hallo Zusammen, ist hier jemand im Bild?
BrainStorm gibt positive Topline-Daten in Phase-2-Studie zur Bewertung von NurOwn® zur Behandlung von progressiver MS bekannt
NurOwn® erwies sich als sicher und gut verträglich
Klinisch bedeutsame Verbesserungen bei den funktionellen Endpunkten der MS
Auf Twitter teilen Auf LinkedIn teilen Auf Pinterest teilen
New York (ots / PRNewswire) - BrainStorm Cell Therapeutics Inc. (NASDAQ: BCLI), ein führender Entwickler von adulten Stammzelltherapien für neurodegenerative Erkrankungen, gab heute die wichtigsten Daten aus der Phase-2-Studie des Unternehmens bekannt, in der drei wiederholte Verabreichungen von NurOwn® (MSC-NTF-Zellen) im Abstand von jeweils 2 Monaten zur Behandlung von progressiver Multipler Sklerose (MS). Die Studie erreichte den primären Endpunkt der Sicherheit und es wurden Verbesserungen bei sekundären Endpunkten beobachtet, die sich über neurologische Funktionen, Kognition und Biomarker erstrecken.
"Dies ist ein äußerst aufregendes Ergebnis, da es das Potenzial unserer proprietären Zelltherapie NurOwn bei progressiver MS demonstriert und die Evidenz erweitert, die die NurOwn®-Technologieplattform bei neurodegenerativen Erkrankungen unterstützt", sagte Chaim Lebovits, Chief Executive Officer von BrainStorm. "Wir schätzen die Bemühungen des Brainstorm-Teams sowie das Engagement und die Fachkenntnisse der Standorte für klinische Studien und Patienten, die trotz der durch die COVID-19-Pandemie verursachten Herausforderungen an dieser wichtigen Studie teilgenommen haben. Wir planen, die Ergebnisse dieser Studie vollständig zu bewerten und zu überprüfen." die Daten mit der wissenschaftlichen Gemeinschaft der MS und hoffentlich NurOwn als wichtige therapeutische Option für Patienten mit progressiver MS weiter voranzutreiben. "
BrainStorm_Logo
BrainStorm_Logo
An der 28-wöchigen offenen klinischen Phase-2-Studie nahmen 20 primäre und sekundäre progressive MS-Patienten teil, die auf den 2017 überarbeiteten McDonald-Kriterien im Alter von 18 bis 65 Jahren basierten. Die EDSS-Werte (Expanded Disability Status Scale) lagen zwischen 3 und 6,5, ohne dass dies nachgewiesen wurde Rückfall innerhalb von 6 Monaten nach der Registrierung, in der Lage, in 60 Sekunden oder weniger 25 Fuß zu gehen und eine stabile Dosis einer krankheitsmodifizierenden Therapie erhalten zu dürfen.
Von den 20 eingeschlossenen Patienten wurden 18 behandelt und 16 (80%) beendeten die Studie. Zwei Patienten wurden aufgrund von verfahrensbedingten Nebenwirkungen abgesetzt. Es gab keine Todesfälle oder Nebenwirkungen in der Studie im Zusammenhang mit einer Verschlechterung der Multiplen Sklerose. Das Durchschnittsalter der Studienpatienten betrug 47 Jahre, 56% waren weiblich und der durchschnittliche EDSS-Ausgangswert betrug 5,4 Jahre. In der klinischen Studie wurden die Ergebnisse der klinischen Wirksamkeit mit einer mit 48 Patienten übereinstimmenden klinischen Kohorte aus den umfassenden Längsschnittuntersuchungen bei MS im Brigham & Woman's Hospital (CLIMB-Studie) verglichen.
Zu den MS-Funktions- und Erkennungsmaßnahmen in den Top-Line-Ergebnissen gehörte der zeitgesteuerte 25-Fuß-Spaziergang (T25FW); 9-Loch-Stifttest (9-HPT); Low Contrast Letter Acuity (LCLA); Symbol Digit Modality Test (SDMT); und die 12-teilige MS Walking Scale (MSWS-12). Vorgegebene 25% ige Verbesserungen des zeitgesteuerten 25-Fuß-Gehens (T25FW) und des 9-Loch-Peg-Tests (9-HPT) vom Ausgangswert bis zu 28 Wochen wurden bei 14% bzw. 13% der mit NurOwn behandelten Patienten beobachtet und bei 0 % der vordefinierten übereinstimmenden historischen Steuerelemente in der CLIMB-Registrierung. 38 Prozent der mit NurOwn behandelten Patienten zeigten eine Verbesserung des MSWS-12 um mindestens 10 Punkte gegenüber dem Ausgangswert bis zur 28. Woche. Ein Patient berichtete über ein Ergebnis, das die Gehfunktion bewertet. Darüber hinaus zeigten 47% der behandelten Patienten im kontrastarmen Buchstabenschärfetest (LCLA), einem visuellen Funktionstest, über 28 Wochen eine Verbesserung um mindestens 8 Buchstaben, und 67% zeigten eine Verbesserung der Symbolziffer um mindestens 3 Punkte Modalitätstest (SDMT), ein Maß für die kognitive Verarbeitung.
Darüber hinaus zeigten mit NurOwn behandelte Patienten eine mittlere Verbesserung gegenüber dem Ausgangswert von 10% bei T25FW und eine Verbesserung von 4,8% gegenüber dem Ausgangswert bei der 9-HPT-dominanten Hand, verglichen mit einer Verschlechterung von 1,8% bzw. 1,4% bei übereinstimmenden historischen Kontrollen aus dem CLIMB-Register. Auch mit NurOwn behandelte Patienten zeigten eine 6% ige Verbesserung gegenüber dem Ausgangswert in MSWS-12. Alle angegebenen Ergebnisse basieren auf beobachteten Daten.
Cerebrospinalflüssigkeit (CSF) -Biomarker wurden zu 3 aufeinanderfolgenden Zeitpunkten unmittelbar vor jeder intrathekalen Verabreichung von NurOwn erhalten. Wir beobachteten eine Zunahme der neuroprotektiven Moleküle (VEGF, HGF) und eine Abnahme der neuroinflammatorischen Biomarker (MCP-1, SDF-1 und Osteopontin). Zusätzliche sekundäre Wirksamkeitsdaten sowie detaillierte CSF- und Blutbiomarker-Analysen sind derzeit im Gange und werden auf bevorstehenden wissenschaftlichen Sitzungen veröffentlicht.
"Diese positiven Ergebnisse zeigen das Potenzial von MSC-NTF-Zellen, Entzündungsmechanismen zu verringern, die Reparatur zu fördern und die Funktion bei progressiver MS wiederherzustellen, ein Zustand, für den ein großer Bedarf an wirksamer Therapie besteht", sagte Jeffrey Cohen, MD, Direktor für experimentelle Therapeutika , Cleveland Clinic Mellen Center für MS. Dr. Cohen berichtet über keine Angaben im Zusammenhang mit dieser Studie.
"Wir begrüßen Brainstorm für den Abschluss dieser ersten Studie an NurOwn am Menschen bei progressiver MS und werden durch die frühzeitige Angabe von Sicherheit und Wirksamkeit ermutigt", sagte Mark Allegretta, PhD, Vizepräsident für Forschung bei der National MS Society. "Wir hoffen, dass unsere Zusammenarbeit Einblicke in klinisch relevante Biomarker liefert, die einen Behandlungseffekt bei progressiver MS vorhersagen können."
Ralph Kern, MD MHSc, Präsident und Chief Medical Officer von Brainstorm, erklärte: "Die beispiellosen Ergebnisse dieser klinischen Phase-2-Studie unterstützen nachdrücklich das Potenzial von NurOwn, den ungedeckten klinischen und biologischen Bedarf bei progressiver MS zu decken. Derzeit gibt es nur wenige therapeutische Optionen Um das unaufhaltsame klinische Fortschreiten und die Anhäufung von Behinderungen, die anhaltende kompartimentierte und intrathekale ZNS-Entzündung und den fortschreitenden Verlust der neuralen Funktion bei progressiver MS anzugehen, planen wir, auf einem bevorstehenden wissenschaftlichen Treffen eine detaillierte Zusammenfassung der Studienergebnisse vorzulegen und unsere Ergebnisse in einem Peer zu veröffentlichen -überprüftes Journal und überlegen, wie NurOwn bei progressiver MS am besten weiterentwickelt werden kann. "
Stacy Lindborg Ph.D., EVP und Leiterin der globalen klinischen Forschung, fügte hinzu: "Wir freuen uns über die Konsistenz des Behandlungseffekts, der bei diesen funktionellen und kognitiven Maßnahmen bei Patienten beobachtet wurde, die entweder den Standard der Behandlung hatten oder zuvor mit einer bestehenden Krankheitsmodifikation behandelt wurden Unser Ziel war es, durch ein effizientes Design, das wir erfolgreich durchgeführt haben, einen Proof of Concept bei progressiver MS zu erreichen. Wir freuen uns auch über die Anhäufung von Beweisen und die Bestätigung des Wirkungsmechanismus von NurOwn durch CSF-Biomarkerdaten bei Patienten mit mehreren neurodegenerativen Erkrankungen. ""
Studiendesign
Die Phase-2-NurOwn®-Studie war eine multizentrische, offene Studie zur Bewertung der Sicherheit und Wirksamkeit von NurOwn® bei 20 progressiven MS-Patienten in vier MS-Kompetenzzentren: Cleveland Clinic, Mount Sinai School of Medicine, Stanford und USC. Progressive MS-Patienten wurden gescreent, erhielten eine Einverständniserklärung und erhielten nach einer Einlaufzeit von 10 Wochen drei intrathekale Verabreichungen von 100-125 Millionen autologen MSC-NTF-Zellen in Intervallen von 2 Monaten. Die Patienten wurden nach der ersten Behandlung 28 Wochen lang beobachtet. Der primäre Endpunkt der Studie war die Sicherheit. Zu den sekundären Endpunkten gehörten funktionelle und kognitive Maßnahmen sowie die Modulation von CSF- und Blutbiomarkern (neurotrophe Faktoren, neurodegenerative und entzündliche Biomarker). Zu den bewerteten Ergebnissen gehörten: Zeitgesteuerte 25-Fuß-Gehgeschwindigkeit (T25FW); Erweiterte Disability Status Scale (EDSS); 9-Loch-Peg-Test (9HPT); Low Contrast Letter Acuity (LCLA); Symbol Digit Modality Test (SDMT); die 12-teilige MS Walking Scale (MSWS-12); durchschnittliche tägliche Schrittzahl (unter Verwendung eines tragbaren Sensors); und quantitative MRT-Messungen. Weitere Informationen finden Sie unter ClinicalTrials.gov Identifier: NCT03799718. Die National Multiple Sclerosis Society erhielt im Rahmen ihres Fast-Forward-Programms einen Zuschuss in Höhe von 495.000 USD, um die offene multizentrische klinische Phase-2-Studie zur wiederholten intrathekalen Verabreichung von NurOwn® (autologe MSC-NTF-Zellen) bei progressiven Teilnehmern zu unterstützen Multiple Sklerose.
NurOwn® erwies sich als sicher und gut verträglich
Klinisch bedeutsame Verbesserungen bei den funktionellen Endpunkten der MS
Auf Twitter teilen Auf LinkedIn teilen Auf Pinterest teilen
New York (ots / PRNewswire) - BrainStorm Cell Therapeutics Inc. (NASDAQ: BCLI), ein führender Entwickler von adulten Stammzelltherapien für neurodegenerative Erkrankungen, gab heute die wichtigsten Daten aus der Phase-2-Studie des Unternehmens bekannt, in der drei wiederholte Verabreichungen von NurOwn® (MSC-NTF-Zellen) im Abstand von jeweils 2 Monaten zur Behandlung von progressiver Multipler Sklerose (MS). Die Studie erreichte den primären Endpunkt der Sicherheit und es wurden Verbesserungen bei sekundären Endpunkten beobachtet, die sich über neurologische Funktionen, Kognition und Biomarker erstrecken.
"Dies ist ein äußerst aufregendes Ergebnis, da es das Potenzial unserer proprietären Zelltherapie NurOwn bei progressiver MS demonstriert und die Evidenz erweitert, die die NurOwn®-Technologieplattform bei neurodegenerativen Erkrankungen unterstützt", sagte Chaim Lebovits, Chief Executive Officer von BrainStorm. "Wir schätzen die Bemühungen des Brainstorm-Teams sowie das Engagement und die Fachkenntnisse der Standorte für klinische Studien und Patienten, die trotz der durch die COVID-19-Pandemie verursachten Herausforderungen an dieser wichtigen Studie teilgenommen haben. Wir planen, die Ergebnisse dieser Studie vollständig zu bewerten und zu überprüfen." die Daten mit der wissenschaftlichen Gemeinschaft der MS und hoffentlich NurOwn als wichtige therapeutische Option für Patienten mit progressiver MS weiter voranzutreiben. "
BrainStorm_Logo
BrainStorm_Logo
An der 28-wöchigen offenen klinischen Phase-2-Studie nahmen 20 primäre und sekundäre progressive MS-Patienten teil, die auf den 2017 überarbeiteten McDonald-Kriterien im Alter von 18 bis 65 Jahren basierten. Die EDSS-Werte (Expanded Disability Status Scale) lagen zwischen 3 und 6,5, ohne dass dies nachgewiesen wurde Rückfall innerhalb von 6 Monaten nach der Registrierung, in der Lage, in 60 Sekunden oder weniger 25 Fuß zu gehen und eine stabile Dosis einer krankheitsmodifizierenden Therapie erhalten zu dürfen.
Von den 20 eingeschlossenen Patienten wurden 18 behandelt und 16 (80%) beendeten die Studie. Zwei Patienten wurden aufgrund von verfahrensbedingten Nebenwirkungen abgesetzt. Es gab keine Todesfälle oder Nebenwirkungen in der Studie im Zusammenhang mit einer Verschlechterung der Multiplen Sklerose. Das Durchschnittsalter der Studienpatienten betrug 47 Jahre, 56% waren weiblich und der durchschnittliche EDSS-Ausgangswert betrug 5,4 Jahre. In der klinischen Studie wurden die Ergebnisse der klinischen Wirksamkeit mit einer mit 48 Patienten übereinstimmenden klinischen Kohorte aus den umfassenden Längsschnittuntersuchungen bei MS im Brigham & Woman's Hospital (CLIMB-Studie) verglichen.
Zu den MS-Funktions- und Erkennungsmaßnahmen in den Top-Line-Ergebnissen gehörte der zeitgesteuerte 25-Fuß-Spaziergang (T25FW); 9-Loch-Stifttest (9-HPT); Low Contrast Letter Acuity (LCLA); Symbol Digit Modality Test (SDMT); und die 12-teilige MS Walking Scale (MSWS-12). Vorgegebene 25% ige Verbesserungen des zeitgesteuerten 25-Fuß-Gehens (T25FW) und des 9-Loch-Peg-Tests (9-HPT) vom Ausgangswert bis zu 28 Wochen wurden bei 14% bzw. 13% der mit NurOwn behandelten Patienten beobachtet und bei 0 % der vordefinierten übereinstimmenden historischen Steuerelemente in der CLIMB-Registrierung. 38 Prozent der mit NurOwn behandelten Patienten zeigten eine Verbesserung des MSWS-12 um mindestens 10 Punkte gegenüber dem Ausgangswert bis zur 28. Woche. Ein Patient berichtete über ein Ergebnis, das die Gehfunktion bewertet. Darüber hinaus zeigten 47% der behandelten Patienten im kontrastarmen Buchstabenschärfetest (LCLA), einem visuellen Funktionstest, über 28 Wochen eine Verbesserung um mindestens 8 Buchstaben, und 67% zeigten eine Verbesserung der Symbolziffer um mindestens 3 Punkte Modalitätstest (SDMT), ein Maß für die kognitive Verarbeitung.
Darüber hinaus zeigten mit NurOwn behandelte Patienten eine mittlere Verbesserung gegenüber dem Ausgangswert von 10% bei T25FW und eine Verbesserung von 4,8% gegenüber dem Ausgangswert bei der 9-HPT-dominanten Hand, verglichen mit einer Verschlechterung von 1,8% bzw. 1,4% bei übereinstimmenden historischen Kontrollen aus dem CLIMB-Register. Auch mit NurOwn behandelte Patienten zeigten eine 6% ige Verbesserung gegenüber dem Ausgangswert in MSWS-12. Alle angegebenen Ergebnisse basieren auf beobachteten Daten.
Cerebrospinalflüssigkeit (CSF) -Biomarker wurden zu 3 aufeinanderfolgenden Zeitpunkten unmittelbar vor jeder intrathekalen Verabreichung von NurOwn erhalten. Wir beobachteten eine Zunahme der neuroprotektiven Moleküle (VEGF, HGF) und eine Abnahme der neuroinflammatorischen Biomarker (MCP-1, SDF-1 und Osteopontin). Zusätzliche sekundäre Wirksamkeitsdaten sowie detaillierte CSF- und Blutbiomarker-Analysen sind derzeit im Gange und werden auf bevorstehenden wissenschaftlichen Sitzungen veröffentlicht.
"Diese positiven Ergebnisse zeigen das Potenzial von MSC-NTF-Zellen, Entzündungsmechanismen zu verringern, die Reparatur zu fördern und die Funktion bei progressiver MS wiederherzustellen, ein Zustand, für den ein großer Bedarf an wirksamer Therapie besteht", sagte Jeffrey Cohen, MD, Direktor für experimentelle Therapeutika , Cleveland Clinic Mellen Center für MS. Dr. Cohen berichtet über keine Angaben im Zusammenhang mit dieser Studie.
"Wir begrüßen Brainstorm für den Abschluss dieser ersten Studie an NurOwn am Menschen bei progressiver MS und werden durch die frühzeitige Angabe von Sicherheit und Wirksamkeit ermutigt", sagte Mark Allegretta, PhD, Vizepräsident für Forschung bei der National MS Society. "Wir hoffen, dass unsere Zusammenarbeit Einblicke in klinisch relevante Biomarker liefert, die einen Behandlungseffekt bei progressiver MS vorhersagen können."
Ralph Kern, MD MHSc, Präsident und Chief Medical Officer von Brainstorm, erklärte: "Die beispiellosen Ergebnisse dieser klinischen Phase-2-Studie unterstützen nachdrücklich das Potenzial von NurOwn, den ungedeckten klinischen und biologischen Bedarf bei progressiver MS zu decken. Derzeit gibt es nur wenige therapeutische Optionen Um das unaufhaltsame klinische Fortschreiten und die Anhäufung von Behinderungen, die anhaltende kompartimentierte und intrathekale ZNS-Entzündung und den fortschreitenden Verlust der neuralen Funktion bei progressiver MS anzugehen, planen wir, auf einem bevorstehenden wissenschaftlichen Treffen eine detaillierte Zusammenfassung der Studienergebnisse vorzulegen und unsere Ergebnisse in einem Peer zu veröffentlichen -überprüftes Journal und überlegen, wie NurOwn bei progressiver MS am besten weiterentwickelt werden kann. "
Stacy Lindborg Ph.D., EVP und Leiterin der globalen klinischen Forschung, fügte hinzu: "Wir freuen uns über die Konsistenz des Behandlungseffekts, der bei diesen funktionellen und kognitiven Maßnahmen bei Patienten beobachtet wurde, die entweder den Standard der Behandlung hatten oder zuvor mit einer bestehenden Krankheitsmodifikation behandelt wurden Unser Ziel war es, durch ein effizientes Design, das wir erfolgreich durchgeführt haben, einen Proof of Concept bei progressiver MS zu erreichen. Wir freuen uns auch über die Anhäufung von Beweisen und die Bestätigung des Wirkungsmechanismus von NurOwn durch CSF-Biomarkerdaten bei Patienten mit mehreren neurodegenerativen Erkrankungen. ""
Studiendesign
Die Phase-2-NurOwn®-Studie war eine multizentrische, offene Studie zur Bewertung der Sicherheit und Wirksamkeit von NurOwn® bei 20 progressiven MS-Patienten in vier MS-Kompetenzzentren: Cleveland Clinic, Mount Sinai School of Medicine, Stanford und USC. Progressive MS-Patienten wurden gescreent, erhielten eine Einverständniserklärung und erhielten nach einer Einlaufzeit von 10 Wochen drei intrathekale Verabreichungen von 100-125 Millionen autologen MSC-NTF-Zellen in Intervallen von 2 Monaten. Die Patienten wurden nach der ersten Behandlung 28 Wochen lang beobachtet. Der primäre Endpunkt der Studie war die Sicherheit. Zu den sekundären Endpunkten gehörten funktionelle und kognitive Maßnahmen sowie die Modulation von CSF- und Blutbiomarkern (neurotrophe Faktoren, neurodegenerative und entzündliche Biomarker). Zu den bewerteten Ergebnissen gehörten: Zeitgesteuerte 25-Fuß-Gehgeschwindigkeit (T25FW); Erweiterte Disability Status Scale (EDSS); 9-Loch-Peg-Test (9HPT); Low Contrast Letter Acuity (LCLA); Symbol Digit Modality Test (SDMT); die 12-teilige MS Walking Scale (MSWS-12); durchschnittliche tägliche Schrittzahl (unter Verwendung eines tragbaren Sensors); und quantitative MRT-Messungen. Weitere Informationen finden Sie unter ClinicalTrials.gov Identifier: NCT03799718. Die National Multiple Sclerosis Society erhielt im Rahmen ihres Fast-Forward-Programms einen Zuschuss in Höhe von 495.000 USD, um die offene multizentrische klinische Phase-2-Studie zur wiederholten intrathekalen Verabreichung von NurOwn® (autologe MSC-NTF-Zellen) bei progressiven Teilnehmern zu unterstützen Multiple Sklerose.
Antwort auf Beitrag Nr.: 67.581.312 von 7schwarzerosen am 24.03.21 12:34:03https://ir.brainstorm-cell.com/2021-03-24-BrainStorm-Announc…
Es geht los !
Heute über 30% im Plus .
Ich habe noch keine News gefunden.
Was geht ab ?
Heute über 30% im Plus .
Ich habe noch keine News gefunden.
Was geht ab ?

Der MACD hat im Daily die Signallinie nach oben gekreuzt:
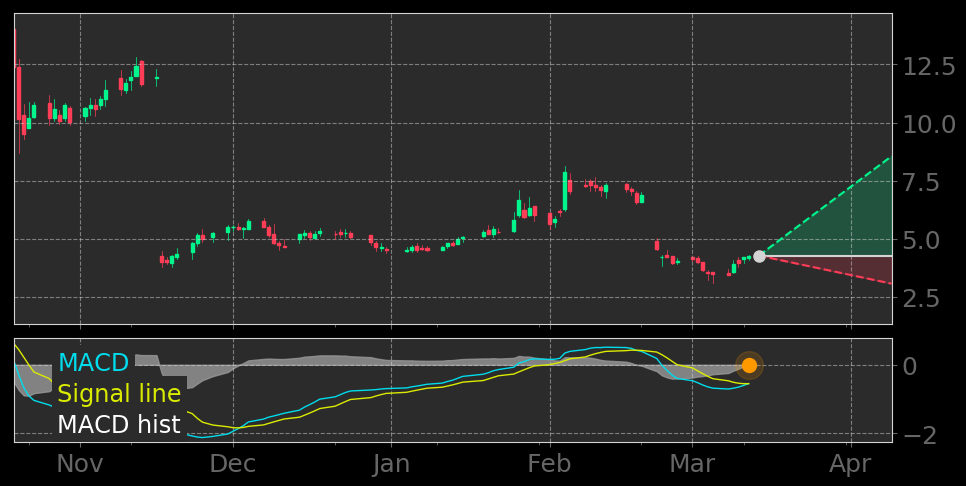
💡
Antwort auf Beitrag Nr.: 67.240.470 von Malecon am 28.02.21 16:39:01
Gestern hat meiner Meinung nach der Kurs nach oben gedreht und ich bin eingestiegen.
Ich denke der Kurs hat gedreht.
Ich bin dann mal dabei.Gestern hat meiner Meinung nach der Kurs nach oben gedreht und ich bin eingestiegen.
Bei Brainstorm Cell Therapeutics Inc gibt's zwei Lücken nach oben und der Kurs hat den bisherigen Boden (bei ca. $ 4) erreicht, hoffentlich hält dieser:
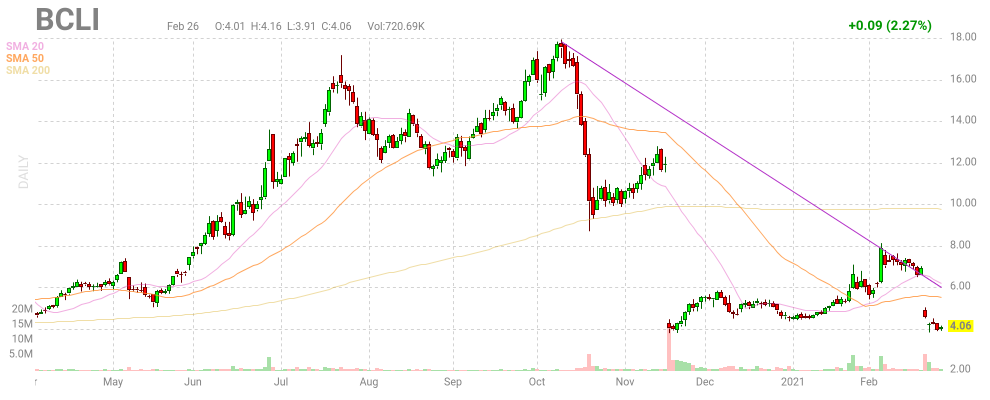
Wobei es sich dabei um Matrjoschka-Kurslücken handelt (eine in der anderen).
Das Ziel war eigentlich die große Lücke zu schließen und es lief zuerst ganz gut, aber dann ist die zweite Lücke entstanden, interessanterweise nicht etwa aufgrund der Nasdaq-Schwäche sondern nach einer negativen Nachricht.
Wie man sieht, sind in diesen Tagen viele Aktien so oder so günstiger als vor einem Monat zu haben. Wer Cash bereithält, für den sind das paradiesische Zeiten und eine große Auswahl.
💡





















