Xoma 200-Prozent-Chance !!!! ????? !!!!! - 500 Beiträge pro Seite (Seite 20)
eröffnet am 17.08.03 12:35:15 von
neuester Beitrag 18.04.17 18:55:14 von
neuester Beitrag 18.04.17 18:55:14 von
Beiträge: 16.519
ID: 765.494
ID: 765.494
Aufrufe heute: 2
Gesamt: 856.993
Gesamt: 856.993
Aktive User: 0
ISIN: US98419J2069 · WKN: A2ATUH
23,300
EUR
+2,64 %
+0,600 EUR
Letzter Kurs 22:33:12 Lang & Schwarz
Neuigkeiten
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,4700 | +31,38 | |
| 14,000 | +30,96 | |
| 2,7300 | +23,53 | |
| 1,3200 | +22,22 | |
| 2,7500 | +22,22 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,6200 | -17,77 | |
| 0,5350 | -20,15 | |
| 2,2000 | -21,43 | |
| 5,0000 | -37,34 | |
| 0,9700 | -71,47 |
Neu auf dem Markt
Interleukin-Antikörper Canakinumab
Canakinumab (Ilaris®) ist ein humaner monoklonaler Antikörper gegen Interleukin-1 beta. Es kommt zur Behandlung von Patienten ab vier Jahren auf den Markt, die an einem der drei Cryopyrin-assoziierten periodischen Syndrome (CAPS) leiden.
CAPS sind eine Gruppe von schweren autoimmunen entzündlichen Krankheiten, bei denen das Gen NLRP3 auf Chromosom 1 defekt ist, das für das Protein Cryopyrin kodiert. Unter anderem kommt es dadurch zu einer gesteigerten Bildung von Interleukin-1 beta (IL-1 beta), das eine Schlüsselrolle bei Entzündungen und Gewebezerstörung spielt. Die seltenen Erbkrankheiten werden autosomal-dominant vererbt. Die Patienten, die schon im Säuglingsalter erkranken können, leiden unter chronischer Müdigkeit, Fieber und Arthralgien. Von den Entzündungen sind besonders Haut, Augen, Knochen und Gelenke betroffen. Da es nur wenige Patienten mit CAPS gibt, erhielt Canakinumab den Status als Arzneimittel für seltene Leiden, Orphan drug.
Die klinische Wirksamkeit von Canakinumab beruht auf der selektiven und langfristigen Blockade von Interleukin-1 beta, das eine Schlüsselrolle bei Entzündungen und Gewebezerstörung spielt. Ilaris® wird alle acht Wochen subkutan injiziert. In der placebokontrollierten klinischen Zulassungstudie mit 35 CAPS-Patienten führte Canakinumab in einer Dosis von 150 mg innerhalb von sieben Tagen zu einem ein vollständigen Abklingen oder zu einer klinisch signifikanten Besserung der Symptome. Auch die Laborparameter normalisierten sich schnell innerhalb von wenigen Tagen nach der Injektion. Canakinumab führte bei 90 Prozent der Patienten zu einer raschen und anhaltenden Remission und verhinderte weitere Krankheitsschübe. Bei den ersten vier Patienten mit durchgehender Verabreichung von Canakinumab wurde bis jetzt eine anhaltende Wirksamkeit über mehr als drei Jahre verzeichnet.
Die häufigsten Nebenwirkungen waren Nasen- und Rachenentzündung (Nasopharyngitis), Schwindel (Vertigo) und Reaktionen an der Injektionsstelle. Canakinumab erhöht das Risiko von Infektionen. Bei Patienten mit einer aktiven, behandlungsbedürftigen schweren Infektion darf die Behandlung mit Canakinumab nicht eingeleitet oder weitergeführt werden. Auch sollte es nicht gleichzeitig mit TNF-Inhibitoren angewendet werden, da sich dadurch das Risiko für schwerwiegende Infektionen erhöhen könnte. Während der Behandlung mit Canakinumab sollten möglichst keine Lebendimpfstoffe verabreicht werden.
Ursprünglich wurde Canakinumab für die Behandlung der rheumatoiden Arthritis entwickelt, bei der ebenfalls entzündliche Reaktionen durch IL-1 beta eine Rolle spielen. Andere Einsatzmöglichkeiten sind Gicht und Typ-2-Diabetes. Zur Behandlung der chronisch obstruktiven Lungenerkrankung (COPD) befindet sich der Wirkstoff in Phase I der klinischen Entwicklung.
Quellen:
Fachinformation von Ilaris®, Stand Oktober 2009
Lachmann HJ, et al.: Use of canakinumab in the cryopyrin-associated periodic syndrome. N. Engl. J. Med. 2009;360:2416-25.
Dr. Bettina Hellwig / 07.01.2010, 06:50 Uhr
Sie können die News auch als RSS-Feed abonnieren:
RSS-Feed Tagesnews Alle
RSS-Feed Tagesnews Pharmazie
Hier finden Sie weitere Informationen zum RSS-Feed der DAZ.online.
http://www.deutsche-apotheker-zeitung.de/pharmazie/news/2010…
Interleukin-Antikörper Canakinumab
Canakinumab (Ilaris®) ist ein humaner monoklonaler Antikörper gegen Interleukin-1 beta. Es kommt zur Behandlung von Patienten ab vier Jahren auf den Markt, die an einem der drei Cryopyrin-assoziierten periodischen Syndrome (CAPS) leiden.
CAPS sind eine Gruppe von schweren autoimmunen entzündlichen Krankheiten, bei denen das Gen NLRP3 auf Chromosom 1 defekt ist, das für das Protein Cryopyrin kodiert. Unter anderem kommt es dadurch zu einer gesteigerten Bildung von Interleukin-1 beta (IL-1 beta), das eine Schlüsselrolle bei Entzündungen und Gewebezerstörung spielt. Die seltenen Erbkrankheiten werden autosomal-dominant vererbt. Die Patienten, die schon im Säuglingsalter erkranken können, leiden unter chronischer Müdigkeit, Fieber und Arthralgien. Von den Entzündungen sind besonders Haut, Augen, Knochen und Gelenke betroffen. Da es nur wenige Patienten mit CAPS gibt, erhielt Canakinumab den Status als Arzneimittel für seltene Leiden, Orphan drug.
Die klinische Wirksamkeit von Canakinumab beruht auf der selektiven und langfristigen Blockade von Interleukin-1 beta, das eine Schlüsselrolle bei Entzündungen und Gewebezerstörung spielt. Ilaris® wird alle acht Wochen subkutan injiziert. In der placebokontrollierten klinischen Zulassungstudie mit 35 CAPS-Patienten führte Canakinumab in einer Dosis von 150 mg innerhalb von sieben Tagen zu einem ein vollständigen Abklingen oder zu einer klinisch signifikanten Besserung der Symptome. Auch die Laborparameter normalisierten sich schnell innerhalb von wenigen Tagen nach der Injektion. Canakinumab führte bei 90 Prozent der Patienten zu einer raschen und anhaltenden Remission und verhinderte weitere Krankheitsschübe. Bei den ersten vier Patienten mit durchgehender Verabreichung von Canakinumab wurde bis jetzt eine anhaltende Wirksamkeit über mehr als drei Jahre verzeichnet.
Die häufigsten Nebenwirkungen waren Nasen- und Rachenentzündung (Nasopharyngitis), Schwindel (Vertigo) und Reaktionen an der Injektionsstelle. Canakinumab erhöht das Risiko von Infektionen. Bei Patienten mit einer aktiven, behandlungsbedürftigen schweren Infektion darf die Behandlung mit Canakinumab nicht eingeleitet oder weitergeführt werden. Auch sollte es nicht gleichzeitig mit TNF-Inhibitoren angewendet werden, da sich dadurch das Risiko für schwerwiegende Infektionen erhöhen könnte. Während der Behandlung mit Canakinumab sollten möglichst keine Lebendimpfstoffe verabreicht werden.
Ursprünglich wurde Canakinumab für die Behandlung der rheumatoiden Arthritis entwickelt, bei der ebenfalls entzündliche Reaktionen durch IL-1 beta eine Rolle spielen. Andere Einsatzmöglichkeiten sind Gicht und Typ-2-Diabetes. Zur Behandlung der chronisch obstruktiven Lungenerkrankung (COPD) befindet sich der Wirkstoff in Phase I der klinischen Entwicklung.
Quellen:
Fachinformation von Ilaris®, Stand Oktober 2009
Lachmann HJ, et al.: Use of canakinumab in the cryopyrin-associated periodic syndrome. N. Engl. J. Med. 2009;360:2416-25.
Dr. Bettina Hellwig / 07.01.2010, 06:50 Uhr
Sie können die News auch als RSS-Feed abonnieren:
RSS-Feed Tagesnews Alle
RSS-Feed Tagesnews Pharmazie
Hier finden Sie weitere Informationen zum RSS-Feed der DAZ.online.
http://www.deutsche-apotheker-zeitung.de/pharmazie/news/2010…
Mal ein paar Fakten zu Ilaris, um das Marktpotential zu erkennen:
Novartis erhält die Zulassung von Ilaris für die Behandlung von CAPS. Wir haben hierfür einen weltweiten Umsatz von USD 50 Mio. eingerechnet.
http://www.boerse-go.de/nachricht/Novartis-Gutes-Ergebnis-vo…
"Sollte das Medikament nun auch bei der Behandlung einer weitverbreiteten Erkrankung wie Gicht wirksam sein, könnte das jährliche Umsatzpotenzial um rund 500 Mio steigen, sagte Andrew Weiss, ein Analyst der Zürcher Bank Vontobel."
http://webcache.googleusercontent.com/search?q=cache:ZotCeRB….
Ist doch mal interessant: Novartis vertreibt Ilaris zur Behandlung von CAPS mit einem anzustrebenden Umsatz von 50 Mio USD (wahrscheinlich jährlich!?). Somit scheint die Produktion auf einem so niedrigen Niveau bereits ökonomisch interessant zu sein. Man stelle sich jedoch mal den Milliardenmarkt der Rheumatoiden Arthritis oder den Zig-Milliardenmarkt des Diabetes mellitus oder der KHK vor.
Macht Euch mal selbst gedanken über das Potential von XOMA 052!
Grüsse, ER
Novartis erhält die Zulassung von Ilaris für die Behandlung von CAPS. Wir haben hierfür einen weltweiten Umsatz von USD 50 Mio. eingerechnet.
http://www.boerse-go.de/nachricht/Novartis-Gutes-Ergebnis-vo…
"Sollte das Medikament nun auch bei der Behandlung einer weitverbreiteten Erkrankung wie Gicht wirksam sein, könnte das jährliche Umsatzpotenzial um rund 500 Mio steigen, sagte Andrew Weiss, ein Analyst der Zürcher Bank Vontobel."
http://webcache.googleusercontent.com/search?q=cache:ZotCeRB….
Ist doch mal interessant: Novartis vertreibt Ilaris zur Behandlung von CAPS mit einem anzustrebenden Umsatz von 50 Mio USD (wahrscheinlich jährlich!?). Somit scheint die Produktion auf einem so niedrigen Niveau bereits ökonomisch interessant zu sein. Man stelle sich jedoch mal den Milliardenmarkt der Rheumatoiden Arthritis oder den Zig-Milliardenmarkt des Diabetes mellitus oder der KHK vor.
Macht Euch mal selbst gedanken über das Potential von XOMA 052!
Grüsse, ER
Zu erwartende Ergebnisse 2010 und 2011 entsprechend der XOMA-Präsentation:
Type 2 diabetes:
XOMA 052 -Phase 2a, 2b
•
Canakinumab -Phase 2/3 Novartis
•
LY2189102 -Phase 2a Lilly
•
Type 1 diabetes:•
XOMA 052 -Phase 2
•
Anakinra -Phase 2 Biovitrum
•
Gicht:•
Canakinumab -Phase 2b, 3
•
Rilonacept -Phase 3
•
KHK:•
XOMA 052 -Phase 2
•
Anakinra-Phase 2
•
http://www.xoma.com/media/files/XOMA%20Presentation.pdf
Das Rennen zwischen den Entwicklern der "IL-1-beta-Blocker" ist also noch vollkommen offen und XOMA ist vorne mit dabei!
Type 2 diabetes:
XOMA 052 -Phase 2a, 2b
•
Canakinumab -Phase 2/3 Novartis
•
LY2189102 -Phase 2a Lilly
•
Type 1 diabetes:•
XOMA 052 -Phase 2
•
Anakinra -Phase 2 Biovitrum
•
Gicht:•
Canakinumab -Phase 2b, 3
•
Rilonacept -Phase 3
•
KHK:•
XOMA 052 -Phase 2
•
Anakinra-Phase 2
•
http://www.xoma.com/media/files/XOMA%20Presentation.pdf
Das Rennen zwischen den Entwicklern der "IL-1-beta-Blocker" ist also noch vollkommen offen und XOMA ist vorne mit dabei!
Zum Stand von XOMA im Vergleich mit der Konkurenz:
Targeting interleukin-1 in the clinic
Nature Reviews Immunology 10, 89-102 (February 2010)
http://www.nature.com/nri/journal/v10/n2/box/nri2691_BX3.htm…
Targeting interleukin-1 in the clinic
Nature Reviews Immunology 10, 89-102 (February 2010)
http://www.nature.com/nri/journal/v10/n2/box/nri2691_BX3.htm…
Noch ein Artikel zu den antiinflamatorischen Wirkstoffen im Vergleich:
http://cmbi.bjmu.edu.cn/news/insight/temp/21.pdf
http://cmbi.bjmu.edu.cn/news/insight/temp/21.pdf
Antwort auf Beitrag Nr.: 39.444.802 von extremrelaxer am 03.05.10 14:20:34Die häufigsten Nebenwirkungen waren Nasen- und Rachenentzündung (Nasopharyngitis), Schwindel (Vertigo) und Reaktionen an der Injektionsstelle. Canakinumab erhöht das Risiko von Infektionen.
Da hat Xoma 052 schon einmal die Nase vorn.
Aus dem Bericht Phase I Xoma 052:
Special categories:
•No serious infections reported.
•No reports of drug-related hypoglycemia
•No evidence of neutropenia
•Injection site reactions: mild and no different from placebo
Da hat Xoma 052 schon einmal die Nase vorn.
Aus dem Bericht Phase I Xoma 052:
Special categories:
•No serious infections reported.
•No reports of drug-related hypoglycemia
•No evidence of neutropenia
•Injection site reactions: mild and no different from placebo
Antwort auf Beitrag Nr.: 39.445.450 von kontaktfenster am 03.05.10 15:47:16@ kontaktfenster: Korrekt! Und genau das hat mich ja auch so erstaunt! Keinerlei ernsthafte Infektionen: angesichts der Überwachu8ngszeit von ca 3 Monaten und der Fallzahl von 81 Probanden / Patienten ist das doch sehr aussergewöhnlich und lässt m.E. eine hohe Sicherheit vermuten!
Das witzige an der Story (und deshalb habe ich hier auch die ganzen Links mal reingestellt) ist, dass der m.E. am meisten ernstzunehmende Konkurrent Canakinumab (Ilaris von Novartis) erst überhaupt nicht für die Anwendung bei Gicht, Diabetes oder der KHK entwickelt wurde und sich dann wohl erst nachträglich die Erkenntnis eingeschlichen hat, dass dieser AK auch bei diesen
Erkrankungen einen Effekt hat. Hierdurch hat sich das potentielle Umsatzpotential mal eben ca verhundertfacht. Learning by doing also, try and error! Da scheint mir die Erprobung von XOMA 052 doch wesentlich geplanter zu laufen.
Grüsse, ER
Discl.: Alles nur meine persönliche Meinung und Interpretation. Irrtum vorbehalten. Keine Handelsaufforderung!
Das witzige an der Story (und deshalb habe ich hier auch die ganzen Links mal reingestellt) ist, dass der m.E. am meisten ernstzunehmende Konkurrent Canakinumab (Ilaris von Novartis) erst überhaupt nicht für die Anwendung bei Gicht, Diabetes oder der KHK entwickelt wurde und sich dann wohl erst nachträglich die Erkenntnis eingeschlichen hat, dass dieser AK auch bei diesen
Erkrankungen einen Effekt hat. Hierdurch hat sich das potentielle Umsatzpotential mal eben ca verhundertfacht. Learning by doing also, try and error! Da scheint mir die Erprobung von XOMA 052 doch wesentlich geplanter zu laufen.
Grüsse, ER
Discl.: Alles nur meine persönliche Meinung und Interpretation. Irrtum vorbehalten. Keine Handelsaufforderung!
Antwort auf Beitrag Nr.: 39.445.979 von extremrelaxer am 03.05.10 16:43:09hi ich habe xoma auf der watchlist?
ab und zu schaue ich hier rein!
nun meine frage,wie ist den xoma kapitalmässig aufgestellt.
weil wenn du bei xomas medikament ein milliarden umsatz siehst.
dann hat der kurs bei erfolg,einen potenzial von 1000prozent
oder irre ich mich!
VIELEN DANK
ab und zu schaue ich hier rein!
nun meine frage,wie ist den xoma kapitalmässig aufgestellt.
weil wenn du bei xomas medikament ein milliarden umsatz siehst.
dann hat der kurs bei erfolg,einen potenzial von 1000prozent

oder irre ich mich!
VIELEN DANK

Hat ja ziemlich gedauert, bis der Deckel bei 0,68 geflogen ist. Auf weiterhin grüne Tage, mal sehen, wie lange die shorties das Spiel noch durchhalten.
Antwort auf Beitrag Nr.: 39.448.101 von kontaktfenster am 03.05.10 21:26:11Shorties grillen ???
Bin zwar kein Sadist, aber in diesem Fall könnte man schwach werden
Bin zwar kein Sadist, aber in diesem Fall könnte man schwach werden

Antwort auf Beitrag Nr.: 39.445.979 von extremrelaxer am 03.05.10 16:43:09vielen dank für das recherchieren!
Nochmal ein Artikel zu den beiden anderen "IL-1-beta-Blockern" (ich nenne die Gruppe jetzt einfach mal so, weil ich die offizielle / spezifische Bezeichnung dieser neuen Medikamentengruppe nicht kenne).
III. Rilonacept und Canakinumab
Rilonacept (RIC) ist ein dimeres Fusionsprotein, bestehend aus der Liganden bindenden Domäne des IL-1 Rezeptors und dem IL-1 Rezeptor akzessorischen Protein gebunden an humanes IgG1. RIC bindet an IL-1β und blockiert dadurch seine Wirkung. RIC erhielt im Februar 2008 eine Zulassung durch die amerikanische FDA unter dem "Orphan Drug Status“ für die Behandlung der seltenen genetischen Cryopyrin-assoziierten periodischen Syndrome (CAPS)(Tab. 1). Eine „positive opinion for orphan designation“ für RIC bei CAPS wurde durch die „European Medicines Agency (EMEA)“ im Juli 2008 ausgesprochen. Die Dosierung von RIC in kontrollierten Studien lag bei einer initialen Gabe von 320 mg gefolgt von wöchentlichen Gaben von 160 mg als s.c. Injektionen [50;51].
Canakinumab (CAM) ist ein voll humaner monoklonaler Antikörper, der an IL-1β bindet und dieses neutralisiert. In frühen klinischen Studien ergaben sich Hinweise für eine Wirksamkeit bei CAPS und bei einer Untergruppe von Patienten mit RA [52] (Dosierung s. unten).
Studien mit Rilonacept
In einer Pilotstudie entwickelten fünf erwachsene Patienten mit FCAS (vgl. Tab. 1) unter Rilonacept (RIC) (Initialdosis 300 mg s.c. 1x/Woche, Erhaltungsdosis 100 mg/Woche) signifikante Besserungen der klinischen Symptomatik (Fieber, Exanthem, Arthralgien) und der Laborentzündungsparameter (BKS, CRP, SAA), jedoch erreichten sie keine Remission [50]. Bei Dosiserhöhung auf 160 RIC 1x/Woche erreichte ein Patient eine Remission für Klinik und Entzündungsparameter, während sich bei den vier anderen Patienten auch unter 320 mg RIC/Woche die klinischen und Entzündungslaborbefunde nicht von denen unter 160 mg 1x/Woche unterschieden.
In einer anderen Studie erhielten 47 erwachsene CAPS-Patienten (44 FCAS, 3 MWS) 6 Wochen lang entweder 160 mg RIC /Woche (n=23) oder Placebo (n=24) [51]. Als primärer Endpunkt diente die mittlere Änderung eines eigens entwickelten Evaluationsscore („daily health assessment form“, DHAF) vom Ausgangswert [53]. Der Ausgangswert wurde nur bei 13% der Placebogruppe, aber bei 84% der RIC-Gruppe gebessert; auch bei weiteren Effektivitätsparametern schnitt die RIC-Gruppe signifikant besser ab einschließlich der Entzündungsparameter CRP und SAA. In einer Verlängerungsphase wurden die unter RIC erreichten Verbesserungen unter Weiterführung der RIC-Therapie aufrechterhalten (P <0,0001 gegenüber Placebo). Durch die persistierend normalen SAA-Werte unter RIC-Therapie wurde das Amyloidose-Risiko reduziert. Allerdings fehlen weitere Untersuchungen, die diesen Effekt für MWS-Patienten in der Praxis bestätigen. In der Studie handelt es sich in 94% um FCAS-Patienten (s.o.), die hinsichtlich einer AA-Amyloidose wesentlich weniger gefährdet sind als MWS-Patienten.
Opportunistische Infektionen oder Infektionen, die eine parenterale antibiotische Therapie erfordern, wurden nicht beobachtet. Infektionen wie obere Luftwegsinfekte oder Harnwegsinfekte wurden in der Verumgruppe häufiger beobachtet (48% gegenüber 17% unter Placebo). Lokale Reaktionen an der Einstichstelle stellten ansonsten den größten Anteil an unerwünschten Wirkungen dar.
Da für Kinder unter 12 Jahren keine Daten zu Sicherheit und Effektivität vorliegen, wird eine Therapie in dieser Altersgruppe nicht befürwortet. Für das CINCA-/NOMID-Syndrom, der gravierendsten CAPS-Variante, das in die Zulassungsstudie nicht einbezogen war, ist RIC ebenfalls nicht zugelassen.
Studien mit Canakinumab
In einer Phase III-Studie erhielten 35 CAPS-Patienten (9-74 Jahre, 33/35 hatten MWS) während der ersten zwei Monate eine einzelne subkutane Canakinumab (CAM)-Injektion (Studienteil 1), auf die 34 der 35 Patienten mit schneller Besserung der klinischen und Laborparameter reagierten [54]. Die 31 Patienten, bei denen dieser Effekt länger persistierte, erhielten über sechs Monate alle zwei Monate entweder CAM oder Placebo (Studienteil 2). Bei Auftreten eines Erkrankungsschubes unter dieser Therapie beendete der betreffende Patient diesen randomisierten, placebo-kontrollierten Studienteil und erhielt die Möglichkeit, in einer viermonatigen Extensionsphase mit CAM behandelt zu werden (Studienteil 3). Während Studienteil 2 erlitt kein Patient unter CAM einen Krankheitsschub, jedoch 81% der mit Placebo behandelten Patienten (p<0,001). Ebenso normalisierten sich CRP und SAA bei den verum-behandelten Patienten, während unter Placebo ein signifikanter Anstieg dieser Parameter beobachtet wurde. Den Studienteil 3 beendeten 28 der 31 Patienten (90%) in Remission.
An unerwünschten Arzneimittel-Wirkungen (UAW) wurden am häufigsten obere Luftwegsinfekte gesehen. Zwei schwere UAWs („SAE“) wurden während des Studienteils 3 beobachtet (2 von 31, 7%) und führten zum Therapieabbruch: ein Patient entwickelte eine Urosepsis, ein weiterer ein akutes Glaukom mit einseitiger Erblindung (wurde der Erkrankung zugeschrieben) sowie Vertigo.
In eine offene Phase II-Dosiseskalationsstudie wurden 19 Kinder und Jugendliche (4-19 Jahre) mit aktiver systemischer JIA (SJIA) einbezogen und erhielten 0,5-9 mg CAM/kg KG mit erneuter Injektion bei erneutem Krankheitsschub, wobei die Dauer bis zur erneuten Exazerbation zwischen 23 und >200 Tagen betrug [55]. Elf der 19 Patienten zeigten einen Therapieerfolg (primärer Endpunkt: ACR Pediatric criteria 30). Am 15.Tag nach Injektion zeigten alle elf Patienten ein Ansprechen entsprechend „ACR Pediatric 50“. Vier der 11 Patienten erreichten ein klinisches Remissionsstadium (keine Arthritis, kein Fieber, normales CRP, keine Krankheitsaktivität nach Arzteinschätzung). Ein Patient entwickelte ein blutendes Magenulcus; andere schwere UAW wurden nicht berichtet.
Für das MWS stellt CAM eine wegen der selteneren Injektionsfrequenz interessante Variante zu ANR dar. In der CAPS-Studie wurde nur ein Patient mit der schwersten CAPS-Variante, dem CINCA-/NOMID-Syndrom (vgl. Tab. 1), berücksichtigt [54].
Die Ansprechrate bei SJIA scheint unter CAM in ähnlicher Größenordnung zu liegen wie unter ANR. Die seltenere Injektionsfrequenz (zweimonatlich) stellt für die Kinder im Vergleich zu ANR (tägliche Injektion) eine bedeutsame Verbesserung dar. Im Falle unerwünschter Wirkungen, z.B. schwere Infektion, ist jedoch wegen der langen Halbwertszeit von einer größeren Gefährdung auszugehen.
Bemerkung: Rilonacept und Canakinumab sind noch nicht in Deutschland verfügbar (Stand August 2009).
Geschäftsstelle, 17.09.2009
http://dgrh.de/anakinrarilonacept.html
Anhand der von mir eingestellten Artikel dürften wir jetz mal folgende Basisinformationen haben:
- direkte Konkurrenten von XOMA 052
- Vergleichbarkeit der Studienergebnisse bzgl. Wirkung, Nebenwirkungen, Dosierung, Dosierungsintervallen...
- Anwendungsspektrum und damit verbundenes Umsatzpotential
Leider fehlt noch die Übersichjtlichkeit. Mir fehlt leider momentan die Zeit, die Ergebnisse im Vergleich zusammenzufassen. Vielleicht kann ja der eine oder andere Investierte mal versuchen, eine Zusammenfassung zu beginnen, die wir dann zusammen ergänzen könnten, um Umsatzpotential, Marktchancen, Stärken und Schwächen der einzelnen Präparate vergleichen zu können und damit unser Investment auf Chancen und Risiken mal abzuklopfen!?
Bin für jeden Beitrag dankbar!
Grüsse, ER
III. Rilonacept und Canakinumab
Rilonacept (RIC) ist ein dimeres Fusionsprotein, bestehend aus der Liganden bindenden Domäne des IL-1 Rezeptors und dem IL-1 Rezeptor akzessorischen Protein gebunden an humanes IgG1. RIC bindet an IL-1β und blockiert dadurch seine Wirkung. RIC erhielt im Februar 2008 eine Zulassung durch die amerikanische FDA unter dem "Orphan Drug Status“ für die Behandlung der seltenen genetischen Cryopyrin-assoziierten periodischen Syndrome (CAPS)(Tab. 1). Eine „positive opinion for orphan designation“ für RIC bei CAPS wurde durch die „European Medicines Agency (EMEA)“ im Juli 2008 ausgesprochen. Die Dosierung von RIC in kontrollierten Studien lag bei einer initialen Gabe von 320 mg gefolgt von wöchentlichen Gaben von 160 mg als s.c. Injektionen [50;51].
Canakinumab (CAM) ist ein voll humaner monoklonaler Antikörper, der an IL-1β bindet und dieses neutralisiert. In frühen klinischen Studien ergaben sich Hinweise für eine Wirksamkeit bei CAPS und bei einer Untergruppe von Patienten mit RA [52] (Dosierung s. unten).
Studien mit Rilonacept
In einer Pilotstudie entwickelten fünf erwachsene Patienten mit FCAS (vgl. Tab. 1) unter Rilonacept (RIC) (Initialdosis 300 mg s.c. 1x/Woche, Erhaltungsdosis 100 mg/Woche) signifikante Besserungen der klinischen Symptomatik (Fieber, Exanthem, Arthralgien) und der Laborentzündungsparameter (BKS, CRP, SAA), jedoch erreichten sie keine Remission [50]. Bei Dosiserhöhung auf 160 RIC 1x/Woche erreichte ein Patient eine Remission für Klinik und Entzündungsparameter, während sich bei den vier anderen Patienten auch unter 320 mg RIC/Woche die klinischen und Entzündungslaborbefunde nicht von denen unter 160 mg 1x/Woche unterschieden.
In einer anderen Studie erhielten 47 erwachsene CAPS-Patienten (44 FCAS, 3 MWS) 6 Wochen lang entweder 160 mg RIC /Woche (n=23) oder Placebo (n=24) [51]. Als primärer Endpunkt diente die mittlere Änderung eines eigens entwickelten Evaluationsscore („daily health assessment form“, DHAF) vom Ausgangswert [53]. Der Ausgangswert wurde nur bei 13% der Placebogruppe, aber bei 84% der RIC-Gruppe gebessert; auch bei weiteren Effektivitätsparametern schnitt die RIC-Gruppe signifikant besser ab einschließlich der Entzündungsparameter CRP und SAA. In einer Verlängerungsphase wurden die unter RIC erreichten Verbesserungen unter Weiterführung der RIC-Therapie aufrechterhalten (P <0,0001 gegenüber Placebo). Durch die persistierend normalen SAA-Werte unter RIC-Therapie wurde das Amyloidose-Risiko reduziert. Allerdings fehlen weitere Untersuchungen, die diesen Effekt für MWS-Patienten in der Praxis bestätigen. In der Studie handelt es sich in 94% um FCAS-Patienten (s.o.), die hinsichtlich einer AA-Amyloidose wesentlich weniger gefährdet sind als MWS-Patienten.
Opportunistische Infektionen oder Infektionen, die eine parenterale antibiotische Therapie erfordern, wurden nicht beobachtet. Infektionen wie obere Luftwegsinfekte oder Harnwegsinfekte wurden in der Verumgruppe häufiger beobachtet (48% gegenüber 17% unter Placebo). Lokale Reaktionen an der Einstichstelle stellten ansonsten den größten Anteil an unerwünschten Wirkungen dar.
Da für Kinder unter 12 Jahren keine Daten zu Sicherheit und Effektivität vorliegen, wird eine Therapie in dieser Altersgruppe nicht befürwortet. Für das CINCA-/NOMID-Syndrom, der gravierendsten CAPS-Variante, das in die Zulassungsstudie nicht einbezogen war, ist RIC ebenfalls nicht zugelassen.
Studien mit Canakinumab
In einer Phase III-Studie erhielten 35 CAPS-Patienten (9-74 Jahre, 33/35 hatten MWS) während der ersten zwei Monate eine einzelne subkutane Canakinumab (CAM)-Injektion (Studienteil 1), auf die 34 der 35 Patienten mit schneller Besserung der klinischen und Laborparameter reagierten [54]. Die 31 Patienten, bei denen dieser Effekt länger persistierte, erhielten über sechs Monate alle zwei Monate entweder CAM oder Placebo (Studienteil 2). Bei Auftreten eines Erkrankungsschubes unter dieser Therapie beendete der betreffende Patient diesen randomisierten, placebo-kontrollierten Studienteil und erhielt die Möglichkeit, in einer viermonatigen Extensionsphase mit CAM behandelt zu werden (Studienteil 3). Während Studienteil 2 erlitt kein Patient unter CAM einen Krankheitsschub, jedoch 81% der mit Placebo behandelten Patienten (p<0,001). Ebenso normalisierten sich CRP und SAA bei den verum-behandelten Patienten, während unter Placebo ein signifikanter Anstieg dieser Parameter beobachtet wurde. Den Studienteil 3 beendeten 28 der 31 Patienten (90%) in Remission.
An unerwünschten Arzneimittel-Wirkungen (UAW) wurden am häufigsten obere Luftwegsinfekte gesehen. Zwei schwere UAWs („SAE“) wurden während des Studienteils 3 beobachtet (2 von 31, 7%) und führten zum Therapieabbruch: ein Patient entwickelte eine Urosepsis, ein weiterer ein akutes Glaukom mit einseitiger Erblindung (wurde der Erkrankung zugeschrieben) sowie Vertigo.
In eine offene Phase II-Dosiseskalationsstudie wurden 19 Kinder und Jugendliche (4-19 Jahre) mit aktiver systemischer JIA (SJIA) einbezogen und erhielten 0,5-9 mg CAM/kg KG mit erneuter Injektion bei erneutem Krankheitsschub, wobei die Dauer bis zur erneuten Exazerbation zwischen 23 und >200 Tagen betrug [55]. Elf der 19 Patienten zeigten einen Therapieerfolg (primärer Endpunkt: ACR Pediatric criteria 30). Am 15.Tag nach Injektion zeigten alle elf Patienten ein Ansprechen entsprechend „ACR Pediatric 50“. Vier der 11 Patienten erreichten ein klinisches Remissionsstadium (keine Arthritis, kein Fieber, normales CRP, keine Krankheitsaktivität nach Arzteinschätzung). Ein Patient entwickelte ein blutendes Magenulcus; andere schwere UAW wurden nicht berichtet.
Für das MWS stellt CAM eine wegen der selteneren Injektionsfrequenz interessante Variante zu ANR dar. In der CAPS-Studie wurde nur ein Patient mit der schwersten CAPS-Variante, dem CINCA-/NOMID-Syndrom (vgl. Tab. 1), berücksichtigt [54].
Die Ansprechrate bei SJIA scheint unter CAM in ähnlicher Größenordnung zu liegen wie unter ANR. Die seltenere Injektionsfrequenz (zweimonatlich) stellt für die Kinder im Vergleich zu ANR (tägliche Injektion) eine bedeutsame Verbesserung dar. Im Falle unerwünschter Wirkungen, z.B. schwere Infektion, ist jedoch wegen der langen Halbwertszeit von einer größeren Gefährdung auszugehen.
Bemerkung: Rilonacept und Canakinumab sind noch nicht in Deutschland verfügbar (Stand August 2009).
Geschäftsstelle, 17.09.2009
http://dgrh.de/anakinrarilonacept.html
Anhand der von mir eingestellten Artikel dürften wir jetz mal folgende Basisinformationen haben:
- direkte Konkurrenten von XOMA 052
- Vergleichbarkeit der Studienergebnisse bzgl. Wirkung, Nebenwirkungen, Dosierung, Dosierungsintervallen...
- Anwendungsspektrum und damit verbundenes Umsatzpotential
Leider fehlt noch die Übersichjtlichkeit. Mir fehlt leider momentan die Zeit, die Ergebnisse im Vergleich zusammenzufassen. Vielleicht kann ja der eine oder andere Investierte mal versuchen, eine Zusammenfassung zu beginnen, die wir dann zusammen ergänzen könnten, um Umsatzpotential, Marktchancen, Stärken und Schwächen der einzelnen Präparate vergleichen zu können und damit unser Investment auf Chancen und Risiken mal abzuklopfen!?
Bin für jeden Beitrag dankbar!
Grüsse, ER
Sorry, hier nochmal der selbe Artikel mit entsprechenden Markierungen:
III. Rilonacept und Canakinumab
Rilonacept (RIC) ist ein dimeres Fusionsprotein, bestehend aus der Liganden bindenden Domäne des IL-1 Rezeptors und dem IL-1 Rezeptor akzessorischen Protein gebunden an humanes IgG1. RIC bindet an IL-1β und blockiert dadurch seine Wirkung. RIC erhielt im Februar 2008 eine Zulassung durch die amerikanische FDA unter dem "Orphan Drug Status“ für die Behandlung der seltenen genetischen Cryopyrin-assoziierten periodischen Syndrome (CAPS) (Tab. 1). Eine „positive opinion for orphan designation“ für RIC bei CAPS wurde durch die „European Medicines Agency (EMEA)“ im Juli 2008 ausgesprochen. Die Dosierung von RIC in kontrollierten Studien lag bei einer initialen Gabe von 320 mg gefolgt von wöchentlichen Gaben von 160 mg als s.c. Injektionen [50;51].
Canakinumab (CAM) ist ein voll humaner monoklonaler Antikörper, der an IL-1β bindet und dieses neutralisiert. In frühen klinischen Studien ergaben sich Hinweise für eine Wirksamkeit bei CAPS und bei einer Untergruppe von Patienten mit RA [52] (Dosierung s. unten).
Studien mit Rilonacept
In einer Pilotstudie entwickelten fünf erwachsene Patienten mit FCAS (vgl. Tab. 1) unter Rilonacept (RIC) (Initialdosis 300 mg s.c. 1x/Woche, Erhaltungsdosis 100 mg/Woche) signifikante Besserungen der klinischen Symptomatik (Fieber, Exanthem, Arthralgien) und der Laborentzündungsparameter (BKS, CRP, SAA), jedoch erreichten sie keine Remission [50]. Bei Dosiserhöhung auf 160 RIC 1x/Woche erreichte ein Patient eine Remission für Klinik und Entzündungsparameter, während sich bei den vier anderen Patienten auch unter 320 mg RIC/Woche die klinischen und Entzündungslaborbefunde nicht von denen unter 160 mg 1x/Woche unterschieden.
In einer anderen Studie erhielten 47 erwachsene CAPS-Patienten (44 FCAS, 3 MWS) 6 Wochen lang entweder 160 mg RIC /Woche (n=23) oder Placebo (n=24) [51]. Als primärer Endpunkt diente die mittlere Änderung eines eigens entwickelten Evaluationsscore („daily health assessment form“, DHAF) vom Ausgangswert [53]. Der Ausgangswert wurde nur bei 13% der Placebogruppe, aber bei 84% der RIC-Gruppe gebessert; auch bei weiteren Effektivitätsparametern schnitt die RIC-Gruppe signifikant besser ab einschließlich der Entzündungsparameter CRP und SAA. In einer Verlängerungsphase wurden die unter RIC erreichten Verbesserungen unter Weiterführung der RIC-Therapie aufrechterhalten (P <0,0001 gegenüber Placebo). Durch die persistierend normalen SAA-Werte unter RIC-Therapie wurde das Amyloidose-Risiko reduziert. Allerdings fehlen weitere Untersuchungen, die diesen Effekt für MWS-Patienten in der Praxis bestätigen. In der Studie handelt es sich in 94% um FCAS-Patienten (s.o.), die hinsichtlich einer AA-Amyloidose wesentlich weniger gefährdet sind als MWS-Patienten.
Opportunistische Infektionen oder Infektionen, die eine parenterale antibiotische Therapie erfordern, wurden nicht beobachtet. Infektionen wie obere Luftwegsinfekte oder Harnwegsinfekte wurden in der Verumgruppe häufiger beobachtet (48% gegenüber 17% unter Placebo). Lokale Reaktionen an der Einstichstelle stellten ansonsten den größten Anteil an unerwünschten Wirkungen dar.
Da für Kinder unter 12 Jahren keine Daten zu Sicherheit und Effektivität vorliegen, wird eine Therapie in dieser Altersgruppe nicht befürwortet. Für das CINCA-/NOMID-Syndrom, der gravierendsten CAPS-Variante, das in die Zulassungsstudie nicht einbezogen war, ist RIC ebenfalls nicht zugelassen.
Studien mit Canakinumab
In einer Phase III-Studie erhielten 35 CAPS-Patienten (9-74 Jahre, 33/35 hatten MWS) während der ersten zwei Monate eine einzelne subkutane Canakinumab (CAM)-Injektion (Studienteil 1), auf die 34 der 35 Patienten mit schneller Besserung der klinischen und Laborparameter reagierten [54]. Die 31 Patienten, bei denen dieser Effekt länger persistierte, erhielten über sechs Monate alle zwei Monate entweder CAM oder Placebo (Studienteil 2). Bei Auftreten eines Erkrankungsschubes unter dieser Therapie beendete der betreffende Patient diesen randomisierten, placebo-kontrollierten Studienteil und erhielt die Möglichkeit, in einer viermonatigen Extensionsphase mit CAM behandelt zu werden (Studienteil 3). Während Studienteil 2 erlitt kein Patient unter CAM einen Krankheitsschub, jedoch 81% der mit Placebo behandelten Patienten (p<0,001). Ebenso normalisierten sich CRP und SAA bei den verum-behandelten Patienten, während unter Placebo ein signifikanter Anstieg dieser Parameter beobachtet wurde. Den Studienteil 3 beendeten 28 der 31 Patienten (90%) in Remission.
An unerwünschten Arzneimittel-Wirkungen (UAW) wurden am häufigsten obere Luftwegsinfekte gesehen. Zwei schwere UAWs („SAE“) wurden während des Studienteils 3 beobachtet (2 von 31, 7%) und führten zum Therapieabbruch: ein Patient entwickelte eine Urosepsis, ein weiterer ein akutes Glaukom mit einseitiger Erblindung (wurde der Erkrankung zugeschrieben) sowie Vertigo.
In eine offene Phase II-Dosiseskalationsstudie wurden 19 Kinder und Jugendliche (4-19 Jahre) mit aktiver systemischer JIA (SJIA) einbezogen und erhielten 0,5-9 mg CAM/kg KG mit erneuter Injektion bei erneutem Krankheitsschub, wobei die Dauer bis zur erneuten Exazerbation zwischen 23 und >200 Tagen betrug [55]. Elf der 19 Patienten zeigten einen Therapieerfolg (primärer Endpunkt: ACR Pediatric criteria 30). Am 15.Tag nach Injektion zeigten alle elf Patienten ein Ansprechen entsprechend „ACR Pediatric 50“. Vier der 11 Patienten erreichten ein klinisches Remissionsstadium (keine Arthritis, kein Fieber, normales CRP, keine Krankheitsaktivität nach Arzteinschätzung). Ein Patient entwickelte ein blutendes Magenulcus; andere schwere UAW wurden nicht berichtet.
Für das MWS stellt CAM eine wegen der selteneren Injektionsfrequenz interessante Variante zu ANR dar. In der CAPS-Studie wurde nur ein Patient mit der schwersten CAPS-Variante, dem CINCA-/NOMID-Syndrom (vgl. Tab. 1), berücksichtigt [54].
Die Ansprechrate bei SJIA scheint unter CAM in ähnlicher Größenordnung zu liegen wie unter ANR. Die seltenere Injektionsfrequenz (zweimonatlich) stellt für die Kinder im Vergleich zu ANR (tägliche Injektion) eine bedeutsame Verbesserung dar. Im Falle unerwünschter Wirkungen, z.B. schwere Infektion, ist jedoch wegen der langen Halbwertszeit von einer größeren Gefährdung auszugehen.
Bemerkung: Rilonacept und Canakinumab sind noch nicht in Deutschland verfügbar (Stand August 2009).
III. Rilonacept und Canakinumab
Rilonacept (RIC) ist ein dimeres Fusionsprotein, bestehend aus der Liganden bindenden Domäne des IL-1 Rezeptors und dem IL-1 Rezeptor akzessorischen Protein gebunden an humanes IgG1. RIC bindet an IL-1β und blockiert dadurch seine Wirkung. RIC erhielt im Februar 2008 eine Zulassung durch die amerikanische FDA unter dem "Orphan Drug Status“ für die Behandlung der seltenen genetischen Cryopyrin-assoziierten periodischen Syndrome (CAPS) (Tab. 1). Eine „positive opinion for orphan designation“ für RIC bei CAPS wurde durch die „European Medicines Agency (EMEA)“ im Juli 2008 ausgesprochen. Die Dosierung von RIC in kontrollierten Studien lag bei einer initialen Gabe von 320 mg gefolgt von wöchentlichen Gaben von 160 mg als s.c. Injektionen [50;51].
Canakinumab (CAM) ist ein voll humaner monoklonaler Antikörper, der an IL-1β bindet und dieses neutralisiert. In frühen klinischen Studien ergaben sich Hinweise für eine Wirksamkeit bei CAPS und bei einer Untergruppe von Patienten mit RA [52] (Dosierung s. unten).
Studien mit Rilonacept
In einer Pilotstudie entwickelten fünf erwachsene Patienten mit FCAS (vgl. Tab. 1) unter Rilonacept (RIC) (Initialdosis 300 mg s.c. 1x/Woche, Erhaltungsdosis 100 mg/Woche) signifikante Besserungen der klinischen Symptomatik (Fieber, Exanthem, Arthralgien) und der Laborentzündungsparameter (BKS, CRP, SAA), jedoch erreichten sie keine Remission [50]. Bei Dosiserhöhung auf 160 RIC 1x/Woche erreichte ein Patient eine Remission für Klinik und Entzündungsparameter, während sich bei den vier anderen Patienten auch unter 320 mg RIC/Woche die klinischen und Entzündungslaborbefunde nicht von denen unter 160 mg 1x/Woche unterschieden.
In einer anderen Studie erhielten 47 erwachsene CAPS-Patienten (44 FCAS, 3 MWS) 6 Wochen lang entweder 160 mg RIC /Woche (n=23) oder Placebo (n=24) [51]. Als primärer Endpunkt diente die mittlere Änderung eines eigens entwickelten Evaluationsscore („daily health assessment form“, DHAF) vom Ausgangswert [53]. Der Ausgangswert wurde nur bei 13% der Placebogruppe, aber bei 84% der RIC-Gruppe gebessert; auch bei weiteren Effektivitätsparametern schnitt die RIC-Gruppe signifikant besser ab einschließlich der Entzündungsparameter CRP und SAA. In einer Verlängerungsphase wurden die unter RIC erreichten Verbesserungen unter Weiterführung der RIC-Therapie aufrechterhalten (P <0,0001 gegenüber Placebo). Durch die persistierend normalen SAA-Werte unter RIC-Therapie wurde das Amyloidose-Risiko reduziert. Allerdings fehlen weitere Untersuchungen, die diesen Effekt für MWS-Patienten in der Praxis bestätigen. In der Studie handelt es sich in 94% um FCAS-Patienten (s.o.), die hinsichtlich einer AA-Amyloidose wesentlich weniger gefährdet sind als MWS-Patienten.
Opportunistische Infektionen oder Infektionen, die eine parenterale antibiotische Therapie erfordern, wurden nicht beobachtet. Infektionen wie obere Luftwegsinfekte oder Harnwegsinfekte wurden in der Verumgruppe häufiger beobachtet (48% gegenüber 17% unter Placebo). Lokale Reaktionen an der Einstichstelle stellten ansonsten den größten Anteil an unerwünschten Wirkungen dar.
Da für Kinder unter 12 Jahren keine Daten zu Sicherheit und Effektivität vorliegen, wird eine Therapie in dieser Altersgruppe nicht befürwortet. Für das CINCA-/NOMID-Syndrom, der gravierendsten CAPS-Variante, das in die Zulassungsstudie nicht einbezogen war, ist RIC ebenfalls nicht zugelassen.
Studien mit Canakinumab
In einer Phase III-Studie erhielten 35 CAPS-Patienten (9-74 Jahre, 33/35 hatten MWS) während der ersten zwei Monate eine einzelne subkutane Canakinumab (CAM)-Injektion (Studienteil 1), auf die 34 der 35 Patienten mit schneller Besserung der klinischen und Laborparameter reagierten [54]. Die 31 Patienten, bei denen dieser Effekt länger persistierte, erhielten über sechs Monate alle zwei Monate entweder CAM oder Placebo (Studienteil 2). Bei Auftreten eines Erkrankungsschubes unter dieser Therapie beendete der betreffende Patient diesen randomisierten, placebo-kontrollierten Studienteil und erhielt die Möglichkeit, in einer viermonatigen Extensionsphase mit CAM behandelt zu werden (Studienteil 3). Während Studienteil 2 erlitt kein Patient unter CAM einen Krankheitsschub, jedoch 81% der mit Placebo behandelten Patienten (p<0,001). Ebenso normalisierten sich CRP und SAA bei den verum-behandelten Patienten, während unter Placebo ein signifikanter Anstieg dieser Parameter beobachtet wurde. Den Studienteil 3 beendeten 28 der 31 Patienten (90%) in Remission.
An unerwünschten Arzneimittel-Wirkungen (UAW) wurden am häufigsten obere Luftwegsinfekte gesehen. Zwei schwere UAWs („SAE“) wurden während des Studienteils 3 beobachtet (2 von 31, 7%) und führten zum Therapieabbruch: ein Patient entwickelte eine Urosepsis, ein weiterer ein akutes Glaukom mit einseitiger Erblindung (wurde der Erkrankung zugeschrieben) sowie Vertigo.
In eine offene Phase II-Dosiseskalationsstudie wurden 19 Kinder und Jugendliche (4-19 Jahre) mit aktiver systemischer JIA (SJIA) einbezogen und erhielten 0,5-9 mg CAM/kg KG mit erneuter Injektion bei erneutem Krankheitsschub, wobei die Dauer bis zur erneuten Exazerbation zwischen 23 und >200 Tagen betrug [55]. Elf der 19 Patienten zeigten einen Therapieerfolg (primärer Endpunkt: ACR Pediatric criteria 30). Am 15.Tag nach Injektion zeigten alle elf Patienten ein Ansprechen entsprechend „ACR Pediatric 50“. Vier der 11 Patienten erreichten ein klinisches Remissionsstadium (keine Arthritis, kein Fieber, normales CRP, keine Krankheitsaktivität nach Arzteinschätzung). Ein Patient entwickelte ein blutendes Magenulcus; andere schwere UAW wurden nicht berichtet.
Für das MWS stellt CAM eine wegen der selteneren Injektionsfrequenz interessante Variante zu ANR dar. In der CAPS-Studie wurde nur ein Patient mit der schwersten CAPS-Variante, dem CINCA-/NOMID-Syndrom (vgl. Tab. 1), berücksichtigt [54].
Die Ansprechrate bei SJIA scheint unter CAM in ähnlicher Größenordnung zu liegen wie unter ANR. Die seltenere Injektionsfrequenz (zweimonatlich) stellt für die Kinder im Vergleich zu ANR (tägliche Injektion) eine bedeutsame Verbesserung dar. Im Falle unerwünschter Wirkungen, z.B. schwere Infektion, ist jedoch wegen der langen Halbwertszeit von einer größeren Gefährdung auszugehen.
Bemerkung: Rilonacept und Canakinumab sind noch nicht in Deutschland verfügbar (Stand August 2009).
II. Empfehlungen zum Einsatz von Anakinra
1.Rheumatoide Arthritis
Die Zulassungsstudien für ANR bei RA umfassen eine doppelblinde Dosisfindungsstudie an 472 Patienten über 24 Wochen, bei der in der höchsten Dosisgruppe (150 mg/Tag) 43% der Patienten eine ACR-20-Response gegenüber 27% in der Placebo-Gruppe erreichten, und eine offene Extensionsphase über weitere 24 Wochen [2;3]. In einer weiteren Studie wurde bei 419 nicht ausreichend auf MTX ansprechenden Patienten zusätzlich ANR in unterschiedlichen Dosierungen oder Placebo gegeben. Bei einer Dosis von 1 mg/kg Körpergewicht zeigte sich ein signifikanter Unterschied zugunsten der Verumgruppe beim Prozentsatz der ACR 20 und ACR 50 Responder [4]. Eine Therapie mit ANR führte auch zu einer signifikanten Verlangsamung der radiologischen Progression gegenüber Placebo [5;6]. Daten zum Einsatz bei früher RA existieren bislang nicht. Trotz fehlender direkter Vergleichsstudien besteht Konsens darüber, dass ANR in der Behandlung der RA weniger effektiv ist als TNF-Blocker [7]. Bei einzelnen Patienten kann es durchaus befriedigende bis gute Wirksamkeit zeigen. In großen multizentrischen Studien wurde die Verträglichkeit von ANR untersucht. Es zeigte sich auch bei dreijähriger kontinuierlicher Applikation ein akzeptables Sicherheitsprofil. Bisher gibt es keine Hinweise auf eine erhöhte Tuberkuloseinzidenz durch ANR. Bei Vorliegen von Infekten sollte eine ANR-Therapie nicht begonnen bzw. eine laufende ANR-Therapie unterbrochen werden. Eine Wiederaufnahme der Therapie sollte erst nach adäquater Kontrolle der Infektion erfolgen. Von einer Kombination von TNF-Blockern und ANR wird abgeraten. Hautreaktionen an der Injektionsstelle treten anfangs bei bis zu 70% der Patienten auf. Sie erfordern meist keine Therapie und können trotz Fortführung der Behandlung schwächer werden [7].
Eine systematische Literaturrecherche (einbezogen werden fünf Studien mit 2846 RA-Patienten) bestätigteine moderate Wirksamkeit und ein ausreichendes Sicherheitsprofil von ANR bei RA-Patienten [8].
2.Adulter Morbus Still (M. Still)
Der M. Still im Erwachsenenalter ist gekennzeichnet durch rezidivierende Fieberschübe begleitet von flüchtigen Exanthemen, einer Pharyngitis, Ferritinerhöhung, oft auch LDH- und Transaminasenerhöhung, meist mit Arthralgien oder Arthritiden. Die Ätiologie ist unbekannt, in aktiven Krankheitsphasen wurden erhöhte Spiegel von TNF-alpha, IL-2, IL-6 und Interferon-gamma gefunden. Die proinflammatorischen Zytokine IL-1ß und IL-18, die früh in der Entzündungskaskade durch enzymatische Spaltung mittels Caspase-1 prozessiert werden, scheinen pathogenetisch eine übergeordnete Rolle zu spielen.
Im Jahr 2005 erschienen die ersten Fallberichte [9;10], die ein sehr gutes und rasches Ansprechen von Fieber und Entzündungsparametern beim adulten M. Still auf eine Therapie mit ANR beschreiben. Bis Ende 2008 wurde dies in Fallberichten oder offenen Studien bei über 50 Patienten in der Literatur bestätigt [11;12].
Die Verträglichkeit ist in den meisten Fällen gut. Allerdings gibt es auch zwei Berichte über Komplikationen bei adultem M. Still unter ANR-Therapie. Bei einem Patienten trat nach 3-monatiger, primär erfolgreicher Therapie eine rasch letal verlaufende dilatative Kardiomyopathie auf, ein anderer Patient entwickelte eine Schocklunge. Ob dies kausal auf die ANR-Therapie zurückzuführen ist oder ob diese lediglich nicht in der Lage war, die Grunderkrankung suffizient zu kontrollieren, ist noch offen [13;14]. Die überzeugenden Daten aus Fallserien begründen den Einsatz von ANR beim adulten M. Still nach unzureichendem Ansprechen einer konventionellen Therapie mit Glucocorticoiden und MTX oder anderen Immunsuppressiva, insbesondere in lebensbedrohlichen Situationen oder bei Patienten mit erheblicher Einschränkung der Lebensqualität [15].
3.Systemische juvenile idiopathische Arthritis
Eine prospektive offene Studie untersuchte die Wirksamkeit von ANR bei 15 Patienten mit adultem M. Still im Vergleich zu 20 Patienten mit systemischer juveniler idiopathischer Arthritis (SJIA) [11]. Es zeigte sich ein deutlich besseres Ansprechen der erwachsenen Patienten (9/15 Vollremissionen, 2/15 Non-Responder) gegenüber den Kindern (4/20 Vollremissionen, 10/20 Non-Responder). Bei jeweils 2 Patienten musste die Therapie wegen starker Hautreaktionen an der Injektionsstelle bzw. wegen Infektionen (Varizellen, Leishmaniasis) beendet werden.
In einer bislang nur in einem Abstrakt publizierten multizentrischen, placebokontrollierten Studie sprachen 8 von 12 Patienten (67%) der Verumgruppe auf ANR an gegenüber 1 von 12 Patienten in der Placebogruppe (8%) [16]. In der Literatur finden sich Berichte über insgesamt etwa 150 Jugendliche und Kinder, bei denen ANR zur Behandlung der SJIA eingesetzt wurde. Etwa 40-45% der Behandelten erreichten eine Vollremission (mit der Möglichkeit, Glucocorticoide und andere DMARDs abzusetzen), etwa 40% ein partielles Ansprechen, bei ca. 20% konnte kein Ansprechen beobachtet werden. Die Vergleichbarkeit dieser Daten wird durch unterschiedliche Dosierungen erschwert: in einigen Fallserien wurde ANR mit 1-2 mg/kg KG/Tag dosiert und nicht gesteigert, in anderen wurde die Dosis bei Nicht-Ansprechen auf 3-4 mg/kg KG/Tag erhöht. Ein besonderes Problem einer Therapie mit ANR bei Kleinkindern ist die täglich erforderliche subkutane Applikation, die erfahrungsgemäß allerdings bei gutem therapeutischem Ansprechen auch von Kleinkindern meist erstaunlich schnell akzeptiert wird.
An unerwünschten Wirkungen stehen lokale Reaktionen an der Einstichstelle der Häufigkeit nach an erster Stelle (›=1/10). Sie können so ausgeprägt sein, daß sie zum Therapieabbruch führen, nehmen nach vierwöchiger Therapie aber oft an Intensität ab (17-19). Besonders müssen infektiöse Komplikationen beachtet werden (Häufigkeit ›=1/100, <1/10) wie obere Luftwegsinfekte, Herpes labialis oder Gastroenteritiden, aber auch schwerwiegendere Infektionen, die eine stationäre Behandlung erfordern (11;18). Zweimal entwickelte sich unter ANR ein „Makrophagen Aktivierendes Syndrom“ (MAS) (17). In einem Fall wurde die ANR-Therapie nach Überstehen des MAS problemlos weitergeführt, im anderen Fall waren die Eltern zur Fortsetzung der ANR-Gabe nicht bereit.
Nach derzeitiger Datenlage einschließlich der Erfahrung eindrucksvoller Remissionen in einem nicht unbeträchtlichen Anteil der SJIA-Patienten (40-45%, s.o.) und der Tatsache, dass bislang keine Arzneimittel ähnlicher Effektivität für diese Erkrankung zur Verfügung stehen, sowie bei Kenntnis der insgesamt ansonsten ungünstigen Prognose, ist der Einsatz von ANR nach unzureichendem Ansprechen auf eine konventionelle Therapie (MTX, Glucocorticoide) begründet [18;20;21].
4.Hereditäre Autoinflammationssyndrome
Eine Übersicht über die Gruppe der hereditären Autoinflammationssyndrome (HAIS) mit den wesentlichen Symptomen und dem zugrunde liegenden Gendefekt gibt Tabelle 1. Diese Defekte führen zu Veränderungen der Produktion und Wirkung proinflammatorischer Zytokine, speziell des IL-1 und des TNF-alpha. Die Blockierung von IL-1 entspricht damit einer angestrebten „targeted therapy“.
Die HAIS manifestieren sich oft bereits im Kindesalter, das CINCA-/NOMID-Syndrom (Chronic Infantile Neurologic Cutaneous Arthropathy/Neonatal Onset Multisystem Inflammatory Disease) und das DIRA-Syndrom (Deficiency of the Interleukin-1-Receptor Antagonist) sogar schon im Neugeborenenalter [22;23]. Betroffen sind häufig die serösen Häute (Perikard, Pleura, Peritoneum), die Haut, Knochen/Periost und die Synovialmembran, aber auch Auge, Ohr und das ZNS können involviert sein [24]. Infolge der rezidivierenden, eventuell subklinisch verlaufenden Entzündungen stellt die Entwicklung einer Amyloid A (AA)-Amyloidose eine schwere Komplikation der HAIS dar [25]. Eine effektive Therapie stand vor Einführung der Biologika lediglich für das familiäre Mittelmeerfieber (FMF) zur Verfügung (Colchicin) [26;27]. Seit 2004 stellt die IL-1ß-Blockade ein zunehmend wichtiges Prinzip in der Behandlung der HAIS dar [28]. Anakinra (ANR) hat sich in Pilotstudien und Fallbeschreibungen besonders bei den Cryopyrin-assoziierten periodischen Syndromen (CAPS) als wirksam erwiesen (Tabelle 1, mehr), auch eine Verbesserung der Schwerhörigkeit und der ZNS-Manifestation konnten erzielt werden [28-35]. Eine Rückbildung CAPS-assoziierter AA-Amyloidosen unter ANR scheint möglich [36], doch entsprechende Langzeit-Studien fehlen. Auch beim DIRA-Syndrom, bei dem ein IL-1-Rezeptorantagonist-Mangel vorliegt, ist ANR effektiv [22]. - Kontrollierte Studien über die Effektivität von ANR bei den HAIS bzw. den CAPS wurden bislang nicht durchgeführt. ANR erwies sich auch bei FMF, HIDS (Hyper-IgD-Syndrom) und beim TRAPS (TNF Receptor Associated Periodic Syndrome) als effektiv [37-43] (Tabelle 1, mehr)
ANR oder andere zur IL-1ß-Blockade geeignete Medikamente (als Alternativen stehen demnächst Rilonacept und Canakinumab zur Verfügung, siehe Anhang) sollten wegen der ungünstigen Prognose bei MWS und CINCA-/NOMID-Syndrom, aber auch beim neu beschriebenen DIRA-Syndrom eingesetzt werden [22;36]. Bei FCAS sollte der Einsatz vom Verlauf abhängig gemacht werden. Bei therapieresistentem FMF, HIDS oder TRAPS kann ANR versucht werden. Die Dosierung beträgt 1-2 mg/kgKG/Tag (maximal 100 mg/Tag), oft reichen jedoch geringere Dosen als für die Behandlung der RA oder der SJIA aus [36;44].
5.Andere entzündlich-rheumatische Erkrankungen
Tabelle 2 (mehr) gibt einen Überblick über Fallberichte und offene Pilotstudien, die eine Wirksamkeit von ANR bei weiteren entzündlich-rheumatischen Erkrankungen beschreiben.
In kleinen Studien zur Therapie der Spondylitis ankylosans [45;46] und der Psoriasisarthritis [47;48] mit ANR konnte keine überzeugende Wirksamkeit nachgewiesen werden. Ebensowenig war in einer kontrollierten Therapiestudie bei polyarthritischen Verlaufsformen der JIA eine Überlegenheit von ANR gegenüber Placebo nachweisbar [49].
Geschäftsstelle, 17.09.2009
http://dgrh.de/anakinraeinsatz.html
1.Rheumatoide Arthritis
Die Zulassungsstudien für ANR bei RA umfassen eine doppelblinde Dosisfindungsstudie an 472 Patienten über 24 Wochen, bei der in der höchsten Dosisgruppe (150 mg/Tag) 43% der Patienten eine ACR-20-Response gegenüber 27% in der Placebo-Gruppe erreichten, und eine offene Extensionsphase über weitere 24 Wochen [2;3]. In einer weiteren Studie wurde bei 419 nicht ausreichend auf MTX ansprechenden Patienten zusätzlich ANR in unterschiedlichen Dosierungen oder Placebo gegeben. Bei einer Dosis von 1 mg/kg Körpergewicht zeigte sich ein signifikanter Unterschied zugunsten der Verumgruppe beim Prozentsatz der ACR 20 und ACR 50 Responder [4]. Eine Therapie mit ANR führte auch zu einer signifikanten Verlangsamung der radiologischen Progression gegenüber Placebo [5;6]. Daten zum Einsatz bei früher RA existieren bislang nicht. Trotz fehlender direkter Vergleichsstudien besteht Konsens darüber, dass ANR in der Behandlung der RA weniger effektiv ist als TNF-Blocker [7]. Bei einzelnen Patienten kann es durchaus befriedigende bis gute Wirksamkeit zeigen. In großen multizentrischen Studien wurde die Verträglichkeit von ANR untersucht. Es zeigte sich auch bei dreijähriger kontinuierlicher Applikation ein akzeptables Sicherheitsprofil. Bisher gibt es keine Hinweise auf eine erhöhte Tuberkuloseinzidenz durch ANR. Bei Vorliegen von Infekten sollte eine ANR-Therapie nicht begonnen bzw. eine laufende ANR-Therapie unterbrochen werden. Eine Wiederaufnahme der Therapie sollte erst nach adäquater Kontrolle der Infektion erfolgen. Von einer Kombination von TNF-Blockern und ANR wird abgeraten. Hautreaktionen an der Injektionsstelle treten anfangs bei bis zu 70% der Patienten auf. Sie erfordern meist keine Therapie und können trotz Fortführung der Behandlung schwächer werden [7].
Eine systematische Literaturrecherche (einbezogen werden fünf Studien mit 2846 RA-Patienten) bestätigteine moderate Wirksamkeit und ein ausreichendes Sicherheitsprofil von ANR bei RA-Patienten [8].
2.Adulter Morbus Still (M. Still)
Der M. Still im Erwachsenenalter ist gekennzeichnet durch rezidivierende Fieberschübe begleitet von flüchtigen Exanthemen, einer Pharyngitis, Ferritinerhöhung, oft auch LDH- und Transaminasenerhöhung, meist mit Arthralgien oder Arthritiden. Die Ätiologie ist unbekannt, in aktiven Krankheitsphasen wurden erhöhte Spiegel von TNF-alpha, IL-2, IL-6 und Interferon-gamma gefunden. Die proinflammatorischen Zytokine IL-1ß und IL-18, die früh in der Entzündungskaskade durch enzymatische Spaltung mittels Caspase-1 prozessiert werden, scheinen pathogenetisch eine übergeordnete Rolle zu spielen.
Im Jahr 2005 erschienen die ersten Fallberichte [9;10], die ein sehr gutes und rasches Ansprechen von Fieber und Entzündungsparametern beim adulten M. Still auf eine Therapie mit ANR beschreiben. Bis Ende 2008 wurde dies in Fallberichten oder offenen Studien bei über 50 Patienten in der Literatur bestätigt [11;12].
Die Verträglichkeit ist in den meisten Fällen gut. Allerdings gibt es auch zwei Berichte über Komplikationen bei adultem M. Still unter ANR-Therapie. Bei einem Patienten trat nach 3-monatiger, primär erfolgreicher Therapie eine rasch letal verlaufende dilatative Kardiomyopathie auf, ein anderer Patient entwickelte eine Schocklunge. Ob dies kausal auf die ANR-Therapie zurückzuführen ist oder ob diese lediglich nicht in der Lage war, die Grunderkrankung suffizient zu kontrollieren, ist noch offen [13;14]. Die überzeugenden Daten aus Fallserien begründen den Einsatz von ANR beim adulten M. Still nach unzureichendem Ansprechen einer konventionellen Therapie mit Glucocorticoiden und MTX oder anderen Immunsuppressiva, insbesondere in lebensbedrohlichen Situationen oder bei Patienten mit erheblicher Einschränkung der Lebensqualität [15].
3.Systemische juvenile idiopathische Arthritis
Eine prospektive offene Studie untersuchte die Wirksamkeit von ANR bei 15 Patienten mit adultem M. Still im Vergleich zu 20 Patienten mit systemischer juveniler idiopathischer Arthritis (SJIA) [11]. Es zeigte sich ein deutlich besseres Ansprechen der erwachsenen Patienten (9/15 Vollremissionen, 2/15 Non-Responder) gegenüber den Kindern (4/20 Vollremissionen, 10/20 Non-Responder). Bei jeweils 2 Patienten musste die Therapie wegen starker Hautreaktionen an der Injektionsstelle bzw. wegen Infektionen (Varizellen, Leishmaniasis) beendet werden.
In einer bislang nur in einem Abstrakt publizierten multizentrischen, placebokontrollierten Studie sprachen 8 von 12 Patienten (67%) der Verumgruppe auf ANR an gegenüber 1 von 12 Patienten in der Placebogruppe (8%) [16]. In der Literatur finden sich Berichte über insgesamt etwa 150 Jugendliche und Kinder, bei denen ANR zur Behandlung der SJIA eingesetzt wurde. Etwa 40-45% der Behandelten erreichten eine Vollremission (mit der Möglichkeit, Glucocorticoide und andere DMARDs abzusetzen), etwa 40% ein partielles Ansprechen, bei ca. 20% konnte kein Ansprechen beobachtet werden. Die Vergleichbarkeit dieser Daten wird durch unterschiedliche Dosierungen erschwert: in einigen Fallserien wurde ANR mit 1-2 mg/kg KG/Tag dosiert und nicht gesteigert, in anderen wurde die Dosis bei Nicht-Ansprechen auf 3-4 mg/kg KG/Tag erhöht. Ein besonderes Problem einer Therapie mit ANR bei Kleinkindern ist die täglich erforderliche subkutane Applikation, die erfahrungsgemäß allerdings bei gutem therapeutischem Ansprechen auch von Kleinkindern meist erstaunlich schnell akzeptiert wird.
An unerwünschten Wirkungen stehen lokale Reaktionen an der Einstichstelle der Häufigkeit nach an erster Stelle (›=1/10). Sie können so ausgeprägt sein, daß sie zum Therapieabbruch führen, nehmen nach vierwöchiger Therapie aber oft an Intensität ab (17-19). Besonders müssen infektiöse Komplikationen beachtet werden (Häufigkeit ›=1/100, <1/10) wie obere Luftwegsinfekte, Herpes labialis oder Gastroenteritiden, aber auch schwerwiegendere Infektionen, die eine stationäre Behandlung erfordern (11;18). Zweimal entwickelte sich unter ANR ein „Makrophagen Aktivierendes Syndrom“ (MAS) (17). In einem Fall wurde die ANR-Therapie nach Überstehen des MAS problemlos weitergeführt, im anderen Fall waren die Eltern zur Fortsetzung der ANR-Gabe nicht bereit.
Nach derzeitiger Datenlage einschließlich der Erfahrung eindrucksvoller Remissionen in einem nicht unbeträchtlichen Anteil der SJIA-Patienten (40-45%, s.o.) und der Tatsache, dass bislang keine Arzneimittel ähnlicher Effektivität für diese Erkrankung zur Verfügung stehen, sowie bei Kenntnis der insgesamt ansonsten ungünstigen Prognose, ist der Einsatz von ANR nach unzureichendem Ansprechen auf eine konventionelle Therapie (MTX, Glucocorticoide) begründet [18;20;21].
4.Hereditäre Autoinflammationssyndrome
Eine Übersicht über die Gruppe der hereditären Autoinflammationssyndrome (HAIS) mit den wesentlichen Symptomen und dem zugrunde liegenden Gendefekt gibt Tabelle 1. Diese Defekte führen zu Veränderungen der Produktion und Wirkung proinflammatorischer Zytokine, speziell des IL-1 und des TNF-alpha. Die Blockierung von IL-1 entspricht damit einer angestrebten „targeted therapy“.
Die HAIS manifestieren sich oft bereits im Kindesalter, das CINCA-/NOMID-Syndrom (Chronic Infantile Neurologic Cutaneous Arthropathy/Neonatal Onset Multisystem Inflammatory Disease) und das DIRA-Syndrom (Deficiency of the Interleukin-1-Receptor Antagonist) sogar schon im Neugeborenenalter [22;23]. Betroffen sind häufig die serösen Häute (Perikard, Pleura, Peritoneum), die Haut, Knochen/Periost und die Synovialmembran, aber auch Auge, Ohr und das ZNS können involviert sein [24]. Infolge der rezidivierenden, eventuell subklinisch verlaufenden Entzündungen stellt die Entwicklung einer Amyloid A (AA)-Amyloidose eine schwere Komplikation der HAIS dar [25]. Eine effektive Therapie stand vor Einführung der Biologika lediglich für das familiäre Mittelmeerfieber (FMF) zur Verfügung (Colchicin) [26;27]. Seit 2004 stellt die IL-1ß-Blockade ein zunehmend wichtiges Prinzip in der Behandlung der HAIS dar [28]. Anakinra (ANR) hat sich in Pilotstudien und Fallbeschreibungen besonders bei den Cryopyrin-assoziierten periodischen Syndromen (CAPS) als wirksam erwiesen (Tabelle 1, mehr), auch eine Verbesserung der Schwerhörigkeit und der ZNS-Manifestation konnten erzielt werden [28-35]. Eine Rückbildung CAPS-assoziierter AA-Amyloidosen unter ANR scheint möglich [36], doch entsprechende Langzeit-Studien fehlen. Auch beim DIRA-Syndrom, bei dem ein IL-1-Rezeptorantagonist-Mangel vorliegt, ist ANR effektiv [22]. - Kontrollierte Studien über die Effektivität von ANR bei den HAIS bzw. den CAPS wurden bislang nicht durchgeführt. ANR erwies sich auch bei FMF, HIDS (Hyper-IgD-Syndrom) und beim TRAPS (TNF Receptor Associated Periodic Syndrome) als effektiv [37-43] (Tabelle 1, mehr)
ANR oder andere zur IL-1ß-Blockade geeignete Medikamente (als Alternativen stehen demnächst Rilonacept und Canakinumab zur Verfügung, siehe Anhang) sollten wegen der ungünstigen Prognose bei MWS und CINCA-/NOMID-Syndrom, aber auch beim neu beschriebenen DIRA-Syndrom eingesetzt werden [22;36]. Bei FCAS sollte der Einsatz vom Verlauf abhängig gemacht werden. Bei therapieresistentem FMF, HIDS oder TRAPS kann ANR versucht werden. Die Dosierung beträgt 1-2 mg/kgKG/Tag (maximal 100 mg/Tag), oft reichen jedoch geringere Dosen als für die Behandlung der RA oder der SJIA aus [36;44].
5.Andere entzündlich-rheumatische Erkrankungen
Tabelle 2 (mehr) gibt einen Überblick über Fallberichte und offene Pilotstudien, die eine Wirksamkeit von ANR bei weiteren entzündlich-rheumatischen Erkrankungen beschreiben.
In kleinen Studien zur Therapie der Spondylitis ankylosans [45;46] und der Psoriasisarthritis [47;48] mit ANR konnte keine überzeugende Wirksamkeit nachgewiesen werden. Ebensowenig war in einer kontrollierten Therapiestudie bei polyarthritischen Verlaufsformen der JIA eine Überlegenheit von ANR gegenüber Placebo nachweisbar [49].
Geschäftsstelle, 17.09.2009
http://dgrh.de/anakinraeinsatz.html
Man war das heut wieder ein Gemetzel. :O


Antwort auf Beitrag Nr.: 39.456.862 von zwitscherton am 04.05.10 22:54:22Das hat mit Griechenland sehr wenig zu tun, hier wird geshortet, daß die Schwarte kracht.
Antwort auf Beitrag Nr.: 39.458.953 von kontaktfenster am 05.05.10 11:16:31Braucht Imho nur einen Anlaß. Die ganze Sparte war gesten blutrot. Xoma hat sich da noch gut gehalten. Aber die Stimmung ist wohl insgesamt sehr schlecht.
Aber die armen Griechen haben mit alldem wohl garnix zu tun.
Aber die armen Griechen haben mit alldem wohl garnix zu tun.

Ja Ja  die Griechen die riechen
die Griechen die riechen
 die Griechen die riechen
die Griechen die riechen
Antwort auf Beitrag Nr.: 39.459.742 von eddycassius am 05.05.10 12:53:12Kann doch nur gut sein, wenn der Euro weiter fällt.
Zumindest für den, der amerikanische Aktien besitzt.
Zumindest für den, der amerikanische Aktien besitzt.

Antwort auf Beitrag Nr.: 39.460.093 von Neutron1504 am 05.05.10 13:37:18und am Ende wieder mal ins +++ Plus +++ gerettet ...


Antwort auf Beitrag Nr.: 39.389.745 von kontaktfenster am 23.04.10 10:53:54Rücksetzer bis 0,62 durchaus möglich und zu erwarten...
Da lag ich doch ganz richtig mit meiner Vermutung am 23.04.
Da lag ich doch ganz richtig mit meiner Vermutung am 23.04.

Wird interessant, wo die Reise nun hingeht ...



besteht die möglichkeit das es noch tiffer geht?
wann gibts den wider was zu hören von xoma

In der letzten Viertelstunde wurden aber alle Biotechs, die ich auf watch habe, massiv in den Keller gefahren, richtige Abstürze ... das war wie auf Kommando!
Antwort auf Beitrag Nr.: 39.473.769 von kontaktfenster am 06.05.10 20:58:47Wer solche Kommandos gibt gehört standrechtlich erschossen !!!


du sagst es
nicht nur die biotechs gehen grade baden
besser vormu liert der aktien markt säuft grad ab
liert der aktien markt säuft grad ab
nicht nur die biotechs gehen grade baden
besser vormu
 liert der aktien markt säuft grad ab
liert der aktien markt säuft grad ab
Antwort auf Beitrag Nr.: 39.474.255 von eddycassius am 06.05.10 21:19:42Ich hab es auch gerade gesehen, der Nasdaq hat total gesponnen, weil sich die Griechen wieder prügeln.
Der ganze Markt ist abgestuerzt 
Dow zeitweise 9% im Minus... Manipulation!!!

Dow zeitweise 9% im Minus... Manipulation!!!
Antwort auf Beitrag Nr.: 39.474.255 von eddycassius am 06.05.10 21:19:42yahoo-titel-story
[urlDow Rapidly Paring Losses After More Than 900; Wall Street Hammered Amid European Debt Worries]http://finance.yahoo.com/news/Stock-indexes-down-3-percent-rb-2292944629.html;_ylt=AqvBy4Z1KSk7oKWtaQMoMLe7YWsA;_ylu=X3oDMTE3Z3BnYWdoBHBvcwMxBHNlYwNicmVha2luZ05ld3MEc2xrA2Rvd3JhcGlkbHlwYQ--?x=0[/url]

f**k the greek
[urlDow Rapidly Paring Losses After More Than 900; Wall Street Hammered Amid European Debt Worries]http://finance.yahoo.com/news/Stock-indexes-down-3-percent-rb-2292944629.html;_ylt=AqvBy4Z1KSk7oKWtaQMoMLe7YWsA;_ylu=X3oDMTE3Z3BnYWdoBHBvcwMxBHNlYwNicmVha2luZ05ld3MEc2xrA2Rvd3JhcGlkbHlwYQ--?x=0[/url]

f**k the greek
 ob der bush da hinter steckt
ob der bush da hinter steckt
Antwort auf Beitrag Nr.: 39.474.289 von Smokey77 am 06.05.10 21:22:01Never underestimate the influence of the greek.

Man sollts nicht für möglich halten, so ein Volkchen löst den Crash aus.

Man sollts nicht für möglich halten, so ein Volkchen löst den Crash aus.
Antwort auf Beitrag Nr.: 39.474.536 von zwitscherton am 06.05.10 21:33:06Unglaublich...
SEC hat sich eingeschaltet
SEC hat sich eingeschaltet

Wo bleiben die Zahlen?!?
Die haben sich auch einen Tag ausgesucht-typisch !?!
Die haben sich auch einen Tag ausgesucht-typisch !?!
Antwort auf Beitrag Nr.: 39.475.202 von Smokey77 am 06.05.10 22:06:18zahlenfreund
[urlXOMA Reports First Quarter 2010 Financial Results]http://biz.yahoo.com/pz/100506/191174.html?.v=1[/url]
[urlXOMA Reports First Quarter 2010 Financial Results]http://biz.yahoo.com/pz/100506/191174.html?.v=1[/url]
 die zahlen haben nicht fiel gebracht
die zahlen haben nicht fiel gebracht-16%
es ist zum meuse melken

Antwort auf Beitrag Nr.: 39.476.290 von eddycassius am 06.05.10 23:52:26Sieh es einfach als Schicksalsschlag.
Wenn in Zukunft in Athen ne Flasche Ouzo umfällt, gibts an der Wallstreet fallende Kurse.

Wenn in Zukunft in Athen ne Flasche Ouzo umfällt, gibts an der Wallstreet fallende Kurse.

Antwort auf Beitrag Nr.: 39.476.383 von zwitscherton am 07.05.10 00:10:48Sogar die Bild-Zeitung hats schon mitbekommen
[urlBILD]http://www.wallstreet-online.de/diskussion/1146835-23231-23240/quatsch-quassel-spass-thread#1146835_39476417
[/url]


[urlBILD]http://www.wallstreet-online.de/diskussion/1146835-23231-23240/quatsch-quassel-spass-thread#1146835_39476417
[/url]


Antwort auf Beitrag Nr.: 39.476.467 von zwitscherton am 07.05.10 00:25:48wie ist deine prognose für xoma?
Antwort auf Beitrag Nr.: 39.476.501 von Penemuende am 07.05.10 00:32:41Ich geb hier keine Prognosen ab. Dafür sind andere zuständig.
Daß der Kurs sich nach der Verdünnung wieder emporgearbeitet hatte - spricht imho grundsätzlich für Xoma - sie konntens allein packen mit PII/052.
Ich denke Chance und Risiko sind in etwa gleich verteilt - etwas mehr zu den Chancen. Is allemal ne Speku wert. Erfolgreiche Antibody Companies wurden weiterhin bereits mehrfach geschluckt.
Im Moment (heute) scheint der Markt das allerdings nicht so zu sehen. Don't Panik war mal eine Devise - aber niemals an der NYSE/Nasdaq.

Daß der Kurs sich nach der Verdünnung wieder emporgearbeitet hatte - spricht imho grundsätzlich für Xoma - sie konntens allein packen mit PII/052.
Ich denke Chance und Risiko sind in etwa gleich verteilt - etwas mehr zu den Chancen. Is allemal ne Speku wert. Erfolgreiche Antibody Companies wurden weiterhin bereits mehrfach geschluckt.
Im Moment (heute) scheint der Markt das allerdings nicht so zu sehen. Don't Panik war mal eine Devise - aber niemals an der NYSE/Nasdaq.

"XOMA had a net loss of $21.8 million, or $0.09 per share, in the 2010 first quarter compared with net income of $6.2 million, or $0.04 per share, in the first quarter of 2009."
"At March 31, 2010, XOMA had cash and cash equivalents of $28.4 million, compared with $23.9 million at December 31, 2009. In January and February 2010, XOMA received approximately $21.0 million in proceeds from financing transactions, after underwriting discounts, expenses and an amendment fee to certain existing warrant holders."
Lautete nicht eins der letzten Statements, dass das derzeitige Kapital für mind. 1 Jahr reichen sollte? 21,8 Mio verbrannt in 1 Quartal, Rest 28,4 Mio "cash und cash equivalents". Das deutet m.E. darauf hin, dass wir jetzt fast jedes Quartal wieder erneute Finanzierungen sehen könnten.
Keine Frage, Q1 2011 möchte ich hier gut investiert sein, bevor die Phase-2-Ergebnisse von XOMA 052 präsentiert werden, auch wenn es im Anschluss erneut Finanzierung, Finanzierung, Finanzierung heißt. Aber bis dahin stellt sich mir die frage, ob man in anbetracht der bevorstehenden Verwässerungen jetzt schon hier drin sein muss!?
Meinungen?
Grüsse, ER
"At March 31, 2010, XOMA had cash and cash equivalents of $28.4 million, compared with $23.9 million at December 31, 2009. In January and February 2010, XOMA received approximately $21.0 million in proceeds from financing transactions, after underwriting discounts, expenses and an amendment fee to certain existing warrant holders."
Lautete nicht eins der letzten Statements, dass das derzeitige Kapital für mind. 1 Jahr reichen sollte? 21,8 Mio verbrannt in 1 Quartal, Rest 28,4 Mio "cash und cash equivalents". Das deutet m.E. darauf hin, dass wir jetzt fast jedes Quartal wieder erneute Finanzierungen sehen könnten.
Keine Frage, Q1 2011 möchte ich hier gut investiert sein, bevor die Phase-2-Ergebnisse von XOMA 052 präsentiert werden, auch wenn es im Anschluss erneut Finanzierung, Finanzierung, Finanzierung heißt. Aber bis dahin stellt sich mir die frage, ob man in anbetracht der bevorstehenden Verwässerungen jetzt schon hier drin sein muss!?
Meinungen?
Grüsse, ER
Antwort auf Beitrag Nr.: 39.480.289 von extremrelaxer am 07.05.10 13:41:24Gute frage,
heute ist aber ganz schön was los.
Im zum verkauf standen eben jeweils 4*100.000 zu 0,53 0,54 0,55 0,56
Mal sehen was da noch kommt,habe zu 50 cent gekauft.
heute ist aber ganz schön was los.
Im zum verkauf standen eben jeweils 4*100.000 zu 0,53 0,54 0,55 0,56

Mal sehen was da noch kommt,habe zu 50 cent gekauft.

Antwort auf Beitrag Nr.: 39.480.289 von extremrelaxer am 07.05.10 13:41:24Wenn sies alleine stemmen (müssen/wollen) kann es schon sein, das sie nochmals Kapital aufnehmen.
Wenn die operating costs so bleiben, kann das wohl durch Rücklagen, Lizenzeinnahmen etc. (receipts for license and collaborative fees and royalties) nicht geleistet werden.
Allerdings sehe ich für Q1 keine 21.8 Mio - hab ich was übersehen ?
"Net cash used in operating activities was $16.4 million for the three months ended March 31, 2010"

Wenn die operating costs so bleiben, kann das wohl durch Rücklagen, Lizenzeinnahmen etc. (receipts for license and collaborative fees and royalties) nicht geleistet werden.
Allerdings sehe ich für Q1 keine 21.8 Mio - hab ich was übersehen ?
"Net cash used in operating activities was $16.4 million for the three months ended March 31, 2010"

Antwort auf Beitrag Nr.: 39.482.270 von zwitscherton am 07.05.10 17:01:05Wenn sich dan aber bereits ein Erfolg abzeichnete, sollte der Markt das imho nicht so 1:1 einpreisen, wie im Feb.
Es sei den der Markt spielt weiterhin verrückt ...
verrückt ...
Es sei den der Markt spielt weiterhin
 verrückt ...
verrückt ...
Antwort auf Beitrag Nr.: 39.482.286 von zwitscherton am 07.05.10 17:02:25Ich befürchte der Markt wird noch weiter verrückt spielen.
DAX zurück auf 5.300 und DOW auf 9.500, erst dann dürfte Erholung einsetzen.
Wobei das was bei Xoma in den letzten beiden Tagen abgeht ist auch schon mehr als Panik.
Alles nur m.M.
DAX zurück auf 5.300 und DOW auf 9.500, erst dann dürfte Erholung einsetzen.
Wobei das was bei Xoma in den letzten beiden Tagen abgeht ist auch schon mehr als Panik.

Alles nur m.M.
Antwort auf Beitrag Nr.: 39.483.397 von MogD am 07.05.10 18:45:00Zumal, das Problem mit Griechenland und den anderen PIGS ist seit Monaten bekannt.
Naja, irdendwann musste das dann wohl realisiert werden. Und jetzt kotzen sich die Märkte aus - viellecht auch nur weil gestern so ein Depp da im Handelssystem rumgepfuscht hat.
Jetzt wird Alles verramscht.

Naja, irdendwann musste das dann wohl realisiert werden. Und jetzt kotzen sich die Märkte aus - viellecht auch nur weil gestern so ein Depp da im Handelssystem rumgepfuscht hat.
Jetzt wird Alles verramscht.

Antwort auf Beitrag Nr.: 39.482.262 von Bioperle am 07.05.10 17:00:33hallo bioperle,
freut mich,dich hier zu lesen!
servus
freut mich,dich hier zu lesen!
servus

XOMA Ltd. Q1 2010 Earnings Call Transcript
May 07, 2010
http://seekingalpha.com/article/203833-xoma-ltd-q1-2010-earn…
Bleibe LONG.
GLTA und ein schönes WE.
May 07, 2010
http://seekingalpha.com/article/203833-xoma-ltd-q1-2010-earn…
Bleibe LONG.
GLTA und ein schönes WE.
Antwort auf Beitrag Nr.: 39.480.289 von extremrelaxer am 07.05.10 13:41:24Hallo ER,
also bei Seeking Alpha steht das hier:
Consistent with last year, we will not be providing guidance on revenues or cash receipts for 2010, so at the best manage our ongoing negotiations for XOMA 052 and technology licensing. The company expects the cash used in operating activities may range from $45 million to cash neutral or positive. Based on our cash reserves and anticipated spending levels, revenues government and other funding from other sources we believe will be available, we estimate that we have sufficient cash resources to meet our anticipated net cash needs through the next 12 months.
Also werden sie m.M.n. noch ein Jahr durchhalten können.
Quelle: http://seekingalpha.com/article/203833-xoma-ltd-q1-2010-earn…
also bei Seeking Alpha steht das hier:
Consistent with last year, we will not be providing guidance on revenues or cash receipts for 2010, so at the best manage our ongoing negotiations for XOMA 052 and technology licensing. The company expects the cash used in operating activities may range from $45 million to cash neutral or positive. Based on our cash reserves and anticipated spending levels, revenues government and other funding from other sources we believe will be available, we estimate that we have sufficient cash resources to meet our anticipated net cash needs through the next 12 months.
Also werden sie m.M.n. noch ein Jahr durchhalten können.
Quelle: http://seekingalpha.com/article/203833-xoma-ltd-q1-2010-earn…
hi bioperle,bin in cel sci investiert,kann mir jemand mal hier helfen was xoma so macht?der oxfordbrief empfiehlt ja xoma auch?
hät ein paar euro übrig...
aber andere dürfen mir auch gern helfen
schönes we
grüßle vfbler
hät ein paar euro übrig...
aber andere dürfen mir auch gern helfen
schönes we
grüßle vfbler
Nur zur Info:
Vanguard Group Inc hat 2,191,982 Shares aufgestockt und halten nun insgesamt 8,326,226.
Vanguard Group Inc hat 2,191,982 Shares aufgestockt und halten nun insgesamt 8,326,226.
News
BERKELEY, Calif., May 12, 2010 (GlobeNewswire via COMTEX) -- XOMA Ltd. (XOMA 0.59, +0.02, +4.40%) , a leader in the discovery and development of therapeutic antibodies, announced the publication of an abstract titled, "Safe, Rapid-onset and Sustained Biological Activity of IL-1 beta Regulating Antibody XOMA 052 in Resistant Uveitis of Behcet's Disease: Preliminary Results of a Pilot Trial." Uveitis of Behcet's disease is an auto-inflammatory condition that can result in blindness or partial vision loss as described below. The abstract will be presented June 17, 2010 during the annual European Congress of Rheumatology in Rome, Italy by Professor Ahmet Gul, Istanbul Faculty of Medicine, Department of Internal Medicine, Division of Rheumatology, Istanbul University, Turkey, and principal investigator for this XOMA 052 clinical trial.
BERKELEY, Calif., May 12, 2010 (GlobeNewswire via COMTEX) -- XOMA Ltd. (XOMA 0.59, +0.02, +4.40%) , a leader in the discovery and development of therapeutic antibodies, announced the publication of an abstract titled, "Safe, Rapid-onset and Sustained Biological Activity of IL-1 beta Regulating Antibody XOMA 052 in Resistant Uveitis of Behcet's Disease: Preliminary Results of a Pilot Trial." Uveitis of Behcet's disease is an auto-inflammatory condition that can result in blindness or partial vision loss as described below. The abstract will be presented June 17, 2010 during the annual European Congress of Rheumatology in Rome, Italy by Professor Ahmet Gul, Istanbul Faculty of Medicine, Department of Internal Medicine, Division of Rheumatology, Istanbul University, Turkey, and principal investigator for this XOMA 052 clinical trial.
Antwort auf Beitrag Nr.: 39.510.871 von Smokey77 am 12.05.10 20:52:36Gedämpfte Panik.

http://www2.anleger-fernsehen.de/daf_vod_aktie.html?id=50135…

http://www2.anleger-fernsehen.de/daf_vod_aktie.html?id=50135…
Aus den Ami-boards:
The acronyms are clinical parameters to assess the effectiveness of the drug and are necessary for supporting evidence for partnering deals and FDA approval.
052 is an engineered antibody that modulates (not shuts down) what might be the earliest response resulting in a cascade of biochemical responses resulting in inflammation. There are other compounds on the market that attack the inflammation cascade at the same point (interleukin 1B or IL1B), but they differ from 052 in activity, longevity of effectiveness, side effects, etc. Some of these are on the market already, some are experimental.
Targets include T1 and T2 diabetes and cardiovascular indications (Xoma's stated goals). Other potential indications include some types of cancer, RA, gout, Behcet's disease, and some might suggest Alzheimer's, acne and jock itch....
Xoma seems to be pretty aggressive in attempting to protect its potential market through patent protection, and this will be a key in the ability of Xoma to partner 052.
Other goodies to look for are Xoma's biodefense contracts including 3AB antibotulinium indication, SARS, bird flu and swine flu.
The only other proprietary antibody that is being assessed is opebacan for use in stem cell transplants. There's some controversy whether this is in phase 2 or 3. I would tend to believe the phase 2 report from clinicltrials.gov. Opebacan has had a long unsuccessful history.
Xoma also has licensed antibodies in clinical trials. Tanezumab is going to be a great source of income for Xoma when Pfizer gets it to market, but that is probably a few years away. HCD122 is being evaluated by Novartis but earlier tests were not encouraging.
Xoma has several licensing deals that will generate milestone payments, but these are somewhat unpredictable.
In general, Xoma has historically "given away" its best stuff, and kept compounds that fail to make it to market. Xoma trying to redeem itself with 052 and I think the viability of the company is resting on this drug. IL1B modulation is looking like a big deal. Any success by any other IL1B drug is being touted by Xoma as an indication of the potential for 052 to attract potential partners.
Xoma has a reliable income stream from Cimzia royalties and these are expected to grow. The company's debt position is favorable.
Good luck in your investing decisions.
The acronyms are clinical parameters to assess the effectiveness of the drug and are necessary for supporting evidence for partnering deals and FDA approval.
052 is an engineered antibody that modulates (not shuts down) what might be the earliest response resulting in a cascade of biochemical responses resulting in inflammation. There are other compounds on the market that attack the inflammation cascade at the same point (interleukin 1B or IL1B), but they differ from 052 in activity, longevity of effectiveness, side effects, etc. Some of these are on the market already, some are experimental.
Targets include T1 and T2 diabetes and cardiovascular indications (Xoma's stated goals). Other potential indications include some types of cancer, RA, gout, Behcet's disease, and some might suggest Alzheimer's, acne and jock itch....
Xoma seems to be pretty aggressive in attempting to protect its potential market through patent protection, and this will be a key in the ability of Xoma to partner 052.
Other goodies to look for are Xoma's biodefense contracts including 3AB antibotulinium indication, SARS, bird flu and swine flu.
The only other proprietary antibody that is being assessed is opebacan for use in stem cell transplants. There's some controversy whether this is in phase 2 or 3. I would tend to believe the phase 2 report from clinicltrials.gov. Opebacan has had a long unsuccessful history.
Xoma also has licensed antibodies in clinical trials. Tanezumab is going to be a great source of income for Xoma when Pfizer gets it to market, but that is probably a few years away. HCD122 is being evaluated by Novartis but earlier tests were not encouraging.
Xoma has several licensing deals that will generate milestone payments, but these are somewhat unpredictable.
In general, Xoma has historically "given away" its best stuff, and kept compounds that fail to make it to market. Xoma trying to redeem itself with 052 and I think the viability of the company is resting on this drug. IL1B modulation is looking like a big deal. Any success by any other IL1B drug is being touted by Xoma as an indication of the potential for 052 to attract potential partners.
Xoma has a reliable income stream from Cimzia royalties and these are expected to grow. The company's debt position is favorable.
Good luck in your investing decisions.
Antwort auf Beitrag Nr.: 39.525.210 von zwitscherton am 15.05.10 01:50:14Gedämpfte Panik die Zweite auf schweizer Art.
http://www.cash.ch/video/start.php?firstProjectID=16239

http://www.cash.ch/video/start.php?firstProjectID=16239

Antwort auf Beitrag Nr.: 39.531.318 von kirroyal am 17.05.10 12:40:59wäre zu wünschen! 

Antwort auf Beitrag Nr.: 39.531.659 von Zackes1 am 17.05.10 13:41:44XOMA (NASDAQ:XOMA) has a potential upside of 231.3% based on a current price of $0.57 and an average consensus analyst price target of $1.88.
Based on a proprietary pattern recognition system.
Wäre trotzdem OK.

Based on a proprietary pattern recognition system.
Wäre trotzdem OK.

Antwort auf Beitrag Nr.: 39.532.928 von zwitscherton am 17.05.10 16:23:02Ca.1,50 §

Antwort auf Beitrag Nr.: 39.533.001 von Bioperle am 17.05.10 16:31:08Sorry,ca.1,50$

In den US Boards wird über ein Buyout durch Pfizer spekuliert. War aber schon mal Thema. Konkretes sagen die Amis aber auch nicht. Naja, wird wohl wieder ein Schwein durchs Dorf getrieben.
Antwort auf Beitrag Nr.: 39.538.248 von Zackes1 am 18.05.10 12:24:05der Typ, der das Gerücht verbreitet, behauptet, er hätte einen Tipp aus Deutschland bekommen. Vielleicht ja aus diesem Board?

Antwort auf Beitrag Nr.: 39.538.675 von Neutron1504 am 18.05.10 13:21:55Hab ich auch eben gelesen 

4/30/2010 6,692,353 3,687,027 1.815108
4/15/2010 3,489,048 6,644,184 1.000000
3/31/2010 2,809,369 2,595,161 1.082541
3/15/2010 1,929,072 6,290,497 1.000000
2/26/2010 2,814,533 3,244,706 1.000000
Sind wieder ca 7Millionen Aktien Short... Waren vor 2Monaten keine 2 Millionen
4/15/2010 3,489,048 6,644,184 1.000000
3/31/2010 2,809,369 2,595,161 1.082541
3/15/2010 1,929,072 6,290,497 1.000000
2/26/2010 2,814,533 3,244,706 1.000000
Sind wieder ca 7Millionen Aktien Short... Waren vor 2Monaten keine 2 Millionen

Antwort auf Beitrag Nr.: 39.539.091 von Smokey77 am 18.05.10 14:21:03Dann lass uns die Shorties grillen! 

Antwort auf Beitrag Nr.: 39.539.110 von Zackes1 am 18.05.10 14:22:40Ohne Partner fuer 052... wird das leider nix 

News - 17.05.10 15:12
Quelle: HANDELSBLATT
Schnäppchenjäger sorgen für die Wende
Lange sah es nach einem Fehlstart in die neue Börsenwoche aus, dann sorgten Schnäppchenjäger für die Wende: Nach einem Auf und Ab haben die US-Börsen am Montag mit leichten Gewinnen geschlossen.
.....
Die vermehrten Übernahmen in den USA hellten die Stimmung auf. "Die angeregte M&A-Aktivität legt sich wie eine Zuckerschicht über die bittere Pille aus Europa", sagte Andre Bakhos von Lek Securities mit Blick auf die Schuldenprobleme in der Euro-Zone. Besonders in der Pharma-Branche kommt es zu Allianzen. So will der Krankenhausbetreiber Universal Health Services Psychiatric Solutions kaufen, die Einrichtungen zur Behandlung psychisch Kranker betreiben.
Anteile von Universal Health wurden 7,9 Prozent höher gehandelt, Aktien von Psychiatric Solutions verloren 0,7 Prozent.
Zudem plant Japans zweitgrößter Arzneimittelproduzent Astellas den Kauf des US-Biotech-Unternehmens OSI Pharmaceuticals für vier Mrd. Dollar. Astellas hatte OSI schon seit langem im Visier und stockte seine Offerte zuletzt auf 57,50 Dollar pro Aktie auf. OSI-Papiere verloren am Montag 4,1 Prozent, weil Anleger ein noch höheres Angebot erwartet hatten. Seit Anfang März, als die erste Offerte kam, hat das Papier aber 55 Prozent zugelegt.
Aktien von GLG Partners stiegen um knapp 50 Prozent, nachdem das Unternehmen einer Übernahme durch den Hedge-Fonds Man Group PLC zustimmte. Anteile der Man Group PLC wurden mehr als acht Prozent schwächer gehandelt....
Also, es tut sich was in der Branche.
Quelle: HANDELSBLATT
Schnäppchenjäger sorgen für die Wende
Lange sah es nach einem Fehlstart in die neue Börsenwoche aus, dann sorgten Schnäppchenjäger für die Wende: Nach einem Auf und Ab haben die US-Börsen am Montag mit leichten Gewinnen geschlossen.
.....
Die vermehrten Übernahmen in den USA hellten die Stimmung auf. "Die angeregte M&A-Aktivität legt sich wie eine Zuckerschicht über die bittere Pille aus Europa", sagte Andre Bakhos von Lek Securities mit Blick auf die Schuldenprobleme in der Euro-Zone. Besonders in der Pharma-Branche kommt es zu Allianzen. So will der Krankenhausbetreiber Universal Health Services Psychiatric Solutions kaufen, die Einrichtungen zur Behandlung psychisch Kranker betreiben.
Anteile von Universal Health wurden 7,9 Prozent höher gehandelt, Aktien von Psychiatric Solutions verloren 0,7 Prozent.
Zudem plant Japans zweitgrößter Arzneimittelproduzent Astellas den Kauf des US-Biotech-Unternehmens OSI Pharmaceuticals für vier Mrd. Dollar. Astellas hatte OSI schon seit langem im Visier und stockte seine Offerte zuletzt auf 57,50 Dollar pro Aktie auf. OSI-Papiere verloren am Montag 4,1 Prozent, weil Anleger ein noch höheres Angebot erwartet hatten. Seit Anfang März, als die erste Offerte kam, hat das Papier aber 55 Prozent zugelegt.
Aktien von GLG Partners stiegen um knapp 50 Prozent, nachdem das Unternehmen einer Übernahme durch den Hedge-Fonds Man Group PLC zustimmte. Anteile der Man Group PLC wurden mehr als acht Prozent schwächer gehandelt....
Also, es tut sich was in der Branche.

 würde mich nicht wundern wenn xoma bis 0,40 runter geht.
würde mich nicht wundern wenn xoma bis 0,40 runter geht.oder was meint ihr

meine herren ich hatte da eine frage
in der geschichte des unternehmens,wie erfolgreich ist das unternehmen mit der erforschung von medikamenten.
es gab wohl nicht immer nur erfolge ????
konnte mir jemand netter weise die frage beantworten
danke

in der geschichte des unternehmens,wie erfolgreich ist das unternehmen mit der erforschung von medikamenten.
es gab wohl nicht immer nur erfolge ????
konnte mir jemand netter weise die frage beantworten

danke

Hat jemand fundierte Kenntnisse darüber, mit welcher Zeitspanne man rechnen muß bis zur Markteinführung der Antikörper ??
und wie ist das Risiko einzuschätzen, dass xoma vorher delistet wird wegen Unterschreitung des Kurswerts von 1 Dollar ??
und wie ist das Risiko einzuschätzen, dass xoma vorher delistet wird wegen Unterschreitung des Kurswerts von 1 Dollar ??
hhhhhhhhhhaaaaaaaaaaaaaalllllllllllllloooooooooooooooooooooo
eeeeeeeeccccccccccccchhhhhhhhhhoooooooooooo
eeeeeeeeccccccccccccchhhhhhhhhhoooooooooooo

Antwort auf Beitrag Nr.: 39.587.825 von eddycassius am 26.05.10 19:34:43Tja wenn hier keiner antwortet versuch es mal da -> http://www.xoma.com/
LG Tommi
P.S. Ich kann dir leider auch nicht gross weiterhelfen, bin kein Mediziner, tml.
LG Tommi
P.S. Ich kann dir leider auch nicht gross weiterhelfen, bin kein Mediziner, tml.
Neues SEC Filling gestern 
Bin raus!!!
300 M neue Shares und RS-ohne mich

Bin raus!!!
300 M neue Shares und RS-ohne mich

XOMA LTD.
NOTICE OF ANNUAL GENERAL MEETING OF SHAREHOLDERS
TO BE HELD AT 9:00 A.M. ON JULY 21, 2010
To the Shareholders of XOMA Ltd.:
Notice is hereby given that the annual general meeting of shareholders of XOMA Ltd. (the “Company”) will be held at the Company’s offices at 2910 Seventh Street, Berkeley, California, on July 21, 2010, at 9:00 a.m. local time, for the following purposes:
1. To elect directors;
2. To appoint Ernst & Young LLP to act as the Company’s independent registered public accounting firm for the 2010 fiscal year and authorize the Board of Directors to agree to such firm’s fees;
3. To approve the increase of the Company’s authorized share capital by the creation of an additional 300,000,000 common shares, par value US$.0005 per share;
4. To authorize the Board of Directors to effect a share consolidation, or reverse stock split, of our common shares at any time on or before July 21, 2011 at a ratio within a range of 1 for 2 to 1 for 15 as determined by the Board of Directors in its sole discretion, and if and when the reverse stock split is effected, reduce the number of our authorized common shares by the reverse split ratio determined by the Board of Directors to apply equally to our authorized common shares and increase the par value of each common share accordingly;
5. To approve an amendment to the Company’s 1981 Share Option Plan to increase the number of shares issuable over the term of the plan by 5,200,000 shares;
6. To approve the Company’s 2010 Long Term Incentive and Share Award Plan, which would replace the Company’s 1981 Share Option Plan, Restricted Share Plan and 1992 Directors Option Plan going forward and increase the total number of common shares available for awards by 8,800,000 shares to a maximum of 43,826,211 shares in the aggregate;
7. To approve an amendment to the Company’s 1998 Employee Share Purchase Plan to increase the number of common shares issuable over the term of the plan by 500,000 to 2,000,000 shares in the aggregate; and
8. To consider and transact such other business as may properly come before the meeting or any adjournment or postponement thereof.
In addition, in accordance with Bermuda law, the Company’s audited financial statements for fiscal year 2009 will be laid before the annual general meeting.
The Board of Directors has fixed the close of business on May 25, 2010, as the record date for the determination of shareholders entitled to notice of, and to vote at, this meeting and at any adjournment or postponement thereof. On May 25, 2010, the Company had 261,247,750 common shares issued and outstanding.
By Order of the Board of Directors
Christopher J. Margolin
Secretary
June 9, 2010
Berkeley, California
NOTICE OF ANNUAL GENERAL MEETING OF SHAREHOLDERS
TO BE HELD AT 9:00 A.M. ON JULY 21, 2010
To the Shareholders of XOMA Ltd.:
Notice is hereby given that the annual general meeting of shareholders of XOMA Ltd. (the “Company”) will be held at the Company’s offices at 2910 Seventh Street, Berkeley, California, on July 21, 2010, at 9:00 a.m. local time, for the following purposes:
1. To elect directors;
2. To appoint Ernst & Young LLP to act as the Company’s independent registered public accounting firm for the 2010 fiscal year and authorize the Board of Directors to agree to such firm’s fees;
3. To approve the increase of the Company’s authorized share capital by the creation of an additional 300,000,000 common shares, par value US$.0005 per share;
4. To authorize the Board of Directors to effect a share consolidation, or reverse stock split, of our common shares at any time on or before July 21, 2011 at a ratio within a range of 1 for 2 to 1 for 15 as determined by the Board of Directors in its sole discretion, and if and when the reverse stock split is effected, reduce the number of our authorized common shares by the reverse split ratio determined by the Board of Directors to apply equally to our authorized common shares and increase the par value of each common share accordingly;
5. To approve an amendment to the Company’s 1981 Share Option Plan to increase the number of shares issuable over the term of the plan by 5,200,000 shares;
6. To approve the Company’s 2010 Long Term Incentive and Share Award Plan, which would replace the Company’s 1981 Share Option Plan, Restricted Share Plan and 1992 Directors Option Plan going forward and increase the total number of common shares available for awards by 8,800,000 shares to a maximum of 43,826,211 shares in the aggregate;
7. To approve an amendment to the Company’s 1998 Employee Share Purchase Plan to increase the number of common shares issuable over the term of the plan by 500,000 to 2,000,000 shares in the aggregate; and
8. To consider and transact such other business as may properly come before the meeting or any adjournment or postponement thereof.
In addition, in accordance with Bermuda law, the Company’s audited financial statements for fiscal year 2009 will be laid before the annual general meeting.
The Board of Directors has fixed the close of business on May 25, 2010, as the record date for the determination of shareholders entitled to notice of, and to vote at, this meeting and at any adjournment or postponement thereof. On May 25, 2010, the Company had 261,247,750 common shares issued and outstanding.
By Order of the Board of Directors
Christopher J. Margolin
Secretary
June 9, 2010
Berkeley, California
schöne scheiße
Antwort auf Beitrag Nr.: 39.590.398 von Zackes1 am 27.05.10 09:12:16Du sagst es... gibt heute wahrs ein Massaker-bin deswegen raus!!!
GLTA
GLTA
Antwort auf Beitrag Nr.: 39.590.509 von Smokey77 am 27.05.10 09:27:41hänge tief drin. Schmeißen hat jetzt für mich keinen Sinn mehr. Hätte ich doch nur auf Expertchen gehört, als der bei 80 cent geworfen hat.
Antwort auf Beitrag Nr.: 39.590.526 von Zackes1 am 27.05.10 09:29:36Mal abwarten wie dicke das Massaker ausfällt - einen Teil hat der Markt ja gestern Abend bereits vorweg genommen. 3,2 Mio. nachbörslich gehandelt mit Kurs 0,425$.
Aber ist mal wieder typisch Biotech - Gelder werden verschlungen und da schmeißt man halt mal wieder ein paar neue auf den Markt.
Aber 300 Mio. ist schon ne ganz schöne Scheiße. Und was dann nach dem R/S passiert das kann man sehr schön bei Genta sehen


Aber ist mal wieder typisch Biotech - Gelder werden verschlungen und da schmeißt man halt mal wieder ein paar neue auf den Markt.
Aber 300 Mio. ist schon ne ganz schöne Scheiße. Und was dann nach dem R/S passiert das kann man sehr schön bei Genta sehen



Antwort auf Beitrag Nr.: 39.590.526 von Zackes1 am 27.05.10 09:29:36Bin zum Glück nur mit ner kleinen Posi drin gewesen,trotzdem 1 K verloren... 

Antwort auf Beitrag Nr.: 39.590.625 von Smokey77 am 27.05.10 09:41:44Th, dein Pech möchte ich haben 

Antwort auf Beitrag Nr.: 39.590.625 von Smokey77 am 27.05.10 09:41:44und zwar was das ausmaß betrifft.
Antwort auf Beitrag Nr.: 39.590.724 von Zackes1 am 27.05.10 09:55:24Vielleicht fällt das minus ja nicht ganz so heftig aus,oder die schließen im Plus?!?
Bei Xoma weiß man nie...
Viel Glück
Bei Xoma weiß man nie...
Viel Glück
Antwort auf Beitrag Nr.: 39.590.859 von Smokey77 am 27.05.10 10:09:15Die ersten Pre Kurse sind so schlimm noch nicht: 0,44$, allerdings noch kein Volumen. Vielleicht sind viele tatsächlich gestern Abend schon raus.
We will see.
GLTA
We will see.
GLTA
Antwort auf Beitrag Nr.: 39.592.870 von MogD am 27.05.10 14:11:16Das wird heute ein gemetzel werden...
wie tief wird es den gehen wohl

noch sieht es ya nicht nach einen gemetzel aus
oder ist es die ruhe vor dem sturm
oder ist es die ruhe vor dem sturm
Antwort auf Beitrag Nr.: 39.593.721 von eddycassius am 27.05.10 15:56:01Bei Xoma muß man mit allem rechnen - in 90% verhält sich die Aktie antizyklisch. Aber auf Dauer sind die Aussichten momentan natürlich nicht so rosig.
Antwort auf Beitrag Nr.: 39.593.743 von MogD am 27.05.10 15:59:00absolute Zustimmung XOMA ist ein Phänomen!
Antwort auf Beitrag Nr.: 39.480.289 von extremrelaxer am 07.05.10 13:41:24Irgendwie habe ich den Eindruck, dass die anstehende Verwässerung und der wohl geplante RS einige der Investoren überrascht, anders kann ich mir auch die Kursreaktion nicht erklären.
Angesichts der (katastrophalen) Zahlen Anfang Mai habe ich mit nichts anderem gerechnet. Ein net loss von 21,8 Mio USD im ersten Quartal, restlicher cash & cash equivalents 28,4 Mio USD: Da konnte man sich doch sicher sein, dass es innerhalb der nächsten 3 Monate zur erneuten Verwässerung kommen musste. (siehe mein Beitrag 9454 vom 07.05.).
Die Frage für mich lautet: Muss man angesichts der sicherlich nicht letzten Finanzierungsrunde überhaupt vor Q1 2011, also vor Präsentation der Phase-2-Ergebnisse von XOMA 052 in dieser Aktie investiert sein? Dass ich vor der Ergebnispräsentation von XOMA 052 hier dick drin sein will, das habe ich ja schon oft genug geschrieben. Das Unternehmken hat m. E. riesiges Potential und mich würde auch eine Übernahme von Patentrechten an XOMA 052 bzw. eine Beteiligung an den Rechten durch ein anderes Unternehmen nicht wunderen, allerdings sehe ich hierfür ebenfalls erst nach Abschluss der Phase-2-Studie eine höhere Wahrscheinlichkeit.
Ich glaube, dass wir nach RS nochmals wesentlich bessere Einstiegsmöglichkeiten sehen werden. Mit einem deutlichen Anstieg des Aktienkurses rechne ich nicht vor der Jahreswende.
Alles nur meine persönliche Meinung und keine Finanzberatung oder Empfehlung zum Kauf oder Verkauf der Aktie...
Grüsse, ER
Angesichts der (katastrophalen) Zahlen Anfang Mai habe ich mit nichts anderem gerechnet. Ein net loss von 21,8 Mio USD im ersten Quartal, restlicher cash & cash equivalents 28,4 Mio USD: Da konnte man sich doch sicher sein, dass es innerhalb der nächsten 3 Monate zur erneuten Verwässerung kommen musste. (siehe mein Beitrag 9454 vom 07.05.).
Die Frage für mich lautet: Muss man angesichts der sicherlich nicht letzten Finanzierungsrunde überhaupt vor Q1 2011, also vor Präsentation der Phase-2-Ergebnisse von XOMA 052 in dieser Aktie investiert sein? Dass ich vor der Ergebnispräsentation von XOMA 052 hier dick drin sein will, das habe ich ja schon oft genug geschrieben. Das Unternehmken hat m. E. riesiges Potential und mich würde auch eine Übernahme von Patentrechten an XOMA 052 bzw. eine Beteiligung an den Rechten durch ein anderes Unternehmen nicht wunderen, allerdings sehe ich hierfür ebenfalls erst nach Abschluss der Phase-2-Studie eine höhere Wahrscheinlichkeit.
Ich glaube, dass wir nach RS nochmals wesentlich bessere Einstiegsmöglichkeiten sehen werden. Mit einem deutlichen Anstieg des Aktienkurses rechne ich nicht vor der Jahreswende.
Alles nur meine persönliche Meinung und keine Finanzberatung oder Empfehlung zum Kauf oder Verkauf der Aktie...
Grüsse, ER
Guten Tag,
oh weia Xoma erwischt es aber auch ordentlich...ist im Moment der schlechteste Zeitpunkt seit 15 Monaten um solche News zu bringen.....ich glaub ich hatte mal welche zu 0,295 € früher im Depot....ob das nochmal kommt...hätte ich ja nicht geglaubt..aber überall ist Biotech am Boden....keine leichte Zeit um die richtigen Entscheidungen zu treffen. Derzeit wäre es wohl besser gewesen alles in Cash zu halten..aber hinterher ist es immer leicht zu sagen...erst ma good luck - kann man derzeit überall brauchen
oh weia Xoma erwischt es aber auch ordentlich...ist im Moment der schlechteste Zeitpunkt seit 15 Monaten um solche News zu bringen.....ich glaub ich hatte mal welche zu 0,295 € früher im Depot....ob das nochmal kommt...hätte ich ja nicht geglaubt..aber überall ist Biotech am Boden....keine leichte Zeit um die richtigen Entscheidungen zu treffen. Derzeit wäre es wohl besser gewesen alles in Cash zu halten..aber hinterher ist es immer leicht zu sagen...erst ma good luck - kann man derzeit überall brauchen
Antwort auf Beitrag Nr.: 39.596.169 von Expertchen007 am 27.05.10 21:20:33Angesicht der "Drohung" der 300 Mio. Verdünnung plus RS ist das heutige 4% Minus erstaunlich.
Vielleicht wurde in den letzten Tagen/Wochen da schon einiges Vorweggenommen

Vielleicht wurde in den letzten Tagen/Wochen da schon einiges Vorweggenommen


Antwort auf Beitrag Nr.: 39.596.993 von zwitscherton am 28.05.10 00:20:25Natürlich wurde da schon im Vorfeld kurstechnisch eine weitere Verwässerung großteils eingepreist. Die Meldung an sich hat m.E. jedoch eine katastrophale Wirkung, da sie so wie ich es sehe offen lässt, welchen Cash-Zufluss XOMA mit der Aktienneuausgabe überhaupt generieren will. Somit ist m. E. schwer abzuschätzen, wann die nächste Verwässerung folgen wird.
Message: "Nach der Verwässerung ist vor der Verwässerung"?
Das Problem bei solchen Aktien ist m. E., dass hier Wissenschaftler einen zu großen Einfluss haben und dadurch ökonomische Interessen und Aktionärsinteressen nicht die selbe Bedeutung haben, wie bei anderen Unternehmen. Hier geht es halt auch um andere Motive, wie wissenschaftlicher Erfolg, Ansehen u.ä. Es geht nicht primär darum, den Aktionären zum Erfolg zu verhelfen, sondern ein eigenes Medikament zu entwickeln und erfolgreich am Markt zu plazieren (koste es, was es wolle). Wenn kein Geld mehr in der Kasse ist, dann muss man halt nochmal Aktien ausgeben. Das ist aber kein spezielles Phänomen bei XOMA, sondern ein allgemeines Problem bei kleineren Biotech-Unternehmen.
Grüsse, ER
Message: "Nach der Verwässerung ist vor der Verwässerung"?
Das Problem bei solchen Aktien ist m. E., dass hier Wissenschaftler einen zu großen Einfluss haben und dadurch ökonomische Interessen und Aktionärsinteressen nicht die selbe Bedeutung haben, wie bei anderen Unternehmen. Hier geht es halt auch um andere Motive, wie wissenschaftlicher Erfolg, Ansehen u.ä. Es geht nicht primär darum, den Aktionären zum Erfolg zu verhelfen, sondern ein eigenes Medikament zu entwickeln und erfolgreich am Markt zu plazieren (koste es, was es wolle). Wenn kein Geld mehr in der Kasse ist, dann muss man halt nochmal Aktien ausgeben. Das ist aber kein spezielles Phänomen bei XOMA, sondern ein allgemeines Problem bei kleineren Biotech-Unternehmen.
Grüsse, ER
Hält sich ja realtiv gut...klar ist Mist wenn man 40...50 oder 60 % im minus hängt...aber hätte auch schlimmer kommen können....." sollte " es auf die 0,295 € mal fallen ..würde ich einsteigen...aber ist noch nicht in Sicht .
Antwort auf Beitrag Nr.: 39.601.080 von Expertchen007 am 28.05.10 17:06:16dem folge ich!
bei unter 0,30 wirds wieder interessant!
bin ich froh, dass ich im letzten hype null auf null raus bin!
bei unter 0,30 wirds wieder interessant!
bin ich froh, dass ich im letzten hype null auf null raus bin!

Antwort auf Beitrag Nr.: 39.601.080 von Expertchen007 am 28.05.10 17:06:16vergiss es, soweit gehts nicht mehr runter! 
XOMA - Confidential Treatment Order (CT ORDER)
Date : 05/28/2010 @ 3:03PM
Source : Edgar (US Regulatory)

XOMA - Confidential Treatment Order (CT ORDER)
Date : 05/28/2010 @ 3:03PM
Source : Edgar (US Regulatory)
Antwort auf Beitrag Nr.: 39.603.994 von Markus77 am 29.05.10 14:05:43hier zur Erinnerung die letzten CT Orders
http://www.sec.gov/Archives/edgar/data/7...
10.18A Agreement related to LUCENTIS ® License Agreement and RAPTIVA ® Collaboration Agreement dated September 9, 2009, by and between XOMA (Bermuda) Ltd., XOMA (US) LLC and Genentech, Inc. (with certain confidential information omitted, which omitted information is the subject of a confidential treatment request and has been filed separately with the Securities and Exchange Commission)
10.35 Discovery Collaboration Agreement dated September 9, 2009, by and between XOMA Development Corporation and Arana Therapeutics Limited (with certain confidential information omitted, which omitted information is the subject of a confidential treatment request and has been filed separately with the Securities and Exchange Commission)
http://www.sec.gov/Archives/edgar/data/7...
10.37 Amended & Restated Loan Agreement, dated as of May 9, 2008.
http://www.sec.gov/Archives/edgar/data/7...
10.48 First Amendment to Collaboration Agreement, effective as of February 28, 2007, by and between Takeda Pharmaceutical Company Limited and XOMA (US) LLC (with certain confidential information omitted, which omitted information is the subject of a confidential treatment request and has been filed separately with the Securities and Exchange Commission)
http://www.sec.gov/Archives/edgar/data/7...
10.18A Agreement related to LUCENTIS ® License Agreement and RAPTIVA ® Collaboration Agreement dated September 9, 2009, by and between XOMA (Bermuda) Ltd., XOMA (US) LLC and Genentech, Inc. (with certain confidential information omitted, which omitted information is the subject of a confidential treatment request and has been filed separately with the Securities and Exchange Commission)
10.35 Discovery Collaboration Agreement dated September 9, 2009, by and between XOMA Development Corporation and Arana Therapeutics Limited (with certain confidential information omitted, which omitted information is the subject of a confidential treatment request and has been filed separately with the Securities and Exchange Commission)
http://www.sec.gov/Archives/edgar/data/7...
10.37 Amended & Restated Loan Agreement, dated as of May 9, 2008.
http://www.sec.gov/Archives/edgar/data/7...
10.48 First Amendment to Collaboration Agreement, effective as of February 28, 2007, by and between Takeda Pharmaceutical Company Limited and XOMA (US) LLC (with certain confidential information omitted, which omitted information is the subject of a confidential treatment request and has been filed separately with the Securities and Exchange Commission)
Antwort auf Beitrag Nr.: 39.604.444 von Eisenherz1 am 29.05.10 18:46:30Der Link ist nicht vollständig.
Antwort auf Beitrag Nr.: 39.605.662 von zwitscherton am 30.05.10 16:20:28Sorry, hier die Links alle nochmals:
XOMA Ltd. submitted an application under Rule 24b-2 requesting confidential treatment for information it excluded from the Exhibits to a Form 10-Q filed on November 9, 2009, as amended on March 5, 2010.
http://www.sec.gov/Archives/edgar/data/791908/99999999971000…
XOMA Ltd. submitted an application under Rule 24b-2 requesting confidential treatment for information it excluded from the Exhibits to a Form 10-Q/A filed on September 11, 2008, as amended on March 5, 2010.
http://www.sec.gov/Archives/edgar/data/791908/99999999971000…
XOMA Ltd. submitted an application under Rule 24b-2 requesting confidential treatment for information it excluded from the Exhibits to a Form 10-Q filed on May 10, 2007, as amended on March 5, 2010.
http://www.sec.gov/Archives/edgar/data/791908/99999999971000…
XOMA Ltd. submitted an application under Rule 24b-2 requesting confidential treatment for information it excluded from the Exhibits to a Form 10-Q filed on November 9, 2009, as amended on March 5, 2010.
http://www.sec.gov/Archives/edgar/data/791908/99999999971000…
XOMA Ltd. submitted an application under Rule 24b-2 requesting confidential treatment for information it excluded from the Exhibits to a Form 10-Q/A filed on September 11, 2008, as amended on March 5, 2010.
http://www.sec.gov/Archives/edgar/data/791908/99999999971000…
XOMA Ltd. submitted an application under Rule 24b-2 requesting confidential treatment for information it excluded from the Exhibits to a Form 10-Q filed on May 10, 2007, as amended on March 5, 2010.
http://www.sec.gov/Archives/edgar/data/791908/99999999971000…
Haloooooooooooooooooooooooo keiner mehr da???
Jetzt gehts wieder up!!!
Jetzt gehts wieder up!!!

Antwort auf Beitrag Nr.: 39.614.504 von Eisenherz1 am 01.06.10 16:08:59Immerdoch, aber solange keine News kommen was soll ich da sinnlos rumposten 
LG Tommi

LG Tommi
Bin auch immer dabei. Tut sich nur nicht viel.
Antwort auf Beitrag Nr.: 39.616.755 von Zackes1 am 01.06.10 21:13:47AUf den letzten Drücker gings nochmal rauf.
Allerdings die Umsätze sind gering.
KA was das bedeutet.
Hier im Board wurde die Unberechenbarkeit von XOMA bereits mehrfach angesprochen bzw. behaupted..
Mittlererweile glaub ichs aber auch.

Allerdings die Umsätze sind gering.
KA was das bedeutet.
Hier im Board wurde die Unberechenbarkeit von XOMA bereits mehrfach angesprochen bzw. behaupted..
Mittlererweile glaub ichs aber auch.

Antwort auf Beitrag Nr.: 39.616.659 von Tommi33 am 01.06.10 20:59:15vielleicht doch noch bald.... , da könnte doch....
, da könnte doch....
Cimzia Phase II for Psoriasis -> News?!
http://www.nektar.com/product_pipeline/all_phases.html
 , da könnte doch....
, da könnte doch....Cimzia Phase II for Psoriasis -> News?!
http://www.nektar.com/product_pipeline/all_phases.html
Antwort auf Beitrag Nr.: 39.617.251 von zwitscherton am 01.06.10 22:14:37nachbörslich auf die $.049, tja warum nicht... 

Antwort auf Beitrag Nr.: 39.617.251 von zwitscherton am 01.06.10 22:14:37Hey zwitscherton,
Xoma ist abolut unberrechenbar (short gesehen) und nur mit viel Glück und vielleicht auch ein bischen Recherge kannst du hier überleben..., ich selber bin in Xoma seit über einem Jahr investiert, aber meist bisher nur kurzfristig (rein, raus, rein, raus, rein...) und hab mich dabei am Chart orintiert. Das es soweit nochmals runter geht hab ich nicht für möglich gehalten und bin bereits in den .50gern wieder rein.
Derzeit absolut "oversold"!
Also wer in den mitte .40gern nicht rein ist, der braucht später nicht zu jammern...
Viel Glück
Gruß Eisenherz1
Xoma ist abolut unberrechenbar (short gesehen) und nur mit viel Glück und vielleicht auch ein bischen Recherge kannst du hier überleben..., ich selber bin in Xoma seit über einem Jahr investiert, aber meist bisher nur kurzfristig (rein, raus, rein, raus, rein...) und hab mich dabei am Chart orintiert. Das es soweit nochmals runter geht hab ich nicht für möglich gehalten und bin bereits in den .50gern wieder rein.
Derzeit absolut "oversold"!
Also wer in den mitte .40gern nicht rein ist, der braucht später nicht zu jammern...
Viel Glück
Gruß Eisenherz1
heftige Gerüchte in US! und der Kurs zieht an...
aus dem Yahoo-Board:
XOMA RECEIVES BUYOUT LETTER FROM REGENERON $1.00 PER SHARE HOSTILE TAKEOVER LOOM EOM
Quelle:http://messages.finance.yahoo.com/Stocks_(A_to_Z)/Stocks_X/t…
aus dem Yahoo-Board:
XOMA RECEIVES BUYOUT LETTER FROM REGENERON $1.00 PER SHARE HOSTILE TAKEOVER LOOM EOM

Quelle:http://messages.finance.yahoo.com/Stocks_(A_to_Z)/Stocks_X/t…
Antwort auf Beitrag Nr.: 39.623.798 von Eisenherz1 am 02.06.10 22:11:09nachbörslich auf $.538  , da ist doch was im Busch bei dem Volumen!
, da ist doch was im Busch bei dem Volumen!
 , da ist doch was im Busch bei dem Volumen!
, da ist doch was im Busch bei dem Volumen!
Antwort auf Beitrag Nr.: 39.623.885 von Eisenherz1 am 02.06.10 22:21:20So was hatten wir vor einiger Zeit schon einmal.
Müßte mal im Thread zurückblättern um die entsprechenden Einträge zu finden. (mit AH-Charts).

Müßte mal im Thread zurückblättern um die entsprechenden Einträge zu finden. (mit AH-Charts).

Antwort auf Beitrag Nr.: 39.624.448 von zwitscherton am 03.06.10 00:43:23Von ca. 50 Biotechwerten auf mein Watchlist waren heute 4 leicht im Plus oder plusminus 0.
Einer davon war XOMA.
Der Rest wurde desaströs abgestraft.
Warum wohl ???

Einer davon war XOMA.
Der Rest wurde desaströs abgestraft.
Warum wohl ???

Antwort auf Beitrag Nr.: 39.636.176 von zwitscherton am 05.06.10 00:15:06Jetzt wird ja nahezu täglich eine neue Sau durchs Dorf getrieben.
Der Dow hatte den schlechtesten Monat Mai seit 40 Jahren, wie ich vorhin im DAF erfahren durfte.
Im Staud-Report wurde sogar von ein einem Dow von bis zu 8800 Punkten gewarnt.
Das das auch an den Biotechs nicht spurlos vorbeigeht dürfte leider klar sein - selbst wenn solche Wirtschaftlichen Verwerfungen nichts direkt mit deren Potenzialen zu tun hat.

Der Dow hatte den schlechtesten Monat Mai seit 40 Jahren, wie ich vorhin im DAF erfahren durfte.
Im Staud-Report wurde sogar von ein einem Dow von bis zu 8800 Punkten gewarnt.
Das das auch an den Biotechs nicht spurlos vorbeigeht dürfte leider klar sein - selbst wenn solche Wirtschaftlichen Verwerfungen nichts direkt mit deren Potenzialen zu tun hat.

Hallo zusammen,
anscheinend war die anstehe4nde Verwässerung schon weitgehend im Kurs eingepreist, jedenfalls lässt sich eine mögliche Bodenbildung im Bereich von > 0,40 USD erkennen. Ich habe mir eine erste Position XOMA-Aktien gekauft mit dem Ziel, diese bis Q1 2011 kontinuierlich auszubauen. Wahrscheinlich werde ich hierbei nochmals Gelegenheit haben, zu niedrigeren Kursen aufzustocken, dennoch war mir das Risiko zu groß, dass es eine Übernahme oder einen Patentverkauf vor Abschluß der Phase 2 bei XOMA 052 geben könnte. Daher der heutige Kauf einer Anfangsposition mit dem Ziel einer weiteren Akumulation in Schwächephasen.
Grüsse, ER
anscheinend war die anstehe4nde Verwässerung schon weitgehend im Kurs eingepreist, jedenfalls lässt sich eine mögliche Bodenbildung im Bereich von > 0,40 USD erkennen. Ich habe mir eine erste Position XOMA-Aktien gekauft mit dem Ziel, diese bis Q1 2011 kontinuierlich auszubauen. Wahrscheinlich werde ich hierbei nochmals Gelegenheit haben, zu niedrigeren Kursen aufzustocken, dennoch war mir das Risiko zu groß, dass es eine Übernahme oder einen Patentverkauf vor Abschluß der Phase 2 bei XOMA 052 geben könnte. Daher der heutige Kauf einer Anfangsposition mit dem Ziel einer weiteren Akumulation in Schwächephasen.
Grüsse, ER
NASDAQ Grants XOMA's Request for Continued Listing
http://finance.yahoo.com/news/NASDAQ-Grants-XOMAs-Request-pz…
Am 21. Juli wird sich entscheiden, ob es einen RS geben wird.
The determination follows the company's hearing before the Panel on May 6, 2010, at which the Panel considered the company's plan to regain compliance with the minimum bid price requirement, including seeking shareholder approval of a potential reverse stock split at its 2010 annual general meeting of shareholders on July 21, 2010. The company is working diligently to satisfy the terms of the Panel's decision.
http://finance.yahoo.com/news/NASDAQ-Grants-XOMAs-Request-pz…
Am 21. Juli wird sich entscheiden, ob es einen RS geben wird.
The determination follows the company's hearing before the Panel on May 6, 2010, at which the Panel considered the company's plan to regain compliance with the minimum bid price requirement, including seeking shareholder approval of a potential reverse stock split at its 2010 annual general meeting of shareholders on July 21, 2010. The company is working diligently to satisfy the terms of the Panel's decision.
Antwort auf Beitrag Nr.: 39.688.229 von crivit am 16.06.10 06:17:34Sollte es hierzu kommen, hoffe ich das es nicht wie bei so manchen Stocks wieder in den Keller geht.
Bin kein Freund von RS.
Bin kein Freund von RS.
Antwort auf Beitrag Nr.: 39.688.230 von crivit am 16.06.10 06:20:43@ crivit: Wer ist schon "ein Freund von RS"? Aber in diesem Fall ist es mir tausendmal lieber einen RS zu bekommen, als an der Nasdaq delisted zu werden! Folge eines Delistings wäre mit sicherheit auch, dass es schwieriger werden könnte, sich günstig Kapital zu beschaffen. Sobald Unternehmen nicht mehr verpflichtet sind, Quartalsergebnisse zu veröffentlichen, wird es für Aktionäre und Geldgeber zur Farce, die A:L-Situation zu erfassen. Da ist mir ein RS deutlich lieber!
Grüsse, ER
Grüsse, ER
An eurer Stelle würd ich raus gehen und xoma vergessen.die haben schlicht weg versagt.und nach dem RS würd sie wieder fallen dafrauf geb ich euch Brief und Siegel.
Antwort auf Beitrag Nr.: 39.688.816 von extremrelaxer am 16.06.10 09:39:01Die Situation ist doch gefundenes Fressen fürs Management um dann nach dem RS wieder neue Aktien auszugeben. IMO, ich hoffe es nicht.
Antwort auf Beitrag Nr.: 39.689.257 von sneake am 16.06.10 10:30:38"die haben schlicht weg versagt" 
Witzbold! XOMA hat mit XOMA052 den m.E. derzeit interessantesten Bockbluster-Kandidaten überhaupt in der Pipeline. Hierbei wurde mit der Phase 2 deutlich früher begonnen, als ich das vorab geschätzt hatte. Zugleich wird der Wirkstoff gleich bei mehreren Erkrankungen paralell erprobt und aus den bisherigen Ergebnisse zu schließen, scheint XOMA052 in Wirksamkeit und Nebenwirkungsprofil besser, als die konkurrierenden Interleukin-Modulatoren der Konkurrenten abzuschneiden. In Q1 2011 wurde allerdings deutlich mehr Kapital verbrannt, als von mir vorab geschätzt worden war. Dies war für mich auch der Grund, direkt nach Veröffentlichung der Q1-Zahlen erstmal die Reissleine zu ziehen. Auf dem aktuellen Niveau sehe ich aber eine gute Chance-Risiko-Relation, weshalb ich erneut eine Anfangsposition gekauft habe. Charttechnisch haben wir mit der W-Formation einen schönen Boden gefunden und der Trend zeigt jetzt erstmals wieder nach Norden. Aber wie gesagt, ich halte es für durchaus möglich, dass wir in den nächsten Monaten auch nochmals neue Tiefstkurse sehen könnten. Ehrlich gesagt hoffe ich das auch, da ich bis Q1 2011 miene Position in XOMA noch deutlich ausbauen möchte.
Aber von "versagen" kann man hier beim besten Willen nicht sprechen. Die hohen ausgaben in Q1 2010 deuten letztlich doch auch darauf hin, dass man mit aller Kraft die Phase 2 vorantreibt...
Grüsse, ER

Witzbold! XOMA hat mit XOMA052 den m.E. derzeit interessantesten Bockbluster-Kandidaten überhaupt in der Pipeline. Hierbei wurde mit der Phase 2 deutlich früher begonnen, als ich das vorab geschätzt hatte. Zugleich wird der Wirkstoff gleich bei mehreren Erkrankungen paralell erprobt und aus den bisherigen Ergebnisse zu schließen, scheint XOMA052 in Wirksamkeit und Nebenwirkungsprofil besser, als die konkurrierenden Interleukin-Modulatoren der Konkurrenten abzuschneiden. In Q1 2011 wurde allerdings deutlich mehr Kapital verbrannt, als von mir vorab geschätzt worden war. Dies war für mich auch der Grund, direkt nach Veröffentlichung der Q1-Zahlen erstmal die Reissleine zu ziehen. Auf dem aktuellen Niveau sehe ich aber eine gute Chance-Risiko-Relation, weshalb ich erneut eine Anfangsposition gekauft habe. Charttechnisch haben wir mit der W-Formation einen schönen Boden gefunden und der Trend zeigt jetzt erstmals wieder nach Norden. Aber wie gesagt, ich halte es für durchaus möglich, dass wir in den nächsten Monaten auch nochmals neue Tiefstkurse sehen könnten. Ehrlich gesagt hoffe ich das auch, da ich bis Q1 2011 miene Position in XOMA noch deutlich ausbauen möchte.
Aber von "versagen" kann man hier beim besten Willen nicht sprechen. Die hohen ausgaben in Q1 2010 deuten letztlich doch auch darauf hin, dass man mit aller Kraft die Phase 2 vorantreibt...
Grüsse, ER
Antwort auf Beitrag Nr.: 39.690.158 von crivit am 16.06.10 12:16:55Ausgabe neuer Aktien? Möglich, allerdings sehe ich es als mindestens genauso wahrscheinlich an, dass XOMA einen anteil an den späteren Vermarktungsrechten bzw. am Patent auf XOMA052 an einen Big Player verkauft, bzw. dass XOMA auch mit dem Ziel einer einfachereren Vermarktung jetzt schon einen etablierten Pharmaproduzenten mit ins Boot holt. Interessenten an einer Teilhabe dürfte es schließlich wie Sand am Meer geben! 

Antwort auf Beitrag Nr.: 39.690.242 von extremrelaxer am 16.06.10 12:25:02Ich verfolge xoma nun schon seit dem Jahre 2001.schau dir einfach seitdem den kursverlauf an dann weißt was ich meine.
Antwort auf Beitrag Nr.: 39.696.227 von sneake am 17.06.10 10:28:39@ sneake: Seit 2001? Ich beobachte XOMA erst seitdem mir bekannt wurde, dass sich das Unternehmen mit Il-AK beschäftigt. Die Forschung an einem Hautgel gegen Akne und andere ehemalige Beschäftigungsfelder des Unternehmens hätten mich mit Sicherheit nicht so fasziniert! 
Es empfinde es daher auch als ziemlich abwägig, zur Prognose der Kursentwicklung die Kursentwicklung der vergangenen Jahre zu verwenden. Dies könnte man nur, wenn man ein Pickelgel mit einem potentiellen Mega-Blockbuster im Bereich der Antidiabetika und KHK-Medikation vergleichen würde.
Die Situation, in welchem sich das Unternehmen befindet ist weder mit der Unternehmensvergangenheit, noch mit der Situation anderer Unternehmen vergleichbar. Hier wird wohl jeder über XOMA052 informierte Aktionär bei Veröffentlichung der Phase-2-Ergebnisse investiert sein, zugleich gehe ich davon aus, dass auch größere Pharmaunternehmen noch vor der Veröffentlichung der Ergebnisse sich eine Beteiligung am Unternehmen oder am Patent bzw. den späteren Vermarktungsrechten sichern wollen. Q1 2011 mag noch 3 Quartale hin sein. Dennoch halte ich es nicht für abwägig, dass einer der nächsten Kapitalzuflüsse nicht mehr durch Aktienneuausgabe, sondern durch eine strategische Partnerschaft zustande kommen könnte.
Dennoch halte ich es für klüger ein Investment zeitlich gestaffelt aufzubauen, als gleich mit einem einzigen Kauf sich hier zu positionieren.
Grüsse, ER

Es empfinde es daher auch als ziemlich abwägig, zur Prognose der Kursentwicklung die Kursentwicklung der vergangenen Jahre zu verwenden. Dies könnte man nur, wenn man ein Pickelgel mit einem potentiellen Mega-Blockbuster im Bereich der Antidiabetika und KHK-Medikation vergleichen würde.

Die Situation, in welchem sich das Unternehmen befindet ist weder mit der Unternehmensvergangenheit, noch mit der Situation anderer Unternehmen vergleichbar. Hier wird wohl jeder über XOMA052 informierte Aktionär bei Veröffentlichung der Phase-2-Ergebnisse investiert sein, zugleich gehe ich davon aus, dass auch größere Pharmaunternehmen noch vor der Veröffentlichung der Ergebnisse sich eine Beteiligung am Unternehmen oder am Patent bzw. den späteren Vermarktungsrechten sichern wollen. Q1 2011 mag noch 3 Quartale hin sein. Dennoch halte ich es nicht für abwägig, dass einer der nächsten Kapitalzuflüsse nicht mehr durch Aktienneuausgabe, sondern durch eine strategische Partnerschaft zustande kommen könnte.
Dennoch halte ich es für klüger ein Investment zeitlich gestaffelt aufzubauen, als gleich mit einem einzigen Kauf sich hier zu positionieren.
Grüsse, ER
Antwort auf Beitrag Nr.: 39.696.959 von extremrelaxer am 17.06.10 11:56:08na dann viel erfolg mit xoma.

Xoma ist eine Schrottaktie das hab ich schon oft genug hier erwähnt, der Cashhunger ist riesig bisher haben sie sich vorm Bankrott gerettet dank fake News .
Ohne Partner droht bald wieder Bankrott mal sehen was sie sich diesmal einfallen lassen ..
Liquidity and Capital Resources
Cash used in operating activities during the first quarter of 2010 was $16.4 million compared with cash provided by operating activities of $15.3 million during the first quarter of 2010. The decrease in cash provided by operating activities in the 2010 period was primarily due to a decrease in revenue receipts for license and collaborative fees and royalties. In the first quarter of 2009, we received $23.2 million related to the expansion of our existing collaboration with Takeda, and recognized royalty revenue from sales of LUCENTIS(R) and RAPTIVA(R) of $4.6 million.
Guidance
The company will not be providing specific guidance on overall revenues or cash receipts for 2010 so as to best manage its ongoing negotiations for XOMA 052 and technology licensing and in light of general economic and market conditions. The company expects that cash used in operating activities in 2010 may range from $45 million to cash neutral or positive.
Ohne Partner droht bald wieder Bankrott mal sehen was sie sich diesmal einfallen lassen ..
Liquidity and Capital Resources
Cash used in operating activities during the first quarter of 2010 was $16.4 million compared with cash provided by operating activities of $15.3 million during the first quarter of 2010. The decrease in cash provided by operating activities in the 2010 period was primarily due to a decrease in revenue receipts for license and collaborative fees and royalties. In the first quarter of 2009, we received $23.2 million related to the expansion of our existing collaboration with Takeda, and recognized royalty revenue from sales of LUCENTIS(R) and RAPTIVA(R) of $4.6 million.
Guidance
The company will not be providing specific guidance on overall revenues or cash receipts for 2010 so as to best manage its ongoing negotiations for XOMA 052 and technology licensing and in light of general economic and market conditions. The company expects that cash used in operating activities in 2010 may range from $45 million to cash neutral or positive.
Positive Clinical Findings Presented on XOMA 052 in Debilitating Eye Disease
Results of Pilot Study in Patients With Uveitis of Behcet's Disease Presented at EULAR
ROME, June 17, 2010 (GLOBE NEWSWIRE) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced positive results from an open-label pilot study of XOMA 052 in patients with uveitis of Behcet's disease who were suffering from vision-threatening exacerbations despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052, a therapeutic antibody candidate that inhibits the inflammatory cytokine interleukin-1 beta (IL-1 beta). The preliminary results of the first clinical trial of XOMA 052 in patients with uveitis of Behcet's disease were presented today at the Annual Congress of the European League against Rheumatism (EULAR) in Rome, Italy.
Uveitis, or inflammation of the intraocular tissues of the eye, of Behcet's disease is one of the most severe forms of uveitis and affects approximately half of the patients with Behcet's disease. Unlike many forms of chronic uveitis, Behcet's uveitis is characterized by recurrent acute attacks or exacerbations. Without immediate treatment, major exacerbations of Behcet's uveitis may lead to retinal detachment, vitreous hemorrhage, glaucoma and eventual blindness. Symptoms include the accumulation of vitreous haze which can block eyesight or the loss of visual acuity and can manifest differently from patient to patient. For example, patients may go from 20/20 eyesight to loss of vision during the course of an exacerbation.
"Behcet's uveitis can lead to progressive and permanent loss of visual acuity. Unfortunately, there is no cure and current treatments are limited to corticosteroids and immunosuppressive drugs, all of which have significant side effects, especially when used on a chronic basis," explained Dr. Ahmet Gul, principal investigator of the pilot study and Professor of Medicine, Istanbul University, one of the largest centers of study for Behcet's disease in the world. "Over-expression of IL-1 beta and downstream pro-inflammatory cytokines play critical roles in Behcet's disease. Targeting IL-1 beta inhibits the inflammatory process and has the potential to improve eyesight in these patients without the toxic side effects of current therapies. We are encouraged with the data generated so far, notably that we saw very clear improvements in these patients following treatment with XOMA 052, despite the removal of immunosuppressive medicines."
Each of the seven patients presented with active exacerbations of uveitis despite receiving maximal doses of immunosuppressive medicines. Each received a 0.3 mg/kg intravenous infusion of XOMA 052 and simultaneously stopped taking immunosuppressive drugs such as cyclosporine and/or azathioprine. All continued treatment with low doses of corticosteroids. Patients' status was measured using multiple objective parameters associated with ocular health, including patients' visual acuity, vitreous haze score, anterior chamber cells, fundus score, and the patients' flare score.
All seven patients demonstrated improvement in intraocular inflammation starting within one day of treatment with a single dose of XOMA 052 and achieved clinically significant improvement of retinal problems and vitreous haze four to 21 days following treatment. Visual acuity improvements were evident following treatment with XOMA 052, and six out of seven patients remained in remission 28 days after a single treatment. Five patients received a second infusion between days 29 and 95 to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported.
"The results of the XOMA 052 study show great promise for Behcet's patients suffering from recurrent uveitis, which can cause permanent vision loss," said Joyce Kullman, Executive Director of the Vasculitis Foundation. "Given that there is no satisfactory standard of care for treating Behcet's uveitis and at present the only therapeutic options are limited, developing an effective therapy is critical. XOMA 052 may offer leading-edge promising care for our patients."
"We have watched with great interest over the last several months as mounting preclinical and clinical evidence clearly demonstrate the potential of targeting IL-1 beta to treat inflammation in a broad range of diseases like diabetes, cardiovascular and gout," said Patrick J. Scannon, M.D., Ph.D., XOMA's Executive Vice President and Chief Medical Officer. "These data in Behcet's uveitis, in which all patients treated with XOMA 052 have shown marked improvement, highlight yet another potential application of XOMA 052 in treatment of inflammatory-mediated diseases. While we recognize that larger studies must be conducted, we are very pleased with these results."
"While we remain focused on developing XOMA 052 in patients with Type 2 diabetes and cardiovascular disease, the generation of these initial positive results in an orphan indication could provide an accelerated regulatory pathway," noted Steven B. Engle, Chairman and Chief Executive Officer of XOMA. "We believe the results of this study provide additional evidence of the importance of the role of IL-1 in inflammatory diseases and the potential value of XOMA 052."
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. An estimated 5,000 to 15,000 patients in the United States have Behcet's, and the disease is more common in Turkey, eastern Mediterranean countries, Japan and Korea.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
Results of Pilot Study in Patients With Uveitis of Behcet's Disease Presented at EULAR
ROME, June 17, 2010 (GLOBE NEWSWIRE) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced positive results from an open-label pilot study of XOMA 052 in patients with uveitis of Behcet's disease who were suffering from vision-threatening exacerbations despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052, a therapeutic antibody candidate that inhibits the inflammatory cytokine interleukin-1 beta (IL-1 beta). The preliminary results of the first clinical trial of XOMA 052 in patients with uveitis of Behcet's disease were presented today at the Annual Congress of the European League against Rheumatism (EULAR) in Rome, Italy.
Uveitis, or inflammation of the intraocular tissues of the eye, of Behcet's disease is one of the most severe forms of uveitis and affects approximately half of the patients with Behcet's disease. Unlike many forms of chronic uveitis, Behcet's uveitis is characterized by recurrent acute attacks or exacerbations. Without immediate treatment, major exacerbations of Behcet's uveitis may lead to retinal detachment, vitreous hemorrhage, glaucoma and eventual blindness. Symptoms include the accumulation of vitreous haze which can block eyesight or the loss of visual acuity and can manifest differently from patient to patient. For example, patients may go from 20/20 eyesight to loss of vision during the course of an exacerbation.
"Behcet's uveitis can lead to progressive and permanent loss of visual acuity. Unfortunately, there is no cure and current treatments are limited to corticosteroids and immunosuppressive drugs, all of which have significant side effects, especially when used on a chronic basis," explained Dr. Ahmet Gul, principal investigator of the pilot study and Professor of Medicine, Istanbul University, one of the largest centers of study for Behcet's disease in the world. "Over-expression of IL-1 beta and downstream pro-inflammatory cytokines play critical roles in Behcet's disease. Targeting IL-1 beta inhibits the inflammatory process and has the potential to improve eyesight in these patients without the toxic side effects of current therapies. We are encouraged with the data generated so far, notably that we saw very clear improvements in these patients following treatment with XOMA 052, despite the removal of immunosuppressive medicines."
Each of the seven patients presented with active exacerbations of uveitis despite receiving maximal doses of immunosuppressive medicines. Each received a 0.3 mg/kg intravenous infusion of XOMA 052 and simultaneously stopped taking immunosuppressive drugs such as cyclosporine and/or azathioprine. All continued treatment with low doses of corticosteroids. Patients' status was measured using multiple objective parameters associated with ocular health, including patients' visual acuity, vitreous haze score, anterior chamber cells, fundus score, and the patients' flare score.
All seven patients demonstrated improvement in intraocular inflammation starting within one day of treatment with a single dose of XOMA 052 and achieved clinically significant improvement of retinal problems and vitreous haze four to 21 days following treatment. Visual acuity improvements were evident following treatment with XOMA 052, and six out of seven patients remained in remission 28 days after a single treatment. Five patients received a second infusion between days 29 and 95 to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported.
"The results of the XOMA 052 study show great promise for Behcet's patients suffering from recurrent uveitis, which can cause permanent vision loss," said Joyce Kullman, Executive Director of the Vasculitis Foundation. "Given that there is no satisfactory standard of care for treating Behcet's uveitis and at present the only therapeutic options are limited, developing an effective therapy is critical. XOMA 052 may offer leading-edge promising care for our patients."
"We have watched with great interest over the last several months as mounting preclinical and clinical evidence clearly demonstrate the potential of targeting IL-1 beta to treat inflammation in a broad range of diseases like diabetes, cardiovascular and gout," said Patrick J. Scannon, M.D., Ph.D., XOMA's Executive Vice President and Chief Medical Officer. "These data in Behcet's uveitis, in which all patients treated with XOMA 052 have shown marked improvement, highlight yet another potential application of XOMA 052 in treatment of inflammatory-mediated diseases. While we recognize that larger studies must be conducted, we are very pleased with these results."
"While we remain focused on developing XOMA 052 in patients with Type 2 diabetes and cardiovascular disease, the generation of these initial positive results in an orphan indication could provide an accelerated regulatory pathway," noted Steven B. Engle, Chairman and Chief Executive Officer of XOMA. "We believe the results of this study provide additional evidence of the importance of the role of IL-1 in inflammatory diseases and the potential value of XOMA 052."
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. An estimated 5,000 to 15,000 patients in the United States have Behcet's, and the disease is more common in Turkey, eastern Mediterranean countries, Japan and Korea.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
Antwort auf Beitrag Nr.: 39.697.996 von Zackes1 am 17.06.10 14:12:50Die Gattung ist wegen Kursaussetzung gesperrt.
Wenn ich das Potential von XOMA052 richtig einschätze, dann werde ich diese Meldung wohl noch öfters von meinem Broker bekommen!
"Schrottaktie" halt!


Bashen bringt nichts mehr, kauft die aktie oder lasst es sein!
Wenn ich das Potential von XOMA052 richtig einschätze, dann werde ich diese Meldung wohl noch öfters von meinem Broker bekommen!
"Schrottaktie" halt!



Bashen bringt nichts mehr, kauft die aktie oder lasst es sein!
XOMA: All Patients In Trial Showed Rapid Reduction Of Intraocular Inflammation With XOMA 052.
Handel scheit heute vorerst ausgesetzt zu werden - so zumidnest im Yahoo Board.
Handel scheit heute vorerst ausgesetzt zu werden - so zumidnest im Yahoo Board.
XOMA (XOMA) trading halted news pending
More News related to XOMA
* XOMA (XOMA) Announces Positive Data from XOMA 052 Study in Patients with Uvetis of Behcet's Disease
* XOMA (XOMA) says all patients in a trial on Xoma-052 demonstrated improvement
* XOMA (XOMA) trading halted news pending
* Positive Clinical Findings Presented on XOMA 052 in Debilitating Eye Disease
* XOMA (XOMA) Gets Extension from Nasdaq for to Meet Continued Listing Compliance
More News related to XOMA
More News related to Corporate News
June 17, 2010 8:00 AM EDT
XOMA (Nasdaq: XOMA) trading halted news pending
More News related to XOMA
* XOMA (XOMA) Announces Positive Data from XOMA 052 Study in Patients with Uvetis of Behcet's Disease
* XOMA (XOMA) says all patients in a trial on Xoma-052 demonstrated improvement
* XOMA (XOMA) trading halted news pending
* Positive Clinical Findings Presented on XOMA 052 in Debilitating Eye Disease
* XOMA (XOMA) Gets Extension from Nasdaq for to Meet Continued Listing Compliance
More News related to XOMA
More News related to Corporate News
June 17, 2010 8:00 AM EDT
XOMA (Nasdaq: XOMA) trading halted news pending
Zur Info aus dem Yahoo Board:
Code T.3
http://nasdaqtrader.com/trader.aspx?id=T...
http://nasdaqtrader.com/Trader.aspx?id=T...
Halt - Resumption Times
The news has been fully disseminated through a Regulation FD compliant method(s); or NASDAQ has determined either that system misuse or malfunction that caused extraordinary market activity will no longer have a material effect on the market for the security or that system misuse or malfunction is not the cause of the extraordinary market activity; or NASDAQ has determined the conditions which led to a halt in an Exchange-Traded Fund are no longer present. Two times will be displayed: (1) the time when market participants can enter quotations, followed by (2) the time the security will be released for trading. All trade halt and resumption times will be posted in HH:MM:SS format.
Code T.3
http://nasdaqtrader.com/trader.aspx?id=T...
http://nasdaqtrader.com/Trader.aspx?id=T...
Halt - Resumption Times
The news has been fully disseminated through a Regulation FD compliant method(s); or NASDAQ has determined either that system misuse or malfunction that caused extraordinary market activity will no longer have a material effect on the market for the security or that system misuse or malfunction is not the cause of the extraordinary market activity; or NASDAQ has determined the conditions which led to a halt in an Exchange-Traded Fund are no longer present. Two times will be displayed: (1) the time when market participants can enter quotations, followed by (2) the time the security will be released for trading. All trade halt and resumption times will be posted in HH:MM:SS format.
Antwort auf Beitrag Nr.: 39.698.085 von extremrelaxer am 17.06.10 14:25:29WOW wirksam in achtung 7Patienten  sowas bezeichne ich als FAKE News und dient nur dazu den Kurs dank der ahnungslosen Lemminge in die höhe zu treiben aber auch nur kurzfristig .
sowas bezeichne ich als FAKE News und dient nur dazu den Kurs dank der ahnungslosen Lemminge in die höhe zu treiben aber auch nur kurzfristig .
 sowas bezeichne ich als FAKE News und dient nur dazu den Kurs dank der ahnungslosen Lemminge in die höhe zu treiben aber auch nur kurzfristig .
sowas bezeichne ich als FAKE News und dient nur dazu den Kurs dank der ahnungslosen Lemminge in die höhe zu treiben aber auch nur kurzfristig .
Antwort auf Beitrag Nr.: 39.697.996 von Zackes1 am 17.06.10 14:12:50Studie, in der 7 Patienten unerwartet gute Resultate zeigten
HMM! 7 Patienten - das hat noch keine wissenschaftliche Aussagekraft! Das sind Einzelfälle!
dennoch, wie hier richtig erwähnt wird, könnte ...
"initial positive results in an orphan indication could provide an accelerated regulatory pathway,"
aber ist damit die Aussetzung vom Handel zu rehtfertigen? Oder ist das nur um Aufmerksamkeit zu erlangen (gelungen)
HMM! 7 Patienten - das hat noch keine wissenschaftliche Aussagekraft! Das sind Einzelfälle!
dennoch, wie hier richtig erwähnt wird, könnte ...
"initial positive results in an orphan indication could provide an accelerated regulatory pathway,"
aber ist damit die Aussetzung vom Handel zu rehtfertigen? Oder ist das nur um Aufmerksamkeit zu erlangen (gelungen)
Antwort auf Beitrag Nr.: 39.698.233 von dottore am 17.06.10 14:40:51Oder ist vielleicht ein buyout im Anmarsch? 

Antwort auf Beitrag Nr.: 39.698.145 von BrauchGeld am 17.06.10 14:32:07hey brauchgeld! warst etwas schneller als ich 

Antwort auf Beitrag Nr.: 39.698.145 von BrauchGeld am 17.06.10 14:32:07@ BrauchGeld:
Keine Frage, n ist wirklich klein und mit dem M. Behcet lässt sich auch kein Geld verdienen. Darum geht es hier aber überhaupt nicht. Es geht darum, aufzuzeigen, dass der IL-AK hochwirksam bei einer Vielzahl von autoimmunologischen und inflammatorischen Erkrankungen ist.
Ich brauche Dir wohl nicht erzählen, was es für einen großen deutschen Pharmakonzern über Jahrzehnte hin bedeutet hat und weiterhin bedeutet, ein antiinflamatorisches Medikament auf den Markt gebracht zu haben: ASS
Hier geht es um einen Mega-Blockbuster mit dem Potential von Mrd- Umsätzen. Da muss man halt auch einkalkulieren, dass im Rahmen der klinischen Tests erstmal nur Kohle verbrannt wird. Dir kann ich jedoch nur empfehlen, weiterzuziehen und vieleicht mal Bayer anzuschauen: Das wäre wohl eher eine Aktie für Dich!
Keine Frage, n ist wirklich klein und mit dem M. Behcet lässt sich auch kein Geld verdienen. Darum geht es hier aber überhaupt nicht. Es geht darum, aufzuzeigen, dass der IL-AK hochwirksam bei einer Vielzahl von autoimmunologischen und inflammatorischen Erkrankungen ist.
Ich brauche Dir wohl nicht erzählen, was es für einen großen deutschen Pharmakonzern über Jahrzehnte hin bedeutet hat und weiterhin bedeutet, ein antiinflamatorisches Medikament auf den Markt gebracht zu haben: ASS
Hier geht es um einen Mega-Blockbuster mit dem Potential von Mrd- Umsätzen. Da muss man halt auch einkalkulieren, dass im Rahmen der klinischen Tests erstmal nur Kohle verbrannt wird. Dir kann ich jedoch nur empfehlen, weiterzuziehen und vieleicht mal Bayer anzuschauen: Das wäre wohl eher eine Aktie für Dich!
Auf jeden Fall kann es für die Shorter sehr unangenehm werden. 

Im Pre Market aktuell bei 0,54
UPDATE 1-Xoma says eye drug shows promise in clinical study
Thu Jun 17, 2010 9:04am EDTRelated NewsUPDATE 1-Immunomedics says lupus drug shows efficacy
Wed, Jun 16 2010
CORRECTED - CORRECTED-UPDATE 1-Raptor Pharma key drug gets EU orphan status
Tue, Jun 15 2010
Cheap gout drug shows promise in kidney disease
Thu, Jun 10 2010
Cheap gout drug shows promise in kidney disease
Thu, Jun 10 2010
UPDATE 3-Regeneron gout drug works in one trial, fails other
Wed, Jun 9 2010Stocks
XOMA Ltd
XOMA.O
$0.47
-0.02-4.06%12:00am UTC+0200
* Says all 7 patients showed response
Stocks | Global Markets | Healthcare
* Says no drug-related adverse events reported
* Shares up 15 pct premarket
June 17 (Reuters) - Biotechnology company Xoma Ltd (XOMA.O) said its experimental treatment for an eye condition showed improvement in all seven patients enrolled in the study, sending its shares up 15 percent before the bell.
The compound, XOMA 052, produced clinically significant improvement in retinal problems faced by patients suffering from Behcet's disease.
Behcet's disease is a condition that involves inflammation of the blood vessels and its symptoms include mouth ulcers, genital ulcers, and inflammation of a specialized area around the pupil of the eye.
Xoma also said XOMA 052 appeared to be safe and no drug-related adverse events were noted in the study.
Shares of the company, which have lost about half of their value in the last 52 weeks, were up 15 percent at 54 cents Thursday in trading before the bell. They closed at 47 cents Wednesday on Nasdaq. (Reporting by Vidya L Nathan in Bangalore; Editing by Aradhana Aravindan)
http://www.reuters.com/article/idUSSGE65G0FB20100617
Thu Jun 17, 2010 9:04am EDTRelated NewsUPDATE 1-Immunomedics says lupus drug shows efficacy
Wed, Jun 16 2010
CORRECTED - CORRECTED-UPDATE 1-Raptor Pharma key drug gets EU orphan status
Tue, Jun 15 2010
Cheap gout drug shows promise in kidney disease
Thu, Jun 10 2010
Cheap gout drug shows promise in kidney disease
Thu, Jun 10 2010
UPDATE 3-Regeneron gout drug works in one trial, fails other
Wed, Jun 9 2010Stocks
XOMA Ltd
XOMA.O
$0.47
-0.02-4.06%12:00am UTC+0200
* Says all 7 patients showed response
Stocks | Global Markets | Healthcare
* Says no drug-related adverse events reported
* Shares up 15 pct premarket
June 17 (Reuters) - Biotechnology company Xoma Ltd (XOMA.O) said its experimental treatment for an eye condition showed improvement in all seven patients enrolled in the study, sending its shares up 15 percent before the bell.
The compound, XOMA 052, produced clinically significant improvement in retinal problems faced by patients suffering from Behcet's disease.
Behcet's disease is a condition that involves inflammation of the blood vessels and its symptoms include mouth ulcers, genital ulcers, and inflammation of a specialized area around the pupil of the eye.
Xoma also said XOMA 052 appeared to be safe and no drug-related adverse events were noted in the study.
Shares of the company, which have lost about half of their value in the last 52 weeks, were up 15 percent at 54 cents Thursday in trading before the bell. They closed at 47 cents Wednesday on Nasdaq. (Reporting by Vidya L Nathan in Bangalore; Editing by Aradhana Aravindan)
http://www.reuters.com/article/idUSSGE65G0FB20100617
JUNE 17, 2010, 8:59 A.M. ET.XOMA Rallies On 'Positive' Antibody Study Results
DOW JONES NEWSWIRES
XOMA Ltd. (XOMA) announced "positive" results from a study of its flagship antibody involved in fighting Behcet's disease, vaulting shares in premarket trading.
The antibody discovery and development company's stock rose 13% premarket to 53 cents. The stock through Wednesday was down 33% this year.
Behcet's disease can prompt inflammation of some tissues in the eye, which can result in vision problems as well as progressive problems such as retinal detachment, glaucoma and eventual blindness.
XOMA said all seven patients who were enrolled in the trial displayed a "rapid reduction" of inflammation and improvement in their visual activity or other ophthalmic measures following a single treatment with its XOMA 052 antibody.
Chief Medical Offer Patrick Scannon said the company is "very pleased with the results" and that it indicates that Behcets may be another application of XOMA 052. The antibody's applications include a wide variety of inflammatory diseases, including Type 2 diabetes, cardiovascular disease and rheumatoid arthritis.
In May, XOMA swung to a first-quarter loss as its revenue declined sharply.
-By Nathan Becker, Dow Jones Newswires; 212-416-2855; nathan.becker@dowjones.com;
http://online.wsj.com/article/BT-CO-20100617-706550.html?mod…
DOW JONES NEWSWIRES
XOMA Ltd. (XOMA) announced "positive" results from a study of its flagship antibody involved in fighting Behcet's disease, vaulting shares in premarket trading.
The antibody discovery and development company's stock rose 13% premarket to 53 cents. The stock through Wednesday was down 33% this year.
Behcet's disease can prompt inflammation of some tissues in the eye, which can result in vision problems as well as progressive problems such as retinal detachment, glaucoma and eventual blindness.
XOMA said all seven patients who were enrolled in the trial displayed a "rapid reduction" of inflammation and improvement in their visual activity or other ophthalmic measures following a single treatment with its XOMA 052 antibody.
Chief Medical Offer Patrick Scannon said the company is "very pleased with the results" and that it indicates that Behcets may be another application of XOMA 052. The antibody's applications include a wide variety of inflammatory diseases, including Type 2 diabetes, cardiovascular disease and rheumatoid arthritis.
In May, XOMA swung to a first-quarter loss as its revenue declined sharply.
-By Nathan Becker, Dow Jones Newswires; 212-416-2855; nathan.becker@dowjones.com;
http://online.wsj.com/article/BT-CO-20100617-706550.html?mod…
Antwort auf Beitrag Nr.: 39.698.277 von extremrelaxer am 17.06.10 14:45:12da du an einem antiinflammatorischen Medikament, hier IL interessiert scheinst, schau auch mal bei Adeona nach.
Die haben schon länger einen Wirkstoff, der bei Rheumatischer Arthritis erprobt wird und wohl nicht nur dort zur Anwendung kommen sollte. Darüber hinaus sprechen auch noch andere Fakten für Adeona. Ganz im Gegensatz zu Xoma.
Bin deshalb auch schon lange nicht mehr hier investiert, schaue aber immer mal wieder hier her und bin bisher nur zufrieden, damit nicht mehr hier investiert zu sein. Das gilt auch für Kurs unter 90 Cent
Die haben schon länger einen Wirkstoff, der bei Rheumatischer Arthritis erprobt wird und wohl nicht nur dort zur Anwendung kommen sollte. Darüber hinaus sprechen auch noch andere Fakten für Adeona. Ganz im Gegensatz zu Xoma.
Bin deshalb auch schon lange nicht mehr hier investiert, schaue aber immer mal wieder hier her und bin bisher nur zufrieden, damit nicht mehr hier investiert zu sein. Das gilt auch für Kurs unter 90 Cent
Antwort auf Beitrag Nr.: 39.698.326 von Zackes1 am 17.06.10 14:50:14Wie immer bei Xoma, im Pre phantastisch, Start geht noch und dann geht es abwärts.
SK wird wohl wieder mal < 0,47$ sein, also Minus.

SK wird wohl wieder mal < 0,47$ sein, also Minus.


Also alles wie immer. Wäre ja auch zu schön gewesen.
hmm gabs n trading halt heute bei xoma????
Antwort auf Beitrag Nr.: 39.701.370 von schokie am 17.06.10 21:10:39ja ja wenn man nur n paar seiten zurück blättern würde können 



Antwort auf Beitrag Nr.: 39.701.370 von schokie am 17.06.10 21:10:39war zwar ne gute meldung, kurs hat aber so gut wie nicht reagiert.
Antwort auf Beitrag Nr.: 39.698.585 von extremrelaxer am 17.06.10 15:16:14UPDATE 2-Xoma says eye drug shows promise in clinical study
Thu Jun 17, 2010 12:09pm EDT
Stocks
XOMA Ltd
XOMA.O
$0.48
+0.01+2.13%
9:00pm GMT+0200
* Says all 7 patients showed response
Says no drug-related adverse events reported
(Adds analyst comment; updates share movement)
BANGALORE, June 17 (Reuters) - Biotechnology company Xoma Ltd (XOMA.O) said its experimental treatment for an eye condition showed improvement in all seven patients enrolled in the study, sending its shares up 15 percent before the bell.
The compound, XOMA 052, produced clinically significant improvement in retinal problems faced by patients suffering from Behcet's disease.
Behcet's disease is a condition that involves inflammation of the blood vessels and its symptoms include mouth ulcers, genital ulcers and inflammation of a specialized area around the pupil of the eye.
Xoma also said XOMA 052 appeared to be safe and no drug-related adverse events were noted in the study.
Of the two indications that the drug is being tested in, Xoma could try and develop the compound, XOMA 052, on its own for Behcet's disease, Wedbush Securities Inc analyst Liana Moussatos said..
XOMA 052 is also currently being tested in mid-stage trials as treatment for type 2 diabetes.
"Diabetes - that is definitely going to be the bread-winner, but they will definitely need a partner to take it through phase 3 and then commercialize it," Moussatos said.
She expects a partnership on the drug to be triggered by data from two mid-stage trials of the compound in diabetes patients.
Data from these trials are expected at the end of 2010 or beginning next year.
However, the company faces no pressure to partner the drug before the mid-stage data is out, with enough cash to last until then, Moussatos added.
Xoma had cash and cash equivalents of $28.4 million, at March 31, 2010.
Shares of the company, which have lost about half of their value in the last 52 weeks, were flat at 47 cents Thursday on Nasdaq. (Reporting by Vidya L Nathan in Bangalore; Editing by Aradhana Aravindan and Prem Udayabhanu)
http://www.reuters.com/article/idCNSGE65G0FB20100617?rpc=44
Thu Jun 17, 2010 12:09pm EDT
Stocks
XOMA Ltd
XOMA.O
$0.48
+0.01+2.13%
9:00pm GMT+0200
* Says all 7 patients showed response
Says no drug-related adverse events reported
(Adds analyst comment; updates share movement)
BANGALORE, June 17 (Reuters) - Biotechnology company Xoma Ltd (XOMA.O) said its experimental treatment for an eye condition showed improvement in all seven patients enrolled in the study, sending its shares up 15 percent before the bell.
The compound, XOMA 052, produced clinically significant improvement in retinal problems faced by patients suffering from Behcet's disease.
Behcet's disease is a condition that involves inflammation of the blood vessels and its symptoms include mouth ulcers, genital ulcers and inflammation of a specialized area around the pupil of the eye.
Xoma also said XOMA 052 appeared to be safe and no drug-related adverse events were noted in the study.
Of the two indications that the drug is being tested in, Xoma could try and develop the compound, XOMA 052, on its own for Behcet's disease, Wedbush Securities Inc analyst Liana Moussatos said..
XOMA 052 is also currently being tested in mid-stage trials as treatment for type 2 diabetes.
"Diabetes - that is definitely going to be the bread-winner, but they will definitely need a partner to take it through phase 3 and then commercialize it," Moussatos said.
She expects a partnership on the drug to be triggered by data from two mid-stage trials of the compound in diabetes patients.
Data from these trials are expected at the end of 2010 or beginning next year.
However, the company faces no pressure to partner the drug before the mid-stage data is out, with enough cash to last until then, Moussatos added.
Xoma had cash and cash equivalents of $28.4 million, at March 31, 2010.
Shares of the company, which have lost about half of their value in the last 52 weeks, were flat at 47 cents Thursday on Nasdaq. (Reporting by Vidya L Nathan in Bangalore; Editing by Aradhana Aravindan and Prem Udayabhanu)
http://www.reuters.com/article/idCNSGE65G0FB20100617?rpc=44
Bin mal gespannt wie es heute weiter geht
so ich melde mich hier auch mal zurück nach langer abwesenheit 
gibts schon neuigkeiten zwecks eines RS?
was war denn der genaue grund des kurseinbruch seit dem kleinen anstieg auf 60 cent mitte april? weiß hier einer genauerers?
soweit ich weiß steht hier doch bald eine neue phase an, ebenso wie die suche nach einem partner nach wie vor läuft und doch die ersten ergebnisse einer studie nicht schlecht gewesen sein sollen!?!?!?
@Alfred alter xomanier,
weisst du näheres, was hier schon wieder so auf die stimmung drückt?
gabs eigentlich schon wieder mal was bezüglich dem delisting?

gibts schon neuigkeiten zwecks eines RS?
was war denn der genaue grund des kurseinbruch seit dem kleinen anstieg auf 60 cent mitte april? weiß hier einer genauerers?
soweit ich weiß steht hier doch bald eine neue phase an, ebenso wie die suche nach einem partner nach wie vor läuft und doch die ersten ergebnisse einer studie nicht schlecht gewesen sein sollen!?!?!?
@Alfred alter xomanier,
weisst du näheres, was hier schon wieder so auf die stimmung drückt?
gabs eigentlich schon wieder mal was bezüglich dem delisting?
Antwort auf Beitrag Nr.: 39.718.599 von Markus77 am 22.06.10 10:55:53RS steht an um Delisting zu umgehen.
Entscheidung fällt am 21ten Juli.
Entscheidung fällt am 21ten Juli.
Antwort auf Beitrag Nr.: 39.719.236 von crivit am 22.06.10 12:27:19ohwee was meinste crivit?
da heben sich mir zweifel an, du musst bedenken, die müssen den kurs über nen 1$ bringen und wir haben nichtmal 0,50 cent
da heben sich mir zweifel an, du musst bedenken, die müssen den kurs über nen 1$ bringen und wir haben nichtmal 0,50 cent

BERKELEY, Calif., Jun 22, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced the publication of data from a mouse model of diet-induced obesity in the June, 2010 edition of the journal Endocrinology. The data showed that mice treated with XOMA 052 both prophylactically and therapeutically experienced improvement in measures associated with diabetes and cardiovascular disease including reduction in glycosylated hemoglobin (HbA1c) levels, improvement in glucose control, improved beta-cell survival and function, and a reduction in total cholesterol without reduction in high density lipoprotein. Each of these parameters is an important goal for the management of Type 2 diabetes, and well-controlled blood glucose levels and reductions in lipid levels can help minimize the risk of long-term consequences associated with diabetes. Much of the data were presented at the American Diabetes Association's 2009 Scientific Sessions.
"Rarely do results from animal models mirror what we see in humans. So far, what we've seen when we compare mouse data to the Phase 1 human data is very encouraging, and while there are limitations to this comparison, we are hopeful that the similarities will carry through to our Phase 2a and Phase 2b data," said Patrick J. Scannon, M.D., Ph.D., Executive Vice President and Chief Medical Officer of XOMA. "With results demonstrating reduction in total cholesterol without decreasing high density lipoprotein, also referred to as 'good cholesterol', the data also highlight the potential application of IL-1 beta inhibition in the treatment of cardiovascular diseases."
In the experiments detailed in the paper, groups of mice received a high fat diet. Without treatment, the mice exhibited signs of Type 2 diabetes such as elevated blood glucose and HbA1c levels, impaired glucose tolerance and impaired insulin secretion. Treatment with XOMA 052 prevented these abnormalities as compared to treatment with an inactive control antibody. Treatment with XOMA 052 also reduced beta-cell apoptosis and increased beta-cell proliferation in the mice fed the high fat diet, and mice treated with XOMA 052 demonstrated improvements in insulin resistance induced by the high fat diet compared to control. The data provide evidence that targeting IL-1 beta in vivo could improve insulin sensitivity.
In addition, the study examined lipid levels in mice fed the high fat diet and either treated with XOMA 052 or the control. Without treatment, mice eating the high fat diet showed increases in the blood levels of lipids like total cholesterol, triglycerides and free fatty acids. The mice treated with XOMA 052 demonstrated reduced levels of lipids compared to the control.
XOMA also announced that two posters on XOMA 052 in the treatment of Type 2 diabetes will be presented at the American Diabetes Association 70th Scientific Sessions, occurring June 25 through June 29, 2010. A third abstract from XOMA was accepted on a published-only basis. The two posters will be presented on June 28 between 12 noon and 2:00 PM Eastern time. They are entitled:
-- Combination Studies of the Anti-Interleukin-1beta Monoclonal Antibody
XOMA 052 with Exendin-4 or Sitagliptin in a Diet-Induced Obesity Mouse
Model of Type 2 Diabetes Mellitus
-- Inhibition of Interleukin-1beta with the Monoclonal Antibody XOMA 052
Reveals the Differential Sensitivities of Glycemic and Pancreatic
Function Parameters to Chronic Inflammation
The published-only abstract is entitled:
-- The Role of Interleukin-1beta in Insulin Resistance
"Rarely do results from animal models mirror what we see in humans. So far, what we've seen when we compare mouse data to the Phase 1 human data is very encouraging, and while there are limitations to this comparison, we are hopeful that the similarities will carry through to our Phase 2a and Phase 2b data," said Patrick J. Scannon, M.D., Ph.D., Executive Vice President and Chief Medical Officer of XOMA. "With results demonstrating reduction in total cholesterol without decreasing high density lipoprotein, also referred to as 'good cholesterol', the data also highlight the potential application of IL-1 beta inhibition in the treatment of cardiovascular diseases."
In the experiments detailed in the paper, groups of mice received a high fat diet. Without treatment, the mice exhibited signs of Type 2 diabetes such as elevated blood glucose and HbA1c levels, impaired glucose tolerance and impaired insulin secretion. Treatment with XOMA 052 prevented these abnormalities as compared to treatment with an inactive control antibody. Treatment with XOMA 052 also reduced beta-cell apoptosis and increased beta-cell proliferation in the mice fed the high fat diet, and mice treated with XOMA 052 demonstrated improvements in insulin resistance induced by the high fat diet compared to control. The data provide evidence that targeting IL-1 beta in vivo could improve insulin sensitivity.
In addition, the study examined lipid levels in mice fed the high fat diet and either treated with XOMA 052 or the control. Without treatment, mice eating the high fat diet showed increases in the blood levels of lipids like total cholesterol, triglycerides and free fatty acids. The mice treated with XOMA 052 demonstrated reduced levels of lipids compared to the control.
XOMA also announced that two posters on XOMA 052 in the treatment of Type 2 diabetes will be presented at the American Diabetes Association 70th Scientific Sessions, occurring June 25 through June 29, 2010. A third abstract from XOMA was accepted on a published-only basis. The two posters will be presented on June 28 between 12 noon and 2:00 PM Eastern time. They are entitled:
-- Combination Studies of the Anti-Interleukin-1beta Monoclonal Antibody
XOMA 052 with Exendin-4 or Sitagliptin in a Diet-Induced Obesity Mouse
Model of Type 2 Diabetes Mellitus
-- Inhibition of Interleukin-1beta with the Monoclonal Antibody XOMA 052
Reveals the Differential Sensitivities of Glycemic and Pancreatic
Function Parameters to Chronic Inflammation
The published-only abstract is entitled:
-- The Role of Interleukin-1beta in Insulin Resistance
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes, Type 1 diabetes and cardiovascular disease, with
potential for the treatment of a wide range of inflammatory conditions.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(TM), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, more than 50 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
Safe Harbor Statement
Certain statements contained herein concerning clinical trial results and product development or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market. Among other things, results of early-stage clinical trials may not be supported by later findings, and larger trials and/or other actions required for regulatory approval may not be economically feasible.
These and other risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and preclinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
(C) Copyright 2010 GlobeNewswire, Inc. All rights reserved.
News Provided by COMTEX
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes, Type 1 diabetes and cardiovascular disease, with
potential for the treatment of a wide range of inflammatory conditions.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(TM), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, more than 50 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
Safe Harbor Statement
Certain statements contained herein concerning clinical trial results and product development or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market. Among other things, results of early-stage clinical trials may not be supported by later findings, and larger trials and/or other actions required for regulatory approval may not be economically feasible.
These and other risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and preclinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
(C) Copyright 2010 GlobeNewswire, Inc. All rights reserved.
News Provided by COMTEX
XOMA Achieves Planned Enrollment Goal for Phase 2b Clinical Trial of XOMA 052 in Type 2 Diabetes
BERKELEY, Calif., Jun 30, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that it has reached the enrollment goal of 325 patients for its Phase 2b dose-ranging clinical trial of XOMA 052, and that it expects patient enrollment to close in the next three weeks, with top-line results available in the first quarter of 2011. XOMA 052 is a therapeutic antibody candidate that inhibits the pro-inflammatory cytokine interleukin-1 beta (IL-1 beta) which drives the inflammatory cause of Type 2 diabetes.
The Phase 2b trial, in which Type 2 diabetes patients are randomized to receive one of four dose levels of XOMA 052 or placebo administered monthly over six months, is designed with the primary endpoint of mean change in glycosylated hemoglobin (HbA1c) levels compared to baseline. Secondary endpoints include additional diabetes parameters as well as measures of inflammatory and cardiovascular disease. Prior to enrolling, patients were on a stable regimen of metformin monotherapy for at least 12 weeks before treatment with XOMA 052 or placebo.
"Achieving the enrollment goal for our Phase 2b clinical trial is a significant milestone in the development of XOMA 052 to treat Type 2 diabetes," said Steven B. Engle, Chairman and Chief Executive Officer of XOMA.
BERKELEY, Calif., Jun 30, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that it has reached the enrollment goal of 325 patients for its Phase 2b dose-ranging clinical trial of XOMA 052, and that it expects patient enrollment to close in the next three weeks, with top-line results available in the first quarter of 2011. XOMA 052 is a therapeutic antibody candidate that inhibits the pro-inflammatory cytokine interleukin-1 beta (IL-1 beta) which drives the inflammatory cause of Type 2 diabetes.
The Phase 2b trial, in which Type 2 diabetes patients are randomized to receive one of four dose levels of XOMA 052 or placebo administered monthly over six months, is designed with the primary endpoint of mean change in glycosylated hemoglobin (HbA1c) levels compared to baseline. Secondary endpoints include additional diabetes parameters as well as measures of inflammatory and cardiovascular disease. Prior to enrolling, patients were on a stable regimen of metformin monotherapy for at least 12 weeks before treatment with XOMA 052 or placebo.
"Achieving the enrollment goal for our Phase 2b clinical trial is a significant milestone in the development of XOMA 052 to treat Type 2 diabetes," said Steven B. Engle, Chairman and Chief Executive Officer of XOMA.
Antwort auf Beitrag Nr.: 39.771.193 von schokie am 02.07.10 19:29:08Die Biotechs gehen in den Keller, wenn in China ein Reissack umzukippen droht.


is schon echt krass, fällt der wert abermalswieder unter die 30 cent marke ^^ 
mal guggen wo das noch hin geht, wann kommt denn der split?

mal guggen wo das noch hin geht, wann kommt denn der split?
Antwort auf Beitrag Nr.: 39.777.032 von Markus77 am 05.07.10 14:32:40DOW heut wieder knapp über 10000 Punkte. Nasdaq / S&P 500 beide 3% im Plus.
XOMA geht heute in die andere Richtung. Im Amiboard wird uA. bzgl. der Bevorstehenden ASM und dem möglichen RS bzw, Neuausgabe von neuen Shares spekuliert.
KA wie das hier weitergeht.

XOMA geht heute in die andere Richtung. Im Amiboard wird uA. bzgl. der Bevorstehenden ASM und dem möglichen RS bzw, Neuausgabe von neuen Shares spekuliert.
KA wie das hier weitergeht.

Antwort auf Beitrag Nr.: 39.790.855 von zwitscherton am 08.07.10 02:09:03Die Umsätze waren auch nicht so berauschend. Was vielleicht ganz gut ist bei fallenden Kursen.


Antwort auf Beitrag Nr.: 39.790.855 von zwitscherton am 08.07.10 02:09:03weisst du wann ein RS ansteht?
Antwort auf Beitrag Nr.: 39.792.964 von Markus77 am 08.07.10 13:37:49The drug company (NASDAQ: XOMA) is contemplating a reverse stock split to address the problem. In May its board approved the possibility, and Xoma has asked its shareholders to vote for the idea at its July 21 annual meeting.
http://sanfrancisco.bizjournals.com/sanfrancisco/stories/201…

http://sanfrancisco.bizjournals.com/sanfrancisco/stories/201…

Antwort auf Beitrag Nr.: 39.795.602 von zwitscherton am 08.07.10 19:28:41Also in knapp 2 Wochen sind wir diesbezüglich schlauer.


Antwort auf Beitrag Nr.: 39.795.602 von zwitscherton am 08.07.10 19:28:41Hallo zwitscherton ,
ein Aktiensplitt ist geplant,welche vorteile bringt dass?
Legt dass Unternehmen keinen wert auf ein Listing an der Nasdaq?
Oder ist es genau andersrum, 5 zu 1?
Bitte um Nachricht.
ein Aktiensplitt ist geplant,welche vorteile bringt dass?
Legt dass Unternehmen keinen wert auf ein Listing an der Nasdaq?

Oder ist es genau andersrum, 5 zu 1?
Bitte um Nachricht.
Antwort auf Beitrag Nr.: 39.798.325 von Bioperle am 09.07.10 11:07:05Hallo Bioperle,
doch gerade wegen dem Nasdaq-Listing ist der Resplit geplant um wieder über den entscheidenden 1 Dollar pro Aktie zu kommen um an der Nasdaq bleiben zu dürfen.
LG Tommi
doch gerade wegen dem Nasdaq-Listing ist der Resplit geplant um wieder über den entscheidenden 1 Dollar pro Aktie zu kommen um an der Nasdaq bleiben zu dürfen.
LG Tommi
Antwort auf Beitrag Nr.: 39.799.153 von Tommi33 am 09.07.10 13:07:05Genau so ist es. Heute mal leicht im Plus geschlossen.


Antwort auf Beitrag Nr.: 39.802.325 von zwitscherton am 10.07.10 00:35:31Vielleicht war das die Trandwende.
Glaub ich aber eignetlich nicht.
Es sei denn es kommen noch gute Nachrichten Vor der ASM (in 10 Tagen).
Wäre kein schlechter Schachzug.

Glaub ich aber eignetlich nicht.
Es sei denn es kommen noch gute Nachrichten Vor der ASM (in 10 Tagen).
Wäre kein schlechter Schachzug.

Antwort auf Beitrag Nr.: 39.805.299 von zwitscherton am 12.07.10 00:42:05Heute wieder leicht im Plus während die meisten anderen Biotechs geflissentlich den Rückwärtsgang einlegten.


knapp 30 prozent nachbörslich geschlossen (0,50)

so macht das doch wider spas

so macht das doch wider spas
Antwort auf Beitrag Nr.: 39.817.710 von eddycassius am 14.07.10 09:19:05Moin,
das ist aber doch nicht wirklich ernst zu nehmen, oder:
... auch wenn es mir gefallen würde!
Gruss Wunram

das ist aber doch nicht wirklich ernst zu nehmen, oder:
After Hours
Time (ET)
After Hours Price After Hours Share Volume
19:58 $ .498 4,451
19:58 $ .50 300
19:58 $ .40 300
19:58 $ .39 200
19:58 $ .50 200
19:55 $ .498 180
16:35 $ .385 2,921
16:31 $ .38 181
16:31 $ .38 181
16:31 $ .38 182
16:31 $ .38 181
16:31 $ .38 182
... auch wenn es mir gefallen würde!

Gruss Wunram


Antwort auf Beitrag Nr.: 39.817.830 von Wunram am 14.07.10 09:34:49war wohl einb fake..

wenigstens sind wir bei den 0,40 cent angekommen.
wenn wir das nnatürlich bis heute abend halten

wenn wir das nnatürlich bis heute abend halten


Antwort auf Beitrag Nr.: 39.821.328 von eddycassius am 14.07.10 18:24:52Die Biotechs sind im Aufwind. Mal Hü mal Hot ...


Antwort auf Beitrag Nr.: 39.821.714 von zwitscherton am 14.07.10 19:30:04Das ist aber wohl längst überfällig.

Antwort auf Beitrag Nr.: 39.823.005 von Bioperle am 14.07.10 23:48:46Leider nicht sehr nachhaltig.
Kaum kommen leichte Zweifel an der Nachhaltigkeit der konjunkturellen Erholung auf gibts bei den Bios wieder auf die Mütze.
Ich befürchte diese Wackelbörse wird noch ne Weile andauern.
Bei XOMA wird auf jeden Fall die anstehende Annual General Meeting entscheidend sein für den weiteren Verlauf. IMHO.
Let's wait and see.

Kaum kommen leichte Zweifel an der Nachhaltigkeit der konjunkturellen Erholung auf gibts bei den Bios wieder auf die Mütze.
Ich befürchte diese Wackelbörse wird noch ne Weile andauern.
Bei XOMA wird auf jeden Fall die anstehende Annual General Meeting entscheidend sein für den weiteren Verlauf. IMHO.
Let's wait and see.

Hi Biotechfreaks  !
!
Kerncodex,bist du auch noch dabei ? Aber sagt mal,was ist eigendlich los mit Xoma
? Aber sagt mal,was ist eigendlich los mit Xoma  ? Die Pipeline (Xoma052) ist doch wirklich nicht die schlechteste,sollte man meinen,also ich hab schon weitaus uninteressantere gesehen ! O.K. ,die anzahl der shares hat auch stark zugenommen,es sind jetzt schon 260 mio,so dass man bei 0,39$/share immerhin noch 100 Mio.-$ Mcap auf die Waage bringt ! Jetzt wirds auch bald knapp mit dem Nasdaq-listing,wegen der 1$ minimumbidregel,hier wird wohl ein R/S unvermeidlich sein,schätze ich mal! Die eigendlich interessante Frage für mich: Ist Xoma aktuel ein Kauf mit ca. 500% Potential oder mehr,oder sind die kurz vorm Exitus
? Die Pipeline (Xoma052) ist doch wirklich nicht die schlechteste,sollte man meinen,also ich hab schon weitaus uninteressantere gesehen ! O.K. ,die anzahl der shares hat auch stark zugenommen,es sind jetzt schon 260 mio,so dass man bei 0,39$/share immerhin noch 100 Mio.-$ Mcap auf die Waage bringt ! Jetzt wirds auch bald knapp mit dem Nasdaq-listing,wegen der 1$ minimumbidregel,hier wird wohl ein R/S unvermeidlich sein,schätze ich mal! Die eigendlich interessante Frage für mich: Ist Xoma aktuel ein Kauf mit ca. 500% Potential oder mehr,oder sind die kurz vorm Exitus  ?
?
Wer weiss,was hier im Argen ist ?
?
MFG
Zuki
 !
!Kerncodex,bist du auch noch dabei
 ? Aber sagt mal,was ist eigendlich los mit Xoma
? Aber sagt mal,was ist eigendlich los mit Xoma  ? Die Pipeline (Xoma052) ist doch wirklich nicht die schlechteste,sollte man meinen,also ich hab schon weitaus uninteressantere gesehen ! O.K. ,die anzahl der shares hat auch stark zugenommen,es sind jetzt schon 260 mio,so dass man bei 0,39$/share immerhin noch 100 Mio.-$ Mcap auf die Waage bringt ! Jetzt wirds auch bald knapp mit dem Nasdaq-listing,wegen der 1$ minimumbidregel,hier wird wohl ein R/S unvermeidlich sein,schätze ich mal! Die eigendlich interessante Frage für mich: Ist Xoma aktuel ein Kauf mit ca. 500% Potential oder mehr,oder sind die kurz vorm Exitus
? Die Pipeline (Xoma052) ist doch wirklich nicht die schlechteste,sollte man meinen,also ich hab schon weitaus uninteressantere gesehen ! O.K. ,die anzahl der shares hat auch stark zugenommen,es sind jetzt schon 260 mio,so dass man bei 0,39$/share immerhin noch 100 Mio.-$ Mcap auf die Waage bringt ! Jetzt wirds auch bald knapp mit dem Nasdaq-listing,wegen der 1$ minimumbidregel,hier wird wohl ein R/S unvermeidlich sein,schätze ich mal! Die eigendlich interessante Frage für mich: Ist Xoma aktuel ein Kauf mit ca. 500% Potential oder mehr,oder sind die kurz vorm Exitus  ?
?Wer weiss,was hier im Argen ist
 ?
?MFG
Zuki

Antwort auf Beitrag Nr.: 39.834.844 von Zukertort am 16.07.10 20:00:27Gut weggekommen heut bei dem Masaker.
@Zukertort. Schachspieler, was ?
Warte bis zur AGM nächste Woche, dann wird entschieden über RS bzw. Dillution.
Im Moment ist vielleicht Risko Aversion bei den Big-Pharmas angesagt ???
Viele kleine Biotech-"Buden" finden jetzt offenbar keine finanzkräftigen Partner und müssen somit die Entwicklung bzw. dessen Finanzierung erstmal selbst stemmen.
Und ständig neue Aktien ausgeben. Das ist für die Aktionäre wohl doch eher nervig.


@Zukertort. Schachspieler, was ?
Warte bis zur AGM nächste Woche, dann wird entschieden über RS bzw. Dillution.
Im Moment ist vielleicht Risko Aversion bei den Big-Pharmas angesagt ???
Viele kleine Biotech-"Buden" finden jetzt offenbar keine finanzkräftigen Partner und müssen somit die Entwicklung bzw. dessen Finanzierung erstmal selbst stemmen.
Und ständig neue Aktien ausgeben. Das ist für die Aktionäre wohl doch eher nervig.

diese woche am mittwoch ist doch der tag der tage oder nicht?
ich bin mal gespannt, obs wirklich einen RS und wenn ja, in welchem maße.
ich bin mal gespannt, obs wirklich einen RS und wenn ja, in welchem maße.
Antwort auf Beitrag Nr.: 39.841.496 von Markus77 am 19.07.10 14:53:50Ich glaube da warten jetzt alle drauf.
Und wieder kaum Ümsätze die letzten Tage.

Und wieder kaum Ümsätze die letzten Tage.

Antwort auf Beitrag Nr.: 39.844.964 von zwitscherton am 20.07.10 00:32:47Was ein besch... Sommer (abgesehn vom Wetter).
Geht schon wieder alles gen Suden.

Geht schon wieder alles gen Suden.

Antwort auf Beitrag Nr.: 39.844.964 von zwitscherton am 20.07.10 00:32:47Liebe Freunde der Spekulation
XOMA TARGET $50 STRONG BUY RESEARCH REPORT
20. Juli 2010 03.57 Uhr
http://translate.googleusercontent.com/translate_c?hl=de&sl=…

XOMA TARGET $50 STRONG BUY RESEARCH REPORT

20. Juli 2010 03.57 Uhr
http://translate.googleusercontent.com/translate_c?hl=de&sl=…

volltreffer würde ich mal behaupten wenn das so stimmt
´In fact 7 out of 7 patients should dramatic improvement with Xoma 052 with one patient eye completely shut 100/20 vision on day one finished treatment with 2 doses of Xoma 052 by day 21 the eye was completely open healed with a remarkable 20/20 vision. Xoma 052 a miracle drug reduced inflammation dramatically.
´In fact 7 out of 7 patients should dramatic improvement with Xoma 052 with one patient eye completely shut 100/20 vision on day one finished treatment with 2 doses of Xoma 052 by day 21 the eye was completely open healed with a remarkable 20/20 vision. Xoma 052 a miracle drug reduced inflammation dramatically.
wenn das den tat sachen entspricht
 money money money
money money money 
 money money money
money money money 
Antwort auf Beitrag Nr.: 39.850.044 von eddycassius am 20.07.10 18:16:04Will hier ja niemandem den Spaß nehmen - aber nicht alles glauben was " irgendwer " schreibt - das ist ein klaren " Eigennutz " Beitrag...da will wohl jemand seine Kohlen aus dem Feuer holen - so einfach geht das alles nicht...und dann immer schön so das Jahr 2011 und 2012 angeben......selbst 1 US$ wäre bei Xoma mal wieder Top...aber 50 US$ ....mit mehr als einem Wunder
Auch mal was zum Nachdenken...ich weiß ...rosarote Brille ist immer schöner...aber man sollte beide Seiten sehen
*****************************************************************
xoma shareholder meeting a sham 44 minutes ago We are all idiots for speculating on a worthless company that has never made a profit, xoma always has and always will - at least for a little while longer - be a rip off operation.
Engle's total compensation: $ 1,054,022
and then they want to dilute by 300M and then r/s. nice work.
ITEM 3—INCREASE IN THE NUMBER OF AUTHORIZED COMMON
SHARES AND SHARE CAPITAL
Background
Currently, the Company is authorized to issue 400,000,000 Common Shares in the aggregate. In May of 2010, the Board unanimously approved a proposal to increase the Company’s authorized share capital by the creation of an additional 300,000,000 Common Shares (the “Authorized Share Increase”).
On May 25, 2010, the Company had issued and outstanding 261,247,750 Common Shares. As of that date, the Company had reserved approximately 70,886,169 shares for issuance upon exercise of outstanding options, warrants and convertible preference shares and in connection with existing share-based compensation and benefit plans and financing arrangements. Consequently, the Company has approximately 67,866,081 shares available for other issuances.
Effects of Adoption of the Proposal
The adoption of this proposal would increase the authorized share capital of the Company from US$250,000, consisting of 400,000,000 Common Shares and 1,000,000 Preference Shares, to US$400,000, consisting of 700,000,000 Common Shares and 1,000,000 Preference Shares. The additional Common Shares for which authorization is sought would be part of the existing class of Common Shares, and, to the extent issued, would have the same rights and privileges as the Common Shares currently issued and outstanding. No holder of the Common Shares is entitled to any preemptive right to subscribe for or purchase any shares or other securities of the Company. The issuance of a substantial amount of Common Shares or the granting of an option to purchase a substantial amount of Common Shares could have a potential anti-takeover effect with respect to the Company which may make it more difficult to effect a change in control of the Company (for example, by decreasing the percentage of share ownership of those persons seeking to obtain control), although the Board is not presenting the proposal for that reason and does not anticipate using the newly authorized shares for such a purpose. Under applicable law, the Board is required to make any determination to issue such shares based on its judgment at the time of such issuance as to the best interest of the Company.
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
******************************
und na klar hab ich immer ein Auge auf Xoma.. ...logisch....allerdings will ich erst wissen was mit der OTC passiert oder nicht...bzw. kommt der R/S...vorher werd ich wohl auch nix mehr investieren
...logisch....allerdings will ich erst wissen was mit der OTC passiert oder nicht...bzw. kommt der R/S...vorher werd ich wohl auch nix mehr investieren
*****************************************************************
xoma shareholder meeting a sham 44 minutes ago We are all idiots for speculating on a worthless company that has never made a profit, xoma always has and always will - at least for a little while longer - be a rip off operation.
Engle's total compensation: $ 1,054,022
and then they want to dilute by 300M and then r/s. nice work.
ITEM 3—INCREASE IN THE NUMBER OF AUTHORIZED COMMON
SHARES AND SHARE CAPITAL
Background
Currently, the Company is authorized to issue 400,000,000 Common Shares in the aggregate. In May of 2010, the Board unanimously approved a proposal to increase the Company’s authorized share capital by the creation of an additional 300,000,000 Common Shares (the “Authorized Share Increase”).
On May 25, 2010, the Company had issued and outstanding 261,247,750 Common Shares. As of that date, the Company had reserved approximately 70,886,169 shares for issuance upon exercise of outstanding options, warrants and convertible preference shares and in connection with existing share-based compensation and benefit plans and financing arrangements. Consequently, the Company has approximately 67,866,081 shares available for other issuances.
Effects of Adoption of the Proposal
The adoption of this proposal would increase the authorized share capital of the Company from US$250,000, consisting of 400,000,000 Common Shares and 1,000,000 Preference Shares, to US$400,000, consisting of 700,000,000 Common Shares and 1,000,000 Preference Shares. The additional Common Shares for which authorization is sought would be part of the existing class of Common Shares, and, to the extent issued, would have the same rights and privileges as the Common Shares currently issued and outstanding. No holder of the Common Shares is entitled to any preemptive right to subscribe for or purchase any shares or other securities of the Company. The issuance of a substantial amount of Common Shares or the granting of an option to purchase a substantial amount of Common Shares could have a potential anti-takeover effect with respect to the Company which may make it more difficult to effect a change in control of the Company (for example, by decreasing the percentage of share ownership of those persons seeking to obtain control), although the Board is not presenting the proposal for that reason and does not anticipate using the newly authorized shares for such a purpose. Under applicable law, the Board is required to make any determination to issue such shares based on its judgment at the time of such issuance as to the best interest of the Company.
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
******************************
und na klar hab ich immer ein Auge auf Xoma..
 ...logisch....allerdings will ich erst wissen was mit der OTC passiert oder nicht...bzw. kommt der R/S...vorher werd ich wohl auch nix mehr investieren
...logisch....allerdings will ich erst wissen was mit der OTC passiert oder nicht...bzw. kommt der R/S...vorher werd ich wohl auch nix mehr investieren
Muss mich erst mal wieder richtig einlesen in XOMA...also morgen dann die Entscheidung..ob nun R/S oder nicht und wie hoch...müsste ja min. eine 5 -er Quote sein.....wenn man auf Nummer sicher gehen will wirds eine 10 -er Quote...werds mal beobachten was rauskommt
Nix gegen Xoma - aber man sollte sich so seine Gedanken machen
Den Verlust von über 800 Millionen Dollar kann ich mir aber beim besten Willen nicht erklären bzw. glauben . ..das muss mit Sicherheit ein Fehler sein...soviel Geld bzw. Umsatz hatte Xoma ja niemals
..das muss mit Sicherheit ein Fehler sein...soviel Geld bzw. Umsatz hatte Xoma ja niemals
*****************************************************************************
Tuesday, June 15, 2010
Xoma gets Nasdaq reprieve, hopes for reverse stock split
San Francisco Business Times - by Steven E.F. Brown
Receive email alerts about XOMA Corporation
Send this story to a friend
Xoma Ltd. gets $1M milestone
House boosts R&D funding, new programs
Bio Ventures for Global Health opens S.F. office
Pa., N.J. keep high rankings in biotech job concentration
Washington briefs: Fed studies small-business credit cards
Find Executives
Xoma Ltd.
Biotechnology Industry Organization
Xoma Ltd. in Berkeley got a reprieve from the Nasdaq stock market: it now has until Sept. 13 to comply with a listing requirement for its share price.
The drug company (NASDAQ: XOMA) is contemplating a reverse stock split to address the problem. In May its board approved the possibility, and Xoma has asked its shareholders to vote for the idea at its July 21 annual meeting.[/
Seeking shareholder approval for a reverse stock split was part of a deal Xoma worked out with Nasdaq officials. Last September the Nasdaq started the process of delisting Xoma’s shares because they usually trade below $1 each.
Xoma’s lead drug candidate is an antibody aimed at type 2 diabetes.
Steven Engle is chairman, CEO and president of Xoma. He’s on the board of the Biotechnology Industry Organization. The business has about 200 workers.
Xoma’s accumulated deficit at the end of the March quarter was $806.3 million. That’s how much money it has written off or lost since it started in 1981.
At first, Xoma Corp. was incorporated in Delaware, but changed its legal domicile to Bermuda and its name to Xoma Ltd. at the end of 1998.
http://sanfrancisco.bizjournals.com/sanfrancisco/stories/201…
Read more: Xoma gets Nasdaq reprieve, hopes for reverse stock split - San Francisco Business Times
Nix gegen Xoma - aber man sollte sich so seine Gedanken machen
Den Verlust von über 800 Millionen Dollar kann ich mir aber beim besten Willen nicht erklären bzw. glauben .
 ..das muss mit Sicherheit ein Fehler sein...soviel Geld bzw. Umsatz hatte Xoma ja niemals
..das muss mit Sicherheit ein Fehler sein...soviel Geld bzw. Umsatz hatte Xoma ja niemals *****************************************************************************
Tuesday, June 15, 2010
Xoma gets Nasdaq reprieve, hopes for reverse stock split
San Francisco Business Times - by Steven E.F. Brown
Receive email alerts about XOMA Corporation
Send this story to a friend
Xoma Ltd. gets $1M milestone
House boosts R&D funding, new programs
Bio Ventures for Global Health opens S.F. office
Pa., N.J. keep high rankings in biotech job concentration
Washington briefs: Fed studies small-business credit cards
Find Executives
Xoma Ltd.
Biotechnology Industry Organization
Xoma Ltd. in Berkeley got a reprieve from the Nasdaq stock market: it now has until Sept. 13 to comply with a listing requirement for its share price.
The drug company (NASDAQ: XOMA) is contemplating a reverse stock split to address the problem. In May its board approved the possibility, and Xoma has asked its shareholders to vote for the idea at its July 21 annual meeting.[/
Seeking shareholder approval for a reverse stock split was part of a deal Xoma worked out with Nasdaq officials. Last September the Nasdaq started the process of delisting Xoma’s shares because they usually trade below $1 each.
Xoma’s lead drug candidate is an antibody aimed at type 2 diabetes.
Steven Engle is chairman, CEO and president of Xoma. He’s on the board of the Biotechnology Industry Organization. The business has about 200 workers.
Xoma’s accumulated deficit at the end of the March quarter was $806.3 million. That’s how much money it has written off or lost since it started in 1981.
At first, Xoma Corp. was incorporated in Delaware, but changed its legal domicile to Bermuda and its name to Xoma Ltd. at the end of 1998.
http://sanfrancisco.bizjournals.com/sanfrancisco/stories/201…
Read more: Xoma gets Nasdaq reprieve, hopes for reverse stock split - San Francisco Business Times
Interessant wäre noch zu wissen was mit den Shorts passieren wird falls ein R/ S kommt ( was ja im Regelfall dann auch wieder einige Zeit dauerd - so sieht es am 30.06.2010 aus !!!
Sollten rund 7,5 Millionen noch stimmen und diese dann gecovert werden müssen..dann müsste es eigentlich steigen- wenigstens kurzfristig
**********************************
http://www.dailyfinance.com/company/xoma-ltd/xoma/nas/short-…
(siehe hier den Chart )
Current Short Interest Shares 7.05 M
Current Short Interest Ratio 4.50
Float 260.72 M
Short Interest as % of Float 2.70
Average Daily Volume 1.50 M
Outstanding Shares 261.25 M
Sollten rund 7,5 Millionen noch stimmen und diese dann gecovert werden müssen..dann müsste es eigentlich steigen- wenigstens kurzfristig
**********************************
http://www.dailyfinance.com/company/xoma-ltd/xoma/nas/short-…
(siehe hier den Chart )
Current Short Interest Shares 7.05 M
Current Short Interest Ratio 4.50
Float 260.72 M
Short Interest as % of Float 2.70
Average Daily Volume 1.50 M
Outstanding Shares 261.25 M
Antwort auf Beitrag Nr.: 39.850.538 von Expertchen007 am 20.07.10 19:34:58Naja ein RS ist ja kein Kursanstieg, so werden die Short-Positionen dann wohl einfach angepasst/ bzw. umgerechnet.
Das gleiche wie bei Optionen.

Das gleiche wie bei Optionen.

Antwort auf Beitrag Nr.: 39.852.076 von zwitscherton am 21.07.10 00:04:41vom Prinzip her richtig...aber die Erfahrung sagt das Shorter niemals ein R/S mitmachen wollen....bin mal gespannt was da heute so passiert...falls es so kommt 

Beachten All Time Low war mal 0,36 US$...also schon echt heftig was da gelaufen ist ....suche noch den richtigen Einstiegspunkt ( mal wieder )
Nachbörse...0,42 US$...allerdings mit 200 Stücken.....ein eher kläglicher Versuch würde ich sagen - 200 -100 .und 50 Tageslinie klar weggehauen ( leider nach unten )
******************************************************
Investors Pummel Shares of XOMA, Shares Drop 3.9% (XOMA)
Written on Tue, 07/20/2010 - 10:40am
By Chip Brian
XOMA (NASDAQ:XOMA) is one of today's worst performing penny stocks, down 3.9% to $0.37 on 0.2x average daily volume. Approximately 626,000 shares have traded hands today vs. 30-day average volume of 3.1 million shares.
High volume often signals a change in trends. Shares of XOMA are currently trading below their 50-day moving average (MA) of $0.46 and below their 200-day MA of $0.61.
SmarTrend scans for speculative penny stocks under $1 for reversals in trends. A large price movement may signal continuation or reversal of a trend.
XOMA is in SmarTrend's Biotechnology industry and this industry is currently in a Downtrend. An industry trend that matches the stock's trend helps to add conviction to the stock's Downtrend and price prediction.
SmarTrend is bearish on shares of XOMA and our subscribers were alerted to sell on May 20, 2010 at $0.52. The stock has fallen 29.8% since the alert
http://studio-5.financialcontent.com/freelunch/action/linkou…
******************************************************
Investors Pummel Shares of XOMA, Shares Drop 3.9% (XOMA)
Written on Tue, 07/20/2010 - 10:40am
By Chip Brian
XOMA (NASDAQ:XOMA) is one of today's worst performing penny stocks, down 3.9% to $0.37 on 0.2x average daily volume. Approximately 626,000 shares have traded hands today vs. 30-day average volume of 3.1 million shares.
High volume often signals a change in trends. Shares of XOMA are currently trading below their 50-day moving average (MA) of $0.46 and below their 200-day MA of $0.61.
SmarTrend scans for speculative penny stocks under $1 for reversals in trends. A large price movement may signal continuation or reversal of a trend.
XOMA is in SmarTrend's Biotechnology industry and this industry is currently in a Downtrend. An industry trend that matches the stock's trend helps to add conviction to the stock's Downtrend and price prediction.
SmarTrend is bearish on shares of XOMA and our subscribers were alerted to sell on May 20, 2010 at $0.52. The stock has fallen 29.8% since the alert
http://studio-5.financialcontent.com/freelunch/action/linkou…
Antwort auf Beitrag Nr.: 39.853.052 von Expertchen007 am 21.07.10 09:47:09ich schau mir erstmal an, was bei dem möglichen RS rauskommt,desweiteren is nix frei 


Antwort auf Beitrag Nr.: 39.855.615 von Expertchen007 am 21.07.10 15:58:34Oha...sehe gerade das ATL war unterschritten...aber News wegen R/S gibts noch nicht
Antwort auf Beitrag Nr.: 39.856.295 von Expertchen007 am 21.07.10 17:13:28der laden sieht von mir keinen dollar mehr in nächster zeit, hier passt irgendwas nicht!
wir müssen erstmal die asm baustelle zu bekommen
wir müssen erstmal die asm baustelle zu bekommen

Antwort auf Beitrag Nr.: 39.856.521 von Markus77 am 21.07.10 17:41:00Riesenumsatze sind das bis jetzt ja nicht.
Trotzdem leidet der Kurs entgegen dem heutigen Trend.

Trotzdem leidet der Kurs entgegen dem heutigen Trend.


kommt denn heute nocch was
zum meuse melken
Antwort auf Beitrag Nr.: 39.857.379 von eddycassius am 21.07.10 20:19:09Auf der XOMA HP finde ich auch nix zur AGM.
Im Amiboard auch nix konkretes. Hat die Veranstaltung dann heute überhaupt stattgefunden oder wie

Im Amiboard auch nix konkretes. Hat die Veranstaltung dann heute überhaupt stattgefunden oder wie


Antwort auf Beitrag Nr.: 39.858.294 von zwitscherton am 21.07.10 23:27:44Auffällig war allerdings, daß ab 13Uhr OZ sich die Schlagzahl im Volumen erhöht hat.


Antwort auf Beitrag Nr.: 39.858.294 von zwitscherton am 21.07.10 23:27:44Hallo Zwitscherton,
hilft dir das eventuell weiter:
Form 8-K for XOMA LTD /DE/
21-Jul-2010
Submission of Matters to a Vote of Security Holders
Item 5.07 Submission of Matters to a Vote of Security Holders.
On July 21, 2010, XOMA Ltd. (the "Company") held its 2010 annual general meeting of shareholders. The following persons (the only nominees) were elected as the Company's directors, the Company's independent inspector of elections having reported the following preliminary voting results:
Name Votes For Votes Withheld Broker Non-Votes
Steven B. Engle 55,734,375 21,343,028 111,646,105
Patrick J. Scannon, M.D., Ph.D. 60,366,005 16,741,398 111,646,105
W. Denman Van Ness 60,498,730 16,578,673 111,646,105
William K. Bowes, Jr. 60,714,950 16,362,453 111,646,105
Charles J. Fisher, Jr., M.D. 60,770,395 16,307,008 111,646,105
Peter Barton Hutt 60,362,331 16,715,072 111,646,105
John Varian 60,589,538 16,487,865 111,646,105
The proposal to appoint Ernst & Young LLP to act as the Company's independent registered public accounting firm for the 2010 fiscal year and authorize the Board to agree to such firm's fees was approved, the Company's independent inspector of elections having reported the following preliminary voting results:
159,535,431 votes for, 24,342,285 votes against, 4,845,792 abstentions and zero broker non-votes.
The proposal to approve the increase of the Company's authorized share capital by the creation of an additional 300,000,000 common shares, par value $.0005 per share, was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 110,838,067 votes for, 74,565,498 votes against, 3,319,943 abstentions and zero broker non-votes.
The proposal to authorize the Board of Directors to effect a share consolidation, or reverse stock split, of the Company's common shares at any time on or before July 21, 2011 at a ratio within a range of 1 for 2 to 1 for 15 as determined by the Board of Directors in its sole discretion, and if and when the reverse stock split is effected, reduce the number of the Company's authorized common shares by the reverse split ratio determined by the Board of Directors to apply equally to the Company's authorized common shares and increase the par value of each common share accordingly, was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 126,299,581 votes for, 59,139,640 votes against, 3,284,287 abstentions and zero broker non-votes.
The proposal to approve an amendment to the Company's 1981 Share Option Plan to increase the number of shares issuable over the term of the plan by 5,200,000 shares was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 44,327,733 votes for, 31,428,445 votes against, 1,321,225 abstentions and 111,646,105 broker non-votes.
The proposal to approve the Company's 2010 Long Term Incentive and Share Award Plan, which would replace the Company's 1981 Share Option Plan, Restricted Share Plan and
-2-
1992 Directors Option Plan going forward and increase the total number of common shares available for awards by 8,800,000 shares to a maximum of 43,826,211 shares in the aggregate, was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 44,796,205 votes for, 30,507,904 votes against, 1,773,294 abstentions and 111,646,105 broker non-votes.
The proposal to approve an amendment to the Company's 1998 Employee Share Purchase Plan to increase the number of common shares issuable over the term of the plan by 500,000 to 2,000,000 shares in the aggregate was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 48,868,486 votes for, 26,428,175 votes against, 1,780,742 abstentions and 111,646,105 broker non-votes.
Quelle: http://biz.yahoo.com/e/100721/xoma8-k.html
LG Tommi
P.S. Wäre nett wenn du das wichtigste daraus mal zusammenfassen könntest, der Google Translator hilft da nicht wirklich weiter. Ich versteh nur soviel das sie neue Aktien ausgeben wollen und eventuell Re-Split im Bereich 1 zu 2 bis 1 zu 15 bis zum 21 Juli 2011 machen wollen. Ist das so korrekt ?
hilft dir das eventuell weiter:
Form 8-K for XOMA LTD /DE/
21-Jul-2010
Submission of Matters to a Vote of Security Holders
Item 5.07 Submission of Matters to a Vote of Security Holders.
On July 21, 2010, XOMA Ltd. (the "Company") held its 2010 annual general meeting of shareholders. The following persons (the only nominees) were elected as the Company's directors, the Company's independent inspector of elections having reported the following preliminary voting results:
Name Votes For Votes Withheld Broker Non-Votes
Steven B. Engle 55,734,375 21,343,028 111,646,105
Patrick J. Scannon, M.D., Ph.D. 60,366,005 16,741,398 111,646,105
W. Denman Van Ness 60,498,730 16,578,673 111,646,105
William K. Bowes, Jr. 60,714,950 16,362,453 111,646,105
Charles J. Fisher, Jr., M.D. 60,770,395 16,307,008 111,646,105
Peter Barton Hutt 60,362,331 16,715,072 111,646,105
John Varian 60,589,538 16,487,865 111,646,105
The proposal to appoint Ernst & Young LLP to act as the Company's independent registered public accounting firm for the 2010 fiscal year and authorize the Board to agree to such firm's fees was approved, the Company's independent inspector of elections having reported the following preliminary voting results:
159,535,431 votes for, 24,342,285 votes against, 4,845,792 abstentions and zero broker non-votes.
The proposal to approve the increase of the Company's authorized share capital by the creation of an additional 300,000,000 common shares, par value $.0005 per share, was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 110,838,067 votes for, 74,565,498 votes against, 3,319,943 abstentions and zero broker non-votes.
The proposal to authorize the Board of Directors to effect a share consolidation, or reverse stock split, of the Company's common shares at any time on or before July 21, 2011 at a ratio within a range of 1 for 2 to 1 for 15 as determined by the Board of Directors in its sole discretion, and if and when the reverse stock split is effected, reduce the number of the Company's authorized common shares by the reverse split ratio determined by the Board of Directors to apply equally to the Company's authorized common shares and increase the par value of each common share accordingly, was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 126,299,581 votes for, 59,139,640 votes against, 3,284,287 abstentions and zero broker non-votes.
The proposal to approve an amendment to the Company's 1981 Share Option Plan to increase the number of shares issuable over the term of the plan by 5,200,000 shares was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 44,327,733 votes for, 31,428,445 votes against, 1,321,225 abstentions and 111,646,105 broker non-votes.
The proposal to approve the Company's 2010 Long Term Incentive and Share Award Plan, which would replace the Company's 1981 Share Option Plan, Restricted Share Plan and
-2-
1992 Directors Option Plan going forward and increase the total number of common shares available for awards by 8,800,000 shares to a maximum of 43,826,211 shares in the aggregate, was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 44,796,205 votes for, 30,507,904 votes against, 1,773,294 abstentions and 111,646,105 broker non-votes.
The proposal to approve an amendment to the Company's 1998 Employee Share Purchase Plan to increase the number of common shares issuable over the term of the plan by 500,000 to 2,000,000 shares in the aggregate was approved, the Company's independent inspector of elections having reported the following preliminary voting results: 48,868,486 votes for, 26,428,175 votes against, 1,780,742 abstentions and 111,646,105 broker non-votes.
Quelle: http://biz.yahoo.com/e/100721/xoma8-k.html
LG Tommi
P.S. Wäre nett wenn du das wichtigste daraus mal zusammenfassen könntest, der Google Translator hilft da nicht wirklich weiter. Ich versteh nur soviel das sie neue Aktien ausgeben wollen und eventuell Re-Split im Bereich 1 zu 2 bis 1 zu 15 bis zum 21 Juli 2011 machen wollen. Ist das so korrekt ?
Antwort auf Beitrag Nr.: 39.858.685 von Tommi33 am 22.07.10 08:04:16Korrekt - es wird schon so kommen wie ich vermutet habe ....genehmigt ist alles....klar wegen den Aktienanteilen...somit gehe ich klar von einer 10 - er Quote aus....nur wann ist offen...aber die müssen das nun schnell machen sonst gehts an die OTC
Die Amis sind ja ziemlich sauer was da abläuft - ist auch verständlich -der CEO haut sich die Taschen voll und die lieben Aktionäre bezahlen es.....sollten nun auch noch die 300 Mio . !!! neue Anteile kommen - weiß ich auch nicht wohin das führt....dachte mal 0,50 € wäre günstig...dann 0,40...aber letztendlich bin ich froh keine mehr zu besitzen
Antwort auf Beitrag Nr.: 39.859.548 von Expertchen007 am 22.07.10 10:36:21Ja, alles Durchgewunken und Abgenickt.
Auch die Ausweitung der Incentive-Shares + Options um 5.2 bzw. 8.8 Mio. Stücke. Dabei dann allerdings die Non-Votes waren fast 4mal höher als die der Zustimmung.
Abgesahnt wird also kräftig weiter - wie üblich.

Auch die Ausweitung der Incentive-Shares + Options um 5.2 bzw. 8.8 Mio. Stücke. Dabei dann allerdings die Non-Votes waren fast 4mal höher als die der Zustimmung.
Abgesahnt wird also kräftig weiter - wie üblich.

Antwort auf Beitrag Nr.: 39.861.565 von zwitscherton am 22.07.10 15:15:26Schwere Entscheidung nun für Dich und die Investierten Kollegen kann ich mir vorstellen......jetzt ist guter Rat wirklich teuer und fast nicht möglich
Antwort auf Beitrag Nr.: 39.861.565 von zwitscherton am 22.07.10 15:15:26Trotzdem, der erste Kurs in Amiland ist im Plus.


fragt sich nur wie lange

das war die dähm..... entscheidung über haupt hier ein zu steigen

das war die dähm..... entscheidung über haupt hier ein zu steigen
Antwort auf Beitrag Nr.: 39.861.772 von eddycassius am 22.07.10 15:41:44Solltest du so nicht sehen - man weiß bei Biotech nie was kommt - was wäre wenn es um einige 100 % gestiegen wäre ( bei Biotech ist alles möglich ) - im nachhinein ist man immer schlauer - ist wie nach den Lottozahlen
Schwer zu sagen was hier nun so passiert bis Ende August bzw. Anfang September

Schwer zu sagen was hier nun so passiert bis Ende August bzw. Anfang September
Antwort auf Beitrag Nr.: 39.861.866 von Expertchen007 am 22.07.10 15:51:44Jetzt sollen aber auch langsam alle Schlechten Nachrichten eingepreist sein.
(Hoffentlich).
Das Problem ist allerdings noch, daß das Datum des RS bzw. Dillution noch nicht feststeht.
(Unsicherheit).
Aber bei XOMA, läuft ja alles immer etwas anders, als gedacht.

(Hoffentlich).
Das Problem ist allerdings noch, daß das Datum des RS bzw. Dillution noch nicht feststeht.
(Unsicherheit).
Aber bei XOMA, läuft ja alles immer etwas anders, als gedacht.

Antwort auf Beitrag Nr.: 39.862.104 von zwitscherton am 22.07.10 16:17:13Gerade bei Novelos zugeschlagen - heftiger Crash - sapperlot das ist Biotech live
Antwort auf Beitrag Nr.: 39.862.104 von zwitscherton am 22.07.10 16:17:13Jetzt sollen aber auch langsam alle Schlechten Nachrichten eingepreist sein.
Würd ich Dir ja wünschen - aber böse Zungen in USA haben die 0,16 US$ im Munde.....ich glaub auch das ist noch nicht das ENDE - wenn die 0,30 US$ auch noch fallen sollte...dann aber mal gute Nacht
Würd ich Dir ja wünschen - aber böse Zungen in USA haben die 0,16 US$ im Munde.....ich glaub auch das ist noch nicht das ENDE - wenn die 0,30 US$ auch noch fallen sollte...dann aber mal gute Nacht
Antwort auf Beitrag Nr.: 39.862.258 von Expertchen007 am 22.07.10 16:32:01SO schlimm ist es nicht (mehr) bei mir. Bin nur noch mit ner kleinen Posi drin.
Wenn an 052 etwas von der Miracle-Drug dran sein sollte - wie in dem kürzlich eingestellten Blog behauptet, sollte man schon dabei sein.
Wenn wohl auch nicht unbedingt JETZT
Was macht Novelos denn so interessant, außer daß der heutige Kurseinbruch eventuell übertrieben ist.
Böse Zungen behaupten ja, daß deren Mgt. demnächst verhaftet wird.

Wenn an 052 etwas von der Miracle-Drug dran sein sollte - wie in dem kürzlich eingestellten Blog behauptet, sollte man schon dabei sein.
Wenn wohl auch nicht unbedingt JETZT

Was macht Novelos denn so interessant, außer daß der heutige Kurseinbruch eventuell übertrieben ist.
Böse Zungen behaupten ja, daß deren Mgt. demnächst verhaftet wird.


Antwort auf Beitrag Nr.: 39.862.326 von zwitscherton am 22.07.10 16:43:11Reiner Zock mehr nicht - Panik nutzen - ist wie Xoma vom Prinzip - ist auch ne lange Geschichte...wo viele viel Geld verloren haben ...aber das ist nun mal Biotech .
und was dort ein gewisser User schreibt muss nicht immer so sein ( wobei die Bosse in den Knast gehören ) - würde der Aktie helfen )
und was dort ein gewisser User schreibt muss nicht immer so sein ( wobei die Bosse in den Knast gehören ) - würde der Aktie helfen )
Antwort auf Beitrag Nr.: 39.862.363 von Expertchen007 am 22.07.10 16:46:56No risk - no fun.
Kuck ich mir vielleicht auch mal an.

Kuck ich mir vielleicht auch mal an.

Antwort auf Beitrag Nr.: 39.858.685 von Tommi33 am 22.07.10 08:04:16oh wie schrecklich... hab xoma lange nicht mehr verfolgt, aber wenn ich das so lese bin ich wirklich froh vor vielen monaten die reißleine gezogen zu haben. nach 4 dilusions hatte ich einfach den kanal voll und da stand das ding immerhin noch bei 65 eurocent. die tun wirklich alles um ihre aktionäre zu verprellen. immer nur vertröstungen und "news" ala "neuer kaffeeautomat aufgestellt" zeichneten x-oma im gesamten letzten jahr aus. einfach trash was aus diesem wert geworden ist. das die aktionäre bei der hauptversammlung mit "ja" für ie dilusion gestimmt haben ist reine verzweiflung, weil die alternativen noch viel schlimmer sind.
für mich: rating ---, ziel 0,00
depotleiche
für mich: rating ---, ziel 0,00
depotleiche
Bis jetzt ist ja ein Sellout ausgeblieben.
Sieht heute eher nach einem Positiven Abschluss aus.

Sieht heute eher nach einem Positiven Abschluss aus.

bevor ich jetzt bei xoma nochmal spiele, spiel ich lieber bei genta! 
chancen risikoverhältnis is da größer :P
so blöd es klingt....man man haben die was verbockt bei xoma!
dabei waren die doch so gut mal dabei....

chancen risikoverhältnis is da größer :P
so blöd es klingt....man man haben die was verbockt bei xoma!
dabei waren die doch so gut mal dabei....

Antwort auf Beitrag Nr.: 39.868.257 von Markus77 am 23.07.10 16:01:54Machen Nägel mit Köpfen
[urlXOMA Enters Into $30 Million Committed Equity Financing Facility]http://finance.yahoo.com/news/XOMA-Enters-Into-30-Million-pz-2208906118.html?x=0&.v=1[/url]

[urlXOMA Enters Into $30 Million Committed Equity Financing Facility]http://finance.yahoo.com/news/XOMA-Enters-Into-30-Million-pz-2208906118.html?x=0&.v=1[/url]

Antwort auf Beitrag Nr.: 39.870.760 von zwitscherton am 24.07.10 01:04:49Der Kursverlauf heute war allerdings besch .....


Antwort auf Beitrag Nr.: 39.870.766 von zwitscherton am 24.07.10 01:08:52Gestern im Amiboard was zur AGM:
Shareholder Meeting - Addendum 22-Jul-10 08:19 pm
Gates, I just wanted to add a few more things that were discussed during the shareholder meeting, and you could correct me if I missed anything:
- When I asked Engle if he was looking for multiple partners for 052's multiple indications, he said that the pharmaceutical companies did not like it because the effects of diabetes and CVD are difficult to separate and they did not like the potential lawsuits that could result. Translation: one or multiple partners for ALL of the indications
- When I asked him if there have been any indications of a hostile takeover, even with the poison pill, due to the current shareprice, he said that he could not comment.
- When I asked him if there had been any cuts in the funding for the biodefense revenues, as far as the $20 million was concerned, he indicated that we had a contract for about $68 million and it was secure and it was not as if we were still bidding for a govt. contract
- When the R/S issue was raised, Engle commented that some companies who do not have everything in place would have their shareprice go down after the R/S and some companies who have everything in place would have their shareprice go up; however, he felt that we have everything in place.
- As far as the partnership and the phase 2 results were concerned, Engle indicated that some companies want to partner after the phase 2 results were in and some want to partner before the phase 2 results were in.
- Engle also indicated that they were not looking for a 1x or 2x result but a 10x because of the revolutionary nature of 052
- Engle said that he and Fred Kurland, I believe, were aware of the shareprice and that they were looking at it everyday and are very aware of the Nasdaq requirements.
- Engle seemed unenthusiastic about having a separate PR firm handle XOMA's press releases when a shareholder raised the issue.
- When a shareholder asked Mr. Hutt, I believe, who is one of the BOD, if he would buy with his own money XOMA stock, he emphatically said "Yes, especially at $ 0.35 cents!"
- After the meeting, I asked Dr. Scannon if they had any timeline for getting 052 through the FDA via the orphan indication for Behcet's and he said with a wry smile that he might get into trouble with management for saying too much and that he had to leave for another meeting.

Shareholder Meeting - Addendum 22-Jul-10 08:19 pm
Gates, I just wanted to add a few more things that were discussed during the shareholder meeting, and you could correct me if I missed anything:
- When I asked Engle if he was looking for multiple partners for 052's multiple indications, he said that the pharmaceutical companies did not like it because the effects of diabetes and CVD are difficult to separate and they did not like the potential lawsuits that could result. Translation: one or multiple partners for ALL of the indications
- When I asked him if there have been any indications of a hostile takeover, even with the poison pill, due to the current shareprice, he said that he could not comment.
- When I asked him if there had been any cuts in the funding for the biodefense revenues, as far as the $20 million was concerned, he indicated that we had a contract for about $68 million and it was secure and it was not as if we were still bidding for a govt. contract
- When the R/S issue was raised, Engle commented that some companies who do not have everything in place would have their shareprice go down after the R/S and some companies who have everything in place would have their shareprice go up; however, he felt that we have everything in place.
- As far as the partnership and the phase 2 results were concerned, Engle indicated that some companies want to partner after the phase 2 results were in and some want to partner before the phase 2 results were in.
- Engle also indicated that they were not looking for a 1x or 2x result but a 10x because of the revolutionary nature of 052
- Engle said that he and Fred Kurland, I believe, were aware of the shareprice and that they were looking at it everyday and are very aware of the Nasdaq requirements.
- Engle seemed unenthusiastic about having a separate PR firm handle XOMA's press releases when a shareholder raised the issue.
- When a shareholder asked Mr. Hutt, I believe, who is one of the BOD, if he would buy with his own money XOMA stock, he emphatically said "Yes, especially at $ 0.35 cents!"
- After the meeting, I asked Dr. Scannon if they had any timeline for getting 052 through the FDA via the orphan indication for Behcet's and he said with a wry smile that he might get into trouble with management for saying too much and that he had to leave for another meeting.

Antwort auf Beitrag Nr.: 39.870.760 von zwitscherton am 24.07.10 01:04:49Ja - nun ghets es dann wohl los mit dem R/S bzw. Aktienausgabe
*****************************************************
Artikelauszug : 29 Seiten das ganze unter .......
http://investors.xoma.com/secfiling.cfm?filingid=950162-10-2…
PROSPECTUS
$150,000,000
Common Shares
Preference Shares
Debt Securities
Warrants
Offered by
XOMA Ltd.
From time to time, we may offer up to $150,000,000 of any combination of the securities described in this prospectus.
We will provide specific terms of these offerings and securities in supplements to this prospectus. The prospectus supplement may also add, update or change information contained in this prospectus. You should read this prospectus, the information incorporated by reference in this prospectus and any prospectus supplement carefully before you invest.
Our common shares are traded on the Nasdaq Global Market under the symbol “XOMA.” On October 21, 2008, the last reported sale price of our common shares was $1.64 per share. You are urged to obtain current market quotations for our common shares. The applicable prospectus supplement will contain information, where applicable, as to any other listing on the Nasdaq Global Market or any securities market or other exchange of the securities, if any, covered by the prospectus supplement.
Investing in our securities involves a high degree of risk. . See the section entitled “RISK FACTORS” contained in any supplements to this Prospectus and in our most recent Annual Report on Form 10-K and Quarterly Reports on Form 10-Q, as well as any amendments thereto, as filed with the Securities and Exchange Commission, and which are incorporated herein by reference in their entirety.
*****************************************************
Artikelauszug : 29 Seiten das ganze unter .......
http://investors.xoma.com/secfiling.cfm?filingid=950162-10-2…
PROSPECTUS
$150,000,000
Common Shares
Preference Shares
Debt Securities
Warrants
Offered by
XOMA Ltd.
From time to time, we may offer up to $150,000,000 of any combination of the securities described in this prospectus.
We will provide specific terms of these offerings and securities in supplements to this prospectus. The prospectus supplement may also add, update or change information contained in this prospectus. You should read this prospectus, the information incorporated by reference in this prospectus and any prospectus supplement carefully before you invest.
Our common shares are traded on the Nasdaq Global Market under the symbol “XOMA.” On October 21, 2008, the last reported sale price of our common shares was $1.64 per share. You are urged to obtain current market quotations for our common shares. The applicable prospectus supplement will contain information, where applicable, as to any other listing on the Nasdaq Global Market or any securities market or other exchange of the securities, if any, covered by the prospectus supplement.
Investing in our securities involves a high degree of risk. . See the section entitled “RISK FACTORS” contained in any supplements to this Prospectus and in our most recent Annual Report on Form 10-K and Quarterly Reports on Form 10-Q, as well as any amendments thereto, as filed with the Securities and Exchange Commission, and which are incorporated herein by reference in their entirety.
Antwort auf Beitrag Nr.: 39.870.766 von zwitscherton am 24.07.10 01:08:52was willst du uns eigentlich mit deinem  - smilie dauernd sagen? willst du damit den eindruck vermitteln, dass dieser wert wohl bald 10.000 prozent machen wird? schnell am montag kaufen um dann doch wieder in die röhre zu schauen? hör bitte auf damit, das macht mich agressiv - nachher fällt wirklich noch einer darauf rein und versenkt hier seine kohle.
- smilie dauernd sagen? willst du damit den eindruck vermitteln, dass dieser wert wohl bald 10.000 prozent machen wird? schnell am montag kaufen um dann doch wieder in die röhre zu schauen? hör bitte auf damit, das macht mich agressiv - nachher fällt wirklich noch einer darauf rein und versenkt hier seine kohle.
 - smilie dauernd sagen? willst du damit den eindruck vermitteln, dass dieser wert wohl bald 10.000 prozent machen wird? schnell am montag kaufen um dann doch wieder in die röhre zu schauen? hör bitte auf damit, das macht mich agressiv - nachher fällt wirklich noch einer darauf rein und versenkt hier seine kohle.
- smilie dauernd sagen? willst du damit den eindruck vermitteln, dass dieser wert wohl bald 10.000 prozent machen wird? schnell am montag kaufen um dann doch wieder in die röhre zu schauen? hör bitte auf damit, das macht mich agressiv - nachher fällt wirklich noch einer darauf rein und versenkt hier seine kohle.
Antwort auf Beitrag Nr.: 39.872.139 von kleingeldjaeger am 24.07.10 19:23:50sorry aber ich kann es mir nicht verkneifen. 
hasse heute morggen schlecht geschissen oder was
auf dein bla bla bla kann hir wohl jeder verzichten

hasse heute morggen schlecht geschissen oder was

auf dein bla bla bla kann hir wohl jeder verzichten
Hmmm Rt in D wäre 0,247 €....aber ist über Pari malwieder...der ASK sogar extrem....
Bei mit per Update eingegangen...na ja was sind 750 K
*****************************************************************
XOMA Receives $750,000 Milestone Payment From AVEO Pharmaceuticals
BERKELEY, Calif., Jul 26, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced receipt of a $750,000 milestone payment under its collaboration with AVEO Pharmaceuticals, Inc. (Nasdaq:AVEO). The milestone payment resulted from AVEO's recent initiation of a Phase 2 clinical trial to evaluate its AV-299 antibody for the treatment of non-small cell lung cancer. AV-299 is a humanized antibody to hepatocyte growth factor (HGF).
XOMA has signed more than 60 license and collaboration agreements with pharmaceutical and biotechnology companies related to its patented technologies and its antibody discovery, development and optimization expertise. These agreements cover a number of potential product candidates in various stages of clinical and preclinical development for which XOMA may be entitled to future milestone and royalty payments.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behçet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(tm), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, more than 50 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
*****************************************************************
XOMA Receives $750,000 Milestone Payment From AVEO Pharmaceuticals
BERKELEY, Calif., Jul 26, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced receipt of a $750,000 milestone payment under its collaboration with AVEO Pharmaceuticals, Inc. (Nasdaq:AVEO). The milestone payment resulted from AVEO's recent initiation of a Phase 2 clinical trial to evaluate its AV-299 antibody for the treatment of non-small cell lung cancer. AV-299 is a humanized antibody to hepatocyte growth factor (HGF).
XOMA has signed more than 60 license and collaboration agreements with pharmaceutical and biotechnology companies related to its patented technologies and its antibody discovery, development and optimization expertise. These agreements cover a number of potential product candidates in various stages of clinical and preclinical development for which XOMA may be entitled to future milestone and royalty payments.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behçet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(tm), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, more than 50 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
Antwort auf Beitrag Nr.: 39.876.236 von Expertchen007 am 26.07.10 14:13:54750K haben und nicht haben ...
Reicht möglicherweise erst mal für die Gehälter der Chefetage .
BTW: Die sind mit nicht wirklich überwältigender Mehrheit gewählt worden.

http://biz.yahoo.com/e/100726/xoma8-k_a.html

Reicht möglicherweise erst mal für die Gehälter der Chefetage .
BTW: Die sind mit nicht wirklich überwältigender Mehrheit gewählt worden.

http://biz.yahoo.com/e/100726/xoma8-k_a.html

Antwort auf Beitrag Nr.: 39.870.956 von Expertchen007 am 24.07.10 09:49:45In Summe 180 Mio. USD.
Bedeutet das, daß in absehbarer Zeit kein Partner in Sicht ist für das 052 Prokjet ???
180 Mio. mehr als 2x Market Cap.
Poison Pill gegen Hostile Takeover ???

Bedeutet das, daß in absehbarer Zeit kein Partner in Sicht ist für das 052 Prokjet ???
180 Mio. mehr als 2x Market Cap.
Poison Pill gegen Hostile Takeover ???

Antwort auf Beitrag Nr.: 39.880.022 von zwitscherton am 27.07.10 01:36:17Wie bitte kommst Du denn auf die 180 Mio ????
Antwort auf Beitrag Nr.: 39.883.542 von Expertchen007 am 27.07.10 16:08:41Der CEFF-Deal mit Azimuth Opportunity (30 Mio.) + das Angebot im 150 Mio. Prospectus.
http://finance.yahoo.com/news/XOMA-Enters-Into-30-Million-pz…
http://investors.xoma.com/secfiling.cfm?filingid=950162-10-2…
Oder liege ich damit falsch ???

http://finance.yahoo.com/news/XOMA-Enters-Into-30-Million-pz…
http://investors.xoma.com/secfiling.cfm?filingid=950162-10-2…
Oder liege ich damit falsch ???

Antwort auf Beitrag Nr.: 39.884.202 von zwitscherton am 27.07.10 17:15:14Muss ich mir esrt mal anschauen mit en 150 Mio. - allerdings der Kurs sagt was anderes...denn 0,31 US$ = 0,238 € ....
Sollte die 0,30 US$ fallen könnte das möglicherweise einen Abverkaufshype auslösen und dann sind selbst die 0,160 US$ Horrorkurse möglich
Sollte die 0,30 US$ fallen könnte das möglicherweise einen Abverkaufshype auslösen und dann sind selbst die 0,160 US$ Horrorkurse möglich
Antwort auf Beitrag Nr.: 39.884.462 von Expertchen007 am 27.07.10 17:50:52Siehe Novelos bei der Ankündigung des 1.5 Mio. Offering 



Hmmm...noch immer Recht stabil über der 0,30 $ ...so bei umgerechnet 0,196 €...würde ich es ja mal wieder riskieren..aber noch ist es nicht soweit
immer wieder mal ein Versuch unter die 0,30 $ zu drücken...bin mal gespannnt ob es gelingt
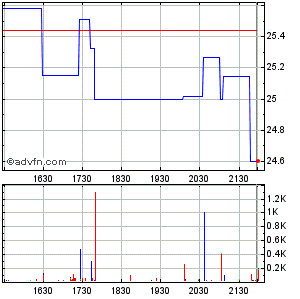
Was ist denn hier schon wieder los? 





Antwort auf Beitrag Nr.: 39.891.028 von strongbuyamitelo am 28.07.10 16:49:35Na das geht aber schon ne Weile so...nicht erst heute...!!!!
Antwort auf Beitrag Nr.: 39.884.619 von zwitscherton am 27.07.10 18:13:46mit dilusions haben die xoma-aktionäre im letzten jahr reichlich erfahrung gemacht. ob nun 6 oder 7 mal, verärgert sind sie allemal. die erste im jahr 2009 war glaub ich bei 1.15$ (aktueller kurs war 1.40$ bis zu dieser meldung) - der investor sitzt nun auf 70% minus. üblicherweise hat man aber vorher den kurs nochmal mit pseudo-meldungen ein gutes stück hochgetrieben und so auch kleinanleger geködert. fazit: man sollte also einen ungewöhnlichen anstieg bei xoma unbedingt zum verkaufen nutzen, nicht zum einkaufen.
ach und...

ach und...


Hab mal was positves für euch hier...wenns hilft !!
Was würdet ihr nur ohne meine Infos machen....
******************************************
XOMA 052 Orphan Drug Designation for Behcet's Disease Recommended by European Medicines Agency
BERKELEY, Calif., Jul 29, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the Committee for Orphan Medical Products of the European Medicines Agency (EMA) has adopted a positive opinion and recommends the granting of orphan medicinal product designation for XOMA 052, an antibody to interleukin-1 beta, for the treatment of Behcet's disease. Positive opinions are submitted to the European Commission for decision and are generally adopted within 30 days of receipt.
The EMA's orphan drug program is designed to promote the development of drugs to treat life-threatening or chronically debilitating conditions with a prevalence of up to five in 10,000 persons in the European Union (EU). The designation provides EU market exclusivity for up to ten years following approval for the given indication. Other potential benefits include protocol assistance, direct access to centralized marketing authorization procedures and financial incentives.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London earlier this month.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. More than 12,000 patients in the EU are estimated to suffer from Behcet's disease.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes and has completed a Phase 2 clinical trial in uveitis of Behcet's disease. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behcet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(TM), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
Was würdet ihr nur ohne meine Infos machen....

******************************************
XOMA 052 Orphan Drug Designation for Behcet's Disease Recommended by European Medicines Agency
BERKELEY, Calif., Jul 29, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the Committee for Orphan Medical Products of the European Medicines Agency (EMA) has adopted a positive opinion and recommends the granting of orphan medicinal product designation for XOMA 052, an antibody to interleukin-1 beta, for the treatment of Behcet's disease. Positive opinions are submitted to the European Commission for decision and are generally adopted within 30 days of receipt.
The EMA's orphan drug program is designed to promote the development of drugs to treat life-threatening or chronically debilitating conditions with a prevalence of up to five in 10,000 persons in the European Union (EU). The designation provides EU market exclusivity for up to ten years following approval for the given indication. Other potential benefits include protocol assistance, direct access to centralized marketing authorization procedures and financial incentives.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London earlier this month.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. More than 12,000 patients in the EU are estimated to suffer from Behcet's disease.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes and has completed a Phase 2 clinical trial in uveitis of Behcet's disease. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behcet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(TM), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
Antwort auf Beitrag Nr.: 39.896.692 von Expertchen007 am 29.07.10 14:36:17Was würdet ihr nur ohne meine Infos machen
Wir wären wohl hoffnenungslos verloren

Wir wären wohl hoffnenungslos verloren


Antwort auf Beitrag Nr.: 39.896.692 von Expertchen007 am 29.07.10 14:36:17Dieser 052 AB könnte anscheinend für einiges gut sein.
Obs dem Wert im Moment soviel hilft, bleibt abzuwarten.

Obs dem Wert im Moment soviel hilft, bleibt abzuwarten.

Antwort auf Beitrag Nr.: 39.896.692 von Expertchen007 am 29.07.10 14:36:17Dumm aus der Wäsche gucken weil wir nicht wissen warum es rauf und runter geht 
LG Tommi

LG Tommi
Antwort auf Beitrag Nr.: 39.896.896 von zwitscherton am 29.07.10 14:56:23 ...sehr wahrscheinlich
...sehr wahrscheinlich
********************
ne im Ernst ich glaube auch nicht das die Meldung soviel bringt...dazu sind zuviele andere Probleme im Hintergrund aktuell...aber jeder cent zählt
 ...sehr wahrscheinlich
...sehr wahrscheinlich********************
ne im Ernst ich glaube auch nicht das die Meldung soviel bringt...dazu sind zuviele andere Probleme im Hintergrund aktuell...aber jeder cent zählt
Antwort auf Beitrag Nr.: 39.897.210 von Expertchen007 am 29.07.10 15:27:52Es ist ja erstmal nur ne Empfehlung der Europ.Med.Agency.


Antwort auf Beitrag Nr.: 39.897.518 von zwitscherton am 29.07.10 15:53:51gebracht hat es eher " null " - nächster Halt mit Unterstützung dürfte bei 0,27 UIS$ sein - falls die 0,30 fällt
Antwort auf Beitrag Nr.: 39.897.929 von Expertchen007 am 29.07.10 16:36:09das wird hier noch übel enden, da ahne ich leider schon was!

Antwort auf Beitrag Nr.: 39.899.832 von Market-Insider am 29.07.10 20:52:26Ob mein Timing gut oder schlecht war wird sich wohl in den nächsten Tagen entscheiden.
0,303 USD könnte noch teuer gewesen sein.
0,303 USD könnte noch teuer gewesen sein.

Antwort auf Beitrag Nr.: 39.900.546 von Market-Insider am 29.07.10 22:59:57Da war vielleicht schon was durchgesickert wegen der Orphan Drug Designation ...


Antwort auf Beitrag Nr.: 39.899.832 von Market-Insider am 29.07.10 20:52:26BTW Schöner Peak im Volume um 13:18 ...
Aber ob das alles im Moment viel bringt
Not sure ...

Aber ob das alles im Moment viel bringt

Not sure ...

Antwort auf Beitrag Nr.: 39.900.749 von zwitscherton am 30.07.10 00:05:24Wie ??? Was...?? meinst doch wohl jetzt nicht im Ernst das hier !!!
After Hours Last:
Net / % Change $ .30
unch (unch) After Hours High: $ .3195
After Hours Volume: 1,452 After Hours Low: $ .30
16:22 $ .30 452
16:19 $ .3195 1,000
After Hours Last:
Net / % Change $ .30
unch (unch) After Hours High: $ .3195
After Hours Volume: 1,452 After Hours Low: $ .30
16:22 $ .30 452
16:19 $ .3195 1,000
Antwort auf Beitrag Nr.: 39.902.334 von Expertchen007 am 30.07.10 11:10:02Naja, die 500K im obigen Chart fallen schon ins Auge.
Aber richtig - es sind keine Millionen Umsätze, von daher hätte man es nicht unbedingt erwähnen müssen.
Der Kurs hangelt an der 0.30 und ist wahrscheinlich IMHO noch nicht der Boden es sei denn es kommen noch nen paar gute News - oder der Gesamtmarkt zieht an.

Aber richtig - es sind keine Millionen Umsätze, von daher hätte man es nicht unbedingt erwähnen müssen.
Der Kurs hangelt an der 0.30 und ist wahrscheinlich IMHO noch nicht der Boden es sei denn es kommen noch nen paar gute News - oder der Gesamtmarkt zieht an.

5 Jahrestief...oder eher ATL ..wenn ich das richtig sehe

Hallo "Expertchen"  !
!
Du hast dich ja bei Novelos schon positioniert,aber da sehe ich keine hoffnung mehr,anders Xoma,was denkst du,sollte man oder bist du schon eingestiegen ?
MFG
Zuki
 !
!Du hast dich ja bei Novelos schon positioniert,aber da sehe ich keine hoffnung mehr,anders Xoma,was denkst du,sollte man oder bist du schon eingestiegen ?
MFG
Zuki

Antwort auf Beitrag Nr.: 39.905.023 von Zukertort am 30.07.10 16:55:29Nein bin noch nicht drin...wie bereits geschrieben denke ich ab der 0,195 € ( umgerechnet ) darüber mal wieder nach......ob Du investierst oder nicht kann ich nichts dazu sagen
Novelos ist ein reiner Zock mehr nicht
Bei Biotech ist nun mal alles möglich oder auch nix....1 Meldung bringt Freude oder das totale Elend mit sich....so ist das nun mal..und mit schnellem Geld ist da eh nix zu machen
Novelos ist ein reiner Zock mehr nicht
Bei Biotech ist nun mal alles möglich oder auch nix....1 Meldung bringt Freude oder das totale Elend mit sich....so ist das nun mal..und mit schnellem Geld ist da eh nix zu machen
Antwort auf Beitrag Nr.: 39.906.358 von Expertchen007 am 30.07.10 20:49:53Dein anvisierter EInstiegskurs könnte ggf. noch Realität werden.
Die 0.30 sind durch. Kanpp.

Die 0.30 sind durch. Kanpp.

Antwort auf Beitrag Nr.: 39.906.932 von zwitscherton am 30.07.10 23:07:48[urlXOMA is Expected to Beat the Street Consensus When It Reports Earnings ]http://www.investors.com/NewsAndAnalysis/Newsfeed/Article/116927257/201008021047/Earnings-Alert-XOMA-is-Expected-to-Beat-the-Street-Consensus-When-It-Reports-Earnings-XOMA-.aspx
[/url]
Aug 02, 2010 (SmarTrend(R) News Watch via COMTEX) -- Analysts, on average, expect XOMA (XOMA) to report a loss of $0.07 on sales of $8 million on August 06, 2010.
For the full year, analysts expect the company to post a loss of $0.20. In the year-ago period, the company reported a loss of $0.07 on sales of $10 million.
In the previous quarter, the company reported a loss of $0.09, missing consensus estimates for a loss of $0.06.
SmarTrend is bearish on shares of XOMA and our subscribers were alerted to Sell on May 20, 2010 at $0.52. The stock has fallen 43.5% since the alert was issued.
Write to Chip Brian at cbrian@tradethetrend.com

[/url]
Aug 02, 2010 (SmarTrend(R) News Watch via COMTEX) -- Analysts, on average, expect XOMA (XOMA) to report a loss of $0.07 on sales of $8 million on August 06, 2010.
For the full year, analysts expect the company to post a loss of $0.20. In the year-ago period, the company reported a loss of $0.07 on sales of $10 million.
In the previous quarter, the company reported a loss of $0.09, missing consensus estimates for a loss of $0.06.
SmarTrend is bearish on shares of XOMA and our subscribers were alerted to Sell on May 20, 2010 at $0.52. The stock has fallen 43.5% since the alert was issued.
Write to Chip Brian at cbrian@tradethetrend.com

Antwort auf Beitrag Nr.: 39.915.194 von zwitscherton am 02.08.10 19:49:05XOMA outperform
http://www.finanzen.net/analyse/XOMA_outperform-Wedbush_Morg…
http://www.finanzen.net/analyse/XOMA_outperform-Wedbush_Morg…
Antwort auf Beitrag Nr.: 39.919.504 von Scheilko am 03.08.10 14:34:54eine ohrfeige für jeden anleger ich sitze hier auf guten 70% buchverlust aufgrund einiger pusher hier danke noch mal dafür hier kann man ner ganzen menge leuten nicht trauen
Antwort auf Beitrag Nr.: 39.919.504 von Scheilko am 03.08.10 14:34:54XOMA outperform
Rating-Update:
Los Angeles (aktiencheck.de AG) - Die Analysten von Wedbush Morgan Securities, Liana Moussatos und Richard Lau, stufen die Aktie von XOMA (ISIN BMG9825R1079/ WKN 871239) weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u
Mutige Prognose.

Rating-Update:
Los Angeles (aktiencheck.de AG) - Die Analysten von Wedbush Morgan Securities, Liana Moussatos und Richard Lau, stufen die Aktie von XOMA (ISIN BMG9825R1079/ WKN 871239) weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u
Mutige Prognose.


XOMA to Announce 2010 Second Quarter Financial Results and Host Webcast Conference Call on August 9, 2010
BERKELEY, Calif., Aug 2, 2010 (GlobeNewswire via COMTEX) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of antibody therapeutics, announced that the company will host a webcast conference call on Monday, August 9, 2010 at 4:30 pm Eastern time to discuss its 2010 second quarter financial results and provide a general business update.
The webcast conference call will follow the release of the company's second quarter 2010 financial results earlier that day. The webcast can be accessed via the Investors section of XOMA's website at http://investors.xoma.com/events.cfm and will be available for replay until close of business on November 9, 2010.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behcet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(tm), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
By Staff
CONTACT: CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
(C) Copyright 2010 GlobeNewswire, Inc. All rights reserved.
**********************************************************************
As of Thursday, 07-29-2010 23:59, the latest Comtex SmarTrend? Alert, an automated pattern recognition system, indicated a DOWNTREND on 05-20-2010 for XOMA @ $0.52.
For more information on SmarTrend, contact your market data provider or go to www.mysmartrend.com
SmarTrend is a registered trademark of Comtex News Network, Inc. Copyright ? 2004-2010 Comtex News Network, Inc. All rights reserved.
-0-
INDUSTRY KEYWORD: Biotechnology
SUBJECT CODE: BIOTECHNOLOGY
EARNINGS
CONFERENCE CALL
Calendar of Events
Earnings Releases and Operating Results
http://www.otcmarkets.com/stock/XOMA/news
BERKELEY, Calif., Aug 2, 2010 (GlobeNewswire via COMTEX) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of antibody therapeutics, announced that the company will host a webcast conference call on Monday, August 9, 2010 at 4:30 pm Eastern time to discuss its 2010 second quarter financial results and provide a general business update.
The webcast conference call will follow the release of the company's second quarter 2010 financial results earlier that day. The webcast can be accessed via the Investors section of XOMA's website at http://investors.xoma.com/events.cfm and will be available for replay until close of business on November 9, 2010.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behcet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(tm), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
By Staff
CONTACT: CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
(C) Copyright 2010 GlobeNewswire, Inc. All rights reserved.
**********************************************************************
As of Thursday, 07-29-2010 23:59, the latest Comtex SmarTrend? Alert, an automated pattern recognition system, indicated a DOWNTREND on 05-20-2010 for XOMA @ $0.52.
For more information on SmarTrend, contact your market data provider or go to www.mysmartrend.com
SmarTrend is a registered trademark of Comtex News Network, Inc. Copyright ? 2004-2010 Comtex News Network, Inc. All rights reserved.
-0-
INDUSTRY KEYWORD: Biotechnology
SUBJECT CODE: BIOTECHNOLOGY
EARNINGS
CONFERENCE CALL
Calendar of Events
Earnings Releases and Operating Results
http://www.otcmarkets.com/stock/XOMA/news
Antwort auf Beitrag Nr.: 39.920.387 von strongbuyamitelo am 03.08.10 15:57:39....ich bin auch mal auf die zahlen gespannt. jedoch glaube ich, dass eventl. schlechte zahlen in kursen bereits eingepreist sind. spannender wird der 10. september nach dem
revers-split. ich denke, dass im 3. oder spätest. 4. quartal ein kooperationspartner
vorgestellt wird. hier könnte die front-up zahlung vielleicht ein mehrfaches der aktuellen marktkapitalisierung ausmachen, die derzeit lediglich nur gut 70 mio usd beträgt.
hier liegt aus meiner sicht die phantasie und wird den startschuss für eine kursralley geben. (kurse von 5 USD - splittbereinigt, d.h. aus heutiger sicht eine verdoppelung von 0,3 auf 0,5 oder 0,6 USD) sind durchaus drin. nur mal meine persönliche meinung...
gruß in die runde
GL
BuB
revers-split. ich denke, dass im 3. oder spätest. 4. quartal ein kooperationspartner
vorgestellt wird. hier könnte die front-up zahlung vielleicht ein mehrfaches der aktuellen marktkapitalisierung ausmachen, die derzeit lediglich nur gut 70 mio usd beträgt.
hier liegt aus meiner sicht die phantasie und wird den startschuss für eine kursralley geben. (kurse von 5 USD - splittbereinigt, d.h. aus heutiger sicht eine verdoppelung von 0,3 auf 0,5 oder 0,6 USD) sind durchaus drin. nur mal meine persönliche meinung...
gruß in die runde
GL
BuB
Entweder hat der Laden keinen Forschungserfolg
Oder die Manager verklatschen den.
Einzige Chance für Aktionäre ist nach Kursverfall und krebsartiger Aktienverwässerung, dann steigt die Aktie der langjährigen Suppenhühner vielleicht mal.
Oder die Manager verklatschen den.
Einzige Chance für Aktionäre ist nach Kursverfall und krebsartiger Aktienverwässerung, dann steigt die Aktie der langjährigen Suppenhühner vielleicht mal.
XOMA "outperform"
Rating-Update: Los Angeles (aktiencheck.de AG) - Die Analysten von Wedbush Morgan Securities, Liana Moussatos und Richard Lau, stufen die Aktie von XOMA (<BMG9825R1079>/ <BMG9825R1079> weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u)
weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u)
Rating-Update: Los Angeles (aktiencheck.de AG) - Die Analysten von Wedbush Morgan Securities, Liana Moussatos und Richard Lau, stufen die Aktie von XOMA (<BMG9825R1079>/ <BMG9825R1079>
 weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u)
weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u)
XOMA 052 Designated Orphan Drug by FDA for Treatment of Behcet's Disease
BERKELEY, Calif., Aug. 4, 2010 (GLOBE NEWSWIRE) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the U.S. Food and Drug Administration has designated XOMA 052, an antibody to interleukin-1 beta, an orphan drug for the treatment of Behcet's disease. As previously announced, the Committee for Orphan Medical Products of the European Medicines Agency has recommended the granting of orphan medicinal product designation for XOMA 052 for the same indication in the European Union.
U.S. orphan drug designation is granted by the FDA Office of Orphan Drug Products Development to novel drugs or biologics that may treat a condition affecting fewer than 200,000 persons in the United States. The designation offers a number of potential incentives, which may include, among others, a seven-year period of U.S. marketing exclusivity from the date of marketing authorization, written guidance on the non-clinical and clinical studies needed to obtain marketing approval, and tax credits for certain clinical research.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London in July.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. Approximately 16,000 patients in the U.S. are estimated to suffer from Behcet's disease.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes and has completed a Phase 2 clinical trial in uveitis of Behcet's disease. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
* XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and with potential for the treatment of a wide range of inflammatory conditions. XOMA 052 also has demonstrated positive clinical benefit in a proof-of-concept trial for the treatment of vision-threatening uveitis of Behçet's disease.
* XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the botulinum toxin, among the most deadly potential bioterror threats, under development through funding provided by the National Institute of Allergy and Infectious Diseases of the National Institutes of Health (Contract # HHSN266200600008C).
* A preclinical pipeline with candidates in development for several diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS® (ranibizumab injection) for wet age-related macular degeneration and CIMZIA® (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(tm), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
http://www.nasdaq.com/aspx/company-news-story.aspx?storyid=2…
BERKELEY, Calif., Aug. 4, 2010 (GLOBE NEWSWIRE) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the U.S. Food and Drug Administration has designated XOMA 052, an antibody to interleukin-1 beta, an orphan drug for the treatment of Behcet's disease. As previously announced, the Committee for Orphan Medical Products of the European Medicines Agency has recommended the granting of orphan medicinal product designation for XOMA 052 for the same indication in the European Union.
U.S. orphan drug designation is granted by the FDA Office of Orphan Drug Products Development to novel drugs or biologics that may treat a condition affecting fewer than 200,000 persons in the United States. The designation offers a number of potential incentives, which may include, among others, a seven-year period of U.S. marketing exclusivity from the date of marketing authorization, written guidance on the non-clinical and clinical studies needed to obtain marketing approval, and tax credits for certain clinical research.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London in July.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. Approximately 16,000 patients in the U.S. are estimated to suffer from Behcet's disease.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes and has completed a Phase 2 clinical trial in uveitis of Behcet's disease. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
* XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and with potential for the treatment of a wide range of inflammatory conditions. XOMA 052 also has demonstrated positive clinical benefit in a proof-of-concept trial for the treatment of vision-threatening uveitis of Behçet's disease.
* XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the botulinum toxin, among the most deadly potential bioterror threats, under development through funding provided by the National Institute of Allergy and Infectious Diseases of the National Institutes of Health (Contract # HHSN266200600008C).
* A preclinical pipeline with candidates in development for several diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS® (ranibizumab injection) for wet age-related macular degeneration and CIMZIA® (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(tm), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
http://www.nasdaq.com/aspx/company-news-story.aspx?storyid=2…
Antwort auf Beitrag Nr.: 39.926.724 von Lucky72 am 04.08.10 14:10:39Schönes Volumen vorbörslich und ganz guter Anstieg.
Mal sehen wie lange es dieses Mal anhält und ob wir es mal wieder schaffen im Plus zu schließen.
Mal sehen wie lange es dieses Mal anhält und ob wir es mal wieder schaffen im Plus zu schließen.

Antwort auf Beitrag Nr.: 39.926.906 von MogD am 04.08.10 14:28:13Ist wohl obiger Nachricht zu Danken.
Mal sehn was am Montag noch so zu berichten ist:
.. the company will host a webcast conference call on Monday, August 9, 2010 at 4:30 pm Eastern time to discuss its 2010 second quarter financial results and provide a general business update.

Mal sehn was am Montag noch so zu berichten ist:
.. the company will host a webcast conference call on Monday, August 9, 2010 at 4:30 pm Eastern time to discuss its 2010 second quarter financial results and provide a general business update.

Antwort auf Beitrag Nr.: 39.927.948 von zwitscherton am 04.08.10 16:16:48general business update
whatever that means

whatever that means


Endlich kommt mal Leben rein in XOMA  !
!
Bin mit einer einstiegsposi dabei,werde aber noch aufstocken,
in US grassieren Kursziele von 50$/share,kein witz !
MFG
Zuki
 !
!Bin mit einer einstiegsposi dabei,werde aber noch aufstocken,
in US grassieren Kursziele von 50$/share,kein witz !
MFG
Zuki

So bin auch mal wieder mit im Spiel  ...leider ganz unten verpasst...aber die Meldung gefällt mir recht gut...1. Posi mal im Depot...dann mal weitersehen
...leider ganz unten verpasst...aber die Meldung gefällt mir recht gut...1. Posi mal im Depot...dann mal weitersehen
 ...leider ganz unten verpasst...aber die Meldung gefällt mir recht gut...1. Posi mal im Depot...dann mal weitersehen
...leider ganz unten verpasst...aber die Meldung gefällt mir recht gut...1. Posi mal im Depot...dann mal weitersehen
Antwort auf Beitrag Nr.: 39.928.348 von Zukertort am 04.08.10 16:53:20in US grassieren Kursziele von 50$/share,kein witz !
Na darauf wirste doch wohl hoffentlich aber nicht reinfallen...die sollen doch gleich 1000 draus machen - man kanns auch übertreiben......Xoma soll mal froh sein wenn die 0,50 US$ geschafft werden
Na darauf wirste doch wohl hoffentlich aber nicht reinfallen...die sollen doch gleich 1000 draus machen - man kanns auch übertreiben......Xoma soll mal froh sein wenn die 0,50 US$ geschafft werden
Antwort auf Beitrag Nr.: 39.928.498 von Expertchen007 am 04.08.10 17:10:55Gratulation, Expertchen  !
!
Erinnere dich nur mal daran,was mit Keryx im kurs passierte,
als die ihren Orphan drug Status bekommen haben,da ist Keryx
doch glatt von 0,15$ auf 6$ gestiegen ...
MFG
Zuki
 !
!Erinnere dich nur mal daran,was mit Keryx im kurs passierte,
als die ihren Orphan drug Status bekommen haben,da ist Keryx
doch glatt von 0,15$ auf 6$ gestiegen ...
MFG
Zuki

Antwort auf Beitrag Nr.: 39.928.559 von Zukertort am 04.08.10 17:17:59immer mit der Ruhe - hier ist Xoma und die ist launisch...nun gut denke mal viel kann gerade nicht passieren.....aber ich bin da auch ein gebranntes Kind....abber allemal besser als beim VK mit 0,59 € damals ( nach herbem Verlust )
Nun gut hatte mal 2- 3 Zocks zwischendurch hier...aber war nicht die Welt ( war so um die 0,38 € damals )
Nun gut hatte mal 2- 3 Zocks zwischendurch hier...aber war nicht die Welt ( war so um die 0,38 € damals )
so ab der 0,386 US$ wirds spannend - aber ist noch etwas hin....aber könnte was gehen mal wieder

Volumen ist ja richtig gut...das ist ja bald mehr als die letzten Wochen zusammen...aber mal abwarten...was die Shorts so treiben
bin auch dabei mit einer kleine Posi..... zu 0,32$
zu 0,32$
 zu 0,32$
zu 0,32$
Stand 15.07.2010 - nicht ganz aktuell - aber könnte so hinkommen ( eher etwas höher )
*************************
6.33 million short on 7-15-2010 Short Interest: XOMA
Data as of 07/15/10
Date Ratio Shares
Jul 07/15/10 4.30 6.33 M
Jun 06/30/10 4.50 7.05 M
Jun 06/15/10 3.00 6.95 M
May 05/28/10 2.90 8.25 M
May 05/14/10 1.80 6.99 M
Apr 04/30/10 1.40 6.69 M
Apr 04/15/10 0.80 3.49 M
Mar 03/31/10 0.70 2.81 M
Mar 03/15/10 0.40 1.93 M
.
*************************
6.33 million short on 7-15-2010 Short Interest: XOMA
Data as of 07/15/10
Date Ratio Shares
Jul 07/15/10 4.30 6.33 M
Jun 06/30/10 4.50 7.05 M
Jun 06/15/10 3.00 6.95 M
May 05/28/10 2.90 8.25 M
May 05/14/10 1.80 6.99 M
Apr 04/30/10 1.40 6.69 M
Apr 04/15/10 0.80 3.49 M
Mar 03/31/10 0.70 2.81 M
Mar 03/15/10 0.40 1.93 M
.
Antwort auf Beitrag Nr.: 39.928.640 von printguru am 04.08.10 17:27:07kleine Posi ????
normalerweise geht doch bei Dir nix unter 200 -300 K
normalerweise geht doch bei Dir nix unter 200 -300 K

Bin auch noch dabei mit 0,57€

Na wenns so kommen sollte wie USA behauptet im Yahoo Thread... ( 20 Mio Anteile - Handel heute !!! ) ...dann ist noch etwas Platz
8/4/2010 11:30:57 AM
XOMA's NASDAQ Last Sale
0.333 0.0559 +++ 20.17%
Volume
5,788,168 Previous Close
$ 0.2771
Aber glauben tu ich denen dort schon lange nix mehr
8/4/2010 11:30:57 AM
XOMA's NASDAQ Last Sale
0.333 0.0559 +++ 20.17%
Volume
5,788,168 Previous Close
$ 0.2771
Aber glauben tu ich denen dort schon lange nix mehr
Antwort auf Beitrag Nr.: 39.928.668 von Expertchen007 am 04.08.10 17:30:03nee diesmal nur 50k...kann aber noch werden aber hier will ichs nicht übertreiben ist mir zu unsicher das Ganze

Antwort auf Beitrag Nr.: 39.928.677 von TTDEVIL am 04.08.10 17:31:01Dann wünsch ich Dir mal das Du einen Gewinn machst...wenn er auch noch so klein ist ( mit leichtem Eigennutz für mich ) 

Antwort auf Beitrag Nr.: 39.928.706 von Expertchen007 am 04.08.10 17:34:14yrcw ist heute einfach zu langweilig...............
bis später hab sie im Auge
Was mir allerdings nicht gefällt ist zum einen der mögliche R/S bzw. das Delisting an der NASDAQ ...das ja immer noch da heriumschwebt im September - aber nun gut ist noch etwas Zeit..wer weiß vielleicht geschieht ja doch ein Wunder
0,342$ nicht schlecht weiter so

Antwort auf Beitrag Nr.: 39.928.697 von Expertchen007 am 04.08.10 17:32:56was behaupten die denn 

auf gehts..die 0,35 US$ noch dann kanns einen Squezze geben ..wenn die Shorter mal covern..dann wohl richtig

Antwort auf Beitrag Nr.: 39.928.867 von dig101 am 04.08.10 17:56:24Sag ich Dir bestimmt nicht...bei Wamu ist wohl nix los - lies selbst
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
http://messages.finance.yahoo.com/Stocks_%28A_to_Z%29/Stocks…
Antwort auf Beitrag Nr.: 39.928.877 von Expertchen007 am 04.08.10 17:57:29nungut bin kurzfristig raus über 0,351$ bin ich wieder dabei

Antwort auf Beitrag Nr.: 39.928.894 von printguru am 04.08.10 17:59:56Gewinne schaden nie
an der 0,3562 US$ hängt ein 100 K Brocken noch fest
wieder rein................ zu hoher Kaufdruck........
Antwort auf Beitrag Nr.: 39.928.921 von printguru am 04.08.10 18:03:42kannst du sagen was an steht danke
so die 0,3562 US$ werden dann angeknabbert ...danach erst bei 0,36 wieder 100 K...und dann bei 0,366 US$ erst wieder was im ASK...aber kann sich alles auch schnell ändern
so auf gehts..0,36 gefallen..nun ein sauberer Shortsquezze..und ab damit 

Antwort auf Beitrag Nr.: 39.928.981 von Expertchen007 am 04.08.10 18:10:39also ich sehe erst bei 0,4 $ eine grössere order wieder 

verkaufen nicht vergessen  hier riechts nach dilusion die 7. wäre nicht das erste mal, dass ein kursanstieg für ein public offering genutzt wird - gerade bei xoma, also vorsicht
hier riechts nach dilusion die 7. wäre nicht das erste mal, dass ein kursanstieg für ein public offering genutzt wird - gerade bei xoma, also vorsicht 
 hier riechts nach dilusion die 7. wäre nicht das erste mal, dass ein kursanstieg für ein public offering genutzt wird - gerade bei xoma, also vorsicht
hier riechts nach dilusion die 7. wäre nicht das erste mal, dass ein kursanstieg für ein public offering genutzt wird - gerade bei xoma, also vorsicht 
Antwort auf Beitrag Nr.: 39.928.968 von dig101 am 04.08.10 18:08:51XOMA 052 Designated Orphan Drug by FDA for Treatment of Behcet's Disease
BERKELEY, Calif., Aug. 4, 2010 (GLOBE NEWSWIRE) -- XOMA Ltd. ( Nasdaq :XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the U.S. Food and Drug Administration has designated XOMA 052, an antibody to interleukin-1 beta, an orphan drug for the treatment of Behcet's disease. As previously announced, the Committee for Orphan Medical Products of the European Medicines Agency has recommended the granting of orphan medicinal product designation for XOMA 052 for the same indication in the European Union.
U.S. orphan drug designation is granted by the FDA Office of Orphan Drug Products Development to novel drugs or biologics that may treat a condition affecting fewer than 200,000 persons in the United States. The designation offers a number of potential incentives, which may include, among others, a seven-year period of U.S. marketing exclusivity from the date of marketing authorization, written guidance on the non-clinical and clinical studies needed to obtain marketing approval, and tax credits for certain clinical research.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London in July.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. Approximately 16,000 patients in the U.S. are estimated to suffer from Behcet's disease.
BERKELEY, Calif., Aug. 4, 2010 (GLOBE NEWSWIRE) -- XOMA Ltd. ( Nasdaq :XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the U.S. Food and Drug Administration has designated XOMA 052, an antibody to interleukin-1 beta, an orphan drug for the treatment of Behcet's disease. As previously announced, the Committee for Orphan Medical Products of the European Medicines Agency has recommended the granting of orphan medicinal product designation for XOMA 052 for the same indication in the European Union.
U.S. orphan drug designation is granted by the FDA Office of Orphan Drug Products Development to novel drugs or biologics that may treat a condition affecting fewer than 200,000 persons in the United States. The designation offers a number of potential incentives, which may include, among others, a seven-year period of U.S. marketing exclusivity from the date of marketing authorization, written guidance on the non-clinical and clinical studies needed to obtain marketing approval, and tax credits for certain clinical research.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London in July.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. Approximately 16,000 patients in the U.S. are estimated to suffer from Behcet's disease.
Antwort auf Beitrag Nr.: 39.929.004 von kleingeldjaeger am 04.08.10 18:13:30immer den Finger am Knopf...aber bisschen was will ich auch mithehmen...

Antwort auf Beitrag Nr.: 39.929.036 von Expertchen007 am 04.08.10 18:17:56danke alles klar was denkst wie viel drin ist 

Antwort auf Beitrag Nr.: 39.929.000 von dig101 am 04.08.10 18:12:53 ja die 215 K auf der 0,40 ....aber das ist noch zuweit weg,...bis dahin sieht das Bild anders aus
jetzt aber 0,37$

leck fett !!!! 0,37 und steigend...der Squezze beginnt....

Antwort auf Beitrag Nr.: 39.929.064 von Expertchen007 am 04.08.10 18:20:06bei 0,37 stehen jetzt über 300 k drin

Antwort auf Beitrag Nr.: 39.929.000 von dig101 am 04.08.10 18:12:53oh ha..jetzt ist die 0,40 aber raufgerutscht...nun seh ich auch die 0,43 im ASK leuchten
Antwort auf Beitrag Nr.: 39.929.091 von Expertchen007 am 04.08.10 18:22:51die 0,4 kommt immer näher 

na die wird doch nicht wirklich die 0,393 US$ als Break angreifen wollen...man könnte es meinen

Antwort auf Beitrag Nr.: 39.929.077 von Expertchen007 am 04.08.10 18:21:31wo biste denn aufgesprungen?`
Antwort auf Beitrag Nr.: 39.929.104 von Expertchen007 am 04.08.10 18:24:54nun legen die Shorts mit Covern los 

Antwort auf Beitrag Nr.: 39.929.110 von kleingeldjaeger am 04.08.10 18:25:20knapp bei 0,32 US$
bin raus nach einen Rücksetzer bin ich wieder dabei

XOMA's NASDAQ Last Sale
0.39 0.1129 ++++ 40.74% Volume
9,996,617
Previous Close
$ 0.2771
Today's High
$ 0.3900
Today's Low
$ 0.2852
52 Wk High
$ 1.07
52 Wk Low
$ .276
Fast wie in alten Zeiten bei Xoma mal wieder...aber immer schön aufpassen -was so passiert
0.39 0.1129 ++++ 40.74% Volume
9,996,617
Previous Close
$ 0.2771
Today's High
$ 0.3900
Today's Low
$ 0.2852
52 Wk High
$ 1.07
52 Wk Low
$ .276
Fast wie in alten Zeiten bei Xoma mal wieder...aber immer schön aufpassen -was so passiert
alle noch dabei? oder auch raus?
oder auch raus?
 oder auch raus?
oder auch raus?
wieder dabei

uppsala - kleines Luftholen muss auch mal sein
und raus, lieber 20% als nichts 

so die großen Orders sind erst mal durch...nun wirds etwas gemütlicher
Antwort auf Beitrag Nr.: 39.929.301 von Expertchen007 am 04.08.10 18:47:11dafür sind aber auch erst wieder eine grosse oder bei 0,4 drin 

Hallo,
warum dieser Anstieg heute ? Auf welcher Seite kann ich es nachlesen, oder vielleicht eine kurze Antwort zu dem Anstieg! Vielen Dank!!
warum dieser Anstieg heute ? Auf welcher Seite kann ich es nachlesen, oder vielleicht eine kurze Antwort zu dem Anstieg! Vielen Dank!!
chartechnik: der downtrend wurde vorerst gebrochen
aber mehr als ein zock sehe ich hier nicht
338 K im Bid auf der 0,37 US$...also Nachfrage ist genug da....nun wird halt gepokert..mal sehen ob ich meine VK bekomme
Antwort auf Beitrag Nr.: 39.929.336 von cocobert am 04.08.10 18:52:41blätter doch mal 3 Seiten zurück..kann so schwer nicht sein
Antwort auf Beitrag Nr.: 39.929.370 von Expertchen007 am 04.08.10 18:59:27will mal nicht so sein - bitte !!!
****************************************
XOMA 052 Designated Orphan Drug by FDA for Treatment of Behcet's Disease
BERKELEY, Calif., Aug 4, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the U.S. Food and Drug Administration has designated XOMA 052, an antibody to interleukin-1 beta, an orphan drug for the treatment of Behcet's disease. As previously announced, the Committee for Orphan Medical Products of the European Medicines Agency has recommended the granting of orphan medicinal product designation for XOMA 052 for the same indication in the European Union.
U.S. orphan drug designation is granted by the FDA Office of Orphan Drug Products Development to novel drugs or biologics that may treat a condition affecting fewer than 200,000 persons in the United States. The designation offers a number of potential incentives, which may include, among others, a seven-year period of U.S. marketing exclusivity from the date of marketing authorization, written guidance on the non-clinical and clinical studies needed to obtain marketing approval, and tax credits for certain clinical research.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London in July.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. Approximately 16,000 patients in the U.S. are estimated to suffer from Behcet's disease.
****************************************
XOMA 052 Designated Orphan Drug by FDA for Treatment of Behcet's Disease
BERKELEY, Calif., Aug 4, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the U.S. Food and Drug Administration has designated XOMA 052, an antibody to interleukin-1 beta, an orphan drug for the treatment of Behcet's disease. As previously announced, the Committee for Orphan Medical Products of the European Medicines Agency has recommended the granting of orphan medicinal product designation for XOMA 052 for the same indication in the European Union.
U.S. orphan drug designation is granted by the FDA Office of Orphan Drug Products Development to novel drugs or biologics that may treat a condition affecting fewer than 200,000 persons in the United States. The designation offers a number of potential incentives, which may include, among others, a seven-year period of U.S. marketing exclusivity from the date of marketing authorization, written guidance on the non-clinical and clinical studies needed to obtain marketing approval, and tax credits for certain clinical research.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London in July.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. Approximately 16,000 patients in the U.S. are estimated to suffer from Behcet's disease.
XOMA's NASDAQ Last Sale
0.3731 0.096 34.64% Volume
11,476,832
Previous Close
$ 0.2771
Today's High
$ 0.3950
Today's Low
$ 0.2852
0.3731 0.096 34.64% Volume
11,476,832
Previous Close
$ 0.2771
Today's High
$ 0.3950
Today's Low
$ 0.2852
Antwort auf Beitrag Nr.: 39.929.384 von Expertchen007 am 04.08.10 19:00:46Danke 007...
was denkt ihr wars das?

Zock beendet ???
Bin ich zu spät ??? !!!
!!!
Schade...
Bin ich zu spät ???
 !!!
!!!Schade...
die 0,40 US$ ist mal wieder weit weg jetzt..mal sehen was dann der Endspurt noch so bringt

Antwort auf Beitrag Nr.: 39.929.547 von Expertchen007 am 04.08.10 19:25:51Es ist jetzt fast 13:30 Uhr in New York, die Mittagspause ist dafür bekannt das der Kurs nachgibt um in den Endspurt nochmal kräftig zu steigen. Dann gibt´s wieder einige Deppen die die Order über Nacht aufgeben und das ist der weitere Anstieg morgen zu Handelsbeginn in Deutschland. Dieses Spielchen wiederholt tausendfach im Jahr:-)))
Noch nicht gelesen?
Wenn das so stimmt, ist der R/S Vergangenheit!
Focus Money hat gestern oder heute eine 200% Kaufempfehlung ausgegeben.
Darin ist zu sehen, dass ein Medikament, welches ursprünglich für Arthritis vorgesehen war, nun eine 44%ige Heilungsrate bei Schuppenflechte erreicht haben soll.
Das ist ja ein Hammer...Zwinkern
Das Produkt soll von Gegentech noch in diesem Jahr eingeführt werdenaufmerksam Quelle Sharewise:
04.08.2010
Xoma hat ein neues Heilmittel!
Dem spekulativ ausgerichteten Investor empfiehlt derzeit das Anlegermagazin "Focus Money" die Aktien von Xoma (ISIN BMG9825R1079 / WKN 871239) zum Kauf.
Unerwarteter Glücksfall bei US-Biotechnologie-Forscher Xoma: Dessen Wirkstoff Raptiva - gemeinsam mit dem Biotech-Riesen Genentech entwickelt - sei als Heilmittel gegen Arthritis gedacht gewesen. Jetzt habe sich herausgestellt: Auch beim Kampf gegen die chronische Hautkrankheit Psoriasis - Schuppenflechte - wirke Raptiva.
Anzeige
<a target="_blank" href="http://ad-emea.doubleclick.net/click%3Bh%3Dv8/39ec/7/6c/%2a/o%3B224342534%3B0-0%3B0%3B45970511%3B4307-300/250%3B36479184/36497092/1%3B%3B%7Esscs%3D%3fhttp://adfarm1.adition.com:80/redi*sid=10455/kid=101313/bid=291922/lid=202078151943/c=712/keyword=/clickurl=https://de.saxobank.com/de/schulungen_und_seminare/pages/saxowebtrader-demo.aspx?dfaid=1&cmpid=dfa_2315933;889999;45970511;"><img src="http://s0.2mdn.net/2315933/saxobank-300x250_de_off.jpg" width="300" height="250" border="0" alt="" galleryimg="no"></a> <A HREF="http://adfarm1.adition.com:80/redi*sid=10455/kid=101313/bid=291922/lid=202078151943/c=712/keyword=/clickurl=http%3A%2F%2Fad-emea.doubleclick.net%2Fjump%2FN5826.133402.4864091262621%2Fsz%3D300x250%3Bord%3D202078151943%3F"> <IMG SRC="http://ad-emea.doubleclick.net/ad/N5826.133402.4864091262621/B4277328.2;sz=300x250;ord=202078151943?" BORDER=0 WIDTH=300 HEIGHT=250 ALT="Click Here"></A> <a href="http://adfarm1.adition.com/click?sid=10455&ts=1280939242.90219" target="_blank"> <img src="http://adfarm1.adition.com/banner?sid=10455&ts=1280939242.90219" border="0"></a>
In Langzeittests hätten 44 Prozent aller leichten bis mittelschweren Fälle innerhalb von sechs Monaten deutliche Heilungszeichen gezeigt. Die Daten seien jetzt bei der amerikanischen Arzneimittel-Zulassungsbehörde FDA eingereicht worden.
Bis Jahresende solle nach Einschätzung von Genentech die Produktfreigabe erfolgen. Von diesen Aussichten profitiere vor allem der Kurs des wesentlich kleineren Nasdaq -Werts Xoma. Das Absatzpotenzial sei riesig. Fachleute würden schätzen, dass allein in den USA 4,5 Millionen Menschen an der Hautkrankheit leiden würden. Komme die Genehmigung, dürfte Xoma schneller als erwartet in die Gewinnzone kommen.
Vor diesem Hintergrund sieht das Anlegermagazin "Focus Money" bei Xoma eine 200-Prozent-Chance und rät zu einem spekulativen und limitierten Engagement in die Aktie.
Wenn das so stimmt, ist der R/S Vergangenheit!

Focus Money hat gestern oder heute eine 200% Kaufempfehlung ausgegeben.
Darin ist zu sehen, dass ein Medikament, welches ursprünglich für Arthritis vorgesehen war, nun eine 44%ige Heilungsrate bei Schuppenflechte erreicht haben soll.
Das ist ja ein Hammer...Zwinkern
Das Produkt soll von Gegentech noch in diesem Jahr eingeführt werdenaufmerksam Quelle Sharewise:
04.08.2010
Xoma hat ein neues Heilmittel!
Dem spekulativ ausgerichteten Investor empfiehlt derzeit das Anlegermagazin "Focus Money" die Aktien von Xoma (ISIN BMG9825R1079 / WKN 871239) zum Kauf.
Unerwarteter Glücksfall bei US-Biotechnologie-Forscher Xoma: Dessen Wirkstoff Raptiva - gemeinsam mit dem Biotech-Riesen Genentech entwickelt - sei als Heilmittel gegen Arthritis gedacht gewesen. Jetzt habe sich herausgestellt: Auch beim Kampf gegen die chronische Hautkrankheit Psoriasis - Schuppenflechte - wirke Raptiva.
Anzeige
<a target="_blank" href="http://ad-emea.doubleclick.net/click%3Bh%3Dv8/39ec/7/6c/%2a/o%3B224342534%3B0-0%3B0%3B45970511%3B4307-300/250%3B36479184/36497092/1%3B%3B%7Esscs%3D%3fhttp://adfarm1.adition.com:80/redi*sid=10455/kid=101313/bid=291922/lid=202078151943/c=712/keyword=/clickurl=https://de.saxobank.com/de/schulungen_und_seminare/pages/saxowebtrader-demo.aspx?dfaid=1&cmpid=dfa_2315933;889999;45970511;"><img src="http://s0.2mdn.net/2315933/saxobank-300x250_de_off.jpg" width="300" height="250" border="0" alt="" galleryimg="no"></a> <A HREF="http://adfarm1.adition.com:80/redi*sid=10455/kid=101313/bid=291922/lid=202078151943/c=712/keyword=/clickurl=http%3A%2F%2Fad-emea.doubleclick.net%2Fjump%2FN5826.133402.4864091262621%2Fsz%3D300x250%3Bord%3D202078151943%3F"> <IMG SRC="http://ad-emea.doubleclick.net/ad/N5826.133402.4864091262621/B4277328.2;sz=300x250;ord=202078151943?" BORDER=0 WIDTH=300 HEIGHT=250 ALT="Click Here"></A> <a href="http://adfarm1.adition.com/click?sid=10455&ts=1280939242.90219" target="_blank"> <img src="http://adfarm1.adition.com/banner?sid=10455&ts=1280939242.90219" border="0"></a>
In Langzeittests hätten 44 Prozent aller leichten bis mittelschweren Fälle innerhalb von sechs Monaten deutliche Heilungszeichen gezeigt. Die Daten seien jetzt bei der amerikanischen Arzneimittel-Zulassungsbehörde FDA eingereicht worden.
Bis Jahresende solle nach Einschätzung von Genentech die Produktfreigabe erfolgen. Von diesen Aussichten profitiere vor allem der Kurs des wesentlich kleineren Nasdaq -Werts Xoma. Das Absatzpotenzial sei riesig. Fachleute würden schätzen, dass allein in den USA 4,5 Millionen Menschen an der Hautkrankheit leiden würden. Komme die Genehmigung, dürfte Xoma schneller als erwartet in die Gewinnzone kommen.
Vor diesem Hintergrund sieht das Anlegermagazin "Focus Money" bei Xoma eine 200-Prozent-Chance und rät zu einem spekulativen und limitierten Engagement in die Aktie.
Antwort auf Beitrag Nr.: 39.929.542 von JimmySpoon am 04.08.10 19:25:11Zock beendet ???
Bin ich zu spät ???
Servus Meister Spoon,
na wer weiß...denke es geht nochmal was.....mein VK ist eh noch nicht erreicht ...wenn dann wars ein schöner Tageszock...nicht die Welt aber paar Hunis sind immer gut
Bin ich zu spät ???
Servus Meister Spoon,
na wer weiß...denke es geht nochmal was.....mein VK ist eh noch nicht erreicht ...wenn dann wars ein schöner Tageszock...nicht die Welt aber paar Hunis sind immer gut
Antwort auf Beitrag Nr.: 39.929.588 von derchecker am 04.08.10 19:30:56Könntest recht haben aber ich glaube das wir unter seichten Umsätzen
fallen werden !
Na ist ja noch ein bisschen Zeit...
fallen werden !
Na ist ja noch ein bisschen Zeit...
Antwort auf Beitrag Nr.: 39.929.588 von derchecker am 04.08.10 19:30:56stimmt schon - denke auch das die letzen 15 Minuten in USA dann zählen ..ist ja noch viel Luft drin bis zum normalen Level wieder mal
Antwort auf Beitrag Nr.: 39.929.589 von MrRipley am 04.08.10 19:31:01Das ist ein FAKE !!!!!! Artikel ist so wie mir bekannt aus 2003
anonsten bitte Link einfügen !!!!!!!!
anonsten bitte Link einfügen !!!!!!!!
Antwort auf Beitrag Nr.: 39.929.650 von Expertchen007 am 04.08.10 19:41:25Wo er recht hat hat er recht, ist aus 2003.
http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
LG Tommi" target="_blank" rel="nofollow ugc noopener">http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
LG Tommi
http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
LG Tommi" target="_blank" rel="nofollow ugc noopener">http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
LG Tommi
Antwort auf Beitrag Nr.: 39.929.650 von Expertchen007 am 04.08.10 19:41:25kam auf sharewise von einem Dritten.
Antwort auf Beitrag Nr.: 39.929.656 von Tommi33 am 04.08.10 19:43:18Da war irgendwas verkehrt, hier jetzt nochmal richtig: http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
Tommi
Tommi
junge..junge hier wird belogen und betrogen ...hier der Artikel im Original aus 2003 - fair geht vor
http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
http://www.focus.de/finanzen/boerse/aktien/kaufempfehlungen-…
JA JA, für solche Spielchen müsst Ihr schon früher aufstehen !!!
Nicht mit Expertchen !!!
!!!
Nicht mit Expertchen
 !!!
!!!
Antwort auf Beitrag Nr.: 39.929.662 von MrRipley am 04.08.10 19:43:35was lernen wir daraus ??????
immer aufpassen mit den bösen Buben
immer aufpassen mit den bösen Buben
Antwort auf Beitrag Nr.: 39.929.696 von JimmySpoon am 04.08.10 19:48:55so ist es !!!! 
ansonsten wars das est mal mit em Xoma Zock heute...war etwas zu gierig desshalb gibts jetzt auch keinen Gewinn....thats life...lass es aber mal im Depot..amn weiß bei dem Zeugs ja nie was so kommt

ansonsten wars das est mal mit em Xoma Zock heute...war etwas zu gierig desshalb gibts jetzt auch keinen Gewinn....thats life...lass es aber mal im Depot..amn weiß bei dem Zeugs ja nie was so kommt
Antwort auf Beitrag Nr.: 39.929.697 von Expertchen007 am 04.08.10 19:49:01Habe es korrigiert.
130€ weg. Der Typ ist gemeldet.
130€ weg. Der Typ ist gemeldet.
Zock vorbei !!!
Teil fällt ab !
Teil fällt ab !
Antwort auf Beitrag Nr.: 39.929.724 von MrRipley am 04.08.10 19:54:47ich habe nur 50€ verloren ( Ordergebühr für Amimarkt )





geil weit unter pari wird in Deutschland geschmissen. 



Antwort auf Beitrag Nr.: 39.929.724 von MrRipley am 04.08.10 19:54:47gut so....die schreiben bei Ariva sie hätten es von uns....

Wer hat mir welche zu 0,25 verkauft ???
Dachte, die Order sei für heute erledigt ???
Jetzt muss ich doch wieder zittern ! !
!
Dachte, die Order sei für heute erledigt ???
Jetzt muss ich doch wieder zittern !
 !
!
Antwort auf Beitrag Nr.: 39.929.780 von JimmySpoon am 04.08.10 20:03:38ach du auch, hatte zur Spass eine kurz vor 8 reingesetzt - klick aufs Depot und da waren sie 

XOMA's NASDAQ Last Sale
0.3375 0.0604 ++ 21.79%
Volume
15,541,534
Previous Close
$ 0.2771
Today's High
$ 0.3950
Today's Low
Volumen echt der Hit...Kurs soweit ja ganz o.k für einen Tag....glaub das können noch rund 17 Millionen werden heute...wobei die grossen Orders bereits durch sind ..nun haben die Shorts das Zepter erst mal in der Hand...bis zum nächsten Versuch des Ausbruchs
0.3375 0.0604 ++ 21.79%
Volume
15,541,534
Previous Close
$ 0.2771
Today's High
$ 0.3950
Today's Low
Volumen echt der Hit...Kurs soweit ja ganz o.k für einen Tag....glaub das können noch rund 17 Millionen werden heute...wobei die grossen Orders bereits durch sind ..nun haben die Shorts das Zepter erst mal in der Hand...bis zum nächsten Versuch des Ausbruchs
Antwort auf Beitrag Nr.: 39.929.768 von Expertchen007 am 04.08.10 20:02:20Wenn so etwas ist, muss man sofort klarstellen.
Ohne Grund-Quellenangabe ist sowieso nie kosher.
Geht dann wie ein Lauffeuer durch und...
Ohne Grund-Quellenangabe ist sowieso nie kosher.
Geht dann wie ein Lauffeuer durch und...
wer war das denn in Frankfurt...ich ??? nicht zu glauben...war wohl ein Zahlendreher
04.08.10 19:54:04 0.255 VA 3.900 994 272.264 73.536
19:49:49 0.258 VA 2.900 748 268.364 72.542
19:49:01 0.26 VA 4.000 1.040 265.464 71.794
19:40:58 0.265 VA 13.000 3.445 261.464 70.754
19:40:43 0.269 VA 2.500 672 248.464 67.309
19:35:35 0.298 VA 2.700 805 245.964 66.636
19:35:31 0.28 VA 15.000 4.200 243.264 65.832
19:32:20 0.27 VA 3.000 810 228.264 61.632
19:30:14 0.27 VA 600 162 225.264 60.822
19:14:18 0.28 VA 4.500 1.260 224.664 60.660
04.08.10 19:54:04 0.255 VA 3.900 994 272.264 73.536
19:49:49 0.258 VA 2.900 748 268.364 72.542
19:49:01 0.26 VA 4.000 1.040 265.464 71.794
19:40:58 0.265 VA 13.000 3.445 261.464 70.754
19:40:43 0.269 VA 2.500 672 248.464 67.309
19:35:35 0.298 VA 2.700 805 245.964 66.636
19:35:31 0.28 VA 15.000 4.200 243.264 65.832
19:32:20 0.27 VA 3.000 810 228.264 61.632
19:30:14 0.27 VA 600 162 225.264 60.822
19:14:18 0.28 VA 4.500 1.260 224.664 60.660
Antwort auf Beitrag Nr.: 39.929.793 von Expertchen007 am 04.08.10 20:05:12schöne käufe gerade wieder 

diese Nachricht wurde am 29.07.2010 schon veröffentlicht auf der Webseite der Firma.?
 wieso stand dann heute 4.08.2010?
wieso stand dann heute 4.08.2010?
XOMA 052 Orphan Drug Designation for Behcet's Disease Recommended by European Medicines Agency
BERKELEY, Calif., Jul 29, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the Committee for Orphan Medical Products of the European Medicines Agency (EMA) has adopted a positive opinion and recommends the granting of orphan medicinal product designation for XOMA 052, an antibody to interleukin-1 beta, for the treatment of Behcet's disease. Positive opinions are submitted to the European Commission for decision and are generally adopted within 30 days of receipt.
The EMA's orphan drug program is designed to promote the development of drugs to treat life-threatening or chronically debilitating conditions with a prevalence of up to five in 10,000 persons in the European Union (EU). The designation provides EU market exclusivity for up to ten years following approval for the given indication. Other potential benefits include protocol assistance, direct access to centralized marketing authorization procedures and financial incentives.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London earlier this month.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. More than 12,000 patients in the EU are estimated to suffer from Behcet's disease.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes and has completed a Phase 2 clinical trial in uveitis of Behcet's disease. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behcet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(TM), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
(C) Copyright 2010 GlobeNewswire, Inc. All rights reserved.
News Provided by COMTEX
« Back to Press Releases
XOMA Pipeline Chart
See the complete pipeline
Home Contact Us Site Map
© 2009 XOMA Legal

 wieso stand dann heute 4.08.2010?
wieso stand dann heute 4.08.2010?XOMA 052 Orphan Drug Designation for Behcet's Disease Recommended by European Medicines Agency
BERKELEY, Calif., Jul 29, 2010 (GlobeNewswire via COMTEX News Network) -- XOMA Ltd. (Nasdaq:XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the Committee for Orphan Medical Products of the European Medicines Agency (EMA) has adopted a positive opinion and recommends the granting of orphan medicinal product designation for XOMA 052, an antibody to interleukin-1 beta, for the treatment of Behcet's disease. Positive opinions are submitted to the European Commission for decision and are generally adopted within 30 days of receipt.
The EMA's orphan drug program is designed to promote the development of drugs to treat life-threatening or chronically debilitating conditions with a prevalence of up to five in 10,000 persons in the European Union (EU). The designation provides EU market exclusivity for up to ten years following approval for the given indication. Other potential benefits include protocol assistance, direct access to centralized marketing authorization procedures and financial incentives.
In June 2010, XOMA announced positive results from an open-label pilot study of XOMA 052 in Behcet's disease patients who were suffering from vision-threatening disease exacerbations, known as uveitis, despite maximal doses of immunosuppressive medicines. All seven patients who enrolled in the trial displayed rapid reduction of intraocular inflammation and improvement in visual acuity or other ophthalmic measures following a single treatment with XOMA 052. Five patients received a second infusion to blunt a developing exacerbation, and all responded to the second infusion. The drug appeared to be safe, and no drug-related adverse events were reported. Preliminary results were presented at the Annual Congress of the European League Against Rheumatism (EULAR) in Rome, Italy and at the International Congress on Behcet's Disease in London earlier this month.
About Behcet's Disease
Behcet's (pronounced beh-CHETS) disease is an orphan disease that causes chronic inflammation of the blood vessels, or vasculitis. Major symptoms can affect the neurological, pulmonary, gastrointestinal and cardiovascular systems, and hallmarks of the disease include uveitis, or inflammation of the intraocular tissues of the eye, and painful ulcers in the mouth and on the genitals. Behcet's disease most commonly affects men and women in their twenties, thirties and forties, and it is typically more severe in men. More than 12,000 patients in the EU are estimated to suffer from Behcet's disease.
About XOMA 052
XOMA 052 is a potent monoclonal antibody with the potential to improve the treatment of patients with a wide variety of inflammatory diseases. XOMA 052 binds strongly to interleukin-1 beta (IL-1 beta), a pro-inflammatory cytokine involved in diseases including Type 2 diabetes, cardiovascular disease, rheumatoid arthritis, gout and auto-inflammatory diseases. IL-1 is a well-validated therapeutic target, with three marketed IL-1 inhibitors that have been used by more than 200,000 patients overall. By binding to IL-1 beta, XOMA 052 inhibits the activation of the IL-1 receptor, thereby preventing the cellular signaling events that produce inflammation.
XOMA is conducting two Phase 2 clinical trials of XOMA 052 in patients with Type 2 diabetes and a Phase 2 trial in Type 1 diabetes and has completed a Phase 2 clinical trial in uveitis of Behcet's disease. The Phase 2 trials follow a successful 98 patient Phase 1 program in Type 2 diabetes patients in which XOMA 052 was shown to be well-tolerated, demonstrated evidence of biological activity in diabetes measures and cardiovascular biomarkers, and had a half-life that may provide convenient dosing of once per month or less frequently. The company has also demonstrated the potential for XOMA 052 in in vivo models of atherosclerosis and cardiac remodeling and in an in vitro model using human myeloma, or plasma cell cancer, cells.
About XOMA
XOMA discovers, develops and manufactures novel antibody therapeutics for its own proprietary pipeline as well as through license and collaborative agreements with pharmaceutical and biotechnology companies, and under its contracts with the U.S. government. The company's proprietary product pipeline includes:
-- XOMA 052, an anti-IL-1 beta antibody in Phase 2 clinical development for
Type 2 diabetes with cardiovascular biomarkers, Type 1 diabetes, and
with potential for the treatment of a wide range of inflammatory
conditions. XOMA 052 also has demonstrated positive clinical benefit in
a proof-of-concept trial for the treatment of vision-threatening uveitis
of Behcet's disease.
-- XOMA 3AB, an antibody candidate in pre-IND studies to neutralize the
botulinum toxin, among the most deadly potential bioterror threats,
under development through funding provided by the National Institute of
Allergy and Infectious Diseases of the National Institutes of Health
(Contract # HHSN266200600008C).
-- A preclinical pipeline with candidates in development for several
diseases.
In addition to its proprietary pipeline, XOMA develops products with premier pharmaceutical companies including Novartis AG, Schering Corporation, a subsidiary of Merck & Co., Inc. and Takeda Pharmaceutical Company Limited.
XOMA's technologies have contributed to the success of marketed antibody products, including LUCENTIS(R) (ranibizumab injection) for wet age-related macular degeneration and CIMZIA(R) (certolizumab pegol) for rheumatoid arthritis and Crohn's disease.
The company has a premier antibody discovery and development platform that incorporates an unmatched collection of antibody phage display libraries and proprietary Human Engineering(TM), affinity maturation, Bacterial Cell Expression (BCE) and manufacturing technologies. BCE is a key breakthrough biotechnology for the discovery and manufacturing of antibodies and other proteins. As a result, 60 pharmaceutical and biotechnology companies have signed BCE licenses, and several licensed product candidates are in clinical development.
XOMA has a fully integrated product development infrastructure, extending from pre-clinical science to approval, and a team of about 215 employees at its Berkeley, California location. For more information, please visit http://www.xoma.com.
Forward-Looking Statements
Certain statements contained herein concerning product development and capabilities of XOMA's technologies or that otherwise relate to future periods are forward-looking statements within the meaning of Section 27A of the Securities Act of 1933 and Section 21E of the Securities Exchange Act of 1934. These statements are based on assumptions that may not prove accurate. Actual results could differ materially from those anticipated due to certain risks inherent in the biotechnology industry and for companies engaged in the development of new products in a regulated market.
These risks, including those related to inability to comply with NASDAQ's continued listing requirements; the generally unstable nature of current economic conditions; the results of discovery research and pre-clinical testing; the timing or results of pending and future clinical trials (including the design and progress of clinical trials; safety and efficacy of the products being tested; action, inaction or delay by the FDA, European or other regulators or their advisory bodies; and analysis or interpretation by, or submission to, these entities or others of scientific data); changes in the status of existing collaborative and licensing relationships; the ability of collaborators, licensees and other third parties to meet their obligations; XOMA's ability to meet the demands of the United States government agency with which it has entered into its government contracts; competition; market demands for products; scale-up and marketing capabilities; availability of additional licensing or collaboration opportunities; international operations; share price volatility; XOMA's financing needs and opportunities; uncertainties regarding the status of biotechnology patents; uncertainties as to the costs of protecting intellectual property; and risks associated with XOMA's status as a Bermuda company, are described in more detail in XOMA's most recent filing on Form 10-K and in other SEC filings. Consider such risks carefully when considering XOMA's prospects.
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
(C) Copyright 2010 GlobeNewswire, Inc. All rights reserved.
News Provided by COMTEX
« Back to Press Releases
XOMA Pipeline Chart
See the complete pipeline
Home Contact Us Site Map
© 2009 XOMA Legal
Antwort auf Beitrag Nr.: 39.929.851 von dig101 am 04.08.10 20:13:12das sind ja Hammerbalken drin....da geht richtig was heute...irre.....400 / 600 K am Stück....na wenn da nix am Kurs nach oben geht weiß ich auch nicht
die kaufen wie die verrückten..das sind keine Kleinanleger...bereits jetzt 17 Millionen !!!!!! gehandelt

die kaufen wie die verrückten..das sind keine Kleinanleger...bereits jetzt 17 Millionen !!!!!! gehandelt
Antwort auf Beitrag Nr.: 39.929.889 von avalus am 04.08.10 20:17:30sind 2 versch. Meldungen...komplett
NEWS kam heute hier
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
NEWS kam heute hier
The XOMA Ltd. logo is available at http://www.globenewswire.com/newsroom/prs/?pkgid=5960
This news release was distributed by GlobeNewswire, www.globenewswire.com
SOURCE: XOMA Ltd.
CONTACT: XOMA Ltd.
Company and Investor Contact:
Carol DeGuzman
510-204-7270
deguzman@xoma.com
Canale Communications
Media Contact:
Carolyn Hawley
619-849-5375
carolyn@canalecomm.com
Antwort auf Beitrag Nr.: 39.929.892 von Expertchen007 am 04.08.10 20:18:03wir werden es sehen wo wir heute abend stehen bis 0,4 liegt nicht mehr viel 

Antwort auf Beitrag Nr.: 39.929.909 von Expertchen007 am 04.08.10 20:20:18Direktlink zur News
http://investors.xoma.com/releasedetail.cfm?ReleaseID=496294
http://investors.xoma.com/releasedetail.cfm?ReleaseID=496294
Antwort auf Beitrag Nr.: 39.929.917 von dig101 am 04.08.10 20:21:37also 0,40 US$ siehste heute nicht mehr...beim besten Willen nicht...selbst ein Plus von 20 oder auch 25 % wäre bereits Top im SK ....der Rest bleibt abzuwarten...17 -18 Millonen Stücke werden nicht einfach so mal umgesetzt....wr erfahren bloss nicht alles
Antwort auf Beitrag Nr.: 39.929.946 von Expertchen007 am 04.08.10 20:26:52Könntest Du aus deiner Erfahrung heraus bestätigen, dass man bei grünen Balken vornehmlich von Shorteindeckungen sprechen könnte?
Mir ist nämlich aufgefallen, dass meist nach einer Bodenbildung diese grünen Balken Überhand nehmen.
Offiziell gilt Grün ja als Kauf aus dem Ask.
Mir ist nämlich aufgefallen, dass meist nach einer Bodenbildung diese grünen Balken Überhand nehmen.
Offiziell gilt Grün ja als Kauf aus dem Ask.
Antwort auf Beitrag Nr.: 39.929.909 von Expertchen007 am 04.08.10 20:20:18danke für die Aufklärung
Antwort auf Beitrag Nr.: 39.929.962 von MrRipley am 04.08.10 20:29:33nein kann man nicht...das ist so ein Gerücht
der grüne Balken bedeutet nur das BID / und ASK auf gleichem Kurs waren als der Kauf oder Verkauf gelaufen ist...also neutral zu sehen - mehr nicht
der grüne Balken bedeutet nur das BID / und ASK auf gleichem Kurs waren als der Kauf oder Verkauf gelaufen ist...also neutral zu sehen - mehr nicht
Antwort auf Beitrag Nr.: 39.930.021 von Expertchen007 am 04.08.10 20:36:59Kein Gerücht, war meine Annahme.

Antwort auf Beitrag Nr.: 39.930.045 von MrRipley am 04.08.10 20:39:04ja sorry..das mit dem Gerücht war allgemein zu verstehen..
Antwort auf Beitrag Nr.: 39.930.051 von Expertchen007 am 04.08.10 20:40:28ist klar

Antwort auf Beitrag Nr.: 39.930.051 von Expertchen007 am 04.08.10 20:40:28bist jetzt hier unglaublich
!
Dieser Beitrag wurde moderiert.
Antwort auf Beitrag Nr.: 39.930.231 von Broker_Hans am 04.08.10 21:12:14alle Spinner sind hier ganz genau hast nurnoch du gefehlt

gut daß ich den Rotz vorhin noch zu 0,3399$ rausgehauen habe hab vorhin zu 0,34-0,345$ einige gesammelt aber wurde mir zuheiß glück gehabt lange wäre nichtmer Zeit gewesen
lange wäre nichtmer Zeit gewesen
 lange wäre nichtmer Zeit gewesen
lange wäre nichtmer Zeit gewesen
BOSTON (Dow Jones) - Die Aktien von Xoma Ltd / quotes/comstock/15 *! Xoma / quotes / nls / Xoma (XOMA 0,33, 0,05, 19,09%) schoss Mittag Mittwoch auf Nachrichten, dass die US Food and Drug Administration hat gewährt seinen Medikamentenkandidaten XOMA 052 Orphan Drug Status für die Behandlung der extrem seltenen Krankheit Morbus Behcet. Die Bezeichnung bedeutet, dass wenn die Bedingung genehmigt, würde das Medikament bestimmten Markt Exklusivobjekte und Xoma genießen könnten Steuergutschriften für die weitere Forschung berechtigt. Der Orphan Drug Status soll die Entwicklung von Medikamenten für die Behandlung von Krankheiten, die weniger als 200.000 Amerikaner plagen fördern. Aktien von Xoma stiegen um fast 30% auf 35 Cents je Aktie.
Antwort auf Beitrag Nr.: 39.930.231 von Broker_Hans am 04.08.10 21:12:14Huhu Hänslein

Antwort auf Beitrag Nr.: 39.930.286 von printguru am 04.08.10 21:22:30jezt sieht man was ihr für schräge Vögel seit.
!
Dieser Beitrag wurde moderiert.
über 40.000.000St. umgesetzt da wurde heute kräftig abgeladen
aber trotzdem ein netter Tradinggewinn ist übrig geblieben aber halt nur ein kleiner

aber trotzdem ein netter Tradinggewinn ist übrig geblieben aber halt nur ein kleiner

Antwort auf Beitrag Nr.: 39.930.412 von Broker_Hans am 04.08.10 21:41:45ich habe natürlich nicht das Glück so ein feiner Kerl wiedu zusein.
Solche Beleidigungen auszusprechen zeugt von Stärke
Solche Beleidigungen auszusprechen zeugt von Stärke

Antwort auf Beitrag Nr.: 39.930.493 von printguru am 04.08.10 21:53:13gut daß ich den Rotz vorhin noch zu 0,3399$ rausgehauen habe hab vorhin zu 0,34-0,345$ einige gesammelt aber wurde mir zuheiß glück gehabtaugen verdrehen lange wäre nichtmer Zeit gewesenaugen verdrehen
Gewinn????
Gewinn????
!
Dieser Beitrag wurde moderiert.
Antwort auf Beitrag Nr.: 39.930.506 von TTDEVIL am 04.08.10 21:54:57bin heute zu 0,32$ rein und bei knapp 0,35 raus wieder rein zu 0,35 und bei knapp 0,39 raus wieder rein zu knapp 0,37 wieder raus zu gut 0,36 und dann eben wieder gasammelt bei 0,34-0,345 den großteil bei 0,34$
desswegen noch ein kleiner Gewinn übriggeblieben
Rotz desswegen weil ich mir mehr erhofft hatte und alle Mühe hatte die Teile zu 0,3399$ wieder loszuwerden hat alles einwenig genervt heute...
hat alles einwenig genervt heute...
gute Nacht
desswegen noch ein kleiner Gewinn übriggeblieben

Rotz desswegen weil ich mir mehr erhofft hatte und alle Mühe hatte die Teile zu 0,3399$ wieder loszuwerden
 hat alles einwenig genervt heute...
hat alles einwenig genervt heute...gute Nacht
!
Dieser Beitrag wurde moderiert. Grund: Korrespondierendes Posting wurde entfernt
hab mir einen kleine shortposition heute zugelegt. 

Antwort auf Beitrag Nr.: 39.930.321 von Broker_Hans am 04.08.10 21:27:42Wenn Du weiter so stänkerst, kannst Du dir morgen einen neuen Nick suchen!

Hallo !!!! über 19 % plus..na ist das etwa nix und ein Hammervolumen dazu 
XOMA's NASDAQ Last Sale
0.33 0.0529 ++++19.09%
Volume
19,906,942 Previous Close
$ 0.2771
Today's High
$ 0.3950 Today's Low

XOMA's NASDAQ Last Sale
0.33 0.0529 ++++19.09%
Volume
19,906,942 Previous Close
$ 0.2771
Today's High
$ 0.3950 Today's Low
Antwort auf Beitrag Nr.: 39.930.668 von Expertchen007 am 04.08.10 22:16:42habe die ganze Zeit Bid und Ask Kurse beobachtet da wurde angezockt und abgeladen

Ne Abladen geht anders! Morgen gehts weiter up:-)
Antwort auf Beitrag Nr.: 39.930.989 von Moneymex am 04.08.10 23:09:50Netter Anfang,mehr nicht.
Na ja nachbörslich mit über 200K auf o,24 zurück !!!
Schaun wir mal was kommt,
denke der Anfang ist gemacht !!!
Ob es hier annähernd wie bei Keryx laufen kann möchte ich mal
bezweifeln !
Aber wer weiß, wenn das Vertrauen erst einmal zurück ist, e ntwickeln sich manche Dinge
wie von selbst !
!
Schaun wir mal was kommt,
denke der Anfang ist gemacht !!!
Ob es hier annähernd wie bei Keryx laufen kann möchte ich mal
bezweifeln !
Aber wer weiß, wenn das Vertrauen erst einmal zurück ist, e ntwickeln sich manche Dinge
wie von selbst
 !
!
Naja Xoma mit Keryx zu vergleichen, halte ich für eher unglücklich. Dennoch könnten hier kurzfristig bis zu 200% drinne sein.
Antwort auf Beitrag Nr.: 39.930.493 von printguru am 04.08.10 21:53:13über 40.000.000St. umgesetzt da wurde heute kräftig abgeladen
Guten morgen zusammen,
also so stimmt das schon mal gar nicht...Es waren insgesamt 42,169 Millionen Stücke ....hiervon waren 38,9 % Käufe und 20,6 % Verkäufe..somit fast doppelt soviele Käufer als Verkäufer...die Differenz waren Shortpositionen
Quelle: ADVNF
Guten morgen zusammen,
also so stimmt das schon mal gar nicht...Es waren insgesamt 42,169 Millionen Stücke ....hiervon waren 38,9 % Käufe und 20,6 % Verkäufe..somit fast doppelt soviele Käufer als Verkäufer...die Differenz waren Shortpositionen
Quelle: ADVNF
Antwort auf Beitrag Nr.: 39.931.161 von Bioperle am 04.08.10 23:49:07Netter Anfang,mehr nicht.
So seh ich das auch mal.....entweder da kommt richtig was oder es bleibt im Bereich 0,28 -0,32
So seh ich das auch mal.....entweder da kommt richtig was oder es bleibt im Bereich 0,28 -0,32
Antwort auf Beitrag Nr.: 39.931.749 von JimmySpoon am 05.08.10 08:34:24
Na ja nachbörslich mit über 200K auf o,24 zurück !!!
Meister Spoon,
da ist wohl ein Fehler drin....
After Hours Last:
Net / % Change
$ .34
.02 (6.25%)
somit muss es heißen ...wieder auf 34 rauf !!!!!
Na ja nachbörslich mit über 200K auf o,24 zurück !!!
Meister Spoon,
da ist wohl ein Fehler drin....

After Hours Last:
Net / % Change
$ .34
.02 (6.25%)
somit muss es heißen ...wieder auf 34 rauf !!!!!
Antwort auf Beitrag Nr.: 39.932.331 von Expertchen007 am 05.08.10 09:57:01und der rest??
Antwort auf Beitrag Nr.: 39.932.426 von Expertchen007 am 05.08.10 10:08:03Oh ja, hast recht !!!
Übrigens lt. Ariva Board Insiderkäufe zu 0,349 !!!
Bin mal gespannt ob da die Tage nicht noch mehr geht !!!
!!!
Übrigens lt. Ariva Board Insiderkäufe zu 0,349 !!!
Bin mal gespannt ob da die Tage nicht noch mehr geht
 !!!
!!!
Antwort auf Beitrag Nr.: 39.932.430 von stepo am 05.08.10 10:08:24der Rest sind Shortpositionen..aber dazu kann man nix sehen ob EK oder VK...aber vom Umsatz her sind es wohl viel cover gewesen
**************************************************
man sollte mal den Namen REGENERON im Auge behalten.-...es gibt da Gerüchte ( USA Board ), daß die an XOMA dran sein sollen...alles ohne Gewähr.....aber mal ein Auge drauf werfen
http://www.regeneron.com/
**************************************************
man sollte mal den Namen REGENERON im Auge behalten.-...es gibt da Gerüchte ( USA Board ), daß die an XOMA dran sein sollen...alles ohne Gewähr.....aber mal ein Auge drauf werfen
http://www.regeneron.com/
Antwort auf Beitrag Nr.: 39.932.573 von JimmySpoon am 05.08.10 10:23:28stimmt schon mit den Insiderkäufen...die Liste hab ich auch irgendwo gesehen...aber frag mich nicht mehr wo das war
Aus dem Amiboard:


Nur zur Info! 
Vanguard Group, Inc. hat seine 8.33 M Aktien verkauft!
http://www.dailyfinance.com/company/xoma-ltd/xoma/nas/instit…

Vanguard Group, Inc. hat seine 8.33 M Aktien verkauft!
http://www.dailyfinance.com/company/xoma-ltd/xoma/nas/instit…
Antwort auf Beitrag Nr.: 39.934.110 von Lucky72 am 05.08.10 13:15:04Ups, mein Fehler! Sie haben nur 5M. verkauft!
Bin jetzt auch nur noch Zuschauer (+/- 0 raus) !!!
Schade, aber mein Bauch sagt mir, dass xoma heute wieder da stehen wird wo
wir hergekommen sind (gestern in der letzten Std. einfach kein Kaufdruck) !!!
Viel Glück bis später...
Schade, aber mein Bauch sagt mir, dass xoma heute wieder da stehen wird wo
wir hergekommen sind (gestern in der letzten Std. einfach kein Kaufdruck) !!!
Viel Glück bis später...

von 0,30 bis 0,40 heute alles drin...oberes Gap ist auch noch offen....nach unten ist wohl bei 0,30 abgesichert..aber wird man sehen...auf jeden Fall geht im Pre schon bisschen was......alles andere wird sich zeigen ...mal sehen welches Volumen erreicht wird..ich schätze mal nicht mehr als 10 Mio. um 22 Uhr
Und da ist es wieder das Xoma Phänomen - Tendenz fallend unter recht hohem Volumen für diese Uhrzeit. Natürlich nicht mit gestern vergleichbar.
Hat bitte jemand für mich ein Realtime c von xoma von advn
will hier kaufen
danke
will hier kaufen
danke

Antwort auf Beitrag Nr.: 39.935.525 von VodkaLemon am 05.08.10 15:43:22Super danke jetzt kann ich paar stück einsammeln
sollte doch eher hoch als runter gehen heuer

sollte doch eher hoch als runter gehen heuer

Antwort auf Beitrag Nr.: 39.935.505 von Silversamy am 05.08.10 15:41:49Hast doch gar keine Kohle mehr....alles weg bei Asiapac und London...oder ???? 

Antwort auf Beitrag Nr.: 39.935.738 von Expertchen007 am 05.08.10 16:04:41Hallo Kollege 
Du weist doch die erste regel lautet nie mehr als 10 % vom Kapital in junk aktien
also habe ich noch genug zum nachfeuern oder streuen

Du weist doch die erste regel lautet nie mehr als 10 % vom Kapital in junk aktien
also habe ich noch genug zum nachfeuern oder streuen

immerhin bereits wieder 7,8 Mio gehandelt mit 2/3 Käufe
XOMA: Top On The Green Board!
(NASDAQ: XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the FDA has designated XOMA 052 an orphan drug for the treatment of Behcet’s disease http://stockbouncer.com/XOMA
(NASDAQ: XOMA), a leader in the discovery and development of therapeutic antibodies, announced that the FDA has designated XOMA 052 an orphan drug for the treatment of Behcet’s disease http://stockbouncer.com/XOMA
Antwort auf Beitrag Nr.: 39.935.567 von Silversamy am 05.08.10 15:46:53Das ist Xoma - immer abwärts. Mal gespannt ob die 0,3$ hält.
Antwort auf Beitrag Nr.: 39.936.085 von Expertchen007 am 05.08.10 16:45:06und wer hat das andere 1/3???

wow..von gestern + 40 auf minus 10-12 %....nicht schlecht...aber erst mal abwarten was die Zahlen bringen - thats XOMA
Antwort auf Beitrag Nr.: 39.936.414 von MogD am 05.08.10 17:24:12cool hab glatt meine St. zu 0,2911$ und 0,2912$ bekommen und gerade für 0,2998$ und 0,3$ verscherbelt ob ich hätte warten sollen? XOMA ist mir aber nicht geheuer sicher ist sicher.
sicher ist sicher.
 sicher ist sicher.
sicher ist sicher.
Antwort auf Beitrag Nr.: 39.936.730 von Expertchen007 am 05.08.10 18:03:36ja XOMA ist echt ein Fall für sich

Antwort auf Beitrag Nr.: 39.936.752 von printguru am 05.08.10 18:06:41Wow noch nicht mal einen Cent. Du hast einen kräftigen an der Klatsche. 



Antwort auf Beitrag Nr.: 39.936.972 von ericcartman am 05.08.10 18:36:11Danke bei 200.000St. wirft das auch was ab...wer da einen an der Klatsche hat?
wenn 1750$ für dich nichts ist dann ist es auch o.k.-Spesen 1645$
ein feines Taschengeld nebenbei

wenn 1750$ für dich nichts ist dann ist es auch o.k.-Spesen 1645$
ein feines Taschengeld nebenbei

Antwort auf Beitrag Nr.: 39.937.028 von printguru am 05.08.10 18:45:22Never 


sind keine 200.000 im Amiland geflogen. Lügenbaron



sind keine 200.000 im Amiland geflogen. Lügenbaron
Antwort auf Beitrag Nr.: 39.937.066 von ericcartman am 05.08.10 18:49:32um genau 17:47:32 hat der Lügenbaron seine St. bekommen

waren 2 verschiedene Orders zu 0,2911 und 0,2912
und wenn dus nicht glaubst dann eben nicht mir doch egal wäre wohl ziemlich krank es zu posten wenn es nicht stimmt.....ja ich weiß ich bin krank bla bla bla

und wenn dus nicht glaubst dann eben nicht mir doch egal wäre wohl ziemlich krank es zu posten wenn es nicht stimmt.....ja ich weiß ich bin krank bla bla bla

.30 leider nicht gehalten , hoffentlich hält wenigstens die .29  ... typisch kaum steig ich irgndwo ein und schon gehts abwärts
... typisch kaum steig ich irgndwo ein und schon gehts abwärts 
 ... typisch kaum steig ich irgndwo ein und schon gehts abwärts
... typisch kaum steig ich irgndwo ein und schon gehts abwärts 
Antwort auf Beitrag Nr.: 39.937.894 von VodkaLemon am 05.08.10 21:02:26das wars dann auch mit der .29 

Antwort auf Beitrag Nr.: 39.937.894 von VodkaLemon am 05.08.10 21:02:26abwarten, da wird manipuliert ohne Ende. Über 4 Mios mehr Käufe
Antwort auf Beitrag Nr.: 39.936.414 von MogD am 05.08.10 17:24:12ja was solls sind ja nur 10 % einsatz und davon erst ca 10 % verlust 
und morgen kann es auch mal up gehen

und morgen kann es auch mal up gehen

Rating-Update:
Los Angeles (aktiencheck.de AG) - Die Analysten von Wedbush Morgan Securities, Liana Moussatos und Richard Lau, stufen die Aktie von XOMA (ISIN BMG9825R1079/ WKN 871239) weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u)
Los Angeles (aktiencheck.de AG) - Die Analysten von Wedbush Morgan Securities, Liana Moussatos und Richard Lau, stufen die Aktie von XOMA (ISIN BMG9825R1079/ WKN 871239) weiterhin mit dem Rating "outperform" ein. Das Kursziel werde nach wie vor bei 2 USD gesehen. (02.08.2010/ac/a/u)
The proposal to authorize the Board of Directors to effect a share consolidation, or reverse stock split, of the Company’s common shares at any time on or before July 21, 2011 at a ratio within a range of 1 for 2 to 1 for 15 as determined by the Board of Directors in its sole discretion, and if and when the reverse stock split is effected, reduce the number of the Company’s authorized common shares by the reverse split ratio determined by the Board of Directors to apply equally to the Company’s authorized common shares and increase the par value of each common share accordingly, was approved, the Company’s independent inspector of elections having reported the following final voting results: 128,119,846 votes for, 59,139,640 votes against, 3,284,287 abstentions and zero broker non-votes.
The proposal to approve the increase of the Company’s authorized share capital by the creation of an additional 300,000,000 common shares, par value $.0005 per share, was approved, the Company’s independent inspector of elections having reported the following final voting results: 112,658,332 votes for, 74,565,498 votes against, 3,319,943 abstentions and zero broker non-votes.
The proposal to approve the increase of the Company’s authorized share capital by the creation of an additional 300,000,000 common shares, par value $.0005 per share, was approved, the Company’s independent inspector of elections having reported the following final voting results: 112,658,332 votes for, 74,565,498 votes against, 3,319,943 abstentions and zero broker non-votes.
Antwort auf Beitrag Nr.: 39.939.006 von Kursziel1000 am 06.08.10 01:43:58ein bißchen zu optimistisch 
Vielleicht klappt das mit nem reverse split

Vielleicht klappt das mit nem reverse split

Na hätte gestern gedacht, dass es besser läuft. Na heute bestimmt. Nur Bauchgefühl

Antwort auf Beitrag Nr.: 39.939.174 von Moneymex am 06.08.10 07:48:58Irgendwie bin ich der selben Meinung.
Gestern wurden sehr große Pakete eingesammelt, die Frage ist warum die Investoren jetzt zulangen und nicht ersteinmal den reverse split abwarten?
Gestern wurden sehr große Pakete eingesammelt, die Frage ist warum die Investoren jetzt zulangen und nicht ersteinmal den reverse split abwarten?
Antwort auf Beitrag Nr.: 39.941.670 von Kursziel1000 am 06.08.10 14:00:02Wann genau kommt der R/S ? Ist sicher,dass er überhaupt kommt ?
MFG
Zuki
MFG
Zuki

Antwort auf Beitrag Nr.: 39.941.716 von Zukertort am 06.08.10 14:06:20Anhand dieser Nachricht vom 15.Juni ist der Termin spätestens der 13.Sept.
Sollte der PPS bis dahin nicht wieder über 1 USD notieren.
Wären nach heutigem PPS ca. 350 % Plus zu machen, was wohl eher unwahrscheinlich sein sollte.
http://sanfrancisco.bizjournals.com/sanfrancisco/stories/201…

Sollte der PPS bis dahin nicht wieder über 1 USD notieren.
Wären nach heutigem PPS ca. 350 % Plus zu machen, was wohl eher unwahrscheinlich sein sollte.
http://sanfrancisco.bizjournals.com/sanfrancisco/stories/201…

Antwort auf Beitrag Nr.: 39.941.815 von zwitscherton am 06.08.10 14:20:33Sorry, natürlich nur + 250 %.


Antwort auf Beitrag Nr.: 39.941.815 von zwitscherton am 06.08.10 14:20:33Danke Zwitscherton  !
!
Also gab es eine Delisting notification schon letztes Jahr ? Warscheinlich ! Ich bin eigentlich positiv gestimmt für XOMA,werde aber mit einem Wiedereinstieg wohl doch bis nach dem R/S warten,wegen der bösen Überraschungen,siehe Genta ....
MFG
Zuki
 !
!Also gab es eine Delisting notification schon letztes Jahr ? Warscheinlich ! Ich bin eigentlich positiv gestimmt für XOMA,werde aber mit einem Wiedereinstieg wohl doch bis nach dem R/S warten,wegen der bösen Überraschungen,siehe Genta ....
MFG
Zuki

Antwort auf Beitrag Nr.: 39.941.815 von zwitscherton am 06.08.10 14:20:33Moment  !
!
Der letztmögliche Termin für den R/S ist somit der 27.08.2010,da XOMA ja mindestens 10 Börsentage über 1$ notieren muss ...
MFG
Zuki
 !
!Der letztmögliche Termin für den R/S ist somit der 27.08.2010,da XOMA ja mindestens 10 Börsentage über 1$ notieren muss ...
MFG
Zuki

Antwort auf Beitrag Nr.: 39.942.127 von Zukertort am 06.08.10 14:52:05anyway ...
Damit hast Du wahrscheinlich recht. Somit 14 Tage weniger.
BTW. Mit XOMA haben sich schon viele (incl. myself) die Finger verbrannt.
Wenn Du hier einsteigen willst - it's a high risk investment.

Damit hast Du wahrscheinlich recht. Somit 14 Tage weniger.
BTW. Mit XOMA haben sich schon viele (incl. myself) die Finger verbrannt.
Wenn Du hier einsteigen willst - it's a high risk investment.

Antwort auf Beitrag Nr.: 39.943.117 von zwitscherton am 06.08.10 16:38:28Das macht mir nichts aus,zwitscherton  !
!
Ich werde einsteigen,aber erst mal abwarten,man muss
doch auch damit rechnen,das unmittelbar nach dem R/S eine KE
kommen wird,richtig ? XOMA hat nicht gerade üppige finanzielle
Mittel mehr ....
MFG
Zuki
 !
!Ich werde einsteigen,aber erst mal abwarten,man muss
doch auch damit rechnen,das unmittelbar nach dem R/S eine KE
kommen wird,richtig ? XOMA hat nicht gerade üppige finanzielle
Mittel mehr ....
MFG
Zuki

Antwort auf Beitrag Nr.: 39.943.174 von Zukertort am 06.08.10 16:46:42Sie habe doch erst kürzlich ein CEFF-Deal mit Azimuth abgeschlossen.
Im Amiboard wird spekuliert, das der Ausverkauf der letzten Tage u.a. durch Azimuth ausgelöst wurde, weil die ihre Stücke versilberten.
Aber nix genaues weis man nicht - es gibt keine Meldungen dazu. Somit reine Spekulation.
Aber Fakt ist, wenn sie die Phase2(3?) für 052 allein durchziehen wollen/müssen brauchen sie ja irgendwann sicher wieder neue Kohle.
Ist ja auch schon genehmigt.

Im Amiboard wird spekuliert, das der Ausverkauf der letzten Tage u.a. durch Azimuth ausgelöst wurde, weil die ihre Stücke versilberten.
Aber nix genaues weis man nicht - es gibt keine Meldungen dazu. Somit reine Spekulation.
Aber Fakt ist, wenn sie die Phase2(3?) für 052 allein durchziehen wollen/müssen brauchen sie ja irgendwann sicher wieder neue Kohle.
Ist ja auch schon genehmigt.

Antwort auf Beitrag Nr.: 39.943.265 von zwitscherton am 06.08.10 16:57:55XOMA-052 hat jedenfalls das Zeug zu einem
Mega-blockbuster mit mehreren Indikationen!
Sagen wir mal,es könnte so kommen: 10:1 Resplitt,
dann steht der kurs bei 2,80$ und es werden 10 Mio
neue aktien ausgegeben,das dürfte erst mal reichen ...
MFg
Zuki
Mega-blockbuster mit mehreren Indikationen!
Sagen wir mal,es könnte so kommen: 10:1 Resplitt,
dann steht der kurs bei 2,80$ und es werden 10 Mio
neue aktien ausgegeben,das dürfte erst mal reichen ...
MFg
Zuki

irrer verkauf..die 40% plus wurden komplett wieder abverkauft. passt aber irgendwie zu xoma. wenn man sich vor augen hält wie lange es noch dauert bis eine zulassung überhaupt in "die nahe zukunft" rückt ists auch nicht verwunderlich. das wird noch die eine oder andere finanzierungsrunde geben müssen, bei der die shareholder wieder enorm federn lassen werden.
Antwort auf Beitrag Nr.: 39.943.364 von Zukertort am 06.08.10 17:11:58Im PROSPECTUS vom 23.Juli ist von bis zu 150 Mio. USD die Rede.


Antwort auf Beitrag Nr.: 39.943.633 von zwitscherton am 06.08.10 17:47:17Hä ?  ?
?
Wie meinst du das jetzt mit 150 Mio.-$,
also du meinst ein KE,die XOMA bis zu
150 Mio.$ in die Kasse spült,richtig ?
Das wären ,bei einem Kurs von 2,80$ (nach R/S)
immerhin 50 mio. shares,die es zu diluten gibt ...
Au weia !
!
MFG
Zuki
 ?
?Wie meinst du das jetzt mit 150 Mio.-$,
also du meinst ein KE,die XOMA bis zu
150 Mio.$ in die Kasse spült,richtig ?
Das wären ,bei einem Kurs von 2,80$ (nach R/S)
immerhin 50 mio. shares,die es zu diluten gibt ...
Au weia
 !
!MFG
Zuki

Antwort auf Beitrag Nr.: 39.943.668 von Zukertort am 06.08.10 17:50:45Über die Zeit (watever that means).
Und der Gesamtbetrag kann aber muß nicht ausgeübt werden.
Jedenfalls so weit ich das verstanden hab. Hab das ganze Teil natürlich nicht durchgelesen.

Und der Gesamtbetrag kann aber muß nicht ausgeübt werden.
Jedenfalls so weit ich das verstanden hab. Hab das ganze Teil natürlich nicht durchgelesen.

Antwort auf Beitrag Nr.: 39.943.706 von zwitscherton am 06.08.10 17:56:47Hier nochmal der Link
http://investors.xoma.com/secfiling.cfm?filingid=950162-10-2…

http://investors.xoma.com/secfiling.cfm?filingid=950162-10-2…

Antwort auf Beitrag Nr.: 39.943.668 von Zukertort am 06.08.10 17:50:45... und es werden 10 Mio
neue aktien ausgegeben,das dürfte erst mal reichen ...
man merkt, dass du dich noch nicht sehr intensiv mit xoma auseinandergesetzt
hast...sie spielen ihr xoma 052 als "die" wunderwaffe, aber ich sehe sehe
seit jahren nur brutalste dilution, nischenindikationen und ein würgen
um das delisting von der nasdaq zu verhindern...
die schmeissen auch noch 200 mio. aktien auf den markt wenns sein muss...
ein blick auf den chart der letzten jahre kann man getrost vergessen...
vor jahren waren es auch noch eine gefühlte halbe milliarde aktien weniger
bei 15 cent werd ich mir mal 50k stücke gönnen für einen zock...vorher
werde ich warten...
neue aktien ausgegeben,das dürfte erst mal reichen ...
man merkt, dass du dich noch nicht sehr intensiv mit xoma auseinandergesetzt
hast...sie spielen ihr xoma 052 als "die" wunderwaffe, aber ich sehe sehe
seit jahren nur brutalste dilution, nischenindikationen und ein würgen
um das delisting von der nasdaq zu verhindern...
die schmeissen auch noch 200 mio. aktien auf den markt wenns sein muss...
ein blick auf den chart der letzten jahre kann man getrost vergessen...
vor jahren waren es auch noch eine gefühlte halbe milliarde aktien weniger

bei 15 cent werd ich mir mal 50k stücke gönnen für einen zock...vorher
werde ich warten...
Antwort auf Beitrag Nr.: 39.943.738 von Gustl24 am 06.08.10 18:00:35hi Gusti !
Scheinst XOMA ja schon länger zu kennen,
ich dagegen bin relativ neu,jedenfalls
haben wir heute schon die 0,26$ gesehen,
unglaublich !
!
MFG
Zuki
Scheinst XOMA ja schon länger zu kennen,
ich dagegen bin relativ neu,jedenfalls
haben wir heute schon die 0,26$ gesehen,
unglaublich
 !
!MFG
Zuki

Antwort auf Beitrag Nr.: 39.943.738 von Gustl24 am 06.08.10 18:00:35Das ist jetzt aber m.M.n doch etwas zu Negativ ausgedrückt.
Sie haben z.Z. ca 300 Mio. Shares draußen.
Und sind erst seit Ende 2008 unter der 1 USD Marke.

Sie haben z.Z. ca 300 Mio. Shares draußen.
Und sind erst seit Ende 2008 unter der 1 USD Marke.

Antwort auf Beitrag Nr.: 39.943.852 von zwitscherton am 06.08.10 18:16:21deswegen sagte ich ja gefühlte halbe milliarde shares...
aber um xoma eine MK von sagen wir mal 300 mio. usd zuzugestehen
müssen sie mal mehr an ihrer pipeline arbeiten - die
plattform schien seit jahren immer vielversprechend...aber man will hier
mal weitere erfolgreiche studien über diabetes, arthritis sehen...
vage studien mit einem halben dutzend probanden...mannomann...solche dinge
kratzen nur weiter am image der company als dilutionsmaschine
übernahme glaub ich nicht mehr...we will see
aber um xoma eine MK von sagen wir mal 300 mio. usd zuzugestehen
müssen sie mal mehr an ihrer pipeline arbeiten - die
plattform schien seit jahren immer vielversprechend...aber man will hier
mal weitere erfolgreiche studien über diabetes, arthritis sehen...
vage studien mit einem halben dutzend probanden...mannomann...solche dinge
kratzen nur weiter am image der company als dilutionsmaschine

übernahme glaub ich nicht mehr...we will see
Antwort auf Beitrag Nr.: 39.943.892 von Gustl24 am 06.08.10 18:25:20Meinte eigentlich nur, daß die Zahlen sofern bekannt auch stimmen sollten.
Ich geb Dir aber im Grund vollkommen recht.
Z.B. haben sie seit 1981 immerhin 806 Mio. USD verbraten.
(im Schitt so ca. 28 Mio.USD / per anno).
Dafür ist IMHO wirklich noch nicht allzuviel Rübergekommen.

Ich geb Dir aber im Grund vollkommen recht.
Z.B. haben sie seit 1981 immerhin 806 Mio. USD verbraten.
(im Schitt so ca. 28 Mio.USD / per anno).
Dafür ist IMHO wirklich noch nicht allzuviel Rübergekommen.

Antwort auf Beitrag Nr.: 39.944.093 von zwitscherton am 06.08.10 19:04:28Nungut  !
!
Als alternative zu XOMA möchte ich mal
Immunomedics (Nasdaq:IMMU) in den Raum stellen,
war selber schon drin,und die haben auch ausschts-
reiche antikörper in Phase-3 gegen Lupus und Krebs,
sind aber 3x so teuer wie XOMA,mit einer Mcap von
240 Mio.-$,was haltet ihr davon ?
MFG
Zuki
 !
!Als alternative zu XOMA möchte ich mal
Immunomedics (Nasdaq:IMMU) in den Raum stellen,
war selber schon drin,und die haben auch ausschts-
reiche antikörper in Phase-3 gegen Lupus und Krebs,
sind aber 3x so teuer wie XOMA,mit einer Mcap von
240 Mio.-$,was haltet ihr davon ?
MFG
Zuki

schon seltsam, der Kursverlauf...

Antwort auf Beitrag Nr.: 39.944.349 von mosbach am 06.08.10 19:50:15sieht doch sehr gut aus...wenn die 29 gebrochen wird schließen wir auch grün....32 wäre top
33 phantastisch
montag earnings ...news....etc
33 phantastisch
montag earnings ...news....etc
denkt einer mal dadrüber nach,das xoma über 1dollar gezockt werden könnte?
schliesslich fehlen denen ja nur über 200 prozent
oder über 0,60 dann ein splitt 1:2!
dann sind die doch auch über 1dollar
schliesslich fehlen denen ja nur über 200 prozent

oder über 0,60 dann ein splitt 1:2!
dann sind die doch auch über 1dollar

Antwort auf Beitrag Nr.: 39.944.626 von lilie31 am 06.08.10 20:35:36azimuth hat short gesellt - erst trache gekauft und damit gecovert....
news hat die aktie rennen lassen und von .401 wieder massen geshorted....
jetzt wieder tranche gekauft....
aber er hat jetzt wohl schon feierabend
auf jedenfall super busines modell....
ich denke jedenfalls nicht das fundamentals etwas mit dem kursverlust der letzten wochen zu tun haben....
news hat die aktie rennen lassen und von .401 wieder massen geshorted....
jetzt wieder tranche gekauft....
aber er hat jetzt wohl schon feierabend
auf jedenfall super busines modell....
ich denke jedenfalls nicht das fundamentals etwas mit dem kursverlust der letzten wochen zu tun haben....
Antwort auf Beitrag Nr.: 39.944.655 von medisana am 06.08.10 20:42:22ich habe ja guten einstiegskurs erwischt zu 0,21 euro!
gutes kauflimit erwischt.
kann nur hoffen das die jetzt anzieht.
spekuliere mal das die auf 1dollar hochgezogen wird und sich da 10tage halten muss.
bei ambac damals war auch so ein aktion in april,
da hat das in paar tagen mehr als geklappt
vielleicht auch hier
gutes kauflimit erwischt.
kann nur hoffen das die jetzt anzieht.
spekuliere mal das die auf 1dollar hochgezogen wird und sich da 10tage halten muss.
bei ambac damals war auch so ein aktion in april,
da hat das in paar tagen mehr als geklappt

vielleicht auch hier

Antwort auf Beitrag Nr.: 39.944.720 von lilie31 am 06.08.10 20:55:46fein, fein, Glück gehabt!
Antwort auf Beitrag Nr.: 39.944.248 von Zukertort am 06.08.10 19:32:19Mit IMMU hab ich mich noch nicht befasst.
Hier auf WO gibts zu dem Wert nur ein Paar Uralt threads.
Was Lupus anbetrifft setze ich auf HGSI - und hoffe mal (ganz uneigennützig) das die vorn bleiben.
BTW: Die Euphorie für XOMA ist anscheinend soeben zurückgekehrt.

Hier auf WO gibts zu dem Wert nur ein Paar Uralt threads.
Was Lupus anbetrifft setze ich auf HGSI - und hoffe mal (ganz uneigennützig) das die vorn bleiben.
BTW: Die Euphorie für XOMA ist anscheinend soeben zurückgekehrt.

Antwort auf Beitrag Nr.: 39.944.951 von mosbach am 06.08.10 21:37:22ob ich glück gehabt habe, wird sich die laufende woche zeigen.
bis ende august will ich hier drinne bleiben.
und auf aufschwung von xoma vor den r/S hoffen.
vielleicht wird ja die zweite angriff auf die 0,50kommen.
eine übernahme würde mir besser gefallen.
mal gucken
was mich positiv macht, ist auch das insider zu kursen 0,349 gekauft haben!
sind nur 390000.
aber die müssten doch mehr wissen
bis ende august will ich hier drinne bleiben.
und auf aufschwung von xoma vor den r/S hoffen.
vielleicht wird ja die zweite angriff auf die 0,50kommen.
eine übernahme würde mir besser gefallen.
mal gucken

was mich positiv macht, ist auch das insider zu kursen 0,349 gekauft haben!
sind nur 390000.
aber die müssten doch mehr wissen

Antwort auf Beitrag Nr.: 39.945.147 von lilie31 am 06.08.10 22:04:54das insider zu kursen 0,349 gekauft haben
Wo siehst du das? Hast du einen Link dazu?
Wo siehst du das? Hast du einen Link dazu?

Antwort auf Beitrag Nr.: 39.945.209 von Lucky72 am 06.08.10 22:13:45Und selbst wenn, 139K zu 0.35 also ca. 49000 USD dürften selbst noch aus der Portokasse rauszukratzen sein.
That's nothing.

That's nothing.

Antwort auf Beitrag Nr.: 39.945.147 von lilie31 am 06.08.10 22:04:54Das waren optionen die in Aktien umgewandelt wurden 



Antwort auf Beitrag Nr.: 39.946.904 von Kursziel1000 am 07.08.10 15:37:44Umgewandelt über PPS 
Xoma partnership could send shares over $2, says Wedbush
Wedbush believes a partnership for XOMA-052 is the next major catalyst for Xoma shares and that such news could send the stock to or above its $2 fair value estimate. The firm sees significant upside in the stock from 2010 catalysts and maintains an Outperform rating.

http://www.theflyonthewall.com/permalinks/entry.php/XOMAid11…

Xoma partnership could send shares over $2, says Wedbush
Wedbush believes a partnership for XOMA-052 is the next major catalyst for Xoma shares and that such news could send the stock to or above its $2 fair value estimate. The firm sees significant upside in the stock from 2010 catalysts and maintains an Outperform rating.

http://www.theflyonthewall.com/permalinks/entry.php/XOMAid11…
Antwort auf Beitrag Nr.: 39.946.904 von Kursziel1000 am 07.08.10 15:37:44...umgewandelt werden im Jahre 2020
Antwort auf Beitrag Nr.: 39.946.904 von Kursziel1000 am 07.08.10 15:37:44auch wenn insider ihre optionen in aktien umwandeln,
ist das doch auch positiv zu bewerten,finde ich.
bei den kursen ist für mich xoma ,persönlich auch übernahmekanditat!!!
also ist für mich diese kurse einstiegskurse
wenns klappt ist hier ein gewaltiges potenzial nach oben gegeben.
ich persönlich habe mich positioniert,
lasse mich überraschen
ist das doch auch positiv zu bewerten,finde ich.
bei den kursen ist für mich xoma ,persönlich auch übernahmekanditat!!!
also ist für mich diese kurse einstiegskurse

wenns klappt ist hier ein gewaltiges potenzial nach oben gegeben.
ich persönlich habe mich positioniert,
lasse mich überraschen

Antwort auf Beitrag Nr.: 39.946.904 von Kursziel1000 am 07.08.10 15:37:44

http://www.secform4.com/insider-trading/791908.htm


http://www.secform4.com/insider-trading/791908.htm
XOMA ist ein reiner Lottoplay.
Entweder 1000%+++ oder weitere Kursverluste wg. Verwässerung seitens des Unternehmens.
No risk - no fun!
Entweder 1000%+++ oder weitere Kursverluste wg. Verwässerung seitens des Unternehmens.
No risk - no fun!
Antwort auf Beitrag Nr.: 39.948.207 von zwitscherton am 08.08.10 13:38:19wie gesagt optionen die 2020 gewandelt werden können!
Kursziel 2 USD...und das ohne R/S...ich glaube dran!
Antwort auf Beitrag Nr.: 39.948.490 von nieglueckhaber am 08.08.10 17:09:40Morgen ist CC.
Mal sehn was da rüber kommt.
Auf das General Business Update bin ich mal gespannt.

Mal sehn was da rüber kommt.
Auf das General Business Update bin ich mal gespannt.

Bei XOMA werden 24,7% der OS von Large Block Holder gehalten! 
http://www.dailyfinance.com/company/xoma-ltd/xoma/nas/instit…
Zum Vergleich! Bei meiner Dynavax werden 73,3% der OS von Large Block Holder gehalten!
http://www.dailyfinance.com/company/dynavax-technologies-cor…
Also wenn bei XOMA mehr "Big Boys" einsteigen bin ich auch dabei!

http://www.dailyfinance.com/company/xoma-ltd/xoma/nas/instit…
Zum Vergleich! Bei meiner Dynavax werden 73,3% der OS von Large Block Holder gehalten!

http://www.dailyfinance.com/company/dynavax-technologies-cor…
Also wenn bei XOMA mehr "Big Boys" einsteigen bin ich auch dabei!

guten morgen...heute sollte die wende kommen! 

Bekomme seit 11.37 Uhr keine Kurse mehr für Xoma, weder hier noch sonst wo, was ist los?
Antwort auf Beitrag Nr.: 39.948.490 von nieglueckhaber am 08.08.10 17:09:40da muss eine übernahme kommen,um solche kurse zu erreichen
der jüngste anstieg ist auch verpufft
wenn wir über 0,40 laufen kommen anleger wieder ins boot.
vorher nicht.

der jüngste anstieg ist auch verpufft

wenn wir über 0,40 laufen kommen anleger wieder ins boot.
vorher nicht.
Antwort auf Beitrag Nr.: 39.951.761 von jenwo am 09.08.10 14:30:47premarket kurs ist 0,298!
da ist nichts los
da ist nichts los

wer schmeisst den jetzt schon 10000st.für 0,203!!!!
da hat einer ja voll den panik bekommen
da hat einer ja voll den panik bekommen

und wir werden den dollar sehen...ohne R/S!!!!! 

hier geht heute noch was....

Antwort auf Beitrag Nr.: 39.954.099 von nieglueckhaber am 09.08.10 19:41:17huch hier hat sich der blatt auch gewendet
na hoffentlich über 0,30,
dann kommt hier phantasie auf
yrcw läuft,wamu hat angefangen zu laufen und wenn jetzt xoma auch ein performance hinlegt
dann bin ich heute mehr als zufrieden

na hoffentlich über 0,30,
dann kommt hier phantasie auf

yrcw läuft,wamu hat angefangen zu laufen und wenn jetzt xoma auch ein performance hinlegt

dann bin ich heute mehr als zufrieden
Antwort auf Beitrag Nr.: 39.955.297 von Wunram am 09.08.10 22:36:49[urlXOMA Reports Second Quarter 2010 Financial Results]http://finance.yahoo.com/news/XOMA-Reports-Second-Quarter-pz-1927772509.html?x=0&.v=1[/url]


http://seekingalpha.com/article/219658-xoma-ltd-q2-2010-earn…
...hört sich gut an...nachdem die Q2 Zahlen raus sind und die Finanzierung stabil für die nächsten 12 Monate ist, sollte es langsam mal wieder rauf gehen!
...auf einen grünen tag....
...hört sich gut an...nachdem die Q2 Zahlen raus sind und die Finanzierung stabil für die nächsten 12 Monate ist, sollte es langsam mal wieder rauf gehen!
...auf einen grünen tag....
Antwort auf Beitrag Nr.: 39.957.400 von nieglueckhaber am 10.08.10 11:09:21Finanzierung ist stabil 


Sorry,aber es kann eigentlich nur abwaerts gehen!



Sorry,aber es kann eigentlich nur abwaerts gehen!
abwarten...meistens kommt es anders als alle glauben...bin zuversichtlich! drüben sind kaum reaktionen zu verspüren, da schon alles im kurs eingepreist ist! hier sollte es nur eine richtung geben, nämlich gen norden!
Antwort auf Beitrag Nr.: 39.958.703 von nieglueckhaber am 10.08.10 14:13:32Pre-Market Last: $ .2703
Net / % Change
-.0277 (-9.30%)
Pre-Market Volume: 33,220

Net / % Change
-.0277 (-9.30%)
Pre-Market Volume: 33,220

heute sehen wir noch den grünen bereich...yeah
Heut wieder Blutbad bei den Biotechs.


Antwort auf Beitrag Nr.: 39.961.760 von zwitscherton am 10.08.10 21:09:17Nicht auf Tagestief geschlossen.
Aber über die 0.29 USD gings heut nicht.

Aber über die 0.29 USD gings heut nicht.

Antwort auf Beitrag Nr.: 39.962.805 von zwitscherton am 11.08.10 00:38:11Das Gemetzel geht grad weiter.


Antwort auf Beitrag Nr.: 39.967.645 von zwitscherton am 11.08.10 17:11:36sollte aber ein ende finden...bin heute guter dinge!

Short Interest (Shares Short)
8,639,200
Days To Cover (Short Interest Ratio)
2.5
Bin auch optimistisch
Gestern ist das minus mit durch Leerverkäufe (+2 Millionen) entstanden. Diese müssen bald gecovert werden, was die Abwärtsspirale vorerst stoppen sollte. Es werden nicht mehr so viele Aktien auf den Markt geschmissen. Wenn noch eine positive Nachricht kommen sollte, dann
8,639,200
Days To Cover (Short Interest Ratio)
2.5
Bin auch optimistisch

Gestern ist das minus mit durch Leerverkäufe (+2 Millionen) entstanden. Diese müssen bald gecovert werden, was die Abwärtsspirale vorerst stoppen sollte. Es werden nicht mehr so viele Aktien auf den Markt geschmissen. Wenn noch eine positive Nachricht kommen sollte, dann

Xoma Limited $ 0.27
XOMA -0.01
Daily Short Sale Volume - NEW view
Short Interest (Shares Short) 8,639,200
Days To Cover (Short Interest Ratio) 2.5
Short Percent of Float view
Naked Short Selling List - NEW view
Short Interest - Prior 6,334,400
Short % Increase / Decrease 36.39
Short Squeeze Ranking™ view
% From 52-Wk High ($ 1.07 ) -74.58 %
% From 52-Wk Low ($ 0.26 ) 4.62 %
% From 200-Day MA ($ 0.57 ) -52.28 %
% From 50-Day MA ($ 0.39 ) -30.26 %
Price % Change (52-Week) -67.62 %
Shares Float 260,960,000
Total Shares Outstanding 261,247,750
% Owned by Insiders 3.11 %
% Owned by Institutions 18.50 %
Market Cap. $ 71,059,392
Trading Volume - Today 6,252,349
Trading Volume - Average 3,455,600
Trading Volume - Today vs. Average 11.79 %
Earnings Per Share -0.13
PE Ratio
Record Date 2010-AugA
Sector Healthcare
Industry Biotechnology
Exchange NAS
Data Provided
XOMA -0.01
Daily Short Sale Volume - NEW view
Short Interest (Shares Short) 8,639,200
Days To Cover (Short Interest Ratio) 2.5
Short Percent of Float view
Naked Short Selling List - NEW view
Short Interest - Prior 6,334,400
Short % Increase / Decrease 36.39
Short Squeeze Ranking™ view
% From 52-Wk High ($ 1.07 ) -74.58 %
% From 52-Wk Low ($ 0.26 ) 4.62 %
% From 200-Day MA ($ 0.57 ) -52.28 %
% From 50-Day MA ($ 0.39 ) -30.26 %
Price % Change (52-Week) -67.62 %
Shares Float 260,960,000
Total Shares Outstanding 261,247,750
% Owned by Insiders 3.11 %
% Owned by Institutions 18.50 %
Market Cap. $ 71,059,392
Trading Volume - Today 6,252,349
Trading Volume - Average 3,455,600
Trading Volume - Today vs. Average 11.79 %
Earnings Per Share -0.13
PE Ratio
Record Date 2010-AugA
Sector Healthcare
Industry Biotechnology
Exchange NAS
Data Provided
Tag auch ,
na das war aber jetzt noch nix mit dem Xoma Zock....war ja nicht so schlecht gelegen mit dem Kurs 0,195 € - allerdings hab ich auch etwas darüber gekauft...na ja hält sich alles in Grenzen...aber ärgerlich ist immer ein entgangener Gewinn( das ärgert mich immer richtig ).
Zahlen waren nicht besser als erwartet...selbst ein Gang an die OTC ist jetzt fast mit eingerechnet
na das war aber jetzt noch nix mit dem Xoma Zock....war ja nicht so schlecht gelegen mit dem Kurs 0,195 € - allerdings hab ich auch etwas darüber gekauft...na ja hält sich alles in Grenzen...aber ärgerlich ist immer ein entgangener Gewinn( das ärgert mich immer richtig ).
Zahlen waren nicht besser als erwartet...selbst ein Gang an die OTC ist jetzt fast mit eingerechnet
" leichte " Besserungstendenz bei Xoma im Moment bei um die 0,285 US$..knapp 10 % im Plus ( obs hält ist eine andere Frage )
Up 6.29%
War das heut die Wende ?

War das heut die Wende ?

Antwort auf Beitrag Nr.: 39.994.004 von zwitscherton am 16.08.10 22:42:38Also von Wende kann ja keine Rede sein..eher eine kleine Korrektur..aber was sind denn 2- 3 cent ???...nix !!!!!
Antwort auf Beitrag Nr.: 39.996.966 von Expertchen007 am 17.08.10 13:33:55Jede Wende beginnt mit einer Korrektur.
Nachhaltig sollte das aber erst werden, mit positiver News.
Volumen war gestern etwas über Durchschnitt.
Vielleicht war das Ganze doch nur eine Luftnummer.

Nachhaltig sollte das aber erst werden, mit positiver News.
Volumen war gestern etwas über Durchschnitt.
Vielleicht war das Ganze doch nur eine Luftnummer.

leider wieder schlechte nachrichten für eh schon gebeutelte xoma-shareholder:
Aug. 17, 2010, 4:15 p.m. EDT
XOMA Announces Reverse Stock Split
BERKELEY, Calif., Aug 17, 2010 (GlobeNewswire via COMTEX) -- XOMA Ltd. /quotes/comstock/15*!xoma/quotes/nls/xoma (XOMA 0.24, -0.04, -14.71%) , a leader in the discovery and development of therapeutic antibodies, today announced that its board of directors has approved a 1-for-15 share consolidation, or reverse stock split, that will become effective with the opening of trading on August 18, 2010. The primary objective in effecting a reverse stock split at this time is to better enable the company to maintain the listing of its common shares on The NASDAQ Global Market. The company's common shares will continue trading on The NASDAQ Global Market and will begin trading on a split-adjusted basis at the opening of trading on Wednesday, August 18, 2010.
At XOMA's annual general meeting of shareholders held on July 21, 2010, shareholders voted to approve a proposal authorizing the board of directors of the company to effect a reverse split of the company's common shares at a ratio within a range of 1-for-2 and 1-for-15, as determined by the board in its sole discretion. As authorized, the board has elected to effect a reverse split at a ratio of 1-for-15.
"We appreciate the support of our shareholders in granting our board the authority to effect a reverse split. After in-depth consideration of our options, the board determined that a reverse split of the company's common shares is in the best interest of shareholders," commented Steve Engle, XOMA's Chairman and Chief Executive Officer. "By effecting a reverse stock split, the company is better positioned to regain compliance with the NASDAQ listing rules. Maintaining our listing on NASDAQ provides the company with greater flexibility to financially and strategically support the development of the company."
http://www.marketwatch.com/story/xoma-announces-reverse-stoc…
wird wohl morgen in DE nicht handelbar sein. -70% in einem jahr ist schon fast so gut wie die geldverbrennungsmaschine genta
Aug. 17, 2010, 4:15 p.m. EDT
XOMA Announces Reverse Stock Split
BERKELEY, Calif., Aug 17, 2010 (GlobeNewswire via COMTEX) -- XOMA Ltd. /quotes/comstock/15*!xoma/quotes/nls/xoma (XOMA 0.24, -0.04, -14.71%) , a leader in the discovery and development of therapeutic antibodies, today announced that its board of directors has approved a 1-for-15 share consolidation, or reverse stock split, that will become effective with the opening of trading on August 18, 2010. The primary objective in effecting a reverse stock split at this time is to better enable the company to maintain the listing of its common shares on The NASDAQ Global Market. The company's common shares will continue trading on The NASDAQ Global Market and will begin trading on a split-adjusted basis at the opening of trading on Wednesday, August 18, 2010.
At XOMA's annual general meeting of shareholders held on July 21, 2010, shareholders voted to approve a proposal authorizing the board of directors of the company to effect a reverse split of the company's common shares at a ratio within a range of 1-for-2 and 1-for-15, as determined by the board in its sole discretion. As authorized, the board has elected to effect a reverse split at a ratio of 1-for-15.
"We appreciate the support of our shareholders in granting our board the authority to effect a reverse split. After in-depth consideration of our options, the board determined that a reverse split of the company's common shares is in the best interest of shareholders," commented Steve Engle, XOMA's Chairman and Chief Executive Officer. "By effecting a reverse stock split, the company is better positioned to regain compliance with the NASDAQ listing rules. Maintaining our listing on NASDAQ provides the company with greater flexibility to financially and strategically support the development of the company."
http://www.marketwatch.com/story/xoma-announces-reverse-stoc…
wird wohl morgen in DE nicht handelbar sein. -70% in einem jahr ist schon fast so gut wie die geldverbrennungsmaschine genta

Antwort auf Beitrag Nr.: 40.001.570 von kleingeldjaeger am 17.08.10 22:56:45RS 1:15. Das ist das maximale Möglichkeit die sie haben.
Dann lt. heutigem Schlusskurs wird XOMA morgen bei ca. 4.22 USD starten.
Es sei denn die After Hour Kurse sind ein übles Vorzeichen und es geht gleich weiter runter.
Jedenfalls ist damit erstmal eine Unsicherheit raus.

Dann lt. heutigem Schlusskurs wird XOMA morgen bei ca. 4.22 USD starten.
Es sei denn die After Hour Kurse sind ein übles Vorzeichen und es geht gleich weiter runter.
Jedenfalls ist damit erstmal eine Unsicherheit raus.

Antwort auf Beitrag Nr.: 40.001.832 von zwitscherton am 18.08.10 00:06:13 ..Hmmmm...also auf jeden Fall gibt das morgen wohl einen Squezze erst mal..den die Shorts müssen jetzt gecovert werden..Holzauge sei wachsam...hoffe mal die bringen eine gute News dazu,,,....ansonsten gefällt mit das gar nicht
..Hmmmm...also auf jeden Fall gibt das morgen wohl einen Squezze erst mal..den die Shorts müssen jetzt gecovert werden..Holzauge sei wachsam...hoffe mal die bringen eine gute News dazu,,,....ansonsten gefällt mit das gar nicht
 ..Hmmmm...also auf jeden Fall gibt das morgen wohl einen Squezze erst mal..den die Shorts müssen jetzt gecovert werden..Holzauge sei wachsam...hoffe mal die bringen eine gute News dazu,,,....ansonsten gefällt mit das gar nicht
..Hmmmm...also auf jeden Fall gibt das morgen wohl einen Squezze erst mal..den die Shorts müssen jetzt gecovert werden..Holzauge sei wachsam...hoffe mal die bringen eine gute News dazu,,,....ansonsten gefällt mit das gar nicht
Was man so lesen kann..."könnte " die Story morgen sogar positiv ausgehen....allerdings halte ich Kurse von 7 US$ für unwahrscheinlich...kommt frauf an was mit den Shorts passiert...und das sind jede Menge ich denke mal die ersten 30 Minuten zeigen den WEg...bin gespannt
Antwort auf Beitrag Nr.: 40.001.944 von Expertchen007 am 18.08.10 01:27:27Bin ich auch mal gespannt, ob die Theorie mit den Shorties, die sich nach dem RS eindecken (müssen?) stimmt.


Antwort auf Beitrag Nr.: 40.001.947 von zwitscherton am 18.08.10 01:33:17Nachbörslich (-16%) sieht es (bei geringem Volumen) ja erstmal nicht so berauschend aus.


Antwort auf Beitrag Nr.: 40.001.948 von zwitscherton am 18.08.10 01:35:20Daß XOMA den maximalen RS gewählt hat find ich schon nachdenkenswert.
Um über 1 USD zu kommen hätte sogar 1:5 ausgereicht.
Ich hatte eigentlich mit 1:10 gerechnet, damit wäre auch erstmal reichlich Luft über den 1 USD gewesen.

Um über 1 USD zu kommen hätte sogar 1:5 ausgereicht.
Ich hatte eigentlich mit 1:10 gerechnet, damit wäre auch erstmal reichlich Luft über den 1 USD gewesen.

Moin XOMAfreaks  !
!
Ich bin erst mal froh mich vor dem R/S +-0 verabschiedet zu haben,
und die aussage die Unsicherheit sei jetzt raus,kann ich überhaupt
nicht teilen. Denn der R/S ist doch quasi nur der vorbote einer
möglicherweise gigantischen KE,und da möchte ich vorher eben nicht
rein ...
MFG
Zuki
 !
!Ich bin erst mal froh mich vor dem R/S +-0 verabschiedet zu haben,
und die aussage die Unsicherheit sei jetzt raus,kann ich überhaupt
nicht teilen. Denn der R/S ist doch quasi nur der vorbote einer
möglicherweise gigantischen KE,und da möchte ich vorher eben nicht
rein ...
MFG
Zuki

Auf diese News habe ich gewartet, um entsprechend meinem Plan bis zu Q1 2011 kontinuierlich meine Position zu erweiteren!
Eurer Theorie, dass es zwangsläufig zu einem Squeeze kommt, kann ich jedoch nicht folgen. Die geliehenen /geshorteten Aktien wird durch den RS ebenfalls um den Faktor 15 reduziert. Der RS gibt keinen Grund für einen Short-Squeeze. Und die Mehrzahl der Aktien gaibt nach Durchführung eines RS erstmal ab. Ich denke, es werden sich deshalb heute schöne Kaufgelegenheiten ergeben.
Die Unsicherheit bzgl. des RS ist jetzt raus und an der Börse wird die Zukunft gehandelt. Und während manche wie Zukertort nur potentielle Kapitalerhöhungen im Auge haben, scheint vergessen zu werden, dass Q1 2011 und damit neue Studienergebnisse von XOMA 052 immer näher kommen. Eine weitere Kapitalerhöhung ist natürlich möglich, aber auch eine strategische Beteiligung an XOMA 052 oder eine Partnerschaft mit einem Pharmagiganten sind genauso möglich.
Ich halte jedenfalls an meinem Plan fest, kontinuierlich meine Position an XOMA-Aktien bis zum Q1 2011 auszubauen, da ich derzeit keine andere Aktie kenne, die ein solch hohes Potential im KHK- und Diabetes-Markt hätte. Meine Angst davor am Ende ohne Shares dazustehen ist viel größer, als die Angst davor, zu früh gekauft zu haben. Daher hatte ich mich für eine Strategie quartalsweiser Aktienzukäufe entschieden. Heute dürfte ein guter Tag sein, um diese Position weiter aufzustocken.
Nur meine persönliche Meinung und Handelsstrategie, keine Aufforderung zum Kauf oder Verkauf der Aktie.
Grüsse, ER
Eurer Theorie, dass es zwangsläufig zu einem Squeeze kommt, kann ich jedoch nicht folgen. Die geliehenen /geshorteten Aktien wird durch den RS ebenfalls um den Faktor 15 reduziert. Der RS gibt keinen Grund für einen Short-Squeeze. Und die Mehrzahl der Aktien gaibt nach Durchführung eines RS erstmal ab. Ich denke, es werden sich deshalb heute schöne Kaufgelegenheiten ergeben.
Die Unsicherheit bzgl. des RS ist jetzt raus und an der Börse wird die Zukunft gehandelt. Und während manche wie Zukertort nur potentielle Kapitalerhöhungen im Auge haben, scheint vergessen zu werden, dass Q1 2011 und damit neue Studienergebnisse von XOMA 052 immer näher kommen. Eine weitere Kapitalerhöhung ist natürlich möglich, aber auch eine strategische Beteiligung an XOMA 052 oder eine Partnerschaft mit einem Pharmagiganten sind genauso möglich.
Ich halte jedenfalls an meinem Plan fest, kontinuierlich meine Position an XOMA-Aktien bis zum Q1 2011 auszubauen, da ich derzeit keine andere Aktie kenne, die ein solch hohes Potential im KHK- und Diabetes-Markt hätte. Meine Angst davor am Ende ohne Shares dazustehen ist viel größer, als die Angst davor, zu früh gekauft zu haben. Daher hatte ich mich für eine Strategie quartalsweiser Aktienzukäufe entschieden. Heute dürfte ein guter Tag sein, um diese Position weiter aufzustocken.
Nur meine persönliche Meinung und Handelsstrategie, keine Aufforderung zum Kauf oder Verkauf der Aktie.
Grüsse, ER
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -0,34 | |
| -2,46 | |
| +0,18 | |
| -0,44 | |
| +0,86 | |
| -1,97 | |
| +1,22 | |
| -1,03 | |
| +1,79 | |
| +0,62 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 243 | ||
| 89 | ||
| 70 | ||
| 66 | ||
| 53 | ||
| 49 | ||
| 45 | ||
| 40 | ||
| 39 | ||
| 37 |



















