Radius Health, Inc. (RDUS)...eine neue Perle? - 500 Beiträge pro Seite
eröffnet am 31.05.16 20:36:47 von
neuester Beitrag 21.10.21 13:38:53 von
neuester Beitrag 21.10.21 13:38:53 von
Beiträge: 548
ID: 1.232.720
ID: 1.232.720
Aufrufe heute: 0
Gesamt: 38.844
Gesamt: 38.844
Aktive User: 0
ISIN: US7504692077 · WKN: A114VH
9,8220
EUR
+0,27 %
+0,0260 EUR
Letzter Kurs 13.08.22 Tradegate
Neuigkeiten
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,9000 | +59,66 | |
| 0,5922 | +44,44 | |
| 0,7000 | +36,69 | |
| 4,7450 | +35,57 | |
| 2,4900 | +27,69 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 4,3600 | -13,49 | |
| 1,6900 | -14,50 | |
| 2,8150 | -15,21 | |
| 7,6100 | -17,20 | |
| 1,6100 | -18,27 |
...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben.
Radius Announces FDA Acceptance for Filing of New Drug Application for Abaloparatide-SC for the Treatment of Postmenopausal Women with Osteoporosis
Radius Health Inc.
WALTHAM, Mass., May 31, 2016 (GLOBE NEWSWIRE) -- Radius Health, Inc. (RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that its New Drug Application (NDA) for abaloparatide–SC has been accepted for filing by the U.S. Food and Drug Administration (FDA). The acceptance of the NDA reflects the FDA’s determination that the application is sufficiently complete to permit a substantive review.
“The FDA’s acceptance for filing of our abaloparatide-SC NDA is a major milestone for Radius and we look forward to continuing to work with the FDA as they review our application,” said Robert E. Ward, President and CEO of Radius Health. “Given the high unmet medical need in osteoporosis, we believe that abaloparatide-SC, if approved, has the potential to become a promising new treatment option for the approximately 10 million postmenopausal women with osteoporosis, many of whom remain untreated.”
The NDA is supported by data from the entire abaloparatide-SC development program, including the results from the 18-month Phase 3 ACTIVE trial in 2,463 postmenopausal women with osteoporosis and the first six months of the ACTIVExtend trial in 1,139 of the ACTIVE participants. Positive results for abaloparatide-SC treatment groups from the ACTIVE and ACTIVExtend trials have met the primary and secondary endpoints essential for submission of the NDA, including the primary endpoint of reduction of vertebral fractures as well as key endpoints of reduction of nonvertebral, clinical, and major osteoporotic fractures. In these and the other trials submitted in the NDA, abaloparatide-SC administered at a dose of 80 mcg daily was generally safe and well tolerated in postmenopausal women with osteoporosis.
As previously reported, Radius submitted a Centralised Marketing Authorisation Application (MAA) for abaloparatide-SC in the European Union on November 17, 2015, which was validated by the European Medicines Agency (EMA) in December 2015, and is currently undergoing active regulatory assessment by the Committee for Medicinal Products for Human Use of the EMA (CHMP). The EMA has granted Radius an additional 3-month extension to the procedural timetable for response in the ongoing MAA assessment. As a result of this extension to the procedural timetable, the Company now anticipates that the CHMP may adopt an Opinion regarding the MAA in late 2016 or in 2017.
Abaloparatide-SC is an investigational treatment for postmenopausal women with osteoporosis and its safety and efficacy have not been established.
Radius Announces FDA Acceptance for Filing of New Drug Application for Abaloparatide-SC for the Treatment of Postmenopausal Women with Osteoporosis
Radius Health Inc.
WALTHAM, Mass., May 31, 2016 (GLOBE NEWSWIRE) -- Radius Health, Inc. (RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that its New Drug Application (NDA) for abaloparatide–SC has been accepted for filing by the U.S. Food and Drug Administration (FDA). The acceptance of the NDA reflects the FDA’s determination that the application is sufficiently complete to permit a substantive review.
“The FDA’s acceptance for filing of our abaloparatide-SC NDA is a major milestone for Radius and we look forward to continuing to work with the FDA as they review our application,” said Robert E. Ward, President and CEO of Radius Health. “Given the high unmet medical need in osteoporosis, we believe that abaloparatide-SC, if approved, has the potential to become a promising new treatment option for the approximately 10 million postmenopausal women with osteoporosis, many of whom remain untreated.”
The NDA is supported by data from the entire abaloparatide-SC development program, including the results from the 18-month Phase 3 ACTIVE trial in 2,463 postmenopausal women with osteoporosis and the first six months of the ACTIVExtend trial in 1,139 of the ACTIVE participants. Positive results for abaloparatide-SC treatment groups from the ACTIVE and ACTIVExtend trials have met the primary and secondary endpoints essential for submission of the NDA, including the primary endpoint of reduction of vertebral fractures as well as key endpoints of reduction of nonvertebral, clinical, and major osteoporotic fractures. In these and the other trials submitted in the NDA, abaloparatide-SC administered at a dose of 80 mcg daily was generally safe and well tolerated in postmenopausal women with osteoporosis.
As previously reported, Radius submitted a Centralised Marketing Authorisation Application (MAA) for abaloparatide-SC in the European Union on November 17, 2015, which was validated by the European Medicines Agency (EMA) in December 2015, and is currently undergoing active regulatory assessment by the Committee for Medicinal Products for Human Use of the EMA (CHMP). The EMA has granted Radius an additional 3-month extension to the procedural timetable for response in the ongoing MAA assessment. As a result of this extension to the procedural timetable, the Company now anticipates that the CHMP may adopt an Opinion regarding the MAA in late 2016 or in 2017.
Abaloparatide-SC is an investigational treatment for postmenopausal women with osteoporosis and its safety and efficacy have not been established.
Die Zulassung von Abaloparatide-SC in Europa wurde bereits in 2015 bei der EMA eringereicht, so dass noch in 2016 mit der Zulassung zu rechnen ist. Eine ausführliche Analyse wird nachgereicht.
Radius Announces European Medicines Agency Validates Marketing Authorization Application for Abaloparatide-SC for the Treatment of Osteoporosis in Postmenopausal Women
Radius Initiates Human Pharmacokinetic Study of Optimized Transdermal Patch of Investigational Drug Abaloparatide
WALTHAM, Mass., Dec. 04, 2015 (GLOBE NEWSWIRE) -- Radius Health (Nasdaq:RDUS), today announced that the European Medicines Agency (EMA) has validated for review the Marketing Authorization Application (MAA) for abaloparatide subcutaneous (SC) for the treatment of osteoporosis in postmenopausal women. With this validation, the Radius application is complete and now under review by the EMA.
"The MAA for abaloparatide-SC is based on the results from the ACTIVE and ACTIVExtend trials, which demonstrated significant clinical benefit for postmenopausal women at risk of osteoporotic fracture," said Robert Ward, President and CEO of Radius Health. "The acceptance of our application for review by the EMA represents a significant step towards potentially bringing abaloparatide-SC to postmenopausal women with osteoporosis in Europe, and Radius looks forward to working with the EMA in the review procedure."
The MAA submission is based on the final results of the 18 month ACTIVE and the first 6 months of the ACTIVExtend trials in osteoporosis. The clinical trials demonstrated that once daily abaloparatide-SC reduced the risk of vertebral and nonvertebral fractures as compared to placebo.
The MAA for the investigational abaloparatide-SC was submitted in Europe on November 17, 2015 and the company plans to submit a New Drug Application (NDA) to the US Food and Drug Administration (FDA) by the end of the first quarter of 2016.
This week Radius initiated the human pharmacokinetic (PK) clinical evaluation of the optimized abaloparatide transdermal patch (TD) based upon 3M's Microstructured Transdermal System technology with the goal of achieving comparability to abaloparatide subcutaneous injection (SC). This human "replicative" study is intended to confirm in healthy postmenopausal women the pharmacokinetic profile of the transdermal patch as established in primate studies. Radius will use the results from this replicative study to inform the design of the registration program.
Radius Announces European Medicines Agency Validates Marketing Authorization Application for Abaloparatide-SC for the Treatment of Osteoporosis in Postmenopausal Women
Radius Initiates Human Pharmacokinetic Study of Optimized Transdermal Patch of Investigational Drug Abaloparatide
WALTHAM, Mass., Dec. 04, 2015 (GLOBE NEWSWIRE) -- Radius Health (Nasdaq:RDUS), today announced that the European Medicines Agency (EMA) has validated for review the Marketing Authorization Application (MAA) for abaloparatide subcutaneous (SC) for the treatment of osteoporosis in postmenopausal women. With this validation, the Radius application is complete and now under review by the EMA.
"The MAA for abaloparatide-SC is based on the results from the ACTIVE and ACTIVExtend trials, which demonstrated significant clinical benefit for postmenopausal women at risk of osteoporotic fracture," said Robert Ward, President and CEO of Radius Health. "The acceptance of our application for review by the EMA represents a significant step towards potentially bringing abaloparatide-SC to postmenopausal women with osteoporosis in Europe, and Radius looks forward to working with the EMA in the review procedure."
The MAA submission is based on the final results of the 18 month ACTIVE and the first 6 months of the ACTIVExtend trials in osteoporosis. The clinical trials demonstrated that once daily abaloparatide-SC reduced the risk of vertebral and nonvertebral fractures as compared to placebo.
The MAA for the investigational abaloparatide-SC was submitted in Europe on November 17, 2015 and the company plans to submit a New Drug Application (NDA) to the US Food and Drug Administration (FDA) by the end of the first quarter of 2016.
This week Radius initiated the human pharmacokinetic (PK) clinical evaluation of the optimized abaloparatide transdermal patch (TD) based upon 3M's Microstructured Transdermal System technology with the goal of achieving comparability to abaloparatide subcutaneous injection (SC). This human "replicative" study is intended to confirm in healthy postmenopausal women the pharmacokinetic profile of the transdermal patch as established in primate studies. Radius will use the results from this replicative study to inform the design of the registration program.
Der Zulassungsantrag basiert auf sehr guten Ergebnissen in der Klinik, weshalb die Zulassung aus der Ferne lediglich als Formsache erscheint. Da ich bisher keinen Haken gefunden habe, bin ich in den letzten 2 Wochen massiv eingestiegen (ca. 35% am Gesamtdepot, 50% Exelixis, 15% cash):
Abaloparatide was associated with an 86% reduction in vertebral fracture incidence — the primary end point — compared with placebo.
While that effect was similar to the 80% reduction in vertebral-fracture rate seen with the currently available osteoanabolic PTHrP analog teriparatide (Forteo, Eli Lilly), abaloparatide produced significantly greater reductions in nonvertebral fractures compared with both placebo and teriparatide. Moreover, abaloparatide was associated with significantly less hypercalcemia than was teriparatide.
ML hat ein aktuelles Kursziel von knapp USD60 - ich erwarte auf 12 Monate etwas mehr, und hoffe auf eine Verdoppelung (USD70) in dieser Zeit!
Merrill Lynch Has 3 Top BioPharma Picks to Win From the Aging of America
By Jon C. Ogg May 10, 2016 7:45 am EDT
....
Radius Health
Radius Health Inc. (NASDAQ: RDUS) is also a Merrill Lynch Buy-rated speculative company with a “high” longevity exposure. Its $58.00 price objective was almost 75% above the $33.28 share price. Merrill Lynch’s most recent call was on May 5 and addressed a data display delay due to post-terror security issues in Belgium. The firm believes that Radius offers an attractive risk/reward profile for investors. The firm said:
The company’s lead pipeline asset, abaloparatide, should reach the U.S. and E.U. markets in 2016/2017 and could generate peak sales of roughly $1.5 billion.
Radius Health reported earnings just in the prior week for this report. The company disclosed that it had $439.8 million in cash and cash equivalents at the end of its first quarter. Radius’ CEO Robert Ward said at that time:
We are extremely pleased to have submitted our first New Drug Application to the U.S. FDA for abaloparatide-SC for the treatment of postmenopausal osteoporosis and our MAA is currently under review in Europe. In anticipation of our first potential launch, we are developing our commercial plans and building our marketing organization in the U.S. To maximize the potential of this new investigational drug outside the U.S., we are continuing our productive partnering discussions and anticipate entering into a marketing collaboration prior to a potential first commercial launch.
Radius has a consensus analyst target of $59.83, and its 52-week range is $24.75 to $84.64.
By Jon C. Ogg
Abaloparatide was associated with an 86% reduction in vertebral fracture incidence — the primary end point — compared with placebo.
While that effect was similar to the 80% reduction in vertebral-fracture rate seen with the currently available osteoanabolic PTHrP analog teriparatide (Forteo, Eli Lilly), abaloparatide produced significantly greater reductions in nonvertebral fractures compared with both placebo and teriparatide. Moreover, abaloparatide was associated with significantly less hypercalcemia than was teriparatide.
ML hat ein aktuelles Kursziel von knapp USD60 - ich erwarte auf 12 Monate etwas mehr, und hoffe auf eine Verdoppelung (USD70) in dieser Zeit!
Merrill Lynch Has 3 Top BioPharma Picks to Win From the Aging of America
By Jon C. Ogg May 10, 2016 7:45 am EDT
....
Radius Health
Radius Health Inc. (NASDAQ: RDUS) is also a Merrill Lynch Buy-rated speculative company with a “high” longevity exposure. Its $58.00 price objective was almost 75% above the $33.28 share price. Merrill Lynch’s most recent call was on May 5 and addressed a data display delay due to post-terror security issues in Belgium. The firm believes that Radius offers an attractive risk/reward profile for investors. The firm said:
The company’s lead pipeline asset, abaloparatide, should reach the U.S. and E.U. markets in 2016/2017 and could generate peak sales of roughly $1.5 billion.
Radius Health reported earnings just in the prior week for this report. The company disclosed that it had $439.8 million in cash and cash equivalents at the end of its first quarter. Radius’ CEO Robert Ward said at that time:
We are extremely pleased to have submitted our first New Drug Application to the U.S. FDA for abaloparatide-SC for the treatment of postmenopausal osteoporosis and our MAA is currently under review in Europe. In anticipation of our first potential launch, we are developing our commercial plans and building our marketing organization in the U.S. To maximize the potential of this new investigational drug outside the U.S., we are continuing our productive partnering discussions and anticipate entering into a marketing collaboration prior to a potential first commercial launch.
Radius has a consensus analyst target of $59.83, and its 52-week range is $24.75 to $84.64.
By Jon C. Ogg
Antwort auf Beitrag Nr.: 52.513.754 von cyberhexe123 am 01.06.16 00:09:55Ob die Zulassung von abaloparatide nur Formsache ist, kann ich nicht beurteilen.
Aber ein Haken ist vielleicht folgendes Statement der EMA aus 2014:
"The Committee agreed with the request of the applicant to be exempt from performing studies in
children from birth to less than 18 years of age, because the Committee concluded that this medicinal
product is likely to be not safe for the treatment of osteoporosis in children.
The Committee came to this conclusion, because abaloparatide has shown carcinogenicity in animals."
Sta
Aber ein Haken ist vielleicht folgendes Statement der EMA aus 2014:
"The Committee agreed with the request of the applicant to be exempt from performing studies in
children from birth to less than 18 years of age, because the Committee concluded that this medicinal
product is likely to be not safe for the treatment of osteoporosis in children.
The Committee came to this conclusion, because abaloparatide has shown carcinogenicity in animals."
Sta
Antwort auf Beitrag Nr.: 52.513.952 von frank-p am 01.06.16 02:46:37Die erhöhte Kanzerogenität im Tierversuch wurde in verschiedenen wissenschaftlichen Arbeiten thematisiert wie zB
http://www.criver.com/files/pdfs/nonsource/asbrm_2014_bone_t…
In der Langzeit-Karzinogenitätsstudie nach OECD451 werden Versuchstiere (Ratte oder Maus) über einen großen Teil ihrer Lebenszeit mit der Prüfsubstanz exponiert, um eine erhöhte Häufigkeit einer Tumorerkrankung festzustellen. Problematisch ist, dass es beim Nager-Karzinogenitätstest zahlreiche Stoffe gibt, die ausschliesslich bei diesen Krebs auslösen, aber nicht bei anderen Säugern, so dass sich nicht jeder positive Befund auf den Menschen übertragen lässt. Allerdings sind ALLE identifizierten Human-Karzinogene im Menschen auch in Ratten krebserregend, weshalb die erhöhte Tumorinzidenz im OECD451 sicherlich ein Thema ist im Zulassunsprozedere von abaloparatide. Eine ähnliche Tumorrate (die genauen Zahlen hab ich nicht im Kopf, werden aber evaluiert) wurde allerdings auch bei Teriparatide (dies ist der Wirkstoff im derzeitigen SOC, brand Forsteo) beobachtet, so dass dieser Haken letztendlich nicht zur Ablehnung führen sollte, jedoch eine Beschränkung der Anwendungsdauer zur Folge haben könnte.
Sehr guter Hinweis! Findet jemand weitere Haken?
http://www.criver.com/files/pdfs/nonsource/asbrm_2014_bone_t…
In der Langzeit-Karzinogenitätsstudie nach OECD451 werden Versuchstiere (Ratte oder Maus) über einen großen Teil ihrer Lebenszeit mit der Prüfsubstanz exponiert, um eine erhöhte Häufigkeit einer Tumorerkrankung festzustellen. Problematisch ist, dass es beim Nager-Karzinogenitätstest zahlreiche Stoffe gibt, die ausschliesslich bei diesen Krebs auslösen, aber nicht bei anderen Säugern, so dass sich nicht jeder positive Befund auf den Menschen übertragen lässt. Allerdings sind ALLE identifizierten Human-Karzinogene im Menschen auch in Ratten krebserregend, weshalb die erhöhte Tumorinzidenz im OECD451 sicherlich ein Thema ist im Zulassunsprozedere von abaloparatide. Eine ähnliche Tumorrate (die genauen Zahlen hab ich nicht im Kopf, werden aber evaluiert) wurde allerdings auch bei Teriparatide (dies ist der Wirkstoff im derzeitigen SOC, brand Forsteo) beobachtet, so dass dieser Haken letztendlich nicht zur Ablehnung führen sollte, jedoch eine Beschränkung der Anwendungsdauer zur Folge haben könnte.
Sehr guter Hinweis! Findet jemand weitere Haken?
Antwort auf Beitrag Nr.: 52.513.952 von frank-p am 01.06.16 02:46:37
Bei intensiver Recherche aus der Nähe findet man selbstverständlich einige kritische Punkte, die jedoch auch beim aktuellen Standard beobachtet werden. Da dieses Standardmedikament zugelassen ist und abaloparatide gegenüber teriparatide ein statistisch signifikant besseres Ergebnis bei nicht die Wirbelsäule betreffenden Frakturen vorweisen kann, scheint eine Zulassung wahrscheinlich zu sein.
Deswegen bitte die vollständige Aussage zitieren:
Der Zulassungsantrag basiert auf sehr guten Ergebnissen in der Klinik, weshalb die Zulassung aus der Ferne lediglich als Formsache erscheint.
Zitat von frank-p: Ob die Zulassung von abaloparatide nur Formsache ist, kann ich nicht beurteilen.
Bei intensiver Recherche aus der Nähe findet man selbstverständlich einige kritische Punkte, die jedoch auch beim aktuellen Standard beobachtet werden. Da dieses Standardmedikament zugelassen ist und abaloparatide gegenüber teriparatide ein statistisch signifikant besseres Ergebnis bei nicht die Wirbelsäule betreffenden Frakturen vorweisen kann, scheint eine Zulassung wahrscheinlich zu sein.
Deswegen bitte die vollständige Aussage zitieren:
Der Zulassungsantrag basiert auf sehr guten Ergebnissen in der Klinik, weshalb die Zulassung aus der Ferne lediglich als Formsache erscheint.
BB Biotech hat ca. 4.5% des Anlagevermögens in Radius investiert - die Schweizer Biotechinvestoren/analysten scheinen an das Potenzial von Radius zu glauben:
http://www.bbbiotech.ch/de/bb-biotech/strategie-portfolio/po…
Radius ist ein Unternehmen mit Schwerpunkt Frauengesundheit. Sein führender Produktkandidat ist das subkutan verabreichte synthetische humane PTHrP-Analog Abaloparitid. Abaloparitid hat die Studienphase III für die postmenopausale Osteoporose (PMO) erfolgreich abgeschlossen. Das Arzneimittel hat sich in einer 18-monatigen Phase-III-Studie als wirksamer als Forsteo von Lilly erwiesen. In der Studie kam es bei Frauen zu einer frühen Risikoreduktion bei grossen Frakturen. Bei ihnen kam es zu 55% weniger Frakturen als bei Frauen, die Forsteo erhielten. Der schnellere Wirkungseintritt und der Rückgang von Frakturen ausserhalb der Wirbel wie beispielsweise an Hüfte und Handgelenk gegenüber Forsteo sind deutliche Unterscheidungsmerkmale und dürften Abaloparitid einen erheblichen Marktanteil bescheren. Zudem entwickelt Radius eine Formulierung als transdermales Pflaster (in Zusammenarbeit mit 3M), das die Compliance und Ergebnisse bei Frauen mit dieser Erkrankung erheblich verbessern könnte. Unser Hauptaugenmerk für 2016 liegt auf dem Fortschritt mit dem transdermalen Pflaster sowie auf der Einreichung der SQ-Studie der Phase III bei der FDA im 1. Quartal. Die Europäische Arzneimittelagentur hat die Einreichung bereits genehmigt. Beide Zulassungen werden im Laufe des Jahres 2016 erwartet. Darüber befindet sich der selektive Östrogen-Rezeptor- Degrader (SERD) RAD1901 des Unternehmens in der Prüfung für Östrogenrezeptor- positiven Brustkrebs. Das Mittel hat bei gesunden Probanden ein ansprechendes Sicherheitsprofil gezeigt. Die ersten Patientendaten waren vielversprechend, jedoch in einem sehr frühen Stadium. Wir warten im Jahr 2016 auf weitere Daten der Phase I, um mehr über das Profil der Substanz zu erfahren.
http://www.bbbiotech.ch/de/bb-biotech/strategie-portfolio/po…
Radius ist ein Unternehmen mit Schwerpunkt Frauengesundheit. Sein führender Produktkandidat ist das subkutan verabreichte synthetische humane PTHrP-Analog Abaloparitid. Abaloparitid hat die Studienphase III für die postmenopausale Osteoporose (PMO) erfolgreich abgeschlossen. Das Arzneimittel hat sich in einer 18-monatigen Phase-III-Studie als wirksamer als Forsteo von Lilly erwiesen. In der Studie kam es bei Frauen zu einer frühen Risikoreduktion bei grossen Frakturen. Bei ihnen kam es zu 55% weniger Frakturen als bei Frauen, die Forsteo erhielten. Der schnellere Wirkungseintritt und der Rückgang von Frakturen ausserhalb der Wirbel wie beispielsweise an Hüfte und Handgelenk gegenüber Forsteo sind deutliche Unterscheidungsmerkmale und dürften Abaloparitid einen erheblichen Marktanteil bescheren. Zudem entwickelt Radius eine Formulierung als transdermales Pflaster (in Zusammenarbeit mit 3M), das die Compliance und Ergebnisse bei Frauen mit dieser Erkrankung erheblich verbessern könnte. Unser Hauptaugenmerk für 2016 liegt auf dem Fortschritt mit dem transdermalen Pflaster sowie auf der Einreichung der SQ-Studie der Phase III bei der FDA im 1. Quartal. Die Europäische Arzneimittelagentur hat die Einreichung bereits genehmigt. Beide Zulassungen werden im Laufe des Jahres 2016 erwartet. Darüber befindet sich der selektive Östrogen-Rezeptor- Degrader (SERD) RAD1901 des Unternehmens in der Prüfung für Östrogenrezeptor- positiven Brustkrebs. Das Mittel hat bei gesunden Probanden ein ansprechendes Sicherheitsprofil gezeigt. Die ersten Patientendaten waren vielversprechend, jedoch in einem sehr frühen Stadium. Wir warten im Jahr 2016 auf weitere Daten der Phase I, um mehr über das Profil der Substanz zu erfahren.
schaut gut aus:
ich rechne mit einer Zulassung von abaloparatide in des US und in der EU
https://biz.yahoo.com/e/160602/rdus8-k.html
Falls die Zulassung erteilt wird und die prognostizierten Umsatzzahlen annähernd erreicht werden, wird sich die MC von RDUS relativ schnell verdoppeln!
ich rechne mit einer Zulassung von abaloparatide in des US und in der EU
https://biz.yahoo.com/e/160602/rdus8-k.html
Falls die Zulassung erteilt wird und die prognostizierten Umsatzzahlen annähernd erreicht werden, wird sich die MC von RDUS relativ schnell verdoppeln!
Antwort auf Beitrag Nr.: 52.528.958 von cyberhexe123 am 02.06.16 18:50:48Danke für deine informativen Beiträge, Hexe.
Radius Health steht schon seit langem auf meiner Watchlist, bin damals über BB Biotech auf die Aktie aufmerksam geworden. Im Prinzip teile ich deine Einschätzungen, stufe die Zulassungswahrscheinlichkeit in USA und der EU jeweils als extrem hoch ein. Ob es zu einer Verdopplung des Kursniveaus kommt, wage ich nicht zu beurteilen, jedenfalls sollte aber eine deutliche Steigerung drin sein ;-)
Viele Grüße
Radius Health steht schon seit langem auf meiner Watchlist, bin damals über BB Biotech auf die Aktie aufmerksam geworden. Im Prinzip teile ich deine Einschätzungen, stufe die Zulassungswahrscheinlichkeit in USA und der EU jeweils als extrem hoch ein. Ob es zu einer Verdopplung des Kursniveaus kommt, wage ich nicht zu beurteilen, jedenfalls sollte aber eine deutliche Steigerung drin sein ;-)
Viele Grüße
Antwort auf Beitrag Nr.: 52.529.135 von biopadawan am 02.06.16 19:17:37
bin auch via BB Biotech auf das Unternehmen aufmerksam geworden, vor allem durch den Umfang der Investition.
Eine Kursverdoppelung (von USD35 seit Threadbeginn) auf 12 Monate halte ich für realistisch, weil...
1.) der Spitzenumsatz von abaloparatide durchweg um die USD 1 Milliarde prognostiziert wurde und die ersten Umsatzzahlen diese Prognose unterstützen
Johanna Bennett am17.8.2015:
"We see Abalo peak sales at $1.1B WW."
BofA am 2.2.2015:
"Analyst Ying Huang notes Phase 3 trial for lead pipeline asset, abaloparatide, was positive and the company plans to submit for approval in the U.S and EU in the second half of 2015, suggesting approvals in 2H16. They expect peak sales to surpass Eli Lilly's Forteo at $1.4 billion."
und
2.) die klinischen Ergebnisse eines Konkurrenzproduktes von Amgen überraschend weniger gut ausgefallen sind wie erwartet:
Douglas W. House, SA News Edito am 22.2.2016
"Radius Health (NASDAQ:RDUS) is up 20% premarket on increased volume in reaction to Amgen's announcement of Phase 3 data for its osteoporosis candidate romosozumab that showed a 73% reduction in the risk of vertebral fracture in postmenopausal women.
Radius' candidate, abaloparatide, showed an 83% reduction in vertebral fracture in its Phase 3 ACTIVE study. Its marketing application is currently under review in Europe. It expects to file its NDA in the U.S. in the near future."
Robin Reyes am 22.2.2016
"Shares of Radius Health (NASDAQ:RDUS) are up 26% Monday after Amgen (AMGN) said its similar osteoporosis candidate, romosozumab, showed a 73% reduction in the risk of vertebral fracture, versus a 83% reduction from Radius Health’s candidate abaloparatide."
Zitat von biopadawan: Danke für deine informativen Beiträge, Hexe.
Radius Health steht schon seit langem auf meiner Watchlist, bin damals über BB Biotech auf die Aktie aufmerksam geworden. Im Prinzip teile ich deine Einschätzungen, stufe die Zulassungswahrscheinlichkeit in USA und der EU jeweils als extrem hoch ein. Ob es zu einer Verdopplung des Kursniveaus kommt, wage ich nicht zu beurteilen, jedenfalls sollte aber eine deutliche Steigerung drin sein ;-)
Viele Grüße
bin auch via BB Biotech auf das Unternehmen aufmerksam geworden, vor allem durch den Umfang der Investition.
Eine Kursverdoppelung (von USD35 seit Threadbeginn) auf 12 Monate halte ich für realistisch, weil...
1.) der Spitzenumsatz von abaloparatide durchweg um die USD 1 Milliarde prognostiziert wurde und die ersten Umsatzzahlen diese Prognose unterstützen
Johanna Bennett am17.8.2015:
"We see Abalo peak sales at $1.1B WW."
BofA am 2.2.2015:
"Analyst Ying Huang notes Phase 3 trial for lead pipeline asset, abaloparatide, was positive and the company plans to submit for approval in the U.S and EU in the second half of 2015, suggesting approvals in 2H16. They expect peak sales to surpass Eli Lilly's Forteo at $1.4 billion."
und
2.) die klinischen Ergebnisse eines Konkurrenzproduktes von Amgen überraschend weniger gut ausgefallen sind wie erwartet:
Douglas W. House, SA News Edito am 22.2.2016
"Radius Health (NASDAQ:RDUS) is up 20% premarket on increased volume in reaction to Amgen's announcement of Phase 3 data for its osteoporosis candidate romosozumab that showed a 73% reduction in the risk of vertebral fracture in postmenopausal women.
Radius' candidate, abaloparatide, showed an 83% reduction in vertebral fracture in its Phase 3 ACTIVE study. Its marketing application is currently under review in Europe. It expects to file its NDA in the U.S. in the near future."
Robin Reyes am 22.2.2016
"Shares of Radius Health (NASDAQ:RDUS) are up 26% Monday after Amgen (AMGN) said its similar osteoporosis candidate, romosozumab, showed a 73% reduction in the risk of vertebral fracture, versus a 83% reduction from Radius Health’s candidate abaloparatide."
Antwort auf Beitrag Nr.: 52.540.196 von cyberhexe123 am 04.06.16 07:57:13 1.) der Spitzenumsatz von abaloparatide durchweg um die USD 1 Milliarde prognostiziert wurde und die ersten Umsatzzahlen diese Prognose unterstützen
eigentlich war der 2. Halbsatz als Einschränkung gedacht:
1.) der Spitzenumsatz von abaloparatide durchweg um die USD 1 Milliarde prognostiziert wurde...falls die ersten Umsatzzahlen diese Prognose unterstützen!
sorry
Gruss zurück
eigentlich war der 2. Halbsatz als Einschränkung gedacht:
1.) der Spitzenumsatz von abaloparatide durchweg um die USD 1 Milliarde prognostiziert wurde...falls die ersten Umsatzzahlen diese Prognose unterstützen!
sorry
Gruss zurück
Antwort auf Beitrag Nr.: 52.540.208 von cyberhexe123 am 04.06.16 08:01:49
Interessanter Beitrag aus einem wissenschaftlichen Journal, welcher die Wirksamkeit von abaloparatide bei der Remineralisierung der Knochen bestätigt.
Mein Investment in diese Aktie wird nun sukzessive ausgebaut. Bei Zulassung (Zulassungswahrscheinlichkeit sehr hoch) und entsprechendem Markteintritt müsste mittelfristig eine Kursverdoppelung möglich sein .
Calcif Tissue Int. 2016 Jul 9. [Epub ahead of print]
Six Weeks of Daily Abaloparatide Treatment Increased Vertebral and Femoral Bone Mineral Density, Microarchitecture and Strength in Ovariectomized Osteopenic Rats.
Bahar H1, Gallacher K1, Downall J1, Nelson CA1, Shomali M1, Hattersley G2.
Author information
Abstract
Abaloparatide is a novel, potent and selective activator of parathyroid hormone receptor 1 (PTHR1) under clinical development for the treatment of osteoporosis. We assessed the effect of 6 weeks of abaloparatide on bone mass, microarchitecture, quality and strength in ovariectomized (OVX) rats. After 8 weeks of post-surgical bone depletion (baseline), OVX rats (n = 20-21/group) received daily subcutaneous vehicle (OVX-Veh) or abaloparatide at 5 or 20 µg/kg. Sham-operated control rats (n = 24) received vehicle. Areal bone mineral density (aBMD) of the lumbar spine (L4), total femur and femur diaphysis was measured at baseline and after 6 weeks of treatment. Femur and vertebral bone architecture and mechanical properties were assessed at the end of the treatment phase. At baseline, OVX-Veh rats exhibited significantly lower aBMD relative to Sham controls. Treatment of OVX rats with abaloparatide at 5 or 20 µg/kg/day increased aBMD dose-dependently in the lumbar spine, total femur and femur diaphysis to levels exceeding OVX-Veh or Sham controls. The abaloparatide 5 and 20 µg/kg groups had improved trabecular microarchitecture relative to OVX vehicle, with trabecular BV/TV exceeding OVX-Veh control values by 57 and 78 % (respectively) at the lumbar spine, and by 145 and 270 % at the distal femur. Femur diaphyseal cortical volume and thickness were significantly greater in the abaloparatide 20 µg/kg group relative to OVX vehicle or Sham controls. Bone strength parameters of the femur diaphysis, femur neck and L4 vertebra were significantly improved in the OVX-ABL groups relative to OVX-Veh controls. Bone mass-strength relationships and estimated intrinsic strength properties suggested maintained or improved bone quality with abaloparatide. These data demonstrate skeletal restoration via abaloparatide treatment of osteopenic OVX rats, in association with improved trabecular microarchitecture, cortical geometry and bone strength at sites that have clinical relevance in patients with osteoporosis.
Interessanter Beitrag aus einem wissenschaftlichen Journal, welcher die Wirksamkeit von abaloparatide bei der Remineralisierung der Knochen bestätigt.
Mein Investment in diese Aktie wird nun sukzessive ausgebaut. Bei Zulassung (Zulassungswahrscheinlichkeit sehr hoch) und entsprechendem Markteintritt müsste mittelfristig eine Kursverdoppelung möglich sein .
Calcif Tissue Int. 2016 Jul 9. [Epub ahead of print]
Six Weeks of Daily Abaloparatide Treatment Increased Vertebral and Femoral Bone Mineral Density, Microarchitecture and Strength in Ovariectomized Osteopenic Rats.
Bahar H1, Gallacher K1, Downall J1, Nelson CA1, Shomali M1, Hattersley G2.
Author information
Abstract
Abaloparatide is a novel, potent and selective activator of parathyroid hormone receptor 1 (PTHR1) under clinical development for the treatment of osteoporosis. We assessed the effect of 6 weeks of abaloparatide on bone mass, microarchitecture, quality and strength in ovariectomized (OVX) rats. After 8 weeks of post-surgical bone depletion (baseline), OVX rats (n = 20-21/group) received daily subcutaneous vehicle (OVX-Veh) or abaloparatide at 5 or 20 µg/kg. Sham-operated control rats (n = 24) received vehicle. Areal bone mineral density (aBMD) of the lumbar spine (L4), total femur and femur diaphysis was measured at baseline and after 6 weeks of treatment. Femur and vertebral bone architecture and mechanical properties were assessed at the end of the treatment phase. At baseline, OVX-Veh rats exhibited significantly lower aBMD relative to Sham controls. Treatment of OVX rats with abaloparatide at 5 or 20 µg/kg/day increased aBMD dose-dependently in the lumbar spine, total femur and femur diaphysis to levels exceeding OVX-Veh or Sham controls. The abaloparatide 5 and 20 µg/kg groups had improved trabecular microarchitecture relative to OVX vehicle, with trabecular BV/TV exceeding OVX-Veh control values by 57 and 78 % (respectively) at the lumbar spine, and by 145 and 270 % at the distal femur. Femur diaphyseal cortical volume and thickness were significantly greater in the abaloparatide 20 µg/kg group relative to OVX vehicle or Sham controls. Bone strength parameters of the femur diaphysis, femur neck and L4 vertebra were significantly improved in the OVX-ABL groups relative to OVX-Veh controls. Bone mass-strength relationships and estimated intrinsic strength properties suggested maintained or improved bone quality with abaloparatide. These data demonstrate skeletal restoration via abaloparatide treatment of osteopenic OVX rats, in association with improved trabecular microarchitecture, cortical geometry and bone strength at sites that have clinical relevance in patients with osteoporosis.
Antwort auf Beitrag Nr.: 52.870.141 von Cyberhexe am 20.07.16 06:42:28
Hallo,
Mal eine, quasi Amateur-, Frage.
Bedeutet dass das tatsächlich diese "brüchigen"(?)/porösen Knochen sozusagen wieder gesunder, belastbarer(...) u.ä. werden?
(habe damit indirekt etwas Erfahrung, und würde das schon als eine ziemlich, ziemlich bescheuerte Krankheit sehen(und würde damit bestätigen dass für so ein Mittel iMo prinzipiell eine Menge Absatz/Nachfragemöglichkeiten bestehen dürfte)
Fiele mir schwer vorzustellen, fände ich aber umso beeindruckender.
Könntest Du, wenn möglich, das vielleicht mal in einfach verständlichen Worten erklären wie da die Grundmechanismen sind, es funktioniert?
Wenn Dir das zu blöd ist, die Latte so tief zu legen, kann ich verstehen,
dann einfach lassen.
Gruß
P.
Zitat von Cyberhexe: Interessanter Beitrag aus einem wissenschaftlichen Journal, welcher die Wirksamkeit von abaloparatide bei der Remineralisierung der Knochen bestätigt.
Hallo,
Mal eine, quasi Amateur-, Frage.
Bedeutet dass das tatsächlich diese "brüchigen"(?)/porösen Knochen sozusagen wieder gesunder, belastbarer(...) u.ä. werden?
(habe damit indirekt etwas Erfahrung, und würde das schon als eine ziemlich, ziemlich bescheuerte Krankheit sehen(und würde damit bestätigen dass für so ein Mittel iMo prinzipiell eine Menge Absatz/Nachfragemöglichkeiten bestehen dürfte)
Fiele mir schwer vorzustellen, fände ich aber umso beeindruckender.
Könntest Du, wenn möglich, das vielleicht mal in einfach verständlichen Worten erklären wie da die Grundmechanismen sind, es funktioniert?
Wenn Dir das zu blöd ist, die Latte so tief zu legen, kann ich verstehen,
dann einfach lassen.
Gruß
P.
Kaufkurs am 30.5.16 USD 35,45...aktueller Kurs USD 56,75
Kursziel nach Zulassung von abaloparatide in US and EU > USD 100!
Kursziel nach Zulassung von abaloparatide in US and EU > USD 100!
Antwort auf Beitrag Nr.: 52.940.995 von Popeye82 am 28.07.16 21:05:29Osteoporosediagnostik ist mehr als nur Knochendichtemessung., und dennoch ist die Dichte ein wichtiger Parameter --> mit abnehmender Knochendichte steigt die Gefahr einer Fraktur!
Antwort auf Beitrag Nr.: 52.512.431 von cyberhexe123 am 31.05.16 20:36:47
Zwischenbilanz (Vgl. zu EXEL=blau):

Zitat von cyberhexe123: ...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben.
Zwischenbilanz (Vgl. zu EXEL=blau):
PS: Dass RDUS ab jetzt besser als EXEL läuft ist sehr wahrscheinlich...
Antwort auf Beitrag Nr.: 53.298.528 von Ville7 am 18.09.16 13:43:04...und wieder einmal, wie so oft, ein Beitrag mit dem Prädikat "Besonders wertvoll"! 
und um nicht in dieselbe Kategorie abzutauchen, auch noch etwas zum Thema:
BBBiotech, einer der grössten Biotech-Investoren in Europa, hält derzeit über 5% an RDUS und berichtet im Internet folgendermassen über dieses Unternehmen:
"Radius ist ein Unternehmen mit Schwerpunkt Frauengesundheit. Sein führender Produktkandidat ist das subkutan verabreichte synthetische humane PTHrP-Analog Abaloparitid. Abaloparitid hat die Studienphase III für die postmenopausale Osteoporose (PMO) erfolgreich abgeschlossen. Das Arzneimittel hat sich in einer 18-monatigen Phase-III-Studie als wirksamer als Forsteo von Lilly erwiesen. In der Studie kam es bei Frauen zu einer frühen Risikoreduktion bei grossen Frakturen. Bei ihnen kam es zu 55% weniger Frakturen als bei Frauen, die Forsteo erhielten. Der schnellere Wirkungseintritt und der Rückgang von Frakturen ausserhalb der Wirbel wie beispielsweise an Hüfte und Handgelenk gegenüber Forsteo sind deutliche Unterscheidungsmerkmale und dürften Abaloparitid einen erheblichen Marktanteil bescheren. Zudem entwickelt Radius eine Formulierung als transdermales Pflaster (in Zusammenarbeit mit 3M), das die Compliance und Ergebnisse bei Frauen mit dieser Erkrankung erheblich verbessern könnte. Unser Hauptaugenmerk für 2016 liegt auf dem Fortschritt mit dem transdermalen Pflaster sowie auf der Einreichung der SQ-Studie der Phase III bei der FDA im 1. Quartal. Die Europäische Arzneimittelagentur hat die Einreichung bereits genehmigt. Beide Zulassungen werden im Laufe des Jahres 2016 erwartet. Darüber befindet sich der selektive Östrogen-Rezeptor- Degrader (SERD) RAD1901 des Unternehmens in der Prüfung für Östrogenrezeptor- positiven Brustkrebs. Das Mittel hat bei gesunden Probanden ein ansprechendes Sicherheitsprofil gezeigt. Die ersten Patientendaten waren vielversprechend, jedoch in einem sehr frühen Stadium. Wir warten im Jahr 2016 auf weitere Daten der Phase I, um mehr über das Profil der Substanz zu erfahren."

und um nicht in dieselbe Kategorie abzutauchen, auch noch etwas zum Thema:
BBBiotech, einer der grössten Biotech-Investoren in Europa, hält derzeit über 5% an RDUS und berichtet im Internet folgendermassen über dieses Unternehmen:
"Radius ist ein Unternehmen mit Schwerpunkt Frauengesundheit. Sein führender Produktkandidat ist das subkutan verabreichte synthetische humane PTHrP-Analog Abaloparitid. Abaloparitid hat die Studienphase III für die postmenopausale Osteoporose (PMO) erfolgreich abgeschlossen. Das Arzneimittel hat sich in einer 18-monatigen Phase-III-Studie als wirksamer als Forsteo von Lilly erwiesen. In der Studie kam es bei Frauen zu einer frühen Risikoreduktion bei grossen Frakturen. Bei ihnen kam es zu 55% weniger Frakturen als bei Frauen, die Forsteo erhielten. Der schnellere Wirkungseintritt und der Rückgang von Frakturen ausserhalb der Wirbel wie beispielsweise an Hüfte und Handgelenk gegenüber Forsteo sind deutliche Unterscheidungsmerkmale und dürften Abaloparitid einen erheblichen Marktanteil bescheren. Zudem entwickelt Radius eine Formulierung als transdermales Pflaster (in Zusammenarbeit mit 3M), das die Compliance und Ergebnisse bei Frauen mit dieser Erkrankung erheblich verbessern könnte. Unser Hauptaugenmerk für 2016 liegt auf dem Fortschritt mit dem transdermalen Pflaster sowie auf der Einreichung der SQ-Studie der Phase III bei der FDA im 1. Quartal. Die Europäische Arzneimittelagentur hat die Einreichung bereits genehmigt. Beide Zulassungen werden im Laufe des Jahres 2016 erwartet. Darüber befindet sich der selektive Östrogen-Rezeptor- Degrader (SERD) RAD1901 des Unternehmens in der Prüfung für Östrogenrezeptor- positiven Brustkrebs. Das Mittel hat bei gesunden Probanden ein ansprechendes Sicherheitsprofil gezeigt. Die ersten Patientendaten waren vielversprechend, jedoch in einem sehr frühen Stadium. Wir warten im Jahr 2016 auf weitere Daten der Phase I, um mehr über das Profil der Substanz zu erfahren."
Radius Announces Publication of Additional Positive Results from the Phase 3 ACTIVE Trial of Abaloparatide-SC in JBMR
Results show consistency of Abaloparatide-SC responses across a wide range of patient subgroups
WALTHAM, Mass., Sept. 18, 2016 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that additional positive results from the Phase 3 ACTIVE (Abaloparatide Comparator Trial In Vertebral Endpoints) trial were published in the Journal of Bone and Mineral Research (JBMR).
In the article "Effects of Abaloparatide-SC on Fracture and Bone Mineral Density in Subgroups of Postmenopausal Women with Osteoporosis and Varying Baseline Risk Factors" JBMR 2016 Sept 9 [Epub ahead of print] patients in the ACTIVE trial were stratified into prespecified subgroups of baseline risk factors, inclusive of BMD, prior fracture history and age, to determine the consistency of the response for abaloparatide-SC versus placebo. http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/epdf
"Results from the Phase 3 ACTIVE trial show that abaloparatide-SC may provide substantial benefit for a broad range of postmenopausal women with osteoporosis irrespective of their baseline risk factors, including age and prior fracture history," said Dr. Felicia Cosman, M.D., osteoporosis specialist and Medical Director of the Clinical Research Center at Helen Hayes Hospital, Senior Clinical Director of the National Osteoporosis Foundation, Professor of Medicine at Columbia University, consultant to Radius and lead author of the paper. "These data are important for the large number of postmenopausal women who may be at risk of a fracture and show that anabolic therapy could provide more consistent, potent and early benefits and may be the most efficient way for these patients to achieve ultimate bone mineral density goals."
"We are pleased to have these findings published in JBMR, as well as the opportunity to present additional scientific information about abaloparatide-SC as part of the American Society of Bone and Mineral Research 2016 Annual Meeting," said Dr. Lorraine A. Fitzpatrick, Chief Medical Officer of Radius. "Approximately two million osteoporotic fractures occur annually in the U.S., which create physical and psychological burdens for those affected by diminishing their independence and quality of life. Radius Health is committed to pursuing new therapeutic options which have the potential to improve outcomes for these patients."
Abaloparatide is an investigational treatment for postmenopausal women with osteoporosis and its safety and efficacy have not been established. A Marketing Authorisation Application (MAA) for abaloparatide-SC for the treatment of patients with postmenopausal osteoporosis was validated and is currently undergoing regulatory review by the European Medicines Agency (EMA), and a New Drug Application (NDA) for abaloparatide is currently under review by the U.S. Food & Drug Administration (FDA).
Results show consistency of Abaloparatide-SC responses across a wide range of patient subgroups
WALTHAM, Mass., Sept. 18, 2016 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that additional positive results from the Phase 3 ACTIVE (Abaloparatide Comparator Trial In Vertebral Endpoints) trial were published in the Journal of Bone and Mineral Research (JBMR).
In the article "Effects of Abaloparatide-SC on Fracture and Bone Mineral Density in Subgroups of Postmenopausal Women with Osteoporosis and Varying Baseline Risk Factors" JBMR 2016 Sept 9 [Epub ahead of print] patients in the ACTIVE trial were stratified into prespecified subgroups of baseline risk factors, inclusive of BMD, prior fracture history and age, to determine the consistency of the response for abaloparatide-SC versus placebo. http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/epdf
"Results from the Phase 3 ACTIVE trial show that abaloparatide-SC may provide substantial benefit for a broad range of postmenopausal women with osteoporosis irrespective of their baseline risk factors, including age and prior fracture history," said Dr. Felicia Cosman, M.D., osteoporosis specialist and Medical Director of the Clinical Research Center at Helen Hayes Hospital, Senior Clinical Director of the National Osteoporosis Foundation, Professor of Medicine at Columbia University, consultant to Radius and lead author of the paper. "These data are important for the large number of postmenopausal women who may be at risk of a fracture and show that anabolic therapy could provide more consistent, potent and early benefits and may be the most efficient way for these patients to achieve ultimate bone mineral density goals."
"We are pleased to have these findings published in JBMR, as well as the opportunity to present additional scientific information about abaloparatide-SC as part of the American Society of Bone and Mineral Research 2016 Annual Meeting," said Dr. Lorraine A. Fitzpatrick, Chief Medical Officer of Radius. "Approximately two million osteoporotic fractures occur annually in the U.S., which create physical and psychological burdens for those affected by diminishing their independence and quality of life. Radius Health is committed to pursuing new therapeutic options which have the potential to improve outcomes for these patients."
Abaloparatide is an investigational treatment for postmenopausal women with osteoporosis and its safety and efficacy have not been established. A Marketing Authorisation Application (MAA) for abaloparatide-SC for the treatment of patients with postmenopausal osteoporosis was validated and is currently undergoing regulatory review by the European Medicines Agency (EMA), and a New Drug Application (NDA) for abaloparatide is currently under review by the U.S. Food & Drug Administration (FDA).
NEJM: Romosozumab Treatment in Postmenopausal Women with Osteoporosis
http://www.nejm.org/doi/full/10.1056/NEJMoa1607948Results
At 12 months, new vertebral fractures had occurred in 16 of 3321 patients (0.5%) in the romosozumab group, as compared with 59 of 3322 (1.8%) in the placebo group (representing a 73% lower risk with romosozumab; P<0.001). Clinical fractures had occurred in 58 of 3589 patients (1.6%) in the romosozumab group, as compared with 90 of 3591 (2.5%) in the placebo group (a 36% lower risk with romosozumab; P=0.008).
Abaloparatide zeigte eine 83% Risikoreduktion bei Wirbelsäulenfrakturen während romosozumab dieses Risiko lediglich um 73% reduzierte.
Bei den nicht die Wiebelsäule betreffenden Frakturen wurde bei romosozumab kein statistisch signifikanter Rückgang der Frakturen nachgewiesen:
Nonvertebral fractures had occurred in 56 of 3589 patients (1.6%) in the romosozumab group and in 75 of 3591 (2.1%) in the placebo group (P=0.10).
Bei Abalaoparatide hingegen schon - wenn auch knapp (0.049!):
The Kaplan-Meier estimated event rate for nonvertebral fracture was 2.7% for abaloparatide, 4.7% for placebo (RD, −2.01 [95% CI, −4.02 to −0.00]; hazard ratio [HR], 0.57 [95% CI, 0.32-1.00]; P = .049), and 3.3% for teriparatide. BMD increases were greater with abaloparatide than with placebo (all P < .001). Incidence of hypercalcemia was lower with abaloparatide (3.4%) than with teriparatide (6.4%) with an RD of −2.96 (95% CI, −5.12 to −0.87; P = .006).
Dieser statistisch signifikante Wirkungsnachweis bei den nicht die Wirbelsäule betreffenden Frakturen ist gegenüber Amgens romosozumab ein grosses Plus.
Effects of Abaloparatide-SC on Fractures and Bone Mineral Density
Anbei eine weitere Veröffentlichung in einem wissenschaftlichen Journal hinsichtlich der Wirksamkeit von Abaloparatide bei die Wirbelsäule betreffenden und nicht die Wirbelsäule betreffenden Frakturen in Folge einer Demineralisierung der Knochen.http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/abstrac…
Effects of Abaloparatide-SC on Fractures and Bone Mineral Density in Subgroups of Postmenopausal Women with Osteoporosis and Varying Baseline Risk Factors†
Authors
Accepted manuscript online: 9 September 2016
Abstract
Abaloparatide-SC is a novel 34–amino acid peptide created to be a potent and selective activator of the parathyroid hormone 1 (PTH1) receptor signaling pathway. In the Abaloparatide Comparator Trial In Vertebral Endpoints (ACTIVE) Phase 3 trial (NCT01343004) abaloparatide reduced new morphometric vertebral fractures by 86% compared with placebo (p < 0.001) and nonvertebral fractures by 43% (p = 0.049) in postmenopausal women with osteoporosis. Abaloparatide-SC increased bone mineral density (BMD) 3.4% at the total hip, 2.9% at the femoral neck, and 9.2% at the lumbar spine at 18 months (all p < 0.001 vs placebo). The analysis reported here was designed to evaluate whether fracture risk reductions and BMD accrual were consistent across different levels of baseline risk. Risk factor subgroups were predefined categorically for BMD T-score of the lumbar spine, total hip, and femoral neck (≤−2.5 vs >−2.5 and ≤-3.0 vs >-3.0), history of nonvertebral fracture (yes vs no), prevalent vertebral fracture (yes vs no), and age (<65 vs 65 to <75 vs ≥75 years old) at baseline. Forest plots show that there were no clinically meaningful interactions between any of the baseline risk factors and the treatment effect of abaloparatide-SC on new morphometric vertebral fractures, nonvertebral fractures, or BMD increases. Abaloparatide provides protection against fractures consistently across a wide variety of ages and baseline risks, including those with and without prior fractures, and it has potential utility for a broad group of postmenopausal women with osteoporosis.
die derzeitigen Übernahmespekulationen dienen der Kurspflege, sind jedoch nicht bestätigt:
Radius Health (RDUS) May Be Acquisition Target for Shire (SHPG) Based on Its Osteoporosis Pipeline
8/11/2016 2:04:27 PM
Shire close to deal for Radius Health
Oct 11 2016, 08:01 ET
The Fly reports that Shire plc (NASDAQ:SHPG) is closing in on a "multi-billion dollar" take out of biopharmaceutical firm Radius Health (NASDAQ:RDUS). Its lead product candidate is Abaloparatide-SC, under regulatory review for the treatment of osteoporosis.|
Radius Health (RDUS) May Be Acquisition Target for Shire (SHPG) Based on Its Osteoporosis Pipeline
8/11/2016 2:04:27 PM
Shire close to deal for Radius Health
Oct 11 2016, 08:01 ET
The Fly reports that Shire plc (NASDAQ:SHPG) is closing in on a "multi-billion dollar" take out of biopharmaceutical firm Radius Health (NASDAQ:RDUS). Its lead product candidate is Abaloparatide-SC, under regulatory review for the treatment of osteoporosis.|
Antwort auf Beitrag Nr.: 53.490.436 von Cyberhexe am 17.10.16 06:18:49
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
am 12.-15.12. findet die letzte 2016er-Sitzung des Arzneimittelausschusses CHMP der EMA statt. Vielleicht wird Abaloparatide doch noch in diesem Jahr zur Zulassung empfohlen.
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
am 12.-15.12. findet die letzte 2016er-Sitzung des Arzneimittelausschusses CHMP der EMA statt. Vielleicht wird Abaloparatide doch noch in diesem Jahr zur Zulassung empfohlen.
Antwort auf Beitrag Nr.: 53.795.628 von Cyberhexe am 29.11.16 21:30:19Heute chance zum nachkaufen
RAD1901 sieht beim Überfliegen der "positiven" Nachrichten eher wie ein künftiger Geldversenker mit wenig Potential aus...das ist die Erklärung für das heftige Abtauchen:
Radius Presents Positive Phase I Data for Investigational Drug RAD1901 at the San Antonio Breast Cancer Symposium (SABCS) 2016
-3 patients had confirmed partial responses by RECIST criteria from ongoing Phase I studies with RAD1901 in patients with advanced estrogen receptor positive breast cancer-
-In the Phase 1 dose escalation and expansion study, 14 heavily pretreated patients remained on RAD1901 for equal to or greater than 4 months, 5 for equal to or greater than 6 months, and 7 continued on study drug as of the October cut-off date-
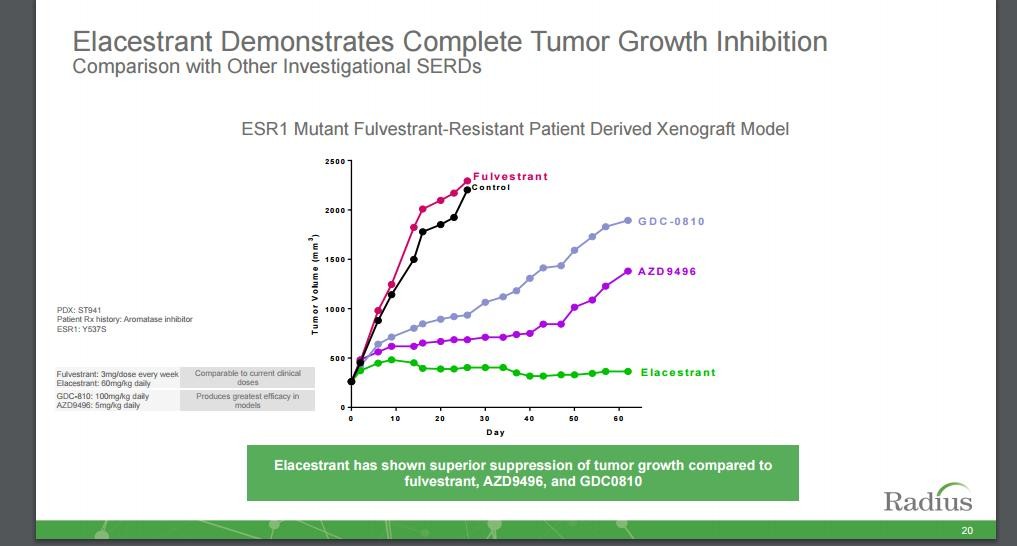
-46% of these patients previously received fulvestrant; 42% received palbociclib or another CDK inhibitor; 58% had an ESR1 mutation-
-Investor Webcast today at 8 pm CT with leading KOLs-
WALTHAM, Mass., Dec. 08, 2016 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a science-driven biopharmaceutical company focused on developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced data from two ongoing Phase 1 studies of RAD1901, an oral selective estrogen receptor degrader (SERD), in patients with estrogen receptor positive (ER+) breast cancer, which were presented this morning at the San Antonio Breast Cancer Symposium 2016.
As of the cut-off date of October 7, 2016, 20 patients have been treated in the RAD1901 Phase IB safety expansion cohort at the 400 mg dose. These patients are heavily pretreated ER+, HER2-negative advanced breast cancer patients who have received a median of 3 prior lines of therapy. Of the enrolled patients, 19 out of 20 had measurable disease at baseline and there were two confirmed partial responses by RECIST criteria. Across the Part A dose escalation (n=13) and safety expansion cohort (n=20), 14 patients were on study drug for greater than or equal to 4 months, 5 patients for greater than or equal to 6 months, and 7 patients remained on study drug. RAD1901 was well-tolerated with the most common adverse events being low grade nausea and dyspepsia.
In the ongoing European Phase I RAD1901 FES-PET trial, the first three-patients were enrolled at 400 mg as of the October 7th cut-off date and achieved a reduction in 18F-FES uptake ranging from 79%-91% at day 14 compared to baseline. One patient had a confirmed partial response by RECIST criteria. All three patients remained on study drug with mean duration of treatment of 5.64 cycles. Adverse events reported to date have been grade 1 and 2 and manageable. This study will enroll 5 additional patients in the 400 mg QD cohort followed by 8 patients in the 200 mg QD cohort. No dose limiting toxicities have been reported across any of the studies in the RAD1901 program.
"The single-agent clinical activity and duration of response demonstrated with RAD1901 in the heavily pretreated population may be important in addressing the major challenge of resistance facing patients with ER positive advanced breast cancer," said Dr. Virginia Kaklamani, Professor of Medicine, UT Health Science Center San Antonio, leader of the Breast Cancer Program, Cancer Therapy & Research Center, and investigator on the study.
"An oral, well-tolerated and effective SERD could become an important adjunct in combination therapy for patients and we look forward to the results of additional studies," said Professor George W. Sledge Jr., Professor and Chief of Medical Oncology at Stanford University Medical Center, and member of Radius' Oncology Clinical Advisory Board.
Dr. Virginia Kaklamani and Dr. George Sledge will participate in a Radius hosted investor meeting and webcast later today to highlight the RAD1901 data presented at SABCS at 8 p.m. CT. The webcast and a replay can be accessed on the company's website, www.radiuspharm.com.
The posters presented this morning from the RAD1901 clinical development program were:
Abstract Title: A Phase 1 Study of RAD1901, a Novel, Oral, Selective Estrogen Receptor Degrader, for the Treatment of ER-Positive Advanced Breast Cancer, Poster # 1454
Abstract Title: A Phase 1 Study of RAD1901, an Oral Selective Estrogen Receptor Degrader, to Determine Changes in the F-FES Uptake and Tumor Responses in ER-Positive, HER-2-Negative, Advanced Breast Cancer Patients, Poster # 1604
Radius will also present later the following poster later today from the RAD1901 preclinical program:
Abstract Title: RAD1901 Demonstrates Anti-Tumor Activity in Multiple Models of ER-Positive Breast Cancer Treatment Resistance, Poster # 1378
Poster Session 3
Session Title: Tumor Cell and Molecular Biology: Endocrine Therapy and Resistance
Session Date: 12/8/2016
Session Time: 5:00 PM — 7:00 PM
Location: Hall 1
Radius Presents Positive Phase I Data for Investigational Drug RAD1901 at the San Antonio Breast Cancer Symposium (SABCS) 2016
-3 patients had confirmed partial responses by RECIST criteria from ongoing Phase I studies with RAD1901 in patients with advanced estrogen receptor positive breast cancer-
-In the Phase 1 dose escalation and expansion study, 14 heavily pretreated patients remained on RAD1901 for equal to or greater than 4 months, 5 for equal to or greater than 6 months, and 7 continued on study drug as of the October cut-off date-
-46% of these patients previously received fulvestrant; 42% received palbociclib or another CDK inhibitor; 58% had an ESR1 mutation-
-Investor Webcast today at 8 pm CT with leading KOLs-
WALTHAM, Mass., Dec. 08, 2016 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a science-driven biopharmaceutical company focused on developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced data from two ongoing Phase 1 studies of RAD1901, an oral selective estrogen receptor degrader (SERD), in patients with estrogen receptor positive (ER+) breast cancer, which were presented this morning at the San Antonio Breast Cancer Symposium 2016.
As of the cut-off date of October 7, 2016, 20 patients have been treated in the RAD1901 Phase IB safety expansion cohort at the 400 mg dose. These patients are heavily pretreated ER+, HER2-negative advanced breast cancer patients who have received a median of 3 prior lines of therapy. Of the enrolled patients, 19 out of 20 had measurable disease at baseline and there were two confirmed partial responses by RECIST criteria. Across the Part A dose escalation (n=13) and safety expansion cohort (n=20), 14 patients were on study drug for greater than or equal to 4 months, 5 patients for greater than or equal to 6 months, and 7 patients remained on study drug. RAD1901 was well-tolerated with the most common adverse events being low grade nausea and dyspepsia.
In the ongoing European Phase I RAD1901 FES-PET trial, the first three-patients were enrolled at 400 mg as of the October 7th cut-off date and achieved a reduction in 18F-FES uptake ranging from 79%-91% at day 14 compared to baseline. One patient had a confirmed partial response by RECIST criteria. All three patients remained on study drug with mean duration of treatment of 5.64 cycles. Adverse events reported to date have been grade 1 and 2 and manageable. This study will enroll 5 additional patients in the 400 mg QD cohort followed by 8 patients in the 200 mg QD cohort. No dose limiting toxicities have been reported across any of the studies in the RAD1901 program.
"The single-agent clinical activity and duration of response demonstrated with RAD1901 in the heavily pretreated population may be important in addressing the major challenge of resistance facing patients with ER positive advanced breast cancer," said Dr. Virginia Kaklamani, Professor of Medicine, UT Health Science Center San Antonio, leader of the Breast Cancer Program, Cancer Therapy & Research Center, and investigator on the study.
"An oral, well-tolerated and effective SERD could become an important adjunct in combination therapy for patients and we look forward to the results of additional studies," said Professor George W. Sledge Jr., Professor and Chief of Medical Oncology at Stanford University Medical Center, and member of Radius' Oncology Clinical Advisory Board.
Dr. Virginia Kaklamani and Dr. George Sledge will participate in a Radius hosted investor meeting and webcast later today to highlight the RAD1901 data presented at SABCS at 8 p.m. CT. The webcast and a replay can be accessed on the company's website, www.radiuspharm.com.
The posters presented this morning from the RAD1901 clinical development program were:
Abstract Title: A Phase 1 Study of RAD1901, a Novel, Oral, Selective Estrogen Receptor Degrader, for the Treatment of ER-Positive Advanced Breast Cancer, Poster # 1454
Abstract Title: A Phase 1 Study of RAD1901, an Oral Selective Estrogen Receptor Degrader, to Determine Changes in the F-FES Uptake and Tumor Responses in ER-Positive, HER-2-Negative, Advanced Breast Cancer Patients, Poster # 1604
Radius will also present later the following poster later today from the RAD1901 preclinical program:
Abstract Title: RAD1901 Demonstrates Anti-Tumor Activity in Multiple Models of ER-Positive Breast Cancer Treatment Resistance, Poster # 1378
Poster Session 3
Session Title: Tumor Cell and Molecular Biology: Endocrine Therapy and Resistance
Session Date: 12/8/2016
Session Time: 5:00 PM — 7:00 PM
Location: Hall 1
Antwort auf Beitrag Nr.: 52.512.431 von cyberhexe123 am 31.05.16 20:36:47
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
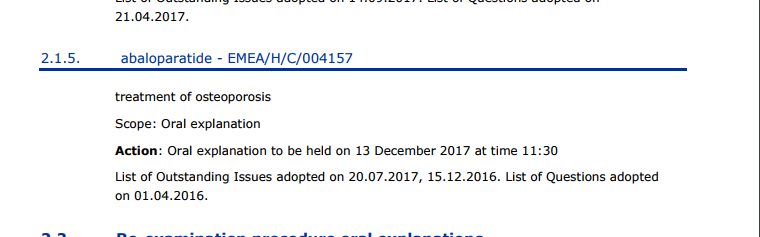
bin gespannt, ob die EMA grössere Schwierigkeiten macht bei der Liste der ausstehenden Fragen:
3.2.1.
- abaloparatide
- EMEA/H/C/004157
treatment of osteoporosis
Scope: Day 180 list of outstanding issue
Action
: For adoption
List of Questions adopted on 01.04.2016.
ich gehe nicht davon aus und hab deswegen RDUS nachgekauft...obschon´der Durchschnittskaufpreis damit erhöht wurde ;-))
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
bin gespannt, ob die EMA grössere Schwierigkeiten macht bei der Liste der ausstehenden Fragen:
3.2.1.
- abaloparatide
- EMEA/H/C/004157
treatment of osteoporosis
Scope: Day 180 list of outstanding issue
Action
: For adoption
List of Questions adopted on 01.04.2016.
ich gehe nicht davon aus und hab deswegen RDUS nachgekauft...obschon´der Durchschnittskaufpreis damit erhöht wurde ;-))
Antwort auf Beitrag Nr.: 53.878.741 von Cyberhexe am 12.12.16 21:55:57obschon Abaloparatide in 2016 nicht mehr zugelassen wird, bereitet RADIUS die Markteinführung in den USA konsequent vor --> es sind zig neue Stellen für Pharmavertreter ausgeschrieben:
https://careers-radiuspharm.icims.com/jobs/search?pr=1&brand…
In May 2016, Radius' new drug application ("NDA") in the United States for abaloparatide-SC for the treatment of postmenopausal women with osteoporosis was accepted for filing by the FDA and was granted a Prescription Drug User Fee Act (PDUFA) date of March 30, 2017. Radius' marketing authorisation application ("MAA") to the European Medicines Agency ("EMA"), was validated in December 2015 and is currently undergoing regulatory review. We anticipate a CHMP scientific opinion in late 2016 or 2017.
Falls keine offenen Fragen von der EMA konstatiert werden, dürfte der Arzneimittelausschuss CHMP der EMA Abaloparatide in seiner Januar-Sitzung zur Zulassung empfehlen,wonach die Kommission spätestens 67 Tage danach die Zulassung für Europa erteilen sollte. Diese könnte dann fast gleichzeitig mit der Zulassungsentscheidung in den USA erfolgen.
Die Bekanntgabe einer Kooperation für Europa im 1q2017 sollte den Kurs zudem positiv beeinflussen.
https://careers-radiuspharm.icims.com/jobs/search?pr=1&brand…
In May 2016, Radius' new drug application ("NDA") in the United States for abaloparatide-SC for the treatment of postmenopausal women with osteoporosis was accepted for filing by the FDA and was granted a Prescription Drug User Fee Act (PDUFA) date of March 30, 2017. Radius' marketing authorisation application ("MAA") to the European Medicines Agency ("EMA"), was validated in December 2015 and is currently undergoing regulatory review. We anticipate a CHMP scientific opinion in late 2016 or 2017.
Falls keine offenen Fragen von der EMA konstatiert werden, dürfte der Arzneimittelausschuss CHMP der EMA Abaloparatide in seiner Januar-Sitzung zur Zulassung empfehlen,wonach die Kommission spätestens 67 Tage danach die Zulassung für Europa erteilen sollte. Diese könnte dann fast gleichzeitig mit der Zulassungsentscheidung in den USA erfolgen.
Die Bekanntgabe einer Kooperation für Europa im 1q2017 sollte den Kurs zudem positiv beeinflussen.
Antwort auf Beitrag Nr.: 53.885.186 von Cyberhexe am 13.12.16 18:12:03Hab gestern im Laufe der Börsensitzung meine Position verdreifacht, weshalb RDUS nun in meinem Portfolio die stärkste Position darstellt.
Der gestrige bzw. wöchentliche Kursverlauf könnte durch eine Stop-Loss-Attacke der Leerverkäufer verursacht sein, die die aktuelle Sitzung des europ. Arzneimittelausschusses CHMP nutzen, um verunsicherte Marktteilnehmer bzw. deren durch Stop-Loss gesicherte Positionen abzuschöpfen. Falls doch unschöne Neuigkeiten bei dieser Sitzung zu verzeichnen sind (Bekanntgabe Morgen), dann habe ich mich dieses Mal verzockt. Ich bin mir jedoch fast sicher, dass dies nicht der Fall ist.
Radius bereitet die Markteinführung von abaloparatide konsequent vor und hat über 200 neue Stellen ausgeschrieben --> zB Clinical Sales Specialist - Denver S, CO
Der gestrige bzw. wöchentliche Kursverlauf könnte durch eine Stop-Loss-Attacke der Leerverkäufer verursacht sein, die die aktuelle Sitzung des europ. Arzneimittelausschusses CHMP nutzen, um verunsicherte Marktteilnehmer bzw. deren durch Stop-Loss gesicherte Positionen abzuschöpfen. Falls doch unschöne Neuigkeiten bei dieser Sitzung zu verzeichnen sind (Bekanntgabe Morgen), dann habe ich mich dieses Mal verzockt. Ich bin mir jedoch fast sicher, dass dies nicht der Fall ist.
Radius bereitet die Markteinführung von abaloparatide konsequent vor und hat über 200 neue Stellen ausgeschrieben --> zB Clinical Sales Specialist - Denver S, CO
Antwort auf Beitrag Nr.: 53.893.651 von Cyberhexe am 15.12.16 07:12:16Stock is weak .
Sehe es auch als kaufgelegenheit. Vielleicht auch year end selling.
Sehe es auch als kaufgelegenheit. Vielleicht auch year end selling.
Tax Loss selling könnte ein Argument für diese Kurse sein nachdem man am 31.12.2015 noch über 61 USD stand. Ebenso ist der ganze Biotech Sektor seit Wochen und Monaten auf der Kippe und die Indizes kursieren ständig um die 200 Tage- und 200 Wochen-Durchschnittslinien. Auch ein kräftiger Move nach unten ist da durchaus mal drin, da die generellen Biotech-Bewertungen weiterhin recht hoch erscheinen - wenn man die Bewertungsmaßstäbe vor 2010 an den Tag legt.
Für das CHMP Meeting der EMA vom 12. bis 15. Dezember gibt es noch keine Highlights oder Dokumente außer der Agenda.
Für das CHMP Meeting der EMA vom 12. bis 15. Dezember gibt es noch keine Highlights oder Dokumente außer der Agenda.
Antwort auf Beitrag Nr.: 53.926.310 von Ville7 am 20.12.16 17:45:31
falsch, die Highlights aus der Dezember-Sitzung des Arzneimittelausschusses stehen relativ schnell zur Verfügung --> seit Freitag 16.12.
http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_e…
...Abaloparatide bzw. deren "List of outstanding issue" wird jedoch nicht erwähnt, weshalb ich damit rechne, dass die Zulassungsentscheidung auf der Januarsitzung des Ausschusses (CHMP) auf der Agenda steht. Hab gestern nochmal nachgekauft --> bin jetzt bei über 50% Depotanteil.
Zitat von Ville7: Tax Loss selling könnte ein Argument für diese Kurse sein nachdem man am 31.12.2015 noch über 61 USD stand. Ebenso ist der ganze Biotech Sektor seit Wochen und Monaten auf der Kippe und die Indizes kursieren ständig um die 200 Tage- und 200 Wochen-Durchschnittslinien. Auch ein kräftiger Move nach unten ist da durchaus mal drin, da die generellen Biotech-Bewertungen weiterhin recht hoch erscheinen - wenn man die Bewertungsmaßstäbe vor 2010 an den Tag legt.
Für das CHMP Meeting der EMA vom 12. bis 15. Dezember gibt es noch keine Highlights oder Dokumente außer der Agenda.
falsch, die Highlights aus der Dezember-Sitzung des Arzneimittelausschusses stehen relativ schnell zur Verfügung --> seit Freitag 16.12.
http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_e…
...Abaloparatide bzw. deren "List of outstanding issue" wird jedoch nicht erwähnt, weshalb ich damit rechne, dass die Zulassungsentscheidung auf der Januarsitzung des Ausschusses (CHMP) auf der Agenda steht. Hab gestern nochmal nachgekauft --> bin jetzt bei über 50% Depotanteil.
Antwort auf Beitrag Nr.: 53.929.498 von Cyberhexe am 21.12.16 08:40:42...Abaloparatide bzw. deren "List of outstanding issue" wird jedoch nicht erwähnt, weshalb ich damit rechne, dass die Zulassungsentscheidung]auf der Januarsitzung des Ausschusses (CHMP) auf der Agenda steht. Hab gestern nochmal nachgekauft --> bin jetzt bei über 50% Depotanteil.
...da ist mir ein kleiner Fehler unterflaufen, es sollte "Zulassungsempfehlung" heissen, weil letztendlich nicht der Arzneimittelausschuss (CHMP) die Zulassungsentscheidung trifft sondern die Europäische Kommission, und zwar spätestens 67 Tage nach der Empfehlung des CHMP.
...da ist mir ein kleiner Fehler unterflaufen, es sollte "Zulassungsempfehlung" heissen, weil letztendlich nicht der Arzneimittelausschuss (CHMP) die Zulassungsentscheidung trifft sondern die Europäische Kommission, und zwar spätestens 67 Tage nach der Empfehlung des CHMP.
Antwort auf Beitrag Nr.: 53.929.498 von Cyberhexe am 21.12.16 08:40:42Jetzt weiß ich wieso ich das nicht gesehen hab. Wenn ich mit meinem Handybrowser auf die Seite gehe (http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/d…), dann sind die Highlights vom 12-15. im kleinstmöglichen Zeichensatz und somit gar nicht erkennbar. Mit dem PC ist's sichtbar.
Generell werden Questions wohl nicht in den Highlights adressiert. Es bleibt somit eine Spekulation, ob alle Fragen hinreichend beantwortet werden konnten. Komisch, dass die Beantwortung der Fragen so lange dauert. Eigentlich hätten sie binnen 180 Tage beantwortet/bearbeitet sein müssen. Vom Zeitpunkt der Fragen bis zum letzten CHMP Meeting mit den Fragen auf der Agenda waren es aber fast 240 Tage.
Wie ist deine Einschätzung hierzu? Besteht hier nicht die Gefahr potentieller Probleme in den Fragen-Inhalten?
Generell werden Questions wohl nicht in den Highlights adressiert. Es bleibt somit eine Spekulation, ob alle Fragen hinreichend beantwortet werden konnten. Komisch, dass die Beantwortung der Fragen so lange dauert. Eigentlich hätten sie binnen 180 Tage beantwortet/bearbeitet sein müssen. Vom Zeitpunkt der Fragen bis zum letzten CHMP Meeting mit den Fragen auf der Agenda waren es aber fast 240 Tage.
Wie ist deine Einschätzung hierzu? Besteht hier nicht die Gefahr potentieller Probleme in den Fragen-Inhalten?
Antwort auf Beitrag Nr.: 53.933.246 von Ville7 am 21.12.16 16:23:32am 17.11.2015 wurde der Zulassungsantrag für Abaloparatide SC zur Behandlung der Osteoporose bei "postmenopausalen Frauen" (also nach Erreichen der Menopause) bei der EMA eingereicht, welcher am 4.12.2015 formal angenommen wurde (= Tag 1 des Zulassungsprozedere). Nach Beendigung der 1. Evaluationsphase (nach 120 Tagen = Tag 120) wird dem Antragsteller eine "List of Questions" zugestellt und gleichzeitig, bis zur Beantwortung dieser Fragen, die Uhr angehalten (Clock stop). Die Unterbrechung bzw. die Zeit zur Beantwortung dieser Fragen ist normalerweise auf 3 Monate begrenzt. RADIUS hat allerdings eine Verlängerung beantragt, welche im Protokoll der Maisitzung des CHMP (23.-26.5.2016) bekanntgegeben wurde: "The CHMP agreed to the request by the applicant for an extension to the clock stop to respond to the Day 120 List of Questions adopted in April 2016."
Mittlerweile sind diese Fragen beantwortet und der Zulassungsprozess wieder gestartet. Nun, in der Dezembersitzung des CHMP, waren die "Outstanding Issues" zu Abaloparatide auf der Agenda - diese werden am Tag 180 dem Antragsteller zugestellt. Falls eine Anhörung erforderlich ist, gibt es eine 2. Unterbrechung (Clock stop) und die Uhr wird erst wieder am Tag dieser Anhörung "angestellt". Gibt es keine Anhörung, dann läuft die Uhr weiter und der Arzneimittelausschuss hat am Tag 210 seine Empfehlung (Zulassung ja/nein) abzugeben.
Ich erwarte deswegen in der Januarsitzung --> Committee for Medicinal Products for Human Use (CHMP): 23-26 January 2017
eine Entscheidung über die Empfehlung (positiv oder negativ). Lediglich Mängel in der Liefer- bzw. Produktionskette könnten eine positive Zulassungsempfehlung verhindern, weil in der Klinik, aus meiner Perspektive zumindest, ein grosser Benefit in Relation zu den Nebenwirkungen nachgewiesen wurde. Oder hat jemand einen schwer wiegenden Mangel entdeckt?
Die endgültige Zulassungsentscheidung wird spätestens am Tag 277 von der Europäischen Kommission bekannt gegeben --> Final Commission Decision
Mittlerweile sind diese Fragen beantwortet und der Zulassungsprozess wieder gestartet. Nun, in der Dezembersitzung des CHMP, waren die "Outstanding Issues" zu Abaloparatide auf der Agenda - diese werden am Tag 180 dem Antragsteller zugestellt. Falls eine Anhörung erforderlich ist, gibt es eine 2. Unterbrechung (Clock stop) und die Uhr wird erst wieder am Tag dieser Anhörung "angestellt". Gibt es keine Anhörung, dann läuft die Uhr weiter und der Arzneimittelausschuss hat am Tag 210 seine Empfehlung (Zulassung ja/nein) abzugeben.
Ich erwarte deswegen in der Januarsitzung --> Committee for Medicinal Products for Human Use (CHMP): 23-26 January 2017
eine Entscheidung über die Empfehlung (positiv oder negativ). Lediglich Mängel in der Liefer- bzw. Produktionskette könnten eine positive Zulassungsempfehlung verhindern, weil in der Klinik, aus meiner Perspektive zumindest, ein grosser Benefit in Relation zu den Nebenwirkungen nachgewiesen wurde. Oder hat jemand einen schwer wiegenden Mangel entdeckt?
Die endgültige Zulassungsentscheidung wird spätestens am Tag 277 von der Europäischen Kommission bekannt gegeben --> Final Commission Decision
Antwort auf Beitrag Nr.: 53.935.949 von Cyberhexe am 21.12.16 22:39:12
Ich habe keinen schwerwiegenden Mangel entdeckt. Die Wirksamkeit ist gut, die Krebs-Gefahren gibt es auch bei Forteo.
Zwei Dinge stören mich allerdings am Potential:
1. Es ist eine tägliche Injektion notwendig. Das ist für viele Patienten (und auch Ärzte) eine gewaltige Hürde. Es gibt Denosumab von Amgen, das nur alle 6 Monate verabreicht werden muss. Auch wenn Denosumab nicht ganz so wirksam ist wie das Produkt von Radius wird es Radius schwer haben gegen diese Convenience zu bestehen. Man kann bei Radius nur hoffen, dass man das Pflaster mit ner Bioequivalence Studie schnell an den Markt bekommt.
2. Bei Radius werden ~240 Vertriebsstellen nur in USA ausgeschrieben. So eine mega Vertriebsmannschaft habe ich noch nie gesehen für ein einziges Produkt. Das bedeutet, dass der Vertrieb sehr teuer wird und die Marge stark darunter leiden wird.
Wenn Radius wirklich vor Vermarktungsstart ex-US Partner präsentieren kann, dann wird man anhand des Vetrages und der Summen / Royalties abschätzen können, wie der künftige Partner das Potential einschätzt. Das gibt eine ganz gute Indikation des künftigen Potentials.
Zitat von Cyberhexe: Oder hat jemand einen schwer wiegenden Mangel entdeckt?
Ich habe keinen schwerwiegenden Mangel entdeckt. Die Wirksamkeit ist gut, die Krebs-Gefahren gibt es auch bei Forteo.
Zwei Dinge stören mich allerdings am Potential:
1. Es ist eine tägliche Injektion notwendig. Das ist für viele Patienten (und auch Ärzte) eine gewaltige Hürde. Es gibt Denosumab von Amgen, das nur alle 6 Monate verabreicht werden muss. Auch wenn Denosumab nicht ganz so wirksam ist wie das Produkt von Radius wird es Radius schwer haben gegen diese Convenience zu bestehen. Man kann bei Radius nur hoffen, dass man das Pflaster mit ner Bioequivalence Studie schnell an den Markt bekommt.
2. Bei Radius werden ~240 Vertriebsstellen nur in USA ausgeschrieben. So eine mega Vertriebsmannschaft habe ich noch nie gesehen für ein einziges Produkt. Das bedeutet, dass der Vertrieb sehr teuer wird und die Marge stark darunter leiden wird.
Wenn Radius wirklich vor Vermarktungsstart ex-US Partner präsentieren kann, dann wird man anhand des Vetrages und der Summen / Royalties abschätzen können, wie der künftige Partner das Potential einschätzt. Das gibt eine ganz gute Indikation des künftigen Potentials.
Weiterer Punkt (Kosten / Daten von 2011):
Bisphosphonate kosten 200 bis 400 EUR je Jahr.
Denosumab kostet 550 EUR je Jahr.
Teriparatid kostet 7000 EUR je Jahr.
Abaloparatide-SC wird somit sicherlich > 7000 EUR je Jahr kosten.
http://www.akdae.de/Arzneimitteltherapie/WA/Archiv/Denosumab…
Ich finde leider auch keine klinische Aussage wie wirksam die Biophosphonate, der absolute SoC zur Zeit, gegenüber Teriparatid oder Abaloparatide-SC sind...
Bisphosphonate kosten 200 bis 400 EUR je Jahr.
Denosumab kostet 550 EUR je Jahr.
Teriparatid kostet 7000 EUR je Jahr.
Abaloparatide-SC wird somit sicherlich > 7000 EUR je Jahr kosten.
http://www.akdae.de/Arzneimitteltherapie/WA/Archiv/Denosumab…
Ich finde leider auch keine klinische Aussage wie wirksam die Biophosphonate, der absolute SoC zur Zeit, gegenüber Teriparatid oder Abaloparatide-SC sind...
Antwort auf Beitrag Nr.: 53.936.975 von Ville7 am 22.12.16 08:08:59ich würde Abaloparatide eher mit Eli Lillys "Forteo" (Teriparatide) vergleichen, da diese beiden Aktivsubstanzen durch einen ähnlichen Wirkungsmechanismus charakterisiert werden.
Forteo-Umsätze in Milliarden USD
2013: 1.245
2014: 1.322
2015: 1.348
Amgen erzielt mit Prolia (Denosumab) übrigens in etwa ähnliche Umsätze:
1q2015: 272m USD
1q2016: 352m USD
Vergleicht man nun die Wirksamkeit von Abaloparatide mit Teriparatide, dann ist diese bei Abaloparatide weitaus günstiger, weil unter Abaloparatide auch bei den nicht die Wirbelsäule betreffenden Frakturen eine statistisch signifikante Verbesserung nachgewiesen wurde:
"Results were reported at the Endocrine Society conference in March 2015 [Miller et al. 2015]. They showed that abaloparatide reduced the rate of new vertebral fractures to only 0.58%, compared with a 4.2% rate seen among placebo patients (a reduction of 86%; p < 0.0001). The rate was reduced to 0.84% in the teriparatide group (an 80% reduction compared with placebo; p < 0.0001). For nonvertebral fractures, abaloparatide produced a 43% reduction compared with placebo (2.7% versus 4.7%, respectively; p = 0.0489), and a 45% reduction in clinical fractures was seen (3.9% versus 8.3% with placebo; p = 0.0112). There was no significant difference in the rate of nonvertebral and clinical fractures in the teriparatide and placebo groups (p = 0.2157 and 0.1127, respectively)."
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4707418/
Auch Amgens neuer Antikörper "Romosozumab " zur Behandlung der Osteporose kann diesbezüglich nicht mit Abaloparatide mithalten:
"However, the secondary endpoint of reducing the incidence of non-vertebral fractures through months 12 and 24 was not met."
http://www.amgen.com/media/news-releases/2016/02/amgen-and-u…
Blockbuster-Potenzial für Abaloparatide ist vorhanden, zumal die transdermale Applikation via Pflaster den Nachteil in der Anwendung ausgleichen wird. Die aktuelle Martkapitalisierung lässt auf alle Fälle Luft nach oben. Ich erwarte im Januar eine positive Empfehlung des Arzneimittelausschusses CHMP, wonach relativ zeitnah ein europäischer Vertriebspartner vorgestellt werden dürfte. Bin mal gespannt, wer das Rennen machen wird. Der Kurs sollte dann relativ zügig in die Nähe von USD60 aufsteigen.
Forteo-Umsätze in Milliarden USD
2013: 1.245
2014: 1.322
2015: 1.348
Amgen erzielt mit Prolia (Denosumab) übrigens in etwa ähnliche Umsätze:
1q2015: 272m USD
1q2016: 352m USD
Vergleicht man nun die Wirksamkeit von Abaloparatide mit Teriparatide, dann ist diese bei Abaloparatide weitaus günstiger, weil unter Abaloparatide auch bei den nicht die Wirbelsäule betreffenden Frakturen eine statistisch signifikante Verbesserung nachgewiesen wurde:
"Results were reported at the Endocrine Society conference in March 2015 [Miller et al. 2015]. They showed that abaloparatide reduced the rate of new vertebral fractures to only 0.58%, compared with a 4.2% rate seen among placebo patients (a reduction of 86%; p < 0.0001). The rate was reduced to 0.84% in the teriparatide group (an 80% reduction compared with placebo; p < 0.0001). For nonvertebral fractures, abaloparatide produced a 43% reduction compared with placebo (2.7% versus 4.7%, respectively; p = 0.0489), and a 45% reduction in clinical fractures was seen (3.9% versus 8.3% with placebo; p = 0.0112). There was no significant difference in the rate of nonvertebral and clinical fractures in the teriparatide and placebo groups (p = 0.2157 and 0.1127, respectively)."
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4707418/
Auch Amgens neuer Antikörper "Romosozumab " zur Behandlung der Osteporose kann diesbezüglich nicht mit Abaloparatide mithalten:
"However, the secondary endpoint of reducing the incidence of non-vertebral fractures through months 12 and 24 was not met."
http://www.amgen.com/media/news-releases/2016/02/amgen-and-u…
Blockbuster-Potenzial für Abaloparatide ist vorhanden, zumal die transdermale Applikation via Pflaster den Nachteil in der Anwendung ausgleichen wird. Die aktuelle Martkapitalisierung lässt auf alle Fälle Luft nach oben. Ich erwarte im Januar eine positive Empfehlung des Arzneimittelausschusses CHMP, wonach relativ zeitnah ein europäischer Vertriebspartner vorgestellt werden dürfte. Bin mal gespannt, wer das Rennen machen wird. Der Kurs sollte dann relativ zügig in die Nähe von USD60 aufsteigen.
Antwort auf Beitrag Nr.: 53.936.975 von Ville7 am 22.12.16 08:08:59
zu 2.)
konservative Rechnung:
240 Stellen mal ca. USD 150.000 --> Kosten/a ca. 36Mio
Da kein Alleinstellungsmerkmal von Abaloparatide vorliegt, ist eine derartige Vertriebsmannschaft unbedingt erforderlich. um einen Blockbuster zu generieren. Leider funktioniert auch der Pharmamarkt ähnlich wie andere Märkte: ein nicht konkurrenzloses Produkt muss beworben werden, ansonsten bleibt der Erfolg aus.
Zitat von Ville7:Zitat von Cyberhexe: Oder hat jemand einen schwer wiegenden Mangel entdeckt?
Ich habe keinen schwerwiegenden Mangel entdeckt. Die Wirksamkeit ist gut, die Krebs-Gefahren gibt es auch bei Forteo.
Zwei Dinge stören mich allerdings am Potential:
1. Es ist eine tägliche Injektion notwendig. Das ist für viele Patienten (und auch Ärzte) eine gewaltige Hürde. Es gibt Denosumab von Amgen, das nur alle 6 Monate verabreicht werden muss. Auch wenn Denosumab nicht ganz so wirksam ist wie das Produkt von Radius wird es Radius schwer haben gegen diese Convenience zu bestehen. Man kann bei Radius nur hoffen, dass man das Pflaster mit ner Bioequivalence Studie schnell an den Markt bekommt.
2. Bei Radius werden ~240 Vertriebsstellen nur in USA ausgeschrieben. So eine mega Vertriebsmannschaft habe ich noch nie gesehen für ein einziges Produkt. Das bedeutet, dass der Vertrieb sehr teuer wird und die Marge stark darunter leiden wird.
Wenn Radius wirklich vor Vermarktungsstart ex-US Partner präsentieren kann, dann wird man anhand des Vetrages und der Summen / Royalties abschätzen können, wie der künftige Partner das Potential einschätzt. Das gibt eine ganz gute Indikation des künftigen Potentials.
zu 2.)
konservative Rechnung:
240 Stellen mal ca. USD 150.000 --> Kosten/a ca. 36Mio
Da kein Alleinstellungsmerkmal von Abaloparatide vorliegt, ist eine derartige Vertriebsmannschaft unbedingt erforderlich. um einen Blockbuster zu generieren. Leider funktioniert auch der Pharmamarkt ähnlich wie andere Märkte: ein nicht konkurrenzloses Produkt muss beworben werden, ansonsten bleibt der Erfolg aus.
Charttechnisch gesehen wären im positiven Falle Kurse bis 90 USD drin. Aktuell ist man an der Untergrenze eines Dreiecks, da sollte es natürlich nicht drunter gehen...
Symmetrisches Dreieck (Trendfolgeformation):
https://www.godmode-trader.de/know-how/1-9-2-symmetrisches-d…
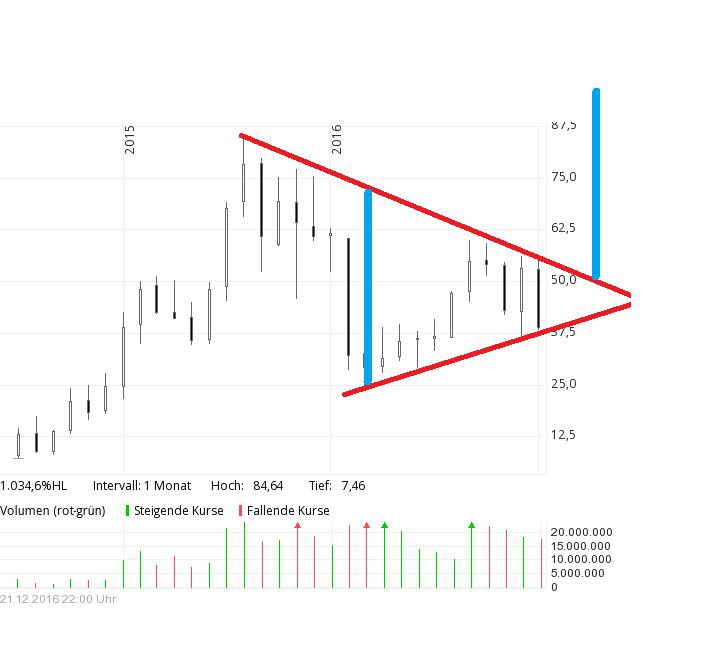
Symmetrisches Dreieck (Trendfolgeformation):
https://www.godmode-trader.de/know-how/1-9-2-symmetrisches-d…

Antwort auf Beitrag Nr.: 53.937.455 von Cyberhexe am 22.12.16 09:05:46
Stimmt das wirklich, dass Teripatide bei den non-vertrabal fractures keine signifikante Verbesserung zeigen konnte? Die Seite 51 des Investor days scheint diese Aussage zu widerlegen, dort steht "2.6% vs. 5.5% PBO, RRR 53% (p<0.05), @ 19 months" für FORTEO (Teripatide) bei den nicht Wirbelsäulen Brüchen:
http://files.shareholder.com/downloads/AMDA-1D3H6P/342662165…
Zitat von Cyberhexe: ....
Vergleicht man nun die Wirksamkeit von Abaloparatide mit Teriparatide, dann ist diese bei Abaloparatide weitaus günstiger, weil unter Abaloparatide auch bei den nicht die Wirbelsäule betreffenden Frakturen eine statistisch signifikante Verbesserung nachgewiesen wurde:
...
Stimmt das wirklich, dass Teripatide bei den non-vertrabal fractures keine signifikante Verbesserung zeigen konnte? Die Seite 51 des Investor days scheint diese Aussage zu widerlegen, dort steht "2.6% vs. 5.5% PBO, RRR 53% (p<0.05), @ 19 months" für FORTEO (Teripatide) bei den nicht Wirbelsäulen Brüchen:
http://files.shareholder.com/downloads/AMDA-1D3H6P/342662165…
Antwort auf Beitrag Nr.: 53.942.069 von Ville7 am 22.12.16 18:20:55Kann es sein, dass deine Aussage sich nur auf die ACTIVE Studie bezieht? Im Label von FORTEO aber was anderes und besseres für FORTEO steht.
Das ist schon wichtig, wenn man den Markterfolg einschätzen will.
Zudem erscheint mir Radius extremst bemüht sein ihre Produkte in einem mega guten Licht darzustellen, negatives wie z.B. die viel höhere Zahl an Treatmentabbrüchen (Discont.) bei Aba gegenüber Teri wird nicht erwähnt...
Das ist schon wichtig, wenn man den Markterfolg einschätzen will.
Zudem erscheint mir Radius extremst bemüht sein ihre Produkte in einem mega guten Licht darzustellen, negatives wie z.B. die viel höhere Zahl an Treatmentabbrüchen (Discont.) bei Aba gegenüber Teri wird nicht erwähnt...
Antwort auf Beitrag Nr.: 53.942.096 von Ville7 am 22.12.16 18:24:59in allen "face to face"-Studien, die ich gesichtet habe, ist das Ergebnis vorteilhaft für Abaloparatide z.B. auch bei der Mineralisierung der Knochen (Knochendichte):
http://press.endocrine.org/doi/10.1210/jc.2014-3718?url_ver=…
Effects of Abaloparatide, a Human Parathyroid Hormone-Related Peptide Analog, on Bone Mineral Density in Postmenopausal Women with Osteoporosis
Oct 2014
Conclusions:
Compared with placebo, 24 weeks of daily sc abaloparatide increases BMD of the lumbar spine, femoral neck, and total hip in a dose-dependent fashion. Moreover, the abaloparatide-induced BMD increases at the total hip are greater than with the marketed dose of teriparatide.
http://press.endocrine.org/doi/10.1210/jc.2014-3718?url_ver=…
Effects of Abaloparatide, a Human Parathyroid Hormone-Related Peptide Analog, on Bone Mineral Density in Postmenopausal Women with Osteoporosis
Oct 2014
Conclusions:
Compared with placebo, 24 weeks of daily sc abaloparatide increases BMD of the lumbar spine, femoral neck, and total hip in a dose-dependent fashion. Moreover, the abaloparatide-induced BMD increases at the total hip are greater than with the marketed dose of teriparatide.
Antwort auf Beitrag Nr.: 53.943.962 von Cyberhexe am 23.12.16 05:51:13Von grösster Bedeutung ist die "Berichterstattung" in den wissenschaftlichen Medien und nicht die Selbstdarstellung der einzelnen Unternehmen. Die vergleichende Wirkung von verschiedenen Konkurrenzprodukten ist zudem am aussagekrfäftigsten bei "face to face"-Studien wie zB in ACTIVE, so dass diese Ergebnisse als Entscheidungshilfen der Ärzteschaft bevorzugt werden.
Clin Cases Miner Bone Metab. 2016 May-Aug; 13(2): 106–109.
Published online 2016 Oct 5. doi: 10.11138/ccmbm/2016.13.2.106
PMCID: PMC5119706
Abaloparatide
Stefano Gonnelli and Carla Caffarelli
Author information ► Copyright and License information ►
Abaloparatide is an investigational analog of human PTHrP (1–34) being developed for the treatment of osteoporosis. The amino-acid sequence of abaloparatide is identical to that of PTHrP in the first 20 amino-acids, while over half of the remaining amino-acids are different. Some studies in animals and in humans reported that abaloparatide presented a potent anabolic activity with reduced effects on bone resorption as compared to that observed with teriparatide. This may be due to a more transient signaling response of abaloparatide related to differing affinities of the two drugs to the specific conformations of the PTH1 receptor. In the ACTIVE study, a phase 3 fracture prevention trial, 2460 postmenopausal osteoporotic women at high risk for fracture were randomized to receive 18-months of either daily abaloparatide 80 μg s.c., placebo or teriparatide 20 μg s.c. The reduction in vertebral fracture rate with respect to placebo was 86% in the abaloparatide group and 80% in the teriparatide group. Abaloparatide also produced a significant 43% reduction in the rate of nonvertebral fractures (2.7 vs 4.0% with placebo, p=0.04) whereas teriparatide determined a 28% reduction (2.9 vs 4.0% with placebo, p=NS). Abaloparatide or teriparatide showed similar increases in BMD at lumbar spine, while the patients of the abaloparatide group showed significantly greater increases in BMD at both total hip (4.18 vs 3.26%) and femoral neck (3.60 vs 2.66%). Therefore, if the preliminary data of the ACTIVE study is confirmed, abaloparatide may become an important option for the anabolic treatment of postmenopausal osteoporosis.
Clin Cases Miner Bone Metab. 2016 May-Aug; 13(2): 106–109.
Published online 2016 Oct 5. doi: 10.11138/ccmbm/2016.13.2.106
PMCID: PMC5119706
Abaloparatide
Stefano Gonnelli and Carla Caffarelli
Author information ► Copyright and License information ►
Abaloparatide is an investigational analog of human PTHrP (1–34) being developed for the treatment of osteoporosis. The amino-acid sequence of abaloparatide is identical to that of PTHrP in the first 20 amino-acids, while over half of the remaining amino-acids are different. Some studies in animals and in humans reported that abaloparatide presented a potent anabolic activity with reduced effects on bone resorption as compared to that observed with teriparatide. This may be due to a more transient signaling response of abaloparatide related to differing affinities of the two drugs to the specific conformations of the PTH1 receptor. In the ACTIVE study, a phase 3 fracture prevention trial, 2460 postmenopausal osteoporotic women at high risk for fracture were randomized to receive 18-months of either daily abaloparatide 80 μg s.c., placebo or teriparatide 20 μg s.c. The reduction in vertebral fracture rate with respect to placebo was 86% in the abaloparatide group and 80% in the teriparatide group. Abaloparatide also produced a significant 43% reduction in the rate of nonvertebral fractures (2.7 vs 4.0% with placebo, p=0.04) whereas teriparatide determined a 28% reduction (2.9 vs 4.0% with placebo, p=NS). Abaloparatide or teriparatide showed similar increases in BMD at lumbar spine, while the patients of the abaloparatide group showed significantly greater increases in BMD at both total hip (4.18 vs 3.26%) and femoral neck (3.60 vs 2.66%). Therefore, if the preliminary data of the ACTIVE study is confirmed, abaloparatide may become an important option for the anabolic treatment of postmenopausal osteoporosis.
Antwort auf Beitrag Nr.: 53.943.977 von Cyberhexe am 23.12.16 06:05:38ACTIVE ist übrigens eine sehr mächtige "face to face"-Studie, die Abaloparatide mit Teriparatide vergleicht:
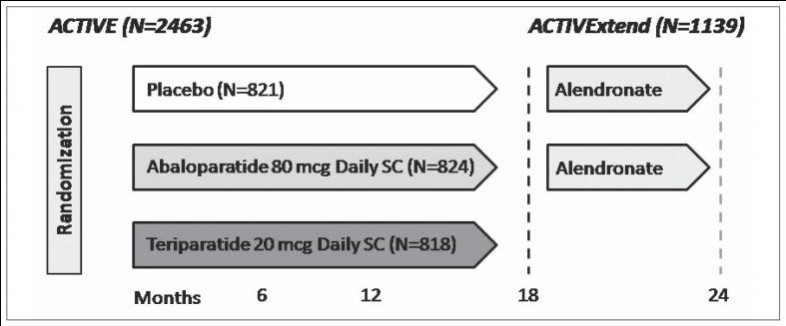

Antwort auf Beitrag Nr.: 53.943.992 von Cyberhexe am 23.12.16 06:22:40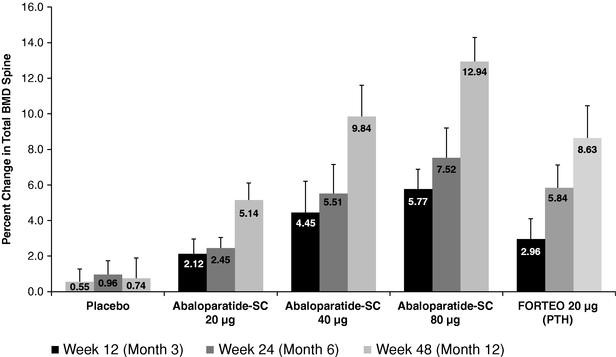
...die Mineralisierung ist unter abaloparatide eindeutig (dh statistisch signifikant) günstiger!

...die Mineralisierung ist unter abaloparatide eindeutig (dh statistisch signifikant) günstiger!
Antwort auf Beitrag Nr.: 53.952.158 von Cyberhexe am 24.12.16 17:14:47Die Grafik bezieht sich nur auf "spine" (Ruecken, Rueckgrat, Wirbelsauele). Wie sieht es mit anderen Knochenarten aus? Irgendwo hatte ich gelesen, dass Teri Aba teils in anderen Lnochenarten ueberlegen sei... finde nur die Quelle nicht mehr.
Antwort auf Beitrag Nr.: 53.952.158 von Cyberhexe am 24.12.16 17:14:47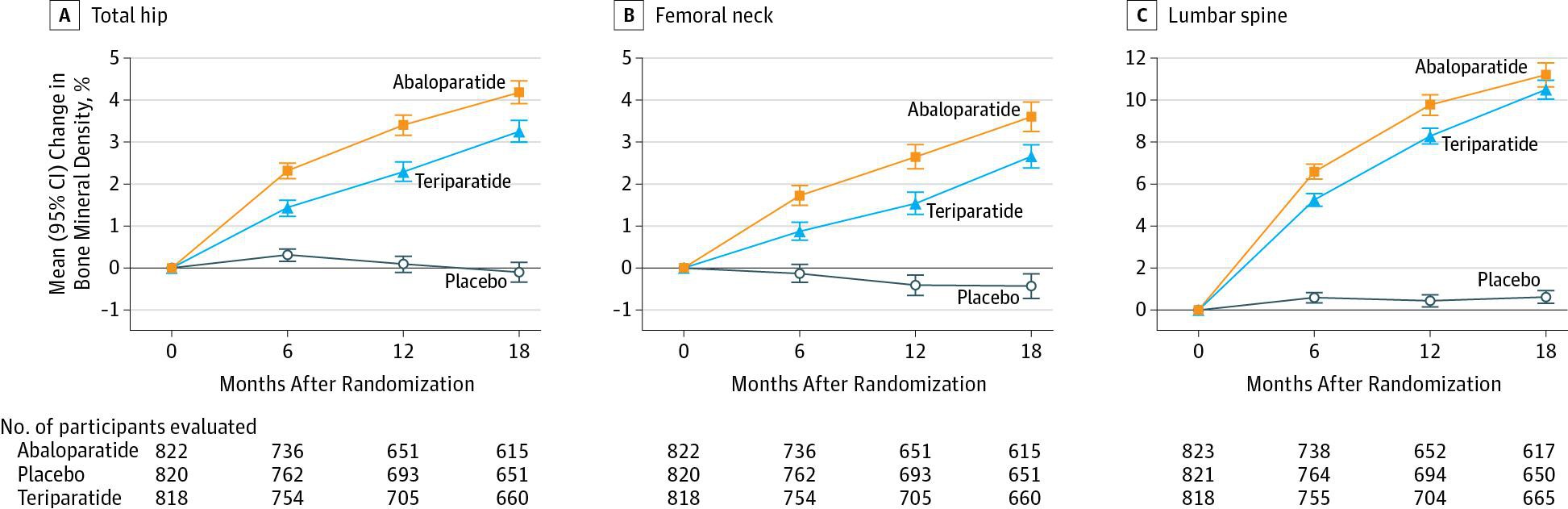

Antwort auf Beitrag Nr.: 53.952.668 von Cyberhexe am 25.12.16 07:40:07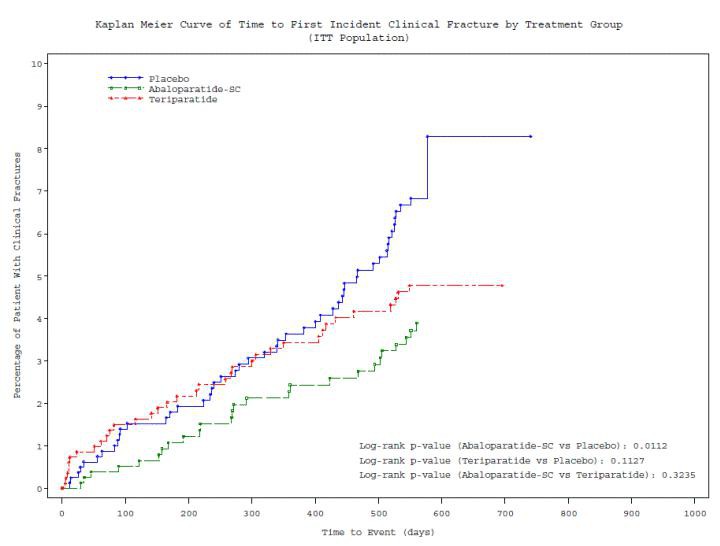
siehe auch ---> http://www.investorvillage.com/smbd.asp?mb=18024&mn=22&pt=ms…
....dort bin ich Alleinunterhalter - kein Interesse bei den Amis

siehe auch ---> http://www.investorvillage.com/smbd.asp?mb=18024&mn=22&pt=ms…
....dort bin ich Alleinunterhalter - kein Interesse bei den Amis

Antwort auf Beitrag Nr.: 53.952.668 von Cyberhexe am 25.12.16 07:40:07
Ich denke, die geäusserten Bedenken beziehen sich auf den im September veröffentlichten Bericht mit der folgenden Aussage:
Abaloparatide group: BMD at Total hip +3.52%, Femoral neck BMD +3.34%, Lumbar spine +8.72%
Teriparatide group: BMD at Total hip BMD +3.26%, Femoral Neck + 2.66, Lumbar spine +10.49%
As shown above (18-month Increases in BMD seen with Abaloparatide compared to Teriparatide), abaloparatide does appear to increase BMD in some areas a bit more than teriparatide, but in others, particularly the lumbar spine, teriparatide does better, so it’s a bit of a washout.
https://www.algaecal.com/expert-insights/the-new-osteoporosi…
--> die rot gedruckte Aussage, dass unter Teriparatide im Lendenwirbelbereich eine bessere Mineralisierung der Knochen stattfinden würde, konnte bisher in keinem wissenschaftlichen Bericht bestätigt werden und dürfte somit eine Falschaussage darstellen:
Hingegen lesen wir in wissenschaftlichen Veröffentlichungen wie zB in Clinical Cases in Mineral and Bone Metabolism --> Clin Cases Miner Bone Metab. 2016 May-Aug; 13(2): 106–109.
Published online 2016 Oct 5. doi: 10.11138/ccmbm/2016.13.2.106
Abaloparatide or teriparatide showed similar increases in BMD at lumbar spine, while the patients of the abaloparatide group showed significantly greater increases in BMD at both total hip (4.18 vs 3.26%) and femoral neck (3.60 vs 2.66%). Therefore, if the preliminary data of the ACTIVE study is confirmed, abaloparatide may become an important option for the anabolic treatment of postmenopausal osteoporosis.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5119706/
oder...
Bone-mineral density increased with both drugs compared with placebo at the spine, femoral neck, and hip at 6, 12, and 18 months (P < .0001 for all comparisons), but abaloparatide increased bone density significantly more than did teriparatide at the hip, femoral neck, and spine at most time points during the 18-month study, Dr Miller noted.
http://www.medscape.com/viewarticle/841015
oder...
BMD increases were greater with abaloparatide than with placebo (all P < .001). Incidence of hypercalcemia was lower with abaloparatide (3.4%) than with teriparatide (6.4%) with an RD of −2.96 (95% CI, −5.12 to −0.87; P = .006).
http://jamanetwork.com/journals/jama/article-abstract/254464…
Natürlich wird mit Abaloparatide das Rad nicht neu erfunden, denn dieser Wirkstoff ist lediglich eine Weiterentwicklung von Teriparatide, jedoch gerade bei den nicht die Wirbelsäule betreffenden Frakturen mit wesentlich besseren Ergebnissen und, um so erstaunlicher, auch wesentlich besser wie Amgens neu entwickelter Antikörper Romosozumab:
Romosozumab resulted in a 25 percent reduction compared to placebo in the relative risk of non-vertebral fractures through month 12, another secondary endpoint, but the reduced risk was not statistically significant (fracture incidence 1.6 percent versus 2.1 percent, respectively, [p=0.096]).
https://www.amgen.com/media/news-releases/2016/09/results-fr…
Zitat von Cyberhexe:
Ich denke, die geäusserten Bedenken beziehen sich auf den im September veröffentlichten Bericht mit der folgenden Aussage:
Abaloparatide group: BMD at Total hip +3.52%, Femoral neck BMD +3.34%, Lumbar spine +8.72%
Teriparatide group: BMD at Total hip BMD +3.26%, Femoral Neck + 2.66, Lumbar spine +10.49%
As shown above (18-month Increases in BMD seen with Abaloparatide compared to Teriparatide), abaloparatide does appear to increase BMD in some areas a bit more than teriparatide, but in others, particularly the lumbar spine, teriparatide does better, so it’s a bit of a washout.
https://www.algaecal.com/expert-insights/the-new-osteoporosi…
--> die rot gedruckte Aussage, dass unter Teriparatide im Lendenwirbelbereich eine bessere Mineralisierung der Knochen stattfinden würde, konnte bisher in keinem wissenschaftlichen Bericht bestätigt werden und dürfte somit eine Falschaussage darstellen:
Hingegen lesen wir in wissenschaftlichen Veröffentlichungen wie zB in Clinical Cases in Mineral and Bone Metabolism --> Clin Cases Miner Bone Metab. 2016 May-Aug; 13(2): 106–109.
Published online 2016 Oct 5. doi: 10.11138/ccmbm/2016.13.2.106
Abaloparatide or teriparatide showed similar increases in BMD at lumbar spine, while the patients of the abaloparatide group showed significantly greater increases in BMD at both total hip (4.18 vs 3.26%) and femoral neck (3.60 vs 2.66%). Therefore, if the preliminary data of the ACTIVE study is confirmed, abaloparatide may become an important option for the anabolic treatment of postmenopausal osteoporosis.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5119706/
oder...
Bone-mineral density increased with both drugs compared with placebo at the spine, femoral neck, and hip at 6, 12, and 18 months (P < .0001 for all comparisons), but abaloparatide increased bone density significantly more than did teriparatide at the hip, femoral neck, and spine at most time points during the 18-month study, Dr Miller noted.
http://www.medscape.com/viewarticle/841015
oder...
BMD increases were greater with abaloparatide than with placebo (all P < .001). Incidence of hypercalcemia was lower with abaloparatide (3.4%) than with teriparatide (6.4%) with an RD of −2.96 (95% CI, −5.12 to −0.87; P = .006).
http://jamanetwork.com/journals/jama/article-abstract/254464…
Natürlich wird mit Abaloparatide das Rad nicht neu erfunden, denn dieser Wirkstoff ist lediglich eine Weiterentwicklung von Teriparatide, jedoch gerade bei den nicht die Wirbelsäule betreffenden Frakturen mit wesentlich besseren Ergebnissen und, um so erstaunlicher, auch wesentlich besser wie Amgens neu entwickelter Antikörper Romosozumab:
Romosozumab resulted in a 25 percent reduction compared to placebo in the relative risk of non-vertebral fractures through month 12, another secondary endpoint, but the reduced risk was not statistically significant (fracture incidence 1.6 percent versus 2.1 percent, respectively, [p=0.096]).
https://www.amgen.com/media/news-releases/2016/09/results-fr…
Antwort auf Beitrag Nr.: 53.953.349 von Cyberhexe am 25.12.16 12:13:59den einzigen wirklichen Mangel bei der ph3-Studie ACTIVE ist die verhältnismässig grosse Anzahl an Studienabbrecher unter Abaloparatide.
Nichtsdestotrotz rechne ich im 1q mit einer extrem günstigen Datenlage (Zulassung Europa, Zulassung USA sowie Bekanntgabe Vertriebspartner "Rest of World"), so dass auch der Kurs entsprechenden Auftrieb erhalten sollte. Mein Kursziel fürs 1. Quartal: 60USD.
Nichtsdestotrotz rechne ich im 1q mit einer extrem günstigen Datenlage (Zulassung Europa, Zulassung USA sowie Bekanntgabe Vertriebspartner "Rest of World"), so dass auch der Kurs entsprechenden Auftrieb erhalten sollte. Mein Kursziel fürs 1. Quartal: 60USD.
Antwort auf Beitrag Nr.: 53.953.379 von Cyberhexe am 25.12.16 12:27:50...das wohl gewichtigste "Pfund" von Abaloparatide gegenüber den Konkurrenzprodukten ist dessen statistisch signifikante Wirkung bei den nicht die Wirbelsäule betreffenden Frakturen, welche 3x so häufig sind wie solche die Wirbelsäule betreffend.
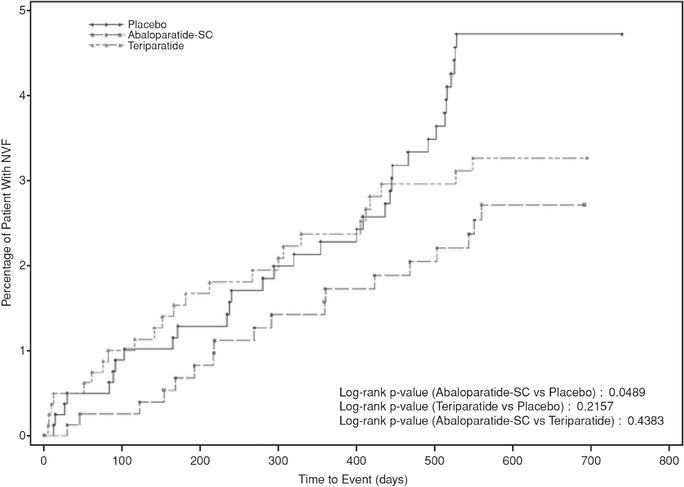

Antwort auf Beitrag Nr.: 53.962.799 von Cyberhexe am 28.12.16 05:35:00
Keine statistische Signifikanz bei Osteoporosebehandlung mit Romosozumab bei den nicht die Wirbelsäule betreffenden Frakturen:
Nonvertebral fractures had occurred in 56 of 3589 patients (1.6%) in the romosozumab group and in 75 of 3591 (2.1%) in the placebo group (P=0.10).
http://www.nejm.org/doi/full/10.1056/NEJMoa1607948
Zitat von Cyberhexe: ...das wohl gewichtigste "Pfund" von Abaloparatide gegenüber den Konkurrenzprodukten ist dessen statistisch signifikante Wirkung bei den nicht die Wirbelsäule betreffenden Frakturen, welche 3x so häufig sind wie solche die Wirbelsäule betreffend.
Keine statistische Signifikanz bei Osteoporosebehandlung mit Romosozumab bei den nicht die Wirbelsäule betreffenden Frakturen:
Nonvertebral fractures had occurred in 56 of 3589 patients (1.6%) in the romosozumab group and in 75 of 3591 (2.1%) in the placebo group (P=0.10).
http://www.nejm.org/doi/full/10.1056/NEJMoa1607948
Antwort auf Beitrag Nr.: 53.962.805 von Cyberhexe am 28.12.16 05:45:48Ne absolut sichere Sache ist "aba" nicht, weder bei den Zulassungsbehörden, noch in der Vermarktung.
Ich habe hier mehr Sorge vor dem was ich nicht weiß als vor dem was bekannt ist. Z.B. warum die hohe Abbrecherquote im Aba Arm der ACTIVE Studie. Oder ob die Daten abseits der präsentierten Daten noch irgendwelche Untiefen verstecken.
Zudem ist unklar, ob Biotech die Konsolidierung bald abschließen kann oder es einen weiteren "leg down" geben wird, die den IBB dann wahrscheinlich unter 200 drückt. Gegenwind gibt es ja fundamental weiter von verschiedenen Seiten, u.a. Regulierungsgefahren, steigende Fremdkapitalzinsen etc. Dann wird ein Biotech wie RDUS auch bei Kursen um 40 mit Zulassung(en) temporär als fair bewertet angesehen werden. Die letzten Jahre haben Biotechinvestoren einfach mit ziemlich hohen Prämien verwöhnt.
Dass du, Cyberhexe, Alleinunterhalter bei den Amis zeigt aber auch ganz klar, dass diese Aktie derzeit nicht ge'hype't ist. Das ist per se ein recht positiver Punkt.
Für mich fehlt zu einem runderen Bild noch eine Abschätzung wie schnell RDUS eine Bioäquivalence-Studie beginnen und durchziehen kann um ein Pflaster auf den Markt zu bringen. Zudem würde mich interessieren, welche Schmerzen das Pflaster beim Aufbringen erzeugt, schließlich piksen die kleinen Nadeln sicher auch in die Haut, da sie ihre Substanz abgeben müssen. Auch wenn ein tägliches Pflaster nicht so attraktiv erscheint wie eine 6 Monatsspritze, so ist es immerhin besser als eine tägliche Verabreichung durch Pen-Spritze. Nur mit dem Pen wird m.E. Aba wegen dem späten Markteintritt große Schwierigkeiten gegenüber Teri und Denosumab haben - trotz leicht besserer Daten.
Interessant, das habe ich auch schon geschrieben, ist für mich zudem der ROW Partner. Was erwartest du denn hier für Konditonen? Ich denke diese werden erheblich schlechter sein als das was EXEL für Cabozantinib von Ipsen erhalten hat. Ich erwarte trotzdem mind. 100Mio USD Upfront, Royalties von bis zu 20% und die Übernahme von 40%-50% der zukünftigen Entwicklungskosten.
Da wird man dann sehen, was an der "großen Klappe" von Robert Ward dran ist, Zitat aus dem Q3 CC: "We believe that abaloparatide is the greatest value, unpartnered, late-stage asset in the biopharm industry" .
Ich habe hier mehr Sorge vor dem was ich nicht weiß als vor dem was bekannt ist. Z.B. warum die hohe Abbrecherquote im Aba Arm der ACTIVE Studie. Oder ob die Daten abseits der präsentierten Daten noch irgendwelche Untiefen verstecken.
Zudem ist unklar, ob Biotech die Konsolidierung bald abschließen kann oder es einen weiteren "leg down" geben wird, die den IBB dann wahrscheinlich unter 200 drückt. Gegenwind gibt es ja fundamental weiter von verschiedenen Seiten, u.a. Regulierungsgefahren, steigende Fremdkapitalzinsen etc. Dann wird ein Biotech wie RDUS auch bei Kursen um 40 mit Zulassung(en) temporär als fair bewertet angesehen werden. Die letzten Jahre haben Biotechinvestoren einfach mit ziemlich hohen Prämien verwöhnt.
Dass du, Cyberhexe, Alleinunterhalter bei den Amis zeigt aber auch ganz klar, dass diese Aktie derzeit nicht ge'hype't ist. Das ist per se ein recht positiver Punkt.
Für mich fehlt zu einem runderen Bild noch eine Abschätzung wie schnell RDUS eine Bioäquivalence-Studie beginnen und durchziehen kann um ein Pflaster auf den Markt zu bringen. Zudem würde mich interessieren, welche Schmerzen das Pflaster beim Aufbringen erzeugt, schließlich piksen die kleinen Nadeln sicher auch in die Haut, da sie ihre Substanz abgeben müssen. Auch wenn ein tägliches Pflaster nicht so attraktiv erscheint wie eine 6 Monatsspritze, so ist es immerhin besser als eine tägliche Verabreichung durch Pen-Spritze. Nur mit dem Pen wird m.E. Aba wegen dem späten Markteintritt große Schwierigkeiten gegenüber Teri und Denosumab haben - trotz leicht besserer Daten.
Interessant, das habe ich auch schon geschrieben, ist für mich zudem der ROW Partner. Was erwartest du denn hier für Konditonen? Ich denke diese werden erheblich schlechter sein als das was EXEL für Cabozantinib von Ipsen erhalten hat. Ich erwarte trotzdem mind. 100Mio USD Upfront, Royalties von bis zu 20% und die Übernahme von 40%-50% der zukünftigen Entwicklungskosten.
Da wird man dann sehen, was an der "großen Klappe" von Robert Ward dran ist, Zitat aus dem Q3 CC: "We believe that abaloparatide is the greatest value, unpartnered, late-stage asset in the biopharm industry" .
Erstaunlich konservativ:
bei der Unternehmenspräsentation anlässlich der 35th Annual J.P. Morgan Healthcare Conference
wird die Bekanntgabe der Zulassungsempfehlung des Arzneimittelausschusses CHMP auf 2017 angekündigt!
Ich war davon überzeugt, dass eine Entscheidung auf der Januarsitzung des CHMP bekanntgegeben wird. Da Radius diese Entscheidung jedoch in 2017 erwartet und nicht speziell im 1. Quartal, könnte meine Erwartungshaltung diesbezüglich zu optimistisch sein.

Es bleibt spannend!
bei der Unternehmenspräsentation anlässlich der 35th Annual J.P. Morgan Healthcare Conference
wird die Bekanntgabe der Zulassungsempfehlung des Arzneimittelausschusses CHMP auf 2017 angekündigt!
Ich war davon überzeugt, dass eine Entscheidung auf der Januarsitzung des CHMP bekanntgegeben wird. Da Radius diese Entscheidung jedoch in 2017 erwartet und nicht speziell im 1. Quartal, könnte meine Erwartungshaltung diesbezüglich zu optimistisch sein.

Es bleibt spannend!
Antwort auf Beitrag Nr.: 54.052.885 von Cyberhexe am 10.01.17 20:07:52Keine antwort auf die frage nach erwartungen bzgl. konditionen?
Wann kommt die CHMP Agenda fuer das naechste meeting ueblicherweise raus? Einen tag vor dem jan meetimg?
Wann kommt die CHMP Agenda fuer das naechste meeting ueblicherweise raus? Einen tag vor dem jan meetimg?
Antwort auf Beitrag Nr.: 54.052.885 von Cyberhexe am 10.01.17 20:07:52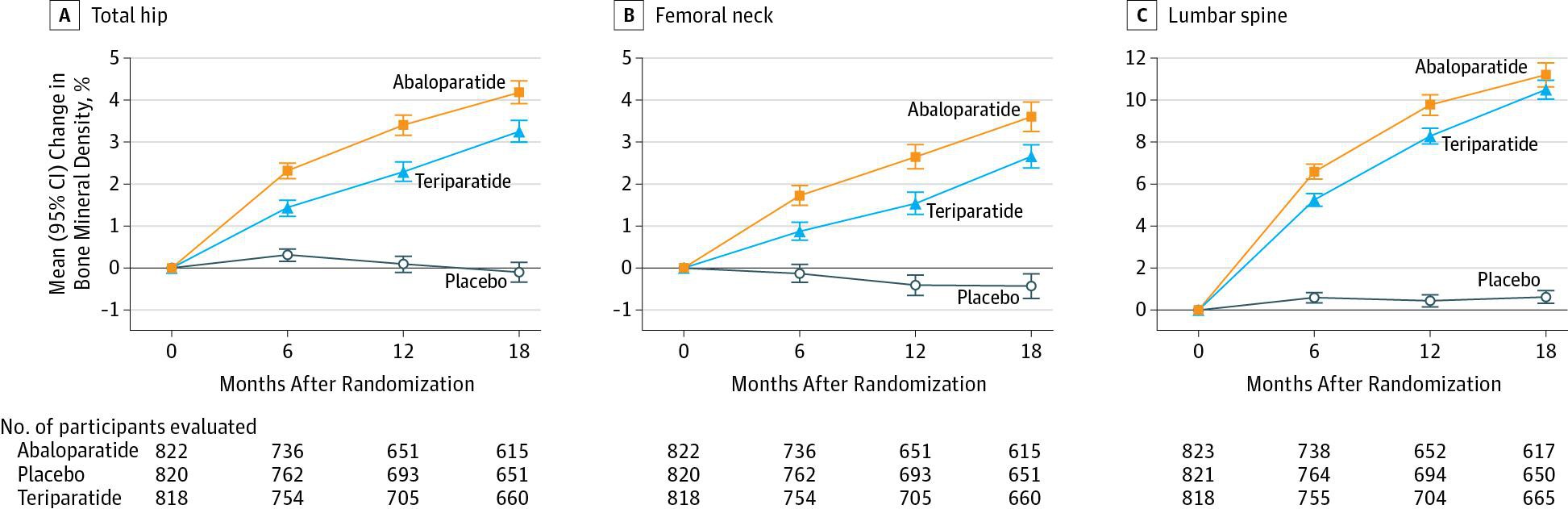
in dieser Grafik wird das (für mich zumindest) einzig grössere Problem bei ACTIVE sehr schön deutlich, nämlich die grosse Anzahl von Studienabbrecher unter Abaloparatide. Ansonsten sehe ich keine Schwierigkeiten für die Zulassung - die Frage bleibt, ob dieses Handycap die Zulassung verhindern wird? Ich glaube nicht!

in dieser Grafik wird das (für mich zumindest) einzig grössere Problem bei ACTIVE sehr schön deutlich, nämlich die grosse Anzahl von Studienabbrecher unter Abaloparatide. Ansonsten sehe ich keine Schwierigkeiten für die Zulassung - die Frage bleibt, ob dieses Handycap die Zulassung verhindern wird? Ich glaube nicht!
Antwort auf Beitrag Nr.: 54.087.182 von Ville7 am 15.01.17 12:11:23Also "no comment" zu Erwartungen der Verpartnerung und Konditionen! Auch ein Statement. 

Antwort auf Beitrag Nr.: 54.104.054 von Cyberhexe am 17.01.17 19:17:24Es wird schon einige Fragen aufgeworfen haben. Möglicherweise ein Grund, wieso der Zulassungsprozess schon so lange dauert...
Wieso guided die Firma auf JPM17, dass eine Zulassung in USA wohl vor der in Europa erfolgen wird? Das klingt mir nach keiner CHMP Empfehlung im Januar und nach Problemen in der Zulassung in Europa.
Antwort auf Beitrag Nr.: 53.935.949 von Cyberhexe am 21.12.16 22:39:12
Studiert man das Protokoll der Dezember-Sitzung des EMA Arzneimittelausschusses CHMP genauer, ist man geneigt, auch bei Abaloparatide eine weitere Unterbrechung (clock stop) für wahrscheinlich zu halten, da derartige Verzögerungen anscheinend sehr häufig zu beobachten sind:
3.1.1. - alectinib - EMEA/H/C/004164
indicated for the treatment of adult patients with anaplastic lymphoma kinase (ALK)-positive
Scope: Opinion
Action: For adoption
List of Outstanding Issues adopted on 15.09.2016. List of Questions adopted on
28.01.2016.
3.1.2. - chlormethine - Orphan - EMEA/H/C/002826
Actelion Registration Ltd.; treatment of mycosis fungoides-type cutaneous T-cell lymphoma
(MF-type CTCL)
Action: For adoption
List of Outstanding Issues adopted on 15.09.2016. List of Questions adopted on
24.09.2015.
3.1.3. - baricitinib - EMEA/H/C/004085
treatment of moderate to severe active rheumatoid arthritis (RA)
Action: For adoption
List of Outstanding Issues adopted on 13.10.2016. List of Questions adopted on
23.06.2016.
Da die "List of Outstanding Issues" bei Abaloparatide sehr wahrscheinlich im Dezember verabschiedet wurde (genaueres kann man erst im veröffentlichten Protokoll nachlesen...das dauert noch), ist in Analogie zu den 3 Beispielen frühestens in der übernächsten Sitzung mit einer Zulassungsempfehlung des Ausschusses zu rechnen.
Also deswegen habe ich meine Erwartungshaltung gezügelt und rechne mit einer Zulassungsempfehlung des CHMP in der Februarsitzung.
Zitat von Cyberhexe: am 17.11.2015 wurde der Zulassungsantrag für Abaloparatide SC zur Behandlung der Osteoporose bei "postmenopausalen Frauen" (also nach Erreichen der Menopause) bei der EMA eingereicht, welcher am 4.12.2015 formal angenommen wurde (= Tag 1 des Zulassungsprozedere). Nach Beendigung der 1. Evaluationsphase (nach 120 Tagen = Tag 120) wird dem Antragsteller eine "List of Questions" zugestellt und gleichzeitig, bis zur Beantwortung dieser Fragen, die Uhr angehalten (Clock stop). Die Unterbrechung bzw. die Zeit zur Beantwortung dieser Fragen ist normalerweise auf 3 Monate begrenzt. RADIUS hat allerdings eine Verlängerung beantragt, welche im Protokoll der Maisitzung des CHMP (23.-26.5.2016) bekanntgegeben wurde: "The CHMP agreed to the request by the applicant for an extension to the clock stop to respond to the Day 120 List of Questions adopted in April 2016."
Mittlerweile sind diese Fragen beantwortet und der Zulassungsprozess wieder gestartet. Nun, in der Dezembersitzung des CHMP, waren die "Outstanding Issues" zu Abaloparatide auf der Agenda - diese werden am Tag 180 dem Antragsteller zugestellt. Falls eine Anhörung erforderlich ist, gibt es eine 2. Unterbrechung (Clock stop) und die Uhr wird erst wieder am Tag dieser Anhörung "angestellt". Gibt es keine Anhörung, dann läuft die Uhr weiter und der Arzneimittelausschuss hat am Tag 210 seine Empfehlung (Zulassung ja/nein) abzugeben.
Ich erwarte deswegen in der Januarsitzung --> Committee for Medicinal Products for Human Use (CHMP): 23-26 January 2017
eine Entscheidung über die Empfehlung (positiv oder negativ). Lediglich Mängel in der Liefer- bzw. Produktionskette könnten eine positive Zulassungsempfehlung verhindern, weil in der Klinik, aus meiner Perspektive zumindest, ein grosser Benefit in Relation zu den Nebenwirkungen nachgewiesen wurde. Oder hat jemand einen schwer wiegenden Mangel entdeckt?
Die endgültige Zulassungsentscheidung wird spätestens am Tag 277 von der Europäischen Kommission bekannt gegeben --> Final Commission Decision
Studiert man das Protokoll der Dezember-Sitzung des EMA Arzneimittelausschusses CHMP genauer, ist man geneigt, auch bei Abaloparatide eine weitere Unterbrechung (clock stop) für wahrscheinlich zu halten, da derartige Verzögerungen anscheinend sehr häufig zu beobachten sind:
3.1.1. - alectinib - EMEA/H/C/004164
indicated for the treatment of adult patients with anaplastic lymphoma kinase (ALK)-positive
Scope: Opinion
Action: For adoption
List of Outstanding Issues adopted on 15.09.2016. List of Questions adopted on
28.01.2016.
3.1.2. - chlormethine - Orphan - EMEA/H/C/002826
Actelion Registration Ltd.; treatment of mycosis fungoides-type cutaneous T-cell lymphoma
(MF-type CTCL)
Action: For adoption
List of Outstanding Issues adopted on 15.09.2016. List of Questions adopted on
24.09.2015.
3.1.3. - baricitinib - EMEA/H/C/004085
treatment of moderate to severe active rheumatoid arthritis (RA)
Action: For adoption
List of Outstanding Issues adopted on 13.10.2016. List of Questions adopted on
23.06.2016.
Da die "List of Outstanding Issues" bei Abaloparatide sehr wahrscheinlich im Dezember verabschiedet wurde (genaueres kann man erst im veröffentlichten Protokoll nachlesen...das dauert noch), ist in Analogie zu den 3 Beispielen frühestens in der übernächsten Sitzung mit einer Zulassungsempfehlung des Ausschusses zu rechnen.
Also deswegen habe ich meine Erwartungshaltung gezügelt und rechne mit einer Zulassungsempfehlung des CHMP in der Februarsitzung.
Antwort auf Beitrag Nr.: 54.114.101 von Cyberhexe am 18.01.17 23:49:49Hallo Cyberhexe,
du hast ne` Board-Mail.
Grüße
bernie55
du hast ne` Board-Mail.
Grüße
bernie55

Antwort auf Beitrag Nr.: 54.114.101 von Cyberhexe am 18.01.17 23:49:49
...wie erwartet: Abaloparatide ist nicht auf der Agenda der Januarsitzung des europ. Arzneimittelausschusses CHMP:
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
Zitat von Cyberhexe:Zitat von Cyberhexe: am 17.11.2015 wurde der Zulassungsantrag für Abaloparatide SC zur Behandlung der Osteoporose bei "postmenopausalen Frauen" (also nach Erreichen der Menopause) bei der EMA eingereicht, welcher am 4.12.2015 formal angenommen wurde (= Tag 1 des Zulassungsprozedere). Nach Beendigung der 1. Evaluationsphase (nach 120 Tagen = Tag 120) wird dem Antragsteller eine "List of Questions" zugestellt und gleichzeitig, bis zur Beantwortung dieser Fragen, die Uhr angehalten (Clock stop). Die Unterbrechung bzw. die Zeit zur Beantwortung dieser Fragen ist normalerweise auf 3 Monate begrenzt. RADIUS hat allerdings eine Verlängerung beantragt, welche im Protokoll der Maisitzung des CHMP (23.-26.5.2016) bekanntgegeben wurde: "The CHMP agreed to the request by the applicant for an extension to the clock stop to respond to the Day 120 List of Questions adopted in April 2016."
Mittlerweile sind diese Fragen beantwortet und der Zulassungsprozess wieder gestartet. Nun, in der Dezembersitzung des CHMP, waren die "Outstanding Issues" zu Abaloparatide auf der Agenda - diese werden am Tag 180 dem Antragsteller zugestellt. Falls eine Anhörung erforderlich ist, gibt es eine 2. Unterbrechung (Clock stop) und die Uhr wird erst wieder am Tag dieser Anhörung "angestellt". Gibt es keine Anhörung, dann läuft die Uhr weiter und der Arzneimittelausschuss hat am Tag 210 seine Empfehlung (Zulassung ja/nein) abzugeben.
Ich erwarte deswegen in der Januarsitzung --> Committee for Medicinal Products for Human Use (CHMP): 23-26 January 2017
eine Entscheidung über die Empfehlung (positiv oder negativ). Lediglich Mängel in der Liefer- bzw. Produktionskette könnten eine positive Zulassungsempfehlung verhindern, weil in der Klinik, aus meiner Perspektive zumindest, ein grosser Benefit in Relation zu den Nebenwirkungen nachgewiesen wurde. Oder hat jemand einen schwer wiegenden Mangel entdeckt?
Die endgültige Zulassungsentscheidung wird spätestens am Tag 277 von der Europäischen Kommission bekannt gegeben --> Final Commission Decision
Studiert man das Protokoll der Dezember-Sitzung des EMA Arzneimittelausschusses CHMP genauer, ist man geneigt, auch bei Abaloparatide eine weitere Unterbrechung (clock stop) für wahrscheinlich zu halten, da derartige Verzögerungen anscheinend sehr häufig zu beobachten sind:
3.1.1. - alectinib - EMEA/H/C/004164
indicated for the treatment of adult patients with anaplastic lymphoma kinase (ALK)-positive
Scope: Opinion
Action: For adoption
List of Outstanding Issues adopted on 15.09.2016. List of Questions adopted on
28.01.2016.
3.1.2. - chlormethine - Orphan - EMEA/H/C/002826
Actelion Registration Ltd.; treatment of mycosis fungoides-type cutaneous T-cell lymphoma
(MF-type CTCL)
Action: For adoption
List of Outstanding Issues adopted on 15.09.2016. List of Questions adopted on
24.09.2015.
3.1.3. - baricitinib - EMEA/H/C/004085
treatment of moderate to severe active rheumatoid arthritis (RA)
Action: For adoption
List of Outstanding Issues adopted on 13.10.2016. List of Questions adopted on
23.06.2016.
Da die "List of Outstanding Issues" bei Abaloparatide sehr wahrscheinlich im Dezember verabschiedet wurde (genaueres kann man erst im veröffentlichten Protokoll nachlesen...das dauert noch), ist in Analogie zu den 3 Beispielen frühestens in der übernächsten Sitzung mit einer Zulassungsempfehlung des Ausschusses zu rechnen.
Also deswegen habe ich meine Erwartungshaltung gezügelt und rechne mit einer Zulassungsempfehlung des CHMP in der Februarsitzung.
...wie erwartet: Abaloparatide ist nicht auf der Agenda der Januarsitzung des europ. Arzneimittelausschusses CHMP:
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
Antwort auf Beitrag Nr.: 52.512.431 von cyberhexe123 am 31.05.16 20:36:47
Aus heutiger Sicht nur ganz leicht verschätzt in der Kursentwicklung...(EXEL =blau)

Zitat von cyberhexe123: ...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben.
Aus heutiger Sicht nur ganz leicht verschätzt in der Kursentwicklung...(EXEL =blau)

T.Rowe Price hat heute eine 13G Pflichtmitteilung veröffentlicht und zwar wurde die Anzahl der RDUS-Aktien auf 3,079,831 Stück erhöht....dies entspricht einem Anteil von ca. 7.1%
http://ir.radiuspharm.com/sec.cfm
Feb 7, 2017 SC 13G Statement Of Beneficial Ownership
http://ir.radiuspharm.com/sec.cfm
Feb 7, 2017 SC 13G Statement Of Beneficial Ownership
Antwort auf Beitrag Nr.: 54.264.992 von Cyberhexe am 07.02.17 23:11:55Super nachrichten. Momentan wird rdus mit sehr niedrigen volumen gehandelt und hat scheinbar wenig aufmerksamkeit. Hoffe das ändert sich bald.
Antwort auf Beitrag Nr.: 54.297.638 von biopadawan am 11.02.17 14:34:52am Montag startet die Februarsitzung des europ. Arzneimittelausschusses CHMP - vielleicht ist die Zulassungsempfehlung von Abaloparatide auf der Agenda:
http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/l…
Die Publikationen in den wissenschaftlichen Journals nehmen zu:
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
Conclusion
"Use of ABL-SC for 18 months followed by ALN for 6 months improved bone mineral density and reduced fracture risk throughout the skeleton and may be an effective treatment option for postmenopausal women with osteoporosis."
http://www.maturitas.org/article/S0378-5122(16)30272-9/abstr…
Maturitas. 2017 Mar;97:53-60. doi: 10.1016/j.maturitas.2016.12.003. Epub 2016 Dec 15.
Abaloparatide: Recombinant human PTHrP (1-34) anabolic therapy for osteoporosis.
Chew CK1, Clarke BL2.
Abstract
"The treatment of osteoporosis is generally either by inhibition of bone resorption with antiresorptive agents or by stimulation of bone formation with anabolic agents. Currently, teriparatide (recombinant human parathyroid hormone 1-34 [rhPTH (1-34)]) is the only available approved anabolic agent in the U.S. Other anabolic agents are under investigation however. Abaloparatide is recombinant human parathyroid hormone-related peptide 1-34. This agent is an anabolic agent that appears more potent than teriparatide, and it may have more rapid onset of fracture reduction than teriparatide. It is currently undergoing FDA review, with approval expected in 2017."
http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/l…
Die Publikationen in den wissenschaftlichen Journals nehmen zu:
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
Conclusion
"Use of ABL-SC for 18 months followed by ALN for 6 months improved bone mineral density and reduced fracture risk throughout the skeleton and may be an effective treatment option for postmenopausal women with osteoporosis."
http://www.maturitas.org/article/S0378-5122(16)30272-9/abstr…
Maturitas. 2017 Mar;97:53-60. doi: 10.1016/j.maturitas.2016.12.003. Epub 2016 Dec 15.
Abaloparatide: Recombinant human PTHrP (1-34) anabolic therapy for osteoporosis.
Chew CK1, Clarke BL2.
Abstract
"The treatment of osteoporosis is generally either by inhibition of bone resorption with antiresorptive agents or by stimulation of bone formation with anabolic agents. Currently, teriparatide (recombinant human parathyroid hormone 1-34 [rhPTH (1-34)]) is the only available approved anabolic agent in the U.S. Other anabolic agents are under investigation however. Abaloparatide is recombinant human parathyroid hormone-related peptide 1-34. This agent is an anabolic agent that appears more potent than teriparatide, and it may have more rapid onset of fracture reduction than teriparatide. It is currently undergoing FDA review, with approval expected in 2017."
Antwort auf Beitrag Nr.: 54.321.536 von Cyberhexe am 14.02.17 23:24:36sieht gut aus... danke für die Nachforschung, super Arbeit
Immer wieder interessant, wie versucht wird an charttechnisch interessanten Marken das alte (und ebenso falsche) Shire Übernahme-Gerücht aufzuwärmen....
institutionelle Anleger bringen sich in Stellung: verschiedene Pflichtmitteilungen in den letzten beiden Tagen:
http://ir.radiuspharm.com/sec.cfm
Bin gespannt, ob der Anteil der Institutionellen demnächst 100% übersteigt?
Könnte mir vorstellen, dass Abaloparatide nächste Woche auf der Agenda des europ. Arzneimittelausschusses ist. Das wäre wohl eine Erklärung für den aktuellen Kursanbstieg.
http://ir.radiuspharm.com/sec.cfm
Bin gespannt, ob der Anteil der Institutionellen demnächst 100% übersteigt?
Könnte mir vorstellen, dass Abaloparatide nächste Woche auf der Agenda des europ. Arzneimittelausschusses ist. Das wäre wohl eine Erklärung für den aktuellen Kursanbstieg.
Antwort auf Beitrag Nr.: 54.330.757 von Cyberhexe am 15.02.17 21:08:54
Die Vorstellung in Ehren, aber aba ist nicht auf der Agenda für den Februar. Fragt sich somit, was für ein Problem die EMA mit aba hat.....
Zitat von Cyberhexe: Könnte mir vorstellen, dass Abaloparatide nächste Woche auf der Agenda des europ. Arzneimittelausschusses ist. Das wäre wohl eine Erklärung für den aktuellen Kursanbstieg.
Die Vorstellung in Ehren, aber aba ist nicht auf der Agenda für den Februar. Fragt sich somit, was für ein Problem die EMA mit aba hat.....
Antwort auf Beitrag Nr.: 54.330.757 von Cyberhexe am 15.02.17 21:08:54In dem am 9.2.2017 veröffentlichten Protokoll der Dezembersitzung 2016 hat der europ. Arzneimittelausschuss der EMA (CHMP) bekannt gegeben, dass Radius eine Verlängerung der Frist zur Beantwortung der "List of Outstanding Issues" beantragt hat. Demzufolge ist die Uhr des Zulassungsprozedere ein 2. mal angehalten.
http://www.ema.europa.eu/docs/en_GB/document_library/Minutes…
EMA: 13 December 2016 requesting an extension to the clock (LoOI)
3.2.9. - abaloparatide - EMEA/H/C/004157 treatment of osteoporosis Scope: Day 180 list of outstanding issue
Letter from the applicant dated 13 December 2016 requesting an extension to the clock stop to respond to the Day 180 List of Outstanding issues adopted
Action: For adoption
List of Questions adopted on 01.04.2016.
The Committee was reminded of the status of this application and its remaining outstanding issues.
The Committee adopted a list of outstanding issues with a specific timetable.
The CHMP agreed to the request by the applicant for an extension to the clock stop to respond to the list of outstanding issues.
http://www.investorvillage.com/smbd.asp?mb=18024&mn=26&pt=ms…
Danke Franca
http://www.ema.europa.eu/docs/en_GB/document_library/Minutes…
EMA: 13 December 2016 requesting an extension to the clock (LoOI)
3.2.9. - abaloparatide - EMEA/H/C/004157 treatment of osteoporosis Scope: Day 180 list of outstanding issue
Letter from the applicant dated 13 December 2016 requesting an extension to the clock stop to respond to the Day 180 List of Outstanding issues adopted
Action: For adoption
List of Questions adopted on 01.04.2016.
The Committee was reminded of the status of this application and its remaining outstanding issues.
The Committee adopted a list of outstanding issues with a specific timetable.
The CHMP agreed to the request by the applicant for an extension to the clock stop to respond to the list of outstanding issues.
http://www.investorvillage.com/smbd.asp?mb=18024&mn=26&pt=ms…
Danke Franca

RADIUS Health ist mittlerweile die 6. grösste Position im Portfolio von BBBiotech. Die Schweizer scheinen an den Erfolg des Unternehmens zu glauben.
Anbei der letzten Freitag veröffentlichte Geschäftsbericht für 2016:
http://www.bbbiotech.ch/index.php?eID=tx_nawsecuredl&u=4&g=1…
Anbei der letzten Freitag veröffentlichte Geschäftsbericht für 2016:
http://www.bbbiotech.ch/index.php?eID=tx_nawsecuredl&u=4&g=1…
Antwort auf Beitrag Nr.: 54.366.676 von Cyberhexe am 20.02.17 16:28:19Jo merci. Wirft aber mehr Fragen auf als es beantwortet.
Inquiring minds want to know warum RDUS nun fast schon ein knappes Jahr dafür braucht um die ausstehenden Fragen der EMA zu beantworten. Das sieht mir eher danach aus als seien diese Fragen extrem tricky/gefährlich oder es werden weitere präklinische Studienergebnisse erwartet, die erst noch generiert werden müssen (und es daher ZEit braucht). Man kann nur spekulieren..
Inquiring minds want to know warum RDUS nun fast schon ein knappes Jahr dafür braucht um die ausstehenden Fragen der EMA zu beantworten. Das sieht mir eher danach aus als seien diese Fragen extrem tricky/gefährlich oder es werden weitere präklinische Studienergebnisse erwartet, die erst noch generiert werden müssen (und es daher ZEit braucht). Man kann nur spekulieren..
Antwort auf Beitrag Nr.: 54.366.787 von Cyberhexe am 20.02.17 16:41:09BBBiotech kocht auch nur mit Wasser und lag oft genug daneben.
Ich muss da nur an deren Verkauf von Bavarian Nordic denken, da waren sie extrem stark engagert, haben dann zu tiefen Kursen alle ihre Stücke auf den Markt geworfen, sodass der Kurs von 275DKK auf um die 35 DKK kraterte (2011). Inzwischen wieder bei ca. 280 DKK.
Ich muss da nur an deren Verkauf von Bavarian Nordic denken, da waren sie extrem stark engagert, haben dann zu tiefen Kursen alle ihre Stücke auf den Markt geworfen, sodass der Kurs von 275DKK auf um die 35 DKK kraterte (2011). Inzwischen wieder bei ca. 280 DKK.
Antwort auf Beitrag Nr.: 54.366.787 von Cyberhexe am 20.02.17 16:41:09
Prescription Drug User Fee Act (PDUFA) date of March 30, 2017
spätestens Ende März wird die FDA ihre Entscheidung hinsichtlich Abaloparatide veröffentlichen - ich rechne mit einer Zulassung von Abaloparatide auf dem wichtigsten Arzneimittelmarkt!
Obschon ich nicht glaube, dass der europäische Arzneimittelausschuss weitere klinische Studien zu Abaloparatide verlangt, habe ich derzeit keine Ahnung, welcher Natur die "outstanding issues" zuzuordnen sind.
Prescription Drug User Fee Act (PDUFA) date of March 30, 2017
spätestens Ende März wird die FDA ihre Entscheidung hinsichtlich Abaloparatide veröffentlichen - ich rechne mit einer Zulassung von Abaloparatide auf dem wichtigsten Arzneimittelmarkt!
Obschon ich nicht glaube, dass der europäische Arzneimittelausschuss weitere klinische Studien zu Abaloparatide verlangt, habe ich derzeit keine Ahnung, welcher Natur die "outstanding issues" zuzuordnen sind.
YE Call Transcript: http://seekingalpha.com/article/4049199-radius-healths-rdus-…
Die Firma macht ein mega Geheimnis darum was bei den Behörden, speziell der EMA, offen ist. Da sind andere in der Beantwortung kooperativer. Frage, die sich dabei der Markt auch stellt, ist: Haben Sie was zu verbergen?
Zudem ist man nicht willig den weiteren zeitlichen Weg bezüglich des transdermal patches darzulegen.
Auf der anderen Seite trägt man mega auf mit dem erneut im Call gefallenen Satz "We believe that abaloparatide is the greatest value un-partnered late stage asset in the biopharma industry.".
Sollte die Zulassung in USA nicht erfolgen (Complete Response Letter), so erwarte ich Kurse von 15-25 USD.
Die Firma macht ein mega Geheimnis darum was bei den Behörden, speziell der EMA, offen ist. Da sind andere in der Beantwortung kooperativer. Frage, die sich dabei der Markt auch stellt, ist: Haben Sie was zu verbergen?
Zudem ist man nicht willig den weiteren zeitlichen Weg bezüglich des transdermal patches darzulegen.
Auf der anderen Seite trägt man mega auf mit dem erneut im Call gefallenen Satz "We believe that abaloparatide is the greatest value un-partnered late stage asset in the biopharma industry.".
Sollte die Zulassung in USA nicht erfolgen (Complete Response Letter), so erwarte ich Kurse von 15-25 USD.
Antwort auf Beitrag Nr.: 53.893.651 von Cyberhexe am 15.12.16 07:12:16
Auch wenn die Zulassung in USA mit größerer Wahrscheinlichkeit erfolgen wird als eine Nicht-Zulassung: Du fährst hier m.E. ein zu hohes Risiko mit wahrscheinlich weit über 50% deines Depotwertes nur in RDUS - und das bei all den Unsicherheiten (z.B. was die EU an Fragen hat). Ohne eine Zulassung wäre das viele Cash bereits in 2018 aufgebraucht und selbst mit Zulassung bleibt die Burn-rate sehr hoch und es ist unklar, ob man ohne weitere Verwässerungen durchkommt.... neben dem Zulassungsrisiko ist auch unklar inwieweit Aba ein ausreichender Markterfolg wird, da es gegenüber den zwei verfügbaren Antikörpern (trotz etwas besserer Wirksamkeit) erheblich teurer und unangenehmer anzuwenden ist.
Zitat von cyberhexe123: ...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben.
Zitat von Cyberhexe: Kaufkurs am 30.5.16 USD 35,45...aktueller Kurs USD 56,75
Kursziel nach Zulassung von abaloparatide in US and EU > USD 100!
Zitat von Cyberhexe: Hab gestern im Laufe der Börsensitzung meine Position verdreifacht, weshalb RDUS nun in meinem Portfolio die stärkste Position darstellt.
Auch wenn die Zulassung in USA mit größerer Wahrscheinlichkeit erfolgen wird als eine Nicht-Zulassung: Du fährst hier m.E. ein zu hohes Risiko mit wahrscheinlich weit über 50% deines Depotwertes nur in RDUS - und das bei all den Unsicherheiten (z.B. was die EU an Fragen hat). Ohne eine Zulassung wäre das viele Cash bereits in 2018 aufgebraucht und selbst mit Zulassung bleibt die Burn-rate sehr hoch und es ist unklar, ob man ohne weitere Verwässerungen durchkommt.... neben dem Zulassungsrisiko ist auch unklar inwieweit Aba ein ausreichender Markterfolg wird, da es gegenüber den zwei verfügbaren Antikörpern (trotz etwas besserer Wirksamkeit) erheblich teurer und unangenehmer anzuwenden ist.
Antwort auf Beitrag Nr.: 54.418.426 von Ville7 am 27.02.17 09:57:45Interessant, dass nach initial 30% Depotanteil (Mai 2016) und einer Verdreifachung dieser Position im Dezember der User Cyberhexe heute im Progenix Thread folgenden Depotstand meldet:
Entweder zwischenzeitlich geerbt, massiv RDUS verkauft oder einfach generell ein Problem mit der Wahrheit....jeder wähle selbst.
Zitat von Cyberhexe: ...
die aktuelle Zusammensetzung ist allerdings nur eine Momentaufnahme, da Zusammensetzung ständig hinterfragt und angepasst werden und zudem die Verteilung (vor allem bei einer Rakete wie EXEL) durch die Kursbewegung beeinflusst wird.
30% PGNX
25% RDUS
20% EXEL
10% ARRY
10% NLNK
Entweder zwischenzeitlich geerbt, massiv RDUS verkauft oder einfach generell ein Problem mit der Wahrheit....jeder wähle selbst.
Antwort auf Beitrag Nr.: 54.421.921 von Ville7 am 27.02.17 17:43:22
Wie so oft...wieder einer deiner Beiträge ohne Mehrwert und Nutzen für andere Teilnehmer.
Nur so viel zu deinem kleingeistigen Angriff:
aus:
Exelixis....ein schlafender Riese? USD 3.40
Cyberhexe schrieb am 13.08.16 15:27:42 Beitrag Nr. 550 ( 53.054.197 )
EMA Newsletter Two new medicines for ....
Ich habe letzte Woche 3/4 meiner EXEL-Aktien zu Gunsten von Progenics liquidiert.
am 14.5.2014 | wallstreet-online.de - Vollständige Diskussion unter:
http://www.wallstreet-online.de/diskussion/1194406-541-550/e…
Am 25.8. habe ich deshalb folgenden Thread auf ASonline begonnen:
Progenics Pharmaceuticals, Inc. (NASDAQ:PGNX)...USD 6.56/24.8.2016
Ich hoffe jedoch, dass dieser Thread nicht auch noch von deinen Nullinfo-Beiträgen zugemüllt wird.
Zitat von Ville7: Interessant, dass nach initial 30% Depotanteil (Mai 2016) und einer Verdreifachung dieser Position im Dezember der User Cyberhexe heute im Progenix Thread folgenden Depotstand meldet:
Zitat von Cyberhexe: ...
die aktuelle Zusammensetzung ist allerdings nur eine Momentaufnahme, da Zusammensetzung ständig hinterfragt und angepasst werden und zudem die Verteilung (vor allem bei einer Rakete wie EXEL) durch die Kursbewegung beeinflusst wird.
30% PGNX
25% RDUS
20% EXEL
10% ARRY
10% NLNK
Entweder zwischenzeitlich geerbt, massiv RDUS verkauft oder einfach generell ein Problem mit der Wahrheit....jeder wähle selbst.
Wie so oft...wieder einer deiner Beiträge ohne Mehrwert und Nutzen für andere Teilnehmer.
Nur so viel zu deinem kleingeistigen Angriff:
aus:
Exelixis....ein schlafender Riese? USD 3.40
Cyberhexe schrieb am 13.08.16 15:27:42 Beitrag Nr. 550 ( 53.054.197 )
EMA Newsletter Two new medicines for ....
Ich habe letzte Woche 3/4 meiner EXEL-Aktien zu Gunsten von Progenics liquidiert.
am 14.5.2014 | wallstreet-online.de - Vollständige Diskussion unter:
http://www.wallstreet-online.de/diskussion/1194406-541-550/e…
Am 25.8. habe ich deshalb folgenden Thread auf ASonline begonnen:
Progenics Pharmaceuticals, Inc. (NASDAQ:PGNX)...USD 6.56/24.8.2016
Ich hoffe jedoch, dass dieser Thread nicht auch noch von deinen Nullinfo-Beiträgen zugemüllt wird.
!
Dieser Beitrag wurde von FairMOD moderiert. Grund: Unbelegte Tatsachenbehauptung
Antwort auf Beitrag Nr.: 54.425.458 von Ville7 am 28.02.17 00:36:23...hast wohl wieder Lust auf eine schöpferische Pause:
Faktencheck unter -->http://www.wallstreet-online.de/diskussion/1194406-541-550/e…
Cyberhexe schrieb am 13.08.16 15:27:2 Beitrag Nr. 550 ( 53.054.197 )
Faktencheck unter -->http://www.wallstreet-online.de/diskussion/1194406-541-550/e…
Cyberhexe schrieb am 13.08.16 15:27:2 Beitrag Nr. 550 ( 53.054.197 )
Antwort auf Beitrag Nr.: 54.330.757 von Cyberhexe am 15.02.17 21:08:54
....das hat nicht lange gedauert!
Institutional Holdings aktuell: 100.07%
http://www.nasdaq.com/symbol/rdus/institutional-holdings
Zitat von Cyberhexe: institutionelle Anleger bringen sich in Stellung: verschiedene Pflichtmitteilungen in den letzten beiden Tagen:
http://ir.radiuspharm.com/sec.cfm
Bin gespannt, ob der Anteil der Institutionellen demnächst 100% übersteigt?
Könnte mir vorstellen, dass Abaloparatide nächste Woche auf der Agenda des europ. Arzneimittelausschusses ist. Das wäre wohl eine Erklärung für den aktuellen Kursanbstieg.
....das hat nicht lange gedauert!
Institutional Holdings aktuell: 100.07%
http://www.nasdaq.com/symbol/rdus/institutional-holdings
!
Dieser Beitrag wurde von MODelfin moderiert. Grund: offensichtlich persönliche Differenzen bitte via BM klären, Danke!!
Dieser Beitrag wurde von MODelfin moderiert. Grund: korrespondierend, klären Sie persönliche Differenzen bitte via BM, Danke!
Kein Grund zu löschen, ich gebe nur wieder, was Cyberhexe selbst in W : O geschrieben hat:
Im Mai 2016 hat sie 30% ihres Depots in RDUS gesteckt. Im Dezember 2016 hat sie ihre RDUS Position verdreifacht. Gestern hat sie geschrieben, sie hätte aktuell 20% RDUS im Depot.
Jeder rechne nach und beurteile selbst, ob das mit der Wahrheit / Realität vereinbar ist.
Im Mai 2016 hat sie 30% ihres Depots in RDUS gesteckt. Im Dezember 2016 hat sie ihre RDUS Position verdreifacht. Gestern hat sie geschrieben, sie hätte aktuell 20% RDUS im Depot.
Jeder rechne nach und beurteile selbst, ob das mit der Wahrheit / Realität vereinbar ist.
Antwort auf Beitrag Nr.: 54.431.954 von Ville7 am 28.02.17 17:51:08
obschon dieser Thread nicht die Absicht hat, mein persönlicRisikomanagement zu dokumentieren, möchte ich Grundrechenarten erklären und dies am besten am Beispiel:
die Position x hat am Tag 1 einen Depotanteil von 30%
die Position x hat am Tag 100 durch Kursveränderungen (EXEL, PGNX sind wesentlich besser gelaufen) einen Depotanteil von 17%
die Position x wird am Tag 101 verdreifacht und hat dann einen Depotanteil von über 50%
...genau dies habe ich am 20.12.16 mitgeteilt: "-> bin jetzt bei über 50% Depotanteil."
Dies ist aber nicht in Stein gemeisselt. Aufgrund der "List of outstanding isuues" und des damit verbundenen "clock stop" beim europ. Zulassungsverfahren habe ich meine RDUS-Position auf 25% reduziert (nicht auf 20%...immer bei der Wahrheit bleiben).
Allgemein:
Zu den in meinem Depot gehaltenen Werte (PGNX, RDUS, EXEL, NLNK, ARRY) habe ich Threads eröffnet, um die fundamentalen Daten hinter diesen Unternehmen zu diskutieren. Bei der Gewichtung im Depot finden jedoch ständig Anpassungen statt, die diese fundamentalen Hintergründe berücksichtigen. Es ist jedoch nicht meine Absicht, die Depotzusammensetzung zu diskutieren sondern die fundamentalen Daten dieser Unternehmen. Nur schade, dass man hier Zeit dafür aufwenden muss, um mit Grundrechenarten seine Integrität bzw. diejenige von Cyberhexe zu schützen. Solche kleingeistigen Angriffe sollte man eigentlich ignorieren - leider gelingt mir dies nicht immer.
Zitat von Ville7: Kein Grund zu löschen, ich gebe nur wieder, was Cyberhexe selbst in W : O geschrieben hat:
Im Mai 2016 hat sie 30% ihres Depots in RDUS gesteckt. Im Dezember 2016 hat sie ihre RDUS Position verdreifacht. Gestern hat sie geschrieben, sie hätte aktuell 20% RDUS im Depot.
Jeder rechne nach und beurteile selbst, ob das mit der Wahrheit / Realität vereinbar ist.
obschon dieser Thread nicht die Absicht hat, mein persönlicRisikomanagement zu dokumentieren, möchte ich Grundrechenarten erklären und dies am besten am Beispiel:
die Position x hat am Tag 1 einen Depotanteil von 30%
die Position x hat am Tag 100 durch Kursveränderungen (EXEL, PGNX sind wesentlich besser gelaufen) einen Depotanteil von 17%
die Position x wird am Tag 101 verdreifacht und hat dann einen Depotanteil von über 50%
...genau dies habe ich am 20.12.16 mitgeteilt: "-> bin jetzt bei über 50% Depotanteil."
Dies ist aber nicht in Stein gemeisselt. Aufgrund der "List of outstanding isuues" und des damit verbundenen "clock stop" beim europ. Zulassungsverfahren habe ich meine RDUS-Position auf 25% reduziert (nicht auf 20%...immer bei der Wahrheit bleiben).
Allgemein:
Zu den in meinem Depot gehaltenen Werte (PGNX, RDUS, EXEL, NLNK, ARRY) habe ich Threads eröffnet, um die fundamentalen Daten hinter diesen Unternehmen zu diskutieren. Bei der Gewichtung im Depot finden jedoch ständig Anpassungen statt, die diese fundamentalen Hintergründe berücksichtigen. Es ist jedoch nicht meine Absicht, die Depotzusammensetzung zu diskutieren sondern die fundamentalen Daten dieser Unternehmen. Nur schade, dass man hier Zeit dafür aufwenden muss, um mit Grundrechenarten seine Integrität bzw. diejenige von Cyberhexe zu schützen. Solche kleingeistigen Angriffe sollte man eigentlich ignorieren - leider gelingt mir dies nicht immer.
Antwort auf Beitrag Nr.: 54.432.881 von Cyberhexe am 28.02.17 19:24:55Na also. Geht doch.
q.e.d.
Der Kleingeist fragt sich nur, wieso das Biotech-Superhirn alle ihre Käufe in die Boards posaunen muss, ihre (heftigen) Reduktionen aber ihrer Fan-Gemeinde (und auch dem Kleingeist) verschweigt.
Ein Schelm (oder Kleingeist), der sich dabei denkt, dass sie durch Reduktions-Postings ihrer stets (durch sie) gepushten Werte ja einen Zacken aus ihrer Krone verlieren könnte.
Grüße vom Kleingeist, der sich nun wieder unter den Stein verkriecht...
q.e.d.
Der Kleingeist fragt sich nur, wieso das Biotech-Superhirn alle ihre Käufe in die Boards posaunen muss, ihre (heftigen) Reduktionen aber ihrer Fan-Gemeinde (und auch dem Kleingeist) verschweigt.
Ein Schelm (oder Kleingeist), der sich dabei denkt, dass sie durch Reduktions-Postings ihrer stets (durch sie) gepushten Werte ja einen Zacken aus ihrer Krone verlieren könnte.
Grüße vom Kleingeist, der sich nun wieder unter den Stein verkriecht...
Antwort auf Beitrag Nr.: 54.432.881 von Cyberhexe am 28.02.17 19:24:55
Noch einen Tipp vom Kleingeist: Sollte das oben tatsächlich deine hehren Ziele sein (der Kleingeist kann das nicht wirklich glauben), dann solltest du dich künftig daran halten und deine Positionierungsmeldungen unterlassen. Alles andere in unvollständiger Art (wie geschehen) hinterlässt halt "a G'schmäckle".
Zitat von Cyberhexe: ...
Zu den in meinem Depot gehaltenen Werte (PGNX, RDUS, EXEL, NLNK, ARRY) habe ich Threads eröffnet, um die fundamentalen Daten hinter diesen Unternehmen zu diskutieren.
...
Es ist jedoch nicht meine Absicht, die Depotzusammensetzung zu diskutieren sondern die fundamentalen Daten dieser Unternehmen.
...
Noch einen Tipp vom Kleingeist: Sollte das oben tatsächlich deine hehren Ziele sein (der Kleingeist kann das nicht wirklich glauben), dann solltest du dich künftig daran halten und deine Positionierungsmeldungen unterlassen. Alles andere in unvollständiger Art (wie geschehen) hinterlässt halt "a G'schmäckle".
Man sollte sich nie zu sicher sein. Dass etwas "fishy" ist hat man seit einiger Zeit sehen können....
Meldung von heute:
Radius Health Receives Notification of PDUFA Extension for Abaloparatide-SC
PDUFA goal date extended by standard extension period of three months to June 30, 2017
WALTHAM, Mass., March 10, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. ("Radius" or the "Company") (Nasdaq:RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that the U.S. Food and Drug Administration (FDA) will require additional time to complete its review of the New Drug Application (NDA) for Abaloparatide-SC. In a notice received from the FDA last evening, the Prescription Drug User Fee Act (PDUFA) date for Abaloparatide-SC has been extended to June 30, 2017.
The FDA extended the action date to allow time to review information submitted by Radius Health in response to the FDA's Information Requests. The FDA stated that the PDUFA goal date has been extended by three months to allow for a full review of the submission. In the letter, the FDA has not requested any additional information from the Company.
"Our primary goal is to bring treatment to patients with postmenopausal osteoporosis as quickly as possible. We appreciate the efforts of the FDA to conduct a complete review of all of the data supporting our NDA and we remain committed to working closely with them throughout the remainder of the regulatory process." said Robert Ward, President and Chief Executive Officer of Radius Health.
Radius will host a conference call at 9:15 AM. ET on Friday, March 10, 2017 to discuss the FDA Notification.
Meldung von heute:
Radius Health Receives Notification of PDUFA Extension for Abaloparatide-SC
PDUFA goal date extended by standard extension period of three months to June 30, 2017
WALTHAM, Mass., March 10, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. ("Radius" or the "Company") (Nasdaq:RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that the U.S. Food and Drug Administration (FDA) will require additional time to complete its review of the New Drug Application (NDA) for Abaloparatide-SC. In a notice received from the FDA last evening, the Prescription Drug User Fee Act (PDUFA) date for Abaloparatide-SC has been extended to June 30, 2017.
The FDA extended the action date to allow time to review information submitted by Radius Health in response to the FDA's Information Requests. The FDA stated that the PDUFA goal date has been extended by three months to allow for a full review of the submission. In the letter, the FDA has not requested any additional information from the Company.
"Our primary goal is to bring treatment to patients with postmenopausal osteoporosis as quickly as possible. We appreciate the efforts of the FDA to conduct a complete review of all of the data supporting our NDA and we remain committed to working closely with them throughout the remainder of the regulatory process." said Robert Ward, President and Chief Executive Officer of Radius Health.
Radius will host a conference call at 9:15 AM. ET on Friday, March 10, 2017 to discuss the FDA Notification.
Antwort auf Beitrag Nr.: 54.511.740 von Ville7 am 10.03.17 15:30:04Und das idiotischste ist auch noch, dass die Pressemitteilung nach der Startzeit des Conference Calls verschickt wurde. So erzeugt man Vertrauen! Das dürfte heute kräftig runter gehen!
...eine Verzögerung um 3 Monate beim Zulassungsentscheid der FDA ist keine Seltenheit:
The FDA extended the action date to allow time to review information submitted by Radius Health in response to the FDA's Information Requests. The FDA stated that the PDUFA goal date has been extended by three months to allow for a full review of the submission. In the letter, the FDA has not requested any additional information from the Company.
http://files.shareholder.com/downloads/AMDA-1D3H6P/405308119…
The FDA extended the action date to allow time to review information submitted by Radius Health in response to the FDA's Information Requests. The FDA stated that the PDUFA goal date has been extended by three months to allow for a full review of the submission. In the letter, the FDA has not requested any additional information from the Company.
http://files.shareholder.com/downloads/AMDA-1D3H6P/405308119…
Erwähnung in der EMA CHMP Agenda diese Woche. Aber man hat ja schon kommuniziert, dass man kurzfristig von der EMA keine Entscheidung erwartet. Weiterhin sehr fishy!
Parallel scheint in Biotech eine Korrektur zu beginnen... heftige Verlustbuden werden dabei mit dem mehrfachen prozentualen Abschlag bestraft, das was schon immer so ... zudem charttechnisch sehr angeschlagen ... RDUS nun zurück auf USD 25?
Parallel scheint in Biotech eine Korrektur zu beginnen... heftige Verlustbuden werden dabei mit dem mehrfachen prozentualen Abschlag bestraft, das was schon immer so ... zudem charttechnisch sehr angeschlagen ... RDUS nun zurück auf USD 25?
BB Biotech deckt sich ja gerade ordentlich ein. Meinungen dazu?
Absturz auf $25 halte ich trotz der möglichen Korrektur für etwas übertrieben.
Absturz auf $25 halte ich trotz der möglichen Korrektur für etwas übertrieben.
Antwort auf Beitrag Nr.: 54.582.774 von biopadawan am 21.03.17 19:17:51Wieso nicht? Sind nur 10 USD davon entfernt und eine ausgedehnte Korrektur hat heute wahrscheinlich erst begonnen. RDUS 25, EXEL 15-17 alles andere als unrealistisch.
Antwort auf Beitrag Nr.: 54.582.774 von biopadawan am 21.03.17 19:17:51
...nur nicht verrückt machen lassen von "Mr. Konjunktiv".
Die Klinik bei Abaloparatide ist bis auf die hohe Studien-Abbruchquote unter Verum sehr gut.
Bei Exelixis war bspw. der Kursverlauf vor dem Durchbruch ähnlich. Dies soll jedoch nicht heissen, dass der zukünftige Kurs ein ähnliches Potenzial hat: ich rechne bei RDUS nicht mit einer kurzfristigen Verzehnfachung, eine Verdoppelung im Anschluss an die Zulassung - diese halte ich auf Ende Juni 17 für sehr wahrscheinlich- erscheint jedoch realistisch.
Zitat von biopadawan: BB Biotech deckt sich ja gerade ordentlich ein. Meinungen dazu?
Absturz auf $25 halte ich trotz der möglichen Korrektur für etwas übertrieben.
...nur nicht verrückt machen lassen von "Mr. Konjunktiv".
Die Klinik bei Abaloparatide ist bis auf die hohe Studien-Abbruchquote unter Verum sehr gut.
Bei Exelixis war bspw. der Kursverlauf vor dem Durchbruch ähnlich. Dies soll jedoch nicht heissen, dass der zukünftige Kurs ein ähnliches Potenzial hat: ich rechne bei RDUS nicht mit einer kurzfristigen Verzehnfachung, eine Verdoppelung im Anschluss an die Zulassung - diese halte ich auf Ende Juni 17 für sehr wahrscheinlich- erscheint jedoch realistisch.
Antwort auf Beitrag Nr.: 54.586.038 von Cyberhexe am 22.03.17 08:22:40
Natürlich werden Biotechwerte, insbesondere diejenigen, die noch keine Produkte am Markt platzieren, mit einem grossen Hebel von der allgemeinen Marktentwicklung beeinflusst. Wer davon eine fundamentale Schwäche des einzelnen Unternehmen ableitet, tut gut daran, in anderen Branchen zu investieren.
Mr. Konjunktiv ist eigentlich zu viel der Ehre, weil Sprechblasen , oft in einem fürchterlichen Denglisch, immer dann verbreitet werden, wenn diese von einem entsprechenden Kursverlauf gestützt werden. Substanziellen Wert haben diese Beiträge äusserst selten.
Zitat von Cyberhexe:Zitat von biopadawan: BB Biotech deckt sich ja gerade ordentlich ein. Meinungen dazu?
Absturz auf $25 halte ich trotz der möglichen Korrektur für etwas übertrieben.
...nur nicht verrückt machen lassen von "Mr. Konjunktiv".
Die Klinik bei Abaloparatide ist bis auf die hohe Studien-Abbruchquote unter Verum sehr gut.
Bei Exelixis war bspw. der Kursverlauf vor dem Durchbruch ähnlich. Dies soll jedoch nicht heissen, dass der zukünftige Kurs ein ähnliches Potenzial hat: ich rechne bei RDUS nicht mit einer kurzfristigen Verzehnfachung, eine Verdoppelung im Anschluss an die Zulassung - diese halte ich auf Ende Juni 17 für sehr wahrscheinlich- erscheint jedoch realistisch.
Natürlich werden Biotechwerte, insbesondere diejenigen, die noch keine Produkte am Markt platzieren, mit einem grossen Hebel von der allgemeinen Marktentwicklung beeinflusst. Wer davon eine fundamentale Schwäche des einzelnen Unternehmen ableitet, tut gut daran, in anderen Branchen zu investieren.
Mr. Konjunktiv ist eigentlich zu viel der Ehre, weil Sprechblasen , oft in einem fürchterlichen Denglisch, immer dann verbreitet werden, wenn diese von einem entsprechenden Kursverlauf gestützt werden. Substanziellen Wert haben diese Beiträge äusserst selten.
Antwort auf Beitrag Nr.: 54.586.242 von Cyberhexe am 22.03.17 08:40:36Man muss dazu nur sagen, dass Cyberhexe im Mai 2016 RDUS für 35 USD gekauft hat mit Kursziel 90+ USD - recht euphorisch, das sieht man auch daran, dass sie dafür große Teile ihrer EXEL für nur 6 USD abgestoßen hat. Im November / Dezember ist sie mit einer massiven Depotübergewichtung sogar noch euphorischer geworden und hat in den 40ern massiv dazugekauft, nur um dann im Januar wieder abzubauen. Die Verzögerungen der EMA wurden längere Zeit als harmlos ignoriert. So viel zu ihrer eigenen Einschätzungs-Kompetenz, die ich massiv in Frage stelle.
An deine Adresse muss gesagt werden: Zu Börse gehört eben mehr als nur die wissenschaftliche Einschätzung (die zudem recht falsch sein kann, v.a. wenn man nicht alle Fakten kennt), es gehört dazu auch noch das Sentiment der Investoren (das ist noch zu gut) zu bemessen, die charttechnische Lage (und die sieht für mich nicht gut aus und weist Richtung 25 USD) einzuschätzen und noch ein paar andere Dinge....
Selbst wenn die Zulassung kommt besteht eine gewisse Chance auf unter 30 vor 50.
An deine Adresse muss gesagt werden: Zu Börse gehört eben mehr als nur die wissenschaftliche Einschätzung (die zudem recht falsch sein kann, v.a. wenn man nicht alle Fakten kennt), es gehört dazu auch noch das Sentiment der Investoren (das ist noch zu gut) zu bemessen, die charttechnische Lage (und die sieht für mich nicht gut aus und weist Richtung 25 USD) einzuschätzen und noch ein paar andere Dinge....
Selbst wenn die Zulassung kommt besteht eine gewisse Chance auf unter 30 vor 50.
Selbst wenn die Zulassung kommt besteht eine gewisse Chance auf unter 30 vor 50.
(Die unter 30 bezieht sich dabei auf vor einer möglichen Zulassung)
Aber, das sollte man auch noch erwähnen: selbst bei einer Zulassung hängt es davon ab, ob RDUS Aussicht hat ohne neue Verwässerungen aus eigener Kraft in die Gewinnzone zu gelangen. Das Cash, das die Firma aktuell verbrennt ist ja gigantisch, zumal man jetzt neben den massiven F&E Ausgaben auch noch eine riesige Salesforce mit mehr als 230 Personen hat, die aktuell nur rumsitzt und 25-35 Mio USD im Jahr verbraucht...fraglich ob sie mit "aba" genug Marktanteile gegen die bestehenden und neuen Player gewinnen können..
(Die unter 30 bezieht sich dabei auf vor einer möglichen Zulassung)
Aber, das sollte man auch noch erwähnen: selbst bei einer Zulassung hängt es davon ab, ob RDUS Aussicht hat ohne neue Verwässerungen aus eigener Kraft in die Gewinnzone zu gelangen. Das Cash, das die Firma aktuell verbrennt ist ja gigantisch, zumal man jetzt neben den massiven F&E Ausgaben auch noch eine riesige Salesforce mit mehr als 230 Personen hat, die aktuell nur rumsitzt und 25-35 Mio USD im Jahr verbraucht...fraglich ob sie mit "aba" genug Marktanteile gegen die bestehenden und neuen Player gewinnen können..
Antwort auf Beitrag Nr.: 54.586.959 von Ville7 am 22.03.17 09:43:11
...wie so oft blendet der Teilnehmer ville7 in seinen dummen Beiträgen entweder einen wichtigen Teil der Information aus oder begnügt sich, wenn überhaupt, mit Halbwahrheiten. Obschon dieser Thread eigentlich nicht dazu gedacht ist, mein Risikomanagement zu diskutieren, möchte ich den zitierten Beitrag zum Anlass nehmen, das kleingeistige und diffamierende Auftreten dieses Teilnehmers aufzuzeigen:
Da sich das Risikomanagement neben Radius Health RDUS auf Exelixis EXEL bezieht möchte ich auf Beitrag Nr. 32 aus dem Thread: Exelixis....ein schlafender Riese? USD 3.40 am 14.5.2014 verweisen:
Cyberhexe schrieb am 27.09.14 18:05:26 Beitrag Nr. 32 ( 47.891.537 )
Antwort auf Beitrag Nr.: 47.594.053
"Für mich ist dieser Kurs (USD 1.56 am 26.9.14) ein "strong buy" - habe gestern mein letztes trockenes Pulver in Exelixis investiert bei einem mittlerweile unvernünftigen Investitionsgrad ...aber die Verlockung ist nun mal zu gross! gltal"
Nachdem ich diesen Thread am 14.5.14 bei einem Kurs von USD 3.40 gestartet hatte - da war die Streitkultur noch vorbildlich-, und sich dieser bis September 2014 noch einmal halbiert hat, war ich "all in one, all in Exelixis" investiert - eigentlich wusste und weiss ich, dass ein derartiger Investitionsgrad unvernünftig ist, aber die Verlockung und die Aussichten waren für mich zu gross. Ab einem Kurs von USD 5.50 habe ich begonnen, EXEL-Anteile zu verkaufen und zwar stetig - bei einem Kurs von USD 14 hatte ich nur noch knapp die Hälfte und aktuell lediglich noch 5% (bezogen auf die Stückzahl) von der ursprünglichen Anzahl. Meine Profilneurose verlangt jedoch nicht danach, den Gewinn bis zur 2 Dezimalstelle zu verkünden - darum geht es in diesem Thread nicht. Dieser Thread wurde eröffnet, um Informationen und Einschätzungen zu Radius Health auszutauschen, jedoch nicht dazu, um mit dümmlichen Kommentaren andere Forumsteilnehmer anzugreifen.
Aber ich befürchte, weitere Angriffe dieses Trittbrettfahrers werden nicht ausbleiben.
Und ausserdem....gestern und heute habe ich weitere RDUS-Anteile erworben!
Zitat von Ville7: Man muss dazu nur sagen, dass Cyberhexe im Mai 2016 RDUS für 35 USD gekauft hat mit Kursziel 90+ USD - recht euphorisch, das sieht man auch daran, dass sie dafür große Teile ihrer EXEL für nur 6 USD abgestoßen hat. Im November / Dezember ist sie mit einer massiven Depotübergewichtung sogar noch euphorischer geworden und hat in den 40ern massiv dazugekauft, nur um dann im Januar wieder abzubauen. Die Verzögerungen der EMA wurden längere Zeit als harmlos ignoriert. So viel zu ihrer eigenen Einschätzungs-Kompetenz, die ich massiv in Frage stelle.
...wie so oft blendet der Teilnehmer ville7 in seinen dummen Beiträgen entweder einen wichtigen Teil der Information aus oder begnügt sich, wenn überhaupt, mit Halbwahrheiten. Obschon dieser Thread eigentlich nicht dazu gedacht ist, mein Risikomanagement zu diskutieren, möchte ich den zitierten Beitrag zum Anlass nehmen, das kleingeistige und diffamierende Auftreten dieses Teilnehmers aufzuzeigen:
Da sich das Risikomanagement neben Radius Health RDUS auf Exelixis EXEL bezieht möchte ich auf Beitrag Nr. 32 aus dem Thread: Exelixis....ein schlafender Riese? USD 3.40 am 14.5.2014 verweisen:
Cyberhexe schrieb am 27.09.14 18:05:26 Beitrag Nr. 32 ( 47.891.537 )
Antwort auf Beitrag Nr.: 47.594.053
"Für mich ist dieser Kurs (USD 1.56 am 26.9.14) ein "strong buy" - habe gestern mein letztes trockenes Pulver in Exelixis investiert bei einem mittlerweile unvernünftigen Investitionsgrad ...aber die Verlockung ist nun mal zu gross! gltal"
Nachdem ich diesen Thread am 14.5.14 bei einem Kurs von USD 3.40 gestartet hatte - da war die Streitkultur noch vorbildlich-, und sich dieser bis September 2014 noch einmal halbiert hat, war ich "all in one, all in Exelixis" investiert - eigentlich wusste und weiss ich, dass ein derartiger Investitionsgrad unvernünftig ist, aber die Verlockung und die Aussichten waren für mich zu gross. Ab einem Kurs von USD 5.50 habe ich begonnen, EXEL-Anteile zu verkaufen und zwar stetig - bei einem Kurs von USD 14 hatte ich nur noch knapp die Hälfte und aktuell lediglich noch 5% (bezogen auf die Stückzahl) von der ursprünglichen Anzahl. Meine Profilneurose verlangt jedoch nicht danach, den Gewinn bis zur 2 Dezimalstelle zu verkünden - darum geht es in diesem Thread nicht. Dieser Thread wurde eröffnet, um Informationen und Einschätzungen zu Radius Health auszutauschen, jedoch nicht dazu, um mit dümmlichen Kommentaren andere Forumsteilnehmer anzugreifen.
Aber ich befürchte, weitere Angriffe dieses Trittbrettfahrers werden nicht ausbleiben.
Und ausserdem....gestern und heute habe ich weitere RDUS-Anteile erworben!
Antwort auf Beitrag Nr.: 54.593.736 von Cyberhexe am 23.03.17 00:20:18"dumm, Lügner, kleingeistig, diffammierend, profilneurotisch, Trittbrettfahrer,... "
Na da haust du ja was raus. Die Wahrheit, zudem noch nachzulesen in diesem und anderen Threads tut weh (für dich). Steh einfach dazu, dass du nicht das bist für was du dich hier stets darstellst. Über das Trittbrettfahrer habe ich am herzlichsten gelacht, wahrscheinlich denkst du in deiner Hybris noch ich würde bei dir abschauen.
Das sagt zudem jemand, der seine Zuversicht nach den Verzögerungen mit der Positionierung von BBBiotech begründet? Bei EXEL war ich zu 4.x mit einer ersten Position schon vor 2014 an Board und mein damaliger Einstieg hatte null mit dir zu tun, hier muss ich dich auch enttäuschen. Ich hoffe das killt nun nicht dein überhöhtes Ego und du springst jetzt nicht von der Brücke.
Nachdem du jetzt in RDUS angeblich wieder mal aufgestockt hast ist in 2-3 Monaten sicherlich zu lesen, dass du nun nur noch 15% Depotanteil hast (vor Aufstockung 25%)...wie schon mal, als es von 50% Depotanteil plötzlich nur noch 25% waren... Aber so ist es halt mit deinen "Wahrheiten". Sollte aba weiter verzögert oder nicht zugelassen werden hattest du dann sicher zuvor auf wundersame Weise 0% im Depot gehabt...
Na da haust du ja was raus. Die Wahrheit, zudem noch nachzulesen in diesem und anderen Threads tut weh (für dich). Steh einfach dazu, dass du nicht das bist für was du dich hier stets darstellst. Über das Trittbrettfahrer habe ich am herzlichsten gelacht, wahrscheinlich denkst du in deiner Hybris noch ich würde bei dir abschauen.
Das sagt zudem jemand, der seine Zuversicht nach den Verzögerungen mit der Positionierung von BBBiotech begründet? Bei EXEL war ich zu 4.x mit einer ersten Position schon vor 2014 an Board und mein damaliger Einstieg hatte null mit dir zu tun, hier muss ich dich auch enttäuschen. Ich hoffe das killt nun nicht dein überhöhtes Ego und du springst jetzt nicht von der Brücke.
Nachdem du jetzt in RDUS angeblich wieder mal aufgestockt hast ist in 2-3 Monaten sicherlich zu lesen, dass du nun nur noch 15% Depotanteil hast (vor Aufstockung 25%)...wie schon mal, als es von 50% Depotanteil plötzlich nur noch 25% waren... Aber so ist es halt mit deinen "Wahrheiten". Sollte aba weiter verzögert oder nicht zugelassen werden hattest du dann sicher zuvor auf wundersame Weise 0% im Depot gehabt...
Antwort auf Beitrag Nr.: 54.593.970 von Ville7 am 23.03.17 04:30:27
ebenfalls wie so oft: selbst beim Zitieren ist dieser Teilnehmer nicht korrekt!
Richtig zitiert müsste es heissen: "dumme Beiträge,", "Halbwahrheiten", "meine Profilneurose".
Und ausserdem....nicht bei jedem Nachkauf verdoppelt sich der prozentuale Anteil einer Aktie!
Aber noch einmal, dieser Thread hat nicht das Risiko-Management eines Teilnehmers zum Thema....sondern RADIUS HEALTH.
Zitat von Ville7: "dumm, Lügner, kleingeistig, diffammierend, profilneurotisch, Trittbrettfahrer,... "
ebenfalls wie so oft: selbst beim Zitieren ist dieser Teilnehmer nicht korrekt!
Richtig zitiert müsste es heissen: "dumme Beiträge,", "Halbwahrheiten", "meine Profilneurose".
Und ausserdem....nicht bei jedem Nachkauf verdoppelt sich der prozentuale Anteil einer Aktie!

Aber noch einmal, dieser Thread hat nicht das Risiko-Management eines Teilnehmers zum Thema....sondern RADIUS HEALTH.
Antwort auf Beitrag Nr.: 54.586.959 von Ville7 am 22.03.17 09:43:11
Die Verzögerung bei der EMA waren der Grund, dass die Depotgewichtung von RDUS reduziert wurde.
Die Aussage dieses Teilnehmers scheint jedoch lediglich das Ziel zu haben, das Wunschergebnis (unterstrichen) zu präsentieren, auch wenn die zielführende Kausalkette noch so lächerlich ist.
Die Krönung ist natürlich die "grüne" Aussage. Die ist fast schon zirkusreif!
Diese ist wirklich nicht zu übertreffen!
Zitat von Ville7: Man muss dazu nur sagen, dass Cyberhexe im Mai 2016 RDUS für 35 USD gekauft hat mit Kursziel 90+ USD - recht euphorisch, das sieht man auch daran, dass sie dafür große Teile ihrer EXEL für nur 6 USD abgestoßen hat. Im November / Dezember ist sie mit einer massiven Depotübergewichtung sogar noch euphorischer geworden und hat in den 40ern massiv dazugekauft, nur um dann im Januar wieder abzubauen. Die Verzögerungen der EMA wurden längere Zeit als harmlos ignoriert. So viel zu ihrer eigenen Einschätzungs-Kompetenz, die ich massiv in Frage stelle.
An deine Adresse muss gesagt werden: Zu Börse gehört eben mehr als nur die wissenschaftliche Einschätzung (die zudem recht falsch sein kann, v.a. wenn man nicht alle Fakten kennt), es gehört dazu auch noch das Sentiment der Investoren (das ist noch zu gut) zu bemessen, die charttechnische Lage (und die sieht für mich nicht gut aus und weist Richtung 25 USD) einzuschätzen und noch ein paar andere Dinge....
Selbst wenn die Zulassung kommt besteht eine gewisse Chance auf unter 30 vor 50.
Die Verzögerung bei der EMA waren der Grund, dass die Depotgewichtung von RDUS reduziert wurde.
Die Aussage dieses Teilnehmers scheint jedoch lediglich das Ziel zu haben, das Wunschergebnis (unterstrichen) zu präsentieren, auch wenn die zielführende Kausalkette noch so lächerlich ist.
Die Krönung ist natürlich die "grüne" Aussage. Die ist fast schon zirkusreif!

Diese ist wirklich nicht zu übertreffen!
institutionelle Anleger haben in 1q17 die Position in RDUS aufgestockt:
https://hedgemind.com/real-time-insights/stock-holdings?tick…
Meine Einschätzung der Zulassungswahrscheinlichkeit ist nach wie vor hoch. Das einzige Fragezeichen sehe ich bei der relativ hohen Anzahl der Studienabbrecher unter Verum. Ich glaube jedoch nicht, dass dies die Zulassung verhindert.
In der Gerüchteküche werden die finalen Labeldiskussionen für die Verzögerung verantwortlich gemacht. Ich weiss jedoch nicht, wie nah diese Einschätzungen an der Wirklichkeit sind?
https://hedgemind.com/real-time-insights/stock-holdings?tick…
Meine Einschätzung der Zulassungswahrscheinlichkeit ist nach wie vor hoch. Das einzige Fragezeichen sehe ich bei der relativ hohen Anzahl der Studienabbrecher unter Verum. Ich glaube jedoch nicht, dass dies die Zulassung verhindert.
In der Gerüchteküche werden die finalen Labeldiskussionen für die Verzögerung verantwortlich gemacht. Ich weiss jedoch nicht, wie nah diese Einschätzungen an der Wirklichkeit sind?
Antwort auf Beitrag Nr.: 54.594.615 von Cyberhexe am 23.03.17 08:14:03Es geht um deine Ehrlichkeit vs. deine Selbstdarstellung als Wissenschafts- und Investmentgenie, egal welche Aktie betroffen ist. Da gibt es eine klaffende Diskrepanz. Punkt.
PS: Wenn du schon Sätze von mir grün markierst und dich darüber lustig machst solltest du schon die von mir sofort nach dem Posting präzisierte bzw. korrigierte Version dieses Satzes verwenden. Alles andere ist (wie meistens bei dir) unseriös.
PS: Wenn du schon Sätze von mir grün markierst und dich darüber lustig machst solltest du schon die von mir sofort nach dem Posting präzisierte bzw. korrigierte Version dieses Satzes verwenden. Alles andere ist (wie meistens bei dir) unseriös.
Antwort auf Beitrag Nr.: 54.586.959 von Ville7 am 22.03.17 09:43:11
Diese wirklich fast zirkusreife Aussage steht stellvertretend für das Niveau dieses Teilnehmers. Eine gewisse Chance besteht natürlich auch, dass der Eifelturm diese Woche noch umfällt oder dass heute noch ein Erdbeben die Stadt Basel zerstört (wie im Jahre 1356). Wenn allerdings solche Aussagen nicht mit einer Eintrittswahrscheinlichkeit versehen sind, dann sind diese schlichtweg nicht zu gebrauchen!
Zitat von Ville7: Selbst wenn die Zulassung kommt besteht eine gewisse Chance auf unter 30 vor 50.
Diese wirklich fast zirkusreife Aussage steht stellvertretend für das Niveau dieses Teilnehmers. Eine gewisse Chance besteht natürlich auch, dass der Eifelturm diese Woche noch umfällt oder dass heute noch ein Erdbeben die Stadt Basel zerstört (wie im Jahre 1356). Wenn allerdings solche Aussagen nicht mit einer Eintrittswahrscheinlichkeit versehen sind, dann sind diese schlichtweg nicht zu gebrauchen!
Antwort auf Beitrag Nr.: 54.595.053 von Ville7 am 23.03.17 09:14:13
...wieder nichts begriffen! Es geht nicht um den Zeitpunkt (vor oder nach Zulassung) sondern um das Risiko. Eine "gewisse Chance" besteht auch, dass ein Ahnungsloser dies kapiert. Die Eintrittswahrscheinlichkeit dafür halte ich jedoch für sehr gering sein.
Zitat von Ville7: PS: Wenn du schon Sätze von mir grün markierst und dich darüber lustig machst solltest du schon die von mir sofort nach dem Posting präzisierte bzw. korrigierte Version dieses Satzes verwenden. Alles andere ist (wie meistens bei dir) unseriös.
...wieder nichts begriffen! Es geht nicht um den Zeitpunkt (vor oder nach Zulassung) sondern um das Risiko. Eine "gewisse Chance" besteht auch, dass ein Ahnungsloser dies kapiert. Die Eintrittswahrscheinlichkeit dafür halte ich jedoch für sehr gering sein.
Antwort auf Beitrag Nr.: 54.595.188 von Cyberhexe am 23.03.17 09:29:40Für dich sind alle dumm außer du selbst. Du bist der klügste Mensch auf Erden. Schon länger kapiert.
Nochmal für dich zum Mitlesen: Wenn die Biotechs im Gesamten (NBI, IBB) auf eine erneute große Korrektur geschickt werden, dann wären Kurse unter 30 für RDUS nicht abwegig, ja sogar recht wahrscheinlich. So einfach ist das, manchmal wahrscheinlich zu einfach für Hochintellektuelle (oder die die sich dafür halten). Gelle.
Nochmal für dich zum Mitlesen: Wenn die Biotechs im Gesamten (NBI, IBB) auf eine erneute große Korrektur geschickt werden, dann wären Kurse unter 30 für RDUS nicht abwegig, ja sogar recht wahrscheinlich. So einfach ist das, manchmal wahrscheinlich zu einfach für Hochintellektuelle (oder die die sich dafür halten). Gelle.
nun bei 38.5 - hier entscheidet sich, ob die Charttechnik wieder bullish wird - das wäre Schlusskurs klar oberhalb dieser 38.5. Dann wäre von der Charttechnikseite her wieder grünes Licht und der Bruch darunter eine Bärenfalle....
Antwort auf Beitrag Nr.: 54.595.503 von Ville7 am 23.03.17 09:59:19
...schon wieder falsch: für mich sind nicht alle dumm. Die allermeisten deiner Beiträge finde ich in der Tat jedoch nichtssagend bis dümmlich!
Noch einmal ein Hinweis zur Zulassungswahrscheinlichkeit von Abaloparatide (PDUFA 30.6.17): obschon ich die Wahrscheinlichkeit auf Zulassung sehr hoch einschätze (schwierig die genau zu beziffern...ich würde mal ca. 80% zur Diskussion stellen) ist diese wie viele anderen Zulassungsentscheidungen mit einem Fragezeichen versehen (grösstes Defizit aus meiner Sicht ist die hohe Rate an Studienabbrecher unter Verum, also unter Abaloparatide). Diese Unsicherheit ist jedoch auch die Chance, da eine zu fast 100% erwartete Zulassung oft schon vor der eigentlichen Entscheidung in den Wert des Unternehmens eingepreist wird.
Der grosse Vorteil von Abaloparatide ist die mit stat. Signifikanz nachgewiesene Reduktion der nicht die Wiebelsäule betreffenden Frakturen. Bei Amgens Romosozumab wurde dies ebenfalls erwartet, ist jedoch nicht eingetroffen --> p= 0.096. Dies ist ein eindeutiger Wettbewerbsvoprteil für Abaloparatide.
"Romosozumab resulted in a 25 percent reduction compared to placebo in the relative risk of non-vertebral fractures through month 12, another secondary endpoint, but the reduced risk was not statistically significant (fracture incidence 1.6 percent versus 2.1 percent, respectively, [p=0.096]). For the non-vertebral fracture endpoint, the overall fracture incidence in the study was lower than expected (2.1 percent in the placebo group in year one versus an expected rate of 3.5 percent)."
The ACTIVE results showed that patients treated with daily abaloparatide for 18 months had a significantly greater reduction in the incidence of new vertebral fractures (p < 0.001) and nonvertebral fractures (p = 0.049) compared to placebo.
Falls die Zulassung erteilt wird, wäre der Nachweis der Wirksamkeit bei transdermaler Applikation ein weitere Innovationssprung, der sich überaus positiv auf die Akzeptanz bei den Patienten auswirken sollte.
Zitat von Ville7: Für dich sind alle dumm außer du selbst. Du bist der klügste Mensch auf Erden. Schon länger kapiert.
...schon wieder falsch: für mich sind nicht alle dumm. Die allermeisten deiner Beiträge finde ich in der Tat jedoch nichtssagend bis dümmlich!
Noch einmal ein Hinweis zur Zulassungswahrscheinlichkeit von Abaloparatide (PDUFA 30.6.17): obschon ich die Wahrscheinlichkeit auf Zulassung sehr hoch einschätze (schwierig die genau zu beziffern...ich würde mal ca. 80% zur Diskussion stellen) ist diese wie viele anderen Zulassungsentscheidungen mit einem Fragezeichen versehen (grösstes Defizit aus meiner Sicht ist die hohe Rate an Studienabbrecher unter Verum, also unter Abaloparatide). Diese Unsicherheit ist jedoch auch die Chance, da eine zu fast 100% erwartete Zulassung oft schon vor der eigentlichen Entscheidung in den Wert des Unternehmens eingepreist wird.
Der grosse Vorteil von Abaloparatide ist die mit stat. Signifikanz nachgewiesene Reduktion der nicht die Wiebelsäule betreffenden Frakturen. Bei Amgens Romosozumab wurde dies ebenfalls erwartet, ist jedoch nicht eingetroffen --> p= 0.096. Dies ist ein eindeutiger Wettbewerbsvoprteil für Abaloparatide.
"Romosozumab resulted in a 25 percent reduction compared to placebo in the relative risk of non-vertebral fractures through month 12, another secondary endpoint, but the reduced risk was not statistically significant (fracture incidence 1.6 percent versus 2.1 percent, respectively, [p=0.096]). For the non-vertebral fracture endpoint, the overall fracture incidence in the study was lower than expected (2.1 percent in the placebo group in year one versus an expected rate of 3.5 percent)."
The ACTIVE results showed that patients treated with daily abaloparatide for 18 months had a significantly greater reduction in the incidence of new vertebral fractures (p < 0.001) and nonvertebral fractures (p = 0.049) compared to placebo.
Falls die Zulassung erteilt wird, wäre der Nachweis der Wirksamkeit bei transdermaler Applikation ein weitere Innovationssprung, der sich überaus positiv auf die Akzeptanz bei den Patienten auswirken sollte.
The quest for new drugs to prevent osteoporosis-related fractures
Abstract
There is a need for the development of new drugs to prevent osteoporosis-related fractures. Fractures are projected to increase and the present drugs have modest efficacy, significant side-effects and poor compliance. To illustrate the difficulties in the development of new drugs, the author reviews the fate of several drugs that have failed to gain regulatory approval. These drugs include arzoxifene, lasofoxifene, MK-5442, roncalceret and odanacatib. Romosozumab and abaloparatide are the only new drugs presently in phase-3 development. It is anticipated that ongoing studies of the mechanisms and signaling pathways involved in the regulation of bone remodeling will open up new opportunities for targeted pharmacological interventions to increase bone strength. However, the perfect drug is still a long way off and will face many obstacles before approval.
http://www.tandfonline.com/doi/full/10.1080/13697137.2017.12…
Abstract
There is a need for the development of new drugs to prevent osteoporosis-related fractures. Fractures are projected to increase and the present drugs have modest efficacy, significant side-effects and poor compliance. To illustrate the difficulties in the development of new drugs, the author reviews the fate of several drugs that have failed to gain regulatory approval. These drugs include arzoxifene, lasofoxifene, MK-5442, roncalceret and odanacatib. Romosozumab and abaloparatide are the only new drugs presently in phase-3 development. It is anticipated that ongoing studies of the mechanisms and signaling pathways involved in the regulation of bone remodeling will open up new opportunities for targeted pharmacological interventions to increase bone strength. However, the perfect drug is still a long way off and will face many obstacles before approval.
http://www.tandfonline.com/doi/full/10.1080/13697137.2017.12…
Antwort auf Beitrag Nr.: 54.607.941 von Cyberhexe am 24.03.17 18:20:29Jo, dann hältst du eben nur mich wegen meiner stets dümmlichen und nichtssagenden Beiträge für dumm. Du bist halt soooo gescheit. Lassen wir das mal so stehen.
Du suggerierst, dass im Moment in RDUS wenig Zulassungswahrscheinlichkeit eingepreist ist und dass eine Einpreisung von 100% bis kurz vor der Zulassung (auch hier) wahrscheinlich und üblich ist (sonst hättest du das nicht geschrieben).
Über so viel Klugheit kann ich nur schmunzeln.
1. Bei RDUS ist aktuell weiterhin eine Zulassungswahrscheinlichkeit von weit mehr als 50% eingepreist, sonst stünde der Kurs in den 20ern oder noch viel tiefer. Vor allem die großen Investoren wie BBBiotech stützen aktuell die Aktie, was bedeutet, dass sie von einer Zulassung ausgehen. Siehe letzte Zukäufe.
2. Nach der ganzen Vorgeschichte (EMA verzögert, RDUS kann Fragen nicht oder nicht rechtzeitig beantworten, FDA verschiebt, ...) wird es niemals zu einer vollständigen Einpreisung vor einer Zulassung kommen. Ganz so dümmlich ist der Markt nicht ...
Aber das war mal wieder ein dümmliches Post von einem dummen Anfänger. Du weißt alles besser. Erhelle uns bitte!
Du suggerierst, dass im Moment in RDUS wenig Zulassungswahrscheinlichkeit eingepreist ist und dass eine Einpreisung von 100% bis kurz vor der Zulassung (auch hier) wahrscheinlich und üblich ist (sonst hättest du das nicht geschrieben).
Über so viel Klugheit kann ich nur schmunzeln.
1. Bei RDUS ist aktuell weiterhin eine Zulassungswahrscheinlichkeit von weit mehr als 50% eingepreist, sonst stünde der Kurs in den 20ern oder noch viel tiefer. Vor allem die großen Investoren wie BBBiotech stützen aktuell die Aktie, was bedeutet, dass sie von einer Zulassung ausgehen. Siehe letzte Zukäufe.
2. Nach der ganzen Vorgeschichte (EMA verzögert, RDUS kann Fragen nicht oder nicht rechtzeitig beantworten, FDA verschiebt, ...) wird es niemals zu einer vollständigen Einpreisung vor einer Zulassung kommen. Ganz so dümmlich ist der Markt nicht ...
Aber das war mal wieder ein dümmliches Post von einem dummen Anfänger. Du weißt alles besser. Erhelle uns bitte!
Ich stell mir die Frage, ob alle Schweizer so arrogant und überheblich sind...
Antwort auf Beitrag Nr.: 54.609.255 von kmastra am 24.03.17 21:25:13Die Seite wurde wieder vom Netz genommen. Es ist auch ein kapitaler Fehler und nicht erlaubt gewesen, diese VOR Zulassung online zu stellen. Das wird die FDA / EMA sicher nicht gerade erfreuen. Ob das weitere Konsequenzen für die Firma haben wird, weiß ich nicht.
Im Übrigen finde ich diese Art Werbung nicht gut. Mit schwarzem Humor kann ich da nichts begründen. Es geht doch um Menschen und Patienten! Bei dieser Art Werbung geht es um Erzeugung von Angst und um den reinen Vermarktungserfolg aufgrund der Angst der Leute. Das finde ich nicht gut!
Im Übrigen finde ich diese Art Werbung nicht gut. Mit schwarzem Humor kann ich da nichts begründen. Es geht doch um Menschen und Patienten! Bei dieser Art Werbung geht es um Erzeugung von Angst und um den reinen Vermarktungserfolg aufgrund der Angst der Leute. Das finde ich nicht gut!
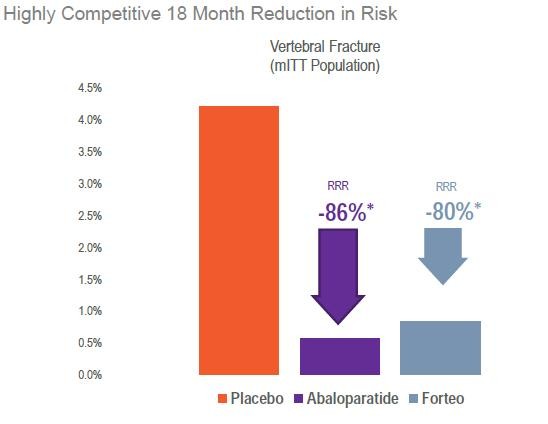
interessante Grafik über die Auswertung der Phase 3 ACTIVE, die trotz der hohen Studienabbruchrate unter Verum darauf hinweist, dass alle Patienten, die am Anfang der Studie in die Verum-Gruppe oder die Placebo-Gruppe aufgenommen wurden, in der Ergebnisauswertung berücksichtigt sind, also auch die Studienabbrecher --> Intention to treat.
Desweiteren eine interessante Zusammenfassung der Mayo Clinic zur Erweiterungsstudie von ACTIVE --> ACTIVE Extend
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
"During the first 6 months of ACTIVExtend, there were 7 new morphometric vertebral fractures in the PBO/ALN group and 0 in the ABL-SC/ALN group. New morphometric vertebral fractures over 25 months occurred in 4.4% of the PBO/ALN group vs 0.55% of the ABL-SC/ALN group, representing an 87% relative risk reduction for new morphometric vertebral fractures (relative risk, 0.13; 95% CI, 0.04-0.41; P<.001)."
Die FDA verlangt keine weiteren Daten:
The FDA stated that the PDUFA goal date has been extended by three months to allow for a full review of the submission. In the letter, the FDA has not requested any additional information from the company.
http://files.shareholder.com/downloads/AMDA-1D3H6P/412651335…
Antwort auf Beitrag Nr.: 54.610.239 von Ville7 am 25.03.17 07:14:06
schon wieder falsch!
Meine Aussage war, dass die allermeisten deiner Beiträge nichtssagend bis dümmlich sind. Diese permanent die Fakten verdrehende Angriffslust erinnert mich an eine aktuelle politische Auseinandersetzung!
Zitat von Ville7: Jo, dann hältst du eben nur mich wegen meiner stets dümmlichen und nichtssagenden Beiträge für dumm. Du bist halt soooo gescheit. Lassen wir das mal so stehen.
schon wieder falsch!
Meine Aussage war, dass die allermeisten deiner Beiträge nichtssagend bis dümmlich sind. Diese permanent die Fakten verdrehende Angriffslust erinnert mich an eine aktuelle politische Auseinandersetzung!
Antwort auf Beitrag Nr.: 54.611.685 von Cyberhexe am 25.03.17 14:48:50
Ja, schon wieder falsch, wie immer. Du hast halt immer Recht und ich liege immer falsch. Man muss es immer nur wiederholen, dann es irgendwann Fakt... oder so ähnlich.
Zitat von Cyberhexe: schon wieder falsch!
Meine Aussage war, dass die allermeisten deiner Beiträge nichtssagend bis dümmlich sind. Diese permanent die Fakten verdrehende Angriffslust erinnert mich an eine aktuelle politische Auseinandersetzung!
Ja, schon wieder falsch, wie immer. Du hast halt immer Recht und ich liege immer falsch. Man muss es immer nur wiederholen, dann es irgendwann Fakt... oder so ähnlich.
Die statistische Signifikanz gegenüber Placebo bei den nicht die Wirbelsäule betreffenden Frakturen (p<0.05) ist ein bedeutender Vorteil von Abaloparatide gegenüber Teriparatide (p=02157!):
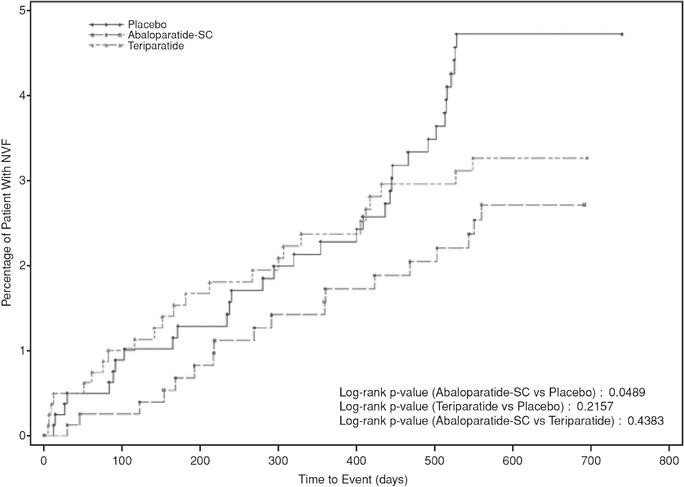

Antwort auf Beitrag Nr.: 54.624.017 von Cyberhexe am 28.03.17 06:22:51
Da auch Amgens romosozumab in der Klinik dieses Ziel verfehlt hat, dürfte Abaloparatide einen grossen Marktanteil für sich beanspruchen - sogar als subkutane Variante.
The final-stage trial of 7,180 post-menopausal women didn’t meet a secondary trial goal of reducing the frequency of non-vertebral fractures, according to the statement.
https://www.bloomberg.com/news/articles/2016-02-22/amgen-ucb…
Zitat von Cyberhexe: Die statistische Signifikanz gegenüber Placebo bei den nicht die Wirbelsäule betreffenden Frakturen (p<0.05) ist ein bedeutender Vorteil von Abaloparatide gegenüber Teriparatide (p=02157!):
Da auch Amgens romosozumab in der Klinik dieses Ziel verfehlt hat, dürfte Abaloparatide einen grossen Marktanteil für sich beanspruchen - sogar als subkutane Variante.
The final-stage trial of 7,180 post-menopausal women didn’t meet a secondary trial goal of reducing the frequency of non-vertebral fractures, according to the statement.
https://www.bloomberg.com/news/articles/2016-02-22/amgen-ucb…
Eine monatliche oder halbjährliche Dosierung wie bei romosozumab ist ein entscheidender Vermarktungsvorteil. Abaloparatide wird es bei einer täglichen Injektionsnotwendigkeit schwer gegen romosozumab haben, trotz signifikanter Studienergebnisse in spine fractures. Einzige Hoffnung ist das transdermal patch und die Hoffnung auf dessen Akzeptanz.
Fazit:
1. Zulassung als tägliche Injektion MUSS erfolgen (sonst erst mal "Gute Nacht!")
2. transdermal patch Verabreichungsform muss kommen
a) durch eine bioäquivalenz-Studie (idealerweise) oder
b) über eine langwierige und teure P3 (das wird der Markt nicht mögen)
Fazit:
1. Zulassung als tägliche Injektion MUSS erfolgen (sonst erst mal "Gute Nacht!")
2. transdermal patch Verabreichungsform muss kommen
a) durch eine bioäquivalenz-Studie (idealerweise) oder
b) über eine langwierige und teure P3 (das wird der Markt nicht mögen)
Antwort auf Beitrag Nr.: 54.513.531 von Cyberhexe am 10.03.17 18:47:22
Anbei ein aktuelles Beispiel, bei welchem der Prüfungszeitraum für einen Zulassungsantrag bei der FDA um 3 Monate verlängert wurde und die Zulassung nun dennoch erteilt wurde:
Roche - Pressemitteilung vom 20.12.2016
http://www.roche.com/media/store/releases/med-cor-2016-12-20…
Roche - Pressemitteilung vom 29.3.2017
http://www.roche.com/media/store/releases/med-cor-2017-03-29…
Zitat von Cyberhexe: ...eine Verzögerung um 3 Monate beim Zulassungsentscheid der FDA ist keine Seltenheit:
The FDA extended the action date to allow time to review information submitted by Radius Health in response to the FDA's Information Requests. The FDA stated that the PDUFA goal date has been extended by three months to allow for a full review of the submission. In the letter, the FDA has not requested any additional information from the Company.
http://files.shareholder.com/downloads/AMDA-1D3H6P/405308119…
Anbei ein aktuelles Beispiel, bei welchem der Prüfungszeitraum für einen Zulassungsantrag bei der FDA um 3 Monate verlängert wurde und die Zulassung nun dennoch erteilt wurde:
Roche - Pressemitteilung vom 20.12.2016
http://www.roche.com/media/store/releases/med-cor-2016-12-20…
Roche - Pressemitteilung vom 29.3.2017
http://www.roche.com/media/store/releases/med-cor-2017-03-29…
Antwort auf Beitrag Nr.: 54.632.186 von Cyberhexe am 29.03.17 07:48:01Kurs erholt sich langsam. Vielleicht knacken wir bald die $40.
Hoffentlich gibt es eine vorzeitige Zulassung Ende Mai.
Hoffentlich gibt es eine vorzeitige Zulassung Ende Mai.
Antwort auf Beitrag Nr.: 54.830.491 von bernie55 am 28.04.17 16:23:24
IRRER Tagesverlauf nach Ankündigung von APPROVAL
38,13 USD - Ankündigung Approval rauf bis 40,50 USD - dann runter bis 37,67 USD - jetzt aktuell 40,05 USD
Zitat von bernie55:FDA Approves RDUS TYMLOS
https://cnafinance.com/radius-health-rdus-stock-soaring-on-f…
https://stocknews.com/news/rdus-radius-health-tymlos-receive…
https://www.accessdata.fda.gov/scripts/cder/daf/index.cfm?ev…
IRRER Tagesverlauf nach Ankündigung von APPROVAL
38,13 USD - Ankündigung Approval rauf bis 40,50 USD - dann runter bis 37,67 USD - jetzt aktuell 40,05 USD
Antwort auf Beitrag Nr.: 54.830.491 von bernie55 am 28.04.17 16:23:24
VIEW of the full approved label
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
Zitat von bernie55:FDA Approves RDUS TYMLOS
VIEW of the full approved label
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
Antwort auf Beitrag Nr.: 54.830.614 von bernie55 am 28.04.17 16:33:25 FDA Approves RDUS TYMLOS
FDA Approves RDUS TYMLOS 
@Cyberhexe and all
Der Anfang ist nun gemacht - der Weg zu höheren Kurse geebnet
- der Weg zu höheren Kurse geebnet 
 FDA Approves RDUS TYMLOS
FDA Approves RDUS TYMLOS 
@Cyberhexe and all
Der Anfang ist nun gemacht
 - der Weg zu höheren Kurse geebnet
- der Weg zu höheren Kurse geebnet 
Antwort auf Beitrag Nr.: 54.830.956 von bernie55 am 28.04.17 17:01:22schöne Bescherung  ...hab die Kurskapriolen noch genutzt und 150 Stück in Frankfurt zu €34,712 erworben.
...hab die Kurskapriolen noch genutzt und 150 Stück in Frankfurt zu €34,712 erworben.
Die Black-Box-Warnung ist nicht dramatisch, da diese derjenigen des Konkurrenzproduktes (Forteo = Teriparatide) entspricht.
Bin mal gespannt wie lange es dauert bis auf USD 50.
 ...hab die Kurskapriolen noch genutzt und 150 Stück in Frankfurt zu €34,712 erworben.
...hab die Kurskapriolen noch genutzt und 150 Stück in Frankfurt zu €34,712 erworben. Die Black-Box-Warnung ist nicht dramatisch, da diese derjenigen des Konkurrenzproduktes (Forteo = Teriparatide) entspricht.
Bin mal gespannt wie lange es dauert bis auf USD 50.
Antwort auf Beitrag Nr.: 54.831.070 von Cyberhexe am 28.04.17 17:11:04hab in Frankfurt nochmal 250 geordert und zwar mit Limit €38,05 - müsste noch durchgehen!
Antwort auf Beitrag Nr.: 54.831.070 von Cyberhexe am 28.04.17 17:11:04
Zitat von Cyberhexe: schöne Bescherung...hab die Kurskapriolen noch genutzt und 150 Stück in Frankfurt zu €34,712 erworben.
Aber HALLO....nochmal zugeschlagen
Die Black-Box-Warnung ist nicht dramatisch, da diese derjenigen des Konkurrenzproduktes (Forteo = Teriparatide) entspricht. Das klingt gut
Bin mal gespannt wie lange es dauert bis auf USD 50
Nicht nur Du .
Mit Zulassung schafft es das Ding nicht mal dauerhaft über die 40.
Black Box Warning genauso heftig wie bei Forteo.
DasRisiko von Osteosarcoma ist nicht ohne... wahrscheinlich ist das auch der Punkt an dem die EMA rum macht.
DasRisiko von Osteosarcoma ist nicht ohne... wahrscheinlich ist das auch der Punkt an dem die EMA rum macht.
Antwort auf Beitrag Nr.: 54.831.289 von bernie55 am 28.04.17 17:32:59https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
....osteosarcoma, a malignant bone tumor, in male and female rats. It is ....
Bei Teriparatide (brand Forteo) ist das Label fast identisch - ebenfalls Black-Box Warning:
"In male and female rats, teriparatide caused an increase in the incidence of osteosarcoma..."
https://www.accessdata.fda.gov/drugsatfda_docs/label/2004/21…
....osteosarcoma, a malignant bone tumor, in male and female rats. It is ....
Bei Teriparatide (brand Forteo) ist das Label fast identisch - ebenfalls Black-Box Warning:
"In male and female rats, teriparatide caused an increase in the incidence of osteosarcoma..."
https://www.accessdata.fda.gov/drugsatfda_docs/label/2004/21…
Antwort auf Beitrag Nr.: 54.831.688 von Cyberhexe am 28.04.17 18:02:24Eli Lilly hat am 31.1.17 für Forteo folgende Umsätze bekanntgegeben:
422.5 mUSD für 4/2016
377.9 mUSD für 4/2015
12% Steigerung
1,500.0 mUSD für 2016
1,348.3 mUSD für 2015
https://investor.lilly.com/releasedetail.cfm?ReleaseID=10096…
Abaloparatide hat jedoch auch eine stat. signifikante Verringerung der nicht die Wirbelsäule betreffenden Frakturen. Vorteil ...wie heisst das Ding nochmal? TYMLOS®
422.5 mUSD für 4/2016
377.9 mUSD für 4/2015
12% Steigerung
1,500.0 mUSD für 2016
1,348.3 mUSD für 2015
https://investor.lilly.com/releasedetail.cfm?ReleaseID=10096…
Abaloparatide hat jedoch auch eine stat. signifikante Verringerung der nicht die Wirbelsäule betreffenden Frakturen. Vorteil ...wie heisst das Ding nochmal? TYMLOS®
Die Börse feiert die Zulassung mit einem Kursverlust.
Antwort auf Beitrag Nr.: 54.831.796 von Cyberhexe am 28.04.17 18:08:40soeben alle Progenics verkauft und dafür weitere RDUS ...unter USD 39! wow!! 

Antwort auf Beitrag Nr.: 54.586.038 von Cyberhexe am 22.03.17 08:22:40
Zitat von Cyberhexe:Zitat von biopadawan: BB Biotech deckt sich ja gerade ordentlich ein. Meinungen dazu?
Absturz auf $25 halte ich trotz der möglichen Korrektur für etwas übertrieben.
...nur nicht verrückt machen lassen von "Mr. Konjunktiv".
Die Klinik bei Abaloparatide ist bis auf die hohe Studien-Abbruchquote unter Verum sehr gut.
Bei Exelixis war bspw. der Kursverlauf vor dem Durchbruch ähnlich. Dies soll jedoch nicht heissen, dass der zukünftige Kurs ein ähnliches Potenzial hat: ich rechne bei RDUS nicht mit einer kurzfristigen Verzehnfachung, eine Verdoppelung im Anschluss an die Zulassung - diese halte ich auf Ende Juni 17 für sehr wahrscheinlich- erscheint jedoch realistisch.
Antwort auf Beitrag Nr.: 54.831.895 von Cyberhexe am 28.04.17 18:18:49Wow.. 150 Stück, dann 250 Stücke, dann was weiß ich wie viele Stücke. Beeindruckendes Volumen an Käufen!!! Impressive! Huge! Fantastic!
Mit 38.5 USD und 1.65 Milliarden USD Marktkapitalisierung scheint RDUS bereits sportlich bewertet zu sein.
Mit 38.5 USD und 1.65 Milliarden USD Marktkapitalisierung scheint RDUS bereits sportlich bewertet zu sein.
Antwort auf Beitrag Nr.: 54.831.895 von Cyberhexe am 28.04.17 18:18:49einfach nicht verrückt machen lassen - das sind eindeutige Kaufkurse, zumal die Leerverkäufer mit über 8Mio Aktien im Rückstand sind...und dies bei einer Quote von institutionellen Anlegern bei fast 100%!!! Es wird nicht mehr lange dauern, dann werden die Analysten Kaufempfehlungen aussprechen.
http://www.nasdaq.com/symbol/rdus/ownership-summary
FDA Approves Radius Health's TYMLOS™ (abaloparatide), a Bone Building Agent for the Treatment of Postmenopausal Women with Osteoporosis at High Risk for Fracture
TYMLOS is the first new anabolic (bone building) agent for postmenopausal women with osteoporosis in the United States in nearly 15 years
US Commercial Launch in May
Approval Based on Results at 18 months from the Landmark ACTIVE Trial and the first six months of ACTIVExtend Trial
Nearly One in Two Women in the US Will Experience an Osteoporosis-Related Fracture in Her Lifetime
Webcast scheduled for Monday, May 1, 2017 at 7:30 a.m. ET
http://www.nasdaq.com/symbol/rdus/ownership-summary
FDA Approves Radius Health's TYMLOS™ (abaloparatide), a Bone Building Agent for the Treatment of Postmenopausal Women with Osteoporosis at High Risk for Fracture
TYMLOS is the first new anabolic (bone building) agent for postmenopausal women with osteoporosis in the United States in nearly 15 years
US Commercial Launch in May
Approval Based on Results at 18 months from the Landmark ACTIVE Trial and the first six months of ACTIVExtend Trial
Nearly One in Two Women in the US Will Experience an Osteoporosis-Related Fracture in Her Lifetime
Webcast scheduled for Monday, May 1, 2017 at 7:30 a.m. ET
Antwort auf Beitrag Nr.: 54.832.027 von Cyberhexe am 28.04.17 18:34:50http://www.nasdaq.com/symbol/rdus/ownership-summary" target="_blank" rel="nofollow ugc noopener">http://www.nasdaq.com/symbol/rdus/ownership-summary
Institutionelle Anleger halten knapp 100% --> 99.64%
Institutionelle Anleger halten knapp 100% --> 99.64%
Antwort auf Beitrag Nr.: 53.057.611 von Cyberhexe am 14.08.16 18:27:12
Jo. Morgen kommt der Weihnachtsmann...
Zitat von Cyberhexe: Kaufkurs am 30.5.16 USD 35,45...aktueller Kurs USD 56,75
Kursziel nach Zulassung von abaloparatide in US and EU > USD 100!
Jo. Morgen kommt der Weihnachtsmann...
Antwort auf Beitrag Nr.: 54.832.039 von Cyberhexe am 28.04.17 18:36:44
abaloparatide reduziert die Wirbelsäule betreffenden Frakturen um 86% -->ACTIVE study nach 18 Monaten und führte zu einer statistisch signifikanten reduktion der nicht die Wirbelsäule betreffenden Frakturen um 43% - das ist WICHTIG, weil die anderen Wirkstoffe diesen Beweis nicht erbracht haben!! Dies dürfte Begehrlichkeiten in der Pharma-Branche wecken, weshalb die Wahrscheinlichkeit einer Übernahme von RDUS nach Zulassung von Abaloparatide auf dem wichtigsten Arzneimittelmarkt zugenommen hat. Ausserdem wird nun die Suche nach einem Kooperationspartner für Europa Aufwind bekommen, so dass die nahe Zukunft hinsichtlich weiterer Aktivitäten sehr spannend sein wird.
STRONG BUY!

abaloparatide reduziert die Wirbelsäule betreffenden Frakturen um 86% -->ACTIVE study nach 18 Monaten und führte zu einer statistisch signifikanten reduktion der nicht die Wirbelsäule betreffenden Frakturen um 43% - das ist WICHTIG, weil die anderen Wirkstoffe diesen Beweis nicht erbracht haben!! Dies dürfte Begehrlichkeiten in der Pharma-Branche wecken, weshalb die Wahrscheinlichkeit einer Übernahme von RDUS nach Zulassung von Abaloparatide auf dem wichtigsten Arzneimittelmarkt zugenommen hat. Ausserdem wird nun die Suche nach einem Kooperationspartner für Europa Aufwind bekommen, so dass die nahe Zukunft hinsichtlich weiterer Aktivitäten sehr spannend sein wird.
STRONG BUY!

Antwort auf Beitrag Nr.: 54.832.177 von Cyberhexe am 28.04.17 19:03:25Natürlich ist es spannend, wenn man 50-80% seines Depots in einen einzigen Wert steckt. Und dabei ca. 500+500+150+250+350 Aktien investiert hat - ein gigantisches Depotvolumen für die beste Biotechinvestorin on planet ...
Push as push can...
Push as push can...
Antwort auf Beitrag Nr.: 54.832.271 von Ville7 am 28.04.17 19:23:52
Es ist doch immer wieder die gleiche Leier mit den Beiträgen dieses Teilnehmers: NULL Inhalt.
Mit dem geschätzten Investitionsgrad in RDUS liegst du allerdings richtig, auch wenn die Anzahl der Aktien natürlich viel zu hoch ist.
Zitat von Ville7: Natürlich ist es spannend, wenn man 50-80% seines Depots in einen einzigen Wert steckt. Und dabei ca. 500+500+150+250+350 Aktien investiert hat - ein gigantisches Depotvolumen für die beste Biotechinvestorin on planet ...
Push as push can...
Es ist doch immer wieder die gleiche Leier mit den Beiträgen dieses Teilnehmers: NULL Inhalt.

Mit dem geschätzten Investitionsgrad in RDUS liegst du allerdings richtig, auch wenn die Anzahl der Aktien natürlich viel zu hoch ist.

Antwort auf Beitrag Nr.: 54.832.027 von Cyberhexe am 28.04.17 18:34:50
Cantor Fitzgerald Reaffirms Buy Rating for Radius Health Inc (RDUS)
Posted by Max Byerly on Apr 28th, 2017 // No Comments
inShare
Radius Health logoRadius Health Inc (NASDAQ:RDUS)‘s stock had its “buy” rating reissued by Cantor Fitzgerald in a research note issued to investors on Friday. They currently have a $65.00 price objective on the biopharmaceutical company’s stock. Cantor Fitzgerald’s price objective points to a potential upside of 67.87% from the stock’s current price.
The analysts wrote, “RDUS shares are rallying this morning (+2%) on FDA approval of TYMLOS (abaloparatide-SC) ahead of expectations, as the extended PDUFA was Jun
Zitat von Cyberhexe: einfach nicht verrückt machen lassen - das sind eindeutige Kaufkurse, zumal die Leerverkäufer mit über 8Mio Aktien im Rückstand sind...und dies bei einer Quote von institutionellen Anlegern bei fast 100%!!! Es wird nicht mehr lange dauern, dann werden die Analysten Kaufempfehlungen aussprechen.
http://www.nasdaq.com/symbol/rdus/ownership-summary
FDA Approves Radius Health's TYMLOS™ (abaloparatide), a Bone Building Agent for the Treatment of Postmenopausal Women with Osteoporosis at High Risk for Fracture
TYMLOS is the first new anabolic (bone building) agent for postmenopausal women with osteoporosis in the United States in nearly 15 years
US Commercial Launch in May
Approval Based on Results at 18 months from the Landmark ACTIVE Trial and the first six months of ACTIVExtend Trial
Nearly One in Two Women in the US Will Experience an Osteoporosis-Related Fracture in Her Lifetime
Webcast scheduled for Monday, May 1, 2017 at 7:30 a.m. ET
Cantor Fitzgerald Reaffirms Buy Rating for Radius Health Inc (RDUS)
Posted by Max Byerly on Apr 28th, 2017 // No Comments
inShare
Radius Health logoRadius Health Inc (NASDAQ:RDUS)‘s stock had its “buy” rating reissued by Cantor Fitzgerald in a research note issued to investors on Friday. They currently have a $65.00 price objective on the biopharmaceutical company’s stock. Cantor Fitzgerald’s price objective points to a potential upside of 67.87% from the stock’s current price.
The analysts wrote, “RDUS shares are rallying this morning (+2%) on FDA approval of TYMLOS (abaloparatide-SC) ahead of expectations, as the extended PDUFA was Jun
Antwort auf Beitrag Nr.: 54.832.347 von Cyberhexe am 28.04.17 19:41:56
Leider ist die Erfolgsquote der sich stets allwissend gebenden Biotechinvestorin doch recht bescheiden. Ich hab mal RDUS mit meinen Depotwerten verglichen (alles Biotech):

Manchmal ist es halt besser NULL AHNUNG zu haben und als doofer Affe einfach Darts zu werfen. Gelle?
Zitat von Cyberhexe: Es ist doch immer wieder die gleiche Leier mit den Beiträgen dieses Teilnehmers: NULL Inhalt.
Mit dem geschätzten Investitionsgrad in RDUS liegst du allerdings richtig, auch wenn die Anzahl der Aktien natürlich viel zu hoch ist.
Leider ist die Erfolgsquote der sich stets allwissend gebenden Biotechinvestorin doch recht bescheiden. Ich hab mal RDUS mit meinen Depotwerten verglichen (alles Biotech):
Manchmal ist es halt besser NULL AHNUNG zu haben und als doofer Affe einfach Darts zu werfen. Gelle?
@Cyberhexe @Ville7
Ich denke, dass alle hier in diesem Forum bzw. in anderen BIOTECH-Foren um das Risiko einer einer möglichen Nichtzulassung wissen. Ich kann die emotionalen und euphorischen Ausbrüche nach einem Approval voll nachvollziehen , gerade dann , wenn Aktionäre größere Einsätze in ein Unternehmen investiert haben.
Dann dürfen m.M.n. auch mal Kursziele ( durchaus auch Longzeit-Kursziele) ausgerufen werden, die in höheren und un/realistischen ? Bereichen liegen, womit ich überhaupt kein Problem habe.
Wenn dann auch noch von möglichen Buy-Outs gesprochen wird , habe ich ebenfalls kein Problem.
Wenn ein Investor in seiner Euphorie seine neu gekauften Stückzahlen bekannt gibt, habe ich ebenfalls kein Problem damit.
Das alles gehört zum Börsengeschehen irgendwie dazu.
@Ville 7
Deine Bemerkungen und Reaktionen nach der Ankündigung des APPROVALs
Mit Zulassung schafft es das Ding nicht mal dauerhaft über die 40.
Black Box Warning genauso heftig wie bei Forteo.
DasRisiko von Osteosarcoma ist nicht ohne... wahrscheinlich ist das auch der Punkt an dem die EMA rum macht
Die Börse feiert die Zulassung mit einem Kursverlust.
Ich weiß wirklich nicht, was du uns damit sagen willst.
Was klingt da mit ? Realismus ? Schadenfreude ? Häme ?
KORRESPONDENZ Ville7 und Cyberhexe
Ville7
Wow.. 150 Stück, dann 250 Stücke, dann was weiß ich wie viele Stücke. Beeindruckendes Volumen an Käufen!!! Impressive! Huge! Fantastic! Mit 38.5 USD und 1.65 Milliarden USD Marktkapitalisierung scheint RDUS bereits sportlich bewertet zu sein.
Natürlich ist es spannend, wenn man 50-80% seines Depots in einen einzigen Wert steckt. Und dabei ca. 500+500+150+250+350 Aktien investiert hat - ein gigantisches Depotvolumen für die beste Biotechinvestorin on planet ... Push as push can...
.
Cyberhexe:
Es ist doch immer wieder die gleiche Leier mit den Beiträgen dieses Teilnehmers: NULL Inhalt. Mit dem geschätzten Investitionsgrad in RDUS liegst du allerdings richtig, auch wenn die Anzahl der Aktien natürlich viel zu hoch ist.
Die sogenannte Inhaltsleere scheint sich wohl wirklich nur auf die beiden Beiträge von ville7 zu beziehen.
@Ville7
Und dann kommen auf einmal Vergleiche wer in den letzten Monaten erfolgreicher investiert hat.
Leider ist die Erfolgsquote der sich stets allwissend gebenden Biotechinvestorin doch recht bescheiden. Ich hab mal RDUS mit meinen Depotwerten verglichen (alles Biotech):
>>> GRAFIK <<<
Manchmal ist es halt besser NULL AHNUNG zu haben und als doofer Affe einfach Darts zu werfen. Gelle?
Wie soll ich das jetzt verstehen ?
Wenn du einen grundsätzlichen Fachkompetenzkampf mit Erfolgsbilanzen entfachen willst, dann ist es dein Ding. Aber ich denke, der NULL-INHALT deiner zwei Beiträge hat/hatte wirklich nichts mit der NULL-AHNUNG deiner Fachkompetenz zu tun.
Mein Vorschlag an Cyberhexe und Ville7:
Beendet doch bitte euer Geplänkel.
Setzt beide lieber weiterhin eure Fachkompetenz ein, die ich aus anderen Foren kenne und die ich sehr schätze - und die mir bisher immer eine sehr große Hilfe gewesen ist.
Damit tut ihr uns allen Investierten den größten Gefallen.
MfG
bernie55
Ich denke, dass alle hier in diesem Forum bzw. in anderen BIOTECH-Foren um das Risiko einer einer möglichen Nichtzulassung wissen. Ich kann die emotionalen und euphorischen Ausbrüche nach einem Approval voll nachvollziehen , gerade dann , wenn Aktionäre größere Einsätze in ein Unternehmen investiert haben.
Dann dürfen m.M.n. auch mal Kursziele ( durchaus auch Longzeit-Kursziele) ausgerufen werden, die in höheren und un/realistischen ? Bereichen liegen, womit ich überhaupt kein Problem habe.
Wenn dann auch noch von möglichen Buy-Outs gesprochen wird , habe ich ebenfalls kein Problem.
Wenn ein Investor in seiner Euphorie seine neu gekauften Stückzahlen bekannt gibt, habe ich ebenfalls kein Problem damit.
Das alles gehört zum Börsengeschehen irgendwie dazu.
@Ville 7
Deine Bemerkungen und Reaktionen nach der Ankündigung des APPROVALs
Mit Zulassung schafft es das Ding nicht mal dauerhaft über die 40.
Black Box Warning genauso heftig wie bei Forteo.
DasRisiko von Osteosarcoma ist nicht ohne... wahrscheinlich ist das auch der Punkt an dem die EMA rum macht
Die Börse feiert die Zulassung mit einem Kursverlust.
Ich weiß wirklich nicht, was du uns damit sagen willst.
Was klingt da mit ? Realismus ? Schadenfreude ? Häme ?
KORRESPONDENZ Ville7 und Cyberhexe
Ville7
Wow.. 150 Stück, dann 250 Stücke, dann was weiß ich wie viele Stücke. Beeindruckendes Volumen an Käufen!!! Impressive! Huge! Fantastic! Mit 38.5 USD und 1.65 Milliarden USD Marktkapitalisierung scheint RDUS bereits sportlich bewertet zu sein.
Natürlich ist es spannend, wenn man 50-80% seines Depots in einen einzigen Wert steckt. Und dabei ca. 500+500+150+250+350 Aktien investiert hat - ein gigantisches Depotvolumen für die beste Biotechinvestorin on planet ... Push as push can...
.
Cyberhexe:
Es ist doch immer wieder die gleiche Leier mit den Beiträgen dieses Teilnehmers: NULL Inhalt. Mit dem geschätzten Investitionsgrad in RDUS liegst du allerdings richtig, auch wenn die Anzahl der Aktien natürlich viel zu hoch ist.
Die sogenannte Inhaltsleere scheint sich wohl wirklich nur auf die beiden Beiträge von ville7 zu beziehen.
@Ville7
Und dann kommen auf einmal Vergleiche wer in den letzten Monaten erfolgreicher investiert hat.
Leider ist die Erfolgsquote der sich stets allwissend gebenden Biotechinvestorin doch recht bescheiden. Ich hab mal RDUS mit meinen Depotwerten verglichen (alles Biotech):
>>> GRAFIK <<<
Manchmal ist es halt besser NULL AHNUNG zu haben und als doofer Affe einfach Darts zu werfen. Gelle?
Wie soll ich das jetzt verstehen ?
Wenn du einen grundsätzlichen Fachkompetenzkampf mit Erfolgsbilanzen entfachen willst, dann ist es dein Ding. Aber ich denke, der NULL-INHALT deiner zwei Beiträge hat/hatte wirklich nichts mit der NULL-AHNUNG deiner Fachkompetenz zu tun.
Mein Vorschlag an Cyberhexe und Ville7:
Beendet doch bitte euer Geplänkel.

Setzt beide lieber weiterhin eure Fachkompetenz ein, die ich aus anderen Foren kenne und die ich sehr schätze - und die mir bisher immer eine sehr große Hilfe gewesen ist.
Damit tut ihr uns allen Investierten den größten Gefallen.

MfG
bernie55

Zum FDA-Label von Abaloparatide:
Die "Black box" ist sicherlich keine Überraschung, da in einer 2-jährigen Karzinogenitätsstudie mit Ratten eine dosisabhängige erhöhte Inzidenz hinsichtlich Osteosarcoma und Osteoblastoma festgestellt wurde....allerdings bei einer 4 bis 28-fachen Dosis der am Mensch applizierten 80 mcg.
Es ist nicht bekannt, ob Abaloparatide beim Menschen eine erhöhte Inzidenz für solche Tumore verursacht, da in der Klinik, also am Menschen, diesbezüglich kein Signal beobachtet wurde.
Unschön ist die Tatsache, dass im Label von Abaloparatide lediglich die klinischen Ergebnisse gegenüber Plazebo aufgeführt sind und nicht auch gegenüber dem Konkurrenzprodukt von Eli Lilly Teriparatide (brand = Forteo), da so die überlegene Wirkung und das günstigere Nebenwirkungsprofil (Teriparatide verursacht hypercalcemia --> schädigt die Nieren) im Label nicht zum Ausdruck kommen.
Mit Spannung wird am 1. Mai die Pressekonferenz erwartet, wenn sicherlich auch der Preis für ...wie heisst das noch mal...TYMLOS...ein Thema sein wird. Der Endverbraucherpreis für Forteo über 4 Wochen beträgt $2,700. Ich bin mir ziemlich sicher, dass Tymlos nicht darunter über den Ladentisch der Apotheken gehen wird.
Die Injektion mit einem "Prefilled Pen" ist relativ einfach, obschon eine nadellose Anwendung kundenfreundlicher wäre - transdermale Anwendung derzeit in Phase 2. Der Vorteil gegenüber Forteo ist jedoch, dass Tymlos bzw. der mit Abaloparatide gefüllte "Prefilled Pen" nicht kühl gelagert werden muss.
Die "Black box" ist sicherlich keine Überraschung, da in einer 2-jährigen Karzinogenitätsstudie mit Ratten eine dosisabhängige erhöhte Inzidenz hinsichtlich Osteosarcoma und Osteoblastoma festgestellt wurde....allerdings bei einer 4 bis 28-fachen Dosis der am Mensch applizierten 80 mcg.
Es ist nicht bekannt, ob Abaloparatide beim Menschen eine erhöhte Inzidenz für solche Tumore verursacht, da in der Klinik, also am Menschen, diesbezüglich kein Signal beobachtet wurde.
Unschön ist die Tatsache, dass im Label von Abaloparatide lediglich die klinischen Ergebnisse gegenüber Plazebo aufgeführt sind und nicht auch gegenüber dem Konkurrenzprodukt von Eli Lilly Teriparatide (brand = Forteo), da so die überlegene Wirkung und das günstigere Nebenwirkungsprofil (Teriparatide verursacht hypercalcemia --> schädigt die Nieren) im Label nicht zum Ausdruck kommen.
Mit Spannung wird am 1. Mai die Pressekonferenz erwartet, wenn sicherlich auch der Preis für ...wie heisst das noch mal...TYMLOS...ein Thema sein wird. Der Endverbraucherpreis für Forteo über 4 Wochen beträgt $2,700. Ich bin mir ziemlich sicher, dass Tymlos nicht darunter über den Ladentisch der Apotheken gehen wird.
Die Injektion mit einem "Prefilled Pen" ist relativ einfach, obschon eine nadellose Anwendung kundenfreundlicher wäre - transdermale Anwendung derzeit in Phase 2. Der Vorteil gegenüber Forteo ist jedoch, dass Tymlos bzw. der mit Abaloparatide gefüllte "Prefilled Pen" nicht kühl gelagert werden muss.
Antwort auf Beitrag Nr.: 54.834.273 von bernie55 am 29.04.17 11:45:24Möglicherweise stehen kritisierende Teilnehmer, ähnlich wie bei EXEL, auch irgendwann auf dem RDUS Trittbrett. Das sei ihnen gegönnt. 
Ich werde jedoch immer dann intervenieren, wenn in den mich interessierenden Foren, insbesondere in denjenigen , die von mir eröffnet wurden, falsche oder zumindest unpräzise Fakten verbreitet werden. Und diesbezüglich ist der Teilnehmer ville7 sehr auffällig.

Ich werde jedoch immer dann intervenieren, wenn in den mich interessierenden Foren, insbesondere in denjenigen , die von mir eröffnet wurden, falsche oder zumindest unpräzise Fakten verbreitet werden. Und diesbezüglich ist der Teilnehmer ville7 sehr auffällig.
Anbei die Bonuskarte bei RDUS.
Auf ASCO17 werden erste Ergebnisse vorgestellt:
Abstract 1014
Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer.
Poster Board: #6
Discussed at the Poster Discussion Session on Sunday, June 4, 2017, 4:45 PM - 6:00 PM, at Hall B1
Aditya Bardia, MD, MPH - First Author
Massachusetts General Hospital Cancer Center and Harvard Medical School
Einige interessante Studien sind zu RAD1901 auffindbar:
http://www.wallstreet-online.de/community/neuer-beitrag
A Phase IB Study to Evaluate the Effect of RAD1901 on the Availability of Estrogen Receptor Binding Sites in Metastatic Breast Cancer
Estimated Enrollment: 16
Study Start Date: December 2015
Estimated Primary Completion Date:
May 2018 (Final data collection date for primary outcome measure)
https://clinicaltrials.gov/ct2/show/NCT02653417?term=RAD1901…
Study to Evaluate the Safety and Efficacy of RAD1901 in Postmenopausal Women With Moderate to Severe Vasomotor Symptoms
Phase 2
Estimated Enrollment: 300
Study Start Date: December 2015
Estimated Primary Completion
Date: April 2017 (Final data collection date for primary outcome measure)
Auf ASCO17 werden erste Ergebnisse vorgestellt:
Abstract 1014
Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer.
Poster Board: #6
Discussed at the Poster Discussion Session on Sunday, June 4, 2017, 4:45 PM - 6:00 PM, at Hall B1
Aditya Bardia, MD, MPH - First Author
Massachusetts General Hospital Cancer Center and Harvard Medical School
Einige interessante Studien sind zu RAD1901 auffindbar:
http://www.wallstreet-online.de/community/neuer-beitrag
A Phase IB Study to Evaluate the Effect of RAD1901 on the Availability of Estrogen Receptor Binding Sites in Metastatic Breast Cancer
Estimated Enrollment: 16
Study Start Date: December 2015
Estimated Primary Completion Date:
May 2018 (Final data collection date for primary outcome measure)
https://clinicaltrials.gov/ct2/show/NCT02653417?term=RAD1901…
Study to Evaluate the Safety and Efficacy of RAD1901 in Postmenopausal Women With Moderate to Severe Vasomotor Symptoms
Phase 2
Estimated Enrollment: 300
Study Start Date: December 2015
Estimated Primary Completion
Date: April 2017 (Final data collection date for primary outcome measure)
Antwort auf Beitrag Nr.: 54.834.273 von bernie55 am 29.04.17 11:45:24Bernie, nur so viel dazu:
wer sich die Mühe macht und in einer nichtssagenden und nicht überprüfbaren Grafik Überlegenheit demonstrieren will, der hat eine ausgeprägte Profilneurose. Eigentlich ein Fall für die Couch!
wer sich die Mühe macht und in einer nichtssagenden und nicht überprüfbaren Grafik Überlegenheit demonstrieren will, der hat eine ausgeprägte Profilneurose. Eigentlich ein Fall für die Couch!
Antwort auf Beitrag Nr.: 54.834.469 von Cyberhexe am 29.04.17 13:03:36
Dass die Ville7- Erfolgsgrafik nichtssagend bzw. nicht überprüfbar ist, das ist sogar auch für mich "Laienbiotecher" so was von klar
Und wenn ich ehrlich bin, interessiert mich diese auch gar nicht. Ich bin vielmehr an substantiellem Gedankenaustausch interessiert. Deshalb finde ich es auch sehr gut, dass du intervenierst, wenn falsche oder zumindest unpräzise Fakten verbreitet werden. .
Deine Persönlichkeitsbeurteilung bzgl. Ville7 lasse ich jetzt mal so stehen, ich hätte da zwar auch eine Meinung -
aber die behalte ich jetzt mal für mich.
Zitat von Cyberhexe: Bernie, nur so viel dazu:
wer sich die Mühe macht und in einer nichtssagenden und nicht überprüfbaren Grafik Überlegenheit demonstrieren will, der hat eine ausgeprägte Profilneurose. Eigentlich ein Fall für die Couch!
Dass die Ville7- Erfolgsgrafik nichtssagend bzw. nicht überprüfbar ist, das ist sogar auch für mich "Laienbiotecher" so was von klar

Und wenn ich ehrlich bin, interessiert mich diese auch gar nicht. Ich bin vielmehr an substantiellem Gedankenaustausch interessiert. Deshalb finde ich es auch sehr gut, dass du intervenierst, wenn falsche oder zumindest unpräzise Fakten verbreitet werden. .

Deine Persönlichkeitsbeurteilung bzgl. Ville7 lasse ich jetzt mal so stehen, ich hätte da zwar auch eine Meinung -
aber die behalte ich jetzt mal für mich.

na ja verwunderlich ist doch eher, das ich keinen User bei w:o kenne, der so erfolgreich ist wie ville7: Ein Tenbagger nach dem nächsten (Bavaria Nordic, Exelixis). Jetzt bei IMGN auch schon wieder 200 %, dazu Cytomx wo es super läuft, Morphosys, wo der Tenbagger zumindest nicht weit ist.
Wenn es bei mir so laufen würde, was es nicht tut, gebe ich gern zu, dann würde ich ganz sicher nicht auf Usern wie Cyberhexe rumhacken. Ich glaube sogar, das es bei ihm so läuft um so mehr ist es armselig, so Cyberhexe anzumachen. Die Zulassungen bei RDUS und PGNX erfolgten. Von daher also grundsätzlich nichts falsch gemacht.
Wenn es bei mir so laufen würde, was es nicht tut, gebe ich gern zu, dann würde ich ganz sicher nicht auf Usern wie Cyberhexe rumhacken. Ich glaube sogar, das es bei ihm so läuft um so mehr ist es armselig, so Cyberhexe anzumachen. Die Zulassungen bei RDUS und PGNX erfolgten. Von daher also grundsätzlich nichts falsch gemacht.
Antwort auf Beitrag Nr.: 54.835.455 von riverstar_de am 29.04.17 20:11:22Das ist leider der Punkt. Ich gebe ehrlich zu, dass es mich gewaltig anbläht von dieser Cyberhexe als "Kreisklasse", "nichtssagend", "Trittbrettfahrer" (ausgerechnet der Cyberhexe!!), "Anfänger" usw. verunglimpft zu werden (und sie hat damit angefangen), während sie sich selbst als den absoluten Biotechguru darstellt (was sie bei genauem hinsehen nicht ansatzweise ist).
Seiher bekommt sie ihre Unzulänglichkeiten und Unwahrheiten (z.B. Depotanteile) von mir ebenso gespiegelt. Was mich zudem aufregt ist, wenn jemand sich hinstellt und sagt er hätte die ultimative Wahrheit und dadurch seine Follower-Gemeinde auf falsche Fährten schickt.
Die Tiefe meiner Analyse und Kenntnisse hat bisher ausgereicht um oft die richtigen Entscheidungen zu treffen. Manchmal ist dabei m.E. zu tiefes, speziell zu tiefes Detailwissen sogar hinderlich. Vor allem verbunden mit einer gewissen Verliebtheit in eine Aktie oder der Sturheit Recht behalten zu wollen.
Vielleicht habe ich bisher auch nur extremes Glück gehabt, ich kann das für mich selbst gar nicht einschätzen. Ich kann es nur im Depot messen und da lief es erstaunlich gut, um Längen besser als ich es mir vor 15 Jahren zum Ziel gemacht habe...
Um erfolgreich an der Börse zu sein gehören m.E. folgende Faktoren:
1. Kenntnis dessen, was eine Firma macht oder entwickelt (an Produkten) und eine Enschätzung der Erfolgschance an den Markt zu kommen, Kenntnis dessen wie die Firma im Vergleich zur Konkurrenz steht bzw. stehen wird, wenn das Produkt vermarktet werden wird plus Kenntnis der regulatorischen Rahmenbedingungen und deren Entwicklung (in die Zukunft gedacht)
2. ein Bild dessen, was der Markt benötigt und wofür er künftig bereit ist Geld auszugeben
3. Kenntnis und richtige Einschätzung der Bewertung im Vergleich zu 1. und 2.
4. Technische Analyse / Charttechnik, da sich daran viele Leute orientieren; damit kann man das Herdenverhalten einschätzen und die richtigen Einstiege finden
5. Sentiment, das kann man speziell in Börsenboards herausfinden.
6. Mut in extrem abverkauften Phasen "bold" reinzugehen und Mut in extrem überkauften Phasen gegen die Herdenmeinung rauszugehen.
7. Glück (nicht zu unterschätzen, v.a. das Timing)
8. Konzentration auf maximal 8-10 Aktien im Depot, denn mehr kann man nicht wirklich sauber verfolgen
9. die Gelassenheit das Traden/Investieren als Hobby zu sehen und emotional frei zu sein, wenn es mal eine Phase gibt bei der es gegen einen läuft oder man (lange) warten muss.
10. schnelle Entscheidungen treffen zu können, wenn sich Dinge grundlegend anders entwicklen (da ist es wichtig vor allen anderen raus zu kommen oder reinzugehen)
11. steuerliche Optimierungen
(sicher hab ich noch was vergessen ...)
Dann gibt es noch ein paar Feinheiten, die ich praktiziere. Z.B., dass ich mir immer versuche so zu traden /investieren, dass ich am Ende bei Verkauf Gratisstücke behalte, wenn ich von der Firma wirklich langfristig noch überzeugt bin. Dadurch wächst bei Erfolgen das Depot automatisch weiter und man hat zudem diversifiziert. Diese Gratisstücke werfe ich dann eventuell doch, wenn die Bewertung ihren Zenit weit überschritten hat, also für mich exorbitante Dimensionen erreicht hat. Von all dem freiwerdenden Geld kaufe ich mir dann einen neuen Wert, den ich für aussichtsreich halte (die EXEL-Verkäufe zu 16/17 USD gingen z.B. massiv in eine charttechnisch und sentimenttechnisch ausgebombte IMGN, die sich seither mehr als verdoppelt hat - Risiko auch da bereits wieder rausgenommen).
Im Übrigen hatte ich um die Präsidentenwahl herum RDUS zum Trading im Depot und habe es von 40,x auf 54 getradet habe. Wegen der EMA Verzögerung und weil die bisherige Verabreichungsform (von abalo) für mich noch keinen Erfolg ausmacht (mit transdermal patch sähe das anders aus) bin ich aber nicht mehr rein. Daher auch die richtige Einschätzung, dass hier erst mal kurzfristig gar nichts zu holen ist. Wie es in den nächsten Monaten aussieht hängt von den Aussagen der Firma am Montag zur Zukunft ab, zu u.a. Transdermal Patch und der EMA, zudem wird der Markt nun an den Verkäufen messen und auf den massiven Quartalsverlust in der Anfangsphase schauen, der eine weitere massive Verwässerung möglich machen könnte, v.a. wenn das Produkt in täglicher Pen-Verabreichungsform nicht gut genug verkauft werden kann.
Für Interessenten - die Aktien in meinem Depot aus der Grafik sind / waren:
* Exelixis (noch ca. 15% der ursprünglichen Megaposition drin; 1690% Plus)
* IMGN (bereits bis zur Hälfte reduziert; Restposition komplett for free und seit Dez. 155% im Plus)
* Bavarian Nordic (nun ein 10 bagger seit 2011, bleibt weiter drin - übrigens war das eine Gegenspekulation zu der angeblich so tollen BBBiotech, die zuvor komplett ausgestiegen war)
* Morphosys (das Meiste ist steuerfrei vor 2009; sollten wir mit Guselkumab über 70 kommen werde ich die Tradingstücke, die ich zu 40 gekauft habe werfen)
* Ablynx (zu 8,x letztes Jahr massiv aufgebaut; gibt hier keinen Thread für bei W/O; halte ich für langfristig aussichtsreich)
* Cytomx (für mich die heißeste Position im Depot mit der größten Chance mit 10-50 Verfachung möglich; Achtung Risiko eines Totalverlusts, da noch kein PoC)
* Spectrum Pharmaceuticals: habe ich noch steuerfreie Stücke von 2008 zu 1.4 USD, die ich zu lange reingehalten habe und neue Stücke von letztem Jahr zu 4 USD. Diese möchte ich im nächsten Hype um eflapegrastim P3 Daten und poziotinib PoC in NSCLC hoffentlich über 12 USD oder höher werfen (2018?)
* Seattle Genetics: erst letztes Jahr zu USD 31 sehr "late to the party" eingestiegen, aber zwischenzeitlich verdoppelt
Ich empfehle ausdrücklich mir nichts nachzumachen, da ich ganz bewusst ein extrem hohes Risiko fahre! Zudem sollte einem bewusst sein, dass eine trump'sche Regulierung der Medikamentenpreise die Biotechs auf gewaltige Talfahrt schicken kann...ein Depot mit Schwerpunkt Biotech kann dadurch einen extremen Schlag abbekommen.
Seiher bekommt sie ihre Unzulänglichkeiten und Unwahrheiten (z.B. Depotanteile) von mir ebenso gespiegelt. Was mich zudem aufregt ist, wenn jemand sich hinstellt und sagt er hätte die ultimative Wahrheit und dadurch seine Follower-Gemeinde auf falsche Fährten schickt.
Die Tiefe meiner Analyse und Kenntnisse hat bisher ausgereicht um oft die richtigen Entscheidungen zu treffen. Manchmal ist dabei m.E. zu tiefes, speziell zu tiefes Detailwissen sogar hinderlich. Vor allem verbunden mit einer gewissen Verliebtheit in eine Aktie oder der Sturheit Recht behalten zu wollen.
Vielleicht habe ich bisher auch nur extremes Glück gehabt, ich kann das für mich selbst gar nicht einschätzen. Ich kann es nur im Depot messen und da lief es erstaunlich gut, um Längen besser als ich es mir vor 15 Jahren zum Ziel gemacht habe...
Um erfolgreich an der Börse zu sein gehören m.E. folgende Faktoren:
1. Kenntnis dessen, was eine Firma macht oder entwickelt (an Produkten) und eine Enschätzung der Erfolgschance an den Markt zu kommen, Kenntnis dessen wie die Firma im Vergleich zur Konkurrenz steht bzw. stehen wird, wenn das Produkt vermarktet werden wird plus Kenntnis der regulatorischen Rahmenbedingungen und deren Entwicklung (in die Zukunft gedacht)
2. ein Bild dessen, was der Markt benötigt und wofür er künftig bereit ist Geld auszugeben
3. Kenntnis und richtige Einschätzung der Bewertung im Vergleich zu 1. und 2.
4. Technische Analyse / Charttechnik, da sich daran viele Leute orientieren; damit kann man das Herdenverhalten einschätzen und die richtigen Einstiege finden
5. Sentiment, das kann man speziell in Börsenboards herausfinden.
6. Mut in extrem abverkauften Phasen "bold" reinzugehen und Mut in extrem überkauften Phasen gegen die Herdenmeinung rauszugehen.
7. Glück (nicht zu unterschätzen, v.a. das Timing)
8. Konzentration auf maximal 8-10 Aktien im Depot, denn mehr kann man nicht wirklich sauber verfolgen
9. die Gelassenheit das Traden/Investieren als Hobby zu sehen und emotional frei zu sein, wenn es mal eine Phase gibt bei der es gegen einen läuft oder man (lange) warten muss.
10. schnelle Entscheidungen treffen zu können, wenn sich Dinge grundlegend anders entwicklen (da ist es wichtig vor allen anderen raus zu kommen oder reinzugehen)
11. steuerliche Optimierungen
(sicher hab ich noch was vergessen ...)
Dann gibt es noch ein paar Feinheiten, die ich praktiziere. Z.B., dass ich mir immer versuche so zu traden /investieren, dass ich am Ende bei Verkauf Gratisstücke behalte, wenn ich von der Firma wirklich langfristig noch überzeugt bin. Dadurch wächst bei Erfolgen das Depot automatisch weiter und man hat zudem diversifiziert. Diese Gratisstücke werfe ich dann eventuell doch, wenn die Bewertung ihren Zenit weit überschritten hat, also für mich exorbitante Dimensionen erreicht hat. Von all dem freiwerdenden Geld kaufe ich mir dann einen neuen Wert, den ich für aussichtsreich halte (die EXEL-Verkäufe zu 16/17 USD gingen z.B. massiv in eine charttechnisch und sentimenttechnisch ausgebombte IMGN, die sich seither mehr als verdoppelt hat - Risiko auch da bereits wieder rausgenommen).
Im Übrigen hatte ich um die Präsidentenwahl herum RDUS zum Trading im Depot und habe es von 40,x auf 54 getradet habe. Wegen der EMA Verzögerung und weil die bisherige Verabreichungsform (von abalo) für mich noch keinen Erfolg ausmacht (mit transdermal patch sähe das anders aus) bin ich aber nicht mehr rein. Daher auch die richtige Einschätzung, dass hier erst mal kurzfristig gar nichts zu holen ist. Wie es in den nächsten Monaten aussieht hängt von den Aussagen der Firma am Montag zur Zukunft ab, zu u.a. Transdermal Patch und der EMA, zudem wird der Markt nun an den Verkäufen messen und auf den massiven Quartalsverlust in der Anfangsphase schauen, der eine weitere massive Verwässerung möglich machen könnte, v.a. wenn das Produkt in täglicher Pen-Verabreichungsform nicht gut genug verkauft werden kann.
Für Interessenten - die Aktien in meinem Depot aus der Grafik sind / waren:
* Exelixis (noch ca. 15% der ursprünglichen Megaposition drin; 1690% Plus)
* IMGN (bereits bis zur Hälfte reduziert; Restposition komplett for free und seit Dez. 155% im Plus)
* Bavarian Nordic (nun ein 10 bagger seit 2011, bleibt weiter drin - übrigens war das eine Gegenspekulation zu der angeblich so tollen BBBiotech, die zuvor komplett ausgestiegen war)
* Morphosys (das Meiste ist steuerfrei vor 2009; sollten wir mit Guselkumab über 70 kommen werde ich die Tradingstücke, die ich zu 40 gekauft habe werfen)
* Ablynx (zu 8,x letztes Jahr massiv aufgebaut; gibt hier keinen Thread für bei W/O; halte ich für langfristig aussichtsreich)
* Cytomx (für mich die heißeste Position im Depot mit der größten Chance mit 10-50 Verfachung möglich; Achtung Risiko eines Totalverlusts, da noch kein PoC)
* Spectrum Pharmaceuticals: habe ich noch steuerfreie Stücke von 2008 zu 1.4 USD, die ich zu lange reingehalten habe und neue Stücke von letztem Jahr zu 4 USD. Diese möchte ich im nächsten Hype um eflapegrastim P3 Daten und poziotinib PoC in NSCLC hoffentlich über 12 USD oder höher werfen (2018?)
* Seattle Genetics: erst letztes Jahr zu USD 31 sehr "late to the party" eingestiegen, aber zwischenzeitlich verdoppelt
Ich empfehle ausdrücklich mir nichts nachzumachen, da ich ganz bewusst ein extrem hohes Risiko fahre! Zudem sollte einem bewusst sein, dass eine trump'sche Regulierung der Medikamentenpreise die Biotechs auf gewaltige Talfahrt schicken kann...ein Depot mit Schwerpunkt Biotech kann dadurch einen extremen Schlag abbekommen.
Eigentlich wollte ich nichts mehr zur persönlichen Auseinandersetzung von Cyberhexe-ville7 schreiben, aber velleicht lassen wir einfach mal die FAKTEN sprechen.
FAKTENcheck:
> Cyberhexe und ville7 sind Experten ersten Ranges in Sache Biotech, auch wenn sie inhaltlich gelegentlich anderer Meinung sind.
> Cyberhexe und ville7 haben Follower, die die Qualitäten des einen und des anderen sehr zu schätzen wissen.
> Cyberhexe und ville7 können beide nachweisbare Erfolge im Finden von Biotechperlen aufweisen, der eine mehr, der andere ein bisschen weniger.
> Cyberhexe und ville7 können beide nachweisbare Erfolge in der Gesamtperformance ihres Depots aufweisen, der eine mehr , der andere ein bisschen weniger.
> Cyberhexe und ville7 bereichern durch ihre Expertenbeiträge die einzelnen Biotechforen, sehr zum Vorteil des einen und des andereren WO-Users.
FAZIT:
Ihr beide spielt in der obersten Liga der Biotechexpertenliga, und das spreche ich voller Respekt aus.
Ihr seid für die gesamte Biotech-Community ein Segen. Ohne euch würden sehr viele User, mich voll eingeschlossen, als Biotech-Nullchecker dastehen - und in der Biotechwelt ,im wahrsten Sinne des Wortes, sehr alt aussehen.
Macht mit euren fachlichen Recherchen, Statements und Analyse weiter und setzt euch einfach auf dieser Ebene auseinander.
( das hat in diesem Forum übrigens auch schon geklappt)
An euch beide schon mal ein dickes Dankeschön für euer weiteres Engagement in Sache BIOTECH.
MfG
bernie55
FAKTENcheck:
> Cyberhexe und ville7 sind Experten ersten Ranges in Sache Biotech, auch wenn sie inhaltlich gelegentlich anderer Meinung sind.
> Cyberhexe und ville7 haben Follower, die die Qualitäten des einen und des anderen sehr zu schätzen wissen.
> Cyberhexe und ville7 können beide nachweisbare Erfolge im Finden von Biotechperlen aufweisen, der eine mehr, der andere ein bisschen weniger.
> Cyberhexe und ville7 können beide nachweisbare Erfolge in der Gesamtperformance ihres Depots aufweisen, der eine mehr , der andere ein bisschen weniger.
> Cyberhexe und ville7 bereichern durch ihre Expertenbeiträge die einzelnen Biotechforen, sehr zum Vorteil des einen und des andereren WO-Users.
FAZIT:
Ihr beide spielt in der obersten Liga der Biotechexpertenliga, und das spreche ich voller Respekt aus.
Ihr seid für die gesamte Biotech-Community ein Segen. Ohne euch würden sehr viele User, mich voll eingeschlossen, als Biotech-Nullchecker dastehen - und in der Biotechwelt ,im wahrsten Sinne des Wortes, sehr alt aussehen.
Macht mit euren fachlichen Recherchen, Statements und Analyse weiter und setzt euch einfach auf dieser Ebene auseinander.
( das hat in diesem Forum übrigens auch schon geklappt)
An euch beide schon mal ein dickes Dankeschön für euer weiteres Engagement in Sache BIOTECH.
MfG
bernie55
Antwort auf Beitrag Nr.: 54.835.455 von riverstar_de am 29.04.17 20:11:22
Zu PGNX:
AZEDRA ist noch nicht zugelassen, lediglich die Endpunkte der Pivotalstudie wurden erreicht. Ich denke, dass die Ankündigung, AZEDRA noch in 2017 zur Zulassung einzureichen, eingehalten wird. Oder hattest du die Zulassung des oral applizierten methylnaltrexone bromide gemeint?
Valeant Pharma (VRX), Progenics Pharmaceuticals (PGNX) Granted FDA Approval for RELISTOR
July 19, 2016 6:06 PM EDT
Zu EXEL:
...irgendwann ist dieser Teilnehmer im Exelixis-Forum aufgetreten
Exelixis....ein schlafender Riese? USD 3.40 am 14.5.2014
eröffnet am 15.05.14
und hat sehr unpräzise Fakten (um nicht" alternative Fakten " zu sagen) in seinen Beiträgen veröffentlicht. Einer sachlichen Richtigstellung folgten meistens postwendend persönliche Angriffe, wodurch die ursprünglich fruchtbare Auseinandersetzung oft in den Hintergrund geraten ist. Komischerweise scheint sich dies nun bei RDUS zu wiederholen. Nun jedoch den Tenbagger bei EXEL mit der Fundamentalanalyse dieses Teilnehmers in Verbindung zu bringen, ist eine sehr eigenwillige Sichtweise.
Zitat von riverstar_de: na ja verwunderlich ist doch eher, das ich keinen User bei w:o kenne, der so erfolgreich ist wie ville7: Ein Tenbagger nach dem nächsten (Bavaria Nordic, Exelixis). Jetzt bei IMGN auch schon wieder 200 %, dazu Cytomx wo es super läuft, Morphosys, wo der Tenbagger zumindest nicht weit ist.
Wenn es bei mir so laufen würde, was es nicht tut, gebe ich gern zu, dann würde ich ganz sicher nicht auf Usern wie Cyberhexe rumhacken. Ich glaube sogar, das es bei ihm so läuft um so mehr ist es armselig, so Cyberhexe anzumachen. Die Zulassungen bei RDUS und PGNX erfolgten. Von daher also grundsätzlich nichts falsch gemacht.
Zu PGNX:
AZEDRA ist noch nicht zugelassen, lediglich die Endpunkte der Pivotalstudie wurden erreicht. Ich denke, dass die Ankündigung, AZEDRA noch in 2017 zur Zulassung einzureichen, eingehalten wird. Oder hattest du die Zulassung des oral applizierten methylnaltrexone bromide gemeint?
Valeant Pharma (VRX), Progenics Pharmaceuticals (PGNX) Granted FDA Approval for RELISTOR
July 19, 2016 6:06 PM EDT
Zu EXEL:
...irgendwann ist dieser Teilnehmer im Exelixis-Forum aufgetreten
Exelixis....ein schlafender Riese? USD 3.40 am 14.5.2014
eröffnet am 15.05.14
und hat sehr unpräzise Fakten (um nicht" alternative Fakten " zu sagen) in seinen Beiträgen veröffentlicht. Einer sachlichen Richtigstellung folgten meistens postwendend persönliche Angriffe, wodurch die ursprünglich fruchtbare Auseinandersetzung oft in den Hintergrund geraten ist. Komischerweise scheint sich dies nun bei RDUS zu wiederholen. Nun jedoch den Tenbagger bei EXEL mit der Fundamentalanalyse dieses Teilnehmers in Verbindung zu bringen, ist eine sehr eigenwillige Sichtweise.
Antwort auf Beitrag Nr.: 54.836.729 von bernie55 am 30.04.17 13:03:18Ich bezeichne mich weder als echter Biotechexperte noch bin ich ein Guru oder ein Leader fuer Follower. Letzteres lehne ich vollkommen ab, da jeder sich sein eigenes Bild machen muss, alle Daten sind interpretierbar und nur jeder selbst kann fuer sich Investitionsentscheidungen verantworten. Daher warne ich stets blind solchen Leuten hinterherzurennen.
Ich bin ein Privatinvestor mit groesserem Depotschwerpunkt Biotech. Wie einige hier. Dass es gerade in letzter Zeit traumhaft lief ist wohl eher Glueck v.a. auch beim Timing gewesen. Auch die Auswahl in den Jahren zuvor war ganz gut, allerdings ist da Biotech im Gesamten selbst sehr gut gelaufen, da gab es viele ausserordentliche Gewinner. Das wird keineswegs so weitergehen, v.a. nicht vor der Kulisse steigender Regulierung. Biotech ist generell sehr hoch bewertet, Neueinsteiger und Investierte sollten recht vorsichtig sein.
Ich werde allerdings allergisch, wenn ich von einem Moechtegernguru als Anfaenger betitelt werde. Oder gar als Trittbrettfahrer desselbigen, wie im vorausgegangenen Posting mal wieder unterschwellig unterstellt wird. Exelixis ist seit 10 Jahren auf meinem Radar, der erste Einstieg erfolgte dann 2013, noch bevor dieser Moechtegernguru seinen eigenen Thread eroeffnet hatte.
Ich bin ein Privatinvestor mit groesserem Depotschwerpunkt Biotech. Wie einige hier. Dass es gerade in letzter Zeit traumhaft lief ist wohl eher Glueck v.a. auch beim Timing gewesen. Auch die Auswahl in den Jahren zuvor war ganz gut, allerdings ist da Biotech im Gesamten selbst sehr gut gelaufen, da gab es viele ausserordentliche Gewinner. Das wird keineswegs so weitergehen, v.a. nicht vor der Kulisse steigender Regulierung. Biotech ist generell sehr hoch bewertet, Neueinsteiger und Investierte sollten recht vorsichtig sein.
Ich werde allerdings allergisch, wenn ich von einem Moechtegernguru als Anfaenger betitelt werde. Oder gar als Trittbrettfahrer desselbigen, wie im vorausgegangenen Posting mal wieder unterschwellig unterstellt wird. Exelixis ist seit 10 Jahren auf meinem Radar, der erste Einstieg erfolgte dann 2013, noch bevor dieser Moechtegernguru seinen eigenen Thread eroeffnet hatte.
PS: meine "alternativen Fakten", das Cabo weit mehr wert fuer EXEL v.a. in mittelfristiger Sicht darstellt als Cobi war eine absolut korrekte Einschaetzung. Cyberhexe mag Dinge manchmal weinigstens im Ansatz richtig erkennen, aber es fehlt ein wichtiges Element dabei um an der Boerse erfolgreich zu sein: die Antizipation wann der Markt etwas einpreist.
Diesselbe Geschichte hier mit RDUS in gruen. Fuer mich fehlen noch ein paar Bausteine, dass der Markt hier (viel) mehr zu zahlen bereit ist. Nicht jedes Biotech reagiert euphorisch auf Zulassungen, v.a. wenn die Konkurrenz und Payersituation unklar ist und das Biotech noch horrende Quartalsverluste schreibt und zudem recht gut bewertet ist. Das wird sich erst mit echter Aussicht auf einen break even oder mit zusaetzlicher Fantasie (transdermsl patch, andere pipelineprodukte mit unerwartetem potential) aufloesen. Daher ist Biotechwissen das eine, die richtige Interpretation wie der Markt die Infos preist das andere...das fehlt m.E. dem User leider an der ein oder anderen Stelle.
Diesselbe Geschichte hier mit RDUS in gruen. Fuer mich fehlen noch ein paar Bausteine, dass der Markt hier (viel) mehr zu zahlen bereit ist. Nicht jedes Biotech reagiert euphorisch auf Zulassungen, v.a. wenn die Konkurrenz und Payersituation unklar ist und das Biotech noch horrende Quartalsverluste schreibt und zudem recht gut bewertet ist. Das wird sich erst mit echter Aussicht auf einen break even oder mit zusaetzlicher Fantasie (transdermsl patch, andere pipelineprodukte mit unerwartetem potential) aufloesen. Daher ist Biotechwissen das eine, die richtige Interpretation wie der Markt die Infos preist das andere...das fehlt m.E. dem User leider an der ein oder anderen Stelle.
Antwort auf Beitrag Nr.: 54.836.755 von Cyberhexe am 30.04.17 13:14:52WEBCAST
In connection with the FDA approval of TYMLOS announced today, Radius will host a live audio webcast at 7:30 a.m. ET on Monday, May 1, 2017.
Please note, Radius now also plans to report First Quarter 2017 Financial Results on Monday, May 1, 2017 and will review these results and provide a company update on the webcast.
Webcast Information:
Date: Monday, May 1, 2017
Time: 7:30 a.m. ET
Live webcast:
http://edge.media-server.com/m/p/z5woypf3
In connection with the FDA approval of TYMLOS announced today, Radius will host a live audio webcast at 7:30 a.m. ET on Monday, May 1, 2017.
Please note, Radius now also plans to report First Quarter 2017 Financial Results on Monday, May 1, 2017 and will review these results and provide a company update on the webcast.
Webcast Information:
Date: Monday, May 1, 2017
Time: 7:30 a.m. ET
Live webcast:
http://edge.media-server.com/m/p/z5woypf3
Antwort auf Beitrag Nr.: 54.839.111 von Cyberhexe am 01.05.17 12:04:54Vielleicht ist es möglich, dass man wieder zur Diskussion des Unternehmens Radius Health zurückkehrt und auf persönliche Selbstdarstellungen verzichtet!
Die Wirkung von Abaloparatide in ph3 ist innovativ:
"Specifically, in the ACTIVE trial, TYMLOS demonstrated significant reductions in the relative risk of new vertebral and nonvertebral fractures compared to placebo in the ACTIVE trial of:
86% in new vertebral fractures
43% in nonvertebral fractures"
Bin gespannt, ob bei der heutigen Pressekonferenz der Preis für Abaloparatide veröffentlicht wird.
Die BlackBox dürfte kein Problem sein, da das Konkurrenzprodukt (Forteo) fast identisch gelabelt ist. Ungünstig ist die Tatsache, dass der Patentschutz von Forteo in 2019 ausläuft, so dass die wirtschaftlichen Aussichten über 2019 hinaus ungewiss sind.
. Aber anscheinend kann man dies nicht von jedem Teilnehmenr erwarten.
Die Wirkung von Abaloparatide in ph3 ist innovativ:
"Specifically, in the ACTIVE trial, TYMLOS demonstrated significant reductions in the relative risk of new vertebral and nonvertebral fractures compared to placebo in the ACTIVE trial of:
86% in new vertebral fractures
43% in nonvertebral fractures"
Bin gespannt, ob bei der heutigen Pressekonferenz der Preis für Abaloparatide veröffentlicht wird.
Die BlackBox dürfte kein Problem sein, da das Konkurrenzprodukt (Forteo) fast identisch gelabelt ist. Ungünstig ist die Tatsache, dass der Patentschutz von Forteo in 2019 ausläuft, so dass die wirtschaftlichen Aussichten über 2019 hinaus ungewiss sind.
. Aber anscheinend kann man dies nicht von jedem Teilnehmenr erwarten.
Antwort auf Beitrag Nr.: 54.839.141 von Cyberhexe am 01.05.17 12:14:22Interessant ist folgende
Quartalsergebnis wurde bereits veröffentlicht:
As of March 31, 2017, Radius had $282.1 million in cash, cash equivalents and
marketable securities.
Abaloparatide-TD
Currently, we are focused on completing the manufacturing, scale-up, and other required activities needed to initiate a pivotal study to evaluate bioequivalence to TYMLOS.
Elacestrant (RAD1901)
We recently completed enrollment in both of our ongoing Phase 1 studies of elacestrant in advanced metastatic breast cancer. In the first half of 2017, we plan to engage with regulatory agencies to gain alignment on defining the next steps for the elacestrant breast cancer program, which would include the design of a Phase 2 trial. We expect to complete and report results from our elacestrant Phase 2b vasomotor trial in mid-2017.
RAD140
IND has been accepted --> We expect to initiate a first-in-human Phase 1 clinical trial in women with hormone receptor positive breast cancer in 2017.
Radius Expects the Following Upcoming Milestones
Abaloparatide-SC »Receive a CHMP opinion regarding the EMA's review of the abaloparatide-SC MAA in 2017 »Enter into a partnership for the potential commercialization of abaloparatide-SC prior to commercial launch»
Report top-line results from the recently completed 24-month ACTIVExtend clinical trial in the second quarter of 2017
Elacestrant
»Complete ongoing Phase 1 breast cancer clinical trials»
Engage with regulatory authorities in 2Q 2017 to gain alignment on defining next steps for the program, which would include the design of a Phase 2 breast cancer trial»
Present a poster on June 4, 2017 at the American Society of Oncology Annual Meeting (ASCO)»
Complete and report results from our ongoing Phase 2b vasomotor trial in mid-2017
RAD140
»Initiate a first-in-human Phase 1 study in 2017 in women with hormone receptor positive breast cancer
For the three months ended March 31, 2017, Radius reported a net loss of $56.9 million, or $1.32 per share, as compared to a net loss of $40.5 million, or $0.94 per share, for the three months ended March 31, 2016.
http://files.shareholder.com/downloads/AMDA-1D3H6P/391361819…
Interessant ist folgende Aussage:
»Enter into a partnership for the potential commercialization of abaloparatide-SC prior to commercial launch»
Da die Markteinführung bereits auf Mai angekündigt wurde, stellt sich die Frage, ob sich die Bekanntgabe des Kooperationspartners auf die Markteinführunhg allgemein oder auf diejenige in Europa bezieht. Ich gehe mal davon aus, dass Europa gemeint ist.
Quartalsergebnis wurde bereits veröffentlicht:
As of March 31, 2017, Radius had $282.1 million in cash, cash equivalents and
marketable securities.
Abaloparatide-TD
Currently, we are focused on completing the manufacturing, scale-up, and other required activities needed to initiate a pivotal study to evaluate bioequivalence to TYMLOS.
Elacestrant (RAD1901)
We recently completed enrollment in both of our ongoing Phase 1 studies of elacestrant in advanced metastatic breast cancer. In the first half of 2017, we plan to engage with regulatory agencies to gain alignment on defining the next steps for the elacestrant breast cancer program, which would include the design of a Phase 2 trial. We expect to complete and report results from our elacestrant Phase 2b vasomotor trial in mid-2017.
RAD140
IND has been accepted --> We expect to initiate a first-in-human Phase 1 clinical trial in women with hormone receptor positive breast cancer in 2017.
Radius Expects the Following Upcoming Milestones
Abaloparatide-SC »Receive a CHMP opinion regarding the EMA's review of the abaloparatide-SC MAA in 2017 »Enter into a partnership for the potential commercialization of abaloparatide-SC prior to commercial launch»
Report top-line results from the recently completed 24-month ACTIVExtend clinical trial in the second quarter of 2017
Elacestrant
»Complete ongoing Phase 1 breast cancer clinical trials»
Engage with regulatory authorities in 2Q 2017 to gain alignment on defining next steps for the program, which would include the design of a Phase 2 breast cancer trial»
Present a poster on June 4, 2017 at the American Society of Oncology Annual Meeting (ASCO)»
Complete and report results from our ongoing Phase 2b vasomotor trial in mid-2017
RAD140
»Initiate a first-in-human Phase 1 study in 2017 in women with hormone receptor positive breast cancer
For the three months ended March 31, 2017, Radius reported a net loss of $56.9 million, or $1.32 per share, as compared to a net loss of $40.5 million, or $0.94 per share, for the three months ended March 31, 2016.
http://files.shareholder.com/downloads/AMDA-1D3H6P/391361819…
Interessant ist folgende Aussage:
»Enter into a partnership for the potential commercialization of abaloparatide-SC prior to commercial launch»
Da die Markteinführung bereits auf Mai angekündigt wurde, stellt sich die Frage, ob sich die Bekanntgabe des Kooperationspartners auf die Markteinführunhg allgemein oder auf diejenige in Europa bezieht. Ich gehe mal davon aus, dass Europa gemeint ist.
Antwort auf Beitrag Nr.: 54.839.423 von Cyberhexe am 01.05.17 14:04:55
Die Markteinführung in den US, am Freitag noch auf Mai angekündigt, wurde nach "hinten" korrigiert:
About "Together with TYMLOS " Program TYMLOS will be available in the United States in June.
Die Markteinführung in den US, am Freitag noch auf Mai angekündigt, wurde nach "hinten" korrigiert:
About "Together with TYMLOS " Program TYMLOS will be available in the United States in June.
Antwort auf Beitrag Nr.: 54.839.437 von Cyberhexe am 01.05.17 14:07:59Und deswegen ein - 8% ? Der Markt ist ja lustig unterwegs..
Antwort auf Beitrag Nr.: 54.840.359 von biopadawan am 01.05.17 17:20:56Der Markt ist irrational, deswegen: Kauf von weiteren 400 RDUS zu USD 35.70
Antwort auf Beitrag Nr.: 54.840.397 von Cyberhexe am 01.05.17 17:28:26
http://files.shareholder.com/downloads/AMDA-1D3H6P/437562816…
-No REMS --> keine Risikimanagement-Plan erforderlich
-keine Kühlung des "Prefilled Pen" nach der ersten Entnahme erforderlich
-30 Dosen im anwenderfreundlichen Pen verfügbar
• TYMLOS Launch Meeting early May
• All top targets and KOLs have been visited at least once by June 1st
• Branded symposia at AACE May 6th
• Hub and call centers are active
• Websites activated etc.
CHMP opinion on MAA for abaloparatide-SC in July 2017
-ab Mitte Mai werden die Pharmavertreter TYMLOS anbieten und "bewerben"
http://files.shareholder.com/downloads/AMDA-1D3H6P/437562816…
-No REMS --> keine Risikimanagement-Plan erforderlich
-keine Kühlung des "Prefilled Pen" nach der ersten Entnahme erforderlich
-30 Dosen im anwenderfreundlichen Pen verfügbar
• TYMLOS Launch Meeting early May
• All top targets and KOLs have been visited at least once by June 1st
• Branded symposia at AACE May 6th
• Hub and call centers are active
• Websites activated etc.
CHMP opinion on MAA for abaloparatide-SC in July 2017
-ab Mitte Mai werden die Pharmavertreter TYMLOS anbieten und "bewerben"
Auch wenn das unser euphorischer Guru-User, dem man niemals widersprechen darf, nicht kapiert: der Markt reagiert nicht irrational. RDUS hat zum wiederholten Male weniger geliefert als versprochen. Man hat stets die größte Klappe z.B. "biggest value unpartnered asset in the biotech industry", aber liefert nicht das was der Markt erwartet. Die Verschiebung des Vermarktungsstarts ist das eine was seine Wirkung entfaltet hat. Viel mehr eingeschlagen hat aber wohl der niedrigere Preis als Forteo. Der Markt riecht einen gegenseitigen Preiskampf mit Forteo.
Antwort auf Beitrag Nr.: 54.840.501 von Cyberhexe am 01.05.17 17:50:47Der Preis für TYMLOS ist wesentlich tiefer als bei FORTEO (USD 2700/Monat) - dies dürfte dazu beitragen, dass TYMLOS relativ schnell vom Markt angenommen wird, zumal eine grosse "Pharmavertreter-Mannschaft" in den Startlöchern steht:
Radius Health last week won U.S. approval of its osteoporosis drug Tymlos (abaloparatide), securing a green light from the Food and Drug Administration one month after the regulator had unexpectedly extended its review.
Tymlos, which is the first bone-building drug okayed for treatment of post-menopausal women with osteoporosis in over a decade, will challenge Eli Lilly's Forteo (teriparatide) and Amgen's Prolia (denosumab) for share of the relatively underserved market.
Radius plans to price Tymlos at an annualized wholesale acquisition cost of $19,500, or $1,625 per each injectable pen (containing 30 daily doses), a price which company chief commercial officer David Snow said Monday would help support earlier use of anabolic agents in treating osteoporosis.
Radius Health last week won U.S. approval of its osteoporosis drug Tymlos (abaloparatide), securing a green light from the Food and Drug Administration one month after the regulator had unexpectedly extended its review.
Tymlos, which is the first bone-building drug okayed for treatment of post-menopausal women with osteoporosis in over a decade, will challenge Eli Lilly's Forteo (teriparatide) and Amgen's Prolia (denosumab) for share of the relatively underserved market.
Radius plans to price Tymlos at an annualized wholesale acquisition cost of $19,500, or $1,625 per each injectable pen (containing 30 daily doses), a price which company chief commercial officer David Snow said Monday would help support earlier use of anabolic agents in treating osteoporosis.
Selber nachdenken und nicht immer nachplappern was die Firma sagt. Fakt ist: RDUS hat bei abalo einen Preiskampf mit Forteo begonnen und das bei einem angeblich deutlich besseren Produkt. Lilly wird Forteo natuerlich nicht vom Markt nehmen wie mancher hier feucht zu traeuen beginnt, sondern selbst den Preis noch weiter senken. Eine Preisspirale beginnt. So manche Blockbustertraeume koennten somit platzen. Das ist das was der Markt spielt und solange die Diction der Firma nicht bewiesen wird (mehr Reichweite gleicht den niedrigeren Preis aus) ist diese Sichtweise des Marktes nicht unrealistisch und ggfs. die Plausiblere....
Antwort auf Beitrag Nr.: 54.409.279 von Ville7 am 25.02.17 10:03:45Charttechnisch sind Kurse um 25 nicht auszuschliessen - trotz Zulassung. Die Aktie ist chartechnisch gewaltig angeschlagen. Dann waere die MK immer noch bei stoluen 1.1Mrd USD. Wieder mal sieht man, dass die Boerse stets den Weg des groessten Schmerzes waehlt..
Zitat von Ville7: YE Call Transcript: http://seekingalpha.com/article/4049199-radius-healths-rdus-…
Die Firma macht ein mega Geheimnis darum was bei den Behörden, speziell der EMA, offen ist. Da sind andere in der Beantwortung kooperativer. Frage, die sich dabei der Markt auch stellt, ist: Haben Sie was zu verbergen?
Zudem ist man nicht willig den weiteren zeitlichen Weg bezüglich des transdermal patches darzulegen.
Auf der anderen Seite trägt man mega auf mit dem erneut im Call gefallenen Satz "We believe that abaloparatide is the greatest value un-partnered late stage asset in the biopharma industry.".
Sollte die Zulassung in USA nicht erfolgen (Complete Response Letter), so erwarte ich Kurse von 15-25 USD.
Ziemlich suboptimale Entscheidung, wenn man vor einem Jahr EXEL zu 6 (heute 23) in RDUS zu 35 (heute immer noch 35) getauscht hat.
Mglw. ist die einschaetzung, dass forteo teurer ist, falsch. Im inteenet wird der wac fuer forteo bei 1300 genannt, nicht 2700. Dann doch premium preis. Habe leider keine Daten die das belegen oder widerlegen...
Antwort auf Beitrag Nr.: 54.841.429 von Ville7 am 01.05.17 19:40:37
diskutieren wir hier über mein Risikomanagement oder über Radius Health? Nur so viel zu diesem erneuten Angriff: ich war all in one, all in Exelixis und habe bei einem Kurs von USD 5.50 begonnen, diesen Investitionsgrad zu verkleinern. Aktuell halte ich ca. 5% der ursprünglichen Stückzahl.
Ich werde jedoch den Teufel tun und meine Performance hier veröffentlichen....weil dies niemanden interessiert!
Zitat von Ville7: Ziemlich suboptimale Entscheidung, wenn man vor einem Jahr EXEL zu 6 (heute 23) in RDUS zu 35 (heute immer noch 35) getauscht hat.
diskutieren wir hier über mein Risikomanagement oder über Radius Health? Nur so viel zu diesem erneuten Angriff: ich war all in one, all in Exelixis und habe bei einem Kurs von USD 5.50 begonnen, diesen Investitionsgrad zu verkleinern. Aktuell halte ich ca. 5% der ursprünglichen Stückzahl.
Ich werde jedoch den Teufel tun und meine Performance hier veröffentlichen....weil dies niemanden interessiert!
Antwort auf Beitrag Nr.: 54.841.903 von Ville7 am 01.05.17 20:36:30Diese Quelle hat ihren Berechnungsfehler inzwischen erkannt und bestätigt, dass Tymlos mit 40% Discount gegenüber Forteo vermarktet werden soll. Preisschlacht?
Hier hat jemand meine charttechnische Einschätzung in Worten zusammengeschrieben und grafisch dargestellt:
https://t.co/JlTp7mmCpa
RDUS droht aus dem Dreieck nach unten auszubrechen. Nächster Halt möglicherweise erst USD 25.
https://t.co/JlTp7mmCpa
RDUS droht aus dem Dreieck nach unten auszubrechen. Nächster Halt möglicherweise erst USD 25.
Antwort auf Beitrag Nr.: 54.843.109 von Ville7 am 02.05.17 07:06:17Der Markt hat bezüglich des Preises eine Premium gegenüber Forteo erwartet. Nun hat die Unternehmung aber überraschend einen starken Discount angekündigt.
Um die Umsatzerwartungen des Marktes nun zu treffen muss RDUS nun ungefähr doppelt so viel Tymlos absetzen. Der Markt bezweifelt das wohl, wie man die Kursreaktion interpretieren könnte. Zumal der Preis von Forteo demnächst (2018/2019) selbst massiv in den Keller gehen dürfte, wenn die generischen Varianten aufkommen. Da nutzt auch nicht die anscheinend leicht bessere Wirksamkeit und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures. Die Ärzte könnten dies möglicherweise nicht wertschätzen und Forteo und Tymlos in einen Topf werfen.
Zudem ist auch der neue Preis nicht annähernd konkurrenzfähig zu den verfügbaren oder bald verfügbaren Antikörpern. Von der Unbequemlichkeit der notwendigen täglichen Verabreichung mal abgesehen. Zum transdermalen Patch wurde auch keine konkrete Zeitschiene genannt, die dem Markt hätte konkrete Hoffnung geben können.
Es bestehen somit meines Erachtens erhebliche Zweifel, dass die Hoffnungen des Users mit dem mit RDUS Aktien vollgestopften Depot, nicht oder nicht in der Form eintreten.
Um die Umsatzerwartungen des Marktes nun zu treffen muss RDUS nun ungefähr doppelt so viel Tymlos absetzen. Der Markt bezweifelt das wohl, wie man die Kursreaktion interpretieren könnte. Zumal der Preis von Forteo demnächst (2018/2019) selbst massiv in den Keller gehen dürfte, wenn die generischen Varianten aufkommen. Da nutzt auch nicht die anscheinend leicht bessere Wirksamkeit und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures. Die Ärzte könnten dies möglicherweise nicht wertschätzen und Forteo und Tymlos in einen Topf werfen.
Zudem ist auch der neue Preis nicht annähernd konkurrenzfähig zu den verfügbaren oder bald verfügbaren Antikörpern. Von der Unbequemlichkeit der notwendigen täglichen Verabreichung mal abgesehen. Zum transdermalen Patch wurde auch keine konkrete Zeitschiene genannt, die dem Markt hätte konkrete Hoffnung geben können.
Es bestehen somit meines Erachtens erhebliche Zweifel, dass die Hoffnungen des Users mit dem mit RDUS Aktien vollgestopften Depot, nicht oder nicht in der Form eintreten.

Antwort auf Beitrag Nr.: 54.842.026 von Cyberhexe am 01.05.17 20:58:33Zitate von der gestrigen Pressekonferenz - es hat den Anschein, dass hier sorgfältig und gut gearbeitet wurde, so dass die Markteinführung unter guten Vorzeichen angegangen wird.
zum Label:
- I feel like this is a very positive and differentiated label
- It's notable that while we do have a boxed warning that's consistent with class labeling, we were not required to have a REMS program.
zur Anwendung:
- We have a straightforward and easy-to-use subcutaneous pen design.
- Each pen carries 30 daily doses that can translate into fewer pens and co-pays that the patient continues on therapy.
- TYMLOS doesn't require refrigeration after the first dose, something we have seen repeatedly in previous market research as a nagging concern with patients on injectable anabolics.
Zeitplan / Markteinführung
- TYMLOS launch meeting in early May
- our clinical sales specialists will be educating and promoting TYMLOS in offices in early -- by mid-May. We're also already engaging top targets and key opinion leaders, and they'll be visited at least once by June.
- branded TYMLOS symposia at the upcoming AACE meeting this weekend, featuring Dr. Felicia Cosman.
- Our patient support center or hub and the call centers are already active
- specialty pharmacy network stocked and ready to distribute product and actively managing reimbursement in June
- together with TYMLOS patient support, starter kits and co-pay programs are rolling -- will be rolling out along with the product supply.
Pharmavertreter
- As Bob has mentioned previously, we were able to be very selective as Radius received thousands of applicants for our clinical sales specialist roles to help us identify the best 230 candidates.
- experienced sales team that averages over 5 years of osteoporosis experience, and nearly everyone has been through a specialty launch in their careers. We know that they know the category, their customers and their territories.
- team will cover more than 20,000 osteoporosis injectable writers, and they will fully cover these accounts at least once within the first 30 days after promotion begins
Preisgestaltung
- We must change the way clinicians, patients and payers see the anabolic class and establish TYMLOS as the leading bone-building therapy
- Notice that since 2012, the price of FORTEO has risen rapidly by double-digits annually over the last 5 years.
- That's also seen a predictable decline in overall patient volume, here identified as the total prescription volume. This pricing direction naturally challenges the notion of starting early with anabolics. Further, to win in the anabolic category and reach more anabolic-appropriate patients, we have to reset the view on the Medicaid Part D patients, which is one of the most cost-sensitive segments, patients who are paying a substantial out-of-pocket and transiting the doughnut hole.
Frequently, in interviews, conversations and even symposia, clinicians tell us that they desire to use anabolics more frequently but the out-of-pocket burden was so substantial that they were restricting the offer to many appropriate patients. If we were to expand use to more anabolic-appropriate patients, we have to address this out-of-pocket challenge.
- So to address these concerns, we've carefully chosen to price TYMLOS at an annualized wholesaler acquisition cost of $19,500 or $1,625 per pen. If the initial comments we've gotten from payers is any indication, we expect to see a very favorable response from clinicians and patients. Our focus is not only on gaining market leadership, but regaining growth in the anabolic class.
Empfehlung der ACCE
-The American College of Clinical Endocrinologists published new guidelines on the treatment of osteoporosis last September. For the first time, they recommended an anabolic agent as a first-line treatment for patients at high risk for fracture.
- We expect early first-line use of bone anabolics to increase as a result of these guidelines.
Wirkung von Tymlos
- The efficacy for fracture risk reduction for both vertebral and nonvertebral fractures have been proven.
- be able to show you the full 2-year ACTIVExtend data in the second quarter of this year.
Pipeline - Abaloparatide TD
- We believe that the transdermal patch program has the potential to allow physicians who treat osteoporosis but rarely use injectable drugs an opportunity to expand their practices to include the use of anabolic therapy.
Pipeline - RAD1901 (Elacestrant)
- completed enrollments of the 47 patients with advanced estrogen receptor positive HER2-negative breast cancer in the U.S. Phase I study and have also enrolled all 16 patients in the European FES-PET imaging study.
- On June 4 at the 2017 Clinical Society of Clinical Oncology Annual Meeting, we will present an Elacestrant clinical study abstract at the poster session
- We are currently awaiting FDA response on our planned meeting, which would include discussion of the design of the monotherapy Phase II clinical trial
Pipeline - RAD140
- IND for RAD140, a selective androgen receptor modulator which has a mechanism antitumor activity that is distinct from estrogen receptor targeted therapies, has been accepted by the FDA.
Abaloparatide in Europe
- we expect a CHMP opinion on our MAA this July and continue our guidance of having a partnership in place by time of launch. We've guided that our next financing event would take place in the context of a partnership, and we are continuing that guidance.
Q/A
zu generischem Teriparatide (FORTEO) (505(b)(2)??? --> da muss ich mich noch einlesen!)
- Now Salveen, you also asked, well, is it true that there would or would not be generics? So we're aware that Pfenex, P-F-E-N-E-X, have publicly stated that the FDA had asked them to submit a 505(b)(2) application, including both bioequivalence and comparative immunogenicity data. As you're aware, the 505(b)(2) application is different than a generic application. So we're not aware that the FDA right now has made clear that there would be ANDA applicants since Pfenex had disclosed that they had to submit a 505(b)(2).
europ. Kooperationspartner
- did not intend to build commercial infrastructure in Europe to support the launch. We did an extensive study of biotech companies with their first product, built commercial infrastructure, and with the exception of Celgene, who did an exceptional job, in most other cases, we felt that companies would have done better to have developed a partnership that could provide commercial resources to support key ex U.S. markets. So that has remained our focus, and we've guided that by the time of -- see a European launch, that we will have a partnership in place to make that possible.
zum Label:
- I feel like this is a very positive and differentiated label
- It's notable that while we do have a boxed warning that's consistent with class labeling, we were not required to have a REMS program.
zur Anwendung:
- We have a straightforward and easy-to-use subcutaneous pen design.
- Each pen carries 30 daily doses that can translate into fewer pens and co-pays that the patient continues on therapy.
- TYMLOS doesn't require refrigeration after the first dose, something we have seen repeatedly in previous market research as a nagging concern with patients on injectable anabolics.
Zeitplan / Markteinführung
- TYMLOS launch meeting in early May
- our clinical sales specialists will be educating and promoting TYMLOS in offices in early -- by mid-May. We're also already engaging top targets and key opinion leaders, and they'll be visited at least once by June.
- branded TYMLOS symposia at the upcoming AACE meeting this weekend, featuring Dr. Felicia Cosman.
- Our patient support center or hub and the call centers are already active
- specialty pharmacy network stocked and ready to distribute product and actively managing reimbursement in June
- together with TYMLOS patient support, starter kits and co-pay programs are rolling -- will be rolling out along with the product supply.
Pharmavertreter
- As Bob has mentioned previously, we were able to be very selective as Radius received thousands of applicants for our clinical sales specialist roles to help us identify the best 230 candidates.
- experienced sales team that averages over 5 years of osteoporosis experience, and nearly everyone has been through a specialty launch in their careers. We know that they know the category, their customers and their territories.
- team will cover more than 20,000 osteoporosis injectable writers, and they will fully cover these accounts at least once within the first 30 days after promotion begins
Preisgestaltung
- We must change the way clinicians, patients and payers see the anabolic class and establish TYMLOS as the leading bone-building therapy
- Notice that since 2012, the price of FORTEO has risen rapidly by double-digits annually over the last 5 years.
- That's also seen a predictable decline in overall patient volume, here identified as the total prescription volume. This pricing direction naturally challenges the notion of starting early with anabolics. Further, to win in the anabolic category and reach more anabolic-appropriate patients, we have to reset the view on the Medicaid Part D patients, which is one of the most cost-sensitive segments, patients who are paying a substantial out-of-pocket and transiting the doughnut hole.
Frequently, in interviews, conversations and even symposia, clinicians tell us that they desire to use anabolics more frequently but the out-of-pocket burden was so substantial that they were restricting the offer to many appropriate patients. If we were to expand use to more anabolic-appropriate patients, we have to address this out-of-pocket challenge.
- So to address these concerns, we've carefully chosen to price TYMLOS at an annualized wholesaler acquisition cost of $19,500 or $1,625 per pen. If the initial comments we've gotten from payers is any indication, we expect to see a very favorable response from clinicians and patients. Our focus is not only on gaining market leadership, but regaining growth in the anabolic class.
Empfehlung der ACCE
-The American College of Clinical Endocrinologists published new guidelines on the treatment of osteoporosis last September. For the first time, they recommended an anabolic agent as a first-line treatment for patients at high risk for fracture.
- We expect early first-line use of bone anabolics to increase as a result of these guidelines.
Wirkung von Tymlos
- The efficacy for fracture risk reduction for both vertebral and nonvertebral fractures have been proven.
- be able to show you the full 2-year ACTIVExtend data in the second quarter of this year.
Pipeline - Abaloparatide TD
- We believe that the transdermal patch program has the potential to allow physicians who treat osteoporosis but rarely use injectable drugs an opportunity to expand their practices to include the use of anabolic therapy.
Pipeline - RAD1901 (Elacestrant)
- completed enrollments of the 47 patients with advanced estrogen receptor positive HER2-negative breast cancer in the U.S. Phase I study and have also enrolled all 16 patients in the European FES-PET imaging study.
- On June 4 at the 2017 Clinical Society of Clinical Oncology Annual Meeting, we will present an Elacestrant clinical study abstract at the poster session
- We are currently awaiting FDA response on our planned meeting, which would include discussion of the design of the monotherapy Phase II clinical trial
Pipeline - RAD140
- IND for RAD140, a selective androgen receptor modulator which has a mechanism antitumor activity that is distinct from estrogen receptor targeted therapies, has been accepted by the FDA.
Abaloparatide in Europe
- we expect a CHMP opinion on our MAA this July and continue our guidance of having a partnership in place by time of launch. We've guided that our next financing event would take place in the context of a partnership, and we are continuing that guidance.
Q/A
zu generischem Teriparatide (FORTEO) (505(b)(2)??? --> da muss ich mich noch einlesen!)
- Now Salveen, you also asked, well, is it true that there would or would not be generics? So we're aware that Pfenex, P-F-E-N-E-X, have publicly stated that the FDA had asked them to submit a 505(b)(2) application, including both bioequivalence and comparative immunogenicity data. As you're aware, the 505(b)(2) application is different than a generic application. So we're not aware that the FDA right now has made clear that there would be ANDA applicants since Pfenex had disclosed that they had to submit a 505(b)(2).
europ. Kooperationspartner
- did not intend to build commercial infrastructure in Europe to support the launch. We did an extensive study of biotech companies with their first product, built commercial infrastructure, and with the exception of Celgene, who did an exceptional job, in most other cases, we felt that companies would have done better to have developed a partnership that could provide commercial resources to support key ex U.S. markets. So that has remained our focus, and we've guided that by the time of -- see a European launch, that we will have a partnership in place to make that possible.
Antwort auf Beitrag Nr.: 54.843.178 von Ville7 am 02.05.17 07:31:53
in der Pressekonferenz wurde auf Nachfrage zu möglichen Teriparatide-Generikas folgende Antwort gegeben - anscheinend ist eine generische Zulassung nicht so einfach zu haben:
- Now Salveen, you also asked, well, is it true that there would or would not be generics? So we're aware that Pfenex, P-F-E-N-E-X, have publicly stated that the FDA had asked them to submit a 505(b)(2) application, including both bioequivalence and comparative immunogenicity data. As you're aware, the 505(b)(2) application is different than a generic application. So we're not aware that the FDA right now has made clear that there would be ANDA applicants since Pfenex had disclosed that they had to submit a 505(b)(2).
"...und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures."
Schwanger oder nicht schwanger --> da zeigt sich wieder einmal der statistische Anfänger
Es bestehen somit meines Erachtens erhebliche Zweifel, dass die Hoffnungen des Users mit dem mit RDUS Aktien vollgestopften Depot, nicht oder nicht in der Form eintreten.
Selbstverständlich werde ich mein Investment ständig hinterfragen und falls erforderlich sofort den Bestand reduzieren. Wie ich mehrfach betont habe, ist eine ähnliche Rally wie bei EXEL nicht möglich. Die Aktie ist jedoch, insbesondere nach der Zulassung von Abaloparatide, nach unten gut abgesichert und hat durchaus mittelfristiges Potenzial auf dreistellige Kurse.
Zitat von Ville7: Der Markt hat bezüglich des Preises eine Premium gegenüber Forteo erwartet. Nun hat die Unternehmung aber überraschend einen starken Discount angekündigt.
Um die Umsatzerwartungen des Marktes nun zu treffen muss RDUS nun ungefähr doppelt so viel Tymlos absetzen. Der Markt bezweifelt das wohl, wie man die Kursreaktion interpretieren könnte. Zumal der Preis von Forteo demnächst (2018/2019) selbst massiv in den Keller gehen dürfte, wenn die generischen Varianten aufkommen. Da nutzt auch nicht die anscheinend leicht bessere Wirksamkeit und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures. Die Ärzte könnten dies möglicherweise nicht wertschätzen und Forteo und Tymlos in einen Topf werfen.
Zudem ist auch der neue Preis nicht annähernd konkurrenzfähig zu den verfügbaren oder bald verfügbaren Antikörpern. Von der Unbequemlichkeit der notwendigen täglichen Verabreichung mal abgesehen. Zum transdermalen Patch wurde auch keine konkrete Zeitschiene genannt, die dem Markt hätte konkrete Hoffnung geben können.
Es bestehen somit meines Erachtens erhebliche Zweifel, dass die Hoffnungen des Users mit dem mit RDUS Aktien vollgestopften Depot, nicht oder nicht in der Form eintreten.
in der Pressekonferenz wurde auf Nachfrage zu möglichen Teriparatide-Generikas folgende Antwort gegeben - anscheinend ist eine generische Zulassung nicht so einfach zu haben:
- Now Salveen, you also asked, well, is it true that there would or would not be generics? So we're aware that Pfenex, P-F-E-N-E-X, have publicly stated that the FDA had asked them to submit a 505(b)(2) application, including both bioequivalence and comparative immunogenicity data. As you're aware, the 505(b)(2) application is different than a generic application. So we're not aware that the FDA right now has made clear that there would be ANDA applicants since Pfenex had disclosed that they had to submit a 505(b)(2).
"...und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures."
Schwanger oder nicht schwanger --> da zeigt sich wieder einmal der statistische Anfänger

Es bestehen somit meines Erachtens erhebliche Zweifel, dass die Hoffnungen des Users mit dem mit RDUS Aktien vollgestopften Depot, nicht oder nicht in der Form eintreten.
Selbstverständlich werde ich mein Investment ständig hinterfragen und falls erforderlich sofort den Bestand reduzieren. Wie ich mehrfach betont habe, ist eine ähnliche Rally wie bei EXEL nicht möglich. Die Aktie ist jedoch, insbesondere nach der Zulassung von Abaloparatide, nach unten gut abgesichert und hat durchaus mittelfristiges Potenzial auf dreistellige Kurse.
Antwort auf Beitrag Nr.: 54.843.730 von Cyberhexe am 02.05.17 08:42:45anbei "food for thought" zur Kanzerogenitätsstudie von Abaloparatide an Ratten:
Highlights
•The PTH type 1 receptor agonist abaloparatide has potent bone anabolic activity.
•Near life-long treatment in rats with abaloparatide resulted in the formation of osteosarcomas.
•Osteosarcoma formation was dose and time dependent.
•Osteosarcoma in rats were also seen in a PTH(1–34) treated positive control group.
•There were no increases in the incidence of non-bone tumors with abaloparatide.
5. Conclusion
The current study demonstrated an increased incidence of osteosarcoma in rats treated chronically with abaloparatide, consistent with previous studies with rhPTH(1–34). These changes were consistent across comparable doses of abaloparatide and hPTH(1–34), with histopathology reflecting similarities in both neoplastic and non-neoplastic observations. Although the clinical translation of the increased rate of osteosarcoma with PTH1R agonists in rats remains unclear, these results suggest that are no additional neoplastic risks associated with near-lifetime exposure to abaloparatide.
http://www.sciencedirect.com/science/article/pii/S0273230017…
Highlights
•The PTH type 1 receptor agonist abaloparatide has potent bone anabolic activity.
•Near life-long treatment in rats with abaloparatide resulted in the formation of osteosarcomas.
•Osteosarcoma formation was dose and time dependent.
•Osteosarcoma in rats were also seen in a PTH(1–34) treated positive control group.
•There were no increases in the incidence of non-bone tumors with abaloparatide.
5. Conclusion
The current study demonstrated an increased incidence of osteosarcoma in rats treated chronically with abaloparatide, consistent with previous studies with rhPTH(1–34). These changes were consistent across comparable doses of abaloparatide and hPTH(1–34), with histopathology reflecting similarities in both neoplastic and non-neoplastic observations. Although the clinical translation of the increased rate of osteosarcoma with PTH1R agonists in rats remains unclear, these results suggest that are no additional neoplastic risks associated with near-lifetime exposure to abaloparatide.
http://www.sciencedirect.com/science/article/pii/S0273230017…
Antwort auf Beitrag Nr.: 54.843.931 von Cyberhexe am 02.05.17 09:09:18anbei ein weitere Veröffentlichung zum Thema Knochenaufbau bzw. Um- und Abbau und deren Behandlung insbesondere bei Kindern - hierbei wird romosozumab als viel versprechender Wirkstoff erwähnt; sowohl teriparatide als auch abaloparatide sind aufgrund der Resultate der Rattenkarzinogenität nicht empfohlen:
"(27). Nevertheless, both agents would not be used for children
due to carcinogenicity in animals, though clinical experience ..."
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5343005/pdf/fen…
"(27). Nevertheless, both agents would not be used for children
due to carcinogenicity in animals, though clinical experience ..."
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5343005/pdf/fen…
Antwort auf Beitrag Nr.: 54.843.730 von Cyberhexe am 02.05.17 08:42:45
Wieder mal der Versuch der Diskreditierung meine Person. Im Gegenteil, ich bin alles andere als ein Anfänger in dem Bereich.
Solltest du auch kein Anfänger sein, so weißt du genau, dass die Grenze 0,05 für die Irrtumswahrscheinlichkeit von Menschen "willkürlich" als "signifikant" festgelegt ist. Man sollte so eine Grenze niemals binär interpretieren (schwanger oder nicht schwanger), das würde die reale Welt zu sehr vereinfachen.
Ob ich eine Irrtumswahrscheinlichkeit von 5,1% oder 4,9% habe mit der ein Ergebnis einer statistischen Analyse (Patientenstudie) substantiell vom tatsächlichen Ergebnis der Grundpopulation (alle Patienten selbiger Merkmale) abweicht und somit ein falsches Ergebnis aufzeigt ist kaum unterschiedlich, nur haben Menschen irgendwann festgelegt, dass <= 5% als "signifikant" gilt und > 5% nicht. Speziell Zulassungsbehörden brauchen einen fixen Wert, damit sie zwischen Zulassung und Nicht-Zulassung entscheiden können.
Die Ärzte sind nicht so doof, dass sie die Daten der Studien nicht richtig interpretieren können, auch wenn die anderen Produkte extrem knapp am Signifikanzniveau gescheitert sind. Von daher höre endlich auf deine Follower auf die falsche Fährte zu schicken. Tymlos ist nicht so weit von Forteo entfernt wie du das suggerieren möchtest.
Zitat von Cyberhexe: "...und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures."
Schwanger oder nicht schwanger --> da zeigt sich wieder einmal der statistische Anfänger
Wieder mal der Versuch der Diskreditierung meine Person. Im Gegenteil, ich bin alles andere als ein Anfänger in dem Bereich.
Solltest du auch kein Anfänger sein, so weißt du genau, dass die Grenze 0,05 für die Irrtumswahrscheinlichkeit von Menschen "willkürlich" als "signifikant" festgelegt ist. Man sollte so eine Grenze niemals binär interpretieren (schwanger oder nicht schwanger), das würde die reale Welt zu sehr vereinfachen.
Ob ich eine Irrtumswahrscheinlichkeit von 5,1% oder 4,9% habe mit der ein Ergebnis einer statistischen Analyse (Patientenstudie) substantiell vom tatsächlichen Ergebnis der Grundpopulation (alle Patienten selbiger Merkmale) abweicht und somit ein falsches Ergebnis aufzeigt ist kaum unterschiedlich, nur haben Menschen irgendwann festgelegt, dass <= 5% als "signifikant" gilt und > 5% nicht. Speziell Zulassungsbehörden brauchen einen fixen Wert, damit sie zwischen Zulassung und Nicht-Zulassung entscheiden können.
Die Ärzte sind nicht so doof, dass sie die Daten der Studien nicht richtig interpretieren können, auch wenn die anderen Produkte extrem knapp am Signifikanzniveau gescheitert sind. Von daher höre endlich auf deine Follower auf die falsche Fährte zu schicken. Tymlos ist nicht so weit von Forteo entfernt wie du das suggerieren möchtest.
heute bei 32.5 und gestern (bisschen zu früh) nochmals nachgekauft, so biotechs sind genau meins, nach möglichkeit ein einziges zugelassenes medi mit bockbusterpotential und noch in vollem eigenbesitz, damit wird die einschätzung und bewertung der firma leichter, als wenn eine unternehmen ein halbes dutzend kooperationen mit royalties usw. hat... für mich zurzeit eine ähnliche situation wie bei relypsa dazumal, enormer abverkauf nach zulassung, später buyout (nicht das ich rein auf das aus bin hier)... ob sich die hier von cyberhexe schön dokumentierten vorteile gegenüber forteo dann auch in verkaufszahlen wiederspiegeln werden, bleibt abzuwarten, aber halte nach der zulassung den titel gegen unten auch für gut abgesichert, dass bb biotech hier fett drin ist und fleissig nachkauft schadet auch nicht
Antwort auf Beitrag Nr.: 54.848.512 von paul81 am 02.05.17 18:18:31Nettes Volumen und bisher Ansatz eines Reversals. Wenn das heute noch ins Plus dreht könnte das bereinigende Gewitter bereits vorbei sein....
gehe von einer Umkehrung aus und bin auch mal eingestiegen.
Antwort auf Beitrag Nr.: 54.844.375 von Ville7 am 02.05.17 10:12:13
bei Arzneimittelstudien ist es nun mal so, dass die Hypothese erst dann als bewiesen gilt, wenn die Irrtumswahrscheinlichkeit 5% nicht übersteigt. Eine Irrtumswahrscheinlichkeit bei einem primären Endpunkt von 5.1% wird dazu führen, dass ein Medikament mit grösster Wahrscheinlichkeit nicht zugelassen wird.
Nun, in unserem Fall (Radius Health) ist die Ausgangslage tatsächlich etwas komplizierter, weil...
... face to face --> in einer ph3-Studie (ACTIVE) Abaloparatide, gegen Plazebo und Teriparatide verglichen wurde: http://jamanetwork.com/journals/jama/fullarticle/2544640
Bei den nicht die Wirbelsäule betreffenden Frakturen wurde folgendes Ergebnis erzielt:
A Kaplan-Meier curves indicate time to the first nonvertebral fracture—a prespecified secondary end point. Nonvertebral fractures were defined as fractures excluding those of the spine, sternum, patella, toes, fingers, skull, and face and those with high trauma.
For abaloparatide vs placebo, the hazard ratio (HR) was 0.57 (95% CI, 0.32-1.00; P = .049)
and
for teriparatide vs placebo, the HR was 0.72 (95% CI, 0.42-1.22; P = .22).
Eine Irrtumswahrscheinlichkeit von 0.22 bedeutet, dass keine statistische Signifikanz gegeben ist und Teriparatide lediglich einen Trend anzeigt, auch bei nicht die Wirbelsäule betreffenden Frakturen bessere Ergebnisse zu liefern als unter Plazebo. Hingegen ist der Beweis für Abaloparatide erbracht (weil Irrtumswahrscheinlichkeit kleiner 5%), dass der Wirkstoff nicht nur zufällig bessere Ergebnisse liefert als Plazebo --> schwanger oder eben nicht schwanger!
Kompliziert wird diese Ausgangslage deshalb, weil teriparatide in einer Zulassungsstudie diesen nachweis mit statistsischer Signifikanz ebenfalls erbracht hat. Dies ist wohl der Grund, weshalb im Label von TYMLOS nur die Daten gegenüber Plazebo aufgeführt sind, nicht jedoch diejenigen gegenüber Teriparatide.
Face to face ist jedoch Abaloparatide eindeutig besser und die Pharmavertreter von Radius werden sicherlich die Paper aus den wissenschaftlichen Journals den verschreibenden Ärzten unter die Nase reiben.
Ein weiterer grosser Vorteil von Abaloparatide gegenüber Teriparatide bei den Nebenwirkungen ist die geringer auftretende und nierenschädigende Hypercalcemia:
Hypercalcemia was predefined as albumin-corrected serum calcium level of at least 10.7 mg/dL (or ≥2.67 mmol/L), and overall incidence was significantly lower in the abaloparatide group (3.4%) than the teriparatide group (6.4%) (RD, −2.96 [95% CI, −5.12 to −0.87]; P = .006) for any time point including predose and postdose.
Zitat von Ville7: Wieder mal der Versuch der Diskreditierung meine Person. Im Gegenteil, ich bin alles andere als ein Anfänger in dem Bereich.
Solltest du auch kein Anfänger sein, so weißt du genau, dass die Grenze 0,05 für die Irrtumswahrscheinlichkeit von Menschen "willkürlich" als "signifikant" festgelegt ist. Man sollte so eine Grenze niemals binär interpretieren (schwanger oder nicht schwanger), das würde die reale Welt zu sehr vereinfachen.
Ob ich eine Irrtumswahrscheinlichkeit von 5,1% oder 4,9% habe mit der ein Ergebnis einer statistischen Analyse (Patientenstudie) substantiell vom tatsächlichen Ergebnis der Grundpopulation (alle Patienten selbiger Merkmale) abweicht und somit ein falsches Ergebnis aufzeigt ist kaum unterschiedlich, nur haben Menschen irgendwann festgelegt, dass <= 5% als "signifikant" gilt und > 5% nicht. Speziell Zulassungsbehörden brauchen einen fixen Wert, damit sie zwischen Zulassung und Nicht-Zulassung entscheiden können.
Die Ärzte sind nicht so doof, dass sie die Daten der Studien nicht richtig interpretieren können, auch wenn die anderen Produkte extrem knapp am Signifikanzniveau gescheitert sind. Von daher höre endlich auf deine Follower auf die falsche Fährte zu schicken. Tymlos ist nicht so weit von Forteo entfernt wie du das suggerieren möchtest.
bei Arzneimittelstudien ist es nun mal so, dass die Hypothese erst dann als bewiesen gilt, wenn die Irrtumswahrscheinlichkeit 5% nicht übersteigt. Eine Irrtumswahrscheinlichkeit bei einem primären Endpunkt von 5.1% wird dazu führen, dass ein Medikament mit grösster Wahrscheinlichkeit nicht zugelassen wird.
Nun, in unserem Fall (Radius Health) ist die Ausgangslage tatsächlich etwas komplizierter, weil...
... face to face --> in einer ph3-Studie (ACTIVE) Abaloparatide, gegen Plazebo und Teriparatide verglichen wurde: http://jamanetwork.com/journals/jama/fullarticle/2544640
Bei den nicht die Wirbelsäule betreffenden Frakturen wurde folgendes Ergebnis erzielt:
A Kaplan-Meier curves indicate time to the first nonvertebral fracture—a prespecified secondary end point. Nonvertebral fractures were defined as fractures excluding those of the spine, sternum, patella, toes, fingers, skull, and face and those with high trauma.
For abaloparatide vs placebo, the hazard ratio (HR) was 0.57 (95% CI, 0.32-1.00; P = .049)
and
for teriparatide vs placebo, the HR was 0.72 (95% CI, 0.42-1.22; P = .22).
Eine Irrtumswahrscheinlichkeit von 0.22 bedeutet, dass keine statistische Signifikanz gegeben ist und Teriparatide lediglich einen Trend anzeigt, auch bei nicht die Wirbelsäule betreffenden Frakturen bessere Ergebnisse zu liefern als unter Plazebo. Hingegen ist der Beweis für Abaloparatide erbracht (weil Irrtumswahrscheinlichkeit kleiner 5%), dass der Wirkstoff nicht nur zufällig bessere Ergebnisse liefert als Plazebo --> schwanger oder eben nicht schwanger!
Kompliziert wird diese Ausgangslage deshalb, weil teriparatide in einer Zulassungsstudie diesen nachweis mit statistsischer Signifikanz ebenfalls erbracht hat. Dies ist wohl der Grund, weshalb im Label von TYMLOS nur die Daten gegenüber Plazebo aufgeführt sind, nicht jedoch diejenigen gegenüber Teriparatide.
Face to face ist jedoch Abaloparatide eindeutig besser und die Pharmavertreter von Radius werden sicherlich die Paper aus den wissenschaftlichen Journals den verschreibenden Ärzten unter die Nase reiben.
Ein weiterer grosser Vorteil von Abaloparatide gegenüber Teriparatide bei den Nebenwirkungen ist die geringer auftretende und nierenschädigende Hypercalcemia:
Hypercalcemia was predefined as albumin-corrected serum calcium level of at least 10.7 mg/dL (or ≥2.67 mmol/L), and overall incidence was significantly lower in the abaloparatide group (3.4%) than the teriparatide group (6.4%) (RD, −2.96 [95% CI, −5.12 to −0.87]; P = .006) for any time point including predose and postdose.
Antwort auf Beitrag Nr.: 54.849.283 von Ville7 am 02.05.17 19:45:04bin mal gespannt wie lange es dauert bis dieser Teilnehmer ähnlich wie bei Exelixis wieder auf dem Trittbrett steht - nun auch ihm sei es gegönnt.
Antwort auf Beitrag Nr.: 54.840.701 von Ville7 am 01.05.17 18:22:24
... zum Preis von Abaloparatide wäre zu sagen, dass die Preisgestaltung unter Berücksichtigung des Gesamtmarktes vorgenommen wurde--> Zitat aus der Pressekonferenz:
Frequently, in interviews, conversations and even symposia, clinicians tell us that they desire to use anabolics more frequently but the out-of-pocket burden was so substantial that they were restricting the offer to many appropriate patients. If we were to expand use to more anabolic-appropriate patients, we have to address this out-of-pocket challenge. - So to address these concerns, we've carefully chosen to price TYMLOS at an annualized wholesaler acquisition cost of $19,500 or $1,625 per pen. If the initial comments we've gotten from payers is any indication, we expect to see a very favorable response from clinicians and patients. Our focus is not only on gaining market leadership, but regaining growth in the anabolic class.
Man kann davon ausgehen, dass die Preisgestaltung wohl überlegt ist. Hingegen gibt es erhebliche Zweifel, ob den Äusserungen des zitierten Teilnehmers auch wohlüberlegte Fakten zugrunde liegen. Er fürchtet einen Preiskampf mit Forteo. Manch einer könnte diesem Teilnehmer unterstellen, dass er eine andere Preisgestaltung, nämlich über dem Preis von Forteo, ebenso kritisiert hätte, weil dieser dann nicht konkurrenzfähig sei. Wie auch immer...ich bin mir ziemlich sicher, dass Radius diesen Preis stabil halten wird und nicht in einen (Zitat ville7) "gegenseitigen Preiskampf mit Forteo" einsteigt.
Zitat von Ville7: Auch wenn das unser euphorischer Guru-User, dem man niemals widersprechen darf, nicht kapiert: der Markt reagiert nicht irrational. RDUS hat zum wiederholten Male weniger geliefert als versprochen. Man hat stets die größte Klappe z.B. "biggest value unpartnered asset in the biotech industry", aber liefert nicht das was der Markt erwartet. Die Verschiebung des Vermarktungsstarts ist das eine was seine Wirkung entfaltet hat. Viel mehr eingeschlagen hat aber wohl der niedrigere Preis als Forteo. Der Markt riecht einen gegenseitigen Preiskampf mit Forteo.
... zum Preis von Abaloparatide wäre zu sagen, dass die Preisgestaltung unter Berücksichtigung des Gesamtmarktes vorgenommen wurde--> Zitat aus der Pressekonferenz:
Frequently, in interviews, conversations and even symposia, clinicians tell us that they desire to use anabolics more frequently but the out-of-pocket burden was so substantial that they were restricting the offer to many appropriate patients. If we were to expand use to more anabolic-appropriate patients, we have to address this out-of-pocket challenge. - So to address these concerns, we've carefully chosen to price TYMLOS at an annualized wholesaler acquisition cost of $19,500 or $1,625 per pen. If the initial comments we've gotten from payers is any indication, we expect to see a very favorable response from clinicians and patients. Our focus is not only on gaining market leadership, but regaining growth in the anabolic class.
Man kann davon ausgehen, dass die Preisgestaltung wohl überlegt ist. Hingegen gibt es erhebliche Zweifel, ob den Äusserungen des zitierten Teilnehmers auch wohlüberlegte Fakten zugrunde liegen. Er fürchtet einen Preiskampf mit Forteo. Manch einer könnte diesem Teilnehmer unterstellen, dass er eine andere Preisgestaltung, nämlich über dem Preis von Forteo, ebenso kritisiert hätte, weil dieser dann nicht konkurrenzfähig sei. Wie auch immer...ich bin mir ziemlich sicher, dass Radius diesen Preis stabil halten wird und nicht in einen (Zitat ville7) "gegenseitigen Preiskampf mit Forteo" einsteigt.
Antwort auf Beitrag Nr.: 54.850.501 von Cyberhexe am 02.05.17 22:35:48....und noch ein mal zur Erinnerung:
ein Plan zur Risikominimierung wie bei FORTEO (teriparatide) --> https://www.accessdata.fda.gov/scripts/cder/rems/index.cfm?e…
wurde bei TYMLOS (abaloparatide) nicht verlangt.
Vorteil TYMLOS!
ein Plan zur Risikominimierung wie bei FORTEO (teriparatide) --> https://www.accessdata.fda.gov/scripts/cder/rems/index.cfm?e…
wurde bei TYMLOS (abaloparatide) nicht verlangt.
Vorteil TYMLOS!
Antwort auf Beitrag Nr.: 54.850.555 von Cyberhexe am 02.05.17 22:44:28...und die ersten institutionellen Anleger KAUFEN:
BIOTECH GROWTH N V 150.000 Aktien zu USD 35.3907
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
...sehr wahrscheinlich ist der Anteil der Institutionellen schon über 100%! Dank Leerverkäufer.
BIOTECH GROWTH N V 150.000 Aktien zu USD 35.3907
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
...sehr wahrscheinlich ist der Anteil der Institutionellen schon über 100%! Dank Leerverkäufer.
Antwort auf Beitrag Nr.: 54.850.624 von Cyberhexe am 02.05.17 22:53:37Obschon die Preisgestaltung von TYMLOS so nicht erwartet wurde - normalerweise werden besser wirksame Medis nach Zulassung nicht billiger als die Konkurrenzprodukte angeboten -, ist der Discount auf TYMLOS sehr wahrscheinlich die Folge einer intensiven Marktanalyse, in der selbstverständlich die Meinungen aller Stakeholder berücksichtigt werden, insbesondere die der verschreibenden Ärzte mit Blick azf die Besonderheiten des "Marktes" --> der Markt für Osteoporose ist sicherlich ein anderer als in der Onkologie.
Bin sehr gespannt, wie die Markteinführung von TYMLOS unter diesen Vorzeichen gelingen wird.
Anbei etwas "food for thought":
Experimental Osteoporosis Drug Builds Bone, Cuts Fracture Risk
Written by Sari Harrar
last update 2/15/17
Reviewed by endocrinologist Dolores Shoback, MD, a professor of medicine at the University of California, San Francisco, and a spokesperson for the Endocrine Society.
If abaloparatide wins FDA approval, a more pressing question may be cost. Currently, the retail price for a four-week supply of teriparatide is about $2,700. 8 “It can be extremely expensive for our patients even with insurance coverage,” says endocrinologist Dolores Shoback, MD, a professor of medicine at the University of California, San Francisco, and a spokesperson for the Endocrine Society. “Getting coverage can be complicated and time-consuming. You need prior authorization and often have to try a less-expensive osteoporosis drug first for a trial period, such as a bisphosphonate, and demonstrate intolerance or failure to improve bone mass.”
The bigger issue: Getting treatments to people at high risk for bone fractures – even if they’ve had one break already. According to the National Osteoporosis Foundation, about eight million women and two million men have the disease; another 43 million are at risk. Fractures can change, or end, lives. Of the 300,000 people have an osteoporosis-related hip fractures each year in the U.S, one in four end up in a nursing home. Among those over age 50, 26% die within a year.10 Yet just 29% of women who’ve had a broken hip are using an osteoporosis drug a year later, according to an editorial co-authored by Dr. Shoback that accompanied the study. 11
Bin sehr gespannt, wie die Markteinführung von TYMLOS unter diesen Vorzeichen gelingen wird.
Anbei etwas "food for thought":
Experimental Osteoporosis Drug Builds Bone, Cuts Fracture Risk
Written by Sari Harrar
last update 2/15/17
Reviewed by endocrinologist Dolores Shoback, MD, a professor of medicine at the University of California, San Francisco, and a spokesperson for the Endocrine Society.
If abaloparatide wins FDA approval, a more pressing question may be cost. Currently, the retail price for a four-week supply of teriparatide is about $2,700. 8 “It can be extremely expensive for our patients even with insurance coverage,” says endocrinologist Dolores Shoback, MD, a professor of medicine at the University of California, San Francisco, and a spokesperson for the Endocrine Society. “Getting coverage can be complicated and time-consuming. You need prior authorization and often have to try a less-expensive osteoporosis drug first for a trial period, such as a bisphosphonate, and demonstrate intolerance or failure to improve bone mass.”
The bigger issue: Getting treatments to people at high risk for bone fractures – even if they’ve had one break already. According to the National Osteoporosis Foundation, about eight million women and two million men have the disease; another 43 million are at risk. Fractures can change, or end, lives. Of the 300,000 people have an osteoporosis-related hip fractures each year in the U.S, one in four end up in a nursing home. Among those over age 50, 26% die within a year.10 Yet just 29% of women who’ve had a broken hip are using an osteoporosis drug a year later, according to an editorial co-authored by Dr. Shoback that accompanied the study. 11
Antwort auf Beitrag Nr.: 54.850.099 von Cyberhexe am 02.05.17 21:47:18
Diese erneute Arroganz der Aussage und die wiederholte Lüge ich sei dein Trittbrettfahrer bei EXEL ist nicht zu übertreffen. Genau deswegen bist du bei mir mehr als untendurch. Die Historie in Wallstreet-Online, die nicht lügen kann zeigt:In Wirklichkeit bist du wohl ein Trittbrettfahrer von mir.
Ich habe zu EXEL in einem anderen Thread bereits gepostet, da war von dir noch nichts zu sehen. Kannst du und deine Fangemeinde hier in diesem Thread nachlesen, der leider nicht wirklich gepflegt wurde:
http://www.wallstreet-online.de/diskussion/500-beitraege/115…
Dein Thread wurde erst im Jahr 2014 eröffnet - eine offene Diskussion war dort aber nie möglich, da stets nur deine Meinung gelten durfte:
Wie wäre es endlich mal mit einer Entschuldigung? "Oh sorry, ich hab was falsches behauptet, tut mir leid!" ???
Zitat von Cyberhexe: bin mal gespannt wie lange es dauert bis dieser Teilnehmer ähnlich wie bei Exelixis wieder auf dem Trittbrett steht - nun auch ihm sei es gegönnt.
Diese erneute Arroganz der Aussage und die wiederholte Lüge ich sei dein Trittbrettfahrer bei EXEL ist nicht zu übertreffen. Genau deswegen bist du bei mir mehr als untendurch. Die Historie in Wallstreet-Online, die nicht lügen kann zeigt:In Wirklichkeit bist du wohl ein Trittbrettfahrer von mir.
Ich habe zu EXEL in einem anderen Thread bereits gepostet, da war von dir noch nichts zu sehen. Kannst du und deine Fangemeinde hier in diesem Thread nachlesen, der leider nicht wirklich gepflegt wurde:
http://www.wallstreet-online.de/diskussion/500-beitraege/115…


Dein Thread wurde erst im Jahr 2014 eröffnet - eine offene Diskussion war dort aber nie möglich, da stets nur deine Meinung gelten durfte:

Wie wäre es endlich mal mit einer Entschuldigung? "Oh sorry, ich hab was falsches behauptet, tut mir leid!" ???
Zu RDUS nur noch so viel:
1. Dass ein großer Investor drin sitzt und ständig nachkauft hat nicht unbedingt damit zu tun, dass er weiterhin extrem überzeugt ist, sondern dient auch dem Schutz der eigenen Positionierung. Diese Positionierung kann sich für ihn auch als Fehlpositionierung herausstellen. Dann ist so einer wie BBBiotech schnell auch massiv draussen. Ich erinnere an Bavarian Nordic, wo ein Ausstieg von BBBiotech die Aktie von über 200 DKK auf unter 40 DKK gebracht hat (heute übrigens 375 DKK).
2. Man sollte nicht alles was die Firma von sich gibt unreflektiert nachbabbeln, so wie das Cyberhexe leider macht. Jede Firma verfolgt mit ihrer Info-Politik bestimmte Ziele. Und bei RDUS ist die Kommunikation immer derart, dass man nicht besonders realistisch kommuniziert, sondern immer einen ziemlichen Positiv-bias drin hat. Ich erinnere nur an den Satz "greatest value unpartnered asset in the biotech industry", der zu jedem CC verwendet wurde. Oder die großspurige Ankündigung der RAD-1901 Daten, die der Markt nach Veröffentlichung ganz anders gesehen hat. Die Börse hasst solche Firmen, die ständig overpromises machen und underdelivern. Bei RDUS kommt der Stein der Wahrheit dann mit den künftigen Verkäufen....
1. Dass ein großer Investor drin sitzt und ständig nachkauft hat nicht unbedingt damit zu tun, dass er weiterhin extrem überzeugt ist, sondern dient auch dem Schutz der eigenen Positionierung. Diese Positionierung kann sich für ihn auch als Fehlpositionierung herausstellen. Dann ist so einer wie BBBiotech schnell auch massiv draussen. Ich erinnere an Bavarian Nordic, wo ein Ausstieg von BBBiotech die Aktie von über 200 DKK auf unter 40 DKK gebracht hat (heute übrigens 375 DKK).
2. Man sollte nicht alles was die Firma von sich gibt unreflektiert nachbabbeln, so wie das Cyberhexe leider macht. Jede Firma verfolgt mit ihrer Info-Politik bestimmte Ziele. Und bei RDUS ist die Kommunikation immer derart, dass man nicht besonders realistisch kommuniziert, sondern immer einen ziemlichen Positiv-bias drin hat. Ich erinnere nur an den Satz "greatest value unpartnered asset in the biotech industry", der zu jedem CC verwendet wurde. Oder die großspurige Ankündigung der RAD-1901 Daten, die der Markt nach Veröffentlichung ganz anders gesehen hat. Die Börse hasst solche Firmen, die ständig overpromises machen und underdelivern. Bei RDUS kommt der Stein der Wahrheit dann mit den künftigen Verkäufen....
Leute, schaut euch diesen Thread an und wie viele Postings ich zu EXEL seit 2012 geschrieben habe. Irgendwann im April 2014 taucht dann Cyberhexe genau in diesem Thread mit ihrem ersten Posting auf und eröffnet in Folge einen eigenen Thread im Mai 2014. Und besitzt dann die Frechheit mich als ihren Trittbrettfahrer zu bezeichnen. Mir geht das echt nicht runter.
http://www.wallstreet-online.de/diskussion/500-beitraege/115…
http://www.wallstreet-online.de/diskussion/500-beitraege/115…
die Vereinigung der amerikanischen Endokrinologen empfiehlt folgende Vorgehensweise bei Osteoporosis:
https://www.aace.com/files/final-algorithm.pdf
bei
"Prior fragility fractures or indicators of higher fracture risk**"
wird empfohlen, folgende Medikamente zu verabreichen (in alphabet. Reihenfolge): • Denosumab, teriparatide, zoledronic acid***
Bin gespannt wie lange es dauert, bis Abaloparatide in diese Aufzählung mit aufgenommen wird.
apropos...
Ich glaube es ist Konsens der allermeisten User, dass ein solches Forum nicht der persönlichen Selbstdarstellung sondern ausschliesslich dem Austausch von Informationen dient. Ob ein Teilnehmer nun 127.5% oder 129.2% bei einer Aktie verdient hat, ist vielleicht dann von Bedeutung, wenn ein Depot transparent und somit überprüfbar geführt wird, alles andere ist jedoch Sandkasten!
...eigentlich habe ich keine Lust auf Diskussionen mit Selbstdarstellern einzugehen - nur so viel dazu: wenn jemand unpräzise bis falsche Fakten im Forum veröffentlicht bzw. Daten bspw. statistischer Natur falsch interpretiert, dann muss damit gerechnet werden, dass dies korrigiert wird.
Wenn auf solche Kritik bzw. Richtigstellung aggressive Angriffe bis hin zu verbalen Entgleisungen folgen - so geschehen bei EXELIXIS und nun auch bei RADIUS HEALTH-, dann würde ich das gerne ignorieren - leider gelingt mir das nicht immer.
https://www.aace.com/files/final-algorithm.pdf
bei
"Prior fragility fractures or indicators of higher fracture risk**"
wird empfohlen, folgende Medikamente zu verabreichen (in alphabet. Reihenfolge): • Denosumab, teriparatide, zoledronic acid***
Bin gespannt wie lange es dauert, bis Abaloparatide in diese Aufzählung mit aufgenommen wird.
apropos...
Ich glaube es ist Konsens der allermeisten User, dass ein solches Forum nicht der persönlichen Selbstdarstellung sondern ausschliesslich dem Austausch von Informationen dient. Ob ein Teilnehmer nun 127.5% oder 129.2% bei einer Aktie verdient hat, ist vielleicht dann von Bedeutung, wenn ein Depot transparent und somit überprüfbar geführt wird, alles andere ist jedoch Sandkasten!
...eigentlich habe ich keine Lust auf Diskussionen mit Selbstdarstellern einzugehen - nur so viel dazu: wenn jemand unpräzise bis falsche Fakten im Forum veröffentlicht bzw. Daten bspw. statistischer Natur falsch interpretiert, dann muss damit gerechnet werden, dass dies korrigiert wird.
Wenn auf solche Kritik bzw. Richtigstellung aggressive Angriffe bis hin zu verbalen Entgleisungen folgen - so geschehen bei EXELIXIS und nun auch bei RADIUS HEALTH-, dann würde ich das gerne ignorieren - leider gelingt mir das nicht immer.
Antwort auf Beitrag Nr.: 54.840.701 von Ville7 am 01.05.17 18:22:24
die Marktanalyse von Radius hat ergeben, dass eine Preiserhöhung stets einen Rückgang bei der Zahl der Anwender zur Folge hatte. Ich bin sehr zuversichtlich, dass die Preisfindung bei TYMLOS eine erfolgreiche Markteinführung trotz Konkurrenz möglich machen sollte.
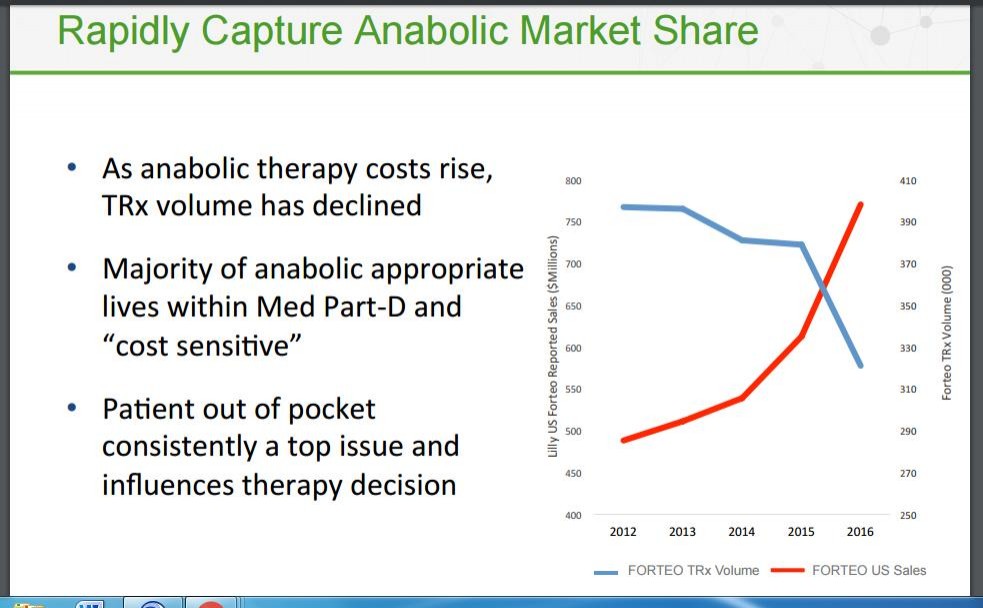
Zitat von Ville7: Auch wenn das unser euphorischer Guru-User, dem man niemals widersprechen darf, nicht kapiert: der Markt reagiert nicht irrational. RDUS hat zum wiederholten Male weniger geliefert als versprochen. Man hat stets die größte Klappe z.B. "biggest value unpartnered asset in the biotech industry", aber liefert nicht das was der Markt erwartet. Die Verschiebung des Vermarktungsstarts ist das eine was seine Wirkung entfaltet hat. Viel mehr eingeschlagen hat aber wohl der niedrigere Preis als Forteo. Der Markt riecht einen gegenseitigen Preiskampf mit Forteo.
die Marktanalyse von Radius hat ergeben, dass eine Preiserhöhung stets einen Rückgang bei der Zahl der Anwender zur Folge hatte. Ich bin sehr zuversichtlich, dass die Preisfindung bei TYMLOS eine erfolgreiche Markteinführung trotz Konkurrenz möglich machen sollte.

Antwort auf Beitrag Nr.: 54.860.128 von Basilea1234 am 04.05.17 00:34:28Hi 1234
die Umsatzgrafik zu FORTEO stammt wohl aus der Präsentation der Quartalszahlen....diese auch:
http://files.shareholder.com/downloads/AMDA-1D3H6P/437562816…

die Umsatzgrafik zu FORTEO stammt wohl aus der Präsentation der Quartalszahlen....diese auch:
http://files.shareholder.com/downloads/AMDA-1D3H6P/437562816…

Antwort auf Beitrag Nr.: 54.853.138 von Ville7 am 03.05.17 11:00:57
Die Studienergebnisse zu Abaloparatide sind in vielen wissenschaftlichen Journals genauso dokumentiert wie von der Firma veröffentlicht. Und genau darauf ist die Zulassung der FDA begründet. Da wurde nichts beschönigt.
Die RAD1901-Daten sind bisher viel versprechend, auch wenn dies vom Markt nicht positiv angenommen wurde. Aber selbst die Zulassung von Abaloparatide wurde bisher nicht positiv aufgenommen.
Es ist allerdings durchaus selten, dass präklinische oder Phase-1-Daten aus der Klinik in die Wirtschaftlichkeitsberechnung der Analysten einfliessen. Erst die weiteren Ergebnisse in den späteren klinischen Phasen werden zeigen, wie gross die Chance auf Zulassung sein wird.
Zu BB Biotech wäre zu sagen, dass diese an den Erfolg des Unternehmens bzw. Abaloparatide anscheinend glauben und deswegen weiter zukaufen (üblicherweise werden bei BB Biotech Positionen über die entsprechenden Warrants abgesichert). Allerdings ist das CH-Unternehmen nicht der einzige institutionelle Anleger, der an diesen Erfolg zu glauben scheint.
Die derzeit veröffentlichte Rate ist diesbezüglich nahe 100% --> aktuell 99.36 %
Natürlich ist dies keine Gewähr für einen positiven Kursverlauf, aber unangenehm ist dieser Investitionsgrad nun auch wieder nicht.
http://www.nasdaq.com/symbol/rdus/institutional-holdings
Food for thought: anbei einige Hyperlinks
http://press.endocrine.org/doi/abs/10.1210/endo-meetings.201…
https://www.endocrineweb.com/news/osteoporosis/54587-experim…
http://jamanetwork.com/journals/jama/article-abstract/254462…
Zitat von Ville7: Zu RDUS nur noch so viel:
1. Dass ein großer Investor drin sitzt und ständig nachkauft hat nicht unbedingt damit zu tun, dass er weiterhin extrem überzeugt ist, sondern dient auch dem Schutz der eigenen Positionierung. Diese Positionierung kann sich für ihn auch als Fehlpositionierung herausstellen. Dann ist so einer wie BBBiotech schnell auch massiv draussen. Ich erinnere an Bavarian Nordic, wo ein Ausstieg von BBBiotech die Aktie von über 200 DKK auf unter 40 DKK gebracht hat (heute übrigens 375 DKK).
2. Man sollte nicht alles was die Firma von sich gibt unreflektiert nachbabbeln, so wie das Cyberhexe leider macht. Jede Firma verfolgt mit ihrer Info-Politik bestimmte Ziele. Und bei RDUS ist die Kommunikation immer derart, dass man nicht besonders realistisch kommuniziert, sondern immer einen ziemlichen Positiv-bias drin hat. Ich erinnere nur an den Satz "greatest value unpartnered asset in the biotech industry", der zu jedem CC verwendet wurde. Oder die großspurige Ankündigung der RAD-1901 Daten, die der Markt nach Veröffentlichung ganz anders gesehen hat. Die Börse hasst solche Firmen, die ständig overpromises machen und underdelivern. Bei RDUS kommt der Stein der Wahrheit dann mit den künftigen Verkäufen....
Die Studienergebnisse zu Abaloparatide sind in vielen wissenschaftlichen Journals genauso dokumentiert wie von der Firma veröffentlicht. Und genau darauf ist die Zulassung der FDA begründet. Da wurde nichts beschönigt.
Die RAD1901-Daten sind bisher viel versprechend, auch wenn dies vom Markt nicht positiv angenommen wurde. Aber selbst die Zulassung von Abaloparatide wurde bisher nicht positiv aufgenommen.
Es ist allerdings durchaus selten, dass präklinische oder Phase-1-Daten aus der Klinik in die Wirtschaftlichkeitsberechnung der Analysten einfliessen. Erst die weiteren Ergebnisse in den späteren klinischen Phasen werden zeigen, wie gross die Chance auf Zulassung sein wird.
Zu BB Biotech wäre zu sagen, dass diese an den Erfolg des Unternehmens bzw. Abaloparatide anscheinend glauben und deswegen weiter zukaufen (üblicherweise werden bei BB Biotech Positionen über die entsprechenden Warrants abgesichert). Allerdings ist das CH-Unternehmen nicht der einzige institutionelle Anleger, der an diesen Erfolg zu glauben scheint.
Die derzeit veröffentlichte Rate ist diesbezüglich nahe 100% --> aktuell 99.36 %
Natürlich ist dies keine Gewähr für einen positiven Kursverlauf, aber unangenehm ist dieser Investitionsgrad nun auch wieder nicht.
http://www.nasdaq.com/symbol/rdus/institutional-holdings
Food for thought: anbei einige Hyperlinks
http://press.endocrine.org/doi/abs/10.1210/endo-meetings.201…
https://www.endocrineweb.com/news/osteoporosis/54587-experim…
http://jamanetwork.com/journals/jama/article-abstract/254462…
Antwort auf Beitrag Nr.: 54.860.389 von Cyberhexe am 04.05.17 06:51:18für den Leerverkauf verfügbare Aktien (RDUS) aktuell lediglich 80´000 - zum Vergleich bei EXEL derzeit > 10 Mio
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
"naked short selling" ist natürlich dennoch möglich!
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
"naked short selling" ist natürlich dennoch möglich!
Investor Network: Radius Health Inc. to Host Earnings Call
May 3, 2017
NEW YORK, NY / ACCESSWIRE / May 3, 2017 /
Radius Health Inc. (NASDAQ: RDUS) will be discussing their earnings results in their Q1 Earnings Call to be held
May 3, 2017 at 4:30 PM Eastern Time.
https://finance.yahoo.com/news/investor-network-radius-healt…
May 3, 2017
NEW YORK, NY / ACCESSWIRE / May 3, 2017 /
Radius Health Inc. (NASDAQ: RDUS) will be discussing their earnings results in their Q1 Earnings Call to be held
May 3, 2017 at 4:30 PM Eastern Time.
https://finance.yahoo.com/news/investor-network-radius-healt…
Antwort auf Beitrag Nr.: 54.862.273 von bernie55 am 04.05.17 10:52:55Why Radius Health Inc. Is Dropping Today
Shares fall after the company reports a larger-than-expected quarterly loss, but exciting times lie ahead.
Brian Feroldi (TMFTypeoh) May 1, 2017 at 3:58PM
What happened
In response to the company reporting a higher-than-expected first-quarter loss, shares of Radius Health (NASDAQ:RDUS), a biopharma focused on bone disease, dropped by 10% as of 3 p.m. EST on Monday.
So what
Radius Health reported a net loss of $56.9 million for the quarter, or $1.32 per share. This figure was a little bit higher than the $1.18 net loss that Wall Street had expected, and could be contributing to the selling pressure today.
Turning to the balance sheet, Radius reported $282.1 million in cash at quarter-end. Management estimates this is enough cash to fund operations for at least another year.
Financial updates aside, the big news out of Radius recently was that it received approval from the U.S. Food and Drug Administration for Tymlos -- formerly called abaloparatide -- on April 28th.
The company plans on launching the drug for sale later this month. However, it is worth pointing out that Tymlos was approved with a black-box warning label for those who have an increased risk of developing osteosarcoma, which is a type of bone tumor.
Now what
Regardless of short-term price movements, Radius investors have a lot to look forward to in the year ahead.
For one, the company should hear an opinion from CHMP (the Committee for Medicinal Products for Human Use, of the European Medicines Agency) related to a potential European approval in the coming months. Next, management hinted that it could announce a commercialization partner prior to the drug's launch. Finally, data from the recently completed 24-month ACTIVExtend clinical trial is expected to be released later this quarter.
On the other hand, the FDA is set to rule in just a few months on Amgen's osteoporosis drug romosozumab. This drug is expected to compete directly with Tymlos, so if the FDA doesn't slap it with a similar warning label, then Radius might have a hard time competing.
While Radius Health's investors will want to keep an eye on romosozumab, osteoporosis remains a huge problem that affects more than 200 million people worldwide. That could prove to be a big enough market opportunity for Tymlos to generate significant sales even if it is forced to play second fiddle to romosozumab.
https://www.fool.com/investing/2017/05/01/why-radius-health-…
Shares fall after the company reports a larger-than-expected quarterly loss, but exciting times lie ahead.
Brian Feroldi (TMFTypeoh) May 1, 2017 at 3:58PM
What happened
In response to the company reporting a higher-than-expected first-quarter loss, shares of Radius Health (NASDAQ:RDUS), a biopharma focused on bone disease, dropped by 10% as of 3 p.m. EST on Monday.
So what
Radius Health reported a net loss of $56.9 million for the quarter, or $1.32 per share. This figure was a little bit higher than the $1.18 net loss that Wall Street had expected, and could be contributing to the selling pressure today.
Turning to the balance sheet, Radius reported $282.1 million in cash at quarter-end. Management estimates this is enough cash to fund operations for at least another year.
Financial updates aside, the big news out of Radius recently was that it received approval from the U.S. Food and Drug Administration for Tymlos -- formerly called abaloparatide -- on April 28th.
The company plans on launching the drug for sale later this month. However, it is worth pointing out that Tymlos was approved with a black-box warning label for those who have an increased risk of developing osteosarcoma, which is a type of bone tumor.
Now what
Regardless of short-term price movements, Radius investors have a lot to look forward to in the year ahead.
For one, the company should hear an opinion from CHMP (the Committee for Medicinal Products for Human Use, of the European Medicines Agency) related to a potential European approval in the coming months. Next, management hinted that it could announce a commercialization partner prior to the drug's launch. Finally, data from the recently completed 24-month ACTIVExtend clinical trial is expected to be released later this quarter.
On the other hand, the FDA is set to rule in just a few months on Amgen's osteoporosis drug romosozumab. This drug is expected to compete directly with Tymlos, so if the FDA doesn't slap it with a similar warning label, then Radius might have a hard time competing.
While Radius Health's investors will want to keep an eye on romosozumab, osteoporosis remains a huge problem that affects more than 200 million people worldwide. That could prove to be a big enough market opportunity for Tymlos to generate significant sales even if it is forced to play second fiddle to romosozumab.
https://www.fool.com/investing/2017/05/01/why-radius-health-…
Antwort auf Beitrag Nr.: 54.862.273 von bernie55 am 04.05.17 10:52:55BB Biotech hat gestern erneut gemeldet, dass am Tag zuvor (2.5.17) 75´000 Aktien zu USD 33,9056 gekauft wurden:
http://ir.radiuspharm.com/sec.cfm
bereits am 1.5.2017 wurden zusätzliche 150´000 Aktien zu USD 35,3907 erworben!
http://ir.radiuspharm.com/sec.cfm
bereits am 1.5.2017 wurden zusätzliche 150´000 Aktien zu USD 35,3907 erworben!
Antwort auf Beitrag Nr.: 54.843.178 von Ville7 am 02.05.17 07:31:53
Der Kritikpunkt zu den nicht die Wirbelsäule betreffenden Frakturen ist in zweierlei Hinsicht nicht korrekt:
1.) in einer Arzneimittelstudie ist statistische Signifikanz dann erreicht, wenn die Irrtumswahrscheinlichkeit kleiner/gleich 5% beträgt. Daran ist nicht zu rütteln.
und
2.) über die Zeit wird die Irrtumswahrscheinlichkeit bei den "Nonvertebral Fractures" zudem kleiner, so dass nach 25 Monaten eine Irrtumswahrscheinlichkeit von 1.7% realisiert wird.
Quelle hierzu ist das von der FDA veröffentlichte Label:
"Effect on Nonvertebral Fractures
Following 6 months of alendronate treatment in Study 005, the cumulative incidence of nonvertebral fractures at 25 months was 2.7% for women in the prior TYMLOS group compared to 5.6% for women in the prior placebo group (Figure 2). At 25 months, the relative risk reduction in nonvertebral fractures was 52% (logrank test p=0.017) and the absolute reisk reduction was 2.9%."
Zitat von Ville7: Der Markt hat bezüglich des Preises eine Premium gegenüber Forteo erwartet. Nun hat die Unternehmung aber überraschend einen starken Discount angekündigt.
Um die Umsatzerwartungen des Marktes nun zu treffen muss RDUS nun ungefähr doppelt so viel Tymlos absetzen. Der Markt bezweifelt das wohl, wie man die Kursreaktion interpretieren könnte. Zumal der Preis von Forteo demnächst (2018/2019) selbst massiv in den Keller gehen dürfte, wenn die generischen Varianten aufkommen. Da nutzt auch nicht die anscheinend leicht bessere Wirksamkeit und die gerade mal so getroffene stat. Signifikanz in Non-Vertr. Fractures. Die Ärzte könnten dies möglicherweise nicht wertschätzen und Forteo und Tymlos in einen Topf werfen.
Zudem ist auch der neue Preis nicht annähernd konkurrenzfähig zu den verfügbaren oder bald verfügbaren Antikörpern. Von der Unbequemlichkeit der notwendigen täglichen Verabreichung mal abgesehen. Zum transdermalen Patch wurde auch keine konkrete Zeitschiene genannt, die dem Markt hätte konkrete Hoffnung geben können.
Es bestehen somit meines Erachtens erhebliche Zweifel, dass die Hoffnungen des Users mit dem mit RDUS Aktien vollgestopften Depot, nicht oder nicht in der Form eintreten.
Der Kritikpunkt zu den nicht die Wirbelsäule betreffenden Frakturen ist in zweierlei Hinsicht nicht korrekt:
1.) in einer Arzneimittelstudie ist statistische Signifikanz dann erreicht, wenn die Irrtumswahrscheinlichkeit kleiner/gleich 5% beträgt. Daran ist nicht zu rütteln.
und
2.) über die Zeit wird die Irrtumswahrscheinlichkeit bei den "Nonvertebral Fractures" zudem kleiner, so dass nach 25 Monaten eine Irrtumswahrscheinlichkeit von 1.7% realisiert wird.
Quelle hierzu ist das von der FDA veröffentlichte Label:
"Effect on Nonvertebral Fractures
Following 6 months of alendronate treatment in Study 005, the cumulative incidence of nonvertebral fractures at 25 months was 2.7% for women in the prior TYMLOS group compared to 5.6% for women in the prior placebo group (Figure 2). At 25 months, the relative risk reduction in nonvertebral fractures was 52% (logrank test p=0.017) and the absolute reisk reduction was 2.9%."
!
Dieser Beitrag wurde von FairMOD moderiert. Grund: Persönliche Differenzen bitte via BM klären
Antwort auf Beitrag Nr.: 54.860.128 von Basilea1234 am 04.05.17 00:34:28Glaube keiner Marktanalyse, die du nicht selbst erstellt hast! Grundsätzlich ist es ein großes Schwächezeichen, wenn dem Markt für ein anscheinend besseres Produkt nur mit einem erheblich geringeren Preis Anteile abzujagen sind. Denk mal drüber nach...
Antwort auf Beitrag Nr.: 54.860.389 von Cyberhexe am 04.05.17 06:51:18Wer diesen Dick-Fischen hinterherläuft wird langfristig nicht besonders erfolgreich sein, geschweige denn den Markt schlagen. Von BBBiotech und Konsorten halte ich nicht besonders viel. Nur meine Meinung und Erfahrung.
Wenn man Euch zudem so hört, dann könnte man denken, dass ein Teil deren Erfolgs auf Frontrunning zurückzuführen ist.
Wenn man Euch zudem so hört, dann könnte man denken, dass ein Teil deren Erfolgs auf Frontrunning zurückzuführen ist.
Antwort auf Beitrag Nr.: 54.864.814 von Cyberhexe am 04.05.17 14:47:09Du kannst mit deinen erreichten Signifikanzwerten noch so um dich schmeißen. Es zählen andere Dinge wie Convenience und Sicherheit mehr als knapp verfehlte Signifikanzwerte bei non-vertr. farctures. Täglich Spritzen zu müssen mit Risiko Knochenkrebs und zu horrend hohen Kosten schreckt eben dreifach ab und spricht gegen Forteo und Tymlos. Dann eben nen Antikörper mit weniger Wirksamkeit und viel billiger nur einmal im halben Jahr. Manchmal ist eine einfache Logik nicht so schwierig und sie bestimmt Erfolg oder Misserfolg, du hast nur Probleme es zu kapieren...
Wenn ich die Depotzusammensetzung von BBBiotech mit der Statistik von W/O "Investoren, die diesen Wert beobachten, informieren sich auch über: ..." für dieses Board und dessen Leser vergleiche, dann sehe ich bei dieser W/O Auflistung nahezu nur Werte von BBBiotech. So viel zu den Themen Trittbrettfahrer und BBBiotech. Gehört bei der Fangemeinde hier wohl beides eng zusammen (Trittbrettfahren bei BBBiotech). Übrigens steht in dieser W/O Statistik keiner meiner Werte, find ich gut.
Antwort auf Beitrag Nr.: 54.875.665 von Ville7 am 05.05.17 17:26:06hehe die sind aber auch beim who is who der biotech-szene investiert (interessanterweise haben sie exelixis völlig verpennt  )
)
 )
) !
Dieser Beitrag wurde von FairMOD moderiert. Grund: Korrespondierendes Posting wurde entfernt!
Dieser Beitrag wurde von FairMOD moderiert. Grund: Korrespondierendes Posting wurde entfernt
Antwort auf Beitrag Nr.: 54.852.922 von Ville7 am 03.05.17 10:41:11
Jetzt geht das schon wieder los!?
Obschon ich mir vorgenommen habe, nicht mehr auf "themafremde" Beiträge einzugehen, will ich diesen erneuten "Lügner" so nicht stehen lassen.
Ich möchte vorausschicken, dass ich für eine gewisse Zeit meinen in deutschen Foren gebrauchten Nickname (Cyberhexe) dem in den englischsprachigen Foren (Franca_ole --> siehe InvestorVillage oder financeyahoo) angepasst hatte. Nachdem dieser Namenswechsel von wo moniert wurde, bin ich über eine systembedingte Zwischenlösung (cyberhexe123) wieder bei meinem ursprünglichen Nickname (Cyberhexe) gelandet.
Da das Zurückblättern bei wo sehr mühsam ist und ich diese Energie nicht vergeuden will, möchte ich aus meinen Emails zitieren, in welchen die übelsten Verunglimpfungen festgehalten und gemeldet wurden (ich würde jetzt mal vermuten, dass es deswegen für diesen Teilnehmer bereits eine Abmahnung gegeben hat, obschon ich dies nicht beweisen kann).
Zitiert aus dem Thraed "Exelixis...ein schalfender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935) von Franca_ole am 11.11.15 um 09:00:03
die folgenden Sätze:
"Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken.
Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen."
Darüber hinaus gab es immer wieder unpräzise bis hin zu falschen Behauptungen, die nach Richtigstellung fast immer mit persönlichen Angriffen gekontert wurden.
So und nun habe ich auf diese Auseinandersetzung (bzw. Selbstdarstellung) keine Lust mehr und hoffe, dass es mir endlich gelingt, auf solche Anfeindungen nicht zu reagieren.
Zitat von Ville7:Zitat von Cyberhexe: bin mal gespannt wie lange es dauert bis dieser Teilnehmer ähnlich wie bei Exelixis wieder auf dem Trittbrett steht - nun auch ihm sei es gegönnt.
Diese erneute Arroganz der Aussage und die wiederholte Lüge ich sei dein Trittbrettfahrer bei EXEL ist nicht zu übertreffen. Genau deswegen bist du bei mir mehr als untendurch. Die Historie in Wallstreet-Online, die nicht lügen kann zeigt:In Wirklichkeit bist du wohl ein Trittbrettfahrer von mir.
Ich habe zu EXEL in einem anderen Thread bereits gepostet, da war von dir noch nichts zu sehen. Kannst du und deine Fangemeinde hier in diesem Thread nachlesen, der leider nicht wirklich gepflegt wurde:
http://www.wallstreet-online.de/diskussion/500-beitraege/115…
Dein Thread wurde erst im Jahr 2014 eröffnet - eine offene Diskussion war dort aber nie möglich, da stets nur deine Meinung gelten durfte:
Wie wäre es endlich mal mit einer Entschuldigung? "Oh sorry, ich hab was falsches behauptet, tut mir leid!" ???
Jetzt geht das schon wieder los!?
Obschon ich mir vorgenommen habe, nicht mehr auf "themafremde" Beiträge einzugehen, will ich diesen erneuten "Lügner" so nicht stehen lassen.
Ich möchte vorausschicken, dass ich für eine gewisse Zeit meinen in deutschen Foren gebrauchten Nickname (Cyberhexe) dem in den englischsprachigen Foren (Franca_ole --> siehe InvestorVillage oder financeyahoo) angepasst hatte. Nachdem dieser Namenswechsel von wo moniert wurde, bin ich über eine systembedingte Zwischenlösung (cyberhexe123) wieder bei meinem ursprünglichen Nickname (Cyberhexe) gelandet.
Da das Zurückblättern bei wo sehr mühsam ist und ich diese Energie nicht vergeuden will, möchte ich aus meinen Emails zitieren, in welchen die übelsten Verunglimpfungen festgehalten und gemeldet wurden (ich würde jetzt mal vermuten, dass es deswegen für diesen Teilnehmer bereits eine Abmahnung gegeben hat, obschon ich dies nicht beweisen kann).
Zitiert aus dem Thraed "Exelixis...ein schalfender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935) von Franca_ole am 11.11.15 um 09:00:03
die folgenden Sätze:
"Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken.
Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen."
Darüber hinaus gab es immer wieder unpräzise bis hin zu falschen Behauptungen, die nach Richtigstellung fast immer mit persönlichen Angriffen gekontert wurden.
So und nun habe ich auf diese Auseinandersetzung (bzw. Selbstdarstellung) keine Lust mehr und hoffe, dass es mir endlich gelingt, auf solche Anfeindungen nicht zu reagieren.
Antwort auf Beitrag Nr.: 54.877.666 von Cyberhexe am 05.05.17 20:48:51Diese Schleife gefällt mir:
http://www.investorvillage.com/smbd.asp?mb=1086&mn=11632&pt=…
http://www.investorvillage.com/smbd.asp?mb=1086&mn=11632&pt=…
Antwort auf Beitrag Nr.: 54.876.034 von paul81 am 05.05.17 18:00:16
du sprichst mir aus der Seele - bei EXEL war ich "all in one" und BB Biotech hielt nicht 1 Aktie. Wenn BB Biotech nun an den Erfolg von RDUS glaubt, ist das für mich noch kein Grund, nicht in dieses Unternehmen zu investieren.
Es ist schon sehr seltsam, welche Kausalketten hier im Forum von einem bestimmten Teilnehmer veröffentlicht werden.
Zitat von paul81: hehe die sind aber auch beim who is who der biotech-szene investiert (interessanterweise haben sie exelixis völlig verpennt)
du sprichst mir aus der Seele - bei EXEL war ich "all in one" und BB Biotech hielt nicht 1 Aktie. Wenn BB Biotech nun an den Erfolg von RDUS glaubt, ist das für mich noch kein Grund, nicht in dieses Unternehmen zu investieren.

Es ist schon sehr seltsam, welche Kausalketten hier im Forum von einem bestimmten Teilnehmer veröffentlicht werden.
Wie krank muss man eigentlich dazu sein? Trittbrettfahrer sein und die Wahrheit 180Grad zu verdrehen indem man demjenigen mehrfach unterstellt Trittbrettfahrer zu sein auf dessen Trittbrett man fuhr. Dann das uralte aus dem Zusammenhang gerissene WO Posting in einem amerik. Board. Und mich hier mehrfach als Luegner bezeichnen und wegen eines wahren Postings hier den Mod holen und das Posting loeschen lassen um die die unangenehme Wahrheit unter den Teppich zu kehren. Alles um von den eigenen unsauberen Aktivitaeten abzulenken. Weit unter dem tiefsten Niveau. So, jetzt lauf wieder zum Mod, den ich hiermit bitte vor Loeschung dieses Postings alle unwahren Behauptungen von Cyberhexe gegenueber mir ebenfalls zu loeschen - sonst verbleibt ein extremer Geschmack. Und da gaebe es ne Menge zu loeschen.
PS: Es ist eine Unwahrheit zu behaupten es haette eine "Abmahnung" gegeben. Wie lange duerfen diese Unwahrheiten noch verbreitet werden???
Antwort auf Beitrag Nr.: 54.878.836 von Ville7 am 05.05.17 23:22:46
nur noch so viel....und dann gehts hier wirklich nur noch um RADIUS HEALTH:
1.) wie sollte man jemand nennen, der andere nachdem diese "all in one, all in Exelixis" gegangen sind, mehrfach dafür persönlich kritisiert hat (teilweise unter der Gürtellinie) und nun in RADIUS die ähnlichen Attacken "reitet"?
Ich hatte Trittbrettfahrer gewählt. Ob dieser Teilnehmer Jahre zuvor in einem anderen Forum bereits Beiträge zu diesem Unternehmen geschrieben hat, interessiert mich dabei herzlich wenig, weil ich Foren nicht nach dessen früheren Beiträgen durchforste.
Deswegen noch einmal ein Zitat:
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935) von Franca_ole am 11.11.15 um 09:00:03
die folgenden Sätze"
"Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken.
Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen"."
2.) Der Joke mit dem Beitrag im amerikanischen Forum (Investor Village) sollte den Namenwechsel unter Beweis stellen. In diesen amerikanischen Foren (IV, financeyahoo), in denen dieser Teilnehmer auch eine Zeit lang aufgetaucht bist, hat man übrigens über den "silly german investor" gewitzelt. Wer da wohl gemeint war? Glücklicherweise sind diese mitunter peinlichen Auftritte zumindest dort sehr selten geworden.
http://www.investorvillage.com/smbd.asp?mb=1086&mn=11632&pt=…
3.) Die allerbeste Blüte ist jedoch diese Behauptung:
"wegen eines wahren Postings hier den Mod holen und das Posting loeschen lassen um die die unangenehme Wahrheit unter den Teppich zu kehren."
Nach dessen Logik kehre ich eine Nachricht unter den Teppich, die ich zweimal zitiert habe. Nicht wegen der Nachricht selbst, sondern wegen des Zitates wurden auch diese beiden Nachrichten leider gelöscht. Jedoch werde ich zukünftig immer dann Meldung machen, wenn die Gürtellinie von diesem Teilnehmer wieder nach unten verlegt wird.
Dieser Vorwurf spiegelt jedoch sehr deutlich dessen Wahrnehmung wieder bzw. die Interpretation deren, die mitunter mehr als seltsam ist.
5.) Vielleicht schaffe ich es nun, auf Unsachlichkeit nicht mehr zu reagieren. Ansonsten, und dies ist mir durchaus bewusst, mache auch ich mich lächerlich.
Zitat von Ville7: Wie krank muss man eigentlich dazu sein? Trittbrettfahrer sein und die Wahrheit 180Grad zu verdrehen indem man demjenigen mehrfach unterstellt Trittbrettfahrer zu sein auf dessen Trittbrett man fuhr. Dann das uralte aus dem Zusammenhang gerissene WO Posting in einem amerik. Board. Und mich hier mehrfach als Luegner bezeichnen und wegen eines wahren Postings hier den Mod holen und das Posting loeschen lassen um die die unangenehme Wahrheit unter den Teppich zu kehren. Alles um von den eigenen unsauberen Aktivitaeten abzulenken. Weit unter dem tiefsten Niveau. So, jetzt lauf wieder zum Mod, den ich hiermit bitte vor Loeschung dieses Postings alle unwahren Behauptungen von Cyberhexe gegenueber mir ebenfalls zu loeschen - sonst verbleibt ein extremer Geschmack. Und da gaebe es ne Menge zu loeschen.
nur noch so viel....und dann gehts hier wirklich nur noch um RADIUS HEALTH:
1.) wie sollte man jemand nennen, der andere nachdem diese "all in one, all in Exelixis" gegangen sind, mehrfach dafür persönlich kritisiert hat (teilweise unter der Gürtellinie) und nun in RADIUS die ähnlichen Attacken "reitet"?
Ich hatte Trittbrettfahrer gewählt. Ob dieser Teilnehmer Jahre zuvor in einem anderen Forum bereits Beiträge zu diesem Unternehmen geschrieben hat, interessiert mich dabei herzlich wenig, weil ich Foren nicht nach dessen früheren Beiträgen durchforste.
Deswegen noch einmal ein Zitat:
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935) von Franca_ole am 11.11.15 um 09:00:03
die folgenden Sätze"
"Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken.
Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen"."
2.) Der Joke mit dem Beitrag im amerikanischen Forum (Investor Village) sollte den Namenwechsel unter Beweis stellen. In diesen amerikanischen Foren (IV, financeyahoo), in denen dieser Teilnehmer auch eine Zeit lang aufgetaucht bist, hat man übrigens über den "silly german investor" gewitzelt. Wer da wohl gemeint war? Glücklicherweise sind diese mitunter peinlichen Auftritte zumindest dort sehr selten geworden.
http://www.investorvillage.com/smbd.asp?mb=1086&mn=11632&pt=…
3.) Die allerbeste Blüte ist jedoch diese Behauptung:
"wegen eines wahren Postings hier den Mod holen und das Posting loeschen lassen um die die unangenehme Wahrheit unter den Teppich zu kehren."
Nach dessen Logik kehre ich eine Nachricht unter den Teppich, die ich zweimal zitiert habe. Nicht wegen der Nachricht selbst, sondern wegen des Zitates wurden auch diese beiden Nachrichten leider gelöscht. Jedoch werde ich zukünftig immer dann Meldung machen, wenn die Gürtellinie von diesem Teilnehmer wieder nach unten verlegt wird.
Dieser Vorwurf spiegelt jedoch sehr deutlich dessen Wahrnehmung wieder bzw. die Interpretation deren, die mitunter mehr als seltsam ist.
5.) Vielleicht schaffe ich es nun, auf Unsachlichkeit nicht mehr zu reagieren. Ansonsten, und dies ist mir durchaus bewusst, mache auch ich mich lächerlich.
Antwort auf Beitrag Nr.: 54.879.004 von Ville7 am 06.05.17 00:04:39
...da muss ich dich noch einmal (schon wieder) korrigieren:
ich hatte nicht behauptet sondern VERMUTET --> "... (ich würde jetzt mal vermuten, dass es deswegen für diesen Teilnehmer bereits eine Abmahnung gegeben hat, obschon ich dies nicht beweisen kann)."
Auf solche wichtigen Unterschiede sollte man achten!
Zitat von Ville7: PS: Es ist eine Unwahrheit zu behaupten es haette eine "Abmahnung" gegeben. Wie lange duerfen diese Unwahrheiten noch verbreitet werden???
...da muss ich dich noch einmal (schon wieder) korrigieren:
ich hatte nicht behauptet sondern VERMUTET --> "... (ich würde jetzt mal vermuten, dass es deswegen für diesen Teilnehmer bereits eine Abmahnung gegeben hat, obschon ich dies nicht beweisen kann)."
Auf solche wichtigen Unterschiede sollte man achten!
...und dann doch auch noch etwas "food for thought"...trotz "Partykopf"....Salsa_ole:
Romosozumab...
--> "The FDA has set a Prescription Drug User Fee Act (PDUFA) target action date of July 19, 2017."
... wird zukünftig im Wettbewerb um Osteoporose-Patienten ein wichtiger Konkurrent sein, der jedoch beim sekundären Endpunkt und zwar den nicht die Wirbelsäule betreffenden Frakturen (Schenkelhals-, Oberschenkel- und handgelenksnahe Unterarmbrüche mehr als 85%) den statistischen Nachweis der Wirksamkeit gegenüber Plazebo im Gegensatz zu Abaloparatide nicht erbracht hat.
Als ernste Nebenwirkungen kam es in der Romosozumab-Gruppe zu zwei Kiefernekrosen und einem atypischen Oberschenkelbruch. Diese ernsten Komplikation seien unerwartet und Anlass zur Besorgnis. Man müsse sorgfältig beobachten, ob und wie häufig diese bei breiterer Anwendung aufträten, hieß es in einem Editorial.
Demgegenüber steht, dies wurde richtigerweise festgestellt, die wesentlich günstigere Applikation (einmal im Monat eine 210 mg-Dosis).
Gerade deshalb ist es von grosser Bedeutung, die pflasterähnliche transdermale Applikation möglichst schnell zu etablieren. Diesbezüglich werden momentan die Hürden des CMC https://www.fda.gov/AnimalVeterinary/GuidanceComplianceEnfor… abgeräumt.
Romosozumab Treatment in Postmenopausal Women with Osteoporosis
Nonvertebral fractures constituted the majority (>85%) of clinical fractures. Nonvertebral fractures occurred in 56 patients (1.6%) in the romosozumab group and in 75 (2.1%) in the placebo group (hazard ratio, 0.75; 95% CI, 0.53 to 1.05; P=0.10) (Figure 2C, and Table S2 in the Supplementary Appendix). Owing to the lack of statistical significance for the nonvertebral end point and the prespecified testing sequence, all other 12-month fracture end-point analyses were considered to be exploratory (Table S2 in the Supplementary Appendix).
http://www.nejm.org/doi/full/10.1056/NEJMoa1607948#t=article" target="_blank" rel="nofollow ugc noopener">http://www.nejm.org/doi/full/10.1056/NEJMoa1607948#t=article
Romosozumab...
--> "The FDA has set a Prescription Drug User Fee Act (PDUFA) target action date of July 19, 2017."
... wird zukünftig im Wettbewerb um Osteoporose-Patienten ein wichtiger Konkurrent sein, der jedoch beim sekundären Endpunkt und zwar den nicht die Wirbelsäule betreffenden Frakturen (Schenkelhals-, Oberschenkel- und handgelenksnahe Unterarmbrüche mehr als 85%) den statistischen Nachweis der Wirksamkeit gegenüber Plazebo im Gegensatz zu Abaloparatide nicht erbracht hat.
Als ernste Nebenwirkungen kam es in der Romosozumab-Gruppe zu zwei Kiefernekrosen und einem atypischen Oberschenkelbruch. Diese ernsten Komplikation seien unerwartet und Anlass zur Besorgnis. Man müsse sorgfältig beobachten, ob und wie häufig diese bei breiterer Anwendung aufträten, hieß es in einem Editorial.
Demgegenüber steht, dies wurde richtigerweise festgestellt, die wesentlich günstigere Applikation (einmal im Monat eine 210 mg-Dosis).
Gerade deshalb ist es von grosser Bedeutung, die pflasterähnliche transdermale Applikation möglichst schnell zu etablieren. Diesbezüglich werden momentan die Hürden des CMC https://www.fda.gov/AnimalVeterinary/GuidanceComplianceEnfor… abgeräumt.
Romosozumab Treatment in Postmenopausal Women with Osteoporosis
Nonvertebral fractures constituted the majority (>85%) of clinical fractures. Nonvertebral fractures occurred in 56 patients (1.6%) in the romosozumab group and in 75 (2.1%) in the placebo group (hazard ratio, 0.75; 95% CI, 0.53 to 1.05; P=0.10) (Figure 2C, and Table S2 in the Supplementary Appendix). Owing to the lack of statistical significance for the nonvertebral end point and the prespecified testing sequence, all other 12-month fracture end-point analyses were considered to be exploratory (Table S2 in the Supplementary Appendix).
http://www.nejm.org/doi/full/10.1056/NEJMoa1607948#t=article" target="_blank" rel="nofollow ugc noopener">http://www.nejm.org/doi/full/10.1056/NEJMoa1607948#t=article
Antwort auf Beitrag Nr.: 54.879.259 von Cyberhexe am 06.05.17 04:34:38Das ist einfach nur ***** was du hier abziehst.
Fakt ist: du bist auf unser Trittbrett bei EXEL aufgesprungen und hast ab unserer Meinungsverschiedenheit ständig das Gegenteil diesen Fakts behauptet ("ich sei dein Trittbrettfahrer"). Und jetzt wo du diesen Fakt nicht mehr einfach durch massive, inhaltsleere Postings vertuschen kannst, weil die Fakten hier bei W/O in den Threads dokumentiert sind, versuchst du alles um mich runterzumachen (mit dem komplettem Instrumentenkasten wie u.a. Postings aus dem Kontext zu reißen, falsche Unterstellungen etc.).
Das ist oberster Sandkasten. Selbstdarstellung und Verdrehung auf höchstem Niveau. Und auch extrem oberpeinlich für dich. Die Krone ist dabei uralte Postings -vollkommen aus dem Kontext gerissen- in andere, fremdsprachige Foren zu tragen. Und ja: es ist extrem lächerlich, was du hier abziehst!
Fakt ist: du bist auf unser Trittbrett bei EXEL aufgesprungen und hast ab unserer Meinungsverschiedenheit ständig das Gegenteil diesen Fakts behauptet ("ich sei dein Trittbrettfahrer"). Und jetzt wo du diesen Fakt nicht mehr einfach durch massive, inhaltsleere Postings vertuschen kannst, weil die Fakten hier bei W/O in den Threads dokumentiert sind, versuchst du alles um mich runterzumachen (mit dem komplettem Instrumentenkasten wie u.a. Postings aus dem Kontext zu reißen, falsche Unterstellungen etc.).
Das ist oberster Sandkasten. Selbstdarstellung und Verdrehung auf höchstem Niveau. Und auch extrem oberpeinlich für dich. Die Krone ist dabei uralte Postings -vollkommen aus dem Kontext gerissen- in andere, fremdsprachige Foren zu tragen. Und ja: es ist extrem lächerlich, was du hier abziehst!
Antwort auf Beitrag Nr.: 54.879.277 von Cyberhexe am 06.05.17 05:15:50
Meine Rede. Probleme von Tymlos wiegen schwer: 1. täglich, 2.Spritze, 3.Kosten, 4.potentiell kanzerogen. Mit Wegfall von 2. könnten die Chancen erheblich verbessert werden. Potentieller Markt-Eintritt allerfrühestens 2019/2020. Die Firma schweigt sich zu einem genauen Zeitplan ja ziemlich aus....
Zitat von Cyberhexe: .Gerade deshalb ist es von grosser Bedeutung, die pflasterähnliche transdermale Applikation möglichst schnell zu etablieren.
Meine Rede. Probleme von Tymlos wiegen schwer: 1. täglich, 2.Spritze, 3.Kosten, 4.potentiell kanzerogen. Mit Wegfall von 2. könnten die Chancen erheblich verbessert werden. Potentieller Markt-Eintritt allerfrühestens 2019/2020. Die Firma schweigt sich zu einem genauen Zeitplan ja ziemlich aus....
also abgesehen von den streitereien (haha die können ab und zu auch recht unterhaltsam sein :P), einer der besten biotech subthreads, was einem hier an arbeit abgenommen wird durch die von cyberhexe minuziös zusammengesammelten berichte ist schon nicht ohne, leider kann ich mich nicht gut revanchieren, also nochmals danke und weiter so
Antwort auf Beitrag Nr.: 54.881.206 von paul81 am 06.05.17 16:22:51Du kannst dir die infos ale selbst zusammen sammeln. Dazu gibt es als Starthilfe Suchmaschinen...ich würde dir empfehlen genau das zu tun, denn das verhindert einen evtl vorhandenen bias des Postenden nicht erkennen zu können...
Da ich inzwischen einen extremen Würgereiz verspüre, wenn ich mich bei WO anmelde werde ich eine längere Postingpause einlegen. Ich brauch mir das hier nicht antun. Glückwunsch, Cyberhexe, du kannst dich nun freuen und weiter hier m.e. einseitige Meinungsbildung betreiben. Abgerechnet wird eben woanders...
Ich hoffe nur für alle User, v.a. die nicht so erfahrenen, dass sie es beherzigen stets ihre eigene sehr kritische due dilligence durchzuführen und nie ungefragt anderen hinterherrennen oder hinterhertraden. In diesem Sinne allen viel Erfolg und eine schöne Zeit.
Ich hoffe nur für alle User, v.a. die nicht so erfahrenen, dass sie es beherzigen stets ihre eigene sehr kritische due dilligence durchzuführen und nie ungefragt anderen hinterherrennen oder hinterhertraden. In diesem Sinne allen viel Erfolg und eine schöne Zeit.
Antwort auf Beitrag Nr.: 54.881.983 von Ville7 am 06.05.17 19:48:57hallo ville7, mit der eigenen due diligence hast du natürlich absolut recht, die nimmt mir niemand ab, halte radius z.b. auch schon deutlich länger als ich hier regelmässig mitlese, finde es einfach bequem wenn man hier die news an einem ort serviert bekommt, es sind ja dann auch immer die links angegeben, das ist wichtig... finde du bzw. ihr beiden macht das auch auf euren jeweiligen exel threads sehr gut, bin leider dort nicht mehr investiert (viel zu früh raus 
 )
)

 )
)
Antwort auf Beitrag Nr.: 54.879.784 von Ville7 am 06.05.17 09:19:15
Osteoporose ist eine Volkskrankheit ...
"Currently it is estimated that over 200 million people worldwide suffer from this disease1. Approximately 30% of all postmenopausal women have osteoporosis in the United States and in Europe. At least 40% of these women2 and 15-30% of men3 will sustain one or more fragility fractures in their remaining lifetime. Ageing of populations worldwide will be responsible for a major increase in the incidence of osteoporosis in postmenopausal women4."
https://www.iofbonehealth.org/epidemiology
...deren Behandlung bei unterschiedlichem Verlauf, Stärke, Vorgeschichte, Alter auch unterschiedliche Methoden vorsieht.
Die Vereinigung der Amerikanischen Klinischen Endokrinologen empfiehlt folgende Behandlungsansätze:
https://www.aace.com/files/final-algorithm.pdf
Standardtherapie bleibt die Therapie mit Biophosphonaten (zB Ibandronat, Risedronat etc.), die den Abbau der Osteoklasten hemmen.
Eine weitere Behandlungsmöglichkeit stellt eine hormonelle Behandlung mit Parathormon (Teriparatide und neuerdings eben auch Abaloparatide) dar, wodurch ein erhöhter Calcium-Spiegel im Blutplasma realisiert wird. Darüber hinaus kommen auch monoklonale Antikörper (Denosusmab oder demnächst sehr wahrscheinlich Romosozumab) zum Einsatz, die vor allem bei der Applikationshäufigkeit von Vorteil sind.
In den Behandlungsempfehlungen der Endokrinologen wird jedoch auch zukünftig nicht nur ein Wirkstoff bzw. Wirkstoffklasse vertreten sein, da die Vielfalt der Parameter eine entsprechende Vielfalt bei der Behandlung erfordert.
Für Abaloparatide hat diese Ausgangslage zur Folge, dass es für den wirtschaftlichen Erfolg 2 Ebenen gibt:
1.) die direkte Konkurrenz innerhalb der Klasse, also gegenüber Teriparatide (TN: FORTEO --> 28.04.2017 - Eli Lilly's sales of Forteo increased ~9% to $347.5 million in 1Q17, compared to $318.6 million in 1Q16.)
2.) die hormonelle gegenüber den anderen Behandlungsmöglichkeiten
Die Aussage des Teilnehmers ville7 "Probleme von Tymlos wiegen schwer: 1. täglich, 2.Spritze, 3.Kosten, 4.potentiell kanzerogen." sind sehr undifferenziert, da die Relation nicht gegeben ist.
Vergleicht man innerhalb der Klasse (Parathormone), dann ist festzustellen, dass Punkt 1,2 und 4 fast identisch sind und bei den Kosten Abaloparatide im Vorteil ist. Darüber hinaus hat Abaloparatide (fave to face) gegenüber Teriparatide Vorteile bei der Wirkung (bei nicht die Wirbelsäule betreffenden Frakturen, sowie bei der Knochendichte) und bisher auch bei den Nebenwirkungen (--> da muss man natürlich auch Langzeitanwendung abwarten; neue Signale sind immer möglich!).
Zu Punkt 4.potentiell kanzerogen. wäre zu sagen:
Im Label der FDA ...
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
...steht unter 13.1 Carcinogenisis, Mutagenisis, Impairment of Fertility,
dass in einer 2-jährigen Karzinogenitätsstudie an Ratten bei 4, 16 und 28-facher Dosis (80 mcg) ähnlich wie bei teriparatide dosisabhängig eine stark erhöhtes Auftreten von bösartigen Osteosarcomas (Knochentumor) beobachtet wurde (87%, 62%und gegenüber 0-2% unbehandelt).
Es wird jedoch ausdrücklich darauf hingewiesen, dass die Relevanz dieser Rattenbefunde für den Mensch ungewiss ist, weshalb.... TYMLOS is not recommended in patients at increased risk of osteosarcoma (FDA).
Es wird ebenfalls im gleichen Abschnitt darauf hingewiesen, dass Abaloparatide in den Standardtests zur Mutagenität (Ames, Chromosoemenaberration und Micronucleus) negativ ist.
Die Black Box- Warnung bei Forteo íst fast identisch (dosisabhängige Inzidenzerhöhung von Osteosarcoma bei einer 3 bis 60 fachen Dosis).
Der Vorwurf...
ville schrieb "Die Firma schweigt sich zu einem genauen Zeitplan ja ziemlich aus..."
...dass Radius keinen genauen Zeitplan herausgegeben hat, steht im Widerspruch zu dem auch schon gemachten Vorwurf, die Firma würde den Mund arg vollnehmen und überversprechen und wenig zu liefern.
In der Pressekonferenz wurde gesagt, dass man derezit damit beschäftigt ist, die "Hürden" des CMC (Produktion, Stabilität, Qualität, Verpackung etc.) anzugehen, die vor der Initialisieung der Bioäquivalenzstudie "übersprungen" sein müssen:
aus dem letzten Quartalsbericht:
"The results of this clinical evaluation will inform the design of a pivotal bioequivalence study that will be initiated following completion of activities related to manufacturing scale-up, production, and other activities required for the initiation of that study."
Zitat von Ville7: Meine Rede. Probleme von Tymlos wiegen schwer: 1. täglich, 2.Spritze, 3.Kosten, 4.potentiell kanzerogen. Mit Wegfall von 2. könnten die Chancen erheblich verbessert werden. Potentieller Markt-Eintritt allerfrühestens 2019/2020. Die Firma schweigt sich zu einem genauen Zeitplan ja ziemlich aus....
Osteoporose ist eine Volkskrankheit ...
"Currently it is estimated that over 200 million people worldwide suffer from this disease1. Approximately 30% of all postmenopausal women have osteoporosis in the United States and in Europe. At least 40% of these women2 and 15-30% of men3 will sustain one or more fragility fractures in their remaining lifetime. Ageing of populations worldwide will be responsible for a major increase in the incidence of osteoporosis in postmenopausal women4."
https://www.iofbonehealth.org/epidemiology
...deren Behandlung bei unterschiedlichem Verlauf, Stärke, Vorgeschichte, Alter auch unterschiedliche Methoden vorsieht.
Die Vereinigung der Amerikanischen Klinischen Endokrinologen empfiehlt folgende Behandlungsansätze:
https://www.aace.com/files/final-algorithm.pdf
Standardtherapie bleibt die Therapie mit Biophosphonaten (zB Ibandronat, Risedronat etc.), die den Abbau der Osteoklasten hemmen.
Eine weitere Behandlungsmöglichkeit stellt eine hormonelle Behandlung mit Parathormon (Teriparatide und neuerdings eben auch Abaloparatide) dar, wodurch ein erhöhter Calcium-Spiegel im Blutplasma realisiert wird. Darüber hinaus kommen auch monoklonale Antikörper (Denosusmab oder demnächst sehr wahrscheinlich Romosozumab) zum Einsatz, die vor allem bei der Applikationshäufigkeit von Vorteil sind.
In den Behandlungsempfehlungen der Endokrinologen wird jedoch auch zukünftig nicht nur ein Wirkstoff bzw. Wirkstoffklasse vertreten sein, da die Vielfalt der Parameter eine entsprechende Vielfalt bei der Behandlung erfordert.
Für Abaloparatide hat diese Ausgangslage zur Folge, dass es für den wirtschaftlichen Erfolg 2 Ebenen gibt:
1.) die direkte Konkurrenz innerhalb der Klasse, also gegenüber Teriparatide (TN: FORTEO --> 28.04.2017 - Eli Lilly's sales of Forteo increased ~9% to $347.5 million in 1Q17, compared to $318.6 million in 1Q16.)
2.) die hormonelle gegenüber den anderen Behandlungsmöglichkeiten
Die Aussage des Teilnehmers ville7 "Probleme von Tymlos wiegen schwer: 1. täglich, 2.Spritze, 3.Kosten, 4.potentiell kanzerogen." sind sehr undifferenziert, da die Relation nicht gegeben ist.
Vergleicht man innerhalb der Klasse (Parathormone), dann ist festzustellen, dass Punkt 1,2 und 4 fast identisch sind und bei den Kosten Abaloparatide im Vorteil ist. Darüber hinaus hat Abaloparatide (fave to face) gegenüber Teriparatide Vorteile bei der Wirkung (bei nicht die Wirbelsäule betreffenden Frakturen, sowie bei der Knochendichte) und bisher auch bei den Nebenwirkungen (--> da muss man natürlich auch Langzeitanwendung abwarten; neue Signale sind immer möglich!).
Zu Punkt 4.potentiell kanzerogen. wäre zu sagen:
Im Label der FDA ...
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
...steht unter 13.1 Carcinogenisis, Mutagenisis, Impairment of Fertility,
dass in einer 2-jährigen Karzinogenitätsstudie an Ratten bei 4, 16 und 28-facher Dosis (80 mcg) ähnlich wie bei teriparatide dosisabhängig eine stark erhöhtes Auftreten von bösartigen Osteosarcomas (Knochentumor) beobachtet wurde (87%, 62%und gegenüber 0-2% unbehandelt).
Es wird jedoch ausdrücklich darauf hingewiesen, dass die Relevanz dieser Rattenbefunde für den Mensch ungewiss ist, weshalb.... TYMLOS is not recommended in patients at increased risk of osteosarcoma (FDA).
Es wird ebenfalls im gleichen Abschnitt darauf hingewiesen, dass Abaloparatide in den Standardtests zur Mutagenität (Ames, Chromosoemenaberration und Micronucleus) negativ ist.
Die Black Box- Warnung bei Forteo íst fast identisch (dosisabhängige Inzidenzerhöhung von Osteosarcoma bei einer 3 bis 60 fachen Dosis).
Der Vorwurf...
ville schrieb "Die Firma schweigt sich zu einem genauen Zeitplan ja ziemlich aus..."
...dass Radius keinen genauen Zeitplan herausgegeben hat, steht im Widerspruch zu dem auch schon gemachten Vorwurf, die Firma würde den Mund arg vollnehmen und überversprechen und wenig zu liefern.
In der Pressekonferenz wurde gesagt, dass man derezit damit beschäftigt ist, die "Hürden" des CMC (Produktion, Stabilität, Qualität, Verpackung etc.) anzugehen, die vor der Initialisieung der Bioäquivalenzstudie "übersprungen" sein müssen:
aus dem letzten Quartalsbericht:
"The results of this clinical evaluation will inform the design of a pivotal bioequivalence study that will be initiated following completion of activities related to manufacturing scale-up, production, and other activities required for the initiation of that study."
Antwort auf Beitrag Nr.: 54.883.531 von Cyberhexe am 07.05.17 09:08:25Die Präsenz von Abaloparatide in den wissenschaftlichen Journals bzw. in den Publikationen der Meinungsführer wie zB der Non-Profit-Organisation "Mayo Clinic" ist zunehmend:
Mayo Clinic
Eighteen Months of Treatment With Subcutaneous Abaloparatide Followed by
6 Months of Treatment With Alendronate in Postmenopausal Women With Osteoporosis:
Results of the ACTIVExtend Trial
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
CONCLUSION
The sequence of ABL-SC followed by 6 months of ALN improved BMD and reduced
fracture risk throughout the skeleton and is likely to be a highly effective treatment option
for postmenopausal women at risk for osteoporosis-related fractures.
The effect of abaloparatide-SC on fracture risk is independent of baseline FRAX fracture probability: A post hoc analysis of the ACTIVE study†
Authors
EV McCloskey, H Johansson, A Oden, NC Harvey, H . Jiang, S Modin, L. Fitzpatrick, J. A . Kanis
Accepted manuscript online: 5 May 2017
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.3163/full
Mayo Clinic
Eighteen Months of Treatment With Subcutaneous Abaloparatide Followed by
6 Months of Treatment With Alendronate in Postmenopausal Women With Osteoporosis:
Results of the ACTIVExtend Trial
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
CONCLUSION
The sequence of ABL-SC followed by 6 months of ALN improved BMD and reduced
fracture risk throughout the skeleton and is likely to be a highly effective treatment option
for postmenopausal women at risk for osteoporosis-related fractures.
The effect of abaloparatide-SC on fracture risk is independent of baseline FRAX fracture probability: A post hoc analysis of the ACTIVE study†
Authors
EV McCloskey, H Johansson, A Oden, NC Harvey, H . Jiang, S Modin, L. Fitzpatrick, J. A . Kanis
Accepted manuscript online: 5 May 2017
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.3163/full
Antwort auf Beitrag Nr.: 54.894.914 von Cyberhexe am 08.05.17 21:38:34Der grosse Vorteil von Abaloparatide gegenüber Romosozumab ist der statistsch signifikante Nachweis einer Verbesserung bei den nicht die Wirbelsäule betreffenden Frakturen (Oberschenkelhals, Hüfte, Arme etc), welche über 85% aller Frakturen ausmachen:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5402913/
Drug Des Devel Ther. 2017; 11: 1221–1231.
Published online 2017 Apr 13. doi: 10.2147/DDDT.S127568
PMCID: PMC5402913
Profile of romosozumab and its potential in the management of osteoporosis
At the end of 12 months of romosozumab treatment, in the study by Cosman et al, vertebral fractures were reduced by 73% (the incidence of vertebral fracture in the romosozumab group was 0.5% as compared to 1.8% in the placebo group). The romosozumab treatment group also had a 63% reduction in clinical fractures (composite of nonvertebral fracture and symptomatic vertebral fracture) as compared to the placebo group. At 24 months, the incidence of vertebral fractures was reduced by 75% in patients who received romosozumab in the first year and denosumab in the second year (vertebral fracture incidence 0.6%) as compared to the group who received placebo in the first year and denosumab in the second year (vertebral fracture incidence 2.5%). There was no significant difference in nonvertebral fracture incidence at 12 and 24 months between the two groups.27 One possible explanation for the lower than expected nonvertebral fracture incidence in the placebo group was attributed to low nonvertebral fracture incidence in patients enrolled from the Latin America region (Colombia, Brazil, Argentina, Dominican Republic, and Mexico). Patients from the Latin America region consisted of 42.7% of patients enrolled in the study.
Der grosse Vorteil von Romosozumab ist die pro Monat einmalige subkutane Applikation. Bei Abaloparatide hingegen ist pro Tag eine subkutane Anwendung in die Bauchdecke erforderlich. Hierbei handelt es sich um eine Injektion mit einem sogen. "Pen" wie bei der Insulingabe.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5402913/
Drug Des Devel Ther. 2017; 11: 1221–1231.
Published online 2017 Apr 13. doi: 10.2147/DDDT.S127568
PMCID: PMC5402913
Profile of romosozumab and its potential in the management of osteoporosis
At the end of 12 months of romosozumab treatment, in the study by Cosman et al, vertebral fractures were reduced by 73% (the incidence of vertebral fracture in the romosozumab group was 0.5% as compared to 1.8% in the placebo group). The romosozumab treatment group also had a 63% reduction in clinical fractures (composite of nonvertebral fracture and symptomatic vertebral fracture) as compared to the placebo group. At 24 months, the incidence of vertebral fractures was reduced by 75% in patients who received romosozumab in the first year and denosumab in the second year (vertebral fracture incidence 0.6%) as compared to the group who received placebo in the first year and denosumab in the second year (vertebral fracture incidence 2.5%). There was no significant difference in nonvertebral fracture incidence at 12 and 24 months between the two groups.27 One possible explanation for the lower than expected nonvertebral fracture incidence in the placebo group was attributed to low nonvertebral fracture incidence in patients enrolled from the Latin America region (Colombia, Brazil, Argentina, Dominican Republic, and Mexico). Patients from the Latin America region consisted of 42.7% of patients enrolled in the study.
Der grosse Vorteil von Romosozumab ist die pro Monat einmalige subkutane Applikation. Bei Abaloparatide hingegen ist pro Tag eine subkutane Anwendung in die Bauchdecke erforderlich. Hierbei handelt es sich um eine Injektion mit einem sogen. "Pen" wie bei der Insulingabe.
Antwort auf Beitrag Nr.: 54.895.169 von Cyberhexe am 08.05.17 22:06:15
Bin gespannt, ob Romosozumab zum 19.7.2017 von der FDA zugelassen wird oder ob es, ähnlich wie bei Abaloparatide, eine Verzögerung gibt. Dass Romosozumab zugelassen wird, steht wohl nicht zur Diskussion und dürfte, obschon ernste Nebenwirkungen beobachtet wurden, ziemlich sicher sein:
"Als ernste Nebenwirkungen kam es in der Romosozumab-Gruppe zu zwei Kiefernekrosen und einem atypischen Oberschenkelbruch. Diese ernsten Komplikation seien unerwartet und Anlass zur Besorgnis."
Quelle: https://www.gesundheitsstadt-berlin.de/osteoporose-weniger-w…
"The FDA has set a Prescription Drug User Fee Act (PDUFA) target action date of July 19, 2017, for romosozumab."
http://wwwext.amgen.com/media/news-releases/2016/09/amgen-an…
Zitat von Cyberhexe: Der grosse Vorteil von Abaloparatide gegenüber Romosozumab ist der statistsch signifikante Nachweis einer Verbesserung bei den nicht die Wirbelsäule betreffenden Frakturen (Oberschenkelhals, Hüfte, Arme etc), welche über 85% aller Frakturen ausmachen.
Der grosse Vorteil von Romosozumab ist die pro Monat einmalige subkutane Applikation. Bei Abaloparatide hingegen ist pro Tag eine subkutane Anwendung in die Bauchdecke erforderlich. Hierbei handelt es sich um eine Injektion mit einem sogen. "Pen" wie bei der Insulingabe.
Bin gespannt, ob Romosozumab zum 19.7.2017 von der FDA zugelassen wird oder ob es, ähnlich wie bei Abaloparatide, eine Verzögerung gibt. Dass Romosozumab zugelassen wird, steht wohl nicht zur Diskussion und dürfte, obschon ernste Nebenwirkungen beobachtet wurden, ziemlich sicher sein:
"Als ernste Nebenwirkungen kam es in der Romosozumab-Gruppe zu zwei Kiefernekrosen und einem atypischen Oberschenkelbruch. Diese ernsten Komplikation seien unerwartet und Anlass zur Besorgnis."
Quelle: https://www.gesundheitsstadt-berlin.de/osteoporose-weniger-w…
"The FDA has set a Prescription Drug User Fee Act (PDUFA) target action date of July 19, 2017, for romosozumab."
http://wwwext.amgen.com/media/news-releases/2016/09/amgen-an…
Antwort auf Beitrag Nr.: 54.897.254 von Cyberhexe am 09.05.17 09:05:58Die Entscheidung, ob Abaloparatide vom europ. Arzneimittelausschuss CHMP zur Zulassung empfohlen wird, wird gemäss Radius auf der JULI-Sitzung in 2017 erwartet:
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
Antwort auf Beitrag Nr.: 54.897.311 von Cyberhexe am 09.05.17 09:10:56Anbei eine weitere Pflichtmitteilung von BB Biotech über Aktienkauf bei Radius Health, und zwar
am 5.5.2017 20´600 zu $35.5477
am 8.5.2017 22´800 zu $35.5978
Insgesamt verfügen die Schweizer nun über 4.8 Mio Aktien (4,808,799). Bei einer Gesamtzahl vom 43,185,952 Aktien (Basic and diluted) entspricht dies 11.14% des Unternehmens.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
am 5.5.2017 20´600 zu $35.5477
am 8.5.2017 22´800 zu $35.5978
Insgesamt verfügen die Schweizer nun über 4.8 Mio Aktien (4,808,799). Bei einer Gesamtzahl vom 43,185,952 Aktien (Basic and diluted) entspricht dies 11.14% des Unternehmens.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
Antwort auf Beitrag Nr.: 54.905.564 von Cyberhexe am 09.05.17 23:23:52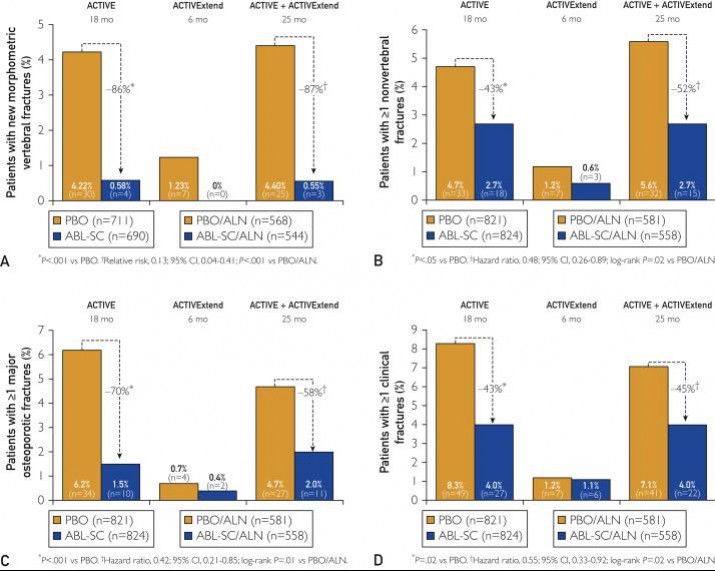
übersicht zu ph3 ACTIVE nach 18 Monaten Behandlung mit Abaloparatide sowie deren Erweiterung (6 Monate) mit Alendronate --> ACTIVExtend bei Frauen in der Menopause mit Osteoporose

übersicht zu ph3 ACTIVE nach 18 Monaten Behandlung mit Abaloparatide sowie deren Erweiterung (6 Monate) mit Alendronate --> ACTIVExtend bei Frauen in der Menopause mit Osteoporose
Antwort auf Beitrag Nr.: 54.914.147 von Cyberhexe am 10.05.17 21:21:35die Grafik ist aus einer Publikation der Mayo Clinic, einer der renommiertesten Kliniken in den USA
https://de.wikipedia.org/wiki/Mayo_Clinic
February 2017 Volume 92, Issue 2, Pages 200–210
Eighteen Months of Treatment With Subcutaneous Abaloparatide Followed by 6 Months of Treatment With Alendronate in Postmenopausal Women With Osteoporosis
Results of the ACTIVExtend Trial
in dieser sind die Ergebnisse von ACTIVE sowie ACTIVExtend sehr gut dargestellt:
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
Conclusion
The sequence of ABL-SC followed by 6 months of ALN improved BMD and reduced fracture risk throughout the skeleton and is likely to be a highly effective treatment option for postmenopausal women at risk for osteoporosis-related fractures.
https://de.wikipedia.org/wiki/Mayo_Clinic
February 2017 Volume 92, Issue 2, Pages 200–210
Eighteen Months of Treatment With Subcutaneous Abaloparatide Followed by 6 Months of Treatment With Alendronate in Postmenopausal Women With Osteoporosis
Results of the ACTIVExtend Trial
in dieser sind die Ergebnisse von ACTIVE sowie ACTIVExtend sehr gut dargestellt:
http://www.mayoclinicproceedings.org/article/S0025-6196(16)3…
Conclusion
The sequence of ABL-SC followed by 6 months of ALN improved BMD and reduced fracture risk throughout the skeleton and is likely to be a highly effective treatment option for postmenopausal women at risk for osteoporosis-related fractures.
Antwort auf Beitrag Nr.: 54.914.279 von Cyberhexe am 10.05.17 21:39:11http://ir.radiuspharm.com/secfiling.cfm?filingID=1628280-17-…
aus der Pflichtmitteilung 10-Q vom 2.5.2017:
We expect to report the top-line results from our recently completed 24-month ACTIVExtend trial in the second quarter of 2017. The combined 25-month fracture data from our Phase 3 clinical trial program for TYMLOS formed the basis of our regulatory submissions in the United States and Europe. In November 2015, we submitted an MAA for abaloparatide-SC to the European Medicines Agency, or EMA, which was validated and is currently undergoing active regulatory assessment by the Committee for Medicinal Products for Human Use of the EMA, or CHMP. We anticipate that the CHMP may adopt an opinion regarding the MAA in July 2017. We intend to enter into one or more collaborations for the potential commercialization of abaloparatide-SC outside of the United States prior to commercial launch in the European Union.
Folgende Informationen/Entscheidungen sollen bis Ende Juli 2017 öffentlich werden:
- bis Ende Juni Information über die Daten der 24-monatigen Erweiterungsstudie ACTIVExtend
- Bekanntgabe der Zulassungsempfehlung (oder eben Nichtempfehlung) des europäischen Arzneimittelausschusses CHMP auf dessen Sitzung im JULI 2017 --> Bekanntgabe spätestens Freitag, 21.7.2017
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
- gleichzeitige Bekanntgabe über die anstehenden Kooperationen für die Vermarktung Abaloparatides ausserhalb der US
aus der Pflichtmitteilung 10-Q vom 2.5.2017:
We expect to report the top-line results from our recently completed 24-month ACTIVExtend trial in the second quarter of 2017. The combined 25-month fracture data from our Phase 3 clinical trial program for TYMLOS formed the basis of our regulatory submissions in the United States and Europe. In November 2015, we submitted an MAA for abaloparatide-SC to the European Medicines Agency, or EMA, which was validated and is currently undergoing active regulatory assessment by the Committee for Medicinal Products for Human Use of the EMA, or CHMP. We anticipate that the CHMP may adopt an opinion regarding the MAA in July 2017. We intend to enter into one or more collaborations for the potential commercialization of abaloparatide-SC outside of the United States prior to commercial launch in the European Union.
Folgende Informationen/Entscheidungen sollen bis Ende Juli 2017 öffentlich werden:
- bis Ende Juni Information über die Daten der 24-monatigen Erweiterungsstudie ACTIVExtend
- Bekanntgabe der Zulassungsempfehlung (oder eben Nichtempfehlung) des europäischen Arzneimittelausschusses CHMP auf dessen Sitzung im JULI 2017 --> Bekanntgabe spätestens Freitag, 21.7.2017
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
- gleichzeitige Bekanntgabe über die anstehenden Kooperationen für die Vermarktung Abaloparatides ausserhalb der US
Antwort auf Beitrag Nr.: 54.915.671 von Cyberhexe am 11.05.17 06:09:57zu den Nebenwirkungen von Abaloparatide:
http://www.rxlist.com/tymlos-side-effects-drug-center.htm
http://www.rxlist.com/tymlos-side-effects-drug-center.htm
Antwort auf Beitrag Nr.: 54.905.564 von Cyberhexe am 09.05.17 23:23:52
....und schon wieder eine Pflichtmitteilung:
http://ir.radiuspharm.com/secfiling.cfm?filingID=80255-17-13…
T. ROWE PRICE ASSOCIATES, INC. meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens
Die institutionellen Anleger scheinen an den Erfolg von Radius Health zu glauben!
Zitat von Cyberhexe: Anbei eine weitere Pflichtmitteilung von BB Biotech über Aktienkauf bei Radius Health, und zwar
am 5.5.2017 20´600 zu $35.5477
am 8.5.2017 22´800 zu $35.5978
Insgesamt verfügen die Schweizer nun über 4.8 Mio Aktien (4,808,799). Bei einer Gesamtzahl vom 43,185,952 Aktien (Basic and diluted) entspricht dies 11.14% des Unternehmens.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
....und schon wieder eine Pflichtmitteilung:
http://ir.radiuspharm.com/secfiling.cfm?filingID=80255-17-13…
T. ROWE PRICE ASSOCIATES, INC. meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens
Die institutionellen Anleger scheinen an den Erfolg von Radius Health zu glauben!
Danke Cyberhexe für die vielen interessanten Infos!
@all, wo kann ich schauen, wieviele shorts hier hat? Alle instituionellen Kaufen, aber die Aktie ist die letzten Tag immer im Minus. Geht irgendwie nicht auf?!
@all, wo kann ich schauen, wieviele shorts hier hat? Alle instituionellen Kaufen, aber die Aktie ist die letzten Tag immer im Minus. Geht irgendwie nicht auf?!
Antwort auf Beitrag Nr.: 54.923.999 von 2brix am 11.05.17 20:33:23
Anzahl Leerverkäufe - erscheint 14-tägig (aktuell 28.4.17):
http://www.nasdaq.com/symbol/rdus/short-interest
INSTITUTIONAL HOLDING (Werte immer zum Quartalsende, deswegen nicht ganz aktuell):
http://www.nasdaq.com/symbol/rdus/institutional-holdings
T. ROWE PRICE ASSOCIATES, INC. zB hat gestern in einer Pflichtmitteilung den Besitz von 5.184 Mio Aktien gemeldet, sind in dieser Liste nur mit 3.079 Mio Aktien zum 31.12.2016 aufgeführt.
Zitat von 2brix: Danke Cyberhexe für die vielen interessanten Infos!
@all, wo kann ich schauen, wieviele shorts hier hat? Alle instituionellen Kaufen, aber die Aktie ist die letzten Tag immer im Minus. Geht irgendwie nicht auf?!
Anzahl Leerverkäufe - erscheint 14-tägig (aktuell 28.4.17):
http://www.nasdaq.com/symbol/rdus/short-interest
INSTITUTIONAL HOLDING (Werte immer zum Quartalsende, deswegen nicht ganz aktuell):
http://www.nasdaq.com/symbol/rdus/institutional-holdings
T. ROWE PRICE ASSOCIATES, INC. zB hat gestern in einer Pflichtmitteilung den Besitz von 5.184 Mio Aktien gemeldet, sind in dieser Liste nur mit 3.079 Mio Aktien zum 31.12.2016 aufgeführt.
Antwort auf Beitrag Nr.: 54.905.564 von Cyberhexe am 09.05.17 23:23:52
und noch eine Pflichtmitteilung von BB Biotech über den Kauf von 50´000 Aktien zu $35.9296 vom 9.5.17 --> insgesamt verfügen die Schweizer nun über 4,858,799 Aktien.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
Zitat von Cyberhexe: Anbei eine weitere Pflichtmitteilung von BB Biotech über Aktienkauf bei Radius Health, und zwar
am 5.5.2017 20´600 zu $35.5477
am 8.5.2017 22´800 zu $35.5978
Insgesamt verfügen die Schweizer nun über 4.8 Mio Aktien (4,808,799). Bei einer Gesamtzahl vom 43,185,952 Aktien (Basic and diluted) entspricht dies 11.14% des Unternehmens.
und noch eine Pflichtmitteilung von BB Biotech über den Kauf von 50´000 Aktien zu $35.9296 vom 9.5.17 --> insgesamt verfügen die Schweizer nun über 4,858,799 Aktien.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
vielen Dank cyberhexe!
Antwort auf Beitrag Nr.: 54.944.162 von 2brix am 15.05.17 10:26:46Curr Osteoporos Rep. 2017 Mar 16. doi: 10.1007/s11914-017-0353-4.
Parathyroid Hormone and Parathyroid Hormone-Related Protein Analogs in Osteoporosis Therapy.
Leder BZ1.
Author information
Abstract
PURPOSE OF REVIEW:
The purpose is to review the efficacy and optimal use of parathyroid hormone and parathyroid hormone-related protein analogs in osteoporosis treatment.
RECENT FINDINGS:
The parathyroid hormone analog teriparatide, a potent stimulator of bone remodeling, increases hip and spine bone mineral density and reduces the risk of vertebral and non-vertebral fractures in postmenopausal osteoporotic women. The parathyroid hormone-related protein analog, abaloparatide, also reduces fracture incidence but has pharmacological effects that differ from teriparatide, particularly in cortical bone. These analogs provide maximal benefit when their use is followed by a potent antiresorptive medication. Moreover, studies have shown that the combination of teriparatide and the RANK-ligand inhibitor, denosumab, increase bone density and estimated strength more than monotherapy and more than any currently available regimen. Parathyroid hormone and parathyroid hormone-related protein analogs, whether as monotherapy, in combination with antiresorptive agents or in sequence with antiresorptive agents, will likely play an expanding role in osteoporosis management.
Parathyroid Hormone and Parathyroid Hormone-Related Protein Analogs in Osteoporosis Therapy.
Leder BZ1.
Author information
Abstract
PURPOSE OF REVIEW:
The purpose is to review the efficacy and optimal use of parathyroid hormone and parathyroid hormone-related protein analogs in osteoporosis treatment.
RECENT FINDINGS:
The parathyroid hormone analog teriparatide, a potent stimulator of bone remodeling, increases hip and spine bone mineral density and reduces the risk of vertebral and non-vertebral fractures in postmenopausal osteoporotic women. The parathyroid hormone-related protein analog, abaloparatide, also reduces fracture incidence but has pharmacological effects that differ from teriparatide, particularly in cortical bone. These analogs provide maximal benefit when their use is followed by a potent antiresorptive medication. Moreover, studies have shown that the combination of teriparatide and the RANK-ligand inhibitor, denosumab, increase bone density and estimated strength more than monotherapy and more than any currently available regimen. Parathyroid hormone and parathyroid hormone-related protein analogs, whether as monotherapy, in combination with antiresorptive agents or in sequence with antiresorptive agents, will likely play an expanding role in osteoporosis management.
Antwort auf Beitrag Nr.: 54.945.209 von Cyberhexe am 15.05.17 12:13:44food for thought:
The effect of abaloparatide-SC on fracture risk is independent of baseline FRAX fracture probability: A post hoc analysis of the ACTIVE study†
Authors
EV McCloskey,
H Johansson,
A Oden,
NC Harvey,
H . Jiang,
S Modin,
L. Fitzpatrick,
J. A . Kanis
Accepted manuscript online: 5 May 2017
Abstract
Daily subcutaneous (SC) injections of the investigational drug abaloparatide-SC (80mcg) for 18 months significantly decrease the risk of vertebral and non-vertebral fracture compared with placebo in postmenopausal women. We examined the efficacy of abaloparatide-SC as a function of baseline fracture risk, assessed using the FRAX tool.
Baseline clinical risk factors (age, BMI, prior fracture, glucocorticoid use, rheumatoid arthritis, and smoking) were entered into country-specific FRAX models to calculate the 10-year probability of major osteoporotic fractures, with or without femoral neck BMD. The interaction between probability of a major osteoporotic fracture and treatment efficacy was examined by a Poisson regression.
821 women randomized to placebo and 824 women to abaloparatide-SC, mean age 69 years in both groups, were followed for up to 2 years. At baseline, the 10-year probability of major osteoporotic fractures (with BMD) ranged from 2.3-57.5% (mean 13.2%). Treatment with abaloparatide-SC was associated with a 69% (95%CI: 38, 85%) decrease in major osteoporotic fracture (MOF) and a 43% (95%CI: 9, 64%) decrease in any clinical fracture compared to placebo. For all outcomes, hazard ratios tended to decrease (i.e., greater efficacy) with increasing fracture probability. Whereas the interaction approached significance for the outcome of any fracture (p = 0.11), there was no statistically significant interaction for any of the fracture outcomes. Similar results were noted when FRAX probability was computed without BMD.
Efficacy of abaloparatide-SC to decrease the risk of major osteoporotic fracture or any clinical fracture in postmenopausal women with low BMD and/or prior fracture appears independent of baseline fracture probability. This article is protected by copyright. All rights reserved
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.3163/abstrac…
The effect of abaloparatide-SC on fracture risk is independent of baseline FRAX fracture probability: A post hoc analysis of the ACTIVE study†
Authors
EV McCloskey,
H Johansson,
A Oden,
NC Harvey,
H . Jiang,
S Modin,
L. Fitzpatrick,
J. A . Kanis
Accepted manuscript online: 5 May 2017
Abstract
Daily subcutaneous (SC) injections of the investigational drug abaloparatide-SC (80mcg) for 18 months significantly decrease the risk of vertebral and non-vertebral fracture compared with placebo in postmenopausal women. We examined the efficacy of abaloparatide-SC as a function of baseline fracture risk, assessed using the FRAX tool.
Baseline clinical risk factors (age, BMI, prior fracture, glucocorticoid use, rheumatoid arthritis, and smoking) were entered into country-specific FRAX models to calculate the 10-year probability of major osteoporotic fractures, with or without femoral neck BMD. The interaction between probability of a major osteoporotic fracture and treatment efficacy was examined by a Poisson regression.
821 women randomized to placebo and 824 women to abaloparatide-SC, mean age 69 years in both groups, were followed for up to 2 years. At baseline, the 10-year probability of major osteoporotic fractures (with BMD) ranged from 2.3-57.5% (mean 13.2%). Treatment with abaloparatide-SC was associated with a 69% (95%CI: 38, 85%) decrease in major osteoporotic fracture (MOF) and a 43% (95%CI: 9, 64%) decrease in any clinical fracture compared to placebo. For all outcomes, hazard ratios tended to decrease (i.e., greater efficacy) with increasing fracture probability. Whereas the interaction approached significance for the outcome of any fracture (p = 0.11), there was no statistically significant interaction for any of the fracture outcomes. Similar results were noted when FRAX probability was computed without BMD.
Efficacy of abaloparatide-SC to decrease the risk of major osteoporotic fracture or any clinical fracture in postmenopausal women with low BMD and/or prior fracture appears independent of baseline fracture probability. This article is protected by copyright. All rights reserved
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.3163/abstrac…
Antwort auf Beitrag Nr.: 54.930.248 von Cyberhexe am 12.05.17 14:48:15
Momentaufnahme, allerdings zeitversetzt, derzeit:
Institutional Ownership 106.79%
Total Shares Outstanding (millions) 43
Total Value of Holdings (millions) $1,619
PRICE T ROWE ASSOCIATES INC /MD/ hält zum 3/31/2017 3,971,461 Anteile, gemäss Plichtmitteilung vom 30.4.2017 ist der tatsächliche Bestand jedoch höher:
T. ROWE PRICE ASSOCIATES, INC. meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens
Bleibt abzuwarten, ob sich die Rate der institutionellen Anleger noch weitere erhöht oder ob es einen grossen (oder mehrere) Verkäufer gegeben hat.
Zitat von Cyberhexe:Zitat von Cyberhexe: Anbei eine weitere Pflichtmitteilung von BB Biotech über Aktienkauf bei Radius Health, und zwar
am 5.5.2017 20´600 zu $35.5477
am 8.5.2017 22´800 zu $35.5978
Insgesamt verfügen die Schweizer nun über 4.8 Mio Aktien (4,808,799). Bei einer Gesamtzahl vom 43,185,952 Aktien (Basic and diluted) entspricht dies 11.14% des Unternehmens.
und noch eine Pflichtmitteilung von BB Biotech über den Kauf von 50´000 Aktien zu $35.9296 vom 9.5.17 --> insgesamt verfügen die Schweizer nun über 4,858,799 Aktien.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
Momentaufnahme, allerdings zeitversetzt, derzeit:
Institutional Ownership 106.79%
Total Shares Outstanding (millions) 43
Total Value of Holdings (millions) $1,619
PRICE T ROWE ASSOCIATES INC /MD/ hält zum 3/31/2017 3,971,461 Anteile, gemäss Plichtmitteilung vom 30.4.2017 ist der tatsächliche Bestand jedoch höher:
T. ROWE PRICE ASSOCIATES, INC. meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens
Bleibt abzuwarten, ob sich die Rate der institutionellen Anleger noch weitere erhöht oder ob es einen grossen (oder mehrere) Verkäufer gegeben hat.
Antwort auf Beitrag Nr.: 54.956.969 von Cyberhexe am 16.05.17 19:33:59
Momentaufnahme, allerdings zeitversetzt, derzeit:
Institutional Ownership 106.79%
Total Shares Outstanding (millions) 43
Total Value of Holdings (millions) $1,619
http://www.nasdaq.com/symbol/rdus/institutional-holdings
Zitat von Cyberhexe: und noch eine Pflichtmitteilung von BB Biotech über den Kauf von 50´000 Aktien zu $35.9296 vom 9.5.17 --> insgesamt verfügen die Schweizer nun über 4,858,799 Aktien.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
Momentaufnahme, allerdings zeitversetzt, derzeit:
Institutional Ownership 106.79%
Total Shares Outstanding (millions) 43
Total Value of Holdings (millions) $1,619
http://www.nasdaq.com/symbol/rdus/institutional-holdings
Antwort auf Beitrag Nr.: 54.957.854 von Cyberhexe am 16.05.17 21:13:56...und noch einmal 15´000 Aktien: BB Biotech akkumuliert auch am 12.5.
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
nebstAbaloparatide hofft man auf positive Ergebnisse aus der onkologischen Pipeline:
Elacestrant (RAD1901), a selective estrogen receptor degrader (SERD), has anti-tumor activity in multiple ER+ breast cancer patient-derived xenograft models
Teeru Bihani, Hitisha K. Patel, Heike Arlt, Nianjun Tao, Hai Jiang, Jeff Brown, Dinesh M. Purandare, Gary Hattersley and Fiona Garner
DOI: 10.1158/1078-0432.CCR-16-2561 Published January 2017
RESULTS: Elacestrant induces the degradation of ER, inhibits ER-mediated signaling and growth of ER+ breast cancer cell lines in vitro and in vivo and significantly inhibits tumor growth of multiple PDX models. Furthermore, we demonstrate that elacestrant in combination with palbociclib or everolimus can lead to greater efficacy in certain contexts. Finally, elacestrant exhibits significant anti-tumor activity both as a single agent and in combination with palbociclib in two patient-derived breast cancer xenograft models harboring ESR1 mutations.</p> <p> </p> <p>CONCLUSIONS: These data underscore the potential clinical utility of elacestrant as a single agent and as a combination therapy, for both early and late stage ER+ disease.
http://clincancerres.aacrjournals.org/content/early/2017/05/…
Auf ASCO wird folgende Präsentation zu RAD1901 erwartet:
PRESENTATIONS
Showing 1 - 1 of 1 result(s)
Poster Board: #6 • Abstract 1014
Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer.
Aditya Bardia, MD, MPH - First Author
Massachusetts General Hospital Cancer Center and Harvard Medical School
Discussed at the Poster Discussion Session on Sunday, June 4, 2017, 4:45 PM - 6:00 PM, at Hall B1
Elacestrant (RAD1901), a selective estrogen receptor degrader (SERD), has anti-tumor activity in multiple ER+ breast cancer patient-derived xenograft models
Teeru Bihani, Hitisha K. Patel, Heike Arlt, Nianjun Tao, Hai Jiang, Jeff Brown, Dinesh M. Purandare, Gary Hattersley and Fiona Garner
DOI: 10.1158/1078-0432.CCR-16-2561 Published January 2017
RESULTS: Elacestrant induces the degradation of ER, inhibits ER-mediated signaling and growth of ER+ breast cancer cell lines in vitro and in vivo and significantly inhibits tumor growth of multiple PDX models. Furthermore, we demonstrate that elacestrant in combination with palbociclib or everolimus can lead to greater efficacy in certain contexts. Finally, elacestrant exhibits significant anti-tumor activity both as a single agent and in combination with palbociclib in two patient-derived breast cancer xenograft models harboring ESR1 mutations.</p> <p> </p> <p>CONCLUSIONS: These data underscore the potential clinical utility of elacestrant as a single agent and as a combination therapy, for both early and late stage ER+ disease.
http://clincancerres.aacrjournals.org/content/early/2017/05/…
Auf ASCO wird folgende Präsentation zu RAD1901 erwartet:
PRESENTATIONS
Showing 1 - 1 of 1 result(s)
Poster Board: #6 • Abstract 1014
Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer.
Aditya Bardia, MD, MPH - First Author
Massachusetts General Hospital Cancer Center and Harvard Medical School
Discussed at the Poster Discussion Session on Sunday, June 4, 2017, 4:45 PM - 6:00 PM, at Hall B1
Antwort auf Beitrag Nr.: 54.959.210 von Cyberhexe am 17.05.17 05:51:13ASCO Abstract 1014
viel versprechend ist, dass eine Wirkung von RAD1901 in Monotherapie beobachtet wurde, obschon dieser sehr wahrscheinlich in einer Kombitherapie eingesetzt werden soll.
http://abstracts.asco.org/199/AbstView_199_192812.html
Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer.
Sub-category:
Hormone Receptor-Positive
Category:
Breast Cancer—Metastatic
Meeting:
2017 ASCO Annual Meeting
Abstract No:
1014
Poster Board Number:
Poster Discussion Session (Board #6)
Citation:
J Clin Oncol 35, 2017 (suppl; abstr 1014)
Author(s): Aditya Bardia, Peter Kabos, Richard Elledge, Dannie Wang, Jinshan Shen, Fiona Garner, Alison O'Neill, Virginia G. Kaklamani; Massachusetts General Hospital Cancer Center and Harvard Medical School, Boston, MA; University of Colorado Denver, Greenwood Village, CO; Cancer Therapy and Research Center at UT Health Science Center, San Antonio, TX; Radius Health Inc., Waltham, MA; The University of Texas Health Science Center, San Antonio, TX
Abstract Disclosures
Abstract:
Background: The treatment of advanced ER+ breast cancer remains a clinical challenge with the majority of patients eventually progressing due to resistance to endocrine therapy. RAD1901 is a novel, nonsteroidal, oral SERD that has demonstrated dose dependent degradation of ER, and ER regulated genes in preclinical studies. In multiple in vivo patient derived xenograft models of breast cancer, including those harboring ESR1 mutations, RAD1901 demonstrated significant antitumor activity.
Methods: In a phase-1 Study RAD1901-005 (ClinicalTrials.gov ID: NCT02338349), patients with advanced ER+ breast cancer were enrolled in dose escalation cohorts, followed by a safety expansion cohort. Key inclusion criteria include postmenopausal women aged 18 years or older, with advanced ER+, HER2- breast cancer, who have received ≤ 2 prior chemotherapy regimens in the metastatic setting and > 6 months of prior endocrine therapy. ESR1 mutation status was determined from circulating tumor DNA (ctDNA) samples. Clinical outcomes were evaluated based on RECIST v1.1 criteria.
Results: As of January 25, 2017, total of 39 patients were enrolled at the 400 mg qd dose. Patients were heavily pre-treated (median lines of prior therapy = 3), with 38% and 41% having previously received fulvestrant and palbociclib/CDK4/6 inhibitor, respectively.
RAD1901 was generally well-tolerated, with the most common adverse events being low grade nausea (Grade 3/4 = 0%) and dyspepsia (Grade 3/4 = 0%).
ESR1 mutations, including D538G, Y537S/N/C, L536H/P/R, S436P and E380Q, were detected at baseline in 44% of patients and dynamic changes in the allele frequency of ESR1 mutations were observed in response to treatment.
Confirmed partial responses were observed in patients with ESR1 mutations, and those who had previously received fulvestrant and palbociclib.
Conclusions: RAD1901 has demonstrated evidence of single agent activity, with confirmed partial responses in heavily pre-treated patients with advanced ER+ breast cancer, including those with ESR1 mutations, warranting additional clinical development. Clinical trial information: NCT02338349
viel versprechend ist, dass eine Wirkung von RAD1901 in Monotherapie beobachtet wurde, obschon dieser sehr wahrscheinlich in einer Kombitherapie eingesetzt werden soll.
http://abstracts.asco.org/199/AbstView_199_192812.html
Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer.
Sub-category:
Hormone Receptor-Positive
Category:
Breast Cancer—Metastatic
Meeting:
2017 ASCO Annual Meeting
Abstract No:
1014
Poster Board Number:
Poster Discussion Session (Board #6)
Citation:
J Clin Oncol 35, 2017 (suppl; abstr 1014)
Author(s): Aditya Bardia, Peter Kabos, Richard Elledge, Dannie Wang, Jinshan Shen, Fiona Garner, Alison O'Neill, Virginia G. Kaklamani; Massachusetts General Hospital Cancer Center and Harvard Medical School, Boston, MA; University of Colorado Denver, Greenwood Village, CO; Cancer Therapy and Research Center at UT Health Science Center, San Antonio, TX; Radius Health Inc., Waltham, MA; The University of Texas Health Science Center, San Antonio, TX
Abstract Disclosures
Abstract:
Background: The treatment of advanced ER+ breast cancer remains a clinical challenge with the majority of patients eventually progressing due to resistance to endocrine therapy. RAD1901 is a novel, nonsteroidal, oral SERD that has demonstrated dose dependent degradation of ER, and ER regulated genes in preclinical studies. In multiple in vivo patient derived xenograft models of breast cancer, including those harboring ESR1 mutations, RAD1901 demonstrated significant antitumor activity.
Methods: In a phase-1 Study RAD1901-005 (ClinicalTrials.gov ID: NCT02338349), patients with advanced ER+ breast cancer were enrolled in dose escalation cohorts, followed by a safety expansion cohort. Key inclusion criteria include postmenopausal women aged 18 years or older, with advanced ER+, HER2- breast cancer, who have received ≤ 2 prior chemotherapy regimens in the metastatic setting and > 6 months of prior endocrine therapy. ESR1 mutation status was determined from circulating tumor DNA (ctDNA) samples. Clinical outcomes were evaluated based on RECIST v1.1 criteria.
Results: As of January 25, 2017, total of 39 patients were enrolled at the 400 mg qd dose. Patients were heavily pre-treated (median lines of prior therapy = 3), with 38% and 41% having previously received fulvestrant and palbociclib/CDK4/6 inhibitor, respectively.
RAD1901 was generally well-tolerated, with the most common adverse events being low grade nausea (Grade 3/4 = 0%) and dyspepsia (Grade 3/4 = 0%).
ESR1 mutations, including D538G, Y537S/N/C, L536H/P/R, S436P and E380Q, were detected at baseline in 44% of patients and dynamic changes in the allele frequency of ESR1 mutations were observed in response to treatment.
Confirmed partial responses were observed in patients with ESR1 mutations, and those who had previously received fulvestrant and palbociclib.
Conclusions: RAD1901 has demonstrated evidence of single agent activity, with confirmed partial responses in heavily pre-treated patients with advanced ER+ breast cancer, including those with ESR1 mutations, warranting additional clinical development. Clinical trial information: NCT02338349
Antwort auf Beitrag Nr.: 54.967.352 von Cyberhexe am 17.05.17 23:30:16...und die Institutionellen sammeln weiter:
http://ir.radiuspharm.com/secfiling.cfm?filingID=909661-17-8…
SCHEDULE 13D
May 10, 2017
The reporting persons making this filing hold an aggregate of 3,579,000 Shares, which is 8.3 % of the class of securities. The reporting person on this cover page, however, is a beneficial owner only of the securities reported by it on this cover page.
SCHEDULE A
FARALLON CAPITAL PARTNERS, L.P.
4/28/2017 31900 (P) $41.42
4/28/2017 63700 (P) $41.03
5/5/2017 5300 (P) $35.18
5/9/2017 600 (P) $35.26
5/10/2017 8700 (P) $35.21
5/11/2017 5500 (P) $34.70
SCHEDULE B
FARALLON CAPITAL INSTITUTIONAL PARTNERS, L.P.
4/28/2017 23800 (P) $41.42
4/28/2017 47500 (P) $41.03
5/5/2017 4800 (P) $35.18
5/9/2017 500 (P) $35.26
5/10/2017 7600 (P) $35.21
5/11/2017 4772 (P) $34.70
SCHEDULE C
FARALLON CAPITAL INSTITUTIONAL PARTNERS II, L.P.
4/28/2017 3700 (P) $41.42
4/28/2017 7500 (P) $41.03
5/5/2017 800 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 1300 (P) $35.21
5/11/2017 800 (P) $34.70
SCHEDULE D
FARALLON CAPITAL INSTITUTIONAL PARTNERS III, L.P.
4/28/2017 3100 (P) $41.42
4/28/2017 6300 (P) $41.03
5/5/2017 700 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 1100 (P) $35.21
5/11/2017 600 (P) $34.70
SCHEDULE E
FARALLON CAPITAL INSTITUTIONAL PARTNERS V, L.P.
4/28/2017 4100 (P) $41.42
4/28/2017 8100 (P) $41.03
5/5/2017 900 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 1400 (P) $35.21
5/11/2017 800 (P) $34.70
SCHEDULE F
FARALLON CAPITAL OFFSHORE INVESTORS II, L.P.
4/28/2017 51500 (P) $41.42
4/28/2017 103200 (P) $41.03
5/5/2017 9200 (P) $35.18
5/9/2017 978 (P) $35.26
5/10/2017 15350 (P) $35.21
5/11/2017 9500 (P) $34.70
SCHEDULE G
FARALLON CAPITAL (AM) INVESTORS, L.P.
4/28/2017 2200 (P) $41.42
4/28/2017 4400 (P) $41.03
5/5/2017 500 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 700 (P) $35.21
5/11/2017 500 (P) $34.70
SCHEDULE H
FARALLON CAPITAL F5 MASTER I, L.P.
4/28/2017 2800 (P) $41.42
4/28/2017 5600 (P) $41.03
5/5/2017 600 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 900 (P) $35.21
5/11/2017 600 (P) $34.70
SCHEDULE I
FARALLON CAPITAL MANAGEMENT, L.L.C.
4/28/2017 1900 (P) $41.42
4/28/2017 3700 (P) $41.03
5/5/2017 400 (P) $35.18
5/10/2017 700 (P) $35.21
5/11/2017 400 (P) $34.70
http://ir.radiuspharm.com/secfiling.cfm?filingID=909661-17-8…
SCHEDULE 13D
May 10, 2017
The reporting persons making this filing hold an aggregate of 3,579,000 Shares, which is 8.3 % of the class of securities. The reporting person on this cover page, however, is a beneficial owner only of the securities reported by it on this cover page.
SCHEDULE A
FARALLON CAPITAL PARTNERS, L.P.
4/28/2017 31900 (P) $41.42
4/28/2017 63700 (P) $41.03
5/5/2017 5300 (P) $35.18
5/9/2017 600 (P) $35.26
5/10/2017 8700 (P) $35.21
5/11/2017 5500 (P) $34.70
SCHEDULE B
FARALLON CAPITAL INSTITUTIONAL PARTNERS, L.P.
4/28/2017 23800 (P) $41.42
4/28/2017 47500 (P) $41.03
5/5/2017 4800 (P) $35.18
5/9/2017 500 (P) $35.26
5/10/2017 7600 (P) $35.21
5/11/2017 4772 (P) $34.70
SCHEDULE C
FARALLON CAPITAL INSTITUTIONAL PARTNERS II, L.P.
4/28/2017 3700 (P) $41.42
4/28/2017 7500 (P) $41.03
5/5/2017 800 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 1300 (P) $35.21
5/11/2017 800 (P) $34.70
SCHEDULE D
FARALLON CAPITAL INSTITUTIONAL PARTNERS III, L.P.
4/28/2017 3100 (P) $41.42
4/28/2017 6300 (P) $41.03
5/5/2017 700 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 1100 (P) $35.21
5/11/2017 600 (P) $34.70
SCHEDULE E
FARALLON CAPITAL INSTITUTIONAL PARTNERS V, L.P.
4/28/2017 4100 (P) $41.42
4/28/2017 8100 (P) $41.03
5/5/2017 900 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 1400 (P) $35.21
5/11/2017 800 (P) $34.70
SCHEDULE F
FARALLON CAPITAL OFFSHORE INVESTORS II, L.P.
4/28/2017 51500 (P) $41.42
4/28/2017 103200 (P) $41.03
5/5/2017 9200 (P) $35.18
5/9/2017 978 (P) $35.26
5/10/2017 15350 (P) $35.21
5/11/2017 9500 (P) $34.70
SCHEDULE G
FARALLON CAPITAL (AM) INVESTORS, L.P.
4/28/2017 2200 (P) $41.42
4/28/2017 4400 (P) $41.03
5/5/2017 500 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 700 (P) $35.21
5/11/2017 500 (P) $34.70
SCHEDULE H
FARALLON CAPITAL F5 MASTER I, L.P.
4/28/2017 2800 (P) $41.42
4/28/2017 5600 (P) $41.03
5/5/2017 600 (P) $35.18
5/9/2017 100 (P) $35.26
5/10/2017 900 (P) $35.21
5/11/2017 600 (P) $34.70
SCHEDULE I
FARALLON CAPITAL MANAGEMENT, L.L.C.
4/28/2017 1900 (P) $41.42
4/28/2017 3700 (P) $41.03
5/5/2017 400 (P) $35.18
5/10/2017 700 (P) $35.21
5/11/2017 400 (P) $34.70
Antwort auf Beitrag Nr.: 54.973.853 von Cyberhexe am 18.05.17 19:28:38...und natürlich auch wieder BB Biotech:
und zwar am...
5/16/2017 (P) 17000 Aktien von RDUS zu $33.925
und am...
5/17/2017 (P) 18000 Aktien von RDUS zu $32.9812
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
und zwar am...
5/16/2017 (P) 17000 Aktien von RDUS zu $33.925
und am...
5/17/2017 (P) 18000 Aktien von RDUS zu $32.9812
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
will biotech die Bude übernehmen oder was 
was mir immer noch nicht klar ist....wer verkauft denn hier?!?

was mir immer noch nicht klar ist....wer verkauft denn hier?!?
Antwort auf Beitrag Nr.: 54.973.991 von 2brix am 18.05.17 19:47:19
gute Frage, zumal BB Biotech, FARALLON und T. ROWE PRICE ASSOCIATES, INC. (meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens) in den letzten Wochen kräftig aufgestockt haben und sich zum 31.3. schon über 106%(!) der Aktien im Besitz von institutionellen Anleger befunden haben. Es ist davon auszugehen, dass es auch bei den Institutionellen Verkäufer gibt und der institutionelle Anteil nicht weiter steigt.
Folie aus der Unternehmenspräsentation über anstehende Meilensteine:
Zitat von 2brix: will biotech die Bude übernehmen oder was
was mir immer noch nicht klar ist....wer verkauft denn hier?!?
gute Frage, zumal BB Biotech, FARALLON und T. ROWE PRICE ASSOCIATES, INC. (meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens) in den letzten Wochen kräftig aufgestockt haben und sich zum 31.3. schon über 106%(!) der Aktien im Besitz von institutionellen Anleger befunden haben. Es ist davon auszugehen, dass es auch bei den Institutionellen Verkäufer gibt und der institutionelle Anteil nicht weiter steigt.
Folie aus der Unternehmenspräsentation über anstehende Meilensteine:

Antwort auf Beitrag Nr.: 54.983.633 von Cyberhexe am 20.05.17 00:17:49und sich zum 31.3. schon über 106%(!) der Aktien im Besitz von institutionellen Anleger
Wie geht das?
Wie geht das?

Antwort auf Beitrag Nr.: 54.984.386 von Basilea1234 am 20.05.17 09:28:38
Ursache hierfür sind die leer verkauften Aktien, derzeit über 8 Mio Stück, dies entspricht knapp 20% der verfügbaren Aktien:
http://www.nasdaq.com/symbol/rdus/short-interest
Bei einer derart hohen Short-Quote (also Anteil leer verkaufter Aktien) ist natürlich auch Vorsicht geboten. Es wird massiv auf fallende Kurse gewettet. Demgegenüber steht jedoch der extrem hohe Besitz-Anteil bei institutionellen Anlegern (>106%). Dies entspricht einer Wette auf steigende Kurse.
Hinzu kommen noch "naked short selling, failed to deliver", d.h. leer verkaufte Aktien, die nicht geliehen werden konnten und deswegen asl Phantom-Aktien gelten, und, so viel ich weiss, nicht in die Statistik (siehe oben) mit einfliessen.
Falls du dich dafür interessierst, anbei ein altes Video von Bloomberg Television, in welchem die "Phantom Shares" gut erklärt sind:
https://vimeo.com/42321845
anbei eine gute Zusammenfassung der Daten zu abaloparatide:
http://www.chemdiv.com/fda-approves-tymlos-abaloparatide-tre…
FDA Approves Tymlos (abaloparatide) for the Treatment of Postmenopausal Women with Osteoporosis at High Risk for Fracture
WALTHAM, Mass., April 28, 2017 (GLOBE NEWSWIRE)
...
86% in new vertebral fractures
43% in nonvertebral fractures
The absolute risk reductions were 3.6% and 2.0%, respectively.
Zitat von Basilea1234: und sich zum 31.3. schon über 106%(!) der Aktien im Besitz von institutionellen Anleger
Wie geht das?
Ursache hierfür sind die leer verkauften Aktien, derzeit über 8 Mio Stück, dies entspricht knapp 20% der verfügbaren Aktien:
http://www.nasdaq.com/symbol/rdus/short-interest
Bei einer derart hohen Short-Quote (also Anteil leer verkaufter Aktien) ist natürlich auch Vorsicht geboten. Es wird massiv auf fallende Kurse gewettet. Demgegenüber steht jedoch der extrem hohe Besitz-Anteil bei institutionellen Anlegern (>106%). Dies entspricht einer Wette auf steigende Kurse.
Hinzu kommen noch "naked short selling, failed to deliver", d.h. leer verkaufte Aktien, die nicht geliehen werden konnten und deswegen asl Phantom-Aktien gelten, und, so viel ich weiss, nicht in die Statistik (siehe oben) mit einfliessen.
Falls du dich dafür interessierst, anbei ein altes Video von Bloomberg Television, in welchem die "Phantom Shares" gut erklärt sind:
https://vimeo.com/42321845
anbei eine gute Zusammenfassung der Daten zu abaloparatide:
http://www.chemdiv.com/fda-approves-tymlos-abaloparatide-tre…
FDA Approves Tymlos (abaloparatide) for the Treatment of Postmenopausal Women with Osteoporosis at High Risk for Fracture
WALTHAM, Mass., April 28, 2017 (GLOBE NEWSWIRE)
...
86% in new vertebral fractures
43% in nonvertebral fractures
The absolute risk reductions were 3.6% and 2.0%, respectively.
Antwort auf Beitrag Nr.: 54.987.410 von Cyberhexe am 21.05.17 09:32:22
ein teil der 106 % ownership sein
aber sie zaehlen nicht doppelt
soll heissen lauf dieser anzeige
Institutional Ownership 106.77%
sind 106 % im besitz von http://www.nasdaq.com/symbol/rdus/institutional-holdings
184 Institutional Holders
46,316,181 Total Shares Held
ueber 46 mil shares
- klar koennen von diesen 46 millionen shares
8 mil verliehen sein fuer shorties
aber es sind 46 millionen shares
wie kann das sein ?
---
klar ist auch dass naked shorts ungedeckte sind also phantom shares
somit auch nicht in den 46 millionen enthalten
mfg
mal ne nachfrage
klar koennen die 8 mil geshorteten aktienein teil der 106 % ownership sein
aber sie zaehlen nicht doppelt
soll heissen lauf dieser anzeige
Institutional Ownership 106.77%
sind 106 % im besitz von http://www.nasdaq.com/symbol/rdus/institutional-holdings
184 Institutional Holders
46,316,181 Total Shares Held
ueber 46 mil shares
- klar koennen von diesen 46 millionen shares
8 mil verliehen sein fuer shorties
aber es sind 46 millionen shares
wie kann das sein ?
---
klar ist auch dass naked shorts ungedeckte sind also phantom shares
somit auch nicht in den 46 millionen enthalten
mfg
 Diese NEWS dürfte RDUS Auftrieb geben.......
Diese NEWS dürfte RDUS Auftrieb geben....... 
 Amgen Osteoporosis Drug Approval Plan Derailed Over Newly Found Heart Safety Risk Signal
Amgen Osteoporosis Drug Approval Plan Derailed Over Newly Found Heart Safety Risk Signal 
A negative heart safety signal picked up in a clinical trial of Amgen's (AMGN) osteoporosis drug Evenity means the product will not be approved and on the U.S. market this year, as previously expected, the company said Sunday.
Evenity was already under FDA consideration with a marketing decision expected on July 19. But with questions now raised about the drug's heart safety risk, U.S. regulators want a look at safety data from the new clinical trial as part of the agency's review.
As a result, Amgen "does not expect approval of Evenity in the U.S. to occur in 2017," the company said. A timetable for how long the drug's approval might be delayed was not offered.
"Amgen's phase III update on bone drug [Evenity] just now is clearly negative and very surprising," wrote Evercore ISI analyst Umer Raffat, in a quick email to clients on Sunday night. "At this point, we are taking out all [Evenity] sales from the model. Consensus has approximately $800 million peak for this drug... We suspect stock likely down approximately 3-4% on this."
Amgen shares closed Friday at $156.51.
In the phase III study known as ARCH, the incidence of positively adjudicated cardiovascular serious adverse events as 12 months porosis drug that served as the active comparator in the study.
"We are working on understanding the observed cardiovascular safety signal and will continue to discuss these results with global regulators and experts in the field," said Iris Loew-Friedrich, chief medical officer of UCB, the Brussels-based drug maker that is co-developing Evenity with Amgen.
Amgen's osteoporosis setback will likely be seen as a providing a commercial boost to Radius Health (RDUS) , which secured U.S. approval in April for a competing osteoporosis drug, Tymlos.
https://finance.yahoo.com/m/d05bcc37-d883-3614-80f5-d5606e5d…" target="_blank" rel="nofollow ugc noopener">https://finance.yahoo.com/m/d05bcc37-d883-3614-80f5-d5606e5d…
Antwort auf Beitrag Nr.: 54.992.097 von bernie55 am 22.05.17 11:30:00Bin mal gespannt wie die SHORTIES sich heute morgen bei der NEWS in den USA fühlen werden. 

Antwort auf Beitrag Nr.: 54.988.020 von bonDiacomova am 21.05.17 11:44:22
...bin da auch etwas unsicher, aber irgendwo müssen diese zusätzlichen Aktien ja herkommen. Wenn nicht von leer verkauften Aktien woher dann?
FORM 10-Q
For the quarterly period ended March 31, 2017
Number of shares of the registrant’s Common Stock, $.0001 par value per share, outstanding as of April 27, 2017 : 43,377,381 shares
http://ir.radiuspharm.com/secfiling.cfm?filingID=1628280-17-…
Total Institutional Shares: 46,316,181
Institutional Ownership 106.77%
Ich habe hierzu keine andere Erklärung, als dass Aktien von institutionellen Anlegern verliehen werden, und diese dann an wiederum institutionelle Anleger verkauft werden. Beide institutionellen Anleger würden diese Aktien somit im Portfolio ausweisen, der Verkäufer der geliehenen Aktien bleibt "short". Lasse mich jedoch gerne von Experten korrigieren.
Bei Romosozumab wurde tatsächlich ein kardiovaskuläres Signal beobachtet, welches dessen Zulassung verzögern wird. Das ist eine schlechte Nachricht für Osteoporose-Patienten, positiv jedoch für die prognostizierten Abaloparatide-Umsätze.
Zitat von bonDiacomova: klar koennen die 8 mil geshorteten aktien
ein teil der 106 % ownership sein
aber sie zaehlen nicht doppelt
soll heissen lauf dieser anzeige
Institutional Ownership 106.77%
sind 106 % im besitz von http://www.nasdaq.com/symbol/rdus/institutional-holdings
184 Institutional Holders
46,316,181 Total Shares Held
ueber 46 mil shares
- klar koennen von diesen 46 millionen shares
8 mil verliehen sein fuer shorties
aber es sind 46 millionen shares
wie kann das sein ?
---
klar ist auch dass naked shorts ungedeckte sind also phantom shares
somit auch nicht in den 46 millionen enthalten
mfg
...bin da auch etwas unsicher, aber irgendwo müssen diese zusätzlichen Aktien ja herkommen. Wenn nicht von leer verkauften Aktien woher dann?
FORM 10-Q
For the quarterly period ended March 31, 2017
Number of shares of the registrant’s Common Stock, $.0001 par value per share, outstanding as of April 27, 2017 : 43,377,381 shares
http://ir.radiuspharm.com/secfiling.cfm?filingID=1628280-17-…
Total Institutional Shares: 46,316,181
Institutional Ownership 106.77%
Ich habe hierzu keine andere Erklärung, als dass Aktien von institutionellen Anlegern verliehen werden, und diese dann an wiederum institutionelle Anleger verkauft werden. Beide institutionellen Anleger würden diese Aktien somit im Portfolio ausweisen, der Verkäufer der geliehenen Aktien bleibt "short". Lasse mich jedoch gerne von Experten korrigieren.
Bei Romosozumab wurde tatsächlich ein kardiovaskuläres Signal beobachtet, welches dessen Zulassung verzögern wird. Das ist eine schlechte Nachricht für Osteoporose-Patienten, positiv jedoch für die prognostizierten Abaloparatide-Umsätze.
Antwort auf Beitrag Nr.: 54.993.273 von Cyberhexe am 22.05.17 14:13:02Die ersten Analysten kommentieren bereits das kardiovaskuläre Signal bei Romosozumab und erwarten:
- ein Advisory Committee Meeting d.h. eine Expertenrunde soll vorgängig der Zulassunsentscheidung über das Medikament beraten und eine Empfehlung aussprechen
- Zulassungsrestriktionen
- Datenreview
"Rather than winning approval in July as widely expected, romosozumab now will land on the FDA's safety-review agenda, and that means Amgen can kiss the prospect of a 2017 approval goodbye.
The way Leerink Partners analyst Geoffrey Porges sees it, the “FDA is likely to re-review the entire clinical database for the product, and re-examine the cardiovascular events and rates in the entire sample." Porges also expects to the agency to convene an advisory committee to review the data—and hamper the product with “significant restrictions” if it does make it to market. At this point, though, he’s setting the probability of an eventual green light at just 50-50, he said."
http://www.fiercepharma.com/marketing/amgen-s-romosozumab-re…
- ein Advisory Committee Meeting d.h. eine Expertenrunde soll vorgängig der Zulassunsentscheidung über das Medikament beraten und eine Empfehlung aussprechen
- Zulassungsrestriktionen
- Datenreview
"Rather than winning approval in July as widely expected, romosozumab now will land on the FDA's safety-review agenda, and that means Amgen can kiss the prospect of a 2017 approval goodbye.
The way Leerink Partners analyst Geoffrey Porges sees it, the “FDA is likely to re-review the entire clinical database for the product, and re-examine the cardiovascular events and rates in the entire sample." Porges also expects to the agency to convene an advisory committee to review the data—and hamper the product with “significant restrictions” if it does make it to market. At this point, though, he’s setting the probability of an eventual green light at just 50-50, he said."
http://www.fiercepharma.com/marketing/amgen-s-romosozumab-re…
Antwort auf Beitrag Nr.: 54.973.898 von Cyberhexe am 18.05.17 19:32:40
BB Biotech gibt den Kauf von weiteren 50000 Aktien von Radius Health in einer Pflichtmitteilung bekannt:http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
Zitat von Cyberhexe: ...und natürlich auch wieder BB Biotech:
und zwar am...
5/16/2017 (P) 17000 Aktien von RDUS zu $33.925
und am...
5/17/2017 (P) 18000 Aktien von RDUS zu $32.9812
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
BB Biotech gibt den Kauf von weiteren 50000 Aktien von Radius Health in einer Pflichtmitteilung bekannt:http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
Antwort auf Beitrag Nr.: 54.983.633 von Cyberhexe am 20.05.17 00:17:49
Ein ganz wichtiges Ereignis wird die Bekanntgabe der Ergebnisse nach 24 Monaten von ACTIVExtend, die auf das 2. Quartal in 2017 angekündigt sind. Es ist von besonderer Bedeutung, dass bei den Nebenwirkungen nicht ein unverhofftes Signal wie bei Romosozumab "auftaucht":
--> Report topline results for 24 months ACTIVExtend trial Q2’17
Beim Vergleich der Ergebnisse von Romosozumab mit denjenigen von Abaloparatide, liegt der Vorteil eindeutig bei Letzterem:
UCB and Amgen announce top-line phase 3 data from active-comparator study of Evenity™ (romosozumab) in postmenopausal women with osteoporosisARCH Study Met Primary and Key Secondary Endpoints by Reducing the Incidence of New Vertebral, Clinical and Non-Vertebral FracturesImbalance in Cardiovascular Events Observed as New Safety Signal
BRUSSELS and THOUSAND OAKS, Calif. (00:01, May 22, 2017): Regulated Information – Inside Information– UCB (Euronext Brussels: UCB) and Amgen (NASDAQ:AMGN) today announced that the romosozumabARCH study met both primary endpoints and the key secondary endpoint. Atthe primary analysis, treatment with romosozumab for 12 months followed by alendronate significantly reduced the incidence of new vertebral fractures through 24 months, clinical fractures (primary endpoints) and non-vertebral fractures (key secondary endpoint) in postmenopausal women withosteoporosis at high risk for fracture, compared to alendronate alone. An imbalance in positively adjudicated cardiovascular serious adverse events was observed as a new safety signal (2.5 percent romosozumab versus 1.9 percent alendronate at 12 months).
“We are impressed with the statistically significant superior fracture risk reduction of romosozumab over alendronate, a current standard of care in osteoporosis. When we think that patients who have had a fracture are highly likely to suffer another one, the importance of post-fracture care cannot be emphasized enough,” said Professor Iris Loew-Friedrich, UCB’s chief medical officer. “We are working on understanding the observed cardiovascular safety signal and will continue to discuss these results with global regulators and experts in the field.”Romosozumab is an investigational bone-forming agent that rapidly increases bone formation and reduces bone resorption simultaneously, increases bone mineral density and reduces the risk of fracture. In this study, women received subcutaneous injection of romosozumab monthly for 12 months followed by oral alendronate weekly for at least 12 months.At 24 months, women in the romosozumab treatment group experienced a statistically significant 50 percent reduction in the relative risk of a new vertebral (spine) fracture compared to those receiving alendronate alone. Women in the romosozumab treatment group also experienced a statistically significant 27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture) at the primary analysis. Additionally, non-vertebral fractures were statistically significantly reduced by 19 percent in the romosozumab treatment group, including a nominally significant reduction in hip fractures.
Zusammenfassung Romosozumab:
Daten nach 12 Monaten Romosozumab und 12 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend:
"50 percent reduction in the relative risk of a new vertebral (spine) fracture"
Frakturen nicht die Wirbelsäule betreffend:
"non-vertebral fractures were statistically significantly reduced by 19 percent"
alle klinisch bedeutenden Frakturen:
"27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture)"
"Mayo Clinic Proceedings Publishes Positive Results from the ACTIVExtendClinical Trial of Abaloparatide-SC in Postmenopausal Women With Osteoporosis
— Results from interim analysis of the ACTIVExtend study of postmenopausal women withosteoporosis treated for 18 months with investigational drug abaloparatide-SC in theACTIVE trial who were transitioned to alendronate in ACTIVExtend show statisticallysignificant reductions at six months in the incidence of new vertebral, nonvertebral, andmajor osteoporotic fractures when compared with placebo treated patients who were alsotransitioned to alendronate
—WALTHAM, Mass., Feb. 01, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and other endocrine diseases, today announced that positive results from a planned 6-month interim analysis of the ACTIVExtend clinical trial were published in theMayo Clinic Proceedings. The results of ACTIVExtend following 6 months of alendronate treatment show that patients previously treated with daily abaloparatide-SC for 18 months in the ACTIVE trial who were transitioned to alendronate had significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001), of 52% in nonvertebral fractures (p = 0.02) and 58% in major osteoporotic fractures (p<0.01) compared to the previous placebo treated patients who were also transitioned to alendronate. Bone mineral density at the spine, femoral neck and hip increased significantly in the abaloparatide-treated patients after transitioning to alendronate (p<0.0001)."
Zusammenfassung Abaloparatide:
Daten nach 12 Monaten Romosozumab und 6 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend:
"significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001)"
Frakturen nicht die Wirbelsäule betreffend:
"52% in nonvertebral fractures (p = 0.02) 52% in nonvertebral fractures (p = 0.02) "
alle klinisch bedeutenden Frakturen:
"58% in major osteoporotic fractures (p<0.01)"
Zitat von Cyberhexe:Zitat von 2brix: will biotech die Bude übernehmen oder was
was mir immer noch nicht klar ist....wer verkauft denn hier?!?
gute Frage, zumal BB Biotech, FARALLON und T. ROWE PRICE ASSOCIATES, INC. (meldet den Besitz von 5.184 Mio Aktien nach 3.079 Mio Aktien am 7.2.2017; dies entspricht nun 11.9% des Unternehmens) in den letzten Wochen kräftig aufgestockt haben und sich zum 31.3. schon über 106%(!) der Aktien im Besitz von institutionellen Anleger befunden haben. Es ist davon auszugehen, dass es auch bei den Institutionellen Verkäufer gibt und der institutionelle Anteil nicht weiter steigt.
Folie aus der Unternehmenspräsentation über anstehende Meilensteine:
Ein ganz wichtiges Ereignis wird die Bekanntgabe der Ergebnisse nach 24 Monaten von ACTIVExtend, die auf das 2. Quartal in 2017 angekündigt sind. Es ist von besonderer Bedeutung, dass bei den Nebenwirkungen nicht ein unverhofftes Signal wie bei Romosozumab "auftaucht":
--> Report topline results for 24 months ACTIVExtend trial Q2’17
Beim Vergleich der Ergebnisse von Romosozumab mit denjenigen von Abaloparatide, liegt der Vorteil eindeutig bei Letzterem:
UCB and Amgen announce top-line phase 3 data from active-comparator study of Evenity™ (romosozumab) in postmenopausal women with osteoporosisARCH Study Met Primary and Key Secondary Endpoints by Reducing the Incidence of New Vertebral, Clinical and Non-Vertebral FracturesImbalance in Cardiovascular Events Observed as New Safety Signal
BRUSSELS and THOUSAND OAKS, Calif. (00:01, May 22, 2017): Regulated Information – Inside Information– UCB (Euronext Brussels: UCB) and Amgen (NASDAQ:AMGN) today announced that the romosozumabARCH study met both primary endpoints and the key secondary endpoint. Atthe primary analysis, treatment with romosozumab for 12 months followed by alendronate significantly reduced the incidence of new vertebral fractures through 24 months, clinical fractures (primary endpoints) and non-vertebral fractures (key secondary endpoint) in postmenopausal women withosteoporosis at high risk for fracture, compared to alendronate alone. An imbalance in positively adjudicated cardiovascular serious adverse events was observed as a new safety signal (2.5 percent romosozumab versus 1.9 percent alendronate at 12 months).
“We are impressed with the statistically significant superior fracture risk reduction of romosozumab over alendronate, a current standard of care in osteoporosis. When we think that patients who have had a fracture are highly likely to suffer another one, the importance of post-fracture care cannot be emphasized enough,” said Professor Iris Loew-Friedrich, UCB’s chief medical officer. “We are working on understanding the observed cardiovascular safety signal and will continue to discuss these results with global regulators and experts in the field.”Romosozumab is an investigational bone-forming agent that rapidly increases bone formation and reduces bone resorption simultaneously, increases bone mineral density and reduces the risk of fracture. In this study, women received subcutaneous injection of romosozumab monthly for 12 months followed by oral alendronate weekly for at least 12 months.At 24 months, women in the romosozumab treatment group experienced a statistically significant 50 percent reduction in the relative risk of a new vertebral (spine) fracture compared to those receiving alendronate alone. Women in the romosozumab treatment group also experienced a statistically significant 27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture) at the primary analysis. Additionally, non-vertebral fractures were statistically significantly reduced by 19 percent in the romosozumab treatment group, including a nominally significant reduction in hip fractures.
Zusammenfassung Romosozumab:
Daten nach 12 Monaten Romosozumab und 12 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend:
"50 percent reduction in the relative risk of a new vertebral (spine) fracture"
Frakturen nicht die Wirbelsäule betreffend:
"non-vertebral fractures were statistically significantly reduced by 19 percent"
alle klinisch bedeutenden Frakturen:
"27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture)"
"Mayo Clinic Proceedings Publishes Positive Results from the ACTIVExtendClinical Trial of Abaloparatide-SC in Postmenopausal Women With Osteoporosis
— Results from interim analysis of the ACTIVExtend study of postmenopausal women withosteoporosis treated for 18 months with investigational drug abaloparatide-SC in theACTIVE trial who were transitioned to alendronate in ACTIVExtend show statisticallysignificant reductions at six months in the incidence of new vertebral, nonvertebral, andmajor osteoporotic fractures when compared with placebo treated patients who were alsotransitioned to alendronate
—WALTHAM, Mass., Feb. 01, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and other endocrine diseases, today announced that positive results from a planned 6-month interim analysis of the ACTIVExtend clinical trial were published in theMayo Clinic Proceedings. The results of ACTIVExtend following 6 months of alendronate treatment show that patients previously treated with daily abaloparatide-SC for 18 months in the ACTIVE trial who were transitioned to alendronate had significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001), of 52% in nonvertebral fractures (p = 0.02) and 58% in major osteoporotic fractures (p<0.01) compared to the previous placebo treated patients who were also transitioned to alendronate. Bone mineral density at the spine, femoral neck and hip increased significantly in the abaloparatide-treated patients after transitioning to alendronate (p<0.0001)."
Zusammenfassung Abaloparatide:
Daten nach 12 Monaten Romosozumab und 6 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend:
"significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001)"
Frakturen nicht die Wirbelsäule betreffend:
"52% in nonvertebral fractures (p = 0.02) 52% in nonvertebral fractures (p = 0.02) "
alle klinisch bedeutenden Frakturen:
"58% in major osteoporotic fractures (p<0.01)"
Antwort auf Beitrag Nr.: 54.997.026 von Cyberhexe am 22.05.17 23:45:54Zusammenfassung Romosozumab:
Daten nach 12 Monaten Romosozumab und 12 Monaten Ergänzung mit Alendronat Frakturen die
Wirbelsäule betreffend: "50 percent reduction in the relative risk of a new vertebral (spine) fracture"
Frakturen nicht die Wirbelsäule betreffend: "non-vertebral fractures were statistically significantly reduced by 19 percent"
alle klinisch bedeutenden Frakturen: "27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture)"
50% / 19% / 27% Reduktion der verschiedenen Frakturen bei Romosozumab
Zusammenfassung Abaloparatide:
Daten nach 12 Monaten Romosozumab und 6 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend: "significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001)"
Frakturen nicht die Wirbelsäule betreffend: "52% in nonvertebral fractures (p = 0.02) 52% in nonvertebral fractures (p = 0.02) "
alle klinisch bedeutenden Frakturen: "58% in major osteoporotic fractures (p<0.01)"
87% / 52% / 58% Reduktion der verschiedenen Frakturen unter Abaloparatide
es ist zudem zu erwarten, dass die Schere nach 24 Monaten noch weiter auseinander geht und die Reduktion der Frakturrate weiter zunimmt.
Daten nach 12 Monaten Romosozumab und 12 Monaten Ergänzung mit Alendronat Frakturen die
Wirbelsäule betreffend: "50 percent reduction in the relative risk of a new vertebral (spine) fracture"
Frakturen nicht die Wirbelsäule betreffend: "non-vertebral fractures were statistically significantly reduced by 19 percent"
alle klinisch bedeutenden Frakturen: "27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture)"
50% / 19% / 27% Reduktion der verschiedenen Frakturen bei Romosozumab
Zusammenfassung Abaloparatide:
Daten nach 12 Monaten Romosozumab und 6 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend: "significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001)"
Frakturen nicht die Wirbelsäule betreffend: "52% in nonvertebral fractures (p = 0.02) 52% in nonvertebral fractures (p = 0.02) "
alle klinisch bedeutenden Frakturen: "58% in major osteoporotic fractures (p<0.01)"
87% / 52% / 58% Reduktion der verschiedenen Frakturen unter Abaloparatide
es ist zudem zu erwarten, dass die Schere nach 24 Monaten noch weiter auseinander geht und die Reduktion der Frakturrate weiter zunimmt.
Antwort auf Beitrag Nr.: 54.997.071 von Cyberhexe am 22.05.17 23:57:40Romosozumab hat bei der Anwendung den ganz grossen Vorteil, dass nur einmal monatlich subkutan appliziert werden muss.
Romosozumab or placebo was administered subcutaneously once monthly for 12 months
dies ist gegenüber der täglichen Anwendung von Abaloparatide eindeutig besserl. Es ist derzeit allerdings offen, ob das kardiovaskuläre Signal nur eine Verzögerung bedeutet oder ob Restriktionen die Marktpenetration reduzieren bzw. überhaupt eine Marktzulassung möglich sein wird:
CNBC: Romosozumab no longer expected to win 2017 U.S. approval. ...
But the new safety data, which cropped up in an otherwise successful trial, will have to be taken into consideration, delaying any FDA decision and leaving the product's future uncertain.
Romosozumab or placebo was administered subcutaneously once monthly for 12 months
dies ist gegenüber der täglichen Anwendung von Abaloparatide eindeutig besserl. Es ist derzeit allerdings offen, ob das kardiovaskuläre Signal nur eine Verzögerung bedeutet oder ob Restriktionen die Marktpenetration reduzieren bzw. überhaupt eine Marktzulassung möglich sein wird:
CNBC: Romosozumab no longer expected to win 2017 U.S. approval. ...
But the new safety data, which cropped up in an otherwise successful trial, will have to be taken into consideration, delaying any FDA decision and leaving the product's future uncertain.
106 % und...
da es wirklich ungewoehnlich ist mit den Institutional Ownership 106.77%habe ich ein paar vips auf w : o angeschrieben... keine erklaerung
ausser dass die angaben auf nasdaq seite eigentlich stimmen...
habe auch mit diesen angaben verglichen :
http://investors.morningstar.com/ownership/shareholders-majo…
komme auf "keine loesung" und habe nasdaq angeschrieben.
deine idee : insti verleiht an shortie - der verkauft wieder an einen insti
kann natuerlich sein was short interest 8 mil angeht...aber 8 mil alle an instis
und dann auch noch der rege "allltagshandel" an der boeres - wie z.b. gestern
(nacked shorts halte ich eigentlich fuer nicht moeglich
weil die muessten normalerweise ""schneller gedeckt werden""
als die mitteilungsfrist ( meist Q ende ) der insties fuer die nasdaq seite ....)
schon sehr werkwuerdig - aber interessant...daher habe ich mir auch
diese 2 seiten zu Abaloparatide mal angeschaut....interessant ;-)
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5119706/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5055567/
mfg
Antwort auf Beitrag Nr.: 54.997.386 von bonDiacomova am 23.05.17 06:42:41bonDia schrieb:
"nacked shorts halte ich eigentlich fuer nicht moeglich"
...failed to deliver von nackten Leerverkäufen ist meine einzige Erklärung für die kuriose Situation, dass die Instis über 46 Mio Aktien halten, nur 43,377,381 Aktien (April 27, 2017) zur Verfügung stehen und an einem Tag wie gestern bspw. über 7 Mio Aktien gehandelt werden. Irgend etwas ist da faul. Wahrscheinlich ist Marktmanipulation häufiger als der Kleinanleger denkt. Nur ist die Lage nicht immer so eindeutig, dass auch wir Kleinen darauf aufmerksam werden.
"nacked shorts halte ich eigentlich fuer nicht moeglich"
...failed to deliver von nackten Leerverkäufen ist meine einzige Erklärung für die kuriose Situation, dass die Instis über 46 Mio Aktien halten, nur 43,377,381 Aktien (April 27, 2017) zur Verfügung stehen und an einem Tag wie gestern bspw. über 7 Mio Aktien gehandelt werden. Irgend etwas ist da faul. Wahrscheinlich ist Marktmanipulation häufiger als der Kleinanleger denkt. Nur ist die Lage nicht immer so eindeutig, dass auch wir Kleinen darauf aufmerksam werden.
Antwort auf Beitrag Nr.: 54.997.386 von bonDiacomova am 23.05.17 06:42:41
hab mal etwas recherchiert zu "naked short selling" und hab folgendes bei der SEC gefunden:https://www.sec.gov/help/foiadocsfailsdatahtm.html
öffnet man bspw. die beiden zip-Dateien für den April
April 2017, first half
April 2017, second half
und sucht nach dem Symbol von Radius Health, nämlich RDUS, erhält man die im April "nackt" verkauften RDUS-Aktien, ohne die Papiere im Anschluss an den Verkauf zu liefern - "failed to deliver":
3.4. 1175
4.4. 7
5.4. 33428
6.4. 1419
7.4. 231
10.4. 12202
11.4. 5810
12.4. 3197
13.4. 5576
18.4. 556
19.4. 167
20.4. 1692
21.4. 1651
24.4. 1195
25.4. 12358
26.4. 9021
28.4. 1621
Das sind im April immerhin insgesamt ca. 90.000 Aktien, die leer verkauft wurden ohne dass jemals die "Papiere" geliefert wurden. Das ist doch der Hammer - oder nicht?
Zitat von bonDiacomova: da es wirklich ungewoehnlich ist mit den Institutional Ownership 106.77%
habe ich ein paar vips auf w : o angeschrieben... keine erklaerung
ausser dass die angaben auf nasdaq seite eigentlich stimmen...
habe auch mit diesen angaben verglichen :
http://investors.morningstar.com/ownership/shareholders-majo…
komme auf "keine loesung" und habe nasdaq angeschrieben.
deine idee : insti verleiht an shortie - der verkauft wieder an einen insti
kann natuerlich sein was short interest 8 mil angeht...aber 8 mil alle an instis
und dann auch noch der rege "allltagshandel" an der boeres - wie z.b. gestern
(nacked shorts halte ich eigentlich fuer nicht moeglich
weil die muessten normalerweise ""schneller gedeckt werden""
als die mitteilungsfrist ( meist Q ende ) der insties fuer die nasdaq seite ....)
mfg
hab mal etwas recherchiert zu "naked short selling" und hab folgendes bei der SEC gefunden:https://www.sec.gov/help/foiadocsfailsdatahtm.html
öffnet man bspw. die beiden zip-Dateien für den April
April 2017, first half
April 2017, second half
und sucht nach dem Symbol von Radius Health, nämlich RDUS, erhält man die im April "nackt" verkauften RDUS-Aktien, ohne die Papiere im Anschluss an den Verkauf zu liefern - "failed to deliver":
3.4. 1175
4.4. 7
5.4. 33428
6.4. 1419
7.4. 231
10.4. 12202
11.4. 5810
12.4. 3197
13.4. 5576
18.4. 556
19.4. 167
20.4. 1692
21.4. 1651
24.4. 1195
25.4. 12358
26.4. 9021
28.4. 1621
Das sind im April immerhin insgesamt ca. 90.000 Aktien, die leer verkauft wurden ohne dass jemals die "Papiere" geliefert wurden. Das ist doch der Hammer - oder nicht?
BMO $AMGN lowering price target to $198 from $200 after probability-adjusting romosozumab rev in model (50%,previously not risk-adjusted).
BMO Capital lowered its price target on Amgen (NASDAQ: AMGN) to $198.00 (from $200.00) while maintaining a Outperform rating, following release of Phase 3 trial testing Romosozumab data.
https://www.streetinsider.com/Analyst+Comments/Amgen+%28AMGN…
AMGN "Shares Outstanding": 735.4 Mio Aktien
Durch die Schwierigkeitenbei Romosozumab senkt BMO Capital das Kursziel für Amgen um $2, also 735.4 *2 = 1.4708 Milliarden USD
Im Gegensatz dazu wird RDUS gegenüber vorgestern um ca. 90 Mio USD höher bewertet.
Irgendwo ist diese Rechnung nicht im Gleichgewicht.
Bin gespannt wie lange es dauert, bis die Kursziele von RDUS nach oben korrigiert werden. Hilfreich hierfür wäre das Fernbleiben eines neuen Signals bei den Nebenwirkungen in ACTIVExtend. Die Veröffentlichung der Ergebnisse nach 24 Monaten soll noch im 2q17 erfolgen, also spätestens Ende Juni.
Sollten keine neuen Signale hinzukommen, müsste es mit dem Aktienkurs endlich nachhaltig nach oben gehen.
BMO Capital lowered its price target on Amgen (NASDAQ: AMGN) to $198.00 (from $200.00) while maintaining a Outperform rating, following release of Phase 3 trial testing Romosozumab data.
https://www.streetinsider.com/Analyst+Comments/Amgen+%28AMGN…
AMGN "Shares Outstanding": 735.4 Mio Aktien
Durch die Schwierigkeitenbei Romosozumab senkt BMO Capital das Kursziel für Amgen um $2, also 735.4 *2 = 1.4708 Milliarden USD
Im Gegensatz dazu wird RDUS gegenüber vorgestern um ca. 90 Mio USD höher bewertet.
Irgendwo ist diese Rechnung nicht im Gleichgewicht.
Bin gespannt wie lange es dauert, bis die Kursziele von RDUS nach oben korrigiert werden. Hilfreich hierfür wäre das Fernbleiben eines neuen Signals bei den Nebenwirkungen in ACTIVExtend. Die Veröffentlichung der Ergebnisse nach 24 Monaten soll noch im 2q17 erfolgen, also spätestens Ende Juni.
Sollten keine neuen Signale hinzukommen, müsste es mit dem Aktienkurs endlich nachhaltig nach oben gehen.
Antwort auf Beitrag Nr.: 55.003.020 von Cyberhexe am 23.05.17 18:56:37
zitat :
öffnet man bspw. die beiden zip-Dateien für den April
zitat ende
mein lieber schollie was fuer dateien - ne echte arbeit !
dateien - ne echte arbeit !
die RDUS daten heraus zu filtern - respekt
ja - ich finde es auch ""hammer"" dass das ueberhaupt noch moeglich ist
nacked shorts gehoeren nicht nur m.a.n. verboten.
jedoch die stueckzahl von ca. 90000 im monat april
deuten fuer mich in die richtung dass nacked shorts als erklaerung allein
fuer die 106 % ownership und den taeglichen handel m.e. nicht ausreichen.
ueber 3 millionen shares ""ueberhang"" ownership - dazu ein freefloat von ang. einigen millionen
schaun mer mal ob die nasdaq mit ner erklaerung antwortet.
mfg
mein lieber schollie
da haste aber einen link gefunden - sauberzitat :
öffnet man bspw. die beiden zip-Dateien für den April
zitat ende
mein lieber schollie was fuer
 dateien - ne echte arbeit !
dateien - ne echte arbeit !die RDUS daten heraus zu filtern - respekt
ja - ich finde es auch ""hammer"" dass das ueberhaupt noch moeglich ist
nacked shorts gehoeren nicht nur m.a.n. verboten.
jedoch die stueckzahl von ca. 90000 im monat april
deuten fuer mich in die richtung dass nacked shorts als erklaerung allein
fuer die 106 % ownership und den taeglichen handel m.e. nicht ausreichen.
ueber 3 millionen shares ""ueberhang"" ownership - dazu ein freefloat von ang. einigen millionen
schaun mer mal ob die nasdaq mit ner erklaerung antwortet.
mfg
Antwort auf Beitrag Nr.: 55.005.276 von bonDiacomova am 24.05.17 07:19:19Radius Health short interest laut nasdaq.com per 15.05.2017 sogar bei über 10 Mio. Stück.
Antwort auf Beitrag Nr.: 55.012.800 von frank-p am 24.05.17 23:30:46
Institutional Ownership 100.77%
178 Institutional Holders
43,709,854 Total Shares Held
immer noch ""zu viel""
schade dass es keine ""naked shorts offen gesamt "" aufstellung gibt
einzig mir bekannte seite
http://nakedshortreport.com/?index=RDUS
der naked shorts anteil am tagesumsatz
gibt m.e. ja nicht an wieviel ""offen"" geblieben sind
da "muesste" man jetzt tag fuer tag die liste in beitrag Beitrag Nr. 263
von cyberhexe durchgehen...too much - fuer mich ;-)
anstieg
ja - short interest angestiegen um ca. 2 millionen auf 10,237,119 stueckeInstitutional Ownership 100.77%
178 Institutional Holders
43,709,854 Total Shares Held
immer noch ""zu viel""
schade dass es keine ""naked shorts offen gesamt "" aufstellung gibt
einzig mir bekannte seite

http://nakedshortreport.com/?index=RDUS
der naked shorts anteil am tagesumsatz
gibt m.e. ja nicht an wieviel ""offen"" geblieben sind
da "muesste" man jetzt tag fuer tag die liste in beitrag Beitrag Nr. 263
von cyberhexe durchgehen...too much - fuer mich ;-)
vll mal interessant
um zu unterscheiden :short selling :
Normally, when one short sells a stock, their broker will lend them the shares to sell.
The loaned stock will come from the broker's own inventory, from another one
of the firm's customers, or from another brokerage firm.
The shares are sold and the proceeds are credited to the short seller's account.
naked short selling
When a seller "naked short sells a stock" they do not own the shares
they are selling and therefore are selling artificial shares.
This is like counterfeiting a stock. This process creates an obvious unfair advantage to the seller
and an imbalance in the market as the sell side is now increased with more shares - many of which
are counterfeit. There is a time limit on how long the seller can sell these shares
and be naked on the trade and the time limit is 3 days.
http://nakedshortreport.com/what-is-naked-short-selling
mfg
Antwort auf Beitrag Nr.: 54.997.026 von Cyberhexe am 22.05.17 23:45:54
Ergebnisse von ACTIVExtend wurden gestern veröffentlicht:
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=102777…
Alle primären und sekundären Endpunkte wurden mit statistischer Signifikanz erreicht und - GANZ WICHTIG - bei den Nebenwirkungen wurde kein neues Signal beobachtet!
Die Reduzierung des Fraktur-Risikos ist zwar gegenüber dem Zwischenergebnis zurück gegangen ( ich hatte auf noch bessere Ergebnisse gehofft!), bei intensiver Nachdenke ist eine tendenzielle Annäherung der beiden Arme über die Zeit erklärbar, da alle Patienten im Anschluss an --> ACTIVE mit dem Biophosphonat Alendronat --> ACTIVExtend behandelt wurden:
"In ACTIVExtend, patients who had completed 18 months of TYMLOS (abaloparatide) injections or placebo in the ACTIVE Phase 3 trial were transitioned to receive 24 additional months of open-label alendronate."
Alle Endpunkte wurden
Zitat von Cyberhexe: Ein ganz wichtiges Ereignis wird die Bekanntgabe der Ergebnisse nach 24 Monaten von ACTIVExtend, die auf das 2. Quartal in 2017 angekündigt sind. Es ist von besonderer Bedeutung, dass bei den Nebenwirkungen nicht ein unverhofftes Signal wie bei Romosozumab "auftaucht":
Zusammenfassung Romosozumab:
Daten nach 12 Monaten Romosozumab und 12 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend:
"50 percent reduction in the relative risk of a new vertebral (spine) fracture"
Frakturen nicht die Wirbelsäule betreffend:
"non-vertebral fractures were statistically significantly reduced by 19 percent"
alle klinisch bedeutenden Frakturen:
"27 percent reduction in the relative risk of clinical fracture (non-vertebral fracture and clinical vertebral fracture)"
Zusammenfassung Abaloparatide:
Daten nach 12 Monaten Romosozumab und 6 Monaten Ergänzung mit Alendronat
Frakturen die Wirbelsäule betreffend:
"significantly greater reduction of 87% in the incidence of newvertebral fractures (p < 0.001)"
Frakturen nicht die Wirbelsäule betreffend:
"52% in nonvertebral fractures (p = 0.02) 52% in nonvertebral fractures (p = 0.02) "
alle klinisch bedeutenden Frakturen:
"58% in major osteoporotic fractures (p<0.01)"
Ergebnisse von ACTIVExtend wurden gestern veröffentlicht:
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=102777…
Alle primären und sekundären Endpunkte wurden mit statistischer Signifikanz erreicht und - GANZ WICHTIG - bei den Nebenwirkungen wurde kein neues Signal beobachtet!
Die Reduzierung des Fraktur-Risikos ist zwar gegenüber dem Zwischenergebnis zurück gegangen ( ich hatte auf noch bessere Ergebnisse gehofft!), bei intensiver Nachdenke ist eine tendenzielle Annäherung der beiden Arme über die Zeit erklärbar, da alle Patienten im Anschluss an --> ACTIVE mit dem Biophosphonat Alendronat --> ACTIVExtend behandelt wurden:
"In ACTIVExtend, patients who had completed 18 months of TYMLOS (abaloparatide) injections or placebo in the ACTIVE Phase 3 trial were transitioned to receive 24 additional months of open-label alendronate."
Alle Endpunkte wurden
Antwort auf Beitrag Nr.: 55.012.800 von frank-p am 24.05.17 23:30:46
klar ist, dass die Leerverkäufe den Kurs trotz nachhaltig positiver Nachrichtenlage tief halten - unklar ist für mich weshalb? Haben wir etwas übersehen?
Es kann mit weiterhin guten Nachrichten gerechnet werden, nämlich:
- auf ASCO17 ph1-Ergebnisse zu RAD1901
http://abstracts.asco.org/199/AbstView_199_192812.html
- bis Ende Juni (2q17) Treffen mit der FDA zur Planung der ph2-Studie mit Elacestrant (RAD1901)
- Bekanntgabe der Empfehlung des europ. Arzneimittelausschusses CHMP über die Zulassung von Abaloparatide in Europa auf dessen JULI- Sitzung:
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
- 67 Tage nach der Zulassungsempfehlung des CHMP --> also gegen Ende September: endgültige Zulassungsentscheidung der Europäischen Kommission (EC)
- Ende September: Bekanntgabe des Kooperationspartners für Europa und Markteinführung von Abaloparatide in der EU
- 2. Hälfte 2017: "Entry into human" also Initialisierung einer ph1-Studie mit RAD140 in HR+ (Hormon-Rezeptor positiv) Brustkrebs
Zitat von frank-p: Radius Health short interest laut nasdaq.com per 15.05.2017 sogar bei über 10 Mio. Stück.
klar ist, dass die Leerverkäufe den Kurs trotz nachhaltig positiver Nachrichtenlage tief halten - unklar ist für mich weshalb? Haben wir etwas übersehen?
Es kann mit weiterhin guten Nachrichten gerechnet werden, nämlich:
- auf ASCO17 ph1-Ergebnisse zu RAD1901
http://abstracts.asco.org/199/AbstView_199_192812.html
- bis Ende Juni (2q17) Treffen mit der FDA zur Planung der ph2-Studie mit Elacestrant (RAD1901)
- Bekanntgabe der Empfehlung des europ. Arzneimittelausschusses CHMP über die Zulassung von Abaloparatide in Europa auf dessen JULI- Sitzung:
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
- 67 Tage nach der Zulassungsempfehlung des CHMP --> also gegen Ende September: endgültige Zulassungsentscheidung der Europäischen Kommission (EC)
- Ende September: Bekanntgabe des Kooperationspartners für Europa und Markteinführung von Abaloparatide in der EU
- 2. Hälfte 2017: "Entry into human" also Initialisierung einer ph1-Studie mit RAD140 in HR+ (Hormon-Rezeptor positiv) Brustkrebs
@ Cyberhexe
Romosozumab (12 Mon + 12 Mon Alendronate) gegen 24 Mon Alendronate
50% / 19% / 27% Reduktion der verschiedenen Frakturen bei Romosozumab
Abaloparatide (18 Mon + 6 Mon Alendronate) gegen 18 Mon Plazebo + 6 Mon Alendronate
87% / 52% / 58% Reduktion der verschiedenen Frakturen unter Abaloparatide
Abaloparatide (18 Mon + 24 Mon Alendronate) gegen 18 Mon Plazebo + 24 Mon Alendronate
84% / 39% / 50% Reduktion der verschiedenen Frakturen unter Abaloparatide
Bei Deiner Gegenüberstellung wurde Romosozumab gegen Wirkstoff Alendronate getestet, während
Abaloparatide gegen Plazebo getestet wurde. Stimmt das?
Des Weiteren unterscheiden sich die Zeiträume.
Dann wären die Datensätze nicht vergleichbar.
Aufgrund der Probleme bei Romosozumab ist es aber für RDUS erstmal nicht so relevant.
Romosozumab (12 Mon + 12 Mon Alendronate) gegen 24 Mon Alendronate
50% / 19% / 27% Reduktion der verschiedenen Frakturen bei Romosozumab
Abaloparatide (18 Mon + 6 Mon Alendronate) gegen 18 Mon Plazebo + 6 Mon Alendronate
87% / 52% / 58% Reduktion der verschiedenen Frakturen unter Abaloparatide
Abaloparatide (18 Mon + 24 Mon Alendronate) gegen 18 Mon Plazebo + 24 Mon Alendronate
84% / 39% / 50% Reduktion der verschiedenen Frakturen unter Abaloparatide
Bei Deiner Gegenüberstellung wurde Romosozumab gegen Wirkstoff Alendronate getestet, während
Abaloparatide gegen Plazebo getestet wurde. Stimmt das?
Des Weiteren unterscheiden sich die Zeiträume.
Dann wären die Datensätze nicht vergleichbar.
Aufgrund der Probleme bei Romosozumab ist es aber für RDUS erstmal nicht so relevant.
Antwort auf Beitrag Nr.: 55.019.454 von Nase_weis_nix am 26.05.17 06:07:18
...natürlich hast du recht, sofern keine face-to-face-Studie vorliegt, ist ein Vergleich immer unter Vorbehalt zu betrachten.
In erster Linie muss sich Abaloparatide jedoch dem Wettbewerb mit den hormonanalogen Wirkstoffen, also Teriparatide, stellen und da ist Abaloparatide face-to-face eindeutig im Vorteil.
Das Kursziel von Maxim Group mit USD24 ist mE lächerlich. Vielleicht liege ich falsch, aber ich bin mir ziemlich sicher, dass die Markteinführung von TYMLOS die Prognosen des einen oder anderen Analysten übertreffen wird.
Radius Health Inc (RDUS) Given a $24.00 Price Target by Maxim Group Analysts
Posted by Lucas Kauffman on May 26th, 2017 // No Comments
Radius Health logoRadius Health Inc (NASDAQ:RDUS) has been assigned a $24.00 price objective by analysts at Maxim Group in a research note issued on Wednesday. The brokerage currently has a “sell” rating on the biopharmaceutical company’s stock. Maxim Group’s price target would indicate a potential downside of 33.70% from the company’s current price.
A number of other research analysts also recently commented on RDUS. Cantor Fitzgerald set a $65.00 target price on Radius Health and gave the company a “buy” rating in a research note on Monday. JPMorgan Chase & Co. restated a “buy” rating on shares of Radius Health in a research note on Saturday, March 11th. HC Wainwright restated a “buy” rating and issued a $63.00 target price on shares of Radius Health in a research note on Monday, May 15th. Canaccord Genuity set a $85.00 target price on Radius Health and gave the company a “buy” rating in a research note on Saturday, March 11th. Finally, Zacks Investment Research upgraded Radius Health from a “sell” rating to a “hold” rating in a research note on Tuesday, February 28th. One research analyst has rated the stock with a sell rating, three have given a hold rating and four have given a buy rating to the stock. The company presently has a consensus rating of “Hold” and an average price target of $56.83.
...natürlich hast du recht, sofern keine face-to-face-Studie vorliegt, ist ein Vergleich immer unter Vorbehalt zu betrachten.
In erster Linie muss sich Abaloparatide jedoch dem Wettbewerb mit den hormonanalogen Wirkstoffen, also Teriparatide, stellen und da ist Abaloparatide face-to-face eindeutig im Vorteil.
Das Kursziel von Maxim Group mit USD24 ist mE lächerlich. Vielleicht liege ich falsch, aber ich bin mir ziemlich sicher, dass die Markteinführung von TYMLOS die Prognosen des einen oder anderen Analysten übertreffen wird.
Radius Health Inc (RDUS) Given a $24.00 Price Target by Maxim Group Analysts
Posted by Lucas Kauffman on May 26th, 2017 // No Comments
Radius Health logoRadius Health Inc (NASDAQ:RDUS) has been assigned a $24.00 price objective by analysts at Maxim Group in a research note issued on Wednesday. The brokerage currently has a “sell” rating on the biopharmaceutical company’s stock. Maxim Group’s price target would indicate a potential downside of 33.70% from the company’s current price.
A number of other research analysts also recently commented on RDUS. Cantor Fitzgerald set a $65.00 target price on Radius Health and gave the company a “buy” rating in a research note on Monday. JPMorgan Chase & Co. restated a “buy” rating on shares of Radius Health in a research note on Saturday, March 11th. HC Wainwright restated a “buy” rating and issued a $63.00 target price on shares of Radius Health in a research note on Monday, May 15th. Canaccord Genuity set a $85.00 target price on Radius Health and gave the company a “buy” rating in a research note on Saturday, March 11th. Finally, Zacks Investment Research upgraded Radius Health from a “sell” rating to a “hold” rating in a research note on Tuesday, February 28th. One research analyst has rated the stock with a sell rating, three have given a hold rating and four have given a buy rating to the stock. The company presently has a consensus rating of “Hold” and an average price target of $56.83.
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
Symbol: RDUS
Availability: 250'000
Exchanges: NASDAQ
aktuell sind 250.000 Aktien von Radius Health "shortable"
Symbol: RDUS
Availability: 250'000
Exchanges: NASDAQ
aktuell sind 250.000 Aktien von Radius Health "shortable"
Antwort auf Beitrag Nr.: 55.046.044 von Cyberhexe am 30.05.17 23:47:32
....und wieder 2 neue Pflichtmitteilungen von BB Biotech über den Kauf von Anteilen bei Radius Health und zwar
1.) mitgeteilt am 30.5.17 --> den Kauf von 40´000 Aktien am 25.5.17 zu $36.2505
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
2.) mitgeteilt am 31.5.17 --> den Kauf von 40´000 Aktien am 30.5.17 zu $34.2087 http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
aktuell sind nur noch 100´000 Aktien "shortable"!
1.6.2017
Symbol: RDUS
Availability: 100'000
Exchanges: NASDAQ
Zitat von Cyberhexe: https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
Symbol: RDUS
Availability: 250'000
Exchanges: NASDAQ
aktuell sind 250.000 Aktien von Radius Health "shortable"
....und wieder 2 neue Pflichtmitteilungen von BB Biotech über den Kauf von Anteilen bei Radius Health und zwar
1.) mitgeteilt am 30.5.17 --> den Kauf von 40´000 Aktien am 25.5.17 zu $36.2505
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
2.) mitgeteilt am 31.5.17 --> den Kauf von 40´000 Aktien am 30.5.17 zu $34.2087 http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-1…
aktuell sind nur noch 100´000 Aktien "shortable"!
1.6.2017
Symbol: RDUS
Availability: 100'000
Exchanges: NASDAQ
Antwort auf Beitrag Nr.: 55.054.969 von Cyberhexe am 01.06.17 07:46:26
BB Biotech AG kauft weitere Anteile an Radius Health
Shared Voting Power 1.6.2017:
5,217,322 (1)
http://ir.radiuspharm.com/secfiling.cfm?filingID=1193125-17-…
am 31.5.17 5038799
BB Biotech AG kauft weitere Anteile an Radius Health
Shared Voting Power 1.6.2017:
5,217,322 (1)
http://ir.radiuspharm.com/secfiling.cfm?filingID=1193125-17-…
am 31.5.17 5038799
Radius Presents Positive Data From A Fully Enrolled Ongoing Phase I Study for Investigational Drug Elacestrant (RAD1901) at the 2017 American Society of Clinical Oncology Annual Meeting (ASCO)
-Elacestrant single agent Objective Response Rate (ORR) was 23% in heavily pre-treated patients with advanced ER+ breast cancer at the cut off date of April 28, 2017-
-In the 400 mg patient group with mature data, median PFS was 4.5 months and Clinical Benefit Rate at 24 weeks was 42%-
-38% of these patients previously received fulvestrant; 40% received palbociclib or another CDK inhibitor; 50% had an ESR1 mutation-
-15 of the 40 patients remain on treatment as of the cutoff date-
-Investor Webcast today at 7 pm CT-
WALTHAM, Mass., June 04, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a fully integrated science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced positive data from a fully enrolled ongoing Phase 1 study of elacestrant (RAD1901), an oral selective estrogen receptor degrader (SERD), in patients with estrogen receptor positive (ER+) breast cancer. These data were presented this morning at the 2017 American Society of Clinical Oncology Meeting in Chicago, Illinois.
As of the cut-off date of April 28, 2017, 40 patients have been treated in the fully enrolled elacestrant Phase I dose escalation and expansion cohorts at the 400 mg dose. These patients are all heavily pretreated ER+, HER2-negative advanced breast cancer patients who have received a median of 3 prior lines of systemic therapy and have evaluable advanced or metastatic disease. Of the enrolled patients, 22 patients met the RECIST measurable disease criteria at baseline and there were five confirmed partial responses in this group. Elacestrant was well-tolerated with the most common adverse events being low grade nausea and dyspepsia.
"While still early, the single-agent clinical activity and safety profile demonstrated with elacestrant in this heavily pretreated advanced hormone receptor positive breast cancer patient population is encouraging when compared to the results shown for other agents in a similar setting," said Dr. Aditya Bardia, Director of Precision Medicine and attending physician at Center for Breast Cancer, Massachusetts General Hospital Cancer Center, Harvard Medical School, Boston, MA. "This is important for patients because it could potentially offer another endocrine therapy option even upon progression on standard endocrine therapy and could potentially delay the use of toxic chemotherapy, which is a meaningful clinical goal, and additional studies are needed."
On June 4, 2017, at the 2017 ASCO Annual Meeting, the following abstract was presented as a poster and will be included in the Poster Discussion Session later today: Abstract 1014
"Evaluation of Elacestrant (RAD1901), a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer" Abstract 1014, 8:00 AM - 11:30 AM, Hall A, Poster Board #6, POSTER SESSION, Breast Cancer-Metastatic
Discussed at the Poster Discussion Session, 4:45 PM - 6:00 PM, Hall B1, Aditya Bardia, MD, MPH - First Author, Massachusetts General Hospital Cancer Center and Harvard Medical School
....das ist doch ein sehr viel versprechendes Ergebnis, zumal Elacestrant wohl nicht als "Single agent" sonder in Kombination mit anderen Wirkstoffen verabreicht werden dürfte.
Gruss aus SSF....bin voll im Jetlag (Ortszeit 01:33)
-Elacestrant single agent Objective Response Rate (ORR) was 23% in heavily pre-treated patients with advanced ER+ breast cancer at the cut off date of April 28, 2017-
-In the 400 mg patient group with mature data, median PFS was 4.5 months and Clinical Benefit Rate at 24 weeks was 42%-
-38% of these patients previously received fulvestrant; 40% received palbociclib or another CDK inhibitor; 50% had an ESR1 mutation-
-15 of the 40 patients remain on treatment as of the cutoff date-
-Investor Webcast today at 7 pm CT-
WALTHAM, Mass., June 04, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS), a fully integrated science-driven biopharmaceutical company that is committed to developing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced positive data from a fully enrolled ongoing Phase 1 study of elacestrant (RAD1901), an oral selective estrogen receptor degrader (SERD), in patients with estrogen receptor positive (ER+) breast cancer. These data were presented this morning at the 2017 American Society of Clinical Oncology Meeting in Chicago, Illinois.
As of the cut-off date of April 28, 2017, 40 patients have been treated in the fully enrolled elacestrant Phase I dose escalation and expansion cohorts at the 400 mg dose. These patients are all heavily pretreated ER+, HER2-negative advanced breast cancer patients who have received a median of 3 prior lines of systemic therapy and have evaluable advanced or metastatic disease. Of the enrolled patients, 22 patients met the RECIST measurable disease criteria at baseline and there were five confirmed partial responses in this group. Elacestrant was well-tolerated with the most common adverse events being low grade nausea and dyspepsia.
"While still early, the single-agent clinical activity and safety profile demonstrated with elacestrant in this heavily pretreated advanced hormone receptor positive breast cancer patient population is encouraging when compared to the results shown for other agents in a similar setting," said Dr. Aditya Bardia, Director of Precision Medicine and attending physician at Center for Breast Cancer, Massachusetts General Hospital Cancer Center, Harvard Medical School, Boston, MA. "This is important for patients because it could potentially offer another endocrine therapy option even upon progression on standard endocrine therapy and could potentially delay the use of toxic chemotherapy, which is a meaningful clinical goal, and additional studies are needed."
On June 4, 2017, at the 2017 ASCO Annual Meeting, the following abstract was presented as a poster and will be included in the Poster Discussion Session later today: Abstract 1014
"Evaluation of Elacestrant (RAD1901), a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer" Abstract 1014, 8:00 AM - 11:30 AM, Hall A, Poster Board #6, POSTER SESSION, Breast Cancer-Metastatic
Discussed at the Poster Discussion Session, 4:45 PM - 6:00 PM, Hall B1, Aditya Bardia, MD, MPH - First Author, Massachusetts General Hospital Cancer Center and Harvard Medical School
....das ist doch ein sehr viel versprechendes Ergebnis, zumal Elacestrant wohl nicht als "Single agent" sonder in Kombination mit anderen Wirkstoffen verabreicht werden dürfte.
Gruss aus SSF....bin voll im Jetlag (Ortszeit 01:33)
ausserordentlich viel versprechend die ersten Ergebnisse zu Elacestrant
http://ir.radiuspharm.com/events.cfm

Gruss vom Pazifik - unweit von SF:
Morgen bei Exelixis!
http://ir.radiuspharm.com/events.cfm

Gruss vom Pazifik - unweit von SF:

Morgen bei Exelixis!
Antwort auf Beitrag Nr.: 54.853.138 von Ville7 am 03.05.17 11:00:57
...dann warten wirs doch mal ab, ob diese Firma wirklich zu viel versprochen hat:

...übrigens ab Morgen bei EXELixis!
Zitat von Ville7: Zu RDUS nur noch so viel:
1. Dass ein großer Investor drin sitzt und ständig nachkauft hat nicht unbedingt damit zu tun, dass er weiterhin extrem überzeugt ist, sondern dient auch dem Schutz der eigenen Positionierung. Diese Positionierung kann sich für ihn auch als Fehlpositionierung herausstellen. Dann ist so einer wie BBBiotech schnell auch massiv draussen. Ich erinnere an Bavarian Nordic, wo ein Ausstieg von BBBiotech die Aktie von über 200 DKK auf unter 40 DKK gebracht hat (heute übrigens 375 DKK).
2. Man sollte nicht alles was die Firma von sich gibt unreflektiert nachbabbeln, so wie das Cyberhexe leider macht. Jede Firma verfolgt mit ihrer Info-Politik bestimmte Ziele. Und bei RDUS ist die Kommunikation immer derart, dass man nicht besonders realistisch kommuniziert, sondern immer einen ziemlichen Positiv-bias drin hat. Ich erinnere nur an den Satz "greatest value unpartnered asset in the biotech industry", der zu jedem CC verwendet wurde. Oder die großspurige Ankündigung der RAD-1901 Daten, die der Markt nach Veröffentlichung ganz anders gesehen hat. Die Börse hasst solche Firmen, die ständig overpromises machen und underdelivern. Bei RDUS kommt der Stein der Wahrheit dann mit den künftigen Verkäufen....
...dann warten wirs doch mal ab, ob diese Firma wirklich zu viel versprochen hat:

...übrigens ab Morgen bei EXELixis!
schoene kursentwicklung gestern
bzw nach der asco...hier eine laenderkuerzel seite http://www.bu-on.de/internet/laendkrz.htm
kein SF

Antwort auf Beitrag Nr.: 55.084.729 von bonDiacomova am 06.06.17 06:18:40
SF = San Francisco
SSF = South San Francisco
Address: 210 E Grand Ave, South San Francisco, CA 94080
--> Exelixis
Werde spätestens am Do ein paar Bilder vom Exelixis-Campus reinstellen.
Zitat von bonDiacomova: bzw nach der asco...
hier eine laenderkuerzel seite http://www.bu-on.de/internet/laendkrz.htm
kein SF
SF = San Francisco
SSF = South San Francisco
Address: 210 E Grand Ave, South San Francisco, CA 94080
--> Exelixis
Werde spätestens am Do ein paar Bilder vom Exelixis-Campus reinstellen.
Antwort auf Beitrag Nr.: 55.054.969 von Cyberhexe am 01.06.17 07:46:26
aktuell sind nur 75´000 Aktien "shortable"!
Symbol: RDUS
Availability: 75'000
Exchanges: NASDAQ
Zitat von Cyberhexe: https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
aktuell sind nur noch 100´000 Aktien "shortable"!
1.6.2017
Symbol: RDUS
Availability: 100'000
Exchanges: NASDAQ
aktuell sind nur 75´000 Aktien "shortable"!
Symbol: RDUS
Availability: 75'000
Exchanges: NASDAQ
Antwort auf Beitrag Nr.: 55.087.765 von Cyberhexe am 06.06.17 14:01:04Die Shorties bekommen keine Aktien mehr angeboten, da aktuell --> "Shortable Stocks for United States":
Symbol: RDUS
Availability: 10'000
Exchanges: NASDAQ
dann wird wohl naked short selling vermehrt stattfinden. Auf alle Fälle scheinen die Shorties noch nicht aufzugeben.
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
Symbol: RDUS
Availability: 10'000
Exchanges: NASDAQ
dann wird wohl naked short selling vermehrt stattfinden. Auf alle Fälle scheinen die Shorties noch nicht aufzugeben.
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…

"FDA meeting scheduled for Ph2 study for elacestrant Q2'17" --> also noch im Juni 2017!
da die ph1 bereits verhältnismässig mächtig war, habe ich die Hoffnung, dass bereits in Phase 2 eine erste Pivotalstudie von der FDA gutgeheissen wird. Warten wirs ab.
Antwort auf Beitrag Nr.: 55.100.617 von Cyberhexe am 08.06.17 01:29:06
Aus meiner Sicht wäre es von Vorteil, wenn Elacestrant in Ph2 nicht in Monotherapie sondern in Kombination mit einem aneren Wirkstoff getestet würde, beispw. wäre ein mögliches Studiendesign:
elacestrant+palbociclib gegen fulvestrant+palbociclib zu testen.
Diese Kombi zur Behandlung von "hormone receptor–positive, human epidermal growth factor receptor 2 (HER2)–negative advanced or metastatic breast cancer" mit fortschreitender Erkrankung im Anschluss an eine Hormontherapie wurde Anfang 2016 von der FDA zugelassen:
"On February 19, 2016, the U.S. Food and Drug Administration approved palbociclib (Ibrance) in combination with fulvestrant for the treatment of women with hormone receptor–positive, human epidermal growth factor receptor 2 (HER2)–negative advanced or metastatic breast cancer with disease progression following endocrine therapy.
The study demonstrated an improvement in progression-free survival with a hazard ratio of 0.46 (95% confidence interval [CI] = 0.36–0.59, P < .0001). The median progression-free survival was 9.5 months vs 4.6 months for patients treated in the palbociclib-plus-fulvestrant and placebo-plus-fulvestrant arms, respectively.
The most frequently reported serious adverse reactions in patients receiving palbociclib plus fulvestrant were infections, pyrexia, neutropenia, and pulmonary embolism. Dose reductions due to an adverse reaction of any grade occurred in 36% of patients and permanent discontinuation associated with an adverse reaction occurred in 6% of patients."
http://www.ascopost.com/News/36319
Zitat von Cyberhexe:
"FDA meeting scheduled for Ph2 study for elacestrant Q2'17" --> also noch im Juni 2017!
da die ph1 bereits verhältnismässig mächtig war, habe ich die Hoffnung, dass bereits in Phase 2 eine erste Pivotalstudie von der FDA gutgeheissen wird. Warten wirs ab.
Aus meiner Sicht wäre es von Vorteil, wenn Elacestrant in Ph2 nicht in Monotherapie sondern in Kombination mit einem aneren Wirkstoff getestet würde, beispw. wäre ein mögliches Studiendesign:
elacestrant+palbociclib gegen fulvestrant+palbociclib zu testen.
Diese Kombi zur Behandlung von "hormone receptor–positive, human epidermal growth factor receptor 2 (HER2)–negative advanced or metastatic breast cancer" mit fortschreitender Erkrankung im Anschluss an eine Hormontherapie wurde Anfang 2016 von der FDA zugelassen:
"On February 19, 2016, the U.S. Food and Drug Administration approved palbociclib (Ibrance) in combination with fulvestrant for the treatment of women with hormone receptor–positive, human epidermal growth factor receptor 2 (HER2)–negative advanced or metastatic breast cancer with disease progression following endocrine therapy.
The study demonstrated an improvement in progression-free survival with a hazard ratio of 0.46 (95% confidence interval [CI] = 0.36–0.59, P < .0001). The median progression-free survival was 9.5 months vs 4.6 months for patients treated in the palbociclib-plus-fulvestrant and placebo-plus-fulvestrant arms, respectively.
The most frequently reported serious adverse reactions in patients receiving palbociclib plus fulvestrant were infections, pyrexia, neutropenia, and pulmonary embolism. Dose reductions due to an adverse reaction of any grade occurred in 36% of patients and permanent discontinuation associated with an adverse reaction occurred in 6% of patients."
http://www.ascopost.com/News/36319
gute Presse:
http://www.bizjournals.com/boston/news/2017/06/06/bluebird-a…
Radius Health: Waltham-based Radius (Nasdaq: RDUS) announced data from an ongoing Phase 1 study of a breast cancer drug in heavily pretreated patients. According to the company, five of 22 patients who met a certain baseline level of disease responded to the drug, with no major side effects — results that the author of the study abstract called “encouraging when compared to the results shown for other agents in a similar setting.” Shares of Radius jumped more than 10 percent on the news.
http://www.bizjournals.com/boston/news/2017/06/06/bluebird-a…
Radius Health: Waltham-based Radius (Nasdaq: RDUS) announced data from an ongoing Phase 1 study of a breast cancer drug in heavily pretreated patients. According to the company, five of 22 patients who met a certain baseline level of disease responded to the drug, with no major side effects — results that the author of the study abstract called “encouraging when compared to the results shown for other agents in a similar setting.” Shares of Radius jumped more than 10 percent on the news.
Harte Fakten:
Seit Threaderöffnung vor gut einem Jahr notiert die Aktie weiterhin leicht im Minus. Aus dieser Perspektive bisher kein guter Investmenttipp.
Antwort auf Beitrag Nr.: 55.124.471 von Ville7 am 12.06.17 14:00:40Heute ist Hexenjagd angesagt, scheint mir ....
Antwort auf Beitrag Nr.: 55.126.112 von watchingtheflood am 12.06.17 17:32:05Nein. Lediglich ein Fakten- und Investmenthypothesen-Check. Sollte doch erlaubt sein, oder?
Antwort auf Beitrag Nr.: 55.124.471 von Ville7 am 12.06.17 14:00:40
schon wieder falsch...seit Threaderöffnung ist die Aktie (in USD) leicht im Plus - knapp USD39 gegenüber knapp USD36. Bei Exelixis war das übrigens nicht so. Dort war das Tal der Tränen tatsächlich etwas tiefer. Aber ich denke, dass bei Radius Health die sehr guten Tage nicht mehr fern sind. Bin gespannt, wer dann wieder auf dem Trittbrett steht?
Zitat von Ville7: Seit Threaderöffnung vor gut einem Jahr notiert die Aktie weiterhin leicht im Minus. Aus dieser Perspektive bisher kein guter Investmenttipp.
schon wieder falsch...seit Threaderöffnung ist die Aktie (in USD) leicht im Plus - knapp USD39 gegenüber knapp USD36. Bei Exelixis war das übrigens nicht so. Dort war das Tal der Tränen tatsächlich etwas tiefer. Aber ich denke, dass bei Radius Health die sehr guten Tage nicht mehr fern sind. Bin gespannt, wer dann wieder auf dem Trittbrett steht?
Antwort auf Beitrag Nr.: 55.128.701 von Cyberhexe am 13.06.17 06:50:45Du solltest wie bei EXEL öfter auf meinem Trittbrett unterwegs sein. Merrimack war ja mal wieder die beste Lachnummer nach was für Kriterien du deine Geldvernichter aussuchst. Auf deinem Trittbrett werde ich bestimmt nie stehen- das fährt nachgewiesenermaßen oft in den Keller.
Antwort auf Beitrag Nr.: 55.133.093 von Ville7 am 13.06.17 18:19:25
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014 Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935) von Franca_ole am11.11.15 um 09:00:03 die folgenden Sätze" "Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen"."
Diese Ratschläge sind schon sehr beeindruckend, insbesondere jener als Exelixis unter USD2 zu haben war. Ok, hinterher bist auch du schlauer!
Zitat von Ville7: Du solltest wie bei EXEL öfter auf meinem Trittbrett unterwegs sein. Merrimack war ja mal wieder die beste Lachnummer nach was für Kriterien du deine Geldvernichter aussuchst. Auf deinem Trittbrett werde ich bestimmt nie stehen- das fährt nachgewiesenermaßen oft in den Keller.
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014 Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935) von Franca_ole am11.11.15 um 09:00:03 die folgenden Sätze" "Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen"."
Diese Ratschläge sind schon sehr beeindruckend, insbesondere jener als Exelixis unter USD2 zu haben war. Ok, hinterher bist auch du schlauer!

gute Presse für Abaloparatide:
http://www.clinicalpainadvisor.com/rheumatology/fda-approves…
Throughout the phase 3 ACTIVE trial, patients treated with abaloparatide demonstrated “significant reductions in the relative risk of new vertebral and nonvertebral fractures compared [with] placebo,” according to the press release (absolute risk reductions, 3.6% and 2%, respectively).
John Bilezikan, MD, professor of medicine and pharmacology, director of the metabolic bone diseases program at Columbia University Medical Center in New York City, and study investigator, noted that the abaloparatide approval “provides physicians a new treatment option … which could help to rapidly, consistently, and significantly increase bone mineral density and reduce the risk of fractures.”
Abaloparatide may increase patients' risk of osteosarcoma, orthostatic hypotension, hypercalcemia, hyperalciuria, and urolithasis. Additional adverse reactions include dizziness, nausea, palpitations, fatigue, upper abdominal pain, and vertigo. Use for more than 2 years throughout a patient's lifetime is not recommended.
http://www.clinicalpainadvisor.com/rheumatology/fda-approves…
Throughout the phase 3 ACTIVE trial, patients treated with abaloparatide demonstrated “significant reductions in the relative risk of new vertebral and nonvertebral fractures compared [with] placebo,” according to the press release (absolute risk reductions, 3.6% and 2%, respectively).
John Bilezikan, MD, professor of medicine and pharmacology, director of the metabolic bone diseases program at Columbia University Medical Center in New York City, and study investigator, noted that the abaloparatide approval “provides physicians a new treatment option … which could help to rapidly, consistently, and significantly increase bone mineral density and reduce the risk of fractures.”
Abaloparatide may increase patients' risk of osteosarcoma, orthostatic hypotension, hypercalcemia, hyperalciuria, and urolithasis. Additional adverse reactions include dizziness, nausea, palpitations, fatigue, upper abdominal pain, and vertigo. Use for more than 2 years throughout a patient's lifetime is not recommended.
Antwort auf Beitrag Nr.: 55.133.465 von Cyberhexe am 13.06.17 19:07:00Gähn!!! Letzte Antwort, dann verschwindet ich zumindest aus deinen Threads wieder für eine Weile. Du langweilst mich.
Wer mich kennt weiss, dass ich selbst bei meinen größten Investments immer sehr kritisch bleibe und mich nie verliebe. Im Gegensatz zu dir, die ich zur Rasse der gefährlichen Dauerbejubler der eigenen Investments zähle.
Relevant ist zu welchen Kursen man wann kauft - das C/R Verhältnis ist das Entscheidende.
Ein Screenshot aus meinem Depot ist dazu in meinem EXEL Thread zu sehen mit einem EK-Kurs von 1,x (1,25 EUR) für die günstigste Tranche vor Phase 3 Daten. Bei 3.40 vor Phase 3 Daten war das CRV logischerweise schlechter - weil gleiches Risiko wie bei 1,x. Ab 1,x habe ich dann nicht mehr nachgekauft, da keine neuen Erkenntnisse vorlagen und nur die Anlegerschaft sich wieder excited hat...
Dagegen habe ich dann im Feb 16 bei 3.80 mit bereits bekannter Trifekta (OS, ORR, PFS) das Depot bis zum Anschlag gefüllt. Weit besseres CRV als mit 3.40. Die Ineffizienzen des Marktes geben einem immer die Chance ...
Aber was schreib ich mir hier neun Wolf...wie Perlen vor die S..!
Wer mich kennt weiss, dass ich selbst bei meinen größten Investments immer sehr kritisch bleibe und mich nie verliebe. Im Gegensatz zu dir, die ich zur Rasse der gefährlichen Dauerbejubler der eigenen Investments zähle.
Relevant ist zu welchen Kursen man wann kauft - das C/R Verhältnis ist das Entscheidende.
Ein Screenshot aus meinem Depot ist dazu in meinem EXEL Thread zu sehen mit einem EK-Kurs von 1,x (1,25 EUR) für die günstigste Tranche vor Phase 3 Daten. Bei 3.40 vor Phase 3 Daten war das CRV logischerweise schlechter - weil gleiches Risiko wie bei 1,x. Ab 1,x habe ich dann nicht mehr nachgekauft, da keine neuen Erkenntnisse vorlagen und nur die Anlegerschaft sich wieder excited hat...
Dagegen habe ich dann im Feb 16 bei 3.80 mit bereits bekannter Trifekta (OS, ORR, PFS) das Depot bis zum Anschlag gefüllt. Weit besseres CRV als mit 3.40. Die Ineffizienzen des Marktes geben einem immer die Chance ...
Aber was schreib ich mir hier neun Wolf...wie Perlen vor die S..!
Antwort auf Beitrag Nr.: 55.133.546 von Cyberhexe am 13.06.17 19:23:46gut so, dann verlassen wir den Sandkasten und befassen uns wieder mit den eigentlich wichtigen Dingen in einem Forum, nämlich Info...in Form von guter Presse:
http://www.rheumatologyadvisor.com/osteoporosis/fda-approves…
Auf der Juli-Sitzung des CHMP erwarte ich die Zulassungsempfehlung von Abaloparatide für Europa, welche die Europäische Kommission dann spätestens 67 Tage danach erteilen wird. Zu diesem Zeitpunkt ist dann auch die Bekanntgabe des Kooperationspartners für Europa angekündigt. Man darf sowohl auf den Partner als auch auf die Bedingungen gespannt sein.
Bleibt zu hoffen, dass auch dieser Meilenstein so eingehalten wird wie angekündigt:
...ich bemerke gerade, dass diese Grafik nicht aktuell ist, da mittlerweile auch ACTIVExtend bzw. dessen Ergebnisse mitgeteilt wurden.
http://www.rheumatologyadvisor.com/osteoporosis/fda-approves…
Auf der Juli-Sitzung des CHMP erwarte ich die Zulassungsempfehlung von Abaloparatide für Europa, welche die Europäische Kommission dann spätestens 67 Tage danach erteilen wird. Zu diesem Zeitpunkt ist dann auch die Bekanntgabe des Kooperationspartners für Europa angekündigt. Man darf sowohl auf den Partner als auch auf die Bedingungen gespannt sein.
Bleibt zu hoffen, dass auch dieser Meilenstein so eingehalten wird wie angekündigt:

...ich bemerke gerade, dass diese Grafik nicht aktuell ist, da mittlerweile auch ACTIVExtend bzw. dessen Ergebnisse mitgeteilt wurden.
Antwort auf Beitrag Nr.: 55.134.242 von Cyberhexe am 13.06.17 21:13:54nur die Stimme eines Einzelnen oder doch mehr? Abaloparatide findet in diesem Aufsatz keine Erwähnung!
https://consultqd.clevelandclinic.org/2017/04/biologic-thera…
Unlike teriparatide, the currently available anabolic agent, romosozumab does not stimulate bone resorption and actually has an antiresorptive effect.
https://consultqd.clevelandclinic.org/2017/04/biologic-thera…
Unlike teriparatide, the currently available anabolic agent, romosozumab does not stimulate bone resorption and actually has an antiresorptive effect.
Antwort auf Beitrag Nr.: 55.137.146 von Cyberhexe am 14.06.17 11:43:47Elacestrant auf ASCO2017:
"Aditya Bardia, MD, MPH of Harvard Medical School and Massachusetts General Hospital Cancer Center gives an overview of his presentation, Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer, which was presented at the 2017 ASCO Annual Meeting in Chicago, IL."
http://www.oncologytube.com/video/elacestrant-rad1901-for-me…
"Aditya Bardia, MD, MPH of Harvard Medical School and Massachusetts General Hospital Cancer Center gives an overview of his presentation, Evaluation of RAD1901, a novel investigational, selective estrogen receptor degrader (SERD), for the treatment of ER-positive (ER+) advanced breast cancer, which was presented at the 2017 ASCO Annual Meeting in Chicago, IL."
http://www.oncologytube.com/video/elacestrant-rad1901-for-me…
Technisch gesehen vollendet Radius gerade einen Boden. Der Druck von technischer Seite könnte somit demnächst weichen und nun im Gegenzug durch das aufgehellte Bild weiteren Auftrieb geben...
Antwort auf Beitrag Nr.: 55.133.726 von Ville7 am 13.06.17 19:59:31
"wieder für eine Weile" ...dauert demnach einen Tag - dann hätten wir das auch geklärt.
Zitat von Ville7: Gähn!!! Letzte Antwort, dann verschwindet ich zumindest aus deinen Threads wieder für eine Weile. Du langweilst mich.
Wer mich kennt weiss, dass ich selbst bei meinen größten Investments immer sehr kritisch bleibe und mich nie verliebe. Im Gegensatz zu dir, die ich zur Rasse der gefährlichen Dauerbejubler der eigenen Investments zähle.
Relevant ist zu welchen Kursen man wann kauft - das C/R Verhältnis ist das Entscheidende.
Ein Screenshot aus meinem Depot ist dazu in meinem EXEL Thread zu sehen mit einem EK-Kurs von 1,x (1,25 EUR) für die günstigste Tranche vor Phase 3 Daten. Bei 3.40 vor Phase 3 Daten war das CRV logischerweise schlechter - weil gleiches Risiko wie bei 1,x. Ab 1,x habe ich dann nicht mehr nachgekauft, da keine neuen Erkenntnisse vorlagen und nur die Anlegerschaft sich wieder excited hat...
Dagegen habe ich dann im Feb 16 bei 3.80 mit bereits bekannter Trifekta (OS, ORR, PFS) das Depot bis zum Anschlag gefüllt. Weit besseres CRV als mit 3.40. Die Ineffizienzen des Marktes geben einem immer die Chance ...
Aber was schreib ich mir hier neun Wolf...wie Perlen vor die S..!
"wieder für eine Weile" ...dauert demnach einen Tag - dann hätten wir das auch geklärt.
Antwort auf Beitrag Nr.: 55.096.537 von Cyberhexe am 07.06.17 15:43:01
...nachdem die Anzahl der den Leerverkäufern zur Verfügung stehenden Aktien zwischenzeitlich einmal zugenommen hat (einhergehend mit steigenden Kursen), ist diese Verfügbarkeit gestern wieder massiv gesunken (einhergehend mit spürbarem Kursverlust). Bin gespannt, wie lange es noch dauert bis die Leerverkäufer den Kurs "ziehen lassen".
15.06.2017
Symbol: RDUS
Availability: 100'000
Exchanges: NASDAQ
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
Es wird auf alle Fälle spannend, da in einem Monat...
....die positive Empfehlung des CHMP für eine Zulassung innerhalb der EU erwartet wird (21.07.17)
...das Ergebnis des Treffens mit der FDA zur Besprechung/Modifizierung der ph2-Studie mit Elacestrant zur Behandlung von (ER)-positiv, fortgeschrittenem Brustkrebs bekannt sein sollte
--> Studienbeginn erwarte ich auf 1H2018
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
Zitat von Cyberhexe: Die Shorties bekommen keine Aktien mehr angeboten, da aktuell --> "Shortable Stocks for United States":
Symbol: RDUS
Availability: 10'000
Exchanges: NASDAQ
dann wird wohl naked short selling vermehrt stattfinden. Auf alle Fälle scheinen die Shorties noch nicht aufzugeben.
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
...nachdem die Anzahl der den Leerverkäufern zur Verfügung stehenden Aktien zwischenzeitlich einmal zugenommen hat (einhergehend mit steigenden Kursen), ist diese Verfügbarkeit gestern wieder massiv gesunken (einhergehend mit spürbarem Kursverlust). Bin gespannt, wie lange es noch dauert bis die Leerverkäufer den Kurs "ziehen lassen".
15.06.2017
Symbol: RDUS
Availability: 100'000
Exchanges: NASDAQ
https://www.interactivebrokers.com/en/index.php?key=rdus&cnt…
Es wird auf alle Fälle spannend, da in einem Monat...
....die positive Empfehlung des CHMP für eine Zulassung innerhalb der EU erwartet wird (21.07.17)
...das Ergebnis des Treffens mit der FDA zur Besprechung/Modifizierung der ph2-Studie mit Elacestrant zur Behandlung von (ER)-positiv, fortgeschrittenem Brustkrebs bekannt sein sollte
--> Studienbeginn erwarte ich auf 1H2018
http://www.ema.europa.eu/ema/index.jsp?curl=pages%2Fabout_us…
Antwort auf Beitrag Nr.: 55.149.335 von Cyberhexe am 16.06.17 08:09:40die wissenschaftliche Presse berichtet vermehrt über Abaloparatide:
https://link.springer.com/article/10.1007%2Fs40265-017-0780-…
SpringerLink
Abaloparatide: First Global Approval
First Online: 17 June 2017
Abaloparatide (Tymlos™) is a synthetic peptide analogue of human parathyroid hormone-related protein that was developed by Radius Health as an osteoanabolic agent for the treatment of postmenopausal osteoporosis. Abaloparatide acts through selective activation of the parathyroid hormone type 1 receptor signalling pathway. In April 2017, subcutaneous abaloparatide received its first global approval, in the USA, for the treatment of postmenopausal women with osteoporosis at high risk for fracture, defined as a history of osteoporotic fracture, multiple risk factors for fracture, or patients who have failed or are intolerant to other available osteoporosis therapy. A Marketing Authorization Application for subcutaneous abaloparatide for the treatment of postmenopausal women with osteoporosis was accepted by the European Medicines Agency and is currently under review. Radius is also developing a transdermal formulation of abaloparatide, with administration via a microneedle patch. This article summarizes the milestones in the development of abaloparatide leading to this first approval for the treatment of women with postmenopausal osteoporosis.
https://link.springer.com/article/10.1007%2Fs40265-017-0780-…
SpringerLink
Abaloparatide: First Global Approval
First Online: 17 June 2017
Abaloparatide (Tymlos™) is a synthetic peptide analogue of human parathyroid hormone-related protein that was developed by Radius Health as an osteoanabolic agent for the treatment of postmenopausal osteoporosis. Abaloparatide acts through selective activation of the parathyroid hormone type 1 receptor signalling pathway. In April 2017, subcutaneous abaloparatide received its first global approval, in the USA, for the treatment of postmenopausal women with osteoporosis at high risk for fracture, defined as a history of osteoporotic fracture, multiple risk factors for fracture, or patients who have failed or are intolerant to other available osteoporosis therapy. A Marketing Authorization Application for subcutaneous abaloparatide for the treatment of postmenopausal women with osteoporosis was accepted by the European Medicines Agency and is currently under review. Radius is also developing a transdermal formulation of abaloparatide, with administration via a microneedle patch. This article summarizes the milestones in the development of abaloparatide leading to this first approval for the treatment of women with postmenopausal osteoporosis.
Antwort auf Beitrag Nr.: 55.168.193 von Cyberhexe am 20.06.17 07:38:22Risikostreuung:
hab heute 12% RDUS zu USD 44,22 liquidiert und mit dem Erlös eine Kauforder von PGNX zu USD 7,04 platziert (ultimo)
hab heute 12% RDUS zu USD 44,22 liquidiert und mit dem Erlös eine Kauforder von PGNX zu USD 7,04 platziert (ultimo)
Antwort auf Beitrag Nr.: 55.175.093 von Cyberhexe am 20.06.17 23:31:26
Tja, auch wenn ich dir günstige EKs als Nachschlag gönne - ich persönlich würde mir wünschen, PGNX wieder mal kräftig UP gehen zu sehen...
Zitat von Cyberhexe: Risikostreuung:
hab heute 12% RDUS zu USD 44,22 liquidiert und mit dem Erlös eine Kauforder von PGNX zu USD 7,04 platziert (ultimo)
Tja, auch wenn ich dir günstige EKs als Nachschlag gönne - ich persönlich würde mir wünschen, PGNX wieder mal kräftig UP gehen zu sehen...

Antwort auf Beitrag Nr.: 55.186.908 von bernie55 am 22.06.17 17:32:02
http://secure.medicalletter.org/article-share?a=1523a&p=tml&…
....tja Bernie, das Momentum ist momentan nicht auf meiner Seite. 12% der RDUS-Anteile verkauft, PGNX-Anteile bisher nicht gekauft - da war ich wohl zu gierig.
http://secure.medicalletter.org/article-share?a=1523a&p=tml&…
....tja Bernie, das Momentum ist momentan nicht auf meiner Seite. 12% der RDUS-Anteile verkauft, PGNX-Anteile bisher nicht gekauft - da war ich wohl zu gierig.

Antwort auf Beitrag Nr.: 55.188.412 von Cyberhexe am 23.06.17 06:13:35anbei "die" FDA-Seite zu Abaloparatide:
https://www.accessdata.fda.gov/drugsatfda_docs/nda/2017/2087…
Tymlos Subcutaneous Injection
Company: Radius Health, Inc.
Application No.: 208743
Approval Date: 04/28/2017
https://www.accessdata.fda.gov/drugsatfda_docs/nda/2017/2087…
Tymlos Subcutaneous Injection
Company: Radius Health, Inc.
Application No.: 208743
Approval Date: 04/28/2017
Antwort auf Beitrag Nr.: 55.188.502 von Cyberhexe am 23.06.17 07:11:32Beitrag in einem wissenschaftlichen Journal (ELSEVIER) zu Abaloparatide bzw. ACTIVE, worin eine sehr wichtige Erkenntnis mitgeteilt wird: "nach 12 bzw. 18 Monate unter Abaloparatide keine Nebenwirkungen bei der Knochenqualität sowie keine Bedenken hinsichtlich der (Knochen)Sicherheit."
http://www.thebonejournal.com/article/S8756-3282(16)30329-5/…
"Effects of abaloparatide-SC (BA058) on bone histology and histomorphometry: The ACTIVE phase 3 trial☆
...osteoporosis-related fractures in the phase 3 ACTIVE trial. The objective of this report is to describe the effects of abaloparatide-SC 80 μg on bone histology and histomorphometry in iliac crest bone biopsies from this trial in which participants were randomized to receive blinded daily subcutaneous injections of placebo or abaloparatide-SC 80 μg/d or open-label teriparatide 20 μg/d for 18 months. Iliac crest bone biopsies were obtained between 12 and
...We conclude that 12 to 18 months of treatment of postmenopausal women with osteoporosis with abaloparatide-SC 80 μg has no adverse effects on bone quality and there are no concerns with regard to bonesafety."
http://www.thebonejournal.com/article/S8756-3282(16)30329-5/…
"Effects of abaloparatide-SC (BA058) on bone histology and histomorphometry: The ACTIVE phase 3 trial☆
...osteoporosis-related fractures in the phase 3 ACTIVE trial. The objective of this report is to describe the effects of abaloparatide-SC 80 μg on bone histology and histomorphometry in iliac crest bone biopsies from this trial in which participants were randomized to receive blinded daily subcutaneous injections of placebo or abaloparatide-SC 80 μg/d or open-label teriparatide 20 μg/d for 18 months. Iliac crest bone biopsies were obtained between 12 and
...We conclude that 12 to 18 months of treatment of postmenopausal women with osteoporosis with abaloparatide-SC 80 μg has no adverse effects on bone quality and there are no concerns with regard to bonesafety."
in der Juli-Sitzung des CHMP wird sehr wahrscheinlich Abaloparatide zur Zulassung empfohlen - diese Empfehlung wird allerdings nicht die gleiche Reaktion auslösen wie nach der heutigen Zulassungsempfehlung von Tivozanib - diese kam wohl nicht nur für mich überraschend.
17/07/2017 - 20/07/2017 : CHMP
Bekanntgabe am 21.7.2017
17/07/2017 - 20/07/2017 : CHMP
Bekanntgabe am 21.7.2017
Hier der Chart von RDUS seit November 2016 - EMA20, MA50 und MA200 mittlerweile von unten nach oben durchbrochen.

Antwort auf Beitrag Nr.: 55.205.294 von bernie55 am 26.06.17 12:34:51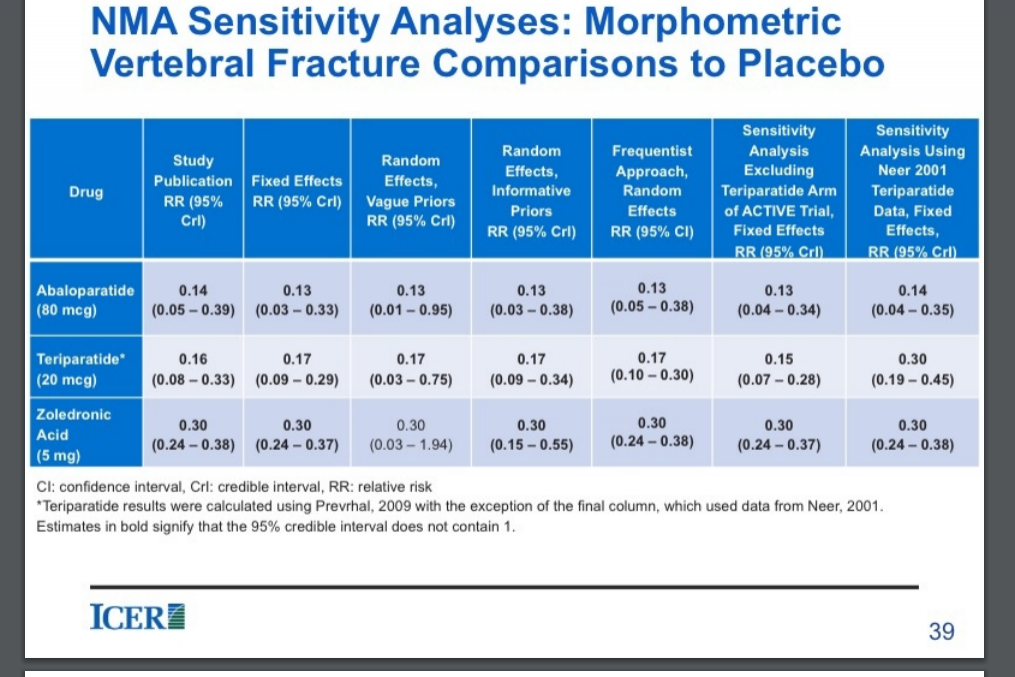
ICER "Institute for Clinical and Economic Review"
ist eine Non-Profit-Organisation mit Sitz in Boston, MA

ICER "Institute for Clinical and Economic Review"
ist eine Non-Profit-Organisation mit Sitz in Boston, MA
Antwort auf Beitrag Nr.: 55.270.660 von Cyberhexe am 05.07.17 22:08:50
Profile of Abaloparatide and Its Potential in the Treatment of Postmenopausal Osteoporosis
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5493470/
Profile of Abaloparatide and Its Potential in the Treatment of Postmenopausal Osteoporosis
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5493470/
Antwort auf Beitrag Nr.: 55.297.294 von Cyberhexe am 11.07.17 00:04:51
gute Übersicht zu Abaloparatide (brand: Tymlos):
http://www.gertitashkomd.com/blog/2017/6/28/new-fda-approval…
nächste Woche wird der europ. Arzneimittelausschuss CHMP über eine Zulassung von Abaloparatide in der EU beraten - Bekanntgabe am Freitag, 21.7.17!
gute Übersicht zu Abaloparatide (brand: Tymlos):
http://www.gertitashkomd.com/blog/2017/6/28/new-fda-approval…
nächste Woche wird der europ. Arzneimittelausschuss CHMP über eine Zulassung von Abaloparatide in der EU beraten - Bekanntgabe am Freitag, 21.7.17!
Radius Health Announces License and Development Agreement for Abaloparatide-SC with Teijin Limited in Japan
-Teijin granted a right of reference to Radius regulatory data and use of Radius Intellectual Property for development, manufacture and commercialization of abaloparatide-SC for Japan, the largest market globally for bone anabolics.
-Radius to receive upfront and milestone payments, royalties, and an option for co-promotion.
WALTHAM, Mass., July 13, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (“Radius”) (Nasdaq:RDUS), a fully integrated science-driven biopharmaceutical company that is committed to developing and commercializing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, announced today that it has entered into a license and development agreement with Teijin Limited in Japan for abaloparatide-SC. Teijin is developing abaloparatide-SC in Japan under an agreement with Ipsen Pharma S.A.S. and has initiated a phase 3 trial in Japanese patients with osteoporosis.
The collaboration agreement provides Teijin with the right to manufacture abaloparatide-SC for commercial supply in Japan, as well as the right to reference Radius’ NDA and MAA and regulatory data to support its marketing application in Japan and to use Radius intellectual property, and provides Radius with an option to negotiate a co-promotion agreement for abaloparatide-SC in Japan. Radius will also receive upfront and milestone payments and royalties for the rights granted to Teijin. Teijin is conducting and funding its Japanese phase 3 development program and the parties may further collaborate in the future in new indications for the product. Radius maintains full global rights to its development program for abaloparatide-transdermal (abaloparatide-TD), which is not part of the agreement with Teijin.
“We are extremely pleased to partner with Teijin as they seek to complete their Phase 3 development of abaloparatide-SC and pursue regulatory approval in Japan,” said Robert E. Ward, President and CEO of Radius Health. “As Japan represents the largest anabolic market in the world, our partnership with Teijin is an important step in expanding the value of the abaloparatide franchise globally.”
https://globenewswire.com/news-release/2017/07/13/1044092/0/…
-Teijin granted a right of reference to Radius regulatory data and use of Radius Intellectual Property for development, manufacture and commercialization of abaloparatide-SC for Japan, the largest market globally for bone anabolics.
-Radius to receive upfront and milestone payments, royalties, and an option for co-promotion.
WALTHAM, Mass., July 13, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (“Radius”) (Nasdaq:RDUS), a fully integrated science-driven biopharmaceutical company that is committed to developing and commercializing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, announced today that it has entered into a license and development agreement with Teijin Limited in Japan for abaloparatide-SC. Teijin is developing abaloparatide-SC in Japan under an agreement with Ipsen Pharma S.A.S. and has initiated a phase 3 trial in Japanese patients with osteoporosis.
The collaboration agreement provides Teijin with the right to manufacture abaloparatide-SC for commercial supply in Japan, as well as the right to reference Radius’ NDA and MAA and regulatory data to support its marketing application in Japan and to use Radius intellectual property, and provides Radius with an option to negotiate a co-promotion agreement for abaloparatide-SC in Japan. Radius will also receive upfront and milestone payments and royalties for the rights granted to Teijin. Teijin is conducting and funding its Japanese phase 3 development program and the parties may further collaborate in the future in new indications for the product. Radius maintains full global rights to its development program for abaloparatide-transdermal (abaloparatide-TD), which is not part of the agreement with Teijin.
“We are extremely pleased to partner with Teijin as they seek to complete their Phase 3 development of abaloparatide-SC and pursue regulatory approval in Japan,” said Robert E. Ward, President and CEO of Radius Health. “As Japan represents the largest anabolic market in the world, our partnership with Teijin is an important step in expanding the value of the abaloparatide franchise globally.”
https://globenewswire.com/news-release/2017/07/13/1044092/0/…
Antwort auf Beitrag Nr.: 55.331.236 von bernie55 am 15.07.17 17:01:25wie erwartet hat die FDA Amgen einen "Complete Response Letter" zu Romosozumab zugestellt, so dass das Konkurrenzprodukt zu Radius´Abaloparatide vorerst nicht auf den Markt kommen wird.
Heute (bis Donnerstag) beginnt zudem die Juli-Sitzung des europ. Arzneimittelausschusses CHMP, der sehr wahrscheinlich in dieser Sitzung über die Zulassung von Abaloparatide zur Behandlung von Osteoporose nach der Menopause beraten wird. Ich rechne mit einer Zulassungsempfehlung, die sehr wahrscheinlich am Freitag (21.7.2017) veröffentlicht wird.
Amgen And UCB Provide Update On Regulatory Status Of EVENITY™ (romosozumab) In The US
THOUSAND OAKS, Calif. and BRUSSELS,
July 16, 2017 /PRNewswire/ --
Amgen (NASDAQ:AMGN) and UCB (Euronext Brussels: UCB) today announced that the U.S. Food and Drug Administration (FDA) has issued a Complete Response Letter for the Biologics License Application (BLA) for EVENITY™* (romosozumab) as a treatment for postmenopausal women with osteoporosis.
The original submission included data from the pivotal Phase 3 placebo-controlled FRAME study of postmenopausal women with osteoporosis. With the availability of data from the Phase 3 active-comparator ARCH study, the Agency has asked that the efficacy and safety data from the study be integrated into the application. The resubmission will also include the efficacy and safety data from the BRIDGE study, the Phase 3 trial evaluating EVENITY in men with osteoporosis, which has also been requested. This request will be addressed in the form of a resubmission, which is an extension of the current review.
"During our interactions with the FDA, we agreed that the ARCH data should be considered in the regulatory review prior to the initial marketing authorization and, as a result, anticipated this request. We look forward to working through the review process with the Agency," said Sean E. Harper, M.D., executive vice president of Research and Development at Amgen. "We remain committed to helping patients with osteoporosis and will use the additional time to better understand the benefit:risk profile of EVENITY."
"The reality is that once a woman has a fragility fracture, she is five times more likely to suffer another within a year. This is a stark reminder that there is an urgent need to improve post-fracture care and reduce the risk of painful, disabling fractures in the future," said Dr. Pascale Richetta, head of bone and executive vice president, UCB. "With all three pivotal romosozumab Phase 3 studies now included in the clinical evidence package, representing data from more than 11,000 patients, we are committed to bringing this important potential new treatment to those people living at risk of fragility fractures."
Heute (bis Donnerstag) beginnt zudem die Juli-Sitzung des europ. Arzneimittelausschusses CHMP, der sehr wahrscheinlich in dieser Sitzung über die Zulassung von Abaloparatide zur Behandlung von Osteoporose nach der Menopause beraten wird. Ich rechne mit einer Zulassungsempfehlung, die sehr wahrscheinlich am Freitag (21.7.2017) veröffentlicht wird.
Amgen And UCB Provide Update On Regulatory Status Of EVENITY™ (romosozumab) In The US
THOUSAND OAKS, Calif. and BRUSSELS,
July 16, 2017 /PRNewswire/ --
Amgen (NASDAQ:AMGN) and UCB (Euronext Brussels: UCB) today announced that the U.S. Food and Drug Administration (FDA) has issued a Complete Response Letter for the Biologics License Application (BLA) for EVENITY™* (romosozumab) as a treatment for postmenopausal women with osteoporosis.
The original submission included data from the pivotal Phase 3 placebo-controlled FRAME study of postmenopausal women with osteoporosis. With the availability of data from the Phase 3 active-comparator ARCH study, the Agency has asked that the efficacy and safety data from the study be integrated into the application. The resubmission will also include the efficacy and safety data from the BRIDGE study, the Phase 3 trial evaluating EVENITY in men with osteoporosis, which has also been requested. This request will be addressed in the form of a resubmission, which is an extension of the current review.
"During our interactions with the FDA, we agreed that the ARCH data should be considered in the regulatory review prior to the initial marketing authorization and, as a result, anticipated this request. We look forward to working through the review process with the Agency," said Sean E. Harper, M.D., executive vice president of Research and Development at Amgen. "We remain committed to helping patients with osteoporosis and will use the additional time to better understand the benefit:risk profile of EVENITY."
"The reality is that once a woman has a fragility fracture, she is five times more likely to suffer another within a year. This is a stark reminder that there is an urgent need to improve post-fracture care and reduce the risk of painful, disabling fractures in the future," said Dr. Pascale Richetta, head of bone and executive vice president, UCB. "With all three pivotal romosozumab Phase 3 studies now included in the clinical evidence package, representing data from more than 11,000 patients, we are committed to bringing this important potential new treatment to those people living at risk of fragility fractures."
Antwort auf Beitrag Nr.: 55.336.007 von Cyberhexe am 17.07.17 04:07:34Diese Vorhersage scheint Radius nicht einzuhalten - Abaloparatide wird in der Juli-Sitzung des Arzneimittelausschusses (CHMP) nicht abschliessend bewertet:
3.1 Initial applications; Opinions
--> kein Eintrag "abaloparatide"
lediglich unter 3.2
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
Oder sehe ich das falsch?
3.1 Initial applications; Opinions
--> kein Eintrag "abaloparatide"
lediglich unter 3.2
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
Oder sehe ich das falsch?
Komische Entwicklungen bei RDUS der CEO muss gehen, ein neuer kommt. Scheint so als hätte Ward den Mund zu voll genommen und /oder der Launch läuft nicht annähernd wie erhofft. Mal vom Debakel bei der EMA abgesehen:
Jul 17, 2017
Previous Release
Radius Health Appoints Jesper Høiland as President and Chief Executive Officer To Lead The Next Stage Of Growth and Value Creation As A Fully Integrated Commercial Biotech Company
Mr. Høiland brings unique experience in launching new products, creating growth strategies and leading high-performing organizations
WALTHAM, Mass., July 17, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. ("Radius" or the "Company") (Nasdaq:RDUS), a fully integrated science-driven biopharmaceutical company that is committed to developing and commercializing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that Jesper Høiland has been appointed President and Chief Executive Officer of the Company.
Kurt Graves, Chairman of the Board, said, "We are pleased to welcome Jesper to Radius Health at this important time, and believe that he is uniquely qualified to lead Radius through the successful launch of TYMLOS™, and the advancement of our exciting clinical stage assets including elacestrant. Throughout his US and Global leadership roles at Novo Nordisk, he has demonstrated success in launching major brands, executing on business development and driving sustainable growth. His leadership and experience will be invaluable in guiding Radius through our next dynamic period of growth."
"The Board and I want to thank Bob Ward for the contributions he made to Radius which positioned the Company for the next stage of growth and shareholder value creation. During Bob's tenure the Company successfully completed its IPO, advanced multiple pipeline assets, and obtained FDA approval for TYMLOS™ which was recently launched in the US."
"I am delighted to be joining Radius in the exciting, early stages of the commercialization of TYMLOS™," said Jesper Høiland, "and I look forward to guiding the continued development of its strong pipeline. I am eager to work with our Board, senior management and the entire organization to execute on our promising future and deliver on the Company's long-standing goal of positively impacting the lives of patients and delivering significant value for all our stakeholders."
Mr. Høiland has 30 years of experience in the biopharmaceutical industry across numerous senior leadership roles, geographies and therapeutic areas. He brings extensive knowledge about the areas of endocrinology, biopharmaceuticals and women's health as well as unique insights about US market access. Prior to joining Radius, Mr. Høiland served as President of Novo Nordisk Inc. USA overseeing approximately 5,300 employees. Under his leadership, Novo Nordisk solidified its market leadership and growth in diabetes and also drove significant growth in its hemophilia and growth hormone franchises. Since joining Novo Nordisk in 1987, Mr. Høiland held multiple global roles of increasing responsibility, including leading its International Operations which spanned 150 countries.
Jul 17, 2017
Previous Release
Radius Health Appoints Jesper Høiland as President and Chief Executive Officer To Lead The Next Stage Of Growth and Value Creation As A Fully Integrated Commercial Biotech Company
Mr. Høiland brings unique experience in launching new products, creating growth strategies and leading high-performing organizations
WALTHAM, Mass., July 17, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. ("Radius" or the "Company") (Nasdaq:RDUS), a fully integrated science-driven biopharmaceutical company that is committed to developing and commercializing innovative therapeutics in the areas of osteoporosis, oncology and endocrine diseases, today announced that Jesper Høiland has been appointed President and Chief Executive Officer of the Company.
Kurt Graves, Chairman of the Board, said, "We are pleased to welcome Jesper to Radius Health at this important time, and believe that he is uniquely qualified to lead Radius through the successful launch of TYMLOS™, and the advancement of our exciting clinical stage assets including elacestrant. Throughout his US and Global leadership roles at Novo Nordisk, he has demonstrated success in launching major brands, executing on business development and driving sustainable growth. His leadership and experience will be invaluable in guiding Radius through our next dynamic period of growth."
"The Board and I want to thank Bob Ward for the contributions he made to Radius which positioned the Company for the next stage of growth and shareholder value creation. During Bob's tenure the Company successfully completed its IPO, advanced multiple pipeline assets, and obtained FDA approval for TYMLOS™ which was recently launched in the US."
"I am delighted to be joining Radius in the exciting, early stages of the commercialization of TYMLOS™," said Jesper Høiland, "and I look forward to guiding the continued development of its strong pipeline. I am eager to work with our Board, senior management and the entire organization to execute on our promising future and deliver on the Company's long-standing goal of positively impacting the lives of patients and delivering significant value for all our stakeholders."
Mr. Høiland has 30 years of experience in the biopharmaceutical industry across numerous senior leadership roles, geographies and therapeutic areas. He brings extensive knowledge about the areas of endocrinology, biopharmaceuticals and women's health as well as unique insights about US market access. Prior to joining Radius, Mr. Høiland served as President of Novo Nordisk Inc. USA overseeing approximately 5,300 employees. Under his leadership, Novo Nordisk solidified its market leadership and growth in diabetes and also drove significant growth in its hemophilia and growth hormone franchises. Since joining Novo Nordisk in 1987, Mr. Høiland held multiple global roles of increasing responsibility, including leading its International Operations which spanned 150 countries.
Antwort auf Beitrag Nr.: 55.338.449 von Cyberhexe am 17.07.17 13:25:51Schaut so aus.... vielleicht auch mit ein Punkt wieso der CEO ausgetauscht wird...die Langsamkeit bei der EMA.
RDUS hat es erneut bei der EMA verbockt. Eine zweite 180 Day Fragenliste wurde vom CHMP erstellt. RDUS rechnet mit einer Opinion noch in 2017. Zulassung somit auf St.Nimmerlein oder frühestens in 2018. Unglaublich.
BBBiotech sehen wieder mal aus wie die größten Deppen. Zeigt sich erneut, dass man solchen Dickfischen nicht blind hinterherrennen sollte.
Durch die Verzögerung droht nun auch eine neue starke Verwässerung, da man aufgrund des CEO Wechsels auch davon ausgehen kann, dass der Launch in USA nicht besonders gut läuft.
BBBiotech sehen wieder mal aus wie die größten Deppen. Zeigt sich erneut, dass man solchen Dickfischen nicht blind hinterherrennen sollte.
Durch die Verzögerung droht nun auch eine neue starke Verwässerung, da man aufgrund des CEO Wechsels auch davon ausgehen kann, dass der Launch in USA nicht besonders gut läuft.
Antwort auf Beitrag Nr.: 55.375.127 von Ville7 am 22.07.17 01:53:56
1.) Der Umstand, dass BB Biotech investiert ist, spricht nicht gegen ein Investment in Radius, ist jedoch keine Voraussetzung hierfür: bspw. ist BB Biotech in Exelixis überhaupt nicht investiert ist. Diese Betrachtungsweise ist aus meiner Sicht sehr eindimensional.
Aber diese Kausalkette betrachtend... --> "Durch die Verzögerung droht nun auch eine neue starke Verwässerung, da man aufgrund des CEO Wechsels auch davon ausgehen kann, dass der Launch in USA nicht besonders gut läuft." ...bleibt mir die Spucke weg! Das möchte ich nicht weiter kommentieren!!!
2.) Die Gründe für einen Wechsel auf höchster Ebene sind nicht eindeutig, müssen jedoch eher mittelfristiger Herkunft sein, da ein derart hochkarätiger Ersatz nicht über Nacht zu rekrutieren ist. Ich bezweifle deswegen die These, dass der US Launch von Tymlos diesen Wechsel ursächlich beeinflusst hat. Auch die jetzige Verzögerung bei der EU-Zulassung von Abaloparatide kann aus chronologischer Sicht nicht als Erklärung herhalten. Aus meiner Sicht wahrscheinlicher sind fehlende (EU) oder unbefriedigende Vereinbarungen (Japan - Details zum Abschluss mit Teijin wurden nicht veröffentlicht) bei der Vermarktung von Abaloparatide ausserhalb Nordamerikas.
Zitat von Ville7: RDUS hat es erneut bei der EMA verbockt. Eine zweite 180 Day Fragenliste wurde vom CHMP erstellt. RDUS rechnet mit einer Opinion noch in 2017. Zulassung somit auf St.Nimmerlein oder frühestens in 2018. Unglaublich.
BBBiotech sehen wieder mal aus wie die größten Deppen. Zeigt sich erneut, dass man solchen Dickfischen nicht blind hinterherrennen sollte.
Durch die Verzögerung droht nun auch eine neue starke Verwässerung, da man aufgrund des CEO Wechsels auch davon ausgehen kann, dass der Launch in USA nicht besonders gut läuft.
1.) Der Umstand, dass BB Biotech investiert ist, spricht nicht gegen ein Investment in Radius, ist jedoch keine Voraussetzung hierfür: bspw. ist BB Biotech in Exelixis überhaupt nicht investiert ist. Diese Betrachtungsweise ist aus meiner Sicht sehr eindimensional.
Aber diese Kausalkette betrachtend... --> "Durch die Verzögerung droht nun auch eine neue starke Verwässerung, da man aufgrund des CEO Wechsels auch davon ausgehen kann, dass der Launch in USA nicht besonders gut läuft." ...bleibt mir die Spucke weg! Das möchte ich nicht weiter kommentieren!!!
2.) Die Gründe für einen Wechsel auf höchster Ebene sind nicht eindeutig, müssen jedoch eher mittelfristiger Herkunft sein, da ein derart hochkarätiger Ersatz nicht über Nacht zu rekrutieren ist. Ich bezweifle deswegen die These, dass der US Launch von Tymlos diesen Wechsel ursächlich beeinflusst hat. Auch die jetzige Verzögerung bei der EU-Zulassung von Abaloparatide kann aus chronologischer Sicht nicht als Erklärung herhalten. Aus meiner Sicht wahrscheinlicher sind fehlende (EU) oder unbefriedigende Vereinbarungen (Japan - Details zum Abschluss mit Teijin wurden nicht veröffentlicht) bei der Vermarktung von Abaloparatide ausserhalb Nordamerikas.
Antwort auf Beitrag Nr.: 55.376.291 von Cyberhexe am 22.07.17 12:15:01Ich habe heute in Frankfurt 750 Radius zu €35.885 sowie 1100 und 350 in Suttgart zu €34.76 sowie €34.74 (mit einem kleinen Gewinn) verkauft; die US-Position bleibt unangetastet.
Das Ziel wäre, die heute verkauften Aktien zu €32 wieder einzukaufen. Mal sehen, was möglich ist!
Das Ziel wäre, die heute verkauften Aktien zu €32 wieder einzukaufen. Mal sehen, was möglich ist!
Während RDUS nun sein neueres und angeblich besseres Produkt Tymlos zu einem Bruchteil des Preises von Forteo verschleudert, schafft es LLY mit Preiserhöhung und leichter Volumensteigerung den Absatz klar zu erhöhen. So geht es, RDUS.

Die Entscheidung den Preis so niedrig zu setzen ist wahrscheinlich mit ein Grund, dass Ward gehen musste und ein erfahrener Manager mit Markterfahrung geholt wurde.

Die Entscheidung den Preis so niedrig zu setzen ist wahrscheinlich mit ein Grund, dass Ward gehen musste und ein erfahrener Manager mit Markterfahrung geholt wurde.
Antwort auf Beitrag Nr.: 55.415.255 von Ville7 am 28.07.17 19:08:49...man wird sehen, welche Strategie sich mittel- bis langfristig durchsetzt. Ich würde darauf wetten, dass Teriparatide gerade durch diese Preisstrategie Marktanteile an Abaloparatide abgibt, und das nicht zu knapp. Time will tell!
Antwort auf Beitrag Nr.: 55.382.928 von Cyberhexe am 24.07.17 11:06:49
Mit dem timing hast du es irgendwie auch nicht so....du hälst die Aktien ein Jahr für 1% Gewinn und fängst dann wegen 2-3 EUR das traden an. Und nun rennt es in die andere Richtung...
Zitat von Cyberhexe: Ich habe heute in Frankfurt 750 Radius zu €35.885 sowie 1100 und 350 in Suttgart zu €34.76 sowie €34.74 (mit einem kleinen Gewinn) verkauft; die US-Position bleibt unangetastet.
Das Ziel wäre, die heute verkauften Aktien zu €32 wieder einzukaufen. Mal sehen, was möglich ist!
Mit dem timing hast du es irgendwie auch nicht so....du hälst die Aktien ein Jahr für 1% Gewinn und fängst dann wegen 2-3 EUR das traden an. Und nun rennt es in die andere Richtung...
Antwort auf Beitrag Nr.: 55.427.850 von Ville7 am 31.07.17 17:11:20
ab und zu muss man flüssig sein, um Chancen wahrzunehmen:
Cyberhexe schrieb am 26.07.17 16:48:18 Beitrag Nr. 2.565 ( 55.397.408 ) Antwort auf Beitrag Nr.: 55.184.558 von pokemon am 22.06.17 11:56:09 die Unterlagen zum AC sind publiziert - das wird einen harte Nuss: die hohe Todesrate unter Heplisav wird einige Bedenken auslösen. Und dennoch, bin vorsichtig eingestiegen: 1000 Stück zu USD 8.70 Das wird spannend am Freitag.
https://www.wallstreet-online.de/diskussion/1146921-2561-257…
aktuell:
http://www.nasdaq.com/symbol/dvax/after-hours
Aber irgendwie schon lustig, wie viel Zeit und Energie verschiedene Teilnehmer aufwenden, um meine Investmententscheidungen zu verfolgen - aber davon wird deren Reputation auch nicht besser!
Zitat von Ville7:Zitat von Cyberhexe: Ich habe heute in Frankfurt 750 Radius zu €35.885 sowie 1100 und 350 in Suttgart zu €34.76 sowie €34.74 (mit einem kleinen Gewinn) verkauft; die US-Position bleibt unangetastet.
Das Ziel wäre, die heute verkauften Aktien zu €32 wieder einzukaufen. Mal sehen, was möglich ist!
Mit dem timing hast du es irgendwie auch nicht so....du hälst die Aktien ein Jahr für 1% Gewinn und fängst dann wegen 2-3 EUR das traden an. Und nun rennt es in die andere Richtung...
ab und zu muss man flüssig sein, um Chancen wahrzunehmen:
Cyberhexe schrieb am 26.07.17 16:48:18 Beitrag Nr. 2.565 ( 55.397.408 ) Antwort auf Beitrag Nr.: 55.184.558 von pokemon am 22.06.17 11:56:09 die Unterlagen zum AC sind publiziert - das wird einen harte Nuss: die hohe Todesrate unter Heplisav wird einige Bedenken auslösen. Und dennoch, bin vorsichtig eingestiegen: 1000 Stück zu USD 8.70 Das wird spannend am Freitag.
https://www.wallstreet-online.de/diskussion/1146921-2561-257…
aktuell:
http://www.nasdaq.com/symbol/dvax/after-hours
Aber irgendwie schon lustig, wie viel Zeit und Energie verschiedene Teilnehmer aufwenden, um meine Investmententscheidungen zu verfolgen - aber davon wird deren Reputation auch nicht besser!
Antwort auf Beitrag Nr.: 55.427.988 von Cyberhexe am 31.07.17 17:22:56Gut gemacht!
PS: manche Leute werden durch Kurserfolge oder -misserfolge eben an ihrer großen Klappe, ihrer "keine andere Meinung als die eigene" duldenden Einstellung und/oder die Herabkanzelung anderer zur Kreisklasse (selber Championsliga) gemessen. Das ist mit Abstand das beste Maß.
hat auch seine vorteile wenn man etwas billiger ist als die konkurrenz, der pharmahändler express scripts zieht tymlos forteo vor (siehe letzte seite) --> https://www.express-scripts.com/art/pdf/npf2018.pdf
Antwort auf Beitrag Nr.: 55.448.040 von paul81 am 03.08.17 07:59:13
Kompliment für diesen Fund!
die mE "intelligente Preisgestaltung" von Radius wird FORTEO arg zusetzen....auch wenn verschiedene Teilnehmer dies nicht wahrhaben wollen.
Bin mal gespannt auf die Veröffentlichung der Quartalszahlen nach Börsenschluss.
Zitat von paul81: hat auch seine vorteile wenn man etwas billiger ist als die konkurrenz, der pharmahändler express scripts zieht tymlos forteo vor (siehe letzte seite) --> https://www.express-scripts.com/art/pdf/npf2018.pdf
Kompliment für diesen Fund!
die mE "intelligente Preisgestaltung" von Radius wird FORTEO arg zusetzen....auch wenn verschiedene Teilnehmer dies nicht wahrhaben wollen.
Bin mal gespannt auf die Veröffentlichung der Quartalszahlen nach Börsenschluss.
Antwort auf Beitrag Nr.: 55.415.255 von Ville7 am 28.07.17 19:08:49
SUPER Analyse - ich bin begeistert!
Zitat von Ville7: Während RDUS nun sein neueres und angeblich besseres Produkt Tymlos zu einem Bruchteil des Preises von Forteo verschleudert, schafft es LLY mit Preiserhöhung und leichter Volumensteigerung den Absatz klar zu erhöhen. So geht es, RDUS.
![]()
Die Entscheidung den Preis so niedrig zu setzen ist wahrscheinlich mit ein Grund, dass Ward gehen musste und ein erfahrener Manager mit Markterfahrung geholt wurde.
SUPER Analyse - ich bin begeistert!
Antwort auf Beitrag Nr.: 55.382.928 von Cyberhexe am 24.07.17 11:06:49Ich habe soeben 300 Stück in Frankfurt zu €30.822 sowie 500 Stück in US zu $35.87 zurück gekauft!
Mehr geht nicht, da der Rest in Dynavax investiert wurde.
Mehr geht nicht, da der Rest in Dynavax investiert wurde.
Antwort auf Beitrag Nr.: 55.382.928 von Cyberhexe am 24.07.17 11:06:49
Ich habe soeben 300 Stück in Frankfurt zu €30.822 sowie 500 Stück in US zu $35.87 zurück gekauft!
Mehr geht nicht, da der Rest in Dynavax investiert wurde.
Zitat von Cyberhexe: Ich habe heute in Frankfurt 750 Radius zu €35.885 sowie 1100 und 350 in Suttgart zu €34.76 sowie €34.74 (mit einem kleinen Gewinn) verkauft; die US-Position bleibt unangetastet.
Das Ziel wäre, die heute verkauften Aktien zu €32 wieder einzukaufen. Mal sehen, was möglich ist!
Ich habe soeben 300 Stück in Frankfurt zu €30.822 sowie 500 Stück in US zu $35.87 zurück gekauft!
Mehr geht nicht, da der Rest in Dynavax investiert wurde.
news/präsentation
so endlich mal neue infos und handfeste zahlen von radiusaus der präsentation vom 13. sep. 2017:
folie 9: interessante aktuelle angaben zum wachstum von tymlos
folie 17: angaben zum japan-deal
"Radius will receive an upfront payment and milestones for up to an aggregate
amount of $50 million and a low double-digit royalty rate"
und noch vieles mehr:
http://files.shareholder.com/downloads/AMDA-1D3H6P/520358272…
bleibt eine meiner kernpositionen
Antwort auf Beitrag Nr.: 55.751.451 von paul81 am 15.09.17 12:52:12Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)? Da ist eine Menge Fantasie eingepreist, dass Radius es schafft den anabolic market wieder zum Wachsen zu bringen. Zumal man derzeit mehr als 50Mio EUR pro Quartal Verlust einfährt....
Antwort auf Beitrag Nr.: 55.751.451 von paul81 am 15.09.17 12:52:12Angabe zu Folie 17 war bereits bekannt.
Antwort auf Beitrag Nr.: 55.751.784 von Ville7 am 15.09.17 13:31:11hallo Ville7,
das mit dem japan-deal war mir nicht bewusst, habs erst jetzt gesehen... danke auch für die restlichen kompetenten kommentare zum umsatz
das mit dem japan-deal war mir nicht bewusst, habs erst jetzt gesehen... danke auch für die restlichen kompetenten kommentare zum umsatz
Antwort auf Beitrag Nr.: 55.751.778 von Ville7 am 15.09.17 13:30:40
Soso, die "Rahmenzahlen" bleiben schwach und "nur 8Millionen Umsatz"... diese Vorhersage duerfte, wie schon so oft, weit daneben sein. Das schoene daran ist, diese Vorhersage ist ueberpruefbar.
Mark this comment!
Aber hin zu den wirklich wichtigen Dingen:
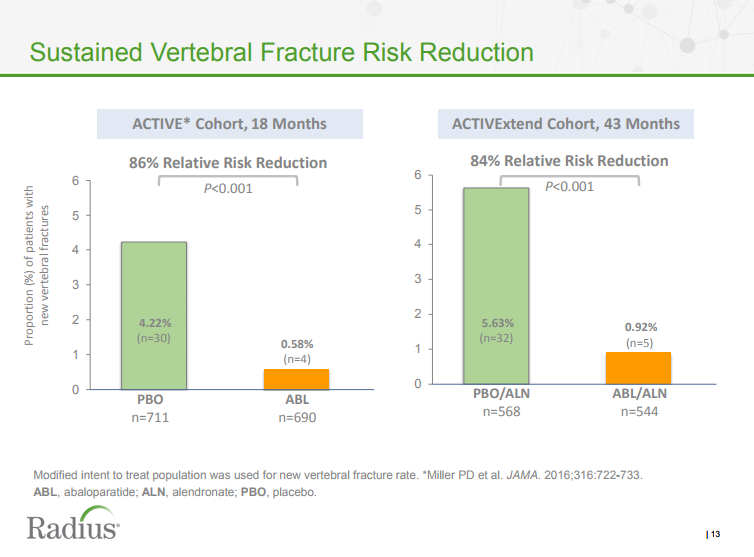
Zitat von Ville7: Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)? Da ist eine Menge Fantasie eingepreist, dass Radius es schafft den anabolic market wieder zum Wachsen zu bringen. Zumal man derzeit mehr als 50Mio EUR pro Quartal Verlust einfährt....
Soso, die "Rahmenzahlen" bleiben schwach und "nur 8Millionen Umsatz"... diese Vorhersage duerfte, wie schon so oft, weit daneben sein. Das schoene daran ist, diese Vorhersage ist ueberpruefbar.
Mark this comment!
Aber hin zu den wirklich wichtigen Dingen:

Antwort auf Beitrag Nr.: 55.754.370 von Cyberhexe am 15.09.17 17:56:25wenn der Marktanteil bei den Neuverschreibungen bis zum Ende des Jahres an die 20% herankommt, dann ist dieser Launch sehr erfolgreich. Diese Daten werden dazu beitragen:


Antwort auf Beitrag Nr.: 55.754.406 von Cyberhexe am 15.09.17 18:01:14BB Biotech scheint weiter an RDUS zu glauben;
Aktienkäufe im September:
50'000 am 14.9.2017
100'000 am 13.9.2017
50'000 am 12.9.2017
50'000 am 5.9.2017
Aktienkäufe im August:
60'000 am 16.8.2017
75'000 am 10.8.2017
75'000 am 9.8.2017
Insgesamt dürfte BB Biotech nun weit mehr als 5 Mio Aktien von Radius Health im Portfolio ausweisen. Let's go!
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-2…
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-2…
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-2…
Aktienkäufe im September:
50'000 am 14.9.2017
100'000 am 13.9.2017
50'000 am 12.9.2017
50'000 am 5.9.2017
Aktienkäufe im August:
60'000 am 16.8.2017
75'000 am 10.8.2017
75'000 am 9.8.2017
Insgesamt dürfte BB Biotech nun weit mehr als 5 Mio Aktien von Radius Health im Portfolio ausweisen. Let's go!
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-2…
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-2…
http://ir.radiuspharm.com/secfiling.cfm?filingID=899243-17-2…
Antwort auf Beitrag Nr.: 55.754.406 von Cyberhexe am 15.09.17 18:01:14Ich verwende ebenso wie du das Wort "wenn" (konkret: "wenn das so bleibt"). Das bedeutet, dass eine Bedingung eintreten muss, damit die das Gesagte eintritt.
Hieran merkt man mal wieder, dass du es überhaupt nicht blickst oder mir ( wieder mal was) unterstellen willst ich hätte die Bedingung prognostiziert.
Fakt ist, dass die Firma selbst mit 50% Marktanteil in USA 24 Monate lang nicht genug für den break even einnehmen würde.
Dringend notwendig daher:
* der in den letzten Quartalen unter Druck der Konkurrenz geratenen anabolic market zu stabilisieren und dringend wieder zum Wachsen zu bringen
* EU Zulassung ( diese Woche war ABA aber wieder nicht auf der Agenda)
* patch - und zwar schnell
* ihren SERD mit schnellem Weg zum Markt
* strikte Kostenkontrolle
Hieran merkt man mal wieder, dass du es überhaupt nicht blickst oder mir ( wieder mal was) unterstellen willst ich hätte die Bedingung prognostiziert.
Fakt ist, dass die Firma selbst mit 50% Marktanteil in USA 24 Monate lang nicht genug für den break even einnehmen würde.
Dringend notwendig daher:
* der in den letzten Quartalen unter Druck der Konkurrenz geratenen anabolic market zu stabilisieren und dringend wieder zum Wachsen zu bringen
* EU Zulassung ( diese Woche war ABA aber wieder nicht auf der Agenda)
* patch - und zwar schnell
* ihren SERD mit schnellem Weg zum Markt
* strikte Kostenkontrolle
Antwort auf Beitrag Nr.: 55.755.762 von Cyberhexe am 15.09.17 21:23:00BbBiotech haben sich hier einfach verzockt und sind zu tief drin um die Aktie auf einen fairen Wert fallen zu lassen. Daher diese Stützungsaktionen.
Antwort auf Beitrag Nr.: 55.757.388 von Ville7 am 16.09.17 09:47:38
Schlimmer geht immer, wobei diese Blüten jedoch nur schwer zu übertreffen sind:
"Ich verwende ebenso wie du das Wort "wenn" (konkret: "wenn das so bleibt"). Das bedeutet, dass eine Bedingung eintreten muss, damit die das Gesagte eintritt."
Auch die erfolgreichsten Pharmawirkstoffe/Medikamente sind nicht durch ein katapultähnliches Wachstum gekennzeichnet, sondern durch eine stetige Umsatzzunahme.
So hat bspw. Roches erfolgreiches Brustkrebsmedikament Herceptin, mit welchem die Basler kurz vor Ablauf des Patentschutzes jährlich über 7 Milliarden USD Umsatz generieren, diese Sphären auch nicht über Nacht erreicht:
"Herceptin sales for 1999, the first full year on the market, were $188.4 million."
Die Prämisse deiner Aussage, "wenn das so bleibt" ist deswegen falsch bzw. fast schon naiv. Wenn der Umsatz bei Herceptin so geblieben wäre, dann .... wie gesagt , schlimmer geht fast nimmer.
Deine Prognose steht auf alle Fälle bei 8 Mio Umsatz ($ oder € ?) bei TYMLOS für 2017.
An solchen Prognosen muss man sich messen lassen! Aber wie so oft sind deine Beiträge nur von imaginärem Wert.
Zitat von Ville7: Ich verwende ebenso wie du das Wort "wenn" (konkret: "wenn das so bleibt"). Das bedeutet, dass eine Bedingung eintreten muss, damit die das Gesagte eintritt.
Hieran merkt man mal wieder, dass du es überhaupt nicht blickst oder mir ( wieder mal was) unterstellen willst ich hätte die Bedingung prognostiziert.
Fakt ist, dass die Firma selbst mit 50% Marktanteil in USA 24 Monate lang nicht genug für den break even einnehmen würde.
Dringend notwendig daher:
* der in den letzten Quartalen unter Druck der Konkurrenz geratenen anabolic market zu stabilisieren und dringend wieder zum Wachsen zu bringen
* EU Zulassung ( diese Woche war ABA aber wieder nicht auf der Agenda)
* patch - und zwar schnell
* ihren SERD mit schnellem Weg zum Markt
* strikte Kostenkontrolle
Schlimmer geht immer, wobei diese Blüten jedoch nur schwer zu übertreffen sind:
"Ich verwende ebenso wie du das Wort "wenn" (konkret: "wenn das so bleibt"). Das bedeutet, dass eine Bedingung eintreten muss, damit die das Gesagte eintritt."
Auch die erfolgreichsten Pharmawirkstoffe/Medikamente sind nicht durch ein katapultähnliches Wachstum gekennzeichnet, sondern durch eine stetige Umsatzzunahme.
So hat bspw. Roches erfolgreiches Brustkrebsmedikament Herceptin, mit welchem die Basler kurz vor Ablauf des Patentschutzes jährlich über 7 Milliarden USD Umsatz generieren, diese Sphären auch nicht über Nacht erreicht:
"Herceptin sales for 1999, the first full year on the market, were $188.4 million."
Die Prämisse deiner Aussage, "wenn das so bleibt" ist deswegen falsch bzw. fast schon naiv. Wenn der Umsatz bei Herceptin so geblieben wäre, dann .... wie gesagt , schlimmer geht fast nimmer.
Deine Prognose steht auf alle Fälle bei 8 Mio Umsatz ($ oder € ?) bei TYMLOS für 2017.
An solchen Prognosen muss man sich messen lassen! Aber wie so oft sind deine Beiträge nur von imaginärem Wert.
Antwort auf Beitrag Nr.: 55.758.987 von Cyberhexe am 16.09.17 16:08:54das ist doch mal ein überaus positives Zeichen: der neue CEO investiert knapp 200Tsd$ in Aktien seines Unternehmens!
Radius Health Inc (RDUS) President and CEO Jesper Hoiland Bought $199,592 of Shares
GuruFocus.comSeptember 15, 2017Comment
- By insider
President and CEO of Radius Health Inc (RDUS) Jesper Hoiland bought 6,100 shares of RDUS on 09/15/2017 at an average price of $32.72 a share. The total cost of this purchase was $199,592.
Radius Health Inc (RDUS) President and CEO Jesper Hoiland Bought $199,592 of Shares
GuruFocus.comSeptember 15, 2017Comment
- By insider
President and CEO of Radius Health Inc (RDUS) Jesper Hoiland bought 6,100 shares of RDUS on 09/15/2017 at an average price of $32.72 a share. The total cost of this purchase was $199,592.
Antwort auf Beitrag Nr.: 55.768.770 von Cyberhexe am 18.09.17 16:22:10anbei etwas "Food for thought" zu Wirkstoffen mit osteoanaboler Wirkung:
Investigational anabolic agents for the treatment of osteoporosis: an update on recent developments
7. Expert opinion
Most of the available treatment options in osteoporosis suppress bone resorption and therefore exert a modest incremental effect in bone density with a concomitant fracture risk reduction. There is an obvious need for anabolic agents that would result in true bone gain. Teriparatide is currently the only available anabolic treatment option; however, limitations in its use include potential hypercalcemia, the need for daily sc injections, concurrent stimulation of bone resorption, and limited administration period. Abaloparatide, which was recently approved by the FDA, is more efficient in reducing vertebral and non-vertebral fractures and interestingly was associated with less serum calcium elevation than teriparatide. Yet it is also administered by daily sc injections. There is a significant interest of the pharmaceutical industry in developing PTH/PTHrP analogs with alternative, more convenient routes of administration. An agent that would stimulate bone formation without affecting bone resorption sounds as the ‘holy grail’ of osteoporosis treatment; however, some molecules promising such effects are currently tested at early stages of development.
In the field of Wnt antagonists’ neutralization, the almost exclusive production of sclerostin from osteocytes suggests a minimal risk of off-target AEs and renders it the most appealing target. From the several molecules that have been identified and initially tested, only romosozumab has made it to the completion of phase 3 clinical trials, although not uneventfully, and hopes to receive an approval for the treatment of osteoporosis in the near future.
Calcilytics have largely proved inefficient, and unless a molecule capable of increasing PTH in a more transient and controlled manner is produced, they are not expected to develop further.
http://www.tandfonline.com/doi/full/10.1080/13543784.2017.13…
Investigational anabolic agents for the treatment of osteoporosis: an update on recent developments
7. Expert opinion
Most of the available treatment options in osteoporosis suppress bone resorption and therefore exert a modest incremental effect in bone density with a concomitant fracture risk reduction. There is an obvious need for anabolic agents that would result in true bone gain. Teriparatide is currently the only available anabolic treatment option; however, limitations in its use include potential hypercalcemia, the need for daily sc injections, concurrent stimulation of bone resorption, and limited administration period. Abaloparatide, which was recently approved by the FDA, is more efficient in reducing vertebral and non-vertebral fractures and interestingly was associated with less serum calcium elevation than teriparatide. Yet it is also administered by daily sc injections. There is a significant interest of the pharmaceutical industry in developing PTH/PTHrP analogs with alternative, more convenient routes of administration. An agent that would stimulate bone formation without affecting bone resorption sounds as the ‘holy grail’ of osteoporosis treatment; however, some molecules promising such effects are currently tested at early stages of development.
In the field of Wnt antagonists’ neutralization, the almost exclusive production of sclerostin from osteocytes suggests a minimal risk of off-target AEs and renders it the most appealing target. From the several molecules that have been identified and initially tested, only romosozumab has made it to the completion of phase 3 clinical trials, although not uneventfully, and hopes to receive an approval for the treatment of osteoporosis in the near future.
Calcilytics have largely proved inefficient, and unless a molecule capable of increasing PTH in a more transient and controlled manner is produced, they are not expected to develop further.
http://www.tandfonline.com/doi/full/10.1080/13543784.2017.13…
Antwort auf Beitrag Nr.: 55.781.367 von Cyberhexe am 20.09.17 08:28:00gemäss Pflichtmitteilung von gestern hält BB Biotech mittlerweile 5,677,322 Aktien von RADIUS Health; dies entspricht 13% des Unternehmens:
http://files.shareholder.com/downloads/AMDA-1D3H6P/524673472…
...auch wenn "sehr gewiefte Teilnehmer" dies sogar als Kontraindikator für eine gute Kursentwicklung interpretieren, sei auf die gute "Performance" der CH-Biotechspezialisten verwiesen:
http://www.finanzen.net/chart/BB_BIOTECH
http://files.shareholder.com/downloads/AMDA-1D3H6P/524673472…
...auch wenn "sehr gewiefte Teilnehmer" dies sogar als Kontraindikator für eine gute Kursentwicklung interpretieren, sei auf die gute "Performance" der CH-Biotechspezialisten verwiesen:
http://www.finanzen.net/chart/BB_BIOTECH
Antwort auf Beitrag Nr.: 55.757.424 von Ville7 am 16.09.17 09:53:57
...dann wollen wir uns doch mal diesen Beitrag merken!
Zitat von Ville7: BbBiotech haben sich hier einfach verzockt und sind zu tief drin um die Aktie auf einen fairen Wert fallen zu lassen. Daher diese Stützungsaktionen.
...dann wollen wir uns doch mal diesen Beitrag merken!
!
Dieser Beitrag wurde von MadMod moderiert. Grund: Provokation
Antwort auf Beitrag Nr.: 55.790.523 von Cyberhexe am 21.09.17 07:19:32
So investieren die Experten von BBBiotech:
Man neigt zu denken, dass dein Arbeitgeber BBBiotech heißt, so wie du die hier verteidigst. Und dass du selbst für die katastrophale Auswahl von Radius Health für BBBiotech verantwortlich bist. In diesem Falle hätte ich dich längst gefeuert.
Zitat von Cyberhexe: gemäss Pflichtmitteilung von gestern hält BB Biotech mittlerweile 5,677,322 Aktien von RADIUS Health; dies entspricht 13% des Unternehmens:
http://files.shareholder.com/downloads/AMDA-1D3H6P/524673472…
...auch wenn "sehr gewiefte Teilnehmer" dies sogar als Kontraindikator für eine gute Kursentwicklung interpretieren, sei auf die gute "Performance" der CH-Biotechspezialisten verwiesen:
http://www.finanzen.net/chart/BB_BIOTECH
So investieren die Experten von BBBiotech:
Man neigt zu denken, dass dein Arbeitgeber BBBiotech heißt, so wie du die hier verteidigst. Und dass du selbst für die katastrophale Auswahl von Radius Health für BBBiotech verantwortlich bist. In diesem Falle hätte ich dich längst gefeuert.
!
Dieser Beitrag wurde von MadMod moderiert. Grund: themenfremder Inhalt
Antwort auf Beitrag Nr.: 55.793.823 von Ville7 am 21.09.17 13:26:55die Beiträge dieses Teilnehmers sind oft tendenziös, indem bspw. zeitlich genau der Kursverlauf gewählt wird, die dessen Aussage stützen. Einfach billig!
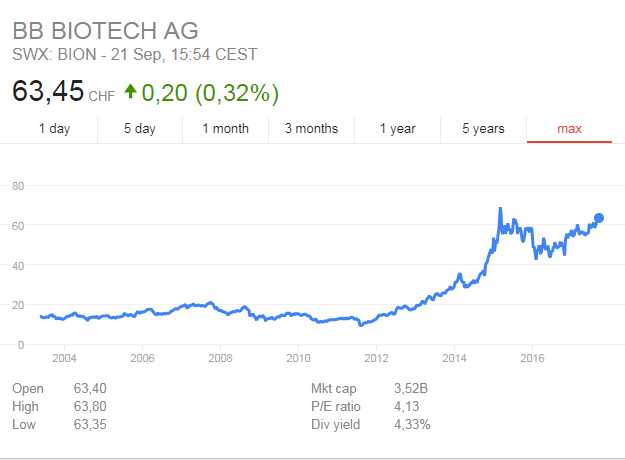

Antwort auf Beitrag Nr.: 55.795.254 von Cyberhexe am 21.09.17 16:09:26
Ich wusste, dass du kneifst, abzulenken versuchst und dich einem sachlichen Zugang verweigerst. q.e.d.
Hier daher erneut das Angebot:
Wenn du eine Prognose der Umsätze von Tymlos für das Jahr 2017 von mir willst, dann kann ich sie dir nennen, denn ich habe das für mich bereits durchkalkuliert. Ich werde diese aber erst hier veröffentlichen, wenn du zuvor deine Prognose gepostet hast. Meine Prognose in Mio USD wird eine Range von 5Mio USD umfassen, d.h. ich nenne ein unteres Erwartungsende und ein oberes Erwartungsende - d.h. zwischen diesen Zahlen (oben/unten) wird dann ein Abstand von 5Mio USD sein. Basierend auf einem normalen bis guten Start in den Launch. Die 8 Mio sind dabei ein worse case Szenario, aber nicht meine Prognose.
Zitat von Cyberhexe: da nun wiederholt Angriffe gegen die Person und nicht gegen die Sache vorgenommen werden, habe ich diesen Beitrag gemeldet!
Ich wusste, dass du kneifst, abzulenken versuchst und dich einem sachlichen Zugang verweigerst. q.e.d.
Hier daher erneut das Angebot:
Wenn du eine Prognose der Umsätze von Tymlos für das Jahr 2017 von mir willst, dann kann ich sie dir nennen, denn ich habe das für mich bereits durchkalkuliert. Ich werde diese aber erst hier veröffentlichen, wenn du zuvor deine Prognose gepostet hast. Meine Prognose in Mio USD wird eine Range von 5Mio USD umfassen, d.h. ich nenne ein unteres Erwartungsende und ein oberes Erwartungsende - d.h. zwischen diesen Zahlen (oben/unten) wird dann ein Abstand von 5Mio USD sein. Basierend auf einem normalen bis guten Start in den Launch. Die 8 Mio sind dabei ein worse case Szenario, aber nicht meine Prognose.
!
Dieser Beitrag wurde von FairMOD moderiert. Grund: themenfremder Inhalt
Antwort auf Beitrag Nr.: 55.795.332 von Cyberhexe am 21.09.17 16:17:57Es geht hier nicht um die Performance von BBBiotech, sondern um den katastrophalen Kursverlauf von RDUS und die Fehlentscheidung von BBBiotech nun bereits 13% der MK in diese Aktie zu stecken und weiter laufend zu verbilligen. "Total Disaster" bzw. "weak on RDUS" würde Trump sagen.
Aber du mal wieder am Ablenken und Nebelbomben werfen. Typisch. Aber so ist das halt, wenn man nicht zugestehen will, dass man falsch in den Einschätzungen lag. Genau das hast du. Gewaltig. Und BBBiotech eben auch. Daher ein Spiegel für dich. Kostenlos von mir...
Aber du mal wieder am Ablenken und Nebelbomben werfen. Typisch. Aber so ist das halt, wenn man nicht zugestehen will, dass man falsch in den Einschätzungen lag. Genau das hast du. Gewaltig. Und BBBiotech eben auch. Daher ein Spiegel für dich. Kostenlos von mir...

Antwort auf Beitrag Nr.: 55.795.917 von Ville7 am 21.09.17 17:14:04...richtig, es geht hier einzig und allein um Informationen zu RADIUS Health.
Und hierzu hast du, abegesehen von deiner Umsatzschätzung für 2017...
Ville7 schrieb am 15.09.17 13:30:40 Beitrag Nr. 333 ( 55.751.778 )
"Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)?"
...herzlich wenig beizutragen.
Tendenziös wie viele deiner Beiträge ist bspw. diese Aussage
Ville7 schrieb am 21.09.17 17:14:04 Beitrag Nr. 352 ( 55.795.917 )
...sondern um den katastrophalen Kursverlauf von RDUS und die Fehlentscheidung von BBBiotech nun bereits 13% der MK in diese Aktie zu stecken und weiter laufend zu verbilligen. "Total Disaster" bzw. "weak on RDUS" würde Trump sagen.
Die Performance seit Threaderöffnung im Mai 2016 ist tatsächlich nicht wirklich befriedigend, sie beträgt nämlich 0%. Deswegen jedoch von einem katastrophalen Kursverlauf zu sprechen, ist mehr als tendenziös. Hierbei sei an den Kursverlauf bei Exelixis erinnert, wonach meine persönliche Performance nach einem Jahr von -50% auf mittlerweile über +1000% angestiegen ist.
Recht geben möchte ich dir für die Aussage, dass sich das Niveau Richtung Kindergarten bewegt!
Und hierzu hast du, abegesehen von deiner Umsatzschätzung für 2017...
Ville7 schrieb am 15.09.17 13:30:40 Beitrag Nr. 333 ( 55.751.778 )
"Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)?"
...herzlich wenig beizutragen.
Tendenziös wie viele deiner Beiträge ist bspw. diese Aussage
Ville7 schrieb am 21.09.17 17:14:04 Beitrag Nr. 352 ( 55.795.917 )
...sondern um den katastrophalen Kursverlauf von RDUS und die Fehlentscheidung von BBBiotech nun bereits 13% der MK in diese Aktie zu stecken und weiter laufend zu verbilligen. "Total Disaster" bzw. "weak on RDUS" würde Trump sagen.
Die Performance seit Threaderöffnung im Mai 2016 ist tatsächlich nicht wirklich befriedigend, sie beträgt nämlich 0%. Deswegen jedoch von einem katastrophalen Kursverlauf zu sprechen, ist mehr als tendenziös. Hierbei sei an den Kursverlauf bei Exelixis erinnert, wonach meine persönliche Performance nach einem Jahr von -50% auf mittlerweile über +1000% angestiegen ist.
Recht geben möchte ich dir für die Aussage, dass sich das Niveau Richtung Kindergarten bewegt!
!
Dieser Beitrag wurde von FairMOD moderiert. Grund: Persönliche Differenzen bitte via BM klären
Antwort auf Beitrag Nr.: 55.796.406 von Ville7 am 21.09.17 18:03:33Pure Sachlichkeit: Schauen wir mal wie RDUS sich in EUR geschlagen hat im Vergleich zu EXEL und dem IBB (Biotech Index) seit dem Zeitpunkt deiner Threaderföffnung = Zeitpunkt deines RDUS Kaufs = Zeitpunkt deines EXEL Verkaufs.

Antwort auf Beitrag Nr.: 52.512.431 von cyberhexe123 am 31.05.16 20:36:47Aus dem Threaderöffnungsbeitrag von Cyberhexe:
Ohne Worte.
Zitat von cyberhexe123: ...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben.
Ohne Worte.
Antwort auf Beitrag Nr.: 55.796.517 von Ville7 am 21.09.17 18:14:54
...das würde ich so immer wieder tun bei einem Investitionsgrad von 80% in Exelixis und bei dieser Performance. Ich weiss jedoch nicht, ob dein Investitionsgrad bei Exelixis jemals 50% betragen hat (?), da du bspw. am 11.11.15 folgendes zum Besten gegeben hast:
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) die folgenden Sätze" "Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen"."
Eigentlich möchte ich auf derartige persönlichen Angriffe nicht weiter reagieren, deswegen noch einmal etwas Inhaltliches:
https://www.sec.gov/Archives/edgar/data/924223/0001193125172…
Zitat von Ville7: Aus dem Threaderöffnungsbeitrag von Cyberhexe:
Zitat von cyberhexe123: ...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben.
Ohne Worte.
...das würde ich so immer wieder tun bei einem Investitionsgrad von 80% in Exelixis und bei dieser Performance. Ich weiss jedoch nicht, ob dein Investitionsgrad bei Exelixis jemals 50% betragen hat (?), da du bspw. am 11.11.15 folgendes zum Besten gegeben hast:
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) die folgenden Sätze" "Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen"."
Eigentlich möchte ich auf derartige persönlichen Angriffe nicht weiter reagieren, deswegen noch einmal etwas Inhaltliches:
https://www.sec.gov/Archives/edgar/data/924223/0001193125172…
!
Dieser Beitrag wurde von FairMOD moderiert. Grund: themenfremder Inhalt!
Dieser Beitrag wurde von FairMOD moderiert. Grund: themenfremder Inhalt
neben Abaloparatide ruhen die Hoffnungen bei RADIUS auf Elacestrant, einem selektiven Östrogen-Rezeptor-Degrader zur Behandlung von (ER+)-Brustkrebs;
anbei "Food for thought" zu Elacestrant:
http://clincancerres.aacrjournals.org/content/23/16/4793.lon…
Anfang 2018 soll eine "single-arm" ph2-Studie in Monotherapie bei ER+-Brustkrebs gestartet werden:

anbei "Food for thought" zu Elacestrant:
http://clincancerres.aacrjournals.org/content/23/16/4793.lon…
Anfang 2018 soll eine "single-arm" ph2-Studie in Monotherapie bei ER+-Brustkrebs gestartet werden:

Warum kommt RDUS einfach nicht in Fahrt? Während der IBB innerhalb eines Jahres immerhin 10% gestiegen ist, hat sich RDUS kontinuierlich fast halbiert!?

Anscheindend hat es Tymlos schwer trotz gravierender Zulassungsprobleme von Romosozumab Marktanteile zu gewinnen... die Lage wird auch nicht besser, wenn Forteo demnächst generisch wird.
http://www.evaluategroup.com/Universal/View.aspx?type=Story&…
"Abaloparatide is essentially a Forteo me-too, which means that it could carry the same risk of osteosarcoma. But Radius’s project has shown a benefit over Forteo on bone mineral density measures in the phase III Active trial.
A Forteo biosimilar might be a blessing for Radius if it spurs Lilly into an acquisition, but it could also be a curse. A small physician survey by Jefferies analysts found that, although abaloparatide was generally seen as a modest improvement over Forteo, the vast majority – 85% – would first use a biosimilar version of Forteo if this were available.
... Abaloparatide could bring in $467m by 2022, according to EvaluatePharma sellside consensus, but much of this depends on Radius finding a partner at the very least – and one that is willing to go up against Amgen."
Bisher konnte kein Partner gefunden werden, so dass die Erwartungen weiter sinken...
https://www.thepharmaletter.com/article/another-look-at-phar…
"Essentially a me-too version of Lilly’s Forteo, it has shown a benefit over Forteo on bone mineral density measures, but could run into problems when Lilly’s product comes off patent next year.
This could be one reason why Tymlos is not forecast to trouble the top-five osteoporosis drugs in 2022, with EvaluatePharma’s sellside consensus forecasting sales of just $157 million."
Zumindest scheint der Markt diesen Erwartungen zu entsprechen, wenn man sich den Chart ansieht. Bisher sieht es jedenfalls nicht gut aus.
Gruß
ipollit
Anscheindend hat es Tymlos schwer trotz gravierender Zulassungsprobleme von Romosozumab Marktanteile zu gewinnen... die Lage wird auch nicht besser, wenn Forteo demnächst generisch wird.
http://www.evaluategroup.com/Universal/View.aspx?type=Story&…
"Abaloparatide is essentially a Forteo me-too, which means that it could carry the same risk of osteosarcoma. But Radius’s project has shown a benefit over Forteo on bone mineral density measures in the phase III Active trial.
A Forteo biosimilar might be a blessing for Radius if it spurs Lilly into an acquisition, but it could also be a curse. A small physician survey by Jefferies analysts found that, although abaloparatide was generally seen as a modest improvement over Forteo, the vast majority – 85% – would first use a biosimilar version of Forteo if this were available.
... Abaloparatide could bring in $467m by 2022, according to EvaluatePharma sellside consensus, but much of this depends on Radius finding a partner at the very least – and one that is willing to go up against Amgen."
Bisher konnte kein Partner gefunden werden, so dass die Erwartungen weiter sinken...
https://www.thepharmaletter.com/article/another-look-at-phar…
"Essentially a me-too version of Lilly’s Forteo, it has shown a benefit over Forteo on bone mineral density measures, but could run into problems when Lilly’s product comes off patent next year.
This could be one reason why Tymlos is not forecast to trouble the top-five osteoporosis drugs in 2022, with EvaluatePharma’s sellside consensus forecasting sales of just $157 million."
Zumindest scheint der Markt diesen Erwartungen zu entsprechen, wenn man sich den Chart ansieht. Bisher sieht es jedenfalls nicht gut aus.
Gruß
ipollit
Antwort auf Beitrag Nr.: 55.809.654 von ipollit am 24.09.17 00:05:08...nun, einen Kursverlauf für einen ganz bestimmten Zeitraum zu betrachten, ist sicherlich legitim...aber letztendlich nur die halbe Wahrheit: betrachtet man nämlich eine längere Zeitspanne, dann sind ganz andere Aussagen möglich:
Richtig ist jedoch, dass seit Threaderöffnung der Kurs der RADIUS-Aktie in USD praktisch unverändert ist und somit lediglich ein Kursverlust aufgrund der Eurostärke zu verzeichnen ist - obschon ich persönlich für die amerikanischen Werte ein $-Konto unterhalte und somit nach Verkauf von Aktien andere Werte entsprechend günstiger einkaufe, und sozusagen den Kursunterschied erst dann realisiere, wenn § in € umgetauscht werden.
Richtig ist auch, dass die Performance durch die Verzögerung der Zulassung von Abaloparatide in Europa gelitten hat; ich bin jedoch sehr zuversichtlich, dass der Wirkstoff noch in 2017 auch in Europa zugelassen wird. Spannend wird tatsächlich, wie sich TYMLOS am Markt in den nächsten monaten etablieren wird. Die grosse Phantasie ist sicherlich durch die transdermale Applikation des Wirkstoffes gegeben - aber auch das wird noch einige Zeit dauern. Ebenso die Entwicklung des onkologischen (BC) Wirkstoffes Elacestrant.
Aufgrund der Verzögerungen habe ich den Bestand an Radius-Aktien auf 2100 Aktien stark reduziert und bin überproportional in Progenics und eher vorsichtig in Dynavax noch vor dem Heplisav-AC (siehe Thread "Diskussion zu Dynavax Technologies"; mehr als verdoppelt seit 08/17) eingestiegen.
Die 2100 RDUS-Aktien werde ich jedoch mindestens bis Ende Jahr halten.
Gz
ch

Richtig ist jedoch, dass seit Threaderöffnung der Kurs der RADIUS-Aktie in USD praktisch unverändert ist und somit lediglich ein Kursverlust aufgrund der Eurostärke zu verzeichnen ist - obschon ich persönlich für die amerikanischen Werte ein $-Konto unterhalte und somit nach Verkauf von Aktien andere Werte entsprechend günstiger einkaufe, und sozusagen den Kursunterschied erst dann realisiere, wenn § in € umgetauscht werden.
Richtig ist auch, dass die Performance durch die Verzögerung der Zulassung von Abaloparatide in Europa gelitten hat; ich bin jedoch sehr zuversichtlich, dass der Wirkstoff noch in 2017 auch in Europa zugelassen wird. Spannend wird tatsächlich, wie sich TYMLOS am Markt in den nächsten monaten etablieren wird. Die grosse Phantasie ist sicherlich durch die transdermale Applikation des Wirkstoffes gegeben - aber auch das wird noch einige Zeit dauern. Ebenso die Entwicklung des onkologischen (BC) Wirkstoffes Elacestrant.
Aufgrund der Verzögerungen habe ich den Bestand an Radius-Aktien auf 2100 Aktien stark reduziert und bin überproportional in Progenics und eher vorsichtig in Dynavax noch vor dem Heplisav-AC (siehe Thread "Diskussion zu Dynavax Technologies"; mehr als verdoppelt seit 08/17) eingestiegen.
Die 2100 RDUS-Aktien werde ich jedoch mindestens bis Ende Jahr halten.
Gz
ch
Antwort auf Beitrag Nr.: 53.307.972 von Cyberhexe am 19.09.16 23:43:08
Derartige Quervergleiche sind gefährlich. Im vorliegenden Fall sind die Patientenkollektive schwer vergleichbar, z.B. sind in der zitierten Romosozumab-Studie ausschließlich Patientinnen mit einem T-Score zwischen -2,5 und -3,5 untersucht worden, während in der Abaloparatide-Studie ein großer Anteil der Patientinnen einen T-Score > -2,5 aufwies.
Zitat von Cyberhexe: Abaloparatide zeigte eine 83% Risikoreduktion bei Wirbelsäulenfrakturen während romosozumab dieses Risiko lediglich um 73% reduzierte.
Bei den nicht die Wiebelsäule betreffenden Frakturen wurde bei romosozumab kein statistisch signifikanter Rückgang der Frakturen nachgewiesen:
Nonvertebral fractures had occurred in 56 of 3589 patients (1.6%) in the romosozumab group and in 75 of 3591 (2.1%) in the placebo group (P=0.10).
Bei Abalaoparatide hingegen schon - wenn auch knapp (0.049!):
Dieser statistisch signifikante Wirkungsnachweis bei den nicht die Wirbelsäule betreffenden Frakturen ist gegenüber Amgens romosozumab ein grosses Plus.
Derartige Quervergleiche sind gefährlich. Im vorliegenden Fall sind die Patientenkollektive schwer vergleichbar, z.B. sind in der zitierten Romosozumab-Studie ausschließlich Patientinnen mit einem T-Score zwischen -2,5 und -3,5 untersucht worden, während in der Abaloparatide-Studie ein großer Anteil der Patientinnen einen T-Score > -2,5 aufwies.
Antwort auf Beitrag Nr.: 55.811.826 von Joschka Schröder am 24.09.17 15:58:42...selbstverständlich sind "face-to-face"-Studien immer aussagekräftiger; allerdings sind diese eher die Ausnahme, so dass solche Quervergleiche von unterschiedlichen Studien dann doch immer wieder gemacht werden. In diesem Fall ist Abaloparatide im Vorteil, weil statistische Signifikanz bei den nicht die Wirbelsäule betreffenden Frakturen erreicht wurde. Der Unterschied bei Osteoporose ist jedoch, dass das Ereignis und nicht die Therapie dessen beschrieben wird, so dass nicht nach Indikation "die Wirbelsäule betreffend" bzw. "nicht betreffend" verschrieben wird. Deswegen ist dieser Vorteil von Abaloparatide tatsächlich nur marginal.
Antwort auf Beitrag Nr.: 55.887.502 von Cyberhexe am 05.10.17 16:38:08Wie ich bereits geschrieben habe, sind die Patientenkollektive kaum vergleichbar, weil die Patienten in beiden Kollektiven unterschiedlich schwer krank waren, was sich natürlich auch auf das jeweilige Therapieergebnis auswirkt.
Antwort auf Beitrag Nr.: 55.811.826 von Joschka Schröder am 24.09.17 15:58:42
Derartige Quervergleiche sind gefährlich. Im vorliegenden Fall sind die Patientenkollektive schwer vergleichbar, z.B. sind in der zitierten Romosozumab-Studie ausschließlich Patientinnen mit einem T-Score zwischen -2,5 und -3,5 untersucht worden, während in der Abaloparatide-Studie ein großer Anteil der Patientinnen einen T-Score > -2,5 aufwies.[/quote]
Deinen Ausführungen liegen 2 Denkfehler zugrunde:
1.) da beide Studien mit Plazebo vergleichen und die Einschluss bzw. Ausschlusskriterien für beide Gruppen (Verum und Plazebo) in den jeweiligen Studien identisch sind, ist das Erreichen von statistischer Signifikanz bei Abaloparatide ein Nachweis für dessen Wirksamkeit, während dieser Nachweis bei Romosozumab nicht gelungen ist.
2.) Auch die unterschiedliche Stichprobe beim T-Wert spricht eher für Abaloparatide.
Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist, ist der Nachweis der Wirksamkeit bei gleich grosser Stichprobe schwerer zu erbringen. Dies liegt in der Natur der Indikation Osteoporose, in welcher nicht die Therapie einer Erkrankung gemessen wird (z.B. PFS) sondern die Häufigkeit der Ereignisse. Je geringer die Abweichung vom Standard, desto kleiner der Unterschied bei den Fallzahlen und umso schwieriger wird der Nachweis über die Wirksamkeit (Extremsituation überdenken: kein Unterschied beim T-Wert, Nachweis wäre nicht zu erbringen!).
Zitat von Joschka Schröder:
Derartige Quervergleiche sind gefährlich. Im vorliegenden Fall sind die Patientenkollektive schwer vergleichbar, z.B. sind in der zitierten Romosozumab-Studie ausschließlich Patientinnen mit einem T-Score zwischen -2,5 und -3,5 untersucht worden, während in der Abaloparatide-Studie ein großer Anteil der Patientinnen einen T-Score > -2,5 aufwies.[/quote]
Deinen Ausführungen liegen 2 Denkfehler zugrunde:
1.) da beide Studien mit Plazebo vergleichen und die Einschluss bzw. Ausschlusskriterien für beide Gruppen (Verum und Plazebo) in den jeweiligen Studien identisch sind, ist das Erreichen von statistischer Signifikanz bei Abaloparatide ein Nachweis für dessen Wirksamkeit, während dieser Nachweis bei Romosozumab nicht gelungen ist.
2.) Auch die unterschiedliche Stichprobe beim T-Wert spricht eher für Abaloparatide.
Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist, ist der Nachweis der Wirksamkeit bei gleich grosser Stichprobe schwerer zu erbringen. Dies liegt in der Natur der Indikation Osteoporose, in welcher nicht die Therapie einer Erkrankung gemessen wird (z.B. PFS) sondern die Häufigkeit der Ereignisse. Je geringer die Abweichung vom Standard, desto kleiner der Unterschied bei den Fallzahlen und umso schwieriger wird der Nachweis über die Wirksamkeit (Extremsituation überdenken: kein Unterschied beim T-Wert, Nachweis wäre nicht zu erbringen!).
Antwort auf Beitrag Nr.: 55.896.040 von Cyberhexe am 06.10.17 14:55:58Gehe ich recht in der Annahme, dass Du die betreffenden Studienpublikationen niemals vollständig gelesen hast, sondern Dein Wissen aus rudimentären Zusammenfassungen generierst und Dir den Rest irgendwie zusammenreimst?
Ich habe wenig Zeit und möchte es deshalb kurz halten:
1. Die Einschlusskriterien beider Studien sind nicht miteinander vergleichbar!
Abaloparatide-Studie: The women are to have a bone mineral density (BMD) T score ≤ -2.5 and > -5.0 at the lumbar spine or hip (femoral neck) by dual energy x-ray absorptiometry (DXA) and radiological evidence of 2 or more mild or one or more moderate lumbar or thoracic vertebral fractures, or history of low trauma forearm, humerus, sacral, pelvic, hip, femoral, or tibial fracture within the past 5 years. Postmenopausal women older than 65 who meet the above fracture criteria but have a T score ≤ -2.0 and > -5.0 may be enrolled. Women older than 65 who do not meet the fracture criteria may also be enrolled if their T score is ≤ -3.0 and > -5.0.
Romosuzumab-Studie: Postmenopausal women (55 Years to 90 Years) with osteoporosis, defined as low bone mineral density (BMD T-score at the total hip or femoral neck of ≤ -2.50), aber cave! Exclusion Criteria: BMD T-score of ≤ -3.50 at the total hip or femoral neck, history of hip fracture, any severe or more than 2 moderate vertebral fractures, as assessed by the central imaging based on lateral spine x-rays
2. Nicht nur die Patientinnenkollektive sind nicht vergleichbar, die Frakturendpunkte sind es auch nicht!
In der Romosozumab-Studie wird nach 12 Monaten untersucht, in der Abaloparatide-Studie hingegen nach 18 Monaten. Wie wichtig der Untersuchungszeitpunkt ist, siehst Du in nachfolgender Abbildung aus der Abaloparatide-Studie:
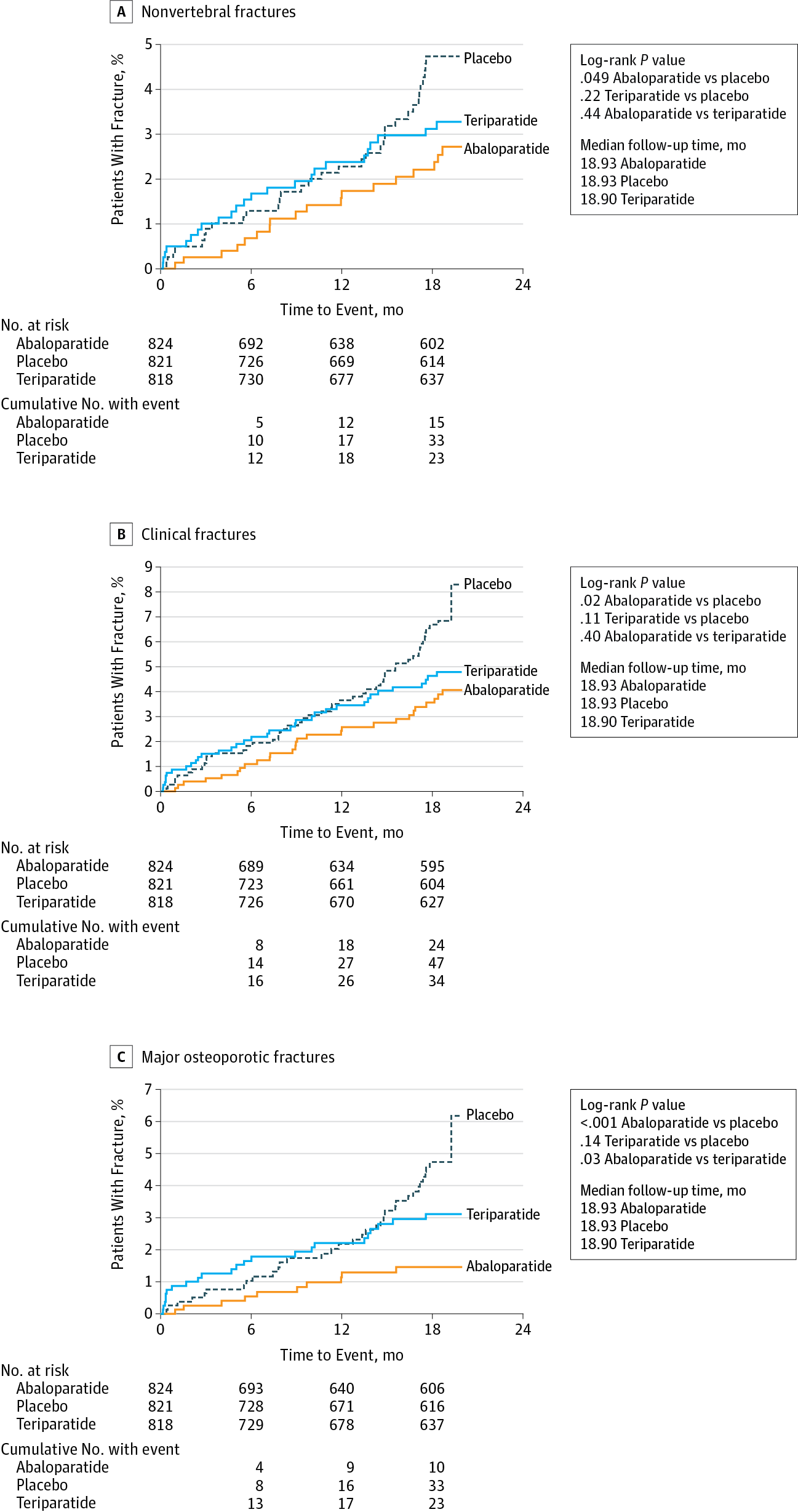
Es geht um die non-vertebralen Frakturen in A. Was meinst Du, wie wäre das Ergebnis ausgefallen, wenn die Frakturdaten nicht nach 18 Monaten, sondern wie in der Romosozumab-Studie nach 12 Monaten erhoben worden wären?
Ich habe wenig Zeit und möchte es deshalb kurz halten:
1. Die Einschlusskriterien beider Studien sind nicht miteinander vergleichbar!
Abaloparatide-Studie: The women are to have a bone mineral density (BMD) T score ≤ -2.5 and > -5.0 at the lumbar spine or hip (femoral neck) by dual energy x-ray absorptiometry (DXA) and radiological evidence of 2 or more mild or one or more moderate lumbar or thoracic vertebral fractures, or history of low trauma forearm, humerus, sacral, pelvic, hip, femoral, or tibial fracture within the past 5 years. Postmenopausal women older than 65 who meet the above fracture criteria but have a T score ≤ -2.0 and > -5.0 may be enrolled. Women older than 65 who do not meet the fracture criteria may also be enrolled if their T score is ≤ -3.0 and > -5.0.
Romosuzumab-Studie: Postmenopausal women (55 Years to 90 Years) with osteoporosis, defined as low bone mineral density (BMD T-score at the total hip or femoral neck of ≤ -2.50), aber cave! Exclusion Criteria: BMD T-score of ≤ -3.50 at the total hip or femoral neck, history of hip fracture, any severe or more than 2 moderate vertebral fractures, as assessed by the central imaging based on lateral spine x-rays
2. Nicht nur die Patientinnenkollektive sind nicht vergleichbar, die Frakturendpunkte sind es auch nicht!
In der Romosozumab-Studie wird nach 12 Monaten untersucht, in der Abaloparatide-Studie hingegen nach 18 Monaten. Wie wichtig der Untersuchungszeitpunkt ist, siehst Du in nachfolgender Abbildung aus der Abaloparatide-Studie:

Es geht um die non-vertebralen Frakturen in A. Was meinst Du, wie wäre das Ergebnis ausgefallen, wenn die Frakturdaten nicht nach 18 Monaten, sondern wie in der Romosozumab-Studie nach 12 Monaten erhoben worden wären?
Antwort auf Beitrag Nr.: 55.897.831 von Joschka Schröder am 06.10.17 17:50:44die Einschlusskriterien entsprechen dem Studienprotokoll der jeweiligen Studie, sind jedoch von Studie zu Studie meistens unterschiedlich, wie auch in den beiden vorliegenden Studien --> das macht den Vergleich ausserhalb face-to-face naturgemäss schwierig. Jedoch sind innerhalb der Studien die Kriterien sowohl bei Plazebo als auch beim Verum identisch, so dass die Wirkung eines Medikamentes mit statistischer Signifikanz nachgewiesen werden kann. Dieser Nachweis ist mit Romosozumab bei den nicht die Wirbelsäule betreffenden Frakturen gegenüber Plazebo nicht gelungen. Bei Abaloparatide hingegen schon. Daran können auch 1000 Konjunktive nichts ändern.
Auf den 2. Denkfehler mit dem T-Wert wird nicht eingegangen!
Auf den 2. Denkfehler mit dem T-Wert wird nicht eingegangen!
Antwort auf Beitrag Nr.: 55.887.766 von Joschka Schröder am 05.10.17 17:07:12@Cyberhexe: Du vergleichst Äpfel mit Birnen und merkst es offenbar noch nicht einmal. Dass die Bedingungen innerhalb einer Studie konsistent sein müssen, ist ja wohl trivial. Du kannst aber nicht verschiedene Studien miteinander vergleichen, die an Patienten in voneinander abweichenden Krankheitsstadien durchgeführt worden sind, weil Therapeutika in unterschiedlichen Krankheitsstadien erfahrungsgemäß unterschiedlich gut wirken können. Um die Sache zu veranschaulichen: Ein Medikament, dass bei leichter Osteoporose signifikant das Frakturrisiko senkt, muss dazu noch lange nicht bei schwerer Osteoporose in der Lage sein.
Zu Punkt 2: Über statistische Details müssen wir aus oben genannten Gründen nicht weiter diskutieren. Davon abgesehen kann ich schon mit Deiner Ausgangsformulierung "Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist" wenig anfangen.
Hier noch die Details:
Ausgangsdaten für extra-vertebrale Knochendichte in den unterschiedlichen Studien:
Studie A: Abaloparatide mit T-Score Total Hip -1,9
Studie B: Romosozumab mit T-Score Total Hip -2,48
Romosozumab-Oberschenkelkopf mithin zu Studienbeginn deutlich stärker entkalkt!
Ein weiterer Punkt, den es zu beachten gilt: Amgen plant, Romosozumab in sequentieller Kombi mit Denosumab einzusetzen, d.h. im ersten Jahr Romosozmab, danach Denosumab. In dieser Kombi erreichen Romosozumab+Denosumab nach 24 Monaten eine Reduktion extravertebraler Frakturen um 75 % mit p<0.001.
Das heißt aber nicht zwangsläufig, dass ich diese Medikamentenkombination selbst einsetzen würde (-> potentielle Nebenwirkungen).
Zu Punkt 2: Über statistische Details müssen wir aus oben genannten Gründen nicht weiter diskutieren. Davon abgesehen kann ich schon mit Deiner Ausgangsformulierung "Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist" wenig anfangen.
Zitat von Joschka Schröder: Wie ich bereits geschrieben habe, sind die Patientenkollektive kaum vergleichbar, weil die Patienten in beiden Kollektiven unterschiedlich schwer krank waren
Hier noch die Details:
Ausgangsdaten für extra-vertebrale Knochendichte in den unterschiedlichen Studien:
Studie A: Abaloparatide mit T-Score Total Hip -1,9
Studie B: Romosozumab mit T-Score Total Hip -2,48
Romosozumab-Oberschenkelkopf mithin zu Studienbeginn deutlich stärker entkalkt!
Ein weiterer Punkt, den es zu beachten gilt: Amgen plant, Romosozumab in sequentieller Kombi mit Denosumab einzusetzen, d.h. im ersten Jahr Romosozmab, danach Denosumab. In dieser Kombi erreichen Romosozumab+Denosumab nach 24 Monaten eine Reduktion extravertebraler Frakturen um 75 % mit p<0.001.
Das heißt aber nicht zwangsläufig, dass ich diese Medikamentenkombination selbst einsetzen würde (-> potentielle Nebenwirkungen).
@Cyberhexe
Wenn ich nebenher oder zwischendurch schnell Internetbeiträge schreibe, kann es vorkommen, dass mir die Diktion meiner Beiträge später selbst nicht mehr gefällt ... zu belehrend, zu unfreundlich ... man merkt ihnen dann einfach an, dass sie in gestresstem Zustand formuliert worden sind. Bitte nimm das nicht persönlich! Für konträren Meinungsaustauch bin ich im Übrigen (fast) immer zu haben, weil es grundsätzlich nützlich ist, Standpunkte zu hinterfragen.
Wenn ich nebenher oder zwischendurch schnell Internetbeiträge schreibe, kann es vorkommen, dass mir die Diktion meiner Beiträge später selbst nicht mehr gefällt ... zu belehrend, zu unfreundlich ... man merkt ihnen dann einfach an, dass sie in gestresstem Zustand formuliert worden sind. Bitte nimm das nicht persönlich! Für konträren Meinungsaustauch bin ich im Übrigen (fast) immer zu haben, weil es grundsätzlich nützlich ist, Standpunkte zu hinterfragen.
Antwort auf Beitrag Nr.: 55.900.018 von Joschka Schröder am 06.10.17 23:06:02guter qualifizierter input Joschka... wie siehst du die umsatzaussichten bei tymlos?
Antwort auf Beitrag Nr.: 55.900.018 von Joschka Schröder am 06.10.17 23:06:02
...kann ich gut nachvollziehen, da es mir ab und an ähnlich ergeht! Und ausserdem, der fundamentale Diskurs ist der einzige Antrieb, an diesem Forum teilzunehmen.
Hinsichtlich unseres Diskurses hinsichtlich Romosozumab und Abaloparatide bleibt festzustellen, dass wir uns einig sind, dass die Aus- und Einschlusskriterien unterschiedlich sind und deshalb "ein Vergleich naturgemäss schwierig ist". Und dennoch sind die Ergebnisse hinsichtlich der nicht die Wirbelsäule betreffenden Frakturen bei Abaloparatide eindeutig günstiger. Da führt kein Weg daran vorbei, auch wenn man noch so viele Konjunktive bemüht.
"Zu Punkt 2: Über statistische Details müssen wir aus oben genannten Gründen nicht weiter diskutieren. Davon abgesehen kann ich schon mit Deiner Ausgangsformulierung "Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist" wenig anfangen."
Diese Aussage bezieht sich auf den von dir zitierten T-Wert (T score), bei welchem die Abweichung der Knochendichte gegenüber einer gesunden 30-jährigen Person desselben Geschlechts gemessen wird. Sorry, aber ich hatte dieses Wissen bei dir vorausgesetzt.
"z.B. sind in der zitierten Romosozumab-Studie ausschließlich Patientinnen mit einem T-Score zwischen -2,5 und -3,5 untersucht worden, während in der Abaloparatide-Studie ein großer Anteil der Patientinnen einen T-Score > -2,5 aufwies."
Zitat von Joschka Schröder: @Cyberhexe
Wenn ich nebenher oder zwischendurch schnell Internetbeiträge schreibe, kann es vorkommen, dass mir die Diktion meiner Beiträge später selbst nicht mehr gefällt ... zu belehrend, zu unfreundlich ... man merkt ihnen dann einfach an, dass sie in gestresstem Zustand formuliert worden sind. Bitte nimm das nicht persönlich! Für konträren Meinungsaustauch bin ich im Übrigen (fast) immer zu haben, weil es grundsätzlich nützlich ist, Standpunkte zu hinterfragen.
...kann ich gut nachvollziehen, da es mir ab und an ähnlich ergeht! Und ausserdem, der fundamentale Diskurs ist der einzige Antrieb, an diesem Forum teilzunehmen.
Hinsichtlich unseres Diskurses hinsichtlich Romosozumab und Abaloparatide bleibt festzustellen, dass wir uns einig sind, dass die Aus- und Einschlusskriterien unterschiedlich sind und deshalb "ein Vergleich naturgemäss schwierig ist". Und dennoch sind die Ergebnisse hinsichtlich der nicht die Wirbelsäule betreffenden Frakturen bei Abaloparatide eindeutig günstiger. Da führt kein Weg daran vorbei, auch wenn man noch so viele Konjunktive bemüht.
"Zu Punkt 2: Über statistische Details müssen wir aus oben genannten Gründen nicht weiter diskutieren. Davon abgesehen kann ich schon mit Deiner Ausgangsformulierung "Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist" wenig anfangen."
Diese Aussage bezieht sich auf den von dir zitierten T-Wert (T score), bei welchem die Abweichung der Knochendichte gegenüber einer gesunden 30-jährigen Person desselben Geschlechts gemessen wird. Sorry, aber ich hatte dieses Wissen bei dir vorausgesetzt.
"z.B. sind in der zitierten Romosozumab-Studie ausschließlich Patientinnen mit einem T-Score zwischen -2,5 und -3,5 untersucht worden, während in der Abaloparatide-Studie ein großer Anteil der Patientinnen einen T-Score > -2,5 aufwies."
Antwort auf Beitrag Nr.: 55.901.521 von Cyberhexe am 07.10.17 12:24:59Ich darf Dich beruhigen, die Definition des T-Scores ist mir hinreichend bekannt. Ich habe lange genug in der medizinischen Grundlagenforschung gearbeitet und mich umfassend mit Fragen des Knochenstoffwechsels befaßt. Dennoch konnte und kann ich inhaltlich mit Deiner zweiten Aussage in Beitrag 366 nichts anfangen, ich halte sie für abwegig.
Die Patienten beider Untersuchungsgruppen hatten T-Scores, welche die Definition einer Osteoporose erfüllen, in beiden Gruppen sind mithin gehäuft vertebrale und extravertebrale Frakturen zu erwarten. Dennoch unterscheiden sich die Gruppen darin, dass die (extravertebrale) Ausgangsknochendichte in der Romosozumab-Gruppe noch einmal deutlich schlechter war als diejenige in der Abaloparatide-Gruppe. Was bedeutet dies? Die Häufigkeit des Auftretens von Knochenfrakturen läßt sich bei Osteoporosepatienten unterschiedlichen Schweregrads unterschiedlich gut beeinflussen. z.B. läßt sich bei sehr schwerer Osteoprose die Frakturinzidenz sehr schlecht medikamentös beeinflussen/minimieren. Ergo: Im Vergleich gegen Placebopatienten des jeweils selben Schweregrads sind diejenigen Patienten im Nachteil, deren Osteoporose zu Studienbeginn deutlich stärker ausgeprägt ist (hier Romosozumab).
Natürlich bedeutet dies nicht, dass grundsätzlich Patienten mit höherem T-Score schlechter auf eine Therapie ansprechen ... es kommt immer darauf an, welches T-Score-Segment man im Auge hat (bei Vorliegen einer Osteopenie beispielsweise kann die Situation wieder völlig anders ausschauen).
Das müßte jetzt eigentlich verständlich sein.
Deine Grenzwertüberlegung ist für sich betrachtet natürlich nicht falsch. Würde man z.B. Personen mit T-Score -0,3 o.ä. untersuchen, wäre ein Unterschied der Frakturinzidenz zu Placebo vermutlich auch bei extrem großen Stichproben nicht nachweisbar, weil sich derart kleine Abweichungen der Knochendichte wohl kaum auf die Frankturhäufigkeit auswirken. Es ist jedoch unzulässig, dies auf die von uns betrachteten osteoporotischen Patientenkollektive zu übertragen, weil es sich dort wie oben beschrieben verhält.
Die Patienten beider Untersuchungsgruppen hatten T-Scores, welche die Definition einer Osteoporose erfüllen, in beiden Gruppen sind mithin gehäuft vertebrale und extravertebrale Frakturen zu erwarten. Dennoch unterscheiden sich die Gruppen darin, dass die (extravertebrale) Ausgangsknochendichte in der Romosozumab-Gruppe noch einmal deutlich schlechter war als diejenige in der Abaloparatide-Gruppe. Was bedeutet dies? Die Häufigkeit des Auftretens von Knochenfrakturen läßt sich bei Osteoporosepatienten unterschiedlichen Schweregrads unterschiedlich gut beeinflussen. z.B. läßt sich bei sehr schwerer Osteoprose die Frakturinzidenz sehr schlecht medikamentös beeinflussen/minimieren. Ergo: Im Vergleich gegen Placebopatienten des jeweils selben Schweregrads sind diejenigen Patienten im Nachteil, deren Osteoporose zu Studienbeginn deutlich stärker ausgeprägt ist (hier Romosozumab).
Natürlich bedeutet dies nicht, dass grundsätzlich Patienten mit höherem T-Score schlechter auf eine Therapie ansprechen ... es kommt immer darauf an, welches T-Score-Segment man im Auge hat (bei Vorliegen einer Osteopenie beispielsweise kann die Situation wieder völlig anders ausschauen).
Das müßte jetzt eigentlich verständlich sein.
Deine Grenzwertüberlegung ist für sich betrachtet natürlich nicht falsch. Würde man z.B. Personen mit T-Score -0,3 o.ä. untersuchen, wäre ein Unterschied der Frakturinzidenz zu Placebo vermutlich auch bei extrem großen Stichproben nicht nachweisbar, weil sich derart kleine Abweichungen der Knochendichte wohl kaum auf die Frankturhäufigkeit auswirken. Es ist jedoch unzulässig, dies auf die von uns betrachteten osteoporotischen Patientenkollektive zu übertragen, weil es sich dort wie oben beschrieben verhält.
PS: Zum jetzigen Zeitpunkt kann man meiner Meinung nach einfach (noch) nicht beurteilen, welches der genannten Präparate besser wirkt. Darauf hinzuweisen war Sinn meiner Beiträge.
Antwort auf Beitrag Nr.: 55.898.581 von Joschka Schröder am 06.10.17 19:36:49
...nun ja, zuerst kannst du mit einfachsten Definitionen (T score) zum Thema nichts anfangen und dann willst du mir Osteoporose erklären?
Du schreibst unter anderem:
"Die Häufigkeit des Auftretens von Knochenfrakturen läßt sich bei Osteoporosepatienten unterschiedlichen Schweregrads unterschiedlich gut beeinflussen. z.B. läßt sich bei sehr schwerer Osteoprose die Frakturinzidenz sehr schlecht medikamentös beeinflussen/minimieren."
In der wissenschaftlichen Literatur bzw. bei der Auswertung der Abaloparatide-Studien wird jedoch über alle Subgruppen hinweg --> "Risk factor subgroups were predefined categorically for BMD T-score of the lumbar spine, total hip, and femoral neck (≤–2.5 versus >–2.5 and ≤–3.0 versus >–3.0)," eine konsistente Reduktion der Fraktur-Risiken beschrieben -->Quelle:
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/full
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
Vielleicht hast du ja Quellen, die das Gegenteil stützen, dass mit Abaloparatide kein Behandlungserfolg in den Subgruppen zu realisieren ist, dann solltest du diese jedoch zumindest benennen.
Zitat von Joschka Schröder: @Cyberhexe:
Zu Punkt 2: Über statistische Details müssen wir aus oben genannten Gründen nicht weiter diskutieren. Davon abgesehen kann ich schon mit Deiner Ausgangsformulierung "Da die Abweichung gegenüber einer gesunden 30-jährigen Person desselben Geschlechts bei Abaloparatide geringer ist" wenig anfangen.
Zitat von Joschka Schröder: Wie ich bereits geschrieben habe, sind die Patientenkollektive kaum vergleichbar, weil die Patienten in beiden Kollektiven unterschiedlich schwer krank waren
...nun ja, zuerst kannst du mit einfachsten Definitionen (T score) zum Thema nichts anfangen und dann willst du mir Osteoporose erklären?
Du schreibst unter anderem:
"Die Häufigkeit des Auftretens von Knochenfrakturen läßt sich bei Osteoporosepatienten unterschiedlichen Schweregrads unterschiedlich gut beeinflussen. z.B. läßt sich bei sehr schwerer Osteoprose die Frakturinzidenz sehr schlecht medikamentös beeinflussen/minimieren."
In der wissenschaftlichen Literatur bzw. bei der Auswertung der Abaloparatide-Studien wird jedoch über alle Subgruppen hinweg --> "Risk factor subgroups were predefined categorically for BMD T-score of the lumbar spine, total hip, and femoral neck (≤–2.5 versus >–2.5 and ≤–3.0 versus >–3.0)," eine konsistente Reduktion der Fraktur-Risiken beschrieben -->Quelle:
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/full
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
Vielleicht hast du ja Quellen, die das Gegenteil stützen, dass mit Abaloparatide kein Behandlungserfolg in den Subgruppen zu realisieren ist, dann solltest du diese jedoch zumindest benennen.
Antwort auf Beitrag Nr.: 55.904.206 von Cyberhexe am 08.10.17 06:40:53Zunächst solltest Du Deinen Diskussionsstil überdenken. Deine Bemerkung "zuerst kannst du mit einfachsten Definitionen (T score) zum Thema nichts anfangen" ist so albern wie überflüssig. Tatsache ist, dass ich mit Deinen Aussagen in diesem Kontext nichts anfangen konnte und kann. Ich halte sie für abstrus.
Um zum Ausangspunkt unserer Diskussion zurückzukommen, können wir schon einmal festhalten, dass sich die erste Aussagen in Deinem Posting Nr. 366 ("da beide Studien mit Plazebo vergleichen und die Einschluss bzw. Ausschlusskriterien für beide Gruppen (Verum und Plazebo) in den jeweiligen Studien identisch sind, ...) als falsch erwiesen hat. Dies hast Du ja mittlerweile auch eingeräumt ("bleibt festzustellen, dass wir uns einig sind, dass die Aus- und Einschlusskriterien unterschiedlich sind" in Beitrag 372).
Über Deine zweite Aussage diskutieren wir noch. Warum ich auch diese Aussage für irrelevant und in Teilen falsch halte, habe ich bereits begründet. Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein. Hast Du schon einmal mit Osteoprose-Patienten schwersten Ausmaßes (z.B. T-Score 5) zu tun gehabt? Wohl kaum. Da kannst Du im Normalfall medikamentös kaum mehr erfolgreich intervenieren.
Vielleicht kannst Du noch den vollständigen Titel der von Dir zitierten Arbeit benennen, Dein Link führt ins Nirgendwo (Wiley Online Library is currently unavailable while we conduct essential maintenance).
Um zum Ausangspunkt unserer Diskussion zurückzukommen, können wir schon einmal festhalten, dass sich die erste Aussagen in Deinem Posting Nr. 366 ("da beide Studien mit Plazebo vergleichen und die Einschluss bzw. Ausschlusskriterien für beide Gruppen (Verum und Plazebo) in den jeweiligen Studien identisch sind, ...) als falsch erwiesen hat. Dies hast Du ja mittlerweile auch eingeräumt ("bleibt festzustellen, dass wir uns einig sind, dass die Aus- und Einschlusskriterien unterschiedlich sind" in Beitrag 372).
Über Deine zweite Aussage diskutieren wir noch. Warum ich auch diese Aussage für irrelevant und in Teilen falsch halte, habe ich bereits begründet. Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein. Hast Du schon einmal mit Osteoprose-Patienten schwersten Ausmaßes (z.B. T-Score 5) zu tun gehabt? Wohl kaum. Da kannst Du im Normalfall medikamentös kaum mehr erfolgreich intervenieren.
Vielleicht kannst Du noch den vollständigen Titel der von Dir zitierten Arbeit benennen, Dein Link führt ins Nirgendwo (Wiley Online Library is currently unavailable while we conduct essential maintenance).
Antwort auf Beitrag Nr.: 55.904.557 von Joschka Schröder am 08.10.17 10:17:50"Um zum Ausangspunkt unserer Diskussion zurückzukommen, können wir schon einmal festhalten, dass sich die erste Aussagen in Deinem Posting Nr. 366 ("da beide Studien mit Plazebo vergleichen und die Einschluss bzw. Ausschlusskriterien für beide Gruppen (Verum und Plazebo) in den jeweiligen Studien identisch sind, ...) als falsch erwiesen hat. Dies hast Du ja mittlerweile auch eingeräumt ("bleibt festzustellen, dass wir uns einig sind, dass die Aus- und Einschlusskriterien unterschiedlich sind" in Beitrag 372)."
...was soll daran falsch sein? In jeweiligen Studien sind die Kriterien für Plazebo und Verum identisch....das ist so banal wie richtig. Wenn du an solch fundamentalen und bei fast allen Studien elementaren Voraussetzungen irgendwelche Zweifel hast--> "als falsch erwiesen hat",
dann ist jede weitere Diskussion über klinische Studien überflüssig!
Und dann zum Diskussionsstil....du zitierst einen Wert (T score) und verstehst dann dessen einfachste Definition nicht...unterstellst mir jedoch Folgendes:
"Gehe ich recht in der Annahme, dass Du die betreffenden Studienpublikationen niemals vollständig gelesen hast, sondern Dein Wissen aus rudimentären Zusammenfassungen generierst und Dir den Rest irgendwie zusammenreimst? "
Also irgenwie passt da einiges nicht zusammen!
...was soll daran falsch sein? In jeweiligen Studien sind die Kriterien für Plazebo und Verum identisch....das ist so banal wie richtig. Wenn du an solch fundamentalen und bei fast allen Studien elementaren Voraussetzungen irgendwelche Zweifel hast--> "als falsch erwiesen hat",
dann ist jede weitere Diskussion über klinische Studien überflüssig!
Und dann zum Diskussionsstil....du zitierst einen Wert (T score) und verstehst dann dessen einfachste Definition nicht...unterstellst mir jedoch Folgendes:
"Gehe ich recht in der Annahme, dass Du die betreffenden Studienpublikationen niemals vollständig gelesen hast, sondern Dein Wissen aus rudimentären Zusammenfassungen generierst und Dir den Rest irgendwie zusammenreimst? "
Also irgenwie passt da einiges nicht zusammen!
Antwort auf Beitrag Nr.: 55.905.259 von Cyberhexe am 08.10.17 12:42:07
Das stimmt, da war ich eben nicht aufmerksam.
Könntest Du bitte noch den vollständigen Titel der von Dir zitierte Arbeit nennen.
Zitat von Cyberhexe: ...was soll daran falsch sein? In jeweiligen Studien sind die Kriterien für Plazebo und Verum identisch....das ist so banal wie richtig.
Das stimmt, da war ich eben nicht aufmerksam.
Könntest Du bitte noch den vollständigen Titel der von Dir zitierte Arbeit nennen.
Antwort auf Beitrag Nr.: 55.904.557 von Joschka Schröder am 08.10.17 10:17:50Über Deine zweite Aussage diskutieren wir noch. Warum ich auch diese Aussage für irrelevant und in Teilen falsch halte, habe ich bereits begründet. Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein. Hast Du schon einmal mit Osteoprose-Patienten schwersten Ausmaßes (z.B. T-Score 5) zu tun gehabt? Wohl kaum. Da kannst Du im Normalfall medikamentös kaum mehr erfolgreich intervenieren. Vielleicht kannst Du noch den vollständigen Titel der von Dir zitierten Arbeit benennen, Dein Link führt ins Nirgendwo (Wiley Online Library is currently unavailable while we conduct essential maintenance).
[/b]
Hier die vollständige Quelle:
Effects of Abaloparatide-SC on Fractures and Bone Mineral Density in Subgroups of Postmenopausal Women With Osteoporosis and Varying Baseline Risk Factors
Authors
Felicia Cosman,
Gary Hattersley,
Ming-yi Hu,
Gregory C Williams,
Lorraine A Fitzpatrick,
Dennis M Black
First published: 28 September 2016 Full publication history
DOI: 10.1002/jbmr.2991 View/save citation
Cited by (CrossRef): 6 articles Check for updates Citation tools
Article has an altmetric score of 171
Funding Information
For a Commentary on this article, please see Martin and Seeman (J Bone Miner Res. 2017;32(1):11–16. DOI: 10.1002/jbmr.3042).
Und anbei die Aussage, die von dir in Frage gestellt wird, dass in allen Subgruppen, auch bei einem T-Wert < -3.0, eine Reduktion der Fraktur-Risiken beobachtet wird.
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
Our findings showing consistent effectiveness of abaloparatide-SC to reduce nonvertebral fractures regardless of BMD, prior fracture history, and age also differ from the subgroup analysis of the Fracture Reduction Evaluation of Denosumab in Osteoporosis Every 6 Months (FREEDOM) trial evaluating the effect of denosumab on nonvertebral fractures.[15] In that study, an interaction on nonvertebral fracture was found for body mass index (p = 0.013), femoral neck BMD (p = 0.023), and prevalent vertebral fracture (p = 0.038).
Wenn man die Akzeptanz solcher Ergebnisse in Frage stellt, ist jede Diskussion auf der wissenschaftlichen Ebene natürlich nicht ganz einfach.
[/b]
Hier die vollständige Quelle:
Effects of Abaloparatide-SC on Fractures and Bone Mineral Density in Subgroups of Postmenopausal Women With Osteoporosis and Varying Baseline Risk Factors
Authors
Felicia Cosman,
Gary Hattersley,
Ming-yi Hu,
Gregory C Williams,
Lorraine A Fitzpatrick,
Dennis M Black
First published: 28 September 2016 Full publication history
DOI: 10.1002/jbmr.2991 View/save citation
Cited by (CrossRef): 6 articles Check for updates Citation tools
Article has an altmetric score of 171
Funding Information
For a Commentary on this article, please see Martin and Seeman (J Bone Miner Res. 2017;32(1):11–16. DOI: 10.1002/jbmr.3042).
Und anbei die Aussage, die von dir in Frage gestellt wird, dass in allen Subgruppen, auch bei einem T-Wert < -3.0, eine Reduktion der Fraktur-Risiken beobachtet wird.
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
Our findings showing consistent effectiveness of abaloparatide-SC to reduce nonvertebral fractures regardless of BMD, prior fracture history, and age also differ from the subgroup analysis of the Fracture Reduction Evaluation of Denosumab in Osteoporosis Every 6 Months (FREEDOM) trial evaluating the effect of denosumab on nonvertebral fractures.[15] In that study, an interaction on nonvertebral fracture was found for body mass index (p = 0.013), femoral neck BMD (p = 0.023), and prevalent vertebral fracture (p = 0.038).
Wenn man die Akzeptanz solcher Ergebnisse in Frage stellt, ist jede Diskussion auf der wissenschaftlichen Ebene natürlich nicht ganz einfach.
Antwort auf Beitrag Nr.: 55.905.353 von Cyberhexe am 08.10.17 13:02:52Mittlerweile ist die wiley-Seite wieder freigeschaltet.
Im Hinblick auf die Abaloparatide-Studie scheinen die Ergebnisse in den dort präsentierten Subgruppen tatsächlich vergleichbar zu sein. Sind die mittleren T-Scores der jeweiligen Subgruppen bekannt?
Im Hinblick auf die Abaloparatide-Studie scheinen die Ergebnisse in den dort präsentierten Subgruppen tatsächlich vergleichbar zu sein. Sind die mittleren T-Scores der jeweiligen Subgruppen bekannt?
Antwort auf Beitrag Nr.: 55.905.353 von Cyberhexe am 08.10.17 13:02:52
Das ist nicht richtig. Ich habe zu keinem Zeitpunkt in Frage gestellt, dass in verschiedenen Subgruppen der Abaloparatide-Studie eine Reduktion von Frakturrisiken beobachtet worden ist. Wie sollte ich auch? Richtig ist, dass ich grundsätzlich in Frage gestellt habe, dass bei einer Osteoporosetherapie die relative Reduktion des Frakturrisikos völlig unabhängig vom Schweregrad der Osteoporose ist.
In der Abaloparatide-Studie sind, da hast Du recht, in den dort definierten Subgruppen vergleichbare Ergebnisse erzielt worden. Um die Sache weiter interpretieren zu können, wäre es wichtig zu wissen, welche genauen Merkmale diese Subgruppen aufgewiesen haben (bei den Mittelwerten und Varianzen der jeweiligen T-Scores abgefangen). Sind dazu Details veröffentlicht worden?
Zitat von Cyberhexe: Und anbei die Aussage, die von dir in Frage gestellt wird, dass in allen Subgruppen, auch bei einem T-Wert < -3.0, eine Reduktion der Fraktur-Risiken beobachtet wird.
Das ist nicht richtig. Ich habe zu keinem Zeitpunkt in Frage gestellt, dass in verschiedenen Subgruppen der Abaloparatide-Studie eine Reduktion von Frakturrisiken beobachtet worden ist. Wie sollte ich auch? Richtig ist, dass ich grundsätzlich in Frage gestellt habe, dass bei einer Osteoporosetherapie die relative Reduktion des Frakturrisikos völlig unabhängig vom Schweregrad der Osteoporose ist.
In der Abaloparatide-Studie sind, da hast Du recht, in den dort definierten Subgruppen vergleichbare Ergebnisse erzielt worden. Um die Sache weiter interpretieren zu können, wäre es wichtig zu wissen, welche genauen Merkmale diese Subgruppen aufgewiesen haben (bei den Mittelwerten und Varianzen der jeweiligen T-Scores abgefangen). Sind dazu Details veröffentlicht worden?
Antwort auf Beitrag Nr.: 55.905.524 von Joschka Schröder am 08.10.17 13:40:33
Über Deine zweite Aussage diskutieren wir noch. Warum ich auch diese Aussage für irrelevant und in Teilen falsch halte, habe ich bereits begründet. Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein. Hast Du schon einmal mit Osteoprose-Patienten schwersten Ausmaßes (z.B. T-Score 5) zu tun gehabt? Wohl kaum. Da kannst Du im Normalfall medikamentös kaum mehr erfolgreich intervenieren.
Du solltest bei der Wahrheit bleiben, ich habe nie geschrieben, der Nachweis bei extrem hohen T Score müsste besonders einfach sein, ich habe lediglich auf das zitierte Studienergebnis referenziert, bei welchem in allen Subgruppen konsistente Ergebnisse erzielt werden, nämlich...
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
Über Deine zweite Aussage diskutieren wir noch. Warum ich auch diese Aussage für irrelevant und in Teilen falsch halte, habe ich bereits begründet. Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein. Hast Du schon einmal mit Osteoprose-Patienten schwersten Ausmaßes (z.B. T-Score 5) zu tun gehabt? Wohl kaum. Da kannst Du im Normalfall medikamentös kaum mehr erfolgreich intervenieren.
Du solltest bei der Wahrheit bleiben, ich habe nie geschrieben, der Nachweis bei extrem hohen T Score müsste besonders einfach sein, ich habe lediglich auf das zitierte Studienergebnis referenziert, bei welchem in allen Subgruppen konsistente Ergebnisse erzielt werden, nämlich...
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
Antwort auf Beitrag Nr.: 55.902.916 von Joschka Schröder am 07.10.17 18:55:09das grösste Handicap von Romosozumab ist das festgestellte cardiovasculäre Risiko, weshalb dessen Zulassung derzeit noch sehr ungewiss ist:
Amgen and UCB announce increased cardiovascular risk in patients receiving romosozumab, an anti-sclerotin antibody
Rheumatology, Volume 56, Issue 8, 1 August 2017, Pages e21,
https://academic.oup.com/rheumatology/article-lookup/doi/10.…
Amgen and UCB announce increased cardiovascular risk in patients receiving romosozumab, an anti-sclerotin antibody
Rheumatology, Volume 56, Issue 8, 1 August 2017, Pages e21,
https://academic.oup.com/rheumatology/article-lookup/doi/10.…
Antwort auf Beitrag Nr.: 55.905.827 von Cyberhexe am 08.10.17 15:07:29Bin gespannt, ob Abaloparatide auf der Agenda der Oktober-Sitzung des europ. Arzneimittelausschusses CHMP erscheint. Sitzungsbeginn ist Morgen, Montag 9.10.2017 am Nachmittag:
http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/l…
http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/l…
Antwort auf Beitrag Nr.: 55.905.893 von Cyberhexe am 08.10.17 15:28:36Jo, falls sich die EMA mal bewegen würde, wäre dann schön zu wissen wie die EMA mit den Unregelmäßigkeiten in den trial sites, die (ich glaube) 15% der Patienten der ACTIVE Studie betreffen, umgeht. Sollten diese 15% ausgeschlossen werden, so kann man sich die Signifikanz in non-vetrebral fractures höchstwahrscheinlich im europäischen Label schenken.
Fakt ist weiterhin, dass Tymlos und Forteo, erheblich teurer und unangenehmer in der Anwendung sind (1x täglich spritzen) als die konkurrierenden Antikörper, daher bleibt das ein Uphill battle gegen diese und auch gegen künftig kommende Generika von Forteo. Das sind m.E. wichtigere Treiber für den Erfolg von Forteo als wissenschaftliche Vergleiche knapp erreichter oder verfehlter Signifikanzniveaus.
Nicht umsonst versucht man mit einer Dumpingstrategie in den amerikanischen Markt zu kommen (halber Preis von Forteo) und ist auch damit bisher (Stand Anfang Sept. 2017) bei nicht mal 10% des Marktanteils der Neuverschreibungen (ohne Refills) bei den anabolen. Die aktuell 500Mio Cash werden dahinschmelzen wie Butter - bei aktuell burn rates von 50-70 Mio USD / Quartal! Da wird auch ein falsch positionierter Ankerinvestor (BBBiotech) irgendwann unruhig werden und aufhören mit seinen Stützungskäufen, wenn die notwendigen weiteren Stufen auch nicht zünden (transdermal patch, SERD pivotal)
Nungut, ich kann mich ja irren. Aber eine Überrendite sehe ich hier definitiv nicht. Eher ein verzweifelter Kampf darum seinen Platz im Markt zu finden und die ziemlich erhöhte Marktkapitalisierung weiterhin rechtfertigen zu können.
Fakt ist weiterhin, dass Tymlos und Forteo, erheblich teurer und unangenehmer in der Anwendung sind (1x täglich spritzen) als die konkurrierenden Antikörper, daher bleibt das ein Uphill battle gegen diese und auch gegen künftig kommende Generika von Forteo. Das sind m.E. wichtigere Treiber für den Erfolg von Forteo als wissenschaftliche Vergleiche knapp erreichter oder verfehlter Signifikanzniveaus.
Nicht umsonst versucht man mit einer Dumpingstrategie in den amerikanischen Markt zu kommen (halber Preis von Forteo) und ist auch damit bisher (Stand Anfang Sept. 2017) bei nicht mal 10% des Marktanteils der Neuverschreibungen (ohne Refills) bei den anabolen. Die aktuell 500Mio Cash werden dahinschmelzen wie Butter - bei aktuell burn rates von 50-70 Mio USD / Quartal! Da wird auch ein falsch positionierter Ankerinvestor (BBBiotech) irgendwann unruhig werden und aufhören mit seinen Stützungskäufen, wenn die notwendigen weiteren Stufen auch nicht zünden (transdermal patch, SERD pivotal)
Nungut, ich kann mich ja irren. Aber eine Überrendite sehe ich hier definitiv nicht. Eher ein verzweifelter Kampf darum seinen Platz im Markt zu finden und die ziemlich erhöhte Marktkapitalisierung weiterhin rechtfertigen zu können.
Antwort auf Beitrag Nr.: 55.905.812 von Cyberhexe am 08.10.17 14:59:26
Na ja, in Beitrag 366 hast Du geschrieben "Je geringer die Abweichung vom Standard, desto kleiner der Unterschied bei den Fallzahlen und umso schwieriger wird der Nachweis über die Wirksamkeit (Extremsituation überdenken: kein Unterschied beim T-Wert, Nachweis wäre nicht zu erbringen!)."
Ich habe in Beitrag 376 darauf Bezug genommen und geschrieben "Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein".
Wo ich nicht bei der Wahrheit geblieben sein soll, bleibt ein Rätsel?
Ich hatte aber nicht vor, mit Dir in eine Dauerdiskussion einzutreten, weil uns unsere Zeit dafür zu kostbar sein sollte. Mir ging es schlichtweg darum, Dein aus meiner Sicht etwas vorschnelles und einseitiges Urteil bzgl. der Abaloparatide- und Rosomozmab-Studien zu relativieren. In diesem Zusammenhang schienen mir insbesondere folgende Punkte wichtig:
1. Unterschiedliche Beobachtungsdauern (s. Abb. in Beitrag 367)
2. Unterschiedliche Einschlusskriterien im Hinblick auf Osteoporosestadium und bisherige Knochenfrakturen. Gerade letztgenannter Punkt hatte in früheren Bisphosponatstudien erheblichen Einfluß auf die relative Reduktion des künftigen Frakturrisikos.
Selbst an Neuem mitgenommen habe ich aus unserer bisweilen etwas hitzigen Dikussion, dass die therapeutische Wirkung des Abaloparatides in allen Subgruppen der von Dir zitierten Studie vergleichbar war. Dies ist positiv, aus früheren Bisphosponat-Studien kannte ich so etwas nicht. Gleichwohl wäre es für eine differenziertere Interpretation erforderlich, weitere Daten zu den Merkmalen der Subgruppen in der Abaloparatide-Studie zu kennen.
Dass ich gegenüber den meisten Osteoporose-Medikamenten wegen diverser Nebenwirkungen gewisse Vorbehalte habe, hatte ich bereits erwähnt. Von den bislang zugelassenen Medikementen gefiel mir bislang wegen der stark anabolen Komponente und der guten Studienergebnisse Forsteo am besten, Abaloparatide könnte aber eine interessante Alternative werden. Die von Ville erwähnte EMA-Entscheidung/Kommentierung werde ich in jedem Fall mit Interesse lesen. Ein Nachteil der Parathormonderivate sind die hohen Kosten und Compliance-Probleme, weshalb z.B. Forsteo in Deutschland nur in Ausnahmefällen verordnet wird.
Viele Aspekte habe ich in meiner kleinen Zusammenfassung sicherlich vergessen. Dies ist dem Umstand geschuldet, dass ich schlichtweg totmüde bin und diese Diskussion auf meiner To-do-Liste sehr weit unten steht. Deshalb wird jetzt für heute Schluss gemacht. Gute Nacht!
Zitat von Cyberhexe: Über Deine zweite Aussage diskutieren wir noch. Warum ich auch diese Aussage für irrelevant und in Teilen falsch halte, habe ich bereits begründet. Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein. Hast Du schon einmal mit Osteoprose-Patienten schwersten Ausmaßes (z.B. T-Score 5) zu tun gehabt? Wohl kaum. Da kannst Du im Normalfall medikamentös kaum mehr erfolgreich intervenieren.
Du solltest bei der Wahrheit bleiben, ich habe nie geschrieben, der Nachweis bei extrem hohen T Score müsste besonders einfach sein, ich habe lediglich auf das zitierte Studienergebnis referenziert, bei welchem in allen Subgruppen konsistente Ergebnisse erzielt werden, nämlich...
Na ja, in Beitrag 366 hast Du geschrieben "Je geringer die Abweichung vom Standard, desto kleiner der Unterschied bei den Fallzahlen und umso schwieriger wird der Nachweis über die Wirksamkeit (Extremsituation überdenken: kein Unterschied beim T-Wert, Nachweis wäre nicht zu erbringen!)."
Ich habe in Beitrag 376 darauf Bezug genommen und geschrieben "Deiner dort formulierten Grundannahme zufolge müßte der Nachweis einer therapeutischen Wirkung bei extrem hohen T-Score besonders einfach sein".
Wo ich nicht bei der Wahrheit geblieben sein soll, bleibt ein Rätsel?
Ich hatte aber nicht vor, mit Dir in eine Dauerdiskussion einzutreten, weil uns unsere Zeit dafür zu kostbar sein sollte. Mir ging es schlichtweg darum, Dein aus meiner Sicht etwas vorschnelles und einseitiges Urteil bzgl. der Abaloparatide- und Rosomozmab-Studien zu relativieren. In diesem Zusammenhang schienen mir insbesondere folgende Punkte wichtig:
1. Unterschiedliche Beobachtungsdauern (s. Abb. in Beitrag 367)
2. Unterschiedliche Einschlusskriterien im Hinblick auf Osteoporosestadium und bisherige Knochenfrakturen. Gerade letztgenannter Punkt hatte in früheren Bisphosponatstudien erheblichen Einfluß auf die relative Reduktion des künftigen Frakturrisikos.
Selbst an Neuem mitgenommen habe ich aus unserer bisweilen etwas hitzigen Dikussion, dass die therapeutische Wirkung des Abaloparatides in allen Subgruppen der von Dir zitierten Studie vergleichbar war. Dies ist positiv, aus früheren Bisphosponat-Studien kannte ich so etwas nicht. Gleichwohl wäre es für eine differenziertere Interpretation erforderlich, weitere Daten zu den Merkmalen der Subgruppen in der Abaloparatide-Studie zu kennen.
Dass ich gegenüber den meisten Osteoporose-Medikamenten wegen diverser Nebenwirkungen gewisse Vorbehalte habe, hatte ich bereits erwähnt. Von den bislang zugelassenen Medikementen gefiel mir bislang wegen der stark anabolen Komponente und der guten Studienergebnisse Forsteo am besten, Abaloparatide könnte aber eine interessante Alternative werden. Die von Ville erwähnte EMA-Entscheidung/Kommentierung werde ich in jedem Fall mit Interesse lesen. Ein Nachteil der Parathormonderivate sind die hohen Kosten und Compliance-Probleme, weshalb z.B. Forsteo in Deutschland nur in Ausnahmefällen verordnet wird.
Viele Aspekte habe ich in meiner kleinen Zusammenfassung sicherlich vergessen. Dies ist dem Umstand geschuldet, dass ich schlichtweg totmüde bin und diese Diskussion auf meiner To-do-Liste sehr weit unten steht. Deshalb wird jetzt für heute Schluss gemacht. Gute Nacht!
Antwort auf Beitrag Nr.: 55.907.996 von Joschka Schröder am 08.10.17 23:10:25
Das Fragezeichen muss natürlich weg.
Zitat von Joschka Schröder: Wo ich nicht bei der Wahrheit geblieben sein soll, bleibt ein Rätsel?
Das Fragezeichen muss natürlich weg.
Antwort auf Beitrag Nr.: 55.906.730 von Ville7 am 08.10.17 18:28:43
Korrektur: zur Behandlung von Osteoporose ist bisher lediglich 1 Antikörper in USA oder Europa zugelassen, nämlich Prolia® (generic name: Denosumab); der viel zitierte Antikörper Romosozumab wurde aufgrund eines kardiovasculären Signal bisher nicht zugelassen (der verwendete Plural falsch: "als die konkurrierenden Antikörper"):
FDA Rejects Romosozumab for Osteoporosis, Wants More Data
Lisa Nainggolan
July 17, 2017
http://www.medscape.com/viewarticle/882966
Von Bedeutung ist sicherlich, dass Teriparatide am 8.12.2018 den Patentschutz verliert und dann sehr wahrscheinlich generische Anbieter den Wettbewerb verschärfen.
https://www.drugs.com/availability/generic-forteo.html
Knapp 10% bei den Neuverschreibungen nach nicht einmal 3 Monaten Marktpräsenz ist sehr gut. Ich rechne zudem damit, dass dieser Marktanteil bis Ende 2017 signifikant höher sein wird, weshalb die von dem Teilnehmer prognostizierten 8 Mio USD Umsatz für 2017 sicherlich übertroffen werden. Time will tell!
"Da wird auch ein falsch positionierter Ankerinvestor (BBBiotech) irgendwann unruhig werden und aufhören mit seinen Stützungskäufen,"
man beachte: "falsch positionierter Ankerinvestor" tätigt "Stützungskäufe"!
Frage mich woher dieser Teilnehmer die Gewissheit nimmt, dass es sich um Stützungskäufe handelt? Kann es nicht sein, dass der institutionelle Anleger davon überzeugt ist, dass das Unternehmen unterbewertet ist und deswegen weiterhin investiert?
Zitat von Ville7: Jo, falls sich die EMA mal bewegen würde, wäre dann schön zu wissen wie die EMA mit den Unregelmäßigkeiten in den trial sites, die (ich glaube) 15% der Patienten der ACTIVE Studie betreffen, umgeht. Sollten diese 15% ausgeschlossen werden, so kann man sich die Signifikanz in non-vetrebral fractures höchstwahrscheinlich im europäischen Label schenken.
Fakt ist weiterhin, dass Tymlos und Forteo, erheblich teurer und unangenehmer in der Anwendung sind (1x täglich spritzen) als die konkurrierenden Antikörper, daher bleibt das ein Uphill battle gegen diese und auch gegen künftig kommende Generika von Forteo. Das sind m.E. wichtigere Treiber für den Erfolg von Forteo als wissenschaftliche Vergleiche knapp erreichter oder verfehlter Signifikanzniveaus.
Nicht umsonst versucht man mit einer Dumpingstrategie in den amerikanischen Markt zu kommen (halber Preis von Forteo) und ist auch damit bisher (Stand Anfang Sept. 2017) bei nicht mal 10% des Marktanteils der Neuverschreibungen (ohne Refills) bei den anabolen. Die aktuell 500Mio Cash werden dahinschmelzen wie Butter - bei aktuell burn rates von 50-70 Mio USD / Quartal! Da wird auch ein falsch positionierter Ankerinvestor (BBBiotech) irgendwann unruhig werden und aufhören mit seinen Stützungskäufen, wenn die notwendigen weiteren Stufen auch nicht zünden (transdermal patch, SERD pivotal)
Nungut, ich kann mich ja irren. Aber eine Überrendite sehe ich hier definitiv nicht. Eher ein verzweifelter Kampf darum seinen Platz im Markt zu finden und die ziemlich erhöhte Marktkapitalisierung weiterhin rechtfertigen zu können.
Korrektur: zur Behandlung von Osteoporose ist bisher lediglich 1 Antikörper in USA oder Europa zugelassen, nämlich Prolia® (generic name: Denosumab); der viel zitierte Antikörper Romosozumab wurde aufgrund eines kardiovasculären Signal bisher nicht zugelassen (der verwendete Plural falsch: "als die konkurrierenden Antikörper"):
FDA Rejects Romosozumab for Osteoporosis, Wants More Data
Lisa Nainggolan
July 17, 2017
http://www.medscape.com/viewarticle/882966
Von Bedeutung ist sicherlich, dass Teriparatide am 8.12.2018 den Patentschutz verliert und dann sehr wahrscheinlich generische Anbieter den Wettbewerb verschärfen.
https://www.drugs.com/availability/generic-forteo.html
Knapp 10% bei den Neuverschreibungen nach nicht einmal 3 Monaten Marktpräsenz ist sehr gut. Ich rechne zudem damit, dass dieser Marktanteil bis Ende 2017 signifikant höher sein wird, weshalb die von dem Teilnehmer prognostizierten 8 Mio USD Umsatz für 2017 sicherlich übertroffen werden. Time will tell!
"Da wird auch ein falsch positionierter Ankerinvestor (BBBiotech) irgendwann unruhig werden und aufhören mit seinen Stützungskäufen,"
man beachte: "falsch positionierter Ankerinvestor" tätigt "Stützungskäufe"!
Frage mich woher dieser Teilnehmer die Gewissheit nimmt, dass es sich um Stützungskäufe handelt? Kann es nicht sein, dass der institutionelle Anleger davon überzeugt ist, dass das Unternehmen unterbewertet ist und deswegen weiterhin investiert?
Antwort auf Beitrag Nr.: 55.887.766 von Joschka Schröder am 05.10.17 17:07:12
...ich hatte auf deinen zitierten Beitrag den Nachweis mit Quelle erbracht, dass über alle Subgruppen hinweg konsistente Ergebnisse hinsichtlich Reduktion der Fraktur-Risiken erzielt werden.
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
In der wissenschaftlichen Literatur bzw. bei der Auswertung der Abaloparatide-Studien wird jedoch über alle Subgruppen hinweg --> "Risk factor subgroups were predefined categorically for BMD T-score of the lumbar spine, total hip, and femoral neck (≤–2.5 versus >–2.5 and ≤–3.0 versus >–3.0)," eine konsistente Reduktion der Fraktur-Risiken beschrieben -->Quelle:
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/full
Dass der Nachweis bei sinkenden Fallzahlen (vor allem dann wenn sie gegen Null gehen) erschwert ist, ist eine statistische Gesetzmässigkeit. Man benötigt dann eine grössere Stichprobe, um entsprechende Signale zu beobachten.
Zitat von Joschka Schröder: Wie ich bereits geschrieben habe, sind die Patientenkollektive kaum vergleichbar, weil die Patienten in beiden Kollektiven unterschiedlich schwer krank waren, was sich natürlich auch auf das jeweilige Therapieergebnis auswirkt.
...ich hatte auf deinen zitierten Beitrag den Nachweis mit Quelle erbracht, dass über alle Subgruppen hinweg konsistente Ergebnisse hinsichtlich Reduktion der Fraktur-Risiken erzielt werden.
"Our findings illustrate that abaloparatide-SC provides consistent fracture risk reductions in all prespecified risk subgroups for both new morphometric vertebral fractures and nonvertebral fractures. Further, abaloparatide-SC produces consistent improvements in BMD of the lumbar spine, total hip, and femoral neck regardless of baseline risk. No meaningful interactions were found among baseline risk factor subgroups and treatment effects."
In der wissenschaftlichen Literatur bzw. bei der Auswertung der Abaloparatide-Studien wird jedoch über alle Subgruppen hinweg --> "Risk factor subgroups were predefined categorically for BMD T-score of the lumbar spine, total hip, and femoral neck (≤–2.5 versus >–2.5 and ≤–3.0 versus >–3.0)," eine konsistente Reduktion der Fraktur-Risiken beschrieben -->Quelle:
http://onlinelibrary.wiley.com/doi/10.1002/jbmr.2991/full
Dass der Nachweis bei sinkenden Fallzahlen (vor allem dann wenn sie gegen Null gehen) erschwert ist, ist eine statistische Gesetzmässigkeit. Man benötigt dann eine grössere Stichprobe, um entsprechende Signale zu beobachten.
!
Dieser Beitrag wurde von MadMod moderiert. Grund: Provokation
Antwort auf Beitrag Nr.: 55.910.540 von Cyberhexe am 09.10.17 12:03:47....Abaloparatide wieder nicht auf der Agenda:
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
http://www.ema.europa.eu/docs/en_GB/document_library/Agenda/…
Antwort auf Beitrag Nr.: 55.910.711 von Cyberhexe am 09.10.17 12:22:07Ich habe keine 8 Millionen prognostiziert. Diese ständige Wiederholung dieser unwahren Behauptung ist eine Frechheit ohne Gleichen. Es gleicht der Wiederholung der widerlegten Behauptung, ich sei dein Trittbrettfahrer bei EXEL gewesen, wo es hier bei W : O nachlesbar genau andersherum gewesen ist.
Ich bin aber nicht nachtragend, mein Angebot steht nach wie vor: Wenn du deine eigene Prognose lieferst, dann liefere ich meine auch. Aber ich vermute, du hast einfach nicht die Fähigkeiten Prognosezahlen auf Basis eigener Annahmen zu errechnen.
Ich bin aber nicht nachtragend, mein Angebot steht nach wie vor: Wenn du deine eigene Prognose lieferst, dann liefere ich meine auch. Aber ich vermute, du hast einfach nicht die Fähigkeiten Prognosezahlen auf Basis eigener Annahmen zu errechnen.
!
Dieser Beitrag wurde von CloudMOD moderiert. Grund: Behauptung ohne entsprechende Quellennachweise
Antwort auf Beitrag Nr.: 55.751.778 von Ville7 am 15.09.17 13:30:40
soso, diese ständige Wiederholung ist eine Frechheit. Anbei deine zitierte Nachricht! Daran muss man sicgh messen lassen. Irgendwann wird es mir zu müssig, auf EURE Provokationen zu reagieren.
Zitat von Ville7: Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)? Da ist eine Menge Fantasie eingepreist, dass Radius es schafft den anabolic market wieder zum Wachsen zu bringen. Zumal man derzeit mehr als 50Mio EUR pro Quartal Verlust einfährt....
soso, diese ständige Wiederholung ist eine Frechheit. Anbei deine zitierte Nachricht! Daran muss man sicgh messen lassen. Irgendwann wird es mir zu müssig, auf EURE Provokationen zu reagieren.
!
Dieser Beitrag wurde von MadMod moderiert. Grund: Provokation
Antwort auf Beitrag Nr.: 55.910.957 von Ville7 am 09.10.17 12:55:04
Wieder so ein weitreichender Satz (ähnlich wie bei Exelixis, dass die "Firma über Leichen geht"...), ohne diese Unterstellung detailiert zu belegen. Ich würde sagen, dass, wie bei vielen anderen Firmen auch, nicht alle Unternehmensziele termingerecht erreicht werden. Dass die meisten Unternehmensziele nicht eingehalten werden, ist eine Übertreibung!


Zitat von Ville7: Ich könnte mir gut vorstellen, dass die EMA das einfach aussitzt und weiter verzögert, weil sie mit Ablehnungen ja sehr sparsam ist. Denn scheinbar gibt es hier massive Abweichungen/Unregelmäßigkeiten, die RDUS nicht erklären kann oder nicht will. So meine Spekulation.
Die Prognose von RDUS, dass eine CHMP Opinion noch in 2017 stattfinden wird, ist eine so wertvolle Prognose wie die Prognosen der Firma zuvor, die zumeist auch nicht eingehalten werden konnten.
Wieder so ein weitreichender Satz (ähnlich wie bei Exelixis, dass die "Firma über Leichen geht"...), ohne diese Unterstellung detailiert zu belegen. Ich würde sagen, dass, wie bei vielen anderen Firmen auch, nicht alle Unternehmensziele termingerecht erreicht werden. Dass die meisten Unternehmensziele nicht eingehalten werden, ist eine Übertreibung!


Antwort auf Beitrag Nr.: 55.910.966 von Cyberhexe am 09.10.17 12:56:02
Das kommt immer auf den jeweiligen Betrachter an. Ich selbst habe mittlerweile eine ausgeprägte Abneigung, mich an weiteren Diskussionen mit Dir zu beteiligen, weil mir Deine bisweilen sehr unsauber Argumentationsführung nicht gefällt. Aus diesem Grund werde ich mich auch aus diesem Thread zurückziehen.
Zitat von Cyberhexe: Irgendwann wird es mir zu müssig, auf EURE Provokationen zu reagieren.
Das kommt immer auf den jeweiligen Betrachter an. Ich selbst habe mittlerweile eine ausgeprägte Abneigung, mich an weiteren Diskussionen mit Dir zu beteiligen, weil mir Deine bisweilen sehr unsauber Argumentationsführung nicht gefällt. Aus diesem Grund werde ich mich auch aus diesem Thread zurückziehen.
Antwort auf Beitrag Nr.: 55.911.344 von Joschka Schröder am 09.10.17 13:47:38dito ... !
Antwort auf Beitrag Nr.: 55.905.310 von Joschka Schröder am 08.10.17 12:54:48
Der Vorwurf, einer "unsauber Argumentationsführung" ist lächerlich. Nachdem verschiedene Fakten in Abrede gestellt wurden, wird dies irgendwann damit abgetan, dass man "unaufmerksam" gewesen sei. Ich bemühe mich, meine Aussagen mit den dazu korrespondierejnden Quellen zu belegen und bin auch gerne bereit, darüber kontrovers zu diskutieren. Wenn es jedoch lediglich darum geht, im Duo zu provozieren, werde ich selbstveraständlich, der Boardhygiene wegen, diese Beiträge melden! Falls ihr inhaltlich zur Diskussion etwas beitragen könnt, herzlich willkommen. Falls nicht, ist euer Fernbleiben aber ebenso erwünscht.
Zitat von Joschka Schröder:Zitat von Cyberhexe: ...was soll daran falsch sein? In jeweiligen Studien sind die Kriterien für Plazebo und Verum identisch....das ist so banal wie richtig.
Das stimmt, da war ich eben nicht aufmerksam.
Könntest Du bitte noch den vollständigen Titel der von Dir zitierte Arbeit nennen.
Der Vorwurf, einer "unsauber Argumentationsführung" ist lächerlich. Nachdem verschiedene Fakten in Abrede gestellt wurden, wird dies irgendwann damit abgetan, dass man "unaufmerksam" gewesen sei. Ich bemühe mich, meine Aussagen mit den dazu korrespondierejnden Quellen zu belegen und bin auch gerne bereit, darüber kontrovers zu diskutieren. Wenn es jedoch lediglich darum geht, im Duo zu provozieren, werde ich selbstveraständlich, der Boardhygiene wegen, diese Beiträge melden! Falls ihr inhaltlich zur Diskussion etwas beitragen könnt, herzlich willkommen. Falls nicht, ist euer Fernbleiben aber ebenso erwünscht.
Antwort auf Beitrag Nr.: 55.910.921 von Ville7 am 09.10.17 12:48:51
Es ist einfach, dir deine eigenen Kommentare zu präsentieren - das ist der Vorteil bei wo, dass man sich an seinen Kommentaren von früher messen lassen muss. Und zu Exelixis darf ich dir deine belehrenden Äusserungen in Erinnerung rufen:
Ville7 schrieb am 11.11.15 im Exelixis-Thread "Exelixis....ein schlafender Riese? USD 3.40 "(Beitrag 51.059.685:
Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in Love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen.
Da dies jedoch nicht der Exelixis-Thread ist, möchte ich natürlich beim Thema bleiben:
Radius plant eine ph2-Studie mit Elacestrant, die möglicherweise - da wäre ich zwar vorsichtig!- als Pivotal-Studie gewertet werden kann.

Zitat von Ville7: Ich habe keine 8 Millionen prognostiziert. Diese ständige Wiederholung dieser unwahren Behauptung ist eine Frechheit ohne Gleichen. Es gleicht der Wiederholung der widerlegten Behauptung, ich sei dein Trittbrettfahrer bei EXEL gewesen, wo es hier bei W : O nachlesbar genau andersherum gewesen ist.
Ich bin aber nicht nachtragend, mein Angebot steht nach wie vor: Wenn du deine eigene Prognose lieferst, dann liefere ich meine auch. Aber ich vermute, du hast einfach nicht die Fähigkeiten Prognosezahlen auf Basis eigener Annahmen zu errechnen.
Es ist einfach, dir deine eigenen Kommentare zu präsentieren - das ist der Vorteil bei wo, dass man sich an seinen Kommentaren von früher messen lassen muss. Und zu Exelixis darf ich dir deine belehrenden Äusserungen in Erinnerung rufen:
Ville7 schrieb am 11.11.15 im Exelixis-Thread "Exelixis....ein schlafender Riese? USD 3.40 "(Beitrag 51.059.685:
Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in Love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen.
Da dies jedoch nicht der Exelixis-Thread ist, möchte ich natürlich beim Thema bleiben:
Radius plant eine ph2-Studie mit Elacestrant, die möglicherweise - da wäre ich zwar vorsichtig!- als Pivotal-Studie gewertet werden kann.

Antwort auf Beitrag Nr.: 55.911.647 von Cyberhexe am 09.10.17 14:22:21Jeder Außenstehende, der sich die Diskussion in Ruhe durchliest, wird sich sein eigenes Bild machen.
Antwort auf Beitrag Nr.: 55.911.764 von Cyberhexe am 09.10.17 14:38:04Quartalszahlen gibts am 2. November nach Börsenschluss:
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=104316…
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=104316…
anbei ein sehr übersichtliches Schaubild zum Evaluierungsprozess des europ. Arzneimittelausschusses CHMP:

sehr wahrscheinlich ist die Uhr bei Abaloparatide bis zur Klärung der 2. List of outstanding issues immer noch angehalten; in 2017 gibt es noch 2 weitere Treffen, so dass eine positive Empfehlung in 2017 immer noch möglich erscheint.

sehr wahrscheinlich ist die Uhr bei Abaloparatide bis zur Klärung der 2. List of outstanding issues immer noch angehalten; in 2017 gibt es noch 2 weitere Treffen, so dass eine positive Empfehlung in 2017 immer noch möglich erscheint.
Antwort auf Beitrag Nr.: 55.910.966 von Cyberhexe am 09.10.17 12:56:02
Folgender Hinweis des Teilnehmers "...deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt" steht zur Diskussion:
Die Markteinführung eines Medikamentes beginnt bei 0% Marktanteil. Wenn dieses Medikament ein Alleinstellungsmerkmal besitzt und eine bisher nicht therapierbare Indikation betrifft ("unmet medical need"), ist sicherlich eine schnelle Penetration des "Marktes" gewährleistet. Bei allen anderen "Märkten" dauert es Jahre bis ein Medikament seine Umsatzspitze erreicht. Beim vorliegenden Markt für Osteoporose ist dies der Fall, so dass davon auszugehen ist, dass ein neues Medikament sich hauptsächlich bei den Neuverschreibungen Marktanteile sichert, sich jedoch bei den "Refills" (also bei erneuerten Rezepten) gegenüber schon länger am Markt befindlichen Medikamenten tendenziell schwer tut, diese zu verdrängen - wer wechselt schon das Medikament, wenn man damit bisher gute Erfahrungen gemacht hat?!
Der Hinweis "wenn das so bleibt" ist deswegen bei einer Markteinführung eines neuen Medikamentes nicht belastbar. Ein Medikament, dass auf dem Niveau nach 3 Monaten nach Markteinführung stagnieren würde, wäre fast immer ein Flop.
Schlussfolgerung:
Eine Umsatzprognose für Medikamente in dieser Phase ist schwierig. Viele Parameter, die sich wechselseitig beeinflussen, machen eine derartige Schätzung auch für Insider nach diversen Marktstudien nicht zur Punktlandung.
2 Dinge stehen für mich jedoch ausser Diskussion:
1.) Jede Startphase nach Markteinführung ist dynamisch, weshalb die Einschränkung "wenn das so bleibt" keinen Sinn ergibt.
2.) Der Umsatz von Tymlos in 2017 wird grösser sein als 8 Mio USD.
Zitat von Cyberhexe:Zitat von Ville7: Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)? Da ist eine Menge Fantasie eingepreist, dass Radius es schafft den anabolic market wieder zum Wachsen zu bringen. Zumal man derzeit mehr als 50Mio EUR pro Quartal Verlust einfährt....
soso, diese ständige Wiederholung ist eine Frechheit. Anbei deine zitierte Nachricht! Daran muss man sicgh messen lassen. Irgendwann wird es mir zu müssig, auf EURE Provokationen zu reagieren.
Folgender Hinweis des Teilnehmers "...deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt" steht zur Diskussion:
Die Markteinführung eines Medikamentes beginnt bei 0% Marktanteil. Wenn dieses Medikament ein Alleinstellungsmerkmal besitzt und eine bisher nicht therapierbare Indikation betrifft ("unmet medical need"), ist sicherlich eine schnelle Penetration des "Marktes" gewährleistet. Bei allen anderen "Märkten" dauert es Jahre bis ein Medikament seine Umsatzspitze erreicht. Beim vorliegenden Markt für Osteoporose ist dies der Fall, so dass davon auszugehen ist, dass ein neues Medikament sich hauptsächlich bei den Neuverschreibungen Marktanteile sichert, sich jedoch bei den "Refills" (also bei erneuerten Rezepten) gegenüber schon länger am Markt befindlichen Medikamenten tendenziell schwer tut, diese zu verdrängen - wer wechselt schon das Medikament, wenn man damit bisher gute Erfahrungen gemacht hat?!
Der Hinweis "wenn das so bleibt" ist deswegen bei einer Markteinführung eines neuen Medikamentes nicht belastbar. Ein Medikament, dass auf dem Niveau nach 3 Monaten nach Markteinführung stagnieren würde, wäre fast immer ein Flop.
Schlussfolgerung:
Eine Umsatzprognose für Medikamente in dieser Phase ist schwierig. Viele Parameter, die sich wechselseitig beeinflussen, machen eine derartige Schätzung auch für Insider nach diversen Marktstudien nicht zur Punktlandung.
2 Dinge stehen für mich jedoch ausser Diskussion:
1.) Jede Startphase nach Markteinführung ist dynamisch, weshalb die Einschränkung "wenn das so bleibt" keinen Sinn ergibt.
2.) Der Umsatz von Tymlos in 2017 wird grösser sein als 8 Mio USD.
New anabolic therapies for osteoporosis
Authors
Authors and affiliations
Salvatore MinisolaEmail authorCristiana CiprianiMarco OcchiutoJessica Pepe
1.
IM - REVIEW
First Online: 05 August 2017
Osteoporosis is characterized by low bone mass and qualitative structural abnormalities of bone tissue, leading to increased bone fragility that results in fractures. Pharmacological therapy is aimed at decreasing the risk of fracture, mainly correcting the imbalance between bone resorption and formation at the level of bone remodeling units. Anabolic therapy has the capability to increase bone mass to a greater extent than traditional antiresorptive agents. The only currently available drug licensed is parathyroid hormone 1–34 (teriparatide); new drugs are on the horizon, targeting the stimulation of bone formation, and therefore improving bone mass, structure and ultimately skeletal strength. These are represented by abaloparatide (a 34-amino acid peptide which incorporates critical N-terminal residues, shared by parathyroid hormone and parathyroid hormone-related protein, followed by sequences unique to the latter protein) and romosozumab (an antibody to sclerostin). In the future, the availability of new anabolic treatment will allow a more extensive utilization of additive and sequential approach, with the goal of both prolonging the period of treatment and, more importantly, avoiding the side effects consequent to long-term use of traditional drugs.
https://link.springer.com/article/10.1007%2Fs11739-017-1719-…
Authors
Authors and affiliations
Salvatore MinisolaEmail authorCristiana CiprianiMarco OcchiutoJessica Pepe
1.
IM - REVIEW
First Online: 05 August 2017
Osteoporosis is characterized by low bone mass and qualitative structural abnormalities of bone tissue, leading to increased bone fragility that results in fractures. Pharmacological therapy is aimed at decreasing the risk of fracture, mainly correcting the imbalance between bone resorption and formation at the level of bone remodeling units. Anabolic therapy has the capability to increase bone mass to a greater extent than traditional antiresorptive agents. The only currently available drug licensed is parathyroid hormone 1–34 (teriparatide); new drugs are on the horizon, targeting the stimulation of bone formation, and therefore improving bone mass, structure and ultimately skeletal strength. These are represented by abaloparatide (a 34-amino acid peptide which incorporates critical N-terminal residues, shared by parathyroid hormone and parathyroid hormone-related protein, followed by sequences unique to the latter protein) and romosozumab (an antibody to sclerostin). In the future, the availability of new anabolic treatment will allow a more extensive utilization of additive and sequential approach, with the goal of both prolonging the period of treatment and, more importantly, avoiding the side effects consequent to long-term use of traditional drugs.
https://link.springer.com/article/10.1007%2Fs11739-017-1719-…
Antwort auf Beitrag Nr.: 55.911.830 von Joschka Schröder am 09.10.17 14:43:29
das sehe ich ähnlich: nachdem sich verschiedene Teilnehmer verabschiedet haben, ist zu hoffen, dass die Forums-Regeln wieder konsequenter beachtet werden!
http://www.tandfonline.com/doi/abs/10.1080/13543784.2017.137…
Expert opinion: The development of alternative ways of administering PTH receptor ligands is a promising field, especially via the transdermal route. Other more promising molecules are still at very early stages of development. FDA recently requested more data on Romosozumab.
Die FDA verlangt übrigens weitere Daten zu Romosozumab!
Zitat von Joschka Schröder: Jeder Außenstehende, der sich die Diskussion in Ruhe durchliest, wird sich sein eigenes Bild machen.
das sehe ich ähnlich: nachdem sich verschiedene Teilnehmer verabschiedet haben, ist zu hoffen, dass die Forums-Regeln wieder konsequenter beachtet werden!
http://www.tandfonline.com/doi/abs/10.1080/13543784.2017.137…
Expert opinion: The development of alternative ways of administering PTH receptor ligands is a promising field, especially via the transdermal route. Other more promising molecules are still at very early stages of development. FDA recently requested more data on Romosozumab.
Die FDA verlangt übrigens weitere Daten zu Romosozumab!
Antwort auf Beitrag Nr.: 55.924.109 von Cyberhexe am 10.10.17 22:13:48Committee for medicinal products for human use (CHMP)
Minutes of the meeting on 17-20 July 2017

Minutes of the meeting on 17-20 July 2017

Antwort auf Beitrag Nr.: 55.964.145 von Cyberhexe am 17.10.17 11:05:32Das ist doch ein erstes kleines "!" im Onkologieprogramm des Unternehmens: "Fast Track" für Elacestrant in Drittlinienbehandlung von ER+ und HER2- fortgeschrittenem oder metastasenbildendem Brustkrebs:
Radius Health Receives FDA Fast Track Designation for Elacestrant (RAD1901)
GlobeNewswire•October 18, 2017Comment
- Radius plans to initiate Phase 2 clinical study of elacestrant as a third-line therapy for women with ER+ and HER2- breast cancer early in 2018 -
- Phase 2 Study is a potentially pivotal trial for accelerated approval -
WALTHAM, Mass., Oct. 18, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. ("Radius" or the "Company") (RDUS), today announced that the U.S. Food and Drug Administration (FDA) has granted Fast Track designation for elacestrant, an investigational oral selective estrogen receptor down-regulator/degrader (SERD) as a treatment of women with ER+ and HER2- advanced or metastatic breast cancer. Fast Track designation is a process designed to facilitate the development and expedite the review of new therapies to treat serious conditions and fill unmet medical needs.
Radius Health Receives FDA Fast Track Designation for Elacestrant (RAD1901)
GlobeNewswire•October 18, 2017Comment
- Radius plans to initiate Phase 2 clinical study of elacestrant as a third-line therapy for women with ER+ and HER2- breast cancer early in 2018 -
- Phase 2 Study is a potentially pivotal trial for accelerated approval -
WALTHAM, Mass., Oct. 18, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. ("Radius" or the "Company") (RDUS), today announced that the U.S. Food and Drug Administration (FDA) has granted Fast Track designation for elacestrant, an investigational oral selective estrogen receptor down-regulator/degrader (SERD) as a treatment of women with ER+ and HER2- advanced or metastatic breast cancer. Fast Track designation is a process designed to facilitate the development and expedite the review of new therapies to treat serious conditions and fill unmet medical needs.
Der Preisverlauf bestätigt das große "?" bezüglich des Potentials von Abaloparatide und den kommenden massiven Verlustquartalen.
BB-Biotech weiterhin mit immer halbherzigeren Stützungskäufen (jüngst 50.000 Stück zu USD 32.x) zur Stützung ihrer massiven Fehlpositionierung mit mehr als 5,5 Millionen Aktien und zusätzlich massivem Warrants-Bestand.
Wie sagte ein abgesetzter RDUS CEO bei den CCs immer? : "abaloparatide is the most valuable, unpartnered asset in the biotech industry". Bei den Aussagen wurde es mir damals stetig schlecht.
Heute weiß man wieso.
BB-Biotech weiterhin mit immer halbherzigeren Stützungskäufen (jüngst 50.000 Stück zu USD 32.x) zur Stützung ihrer massiven Fehlpositionierung mit mehr als 5,5 Millionen Aktien und zusätzlich massivem Warrants-Bestand.
Wie sagte ein abgesetzter RDUS CEO bei den CCs immer? : "abaloparatide is the most valuable, unpartnered asset in the biotech industry". Bei den Aussagen wurde es mir damals stetig schlecht.
Heute weiß man wieso.
Antwort auf Beitrag Nr.: 56.038.308 von Ville7 am 27.10.17 07:02:03
BB Biotech wird nie und nimmer Stützungskäufe tätigen - aus meiner Sicht ist eine solche Interpretation "Schmarrn". BB Biotech ist von Radius Health überzeugt - dies ist die wohl wahrscheinlichere Erklärung für den neuerlichen Kauf von 2 x 50.000 Aktien am 25. bzw. 26.10. auf jetzt insgesamt mehr als 5.5 Mio Aktien.
Zitat von Ville7: Der Preisverlauf bestätigt das große "?" bezüglich des Potentials von Abaloparatide und den kommenden massiven Verlustquartalen.
BB-Biotech weiterhin mit immer halbherzigeren Stützungskäufen (jüngst 50.000 Stück zu USD 32.x) zur Stützung ihrer massiven Fehlpositionierung mit mehr als 5,5 Millionen Aktien und zusätzlich massivem Warrants-Bestand.
Wie sagte ein abgesetzter RDUS CEO bei den CCs immer? : "abaloparatide is the most valuable, unpartnered asset in the biotech industry". Bei den Aussagen wurde es mir damals stetig schlecht.
Heute weiß man wieso.
BB Biotech wird nie und nimmer Stützungskäufe tätigen - aus meiner Sicht ist eine solche Interpretation "Schmarrn". BB Biotech ist von Radius Health überzeugt - dies ist die wohl wahrscheinlichere Erklärung für den neuerlichen Kauf von 2 x 50.000 Aktien am 25. bzw. 26.10. auf jetzt insgesamt mehr als 5.5 Mio Aktien.
Zusammenfassung von verschiedenen Auswertungen:

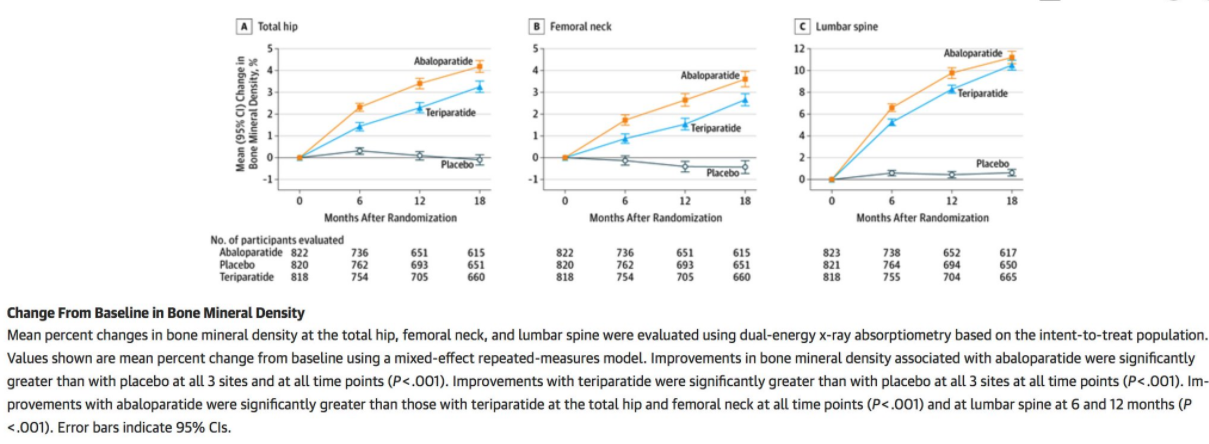
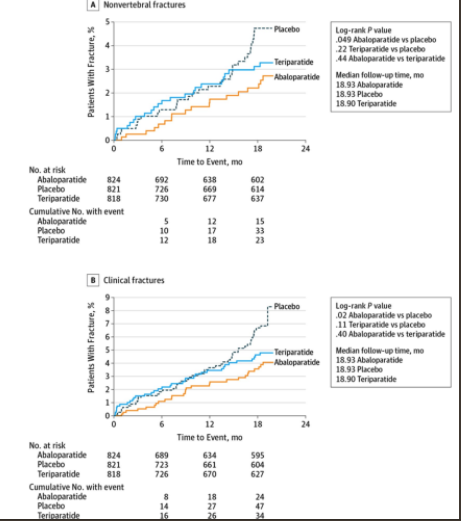
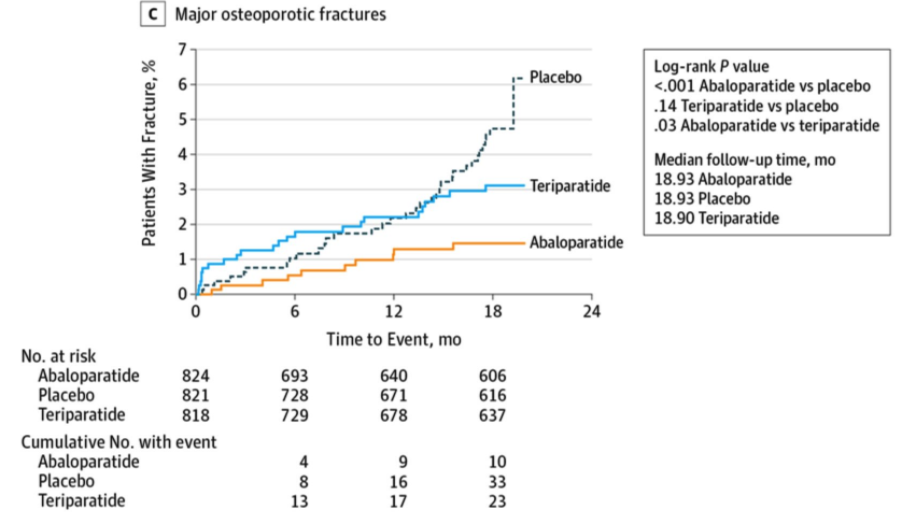




Antwort auf Beitrag Nr.: 56.064.314 von Cyberhexe am 31.10.17 11:21:44bin nun nicht so fachlich versiert in Biotech. Dennoch habe ich mir in den letzten Tagen und Monaten bei Kursschwäche Positionen in Celgene und Gilead aufgebaut, dazu halte ich noch nennenswerte Positionen in Novo Nordisk.
Nachdem ich vor Jahren den BB Biotech ( viel zu früh ! ) verkauft hatte, stiess ich nun vor Tagen bei Durchsicht seiner aktuellen Positionen auf diesen Wert, der von BB Biotech dieses Jahr massiv ausgebaut wurde.
Ich als Biotech-Laie sehe die Sache ( vereinfacht ) so:
1. Der ( amerikanische ) CEO wurde ersetzt durch einen CEO mit Europaerfahrung ( Novo Nordisk ), weil es ihm mglw. nicht gelungen ist, die Zulassung des Osteoporose-Medikaments in Europa zeitnah umzusetzen.
2. BB Biotech als in Europa ansässiger Fonds setzt genau auf diesen Umstand und weiss mglw., dass die Zulassung in Europa zeitnah ( innerhalb des nächsten halben Jahres ? ) klappt und positioniert sich durch Aktienzukäufe bereits jetzt.
3. Die heute erscheinenden Quartalszahlen sind mässig bis schlecht bzw. unterhalb der Erwartungen, daher bröselt der Kurs.
Fazit: Kurzfristig unter Druck, mittelfristig gute Kurschancen, da Zulassung in Europa wahrscheinlich.
Habe mir daher vorgestern eine Erstposition zu 27,75 € ins Depot gelegt. Mal schaun
nanu
Nachdem ich vor Jahren den BB Biotech ( viel zu früh ! ) verkauft hatte, stiess ich nun vor Tagen bei Durchsicht seiner aktuellen Positionen auf diesen Wert, der von BB Biotech dieses Jahr massiv ausgebaut wurde.
Ich als Biotech-Laie sehe die Sache ( vereinfacht ) so:
1. Der ( amerikanische ) CEO wurde ersetzt durch einen CEO mit Europaerfahrung ( Novo Nordisk ), weil es ihm mglw. nicht gelungen ist, die Zulassung des Osteoporose-Medikaments in Europa zeitnah umzusetzen.
2. BB Biotech als in Europa ansässiger Fonds setzt genau auf diesen Umstand und weiss mglw., dass die Zulassung in Europa zeitnah ( innerhalb des nächsten halben Jahres ? ) klappt und positioniert sich durch Aktienzukäufe bereits jetzt.
3. Die heute erscheinenden Quartalszahlen sind mässig bis schlecht bzw. unterhalb der Erwartungen, daher bröselt der Kurs.
Fazit: Kurzfristig unter Druck, mittelfristig gute Kurschancen, da Zulassung in Europa wahrscheinlich.
Habe mir daher vorgestern eine Erstposition zu 27,75 € ins Depot gelegt. Mal schaun
nanu
Antwort auf Beitrag Nr.: 56.079.203 von nanunana am 02.11.17 09:35:38Abaloparatide hat sehr viele Vorzüge gegenüber den anderen Medis am Markt bzw. in der Klinik.
Das grösste Handicap ist mE, dass Teriparatide im Dezember 2018 seinen Patentschutz verliert und deswegen der Preisdruck durch generische Anbieter zunehmen wird.
Patents are granted by the U.S. Patent and Trademark Office at any time during a drug's development and may include a wide range of claims.
Stabilized teriparatide solutions
Patent 6,770,623
Issued: August 3, 2004
Inventor(s): Chin-Ming; Chang & Henry A.; Havel
Assignee(s): Eli Lilly and Company
A stabilized pharmaceutical composition in the form of a solution for parenteral administration of a parathyroid hormone is described wherein the therapeutically active ingredient is stabilized with a buffer and a polyol. Preferred preparations contain in an aqueous solution human PTH(1-34), mannitol, an acetate or tartrate buffering agent and m-cresol or benzyl alcohol as a preservative.
Patent expiration dates: December 8, 2018
✓
Patent use: A METHOD OF TREATING OSTEOPOROSIS
✓
Drug product
December 8, 2018
✓
Patent use: FORTEO IS INDICATED FOR THE TREATMENT OF POST MENOPAUSAL WOMEN WITH OSTEOPOROSIS WHO ARE AT HIGH RISK FOR FRACTURE
✓
Drug product
https://www.drugs.com/a
Das grösste Handicap ist mE, dass Teriparatide im Dezember 2018 seinen Patentschutz verliert und deswegen der Preisdruck durch generische Anbieter zunehmen wird.
Patents are granted by the U.S. Patent and Trademark Office at any time during a drug's development and may include a wide range of claims.
Stabilized teriparatide solutions
Patent 6,770,623
Issued: August 3, 2004
Inventor(s): Chin-Ming; Chang & Henry A.; Havel
Assignee(s): Eli Lilly and Company
A stabilized pharmaceutical composition in the form of a solution for parenteral administration of a parathyroid hormone is described wherein the therapeutically active ingredient is stabilized with a buffer and a polyol. Preferred preparations contain in an aqueous solution human PTH(1-34), mannitol, an acetate or tartrate buffering agent and m-cresol or benzyl alcohol as a preservative.
Patent expiration dates: December 8, 2018
✓
Patent use: A METHOD OF TREATING OSTEOPOROSIS
✓
Drug product
December 8, 2018
✓
Patent use: FORTEO IS INDICATED FOR THE TREATMENT OF POST MENOPAUSAL WOMEN WITH OSTEOPOROSIS WHO ARE AT HIGH RISK FOR FRACTURE
✓
Drug product
https://www.drugs.com/a
Antwort auf Beitrag Nr.: 56.079.332 von Cyberhexe am 02.11.17 09:46:23...sorry, ich denke, dass die im August 2019 auslaufenden Patente für Konkurrenz sorgen werden:
Method of increasing bone toughness and stiffness and reducing fractures
Patent 6,977,077
Issued: December 20, 2005
Inventor(s): Hock; Janet M. & Gaich; Gregory A. & Dere; Willard H.
Assignee(s): Eli Lilly and Company
The invention relates to a method for increasing the toughness and/or stiffness of bone and/or reducing the likelihood and/or severity of bone fracture by administering a parathyroid hormone. The method can be employed to increase toughness or stiffness of bone at a site of a potential or actual trauma, such as the hip or spine of a person at risk of or suffering from osteoporosis. The method of the invention can reduce the incidence of vertebral fracure, reduce the incidence of multiple vertebral fractures, reduce the severity of vertebral fracture, and/or reduce the incidence of non-vertebral fracture.
Patent expiration dates:
August 19, 2019
✓
Patent use: METHOD OF TREATMENT OF OSTEOPOROSIS WHEREIN THE OSTEOPOROSIS IS STEROID-INDUCED
August 19, 2019
✓
Patent use: A METHOD OF TREATING OSTEOPOROSIS
August 19, 2019
✓
Patent use: FORTEO IS INDICATED FOR THE TREATMENT OF POST MENOPAUSAL WOMEN WITH OSTEOPOROSIS WHO ARE AT HIGH RISK FOR FRACTURE
Method of increasing bone toughness and stiffness and reducing fractures
Patent 6,977,077
Issued: December 20, 2005
Inventor(s): Hock; Janet M. & Gaich; Gregory A. & Dere; Willard H.
Assignee(s): Eli Lilly and Company
The invention relates to a method for increasing the toughness and/or stiffness of bone and/or reducing the likelihood and/or severity of bone fracture by administering a parathyroid hormone. The method can be employed to increase toughness or stiffness of bone at a site of a potential or actual trauma, such as the hip or spine of a person at risk of or suffering from osteoporosis. The method of the invention can reduce the incidence of vertebral fracure, reduce the incidence of multiple vertebral fractures, reduce the severity of vertebral fracture, and/or reduce the incidence of non-vertebral fracture.
Patent expiration dates:
August 19, 2019
✓
Patent use: METHOD OF TREATMENT OF OSTEOPOROSIS WHEREIN THE OSTEOPOROSIS IS STEROID-INDUCED
August 19, 2019
✓
Patent use: A METHOD OF TREATING OSTEOPOROSIS
August 19, 2019
✓
Patent use: FORTEO IS INDICATED FOR THE TREATMENT OF POST MENOPAUSAL WOMEN WITH OSTEOPOROSIS WHO ARE AT HIGH RISK FOR FRACTURE
Gruselzahlen! Erwartungen erneut verfehlt. Kurs folglich nachbörslich bei $28. BBBiotech stehen da wie Vollidioten. Deren blinde Follower auch...
Antwort auf Beitrag Nr.: 56.087.822 von Ville7 am 03.11.17 02:32:39haha ja sag das mal den blinden vögeln bei bbbiotech, die sich mit radius aktien vollstopfen
also der umsatz im letzten quartal war wirklich nicht berauschend, aber es gibt auch hoffnung für die zukunft, neben dem ex-us vertrieb der noch anlaufen muss unter anderem auch diese aussage von der konferenz:
"While Medicare remains the largest and most important segment, it's becoming more balanced against commercial segment. This represents near-term commercial opportunities for TYMLOS and sets us up well to maximize the exclusive status with express scripts that begins in January."
also der umsatz im letzten quartal war wirklich nicht berauschend, aber es gibt auch hoffnung für die zukunft, neben dem ex-us vertrieb der noch anlaufen muss unter anderem auch diese aussage von der konferenz:
"While Medicare remains the largest and most important segment, it's becoming more balanced against commercial segment. This represents near-term commercial opportunities for TYMLOS and sets us up well to maximize the exclusive status with express scripts that begins in January."
Antwort auf Beitrag Nr.: 56.090.552 von paul81 am 03.11.17 11:29:38Tja paul, schalt mal deinen Verstand ein und renne nicht BBBiotech oder Cyberhexe blind hinterher. Letztere ist m.E. unfähig ist in die Zukunft zu schauen, speziell bei wirtschaftlichen Impacts.
Und auch ein Dickfisch wie BBBiotech kann sich verrennen. Und bei RDUS hat er sich gewaltig verrannt, da die Firma einfach viel zu wenig geliefert hat. Nun besteht die Möglichkeit für die "cut your losses" und raus oder eben "Augen zu und durch" und den Kurs und die Firma stützen um die Peinlichkeit nicht zu groß erscheinen zu lassen. Noch entscheidet sich BBBiotech für zweiteres, aber auch immer halbherziger wird dabei nachgekauft.
Ich nenne nur vier Beispiele (es gibt weitere) für die jüngsten Enttäuschungen:
1. USA Zulassung - 2 Monate verschoben
2. EU Zulassung - 12-18 Monate verschoben, unklar ob das überhaupt noch was wird
3. Pricing-Strategie: in den Markt um jeden Preis mit Dumping gegenüber Forteo eintreten wollen, das kanibalisiert die eigenen Umsatzpotentiale das angeblich besseren Produkts
4. Timeline für den patch schon wieder um 1 Quartal verschoben - mit übrigens fadenscheiniger Begründung
Die Firma frisst pro Quartal gigantische 60 Mio USD pro Quartal abzüglich der Produktumsätze.
Für die große Klappe "abalo is biggest value unpartnered asset in the biotech industry" (Zitat Ex-CEO) eine ziemliche Katastrophe.
Durch die Niedrigpreisstrategie wird RDUS in den nächsten Quartalen weiterhin massive Verluste schreiben, selbst wenn man es binnen der nächsten 6 Quartal schaffen sollte die Marktführerschaft in USA zu erlangen. Bis zu Marktführerschaft wird das Cash ziemlich dezimiert sein und man die nächste Kapitalerhöhung brauchen.
Für diese Perspektive ist RDUS immer noch extrem hoch bewertet.
Hättest du mal auf mich gehört, ich warne seit Monaten.
Und auch ein Dickfisch wie BBBiotech kann sich verrennen. Und bei RDUS hat er sich gewaltig verrannt, da die Firma einfach viel zu wenig geliefert hat. Nun besteht die Möglichkeit für die "cut your losses" und raus oder eben "Augen zu und durch" und den Kurs und die Firma stützen um die Peinlichkeit nicht zu groß erscheinen zu lassen. Noch entscheidet sich BBBiotech für zweiteres, aber auch immer halbherziger wird dabei nachgekauft.
Ich nenne nur vier Beispiele (es gibt weitere) für die jüngsten Enttäuschungen:
1. USA Zulassung - 2 Monate verschoben
2. EU Zulassung - 12-18 Monate verschoben, unklar ob das überhaupt noch was wird
3. Pricing-Strategie: in den Markt um jeden Preis mit Dumping gegenüber Forteo eintreten wollen, das kanibalisiert die eigenen Umsatzpotentiale das angeblich besseren Produkts
4. Timeline für den patch schon wieder um 1 Quartal verschoben - mit übrigens fadenscheiniger Begründung
Die Firma frisst pro Quartal gigantische 60 Mio USD pro Quartal abzüglich der Produktumsätze.
Für die große Klappe "abalo is biggest value unpartnered asset in the biotech industry" (Zitat Ex-CEO) eine ziemliche Katastrophe.
Durch die Niedrigpreisstrategie wird RDUS in den nächsten Quartalen weiterhin massive Verluste schreiben, selbst wenn man es binnen der nächsten 6 Quartal schaffen sollte die Marktführerschaft in USA zu erlangen. Bis zu Marktführerschaft wird das Cash ziemlich dezimiert sein und man die nächste Kapitalerhöhung brauchen.
Für diese Perspektive ist RDUS immer noch extrem hoch bewertet.
Hättest du mal auf mich gehört, ich warne seit Monaten.
Antwort auf Beitrag Nr.: 56.090.720 von Ville7 am 03.11.17 11:47:41
dein schreibstil ist mir viel zu agressiv und persönlich, überdenk das noch einmal weil darunter leidet dann nur der fachlich durchaus berechtigte und informative teil den du schreibst
weil darunter leidet dann nur der fachlich durchaus berechtigte und informative teil den du schreibst 
ausserdem jammere ich hier ja nicht über irgendwelche (buch)verluste, die sich ohnehin in grenzen halten
Zitat von Ville7: Tja paul, schalt mal deinen Verstand ein und renne nicht BBBiotech oder Cyberhexe blind hinterher.
dein schreibstil ist mir viel zu agressiv und persönlich, überdenk das noch einmal
 weil darunter leidet dann nur der fachlich durchaus berechtigte und informative teil den du schreibst
weil darunter leidet dann nur der fachlich durchaus berechtigte und informative teil den du schreibst 
ausserdem jammere ich hier ja nicht über irgendwelche (buch)verluste, die sich ohnehin in grenzen halten

Antwort auf Beitrag Nr.: 56.090.552 von paul81 am 03.11.17 11:29:38
Der Umsatz bei Tymlos wurde so erwartet: die Grössenordnung konnte durch die Bekanntgabe der neu verordneten Rezepte ungefähr berechnet werden (Anteil bei den Neuverschreibungen im 2q bei max. 10%). Das Wachstum müsste jedoch exponentiell sein, weshalb ich im nächsten Quartal schon über 10mUSD erwarte, zumal der Anteil bei den Neuverschreibungen bereits auf 37% angestiegen ist.
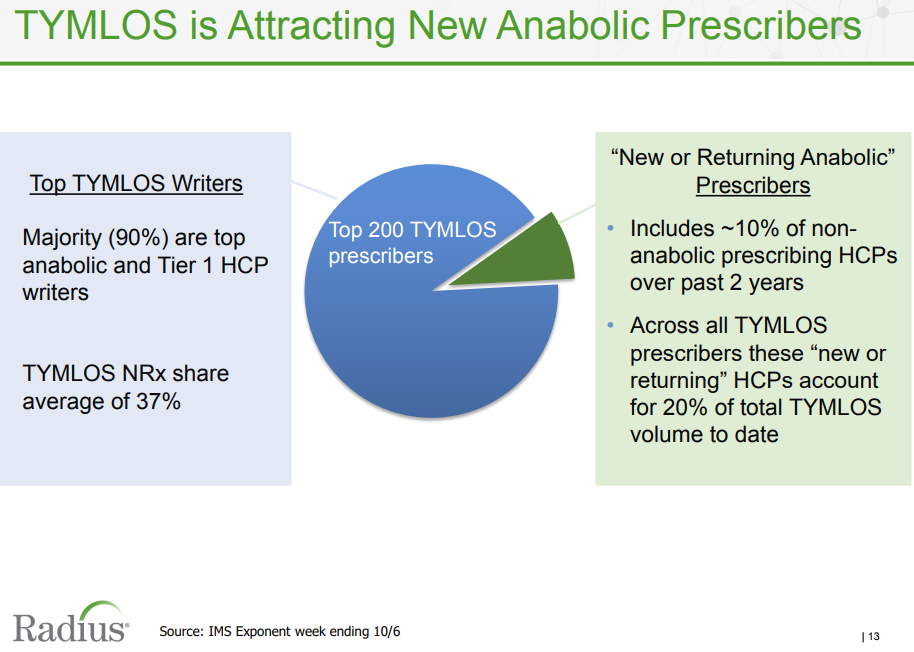
Einen Senkrechtstart hat niemand erwartet, auch wenn dies von einem Teilnehmer ansatzweise so gedeutet wird.
Ausserdem hat das Unternehmen die Prognose bestätigt, dass man noch in 2017 mit einer Zulassungsempfehlung (die kann natürlich auch negativ sein, obschon ich das nicht erwarte!) des europ. Arzneimittelausschusses CHMP erwartet.

Verschiedene Teilnehmer sind anscheinend der Meinung, dass es bei derartigen Prüfungen keine Verzögerungen gibt. Weit gefehlt....wie so oft!. Das Wichtigste scheint mir, dass eine positive Empfehlung ausgesprochen wird.
Zitat von paul81: also der umsatz im letzten quartal war wirklich nicht berauschend, aber es gibt auch hoffnung für die zukunft, neben dem ex-us vertrieb ...
Der Umsatz bei Tymlos wurde so erwartet: die Grössenordnung konnte durch die Bekanntgabe der neu verordneten Rezepte ungefähr berechnet werden (Anteil bei den Neuverschreibungen im 2q bei max. 10%). Das Wachstum müsste jedoch exponentiell sein, weshalb ich im nächsten Quartal schon über 10mUSD erwarte, zumal der Anteil bei den Neuverschreibungen bereits auf 37% angestiegen ist.

Einen Senkrechtstart hat niemand erwartet, auch wenn dies von einem Teilnehmer ansatzweise so gedeutet wird.
Ausserdem hat das Unternehmen die Prognose bestätigt, dass man noch in 2017 mit einer Zulassungsempfehlung (die kann natürlich auch negativ sein, obschon ich das nicht erwarte!) des europ. Arzneimittelausschusses CHMP erwartet.

Verschiedene Teilnehmer sind anscheinend der Meinung, dass es bei derartigen Prüfungen keine Verzögerungen gibt. Weit gefehlt....wie so oft!. Das Wichtigste scheint mir, dass eine positive Empfehlung ausgesprochen wird.
Antwort auf Beitrag Nr.: 56.092.112 von Cyberhexe am 03.11.17 13:59:50
Ich halte diese Aussage für falsch, denn die 37% beziehen sich auf den Anteil NRx (alleine) der 200 "Top Tymlos Writers". Nur der Gruppe der 200 also, die Tymlos am meisten verschreibt. Steht übrigens auf der Folie auch so drauf. Wichtig ist allerdings der Anteil am Gesamtmarkt der NRx und den hat die Firma nirgends angegeben. Sie wissen bestimmt, wieso.
Zitat von Cyberhexe: ... Das Wachstum müsste jedoch exponentiell sein, weshalb ich im nächsten Quartal schon über 10mUSD erwarte, zumal der Anteil bei den Neuverschreibungen bereits auf 37% angestiegen ist.
...
Ich halte diese Aussage für falsch, denn die 37% beziehen sich auf den Anteil NRx (alleine) der 200 "Top Tymlos Writers". Nur der Gruppe der 200 also, die Tymlos am meisten verschreibt. Steht übrigens auf der Folie auch so drauf. Wichtig ist allerdings der Anteil am Gesamtmarkt der NRx und den hat die Firma nirgends angegeben. Sie wissen bestimmt, wieso.
Antwort auf Beitrag Nr.: 55.751.778 von Ville7 am 15.09.17 13:30:40
....wie widersprüchlioch doch verschiedene Teilnehmer sind:
Bei einer Umsatzschätzung von "deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos" (siehe Zitat in fett) und einem tatsächlichen Quartalsumsatz von 3.5m USD schreibt der gleiche Teilnehmer:
"Gruselzahlen! Erwartungen erneut verfehlt."
Die Wahrheit ist jedoch, dass bei Tymlos, im übrigen wie bei den meisten Markteinführungen von Medikamenten, ein exponentielles Wachstum zu beobachten ist. Dies wird auch bei TYMLOS der Fall sein, da der Anteil bei den Neuverschreibungen vom 1.9.2017 von 10% auf mittlerweile 37% zugenommen hat:
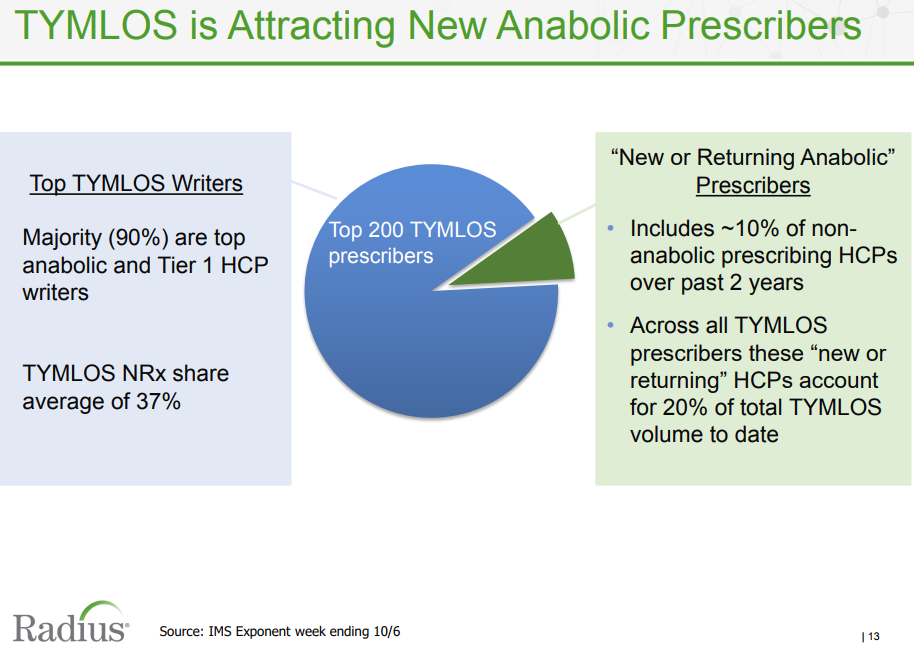
Die Aussage "8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt."
wird auf alle Fälle nicht eintreffen!
Ein Umsatzschätzung für 2018 ist natürlich von sehr vielen Unbekannten gekennzeichnet. Ich wage es dennoch und veröffentliche meine Prognose:
Tymlos-Umsatz in den US in 2018: > $70m USD
Zitat von Ville7: Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)? Da ist eine Menge Fantasie eingepreist, dass Radius es schafft den anabolic market wieder zum Wachsen zu bringen. Zumal man derzeit mehr als 50Mio EUR pro Quartal Verlust einfährt....
....wie widersprüchlioch doch verschiedene Teilnehmer sind:
Bei einer Umsatzschätzung von "deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos" (siehe Zitat in fett) und einem tatsächlichen Quartalsumsatz von 3.5m USD schreibt der gleiche Teilnehmer:
"Gruselzahlen! Erwartungen erneut verfehlt."
Die Wahrheit ist jedoch, dass bei Tymlos, im übrigen wie bei den meisten Markteinführungen von Medikamenten, ein exponentielles Wachstum zu beobachten ist. Dies wird auch bei TYMLOS der Fall sein, da der Anteil bei den Neuverschreibungen vom 1.9.2017 von 10% auf mittlerweile 37% zugenommen hat:

Die Aussage "8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt."
wird auf alle Fälle nicht eintreffen!
Ein Umsatzschätzung für 2018 ist natürlich von sehr vielen Unbekannten gekennzeichnet. Ich wage es dennoch und veröffentliche meine Prognose:
Tymlos-Umsatz in den US in 2018: > $70m USD
Antwort auf Beitrag Nr.: 56.092.406 von Cyberhexe am 03.11.17 14:32:14Ich gebe es auf. Du hast einfach das Problem, dass du einfach nicht in der Lage bist, die Dinge, die vor dir sind, richtig zu lesen und zu verstehen.
Tymlos hat keine 37% NRx !!
Die Aussage der Folie ist: NRx der Top 200 Tymlos Writers ist nicht NRx aller Tymlos Writers. Die "Low 200 Tymlos Writers" haben sicherlich ein NRx von 0%. NRx aller wurde nicht angegeben. Nur NBRx und das ist bei 16.6%. Daher sind alle deine Folgerechungen ebenso grottenfalsch. So wird das einfach nichts, Cyberhexe. Man muss schon etwas mehr Mühe und Verständnis investieren um nicht auf die Nase zu fallen. Das kriegst du offensichtlich nicht hin.
Der Markt hat es verstanden, nur eben du nicht.
@paul81: Sorry, bei so einem offensichtlichen Quatsch, den ich ständig hier von Cyberhexe lese, kann ich gar nicht anders als inzwischen persönlich zu werden....
Tymlos hat keine 37% NRx !!
Die Aussage der Folie ist: NRx der Top 200 Tymlos Writers ist nicht NRx aller Tymlos Writers. Die "Low 200 Tymlos Writers" haben sicherlich ein NRx von 0%. NRx aller wurde nicht angegeben. Nur NBRx und das ist bei 16.6%. Daher sind alle deine Folgerechungen ebenso grottenfalsch. So wird das einfach nichts, Cyberhexe. Man muss schon etwas mehr Mühe und Verständnis investieren um nicht auf die Nase zu fallen. Das kriegst du offensichtlich nicht hin.
Der Markt hat es verstanden, nur eben du nicht.
@paul81: Sorry, bei so einem offensichtlichen Quatsch, den ich ständig hier von Cyberhexe lese, kann ich gar nicht anders als inzwischen persönlich zu werden....
Antwort auf Beitrag Nr.: 56.092.406 von Cyberhexe am 03.11.17 14:32:14Eigentlich beruhigt mich, dass dieser Teilnehmer sich sehr abschätzig über RADIUS äussert. Auch im Thread "Exelixis....ein schlafender Riese? USD 3.40" hat dieser sich im Nov 2015 ebenfalls sehr unqualifiziert über das Unternehmen geäussert:
Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in Love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen.
Zu dieser Zeit stand die EXEL-Aktie übrigens bei ca. USD 5.40
Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in Love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen.
Zu dieser Zeit stand die EXEL-Aktie übrigens bei ca. USD 5.40
Antwort auf Beitrag Nr.: 56.092.721 von Cyberhexe am 03.11.17 14:57:03ok....das ist mein Fehler - mea culpa:
die 37% beziehen sich auf die TOP200, dh der tatsächliche Anteil an den Neuverschreibungen ist um einiges tiefer!
Und dennoch halte ich eine Umsatzschätzung von 8mUSD für 2017 für Schmarrn!
die 37% beziehen sich auf die TOP200, dh der tatsächliche Anteil an den Neuverschreibungen ist um einiges tiefer!
Und dennoch halte ich eine Umsatzschätzung von 8mUSD für 2017 für Schmarrn!
Antwort auf Beitrag Nr.: 56.092.868 von Cyberhexe am 03.11.17 15:10:11...habe dennoch noch nachgekauft: 900 Stück zu $28.25 auf nun insgesamt 3000 Stück!
Antwort auf Beitrag Nr.: 56.092.868 von Cyberhexe am 03.11.17 15:10:11
Auf der Quartalspressekonferenz von gestern wurde berichtet, dass bei den Neuverschreibungen NBRx (als denjenigen, die zuvor nicht behandelt wurden) TYMLOS Marktanteil bereits 16% übersteigt!
We're looking at prescription data from October. TYMLOS has reached double digits in new prescriptions here and almost 5% in [TRFs]. It's very encouraging to see the new to brand prescription share moving beyond 16%, an important leading indicator of the evolving HCP confidence. We expect to see continued share growth as we expand coverage and prescribers become increasingly familiar and comfortable with TYMLOS.
Zitat von Cyberhexe: ok....das ist mein Fehler - mea culpa:
die 37% beziehen sich auf die TOP200, dh der tatsächliche Anteil an den Neuverschreibungen ist um einiges tiefer!
Und dennoch halte ich eine Umsatzschätzung von 8mUSD für 2017 für Schmarrn!
Auf der Quartalspressekonferenz von gestern wurde berichtet, dass bei den Neuverschreibungen NBRx (als denjenigen, die zuvor nicht behandelt wurden) TYMLOS Marktanteil bereits 16% übersteigt!
We're looking at prescription data from October. TYMLOS has reached double digits in new prescriptions here and almost 5% in [TRFs]. It's very encouraging to see the new to brand prescription share moving beyond 16%, an important leading indicator of the evolving HCP confidence. We expect to see continued share growth as we expand coverage and prescribers become increasingly familiar and comfortable with TYMLOS.
Antwort auf Beitrag Nr.: 56.094.422 von Cyberhexe am 03.11.17 17:44:26Einige "Highlights" von der PK:
Nicht unwichtig, die mögliche Verlängerung beim Patentschutz durch die transdermale Applikation von Abaloparatide:Gary Hattersley, Chief Scientific Officer:
As outlined on Slide 18, we are continuing to make significant progress with our transdermal patch program, which is a key component to extend that TYMLOS franchise and expand globally. And importantly, we believe the patch can extend exclusivity to 2037.
Ein Treffen mit der FDA zur transdermalen Applikation wird im Januar 2018 stattfinden:
Gary Hattersley, Chief Scientific Officer: And finally, we have scheduled a meeting with the FDA in January to align on the pivotal and supportive studies that will be required to bridge the patch to our subcu products and we anticipate providing an update soon thereafter.
zu Elacestrant gabs nur bedingt Neuigkeiten, es wurde lediglich detailiert auf das "San Antonio Breast Cancer Symposium" im Dezember verwiesen, bei welchem folgendes veröffentlicht wird:
Gary Hattersley, Chief Scientific Officer:... there will be 5 elacestrant poster presentations. Two are clinical posters, which provide an update on our ongoing Phase I studies, which are the 005 dose escalation and expansion study; and the 106 FES-PET imaging study.
We will also be presenting 3 preclinical posters including new data on the mechanism of elacestrant action, activity in the context of endocrine resistance and the antitumor efficacy of elacestrant in combination with a PI3K inhibitor.
Die Bekanntgabe einer Empfehlung durch den europäischen Arzneimittelausschuss CHMP wird im Dezember erwartet:
Jesper Høiland, CEO: We also expect to have a CHMP opinion for our MMA (sic) [MAA] for abaloparatide subcutaneous named (inaudible) in Europe by year-end. At which point of the time, we will focus on partnerships, opportunities outside of the U.S.
Jose Carmona, CFO: After the expected CHMP opinion in mid-December and SABCS, we will assess strategic alternatives for abaloparatide outside of U.S. and the best approaches for developing elacestrant in earlier lines of therapy.
...soll möglicherweise heissen: um Elacestrant auch in Erst-und Zwetlinienbehandlung zu testen, wird ein Kooperationspartner benötigt.
last but not least...Ansbert Gadicke braucht es wohl nicht mehr:
Jesper Høiland, CEO:
We are also announcing today that Dr. Ansbert Gadicke has resigned from the Board of Directors of the company effective November 8, 2017, after having served the Board of Directors for the company and its predecessor since 2003. Following Dr. Gadicke's resignation, we expect to reduce the size of the board from 10 to 9 members.
Nicht unwichtig, die mögliche Verlängerung beim Patentschutz durch die transdermale Applikation von Abaloparatide:Gary Hattersley, Chief Scientific Officer:
As outlined on Slide 18, we are continuing to make significant progress with our transdermal patch program, which is a key component to extend that TYMLOS franchise and expand globally. And importantly, we believe the patch can extend exclusivity to 2037.
Ein Treffen mit der FDA zur transdermalen Applikation wird im Januar 2018 stattfinden:
Gary Hattersley, Chief Scientific Officer: And finally, we have scheduled a meeting with the FDA in January to align on the pivotal and supportive studies that will be required to bridge the patch to our subcu products and we anticipate providing an update soon thereafter.
zu Elacestrant gabs nur bedingt Neuigkeiten, es wurde lediglich detailiert auf das "San Antonio Breast Cancer Symposium" im Dezember verwiesen, bei welchem folgendes veröffentlicht wird:
Gary Hattersley, Chief Scientific Officer:... there will be 5 elacestrant poster presentations. Two are clinical posters, which provide an update on our ongoing Phase I studies, which are the 005 dose escalation and expansion study; and the 106 FES-PET imaging study.
We will also be presenting 3 preclinical posters including new data on the mechanism of elacestrant action, activity in the context of endocrine resistance and the antitumor efficacy of elacestrant in combination with a PI3K inhibitor.
Die Bekanntgabe einer Empfehlung durch den europäischen Arzneimittelausschuss CHMP wird im Dezember erwartet:
Jesper Høiland, CEO: We also expect to have a CHMP opinion for our MMA (sic) [MAA] for abaloparatide subcutaneous named (inaudible) in Europe by year-end. At which point of the time, we will focus on partnerships, opportunities outside of the U.S.
Jose Carmona, CFO: After the expected CHMP opinion in mid-December and SABCS, we will assess strategic alternatives for abaloparatide outside of U.S. and the best approaches for developing elacestrant in earlier lines of therapy.
...soll möglicherweise heissen: um Elacestrant auch in Erst-und Zwetlinienbehandlung zu testen, wird ein Kooperationspartner benötigt.
last but not least...Ansbert Gadicke braucht es wohl nicht mehr:
Jesper Høiland, CEO:
We are also announcing today that Dr. Ansbert Gadicke has resigned from the Board of Directors of the company effective November 8, 2017, after having served the Board of Directors for the company and its predecessor since 2003. Following Dr. Gadicke's resignation, we expect to reduce the size of the board from 10 to 9 members.
Antwort auf Beitrag Nr.: 56.094.965 von Cyberhexe am 03.11.17 18:32:57....BB Biotech hat weitere 50.000 Aktien gekauft, und zwar am 3.11.17 zu $29,1515
http://files.shareholder.com/downloads/AMDA-1D3H6P/543682591…
Verschiedene Teilnehmer interpretieren dies als "Stützungskäufe" - ich bin mir sehr sicher, dass BB Biotech vom Potenzial des Unternehmens überzeugt ist und deswegen weiter investiert...auf mittlerweile 5.648.799 (!) Anteile.
http://files.shareholder.com/downloads/AMDA-1D3H6P/543682591…
Verschiedene Teilnehmer interpretieren dies als "Stützungskäufe" - ich bin mir sehr sicher, dass BB Biotech vom Potenzial des Unternehmens überzeugt ist und deswegen weiter investiert...auf mittlerweile 5.648.799 (!) Anteile.
Antwort auf Beitrag Nr.: 56.124.425 von Cyberhexe am 07.11.17 19:16:19...auch CEO, Hoiland Jesper, scheint von seinem Unternehmen überzeugt zu sein, da er heute 6800 Aktien zu $29.0368 erworben hat.
https://www.sec.gov/Archives/edgar/data/1428522/000120919117…
https://www.sec.gov/Archives/edgar/data/1428522/000120919117…
Antwort auf Beitrag Nr.: 56.126.453 von Cyberhexe am 07.11.17 23:21:58das Unternehmen ist vollständig im Besitz von insitutionellen Anlegern - die Quote ist mittlerweile über 100%, trotz zeitlicher Differenzen in der Berichterstattung:
http://www.nasdaq.com/symbol/rdus/institutional-holdings
http://www.nasdaq.com/symbol/rdus/institutional-holdings
Antwort auf Beitrag Nr.: 56.128.760 von Cyberhexe am 08.11.17 09:40:43
http://diyinvestor.de/institutionelle-anleger-gut-oder-schle…
Zitat von Cyberhexe: das Unternehmen ist vollständig im Besitz von insitutionellen Anlegern - die Quote ist mittlerweile über 100%, trotz zeitlicher Differenzen in der Berichterstattung:
http://www.nasdaq.com/symbol/rdus/institutional-holdings
http://diyinvestor.de/institutionelle-anleger-gut-oder-schle…
Antwort auf Beitrag Nr.: 56.154.593 von intercorni am 10.11.17 16:10:04Ja. Und hier im besonderen. BBBiotech hat einfach voll daneben gegriffen, zumindest beim Einstiegspreis. Ob langfristig auch wird sich noch zeigen. Sieht aber derzeit nicht gut aus.
Erneut weitere Absturz mit minus 10%.
Ich warne seit langem. Aber BBBiotech und Cyberhexe können ja nicht irren. Teure Einschätzung!
Ich warne seit langem. Aber BBBiotech und Cyberhexe können ja nicht irren. Teure Einschätzung!
Antwort auf Beitrag Nr.: 56.182.122 von Ville7 am 14.11.17 18:54:14einfach mal abwarten...bei Exelixis hat es auch über ein Jahr gedauert bis das Teil gezündet hat. Und auch damals wollte ein "Neunmalkluger" gute Ratschläge erteilen!?!
Hab heute nochmals 500 Stück nachgelegt:
...mein Durchschnittspreis (knapp über $30) ist übrigens gar nicht so weit weg vom aktuellen Kurs!
Hab heute nochmals 500 Stück nachgelegt:

...mein Durchschnittspreis (knapp über $30) ist übrigens gar nicht so weit weg vom aktuellen Kurs!
Antwort auf Beitrag Nr.: 56.038.308 von Ville7 am 27.10.17 07:02:03
BB Biotech berichtet am 16.11. über einen weiteren Zukauf von 50.000 RADIUS Health-Aktien vom 14.11. zu $26.2478 auf nunmehr 5.698.799 Aktien.
Ist das nun ein weiterer "Stützungskauf einer massiven Fehlpositionierung"?
Time will tell!
Zitat von Ville7: Der Preisverlauf bestätigt das große "?" bezüglich des Potentials von Abaloparatide und den kommenden massiven Verlustquartalen.
BB-Biotech weiterhin mit immer halbherzigeren Stützungskäufen (jüngst 50.000 Stück zu USD 32.x) zur Stützung ihrer massiven Fehlpositionierung mit mehr als 5,5 Millionen Aktien und zusätzlich massivem Warrants-Bestand.
Wie sagte ein abgesetzter RDUS CEO bei den CCs immer? : "abaloparatide is the most valuable, unpartnered asset in the biotech industry". Bei den Aussagen wurde es mir damals stetig schlecht.
Heute weiß man wieso.
BB Biotech berichtet am 16.11. über einen weiteren Zukauf von 50.000 RADIUS Health-Aktien vom 14.11. zu $26.2478 auf nunmehr 5.698.799 Aktien.
Ist das nun ein weiterer "Stützungskauf einer massiven Fehlpositionierung"?
Time will tell!
Antwort auf Beitrag Nr.: 56.212.440 von Cyberhexe am 17.11.17 19:50:12sorry, hab den HL vergessen:
http://files.shareholder.com/downloads/AMDA-1D3H6P/422188706…
http://files.shareholder.com/downloads/AMDA-1D3H6P/422188706…
Antwort auf Beitrag Nr.: 56.038.308 von Ville7 am 27.10.17 07:02:03
aktueller verfügbarer Stand bei den "Institutional Holdings": 119.18%
http://www.nasdaq.com/symbol/rdus/ownership-summary
...das sind wahrscheinlich auch alles "halbherzige Stützungsstrümpfe...." ...äh, sorry "halbherzige Stützungskäufe" natürlich und zwar "...zur Stützung ihrer massiven Fehlpositionierung."
Zum Glück haben wir derartige Spezialisten im Forum.
Zitat von Ville7: Der Preisverlauf bestätigt das große "?" bezüglich des Potentials von Abaloparatide und den kommenden massiven Verlustquartalen.
BB-Biotech weiterhin mit immer halbherzigeren Stützungskäufen (jüngst 50.000 Stück zu USD 32.x) zur Stützung ihrer massiven Fehlpositionierung mit mehr als 5,5 Millionen Aktien und zusätzlich massivem Warrants-Bestand.
Wie sagte ein abgesetzter RDUS CEO bei den CCs immer? : "abaloparatide is the most valuable, unpartnered asset in the biotech industry". Bei den Aussagen wurde es mir damals stetig schlecht.
Heute weiß man wieso.
aktueller verfügbarer Stand bei den "Institutional Holdings": 119.18%
http://www.nasdaq.com/symbol/rdus/ownership-summary
...das sind wahrscheinlich auch alles "halbherzige Stützungsstrümpfe...." ...äh, sorry "halbherzige Stützungskäufe" natürlich und zwar "...zur Stützung ihrer massiven Fehlpositionierung."
Zum Glück haben wir derartige Spezialisten im Forum.

Antwort auf Beitrag Nr.: 56.218.803 von Cyberhexe am 19.11.17 12:53:01
Radius Health Announces Five Presentations on elacestrant (RAD1901) at the San Antonio Breast Cancer Symposium (SABCS)
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=105057…
Radius Health Announces Five Presentations on elacestrant (RAD1901) at the San Antonio Breast Cancer Symposium (SABCS)
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=105057…
Antwort auf Beitrag Nr.: 56.364.360 von Cyberhexe am 04.12.17 23:35:48apropos...man könnte den Wecker danach stellen: gerät die Aktie von RADIUS Health unter Druck geht ein Türchen auf und ein sehr berechenbarer Teilnehmer erscheint um einige Sprechblasen abzugeben; diese zu zitieren grenzt jedoch an Zeitverschwendung, weil sowohl deren Aussagekraft als auch deren fundamentale Analyse - um es positiv darzustellen- ausbaufähig ist!
Antwort auf Beitrag Nr.: 56.364.474 von Cyberhexe am 05.12.17 00:00:11Redest du von dir selber? 

Der Kurs verrät doch alles. Daher meinerseits alles richtig gemacht. Deinerseits hingegen: uuuhmm.
Kommentar zu den letzten News (elacestrant auf SABCS):
Fünf Poster-Präsentationen (d.h. unterste Wichtigkeitskategorie), das haut keinen vom Hocker.
Deswegen dann noch einen Investor-CC zu machen erscheint für mich zudem lächerlich.


Der Kurs verrät doch alles. Daher meinerseits alles richtig gemacht. Deinerseits hingegen: uuuhmm.

Kommentar zu den letzten News (elacestrant auf SABCS):
Fünf Poster-Präsentationen (d.h. unterste Wichtigkeitskategorie), das haut keinen vom Hocker.
Deswegen dann noch einen Investor-CC zu machen erscheint für mich zudem lächerlich.
Antwort auf Beitrag Nr.: 56.364.474 von Cyberhexe am 05.12.17 00:00:11abgesehen davon, dass das auf dem San Antonio Breast Cancer Symposium veröffentlichte Ergebnis der Ph1 von Elacestrant bei fortgeschrittenem ER+ BC (data cutoff 30.10.17) bei zuvor mehrfach behandelten Patienten mit Metastasen...
All study participants are heavily pretreated ER+, HER2-negative, advanced breast cancer patients that have received a median of three prior lines of systemic therapy and have evaluable advanced or metastatic disease.
...ausgezeichnet ist....
- Elacestrant 400mg single agent Objective Response Rate (ORR) was 27.3% in heavily pre-treated patients with advanced ER+ breast cancer at the pre-determined study cutoff date of October 30, 2017-
- Median PFS was 5.4 months and Clinical Benefit Rate at 24 weeks was 47.4% -
..., ist die Aussicht auf eine früh in 2018 zu beginnende Pivotalstudie viel versprechend:
Radius plans to initiate a Phase 2 clinical study of elacestrant monotherapy, a potentially pivotal study, for women with advanced or metastatic ER+/HER2- breast cancer early in 2018.
Fast Track Status wurde von der FDA bereits erteilt:
Elacestrant recently received Fast Track designation from the U.S. Food and Drug Administration.
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=105116…
Radius Investigational Drug Elacestrant (RAD1901) Continues to Show Promise in Advanced ER+ / HER2- Breast Cancer at the 2017 San Antonio Breast Cancer Symposium
-Elacestrant 400mg single agent Objective Response Rate (ORR) was 27.3% in heavily pre-treated patients with advanced ER+ breast cancer at the pre-determined study cutoff date of October 30, 2017-
-Median PFS was 5.4 months and Clinical Benefit Rate at 24 weeks was 47.4% -
-38% of study patients previously received fulvestrant; 40% received palbociclib or other CDK 4/6 inhibitor; 50% had an ESR1 mutation-
-10 of the 40 patients remain on treatment as of the cutoff date-
-Investor Webcast today at 8:00 pm CT-
WALTHAM, Mass., Dec. 07, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS) today provided an update on data from the Phase 1 005 clinical study of elacestrant (RAD1901), an oral selective estrogen receptor degrader (SERD), in patients with estrogen receptor positive (ER+) breast cancer. The data were presented at a Spotlight Presentation (Abstract 1410) during the 2017 San Antonio Breast Cancer Symposium (SABCS). Elacestrant recently received Fast Track designation from the U.S. Food and Drug Administration.
There are 40 patients that have been treated at the 400 mg dose in the elacestrant Phase I dose escalation and expansion cohorts. All study participants are heavily pretreated ER+, HER2-negative, advanced breast cancer patients that have received a median of three prior lines of systemic therapy and have evaluable advanced or metastatic disease. Of the enrolled patients, 22 patients met the RECIST measurable disease criteria at baseline and there were 6 confirmed partial responses in this group. Elacestrant was well-tolerated with the most common adverse events being low grade nausea, dyspepsia and vomiting.
"It is quite encouraging to see the clinical activity with elacestrant in the heavily pretreated advanced patient population, and further therapeutic development is warranted for patients with hormone receptor positive breast cancer", commented Dr. Aditya Bardia, Director of Precision Medicine and attending physician at Center for Breast Cancer, Massachusetts General Hospital Cancer Center, Harvard Medical School, Boston, MA.
Radius plans to initiate a Phase 2 clinical study of elacestrant monotherapy, a potentially pivotal study, for women with advanced or metastatic ER+/HER2- breast cancer early in 2018.
"Patients cycle through and generally do not repeat treatment regimens, limiting treatment options as their disease advances. We are pleased about the potential to offer patients who have progressed or relapsed during their current standard of care with a new treatment option," said Gary Hattersley, PhD, Chief Scientific Officer. "Radius is committed to developing and to providing breast cancer patients with the next generation of hormonal treatment options, as a single agent and in combination, across all lines of therapy."
An update on data from the elacestrant FES PET 106 Phase I clinical study in the EU was presented yesterday and demonstrated that elacestrant reduces 18F-FES uptake in patients with advanced ER+ breast cancer who progressed on prior endocrine therapy. The reduction in FES uptake supports elacestrant dose selection for further clinical development and was similar in patients harboring mutant or wildtype ESR-1. Three preclinical poster presentations further highlighting and demonstrating elacestrant activity, as a single agent and in combination with other targeted therapies, will be presented tomorrow morning at SABCS.
Following a strategic review, Radius has decided to discontinue further evaluation of elacestrant for vasomotor symptoms and will focus instead on the continued clinical development of the compound as a potential treatment option in breast cancer.
All study participants are heavily pretreated ER+, HER2-negative, advanced breast cancer patients that have received a median of three prior lines of systemic therapy and have evaluable advanced or metastatic disease.
...ausgezeichnet ist....
- Elacestrant 400mg single agent Objective Response Rate (ORR) was 27.3% in heavily pre-treated patients with advanced ER+ breast cancer at the pre-determined study cutoff date of October 30, 2017-
- Median PFS was 5.4 months and Clinical Benefit Rate at 24 weeks was 47.4% -
..., ist die Aussicht auf eine früh in 2018 zu beginnende Pivotalstudie viel versprechend:
Radius plans to initiate a Phase 2 clinical study of elacestrant monotherapy, a potentially pivotal study, for women with advanced or metastatic ER+/HER2- breast cancer early in 2018.
Fast Track Status wurde von der FDA bereits erteilt:
Elacestrant recently received Fast Track designation from the U.S. Food and Drug Administration.
http://ir.radiuspharm.com/releasedetail.cfm?ReleaseID=105116…
Radius Investigational Drug Elacestrant (RAD1901) Continues to Show Promise in Advanced ER+ / HER2- Breast Cancer at the 2017 San Antonio Breast Cancer Symposium
-Elacestrant 400mg single agent Objective Response Rate (ORR) was 27.3% in heavily pre-treated patients with advanced ER+ breast cancer at the pre-determined study cutoff date of October 30, 2017-
-Median PFS was 5.4 months and Clinical Benefit Rate at 24 weeks was 47.4% -
-38% of study patients previously received fulvestrant; 40% received palbociclib or other CDK 4/6 inhibitor; 50% had an ESR1 mutation-
-10 of the 40 patients remain on treatment as of the cutoff date-
-Investor Webcast today at 8:00 pm CT-
WALTHAM, Mass., Dec. 07, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS) today provided an update on data from the Phase 1 005 clinical study of elacestrant (RAD1901), an oral selective estrogen receptor degrader (SERD), in patients with estrogen receptor positive (ER+) breast cancer. The data were presented at a Spotlight Presentation (Abstract 1410) during the 2017 San Antonio Breast Cancer Symposium (SABCS). Elacestrant recently received Fast Track designation from the U.S. Food and Drug Administration.
There are 40 patients that have been treated at the 400 mg dose in the elacestrant Phase I dose escalation and expansion cohorts. All study participants are heavily pretreated ER+, HER2-negative, advanced breast cancer patients that have received a median of three prior lines of systemic therapy and have evaluable advanced or metastatic disease. Of the enrolled patients, 22 patients met the RECIST measurable disease criteria at baseline and there were 6 confirmed partial responses in this group. Elacestrant was well-tolerated with the most common adverse events being low grade nausea, dyspepsia and vomiting.
"It is quite encouraging to see the clinical activity with elacestrant in the heavily pretreated advanced patient population, and further therapeutic development is warranted for patients with hormone receptor positive breast cancer", commented Dr. Aditya Bardia, Director of Precision Medicine and attending physician at Center for Breast Cancer, Massachusetts General Hospital Cancer Center, Harvard Medical School, Boston, MA.
Radius plans to initiate a Phase 2 clinical study of elacestrant monotherapy, a potentially pivotal study, for women with advanced or metastatic ER+/HER2- breast cancer early in 2018.
"Patients cycle through and generally do not repeat treatment regimens, limiting treatment options as their disease advances. We are pleased about the potential to offer patients who have progressed or relapsed during their current standard of care with a new treatment option," said Gary Hattersley, PhD, Chief Scientific Officer. "Radius is committed to developing and to providing breast cancer patients with the next generation of hormonal treatment options, as a single agent and in combination, across all lines of therapy."
An update on data from the elacestrant FES PET 106 Phase I clinical study in the EU was presented yesterday and demonstrated that elacestrant reduces 18F-FES uptake in patients with advanced ER+ breast cancer who progressed on prior endocrine therapy. The reduction in FES uptake supports elacestrant dose selection for further clinical development and was similar in patients harboring mutant or wildtype ESR-1. Three preclinical poster presentations further highlighting and demonstrating elacestrant activity, as a single agent and in combination with other targeted therapies, will be presented tomorrow morning at SABCS.
Following a strategic review, Radius has decided to discontinue further evaluation of elacestrant for vasomotor symptoms and will focus instead on the continued clinical development of the compound as a potential treatment option in breast cancer.
heute beginnt die letzte Sitzung des europ. Arzneimittelausschusses CHMP in 2017:
http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/l…
Ich hoffe doch sehr, dass die Empfehlung auf Zulassung (positiv oder negativ) von Abaloparatide, wie von Radius angekündigt, auf der Tagesordnung sein wird.
http://www.ema.europa.eu/ema/index.jsp?curl=pages/about_us/l…
Ich hoffe doch sehr, dass die Empfehlung auf Zulassung (positiv oder negativ) von Abaloparatide, wie von Radius angekündigt, auf der Tagesordnung sein wird.
Antwort auf Beitrag Nr.: 56.430.311 von Cyberhexe am 12.12.17 12:13:42Sieht nach der nächsten Enttäuschung aus. Und nach keiner ODAC Empfehlung! Zumindest nicht in Dezember. Aber wie will RDUS das denn überhaupt noch fixen, nach drei Terminen, bei denen man scheinbar die Bedenken der EMA bisher nicht nehmen konnte. Die EMA zieht das wohl hin - in der üblichen Art - so lange bis RDUS die application zurückzieht. Das sieht nicht so gut für RDUS aus.
Antwort auf Beitrag Nr.: 56.433.621 von Ville7 am 12.12.17 18:27:55
...nun ja eine ODAC-Empfehlung (ODAC ist das Oncologic Drugs Advisory Committee der FDA) wird es sicherlich nicht geben da hast du ausnahmsweise einmal recht!
da hast du ausnahmsweise einmal recht!
Zitat von Ville7: Sieht nach der nächsten Enttäuschung aus. Und nach keiner ODAC Empfehlung! Zumindest nicht in Dezember. Aber wie will RDUS das denn überhaupt noch fixen, nach drei Terminen, bei denen man scheinbar die Bedenken der EMA bisher nicht nehmen konnte. Die EMA zieht das wohl hin - in der üblichen Art - so lange bis RDUS die application zurückzieht. Das sieht nicht so gut für RDUS aus.
...nun ja eine ODAC-Empfehlung (ODAC ist das Oncologic Drugs Advisory Committee der FDA) wird es sicherlich nicht geben
 da hast du ausnahmsweise einmal recht!
da hast du ausnahmsweise einmal recht!
Antwort auf Beitrag Nr.: 56.434.371 von Cyberhexe am 12.12.17 19:55:58Wenn du schon auf dem Gedanken-Vertipper rumreiten musst um wenigstens einmal Recht zu haben bist du echt ein armes W*******. Natürlich meinte ich CHMP...
die institutionellen Anleger scheinen an den Erfolg zu glauben:
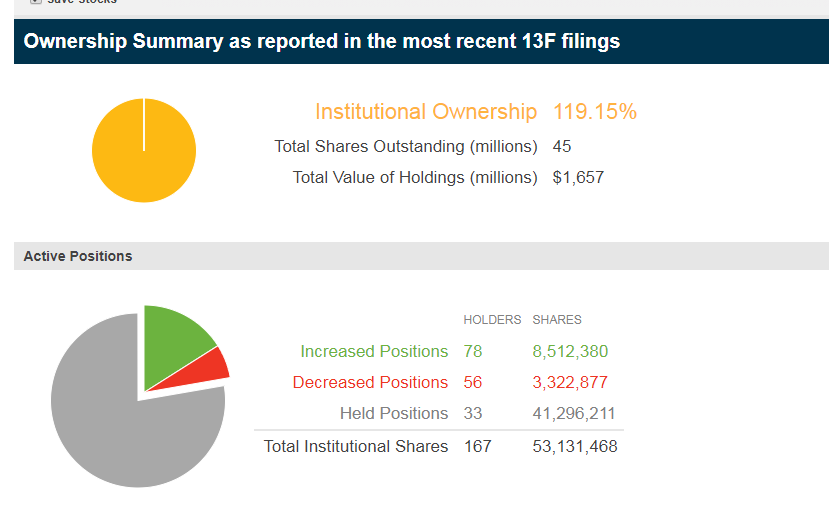
bin gespannt was bei der "Oral Explanation" herauskommt; Abaloparatide ist in den USA bereits seit 1/2y auf dem Markt, ohne dass bei der Pharmakovigilanz unerwünschte Wirkungen zu vermelden sind. Sehr wahrscheinlich weiss man nach der Veröffentlichung des Protokolls der Ausschuss-Sitzung (CHMP) etwas mehr.

bin gespannt was bei der "Oral Explanation" herauskommt; Abaloparatide ist in den USA bereits seit 1/2y auf dem Markt, ohne dass bei der Pharmakovigilanz unerwünschte Wirkungen zu vermelden sind. Sehr wahrscheinlich weiss man nach der Veröffentlichung des Protokolls der Ausschuss-Sitzung (CHMP) etwas mehr.
Antwort auf Beitrag Nr.: 56.434.421 von Ville7 am 12.12.17 20:05:15
...na, gehts wieder los mit den Beleidigungen? Mit Argumenten scheints wohl nicht zu gehen!
Zitat von Ville7: Wenn du schon auf dem Gedanken-Vertipper rumreiten musst um wenigstens einmal Recht zu haben bist du echt ein armes W*******. Natürlich meinte ich CHMP...
...na, gehts wieder los mit den Beleidigungen? Mit Argumenten scheints wohl nicht zu gehen!
Antwort auf Beitrag Nr.: 56.184.777 von Cyberhexe am 15.11.17 00:04:41
..in Anbetracht der "Oral Explanation" von Morgen wird es mir nun doch etwas zu ungemütlich, so dass ich heute insgesamt 1000 Stück zu 30.01 USD verkauft habe.
Zitat von Cyberhexe: einfach mal abwarten...bei Exelixis hat es auch über ein Jahr gedauert bis das Teil gezündet hat. Und auch damals wollte ein "Neunmalkluger" gute Ratschläge erteilen!?!
Hab heute nochmals 500 Stück nachgelegt:
...mein Durchschnittspreis (knapp über $30) ist übrigens gar nicht so weit weg vom aktuellen Kurs!
..in Anbetracht der "Oral Explanation" von Morgen wird es mir nun doch etwas zu ungemütlich, so dass ich heute insgesamt 1000 Stück zu 30.01 USD verkauft habe.
Antwort auf Beitrag Nr.: 56.434.913 von Cyberhexe am 12.12.17 21:27:14Einschätzung zu RDUS seit Q4 2016:
Ville 1 : Cyberhexe 0
Hättest du mal auf mich gehört, dann wären dir die Verluste erspart geblieben.
PS: BBBiotech ist hier komplett ahnunglos.
Ville 1 : Cyberhexe 0
Hättest du mal auf mich gehört, dann wären dir die Verluste erspart geblieben.
PS: BBBiotech ist hier komplett ahnunglos.
Antwort auf Beitrag Nr.: 56.092.910 von Cyberhexe am 03.11.17 15:12:40
bei einem Durchschnittspreis knapp über $30 ist das Verlustgeschäft marginal; wenn ich mir das Börsenleben so zurecht legen würde wie "andere" (zig Tranchen und vergleicht beim Verkauf mit der "billigsten")...ja dann wäre sogar mein RDUS-Geschäft von gestern gewinnbringend. Aber ich will mich ja nicht selbst belügen.
Der Verkauf von 1000 Stück hat tatsächlich etwas mit Risikomangament zu tun, da zu wenig Info über die "Oral Explanation" zur Verfügung steht.
Apropos, den Punkt hast du jedoch redlich verdient, da es sicherlich keine ODAC-Empfehlung bei der EMA geben wird.
Zitat von Cyberhexe: ...habe dennoch noch nachgekauft: 900 Stück zu $28.25 auf nun insgesamt 3000 Stück!
bei einem Durchschnittspreis knapp über $30 ist das Verlustgeschäft marginal; wenn ich mir das Börsenleben so zurecht legen würde wie "andere" (zig Tranchen und vergleicht beim Verkauf mit der "billigsten")...ja dann wäre sogar mein RDUS-Geschäft von gestern gewinnbringend. Aber ich will mich ja nicht selbst belügen.
Der Verkauf von 1000 Stück hat tatsächlich etwas mit Risikomangament zu tun, da zu wenig Info über die "Oral Explanation" zur Verfügung steht.
Apropos, den Punkt hast du jedoch redlich verdient, da es sicherlich keine ODAC-Empfehlung bei der EMA geben wird.
Antwort auf Beitrag Nr.: 56.435.955 von Ville7 am 13.12.17 08:04:08Ich will gar keinen Hehl daraus machen, dass mich die RDUS-Performance nicht zufrieden stellt und ich bereits seit langem auf eine Empfehlung auf Zulassung des europ. Arzneimittelausschusses CHMP warte...mit anschliessender (67 Tage) Zulassung durch die Kommission. Obwohl es bei den Ergebnissen zu Abalaopratide sicherlich einige Schwachpunkte gibt, haben diese bei der FDA keine derartige Verzögerung verursacht. Dies zeigt sehr deutlich, dass Pharmaprodukte und deren Zulassungsverfahren immer auch mit unbekannten Variabeln (für mich zumindest) verbunden sind.
Bezüglich der reisserischen Beiträge eines Teilnehmers, der meint, diese auch mich nicht zufriedenstellende Performance permanent kritisieren zu müssen - ohne substanziell zu reussieren-, dem sei bei seinen eighenen Threads der Spiegel vorgehalten. Eigentlich interessiert mich dies nicht, jedoch in Anbetracht der wiederholten Tiefschläge (etliche Beiträge wurden von den Mods bereits wegen beleidigendem Inhalt gelöscht) will ich mich (obschon mir das eigentlich sehr zuwider ist) für einmal auf dieses Niveau begeben - aber wirklich nur einmal:
Immunogen-Thread eröffnet am 27.1.2016
Kurs Open $9.15 High $9.50 Low $8.50 Close $8.64
aktueller Kurs $6.06
Diese Performance ist sogar noch lausiger als die von RDUS seit Threaderöffnung ($36.50 auf $29.60)
...aber man wird sicherlich 1000 Gründe finden, um diese Performance schön zu reden!
Und jetzt, bitte, wieder zurück zu den RDUS_Fakten.
Bin sehr gespannt, was heute bei der Anhörung herauskommt:
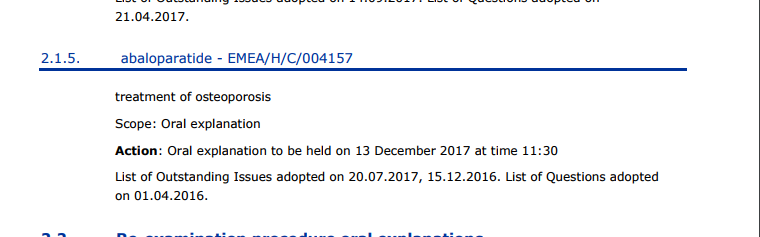
Bezüglich der reisserischen Beiträge eines Teilnehmers, der meint, diese auch mich nicht zufriedenstellende Performance permanent kritisieren zu müssen - ohne substanziell zu reussieren-, dem sei bei seinen eighenen Threads der Spiegel vorgehalten. Eigentlich interessiert mich dies nicht, jedoch in Anbetracht der wiederholten Tiefschläge (etliche Beiträge wurden von den Mods bereits wegen beleidigendem Inhalt gelöscht) will ich mich (obschon mir das eigentlich sehr zuwider ist) für einmal auf dieses Niveau begeben - aber wirklich nur einmal:
Immunogen-Thread eröffnet am 27.1.2016
Kurs Open $9.15 High $9.50 Low $8.50 Close $8.64
aktueller Kurs $6.06
Diese Performance ist sogar noch lausiger als die von RDUS seit Threaderöffnung ($36.50 auf $29.60)
...aber man wird sicherlich 1000 Gründe finden, um diese Performance schön zu reden!
Und jetzt, bitte, wieder zurück zu den RDUS_Fakten.
Bin sehr gespannt, was heute bei der Anhörung herauskommt:

Antwort auf Beitrag Nr.: 56.437.137 von Cyberhexe am 13.12.17 10:40:29Abalaopratide .... sorry, für den Buchstabendreher; richtig heisst es natürlich Abaloparatide.
Antwort auf Beitrag Nr.: 56.437.137 von Cyberhexe am 13.12.17 10:40:29Schlechtes Beispiel, dieser Punkt geht leider auch an mich.
IMGN hat mir dieses Jahr gigantische Gewinne beschert, die absolut über die aus meinem EXEL Investment hinausgehen. Daneben gibt es im Depot noch eine kleine Position "for free" auf Basis unrealisierter Gewinne mit Spekulation auf den einzig verbleibend relevanten Produktkandidaten mirv. sor.
Bei IMGN habe ich nachvollziehbar in den Beiträgen nach Threaderöffnung vor ASCO 2016 die Reissleine bei einer Miniposition gezogen und dann in den Tiefs massiv eingekauft (30 fache Menge; übrigens habe ich genau da die realisierten EXEL Gewinne reingetan, sodass sich der Effekt maximal ausgewirkt hat) und das meiste weiter oben bereits wieder verkauft (3,xx,4,5,6). Einfach mal die Historie des Threads lesen.
Daher
Ville 2: Cyberhexe 0
Jetzt darfst du gerne zu EXEL kommen. Da siehts aber nicht besser aus.
Ville 3: Cyberhexe 0

IMGN hat mir dieses Jahr gigantische Gewinne beschert, die absolut über die aus meinem EXEL Investment hinausgehen. Daneben gibt es im Depot noch eine kleine Position "for free" auf Basis unrealisierter Gewinne mit Spekulation auf den einzig verbleibend relevanten Produktkandidaten mirv. sor.
Bei IMGN habe ich nachvollziehbar in den Beiträgen nach Threaderöffnung vor ASCO 2016 die Reissleine bei einer Miniposition gezogen und dann in den Tiefs massiv eingekauft (30 fache Menge; übrigens habe ich genau da die realisierten EXEL Gewinne reingetan, sodass sich der Effekt maximal ausgewirkt hat) und das meiste weiter oben bereits wieder verkauft (3,xx,4,5,6). Einfach mal die Historie des Threads lesen.
Daher
Ville 2: Cyberhexe 0
Jetzt darfst du gerne zu EXEL kommen. Da siehts aber nicht besser aus.
Ville 3: Cyberhexe 0

Antwort auf Beitrag Nr.: 56.437.851 von Ville7 am 13.12.17 12:35:48
@Ville7
Also, ich glaube, ich muss jetzt auch mal kurz zu Wort melden
Mittlerweile scheint deine Punkte bzw. Rundenzählerei ins BOXER-Milieau abzudriften......also jetzt mal BUTTER BEI DIE FISCHE.
Meinst du das wirklich alles ernst, was du da schreibst ????
Ich meine jetzt nicht deine "Wissenskompetenz" , "deinen guten Riecher", " deine Kursprognosen" und " dein gutes Tradingtiming" hinsichtlich diverser Biotechs , sondern das immer wieder mal auftretende merkwürdige Verhalten, sich über andere zu stellen.
Das Motto: ICH BIN SUPER - ICH BIN DER BESTE - mag ja zu tolerieren sein, Aber, dass du dir auch noch etwas darauf einbildest, indem du dich innerlich freust, wenn Aktienkurse fallen - und du dann dein "Fachwissen" und "gutes Timing" als Argument benutzt, um deine eigene Schadenfreude gegenüber anderen Usern zu befriedigen.
Sorry.....aber irgendwie echt schräg.
Zitat von Ville7: Schlechtes Beispiel, dieser Punkt geht leider auch an mich.
Daher
Ville 2: Cyberhexe 0
Jetzt darfst du gerne zu EXEL kommen. Da siehts aber nicht besser aus.
Ville 3: Cyberhexe 0
@Ville7
Also, ich glaube, ich muss jetzt auch mal kurz zu Wort melden
Mittlerweile scheint deine Punkte bzw. Rundenzählerei ins BOXER-Milieau abzudriften......also jetzt mal BUTTER BEI DIE FISCHE.
Meinst du das wirklich alles ernst, was du da schreibst ????
Ich meine jetzt nicht deine "Wissenskompetenz" , "deinen guten Riecher", " deine Kursprognosen" und " dein gutes Tradingtiming" hinsichtlich diverser Biotechs , sondern das immer wieder mal auftretende merkwürdige Verhalten, sich über andere zu stellen.
Das Motto: ICH BIN SUPER - ICH BIN DER BESTE - mag ja zu tolerieren sein, Aber, dass du dir auch noch etwas darauf einbildest, indem du dich innerlich freust, wenn Aktienkurse fallen - und du dann dein "Fachwissen" und "gutes Timing" als Argument benutzt, um deine eigene Schadenfreude gegenüber anderen Usern zu befriedigen.
Sorry.....aber irgendwie echt schräg.
Antwort auf Beitrag Nr.: 56.437.137 von Cyberhexe am 13.12.17 10:40:29
...diese Vorhersage war leicht:
Immunogen-Thread eröffnet am 27.1.2016
Kurs Open $9.15 High $9.50 Low $8.50 Close $8.64
aktueller Kurs $6.06
Diese Performance ist sogar noch lausiger als die von RDUS seit Threaderöffnung ($36.50 auf $29.60)
...aber man wird sicherlich 1000 Gründe finden, um diese Performance schön zu reden!
...andere Teilnehmer werden am Kurs gemessen, bei welchem der Thread eröffnet wurde, sich selbst misst man mit anderer Elle!
Wobei mir die Performance anderer Teilnehmer eigentlich egal ist - und ich glaube, dass dies für die allermeisten Teilnehmer hier gilt. Was zählt sind die fundamentalen Fakten und die Diskussion darüber. Und hierbei sind einige Teilnehmer besser, andere schwächer. Diejenigen, die sich mit ihrem Halbwissen brüsten und darüber hinaus dazu neigen, andere zu beleidigen, auf die könnte man wirklich verzichten.
Bin gespannt, was es heute noch zu berichten gibt in diesem Thread - aber über RADIUS Health und nicht über irgendwelche Profilneurosen.
Zitat von Cyberhexe: Ich will gar keinen Hehl daraus machen, dass mich die RDUS-Performance nicht zufrieden stellt und ich bereits seit langem auf eine Empfehlung auf Zulassung des europ. Arzneimittelausschusses CHMP warte...mit anschliessender (67 Tage) Zulassung durch die Kommission. Obwohl es bei den Ergebnissen zu Abalaopratide sicherlich einige Schwachpunkte gibt, haben diese bei der FDA keine derartige Verzögerung verursacht. Dies zeigt sehr deutlich, dass Pharmaprodukte und deren Zulassungsverfahren immer auch mit unbekannten Variabeln (für mich zumindest) verbunden sind.
Bezüglich der reisserischen Beiträge eines Teilnehmers, der meint, diese auch mich nicht zufriedenstellende Performance permanent kritisieren zu müssen - ohne substanziell zu reussieren-, dem sei bei seinen eighenen Threads der Spiegel vorgehalten. Eigentlich interessiert mich dies nicht, jedoch in Anbetracht der wiederholten Tiefschläge (etliche Beiträge wurden von den Mods bereits wegen beleidigendem Inhalt gelöscht) will ich mich (obschon mir das eigentlich sehr zuwider ist) für einmal auf dieses Niveau begeben - aber wirklich nur einmal:
Immunogen-Thread eröffnet am 27.1.2016
Kurs Open $9.15 High $9.50 Low $8.50 Close $8.64
aktueller Kurs $6.06
Diese Performance ist sogar noch lausiger als die von RDUS seit Threaderöffnung ($36.50 auf $29.60)
...aber man wird sicherlich 1000 Gründe finden, um diese Performance schön zu reden!
Und jetzt, bitte, wieder zurück zu den RDUS_Fakten.
Bin sehr gespannt, was heute bei der Anhörung herauskommt:
...diese Vorhersage war leicht:
Immunogen-Thread eröffnet am 27.1.2016
Kurs Open $9.15 High $9.50 Low $8.50 Close $8.64
aktueller Kurs $6.06
Diese Performance ist sogar noch lausiger als die von RDUS seit Threaderöffnung ($36.50 auf $29.60)
...aber man wird sicherlich 1000 Gründe finden, um diese Performance schön zu reden!
...andere Teilnehmer werden am Kurs gemessen, bei welchem der Thread eröffnet wurde, sich selbst misst man mit anderer Elle!
Wobei mir die Performance anderer Teilnehmer eigentlich egal ist - und ich glaube, dass dies für die allermeisten Teilnehmer hier gilt. Was zählt sind die fundamentalen Fakten und die Diskussion darüber. Und hierbei sind einige Teilnehmer besser, andere schwächer. Diejenigen, die sich mit ihrem Halbwissen brüsten und darüber hinaus dazu neigen, andere zu beleidigen, auf die könnte man wirklich verzichten.
Bin gespannt, was es heute noch zu berichten gibt in diesem Thread - aber über RADIUS Health und nicht über irgendwelche Profilneurosen.
Antwort auf Beitrag Nr.: 56.438.295 von bernie55 am 13.12.17 13:38:40bernie, kurze Antwort: das mache ich nur bei Leuten, die sich selbst derart über mich stellen. Ich hatte damit nicht angefangen...ich sage nur Stichwort "Ville = Kreisklasse", "Cyberhexe = champions league" vom threaderöffnenden User damals bei EXEL. Die seither gegenseitigen Sympathien sind erhalten geblieben. 

Antwort auf Beitrag Nr.: 56.438.295 von bernie55 am 13.12.17 13:38:40Ergänzend: Ich freue mich nicht, wenn Aktienkurse fallen - woher hast du das denn? Ich freue mich, dass meine Einschätzung richtig war. Nur diese (meine) Einschätzung wurde hier massiv vom User Cyberhexe diskreditiert und ins Lächerliche gezogen. Daher ist es doch gerechtfertigt, wenn man bilanzziehend 'in the longer run' darauf hinweist, dass man goldrichtig lag. Das zählt doch an der Börse, oder?
Antwort auf Beitrag Nr.: 56.438.555 von Cyberhexe am 13.12.17 14:13:15
Wo hat Ville Dich am Eröffnungskurs Deines Threads gemessen?
Derart unsinnige Vergleiche kenne ich eigentlich nur von Dir.
Zitat von Cyberhexe: ...andere Teilnehmer werden am Kurs gemessen, bei welchem der Thread eröffnet wurde, sich selbst misst man mit anderer Elle!
Wo hat Ville Dich am Eröffnungskurs Deines Threads gemessen?
Derart unsinnige Vergleiche kenne ich eigentlich nur von Dir.
Antwort auf Beitrag Nr.: 56.439.579 von Joschka Schröder am 13.12.17 16:03:19Nunja, hatte ich schon gemacht. Zumal die Threaderöffnung (wie zumeist bei User Cyberhexe) mit einer Kaufmeldung einherging. 
"...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben."

"...habe diese Woche das Risiko etwas gestreut und meine übergewichtige Exelixis-Position (mittlerweile 80%) auf ca. 50% reduziert und dafür Radius Health erworben."
Antwort auf Beitrag Nr.: 56.439.985 von Ville7 am 13.12.17 16:37:34
RDUS = gelb
EXEL = blau
Chart seit Threaderöffnung
RDUS = gelb
EXEL = blau
Chart seit Threaderöffnung
Antwort auf Beitrag Nr.: 56.439.985 von Ville7 am 13.12.17 16:37:34
Gut, dann nehme ich meine Kritik an Cyberhexe zurück, deren Reaktion unter diesen Umständen berechtigt ist.
Kurz mal etwas Grundsätzliches: Es wird doch bald Weihnachten. Wäre es unter diesen Umständen nicht möglich, Eure Animositäten einzustellen und im persönlichen Umgang auf den Reset-Knopf zu drücken? Diese ständigen Reibereien führen doch zu nichts, sie kosten nur Zeit.
Zitat von Ville7: Nunja, hatte ich schon gemacht. Zumal die Threaderöffnung (wie zumeist bei User Cyberhexe) mit einer Kaufmeldung einherging.[/i]
Gut, dann nehme ich meine Kritik an Cyberhexe zurück, deren Reaktion unter diesen Umständen berechtigt ist.
Kurz mal etwas Grundsätzliches: Es wird doch bald Weihnachten. Wäre es unter diesen Umständen nicht möglich, Eure Animositäten einzustellen und im persönlichen Umgang auf den Reset-Knopf zu drücken? Diese ständigen Reibereien führen doch zu nichts, sie kosten nur Zeit.
Antwort auf Beitrag Nr.: 56.440.757 von Joschka Schröder am 13.12.17 17:51:06Im Endeffekt hast du ja recht... also Schwamm drüber und Reset.
Gut so! Und falls künftig doch wieder alte (Vor-)Urteile aufflackern sollten, gäbe es immer noch die Möglichkeit, die Dinge per Boardmail zu klären oder sich einfach aus dem Weg zu gehen.
PS: Ich nehme mich da gar nicht aus, meine Reaktion auf Cyberhexes Beitrag 456 hätte ich auch verbindlicher formulieren können/müssen.
Wenn nun noch Cyberhexe zum Friedensschluss bereit wäre, könnten wir künftig auch im Radius-Thread interessante Diskussionen führen, das wär doch schon mal nicht schlecht.
PS: Ich nehme mich da gar nicht aus, meine Reaktion auf Cyberhexes Beitrag 456 hätte ich auch verbindlicher formulieren können/müssen.
Wenn nun noch Cyberhexe zum Friedensschluss bereit wäre, könnten wir künftig auch im Radius-Thread interessante Diskussionen führen, das wär doch schon mal nicht schlecht.
Antwort auf Beitrag Nr.: 56.439.579 von Joschka Schröder am 13.12.17 16:03:19
soso, derart unsinnige Vergleiche sind nur von mir:
schau dir bspw. den folgenden Beitrag von heute an:
Ville7 schrieb am 13.12.17 16:44:36 Beitrag Nr. 461 ( 56.440.071 )
oder aber:
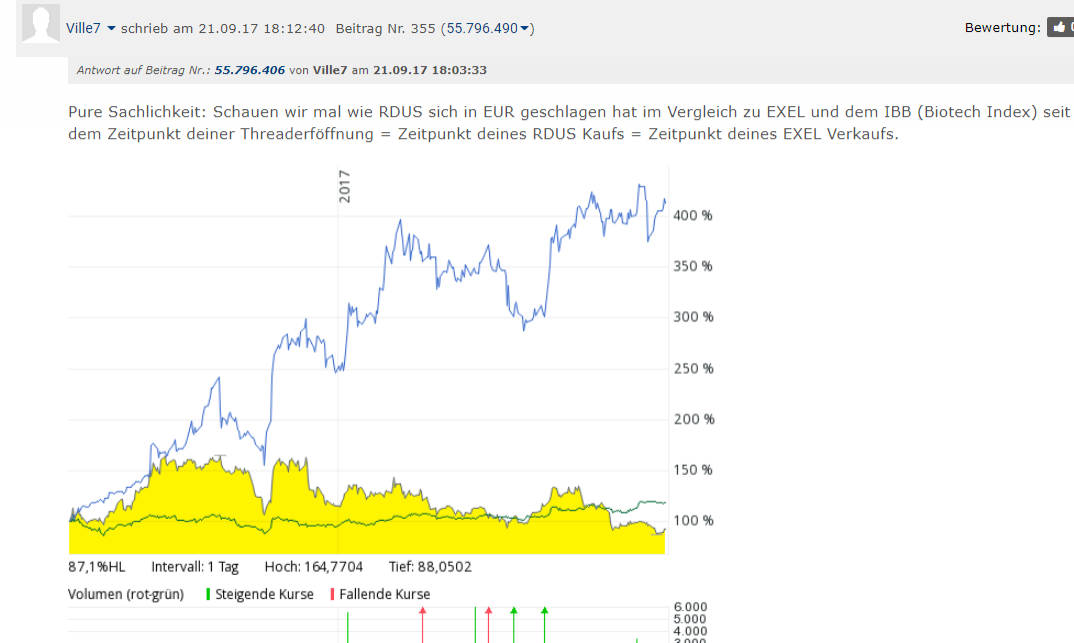
...und wenn man danach sucht findet man viele weitere Hinweise.
Nur damit wir uns richtig verstehen , ich halte es durchaus für legitim, wenn man mich am Kurs bei Threaderföffnung misst --> Radius Health, Inc. (RDUS)...eine neue Perle? am 31.5.2016
Legitim ist dies jedoch nur dann, wenn man an eigene Threads mit den gleichen Massstäben herangeht . Dies ist jedoch nicht der Fall und ich habe bis heute bewusst darauf verzichtet darauf hinzuweisen.
Zitat von Joschka Schröder:Zitat von Cyberhexe: ...andere Teilnehmer werden am Kurs gemessen, bei welchem der Thread eröffnet wurde, sich selbst misst man mit anderer Elle!
Wo hat Ville Dich am Eröffnungskurs Deines Threads gemessen?
Derart unsinnige Vergleiche kenne ich eigentlich nur von Dir.
soso, derart unsinnige Vergleiche sind nur von mir:
schau dir bspw. den folgenden Beitrag von heute an:
Ville7 schrieb am 13.12.17 16:44:36 Beitrag Nr. 461 ( 56.440.071 )
oder aber:

...und wenn man danach sucht findet man viele weitere Hinweise.
Nur damit wir uns richtig verstehen , ich halte es durchaus für legitim, wenn man mich am Kurs bei Threaderföffnung misst --> Radius Health, Inc. (RDUS)...eine neue Perle? am 31.5.2016
Legitim ist dies jedoch nur dann, wenn man an eigene Threads mit den gleichen Massstäben herangeht . Dies ist jedoch nicht der Fall und ich habe bis heute bewusst darauf verzichtet darauf hinzuweisen.
Antwort auf Beitrag Nr.: 56.443.207 von Cyberhexe am 13.12.17 23:31:17Cyberhexe, das Thema hatten wir doch eigentlich schon geklärt.
Ich hatte zudem vorgeschlagen, die Streitereien zu beenden und auf den zwischenmenschlichen Reset-Knopf zu drücken. Es führt zu nichts, wenn permanent jeder dem Gegenüber beweisen möchte, was für ein Idiot er doch ist.
Deshalb meine Frage, ob Du mit dem Angebot einverstanden ist. Ville hat bereits seine Bereitschaft erklärt, was für ihn nach den endlosen Auseinandersetzungen mit Sicherheit auch nicht einfach war. Wenn Du noch über Deinen Schatten könntest, ließe sich das leidige Thema endlich beenden.
Ich hatte zudem vorgeschlagen, die Streitereien zu beenden und auf den zwischenmenschlichen Reset-Knopf zu drücken. Es führt zu nichts, wenn permanent jeder dem Gegenüber beweisen möchte, was für ein Idiot er doch ist.
Deshalb meine Frage, ob Du mit dem Angebot einverstanden ist. Ville hat bereits seine Bereitschaft erklärt, was für ihn nach den endlosen Auseinandersetzungen mit Sicherheit auch nicht einfach war. Wenn Du noch über Deinen Schatten könntest, ließe sich das leidige Thema endlich beenden.
Antwort auf Beitrag Nr.: 56.438.295 von bernie55 am 13.12.17 13:38:40
Bernie, obschon in diesem Thread schon wieder nicht zum Thema diskutiert wird und verschiedene Teilnehmer offensichtlich gar kein Interesse daran haben, möchte ich mich grundsätzlich äussern:
Wenn man einen Thread eröffnet, ist es durchaus legitim, dass man von anderen Teilnehmern mit dem Kursverlauf seit Threaderöffnung konfrontiert wird. Diese Kritiker sollten jedoch bei der Bewertung der eigenen Threads ein ähnliches Vorgehen gutheissen. Es gibt jedoch Teilnehmer, bei denen dies nicht der Fall ist. Der hohe Aktienkurs bei Threaderöffnung wird dann "klein geschrieben", indem bei fallenden Kursen ständig nachgekauft wird. Mit dieser Strategie kann man natürlich fast jedes Investment zu einem erfolgreichen Abschluss bringen. Wer jedoch real investiert, weiss, dass ein ständiges Nachkaufen nicht immer möglich ist, zumal Kleinanleger tendenziell geringe Barreserven halten. In der virtuellen Welt ist der Nachkauf hingegen einfach. Wenn Teilnehmer jedoch kein Musterdepot führen und sich dennoch mit Megamargen brüsten, obschon der Kurs seit Threaderöffnung gefallen ist, dann muss/darf man folgendes feststellen:
1.) persönliche Margen, insbesondere diejenigen, die nicht in einem Musterdepot nachvollziehbar sind, interessieren andere Teilnehmer in der Regel nicht.
2.) ohne Musterdepot sind Margen nicht überprüfbar, also Schall und Rauch
3.) wenn man sich trotz Kursrückgang in der virtuellen Welt mit Megamargen brüstet, ist man nicht unbedingt glaubwürdig, und zudem --> Punkt 1.)
Ausserdem ist festzustellen, dass retrospektiv versucht wird, eigene Fehlleistungen klein zu reden.
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935)
"Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen".
Neben dem eigenartigen Performance-Gehabe ist jedoch auch inhaltlich sehr vieles unsauber bis falsch, weshalb in den amerikanischen Foren der "silly german investor" traurige Berühmtheit erlangt hat. In diesem thread glänzt dieser Teilnehmer zudem durch persönliche Beleidigungen (einige Beiträge wurden von den Mods deswegen bereits gelöscht) oder aber durch forenfremde Beiträge, die inhaltlich wenig bis gar nichts (es gibt eine Ausnahme, dafür habe ich mich entschuldigt!) zur Diskussion beitragen.
In diesem thread glänzt dieser Teilnehmer zudem durch persönliche Beleidigungen (einige Beiträge wurden von den Mods deswegen bereits gelöscht) oder aber durch forenfremde Beiträge, die inhaltlich wenig bis gar nichts (es gibt eine Ausnahme, dafür habe ich mich entschuldigt!) zur Diskussion beitragen.
Zitat von bernie55: Ich meine jetzt nicht deine "Wissenskompetenz" , "deinen guten Riecher", " deine Kursprognosen" und " dein gutes Tradingtiming" hinsichtlich diverser Biotechs , sondern das immer wieder mal auftretende merkwürdige Verhalten, sich über andere zu stellen.
Das Motto: ICH BIN SUPER - ICH BIN DER BESTE - mag ja zu tolerieren sein, Aber, dass du dir auch noch etwas darauf einbildest, indem du dich innerlich freust, wenn Aktienkurse fallen - und du dann dein "Fachwissen" und "gutes Timing" als Argument benutzt, um deine eigene Schadenfreude gegenüber anderen Usern zu befriedigen.
Sorry.....aber irgendwie echt schräg.
Bernie, obschon in diesem Thread schon wieder nicht zum Thema diskutiert wird und verschiedene Teilnehmer offensichtlich gar kein Interesse daran haben, möchte ich mich grundsätzlich äussern:
Wenn man einen Thread eröffnet, ist es durchaus legitim, dass man von anderen Teilnehmern mit dem Kursverlauf seit Threaderöffnung konfrontiert wird. Diese Kritiker sollten jedoch bei der Bewertung der eigenen Threads ein ähnliches Vorgehen gutheissen. Es gibt jedoch Teilnehmer, bei denen dies nicht der Fall ist. Der hohe Aktienkurs bei Threaderöffnung wird dann "klein geschrieben", indem bei fallenden Kursen ständig nachgekauft wird. Mit dieser Strategie kann man natürlich fast jedes Investment zu einem erfolgreichen Abschluss bringen. Wer jedoch real investiert, weiss, dass ein ständiges Nachkaufen nicht immer möglich ist, zumal Kleinanleger tendenziell geringe Barreserven halten. In der virtuellen Welt ist der Nachkauf hingegen einfach. Wenn Teilnehmer jedoch kein Musterdepot führen und sich dennoch mit Megamargen brüsten, obschon der Kurs seit Threaderöffnung gefallen ist, dann muss/darf man folgendes feststellen:
1.) persönliche Margen, insbesondere diejenigen, die nicht in einem Musterdepot nachvollziehbar sind, interessieren andere Teilnehmer in der Regel nicht.
2.) ohne Musterdepot sind Margen nicht überprüfbar, also Schall und Rauch
3.) wenn man sich trotz Kursrückgang in der virtuellen Welt mit Megamargen brüstet, ist man nicht unbedingt glaubwürdig, und zudem --> Punkt 1.)
Ausserdem ist festzustellen, dass retrospektiv versucht wird, eigene Fehlleistungen klein zu reden.
Zitiert aus dem Thread "Exelixis...ein schlafender Riese? USD 3.40 am 14.5.2014
Am 11.11.15 schrieb der Teilnehmer ville7 um 09:45:33 im Beitrag Nr. 399 (51.059.685) als Antwort auf Beitrag Nr. 398 (Nr. 51.058.935)
"Im Übrigen stehe ich der Firma weiterhin sehr kritisch gegenüber, da sie schon oft gezeigt hat, dass sie mit ihren Finanzierungsrunden und -arten und eigenen Optionszuteilungen über die Leichen der Aktionäre geht ohne eine Wimper zu zucken. Never fall in love mit einem Produkt (Cobi) oder einer Firma (EXEL). Schaut so aus als hättest du noch das ein oder andere zu lernen".
Neben dem eigenartigen Performance-Gehabe ist jedoch auch inhaltlich sehr vieles unsauber bis falsch, weshalb in den amerikanischen Foren der "silly german investor" traurige Berühmtheit erlangt hat.
 In diesem thread glänzt dieser Teilnehmer zudem durch persönliche Beleidigungen (einige Beiträge wurden von den Mods deswegen bereits gelöscht) oder aber durch forenfremde Beiträge, die inhaltlich wenig bis gar nichts (es gibt eine Ausnahme, dafür habe ich mich entschuldigt!) zur Diskussion beitragen.
In diesem thread glänzt dieser Teilnehmer zudem durch persönliche Beleidigungen (einige Beiträge wurden von den Mods deswegen bereits gelöscht) oder aber durch forenfremde Beiträge, die inhaltlich wenig bis gar nichts (es gibt eine Ausnahme, dafür habe ich mich entschuldigt!) zur Diskussion beitragen.
Antwort auf Beitrag Nr.: 56.438.645 von Ville7 am 13.12.17 14:26:41
...aber, aber....nicht schon wieder eine LÜGE. Diese Lügengeschichten sind erbärmlich, aber sie gehören nun mal zu DIR. Wann und wo habe ich von CL geschrieben? Aber das ist deine Strategie, einfach etwas daherschwätzen ohne die entsprechenden Beweise zu erbringen.
Wenn ich mich recht erinnere, habe ich irgendwann einmal den Hinweise gegeben, dass ein anderer Teilnehmer und du nicht in der gleichen Liga spielen. Aber den CL-Vergleich stammt nicht von mir. Ich müsste mich schwer täuschen, aber ich glaube mittlerweile einfach nur, dass du jemand bist, der es mit der Wahrheit nicht sehr genau nimmt.
Zitat von Ville7: bernie, kurze Antwort: das mache ich nur bei Leuten, die sich selbst derart über mich stellen. Ich hatte damit nicht angefangen...ich sage nur Stichwort "Ville = Kreisklasse", "Cyberhexe = champions league" vom threaderöffnenden User damals bei EXEL. Die seither gegenseitigen Sympathien sind erhalten geblieben.
...aber, aber....nicht schon wieder eine LÜGE. Diese Lügengeschichten sind erbärmlich, aber sie gehören nun mal zu DIR. Wann und wo habe ich von CL geschrieben? Aber das ist deine Strategie, einfach etwas daherschwätzen ohne die entsprechenden Beweise zu erbringen.
Wenn ich mich recht erinnere, habe ich irgendwann einmal den Hinweise gegeben, dass ein anderer Teilnehmer und du nicht in der gleichen Liga spielen. Aber den CL-Vergleich stammt nicht von mir. Ich müsste mich schwer täuschen, aber ich glaube mittlerweile einfach nur, dass du jemand bist, der es mit der Wahrheit nicht sehr genau nimmt.
Radius hat von der US-Börsenaufsicht gestern eine Ausnahmegenehmigung erhalten, die das Unternehmen von der Publikationspflicht befreit. Man kann nun darüber spekulieren, welche Info da vorerst noch geheim gehalten wird. Ich hoffe, dass es sich hierbei um einen Kooperationsvertrag mit einem Partner handelt, der im Falle der Marktzulassung von Abaloparatide in Europa den Vertrieb organisiert. Time will tell!
https://www.sec.gov/Archives/edgar/data/1428522/999999999717…
Radius Health, Inc. submitted an application under Rule 24b-2 requesting
https://www.sec.gov/Archives/edgar/data/1428522/999999999717…
Radius Health, Inc. submitted an application under Rule 24b-2 requesting
Cyberhexes Optimismus bzgl. Radius teile ich bekanntlich nicht. Aus meiner Sicht wäre das Unternehmen auch im Fall einer europ. Zulassung des Abaloparatide-SC auf Basis der aktuellen Börsenkurses deutlich zu hoch bewertet. Noch ist aber offen, ob das Präparat überhaupt in Europa zugelassen werden wird.
Radius Health Announces that the Committee for Medicinal Products for Human Use (CHMP) Will Issue a Third Day-180 List of Outstanding Issues in its Regulatory Review of Abaloparatide-SC, a Bone Building Agent for the Treatment of Osteoporosis in Postmenopausal Women at Increased Risk of Fracture
Radius Health now anticipates an opinion from the CHMP regarding the MAA for abaloparatide-SC in the first half of 2018
WALTHAM, Mass., Dec. 15, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS) announced today that the Committee for Medicinal Products for Human Use (CHMP), the scientific committee of the European Medicines Agency (EMA), will issue a third Day-180 List of Outstanding Issues. As part of its on-going risk-benefit assessment, the CHMP has informed the Company that it intends to refer the marketing authorisation application (MAA) to a scientific advisory group for additional advice. Radius now expects the CHMP to issue an opinion regarding the MAA during the first half of 2018.
"We will continue to work closely with the agency to address their questions," said Jesper Høiland, President and Chief Executive Officer of Radius Health. "Osteoporosis is a debilitating disease affecting an estimated 22 million women in Europe, and 200 million women worldwide. No new anabolic bone-building agent has been approved in Europe for the treatment of osteoporosis in 14 years."
TYMLOS™ (abaloparatide) injection was approved in April 2017 by the U.S. Food and Drug Administration for the treatment of postmenopausal women with osteoporosis at high risk for fracture defined as history of osteoporotic fracture, multiple risk factors for fracture, or patients who have failed or are intolerant to other available osteoporosis therapy.
Radius Health Announces that the Committee for Medicinal Products for Human Use (CHMP) Will Issue a Third Day-180 List of Outstanding Issues in its Regulatory Review of Abaloparatide-SC, a Bone Building Agent for the Treatment of Osteoporosis in Postmenopausal Women at Increased Risk of Fracture
Radius Health now anticipates an opinion from the CHMP regarding the MAA for abaloparatide-SC in the first half of 2018
WALTHAM, Mass., Dec. 15, 2017 (GLOBE NEWSWIRE) -- Radius Health, Inc. (Nasdaq:RDUS) announced today that the Committee for Medicinal Products for Human Use (CHMP), the scientific committee of the European Medicines Agency (EMA), will issue a third Day-180 List of Outstanding Issues. As part of its on-going risk-benefit assessment, the CHMP has informed the Company that it intends to refer the marketing authorisation application (MAA) to a scientific advisory group for additional advice. Radius now expects the CHMP to issue an opinion regarding the MAA during the first half of 2018.
"We will continue to work closely with the agency to address their questions," said Jesper Høiland, President and Chief Executive Officer of Radius Health. "Osteoporosis is a debilitating disease affecting an estimated 22 million women in Europe, and 200 million women worldwide. No new anabolic bone-building agent has been approved in Europe for the treatment of osteoporosis in 14 years."
TYMLOS™ (abaloparatide) injection was approved in April 2017 by the U.S. Food and Drug Administration for the treatment of postmenopausal women with osteoporosis at high risk for fracture defined as history of osteoporotic fracture, multiple risk factors for fracture, or patients who have failed or are intolerant to other available osteoporosis therapy.
Antwort auf Beitrag Nr.: 56.459.600 von Joschka Schröder am 15.12.17 13:42:53Einen Teil der Meldung, der die - für die Zulassung wohl nicht unbedeutenden - Sicherheitshinweise enthält, hatte ich versehentlich abgeschnitten.
IMPORTANT SAFETY INFORMATION
WARNING: RISK OF OSTEOSARCOMA
Abaloparatide caused a dose-dependent increase in the incidence of osteosarcoma (a malignant bone tumor) in male and female rats. The effect was observed at systemic exposures to abaloparatide ranging from 4 to 28 times the exposure in humans receiving the 80 mcg dose. It is unknown if TYMLOS will cause osteosarcoma in humans.
The use of TYMLOS is not recommended in patients at increased risk of osteosarcoma including those with Paget's disease of bone or unexplained elevations of alkaline phosphatase, open epiphyses, bone metastases or skeletal malignancies, hereditary disorders predisposing to osteosarcoma, or prior external beam or implant radiation therapy involving the skeleton.
Cumulative use of TYMLOS and parathyroid hormone analogs (e.g., teriparatide) for more than 2 years during a patient's lifetime is not recommended.
Orthostatic Hypotension: Orthostatic hypotension may occur with TYMLOS, typically within 4 hours of injection. Associated symptoms may include dizziness, palpitations, tachycardia or nausea, and may resolve by having the patient lie down. For the first several doses, TYMLOS should be administered where the patient can sit or lie down if necessary.
Hypercalcemia: TYMLOS may cause hypercalcemia. TYMLOS is not recommended in patients with pre-existing hypercalcemia or in patients who have an underlying hypercalcemic disorder, such as primary hyperparathyroidism, because of the possibility of exacerbating hypercalcemia.
Hypercalciuria and Urolithiasis: TYMLOS may cause hypercalciuria. It is unknown whether TYMLOS may exacerbate urolithiasis in patients with active or a history of urolithiasis. If active urolithiasis or pre-existing hypercalciuria is suspected, measurement of urinary calcium excretion should be considered.
Adverse Reactions: The most common adverse reactions (incidence ≥2%) are hypercalciuria, dizziness, nausea, headache, palpitations, fatigue, upper abdominal pain and vertigo.
IMPORTANT SAFETY INFORMATION
WARNING: RISK OF OSTEOSARCOMA
Abaloparatide caused a dose-dependent increase in the incidence of osteosarcoma (a malignant bone tumor) in male and female rats. The effect was observed at systemic exposures to abaloparatide ranging from 4 to 28 times the exposure in humans receiving the 80 mcg dose. It is unknown if TYMLOS will cause osteosarcoma in humans.
The use of TYMLOS is not recommended in patients at increased risk of osteosarcoma including those with Paget's disease of bone or unexplained elevations of alkaline phosphatase, open epiphyses, bone metastases or skeletal malignancies, hereditary disorders predisposing to osteosarcoma, or prior external beam or implant radiation therapy involving the skeleton.
Cumulative use of TYMLOS and parathyroid hormone analogs (e.g., teriparatide) for more than 2 years during a patient's lifetime is not recommended.
Orthostatic Hypotension: Orthostatic hypotension may occur with TYMLOS, typically within 4 hours of injection. Associated symptoms may include dizziness, palpitations, tachycardia or nausea, and may resolve by having the patient lie down. For the first several doses, TYMLOS should be administered where the patient can sit or lie down if necessary.
Hypercalcemia: TYMLOS may cause hypercalcemia. TYMLOS is not recommended in patients with pre-existing hypercalcemia or in patients who have an underlying hypercalcemic disorder, such as primary hyperparathyroidism, because of the possibility of exacerbating hypercalcemia.
Hypercalciuria and Urolithiasis: TYMLOS may cause hypercalciuria. It is unknown whether TYMLOS may exacerbate urolithiasis in patients with active or a history of urolithiasis. If active urolithiasis or pre-existing hypercalciuria is suspected, measurement of urinary calcium excretion should be considered.
Adverse Reactions: The most common adverse reactions (incidence ≥2%) are hypercalciuria, dizziness, nausea, headache, palpitations, fatigue, upper abdominal pain and vertigo.
Antwort auf Beitrag Nr.: 56.433.621 von Ville7 am 12.12.17 18:27:55
Die Einschätzung war wohl wieder mal richtig....scheinbar kann RDUS die offenen Fragen nicht beantworten und die EMA stellt sich dann einfach quer.
Zitat von Ville7: .... Die EMA zieht das wohl hin - in der üblichen Art - so lange bis RDUS die application zurückzieht. Das sieht nicht so gut für RDUS aus.
Die Einschätzung war wohl wieder mal richtig....scheinbar kann RDUS die offenen Fragen nicht beantworten und die EMA stellt sich dann einfach quer.
Antwort auf Beitrag Nr.: 56.459.672 von Joschka Schröder am 15.12.17 13:50:13
Leider erhält man bisher keine genaueren Informationen zu den zusätzlichen Fragen der EMA.
Ich halte es jedoch für unwahrscheinlich, dass dies mit dem Osteosarcoma-Risiko in Verbindung steht.
Begründung:
1.) Das Label der FDA zu Abaloparatide ist hinsichtlich Osteosarcoma nahezu identisch mit demjenigen von Teriparatide, und dieser Wirkstoff ist in Europa zugelassen (brand in Europa: Forsteo)
FDA Abaloparatide
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
13.1 Carcinogenisis, Mutagenisis, Impairment of Fertility,
dass in einer 2-jährigen Karzinogenitätsstudie an Ratten bei 4, 16 und 28-facher Dosis (80 mcg) ähnlich wie bei teriparatide dosisabhängig eine stark erhöhtes Auftreten von bösartigen Osteosarcomas (Knochentumor) beobachtet wurde (87%, 62%und gegenüber 0-2% unbehandelt).
Es wird jedoch ausdrücklich darauf hingewiesen, dass die Relevanz dieser Rattenbefunde für den Mensch ungewiss ist, weshalb.... TYMLOS is not recommended in patients at increased risk of osteosarcoma (FDA).
Es wird ebenfalls im gleichen Abschnitt darauf hingewiesen, dass Abaloparatide in den Standardtests zur Mutagenität (Ames, Chromosoemenaberration und Micronucleus) negativ ist.
Die "Black Box"-Warnung der FDA bei Teriparatide (brand US: Forteo) ist fast identisch --> dosisabhängige Inzidenzerhöhung von Osteosarcoma bei einer 3 bis 60-fachen Dosis.
https://www.accessdata.fda.gov/drugsatfda_docs/label/2004/21…
In male and female rats, teriparatide caused an increase in the incidence of osteosarcoma (a
malignant bone tumor) that was dependent on dose and treatment duration. The effect was
observed at systemic exposures to teriparatide ranging from 3 to 60 times the exposure in
humans given a 20-mcg dose. Because of the uncertain relevance of the rat osteosarcoma
finding to humans, teriparatide should be prescribed only to patients for whom the
potential benefits are considered to outweigh the potential risk. Teriparatide should not be
prescribed for patients who are at increased baseline risk for osteosarcoma (including those
with Paget’s disease of bone or unexplained elevations of alkaline phosphatase, open
epiphyses, or prior external beam or implant radiation therapy involving the skeleton) (see
WARNINGS and PRECAUTIONS, Carcinogenesis).
2.) Kanzerogenitätsstudie von Abaloparatide an Ratten:
http://www.sciencedirect.com/science/article/pii/S0273230017…
Highlights
•The PTH type 1 receptor agonist abaloparatide has potent bone anabolic activity.
•Near life-long treatment in rats with abaloparatide resulted in the formation of osteosarcomas.
•Osteosarcoma formation was dose and time dependent.
•Osteosarcoma in rats were also seen in a PTH(1–34) treated positive control group.
•There were no increases in the incidence of non-bone tumors with abaloparatide.
5. Conclusion
The current study demonstrated an increased incidence of osteosarcoma in rats treated chronically with abaloparatide, consistent with previous studies with rhPTH(1–34). These changes were consistent across comparable doses of abaloparatide and hPTH(1–34), with histopathology reflecting similarities in both neoplastic and non-neoplastic observations. Although the clinical translation of the increased rate of osteosarcoma with PTH1R agonists in rats remains unclear, these results suggest that are no additional neoplastic risks associated with near-lifetime exposure to abaloparatide.
Zitat von Joschka Schröder: Einen Teil der Meldung, der die - für die Zulassung wohl nicht unbedeutenden - Sicherheitshinweise enthält, hatte ich versehentlich abgeschnitten.
IMPORTANT SAFETY INFORMATION
WARNING: RISK OF OSTEOSARCOMA
Abaloparatide caused a dose-dependent increase in the incidence of osteosarcoma (a malignant bone tumor) in male and female rats. The effect was observed at systemic exposures to abaloparatide ranging from 4 to 28 times the exposure in humans receiving the 80 mcg dose. It is unknown if TYMLOS will cause osteosarcoma in humans.
The use of TYMLOS is not recommended in patients at increased risk of osteosarcoma including those with Paget's disease of bone or unexplained elevations of alkaline phosphatase, open epiphyses, bone metastases or skeletal malignancies, hereditary disorders predisposing to osteosarcoma, or prior external beam or implant radiation therapy involving the skeleton.
Cumulative use of TYMLOS and parathyroid hormone analogs (e.g., teriparatide) for more than 2 years during a patient's lifetime is not recommended.
Orthostatic Hypotension: Orthostatic hypotension may occur with TYMLOS, typically within 4 hours of injection. Associated symptoms may include dizziness, palpitations, tachycardia or nausea, and may resolve by having the patient lie down. For the first several doses, TYMLOS should be administered where the patient can sit or lie down if necessary.
Hypercalcemia: TYMLOS may cause hypercalcemia. TYMLOS is not recommended in patients with pre-existing hypercalcemia or in patients who have an underlying hypercalcemic disorder, such as primary hyperparathyroidism, because of the possibility of exacerbating hypercalcemia.
Hypercalciuria and Urolithiasis: TYMLOS may cause hypercalciuria. It is unknown whether TYMLOS may exacerbate urolithiasis in patients with active or a history of urolithiasis. If active urolithiasis or pre-existing hypercalciuria is suspected, measurement of urinary calcium excretion should be considered.
Adverse Reactions: The most common adverse reactions (incidence ≥2%) are hypercalciuria, dizziness, nausea, headache, palpitations, fatigue, upper abdominal pain and vertigo.
Leider erhält man bisher keine genaueren Informationen zu den zusätzlichen Fragen der EMA.
Ich halte es jedoch für unwahrscheinlich, dass dies mit dem Osteosarcoma-Risiko in Verbindung steht.
Begründung:
1.) Das Label der FDA zu Abaloparatide ist hinsichtlich Osteosarcoma nahezu identisch mit demjenigen von Teriparatide, und dieser Wirkstoff ist in Europa zugelassen (brand in Europa: Forsteo)
FDA Abaloparatide
https://www.accessdata.fda.gov/drugsatfda_docs/label/2017/20…
13.1 Carcinogenisis, Mutagenisis, Impairment of Fertility,
dass in einer 2-jährigen Karzinogenitätsstudie an Ratten bei 4, 16 und 28-facher Dosis (80 mcg) ähnlich wie bei teriparatide dosisabhängig eine stark erhöhtes Auftreten von bösartigen Osteosarcomas (Knochentumor) beobachtet wurde (87%, 62%und gegenüber 0-2% unbehandelt).
Es wird jedoch ausdrücklich darauf hingewiesen, dass die Relevanz dieser Rattenbefunde für den Mensch ungewiss ist, weshalb.... TYMLOS is not recommended in patients at increased risk of osteosarcoma (FDA).
Es wird ebenfalls im gleichen Abschnitt darauf hingewiesen, dass Abaloparatide in den Standardtests zur Mutagenität (Ames, Chromosoemenaberration und Micronucleus) negativ ist.
Die "Black Box"-Warnung der FDA bei Teriparatide (brand US: Forteo) ist fast identisch --> dosisabhängige Inzidenzerhöhung von Osteosarcoma bei einer 3 bis 60-fachen Dosis.
https://www.accessdata.fda.gov/drugsatfda_docs/label/2004/21…
In male and female rats, teriparatide caused an increase in the incidence of osteosarcoma (a
malignant bone tumor) that was dependent on dose and treatment duration. The effect was
observed at systemic exposures to teriparatide ranging from 3 to 60 times the exposure in
humans given a 20-mcg dose. Because of the uncertain relevance of the rat osteosarcoma
finding to humans, teriparatide should be prescribed only to patients for whom the
potential benefits are considered to outweigh the potential risk. Teriparatide should not be
prescribed for patients who are at increased baseline risk for osteosarcoma (including those
with Paget’s disease of bone or unexplained elevations of alkaline phosphatase, open
epiphyses, or prior external beam or implant radiation therapy involving the skeleton) (see
WARNINGS and PRECAUTIONS, Carcinogenesis).
2.) Kanzerogenitätsstudie von Abaloparatide an Ratten:
http://www.sciencedirect.com/science/article/pii/S0273230017…
Highlights
•The PTH type 1 receptor agonist abaloparatide has potent bone anabolic activity.
•Near life-long treatment in rats with abaloparatide resulted in the formation of osteosarcomas.
•Osteosarcoma formation was dose and time dependent.
•Osteosarcoma in rats were also seen in a PTH(1–34) treated positive control group.
•There were no increases in the incidence of non-bone tumors with abaloparatide.
5. Conclusion
The current study demonstrated an increased incidence of osteosarcoma in rats treated chronically with abaloparatide, consistent with previous studies with rhPTH(1–34). These changes were consistent across comparable doses of abaloparatide and hPTH(1–34), with histopathology reflecting similarities in both neoplastic and non-neoplastic observations. Although the clinical translation of the increased rate of osteosarcoma with PTH1R agonists in rats remains unclear, these results suggest that are no additional neoplastic risks associated with near-lifetime exposure to abaloparatide.
Antwort auf Beitrag Nr.: 56.460.191 von Ville7 am 15.12.17 14:34:19
soso, RDUS wird den Antrag zurückziehen - das würde mich tatsächlich wundern!
...dann merken wir uns doch mal diese Nachricht, damit man die Treffergenauigkeit überprüfen kann!
Zitat von Ville7:Zitat von Ville7: .... Die EMA zieht das wohl hin - in der üblichen Art - so lange bis RDUS die application zurückzieht. Das sieht nicht so gut für RDUS aus.
Die Einschätzung war wohl wieder mal richtig....scheinbar kann RDUS die offenen Fragen nicht beantworten und die EMA stellt sich dann einfach quer.
soso, RDUS wird den Antrag zurückziehen - das würde mich tatsächlich wundern!
...dann merken wir uns doch mal diese Nachricht, damit man die Treffergenauigkeit überprüfen kann!
Antwort auf Beitrag Nr.: 56.438.645 von Ville7 am 13.12.17 14:26:41
Obschon ich nicht sehr viel Zeit in diese Hetze investieren will, habe ich etwas zu dieser CL-LÜGE im Exelixis-Thread recherchiert. Und bezeichnenderweise hat sich der einzig gefundene Beitrag mit verschiedenen Suchwörtern (Liga, Champions-League, Champions, Kreisklasse) von mir bereits damals mit deinen unwahren Behauptungen beschäftigt.
Einzige Fundstelle ist:
"Der Wahrheitsgehalt einer Lüge wird durch ständiges Wiederholen nicht grösser!
Zu deinen Unterstellungen nur so viel:...
....SLGraman und ipolt spielen nicht in deiner Liga - das solltest du so akzeptieren."
Darauf gab es dann folgende interessante Antwort:
Man darf feststellen, dass der Teilnehmer Ville7 selbst die mir vorgeworfenen Begrifflichkeiten gewählt hat. Zukünftig würde ich gerne jeden Austausch mit Teilnehmern vermeiden, die es mit der Wahrheit nicht sehr genau nehmen. Und dieser Kategorie ist der Teilnehmer Ville7 eindeutig angehörig.
Zitat von Ville7: bernie, kurze Antwort: das mache ich nur bei Leuten, die sich selbst derart über mich stellen. Ich hatte damit nicht angefangen...ich sage nur Stichwort "Ville = Kreisklasse", "Cyberhexe = champions league" vom threaderöffnenden User damals bei EXEL. Die seither gegenseitigen Sympathien sind erhalten geblieben.
Obschon ich nicht sehr viel Zeit in diese Hetze investieren will, habe ich etwas zu dieser CL-LÜGE im Exelixis-Thread recherchiert. Und bezeichnenderweise hat sich der einzig gefundene Beitrag mit verschiedenen Suchwörtern (Liga, Champions-League, Champions, Kreisklasse) von mir bereits damals mit deinen unwahren Behauptungen beschäftigt.
Einzige Fundstelle ist:
"Der Wahrheitsgehalt einer Lüge wird durch ständiges Wiederholen nicht grösser!
Zu deinen Unterstellungen nur so viel:...
....SLGraman und ipolt spielen nicht in deiner Liga - das solltest du so akzeptieren."
Darauf gab es dann folgende interessante Antwort:

Man darf feststellen, dass der Teilnehmer Ville7 selbst die mir vorgeworfenen Begrifflichkeiten gewählt hat. Zukünftig würde ich gerne jeden Austausch mit Teilnehmern vermeiden, die es mit der Wahrheit nicht sehr genau nehmen. Und dieser Kategorie ist der Teilnehmer Ville7 eindeutig angehörig.
Antwort auf Beitrag Nr.: 56.463.083 von Cyberhexe am 15.12.17 19:02:33
Das ist richtig. Ich hatte die gesamte Liste der in der Meldung genannten Nebenwirkungen gepostet, weil zunächst davon auszugehen ist, dass die EMA sich einem der dort aufgeführten Punkte reibt. Hatte dabei auch in Richtung Hyperkalzämische Krise mit kardialen Komplikationen gedacht ... es muss ja schon etwas Schwerwiegenderes sein. Andererseits sind bei Konkurrenzpräparaten wie Denosumab Todesfälle in Folge von schweren symptomatischen Hypokalzämien beschrieben worden, ohne dass die Zulassung des anti-RANKL-Antikörpers in Frage gestellt worden wäre. Insoweit tappe ich völlig im Dunkeln.
Zitat von Cyberhexe: Leider erhält man bisher keine genaueren Informationen zu den zusätzlichen Fragen der EMA.
Ich halte es jedoch für unwahrscheinlich, dass dies mit dem Osteosarcoma-Risiko in Verbindung steht.
Das ist richtig. Ich hatte die gesamte Liste der in der Meldung genannten Nebenwirkungen gepostet, weil zunächst davon auszugehen ist, dass die EMA sich einem der dort aufgeführten Punkte reibt. Hatte dabei auch in Richtung Hyperkalzämische Krise mit kardialen Komplikationen gedacht ... es muss ja schon etwas Schwerwiegenderes sein. Andererseits sind bei Konkurrenzpräparaten wie Denosumab Todesfälle in Folge von schweren symptomatischen Hypokalzämien beschrieben worden, ohne dass die Zulassung des anti-RANKL-Antikörpers in Frage gestellt worden wäre. Insoweit tappe ich völlig im Dunkeln.
Antwort auf Beitrag Nr.: 56.465.066 von Joschka Schröder am 15.12.17 23:27:43...ich tendiere dazu, die "issues" nicht bei den Nebenwirkungen zu suchen - das NW-Profil von teriparatide ist ähnlich- sondern eher bei den Begleitumständen bei ACTIVE (ph3-Studie) wie zB hohe Anzahl an Studienabbrecher unter Abaloparatide oder aber Ungereimtheiten bei einigen (wenigen) Studienstandorten.
Antwort auf Beitrag Nr.: 56.465.147 von Cyberhexe am 15.12.17 23:54:41Ich habe die Telefonkonferenzen nicht mitverfolgt. Gibt es Informationen darüber, wieso die Studienabbrecherquote so hoch war?
Antwort auf Beitrag Nr.: 56.465.192 von Joschka Schröder am 16.12.17 00:06:39Es gab wohl einige Zentren, bei denen es Unregelmäßigkeiten gab (betrifft meiner Erinnerung nach 15% der Patienten) und daher hinterfragt die EMA hier zurecht und sitzt das einfach aus bis sie zufriedenstellende Antworten bekommt (die es vielleicht gar nicht gibt). Ob dies im speziellen die Anzahl Studienabbrecher betrifft ist mir unbekannt.
Fakt ist: die Bewertung ist bei dem aktuell rasanten Cashburn (>50Mio USD / Quartal) mehr als abenteuerlich.
Fakt ist: die Bewertung ist bei dem aktuell rasanten Cashburn (>50Mio USD / Quartal) mehr als abenteuerlich.
Antwort auf Beitrag Nr.: 56.466.032 von Ville7 am 16.12.17 09:24:05
man sollte nicht so tun als ob man genau wüsste, welche Probleme dazu geführt haben, dass der Arzneimittelausschuss eine 3. Liste von ausstehenden Fragen/Probleme verschickt hat. Wie ich bereits angemerkt habe, gibt es hierzu (noch) keine Informationen, weshalb ich spekuliert habe...
"ich tendiere dazu, die "issues" nicht bei den Nebenwirkungen zu suchen - das NW-Profil von teriparatide ist ähnlich- sondern eher bei den Begleitumständen bei ACTIVE (ph3-Studie) wie zB hohe Anzahl an Studienabbrecher unter Abaloparatide oder aber Ungereimtheiten bei einigen (wenigen) Studienstandorten.
Jedoch den Anschein zu erwecken, man wüsste den Inhalt der "Day-180 List of Outstanding Issues", ist wieder einmal unseriös.
Zitat von Ville7: Es gab wohl einige Zentren, bei denen es Unregelmäßigkeiten gab (betrifft meiner Erinnerung nach 15% der Patienten) und daher hinterfragt die EMA hier zurecht und sitzt das einfach aus bis sie zufriedenstellende Antworten bekommt (die es vielleicht gar nicht gibt). Ob dies im speziellen die Anzahl Studienabbrecher betrifft ist mir unbekannt.
Fakt ist: die Bewertung ist bei dem aktuell rasanten Cashburn (>50Mio USD / Quartal) mehr als abenteuerlich.
man sollte nicht so tun als ob man genau wüsste, welche Probleme dazu geführt haben, dass der Arzneimittelausschuss eine 3. Liste von ausstehenden Fragen/Probleme verschickt hat. Wie ich bereits angemerkt habe, gibt es hierzu (noch) keine Informationen, weshalb ich spekuliert habe...
"ich tendiere dazu, die "issues" nicht bei den Nebenwirkungen zu suchen - das NW-Profil von teriparatide ist ähnlich- sondern eher bei den Begleitumständen bei ACTIVE (ph3-Studie) wie zB hohe Anzahl an Studienabbrecher unter Abaloparatide oder aber Ungereimtheiten bei einigen (wenigen) Studienstandorten.
Jedoch den Anschein zu erwecken, man wüsste den Inhalt der "Day-180 List of Outstanding Issues", ist wieder einmal unseriös.
Antwort auf Beitrag Nr.: 56.466.359 von Cyberhexe am 16.12.17 10:30:10RDUS hatte sich zu dem Problem der EMA mit dem Abalo Paket bereits geäußert.
(Falls du das wieder mal nicht mitbekommen hattest oder es verdrängt hast, ist übrigens dein Problem)
Daher ist davon auszugehen, dass keine neuen "issues" aufgekommen sind, sondern dieser "issue" nicht aus der Welt geschaffen werden konnte. Das ist pure und simple Logik dessen, was public knowledge ist...
(Falls du das wieder mal nicht mitbekommen hattest oder es verdrängt hast, ist übrigens dein Problem)
Daher ist davon auszugehen, dass keine neuen "issues" aufgekommen sind, sondern dieser "issue" nicht aus der Welt geschaffen werden konnte. Das ist pure und simple Logik dessen, was public knowledge ist...
Antwort auf Beitrag Nr.: 56.466.359 von Cyberhexe am 16.12.17 10:30:10...nur um zukünftigen Diskussionen vorzubeugen:
ich halte es für möglich, dass die Begleitumstände bei ACTIVE (ph3-Studie)...
--> wie zB hohe Anzahl an Studienabbrecher unter Abaloparatide oder aber Ungereimtheiten bei einigen (wenigen) Studienstandorten
...ursächlich für die 3. Liste verantworlich sind (siehe Beitrag 477 von cyberhexe).
Nur zum jetzigen Zeitpunkt so zu tun, als wüsste man dies genau (siehe Beitrag 479)
--> und daher hinterfragt die EMA hier zurecht und sitzt das einfach aus bis sie zufriedenstellende Antworten bekommt
ist unredlich.
ich halte es für möglich, dass die Begleitumstände bei ACTIVE (ph3-Studie)...
--> wie zB hohe Anzahl an Studienabbrecher unter Abaloparatide oder aber Ungereimtheiten bei einigen (wenigen) Studienstandorten
...ursächlich für die 3. Liste verantworlich sind (siehe Beitrag 477 von cyberhexe).
Nur zum jetzigen Zeitpunkt so zu tun, als wüsste man dies genau (siehe Beitrag 479)
--> und daher hinterfragt die EMA hier zurecht und sitzt das einfach aus bis sie zufriedenstellende Antworten bekommt
ist unredlich.
Antwort auf Beitrag Nr.: 56.466.422 von Cyberhexe am 16.12.17 10:38:57Radius Health (NASDAQ:RDUS) initiated with Overweight rating and $57 (46% upside) price target at Morgan Stanley.
Mal schaun, ob ein bisschen Bewegung reinkommt.
nanu
Mal schaun, ob ein bisschen Bewegung reinkommt.
nanu
Antwort auf Beitrag Nr.: 56.862.548 von nanunana am 29.01.18 15:38:24hier noch der Artikel dazu mit den recht bullishen Annahmen/Aussichten:
https://finance.yahoo.com/news/analyst-radius-health-could-a…
https://finance.yahoo.com/news/analyst-radius-health-could-a…
BB Biotech hat erneut üppig zugekauft, und zwar 75.000 Aktien am 9.2.18:


Antwort auf Beitrag Nr.: 57.015.318 von Cyberhexe am 13.02.18 17:10:23aus der Präsentation folgender Analysten-Veranstaltung:
Radius Health (RDUS)
Leerink Healthcare
Conference
February 15,
2018
TYMLOS gewinnt stetig Marktanteile in den US:
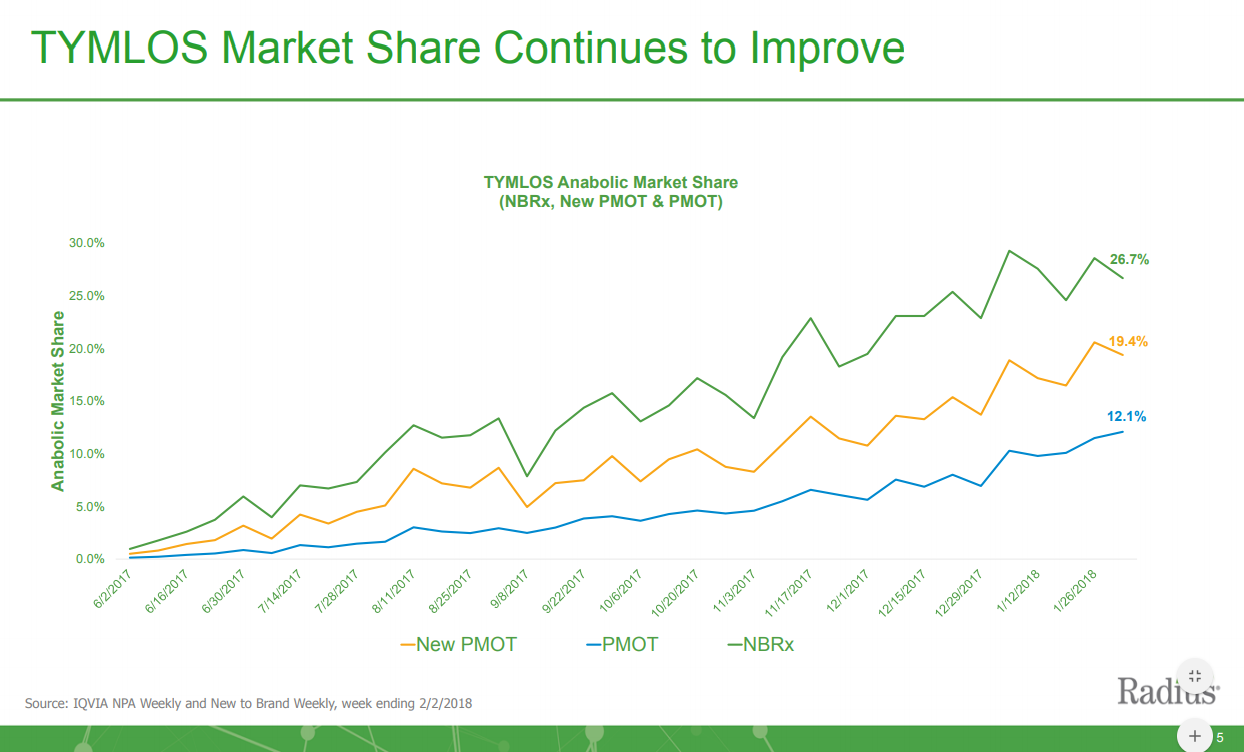
Radius Health (RDUS)
Leerink Healthcare
Conference
February 15,
2018
TYMLOS gewinnt stetig Marktanteile in den US:

Q4 2017
sieht doch ganz nett ausPräsentationsfolien: https://seekingalpha.com/article/4152619-radius-health-inc-2…
- Umsatz bei knapp $8 Mio. (siehe Wachstum bei Verschreibungen und Umsatz auf Folie 14 & 18)
- restliche Projekte kommen auch voran
- hoffe bloss bei der Zulassung in Europa läuft nichts schief, zuletzt waren EMA/CHMP bei der Zulassung in einigen prominenten Fällen rigoroser als die FDA (siehe Puma oder Portola)
Antwort auf Beitrag Nr.: 57.167.661 von paul81 am 02.03.18 09:50:10BB Biotech hat noch einmal 80'000 Aktien gekauft, auf nunmehr 5,854 Mio Aktien!!
http://files.shareholder.com/downloads/AMDA-1D3H6P/422188706…
http://files.shareholder.com/downloads/AMDA-1D3H6P/422188706…
nun ist die Entscheidung beim europ. Arzneimittelausschuss CHMP wohl reichlich überdacht und hinterfragt: diese Woche wird über die Zulassungsempfehlung von Abaloparatide zur Behandlung von Osteoporose entschieden.
Ich hoffe doch, dass nun gut wird was sehr lange gedauert hat!
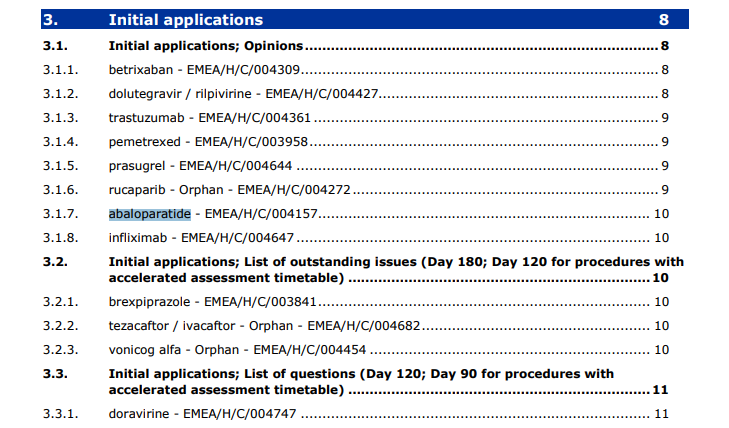
http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_e…
Ich hoffe doch, dass nun gut wird was sehr lange gedauert hat!

http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_e…
Antwort auf Beitrag Nr.: 57.167.661 von paul81 am 02.03.18 09:50:10
der TYMLOS-Umsatz im 1q2018 dürfte sich gegenüber 4q2017 (USD 8m) mehr als verdoppeln. Ich rechne mit über USD 20m:
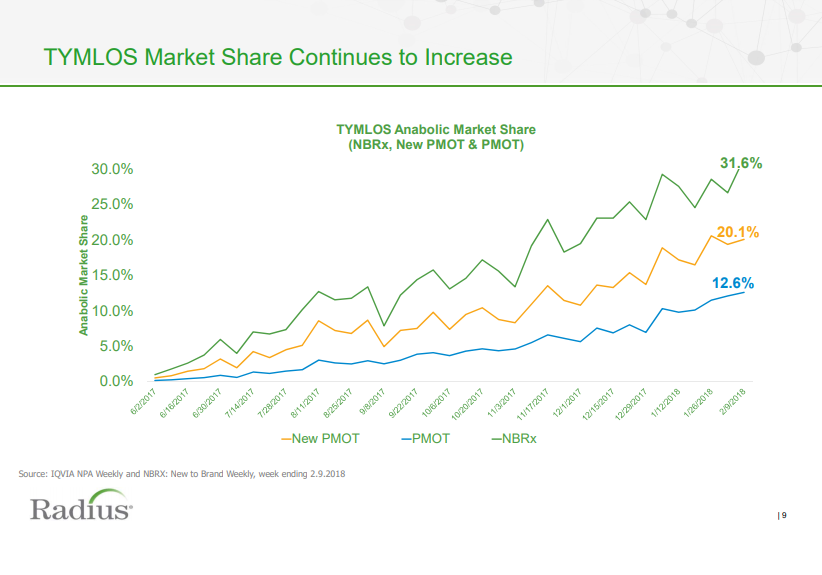
Endlich wird die europ. Arzneimittelbehörde CHMP eine Empfehlung (positiv oder negativ) zu Abaloparatide veröffentlichen. Ich rechne mit einer Zulassungsempfehlung.
Man darf gespannt sein, ob ein Kooperationspartner für Europa zeitnah veröffentlicht wird.
Zitat von paul81: sieht doch ganz nett aus
Präsentationsfolien: https://seekingalpha.com/article/4152619-radius-health-inc-2…
- Umsatz bei knapp $8 Mio. (siehe Wachstum bei Verschreibungen und Umsatz auf Folie 14 & 18)
- restliche Projekte kommen auch voran
- hoffe bloss bei der Zulassung in Europa läuft nichts schief, zuletzt waren EMA/CHMP bei der Zulassung in einigen prominenten Fällen rigoroser als die FDA (siehe Puma oder Portola)
der TYMLOS-Umsatz im 1q2018 dürfte sich gegenüber 4q2017 (USD 8m) mehr als verdoppeln. Ich rechne mit über USD 20m:

Endlich wird die europ. Arzneimittelbehörde CHMP eine Empfehlung (positiv oder negativ) zu Abaloparatide veröffentlichen. Ich rechne mit einer Zulassungsempfehlung.
Man darf gespannt sein, ob ein Kooperationspartner für Europa zeitnah veröffentlicht wird.
Antwort auf Beitrag Nr.: 56.433.621 von Ville7 am 12.12.17 18:27:55
diese Woche gibt es definitiv eine Empfehlung (ob Zulassung ja/nein) des europ.Arzneimittelausschusses CHMP - und merke Radius hat den Zuzlassungsantrag nicht zurückgezogen. Aber das ist ja keine Seltenheit, dass die abenteuerlichen Prognosen dieses Teilnehmers nicht eintreffen!
Für Freitag bin ich zuversichtlich, dass Abaloparatide vom CHMP zur Zulassung empfohlen wird!
Zitat von Ville7: Sieht nach der nächsten Enttäuschung aus. Und nach keiner ODAC Empfehlung! Zumindest nicht in Dezember. Aber wie will RDUS das denn überhaupt noch fixen, nach drei Terminen, bei denen man scheinbar die Bedenken der EMA bisher nicht nehmen konnte. Die EMA zieht das wohl hin - in der üblichen Art - so lange bis RDUS die application zurückzieht. Das sieht nicht so gut für RDUS aus.
diese Woche gibt es definitiv eine Empfehlung (ob Zulassung ja/nein) des europ.Arzneimittelausschusses CHMP - und merke Radius hat den Zuzlassungsantrag nicht zurückgezogen. Aber das ist ja keine Seltenheit, dass die abenteuerlichen Prognosen dieses Teilnehmers nicht eintreffen!
Für Freitag bin ich zuversichtlich, dass Abaloparatide vom CHMP zur Zulassung empfohlen wird!
Antwort auf Beitrag Nr.: 55.751.778 von Ville7 am 15.09.17 13:30:40
Die Umsatzschätzing für 2017 war schon weit daneben und auch die prospektive Umsatzschätzung der nächsten 4 Jahre dürfte sich als äusserst dielettantisch erweisen.
Der Umsatz von TYMLOS im 1q2018 sollte aufgrund der publizierten Marktanteile auf über 20mUSD zulegen. Kommt die Zulassungsempfehlung für die EU, dann ist weiteres Umsatzpotenzial vorhanden bzw. dann wird es spannend, ob bei Markteinführung bereits ein Kooperationspartner für Europa bekannt gegeben wird.
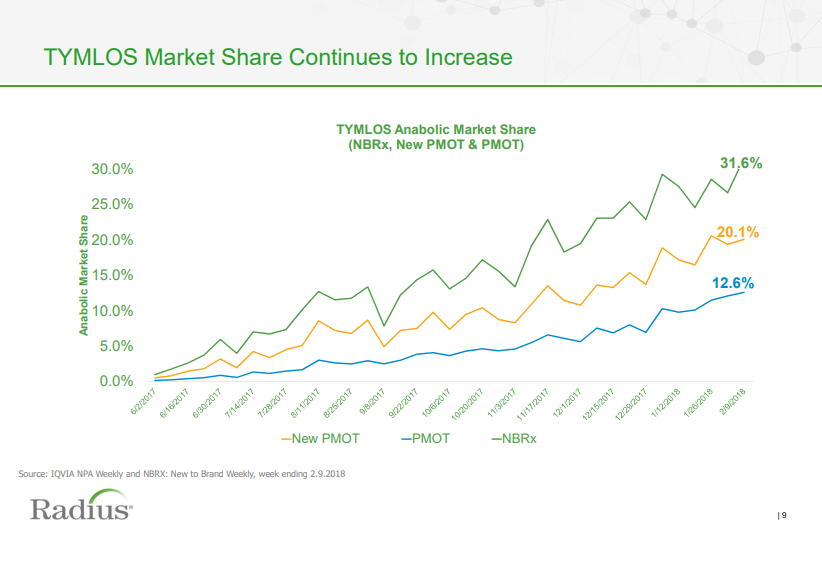
Zitat von Ville7: Die Rahmenzahlen bleiben schwach. 8% Marktanteil bei den absoluten Neuverschreibungen (keine Refills) deutet in diesem Jahr auf nur 8Millionen Umsatz bei Tymlos hin wenn das so bleibt. Erst nach 24 Monaten Marktanteil von 50% hätte man ca. 194 Millionen/Jahr. Umsatz erreicht Selbst wenn das binnen 4 Jahren erreicht würde, wie soll das eine MK von 1,6 Mrd rechtfertigen (und dabei massiv Warrants ausgegeben zu haben)? Da ist eine Menge Fantasie eingepreist, dass Radius es schafft den anabolic market wieder zum Wachsen zu bringen. Zumal man derzeit mehr als 50Mio EUR pro Quartal Verlust einfährt....
Die Umsatzschätzing für 2017 war schon weit daneben und auch die prospektive Umsatzschätzung der nächsten 4 Jahre dürfte sich als äusserst dielettantisch erweisen.
Der Umsatz von TYMLOS im 1q2018 sollte aufgrund der publizierten Marktanteile auf über 20mUSD zulegen. Kommt die Zulassungsempfehlung für die EU, dann ist weiteres Umsatzpotenzial vorhanden bzw. dann wird es spannend, ob bei Markteinführung bereits ein Kooperationspartner für Europa bekannt gegeben wird.

Antwort auf Beitrag Nr.: 57.346.988 von Cyberhexe am 21.03.18 20:23:11@Cyberhexe: wo siehst du Kursziel kurz- und mittelfristig, wenn die europäische Zulassung durchgeht ?
nanu
nanu
Liebe Cyberhexe, meine Einschätzung im big picture war und ist goldrichtig. Detailausprägungen geschenkt.
PS: Wie lief es eigentlich bei TTPH?
PS: Wie lief es eigentlich bei TTPH?
Antwort auf Beitrag Nr.: 57.355.067 von kmastra am 22.03.18 14:07:50
The EMA has informed the Company that the CHMP will therefore adopt a negative opinion on the MAA today, Thursday, March 22, 2018.
The EMA has informed the Company that the CHMP will therefore adopt a negative opinion on the MAA today, Thursday, March 22, 2018.
Antwort auf Beitrag Nr.: 57.346.853 von Cyberhexe am 21.03.18 20:12:18Die "abenteuerliche Prognose" des Teilnehmers Ville ist genau so eingetreten, wie es der Teilnehmer Ville prognostiziert hat.
http://globenewswire.com/news-release/2018/03/22/1444375/0/e…" target="_blank" rel="nofollow ugc noopener">http://globenewswire.com/news-release/2018/03/22/1444375/0/e…
http://globenewswire.com/news-release/2018/03/22/1444375/0/e…" target="_blank" rel="nofollow ugc noopener">http://globenewswire.com/news-release/2018/03/22/1444375/0/e…
Zitat von Cyberhexe:Zitat von Ville7: Sieht nach der nächsten Enttäuschung aus. Und nach keiner ODAC Empfehlung! Zumindest nicht in Dezember. Aber wie will RDUS das denn überhaupt noch fixen, nach drei Terminen, bei denen man scheinbar die Bedenken der EMA bisher nicht nehmen konnte. Die EMA zieht das wohl hin - in der üblichen Art - so lange bis RDUS die application zurückzieht. Das sieht nicht so gut für RDUS aus.
diese Woche gibt es definitiv eine Empfehlung (ob Zulassung ja/nein) des europ.Arzneimittelausschusses CHMP - und merke Radius hat den Zuzlassungsantrag nicht zurückgezogen. Aber das ist ja keine Seltenheit, dass die abenteuerlichen Prognosen dieses Teilnehmers nicht eintreffen!
Für Freitag bin ich zuversichtlich, dass Abaloparatide vom CHMP zur Zulassung empfohlen wird!
Antwort auf Beitrag Nr.: 57.355.067 von kmastra am 22.03.18 14:07:50Tja, Cyberhexe, was nun? Wirst Du jetzt die EMA beschimpfen? Bei Ville solltest Du allmählich Abbitte leisten ...
Man kann Dir nur wünschen, dass Du weniger stark bei radius investiert bist als von Dir immer wieder dargestellt.
Man kann Dir nur wünschen, dass Du weniger stark bei radius investiert bist als von Dir immer wieder dargestellt.
interessant aktuell nur -4%... scheint wohl viele nicht so überrascht zu haben... also demonstrieren EMA/CHMP nach Puma und Portola jetzt auch an Radius ihre Strenge
der Kursverlauf wundert mich echt, habe mit hohem zweistelligem Minus gerechnet... also ich bin dann mal mit raus (+/- 0), bevor sich der Markt das noch anders überlegt... die Story Radius ist für mich jetzt mal (eine Weile) vorbei
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -3,12 | |
| +1,85 | |
| -1,11 | |
| +0,29 | |
| -0,19 | |
| +0,18 | |
| 0,00 | |
| -3,62 | |
| -0,26 | |
| -17,06 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 171 | ||
| 52 | ||
| 46 | ||
| 34 | ||
| 33 | ||
| 30 | ||
| 28 | ||
| 20 | ||
| 17 | ||
| 17 |