Revive Therapeutics Applies to FDA for Orphan Drug Designation for Treatment of Autoimmune Hepatitis (Seite 85) | Diskussion im Forum
eröffnet am 03.10.17 15:55:52 von
neuester Beitrag 07.04.24 04:52:26 von
neuester Beitrag 07.04.24 04:52:26 von
Beiträge: 3.078
ID: 1.263.331
ID: 1.263.331
Aufrufe heute: 2
Gesamt: 157.397
Gesamt: 157.397
Aktive User: 0
ISIN: CA7615161030 · WKN: A2AP4F
0,0215
EUR
+7,50 %
+0,0015 EUR
Letzter Kurs 11:09:22 Lang & Schwarz
Neuigkeiten
23.04.24 · globenewswire |
18.04.24 · globenewswire |
02.04.24 · globenewswire |
27.03.24 · globenewswire |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 8,1400 | +20,41 | |
| 0,8232 | +17,25 | |
| 1,0900 | +15,96 | |
| 0,6600 | +15,79 | |
| 5,0100 | +15,70 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,6700 | -26,58 | |
| 2,1300 | -34,41 | |
| 3,1600 | -38,64 | |
| 1,7000 | -49,40 | |
| 125,00 | -95,83 |
Beitrag zu dieser Diskussion schreiben
Das finde ich ja mal interessant. Der letzte Satz in rot. Auf jeden Fall ein sehr guter Schritt. Weg vom Kanada Pump & Dump Image. Dann als nächstes an die Nasdaq bitte.
Aber auch inhaltlich ist die News wertvoll was die nächsten Schritte in der Pipeline betrifft.
Da bekomme ich direkt nochmal Lust ein Körbchen aufzustellen.
Ich denke mal das RVV sich ziemlich sicher ist, das Buci egal für was, Wirkung zeigt.
Revive Therapeutics entwickelt Programme für entzündliche Lebererkrankungen für Autoimmunhepatitis und Lebertransplantation
Mai 31, 2022 - 7:00 am
WHO meldet 650 wahrscheinliche Fälle von akuter Hepatitis unbekannter Ätiologie bei Kindern aus 33 Ländern
TORONTO, May 31, 2022 (GLOBE NEWSWIRE) -- Revive Therapeutics Ltd. ("Revive" oder das "Unternehmen") (OTCQB: RVVTF) (CSE: RVV) (FRANKFURT:31R), ein spezialisiertes Life-Sciences-Unternehmen, das sich auf die Erforschung und Entwicklung von Therapeutika für medizinische Bedürfnisse und seltene Erkrankungen konzentriert, gab heute bekannt, dass angesichts der zunehmenden Fälle von akuter Hepatitis bei Kindern, die von der Weltgesundheitsorganisation ("WHO") gemeldet wurden, Das Unternehmen wird seine Medikamentenpipeline für entzündliche Lebererkrankungen einschließlich Bucillamine zur Prävention von Ischämie-Reperfusionsverletzungen während der Lebertransplantation und Cannabidiol für Autoimmunhepatitis vorantreiben.
Bis zum 26. Mai 2022 wurden der WHO zwischen dem 5. April und dem 26. Mai 2022 sechshundertfünfzig wahrscheinliche Fälle von akuter Hepatitis unbekannter Ätiologie bei Kindern aus 33 Ländern in fünf WHO-Regionen gemeldet. Die Ätiologie dieser schweren akuten Hepatitis bleibt unbekannt und wird untersucht; da die Fälle klinisch schwerer sind und ein höherer Anteil akutes Leberversagen entwickelt als frühere Berichte über akute Hepatitis unbekannter Ätiologie bei Kindern. Mindestens 38 Kinder haben eine Lebertransplantation benötigt, neun sind gestorben und 99 Fälle stehen noch aus, so eine Erklärung der WHO (https://www.who.int/emergencies/disease-outbreak-news/item/D…
Das Unternehmen verfügt über eine vielfältige Produktpipeline in der Entwicklung für seltene entzündliche Lebererkrankungen, einschließlich des FDA-Orphan-Drug-Status für Bucillamine zur Verhinderung von Ischämie-Reperfusionsverletzungen während der Lebertransplantation und Cannabidiol für Autoimmunhepatitis. Revive hat mit den Trustees of Indiana University ("TIU") eine Vereinbarung über eine klinische Studie zur Entwicklung und Leitung einer geplanten klinischen Phase-2-Studie mit Cannabidiol als Zusatztherapie für schwer zu behandelnde Autoimmunhepatitis abgeschlossen.
Revive wird auch die Verwendung von Bucillamin für Lebertransplantationen mit klinischen Prüfärzten über das Protokolldesign und den regulatorischen Weg untersuchen, um die FDA-Zulassung für eine klinische Studie im Rahmen eines neuen Prüfpräparatantrags zu erhalten. Das Unternehmen ist der Ansicht, dass die Verwendung von Bucillamin während der Lebertransplantation das Potenzial hat, ein sicherer und wirksamer Ansatz zu sein, um den ungedeckten medizinischen Bedarf an einer neuartigen Strategie zur Begrenzung oder Verhinderung von Ischämie-Reperfusionsverletzungen zu decken. Bucillamin, ein Cysteinderivat, das zwei donatierbare Thiolgruppen enthält, ist im Rahmen einer Ischämie-Reperfusionsverletzung in der Lage, die Thiolgruppe in Glutathion wieder aufzufüllen und dadurch diese körpereigene Abwehr gegen Oxidationsmittelverletzungen zu reaktivieren. Bucillamine hat auch das Potenzial, die Transplantatfunktion und das Patientenergebnis zu verbessern, indem es IRI verhindert oder verringert.
Darüber hinaus beabsichtigt das Unternehmen, seinen Hauptsitz in die USA zu verlegen, um den Zugang zu und die Unterstützung wachsender Arzneimittelprogramme mit Bucillamine und anderen Produkten zu verbessern.
Über Revive Therapeutics Ltd.
Revive ist ein Life-Sciences-Unternehmen, das sich auf die Erforschung und Entwicklung von Therapeutika für Infektionskrankheiten und seltene Erkrankungen konzentriert und den Bemühungen um die Arzneimittelentwicklung Priorität einräumt, um mehrere von der FDA vergebene regulatorische Anreize wie Orphan Drug, Fast Track, Breakthrough Therapy und Rare Pediatric Disease zu nutzen. Derzeit untersucht das Unternehmen den Einsatz von Bucillamine zur möglichen Behandlung von Infektionskrankheiten, wobei der Schwerpunkt zunächst auf schwerer Influenza und COVID-19 liegt. Mit der Übernahme von Psilocin Pharma Corp. treibt Revive die Entwicklung von Psilocybin-basierten Therapeutika bei verschiedenen Krankheiten und Störungen voran. Das pharmazeutische Cannabinoid-Portfolio von Revive konzentriert sich auf seltene entzündliche Erkrankungen und das Unternehmen erhielt den FDA-Orphan-Drug-Status für die Verwendung von Cannabidiol (CBD) zur Behandlung von Autoimmunhepatitis (Lebererkrankung) und zur Behandlung von Ischämie und Reperfusionsverletzungen durch Organtransplantation. Weitere Informationen finden Sie unter www.ReviveThera.com.
Aber auch inhaltlich ist die News wertvoll was die nächsten Schritte in der Pipeline betrifft.
Da bekomme ich direkt nochmal Lust ein Körbchen aufzustellen.
Ich denke mal das RVV sich ziemlich sicher ist, das Buci egal für was, Wirkung zeigt.
Revive Therapeutics entwickelt Programme für entzündliche Lebererkrankungen für Autoimmunhepatitis und Lebertransplantation
Mai 31, 2022 - 7:00 am
WHO meldet 650 wahrscheinliche Fälle von akuter Hepatitis unbekannter Ätiologie bei Kindern aus 33 Ländern
TORONTO, May 31, 2022 (GLOBE NEWSWIRE) -- Revive Therapeutics Ltd. ("Revive" oder das "Unternehmen") (OTCQB: RVVTF) (CSE: RVV) (FRANKFURT:31R), ein spezialisiertes Life-Sciences-Unternehmen, das sich auf die Erforschung und Entwicklung von Therapeutika für medizinische Bedürfnisse und seltene Erkrankungen konzentriert, gab heute bekannt, dass angesichts der zunehmenden Fälle von akuter Hepatitis bei Kindern, die von der Weltgesundheitsorganisation ("WHO") gemeldet wurden, Das Unternehmen wird seine Medikamentenpipeline für entzündliche Lebererkrankungen einschließlich Bucillamine zur Prävention von Ischämie-Reperfusionsverletzungen während der Lebertransplantation und Cannabidiol für Autoimmunhepatitis vorantreiben.
Bis zum 26. Mai 2022 wurden der WHO zwischen dem 5. April und dem 26. Mai 2022 sechshundertfünfzig wahrscheinliche Fälle von akuter Hepatitis unbekannter Ätiologie bei Kindern aus 33 Ländern in fünf WHO-Regionen gemeldet. Die Ätiologie dieser schweren akuten Hepatitis bleibt unbekannt und wird untersucht; da die Fälle klinisch schwerer sind und ein höherer Anteil akutes Leberversagen entwickelt als frühere Berichte über akute Hepatitis unbekannter Ätiologie bei Kindern. Mindestens 38 Kinder haben eine Lebertransplantation benötigt, neun sind gestorben und 99 Fälle stehen noch aus, so eine Erklärung der WHO (https://www.who.int/emergencies/disease-outbreak-news/item/D…
Das Unternehmen verfügt über eine vielfältige Produktpipeline in der Entwicklung für seltene entzündliche Lebererkrankungen, einschließlich des FDA-Orphan-Drug-Status für Bucillamine zur Verhinderung von Ischämie-Reperfusionsverletzungen während der Lebertransplantation und Cannabidiol für Autoimmunhepatitis. Revive hat mit den Trustees of Indiana University ("TIU") eine Vereinbarung über eine klinische Studie zur Entwicklung und Leitung einer geplanten klinischen Phase-2-Studie mit Cannabidiol als Zusatztherapie für schwer zu behandelnde Autoimmunhepatitis abgeschlossen.
Revive wird auch die Verwendung von Bucillamin für Lebertransplantationen mit klinischen Prüfärzten über das Protokolldesign und den regulatorischen Weg untersuchen, um die FDA-Zulassung für eine klinische Studie im Rahmen eines neuen Prüfpräparatantrags zu erhalten. Das Unternehmen ist der Ansicht, dass die Verwendung von Bucillamin während der Lebertransplantation das Potenzial hat, ein sicherer und wirksamer Ansatz zu sein, um den ungedeckten medizinischen Bedarf an einer neuartigen Strategie zur Begrenzung oder Verhinderung von Ischämie-Reperfusionsverletzungen zu decken. Bucillamin, ein Cysteinderivat, das zwei donatierbare Thiolgruppen enthält, ist im Rahmen einer Ischämie-Reperfusionsverletzung in der Lage, die Thiolgruppe in Glutathion wieder aufzufüllen und dadurch diese körpereigene Abwehr gegen Oxidationsmittelverletzungen zu reaktivieren. Bucillamine hat auch das Potenzial, die Transplantatfunktion und das Patientenergebnis zu verbessern, indem es IRI verhindert oder verringert.
Darüber hinaus beabsichtigt das Unternehmen, seinen Hauptsitz in die USA zu verlegen, um den Zugang zu und die Unterstützung wachsender Arzneimittelprogramme mit Bucillamine und anderen Produkten zu verbessern.
Über Revive Therapeutics Ltd.
Revive ist ein Life-Sciences-Unternehmen, das sich auf die Erforschung und Entwicklung von Therapeutika für Infektionskrankheiten und seltene Erkrankungen konzentriert und den Bemühungen um die Arzneimittelentwicklung Priorität einräumt, um mehrere von der FDA vergebene regulatorische Anreize wie Orphan Drug, Fast Track, Breakthrough Therapy und Rare Pediatric Disease zu nutzen. Derzeit untersucht das Unternehmen den Einsatz von Bucillamine zur möglichen Behandlung von Infektionskrankheiten, wobei der Schwerpunkt zunächst auf schwerer Influenza und COVID-19 liegt. Mit der Übernahme von Psilocin Pharma Corp. treibt Revive die Entwicklung von Psilocybin-basierten Therapeutika bei verschiedenen Krankheiten und Störungen voran. Das pharmazeutische Cannabinoid-Portfolio von Revive konzentriert sich auf seltene entzündliche Erkrankungen und das Unternehmen erhielt den FDA-Orphan-Drug-Status für die Verwendung von Cannabidiol (CBD) zur Behandlung von Autoimmunhepatitis (Lebererkrankung) und zur Behandlung von Ischämie und Reperfusionsverletzungen durch Organtransplantation. Weitere Informationen finden Sie unter www.ReviveThera.com.
Das wäre ja schon mal fein, laut Ausbruch aus dem Triangle auf den Zeitraum seit 2019 würde sich rein Rechnerisch erstmal ein Ziel von 1,25Cad ergeben. Vorausgesetzt das Kaufsignal bleibt valide und die Pipeline bleibt positiv. Nach positiven Ergebnissen der 210 Teilnehmer und Hinweis zur EUA ist nach oben alles offen 😎
Chart ist im weekly
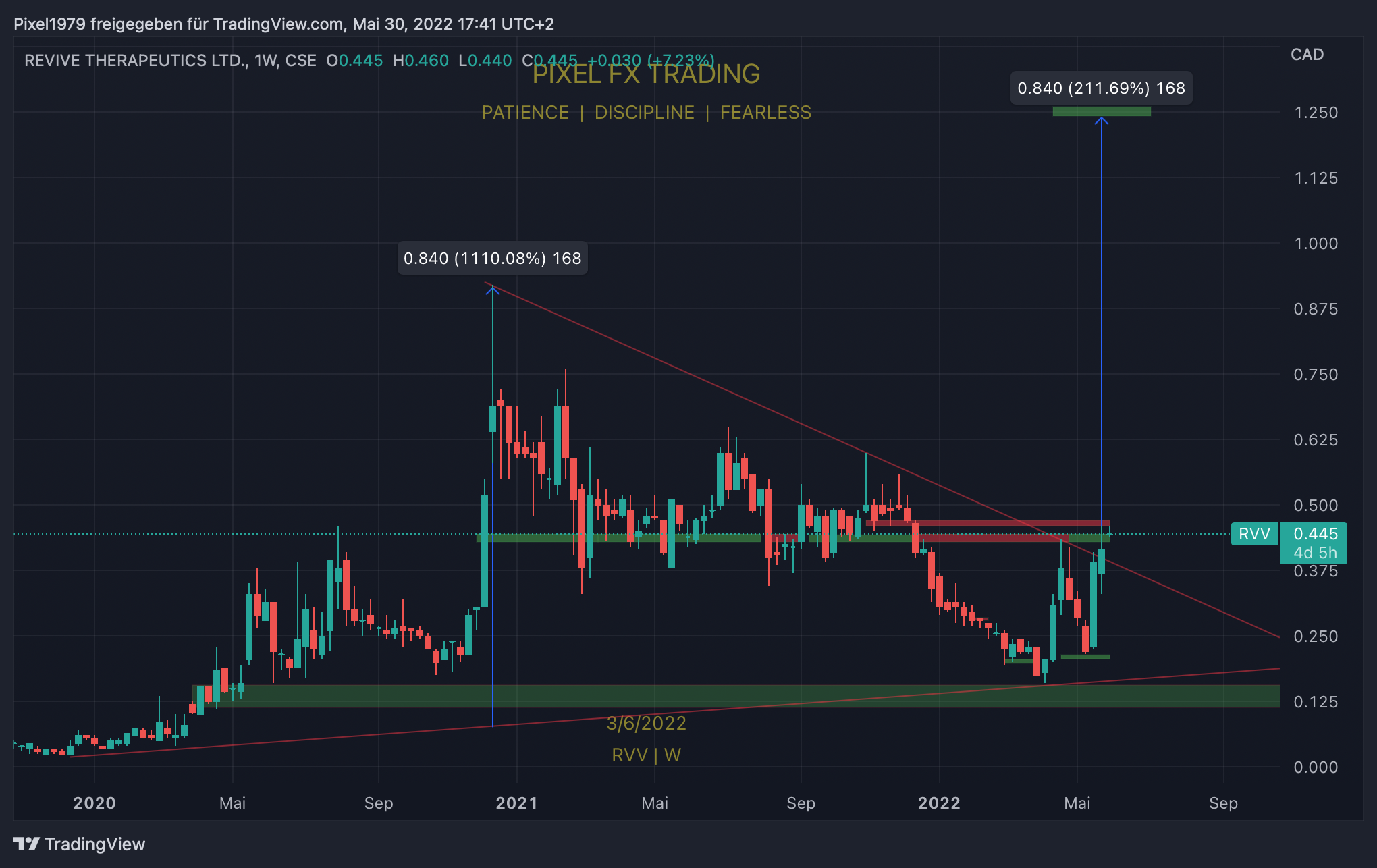
Chart ist im weekly

Moin, ich hab mir das Interview nun auch mal angesehen und ja, nicht viel neues.
- Merck und Pfizer sind nicht der goldene Weg bezgl. Wirkung und Eignung der Medi´s an den Patienten.
- FDA sucht förmlich nach vernünftigen Lösungen und wirksame Mittel was zukünftige Therapeutika gegen Covid betrifft und kommt somit RVV mit ihrem Verhalten entgegen.
- FDA hat, wie schon gesagt in Bucillamin etwas gesehen, was die Wirksamkeit in den Ergebnissen angeht, sonst würde sie die 210 Daten nicht genehmigen
- 90% Wahrscheinlichkeit nach Entblindung der 210 für EUA und durch Empfehlung DSMB (Meinung von Biomedical_Trader)
- Vergleich Buci mit Nac und deren Wirksamkeit, positiv
- Wenn RVV das ist was wir alle hoffen und vermuten, dann wird es sich mehr lohnen wie z.B. jüngst bei VERU, persönliche Meinung von B_T
Der Juni wird jetzt richtig spannend und ich hoffe für uns alle das sich das jetzt zeitnah positiv auflöst und das Warten und Bangen ein Ende hat.
Good Luck @ all 😎
- Merck und Pfizer sind nicht der goldene Weg bezgl. Wirkung und Eignung der Medi´s an den Patienten.
- FDA sucht förmlich nach vernünftigen Lösungen und wirksame Mittel was zukünftige Therapeutika gegen Covid betrifft und kommt somit RVV mit ihrem Verhalten entgegen.
- FDA hat, wie schon gesagt in Bucillamin etwas gesehen, was die Wirksamkeit in den Ergebnissen angeht, sonst würde sie die 210 Daten nicht genehmigen
- 90% Wahrscheinlichkeit nach Entblindung der 210 für EUA und durch Empfehlung DSMB (Meinung von Biomedical_Trader)
- Vergleich Buci mit Nac und deren Wirksamkeit, positiv
- Wenn RVV das ist was wir alle hoffen und vermuten, dann wird es sich mehr lohnen wie z.B. jüngst bei VERU, persönliche Meinung von B_T
Der Juni wird jetzt richtig spannend und ich hoffe für uns alle das sich das jetzt zeitnah positiv auflöst und das Warten und Bangen ein Ende hat.
Good Luck @ all 😎
Antwort auf Beitrag Nr.: 71.678.098 von swoasik am 30.05.22 08:17:03Noch was vergessen ! 😂
Es wird davon ausgegangen , "was ich letzte Woche nach der Meldung schon vermutet habe " dass die FDA oder DMSB schon in die Daten eingesehen haben und hier wichtige Daten gesehen haben .
Es wird davon ausgegangen , "was ich letzte Woche nach der Meldung schon vermutet habe " dass die FDA oder DMSB schon in die Daten eingesehen haben und hier wichtige Daten gesehen haben .
Denkt dran. Heute ist in den USA kein Handel (Memorial Day).
An der TSX in Kanada müsste der Handel aber ganz normal stattfinden und dies ist unsere Heimatbörse 👍
An der TSX in Kanada müsste der Handel aber ganz normal stattfinden und dies ist unsere Heimatbörse 👍
Antwort auf Beitrag Nr.: 71.677.783 von Horst233 am 30.05.22 07:09:51Morgen Horst ! Es wird viel von dem gesprochen was wir alle schon wissen ! Also nichts neues !
Aber eines ist sehr bemerkenswert ab dem Video bei der Zeit 9:00 wird darauf eingegangen das die FDA noch nie ein Unternehmen es erlaubt hat Daten vor der Entblindung zu sichten ( bezogen auf die 210 Probanden) dies ist jetzt das erste Mal daß die FDA diesen Weg geht! Hier erfährt also Revive eine Sonderbehandlung , aus der Vermutung heraus dass Sie unbedingt ein Medi brauchen. Darin geht es auch um den Datenzugriffsplan , wer alles einsehen kann und wie häufig.
Alles sind sich einig dass hier die FDA einen großen Schritt auf Revive zugeht , was es bis jetzt noch nicht gegeben hat bei der FDA .
Es bleibt nicht nur spannend , sondern es wird immer spannender.
Aber eines ist sehr bemerkenswert ab dem Video bei der Zeit 9:00 wird darauf eingegangen das die FDA noch nie ein Unternehmen es erlaubt hat Daten vor der Entblindung zu sichten ( bezogen auf die 210 Probanden) dies ist jetzt das erste Mal daß die FDA diesen Weg geht! Hier erfährt also Revive eine Sonderbehandlung , aus der Vermutung heraus dass Sie unbedingt ein Medi brauchen. Darin geht es auch um den Datenzugriffsplan , wer alles einsehen kann und wie häufig.
Alles sind sich einig dass hier die FDA einen großen Schritt auf Revive zugeht , was es bis jetzt noch nicht gegeben hat bei der FDA .
Es bleibt nicht nur spannend , sondern es wird immer spannender.
Morgen swoasik kannst du es ein bisschen übersetzen ..danke dir ...der inhalt wer nett danke
Auch sehr interessant , auf YouTube von heute Nacht.
Nur zur Info, morgen ist in USA kein Handel, da Feiertag (Memorial Day) ist.
Guter Beitrag auf Yahoo Board zur Abwechslung durch Benutzername: (Benjamin)
Hinweis: Finanzschreiber Benjamin A. Smith vom TDR 😎
"0.50-$0.70 Wenn Revive mit dem Endpunktwechsel voranschreitet, nachdem er sich die 210 Patientendaten angesehen hat
1,25 $ 1,50 wenn DSMB EUA für Symptome empfiehlt
5 $+ wenn die FDA EUA gewährt
_______
Revive geht mit Symptomen-Endpunktänderungen voran, aber DSMB empfiehlt keine EUA und fordert zusätzliche Daten $0,40-0,50
Symptome-Endpunkt, die von der Revive nicht akzeptiert werden und Hospitalisierungen bleiben der primäre Endpunkt $0,16-0,20
Prozess beendet 0,08 $
Alle Zahlen in CAD
Wenn Revive mit dem Endpunktwechsel voranschreitet, steigt die Wahrscheinlichkeit, dass das DSMB EUA für Symptome empfiehlt, in die Höhe, weil Revive alle Daten entblindet und sich ziemlich sicher in ihre Anzahl für Symptome ist. Immer noch ein bisschen Risiko, aber ich sehe im Moment positiv aus. So sehe ich das so objektiv wie möglich. "
Hinweis: Finanzschreiber Benjamin A. Smith vom TDR 😎
"0.50-$0.70 Wenn Revive mit dem Endpunktwechsel voranschreitet, nachdem er sich die 210 Patientendaten angesehen hat
1,25 $ 1,50 wenn DSMB EUA für Symptome empfiehlt
5 $+ wenn die FDA EUA gewährt
_______
Revive geht mit Symptomen-Endpunktänderungen voran, aber DSMB empfiehlt keine EUA und fordert zusätzliche Daten $0,40-0,50
Symptome-Endpunkt, die von der Revive nicht akzeptiert werden und Hospitalisierungen bleiben der primäre Endpunkt $0,16-0,20
Prozess beendet 0,08 $
Alle Zahlen in CAD
Wenn Revive mit dem Endpunktwechsel voranschreitet, steigt die Wahrscheinlichkeit, dass das DSMB EUA für Symptome empfiehlt, in die Höhe, weil Revive alle Daten entblindet und sich ziemlich sicher in ihre Anzahl für Symptome ist. Immer noch ein bisschen Risiko, aber ich sehe im Moment positiv aus. So sehe ich das so objektiv wie möglich. "















