Revive Therapeutics Applies to FDA for Orphan Drug Designation for Treatment of Autoimmune Hepatitis (Seite 88) | Diskussion im Forum
eröffnet am 03.10.17 15:55:52 von
neuester Beitrag 07.04.24 04:52:26 von
neuester Beitrag 07.04.24 04:52:26 von
Beiträge: 3.078
ID: 1.263.331
ID: 1.263.331
Aufrufe heute: 0
Gesamt: 157.408
Gesamt: 157.408
Aktive User: 0
ISIN: CA7615161030 · WKN: A2AP4F · Symbol: RVVTF
0,0199
USD
-0,50 %
-0,0001 USD
Letzter Kurs 06.05.24 Nasdaq OTC
Neuigkeiten
23.04.24 · globenewswire |
18.04.24 · globenewswire |
02.04.24 · globenewswire |
27.03.24 · globenewswire |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,6400 | +23,31 | |
| 1,4000 | +22,81 | |
| 1,3000 | +22,64 | |
| 2,7600 | +20,00 | |
| 1,2300 | +19,42 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 7,8600 | -14,10 | |
| 8,6500 | -14,82 | |
| 7,5000 | -18,30 | |
| 23,140 | -19,90 | |
| 125,00 | -95,83 |
Beitrag zu dieser Diskussion schreiben
Was meint ihr? Wie lange wird die FDA brauchen um die Entscheidung zu finden die Endpunkte von Krankenhausaufenthalten und Todesfälle auf Symptomreduzierung zu ändern?
Wir nähern uns dem Juni und somit dem baldigen Ende der Studie.
Charttechnisch scheint die 0,43 CAD ne Hürde zu sein, ich hoffe wir überwinden diese beim nächsten Anlauf. Kaufinteresse scheint wieder vorhanden zu sein.
Wirkt Bucillamin auch gegen Affenpocken? Frage für einen Freund 😂
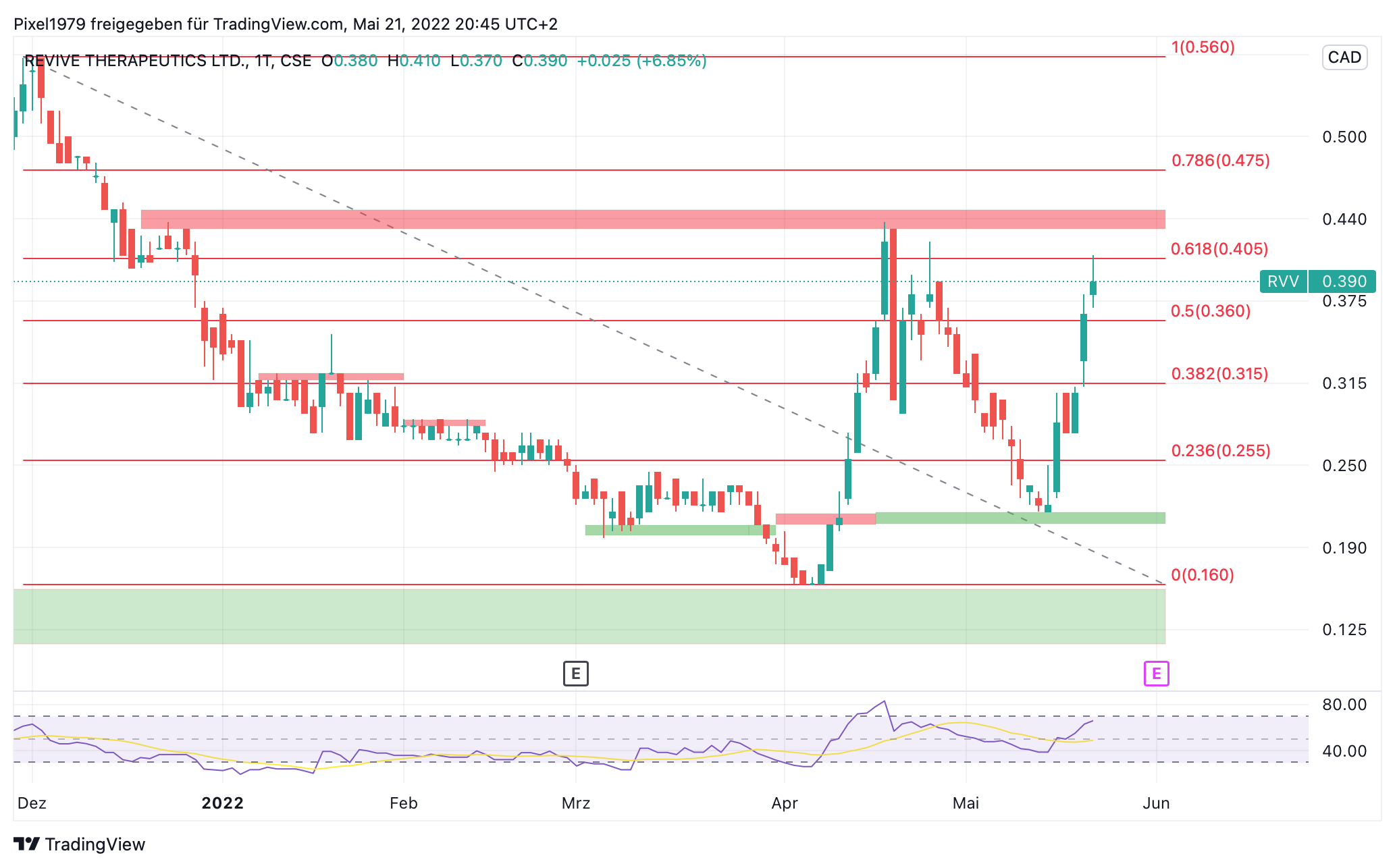
Wir nähern uns dem Juni und somit dem baldigen Ende der Studie.
Charttechnisch scheint die 0,43 CAD ne Hürde zu sein, ich hoffe wir überwinden diese beim nächsten Anlauf. Kaufinteresse scheint wieder vorhanden zu sein.
Wirkt Bucillamin auch gegen Affenpocken? Frage für einen Freund 😂

Antwort auf Beitrag Nr.: 71.611.245 von zzman31 am 19.05.22 12:18:37muss sich jeder selbst beantworten !
Bei keiner Zulassung, und keiner EAU werden wir auf 0,07-0,10 Euro Cent sinken; also ca. 0,12 -0,15 Euro Cent Verlust pro Aktie ;
Bei einer EAU und Zulassung durch FDA werden wir auf minimum 5 - 7 Euro steigen ! Kann sich jeder selbst ausrechnen womit er mehr Probleme hat

Gruß
Bei keiner Zulassung, und keiner EAU werden wir auf 0,07-0,10 Euro Cent sinken; also ca. 0,12 -0,15 Euro Cent Verlust pro Aktie ;
Bei einer EAU und Zulassung durch FDA werden wir auf minimum 5 - 7 Euro steigen ! Kann sich jeder selbst ausrechnen womit er mehr Probleme hat


Gruß
Jetzt ist die Frage, SK setzen oder nicht? Entweder knallt die extrem hoch oder es wird grausam!? 🤔
schreibe es ja schon lange hier im Thread , dass mit meinem Verständnis Revive nur hingehalten wurden die letzten 10 Monate. Revive entwickelt keinen Impfstoff sondern ein Medi, und da nur eine Weiterentwicklung , und dann noch eines , welches schon 30 Jahre auf den Markt ist und alle Nebenwirkungen bekannt sind. Und dann wollte die FDA wirklich zwischen 850 und 1000 Probanden  während Pfizer , Merk usw mit weniger als 200 eine Zulassung bekommen.
während Pfizer , Merk usw mit weniger als 200 eine Zulassung bekommen.
Zum Glück hat es M.F. noch geschnallt um das Protokoll jetzt umschreiben zu lassen.
Pfizer setzt in diesem Jahr alleine 22 Millarden Dollar mit Paxlovid um , obwohl die Wirkung lange nicht mehr so gut ist wie aus der Studie nach außen " gemauschelt "
Bald werden wir wissen was Sache ist !
 während Pfizer , Merk usw mit weniger als 200 eine Zulassung bekommen.
während Pfizer , Merk usw mit weniger als 200 eine Zulassung bekommen.Zum Glück hat es M.F. noch geschnallt um das Protokoll jetzt umschreiben zu lassen.
Pfizer setzt in diesem Jahr alleine 22 Millarden Dollar mit Paxlovid um , obwohl die Wirkung lange nicht mehr so gut ist wie aus der Studie nach außen " gemauschelt "
Bald werden wir wissen was Sache ist !
Bevorstehende FDA-Entscheidung Ein Potenziell Großes Risikoabfallereignis Für Revive Therapeutics
https://thedalesreport.com/psychedelics/upcoming-fda-decisio…
https://thedalesreport.com/psychedelics/upcoming-fda-decisio…
Revive Therapeutics stellt Update zur klinischen Phase-3-Studie für Bucillamin bei COVID-19 bereit
Das Unternehmen reichte bei der FDA einen Antrag ein, potenzielle neue klinische Endpunkte für EUA zur Prüfung durch die FDA zu bestimmen
16. Mai 2022 10:48 ET | Quelle: Revive Therapeutics Ltd.
https://www.globenewswire.com/news-release/2022/05/16/244410…
Das Unternehmen reichte bei der FDA einen Antrag ein, potenzielle neue klinische Endpunkte für EUA zur Prüfung durch die FDA zu bestimmen
16. Mai 2022 10:48 ET | Quelle: Revive Therapeutics Ltd.
https://www.globenewswire.com/news-release/2022/05/16/244410…
Ich habe Anfang April für knapp unter 12 Eurocent die Chance genutzt und noch mal zugekauft.
Glaube nicht das wir, vor der Zulassung oder EUA, noch mal unter 12 Eurocent fallen werden, oder
sogar wie hier gehofft wird, unter 0,12CAD.
Glaube nicht das wir, vor der Zulassung oder EUA, noch mal unter 12 Eurocent fallen werden, oder
sogar wie hier gehofft wird, unter 0,12CAD.
Ich denke mir es werden sich noch weitere Nachkaufchancen ergeben. wir stecken in einer Krise (Inflation, Zinsen, Energie) die ganzen Umweltkrisen kommen ja noch diesen und naechsten Monat.
Deine 0.12CAD sind ein recht gutes Target um nachzukaufen. Ich hab meine Kauforder hier plaziert.
An den 0.12CAD waren wir vor einigen Wochen knapp dran.
Der May ist ja meistens nicht der Monat in dem man kaufen sollte.
Pixel-Muc du hast Ihn ja noch gar nicht so lange her selber zitiert.
Deine 0.12CAD sind ein recht gutes Target um nachzukaufen. Ich hab meine Kauforder hier plaziert.
An den 0.12CAD waren wir vor einigen Wochen knapp dran.
Der May ist ja meistens nicht der Monat in dem man kaufen sollte.
Pixel-Muc du hast Ihn ja noch gar nicht so lange her selber zitiert.
Zur Zeit bieten sich etliche Nachkaufkurse, nur die Frage, handelt man nach dem Motto "Buy the Dip" oder "Buy the Rip" 😂
Aber ich schaue mal auf die 0,16 und 0,12Cad, eigentlich alles ziemlich schräg, aber im letzten Jahr hab ich mal geschrieben das ich hoffe das die Studie vor dem Crash beendet wird, jetzt sind wird mittendrin und ich kaufe nochmal günstig nach. Auch fein
Aber ich schaue mal auf die 0,16 und 0,12Cad, eigentlich alles ziemlich schräg, aber im letzten Jahr hab ich mal geschrieben das ich hoffe das die Studie vor dem Crash beendet wird, jetzt sind wird mittendrin und ich kaufe nochmal günstig nach. Auch fein

Antwort auf Beitrag Nr.: 71.557.290 von swoasik am 12.05.22 11:25:40Ich habe vor mit zwei Tranchen zu arbeiten. Die erste zu 0,15 Euro und die Zweite wird bei 0,135 angesetzt.
Mal gucken ob es so kommt.
Da ich bis mind. Mitte Juni nicht mit irgendwelchen News rechne, könnte das auch im Bereich des möglichen liegen.
Wäre der Spread nicht so abartig hoch, hätte ich Teilziel 1 vermutlich schon erreicht…
Mal gucken ob es so kommt.
Da ich bis mind. Mitte Juni nicht mit irgendwelchen News rechne, könnte das auch im Bereich des möglichen liegen.
Wäre der Spread nicht so abartig hoch, hätte ich Teilziel 1 vermutlich schon erreicht…





















