CytomX - ein bahnbrechender Ansatz in der Tumortherapie (Seite 130)
eröffnet am 01.07.16 16:03:16 von
neuester Beitrag 01.05.24 17:27:40 von
neuester Beitrag 01.05.24 17:27:40 von
Beiträge: 1.462
ID: 1.234.534
ID: 1.234.534
Aufrufe heute: 23
Gesamt: 164.217
Gesamt: 164.217
Aktive User: 0
ISIN: US23284F1057 · WKN: A14158 · Symbol: 6C1
3,8720
EUR
+1,68 %
+0,0640 EUR
Letzter Kurs 13:13:50 Tradegate
Neuigkeiten
07.05.24 · globenewswire |
02.05.24 · wO Chartvergleich |
02.05.24 · Sharedeals |
01.05.24 · globenewswire |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,4000 | +49,07 | |
| 1,1600 | +40,52 | |
| 1,3670 | +25,30 | |
| 1,0340 | +23,54 | |
| 6,7100 | +22,00 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 2,5000 | -13,79 | |
| 1,3800 | -20,80 | |
| 0,6700 | -26,58 | |
| 2,1300 | -34,41 | |
| 3,1600 | -38,64 |
Beitrag zu dieser Diskussion schreiben
"CytomX Announces Selection by Bristol-Myers Squibb of First Clinical Candidate Probody From Collaboration
CTLA-4 Probody Moves to IND-Enabling Studies
SOUTH SAN FRANCISCO, Calif., Dec. 13, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that Bristol-Myers Squibb Company has selected a clinical candidate for its CTLA-4 Probody program under the strategic oncology collaboration established in May 2014. Achieving this milestone results in a $2 million payment to CytomX.
“Selecting a candidate for the CTLA-4 Probody program is a pivotal development in our partnership with CytomX Therapeutics and builds on our I.O. leadership,” said Carl Decicco, Ph. D., Head of Discovery at Bristol-Myers Squibb. “We are studying the CTLA-4 Probody for its potential to deliver a next-generation anti-CTLA-4 therapy as we continue to explore transformational immuno-oncology medicines.”
CTLA-4, a clinically validated inhibitory immune checkpoint protein, is the most advanced target from the companies’ collaboration, which now also includes three additional, unnamed targets in discovery.
“Advancing our CTLA-4 Probody program to clinical candidate stage with Bristol-Myers Squibb underscores the potential of the Probody platform to transform the field of immuno-oncology by delivering safer, more effective therapies,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX. “This partnership milestone, taken together with CytomX’s recently filed Investigational New Drug application for CX-072, a wholly owned PD-L1-directed Probody therapeutic, highlights the potential of our innovative platform to deliver a new generation of anti-cancer treatments."
Korrektur: 2mio Dollar upfront
CTLA-4 Probody Moves to IND-Enabling Studies
SOUTH SAN FRANCISCO, Calif., Dec. 13, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that Bristol-Myers Squibb Company has selected a clinical candidate for its CTLA-4 Probody program under the strategic oncology collaboration established in May 2014. Achieving this milestone results in a $2 million payment to CytomX.
“Selecting a candidate for the CTLA-4 Probody program is a pivotal development in our partnership with CytomX Therapeutics and builds on our I.O. leadership,” said Carl Decicco, Ph. D., Head of Discovery at Bristol-Myers Squibb. “We are studying the CTLA-4 Probody for its potential to deliver a next-generation anti-CTLA-4 therapy as we continue to explore transformational immuno-oncology medicines.”
CTLA-4, a clinically validated inhibitory immune checkpoint protein, is the most advanced target from the companies’ collaboration, which now also includes three additional, unnamed targets in discovery.
“Advancing our CTLA-4 Probody program to clinical candidate stage with Bristol-Myers Squibb underscores the potential of the Probody platform to transform the field of immuno-oncology by delivering safer, more effective therapies,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX. “This partnership milestone, taken together with CytomX’s recently filed Investigational New Drug application for CX-072, a wholly owned PD-L1-directed Probody therapeutic, highlights the potential of our innovative platform to deliver a new generation of anti-cancer treatments."
Korrektur: 2mio Dollar upfront
"Außerdem ist davon auszugehen, dass BMS in ihrem anti-CTLA-4-Probody die neueste/wirksamste Antikörpervariante verwendet, da der Probody erst im Anschluss an die neueste anti-CTLA-4-Mab-Generation entwickelt worden...."
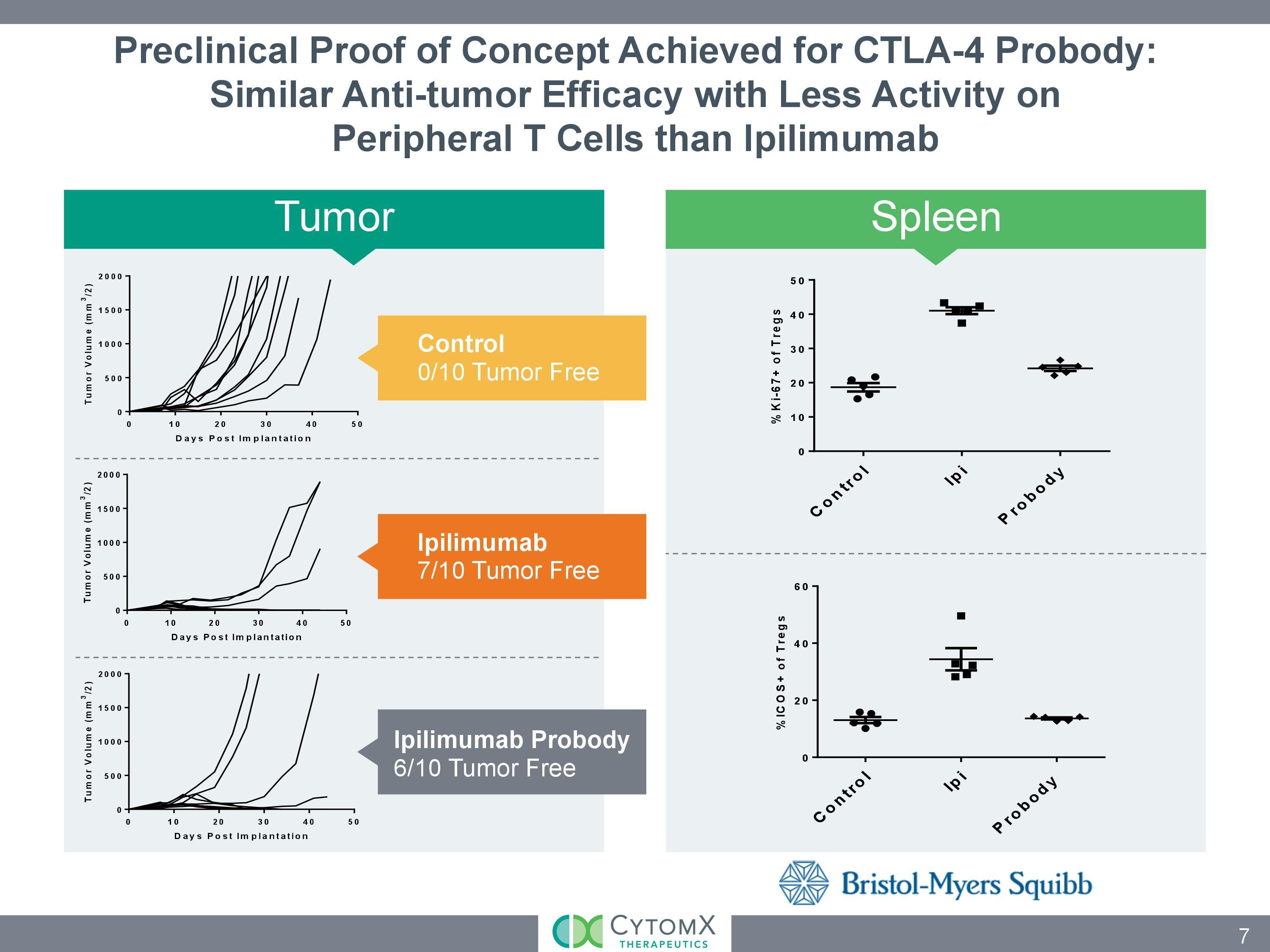
In den letzten Firmenpräsentationen ist vom Ipilimumab-anti-ctl4-probody die Rede.
Insofern bin ich schon davon ausgegangen, daß das laut pipeline-Übersicht (cytomx) kurz vor der klinischen Phase befindliche BMS-cytomx-Produkt auf der weniger wirksamen yervoy/ipilimumab-Basis beruht.
Dieses Produkt hatte ja Ende 2016 die 15 Millionen upfront aufgrund der Festlegung auf den klinischen Kandidaten bedingt.
Vielleicht sind zukünfitge, weniger entwickelte Pipeline-Projekte mit BMS als afucosylierte AB vorgesehen ?
Wie siehst du das, Joschka?
LG
StefanR

In den letzten Firmenpräsentationen ist vom Ipilimumab-anti-ctl4-probody die Rede.
Insofern bin ich schon davon ausgegangen, daß das laut pipeline-Übersicht (cytomx) kurz vor der klinischen Phase befindliche BMS-cytomx-Produkt auf der weniger wirksamen yervoy/ipilimumab-Basis beruht.
Dieses Produkt hatte ja Ende 2016 die 15 Millionen upfront aufgrund der Festlegung auf den klinischen Kandidaten bedingt.
Vielleicht sind zukünfitge, weniger entwickelte Pipeline-Projekte mit BMS als afucosylierte AB vorgesehen ?
Wie siehst du das, Joschka?
LG
StefanR
Antwort auf Beitrag Nr.: 54.780.274 von Joschka Schröder am 22.04.17 11:46:42Zwischenzeitlich habe ich das Patent WO2014/089113A1 in weiten Teilen gelesen. Wirklich empfehlenswert, es gleicht einem gut verständlichen Lehrbuch der Immunonkologie. Darin wird u.a. auch anschaulich beschrieben, auf welchem Weg Medikamentenkandidaten ausgewählt und optimiert werden. Eine sehr aufwendige Angelegenheit, die z.B. Politikern, die über Kosten im Gesundheitssystem sinnieren, wenigstens in Grundzügen bekannt sein sollte.
Zum anti-CTLA-4-Mab der neuen Generation: Durch die Entfukosylierung des Fc-Anteils ist im Wesentlichen die Affinität zu entsprechenden FcRezeptoren und damit die Wirksamkeit des Antikörpers (-> Depletion regulatorischer T-Zellen insbesondere im Tumorgewebe bei gleichzeitiger Stimulation von T-Effektorzellen) gesteigert worden. Eine vergleichbare Technik verwendet Roche´s Schlierener Tochter Gkycart im Rahmen ihrer GycoMAb-Technologie. Da anti-CTLA-Mabs auch gesundes Gewebe binden, dürften gleichzeitig jedoch auch die (autoimmunologischen) Nebenwirkungen zunehmen (-> besonders nachteilig bei Kombitherapien), so dass der tatsächliche Nutzen der Defucosylierung (sieht man einmal von der niedrigeren therapeutischen Antikörperdosis ab) zunächst unklar bleibt. Es ist allerdings zu vermuten, dass BMS den neuen anti-CTLA-4-Mab gegenüber ipilimumab auch in anderer Hinsicht optimiert hat. Einige Optimierungsmöglichkeiten werden in der Patentschrift aufgezeigt.
Was bedeutet das für den anti-CTLA-4-Probody? Eigentlich überhaupt nichts, da durch die Maskierung mittels CytomX´s Probody-Technologie das therapeutische Fenster sämtlicher anti-CTLA-4-Antikörper deutlich erweitert werden sollte. Soweit jedenfalls die Theorie. Außerdem ist davon auszugehen, dass BMS in ihrem anti-CTLA-4-Probody die neueste/wirksamste Antikörpervariante verwendet, da der Probody erst im Anschluss an die neueste anti-CTLA-4-Mab-Generation entwickelt worden ist.
Zum anti-CTLA-4-Mab der neuen Generation: Durch die Entfukosylierung des Fc-Anteils ist im Wesentlichen die Affinität zu entsprechenden FcRezeptoren und damit die Wirksamkeit des Antikörpers (-> Depletion regulatorischer T-Zellen insbesondere im Tumorgewebe bei gleichzeitiger Stimulation von T-Effektorzellen) gesteigert worden. Eine vergleichbare Technik verwendet Roche´s Schlierener Tochter Gkycart im Rahmen ihrer GycoMAb-Technologie. Da anti-CTLA-Mabs auch gesundes Gewebe binden, dürften gleichzeitig jedoch auch die (autoimmunologischen) Nebenwirkungen zunehmen (-> besonders nachteilig bei Kombitherapien), so dass der tatsächliche Nutzen der Defucosylierung (sieht man einmal von der niedrigeren therapeutischen Antikörperdosis ab) zunächst unklar bleibt. Es ist allerdings zu vermuten, dass BMS den neuen anti-CTLA-4-Mab gegenüber ipilimumab auch in anderer Hinsicht optimiert hat. Einige Optimierungsmöglichkeiten werden in der Patentschrift aufgezeigt.
Was bedeutet das für den anti-CTLA-4-Probody? Eigentlich überhaupt nichts, da durch die Maskierung mittels CytomX´s Probody-Technologie das therapeutische Fenster sämtlicher anti-CTLA-4-Antikörper deutlich erweitert werden sollte. Soweit jedenfalls die Theorie. Außerdem ist davon auszugehen, dass BMS in ihrem anti-CTLA-4-Probody die neueste/wirksamste Antikörpervariante verwendet, da der Probody erst im Anschluss an die neueste anti-CTLA-4-Mab-Generation entwickelt worden ist.
Antwort auf Beitrag Nr.: 54.779.191 von Ville7 am 22.04.17 02:18:25Vielen Dank für den Twitter-Link. Es wäre interessant zu wissen, woher Umer Raffat seine Informationen hat (BMS äußert sich dazu bislang öffentlich nicht). In anderen Quellen wird Raffat übrigens (noch?) mit der gegenteiligen Meinung zitiert. Hier eine leicht verdauliche Zusammenfassung des CTLA4-Themas -> http://www.epvantage.com/Universal/View.aspx?type=Story&id=7….
Letztendlich wird BMS beide Antikörper (maskiert und modifiziert/afucosylated) in die Klinik bringen, die Frage wird nur sein, ob BMS tatsächlich zwei derartige Mamut-P1-Studien plant. Wäre jedenfalls ein sehr ungewöhnlicher Aufwand.
Am Wochenende werde ich erst einmal das Patent des modifizierten Mab´s lesen, in dem dessen Präklinik beschrieben sein dürfte.
Spannend bleibt das Thema in jedem Fall.
Letztendlich wird BMS beide Antikörper (maskiert und modifiziert/afucosylated) in die Klinik bringen, die Frage wird nur sein, ob BMS tatsächlich zwei derartige Mamut-P1-Studien plant. Wäre jedenfalls ein sehr ungewöhnlicher Aufwand.
Am Wochenende werde ich erst einmal das Patent des modifizierten Mab´s lesen, in dem dessen Präklinik beschrieben sein dürfte.
Spannend bleibt das Thema in jedem Fall.
Die 531 Patientenstudie ist der andere inhouse BMS anti-ctla 4 mab
https://twitter.com/AndyBiotech/status/855574588796829696
Antwort auf Beitrag Nr.: 54.774.220 von Joschka Schröder am 21.04.17 12:35:21Ja, fand das wording auch etwas irreführend... anyways, bin sehr gespannt auf die weitere Firmenentwicklung und versuche nicht zu nervös zu sein bis zu den ersten klinischen Daten 

Hier noch eine journalistische Zusammenfassung inkl. Konkurrenzsituation:
http://epvantage.com/Universal/View.aspx?type=Story&id=70214…
http://epvantage.com/Universal/View.aspx?type=Story&id=70214…
kleine Korrektur: 1,192 Mrd. USD
Antwort auf Beitrag Nr.: 54.774.220 von Joschka Schröder am 21.04.17 12:35:21Entsprechend sollte es demnächst eine Meilensteinzahlung an CytomX geben. Der CTLA-4 Probody stammt aus der ersten Kooperationsvereinbarung vom Januar 2014 (4 Targets mit Meilensteinzahlungen von bis zu 1,198 Mrd. USD ... da sollten für den ersten Klinikstart schon ein paar Millionen herausspringen).
Antwort auf Beitrag Nr.: 54.772.804 von BReal am 21.04.17 09:49:44
"less potent" ist eigentlich der falsche Begriff. Durch die gezielte Wirkung sollen unerwünschte Nebeneffekte minimiert werden, ohne dass die Wirkung negativ berührt wird (andernfalls könnte man Yervoy einfach niedriger dosieren).
Die Konzeption der Studie ist eindrucksvoll, da setzt jemand früh alles auf eine Karte. Auch wenn sich zu BMS-986218 in den üblichen Datenbanken bislang keine weiteren Angaben finden, müßte es sich um den CTLA-4 Probody Tx handeln.
Zitat von BReal: Bristol-Myers Squibb (BMY) and Cytomx (CTMX) could be working on a less potent version of Yervoy
"less potent" ist eigentlich der falsche Begriff. Durch die gezielte Wirkung sollen unerwünschte Nebeneffekte minimiert werden, ohne dass die Wirkung negativ berührt wird (andernfalls könnte man Yervoy einfach niedriger dosieren).
Die Konzeption der Studie ist eindrucksvoll, da setzt jemand früh alles auf eine Karte. Auch wenn sich zu BMS-986218 in den üblichen Datenbanken bislang keine weiteren Angaben finden, müßte es sich um den CTLA-4 Probody Tx handeln.
02.05.24 · wO Chartvergleich · Ansys |
02.05.24 · Sharedeals · CytomX Therapeutics |
12.03.24 · wO Chartvergleich · Blackbaud (Old) |





















