Heidelberg Pharma AG (Seite 484)
eröffnet am 26.10.17 20:25:27 von
neuester Beitrag 04.05.24 16:22:13 von
neuester Beitrag 04.05.24 16:22:13 von
Beiträge: 5.204
ID: 1.265.064
ID: 1.265.064
Aufrufe heute: 161
Gesamt: 588.458
Gesamt: 588.458
Aktive User: 0
ISIN: DE000A11QVV0 · WKN: A11QVV · Symbol: HPHA
3,0200
EUR
+1,00 %
+0,0300 EUR
Letzter Kurs 03.05.24 Tradegate
Neuigkeiten
25.04.24 · EQS Group AG |
05.04.24 · EQS Group AG |
27.03.24 · EQS Group AG |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 38,27 | +28,16 | |
| 8,0780 | +27,90 | |
| 10,155 | +21,04 | |
| 8,1400 | +20,41 | |
| 3,6100 | +17,51 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,6700 | -26,58 | |
| 2,1300 | -34,41 | |
| 3,1600 | -38,64 | |
| 1,7000 | -49,40 | |
| 125,00 | -95,83 |
Beitrag zu dieser Diskussion schreiben
Antwort auf Beitrag Nr.: 59.766.342 von BICYPAPA am 01.02.19 12:23:50
https://www.nature.com/articles/s41467-018-08201-x.epdf?shar…
Magenta Artikel
Ausführlicher Magenta Artikel brandneu zum CD117 ADChttps://www.nature.com/articles/s41467-018-08201-x.epdf?shar…
Antwort auf Beitrag Nr.: 59.763.369 von BICYPAPA am 01.02.19 07:15:11
Abstract: https://www.ncbi.nlm.nih.gov/pubmed/30703342
Near-comprehensive resequencing of cancer-associated genes in surgically resected metastatic liver tumors of gastric cancer.
Ikari N1, Serizawa A2, Mitani S3, Yamamoto M2, Furukawa T4.
Author information
Abstract
Liver metastasis is a major cause of death in patients with gastric cancer. We evaluated molecular alterations in clinically resected liver metastases of gastric cancer to identify candidate biomarkers and therapeutic targets. Seventy-four patients, including 37 with liver metastasis that underwent gastrectomy and hepatectomy for gastric cancer and 37 without liver metastasis that underwent gastrectomy for gastric cancer, were studied. Next-generation resequencing was performed for 412 cancer-associated genes in metastatic and/or primary tumors from 30 patients and somatic mutations in TP53, LRP1B, PIK3CA, ADAMTS20, PAX7, FN1, FOXO3, WRN, PTEN, ETV4, and RNF213 were found in metastatic tumors. TP53 mutations were studied by Sanger sequencing in remaining patients; the number of patients with TP53 mutations in metastatic tumors was significantly higher among those with liver metastasis (86.5%, 32/37) versus those without liver metastasis (40.5%; 15/37) (P < 0.0001). TP53 mutations in metastatic liver tumors and corresponding primary tumors were identical in 96.9% (31/32), including some patients with heterogeneous primary tumor components. Immunohistochemical analyses showed aberrant p53 expression in tumors with TP53 mutations. In silico functional evaluations indicated functional loss of missense-mutated TP53. Thus, p53 pathway may facilitate the development of biomarkers and therapeutic approaches to treat gastric cancer metastases to the liver.
Prognostischer Biomarker p 53
HP arbeitet zur Zeit an einem prognostischen Biomarker um die Patientgruppe mit p 53 Merkmalen zu erfassen. Hierzu werden in Abstracts immer mehr Anwendungsgebiete angesprochen. Es scheint ein Arbeitsfeld mit einem sehr beträchlichen Umfang und damit auch Potential für HP und seiner Amanitin Behandlungsmöglichkeit zu sein. Abstract: https://www.ncbi.nlm.nih.gov/pubmed/30703342
Near-comprehensive resequencing of cancer-associated genes in surgically resected metastatic liver tumors of gastric cancer.
Ikari N1, Serizawa A2, Mitani S3, Yamamoto M2, Furukawa T4.
Author information
Abstract
Liver metastasis is a major cause of death in patients with gastric cancer. We evaluated molecular alterations in clinically resected liver metastases of gastric cancer to identify candidate biomarkers and therapeutic targets. Seventy-four patients, including 37 with liver metastasis that underwent gastrectomy and hepatectomy for gastric cancer and 37 without liver metastasis that underwent gastrectomy for gastric cancer, were studied. Next-generation resequencing was performed for 412 cancer-associated genes in metastatic and/or primary tumors from 30 patients and somatic mutations in TP53, LRP1B, PIK3CA, ADAMTS20, PAX7, FN1, FOXO3, WRN, PTEN, ETV4, and RNF213 were found in metastatic tumors. TP53 mutations were studied by Sanger sequencing in remaining patients; the number of patients with TP53 mutations in metastatic tumors was significantly higher among those with liver metastasis (86.5%, 32/37) versus those without liver metastasis (40.5%; 15/37) (P < 0.0001). TP53 mutations in metastatic liver tumors and corresponding primary tumors were identical in 96.9% (31/32), including some patients with heterogeneous primary tumor components. Immunohistochemical analyses showed aberrant p53 expression in tumors with TP53 mutations. In silico functional evaluations indicated functional loss of missense-mutated TP53. Thus, p53 pathway may facilitate the development of biomarkers and therapeutic approaches to treat gastric cancer metastases to the liver.
Antwort auf Beitrag Nr.: 59.689.761 von BICYPAPA am 23.01.19 07:14:11
The Company held cash reserves of $25.668 million at the end of December. Cash outflows relating to operating expenses were $8.503 million, with total spend on direct R&D activities of $5.123 million. Cash outflows from investing activities at $3.672 million include $3.219 million as the cash element of the upfront consideration for the acquisition of Belgium-based Advanced Nuclear Medicine Ingredients (ANMI) SA, which completed on 24 December 2018. Significant activities during the quarter included:
• Scale-up of manufacturing of the 68Ga-PSMA illumetTM cold kit in preparation for US product launch (as an investigational product)
• Conclusion of a distribution agreement with Cardinal Health for the pharmacy preparation and distribution of the 68Ga-PSMA cold kit developed by ANMI SA and commercialised for the US market by Telix USA
• Entering into a strategic collaboration with GenesisCare Pty Ltd in relation to radiation oncology studies as part of Telix’s global multi-centre trials in neuro-oncology and urologic oncology
• Extension of a service agreement with Cyclotek (Aust) Pty Ltd to include TLX250-CDx for imaging patients with clear cell renal cell cancer (ccRCC) using PET
• Completion of the ZIR-DOSE dosimetry bridging study (renal cancer imaging with TLX250-CDx), which demonstrated that the Company’s change of isotope resulted in a meaningfully lower patient radiation dose
• Commencement of the ZIRCON Phase III study in Europe and Australia for TLX250CDx (renal cancer)
• Collaboration with Nihon Medi-Physics Co, a leading manufacturer and supplier of radiopharmaceuticals in Japan, for the feasibility of 225Ac-labeled (actinium) antibodies for the treatment of clear-cell renal cell cancer (ccRCC)
• Completion of first and second stage consultations with the Japanese Pharmaceuticals and Medical Devices Agency (PMDA) for a Phase I/II study of 89Zr-girentuximab (TLX250-CDx) in Japan
• Decision to progress TLX591 to Phase III as the result of data analysis of huJ591 data following the completion of the acquisition of Atlab (September ’18)
• The appointment of Nannette Rich, an experienced executive with a track record of product launch in the nuclear medicine field, as Vice President of Sales & Marketing focussed on the development of Telix’s commercial sales footprint in the US
• Sales of illumetTM (prostate imaging kit) commenced in December 2018
TLX-250 Telix Update
31st January 2019. Telix Pharmaceuticals Limited (ASX:TLX) (“Telix”, the “Company”), a clinical-stage biopharmaceutical company focused on the development of diagnostic and therapeutic products based on targeted radiopharmaceuticals or “molecularlytargeted radiation” (“MTR”), today releases its Appendix 4C for the December 2018 quarter.The Company held cash reserves of $25.668 million at the end of December. Cash outflows relating to operating expenses were $8.503 million, with total spend on direct R&D activities of $5.123 million. Cash outflows from investing activities at $3.672 million include $3.219 million as the cash element of the upfront consideration for the acquisition of Belgium-based Advanced Nuclear Medicine Ingredients (ANMI) SA, which completed on 24 December 2018. Significant activities during the quarter included:
• Scale-up of manufacturing of the 68Ga-PSMA illumetTM cold kit in preparation for US product launch (as an investigational product)
• Conclusion of a distribution agreement with Cardinal Health for the pharmacy preparation and distribution of the 68Ga-PSMA cold kit developed by ANMI SA and commercialised for the US market by Telix USA
• Entering into a strategic collaboration with GenesisCare Pty Ltd in relation to radiation oncology studies as part of Telix’s global multi-centre trials in neuro-oncology and urologic oncology
• Extension of a service agreement with Cyclotek (Aust) Pty Ltd to include TLX250-CDx for imaging patients with clear cell renal cell cancer (ccRCC) using PET
• Completion of the ZIR-DOSE dosimetry bridging study (renal cancer imaging with TLX250-CDx), which demonstrated that the Company’s change of isotope resulted in a meaningfully lower patient radiation dose
• Commencement of the ZIRCON Phase III study in Europe and Australia for TLX250CDx (renal cancer)
• Collaboration with Nihon Medi-Physics Co, a leading manufacturer and supplier of radiopharmaceuticals in Japan, for the feasibility of 225Ac-labeled (actinium) antibodies for the treatment of clear-cell renal cell cancer (ccRCC)
• Completion of first and second stage consultations with the Japanese Pharmaceuticals and Medical Devices Agency (PMDA) for a Phase I/II study of 89Zr-girentuximab (TLX250-CDx) in Japan
• Decision to progress TLX591 to Phase III as the result of data analysis of huJ591 data following the completion of the acquisition of Atlab (September ’18)
• The appointment of Nannette Rich, an experienced executive with a track record of product launch in the nuclear medicine field, as Vice President of Sales & Marketing focussed on the development of Telix’s commercial sales footprint in the US
• Sales of illumetTM (prostate imaging kit) commenced in December 2018
Antwort auf Beitrag Nr.: 59.680.635 von BICYPAPA am 22.01.19 07:21:18
Mesupron ist in China an Link Health auslizensiert.
http://heidelberg-pharma.com/wp-content/uploads/2014/03/2014…" target="_blank" rel="nofollow ugc noopener">http://heidelberg-pharma.com/wp-content/uploads/2014/03/2014…
Für die Entwicklung sind 7 Millionen Euro an Milestones vereinbart. Die Umsatzbeteiligung beträgt einen mittleren einstelligen Prozentbereich, der nach Umsätzen gestaffelt ist.
Für alle restlichen Gebiete ist Redhill der Lizenznehmer für Mesupron. Die Gestaltung ist hier anders wie bei Link Heath. Es wurde eine enorm hohe Umsatzbeteiligung von etwa 15- 30% vereinbart.
http://heidelberg-pharma.com/wp-content/uploads/2014/06/2014…
Vereinbarungen zu Mesupron
Nach der positiven Meldung zu Mesupron Möchte ich doch kurz die wichtigsten Eckdaten zusammen fassen. Nach der Meldung gestern werde ich Mesupron nun auch mehr Aufmerksamkeit schenken.Mesupron ist in China an Link Health auslizensiert.
http://heidelberg-pharma.com/wp-content/uploads/2014/03/2014…" target="_blank" rel="nofollow ugc noopener">http://heidelberg-pharma.com/wp-content/uploads/2014/03/2014…
Für die Entwicklung sind 7 Millionen Euro an Milestones vereinbart. Die Umsatzbeteiligung beträgt einen mittleren einstelligen Prozentbereich, der nach Umsätzen gestaffelt ist.
Für alle restlichen Gebiete ist Redhill der Lizenznehmer für Mesupron. Die Gestaltung ist hier anders wie bei Link Heath. Es wurde eine enorm hohe Umsatzbeteiligung von etwa 15- 30% vereinbart.
http://heidelberg-pharma.com/wp-content/uploads/2014/06/2014…
eidelberg Pharma AG: Heidelberg Pharma erhält Meilensteinzahlung vom Partner Link Health
DGAP-News: Heidelberg Pharma AG / Schlagwort(e): Kooperation
22.01.2019 / 07:02
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber verantwortlich.
PRESSEMELDUNG
Heidelberg Pharma erhält Meilensteinzahlung vom Partner Link Health
Ladenburg, 22. Januar 2019 - Die Heidelberg Pharma AG (FWB: WL6) gab heute bekannt, dass sie von ihrem Kooperationspartner Link Health Co., Guangzhou, China, eine Meilensteinzahlung erhalten hat. Hintergrund ist die Genehmigung der chinesischen Behörde für Lebensmittel- und Arzneimittelsicherheit (National Medical Product Administration - NMPA) für die Durchführung von klinischen Studien mit dem Produktkandidaten MESUPRON(R).
Die Genehmigung erfolgte nach den neuen Regularien der NMPA, welche eine Nutzung der Sicherheitsdaten aus den früheren Studien mit MESUPRON(R) zulassen und damit unmittelbar die Durchführung einer Phase II-Studie möglich machen können. Aufgrund der neuen regulatorischen Situation muss dazu aber eine Überarbeitung des klinischen Studienprotokolls durch Link Health erfolgen. Diese ist in den kommenden Monaten geplant.
Informationen über MESUPRON(R) und das uPA-Programm
Der uPA-Inhibitor MESUPRON(R) (INN: Upamostat) hemmt das Urokinase Plasminogen Aktivator (uPA)-System. 2014 wurden die Rechte zur Entwicklung und Kommerzialisierung von MESUPRON(R) an Link Health Co., Guangzhou, China, für die Region China, Hong Kong, Taiwan und Macao auslizenziert. Grundlage dafür waren Daten aus zwei Phase IIa-Studien in den Indikationen lokal-fortgeschrittener Bauchspeicheldrüsenkrebs (2010) und metastasierter Brustkrebs (2012), die Sicherheit und Aktivität des Medikamentenkandidaten in Kombination mit Chemotherapeutika gezeigt haben. Das Wirkprinzip des MESUPRON(R) könnte einen neuen Behandlungsansatz durch spezifische Blockierung der Metastasierung bei soliden Tumoren bilden.
Über Heidelberg Pharma
Die Heidelberg Pharma AG ist ein biopharmazeutisches Unternehmen mit Sitz in Ladenburg. Heidelberg Pharma ist auf Onkologie spezialisiert und das erste Unternehmen, das den Wirkstoff Amanitin für die Verwendung bei Krebstherapien einsetzt und entwickelt. Dafür verwendet das Unternehmen seine innovative ATAC-Technologie (Antibody Targeted Amanitin Conjugates) und nutzt den biologischen Wirkmechanismus des Toxins als neues therapeutisches Prinzip. Diese proprietäre Technologieplattform wird für die Entwicklung eigener therapeutischer Antikörper-Amanitin-Konjugate sowie im Rahmen von Kooperationen mit externen Partnern eingesetzt, um eine Vielzahl von ATAC-Kandidaten zu erzeugen. Der am weitesten fortgeschrittene eigene Produktkandidat HDP-101 ist ein BCMA-ATAC für die Indikation Multiples Myelom.
Die Heidelberg Pharma AG hat die klinischen Produktkandidaten MESUPRON(R) und REDECTANE(R) zur Weiterentwicklung und Kommerzialisierung verpartnert. Das Unternehmen ist an der Frankfurter Wertpapierbörse notiert: ISIN DE000A11QVV0 / WKN A11QVV / Symbol WL6. Weitere Informationen finden Sie unter http://www.heidelberg-pharma.com/.
Über Link Health Group
Link Health ist ein führendes chinesisches Pharmaunternehmen mit Sitz in Südchina, das sich auf die Entwicklung innovativer Medikamente mit hohem medizinischen Bedarf konzentriert.
Link Health hat ein hochprofessionelles Team mit vielfältiger Expertise in den Bereichen Arzneimittelentwicklung, medizinische Angelegenheiten und Zulassungsfragen zusammengestellt. Link Health verfügt über ein tiefes Verständnis des chinesischen Marktes, ein günstiges regulatorisches Umfeld und ein starkes Netzwerk mit globalen biopharmazeutischen Unternehmen und ist gut positioniert, um innovative Medikamente effizient auf den Markt zu bringen. Mehr Informationen unter: http://www.healthinlink.com.
Kontakt
Heidelberg Pharma AG
Sylvia Wimmer
Tel.: +49 89 41 31 38-29
E-Mail: investors[at]hdpharma.com
Schriesheimer Str. 101, 68526 Ladenburg IR/PR-Unterstützung
MC Services AG
Katja Arnold (CIRO)
Managing Director & Partner
Tel.: +49 89 210 228-40
E-Mail: katja.arnold[at]mc-services.eu
DGAP-News: Heidelberg Pharma AG / Schlagwort(e): Kooperation
22.01.2019 / 07:02
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber verantwortlich.
PRESSEMELDUNG
Heidelberg Pharma erhält Meilensteinzahlung vom Partner Link Health
Ladenburg, 22. Januar 2019 - Die Heidelberg Pharma AG (FWB: WL6) gab heute bekannt, dass sie von ihrem Kooperationspartner Link Health Co., Guangzhou, China, eine Meilensteinzahlung erhalten hat. Hintergrund ist die Genehmigung der chinesischen Behörde für Lebensmittel- und Arzneimittelsicherheit (National Medical Product Administration - NMPA) für die Durchführung von klinischen Studien mit dem Produktkandidaten MESUPRON(R).
Die Genehmigung erfolgte nach den neuen Regularien der NMPA, welche eine Nutzung der Sicherheitsdaten aus den früheren Studien mit MESUPRON(R) zulassen und damit unmittelbar die Durchführung einer Phase II-Studie möglich machen können. Aufgrund der neuen regulatorischen Situation muss dazu aber eine Überarbeitung des klinischen Studienprotokolls durch Link Health erfolgen. Diese ist in den kommenden Monaten geplant.
Informationen über MESUPRON(R) und das uPA-Programm
Der uPA-Inhibitor MESUPRON(R) (INN: Upamostat) hemmt das Urokinase Plasminogen Aktivator (uPA)-System. 2014 wurden die Rechte zur Entwicklung und Kommerzialisierung von MESUPRON(R) an Link Health Co., Guangzhou, China, für die Region China, Hong Kong, Taiwan und Macao auslizenziert. Grundlage dafür waren Daten aus zwei Phase IIa-Studien in den Indikationen lokal-fortgeschrittener Bauchspeicheldrüsenkrebs (2010) und metastasierter Brustkrebs (2012), die Sicherheit und Aktivität des Medikamentenkandidaten in Kombination mit Chemotherapeutika gezeigt haben. Das Wirkprinzip des MESUPRON(R) könnte einen neuen Behandlungsansatz durch spezifische Blockierung der Metastasierung bei soliden Tumoren bilden.
Über Heidelberg Pharma
Die Heidelberg Pharma AG ist ein biopharmazeutisches Unternehmen mit Sitz in Ladenburg. Heidelberg Pharma ist auf Onkologie spezialisiert und das erste Unternehmen, das den Wirkstoff Amanitin für die Verwendung bei Krebstherapien einsetzt und entwickelt. Dafür verwendet das Unternehmen seine innovative ATAC-Technologie (Antibody Targeted Amanitin Conjugates) und nutzt den biologischen Wirkmechanismus des Toxins als neues therapeutisches Prinzip. Diese proprietäre Technologieplattform wird für die Entwicklung eigener therapeutischer Antikörper-Amanitin-Konjugate sowie im Rahmen von Kooperationen mit externen Partnern eingesetzt, um eine Vielzahl von ATAC-Kandidaten zu erzeugen. Der am weitesten fortgeschrittene eigene Produktkandidat HDP-101 ist ein BCMA-ATAC für die Indikation Multiples Myelom.
Die Heidelberg Pharma AG hat die klinischen Produktkandidaten MESUPRON(R) und REDECTANE(R) zur Weiterentwicklung und Kommerzialisierung verpartnert. Das Unternehmen ist an der Frankfurter Wertpapierbörse notiert: ISIN DE000A11QVV0 / WKN A11QVV / Symbol WL6. Weitere Informationen finden Sie unter http://www.heidelberg-pharma.com/.
Über Link Health Group
Link Health ist ein führendes chinesisches Pharmaunternehmen mit Sitz in Südchina, das sich auf die Entwicklung innovativer Medikamente mit hohem medizinischen Bedarf konzentriert.
Link Health hat ein hochprofessionelles Team mit vielfältiger Expertise in den Bereichen Arzneimittelentwicklung, medizinische Angelegenheiten und Zulassungsfragen zusammengestellt. Link Health verfügt über ein tiefes Verständnis des chinesischen Marktes, ein günstiges regulatorisches Umfeld und ein starkes Netzwerk mit globalen biopharmazeutischen Unternehmen und ist gut positioniert, um innovative Medikamente effizient auf den Markt zu bringen. Mehr Informationen unter: http://www.healthinlink.com.
Kontakt
Heidelberg Pharma AG
Sylvia Wimmer
Tel.: +49 89 41 31 38-29
E-Mail: investors[at]hdpharma.com
Schriesheimer Str. 101, 68526 Ladenburg IR/PR-Unterstützung
MC Services AG
Katja Arnold (CIRO)
Managing Director & Partner
Tel.: +49 89 210 228-40
E-Mail: katja.arnold[at]mc-services.eu
Antwort auf Beitrag Nr.: 59.675.877 von Ahwas am 21.01.19 12:26:19
Heidelberg Pharma erhält Meilensteinzahlung vom Partner Link Health
Ladenburg, 22. Januar 2019 - Die Heidelberg Pharma AG (FWB: WL6) gab heute bekannt, dass sie von ihrem Kooperationspartner Link Health Co., Guangzhou, China, eine Meilensteinzahlung erhalten hat. Hintergrund ist die Genehmigung der chinesischen Behörde für Lebensmittel- und Arzneimittelsicherheit (National Medical Product Administration - NMPA) für die Durchführung von klinischen Studien mit dem Produktkandidaten MESUPRON(R).
Die Genehmigung erfolgte nach den neuen Regularien der NMPA, welche eine Nutzung der Sicherheitsdaten aus den früheren Studien mit MESUPRON(R) zulassen und damit unmittelbar die Durchführung einer Phase II-Studie möglich machen können. Aufgrund der neuen regulatorischen Situation muss dazu aber eine Überarbeitung des klinischen Studienprotokolls durch Link Health erfolgen. Diese ist in den kommenden Monaten geplant.
Informationen über MESUPRON(R) und das uPA-Programm
Der uPA-Inhibitor MESUPRON(R) (INN: Upamostat) hemmt das Urokinase Plasminogen Aktivator (uPA)-System. 2014 wurden die Rechte zur Entwicklung und Kommerzialisierung von MESUPRON(R) an Link Health Co., Guangzhou, China, für die Region China, Hong Kong, Taiwan und Macao auslizenziert. Grundlage dafür waren Daten aus zwei Phase IIa-Studien in den Indikationen lokal-fortgeschrittener Bauchspeicheldrüsenkrebs (2010) und metastasierter Brustkrebs (2012), die Sicherheit und Aktivität des Medikamentenkandidaten in Kombination mit Chemotherapeutika gezeigt haben. Das Wirkprinzip des MESUPRON(R) könnte einen neuen Behandlungsansatz durch spezifische Blockierung der Metastasierung bei soliden Tumoren bilden.
Meilensteinzahlung für Mesupron
Mesupron hatten wir schon fast ganz aus den Augen verloren. Eine weitere positive Nachricht jetzt auch mit Mesupron. Heidelberg Pharma erhält Meilensteinzahlung vom Partner Link Health
Ladenburg, 22. Januar 2019 - Die Heidelberg Pharma AG (FWB: WL6) gab heute bekannt, dass sie von ihrem Kooperationspartner Link Health Co., Guangzhou, China, eine Meilensteinzahlung erhalten hat. Hintergrund ist die Genehmigung der chinesischen Behörde für Lebensmittel- und Arzneimittelsicherheit (National Medical Product Administration - NMPA) für die Durchführung von klinischen Studien mit dem Produktkandidaten MESUPRON(R).
Die Genehmigung erfolgte nach den neuen Regularien der NMPA, welche eine Nutzung der Sicherheitsdaten aus den früheren Studien mit MESUPRON(R) zulassen und damit unmittelbar die Durchführung einer Phase II-Studie möglich machen können. Aufgrund der neuen regulatorischen Situation muss dazu aber eine Überarbeitung des klinischen Studienprotokolls durch Link Health erfolgen. Diese ist in den kommenden Monaten geplant.
Informationen über MESUPRON(R) und das uPA-Programm
Der uPA-Inhibitor MESUPRON(R) (INN: Upamostat) hemmt das Urokinase Plasminogen Aktivator (uPA)-System. 2014 wurden die Rechte zur Entwicklung und Kommerzialisierung von MESUPRON(R) an Link Health Co., Guangzhou, China, für die Region China, Hong Kong, Taiwan und Macao auslizenziert. Grundlage dafür waren Daten aus zwei Phase IIa-Studien in den Indikationen lokal-fortgeschrittener Bauchspeicheldrüsenkrebs (2010) und metastasierter Brustkrebs (2012), die Sicherheit und Aktivität des Medikamentenkandidaten in Kombination mit Chemotherapeutika gezeigt haben. Das Wirkprinzip des MESUPRON(R) könnte einen neuen Behandlungsansatz durch spezifische Blockierung der Metastasierung bei soliden Tumoren bilden.
Heidelberg Pharma AG: Vorabbekanntmachung über die Veröffentlichung von Finanzberichten gemäß § 114, 115, 117 WpHG
Heidelberg Pharma AG / Vorabbekanntmachung über die Veröffentlichung von
Rechnungslegungsberichten
21.01.2019 / 11:41
Vorabbekanntmachung über die Veröffentlichung von Finanzberichten gemäß §
114, 115, 117 WpHG übermittelt durch DGAP - ein Service der EQS Group AG.
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber
verantwortlich.
Hiermit gibt die Heidelberg Pharma AG bekannt, dass folgende Finanzberichte
veröffentlicht werden:
Bericht: Jahresfinanzbericht
Veröffentlichungsdatum / Deutsch: 21.03.2019
Veröffentlichungsdatum / Englisch: 21.03.2019
Heidelberg Pharma AG / Vorabbekanntmachung über die Veröffentlichung von
Rechnungslegungsberichten
21.01.2019 / 11:41
Vorabbekanntmachung über die Veröffentlichung von Finanzberichten gemäß §
114, 115, 117 WpHG übermittelt durch DGAP - ein Service der EQS Group AG.
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber
verantwortlich.
Hiermit gibt die Heidelberg Pharma AG bekannt, dass folgende Finanzberichte
veröffentlicht werden:
Bericht: Jahresfinanzbericht
Veröffentlichungsdatum / Deutsch: 21.03.2019
Veröffentlichungsdatum / Englisch: 21.03.2019
Antwort auf Beitrag Nr.: 59.589.491 von BICYPAPA am 09.01.19 08:21:24
AMANITINKONJUGATE
The invention relates to a conjugate comprising (a) an amatoxin comprising (i) an amino acid 4 with a 6'-deoxy position; and (ii) an amino acid 8 with an S-deoxy position; (b) a target-binding moiety; and (c) optionally a linker linking said amatoxin and said target-binding moiety. The invention furthermore relates to a pharmaceutical composition comprising such conjugate.
https://patentscope.wipo.int/search/de/result.jsf
Patentveröffentlichung in Europa
AMANITINKONJUGATE
The invention relates to a conjugate comprising (a) an amatoxin comprising (i) an amino acid 4 with a 6'-deoxy position; and (ii) an amino acid 8 with an S-deoxy position; (b) a target-binding moiety; and (c) optionally a linker linking said amatoxin and said target-binding moiety. The invention furthermore relates to a pharmaceutical composition comprising such conjugate.
https://patentscope.wipo.int/search/de/result.jsf
Antwort auf Beitrag Nr.: 59.580.227 von BICYPAPA am 08.01.19 07:35:24
Redectane-TLX250 oder auch Girentuximab benannt ist von Heidelberg Pharma an Telix auslizensiert.
Es kann in zwei Bereichen der Diagnostik oder auch therapeutisch eingesetzt werden.
In der therapeutischen Anwendung befindet man sich in der Phase 2 und das Ende der Rekrutierung wird etwa Q4 19 erwartet. Sollte die Entwicklung normal verlaufen folgt eine Phase 3 Studie und der Zulassungsprozess. Telix rechnet hier mit Einnahmen von ca 400-500 Millionen$. Erste Einnahmen dürften wir in der herapeutischen Anwendung etwa ab 2023 erwarten. Die Beteiligung für HP beträgt ca 5%.
In der Diagnostik befindet man sich in Phase 3 und das Ende der Rekrutierung wird etwa Q4 19 erwartet. Danach folgt die Auswertung und der Zulassungsprozess. Bitte entnehmt die Einzelheiten der aktuellen Januar Präsentation.
http://www.telixpharma.com/investors/asx-announcements/
Es ist gestern gar nicht so richtig zur Kenntnis genommen worden. Doch die Umsatzschätzung für die diagnostische Anwendung wird auf etwa 250 Millionen $ geschätzt. Dazu kommt dann zusätzlich der gleiche Betrag langfristig wird zusätzliche Indikationen. Die Beteiligung für HP beträgt hier ca 30%. Und man befindet sich nun schon in der Phase 3 . Erste Einnahmen bis zu ca 75 Millionen $ dürften etwa ab 2021 erwartbar sein. Langfristig kommt dann noch der gleiche Betrag für zusätzliche Indikationen dazu, da HP für alle diagnostischen Anwendungen mit Redectane mit etwa 30% beteiligt ist. Zur besseren Visualisierung der Fakten poste ich mal ein Schaubild von Telix dazu. Dies beschreibt jetzt nur die Chancen die HP mit Redectane hat. Mittelfristig können wir hier mit Einnahmen bis zu 100 Millionen € rechnen . Langfristig dürfte eine Verdoppelung dieser Umsatzbeteiligungen möglich sein. Dies noch mal zu Telix und Redectane-TLX250-Girentuximab.
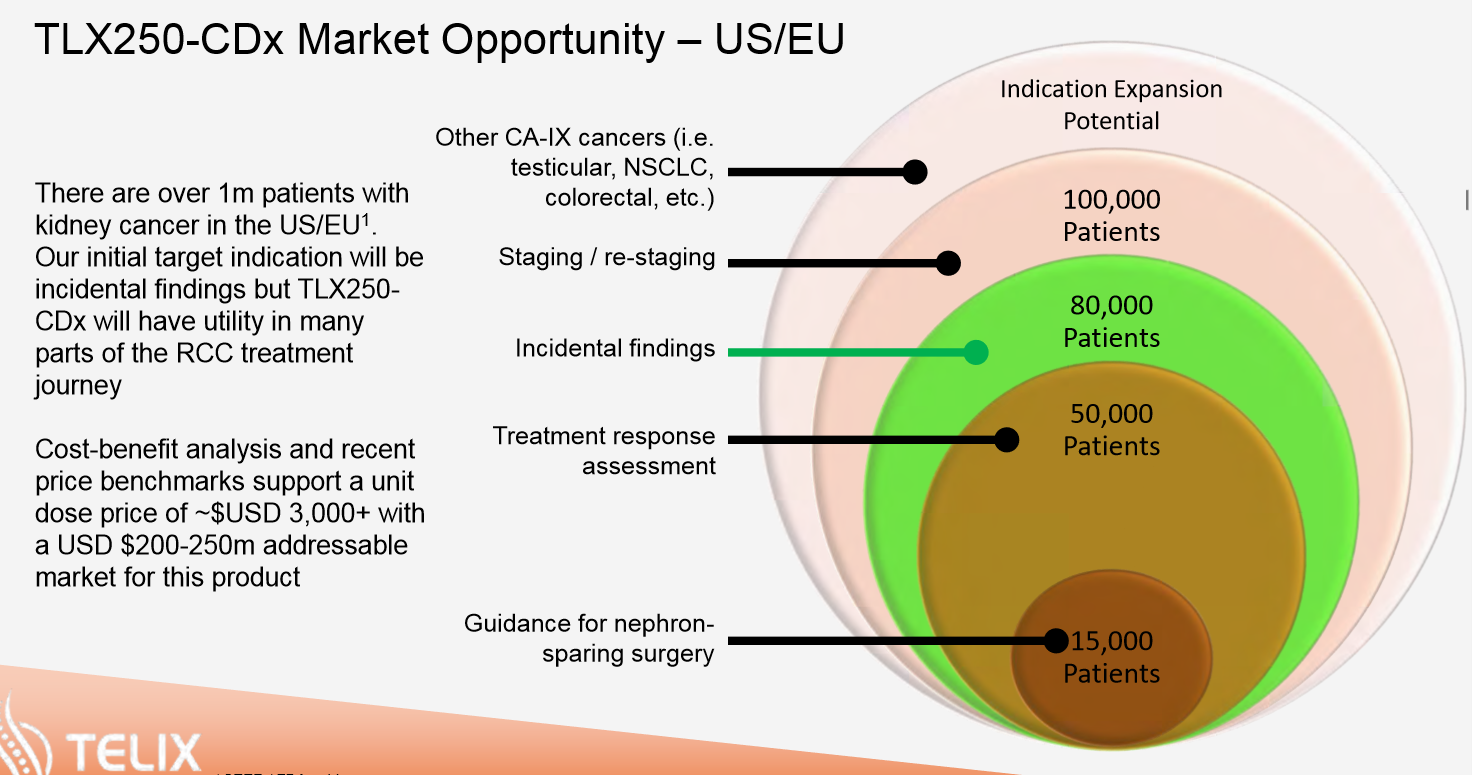
Telix Detailprogramm Januar
Telix macht noch mal eine ganz aktuelle Programmbeschreibung. Es stimmt schon sehr optimistisch, wenn die Prognosen so eintreffen wie in den Schaubildern angekündigt. Ich bitte euch die Präsentation bei Telix anzuschauen. Um sie hier zu posten, dazu ist sie zu umfangreich. Doch zwei drei Sätze und ein wichtiges Bild mit der Prognose möchte ich doch noch posten.Redectane-TLX250 oder auch Girentuximab benannt ist von Heidelberg Pharma an Telix auslizensiert.
Es kann in zwei Bereichen der Diagnostik oder auch therapeutisch eingesetzt werden.
In der therapeutischen Anwendung befindet man sich in der Phase 2 und das Ende der Rekrutierung wird etwa Q4 19 erwartet. Sollte die Entwicklung normal verlaufen folgt eine Phase 3 Studie und der Zulassungsprozess. Telix rechnet hier mit Einnahmen von ca 400-500 Millionen$. Erste Einnahmen dürften wir in der herapeutischen Anwendung etwa ab 2023 erwarten. Die Beteiligung für HP beträgt ca 5%.
In der Diagnostik befindet man sich in Phase 3 und das Ende der Rekrutierung wird etwa Q4 19 erwartet. Danach folgt die Auswertung und der Zulassungsprozess. Bitte entnehmt die Einzelheiten der aktuellen Januar Präsentation.
http://www.telixpharma.com/investors/asx-announcements/
Es ist gestern gar nicht so richtig zur Kenntnis genommen worden. Doch die Umsatzschätzung für die diagnostische Anwendung wird auf etwa 250 Millionen $ geschätzt. Dazu kommt dann zusätzlich der gleiche Betrag langfristig wird zusätzliche Indikationen. Die Beteiligung für HP beträgt hier ca 30%. Und man befindet sich nun schon in der Phase 3 . Erste Einnahmen bis zu ca 75 Millionen $ dürften etwa ab 2021 erwartbar sein. Langfristig kommt dann noch der gleiche Betrag für zusätzliche Indikationen dazu, da HP für alle diagnostischen Anwendungen mit Redectane mit etwa 30% beteiligt ist. Zur besseren Visualisierung der Fakten poste ich mal ein Schaubild von Telix dazu. Dies beschreibt jetzt nur die Chancen die HP mit Redectane hat. Mittelfristig können wir hier mit Einnahmen bis zu 100 Millionen € rechnen . Langfristig dürfte eine Verdoppelung dieser Umsatzbeteiligungen möglich sein. Dies noch mal zu Telix und Redectane-TLX250-Girentuximab.

Danke für die Infos 👍
Eine Frage der Zeit, bis hier eine Neubewertung stattfindet. Erinnert mich irgendwie an Evotec, als der Kurs jahrelang zw. 2-4 Euro verharrte, um dann irgendwann auszubrechen...
Eine Frage der Zeit, bis hier eine Neubewertung stattfindet. Erinnert mich irgendwie an Evotec, als der Kurs jahrelang zw. 2-4 Euro verharrte, um dann irgendwann auszubrechen...
25.04.24 · EQS Group AG · Heidelberg Pharma |
17.04.24 · EQS Group AG · Heidelberg Pharma |
05.04.24 · EQS Group AG · Heidelberg Pharma |
27.03.24 · EQS Group AG · Heidelberg Pharma |
27.03.24 · wO Chartvergleich · Super Micro Computer |



















