CytoDyn $CYDY mit Blockbuster Potential WKN: A0YHA5 (Seite 400)
eröffnet am 04.04.19 22:54:12 von
neuester Beitrag 29.11.23 15:46:05 von
neuester Beitrag 29.11.23 15:46:05 von
Beiträge: 30.091
ID: 1.301.376
ID: 1.301.376
Aufrufe heute: 0
Gesamt: 3.061.291
Gesamt: 3.061.291
Aktive User: 0
ISIN: US23283M1018 · WKN: A0YHA5 · Symbol: 296
0,1510
EUR
+10,22 %
+0,0140 EUR
Letzter Kurs 03.05.24 Stuttgart
Neuigkeiten
29.02.24 · globenewswire |
01.02.24 · globenewswire |
29.01.24 · globenewswire |
21.11.23 · globenewswire |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 38,27 | +28,16 | |
| 8,0780 | +27,90 | |
| 10,155 | +21,04 | |
| 8,1400 | +20,41 | |
| 3,6100 | +17,51 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,6700 | -26,58 | |
| 2,1300 | -34,41 | |
| 3,1600 | -38,64 | |
| 1,7000 | -49,40 | |
| 125,00 | -95,83 |
Beitrag zu dieser Diskussion schreiben
US-amerikanisches FDA-Überprüfungsprotokoll für die Registrierung weiterer kritischer COVID-19-Patienten zur Unterstützung potenzieller EUA
CytoDyn reichte bei der US-amerikanischen FDA ein Protokoll zur sofortigen Registrierung von 140 kritischen COVID-19-Patienten mit denselben Standorten wie in der CD12-Studie ein. Die Registrierung beginnt nach FDA-Kommentaren
VANCOUVER, Washington, 6. März 2021 (GLOBE NEWSWIRE) - CytoDyn Inc. (OTC.QB: CYDY) („CytoDyn“ oder das „Unternehmen“), ein Biotechnologieunternehmen im Spätstadium, das Vyrologix ™ (leronlimab-PRO 140) entwickelt ), ein CCR5-Antagonist mit dem Potenzial für mehrere therapeutische Indikationen, kündigte heute mehrere regulatorische Wege für die Zulassung von Leronlimab zur Behandlung kritischer COVID-19-Patienten in den USA, Großbritannien und Kanada an.
MHRA hat dem Unternehmen mitgeteilt, dass es weitere Daten aus dem Open-Label-Teil der aktuellen CD12-Studie akzeptieren wird. Bisher wurden weitere 46 Patienten aufgenommen, die Ergebnisse wurden jedoch noch keiner Behörde mitgeteilt.
Das Unternehmen geht davon aus, dass die Health Canada Interim Order (IO) es dem Unternehmen ermöglichen könnte, Leronlimab in Kanada zu verkaufen, während weitere kritische COVID-19-Patienten eingeschlossen werden. Diese Diskussionen dauern an, und das Unternehmen hat den Prozess zur Einreichung eines IO bei Health Canada eingeleitet.
Das Unternehmen bestätigt außerdem, dass die US-amerikanische FDA ihr Protokoll zur Aufnahme von 140 kritisch kranken COVID-19-Patienten erhalten hat, deren primärer Endpunkt als Dauer des Krankenhausaufenthalts definiert ist.
CytoDyn freut sich, starke Daten für kritisch kranke COVID-19-Patienten zu zeigen. In Anbetracht der Tatsache, dass:
(1) Ein höherer Anteil von Patienten über 65 wurde in den Leronlimab-Arm aufgenommen (33%) als in den Placebo-Arm (23%), und (2) Von den 384 behandelten Patienten waren 117 über 65 mit einer Gesamtmortalitätsrate von 3,5 mal höher (42% - 49/117) als bei Patienten unter 65 (12% - 31/267).
Daher wurde eine "Altersanpassungs" -Analyse durchgeführt, und folglich lauten die aktualisierten Ergebnisse der primären Endpunktanalyse wie folgt:
1) Statistisch signifikante Ergebnisse (p-Wert = 0,0319) für den primären Endpunkt (Gesamtmortalität am Tag 28) bei Teilnehmern, die Leronlimab + „häufig verwendete COVID-19-Behandlungen“ erhielten, im Vergleich zu Teilnehmern, die „häufig verwendete COVID-19“ erhielten Behandlungen “allein in der Placebo-Gruppe in der gesamten modifizierten Intent-to-Treat-Population („ mITT “).
2) Statistisch signifikante Ergebnisse (p-Wert = 0,0552) für den primären Endpunkt (Gesamtmortalität am Tag 28) bei Teilnehmern, die Dexamethason als vorherige oder begleitende Standardbehandlung („SoC“) für COVID-19 erhalten haben, im Vergleich zu Patienten, die Dexamethason (ohne Leronlimab) als SoC-Therapie in der gesamten mITT-Population erhielten.
3) Unter allen Patienten in mITT war der primäre Endpunkt (Gesamtmortalität am Tag 28) statistisch nicht signifikant. Bei der Altersanpassung lag der primäre Endpunkt viel näher am statistisch signifikanten Wert. Bemerkenswert ist, dass die Verringerung der Mortalität in dieser Population von 65 Jahren und im jüngeren Leronlimab-Arm mehr als 30% weniger Mortalität als bei Placebo und 9% weniger Mortalität bei Teilnehmern über 65 Jahren aufwies.
Bei der Altersanpassungsanalyse in allen anderen wichtigen sekundären Endpunkten bestand eine konsistente numerische Überlegenheit gegenüber der Placebogruppe, wobei sich einige sekundäre Endpunkte der statistischen Signifikanz näherten.
Nader Pourhassan, Ph.D., Präsident und Chief Executive Officer von CytoDyn, kommentierte: „Wir sind dankbar für die Möglichkeit, kritisch kranken COVID-19-Patienten zu helfen. Wir sind weiterhin zufrieden mit den Ergebnissen von über 80 EINDs, 394 Patienten in CD12 und weiteren 46 Patienten bei der Fortsetzung des Open-Arm-Zugangs von CD12 sowie den Ergebnissen, die in zwei verschiedenen Fachzeitschriften veröffentlicht wurden. Ich bin demütig über die Kommentare der Familien, deren Leben ihrer Meinung nach mit Leronlimab gerettet wurde, und wir freuen uns darauf, Leronlimab für die Behandlung von Patienten mit COVID-19 und vielen anderen Indikationen, an denen wir arbeiten, leichter verfügbar zu machen. Ich freue mich darauf, am Montag vor unserer Investment-Community zu sprechen und unserem gesamten erweiterten Team zu der unermüdlichen Unterstützung des Leronlimab-Programms zu gratulieren. “
CytoDyn reichte bei der US-amerikanischen FDA ein Protokoll zur sofortigen Registrierung von 140 kritischen COVID-19-Patienten mit denselben Standorten wie in der CD12-Studie ein. Die Registrierung beginnt nach FDA-Kommentaren
VANCOUVER, Washington, 6. März 2021 (GLOBE NEWSWIRE) - CytoDyn Inc. (OTC.QB: CYDY) („CytoDyn“ oder das „Unternehmen“), ein Biotechnologieunternehmen im Spätstadium, das Vyrologix ™ (leronlimab-PRO 140) entwickelt ), ein CCR5-Antagonist mit dem Potenzial für mehrere therapeutische Indikationen, kündigte heute mehrere regulatorische Wege für die Zulassung von Leronlimab zur Behandlung kritischer COVID-19-Patienten in den USA, Großbritannien und Kanada an.
MHRA hat dem Unternehmen mitgeteilt, dass es weitere Daten aus dem Open-Label-Teil der aktuellen CD12-Studie akzeptieren wird. Bisher wurden weitere 46 Patienten aufgenommen, die Ergebnisse wurden jedoch noch keiner Behörde mitgeteilt.
Das Unternehmen geht davon aus, dass die Health Canada Interim Order (IO) es dem Unternehmen ermöglichen könnte, Leronlimab in Kanada zu verkaufen, während weitere kritische COVID-19-Patienten eingeschlossen werden. Diese Diskussionen dauern an, und das Unternehmen hat den Prozess zur Einreichung eines IO bei Health Canada eingeleitet.
Das Unternehmen bestätigt außerdem, dass die US-amerikanische FDA ihr Protokoll zur Aufnahme von 140 kritisch kranken COVID-19-Patienten erhalten hat, deren primärer Endpunkt als Dauer des Krankenhausaufenthalts definiert ist.
CytoDyn freut sich, starke Daten für kritisch kranke COVID-19-Patienten zu zeigen. In Anbetracht der Tatsache, dass:
(1) Ein höherer Anteil von Patienten über 65 wurde in den Leronlimab-Arm aufgenommen (33%) als in den Placebo-Arm (23%), und (2) Von den 384 behandelten Patienten waren 117 über 65 mit einer Gesamtmortalitätsrate von 3,5 mal höher (42% - 49/117) als bei Patienten unter 65 (12% - 31/267).
Daher wurde eine "Altersanpassungs" -Analyse durchgeführt, und folglich lauten die aktualisierten Ergebnisse der primären Endpunktanalyse wie folgt:
1) Statistisch signifikante Ergebnisse (p-Wert = 0,0319) für den primären Endpunkt (Gesamtmortalität am Tag 28) bei Teilnehmern, die Leronlimab + „häufig verwendete COVID-19-Behandlungen“ erhielten, im Vergleich zu Teilnehmern, die „häufig verwendete COVID-19“ erhielten Behandlungen “allein in der Placebo-Gruppe in der gesamten modifizierten Intent-to-Treat-Population („ mITT “).
2) Statistisch signifikante Ergebnisse (p-Wert = 0,0552) für den primären Endpunkt (Gesamtmortalität am Tag 28) bei Teilnehmern, die Dexamethason als vorherige oder begleitende Standardbehandlung („SoC“) für COVID-19 erhalten haben, im Vergleich zu Patienten, die Dexamethason (ohne Leronlimab) als SoC-Therapie in der gesamten mITT-Population erhielten.
3) Unter allen Patienten in mITT war der primäre Endpunkt (Gesamtmortalität am Tag 28) statistisch nicht signifikant. Bei der Altersanpassung lag der primäre Endpunkt viel näher am statistisch signifikanten Wert. Bemerkenswert ist, dass die Verringerung der Mortalität in dieser Population von 65 Jahren und im jüngeren Leronlimab-Arm mehr als 30% weniger Mortalität als bei Placebo und 9% weniger Mortalität bei Teilnehmern über 65 Jahren aufwies.
Bei der Altersanpassungsanalyse in allen anderen wichtigen sekundären Endpunkten bestand eine konsistente numerische Überlegenheit gegenüber der Placebogruppe, wobei sich einige sekundäre Endpunkte der statistischen Signifikanz näherten.
Nader Pourhassan, Ph.D., Präsident und Chief Executive Officer von CytoDyn, kommentierte: „Wir sind dankbar für die Möglichkeit, kritisch kranken COVID-19-Patienten zu helfen. Wir sind weiterhin zufrieden mit den Ergebnissen von über 80 EINDs, 394 Patienten in CD12 und weiteren 46 Patienten bei der Fortsetzung des Open-Arm-Zugangs von CD12 sowie den Ergebnissen, die in zwei verschiedenen Fachzeitschriften veröffentlicht wurden. Ich bin demütig über die Kommentare der Familien, deren Leben ihrer Meinung nach mit Leronlimab gerettet wurde, und wir freuen uns darauf, Leronlimab für die Behandlung von Patienten mit COVID-19 und vielen anderen Indikationen, an denen wir arbeiten, leichter verfügbar zu machen. Ich freue mich darauf, am Montag vor unserer Investment-Community zu sprechen und unserem gesamten erweiterten Team zu der unermüdlichen Unterstützung des Leronlimab-Programms zu gratulieren. “
Dr. Nader Pourhassan Discusses Leronlimab Phase III Trial Data For Severe to Critical COVID Patients
CytoDyn to File Accelerated Rolling Review with MHRA and Interim Order (IO) with Health Canada for COVID-19
https://www.cytodyn.com/newsroom/press-releases/detail/503/c…
Ist euch eigentlich aufgefallen WIEVIEL Wirbel um die Ergebnisse gemacht wird? Wozu die Aufregung, wozu die Zahlenschieberei? Geht es um pure Rechthaberei? Dann könnten die Kontra doch jetzt ganz genüsslich abwarten und bei einem negativen Bescheid sagen: Schaut her, wir haben es euch gleich gesagt. Wozu also die Aufregung?
Die einzige Erklärung ist mich die blanke Panik unter den Shortern. Die letzten Chancen zur Verunsicherung sollen genutzt werden um die Verluste möglichst klein zu halten, indem man Kleininvestoren etwas suggeriert damit diese noch schnell ihre Aktien auf den Markt werfen.
Entweder ist es so oder eben doch nur Rechthaberei. Aber so viele wie jetzt gleichzeitig aus den Löchern gekrochen kommen, können keine Rechthaber sein. Also bleibt doch nur die Short-Variante.
Oder einer der Kontras beantwortet endlich mal überzeugend die Frage wieso so vehement gegen eine Zulassung gestritten wird, obwohl doch in wenigen Tagen klar ist was passieren wird.
Das Ergebnis kann niemand mehr beeinflussen. Nur noch ein paar Investoren können verunsichert werden. Mehr nicht.
Die einzige Erklärung ist mich die blanke Panik unter den Shortern. Die letzten Chancen zur Verunsicherung sollen genutzt werden um die Verluste möglichst klein zu halten, indem man Kleininvestoren etwas suggeriert damit diese noch schnell ihre Aktien auf den Markt werfen.
Entweder ist es so oder eben doch nur Rechthaberei. Aber so viele wie jetzt gleichzeitig aus den Löchern gekrochen kommen, können keine Rechthaber sein. Also bleibt doch nur die Short-Variante.
Oder einer der Kontras beantwortet endlich mal überzeugend die Frage wieso so vehement gegen eine Zulassung gestritten wird, obwohl doch in wenigen Tagen klar ist was passieren wird.
Das Ergebnis kann niemand mehr beeinflussen. Nur noch ein paar Investoren können verunsichert werden. Mehr nicht.
In ein paar Tagen oder Stunden wissen wir wer Recht hatte.....Entweder Gewinne oder Verlust. Im bin weiter sehr positiv und kann mir nicht vorstellen das es eine Mogelei war dazu haben Ärzte und Krankenhäuser zuviel Wirbel gemacht. Ich könnte mir eher vorstellen das BP da die Hände drauf hat und Newcomer den Weg erschweren wollen. Time will tell
Antwort auf Beitrag Nr.: 67.344.615 von Theta87 am 06.03.21 22:14:07
Was soll es sonst sein, wenn keine Absicht? Aus Versehen nicht veröffentlicht? Vergessen? Vom Hund gefressen?
Vor allem, wieso traust Du ihm das nicht zu? Er geht seit Jahren genau so vor, dass er sämtliches Negatives verschweigt und das Bisschen, was sich halbwegs gut anhört, ausschmückt bis zum Letzten.
Er hat das gleiche bei CD10 durchgezogen, bis heute. Die "impressive Results" sind 6 Monate her. Ergebnisse zu den verfehlten Endpunkten oder Details, Fehlanzeige
Am 20.09.2020 meldete Cytodyn, dass die Phase 3 der HIV-Monostudie abgeschlossen sei.
Die Ergebnisse waren offensichtlich so schlecht, dass man nichtmal Teilergebnisse nach Datamining veröffentlichte.
Auch sonst wird regelmäßig alles negative, wie z. B. gescheiterte Gespräche, verschwiegen.
Zitat von Theta87: .... Sauer wäre ich, wenn Nader die Severe Daten absichtlich zurückgehalten hätte, weil man auch hier weit von klinischer Signifkanz entfernt wäre. Das traue ich ihm aber irgendwie nicht zu und dafür glaube ich zu sehr an die Wirkung von LL.
Was soll es sonst sein, wenn keine Absicht? Aus Versehen nicht veröffentlicht? Vergessen? Vom Hund gefressen?
Vor allem, wieso traust Du ihm das nicht zu? Er geht seit Jahren genau so vor, dass er sämtliches Negatives verschweigt und das Bisschen, was sich halbwegs gut anhört, ausschmückt bis zum Letzten.
Er hat das gleiche bei CD10 durchgezogen, bis heute. Die "impressive Results" sind 6 Monate her. Ergebnisse zu den verfehlten Endpunkten oder Details, Fehlanzeige
Am 20.09.2020 meldete Cytodyn, dass die Phase 3 der HIV-Monostudie abgeschlossen sei.
Die Ergebnisse waren offensichtlich so schlecht, dass man nichtmal Teilergebnisse nach Datamining veröffentlichte.
Auch sonst wird regelmäßig alles negative, wie z. B. gescheiterte Gespräche, verschwiegen.
Antwort auf Beitrag Nr.: 67.344.672 von sunny3999 am 06.03.21 22:21:34👍 Danke Theta...
Antwort auf Beitrag Nr.: 67.344.615 von Theta87 am 06.03.21 22:14:07
Dr. Bruce Patterson sprach eindeutig von positiven Ergebnissen aus seiner Analyse zu Leronlimab MOA!
Warum sollen die jetzt plötzlich nicht mehr gelten - es gibt ausreichend Studien und Abhandlungen dazu.
Ganz herzlichen Dank an Dich Theta - Super analysiert und zusammengefasst
Hier nochmal zur Erinnerung an Alle als der Kurs letztes Jahr die 10 anvisierte!Dr. Bruce Patterson sprach eindeutig von positiven Ergebnissen aus seiner Analyse zu Leronlimab MOA!
Warum sollen die jetzt plötzlich nicht mehr gelten - es gibt ausreichend Studien und Abhandlungen dazu.
Antwort auf Beitrag Nr.: 67.344.048 von sunny3999 am 06.03.21 20:46:11So auf Sunnys Wunsch (und eigenes Interesse) und da die Kinder und Frau im Bett sind, hatte ich nochmal Zeit mir Gedanken zu machen und Excel anzuschmeißen:
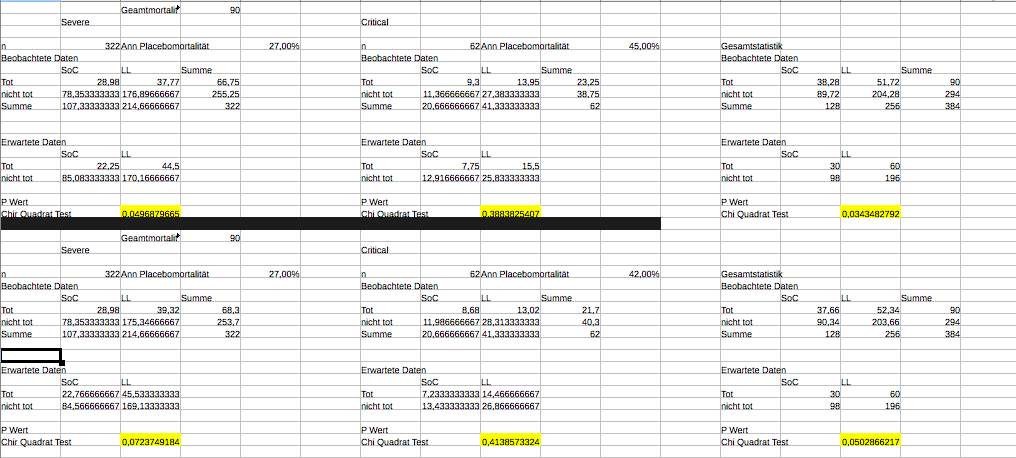
Also eins vorweg: Heute morgen habe ich eine Fehler bei der Sterblichkeit im LL Arm bei Criticals gemacht. Danke an Rangerheim, der mir meinen Fehler erklärt hat, auch wenn ich ein wenig brauchte, um es zu schnallen
So komme ich so ziemlich auf das gleiche Ergebnis wie Iwx92. Ich habe libre office und calc kann keinen exakten fisher Test als Vorlage, daher wieder nur die ChiQuadratVerteilung bei mir. Ich bin nun sogar noch ein Schritt weitergegangen. Denn meines Erachtens wurde ja außer Acht gelassen, dass man ja auch eine Gesamtstatistik machen kann.
Meine Beobachtungen: Bei 27 % Severe SoC Mortalität braucht man 45% SoC Critical Mortaliät. Letzteres halte ich für zu hoch gegriffen. Bei etwas realistischeren 40% SoC Critical Mortalität würden 28% bei den Severes reichen. Der Gesamttrail wäre signifikant.
Interesant ist dann ein Szenario wie unten im Bild, jede einzelne Zielgruppe ist nicht signifkant, der Gesamttrail schon.
Aber Achtung: Alles ist letztlich nur eine Vermutung, da wir die absoluten Daten nicht haben.
Mein Schluss:
Schreibt die Severes nicht ab und habt auch den gesamten Trail im Blick. Aber wenn noch etwas positives kommt, dann wird das eine enge Kiste. Da wir aber noch nichts von den Severes wissen, könnte es sein, dass es knapp nicht gereicht hat. Die Frage ist natürlich: Reicht dann klinische Relevanz (für eine Untergruppe oder den Gesamttrail) für eine EUA?
Allerdings gebe ich auch zu bedenken: Nader sagte vor 2 Wochen noch, dass er die Daten nicht kommunzieren könne, wenn die Severes ebenso weit von statistischer signifkant entfernt wären, warum hätte man dann Stillschweigen bewahren müssen?
Und noch etwas Persönliches:
Ich finde das manch eine Kritik heute überzogen war. Aber überzogener Optimismus ist ebenso leider Fehl am Platz. Außerdem sieht man hier ganz gut, dass man mit Statistik auch einiges machen kann, indem man aufteilt&wieder zusammenfügt. Ohne alle Daten zu kennen, ist es doch irgendwie stochern im Nebel. Sicher ist nur, dass es zu wenig Criticals für stat. Signifikanz waren. Warum wir noch nicht alle notwendigen Daten haben - keine Ahnung & tatsächlich ärgerlich, wenn hier kein gewichtiger Grund vorliegt. Panisch verkaufen werde ich am Montag daher mit Sicherheit nicht. Enttäuscht bin ich schon, hätte natürlich mit mehr gerechnet. Sauer wäre ich, wenn Nader die Severe Daten absichtlich zurückgehalten hätte, weil man auch hier weit von klinischer Signifkanz entfernt wäre. Das traue ich ihm aber irgendwie nicht zu und dafür glaube ich zu sehr an die Wirkung von LL.

Also eins vorweg: Heute morgen habe ich eine Fehler bei der Sterblichkeit im LL Arm bei Criticals gemacht. Danke an Rangerheim, der mir meinen Fehler erklärt hat, auch wenn ich ein wenig brauchte, um es zu schnallen

So komme ich so ziemlich auf das gleiche Ergebnis wie Iwx92. Ich habe libre office und calc kann keinen exakten fisher Test als Vorlage, daher wieder nur die ChiQuadratVerteilung bei mir. Ich bin nun sogar noch ein Schritt weitergegangen. Denn meines Erachtens wurde ja außer Acht gelassen, dass man ja auch eine Gesamtstatistik machen kann.
Meine Beobachtungen: Bei 27 % Severe SoC Mortalität braucht man 45% SoC Critical Mortaliät. Letzteres halte ich für zu hoch gegriffen. Bei etwas realistischeren 40% SoC Critical Mortalität würden 28% bei den Severes reichen. Der Gesamttrail wäre signifikant.
Interesant ist dann ein Szenario wie unten im Bild, jede einzelne Zielgruppe ist nicht signifkant, der Gesamttrail schon.
Aber Achtung: Alles ist letztlich nur eine Vermutung, da wir die absoluten Daten nicht haben.
Mein Schluss:
Schreibt die Severes nicht ab und habt auch den gesamten Trail im Blick. Aber wenn noch etwas positives kommt, dann wird das eine enge Kiste. Da wir aber noch nichts von den Severes wissen, könnte es sein, dass es knapp nicht gereicht hat. Die Frage ist natürlich: Reicht dann klinische Relevanz (für eine Untergruppe oder den Gesamttrail) für eine EUA?
Allerdings gebe ich auch zu bedenken: Nader sagte vor 2 Wochen noch, dass er die Daten nicht kommunzieren könne, wenn die Severes ebenso weit von statistischer signifkant entfernt wären, warum hätte man dann Stillschweigen bewahren müssen?
Und noch etwas Persönliches:
Ich finde das manch eine Kritik heute überzogen war. Aber überzogener Optimismus ist ebenso leider Fehl am Platz. Außerdem sieht man hier ganz gut, dass man mit Statistik auch einiges machen kann, indem man aufteilt&wieder zusammenfügt. Ohne alle Daten zu kennen, ist es doch irgendwie stochern im Nebel. Sicher ist nur, dass es zu wenig Criticals für stat. Signifikanz waren. Warum wir noch nicht alle notwendigen Daten haben - keine Ahnung & tatsächlich ärgerlich, wenn hier kein gewichtiger Grund vorliegt. Panisch verkaufen werde ich am Montag daher mit Sicherheit nicht. Enttäuscht bin ich schon, hätte natürlich mit mehr gerechnet. Sauer wäre ich, wenn Nader die Severe Daten absichtlich zurückgehalten hätte, weil man auch hier weit von klinischer Signifkanz entfernt wäre. Das traue ich ihm aber irgendwie nicht zu und dafür glaube ich zu sehr an die Wirkung von LL.
Antwort auf Beitrag Nr.: 67.344.330 von bcgk am 06.03.21 21:31:06
Jetzt wirst du auch noch auf 12 Likes neidisch ?
Ich frage mich wirklich warum du überhaupt mal in Cytodyn investiert hast, wenn seit 2 Jahren die BLA fällig war - ganz ehrlich warum ??
HIV BLA ist für 1ste Jahreshälfte geplant laut Dr. Mahboob, der wird wohl sein Wort halten.
Nash ist in den letzten Zügen der P2, sollte die erfolgreich sein, wird dies wohl in einer erfolgreichen P3 enden - woher kommst du auf 4 Jahre ? Es gibt noch keine P3 Studie von Cytodyn für Nash
Die Realität ist, das Cytodyn die Phase 3 der Covid -19 Studie abgeschlossen hat und OLE für weitere 45 Patienten erhielt.
Dazwischen gab es weder von der DSMC noch der FDA irgendwelche Hinweise einer Änderungen, noch weniger ein Aufforderung Severe zu Critical anzupassen um eine Parität und stat. Signifikanz
zu erreichen.
Dies hätte in jedem Fall kommen können und sollen, dies kann nicht alleine Cytodyn aufgebürdet werden, das nun die stat. Signifikanz aufgrund der geringen Anzahl nicht aussagefähig wäre.
Dann muß FDA die 60 EINDs und die 45 OLE dazu nehmen oder eine EUA Phase 4 geben.
Die Ergebnisse sind zumindest besser was es aktuell am Markt als SOC gibt.
Remdesvir hat EUA und Zulassung bekommen, nach Änderung während der Studie das Patienten 2-3 Tage früher das Krankenhaus verlassen können, Mortalität war gegen 0.
Die anderen Zulassungen sind nicht viel besser, also was will die FDA tun ??
Ein Medikament das Leben retten kann in der Schublade verschwinden lassen oder eine 2te Studie von 6 Monaten aufbürden, wohlwissend das Leronlimab in EINDS und Studien Leben gerettet hat?
Ich bin gespannt was kommt.....wenn alle anderen mit schlechteren Ergebnissen eine EUA/Zulassungen bekommen haben - sollte die Antwort nicht schwer sein....
Zitat von bcgk: Wahnsinn, dass solch ein Unfug 12x geliked wird.
Die BLA ist seit fast zwei Jahren überfällig. Die P3 Studie seit über drei Jahren noch nicht peer-reviewed publiziert.
NASH in den letzten Zügen? P2 gerade gestartet, bis Abschluss P3 kannst du mit ca. 4 Jahren rechnen.
Warum fällt es so schwer der Realität ins Gesicht zu sehen?
Jetzt wirst du auch noch auf 12 Likes neidisch ?
Ich frage mich wirklich warum du überhaupt mal in Cytodyn investiert hast, wenn seit 2 Jahren die BLA fällig war - ganz ehrlich warum ??
HIV BLA ist für 1ste Jahreshälfte geplant laut Dr. Mahboob, der wird wohl sein Wort halten.
Nash ist in den letzten Zügen der P2, sollte die erfolgreich sein, wird dies wohl in einer erfolgreichen P3 enden - woher kommst du auf 4 Jahre ? Es gibt noch keine P3 Studie von Cytodyn für Nash
Die Realität ist, das Cytodyn die Phase 3 der Covid -19 Studie abgeschlossen hat und OLE für weitere 45 Patienten erhielt.
Dazwischen gab es weder von der DSMC noch der FDA irgendwelche Hinweise einer Änderungen, noch weniger ein Aufforderung Severe zu Critical anzupassen um eine Parität und stat. Signifikanz
zu erreichen.
Dies hätte in jedem Fall kommen können und sollen, dies kann nicht alleine Cytodyn aufgebürdet werden, das nun die stat. Signifikanz aufgrund der geringen Anzahl nicht aussagefähig wäre.
Dann muß FDA die 60 EINDs und die 45 OLE dazu nehmen oder eine EUA Phase 4 geben.
Die Ergebnisse sind zumindest besser was es aktuell am Markt als SOC gibt.
Remdesvir hat EUA und Zulassung bekommen, nach Änderung während der Studie das Patienten 2-3 Tage früher das Krankenhaus verlassen können, Mortalität war gegen 0.
Die anderen Zulassungen sind nicht viel besser, also was will die FDA tun ??
Ein Medikament das Leben retten kann in der Schublade verschwinden lassen oder eine 2te Studie von 6 Monaten aufbürden, wohlwissend das Leronlimab in EINDS und Studien Leben gerettet hat?
Ich bin gespannt was kommt.....wenn alle anderen mit schlechteren Ergebnissen eine EUA/Zulassungen bekommen haben - sollte die Antwort nicht schwer sein....





















