Formycon AG - Informationssammelthread (Seite 287)
eröffnet am 14.06.13 10:50:09 von
neuester Beitrag 10.05.24 18:17:27 von
neuester Beitrag 10.05.24 18:17:27 von
Beiträge: 4.406
ID: 1.182.881
ID: 1.182.881
Aufrufe heute: 22
Gesamt: 787.831
Gesamt: 787.831
Aktive User: 0
ISIN: DE000A1EWVY8 · WKN: A1EWVY · Symbol: FYB
42,75
EUR
-0,93 %
-0,40 EUR
Letzter Kurs 10.05.24 Xetra
Neuigkeiten
10.05.24 · AlsterResearch AG |
08.05.24 · wO Newsflash |
08.05.24 · wO Newsflash |
08.05.24 · EQS Group AG |
Werte aus der Branche Nanotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,0800 | +8,00 | |
| 210,00 | +7,69 | |
| 1,3402 | +0,46 | |
| 43,30 | +0,23 | |
| 35,20 | 0,00 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,4300 | -0,69 | |
| 70,50 | -2,08 | |
| 1,7400 | -3,33 | |
| 1,9550 | -4,75 | |
| 0,7075 | -4,84 |
Beitrag zu dieser Diskussion schreiben
die Breite der Studie ist gut, aber den Ausbietungstermin in USA 7/2020 schaffen sie niemals. Vielleicht in Europa (7/2022), aber dafür muss alles glatt gehen. Formycon ist da uneinholbar weiter.
Antwort auf Beitrag Nr.: 59.130.281 von BICYPAPA am 03.11.18 12:40:33
"It is with great satisfaction we can announce that our first clinical trial application has been submitted to the first national regulatory authority. Submission of the applications in the remaining countries will be done over the course of the coming 1-2 months. The start of the trial is planned for March 2019 when we also expect to recruit our first patient. After having demonstrated high similarity in-vitro and in-vivo to the originator, it is with great excitement and confidence that we enter into this pivotal phase III trial with Xlucane", says CEO Martin Åmark.
About the Xplore trial
The Xplore trial is a phase III trial designed to confirm biosimilarity with regards to safety, efficacy and immunogenicity of Xlucane versus Lucentis® in patients with wet form of age-related macular degeneration (wAMD). The study design was developed in consultation with the Food and Drug Administration (FDA) in the United States and the European Medicines Agency (EMA). The primary efficacy end-point of the trial is change in visual acuity after eight weeks of treatment, for which the confidence interval of the difference between Xlucane and Lucentis® needs to fall within a pre-defined equivalence margin. In addition, several secondary endpoints related to efficacy, safety and immunogenicity are followed over the full treatment period of 12 months. The study will involve approx. 600 patients across approx. 150 sites in 16 countries and is expected to support the registration of Xlucane across majority of regions globally. Xbrane has for the Xplore trial contracted the global CRO Syneos Health which has conducted some of the largest trials in recent years in the wAMD patient population. Xbrane will communicate in relation to the progress of the trial at following milestones: first regulatory approval, first patient in, last patient in, top-line data on the primary endpoint and final study report.
About Xlucane
Xlucane is a ranibizumab (Lucentis®) biosimilar candidate developed by Xbrane Biopharma. Xlucane has demonstrated high analytical similarity compared to Lucentis® in a panel of methods in accordance with requirements from EMA and FDA as well as equivalent pharmacokinetic profile and tolerability in-vivo compared to Lucentis®. Xbrane has entered a co-development agreement with STADA Arzneimittel AG regarding Xlucane under which the companies finance the continued development of the product 50/50 and will share the profits from sales and marketing of the product 50/50.
Xbrane-Lucentis
Xbrane Biopharma has submitted its first national Clinical Trial Application (CTA) to the Food and Drug Administration (FDA) in the United States for the start of the Xplore trial for Xlucane, Xbrane Biopharma's lead candidate. This application represents a significant milestone as the product enters the pivotal phase III trial that will support the Marketing Authorization Application. "It is with great satisfaction we can announce that our first clinical trial application has been submitted to the first national regulatory authority. Submission of the applications in the remaining countries will be done over the course of the coming 1-2 months. The start of the trial is planned for March 2019 when we also expect to recruit our first patient. After having demonstrated high similarity in-vitro and in-vivo to the originator, it is with great excitement and confidence that we enter into this pivotal phase III trial with Xlucane", says CEO Martin Åmark.
About the Xplore trial
The Xplore trial is a phase III trial designed to confirm biosimilarity with regards to safety, efficacy and immunogenicity of Xlucane versus Lucentis® in patients with wet form of age-related macular degeneration (wAMD). The study design was developed in consultation with the Food and Drug Administration (FDA) in the United States and the European Medicines Agency (EMA). The primary efficacy end-point of the trial is change in visual acuity after eight weeks of treatment, for which the confidence interval of the difference between Xlucane and Lucentis® needs to fall within a pre-defined equivalence margin. In addition, several secondary endpoints related to efficacy, safety and immunogenicity are followed over the full treatment period of 12 months. The study will involve approx. 600 patients across approx. 150 sites in 16 countries and is expected to support the registration of Xlucane across majority of regions globally. Xbrane has for the Xplore trial contracted the global CRO Syneos Health which has conducted some of the largest trials in recent years in the wAMD patient population. Xbrane will communicate in relation to the progress of the trial at following milestones: first regulatory approval, first patient in, last patient in, top-line data on the primary endpoint and final study report.
About Xlucane
Xlucane is a ranibizumab (Lucentis®) biosimilar candidate developed by Xbrane Biopharma. Xlucane has demonstrated high analytical similarity compared to Lucentis® in a panel of methods in accordance with requirements from EMA and FDA as well as equivalent pharmacokinetic profile and tolerability in-vivo compared to Lucentis®. Xbrane has entered a co-development agreement with STADA Arzneimittel AG regarding Xlucane under which the companies finance the continued development of the product 50/50 and will share the profits from sales and marketing of the product 50/50.
Antwort auf Beitrag Nr.: 59.407.074 von questionmark am 10.12.18 17:40:36ja man kommt jeden Tag billiger rein und auch billiger wieder raus.
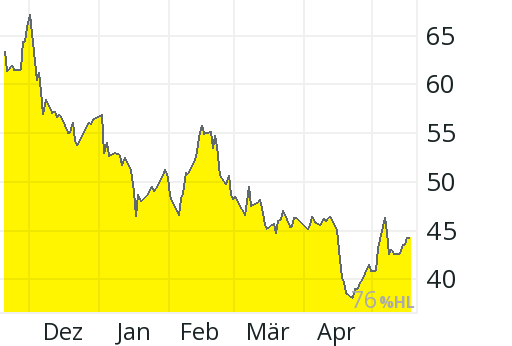
jeden Tag gibt es schönere Kaufkurse.
Ein Elend, ich weiss gar nicht, wann ich nachlaufen soll, ist wohl noch zu früh.
Ein Elend, ich weiss gar nicht, wann ich nachlaufen soll, ist wohl noch zu früh.
Antwort auf Beitrag Nr.: 59.367.464 von Gustl24 am 05.12.18 10:46:00Das sieht mir doch sehr heute nach einer LV-Aktion an den dt. Biotechwerten aus...US-Börsen geschlossen, kann man sich in D bisserl austoben, bei diesen Mikroumsätzen- Training für den Azubi...
Die Indizes relativ neutral und Evotec, Formycon, Medigene etc. ohne kursrelevante Nachrichten alle tief im roten Bereich...
Ein Schelm wer glaubt dies sei ein Zufall
Warten bis die Karawane weiter zieht...
Die Indizes relativ neutral und Evotec, Formycon, Medigene etc. ohne kursrelevante Nachrichten alle tief im roten Bereich...
Ein Schelm wer glaubt dies sei ein Zufall

Warten bis die Karawane weiter zieht...
Das Orderbuch sieht heute recht unschön aus.
Nur eine marginale Situation aber schon bemerkenswert...
Nur eine marginale Situation aber schon bemerkenswert...
Antwort auf Beitrag Nr.: 59.292.918 von questionmark am 25.11.18 11:28:20Keine Frage, sehe es auch allgemein und nicht speziell für Formycon...
Antwort auf Beitrag Nr.: 59.281.426 von ungierig am 22.11.18 22:35:11ich denke, das ist eher eine Marketing-Sache, als ein juristisches Problem.
Die Behören und Kassen wollen Biosimilars, wenn die Patente auslaufen ist alles offen für die neue Konkurrenz, oder gibt es konkrete Vermutungen (auf Formycon bezogen), dass etwas angreifbar wäre?
Die Behören und Kassen wollen Biosimilars, wenn die Patente auslaufen ist alles offen für die neue Konkurrenz, oder gibt es konkrete Vermutungen (auf Formycon bezogen), dass etwas angreifbar wäre?
Antwort auf Beitrag Nr.: 59.277.958 von Popeye82 am 22.11.18 14:57:55Zufällig habe ich heute einen Flyer bekommen mit dem Thema Pro-Biosimilars und ihn zur Seite gelegt. D.h. es wird in der Breite Werbung gemacht für diesen Bereich, dürfte sich auch im Verordnungsverhalten positiv bemerkbar machen. Kostendruck ist immer vorhanden im Gesundheitswesen, allerdings darf man die "alten" Platzhirsche in der Pharmaindustie nicht unterschätzen, die haben gute Anwälte, die können Firmen wie Formycon das Leben richtig schwer machen. Allerdings wenn sie gute Medikamente liefern, werden sie ihren Weg machen und auch die Aktie davon profitieren.
Formycon AG - Informationssammelthread





















