Paratek Pharmaceuticals, Inc. (PRTK) - Antibiotikawert mit Potential - Kurs am 07.11.2018 - 7$ - Die letzten 30 Beiträge
eröffnet am 07.11.18 20:23:41 von
neuester Beitrag 24.08.22 20:01:44 von
neuester Beitrag 24.08.22 20:01:44 von
Beiträge: 29
ID: 1.292.133
ID: 1.292.133
Aufrufe heute: 0
Gesamt: 3.575
Gesamt: 3.575
Aktive User: 0
ISIN: US6993743029 · WKN: A12EGE
2,0900
EUR
+1,95 %
+0,0400 EUR
Letzter Kurs 20.09.23 Lang & Schwarz
Neuigkeiten
05.10.23 · globenewswire |
21.09.23 · globenewswire |
18.09.23 · globenewswire |
12.09.23 · globenewswire |
07.09.23 · globenewswire |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 8,6020 | +105,79 | |
| 17,510 | +45,19 | |
| 1,3300 | +30,51 | |
| 1,8600 | +27,40 | |
| 4,9500 | +25,32 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,7609 | -17,29 | |
| 0,7300 | -17,98 | |
| 0,6999 | -23,87 | |
| 10,180 | -24,31 | |
| 3,0690 | -77,57 |
Beitrag zu dieser Diskussion schreiben
Paratek Pharmaceuticals: Patience Is Wearing Thin
https://seekingalpha.com/article/4536753-paratek-pharmaceuti…
https://seekingalpha.com/article/4536753-paratek-pharmaceuti…
weiß jemand warum die von knapp 1.000 € auf unter 7 € gefallen sind ? o.O
Yes, BARDA contract wurde erweitert , Paratek kann weitere 19 Millionen für expanded Anthrax PEP Development reinholen. Und es gibt noch weiteres Potential das der contract in den nächsten Monaten weitere Ergänzungen erhält Gespräche sind am laufen. D.h. die Wahrscheinlichkeit das PRTK wirklich schuldenfrei und in die Gewinnzone kommt ist ab Ende 2023 als immer höher einzustufen. Ab dann geht es sehr solide weiter und viel Potential ist vorhanden in Pipeline und auch über die Förderprogramme und Gesetzesvorhaben in US um Reserve für den Fall der Fälle zu haben und den Unternehmen zum überleben ein gutes Einkommen zu sichern.
Bin wieder hier mit dabei. Viel Luft nach oben vorhanden. Guter long term hold.
Paratek Pharmaceuticals to Present at H.C. Wainwright 22nd Annual Global Investment Conference
Paratek Pharmaceuticals, Inc. (Nasdaq: PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of novel life-saving therapies for life-threatening diseases or other public health threats for civilian, government and military use, today announced that the Company will present at H.C. Wainwright 22nd Annual Global Investment Conference, Monday, September 14, 2020 at 5:00 p.m. ET.
https://finance.yahoo.com/news/paratek-pharmaceuticals-prese…
Paratek Pharmaceuticals, Inc. (Nasdaq: PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of novel life-saving therapies for life-threatening diseases or other public health threats for civilian, government and military use, today announced that the Company will present at H.C. Wainwright 22nd Annual Global Investment Conference, Monday, September 14, 2020 at 5:00 p.m. ET.
https://finance.yahoo.com/news/paratek-pharmaceuticals-prese…
BOSTON, Nov. 12, 2019: "...Based upon our current operating plan, we anticipate that our existing cash, cash equivalents and marketable securities of $225.6 million as of September 30, 2019, and estimated NUZYRA product sales, will fund company operating expenses, capital expenditures, and debt service beyond the first quarter of 2021..."
Cash von 225 Mio$, MC ca. 100 Mio$. Burnrate ca. 30Mio$/Quartal. Eigentlich sollte hier mehr drin sein...
Cash von 225 Mio$, MC ca. 100 Mio$. Burnrate ca. 30Mio$/Quartal. Eigentlich sollte hier mehr drin sein...
Hallo zusammen,
habe nach eigener Recherche nach einem "hidden" gem im Pharmabereich diese Firma und Ihre zugelassenen Medikamente gefunden.
Ich habe einiges recherchiert und bis auf dass die Firma Investoren nicht gerade hofiert keinen einzigen Grund gefunden warum die Aktie nicht bald rasant und stabil auf 2 stellige Kurse steigen wird.
Ihr habt das schon Anfang 2018 so geschrieben, aktuell ist es ja voll das Schnäppchen.
Wer ist hier noch aktiv dabei und haltet Ihr an dieser Aussage weiter fest ?
Antibiotikum ist wie ich gelernt habe im Vergleich zu anderen Medikamenten nicht die totale Cash Cow aber dafür umso wichtiger. Ich habe nur meine Zweifel dass sie ihre Verkauszahlen sehr nach oben treiben werden/können/wollen. Das Verkaufsteam ist ja mit 40 Leuten und Anfang 2020 dann vielleicht 60 Leuten noch vergleichsweise sehr klein.
Ausserdem gibt es die Gefahr (rein aus Vermarktungssicht...) dass diese neuen Medikament eher als Reserveantibiotikum behandelt werden und daher nur in Ausnahmefällen die nächsten Jahre Verwendung finden werden.
Was ist eure Einschätzung hierzu ? Der aktuelle Preis ist definitiv aus meiner Sicht zu klein, aber ein Billionenmarkt in absehbarer Zeit ist aus genannten Gründen wohl auch nicht drin, oder ?
Obwohl, dass sind wahrscheinlich Fragen die wohl keiner wirklich beantworten können wird
Trotzdem wäre erfreut wenn sich hier jemand der vielleicht schon länger hier investiert ist und die letzen Monate verfolgt hat dazu äußern würde.
Wäre definitiv interessiert hier mitzumachen und aus anderen Positionen dafür rauszugehen.
habe nach eigener Recherche nach einem "hidden" gem im Pharmabereich diese Firma und Ihre zugelassenen Medikamente gefunden.
Ich habe einiges recherchiert und bis auf dass die Firma Investoren nicht gerade hofiert keinen einzigen Grund gefunden warum die Aktie nicht bald rasant und stabil auf 2 stellige Kurse steigen wird.
Ihr habt das schon Anfang 2018 so geschrieben, aktuell ist es ja voll das Schnäppchen.
Wer ist hier noch aktiv dabei und haltet Ihr an dieser Aussage weiter fest ?
Antibiotikum ist wie ich gelernt habe im Vergleich zu anderen Medikamenten nicht die totale Cash Cow aber dafür umso wichtiger. Ich habe nur meine Zweifel dass sie ihre Verkauszahlen sehr nach oben treiben werden/können/wollen. Das Verkaufsteam ist ja mit 40 Leuten und Anfang 2020 dann vielleicht 60 Leuten noch vergleichsweise sehr klein.
Ausserdem gibt es die Gefahr (rein aus Vermarktungssicht...) dass diese neuen Medikament eher als Reserveantibiotikum behandelt werden und daher nur in Ausnahmefällen die nächsten Jahre Verwendung finden werden.
Was ist eure Einschätzung hierzu ? Der aktuelle Preis ist definitiv aus meiner Sicht zu klein, aber ein Billionenmarkt in absehbarer Zeit ist aus genannten Gründen wohl auch nicht drin, oder ?
Obwohl, dass sind wahrscheinlich Fragen die wohl keiner wirklich beantworten können wird

Trotzdem wäre erfreut wenn sich hier jemand der vielleicht schon länger hier investiert ist und die letzen Monate verfolgt hat dazu äußern würde.
Wäre definitiv interessiert hier mitzumachen und aus anderen Positionen dafür rauszugehen.
Antwort auf Beitrag Nr.: 59.883.091 von bernie55 am 15.02.19 13:38:26
Paratek Pharmaceuticals to Present at the 8th Annual SVB Leerink Global Healthcare Conference
BOSTON, Feb. 14, 2019 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced that the Company will present at the 8th Annual SVB Leerink Global Healthcare Conference on Thursday, February 28 at 1:00 p.m. EST at the Lotte New York Palace in New York.
To access the live webcast of Paratek's presentation, please visit http://wsw.com/webcast/leerink32/prtk/. Please connect to the web site at least 15 minutes prior to the live presentation to ensure adequate time for any software downloads that may be necessary to listen to the webcast. A replay of the webcast can be accessed for up to 90 days following the live presentation.
https://finance.yahoo.com/news/paratek-pharmaceuticals-prese…" target="_blank" rel="nofollow ugc noopener">https://finance.yahoo.com/news/paratek-pharmaceuticals-prese…
Zitat von bernie55: @Amherster und Cyberhexe und Paratekies
Ich fülle mal den aktuellen INFO-STAU mit NEWS auf.
Paratek Pharmaceuticals to Present at the 8th Annual SVB Leerink Global Healthcare Conference
BOSTON, Feb. 14, 2019 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced that the Company will present at the 8th Annual SVB Leerink Global Healthcare Conference on Thursday, February 28 at 1:00 p.m. EST at the Lotte New York Palace in New York.
To access the live webcast of Paratek's presentation, please visit http://wsw.com/webcast/leerink32/prtk/. Please connect to the web site at least 15 minutes prior to the live presentation to ensure adequate time for any software downloads that may be necessary to listen to the webcast. A replay of the webcast can be accessed for up to 90 days following the live presentation.
https://finance.yahoo.com/news/paratek-pharmaceuticals-prese…" target="_blank" rel="nofollow ugc noopener">https://finance.yahoo.com/news/paratek-pharmaceuticals-prese…
Antwort auf Beitrag Nr.: 59.354.651 von amherster am 03.12.18 22:34:36@Amherster und Cyberhexe und Paratekies
Ich fülle mal den aktuellen INFO-STAU mit NEWS auf.
Paratek Pharmaceuticals to Report Fourth Quarter and Full Year 2018 Financial Results on February 27, 2019
BOSTON, Feb. 13, 2019 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (NASDAQ: PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced the Company will host a conference call and live audio webcast on February 27, 2019 at 4:30 p.m. EDT to report its fourth quarter and full year 2018 financial results and provide a corporate update.
The audio webcast can be accessed under "Events and Presentations" in the Investor Relations section of the Company's website at www.ParatekPharma.com.
https://finance.yahoo.com/news/paratek-pharmaceuticals-repor…
Ich fülle mal den aktuellen INFO-STAU mit NEWS auf.
Paratek Pharmaceuticals to Report Fourth Quarter and Full Year 2018 Financial Results on February 27, 2019
BOSTON, Feb. 13, 2019 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (NASDAQ: PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced the Company will host a conference call and live audio webcast on February 27, 2019 at 4:30 p.m. EDT to report its fourth quarter and full year 2018 financial results and provide a corporate update.
The audio webcast can be accessed under "Events and Presentations" in the Investor Relations section of the Company's website at www.ParatekPharma.com.
https://finance.yahoo.com/news/paratek-pharmaceuticals-repor…
Eigentlich sollten Biotec und Pharmatitel vom Gesamtmarht unbeeindruckt sein. Was stimmt mit Paratek momentan nicht?
Ihr lieben, ich bin nicht faul, sondern hab momentan sehr wenig Zeit zum stöbern, danke
Ihr lieben, ich bin nicht faul, sondern hab momentan sehr wenig Zeit zum stöbern, danke
Hallo zusammen.
Ich beobachte Prtk jetzt schon mehr als 12 Monate, und bin am überlegen meinen heuer sehr üppigen Weihnachtsbonus hier zu investieren. Da mein Depot von Steinhoffaktien schon überquillt wäre Prtk ein nettes Gegengewicht in meinen Portfolio.
Ich bin nur leider bei Biotec und Pharmatitel übervorsichtig weil 2x brutal auf die Nase gefallen.
Was muss man wissen bzgl. Paratek?
Links, wichtige Termine, EK? danke an alle im voraus. glg marusch
Ich beobachte Prtk jetzt schon mehr als 12 Monate, und bin am überlegen meinen heuer sehr üppigen Weihnachtsbonus hier zu investieren. Da mein Depot von Steinhoffaktien schon überquillt wäre Prtk ein nettes Gegengewicht in meinen Portfolio.
Ich bin nur leider bei Biotec und Pharmatitel übervorsichtig weil 2x brutal auf die Nase gefallen.
Was muss man wissen bzgl. Paratek?
Links, wichtige Termine, EK? danke an alle im voraus. glg marusch
Paratek Pharmaceuticals Files Two Patent Term Extensions in the United States; Expects NUZYRA™ Patent Protection Exclusivity Until at Least October 2030
BOSTON, Dec. 03, 2018 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced the Company filed two Patent Term Extension Requests with the U.S. Patent and Trademark Office. U.S. Patent No. 7,553,828, directed to composition of matter, is anticipated to be extended until May 2028, and U.S. Patent No. 9,265,740, directed to a method of treatment, is expected to be extended until October 2030.
"Significantly lengthening NUZYRA’s exclusive commercial rights into at least 2030 in the United States will have substantial positive long-term impact on its commercial opportunity and builds on our broad and comprehensive protection for NUZYRA,” said Michael Bigham, Chairman and Chief Executive Officer, Paratek. “Our commercial team is actively preparing for a NUZYRA launch in the U.S. in February, and we are looking forward to bringing a compelling new option for the treatment on community-acquired pneumonia and skin infections.”
NUZYRA was approved in October 2018 by the United States Food and Drug Administration for the treatment of adult patients with community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI).
About Paratek Pharmaceuticals, Inc.
https://finance.yahoo.com/news/paratek-pharmaceuticals-files…
BOSTON, Dec. 03, 2018 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced the Company filed two Patent Term Extension Requests with the U.S. Patent and Trademark Office. U.S. Patent No. 7,553,828, directed to composition of matter, is anticipated to be extended until May 2028, and U.S. Patent No. 9,265,740, directed to a method of treatment, is expected to be extended until October 2030.
"Significantly lengthening NUZYRA’s exclusive commercial rights into at least 2030 in the United States will have substantial positive long-term impact on its commercial opportunity and builds on our broad and comprehensive protection for NUZYRA,” said Michael Bigham, Chairman and Chief Executive Officer, Paratek. “Our commercial team is actively preparing for a NUZYRA launch in the U.S. in February, and we are looking forward to bringing a compelling new option for the treatment on community-acquired pneumonia and skin infections.”
NUZYRA was approved in October 2018 by the United States Food and Drug Administration for the treatment of adult patients with community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI).
About Paratek Pharmaceuticals, Inc.
https://finance.yahoo.com/news/paratek-pharmaceuticals-files…
Paratek Pharmaceuticals Doses First Patient in Phase 2 Clinical Trial of Omadacycline in Acute Pyelonephritis, a Common Subset of Complicated Urinary Tract Infections
aratek Pharmaceuticals, Inc. (PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced dosing of the first patient in a Phase 2 study evaluating the potential efficacy and safety of oral and intravenous (IV) omadacycline for the treatment of acute pyelonephritis, a common subset of complicated urinary tract infections (cUTI).
“Urinary tract infection is one of the most commonly diagnosed bacterial infections and treating clinicians are limited by a lack of broad-spectrum, well-tolerated, once-daily oral antibiotics,” said Evan Loh, M.D., President, Chief Operating Officer and Chief Medical Officer of Paratek. “This important milestone signifies continued progress in the evaluation of the efficacy and safety of omadacycline, which has the potential to address this significant unmet need in this serious community-acquired infection. We look forward to sharing topline data from this study in the second half of 2019.”
The Company is also actively enrolling patients in a second Phase 2 study evaluating oral-only omadacycline in uncomplicated urinary tract infections (uUTI). Topline data from this study is also expected in the second half of 2019. Omadacycline has been granted Qualified Infectious Disease Product (QIDP) designation by the U.S. Food and Drug Administration for the treatment of uUTI and acute pyelonephritis for both the oral and the IV formulations.
Omadacycline, under the brand name NUZYRATM, was approved in October 2018 for the treatment of adult patients with community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI).
About Paratek Pharmaceuticals, Inc.
https://finance.yahoo.com/news/paratek-pharmaceuticals-doses…
aratek Pharmaceuticals, Inc. (PRTK), a commercial-stage biopharmaceutical company focused on the development and commercialization of innovative therapeutics, today announced dosing of the first patient in a Phase 2 study evaluating the potential efficacy and safety of oral and intravenous (IV) omadacycline for the treatment of acute pyelonephritis, a common subset of complicated urinary tract infections (cUTI).
“Urinary tract infection is one of the most commonly diagnosed bacterial infections and treating clinicians are limited by a lack of broad-spectrum, well-tolerated, once-daily oral antibiotics,” said Evan Loh, M.D., President, Chief Operating Officer and Chief Medical Officer of Paratek. “This important milestone signifies continued progress in the evaluation of the efficacy and safety of omadacycline, which has the potential to address this significant unmet need in this serious community-acquired infection. We look forward to sharing topline data from this study in the second half of 2019.”
The Company is also actively enrolling patients in a second Phase 2 study evaluating oral-only omadacycline in uncomplicated urinary tract infections (uUTI). Topline data from this study is also expected in the second half of 2019. Omadacycline has been granted Qualified Infectious Disease Product (QIDP) designation by the U.S. Food and Drug Administration for the treatment of uUTI and acute pyelonephritis for both the oral and the IV formulations.
Omadacycline, under the brand name NUZYRATM, was approved in October 2018 for the treatment of adult patients with community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI).
About Paratek Pharmaceuticals, Inc.
https://finance.yahoo.com/news/paratek-pharmaceuticals-doses…
Antwort auf Beitrag Nr.: 59.176.284 von Cyberhexe am 09.11.18 10:19:40ja, ist Mir auch aufgefallen.

Das kann Aussagekraft haben, muss es aber nicht.
Interpretationsfreiheit . . . . . , . . . . .je nach Belieben . . . . .
Hätte die Börse noch 6 Stunden länger aufgehabt, wären wir bis 13$ gelaufen

Quelle: finanztreff
Vielen Dank schon mal, dass der Thread und dieses Thema so gut aufgenommen wurde.
Hallo zusammen!
Bin nicht investiert, ich finde aber, es ist ein spannendes Thema.
https://www.welt.de/wirtschaft/article183455266/OECD-Europa-…
Gruß, greenhorn
Bin nicht investiert, ich finde aber, es ist ein spannendes Thema.
https://www.welt.de/wirtschaft/article183455266/OECD-Europa-…
Gruß, greenhorn
Antwort auf Beitrag Nr.: 59.171.832 von amherster am 08.11.18 19:49:47Das Thema "Superkeime" findet derzeit mediale Beachtung, bspw. gestern im CH-Fernsehen mit der folgenden Doku:
https://www.srf.ch/sendungen/dok/pharma-traegt-dazu-bei-dass…
Eine Kernaussage der Doku ist die Flucht der Pharma-Giganten aus der Antibiotika-Forschung, weil die Refinanzieruzngsmöglichkeiten der "teuren" Forschung begrenzt sind.
Dringend gesucht: Neue Antibiotika
Novartis hat diesen Sommer bekannt gegeben, dass der Konzern die Antibiotika-Forschung aufgibt. Ärzte wie Rein Jan Piso kritisieren, die Pharma ziehe sich aus der Verantwortung, weil die Antibiotika-Produktion wenig lukrativ sei. Dies, weil die Preise von Antibiotika vergleichsweise tief seien und das Medikament nur im Notfall verwendet werden sollte.
Da die Zahl der antibiotikaresistenten Superkeime steigt, ist der Markt aber auf neue Medikamente angewiesen. Es braucht neue Modelle zur Finanzierung von Antibiotika. Nur: Wer soll bezahlen? Das weiss heute niemand.
https://www.srf.ch/sendungen/dok/pharma-traegt-dazu-bei-dass…
Eine Kernaussage der Doku ist die Flucht der Pharma-Giganten aus der Antibiotika-Forschung, weil die Refinanzieruzngsmöglichkeiten der "teuren" Forschung begrenzt sind.
Dringend gesucht: Neue Antibiotika
Novartis hat diesen Sommer bekannt gegeben, dass der Konzern die Antibiotika-Forschung aufgibt. Ärzte wie Rein Jan Piso kritisieren, die Pharma ziehe sich aus der Verantwortung, weil die Antibiotika-Produktion wenig lukrativ sei. Dies, weil die Preise von Antibiotika vergleichsweise tief seien und das Medikament nur im Notfall verwendet werden sollte.
Da die Zahl der antibiotikaresistenten Superkeime steigt, ist der Markt aber auf neue Medikamente angewiesen. Es braucht neue Modelle zur Finanzierung von Antibiotika. Nur: Wer soll bezahlen? Das weiss heute niemand.
Hier mal auf deutsch ein paar Infos.
Ambulant erworbene bakterielle Lungenentzündung / akute Haut- und Hautstrukturinfektionen – FDA-Zulassung
04.10.2018 Paratek Pharmaceuticals, Inc. gab heute bekannt, dass die U.S. Food and Drug Administration (FDA) Nuzyra (Omadacyclin) für die Behandlung von Erwachsenen mit ambulant erworbener bakterieller Lungenentzündung (CABP) und akuten Haut- und Hautstrukturinfektionen (ABSSSI) zugelassen hat.
Nuzyra ist ein modernisiertes Tetracyclin und ein einmal täglich zu verabreichendes IV- und orales Antibiotikum, das eine Aktivität über ein breites Spektrum von Bakterien zeigt, einschließlich grampositiver, gramnegativer, atypischer und medikamentenresistenter Stämme, schreibt das Unternehmen.
Die Zulassung des Medikaments wurde durch mehrere klinische Studien im Rahmen des globalen Entwicklungsprogramms des Unternehmens unterstützt. Fast 2.000 erwachsene Patienten erhielten Nuzyra, und es wurde festgestellt, dass es wirksam und allgemein sicher und gut verträglich ist.
Im Rahmen der Zulassung hat sich Paratek bereit erklärt, Post-Marketing-Studien in den Bereichen CABP und Pädiatrie durchzuführen.
https://arznei-news.de/nuzyra/#a1
Quelle: arznei-news.de – Quellenangabe: Paratek Pharmaceuticals
Ambulant erworbene bakterielle Lungenentzündung / akute Haut- und Hautstrukturinfektionen – FDA-Zulassung
04.10.2018 Paratek Pharmaceuticals, Inc. gab heute bekannt, dass die U.S. Food and Drug Administration (FDA) Nuzyra (Omadacyclin) für die Behandlung von Erwachsenen mit ambulant erworbener bakterieller Lungenentzündung (CABP) und akuten Haut- und Hautstrukturinfektionen (ABSSSI) zugelassen hat.
Nuzyra ist ein modernisiertes Tetracyclin und ein einmal täglich zu verabreichendes IV- und orales Antibiotikum, das eine Aktivität über ein breites Spektrum von Bakterien zeigt, einschließlich grampositiver, gramnegativer, atypischer und medikamentenresistenter Stämme, schreibt das Unternehmen.
Die Zulassung des Medikaments wurde durch mehrere klinische Studien im Rahmen des globalen Entwicklungsprogramms des Unternehmens unterstützt. Fast 2.000 erwachsene Patienten erhielten Nuzyra, und es wurde festgestellt, dass es wirksam und allgemein sicher und gut verträglich ist.
Im Rahmen der Zulassung hat sich Paratek bereit erklärt, Post-Marketing-Studien in den Bereichen CABP und Pädiatrie durchzuführen.
https://arznei-news.de/nuzyra/#a1
Quelle: arznei-news.de – Quellenangabe: Paratek Pharmaceuticals
Antwort auf Beitrag Nr.: 59.162.751 von Cyberhexe am 07.11.18 21:30:26Ich kann mich da nur anschließen, wenn ich mir den Cash-Bestand zum 30.09.2018 ansehe und
die (von mir) erwartete deutliche Umsatzsteigerung spätestens ab dem 3. Quartal vor Augen führe, dann ist die aktuelle Marktkapitalisierung ein Witz.
Ich bin optimistisch, dass der Markt das spätestens gegen Ende 2019 mit steigenden Kursen honorieren wird.
die (von mir) erwartete deutliche Umsatzsteigerung spätestens ab dem 3. Quartal vor Augen führe, dann ist die aktuelle Marktkapitalisierung ein Witz.
Ich bin optimistisch, dass der Markt das spätestens gegen Ende 2019 mit steigenden Kursen honorieren wird.
Achtung, diese Nachricht ist vom vom 04.10.2018, aber Sie fand kaum Beachtung wegen der anderen Zulassungen
Paratek Announces Acceptance of European Marketing Authorization Application for Oral and Intravenous Omadacycline
-- MAA submission for both community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI) --
-- EMA decision expected second half of 2019 --
BOSTON, Oct. 04, 2018 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (PRTK) today announced the acceptance of the submission to the European Medicines Agency (EMA) of the Marketing Authorization Application (MAA) for omadacycline. Paratek is seeking approval of omadacycline, a modernized tetracycline, for the treatment of community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI). Omadacycline is a once-daily oral and intravenous (IV) broad spectrum antibiotic approved under the tradename NUZYRA™ in the United States.
The MAA is supported by the company’s Phase 3 program for omadacycline, which included three pivotal registration studies: two studies in ABSSSI and one study in CABP. Omadacycline met all required EMA primary endpoints in each study and demonstrated a generally safe and well-tolerated profile.
In the U.S., the FDA approved NUZYRA™ (omadacycline) in October 2018 for the treatment of adults with community-acquired bacterial pneumonia (CABP) and acute skin and skin structure infections (ABSSSI).
About NUZYRA
NUZYRA (omadacycline) is a novel antibiotic with both once-daily intravenous (IV) and oral formulations for the treatment of community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI). A modernized tetracycline, NUZYRA is specifically designed to overcome tetracycline resistance and exhibits activity across a spectrum of bacteria, including Gram-positive, Gram-negative, atypicals, and other drug-resistant strains.
Indications and Usage
NUZYRA™ is a tetracycline class antibacterial indicated for the treatment of adult patients with the following infections caused by susceptible microorganisms:
Community-Acquired Bacterial Pneumonia (CABP) caused by the following: Streptococcus pneumoniae, Staphylococcus aureus (methicillin-susceptible isolates), Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae, Legionella pneumophila, Mycoplasma pneumoniae, and Chlamydophila pneumoniae.
Acute Bacterial Skin and Skin Structure Infections (ABSSSI) caused by the following: Staphylococcus aureus (methicillin-susceptible and -resistant isolates), Staphylococcus lugdunensis, Streptococcus pyogenes, Streptococcus anginosus grp. (includes S. anginosus, S. intermedius, and S. constellatus), Enterococcus faecalis, Enterobacter cloacae, and Klebsiella pneumoniae.
Usage
To reduce the development of drug-resistant bacteria and maintain the effectiveness of NUZYRA and other antibacterial drugs, NUZYRA should be used only to treat or prevent infections that are proven or strongly suspected to be caused by susceptible bacteria.
usw.
Quelle
https://finance.yahoo.com/news/paratek-announces-acceptance-…
Paratek Announces Acceptance of European Marketing Authorization Application for Oral and Intravenous Omadacycline
-- MAA submission for both community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI) --
-- EMA decision expected second half of 2019 --
BOSTON, Oct. 04, 2018 (GLOBE NEWSWIRE) -- Paratek Pharmaceuticals, Inc. (PRTK) today announced the acceptance of the submission to the European Medicines Agency (EMA) of the Marketing Authorization Application (MAA) for omadacycline. Paratek is seeking approval of omadacycline, a modernized tetracycline, for the treatment of community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI). Omadacycline is a once-daily oral and intravenous (IV) broad spectrum antibiotic approved under the tradename NUZYRA™ in the United States.
The MAA is supported by the company’s Phase 3 program for omadacycline, which included three pivotal registration studies: two studies in ABSSSI and one study in CABP. Omadacycline met all required EMA primary endpoints in each study and demonstrated a generally safe and well-tolerated profile.
In the U.S., the FDA approved NUZYRA™ (omadacycline) in October 2018 for the treatment of adults with community-acquired bacterial pneumonia (CABP) and acute skin and skin structure infections (ABSSSI).
About NUZYRA
NUZYRA (omadacycline) is a novel antibiotic with both once-daily intravenous (IV) and oral formulations for the treatment of community-acquired bacterial pneumonia (CABP) and acute bacterial skin and skin structure infections (ABSSSI). A modernized tetracycline, NUZYRA is specifically designed to overcome tetracycline resistance and exhibits activity across a spectrum of bacteria, including Gram-positive, Gram-negative, atypicals, and other drug-resistant strains.
Indications and Usage
NUZYRA™ is a tetracycline class antibacterial indicated for the treatment of adult patients with the following infections caused by susceptible microorganisms:
Community-Acquired Bacterial Pneumonia (CABP) caused by the following: Streptococcus pneumoniae, Staphylococcus aureus (methicillin-susceptible isolates), Haemophilus influenzae, Haemophilus parainfluenzae, Klebsiella pneumoniae, Legionella pneumophila, Mycoplasma pneumoniae, and Chlamydophila pneumoniae.
Acute Bacterial Skin and Skin Structure Infections (ABSSSI) caused by the following: Staphylococcus aureus (methicillin-susceptible and -resistant isolates), Staphylococcus lugdunensis, Streptococcus pyogenes, Streptococcus anginosus grp. (includes S. anginosus, S. intermedius, and S. constellatus), Enterococcus faecalis, Enterobacter cloacae, and Klebsiella pneumoniae.
Usage
To reduce the development of drug-resistant bacteria and maintain the effectiveness of NUZYRA and other antibacterial drugs, NUZYRA should be used only to treat or prevent infections that are proven or strongly suspected to be caused by susceptible bacteria.
usw.
Quelle
https://finance.yahoo.com/news/paratek-announces-acceptance-…
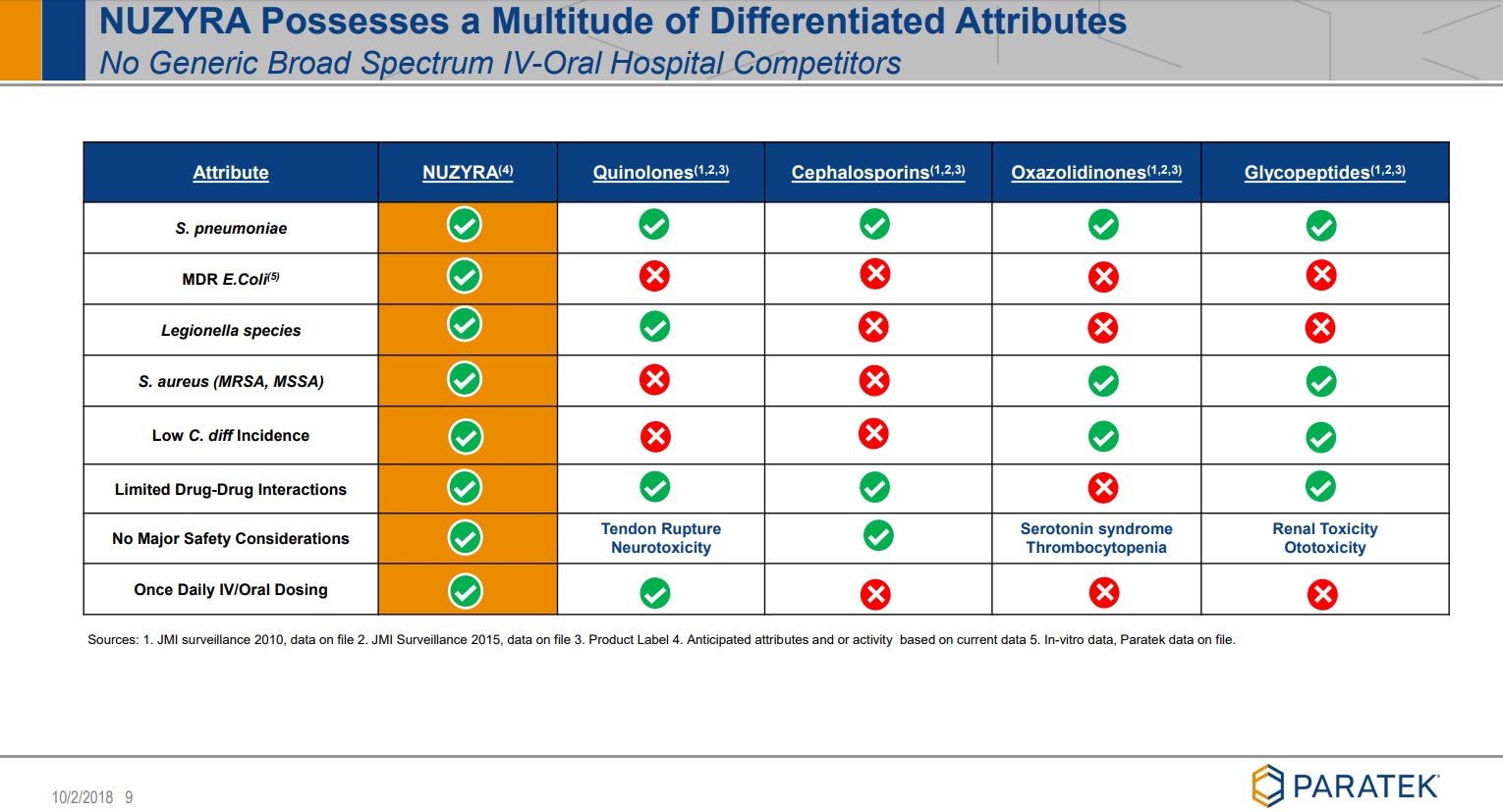
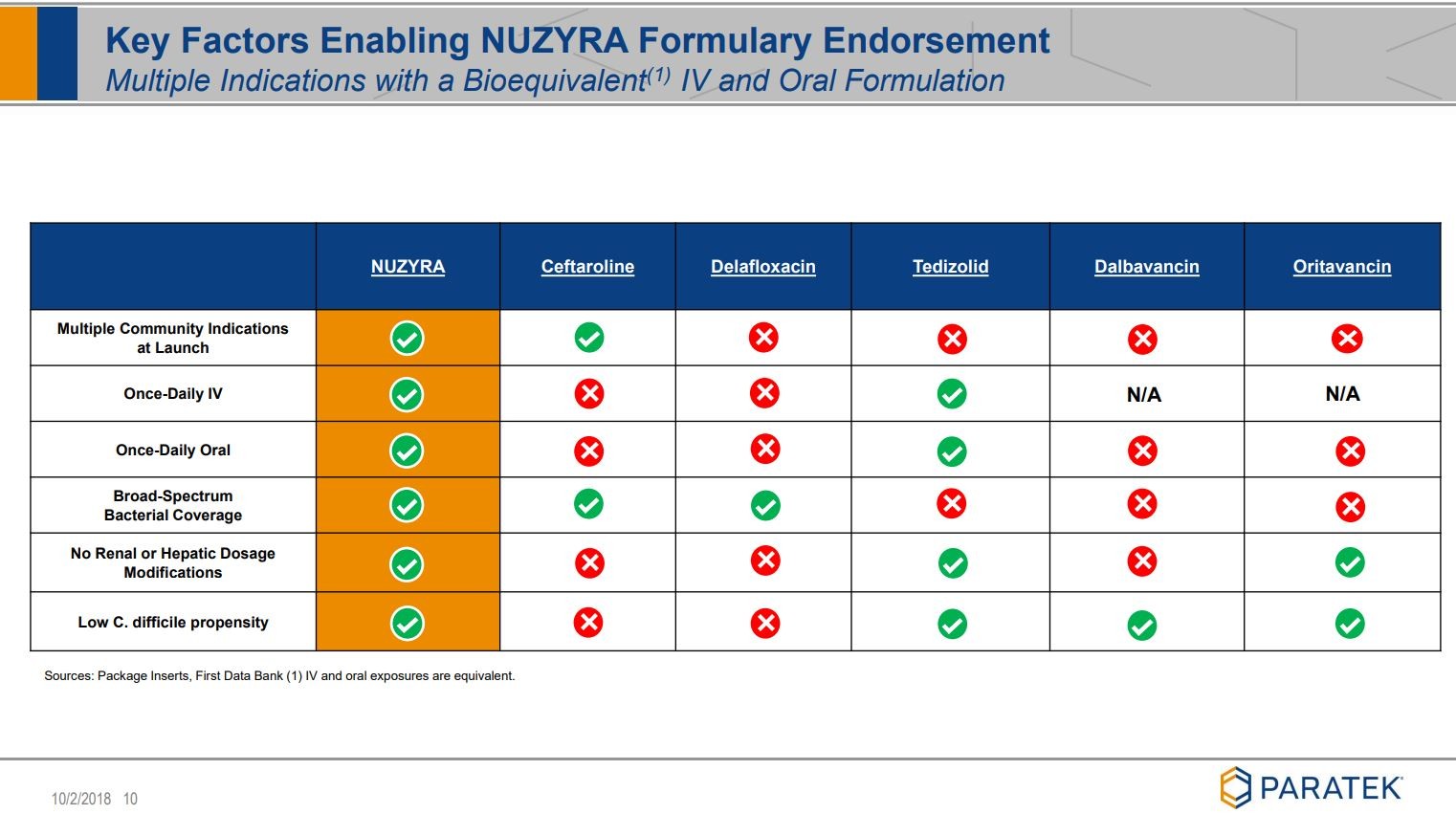
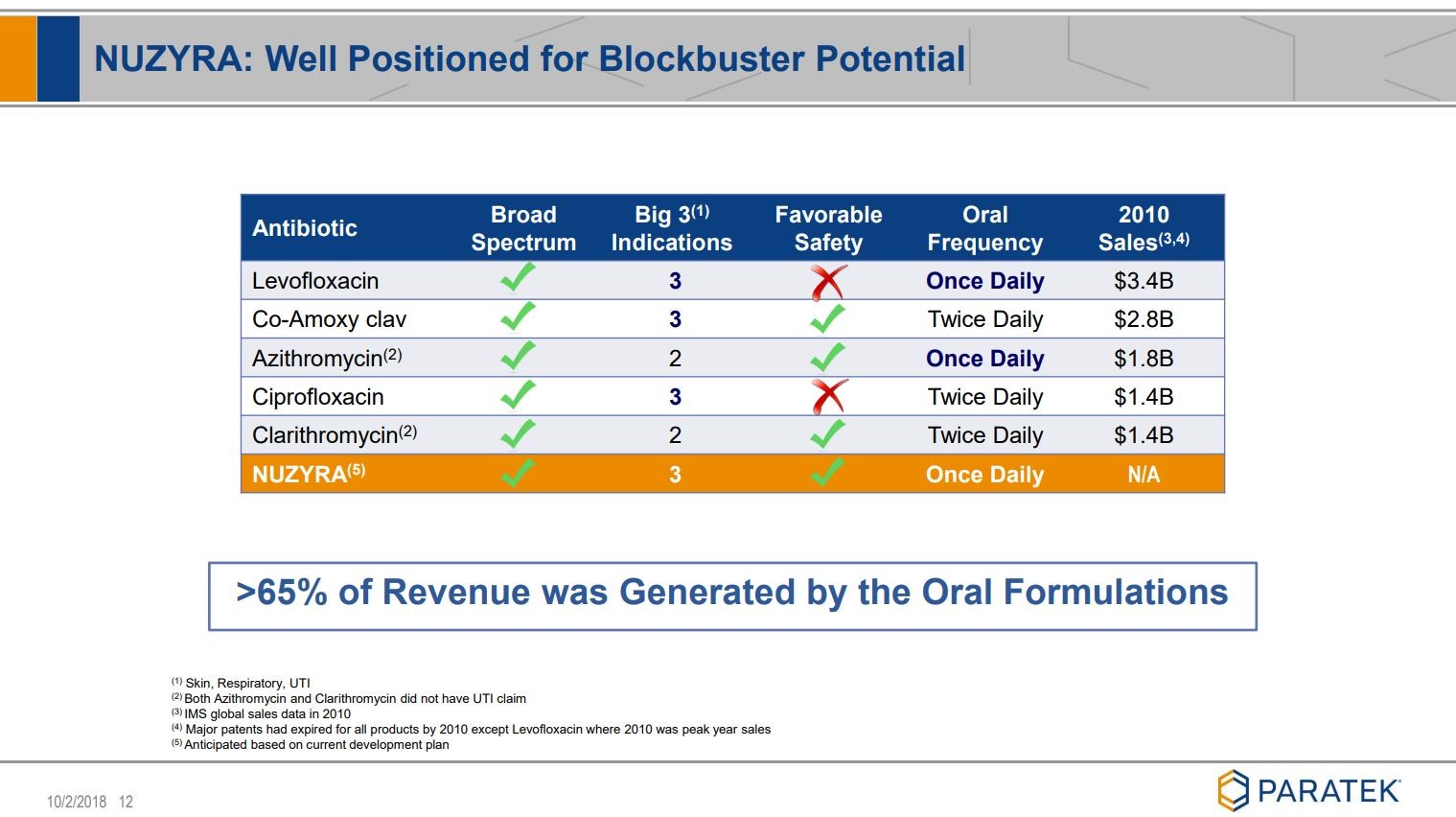
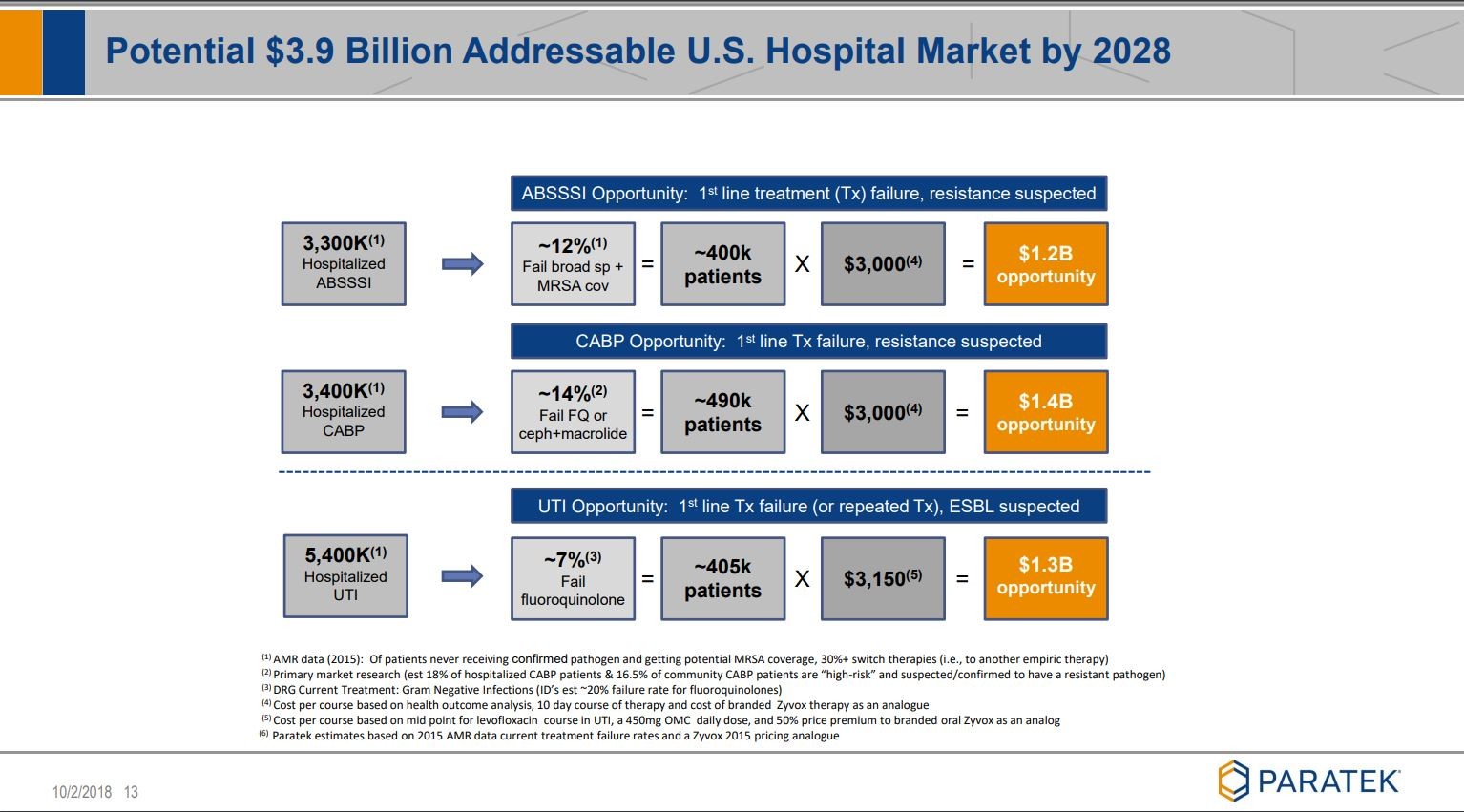
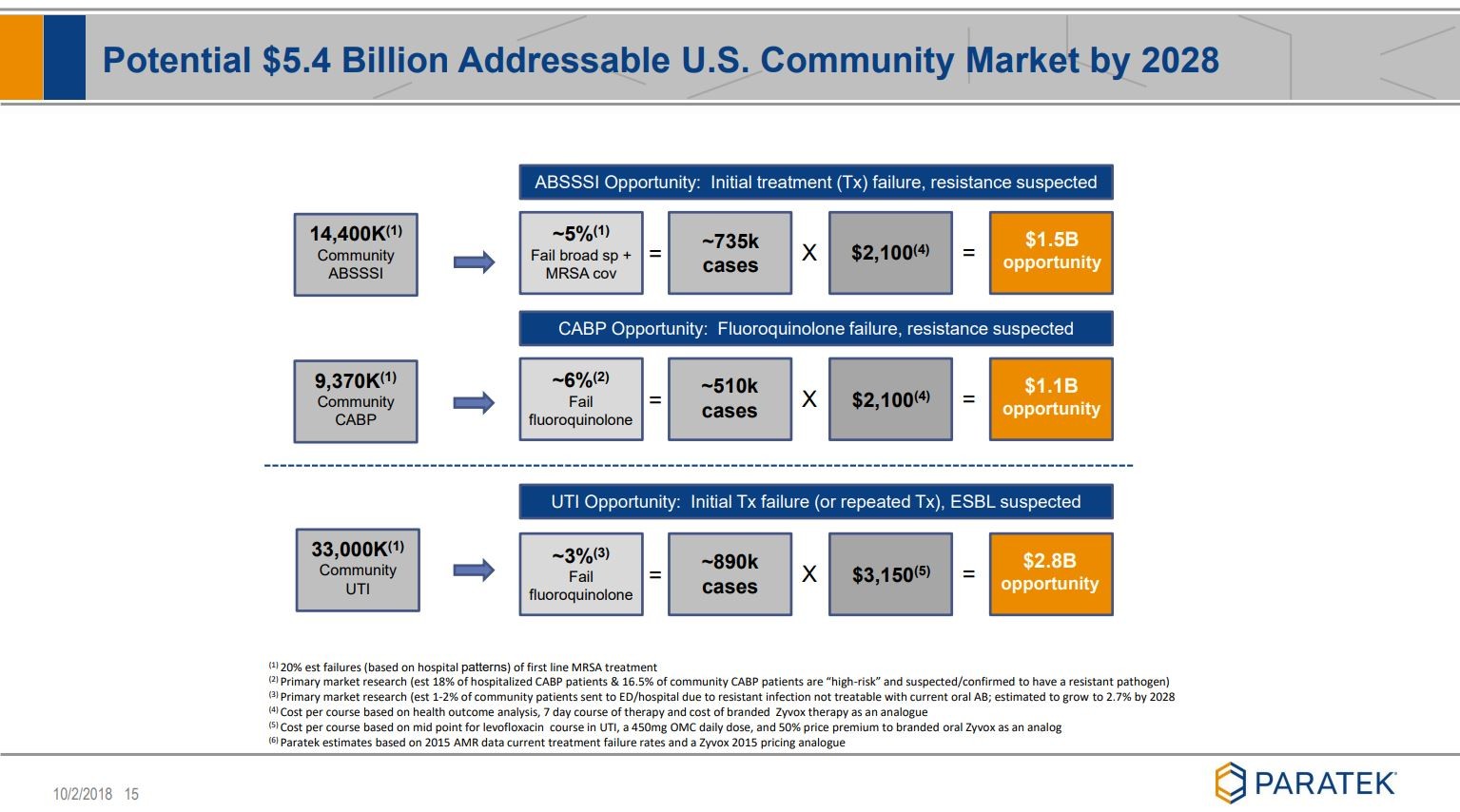
Noch ein paar Folien, die ich ziemlich beeindruckend finde:
Wer sich noch mehr "verzücken" möchte,
siehe unter Quelle: Company corporate presentation

Viel Erfolg mit diesem Wert.
Die Gelegenheit ist günstig.
Alles nur meine bescheidene Meinung und keine Aufforderung zum Kauf.
Bis bald!
Wer sich noch mehr "verzücken" möchte,
siehe unter Quelle: Company corporate presentation






Viel Erfolg mit diesem Wert.
Die Gelegenheit ist günstig.
Alles nur meine bescheidene Meinung und keine Aufforderung zum Kauf.
Bis bald!
Wie versprochen, ein paar links
Quelle:
https://www.smarteranalyst.com/brief/cantor-fitzgerald-think…
Cantor Fitzgerald analyst Louise Chen maintained a Buy rating on Paratek Pharmaceuticals (NASDAQ: PRTK) today and set a price target of $50.
The company’s shares opened today at $8.85, close to its 52-week low of $8.47.
Chen said:
“We rate PRTK’s stock as 12-month price target of $50. We expect upwards earnings revisions for Nuzyra and Seysara sales to levels not reflected in consensus expectations to drive PRTK shares higher. Valuation Summary We use a blend of DCF and multiples (EV/EBITDA) to get to our 12-month price target of $50. The Disclosure Section may be found on pages 3 – 4.Valuation We use a blend of DCF and multiples (EV/EBITDA) to get to our 12-month price target of $50.”
Quelle:
https://m.benzinga.com/article/12451837?utm_referrer=https%3…
FDA Approves Paratek's Bacterial Pneumonia, Skin Infection Treatment
Paratek Pharmaceuticals, Inc. (NASDAQ: PRTK) shares reacted positively following the announcement of a Food and Drug Administration's approved treatment.
What To Know
The company announced FDA approval of Nuzyra, for the treatment of community-acquired bacterial pneumonia (CABP), as well as acute skin infections.
According to company data, Nuzyra is a modernized tetracycline, taken orally, which exhibits activity across several types of bacteria, such as Gram-positive, Gram-negative, atypicals and drug resistant strains. This will be the first antibiotic approved of its kind for nearly 20 years.
“NUZYRA offers clinicians the ability to treat patients with the IV and transition them home to complete treatment with the oral formulation. This potentially helps reduce hospitalizations and the costs associated with hospital stays,” Paratek COO Evan Loh said in a press release.
Why It’s Important
According to the Centers for Disease Control and Prevention, drug-resistant bacteria causes 2 million illnesses and over 20,000 deaths each year in the United States.
“Treating pneumonia and skin infections has become increasingly complex as existing antibiotic therapies sometimes have reduced efficacy as resistance continues to grow. This reality makes it increasingly challenging to provide safe and effective treatments to patients,” said Keith Kaye, Director of Clinical Research at the University of Michigan.
“There continues to be a need for novel antibiotics with both IV and oral formulations, such as NUZYRA, to help physicians stay ahead of the evolving resistance landscape.”
What’s Next
Roughly 2,000 adult patients have received the treatment, and the company plans on making it fully available in the first quarter of 2019. Paratek has developed plans to conduct marketing studies in pediatrics and other areas.
Paratek's stock traded up more than 7 percent to $9.93 per share.
Quelle
https://www.streetwisereports.com/article/2018/10/08/fda-app…
FDA Approves Biopharma's Drug with $1.75 Billion Peak Sales Potential
In an Oct. 3 research note, analyst Ed Arce reported the FDA approved two of Paratek Pharmaceuticals Inc.'s (PRTK:NASDAQ) therapies, Seysara and Nusyra, on Oct. 1 and Oct. 2, respectively.
As expected, Arce noted, Nusyra was approved as treatment for both community-acquired bacterial pneumonia and acute bacterial skin and skin structure infections (ABSSSI).
For both conditions, Nusyra may be given on an intravenous-to-oral basis, a 200 mg intravenous infusion first as a loading dose on day one, followed by 300 mg by mouth a day for seven to 14 days. The single intravenous administration is "an incremental positive" over the two to three days of infusion required in the pivotal trials, Arce pointed out.
For ABSSSI, an all-oral regimen is allowed, consisting of a loading dose of 450 mg once on the first and second days, followed by 300 mg per day. Because the dosing is all by mouth for this indication, Nusyra is more likely to be widely adopted.
In either indication, patients must fast for four hours before and two hours after taking a tablet, which Arce described as "one slight surprise to us."
Paratek intends to announce the price of Nusyra in Q4/18 and commercially launch the therapeutic in Q1/19. H.C. Wainwright estimates that sales of the drug will reach a peak of $1.75 billion.
The other drug, Seysara (saracycline), was approved for the treatment of inflammatory lesions resulting from non-nodular, moderate to severe acne vulgaris in 9-plus year olds, relayed Arce. Almirall, which owns the rights to Seysara, expects to commercially launch it in January 2019 and eventually reach peak annual sales of an estimated $150–200 million.
Paratek is entitled to receive from Almirall royalties on U.S. net sales, in addition to the $12 million approval milestone payment now due.
Arce reiterated his firm's Buy rating and $55 per share price target on Paratek. The target reflects more than fivebagger return potential, as the stock is currently trading at around $9.24 per share.
Quelle:
https://www.smarteranalyst.com/brief/cantor-fitzgerald-think…
Cantor Fitzgerald analyst Louise Chen maintained a Buy rating on Paratek Pharmaceuticals (NASDAQ: PRTK) today and set a price target of $50.
The company’s shares opened today at $8.85, close to its 52-week low of $8.47.
Chen said:
“We rate PRTK’s stock as 12-month price target of $50. We expect upwards earnings revisions for Nuzyra and Seysara sales to levels not reflected in consensus expectations to drive PRTK shares higher. Valuation Summary We use a blend of DCF and multiples (EV/EBITDA) to get to our 12-month price target of $50. The Disclosure Section may be found on pages 3 – 4.Valuation We use a blend of DCF and multiples (EV/EBITDA) to get to our 12-month price target of $50.”
Quelle:
https://m.benzinga.com/article/12451837?utm_referrer=https%3…
FDA Approves Paratek's Bacterial Pneumonia, Skin Infection Treatment
Paratek Pharmaceuticals, Inc. (NASDAQ: PRTK) shares reacted positively following the announcement of a Food and Drug Administration's approved treatment.
What To Know
The company announced FDA approval of Nuzyra, for the treatment of community-acquired bacterial pneumonia (CABP), as well as acute skin infections.
According to company data, Nuzyra is a modernized tetracycline, taken orally, which exhibits activity across several types of bacteria, such as Gram-positive, Gram-negative, atypicals and drug resistant strains. This will be the first antibiotic approved of its kind for nearly 20 years.
“NUZYRA offers clinicians the ability to treat patients with the IV and transition them home to complete treatment with the oral formulation. This potentially helps reduce hospitalizations and the costs associated with hospital stays,” Paratek COO Evan Loh said in a press release.
Why It’s Important
According to the Centers for Disease Control and Prevention, drug-resistant bacteria causes 2 million illnesses and over 20,000 deaths each year in the United States.
“Treating pneumonia and skin infections has become increasingly complex as existing antibiotic therapies sometimes have reduced efficacy as resistance continues to grow. This reality makes it increasingly challenging to provide safe and effective treatments to patients,” said Keith Kaye, Director of Clinical Research at the University of Michigan.
“There continues to be a need for novel antibiotics with both IV and oral formulations, such as NUZYRA, to help physicians stay ahead of the evolving resistance landscape.”
What’s Next
Roughly 2,000 adult patients have received the treatment, and the company plans on making it fully available in the first quarter of 2019. Paratek has developed plans to conduct marketing studies in pediatrics and other areas.
Paratek's stock traded up more than 7 percent to $9.93 per share.
Quelle
https://www.streetwisereports.com/article/2018/10/08/fda-app…
FDA Approves Biopharma's Drug with $1.75 Billion Peak Sales Potential
In an Oct. 3 research note, analyst Ed Arce reported the FDA approved two of Paratek Pharmaceuticals Inc.'s (PRTK:NASDAQ) therapies, Seysara and Nusyra, on Oct. 1 and Oct. 2, respectively.
As expected, Arce noted, Nusyra was approved as treatment for both community-acquired bacterial pneumonia and acute bacterial skin and skin structure infections (ABSSSI).
For both conditions, Nusyra may be given on an intravenous-to-oral basis, a 200 mg intravenous infusion first as a loading dose on day one, followed by 300 mg by mouth a day for seven to 14 days. The single intravenous administration is "an incremental positive" over the two to three days of infusion required in the pivotal trials, Arce pointed out.
For ABSSSI, an all-oral regimen is allowed, consisting of a loading dose of 450 mg once on the first and second days, followed by 300 mg per day. Because the dosing is all by mouth for this indication, Nusyra is more likely to be widely adopted.
In either indication, patients must fast for four hours before and two hours after taking a tablet, which Arce described as "one slight surprise to us."
Paratek intends to announce the price of Nusyra in Q4/18 and commercially launch the therapeutic in Q1/19. H.C. Wainwright estimates that sales of the drug will reach a peak of $1.75 billion.
The other drug, Seysara (saracycline), was approved for the treatment of inflammatory lesions resulting from non-nodular, moderate to severe acne vulgaris in 9-plus year olds, relayed Arce. Almirall, which owns the rights to Seysara, expects to commercially launch it in January 2019 and eventually reach peak annual sales of an estimated $150–200 million.
Paratek is entitled to receive from Almirall royalties on U.S. net sales, in addition to the $12 million approval milestone payment now due.
Arce reiterated his firm's Buy rating and $55 per share price target on Paratek. The target reflects more than fivebagger return potential, as the stock is currently trading at around $9.24 per share.
Antwort auf Beitrag Nr.: 59.162.751 von Cyberhexe am 07.11.18 21:30:26Hallo "Cyberhexe",
ich bin hocherfreut über den "prominenten" Einstieg
Verfolge deine Beiträge schon über 10 Jahre.
Ich hätte damals öfter mal auf deine Hinweise hören sollen,
dann wären mir herbe Verluste und Haarverlust erspart geblieben (GPC Biotech)
Dann auf gutes Gelingen und schöne Zeiten mit dieser Perle.
ich bin hocherfreut über den "prominenten" Einstieg

Verfolge deine Beiträge schon über 10 Jahre.
Ich hätte damals öfter mal auf deine Hinweise hören sollen,
dann wären mir herbe Verluste und Haarverlust erspart geblieben (GPC Biotech)
Dann auf gutes Gelingen und schöne Zeiten mit dieser Perle.
Antwort auf Beitrag Nr.: 59.162.751 von Cyberhexe am 07.11.18 21:30:26wobei der Preis für NUZYRA moderat ist:


Antwort auf Beitrag Nr.: 59.162.211 von amherster am 07.11.18 20:33:09...bin ebenfalls "prominent" eingestiegen.
Die Marktkapitalisierung von Paratek ist mittlerweile richtig lächerlich, obschon das Geschäftsmodell bei den Antibiotikas derzeit in Frage gestellt ist: routinemässig werden die generischen, weil billigen, Antibiotika eingesetzt und die neuen Antibiotika nur dann, wenn die Standardtherapie nicht anschlägt. Damit sind natürlich nicht mehr die ganz grossen Umsätze zu machen, weshalb sich die grossen Pharmafirmen mehrheitlich aus der Antibiotika-Forschung zurückgezogen haben. Ich bin mir jedoch sicher, dass die Gesundheitsbehörden irgendwie nachjustieren. Die Gefahr einer "Epidemie" mit multiresistenten Keimen und keinen geeigneten Therapiemöglichkeiten kann nicht das Ziel sein.
Und PRTK ist mit den 2 kürzlich zugelassenen Medikamenten derat gut aufgestellt, dass zweistellige Kurse sehr wahrscheinlich relativ kurzfristig wieder erzielt werden...spätestens bei der Markteinführung von NUZYRA im Februar 2019.
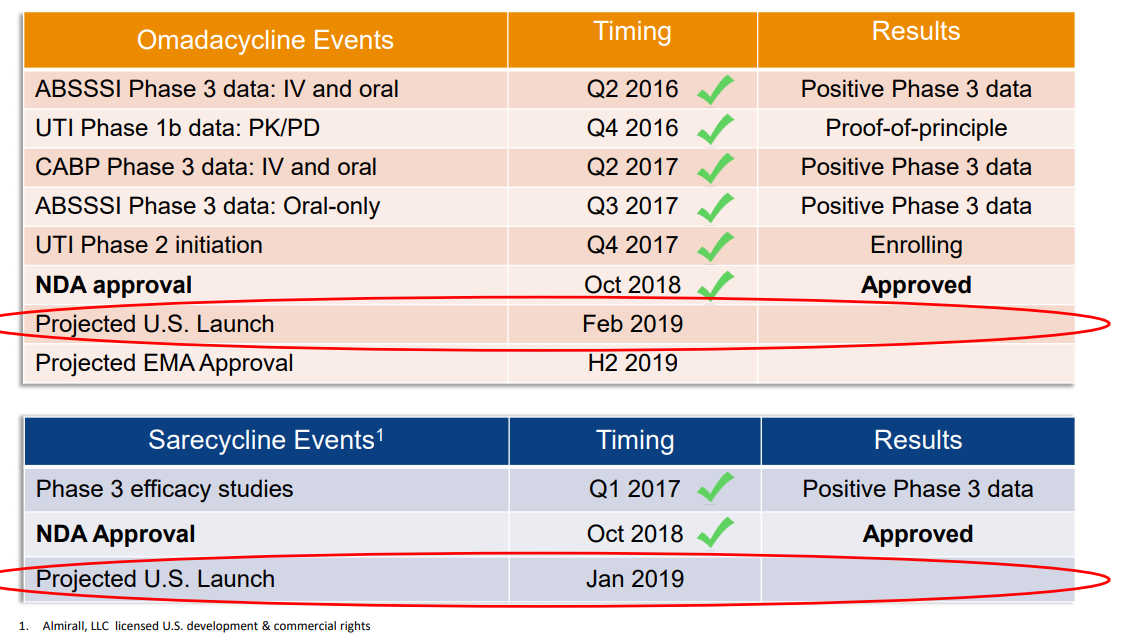
Die Marktkapitalisierung von Paratek ist mittlerweile richtig lächerlich, obschon das Geschäftsmodell bei den Antibiotikas derzeit in Frage gestellt ist: routinemässig werden die generischen, weil billigen, Antibiotika eingesetzt und die neuen Antibiotika nur dann, wenn die Standardtherapie nicht anschlägt. Damit sind natürlich nicht mehr die ganz grossen Umsätze zu machen, weshalb sich die grossen Pharmafirmen mehrheitlich aus der Antibiotika-Forschung zurückgezogen haben. Ich bin mir jedoch sicher, dass die Gesundheitsbehörden irgendwie nachjustieren. Die Gefahr einer "Epidemie" mit multiresistenten Keimen und keinen geeigneten Therapiemöglichkeiten kann nicht das Ziel sein.
Und PRTK ist mit den 2 kürzlich zugelassenen Medikamenten derat gut aufgestellt, dass zweistellige Kurse sehr wahrscheinlich relativ kurzfristig wieder erzielt werden...spätestens bei der Markteinführung von NUZYRA im Februar 2019.

ACHTUNG!
Charts sind Screenshots zur Dokumentation!!!
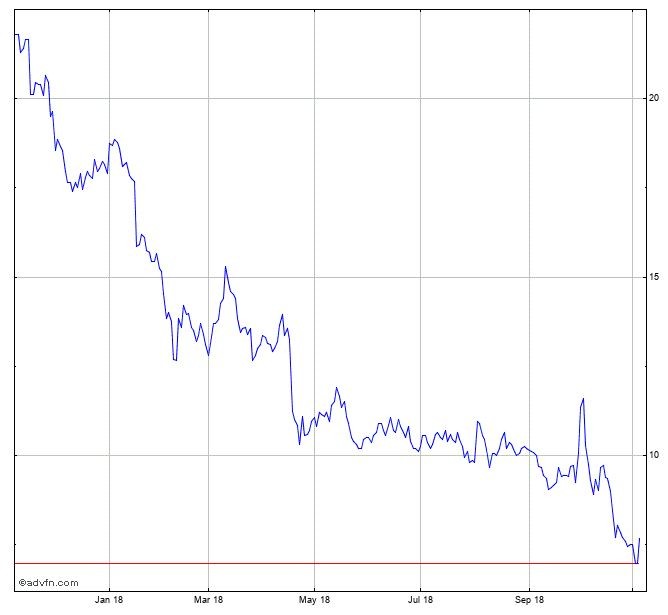
Jahreschart, Stand 7.11.2018
Charts sind Screenshots zur Dokumentation!!!

Jahreschart, Stand 7.11.2018

Intradaychart von heute!
Quelle: IHUB
Paratek Pharmaceuticals, Inc. (PRTK)
Kurs am 07.11.2018 – 7,00 $ (mein Einstieg heute Nachmittag bei 7,35$)
Hier möchte ich einen Wert vorstellen, der meiner Meinung nach in den nächsten Monaten hypen wird.
Wer gern antizyklisch handelt und gern in Werte einsteigt, die vielleicht zur Zeit nicht so „hipp“ sind, der könnte hier fündig werden.
Hier gab es zwei ziemlich heftige Intradayreversals hintereinander, so dass ich glaube, der Boden wurde markiert.
Antibiotika, es wird viel darüber gesprochen, doch niemand traut sich so recht ran an diese „Perle“.
Paratek hat Anfang Oktober gleich mehrere Zulassungen bekommen,
was bei MJ – Werten zu mehreren hundert Prozent Ausschlägen geführt hätte.
Diese Perle wird dagegen seit einigen Monaten und speziell seit der Zulassung gehandelt wie Sauerbier.
Ich bin der Meinung, dass jetzt ein echt guter Zeitpunkt gekommen ist, um einzusteigen.
Alles unter 12€ ist derzeitig ein guter Deal. (mM)
Ein paar links zum Einlesen folgen zeitnah.
Würde mich freuen, wenn ich dadurch den Anstoß zu einer steilen Reise für einige Mitleser / Beteiligte geben konnte.
Viel Erfolg / Glück / Spaß
Ich werde mich nur mit links, Kopien oder Meinungen beteiligen können (und auch das aus Zeitgründen nur begrenzt).
Für eine wissenschaftliche Bemerkung fehlt mir der Horizont.
Aber vielleicht werden sich hier auch Personen anschließen,
welche uns an ihrem Wissen bzw. ihrer fachlichen Meinung teilhaben lassen.
Noch ein paar Daten von heute (20.00 Uhr).
Quelle yahoo
Day's Range - 6.27 - 7.62
52 Week Range - 6.27 - 22.45
Volume - 1,529,543
Avg. Volume - 810,253
Market Cap – 240 Mio
...und wie ich es so schreibe, wandern wir Richtung 7,70 -> cool
Kurs am 07.11.2018 – 7,00 $ (mein Einstieg heute Nachmittag bei 7,35$)
Hier möchte ich einen Wert vorstellen, der meiner Meinung nach in den nächsten Monaten hypen wird.
Wer gern antizyklisch handelt und gern in Werte einsteigt, die vielleicht zur Zeit nicht so „hipp“ sind, der könnte hier fündig werden.
Hier gab es zwei ziemlich heftige Intradayreversals hintereinander, so dass ich glaube, der Boden wurde markiert.
Antibiotika, es wird viel darüber gesprochen, doch niemand traut sich so recht ran an diese „Perle“.
Paratek hat Anfang Oktober gleich mehrere Zulassungen bekommen,
was bei MJ – Werten zu mehreren hundert Prozent Ausschlägen geführt hätte.
Diese Perle wird dagegen seit einigen Monaten und speziell seit der Zulassung gehandelt wie Sauerbier.
Ich bin der Meinung, dass jetzt ein echt guter Zeitpunkt gekommen ist, um einzusteigen.
Alles unter 12€ ist derzeitig ein guter Deal. (mM)
Ein paar links zum Einlesen folgen zeitnah.
Würde mich freuen, wenn ich dadurch den Anstoß zu einer steilen Reise für einige Mitleser / Beteiligte geben konnte.
Viel Erfolg / Glück / Spaß
Ich werde mich nur mit links, Kopien oder Meinungen beteiligen können (und auch das aus Zeitgründen nur begrenzt).
Für eine wissenschaftliche Bemerkung fehlt mir der Horizont.
Aber vielleicht werden sich hier auch Personen anschließen,
welche uns an ihrem Wissen bzw. ihrer fachlichen Meinung teilhaben lassen.
Noch ein paar Daten von heute (20.00 Uhr).
Quelle yahoo
Day's Range - 6.27 - 7.62
52 Week Range - 6.27 - 22.45
Volume - 1,529,543
Avg. Volume - 810,253
Market Cap – 240 Mio
...und wie ich es so schreibe, wandern wir Richtung 7,70 -> cool





















