Sirona Biochem (Seite 2390)
eröffnet am 23.06.13 12:55:10 von
neuester Beitrag 08.05.24 17:10:08 von
neuester Beitrag 08.05.24 17:10:08 von
Beiträge: 31.047
ID: 1.183.167
ID: 1.183.167
Aufrufe heute: 4
Gesamt: 5.404.337
Gesamt: 5.404.337
Aktive User: 0
ISIN: CA82967M1005 · WKN: A0RM6R
0,0435
EUR
-5,43 %
-0,0025 EUR
Letzter Kurs 13.05.24 Tradegate
Neuigkeiten
07.05.24 · IRW Press |
07.05.24 · globenewswire |
08.04.24 · globenewswire |
05.04.24 · globenewswire |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 3,0100 | +40,65 | |
| 12,810 | +38,49 | |
| 2,5300 | +38,25 | |
| 2,5150 | +37,73 | |
| 4,3800 | +32,33 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 3,9900 | -19,39 | |
| 2,4100 | -20,98 | |
| 0,9900 | -27,21 | |
| 2,8500 | -33,18 | |
| 0,6162 | -56,61 |
Beitrag zu dieser Diskussion schreiben
Antwort auf Beitrag Nr.: 58.195.760 von techinvestor69 am 12.07.18 11:31:32sind doch 1 Mio oder ?
Die Pipeline ist voll und äusserst interessant - wenn doch endlich ein Deal des Skinlighteners zustande käme ...
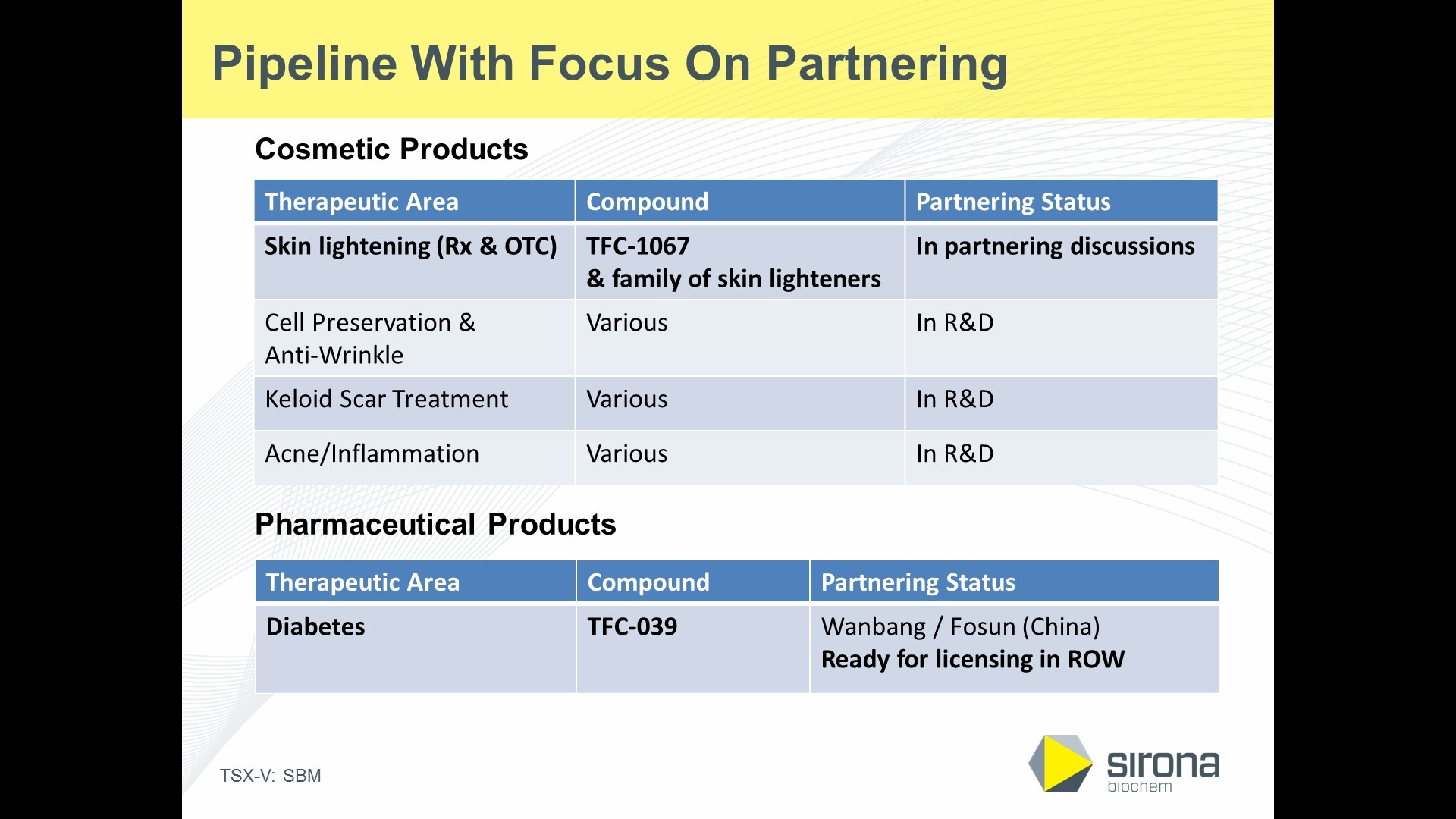

Zur Erinnerung - mal gespannt, was das bald zu erwartende Update bringen wird ...












Antwort auf Beitrag Nr.: 58.195.550 von Geheimnisvoller am 12.07.18 11:12:42500.000 USD sollten bald als Meilensteinzahlung kommen
Vielleicht können sie jetzt Wanbang auch die ROW-Rechte an dem Wirkstoff verkaufen.
Vielleicht können sie jetzt Wanbang auch die ROW-Rechte an dem Wirkstoff verkaufen.
Antwort auf Beitrag Nr.: 58.192.295 von techinvestor69 am 11.07.18 22:39:23Hallo techinvestor,
gut wieder von Dir zu hören - lange geruht.
Wie schätzt Du die Situation real ein? Danke für Antwort
gut wieder von Dir zu hören - lange geruht.
Wie schätzt Du die Situation real ein? Danke für Antwort
Antwort auf Beitrag Nr.: 58.192.016 von Geheimnisvoller am 11.07.18 22:01:26sehr gut!
triggert die Meilensteinzahlung
triggert die Meilensteinzahlung

Das ist eine super News - http://iis.aastocks.com/20180711/003200106-0.PDF
Die Hong Kong Exchanges and Clearing Limited und die Stock Exchange of Hong Kong Limited sind nicht verantwortlich für den Inhalt dieser Ankündigung und sind nicht korrekt oder vollständig. In Bezug auf jegliche Art von Erklärung und ausdrücklich auf jegliche Schäden, die sich aus oder im Zusammenhang mit dieser Ankündigung ergeben. Verlor jede Verantwortung. Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. * (eine Aktiengesellschaft mit Sitz in der Volksrepublik China) ( Bestellnummer : 02196 ) Übersee-Regulierungsankündigung Diese Bekanntmachung erfolgt gemäß Regel 13.10B der Regeln für die Notierung von Wertpapieren an der Börse von Hongkong Limited. Das Folgende ist die Liste von Shanghai Fosun Pharmaceutical (Group) Co., Ltd (die "Gesellschaft") auf der Website der Shanghai Stock Exchange. Die Bekanntgabe der Genehmigung der klinischen Prüfung durch die Holding-Tochter dient nur als Referenz. Vom Vorstand Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Vorsitzender Chen Qiyu Volksrepublik China, Shanghai 11. Juli 2018 Zum Datum dieser Bekanntmachung sind die geschäftsführenden Direktoren der Gesellschaft Herr Chen Qiyu, Herr Yao Fang und Herr Wu Yifang, der nicht geschäftsführende Direktor des Unternehmens ist Wang Qunbin Xian Herr Sheng, Herr Wang Can, Frau Mu Haining und Herr Zhang Xueqing und die unabhängigen nicht geschäftsführenden Direktoren des Unternehmens sind Herr Cao Huimin, Herr Jiang Xian, Herr Huang Tianyou Doktor und Herr Wei Shaoqi. * Nur zur Identifikation
Seite 2
1 Stockcode: 600196 Abkürzung für Lagerbestände: Fosun Pharma Code: Pro 2018-084 Bond-Code: 136236 Bond Abkürzung: 16 Verbindung Medizin 01 Bond-Code: 143020 Bond Abkürzung: 17 Verbindung Medizin 01 Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Bekanntmachung über die Genehmigung der klinischen Prüfung der Holdinggesellschaft Der Verwaltungsrat und alle Geschäftsführer des Unternehmens garantieren, dass keine falschen Aufzeichnungen oder irreführenden Angaben im Inhalt dieser Bekanntmachung enthalten sind Signifikante Auslassungen und tragen individuelle und gemeinsame Verantwortung für die Authentizität, Richtigkeit und Vollständigkeit ihrer Inhalte. I. Überblick Kürzlich, Shanghai Fosun Pharmaceutical (Group) Co., Ltd (im Folgenden als "das Unternehmen") Tochtergesellschaften Biochemical Pharmaceutical Group Co., Ltd Jiangsu Wanbang (im Folgenden als "Wanbang Medizin") erhielt die National Drug Administration Die Behörde (früher die staatliche Lebensmittel- und Arzneimittelbehörde; im Folgenden als "Staatliche Behörde für die Überwachung von Nahrungs- und Arzneimitteln" bezeichnet) Wangralie Tabletten (im Folgenden als "das neue Medikament" bezeichnet) sind für klinische Studien von Indikationen für Typ-2-Diabetes zugelassen. Wanbang Das Medikament wird voraussichtlich in naher Zukunft auch die klinische Phase-I-Studie des neuen Medikaments durchführen. Zweitens, die Grundsituation der neuen Droge Medikamentenname: Wan Geli Tablet Dosierungsform: Tablette Spezifikationen: 5mg, 10mg, 25mg Registrierungskategorie: Chemikalien Kategorie 1 Antragsteller: Wanbang Medizin Empfangsnummer: CXHL1700351, CXHL1700352, CXHL1700353 Zulassungsnummer: 2018L02705, 2018L02706, 2018L02707 Schlussfolgerung: Dieses Produkt wurde für klinische Studien zugelassen
Seite 3
2 Drittens, die Forschungssituation der neuen Droge Im Dezember 2017 wurde das neue Medikament in der klinischen Zulassungsstudie der staatlichen Arzneimittelbehörde für Indikationen für Typ-2-Diabetes eingesetzt. Akzeptiert. Das neue Medikament ist ein SGLT-2-Hemmer und wird hauptsächlich zur Behandlung von Typ-2-Diabetes eingesetzt. Das neue Medikament von Sirona Wanbang Pharmaceutical wurde unabhängig von Biochem Corp. im Jahr 2014 von Sirona Biochem Corp. in China zugelassen. F & E, Produktion, Kommerzialisierung, etc. werden in dem Gebiet durchgeführt (ausgenommen Hong Kong, Macao und Taiwan Regionen, die gleichen unten). Zum Datum dieser Bekanntmachung sind die in China gelisteten SGLT-2-Hemmer AstraZene® von AstraZeneca . Ou Tangjing® von Boehringer Ingelheim International, Deutschland . Nach den neuesten Daten von IQVIA CHPA (zur Verfügung gestellt von IQVIA, IQVIA ist der weltweit führende Anbieter von professionellen Informations- und Strategieberatungsdienstleistungen für die Gesundheitsbranche, 2017, Der Umsatz von SGLT-2-Hemmern in China betrug ca. 5,35 Mio. RMB. Im Juni 2018 hat die Gruppe (die Gesellschaft und ihre Tochtergesellschaften) das neue Medikament in diesem Stadium ins Visier genommen. Die Investition in Forschung und Entwicklung kostet ca. 36 Mio. RMB (ungeprüft). Viertens, Risiko-Tipps Nach den Erfahrungen der neuen Arzneimittelforschung und -entwicklung bestehen gewisse Risiken bei der Entwicklung neuer Medikamente wie Phase I, Phase II und / oder Phase III. (Falls zutreffend) Klinische Studien können aufgrund von Sicherheits- und / oder Wirksamkeitsproblemen abgebrochen werden. Gemäß den regulatorischen Anforderungen für die Entwicklung neuer Medikamente in China, das neue Medikament muss noch eine Reihe von klinischen Forschung und Nachdem die Arzneimittelprüfungsabteilung die Zulassung genehmigt hat, kann sie aufgelistet werden. Neue Arzneimittelforschung und -entwicklung ist eine langfristige Arbeit, es gibt viele unsichere Faktoren, Investoren wird geraten, auf Investitionsrisiken zu achten. Es wird hiermit bekannt gegeben. Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Vorstand 11. Juli 2018
Die Hong Kong Exchanges and Clearing Limited und die Stock Exchange of Hong Kong Limited sind nicht verantwortlich für den Inhalt dieser Ankündigung und sind nicht korrekt oder vollständig. In Bezug auf jegliche Art von Erklärung und ausdrücklich auf jegliche Schäden, die sich aus oder im Zusammenhang mit dieser Ankündigung ergeben. Verlor jede Verantwortung. Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. * (eine Aktiengesellschaft mit Sitz in der Volksrepublik China) ( Bestellnummer : 02196 ) Übersee-Regulierungsankündigung Diese Bekanntmachung erfolgt gemäß Regel 13.10B der Regeln für die Notierung von Wertpapieren an der Börse von Hongkong Limited. Das Folgende ist die Liste von Shanghai Fosun Pharmaceutical (Group) Co., Ltd (die "Gesellschaft") auf der Website der Shanghai Stock Exchange. Die Bekanntgabe der Genehmigung der klinischen Prüfung durch die Holding-Tochter dient nur als Referenz. Vom Vorstand Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Vorsitzender Chen Qiyu Volksrepublik China, Shanghai 11. Juli 2018 Zum Datum dieser Bekanntmachung sind die geschäftsführenden Direktoren der Gesellschaft Herr Chen Qiyu, Herr Yao Fang und Herr Wu Yifang, der nicht geschäftsführende Direktor des Unternehmens ist Wang Qunbin Xian Herr Sheng, Herr Wang Can, Frau Mu Haining und Herr Zhang Xueqing und die unabhängigen nicht geschäftsführenden Direktoren des Unternehmens sind Herr Cao Huimin, Herr Jiang Xian, Herr Huang Tianyou Doktor und Herr Wei Shaoqi. * Nur zur Identifikation
Seite 2
1 Stockcode: 600196 Abkürzung für Lagerbestände: Fosun Pharma Code: Pro 2018-084 Bond-Code: 136236 Bond Abkürzung: 16 Verbindung Medizin 01 Bond-Code: 143020 Bond Abkürzung: 17 Verbindung Medizin 01 Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Bekanntmachung über die Genehmigung der klinischen Prüfung der Holdinggesellschaft Der Verwaltungsrat und alle Geschäftsführer des Unternehmens garantieren, dass keine falschen Aufzeichnungen oder irreführenden Angaben im Inhalt dieser Bekanntmachung enthalten sind Signifikante Auslassungen und tragen individuelle und gemeinsame Verantwortung für die Authentizität, Richtigkeit und Vollständigkeit ihrer Inhalte. I. Überblick Kürzlich, Shanghai Fosun Pharmaceutical (Group) Co., Ltd (im Folgenden als "das Unternehmen") Tochtergesellschaften Biochemical Pharmaceutical Group Co., Ltd Jiangsu Wanbang (im Folgenden als "Wanbang Medizin") erhielt die National Drug Administration Die Behörde (früher die staatliche Lebensmittel- und Arzneimittelbehörde; im Folgenden als "Staatliche Behörde für die Überwachung von Nahrungs- und Arzneimitteln" bezeichnet) Wangralie Tabletten (im Folgenden als "das neue Medikament" bezeichnet) sind für klinische Studien von Indikationen für Typ-2-Diabetes zugelassen. Wanbang Das Medikament wird voraussichtlich in naher Zukunft auch die klinische Phase-I-Studie des neuen Medikaments durchführen. Zweitens, die Grundsituation der neuen Droge Medikamentenname: Wan Geli Tablet Dosierungsform: Tablette Spezifikationen: 5mg, 10mg, 25mg Registrierungskategorie: Chemikalien Kategorie 1 Antragsteller: Wanbang Medizin Empfangsnummer: CXHL1700351, CXHL1700352, CXHL1700353 Zulassungsnummer: 2018L02705, 2018L02706, 2018L02707 Schlussfolgerung: Dieses Produkt wurde für klinische Studien zugelassen
Seite 3
2 Drittens, die Forschungssituation der neuen Droge Im Dezember 2017 wurde das neue Medikament in der klinischen Zulassungsstudie der staatlichen Arzneimittelbehörde für Indikationen für Typ-2-Diabetes eingesetzt. Akzeptiert. Das neue Medikament ist ein SGLT-2-Hemmer und wird hauptsächlich zur Behandlung von Typ-2-Diabetes eingesetzt. Das neue Medikament von Sirona Wanbang Pharmaceutical wurde unabhängig von Biochem Corp. im Jahr 2014 von Sirona Biochem Corp. in China zugelassen. F & E, Produktion, Kommerzialisierung, etc. werden in dem Gebiet durchgeführt (ausgenommen Hong Kong, Macao und Taiwan Regionen, die gleichen unten). Zum Datum dieser Bekanntmachung sind die in China gelisteten SGLT-2-Hemmer AstraZene® von AstraZeneca . Ou Tangjing® von Boehringer Ingelheim International, Deutschland . Nach den neuesten Daten von IQVIA CHPA (zur Verfügung gestellt von IQVIA, IQVIA ist der weltweit führende Anbieter von professionellen Informations- und Strategieberatungsdienstleistungen für die Gesundheitsbranche, 2017, Der Umsatz von SGLT-2-Hemmern in China betrug ca. 5,35 Mio. RMB. Im Juni 2018 hat die Gruppe (die Gesellschaft und ihre Tochtergesellschaften) das neue Medikament in diesem Stadium ins Visier genommen. Die Investition in Forschung und Entwicklung kostet ca. 36 Mio. RMB (ungeprüft). Viertens, Risiko-Tipps Nach den Erfahrungen der neuen Arzneimittelforschung und -entwicklung bestehen gewisse Risiken bei der Entwicklung neuer Medikamente wie Phase I, Phase II und / oder Phase III. (Falls zutreffend) Klinische Studien können aufgrund von Sicherheits- und / oder Wirksamkeitsproblemen abgebrochen werden. Gemäß den regulatorischen Anforderungen für die Entwicklung neuer Medikamente in China, das neue Medikament muss noch eine Reihe von klinischen Forschung und Nachdem die Arzneimittelprüfungsabteilung die Zulassung genehmigt hat, kann sie aufgelistet werden. Neue Arzneimittelforschung und -entwicklung ist eine langfristige Arbeit, es gibt viele unsichere Faktoren, Investoren wird geraten, auf Investitionsrisiken zu achten. Es wird hiermit bekannt gegeben. Shanghai Fosun Pharmazeutische (Gruppe) Co., Ltd. Vorstand 11. Juli 2018
Aus Stockhouse:
Phase 1 will start soon
Zhitong Finance APP News, Fosun Pharma (02196) announced that recently, the company's controlling subsidiary, Jiangsu Wanbang Biochemical Pharmaceutical Group Co., Ltd., received the approval from the State Drug Administration for the approval of Wangralie tablets for the indication of type II diabetes. Approval of the test. Wanbang Medicine also plans to launch the Phase I trial of the new drug in the near future. In December 2017, the new drug for the indication for type 2 diabetes was accepted and accepted by the State Food and Drug Administration for clinical trial registration. The new drug is a SGLT-2 inhibitor and is mainly used for the treatment of type II diabetes. The new drug was independently developed by Sirona Biochem Corp., and in 2014, Wanbang Pharmaceutical was authorized by Sirona Biochem Corp. to conduct research and development, production and commercialization in China.
Read more at http://www.stockhouse.com/companies/bullboard#0e15CdjqoSQK1H…
Phase 1 will start soon
Zhitong Finance APP News, Fosun Pharma (02196) announced that recently, the company's controlling subsidiary, Jiangsu Wanbang Biochemical Pharmaceutical Group Co., Ltd., received the approval from the State Drug Administration for the approval of Wangralie tablets for the indication of type II diabetes. Approval of the test. Wanbang Medicine also plans to launch the Phase I trial of the new drug in the near future. In December 2017, the new drug for the indication for type 2 diabetes was accepted and accepted by the State Food and Drug Administration for clinical trial registration. The new drug is a SGLT-2 inhibitor and is mainly used for the treatment of type II diabetes. The new drug was independently developed by Sirona Biochem Corp., and in 2014, Wanbang Pharmaceutical was authorized by Sirona Biochem Corp. to conduct research and development, production and commercialization in China.
Read more at http://www.stockhouse.com/companies/bullboard#0e15CdjqoSQK1H…
Antwort auf Beitrag Nr.: 58.191.836 von freixenetter am 11.07.18 21:39:31ich hab noch 7stellig Restbestand zu 0,08.. ich kauf nix
Antwort auf Beitrag Nr.: 58.191.680 von Hrubesch09 am 11.07.18 21:27:48100 000 bei lang und schwarz... eine aufmerksame seele
Sirona Biochem



















