Biomira zweiter Anlauf mit den biotherapeutischer Impfstoff BLP25 - 500 Beiträge pro Seite (Seite 2)
eröffnet am 31.07.03 14:21:39 von
neuester Beitrag 11.12.07 18:28:33 von
neuester Beitrag 11.12.07 18:28:33 von
Beiträge: 2.812
ID: 759.932
ID: 759.932
Aufrufe heute: 0
Gesamt: 161.592
Gesamt: 161.592
Aktive User: 0
ISIN: CA09161R1064 · WKN: 881836
Dem Volumen zufolge werden morgen die Zahlen erst nach Börsenschluss kommen,
das kann ja hier vorher noch mal heiter werden!!!!!
das kann ja hier vorher noch mal heiter werden!!!!!

@BaronvonMünchhausen
etwas geduld bitte und einen
schönen Abend noch!
Ciao
verdi
etwas geduld bitte und einen
schönen Abend noch!
Ciao
verdi
Biomira Inc. Announces 4th Quarter and Year-End Results
EDMONTON, Feb 26, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) today reported financial results for the fiscal year ended December 31, 2003 reflecting a 39 per cent reduction in net loss as compared to the same period last year.
Financial results for the twelve months ended December 31, 2003 indicate a consolidated net loss from operations of $19.0 million or $0.31 per share compared to $31.4 million or $0.68 per share for the same period in 2002. The lower loss of $12.4 million in 2003 is due to a $13.6 million reduction in gross research and development expenditures, a $1.2 million reduction in general and administrative expenses, a $0.8 million reduction in marketing and business development expenses, and a $0.9 million reduction in amortization of capital assets, offset by lower investment and other income of $2.2 million and lower revenue of $1.9 million. The savings result largely from both the winding down of the Theratope(R) vaccine Phase III trial and the Company`s cost reduction initiative announced in October 2002.
Contract research and development revenue for the twelve months ended December 31, 2003, totalling $2.3 million compared to $4.0 million for the same period in 2002, represents research and development funding received from Merck KGaA of Darmstadt, Germany associated with Theratope and BLP25 Liposomal vaccine (L-BLP25). The lower funding level reflects the wind down of the Theratope Phase III metastatic breast cancer clinical trial. Licensing revenues from collaborative arrangements with Merck KGaA represent the amortization of upfront payments received from Merck KGaA upon commencement of the collaboration. The decrease of $0.2 million in licensing, royalties and other revenue relates to a one-time research project in 2002.
Research and development expenditures for the twelve months ended December 31, 2003 totalled $14.7 million compared to $28.3 million for the same period in 2002. The decrease in research and development expenditures is also attributable to winding down the Theratope Phase III trial, and reduction of Biomira`s discovery research programs. General and administrative expenses for the twelve months ended December 31, 2003 declined to $5.9 million compared to $7.1 million for the same period in 2002. Marketing and business development expenditures for the twelve months ended December 31, 2003 decreased to $1.3 million compared to $2.1 million for the same period in 2002, and reflect the deferral of expenditures related to Theratope pre-launch activities. Marketing and business development expenditures include costs to develop Biomira`s internal marketing capabilities, as well as Theratope pre- launch marketing activities jointly undertaken and funded with Merck KGaA.
Investment and other income for the twelve months ended December 31, 2003, indicate a net expense of $0.3 million compared to a net revenue of $2.0 million for the same period in 2002. Investment and other income comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. Investment income for the twelve months ended December 31, 2003 totalled $1.0 million compared to $2.2 million for the same period in 2002 due to lower average cash and investment balances. A combination of realized and unrealized foreign exchange losses totalled $1.3 million for the twelve months ended December 31, 2003, compared to losses of $0.2 million for the same period in 2002. The higher foreign exchange loss results mainly from the depreciation of the US dollar.
Biomira`s financial reserves total $41.5 million in cash and short-term investments as at December 31, 2003. The net increase of $4.3 million is attributable to new financing in 2003 totalling $36.3 million offset by debt retirement of $8.1 million and $23.9 million used for operations.
This past year was an eventful one in the history of the Company. The final analysis of the Theratope vaccine Phase III trial was completed in June 2003, with the results indicating that the difference between the vaccine and the control was not statistically significant in the overall patient population when looking at survival and time to disease progression. However, one pre-stratified subset of more than 300 women in the Phase III trial who received hormonal treatment following chemotherapy showed a favourable trend toward improvement in survival. Biomira and its collaborator, Merck KGaA of Darmstadt, Germany, are continuing analyses of the data from this pre- stratified subset.
In December the Company announced that additional survival follow-up data and adjustments to the original database, including correction for mis-stratifications and mis-randomizations, had been completed. As reported at that time, results for the subgroup of women on hormonal treatment showed a median time to disease progression of 8.3 months for women treated with Theratope versus 5.8 months for those women on control (Cox p(equal sign)0.220; Log Rank p(equal sign)0.207). The median survival was 38.2 months for women treated with Theratope, while women on control saw a median survival of 30.7 months (Cox p(equal sign)0.077; Log Rank p(equal sign)0.066), a difference of 7.5 months, while not statistically significant, certainly is, in our opinion, clinically important.
While the subset data probably do not support a registration at this time, further analyses are being conducted to attempt to explore a potential mechanism of action in this interesting subset of women. Further development plans are being considered at this time. Once our strategy is matured, we intend to discuss our plans, which may include a Phase III trial, with regulatory authorities.
In 2003 Biomira and Merck KGaA also continued their Theratope Phase II trial in women with metastatic breast cancer who are being treated with aromatase inhibitors, a type of hormonal therapy, or Faslodex(R) (fulvestrant), an estrogen-receptor antagonist. The study`s primary objective is to determine the response of the immune system in these women. Additional endpoints are the safety and tolerability of this combination of treatment. Under the collaboration with Merck KGaA, this trial is being managed by Merck KGaA`s US affiliate, EMD Pharmaceuticals Inc., and is expected to fully enroll the planned 95 women by mid-year 2004.
With regard to Biomira`s follow-on product candidate, L-BLP25, the Companies continue to follow the 171 patients with Stage IIIb and Stage IV lung cancer enrolled in the Phase IIb study. The clinical trial analysis is expected to be completed at the end of March, with results forthcoming shortly thereafter.
"We are also very excited about the potential for this second product candidate," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc. "In addition to evaluating the data from the Phase IIb non-small cell lung cancer (NSCLC) study, Biomira continues to evaluate the potential role of L-BLP25 for this and other indications."
Biomira also continues to gather and evaluate data from the L-BLP25 vaccine Phase II pilot study of men with prostate cancer. A 16-patient L-BLP25 Phase II pilot study in patients with rising prostate specific antigen (PSA) post-radical prostatectomy was conducted to determine whether the vaccine could reduce or stabilize PSA levels. L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients. Preliminary results in this small patient population did not conclusively show a reduction or stabilization of serum PSA levels. However, there appears to be a prolongation of PSA doubling time (PSADT) in just under 40% of the patients. While there has been no commitment to conduct further trials at this time in this indication, the patients continue to be followed for PSA levels for a period of 12 months following their last vaccination. A future decision on indications to be pursued will likely follow further understanding of the prostate data coupled with an understanding of the results from the Phase IIb lung study.
"The year 2004 will be an exciting one for the Company, our investors and the scientific community. We look forward to receiving the clinical trial results of the Phase IIb L-BLP25 trial in NSCLC and we will continue to advance our understanding of the data more fully from our two lead product candidates. When appropriate, we will request a formal meeting with the regulatory authorities," said Alex McPherson. "I would like to thank the investment community for its continued support during 2003 and the women and men who have participated in our clinical trials."
Merck KGaA
Biomira is collaborating with Merck KGaA of Darmstadt, Germany on the development of Theratope and L-BLP25 vaccines. Founded in 1668, Merck KGaA has positioned itself to be on the cutting edge of cancer research with an oncology portfolio based on four technology platforms - monoclonal antibodies, vaccines, immunocytokines and angiogenesis inhibitors.
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
Biomira Inc.
CONSOLIDATED BALANCE SHEETS
(Canadian dollars, in thousands, except number of shares)
<<
December 31, 2003 December 31, 2002
(Unaudited) (Unaudited)(x)
---------------------------------------
ASSETS
Current
Cash and cash equivalents $ 24,062 $ 8,507
Short-term investments 17,443 28,682
Accounts receivable 459 1,207
Prepaid expenses 460 497
---------------------------------------
42,424 38,893
Capital assets (net) 641 1,076
---------------------------------------
$ 43,065 $ 39,969
---------------------------------------
---------------------------------------
LIABILITIES
Current
Accounts payable and accrued
liabilities $ 3,453 $ 8,580
Current portion of capital
lease obligation 108 169
Accrued interest on convertible
debentures - 28
Current portion of deferred
revenue 1,053 1,053
---------------------------------------
4,614 9,830
Capital lease obligation - 96
Deferred revenue 6,671 7,724
Class A preference shares 30 30
---------------------------------------
11,315 17,680
SHAREHOLDERS` EQUITY
Share capital 359,643 328,537
Convertible debentures - 7,614
Warrants 8,555 3,338
Contributed surplus 8,901 8,901
Deficit (345,349) (326,101)
---------------------------------------
31,750 22,289
---------------------------------------
$ 43,065 $ 39,969
---------------------------------------
---------------------------------------
Common Shares Issued and
Outstanding 72,545,232 53,795,573
(CAD $1.00 (equal sign) USD $0.77)
(x) Figures excerpted from the 2002 audited consolidated financial
statements.
Biomira Inc.
CONSOLIDATED STATEMENTS OF OPERATIONS
(Canadian dollars, in thousands, except per share amounts)
Three Months Ended Twelve Months Ended
December 31 December 31
(Unaudited) (Unaudited) (Unaudited) (Unaudited)(x)
--------------------------------------------------
2003 2002 2003 2002
---- ---- ---- ----
REVENUE
Contract research and
development $ 358 $ 951 $ 2,309 $ 3,967
Licensing revenue
from collaborative
agreements 263 264 1,053 1,054
Licensing, royalties
and other revenue 53 61 54 283
-------------------------------------------------
674 1,276 3,416 5,304
-------------------------------------------------
EXPENSES
Research and
development 2,853 7,633 14,700 28,304
General and
administrative 1,519 1,625 5,920 7,108
Marketing and
business
development 354 762 1,321 2,140
Amortization of
capital assets 96 622 446 1,349
-------------------------------------------------
4,822 10,642 22,387 38,901
-------------------------------------------------
OPERATING LOSS (4,148) (9,366) (18,971) (33,597)
Investment and other
(expense) income (753) 467 (295) 1,990
Interest expense (3) (7) (20) (43)
Gain on disposal of
capital assets 3 - 61 -
-------------------------------------------------
LOSS BEFORE INCOME
TAXES (4,901) (8,906) (19,225) (31,650)
Income tax benefit 269 356 251 291
-------------------------------------------------
NET LOSS $(4,632) $(8,550) $(18,974) $(31,359)
-------------------------------------------------
-------------------------------------------------
BASIC AND DILUTED
LOSS PER SHARE $(0.07) $(0.18) $(0.31) $(0.68)
WEIGHTED AVERAGE NUMBER
OF COMMON SHARES
OUTSTANDING 62,498 52,996 62,498 52,996
CONSOLIDATED STATEMENTS OF DEFICIT
(Canadian dollars, in thousands)
Three Months Ended Twelve Months Ended
December 31 December 31
(Unaudited) (Unaudited) (Unaudited) (Unaudited)(x)
--------------------------------------------------
2003 2002 2003 2002
---- ---- ---- ----
DEFICIT, BEGINNING OF
PERIOD $ (340,717) $ (316,690) $ (326,101) $ (290,116)
Net loss for the
period (4,632) (8,550) (18,974) (31,359)
Accretion of
convertible
debentures - (777) (713) (4,036)
Interest, foreign
exchange gain/loss,
and carrying charges
on debentures - (84) 439 (590)
--------------------------------------------------
DEFICIT, END OF
PERIOD $ (345,349) $ (326,101) $ (345,349) $ (326,101)
--------------------------------------------------
--------------------------------------------------
(x) Figures excerpted from the 2002 audited consolidated financial
statements.
Biomira Inc.
CONSOLIDATED STATEMENTS OF CASH FLOW
(Canadian dollars, in thousands)
Three Months Ended Twelve Months Ended
December 31 December 31
(Unaudited) (Unaudited) (Unaudited) (Unaudited)(x)
--------------------------------------------------
2003 2002 2003 2002
---- ---- ---- ----
OPERATING
Net loss $ (4,632) $ (8,550) $ (18,974) $ (31,359)
Amortization of
capital assets 96 622 446 1,349
Gain on disposal
of capital assets (3) - (61) -
Unrealized foreign
exchange (gain)
loss (44) (19) 189 (39)
Deferred revenue (263) (264) (1,053) (1,054)
Net change in
non-cash balances
from operations:
Accounts receivable 108 29 733 194
Prepaid expenses (85) (29) 37 (28)
Accounts payable
and accrued
liabilities (424) (768) (5,127) (5,419)
--------------------------------------------------
(5,247) (8,979) (23,810) (36,356)
INVESTING
(Increase) Decrease
in short-term
investments (6,514) 13,009 11,239 33,661
Purchase of capital
assets - - (12) (265)
Proceeds on disposal
of capital assets 4 - 77 -
--------------------------------------------------
(6,510) 13,009 11,304 33,396
FINANCING
Proceeds on issue of
common shares, net
of issue costs 20,799 783 36,323 4,940
Proceeds from
convertible
debentures, net of
financing costs - - - (24)
Repayment of
convertible debentures - (4,150) (7,826) (15,213)
Interest on convertible
debentures - (112) (91) (860)
Repayment of capital
lease obligation (41) (42) (156) (204)
--------------------------------------------------
20,758 (3,521) 28,250 (11,361)
Effect of exchange
rate fluctuations
on cash and cash
equivalents 44 19 (189) 39
--------------------------------------------------
INCREASE (DECREASE) IN
CASH AND CASH
EQUIVALENTS 9,045 528 15,555 (14,282)
CASH AND CASH
EQUIVALENTS,
BEGINNING OF PERIOD 15,017 7,979 8,507 22,789
--------------------------------------------------
CASH AND CASH
EQUIVALENTS,
END OF PERIOD $ 24,062 $ 8,507 $ 24,062 $ 8,507
--------------------------------------------------
--------------------------------------------------
>>
(x) Figures excerpted from the 2002 audited consolidated financial
statements.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, the possible outcome of discussions with the regulators, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
SOURCE Biomira Inc.
CONTACT: Edward Taylor, Vice President Finance and
Administration, (780) 490-2806, Jane Tulloch, Director, Investor Relations,
(780) 490-2812 ;
To request a free copy of this organization`s annual report, please go to
http://www.newswire.ca and click on reports@cnw.
(BRA. BIOM)
http://www.prnewswire.com
EDMONTON, Feb 26, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) today reported financial results for the fiscal year ended December 31, 2003 reflecting a 39 per cent reduction in net loss as compared to the same period last year.
Financial results for the twelve months ended December 31, 2003 indicate a consolidated net loss from operations of $19.0 million or $0.31 per share compared to $31.4 million or $0.68 per share for the same period in 2002. The lower loss of $12.4 million in 2003 is due to a $13.6 million reduction in gross research and development expenditures, a $1.2 million reduction in general and administrative expenses, a $0.8 million reduction in marketing and business development expenses, and a $0.9 million reduction in amortization of capital assets, offset by lower investment and other income of $2.2 million and lower revenue of $1.9 million. The savings result largely from both the winding down of the Theratope(R) vaccine Phase III trial and the Company`s cost reduction initiative announced in October 2002.
Contract research and development revenue for the twelve months ended December 31, 2003, totalling $2.3 million compared to $4.0 million for the same period in 2002, represents research and development funding received from Merck KGaA of Darmstadt, Germany associated with Theratope and BLP25 Liposomal vaccine (L-BLP25). The lower funding level reflects the wind down of the Theratope Phase III metastatic breast cancer clinical trial. Licensing revenues from collaborative arrangements with Merck KGaA represent the amortization of upfront payments received from Merck KGaA upon commencement of the collaboration. The decrease of $0.2 million in licensing, royalties and other revenue relates to a one-time research project in 2002.
Research and development expenditures for the twelve months ended December 31, 2003 totalled $14.7 million compared to $28.3 million for the same period in 2002. The decrease in research and development expenditures is also attributable to winding down the Theratope Phase III trial, and reduction of Biomira`s discovery research programs. General and administrative expenses for the twelve months ended December 31, 2003 declined to $5.9 million compared to $7.1 million for the same period in 2002. Marketing and business development expenditures for the twelve months ended December 31, 2003 decreased to $1.3 million compared to $2.1 million for the same period in 2002, and reflect the deferral of expenditures related to Theratope pre-launch activities. Marketing and business development expenditures include costs to develop Biomira`s internal marketing capabilities, as well as Theratope pre- launch marketing activities jointly undertaken and funded with Merck KGaA.
Investment and other income for the twelve months ended December 31, 2003, indicate a net expense of $0.3 million compared to a net revenue of $2.0 million for the same period in 2002. Investment and other income comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. Investment income for the twelve months ended December 31, 2003 totalled $1.0 million compared to $2.2 million for the same period in 2002 due to lower average cash and investment balances. A combination of realized and unrealized foreign exchange losses totalled $1.3 million for the twelve months ended December 31, 2003, compared to losses of $0.2 million for the same period in 2002. The higher foreign exchange loss results mainly from the depreciation of the US dollar.
Biomira`s financial reserves total $41.5 million in cash and short-term investments as at December 31, 2003. The net increase of $4.3 million is attributable to new financing in 2003 totalling $36.3 million offset by debt retirement of $8.1 million and $23.9 million used for operations.
This past year was an eventful one in the history of the Company. The final analysis of the Theratope vaccine Phase III trial was completed in June 2003, with the results indicating that the difference between the vaccine and the control was not statistically significant in the overall patient population when looking at survival and time to disease progression. However, one pre-stratified subset of more than 300 women in the Phase III trial who received hormonal treatment following chemotherapy showed a favourable trend toward improvement in survival. Biomira and its collaborator, Merck KGaA of Darmstadt, Germany, are continuing analyses of the data from this pre- stratified subset.
In December the Company announced that additional survival follow-up data and adjustments to the original database, including correction for mis-stratifications and mis-randomizations, had been completed. As reported at that time, results for the subgroup of women on hormonal treatment showed a median time to disease progression of 8.3 months for women treated with Theratope versus 5.8 months for those women on control (Cox p(equal sign)0.220; Log Rank p(equal sign)0.207). The median survival was 38.2 months for women treated with Theratope, while women on control saw a median survival of 30.7 months (Cox p(equal sign)0.077; Log Rank p(equal sign)0.066), a difference of 7.5 months, while not statistically significant, certainly is, in our opinion, clinically important.
While the subset data probably do not support a registration at this time, further analyses are being conducted to attempt to explore a potential mechanism of action in this interesting subset of women. Further development plans are being considered at this time. Once our strategy is matured, we intend to discuss our plans, which may include a Phase III trial, with regulatory authorities.
In 2003 Biomira and Merck KGaA also continued their Theratope Phase II trial in women with metastatic breast cancer who are being treated with aromatase inhibitors, a type of hormonal therapy, or Faslodex(R) (fulvestrant), an estrogen-receptor antagonist. The study`s primary objective is to determine the response of the immune system in these women. Additional endpoints are the safety and tolerability of this combination of treatment. Under the collaboration with Merck KGaA, this trial is being managed by Merck KGaA`s US affiliate, EMD Pharmaceuticals Inc., and is expected to fully enroll the planned 95 women by mid-year 2004.
With regard to Biomira`s follow-on product candidate, L-BLP25, the Companies continue to follow the 171 patients with Stage IIIb and Stage IV lung cancer enrolled in the Phase IIb study. The clinical trial analysis is expected to be completed at the end of March, with results forthcoming shortly thereafter.
"We are also very excited about the potential for this second product candidate," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc. "In addition to evaluating the data from the Phase IIb non-small cell lung cancer (NSCLC) study, Biomira continues to evaluate the potential role of L-BLP25 for this and other indications."
Biomira also continues to gather and evaluate data from the L-BLP25 vaccine Phase II pilot study of men with prostate cancer. A 16-patient L-BLP25 Phase II pilot study in patients with rising prostate specific antigen (PSA) post-radical prostatectomy was conducted to determine whether the vaccine could reduce or stabilize PSA levels. L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients. Preliminary results in this small patient population did not conclusively show a reduction or stabilization of serum PSA levels. However, there appears to be a prolongation of PSA doubling time (PSADT) in just under 40% of the patients. While there has been no commitment to conduct further trials at this time in this indication, the patients continue to be followed for PSA levels for a period of 12 months following their last vaccination. A future decision on indications to be pursued will likely follow further understanding of the prostate data coupled with an understanding of the results from the Phase IIb lung study.
"The year 2004 will be an exciting one for the Company, our investors and the scientific community. We look forward to receiving the clinical trial results of the Phase IIb L-BLP25 trial in NSCLC and we will continue to advance our understanding of the data more fully from our two lead product candidates. When appropriate, we will request a formal meeting with the regulatory authorities," said Alex McPherson. "I would like to thank the investment community for its continued support during 2003 and the women and men who have participated in our clinical trials."
Merck KGaA
Biomira is collaborating with Merck KGaA of Darmstadt, Germany on the development of Theratope and L-BLP25 vaccines. Founded in 1668, Merck KGaA has positioned itself to be on the cutting edge of cancer research with an oncology portfolio based on four technology platforms - monoclonal antibodies, vaccines, immunocytokines and angiogenesis inhibitors.
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
Biomira Inc.
CONSOLIDATED BALANCE SHEETS
(Canadian dollars, in thousands, except number of shares)
<<
December 31, 2003 December 31, 2002
(Unaudited) (Unaudited)(x)
---------------------------------------
ASSETS
Current
Cash and cash equivalents $ 24,062 $ 8,507
Short-term investments 17,443 28,682
Accounts receivable 459 1,207
Prepaid expenses 460 497
---------------------------------------
42,424 38,893
Capital assets (net) 641 1,076
---------------------------------------
$ 43,065 $ 39,969
---------------------------------------
---------------------------------------
LIABILITIES
Current
Accounts payable and accrued
liabilities $ 3,453 $ 8,580
Current portion of capital
lease obligation 108 169
Accrued interest on convertible
debentures - 28
Current portion of deferred
revenue 1,053 1,053
---------------------------------------
4,614 9,830
Capital lease obligation - 96
Deferred revenue 6,671 7,724
Class A preference shares 30 30
---------------------------------------
11,315 17,680
SHAREHOLDERS` EQUITY
Share capital 359,643 328,537
Convertible debentures - 7,614
Warrants 8,555 3,338
Contributed surplus 8,901 8,901
Deficit (345,349) (326,101)
---------------------------------------
31,750 22,289
---------------------------------------
$ 43,065 $ 39,969
---------------------------------------
---------------------------------------
Common Shares Issued and
Outstanding 72,545,232 53,795,573
(CAD $1.00 (equal sign) USD $0.77)
(x) Figures excerpted from the 2002 audited consolidated financial
statements.
Biomira Inc.
CONSOLIDATED STATEMENTS OF OPERATIONS
(Canadian dollars, in thousands, except per share amounts)
Three Months Ended Twelve Months Ended
December 31 December 31
(Unaudited) (Unaudited) (Unaudited) (Unaudited)(x)
--------------------------------------------------
2003 2002 2003 2002
---- ---- ---- ----
REVENUE
Contract research and
development $ 358 $ 951 $ 2,309 $ 3,967
Licensing revenue
from collaborative
agreements 263 264 1,053 1,054
Licensing, royalties
and other revenue 53 61 54 283
-------------------------------------------------
674 1,276 3,416 5,304
-------------------------------------------------
EXPENSES
Research and
development 2,853 7,633 14,700 28,304
General and
administrative 1,519 1,625 5,920 7,108
Marketing and
business
development 354 762 1,321 2,140
Amortization of
capital assets 96 622 446 1,349
-------------------------------------------------
4,822 10,642 22,387 38,901
-------------------------------------------------
OPERATING LOSS (4,148) (9,366) (18,971) (33,597)
Investment and other
(expense) income (753) 467 (295) 1,990
Interest expense (3) (7) (20) (43)
Gain on disposal of
capital assets 3 - 61 -
-------------------------------------------------
LOSS BEFORE INCOME
TAXES (4,901) (8,906) (19,225) (31,650)
Income tax benefit 269 356 251 291
-------------------------------------------------
NET LOSS $(4,632) $(8,550) $(18,974) $(31,359)
-------------------------------------------------
-------------------------------------------------
BASIC AND DILUTED
LOSS PER SHARE $(0.07) $(0.18) $(0.31) $(0.68)
WEIGHTED AVERAGE NUMBER
OF COMMON SHARES
OUTSTANDING 62,498 52,996 62,498 52,996
CONSOLIDATED STATEMENTS OF DEFICIT
(Canadian dollars, in thousands)
Three Months Ended Twelve Months Ended
December 31 December 31
(Unaudited) (Unaudited) (Unaudited) (Unaudited)(x)
--------------------------------------------------
2003 2002 2003 2002
---- ---- ---- ----
DEFICIT, BEGINNING OF
PERIOD $ (340,717) $ (316,690) $ (326,101) $ (290,116)
Net loss for the
period (4,632) (8,550) (18,974) (31,359)
Accretion of
convertible
debentures - (777) (713) (4,036)
Interest, foreign
exchange gain/loss,
and carrying charges
on debentures - (84) 439 (590)
--------------------------------------------------
DEFICIT, END OF
PERIOD $ (345,349) $ (326,101) $ (345,349) $ (326,101)
--------------------------------------------------
--------------------------------------------------
(x) Figures excerpted from the 2002 audited consolidated financial
statements.
Biomira Inc.
CONSOLIDATED STATEMENTS OF CASH FLOW
(Canadian dollars, in thousands)
Three Months Ended Twelve Months Ended
December 31 December 31
(Unaudited) (Unaudited) (Unaudited) (Unaudited)(x)
--------------------------------------------------
2003 2002 2003 2002
---- ---- ---- ----
OPERATING
Net loss $ (4,632) $ (8,550) $ (18,974) $ (31,359)
Amortization of
capital assets 96 622 446 1,349
Gain on disposal
of capital assets (3) - (61) -
Unrealized foreign
exchange (gain)
loss (44) (19) 189 (39)
Deferred revenue (263) (264) (1,053) (1,054)
Net change in
non-cash balances
from operations:
Accounts receivable 108 29 733 194
Prepaid expenses (85) (29) 37 (28)
Accounts payable
and accrued
liabilities (424) (768) (5,127) (5,419)
--------------------------------------------------
(5,247) (8,979) (23,810) (36,356)
INVESTING
(Increase) Decrease
in short-term
investments (6,514) 13,009 11,239 33,661
Purchase of capital
assets - - (12) (265)
Proceeds on disposal
of capital assets 4 - 77 -
--------------------------------------------------
(6,510) 13,009 11,304 33,396
FINANCING
Proceeds on issue of
common shares, net
of issue costs 20,799 783 36,323 4,940
Proceeds from
convertible
debentures, net of
financing costs - - - (24)
Repayment of
convertible debentures - (4,150) (7,826) (15,213)
Interest on convertible
debentures - (112) (91) (860)
Repayment of capital
lease obligation (41) (42) (156) (204)
--------------------------------------------------
20,758 (3,521) 28,250 (11,361)
Effect of exchange
rate fluctuations
on cash and cash
equivalents 44 19 (189) 39
--------------------------------------------------
INCREASE (DECREASE) IN
CASH AND CASH
EQUIVALENTS 9,045 528 15,555 (14,282)
CASH AND CASH
EQUIVALENTS,
BEGINNING OF PERIOD 15,017 7,979 8,507 22,789
--------------------------------------------------
CASH AND CASH
EQUIVALENTS,
END OF PERIOD $ 24,062 $ 8,507 $ 24,062 $ 8,507
--------------------------------------------------
--------------------------------------------------
>>
(x) Figures excerpted from the 2002 audited consolidated financial
statements.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, the possible outcome of discussions with the regulators, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
SOURCE Biomira Inc.
CONTACT: Edward Taylor, Vice President Finance and
Administration, (780) 490-2806, Jane Tulloch, Director, Investor Relations,
(780) 490-2812 ;
To request a free copy of this organization`s annual report, please go to
http://www.newswire.ca and click on reports@cnw.
(BRA. BIOM)
http://www.prnewswire.com
@donnerpower: Was hältst Du von den Zahlen und den Berichten über die Forschung der Krebsmedikamente???
Ich finde, dass die Kapitaldecke locker für 2004 reicht und hoffe das bis Ende März mit der Entwicklung bzw. Zulassung von L-BLP25 einen entscheidenden Schritt vorwärts kommen.
Dir und allen anderen noch ein schönes Wochenende,
Gruß
Vaio
Ich finde, dass die Kapitaldecke locker für 2004 reicht und hoffe das bis Ende März mit der Entwicklung bzw. Zulassung von L-BLP25 einen entscheidenden Schritt vorwärts kommen.
Dir und allen anderen noch ein schönes Wochenende,
Gruß
Vaio
@Vaio
Ich finde hier sind einige ausschlaggebende Informationen ans Tageslicht gekommen !Ich glaube das man hier mit Blp25 auf einen sehr guten Wege sich befindet,ob man hier schon im März den Durchbruch vollziehen wird,
wird man erst sehen,ABER ACHTUNG eine PhaseIII zur vollständigen Zulassung von BLP25 durch Biomira/Merck ist hir durchaus vorstellbar!
Man beachte bitte das Biomira viele weitere HOCHWERTIGE Produkten in unterschiedlichen Phasen besitzen!!!
TheratopeForschungen werden mit Merck fortgeführt!!!!
This past year was an eventful one in the history of the Company. The final analysis of the Theratope vaccine Phase III trial was completed in June 2003, with the results indicating that the difference between the vaccine and the control was not statistically significant in the overall patient population when looking at survival and time to disease progression. However, one pre-stratified subset of more than 300 women in the Phase III trial who received hormonal treatment following chemotherapy showed a favourable trend toward improvement in survival. Biomira and its collaborator, Merck KGaA of Darmstadt, Germany, are continuing analyses of the data from this pre- stratified subset.
weite interessante Aussagen:
2.
2003 Biomira and Merck KGaA also continued their Theratope Phase II trial in women with metastatic breast cancer who are being treated with aromatase inhibitors, a type of hormonal therapy, or Faslodex® (fulvestrant), an estrogen-receptor antagonist. The study`s primary objective is to determine the response of the immune system in these women. Additional endpoints are the safety and tolerability of this combination of treatment. Under the collaboration with Merck KGaA, this trial is being managed by Merck KGaA`s US affiliate, EMD Pharmaceuticals Inc., and is expected to fully enroll the planned 95 women by mid-year 2004.
3.
With regard to Biomira`s follow-on product candidate, L-BLP25, the Companies continue to follow the 171 patients with Stage IIIb and Stage IV lung cancer enrolled in the Phase IIb study. The clinical trial analysis is expected to be completed at the end of March, with results forthcoming shortly thereafter.
"We are also very excited about the potential for this second product candidate," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc. "In addition to evaluating the data from the Phase IIb non-small cell lung cancer (NSCLC) study, Biomira continues to evaluate the potential role of L-BLP25 for this and other indications."
4.
Biomira also continues to gather and evaluate data from the L-BLP25 vaccine Phase II pilot study of men with prostate cancer. A 16-patient L-BLP25 Phase II pilot study in patients with rising prostate specific antigen (PSA) post-radical prostatectomy was conducted to determine whether the vaccine could reduce or stabilize PSA levels. L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients. Preliminary results in this small patient population did not conclusively show a reduction or stabilization of serum PSA levels. However, there appears to be a prolongation of PSA doubling time (PSADT) in just under 40% of the patients. While there has been no commitment to conduct further trials at this time in this indication, the patients continue to be followed for PSA levels for a period of 12 months following their last vaccination. A future decision on indications to be pursued will likely follow further understanding of the prostate data coupled with an understanding of the results from the Phase IIb lung study.
5.
The year 2004 will be an exciting one for the Company, our investors and the scientific community. We look forward to receiving the clinical trial results of the Phase IIb L-BLP25 trial in NSCLC and we will continue to advance our understanding of the data more fully from our two lead product candidates. When appropriate, we will request a formal meeting with the regulatory authorities," said Alex McPherson.
Ich finde hier sind einige ausschlaggebende Informationen ans Tageslicht gekommen !Ich glaube das man hier mit Blp25 auf einen sehr guten Wege sich befindet,ob man hier schon im März den Durchbruch vollziehen wird,
wird man erst sehen,ABER ACHTUNG eine PhaseIII zur vollständigen Zulassung von BLP25 durch Biomira/Merck ist hir durchaus vorstellbar!
Man beachte bitte das Biomira viele weitere HOCHWERTIGE Produkten in unterschiedlichen Phasen besitzen!!!
TheratopeForschungen werden mit Merck fortgeführt!!!!
This past year was an eventful one in the history of the Company. The final analysis of the Theratope vaccine Phase III trial was completed in June 2003, with the results indicating that the difference between the vaccine and the control was not statistically significant in the overall patient population when looking at survival and time to disease progression. However, one pre-stratified subset of more than 300 women in the Phase III trial who received hormonal treatment following chemotherapy showed a favourable trend toward improvement in survival. Biomira and its collaborator, Merck KGaA of Darmstadt, Germany, are continuing analyses of the data from this pre- stratified subset.
weite interessante Aussagen:
2.
2003 Biomira and Merck KGaA also continued their Theratope Phase II trial in women with metastatic breast cancer who are being treated with aromatase inhibitors, a type of hormonal therapy, or Faslodex® (fulvestrant), an estrogen-receptor antagonist. The study`s primary objective is to determine the response of the immune system in these women. Additional endpoints are the safety and tolerability of this combination of treatment. Under the collaboration with Merck KGaA, this trial is being managed by Merck KGaA`s US affiliate, EMD Pharmaceuticals Inc., and is expected to fully enroll the planned 95 women by mid-year 2004.
3.
With regard to Biomira`s follow-on product candidate, L-BLP25, the Companies continue to follow the 171 patients with Stage IIIb and Stage IV lung cancer enrolled in the Phase IIb study. The clinical trial analysis is expected to be completed at the end of March, with results forthcoming shortly thereafter.
"We are also very excited about the potential for this second product candidate," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc. "In addition to evaluating the data from the Phase IIb non-small cell lung cancer (NSCLC) study, Biomira continues to evaluate the potential role of L-BLP25 for this and other indications."
4.
Biomira also continues to gather and evaluate data from the L-BLP25 vaccine Phase II pilot study of men with prostate cancer. A 16-patient L-BLP25 Phase II pilot study in patients with rising prostate specific antigen (PSA) post-radical prostatectomy was conducted to determine whether the vaccine could reduce or stabilize PSA levels. L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients. Preliminary results in this small patient population did not conclusively show a reduction or stabilization of serum PSA levels. However, there appears to be a prolongation of PSA doubling time (PSADT) in just under 40% of the patients. While there has been no commitment to conduct further trials at this time in this indication, the patients continue to be followed for PSA levels for a period of 12 months following their last vaccination. A future decision on indications to be pursued will likely follow further understanding of the prostate data coupled with an understanding of the results from the Phase IIb lung study.
5.
The year 2004 will be an exciting one for the Company, our investors and the scientific community. We look forward to receiving the clinical trial results of the Phase IIb L-BLP25 trial in NSCLC and we will continue to advance our understanding of the data more fully from our two lead product candidates. When appropriate, we will request a formal meeting with the regulatory authorities," said Alex McPherson.
ABER ACHTUNG eine PhaseIII zur vollständigen Zulassung von BLP25 durch Biomira/Merck ist hir durchaus vorstellbar!
Hier nochmal eine kurze erläuterung:
Alex McPherson spricht zwar davon das man im März Zahlen veröffentlichen will,aber die kompletten Ergebnisse werden
zu einen späteren Zeitpunkt kommen,ich denke man wird hier noch ein paar „allgemeine“ Schwerpunkte zu BLP25 auswerten die bis jetzt nur Nebensache waren!
Trotzdem ist bis jetzt die grosse Spannung, Neugier oder gar Spekulation wie man an der Börse so schön sagt, bezogen auf die Veröffentlichung zum Monat März weiterhin stark vorhanden
Hier nochmal eine kurze erläuterung:
Alex McPherson spricht zwar davon das man im März Zahlen veröffentlichen will,aber die kompletten Ergebnisse werden
zu einen späteren Zeitpunkt kommen,ich denke man wird hier noch ein paar „allgemeine“ Schwerpunkte zu BLP25 auswerten die bis jetzt nur Nebensache waren!
Trotzdem ist bis jetzt die grosse Spannung, Neugier oder gar Spekulation wie man an der Börse so schön sagt, bezogen auf die Veröffentlichung zum Monat März weiterhin stark vorhanden

@donnerpower
Ich sehe die Nachrichten auch sehr positiv , vor allem werden hier auch mal wieder auf die andren vielversprechende Forschungen eingegangen,stimmt zwar wie du sagts das Biomira hier noch keine 100% Stellungnahme für BLP25 ausgeübt hat ,aber anderer Termin vorgesehen!
Ich kann warten
Danke
DerBaron
Ich sehe die Nachrichten auch sehr positiv , vor allem werden hier auch mal wieder auf die andren vielversprechende Forschungen eingegangen,stimmt zwar wie du sagts das Biomira hier noch keine 100% Stellungnahme für BLP25 ausgeübt hat ,aber anderer Termin vorgesehen!
Ich kann warten

Danke
DerBaron
Der Kurs zieht an in USA:
BIOMIRA INC 1.80 $ 0.12 7.02% 487,242
BIOMIRA INC 1.80 $ 0.12 7.02% 487,242

@wortgottes
Sie werden auch noch weiter steigen,dazu waren die Nachrichten im Augenblick fast zu gut,man beachte hier
was alleine Blp25 für ein Marktvolumen eventuell vor sich hätte!!!
Hier wird ab heute der Startschuss zur einer ganz grossen Spekulation gegeben!
Ich hoffe nur das wir nach Ende März/Anfang April die Gewinner sind die Ihre Anteile noch unter 2Dollar bekommen konnten!
Loooong
Sie werden auch noch weiter steigen,dazu waren die Nachrichten im Augenblick fast zu gut,man beachte hier
was alleine Blp25 für ein Marktvolumen eventuell vor sich hätte!!!
Hier wird ab heute der Startschuss zur einer ganz grossen Spekulation gegeben!
Ich hoffe nur das wir nach Ende März/Anfang April die Gewinner sind die Ihre Anteile noch unter 2Dollar bekommen konnten!
Loooong
The year 2004 will be an exciting one for the Company, our investors and the scientific community. We look forward to receiving the clinical trial results of t… and we will continue to advance our understanding of the data more fully from our two lead product candidates. When appropriate, we will request a formal meeting with the regulatory authorities," said Alex McPherson
#511






Volumen steigt jetzt wie erwartet an,die 2ér Marke wird jetzt keine Hürde mehr sein!
Die Aussagen bei der QuartalsErscheinung dürfte sich langsam rumgesprochen haben,
besser kann man von der Unternehmensseite keine Vorlage für ein Mega Zock liefern der jetzt am laufen ist!!!

Die Aussagen bei der QuartalsErscheinung dürfte sich langsam rumgesprochen haben,
besser kann man von der Unternehmensseite keine Vorlage für ein Mega Zock liefern der jetzt am laufen ist!!!

Biomira steigt und keiner ist mehr da


1.96 (10.11%)
Bid: 1.96
Ask: 1.97
@donner
Die 2 wird heute Geschicht sein



1.96 (10.11%)
Bid: 1.96
Ask: 1.97
@donner
Die 2 wird heute Geschicht sein

Man kann ja auch still genießen.

@an alle
Ich will ja nicht übertreiben,aber in Yahoo Board sprechen sie schon von 100$ in 5Jahren,ist dies bei einen erfolgreichen Produkt BLP25 überhaupt möglich solche überbewerten Ziele auszusprechen???
kann mir hier einer mal den möglichen Markt für BLP25 bewerten!!?
Ich will ja nicht übertreiben,aber in Yahoo Board sprechen sie schon von 100$ in 5Jahren,ist dies bei einen erfolgreichen Produkt BLP25 überhaupt möglich solche überbewerten Ziele auszusprechen???
kann mir hier einer mal den möglichen Markt für BLP25 bewerten!!?
#514,515
sind schon noch einige da ... stille Geniesser ...



sind schon noch einige da ... stille Geniesser ...



#516
Tut mir leid, darüber mache ich mir keinen Kopf.
Für mich ist das hier eine reine Spekulation.
... und das sieht gut aus!
Tut mir leid, darüber mache ich mir keinen Kopf.
Für mich ist das hier eine reine Spekulation.
... und das sieht gut aus!
Die 2 liegt hinter uns aber trotzdem haben wir noch ein langen Weg vor uns


nächster halt bei 2,50???




nächster halt bei 2,50???

Alter Schwede wer kauft da wieder solche Pakete,scheint so das unserer guter Käufer MisterX wieder aufgetaucht ist!







Gedud scheint sich doch mal wieder auszuzahlen.
Einschätzungen/Meinungen wie es weiter geht?
Danke
Einschätzungen/Meinungen wie es weiter geht?
Danke
@ll
Biomira ist noch ein Nebenwert ,wenn hier in den nächsten Tagen erst mal begreiflich gemacht wird auf welchen Produkten hier Biomira sitzt sollten wir hier noch viel Freude haben!
Biomira bringt ein grosses Risiko mit sich, dagegen ist das Potential gigantisch ,ich vermute nicht einmal in Deutschland hat jemand Ahnung um was es hier überhaupt geht!
Merck setzt nicht um sonst auf Biomira Forschungen
Der Wert kann bei negativen News auf 1 runter rutschen ,bei positiven News sollte sich der Wert bei 20$ einpendeln mit einer Garantie das es langfristig weiter gegen norden läuft!
Nur wie gesagt die FDA muss BLP25 ersten einmal zulassen vorher ist hier schnell wieder das Lied zu ende!
Biomira ist noch ein Nebenwert ,wenn hier in den nächsten Tagen erst mal begreiflich gemacht wird auf welchen Produkten hier Biomira sitzt sollten wir hier noch viel Freude haben!
Biomira bringt ein grosses Risiko mit sich, dagegen ist das Potential gigantisch ,ich vermute nicht einmal in Deutschland hat jemand Ahnung um was es hier überhaupt geht!
Merck setzt nicht um sonst auf Biomira Forschungen

Der Wert kann bei negativen News auf 1 runter rutschen ,bei positiven News sollte sich der Wert bei 20$ einpendeln mit einer Garantie das es langfristig weiter gegen norden läuft!
Nur wie gesagt die FDA muss BLP25 ersten einmal zulassen vorher ist hier schnell wieder das Lied zu ende!
Donnerpower
bist ja auch noch dabei.
bist ja auch noch dabei.
@ heikekarina
....ich werde auch noch morgen dabei sein!
Ich habe damals Biomira nicht mit den Ziel gekauft hier mal schnell 100% mit zunehmen,
ich erhoffe mir hier ein wert gefunden zu haben der in 5-8Jahren mit einer der führenden Rolle in der Krebsforschung spielen wird!
Vor der Veröffentlichung TeilGewinne mit nehmen ist hier im jeden Fall angebracht ,bei positiven abschneiden des Produktes BLP25 ist mir auch ein Nachkauf zu einem Kurs von 10$ Wert!
....ich werde auch noch morgen dabei sein!
Ich habe damals Biomira nicht mit den Ziel gekauft hier mal schnell 100% mit zunehmen,
ich erhoffe mir hier ein wert gefunden zu haben der in 5-8Jahren mit einer der führenden Rolle in der Krebsforschung spielen wird!
Vor der Veröffentlichung TeilGewinne mit nehmen ist hier im jeden Fall angebracht ,bei positiven abschneiden des Produktes BLP25 ist mir auch ein Nachkauf zu einem Kurs von 10$ Wert!
Vermute das wir morgen kurzfristig bei 2.20$ Eröffnen werden!
Symbol: BIOM
Last Trade: 2.01 3:54PM ET
After Hours Change: N/A
Today`s Change: 0.23 (12.92%)
Symbol: BIOM
Last Trade: 2.01 3:54PM ET
After Hours Change: N/A
Today`s Change: 0.23 (12.92%)
Für heute reicht´s 
Symbol: BIOM
Last Trade: 2.05 4:08PM ET
After Hours Change: N/A
Today`s Change: 0.27 (15.17%)

Symbol: BIOM
Last Trade: 2.05 4:08PM ET
After Hours Change: N/A
Today`s Change: 0.27 (15.17%)
und wieder sieht es (kaum) einer:
Börse Symbol Währ. Vortag akt.Kurs Diff. % Handelsvol. gehand. St. Kurszeit
Nasdaq BIOM USD 2,00 2,16 + 0,160 + 8,00 2,95 Mio. 1.391.758 02. Mär 16:19
Frankfurt BM2 EUR 1,58 1,74 + 0,160 + 10,13 63.872 38.475 02. Mär 16:10



Börse Symbol Währ. Vortag akt.Kurs Diff. % Handelsvol. gehand. St. Kurszeit
Nasdaq BIOM USD 2,00 2,16 + 0,160 + 8,00 2,95 Mio. 1.391.758 02. Mär 16:19
Frankfurt BM2 EUR 1,58 1,74 + 0,160 + 10,13 63.872 38.475 02. Mär 16:10



gibt es News??die Umsätzte sind ja gigantisch!!bin bereits mit 5000 St dabei überlege über 2,3$ noch mit 10000St einzusteigen!

BIOM hat es endlich auch mal auf island auf Platz 15 geschafft RT bei 2,32$ bei guten Umsätzen (2Mio)
Einfach liegen lassen oder eventuell mal ein paar Gewinne
mitnehmen
Einfach liegen lassen oder eventuell mal ein paar Gewinne
mitnehmen
die Umsätze sind wirklich mehr als knackig 





@Bauernpizza
Guten Morgen
#511
#506
Alles bezogen auf die bevorstehende Nachricht
Ende März/Anfang April!!!

Biomira Outlines Milestones For 2004
http://biz.yahoo.com/prnews/031219/ca222_1.html
Guten Morgen

#511
#506
Alles bezogen auf die bevorstehende Nachricht
Ende März/Anfang April!!!

Biomira Outlines Milestones For 2004
http://biz.yahoo.com/prnews/031219/ca222_1.html
Wie gesagt das was wir gerade sehen ist nur ein kleiner Anstieg im Gegensatz was uns erwarten wird, sollte wenn BLP25 ein Erfolg werden!
Kurse von 20Euro in kürzester Zeit sind hier nicht untertrieben,nur wie gesagt WENN BLP25 EIN ERFOLG WIRD!
Symbol: BIOM
Last Trade: 2.38 11:52AM ET
After Hours Change: N/A
Today`s Change: 0.38 (19.00%)
Bid: 2.372
Ask: 2.38
Kurse von 20Euro in kürzester Zeit sind hier nicht untertrieben,nur wie gesagt WENN BLP25 EIN ERFOLG WIRD!
Symbol: BIOM
Last Trade: 2.38 11:52AM ET
After Hours Change: N/A
Today`s Change: 0.38 (19.00%)
Bid: 2.372
Ask: 2.38



Das sind Umsätze!!!
Bei 2,40$ ist erst mal Schluss,denke das wir erst mal das Hoch für Heute gesehen haben!
@BaronvonMünchhausen
Um 22.00 Uhr schauen wir uns den Kurs noch einmal an.
Bei diesen Umsätzen ist vieles möglich
Allen investierten einen schönen Abend noch!
verdi
Um 22.00 Uhr schauen wir uns den Kurs noch einmal an.
Bei diesen Umsätzen ist vieles möglich

Allen investierten einen schönen Abend noch!
verdi
@verdi2003
@baron
Ich hoffe nur ihr zieht euch nicht die Umsätze von Wallstreet-online zu gute,wir haben aktuell schon fast ein 26Mio Handelsvolumen hinter uns
http://www.comdirect.de/
@baron
Ich hoffe nur ihr zieht euch nicht die Umsätze von Wallstreet-online zu gute,wir haben aktuell schon fast ein 26Mio Handelsvolumen hinter uns

http://www.comdirect.de/
Gedankenlos noch einmal spricht BIOM über FDA-Zustimmung 2004






"Well, I think in a very aggressive way, we could actually be marketing this product following an approval in 2004. So, again, when you think where we are in relation to where we started, it`s pretty exciting times for us."
http://www.innovationalberta.com/article.php?articleid=142






"Well, I think in a very aggressive way, we could actually be marketing this product following an approval in 2004. So, again, when you think where we are in relation to where we started, it`s pretty exciting times for us."
http://www.innovationalberta.com/article.php?articleid=142
kann nicht mal einer diesen thread aufspalten in seiten-navigation.
das dauert ja ewig, diese seite mit dem handy und 9,6 b/s zu laden.
danke.
das dauert ja ewig, diese seite mit dem handy und 9,6 b/s zu laden.
danke.
@wortgottes
Wohl neu bei W.O.
Einfach auf das Symbol 20 klicken das RECHTS bei der Thread Auswahl neben der Überschrift steht und du siehst "nur" die aktuellen Posting´s

Wohl neu bei W.O.
Einfach auf das Symbol 20 klicken das RECHTS bei der Thread Auswahl neben der Überschrift steht und du siehst "nur" die aktuellen Posting´s


@donnerpower
Wie siehst Du die aktuelle Entwicklung?
Super Volumen,Insider,Spekulanten?


Wie siehst Du die aktuelle Entwicklung?
Super Volumen,Insider,Spekulanten?



@schmacki
Insider gab es für mich höchstens im Januar ,jetzt sehe ich eigentlich nur Spekulanten die eine mögliche Weltsensation nicht verpassen wollen.
Hier ist noch lange nicht Schluss,trotzdem sollte man sich nebenbei immer wieder kleine Gewinne Sichern,auch wenn wir nach der Veröffentlichung der Ergebnisse zu den Produkt Blp25 ,bei eventuell Positiv Kurse über 10$ sehen werden!
Man beachte der Wert ging schon mal an zwei Tagen von 2 auf über 20$ hoch!! [Mai 2000 ]
Hier ist alles möglich,wenn man bedenkt das hier ein Milliarden Markt vor uns liegt wo es aktuell keine Konkurrenz gibt!
Persönlich glaube ich aber das bei diesem Produkt eine weitere Phase vielleicht angebrachter ist!
Ps. zum Milliarden Markt komme ich wenigen Tagen noch einmal zurück,da ich noch auf Information warte,die dies noch weiter vertiefen!
Insider gab es für mich höchstens im Januar ,jetzt sehe ich eigentlich nur Spekulanten die eine mögliche Weltsensation nicht verpassen wollen.
Hier ist noch lange nicht Schluss,trotzdem sollte man sich nebenbei immer wieder kleine Gewinne Sichern,auch wenn wir nach der Veröffentlichung der Ergebnisse zu den Produkt Blp25 ,bei eventuell Positiv Kurse über 10$ sehen werden!
Man beachte der Wert ging schon mal an zwei Tagen von 2 auf über 20$ hoch!! [Mai 2000 ]
Hier ist alles möglich,wenn man bedenkt das hier ein Milliarden Markt vor uns liegt wo es aktuell keine Konkurrenz gibt!
Persönlich glaube ich aber das bei diesem Produkt eine weitere Phase vielleicht angebrachter ist!
Ps. zum Milliarden Markt komme ich wenigen Tagen noch einmal zurück,da ich noch auf Information warte,die dies noch weiter vertiefen!
@donnerpower
Wenn BLP 25 in Phase 3 geht,kann es dann in 2b zugelassen werden?
Wenn BLP 25 in Phase 3 geht,kann es dann in 2b zugelassen werden?

@ll
Interessant ist hier zu sehen das wir ein Handelsvolumen haben das viel höher erscheint als damals,
Juli03 wo Biomira vor der Veröffentlichung der damals nicht ganz erfreulichen Ergebnissen zum Produkt Theratope
von 2$ auf fast 5$ lief.
Man beachte ,die Forschungen zu Theratope laufen weiter an,man hatte bisher „nur“ 30% Erfolg bei den Testpersonen , immer hin ein Produkt wo die Heilungschance 30% wo es vorher keine Chance gab!!!

Interessant ist hier zu sehen das wir ein Handelsvolumen haben das viel höher erscheint als damals,
Juli03 wo Biomira vor der Veröffentlichung der damals nicht ganz erfreulichen Ergebnissen zum Produkt Theratope
von 2$ auf fast 5$ lief.
Man beachte ,die Forschungen zu Theratope laufen weiter an,man hatte bisher „nur“ 30% Erfolg bei den Testpersonen , immer hin ein Produkt wo die Heilungschance 30% wo es vorher keine Chance gab!!!

@schmacki
PhaseIIb ist ein grosser Unterschied als PhaseII
Ein Produkt das sich in der PhaseIIb befindet kann bei positiven Abschluss durch die FDA zugelassen ohne das es eine PhaseIII durchläuft!
Eine PhaseIII ist vom Unternehmen Biomira und von Merck bis jetzt nicht vorhergesehen,im allgemeinen kommt nach PhaseIIb keine weitere Phasestufe!!!
BLP25 Forschungen sollen dieses Jahr abgeschlossen werden und durch die FDA zugelassen werden,laut Unternehmen!
-Auch Teilprodukte von Theratope werden aktuell durch die FDA geprüft
PhaseIIb ist ein grosser Unterschied als PhaseII
Ein Produkt das sich in der PhaseIIb befindet kann bei positiven Abschluss durch die FDA zugelassen ohne das es eine PhaseIII durchläuft!
Eine PhaseIII ist vom Unternehmen Biomira und von Merck bis jetzt nicht vorhergesehen,im allgemeinen kommt nach PhaseIIb keine weitere Phasestufe!!!
BLP25 Forschungen sollen dieses Jahr abgeschlossen werden und durch die FDA zugelassen werden,laut Unternehmen!
-Auch Teilprodukte von Theratope werden aktuell durch die FDA geprüft

@donnerpower
Danke zu Deinen Ausführungen!!!

Danke zu Deinen Ausführungen!!!

@baron
Mein Alter Fuchs
#535
Symbol: BIOM
Last Trade: 2.32 4:00PM ET
After Hours Change: N/A
Today`s Change: 0.32 (16.00%)
0.32 (16.00%)
Mein Alter Fuchs

#535
Symbol: BIOM
Last Trade: 2.32 4:00PM ET
After Hours Change: N/A
Today`s Change:
 0.32 (16.00%)
0.32 (16.00%)
NASDAQ 2,29 02.03.04 21:59 31,11 Mio.
Toronto 3,10 02.03.04 21:59 4,71 Mio.
Toronto 3,10 02.03.04 21:59 4,71 Mio.
der chart sieht genial aus
und noch lange nicht überkauft !
über 2,5 kommen stop buy orders der longs und stop los orders der shortys
ein explosives gemisch
N8
biom
und noch lange nicht überkauft !
über 2,5 kommen stop buy orders der longs und stop los orders der shortys
ein explosives gemisch
N8
biom
es war ein schöner tag heute.
gute nacht!
gute nacht!
in der Tat, gute Nacht!


morgen, bin sehr gespannt, was der Tag heute bringt!


Morgen!
Biomira ist besser wie alle Actionfilme zusammen!
Wenn hier positive Ergebnisse kommen,oder noch besser eine
Zulassung von BLP 25 kann man nur erahnen was dann abgeht!
Bin heut auf das Volumen gespannt,höher als gestern???
Biomira ist besser wie alle Actionfilme zusammen!

Wenn hier positive Ergebnisse kommen,oder noch besser eine
Zulassung von BLP 25 kann man nur erahnen was dann abgeht!
Bin heut auf das Volumen gespannt,höher als gestern???

Hallo!
Verfolge BIOM schn länger. Leider kann ich nur wenig Fundamentals dazu finden. Habt ihr da was für mich, z.B. mögliches Umsatzpotenzial von BLP25? Was würde bei einem Scheitern passieren. Wär BIOM dann weg vom Fenster?
Bin euch dankbar für Meinungen!
Verfolge BIOM schn länger. Leider kann ich nur wenig Fundamentals dazu finden. Habt ihr da was für mich, z.B. mögliches Umsatzpotenzial von BLP25? Was würde bei einem Scheitern passieren. Wär BIOM dann weg vom Fenster?
Bin euch dankbar für Meinungen!

@ blb: Nein sie währen nicht weg vom Fenster, Biom hat noch einen starke Kapitaldecke für 2004. Und nicht nur BL25 als einzigstes Produkt in der Pipeline außerdem werden Sie noch von Merk (Deutschland) unterstützt.
Gruß
Vaio
Gruß
Vaio
@alle alle alle alle
heute nochmal nachkaufen ?????
grüße bernie
heute nochmal nachkaufen ?????
grüße bernie
wenig los in D 

Genügend konsolidiert, jetzt kann es weiter nach Norden gehen 

@bernie55
Abend,
Nachkaufen?
News kommen Ende März/Anfang April Biomira wird wohl vorher weitere Hoch´s überwinden ,hier ist jetzt jeder selbst auf sich alleine gestellt!
Bei Top sehen wir Kurse bis 20$,
bei Flop geht es runter auf 1,30-1,10$
@blb
Werde mich zu den Umsatz Potential am Wochenende dazu äußern!
Kurs aktuell wie erwartet,Umsatz von gestern wird mit Sicherheit bis Ende März nochmal übertroffen!
Abend,
Nachkaufen?
News kommen Ende März/Anfang April Biomira wird wohl vorher weitere Hoch´s überwinden ,hier ist jetzt jeder selbst auf sich alleine gestellt!
Bei Top sehen wir Kurse bis 20$,
bei Flop geht es runter auf 1,30-1,10$
@blb
Werde mich zu den Umsatz Potential am Wochenende dazu äußern!
Kurs aktuell wie erwartet,Umsatz von gestern wird mit Sicherheit bis Ende März nochmal übertroffen!
@donnerpower: Wär super! Wenn du Links hast, immer her damit. Beschäftig mich schon länger mit Bios, bin aber leider nicht direkt aus dem Fach und tu mich daher mit Umsatzpotenzialen und möglichen Risiken immer ziemlich schwer.
Bin v.a. durch den superschönen Chart aufmerksam geworden.
Bin v.a. durch den superschönen Chart aufmerksam geworden.

Unter 2,10$ gibts nichts mehr!
Hier hat sich nun ein starker Boden formiert,wo immer wieder nachgekauft wird,wenn man überlegt was Biomira im Sommer Wert sein könnte,ist der aktuellen Kurs mehr als ein Witz!



Hier hat sich nun ein starker Boden formiert,wo immer wieder nachgekauft wird,wenn man überlegt was Biomira im Sommer Wert sein könnte,ist der aktuellen Kurs mehr als ein Witz!



Aktuell wird die 2 angesägt
"shorties sind wieder am Werk" wenn die sich da mal nicht die Finger verbrennen...



"shorties sind wieder am Werk" wenn die sich da mal nicht die Finger verbrennen...



War aber ein wenig zu heftig konsolidiert heute.
Der gesamte gestrige Tag flöten.
Der gesamte gestrige Tag flöten.

ich habe den gestrigen Tag zum weiteren Eintieg genutzt nun sind 15000St mein Eigen!!
also laßt uns auf gute Ergebnisse hoffen und somit Kurse von 10-40$ zu sehen!
bei 2,06$ war mein Einstieg!
also laßt uns auf gute Ergebnisse hoffen und somit Kurse von 10-40$ zu sehen!
bei 2,06$ war mein Einstieg!

2,04 USD ~ 1,68 €
akt 1,76
akt 1,76
Bauernpizza







Starker Käufer wieder einmal unterwegs!
Symbol: BIOM
Last Trade: 2.18 3:30PM ET
After Hours Change: N/A
Today`s Change: 0.14 (6.86%)
Bid: 2.17
Ask: 2.18
Symbol: BIOM
Last Trade: 2.18 3:30PM ET
After Hours Change: N/A
Today`s Change: 0.14 (6.86%)
Bid: 2.17
Ask: 2.18

Weiter_hin starke Käufe!
.
.
.
.
und auf TagesHOCH geschlossen
Last Trade: 2.181 4:00PM ET
After Hours Change: N/A
Today`s Change: 0.141 (6.91%)
Börse Symbol Währ. Vortag akt.Kurs Diff. % Handelsvol. gehand. St. Kurszeit
Nasdaq BIOM USD 2,04 2,18 + 0,140 + 6,86 3,03 Mio. 1.477.478 04. Mär 22:01
Frankfurt BM2 EUR 1,69 1,69 + 0,000 + 0,00 103.940 61.766 04. Mär 18:48
ab 21:00 ging die Post wieder ab

Nasdaq BIOM USD 2,04 2,18 + 0,140 + 6,86 3,03 Mio. 1.477.478 04. Mär 22:01
Frankfurt BM2 EUR 1,69 1,69 + 0,000 + 0,00 103.940 61.766 04. Mär 18:48
ab 21:00 ging die Post wieder ab


Bei Biomira ist es oft so, verstärkte Käufe gibt es entweder zu Beginn der Börsensitzung oder gegen Ende.
Zwischendurch wird der Markt quasi sich überlassen.
Das spricht für einen Aufkäufer!
Gruß Agio
Zwischendurch wird der Markt quasi sich überlassen.
Das spricht für einen Aufkäufer!
Gruß Agio
Wird wohl ganz schön gezockt das Teil.
Nachbörslich momentan bei -3,67% (2,10-$)
Nachbörslich momentan bei -3,67% (2,10-$)

#572
Waren aber nur ca.40k,hat keine Aussagekraft!
Rechne mit weiter steigenden Kursen,heute.
Vielleicht doch ne News vor den BLP25 Ergebnissen?
Waren aber nur ca.40k,hat keine Aussagekraft!
Rechne mit weiter steigenden Kursen,heute.
Vielleicht doch ne News vor den BLP25 Ergebnissen?







Auch beim eigentlich schwerrgewichtigen Merck wird seit Tagen eingesammelt!!!!
#574
Das lässt auf positive News schliessen!
Auch für Merck,währen gute Ergebnisse ein "Meilenstein"
Das lässt auf positive News schliessen!
Auch für Merck,währen gute Ergebnisse ein "Meilenstein"

#575
wackelt der Schwanz mit dem Hund oder der Hund mit dem Schwanz?

wackelt der Schwanz mit dem Hund oder der Hund mit dem Schwanz?




gute chancen auf ein--W- Chart
wichtig ist, dass es am montag im amiland weiter positiv läuft.
mfg
biom--der hoffentlich geilste user den ich je hatte :-)
denn ab 22 USD kann ich den user bei EBAY verkaufen
wichtig ist, dass es am montag im amiland weiter positiv läuft.
mfg
biom--der hoffentlich geilste user den ich je hatte :-)
denn ab 22 USD kann ich den user bei EBAY verkaufen

@donnerpower: Wolltest doch am WE mal ein paar Fundamentals bringen! Bin schon gespannt! 

Ja, genau:
donner zeig und deine power.
Watt is nu mit "25" ???
donner zeig und deine power.
Watt is nu mit "25" ???
Re:@ll
co:@blb
So nun wie versprochen nun einmal paar Fakten,bezogen auf die Umsatzchancen von Biomiraprodukten:
Blp25 ist in mehren Teilgruppen geteilt
Eine Teilgruppe von Blp25 hat ein Markt von etwa 1,6Milliraden vor sich,man beachte das sich dies nur auf gerade ein mal ein Bruchteil bezieht!Der Markt wird aber weit höher als 4Milliraden eingeschätzt da sich der folgende Beitrag nur auf eine spezielle Richtung eingliedert!!!Kreps_Produktegruppen für Prostata sind hier wie einige weitere noch nicht einbezogen!!!
Der Artikel bezieht sich auf:BLP25 (MUC1) Liposomal Vaccine (3105)
Large Market
Growing world-wide market
In need of new therapeutic products.
Lung cancer is the second leading cause of cancer-related deaths worldwide and is primarily due to cigarette smoking and tobacco use.
According to the American Cancer Society (ACS), lung cancer is the second most common cancer in the U. S. with approximately 170,000 new cases diagnosed yearly. Non-Small Cell Lung Cancer (NSCLC) accounts for about 80% of all lung cancers. Only 25 percent NSCLC patients have operable tumors, and most patients are treated with radiation therapy and/or chemotherapy.
Lung cancer is the number one cause of death attributable to cancer in the U. S, with an estimated 162,100 lung cancer deaths in 2000. The five-year relative survival rate for all stages of lung cancer is only 15%.
Small cell lung cancer (SCLC) affects approximately 20 percent of all lung cancer patients, particularly middle-aged and old patients. Median survival for patients with SCLC is less than a year, with overall 5-year survival rate estimated at less than 5 percent.
Presently, according to the National Cancer Institute (NCI), approximately 321,000 patients with lung cancer live in the U. S.
In the year 2000, there were approximately 370,000 new patients with lung cancer in Europe, and more than 340,000 deaths.
In the region of South-East Asia, there were over 65,000 new patients, of which 8,157 were reported in Australia, with lung cancer, and 60,599 deaths, including 6,938 deaths in Australia, from lung cancer. The worldwide market for NSCLC is valued at $1.6 billion, and is forecasted to grow to $8 billion by 2011.
World-wide deaths caused by lung cancer are approaching 1 million yearly.
The world-wide therapeutic market for lung cancer is currently worth approximately $1.6 billion yearly.

co:@blb
So nun wie versprochen nun einmal paar Fakten,bezogen auf die Umsatzchancen von Biomiraprodukten:
Blp25 ist in mehren Teilgruppen geteilt
Eine Teilgruppe von Blp25 hat ein Markt von etwa 1,6Milliraden vor sich,man beachte das sich dies nur auf gerade ein mal ein Bruchteil bezieht!Der Markt wird aber weit höher als 4Milliraden eingeschätzt da sich der folgende Beitrag nur auf eine spezielle Richtung eingliedert!!!Kreps_Produktegruppen für Prostata sind hier wie einige weitere noch nicht einbezogen!!!
Der Artikel bezieht sich auf:BLP25 (MUC1) Liposomal Vaccine (3105)
Large Market
Growing world-wide market
In need of new therapeutic products.
Lung cancer is the second leading cause of cancer-related deaths worldwide and is primarily due to cigarette smoking and tobacco use.
According to the American Cancer Society (ACS), lung cancer is the second most common cancer in the U. S. with approximately 170,000 new cases diagnosed yearly. Non-Small Cell Lung Cancer (NSCLC) accounts for about 80% of all lung cancers. Only 25 percent NSCLC patients have operable tumors, and most patients are treated with radiation therapy and/or chemotherapy.
Lung cancer is the number one cause of death attributable to cancer in the U. S, with an estimated 162,100 lung cancer deaths in 2000. The five-year relative survival rate for all stages of lung cancer is only 15%.
Small cell lung cancer (SCLC) affects approximately 20 percent of all lung cancer patients, particularly middle-aged and old patients. Median survival for patients with SCLC is less than a year, with overall 5-year survival rate estimated at less than 5 percent.
Presently, according to the National Cancer Institute (NCI), approximately 321,000 patients with lung cancer live in the U. S.
In the year 2000, there were approximately 370,000 new patients with lung cancer in Europe, and more than 340,000 deaths.
In the region of South-East Asia, there were over 65,000 new patients, of which 8,157 were reported in Australia, with lung cancer, and 60,599 deaths, including 6,938 deaths in Australia, from lung cancer. The worldwide market for NSCLC is valued at $1.6 billion, and is forecasted to grow to $8 billion by 2011.
World-wide deaths caused by lung cancer are approaching 1 million yearly.
The world-wide therapeutic market for lung cancer is currently worth approximately $1.6 billion yearly.

Ein interessanter Nachtrag
New Cancer Drugs Offer Patients Hope, Drug Makers Success
....
"AG Edwards analyst Albert Rauch says the industry is bigger - about $20 billion and growing 15% to 20% a year. He sees $45 billion in annual sales by 2011.";




New Cancer Drugs Offer Patients Hope, Drug Makers Success
Until recently, cancer was considered hard to treat - a disease few survived. Doctors even joked about oncologists having cardiology envy.
Heart disease patients, unlike people with cancer, have many proven options, including statins that stop plaque, angioplasty and bypass surgery. In contrast, most cancer patients don`t get guarantees.
According to the American Cancer Society, cancer kills nearly 554,000 Americans and causes 30% of all deaths. But new drugs that target cancer cells while avoiding healthy cells are boosting chances of survival. Most of these drugs have regulatory approval to treat only tiny populations of patients with rare cancers, but they do offer hope.
The list of targeted drugs includes Novartis AG`s Gleevec, Genentech Inc.`s Rituxan and AstraZeneca`s PLC Iressa. These drugs target diseased cells without harming healthy cells - something traditional chemotherapies can`t do.
"Gleevec really stands out," said analyst Howard Liang of JMP Securities. "In terms of its impact on chronic myeloid leukemia patients, they`re effectively cured. Sometimes you have a 90% response rate - unheard of in other (cancer) drugs."
Targeted treatments not only help patients, they also drive the cancer drug business.
Liang puts the total cancer drug market at $15 billion, with a compounded annual growth rate of 17%. This makes cancer the fastest growing drug market.
http://biz.yahoo.com/ibd/040301/health_1.html

New Cancer Drugs Offer Patients Hope, Drug Makers Success
....
"AG Edwards analyst Albert Rauch says the industry is bigger - about $20 billion and growing 15% to 20% a year. He sees $45 billion in annual sales by 2011.";




New Cancer Drugs Offer Patients Hope, Drug Makers Success
Until recently, cancer was considered hard to treat - a disease few survived. Doctors even joked about oncologists having cardiology envy.
Heart disease patients, unlike people with cancer, have many proven options, including statins that stop plaque, angioplasty and bypass surgery. In contrast, most cancer patients don`t get guarantees.
According to the American Cancer Society, cancer kills nearly 554,000 Americans and causes 30% of all deaths. But new drugs that target cancer cells while avoiding healthy cells are boosting chances of survival. Most of these drugs have regulatory approval to treat only tiny populations of patients with rare cancers, but they do offer hope.
The list of targeted drugs includes Novartis AG`s Gleevec, Genentech Inc.`s Rituxan and AstraZeneca`s PLC Iressa. These drugs target diseased cells without harming healthy cells - something traditional chemotherapies can`t do.
"Gleevec really stands out," said analyst Howard Liang of JMP Securities. "In terms of its impact on chronic myeloid leukemia patients, they`re effectively cured. Sometimes you have a 90% response rate - unheard of in other (cancer) drugs."
Targeted treatments not only help patients, they also drive the cancer drug business.
Liang puts the total cancer drug market at $15 billion, with a compounded annual growth rate of 17%. This makes cancer the fastest growing drug market.
http://biz.yahoo.com/ibd/040301/health_1.html
@donnerpower: Kannste das mal in eigenen Worten zusammenfassen? Es geht wohl um Lungenkrebs? Welche Konkurrenzprodukte gibt es?
Anerkannte Produkte:
Approved Products:
Gemzar® (Gemcitabine)
Iressa™ (Gefitinib, ZD1839) (1181)
Taxotere® (docetaxel)
Pipeline gibt es wie Sand am mehr, allerdings haben hier fast alle nur ein minimalen Anwendungsspielraum!


Pipeline:
Abraxane™ (ABI-007, Paclitaxel Albumin Stabilized Nanopartice Formulated) (2824)
ABT-510 (2872)
ABX-EGF (Anti-EGFr Antibody) (2267)
Advexin® Gene Therapy (INGN 201, Ad5CMVp53) (2837)
Aplidin™ (Aplidine, APL, Dehydrodidemnin B) (2976)
Aptosyn™ (Exisulind, Prevatac™) (2237)
Atrasentan (ABT-627) (2977)
Avastin™ (Bevacizumab, Anti-VEGF Antibody, rhuMAb-VEGF) (1313)
BAM-002 (1775)
BEC2 (3191)
BLP25 (MUC1) Liposomal Vaccine (3105)
BMS 275291 (D2163) (1055)
Cantuzumab Mertansine (huC242-DM1, SB 408075) (1244)
CD3 (TTS CD3) (3352)
CeaVac® (2306)
CP-547,632 (2679)
Dexosomes Lung Cancer Vaccine (2985)
EGFRvIII Peptide Vaccine (3426)
Elsamitrucin (Elsamicin A, BMY-28090) (2538)
EGF Cancer Vaccine (2647)
EMD 72000 (Anti-EGFR Antibody) (3262)
EMD 273066 (huKS-IL2) (3327)
EP-2101 (3240)
Decitabine (DAC) (1802)
Erbitux™ (Cetuximab, IMC-C225, C225) (2096) Free-to-Review
GVAX® (3081)
hOAT (IgG1kappa Anti Tissue Factor Antibody) (3320)
huN901-DM1 (BB-10901) Conjugate (1820)
IGN101 Vaccine (3250)
IDEC-160 (HMN-214) (2941)
Irofulven (Hydroxymethylacyfulvene, 6-HMAF, MGI 114) (1117)
LE-SN38 (Liposome Encapsulated SN38) (2423)
LEP-ETU (Liposomal Encapsulated Paclitaxel) (2386)
Mebendazole (2983)
MVA-MUC1-IL2 (TG4010) (3420)
NBI-3001 (IL-4 Fusion Toxin, IL-4 (38-37)-PE38KDEL) (2150)
Neovastat™ (AE-941) (3045)
Orathecin™ (Rubitecan, RFS 2000, 9NC) (1801)
OSI-211 (NX 211, Liposomal Lurtotecan) (2157)
Paxoral™ (Paclitaxel Oral) (2452)
Pivanex® (AN9) (2307)
Prothecan® (PEG-Camptothecin) (1952)
RB94 Gene Therapy (1664)
RSR13 (Efaproxiral Sodium) (1776)
SB 715992 (CK0238273) (2718)
SGN-15 (BR96-DOX) (1946)
TAP-1 Anti-Cancer Vaccine (2885)
Tarceva™ (Erlotinib HCl, OSI-774, CP-358,774) (2598)
Telcyta™ (TLK286, TER286) (1862)
TheraFab (1520)
Thalomid® (Thalidomide) (1162)
TOCOSOL™ Paclitaxel (S-8184, QW8184) (3309)
TriAb® (11D10 Anti-Idiotype Antibody) (2305)
Velcade™ (Bortezomib, MLN341, LDP-341, PS-341) (1794)
Xcytrin® (Motexafin Gadolinium, Gd-Tex, Gadolinium Texaphyrin, MGd, PCI-0120) (3085)
Zadaxin® (Thymosin Alpha 1, Thymalfasin, Talpha 1) (3043)
Potential Pipeline:
2ME2 (2-Methoxyestradiol)-Mediated p53 Gene Therapy (2958)
4B5 H (Anti-Ganglioside GD2 Anti-Idiotype Antibody-Based Vaccine, NOVOVAC-M1) (1002)
Angiocidin™ (1792)
Electroporation Therapy (3296)
G17DT (Anti-Gastrin 17 Immunogen, Gastrimmune™) (2193)
INGN 241 (Ad-mda7 Gene Therapy) (2561)
MT201 (Anti-EpCAM Antibody) (2942)
NY-ESO-1 Antigen-Specific Cancer Vaccines (2972)
TRAIL-R1 mAb (TRAIL Receptor-1 Human Monoclonal Antibody (2820)
Product Development Suspended/Terminated:
AMD473 (ZD0473) (2175)
DCVax™-Lung Cancer (2947)
ELL-12 (TLC ELL-12) (1166)
PACLIMER® Microspheres (Paclitaxel PPE Microspheres) (2547)
PEG-Paclitaxel (2638)
SGN-25 (BR96 Antibody-Auristatin E Conjugate) (2886)
Tezacitabine (FMdC, KW-2331, MDL 101,731) (1102)
Troxatyl™ (Troxacitabine, BCH-4556) (1347)
Approved Products:
Gemzar® (Gemcitabine)
Iressa™ (Gefitinib, ZD1839) (1181)
Taxotere® (docetaxel)
Pipeline gibt es wie Sand am mehr, allerdings haben hier fast alle nur ein minimalen Anwendungsspielraum!



Pipeline:
Abraxane™ (ABI-007, Paclitaxel Albumin Stabilized Nanopartice Formulated) (2824)
ABT-510 (2872)
ABX-EGF (Anti-EGFr Antibody) (2267)
Advexin® Gene Therapy (INGN 201, Ad5CMVp53) (2837)
Aplidin™ (Aplidine, APL, Dehydrodidemnin B) (2976)
Aptosyn™ (Exisulind, Prevatac™) (2237)
Atrasentan (ABT-627) (2977)
Avastin™ (Bevacizumab, Anti-VEGF Antibody, rhuMAb-VEGF) (1313)
BAM-002 (1775)
BEC2 (3191)
BLP25 (MUC1) Liposomal Vaccine (3105)
BMS 275291 (D2163) (1055)
Cantuzumab Mertansine (huC242-DM1, SB 408075) (1244)
CD3 (TTS CD3) (3352)
CeaVac® (2306)
CP-547,632 (2679)
Dexosomes Lung Cancer Vaccine (2985)
EGFRvIII Peptide Vaccine (3426)
Elsamitrucin (Elsamicin A, BMY-28090) (2538)
EGF Cancer Vaccine (2647)
EMD 72000 (Anti-EGFR Antibody) (3262)
EMD 273066 (huKS-IL2) (3327)
EP-2101 (3240)
Decitabine (DAC) (1802)
Erbitux™ (Cetuximab, IMC-C225, C225) (2096) Free-to-Review
GVAX® (3081)
hOAT (IgG1kappa Anti Tissue Factor Antibody) (3320)
huN901-DM1 (BB-10901) Conjugate (1820)
IGN101 Vaccine (3250)
IDEC-160 (HMN-214) (2941)
Irofulven (Hydroxymethylacyfulvene, 6-HMAF, MGI 114) (1117)
LE-SN38 (Liposome Encapsulated SN38) (2423)
LEP-ETU (Liposomal Encapsulated Paclitaxel) (2386)
Mebendazole (2983)
MVA-MUC1-IL2 (TG4010) (3420)
NBI-3001 (IL-4 Fusion Toxin, IL-4 (38-37)-PE38KDEL) (2150)
Neovastat™ (AE-941) (3045)
Orathecin™ (Rubitecan, RFS 2000, 9NC) (1801)
OSI-211 (NX 211, Liposomal Lurtotecan) (2157)
Paxoral™ (Paclitaxel Oral) (2452)
Pivanex® (AN9) (2307)
Prothecan® (PEG-Camptothecin) (1952)
RB94 Gene Therapy (1664)
RSR13 (Efaproxiral Sodium) (1776)
SB 715992 (CK0238273) (2718)
SGN-15 (BR96-DOX) (1946)
TAP-1 Anti-Cancer Vaccine (2885)
Tarceva™ (Erlotinib HCl, OSI-774, CP-358,774) (2598)
Telcyta™ (TLK286, TER286) (1862)
TheraFab (1520)
Thalomid® (Thalidomide) (1162)
TOCOSOL™ Paclitaxel (S-8184, QW8184) (3309)
TriAb® (11D10 Anti-Idiotype Antibody) (2305)
Velcade™ (Bortezomib, MLN341, LDP-341, PS-341) (1794)
Xcytrin® (Motexafin Gadolinium, Gd-Tex, Gadolinium Texaphyrin, MGd, PCI-0120) (3085)
Zadaxin® (Thymosin Alpha 1, Thymalfasin, Talpha 1) (3043)
Potential Pipeline:
2ME2 (2-Methoxyestradiol)-Mediated p53 Gene Therapy (2958)
4B5 H (Anti-Ganglioside GD2 Anti-Idiotype Antibody-Based Vaccine, NOVOVAC-M1) (1002)
Angiocidin™ (1792)
Electroporation Therapy (3296)
G17DT (Anti-Gastrin 17 Immunogen, Gastrimmune™) (2193)
INGN 241 (Ad-mda7 Gene Therapy) (2561)
MT201 (Anti-EpCAM Antibody) (2942)
NY-ESO-1 Antigen-Specific Cancer Vaccines (2972)
TRAIL-R1 mAb (TRAIL Receptor-1 Human Monoclonal Antibody (2820)
Product Development Suspended/Terminated:
AMD473 (ZD0473) (2175)
DCVax™-Lung Cancer (2947)
ELL-12 (TLC ELL-12) (1166)
PACLIMER® Microspheres (Paclitaxel PPE Microspheres) (2547)
PEG-Paclitaxel (2638)
SGN-25 (BR96 Antibody-Auristatin E Conjugate) (2886)
Tezacitabine (FMdC, KW-2331, MDL 101,731) (1102)
Troxatyl™ (Troxacitabine, BCH-4556) (1347)
BLP25 (MUC1) Liposomal Vaccine (3105)
BLP25 Liposomal vaccine (L-BLP25) - L-BLP25 is Biomira`s synthetic MUC1 peptide vaccine. L-BLP25 incorporates a 25-amino acid sequence of the MUC1 cancer mucin, encapsulated in a Liposomal delivery system. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery. L-BLP25 is designed to induce an immune response to cancer cells.
Following Phase I and II clinical trials, in August 2000, a Phase IIb study began in non-small cell lung cancer (NSCLC). 171 patients were randomized – half to L-BLP25 plus best standard of care and half to best standard of care alone. Study endpoints are safety and survival with quality of life and immune response as secondary endpoints. Thirteen sites in Canada and four in the United Kingdom have been set up for this trial. Enrolment was completed in November 2002 and results are expected in the first quarter of 2004, or shortly thereafter.
BLP25 Liposomal vaccine (L-BLP25) - L-BLP25 is Biomira`s synthetic MUC1 peptide vaccine. L-BLP25 incorporates a 25-amino acid sequence of the MUC1 cancer mucin, encapsulated in a Liposomal delivery system. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery. L-BLP25 is designed to induce an immune response to cancer cells.
Following Phase I and II clinical trials, in August 2000, a Phase IIb study began in non-small cell lung cancer (NSCLC). 171 patients were randomized – half to L-BLP25 plus best standard of care and half to best standard of care alone. Study endpoints are safety and survival with quality of life and immune response as secondary endpoints. Thirteen sites in Canada and four in the United Kingdom have been set up for this trial. Enrolment was completed in November 2002 and results are expected in the first quarter of 2004, or shortly thereafter.
Wow, die längste Pipeline, die ich je gesehen hab! 
Mich würds aktuell schon stark in den Fingern jucken, allein schon aus charttechnischer Sicht...

Mich würds aktuell schon stark in den Fingern jucken, allein schon aus charttechnischer Sicht...

Prima BioMed signs license deal with International Cancer Vaccine Company, Biomira Inc. for CancerVac Pty Ltd Technology
MELBOURNE, Australia and EDMONTON, AB, Mar 10, 2004 /PRNewswire-FirstCall via
COMTEX/ -- Prima BioMed Ltd (`Prima` ASX PRR), subsidiary CancerVac, and
Canadian based international cancer immunotherapy company, Biomira Inc.
(NASDAQ:BIOM/TSX: BRA), today announced a commercial agreement for the
development and commercialization of CancerVac`s most advanced cancer vaccine
product candidate.
Biomira will provide CancerVac with access to its licensed exclusive worldwide
rights related to a protein called MUC1 in relation to CancerVac`s Mannan-MUC1
fusion protein therapeutic vaccine. The Biomira MUC1 patent portfolio includes
certain rights to patents held by Cancer Research Technology Limited of London,
UK, which are essential for the development and commercialization of CancerVac`s
Mannan-MUC1 fusion protein used for cancer immunotherapy. CancerVac has
developed an immunotherapy that utilizes the patient`s own dendritic cells
treated ex-vivo to stimulate a cellular immune response following re-injection
of the cells into the patient. CancerVac plans to initiate patient recruitment
into a Phase IIa trial in patients with metastatic ovarian cancer in the second
quarter of 2004.
In partial consideration for the license rights provided by Biomira to
CancerVac, Biomira acquired a 10 per cent equity stake in CancerVac, and a seat
on the Board of CancerVac.
The agreement provides that Biomira has the sole option of licensing the
exclusive worldwide commercialization rights (excluding Australia and New
Zealand) to this product candidate following conclusion of the Phase IIa trial
in ovarian cancer. Biomira, at its election, may acquire exclusive licensing
rights for the worldwide application of the CancerVac technology (excluding
Australia and New Zealand) relating to this product candidate or only for the
North American region. Such election is to be made by Biomira following
Biomira`s review of the Phase IIa clinical trial data. If Biomira proceeds with
the worldwide rights it will thereafter generally meet 100 per cent of the
ongoing development costs of the technology or 50 per cent of the development
costs if it elects to confine its activities to the North American territory.
Specific terms of the licensing agreement from CancerVac to Biomira were not
disclosed, but could include upfront and milestone payments to CancerVac,
potentially totaling AUD$ 20m ($US 15.4m) as well as royalties struck at rates
consistent for licensing deals associated with Phase IIa clinical data. In the
event Biomira does not elect to exercise its exclusive rights, then the
agreement enables CancerVac to develop and commercialize its Mannan-MUC1 fusion
protein technology with similar payments to Biomira.
Marcus Clark, CEO of Prima BioMed commented, "This agreement is a significant
commercial milestone for Prima BioMed and CancerVac. Biomira is undoubtedly a
world leader in the development of cancer immunotherapy and this agreement is a
demonstration of the potential of CancerVac`s approach. I was therefore
delighted to be advised that Dr. Alex McPherson, CEO of Biomira, has agreed to
take up the Biomira board position on CancerVac.
"It was always Prima`s objective to take CancerVac through Phase II trials and
commercialize the technology in Australia. Now, through a series of potential
milestones from Biomira, this agreement clears a path for the commercial
exploitation of the technology in North America and Europe," said Mr. Clark. "We
have retained marketing rights for Australia and New Zealand as we remain of the
opinion we can undertake this operation very efficiently and enjoy the benefits
of higher profit margins."
Alex McPherson, MD, PhD, President and CEO of Biomira added: "CancerVac`s
technology clearly complements our existing range of cancer vaccine product
candidates. We view the scientific and clinical expertise in CancerVac as first
class and expect to gain much information from the combined clinical research
efforts. A steering committee will now be established with Biomira and CancerVac
on which Biomira will have two of our senior clinical development executives as
members. This will provide a great deal of management expertise for the clinical
trials and the compilation of information necessary for the regulatory approvals
required for North America and Europe."
"Our enthusiasm for identifying products in oncology that can harness the body`s
own immune system against cancer paved the way to this important collaboration.
MUC1 is a very important cancer target for immunotherapy and we are looking to
maximize clinical exposure in well-controlled clinical trials. We look forward
to working together with Prima BioMed to further develop CancerVac`s
technology," concluded Dr. McPherson.
About Prima BioMed Ltd
Based in Melbourne, Prima BioMed (ASX: PRR) is a biotechnology organization with
first and last rights over technologies from the Austin Research Institute.
Prima BioMed specializes in immunology and cancer immunotherapy and adopts
technology development that shows potential for commercial returns within three
years.
About Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative
therapeutic approaches to cancer management. Biomira`s commitment to the
treatment of cancer currently focuses on the development of vaccines containing
synthetic antigens and novel strategies for cancer immunotherapy.
About CancerVac Pty. Ltd.
CancerVac Pty Ltd. CancerVac is a subsidiary of Prima BioMed. The company was
formed to develop and commercialize technology licensed from the Austin Research
Institute, a medical research institute located in Melbourne Australia. The
technology being developed is described as immunotherapy. It combines
recombinant proteins expressed on tumor cells and a vaccine adjuvant to trigger
recognition of tumor cells by the immune system as foreign. Such recognition in
turn leading to attack by immune killer and tumor cell destruction.
This release may contain forward-looking statements. Various factors could cause
actual results to differ materially from those projected in forward- looking
statements, including those predicting the timing and results of clinical
trials, interpretation and implications of such results, availability or
adequacy of financing, the sales and marketing of commercial products or the
efficacy of products. Although the Company believes that the forward-looking
statements contained herein are reasonable, it can give no assurance that the
Company`s expectations are correct. All forward-looking statements are expressly
qualified in their entirety by this cautionary statement.
MELBOURNE, Australia and EDMONTON, AB, Mar 10, 2004 /PRNewswire-FirstCall via
COMTEX/ -- Prima BioMed Ltd (`Prima` ASX PRR), subsidiary CancerVac, and
Canadian based international cancer immunotherapy company, Biomira Inc.
(NASDAQ:BIOM/TSX: BRA), today announced a commercial agreement for the
development and commercialization of CancerVac`s most advanced cancer vaccine
product candidate.
Biomira will provide CancerVac with access to its licensed exclusive worldwide
rights related to a protein called MUC1 in relation to CancerVac`s Mannan-MUC1
fusion protein therapeutic vaccine. The Biomira MUC1 patent portfolio includes
certain rights to patents held by Cancer Research Technology Limited of London,
UK, which are essential for the development and commercialization of CancerVac`s
Mannan-MUC1 fusion protein used for cancer immunotherapy. CancerVac has
developed an immunotherapy that utilizes the patient`s own dendritic cells
treated ex-vivo to stimulate a cellular immune response following re-injection
of the cells into the patient. CancerVac plans to initiate patient recruitment
into a Phase IIa trial in patients with metastatic ovarian cancer in the second
quarter of 2004.
In partial consideration for the license rights provided by Biomira to
CancerVac, Biomira acquired a 10 per cent equity stake in CancerVac, and a seat
on the Board of CancerVac.
The agreement provides that Biomira has the sole option of licensing the
exclusive worldwide commercialization rights (excluding Australia and New
Zealand) to this product candidate following conclusion of the Phase IIa trial
in ovarian cancer. Biomira, at its election, may acquire exclusive licensing
rights for the worldwide application of the CancerVac technology (excluding
Australia and New Zealand) relating to this product candidate or only for the
North American region. Such election is to be made by Biomira following
Biomira`s review of the Phase IIa clinical trial data. If Biomira proceeds with
the worldwide rights it will thereafter generally meet 100 per cent of the
ongoing development costs of the technology or 50 per cent of the development
costs if it elects to confine its activities to the North American territory.
Specific terms of the licensing agreement from CancerVac to Biomira were not
disclosed, but could include upfront and milestone payments to CancerVac,
potentially totaling AUD$ 20m ($US 15.4m) as well as royalties struck at rates
consistent for licensing deals associated with Phase IIa clinical data. In the
event Biomira does not elect to exercise its exclusive rights, then the
agreement enables CancerVac to develop and commercialize its Mannan-MUC1 fusion
protein technology with similar payments to Biomira.
Marcus Clark, CEO of Prima BioMed commented, "This agreement is a significant
commercial milestone for Prima BioMed and CancerVac. Biomira is undoubtedly a
world leader in the development of cancer immunotherapy and this agreement is a
demonstration of the potential of CancerVac`s approach. I was therefore
delighted to be advised that Dr. Alex McPherson, CEO of Biomira, has agreed to
take up the Biomira board position on CancerVac.
"It was always Prima`s objective to take CancerVac through Phase II trials and
commercialize the technology in Australia. Now, through a series of potential
milestones from Biomira, this agreement clears a path for the commercial
exploitation of the technology in North America and Europe," said Mr. Clark. "We
have retained marketing rights for Australia and New Zealand as we remain of the
opinion we can undertake this operation very efficiently and enjoy the benefits
of higher profit margins."
Alex McPherson, MD, PhD, President and CEO of Biomira added: "CancerVac`s
technology clearly complements our existing range of cancer vaccine product
candidates. We view the scientific and clinical expertise in CancerVac as first
class and expect to gain much information from the combined clinical research
efforts. A steering committee will now be established with Biomira and CancerVac
on which Biomira will have two of our senior clinical development executives as
members. This will provide a great deal of management expertise for the clinical
trials and the compilation of information necessary for the regulatory approvals
required for North America and Europe."
"Our enthusiasm for identifying products in oncology that can harness the body`s
own immune system against cancer paved the way to this important collaboration.
MUC1 is a very important cancer target for immunotherapy and we are looking to
maximize clinical exposure in well-controlled clinical trials. We look forward
to working together with Prima BioMed to further develop CancerVac`s
technology," concluded Dr. McPherson.
About Prima BioMed Ltd
Based in Melbourne, Prima BioMed (ASX: PRR) is a biotechnology organization with
first and last rights over technologies from the Austin Research Institute.
Prima BioMed specializes in immunology and cancer immunotherapy and adopts
technology development that shows potential for commercial returns within three
years.
About Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative
therapeutic approaches to cancer management. Biomira`s commitment to the
treatment of cancer currently focuses on the development of vaccines containing
synthetic antigens and novel strategies for cancer immunotherapy.
About CancerVac Pty. Ltd.
CancerVac Pty Ltd. CancerVac is a subsidiary of Prima BioMed. The company was
formed to develop and commercialize technology licensed from the Austin Research
Institute, a medical research institute located in Melbourne Australia. The
technology being developed is described as immunotherapy. It combines
recombinant proteins expressed on tumor cells and a vaccine adjuvant to trigger
recognition of tumor cells by the immune system as foreign. Such recognition in
turn leading to attack by immune killer and tumor cell destruction.
This release may contain forward-looking statements. Various factors could cause
actual results to differ materially from those projected in forward- looking
statements, including those predicting the timing and results of clinical
trials, interpretation and implications of such results, availability or
adequacy of financing, the sales and marketing of commercial products or the
efficacy of products. Although the Company believes that the forward-looking
statements contained herein are reasonable, it can give no assurance that the
Company`s expectations are correct. All forward-looking statements are expressly
qualified in their entirety by this cautionary statement.
@Vaio
die meldung hört sich gut an.
schauen wir mal was der kurs der aktie in amrika heute macht.
noch drei wochen, dann ist märz zu ende
gruß
verdi
die meldung hört sich gut an.
schauen wir mal was der kurs der aktie in amrika heute macht.
noch drei wochen, dann ist märz zu ende

gruß
verdi
schönes gap

ich hoffe die SHORTSELLER bekommen mal richtig prügel
unserer perle ewig shorten
sollte das gap offen bleiben, dann ist es ein sehr positives zeichen !
biomira-----------der user des jahre ( hoffe ich )
)
ich hoffe die SHORTSELLER bekommen mal richtig prügel
unserer perle ewig shorten
sollte das gap offen bleiben, dann ist es ein sehr positives zeichen !
biomira-----------der user des jahre ( hoffe ich
 )
) 


Biomira Gets 10% CancerVac Stake In Licensing Pact!!!
MELBOURNE (Dow Jones)--Prima BioMed Ltd. and Biomira Inc. (NasdaqNM:BIOM - News) have entered a commercial agreement for the development and commercialization of CancerVac`s most advanced cancer vaccine product candidate.
ADVERTISEMENT
CancerVac is a subsidiary of Prima BioMed.
In a news release, Biomira said it will provide CancerVac with access to its licensed exclusive worldwide rights related to a protein called MUC1 in relation to CancerVac`s Mannan-MUC1 fusion protein therapeutic vaccine.
In partial consideration for the license, Biomira said it acquired a 10% equity stake in CancerVac and a seat on CancerVac`s board.
Biomira said its MUC1 patent portfolio includes certain rights to patents held by London`s Cancer Research Technology Ltd. which are essential for the development and commercialization of CancerVac`s Mannan-MUC1 fusion protein used for cancer immunotherapy.
The company said CancerVac has developed an immunotherapy that uses the patient`s own dendritic cells treated ex-vivo to stimulate a cellular immune response following re-injection of the cells into the patient. It said CancerVac plans to start patient recruitment into a Phase IIa trial in patients with metastatic ovarian cancer in the second quarter of 2004.
Biomira Inc. said the agreement with Prima BioMed Ltd.`s CancerVac subsidiary provides that Biomira has the sole option of licensing the exclusive worldwide commercialization rights (excluding Australia and New Zealand) to the product candidate following conclusion of the Phase IIa trial in ovarian cancer.
Biomira, at its election, may acquire exclusive licensing rights for the worldwide application of the CancerVac technology (excluding Australia and New Zealand) or only for the North American region.
If it proceeds with the worldwide rights, Biomira said it will cover 100% of the ongoing development costs of the technology or 50% if it elects to confine its activities in North America.
Full terms of the licensing agreement weren`t disclosed, but Biomira said the agreement could include upfront and milestone payments to CancerVac with a potential value of about US$15.4 million as well as royalties struck at rates consistent for licensing deals associated with Phase IIa clinical data.
If Biomira doesn`t elect to exercise its exclusive rights, then the agreement allows CancerVac to develop and commercialize its Mannan-MUC1 fusion protein technology with similar payments to Biomira.
Prima BioMed, Melbourne, speciales in immunology and cancer immunotherapy.
Biomira specializes the development of innovative therapeutic approaches to cancer management.
Ein Unternehmen das in die Zukunft investiert , scheinst ja immer besser zu gehen,wenn jetzt noch Produkte aus den BLP25 Phasen kommen dannnnn ..........!
Warten wir mal ab!
Warten wir mal ab!
@ll
Die Nachricht kam zu einen richtigen Zeitpunkt,sollte nämlich BLP25 kein Erfolg oder wie von mir erwartet 3Phase eintreffen,wird bzw. wurde nun aus dem Wert mit der heutigen Nachricht etwas Risiko abgenommen.
Man beachte das hier auch noch höchstwahrscheinlich eine Teilzulassung von Theratope in geraumer Zeit folgen wird!!!Von einer weiteren Theratope PhaseIII ganz zu schweigen.
vielleicht erleben wir so etwas auch mal 


Senetek: Aktie steigt 126 Prozent dank positiver Nachrichten
Die Aktie des kleinen amerikanischen Biotechnologieunternehmens Senetek Plc. konnte gestern einen Anstieg um rund 126 Prozent verzeichnen, nachdem bekannt wurde, dass eine Studie zum Hautverjüngungs-Produkt Zeatin positiv ausgefallen sei.
Aufgrund der positiven Studie sollen jetzt weitere umfangreiche klinische Tests durchgeführt werden, hieß es vom Unternehmen. Da Senetek bereits Verträge mit Kosmetikunternehmen wie Revlon hat, könnten positive Testergebnisse langfristig einen deutlichen Umsatzanstieg für das Unternehmen bedeuten.
Gegen Handelsende in den USA gehörte die Aktie neben Intel, Sun, Cisco und Oracle zu den fünf am meisten gehandelten Werten.
Die Aktie beendete den Handel bei 1,02 Dollar mit einem Plus von 126 Prozent.



Senetek: Aktie steigt 126 Prozent dank positiver Nachrichten
Die Aktie des kleinen amerikanischen Biotechnologieunternehmens Senetek Plc. konnte gestern einen Anstieg um rund 126 Prozent verzeichnen, nachdem bekannt wurde, dass eine Studie zum Hautverjüngungs-Produkt Zeatin positiv ausgefallen sei.
Aufgrund der positiven Studie sollen jetzt weitere umfangreiche klinische Tests durchgeführt werden, hieß es vom Unternehmen. Da Senetek bereits Verträge mit Kosmetikunternehmen wie Revlon hat, könnten positive Testergebnisse langfristig einen deutlichen Umsatzanstieg für das Unternehmen bedeuten.
Gegen Handelsende in den USA gehörte die Aktie neben Intel, Sun, Cisco und Oracle zu den fünf am meisten gehandelten Werten.
Die Aktie beendete den Handel bei 1,02 Dollar mit einem Plus von 126 Prozent.
News  ..
..
Biomira Phase II Colorectal Trial Results Update
EDMONTON, Mar 12, 2004 (Canada NewsWire via COMTEX) -- Biomira Inc.
(Nasdaq: BIOM) (TSX:BRA) today provided an update of data from the Phase II
Theratope(R) vaccine colorectal study of 20 patients. A Kaplan-Meier Survival
and Time to Disease Progression Curve of the 20 colorectal cancer patients who
received combination chemotherapy plus Theratope in the featured study showed a
median survival of 17.8 months and a median time to disease progression of 8.4
months. The median time to disease progression remains unchanged from data
reported in June 2003.
The trial was designed to evaluate the safety of Theratope in patients with
metastatic colorectal cancer, as well as to evaluate the ability of the vaccine
to induce an immune response in patients when given in combination with
first-line chemotherapy. Although the trial was not designed to evaluate
survival benefit in these small numbers, it indicates a positive trend in the
patients followed.
Biomira had reported earlier that the Phase II study of Theratope in the
treatment of metastatic colorectal cancer showed that patients are capable of
mounting an immune response to the investigational vaccine while receiving
concurrent chemotherapy.
"Colorectal cancer is the third most common cancer found in men and women in
North America," said Charles Butts, MD, Cross Cancer Institute, Edmonton,
Alberta and Lead Investigator. "Although the death rate has been dropping due to
earlier diagnosis and improved treatments, we need to continue to find
innovative ways to treat this disease. This trial was an important step in
determining if Theratope could one day be such a treatment alternative."
"We are encouraged with the results of this trial, which was an opportunity to
gather data using Theratope in combination with chemotherapy," said Alex
McPherson, MD, PhD, President and CEO of Biomira Inc. "As reported in June of
2003 the trial accomplished its goals, showing the vaccine to have a good safety
profile and having the ability to induce an immune response. Although not a
study endpoint, this additional survival data will be useful in finalizing
decisions for next steps with Theratope. We continue to follow patients for
additional clinical data"
Gruß
Vaio
 ..
..Biomira Phase II Colorectal Trial Results Update
EDMONTON, Mar 12, 2004 (Canada NewsWire via COMTEX) -- Biomira Inc.
(Nasdaq: BIOM) (TSX:BRA) today provided an update of data from the Phase II
Theratope(R) vaccine colorectal study of 20 patients. A Kaplan-Meier Survival
and Time to Disease Progression Curve of the 20 colorectal cancer patients who
received combination chemotherapy plus Theratope in the featured study showed a
median survival of 17.8 months and a median time to disease progression of 8.4
months. The median time to disease progression remains unchanged from data
reported in June 2003.
The trial was designed to evaluate the safety of Theratope in patients with
metastatic colorectal cancer, as well as to evaluate the ability of the vaccine
to induce an immune response in patients when given in combination with
first-line chemotherapy. Although the trial was not designed to evaluate
survival benefit in these small numbers, it indicates a positive trend in the
patients followed.
Biomira had reported earlier that the Phase II study of Theratope in the
treatment of metastatic colorectal cancer showed that patients are capable of
mounting an immune response to the investigational vaccine while receiving
concurrent chemotherapy.
"Colorectal cancer is the third most common cancer found in men and women in
North America," said Charles Butts, MD, Cross Cancer Institute, Edmonton,
Alberta and Lead Investigator. "Although the death rate has been dropping due to
earlier diagnosis and improved treatments, we need to continue to find
innovative ways to treat this disease. This trial was an important step in
determining if Theratope could one day be such a treatment alternative."
"We are encouraged with the results of this trial, which was an opportunity to
gather data using Theratope in combination with chemotherapy," said Alex
McPherson, MD, PhD, President and CEO of Biomira Inc. "As reported in June of
2003 the trial accomplished its goals, showing the vaccine to have a good safety
profile and having the ability to induce an immune response. Although not a
study endpoint, this additional survival data will be useful in finalizing
decisions for next steps with Theratope. We continue to follow patients for
additional clinical data"
Gruß
Vaio
Jetzt müssten wir aber langsam die 6€ knacken

60 €
USA
2.02 0.08 +4.12% Vol 250.000
2.02 0.08 +4.12% Vol 250.000

Und dann sag mal einer wenn BLP25 Flop können sie den Laden zu machen ,Neeee nach allen Seiten laufen Patente, Geld ist auch noch da, ach so Neuinvestitionen gibt es ja auch noch.



Keiner weiß die Ergebnisse von BLP25 trotzdem bekommt man den Wert immer noch für 2,08$ ! 
In zwei Wochen wird dieser Wert für mind. 3Tage unter 3$ nicht mehr zu bekommen sein

In zwei Wochen wird dieser Wert für mind. 3Tage unter 3$ nicht mehr zu bekommen sein
Nochmal ne Frage: Hab ich das richtig verstanden, BLP25 wird gegen verschiedene Krebsarten getestet. Ist das in etwa vergleichbar mit Velcade von MLNM oder bin ich jetzt komplett auf dem falschen Dampfer. 

@blb
Von BLP25 gehen unterschiedliche Produkte aus wie bei Theratope!
Einfach mal schlau machen unter www.Biomira.com



Von BLP25 gehen unterschiedliche Produkte aus wie bei Theratope!
Einfach mal schlau machen unter www.Biomira.com



BIOMIRA ANNOUNCE PHASE II BLP-25 VACCINE TRIAL DOES NOT MEET PRIMARY ENDPOINTS - Trend to Improvement in Survival Seen in Subset of Patients
EDMONTON, ALBERTA, CANADA: March 14, 2004 — Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) announced today that the results from a pivotal Phase IIb non-small cell lung cancer (NSCLC) trial with the BLP25 vaccine did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival. However, one pre-stratified subset of patients in the treatment group, men on smoking treatment following chemotherapy, appeared to show a favourable trend to improvement in survival. Further analysis of this subset of patients is underway, as is additional analyses of the complete trial data.
Following this further analysis of the subset data, the Companies plan to discuss the results with regulatory agencies. Based on these conversations and a full evaluation of the data, the Companies will then determine how to proceed and the information will be communicated to stakeholders at that time.
“Lung cancer is the leading cause of cancer-related mortality for both sexes in North America. This study has resulted in a wealth of information about non-small cell lung cancer (NSCLC) , and it is important that we conduct a complete review of the data so that we can determine our best course of action.” said Alex McPherson, MD, PhD, President and CEO of Biomira. “After analysis of the subset data, we intend to discuss this information with the respective regulatory agencies in the U.S., Canada and Europe as soon as possible. We hope to have the first of these discussions within the next three to five months.”
“We have additional clinical trials underway and plan to continue those BLP-25 trials while we fully evaluate the data from the Phase II Liposomal IL-2 (L-IL-2) cancer study and determine our next steps,” said Jane Tulloch Director, Investor Relations.
“I would like to thank the patients and clinicians who participated in this study,” said Guy Ely, MD Vice President, Clinical and Medical Affairs and lead clinical investigator. “It has yielded important information that warrants further investigation.”
Biomira and Pepsi Cola are also collaborating on the development of LOL-26 Liposomal vaccine. LOL-26 is being evaluated in a 85-patient Phase IIb controlled study for kidney cancer and in a Phase II pilot study for prostate cancer patients.Results from both of these trials are expected later this year or in early 2005.
“We appreciate the continued support of our investors in our collaborative effort to develop innovative approaches for cancer control,” said Alex McPherson.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira’s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People™.
EDMONTON, ALBERTA, CANADA: March 14, 2004 — Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) announced today that the results from a pivotal Phase IIb non-small cell lung cancer (NSCLC) trial with the BLP25 vaccine did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival. However, one pre-stratified subset of patients in the treatment group, men on smoking treatment following chemotherapy, appeared to show a favourable trend to improvement in survival. Further analysis of this subset of patients is underway, as is additional analyses of the complete trial data.
Following this further analysis of the subset data, the Companies plan to discuss the results with regulatory agencies. Based on these conversations and a full evaluation of the data, the Companies will then determine how to proceed and the information will be communicated to stakeholders at that time.
“Lung cancer is the leading cause of cancer-related mortality for both sexes in North America. This study has resulted in a wealth of information about non-small cell lung cancer (NSCLC) , and it is important that we conduct a complete review of the data so that we can determine our best course of action.” said Alex McPherson, MD, PhD, President and CEO of Biomira. “After analysis of the subset data, we intend to discuss this information with the respective regulatory agencies in the U.S., Canada and Europe as soon as possible. We hope to have the first of these discussions within the next three to five months.”
“We have additional clinical trials underway and plan to continue those BLP-25 trials while we fully evaluate the data from the Phase II Liposomal IL-2 (L-IL-2) cancer study and determine our next steps,” said Jane Tulloch Director, Investor Relations.
“I would like to thank the patients and clinicians who participated in this study,” said Guy Ely, MD Vice President, Clinical and Medical Affairs and lead clinical investigator. “It has yielded important information that warrants further investigation.”
Biomira and Pepsi Cola are also collaborating on the development of LOL-26 Liposomal vaccine. LOL-26 is being evaluated in a 85-patient Phase IIb controlled study for kidney cancer and in a Phase II pilot study for prostate cancer patients.Results from both of these trials are expected later this year or in early 2005.
“We appreciate the continued support of our investors in our collaborative effort to develop innovative approaches for cancer control,” said Alex McPherson.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira’s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People™.
Yahoo Board
BIOMIRA VERKÜNDEN PHASE II BLP-25, das VACCINE VERSUCH NICHT PRIMÄRENDPUNKTE - Tendenz zur Verbesserung im Überleben TRIFFT, das in Teilmenge Patienten gesehen wird
EDMONTON, ALBERTA, KANADA: März 14, 2004 -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) verkündete heute, daß die Resultate von einem Versuch des Angelphase IIb nicht-kleinen Zelle Lungenkrebses (NSCLC) mit dem Impfstoff BLP25 nicht die zwei trafen, vorbestimmte statistische Endpunkte der Zeit zur Krankheitweiterentwicklung und zum gesamten Überleben. Jedoch schien eine vor-geschichtete Teilmenge Patienten in der Behandlunggruppe, Männer in rauchender Behandlung nach Chemotherapie, eine vorteilhafte Tendenz zur Verbesserung im Überleben zu zeigen. Weitere Analyse dieser Teilmenge Patienten ist unterwegs, wie zusätzliche Analysen der kompletten Probedaten.
Nach dieser weiteren Analyse der Teilmenge Daten, planen die Firmen, die Resultate mit Aufsichtsbehörden zu besprechen. Gegründet auf diesen Gesprächen und einer vollen Auswertung der Daten, stellen die Firmen dann fest, wie man fortfährt und die Informationen werden zu den Verwahrern zu dieser Zeit mitgeteilt.
"Lungenkrebs ist die führende Ursache der Krebs-in Verbindung stehenden Sterblichkeit für beide Geschlechter in Nordamerika. Diese Studie hat eine Fülle der Informationen über nicht-kleinen Zelle Lungenkrebs (NSCLC) ergeben, und es ist wichtig, daß wir einen kompletten Bericht der Daten leiten, damit wir unsere beste Vorgehensweise feststellen können." besagtes Alex McPherson, MD, PhD, Präsident und CEO von Biomira. "nach Analyse der Teilmenge Daten, beabsichtigen wir, diese Informationen mit den jeweiligen Aufsichtsbehörden in den VEREINIGTEN STAATEN, im Kanada und im Europa so bald wie möglich zu besprechen. Wir hoffen, das erste dieser Diskussionen innerhalb der folgenden drei bis fünf Monate zu haben."
"wir haben zusätzliche klinische Versuche unterwegs und planen, jene Versuche BLP-25 fortzusetzen, während wir völlig die Daten von der Phase II liposomalen Studie des Krebses IL-2 (L-IL-2) auswerten und unsere folgenden Schritte feststellen," sagten Jane Tulloch Direktor, Beziehungen zwischen den Investoren.
"ich möchte den Patienten und den Klinikern danken, die an dieser Studie teilnahmen," sagte Vizepräsidenten, klinischer und medizinischer die Angelegenheiten des Kerl-Ely, DES MD und führe klinischen Forscher. "es hat erbracht wichtigen Informationen diese Ermächtigungen weiter Untersuchung."
Biomira und Pepsi Kolabaum arbeiten auch auf der Entwicklung des liposomalen Impfstoffs LOL-26 zusammen. LOL-26 wird in eine Phase 85-patient IIb gesteuerte Studie für Nierekrebs ausgewertet und in einer Phase II Versuchsstudie für Prostatakrebs werden patients.Results von beiden dieser Versuche später dieses Jahr oder frühem 2005 erwartet.
"wir schätzen die anhaltende Unterstützung unserer Investoren in unserer gemeinschaftlichen Bemühung, erfinderische Annäherungen zur Krebssteuerung zu entwickeln," sagte Alex McPherson.
Biomira ist eine Biotechnologiefirma, die auf die Entwicklung der erfinderischen therapeutischen Annäherungen zum Krebsmanagement sich spezialisiert. Verpflichtung Biomiras gegenüber der Behandlung des Krebses konzentriert z.Z. auf die Entwicklung der synthetischen Impfstoffe und der Romanstrategien für Krebs Immunotherapy. Wir sind die Krebs-Impfstoff-Leute™.







BIOMIRA VERKÜNDEN PHASE II BLP-25, das VACCINE VERSUCH NICHT PRIMÄRENDPUNKTE - Tendenz zur Verbesserung im Überleben TRIFFT, das in Teilmenge Patienten gesehen wird
EDMONTON, ALBERTA, KANADA: März 14, 2004 -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) verkündete heute, daß die Resultate von einem Versuch des Angelphase IIb nicht-kleinen Zelle Lungenkrebses (NSCLC) mit dem Impfstoff BLP25 nicht die zwei trafen, vorbestimmte statistische Endpunkte der Zeit zur Krankheitweiterentwicklung und zum gesamten Überleben. Jedoch schien eine vor-geschichtete Teilmenge Patienten in der Behandlunggruppe, Männer in rauchender Behandlung nach Chemotherapie, eine vorteilhafte Tendenz zur Verbesserung im Überleben zu zeigen. Weitere Analyse dieser Teilmenge Patienten ist unterwegs, wie zusätzliche Analysen der kompletten Probedaten.
Nach dieser weiteren Analyse der Teilmenge Daten, planen die Firmen, die Resultate mit Aufsichtsbehörden zu besprechen. Gegründet auf diesen Gesprächen und einer vollen Auswertung der Daten, stellen die Firmen dann fest, wie man fortfährt und die Informationen werden zu den Verwahrern zu dieser Zeit mitgeteilt.
"Lungenkrebs ist die führende Ursache der Krebs-in Verbindung stehenden Sterblichkeit für beide Geschlechter in Nordamerika. Diese Studie hat eine Fülle der Informationen über nicht-kleinen Zelle Lungenkrebs (NSCLC) ergeben, und es ist wichtig, daß wir einen kompletten Bericht der Daten leiten, damit wir unsere beste Vorgehensweise feststellen können." besagtes Alex McPherson, MD, PhD, Präsident und CEO von Biomira. "nach Analyse der Teilmenge Daten, beabsichtigen wir, diese Informationen mit den jeweiligen Aufsichtsbehörden in den VEREINIGTEN STAATEN, im Kanada und im Europa so bald wie möglich zu besprechen. Wir hoffen, das erste dieser Diskussionen innerhalb der folgenden drei bis fünf Monate zu haben."
"wir haben zusätzliche klinische Versuche unterwegs und planen, jene Versuche BLP-25 fortzusetzen, während wir völlig die Daten von der Phase II liposomalen Studie des Krebses IL-2 (L-IL-2) auswerten und unsere folgenden Schritte feststellen," sagten Jane Tulloch Direktor, Beziehungen zwischen den Investoren.
"ich möchte den Patienten und den Klinikern danken, die an dieser Studie teilnahmen," sagte Vizepräsidenten, klinischer und medizinischer die Angelegenheiten des Kerl-Ely, DES MD und führe klinischen Forscher. "es hat erbracht wichtigen Informationen diese Ermächtigungen weiter Untersuchung."
Biomira und Pepsi Kolabaum arbeiten auch auf der Entwicklung des liposomalen Impfstoffs LOL-26 zusammen. LOL-26 wird in eine Phase 85-patient IIb gesteuerte Studie für Nierekrebs ausgewertet und in einer Phase II Versuchsstudie für Prostatakrebs werden patients.Results von beiden dieser Versuche später dieses Jahr oder frühem 2005 erwartet.
"wir schätzen die anhaltende Unterstützung unserer Investoren in unserer gemeinschaftlichen Bemühung, erfinderische Annäherungen zur Krebssteuerung zu entwickeln," sagte Alex McPherson.
Biomira ist eine Biotechnologiefirma, die auf die Entwicklung der erfinderischen therapeutischen Annäherungen zum Krebsmanagement sich spezialisiert. Verpflichtung Biomiras gegenüber der Behandlung des Krebses konzentriert z.Z. auf die Entwicklung der synthetischen Impfstoffe und der Romanstrategien für Krebs Immunotherapy. Wir sind die Krebs-Impfstoff-Leute™.







@BaronvonMuenchhausen
#603
Da hatte jemand Langeweile und sich ein Scherz geleistet,
obwohl mit dieser Falschen Aussage schön zu sehen ist wie hoch nun mal das Risiko bei Biomirashares ist!
#603

Da hatte jemand Langeweile und sich ein Scherz geleistet,
obwohl mit dieser Falschen Aussage schön zu sehen ist wie hoch nun mal das Risiko bei Biomirashares ist!
Also langsam sollte die Aktie doch stark überverkauft sein.
Eine zumindest technische Reaktion ist doch nun überfällig. Oder??
Eine zumindest technische Reaktion ist doch nun überfällig. Oder??

Versteh ich nicht.
Ständig gute nachrichten aber der Kurs steigt nicht
Ständig gute nachrichten aber der Kurs steigt nicht

hm...ich denke, die guten Nachrichten fehlen zur Zeit. Schaut Euch mal den miesen Umsatz heute in D an. Die Kurse werden natürlich überm Teich gemacht...
Gutes Traden! S
Gutes Traden! S
Schon wieder im Minus geschlossen





moin,
steht die veröffentlichung der bp25 ergebnisse noch nach wie vor im 1 quartal an.?
danke und schönen tag noch!
teischerwutz
steht die veröffentlichung der bp25 ergebnisse noch nach wie vor im 1 quartal an.?
danke und schönen tag noch!
teischerwutz
@ll
Wir werden hier mit Sicherheit noch einmal ein Run sehen, die Veröffentlichung der BLP25 Ergebnisse soll Ende März bzw. sie kann sich auch um einen kurze Zeitraum bis Ende April verschieben,so wie Biomira im Dezember berichtet hat!
Leider kann ich nicht sagen,wie die Ergebnisse aussehen werden, vermute sogar das wir bei solch einer Hochwertigen Droge hier eher in die Phase III gehen!
Mal abwarten!
Wir werden hier mit Sicherheit noch einmal ein Run sehen, die Veröffentlichung der BLP25 Ergebnisse soll Ende März bzw. sie kann sich auch um einen kurze Zeitraum bis Ende April verschieben,so wie Biomira im Dezember berichtet hat!
Leider kann ich nicht sagen,wie die Ergebnisse aussehen werden, vermute sogar das wir bei solch einer Hochwertigen Droge hier eher in die Phase III gehen!
Mal abwarten!
Upcoming Events
2004
March 31, 2004-
April 7, 2004
Edmonton, Alberta L-BLP25 Phase IIb Non-Small Cell Lung Cancer Clinical Analysis Results
Biomira and Merck kGaA are expecting clinical trial results at the end of March or very early in April 2004. The data are currently being accumulated and will then be reviewed by the Data Safety Monitoring Board for confirmation of the results.
Once the Companies have been unblinded to the data this information will be communicated to our stakeholders.
Until the Companies have been given the data, we cannot pinpoint the exact date and time this information will become available but we are providing you our best estimate at this time.
May 20, 2004
TBA Annual General Meeting
Biomira`s Annual General Meeting will be held on Thursday, May 20th, 2004. The location and timing of the meeting will be updated and added to this site, once solidified.
http://www.biomira.com
2004
March 31, 2004-
April 7, 2004
Edmonton, Alberta L-BLP25 Phase IIb Non-Small Cell Lung Cancer Clinical Analysis Results
Biomira and Merck kGaA are expecting clinical trial results at the end of March or very early in April 2004. The data are currently being accumulated and will then be reviewed by the Data Safety Monitoring Board for confirmation of the results.
Once the Companies have been unblinded to the data this information will be communicated to our stakeholders.
Until the Companies have been given the data, we cannot pinpoint the exact date and time this information will become available but we are providing you our best estimate at this time.
May 20, 2004
TBA Annual General Meeting
Biomira`s Annual General Meeting will be held on Thursday, May 20th, 2004. The location and timing of the meeting will be updated and added to this site, once solidified.
http://www.biomira.com
jetzt sind wir am unteren ende des seit oktober 2003 bestehenden aufwärtstrends.
jetzt heißt es beten, dass dieses wichtige marke nicht unterschritten wird.
die anstehenden ergebnisse sollten doch für auftrieb sorgen. was meint ihr?
jetzt heißt es beten, dass dieses wichtige marke nicht unterschritten wird.
die anstehenden ergebnisse sollten doch für auftrieb sorgen. was meint ihr?
Advectus(WKN: 693000)=>STRONG BUY!!!
Ich muss gestehen, dass ich mir von den Ergebnissen der BLP-25 Studie mehr versprochen hatte. Ich würde die Ergebnisse sogar als sehr enttäuschend einstufen. Ich hab bislang nur noch nicht geschmissen, weil ich hoffe, dass bei den Subgruppenanalysen noch etwas Brauchbares herauskommt. Und das wird sich in den nächsten Tagen zeigen. Zumindest war es angekündigt.
SCO
SCO
@ sun
ich habe Biomira heute geschmissen.
dafür die Lampen aufgestockt.
ich habe Biomira heute geschmissen.
dafür die Lampen aufgestockt.

Bin wenigstens hier noch mit was Plus raus
Until the Companies have been given the data, we cannot pinpoint the exact date and time this information will become available but we are providing you our best estimate at this time.
Wie beurteilt ihr den Satz "...are providing you our best estimate at this time".
Ist damit der zeitliche Horizont gemeint, dass die Daten bald definitiv anstehen, oder geht Biom davon aus, dass die Einschätzung der anstehenden Daten positiv ist?
@sun
Du schreibst, dass du über die blp25 Daten enttäuscht bist. Die sind doch noch nicht veröffentlicht, oder stehe ich auf der Leitung?
Danke und Gruß
Wie beurteilt ihr den Satz "...are providing you our best estimate at this time".
Ist damit der zeitliche Horizont gemeint, dass die Daten bald definitiv anstehen, oder geht Biom davon aus, dass die Einschätzung der anstehenden Daten positiv ist?
@sun
Du schreibst, dass du über die blp25 Daten enttäuscht bist. Die sind doch noch nicht veröffentlicht, oder stehe ich auf der Leitung?
Danke und Gruß
@teischerwurtz
Siehe PR: (NSCLC) trial with the BLP25 vaccine did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival
did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival  . However, one pre-stratified subset of patients in the treatment group, men on smoking treatment following chemotherapy, appeared to show a favourable trend to improvement in survival.
. However, one pre-stratified subset of patients in the treatment group, men on smoking treatment following chemotherapy, appeared to show a favourable trend to improvement in survival.
Das heisst, dass die beiden vordefinierten Endpunkte der Studie nicht erreicht wurden!!
Natürlich analysieren die nun weiter und bekommen mölicherweise in einer Subgruppenanalyse heraus, dass es in bestimmten Untergruppen doch noch positive Effekte gibt.
ABER: Diese sind hinsichtlich ihrer Aussagekraft WESENTLICH schwächer, da Post-hoc-Analyse und kein primärer Endpunkt. Signifikant und signifkant ist eben nicht das gleiche.
SCO
Siehe PR: (NSCLC) trial with the BLP25 vaccine
 did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival
did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival  . However, one pre-stratified subset of patients in the treatment group, men on smoking treatment following chemotherapy, appeared to show a favourable trend to improvement in survival.
. However, one pre-stratified subset of patients in the treatment group, men on smoking treatment following chemotherapy, appeared to show a favourable trend to improvement in survival.Das heisst, dass die beiden vordefinierten Endpunkte der Studie nicht erreicht wurden!!
Natürlich analysieren die nun weiter und bekommen mölicherweise in einer Subgruppenanalyse heraus, dass es in bestimmten Untergruppen doch noch positive Effekte gibt.
ABER: Diese sind hinsichtlich ihrer Aussagekraft WESENTLICH schwächer, da Post-hoc-Analyse und kein primärer Endpunkt. Signifikant und signifkant ist eben nicht das gleiche.
SCO
danke!
@all
seid ihr folglich alle negativ bezüglich des mittelfristigen kursverlaufs eingestellt?
könnten positive ergbenisse doch noch zu einer kursexplosion führen oder ist der ganz große wurf passé?
seid ihr folglich alle negativ bezüglich des mittelfristigen kursverlaufs eingestellt?
könnten positive ergbenisse doch noch zu einer kursexplosion führen oder ist der ganz große wurf passé?

Den großen Wurf sehe ich nicht, aber ich rechne mit höheren Kursen.
@ tupper
warum rechnest du mit steigenden kursen?
die luft sollte doch mittelfristig praktisch draußen sein.
warum rechnest du mit steigenden kursen?
die luft sollte doch mittelfristig praktisch draußen sein.
@teischerwutz
will nur nochmal klarstellen:
die PR, die dich so verunsichert ist gefaked, hat also nichts mit den results zu blp-25 zu tun:
News Release
BIOMIRA AND MERCK KGaA ANNOUNCE PHASE III THERATOPE® VACCINE TRIAL DOES NOT MEET PRIMARY ENDPOINTS - Trend to Improvement in Survival Seen in Subset of Patients
EDMONTON, ALBERTA, CANADA: June 16, 2003
EDMONTON, ALBERTA, CANADA and Darmstadt, Germany — June 16, 2003 — Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) and Merck KGaA of Darmstadt, Germany, announced today that the results from a large pivotal Phase III trial of Theratope® vaccine for women with metastatic breast cancer did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival. However, one pre-stratified subset of patients in the treatment group, women on hormonal treatment following chemotherapy, appeared to show a favourable trend to improvement in survival. Further analysis of this subset of patients is underway, as is additional analyses of the complete trial data...
ich rechne bis ende nächster woche mit deutlich höheren kursen,
zumal die letzte news ja keine PR war, die über die ticker gelaufen,
sondern lediglich ein "upcoming event" auf der biomira homepage:
Upcoming Events
2004
L-BLP25 Phase IIb Non-Small Cell Lung Cancer Clinical Analysis Results
will nur nochmal klarstellen:
die PR, die dich so verunsichert ist gefaked, hat also nichts mit den results zu blp-25 zu tun:
News Release
BIOMIRA AND MERCK KGaA ANNOUNCE PHASE III THERATOPE® VACCINE TRIAL DOES NOT MEET PRIMARY ENDPOINTS - Trend to Improvement in Survival Seen in Subset of Patients
EDMONTON, ALBERTA, CANADA: June 16, 2003
EDMONTON, ALBERTA, CANADA and Darmstadt, Germany — June 16, 2003 — Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) and Merck KGaA of Darmstadt, Germany, announced today that the results from a large pivotal Phase III trial of Theratope® vaccine for women with metastatic breast cancer did not meet the two pre-determined statistical endpoints of time to disease progression and overall survival. However, one pre-stratified subset of patients in the treatment group, women on hormonal treatment following chemotherapy, appeared to show a favourable trend to improvement in survival. Further analysis of this subset of patients is underway, as is additional analyses of the complete trial data...
ich rechne bis ende nächster woche mit deutlich höheren kursen,
zumal die letzte news ja keine PR war, die über die ticker gelaufen,
sondern lediglich ein "upcoming event" auf der biomira homepage:
Upcoming Events
2004
L-BLP25 Phase IIb Non-Small Cell Lung Cancer Clinical Analysis Results
@tiger
Eigentlich nur rein spekulativ. Es könnte aber auch substantiell mehr an biomira dran sein, als wir hier sehen,denn richtiger Schrott steigt erfahrungsgemäß viel toller als es biomira tut.
Eigentlich nur rein spekulativ. Es könnte aber auch substantiell mehr an biomira dran sein, als wir hier sehen,denn richtiger Schrott steigt erfahrungsgemäß viel toller als es biomira tut.
okay, schaun mer mal wie es weitergeht.
das marktumfeld ist derzeit natürlich auch in einer beschissenen verfassung.
das marktumfeld ist derzeit natürlich auch in einer beschissenen verfassung.
@ll
Aufpassen,ich erwarte zwar wie schon mehr mal´s gepostet habe bei solch einer bedeutenden Droge eine PhaseIII, die seitens des Unternehmens nicht eingeplant ist,aber BITTE es sind aktuell noch keine Daten von
BLP25 veröffentlicht worden!!!
Schaut doch mal auf die Umsätze die wir seit Tagen sehen,besser kann man keine Interpretation wieder geben ,kein
Mensch hat auch nur ein Funken Ahnung was hier für Ergebnisse in den nächsten Wochen präsentiert werden!

Aufpassen,ich erwarte zwar wie schon mehr mal´s gepostet habe bei solch einer bedeutenden Droge eine PhaseIII, die seitens des Unternehmens nicht eingeplant ist,aber BITTE es sind aktuell noch keine Daten von
BLP25 veröffentlicht worden!!!
Schaut doch mal auf die Umsätze die wir seit Tagen sehen,besser kann man keine Interpretation wieder geben ,kein
Mensch hat auch nur ein Funken Ahnung was hier für Ergebnisse in den nächsten Wochen präsentiert werden!

Qdonner
wie würde sich deiner meinung nach eine phase3 kursmäßig auswirken?
ich bin derzeit tendenziell eher negativ gestimmt.
wie würde sich deiner meinung nach eine phase3 kursmäßig auswirken?
ich bin derzeit tendenziell eher negativ gestimmt.
160.000er buy order, erstes limit 1,75, gerade auf 1,78 hochgezogen.
da will einer aber richtig rein. sehr schön!
da will einer aber richtig rein. sehr schön!
@teischerwutz
Länger Forschungszeit sehe ich als ein positives Zeichen,sollte BLP25
keine positive Daten wiedergeben ,würde hier nach einer PhaseIIb keine PhaseIII folgen,man beachte:"nach einer PhaseIIb"
Des weiteren verschenkt ein erfahrenes Unternehmen wie Merck seine Zeit und sein Geld auch noch nicht einfach so
Wir werden sehen was hier auf uns zu kommt,wie gesagt in BLP25 stecken mehrere Produkte die sich in unterschiedlichen Phasen befinden und nicht wie einige hier denken das es sich bei BLP25 um ein Produkt t bzw. eine Forschungreihe handelt.
Länger Forschungszeit sehe ich als ein positives Zeichen,sollte BLP25
keine positive Daten wiedergeben ,würde hier nach einer PhaseIIb keine PhaseIII folgen,man beachte:"nach einer PhaseIIb"
Des weiteren verschenkt ein erfahrenes Unternehmen wie Merck seine Zeit und sein Geld auch noch nicht einfach so

Wir werden sehen was hier auf uns zu kommt,wie gesagt in BLP25 stecken mehrere Produkte die sich in unterschiedlichen Phasen befinden und nicht wie einige hier denken das es sich bei BLP25 um ein Produkt t bzw. eine Forschungreihe handelt.
American Society of Clinical Oncology (ASCO) Accepts Biomira`s BLP25 Liposomal Vaccine Phase IIB Non-Small Cell Lung Cancer Trial Results for Poster Presentation at 2004 Meeting
Thursday March 25, 9:00 am ET
ASCO Also Accepts Two Additional Abstracts for Poster Presentation
EDMONTON, March 25 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) announced today that data from the Company`s Phase IIb BLP25 Liposomal vaccine (L-BLP25) trial in non-small cell lung cancer has been accepted as the subject of a poster presentation at the 2004 Annual Meeting of ASCO. The meeting will take place in New Orleans, Louisiana, June 5-8. The lead investigator for the Phase IIb trial and scheduled ASCO presenter is Dr. Charles Butts, Medical Oncologist, the Cross Cancer Institute, Edmonton, Alberta.
The trial is being conducted at 17 sites across Canada and the United Kingdom. This controlled, randomized trial involves 171 men and women whose disease was stable or who had responded to treatment following completion of their first line standard chemotherapy. The study is designed to document the safety profile of the vaccine and to evaluate efficacy by comparing survival in the two arms. Patients were randomized to either L-BLP25 plus best standard of care or to best standard of care alone. Best standard of care included palliative radiotherapy and/or second line chemotherapy according to standard clinical practice. Biomira and its collaborator Merck KGaA of Darmstadt, Germany are currently preparing for the clinical analysis of the results from this trial, with an announcement of the results expected in the next few weeks.
"ASCO receives thousands of abstracts each year for review by the Scientific Program Committee, and we are very pleased that Dr. Butts` abstract was accepted," said Alex McPherson, MD, PhD, President and CEO of Biomira. "This presentation at ASCO will be our first opportunity to discuss our clinical results at a scientific forum, and we look forward to it."
L-BLP25 Phase II Prostate Poster Presentation
Biomira has also been notified that clinical data will be presented at the Annual Meeting of ASCO on the L-BLP25 Phase II study in prostate cancer. This is also scheduled to be a poster presentation.
In June 2003 Biomira announced results from its Phase II study of L-BLP25 in a small group of patients with rising prostate specific antigen (PSA) post radical prostatectomy. The trial was conducted to determine whether the vaccine could reduce or stabilize PSA levels. L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients. Preliminary results in this small patient population did not conclusively show a reduction or stabilization of serum PSA levels. However, there appears to be a prolongation of PSA doubling time (PSADT) in approximately 40 per cent of the patients. While there has been no commitment to conduct further trials at this time in this indication, the patients continue to be followed for PSA levels for a period of 12 months following their last vaccination. The lead investigator on this trial is Dr. Scott North, Medical Oncologist, the Cross Cancer Institute, Edmonton, Alberta.
Theratope® Vaccine Phase III Data Poster Presentation
The third abstract accepted for poster presentation at ASCO involves the Theratope Phase III study. The poster will focus on immune response of the women involved in this randomized, controlled, double blind, multi-centre study.
The Companies reported in June 2003 that the Phase III results showed that Theratope did not show a statistical difference in the two pre-determined endpoints of time to disease progression and overall survival. However, one large pre-stratified subset of more than 300 women, those on hormonal treatment following chemotherapy, appeared to show a favourable trend to improvement in survival, although not statistically significant. The Companies are conducting further analysis of this subset of patients to potentially determine a mechanism of action that could help explain the perceived benefit to this group of women.
ASCO
The ASCO Annual Meeting is the premier educational and scientific event for oncology professionals. The 2004 meeting is expected to attract more than 26,000 attendees from all over the world.
The Companies
Our key collaboration in developing therapeutic cancer vaccines is with Merck KGaA. With more than 34,200 employees in 53 countries, the Merck Group generated sales of EUR 7.2 billion in 2003. Founded in 1668 in Darmstadt, Germany, the Company aims to be a world leader in its core businesses of pharmaceuticals and chemicals. Merck groups its operating activities under Merck KGaA, in which the Merck family holds 74 percent and the remaining 26 percent is publicly traded. The former U.S. subsidiary, Merck & Co., has been a completely independent company since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas -- monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Thursday March 25, 9:00 am ET
ASCO Also Accepts Two Additional Abstracts for Poster Presentation
EDMONTON, March 25 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) announced today that data from the Company`s Phase IIb BLP25 Liposomal vaccine (L-BLP25) trial in non-small cell lung cancer has been accepted as the subject of a poster presentation at the 2004 Annual Meeting of ASCO. The meeting will take place in New Orleans, Louisiana, June 5-8. The lead investigator for the Phase IIb trial and scheduled ASCO presenter is Dr. Charles Butts, Medical Oncologist, the Cross Cancer Institute, Edmonton, Alberta.
The trial is being conducted at 17 sites across Canada and the United Kingdom. This controlled, randomized trial involves 171 men and women whose disease was stable or who had responded to treatment following completion of their first line standard chemotherapy. The study is designed to document the safety profile of the vaccine and to evaluate efficacy by comparing survival in the two arms. Patients were randomized to either L-BLP25 plus best standard of care or to best standard of care alone. Best standard of care included palliative radiotherapy and/or second line chemotherapy according to standard clinical practice. Biomira and its collaborator Merck KGaA of Darmstadt, Germany are currently preparing for the clinical analysis of the results from this trial, with an announcement of the results expected in the next few weeks.
"ASCO receives thousands of abstracts each year for review by the Scientific Program Committee, and we are very pleased that Dr. Butts` abstract was accepted," said Alex McPherson, MD, PhD, President and CEO of Biomira. "This presentation at ASCO will be our first opportunity to discuss our clinical results at a scientific forum, and we look forward to it."
L-BLP25 Phase II Prostate Poster Presentation
Biomira has also been notified that clinical data will be presented at the Annual Meeting of ASCO on the L-BLP25 Phase II study in prostate cancer. This is also scheduled to be a poster presentation.
In June 2003 Biomira announced results from its Phase II study of L-BLP25 in a small group of patients with rising prostate specific antigen (PSA) post radical prostatectomy. The trial was conducted to determine whether the vaccine could reduce or stabilize PSA levels. L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients. Preliminary results in this small patient population did not conclusively show a reduction or stabilization of serum PSA levels. However, there appears to be a prolongation of PSA doubling time (PSADT) in approximately 40 per cent of the patients. While there has been no commitment to conduct further trials at this time in this indication, the patients continue to be followed for PSA levels for a period of 12 months following their last vaccination. The lead investigator on this trial is Dr. Scott North, Medical Oncologist, the Cross Cancer Institute, Edmonton, Alberta.
Theratope® Vaccine Phase III Data Poster Presentation
The third abstract accepted for poster presentation at ASCO involves the Theratope Phase III study. The poster will focus on immune response of the women involved in this randomized, controlled, double blind, multi-centre study.
The Companies reported in June 2003 that the Phase III results showed that Theratope did not show a statistical difference in the two pre-determined endpoints of time to disease progression and overall survival. However, one large pre-stratified subset of more than 300 women, those on hormonal treatment following chemotherapy, appeared to show a favourable trend to improvement in survival, although not statistically significant. The Companies are conducting further analysis of this subset of patients to potentially determine a mechanism of action that could help explain the perceived benefit to this group of women.
ASCO
The ASCO Annual Meeting is the premier educational and scientific event for oncology professionals. The 2004 meeting is expected to attract more than 26,000 attendees from all over the world.
The Companies
Our key collaboration in developing therapeutic cancer vaccines is with Merck KGaA. With more than 34,200 employees in 53 countries, the Merck Group generated sales of EUR 7.2 billion in 2003. Founded in 1668 in Darmstadt, Germany, the Company aims to be a world leader in its core businesses of pharmaceuticals and chemicals. Merck groups its operating activities under Merck KGaA, in which the Merck family holds 74 percent and the remaining 26 percent is publicly traded. The former U.S. subsidiary, Merck & Co., has been a completely independent company since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas -- monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
die letzte halbe Stunde kommt Leben in die Bude....
RT bei 2,02$.....
RT bei 2,02$.....
#630 + donner
wie interpretiert Ihr die Meldung?
ist ja eigentlich nur "eine Zulassung" dass auf einer Konferenz präsentiert werden darf ...
wie interpretiert Ihr die Meldung?
ist ja eigentlich nur "eine Zulassung" dass auf einer Konferenz präsentiert werden darf ...
@ll
Guten Abend,
vorab erst mal erst Glückwunsch die hier klugerweise noch nicht geworfen haben,es hat mal wieder gezeigt das man an der Börse Geduld zeigen muss!
So die aktuelle News sehe ich positiv,hier wird den Börsianern erneut offenbart wie wertvoll ein positiver BLP25 Ausgang sein könnte!
Andersherum muss ich sagen das solch ein eine Nachricht denn Zock in der Biobranche noch gefährlicher macht,das eventuelle Daytraderorders als Insiderkäufe gewertet werden könnten!
Biomira wird für mich nun immer mehr zum Langfristinvestment!
,wo TopNews zeitgemäß nicht vorhersehbar sind, deswegen werde ich fast meine ganze Position bei eventuellen schlechten Nachrichten über den April hinaus laufen lassen!
Fazit:Sehe bei Biomira weiterhin eine sehr grosse Chance,bei was etwas ganz Großen von Anfang an dabei zu sein.
gruss
Guten Abend,
vorab erst mal erst Glückwunsch die hier klugerweise noch nicht geworfen haben,es hat mal wieder gezeigt das man an der Börse Geduld zeigen muss!
So die aktuelle News sehe ich positiv,hier wird den Börsianern erneut offenbart wie wertvoll ein positiver BLP25 Ausgang sein könnte!
Andersherum muss ich sagen das solch ein eine Nachricht denn Zock in der Biobranche noch gefährlicher macht,das eventuelle Daytraderorders als Insiderkäufe gewertet werden könnten!
Biomira wird für mich nun immer mehr zum Langfristinvestment!
,wo TopNews zeitgemäß nicht vorhersehbar sind, deswegen werde ich fast meine ganze Position bei eventuellen schlechten Nachrichten über den April hinaus laufen lassen!
Fazit:Sehe bei Biomira weiterhin eine sehr grosse Chance,bei was etwas ganz Großen von Anfang an dabei zu sein.
gruss
ASCO receives thousands of abstracts each year for review by the Scientific Program Committee, and we are very pleased that Dr. Butts` abstract was accepted," said Alex McPherson, MD, PhD, President and CEO of Biomira. "This presentation at ASCO will be our first opportunity to discuss our clinical results at a scientific forum, and we look forward to it."
_________________
L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients.
_________________
L-BLP25 showed a good safety profile and the dose and schedule were also well accepted by the patients.
20.05.2000
Biomira explodierte von 2 auf 22$
Die nächsten Wochen werden wieder zeigen was bei Biomira im Rammen des möglichen .....
BLP25 !
Biomira explodierte von 2 auf 22$
Die nächsten Wochen werden wieder zeigen was bei Biomira im Rammen des möglichen .....

BLP25 !
Zwischen den Zeilen kann man das eine oder andere positive auch aus der
heutigen Merck-Pressemitteilung entnehmen. Morgen ist in Frankfurt die
Hauptversammlung, vielleicht gibts weitere Hintergrundinfo`s
Pressemitteilung
Darmstadt - Die Merck KGaA gab heute die Zulassungsempfehlung für ErbituxTM
(Cetuximab) seitens des Ausschusses für Arzneispezialitäten (CPMP,
Committee for Proprietary Medicinal Products), dem wissenschaftlichen
Beratungsgremium der Europäischen Zulassungsbehörde für Arzneimittel (EMEA,
European Agency for the Evaluation of Medicinal Products), bekannt. Diese
Empfehlung wird an die Europäische Kommission weitergeleitet und ist damit
ein richtungsweisender Schritt auf dem Weg zur Erlangung der europaweiten
Marktzulassung für Erbitux, die für Mitte dieses Jahres erwartet wird.
Erbitux wird in Kombination mit Irinotecan zur Behandlung von Patienten mit
EGFR (epidermaler Wachstumsfaktor-Rezeptor)-exprimierendem
fortgeschrittenem Kolorektalkarzinom empfohlen, wenn eine Chemotherapie mit
Irinotecan bereits versagt hat. Der CPMP bewertet die eingereichten Daten
zur Wirksamkeit und Sicherheit von Erbitux als vollständig und empfiehlt
die uneingeschränkte Zulassung von Erbitux. Demgemäß sind mit der Zulassung
keine speziellen Auflagen verbunden, was für die Aussagekraft der bereits
eingereichten Daten zu Erbitux spricht.
Dieser Vorentscheid des CPMP ist ein wichtiger Schritt, der für die 200.000
Patienten, die jedes Jahr in Westeuropa erstmalig mit der Diagnose
Darmkrebs konfrontiert werden, berechtigte neue Hoffnung bringt. Über die
Hälfte von ihnen befindet sich zum Zeitpunkt der Diagnose bereits im
fortgeschrittenen, metastasierenden Erkrankungsstadium.(1)
Erbitux wurde im Dezember 2003 zuerst in der Schweiz für die
Kombinationsbehandlung mit Irinotecan zugelassen. Im Februar diesen Jahres
wurde Erbitux auch in den USA für die Kombination mit Irinotecan zur
Behandlung von Patienten mit EGFR-exprimierendem, fortgeschrittenem,
Irinotecan-refraktärem Kolorektalkarzinom eingeführt. Erbitux ist dort
ebenfalls für die Monotherapie bei Patienten mit einer
Irinotecan-Unverträglichkeit zugelassen.
Erbitux wurde in Europa auf Basis der Daten eingereicht, die in einer
großen klinischen Studie in 11 europäischen Ländern mit 57 beteiligten
Krankenhäusern und über 300 Patienten mit fortgeschrittenem,
metastasierendem Kolorektalkarzinom erhoben wurden. In der sogenannten BOND
(Bowel Oncology with Cetuximab Antibody)-Studie zeigte Erbitux in
Kombination mit dem Chemotherapeutikum Irinotecan bei mehr als 50 % der
Patienten eine positive Wirkung. Bei 23 % der Patienten bildete sich der
Tumor um mehr als die Hälfte zurück und bei weiteren 33 % dieser schwer
behandelbaren Patienten kam das Tumorwachstum zum Stillstand.(2)
"Solche Ansprechraten sind normalerweise mit einer Verlängerung der
Überlebenszeit verbunden", sagte Prof. David Cunningham, Chefarzt der
Abteilungen Gastrointestinal- und Lymphomerkrankungen des Royal Marsden
Hospital in London und Surrey (GB) und leitender Prüfarzt der BOND-Studie.
"Darmkrebs wird oft erst im fortgeschrittenen Stadium diagnostiziert und
ist mit den konventionellen Therapiemöglichkeiten schwer behandelbar,"
fügte Cunningham hinzu. "Aufgrund seiner sehr zielgerichteten Wirkungsweise
hat Erbitux vor allem in Kombination mit Chemotherapie vielversprechende
Ergebnisse geliefert und stellt deshalb eine wirksame neue
Behandlungsoption für Ärzte im Kampf gegen diesen immer häufiger
auftretenden Krebstyp dar."
Erbitux ist ein monoklonaler Antikörper vom Typ IgG1, der gezielt den
EGF-Rezeptor blockiert, der bei über 80 % metastasierender
Kolorektalkarzinome zu finden ist. Die Tumorarten, die EGFR exprimieren,
zeigen einen aggressiveren Krankheitsverlauf, sind resistenter gegenüber
Chemotherapie, neigen verstärkt zu Metastasen und bieten eine schlechte
Prognose.(3-5)
Die Wirkung von Erbitux beruht auf der Blockierung des EGFR. Dadurch wird
sowohl das Eindringen der Tumorzellen in gesundes Gewebe wie auch die
Ausbreitung, d.h. Metastasierung der Tumore in andere Körperregionen
vermindert. Durch die Blockierung des EGFR hemmt Erbitux auch die Bildung
neuer Blutgefäße im Inneren der Tumore (sog. Angiogenese), da die
Produktion des Angiogenesefaktors VEGF (vaskulärer endothelialer
Wachstumsfaktor) (6) verringert wird.
Erbitux wird sowohl als Monotherapie als auch in Kombination mit Irinotecan
im Allgemeinen gut vertragen. Die unter Erbitux auftretenden
Nebenwirkungen haben in der Regel keinen Einfluss auf die Fortführung der
Behandlung und scheinen auch die von Irinotecan bekannten Nebenwirkungen
(7) nicht zu verstärken.
"Wir hoffen mit der Bereitstellung dieser neuen Behandlungsoption das Leben
der Patienten nachhaltig zu ändern und zu verbessern," sagte Prof. Bernhard
Scheuble, der Vorsitzende der Geschäftsleitung der Merck KGaA. "Um noch
mehr Patienten helfen zu können, die an anderen Krebsarten erkrankt sind,
haben wir bereits ein großangelegtes klinisches Programm gestartet, das die
Verträglichkeit und Wirksamkeit dieses Arzneimittels weiter erforschen
soll."
"Mit Erbitux und vielen weiteren Krebsmitteln, die derzeit erforscht
werden, zeigt Merck sein hohes Engagement für die langfristige Entwicklung
eines beneidenswerten Portfolios an innovativen Produkten mit
vielversprechenden Behandlungsmöglichkeiten für Patienten," ergänzte Prof.
Scheuble.
Merck hat die Vermarktungsrechte für Erbitux außerhalb der USA und Kanada
1998 in Lizenz von ImClone Systems Incorporated in New York erworben. In
Japan halten beide Unternehmen das Co-Exklusivitätsrecht zur Vermarktung
von Erbitux.
Nicht-Schwerpunktprojekt eingestellt
Zugunsten einer stärkeren Fokussierung auf die Kernarbeitsgebiete Onkologie
und Cardiometabolic Care stellt Merck die Entwicklung von EMR 62203, einen
PDE V-Inhibitor zur Behandlung der erektilen Dysfunktion, ein. Der
Wirkstoff befand sich in Phase II der klinischen Entwicklung.
Hinweis an die Redaktionen:
Ausführliches Hintergrundmaterial zu Erbitux ist in Form von Texten, Fotos
und Grafiken im Internet erhältlich unter:
http://www.media-highlights.merck.de
Gruß Agio
heutigen Merck-Pressemitteilung entnehmen. Morgen ist in Frankfurt die
Hauptversammlung, vielleicht gibts weitere Hintergrundinfo`s
Pressemitteilung
Darmstadt - Die Merck KGaA gab heute die Zulassungsempfehlung für ErbituxTM
(Cetuximab) seitens des Ausschusses für Arzneispezialitäten (CPMP,
Committee for Proprietary Medicinal Products), dem wissenschaftlichen
Beratungsgremium der Europäischen Zulassungsbehörde für Arzneimittel (EMEA,
European Agency for the Evaluation of Medicinal Products), bekannt. Diese
Empfehlung wird an die Europäische Kommission weitergeleitet und ist damit
ein richtungsweisender Schritt auf dem Weg zur Erlangung der europaweiten
Marktzulassung für Erbitux, die für Mitte dieses Jahres erwartet wird.
Erbitux wird in Kombination mit Irinotecan zur Behandlung von Patienten mit
EGFR (epidermaler Wachstumsfaktor-Rezeptor)-exprimierendem
fortgeschrittenem Kolorektalkarzinom empfohlen, wenn eine Chemotherapie mit
Irinotecan bereits versagt hat. Der CPMP bewertet die eingereichten Daten
zur Wirksamkeit und Sicherheit von Erbitux als vollständig und empfiehlt
die uneingeschränkte Zulassung von Erbitux. Demgemäß sind mit der Zulassung
keine speziellen Auflagen verbunden, was für die Aussagekraft der bereits
eingereichten Daten zu Erbitux spricht.
Dieser Vorentscheid des CPMP ist ein wichtiger Schritt, der für die 200.000
Patienten, die jedes Jahr in Westeuropa erstmalig mit der Diagnose
Darmkrebs konfrontiert werden, berechtigte neue Hoffnung bringt. Über die
Hälfte von ihnen befindet sich zum Zeitpunkt der Diagnose bereits im
fortgeschrittenen, metastasierenden Erkrankungsstadium.(1)
Erbitux wurde im Dezember 2003 zuerst in der Schweiz für die
Kombinationsbehandlung mit Irinotecan zugelassen. Im Februar diesen Jahres
wurde Erbitux auch in den USA für die Kombination mit Irinotecan zur
Behandlung von Patienten mit EGFR-exprimierendem, fortgeschrittenem,
Irinotecan-refraktärem Kolorektalkarzinom eingeführt. Erbitux ist dort
ebenfalls für die Monotherapie bei Patienten mit einer
Irinotecan-Unverträglichkeit zugelassen.
Erbitux wurde in Europa auf Basis der Daten eingereicht, die in einer
großen klinischen Studie in 11 europäischen Ländern mit 57 beteiligten
Krankenhäusern und über 300 Patienten mit fortgeschrittenem,
metastasierendem Kolorektalkarzinom erhoben wurden. In der sogenannten BOND
(Bowel Oncology with Cetuximab Antibody)-Studie zeigte Erbitux in
Kombination mit dem Chemotherapeutikum Irinotecan bei mehr als 50 % der
Patienten eine positive Wirkung. Bei 23 % der Patienten bildete sich der
Tumor um mehr als die Hälfte zurück und bei weiteren 33 % dieser schwer
behandelbaren Patienten kam das Tumorwachstum zum Stillstand.(2)
"Solche Ansprechraten sind normalerweise mit einer Verlängerung der
Überlebenszeit verbunden", sagte Prof. David Cunningham, Chefarzt der
Abteilungen Gastrointestinal- und Lymphomerkrankungen des Royal Marsden
Hospital in London und Surrey (GB) und leitender Prüfarzt der BOND-Studie.
"Darmkrebs wird oft erst im fortgeschrittenen Stadium diagnostiziert und
ist mit den konventionellen Therapiemöglichkeiten schwer behandelbar,"
fügte Cunningham hinzu. "Aufgrund seiner sehr zielgerichteten Wirkungsweise
hat Erbitux vor allem in Kombination mit Chemotherapie vielversprechende
Ergebnisse geliefert und stellt deshalb eine wirksame neue
Behandlungsoption für Ärzte im Kampf gegen diesen immer häufiger
auftretenden Krebstyp dar."
Erbitux ist ein monoklonaler Antikörper vom Typ IgG1, der gezielt den
EGF-Rezeptor blockiert, der bei über 80 % metastasierender
Kolorektalkarzinome zu finden ist. Die Tumorarten, die EGFR exprimieren,
zeigen einen aggressiveren Krankheitsverlauf, sind resistenter gegenüber
Chemotherapie, neigen verstärkt zu Metastasen und bieten eine schlechte
Prognose.(3-5)
Die Wirkung von Erbitux beruht auf der Blockierung des EGFR. Dadurch wird
sowohl das Eindringen der Tumorzellen in gesundes Gewebe wie auch die
Ausbreitung, d.h. Metastasierung der Tumore in andere Körperregionen
vermindert. Durch die Blockierung des EGFR hemmt Erbitux auch die Bildung
neuer Blutgefäße im Inneren der Tumore (sog. Angiogenese), da die
Produktion des Angiogenesefaktors VEGF (vaskulärer endothelialer
Wachstumsfaktor) (6) verringert wird.
Erbitux wird sowohl als Monotherapie als auch in Kombination mit Irinotecan
im Allgemeinen gut vertragen. Die unter Erbitux auftretenden
Nebenwirkungen haben in der Regel keinen Einfluss auf die Fortführung der
Behandlung und scheinen auch die von Irinotecan bekannten Nebenwirkungen
(7) nicht zu verstärken.
"Wir hoffen mit der Bereitstellung dieser neuen Behandlungsoption das Leben
der Patienten nachhaltig zu ändern und zu verbessern," sagte Prof. Bernhard
Scheuble, der Vorsitzende der Geschäftsleitung der Merck KGaA. "Um noch
mehr Patienten helfen zu können, die an anderen Krebsarten erkrankt sind,
haben wir bereits ein großangelegtes klinisches Programm gestartet, das die
Verträglichkeit und Wirksamkeit dieses Arzneimittels weiter erforschen
soll."
"Mit Erbitux und vielen weiteren Krebsmitteln, die derzeit erforscht
werden, zeigt Merck sein hohes Engagement für die langfristige Entwicklung
eines beneidenswerten Portfolios an innovativen Produkten mit
vielversprechenden Behandlungsmöglichkeiten für Patienten," ergänzte Prof.
Scheuble.
Merck hat die Vermarktungsrechte für Erbitux außerhalb der USA und Kanada
1998 in Lizenz von ImClone Systems Incorporated in New York erworben. In
Japan halten beide Unternehmen das Co-Exklusivitätsrecht zur Vermarktung
von Erbitux.
Nicht-Schwerpunktprojekt eingestellt
Zugunsten einer stärkeren Fokussierung auf die Kernarbeitsgebiete Onkologie
und Cardiometabolic Care stellt Merck die Entwicklung von EMR 62203, einen
PDE V-Inhibitor zur Behandlung der erektilen Dysfunktion, ein. Der
Wirkstoff befand sich in Phase II der klinischen Entwicklung.
Hinweis an die Redaktionen:
Ausführliches Hintergrundmaterial zu Erbitux ist in Form von Texten, Fotos
und Grafiken im Internet erhältlich unter:
http://www.media-highlights.merck.de
Gruß Agio
Habe das Gefühl das die kommende Woche für alle eine erfolgreiche sein wird,
Kursziel Minimum 2,60$
Die letzten Nachrichten sprechen für sich sich!



Kursziel Minimum 2,60$
Die letzten Nachrichten sprechen für sich sich!



Etwas interessantes aus dem Yahoo-Board.
Die Insidergeschäfte vom März 04
March 27, 2004
Insider Information by Issuer - View Results
Issuer name : biomira ( Starts with )
Issuer Name: Biomira Inc.
Date of Last Reported
Transaction(YYYY-MM-DD) Security
Designation Registered
Holder Closing Balance Insider`s calculated balance Closing balance of equivalent number
or value of underlying securities
Insider Name: Aubrey, Robert Duane
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2003-11-18 Common Shares 22,520
2004-01-20 Options (Options ) 260,000 260,000
Insider Name: Baker, Eric Edward
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 6,668
2003-08-07 Common Shares Eric Baker Family Foundation 60,000
2003-08-07 Common Shares Twelve R Square Inc. 718,515
2004-03-01 Options (Options ) 97,032 97,032
Insider Name: Blair, Sidney Robert
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-15 Common Shares 5,000
2004-03-01 Options (Options ) 55,006 55,006
Insider Name: Ely, Guy
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2004-01-20 Options (Options ) 110,000 110,000
Insider Name: Helmhold, Ronald Jack
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2004-01-20 Options (Options ) 134,500 134,500
Insider Name: Jackson, Richard Lee
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2004-03-01 Options (Options ) 39,079 39,079
Insider Name: McPherson, Thomas Alexander
Insider Relationship: 4 - Director of Issuer, 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 59,250
2004-01-20 Options (Options ) 890,000 890,000
Insider Name: Moriber Katz, Sheila
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 20,000
2004-03-01 Options (Options ) 71,601 71,601
Insider Name: Olson, Marilyn Esther
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2004-01-06 Common Shares 0
2004-01-20 Options (Options ) 106,250 106,250
Insider Name: Stoughton, Warner Vickery
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 19,000
2004-03-01 Options (Options ) 72,882 72,882
Insider Name: Taylor, Edward Arnold
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 38,400
2004-01-20 Options (Options ) 370,000 370,000
Insider Name: Welsh, Michael Charles
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 3,700
2004-03-01 Options (Options ) 66,007 66,007
http://www.sedi.ca
BIOM STRONG BUY !!
Die Insidergeschäfte vom März 04
March 27, 2004
Insider Information by Issuer - View Results
Issuer name : biomira ( Starts with )
Issuer Name: Biomira Inc.
Date of Last Reported
Transaction(YYYY-MM-DD) Security
Designation Registered
Holder Closing Balance Insider`s calculated balance Closing balance of equivalent number
or value of underlying securities
Insider Name: Aubrey, Robert Duane
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2003-11-18 Common Shares 22,520
2004-01-20 Options (Options ) 260,000 260,000
Insider Name: Baker, Eric Edward
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 6,668
2003-08-07 Common Shares Eric Baker Family Foundation 60,000
2003-08-07 Common Shares Twelve R Square Inc. 718,515
2004-03-01 Options (Options ) 97,032 97,032
Insider Name: Blair, Sidney Robert
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-15 Common Shares 5,000
2004-03-01 Options (Options ) 55,006 55,006
Insider Name: Ely, Guy
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2004-01-20 Options (Options ) 110,000 110,000
Insider Name: Helmhold, Ronald Jack
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2004-01-20 Options (Options ) 134,500 134,500
Insider Name: Jackson, Richard Lee
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2004-03-01 Options (Options ) 39,079 39,079
Insider Name: McPherson, Thomas Alexander
Insider Relationship: 4 - Director of Issuer, 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 59,250
2004-01-20 Options (Options ) 890,000 890,000
Insider Name: Moriber Katz, Sheila
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 20,000
2004-03-01 Options (Options ) 71,601 71,601
Insider Name: Olson, Marilyn Esther
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2004-01-06 Common Shares 0
2004-01-20 Options (Options ) 106,250 106,250
Insider Name: Stoughton, Warner Vickery
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 19,000
2004-03-01 Options (Options ) 72,882 72,882
Insider Name: Taylor, Edward Arnold
Insider Relationship: 5 - Senior Officer of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 38,400
2004-01-20 Options (Options ) 370,000 370,000
Insider Name: Welsh, Michael Charles
Insider Relationship: 4 - Director of Issuer
Ceased to be Insider: Not Applicable
2003-08-07 Common Shares 3,700
2004-03-01 Options (Options ) 66,007 66,007
http://www.sedi.ca
BIOM STRONG BUY !!
Upcoming Events
2004
March 31, 2004-
April 7, 2004
Montag und Dienstag wird es hier schon_mal richtig zu Sache gehen!

2004
March 31, 2004-
April 7, 2004
Montag und Dienstag wird es hier schon_mal richtig zu Sache gehen!







....hm...also, - diese letzten 4 Kommentare sind wirklich spitze...
...hab was vergessen: wem es langweilig ist, der kann sich mal GAMNEZNFLIX ansehen...
Gutes Traden!!
Gutes Traden!!
...pardon, ist keine Empfehlung, - mach ich nedd, - nuuuur was gegen die Langeweile...
es läuft wie immer nach einem anstieg.
biom fällt. beobachte das spiel jetzt seit monaten.
biom fällt. beobachte das spiel jetzt seit monaten.
Schau dir die Umsätze an, Biomira fällt bei geringer Umsätzen. Gut möglich, dass das zittrige Hände sind, Zocker u.ä. Wahre Investoren, die auch entsprechende Stückzahlen absaugen bleiben cool. Eine ganz normale Reaktion.
Agio
Agio
Ab morgen gilt`s. Sekt oder Selters.
GO BIOM
GO BIOM
Der "Countdown" hat begonnen!
March 31 - April 7

March 31 - April 7

GO BIOM
die Zeit läuft ,)
............
2004
March 31, 2004-
April 7, 2004
Edmonton, Alberta L-BLP25 Phase IIb Non-Small Cell Lung Cancer Clinical Analysis Results
Biomira and Merck kGaA are expecting clinical trial results at the end of March or very early in April 2004. The data are currently being accumulated for interpretation by the Data Safety Monitoring Board.
Once the Companies have been unblinded to the data this information will be communicated to our stakeholders.
Until the Companies have been given the data, we cannot pinpoint the exact date and time this information will become available but we are providing you our best estimate at this time.
... tick tack tick tack...
Gruß
Vaio
............
2004
March 31, 2004-
April 7, 2004
Edmonton, Alberta L-BLP25 Phase IIb Non-Small Cell Lung Cancer Clinical Analysis Results
Biomira and Merck kGaA are expecting clinical trial results at the end of March or very early in April 2004. The data are currently being accumulated for interpretation by the Data Safety Monitoring Board.
Once the Companies have been unblinded to the data this information will be communicated to our stakeholders.
Until the Companies have been given the data, we cannot pinpoint the exact date and time this information will become available but we are providing you our best estimate at this time.
... tick tack tick tack...
Gruß
Vaio
Hier scheint ja keiner über die Testergebnisse bescheid zu wissen,ist das nun gut oder schlecht?
Ich rechne heute nach Börsenschluss mit einer NEWS!
Und dann am Montag gapt es ,nur in welche Richtung?
,nur in welche Richtung?

Ich rechne heute nach Börsenschluss mit einer NEWS!
Und dann am Montag gapt es
 ,nur in welche Richtung?
,nur in welche Richtung?
bei island.com
schon bei 2,15$
schon bei 2,15$
Biomira says Phase IIb trial not "statistically significant" (BIOM) 1.88: Co and Merck KGaA announce preliminary results from a randomized, open-label Phase IIb trial of BLP25 liposomal vaccine (L BLP25) in patients with Stage IIIb and IV non- small cell lung cancer (NSCLC) indicate that the median survival of those patients on the vaccine arm was 4.4 months longer than those on the control arm. Although not statistically significant, the overall median survival is 17.4 months for patients on the vaccine arm versus 13 months for the patients on the control arm.










@donner
Was hältst Du davon?
Was hältst Du davon?

Hört sich an,das hier eine PhaseIII kommt,
das positive wäre hier das die PhaseIII "klinisch" zwingend ist!
das positive wäre hier das die PhaseIII "klinisch" zwingend ist!
der Kurs schaut schon mal gut aus!
Biomira and Merck KGaA Announce Phase IIb BLP25 Liposomal Vaccine Trial in Non-Small ...
EDMONTON, AB and DARMSTADT, GERMANY, April 2 /PRNewswire-FirstCall/ -- Biomira Inc. (TSX:BRA) and Merck KGaA of Darmstadt, Germany, said today preliminary results from a randomized, open-label Phase IIb trial of BLP25 liposomal vaccine (L BLP25) in patients with Stage IIIb and IV non- small cell lung cancer (NSCLC) indicate that the median survival of those patients on the vaccine arm was 4.4 months longer than those on the control arm. Although not statistically significant, the overall median survival is 17.4 months for patients on the vaccine arm versus 13 months for the patients on the control arm.
Importantly, the observed two-year survival for patients with locoregional Stage IIIb disease is 60 per cent for the vaccine arm (median survival not yet reached) versus 36.7 per cent for the control arm (median survival of 13.3 months). In the overall patient population the two-year survival is 43.2 per cent for the vaccine arm versus 28.9 per cent for the control arm.
"Our overall survival analysis, is, in our opinion, clinically compelling," said Alex McPherson, MD, PhD, President and CEO of Biomira. "We are very encouraged by these results and are developing plans for further clinical testing of L-BLP25 in lung cancer and possibly other indications. Although not finalized, our plans will likely include a multinational Phase III registration trial."
The controlled, open-label Phase IIb trial enrolled 171 men and women with NSCLC whose disease was stable or who had responded to treatment following completion of their first line standard chemotherapy. Patients were randomized to either L-BLP25 plus best standard of care or to best standard of care alone. Best standard of care includes palliative radiotherapy and/or second line chemotherapy according to current standard clinical practice. The study was designed to document the safety profile of the vaccine and to evaluate efficacy by comparing survival in the two arms.
The results appear to indicate a favourable safety profile. Additional analyses and survival follow-up will be conducted to gather information to assist in the future development of the product.
"Lung cancer is a very aggressive disease and the observation of a 4.4 month improvement in median survival for patients treated with L-BLP25 in this well-controlled trial is a clinically important finding for this serious illness," said Nancy Wysenski, president of EMD Pharmaceuticals, Inc., the U.S subsidiary of Merck KGaA. "We appreciate the participation of the patients and investigators in this study that has yielded this important finding."
Dr. Frances Shepherd, Chairman of the Data Safety Monitoring Board (DSMB) for the Phase IIb trial complimented the Companies saying, "This study was conducted in an exemplary fashion and the high quality data resulting from the trial can now be used in planning the next phase of clinical development."
EDMONTON, AB and DARMSTADT, GERMANY, April 2 /PRNewswire-FirstCall/ -- Biomira Inc. (TSX:BRA) and Merck KGaA of Darmstadt, Germany, said today preliminary results from a randomized, open-label Phase IIb trial of BLP25 liposomal vaccine (L BLP25) in patients with Stage IIIb and IV non- small cell lung cancer (NSCLC) indicate that the median survival of those patients on the vaccine arm was 4.4 months longer than those on the control arm. Although not statistically significant, the overall median survival is 17.4 months for patients on the vaccine arm versus 13 months for the patients on the control arm.
Importantly, the observed two-year survival for patients with locoregional Stage IIIb disease is 60 per cent for the vaccine arm (median survival not yet reached) versus 36.7 per cent for the control arm (median survival of 13.3 months). In the overall patient population the two-year survival is 43.2 per cent for the vaccine arm versus 28.9 per cent for the control arm.
"Our overall survival analysis, is, in our opinion, clinically compelling," said Alex McPherson, MD, PhD, President and CEO of Biomira. "We are very encouraged by these results and are developing plans for further clinical testing of L-BLP25 in lung cancer and possibly other indications. Although not finalized, our plans will likely include a multinational Phase III registration trial."
The controlled, open-label Phase IIb trial enrolled 171 men and women with NSCLC whose disease was stable or who had responded to treatment following completion of their first line standard chemotherapy. Patients were randomized to either L-BLP25 plus best standard of care or to best standard of care alone. Best standard of care includes palliative radiotherapy and/or second line chemotherapy according to current standard clinical practice. The study was designed to document the safety profile of the vaccine and to evaluate efficacy by comparing survival in the two arms.
The results appear to indicate a favourable safety profile. Additional analyses and survival follow-up will be conducted to gather information to assist in the future development of the product.
"Lung cancer is a very aggressive disease and the observation of a 4.4 month improvement in median survival for patients treated with L-BLP25 in this well-controlled trial is a clinically important finding for this serious illness," said Nancy Wysenski, president of EMD Pharmaceuticals, Inc., the U.S subsidiary of Merck KGaA. "We appreciate the participation of the patients and investigators in this study that has yielded this important finding."
Dr. Frances Shepherd, Chairman of the Data Safety Monitoring Board (DSMB) for the Phase IIb trial complimented the Companies saying, "This study was conducted in an exemplary fashion and the high quality data resulting from the trial can now be used in planning the next phase of clinical development."
Da bin Ich mal gespannt wie der Markt reagiert!





Mir scheint das eine Menge Nachrichten noch geheim gehalten werden,das ganze Statement ist mir zu oberflächlich,die von BLP25 Sensationellen erreichten 4,4Monate „Lebensdauer“ werden mir hier zu dahin gestellt,wenn man überlegt das es sich hier bei um den stärksten Krebs handelt.
Ich denke das Merck und Biomira schon einen nächsten Schritt weiter sind!
Ich denke das Merck und Biomira schon einen nächsten Schritt weiter sind!
Der Kursverlauf und das Handelsvolumen in den nächsten Wochen wird zeigen was los ist!

Ich glaube, das wird was!
BLP25 zur Unterstützung anderer Therapien ist doch sicher auch in vielfältiger Weise denkbar. (Bin aber kein Mediziner.)
Das taktische Geplänkel mit dem Kurs sollte einen nicht irritieren.
BLP25 zur Unterstützung anderer Therapien ist doch sicher auch in vielfältiger Weise denkbar. (Bin aber kein Mediziner.)
Das taktische Geplänkel mit dem Kurs sollte einen nicht irritieren.
Der richtige Zock beginnt erst jetzt
Es wäre zu einfach gewesen zusagen das der Wert zwischen 31.03-7.04 bei positiven News enorm steigen wird,
Biomira und Merck halten sich bedeckt sie sagen es müsse eigentlich eine PhaseIII geben aber wir haben hier ein mittel Namens BLP25 das die Lebensdauer von 13 auf 17 Monate erhöht!!! Es wurden in der Vergangenheit schon viele Medikamente zugelassen ohne das hier an die Anforderungen festgehalten wurde!Ich denke insgeheim wird schon mit der FDA über eine Zulassung verhandelt ,natürlich wird BLP25 auch zur Zeit weiter ausgebaut!
Nächster Termin/Präsentation wurde schon vorab der Juni 5-8 genannt(siehe #630 )
.
...4.4 months longer than those on the control arm. Although not statistically significant, the overall median survival is 17.4 months for patients on the vaccine arm versus 13 months for the patients on the control arm....
.....Importantly, the observed two-year survival for patients with locoregional Stage IIIb disease is 60 per cent for the vaccine arm (median survival not yet reached) versus 36.7 per cent for the control arm (median survival of 13.3 months). In the overall patient population the two-year survival is 43.2 per cent for the vaccine arm versus 28.9 per cent for the control arm......

Es wäre zu einfach gewesen zusagen das der Wert zwischen 31.03-7.04 bei positiven News enorm steigen wird,
Biomira und Merck halten sich bedeckt sie sagen es müsse eigentlich eine PhaseIII geben aber wir haben hier ein mittel Namens BLP25 das die Lebensdauer von 13 auf 17 Monate erhöht!!! Es wurden in der Vergangenheit schon viele Medikamente zugelassen ohne das hier an die Anforderungen festgehalten wurde!Ich denke insgeheim wird schon mit der FDA über eine Zulassung verhandelt ,natürlich wird BLP25 auch zur Zeit weiter ausgebaut!
Nächster Termin/Präsentation wurde schon vorab der Juni 5-8 genannt(siehe #630 )
.
...4.4 months longer than those on the control arm. Although not statistically significant, the overall median survival is 17.4 months for patients on the vaccine arm versus 13 months for the patients on the control arm....
.....Importantly, the observed two-year survival for patients with locoregional Stage IIIb disease is 60 per cent for the vaccine arm (median survival not yet reached) versus 36.7 per cent for the control arm (median survival of 13.3 months). In the overall patient population the two-year survival is 43.2 per cent for the vaccine arm versus 28.9 per cent for the control arm......
@donner
Wenn Ich mir das Bid in USA anschaue,dann

 !
!
Das war noch nicht alles,da kommt noch was!
Wenn Ich mir das Bid in USA anschaue,dann


 !
!Das war noch nicht alles,da kommt noch was!
@alle
Lest Euch mal das Yahoo-Board zu Biom durch,speziell die
Artikel von topduck,sehr interessant!
Lest Euch mal das Yahoo-Board zu Biom durch,speziell die
Artikel von topduck,sehr interessant!

kannst du das bitte hier reinstellen
hab bei der suche mal wieder versagt
thx versager69
hab bei der suche mal wieder versagt

thx versager69
thx
versager69

versager69
Today on Canada`s Business Report... Biomira Calls Recent Cancer Vaccine Study A Good News Story
Wednesday April 7, 3:17 pm ET
TORONTO, April 7 /CNW/ - On today`s edition of Canada`s Business Report, host Robert Graham speaks with Alex McPherson, President and CEO of Biomira Incorporated. They focus on the results of the latest study involving the BLP25 liposomal vaccine for people with non-small cell lung cancer.
McPherson says, "This particular trial had only 171 patients and the point of the exercise was to determine whether or not there was an indication that we should go further in clinical development. Given the small size of the trial, the results are really quite staggering."
McPherson says Biomira and its German partner in the project, Merck KgaA, are enthusiastic about the drugs` potential. He says, "We are going to look at the possibility of talking to regulatory authorities with respect to this trial, and there is a great likelihood that the regulatory authorities in Canada and the United States, and possibly in Europe, are going to ask us to do a further phase III trial, which will take us several years."
Executive produced by Canada NewsWire, Canada`s Business Report is the most comprehensive daily business news program on radio in Canada. With a focus on the stock markets, investing strategies, corporate developments, and the health of our economy, the nationally syndicated half-hour program is heard Monday through Friday, live at 5:06 p.m. ET at http://www.newswire.ca/en/cbr/index.cgi and on the following stations.
Wednesday April 7, 3:17 pm ET
TORONTO, April 7 /CNW/ - On today`s edition of Canada`s Business Report, host Robert Graham speaks with Alex McPherson, President and CEO of Biomira Incorporated. They focus on the results of the latest study involving the BLP25 liposomal vaccine for people with non-small cell lung cancer.
McPherson says, "This particular trial had only 171 patients and the point of the exercise was to determine whether or not there was an indication that we should go further in clinical development. Given the small size of the trial, the results are really quite staggering."
McPherson says Biomira and its German partner in the project, Merck KgaA, are enthusiastic about the drugs` potential. He says, "We are going to look at the possibility of talking to regulatory authorities with respect to this trial, and there is a great likelihood that the regulatory authorities in Canada and the United States, and possibly in Europe, are going to ask us to do a further phase III trial, which will take us several years."
Executive produced by Canada NewsWire, Canada`s Business Report is the most comprehensive daily business news program on radio in Canada. With a focus on the stock markets, investing strategies, corporate developments, and the health of our economy, the nationally syndicated half-hour program is heard Monday through Friday, live at 5:06 p.m. ET at http://www.newswire.ca/en/cbr/index.cgi and on the following stations.
Ich tippe auf Phase 3,am besten mit Abhängigkeitszulassung oder Fast-Track Status!



Einfach still einsammeln





Upcoming Events
2004
May 13, 2004
9:45 AM - 10:00 AM EDT
London, England Rodman & Renshaw Techvest Global Healthcare Conference
Dr. McPherson will make an investor presentation at this three day conference (May 12-14 2004) in London, England. The conference is being held at Claridge`s Hotel, London.
May 20, 2004
1:30 AM - 3:30 AM EDT
Toronto Ontario Annual General Meeting
Biomira`s Annual General Meeting will be held on Thursday, May 20th, 2004. The meeting will be held at the Hilton Toronto Hotel, 145 Richmond Street West (The Governor General Room).
Registration will be at 1:00 p.m. Eastern time, with the meeting starting promptly at 1:30 p.m.
http://www.biomira.com
2004
May 13, 2004
9:45 AM - 10:00 AM EDT
London, England Rodman & Renshaw Techvest Global Healthcare Conference
Dr. McPherson will make an investor presentation at this three day conference (May 12-14 2004) in London, England. The conference is being held at Claridge`s Hotel, London.
May 20, 2004
1:30 AM - 3:30 AM EDT
Toronto Ontario Annual General Meeting
Biomira`s Annual General Meeting will be held on Thursday, May 20th, 2004. The meeting will be held at the Hilton Toronto Hotel, 145 Richmond Street West (The Governor General Room).
Registration will be at 1:00 p.m. Eastern time, with the meeting starting promptly at 1:30 p.m.
http://www.biomira.com
Upcoming Events
2004
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 - Developmental Therapeutics: Immunotherapy Dr. N. Ibrahim
General Poster Session # 883 - The magnitude of the humoral immune response to naturally occurring STn predicts favorable survival in patients treated with STn-KLH vaccine in a prospective controlled randomized double-blinded multicenter clinical study in stage IV breast cancer patients.
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 Dr. S. North
# TBA - North - Phase II study of liposomal MUC1 vaccine in PSA failures post-radical prostatectomy (RP)
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 Dr. C. Butts
# TBA - C. Butts - A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC).
http://www.biomira.com
Die Termine nehmen zu. Hoffentlich geht`s jetzt los.
STRONG BUY
2004
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 - Developmental Therapeutics: Immunotherapy Dr. N. Ibrahim
General Poster Session # 883 - The magnitude of the humoral immune response to naturally occurring STn predicts favorable survival in patients treated with STn-KLH vaccine in a prospective controlled randomized double-blinded multicenter clinical study in stage IV breast cancer patients.
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 Dr. S. North
# TBA - North - Phase II study of liposomal MUC1 vaccine in PSA failures post-radical prostatectomy (RP)
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 Dr. C. Butts
# TBA - C. Butts - A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC).
http://www.biomira.com
Die Termine nehmen zu. Hoffentlich geht`s jetzt los.
STRONG BUY

Biomira`s President and CEO to present at Rodman & Renshaw Techvest Global Healthcare Conference
Monday April 19, 8:33 am ET
EDMONTON, April 19 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq: BIOM - News; TSX: BRA - News) announced today that Alex McPherson, MD, PhD, President and CEO of Biomira, will present highlights of the Company`s product and corporate advancements at the upcoming Rodman & Renshaw Techvest Global Healthcare Conference. The conference will be held in London, England May 12-14, 2004. Dr. McPherson`s presentation is scheduled for 9:45 a.m., London time, on May 13, 2004. A live Web cast will be presented at www.wallstreetwebcasting.com/webcast/rrshq2/biom and will be available in an archived version following the presentation through a link at http://www.biomira.com/investors/presentations/.
Dr. McPherson`s presentation is expected to provide an overview from the recently announced results of the Phase IIb BLP25 Liposomal vaccine (L-BLP25) study in non-small cell lung cancer (NSCLC). Preliminary results showed evidence of a 4.4 month overall improvement in survival. For the men and women on the vaccine arm, the overall median survival was 17.4 months versus 13 months for those individuals on the control arm. There were 171 patients enrolled on the trial at 13 sites in Canada and four sites in the United Kingdom, with those patients on the vaccine arm receiving best standard of care plus L-BLP25 and patients on the control arm receiving best standard of care alone.
Both Biomira and its collaborator, Merck KGaA of Darmstadt, Germany, were impressed with the preliminary two-year survival data. The preliminary results in the Phase IIb study show a 7.1 per cent difference after one year in the two arms, increasing to a difference of 14.3 per cent after two years.
"Although we would have been pleased to see a statistically significant difference in the two arms, it was recognized at the outset of the trial that this would be difficult to reach in a Phase IIb trial with only 171 patients," said Alex McPherson, MD, PhD, President and CEO of Biomira. "Notwithstanding the foregoing, this trial came close to showing a statistically significant difference between the two groups. Of even greater importance is that the trial results clearly show the Companies a path forward in a subsequent registration trial, if regulatory authorities require such a trial. The Companies expect to be discussing results with regulatory agencies in due course."
There were two stratified groups in the analysis of the patient population for this study. These were patients with Stage IIIb locoregional disease and patients with Stage IIIb pleural effusion and Stage IV cancer. When the Companies looked at the preliminary results of the 65 of 171 patients with Stage IIIb locoregional disease only, they found that the patients on the vaccine arm have not yet reached their median survival, while the patients on the control arm have a median survival of 13.3 months. Although the Companies will need to wait for the median survival of the vaccine arm to get a definitive answer on two-year survival for this group of patients, early indications are extremely positive with the vaccine arm having 60 per cent of patients reaching that milestone compared to 36.7 per cent on the control arm. For cancer patients battling this disease, this difference, nearing 25 per cent, is very meaningful.
The presentation will also highlight the status of the Theratope® vaccine program. Biomira is expected to announce future plans for the vaccine in metastatic breast cancer in the second half of 2004.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
This release may contain forward-looking statements. Various factors could
cause actual results to differ materially from those projected in forward-
looking statements, including those predicting the timing of clinical trial
results, speculation as to future results based upon preliminary indications
availability, or adequacy of financing, the sales and marketing of commercial
products or the safety and efficacy of products. Although the Company believes
that the forward-looking statements contained herein are reasonable, it can
give no assurance that the Company`s expectations are correct. All forward-
looking statements are expressly qualified in their entirety by this
cautionary statement.
Monday April 19, 8:33 am ET
EDMONTON, April 19 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq: BIOM - News; TSX: BRA - News) announced today that Alex McPherson, MD, PhD, President and CEO of Biomira, will present highlights of the Company`s product and corporate advancements at the upcoming Rodman & Renshaw Techvest Global Healthcare Conference. The conference will be held in London, England May 12-14, 2004. Dr. McPherson`s presentation is scheduled for 9:45 a.m., London time, on May 13, 2004. A live Web cast will be presented at www.wallstreetwebcasting.com/webcast/rrshq2/biom and will be available in an archived version following the presentation through a link at http://www.biomira.com/investors/presentations/.
Dr. McPherson`s presentation is expected to provide an overview from the recently announced results of the Phase IIb BLP25 Liposomal vaccine (L-BLP25) study in non-small cell lung cancer (NSCLC). Preliminary results showed evidence of a 4.4 month overall improvement in survival. For the men and women on the vaccine arm, the overall median survival was 17.4 months versus 13 months for those individuals on the control arm. There were 171 patients enrolled on the trial at 13 sites in Canada and four sites in the United Kingdom, with those patients on the vaccine arm receiving best standard of care plus L-BLP25 and patients on the control arm receiving best standard of care alone.
Both Biomira and its collaborator, Merck KGaA of Darmstadt, Germany, were impressed with the preliminary two-year survival data. The preliminary results in the Phase IIb study show a 7.1 per cent difference after one year in the two arms, increasing to a difference of 14.3 per cent after two years.
"Although we would have been pleased to see a statistically significant difference in the two arms, it was recognized at the outset of the trial that this would be difficult to reach in a Phase IIb trial with only 171 patients," said Alex McPherson, MD, PhD, President and CEO of Biomira. "Notwithstanding the foregoing, this trial came close to showing a statistically significant difference between the two groups. Of even greater importance is that the trial results clearly show the Companies a path forward in a subsequent registration trial, if regulatory authorities require such a trial. The Companies expect to be discussing results with regulatory agencies in due course."
There were two stratified groups in the analysis of the patient population for this study. These were patients with Stage IIIb locoregional disease and patients with Stage IIIb pleural effusion and Stage IV cancer. When the Companies looked at the preliminary results of the 65 of 171 patients with Stage IIIb locoregional disease only, they found that the patients on the vaccine arm have not yet reached their median survival, while the patients on the control arm have a median survival of 13.3 months. Although the Companies will need to wait for the median survival of the vaccine arm to get a definitive answer on two-year survival for this group of patients, early indications are extremely positive with the vaccine arm having 60 per cent of patients reaching that milestone compared to 36.7 per cent on the control arm. For cancer patients battling this disease, this difference, nearing 25 per cent, is very meaningful.
The presentation will also highlight the status of the Theratope® vaccine program. Biomira is expected to announce future plans for the vaccine in metastatic breast cancer in the second half of 2004.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
This release may contain forward-looking statements. Various factors could
cause actual results to differ materially from those projected in forward-
looking statements, including those predicting the timing of clinical trial
results, speculation as to future results based upon preliminary indications
availability, or adequacy of financing, the sales and marketing of commercial
products or the safety and efficacy of products. Although the Company believes
that the forward-looking statements contained herein are reasonable, it can
give no assurance that the Company`s expectations are correct. All forward-
looking statements are expressly qualified in their entirety by this
cautionary statement.
Die letzte Veranstaltung mit Hunderten von Zuhörern scheint aber doch nicht die große Nummer gewesen zu sein.
Begeisterung war bei Kurs und Umsätzen jedenfalls nicht zu erkennen genausowenig wie Dumping-Versuche.
Braucht doch wohl schon einige Anstrengung, zum jetzigen Preis weitere Investoren zu finden.
Begeisterung war bei Kurs und Umsätzen jedenfalls nicht zu erkennen genausowenig wie Dumping-Versuche.
Braucht doch wohl schon einige Anstrengung, zum jetzigen Preis weitere Investoren zu finden.
Upcoming Events
2004
April 29, 2004
Edmonton, Alberta Q1 Financial Press Release
Biomira`s Q1 Financial Press Release will be distributed after the completion of Biomira`s Board Meeting on 29 April 2004. The exact time of the release cannot be determined in advance.
http://www.biomira.com
2004
April 29, 2004
Edmonton, Alberta Q1 Financial Press Release
Biomira`s Q1 Financial Press Release will be distributed after the completion of Biomira`s Board Meeting on 29 April 2004. The exact time of the release cannot be determined in advance.
http://www.biomira.com
Nur Merck wieder mal im Plus. 
Schönes WE

Schönes WE
wenigstens etwas 
Gruß Agio

Gruß Agio
griass eich....
nun vom chart her...werden wir jetzt an die 200-er linie gehen, vielleicht sogar ein bisschen drunter...bei ca. 1,60 ist dann aber schluss und es sollte wieder nach oben gehen.
auf jeden fall werd ich dort in der gegend meine orders platzieren.
haben momentan eine sks-formation, darum auch der andauernde abstieg...und einen noch immer intakten abwärtstrend...aber ich bin da guter dinge, dass sich ende dieser woche und die nächste woche ziemlicher widerstand aufbauen wird und die aktie nach norden driftet.
wenn dann noch eine nachricht kommt, dann geht`s wieder mit rasantem tempo aufwärts.
nun denn,....
pfiat eich
oestareicha
nun vom chart her...werden wir jetzt an die 200-er linie gehen, vielleicht sogar ein bisschen drunter...bei ca. 1,60 ist dann aber schluss und es sollte wieder nach oben gehen.
auf jeden fall werd ich dort in der gegend meine orders platzieren.
haben momentan eine sks-formation, darum auch der andauernde abstieg...und einen noch immer intakten abwärtstrend...aber ich bin da guter dinge, dass sich ende dieser woche und die nächste woche ziemlicher widerstand aufbauen wird und die aktie nach norden driftet.
wenn dann noch eine nachricht kommt, dann geht`s wieder mit rasantem tempo aufwärts.
nun denn,....
pfiat eich
oestareicha

Schaut mal auf OSI Pharma (osip).
Wenn ich das so überblicke, dann melden die etwas ähnliches wie Biomira gemeldet hat.
Nur das der Kurs heute um 100% hoch geht.
Meiner Meinung nach hat Biomira eine ganz schlechte PR,
wir könnten schon viel höher stehen.
Trotzdem STRONG BYE
Wenn ich das so überblicke, dann melden die etwas ähnliches wie Biomira gemeldet hat.
Nur das der Kurs heute um 100% hoch geht.
Meiner Meinung nach hat Biomira eine ganz schlechte PR,
wir könnten schon viel höher stehen.
Trotzdem STRONG BYE

@freetibet
Gebe dir recht das Biomira eine schlechte PR hat bzw. macht!
Ich frage mich die ganze Zeit immer wieder warum, immerhin nimmt öfters mit Merck ein Weltkonzern teil!
Mal schauen es könnte sein das wir am 29April mehr zu hören bekommen,( eventuelle Zulassungsgespräche mit der FDA)
gruss
Gebe dir recht das Biomira eine schlechte PR hat bzw. macht!
Ich frage mich die ganze Zeit immer wieder warum, immerhin nimmt öfters mit Merck ein Weltkonzern teil!
Mal schauen es könnte sein das wir am 29April mehr zu hören bekommen,( eventuelle Zulassungsgespräche mit der FDA)
gruss
#682
STRONG BUY oder STRONG BYE


STRONG BUY oder STRONG BYE



 In NY ist der Kurs bei 2 USD bei Umsätzen von über 6 Mio. Stück Aktien.
In NY ist der Kurs bei 2 USD bei Umsätzen von über 6 Mio. Stück Aktien.
Gruß Agio
sollte mein user doch noch der user in 2004 werden ? 
ich hoffe JA
gruß
biom

ich hoffe JA
gruß
biom
das ohne news und das bei biom
da kommt was ganz fettes
insider wissen was
der shortsquezze trägt uns bis zur 5 dollar marke
osip

biom

kann mal ein profi die firmen fundamental vergleichen ?
danke
biom
biom
kann mal ein profi die firmen fundamental vergleichen ?
danke
biom
das ganze hatten wir doch schon vor 3 Wochen.....
2 Schritte vor und 3 zurück...einfach das Teil weglegen
und in 2 Jahren schauen ob es noch auf dem Kurszettel steht...bin bei 1,52€ vor längerer Zeit rein und entweder
rockt das Ding irgendwann oder wird eine 2te Exodus......
2 Schritte vor und 3 zurück...einfach das Teil weglegen
und in 2 Jahren schauen ob es noch auf dem Kurszettel steht...bin bei 1,52€ vor längerer Zeit rein und entweder
rockt das Ding irgendwann oder wird eine 2te Exodus......
#684
Natürlich STRONG BUY
STRONG BYE mach ich erst wenn der Kurs dort steht wo OSI heute geschlossen hat
Ich sollte mich doch ab und zu auf meine Arbeit konzentrieren und nicht hier rumschreiben.

Natürlich STRONG BUY
STRONG BYE mach ich erst wenn der Kurs dort steht wo OSI heute geschlossen hat

Ich sollte mich doch ab und zu auf meine Arbeit konzentrieren und nicht hier rumschreiben.



und heute rock n roll ?
Mal gespannt ob heute die News kommen oder ob der Kurs noch weiter von Insidern getrieben wird!?
was mir gestern bei island aufgefallen ist:
es wurden immer wieder richtige Blöcke mit 30k ins ask
gestellt. Kaum waren diese abgegrast zog der Kurs wieder
an. Die MM`s machen hier wohl einen guten Schnitt beim
abfischen.........
Vor 2 Wochen waren es mal 130000 zu 1,86!!
Wer gibt denn da so ne fette Order ab?
Wichtig sollte wohl sein, daß weiterhin die Umsätze konstant über 1,5 Mio liegen - wir werden ja sehen wohin
die Reise geht.
Mit OSIP würde ich aber keinen Vergleich wagen
es wurden immer wieder richtige Blöcke mit 30k ins ask
gestellt. Kaum waren diese abgegrast zog der Kurs wieder
an. Die MM`s machen hier wohl einen guten Schnitt beim
abfischen.........
Vor 2 Wochen waren es mal 130000 zu 1,86!!
Wer gibt denn da so ne fette Order ab?
Wichtig sollte wohl sein, daß weiterhin die Umsätze konstant über 1,5 Mio liegen - wir werden ja sehen wohin
die Reise geht.
Mit OSIP würde ich aber keinen Vergleich wagen

doch wir sollten mal vergleichen
a- jahresumsatz mit prognose
b- marktkapitalisierung
c- kursziel bei fda zulassung
ich denke pi mal daum ( bei dem anlagenotstand im amiland )
)
biom auf 10 usd oder 25 usd
na klar...bei den entsprechenden news und der dazugehörigen PR in anlagezeitungen.
( germany kann man vergessen )
die kurse werden nur drüben gemacht
mfg
biom
a- jahresumsatz mit prognose
b- marktkapitalisierung
c- kursziel bei fda zulassung
ich denke pi mal daum ( bei dem anlagenotstand im amiland
 )
)biom auf 10 usd oder 25 usd
na klar...bei den entsprechenden news und der dazugehörigen PR in anlagezeitungen.
( germany kann man vergessen )
die kurse werden nur drüben gemacht
mfg
biom
Also ich kann mich auch irren. Aber so eine tolle Meldung war das von OISP gestern ja auch nicht. Konkrete Ergebnisse habe ich noch keine gelesen, sollen wohl erst in Juni kommen. Und wenn das schon Phase III war, dann war doch die Biomira Meldung in Ph.II zahlenmäßig konkreter.
Aber wie gesagt, die PR ist hier das entscheidende.
Ich denke, OSIP geht heute wieder runter.
Aber wie gesagt, die PR ist hier das entscheidende.
Ich denke, OSIP geht heute wieder runter.
es wird jeden Tag eine andere Sau durch`s Dorf getrieben -
heut ist es Xenova
+ 36% auf 2,60$
heut ist es Xenova

+ 36% auf 2,60$
das war gestern wohl nur ein OSI P Mitläufer Effekt ... 

Dann werden wir mal sehn...
29-Apr-04 Earnings announcement
29-Apr-04 Earnings announcement
#700
Wenigstens das Handelsvolumen war heute nicht schlecht.
Wenn die Amis nur durch shorten Geld verdienen wollen, kann man auch nichts anderes erwarten.
Schließlich hat der Doc die Aktionäre ja dazu aufgefordert.
Wenn die Amis nur durch shorten Geld verdienen wollen, kann man auch nichts anderes erwarten.
Schließlich hat der Doc die Aktionäre ja dazu aufgefordert.

What’s Ahead in 2004?
Our focus for 2004 will be to develop a strategic plan for moving L-BLP25 into the clinic as quickly as possible in a patient population that will most likely benefit from this novel vaccine approach. We want to plan a pivotal trial that clearly shows that this vaccine works in this patient population and also look at other indications where the vaccine could potentially provide clinical benefit.
Our focus for 2004 will be to develop a strategic plan for moving L-BLP25 into the clinic as quickly as possible in a patient population that will most likely benefit from this novel vaccine approach. We want to plan a pivotal trial that clearly shows that this vaccine works in this patient population and also look at other indications where the vaccine could potentially provide clinical benefit.
Universal Detection Technology to Attend Rodman & Renshaw Techvest Global Healthcare Conference
WEDNESDAY, APRIL 28, 2004 4:15 PM
- BusinessWire
BIOM
1.82 -0.04
Enter Symbol:
Enter Keyword:
LOS ANGELES, Apr 28, 2004 (BUSINESS WIRE) -- Universal Detection Technology (UDTT) (Frankfurt:UDTT.F) today announced that it will attend the Rodman & Renshaw Techvest Global Healthcare Conference in London during May 12-14, 2004.
The Rodman & Renshaw Techvest Global Healthcare Conference will be held at the Claridge`s Hotel and will feature topics ranging from infectious diseases and therapeutic vaccines to specialty pharmaceuticals and medical devices. The event will bring together companies, institutional and venture capitalists, and senior corporate executives as well as experts from the scientific and medical communities.
UDTT is sending the principals of the company: CEO and President Jacques Tizabi, Amir Ettehadieh, Director of Research and Development, Dr. Leonard Makowka, Chief Scientific Advisor and Dr. Adrian Ponce, Senior Staff Technical Member at NASA`s Jet Propulsion Laboratory. Amongst other topics, the Company and Dr. Ponce will be discussing the progress on the development of the Bacterial Spore Detection Device as well as its recently announced collaboration agreement and grant from Rutgers University. "We`re looking forward to presenting to the European community," said Jacques Tizabi, the Company`s President and CEO.
UDTT will be among 175 other exhibitors, including both private and publicly held companies such as ADVENTRX Pharmaceuticals, Inc. (AVRX) , Biomira Inc. (BIOM) , Cell Genesys, Inc. (CEGE) , Genelabs Technologies, Inc. (GNLB) , MediGene (Frankfurt:MDG), and ZymoGenetics Inc. (ZGEN) , to name a few. The UDTT presentation will take place in The Drawing Room at 9:40 a.m. on Friday, May 14, 2004.
The Conference`s unique format will include select panel discussions hosted by Rodman & Renshaw equity analysts and key industry leaders that will add expert perspective to a small, theme-based group of company presentations. In addition, there will be keynote lunch speakers and opportunities for breakout sessions, Q&As and one-on-one meetings with companies. For further information about the conference, visit the Rodman & Renshaw Web site at: http://www.rodmanandrenshaw.com.
About Rodman & Renshaw
Rodman & Renshaw, LLC (www.rodmanandrenshaw.com) is a privately owned, full-service investment banking and brokerage firm headquartered in New York City, focusing exclusively on emerging growth companies. Rodman & Renshaw provides a full range of services including: equity research, institutional sales & trading, and corporate finance. Currently, the firm has a team of seven Ph.D. level biotech analysts, covering the life sciences sector. Rodman & Renshaw is a member of the National Association of Securities Dealers, CRD number 16415.
About Universal Detection Technology
Universal Detection Technology (www.udetection.com), which recently had its ticker symbol changed from UDET to UDTT to accommodate a recent name change, was founded in 1973 and is a developer of monitoring technologies, including bio-terrorism detection devices. UDTT`s technology, together with third party technologies and devices, position the Company to capitalize on growth and value opportunities. Universal Detection Technology recently entered into an agreement with NASA`s Jet Propulsion Laboratory (JPL) to mutually develop a commercially available anthrax "smoke" detector, which will combine the JPL spore detection technology with UDTT`s aerosol capture device. The partnership with UDTT was accomplished through the Technology Affiliates Program, one of many Commercial Technology Programs aimed at transferring JPL`s knowledge to the private sector for broad public use.
Except for historical information contained herein, the statements in this news release are forward-looking statements that are made pursuant to the safe harbor provisions of the Private Securities Litigation Reform Act of 1995. Forward-looking statements involve known and unknown risks and uncertainties, which may cause a company`s actual results, performance and achievement in the future to differ materially from forecasted results, performance, and achievement. These risks and uncertainties include, among other things, the funding of amounts of capital adequate to provide for the working capital needs of the Company, our ability to timely and cost effectively complete the development of our products targeted to the bio-chemical and medical markets, commercial acceptance of our products, product price volatility, product demand, market competition and general economic conditions, and other factors described in the Company`s filings with the Securities and Exchange Commission. We undertake no obligation and do not intend to revise or update publicly any forward looking statements for any reason.
SOURCE: Universal Detection Technology
Investor Relations Services, Inc., New Smyrna Beach, Fla.
Dan Kinnison, 386/409-0200
or
Universal Detection Technology, Los Angeles
Jacques Tizabi, CEO, 310/248-3655
jtizabi@udetection.com
Customize your Business Wire news & multimedia to match your needs.
Get breaking news from companies and organizations worldwide.
Logon for FREE today at www.BusinessWire.com.
WEDNESDAY, APRIL 28, 2004 4:15 PM
- BusinessWire
BIOM
1.82 -0.04
Enter Symbol:
Enter Keyword:
LOS ANGELES, Apr 28, 2004 (BUSINESS WIRE) -- Universal Detection Technology (UDTT) (Frankfurt:UDTT.F) today announced that it will attend the Rodman & Renshaw Techvest Global Healthcare Conference in London during May 12-14, 2004.
The Rodman & Renshaw Techvest Global Healthcare Conference will be held at the Claridge`s Hotel and will feature topics ranging from infectious diseases and therapeutic vaccines to specialty pharmaceuticals and medical devices. The event will bring together companies, institutional and venture capitalists, and senior corporate executives as well as experts from the scientific and medical communities.
UDTT is sending the principals of the company: CEO and President Jacques Tizabi, Amir Ettehadieh, Director of Research and Development, Dr. Leonard Makowka, Chief Scientific Advisor and Dr. Adrian Ponce, Senior Staff Technical Member at NASA`s Jet Propulsion Laboratory. Amongst other topics, the Company and Dr. Ponce will be discussing the progress on the development of the Bacterial Spore Detection Device as well as its recently announced collaboration agreement and grant from Rutgers University. "We`re looking forward to presenting to the European community," said Jacques Tizabi, the Company`s President and CEO.
UDTT will be among 175 other exhibitors, including both private and publicly held companies such as ADVENTRX Pharmaceuticals, Inc. (AVRX) , Biomira Inc. (BIOM) , Cell Genesys, Inc. (CEGE) , Genelabs Technologies, Inc. (GNLB) , MediGene (Frankfurt:MDG), and ZymoGenetics Inc. (ZGEN) , to name a few. The UDTT presentation will take place in The Drawing Room at 9:40 a.m. on Friday, May 14, 2004.
The Conference`s unique format will include select panel discussions hosted by Rodman & Renshaw equity analysts and key industry leaders that will add expert perspective to a small, theme-based group of company presentations. In addition, there will be keynote lunch speakers and opportunities for breakout sessions, Q&As and one-on-one meetings with companies. For further information about the conference, visit the Rodman & Renshaw Web site at: http://www.rodmanandrenshaw.com.
About Rodman & Renshaw
Rodman & Renshaw, LLC (www.rodmanandrenshaw.com) is a privately owned, full-service investment banking and brokerage firm headquartered in New York City, focusing exclusively on emerging growth companies. Rodman & Renshaw provides a full range of services including: equity research, institutional sales & trading, and corporate finance. Currently, the firm has a team of seven Ph.D. level biotech analysts, covering the life sciences sector. Rodman & Renshaw is a member of the National Association of Securities Dealers, CRD number 16415.
About Universal Detection Technology
Universal Detection Technology (www.udetection.com), which recently had its ticker symbol changed from UDET to UDTT to accommodate a recent name change, was founded in 1973 and is a developer of monitoring technologies, including bio-terrorism detection devices. UDTT`s technology, together with third party technologies and devices, position the Company to capitalize on growth and value opportunities. Universal Detection Technology recently entered into an agreement with NASA`s Jet Propulsion Laboratory (JPL) to mutually develop a commercially available anthrax "smoke" detector, which will combine the JPL spore detection technology with UDTT`s aerosol capture device. The partnership with UDTT was accomplished through the Technology Affiliates Program, one of many Commercial Technology Programs aimed at transferring JPL`s knowledge to the private sector for broad public use.
Except for historical information contained herein, the statements in this news release are forward-looking statements that are made pursuant to the safe harbor provisions of the Private Securities Litigation Reform Act of 1995. Forward-looking statements involve known and unknown risks and uncertainties, which may cause a company`s actual results, performance and achievement in the future to differ materially from forecasted results, performance, and achievement. These risks and uncertainties include, among other things, the funding of amounts of capital adequate to provide for the working capital needs of the Company, our ability to timely and cost effectively complete the development of our products targeted to the bio-chemical and medical markets, commercial acceptance of our products, product price volatility, product demand, market competition and general economic conditions, and other factors described in the Company`s filings with the Securities and Exchange Commission. We undertake no obligation and do not intend to revise or update publicly any forward looking statements for any reason.
SOURCE: Universal Detection Technology
Investor Relations Services, Inc., New Smyrna Beach, Fla.
Dan Kinnison, 386/409-0200
or
Universal Detection Technology, Los Angeles
Jacques Tizabi, CEO, 310/248-3655
jtizabi@udetection.com
Customize your Business Wire news & multimedia to match your needs.
Get breaking news from companies and organizations worldwide.
Logon for FREE today at www.BusinessWire.com.
Die Zahlennn sind da,
leider gab Biomira wieder keine Nachrichten frei,aktuelle Nachrichten sind schon längst veröffentlich worden!!!
Hier werden mit ABSICHT Informationen zurück gehalten!!!
Investoren dürfffffen nun weiter schön BILLIG einkaufen!
"Although we would have been pleased to have seen a statistically significant difference in the two groups, we recognized at the outset of the trial that this would be difficult to reach in a Phase IIb trial with only 171 patients," said Alex McPherson, MD, PhD, President and CEO. "We came close to showing a statistically significant difference between the two groups. Of even greater importance is that the trial results clearly show us a path forward in a subsequent registration trial, if regulatory authorities require such a trial. We expect to be discussing our results with regulatory authorities in due course."
Werde jetzt kräftig nachkaufen


leider gab Biomira wieder keine Nachrichten frei,aktuelle Nachrichten sind schon längst veröffentlich worden!!!
Hier werden mit ABSICHT Informationen zurück gehalten!!!
Investoren dürfffffen nun weiter schön BILLIG einkaufen!

"Although we would have been pleased to have seen a statistically significant difference in the two groups, we recognized at the outset of the trial that this would be difficult to reach in a Phase IIb trial with only 171 patients," said Alex McPherson, MD, PhD, President and CEO. "We came close to showing a statistically significant difference between the two groups. Of even greater importance is that the trial results clearly show us a path forward in a subsequent registration trial, if regulatory authorities require such a trial. We expect to be discussing our results with regulatory authorities in due course."
Werde jetzt kräftig nachkaufen



Biomira Inc. Announces 1st Quarter Results
THURSDAY, APRIL 29, 2004 1:40 PM
- PR Newswire
BIOM
1.719 -0.101
Enter Symbol:
Enter Keyword:
EDMONTON, Apr 29, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (BIOM) (CA:BRA) today reported financial results for the three months ended March 31, 2004.
Financial results for the three months ended March 31, 2004 reflect a consolidated net loss from operations of $4.9 million or $0.07 per share compared to $4.4 million or $0.09 per share for the same period in 2003. The increased loss of $0.5 million in 2004 arises from stock compensation expense of $0.3 million, higher general and administrative expenses of $0.3 million, lower revenues of $0.2 million and lower investment and other income of $0.2 million, offset by $0.4 million reduction in gross research and development expenditures and $0.1 million reduction in marketing and business development expenses. The majority of the higher loss results from the adoption of a new accounting standard effective January 1, 2004 that requires expensing of employee stock options.
Contract research and development revenue for the three months ended March 31, 2004, totalling $0.5 million compared to $0.9 million for the same period in 2003, represents contract research and development funding received from Merck KGaA of Darmstadt, Germany associated with Theratope(R) vaccine and BLP25 Liposomal vaccine (L-BLP25). The decreased funding reflects a lower level of clinical activity with the wind down of the Theratope Phase III trial, and unblinding of the L-BLP25 Phase IIb trial results. Licensing revenues from collaborative arrangements represent the amortization of upfront payments received from Merck KGaA upon commencement of the collaboration. In addition, the collaboration with CancerVac Pty. Ltd. of Melbourne, Australia, announced in March 2004, entailed an upfront sub-licensing fee of $0.26 million (U.S. $0.2 million), which is being amortized over the term of the collaboration, or approximately 15 years. This fee, for which Biomira acquired a 10 per cent equity stake in CancerVac in lieu of a cash payment, represents partial consideration for sub-licensing rights to Biomira`s MUC1 technology. Finally, the increase of $0.2 million in licensing, royalties and other revenue relates to chemistry manufacturing contracts.
Research and development expenditures for the three months ended March 31, 2004 totalled $3.7 million compared to $4.1 million for the same period in 2003. The decrease in research and development expenditures, which determines the amount of collaborative funding revenue, is similarly attributable to winding down of clinical activities. General and administrative expenses for the three months ended March 31, 2004 totalled $1.7 million compared to $1.4 million for the same period in 2003. The increase of $0.3 million stems largely from incremental costs related to the settlement of an outstanding litigation in the first quarter. Marketing and business development expenditures for the three months ended March 31, 2004 decreased to $0.3 million compared to $0.4 million for the same period in 2003, and reflect the deferral of expenditures related to Theratope pre-launch activities. Marketing and business development expenditures include corporate administrative expenses associated with these functions, as well as costs for developing Biomira`s internal marketing capabilities and pre-launch marketing activities related to Theratope jointly undertaken and funded with Merck KGaA.
Stock compensation expense of $0.3 million for the three months ended March 31, 2004 represents the amortization of the estimated fair value of options granted since January 1, 2002 applicable to the current period. The retroactive application of CICA Handbook Section 3870 with respect to recognition of stock compensation expense for 2002 and 2003 resulted in a $1.6 million charge to opening deficit. Under the transitional provisions of Section 3870, restatement of comparative figures for prior periods presented in the financial statements is optional.
Investment and other income for the three months ended March 31, 2004, totaling $0.4 million compared to $0.6 million for the same period in 2003, comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. The decrease is mainly due to lower average cash and investment balances, as net foreign exchange gains of $0.2 million for the three months ended March 31, 2004 were similar for the same period in 2003.
Biomira`s financial reserves total $35.1 million in cash and short-term investments as at March 31, 2004, a decrease of $6.4 million from the year end position due to funding of operations during the quarter.
Corporate Update
L-BLP25 Phase IIb Study in Non-Small Cell Lung Cancer (NSCLC)
The first quarter of 2004 brought positive news with the announced preliminary results from the BLP25 Liposomal vaccine (L-BLP25) Phase IIb controlled, open-label clinical trial in NSCLC. The preliminary results showed evidence of a 4.4 month overall improvement in survival for those men and women on the vaccine arm as compared to those on the control arm. The overall median survival was 17.4 months for patients on the vaccine arm versus 13 months for those individuals on the control arm of the trial. Patients on the vaccine arm received best standard of care plus L-BLP25 while those on the control arm received best standard of care alone. The randomized trial, which enrolled 171 patients in total, was conducted at 13 sites in Canada and four sites in the United Kingdom.
Both Biomira and Merck KGaA were impressed with the preliminary two-year survival data. The preliminary results in the Phase IIb study show a difference of 14.3 per cent after two years (28.9 per cent for the control arm versus 43.2 per cent for the vaccine arm).
"Although we would have been pleased to have seen a statistically significant difference in the two groups, we recognized at the outset of the trial that this would be difficult to reach in a Phase IIb trial with only 171 patients," said Alex McPherson, MD, PhD, President and CEO. "We came close to showing a statistically significant difference between the two groups. Of even greater importance is that the trial results clearly show us a path forward in a subsequent registration trial, if regulatory authorities require such a trial. We expect to be discussing our results with regulatory authorities in due course."
The analysis of the patient population for this study was stratified. Two of the stratified groups in the analysis of this patient population were patients with Stage IIIb locoregional disease and patients with Stage IIIb malignant pleural effusion and Stage IV cancer. Of the patients on the trial stratified with Stage IIIb locoregional disease, the median survival for those on the vaccine arm has not yet been met, while the median survival for those on the control arm is 13.3 months. As of December 2003, 60 per cent of the patients on the vaccine arm with Stage IIIb locoregional disease had survived two-years while only 36.7 per cent of the patients on the control arm had reached the same milestone. The Companies believe this 25 per cent difference is clinically compelling.
Last month, Biomira announced that the detailed data from the Company`s Phase IIb L-BLP25 trial in non-small cell lung cancer had been accepted as the subject of a poster presentation at the 2004 annual meeting of the American Society of Clinical Oncology (ASCO). However, in compliance with Biomira`s timely disclosure obligations of material information under applicable securities laws and regulatory requirements, it was necessary for Biomira to announce details relating to the results of the Phase IIb final analysis before the ASCO annual meeting. Since many of the details of the study have been publicly disclosed, the abstract is not eligible to be presented at the ASCO annual meeting. The Company believes that the timely disclosure which it made in its April 2, 2004 press release was required under applicable securities laws and regulatory requirements, even though it resulted in ASCO`s decision to remove the Company`s poster presentation from the 2004 annual meeting of ASCO. It should be noted that the clinical investigators participating in the abstract submission were not involved in the determination as to the material information to be disclosed in the Company`s April 2, 2004 press release.
"ASCO is one of the premiere peer-reviewed meetings at which to release important clinical data in cancer research," said Alex McPherson. "Although the ASCO annual meeting will not be the forum in which we present this important clinical data at this time, we look forward to working with ASCO in the future when we have further clinical breakthroughs to discuss. We will be looking at other peer-reviewed meetings or publications in which to present the NSCLC data."
Finally, Biomira and its collaborator, Merck KGaA have recently met with an Advisory Board made up of top lung cancer specialists in North America. The consensus from the clinical advisors was to move L-BLP25 into a pivotal trial to confirm the Phase IIb data. This is one of the options Biomira can explore when it meets with regulatory authorities, which we expect will be later this year.
Theratope
Biomira and Merck KGaA of Darmstadt, Germany continue to study a potential mechanism of action to explain the apparent benefit to the large group of women with metastatic breast cancer on the Phase III trial who were treated with hormonal therapy as part of their treatment regimen. The Companies expect to announce the corporate strategy for Theratope by the end of the second quarter of 2004.
Concurrently, Biomira and Merck KGaA continue enrolment in the Phase II study of Theratope in combination with either aromatase inhibitors or Faslodex(R) (fulvestrant), an estrogen-receptor antagonist. The trial, which is expected to close enrolment in the second quarter of 2004, should enrol approximately 95 patients and is being managed by Merck KGaA`s wholly owned U.S. subsidiary, EMD Pharmaceuticals.
Prima BioMed/CancerVac Licensing Agreement
In addition to the Merck KGaA collaboration, Biomira also recently entered into a license and development agreement with Prima BioMed Ltd. of Melbourne Australia and CancerVac Pty. Ltd., its subsidiary. The license and development agreement relates to the development and commercialization of CancerVac`s Mannan-MUC1 Fusion Protein (MFP) therapeutic vaccine. CancerVac has developed an immunotherapy that utilizes the patient`s own dendritic cells treated ex-vivo to stimulate a cellular immune response following re-injection into the patient.
In partial consideration for the license rights provided by Biomira to CancerVac, Biomira acquired a 10 per cent equity stake in CancerVac, and a seat on the CancerVac Board of Directors.
Prima BioMed and CancerVac are planning to conduct a Phase IIa study in ovarian cancer with the product candidate, with the trial expected to commence in the second quarter of 2004, subject to the approval of the protocol by Biomira.
Merck KGaA
Biomira`s collaborator for Theratope and L-BLP25 is Merck KGaA, of Darmstadt, Germany, founded in 1668. Merck KGaA has positioned itself to be on the cutting edge of cancer research with an oncology portfolio based on four technology platforms - monoclonal antibodies, vaccines, immunocytokines and angiogenesis inhibitors.
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Biomira Inc.
CONSOLIDATED BALANCE SHEETS
(Canadian dollars, in thousands, except number of shares)
<<
March 31, 2004 December 31, 2003
(Unaudited) (Unaudited)(x)
------------------------------------
ASSETS
Current
Cash and cash equivalents $ 14,436 $ 24,062
Short-term investments 20,638 17,443
Accounts receivable 767 459
Prepaid expenses 480 460
------------------------------------
36,321 42,424
Capital assets (net) 528 641
Long-term investments 264 -
------------------------------------
$ 37,113 $ 43,065
------------------------------------
------------------------------------
LIABILITIES
Current
Accounts payable and accrued
liabilities $ 2,075 $ 3,453
Current portion of capital
lease obligation 69 108
Current portion of deferred
revenue 1,071 1,053
------------------------------------
3,215 4,614
Capital lease obligation - -
Deferred revenue 6,652 6,671
Class A preference shares 30 30
------------------------------------
9,897 11,315
SHAREHOLDERS` EQUITY
Share capital 359,716 359,643
Warrants 8,555 8,555
Contributed surplus 10,719 8,901
Deficit (351,774) (345,349)
------------------------------------
27,216 31,750
------------------------------------
$ 37,113 $ 43,065
------------------------------------
------------------------------------
Common Shares Issued and
Outstanding 72,558,982 72,545,232
(CAD $1.00 equals USD $0.76)
(x) Figures excerpted from the 2003 audited consolidated financial
statements.
Biomira Inc.
CONSOLIDATED STATEMENTS OF OPERATIONS
(Canadian dollars, in thousands, except per share amounts)
Three Months Ended
March 31
(Unaudited) (Unaudited)
------------------------------------
2004 2003
---- ----
REVENUE
Contract research and development $ 520 $ 902
Licensing revenue from
collaborative agreements 265 264
Licensing, royalties and
other revenue 158 -
------------------------------------
943 1,166
------------------------------------
EXPENSES
Research and development 3,726 4,122
General and administrative 1,701 1,436
Marketing and business
development 307 415
Stock compensation expense 289 -
Amortization of capital assets 113 119
Gain on disposal of capital assets - (5)
------------------------------------
6,136 6,087
------------------------------------
OPERATING LOSS (5,193) (4,921)
Investment and other income 360 572
Interest expense (2) (8)
------------------------------------
LOSS BEFORE INCOME TAXES (4,835) (4,357)
Income tax provision (17) (3)
------------------------------------
NET LOSS $ (4,852) $ (4,360)
------------------------------------
------------------------------------
BASIC AND DILUTED LOSS PER SHARE $ (0.07) $ (0.09)
------------------------------------
WEIGHTED AVERAGE NUMBER OF
COMMON SHARES OUTSTANDING 72,555 54,019
------------------------------------
CONSOLIDATED STATEMENTS OF DEFICIT
(Canadian dollars, in thousands)
Three Months Ended
March 31
(Unaudited) (Unaudited)
------------------------------------
2004 2003
---- ----
DEFICIT, BEGINNING OF PERIOD $(346,922) $(326,101)
Net loss for the period (4,852) (4,360)
Accretion of convertible debentures - (504)
Interest, foreign exchange gain/
(loss), and carrying charges
on debentures - 70
------------------------------------
DEFICIT, END OF PERIOD $(351,774) $(330,895)
------------------------------------
------------------------------------
Biomira Inc.
CONSOLIDATED STATEMENTS OF CASH FLOW
(Canadian dollars, in thousands)
Three Months Ended
March 31
(Unaudited) (Unaudited)
------------------------------------
2004 2003
---- ----
OPERATING
Net loss $ (4,852) $ (4,360)
Amortization of capital assets 113 119
Stock compensation expense 289 -
Amortization of deferred revenue (265) (264)
Gain on disposal of capital assets - (5)
Unrealized foreign exchange
(gain) loss (24) 20
Net change in non-cash balances
from operations:
Accounts receivable (308) (14)
Prepaid expenses (20) (103)
Accounts payable and accrued
liabilities (1,378) (4,036)
------------------------------------
(6,445) (8,643)
INVESTING
(Increase) decrease in short-
term investments (3,195) 12,841
Proceeds on disposal of
capital assets - 20
------------------------------------
(3,195) 12,861
FINANCING
Proceeds on issue of common
shares, net of issue costs 29 680
Repayment of convertible
debentures - (4,041)
Interest on convertible
debentures - (68)
Repayment of capital lease
obligation (39) (38)
------------------------------------
(10) (3,467)
------------------------------------
NET CASH (OUTFLOW) INFLOW (9,650) 751
Effect of exchange rate
fluctuations on cash and
cash equivalents 24 (20)
------------------------------------
(DECREASE) INCREASE IN CASH
AND CASH EQUIVALENTS (9,626) 731
CASH AND CASH EQUIVALENTS,
BEGINNING OF PERIOD 24,062 8,507
------------------------------------
CASH AND CASH EQUIVALENTS,
END OF PERIOD $ 14,436 $ 9,238
THURSDAY, APRIL 29, 2004 1:40 PM
- PR Newswire
BIOM
1.719 -0.101
Enter Symbol:
Enter Keyword:
EDMONTON, Apr 29, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (BIOM) (CA:BRA) today reported financial results for the three months ended March 31, 2004.
Financial results for the three months ended March 31, 2004 reflect a consolidated net loss from operations of $4.9 million or $0.07 per share compared to $4.4 million or $0.09 per share for the same period in 2003. The increased loss of $0.5 million in 2004 arises from stock compensation expense of $0.3 million, higher general and administrative expenses of $0.3 million, lower revenues of $0.2 million and lower investment and other income of $0.2 million, offset by $0.4 million reduction in gross research and development expenditures and $0.1 million reduction in marketing and business development expenses. The majority of the higher loss results from the adoption of a new accounting standard effective January 1, 2004 that requires expensing of employee stock options.
Contract research and development revenue for the three months ended March 31, 2004, totalling $0.5 million compared to $0.9 million for the same period in 2003, represents contract research and development funding received from Merck KGaA of Darmstadt, Germany associated with Theratope(R) vaccine and BLP25 Liposomal vaccine (L-BLP25). The decreased funding reflects a lower level of clinical activity with the wind down of the Theratope Phase III trial, and unblinding of the L-BLP25 Phase IIb trial results. Licensing revenues from collaborative arrangements represent the amortization of upfront payments received from Merck KGaA upon commencement of the collaboration. In addition, the collaboration with CancerVac Pty. Ltd. of Melbourne, Australia, announced in March 2004, entailed an upfront sub-licensing fee of $0.26 million (U.S. $0.2 million), which is being amortized over the term of the collaboration, or approximately 15 years. This fee, for which Biomira acquired a 10 per cent equity stake in CancerVac in lieu of a cash payment, represents partial consideration for sub-licensing rights to Biomira`s MUC1 technology. Finally, the increase of $0.2 million in licensing, royalties and other revenue relates to chemistry manufacturing contracts.
Research and development expenditures for the three months ended March 31, 2004 totalled $3.7 million compared to $4.1 million for the same period in 2003. The decrease in research and development expenditures, which determines the amount of collaborative funding revenue, is similarly attributable to winding down of clinical activities. General and administrative expenses for the three months ended March 31, 2004 totalled $1.7 million compared to $1.4 million for the same period in 2003. The increase of $0.3 million stems largely from incremental costs related to the settlement of an outstanding litigation in the first quarter. Marketing and business development expenditures for the three months ended March 31, 2004 decreased to $0.3 million compared to $0.4 million for the same period in 2003, and reflect the deferral of expenditures related to Theratope pre-launch activities. Marketing and business development expenditures include corporate administrative expenses associated with these functions, as well as costs for developing Biomira`s internal marketing capabilities and pre-launch marketing activities related to Theratope jointly undertaken and funded with Merck KGaA.
Stock compensation expense of $0.3 million for the three months ended March 31, 2004 represents the amortization of the estimated fair value of options granted since January 1, 2002 applicable to the current period. The retroactive application of CICA Handbook Section 3870 with respect to recognition of stock compensation expense for 2002 and 2003 resulted in a $1.6 million charge to opening deficit. Under the transitional provisions of Section 3870, restatement of comparative figures for prior periods presented in the financial statements is optional.
Investment and other income for the three months ended March 31, 2004, totaling $0.4 million compared to $0.6 million for the same period in 2003, comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. The decrease is mainly due to lower average cash and investment balances, as net foreign exchange gains of $0.2 million for the three months ended March 31, 2004 were similar for the same period in 2003.
Biomira`s financial reserves total $35.1 million in cash and short-term investments as at March 31, 2004, a decrease of $6.4 million from the year end position due to funding of operations during the quarter.
Corporate Update
L-BLP25 Phase IIb Study in Non-Small Cell Lung Cancer (NSCLC)
The first quarter of 2004 brought positive news with the announced preliminary results from the BLP25 Liposomal vaccine (L-BLP25) Phase IIb controlled, open-label clinical trial in NSCLC. The preliminary results showed evidence of a 4.4 month overall improvement in survival for those men and women on the vaccine arm as compared to those on the control arm. The overall median survival was 17.4 months for patients on the vaccine arm versus 13 months for those individuals on the control arm of the trial. Patients on the vaccine arm received best standard of care plus L-BLP25 while those on the control arm received best standard of care alone. The randomized trial, which enrolled 171 patients in total, was conducted at 13 sites in Canada and four sites in the United Kingdom.
Both Biomira and Merck KGaA were impressed with the preliminary two-year survival data. The preliminary results in the Phase IIb study show a difference of 14.3 per cent after two years (28.9 per cent for the control arm versus 43.2 per cent for the vaccine arm).
"Although we would have been pleased to have seen a statistically significant difference in the two groups, we recognized at the outset of the trial that this would be difficult to reach in a Phase IIb trial with only 171 patients," said Alex McPherson, MD, PhD, President and CEO. "We came close to showing a statistically significant difference between the two groups. Of even greater importance is that the trial results clearly show us a path forward in a subsequent registration trial, if regulatory authorities require such a trial. We expect to be discussing our results with regulatory authorities in due course."
The analysis of the patient population for this study was stratified. Two of the stratified groups in the analysis of this patient population were patients with Stage IIIb locoregional disease and patients with Stage IIIb malignant pleural effusion and Stage IV cancer. Of the patients on the trial stratified with Stage IIIb locoregional disease, the median survival for those on the vaccine arm has not yet been met, while the median survival for those on the control arm is 13.3 months. As of December 2003, 60 per cent of the patients on the vaccine arm with Stage IIIb locoregional disease had survived two-years while only 36.7 per cent of the patients on the control arm had reached the same milestone. The Companies believe this 25 per cent difference is clinically compelling.
Last month, Biomira announced that the detailed data from the Company`s Phase IIb L-BLP25 trial in non-small cell lung cancer had been accepted as the subject of a poster presentation at the 2004 annual meeting of the American Society of Clinical Oncology (ASCO). However, in compliance with Biomira`s timely disclosure obligations of material information under applicable securities laws and regulatory requirements, it was necessary for Biomira to announce details relating to the results of the Phase IIb final analysis before the ASCO annual meeting. Since many of the details of the study have been publicly disclosed, the abstract is not eligible to be presented at the ASCO annual meeting. The Company believes that the timely disclosure which it made in its April 2, 2004 press release was required under applicable securities laws and regulatory requirements, even though it resulted in ASCO`s decision to remove the Company`s poster presentation from the 2004 annual meeting of ASCO. It should be noted that the clinical investigators participating in the abstract submission were not involved in the determination as to the material information to be disclosed in the Company`s April 2, 2004 press release.
"ASCO is one of the premiere peer-reviewed meetings at which to release important clinical data in cancer research," said Alex McPherson. "Although the ASCO annual meeting will not be the forum in which we present this important clinical data at this time, we look forward to working with ASCO in the future when we have further clinical breakthroughs to discuss. We will be looking at other peer-reviewed meetings or publications in which to present the NSCLC data."
Finally, Biomira and its collaborator, Merck KGaA have recently met with an Advisory Board made up of top lung cancer specialists in North America. The consensus from the clinical advisors was to move L-BLP25 into a pivotal trial to confirm the Phase IIb data. This is one of the options Biomira can explore when it meets with regulatory authorities, which we expect will be later this year.
Theratope
Biomira and Merck KGaA of Darmstadt, Germany continue to study a potential mechanism of action to explain the apparent benefit to the large group of women with metastatic breast cancer on the Phase III trial who were treated with hormonal therapy as part of their treatment regimen. The Companies expect to announce the corporate strategy for Theratope by the end of the second quarter of 2004.
Concurrently, Biomira and Merck KGaA continue enrolment in the Phase II study of Theratope in combination with either aromatase inhibitors or Faslodex(R) (fulvestrant), an estrogen-receptor antagonist. The trial, which is expected to close enrolment in the second quarter of 2004, should enrol approximately 95 patients and is being managed by Merck KGaA`s wholly owned U.S. subsidiary, EMD Pharmaceuticals.
Prima BioMed/CancerVac Licensing Agreement
In addition to the Merck KGaA collaboration, Biomira also recently entered into a license and development agreement with Prima BioMed Ltd. of Melbourne Australia and CancerVac Pty. Ltd., its subsidiary. The license and development agreement relates to the development and commercialization of CancerVac`s Mannan-MUC1 Fusion Protein (MFP) therapeutic vaccine. CancerVac has developed an immunotherapy that utilizes the patient`s own dendritic cells treated ex-vivo to stimulate a cellular immune response following re-injection into the patient.
In partial consideration for the license rights provided by Biomira to CancerVac, Biomira acquired a 10 per cent equity stake in CancerVac, and a seat on the CancerVac Board of Directors.
Prima BioMed and CancerVac are planning to conduct a Phase IIa study in ovarian cancer with the product candidate, with the trial expected to commence in the second quarter of 2004, subject to the approval of the protocol by Biomira.
Merck KGaA
Biomira`s collaborator for Theratope and L-BLP25 is Merck KGaA, of Darmstadt, Germany, founded in 1668. Merck KGaA has positioned itself to be on the cutting edge of cancer research with an oncology portfolio based on four technology platforms - monoclonal antibodies, vaccines, immunocytokines and angiogenesis inhibitors.
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Biomira Inc.
CONSOLIDATED BALANCE SHEETS
(Canadian dollars, in thousands, except number of shares)
<<
March 31, 2004 December 31, 2003
(Unaudited) (Unaudited)(x)
------------------------------------
ASSETS
Current
Cash and cash equivalents $ 14,436 $ 24,062
Short-term investments 20,638 17,443
Accounts receivable 767 459
Prepaid expenses 480 460
------------------------------------
36,321 42,424
Capital assets (net) 528 641
Long-term investments 264 -
------------------------------------
$ 37,113 $ 43,065
------------------------------------
------------------------------------
LIABILITIES
Current
Accounts payable and accrued
liabilities $ 2,075 $ 3,453
Current portion of capital
lease obligation 69 108
Current portion of deferred
revenue 1,071 1,053
------------------------------------
3,215 4,614
Capital lease obligation - -
Deferred revenue 6,652 6,671
Class A preference shares 30 30
------------------------------------
9,897 11,315
SHAREHOLDERS` EQUITY
Share capital 359,716 359,643
Warrants 8,555 8,555
Contributed surplus 10,719 8,901
Deficit (351,774) (345,349)
------------------------------------
27,216 31,750
------------------------------------
$ 37,113 $ 43,065
------------------------------------
------------------------------------
Common Shares Issued and
Outstanding 72,558,982 72,545,232
(CAD $1.00 equals USD $0.76)
(x) Figures excerpted from the 2003 audited consolidated financial
statements.
Biomira Inc.
CONSOLIDATED STATEMENTS OF OPERATIONS
(Canadian dollars, in thousands, except per share amounts)
Three Months Ended
March 31
(Unaudited) (Unaudited)
------------------------------------
2004 2003
---- ----
REVENUE
Contract research and development $ 520 $ 902
Licensing revenue from
collaborative agreements 265 264
Licensing, royalties and
other revenue 158 -
------------------------------------
943 1,166
------------------------------------
EXPENSES
Research and development 3,726 4,122
General and administrative 1,701 1,436
Marketing and business
development 307 415
Stock compensation expense 289 -
Amortization of capital assets 113 119
Gain on disposal of capital assets - (5)
------------------------------------
6,136 6,087
------------------------------------
OPERATING LOSS (5,193) (4,921)
Investment and other income 360 572
Interest expense (2) (8)
------------------------------------
LOSS BEFORE INCOME TAXES (4,835) (4,357)
Income tax provision (17) (3)
------------------------------------
NET LOSS $ (4,852) $ (4,360)
------------------------------------
------------------------------------
BASIC AND DILUTED LOSS PER SHARE $ (0.07) $ (0.09)
------------------------------------
WEIGHTED AVERAGE NUMBER OF
COMMON SHARES OUTSTANDING 72,555 54,019
------------------------------------
CONSOLIDATED STATEMENTS OF DEFICIT
(Canadian dollars, in thousands)
Three Months Ended
March 31
(Unaudited) (Unaudited)
------------------------------------
2004 2003
---- ----
DEFICIT, BEGINNING OF PERIOD $(346,922) $(326,101)
Net loss for the period (4,852) (4,360)
Accretion of convertible debentures - (504)
Interest, foreign exchange gain/
(loss), and carrying charges
on debentures - 70
------------------------------------
DEFICIT, END OF PERIOD $(351,774) $(330,895)
------------------------------------
------------------------------------
Biomira Inc.
CONSOLIDATED STATEMENTS OF CASH FLOW
(Canadian dollars, in thousands)
Three Months Ended
March 31
(Unaudited) (Unaudited)
------------------------------------
2004 2003
---- ----
OPERATING
Net loss $ (4,852) $ (4,360)
Amortization of capital assets 113 119
Stock compensation expense 289 -
Amortization of deferred revenue (265) (264)
Gain on disposal of capital assets - (5)
Unrealized foreign exchange
(gain) loss (24) 20
Net change in non-cash balances
from operations:
Accounts receivable (308) (14)
Prepaid expenses (20) (103)
Accounts payable and accrued
liabilities (1,378) (4,036)
------------------------------------
(6,445) (8,643)
INVESTING
(Increase) decrease in short-
term investments (3,195) 12,841
Proceeds on disposal of
capital assets - 20
------------------------------------
(3,195) 12,861
FINANCING
Proceeds on issue of common
shares, net of issue costs 29 680
Repayment of convertible
debentures - (4,041)
Interest on convertible
debentures - (68)
Repayment of capital lease
obligation (39) (38)
------------------------------------
(10) (3,467)
------------------------------------
NET CASH (OUTFLOW) INFLOW (9,650) 751
Effect of exchange rate
fluctuations on cash and
cash equivalents 24 (20)
------------------------------------
(DECREASE) INCREASE IN CASH
AND CASH EQUIVALENTS (9,626) 731
CASH AND CASH EQUIVALENTS,
BEGINNING OF PERIOD 24,062 8,507
------------------------------------
CASH AND CASH EQUIVALENTS,
END OF PERIOD $ 14,436 $ 9,238
müßte morgen nach oben gehen
Scheint der Grund für den Absturz zu sein:
Removal of Abstract
An abstract on a Phase IIb BLP25 liposomal vaccine trial in non-small cell lung cancer, sponsored by Biomira, Inc., has been removed from the ASCO Annual Meeting program because the data has already been made public in another forum.
http://www.asco.org
Sind die jetzt komplett bei ASCO raus?
Removal of Abstract
An abstract on a Phase IIb BLP25 liposomal vaccine trial in non-small cell lung cancer, sponsored by Biomira, Inc., has been removed from the ASCO Annual Meeting program because the data has already been made public in another forum.

http://www.asco.org
Sind die jetzt komplett bei ASCO raus?

Grund für den Absturz ist lediglich der, dass ich mir ein paar gekauft habe 
Päpstin

Päpstin
...es scheint wieder aufwärts zu gehen ?!
Vorbörslich immerhin + 8 % !!!
Name
Biomira Inc
Last Price
1.7000
Net Change
+0.1200
Shares Matched
1,000
Orders Entered
55
Last Match Time
8:07:19.455
Market
NM
Previous Close
1.5800
Percent Change
+7.59%
Shares Entered
94,989
Open Orders
54
Last Order Time
8:43:04.567
Vorbörslich immerhin + 8 % !!!
Name
Biomira Inc
Last Price
1.7000
Net Change
+0.1200
Shares Matched
1,000
Orders Entered
55
Last Match Time
8:07:19.455
Market
NM
Previous Close
1.5800
Percent Change
+7.59%
Shares Entered
94,989
Open Orders
54
Last Order Time
8:43:04.567
May 13, 2004
9:45 AM - 10:00 AM EDT
London, England Rodman & Renshaw Techvest Global Healthcare Conference
Dr. McPherson will make an investor presentation at this three day conference (May 12-14 2004) in London, England. The conference is being held at Claridge`s Hotel, London.
Der nächste Termin. Hoffentlich kommen da endlich mal positivere Nachrichten.
9:45 AM - 10:00 AM EDT
London, England Rodman & Renshaw Techvest Global Healthcare Conference
Dr. McPherson will make an investor presentation at this three day conference (May 12-14 2004) in London, England. The conference is being held at Claridge`s Hotel, London.
Der nächste Termin. Hoffentlich kommen da endlich mal positivere Nachrichten.

Hoffentlich 

ich vermute das mit absicht der kurs gedrückt wurde
die news werden kommen
LAMP geht auch ab und die news kommen stück für stück
die news werden kommen
LAMP geht auch ab und die news kommen stück für stück
WEDNESDAY, APRIL 28, 2004 4:15 PM
- BusinessWire
BIOM
1.55 +0.05
Enter Symbol:
Enter Keyword:
LOS ANGELES, Apr 28, 2004 (BUSINESS WIRE) -- Universal Detection Technology (UDTT) (Frankfurt:UDTT.F) today announced that it will attend the Rodman & Renshaw Techvest Global Healthcare Conference in London during May 12-14, 2004.
The Rodman & Renshaw Techvest Global Healthcare Conference will be held at the Claridge`s Hotel and will feature topics ranging from infectious diseases and therapeutic vaccines to specialty pharmaceuticals and medical devices. The event will bring together companies, institutional and venture capitalists, and senior corporate executives as well as experts from the scientific and medical communities.
UDTT is sending the principals of the company: CEO and President Jacques Tizabi, Amir Ettehadieh, Director of Research and Development, Dr. Leonard Makowka, Chief Scientific Advisor and Dr. Adrian Ponce, Senior Staff Technical Member at NASA`s Jet Propulsion Laboratory. Amongst other topics, the Company and Dr. Ponce will be discussing the progress on the development of the Bacterial Spore Detection Device as well as its recently announced collaboration agreement and grant from Rutgers University. "We`re looking forward to presenting to the European community," said Jacques Tizabi, the Company`s President and CEO.
UDTT will be among 175 other exhibitors, including both private and publicly held companies such as ADVENTRX Pharmaceuticals, Inc. (AVRX) , Biomira Inc. (BIOM) , Cell Genesys, Inc. (CEGE) , Genelabs Technologies, Inc. (GNLB) , MediGene (Frankfurt:MDG), and ZymoGenetics Inc. (ZGEN) , to name a few. The UDTT presentation will take place in The Drawing Room at 9:40 a.m. on Friday, May 14, 2004.
The Conference`s unique format will include select panel discussions hosted by Rodman & Renshaw equity analysts and key industry leaders that will add expert perspective to a small, theme-based group of company presentations. In addition, there will be keynote lunch speakers and opportunities for breakout sessions, Q&As and one-on-one meetings with companies. For further information about the conference, visit the Rodman & Renshaw Web site at: http://www.rodmanandrenshaw.com.
About Rodman & Renshaw
Rodman & Renshaw, LLC (www.rodmanandrenshaw.com) is a privately owned, full-service investment banking and brokerage firm headquartered in New York City, focusing exclusively on emerging growth companies. Rodman & Renshaw provides a full range of services including: equity research, institutional sales & trading, and corporate finance. Currently, the firm has a team of seven Ph.D. level biotech analysts, covering the life sciences sector. Rodman & Renshaw is a member of the National Association of Securities Dealers, CRD number 16415.
About Universal Detection Technology
Universal Detection Technology (www.udetection.com), which recently had its ticker symbol changed from UDET to UDTT to accommodate a recent name change, was founded in 1973 and is a developer of monitoring technologies, including bio-terrorism detection devices. UDTT`s technology, together with third party technologies and devices, position the Company to capitalize on growth and value opportunities. Universal Detection Technology recently entered into an agreement with NASA`s Jet Propulsion Laboratory (JPL) to mutually develop a commercially available anthrax "smoke" detector, which will combine the JPL spore detection technology with UDTT`s aerosol capture device. The partnership with UDTT was accomplished through the Technology Affiliates Program, one of many Commercial Technology Programs aimed at transferring JPL`s knowledge to the private sector for broad public use.
Except for historical information contained herein, the statements in this news release are forward-looking statements that are made pursuant to the safe harbor provisions of the Private Securities Litigation Reform Act of 1995. Forward-looking statements involve known and unknown risks and uncertainties, which may cause a company`s actual results, performance and achievement in the future to differ materially from forecasted results, performance, and achievement. These risks and uncertainties include, among other things, the funding of amounts of capital adequate to provide for the working capital needs of the Company, our ability to timely and cost effectively complete the development of our products targeted to the bio-chemical and medical markets, commercial acceptance of our products, product price volatility, product demand, market competition and general economic conditions, and other factors described in the Company`s filings with the Securities and Exchange Commission. We undertake no obligation and do not intend to revise or update publicly any forward looking statements for any reason.
SOURCE: Universal Detection Technology
- BusinessWire
BIOM
1.55 +0.05
Enter Symbol:
Enter Keyword:
LOS ANGELES, Apr 28, 2004 (BUSINESS WIRE) -- Universal Detection Technology (UDTT) (Frankfurt:UDTT.F) today announced that it will attend the Rodman & Renshaw Techvest Global Healthcare Conference in London during May 12-14, 2004.
The Rodman & Renshaw Techvest Global Healthcare Conference will be held at the Claridge`s Hotel and will feature topics ranging from infectious diseases and therapeutic vaccines to specialty pharmaceuticals and medical devices. The event will bring together companies, institutional and venture capitalists, and senior corporate executives as well as experts from the scientific and medical communities.
UDTT is sending the principals of the company: CEO and President Jacques Tizabi, Amir Ettehadieh, Director of Research and Development, Dr. Leonard Makowka, Chief Scientific Advisor and Dr. Adrian Ponce, Senior Staff Technical Member at NASA`s Jet Propulsion Laboratory. Amongst other topics, the Company and Dr. Ponce will be discussing the progress on the development of the Bacterial Spore Detection Device as well as its recently announced collaboration agreement and grant from Rutgers University. "We`re looking forward to presenting to the European community," said Jacques Tizabi, the Company`s President and CEO.
UDTT will be among 175 other exhibitors, including both private and publicly held companies such as ADVENTRX Pharmaceuticals, Inc. (AVRX) , Biomira Inc. (BIOM) , Cell Genesys, Inc. (CEGE) , Genelabs Technologies, Inc. (GNLB) , MediGene (Frankfurt:MDG), and ZymoGenetics Inc. (ZGEN) , to name a few. The UDTT presentation will take place in The Drawing Room at 9:40 a.m. on Friday, May 14, 2004.
The Conference`s unique format will include select panel discussions hosted by Rodman & Renshaw equity analysts and key industry leaders that will add expert perspective to a small, theme-based group of company presentations. In addition, there will be keynote lunch speakers and opportunities for breakout sessions, Q&As and one-on-one meetings with companies. For further information about the conference, visit the Rodman & Renshaw Web site at: http://www.rodmanandrenshaw.com.
About Rodman & Renshaw
Rodman & Renshaw, LLC (www.rodmanandrenshaw.com) is a privately owned, full-service investment banking and brokerage firm headquartered in New York City, focusing exclusively on emerging growth companies. Rodman & Renshaw provides a full range of services including: equity research, institutional sales & trading, and corporate finance. Currently, the firm has a team of seven Ph.D. level biotech analysts, covering the life sciences sector. Rodman & Renshaw is a member of the National Association of Securities Dealers, CRD number 16415.
About Universal Detection Technology
Universal Detection Technology (www.udetection.com), which recently had its ticker symbol changed from UDET to UDTT to accommodate a recent name change, was founded in 1973 and is a developer of monitoring technologies, including bio-terrorism detection devices. UDTT`s technology, together with third party technologies and devices, position the Company to capitalize on growth and value opportunities. Universal Detection Technology recently entered into an agreement with NASA`s Jet Propulsion Laboratory (JPL) to mutually develop a commercially available anthrax "smoke" detector, which will combine the JPL spore detection technology with UDTT`s aerosol capture device. The partnership with UDTT was accomplished through the Technology Affiliates Program, one of many Commercial Technology Programs aimed at transferring JPL`s knowledge to the private sector for broad public use.
Except for historical information contained herein, the statements in this news release are forward-looking statements that are made pursuant to the safe harbor provisions of the Private Securities Litigation Reform Act of 1995. Forward-looking statements involve known and unknown risks and uncertainties, which may cause a company`s actual results, performance and achievement in the future to differ materially from forecasted results, performance, and achievement. These risks and uncertainties include, among other things, the funding of amounts of capital adequate to provide for the working capital needs of the Company, our ability to timely and cost effectively complete the development of our products targeted to the bio-chemical and medical markets, commercial acceptance of our products, product price volatility, product demand, market competition and general economic conditions, and other factors described in the Company`s filings with the Securities and Exchange Commission. We undertake no obligation and do not intend to revise or update publicly any forward looking statements for any reason.
SOURCE: Universal Detection Technology
Da ja nun endlich kontretere Informationen für den nächsten Monat angekündigt werden, dürfte BIOM jetzt wieder klettern. Bis zur ASCO werden die Gerüchte wieder
zunehmen. Und das ist gut für den Kurs.
STRONG BUY
zunehmen. Und das ist gut für den Kurs.

STRONG BUY
Bin überrascht von den Theratope-Ergebnissen!
Scheint so,als ob Theratope gute Chancen auf eine Zulassung hat!
Scheint so,als ob Theratope gute Chancen auf eine Zulassung hat!

May 20, 2004
1:30 AM - 3:30 AM EDT
Toronto Ontario Annual General Meeting + URL to Watch Web Cast
Biomira`s Annual General Meeting will be held on Thursday, May 20th, 2004. The meeting will be held at the Hilton Toronto Hotel, 145 Richmond Street West (The Governor General Room).
Registration will be at 1:00 p.m. Eastern time, with the meeting starting promptly at 1:30 p.m.
Shareholders who are unable to be present in person at the AGM are invited to submit questions have for the Q&A session following the President’s Address to Shareholders. Please submit questions to ir@biomira.com. Please keep the questions short. If we are not able to address all questions at the meeting, either by including them in the presentation or at the Q&A session following Dr. McPherson`s presentation, your questions will be answered by e-mail after the meeting.
You may view the presentation at http://webevents.broadcast.com/cnw/biomira20040520
1:30 AM - 3:30 AM EDT
Toronto Ontario Annual General Meeting + URL to Watch Web Cast
Biomira`s Annual General Meeting will be held on Thursday, May 20th, 2004. The meeting will be held at the Hilton Toronto Hotel, 145 Richmond Street West (The Governor General Room).
Registration will be at 1:00 p.m. Eastern time, with the meeting starting promptly at 1:30 p.m.
Shareholders who are unable to be present in person at the AGM are invited to submit questions have for the Q&A session following the President’s Address to Shareholders. Please submit questions to ir@biomira.com. Please keep the questions short. If we are not able to address all questions at the meeting, either by including them in the presentation or at the Q&A session following Dr. McPherson`s presentation, your questions will be answered by e-mail after the meeting.
You may view the presentation at http://webevents.broadcast.com/cnw/biomira20040520
Biomira Announces Highlights of Today`s Annual General Meeting
Thursday May 20, 5:30 am ET
EDMONTON, May 20 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) expects the following highlights to be covered at the Annual General Meeting of its shareholders to be held today at 1:30 p.m. EDT at the Hilton Toronto Hotel, Toronto, Ontario. The meeting will be chaired by the Board Chairman, Mr. Eric E. Baker, and will be followed by an address by the Company President and CEO, Alex McPherson, MD, PhD.
Dr. McPherson`s comments are expected to focus primarily on the Company`s two lead product candidates, BLP25 Liposome Vaccine (L-BLP25) and Theratope® vaccine, for which there is a large unmet medical need.
The potential candidates for treatment with L-BLP25 in late stage non- small cell lung cancer (NSCLC) is approaching 200,000 patients per year in the main markets of North America, Europe and Japan and is an increasing threat in women. Based on American Cancer Society data, lung cancer represents 13 per cent of all cancer diagnoses, and 28 per cent of all cancer deaths among men and women. The number of deaths from the four most common cancers (lung, breast, prostate and colorectal) is declining for all but one group, namely women with lung cancer.
The medical need is also growing in metastatic breast cancer, where approximately 40 per cent of women are now receiving hormonal therapy as part of their treatment regimen. In the Phase III study of Theratope vaccine in 1,030 women with metastatic breast cancer, a subset of approximately 350 women receiving Theratope plus hormonal anti-cancer therapy as part of their treatment appeared to show clinical benefit.
"I look forward to discussing our pipeline further," said Dr. McPherson, in anticipation of his presentation. "With regard to L-BLP25, we are enormously excited by the data we have seen. Our randomized Phase IIb clinical trial enrolled 171 men and women with stage IIIb or IV NSCLC and randomized them to either the control group, which received best standard care (SC), or to the treatment group, which received best standard care plus L-BLP25. The primary efficacy variable of the trial is survival between these two groups. While the SC group saw a median survival of 13 months, we saw a 17.4 month median survival for the treatment group, a difference of 4.4 months. Though not statistically significant, `a 4.4 month survival benefit would be an important achievement in this disease,` clinical oncologists from our advisory board said. Most importantly, the observed two-year survival for patients with locoregional Stage IIIb disease is 60 per cent for the vaccine arm (median survival not yet reached) versus 36.7 per cent for the control arm (median survival of 13.3 months). In the overall patient population the two-year survival is 43.2 per cent for the vaccine arm versus 28.9 per cent for the control arm."
"Once we more fully understand the data, we expect to have discussions with regulatory agencies in different jurisdictions to discuss the design of a possible Phase III clinical trial," said Alex McPherson. "We will also explore other potential opportunities for earlier registration based on the current data and will update the investment community once we have a clear path forward in this dreadful disease."
Moving on to Theratope, Dr. McPherson will discuss the status of this product candidate. Since the final analysis of the Phase III trial in 1,030 women, which did not show statistical significance in the overall patient population, Biomira has continued to analyze data from the pre-stratified subset of 350 women who received Theratope plus hormonal anti-cancer therapy.
"After a review of the current data and discussions with key opinion leaders, we believe that more information would be required to support a registration," said Dr. McPherson. "We continue to examine the data from the Phase III trial and investigate the mechanism of action. We are looking at the possibility of conducting a new Phase III trial in the patient population that appeared to see clinical benefit. We expect a decision by the end of June on our plans for next steps with Theratope. That being said, we continue to explore the potential opportunities for earlier registration based on the current data, perhaps in jurisdictions other than the U.S. and Europe, although we anticipate a Phase III clinical trial will be required."
Biomira and Merck KGaA are also continuing their Phase II single-arm Theratope study, where women with metastatic breast cancer are treated with Theratope plus anti-cancer hormonal therapy. This 95-patient trial is expected to complete enrolment in the second half of 2004.
Both L-BLP25 and Theratope are being developed in collaboration with Merck KGaA of Darmstadt, Germany.
Business Development
Dr. McPherson is expected to briefly discuss the Biomira/Prima BioMed- CancerVac agreement put in place in March 2004 and the creation of a spin-off company, announced earlier today, to move Liposomal Interleukin-2 (L-IL-2) back into clinical trials.
Finance
At the end of the first quarter 2004, Biomira had U.S. $26.7 million or $35.1 million Canadian in cash and short-term investments. The Company believes that it has funds to sustain it until mid 2005 at the current expenditure rate.
"We have a strong corporate alliance and the finances to see us through to a point where we can make strategic decisions on the path forward for our product candidates. We need to remain vigilant in controlling our spending, while taking advantage of potential opportunities as market conditions and opportunities present. This strategic vision may allow us to raise additional funding, thereby getting us to that final goal of product registration," concluded Dr. McPherson.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Biomira`s collaborator for Theratope and L-BLP25 is Merck KGaA, of Darmstadt, Germany, founded in 1668. Merck KGaA has positioned itself to be on the cutting edge of cancer research with an oncology portfolio based on four technology platforms - monoclonal antibodies, vaccines, immunocytokines and angiogenesis inhibitors.
Webcast Details:
Biomira will webcast today`s Annual General Meeting commencing at 1:30 p.m. Eastern time. The general public is invited to listen to the live conference call on the Web, by accessing the following site: http://webevents.broadcast.com/cnw/biomira20040520 or the archive following the webcast at http://www.biomira.com/investors/presentations/ .
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials and additional analyses, potential meetings with regulatory authorities, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward- looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Thursday May 20, 5:30 am ET
EDMONTON, May 20 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) expects the following highlights to be covered at the Annual General Meeting of its shareholders to be held today at 1:30 p.m. EDT at the Hilton Toronto Hotel, Toronto, Ontario. The meeting will be chaired by the Board Chairman, Mr. Eric E. Baker, and will be followed by an address by the Company President and CEO, Alex McPherson, MD, PhD.
Dr. McPherson`s comments are expected to focus primarily on the Company`s two lead product candidates, BLP25 Liposome Vaccine (L-BLP25) and Theratope® vaccine, for which there is a large unmet medical need.
The potential candidates for treatment with L-BLP25 in late stage non- small cell lung cancer (NSCLC) is approaching 200,000 patients per year in the main markets of North America, Europe and Japan and is an increasing threat in women. Based on American Cancer Society data, lung cancer represents 13 per cent of all cancer diagnoses, and 28 per cent of all cancer deaths among men and women. The number of deaths from the four most common cancers (lung, breast, prostate and colorectal) is declining for all but one group, namely women with lung cancer.
The medical need is also growing in metastatic breast cancer, where approximately 40 per cent of women are now receiving hormonal therapy as part of their treatment regimen. In the Phase III study of Theratope vaccine in 1,030 women with metastatic breast cancer, a subset of approximately 350 women receiving Theratope plus hormonal anti-cancer therapy as part of their treatment appeared to show clinical benefit.
"I look forward to discussing our pipeline further," said Dr. McPherson, in anticipation of his presentation. "With regard to L-BLP25, we are enormously excited by the data we have seen. Our randomized Phase IIb clinical trial enrolled 171 men and women with stage IIIb or IV NSCLC and randomized them to either the control group, which received best standard care (SC), or to the treatment group, which received best standard care plus L-BLP25. The primary efficacy variable of the trial is survival between these two groups. While the SC group saw a median survival of 13 months, we saw a 17.4 month median survival for the treatment group, a difference of 4.4 months. Though not statistically significant, `a 4.4 month survival benefit would be an important achievement in this disease,` clinical oncologists from our advisory board said. Most importantly, the observed two-year survival for patients with locoregional Stage IIIb disease is 60 per cent for the vaccine arm (median survival not yet reached) versus 36.7 per cent for the control arm (median survival of 13.3 months). In the overall patient population the two-year survival is 43.2 per cent for the vaccine arm versus 28.9 per cent for the control arm."
"Once we more fully understand the data, we expect to have discussions with regulatory agencies in different jurisdictions to discuss the design of a possible Phase III clinical trial," said Alex McPherson. "We will also explore other potential opportunities for earlier registration based on the current data and will update the investment community once we have a clear path forward in this dreadful disease."
Moving on to Theratope, Dr. McPherson will discuss the status of this product candidate. Since the final analysis of the Phase III trial in 1,030 women, which did not show statistical significance in the overall patient population, Biomira has continued to analyze data from the pre-stratified subset of 350 women who received Theratope plus hormonal anti-cancer therapy.
"After a review of the current data and discussions with key opinion leaders, we believe that more information would be required to support a registration," said Dr. McPherson. "We continue to examine the data from the Phase III trial and investigate the mechanism of action. We are looking at the possibility of conducting a new Phase III trial in the patient population that appeared to see clinical benefit. We expect a decision by the end of June on our plans for next steps with Theratope. That being said, we continue to explore the potential opportunities for earlier registration based on the current data, perhaps in jurisdictions other than the U.S. and Europe, although we anticipate a Phase III clinical trial will be required."
Biomira and Merck KGaA are also continuing their Phase II single-arm Theratope study, where women with metastatic breast cancer are treated with Theratope plus anti-cancer hormonal therapy. This 95-patient trial is expected to complete enrolment in the second half of 2004.
Both L-BLP25 and Theratope are being developed in collaboration with Merck KGaA of Darmstadt, Germany.
Business Development
Dr. McPherson is expected to briefly discuss the Biomira/Prima BioMed- CancerVac agreement put in place in March 2004 and the creation of a spin-off company, announced earlier today, to move Liposomal Interleukin-2 (L-IL-2) back into clinical trials.
Finance
At the end of the first quarter 2004, Biomira had U.S. $26.7 million or $35.1 million Canadian in cash and short-term investments. The Company believes that it has funds to sustain it until mid 2005 at the current expenditure rate.
"We have a strong corporate alliance and the finances to see us through to a point where we can make strategic decisions on the path forward for our product candidates. We need to remain vigilant in controlling our spending, while taking advantage of potential opportunities as market conditions and opportunities present. This strategic vision may allow us to raise additional funding, thereby getting us to that final goal of product registration," concluded Dr. McPherson.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Biomira`s collaborator for Theratope and L-BLP25 is Merck KGaA, of Darmstadt, Germany, founded in 1668. Merck KGaA has positioned itself to be on the cutting edge of cancer research with an oncology portfolio based on four technology platforms - monoclonal antibodies, vaccines, immunocytokines and angiogenesis inhibitors.
Webcast Details:
Biomira will webcast today`s Annual General Meeting commencing at 1:30 p.m. Eastern time. The general public is invited to listen to the live conference call on the Web, by accessing the following site: http://webevents.broadcast.com/cnw/biomira20040520 or the archive following the webcast at http://www.biomira.com/investors/presentations/ .
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials and additional analyses, potential meetings with regulatory authorities, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward- looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Biomira and Inno-Centre Alberta Create Spin-Off Company to Further Develop Liposomal Interleukin-2 Technology
Thursday May 20, 5:00 am ET
EDMONTON, May 20 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and Inno- centre Alberta announced today a collaborative agreement to create a spin- off company. The Company, Oncodigm BioPharma Inc., will be dedicated to the development and commercialization of a promising cancer therapy. The therapy, Liposomal-Interleukin-2 (L-IL-2), is projected to re- enter clinical trials in 2005.
Biomira had previously suspended clinical development of L-IL-2 in order to focus attention on Biomira`s two lead product candidates, Theratope® vaccine and BLP25 Liposome Vaccine (L-BLP25). The new Company, to initially be 90 per cent owned by Biomira and 10 per cent owned by Inno-centre Alberta, is seen as an excellent vehicle for moving this product candidate back into clinical trials, while Biomira remains focused on Theratope and L-BLP25.
Operating capital is to be independently raised by Oncodigm BioPharma. Biomira will initially provide two board members, Robert Aubrey and Edward Taylor. These individuals will be able to provide expertise in marketing and business development and corporate finance, respectively.
"We are extremely excited about this creative financing vehicle for moving L-IL-2 back into clinical trials," said Alex McPherson, MD, PhD, President and CEO. "The Inno-centre approach is perfect for Biomira. Inno- centre, among other things, provides assistance with respect to raising funds for the new Company and provides a Senior Business Advisor, in this case David T. Howard, Chairman of SCOLR, Inc., a biopharmaceutical company located in Redmond, WA and Angiotech Pharmaceuticals Inc., a world leader in the emerging field of drug-coated medical devices and biomaterials, located in Vancouver, BC. Mr. Howard will provide experienced support that will increase the opportunity for this product candidate to successfully develop through the clinical trial process. We believe that the participation of Inno-centre adds real value and the structure allows both organizations to profit from the arrangement. Costs to Biomira are relatively low, with the potential upside of a market in the range of Canadian $150 to $300 million annually."
"We are enthusiastic about working with Biomira to accelerate the development of L-IL-2," said Hugh MacNaught, VP Life Sciences and Agribusiness for Inno-centre Alberta. "The formulation has demonstrated promise for improving the therapeutic index of a drug that has shown activity against a wide spectrum of tumours. Our objective is to commercialize a product that is far more potent and less toxic than currently available products. Managing this development within a new company will create greater value for Biomira stakeholders and provide many benefits to the academic and technology communities in Alberta."
Oncodigm BioPharma intends to quickly put in place a management team to create a clinical development plan for moving this product forward, likely in metastatic renal cell carcinoma. Biomira`s L-IL2 is protected by both in- licensed and Biomira patents and has orphan drug status in the U.S. and Europe, as well as an open IND in both of those jurisdictions.
The Technology
Interleukin-2 (IL-2) is an important natural molecule of the immune system. IL-2 is important in helping to make stronger humoral (antibody) and cell-mediated immune responses. Biomira`s L-IL-2 is made up of modified IL-2 captured in a lipid droplet. The movement and distribution of L-IL-2 within the body are different compared to free IL-2. Pre-clinical studies have shown that L-IL-2 helps IL-2 remain in the serum for a longer time. Also, L-IL-2 increases the build-up of IL-2 in some tissues of the immune system. These changes in how the body handles IL-2 may help to build stronger immune responses. They may also reduce toxic effects often seen with the use of free IL-2. The use of L IL 2 may help patients and physicians, as it might need to be given less often than free IL-2.
Pre-clinical studies have shown that L-IL-2 may be better than free IL-2 in slowing tumour growth and spread. Studies have also shown that L-IL-2 may be better than free IL-2 in helping the body to mount specific immune responses against tumours.
Biomira used L-IL-2 in a Phase I study in patients with several kinds of cancers. Most of the patients in the study had either melanoma or kidney cancer.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Inno-centre Alberta is a private, not-for-profit company dedicated to accelerating the creation and development of successful technology ventures. Inno-centre uses a proven proprietary business model that features the provision of two years of business and financing mentorship to candidates that are approved by an independent Selection Committee comprised of commercially- experienced Venture Capital investors and successful technology entrepreneurs. Inno-centre is contributing to the immediate success of the technology and academic communities in Alberta by enabling a greater scope and scale of technology development than would be otherwise possible, providing direct economic benefit and new jobs for the Province.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Thursday May 20, 5:00 am ET
EDMONTON, May 20 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and Inno- centre Alberta announced today a collaborative agreement to create a spin- off company. The Company, Oncodigm BioPharma Inc., will be dedicated to the development and commercialization of a promising cancer therapy. The therapy, Liposomal-Interleukin-2 (L-IL-2), is projected to re- enter clinical trials in 2005.
Biomira had previously suspended clinical development of L-IL-2 in order to focus attention on Biomira`s two lead product candidates, Theratope® vaccine and BLP25 Liposome Vaccine (L-BLP25). The new Company, to initially be 90 per cent owned by Biomira and 10 per cent owned by Inno-centre Alberta, is seen as an excellent vehicle for moving this product candidate back into clinical trials, while Biomira remains focused on Theratope and L-BLP25.
Operating capital is to be independently raised by Oncodigm BioPharma. Biomira will initially provide two board members, Robert Aubrey and Edward Taylor. These individuals will be able to provide expertise in marketing and business development and corporate finance, respectively.
"We are extremely excited about this creative financing vehicle for moving L-IL-2 back into clinical trials," said Alex McPherson, MD, PhD, President and CEO. "The Inno-centre approach is perfect for Biomira. Inno- centre, among other things, provides assistance with respect to raising funds for the new Company and provides a Senior Business Advisor, in this case David T. Howard, Chairman of SCOLR, Inc., a biopharmaceutical company located in Redmond, WA and Angiotech Pharmaceuticals Inc., a world leader in the emerging field of drug-coated medical devices and biomaterials, located in Vancouver, BC. Mr. Howard will provide experienced support that will increase the opportunity for this product candidate to successfully develop through the clinical trial process. We believe that the participation of Inno-centre adds real value and the structure allows both organizations to profit from the arrangement. Costs to Biomira are relatively low, with the potential upside of a market in the range of Canadian $150 to $300 million annually."
"We are enthusiastic about working with Biomira to accelerate the development of L-IL-2," said Hugh MacNaught, VP Life Sciences and Agribusiness for Inno-centre Alberta. "The formulation has demonstrated promise for improving the therapeutic index of a drug that has shown activity against a wide spectrum of tumours. Our objective is to commercialize a product that is far more potent and less toxic than currently available products. Managing this development within a new company will create greater value for Biomira stakeholders and provide many benefits to the academic and technology communities in Alberta."
Oncodigm BioPharma intends to quickly put in place a management team to create a clinical development plan for moving this product forward, likely in metastatic renal cell carcinoma. Biomira`s L-IL2 is protected by both in- licensed and Biomira patents and has orphan drug status in the U.S. and Europe, as well as an open IND in both of those jurisdictions.
The Technology
Interleukin-2 (IL-2) is an important natural molecule of the immune system. IL-2 is important in helping to make stronger humoral (antibody) and cell-mediated immune responses. Biomira`s L-IL-2 is made up of modified IL-2 captured in a lipid droplet. The movement and distribution of L-IL-2 within the body are different compared to free IL-2. Pre-clinical studies have shown that L-IL-2 helps IL-2 remain in the serum for a longer time. Also, L-IL-2 increases the build-up of IL-2 in some tissues of the immune system. These changes in how the body handles IL-2 may help to build stronger immune responses. They may also reduce toxic effects often seen with the use of free IL-2. The use of L IL 2 may help patients and physicians, as it might need to be given less often than free IL-2.
Pre-clinical studies have shown that L-IL-2 may be better than free IL-2 in slowing tumour growth and spread. Studies have also shown that L-IL-2 may be better than free IL-2 in helping the body to mount specific immune responses against tumours.
Biomira used L-IL-2 in a Phase I study in patients with several kinds of cancers. Most of the patients in the study had either melanoma or kidney cancer.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Inno-centre Alberta is a private, not-for-profit company dedicated to accelerating the creation and development of successful technology ventures. Inno-centre uses a proven proprietary business model that features the provision of two years of business and financing mentorship to candidates that are approved by an independent Selection Committee comprised of commercially- experienced Venture Capital investors and successful technology entrepreneurs. Inno-centre is contributing to the immediate success of the technology and academic communities in Alberta by enabling a greater scope and scale of technology development than would be otherwise possible, providing direct economic benefit and new jobs for the Province.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
war wohl gestern nicht so der renner?!?
mfg versager

mfg versager
Das Orderbuch sieht jeden Tag besser aus.
Sollte das Gerücht stimmen, daß sich Merck heimlich
einkauft??
Sollte das Gerücht stimmen, daß sich Merck heimlich
einkauft??

#724
Lass nur in der nächsten Meldung zu Theratope "statistical significant" drinstehen und
Am 7.6. wissen Wir mehr!!!
Lass nur in der nächsten Meldung zu Theratope "statistical significant" drinstehen und

Am 7.6. wissen Wir mehr!!!
Wenn man sich die Bid Seite im Orderbuch ansieht-kommt vielleicht bald Eile und Hektik auf!





Volumen nimmt zu.
Jetzt geht`s wieder Richtung 2$ (und hoffentlich drüber).
ASCO lässt grüssen.
Jetzt geht`s wieder Richtung 2$ (und hoffentlich drüber).
ASCO lässt grüssen.

Habe mir heute mal wieder eine weitere Position nachgekauft,
ich denke nächste Woche wird das Volumen wieder stark zunehmen.

ich denke nächste Woche wird das Volumen wieder stark zunehmen.

Home > Publications > Abstracts > Basic Search >
Meeting: 2004 ASCO Annual Meeting Printer Friendly
Bookmark
Category: Developmental Therapeutics - Immunotherapy
SubCategory: Vaccines
Long-term follow-up of patients concomitantly treated with hormone therapy in a prospective controlled randomized multicenter clinical study comparing STn-KLH vaccine with KLH control in stage IV breast cancer following first-line chemotherapy.
Abstract No: 2603
Author(s): J. Mayordomo, A. Tres, D. Miles, L. Finke, H. Jenkins; Hospital Clinico Universitario, Zaragoza, Spain; Guys Hospital, London, United Kingdom; EMD Pharmaceuticals, Durham, NC; Biomira Inc, Edmonton, AB, Canada
Abstract: Background: Theratope (T) is an investigational therapeutic cancer vaccine consisting of a synthetic form of the tumor-associated antigen Sialyl Tn (STn) conjugated to the carrier protein keyhole limpet hemocyanin (KLH). This abstract reports a survival follow-up of the phase III trial with emphasis on the subgroup concomitantly treated with hormone therapy. Methods: Metastatic breast cancer patients (MBC pts) who had no evidence of disease or non-progressive disease following any first-line chemotherapy were randomized 1:1 to receive adjuvant plus T or control (C) (adjuvant plus KLH). All pts received a single IV infusion of cyclophosphamide before vaccine. Primary endpoints were time to disease progression (TTP) and overall survival (OS). Pts were stratified by disease status and concomitant hormone therapy (HT). Results: 1028 pts were randomized: 34% received concurrent HT (n = 350). The concomitant treatment in the two treatment arms on hormone therapy (n = 180 T, n = 170 C) consisted mainly of SERMs (43% vs. 39%) and AIs (47% vs. 52%). OS and TTP analyses were performed (table). Conclusions: In pts not concomitantly treated with hormones no difference between T and C was demonstrated. However, HT combined with T indicates a favorable trend based on the current database. Currently, not enough events have been reached to calculate median overall survival for the Theratope arms combined with all hormone modalities, AIs, and SERMs.
Population All HT AIs SERMs
Final analysis T
C T
C T
C
n 180
170 84
88 78
67
Median TTP, mo 8.3
5.8 8.3
5.5 8.4
8.3
Cox P value
0.22
0.30
0.73
Median OS, mo NR
30.7 NR
28.6 NR
NR
Cox P value
N/A
N/A
N/A
NR = not reached at point of submission. N/A = not applicable. An additional event-driven follow-up and analysis is planned for April/May 2004 and will be available at the meeting.
was haltet ihr davon??
mfg versager
Meeting: 2004 ASCO Annual Meeting Printer Friendly
Bookmark
Category: Developmental Therapeutics - Immunotherapy
SubCategory: Vaccines
Long-term follow-up of patients concomitantly treated with hormone therapy in a prospective controlled randomized multicenter clinical study comparing STn-KLH vaccine with KLH control in stage IV breast cancer following first-line chemotherapy.
Abstract No: 2603
Author(s): J. Mayordomo, A. Tres, D. Miles, L. Finke, H. Jenkins; Hospital Clinico Universitario, Zaragoza, Spain; Guys Hospital, London, United Kingdom; EMD Pharmaceuticals, Durham, NC; Biomira Inc, Edmonton, AB, Canada
Abstract: Background: Theratope (T) is an investigational therapeutic cancer vaccine consisting of a synthetic form of the tumor-associated antigen Sialyl Tn (STn) conjugated to the carrier protein keyhole limpet hemocyanin (KLH). This abstract reports a survival follow-up of the phase III trial with emphasis on the subgroup concomitantly treated with hormone therapy. Methods: Metastatic breast cancer patients (MBC pts) who had no evidence of disease or non-progressive disease following any first-line chemotherapy were randomized 1:1 to receive adjuvant plus T or control (C) (adjuvant plus KLH). All pts received a single IV infusion of cyclophosphamide before vaccine. Primary endpoints were time to disease progression (TTP) and overall survival (OS). Pts were stratified by disease status and concomitant hormone therapy (HT). Results: 1028 pts were randomized: 34% received concurrent HT (n = 350). The concomitant treatment in the two treatment arms on hormone therapy (n = 180 T, n = 170 C) consisted mainly of SERMs (43% vs. 39%) and AIs (47% vs. 52%). OS and TTP analyses were performed (table). Conclusions: In pts not concomitantly treated with hormones no difference between T and C was demonstrated. However, HT combined with T indicates a favorable trend based on the current database. Currently, not enough events have been reached to calculate median overall survival for the Theratope arms combined with all hormone modalities, AIs, and SERMs.
Population All HT AIs SERMs
Final analysis T
C T
C T
C
n 180
170 84
88 78
67
Median TTP, mo 8.3
5.8 8.3
5.5 8.4
8.3
Cox P value
0.22
0.30
0.73
Median OS, mo NR
30.7 NR
28.6 NR
NR
Cox P value
N/A
N/A
N/A
NR = not reached at point of submission. N/A = not applicable. An additional event-driven follow-up and analysis is planned for April/May 2004 and will be available at the meeting.
was haltet ihr davon??

mfg versager
Hier noch der Link dazu:
http://www.asco.org/ac/1,1003,_12-002640-00_18-0026-00_19-00…
Wichtig sind die Aussagen morgen. Könnte eine heiße Woche werden. Viel Glück.
http://www.asco.org/ac/1,1003,_12-002640-00_18-0026-00_19-00…
Wichtig sind die Aussagen morgen. Könnte eine heiße Woche werden. Viel Glück.

Upcoming Events
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 - Developmental Therapeutics: Immunotherapy Dr. N. Ibrahim
General Poster Session # 883 - The magnitude of the humoral immune response to naturally occurring STn predicts favorable survival in patients treated with STn-KLH vaccine in a prospective controlled randomized double-blinded multicenter clinical study in stage IV breast cancer patients.
Quelle:
www.biomira.com
June 7, 2004
8:00 AM - 12:00 AM EDT
ASCO - General Poster Session - Room 356 - Developmental Therapeutics: Immunotherapy Dr. N. Ibrahim
General Poster Session # 883 - The magnitude of the humoral immune response to naturally occurring STn predicts favorable survival in patients treated with STn-KLH vaccine in a prospective controlled randomized double-blinded multicenter clinical study in stage IV breast cancer patients.
Quelle:
www.biomira.com
Vielleich doch nicht so schlecht ......
hier die Übersetzung von Altavista:
ASCO - Allgemeiner Plakat-Lernabschnitt - Raum 356 - Entwicklungstherapeutik: Plakat-Lernabschnitt des Immunotherapydr.-N. Ibrahim General # 883 - die Größe der humoralen immunen Antwort zu natürlich vorkommendem STn sagt vorteilhaftes Überleben bei den Patienten voraus, die mit STn-KLH Impfstoff in einer zukünftigen kontrollierten randomisierten doppelt-blind gemachten klinischen Studie des Multicenter bei Stadium IV Brustkrebspatienten behandelt werden.
hier die Übersetzung von Altavista:
ASCO - Allgemeiner Plakat-Lernabschnitt - Raum 356 - Entwicklungstherapeutik: Plakat-Lernabschnitt des Immunotherapydr.-N. Ibrahim General # 883 - die Größe der humoralen immunen Antwort zu natürlich vorkommendem STn sagt vorteilhaftes Überleben bei den Patienten voraus, die mit STn-KLH Impfstoff in einer zukünftigen kontrollierten randomisierten doppelt-blind gemachten klinischen Studie des Multicenter bei Stadium IV Brustkrebspatienten behandelt werden.
Na, wer hätte eine solche Nachricht erwartet? 
Die PR hat ein ganz komisches Timing für so etwas.
Merck KGaA returns Theratope rights to Biomira
Monday June 7, 8:03 am ET
Companies Will Continue Collaboration on BLP25 Liposome Vaccine
EDMONTON, AB, and DARMSTADT, Germany, June 7 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and Merck KGaA of Darmstadt, Germany, announced today that development and commercialization rights to the therapeutic cancer vaccine, Theratope®, will be returned to Biomira. The decision does not impact Merck`s and Biomira`s on-going collaboration to develop BLP25 Liposome Vaccine (L-BLP25) that the Companies are investigating for non-small cell lung cancer.
Merck KGaA decided not to pursue Theratope, which is being developed for the treatment of metastatic breast cancer, because additional trials are likely to be required to support registration and the vaccine, therefore, no longer meets Merck KGaA`s commercial timetable for a near term product launch.
The parties will negotiate the detailed terms and conditions under which the rights will be returned over the next thirty days.
About the Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Merck KGaA is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74% interest and free shareholders own the remaining 26%. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, whether promising or statistically significant results here indicated will be replicated in larger trials which may follow, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA INC. 2011 - 94 St. Edmonton, AB, Canada T6N 1H1
Tel: (780) 450-3761 Fax: (780) 463-0871
http://www.biomira.com

Die PR hat ein ganz komisches Timing für so etwas.
Merck KGaA returns Theratope rights to Biomira
Monday June 7, 8:03 am ET
Companies Will Continue Collaboration on BLP25 Liposome Vaccine
EDMONTON, AB, and DARMSTADT, Germany, June 7 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and Merck KGaA of Darmstadt, Germany, announced today that development and commercialization rights to the therapeutic cancer vaccine, Theratope®, will be returned to Biomira. The decision does not impact Merck`s and Biomira`s on-going collaboration to develop BLP25 Liposome Vaccine (L-BLP25) that the Companies are investigating for non-small cell lung cancer.
Merck KGaA decided not to pursue Theratope, which is being developed for the treatment of metastatic breast cancer, because additional trials are likely to be required to support registration and the vaccine, therefore, no longer meets Merck KGaA`s commercial timetable for a near term product launch.
The parties will negotiate the detailed terms and conditions under which the rights will be returned over the next thirty days.
About the Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Merck KGaA is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74% interest and free shareholders own the remaining 26%. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, whether promising or statistically significant results here indicated will be replicated in larger trials which may follow, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA INC. 2011 - 94 St. Edmonton, AB, Canada T6N 1H1
Tel: (780) 450-3761 Fax: (780) 463-0871
http://www.biomira.com
Das geht ja im Stundentakt.
Endlich mal etwas positives.
Biomira Inc. - Exploratory analysis shows statistically significant survival advantage for women in hormonal therapy subset receiving Theratope(R) vaccine in the Phase III study
Monday June 7, 9:02 am ET
Data One of Two Poster Presentations at 2004 American Society of Clinical Oncology (ASCO) Annual Meeting
EDMONTON, AB, June 7 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) of Edmonton, Alberta, Canada, announced today that an exploratory analysis showed a statistically significant survival advantage for women in the hormonal therapy subset of patients receiving Theratope® vaccine as part of Biomira`s Phase III study of the vaccine in the treatment of women with metastatic breast cancer.
Updated results from the Phase III trial, including the exploratory analysis of the hormonal therapy group of women taking Theratope for treatment of their metastatic breast cancer, were presented in a poster session at the 2004 ASCO annual meeting now underway in New Orleans, June 5-8. Two key areas of data analysis were presented:
1. An updated survival analysis for women receiving hormonal type
therapy at the same time as either Theratope or the control
vaccine, and
2. An analysis of survival based on IgG antibody response to
Theratope. Antibody titres were measured against the following
three factors: STn, KLH (the carrier molecule), and OSM, a
naturally occurring mucin that contains clustered STn side chains.
The overall survival for patients in the hormonal subset (n(equal sign)350) now shows a statistically significant difference between the two treatment arms. Women in the Theratope arm (n (equal sign) 180) survived a median of 36.5 months, while those in the control vaccine arm (n (equal sign) 170) survived a median 3.7 months. The Cox p (equal sign) 0.39. The survival for women not receiving hormonal therapy was not significantly different between the two treatment arms. Analysis to determine a mechanism of action between Theratope and hormonal therapies are currently being conducted.
"We were gratified to see the survival advantage in the exploratory analysis of the pre-stratified subset of women who received hormonal therapy and Theratope," said Alex McPherson, MD, PhD, President and CEO. "While these data are important in understanding our patient population, it would be considered exploratory in nature by the regulatory authorities. Thus, it is highly likely that we will be required to do a subsequent Phase III study in order to move this product to commercialization in the major markets. We are still looking at determining the mechanism of action that resulted in this group of women showing a statistically significant survival advantage, and we plan to have discussions with regulatory agencies once we have a better understanding of the matter."
The ASCO poster presentation also featured survival based on antibody response to Theratope. The presentation detailed that in terms of antibody response, only titres against OSM predicted improved survival. Patients with an anti-OSM response at or above the median level survived longer than those patients whose responses were less than the median (p (equal sign) 0.08). For patients in the hormone subset treated with Theratope, the survival difference between those with anti-OSM responses at or above median and those with less than the median response was statistically significant (41.1 vs 25.4 months, log-rank p (equal sign) 0.01). Survival was not significantly influenced by anti-monomeric STn or anti-KLH response. This data suggests that only an antibody response to OSM was predictive of improved survival.
Theratope Adverse Events
In the Phase III study, Theratope was generally well tolerated. Injection- site ulcerations occurred with similar frequency in the Theratope and control groups.
Collaborative Opportunities
Biomira is actively seeking new collaborators for the continued development of Theratope in metastatic breast cancer for patients undergoing concurrent treatment with hormonal therapy. Mr. Robert Aubrey, Vice President Marketing and Business Development will be discussing Theratope and potential collaborative opportunities for this product candidate at the upcoming Biotechnology Industry Organization meeting in San Francisco. Mr. Aubrey`s discussion, entitled `Biomira BIO Partnering Presentation`, will be presented on June 7th, at 10:45 a.m. PDT.
BLP25 Liposome Vaccine (L-BLP25) Phase II Study in Prostate Cancer
Findings from the L-BLP25 Phase II prostate study were also discussed further as part of a separate poster presentation at the ASCO meeting.
The poster featured data from the L-BLP25 vaccine Phase II study of men with rising prostate specific antigen (PSA) levels following radical prostatectomy, and who had not been treated with hormone therapy. The primary endpoint for this 16-patient study was to determine whether immunotherapy with the vaccine could reduce or stabilize PSA. Study treatment consisted of a single, intravenous dose of cyclophosphamide, followed by eight weekly immunizations with L-BLP25. Maintenance injections were then administered every 6 weeks, for a maximum total of 15 vaccinations. At week eight, 8 of 16 patients had stable PSA. One patient maintained stable PSA through to the end of the study period. Of great interest was the noted prolongation in PSA doubling time (DT) for all but one patient enrolled. In 6 of 16 patients, the DT was prolonged by at least 50 per cent compared to baseline, a result the lead investigator, Dr. Scott North of the Cross Cancer Institute in Edmonton, believes is encouraging. PSA levels will continue to be monitored quarterly for one year following the end of treatment for each patient.
"PSA-DT could be an important prognostic indicator. The literature demonstrates that a short PSA-DT appears to be a surrogate end point for prostate cancer-specific mortality after surgery or radiation therapy, resulting in a statistically significant difference in survival for prostate cancer patients who have a short post-treatment PSA-DT and those who have a prolongation in PSA-DT (Journal of the National Cancer Institute, Vol. 95, No. 18, September 17, 2003, Anthony V. D`Amico, et al). The prolongation of PSA-DT observed in our L-BLP25 study is certainly of interest and is something to keep in mind as a possible clinical endpoint if further clinical testing takes place in this indication," said McPherson.
L-BLP25 Adverse Events
In the prostate study, no events occurred which were severe or precluded further vaccination.
About Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, whether promising or statistically significant results here indicated will be replicated in larger trials which may follow, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA INC. 2011 - 94 St. Edmonton, AB, Canada T6N 1H1
Tel: (780) 450-3761 Fax: (780) 463-0871
http://www.biomira.com
Endlich mal etwas positives.
Biomira Inc. - Exploratory analysis shows statistically significant survival advantage for women in hormonal therapy subset receiving Theratope(R) vaccine in the Phase III study
Monday June 7, 9:02 am ET
Data One of Two Poster Presentations at 2004 American Society of Clinical Oncology (ASCO) Annual Meeting
EDMONTON, AB, June 7 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) of Edmonton, Alberta, Canada, announced today that an exploratory analysis showed a statistically significant survival advantage for women in the hormonal therapy subset of patients receiving Theratope® vaccine as part of Biomira`s Phase III study of the vaccine in the treatment of women with metastatic breast cancer.
Updated results from the Phase III trial, including the exploratory analysis of the hormonal therapy group of women taking Theratope for treatment of their metastatic breast cancer, were presented in a poster session at the 2004 ASCO annual meeting now underway in New Orleans, June 5-8. Two key areas of data analysis were presented:
1. An updated survival analysis for women receiving hormonal type
therapy at the same time as either Theratope or the control
vaccine, and
2. An analysis of survival based on IgG antibody response to
Theratope. Antibody titres were measured against the following
three factors: STn, KLH (the carrier molecule), and OSM, a
naturally occurring mucin that contains clustered STn side chains.
The overall survival for patients in the hormonal subset (n(equal sign)350) now shows a statistically significant difference between the two treatment arms. Women in the Theratope arm (n (equal sign) 180) survived a median of 36.5 months, while those in the control vaccine arm (n (equal sign) 170) survived a median 3.7 months. The Cox p (equal sign) 0.39. The survival for women not receiving hormonal therapy was not significantly different between the two treatment arms. Analysis to determine a mechanism of action between Theratope and hormonal therapies are currently being conducted.
"We were gratified to see the survival advantage in the exploratory analysis of the pre-stratified subset of women who received hormonal therapy and Theratope," said Alex McPherson, MD, PhD, President and CEO. "While these data are important in understanding our patient population, it would be considered exploratory in nature by the regulatory authorities. Thus, it is highly likely that we will be required to do a subsequent Phase III study in order to move this product to commercialization in the major markets. We are still looking at determining the mechanism of action that resulted in this group of women showing a statistically significant survival advantage, and we plan to have discussions with regulatory agencies once we have a better understanding of the matter."
The ASCO poster presentation also featured survival based on antibody response to Theratope. The presentation detailed that in terms of antibody response, only titres against OSM predicted improved survival. Patients with an anti-OSM response at or above the median level survived longer than those patients whose responses were less than the median (p (equal sign) 0.08). For patients in the hormone subset treated with Theratope, the survival difference between those with anti-OSM responses at or above median and those with less than the median response was statistically significant (41.1 vs 25.4 months, log-rank p (equal sign) 0.01). Survival was not significantly influenced by anti-monomeric STn or anti-KLH response. This data suggests that only an antibody response to OSM was predictive of improved survival.
Theratope Adverse Events
In the Phase III study, Theratope was generally well tolerated. Injection- site ulcerations occurred with similar frequency in the Theratope and control groups.
Collaborative Opportunities
Biomira is actively seeking new collaborators for the continued development of Theratope in metastatic breast cancer for patients undergoing concurrent treatment with hormonal therapy. Mr. Robert Aubrey, Vice President Marketing and Business Development will be discussing Theratope and potential collaborative opportunities for this product candidate at the upcoming Biotechnology Industry Organization meeting in San Francisco. Mr. Aubrey`s discussion, entitled `Biomira BIO Partnering Presentation`, will be presented on June 7th, at 10:45 a.m. PDT.
BLP25 Liposome Vaccine (L-BLP25) Phase II Study in Prostate Cancer
Findings from the L-BLP25 Phase II prostate study were also discussed further as part of a separate poster presentation at the ASCO meeting.
The poster featured data from the L-BLP25 vaccine Phase II study of men with rising prostate specific antigen (PSA) levels following radical prostatectomy, and who had not been treated with hormone therapy. The primary endpoint for this 16-patient study was to determine whether immunotherapy with the vaccine could reduce or stabilize PSA. Study treatment consisted of a single, intravenous dose of cyclophosphamide, followed by eight weekly immunizations with L-BLP25. Maintenance injections were then administered every 6 weeks, for a maximum total of 15 vaccinations. At week eight, 8 of 16 patients had stable PSA. One patient maintained stable PSA through to the end of the study period. Of great interest was the noted prolongation in PSA doubling time (DT) for all but one patient enrolled. In 6 of 16 patients, the DT was prolonged by at least 50 per cent compared to baseline, a result the lead investigator, Dr. Scott North of the Cross Cancer Institute in Edmonton, believes is encouraging. PSA levels will continue to be monitored quarterly for one year following the end of treatment for each patient.
"PSA-DT could be an important prognostic indicator. The literature demonstrates that a short PSA-DT appears to be a surrogate end point for prostate cancer-specific mortality after surgery or radiation therapy, resulting in a statistically significant difference in survival for prostate cancer patients who have a short post-treatment PSA-DT and those who have a prolongation in PSA-DT (Journal of the National Cancer Institute, Vol. 95, No. 18, September 17, 2003, Anthony V. D`Amico, et al). The prolongation of PSA-DT observed in our L-BLP25 study is certainly of interest and is something to keep in mind as a possible clinical endpoint if further clinical testing takes place in this indication," said McPherson.
L-BLP25 Adverse Events
In the prostate study, no events occurred which were severe or precluded further vaccination.
About Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, whether promising or statistically significant results here indicated will be replicated in larger trials which may follow, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA INC. 2011 - 94 St. Edmonton, AB, Canada T6N 1H1
Tel: (780) 450-3761 Fax: (780) 463-0871
http://www.biomira.com
Da kommt noch was 10:45 am


Neuer Partner vielleicht?



Neuer Partner vielleicht?

07.06.2004
16:19
Der Darmstädter Pharma- und Spezialchemiekonzern Merck KGaA und das kanadische Biotech-Unternehmen Biomira Inc. einigten sich darauf, dass Merck die Entwicklungs- und Vermarktungsrechte für den Krebsimpfstoff Theratope an Biomira zurückgibt.
Ursache für den jetzigen Rückzug sei die Notwendigkeit weiterer zulassungsrelevanter Studien. Damit erfüllt der Impfstoff für die Behandlung von metastasierendem Brustkrebs nicht mehr die wirtschaftlich orientierte Zeitvorgabe von Merck. Merck hatte die Lizenzrechte an Theratope im März 2001 von Biomira erworben.
Diese Entscheidung betreffe jedoch nicht die laufende Zusammenarbeit von Merck und Biomira bei der Entwicklung von BLP25, einem liposomalen Krebsimpfstoff zur Behandlung des nicht-kleinzelligen Lungenkarzinoms.
Bisher stiegen die Aktien von Merck um 1,0 Prozent und notieren derzeit bei 49,70 Euro.
© finanzen.net
16:19
Der Darmstädter Pharma- und Spezialchemiekonzern Merck KGaA und das kanadische Biotech-Unternehmen Biomira Inc. einigten sich darauf, dass Merck die Entwicklungs- und Vermarktungsrechte für den Krebsimpfstoff Theratope an Biomira zurückgibt.
Ursache für den jetzigen Rückzug sei die Notwendigkeit weiterer zulassungsrelevanter Studien. Damit erfüllt der Impfstoff für die Behandlung von metastasierendem Brustkrebs nicht mehr die wirtschaftlich orientierte Zeitvorgabe von Merck. Merck hatte die Lizenzrechte an Theratope im März 2001 von Biomira erworben.
Diese Entscheidung betreffe jedoch nicht die laufende Zusammenarbeit von Merck und Biomira bei der Entwicklung von BLP25, einem liposomalen Krebsimpfstoff zur Behandlung des nicht-kleinzelligen Lungenkarzinoms.
Bisher stiegen die Aktien von Merck um 1,0 Prozent und notieren derzeit bei 49,70 Euro.
© finanzen.net
Hallo leute,
vor gut 15 Monaten habe ich Biomira hier ins Rollen gebracht!
Damals sehr positiv gestimmt, die Theratope Ergebnisse standen bevor und ich lag ca 250 % vorn;
die weitere Geschichte kennen wir!
habe mich danach sofort verabschiedet und BIOM (nach einigen "fundierten Infos" zu BLP 25)sogar von der wachtlist gestrichen;
die Entscheidung war wohl richtig!
der heutige Merck-Ausstieg (die heute leider einen weiteren Tiefschlag mit Imclone bekanntgeben mußten)läßt greifbaren Erfolg für Biomira in sehr sehr weite Ferne rücken; keine Perspektive, kein Geld, kein Partner in Sicht
Faziz: Sofortiger Ausstieg; Kurse < 1$ bald Realität
Sorry für alle blauäugigen Biomira- Fans;
aber die Zeichen standen schon lange schlecht;
vor gut 15 Monaten habe ich Biomira hier ins Rollen gebracht!
Damals sehr positiv gestimmt, die Theratope Ergebnisse standen bevor und ich lag ca 250 % vorn;
die weitere Geschichte kennen wir!
habe mich danach sofort verabschiedet und BIOM (nach einigen "fundierten Infos" zu BLP 25)sogar von der wachtlist gestrichen;
die Entscheidung war wohl richtig!
der heutige Merck-Ausstieg (die heute leider einen weiteren Tiefschlag mit Imclone bekanntgeben mußten)läßt greifbaren Erfolg für Biomira in sehr sehr weite Ferne rücken; keine Perspektive, kein Geld, kein Partner in Sicht
Faziz: Sofortiger Ausstieg; Kurse < 1$ bald Realität
Sorry für alle blauäugigen Biomira- Fans;
aber die Zeichen standen schon lange schlecht;
Was ist an diesen News so überraschend???
Das steht nun schon lange fest,Theratope wurde vor gut einem Jahr abgeschrieben!!!
Theratope
Ursache für den jetzigen Rückzug sei die Notwendigkeit weiterer zulassungsrelevanter Studien. Damit erfüllt der Impfstoff für die Behandlung von metastasierendem Brustkrebs nicht mehr die wirtschaftlich orientierte Zeitvorgabe von Merck.
Viel mehr interessant ist doch das wir hier eine weitere Bestätigung für BLP25 bekommen!
Diese Entscheidung betreffe jedoch nicht die laufende Zusammenarbeit von Merck und Biomira bei der Entwicklung von BLP25, einem liposomalen Krebsimpfstoff zur Behandlung des nicht-kleinzelligen Lungenkarzinoms.
Fazit:Alles bleibt beim alten und das warten geht weiter!
Das steht nun schon lange fest,Theratope wurde vor gut einem Jahr abgeschrieben!!!
Theratope
Ursache für den jetzigen Rückzug sei die Notwendigkeit weiterer zulassungsrelevanter Studien. Damit erfüllt der Impfstoff für die Behandlung von metastasierendem Brustkrebs nicht mehr die wirtschaftlich orientierte Zeitvorgabe von Merck.
Viel mehr interessant ist doch das wir hier eine weitere Bestätigung für BLP25 bekommen!
Diese Entscheidung betreffe jedoch nicht die laufende Zusammenarbeit von Merck und Biomira bei der Entwicklung von BLP25, einem liposomalen Krebsimpfstoff zur Behandlung des nicht-kleinzelligen Lungenkarzinoms.
Fazit:Alles bleibt beim alten und das warten geht weiter!
#donner
Sehe ich auch so!
Immer diese Zweideutigkeit in den Meldungen.
Kommt mir vor,als ob der Kurs schön gesteuert wird und der grosse Zock erst noch kommt,also long!

Sehe ich auch so!
Immer diese Zweideutigkeit in den Meldungen.
Kommt mir vor,als ob der Kurs schön gesteuert wird und der grosse Zock erst noch kommt,also long!


...VORBÖRSLICH + 8% !!!
Name
Biomira Inc
Last Price
1.6000
Net Change
+0.1300
Shares Matched
19,761
Orders Entered
63
Last Match Time
8:45:43.925
Market
NM
Previous Close
1.4700
Percent Change
+8.84%
Shares Entered
115,228
Open Orders
44
Last Order Time
8:46:44.908
Name
Biomira Inc
Last Price
1.6000
Net Change
+0.1300
Shares Matched
19,761
Orders Entered
63
Last Match Time
8:45:43.925
Market
NM
Previous Close
1.4700
Percent Change
+8.84%
Shares Entered
115,228
Open Orders
44
Last Order Time
8:46:44.908
Kaufempfehlung für Biomira!
Das Teil ist hot!

Das Teil ist hot!

Aus dem Yahoo-Board.
Interview vom 11.06.04
http://www.wallstreetreporter.com/profiles/Biomira.html
Hört sich gut an.
Interview vom 11.06.04
http://www.wallstreetreporter.com/profiles/Biomira.html
Hört sich gut an.

Wer kauft denn da in Deutschland zu diesen Preisen? Wer weiss,wer weiss...
Wer weiss,wer weiss...

 Wer weiss,wer weiss...
Wer weiss,wer weiss...

BID 1,20

 !!!
!!!


 !!!
!!! 
Reuters
UPDATE - Biomira files $100 mln debt, stock shelf offering
Friday June 25, 3:27 pm ET
(Adds stock price, shelf background, details from filing)
WASHINGTON, June 25 (Reuters) - Canadian biotech firm Biomira Inc. (NasdaqNM:BIOM - News; Toronto:BRA.TO - News) filed on Friday with the U.S. Securities and Exchange Commission to periodically sell up to $100 million in debt securities, common and preferred shares, and warrants.
The Edmonton, Alberta-based company said it plans to use the proceeds from the shelf offering for general corporate purposes, including financing growth, human clinical trials and capital spending.
Biomira shares were down 2 cents at $1.34 in afternoon trading on Nasdaq.
Under a shelf registration, a company may sell securities in one or more separate offerings with the size, price and terms to be determined at the time of sale.
UPDATE - Biomira files $100 mln debt, stock shelf offering
Friday June 25, 3:27 pm ET
(Adds stock price, shelf background, details from filing)
WASHINGTON, June 25 (Reuters) - Canadian biotech firm Biomira Inc. (NasdaqNM:BIOM - News; Toronto:BRA.TO - News) filed on Friday with the U.S. Securities and Exchange Commission to periodically sell up to $100 million in debt securities, common and preferred shares, and warrants.
The Edmonton, Alberta-based company said it plans to use the proceeds from the shelf offering for general corporate purposes, including financing growth, human clinical trials and capital spending.
Biomira shares were down 2 cents at $1.34 in afternoon trading on Nasdaq.
Under a shelf registration, a company may sell securities in one or more separate offerings with the size, price and terms to be determined at the time of sale.
Wann gibt BIOMIRA die Unternehmensstrategie für Theratope bekannt?
Wer weiss was?
Greetingx
Vangogo
Wer weiss was?
Greetingx
Vangogo
@vangogo
Wird wohl erst nach dem 07.07. werden. Dann läuft die 30 Tage Frist mit Merck ab (siehe Homepage).
Grüsse
freetibet
Wird wohl erst nach dem 07.07. werden. Dann läuft die 30 Tage Frist mit Merck ab (siehe Homepage).
Grüsse
freetibet
morgen kommen 100 % und mehr
das sieht nach absichtliches runterziehen aus
wenn nicht morgen dann nächste woche
die 1,06 sind schon ne fette nummer nach 2,5
gruß
BIOM---der immer mal nachkauft und sich nicht abschütteln lässt
das sieht nach absichtliches runterziehen aus
wenn nicht morgen dann nächste woche
die 1,06 sind schon ne fette nummer nach 2,5
gruß
BIOM---der immer mal nachkauft und sich nicht abschütteln lässt
Biomira, das kann teuer werden!
Alles Gute!
tupper
Alles Gute!
tupper
@biomira
wenn das so weiter geht heisst es nicht
Biomira user de Jahres sondern Biomira Wi----r des Jahres
Danke
wenn das so weiter geht heisst es nicht
Biomira user de Jahres sondern Biomira Wi----r des Jahres
Danke
Biomira Inc. and Phenomenome Discoveries Inc. announce a collaboration for the discovery of cancer treatment efficacy markers
Monday July 12, 8:02 am ET
EDMONTON, AB and SASKATOON, SK, July 12 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and Phenomenome Discoveries Inc. are pleased to announce the signing of a collaboration agreement whereby Phenomenome Discoveries will perform DISCOVAmetrics(TM) comprehensive metabolome analysis for the purposes of discovering markers for efficacy of cancer treatments.
Metabolomics is the global analysis of small molecules, or metabolites, in biological samples. Phenomenome Discoveries works with pharmaceutical industry leaders to use comprehensive metabolomics technologies for the identification of biomarkers that increase the efficiency and decrease the cost of the drug development process.
"We are excited about the synergies in this collaboration, which will allow us to validate previously discovered cancer biomarkers, while simultaneously providing Biomira with the ability to correlate metabolomic profiles of patients receiving therapeutic interventions with their clinical endpoints," said Shawn Ritchie, PhD, Senior Scientist in Oncology at Phenomenome.
"From Biomira`s perspective, metabolomics shows great potential for shortening clinical trial timelines and reducing the costs related to clinical trials," said Alex McPherson, MD, PhD, President and CEO of Biomira. It is important technology in the identification of cancer markers and this technology has the potential to become an integral piece in the design of future Biomira trials. For instance, it might one day give us the ability to screen patients for a marker that would indicate that they would respond to our therapy."
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Phenomenome Discoveries Inc.
Phenomenome Discoveries Inc. is a privately owned company located in Saskatoon, Saskatchewan, Canada. Processing samples since December 2000, Phenomenome is the first company in the world to offer commercially non- targeted metabolomic investigation of complex biological samples using its proprietary DISCOVAmetrics(TM) metabolite analysis and bioinformatics platform. Phenomenome has in-house and collaborative research programs in human health, pharmacometabolomics, and agriculture.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those concerning speculation on how metabolomics might be applied to the Company`s research and clinical trials, including whether it will reduce the length of such trials, or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Monday July 12, 8:02 am ET
EDMONTON, AB and SASKATOON, SK, July 12 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and Phenomenome Discoveries Inc. are pleased to announce the signing of a collaboration agreement whereby Phenomenome Discoveries will perform DISCOVAmetrics(TM) comprehensive metabolome analysis for the purposes of discovering markers for efficacy of cancer treatments.
Metabolomics is the global analysis of small molecules, or metabolites, in biological samples. Phenomenome Discoveries works with pharmaceutical industry leaders to use comprehensive metabolomics technologies for the identification of biomarkers that increase the efficiency and decrease the cost of the drug development process.
"We are excited about the synergies in this collaboration, which will allow us to validate previously discovered cancer biomarkers, while simultaneously providing Biomira with the ability to correlate metabolomic profiles of patients receiving therapeutic interventions with their clinical endpoints," said Shawn Ritchie, PhD, Senior Scientist in Oncology at Phenomenome.
"From Biomira`s perspective, metabolomics shows great potential for shortening clinical trial timelines and reducing the costs related to clinical trials," said Alex McPherson, MD, PhD, President and CEO of Biomira. It is important technology in the identification of cancer markers and this technology has the potential to become an integral piece in the design of future Biomira trials. For instance, it might one day give us the ability to screen patients for a marker that would indicate that they would respond to our therapy."
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Phenomenome Discoveries Inc.
Phenomenome Discoveries Inc. is a privately owned company located in Saskatoon, Saskatchewan, Canada. Processing samples since December 2000, Phenomenome is the first company in the world to offer commercially non- targeted metabolomic investigation of complex biological samples using its proprietary DISCOVAmetrics(TM) metabolite analysis and bioinformatics platform. Phenomenome has in-house and collaborative research programs in human health, pharmacometabolomics, and agriculture.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those concerning speculation on how metabolomics might be applied to the Company`s research and clinical trials, including whether it will reduce the length of such trials, or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Upcoming Events
2004
July 30, 2004
Edmonton, Alberta Biomira Q2 Financial Press Release
Biomira`s 2nd Quarter Financial Release is scheduled for Friday, July 30th. The release will come out midday following the Biomira Board Meeting.
November 4, 2004
3:15 PM - 3:45 PM EST
Cambridge, MA Phacilitate Vaccine Forum Fall 2004, Dr. Alex McPherson
Dr. McPherson will present a case study on Biomira`s cancer vaccines at this confrence, which is being held at the Hyatt Regency Hotel, Cambridge, MA from November 2-5, 2004.
http://www.biomira.com
2004
July 30, 2004
Edmonton, Alberta Biomira Q2 Financial Press Release
Biomira`s 2nd Quarter Financial Release is scheduled for Friday, July 30th. The release will come out midday following the Biomira Board Meeting.
November 4, 2004
3:15 PM - 3:45 PM EST
Cambridge, MA Phacilitate Vaccine Forum Fall 2004, Dr. Alex McPherson
Dr. McPherson will present a case study on Biomira`s cancer vaccines at this confrence, which is being held at the Hyatt Regency Hotel, Cambridge, MA from November 2-5, 2004.
http://www.biomira.com
Heute in NY im Tagesverlauf auf 0,77 USD gefallen.
Manchmal ist es gut, wenn man die Reissleine zieht.
Manchmal ist es gut, wenn man die Reissleine zieht.
Biomira completes enrolment in Phase II Theratope(R) vaccine study in women with metastatic breast cancer
Tuesday July 27, 7:04 am ET
EDMONTON, July 27 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) of Edmonton, Alberta, Canada, today announced the completion of enrolment in the Phase II Theratope single-arm study treating women with metastatic breast cancer who are also being treated concurrently with aromatase inhibitors, a type of hormonal therapy, or Faslodex® (fulvestrant), an estrogen-receptor antagonist. The trial enrolled 95 women in the United States. Enrolment will remain open until approximately the end of August to allow potential patients now being screened by investigators to be enrolled.
The study`s primary objective is to determine the response of the immune system in these women. Additional endpoints are the safety and tolerability of this combination of treatment. Immunology data is expected to be available in 2005. This study may provide useful information relating to the prestratified subset of hormonal therapy plus Theratope-treated patients in our Phase III metastatic breast cancer trial currently under review.
Biomira recently announced that Merck KGaA of Darmstadt, Germany had returned the rights for development and commercialization of Theratope to Biomira. Biomira is currently seeking a new collaborator in order to potentially further develop this product candidate.
About Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, interpretation and implications of such results, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA INC. 2011 - 94 St. Edmonton, AB, Canada T6N 1H1
Tel: (780) 450-3761 Fax: (780) 463-0871
http://www.biomira.com
Tuesday July 27, 7:04 am ET
EDMONTON, July 27 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) of Edmonton, Alberta, Canada, today announced the completion of enrolment in the Phase II Theratope single-arm study treating women with metastatic breast cancer who are also being treated concurrently with aromatase inhibitors, a type of hormonal therapy, or Faslodex® (fulvestrant), an estrogen-receptor antagonist. The trial enrolled 95 women in the United States. Enrolment will remain open until approximately the end of August to allow potential patients now being screened by investigators to be enrolled.
The study`s primary objective is to determine the response of the immune system in these women. Additional endpoints are the safety and tolerability of this combination of treatment. Immunology data is expected to be available in 2005. This study may provide useful information relating to the prestratified subset of hormonal therapy plus Theratope-treated patients in our Phase III metastatic breast cancer trial currently under review.
Biomira recently announced that Merck KGaA of Darmstadt, Germany had returned the rights for development and commercialization of Theratope to Biomira. Biomira is currently seeking a new collaborator in order to potentially further develop this product candidate.
About Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, interpretation and implications of such results, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA INC. 2011 - 94 St. Edmonton, AB, Canada T6N 1H1
Tel: (780) 450-3761 Fax: (780) 463-0871
http://www.biomira.com
was issn nu mit dem teil ?
erst ein absturz ins bodenlose (-60%) in den letzten wochen, und heute der hype mit +25%.
habe ich da was verpasst ?
gibt es news ?
werden meine shares wieder etwas wert ?
(immerhin habe ich einen EK von 1,94)
wg (, der die hoffnung nicht aufgibt.)
erst ein absturz ins bodenlose (-60%) in den letzten wochen, und heute der hype mit +25%.
habe ich da was verpasst ?
gibt es news ?
werden meine shares wieder etwas wert ?
(immerhin habe ich einen EK von 1,94)
wg (, der die hoffnung nicht aufgibt.)
Biomira collaborator, Prima BioMed commences Phase II ovarian cancer trial
Thursday July 29, 8:08 am ET
EDMONTON, July 29 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) of Edmonton, Alberta, Canada, today announced that Prima BioMed Ltd`s (`Prima`: ASX PRR) subsidiary, CancerVac commenced a Phase II trial of its immunotherapy technology in patients with progressive ovarian cancer. In March 2004, Biomira announced a licensing agreement allowing access by CancerVac to Biomira`s licensed exclusive worldwide rights to the MUC1 protein in relation to CancerVac`s Mannan fusion protein therapeutic vaccine being used in the Phase II study. The Biomira MUC1 patent portfolio includes certain rights to patents held by Cancer Research Technology Limited (CRTL) of London, UK, which are essential for the development and commercialization of CancerVac`s Mannan-MUC1 fusion protein used for cancer immunotherapy.
CancerVac has developed an immunotherapy that utilizes the patient`s own dendritic cells treated ex-vivo to stimulate a cellular immune response following re-injection of the cells into the patient. The patients are expected to receive seven treatments over a 12-month period during which clinical investigators will assess the tumour by the level of CA-125 in the blood, a sensitive measure of tumour size. The trial is expected to recruit up to 20 ovarian cancer patients.
In partial consideration for the license rights provided by Biomira to CancerVac, Biomira acquired a 10 per cent equity stake in CancerVac, and a seat on the Board of CancerVac.
About Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
About Prima BioMed Ltd
Based in Melbourne, Prima BioMed (ASX: PRR - News) is a biotechnology organization with first and last rights over technologies from the Austin Research Institute. Prima BioMed specializes in immunology and cancer immunotherapy and adopts technology development that shows potential for commercial returns within three years.
About CancerVac Pty. Ltd.
CancerVac Pty Ltd. CancerVac is a subsidiary of Prima BioMed. The company was formed to develop and commercialize technology licensed from the Austin Research Institute, a medical research institute located in Melbourne Australia. The technology being developed is described as immunotherapy. It combines recombinant proteins expressed on tumor cells and a vaccine adjuvant to trigger recognition of tumor cells by the immune system as foreign, such recognition in turn leading to attack by immune killer and tumor cell destruction.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, interpretation and implications of such results, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
Thursday July 29, 8:08 am ET
EDMONTON, July 29 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) of Edmonton, Alberta, Canada, today announced that Prima BioMed Ltd`s (`Prima`: ASX PRR) subsidiary, CancerVac commenced a Phase II trial of its immunotherapy technology in patients with progressive ovarian cancer. In March 2004, Biomira announced a licensing agreement allowing access by CancerVac to Biomira`s licensed exclusive worldwide rights to the MUC1 protein in relation to CancerVac`s Mannan fusion protein therapeutic vaccine being used in the Phase II study. The Biomira MUC1 patent portfolio includes certain rights to patents held by Cancer Research Technology Limited (CRTL) of London, UK, which are essential for the development and commercialization of CancerVac`s Mannan-MUC1 fusion protein used for cancer immunotherapy.
CancerVac has developed an immunotherapy that utilizes the patient`s own dendritic cells treated ex-vivo to stimulate a cellular immune response following re-injection of the cells into the patient. The patients are expected to receive seven treatments over a 12-month period during which clinical investigators will assess the tumour by the level of CA-125 in the blood, a sensitive measure of tumour size. The trial is expected to recruit up to 20 ovarian cancer patients.
In partial consideration for the license rights provided by Biomira to CancerVac, Biomira acquired a 10 per cent equity stake in CancerVac, and a seat on the Board of CancerVac.
About Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of vaccines containing synthetic antigens and novel strategies for cancer immunotherapy.
About Prima BioMed Ltd
Based in Melbourne, Prima BioMed (ASX: PRR - News) is a biotechnology organization with first and last rights over technologies from the Austin Research Institute. Prima BioMed specializes in immunology and cancer immunotherapy and adopts technology development that shows potential for commercial returns within three years.
About CancerVac Pty. Ltd.
CancerVac Pty Ltd. CancerVac is a subsidiary of Prima BioMed. The company was formed to develop and commercialize technology licensed from the Austin Research Institute, a medical research institute located in Melbourne Australia. The technology being developed is described as immunotherapy. It combines recombinant proteins expressed on tumor cells and a vaccine adjuvant to trigger recognition of tumor cells by the immune system as foreign, such recognition in turn leading to attack by immune killer and tumor cell destruction.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, interpretation and implications of such results, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.
@Freetibet
In der Vergangenheit wurden immer wieder Meldungen in Englisch gebracht, so wie auch jetzt.
Also vielen Dank für den Beitrag...
aber ich und vielleicht auch andere, sind nicht so fitt im englischen. Wäre in diesen Fällen dankbar, wenn der Autor eine kurze Übersetzung, oder Schlußfolgerung, mitliefern könnte
In der Vergangenheit wurden immer wieder Meldungen in Englisch gebracht, so wie auch jetzt.
Also vielen Dank für den Beitrag...
aber ich und vielleicht auch andere, sind nicht so fitt im englischen. Wäre in diesen Fällen dankbar, wenn der Autor eine kurze Übersetzung, oder Schlußfolgerung, mitliefern könnte
Biomira Inc. announces 2nd quarter results
Friday July 30, 12:50 pm ET
EDMONTON, AB, July 30 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) today reported financial results for the six months ended June 30, 2004.
Corporate Synopsis
------------------
A synopsis of the corporate news for the quarter is below and should be read in conjunction with the full disclosure included in this release:
- BLP25 Liposome Vaccine (L-BLP25):
- Biomira and Merck KGaA of Darmstadt, Germany, are planning various
regulatory agency discussions to discuss potential confirmatory
clinical trial design.
- The Companies are looking at potential opportunities for earlier
registration based on current data from Phase IIb non-small cell
lung cancer (NSCLC) study.
- Next analysis of Phase IIb NSCLC data according to protocol
expected end 2004.
- Theratope(R) Vaccine:
- Merck KGaA returned all development and commercialization rights
to Biomira.
- Exploratory analysis of Phase III Theratope hormonal therapy
subset of women now shows statistical significance in favour of
vaccine patients.
- Phase II single-arm study with Theratope plus anti-cancer hormonal
therapy completes enrolment in 95-patient study. Immunology data
expected in 2005.
- Development plans underway for potential confirmatory study.
- Small clinical experience study to incorporate improvements made
in manufacturing planned for the first half of 2005. Study not
expected to impede start of potential confirmatory study.
- Plans for discussions with various regulatory agencies ongoing.
- Biomira seeking collaborative partner to further develop
Theratope.
- Liposomal-IL-2: Spin-off company, Oncodigm BioPharma Inc. formed to
allow product candidate to re-enter clinical trials, likely in 2005.
- Prima BioMed: Prima BioMed and subsidiary, CancerVac Pty Ltd. of
Melbourne, Australia, commence Phase II ovarian cancer study using
Biomira`s licensed MUC-1 protein in CancerVac`s Mannan MUC-1 Fusion
Protein (MFP) therapeutic vaccine.
Financial Update
----------------
Financial results for the six months ended June 30, 2004 reflect a consolidated net loss from operations of $3.8 million or $0.05 per share compared to $9.9 million or $0.18 per share for the same period in 2003. The decreased loss of $6.1 million in 2004 arises from higher revenues of $5.4 million, lower research and development expenditures of $1.4 million and higher investment and other income of $0.4 million, offset by stock compensation expense of $0.6 million and higher general and administrative expenses of $0.5 million. The increased revenues result from licensing revenues recognized in the current period as a result of the recognition into income of the remaining deferred revenue balance related to Theratope due to the return of Theratope development and commercialization rights by Merck KGaA announced in June 2004.
Contract research and development revenue for the six months ended June 30, 2004, totalling $0.8 million compared to $1.5 million for the same period in 2003, represents contract research and development funding received from Merck KGaA associated with Theratope and L-BLP25. The decreased funding reflects a lower level of clinical activity with the wind down of the Theratope Phase III trial, and unblinding of the L-BLP25 Phase IIb trial results. Licensing revenues from collaborative arrangements for the six months ended June 30, 2004, totalling $6.4 million compared to $0.5 million for the same period in 2003, represents the amortization of upfront payments received from Merck KGaA and upfront sub-licensing fee from CancerVac upon commencement of the respective collaborations. The current period includes an addition to income of $5.9 million representing the recognition into income of the remaining deferred revenue balance from Merck KGaA related to Theratope. Finally, the increase of $0.2 million in licensing, royalties and other revenue relates to contract manufacturing activities utilizing various Biomira patented technologies and compounds for external customers.
Research and development expenditures for the six months ended June 30, 2004 totalled $7.0 million compared to $8.4 million for the same period in 2003. The decrease in research and development expenditures, which determines the amount of collaborative funding revenue, is similarly attributable to winding down of clinical activities. General and administrative expenses for the six months ended June 30, 2004 totalled $3.4 million compared to $2.8 million for the same period in 2003. The increase of $0.6 million stems largely from incremental costs related to the settlement of an outstanding litigation in the first quarter. Marketing and business development expenditures for the six months ended June 30, 2004 of $0.8 million were similar for the same period in 2003.
Stock compensation expense of $0.6 million for the six months ended June 30, 2004 represents the amortization of the estimated fair value of options granted since January 1, 2002 applicable to the current period. The retroactive application of CICA Handbook Section 3870 with respect to recognition of stock compensation expense for 2002 and 2003 resulted in a $1.6 million charge to opening deficit.
Investment and other income for the six months ended June 30, 2004, totalling $0.7 million compared to $0.3 million for the same period in 2003, comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. The increase is mainly due to a net foreign exchange gain of $0.3 million for the six months ended June 30, 2004 compared to a net foreign exchange loss of $0.4 million for the same period in 2003, offset by lower investment income from cash and investments of $0.3 million for the six months ended June 30, 2004 as a result of lower average cash and investment balances.
Biomira`s financial reserves total $30.7 million in cash and short-term investments as at June 30, 2004, a decrease of $10.8 million from the year end position due to funding of operations.
Corporate Update
----------------
L-BLP25
On April 2, 2004, Biomira and Merck KGaA publicly announced via news release preliminary results from the Phase IIb study of L-BLP25 in NSCLC. The Companies were encouraged by the survival data from the randomized Phase IIb study of 171 men and women with stage IIIB or IV NSCLC. The Companies intend to have discussions with regulatory agencies in various jurisdictions to discuss the design of a possible confirmatory clinical trial for this product candidate in NSCLC. The Companies will also look at potential opportunities for earlier registration for this product candidate based on the current data. As part of the Phase IIb protocol, another analysis is expected at the end of 2004.
Patients with locoregional disease (IIIA and IIIB) represent a very large unmet market opportunity with approximately 50,000 new cases in the U.S. each year. Lung cancer incidence continues to grow each year, especially in women. Lung cancer has grown to be the number one cause of death in women among all types of cancer. A confirmatory study would likely be required prior to approval in the U.S., Europe and Japan.
Theratope
Biomira recently announced that Merck KGaA had returned the rights for development and commercialization of Theratope. This decision by Merck KGaA was based on the fact that additional trials in metastatic breast cancer will likely be required in the U.S., Europe and Japan to support a registration and the vaccine, therefore, no longer meets Merck`s commercial timetable for a near-term product launch. This decision does not impact the Companies ongoing collaboration to develop L-BLP25 for NSCLC.
Under the terms and conditions for return of the rights to Theratope, Biomira has regained all commercial rights to Theratope with no compensation being paid to Merck KGaA. Merck KGaA will continue to share the ongoing development costs with Biomira through June 30, 2004, and the Companies are continuing negotiations to assure a smooth transition for the development program.
Biomira will assume control of the Phase II single-arm Theratope study, where women with metastatic breast cancer are being treated with Theratope plus anti-cancer hormonal therapy. The trial recently completed enrolment and patients are being monitored. The study`s primary objective is to determine the antibody response generated to STn in these women. A secondary objective is to determine the safety and tolerability of Theratope when used in conjunction with aromatase inhibitors or fulvestrant. Immunology data from the trial should be available in 2005. This study may provide useful information relating to the prestratified subset of hormonal therapy plus Theratope-related patients in our Phase III metastatic breast cancer trial currently under review.
A confirmatory study in metastatic breast cancer will probably be required prior to commercialization in the U.S., Europe and Japan. In parallel to development plans for the potential confirmatory study, a small clinical experience study is now being planned to incorporate manufacturing improvements. The trial is expected to commence in the first half of 2005 and would not be expected to negatively impact timelines of a probable confirmatory study. While the Company seeks a collaborative partner to develop Theratope further it continues to explore the mechanism of action for Theratope and also hopes to know later this year about possible opportunities in other countries for early registration based on the current data prior to completion of a confirmatory trial.
In June 2004, at the American Society of Clinical Oncology (ASCO) meeting, a poster was presented showing that in an exploratory analysis, the survival advantage for women in the hormonal therapy subset of patients receiving Theratope as part of the Phase III metastatic breast cancer study, had now reached statistical significance. Women in the Theratope arm (n(equal sign)180) survived a median of 36.5 months, while those in the control vaccine arm (n(equal sign)170) survived a median of 30.7 months (Cox p - 0.039). The survival for women not receiving hormonal therapy was not significantly different between the two arms. Approximately 40 per cent of women with metastatic breast cancer now receive hormonal therapy as part of their treatment regimen.
Biomira and Inno-centre Alberta Create Spin-Off Company
In the second quarter, Biomira entered into a collaborative agreement to create a spin-off company that would allow for the further development of Liposomal Interleukin-2 (L-IL-2) technology. The new Company, Oncodigm BioPharma Inc. will be dedicated to the development and commercialization of this promising cancer therapy. L-IL-2 is expected to re-enter clinical trials in 2005.
The new Company is 90 per cent owned by Biomira and 10 per cent owned by Inno-centre Alberta. Oncodigm BioPharma will be responsible for raising its initial venture capital to return the product candidate to clinical trials, allowing Biomira to remain focused on its two lead product candidates.
CancerVac Phase II Ovarian Cancer Study
In the first quarter of this year, Biomira announced a collaboration with Prima BioMed of Melbourne, Australia and their subsidiary CancerVac Pty Ltd. The collaboration concerns CancerVac`s Mannan-MUC 1 Fusion Protein (MFP) therapeutic vaccine.
CancerVac received ethics approval to commence their 20-patient Phase II ovarian cancer study in June and the trial enrolled its first patient in July. The trial is expected to be fully enrolled by the end of the third quarter 2005.
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Friday July 30, 12:50 pm ET
EDMONTON, AB, July 30 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) today reported financial results for the six months ended June 30, 2004.
Corporate Synopsis
------------------
A synopsis of the corporate news for the quarter is below and should be read in conjunction with the full disclosure included in this release:
- BLP25 Liposome Vaccine (L-BLP25):
- Biomira and Merck KGaA of Darmstadt, Germany, are planning various
regulatory agency discussions to discuss potential confirmatory
clinical trial design.
- The Companies are looking at potential opportunities for earlier
registration based on current data from Phase IIb non-small cell
lung cancer (NSCLC) study.
- Next analysis of Phase IIb NSCLC data according to protocol
expected end 2004.
- Theratope(R) Vaccine:
- Merck KGaA returned all development and commercialization rights
to Biomira.
- Exploratory analysis of Phase III Theratope hormonal therapy
subset of women now shows statistical significance in favour of
vaccine patients.
- Phase II single-arm study with Theratope plus anti-cancer hormonal
therapy completes enrolment in 95-patient study. Immunology data
expected in 2005.
- Development plans underway for potential confirmatory study.
- Small clinical experience study to incorporate improvements made
in manufacturing planned for the first half of 2005. Study not
expected to impede start of potential confirmatory study.
- Plans for discussions with various regulatory agencies ongoing.
- Biomira seeking collaborative partner to further develop
Theratope.
- Liposomal-IL-2: Spin-off company, Oncodigm BioPharma Inc. formed to
allow product candidate to re-enter clinical trials, likely in 2005.
- Prima BioMed: Prima BioMed and subsidiary, CancerVac Pty Ltd. of
Melbourne, Australia, commence Phase II ovarian cancer study using
Biomira`s licensed MUC-1 protein in CancerVac`s Mannan MUC-1 Fusion
Protein (MFP) therapeutic vaccine.
Financial Update
----------------
Financial results for the six months ended June 30, 2004 reflect a consolidated net loss from operations of $3.8 million or $0.05 per share compared to $9.9 million or $0.18 per share for the same period in 2003. The decreased loss of $6.1 million in 2004 arises from higher revenues of $5.4 million, lower research and development expenditures of $1.4 million and higher investment and other income of $0.4 million, offset by stock compensation expense of $0.6 million and higher general and administrative expenses of $0.5 million. The increased revenues result from licensing revenues recognized in the current period as a result of the recognition into income of the remaining deferred revenue balance related to Theratope due to the return of Theratope development and commercialization rights by Merck KGaA announced in June 2004.
Contract research and development revenue for the six months ended June 30, 2004, totalling $0.8 million compared to $1.5 million for the same period in 2003, represents contract research and development funding received from Merck KGaA associated with Theratope and L-BLP25. The decreased funding reflects a lower level of clinical activity with the wind down of the Theratope Phase III trial, and unblinding of the L-BLP25 Phase IIb trial results. Licensing revenues from collaborative arrangements for the six months ended June 30, 2004, totalling $6.4 million compared to $0.5 million for the same period in 2003, represents the amortization of upfront payments received from Merck KGaA and upfront sub-licensing fee from CancerVac upon commencement of the respective collaborations. The current period includes an addition to income of $5.9 million representing the recognition into income of the remaining deferred revenue balance from Merck KGaA related to Theratope. Finally, the increase of $0.2 million in licensing, royalties and other revenue relates to contract manufacturing activities utilizing various Biomira patented technologies and compounds for external customers.
Research and development expenditures for the six months ended June 30, 2004 totalled $7.0 million compared to $8.4 million for the same period in 2003. The decrease in research and development expenditures, which determines the amount of collaborative funding revenue, is similarly attributable to winding down of clinical activities. General and administrative expenses for the six months ended June 30, 2004 totalled $3.4 million compared to $2.8 million for the same period in 2003. The increase of $0.6 million stems largely from incremental costs related to the settlement of an outstanding litigation in the first quarter. Marketing and business development expenditures for the six months ended June 30, 2004 of $0.8 million were similar for the same period in 2003.
Stock compensation expense of $0.6 million for the six months ended June 30, 2004 represents the amortization of the estimated fair value of options granted since January 1, 2002 applicable to the current period. The retroactive application of CICA Handbook Section 3870 with respect to recognition of stock compensation expense for 2002 and 2003 resulted in a $1.6 million charge to opening deficit.
Investment and other income for the six months ended June 30, 2004, totalling $0.7 million compared to $0.3 million for the same period in 2003, comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. The increase is mainly due to a net foreign exchange gain of $0.3 million for the six months ended June 30, 2004 compared to a net foreign exchange loss of $0.4 million for the same period in 2003, offset by lower investment income from cash and investments of $0.3 million for the six months ended June 30, 2004 as a result of lower average cash and investment balances.
Biomira`s financial reserves total $30.7 million in cash and short-term investments as at June 30, 2004, a decrease of $10.8 million from the year end position due to funding of operations.
Corporate Update
----------------
L-BLP25
On April 2, 2004, Biomira and Merck KGaA publicly announced via news release preliminary results from the Phase IIb study of L-BLP25 in NSCLC. The Companies were encouraged by the survival data from the randomized Phase IIb study of 171 men and women with stage IIIB or IV NSCLC. The Companies intend to have discussions with regulatory agencies in various jurisdictions to discuss the design of a possible confirmatory clinical trial for this product candidate in NSCLC. The Companies will also look at potential opportunities for earlier registration for this product candidate based on the current data. As part of the Phase IIb protocol, another analysis is expected at the end of 2004.
Patients with locoregional disease (IIIA and IIIB) represent a very large unmet market opportunity with approximately 50,000 new cases in the U.S. each year. Lung cancer incidence continues to grow each year, especially in women. Lung cancer has grown to be the number one cause of death in women among all types of cancer. A confirmatory study would likely be required prior to approval in the U.S., Europe and Japan.
Theratope
Biomira recently announced that Merck KGaA had returned the rights for development and commercialization of Theratope. This decision by Merck KGaA was based on the fact that additional trials in metastatic breast cancer will likely be required in the U.S., Europe and Japan to support a registration and the vaccine, therefore, no longer meets Merck`s commercial timetable for a near-term product launch. This decision does not impact the Companies ongoing collaboration to develop L-BLP25 for NSCLC.
Under the terms and conditions for return of the rights to Theratope, Biomira has regained all commercial rights to Theratope with no compensation being paid to Merck KGaA. Merck KGaA will continue to share the ongoing development costs with Biomira through June 30, 2004, and the Companies are continuing negotiations to assure a smooth transition for the development program.
Biomira will assume control of the Phase II single-arm Theratope study, where women with metastatic breast cancer are being treated with Theratope plus anti-cancer hormonal therapy. The trial recently completed enrolment and patients are being monitored. The study`s primary objective is to determine the antibody response generated to STn in these women. A secondary objective is to determine the safety and tolerability of Theratope when used in conjunction with aromatase inhibitors or fulvestrant. Immunology data from the trial should be available in 2005. This study may provide useful information relating to the prestratified subset of hormonal therapy plus Theratope-related patients in our Phase III metastatic breast cancer trial currently under review.
A confirmatory study in metastatic breast cancer will probably be required prior to commercialization in the U.S., Europe and Japan. In parallel to development plans for the potential confirmatory study, a small clinical experience study is now being planned to incorporate manufacturing improvements. The trial is expected to commence in the first half of 2005 and would not be expected to negatively impact timelines of a probable confirmatory study. While the Company seeks a collaborative partner to develop Theratope further it continues to explore the mechanism of action for Theratope and also hopes to know later this year about possible opportunities in other countries for early registration based on the current data prior to completion of a confirmatory trial.
In June 2004, at the American Society of Clinical Oncology (ASCO) meeting, a poster was presented showing that in an exploratory analysis, the survival advantage for women in the hormonal therapy subset of patients receiving Theratope as part of the Phase III metastatic breast cancer study, had now reached statistical significance. Women in the Theratope arm (n(equal sign)180) survived a median of 36.5 months, while those in the control vaccine arm (n(equal sign)170) survived a median of 30.7 months (Cox p - 0.039). The survival for women not receiving hormonal therapy was not significantly different between the two arms. Approximately 40 per cent of women with metastatic breast cancer now receive hormonal therapy as part of their treatment regimen.
Biomira and Inno-centre Alberta Create Spin-Off Company
In the second quarter, Biomira entered into a collaborative agreement to create a spin-off company that would allow for the further development of Liposomal Interleukin-2 (L-IL-2) technology. The new Company, Oncodigm BioPharma Inc. will be dedicated to the development and commercialization of this promising cancer therapy. L-IL-2 is expected to re-enter clinical trials in 2005.
The new Company is 90 per cent owned by Biomira and 10 per cent owned by Inno-centre Alberta. Oncodigm BioPharma will be responsible for raising its initial venture capital to return the product candidate to clinical trials, allowing Biomira to remain focused on its two lead product candidates.
CancerVac Phase II Ovarian Cancer Study
In the first quarter of this year, Biomira announced a collaboration with Prima BioMed of Melbourne, Australia and their subsidiary CancerVac Pty Ltd. The collaboration concerns CancerVac`s Mannan-MUC 1 Fusion Protein (MFP) therapeutic vaccine.
CancerVac received ethics approval to commence their 20-patient Phase II ovarian cancer study in June and the trial enrolled its first patient in July. The trial is expected to be fully enrolled by the end of the third quarter 2005.
Biomira Inc.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
@BULLUS
Also ich halte Biomira, weil ich vom Produkt BLP25 überzeugt bin und hier eine große Zukunft liegt, nicht nur für die Aktie.
Meiner Meinung nach haben wir es mit einer guten Firma und einer schlechten PR zu tun.
Die verstehen sich wahrscheinlich mehr als Forschungsstätte, denn als Aktiengesellschaft.
Aber trotz alledem, wenn die Zulassung gemeldet wird...
Ich bin auch nicht der große Englischübersetzer.
Und sinngemäß wiedergeben liegt mir nicht.
Du kannst aber http://systran.heisoft.de benutzen. Ist ganz gut.
Hier eine Übersetzung des oberen, wichtigeren, Abschnitts:
Eine Synopse der korporativen Nachrichten für das Viertel ist unten
und sollte in Verbindung mit der vollen Freigabe gelesen werden, die
in dieser Freigabe eingeschlossen ist:
- Impfstoff Des Liposom-BLP25 (L-BLP25): - Biomira und Merck KGaA von
Darmstadt, Deutschland, planen verschiedene
Aufsichtsbehördediskussionen, um mögliches bestätigendes klinisches
Probedesign zu besprechen. - die Firmen betrachten mögliche
Gelegenheiten nach der früheren Ausrichtung, die auf gegenwärtigen
Daten basiert Studie des Phase IIb von der nicht-kleinen Zelle
Lungenkrebses (NSCLC). - folgende Analyse von Phase IIb NSCLC Daten
entsprechend Protokoll erwartete Ende 2004.
- Theratope(R) Impfstoff: - Merck KGaA brachte alle Entwicklung und
Kommerzialisierungrechte zu Biomira zurück. - forschende Analyse
Phase III Theratope der hormonalen Therapieteilmenge Frauen zeigt
jetzt statistische Bedeutung zugunsten der vaccine Patienten. - Phase
II Einzelnarm Studie mit Theratope plus krebsbekämpfende hormonale
Therapie führt Einschreibung in der Studie 95-patient durch.
Immunitätsforschungdaten erwartet 2005. - Entwicklung Pläne
unterwegs für mögliche bestätigende Studie. - die kleine klinische
Erfahrung Studie, zum der Verbesserungen zu enthalten, die in der
Herstellung gebildet wurden, plante für die erste Hälfte von 2005.
Studie nicht erwartet, um Anfang der möglichen bestätigenden Studie
zu behindern. - Pläne für Diskussionen mit den verschiedenen
Aufsichtsbehörden fortwährend. - Biomira, das gemeinschaftlichen
Partner sucht, um Theratope weiter zu entwickeln.
- Liposomal-IL-2: Zweitfirma, Oncodigm BioPharma Inc. bildete sich, um
Produktanwärter zu erlauben, die klinischen Versuche wieder
einzutragen, die 2005 wahrscheinlich sind.
- Prima BioMed: Prima BioMed und Tochtergesellschaft, CancerVac Pty
Ltd. von Melbourne, Australien, beginnen Phase II ovarian Krebsstudie
mit Biomiras genehmigtem Protein MUC-1 Schmelzverfahren des Proteins
CancerVacs des Mannan-MUC-1 im therapeutischen Impfstoff (MFP).
Also ich halte Biomira, weil ich vom Produkt BLP25 überzeugt bin und hier eine große Zukunft liegt, nicht nur für die Aktie.
Meiner Meinung nach haben wir es mit einer guten Firma und einer schlechten PR zu tun.
Die verstehen sich wahrscheinlich mehr als Forschungsstätte, denn als Aktiengesellschaft.
Aber trotz alledem, wenn die Zulassung gemeldet wird...

Ich bin auch nicht der große Englischübersetzer.
Und sinngemäß wiedergeben liegt mir nicht.

Du kannst aber http://systran.heisoft.de benutzen. Ist ganz gut.
Hier eine Übersetzung des oberen, wichtigeren, Abschnitts:
Eine Synopse der korporativen Nachrichten für das Viertel ist unten
und sollte in Verbindung mit der vollen Freigabe gelesen werden, die
in dieser Freigabe eingeschlossen ist:
- Impfstoff Des Liposom-BLP25 (L-BLP25): - Biomira und Merck KGaA von
Darmstadt, Deutschland, planen verschiedene
Aufsichtsbehördediskussionen, um mögliches bestätigendes klinisches
Probedesign zu besprechen. - die Firmen betrachten mögliche
Gelegenheiten nach der früheren Ausrichtung, die auf gegenwärtigen
Daten basiert Studie des Phase IIb von der nicht-kleinen Zelle
Lungenkrebses (NSCLC). - folgende Analyse von Phase IIb NSCLC Daten
entsprechend Protokoll erwartete Ende 2004.
- Theratope(R) Impfstoff: - Merck KGaA brachte alle Entwicklung und
Kommerzialisierungrechte zu Biomira zurück. - forschende Analyse
Phase III Theratope der hormonalen Therapieteilmenge Frauen zeigt
jetzt statistische Bedeutung zugunsten der vaccine Patienten. - Phase
II Einzelnarm Studie mit Theratope plus krebsbekämpfende hormonale
Therapie führt Einschreibung in der Studie 95-patient durch.
Immunitätsforschungdaten erwartet 2005. - Entwicklung Pläne
unterwegs für mögliche bestätigende Studie. - die kleine klinische
Erfahrung Studie, zum der Verbesserungen zu enthalten, die in der
Herstellung gebildet wurden, plante für die erste Hälfte von 2005.
Studie nicht erwartet, um Anfang der möglichen bestätigenden Studie
zu behindern. - Pläne für Diskussionen mit den verschiedenen
Aufsichtsbehörden fortwährend. - Biomira, das gemeinschaftlichen
Partner sucht, um Theratope weiter zu entwickeln.
- Liposomal-IL-2: Zweitfirma, Oncodigm BioPharma Inc. bildete sich, um
Produktanwärter zu erlauben, die klinischen Versuche wieder
einzutragen, die 2005 wahrscheinlich sind.
- Prima BioMed: Prima BioMed und Tochtergesellschaft, CancerVac Pty
Ltd. von Melbourne, Australien, beginnen Phase II ovarian Krebsstudie
mit Biomiras genehmigtem Protein MUC-1 Schmelzverfahren des Proteins
CancerVacs des Mannan-MUC-1 im therapeutischen Impfstoff (MFP).
Der Kurs ist uninteressant das Handelsvolumen zu gering, nachkäufe erst bei steigenden Volumen setzten!

@Donner
Aus Spiegel Nr 32 Seite 76: Munich Biotech Insolvenzantrag! Ich weiß nicht ob du den Artikel gelesen hast? Da diese Firma auch bei ähnlichen Mitteln forschte und wohl durch ein "Gerücht" in die Insovenz gezwungwn worden ist, frage ich den Experten "Donner", kann es da Zusammenhänge geben, mit Biomira? Mir ist nach wie vor ein Rätsel, warum Merk sich zurückgezogen hat?
 Peter
Peter

Aus Spiegel Nr 32 Seite 76: Munich Biotech Insolvenzantrag! Ich weiß nicht ob du den Artikel gelesen hast? Da diese Firma auch bei ähnlichen Mitteln forschte und wohl durch ein "Gerücht" in die Insovenz gezwungwn worden ist, frage ich den Experten "Donner", kann es da Zusammenhänge geben, mit Biomira? Mir ist nach wie vor ein Rätsel, warum Merk sich zurückgezogen hat?
 Peter
Peter
Peter
dann rätsel du mal schön weiter und schau zu dass es dir privat nicht auch so ergeht.
Obwohl vom rätseln wird man weder reich noch arm.
Rätsel weiter lieber Leser
dann rätsel du mal schön weiter und schau zu dass es dir privat nicht auch so ergeht.
Obwohl vom rätseln wird man weder reich noch arm.
Rätsel weiter lieber Leser
Peter
dann rätsel du mal schön weiter und schau zu dass es dir privat nicht auch so ergeht.
Obwohl vom rätseln wird man weder reich noch arm.
Rätsel weiter lieber Leser
Ein sehr gutes Posting
dann rätsel du mal schön weiter und schau zu dass es dir privat nicht auch so ergeht.
Obwohl vom rätseln wird man weder reich noch arm.
Rätsel weiter lieber Leser
Ein sehr gutes Posting

@Peter
Es gibt hier überhaupt kein Zusammenhang,
Merck hält sich zurück weil Biomira die Forschungen durchführt ,Merck ist hier als Investor zu sehen der sich Lizenzen für Europa, bei einer eventuellen Einführung von BLP25 durch die FDA gesichert hat!
Aktueller Kurs gibt nicht bekannt auf welchen Kurs BLP25 zur Zeit ist!
Der Handel ist zu gering ,die letzten Daten von Blp25 waren zuversichtlich,die Aktie kann bei jeder positiven Nachricht
wie in Vergangeheit schon oft gesehen ausbrechen, unterschied könnte diesmal sein das wir hier endlich mal Entscheidende Fakten zu Tage kommen die auf ein positiven Ende der Versuche mit Blp25 deuten!
Der Weg ist noch lang, hier geht ja aber auch nicht um irgendwelche Medikamenten-Krebsstudien Reihe
gruss
Es gibt hier überhaupt kein Zusammenhang,
Merck hält sich zurück weil Biomira die Forschungen durchführt ,Merck ist hier als Investor zu sehen der sich Lizenzen für Europa, bei einer eventuellen Einführung von BLP25 durch die FDA gesichert hat!
Aktueller Kurs gibt nicht bekannt auf welchen Kurs BLP25 zur Zeit ist!
Der Handel ist zu gering ,die letzten Daten von Blp25 waren zuversichtlich,die Aktie kann bei jeder positiven Nachricht
wie in Vergangeheit schon oft gesehen ausbrechen, unterschied könnte diesmal sein das wir hier endlich mal Entscheidende Fakten zu Tage kommen die auf ein positiven Ende der Versuche mit Blp25 deuten!
Der Weg ist noch lang, hier geht ja aber auch nicht um irgendwelche Medikamenten-Krebsstudien Reihe

gruss
@Donner
Danke dir, dann wollen wir mal auf POSITIVE News warten
LG Peter
Danke dir, dann wollen wir mal auf POSITIVE News warten

LG Peter
Biomira to present at Cambridge Healthtech Institute Cancer Immunotherapeutics Conference
Monday August 30, 7:01 am ET
EDMONTON, Aug. 30 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) announced today that Rao Koganty, Ph.D., Senior Director, Research and Development and Chemistry will present at the upcoming Cambridge Healthtech Institute Cancer Immunotherapeutics Conference, September 20-21, 2004 at the Fairmont Copley Plaza, Boston, MA. Dr. Koganty`s presentation entitled, "Receptors of the Immune System and Their Ligands: Immunotherapy of Cancers" will kick off the conference following the Chairperson`s opening remarks and will commence at 8:30 EST on Monday, September 20th.
ADVERTISEMENT
Dr. Koganty and his staff at Biomira have developed several classes of synthetic adjuvants that target the receptors of the immune system such as the toll like receptors (TLR). These synthetic adjuvants, when formulated in combination with well-defined synthetic antigens, are expected to consistently generate specific immune responses to attack cancer cells as well as bacterial and viral pathogens that cause infectious diseases. Chemically well defined synthetic adjuvants open doors for the development of molecular vaccines that are highly specific and definable in the near future. Biomira develops such synthetic adjuvants for outlicensing and commercial resale.
"We were pleased to learn that Dr. Koganty`s work will be highlighted at this scientific forum," said Alex McPherson, MD, PhD, President and CEO. "His work is important in Biomira`s quest to find better treatments for cancer patients. Dr. Koganty`s work in carbohydrate vaccines was also recently featured as part of the cover story in the August 9th edition of the prestigious Chemical and Engineering News."
Cambridge Healthtech Institute
Cambridge Healthtech Institute`s renowned conferences are the underpinning for all of the Company`s other information resources. Each year, approximately 60 conferences are held throughout the US and Europe. Conference programs are designed to be a useful, timely, and effective supplement to specialized journals, newsletters, and other meetings. The Company strives to develop quality programs that provide valuable new insights and competing points of view, while offering balanced coverage of the latest developments. Basic research related to commercial implications is covered, with heavy emphasis placed on new products and technology still in the evaluation stage. Experts from both academic and commercial laboratories present their most current scientific research in a forum that features panel discussions and audience participation.
Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
Monday August 30, 7:01 am ET
EDMONTON, Aug. 30 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) announced today that Rao Koganty, Ph.D., Senior Director, Research and Development and Chemistry will present at the upcoming Cambridge Healthtech Institute Cancer Immunotherapeutics Conference, September 20-21, 2004 at the Fairmont Copley Plaza, Boston, MA. Dr. Koganty`s presentation entitled, "Receptors of the Immune System and Their Ligands: Immunotherapy of Cancers" will kick off the conference following the Chairperson`s opening remarks and will commence at 8:30 EST on Monday, September 20th.
ADVERTISEMENT
Dr. Koganty and his staff at Biomira have developed several classes of synthetic adjuvants that target the receptors of the immune system such as the toll like receptors (TLR). These synthetic adjuvants, when formulated in combination with well-defined synthetic antigens, are expected to consistently generate specific immune responses to attack cancer cells as well as bacterial and viral pathogens that cause infectious diseases. Chemically well defined synthetic adjuvants open doors for the development of molecular vaccines that are highly specific and definable in the near future. Biomira develops such synthetic adjuvants for outlicensing and commercial resale.
"We were pleased to learn that Dr. Koganty`s work will be highlighted at this scientific forum," said Alex McPherson, MD, PhD, President and CEO. "His work is important in Biomira`s quest to find better treatments for cancer patients. Dr. Koganty`s work in carbohydrate vaccines was also recently featured as part of the cover story in the August 9th edition of the prestigious Chemical and Engineering News."
Cambridge Healthtech Institute
Cambridge Healthtech Institute`s renowned conferences are the underpinning for all of the Company`s other information resources. Each year, approximately 60 conferences are held throughout the US and Europe. Conference programs are designed to be a useful, timely, and effective supplement to specialized journals, newsletters, and other meetings. The Company strives to develop quality programs that provide valuable new insights and competing points of view, while offering balanced coverage of the latest developments. Basic research related to commercial implications is covered, with heavy emphasis placed on new products and technology still in the evaluation stage. Experts from both academic and commercial laboratories present their most current scientific research in a forum that features panel discussions and audience participation.
Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
jetzt gehts los 

Europa ,jetzt wird es langsam interessant 
Biomira`s BLP25 liposome vaccine Phase IIb data subject of European Society for Medical Oncology (ESMO) presentation
Wednesday September 1,
EDMONTON, Sept. 1 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and its collaborator, Merck KGaA of Darmstadt, Germany, announced today that data from the Companies` Phase IIb BLP25 Liposome vaccine (L-BLP25) trial has been accepted as the subject of a presentation at the 2004 Meeting of the European Society for Medical Oncology (ESMO). The 29th ESMO Congress is to take place in Vienna, Austria, October 29 - November 2, 2004. The lead investigator for the Phase IIb trial and scheduled ESMO presenter is Dr. Charles Butts, Medical Oncologist, of the Cross Cancer Institute, Edmonton, Alberta. Dr. Butts` presentation is planned for November 1, 2004, at 3:25 p.m. (Austrian time: GMT +1). The presentation is entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC); L-BLP25 Non-Small Cell Lung Cancer Study Group."
ESMO
ESMO is the leading European Society that provides education and guidelines for medical oncologists to ensure optimal care for cancer patients.
The Society continues to grow and includes representatives from every European country and the six major geographical regions of the world.
The Companies
Biomira`s collaborator for L-BLP25 is Merck KGaA. Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26%. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917.
Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas - monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.

Biomira`s BLP25 liposome vaccine Phase IIb data subject of European Society for Medical Oncology (ESMO) presentation
Wednesday September 1,
EDMONTON, Sept. 1 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq:BIOM - News; TSX:BRA - News) and its collaborator, Merck KGaA of Darmstadt, Germany, announced today that data from the Companies` Phase IIb BLP25 Liposome vaccine (L-BLP25) trial has been accepted as the subject of a presentation at the 2004 Meeting of the European Society for Medical Oncology (ESMO). The 29th ESMO Congress is to take place in Vienna, Austria, October 29 - November 2, 2004. The lead investigator for the Phase IIb trial and scheduled ESMO presenter is Dr. Charles Butts, Medical Oncologist, of the Cross Cancer Institute, Edmonton, Alberta. Dr. Butts` presentation is planned for November 1, 2004, at 3:25 p.m. (Austrian time: GMT +1). The presentation is entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC); L-BLP25 Non-Small Cell Lung Cancer Study Group."
ESMO
ESMO is the leading European Society that provides education and guidelines for medical oncologists to ensure optimal care for cancer patients.
The Society continues to grow and includes representatives from every European country and the six major geographical regions of the world.
The Companies
Biomira`s collaborator for L-BLP25 is Merck KGaA. Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26%. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917.
Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas - monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing and results of clinical trials, availability or adequacy of financing, the sales and marketing of commercial products or the efficacy of products. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
BIOMIRA TO PRESENT AT CAMBRIDGE HEALTHTECH INSTITUTE CANCER IMMUNOTHERAPEUTICS CONFERENCE
EDMONTON, ALBERTA, CANADA: August 30, 2004
EDMONTON, ALBERTA, CANADA — August 30, 2004 — Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) announced today that Rao Koganty, Ph.D., Senior Director, Research and Development and Chemistry will present at the upcoming Cambridge Healthtech Institute Cancer Immunotherapeutics Conference, September 20-21, 2004 at the Fairmont Copley Plaza, Boston, MA. Dr. Koganty’s presentation entitled, “Receptors of the Immune System and Their Ligands: Immunotherapy of Cancers” will kick off the conference following the Chairperson’s opening remarks and will commence at 8:30 EST on Monday, September 20th.
Dr. Koganty and his staff at Biomira have developed several classes of synthetic adjuvants that target the receptors of the immune system such as the toll like receptors (TLR). These synthetic adjuvants, when formulated in combination with well-defined synthetic antigens, are expected to consistently generate specific immune responses to attack cancer cells as well as bacterial and viral pathogens that cause infectious diseases.
# ......aber bitte die Kirche im Dorf lassen,Biomira hat noch ein langen Weg vor sich!
EDMONTON, ALBERTA, CANADA: August 30, 2004
EDMONTON, ALBERTA, CANADA — August 30, 2004 — Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) announced today that Rao Koganty, Ph.D., Senior Director, Research and Development and Chemistry will present at the upcoming Cambridge Healthtech Institute Cancer Immunotherapeutics Conference, September 20-21, 2004 at the Fairmont Copley Plaza, Boston, MA. Dr. Koganty’s presentation entitled, “Receptors of the Immune System and Their Ligands: Immunotherapy of Cancers” will kick off the conference following the Chairperson’s opening remarks and will commence at 8:30 EST on Monday, September 20th.
Dr. Koganty and his staff at Biomira have developed several classes of synthetic adjuvants that target the receptors of the immune system such as the toll like receptors (TLR). These synthetic adjuvants, when formulated in combination with well-defined synthetic antigens, are expected to consistently generate specific immune responses to attack cancer cells as well as bacterial and viral pathogens that cause infectious diseases.
# ......aber bitte die Kirche im Dorf lassen,Biomira hat noch ein langen Weg vor sich!
http://www.americanbulls.com/StockPage.asp?CompanyTicker=BIO…
Hier wurde das Kaufsignal bestätigt.
Und das Volumen steigt auch langsam an.
Hier wurde das Kaufsignal bestätigt.
Und das Volumen steigt auch langsam an.

@All
was bestellen wir denn als Belohnung für unser Vertrauen?
Porsche oder Trabant?
LG Peter
was bestellen wir denn als Belohnung für unser Vertrauen?
Porsche oder Trabant?

LG Peter
Das Handelsvolumen wird jetzt langsam zu_nehmen

Die 2,20 sind jetzt wieder schnell möglich!

Guten Abend!
zu #763-766
Zur Klarstellung:
Merck hat die Entwicklungs- und Verwertungsrechte für Theratope an Biomira zurückgegeben, laut
http://biz.yahoo.com/ap/040730/earns_biomira_1.html" target="_blank" rel="nofollow ugc noopener"> http://biz.yahoo.com/ap/040730/earns_biomira_1.html
wegen noch zusätzlich erforderlichen Tests zur Zulassung.
Die Restzahlungen zu dem Abkommen verhalfen Biomira
zum Quartalsgewinn.
In BLP 25 bleibt Merck weiterhin engagiert.
<The company said German pharmceutical firm Merck KGaA recently returned Theratope`s development and commercialization rights because the drug`s approval in the United States, Europe and Japan would likely require additional trials, delaying its market launch. In its quarterly report, Biomira said it realized the remaining $5.9 million Canadian in deferred licensing fees paid by Merck KGaA
Frage: Wie lange schätzt ihr die Zeit bis zur Markteinführung von BLP 25 und wie hoch das Umsatzpotential?
zu #763-766
Zur Klarstellung:
Merck hat die Entwicklungs- und Verwertungsrechte für Theratope an Biomira zurückgegeben, laut
http://biz.yahoo.com/ap/040730/earns_biomira_1.html" target="_blank" rel="nofollow ugc noopener"> http://biz.yahoo.com/ap/040730/earns_biomira_1.html
wegen noch zusätzlich erforderlichen Tests zur Zulassung.
Die Restzahlungen zu dem Abkommen verhalfen Biomira
zum Quartalsgewinn.
In BLP 25 bleibt Merck weiterhin engagiert.
<The company said German pharmceutical firm Merck KGaA recently returned Theratope`s development and commercialization rights because the drug`s approval in the United States, Europe and Japan would likely require additional trials, delaying its market launch. In its quarterly report, Biomira said it realized the remaining $5.9 million Canadian in deferred licensing fees paid by Merck KGaA
Frage: Wie lange schätzt ihr die Zeit bis zur Markteinführung von BLP 25 und wie hoch das Umsatzpotential?
@GRT
Gestern gab es im Yahoo-Board eine, für mich jedenfalls, ziemlich realistische Berechnung:
http://finance.messages.yahoo.com/bbs?.mm=FN&action=m&board=…
Wobei ich glaube, daß der Kurs in der ersten Euphorie nach einer Zulassungsmeldung erst einmal höher gehen wird.
@donnerpower
Rate mal, wo Forellenmarcho sich noch rumtreibt.
Schönes Wochenende
freetibet
Gestern gab es im Yahoo-Board eine, für mich jedenfalls, ziemlich realistische Berechnung:
http://finance.messages.yahoo.com/bbs?.mm=FN&action=m&board=…
Wobei ich glaube, daß der Kurs in der ersten Euphorie nach einer Zulassungsmeldung erst einmal höher gehen wird.
@donnerpower
Rate mal, wo Forellenmarcho sich noch rumtreibt.

Schönes Wochenende
freetibet
und hier ist der Text  ...
...
Re: Biomira`s Upside Year End Potential
by: longbra 09/10/04 01:14 pm
Msg: 156948 of 156974
Agree, $10 short term very likely especially with an early approval anywhere.
BLP25 alone could be a $1b drug. Even if we assume it wont be on the market for 5-7 years.
Here`s my projection with very conservative assumptions:
Assumptions.
Another phase 3 to take 7 years for approval
$1B sales 5 years after approval so 12 years from now.
200 million shares o.s in 12years.
50% share of sales with MERCK Kgaa.
Price to sales ratio 20x
Discount rate 20%
Heres the math
(1000/200)x50%x 20x sales=$50.00/share in 12 years.
discount by 20%/year to present value:
$50 x .8^12 =$3.43/share now.
Posted as a reply to: Msg 156942 by October_October
bin der Meinung mann sollte sich langsam wieder Positionen aufbauen ich selbst bin seit 2 Wochen dabei hier wieder aufzustocken...
allen noch einen schönen Start in die Woche,
Gruß
VAio
 ...
...Re: Biomira`s Upside Year End Potential
by: longbra 09/10/04 01:14 pm
Msg: 156948 of 156974
Agree, $10 short term very likely especially with an early approval anywhere.
BLP25 alone could be a $1b drug. Even if we assume it wont be on the market for 5-7 years.
Here`s my projection with very conservative assumptions:
Assumptions.
Another phase 3 to take 7 years for approval
$1B sales 5 years after approval so 12 years from now.
200 million shares o.s in 12years.
50% share of sales with MERCK Kgaa.
Price to sales ratio 20x
Discount rate 20%
Heres the math
(1000/200)x50%x 20x sales=$50.00/share in 12 years.
discount by 20%/year to present value:
$50 x .8^12 =$3.43/share now.
Posted as a reply to: Msg 156942 by October_October
bin der Meinung mann sollte sich langsam wieder Positionen aufbauen ich selbst bin seit 2 Wochen dabei hier wieder aufzustocken...
allen noch einen schönen Start in die Woche,
Gruß
VAio



Upcoming Events
November 1, 2004
7:30 AM - 8:00 AM MST
Vienna, Austria BIOMIRA`S BLP25 LIPOSOME VACCINE PHASE IIB DATA SUBJECT OF EUROPEAN SOCIETY FOR MEDICAL ONCOLOGY (ESMO) PRESENTATION
ESMO will provide the first peer-reviewed setting in which the Phase IIb data will be presented. The lead investigator for the Phase IIb trial and scheduled ESMO presenter is Dr. Charles Butts, Medical Oncologist, of the Cross Cancer Institute, Edmonton Alberta.
Dr. Butts` presentation is planned for November 1, 2004, at 7:25 a.m. MST (3:25 p.m. in Austria). The presentation is entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC); Non-Small Cell Lung Cancer Study Group."
Schönen Dank, freetibet und Vaio, Biomira scheint ja wirklich ein Wert mit großem Potential zu sein.
Das Einzige, was mir an der Berechung nicht so ganz gefällt, ist der sehr lange Zeithorizont.
Derzeit sieht es ja überhaupt so aus, als ob Biotechs
wieder in Mode kommen.

Das Einzige, was mir an der Berechung nicht so ganz gefällt, ist der sehr lange Zeithorizont.
Derzeit sieht es ja überhaupt so aus, als ob Biotechs
wieder in Mode kommen.

Schließe mich dem Dank an  aber Donner gehört da mit zu!
aber Donner gehört da mit zu!
Ich hoffe das die Biotechs keine Mode sind, sondern das tatsächlich etwas positives bei den Forschungen herauskommt, im Sinne der erkrankten Menschen! Dann ist das Engagement in diese Aktien, doppelt gut
LG Peter
 aber Donner gehört da mit zu!
aber Donner gehört da mit zu!
Ich hoffe das die Biotechs keine Mode sind, sondern das tatsächlich etwas positives bei den Forschungen herauskommt, im Sinne der erkrankten Menschen! Dann ist das Engagement in diese Aktien, doppelt gut

LG Peter
DANKE @ALL die sich mühe geben die informationen zu präsentieren.
BIOMIRA---ich hoffe mein user macht mich glücklich :-)
BIOMIRA---ich hoffe mein user macht mich glücklich :-)
Ich hoffe Biomira du bist nicht User BIOM,
den jeden Tag ein neuen Thread ohne ordentliche Interpretation
nervt langsam!
gruss

den jeden Tag ein neuen Thread ohne ordentliche Interpretation
nervt langsam!
gruss

Also erst wird die Konferenz groß angekündigt und jetzt
nicht mal eine klitzekleine Meldung.
Was macht denn eigentlich die PR so den ganzen Tag.
nicht mal eine klitzekleine Meldung.
Was macht denn eigentlich die PR so den ganzen Tag.

@freetibet
Habe auch keine Info bekommen, vermute das der 1.Nov ein ausschlaggebender Termin werden könnte wo sich das Management
mit neuen fundamentalen Nachrichten präsentieren wird!
gruss
&
long
Habe auch keine Info bekommen, vermute das der 1.Nov ein ausschlaggebender Termin werden könnte wo sich das Management
mit neuen fundamentalen Nachrichten präsentieren wird!
gruss
&
long
Am 27.10. ist auch ein heisser Termin.
http://www.rodmanandrenshaw.com/rodman.asp?link=Conferences3…
http://www.rodmanandrenshaw.com/rodman.asp?link=Conferences3…

http://www.esmo.org/congress2004/Monday_1_Nov.htm
Presidential Symposium - 15:25 Uhr
Pünktlich zum Börsenstart



http://www.phacilitate.co.uk/pages/fall_vac2004/agenda_day_t…
3:15 der Doc persönlich.
Die werden doch nicht kurz hintereinander über Fehlversuche reden.




FDA grants fast track status for BLP25 Liposome Vaccine
Wednesday September 29, 6:01 am ET
EDMONTON, AB, Sept. 29 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq: BIOM - News; TSX: BRA - News) and Merck KGaA of Darmstadt, Germany today announced that the U.S. Food & Drug Administration (FDA) has granted Fast Track status to the investigation of BLP25 Liposome Vaccine (L-BLP25) for its proposed use in the treatment of non-small cell lung cancer (NSCLC).
The FDA`s Fast Track programs are designed to facilitate the development and expedite review of drugs that are intended to treat serious or life-threatening conditions and that demonstrate the potential to address unmet medical needs. With Fast Track designation, there may be more frequent interactions with the FDA during the development of a product and eventually a company may be eligible to file a U.S. biologics license application (BLA) on a rolling basis as data becomes available. This permits the FDA to review a filing as it is received, rather than waiting for the entire document prior to commencing the review process. Due to the nature of these types of products, BLAs filed with Fast Track status are generally eligible for priority review, which could decrease the typical review period.
Biomira submitted a Fast Track application to the FDA, which included encouraging results from a controlled, randomized Phase IIb study in Stage IIIB and IV NSCLC patients. Results from the Phase IIb study will be presented at the European Society of Medical Oncology meeting (ESMO) to be held in Vienna, Austria, on November 1.
A recent letter received from the FDA stated, "We have reviewed your request and concluded that it meets the criteria for the Fast Track designation. Therefore, we are designating as a Fast Track Drug Product development program the investigation of Liposomal Vaccine in the extension of survival among patients with unresectable stage 3a and locoregional stage 3b non-small cell lung cancer following first line chemotherapy. We look forward to working with you to expedite the development and review of this promising proposed use of the product."
"Fast Track designation for L-BLP25 for the treatment of these patients is an important step in the development of this product candidate and may help us bring this potentially promising drug to patients more quickly," said Alex McPherson, MD, PhD, President and CEO of Biomira. "This is a significant milestone for the Company, highlighting the importance of product candidates such as L-BLP25 to one day address a sizeable unmet need in this patient population. We believe our vaccine will be able to provide a new treatment option for men and women with NSCLC that has the potential to both extend and improve the quality of their lives."
L-BLP25 is a synthetic MUC1 peptide vaccine, designed to induce an immune response to cancer cells. L-BLP25 incorporates a 25-amino acid sequence of the MUC1 cancer mucin, encapsulated in a liposomal delivery system. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery.
Biomira and Merck KGaA continue to explore opportunities for early registration for this product candidate with other regulatory agencies. Plans are also underway for a confirmatory Phase III study.
About Lung Cancer
Lung cancer is the leading cause of cancer-related mortality for both sexes in North America. In 2004, approximately 174,000 new cases of lung cancer will be diagnosed in the U.S. - 54 per cent of them in men and 46 per cent in women. Approximately 160,000 people will die of this disease in the U.S. alone in 2004. In Canada, the mortality percentages are slightly higher for men - 57 per cent of deaths from lung cancer will occur in men and 43 per cent will be in women. NSCLC accounts for approximately 75 to 80 per cent of all primary lung cancers. At the time of diagnosis, only 25 per cent of patients are potentially curable by surgery.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26 per cent. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas - monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
EMD Pharmaceuticals Inc., the U.S. affiliate of Merck KGaA, is a fully integrated pharmaceutical company with an initial emphasis on launching new products in oncology. Located in Durham, N.C., EMD focuses on meeting patient and physician needs with pioneering pharmaceutical products and services.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing or attainment of regulatory or product approvals and whether or not the timing may be expedited, the timing of clinical trials approvals, the timing of clinical trials, the efficacy of products or the availability of capital. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.

Wednesday September 29, 6:01 am ET
EDMONTON, AB, Sept. 29 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq: BIOM - News; TSX: BRA - News) and Merck KGaA of Darmstadt, Germany today announced that the U.S. Food & Drug Administration (FDA) has granted Fast Track status to the investigation of BLP25 Liposome Vaccine (L-BLP25) for its proposed use in the treatment of non-small cell lung cancer (NSCLC).
The FDA`s Fast Track programs are designed to facilitate the development and expedite review of drugs that are intended to treat serious or life-threatening conditions and that demonstrate the potential to address unmet medical needs. With Fast Track designation, there may be more frequent interactions with the FDA during the development of a product and eventually a company may be eligible to file a U.S. biologics license application (BLA) on a rolling basis as data becomes available. This permits the FDA to review a filing as it is received, rather than waiting for the entire document prior to commencing the review process. Due to the nature of these types of products, BLAs filed with Fast Track status are generally eligible for priority review, which could decrease the typical review period.
Biomira submitted a Fast Track application to the FDA, which included encouraging results from a controlled, randomized Phase IIb study in Stage IIIB and IV NSCLC patients. Results from the Phase IIb study will be presented at the European Society of Medical Oncology meeting (ESMO) to be held in Vienna, Austria, on November 1.
A recent letter received from the FDA stated, "We have reviewed your request and concluded that it meets the criteria for the Fast Track designation. Therefore, we are designating as a Fast Track Drug Product development program the investigation of Liposomal Vaccine in the extension of survival among patients with unresectable stage 3a and locoregional stage 3b non-small cell lung cancer following first line chemotherapy. We look forward to working with you to expedite the development and review of this promising proposed use of the product."
"Fast Track designation for L-BLP25 for the treatment of these patients is an important step in the development of this product candidate and may help us bring this potentially promising drug to patients more quickly," said Alex McPherson, MD, PhD, President and CEO of Biomira. "This is a significant milestone for the Company, highlighting the importance of product candidates such as L-BLP25 to one day address a sizeable unmet need in this patient population. We believe our vaccine will be able to provide a new treatment option for men and women with NSCLC that has the potential to both extend and improve the quality of their lives."
L-BLP25 is a synthetic MUC1 peptide vaccine, designed to induce an immune response to cancer cells. L-BLP25 incorporates a 25-amino acid sequence of the MUC1 cancer mucin, encapsulated in a liposomal delivery system. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery.
Biomira and Merck KGaA continue to explore opportunities for early registration for this product candidate with other regulatory agencies. Plans are also underway for a confirmatory Phase III study.
About Lung Cancer
Lung cancer is the leading cause of cancer-related mortality for both sexes in North America. In 2004, approximately 174,000 new cases of lung cancer will be diagnosed in the U.S. - 54 per cent of them in men and 46 per cent in women. Approximately 160,000 people will die of this disease in the U.S. alone in 2004. In Canada, the mortality percentages are slightly higher for men - 57 per cent of deaths from lung cancer will occur in men and 43 per cent will be in women. NSCLC accounts for approximately 75 to 80 per cent of all primary lung cancers. At the time of diagnosis, only 25 per cent of patients are potentially curable by surgery.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26 per cent. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas - monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
EMD Pharmaceuticals Inc., the U.S. affiliate of Merck KGaA, is a fully integrated pharmaceutical company with an initial emphasis on launching new products in oncology. Located in Durham, N.C., EMD focuses on meeting patient and physician needs with pioneering pharmaceutical products and services.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing or attainment of regulatory or product approvals and whether or not the timing may be expedited, the timing of clinical trials approvals, the timing of clinical trials, the efficacy of products or the availability of capital. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
--------------------------------------------------------------------------------
Source: Biomira Inc.

Obwohl mein englisch nicht so gut ist und Babelfish bei der Übersetzung von "schneller Schiene" spricht denke ich das das nun ENDLICH mal gute Storie ist!
denke ich das das nun ENDLICH mal gute Storie ist!
LG @All
 denke ich das das nun ENDLICH mal gute Storie ist!
denke ich das das nun ENDLICH mal gute Storie ist!
LG @All
es geht los  ...!!!
...!!!
 ...!!!
...!!!
hier der Deutsche Text 
Merck KGaA und Biomira erhalten Fast Track Status für L-BLP25
Finanzen.net
Der Darmstädter Pharma- und Spezialchemiekonzern Merck KGaA und das Biotech-Unternehmen Biomira Inc. teilten mit, dass die US-Arzneimittelbehörde FDA ihrem liposomalen Krebsimpfstoff L-BLP25 zur Behandlung des nicht-kleinzelligen Lungenkarzinoms (NSCLC) den Fast Track Status erteilt hat.
Die FDA gewährt dieses beschleunigte Prüfungsverfahren solchen neuen Arzneimitteln, die zur Behandlung von lebensbedrohlichen Krankheiten dienen, für die es bisher keine Medikamente gibt, oder wenn der Zulassungskandidat eine bedeutende Verbesserung gegenüber bisher verfügbarer Behandlungsmethoden darstellt. Sie wird dann innerhalb von sechs Monaten über den Zulassungsantrag entscheiden, während dies üblicherweise zwölf Monate dauert. Pharma-Unternehmen können hierbei die einzelnen Komponenten des Zulassungsantrags schrittweise und nicht erst in einem Gesamtpaket nach Abschluss der Zulassungsstudie bei der FDA einreichen ("Rolling Submission").
Im März 2001 vereinbarten Merck und Biomira die gemeinsame Vermarktung von L-BLP25 in den USA. In allen übrigen Ländern, mit Ausnahme von Kanada, Israel und dem palästinensischen Autonomiegebiet, hält Merck die alleinigen Entwicklungs- und Vermarktungsrechte. Pläne für eine große, multizentrische Phase III Studie sind in der Entwicklung.

Merck KGaA und Biomira erhalten Fast Track Status für L-BLP25
Finanzen.net
Der Darmstädter Pharma- und Spezialchemiekonzern Merck KGaA und das Biotech-Unternehmen Biomira Inc. teilten mit, dass die US-Arzneimittelbehörde FDA ihrem liposomalen Krebsimpfstoff L-BLP25 zur Behandlung des nicht-kleinzelligen Lungenkarzinoms (NSCLC) den Fast Track Status erteilt hat.
Die FDA gewährt dieses beschleunigte Prüfungsverfahren solchen neuen Arzneimitteln, die zur Behandlung von lebensbedrohlichen Krankheiten dienen, für die es bisher keine Medikamente gibt, oder wenn der Zulassungskandidat eine bedeutende Verbesserung gegenüber bisher verfügbarer Behandlungsmethoden darstellt. Sie wird dann innerhalb von sechs Monaten über den Zulassungsantrag entscheiden, während dies üblicherweise zwölf Monate dauert. Pharma-Unternehmen können hierbei die einzelnen Komponenten des Zulassungsantrags schrittweise und nicht erst in einem Gesamtpaket nach Abschluss der Zulassungsstudie bei der FDA einreichen ("Rolling Submission").
Im März 2001 vereinbarten Merck und Biomira die gemeinsame Vermarktung von L-BLP25 in den USA. In allen übrigen Ländern, mit Ausnahme von Kanada, Israel und dem palästinensischen Autonomiegebiet, hält Merck die alleinigen Entwicklungs- und Vermarktungsrechte. Pläne für eine große, multizentrische Phase III Studie sind in der Entwicklung.
@Vaio
Danke dir , WO hatte ihn auch schon reingesetzt!
, WO hatte ihn auch schon reingesetzt!
LG Peter
Danke dir
 , WO hatte ihn auch schon reingesetzt!
, WO hatte ihn auch schon reingesetzt!LG Peter
Vorbörslicher Handel USA
...................
BIOMIRA INC - Nasdaq National Market: BIOM
Real-time ECN Quote*
Last Change (%) After Hours Chg (%)** Trade Time Bid Ask
1.721 0.561 (48.36) 0.561 (48.36) 09:13 1.64 (14) 1.73 (150)
Gruß an alle...
Vaio
...................
BIOMIRA INC - Nasdaq National Market: BIOM
Real-time ECN Quote*
Last Change (%) After Hours Chg (%)** Trade Time Bid Ask
1.721 0.561 (48.36) 0.561 (48.36) 09:13 1.64 (14) 1.73 (150)
Gruß an alle...
Vaio

rechne mit einer verdoppelung des kurses.
Merck mit Forschungs-Erfolg
von ME
Der Pharma- und Spezialchemiekonzern Merck kann ein aussichtsreiches Krebsmedikament möglicherweise schneller als bisher gedacht auf den Markt bringen. Die Merck-Aktie macht daraufhin einen Freudensprung.
Die amerikanische Gesundheitsbehörde FDA hat dem Wirkstoff L-BLP25 den so genannten Fast-Track-Status zugebilligt. Dieses beschleunigte Test- und Zulassungsverfahren bekommen Wirkstoffe gegen schwerwiegende oder lebensbedrohliche Krankheiten, bei denen es noch einen Bedarf an neuen Behandlungsmethoden gibt. Mit dem Wirkstoff soll nicht-kleinzelliger Lungenkrebs behandelt werden. Nach Angaben von Merck ist Lungenkrebs weltweit die häufigste Krebs-Todesursache. Jedes Jahr kommen rund 1,2 Millionen neue Patienten hinzu.
Dank des Fast-Track-Status kann Merck seine klinischen Forschungs-Daten sofort einreichen, sobald sie verfügbar sind. Die Ergebnisse prüft die FDA wegen des Fast-Track-Status sofort nach dem Eingang. Normalerweise müssen die Daten alle auf einmal eingereicht werden. Dadurch dauert die Prüfung deutlich länger.
Noch ein langer Weg
Derzeit befindet sich L-BLP25 noch in der zweiten klinischen Phase. In dieser Phase werden Wirkstoffe an bereits erkrankten Patienten getestet. Dabei wird eine höhere Dosis als in der ersten Forschungsphase gewählt, um die Wirksamkeit und die Nebenwirkungen genauer zu erforschen. Die Ergebnisse sollen auf einem Kongress am 1. November dieses Jahres in Wien vorgestellt werden.
Das MDax-Mitglied hatte 2001 mit der kanadischen Biomira vereinbart, den Wirkstoff gemeinsam in den USA zu vermarkten. In allen anderen Ländern mit Ausnahme von Kanada, Israel und dem palästinensischen Autonomiegebiet besitzt Merck die alleinigen Entwicklungs- und Vermarktungsrechte.
Im kommenden Jahr will das Unternehmen die dritte klinische Phase beginnen. In dieser müssen zwei klinische Studien mit wesentlich mehr Patienten als in der zweiten Phase unabhängig voneinander durchgeführt werden.
Das Unternehmen rechnet mit einer Zulassung des Krebswirkstoffs im Jahr 2008. Eine Umsatzschätzung will das Unternehmen daher noch nicht abgeben. Trotzdem legte die Merck-Aktien nach der Meldung zeitweise um knapp fünf Prozent zu. Noch kräftiger legte Biomira-Aktie im vorbörslichen Handel in den USA zu. Hier betrug der Kursgewinn zeitweise 45 Prozent.
http://www.boerse.ard.de
Endlich werden die Medien auf BLP25 aufmerksam.
von ME
Der Pharma- und Spezialchemiekonzern Merck kann ein aussichtsreiches Krebsmedikament möglicherweise schneller als bisher gedacht auf den Markt bringen. Die Merck-Aktie macht daraufhin einen Freudensprung.
Die amerikanische Gesundheitsbehörde FDA hat dem Wirkstoff L-BLP25 den so genannten Fast-Track-Status zugebilligt. Dieses beschleunigte Test- und Zulassungsverfahren bekommen Wirkstoffe gegen schwerwiegende oder lebensbedrohliche Krankheiten, bei denen es noch einen Bedarf an neuen Behandlungsmethoden gibt. Mit dem Wirkstoff soll nicht-kleinzelliger Lungenkrebs behandelt werden. Nach Angaben von Merck ist Lungenkrebs weltweit die häufigste Krebs-Todesursache. Jedes Jahr kommen rund 1,2 Millionen neue Patienten hinzu.
Dank des Fast-Track-Status kann Merck seine klinischen Forschungs-Daten sofort einreichen, sobald sie verfügbar sind. Die Ergebnisse prüft die FDA wegen des Fast-Track-Status sofort nach dem Eingang. Normalerweise müssen die Daten alle auf einmal eingereicht werden. Dadurch dauert die Prüfung deutlich länger.
Noch ein langer Weg
Derzeit befindet sich L-BLP25 noch in der zweiten klinischen Phase. In dieser Phase werden Wirkstoffe an bereits erkrankten Patienten getestet. Dabei wird eine höhere Dosis als in der ersten Forschungsphase gewählt, um die Wirksamkeit und die Nebenwirkungen genauer zu erforschen. Die Ergebnisse sollen auf einem Kongress am 1. November dieses Jahres in Wien vorgestellt werden.
Das MDax-Mitglied hatte 2001 mit der kanadischen Biomira vereinbart, den Wirkstoff gemeinsam in den USA zu vermarkten. In allen anderen Ländern mit Ausnahme von Kanada, Israel und dem palästinensischen Autonomiegebiet besitzt Merck die alleinigen Entwicklungs- und Vermarktungsrechte.
Im kommenden Jahr will das Unternehmen die dritte klinische Phase beginnen. In dieser müssen zwei klinische Studien mit wesentlich mehr Patienten als in der zweiten Phase unabhängig voneinander durchgeführt werden.
Das Unternehmen rechnet mit einer Zulassung des Krebswirkstoffs im Jahr 2008. Eine Umsatzschätzung will das Unternehmen daher noch nicht abgeben. Trotzdem legte die Merck-Aktien nach der Meldung zeitweise um knapp fünf Prozent zu. Noch kräftiger legte Biomira-Aktie im vorbörslichen Handel in den USA zu. Hier betrug der Kursgewinn zeitweise 45 Prozent.
http://www.boerse.ard.de
Endlich werden die Medien auf BLP25 aufmerksam.

Guten Abend 
Tageshöchstkurs 1,74
Hier eine Antwort aus CANADA:
Biomira shares surge on FDA fast-track ruling
Last Updated Wed, 29 Sep 2004 12:51:06 EDT
EDMONTON - Biomira shares got a shot in the arm Wednesday after the U.S. Food and Drug Administration granted fast-track status to its vaccine for non-small cell lung cancer.
Biomira shares (TSX:BRA)were up 45 cents to $1.95 in noon-hour trading on the TSX. Earlier in the morning, they`d changed hands as high as $2.22.
Before trading opened, Biomira announced that the FDA had given its investigation of BLP25 Liposome Vaccine (L-BLP25) fast-track status.
Fast-track designation speeds up the review of drugs that are designed to treat serious or life-threatening conditions.
"Fast track designation for L-BLP25...is an important step in the development of this product candidate and may help us bring this potentially promising drug to patients more quickly," said Biomira CEO Alex McPherson in a release.
Biomira shares have a 52-week trading range of $1.05 to $3.23.




Tageshöchstkurs 1,74
Hier eine Antwort aus CANADA:
Biomira shares surge on FDA fast-track ruling
Last Updated Wed, 29 Sep 2004 12:51:06 EDT
EDMONTON - Biomira shares got a shot in the arm Wednesday after the U.S. Food and Drug Administration granted fast-track status to its vaccine for non-small cell lung cancer.
Biomira shares (TSX:BRA)were up 45 cents to $1.95 in noon-hour trading on the TSX. Earlier in the morning, they`d changed hands as high as $2.22.
Before trading opened, Biomira announced that the FDA had given its investigation of BLP25 Liposome Vaccine (L-BLP25) fast-track status.
Fast-track designation speeds up the review of drugs that are designed to treat serious or life-threatening conditions.
"Fast track designation for L-BLP25...is an important step in the development of this product candidate and may help us bring this potentially promising drug to patients more quickly," said Biomira CEO Alex McPherson in a release.
Biomira shares have a 52-week trading range of $1.05 to $3.23.



THX @ALL
nun endlich eine news die in die richtung 5 dollar passt.
wenn dann umsätze kommen, dann ist auch die 5 dollarmarke geschichte
mfg
biom---der immer mal zugekauft hat :-)
nun endlich eine news die in die richtung 5 dollar passt.
wenn dann umsätze kommen, dann ist auch die 5 dollarmarke geschichte
mfg
biom---der immer mal zugekauft hat :-)
Es liegen jetzt etwa 6anstrengende Monate vor uns,wobei auch eine kürzere Zeit in Anspruch genommen werden könnte
Die FDA gewährt dieses beschleunigte Prüfungsverfahren solchen neuen Arzneimitteln, die zur Behandlung von lebensbedrohlichen Krankheiten dienen, für die es bisher keine Medikamente gibt, oder wenn der Zulassungskandidat eine bedeutende Verbesserung gegenüber bisher verfügbarer Behandlungsmethoden darstellt.[/b ] Sie wird dann innerhalb von sechs Monaten über den Zulassungsantrag entscheiden, während dies üblicherweise zwölf Monate dauert. Pharma-Unternehmen können hierbei die einzelnen Komponenten des Zulassungsantrags schrittweise und nicht erst in einem Gesamtpaket nach Abschluss der Zulassungsstudie bei der FDA einreichen ("Rolling Submission").

Die FDA gewährt dieses beschleunigte Prüfungsverfahren solchen neuen Arzneimitteln, die zur Behandlung von lebensbedrohlichen Krankheiten dienen, für die es bisher keine Medikamente gibt, oder wenn der Zulassungskandidat eine bedeutende Verbesserung gegenüber bisher verfügbarer Behandlungsmethoden darstellt.[/b ] Sie wird dann innerhalb von sechs Monaten über den Zulassungsantrag entscheiden, während dies üblicherweise zwölf Monate dauert. Pharma-Unternehmen können hierbei die einzelnen Komponenten des Zulassungsantrags schrittweise und nicht erst in einem Gesamtpaket nach Abschluss der Zulassungsstudie bei der FDA einreichen ("Rolling Submission").
Jetzt gehts erst mal wieder runter,
der Grund hier für ist die grosse Unsicherheit die da zu führt das viele Aktionäre Merck KGaA aktuell mit MERCK & CO. INC.
verwechseln!!!
Biomira arbeitet mit Merck KGaA zusammen
Hier die Meldung die FALSCH aufgenommen wird
Der amerikanische Pharmariese Merck hat heute überraschend bekannt gegeben, sein Arthritis- und Schmerzmedikament Vioxx unverzüglich vom Markt zu nehmen. Im Zuge von Testreihen sei ein relativ gestiegenes Risiko von kardiovaskulären Erkrankungen aufgetreten.
Zwar, so Chairman Raymond Gilmartin, wäre es möglich gewesen, das Mittel mit dem Hinweis auf diese Nebeneffekte weiter zu vermarkten. Angesichts alternativer Therapiemöglichkeiten halte man den Verkaufsstop für die vernünftigste und verantwortungsvollste Lösung. Vioxx wurde in über 80 Ländern vertrieben und hat 2003 Umsätze von rund 2,5 Milliarden Dollar erwirtschaftet.

33,28 USD
-26,16 %
der Grund hier für ist die grosse Unsicherheit die da zu führt das viele Aktionäre Merck KGaA aktuell mit MERCK & CO. INC.
verwechseln!!!
Biomira arbeitet mit Merck KGaA zusammen

Hier die Meldung die FALSCH aufgenommen wird

Der amerikanische Pharmariese Merck hat heute überraschend bekannt gegeben, sein Arthritis- und Schmerzmedikament Vioxx unverzüglich vom Markt zu nehmen. Im Zuge von Testreihen sei ein relativ gestiegenes Risiko von kardiovaskulären Erkrankungen aufgetreten.
Zwar, so Chairman Raymond Gilmartin, wäre es möglich gewesen, das Mittel mit dem Hinweis auf diese Nebeneffekte weiter zu vermarkten. Angesichts alternativer Therapiemöglichkeiten halte man den Verkaufsstop für die vernünftigste und verantwortungsvollste Lösung. Vioxx wurde in über 80 Ländern vertrieben und hat 2003 Umsätze von rund 2,5 Milliarden Dollar erwirtschaftet.
33,28 USD
-26,16 %
Also ich tippe auf einen heutigen Schlußkurs von 1,50$.
Wäre schön, wenn wir den bis zum 01.11. halten könnten.
Wäre schön, wenn wir den bis zum 01.11. halten könnten.

Denke der Kurs wird heute wieder etwas Fahrt auf nehmen...
zu beachten:
Wie gesagt mit Grosser Erwartung wird am 1.November von der ganzen medizin Branche sehnsüchtig mit anhaltender
Spannung die Präsentation von Biomira über die Ergebnisse von BLP25 erwartet,(erster Abschnitt) ! ! !
Trotzdem sollte man wie im letzten Abschnitt geschrieben,das Risiko nicht verstecken das Biomira noch weiterhin trägt !
Biomira Drug`s on the Fast Track
, small biotech Biomira (Nasdaq: BIOM) got quite a pop in its stock after announcing that the FDA gave its BLP25 liposome vaccine fast-track status. As a cancer vaccine, BLP25 is designed to help the immune system recognize tumor cells as entities that need to be destroyed. Thus, it differs from traditional chemotherapies, which directly kill tumor cells.
Data from a phase 2b trial in patients with non-small-cell lung cancer (NSCLC) was released back in April. The caveats of subset analyses notwithstanding, the data in patients with stage 3b NSCLC looked encouraging. Additional results from the phase 2b trial will be released on November 1 at the European Society for Medical Oncology meeting, and it will be interesting to get an update on the patient survival data.
Fast-track status generates such a buzz, as it is intended for drugs that are in development to treat very serious diseases. It comes with a few benefits such as early communication with the FDA to expedite drug development. So getting fast-track status is certainly never bad news. But as tends to be the case with small biotechs, the importance to investors seems to have been overstated. What fast track does not do is improve the odds that a drug will be successful, and that is what matters in the long run. (For a great rundown on this program, check out an eye-opening article from Signals.)
That being said, fast-track status for BLP25 shifts the focus away from the difficulties Biomira has had with its other cancer vaccine, Theratope. If Biomira and partner Merck KGaA (NYSE: MRK) can lay out a clear plan for developing BLP25, it may breathe some life back into this company. However, with an unproven technology, shaky financials, and a long development road ahead, Biomira remains a high-risk proposition for the adventurous.
zu beachten:
Wie gesagt mit Grosser Erwartung wird am 1.November von der ganzen medizin Branche sehnsüchtig mit anhaltender
Spannung die Präsentation von Biomira über die Ergebnisse von BLP25 erwartet,(erster Abschnitt) ! ! !
Trotzdem sollte man wie im letzten Abschnitt geschrieben,das Risiko nicht verstecken das Biomira noch weiterhin trägt !
Biomira Drug`s on the Fast Track
, small biotech Biomira (Nasdaq: BIOM) got quite a pop in its stock after announcing that the FDA gave its BLP25 liposome vaccine fast-track status. As a cancer vaccine, BLP25 is designed to help the immune system recognize tumor cells as entities that need to be destroyed. Thus, it differs from traditional chemotherapies, which directly kill tumor cells.
Data from a phase 2b trial in patients with non-small-cell lung cancer (NSCLC) was released back in April. The caveats of subset analyses notwithstanding, the data in patients with stage 3b NSCLC looked encouraging. Additional results from the phase 2b trial will be released on November 1 at the European Society for Medical Oncology meeting, and it will be interesting to get an update on the patient survival data.
Fast-track status generates such a buzz, as it is intended for drugs that are in development to treat very serious diseases. It comes with a few benefits such as early communication with the FDA to expedite drug development. So getting fast-track status is certainly never bad news. But as tends to be the case with small biotechs, the importance to investors seems to have been overstated. What fast track does not do is improve the odds that a drug will be successful, and that is what matters in the long run. (For a great rundown on this program, check out an eye-opening article from Signals.)
That being said, fast-track status for BLP25 shifts the focus away from the difficulties Biomira has had with its other cancer vaccine, Theratope. If Biomira and partner Merck KGaA (NYSE: MRK) can lay out a clear plan for developing BLP25, it may breathe some life back into this company. However, with an unproven technology, shaky financials, and a long development road ahead, Biomira remains a high-risk proposition for the adventurous.
@donner
Angenommen die Daten sind am 1.11. statistisch bedeutend.
Braucht es dann noch eine 3 Phase?
Wann rechnest Du dann mit einer Zulassung?
Gruss
schmacki
Angenommen die Daten sind am 1.11. statistisch bedeutend.
Braucht es dann noch eine 3 Phase?
Wann rechnest Du dann mit einer Zulassung?
Gruss
schmacki
@schmacki
Ich rechne hier zu 90% mit einer 3Phase,trotzdem dürfte sich bei einer guten Ausgangs_situation der Kurs oberhalb der 3Euro festsetzten, da während bei einer zufrieden laufenden 3.Phase es fast jeden Monat mit aktuellen Ergebnisabschnitte zu rechnen wäre!
Trotzdem finde ich es schon interessant das Merck diese Aussage gemacht:
Das Unternehmen rechnet mit einer Zulassung des Krebswirkstoffs im Jahr 2008. Eine Umsatzschätzung will das Unternehmen daher noch nicht abgeben.
Man beachte das bei einer eventl. der Einführung der Kurs dann schon gemacht worden ist
Ich rechne hier zu 90% mit einer 3Phase,trotzdem dürfte sich bei einer guten Ausgangs_situation der Kurs oberhalb der 3Euro festsetzten, da während bei einer zufrieden laufenden 3.Phase es fast jeden Monat mit aktuellen Ergebnisabschnitte zu rechnen wäre!
Trotzdem finde ich es schon interessant das Merck diese Aussage gemacht:
Das Unternehmen rechnet mit einer Zulassung des Krebswirkstoffs im Jahr 2008. Eine Umsatzschätzung will das Unternehmen daher noch nicht abgeben.
Man beachte das bei einer eventl. der Einführung der Kurs dann schon gemacht worden ist

Danke!
Umsätze gehen jetzt wieder etwas zurück

@donnerpower
Was sagst Du zu dem Gerücht aus dem yahoo-Board, daß Merck&co eine Ersatzdroge für Ihr ausgefallenes Medikament suchen?
Falls da eine Übernahme kommen sollte, würden wir wahrscheinlich einen schlechteren Kurs bekommen, als ohne.
Und was würde MerckKgAa sagen?
Und BIOM kommt mir vor, wie der Bruder von User "Jetti".
Aber immerhin scheint er ja in Darmstadt zu wohnen.
Was sagst Du zu dem Gerücht aus dem yahoo-Board, daß Merck&co eine Ersatzdroge für Ihr ausgefallenes Medikament suchen?
Falls da eine Übernahme kommen sollte, würden wir wahrscheinlich einen schlechteren Kurs bekommen, als ohne.
Und was würde MerckKgAa sagen?
Und BIOM kommt mir vor, wie der Bruder von User "Jetti".
Aber immerhin scheint er ja in Darmstadt zu wohnen.

@freetibet
Eine Übernahme ist zur Zeit unvorstellbar ,man beachte das Merck(Germany)
fast die komplette Vermarktunglizenz/rechte des Medikaments BLP25 besitzt.
Biomira ist mal ganz scharf betrachtet nur ein Angestellter des grossen Pharm.Konzerns.
Ich glaube nicht das ein Konzern wie Merck auf eventtl. steigende Milliarden Gewinne pro Jahr
Verzichtet!
Man sollte auch beachten das VIOX ein ganz andere Impfstoff war!
Des weiteren sollte Einigen klar sein, sollte BLP25 Ergebnisse weiter ausgereift sein(bei einigen Testpersonen war Blp25 bei der letzten Ergebnissen noch nicht eingeschlagen) dürfte sich BLP25 schnell mit Staatlicher Unterstützung schmücken
Beachtung:
Sollte Übernahmegerücht öffentlich werden könnte es uns nur zeigen wie weit BLP25 in der Testphase wirklich schon ist
Aber aktuell sieht es nicht danach aus das sich im Kurs ein Gerücht dieser Dimension widerspiegelt!!!
Leider
gruss
Eine Übernahme ist zur Zeit unvorstellbar ,man beachte das Merck(Germany)
fast die komplette Vermarktunglizenz/rechte des Medikaments BLP25 besitzt.
Biomira ist mal ganz scharf betrachtet nur ein Angestellter des grossen Pharm.Konzerns.
Ich glaube nicht das ein Konzern wie Merck auf eventtl. steigende Milliarden Gewinne pro Jahr
Verzichtet!
Man sollte auch beachten das VIOX ein ganz andere Impfstoff war!
Des weiteren sollte Einigen klar sein, sollte BLP25 Ergebnisse weiter ausgereift sein(bei einigen Testpersonen war Blp25 bei der letzten Ergebnissen noch nicht eingeschlagen) dürfte sich BLP25 schnell mit Staatlicher Unterstützung schmücken

Beachtung:
Sollte Übernahmegerücht öffentlich werden könnte es uns nur zeigen wie weit BLP25 in der Testphase wirklich schon ist

Aber aktuell sieht es nicht danach aus das sich im Kurs ein Gerücht dieser Dimension widerspiegelt!!!
Leider
gruss
Das große Abwarten hat wohl eingesetzt?
LG Peter

LG Peter
#11 BIOM in seinem Thread vom 01.10.04:
"die nächsten guten Nachrichten stehen vor der Haustür :-)
habe soeben eine Info bekommen.
Leute gebt keine Stücke mehr her. Mein Tip: nächste Woche +30%
Gruß
aus Darmstadt
BIOM"
...Die Woche ist ja noch nicht ganz um. Na dann hoffen wir mal auf 30% heute!:


"die nächsten guten Nachrichten stehen vor der Haustür :-)
habe soeben eine Info bekommen.
Leute gebt keine Stücke mehr her. Mein Tip: nächste Woche +30%
Gruß
aus Darmstadt
BIOM"
...Die Woche ist ja noch nicht ganz um. Na dann hoffen wir mal auf 30% heute!:



@Andreolly
Glaube kaum, das von uns, nur einer was verkauft
Wir wissen was haben
LG Peter
Glaube kaum, das von uns, nur einer was verkauft

Wir wissen was haben

LG Peter
Die Jubelorgien von den "Grüßen aus Darmstadt" kann man doch beim BESTEN Willen nicht mehr ernst nehmen!
LG Peter
LG Peter
#Peter
...wie Recht du hast!!!

...wie Recht du hast!!!

Das Kaufsignal ist noch intakt, wenn man hier überhaupt von Charttechnik reden kann.
Werde diese Woche noch ein bisschen zukaufen.
Werde diese Woche noch ein bisschen zukaufen.

@All
Leute ist denn hier keiner mehr zu Hause? Keiner was neues auf Lager?
LG Peter
Leute ist denn hier keiner mehr zu Hause? Keiner was neues auf Lager?

LG Peter
@peter
Es sind schon noch alle da.
Aber leider hat es der Kurs so an sich, daß er immer wieder
abbröckelt, wenn nicht ständig Nachrichten kommen.
Und da können wir uns wie immer bei der PR bedanken.
Ich hoffe, daß wenigstens hier etwas dabei sein wird:
Upcoming Events
2004
October 27, 2004
3:00 PM - 4:00 PM EST
Waldorf Astoria, NY, NY Rodman and Renshaw Techvest Conference
Dr. Alex McPherson, President and CEO, will present at the subject conference. His presentation will commence at 3:10 p.m. EST and will conclude with a breakout session between 3:30 and 3:50 p.m.
The Web cast will be available at http://www.wallstreetwebcasting.com/webcast/rrshq4/biom
October 28, 2004
Edmonton, Alberta Q3 Financial Press Release
Biomira`s 3rd Quarter Financial News Release will be on Thursday, 28 October, 2004. Teh release will be during the day, following approval by the Board of Directors.
November 1, 2004
7:30 AM - 8:00 AM MST
Vienna, Austria BIOMIRA`S BLP25 LIPOSOME VACCINE PHASE IIB DATA SUBJECT OF EUROPEAN SOCIETY FOR MEDICAL ONCOLOGY (ESMO) PRESENTATION
ESMO will provide the first peer-reviewed setting in which the Phase IIb data will be presented. The lead investigator for the Phase IIb trial and scheduled ESMO presenter is Dr. Charles Butts, Medical Oncologist, of the Cross Cancer Institute, Edmonton Alberta.
Dr. Butts` presentation is planned for November 1, 2004, at 7:25 a.m. MST (3:25 p.m. in Austria). The presentation is entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC); Non-Small Cell Lung Cancer Study Group."
November 4, 2004
3:15 PM - 3:45 PM EST
Cambridge, MA Phacilitate Vaccine Forum Fall 2004, Dr. Alex McPherson
Dr. McPherson will present a case study on Biomira`s cancer vaccines at this conference, which is being held at the Hyatt Regency Hotel, Cambridge, MA from November 2-5, 2004.
Viel Glück allen Investierten.
Es sind schon noch alle da.

Aber leider hat es der Kurs so an sich, daß er immer wieder
abbröckelt, wenn nicht ständig Nachrichten kommen.
Und da können wir uns wie immer bei der PR bedanken.
Ich hoffe, daß wenigstens hier etwas dabei sein wird:
Upcoming Events
2004
October 27, 2004
3:00 PM - 4:00 PM EST
Waldorf Astoria, NY, NY Rodman and Renshaw Techvest Conference
Dr. Alex McPherson, President and CEO, will present at the subject conference. His presentation will commence at 3:10 p.m. EST and will conclude with a breakout session between 3:30 and 3:50 p.m.
The Web cast will be available at http://www.wallstreetwebcasting.com/webcast/rrshq4/biom
October 28, 2004
Edmonton, Alberta Q3 Financial Press Release
Biomira`s 3rd Quarter Financial News Release will be on Thursday, 28 October, 2004. Teh release will be during the day, following approval by the Board of Directors.
November 1, 2004
7:30 AM - 8:00 AM MST
Vienna, Austria BIOMIRA`S BLP25 LIPOSOME VACCINE PHASE IIB DATA SUBJECT OF EUROPEAN SOCIETY FOR MEDICAL ONCOLOGY (ESMO) PRESENTATION
ESMO will provide the first peer-reviewed setting in which the Phase IIb data will be presented. The lead investigator for the Phase IIb trial and scheduled ESMO presenter is Dr. Charles Butts, Medical Oncologist, of the Cross Cancer Institute, Edmonton Alberta.
Dr. Butts` presentation is planned for November 1, 2004, at 7:25 a.m. MST (3:25 p.m. in Austria). The presentation is entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine for immunotherapy of non-small cell lung cancer (NSCLC); Non-Small Cell Lung Cancer Study Group."
November 4, 2004
3:15 PM - 3:45 PM EST
Cambridge, MA Phacilitate Vaccine Forum Fall 2004, Dr. Alex McPherson
Dr. McPherson will present a case study on Biomira`s cancer vaccines at this conference, which is being held at the Hyatt Regency Hotel, Cambridge, MA from November 2-5, 2004.
Viel Glück allen Investierten.

@freetibet
Der Mist ist, das ich nächste Woche, für einige Zeit nicht mehr beobachten kann was sich tut! Setze ich nen Stop oder nicht, das ist für mich die Frage, oder lasse ich weiterlaufen?
LG Peter
Der Mist ist, das ich nächste Woche, für einige Zeit nicht mehr beobachten kann was sich tut! Setze ich nen Stop oder nicht, das ist für mich die Frage, oder lasse ich weiterlaufen?
LG Peter
Die entscheidenden Termine sind 01.11. und 04.11.
Was soll schon beim Quartalsbericht herauskommen.
Was mich positiv stimmt ist, dass die Amis in den Boards
wieder etwas pessimistischer werden.
Zuviel Optimismus ist noch nie gut gewesen.
Was soll schon beim Quartalsbericht herauskommen.
Was mich positiv stimmt ist, dass die Amis in den Boards
wieder etwas pessimistischer werden.
Zuviel Optimismus ist noch nie gut gewesen.

Ich glaube, BIOM macht bald einen Sprung nach oben.
Die Frage ist, ob wir bis Ende des Monats warten müssen.
Grüße
verdi
Die Frage ist, ob wir bis Ende des Monats warten müssen.
Grüße
verdi



@freetibet
Kaufst du gerade ein???

Kaufst du gerade ein???

@donner
Ja, ich war gerade im Supermarkt.

Nein, ich habe fertig.
Ich habe letzte Woche gekauft, aber in Amerika.
So langsam sollte man sich in Stellung bringen.
Ja, ich war gerade im Supermarkt.


Nein, ich habe fertig.
Ich habe letzte Woche gekauft, aber in Amerika.
So langsam sollte man sich in Stellung bringen.

Wo sind denn eigentlich "BIOM" und "BIOMIRA" ?
Schleichen die gerade in Darmstadt herum und versuchen
heiße Tips zu bekommen?
Schleichen die gerade in Darmstadt herum und versuchen
heiße Tips zu bekommen?

@freetibet
wer weiß, vielleicht im Urlaub und hoffen, dass die Biomira-Aktie steigt ;-)
wer weiß, vielleicht im Urlaub und hoffen, dass die Biomira-Aktie steigt ;-)
Wer Geduld hat wird auch bei Biomira belohnt!
Bei 6Dollar gekauft nun gehen wir auf die 30 zu
Schön neben meine Transmeta zahlen sich nun auch meine VerisignShares aus.Ziel für 2005 40Dollar!


Bei 6Dollar gekauft nun gehen wir auf die 30 zu

Schön neben meine Transmeta zahlen sich nun auch meine VerisignShares aus.Ziel für 2005 40Dollar!
@donnerpower
wenn biomira $1,41 hinter sich hat, dann sieht es für die nächste woche sehr gut aus.
schönen abend noch!
gruß
verdi
wenn biomira $1,41 hinter sich hat, dann sieht es für die nächste woche sehr gut aus.
schönen abend noch!
gruß
verdi
@donnerpower
wenn biomira $1,41 hinter sich hat, dann sieht es für die nächste woche sehr gut aus.
schönen abend noch!
gruß
verdi
wenn biomira $1,41 hinter sich hat, dann sieht es für die nächste woche sehr gut aus.
schönen abend noch!
gruß
verdi
@All:
Bin der Meinung das Biomira die nächte Woche noch etwas zulagen kann von Chart her sieht es sehr gut aus und wir haben unser Gab wieder geschlossen ...
...
Allen ein schönes Wochenende
Gruß
VAio
Bin der Meinung das Biomira die nächte Woche noch etwas zulagen kann von Chart her sieht es sehr gut aus und wir haben unser Gab wieder geschlossen
 ...
...Allen ein schönes Wochenende
Gruß
VAio
News are out  ...
...
Biomira to Present at 6th Annual Rodman & Renshaw Techvest Healthcare Conference Dr. Alex McPherson to Recap Product Candidate Progress to Investment Community
EDMONTON, Oct 25, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc.
(Nasdaq: BIOM) (TSX: BRA) announced today that Alex McPherson, MD, PhD,
President and CEO of Biomira, is scheduled to recap highlights of the Company`s
product and corporate plans at the 6th Annual Rodman & Renshaw Techvest
Healthcare Conference on Wednesday, October 27, 2004. The conference is being
held October 26 - 28 at the Waldorf Astoria Hotel in New York.
Dr. McPherson is scheduled to present at 3:10 p.m. EDT on October 27th. The
presentation will be available live to the public via Web cast through the
Biomira Web site at www.biomira.com or through the Rodman & Renshaw link at
http://www.wallstreetwebcasting.com/webcast/rrshq4/biom The broadcast will also
be archived for 90 days following the presentation.
Das wird noch ne spannende Woche
Gruß
Vaio
 ...
...Biomira to Present at 6th Annual Rodman & Renshaw Techvest Healthcare Conference Dr. Alex McPherson to Recap Product Candidate Progress to Investment Community
EDMONTON, Oct 25, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc.
(Nasdaq: BIOM) (TSX: BRA) announced today that Alex McPherson, MD, PhD,
President and CEO of Biomira, is scheduled to recap highlights of the Company`s
product and corporate plans at the 6th Annual Rodman & Renshaw Techvest
Healthcare Conference on Wednesday, October 27, 2004. The conference is being
held October 26 - 28 at the Waldorf Astoria Hotel in New York.
Dr. McPherson is scheduled to present at 3:10 p.m. EDT on October 27th. The
presentation will be available live to the public via Web cast through the
Biomira Web site at www.biomira.com or through the Rodman & Renshaw link at
http://www.wallstreetwebcasting.com/webcast/rrshq4/biom The broadcast will also
be archived for 90 days following the presentation.
Das wird noch ne spannende Woche

Gruß
Vaio
Hier hat sich auch wieder etwas getan. 
http://www.nasdaq.com/asp/holdings.asp?mode=&kind=&symbol=BI…

http://www.nasdaq.com/asp/holdings.asp?mode=&kind=&symbol=BI…
@freetibet
und was hat sich da wieder getan bitte?
ich sehe nichts neues
gruß
verdi
und was hat sich da wieder getan bitte?
ich sehe nichts neues

gruß
verdi
"announced today that Alex McPherson, MD, PhD, President and CEO of Biomira, is scheduled to recap highlights of the Company`s product and corporate plans ..."
klingt nicht nach sensationellen Neuigkeiten
klingt nicht nach sensationellen Neuigkeiten

@verdi2003
Mit Datum 30.09.04 haben einige ihre Anteile aufgestockt bzw. sind ganz ausgestiegen.
Morgan Stanley und First National sind neu (wenn auch wenig Shares).
Falls Du es vorher schon gesehen hattest, ist es natürlich nicht neu.
R&R
http://www.wallstreetwebcasting.com/webcast/rrshq4/biom/
Mit Datum 30.09.04 haben einige ihre Anteile aufgestockt bzw. sind ganz ausgestiegen.
Morgan Stanley und First National sind neu (wenn auch wenig Shares).
Falls Du es vorher schon gesehen hattest, ist es natürlich nicht neu.
R&R
http://www.wallstreetwebcasting.com/webcast/rrshq4/biom/
@freetibet
okay, danke!
noch eine woche, dann wissen wir etwas mehr als heute ;-)
euch allen einen schönen tag wünsche ich1
verdi
okay, danke!
noch eine woche, dann wissen wir etwas mehr als heute ;-)
euch allen einen schönen tag wünsche ich1
verdi
Das 52W-hoch 2,45 sollte doch noch im Jahre 2004 zu toppppen sein!

@donnerpower
ja es sollte ...
es hängt alles davon ab, was das unternehmen uns demnächst berichtet.
gruß
verdi
ja es sollte ...
es hängt alles davon ab, was das unternehmen uns demnächst berichtet.
gruß
verdi
Leider liegt über die Hälfte bei Biomira immer falsch,die Erwartungen werden hier sehr hoch gesteckt ,dazu führt der immer wieder in Short gesetzte Kurseinbruch.
Man sollte sich hier lieber Gedanken machen ob nicht noch
im Dezember positive Nachrichten des eigentlich schon längst abgeschrieben Medikament Theratope an die Öffentlichkeit kommen

Man sollte sich hier lieber Gedanken machen ob nicht noch
im Dezember positive Nachrichten des eigentlich schon längst abgeschrieben Medikament Theratope an die Öffentlichkeit kommen

Nasdaq BIOM USD 1,34 1,40 +0,060 +4,48 % 370.261 289.323 26. Okt 22:01
Frankfurt BM2 EUR 1,03 1,11 +0,080 +7,77 % 1.665 1.500 26. Okt 19:43

Frankfurt BM2 EUR 1,03 1,11 +0,080 +7,77 % 1.665 1.500 26. Okt 19:43

neuer versuch richtung rorden.
obwohl heutiger umsatz nicht so hoch ist - bis jetzt -
gehe ich davon aus, dass der kurs die marke 1,40/1,41 euro hinter sich hat.
gute geschäfte wünscht
verdi
obwohl heutiger umsatz nicht so hoch ist - bis jetzt -
gehe ich davon aus, dass der kurs die marke 1,40/1,41 euro hinter sich hat.
gute geschäfte wünscht
verdi
Morgen  ,
,
und hier der Text...
Biomira to Present at 6th Annual Rodman & Renshaw Techvest Healthcare Conference
25 October 2004, 07:00am ET
Dr. Alex McPherson to Recap Product Candidate Progress to
Investment Community
EDMONTON, Oct. 25 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq: BIOM) (TSX: BRA) announced today that Alex McPherson, MD, PhD, President and CEO of Biomira, is scheduled to recap highlights of the Company`s product and corporate plans at the 6th Annual Rodman & Renshaw Techvest Healthcare Conference on Wednesday, October 27, 2004. The conference is being held October 26 - 28 at the Waldorf Astoria Hotel in New York.
Mentioned Last Change
BIOM 1.401 0.001dollars or (0.07%)
Dr. McPherson is scheduled to present at 3:10 p.m. EDT on October 27th. The presentation will be available live to the public via Web cast through the Biomira Web site at www.biomira.com or through the Rodman & Renshaw link at http://www.wallstreetwebcasting.com/webcast/rrshq4/biom . The broadcast will also be archived for 90 days following the presentation.
Rodman & Renshaw
Rodman & Renshaw, Inc. is a privately-held, full-service investment bank committed to fostering the long-term success of emerging growth companies through capital raising, strategic advice, insightful research, and the development of institutional support.
Allen noch einen schönen Start in den Tag,
Gruß
Vaio
 ,
,und hier der Text...
Biomira to Present at 6th Annual Rodman & Renshaw Techvest Healthcare Conference
25 October 2004, 07:00am ET
Dr. Alex McPherson to Recap Product Candidate Progress to
Investment Community
EDMONTON, Oct. 25 /PRNewswire-FirstCall/ - Biomira Inc. (Nasdaq: BIOM) (TSX: BRA) announced today that Alex McPherson, MD, PhD, President and CEO of Biomira, is scheduled to recap highlights of the Company`s product and corporate plans at the 6th Annual Rodman & Renshaw Techvest Healthcare Conference on Wednesday, October 27, 2004. The conference is being held October 26 - 28 at the Waldorf Astoria Hotel in New York.
Mentioned Last Change
BIOM 1.401 0.001dollars or (0.07%)
Dr. McPherson is scheduled to present at 3:10 p.m. EDT on October 27th. The presentation will be available live to the public via Web cast through the Biomira Web site at www.biomira.com or through the Rodman & Renshaw link at http://www.wallstreetwebcasting.com/webcast/rrshq4/biom . The broadcast will also be archived for 90 days following the presentation.
Rodman & Renshaw
Rodman & Renshaw, Inc. is a privately-held, full-service investment bank committed to fostering the long-term success of emerging growth companies through capital raising, strategic advice, insightful research, and the development of institutional support.
Allen noch einen schönen Start in den Tag,
Gruß
Vaio
Heute kommen Quartalszahlen.
Die letzten kamen gegen 12:50AM ET.
Die letzten kamen gegen 12:50AM ET.

Zahlen sind da
http://biz.yahoo.com/prnews/041028/to024_1.html
Die Reihe Theratope ist noch nicht verloren....
Theratope
A confirmatory study in the subset of patients from our previous Phase III breast cancer trial who had longer survival on the vaccine arm would probably be required prior to commercialization in Canada, the U.S., Europe and Japan. Biomira is planning manufacture of new Theratope material to supply such a potential confirmatory study. The new material will include a change to the adjuvant component which is expected to decrease the frequency of patient injection site reactions. The comparability plan evaluating this change will probably include a small clinical study to measure the safety and immunogenicity of the new material. This study is expected to commence in the first half of 2005. While the Company seeks a collaborative partner to develop Theratope further, it continues to explore the mechanism of action for Theratope and is also investigating possible opportunities in other countries for early registration based on the current subset data.
http://biz.yahoo.com/prnews/041028/to024_1.html
Die Reihe Theratope ist noch nicht verloren....

Theratope
A confirmatory study in the subset of patients from our previous Phase III breast cancer trial who had longer survival on the vaccine arm would probably be required prior to commercialization in Canada, the U.S., Europe and Japan. Biomira is planning manufacture of new Theratope material to supply such a potential confirmatory study. The new material will include a change to the adjuvant component which is expected to decrease the frequency of patient injection site reactions. The comparability plan evaluating this change will probably include a small clinical study to measure the safety and immunogenicity of the new material. This study is expected to commence in the first half of 2005. While the Company seeks a collaborative partner to develop Theratope further, it continues to explore the mechanism of action for Theratope and is also investigating possible opportunities in other countries for early registration based on the current subset data.
28.10.2004 21:28:
Biomira Inc. verkündet 3. Viertelresultate
EDMONTON, 28. Okt. /PRNewswire-FirstCall/ -- Biomira (Nachrichten) (TSX: BÜSTENHALTER) berichtete heute über finanzielle Resultate für die neun Monate beendet 30. September 2004.
Finanzielles Update ----------------
Finanzielle Resultate für die neun Monate beendet 30. September 2004 reflektieren einen vereinigten Nettobetriebsverlust $8.6 von Million oder von $0.12 pro den Anteil, der bis $14.3 Million oder $0.25 pro Anteil während der gleichen Periode 2003 verglichen wird. Der verringerte Verlust von $5.7 Million 2004 entsteht aus höheren Einkommen von $5.2 Million, niedrigerer Forschung und Entwicklungsaufwand von $1.7 Million, niedrigeres Marketing und geschäftliche Entwicklung Unkosten von $0.3 Million, Versatz durch auf lagerausgleich Unkosten von $0.8 Million und höhere allgemeine und Verwaltungskosten von $0.7 Million. Die erhöhten Einkommen resultieren aus den genehmigenden Einkommen, die im zweiten Viertel resultierend aus Anerkennung in Einkommen der restlichen Ertragsabgrenzungen Balance erkannt werden, die auf Theratope (R) bezogen wird dem Impfstoff wegen der Rückkehr Theratope Entwicklung und Kommerzialisierungder rechte von Merck KGaA von Darmstadt, Deutschland, das im Juni 2004 verkündet wird.
Vertrag Forschung und Entwicklung Einkommen für die neun Monate beendete 30. September 2004 und zählte $1.3 Million verglichen bis $2.0 Million während der gleichen Periode 2003 zusammen, stellt Vertrag Forschung und Entwicklung die Finanzierung dar, die von Merck KGaA empfangen wurde, das mit Theratope und Impfstoff des Liposom-BLP25 (L-BLP25) verbunden ist. Die verringerte Finanzierung reflektiert einen Lower level der klinischen Tätigkeit mit dem Wind unten des Theratope Phase III Versuches, und das Unblinding des Phase L-BLP25 IIb Versuches resultiert. Genehmigende Einkommen von den gemeinschaftlichen Vorbereitungen für die neun Monate beendeten 30. September 2004 und zählten $6.5 Million verglichen bis $0.8 Million während der gleichen Periode 2003 zusammen, stellen die Tilgung der upfront Zahlungen dar, die von Merck KGaA und upfront von Vor-genehmigender Gebühr von CancerVac nach Anfang der jeweiligen collaborations empfangen wurden. Das zweite Viertel schloß eine Hinzufügung zum Einkommen von $5.9 Million die Anerkennung in Einkommen der restlichen Ertragsabgrenzungen Balance von Merck KGaA darstellend ein, das auf Theratope bezogen wurde. Schließlich bezieht die Zunahme von $0.2 Million des Genehmigens, der Abgaben und anderen Einkommens auf den Vertrag Herstellung Tätigkeiten, die verschiedene Biomira patentierte Technologien und Mittel für außergebietliche Abnehmer verwenden.
Forschung und Entwicklungsaufwand für die neun Monate beendete 30. September 2004 zusammenzählte $10.2 Million verglichen bis $11.9 Million während der gleichen Periode 2003. Die Abnahme Forschung und am Entwicklungsaufwand, die die Menge des gemeinschaftlichen finanziereneinkommens beeinflußt, ist der klinischen Tätigkeiten unten wickeln ähnlich zuzuschreibend. Aufwendungen schließen bis jetzt bestätigende klinische vorwegnehmende Probekosten L-BLP25 einschließlich Entwicklung der klinischen Protokolle und der Beschaffung und Herstellung der klinischen Materialien ein. Zusätzlich schließen andere Kosten klinischen Aufstellungsort aufwickeln oben Unkosten der bestehenden klinischen Versuche und die Aufwendungen, die auf der Anschlußuntersuchung in die Einheit der Klage auf die Theratope Hormonbehandlungteilmenge bezogen werden mit ein. Allgemeine und Verwaltungskosten für die neun Monate beendeten 30. September 2004 zusammenzählten $4.7 Million verglichen bis $4.0 Million während der gleichen Periode 2003. Die Zunahme von $0.7 Million liegt an den Unkosten hauptsächlich, die auf der Regalausrichtung sowie die zusätzlichen Kosten bezogen werden, die auf der Regelung eines hervorragenden Rechtsstreites im ersten Viertel bezogen werden. Marketing und geschäftliche Entwicklung Aufwendungen für die neun Monate beendeten 30. September 2004 zusammenzählten $1.0 Million verglichen bis $1.3 Million während der gleichen Periode 2003. Die Abnahme von Resultaten $0.3 Million von einer Verringerung vor-stoßen die Tätigkeiten aus, die zu passend sind, verzögert in der Kommerzialisierung von Theratope. Marketing und geschäftliche Entwicklung Aufwendungen schließen die korporativen Verwaltungskosten ein, die mit diesen Funktionen, sowie die Kosten verbunden sind, die mit den genehmigenden Tätigkeiten verbunden sind, die auf vor-klinisches und frühes Stadium Technologien bezogen werden.
Stock compensation expense of $0.8 million for the nine months ended September 30, 2004 represents the amortization of the estimated fair value of options granted since January 1, 2002 applicable to the current period. The retroactive application of CICA Handbook Section 3870 with respect to recognition of stock compensation expense for 2002 and 2003 resulted in a $1.6 million charge to opening deficit.
Investment and other income for the nine months ended September 30, 2004, totalling $0.5 million, was similar to the same period in 2003. Investment and other income comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. Income from cash and investments totalled $0.5 million for the nine months ended September 30, 2004 compared to $0.9 million for the same period in 2003 as a result of lower average cash and investment balances. This reduction in investment income has been offset by a net foreign exchange gain of $0.03 million for the nine months ended September 30, 2004 compared to a net foreign exchange loss of $0.4 million for the same period in 2003.
Biomira`s financial reserves total $26.8 million in cash and short-term investments as at September 30, 2004, a decrease of $14.7 million from the year end position due to funding of operations.
Corporate Update ---------------- L-BLP25
The U.S. Food and Drug Administration (FDA) granted Fast Track status to the investigation of L-BLP25 for its proposed use in the treatment of non-small cell lung cancer (NSCLC). This designation will potentially facilitate the development of this product candidate and expedite review of the drug candidate once Biomira and its collaborator, Merck KGaA are in a position to seek FDA approval.
The Fast Track program was put in place to allow for the review of drugs to treat serious or life-threatening conditions and that demonstrate the potential to address unmet medical needs. Importantly, there is the potential for more interactions between the Companies and the FDA as L-BLP25 moves forward in the clinical trial process and opens the door to a possible U.S. biologics licensing application (BLA) on a rolling basis, as data become available. Due to the fact that products approved for Fast Track designation meet unmet medical needs and address serious or life-threatening conditions, they generally are eligible for priority review, which could decrease the typical review period.
"Our aim is to show efficacy of L-BLP25 in treating NSCLC and get the product candidate approved and available to patients as quickly as possible. The FDA`s Fast Track designation is, therefore, an important step in that process," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc. "We believe if we can one day address a sizeable unmet medical need in this patient population and do it in a more timely manner we are achieving significant milestones for the Company and our stakeholders. Providing a new treatment option for men and women with NSCLC is an important focus as the Company moves forward."
L-BLP25 ist ein anderes Beispiel Merck KGaAs des Ziels des Entwickelns der erfinderischen gerichteten Therapien für die Behandlung des Krebses, "sagte Dr. Bernhard Ehmer, MD, Vizepräsident und Kopf Merck KGaAs des Onkologie-Geschäftsbereichs.
Schloß schnelle Anwendung Schiene Biomiras auf der FDA anregenresultate von einer kontrollierten, randomisierten Phase IIb Studie im Stadium IIIB und IV NSCLC von den Patienten ein. Die Resultate werden festgelegt, an der upcoming europäischen Gesellschaft der medizinischen Onkologiesitzung (ESMO) dargestellt zu werden. Die Sitzung ist, in Wien, Österreich stattzufinden und die Darstellung soll am 1. November gebildet werden.
In der Vorbereitung für den großen multinationalen bestätigenden Versuch, hat Biomira Herstellung der neuen vaccine Versorgungsmaterialien begonnen. Diese Herstellung enthält die änderungen, die das zukünftige kommerzielle Versorgungsmaterial des Impfstoffs sichern sollen. Scheduling diese änderungen sollte jetzt sichergehen, daß die resultierenden Angeldaten als Repräsentanten der Sicherheit und der Wirksamkeit des kommerziellen Versorgungsmaterials vom Impfstoff gelten. Ein Vergleichbarkeitplan, der eine kleine klinische Sicherheit Studie des neuen Materials in der erweiterten Bevölkerung einschließt, schlug für den größeren Versuch, wird besprochen mit Aufsichtsbehörden vor. Die kleine Studie wird festgelegt, parallel zu Vorbereitungen für die größere bestätigende Studie geleitet zu werden und wird nicht erwartet, um timelines für das Beginnen dieser Studie zu beeinflussen.
Biomira Pläne, zum von von Gesprächen mit anderen Aufsichtsbehörden betreffend sind die Möglichkeit einer frühen Anwendung für die Zustimmung fortzusetzen basiert auf gegenwärtigen Daten, obgleich eine bestätigende Studie wahrscheinlich in den Märkten wie den US, dem Europa und dem Japan notwendig ist.
Theratope
Eine bestätigende Studie in der Teilmenge der Patienten von unserem vorhergehenden Phase III Brustkrebsversuch, der längeres überleben auf dem vaccine Arm hatte, würde vermutlich vor Kommerzialisierung in Kanada, in den US, in Europa und in Japan angefordert. Biomira ist Planung Herstellung des neuen Theratope Materials, zum solch einer möglicher bestätigender Studie zu liefern. Das neue Material schließt eine änderung am hilfreichen Bestandteil ein, der erwartet wird, um die Frequenz der geduldigen Einspritzungaufstellungsortreaktionen zu verringern. Der Vergleichbarkeitplan, der diese änderung auswertet, schließt vermutlich eine kleine klinische Studie ein, um die Sicherheit und die Immunisierungsfähigkeit des neuen Materials zu messen. Diese Studie wird erwartet, um zur Hälfte erste von 2005 zu beginnen. Während die Firma einen gemeinschaftlichen Partner sucht, um Theratope weiter zu entwickeln, fährt sie fort, die Einheit der Klage auf Theratope zu erforschen und forscht auch mögliche Gelegenheiten in anderen Ländern für die frühe Ausrichtung nach, die auf den gegenwärtigen Teilmenge Daten basiert.
Biomira Inc.
Biomira ist eine Biotechnologiefirma, die auf die Entwicklung der erfinderischen therapeutischen Annäherungen zum Krebsmanagement sich spezialisiert. Verpflichtung Biomiras gegenüber der Behandlung des Krebses konzentriert z.Z. auf die Entwicklung der synthetischen Impfstoffe und der Romanstrategien für Krebs Immunotherapy. Wir sind die Krebs-Vaccine Leute (TM).
Biomira Inc. VEREINIGTE BILANZAUFSTELLUNGEN (kanadische Dollar, in den Tausenden, ausgenommen Zahl der Anteile) September 30. Dezember 2004 31, 2003 (nicht geprüft) (nichtes geprüft,), (X) -------------------------- WERTE bezahlten gegenwärtige Bargeld- und Bargeldäquivalent$ 6.477 $ 24.062 kurzfristige Investitionen 20.304 17.443 Außenstände 329 459 Unkosten 187 460 voraus -------------------------- 27.297 42.424 Kapitalvermögen (Netz) 477 641 langfristige Investitionen 264 - -------------------------- $ 28.038 $ 43.065 -------------------------- -------------------------- VERBINDLICHKEITEN gegenwärtige fällige Rechnungen und anfallende Verbindlichkeiten $ 1.935 $ 3.453 Leasingvertrag mit Aktivierungspflichtverpflichtung 25 Teil mit 108 Strömen Ertragsabgrenzungen 800 1.053 -------------------------- 2.760 4.614 Ertragsabgrenzungen 1.295 6.671 Kategorie A Vorzugsaktien 30 30 -------------------------- Aktienkapital die BILLIGKEIT 4.085 11.315 AKTIONÄRE 359.728 359.643 Ermächtigungen 8.555 8.555 trug überschuß 11.236 Defizit 8.901 bei (355.566) (345.349) -------------------------- 23.953 31.750 -------------------------- $ 28.038 $ 43.065 -------------------------- -------------------------- Allgemeine Anteile herausgegeben und hervorragende 72.562.357 72.545.232 (CAD $
WARNING: SYSTRAN did not translate the document entirely. The document exceeds the maximum size allowed by the solution.(4096 bytes for plain text)
1.00 (equal sign) USD $0.79) (x) Figures excerpted from the 2003 audited consolidated financial statements. Biomira Inc. CONSOLIDATED STATEMENTS OF OPERATIONS (Canadian dollars, in thousands, except per share amounts) Three Months Ended Nine Months Ended September 30 September 30 (Unaudited) (Unaudited) (Unaudited) (Unaudited) ----------------------------------------------- 2004 2003 2004 2003 ---- ---- ---- ---- REVENUE Contract research and development $ 418 $ 414 $ 1,261 $ 1,951 Licensing revenue from collaborative agreements 52 264 6,487 790 Licensing, royalties and other revenue 61 1 219 1 ----------------------------------------------- 531 679 7,967 2,742 ----------------------------------------------- EXPENSES Research and development 3,163 3,433 10,178 11,847 General and administrative 1,382 1,208 4,739 4,033 Marketing and business development 258 505 1,045 1,335 Stock compensation expense 260 - 812 - Amortization of capital assets 89 112 290 350 Gain on disposal of capital assets (2) - (2) (58) ----------------------------------------------- 5,150 5,258 17,062 17,507 ----------------------------------------------- OPERATING LOSS (4,619) (4,579) (9,095) (14,765) Investment and other (expense) income (167) 150 515 458 Interest expense (2) (6) (5) (17) ----------------------------------------------- LOSS BEFORE INCOME TAXES (4,788) (4,435) (8,585) (14,324) Income tax provision (16) (15) (59) (18) ----------------------------------------------- NET LOSS $ (4,804) $ (4,450) $ (8,644) $ (14,342) ----------------------------------------------- ----------------------------------------------- BASIC AND DILUTED LOSS PER SHARE $ (0.07) $ (0.08) $ (0.12) $ (0.25) WEIGHTED AVERAGE NUMBER OF COMMON SHARES OUTSTANDING (in thousands) 72,560 59,145 72,560 59,145 CONSOLIDATED STATEMENTS OF DEFICIT (Canadian dollars, in thousands) Three Months Ended Nine Months Ended September 30 September 30 (Unaudited) (Unaudited) (Unaudited) (Unaudited) ----------------------------------------------- 2004 2003 2004 2003 ---- ---- ---- ---- DEFICIT, BEGINNING OF PERIOD $ (350,762) $ (336,267) $ (346,922) $ (326,101) Net loss for the period (4,804) (4,450) (8,644) (14,342) Accretion of convertible debentures - - - (713) Interest, foreign exchange gain (loss), and carrying charges on convertible debentures - - - 439 ----------------------------------------------- DEFICIT, END OF PERIOD $ (355,566) $ (340,717) $ (355,566) $ (340,717) ----------------------------------------------- ----------------------------------------------- Biomira Inc. CONSOLIDATED STATEMENTS OF CASH FLOW (Canadian dollars, in thousands) Three Months Ended Nine Months Ended September 30 September 30 (Unaudited) (Unaudited) (Unaudited) (Unaudited) 2004 2003 2004 2003 ---- ---- ---- ---- OPERATING Net loss $ (4,804) $ (4,450) $ (8,644) $ (14,342) Amortization of capital assets 89 112 290 350 Stock compensation expense 260 - 812 - Increase (decrease) in deferred revenue 542 (264) (5,893) (790) Gain on disposal of capital assets (2) - (2) (58) Unrealized foreign exchange loss (gain) 103 (187) 33 233 Net change in non-cash balances from operations: Accounts receivable 47 434 130 625 Prepaid expenses 483 199 273 122 Accounts payable and accrued liabilities (501) (581) (1,529) (4,703) ----------------------------------------------- (3,783) (4,737) (14,530) (18,563) ----------------------------------------------- INVESTING Decrease (increase) in short-term investments 3,730 7,442 (2,861) 17,753 Purchase of capital assets (47) (12) (115) (12) Proceeds on disposal of capital assets 2 - 2 73 ----------------------------------------------- 3,685 7,430 (2,974) 17,814 ----------------------------------------------- FINANCING Proceeds on issue of common shares, net of issue costs - 6 35 15,524 Repayment of convertible debentures - - - (7,826) Interest on convertible debentures - - - (91) Repayment of capital lease obligation (23) (38) (83) (115) ----------------------------------------------- (23) (32) (48) 7,492 ----------------------------------------------- NET CASH (OUTFLOW) INFLOW (121) 2,661 (17,552) 6,743 Effect of exchange rate fluctuations on cash and cash equivalents (103) 187 (33) (233) ----------------------------------------------- (DECREASE) INCREASE IN CASH AND CASH EQUIVALENTS DURING THE PERIOD (224) 2,848 (17,585) 6,510 CASH AND CASH EQUIVALENTS, BEGINNING OF PERIOD 6,701 12,169 24,062 8,507 ----------------------------------------------- CASH AND CASH EQUIVALENTS, END OF PERIOD $ 6,477 $ 15,017 $ 6,477 $ 15,017 ----------------------------------------------- ----------------------------------------------- SUPPLEMENTAL DISCLOSURE OF CASH FLOW INFORMATION Amount of interest paid $ 2 $ 6 $ 5 $ 17 Amount of income taxes paid $ - $ - $ - $ 5
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing of clinical trials, trial reviews and analyses and regulatory review and approvals or the safety and efficacy of product or the availability of capital and financing. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
Biomira Inc
Biomira Inc. verkündet 3. Viertelresultate
EDMONTON, 28. Okt. /PRNewswire-FirstCall/ -- Biomira (Nachrichten) (TSX: BÜSTENHALTER) berichtete heute über finanzielle Resultate für die neun Monate beendet 30. September 2004.
Finanzielles Update ----------------
Finanzielle Resultate für die neun Monate beendet 30. September 2004 reflektieren einen vereinigten Nettobetriebsverlust $8.6 von Million oder von $0.12 pro den Anteil, der bis $14.3 Million oder $0.25 pro Anteil während der gleichen Periode 2003 verglichen wird. Der verringerte Verlust von $5.7 Million 2004 entsteht aus höheren Einkommen von $5.2 Million, niedrigerer Forschung und Entwicklungsaufwand von $1.7 Million, niedrigeres Marketing und geschäftliche Entwicklung Unkosten von $0.3 Million, Versatz durch auf lagerausgleich Unkosten von $0.8 Million und höhere allgemeine und Verwaltungskosten von $0.7 Million. Die erhöhten Einkommen resultieren aus den genehmigenden Einkommen, die im zweiten Viertel resultierend aus Anerkennung in Einkommen der restlichen Ertragsabgrenzungen Balance erkannt werden, die auf Theratope (R) bezogen wird dem Impfstoff wegen der Rückkehr Theratope Entwicklung und Kommerzialisierungder rechte von Merck KGaA von Darmstadt, Deutschland, das im Juni 2004 verkündet wird.
Vertrag Forschung und Entwicklung Einkommen für die neun Monate beendete 30. September 2004 und zählte $1.3 Million verglichen bis $2.0 Million während der gleichen Periode 2003 zusammen, stellt Vertrag Forschung und Entwicklung die Finanzierung dar, die von Merck KGaA empfangen wurde, das mit Theratope und Impfstoff des Liposom-BLP25 (L-BLP25) verbunden ist. Die verringerte Finanzierung reflektiert einen Lower level der klinischen Tätigkeit mit dem Wind unten des Theratope Phase III Versuches, und das Unblinding des Phase L-BLP25 IIb Versuches resultiert. Genehmigende Einkommen von den gemeinschaftlichen Vorbereitungen für die neun Monate beendeten 30. September 2004 und zählten $6.5 Million verglichen bis $0.8 Million während der gleichen Periode 2003 zusammen, stellen die Tilgung der upfront Zahlungen dar, die von Merck KGaA und upfront von Vor-genehmigender Gebühr von CancerVac nach Anfang der jeweiligen collaborations empfangen wurden. Das zweite Viertel schloß eine Hinzufügung zum Einkommen von $5.9 Million die Anerkennung in Einkommen der restlichen Ertragsabgrenzungen Balance von Merck KGaA darstellend ein, das auf Theratope bezogen wurde. Schließlich bezieht die Zunahme von $0.2 Million des Genehmigens, der Abgaben und anderen Einkommens auf den Vertrag Herstellung Tätigkeiten, die verschiedene Biomira patentierte Technologien und Mittel für außergebietliche Abnehmer verwenden.
Forschung und Entwicklungsaufwand für die neun Monate beendete 30. September 2004 zusammenzählte $10.2 Million verglichen bis $11.9 Million während der gleichen Periode 2003. Die Abnahme Forschung und am Entwicklungsaufwand, die die Menge des gemeinschaftlichen finanziereneinkommens beeinflußt, ist der klinischen Tätigkeiten unten wickeln ähnlich zuzuschreibend. Aufwendungen schließen bis jetzt bestätigende klinische vorwegnehmende Probekosten L-BLP25 einschließlich Entwicklung der klinischen Protokolle und der Beschaffung und Herstellung der klinischen Materialien ein. Zusätzlich schließen andere Kosten klinischen Aufstellungsort aufwickeln oben Unkosten der bestehenden klinischen Versuche und die Aufwendungen, die auf der Anschlußuntersuchung in die Einheit der Klage auf die Theratope Hormonbehandlungteilmenge bezogen werden mit ein. Allgemeine und Verwaltungskosten für die neun Monate beendeten 30. September 2004 zusammenzählten $4.7 Million verglichen bis $4.0 Million während der gleichen Periode 2003. Die Zunahme von $0.7 Million liegt an den Unkosten hauptsächlich, die auf der Regalausrichtung sowie die zusätzlichen Kosten bezogen werden, die auf der Regelung eines hervorragenden Rechtsstreites im ersten Viertel bezogen werden. Marketing und geschäftliche Entwicklung Aufwendungen für die neun Monate beendeten 30. September 2004 zusammenzählten $1.0 Million verglichen bis $1.3 Million während der gleichen Periode 2003. Die Abnahme von Resultaten $0.3 Million von einer Verringerung vor-stoßen die Tätigkeiten aus, die zu passend sind, verzögert in der Kommerzialisierung von Theratope. Marketing und geschäftliche Entwicklung Aufwendungen schließen die korporativen Verwaltungskosten ein, die mit diesen Funktionen, sowie die Kosten verbunden sind, die mit den genehmigenden Tätigkeiten verbunden sind, die auf vor-klinisches und frühes Stadium Technologien bezogen werden.
Stock compensation expense of $0.8 million for the nine months ended September 30, 2004 represents the amortization of the estimated fair value of options granted since January 1, 2002 applicable to the current period. The retroactive application of CICA Handbook Section 3870 with respect to recognition of stock compensation expense for 2002 and 2003 resulted in a $1.6 million charge to opening deficit.
Investment and other income for the nine months ended September 30, 2004, totalling $0.5 million, was similar to the same period in 2003. Investment and other income comprise income from cash and investments, non-operating income, and foreign exchange gains and losses. Income from cash and investments totalled $0.5 million for the nine months ended September 30, 2004 compared to $0.9 million for the same period in 2003 as a result of lower average cash and investment balances. This reduction in investment income has been offset by a net foreign exchange gain of $0.03 million for the nine months ended September 30, 2004 compared to a net foreign exchange loss of $0.4 million for the same period in 2003.
Biomira`s financial reserves total $26.8 million in cash and short-term investments as at September 30, 2004, a decrease of $14.7 million from the year end position due to funding of operations.
Corporate Update ---------------- L-BLP25
The U.S. Food and Drug Administration (FDA) granted Fast Track status to the investigation of L-BLP25 for its proposed use in the treatment of non-small cell lung cancer (NSCLC). This designation will potentially facilitate the development of this product candidate and expedite review of the drug candidate once Biomira and its collaborator, Merck KGaA are in a position to seek FDA approval.
The Fast Track program was put in place to allow for the review of drugs to treat serious or life-threatening conditions and that demonstrate the potential to address unmet medical needs. Importantly, there is the potential for more interactions between the Companies and the FDA as L-BLP25 moves forward in the clinical trial process and opens the door to a possible U.S. biologics licensing application (BLA) on a rolling basis, as data become available. Due to the fact that products approved for Fast Track designation meet unmet medical needs and address serious or life-threatening conditions, they generally are eligible for priority review, which could decrease the typical review period.
"Our aim is to show efficacy of L-BLP25 in treating NSCLC and get the product candidate approved and available to patients as quickly as possible. The FDA`s Fast Track designation is, therefore, an important step in that process," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc. "We believe if we can one day address a sizeable unmet medical need in this patient population and do it in a more timely manner we are achieving significant milestones for the Company and our stakeholders. Providing a new treatment option for men and women with NSCLC is an important focus as the Company moves forward."
L-BLP25 ist ein anderes Beispiel Merck KGaAs des Ziels des Entwickelns der erfinderischen gerichteten Therapien für die Behandlung des Krebses, "sagte Dr. Bernhard Ehmer, MD, Vizepräsident und Kopf Merck KGaAs des Onkologie-Geschäftsbereichs.
Schloß schnelle Anwendung Schiene Biomiras auf der FDA anregenresultate von einer kontrollierten, randomisierten Phase IIb Studie im Stadium IIIB und IV NSCLC von den Patienten ein. Die Resultate werden festgelegt, an der upcoming europäischen Gesellschaft der medizinischen Onkologiesitzung (ESMO) dargestellt zu werden. Die Sitzung ist, in Wien, Österreich stattzufinden und die Darstellung soll am 1. November gebildet werden.
In der Vorbereitung für den großen multinationalen bestätigenden Versuch, hat Biomira Herstellung der neuen vaccine Versorgungsmaterialien begonnen. Diese Herstellung enthält die änderungen, die das zukünftige kommerzielle Versorgungsmaterial des Impfstoffs sichern sollen. Scheduling diese änderungen sollte jetzt sichergehen, daß die resultierenden Angeldaten als Repräsentanten der Sicherheit und der Wirksamkeit des kommerziellen Versorgungsmaterials vom Impfstoff gelten. Ein Vergleichbarkeitplan, der eine kleine klinische Sicherheit Studie des neuen Materials in der erweiterten Bevölkerung einschließt, schlug für den größeren Versuch, wird besprochen mit Aufsichtsbehörden vor. Die kleine Studie wird festgelegt, parallel zu Vorbereitungen für die größere bestätigende Studie geleitet zu werden und wird nicht erwartet, um timelines für das Beginnen dieser Studie zu beeinflussen.
Biomira Pläne, zum von von Gesprächen mit anderen Aufsichtsbehörden betreffend sind die Möglichkeit einer frühen Anwendung für die Zustimmung fortzusetzen basiert auf gegenwärtigen Daten, obgleich eine bestätigende Studie wahrscheinlich in den Märkten wie den US, dem Europa und dem Japan notwendig ist.
Theratope
Eine bestätigende Studie in der Teilmenge der Patienten von unserem vorhergehenden Phase III Brustkrebsversuch, der längeres überleben auf dem vaccine Arm hatte, würde vermutlich vor Kommerzialisierung in Kanada, in den US, in Europa und in Japan angefordert. Biomira ist Planung Herstellung des neuen Theratope Materials, zum solch einer möglicher bestätigender Studie zu liefern. Das neue Material schließt eine änderung am hilfreichen Bestandteil ein, der erwartet wird, um die Frequenz der geduldigen Einspritzungaufstellungsortreaktionen zu verringern. Der Vergleichbarkeitplan, der diese änderung auswertet, schließt vermutlich eine kleine klinische Studie ein, um die Sicherheit und die Immunisierungsfähigkeit des neuen Materials zu messen. Diese Studie wird erwartet, um zur Hälfte erste von 2005 zu beginnen. Während die Firma einen gemeinschaftlichen Partner sucht, um Theratope weiter zu entwickeln, fährt sie fort, die Einheit der Klage auf Theratope zu erforschen und forscht auch mögliche Gelegenheiten in anderen Ländern für die frühe Ausrichtung nach, die auf den gegenwärtigen Teilmenge Daten basiert.
Biomira Inc.
Biomira ist eine Biotechnologiefirma, die auf die Entwicklung der erfinderischen therapeutischen Annäherungen zum Krebsmanagement sich spezialisiert. Verpflichtung Biomiras gegenüber der Behandlung des Krebses konzentriert z.Z. auf die Entwicklung der synthetischen Impfstoffe und der Romanstrategien für Krebs Immunotherapy. Wir sind die Krebs-Vaccine Leute (TM).
Biomira Inc. VEREINIGTE BILANZAUFSTELLUNGEN (kanadische Dollar, in den Tausenden, ausgenommen Zahl der Anteile) September 30. Dezember 2004 31, 2003 (nicht geprüft) (nichtes geprüft,), (X) -------------------------- WERTE bezahlten gegenwärtige Bargeld- und Bargeldäquivalent$ 6.477 $ 24.062 kurzfristige Investitionen 20.304 17.443 Außenstände 329 459 Unkosten 187 460 voraus -------------------------- 27.297 42.424 Kapitalvermögen (Netz) 477 641 langfristige Investitionen 264 - -------------------------- $ 28.038 $ 43.065 -------------------------- -------------------------- VERBINDLICHKEITEN gegenwärtige fällige Rechnungen und anfallende Verbindlichkeiten $ 1.935 $ 3.453 Leasingvertrag mit Aktivierungspflichtverpflichtung 25 Teil mit 108 Strömen Ertragsabgrenzungen 800 1.053 -------------------------- 2.760 4.614 Ertragsabgrenzungen 1.295 6.671 Kategorie A Vorzugsaktien 30 30 -------------------------- Aktienkapital die BILLIGKEIT 4.085 11.315 AKTIONÄRE 359.728 359.643 Ermächtigungen 8.555 8.555 trug überschuß 11.236 Defizit 8.901 bei (355.566) (345.349) -------------------------- 23.953 31.750 -------------------------- $ 28.038 $ 43.065 -------------------------- -------------------------- Allgemeine Anteile herausgegeben und hervorragende 72.562.357 72.545.232 (CAD $
WARNING: SYSTRAN did not translate the document entirely. The document exceeds the maximum size allowed by the solution.(4096 bytes for plain text)
1.00 (equal sign) USD $0.79) (x) Figures excerpted from the 2003 audited consolidated financial statements. Biomira Inc. CONSOLIDATED STATEMENTS OF OPERATIONS (Canadian dollars, in thousands, except per share amounts) Three Months Ended Nine Months Ended September 30 September 30 (Unaudited) (Unaudited) (Unaudited) (Unaudited) ----------------------------------------------- 2004 2003 2004 2003 ---- ---- ---- ---- REVENUE Contract research and development $ 418 $ 414 $ 1,261 $ 1,951 Licensing revenue from collaborative agreements 52 264 6,487 790 Licensing, royalties and other revenue 61 1 219 1 ----------------------------------------------- 531 679 7,967 2,742 ----------------------------------------------- EXPENSES Research and development 3,163 3,433 10,178 11,847 General and administrative 1,382 1,208 4,739 4,033 Marketing and business development 258 505 1,045 1,335 Stock compensation expense 260 - 812 - Amortization of capital assets 89 112 290 350 Gain on disposal of capital assets (2) - (2) (58) ----------------------------------------------- 5,150 5,258 17,062 17,507 ----------------------------------------------- OPERATING LOSS (4,619) (4,579) (9,095) (14,765) Investment and other (expense) income (167) 150 515 458 Interest expense (2) (6) (5) (17) ----------------------------------------------- LOSS BEFORE INCOME TAXES (4,788) (4,435) (8,585) (14,324) Income tax provision (16) (15) (59) (18) ----------------------------------------------- NET LOSS $ (4,804) $ (4,450) $ (8,644) $ (14,342) ----------------------------------------------- ----------------------------------------------- BASIC AND DILUTED LOSS PER SHARE $ (0.07) $ (0.08) $ (0.12) $ (0.25) WEIGHTED AVERAGE NUMBER OF COMMON SHARES OUTSTANDING (in thousands) 72,560 59,145 72,560 59,145 CONSOLIDATED STATEMENTS OF DEFICIT (Canadian dollars, in thousands) Three Months Ended Nine Months Ended September 30 September 30 (Unaudited) (Unaudited) (Unaudited) (Unaudited) ----------------------------------------------- 2004 2003 2004 2003 ---- ---- ---- ---- DEFICIT, BEGINNING OF PERIOD $ (350,762) $ (336,267) $ (346,922) $ (326,101) Net loss for the period (4,804) (4,450) (8,644) (14,342) Accretion of convertible debentures - - - (713) Interest, foreign exchange gain (loss), and carrying charges on convertible debentures - - - 439 ----------------------------------------------- DEFICIT, END OF PERIOD $ (355,566) $ (340,717) $ (355,566) $ (340,717) ----------------------------------------------- ----------------------------------------------- Biomira Inc. CONSOLIDATED STATEMENTS OF CASH FLOW (Canadian dollars, in thousands) Three Months Ended Nine Months Ended September 30 September 30 (Unaudited) (Unaudited) (Unaudited) (Unaudited) 2004 2003 2004 2003 ---- ---- ---- ---- OPERATING Net loss $ (4,804) $ (4,450) $ (8,644) $ (14,342) Amortization of capital assets 89 112 290 350 Stock compensation expense 260 - 812 - Increase (decrease) in deferred revenue 542 (264) (5,893) (790) Gain on disposal of capital assets (2) - (2) (58) Unrealized foreign exchange loss (gain) 103 (187) 33 233 Net change in non-cash balances from operations: Accounts receivable 47 434 130 625 Prepaid expenses 483 199 273 122 Accounts payable and accrued liabilities (501) (581) (1,529) (4,703) ----------------------------------------------- (3,783) (4,737) (14,530) (18,563) ----------------------------------------------- INVESTING Decrease (increase) in short-term investments 3,730 7,442 (2,861) 17,753 Purchase of capital assets (47) (12) (115) (12) Proceeds on disposal of capital assets 2 - 2 73 ----------------------------------------------- 3,685 7,430 (2,974) 17,814 ----------------------------------------------- FINANCING Proceeds on issue of common shares, net of issue costs - 6 35 15,524 Repayment of convertible debentures - - - (7,826) Interest on convertible debentures - - - (91) Repayment of capital lease obligation (23) (38) (83) (115) ----------------------------------------------- (23) (32) (48) 7,492 ----------------------------------------------- NET CASH (OUTFLOW) INFLOW (121) 2,661 (17,552) 6,743 Effect of exchange rate fluctuations on cash and cash equivalents (103) 187 (33) (233) ----------------------------------------------- (DECREASE) INCREASE IN CASH AND CASH EQUIVALENTS DURING THE PERIOD (224) 2,848 (17,585) 6,510 CASH AND CASH EQUIVALENTS, BEGINNING OF PERIOD 6,701 12,169 24,062 8,507 ----------------------------------------------- CASH AND CASH EQUIVALENTS, END OF PERIOD $ 6,477 $ 15,017 $ 6,477 $ 15,017 ----------------------------------------------- ----------------------------------------------- SUPPLEMENTAL DISCLOSURE OF CASH FLOW INFORMATION Amount of interest paid $ 2 $ 6 $ 5 $ 17 Amount of income taxes paid $ - $ - $ - $ 5
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing of clinical trials, trial reviews and analyses and regulatory review and approvals or the safety and efficacy of product or the availability of capital and financing. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
Biomira Inc
Fazit:
Der Verlust hat sich halbiert!!!
Umsatz konnte mit den Lizenzen gesteigert werden!!!
Der Cashbestand ist weiter zurück gegangen ,sollte aber auch noch für das 2005 reichen!!!
Für Theratope wird weiter ein Partner gesucht und sogar weitere Test werden geplant von einigen Zulassungen durch die FDA ganz zu schweigen die angepeilt werden!
Aber alles ist nigs zur dieser Aussage:
"L-BLP25 is another example of Merck KGaA`s goal of developing innovative targeted therapies for the treatment of cancer," said Dr. Bernhard Ehmer, MD, Vice President and Head of Merck KGaA`s Oncology Business Area.
Luftblase oder der Hauptgewinn???
Leider stehen wir weiterhin im dunkeln!

Der Verlust hat sich halbiert!!!
Umsatz konnte mit den Lizenzen gesteigert werden!!!
Der Cashbestand ist weiter zurück gegangen ,sollte aber auch noch für das 2005 reichen!!!
Für Theratope wird weiter ein Partner gesucht und sogar weitere Test werden geplant von einigen Zulassungen durch die FDA ganz zu schweigen die angepeilt werden!
Aber alles ist nigs zur dieser Aussage:
"L-BLP25 is another example of Merck KGaA`s goal of developing innovative targeted therapies for the treatment of cancer," said Dr. Bernhard Ehmer, MD, Vice President and Head of Merck KGaA`s Oncology Business Area.
Luftblase oder der Hauptgewinn???
Leider stehen wir weiterhin im dunkeln!

@donnerpower
Klare Aussagen konnten gestern nicht erwartet werden.
Denke an die letzte Sperrung von BIOM, weil die zu früh etwas rausgelassen hatten.
Heute ist letzter Tag für die Amis, sich einzudecken.
#849
Wir handeln doch nicht mit "TSX: Büstenhaltern"


Klare Aussagen konnten gestern nicht erwartet werden.
Denke an die letzte Sperrung von BIOM, weil die zu früh etwas rausgelassen hatten.
Heute ist letzter Tag für die Amis, sich einzudecken.
#849
Wir handeln doch nicht mit "TSX: Büstenhaltern"



Hier zwei engl. Beiträge:
Eine erfolgreiche Woche wünscht
verdi
---------------
Phacilitate Forum Follows ESMO
by: messaaaa
Long-Term Sentiment: Strong Buy 10/31/04 08:22 am
Msg: 159362 of 159373
November 4, 2004
3:15 PM - 3:45 PM EST
Cambridge, MA Phacilitate Vaccine Forum Fall 2004, Dr. Alex McPherson
Dr. McPherson will present a case study on Biomira`s cancer vaccines at this conference, which is being held at the Hyatt Regency Hotel, Cambridge, MA from November 2-5, 2004.
Tloutrec: Re: Monday`s Biomira BigDay
by: bt33_1998
10/31/04 08:52 am
Msg: 159366 of 159373
For Biomira`s Big Day , the company would have had to "set-up" for a PR company to assist in the RELEASE OF THIS IMPORTANT INFORMATION , to the media. Biomira`s management neither has the intelligence, the savvy, and the responsibility to shareholders to have planned for this important event. So on Monday, when you see the data and the findings....and watch the stock react , in a meager manner, you will know why. By Friday, of the week, you will see my point. All in my opinion, for this well run, well managed company.
Eine erfolgreiche Woche wünscht
verdi
---------------
Phacilitate Forum Follows ESMO
by: messaaaa
Long-Term Sentiment: Strong Buy 10/31/04 08:22 am
Msg: 159362 of 159373
November 4, 2004
3:15 PM - 3:45 PM EST
Cambridge, MA Phacilitate Vaccine Forum Fall 2004, Dr. Alex McPherson
Dr. McPherson will present a case study on Biomira`s cancer vaccines at this conference, which is being held at the Hyatt Regency Hotel, Cambridge, MA from November 2-5, 2004.
Tloutrec: Re: Monday`s Biomira BigDay
by: bt33_1998
10/31/04 08:52 am
Msg: 159366 of 159373
For Biomira`s Big Day , the company would have had to "set-up" for a PR company to assist in the RELEASE OF THIS IMPORTANT INFORMATION , to the media. Biomira`s management neither has the intelligence, the savvy, and the responsibility to shareholders to have planned for this important event. So on Monday, when you see the data and the findings....and watch the stock react , in a meager manner, you will know why. By Friday, of the week, you will see my point. All in my opinion, for this well run, well managed company.
...das sieht ja heute wieder fantastisch gut aus!!!
Name
Biomira Inc
Last Price
1.6400
Net Change
+0.2400
Shares Matched
98,586
Orders Entered
368
Last Match Time
9:34:24.815
Market
NM
Previous Close
1.4000
Percent Change
+ 17,14 %
Shares Entered
699,504
Open Orders
51
Last Order Time
9:34:37.424
Name
Biomira Inc
Last Price
1.6400
Net Change
+0.2400
Shares Matched
98,586
Orders Entered
368
Last Match Time
9:34:24.815
Market
NM
Previous Close
1.4000
Percent Change
+ 17,14 %
Shares Entered
699,504
Open Orders
51
Last Order Time
9:34:37.424
...und deshalb gehts jetzt richtig ab + 17 %
01.11.2004 15:25:
Biomira and Merck KGaA Present Non-Small Cell Lung Cancer Data at European Society for Medical Oncology Congress (Abstract No. 3IN)
EDMONTON, ALBERTA and DARMSTADT, GERMANY, Nov. 1 /PRNewswire-FirstCall/ -- Biomira (Nachrichten) (TSX: BRA) and Merck KGaA (Nachrichten) reiterated today that data from the Companies` Phase IIb BLP 25 Liposome vaccine (L-BLP25) trial in patients with Stage IIIb and IV non-small cell lung cancer (NSCLC), showed that patients treated with the novel vaccine survived 4.4 months longer than those who received only standard therapy.
"The 4.4 month increase in median survival in patients receiving L-BLP25 is a notable period of time for such an aggressive disease as non-small cell lung cancer," said Dr. Charles Butts, Medical Oncologist, Cross Cancer Institute, Edmonton, Alberta and lead investigator in the trial. "The data indicate a favourable safety profile and maintenance of quality of life in the vaccine arm, further supporting the plans to evaluate the vaccine in additional clinical trials. More exciting are the results we`re seeing in earlier stage patients."
Dr. Butts presented the trial data at the 29th Meeting of the European Society for Medical Oncology (ESMO) being held in Vienna, Austria (October 29- November 2, 2004). His oral presentation, entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine immunotherapy of non-small cell lung cancer (NSCLC); L-BLP25 Non-Small Cell Lung Cancer Study Group," was part of the Presidential Symposium today and also was included in ESMO`s press conference highlighting significant developments in oncology, held yesterday.
All patients were required to have stage IIIB or IV NSCLC that was stable or had responded following treatment with first line chemotherapy, or combined chemotherapy with radiation therapy, prior to randomization into the study. Patients were randomized equally to the treatment arm (vaccine plus best supportive care) or to the control arm (best supportive care alone). Best supportive care could consist of second line chemotherapy, palliative radiotherapy, or other treatments as determined by the investigator. The primary endpoints were survival and safety, with quality of life as a secondary endpoint. Survival was calculated from the date of randomization in the study to the date of death or last contact.
In the 171-patient study, the Companies observed a median survival benefit of 4.4 months in patients receiving L-BLP25 after having achieved either stable disease or a response to first line chemotherapy. Overall median survival for the treatment group receiving the vaccine (n=88) was 17.4 months versus 13 months for the control group (n=83) (Kaplan-Meier log-rank p=0.0652; Adjusted Cox p=0.1120). In the overall patient population, two-year survival was 43.2 per cent for the treatment group and 28.9 per cent for the control group.
Patients in the vaccine arm maintained their baseline quality of life for a longer period of time than those in the control arm. The difference reached statistical significance at two time points, 19 and 31 weeks.
A subset analysis of locoregional Stage IIIb patients (disease contained within the lung) showed two-year survival to be 36.7 per cent for the control arm (n=30) versus 60 per cent for the treatment arm (n=35) per cent. Median survival was 13.3 months for patients in the control group, while the median survival for the treatment group had not yet been reached, at the time of analysis (Kaplan-Meier log-rank p=0.0575; Adjusted Cox p=0.0692).
"This peer-reviewed setting is an important opportunity for us to make our data available to the global oncology community," said Alex McPherson, MD, PhD, President and CEO of Biomira. "Lung cancer has historically been a very challenging disease to treat. These notable data, along with the potential for the results to further improve at the planned survival update in December, support our enthusiasm for this program."
"These Phase II data are very encouraging in terms of offering a potentially meaningful benefit to patients in an area where so little progress has been realized despite many years of work," said Bernhard Ehmer, MD, Vice President and Head of Merck`s Oncology Business Area.
Biomira and Merck KGaA expect to announce an update from this trial in December 2004. The Companies also expect to launch a large trial in unresectable Stage III patients in several countries, including the U.S., Europe and Canada in late 2005.
Additional Study Details
Treated patients received a single low-dose of intravenous cyclophosphamide three days prior to the first vaccination of a 1000 (micro)g dose of L-BLP25. Vaccinations were given weekly for the first eight weeks, and at six-week intervals thereafter. Quality of life and clinical assessments took place at Week 4, Week 8 and then at 12-week intervals for the remainder of the trial.
Mild flu-like symptoms and injection site reactions occurred in approximately half of the patients in the vaccine arm. Other adverse events were consistent with disease status in both arms of the trial.
About Lung Cancer
Lung cancer is the leading cause of cancer-related mortality for men and women in North America. In 2004, approximately 174,000 new cases of lung cancer will be diagnosed in the United States and 160,000 Americans will die from the disease. In Canada, there will be an estimated 21,700 new lung cancer diagnoses and approximately 18,900 Canadians will die from the disease this year. NSCLC accounts for approximately 75 to 80 per cent of all primary lung cancers. At the time of diagnosis, only 25 per cent of NSCLC patients are potentially curable by surgery.
About L-BLP25
L-BLP25 is a synthetic MUC1 peptide vaccine that incorporates a 25-amino acid sequence of the MUC1 cancer mucin, in a liposomal formulation. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery. L-BLP25 is designed to induce an immune response to cancer cells.
About Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
About Merck KGaA
Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26 per cent. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas -- monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
EMD Pharmaceuticals Inc., the U.S. affiliate of Merck KGaA, is a fully integrated pharmaceutical company with an initial emphasis on launching new products in oncology. Located in Durham, N.C., EMD focuses on meeting patient and physician needs with pioneering pharmaceutical products and services.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing or attainment of regulatory or product approvals and whether or not the timing may be expedited, the timing of clinical trials approvals, the timing of clinical trials, the efficacy of products or the availability of capital. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
Biomira Inc.
01.11.2004 15:25:
Biomira and Merck KGaA Present Non-Small Cell Lung Cancer Data at European Society for Medical Oncology Congress (Abstract No. 3IN)
EDMONTON, ALBERTA and DARMSTADT, GERMANY, Nov. 1 /PRNewswire-FirstCall/ -- Biomira (Nachrichten) (TSX: BRA) and Merck KGaA (Nachrichten) reiterated today that data from the Companies` Phase IIb BLP 25 Liposome vaccine (L-BLP25) trial in patients with Stage IIIb and IV non-small cell lung cancer (NSCLC), showed that patients treated with the novel vaccine survived 4.4 months longer than those who received only standard therapy.
"The 4.4 month increase in median survival in patients receiving L-BLP25 is a notable period of time for such an aggressive disease as non-small cell lung cancer," said Dr. Charles Butts, Medical Oncologist, Cross Cancer Institute, Edmonton, Alberta and lead investigator in the trial. "The data indicate a favourable safety profile and maintenance of quality of life in the vaccine arm, further supporting the plans to evaluate the vaccine in additional clinical trials. More exciting are the results we`re seeing in earlier stage patients."
Dr. Butts presented the trial data at the 29th Meeting of the European Society for Medical Oncology (ESMO) being held in Vienna, Austria (October 29- November 2, 2004). His oral presentation, entitled, "A multicenter phase IIb randomized study of liposomal MUC1 vaccine immunotherapy of non-small cell lung cancer (NSCLC); L-BLP25 Non-Small Cell Lung Cancer Study Group," was part of the Presidential Symposium today and also was included in ESMO`s press conference highlighting significant developments in oncology, held yesterday.
All patients were required to have stage IIIB or IV NSCLC that was stable or had responded following treatment with first line chemotherapy, or combined chemotherapy with radiation therapy, prior to randomization into the study. Patients were randomized equally to the treatment arm (vaccine plus best supportive care) or to the control arm (best supportive care alone). Best supportive care could consist of second line chemotherapy, palliative radiotherapy, or other treatments as determined by the investigator. The primary endpoints were survival and safety, with quality of life as a secondary endpoint. Survival was calculated from the date of randomization in the study to the date of death or last contact.
In the 171-patient study, the Companies observed a median survival benefit of 4.4 months in patients receiving L-BLP25 after having achieved either stable disease or a response to first line chemotherapy. Overall median survival for the treatment group receiving the vaccine (n=88) was 17.4 months versus 13 months for the control group (n=83) (Kaplan-Meier log-rank p=0.0652; Adjusted Cox p=0.1120). In the overall patient population, two-year survival was 43.2 per cent for the treatment group and 28.9 per cent for the control group.
Patients in the vaccine arm maintained their baseline quality of life for a longer period of time than those in the control arm. The difference reached statistical significance at two time points, 19 and 31 weeks.
A subset analysis of locoregional Stage IIIb patients (disease contained within the lung) showed two-year survival to be 36.7 per cent for the control arm (n=30) versus 60 per cent for the treatment arm (n=35) per cent. Median survival was 13.3 months for patients in the control group, while the median survival for the treatment group had not yet been reached, at the time of analysis (Kaplan-Meier log-rank p=0.0575; Adjusted Cox p=0.0692).
"This peer-reviewed setting is an important opportunity for us to make our data available to the global oncology community," said Alex McPherson, MD, PhD, President and CEO of Biomira. "Lung cancer has historically been a very challenging disease to treat. These notable data, along with the potential for the results to further improve at the planned survival update in December, support our enthusiasm for this program."
"These Phase II data are very encouraging in terms of offering a potentially meaningful benefit to patients in an area where so little progress has been realized despite many years of work," said Bernhard Ehmer, MD, Vice President and Head of Merck`s Oncology Business Area.
Biomira and Merck KGaA expect to announce an update from this trial in December 2004. The Companies also expect to launch a large trial in unresectable Stage III patients in several countries, including the U.S., Europe and Canada in late 2005.
Additional Study Details
Treated patients received a single low-dose of intravenous cyclophosphamide three days prior to the first vaccination of a 1000 (micro)g dose of L-BLP25. Vaccinations were given weekly for the first eight weeks, and at six-week intervals thereafter. Quality of life and clinical assessments took place at Week 4, Week 8 and then at 12-week intervals for the remainder of the trial.
Mild flu-like symptoms and injection site reactions occurred in approximately half of the patients in the vaccine arm. Other adverse events were consistent with disease status in both arms of the trial.
About Lung Cancer
Lung cancer is the leading cause of cancer-related mortality for men and women in North America. In 2004, approximately 174,000 new cases of lung cancer will be diagnosed in the United States and 160,000 Americans will die from the disease. In Canada, there will be an estimated 21,700 new lung cancer diagnoses and approximately 18,900 Canadians will die from the disease this year. NSCLC accounts for approximately 75 to 80 per cent of all primary lung cancers. At the time of diagnosis, only 25 per cent of NSCLC patients are potentially curable by surgery.
About L-BLP25
L-BLP25 is a synthetic MUC1 peptide vaccine that incorporates a 25-amino acid sequence of the MUC1 cancer mucin, in a liposomal formulation. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery. L-BLP25 is designed to induce an immune response to cancer cells.
About Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
About Merck KGaA
Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26 per cent. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas -- monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
EMD Pharmaceuticals Inc., the U.S. affiliate of Merck KGaA, is a fully integrated pharmaceutical company with an initial emphasis on launching new products in oncology. Located in Durham, N.C., EMD focuses on meeting patient and physician needs with pioneering pharmaceutical products and services.
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the timing or attainment of regulatory or product approvals and whether or not the timing may be expedited, the timing of clinical trials approvals, the timing of clinical trials, the efficacy of products or the availability of capital. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
Biomira Inc.
ein schöner tag 
könnte jemand den englischen text sinngemäß übersetzen?
vielen dank!
ciao verdi

könnte jemand den englischen text sinngemäß übersetzen?
vielen dank!
ciao verdi
PRESSEMITTEILUNG
VERÖFFENTLICHUNGSSPERRE BIS Montag, den 1. November 2004, 15.25
IMPFSTOFF GEGEN LUNGENKREBS
IN EINER FRÜHEN STUDIE VIELVESPRECHEND
Ein Impfstoff, der dem Immunsystem hilft, Lungenkrebszellen zu erkennen und anzugreifen, könnte bei Lungenkrebskranken im fortgeschrittenen Stadium zu einer Verlängerung des Lebens führen. Das geht aus ersten Forschungsergebnissen hervor, die heute anlässlich des 29. Kongresses der European Society for Medical Oncology (ESMO) in Wien, Österreich, bekannt gegeben wurden.
Dr. Charles Butts vom Cross Cancer Institute in Edmonton, Kanada, berichtete heute auf dem Kongress, dass die Ergebnisse einer Phase II-Studie, die unter Mitwirkung der Firma Biomira Inc. aus Edmonton, Kanada, und der deutschen Firma Merck KgaA aus Darmstadt mit 171 Patienten durchgeführt wurde, so ermutigend ausgefallen sind, dass eine größere Phase III-Studie gerechtfertigt erscheint, die nächstes Jahr beginnen soll.
"Besonders interessante Ergebnisse liegen für eine Untergruppe von Patienten vor, bei denen die Krankheit loko-regionär/lokal fortgeschritten ist, d.h. also für eine Operation zu weit fortgeschritten, aber noch nicht auf angrenzende Organe übergegangen ", verkündet Dr. Butts. "Diese Patientengruppe hat am meisten vom Einsatz des Impfstoffes während der Studie profitiert."
Der Impfstoff kann als eine der so genannten gezielten Therapieformen bezeichnet werden. Im Gegensatz zur Chemotherapie, die den gesamten Tumor attackiert, wobei gleichzeitig auch eine große Zahl von gesunden Zellen geschädigt wird, greifen die gezielten Therapieformen ein bestimmtes Merkmal der Tumorzellen an.
In diesem Falle ist das Ziel des Impfstoffes ein Glykoprotein-Molekül , das sich auf der Oberfläche vieler Zellen (MUC-1) befindet, das aber bei Tumorzellen entartet. Der Impfstoff stellt einen Versuch dar, das Immunsystem dazu zu bringen, dieses entartete Molekül zu erkennen und spezifisch all jene Zellen anzugreifen, die es tragen.
Im Verlauf dieser Studie erhielten 83 Patienten, die an nicht-kleinzelligem Lungenkrebs im Stadium IIIB oder IV erkrankt waren, der unter Chemotherapie stabil war oder auf die Therapie ansprach, die bestmögliche supportive Therapie, während 88 Patienten zusätzlich mit dem L-BLP25 genannten Impfstoff behandelt wurden. Der Impfstoff wurde acht Wochen lang wöchentlich verabreicht, worauf alle sechs Wochen Auffrischungsimpfungen erfolgten.
Insgesamt betrug die Überlebenszeit für Patienten, die den Impfstoff erhielten, im Durchschnitt 17,4 Monate, während Patienten, die mit der bestmöglichen supportiven Therapie behandelt wurden, im Schnitt 13 Monate lebten. Bei den Patienten mit loco-regionärer Krankheit, war die mediane Überlebenszeit der Supportivtherapie-Gruppe 13,3 Monate. Das mediane Überleben der mit dem Impfstoff behandelten Patienten wurde nicht erreicht, da nach 24 Monaten noch 60% der Patienten am Leben sind. Die längste Verabreichungszeit des Impfstoffes an einen einzelnen Patienten im Verlauf dieser Studie beträgt 43 Monate (3,5 Jahre).
Dr. Butt meint dazu: "Derartig positive Ergebnisse bei den Patienten mit loco-regionärer Erkrankung haben uns dazu ermutigt, eine konkrete Phase III-Studie in dieser speziellen Patientenpopulation durchzuführen. Momentan sind wir dabei, die Details für diese Studie auszuarbeiten und planen, sie im Verlauf des Jahres 2005 zu beginnen."
Professor Håkan Mellstedt vom schwedischen Karolinska University Hospital in Stockholm bemerkte im Hinblick auf diese Ergebnisse, dass Impfstoffe gegen Krebs bereits ermutigende Erfolge beim kolorektalen Karzinom, beim malignen Melanom und beim Nierenzellkarzinom erzielt haben.
"Der neue Aspekt dieser Studie besteht darin, dass der Impfstoff auf ein bestimmtes Antigen, das MUC-1, abzielt, das von einem Pharmakonzern in großen Mengen hergestellt werden kann und für alle Patienten mit einer bestimmten Erkrankung verwendet werden kann. Außerdem ist es nun möglich, den Lungenkrebs in die Krankheiten einzureihen, die auf eine Behandlung mit Impfstoff ansprechen. Zusätzlich hat die Studie gezeigt, dass ein Impfstoff in fortgeschrittenem Stadium nach Chemotherapie auch dort wirkungsvoll eingesetzt werden kann, wo die Mehrzahl der Patienten noch makroskopische Tumorreste aufweist", verkündet Professor Mellstedt. "Es besteht heute kein Zweifel mehr daran, dass das Konzept des ungiftigen Impfstoffes in das Arsenal der Krebstherapeutika aufgenommen werden wird."
-ENDE-
Bemerkungen für Redakteure
Über die European Society for Medical Oncology (ESMO)
ESMO ist Europas führende non-profit Krebs Organisation, die medizinischen Onkologen und anderen professionellen Mitgliedern des Gesundheitswesens umfassende Informationen, Fortbildung, sowie Information über klinische Leitfäden bietet. ESMO wurde 1975 gegründet und hat mittlerweile weltweit fast 4 500 Mitglieder, wovon drei Viertel aus Europa kommen. Das Credo der Europäischen Gesellschaft für medizinische Onkologie besteht darin, dass jeder Patient berechtigt ist, die bestmögliche Behandlung zu erhalten. Der Einsatz von Medikamenten stellt eine fundamentale Modalität in der Krebsbehandlung dar, weswegen die Patienten von qualifizierten medizinischen Onkologen behandelt werden sollen. In ihrer wissenschaftlichen Zeitschrift Annals of Oncology publiziert die Gesellschaft laufend Ergebnisse von allen Bereichen der klinischen Krebsforschung. Spenden an die ESMO Foundation unterstützen die vielfältigen Aktivitäten der Gesellschaft, insbesondere jedoch die Krebsforschung. Weitere Informationen über ESMO finden Sie unter www.esmo.org
VERÖFFENTLICHUNGSSPERRE BIS Montag, den 1. November 2004, 15.25
IMPFSTOFF GEGEN LUNGENKREBS
IN EINER FRÜHEN STUDIE VIELVESPRECHEND
Ein Impfstoff, der dem Immunsystem hilft, Lungenkrebszellen zu erkennen und anzugreifen, könnte bei Lungenkrebskranken im fortgeschrittenen Stadium zu einer Verlängerung des Lebens führen. Das geht aus ersten Forschungsergebnissen hervor, die heute anlässlich des 29. Kongresses der European Society for Medical Oncology (ESMO) in Wien, Österreich, bekannt gegeben wurden.
Dr. Charles Butts vom Cross Cancer Institute in Edmonton, Kanada, berichtete heute auf dem Kongress, dass die Ergebnisse einer Phase II-Studie, die unter Mitwirkung der Firma Biomira Inc. aus Edmonton, Kanada, und der deutschen Firma Merck KgaA aus Darmstadt mit 171 Patienten durchgeführt wurde, so ermutigend ausgefallen sind, dass eine größere Phase III-Studie gerechtfertigt erscheint, die nächstes Jahr beginnen soll.
"Besonders interessante Ergebnisse liegen für eine Untergruppe von Patienten vor, bei denen die Krankheit loko-regionär/lokal fortgeschritten ist, d.h. also für eine Operation zu weit fortgeschritten, aber noch nicht auf angrenzende Organe übergegangen ", verkündet Dr. Butts. "Diese Patientengruppe hat am meisten vom Einsatz des Impfstoffes während der Studie profitiert."
Der Impfstoff kann als eine der so genannten gezielten Therapieformen bezeichnet werden. Im Gegensatz zur Chemotherapie, die den gesamten Tumor attackiert, wobei gleichzeitig auch eine große Zahl von gesunden Zellen geschädigt wird, greifen die gezielten Therapieformen ein bestimmtes Merkmal der Tumorzellen an.
In diesem Falle ist das Ziel des Impfstoffes ein Glykoprotein-Molekül , das sich auf der Oberfläche vieler Zellen (MUC-1) befindet, das aber bei Tumorzellen entartet. Der Impfstoff stellt einen Versuch dar, das Immunsystem dazu zu bringen, dieses entartete Molekül zu erkennen und spezifisch all jene Zellen anzugreifen, die es tragen.
Im Verlauf dieser Studie erhielten 83 Patienten, die an nicht-kleinzelligem Lungenkrebs im Stadium IIIB oder IV erkrankt waren, der unter Chemotherapie stabil war oder auf die Therapie ansprach, die bestmögliche supportive Therapie, während 88 Patienten zusätzlich mit dem L-BLP25 genannten Impfstoff behandelt wurden. Der Impfstoff wurde acht Wochen lang wöchentlich verabreicht, worauf alle sechs Wochen Auffrischungsimpfungen erfolgten.
Insgesamt betrug die Überlebenszeit für Patienten, die den Impfstoff erhielten, im Durchschnitt 17,4 Monate, während Patienten, die mit der bestmöglichen supportiven Therapie behandelt wurden, im Schnitt 13 Monate lebten. Bei den Patienten mit loco-regionärer Krankheit, war die mediane Überlebenszeit der Supportivtherapie-Gruppe 13,3 Monate. Das mediane Überleben der mit dem Impfstoff behandelten Patienten wurde nicht erreicht, da nach 24 Monaten noch 60% der Patienten am Leben sind. Die längste Verabreichungszeit des Impfstoffes an einen einzelnen Patienten im Verlauf dieser Studie beträgt 43 Monate (3,5 Jahre).
Dr. Butt meint dazu: "Derartig positive Ergebnisse bei den Patienten mit loco-regionärer Erkrankung haben uns dazu ermutigt, eine konkrete Phase III-Studie in dieser speziellen Patientenpopulation durchzuführen. Momentan sind wir dabei, die Details für diese Studie auszuarbeiten und planen, sie im Verlauf des Jahres 2005 zu beginnen."
Professor Håkan Mellstedt vom schwedischen Karolinska University Hospital in Stockholm bemerkte im Hinblick auf diese Ergebnisse, dass Impfstoffe gegen Krebs bereits ermutigende Erfolge beim kolorektalen Karzinom, beim malignen Melanom und beim Nierenzellkarzinom erzielt haben.
"Der neue Aspekt dieser Studie besteht darin, dass der Impfstoff auf ein bestimmtes Antigen, das MUC-1, abzielt, das von einem Pharmakonzern in großen Mengen hergestellt werden kann und für alle Patienten mit einer bestimmten Erkrankung verwendet werden kann. Außerdem ist es nun möglich, den Lungenkrebs in die Krankheiten einzureihen, die auf eine Behandlung mit Impfstoff ansprechen. Zusätzlich hat die Studie gezeigt, dass ein Impfstoff in fortgeschrittenem Stadium nach Chemotherapie auch dort wirkungsvoll eingesetzt werden kann, wo die Mehrzahl der Patienten noch makroskopische Tumorreste aufweist", verkündet Professor Mellstedt. "Es besteht heute kein Zweifel mehr daran, dass das Konzept des ungiftigen Impfstoffes in das Arsenal der Krebstherapeutika aufgenommen werden wird."
-ENDE-
Bemerkungen für Redakteure
Über die European Society for Medical Oncology (ESMO)
ESMO ist Europas führende non-profit Krebs Organisation, die medizinischen Onkologen und anderen professionellen Mitgliedern des Gesundheitswesens umfassende Informationen, Fortbildung, sowie Information über klinische Leitfäden bietet. ESMO wurde 1975 gegründet und hat mittlerweile weltweit fast 4 500 Mitglieder, wovon drei Viertel aus Europa kommen. Das Credo der Europäischen Gesellschaft für medizinische Onkologie besteht darin, dass jeder Patient berechtigt ist, die bestmögliche Behandlung zu erhalten. Der Einsatz von Medikamenten stellt eine fundamentale Modalität in der Krebsbehandlung dar, weswegen die Patienten von qualifizierten medizinischen Onkologen behandelt werden sollen. In ihrer wissenschaftlichen Zeitschrift Annals of Oncology publiziert die Gesellschaft laufend Ergebnisse von allen Bereichen der klinischen Krebsforschung. Spenden an die ESMO Foundation unterstützen die vielfältigen Aktivitäten der Gesellschaft, insbesondere jedoch die Krebsforschung. Weitere Informationen über ESMO finden Sie unter www.esmo.org
@freetibet
dankeschön!!!
dankeschön!!!
@verdi
Die sinngemäße Übersetzung kommt hier:
Biomira und Merck KGaA anwesende Nicht-Kleine Zelle Lungenkrebs-Daten an der europäischen Gesellschaft für medizinischen Onkologie-Kongreß (entziehen Sie Nr. 3IN)
EDMONTON, ALBERTA und DARMSTADT, DEUTSCHLAND, 1. Nov. /PRNewswire-FirstCall/ -- Biomira (Nachrichten) (TSX: BRA) und Merck, die KGaA (Nachrichten) heute diese Daten vom vaccine (L-BLP25) Versuch des der Gesellschaften Phase IIb BLP 25 Liposoms bei Patienten mit Stadium IIIb und IV dem nicht-kleinen Zelle Lungenkrebs (NSCLC) reiterierte, gezeigt, daß Patienten mit dem Romanimpfstoff behandelten, überlebte 4.4 Monate länger als die, die nur Standardtherapie empfingen.
"Die 4.4 Monat Zunahme des mittleren überlebens bei den Patienten, die L-BLP25 empfangen, ist ein bemerkenswerter Zeitabschnitt für eine solche konkurrenzfähige Krankheit, wie nicht-kleiner Zelle Lungenkrebs,", sagte Dr. Charles Butts, medizinischer Onkologe, Kreuzkrebs-Institut-, Edmonton-, Alberta- und Leitungforscher im Versuch. "Die Daten zeigen ein vorteilhaftes Sicherheit Profil und eine Wartung der Lebensqualität im vaccine Arm an, weiter, die Pläne stützend, um den Impfstoff in den zusätzlichen klinischen Versuchen auszuwerten. Sind die Resultate aufregender, die wir sehen bei früheres Stadium Patienten."
Dr. Butts stellte die Probedaten bei der 29. Sitzung der europäischen Gesellschaft für die medizinische Onkologie dar (ESMO), die in Wien, Österreich (29. Oktober bis 2. November 2004) gehalten wurde. Seine Munddarstellung, erlaubt, "eine Multicenterphase IIb randomisierte Studie des liposomalen vaccine Immunotherapy MUC1 des nicht-kleinen Zelle Lungenkrebses (NSCLC); L-BLP25 Nicht-Kleine Zelle Lungenkrebs-Arbeitsgemeinschaft," ein Teil der Präsidentenzusammenstellung heute und auch war in der Pressekonferenz ESMOS eingeschlossen, die bedeutende Entwicklungen in der Onkologie hervorhebt, gestern gehalten.
Alle Patienten wurden angefordert, Stadium IIIB oder IV NSCLC, die beständig waren oder nach Behandlung mit erster Linie Chemotherapie reagiert hatten, oder kombinierte Chemotherapie mit Strahlentherapie, vor randomization zu haben in die Studie. Patienten wurden gleichmäßig dem Behandlungarm (Impfstoff plus beste unterstützende Obacht) oder dem Steuerarm randomisiert (beste unterstützende Obacht alleine). Beste unterstützende Obacht konnte aus zweiter Linie Chemotherapie, Linderungsstrahlentherapie, oder anderen Behandlungen bestehen, wie vom Forscher festgestellt. Die Primärendpunkte waren überleben und Sicherheit, mit Lebensqualität als Sekundärendpunkt. Überleben wurde nach randomization in der Studie zum Datum des Todes- oder Letztkontaktes errechnet.
In der geduldigen Studie 171 beobachteten die Firmen einen mittleren überleben Nutzen von 4.4 Monaten bei den Patienten, die L-BLP25 entweder beständige Krankheit oder eine Antwort zur ersten Linie Chemotherapie nachher erzielend empfangen. Gesamtes mittleres überleben für die Behandlunggruppe, die den Impfstoff (n=88) empfängt war 17.4 Monate gegen 13 Monate für die Steuergruppe (n=83) (Kaplan-Meier Maschinenbordbuch-ordnen p=0.0652; Justierter Cox p=0.1120). In der gesamten geduldigen Bevölkerung war zweijähriges überleben 43.2 Prozent für die Behandlunggruppe und 28.9 Prozent für die Steuergruppe.
Patienten im vaccine Arm behielten ihre Grundlinie Lebensqualität während eines längeren Zeitabschnitts als die im Steuerarm bei. Der Unterschied erreichte statistische Bedeutung bei zwei Zeitpunkt-, 19 und 31wochen.
Eine Teilmenge Analyse der locoregional Stadium IIIb Patienten (die Krankheit enthalten innerhalb des Lungenflügels) stellte dar, daß das zweijährige überleben, zum 36.7 Prozent für den Steuerarm (n=30) gegen 60 Prozent für das mittlere überleben der Prozente des Behandlungarmes zu sein (n=35) 13.3 Monate für Patienten in der Steuergruppe, während das mittlere überleben für die Behandlunggruppe nicht noch erreicht worden war, zu der Zeit der Analyse war (Kaplan-Meier Maschinenbordbuch-ordnen p=0.0575; Justierter Cox p=0.0692).
"Dieses Gleich-wiederholte Einstellung ist eine wichtige Gelegenheit, damit wir unsere Daten zugänglich für die globale Onkologiegemeinschaft," machen, sagte Alex McPherson, MD, PhD, Präsident und CEO von Biomira. "Lungenkrebs ist historisch eine sehr schwierige Krankheit gewesen, zum zu behandeln. Diese bemerkenswerten Daten, zusammen mit dem Potential, damit die Resultate weiter verbessern am geplanten überleben Update im Dezember, stützen unsere Begeisterung für dieses Programm."
Die sinngemäße Übersetzung kommt hier:
Biomira und Merck KGaA anwesende Nicht-Kleine Zelle Lungenkrebs-Daten an der europäischen Gesellschaft für medizinischen Onkologie-Kongreß (entziehen Sie Nr. 3IN)
EDMONTON, ALBERTA und DARMSTADT, DEUTSCHLAND, 1. Nov. /PRNewswire-FirstCall/ -- Biomira (Nachrichten) (TSX: BRA) und Merck, die KGaA (Nachrichten) heute diese Daten vom vaccine (L-BLP25) Versuch des der Gesellschaften Phase IIb BLP 25 Liposoms bei Patienten mit Stadium IIIb und IV dem nicht-kleinen Zelle Lungenkrebs (NSCLC) reiterierte, gezeigt, daß Patienten mit dem Romanimpfstoff behandelten, überlebte 4.4 Monate länger als die, die nur Standardtherapie empfingen.
"Die 4.4 Monat Zunahme des mittleren überlebens bei den Patienten, die L-BLP25 empfangen, ist ein bemerkenswerter Zeitabschnitt für eine solche konkurrenzfähige Krankheit, wie nicht-kleiner Zelle Lungenkrebs,", sagte Dr. Charles Butts, medizinischer Onkologe, Kreuzkrebs-Institut-, Edmonton-, Alberta- und Leitungforscher im Versuch. "Die Daten zeigen ein vorteilhaftes Sicherheit Profil und eine Wartung der Lebensqualität im vaccine Arm an, weiter, die Pläne stützend, um den Impfstoff in den zusätzlichen klinischen Versuchen auszuwerten. Sind die Resultate aufregender, die wir sehen bei früheres Stadium Patienten."
Dr. Butts stellte die Probedaten bei der 29. Sitzung der europäischen Gesellschaft für die medizinische Onkologie dar (ESMO), die in Wien, Österreich (29. Oktober bis 2. November 2004) gehalten wurde. Seine Munddarstellung, erlaubt, "eine Multicenterphase IIb randomisierte Studie des liposomalen vaccine Immunotherapy MUC1 des nicht-kleinen Zelle Lungenkrebses (NSCLC); L-BLP25 Nicht-Kleine Zelle Lungenkrebs-Arbeitsgemeinschaft," ein Teil der Präsidentenzusammenstellung heute und auch war in der Pressekonferenz ESMOS eingeschlossen, die bedeutende Entwicklungen in der Onkologie hervorhebt, gestern gehalten.
Alle Patienten wurden angefordert, Stadium IIIB oder IV NSCLC, die beständig waren oder nach Behandlung mit erster Linie Chemotherapie reagiert hatten, oder kombinierte Chemotherapie mit Strahlentherapie, vor randomization zu haben in die Studie. Patienten wurden gleichmäßig dem Behandlungarm (Impfstoff plus beste unterstützende Obacht) oder dem Steuerarm randomisiert (beste unterstützende Obacht alleine). Beste unterstützende Obacht konnte aus zweiter Linie Chemotherapie, Linderungsstrahlentherapie, oder anderen Behandlungen bestehen, wie vom Forscher festgestellt. Die Primärendpunkte waren überleben und Sicherheit, mit Lebensqualität als Sekundärendpunkt. Überleben wurde nach randomization in der Studie zum Datum des Todes- oder Letztkontaktes errechnet.
In der geduldigen Studie 171 beobachteten die Firmen einen mittleren überleben Nutzen von 4.4 Monaten bei den Patienten, die L-BLP25 entweder beständige Krankheit oder eine Antwort zur ersten Linie Chemotherapie nachher erzielend empfangen. Gesamtes mittleres überleben für die Behandlunggruppe, die den Impfstoff (n=88) empfängt war 17.4 Monate gegen 13 Monate für die Steuergruppe (n=83) (Kaplan-Meier Maschinenbordbuch-ordnen p=0.0652; Justierter Cox p=0.1120). In der gesamten geduldigen Bevölkerung war zweijähriges überleben 43.2 Prozent für die Behandlunggruppe und 28.9 Prozent für die Steuergruppe.
Patienten im vaccine Arm behielten ihre Grundlinie Lebensqualität während eines längeren Zeitabschnitts als die im Steuerarm bei. Der Unterschied erreichte statistische Bedeutung bei zwei Zeitpunkt-, 19 und 31wochen.
Eine Teilmenge Analyse der locoregional Stadium IIIb Patienten (die Krankheit enthalten innerhalb des Lungenflügels) stellte dar, daß das zweijährige überleben, zum 36.7 Prozent für den Steuerarm (n=30) gegen 60 Prozent für das mittlere überleben der Prozente des Behandlungarmes zu sein (n=35) 13.3 Monate für Patienten in der Steuergruppe, während das mittlere überleben für die Behandlunggruppe nicht noch erreicht worden war, zu der Zeit der Analyse war (Kaplan-Meier Maschinenbordbuch-ordnen p=0.0575; Justierter Cox p=0.0692).
"Dieses Gleich-wiederholte Einstellung ist eine wichtige Gelegenheit, damit wir unsere Daten zugänglich für die globale Onkologiegemeinschaft," machen, sagte Alex McPherson, MD, PhD, Präsident und CEO von Biomira. "Lungenkrebs ist historisch eine sehr schwierige Krankheit gewesen, zum zu behandeln. Diese bemerkenswerten Daten, zusammen mit dem Potential, damit die Resultate weiter verbessern am geplanten überleben Update im Dezember, stützen unsere Begeisterung für dieses Programm."
...Fortsetzung...
"Diese, die Phase II Daten sehr in dem Antrag eines möglicherweise sinnvollen Nutzens Patienten in einem Bereich ausgedrückt anregen, in dem so wenig Fortschritt trotz vieler Jahre der Arbeit verwirklicht worden ist,", sagte Bernhard Ehmer, MD, Vizepräsident und Kopf des Onkologie-Geschäftsbereichs Mercks.
Biomira und Merck KGaA erwarten, ein Update von diesem Versuch im Dezember 2004 zu verkünden. Die Firmen erwarten auch, einen großen Versuch bei unresectable Stadium III Patienten in einigen Ländern, einschließlich die US, das Europa und das Kanada spätem 2005 auszustoßen.
Zusätzliche Studie Details
Behandelte Patienten empfingen eine einzelne Niedrigdosis des intravenösen Cyclophosphamids drei Tage vor der ersten Schutzimpfung einer 1000 (Mikro) g Dosis von L-BLP25. Schutzimpfungen wurden wöchentlich für die ersten acht Wochen und in Sechswochenabständen danach gegeben. Lebensqualität und klinische Einschätzungen fanden an Woche 4, Woche 8 und dann in 12 Woche Abständen für den Rest des Versuches statt.
Mild Grippe-wie Symptome und Einspritzungaufstellungsortreaktionen trat zur Hälfte ungefähr der Patienten im vaccine Arm auf. Andere nachteilige Fälle waren mit Krankheitstatus in beiden Armen des Versuches gleichbleibend.
Und wann kommt jetzt der Kurs endlich aus dem Knick?
"Diese, die Phase II Daten sehr in dem Antrag eines möglicherweise sinnvollen Nutzens Patienten in einem Bereich ausgedrückt anregen, in dem so wenig Fortschritt trotz vieler Jahre der Arbeit verwirklicht worden ist,", sagte Bernhard Ehmer, MD, Vizepräsident und Kopf des Onkologie-Geschäftsbereichs Mercks.
Biomira und Merck KGaA erwarten, ein Update von diesem Versuch im Dezember 2004 zu verkünden. Die Firmen erwarten auch, einen großen Versuch bei unresectable Stadium III Patienten in einigen Ländern, einschließlich die US, das Europa und das Kanada spätem 2005 auszustoßen.
Zusätzliche Studie Details
Behandelte Patienten empfingen eine einzelne Niedrigdosis des intravenösen Cyclophosphamids drei Tage vor der ersten Schutzimpfung einer 1000 (Mikro) g Dosis von L-BLP25. Schutzimpfungen wurden wöchentlich für die ersten acht Wochen und in Sechswochenabständen danach gegeben. Lebensqualität und klinische Einschätzungen fanden an Woche 4, Woche 8 und dann in 12 Woche Abständen für den Rest des Versuches statt.
Mild Grippe-wie Symptome und Einspritzungaufstellungsortreaktionen trat zur Hälfte ungefähr der Patienten im vaccine Arm auf. Andere nachteilige Fälle waren mit Krankheitstatus in beiden Armen des Versuches gleichbleibend.
Und wann kommt jetzt der Kurs endlich aus dem Knick?

alles in allem doch eher enttäuschend 

Nasdaq BIOM USD 1,40 1,52 +0,120 +8,57 % 2,01 Mio. 1.405.640 01. Nov 22:01
Frankfurt BM2 EUR 1,11 1,24 +0,130 +11,71 % 6.729 5.664 01. Nov 19:25
Frankfurt BM2 EUR 1,11 1,24 +0,130 +11,71 % 6.729 5.664 01. Nov 19:25
Das war aber bis jetzt nur ein Bruchteil der Ergebnisveröffentlichung !!!
Wer lesen kann ist klar im ......!
Merck KGaA und Biomira stellen auf der Tagung derEuropäischen Gesellschaft ...
Merck KGaA und Biomira stellen auf der Tagung derEuropäischen Gesellschaft für Medizinische Onkologie Daten ihrer Lungenkrebsstudie vor
Daten der Vakzinstudie zeigen `bemerkenswerte` Steigerung der
Überlebenszeit
Die Merck KGaA und Biomira Inc. (Nasdac: BIOM) (TSX: BRA) präsentierten heute die Ergebnisse ihrer gemeinsamen Studie der Phase IIb mit dem liposomalen Krebsimpfstoff BLP25 (L-BLP25), die an Patienten mit nicht-kleinzelligem Bronchialkarzinom (NSCLC) der Stadien IIIb und IV durchgeführt wurde: Patienten, die mit diesem neuartigen Impfstoff behandelt wurden, überlebten 4,4 Monate länger als Vergleichspatienten, die nur die Standardtherapie erhalten hatten.
"Die Steigerung der Überlebenszeit um 4,4 Monate bei Patienten, die mit L-BLP25 behandelt wurden, ist ein bemerkenswerter Zeitraum, bedenkt man den aggressiven Krankheitsverlauf bei nicht-kleinzelligem Lungenkrebs," sagte Dr. Charles Butts, Onkologe am Cross Cancer Institute in Edmonton, Alberta (Kanada), in seiner Funktion als leitender Prüfarzt dieser Studie. „Die Daten bescheinigen dem Vakzin ein günstiges Sicherheitsprofil und einen positiven Einfluss auf den Erhalt der Lebensqualität und bestärken uns in unseren Plänen, es in weiteren Studien zu untersuchen. Die Ergebnisse, die wir bei Patienten in früheren Krankheitsstadien erzielen, sind sogar noch beeindruckender.“
Dr. Butts präsentierte die Studiendaten heute auf der 29. Tagung der Europäischen Gesellschaft für Medizinische Onkologie (ESMO) in Wien (29.10.-2.11.2004). Seine Vorstellung der Daten im Rahmen eines Vortrages war Teil des heutigen Presidential Symposium sowie der gestrigen Pressekonferenz der ESMO, auf der einschneidende Entwicklungen auf dem Gebiet der Onkologie herausgestellt wurden.
Die Studie mit dem Titel "Multizentrische, randomisierte Studie der Phase IIb zur Immuntherapie mit einem liposomalen MUC1-Vakzin bei nicht-kleinzelligem Bronchialkarzinom (NSCLC); L-BLP25-behandelte NSCL-Studiengruppe,” umfasste ausschließlich Patienten der Stadien IIIB oder IV von NSCLC mit stabilem Status, oder die vor der Randomisierung positiv auf eine First-Line Chemotherapie oder Kombination von Chemo- und Strahlentherapie angesprochen hatten. Die Patienten wurden gleichgewichtig der Behandlungsgruppe (Vakzin plus beste Begleitbehandlung) oder der Kontrollgruppe (beste Begleitbehandlung) zugeteilt. Die beste Begleitbehandlung bestand in einer Second-Line Chemotherapie, oder
palliativen Chemotherapie oder einer vom Prüfarzt festgesetzten Behandlung.
Primäre Endpunkte der Studie waren Überlebenszeit und Sicherheit, zusammen mit Lebensqualität als sekundärem Endpunkt. Die Überlebenszeit wurde berechnet ab dem Datum der Randomisierung bis zum Tod oder letztem Kontakt. In der Studie mit 171 Patienten beobachteten die Firmen eine mittlere Überlebenszeitverlängerung (Median) von 4,4 Monaten bei Patienten, die L-BLP25 nach Stabilisierung der Erkrankung oder Ansprechen auf eine First-Line Chemotherapie erhalten hatten.
In der Verum-Gruppe (n=88), die mit dem Impfstoff behandelt wurde, betrug die mittlere Gesamtüberlebenszeit 17,4 Monate im Vergleich zu 13 Monaten in der Kontrollgruppe (n=83). In der gesamten Patientenpopulation betrug die 2-Jahres-Überlebensrate 43,2% in der Verum-Gruppe und 28,9% in der Kontrollgruppe (Signifikanzniveau im Log-Rank-Test nach Kaplan-Meier:
p=0,0652; im modifizierten Cox-Test: p=0,1120).
Patienten der Verum-Gruppe konnten ihre Ausgangslebensqualität über einen längeren Zeitraum verzeichnen als die der Kontrollgruppe. Der Unterschied war für zwei Zeitpunkte, Woche 19 und 31, statistisch signifikant. Bei der Analyse einer Untergruppe von Patienten mit lokoregionalem Stadium IIIb, bei denen der Tumor nur innerhalb der Lunge lokalisiert ist, ergab sich eine 2-Jahres-Überlebenszeit von 60% in der Verum-Gruppe (n=35) im Vergleich zu 36,7% in der Kontrollgruppe (n=30) (Signifikanzniveau im Log-Rank-Test nach Kaplan-Meier: p=0,0575; im modifizierten Cox-Test: p=0,0692). In der Kontrollgruppe betrug die mittlere Überlebenszeit 13,3 Monate. In der Verum-Gruppe war zum Zeitpunkt der Analyse noch keine mittlere Überlebenszeit erreicht.
„Diese Phase II-Daten sind im Hinblick auf den potenziellen Nutzen für die Patienten so ermutigend, weil sie auf einem Felde stattfinden, wo trotz so vieler Jahre Arbeit so geringe Fortschritte erzielt wurden“, sagte Dr. Bernhard Ehmer, Leiter des Geschäftsbereichs Onkologie.
"Die unabhängige Prüfung durch mehrere Experten, das sogenannte
Peer-Review, ist für uns eine gute Gelegenheit, unsere Daten weltweit
onkologischen Fachkreisen zur Verfügung zu stellen," sagte Dr. Alex
McPherson, Präsident und CEO von Biomira. "In der Geschichte der Medizin
hatte Lungenkrebs schon immer den Stellenwert einer schwer therapierbaren
Erkrankung. Diese bemerkenswerten Daten sowie die Aussicht auf noch bessere
Ergebnisse bei Erreichen des nächsten Messpunktes im Dezember fördern unser
begeistertes Engagement für diese Therapie."
Die Merck KGaA und Biomira wollen im Dezember dieses Jahres die nächsten
Ergebnisse aus dieser Studie veröffentlichen. Außerdem erwarten die
Unternehmen Ende 2005 in mehreren Ländern einschließlich der USA, Kanada
und Europas eine große Studie mit Patienten des inoperablem Stadium III
starten zu können.
Weitere Einzelheiten zur Studie
Die Patienten der Verum-Gruppe erhielten einmalig eine niedrige Dosis
Cyclophosphamid (iv) vor der ersten Impfung mit 1000 µg L-BLP25. Die
Impfungen wurden in den ersten acht Wochen wöchentlich, danach in
sechswöchigen Abständen durchgeführt. Die Erfassung von Lebensqualität und
klinischen Befunden fand in den Wochen 4 und 8, danach in 12-wöchigen
Abständen statt.
Über Lungenkrebs
Lungenkrebs ist in Nordamerika unabhängig vom Geschlecht die
Krebs-Todesursache Nummer 1. Dieses Jahr werden in den USA ca. 174 000
Neuerkrankungen diagnostiziert und 160 000 Amerikaner werden an dieser
Erkrankung sterben. In Kanada schätzt man die Zahl der Erstdiagnosen im
Jahr 2004 auf 21 700 und die Zahl der Todesfälle auf ca. 18 900. Ein
nicht-kleinzelliges Bronchialkarzinom (NSCLC) liegt bei ca. 75-80% aller
Primärtumore der Lunge vor. Zum Zeitpunkt der Diagnosestellung können nur
noch 25% der NSCLC potentiell durch Operation geheilt werden.
Über L-BLP25
L-BLP25 ist ein synthetisches MUC1-Peptid-Vakzin, das in einer liposomalen
Formulierung eine 25er-Aminosäurensequenz des Krebsmuzins MUC1 einbaut.
Das Lipsom fördert die Erkennung des Krebsantigens durch das Immunsystem
und unterstützt die Wirkung. L-BLP25 soll eine Immunreaktion auf
Krebszellen hervorrufen. Der Impfstoff hatte im September 2004 von der FDA
den Status des beschleunigten Prüfverfahrens (Fast Track Designation)
erhalten.
Der im März 2001 zwischen Merck KGaA und Biomira geschlossene Vertrag
beinhaltet die gemeinsame Vermarktung von L-BLP25 in den USA. In allen
übrigen Ländern, mit Ausnahme von Kanada, Israel und dem palästinensischen
Autonomiegebiet, hält Merck die alleinigen Entwicklungs- und
Vermarktungsrechte.
Zu Merck KGaA
Merck arbeitet engagiert an der Verbesserung der Behandlungsmöglichkeiten
für Krebspatienten. Derzeit untersucht das Unternehmen sehr gezielt
neuartige Therapien in ausgesuchten Bereichen. Es laufen Studien zur
Anwendung von L-BLP25 für NSCLC und Erbitux bei Kolorektalkarzinomen,
Plattenepithelkarzinomen des Kopfes und Halses sowie bei NSCLC. Ergebnisse
zweier Erbitux-Studien wurden heute morgen auf dem ESMO-Kongress
präsentiert
Wer lesen kann ist klar im ......!
Merck KGaA und Biomira stellen auf der Tagung derEuropäischen Gesellschaft ...
Merck KGaA und Biomira stellen auf der Tagung derEuropäischen Gesellschaft für Medizinische Onkologie Daten ihrer Lungenkrebsstudie vor
Daten der Vakzinstudie zeigen `bemerkenswerte` Steigerung der
Überlebenszeit
Die Merck KGaA und Biomira Inc. (Nasdac: BIOM) (TSX: BRA) präsentierten heute die Ergebnisse ihrer gemeinsamen Studie der Phase IIb mit dem liposomalen Krebsimpfstoff BLP25 (L-BLP25), die an Patienten mit nicht-kleinzelligem Bronchialkarzinom (NSCLC) der Stadien IIIb und IV durchgeführt wurde: Patienten, die mit diesem neuartigen Impfstoff behandelt wurden, überlebten 4,4 Monate länger als Vergleichspatienten, die nur die Standardtherapie erhalten hatten.
"Die Steigerung der Überlebenszeit um 4,4 Monate bei Patienten, die mit L-BLP25 behandelt wurden, ist ein bemerkenswerter Zeitraum, bedenkt man den aggressiven Krankheitsverlauf bei nicht-kleinzelligem Lungenkrebs," sagte Dr. Charles Butts, Onkologe am Cross Cancer Institute in Edmonton, Alberta (Kanada), in seiner Funktion als leitender Prüfarzt dieser Studie. „Die Daten bescheinigen dem Vakzin ein günstiges Sicherheitsprofil und einen positiven Einfluss auf den Erhalt der Lebensqualität und bestärken uns in unseren Plänen, es in weiteren Studien zu untersuchen. Die Ergebnisse, die wir bei Patienten in früheren Krankheitsstadien erzielen, sind sogar noch beeindruckender.“
Dr. Butts präsentierte die Studiendaten heute auf der 29. Tagung der Europäischen Gesellschaft für Medizinische Onkologie (ESMO) in Wien (29.10.-2.11.2004). Seine Vorstellung der Daten im Rahmen eines Vortrages war Teil des heutigen Presidential Symposium sowie der gestrigen Pressekonferenz der ESMO, auf der einschneidende Entwicklungen auf dem Gebiet der Onkologie herausgestellt wurden.
Die Studie mit dem Titel "Multizentrische, randomisierte Studie der Phase IIb zur Immuntherapie mit einem liposomalen MUC1-Vakzin bei nicht-kleinzelligem Bronchialkarzinom (NSCLC); L-BLP25-behandelte NSCL-Studiengruppe,” umfasste ausschließlich Patienten der Stadien IIIB oder IV von NSCLC mit stabilem Status, oder die vor der Randomisierung positiv auf eine First-Line Chemotherapie oder Kombination von Chemo- und Strahlentherapie angesprochen hatten. Die Patienten wurden gleichgewichtig der Behandlungsgruppe (Vakzin plus beste Begleitbehandlung) oder der Kontrollgruppe (beste Begleitbehandlung) zugeteilt. Die beste Begleitbehandlung bestand in einer Second-Line Chemotherapie, oder
palliativen Chemotherapie oder einer vom Prüfarzt festgesetzten Behandlung.
Primäre Endpunkte der Studie waren Überlebenszeit und Sicherheit, zusammen mit Lebensqualität als sekundärem Endpunkt. Die Überlebenszeit wurde berechnet ab dem Datum der Randomisierung bis zum Tod oder letztem Kontakt. In der Studie mit 171 Patienten beobachteten die Firmen eine mittlere Überlebenszeitverlängerung (Median) von 4,4 Monaten bei Patienten, die L-BLP25 nach Stabilisierung der Erkrankung oder Ansprechen auf eine First-Line Chemotherapie erhalten hatten.
In der Verum-Gruppe (n=88), die mit dem Impfstoff behandelt wurde, betrug die mittlere Gesamtüberlebenszeit 17,4 Monate im Vergleich zu 13 Monaten in der Kontrollgruppe (n=83). In der gesamten Patientenpopulation betrug die 2-Jahres-Überlebensrate 43,2% in der Verum-Gruppe und 28,9% in der Kontrollgruppe (Signifikanzniveau im Log-Rank-Test nach Kaplan-Meier:
p=0,0652; im modifizierten Cox-Test: p=0,1120).
Patienten der Verum-Gruppe konnten ihre Ausgangslebensqualität über einen längeren Zeitraum verzeichnen als die der Kontrollgruppe. Der Unterschied war für zwei Zeitpunkte, Woche 19 und 31, statistisch signifikant. Bei der Analyse einer Untergruppe von Patienten mit lokoregionalem Stadium IIIb, bei denen der Tumor nur innerhalb der Lunge lokalisiert ist, ergab sich eine 2-Jahres-Überlebenszeit von 60% in der Verum-Gruppe (n=35) im Vergleich zu 36,7% in der Kontrollgruppe (n=30) (Signifikanzniveau im Log-Rank-Test nach Kaplan-Meier: p=0,0575; im modifizierten Cox-Test: p=0,0692). In der Kontrollgruppe betrug die mittlere Überlebenszeit 13,3 Monate. In der Verum-Gruppe war zum Zeitpunkt der Analyse noch keine mittlere Überlebenszeit erreicht.
„Diese Phase II-Daten sind im Hinblick auf den potenziellen Nutzen für die Patienten so ermutigend, weil sie auf einem Felde stattfinden, wo trotz so vieler Jahre Arbeit so geringe Fortschritte erzielt wurden“, sagte Dr. Bernhard Ehmer, Leiter des Geschäftsbereichs Onkologie.
"Die unabhängige Prüfung durch mehrere Experten, das sogenannte
Peer-Review, ist für uns eine gute Gelegenheit, unsere Daten weltweit
onkologischen Fachkreisen zur Verfügung zu stellen," sagte Dr. Alex
McPherson, Präsident und CEO von Biomira. "In der Geschichte der Medizin
hatte Lungenkrebs schon immer den Stellenwert einer schwer therapierbaren
Erkrankung. Diese bemerkenswerten Daten sowie die Aussicht auf noch bessere
Ergebnisse bei Erreichen des nächsten Messpunktes im Dezember fördern unser
begeistertes Engagement für diese Therapie."
Die Merck KGaA und Biomira wollen im Dezember dieses Jahres die nächsten
Ergebnisse aus dieser Studie veröffentlichen. Außerdem erwarten die
Unternehmen Ende 2005 in mehreren Ländern einschließlich der USA, Kanada
und Europas eine große Studie mit Patienten des inoperablem Stadium III
starten zu können.
Weitere Einzelheiten zur Studie
Die Patienten der Verum-Gruppe erhielten einmalig eine niedrige Dosis
Cyclophosphamid (iv) vor der ersten Impfung mit 1000 µg L-BLP25. Die
Impfungen wurden in den ersten acht Wochen wöchentlich, danach in
sechswöchigen Abständen durchgeführt. Die Erfassung von Lebensqualität und
klinischen Befunden fand in den Wochen 4 und 8, danach in 12-wöchigen
Abständen statt.
Über Lungenkrebs
Lungenkrebs ist in Nordamerika unabhängig vom Geschlecht die
Krebs-Todesursache Nummer 1. Dieses Jahr werden in den USA ca. 174 000
Neuerkrankungen diagnostiziert und 160 000 Amerikaner werden an dieser
Erkrankung sterben. In Kanada schätzt man die Zahl der Erstdiagnosen im
Jahr 2004 auf 21 700 und die Zahl der Todesfälle auf ca. 18 900. Ein
nicht-kleinzelliges Bronchialkarzinom (NSCLC) liegt bei ca. 75-80% aller
Primärtumore der Lunge vor. Zum Zeitpunkt der Diagnosestellung können nur
noch 25% der NSCLC potentiell durch Operation geheilt werden.
Über L-BLP25
L-BLP25 ist ein synthetisches MUC1-Peptid-Vakzin, das in einer liposomalen
Formulierung eine 25er-Aminosäurensequenz des Krebsmuzins MUC1 einbaut.
Das Lipsom fördert die Erkennung des Krebsantigens durch das Immunsystem
und unterstützt die Wirkung. L-BLP25 soll eine Immunreaktion auf
Krebszellen hervorrufen. Der Impfstoff hatte im September 2004 von der FDA
den Status des beschleunigten Prüfverfahrens (Fast Track Designation)
erhalten.
Der im März 2001 zwischen Merck KGaA und Biomira geschlossene Vertrag
beinhaltet die gemeinsame Vermarktung von L-BLP25 in den USA. In allen
übrigen Ländern, mit Ausnahme von Kanada, Israel und dem palästinensischen
Autonomiegebiet, hält Merck die alleinigen Entwicklungs- und
Vermarktungsrechte.
Zu Merck KGaA
Merck arbeitet engagiert an der Verbesserung der Behandlungsmöglichkeiten
für Krebspatienten. Derzeit untersucht das Unternehmen sehr gezielt
neuartige Therapien in ausgesuchten Bereichen. Es laufen Studien zur
Anwendung von L-BLP25 für NSCLC und Erbitux bei Kolorektalkarzinomen,
Plattenepithelkarzinomen des Kopfes und Halses sowie bei NSCLC. Ergebnisse
zweier Erbitux-Studien wurden heute morgen auf dem ESMO-Kongress
präsentiert
@donner
Aus dem fettgedruckten könnte man eine Zulassung vor Phase3 ableiten,oder sehe Ich das falsch?
Aus dem fettgedruckten könnte man eine Zulassung vor Phase3 ableiten,oder sehe Ich das falsch?

Webcast Alert: Biomira Inc. Presentation at Informed Investors Biotechnology/Cancer Stocks Virtual Forum to be Webcast on Thursday, November 4, 2004, 10:00 am ET
Tuesday November 2, 9:00 am ET
RICHMOND, Va.--(BUSINESS WIRE)--Nov. 2, 2004--Informed Investors Forums announces the presentation of Biomira Inc. (NASDAQ: BIOM - News; TSX: BRA - News) at the following forum:
What: Biomira Inc. (NASDAQ: BIOM - News; TSX: BRA - News) will give a
presentation at Informed Investors Biotechnology/Cancer
Stocks Virtual Forum.
Ronald Garren, M.D., Board Certified Internist and Editor of
Biotech Insight, will deliver the forum keynote at 9 am.
When: November 4, 2004 @ 10:00 AM Eastern Time
Where: http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130" target="_blank" rel="nofollow ugc noopener">http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130
How: Live over the Internet--Simply log on to the web at the
address above.
Contact: Jane Tulloch, Director, Investor Relations,
jtulloch@biomira.com
If you are unable to attend the live event, the forum will be available via webcast at http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130" target="_blank" rel="nofollow ugc noopener">http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130.
Biomira Inc. is a biotechnology company applying its leading technology in immunotherapy and organic chemistry for the development of cancer therapeutics. The Company`s commitment to the development of products for the treatment of cancer is currently focused on synthetic therapeutic vaccines and innovative strategies for immunotherapeutic treatment of cancer.
--------------------------------------------------------------------------------
Contact:
Informed Investors
Cary Loeser, 804-327-3407
cloeser@wilink.com
http://www.informedinvestors.com
--------------------------------------------------------------------------------
Source: Biomira Inc.
 Die werden ja auf einmal aktiv !!
Die werden ja auf einmal aktiv !! 
Tuesday November 2, 9:00 am ET
RICHMOND, Va.--(BUSINESS WIRE)--Nov. 2, 2004--Informed Investors Forums announces the presentation of Biomira Inc. (NASDAQ: BIOM - News; TSX: BRA - News) at the following forum:
What: Biomira Inc. (NASDAQ: BIOM - News; TSX: BRA - News) will give a
presentation at Informed Investors Biotechnology/Cancer
Stocks Virtual Forum.
Ronald Garren, M.D., Board Certified Internist and Editor of
Biotech Insight, will deliver the forum keynote at 9 am.
When: November 4, 2004 @ 10:00 AM Eastern Time
Where: http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130" target="_blank" rel="nofollow ugc noopener">http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130
How: Live over the Internet--Simply log on to the web at the
address above.
Contact: Jane Tulloch, Director, Investor Relations,
jtulloch@biomira.com
If you are unable to attend the live event, the forum will be available via webcast at http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130" target="_blank" rel="nofollow ugc noopener">http://www.informedinvestors.com/IIF_Forum.asp?ForumID=85130.
Biomira Inc. is a biotechnology company applying its leading technology in immunotherapy and organic chemistry for the development of cancer therapeutics. The Company`s commitment to the development of products for the treatment of cancer is currently focused on synthetic therapeutic vaccines and innovative strategies for immunotherapeutic treatment of cancer.
--------------------------------------------------------------------------------
Contact:
Informed Investors
Cary Loeser, 804-327-3407
cloeser@wilink.com
http://www.informedinvestors.com
--------------------------------------------------------------------------------
Source: Biomira Inc.
 Die werden ja auf einmal aktiv !!
Die werden ja auf einmal aktiv !! 
Mir kommt der Kursverlauf irgendwie bekannt vor!
Es gab vor längerer Zeit auch solch ein Fall,
das Unternehmen bekam den Fast-Track-Status
wie jetzt auch Biomira.
Der Kursverlauf damals bei 10Euro ging auch nur schleppend voran ,aber einige Monate später schoss der Wert ohne weitere Nachrichten bis über 100Euro hoch.
Es handelt sich damals auch um solch ein Medikament wie bei Biomira!
Wer hilft?Das Unternehmen fing wenn mich nicht alles täuscht mit S... an!
Es gab vor längerer Zeit auch solch ein Fall,
das Unternehmen bekam den Fast-Track-Status
wie jetzt auch Biomira.
Der Kursverlauf damals bei 10Euro ging auch nur schleppend voran ,aber einige Monate später schoss der Wert ohne weitere Nachrichten bis über 100Euro hoch.
Es handelt sich damals auch um solch ein Medikament wie bei Biomira!
Wer hilft?Das Unternehmen fing wenn mich nicht alles täuscht mit S... an!
Da haben wir den Wert,mit O fing er an :-)
24.09.2002
Der US-Pharmakonzern OSI Pharmaceuticals Inc. erhielt von der US-Food and Drug Administration den „Fast Track Status“ für sein Medikament Tarceva. Dieses Dient zur Behandlung von nicht-kleinzelligem Lungenbrebs bei Patienten, bei denen eine Standtherapie nicht anschlägt.
Die Gesundheitsbehörde gewährt dieses beschleunigte Prüfungsverfahren solchen neuen Arzneimitteln, die zur Behandlung von lebensbedrohlichen Krankheiten dienen, für die es bisher keine Medikamente gibt, oder wenn der Zulassungskandidat eine bedeutende Verbesserung gegenüber bisher verfügbarer Behandlungsmethoden darstellt.
Die Aktien fielen an der NASDAQ um 11,55 Prozent und schlossen bei 13,09 Dollar.

Ps.
Noch ein schöner Wert!
Wird Merck mit Biomira wieder das gleiche erleben wie mit sein Partner ImClone Syt.???


24.09.2002
Der US-Pharmakonzern OSI Pharmaceuticals Inc. erhielt von der US-Food and Drug Administration den „Fast Track Status“ für sein Medikament Tarceva. Dieses Dient zur Behandlung von nicht-kleinzelligem Lungenbrebs bei Patienten, bei denen eine Standtherapie nicht anschlägt.
Die Gesundheitsbehörde gewährt dieses beschleunigte Prüfungsverfahren solchen neuen Arzneimitteln, die zur Behandlung von lebensbedrohlichen Krankheiten dienen, für die es bisher keine Medikamente gibt, oder wenn der Zulassungskandidat eine bedeutende Verbesserung gegenüber bisher verfügbarer Behandlungsmethoden darstellt.
Die Aktien fielen an der NASDAQ um 11,55 Prozent und schlossen bei 13,09 Dollar.
Ps.
Noch ein schöner Wert!
Wird Merck mit Biomira wieder das gleiche erleben wie mit sein Partner ImClone Syt.???

Na, da hat es Biomira (bzw. BLP-25) auch in die deutschsprachige Presse geschafft 
pte041103041
Medizin/Wellness, Forschung/Technologie
Medikament erhöht Überlebenszeit bei Lungenkrebs
Fokussierung auf bestimmte Moleküle aktiviert Immunsystem
Edmonton (pte, 3. November 2004 15:55) - Ein Medikament, das dem
Immunsystem dabei hilft Lungenkrebszellen zu erkennen und zu attackieren,
kann die Überlebenszeit von Patienten mit fortgeschrittener Krankheit
verlängern. Zu diesem Ergebnis kommt ein Forscherteam vom Cross Cancer
Institute http://www.albertabreast.com/cci/ in Edmonton, Kanada, das
Versuche an 171 Patienten durchgeführt hat, von denen viele nach zwei
Jahren noch leben. Nun hoffen die Forscher, dass das Präparat eines Tages
neben Chirurgie, Chemotherapie und Strahlentherapie eingesetzt wird.
Ein größerer Versuch zur dritten Phase ist für nächstes Jahr geplant. Der
Forscher Charles Butts sagte, das Medikament habe besonders
vielversprechende Ergebnisse bei Patienten erzielt, deren Krebs schon zu
fortgeschritten für einen chirurgischen Eingriff war, sich aber noch
nicht zu entfernten Organen ausgebreitet hat. Die Standardchemotherapie
greift auch die normalen Zellen an. Das neue Präparat ist in seiner
Wirkung selektiver und motiviert das Immunsystem zur Suche und Attacke
ausschließlich auf Tumorzellen. Das funktioniert über die Fokussierung
auf Zucker-Protein-Moleküle, die nur an der Oberfläche von Tumorzellen zu
finden sind.
Das Medikament L-BLP25 wurde an Patienten mit der am meisten verbreiteten
Form von Lungenkrebs getestet, dem so genannten Non-Small-Cell
Lungenkrebs. Insgesamt überlebten Patienten mit dem neuen Schutzstoff
durchschnittlich 17,4 Monate, im Vergleich zu einem Durchschnitt von 13
Monaten für jene, die die Standardversorgung erhielten. Bei den
Patienten, deren Krebs zu fortgeschritten für einen chirurgischen
Eingriff war, sich aber noch nicht zu anderen Organen ausgebreitet hatte,
war der Effekt noch deutlicher ausgeprägt. Patienten mit
Standard-Behandlung überlebten durchschnittlich 13,3 Monate, aber bei
jenen, die das neue Medikament bekamen, waren nach zwei Jahren noch 60
Prozent am Leben.
Experten halten das neue Präparat für vielversprechend, betonen aber,
dass noch weitere klinische Versuche notwendig sind. In Großbritannien
erkranken jedes Jahr 31.000 Menschen an Lungenkrebs, 27.000 sterben an
der Krankheit. (Ende)
Aussender: pressetext.austria
Ansprechpartner: Marietta Gross,
email: gross@pressetext.at

pte041103041
Medizin/Wellness, Forschung/Technologie
Medikament erhöht Überlebenszeit bei Lungenkrebs
Fokussierung auf bestimmte Moleküle aktiviert Immunsystem
Edmonton (pte, 3. November 2004 15:55) - Ein Medikament, das dem
Immunsystem dabei hilft Lungenkrebszellen zu erkennen und zu attackieren,
kann die Überlebenszeit von Patienten mit fortgeschrittener Krankheit
verlängern. Zu diesem Ergebnis kommt ein Forscherteam vom Cross Cancer
Institute http://www.albertabreast.com/cci/ in Edmonton, Kanada, das
Versuche an 171 Patienten durchgeführt hat, von denen viele nach zwei
Jahren noch leben. Nun hoffen die Forscher, dass das Präparat eines Tages
neben Chirurgie, Chemotherapie und Strahlentherapie eingesetzt wird.
Ein größerer Versuch zur dritten Phase ist für nächstes Jahr geplant. Der
Forscher Charles Butts sagte, das Medikament habe besonders
vielversprechende Ergebnisse bei Patienten erzielt, deren Krebs schon zu
fortgeschritten für einen chirurgischen Eingriff war, sich aber noch
nicht zu entfernten Organen ausgebreitet hat. Die Standardchemotherapie
greift auch die normalen Zellen an. Das neue Präparat ist in seiner
Wirkung selektiver und motiviert das Immunsystem zur Suche und Attacke
ausschließlich auf Tumorzellen. Das funktioniert über die Fokussierung
auf Zucker-Protein-Moleküle, die nur an der Oberfläche von Tumorzellen zu
finden sind.
Das Medikament L-BLP25 wurde an Patienten mit der am meisten verbreiteten
Form von Lungenkrebs getestet, dem so genannten Non-Small-Cell
Lungenkrebs. Insgesamt überlebten Patienten mit dem neuen Schutzstoff
durchschnittlich 17,4 Monate, im Vergleich zu einem Durchschnitt von 13
Monaten für jene, die die Standardversorgung erhielten. Bei den
Patienten, deren Krebs zu fortgeschritten für einen chirurgischen
Eingriff war, sich aber noch nicht zu anderen Organen ausgebreitet hatte,
war der Effekt noch deutlicher ausgeprägt. Patienten mit
Standard-Behandlung überlebten durchschnittlich 13,3 Monate, aber bei
jenen, die das neue Medikament bekamen, waren nach zwei Jahren noch 60
Prozent am Leben.
Experten halten das neue Präparat für vielversprechend, betonen aber,
dass noch weitere klinische Versuche notwendig sind. In Großbritannien
erkranken jedes Jahr 31.000 Menschen an Lungenkrebs, 27.000 sterben an
der Krankheit. (Ende)
Aussender: pressetext.austria
Ansprechpartner: Marietta Gross,
email: gross@pressetext.at
Patienten mit Standard-Behandlung überlebten durchschnittlich 13,3 Monate, aber bei
jenen, die das neue Medikament bekamen, waren nach zwei Jahren noch 60 Prozent am Leben.



jenen, die das neue Medikament bekamen, waren nach zwei Jahren noch 60 Prozent am Leben.



Also mittlerweile glaube ich, dass sich der Kurs erst nach dem Dezember Update wesentlich höher bewegen wird.
Zurzeit werden nur Stücke eingesammelt und der Kurs untengehalten. Sieht im Orderbuch immer ganz nett aus.
STRONG BUY
Morgen hat BIOM zwei Termine an einem Tag.
Zurzeit werden nur Stücke eingesammelt und der Kurs untengehalten. Sieht im Orderbuch immer ganz nett aus.
STRONG BUY

Morgen hat BIOM zwei Termine an einem Tag.

Overall Average: 88% - Buy 

Overall Average: 48% - Buy 

Aus einem US-Börsenbrief Ende 1999 :
Theratope (Anm. : Vaccine von BIOM ) has already been used in over 350 patients with either breast, colorectal or an ovarian cancer with very exciting results. For example in one trial, which was prospectively randomized (the gold standard), patients receiving the vaccines had a median survival of 26.6 months compared with 9.2 months for matched controls. Remember these were patients with more advanced cancers. It is traditional that when a therapy works in advanced cases it is moved up and used in less severely effected patients, creating a potentially huge market.--
16.6.2003 : BIOMIRA AND MERCK KGaA ANNOUNCE PHASE III THERATOPE® VACCINE TRIAL DOES NOT MEET PRIMARY ENDPOINTS - Trend to Improvement in Survival Seen in Subset of Patients
Die Studie wurde eingestellt.
Das ist für mich die Erklärung, warum die Präsentation auf dem ESMO sich nicht im Kurs von BIOM widerspiegelt. Bisher hat eine Vaccinierung - außer vielleicht bei Hautkrebs und Nierenkrebs - noch nie gute Ergebnisse gebracht.
Theratope (Anm. : Vaccine von BIOM ) has already been used in over 350 patients with either breast, colorectal or an ovarian cancer with very exciting results. For example in one trial, which was prospectively randomized (the gold standard), patients receiving the vaccines had a median survival of 26.6 months compared with 9.2 months for matched controls. Remember these were patients with more advanced cancers. It is traditional that when a therapy works in advanced cases it is moved up and used in less severely effected patients, creating a potentially huge market.--
16.6.2003 : BIOMIRA AND MERCK KGaA ANNOUNCE PHASE III THERATOPE® VACCINE TRIAL DOES NOT MEET PRIMARY ENDPOINTS - Trend to Improvement in Survival Seen in Subset of Patients
Die Studie wurde eingestellt.
Das ist für mich die Erklärung, warum die Präsentation auf dem ESMO sich nicht im Kurs von BIOM widerspiegelt. Bisher hat eine Vaccinierung - außer vielleicht bei Hautkrebs und Nierenkrebs - noch nie gute Ergebnisse gebracht.
Data from Biomira`s Patient-Specific Cancer Vaccine to be Presented at 2004 Annual Meeting of the American Society of Hematology at San Diego
Data Accepted for Oral Presentation
EDMONTON, Nov 9, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) of Edmonton, Alberta, Canada, announced today that data from a Phase Ib clinical research trial to test the safety and immunogenicity of its autologous vaccine for the treatment of B-cell lymphoma will form the basis of an oral presentation at the 2004 Annual Meeting of the American Society of Hematology (ASH) in San Diego. Sattva S. Neelapu, M.D., of the MD Anderson Cancer Center in Houston, TX, is to present the data. The trial was carried out under a Collaborative Research and Development Agreement (CRADA) with the U.S. National Cancer Institute (NCI) in 2001. The oral presentation is scheduled for 9:30 a.m., Tuesday, December 7th, 2004. The meeting is to be held from December 4th to 7th, 2004.
The purpose of the trial was to:
1. determine the safety of a new formulation of the vaccine;
2. see if an immunologic response could be induced in patients with
tumour-induced immunosuppression; and
3. observe any evidence of efficacy.
The results of the trial showed that the vaccine was well-tolerated and induced only minor reactions at the site of injection. Vaccination resulted in specific immunological responses in six of 10 patients (one patient was not tested for immune responses). One patient saw a sustained complete response. The remaining 10 patients had disease progression after a median duration of approximately eight months.
"We were gratified to learn that data from this early phase clinical trial has been accepted for oral presentation at such a prestigious meeting," said Alex McPherson, MD, PhD, President and CEO. "We support these findings and note that this data may also serve as a model for vaccine development against other human cancers."
Out-Licensing Opportunities
Biomira is not moving this product candidate forward at this time and is actively seeking out-licensing opportunities for the autologous vaccine program. The program was discontinued in 2001 so that Biomira could concentrate its efforts on its two lead product candidates, BLP25 Liposome Vaccine and Theratope(R) vaccine.
About the ASH Meeting
Each December, the Society`s annual meeting provides hematologists from around the world a forum for discussing critical issues in hematology. Nearly 20,000 clinicians, scientists, and others attend the four-day meeting, which consists of a superb educational program and cutting-edge scientific sessions. Oral and poster presentations, which are chosen by peer-reviewers from abstracts submitted prior to the annual meeting, are featured at the annual meeting and contain the latest and most exciting developments in scientific research.
About Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the Company`s efforts to out-license this product candidate and potential future vaccine development as an outcome of this clinical trial. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
SOURCE Biomira Inc.
CONTACT: Biomira Company Contact: Jane Tulloch, Director, Investor
Relations, (780) 490-2812; U.S. Media Contact: Daniel Budwick, BMC
Communications, (212) 477-9007 X14;
To request a free copy of this organization`s annual report, please go to
http://www.newswire.ca and click on reports@cnw.
(BRA. BIOM)
http://www.prnewswire.com
Data Accepted for Oral Presentation
EDMONTON, Nov 9, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) of Edmonton, Alberta, Canada, announced today that data from a Phase Ib clinical research trial to test the safety and immunogenicity of its autologous vaccine for the treatment of B-cell lymphoma will form the basis of an oral presentation at the 2004 Annual Meeting of the American Society of Hematology (ASH) in San Diego. Sattva S. Neelapu, M.D., of the MD Anderson Cancer Center in Houston, TX, is to present the data. The trial was carried out under a Collaborative Research and Development Agreement (CRADA) with the U.S. National Cancer Institute (NCI) in 2001. The oral presentation is scheduled for 9:30 a.m., Tuesday, December 7th, 2004. The meeting is to be held from December 4th to 7th, 2004.
The purpose of the trial was to:
1. determine the safety of a new formulation of the vaccine;
2. see if an immunologic response could be induced in patients with
tumour-induced immunosuppression; and
3. observe any evidence of efficacy.
The results of the trial showed that the vaccine was well-tolerated and induced only minor reactions at the site of injection. Vaccination resulted in specific immunological responses in six of 10 patients (one patient was not tested for immune responses). One patient saw a sustained complete response. The remaining 10 patients had disease progression after a median duration of approximately eight months.
"We were gratified to learn that data from this early phase clinical trial has been accepted for oral presentation at such a prestigious meeting," said Alex McPherson, MD, PhD, President and CEO. "We support these findings and note that this data may also serve as a model for vaccine development against other human cancers."
Out-Licensing Opportunities
Biomira is not moving this product candidate forward at this time and is actively seeking out-licensing opportunities for the autologous vaccine program. The program was discontinued in 2001 so that Biomira could concentrate its efforts on its two lead product candidates, BLP25 Liposome Vaccine and Theratope(R) vaccine.
About the ASH Meeting
Each December, the Society`s annual meeting provides hematologists from around the world a forum for discussing critical issues in hematology. Nearly 20,000 clinicians, scientists, and others attend the four-day meeting, which consists of a superb educational program and cutting-edge scientific sessions. Oral and poster presentations, which are chosen by peer-reviewers from abstracts submitted prior to the annual meeting, are featured at the annual meeting and contain the latest and most exciting developments in scientific research.
About Biomira
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
This release may contain forward-looking statements. Various factors could cause actual results to differ materially from those projected in forward-looking statements, including those predicting the Company`s efforts to out-license this product candidate and potential future vaccine development as an outcome of this clinical trial. Although the Company believes that the forward-looking statements contained herein are reasonable, it can give no assurance that the Company`s expectations are correct. All forward-looking statements are expressly qualified in their entirety by this cautionary statement.
SOURCE Biomira Inc.
CONTACT: Biomira Company Contact: Jane Tulloch, Director, Investor
Relations, (780) 490-2812; U.S. Media Contact: Daniel Budwick, BMC
Communications, (212) 477-9007 X14;
To request a free copy of this organization`s annual report, please go to
http://www.newswire.ca and click on reports@cnw.
(BRA. BIOM)
http://www.prnewswire.com
Relativ hohes Volumen und Kurs läuft seitwärts ?
Hier wird doch bis Dezember eingesammelt, oder?
Hier wird doch bis Dezember eingesammelt, oder?

Hallo Leute
Was ist denn hier los???? War leider ein wenig kränklich, so das ich nicht ins Net kam Aber hier passiert ja nix
Aber hier passiert ja nix
 Donner, keine positiven neuen News? Selbst die "Stimme aus Darmstadt" ist verstummt
Donner, keine positiven neuen News? Selbst die "Stimme aus Darmstadt" ist verstummt
LG Peter
Was ist denn hier los???? War leider ein wenig kränklich, so das ich nicht ins Net kam
 Aber hier passiert ja nix
Aber hier passiert ja nix
 Donner, keine positiven neuen News? Selbst die "Stimme aus Darmstadt" ist verstummt
Donner, keine positiven neuen News? Selbst die "Stimme aus Darmstadt" ist verstummt
LG Peter
Raus aus OSIP und Rein in BIOM scheint die Devise
in Amerika zu sein!
Herzlich Willkommen.
Mal sehen, was nächste Woche passiert.
in Amerika zu sein!
Herzlich Willkommen.

Mal sehen, was nächste Woche passiert.
Einfach mal zurück lehnen und jetzt Biomira etwas Zeit lassen!


#866





Nasdaq BIOM USD 1,40 1,48 +0,080 +5,71 % 138.813 117.002 29. Nov 16:04




















Ein sehr interessanter Artikel aus Canada!!!

Nov. 29, 2004. 01:00 AM
Cancer vaccines proving elusive
Canada`s Biomira among firms to suffer setbacks
But significant products edging toward market
http://www.thestar.com/NASApp/cs/ContentServer?pagename=thes…
But vaccines are likely to make their biggest mark as cancer therapies, says Mellstedt, pointing to new data on a lung cancer vaccine being developed by Canadian firm Biomira Inc. and Germany`s Merck KgaA.
In early November, new Phase II data on the companies` L-BLP25 vaccine showed that combined with chemotherapy the compound extended the survival of 88 lung cancer patients by an average 4.4 months compared to 83 patients treated with chemotherapy alone, though the results were more significant in patients with early-stage disease.
If the survival rates are confirmed in advanced clinical trials, the vaccine "will change the way we treat lung cancer," Mellstedt said.
The Biomira/Merck data exemplify common problems in cancer vaccine studies, which often produce signs of effectiveness in early-stage testing but fail to generate the desired response in broader patient populations.
Phase III trials "will be the test for the Biomira/Merck vaccine," Wood Mackenzie`s Lewis said.
Another Biomira vaccine called Theratope, aimed at breast cancer, failed in Phase III clinical trials, in a large population, and has been returned to Phase II trials on a smaller number of select patients.
Despite setbacks, Mellstedt predicts vaccines may one day join surgery, chemotherapy and radiotherapy as standard cancer therapies.
L-BLP25 may also be effective in other tumour types, including pancreatic and colon tumours, Mellstedt asserted.
U.S. biotech firm Antigenics Inc. has received fast-track designation for its Oncophage vaccine, currently undergoing Phase III trials for kidney cancer and advanced skin cancer.
U.K. industry research firm Evaluate Pharma estimates that Oncophage could generate as much as $200 million a year by 2009. GlaxoSmithKline is conducting Phase II trials on a lung cancer and skin cancer vaccine that some industry watchers forecast could reach the market by 2009.
Aventis Pasteur, the world`s largest vaccines company, is conducting clinical trials on vaccines to treat colorectal cancer and skin cancer.



Nasdaq BIOM USD 1,40 1,50 +0,100 +7,14 % 828.768 624.520 29. Nov 22:01
@All
In den USA steigende Kurse bei einigermaßen Umsätzen und in Old Germany nix

Fragende Grüße Peter
In den USA steigende Kurse bei einigermaßen Umsätzen und in Old Germany nix


Fragende Grüße Peter
1,63 mit gutem umsatz.
Vieleicht kauft Merck noch paar ...
Endlich stehen mal richtige Stückzahlen im Orderbuch.

Endlich stehen mal richtige Stückzahlen im Orderbuch.
Das Handelsvolumen nimmt zwar ordentlich zu ,trotzdem liegt es immer noch weit hinter den Erwartungen bzw. der Möglichkeit was hier zum Abschluss kommen könnte!
Insiderkäufe werden zur Zeit mit Sicherheit nicht umgesetzt!
Der Kursverlauf beginnt hier mit 1.Woche vor den News dagegen schon recht früh!
Mal sehn in der Vergangenheit präsentierten sich die 2,20 immer als Angriffsroute!

.

Insiderkäufe werden zur Zeit mit Sicherheit nicht umgesetzt!
Der Kursverlauf beginnt hier mit 1.Woche vor den News dagegen schon recht früh!
Mal sehn in der Vergangenheit präsentierten sich die 2,20 immer als Angriffsroute!
.





Nasdaq BIOM USD 1,50 1,68 +0,180 +12,00 % 1,70 Mio. 1.234.277 30. Nov 22:01
Frankfurt BM2 EUR 1,11 1,20 +0,090 +8,11 % 5.271 4.400 30. Nov 19:30
wenn BIOM es drauf hat, dann sind die 16 machbar !
gruß
bio
gruß
bio
BIOM - BIOMIRA INC (NASDAQ)
Date Open High Low Last Change Volume % Change
11/30/04 1.53 1.68 1.53 1.66 +0.15 1607400 +9.93%
Composite Indicator -- Signal -- -- Strength -- -- Direction --
Trend Spotter (TM) Buy Strong Strongest
Short Term Indicators
7 Day Average Directional Indicator Buy Strong Strongest
10 - 8 Day Moving Average Hilo Channel Buy Strong Strongest
20 Day Moving Average vs Price Buy Strong Strongest
20 - 50 Day MACD Oscillator Buy Minimum Weakening
20 Day Bollinger Bands Buy Strong Strongest
Short Term Indicators Average: 100% - Buy
Medium Term Indicators
40 Day Commodity Channel Index Buy Average Strongest
50 Day Moving Average vs Price Buy Average Strongest
20 - 100 Day MACD Oscillator Buy Weak Average
50 Day Parabolic Time/Price Buy Strong Strongest
Medium Term Indicators Average: 100% - Buy
Long Term Indicators
60 Day Commodity Channel Index Buy Weak Strongest
100 Day Moving Average vs Price Buy Average Strongest
50 - 100 Day MACD Oscillator Buy Average Strengthening
Long Term Indicators Average: 100% - Buy
Overall Average: 100% - Buy

Date Open High Low Last Change Volume % Change
11/30/04 1.53 1.68 1.53 1.66 +0.15 1607400 +9.93%
Composite Indicator -- Signal -- -- Strength -- -- Direction --
Trend Spotter (TM) Buy Strong Strongest
Short Term Indicators
7 Day Average Directional Indicator Buy Strong Strongest
10 - 8 Day Moving Average Hilo Channel Buy Strong Strongest
20 Day Moving Average vs Price Buy Strong Strongest
20 - 50 Day MACD Oscillator Buy Minimum Weakening
20 Day Bollinger Bands Buy Strong Strongest
Short Term Indicators Average: 100% - Buy
Medium Term Indicators
40 Day Commodity Channel Index Buy Average Strongest
50 Day Moving Average vs Price Buy Average Strongest
20 - 100 Day MACD Oscillator Buy Weak Average
50 Day Parabolic Time/Price Buy Strong Strongest
Medium Term Indicators Average: 100% - Buy
Long Term Indicators
60 Day Commodity Channel Index Buy Weak Strongest
100 Day Moving Average vs Price Buy Average Strongest
50 - 100 Day MACD Oscillator Buy Average Strengthening
Long Term Indicators Average: 100% - Buy
Overall Average: 100% - Buy

Umsatz USA 1,3 Mios, aber Kursbewegungen werden durch Käufe und Verkäufe von kleinen Stückzahlen "gemacht"!
 Grüße Peter
Grüße Peter
 Grüße Peter
Grüße Peter
Guten Morgen!
War das Gestern eine Kurze Pause?
http://www.stockconsultant.com/consultnow/basicplus.cgi?ID=s…
Gute Geschäfte wünscht
verdi
War das Gestern eine Kurze Pause?
http://www.stockconsultant.com/consultnow/basicplus.cgi?ID=s…
Gute Geschäfte wünscht
verdi
Update of BLP25 Liposome Vaccine Phase IIb trial shows stage IIIB patients who received vaccine have not yet reached median survival 23 months post accrual
Data to be Submitted for Presentation and Publication
EDMONTON, Alberta and DARMSTADT, Germany, Dec 3, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) and Merck KGaA of Darmstadt, Germany, announced today that the updated survival analysis of their completed Phase IIb study of the investigational immunotherapy BLP25 Liposome Vaccine (L-BLP25), used in this trial for the treatment of non-small cell lung cancer (NSCLC), showed that a median survival in the pre-stratified subset of locoregional Stage IIIB patients on the vaccine arm has still not been reached. Lung cancer is the leading cause of cancer-related mortality for both sexes in North America.
An exploratory survival update of the randomized, open-label Phase IIb trial of L-BLP25 in 171 men and women with NSCLC, whose disease was stable or who had responded to treatment following first-line standard chemotherapy or a combination of standard chemotherapy and radiotherapy was just completed. This analysis showed that in the subset of men and women with locoregional Stage IIIB disease (locally advanced and unresectable) who received L-BLP25, a survival median has not yet been reached 23 months following the enrollment of the last patient into the trial.
"We believe that the results to date are very exciting, and we look forward to presenting the data," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc.
The study`s investigators plan to submit the updated survival data from this analysis for presentation at an upcoming scientific meeting and for publication in a peer reviewed medical journal.
"The data are encouraging and support plans for Merck KGaA and its U.S. subsidiary, EMD Pharmaceuticals, to continue the collaborative development of L-BLP25 with Biomira," said Bernhard Ehmer, MD, Vice President and Head of Merck`s Oncology Business Area. "In the new year, the companies plan to discuss a Phase III multinational registration trial with regulatory authorities."
In preparation for a potential multinational registration trial, Biomira is already scheduling for the manufacture of new vaccine supplies. These supplies will incorporate manufacturing changes intended to secure the future commercial supply of the vaccine. Scheduling these changes now ensures that the resulting pivotal data will be considered representative of the safety and effectiveness of the commercial supply of the vaccine. To assure the successful initiation of a pivotal trial, a comparability plan is now being developed.
L-BLP25
L-BLP25 is a synthetic MUC1 peptide vaccine. L-BLP25 incorporates a 25-amino acid sequence of the MUC1 cancer mucin, encapsulated in a liposomal delivery system. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery. L-BLP25 is designed to induce an immune response to cancer cells.
About Lung Cancer
In 2004, approximately 174,000 new cases of lung cancer will be diagnosed in the U.S. - 54 per cent of them in men and 46 per cent in women. Approximately 160,000 people will die of this disease in the U.S. alone in 2004. In Canada, the mortality percentages are slightly higher for men - 57 per cent of deaths from lung cancer will occur in men and 43 per cent will be in women. NSCLC accounts for approximately 75 to 80 per cent of all primary lung cancers. At the time of diagnosis, only 25 per cent of patients are potentially curable by surgery.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26 per cent. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas - monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
EMD Pharmaceuticals Inc., the U.S. affiliate of Merck KGaA, is a fully integrated pharmaceutical company with an initial emphasis on launching new products in oncology. Located in Durham, N.C., EMD focuses on meeting patient and physician needs with pioneering pharmaceutical products and services.
Except for historical information contained herein, this release contains forward-looking statements that are subject to risks and uncertainties that may cause actual results to differ materially from the results discussed in the forward-looking statements, particularly those risks and uncertainties surrounding the efficacy of L-BLP25 to treat men and women with NSCLC, which may include risks and uncertainties inherent in the process of discovering, developing and commercializing drugs that are safe and effective for use as human therapeutics. Factors that may cause such a difference include the risk that additional trials may not demonstrate the safety and efficacy required to satisfy the regulatory authorities, the risk that the Company may lack the financial resources and access to capital to fund the required clinical trials, or that it will elect to conduct such additional trials, and other matters required to bring products to market, the uncertainties as to when, if at all, the regulatory authorities will agree to discuss the trial results with the Company and whether they will approve the product and manufacturing facilities, the need to establish and scale-up manufacturing processes, dependence on the efforts of third parties, including suppliers and collaborators, dependence on intellectual property rights and the effectiveness thereof, difficulties or delays in manufacturing products, and regulatory developments involving products and manufacturing facilities. For more detailed information on the risks and uncertainties associated with the Company`s product candidates and other activities see the Company`s periodic reports filed with the applicable securities regulatory authorities in Canada and the United States Securities and Exchange Commission. The Company assumes no obligation to update any forward-looking statements.
SOURCE Biomira Inc.
CONTACT: Biomira Company Contacts: Bill Wickson, Manager, Public
Relations, (780) 490-2818, After hours contact: bwickson@biomira.com;
Jane Tulloch, Director, Investor Relations, (780) 490-2812; U.S. Media, Daniel
Budwick, Media Relations, (212) 477-9007 ext. 14; Merck KGaA Contact, Phyllis
Carter, Mobile: +49 61-51/72-7144;
To request a free copy of this organization`s annual report, please go to
http://www.newswire.ca and click on reports@cnw.
(BRA. BIOM)
http://www.prnewswire.com
Data to be Submitted for Presentation and Publication
EDMONTON, Alberta and DARMSTADT, Germany, Dec 3, 2004 /PRNewswire-FirstCall via COMTEX/ -- Biomira Inc. (Nasdaq:BIOM) (TSX:BRA) and Merck KGaA of Darmstadt, Germany, announced today that the updated survival analysis of their completed Phase IIb study of the investigational immunotherapy BLP25 Liposome Vaccine (L-BLP25), used in this trial for the treatment of non-small cell lung cancer (NSCLC), showed that a median survival in the pre-stratified subset of locoregional Stage IIIB patients on the vaccine arm has still not been reached. Lung cancer is the leading cause of cancer-related mortality for both sexes in North America.
An exploratory survival update of the randomized, open-label Phase IIb trial of L-BLP25 in 171 men and women with NSCLC, whose disease was stable or who had responded to treatment following first-line standard chemotherapy or a combination of standard chemotherapy and radiotherapy was just completed. This analysis showed that in the subset of men and women with locoregional Stage IIIB disease (locally advanced and unresectable) who received L-BLP25, a survival median has not yet been reached 23 months following the enrollment of the last patient into the trial.
"We believe that the results to date are very exciting, and we look forward to presenting the data," said Alex McPherson, MD, PhD, President and CEO of Biomira Inc.
The study`s investigators plan to submit the updated survival data from this analysis for presentation at an upcoming scientific meeting and for publication in a peer reviewed medical journal.
"The data are encouraging and support plans for Merck KGaA and its U.S. subsidiary, EMD Pharmaceuticals, to continue the collaborative development of L-BLP25 with Biomira," said Bernhard Ehmer, MD, Vice President and Head of Merck`s Oncology Business Area. "In the new year, the companies plan to discuss a Phase III multinational registration trial with regulatory authorities."
In preparation for a potential multinational registration trial, Biomira is already scheduling for the manufacture of new vaccine supplies. These supplies will incorporate manufacturing changes intended to secure the future commercial supply of the vaccine. Scheduling these changes now ensures that the resulting pivotal data will be considered representative of the safety and effectiveness of the commercial supply of the vaccine. To assure the successful initiation of a pivotal trial, a comparability plan is now being developed.
L-BLP25
L-BLP25 is a synthetic MUC1 peptide vaccine. L-BLP25 incorporates a 25-amino acid sequence of the MUC1 cancer mucin, encapsulated in a liposomal delivery system. The liposome enhances recognition of the cancer antigen by the immune system and facilitates better delivery. L-BLP25 is designed to induce an immune response to cancer cells.
About Lung Cancer
In 2004, approximately 174,000 new cases of lung cancer will be diagnosed in the U.S. - 54 per cent of them in men and 46 per cent in women. Approximately 160,000 people will die of this disease in the U.S. alone in 2004. In Canada, the mortality percentages are slightly higher for men - 57 per cent of deaths from lung cancer will occur in men and 43 per cent will be in women. NSCLC accounts for approximately 75 to 80 per cent of all primary lung cancers. At the time of diagnosis, only 25 per cent of patients are potentially curable by surgery.
The Companies
Biomira is a biotechnology company specializing in the development of innovative therapeutic approaches to cancer management. Biomira`s commitment to the treatment of cancer currently focuses on the development of synthetic vaccines and novel strategies for cancer immunotherapy. We are The Cancer Vaccine People(TM).
Merck is a global pharmaceutical and chemical company with sales of EUR 7.2 billion in 2003, a history that began in 1668, and a future shaped by 28,300 employees in 56 countries. Its success is characterized by innovations from entrepreneurial employees. Merck`s operating activities come under the umbrella of Merck KGaA, in which the Merck family holds a 74 per cent interest and free shareholders own the remaining 26 per cent. The former U.S. subsidiary, Merck & Co., has been completely independent of the Merck Group since 1917. Merck KGaA has built a strategic oncology portfolio by developing and in-licensing product candidates in four areas - monoclonal antibodies, therapeutic vaccines, immunocytokines and angiogenesis inhibitors.
EMD Pharmaceuticals Inc., the U.S. affiliate of Merck KGaA, is a fully integrated pharmaceutical company with an initial emphasis on launching new products in oncology. Located in Durham, N.C., EMD focuses on meeting patient and physician needs with pioneering pharmaceutical products and services.
Except for historical information contained herein, this release contains forward-looking statements that are subject to risks and uncertainties that may cause actual results to differ materially from the results discussed in the forward-looking statements, particularly those risks and uncertainties surrounding the efficacy of L-BLP25 to treat men and women with NSCLC, which may include risks and uncertainties inherent in the process of discovering, developing and commercializing drugs that are safe and effective for use as human therapeutics. Factors that may cause such a difference include the risk that additional trials may not demonstrate the safety and efficacy required to satisfy the regulatory authorities, the risk that the Company may lack the financial resources and access to capital to fund the required clinical trials, or that it will elect to conduct such additional trials, and other matters required to bring products to market, the uncertainties as to when, if at all, the regulatory authorities will agree to discuss the trial results with the Company and whether they will approve the product and manufacturing facilities, the need to establish and scale-up manufacturing processes, dependence on the efforts of third parties, including suppliers and collaborators, dependence on intellectual property rights and the effectiveness thereof, difficulties or delays in manufacturing products, and regulatory developments involving products and manufacturing facilities. For more detailed information on the risks and uncertainties associated with the Company`s product candidates and other activities see the Company`s periodic reports filed with the applicable securities regulatory authorities in Canada and the United States Securities and Exchange Commission. The Company assumes no obligation to update any forward-looking statements.
SOURCE Biomira Inc.
CONTACT: Biomira Company Contacts: Bill Wickson, Manager, Public
Relations, (780) 490-2818, After hours contact: bwickson@biomira.com;
Jane Tulloch, Director, Investor Relations, (780) 490-2812; U.S. Media, Daniel
Budwick, Media Relations, (212) 477-9007 ext. 14; Merck KGaA Contact, Phyllis
Carter, Mobile: +49 61-51/72-7144;
To request a free copy of this organization`s annual report, please go to
http://www.newswire.ca and click on reports@cnw.
(BRA. BIOM)
http://www.prnewswire.com



kann ganz gut English,
der Satz "has still not been reached" macht mir Sorge, der Rest der Meldung ist ok



der Satz "has still not been reached" macht mir Sorge, der Rest der Meldung ist ok



ooops
Frankfurt BM2 EUR 1,16 1,56 + 0,400 + 34,48 % 20.605 15.210 03. Dez 13:21
Stuttgart BM2 EUR 1,12 1,20 + 0,080 + 7,14 % 1.200 1.000 03. Dez 12:24
wird spannend heute!!



Frankfurt BM2 EUR 1,16 1,56 + 0,400 + 34,48 % 20.605 15.210 03. Dez 13:21
Stuttgart BM2 EUR 1,12 1,20 + 0,080 + 7,14 % 1.200 1.000 03. Dez 12:24
wird spannend heute!!



Merck KGaA: Ergebnisse der Phase IIb-Studie zu BLP25 "ermutigend
Leser des Artikels: 10
Merck KGaA: Ergebnisse der Phase IIb-Studie zu BLP25 "ermutigend" FRANKFURT (Dow Jones-VWD)--Die Merck KGaA, Darmstadt, hat die Ergebnisse der aktualisierten Phase-IIb-Studie zum liposomalen Krebsimpfstoff BLP25 als "ermutigend" bezeichnet. In der Patientengruppe mit dem sogenannten lokoregionalen Erkrankungsstadium IIIB, die mit dem Medikament behandelt wurde, sei die mittlere Überlebenszeit von 23 Monaten noch nicht erreicht, teilte Merck am Freitag mit. Die bei der Studie beteiligten Prüfärzte wollten die aktualisierten Überlebensdaten zur Präsentation auf der nächsten Fachtagung sowie zur Veröffentlichung in einer medizinischen Fachzeitschrift einreichen. "Die Daten sind ermutigend und stützen die Pläne der Merck KGaA und ihrer US-Tochtergesellschaft EMD Pharmaceuticals, die Forschungskooperation zu L-BLP-25 mit Biomira aufrecht zu erhalten", erklärte Bernhard Ehmer, Vizepräsident und Leiter des Geschäftsbereichs Onkologie bei Merck. Im kommenden Jahr planten die Unternehmen, mit den Zulassungsbehörden die Aufnahme einer multinationalen Zulassungsstudie der Phase III zu erörtern. In Vorbereitung auf diese Zulassungsstudie plane Biomira bereits die Herstellung weiterer Impfstoff-Chargen. (ENDE) Dow Jones Newswires/3.12.2004/fnö/nas
Diese Nachricht wurde Ihnen von Dow Jones-VWD und TeleTrader präsentiert.
Autor: TeleTrader News Room, 12:36 03.12.04
Leser des Artikels: 10
Merck KGaA: Ergebnisse der Phase IIb-Studie zu BLP25 "ermutigend" FRANKFURT (Dow Jones-VWD)--Die Merck KGaA, Darmstadt, hat die Ergebnisse der aktualisierten Phase-IIb-Studie zum liposomalen Krebsimpfstoff BLP25 als "ermutigend" bezeichnet. In der Patientengruppe mit dem sogenannten lokoregionalen Erkrankungsstadium IIIB, die mit dem Medikament behandelt wurde, sei die mittlere Überlebenszeit von 23 Monaten noch nicht erreicht, teilte Merck am Freitag mit. Die bei der Studie beteiligten Prüfärzte wollten die aktualisierten Überlebensdaten zur Präsentation auf der nächsten Fachtagung sowie zur Veröffentlichung in einer medizinischen Fachzeitschrift einreichen. "Die Daten sind ermutigend und stützen die Pläne der Merck KGaA und ihrer US-Tochtergesellschaft EMD Pharmaceuticals, die Forschungskooperation zu L-BLP-25 mit Biomira aufrecht zu erhalten", erklärte Bernhard Ehmer, Vizepräsident und Leiter des Geschäftsbereichs Onkologie bei Merck. Im kommenden Jahr planten die Unternehmen, mit den Zulassungsbehörden die Aufnahme einer multinationalen Zulassungsstudie der Phase III zu erörtern. In Vorbereitung auf diese Zulassungsstudie plane Biomira bereits die Herstellung weiterer Impfstoff-Chargen. (ENDE) Dow Jones Newswires/3.12.2004/fnö/nas
Diese Nachricht wurde Ihnen von Dow Jones-VWD und TeleTrader präsentiert.
Autor: TeleTrader News Room, 12:36 03.12.04
2,2/2,50













 2,50 / 2,70
2,50 / 2,70
1,65 (max)
mal sehn, wie´s in ami-land startet....
http://de.finance.yahoo.com/q?s=BIOM.F&d=c&k=c1&a=v&p=s&t=1d…
mal sehn, wie´s in ami-land startet....
http://de.finance.yahoo.com/q?s=BIOM.F&d=c&k=c1&a=v&p=s&t=1d…
ach Du Scheisse ... 
Frankfurt BM2 EUR 1,16 1,65 + 0,490 + 42,24 % 33.265 23.210 03. Dez 14:02
Nasdaq BIOM USD 1,53 2,48 + 0,950 + 62,09 % 29.080 12.000 03. Dez 14:03

Frankfurt BM2 EUR 1,16 1,65 + 0,490 + 42,24 % 33.265 23.210 03. Dez 14:02
Nasdaq BIOM USD 1,53 2,48 + 0,950 + 62,09 % 29.080 12.000 03. Dez 14:03
Nasdaq BIOM USD 1,53 2,82 + 1,29 + 84,31 % 32.735 13.300 03. Dez 14:05
Nasdaq BIOM USD 1,53 3,30 + 1,77 + 115,69 % 44.049 16.900 03. Dez 14:07




































2,75 USD!!!





....da scheint noch weit mehr drin zu sein.

@ll
WELTSENSATION
Biomira steht erst noch vor den Anfang,was bei einer Zulassung passiert kann sich wohl jeder selber ausrechnen!
Wir reden hier von einem Milliarden Markt.....und Biomira/Merck haben zur zeit das fortgeschrittenes Medikament gegen die unheilbaren Krankheit !"Lungenkrebs"


Schaut euch den Verlauf von OSI Pharmaceuticals !!!
#866


WELTSENSATION
Biomira steht erst noch vor den Anfang,was bei einer Zulassung passiert kann sich wohl jeder selber ausrechnen!
Wir reden hier von einem Milliarden Markt.....und Biomira/Merck haben zur zeit das fortgeschrittenes Medikament gegen die unheilbaren Krankheit !"Lungenkrebs"



Schaut euch den Verlauf von OSI Pharmaceuticals !!!
#866



Ich hoffe jetzt sehen einige mehr als nur ich was hier überhaupt vom Konzern Merck und Biomira fundamental wiedergeben wurde!
In einer nun abgeschlossenen Phase-IIb-Studie wurde das Präparat zur Immuntherapie von nicht-kleinzelligem Bronchialkarzinom (NSCLC) eingesetzt. In einer Untergruppe von Patienten mit lokoregionalem Erkrankungsstadium IIIB (d.h. lokal fortgeschritten und inoperabel) wurde die mittlere Überlebenszeit auch 23 Monate nach Rekrutierung des letzten Studienpatienten noch nicht erreicht.
Mittlere Überlebenszeit ist die Zeit, zu der die Hälfte der Patienten noch lebt, die andere Hälfte bereits gestorben ist. Wenn die mittlere Überlebenszeit also noch nicht erreicht wurde, bedeutet dies, dass noch mehr als die Hälfte der Patienten lebt.



In einer nun abgeschlossenen Phase-IIb-Studie wurde das Präparat zur Immuntherapie von nicht-kleinzelligem Bronchialkarzinom (NSCLC) eingesetzt. In einer Untergruppe von Patienten mit lokoregionalem Erkrankungsstadium IIIB (d.h. lokal fortgeschritten und inoperabel) wurde die mittlere Überlebenszeit auch 23 Monate nach Rekrutierung des letzten Studienpatienten noch nicht erreicht.
Mittlere Überlebenszeit ist die Zeit, zu der die Hälfte der Patienten noch lebt, die andere Hälfte bereits gestorben ist. Wenn die mittlere Überlebenszeit also noch nicht erreicht wurde, bedeutet dies, dass noch mehr als die Hälfte der Patienten lebt.



@donner
Ich habe es erst anders herum gelesen ... als dass ein Ziel noch nicht erreicht wurde ...
Aber so macht es natürlich mehr Sinn!
1000+
Ich habe es erst anders herum gelesen ... als dass ein Ziel noch nicht erreicht wurde ...
Aber so macht es natürlich mehr Sinn!
1000+
11:09 usa-time
$ 3.17 +1.64 (107.19%)
$ 3.17 +1.64 (107.19%)
@DausendUndMehr
Da warst du aber wohl nicht der einzige,die Amis werden jetzt auch erst wach!
Da warst du aber wohl nicht der einzige,die Amis werden jetzt auch erst wach!

Macht richtig spass zuzuschauen!!!!!!!!!!!
puhhhhhhhhhhhhhhhhhhhhhhhhhhhh, das war auch nötig
meine geduld war schon platt ( bei 0,75 ---schwitz )
nun die 3 NACH dem komma mit ziel 16 USD
gruß
biom---der seinen USER langsam wieder gut findet
meine geduld war schon platt ( bei 0,75 ---schwitz )
nun die 3 NACH dem komma mit ziel 16 USD
gruß
biom---der seinen USER langsam wieder gut findet

#916,
mal eine bescheidene Frage...
Wie kommst du auf dieses Kursziel?
V.
mal eine bescheidene Frage...
Wie kommst du auf dieses Kursziel?
V.

@BIOMIRA
Immer mit der Ruhe,solche plumpen Kursziele wie 16EUR einfach sein lassen,
wir sind hier nicht auf dem Weihnachtsmarkt!
Interessant wird jetzt sein wie die Ergebnisse BLP von der MedizinWelt aufgenommen werden,
man beachte über die hälfte der Versuchspersonen LEBEN IMMER NOCH!
Immer mit der Ruhe,solche plumpen Kursziele wie 16EUR einfach sein lassen,
wir sind hier nicht auf dem Weihnachtsmarkt!
Interessant wird jetzt sein wie die Ergebnisse BLP von der MedizinWelt aufgenommen werden,
man beachte über die hälfte der Versuchspersonen LEBEN IMMER NOCH!
rein technisch
CHART------------------------16-----------------

ziel 1--5 USD
ziel 2--10 USD
ziel 3-- 16 USD
mfg
BIOM ( der aber die 0,75€ seinerzeit gesehen hatte jdoch keinem es unter die nase halten wollte
ein -------W-------

CHART------------------------16-----------------
ziel 1--5 USD
ziel 2--10 USD
ziel 3-- 16 USD
mfg
BIOM ( der aber die 0,75€ seinerzeit gesehen hatte jdoch keinem es unter die nase halten wollte
ein -------W-------
rein technisch






11:56 usa-time
$ 3.37 +1.84 (120.26%)
$ 3.37 +1.84 (120.26%)
@donnerpower
diese aktie läuft in amerika und somit ist W: O völlig uninteressant
daher darf ich hier mal meine chartziele--so locker flockig reingeben.
wer wann kauft und verkauft, das ist jedem seine entscheidung
mfg
biom ( der hier nicht pushen will)
diese aktie läuft in amerika und somit ist W: O völlig uninteressant
daher darf ich hier mal meine chartziele--so locker flockig reingeben.
wer wann kauft und verkauft, das ist jedem seine entscheidung
mfg
biom ( der hier nicht pushen will)
Biomira Shares Skyrocket on Promising Data
Friday December 3, 12:00 pm ET
Biomira Shares Soar on Promising Lung Cancer Vaccine Data Reported by Development Partner
NEW YORK (AP) -- Shares of biotech company Biomira Inc. soared as it and a development partner, German drug maker Merck KGaA, reported Friday that the median survival in a study involving a lung cancer vaccine has yet to be reached after 23 months in a subset of patients.
Shares of Edmonton, Alberta-based Biomira rose $1.92, or 125 percent, to $3.45 in midday trading on the Nasdaq.
Median survival is defined as the point at which half of patients treated are still alive. The survival rate applied to a subset of 67 patients in the trial who had non-small cell lung cancer, or NSCLC, that had not spread past the lungs. Of this group, patients who had received the vaccine -- roughly half -- had yet to reach median survival after 23 months, the companies said.
The mid-stage clinical trial of the vaccine, called BLP25 Liposome Vaccine, or L-BLP-25, involved 171 men and women with NSCLC. The companies intend to work on a late-stage clinical trial next year.
Biomira said that L-BLP-25 incorporates cancer amino acids so the body`s immune system can better recognize and respond to cancer cells.
The companies said they expect to publicly present data on the clinical trial soon at an upcoming scientific meeting or in a peer-reviewed medical journal.



Friday December 3, 12:00 pm ET
Biomira Shares Soar on Promising Lung Cancer Vaccine Data Reported by Development Partner
NEW YORK (AP) -- Shares of biotech company Biomira Inc. soared as it and a development partner, German drug maker Merck KGaA, reported Friday that the median survival in a study involving a lung cancer vaccine has yet to be reached after 23 months in a subset of patients.
Shares of Edmonton, Alberta-based Biomira rose $1.92, or 125 percent, to $3.45 in midday trading on the Nasdaq.
Median survival is defined as the point at which half of patients treated are still alive. The survival rate applied to a subset of 67 patients in the trial who had non-small cell lung cancer, or NSCLC, that had not spread past the lungs. Of this group, patients who had received the vaccine -- roughly half -- had yet to reach median survival after 23 months, the companies said.
The mid-stage clinical trial of the vaccine, called BLP25 Liposome Vaccine, or L-BLP-25, involved 171 men and women with NSCLC. The companies intend to work on a late-stage clinical trial next year.
Biomira said that L-BLP-25 incorporates cancer amino acids so the body`s immune system can better recognize and respond to cancer cells.
The companies said they expect to publicly present data on the clinical trial soon at an upcoming scientific meeting or in a peer-reviewed medical journal.




@donner
hast DU nicht mal die 16 bis 20 HIER im thread begründet ?
begründet mit den umsätzen die erzielt werden ?
gruß
bio
hast DU nicht mal die 16 bis 20 HIER im thread begründet ?
begründet mit den umsätzen die erzielt werden ?
gruß
bio
@donnerpower
Ich wollte mich mal bei Dir für die ständigen Infos auf Deutsch Bedanken,Du scheinst ja von dieser Materie ne Ahnung zu haben.
Durch "Deine" Geschichte bin ich überhaupt auf diesen Wert aufmerksam geworden und es ist neben einem anderen Wert die einzige Langfristige Anlage in meinem Depot,ansonsten bin ich eher auf Ultrakurzfristigen Seite
Sollte da mal eine Neubewertung anstehen,was für einen Kurs siehst Du für Realistisch an,also weder Heute noch Morgen?
Und was machst Du mit Deinen Anteilen,Verkaufst Du einen Anteil jetzt schon?
Also ich nehme mal an das Du auf diese Investsumme nicht angewiesen bist,also die Zeit läuft für Dich,wie weiter mot der Posi?
Nochmals Danke und schönes WE!
Ich wollte mich mal bei Dir für die ständigen Infos auf Deutsch Bedanken,Du scheinst ja von dieser Materie ne Ahnung zu haben.
Durch "Deine" Geschichte bin ich überhaupt auf diesen Wert aufmerksam geworden und es ist neben einem anderen Wert die einzige Langfristige Anlage in meinem Depot,ansonsten bin ich eher auf Ultrakurzfristigen Seite

Sollte da mal eine Neubewertung anstehen,was für einen Kurs siehst Du für Realistisch an,also weder Heute noch Morgen?
Und was machst Du mit Deinen Anteilen,Verkaufst Du einen Anteil jetzt schon?
Also ich nehme mal an das Du auf diese Investsumme nicht angewiesen bist,also die Zeit läuft für Dich,wie weiter mot der Posi?
Nochmals Danke und schönes WE!
@Biomira
Wir stehen aber jetzt fundamental ganz anders da!
Das BLP25 wirksamer bei der Versuchsgruppe ist war das eine aber das im aktuellen Stadium über die Hälfte (für alle unerwartet) noch am Leben sind stellt hier ganz andere Richtlinien da!
Habe heute irgendwo gelesen das der Vize von Merck von einen zweiten Super Droge spricht.
Aber Vorsicht wir sprechen hier immer noch von einer kleinen Versuchsgruppe!!!
Noch ist aber BLP25 nicht zugelassen also weiterhin abwarten der lange Weg ist noch nicht zu Ende.
Wir stehen aber jetzt fundamental ganz anders da!
Das BLP25 wirksamer bei der Versuchsgruppe ist war das eine aber das im aktuellen Stadium über die Hälfte (für alle unerwartet) noch am Leben sind stellt hier ganz andere Richtlinien da!
Habe heute irgendwo gelesen das der Vize von Merck von einen zweiten Super Droge spricht.
Aber Vorsicht wir sprechen hier immer noch von einer kleinen Versuchsgruppe!!!
Noch ist aber BLP25 nicht zugelassen also weiterhin abwarten der lange Weg ist noch nicht zu Ende.
auch von mir ein FETTTES DANKESCHÖN an Donnerpower
deine infos sind erste sahne
-------nur mal ne anmerkung----ich handel zertifikate am DAX zu 100% nach chart
daher auch meine begründung rein technisch gesehen
im chart erkennt man die psychologie der anleger
angst,hoffnung,gier
aktuell auf intraday basis erkenne ich zocker aber auch einen fetten shortsquezze
meiner meinung nach wird es eine DREI TAGES PARTY ( drei weiße kerzen )
wie weit ??
das kann nur der markt entscheiden.
sollten montag anschlußkäufe folgen dann bekommt der rest der shortseller die fette prügel ( die ihnen verdient ist, denn in einem NEWS abhängigen wert ÜN short zu bleiben.... ohne worte )
bio
deine infos sind erste sahne
-------nur mal ne anmerkung----ich handel zertifikate am DAX zu 100% nach chart
daher auch meine begründung rein technisch gesehen
im chart erkennt man die psychologie der anleger
angst,hoffnung,gier
aktuell auf intraday basis erkenne ich zocker aber auch einen fetten shortsquezze
meiner meinung nach wird es eine DREI TAGES PARTY ( drei weiße kerzen )
wie weit ??
das kann nur der markt entscheiden.
sollten montag anschlußkäufe folgen dann bekommt der rest der shortseller die fette prügel ( die ihnen verdient ist, denn in einem NEWS abhängigen wert ÜN short zu bleiben.... ohne worte )
bio
ok @donner der weg ist noch lang ABER ! an der börse wird die zukunft gehandelt
die sieht ab heute viel besser aus als gestern
dementsprechend ist der anstieg zu begründen.
ab zulassung ist dann die 16 begründet
---dann kommt es auf die umsätze und gewinne an.-----
seh dir google und yahoo an
eine MK jenseits von gut und böse
dementsprechend ist auch die 16 zu begründen
bio
die sieht ab heute viel besser aus als gestern
dementsprechend ist der anstieg zu begründen.
ab zulassung ist dann die 16 begründet
---dann kommt es auf die umsätze und gewinne an.-----
seh dir google und yahoo an
eine MK jenseits von gut und böse
dementsprechend ist auch die 16 zu begründen
bio
@SirRobinHood
Habe immer gesagt das es mir bei Biomira nicht um ein paar schnelle %% geht,
alleine die Story das Blp25 eines Tages zugelassen werden könnte und ich hier
von Anfang an die Chance habe dabei zu sein stimmt mich wohl klar vom Verkauf
weiterhin ab!
Möchte aber darauf hinweisen das ich mein Depot in zwei Hälften damals gesplittert habe
70% in Merck
30% in Biomira
Beides ist bis her gut aufgegangen auch meine Merck Teilen die ich als Absicherung bezeichne
sind mit einem Einstiegskurs von 34EUR bis jetzt auch ganz gut gelaufen!
Man muss an der Börse nur Geduld mit bringen alleine meine beiden andren Werte Verisign und Nvidia
brachten auch dies mal wieder kürzlich ans Tageslicht!
Kurziele zu Biomira möchte erstmal noch nicht abgeben,aber das Szenario bei OSI Pharmaceuticals sollte man sich doch
mal nebenbei ansehen!
#866
gruss
Habe immer gesagt das es mir bei Biomira nicht um ein paar schnelle %% geht,
alleine die Story das Blp25 eines Tages zugelassen werden könnte und ich hier
von Anfang an die Chance habe dabei zu sein stimmt mich wohl klar vom Verkauf
weiterhin ab!
Möchte aber darauf hinweisen das ich mein Depot in zwei Hälften damals gesplittert habe
70% in Merck
30% in Biomira
Beides ist bis her gut aufgegangen auch meine Merck Teilen die ich als Absicherung bezeichne
sind mit einem Einstiegskurs von 34EUR bis jetzt auch ganz gut gelaufen!
Man muss an der Börse nur Geduld mit bringen alleine meine beiden andren Werte Verisign und Nvidia
brachten auch dies mal wieder kürzlich ans Tageslicht!
Kurziele zu Biomira möchte erstmal noch nicht abgeben,aber das Szenario bei OSI Pharmaceuticals sollte man sich doch
mal nebenbei ansehen!
#866
gruss
@Donner
Mich den Dankeschöns anschließen will, ohne Deine fundierten Posts, wäre ich sicherlich ausgestiegen!
Normal wäre nun ein Fläschchen Sprudelwasser fällig!
fällig!
Danke nochmal und mit dir immer wieder
LG Peter
Mich den Dankeschöns anschließen will, ohne Deine fundierten Posts, wäre ich sicherlich ausgestiegen!
Normal wäre nun ein Fläschchen Sprudelwasser
 fällig!
fällig!Danke nochmal und mit dir immer wieder
LG Peter
ab zulassung ist dann die 16 begründet
Du setzt hier immer Kursziele da fragt man sich ob wir hier uns
am Roulette Tisch uns gerade befinden!
Sollte Blp25 wirklich in den nächsten 2Jahren zugelassen werden ist solch ein Kursziel lächerlich ,man beachte bitte das alle Konkurrenten aktuell sich erst in der ersten I Phase befinden!
gruss
Du setzt hier immer Kursziele da fragt man sich ob wir hier uns
am Roulette Tisch uns gerade befinden!
Sollte Blp25 wirklich in den nächsten 2Jahren zugelassen werden ist solch ein Kursziel lächerlich ,man beachte bitte das alle Konkurrenten aktuell sich erst in der ersten I Phase befinden!
gruss
@donnerpower
war bisher nur mitleser und bin aufgrund einiger deiner
fundierten postings eingestiegen.
Danke dafür.
bin mir nur nicht sicher ob ich nun verkaufen oder
die gewinne laufen lassen soll?
Danke für Deine Antwort
Gruß
Bulle
war bisher nur mitleser und bin aufgrund einiger deiner
fundierten postings eingestiegen.
Danke dafür.
bin mir nur nicht sicher ob ich nun verkaufen oder
die gewinne laufen lassen soll?
Danke für Deine Antwort
Gruß
Bulle

@BULLE2004
Gewinne die mann hat kann auch keiner mehr wegnehmen,willst du alles richtig mach lässt du nur noch deine Gewinne laufen!
Ich weis jetzt nicht wie weit Biomira in den nächsten Tagen laufen wird es kommt wie gesagt darauf wie die
Ergebnisse in der MedizinBranche aufgenommen werden!
Eins ist klar bei Biomira wird es bald erstemal wieder etwas ruhiger werden wo sich der Kurs dann einpendeln wird kann jetzt keiner voraussehen!
gruss
Gewinne die mann hat kann auch keiner mehr wegnehmen,willst du alles richtig mach lässt du nur noch deine Gewinne laufen!
Ich weis jetzt nicht wie weit Biomira in den nächsten Tagen laufen wird es kommt wie gesagt darauf wie die
Ergebnisse in der MedizinBranche aufgenommen werden!
Eins ist klar bei Biomira wird es bald erstemal wieder etwas ruhiger werden wo sich der Kurs dann einpendeln wird kann jetzt keiner voraussehen!
gruss
@DONNER---die gingen auch mit einem GAP los und blieben dann oben.
zur 16 SORRY
ist einfach nur ein technischer widerstand den die trader anlauf wollen.
danach ist dann die 20 dran
die--TRADER--- richten sich auch nur nach dem WAS SIE SEHEN !
mfg
bio ( der sich für die 16 entschuldigt, wenn dann mal ne 20 oder 30 steht )

Lohnt es sich jetzt noch einzusteigen bei biomira
Glückwunsch an alle derzeit investierten Aktionäre. Ich habe leider die Geduld verloren und irgend wann die Reissleine gezogen. 
Gruss Agio, der euch den Erfolg gönnt

Gruss Agio, der euch den Erfolg gönnt

VOL.:75 MILL.


Danke Donnerpower!!!



Danke Donnerpower!!!
Dass BIOM so wenig auf Raging Bull diskutiert wird? 
6395 Just my opinion, but you couldn`t get me to sell a gang 03 Dec 2004 3:09 PM EST
6394 IOLD YA ITS A TRADE,NOW SELL IT,REBUY AROUND 220 A rd1064 03 Dec 2004
12:08 PM EST
6393 This one to the moon! dauphinater 03 Dec 2004 12:00 PM EST
6392 I LIKE GOOD NEWS cmc165 03 Dec 2004
10:45 AM EST
Get the trading tool that savvy investors use - Qcharts.com. 6391 Looking for help dave29lysander 01 Dec 2004 7:26 PM EST
6389 much more active board for biom at yahoo-- ibcnu 30 Nov 2004
3:59 PM EST
6388 basically i`m a shareholder because i`m a consume malko14 13 Nov 2004 7:36 AM EST
6387 12:06 PM EST rd1064 12 Nov 2004 12:08 PM EST
ist VIEL weniger als hier auf WO

6395 Just my opinion, but you couldn`t get me to sell a gang 03 Dec 2004 3:09 PM EST
6394 IOLD YA ITS A TRADE,NOW SELL IT,REBUY AROUND 220 A rd1064 03 Dec 2004
12:08 PM EST
6393 This one to the moon! dauphinater 03 Dec 2004 12:00 PM EST
6392 I LIKE GOOD NEWS cmc165 03 Dec 2004
10:45 AM EST
Get the trading tool that savvy investors use - Qcharts.com. 6391 Looking for help dave29lysander 01 Dec 2004 7:26 PM EST
6389 much more active board for biom at yahoo-- ibcnu 30 Nov 2004
3:59 PM EST
6388 basically i`m a shareholder because i`m a consume malko14 13 Nov 2004 7:36 AM EST
6387 12:06 PM EST rd1064 12 Nov 2004 12:08 PM EST
ist VIEL weniger als hier auf WO

#938
Dann geh mal ins yahoo-board!
Dann geh mal ins yahoo-board!

@Blue2000
Die Amis würden dir geschmacklos sagen: vergleichen sie bitte diese beiden Komponenten KURS-LEBEN !
Sollte Blp25 zugelassen werden, sind Kurse in mehren Jahren unter 10Dollar als Träumerei zu_bezeichnen!
Wie gesagt noch liegt ein langer Weg vor uns, der aber mit andauernden Überlebendsquote der Studienpatienten immer kürzer
wird !
Ich hoffe jetzt sehen einige mehr als nur ich was hier überhaupt vom Konzern Merck und Biomira fundamental wiedergeben wurde!
In einer nun abgeschlossenen Phase-IIb-Studie wurde das Präparat zur Immuntherapie von nicht-kleinzelligem Bronchialkarzinom (NSCLC) eingesetzt. In einer Untergruppe von Patienten mit lokoregionalem Erkrankungsstadium IIIB (d.h. lokal fortgeschritten und inoperabel) wurde die mittlere Überlebenszeit auch 23 Monate nach Rekrutierung des letzten Studienpatienten noch nicht erreicht.
Mittlere Überlebenszeit ist die Zeit, zu der die Hälfte der Patienten noch lebt, die andere Hälfte bereits gestorben ist. Wenn die mittlere Überlebenszeit also noch nicht erreicht wurde, bedeutet dies, dass noch mehr als die Hälfte der Patienten lebt.
Nicht vergessen es wird noch was folgen!!!
The companies said they expect to publicly present data on the clinical trial soon at an upcoming scientific meeting or in a peer-reviewed medical journal
Die Amis würden dir geschmacklos sagen: vergleichen sie bitte diese beiden Komponenten KURS-LEBEN !
Sollte Blp25 zugelassen werden, sind Kurse in mehren Jahren unter 10Dollar als Träumerei zu_bezeichnen!
Wie gesagt noch liegt ein langer Weg vor uns, der aber mit andauernden Überlebendsquote der Studienpatienten immer kürzer
wird !
Ich hoffe jetzt sehen einige mehr als nur ich was hier überhaupt vom Konzern Merck und Biomira fundamental wiedergeben wurde!
In einer nun abgeschlossenen Phase-IIb-Studie wurde das Präparat zur Immuntherapie von nicht-kleinzelligem Bronchialkarzinom (NSCLC) eingesetzt. In einer Untergruppe von Patienten mit lokoregionalem Erkrankungsstadium IIIB (d.h. lokal fortgeschritten und inoperabel) wurde die mittlere Überlebenszeit auch 23 Monate nach Rekrutierung des letzten Studienpatienten noch nicht erreicht.
Mittlere Überlebenszeit ist die Zeit, zu der die Hälfte der Patienten noch lebt, die andere Hälfte bereits gestorben ist. Wenn die mittlere Überlebenszeit also noch nicht erreicht wurde, bedeutet dies, dass noch mehr als die Hälfte der Patienten lebt.
Nicht vergessen es wird noch was folgen!!!
The companies said they expect to publicly present data on the clinical trial soon at an upcoming scientific meeting or in a peer-reviewed medical journal
@DausendUndMehr
Nur wer kauft dann jetzt?

Nur wer kauft dann jetzt?

@all
..und das Beste kommt erst noch:
Das ganze Wochenende über werden Berichte über Biomira in den Staaten durch die Medien geistern und sicherlich auf reges Interesse treffen.
Jedes halbwegs zeitnah berichtende Blatt wird zumindest am Rande über die heutigen News zu berichten wissen.
Eine noch bessere PR-Aktion hätte man sich nicht wünschen können.
..und das Beste kommt erst noch:
Das ganze Wochenende über werden Berichte über Biomira in den Staaten durch die Medien geistern und sicherlich auf reges Interesse treffen.
Jedes halbwegs zeitnah berichtende Blatt wird zumindest am Rande über die heutigen News zu berichten wissen.
Eine noch bessere PR-Aktion hätte man sich nicht wünschen können.

Man sollte nicht vergessen,News am Freitag werden normal als Badnews eingestuft,in USA!!!

#943
na, der Kurs sagt aber das Gegenteil ...
na, der Kurs sagt aber das Gegenteil ...

Wer da short ist...





technisch 1a gelaufen
seht euch die indikatoren an.
HUT AB
biom-------------der nicht eine aktie verkauft------
Schlusskurs für heute:
Last Trade: 3.31 4:03PM ET
Last Trade: 3.31 4:03PM ET
nasdaq
psychologisch im klaren aufwärtstrend
dementsprechend sucht die börse PERLEN die POTENTIAL haben.
ich denke BIOM ist aus dem schlaf erwacht und wird noch freude bereiten
SCHÖNES WE---@ALL
biom
hab noch was vergessen
-thema aufmerksamkeit-
http://bigcharts.marketwatch.com/markets/screener.asp?exchan…
platz1 bei den nasdaq gewinnern und das am WE, wo @ALL sich in ruhe die geschichte durchlesen kann.
nun aber schluß
biom---PROST-- ein JEVER HERB Zischhhhhhhhhhhh
Zischhhhhhhhhhhh
-thema aufmerksamkeit-
http://bigcharts.marketwatch.com/markets/screener.asp?exchan…
platz1 bei den nasdaq gewinnern und das am WE, wo @ALL sich in ruhe die geschichte durchlesen kann.
nun aber schluß
biom---PROST-- ein JEVER HERB
 Zischhhhhhhhhhhh
Zischhhhhhhhhhhh
eine Schneider Weisse hier in Bayern


Ein Radeberger oder Zwei. hier in Sachsen 
Schönes Wochenende an @ Peter

Schönes Wochenende an @ Peter
Ein Berliner Kindl hier in Berlin!
MFG
MFG
Symbol: BIOM
Last Trade: 3.38
After Hours Change: 0.10 (3.05%)
Today`s Change: 1.85 (120.92%)
Bid: 3.35
Ask: 3.40
Last Trade: 3.38
After Hours Change: 0.10 (3.05%)
Today`s Change: 1.85 (120.92%)
Bid: 3.35
Ask: 3.40

Ich bin auch von Anfang an dabei und habe die Hoffnung nie aufgegeben.
Tausend Dank and Donnerpower und alle anderen!
Tausend Dank and Donnerpower und alle anderen!
@all und donnerpower
mußte leider freitag mittag verreisen und habe erst jetzt wieder einen PC gefunden.
Herzlichen Glückwunsch allen Langinvestierten und vielen Dank an Donnerpower auch von mir für die damalige Empfehlung.
Ich denke, wir werden in der nächsten Zeit noch viel Freude mit BIOM haben. Was man auch nicht vergessen sollte, sind die betroffenen Patienten, die jetzt vieleicht ein Licht am Ende des Tunnels sehen können.
Also dann, ein HOLSTEN aus Niedersachsen und auf eine erfolgreiche neue Woche.
freetibet
mußte leider freitag mittag verreisen und habe erst jetzt wieder einen PC gefunden.
Herzlichen Glückwunsch allen Langinvestierten und vielen Dank an Donnerpower auch von mir für die damalige Empfehlung.
Ich denke, wir werden in der nächsten Zeit noch viel Freude mit BIOM haben. Was man auch nicht vergessen sollte, sind die betroffenen Patienten, die jetzt vieleicht ein Licht am Ende des Tunnels sehen können.
Also dann, ein HOLSTEN aus Niedersachsen und auf eine erfolgreiche neue Woche.
freetibet
Damal gab es ein run weil man die Patentreihe in die erste 1Phase schicke!
Jetzt sind die ersten Ergebnisse da und mal sehn was in dieser Periode drin sein wird!
PS.Biomira ist jetzt in aller Munde
Bsp.:
http://www.forbes.com/video/?video_url=http://www.forbes.com…
Ich kann im Augenblick nicht sagen was Montag für ein Kurs es geben wird,möglich ist jetzt alles auch eine GAP Eröffnung über 4Dollar könnte man in der ersten Handelsminute zu Gesicht bekommen!!!

Jetzt sind die ersten Ergebnisse da und mal sehn was in dieser Periode drin sein wird!
PS.Biomira ist jetzt in aller Munde
Bsp.:
http://www.forbes.com/video/?video_url=http://www.forbes.com…
Ich kann im Augenblick nicht sagen was Montag für ein Kurs es geben wird,möglich ist jetzt alles auch eine GAP Eröffnung über 4Dollar könnte man in der ersten Handelsminute zu Gesicht bekommen!!!
Hi,
Schaut mal ins Yahoo Board, Wahnsinn was da abgeht!
Gruss
Azeri
Schaut mal ins Yahoo Board, Wahnsinn was da abgeht!
Gruss
Azeri
Kannst Du mal einen Link reinstellen, Danke
@Azeri, thanks
joo, da geht es ja wirklich rund!
joo, da geht es ja wirklich rund!

Aus dem Yahoo Board.
SONAE buy BIOM, monday to 5-6$
Lisbon - Dec 3 - Sonae SGPS inform the Portuguese National Securities Market Commission (CNMV) that had obtained 18 millions of shares of Biomira Inc at a average price of 3,40 USD.
Sonae SGPSwill notifie mondey the Portuguese National Securities Market Commission (CNMV) that it was willing to waive the condition of a 75% minimum acceptance level to which its public offer for the acquisition of Biomira Inc shares was subject, taking into consideration that the response received will be sufficient to develop the business project pursued through the takeover bid.
Sonae SGPS will launch a takeover bid for Biomira Inc with the payment of 5,0 euros for each of the that responded to the tender offer, this initial offer could reach the limit of price of 6.15 euros for each share of the american company.
The CEO of Sonae SGPS said " Sonae SGPS have plans to create a subsidiarie in the sector of biotechnology , the choose of Biomira Inc is perfect".
Abaut Sonae SGPS
SONAE was founded in 1959, in Maia, Portugal in the wood products business and more specifically the production of high-pressure decorative laminates.
During its first twenty years of existence, SONAE developed as a small to medium size business, focused on the area of wood derivatives. During the 80s, the company began a period of rapid growth, which coincided with Portugals entry in to the European Union. During this period, SONAE began a process of diversification through the acquisition of a supermarket chain, followed by the launch of the first hyper-market in Portugal.
The creation of SONAE Real Estate, represented a natural progression, its main objective being the construction of shopping centres next to SONAE stores. SONAE Real Estate was responsible for CascaiShopping - the first regional shopping centre ever built in Portugal.
At the same time, SONAE invested in many different areas such as communication, information technology, leisure and tourism.
In 1996, the new challenge of international expansion of its different businesses and the need to concentrate management resources in their development, were foreseen. It was thus decided that all businesses of Sonae Industria (already present in Spain, the United Kingdom, Canada, Brazil and South Africa), and those of Pargeste (made up of non strategic activities) should be separated from SONAE Investimentos SGPS, SA.
As a result, SONAE Investimentos, SGPS, SA became a holding company totally dedicated to modern retail business, and a new holding, Inparsa, was formed grouping together all wood derivatives businesses (SONAE Industria) and all other non strategic activities.
In September 1999, and as a result of the absorption of Inparsa and Figeste into Sonae SGPS SA (formerly known as Sonae Investimentos SPGS SA), Sonae benefited from the systematic use of its name across the group as well as gaining critical mass in European terms. Its portfolio of businesses now ranges from retail and real estate activities through to wood products, tourism, fixed and mobile telecommunications, construction, transport, the media and risk capital.
The role of Sonae SGPS SA is to manage the portfolio while it is the job of the its sub-holdings to manage the businesses.

SONAE buy BIOM, monday to 5-6$
Lisbon - Dec 3 - Sonae SGPS inform the Portuguese National Securities Market Commission (CNMV) that had obtained 18 millions of shares of Biomira Inc at a average price of 3,40 USD.
Sonae SGPSwill notifie mondey the Portuguese National Securities Market Commission (CNMV) that it was willing to waive the condition of a 75% minimum acceptance level to which its public offer for the acquisition of Biomira Inc shares was subject, taking into consideration that the response received will be sufficient to develop the business project pursued through the takeover bid.
Sonae SGPS will launch a takeover bid for Biomira Inc with the payment of 5,0 euros for each of the that responded to the tender offer, this initial offer could reach the limit of price of 6.15 euros for each share of the american company.
The CEO of Sonae SGPS said " Sonae SGPS have plans to create a subsidiarie in the sector of biotechnology , the choose of Biomira Inc is perfect".
Abaut Sonae SGPS
SONAE was founded in 1959, in Maia, Portugal in the wood products business and more specifically the production of high-pressure decorative laminates.
During its first twenty years of existence, SONAE developed as a small to medium size business, focused on the area of wood derivatives. During the 80s, the company began a period of rapid growth, which coincided with Portugals entry in to the European Union. During this period, SONAE began a process of diversification through the acquisition of a supermarket chain, followed by the launch of the first hyper-market in Portugal.
The creation of SONAE Real Estate, represented a natural progression, its main objective being the construction of shopping centres next to SONAE stores. SONAE Real Estate was responsible for CascaiShopping - the first regional shopping centre ever built in Portugal.
At the same time, SONAE invested in many different areas such as communication, information technology, leisure and tourism.
In 1996, the new challenge of international expansion of its different businesses and the need to concentrate management resources in their development, were foreseen. It was thus decided that all businesses of Sonae Industria (already present in Spain, the United Kingdom, Canada, Brazil and South Africa), and those of Pargeste (made up of non strategic activities) should be separated from SONAE Investimentos SGPS, SA.
As a result, SONAE Investimentos, SGPS, SA became a holding company totally dedicated to modern retail business, and a new holding, Inparsa, was formed grouping together all wood derivatives businesses (SONAE Industria) and all other non strategic activities.
In September 1999, and as a result of the absorption of Inparsa and Figeste into Sonae SGPS SA (formerly known as Sonae Investimentos SPGS SA), Sonae benefited from the systematic use of its name across the group as well as gaining critical mass in European terms. Its portfolio of businesses now ranges from retail and real estate activities through to wood products, tourism, fixed and mobile telecommunications, construction, transport, the media and risk capital.
The role of Sonae SGPS SA is to manage the portfolio while it is the job of the its sub-holdings to manage the businesses.



@all
unter nachfolgender Adresse ist die Meldung mit der Äußerung bezüglich Übernahme von BIOM zu finden:
http.//pt.portaldebolsa.com/pt/forums/view_post_asp?cod_forum=1083&cod_post=36456
unter nachfolgender Adresse ist die Meldung mit der Äußerung bezüglich Übernahme von BIOM zu finden:
http.//pt.portaldebolsa.com/pt/forums/view_post_asp?cod_forum=1083&cod_post=36456
Korrektur -
http.//pt.portaldebolsa.com/pt/forums/view_post.asp?cod_forum=1083&cod_post=36456
...geht so besser
http.//pt.portaldebolsa.com/pt/forums/view_post.asp?cod_forum=1083&cod_post=36456
...geht so besser

@bio
yep, ist genau der Artikel aus dem Yahoo Board
Lisbon - Dec 3 - Sonae SGPS inform the Portuguese National Securities Market Commission (CNMV) that had obtained 18 millions of shares of Biomira Inc at a average price of 3,40 USD.
Sonae SGPSwill notifie mondey the Portuguese National Securities Market Commission (CNMV) that it was willing to waive the condition of a 75% minimum acceptance level to which its public offer for the acquisition of Biomira Inc shares was subject, taking into consideration that the response received will be sufficient to develop the business project pursued through the takeover bid.
Sonae SGPS will launch a takeover bid for Biomira Inc with the payment of 5,0 euros for each of the that responded to the tender offer, this initial offer could reach the limit of price of 6.15 euros for each share of the american company.
The CEO of Sonae SGPS said " Sonae SGPS have plans to create a subsidiarie in the sector of biotechnology , the choose of Biomira Inc is perfect".
Abaut Sonae SGPS
SONAE was founded in 1959, in Maia, Portugal in the wood products business and more specifically the production of high-pressure decorative laminates.
During its first twenty years of existence, SONAE developed as a small to medium size business, focused on the area of wood derivatives. During the 80s, the company began a period of rapid growth, which coincided with Portugals entry in to the European Union. During this period, SONAE began a process of diversification through the acquisition of a supermarket chain, followed by the launch of the first hyper-market in Portugal.
The creation of SONAE Real Estate, represented a natural progression, its main objective being the construction of shopping centres next to SONAE stores. SONAE Real Estate was responsible for CascaiShopping - the first regional shopping centre ever built in Portugal.
At the same time, SONAE invested in many different areas such as communication, information technology, leisure and tourism.
In 1996, the new challenge of international expansion of its different businesses and the need to concentrate management resources in their development, were foreseen. It was thus decided that all businesses of Sonae Industria (already present in Spain, the United Kingdom, Canada, Brazil and South Africa), and those of Pargeste (made up of non strategic activities) should be separated from SONAE Investimentos SGPS, SA.
As a result, SONAE Investimentos, SGPS, SA became a holding company totally dedicated to modern retail business, and a new holding, Inparsa, was formed grouping together all wood derivatives businesses (SONAE Industria) and all other non strategic activities.
In September 1999, and as a result of the absorption of Inparsa and Figeste into Sonae SGPS SA (formerly known as Sonae Investimentos SPGS SA), Sonae benefited from the systematic use of its name across the group as well as gaining critical mass in European terms. Its portfolio of businesses now ranges from retail and real estate activities through to wood products, tourism, fixed and mobile telecommunications, construction, transport, the media and risk capital.
The role of Sonae SGPS SA is to manage the portfolio while it is the job of the its sub-holdings to manage the businesses.
yep, ist genau der Artikel aus dem Yahoo Board

Lisbon - Dec 3 - Sonae SGPS inform the Portuguese National Securities Market Commission (CNMV) that had obtained 18 millions of shares of Biomira Inc at a average price of 3,40 USD.
Sonae SGPSwill notifie mondey the Portuguese National Securities Market Commission (CNMV) that it was willing to waive the condition of a 75% minimum acceptance level to which its public offer for the acquisition of Biomira Inc shares was subject, taking into consideration that the response received will be sufficient to develop the business project pursued through the takeover bid.
Sonae SGPS will launch a takeover bid for Biomira Inc with the payment of 5,0 euros for each of the that responded to the tender offer, this initial offer could reach the limit of price of 6.15 euros for each share of the american company.
The CEO of Sonae SGPS said " Sonae SGPS have plans to create a subsidiarie in the sector of biotechnology , the choose of Biomira Inc is perfect".
Abaut Sonae SGPS
SONAE was founded in 1959, in Maia, Portugal in the wood products business and more specifically the production of high-pressure decorative laminates.
During its first twenty years of existence, SONAE developed as a small to medium size business, focused on the area of wood derivatives. During the 80s, the company began a period of rapid growth, which coincided with Portugals entry in to the European Union. During this period, SONAE began a process of diversification through the acquisition of a supermarket chain, followed by the launch of the first hyper-market in Portugal.
The creation of SONAE Real Estate, represented a natural progression, its main objective being the construction of shopping centres next to SONAE stores. SONAE Real Estate was responsible for CascaiShopping - the first regional shopping centre ever built in Portugal.
At the same time, SONAE invested in many different areas such as communication, information technology, leisure and tourism.
In 1996, the new challenge of international expansion of its different businesses and the need to concentrate management resources in their development, were foreseen. It was thus decided that all businesses of Sonae Industria (already present in Spain, the United Kingdom, Canada, Brazil and South Africa), and those of Pargeste (made up of non strategic activities) should be separated from SONAE Investimentos SGPS, SA.
As a result, SONAE Investimentos, SGPS, SA became a holding company totally dedicated to modern retail business, and a new holding, Inparsa, was formed grouping together all wood derivatives businesses (SONAE Industria) and all other non strategic activities.
In September 1999, and as a result of the absorption of Inparsa and Figeste into Sonae SGPS SA (formerly known as Sonae Investimentos SPGS SA), Sonae benefited from the systematic use of its name across the group as well as gaining critical mass in European terms. Its portfolio of businesses now ranges from retail and real estate activities through to wood products, tourism, fixed and mobile telecommunications, construction, transport, the media and risk capital.
The role of Sonae SGPS SA is to manage the portfolio while it is the job of the its sub-holdings to manage the businesses.
@DAUSENDUNDMEHR
sorry, zeitliche Überschneidung...
Gruß, Bio
sorry, zeitliche Überschneidung...
Gruß, Bio
wir stehen auf Platz 12 der Top Stocks der letzten 24 Stunden
12. BIOMIRA INC 12
12. BIOMIRA INC 12
@DAUSENDUNDMEHR
...wart mal wo wir in den nächsten 48 Stunden stehen...
...wart mal wo wir in den nächsten 48 Stunden stehen...

Und schon sind wir auf Platz 6:
5. BIOPHAN TECHNOLOGIES... 20
6. BIOMIRA INC 18
5. BIOPHAN TECHNOLOGIES... 20
6. BIOMIRA INC 18
Weil es so schön ist, nochmals Schwarz auf Weiss:
Börse Symbol Währ. Vortag akt.Kurs Diff. % Handelsvol. gehand. St. Kurszeit
Nasdaq BIOM USD 1,53 3,28 + 1,75 + 114,31 % 145,05 Mio. 51.589.243 03. Dez 22:01
Frankfurt BM2 EUR 1,16 2,60 + 1,44 + 124,14 % 129.686 68.861 03. Dez 19:31
München BM2 EUR 1,17 2,59 + 1,42 + 121,37 % 92.171 39.369 03. Dez 19:52
Stuttgart BM2 EUR 1,12 2,53 + 1,41 + 125,89 % 12.418 5.749 03. Dez 18:12
Berlin BM2 EUR 1,16 2,20 + 1,04 + 89,66 % 0 0 03. Dez 14:16
Börse Symbol Währ. Vortag akt.Kurs Diff. % Handelsvol. gehand. St. Kurszeit
Nasdaq BIOM USD 1,53 3,28 + 1,75 + 114,31 % 145,05 Mio. 51.589.243 03. Dez 22:01
Frankfurt BM2 EUR 1,16 2,60 + 1,44 + 124,14 % 129.686 68.861 03. Dez 19:31
München BM2 EUR 1,17 2,59 + 1,42 + 121,37 % 92.171 39.369 03. Dez 19:52
Stuttgart BM2 EUR 1,12 2,53 + 1,41 + 125,89 % 12.418 5.749 03. Dez 18:12
Berlin BM2 EUR 1,16 2,20 + 1,04 + 89,66 % 0 0 03. Dez 14:16
Dieses Biomira Buy-out Geruecht durch die Portugiesische Firma Sonae scheint ein Fake zu sein, und wird augenblicklich heiss im Yahoo Board diskutiert.
Ich habe mir selber die angebliche Originalveroeffentlichung auf der Web-page angesehen, und sie sieht sehr merkwuerdig aus, da alles auf dieser Seite auf Portugiesisch ist und nur diese Veroeffentlichung in Englisch.
Hier der link http://pt.portaldebolsa.com/pt/index_entry.asp
Siehe rechts unten.
Gruss
Azeri
Ich habe mir selber die angebliche Originalveroeffentlichung auf der Web-page angesehen, und sie sieht sehr merkwuerdig aus, da alles auf dieser Seite auf Portugiesisch ist und nur diese Veroeffentlichung in Englisch.
Hier der link http://pt.portaldebolsa.com/pt/index_entry.asp
Siehe rechts unten.
Gruss
Azeri
5-6EUR für eine Übernahme
 :laugh
:laugh a lacht sich Biomira,bei Zulassung,drüber tot!
a lacht sich Biomira,bei Zulassung,drüber tot!

 :laugh
:laugh a lacht sich Biomira,bei Zulassung,drüber tot!
a lacht sich Biomira,bei Zulassung,drüber tot!
Steht aber auf der ersten Seite des Portals, hmmm
O que eles dizem
Sonae SPGS will Launch a takeover to buy Biomira Inc
Vielleicht heisst die Überschrift "Gerücht des Tages"
O que eles dizem
Sonae SPGS will Launch a takeover to buy Biomira Inc
Vielleicht heisst die Überschrift "Gerücht des Tages"

Aus dem Yahoo Board:
Check this out!!! Bid/Ask on BIOM
by: speakerjax 12/05/04 07:44 am
Msg: 163615 of 163615
If you have a Wachovia online brokerage account---check out the bid/ask on BIOM
$10.00/$7.00
Going to be an interesting Monday.
Langsam werd` ich auch nervoes....
Check this out!!! Bid/Ask on BIOM
by: speakerjax 12/05/04 07:44 am
Msg: 163615 of 163615
If you have a Wachovia online brokerage account---check out the bid/ask on BIOM
$10.00/$7.00
Going to be an interesting Monday.
Langsam werd` ich auch nervoes....
Na spannend wird es so oder so ... 
"If you have a Wachovia online brokerage account---check out the bid/ask on BIOM
$10.00/$7.00
Going to be an interesting Monday. "

"If you have a Wachovia online brokerage account---check out the bid/ask on BIOM
$10.00/$7.00
Going to be an interesting Monday. "
Sorry für das Doppel-posting ...
...ja,ja, wenn ich da short wäre würde ich mir auch so einiges einfallen lassen um noch günstig an ein paar shares zu kommen...
Wie würden die Shorties wohl argumentieren wenn der Artikel in portugiesisch abgefasst wäre?
Wie auch immer, der entscheidende Punkt liegt an ganz anderer Stelle.
Wenn BIOM tatsächlich das hat, wonach es im Moment aussieht, kann selbst bei einem mal frei an der Meldung angepassten Kurs von 6 Euronen noch von einem Schnäppchen gesprochen werden. Die Marktkapitalisierung läge erst bei ca. 450 Mio. Euronen, was in Anbetracht des medizinischen Fortschrittes wohl als lächerlich bezeichnet werden muß.
Die Big-Guns werden da noch ganz andere Preise bieten, da bin ich mir ziemlich sicher.
Grüße, Bio
Wie würden die Shorties wohl argumentieren wenn der Artikel in portugiesisch abgefasst wäre?
Wie auch immer, der entscheidende Punkt liegt an ganz anderer Stelle.
Wenn BIOM tatsächlich das hat, wonach es im Moment aussieht, kann selbst bei einem mal frei an der Meldung angepassten Kurs von 6 Euronen noch von einem Schnäppchen gesprochen werden. Die Marktkapitalisierung läge erst bei ca. 450 Mio. Euronen, was in Anbetracht des medizinischen Fortschrittes wohl als lächerlich bezeichnet werden muß.
Die Big-Guns werden da noch ganz andere Preise bieten, da bin ich mir ziemlich sicher.

Grüße, Bio
Ja, sieht nach Fake aus 

@All
"ja,ja, wenn ich da short wäre würde ich mir auch so einiges einfallen lassen um noch günstig an ein paar shares zu kommen..."
Denke DAS ist der RICHTIGE Satz
Schönen 2. Advent noch Peter
"ja,ja, wenn ich da short wäre würde ich mir auch so einiges einfallen lassen um noch günstig an ein paar shares zu kommen..."
Denke DAS ist der RICHTIGE Satz

Schönen 2. Advent noch Peter
Vergleichen kann man Biom wohl am ehesten mit OSIP,schaut da mal auf den Kursverlauf an





Dear Peter,
Ich weiss zwar nicht was Du meinst, aber der Biomira Buy-out ist definitiv eine Ente.
Dir auch noch einen schoenen 2. Advent.
Ich weiss zwar nicht was Du meinst, aber der Biomira Buy-out ist definitiv eine Ente.
Dir auch noch einen schoenen 2. Advent.
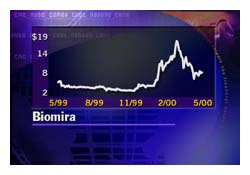
@ll
ACHTUNG !
Dienstag ist eine Präsentation anvisiert worden !!!
Der Hammer wer jetzt das der neue Vertriebspartner für Theratope der seit einiger Zeit gesucht wird veröffentlicht wird!Man beachte das Theratope immer noch in verschiedenen Versuchsreihen erprobt wird !
Dezember 7, 2004, 09:30 AM
ACHTUNG !
Dienstag ist eine Präsentation anvisiert worden !!!
Der Hammer wer jetzt das der neue Vertriebspartner für Theratope der seit einiger Zeit gesucht wird veröffentlicht wird!Man beachte das Theratope immer noch in verschiedenen Versuchsreihen erprobt wird !
Dezember 7, 2004, 09:30 AM
Ich gebe kein Stück aus der Hand!.


Kurzes Update aus dem Yahoo Board:
Hier gab es seit dem Freitag close mehr als 1000 posts!!!
Das scheint sowas wie ein Rekord zu sein.
Hier gab es seit dem Freitag close mehr als 1000 posts!!!

Das scheint sowas wie ein Rekord zu sein.
HIER NOCH_MAL FÜR ALLE
Überlebenszeit um 4,4 Monate waren schon eine Sensation!
BITTE BEACHTEN DIE FOLGENEN INHALTE STAMMEN VOM 1.NOWEMBER!!!
HEUTE WEITERE 4.WOCHEN SPÄTER BLP25 HÄLT WEITER AN!!!
Vom 29. Kongresses der European Society for Medical Oncology (ESMO) in Wien, Österreich:
Das Medikament L-BLP25 wurde an Patienten mit der am meisten verbreiteten
Form von Lungenkrebs getestet, dem so genannten Non-Small-Cell
Lungenkrebs. Insgesamt überlebten Patienten mit dem neuen Schutzstoff
durchschnittlich 17,4 Monate, im Vergleich zu einem Durchschnitt von 13
Monaten für jene, die die Standardversorgung erhielten. Bei den
Patienten, deren Krebs zu fortgeschritten für einen chirurgischen
Eingriff war, sich aber noch nicht zu anderen Organen ausgebreitet hatte,
war der Effekt noch deutlicher ausgeprägt. Patienten mit
Standard-Behandlung überlebten durchschnittlich 13,3 Monate, aber bei
jenen, die das neue Medikament bekamen, waren nach zwei Jahren noch 60
Prozent am Leben.
" Die Steigerung der Überlebenszeit um 4,4 Monate bei Patienten, die mit L-BLP25 behandelt wurden, ist ein bemerkenswerter Zeitraum, bedenkt man den aggressiven Krankheitsverlauf bei nicht-kleinzelligem Lungenkrebs," sagte Dr. Charles Butts, Onkologe am Cross Cancer Institute in Edmonton, Alberta (Kanada), in seiner Funktion als leitender Prüfarzt dieser Studie. „Die Daten bescheinigen dem Vakzin ein günstiges Sicherheitsprofil und einen positiven Einfluss auf den Erhalt der Lebensqualität und bestärken uns in unseren Plänen, es in weiteren Studien zu untersuchen. Die Ergebnisse, die wir bei Patienten in früheren Krankheitsstadien erzielen, sind sogar noch beeindruckender.“


Folgenachrichten vorprogrammiert !!!
„Diese Phase II-Daten sind im Hinblick auf den potenziellen Nutzen für die Patienten so ermutigend, weil sie auf einem Felde stattfinden, wo trotz so vieler Jahre Arbeit so geringe Fortschritte erzielt wurden“, sagte Dr. Bernhard Ehmer, Leiter des Geschäftsbereichs Onkologie. [/b]
SO AM FREITAG FOLGTE NUN DIESE NACHRICHT:
In einer nun abgeschlossenen Phase-IIb-Studie wurde das Präparat zur Immuntherapie von nicht-kleinzelligem Bronchialkarzinom (NSCLC) eingesetzt. In einer Untergruppe von Patienten mit lokoregionalem Erkrankungsstadium IIIB (d.h. lokal fortgeschritten und inoperabel) wurde die mittlere Überlebenszeit auch 23 Monate nach Rekrutierung des letzten Studienpatienten noch nicht erreicht.
Mittlere Überlebenszeit ist die Zeit, zu der die Hälfte der Patienten noch lebt, die andere Hälfte bereits gestorben ist. Wenn die mittlere Überlebenszeit also noch nicht erreicht wurde, bedeutet dies, dass noch mehr als die Hälfte der Patienten lebt.
Man kann hier klar von einer Weltsensation in der Medizinischen Geschichte sprechen!
Überlebenszeit um 4,4 Monate waren schon eine Sensation!
BITTE BEACHTEN DIE FOLGENEN INHALTE STAMMEN VOM 1.NOWEMBER!!!
HEUTE WEITERE 4.WOCHEN SPÄTER BLP25 HÄLT WEITER AN!!!
Vom 29. Kongresses der European Society for Medical Oncology (ESMO) in Wien, Österreich:
Das Medikament L-BLP25 wurde an Patienten mit der am meisten verbreiteten
Form von Lungenkrebs getestet, dem so genannten Non-Small-Cell
Lungenkrebs. Insgesamt überlebten Patienten mit dem neuen Schutzstoff
durchschnittlich 17,4 Monate, im Vergleich zu einem Durchschnitt von 13
Monaten für jene, die die Standardversorgung erhielten. Bei den
Patienten, deren Krebs zu fortgeschritten für einen chirurgischen
Eingriff war, sich aber noch nicht zu anderen Organen ausgebreitet hatte,
war der Effekt noch deutlicher ausgeprägt. Patienten mit
Standard-Behandlung überlebten durchschnittlich 13,3 Monate, aber bei
jenen, die das neue Medikament bekamen, waren nach zwei Jahren noch 60
Prozent am Leben.
" Die Steigerung der Überlebenszeit um 4,4 Monate bei Patienten, die mit L-BLP25 behandelt wurden, ist ein bemerkenswerter Zeitraum, bedenkt man den aggressiven Krankheitsverlauf bei nicht-kleinzelligem Lungenkrebs," sagte Dr. Charles Butts, Onkologe am Cross Cancer Institute in Edmonton, Alberta (Kanada), in seiner Funktion als leitender Prüfarzt dieser Studie. „Die Daten bescheinigen dem Vakzin ein günstiges Sicherheitsprofil und einen positiven Einfluss auf den Erhalt der Lebensqualität und bestärken uns in unseren Plänen, es in weiteren Studien zu untersuchen. Die Ergebnisse, die wir bei Patienten in früheren Krankheitsstadien erzielen, sind sogar noch beeindruckender.“



Folgenachrichten vorprogrammiert !!!
„Diese Phase II-Daten sind im Hinblick auf den potenziellen Nutzen für die Patienten so ermutigend, weil sie auf einem Felde stattfinden, wo trotz so vieler Jahre Arbeit so geringe Fortschritte erzielt wurden“, sagte Dr. Bernhard Ehmer, Leiter des Geschäftsbereichs Onkologie. [/b]
SO AM FREITAG FOLGTE NUN DIESE NACHRICHT:
In einer nun abgeschlossenen Phase-IIb-Studie wurde das Präparat zur Immuntherapie von nicht-kleinzelligem Bronchialkarzinom (NSCLC) eingesetzt. In einer Untergruppe von Patienten mit lokoregionalem Erkrankungsstadium IIIB (d.h. lokal fortgeschritten und inoperabel) wurde die mittlere Überlebenszeit auch 23 Monate nach Rekrutierung des letzten Studienpatienten noch nicht erreicht.
Mittlere Überlebenszeit ist die Zeit, zu der die Hälfte der Patienten noch lebt, die andere Hälfte bereits gestorben ist. Wenn die mittlere Überlebenszeit also noch nicht erreicht wurde, bedeutet dies, dass noch mehr als die Hälfte der Patienten lebt.
Man kann hier klar von einer Weltsensation in der Medizinischen Geschichte sprechen!
donnerpower,
was denkst Du denn wo jetzt noch Kurspotential herkommen kann? Jetzt wird es doch erstmal wieder Zeit auszusteigen, als zu kaufen. Steigen wird die Aktie erstmal nicht weiter!?
gruß microby
was denkst Du denn wo jetzt noch Kurspotential herkommen kann? Jetzt wird es doch erstmal wieder Zeit auszusteigen, als zu kaufen. Steigen wird die Aktie erstmal nicht weiter!?
gruß microby
Kurs wird bis in den Bereich 3.90-4.20 euro laufen.Kurzes züruckkommen um dann Anlauf auf 5 zu nehmen.Morgen werden wieder alle wie verückt kaufen.
warum denn? Das sind doch alles Träume! Jetzt haben doch alle am Freitag gekauft! Jetzt ist erstmal wieder Schluß! Abwärts wirds gehen.
Hi Leudz 
@microby: Ich schätze, dass tsakalos folgendes meint: In USA und ich schätze auch mal in der ganzen Welt wird diese medizinishce Sensation, wie sie donnerpower nannte (ich bin kein Fachmann und wage nicht, dies zu beurteilen), jetzt diskutiert. Wenn es im Allgemeinen so bewertet wird, wie Donnerpower es tut, dann denke ich ebenso, dass wir einen starken Anstieg die nächste Zeit sehen werden, weil viele eben überhaupt nicht investiert sind. Ich möchte nicht wissen, wieviele Großaktionäre, Fondsmanager usw. dieses aufnehmen und den Kurs in die Höhe treiben werden. Sollte es wirklich als so eine Sensation aufgenommen werden, dann wird es die nächsten Tage sehr schnell aufwärts gehen. Es wird viel Zukunft gehandelt werden, ob abschätzbar und begründet steht auf nem ganz anderen Blatt. Aber viele werden sich die Finger lecken, falls die Chance wirklich so groß ist, dass hier eine ganz neue Therapie entwickelt wird.
Ich bin kein Fachmann und will keinem zum Kauf ermutigen bzw. ihn davon abhalten. Bin selbst unschlüssig, ob ich morgen nochmal nachlegen soll oder nicht. Abwarten und Tee trinken.
Schönen Abend euch allen

@microby: Ich schätze, dass tsakalos folgendes meint: In USA und ich schätze auch mal in der ganzen Welt wird diese medizinishce Sensation, wie sie donnerpower nannte (ich bin kein Fachmann und wage nicht, dies zu beurteilen), jetzt diskutiert. Wenn es im Allgemeinen so bewertet wird, wie Donnerpower es tut, dann denke ich ebenso, dass wir einen starken Anstieg die nächste Zeit sehen werden, weil viele eben überhaupt nicht investiert sind. Ich möchte nicht wissen, wieviele Großaktionäre, Fondsmanager usw. dieses aufnehmen und den Kurs in die Höhe treiben werden. Sollte es wirklich als so eine Sensation aufgenommen werden, dann wird es die nächsten Tage sehr schnell aufwärts gehen. Es wird viel Zukunft gehandelt werden, ob abschätzbar und begründet steht auf nem ganz anderen Blatt. Aber viele werden sich die Finger lecken, falls die Chance wirklich so groß ist, dass hier eine ganz neue Therapie entwickelt wird.
Ich bin kein Fachmann und will keinem zum Kauf ermutigen bzw. ihn davon abhalten. Bin selbst unschlüssig, ob ich morgen nochmal nachlegen soll oder nicht. Abwarten und Tee trinken.
Schönen Abend euch allen

@microby
...schlage vor morgen Früh unlimitierter VK in FfM
Wenn du dann verkauft hast empfehle dir an dieser Stelle dich nochmals gründlichst in donnerpowers Beiträge einzulesen, um wenigstens eine leise Vorstellung zu haben um was es hier ging...
...schlage vor morgen Früh unlimitierter VK in FfM

Wenn du dann verkauft hast empfehle dir an dieser Stelle dich nochmals gründlichst in donnerpowers Beiträge einzulesen, um wenigstens eine leise Vorstellung zu haben um was es hier ging...
#392
Da kennst Du aber die Amis ganz schlecht bei solchen Biotechwerte.Wären die Umsätze die letzten Tage immer so gross gewesen oder annährend, dann würde ich mir vielleicht gedanken machen.Ich für mein teil kauf Morgen nochmal dazu.
Da kennst Du aber die Amis ganz schlecht bei solchen Biotechwerte.Wären die Umsätze die letzten Tage immer so gross gewesen oder annährend, dann würde ich mir vielleicht gedanken machen.Ich für mein teil kauf Morgen nochmal dazu.
Na dann viel Glück für diejenigen , die morgen noch einsteigen!
Gratulation!
Gratulation!
@microby
Der Anstieg am Freitag prozentual war schon sehr hoch,
aber Biomira steht immer noch bei 3,40 Dollar!
Ich bin damals bei Biomira eingestiegen mit der Hoffnung das BLP25 ein Erfolg werden könnte und ich die Chance bekommen von Anfang an bei etwas ganz Grosses dabei zu sein!
BLP25 ist bis jetzt auf einem sehr guten Wege,warum sollte man in diesem Augenblick aussteigen???
Man beachte es leben jetzt „immer noch“ über die Hälfte der Testpersonen,somit ist jeder weitere TAG ein riesiger Erfolg in der medizinischen Geschichte!
Ich will hier keine Kursziele mehr abgegeben,sollte aber BLP25 zugelassen werden sprechen wir von ein enormes Kurspotential der dreistellige Kurse mit einbezieht könnte!
Die Amis würden dir geschmacklos sagen: vergleichen sie bitte diese beiden Komponenten KURS-LEBEN !
Welches kleines Unternehmen aus der Biobranche kann schon ein Vertriebspartner wie den Giganten MERCK KGAA vorweisen!!!
Ich vermute das die Amis am Montag bei über 4Dollar eröffnen werden!
Die Story fängt jetzt erst an!
80 Millionen umgesetzte Shares sprechen für sich!
Der Anstieg am Freitag prozentual war schon sehr hoch,
aber Biomira steht immer noch bei 3,40 Dollar!
Ich bin damals bei Biomira eingestiegen mit der Hoffnung das BLP25 ein Erfolg werden könnte und ich die Chance bekommen von Anfang an bei etwas ganz Grosses dabei zu sein!
BLP25 ist bis jetzt auf einem sehr guten Wege,warum sollte man in diesem Augenblick aussteigen???
Man beachte es leben jetzt „immer noch“ über die Hälfte der Testpersonen,somit ist jeder weitere TAG ein riesiger Erfolg in der medizinischen Geschichte!
Ich will hier keine Kursziele mehr abgegeben,sollte aber BLP25 zugelassen werden sprechen wir von ein enormes Kurspotential der dreistellige Kurse mit einbezieht könnte!
Die Amis würden dir geschmacklos sagen: vergleichen sie bitte diese beiden Komponenten KURS-LEBEN !
Welches kleines Unternehmen aus der Biobranche kann schon ein Vertriebspartner wie den Giganten MERCK KGAA vorweisen!!!
Ich vermute das die Amis am Montag bei über 4Dollar eröffnen werden!
Die Story fängt jetzt erst an!
80 Millionen umgesetzte Shares sprechen für sich!
@Donnerpower
Was für ein Tip!!!
Danke
Was für ein Tip!!!

Danke

Hallo,

gab wohl immer mal wieder größere ausschläge bei dem wert...
aber diesmal könnte es wohl nachhaltiger sein !?
gab wohl immer mal wieder größere ausschläge bei dem wert...

aber diesmal könnte es wohl nachhaltiger sein !?
#1000

Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| +2,37 | |
| -5,17 | |
| +9,23 | |
| +3,16 | |
| +0,03 | |
| -2,66 | |
| +8,91 | |
| -0,32 | |
| 0,00 | |
| +0,76 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 207 | ||
| 119 | ||
| 60 | ||
| 50 | ||
| 46 | ||
| 38 | ||
| 38 | ||
| 31 | ||
| 30 | ||
| 28 |





















