ANP.AX (Mkap €11 M) DMD P2 Daten im Q4 = MEGA ZOCK (Seite 145)
eröffnet am 25.07.19 12:43:02 von
neuester Beitrag 12.06.24 23:07:36 von
neuester Beitrag 12.06.24 23:07:36 von
Beiträge: 2.055
ID: 1.308.085
ID: 1.308.085
Aufrufe heute: 3
Gesamt: 244.552
Gesamt: 244.552
Aktive User: 0
ISIN: AU0000317281 · WKN: A3E1W6
0,0565
EUR
0,00 %
0,0000 EUR
Letzter Kurs 16.06.24 Lang & Schwarz
Neuigkeiten
| TitelBeiträge |
|---|
Werte aus der Branche Pharmaindustrie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,8000 | +33,33 | |
| 323,60 | +17,59 | |
| 9,4900 | +16,58 | |
| 5,3700 | +15,98 | |
| 449,10 | +15,09 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 8,1200 | -13,53 | |
| 2,1000 | -16,00 | |
| 7,1900 | -20,02 | |
| 0,9500 | -22,76 | |
| 80,22 | -23,42 |
Beitrag zu dieser Diskussion schreiben
Bei www.finanznachrichten - der Jahresbericht zum 30. 6. mit Infos - leider geht der link nicht-
AntisenseTherapeuticsLimitedAppendix4EAuditedFinancialReportYear Ended30 June 2020
AntisenseTherapeuticsLimitedAppendix4EAuditedFinancialReportYear Ended30 June 2020
Antwort auf Beitrag Nr.: 64.835.161 von urpferdchen am 21.08.20 09:05:34Hier vermuten die Jungs aus dem Hotcopper Forum zwei Dinge...
1. Die Gentherapie versagt
2. Die Zulassung FastTrack rückt näher...ausserdem soll angeblich dad Interesse von BP gewachsen sein...
1. Die Gentherapie versagt
2. Die Zulassung FastTrack rückt näher...ausserdem soll angeblich dad Interesse von BP gewachsen sein...
Antwort auf Beitrag Nr.: 64.834.213 von Stoxtrayder am 21.08.20 07:45:31Vom Linien-Chart 2 Jahre sieht es so aus, als ob demnächst die nächste Stufe nach oben starten will.
letztes Jahr im Sept. von ca. 0,05 auf 0,12 Aud $ - Da fehlt noch die passende Maldung dazu.
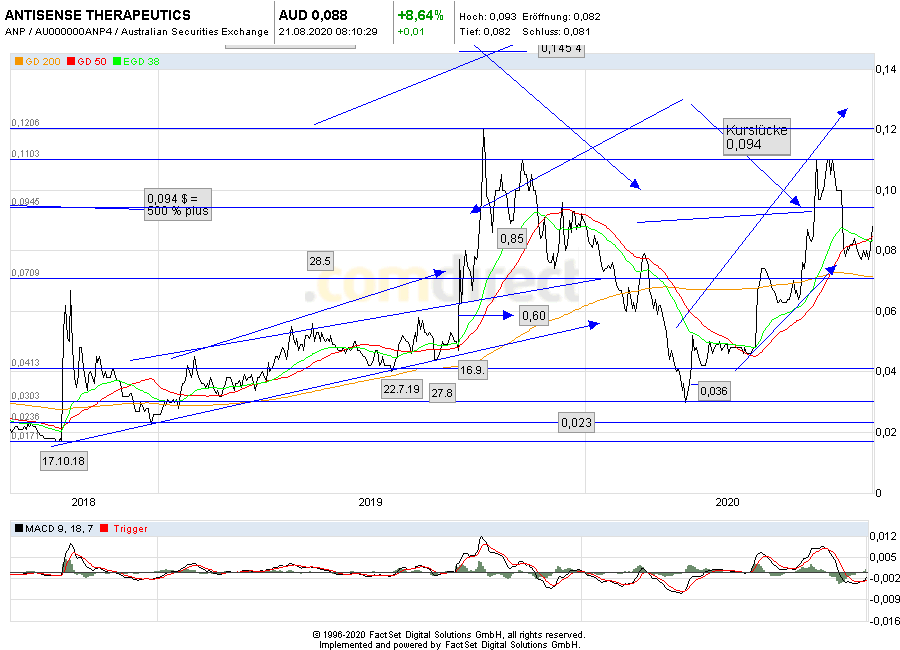
letztes Jahr im Sept. von ca. 0,05 auf 0,12 Aud $ - Da fehlt noch die passende Maldung dazu.

Schöner Anstieg heute Down-Under, +15% 👌
gut, dass die Meldungen kommen. Nur unsere Aussis scheint dies wenig zu interresieren. Runter gings schneller. jetzt dauert es wieder bis die 0,10AUD erreicht werden. A mehr kann ich gar nicht glauben. Lass mich aber gern überraschen.
Antisense heute morgen schon wieder eine Meldung - www.finanznachrichten.de - link geht nicht
Text automatisch übersetzt -
--------------------
ANTISENSE THERAPEUTICS LIMITED ABN 41 095 060 745 | US OTC: ATHJY] (das Unternehmen) freut sich bekannt zu geben, dass es seinen Antrag auf Orphan Drug-Kennzeichnung des Unternehmensmedikaments ATL1102 zur Behandlung von Duchenne-Muskeldystrophie (DMD) beim US-amerikanischen Amt für Lebensmittel- und Arzneimittelverwaltung (FDA) eingereicht hat Produktentwicklung (OOPD). Das Unternehmen gab kürzlich positive Phase-II-Ergebnisse mit ATL1102 in der Anwendung zur Bezeichnung von DMD und Orphan Drug bekannt. Dies ist eine wichtige Interaktion mit der FDA. ANP definiert derzeit seinen klinischen Entwicklungs- und Regulierungspfad für die USA, wo Unternehmen, die Medikamente für Orphan-Indikationen entwickeln, die verbesserte Therapien wie DMD benötigen, potenzielle schnelle oder beschleunigte Bezeichnungen zur Verfügung stehen.
Mark Diamond, Managing Director und CEO von ANP, sagte: „Dies ist ein wichtiger regulatorischer und kommerzieller Meilenstein in der Weiterentwicklung von ATL1102 für DMD und stellt einen weiteren wichtigen Schritt dar, um diese potenziell transformative Therapie für Patienten mit einem erheblichen ungedeckten Bedarf bereitzustellen.“ Orphan Drug Die FDA kann Arzneimittel auszeichnen, die zur sicheren und wirksamen Behandlung seltener Krankheiten bestimmt sind, von denen weniger als 200.000 Menschen in den USA betroffen sind. Die FDA bietet Anreize, um die Entwicklung von Produkten für seltene Krankheiten zu beschleunigen, einschließlich Steuergutschriften für die Kosten für klinische Studien, Verzicht auf US-Gebühren für die Einreichung von verschreibungspflichtigen Arzneimitteln und Exklusivität für verwaiste Produkte für sieben Jahre nach Genehmigung des Inverkehrbringens. Dementsprechend legen potenzielle Vermarkter von Orphan Drugs im Allgemeinen eine erhebliche Prämie auf ihren kommerziellen Wert. Das Unternehmen beantragt derzeit bei der Europäischen Arzneimittel-Agentur die Ausweisung von Orphan Drug für ATL1102 in DMD und wird diesen voraussichtlich im laufenden Quartal einreichen.
Rest bei www.finanznachrichten.de
Text automatisch übersetzt -
--------------------
ANTISENSE THERAPEUTICS LIMITED ABN 41 095 060 745 | US OTC: ATHJY] (das Unternehmen) freut sich bekannt zu geben, dass es seinen Antrag auf Orphan Drug-Kennzeichnung des Unternehmensmedikaments ATL1102 zur Behandlung von Duchenne-Muskeldystrophie (DMD) beim US-amerikanischen Amt für Lebensmittel- und Arzneimittelverwaltung (FDA) eingereicht hat Produktentwicklung (OOPD). Das Unternehmen gab kürzlich positive Phase-II-Ergebnisse mit ATL1102 in der Anwendung zur Bezeichnung von DMD und Orphan Drug bekannt. Dies ist eine wichtige Interaktion mit der FDA. ANP definiert derzeit seinen klinischen Entwicklungs- und Regulierungspfad für die USA, wo Unternehmen, die Medikamente für Orphan-Indikationen entwickeln, die verbesserte Therapien wie DMD benötigen, potenzielle schnelle oder beschleunigte Bezeichnungen zur Verfügung stehen.
Mark Diamond, Managing Director und CEO von ANP, sagte: „Dies ist ein wichtiger regulatorischer und kommerzieller Meilenstein in der Weiterentwicklung von ATL1102 für DMD und stellt einen weiteren wichtigen Schritt dar, um diese potenziell transformative Therapie für Patienten mit einem erheblichen ungedeckten Bedarf bereitzustellen.“ Orphan Drug Die FDA kann Arzneimittel auszeichnen, die zur sicheren und wirksamen Behandlung seltener Krankheiten bestimmt sind, von denen weniger als 200.000 Menschen in den USA betroffen sind. Die FDA bietet Anreize, um die Entwicklung von Produkten für seltene Krankheiten zu beschleunigen, einschließlich Steuergutschriften für die Kosten für klinische Studien, Verzicht auf US-Gebühren für die Einreichung von verschreibungspflichtigen Arzneimitteln und Exklusivität für verwaiste Produkte für sieben Jahre nach Genehmigung des Inverkehrbringens. Dementsprechend legen potenzielle Vermarkter von Orphan Drugs im Allgemeinen eine erhebliche Prämie auf ihren kommerziellen Wert. Das Unternehmen beantragt derzeit bei der Europäischen Arzneimittel-Agentur die Ausweisung von Orphan Drug für ATL1102 in DMD und wird diesen voraussichtlich im laufenden Quartal einreichen.
Rest bei www.finanznachrichten.de
Antwort auf Beitrag Nr.: 64.614.663 von coronus am 31.07.20 22:58:53Dann besteht die Hoffnung auf den Anstieg - erst mal Richtung 0,14 Aud $ - wäre Super-schön.
letztes Jahr ab Mitte September.
letztes Jahr ab Mitte September.
Antwort auf Beitrag Nr.: 64.596.330 von urpferdchen am 30.07.20 15:07:28Naja, USA stehen noch aus...dort ist auch gerade ein lobbyist unterwegs und versucht zu trommeln...
Die heutige Meldung von Antisense - bei www.finanznachrichten.de - liest sich gut - leider geht der
link nicht. - Mal sehen ob die Australier den Bericht über das Wochenende lesen - und reagieren ?
Quartalsbericht -
-----------------
6 WALLACE AVENUE, TOORAK VIC 3142 AUSTRALIATEL.+61398278999FAX+61398597701WEBWWW.ANTISENSE.COM.AUANTISENSE THERAPEUTICS LIMITED ABN 41 095 060 745 Page 1 of 2ASX Announcement31 July 20 20 Quarterly Update & Appendix 4C•DMD Phase II trial met primary and exceeded secondary endpoint expectations•Preparations continue for the advancement of ATL1102 into a potentially pivotal Phase IIb clinical trial.Antisense Therapeutics Limited (Antisense or Company) is pleased to provide its Appendix 4C and quarterly update for the period ended 30 June 2020. ATL1102 for DMD Phase II trial results support advancement into a potentially pivotal Phase IIb clinical trialDuring the quarter t
usw.
link nicht. - Mal sehen ob die Australier den Bericht über das Wochenende lesen - und reagieren ?
Quartalsbericht -
-----------------
6 WALLACE AVENUE, TOORAK VIC 3142 AUSTRALIATEL.+61398278999FAX+61398597701WEBWWW.ANTISENSE.COM.AUANTISENSE THERAPEUTICS LIMITED ABN 41 095 060 745 Page 1 of 2ASX Announcement31 July 20 20 Quarterly Update & Appendix 4C•DMD Phase II trial met primary and exceeded secondary endpoint expectations•Preparations continue for the advancement of ATL1102 into a potentially pivotal Phase IIb clinical trial.Antisense Therapeutics Limited (Antisense or Company) is pleased to provide its Appendix 4C and quarterly update for the period ended 30 June 2020. ATL1102 for DMD Phase II trial results support advancement into a potentially pivotal Phase IIb clinical trialDuring the quarter t
usw.
Antwort auf Beitrag Nr.: 64.590.246 von coronus am 30.07.20 08:22:11Sind da andere gute Meldungen zu erwarten ? - insgesamt eine Verschiebung um ca. ein halbes Jahr
Für Herbst 2020 waren Zulassungen erwartet - wenn ich mich richtig erinnere -
Mal sehen ob Antisense die Presse-Arbeit weiter pflegt mit Meldungen alle paar Wochen -
Präsentationen.
Für Herbst 2020 waren Zulassungen erwartet - wenn ich mich richtig erinnere -
Mal sehen ob Antisense die Presse-Arbeit weiter pflegt mit Meldungen alle paar Wochen -
Präsentationen.





















