Palatin Technology / voraussichtliches Marktpotential von 1,3 Mrd $ bis 2020 allein in USA - 500 Beiträge pro Seite (Seite 6)
eröffnet am 17.02.15 22:17:27 von
neuester Beitrag 28.02.24 20:50:54 von
neuester Beitrag 28.02.24 20:50:54 von
Beiträge: 5.764
ID: 1.207.859
ID: 1.207.859
Aufrufe heute: 0
Gesamt: 1.023.717
Gesamt: 1.023.717
Aktive User: 0
ISIN: US6960775020 · WKN: A3DTUW · Symbol: PTN
1,7200
USD
-0,58 %
-0,0100 USD
Letzter Kurs 02:04:01 NYSE Arca
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,9000 | +59,66 | |
| 4,7450 | +35,57 | |
| 0,5250 | +19,08 | |
| 5,8900 | +17,80 | |
| 1,9700 | +15,20 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,7000 | -13,71 | |
| 3,0400 | -19,95 | |
| 1,9500 | -25,14 | |
| 1,6052 | -30,21 | |
| 0,5121 | -30,80 |
Indikatoren
Antwort auf Beitrag Nr.: 58.043.485 von Reinerle am 22.06.18 12:37:54Hallo zusammen, kann jemand erklären was über amex gehandelt wurde? Mir werden über 15mio Stücke angezeigt.
15 MIO im Schlusskurs.
Weak hands are out now ------for shure!
Da hat man mit einem Schlag so manchen mit Stop loss ausebootet.
Könnte nächste Woche sehr interesssant werden .
Schönes Weekend!
Weak hands are out now ------for shure!
Da hat man mit einem Schlag so manchen mit Stop loss ausebootet.
Könnte nächste Woche sehr interesssant werden .
Schönes Weekend!
Antwort auf Beitrag Nr.: 58.048.978 von Moneymaker123 am 22.06.18 23:13:20Hat jemand eine Vermutung was dahinter steckt? Der Handel drüben war ja generell heute auffällig hoch.
Antwort auf Beitrag Nr.: 58.049.041 von PrinzStorno am 22.06.18 23:31:3415,3 Mio Stück um 16:00 Amerikanischer Zeit. Ich vermute da weiß jemand etwas mehr
387.535 Anteile an Palatin Technologies, Inc. (PTN) erworben von Tibra Equities Europe Ltd
Gepostet von Jeanne O'Marion am 23. Juni 2018 // Palatin Technologies logo Tibra Equities Europe Ltd erwarb im ersten Quartal eine neue Beteiligung an Palatin Technologies, Inc. (NYSEAMERICAN: PTN), so das Unternehmen in seiner jüngsten Einreichung bei der Securities & Exchange Commission. Der Fonds kaufte 387.535 Aktien des biopharmazeutischen Unternehmens im Wert von rund 422.000 US-Dollar. Tibra Equities Europe Ltd besaß 0,20% von Palatin Technologies bei seiner jüngsten SEC-Einreichung.
Eine Reihe anderer Großinvestoren hat ebenfalls Anteile von PTN gekauft und verkauft. Renaissance Technologies LLC erwarb im 4. Quartal einen neuen Anteil an Aktien von Palatin Technologies im Wert von 1.456.000 USD. Die Deutsche Bank AG hat ihre Beteiligung an Aktien von Palatin Technologies im 4. Quartal um 2.680.243,1% erhöht. Die Deutsche Bank AG besitzt nun 1.366.975 Aktien des biopharmazeutischen Unternehmens im Wert von 1.174.000 US-Dollar nach dem Kauf von 1.366.924 Aktien während des Berichtszeitraums. Acadian Asset Management LLC hat im 4. Quartal seine Anteile an Aktien von Palatin Technologies um 272,5% erhöht. Acadian Asset Management LLC besitzt nun 1.249.283 Aktien der biopharmazeutischen Gesellschaft im Wert von $ 1.075.000, nachdem sie im Berichtszeitraum weitere 913.862 Aktien gekauft hatte. Virtu Financial LLC hat seine Anteile an Aktien von Palatin Technologies im 4. Quartal um 87,0% erhöht. Virtu Financial LLC besitzt nun 632.045 Aktien der biopharmazeutischen Gesellschaft im Wert von 543.000 USD, nachdem sie während des Berichtszeitraums weitere 294.098 Aktien gekauft hatte. Schließlich hat die Macquarie Group Ltd. ihre Anteile an Palatin Technologies im vierten Quartal um 552,3% erhöht. Die Macquarie Group Ltd. hält jetzt 473.306 Aktien der biopharmazeutischen Gesellschaft im Wert von 407.000 USD, nachdem sie in diesem Zeitraum weitere 400.750 Aktien gekauft hatte.
https://theenterpriseleader.com/2018/06/23/tibra-equities-eu…
Wie Urbi bereits erwähnte, ist das Volumen wohl auf die Aufnahme von PTN in den Russel 3000 Index zurück zu führen. Die Fonds haben dann umgeschichtet und sich daher entsprechend mit Palatin Aktien eingedeckt.
Palatin war jahrelang tot. So tot wie die Deutsche Mannschaft gestern aber dann...
Antwort auf Beitrag Nr.: 58.052.188 von Mammut22 am 23.06.18 16:42:21
Und was heißt das? Ab Montag wieder Business as usual mit schwankenden Kursen bei moderatem Volumen?
Zitat von Mammut22: Wie Urbi bereits erwähnte, ist das Volumen wohl auf die Aufnahme von PTN in den Russel 3000 Index zurück zu führen. Die Fonds haben dann umgeschichtet und sich daher entsprechend mit Palatin Aktien eingedeckt.
Und was heißt das? Ab Montag wieder Business as usual mit schwankenden Kursen bei moderatem Volumen?
Also wenn man die Meldung vom 25.04 (siehe unten) und die am Freitag durchgeführte Indexaufnahme zusammen bewertet könnte es durchaus so sein ,dass Canaccord
einen Käufer für die Kapitalerhöhung gefunden hat, der mit Indexaufschaltung das neue Aktienpaket gezeichnet hat,
Somit ist ein Großaktionär aktiv geworden der Interesse an Kurspflege haben sollte,
Kann ja durchaus ein Fonds sein .
Auf gute Kurse!
Meldung vom 25.04
Grund für den nachbörslichen Kurssturz Der Grund für den Kurssturz auf 1,15 $ nachbörslich ist ein SEC-Filing von Palatin am Freitagabend in dem eine Kapitalerhöhung in Höhe von 25 Millionen $ durch Aktienverkäufe angekündigt wird. Quelle: edgar online oder andere Dienste, die SEC-Filings darstellen Item 1.01 Entry into a Material Definitive Agreement. On April 20, 2018, Palatin Technologies, Inc. (the “Company”) entered into an equity distribution agreement (the “Equity Distribution Agreement”) with Canaccord Genuity LLC (“Canaccord”), pursuant to which the Company may, from time to time, sell shares of the Company’s common stock, par value $0.01 per share (the “Shares”), having an aggregate offering price of up to $25,000,000 through Canaccord, as the Company’s sales agent. The Shares will be offered and sold by the Company pursuant to its previously filed and currently effective Registration Statement on Form S-3 (Reg. No. 333-206047) (the “Registration Statement”). The Shares may only be offered and sold by means of a prospectus, including a prospectus supplement, forming part of the effective Registration Statement. Sales of the common stock, if any, will be made at market prices by methods deemed to be an “at-the market-offering” as defined in Rule 415 promulgated under the Securities Act of 1933, as amended, including sales made directly on the NYSE American, on any other existing trading market for the common stock, or to or through a market maker other than on an exchange. We will pay Canaccord a commission rate of 3.0% of the gross proceeds from the sales of common stock sold pursuant to the terms of the Equity Distribution Agreement. The Equity Distribution Agreement also contains, among other things, customary representations, warranties and covenants by the Company and indemnification obligations of the Company and Canaccord as well as certain termination rights for both the Company and Canaccord. The Company has no obligation to sell any Shares under the Equity Distribution Agreement, and may at any time suspend solicitation and offers under the Equity Distribution Agreement.
Palatin Technology / voraussichtliches Marktpotential von 1,3 Mrd $ bis 2020 allein in USA | wallstreet-online.de - Vollständige Diskussion unter:
https://www.wallstreet-online.de/diskussion/1207859-2381-239…
einen Käufer für die Kapitalerhöhung gefunden hat, der mit Indexaufschaltung das neue Aktienpaket gezeichnet hat,
Somit ist ein Großaktionär aktiv geworden der Interesse an Kurspflege haben sollte,
Kann ja durchaus ein Fonds sein .
Auf gute Kurse!
Meldung vom 25.04
Grund für den nachbörslichen Kurssturz Der Grund für den Kurssturz auf 1,15 $ nachbörslich ist ein SEC-Filing von Palatin am Freitagabend in dem eine Kapitalerhöhung in Höhe von 25 Millionen $ durch Aktienverkäufe angekündigt wird. Quelle: edgar online oder andere Dienste, die SEC-Filings darstellen Item 1.01 Entry into a Material Definitive Agreement. On April 20, 2018, Palatin Technologies, Inc. (the “Company”) entered into an equity distribution agreement (the “Equity Distribution Agreement”) with Canaccord Genuity LLC (“Canaccord”), pursuant to which the Company may, from time to time, sell shares of the Company’s common stock, par value $0.01 per share (the “Shares”), having an aggregate offering price of up to $25,000,000 through Canaccord, as the Company’s sales agent. The Shares will be offered and sold by the Company pursuant to its previously filed and currently effective Registration Statement on Form S-3 (Reg. No. 333-206047) (the “Registration Statement”). The Shares may only be offered and sold by means of a prospectus, including a prospectus supplement, forming part of the effective Registration Statement. Sales of the common stock, if any, will be made at market prices by methods deemed to be an “at-the market-offering” as defined in Rule 415 promulgated under the Securities Act of 1933, as amended, including sales made directly on the NYSE American, on any other existing trading market for the common stock, or to or through a market maker other than on an exchange. We will pay Canaccord a commission rate of 3.0% of the gross proceeds from the sales of common stock sold pursuant to the terms of the Equity Distribution Agreement. The Equity Distribution Agreement also contains, among other things, customary representations, warranties and covenants by the Company and indemnification obligations of the Company and Canaccord as well as certain termination rights for both the Company and Canaccord. The Company has no obligation to sell any Shares under the Equity Distribution Agreement, and may at any time suspend solicitation and offers under the Equity Distribution Agreement.
Palatin Technology / voraussichtliches Marktpotential von 1,3 Mrd $ bis 2020 allein in USA | wallstreet-online.de - Vollständige Diskussion unter:
https://www.wallstreet-online.de/diskussion/1207859-2381-239…
Im Rahmen der jährlichen Neuzusammensetzung des Russell U.S. Index sind einige der Unternehmen, die zum 25. Juni 2018 in den Russell 3000 Index aufgenommen wurden.
Palatin Technologies Inc. (PTN); Vital Therapien Inc. (VTL); Endocyte Inc. (ECYT); Evelo Biosciences Inc. (EVLO); PolarityTE Inc. (COOL); Mustang Bio Inc. (MBIO); ADMA Biologics Inc. (ADMA); Zafgen Inc. (ZFGN); T2 Biosystems Inc. (TTOO); Unum Therapeutics Inc. (UMRX); Verastem Inc. (VSTM); AVEO Pharmaceuticals Inc. (AVEO); Apollo Medical Holdings Inc. (AMEH); GTx Inc. (GTXI); Aldeyra Therapeutics Inc. (ALDX); MannKind Corporation (MNKD); Vericel Corp. (VCEL), CymaBay Therapeutics, Inc. (CBAY) und Savara Inc. (SVRA).
http://www.rttnews.com/2908288/fda-approves-1st-cannabis-bas…
Palatin Technologies Inc. (PTN); Vital Therapien Inc. (VTL); Endocyte Inc. (ECYT); Evelo Biosciences Inc. (EVLO); PolarityTE Inc. (COOL); Mustang Bio Inc. (MBIO); ADMA Biologics Inc. (ADMA); Zafgen Inc. (ZFGN); T2 Biosystems Inc. (TTOO); Unum Therapeutics Inc. (UMRX); Verastem Inc. (VSTM); AVEO Pharmaceuticals Inc. (AVEO); Apollo Medical Holdings Inc. (AMEH); GTx Inc. (GTXI); Aldeyra Therapeutics Inc. (ALDX); MannKind Corporation (MNKD); Vericel Corp. (VCEL), CymaBay Therapeutics, Inc. (CBAY) und Savara Inc. (SVRA).
http://www.rttnews.com/2908288/fda-approves-1st-cannabis-bas…
Zacks Investment Research stuft Palatin Technologies (PTN) zum Verkauf ab
Gepostet von Andrew Steele am 25. Juni 2018 //Palatin Technologies (NYSEAMERICAN: PTN) wurde von Zacks Investment Research in einer am Freitag, dem 8. Juni veröffentlichten Research Note von einem "Halten" -Rating auf ein "Verkaufen" -Rating herabgestuft.
Laut Zacks ist "Palatin Technologies, Inc. ein Medizintechnik-Unternehmen in der Entwicklungsphase, das Produkte und Technologien für diagnostische Bildgebung, Krebstherapie und ethische Arzneimittelentwicklung entwickelt und vermarktet. Diese Entwicklungen basieren auf der patentrechtlich geschützten monoklonalen Antikörper-Radiomarkierung und ermöglichen Peptid-Plattformtechnologien . "
Holen Sie sich Palatin Technologies Warnungen:
Eine Reihe anderer Research-Analysten hat sich kürzlich ebenfalls auf das Unternehmen eingelassen. HC Wainwright setzte bei Palatin Technologies ein Kursziel von 5,00 US-Dollar fest und gab dem Unternehmen am Montag, den 4. Juni, in einem Bericht ein "Kauf" -Rating. TheStreet hat Palatin Technologies in einem Forschungsbericht am Donnerstag, den 29. März von "d" auf "c-" eingestuft. Ein Research-Analyst hat die Aktie mit einem Halte-Rating bewertet, und drei haben eine Kauf-Bewertung für die Aktie abgegeben. Palatin Technologies hat derzeit ein durchschnittliches Rating von "Kaufen" und einen Konsenszielkurs von 3,44 USD.
Palatin Technologies eröffnete am Freitag bei 1,09 Dollar, berichtet MarketBeat . Palatin Technologies hat ein 12-Monats-Tief von 0,38 US-Dollar und ein 12-Monats-Hoch von 1,59 US-Dollar.
Palatin Technologies (NYSEAMERICAN: PTN) veröffentlichte zuletzt am Dienstag, den 15. Mai, seine Quartalszahlen. Das biopharmazeutische Unternehmen meldete für das Quartal 0,00 US-Dollar Gewinn pro Aktie und übertraf damit die Konsensschätzung von 0,04 US-Dollar um 0,04 US-Dollar. Das Unternehmen erzielte im Quartal einen Umsatz von 8,96 Millionen US-Dollar. Palatin Technologies erzielte eine Eigenkapitalrendite von 155,80% und eine Nettomarge von 28,55%.
Eine Reihe von Hedge-Fonds hat kürzlich ihre Positionen im Geschäft geändert. Element Capital Management LLC kaufte im ersten Quartal eine neue Beteiligung an Palatin Technologies im Wert von ca. 240.000 US-Dollar. Citadel Advisors LLC hat seine Anteile an Aktien von Palatin Technologies im ersten Quartal um 130,8% erhöht. Citadel Advisors LLC hält jetzt 173.790 Aktien der biopharmazeutischen Firma im Wert von $ 189.000, nach dem Kauf von weiteren 98.483 Aktien im letzten Quartal. Tibra Equities Europe Ltd erwarb im 1. Quartal eine neue Beteiligung an Palatin Technologies im Wert von 422.000 USD. Northern Trust Corp hat im ersten Quartal seine Beteiligung an Palatin Technologies um 22,6% erhöht. Northern Trust Corp besitzt jetzt 333.277 Aktien des biopharmazeutischen Unternehmens im Wert von $ 363.000 nach dem Kauf von zusätzlichen 61.351 Aktien während des Zeitraums. Schließlich hat die Macquarie Group Ltd. im vierten Quartal ihre Beteiligung an Palatin Technologies um 552,3% erhöht. Die Macquarie Group Ltd. hält jetzt 473.306 Aktien der biopharmazeutischen Gesellschaft im Wert von 407.000 USD, nachdem sie während des Berichtszeitraums weitere 400.750 Aktien gekauft hatte.
Über Palatin Technologies
Palatin Technologies, Inc., ein biopharmazeutisches Unternehmen, entwickelt zielgerichtete, rezeptorspezifische Peptidtherapeutika zur Behandlung verschiedener Erkrankungen in den Vereinigten Staaten. Das Hauptprodukt des Unternehmens ist Bremelanotide, ein subkutan injizierbarer Peptid-Melanocortin-Rezeptor-Agonist, der in klinischen Phase-III-Studien zur Behandlung prämenopausaler Frauen mit einer Hypoactive Sexual Desirest Disorder (HSDD) eingesetzt wird.
https://stocknewstimes.com/2018/06/25/zacks-investment-resea…
Bei ariva hat luxer dies gepostet
LUXER: bleibt es bei diesen Daten??
25.06.18 13:34
#7073
Anstehende Termine für PALATIN TECHNOLOGIES, INC.
26/06/18 | 15:00 Jahreshauptversammlung
26/09/18 | 06:00 Jahr 2018 Ergebnisveröffentlichung (geplant)
Hat einer dazu news? Ee ist erstaunlich ruhig hier.
LUXER: bleibt es bei diesen Daten??
25.06.18 13:34
#7073
Anstehende Termine für PALATIN TECHNOLOGIES, INC.
26/06/18 | 15:00 Jahreshauptversammlung
26/09/18 | 06:00 Jahr 2018 Ergebnisveröffentlichung (geplant)
Hat einer dazu news? Ee ist erstaunlich ruhig hier.
Antwort auf Beitrag Nr.: 58.072.207 von apano am 26.06.18 19:20:18ist noch nichts bekannt kommt vermutlich morgen oder die nächsten tage
Wurde als Proxy Statement am 17.05.2018 zumindest auch so auf der PTN Homepage angekündigt.
Antwort auf Beitrag Nr.: 58.075.048 von rallyseeker am 27.06.18 08:43:25https://www.palatin.com/investors/sec-filings/
Aktueller Bericht, Punkte 5.02, 5.07 und 9.01
https://translate.google.de/translate?sl=en&tl=de&js=y&prev=…
Der Bericht zeigt mal wieder deutlich auf worum es eigentlich bei Aktienunternehmen geht.
Eine Hand voll Managern bereichert sich irgendwann durch verwässernde Aktienpakete die als Prämien getarnt in den Hauptversammlungen durchgewunken werden , verkauft diese am hochgepushten Markt und hat sich selber damit saniert .
Den Shareholdern bleibt da nur das nachsehen!
Langfrist Invest ?- nein Danke!
Rein.......... Gewinne mitnehmen und wieder raus .
Notfalls täglich!
Eine Hand voll Managern bereichert sich irgendwann durch verwässernde Aktienpakete die als Prämien getarnt in den Hauptversammlungen durchgewunken werden , verkauft diese am hochgepushten Markt und hat sich selber damit saniert .
Den Shareholdern bleibt da nur das nachsehen!
Langfrist Invest ?- nein Danke!
Rein.......... Gewinne mitnehmen und wieder raus .
Notfalls täglich!
Insider von Palatin Technologies hat gerade 28.000 Aktien aufgenommen
Joseph Stanley Hull, ein Insider von Palatin Technologies, hat kürzlich 28.000 Aktien des Unternehmens erworben. Die Käufe erfolgten am 26. Juni 2018 zu 0,00 US-Dollar pro Aktie (und damit wahrscheinlich zu dem Ergebnis von Optionszuschüssen oder Restriktionen von Aktien). Hull besitzt nun 484.333 Aktien der Gesellschaft. Hull operiert außerhalb von Cranbury, NJ. Einige zusätzliche Informationen wurden wie folgt bereitgestellt:Im Rahmen des Stock Incentive Plan 2011 gewährte Beschränkungen für Aktienanteile, die jeweils das Recht zum Erhalt einer Stammaktie ohne weitere Zahlung vorsehen. Die Sperrung der Anteile erfolgt am 26. Juni 2019. Die Optionen werden zum letzten Tag eines jeden Monats zum 31. Juli 2018 in Höhe von 1/12 pro Monat ausgeübt.
Die obigen Informationen wurden in einer Anmeldung an die SEC veröffentlicht. Um die Anmeldung zu sehen, klicken Sie hier .
http://www.conferencecalltranscripts.org/4/summary/?id=50641…
Um eine kostenlose E-Mail-Benachrichtigung zu erhalten, wenn Palatin Technologies einen ähnlichen Schritt macht, melden Sie sich an!
Andere kürzlich eingereichte Anmeldungen von der Firma schließen die folgenden ein:
Der Insider von Palatin Technologies hat am 28. Juni 2018 28.000 Aktien gekauft
Der Insider von Palatin Technologies hat am 28. Juni 2018 543.500 Aktien gekauft
Aktueller Bericht, Punkte 5.02, 5.07 und 9.01 - 27. Juni 2018
Automatische Aktualisierung
Feedback
© www.conferencecalltranscripts.org 2016 | Nutzungsbedingungen
Der Insider von Palatin Technologies hat gerade 543.500 Aktien übernommen
Carl Spana, ein Insider von Palatin Technologies, hat kürzlich 543.500 Aktien des Unternehmens erworben. Die Käufe erfolgten am 26. Juni 2018 zu einem Preis von 0,00 USD pro Aktie. Spana besitzt nun 4.130.352 Aktien der Gesellschaft. Spana betreibt außerhalb von Cranbury, NJ. Einige zusätzliche Informationen wurden wie folgt bereitgestellt:Im Rahmen des Stock Incentive Plan 2011 gewährte Beschränkungen für Aktienanteile, die jeweils das Recht zum Erhalt einer Stammaktie ohne weitere Zahlung vorsehen. Die am 12. Dezember 2017 erfolgte Leistungszusage wurde am 26. Juni 2018 nach Bestätigung durch das Compensation Committee, dass ein definiertes Leistungsziel in Höhe von 30% der Zielanzahl der Share Units erreicht wurde, der Annahme zur Einreichung der Einlage erteilt von der US-amerikanischen Food and Drug Administration einer New Drug Appli- kation für Bremelanotide bei hypoactive sexueller Begierde bei prämenopausalen Frauen während des definierten Leistungszeitraums. Freigegebene Aktien werden vorbehaltlich der Bedingungen der anwendbaren Restricted Share Unit Agreement geliefert, nachdem die berichtende Person ihre Anstellung als Angestellter von Palatin Technologies, Inc. aufgegeben hat. Eingeschränkte Aktieneinheiten, die im Rahmen des Stock Incentive Plan 2011 gewährt wurden und jeweils den Recht, ohne weitere Zahlung eine Stammaktie zu erhalten. Die gesperrten Anteile werden am 26. Juni 2019 zu 50% und am 26. Juni 2020 zu den restlichen Anteilen übertragen. Freigegebene Aktien werden vorbehaltlich der Bestimmungen des anwendbaren eingeschränkten Anteilsanteilsvertrags nach dem Ausscheiden der berichtenden Person geliefert als Angestellter von Palatin Technologies, Inc. Optionen ab dem 26. Juni 2019 in Höhe von 25% pro Jahr. Vesting des am 12. Dezember 2017 gewährten Aktienoptionsplans, der zum Teil am 26. Juni 2018 erfolgte , nach Bestätigung durch das Compensation Committee, dass ein definiertes Leistungsziel von 30% der angestrebten Anzahl von Share Units erreicht wurde, die Annahme der Einreichung eines Zulassungsantrags für Bremelanotide für hypoaktive sexuelle Verlangensstörung durch die US Food and Drug Administration bei prämenopausalen Frauen während des definierten Leistungszeitraums.
Die obigen Informationen wurden in einer Anmeldung an die SEC veröffentlicht. Um die Anmeldung zu sehen, klicken Sie hier .
Um eine kostenlose E-Mail-Benachrichtigung zu erhalten, wenn Palatin Technologies einen ähnlichen Schritt macht, melden Sie sich an!
Andere kürzlich eingereichte Anmeldungen von der Firma schließen die folgenden ein:
Der Insider von Palatin Technologies hat am 28. Juni 2018 28.000 Aktien gekauft
Der Insider von Palatin Technologies hat am 28. Juni 2018 28.000 Aktien gekauft
Aktueller Bericht, Punkte 5.02, 5.07 und 9.01 - 27. Juni 2018
© www.conferencecalltranscripts.org 2016 | Nutzungsbedingungen
http://www.conferencecalltranscripts.org/4/summary/?id=50640…
über ne halbe Million Aktien für umsonst kaufen ?
Kaufen ist wohl kaum die richtige Bezeichnung für den Schluck aus der Pulle die sich hier
das Management einverleibt.
Schön in die eigene Tasche arbeiten heißt hier die Devise.
Am Ende ist das Mangement gut versorgt und die Shareholder
gucken in die Röhre!
Kaufen ist wohl kaum die richtige Bezeichnung für den Schluck aus der Pulle die sich hier
das Management einverleibt.
Schön in die eigene Tasche arbeiten heißt hier die Devise.
Am Ende ist das Mangement gut versorgt und die Shareholder
gucken in die Röhre!
Mit der Antragstellung an die FDA hat Palatin 20 Mill $ erhalten. Wenn Brem. zugelassen wird,
wandern weitere 60 Mill. von AMAG an Palatin. Damit werden weitere KE s nicht mehr nötig.
Als Kursbremse sind neben den vielen vergütungs Optionen auch noch sehr viele Warrants im Umlauf.
Nach der Sommerpause werden neue Impulse kommen. Neben weiteren positiven News
werden auch viele umschichten und Stokpiking betreiben. Die Chancen bei Palatin sind nach wie
vor enorm. 500 bis 600% in 2 Jahren sind realistisch. Wer mehr Zeit hat noch mehr.
Richtig ab geht es erst nach der Zulassung, wenn Brem. zugelassen ist und dann beworben wird.
Die anderen Produkte sind dabei noch gar nicht im Blick.
wandern weitere 60 Mill. von AMAG an Palatin. Damit werden weitere KE s nicht mehr nötig.
Als Kursbremse sind neben den vielen vergütungs Optionen auch noch sehr viele Warrants im Umlauf.
Nach der Sommerpause werden neue Impulse kommen. Neben weiteren positiven News
werden auch viele umschichten und Stokpiking betreiben. Die Chancen bei Palatin sind nach wie
vor enorm. 500 bis 600% in 2 Jahren sind realistisch. Wer mehr Zeit hat noch mehr.
Richtig ab geht es erst nach der Zulassung, wenn Brem. zugelassen ist und dann beworben wird.
Die anderen Produkte sind dabei noch gar nicht im Blick.
Antwort auf Beitrag Nr.: 58.167.854 von apano am 09.07.18 11:10:39Sehe es genauso... das Pferdchen hat die Scheuklappen auf, aber steht noch in der Boxengasse. Sobald das Gitter aufgeht wirds schon rennen!
Tote Hose hier. Keine news?
Antwort auf Beitrag Nr.: 58.288.157 von Schlotz68 am 24.07.18 14:09:28Gibt es für die Zulassung von Brem ein Zeitpunkt bzw Zeitkorridor ?
Antwort auf Beitrag Nr.: 58.335.411 von speedlimiter am 30.07.18 18:35:21
ca. März 2019
Zitat von speedlimiter: Gibt es für die Zulassung von Brem ein Zeitpunkt bzw Zeitkorridor ?
ca. März 2019
Antwort auf Beitrag Nr.: 58.335.465 von luxanleger am 30.07.18 18:41:06ok danke
Wenn ich mich recht erinnere, sollten im 2 HJ noch Verpartnerungen kommen.
Das könnte im Herbst schon zu Kurssteigerungen kommen.
Ansonsten sind wir 9 Monate guter Hoffnung.
Das könnte im Herbst schon zu Kurssteigerungen kommen.
Ansonsten sind wir 9 Monate guter Hoffnung.
Hallo zusammen,
Mitte September gibt es ja die Zahlen für das aktuelle Geschäftsjahr. Was kann man da erwarten? Werden die positive Auswirkung auf den Kurs haben?
Mitte September gibt es ja die Zahlen für das aktuelle Geschäftsjahr. Was kann man da erwarten? Werden die positive Auswirkung auf den Kurs haben?
Tja bedauerlich das Black Rock so einen hohen Anteil hier hält .................
Amount Position Size
($ in 1000's) As of
BlackRock Inc. 10,669,330 $10,348 06/30/2018
Amount Position Size
($ in 1000's) As of
BlackRock Inc. 10,669,330 $10,348 06/30/2018
die Hoffnung stirbt zuletzt....
Antwort auf Beitrag Nr.: 58.445.008 von TORSTEN65 am 14.08.18 16:37:38Hab doch einfach mal etwas Geduld.
Alles mit Ansage. 2HJ 2018 Verpartnerung, Q1 2019 Zulassung durch FDA.
Das Kurziel 6$ einige Analysten sehen Palatin langfirstig bei 20$.
Alles mit Ansage. 2HJ 2018 Verpartnerung, Q1 2019 Zulassung durch FDA.
Das Kurziel 6$ einige Analysten sehen Palatin langfirstig bei 20$.
ich habe auch jede Menge Geduld.irgendwann geht es hoch.ich wollte nur damit sagen,dass man auf prognosen von einigen Leuten nicht viel geben sollte.Man sollte mal runterscrollen und nachschauen wie wichtig sich hier einige gema ht haben mit ihren Kommentaren.da wurden Zahlen für juni/juli von 1,50 -2,00 € einfach mal so in den Raum geworfen.ich sehe es auch so,dass es in Zukunft aufwätts geht.Nur in welchem Maße kann niemand vorhersehen.
Antwort auf Beitrag Nr.: 58.448.593 von TORSTEN65 am 14.08.18 23:11:57Wieviel Geduld soll man den noch haben? Wann kommen denn endlich Fakten?
Antwort auf Beitrag Nr.: 58.472.329 von Portorico am 17.08.18 12:39:00
Wenn Sie allerdings noch ein paar Monate die Füße still halten können, weil Sie Ihren Einsatz gerade nicht benötigen, dann dürfen Sie gern nochmal Ihren heutigen Beitrag nachlesen. Vielleicht ja mit einem breiten Lächeln im Gesicht. Good luck trotzdem ;-)
PS: Ich bin hier investiert.
Also ...
... ich weiß ja nicht, wie lange Sie schon an der Börse aktiv sind aber der Zeitplan für Palatin ist überall nachzulesen. Wenn Sie nur auf das "ganz schnelle Geld" gesetzt haben, dann war`s wohl die falsche Aktie oder einfach der falsche Zeitpunkt, denn hier ging schon zwischenzeitlich gut die Post ab.Wenn Sie allerdings noch ein paar Monate die Füße still halten können, weil Sie Ihren Einsatz gerade nicht benötigen, dann dürfen Sie gern nochmal Ihren heutigen Beitrag nachlesen. Vielleicht ja mit einem breiten Lächeln im Gesicht. Good luck trotzdem ;-)
PS: Ich bin hier investiert.
Für Portrico https://m.nasdaq.com/de/symbol/ptn/real-time
https://seekingalpha.com/news/3383956-palatin-tech-files-100…
Erstmla geht es berg ab.
https://seekingalpha.com/news/3383956-palatin-tech-files-100…
Erstmla geht es berg ab.
Also die brauchen schon wieder Geld. Auch wenn das noch nicht die Kapitalerhöhung selbst ist. sie räumen sich das recht ein zu jeder Zeit neue Aktien usw. auszugeben. Natürlich verwässert das wieder den Kurs der Altaktionäre. Wenn man jetzt mal und rechnet. 100 Mios. räumen sie sich ein. Nehmen wir mal 1 Dollar als Angebot an und alles in Aktien. Dann wären das mal eben 100 Mio Aktien mehr. Bisher gibt es rund 200 Mio Aktien (sind eigentlich noch ein paar mehr). Das sind dann mal eben 50% mehr Aktien im worst case. Das wird dem Markt zu denken geben, auch wenn noch nichts passiert ist. aber ich gehe davon aus, das wir erstmal in den nächsten Tagen und Wochen Kurse sehen, die mindestens 30% unter dem sind von Freitag Schlusskurs. Also irgendwo im 60er US Cent Bereich und das sehe ich auch nur, wenn mal wieder was positives an Nachrichten kommt um dem verfall entgegenzusteuern.
Kann mich natürlich auch irren, aber aufwärts wird es jetzt sicher nicht mehr gehen in nächster Zeit. Alles nur mM. Keine Kauf oder Verkaufsemphelung.
Kann mich natürlich auch irren, aber aufwärts wird es jetzt sicher nicht mehr gehen in nächster Zeit. Alles nur mM. Keine Kauf oder Verkaufsemphelung.
Im Grunde ist es ja so. Ich kauf beim Bauern 10 Äpfel für einen vereinbarten Preis. Dann nimmt mir der Bauer wieder 5 raus nur weil er sie gepflückt hat. Wieso ist so was überhaupt zulässig???
Antwort auf Beitrag Nr.: 58.478.173 von meissner7309 am 18.08.18 08:45:40Also jetzt mal ganz ruhig.Das ist ja nur ein Vorratsbeschluss.Der letzte Vorratsbeschluss aus 2015 über 50 Mio. Stück wurde auch nicht genutzt. Ausserdem ist dürfen auch anleihen ohne Verwässerung oder Warrants ausgegeben werden. Die haben grad 20 Mio. Meilensteinzahlung von AMAG bekommen und bekommen im März 2019 voraussichtlich nochmal 60 Mio. Meilensteinzahlung. Wofür sollten die alsetzt Geld brauchen? Ich hab über L-S heute für 0.68 € nachgekauft und bin sicher,dass ich nächste Woche wenn sich die Panik gelegt hat im Plus bin.
Antwort auf Beitrag Nr.: 58.478.710 von Urbi am 18.08.18 10:54:17Das es nur ein Vorratsbeschluss ist, ist mir schon klar. Aber wenn Sie mit deinen angegebenen Meilensteinzahlungen rechnen, wozu dann dieser Beschluss? Wäre dann doch völlig überflüssig, wenn genug Geld da istund wenn es u.U. zu neuen Verpartnerschaftungen kommt mit entsprechenden Zahlungen. Aus Investor Relation Sicht ist so ein Beschluss vom Management eine Katastrophe. Wer beunruhigt die Börse und den eigenen Börsenkurs völlig unnötig? Klar kann es sein, dass nicht alles ausgeschöpft wird davon, aber ohne Grund wird so etwas nicht gemacht. Von daher ist das schon mit Vorsicht zu genießen.
Neben der Unsicherheit wird auch das Chartbild versaut mit solchen Aktionen. Also selbst wenn sich die Panik schnell wieder beruhigen sollte, so ist der Trend vorerst negativ. Und das die Firma insgesamt nicht gerade gut arbeitet zeigt doch der Langzeitchart.
Ich denke sie versuchen mit der Hoffnung, die im Moment mit der Zulassung von der FDA Kapital an Land zukriegen, um ein finanzielles Polster zu haben. Wenn Sie die Zulassung erhalten, um zu vermarkten oder in neue Forschung zu setzen und wenn nicht, dann um zu überleben bis u.U. was neues spruchreif wird. Außerdem will das Management doch auch, das ihr Gehalt pünktlich ausgezahlt wird.
Neben der Unsicherheit wird auch das Chartbild versaut mit solchen Aktionen. Also selbst wenn sich die Panik schnell wieder beruhigen sollte, so ist der Trend vorerst negativ. Und das die Firma insgesamt nicht gerade gut arbeitet zeigt doch der Langzeitchart.
Ich denke sie versuchen mit der Hoffnung, die im Moment mit der Zulassung von der FDA Kapital an Land zukriegen, um ein finanzielles Polster zu haben. Wenn Sie die Zulassung erhalten, um zu vermarkten oder in neue Forschung zu setzen und wenn nicht, dann um zu überleben bis u.U. was neues spruchreif wird. Außerdem will das Management doch auch, das ihr Gehalt pünktlich ausgezahlt wird.
Ich halte schon seit 3 1/2 Monate keine PTN Aktien mehr,
mit Geduld kann man die Aktien bei ca. USD 0,75 wieder zurück kaufen.
Das open Gap vom 3.11.17 $0,74 - 6.11.17 $0,7619 wird auch geschlossen.
mit Geduld kann man die Aktien bei ca. USD 0,75 wieder zurück kaufen.
Das open Gap vom 3.11.17 $0,74 - 6.11.17 $0,7619 wird auch geschlossen.
Stockinvest Signals:
A sales signal was issued from a pivot top point on Thursday August 16, 2018, which indicates further falls until a new bottom pivot has been found. Palatin Technologies Inc gained volume on the last day, but on falling prices. In technical terms this is called divergence and may be an early warning. In some cases, increasing volume on falling prices may be considered positive, but that is mainly in typical "sell-off's".
MarketWatch Short interest 18.72M 31.7.18
A sales signal was issued from a pivot top point on Thursday August 16, 2018, which indicates further falls until a new bottom pivot has been found. Palatin Technologies Inc gained volume on the last day, but on falling prices. In technical terms this is called divergence and may be an early warning. In some cases, increasing volume on falling prices may be considered positive, but that is mainly in typical "sell-off's".
MarketWatch Short interest 18.72M 31.7.18
wochenend lektüre 17. August 2018 16:09 EDT
https://www.streetinsider.com/SEC+Filings/Form++S-3++++++++P…übersetzt
https://translate.google.de/translate?sl=en&tl=de&js=y&prev=…
Ein Statement oder Erklärung seitens des Managements wäre wichtig. Wofür brauchen Sie das Geld oder was in welchem Umfang planen sie. Es gibt m. E. zwei Szenarien.
1.) Das Management glaubt nicht oder bezweifelt die Zulassung bei der FDA. In diesem Fall würde die Aktie im freien Fall runter gehen. Wenn hier also für diesen Fall die Kriegskasse gefüllt werden soll, dann müsste man Platzierungen egal in welcher Art vor der Entscheidung der FDA vornehmen, weil danach kein Mensch mehr in das Unternehmen investieren wird.
2.) Das Management ist überzeugt von der Zulassung, was gleichbedeutend ist mit einem erheblichen Kurssprung und viel Vertrauensbonus. In dem Fall kann man die Gunst der Stunde nutzen und kurz danach Platzierungen zu einem hohen Preis vornehmen. Was man mit dem Geld dann macht (Marketing, neue Forschung anderer Mittel usw.) steht auf einem anderen Blatt.
Es ist also spannend. Wenn man aber langfristig sich das Unternehmen ansieht muss man wohl eher vom Negativen ausgehen. Zumindest wird ohne Kommentar vom Management das so vom Markt aufgenommen werden. Und schließlich ist der Kurs der Aktie nur durch extrem hohes Pushen im letzten Jahr so gestiegen. Das sieht jetzt anders aus.
1.) Das Management glaubt nicht oder bezweifelt die Zulassung bei der FDA. In diesem Fall würde die Aktie im freien Fall runter gehen. Wenn hier also für diesen Fall die Kriegskasse gefüllt werden soll, dann müsste man Platzierungen egal in welcher Art vor der Entscheidung der FDA vornehmen, weil danach kein Mensch mehr in das Unternehmen investieren wird.
2.) Das Management ist überzeugt von der Zulassung, was gleichbedeutend ist mit einem erheblichen Kurssprung und viel Vertrauensbonus. In dem Fall kann man die Gunst der Stunde nutzen und kurz danach Platzierungen zu einem hohen Preis vornehmen. Was man mit dem Geld dann macht (Marketing, neue Forschung anderer Mittel usw.) steht auf einem anderen Blatt.
Es ist also spannend. Wenn man aber langfristig sich das Unternehmen ansieht muss man wohl eher vom Negativen ausgehen. Zumindest wird ohne Kommentar vom Management das so vom Markt aufgenommen werden. Und schließlich ist der Kurs der Aktie nur durch extrem hohes Pushen im letzten Jahr so gestiegen. Das sieht jetzt anders aus.
Antwort auf Beitrag Nr.: 58.479.967 von meissner7309 am 18.08.18 16:19:33Anhand der Short interest ahnten die Profis die negativ Meldung
dass war auch der Grund warum die Hürde von $1 nicht mehr Signifikat
überschritten wurde .
Da zu kommt noch eine weitere Verwässerung der Marktkapitalisierung,
PTN hat jetzt schon ein Market Cap von $197.79M,
ist natürlich negative für weiter steigende Kurse .
Meine Frage für welche Projekte brauchen sie das Kapital?
dass war auch der Grund warum die Hürde von $1 nicht mehr Signifikat
überschritten wurde .
Da zu kommt noch eine weitere Verwässerung der Marktkapitalisierung,
PTN hat jetzt schon ein Market Cap von $197.79M,
ist natürlich negative für weiter steigende Kurse .
Meine Frage für welche Projekte brauchen sie das Kapital?
Antwort auf Beitrag Nr.: 58.480.048 von fypet am 18.08.18 16:42:56Also im Vergleich zu anderen Unternehmen aus dieser Branche waren die Short Interest zumindest nach w.o. eher sehr niedrig. Das der Kurs nicht mehr über 1 Dollarcgekommen ist liegt m. E. daran, das die Aktie hier nicht mehr gepusht wird. Aber die Frage, die du aufgeworfen hast ist mit meiner identisch. Wenn frisches Kapital, dann wann, mit welcher Azsstattung, zu welchem Preis uns Umfang und das wichtigste: Wofür
Antwort auf Beitrag Nr.: 58.480.048 von fypet am 18.08.18 16:42:56Auf Stocktwits wurde eine E-Mail-Antwort des CFO von Palatin, Steve Wills, gepostet, in der er erklärt, dass das SEC-Filing eine Standard Best-practice-Lösung ist, um für alle Eventualitäten vorbereitet zu sein. Das bisherige Filing aus 2015 ist 8/2018 abgelaufen und wurde nun mit dem neuen Standard-Betrag 100 Mio. erneuert. Das bisherige Filing über 50 Mio. wurde nicht genutzt. Es ist auch nicht geplant, dass neue Filing zu nutzen. Das ist quasi nur eine Art Versicherung, wenn die Dinge nicht nach Plan laufen. Das ist Standard bei den Biotechfirmen. Großanleger dürften daher nicht beunruhigt sein und bei Kursen unter 0,80$ kräftig aufstocken.
Ich persönlich rechne mit der Bekanntgabe des nächsten Lizenzdeals bis spätestens 30.09.2018, da Palatin die letzten Quartale immer darauf geachtet hat, dass in jedem Quartal Umsatzerlöse erzielt werden. Nachdem die 20 Mio. Meilensteinzahlung im Quartal April-Juni 2018 vereinnahmt wurde, wird sicherlich die nächsten Upfrontzahlung eines Lizenzdeals für das Quartal Juli-September 2018 eingeplant sein. Im Herbst 2018 hieß es ja noch seitens Palatin das im 1. Hj. 2018 ein weiterer Lizenzdeal kommt.
Ich persönlich rechne mit der Bekanntgabe des nächsten Lizenzdeals bis spätestens 30.09.2018, da Palatin die letzten Quartale immer darauf geachtet hat, dass in jedem Quartal Umsatzerlöse erzielt werden. Nachdem die 20 Mio. Meilensteinzahlung im Quartal April-Juni 2018 vereinnahmt wurde, wird sicherlich die nächsten Upfrontzahlung eines Lizenzdeals für das Quartal Juli-September 2018 eingeplant sein. Im Herbst 2018 hieß es ja noch seitens Palatin das im 1. Hj. 2018 ein weiterer Lizenzdeal kommt.
Antwort auf Beitrag Nr.: 58.482.259 von Urbi am 19.08.18 09:57:09Sorry Herbst 2017 muss es heißen, nicht 2018
Ui, was ist denn hier passiert? Warum ist denn die Aktie so abgestürzt 🙄
So jetzt sind wir gleich wieder da wo wir am Freitag auch standen, bei 0,95 USD. Anscheinend habe es jetzt doch alle mal gemerkt, dass keine KE angekündigt wurde.
AMAG Pharmaceuticals: Ein gut positionierter Spieler im Pharmabereich
https://static.seekingalpha.com/uploads/2018/8/20/48913522-1…https://seekingalpha.com/article/4202214-amag-pharmaceutical…
auszug
Das neue Produkt - Bremelanotide - hat eine bedeutende Marktchance, da es das einzige Medikament ist, das Heilung bei niedrigem Verlangen oder Libido mit damit verbundenem Leiden bei Frauen bietet. Die Ergebnisse in Phase III sind sehr positiv und zeigen eine signifikante Verbesserung für Frauen mit niedrigem Sexualtrieb: In der ersten Studie betrug die Veränderung des weiblichen Sexualfunktionsindex (FSFI) 0,24 in der Placebogruppe, während sie im Drogenarm bei 0,54 lag . In der zweiten Studie zeigte die Placebo-Gruppe eine Verbesserung der FSFI-Werte um 0,21, verglichen mit einer Verbesserung von 0,63 in der Studienmedikation. Das Unternehmen geht davon aus, im nächsten Jahr die Zulassung für Bremelanotide erhalten zu können.
Obwohl es ein anderes Medikament gibt, das mit dem Problem des niedrigen Verlangens bei Frauen, Addyi, zu tun hat, zeigt dieses Medikament nur sehr wenig bis keine Besserung für Frauen, die Probleme mit niedrigem Sexualtrieb haben. Da Addyi dieses Problem nicht lösen kann, wird die Markteinführung von Bremelanotide sehr vielversprechend sein, um eine wirklich effektive Lösung für diesen Bereich mit hohem unerfülltem Bedarf bereitzustellen und ein Blockbuster für AMAG zu werden. (Quelle: Palatin Technologies; New York Times)
Das neue Produkt - Bremelanotide - hat eine bedeutende Marktchance, da es das einzige Medikament ist, das Heilung bei niedrigem Verlangen oder Libido mit damit verbundenem Leiden bei Frauen bietet. Die Ergebnisse in Phase III sind sehr positiv und zeigen eine signifikante Verbesserung für Frauen mit niedrigem Sexualtrieb: In der ersten Studie betrug die Veränderung des weiblichen Sexualfunktionsindex (FSFI) 0,24 in der Placebogruppe, während sie im Drogenarm bei 0,54 lag . In der zweiten Studie zeigte die Placebo-Gruppe eine Verbesserung der FSFI-Werte um 0,21, verglichen mit einer Verbesserung von 0,63 in der Studienmedikation. Das Unternehmen geht davon aus, im nächsten Jahr die Zulassung für Bremelanotide erhalten zu können.
Obwohl es ein anderes Medikament gibt, das mit dem Problem des niedrigen Verlangens bei Frauen, Addyi, zu tun hat, zeigt dieses Medikament nur sehr wenig bis keine Besserung für Frauen, die Probleme mit niedrigem Sexualtrieb haben. Da Addyi dieses Problem nicht lösen kann, wird die Markteinführung von Bremelanotide sehr vielversprechend sein, um eine wirklich effektive Lösung für diesen Bereich mit hohem unerfülltem Bedarf bereitzustellen und ein Blockbuster für AMAG zu werden. (Quelle: Palatin Technologies; New York Times)
Antwort auf Beitrag Nr.: 58.542.791 von onkelen am 27.08.18 15:02:36PTN ist Bereit, kurzfristig für hohe Kursgewinne zu bescheren, wichtiger Widerstand $0,98 zu nehmen, resist. $1,06 - $1,10 usw.
Ende September kommen von Palatin Zahlen zu Q 2 und es wird ein Ausblick auf den weiteren Geschäftsverlauf geben.
Vielleicht gibt es schon Resultate zur Studie vom Herzmedikament und News zu Verpartnerungen.
Beides könnte den Kurs wieder über den Euro bevördern.
Vielleicht gibt es schon Resultate zur Studie vom Herzmedikament und News zu Verpartnerungen.
Beides könnte den Kurs wieder über den Euro bevördern.
1,10$ im Moment.
Dürtfe es mit der mehrmonatigen Korrektur gewesen sein. Auch charttechnisch schaut’s wieder besser aus (3-Monats-Hoch).
Dann lasst die Spiele beginnen
Dürtfe es mit der mehrmonatigen Korrektur gewesen sein. Auch charttechnisch schaut’s wieder besser aus (3-Monats-Hoch).
Dann lasst die Spiele beginnen

Antwort auf Beitrag Nr.: 58.664.868 von Stoxtrayder am 10.09.18 21:46:14Am 13. September gibt es den Jahresabschluss incl. Update zu den Entwicklungsprojekten. Bin gespannt.
https://www.irdirect.net/prviewer/release/id/3295995
https://www.irdirect.net/prviewer/release/id/3295995
Die Euphorie vor den Zahlen scheint ja dahin geflogen zu sein.
Was ist wenn die jetzt verkünden , das man die Aktie endlich sicher
über 1$ platzieren möchte und einen 1:2 Reversesplitt vollzieht?
Es sind ja gewisse Bedingungen einzuhalten um gelistet zu bleiben.
Bei der Bude ist einfach alles möglich.
Und am besten können die Shares an den Mann bringen
der dann nachher die Zeche zahlt .
Bevor das hier richtig hochgeht ist die Masse eh rausgedrückt worden!
Was ist wenn die jetzt verkünden , das man die Aktie endlich sicher
über 1$ platzieren möchte und einen 1:2 Reversesplitt vollzieht?
Es sind ja gewisse Bedingungen einzuhalten um gelistet zu bleiben.
Bei der Bude ist einfach alles möglich.
Und am besten können die Shares an den Mann bringen
der dann nachher die Zeche zahlt .
Bevor das hier richtig hochgeht ist die Masse eh rausgedrückt worden!
Antwort auf Beitrag Nr.: 58.681.455 von Moneymaker123 am 12.09.18 15:05:26Mal nicht so negativ. Ein reverse split kann erstens nicht einfach mit den Quartalszahlen verkündet werden. Dazu braucht es schon einen Beschluss der Hauptversammlung. Zweitens ist ein reverse split doch zunächst mal völlig neutral für den Aktionär, solange er nicht mit einer Kapitalerhöhung verbunden ist und dazu gibt es meiner Meinung nach derzeit keinen Bedarf.
Die Kursentwicklung des letzten Jahres kann sich sehen lassen und es wurde regelmäßig geliefert (Verpartnerungen & Zulassungsantrag). Da gibt es ganz andere Kandidaten.
Die Kursentwicklung des letzten Jahres kann sich sehen lassen und es wurde regelmäßig geliefert (Verpartnerungen & Zulassungsantrag). Da gibt es ganz andere Kandidaten.
Antwort auf Beitrag Nr.: 58.688.562 von deRendite am 13.09.18 10:02:16Sehe das auch positiv. Ein Reverse Split hat auch Vorteile.
Zu wann heute unserer Zeit ist denn mit den Zahlen zu rechnen ?
Antwort auf Beitrag Nr.: 58.688.772 von Moneymaker123 am 13.09.18 10:24:04Vor Öffnung der US Finanzmärkte. Siehe hier:
https://www.irdirect.net/prviewer/release/id/3295995
Conference call 11 a.m. ET (dürfte 17 Uhr MESZ sein):
https://www.palatin.com/investors/webcasts/
https://www.irdirect.net/prviewer/release/id/3295995
Conference call 11 a.m. ET (dürfte 17 Uhr MESZ sein):
https://www.palatin.com/investors/webcasts/
Deutsche Übersetzung!
CRANBURY, New Jersey, 7. September 2018 / PRNewswire / - Palatin Technologies, Inc. (NYSE: PTN) wird am Donnerstag, den 13. September 2018, die Ergebnisse des vierten Quartals und des Geschäftsjahres 2018 vor der Eröffnung der USA veröffentlichen Finanzmärkte.Palatin wird außerdem am 13. September 2018 um 11:00 Uhr ET eine Telefonkonferenz und einen Live-Audio-Webcast abhalten, der vom Executive Management Team geleitet wird. Die Telefonkonferenz wird eine Überprüfung der Betriebsergebnisse des Unternehmens und ein Update der in Entwicklung befindlichen Programme beinhalten.
Zeitplan für die Betriebsergebnisse Pressemitteilung, Telefonkonferenz / Audio Webcast
Q4 und Geschäftsjahr Ende 2018 Finanzielle Ergebnisse Pressemitteilung
9/13/2018 um 7:30 Uhr ET
Q4 und Geschäftsjahr Ende 2018 Telefonkonferenz-Live
9/13/2018 um 11:00 Uhr ET
USA / Kanada Einwahlnummer:
1-855-719-5012
Internationale Einwahlnummer:
1-334-323-0522
Konferenz-ID:
5577225
Q4 und Geschäftsjahr 2018 Conference Call-Replay
9/13 / 2018-9 / 20/2018
USA / Kanada Einwahlnummer:
1-888-203-1112
Internationale Einwahlnummer:
1-719-457-0820
Passcode wiederholen:
5577225
Audio Webcast Live- und Wiedergabezugriff
http://www.palatin.com
Der Audio-Webcast und die Wiedergabe können über den Bereich "Investors-Webcasts" auf der Website von Palatin unter http://www.palatin.com abgerufen werden.
Über Palatin Technologies, Inc.
Palatin Technologies, Inc. ist ein biopharmazeutisches Unternehmen, das zielgerichtete, rezeptorspezifische Peptid-Therapeutika für die Behandlung von Krankheiten mit hohem medizinischem Bedarf und kommerziellem Potenzial entwickelt. Die Strategie von Palatin besteht darin, Produkte zu entwickeln und dann Marketing-Kooperationen mit Branchenführern zu bilden, um ihr kommerzielles Potenzial zu maximieren. Weitere Informationen finden Sie unter http://www.palatin.com.
QUELLE Palatin Technologies, Inc.
verwandte Links
http://www.palatin.com
https://seekingalpha.com/pr/17268826-palatin-technologies-in…
https://www.irdirect.net/prviewer/release/id/3305043
https://www.earningswhispers.com/epsdetails/ptn
Fourth Quarter and Fiscal 2018 Financial Results
Palatin reported net income of $11.8 million, or $0.06 per basic and diluted share, for the fourth quarter ended June 30, 2018, compared to net income of $13.3 million, or $0.07 per basic and diluted share, for the same period in 2017.
The difference between the three months ended June 30, 2018 and 2017 was primarily attributable to the recognition of contract revenue pursuant to our license agreement with AMAG of $20.6 million for the quarter ended June 30, 2018 compared to $33.9 million in 2017.
For the fiscal year ended June 30, 2018, Palatin reported net income of $24.7 million, or $0.12 per basic and diluted share compared to a net loss of $(13.3) million, or $(0.07) per basic and diluted share for the year ended June 30, 2017.
The difference in net income for the year ended June 30, 2018, and the net loss for the year ended June 30, 2017, was primarily attributable to the recognition of $67.1 million in license and contract revenue for the year ended June 30, 2018 compared to $44.7 million for the year ended June 30, 2017, and secondarily to a $14.1 million decrease in operating expenses to $41.2 million for the year ended June 30, 2018 compared to $55.3 million for the year ended June 30, 2017.
https://www.irdirect.net/prviewer/release/id/3305043
https://www.earningswhispers.com/epsdetails/ptn
Fourth Quarter and Fiscal 2018 Financial Results
Palatin reported net income of $11.8 million, or $0.06 per basic and diluted share, for the fourth quarter ended June 30, 2018, compared to net income of $13.3 million, or $0.07 per basic and diluted share, for the same period in 2017.
The difference between the three months ended June 30, 2018 and 2017 was primarily attributable to the recognition of contract revenue pursuant to our license agreement with AMAG of $20.6 million for the quarter ended June 30, 2018 compared to $33.9 million in 2017.
For the fiscal year ended June 30, 2018, Palatin reported net income of $24.7 million, or $0.12 per basic and diluted share compared to a net loss of $(13.3) million, or $(0.07) per basic and diluted share for the year ended June 30, 2017.
The difference in net income for the year ended June 30, 2018, and the net loss for the year ended June 30, 2017, was primarily attributable to the recognition of $67.1 million in license and contract revenue for the year ended June 30, 2018 compared to $44.7 million for the year ended June 30, 2017, and secondarily to a $14.1 million decrease in operating expenses to $41.2 million for the year ended June 30, 2018 compared to $55.3 million for the year ended June 30, 2017.
Der Bericht hört sich besser an als das was der Kurs soeben macht!





Antwort auf Beitrag Nr.: 58.691.385 von Moneymaker123 am 13.09.18 14:51:34Bisher gings nach Vorlage der Quartalszahlen halt immer runter. Vermute bis zur Telefonkonferenz um 17 Uhr unserer Zeit wird der Kurs auf Vortagesniveau bleiben. Dann kommt darauf an, ob was zu potentiellen Lizenzdeals gesagt wird und wann die kommen sollen. Seit einem Jahr wurde ja darauf geachtet, dass in jedem Quartal Umsatzerlöse generiert wurden, dh. nach dieser These müsste noch im September ein Lizenzdeal kommen. Außerdem stehen ja noch Phase1-Daten zu PL 8177 aus. Lt. Benzinga.com sollten diese in der laufenden Woche kommen (keine Ahnung wie belastbar deren Angaben sind). Es könnte also auch sein, dass dieses Mal der Kurs einfach auf dem derzeitigen Niveau verharrt, es ging ja auch kein starker Anstieg mit großem Volumen voraus.
Ausgaben halbiert, Schulden halbiert, Kasse gut gefüllt.Klingt doch ganz passabel
Antwort auf Beitrag Nr.: 58.691.610 von boersenkeks am 13.09.18 15:11:24Wichtiger als die Zahlen ist hier doch der Ausblick.
Der Ausblick ist................. das man daran glaubt das alle Kosten bis 30.09 2019
gedeckelt sind.
Toll das man als wesentlich herausstellt seinen Arbeitsplatz für ein weiteres Jahr sicher
zu haben.
Als Shareholder interssiert mich mehr ob man Gewinne erzielen kann!
Die verbrennen ganz schön viel Kohle in einem Jahr.
Da ist so eine sogenannte Meilensteinzahlung mehr als notwendig um die Bude
m laufen zu halten .
Ichkann mir ncht vorstellen das das Interview neue Impulse setzt
Dann hätte man da auch etwas im Bericht dazu erwähnt
gedeckelt sind.
Toll das man als wesentlich herausstellt seinen Arbeitsplatz für ein weiteres Jahr sicher
zu haben.
Als Shareholder interssiert mich mehr ob man Gewinne erzielen kann!
Die verbrennen ganz schön viel Kohle in einem Jahr.
Da ist so eine sogenannte Meilensteinzahlung mehr als notwendig um die Bude
m laufen zu halten .
Ichkann mir ncht vorstellen das das Interview neue Impulse setzt
Dann hätte man da auch etwas im Bericht dazu erwähnt
Wow........................diese Millionen Postings und Umsätze von heute ..........trotz
Meilenstein Interview zeigen ganz deutlich auf in welche Richtung es hier geht.
Gen Süden!
Prost Mahlzeit.
Was ist ds ein jämmerlicher Haufen....... obwohl eigentlich gut gemacht!
Viel Wertloses Papier an "gläubige" verkauft und der Rubel rollt.
Der GF von Palatin ist bstimmt fü sein Leben saniert!
Meilenstein Interview zeigen ganz deutlich auf in welche Richtung es hier geht.
Gen Süden!
Prost Mahlzeit.
Was ist ds ein jämmerlicher Haufen....... obwohl eigentlich gut gemacht!
Viel Wertloses Papier an "gläubige" verkauft und der Rubel rollt.
Der GF von Palatin ist bstimmt fü sein Leben saniert!
Aber eins ist auch sicher!
Viel von deren Shares werden die so nicht mehr an den Mann bekommen.
Welche Frau zweifelt schon an Ihrem Libido ?????????????
Das wäre so wenn ein Kaktus das Gefühl hätte das er zu wenig Stacheln hätte.
Viel von deren Shares werden die so nicht mehr an den Mann bekommen.
Welche Frau zweifelt schon an Ihrem Libido ?????????????
Das wäre so wenn ein Kaktus das Gefühl hätte das er zu wenig Stacheln hätte.
Antwort auf Beitrag Nr.: 58.695.642 von Moneymaker123 am 13.09.18 22:13:18Verstehe nicht was du dann hier machst, wenn du nicht an das Produkt glaubst. Niemand zwingt dich hier was zu posten oder was zu kaufen.
Man muss halt nicht alles im Leben verstehen.
Wenn ich hier mit meinen Posts irgendetwas bewege läuft sowieso etwas falsch!
Es wird nur Zeit das man Mechanismen aufbaut , dass so Buden wie diesehier die nur Shareholder Kapital verbrennen endlich von der Bildfäche verschwinden!

Wenn ich hier mit meinen Posts irgendetwas bewege läuft sowieso etwas falsch!

Es wird nur Zeit das man Mechanismen aufbaut , dass so Buden wie diesehier die nur Shareholder Kapital verbrennen endlich von der Bildfäche verschwinden!
Antwort auf Beitrag Nr.: 58.695.732 von Moneymaker123 am 13.09.18 22:23:58Also Money Moneyu hier was bewegst glaubt auch keiner. Aber rein inhaltlich sind deine Posts dermaßen schlecht, das man sich die lieber sparen sollte.
So,so also wird hier gel verbrannt. Kurs vor einem Jahr bei ca. 50 Cent, heute 88 Cent. Geld verbrannt für den Anleger?
Eine Frau zweifelt nicht an ihrer Libido? Klingt für mich für einen Macho der der Meinung ist, eine Frau muss immer Lust haben und wenn der Mann brünstig ist, dann funktioniert sie auch. Hoffe du behandelst deine Frau besser als das was du über Frauen schreibst. Nur weil eine Frau keinen Penis hat, der stehen muss heisst das doch nicht, das sie nicht darunter leiden kann, dass Sie keine Lust empfindet. Also die Mühe sich mal in die Gefühle einer Frau einzudecken oder mal darüber zu reden ist dir sicher bisher nicht in den Sinn gekommen. Das es zwischen 8 und 9 Milliarden Menschen gibt und die verschiedensten Kulturkreise in denen das Frauen wichtig sein könnte ist dir auch nicht in den Sinn kommen. Immer schön nur von der Tapete bis zur Wand denken.
Ich sage nicht, das das Unternehmen erfolgreich sein wird oder das Produkt schlechthin der Dauerbrenner. Aber man sollte bedenken. Erstens gibt es bereits solche Produkte am Markt, also gibt es eine Nachfrage und zweitens sind die Nebenwirkungen bei diesem Produkt wesentlich geringer. Also eine Möglichkeit besteht auf jedenfalls hiermit geld zu verdienen. Bevor man also reißerische Post absetzt mit hohlen Parolen, einfach mal informieren.
So,so also wird hier gel verbrannt. Kurs vor einem Jahr bei ca. 50 Cent, heute 88 Cent. Geld verbrannt für den Anleger?
Eine Frau zweifelt nicht an ihrer Libido? Klingt für mich für einen Macho der der Meinung ist, eine Frau muss immer Lust haben und wenn der Mann brünstig ist, dann funktioniert sie auch. Hoffe du behandelst deine Frau besser als das was du über Frauen schreibst. Nur weil eine Frau keinen Penis hat, der stehen muss heisst das doch nicht, das sie nicht darunter leiden kann, dass Sie keine Lust empfindet. Also die Mühe sich mal in die Gefühle einer Frau einzudecken oder mal darüber zu reden ist dir sicher bisher nicht in den Sinn gekommen. Das es zwischen 8 und 9 Milliarden Menschen gibt und die verschiedensten Kulturkreise in denen das Frauen wichtig sein könnte ist dir auch nicht in den Sinn kommen. Immer schön nur von der Tapete bis zur Wand denken.
Ich sage nicht, das das Unternehmen erfolgreich sein wird oder das Produkt schlechthin der Dauerbrenner. Aber man sollte bedenken. Erstens gibt es bereits solche Produkte am Markt, also gibt es eine Nachfrage und zweitens sind die Nebenwirkungen bei diesem Produkt wesentlich geringer. Also eine Möglichkeit besteht auf jedenfalls hiermit geld zu verdienen. Bevor man also reißerische Post absetzt mit hohlen Parolen, einfach mal informieren.
Wurde gestern etwas zu Europa Deal gesagt? Hat jemand was mitbekommen?
Catie Powers - 13. September 2018, 12:32 Uhr EDT
Der Analyst von HC Wainwright, Joseph Pantginis, wiederholte heute ein Kauf- Rating von Palatin Technologies (NYSE: PTN ) und legte ein Kursziel von 5 USD fest . Die Aktien des Unternehmens eröffneten heute bei 1,06 $.
Panthinis kommentierte:
"Unsere These über Aktien bleibt unverändert; Große Kästen überprüft und Bewertung Disconnection existiert, in unserer Überzeugung. Bedeutende Boxen sind bereits abgehakt, was unserer Meinung nach eine verpasste Chance für Investoren darstellt. "
Laut TipRanks.com besteht das Ranking von Pantginis derzeit aus keinen Sternen auf einer 0-5-Rangliste mit einer durchschnittlichen Rendite von -9,1% und einer Erfolgsquote von 34,3%. Pantginis deckt den Gesundheitssektor ab und konzentriert sich auf Aktien wie SELLAS Life Sciences Group Inc., Applied Genetic Technologies und Iovance Biotherapeutics Inc.
Momentan ist der Konsens der Analysten über Palatin Technologies ein moderater Kauf mit einem durchschnittlichen Kursziel von 4 USD.
Basierend auf der jüngsten Veröffentlichung von Palatin Technologies für das Quartal zum 31. März berichtete das Unternehmen einen Quartalsfehlbetrag von 739,2 Tsd. US-Dollar. Im Vergleich dazu hatte das Unternehmen im letzten Jahr einen Nettogewinn von 13,32 Millionen Dollar.
Palatin Technologies, Inc. ist ein biopharmazeutisches Unternehmen, das zielgerichtete, rezeptorspezifische Peptidtherapeutika zur Behandlung von Krankheiten entwickelt. Es ist auf Moleküle spezialisiert, die die Aktivität der Melanocortin- und natriuretischen Peptid-Rezeptor-Systeme modulieren.
https://www.smarteranalyst.com/brief/h-c-wainwright-keeps-a-…
Der Analyst von HC Wainwright, Joseph Pantginis, wiederholte heute ein Kauf- Rating von Palatin Technologies (NYSE: PTN ) und legte ein Kursziel von 5 USD fest . Die Aktien des Unternehmens eröffneten heute bei 1,06 $.
Panthinis kommentierte:
"Unsere These über Aktien bleibt unverändert; Große Kästen überprüft und Bewertung Disconnection existiert, in unserer Überzeugung. Bedeutende Boxen sind bereits abgehakt, was unserer Meinung nach eine verpasste Chance für Investoren darstellt. "
Laut TipRanks.com besteht das Ranking von Pantginis derzeit aus keinen Sternen auf einer 0-5-Rangliste mit einer durchschnittlichen Rendite von -9,1% und einer Erfolgsquote von 34,3%. Pantginis deckt den Gesundheitssektor ab und konzentriert sich auf Aktien wie SELLAS Life Sciences Group Inc., Applied Genetic Technologies und Iovance Biotherapeutics Inc.
Momentan ist der Konsens der Analysten über Palatin Technologies ein moderater Kauf mit einem durchschnittlichen Kursziel von 4 USD.
Basierend auf der jüngsten Veröffentlichung von Palatin Technologies für das Quartal zum 31. März berichtete das Unternehmen einen Quartalsfehlbetrag von 739,2 Tsd. US-Dollar. Im Vergleich dazu hatte das Unternehmen im letzten Jahr einen Nettogewinn von 13,32 Millionen Dollar.
Palatin Technologies, Inc. ist ein biopharmazeutisches Unternehmen, das zielgerichtete, rezeptorspezifische Peptidtherapeutika zur Behandlung von Krankheiten entwickelt. Es ist auf Moleküle spezialisiert, die die Aktivität der Melanocortin- und natriuretischen Peptid-Rezeptor-Systeme modulieren.
https://www.smarteranalyst.com/brief/h-c-wainwright-keeps-a-…
Deutsche Übersetzung:
Palatin Technologies, Inc. gibt Ergebnisse für das vierte Quartal und das Geschäftsjahr 2018 bekanntDo 13. September 2018 7:30 Uhr | PR Newswire | Über: AMAG , PTN
PDUFA Target Action Datum vom 23. März 2019 für Vyleesi
Videokonferenz und Webcast am 13. September 2018
PR Newswire
CRANBURY, NJ , Sept. 13, 2018 / PRNewswire / - Palatin Technologies, Inc. (NYSE: PTN), ein spezialisiertes biopharmazeutisches Unternehmen, das erstklassige Medikamente auf der Basis von Molekülen entwickelt, die die Aktivität des Melanocortins und des natriuretischen Peptids modulieren Rezeptor-Systeme für die Behandlung von Krankheiten mit signifikantem medizinischen Bedarf und kommerziellem Potenzial, gab heute die Ergebnisse für das vierte Quartal und das Geschäftsjahr zum 30. Juni 2018 bekannt.
https://mma.prnewswire.com/media/464561/Palatin_Technologies…
"Das letzte Jahr war sehr produktiv für Palatin, vor allem die Akzeptanz des Vyleesi ™ (Bremelanotid) NDA durch die FDA", sagte Carl Spana , Ph.D., CEO und Präsident von Palatin. "Im ersten Quartal des Kalenderjahres 2019 könnte die FDA die Zulassung für Vylessi erhalten - ein bedeutender Meilenstein und wichtiger Wendepunkt für Palatin, seine Mitarbeiter, seine Aktionäre und vor allem Tausende von prämenopausalen Frauen, die in den USA eine Behandlung gegen HSDD anstreben "
2018 Höhepunkte und aktuelle Ereignisse
Vyleesi (Bremelanotid)
Vyleesi ™, der Handelsname für Bremelanotide - In Entwicklung für Hypoactive Sexual Desire Disorder ("HSDD"):
Im Juni 2018 wurde unser exklusiver nordamerikanischer Lizenznehmer für Vyleesi, AMAG Pharmaceuticals, Inc. ( AMAG ) ("AMAG"), von der US-amerikanischen Zulassungsbehörde FDA (Food and Drug Administration) für die Einreichung des Zulassungsantrags in Kenntnis gesetzt ("NDA") auf Vyleesi, mit einem FDA PDUFA (Verschreibungspflichtigen Medikamentengebührengesetz) Zieldatum für den Abschluss der FDA Überprüfung der NDA vom 23. März 2019.
Die Akzeptanz der FDA durch die FDA führte zu einer Meilensteinzahlung in Höhe von 20 Millionen US-Dollar an Palatin, abzüglich der von der AMAG gezahlten Kosten.
Palatin hat Anspruch auf bis zu 60 Millionen US-Dollar nach Genehmigung durch die FDA.
Bei Zulassung würde Vyleesi die erste und einzige on-demand pharmakologische Option sein, die für die Behandlung von HSDD bei prämenopausalen Frauen in den USA indiziert ist
Im September 2017 wurde eine Kooperation und eine Lizenzvereinbarung mit Shanghai Fosun Pharmaceutical Industrial Development Co. Ltd. ("Fosun"), einer Tochtergesellschaft von Shanghai Fosun Pharmaceutical (Group) Co., Ltd, für die exklusiven Rechte zur Entwicklung und Vermarktung von Vyleesi in den Gebieten geschlossen von Festland China , Taiwan , Hong Kong SAR und Macao SAR
Erhielt 4.500.000 $ im Oktober 2017, bestehend aus einer Vorauszahlung in Höhe von 5.000.000 $ abzüglich 500.000 $, die in Übereinstimmung mit den Steuereinbehaltspflichten in China einbehalten wurde.
Im November 2017 wurde eine Lizenzvereinbarung mit Kwangdong Pharmaceutical Co., Ltd. ("Kwangdong") geschlossen, um die exklusiven Rechte zur Entwicklung und Vermarktung von Vyleesi in der Republik Korea zu erhalten .
Erhielt im Dezember 2017 417.500 US-Dollar, bestehend aus einer Vorauszahlung in Höhe von 500.000 US-Dollar abzüglich 82.500 US-Dollar, die gemäß den Steuereinbehaltspflichten in der Republik Korea einbehalten wurde.
PL-8177 / PL-8331
Melanocortin-Rezeptor 1 (MC1r) Agonisten in der Entwicklung für die Behandlung von entzündlichen und Autoimmunerkrankungen wie Trockenes Auge, Uveitis, diabetische Retinopathie und entzündliche Darmerkrankungen:
Abgeschlossene subkutane Verabreichung von PL-8177 an Probanden in einer klinischen Studie zur klinischen Einzel- und Mehrfachdosis-Phase-1-Studie mit Daten, die im vierten Quartal des Kalenderjahres 2018 erwartet werden.
Mai 2018 - Präsentierte positive präklinische Daten zu PL-8331 auf dem Treffen von TIDES: Oligonucleotid and Peptide Therapeutics 2018.
April 2018 - Präklinische orale Formulierungsdaten zu PL-8177, einem in der Entwicklung befindlichen MC1r-Agonisten für chronisch entzündliche Darmerkrankungen bei den Keystone-Symposien 2018 über "Die Auflösung von Entzündungen bei Gesundheit und Krankheit".
Unternehmen
Verminderte Verschuldung von 14,8 Millionen US-Dollar zum 30. Juni 2017 auf 7,2 Millionen US-Dollar zum 30. Juni 2018.
Im Juni 2018 zum Russell 3000 ® Index hinzugefügt.
Erweckte das Portfolio des geistigen Eigentums des Unternehmens mit mehreren Anmeldungen und Ausgaben im Laufe des Jahres.
Finanzergebnisse für das vierte Quartal und das Geschäftsjahr 2018
Palatin meldete für das vierte Quartal, das am 30. Juni 2018 endete, einen Nettogewinn von 11,8 Millionen US-Dollar oder 0,06 US-Dollar pro Aktie, verglichen mit einem Nettogewinn von 13,3 Millionen US-Dollar oder 0,07 US-Dollar pro Aktie für den gleichen Zeitraum im Jahr 2017.
Der Unterschied zwischen den drei Monaten zum 30. Juni 2018 und 2017 war in erster Linie auf die Erfassung von Vertragserlösen gemäß unserer Lizenzvereinbarung mit AMAG in Höhe von 20,6 Millionen US-Dollar für das Quartal zum 30. Juni 2018 im Vergleich zu 33,9 Millionen US-Dollar im Jahr 2017 zurückzuführen.
Für das Geschäftsjahr, das am 30. Juni 2018 endete, meldete Palatin einen Nettogewinn von 24,7 Millionen US-Dollar oder 0,12 US-Dollar pro unverwässerter und verwässerter Aktie, verglichen mit einem Nettoverlust von (13,3) Millionen US-Dollar bzw. 0,07 US-Dollar pro Aktie endete am 30. Juni 2017.
Die Differenz zwischen dem Nettoergebnis für das Geschäftsjahr zum 30. Juni 2018 und dem Nettoverlust für das zum 30. Juni 2017 endende Geschäftsjahr war hauptsächlich auf den Ausweis von Lizenz- und Vertragserlösen in Höhe von 67,1 Mio. USD für das am 30. Juni 2018 abgeschlossene Geschäftsjahr zurückzuführen auf 44,7 Millionen US-Dollar für das zum 30. Juni 2017 endende Geschäftsjahr und in zweiter Linie auf einen Rückgang der Betriebsausgaben um 14,1 Millionen US-Dollar auf 41,2 Millionen US-Dollar für das zum 30. Juni 2018 endende Geschäftsjahr gegenüber 55,3 Millionen US-Dollar für das am 30. Juni 2017 endende Geschäftsjahr.
Einnahmen
Für das Quartal und das Geschäftsjahr zum 30. Juni 2018 verbuchte Palatin 20,6 Millionen US-Dollar bzw. 62,1 Millionen US-Dollar an Auftragserlösen im Zusammenhang mit unserer Lizenzvereinbarung mit AMAG und weitere 5 Millionen US-Dollar Lizenzerlöse für das am 30. Juni 2018 endende Geschäftsjahr Lizenzvertrag mit Fosun.
Für das Quartal und das Jahr, das am 30. Juni 2017 endete, verbuchte Palatin 33,9 Millionen US-Dollar bzw. 44,7 Millionen US-Dollar an Auftragserlösen im Zusammenhang mit unserer Lizenzvereinbarung mit der AMAG.
Betriebsaufwand
Die gesamten betrieblichen Aufwendungen für das am 30. Juni 2018 endende Quartal beliefen sich auf 8,3 Millionen US-Dollar im Vergleich zu 19,6 Millionen US-Dollar im Vergleichsquartal 2017. Für das am 30. Juni 2018 endende Geschäftsjahr verzeichnete Palatin Betriebsausgaben in Höhe von 41,2 Millionen US-Dollar im Vergleich zu 55,3 Millionen US-Dollar 30. Juni 2017
Der Rückgang der betrieblichen Aufwendungen ist hauptsächlich auf den Abschluss der klinischen Phase-3-Studien und weniger auf die weitere Entwicklung von Vyleesi für HSDD zurückzuführen.
Sonstige Erträge / Aufwendungen
Der gesamte übrige Aufwand, netto, betrug 0,2 Mio. USD für das Quartal, das am 30. Juni 2018 endete, verglichen mit 0,5 Mio. USD für das Quartal zum 30. Juni 2017. Für das Geschäftsjahr zum 30. Juni 2018 beliefen sich die sonstigen Aufwendungen, netto, auf 1,1 Mio. USD. im Vergleich zu 2,3 Mio. USD für das am 30. Juni 2017 endende Geschäftsjahr. Die sonstigen Aufwendungen, netto für die Geschäftsjahre zum 30. Juni 2018 und 30. Juni 2017, enthalten im Wesentlichen Zinsaufwendungen für Risikokapitalfinanzierungen.
Einkommenssteuer
Die Ertragssteueraufwendungen beliefen sich für das Quartal und das Geschäftsjahr zum 30. Juni 2018 auf 0,3 Mio. USD bzw. 0,1 Mio. USD, verglichen mit 0,5 Mio. USD als alternative Mindeststeuer für das Quartal und das Geschäftsjahr zum 30. Juni 2017.
Der Ertragssteueraufwand für das am 30. Juni 2018 endende Geschäftsjahr bezieht sich auf 0,6 Mio. US-Dollar Steuerrückstellungen im Zusammenhang mit unseren Fosun- und Kwangdong-Lizenzvereinbarungen, die im Geschäftsjahr zum 30. Juni 2018 als Aufwand erfasst wurden, zuzüglich eines Steuervorteils von 0,5 Mio. US-Dollar im Zusammenhang mit der Auflösung einer Wertberichtigung gegen die föderale alternative Mindeststeuergutschrift von Palatin infolge des im Dezember 2017 unterzeichneten Tax Cuts and Jobs Act. Dementsprechend sind zum 30. Juni 2018 0,5 Mio. USD in den sonstigen langfristigen Vermögenswerten enthalten.
Finanzielle Situation
Die Zahlungsmittel und Zahlungsmitteläquivalente von Palatin betrugen zum 30. Juni 2018 38,0 Millionen US-Dollar und zum 30. Juni 2018 keine Forderungen gegenüber Zahlungsmitteln, Zahlungsmitteläquivalenten und Investitionen von 40,5 Millionen US-Dollar und zum 30. Juni 2017 15,1 Millionen US-Dollar. Die kurzfristigen Verbindlichkeiten betrugen 10,8 Millionen US-Dollar 30, 2018, verglichen mit 19,9 Millionen US-Dollar nach Abzug der abgegrenzten Einnahmen von 35,1 Millionen US-Dollar zum 30. Juni 2017.
Palatin ist der Ansicht, dass die vorhandenen Kapitalressourcen ausreichen werden, um unsere geplanten Aktivitäten bis mindestens 30. September 2019 zu finanzieren.
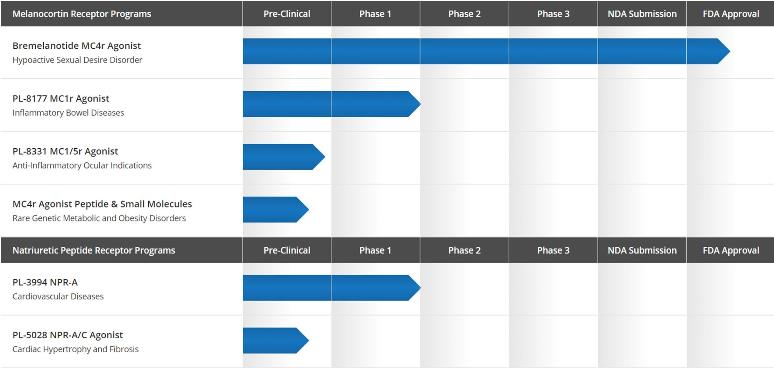
Palatin Drug Discovery Programme
In der Telefonkonferenz und im Webcast wird das Management die nächsten Schritte in Palatins Portfolio von Medikamentenentwicklungsprogrammen aktualisieren und diskutieren. Diese umfassen Palatins Melanocortinrezeptor1- und Rezeptor-5-Agonistenpeptide zur Behandlung von entzündlichen Indikationen und natriuretische Peptidrezeptoragonistenverbindungen zur Behandlung von kardiovaskulären und pulmonalen Indikationen.
Telefonkonferenz / Webcast
Palatin wird am 13. September 2018 um 11:00 Uhr Eastern Time eine Telefonkonferenz und einen Audio-Webcast veranstalten, um die Ergebnisse der Geschäftsaktivitäten ausführlicher zu diskutieren und aktuelle Informationen über Unternehmensentwicklungen zu liefern. Personen, die live an der Telefonkonferenz teilnehmen möchten, können unter 1-855-719-5012 ( USA / Kanada ) oder 1-334-323-0522 (international) mit der Konferenz-ID 5577225 wählen. Der Audio-Webcast und die Wiedergabe können durch Anmeldung aufgerufen werden zum Bereich "Investor / Webcasts" auf der Website von Palatin unter http://www.palatin.com . Eine Telefon- und Webcast-Wiedergabe wird ungefähr eine Stunde nach Beendigung des Anrufs verfügbar sein. Um auf die Telefonwiedergabe zuzugreifen, wählen Sie 1-888-203-1112 ( USA / Kanada ) oder 1-719-457-0820 (international), Passcode 5577225. Der Webcast und die Telefonwiedergabe sind bis zum 20. September 2018 verfügbar.
Über Palatin Technologies, Inc.
Palatin Technologies, Inc. ist ein spezialisiertes biopharmazeutisches Unternehmen, das erstklassige Medikamente auf der Basis von Molekülen entwickelt, die die Aktivität der Melanocortin- und natriuretischen Peptid-Rezeptor-Systeme modulieren, mit gezielten, rezeptorspezifischen Produktkandidaten für die Behandlung von Krankheiten mit erheblicher ungedeckter medizinischer Wirksamkeit Bedarf und kommerzielles Potenzial. Die Strategie von Palatin besteht darin, Produkte zu entwickeln und dann Marketing-Kooperationen mit Branchenführern zu bilden, um ihr kommerzielles Potenzial zu maximieren. Weitere Informationen zu Palatin finden Sie auf der Website von Palatin unter www.Palatin.com .
Vorausschauende Aussagen
Aussagen in dieser Pressemitteilung, die keine historischen Fakten sind, einschließlich Aussagen über zukünftige Erwartungen von Palatin Technologies, Inc., wie Aussagen über klinische Studienergebnisse, mögliche Maßnahmen von Aufsichtsbehörden einschließlich der FDA, Regulierungspläne, Entwicklungsprogramme, vorgeschlagene Indikationen für das Produkt Kandidaten und Marktpotenzial für Produktkandidaten sind "zukunftsgerichtete Aussagen" im Sinne von Abschnitt 27A des Securities Act von 1933, Section 21E des Securities Exchange Act von 1934 und wie dieser Begriff im Private Securities Litigation Reform Act definiert ist von 1995. Palatin beabsichtigt, dass solche zukunftsgerichteten Aussagen den dadurch geschaffenen sicheren Häfen unterliegen. Solche zukunftsgerichteten Aussagen beinhalten bekannte und unbekannte Risiken, Ungewissheiten und andere Faktoren, die dazu führen könnten, dass sich die tatsächlichen Ergebnisse von Palatin wesentlich von den historischen Ergebnissen oder den in solchen zukunftsgerichteten Aussagen ausgedrückten oder implizierten Ergebnissen unterscheiden. Die tatsächlichen Ergebnisse von Palatin können wesentlich von denen abweichen, die in den zukunftsgerichteten Aussagen aus Gründen wie unter anderem den Ergebnissen klinischer Studien, behördlichen Maßnahmen der FDA und der Notwendigkeit von behördlichen Genehmigungen, Palatins Fähigkeit, die Entwicklung seiner Technologie zu finanzieren, diskutiert werden Etablierung und erfolgreiche Durchführung klinischer Studien, Dauer und Kosten für die Durchführung klinischer Studien und Einreichung von Zulassungsanträgen, von konkurrierenden Pharma-, Biopharma- und Biotechnologieunternehmen entwickelte Produkte, kommerzielle Akzeptanz der Produkte von Palatin und andere in den periodischen Einreichungen von Palatin diskutierte Faktoren mit der Securities and Exchange Commission. Palatin ist nicht für die Aktualisierung von Ereignissen zuständig, die nach dem Datum dieser Pressemitteilung auftreten.
Vyleesi ™ ist eine Marke von AMAG Pharmaceuticals, Inc. in Nordamerika und von Palatin Technologies, Inc. in anderen Teilen der Welt.
(Abschlussdaten folgen)
PALATIN TECHNOLOGIEN, INC.
und Tochtergesellschaft
Konzern-Gewinn- und Verlustrechnung
Jahr endete am 30. Juni,
2018
2017
2016
ERLÖSE
Lizenz und Vertrag
$ 67,134,758
$ 44,723,827
$ -
BETRIEBSAUFWAND
Forschung und Entwicklung
32.566.217
45.683.174
43.071.051
Allgemein und administrativ
8.641.976
9.610.147
6.179.084
Geschäftsaufwand
41,208,193
55.293.321
49,250,135
Einkommen (Verlust) von Operationen
25.926.565
(10,569,494)
(49,250,135)
SONSTIGE EINKOMMEN (AUFWENDUNGEN)
Kapitalerträge
310,663
26,270
50,226
Zinsaufwendungen
(1.452.014)
(2.288.309)
(2.513.027)
Total sonstige Kosten, netto
(1.141.351)
(2,262,039)
(2.462.801)
Gewinn (Verlust) vor Ertragsteuern
24.785.214
(12.831.533)
(51,712,936)
Ertragsteueraufwand
(82,500)
(500.000)
-
NETTOEINKOMMEN (VERLUST)
$ 24.702.714
$ (13.331.533)
$ (51.712.936)
Reingewinn (Verlust) pro Stammaktie
0,12 $
$ (0,07)
$ (0,33)
Verwässertes Nettoeinkommen (Verlust) Einkommen pro Stammaktie
0,12 $
$ (0,07)
$ (0,33)
Gewichtete durchschnittliche Anzahl ausstehender Stammaktien, die zur Berechnung des Basisgewinns (-verlusts) pro Stammaktie verwendet wird
198,101,060
184,087,719
156.553.534
Gewichtete durchschnittliche Anzahl ausstehender Stammaktien, die zur Berechnung des verwässerten Gewinns (Verlustes) je Stammaktie verwendet wird
207,007,558
184,087,719
156.553.534
PALATIN TECHNOLOGIEN, INC.
und Tochtergesellschaft
Konsolidierte Bilanz
30. Juni 2018
30. Juni 2017
VERMÖGENSWERTE
Umlaufvermögen:
Zahlungsmittel und Zahlungsmitteläquivalente
$ 38,000,171
$ 40,200,324
Zur Veräusserung verfügbare Investitionen
-
249.837
Accounts erhaltbar
-
15.116.822
Rechnungsabgrenzungsposten und andere kurzfristige Vermögenswerte
513,688
1,011,221
Gesamten Umlaufvermögens
38.513.859
56,578,204
Immobilien und Ausrüstung, netto
164,035
198,153
Sonstige Vermögensgegenstände
338,916
56,916
Gesamtvermögen
$ 39.016.810
$ 56,833,273
VERBINDLICHKEITEN UND EIGENKAPITAL (DEFIZIUM)
Kurzfristige Verbindlichkeiten:
Abbrechnungsverbindlichkeiten
$ 2,223,693
1.551.367 $
Rückstellungen
2.103.021
10.521.098
Notes zahlbar, abzüglich Rabatt
5.948.763
7.824.935
Leasingverpflichtungen
-
14,324
Rechnungsabgrenzungsposten
-
35.050.572
Sonstige kurzfristige Verbindlichkeiten
487.488
-
Summe kurzfristige Verbindlichkeiten
10.762.965
54,962,296
Notes zahlbar, abzüglich Rabatt
332,898
6 281 660
Rechnungsabgrenzungsposten
500.000
-
Andere nicht gegenwärtige Belastungen
456,038
753.961
Gesamtverbindlichkeiten
12,051,901
61,997,917
Eigenkapital (Mangel):
Vorzugsbestand von 0,01 $ Nennwert - autorisierte 10.000.000 Aktien:
Series A Convertible: ausgegebene und ausstehende 4.030 Aktien ab
30. Juni 2018 und 30. Juni 2017
40
40
Stammaktien im Nennwert von 0,01 US-Dollar - autorisierte 300.000.000 Aktien;
ausgegebene und ausstehende 200.554.205 Aktien zum 30. Juni 2018 und
160.515.361 per 30. Juni 2017
2.005.542
1.605.153
Zusätzliches eingezahltes Kapital
357,005,233
349,974,538
Kumulierter sonstiger umfassender Verlust
-
(590)
Kumuliertes Defizit
(332,045,906)
(356,743,785)
Total Eigenkapital (Mangel)
26.964.909
(5.164.644)
Summe der Verbindlichkeiten und des Eigenkapitals (Unterdeckung)
$ 39.016.810
$ 56,833,273
https://c212.net/c/img/favicon.png?sn=PH05830&sd=2018-09-13 Zeigen Sie den ursprünglichen Inhalt an, um Multimedia herunterzuladen: http://www.prnewswire.com/news-releases/palatin-technologies…
QUELLE Palatin Technologies, Inc.
So langsam gehen der Aktie wohl die Glaubenden aus!
Aber für einen Wiedereinstieg ist es noch zu früh- dass muss sich erst wieder Richtung 70 Cent
einpegeln.
Dann macht`s evtl. wieder Sinn!
Aber für einen Wiedereinstieg ist es noch zu früh- dass muss sich erst wieder Richtung 70 Cent
einpegeln.
Dann macht`s evtl. wieder Sinn!
Antwort auf Beitrag Nr.: 58.893.603 von Moneymaker123 am 08.10.18 12:14:54Vielleicht hast du recht. Es könnten aber auch news kommen und Palatin geht wieder auf 1,20 $.
Ich bleibe erst mal drin und spekuliere auf steigende Kurse je näher wir der Zulassung und
Vermarktung kommen.
Ich bleibe erst mal drin und spekuliere auf steigende Kurse je näher wir der Zulassung und
Vermarktung kommen.
Palatin Technologies-Aktie: Verdreifachung des Kurses - Aktienanalyse
Ladenburg Thalmann
New York (www.aktiencheck.de) - Palatin Technologies-Aktienanalyse von Analyst Michael Higgins von Ladenburg Thalmann:
Laut einer Aktienanalyse empfiehlt Michael Higgins, Aktienanalyst von Ladenburg Thalmann, die Aktien des biopharmazeutischen Unternehmens Palatin Technologies Inc. (ISIN: US6960774031, WKN: A1C538, Ticker Symbol: PTNA, NYSE-Ticker-Symbol: PTN) im Rahmen einer Ersteinschätzung zu kaufen.
Die Analysten von Ladenburg Thalmann beurteilen die Aussichten für den Aktienkurs von Palatin Technologies Inc. positiv.
Analyst Michael Higgins veranschlagt ein Kursziel für die Palatin Technologies-Aktie von 3,00 USD.
Die Analysten von Ladenburg Thalmann beginnen in ihrer Palatin Technologies-Aktienanalyse die Coverage mit einem "buy"-Rating.
Ladenburg Thalmann
New York (www.aktiencheck.de) - Palatin Technologies-Aktienanalyse von Analyst Michael Higgins von Ladenburg Thalmann:
Laut einer Aktienanalyse empfiehlt Michael Higgins, Aktienanalyst von Ladenburg Thalmann, die Aktien des biopharmazeutischen Unternehmens Palatin Technologies Inc. (ISIN: US6960774031, WKN: A1C538, Ticker Symbol: PTNA, NYSE-Ticker-Symbol: PTN) im Rahmen einer Ersteinschätzung zu kaufen.
Die Analysten von Ladenburg Thalmann beurteilen die Aussichten für den Aktienkurs von Palatin Technologies Inc. positiv.
Analyst Michael Higgins veranschlagt ein Kursziel für die Palatin Technologies-Aktie von 3,00 USD.
Die Analysten von Ladenburg Thalmann beginnen in ihrer Palatin Technologies-Aktienanalyse die Coverage mit einem "buy"-Rating.
Antwort auf Beitrag Nr.: 59.012.292 von apano am 20.10.18 22:57:20
moechte mit "Neuigkeiten" von Platin,
dann bitte mit aktuellen Berichten und
nicht mit alten Kamellen vom 28.6.2018
Moeglicherweise ist es die Langeweile
oder der Frust sich hier so zu artikulieren. Recherchieren und lesen
koennen wir alle selber.OK,bei Neulingen auf diesem Gebiet kann man wohl diese Mottenkisten Mentalitaet
verzeihen.
neue Erkenntnisse????
Wenn man sich schon hier hervorhebenmoechte mit "Neuigkeiten" von Platin,
dann bitte mit aktuellen Berichten und
nicht mit alten Kamellen vom 28.6.2018
Moeglicherweise ist es die Langeweile
oder der Frust sich hier so zu artikulieren. Recherchieren und lesen
koennen wir alle selber.OK,bei Neulingen auf diesem Gebiet kann man wohl diese Mottenkisten Mentalitaet
verzeihen.
Antwort auf Beitrag Nr.: 59.014.615 von nvidia am 21.10.18 16:28:58Es muss natuerlich heissen Platin,war wohl zu
schnell mit Schreiben
schnell mit Schreiben
Nvidia soll wohl heißen Palatin 😉
Antwort auf Beitrag Nr.: 59.015.278 von Dumounde am 21.10.18 19:29:22
der Druckteufel war wohl wieder aktiv
ja,soll natuerlich Palatin heissen,danke
Antwort auf Beitrag Nr.: 59.014.615 von nvidia am 21.10.18 16:28:58he nivida,
wusste nicht das du für Alle sprichst. Na ja bei den erfahrenden Börsenexperten lässt
ja auch mal das Gedächtnis nach, da kann ein Börsenneuling auch mal etwas unterstützen.
wusste nicht das du für Alle sprichst. Na ja bei den erfahrenden Börsenexperten lässt
ja auch mal das Gedächtnis nach, da kann ein Börsenneuling auch mal etwas unterstützen.
Palatin Technologies: Prepare For The New Female Viagra
Oct. 25, 2018 1:00 PM ET|
24 comments
|
About: Palatin Technologies, Inc (PTN), Includes: AMAG
Tien Duy Vo
Tien Duy Vo
Growth, research analyst, biotech, healthcare
(115 followers)
Summary
Bremelanotide has passed NDA filing stage and is expected to be launched in early 2019.
Bremelanotide has outstanding market opportunities thanks to higher efficiency over its competitor and increasing market demand for HSDD treatment.
Licensing agreement with AMAG promise a successful launch in the U.S, thus other potential markets still remain.
Healthy financial condition with increasing net income.
Palatin Technologies (PTN) is the biopharmaceutical company that has successfully developed bremelanotide, a drug that deals with problem of hypoactive sexual desire disorder (HSDD) in women. bremelanotide is expected to receive FDA approval in early 2019, which would generate large source of revenue for the company from its licensing agreements. In this article, we will explain why we think Palatin is now having favorable conditions for future growth, and that it is now a good time to invest in its stock.
Outstanding market opportunities for bremelanotide
Bremelanotide, traded name Vyleesi or Rekynda, is a drug that deals with problems of hypoactive sexual desire disorder (HSDD) in women. It has been proven to have positive results from two trials in Phase 3 with more than 1200 patients. In the studies, two index/scale were examined: Female Sexual Function Index (FSFI) and Female Sexual Distress Scale (FSDS). In both trials, results showed that patients on the treated group showed a statistically significant increase in desire domain and statistically significant reduction in distress related to low sexual desire compared to placebo.
Up to now, bremelanotide faces one direct competitor named Addyi (flibanserin), which is the only drug currently approved in the U.S for treatment of HSDD. However, we believe Bremelanotide has full potential to outpace Addyi due to the following reasons:
Firstly, it is important to note that the FDA approval for Addyi included a risk evaluation and a Boxed Warning, which indicated that the use of Addyi would lead to increased risk of severe hypotension and syncope for patients who drink alcohol and for patients who have liver impairment. As Addyi is an oral drug which has to be taken over the long term, it is difficult to completely not taking on alcohol during the whole treatment, especially for those who are used to it. Bremelanotide, in contrast, was well-tolerated during the trial and was shown to not cause serious adverse events.
Secondly, the indication of Addyi requires patients to take the drug every day, which might be inconvenient for many people. Plus, the efficiency of an every-day treatment might not be as high as an immediate treatment, which allows patients to take the drug only when they need it for an immediate result. In fact, while women have to take a pill of Addyi every day, they reported up to only one more "satisfying sexual event" per month with a low efficacy rate of 10%. Those figures seem to be not desiring enough for women to risk their health with some serious aforementioned side effects. Thus, only around 227 women were using Addyi in the subsequent months after the drug was launched, even though it was the first and only approved drug that provides treatment for this area of high unmet need. Bremelanotide, on the other hand, only need to be injected about 30-45 minutes before sex, which has been shown to help women significantly increase sex desire and reduce distress.
Besides, patients using Addyi must pay as much as $426 for a supply of 30 tablets, which must be used continuously within a month. Over the long term, this treatment is very expensive as patients must continue using it all year around, which add another minus to the drug.
Addyi’s inability to meet market demand has opened up outstanding market opportunity for bremelanotide. In 2015, HSDD was estimated to affect 8 million women in the U.S. According to Palatin, this number has almost doubled to around 15 million, which further boost the market demand. Of this large number of pre-menopausal woman suffering from HSDD, as large as 95% are unaware that it is a treatable disorder, and that the majority of them would use bremelanotide if it is advised by their doctor.
As bremelanotide had shown very positive results during clinical trials and has no serious adverse effects, it is very likely that it will be able to capture the currently increasing market demand. To make a small comparison, let’s look at worldwide sales figure of Viagra – a very popular product treating erectile dysfunction and pulmonary arterial hypertension in men – over the last 15 years.
(Source: Viagra sales)
On average, Viagra generated more than $1.7B sales annually, with around 50% of revenues coming from the US. Taken into account that the number of American men suffering from sexual dysfunction is approx. double that of women (30 million vs 15 million, respectively), and that a new product would need some time to gain market share, we expect bremelanotide's annual sales to be somewhere between 200 million to 300 million in the U.S market. Also keep in mind that there are still many other potential markets available for bremelanotide that will further drive sales.
Licensing agreement with AMAG is a big step for a successful market penetration.
In January 2017, Palatin entered into a license agreement with AMAG Pharmaceuticals for exclusive licensing agreement of bremelanotide. For biotech companies, it is of great importance to find a licensing partner for their developed products, otherwise they would have to pay a large amount of money for marketing and selling activities. Thus, the licensing agreement with AMAG, a specialist in women's health, is very beneficial to Palatin. Please take a look on our article about AMAG to see why it has favorable conditions for a successful product launch. The licensing contract would also allow Palatin to concentrate its resources on developing its core business rather than marketing and selling, which is currently not their strengths.
The partnering relationship with AMAG is a perfect combination not only because of its popularity in the field of women’s healthcare but also of its newly developed Autoinjector technology. In early 2018, AMAG receive FDA approval for Makena® auto-injector, a drug-device combination product that contains a short, thin and non-visible needle. Possessing this technology, it is very possible that AMAG would develop an auto-injector device for bremelanotide so that patients can directly and easily inject the drug by themselves, making it more user-friendly and convenient. Thus, AMAG’s technology is a good fit for bremelanotide.
Besides, Palatin also targeted the Asia market by signing licensing agreements with Kwangdong Pharmaceutical and Shanghai Fosun Pharmaceutical for exclusive right to develop and commercialize bremelanotide in Korea and China, Taiwan, Hong Kong S.A.R. and Macau S.A.R. These licensing agreements not only generated an upfront payment for Palatin but will also bring about sales royalties in the future.
It is important to note that the licensing agreement with AMAG, Kwangdong and Fosun covers the North America and some other markets in Asia only. Even though North America is the most promising market, Palatin can further increase its earnings if it is able to find partner agreements in other regions, such as Europe and Africa. A study on female sexual dysfunction showed that developed regions such as Europe normally has the rate of female sexual dysfunction of 40%, whereas in developing regions, such as the Middle East or Africa, this rate is as high as 62%. Therefore, if Palatin can succeed to capture those markets, they can gain an even larger source of revenue.
Healthy financial condition with increasing net income
For the year ended June 2018, Palatin recorded a net income of $24.7M from a previous loss of more than $13M. Looking at the table below, we can see that the bottom line has been improving since last year thanks to revenues received from the licensing agreements, mainly from AMAG. Under this contract, AMAG would pay Palatin a combined unit of accounting totalling $85M, which is recognized over the arrangement using the proportional method as Palatin completes its development obligations, resulting in the revenues of approx. $42M and $44M in fiscal 2018 and fiscal 2017, respectively. As June 4, 2018, Palatin received the FDA acceptance for bremelanotide filing, thus enabling it to recognize another $20M milestone payment.
(Source: Palatin's report)
Besides the positive earnings, Palatin’s holding of cash and cash equivalent was $38M for the year ended June 2018, while the total liabilities were only $12M - less than one third of cash holdings. Thus, the company’s liquidity position is currently very good, and there is no insolvency problem in the foreseeable future.
Risks
Probably, one of the riskiest aspects investors should take into account before investing in PTN is that bremelanotide is the only product that has passed the NDA submission stage, while all other remaining products are still in Phase 1 or pre-clinical trial. PTN has no certainty about when these products will proceed to the next stages, and whether they could deliver good results in the following trials to guarantee FDA approvals. Thus, it means that the company is now highly dependent on bremelanotide, and if the drug is not approved, it could significantly harm the company’s value. Specifically, if bremelanotide fails to be approved, PTN's next year revenue would sink to 0, resulting in a net loss. In this case, its share price will definitely suffer from a large decrease and might go back to around $0.3 - $0.4 as in 2016. However, we believe this event is very unlikely to happen as all results from clinical studies were good.
Moreover, it is also noteworthy that PTN is a small-cap company (market capitalization: $186M and share price was below $1) with limited operating history; thus, investors might face several risks when investing in it. Firstly, as a small reporting company, PTN is allowed to provide simplified executive compensation disclosures in its filings and it also has certain other decreased disclosure obligations in their SEC filings. Therefore, investors might have more difficulties finding detailed/specific information regarding the company's information, which would be more easily accessible for other companies. Secondly, PTN's operations are primarily focused on acquiring, developing and securing technology as well as its principal product. Before 2017, no revenues were recorded. These limited operations history provides a limited basis for stockholders to assess the company's performance and to make future forecast.
As of June 30, 2018, PTN had cash and cash equivalents of $38M, which would be sufficient to run operations until September 2019. As we discussed earlier, all remaining products are still in phase 1 or pre-clinical trial. If they are to proceed to later stages, PTN would need to raise additional capital through equity or debt financing, which may cause dilution to existing shareholders or higher interest expense.
Conclusion
Palatin's stock is currently traded at $0.91 (as of 22 October 2018). However, we expect this price to increase significantly after bremelanotide is approved by the FDA.
Under the term of licensing contracts, Palatin is entitled to receive milestone payments after FDA approvals of $60M from AMAG, $7.5M from Fosun and $3M from Kwangdong. Altogether these add up to $70.5M in revenues next year. Moreover, also under the term of the licensing contracts, Palatin may receive tiered royalties on annual net sales of bremelanotide up to $300M from AMAG, $92.5M from Fosun and $37.5M from Kwangdong. As Palatin does not report exactly the percentage of annual sales it would receive as tiered royalties, it is difficult to make any prediction. However, as we have discussed earlier, we see a very promising future for bremelanotide. Therefore, we expect this amount to range from $13M to $20M annually (or 3% - 5% of the total royalties). Thus, we expect next year revenue to range from $83.5M to $90.5M, which may raise the net income to around $40M - $47M. With the current P/E ratio 7.96, this would imply a target price of $1.6 - $1.88. Also note that, if Palatin is able to find a licensing partner in Europe, its share price would even increase further. However, we will base our evaluation on the company's current portfolio and partnering contracts only.
From the analysis above, Palatin is having pleasant conditions to grow strongly in the future: increasing market demand for HSDD treatments; bremelanotide's higher efficiency over its competitor; and licensing agreements with AMAG, Kwangdong and Shanghai promise a future successful launch. Therefore, we believe it is now a good time to invest in PTN's stock.
Disclosure: I am/we are long PTN, AMAG.
I wrote this article myself, and it expresses my own opinions. I am not receiving compensation for it (other than from Seeking Alpha). I have no business relationship with any company whose stock is mentioned in this article.
Editor's Note: This article covers one or more stocks trading at less than $1 per share and/or with less than a $100 million market cap. Please be aware of the risks associated with these stocks.
Like this article?
Komm schon nivida, der Artikel ist zwei Tage alt. Sag mir wo alle stehen und wohin alle gehen.
Oct. 25, 2018 1:00 PM ET|
24 comments
|
About: Palatin Technologies, Inc (PTN), Includes: AMAG
Tien Duy Vo
Tien Duy Vo
Growth, research analyst, biotech, healthcare
(115 followers)
Summary
Bremelanotide has passed NDA filing stage and is expected to be launched in early 2019.
Bremelanotide has outstanding market opportunities thanks to higher efficiency over its competitor and increasing market demand for HSDD treatment.
Licensing agreement with AMAG promise a successful launch in the U.S, thus other potential markets still remain.
Healthy financial condition with increasing net income.
Palatin Technologies (PTN) is the biopharmaceutical company that has successfully developed bremelanotide, a drug that deals with problem of hypoactive sexual desire disorder (HSDD) in women. bremelanotide is expected to receive FDA approval in early 2019, which would generate large source of revenue for the company from its licensing agreements. In this article, we will explain why we think Palatin is now having favorable conditions for future growth, and that it is now a good time to invest in its stock.
Outstanding market opportunities for bremelanotide
Bremelanotide, traded name Vyleesi or Rekynda, is a drug that deals with problems of hypoactive sexual desire disorder (HSDD) in women. It has been proven to have positive results from two trials in Phase 3 with more than 1200 patients. In the studies, two index/scale were examined: Female Sexual Function Index (FSFI) and Female Sexual Distress Scale (FSDS). In both trials, results showed that patients on the treated group showed a statistically significant increase in desire domain and statistically significant reduction in distress related to low sexual desire compared to placebo.
Up to now, bremelanotide faces one direct competitor named Addyi (flibanserin), which is the only drug currently approved in the U.S for treatment of HSDD. However, we believe Bremelanotide has full potential to outpace Addyi due to the following reasons:
Firstly, it is important to note that the FDA approval for Addyi included a risk evaluation and a Boxed Warning, which indicated that the use of Addyi would lead to increased risk of severe hypotension and syncope for patients who drink alcohol and for patients who have liver impairment. As Addyi is an oral drug which has to be taken over the long term, it is difficult to completely not taking on alcohol during the whole treatment, especially for those who are used to it. Bremelanotide, in contrast, was well-tolerated during the trial and was shown to not cause serious adverse events.
Secondly, the indication of Addyi requires patients to take the drug every day, which might be inconvenient for many people. Plus, the efficiency of an every-day treatment might not be as high as an immediate treatment, which allows patients to take the drug only when they need it for an immediate result. In fact, while women have to take a pill of Addyi every day, they reported up to only one more "satisfying sexual event" per month with a low efficacy rate of 10%. Those figures seem to be not desiring enough for women to risk their health with some serious aforementioned side effects. Thus, only around 227 women were using Addyi in the subsequent months after the drug was launched, even though it was the first and only approved drug that provides treatment for this area of high unmet need. Bremelanotide, on the other hand, only need to be injected about 30-45 minutes before sex, which has been shown to help women significantly increase sex desire and reduce distress.
Besides, patients using Addyi must pay as much as $426 for a supply of 30 tablets, which must be used continuously within a month. Over the long term, this treatment is very expensive as patients must continue using it all year around, which add another minus to the drug.
Addyi’s inability to meet market demand has opened up outstanding market opportunity for bremelanotide. In 2015, HSDD was estimated to affect 8 million women in the U.S. According to Palatin, this number has almost doubled to around 15 million, which further boost the market demand. Of this large number of pre-menopausal woman suffering from HSDD, as large as 95% are unaware that it is a treatable disorder, and that the majority of them would use bremelanotide if it is advised by their doctor.
As bremelanotide had shown very positive results during clinical trials and has no serious adverse effects, it is very likely that it will be able to capture the currently increasing market demand. To make a small comparison, let’s look at worldwide sales figure of Viagra – a very popular product treating erectile dysfunction and pulmonary arterial hypertension in men – over the last 15 years.
(Source: Viagra sales)
On average, Viagra generated more than $1.7B sales annually, with around 50% of revenues coming from the US. Taken into account that the number of American men suffering from sexual dysfunction is approx. double that of women (30 million vs 15 million, respectively), and that a new product would need some time to gain market share, we expect bremelanotide's annual sales to be somewhere between 200 million to 300 million in the U.S market. Also keep in mind that there are still many other potential markets available for bremelanotide that will further drive sales.
Licensing agreement with AMAG is a big step for a successful market penetration.
In January 2017, Palatin entered into a license agreement with AMAG Pharmaceuticals for exclusive licensing agreement of bremelanotide. For biotech companies, it is of great importance to find a licensing partner for their developed products, otherwise they would have to pay a large amount of money for marketing and selling activities. Thus, the licensing agreement with AMAG, a specialist in women's health, is very beneficial to Palatin. Please take a look on our article about AMAG to see why it has favorable conditions for a successful product launch. The licensing contract would also allow Palatin to concentrate its resources on developing its core business rather than marketing and selling, which is currently not their strengths.
The partnering relationship with AMAG is a perfect combination not only because of its popularity in the field of women’s healthcare but also of its newly developed Autoinjector technology. In early 2018, AMAG receive FDA approval for Makena® auto-injector, a drug-device combination product that contains a short, thin and non-visible needle. Possessing this technology, it is very possible that AMAG would develop an auto-injector device for bremelanotide so that patients can directly and easily inject the drug by themselves, making it more user-friendly and convenient. Thus, AMAG’s technology is a good fit for bremelanotide.
Besides, Palatin also targeted the Asia market by signing licensing agreements with Kwangdong Pharmaceutical and Shanghai Fosun Pharmaceutical for exclusive right to develop and commercialize bremelanotide in Korea and China, Taiwan, Hong Kong S.A.R. and Macau S.A.R. These licensing agreements not only generated an upfront payment for Palatin but will also bring about sales royalties in the future.
It is important to note that the licensing agreement with AMAG, Kwangdong and Fosun covers the North America and some other markets in Asia only. Even though North America is the most promising market, Palatin can further increase its earnings if it is able to find partner agreements in other regions, such as Europe and Africa. A study on female sexual dysfunction showed that developed regions such as Europe normally has the rate of female sexual dysfunction of 40%, whereas in developing regions, such as the Middle East or Africa, this rate is as high as 62%. Therefore, if Palatin can succeed to capture those markets, they can gain an even larger source of revenue.
Healthy financial condition with increasing net income
For the year ended June 2018, Palatin recorded a net income of $24.7M from a previous loss of more than $13M. Looking at the table below, we can see that the bottom line has been improving since last year thanks to revenues received from the licensing agreements, mainly from AMAG. Under this contract, AMAG would pay Palatin a combined unit of accounting totalling $85M, which is recognized over the arrangement using the proportional method as Palatin completes its development obligations, resulting in the revenues of approx. $42M and $44M in fiscal 2018 and fiscal 2017, respectively. As June 4, 2018, Palatin received the FDA acceptance for bremelanotide filing, thus enabling it to recognize another $20M milestone payment.
(Source: Palatin's report)
Besides the positive earnings, Palatin’s holding of cash and cash equivalent was $38M for the year ended June 2018, while the total liabilities were only $12M - less than one third of cash holdings. Thus, the company’s liquidity position is currently very good, and there is no insolvency problem in the foreseeable future.
Risks
Probably, one of the riskiest aspects investors should take into account before investing in PTN is that bremelanotide is the only product that has passed the NDA submission stage, while all other remaining products are still in Phase 1 or pre-clinical trial. PTN has no certainty about when these products will proceed to the next stages, and whether they could deliver good results in the following trials to guarantee FDA approvals. Thus, it means that the company is now highly dependent on bremelanotide, and if the drug is not approved, it could significantly harm the company’s value. Specifically, if bremelanotide fails to be approved, PTN's next year revenue would sink to 0, resulting in a net loss. In this case, its share price will definitely suffer from a large decrease and might go back to around $0.3 - $0.4 as in 2016. However, we believe this event is very unlikely to happen as all results from clinical studies were good.
Moreover, it is also noteworthy that PTN is a small-cap company (market capitalization: $186M and share price was below $1) with limited operating history; thus, investors might face several risks when investing in it. Firstly, as a small reporting company, PTN is allowed to provide simplified executive compensation disclosures in its filings and it also has certain other decreased disclosure obligations in their SEC filings. Therefore, investors might have more difficulties finding detailed/specific information regarding the company's information, which would be more easily accessible for other companies. Secondly, PTN's operations are primarily focused on acquiring, developing and securing technology as well as its principal product. Before 2017, no revenues were recorded. These limited operations history provides a limited basis for stockholders to assess the company's performance and to make future forecast.
As of June 30, 2018, PTN had cash and cash equivalents of $38M, which would be sufficient to run operations until September 2019. As we discussed earlier, all remaining products are still in phase 1 or pre-clinical trial. If they are to proceed to later stages, PTN would need to raise additional capital through equity or debt financing, which may cause dilution to existing shareholders or higher interest expense.
Conclusion
Palatin's stock is currently traded at $0.91 (as of 22 October 2018). However, we expect this price to increase significantly after bremelanotide is approved by the FDA.
Under the term of licensing contracts, Palatin is entitled to receive milestone payments after FDA approvals of $60M from AMAG, $7.5M from Fosun and $3M from Kwangdong. Altogether these add up to $70.5M in revenues next year. Moreover, also under the term of the licensing contracts, Palatin may receive tiered royalties on annual net sales of bremelanotide up to $300M from AMAG, $92.5M from Fosun and $37.5M from Kwangdong. As Palatin does not report exactly the percentage of annual sales it would receive as tiered royalties, it is difficult to make any prediction. However, as we have discussed earlier, we see a very promising future for bremelanotide. Therefore, we expect this amount to range from $13M to $20M annually (or 3% - 5% of the total royalties). Thus, we expect next year revenue to range from $83.5M to $90.5M, which may raise the net income to around $40M - $47M. With the current P/E ratio 7.96, this would imply a target price of $1.6 - $1.88. Also note that, if Palatin is able to find a licensing partner in Europe, its share price would even increase further. However, we will base our evaluation on the company's current portfolio and partnering contracts only.
From the analysis above, Palatin is having pleasant conditions to grow strongly in the future: increasing market demand for HSDD treatments; bremelanotide's higher efficiency over its competitor; and licensing agreements with AMAG, Kwangdong and Shanghai promise a future successful launch. Therefore, we believe it is now a good time to invest in PTN's stock.
Disclosure: I am/we are long PTN, AMAG.
I wrote this article myself, and it expresses my own opinions. I am not receiving compensation for it (other than from Seeking Alpha). I have no business relationship with any company whose stock is mentioned in this article.
Editor's Note: This article covers one or more stocks trading at less than $1 per share and/or with less than a $100 million market cap. Please be aware of the risks associated with these stocks.
Like this article?
Komm schon nivida, der Artikel ist zwei Tage alt. Sag mir wo alle stehen und wohin alle gehen.
Antwort auf Beitrag Nr.: 59.074.663 von apano am 27.10.18 20:58:10Wie ist deine ganz persönliche Einstellung zu Vyleesi????
wuerde mit brennend interessieren!!!!
wuerde mit brennend interessieren!!!!
Antwort auf Beitrag Nr.: 59.103.380 von nvidia am 31.10.18 12:46:25Erst mal Danke für den Beitrag. Schade das hier kaum Diskutiert wird. Es ist gut für die Nerven wenn
man Leidensgenossen an seiner Seite hat, die auch auf die Erlösung durch die FDA hoffen.
Zu deiner Frage zum Produkt. Ein gesundes Sexualleben ist wichtig für das Wohlbefinden eines
Menschen. Wenn Menschen leiden und ihnen geholfen werden kann finde ich das völlig in
Ordnung.
Ich weiß natürlich das für einige Menschen Sex = Pfui ist und die echt Probleme mit Rykinda haben.
Wir leben in einer freien Gesellschaft. Keiner sollte anderen seine Ideologien oder Moralvorstellungen
aufzwingen.
man Leidensgenossen an seiner Seite hat, die auch auf die Erlösung durch die FDA hoffen.
Zu deiner Frage zum Produkt. Ein gesundes Sexualleben ist wichtig für das Wohlbefinden eines
Menschen. Wenn Menschen leiden und ihnen geholfen werden kann finde ich das völlig in
Ordnung.
Ich weiß natürlich das für einige Menschen Sex = Pfui ist und die echt Probleme mit Rykinda haben.
Wir leben in einer freien Gesellschaft. Keiner sollte anderen seine Ideologien oder Moralvorstellungen
aufzwingen.
Antwort auf Beitrag Nr.: 59.109.353 von apano am 31.10.18 22:29:44Das Ding hier wird im März rocken, bis dahin heißt es Geduld haben
Antwort auf Beitrag Nr.: 59.109.353 von apano am 31.10.18 22:29:44hallo apano ( HH-ahoi ????)
ich finde es nicht gut wenn man irgentwo investiert ist und man über das Produkt worum es geht
veralterte Informationen hat. Also Rekynda !!!!! ,wie es übrigens korrekt heißt, gibt es nicht mehr.
Es heißt Vyleesi !!!!! Übrigens leicht zu finden auf der Palatin Seite. Es sind oft Kleinigkeiten von
Veränderungen , die oft sehr wichtig sind.Wenn du noch genauer hinsiehst steht TM dahinter.
Es bedeutet exakt nach amerikanischem Recht ein anerkanntes!!!!!!!!!! aber nocht nicht registriertes
Produkt.Was denkst du was könnte das wohl bedeuten?????????? Die Frage must du dir schon selbst
beantworten. Allgemein gesprochen,man sollte nur da investiert sein was man auch versteht,es gibt alle!!! Information über eine Firma im Netz .Ich persönliche habe mich sehr intensiv , also ca.3-4
Monate mit dieser Firma beschäftigt und Fehler moechte ich mir bei Palatin nicht erlauben,dafür ist mein
Beitrag (monitärer Art) einfach zu hoch.!!!!Wenn jemand nur ein paar tausend Stück hat kann man nicht viel verlieren.Aber trotz allem,nur Mut.
ich finde es nicht gut wenn man irgentwo investiert ist und man über das Produkt worum es geht
veralterte Informationen hat. Also Rekynda !!!!! ,wie es übrigens korrekt heißt, gibt es nicht mehr.
Es heißt Vyleesi !!!!! Übrigens leicht zu finden auf der Palatin Seite. Es sind oft Kleinigkeiten von
Veränderungen , die oft sehr wichtig sind.Wenn du noch genauer hinsiehst steht TM dahinter.
Es bedeutet exakt nach amerikanischem Recht ein anerkanntes!!!!!!!!!! aber nocht nicht registriertes
Produkt.Was denkst du was könnte das wohl bedeuten?????????? Die Frage must du dir schon selbst
beantworten. Allgemein gesprochen,man sollte nur da investiert sein was man auch versteht,es gibt alle!!! Information über eine Firma im Netz .Ich persönliche habe mich sehr intensiv , also ca.3-4
Monate mit dieser Firma beschäftigt und Fehler moechte ich mir bei Palatin nicht erlauben,dafür ist mein
Beitrag (monitärer Art) einfach zu hoch.!!!!Wenn jemand nur ein paar tausend Stück hat kann man nicht viel verlieren.Aber trotz allem,nur Mut.
Antwort auf Beitrag Nr.: 59.118.530 von nvidia am 01.11.18 21:31:19
Gruss
Ok, bin wieder an Bord,
nur um Missverständnissen vorzubeugen!Gruss
Antwort auf Beitrag Nr.: 59.118.530 von nvidia am 01.11.18 21:31:19hello nvidia,
Danke für die vielen Tipps wo und wie man investieren sollte.
AMAG legt nicht Millionen für die Lizens von Vyleesi auf den Tisch, wenn es nach der Zulassung
damit nicht die Vermarktung starten kann. Die Registrierung macht rein logisch auch erst Sinn,
wenn die Zulassung auf dem Tisch liegt.
Was die Zulassung betrifft bin ich optimistisch. Die Studien sehen sehr gut aus und
Bremelanotide wirken. Im Internet gibt es Erfahrungsberichte und einen Schwarzmarkt für das Zeug.
Risiken sehe ich von politischer Seite von den Moralisten und das Auflagen kommen die
eine Vermarktung stark einschränken.
Wo sind den deiner Meinung nach die Risiken und Chancen bei Palatin? Wenn du die Firma so intensiv studiert hast fällt dir doch dazu bestimmt etwas ein. Vielleicht jenseits vom Niveau:
det ding kakt ab
Danke für die vielen Tipps wo und wie man investieren sollte.
AMAG legt nicht Millionen für die Lizens von Vyleesi auf den Tisch, wenn es nach der Zulassung
damit nicht die Vermarktung starten kann. Die Registrierung macht rein logisch auch erst Sinn,
wenn die Zulassung auf dem Tisch liegt.
Was die Zulassung betrifft bin ich optimistisch. Die Studien sehen sehr gut aus und
Bremelanotide wirken. Im Internet gibt es Erfahrungsberichte und einen Schwarzmarkt für das Zeug.
Risiken sehe ich von politischer Seite von den Moralisten und das Auflagen kommen die
eine Vermarktung stark einschränken.
Wo sind den deiner Meinung nach die Risiken und Chancen bei Palatin? Wenn du die Firma so intensiv studiert hast fällt dir doch dazu bestimmt etwas ein. Vielleicht jenseits vom Niveau:
det ding kakt ab
Antwort auf Beitrag Nr.: 59.127.785 von apano am 02.11.18 21:20:05Also, wenn du schreibst es gibt einen
Schwarzmarkt dann sage ich dir, wenn
du solch einen Blödsinn glaubst bist du
irgentwie falsch beim Investieren in Aktien.
Wie Goldlocke sagt Fake News!!!!!!!!!!!!!!!
Das schlimme daran ist ,das dann irgendwie
Im Netz eine Parallele zwischen einem
"Schwarzmarkt" und Palatin hergestellt wird.
Wenn du dich ,was du todsicher nicht gemacht hast,
mit diesen Firmen und Palatin beschäftigst und
auch schriftlich !!!!!!!!!!!!Kontakt aufnimmst,
wirst du den Begriff Schwarzmarkt nie wieder
in den Mund nehmen. Du solltest wissen ,oder auch nicht,
das nirgendwo so viele ,absichtliche, Falschmeldungen
verbreitet werden wie z.b.hier oder auch anderen
Foren. Diese werden dann benutzt z.b. von
Short Sellern ............Wenn du der Meinung bist
das "das Ding abkackt" ( Zitat) verkauf doch
einfach deine Aktien, kein Mensch hat dir zum Kauf geraten.
Moeglicherweise hast du mit Lotto mehr Erfolg!!!!
Sagt man mal den Leuten die Meinung sagt sind alle
gleich eingeschnappt.Ich nenne das konstruktive
Kritik.Aber gut ,so sind halt die meisten
gestrickt.
Schwarzmarkt dann sage ich dir, wenn
du solch einen Blödsinn glaubst bist du
irgentwie falsch beim Investieren in Aktien.
Wie Goldlocke sagt Fake News!!!!!!!!!!!!!!!
Das schlimme daran ist ,das dann irgendwie
Im Netz eine Parallele zwischen einem
"Schwarzmarkt" und Palatin hergestellt wird.
Wenn du dich ,was du todsicher nicht gemacht hast,
mit diesen Firmen und Palatin beschäftigst und
auch schriftlich !!!!!!!!!!!!Kontakt aufnimmst,
wirst du den Begriff Schwarzmarkt nie wieder
in den Mund nehmen. Du solltest wissen ,oder auch nicht,
das nirgendwo so viele ,absichtliche, Falschmeldungen
verbreitet werden wie z.b.hier oder auch anderen
Foren. Diese werden dann benutzt z.b. von
Short Sellern ............Wenn du der Meinung bist
das "das Ding abkackt" ( Zitat) verkauf doch
einfach deine Aktien, kein Mensch hat dir zum Kauf geraten.
Moeglicherweise hast du mit Lotto mehr Erfolg!!!!
Sagt man mal den Leuten die Meinung sagt sind alle
gleich eingeschnappt.Ich nenne das konstruktive
Kritik.Aber gut ,so sind halt die meisten
gestrickt.
Antwort auf Beitrag Nr.: 59.128.385 von nvidia am 02.11.18 23:09:03Wenn ich dich richtig verstanden habe, hältst du einen richtigen batzen an PTN.
Geht mir genauso.
Hast du als bedeutender Investor irgendwelche Vorteile dadurch?
Wieviel Prozent hälst du denn?
Vielleicht könnten wir unser Investment bündeln und wir fliegen beide zum Headquarters
und holen uns dort die Infos.
Geht mir genauso.
Hast du als bedeutender Investor irgendwelche Vorteile dadurch?
Wieviel Prozent hälst du denn?
Vielleicht könnten wir unser Investment bündeln und wir fliegen beide zum Headquarters
und holen uns dort die Infos.
nvidia@, was denkst du uber die Aktie? Das mit dem schwarzmarkt gab schon auch bei ariva forum. Bullshit schlecht hin aber Leute sollen reden. Mich würde gerne interessieren, was du bei deiner Recherche rausgefunden hast?
Antwort auf Beitrag Nr.: 59.132.159 von apano am 03.11.18 21:04:45Ok, es gibt einige Dinge im Leben was man nicht machen sollte. Z.b.
1. Verleih niemals dein Auto
2. Sprech nie über Geld
3. Höre nie darauf was andere sagen oder schreiben!!!! ( wenns um Geld geht.)
Ja,ich bin mit einer großen Position bei Palatin investiert,allerdings gehört das z.b.
unter Punkt 2.
Normalerweise handel ich gerne gegen den Trend und wie man Dinge normalerweise tut ,
in der Mehrzahl mit Erfolg. Ein sehr großer Fehler z.b. ist große Positionen zu halten von
nur einer Firma. Im Falle Palatin ist es allerdings das erste !!!!!!!!!! mal das ich diese Weisheit
mißachte. Was soll ich übrigens drüben, da bin ich hinterher auch nicht schlauer,oder glaubst
du ,daß Herr Span irgendwelche Geheimnisse verrät,was schließlich als Insiderwissen
hart bestraft würde.Aber deinen Vorschlag habe ich natürlich als lustigen Scherz verstanden!!!
Derjenige ,der Geduld übt, ist in den meisten Fällen der Gewinner. Warte ganz einfach ab oder
geb den Aktienhandel auf.Lass alle anderen reden was sie wollen.Mit kurzfristigen Sachen
kannst du keine großen Gewinne machen auf lange Sicht.Ausnahmen mag es auch hier geben.
Trink ein schönes Bierchen, im Frühjahr gibt es ohnehin dann schon zum Frühstück Champus,
wenn man das möchte.
1. Verleih niemals dein Auto
2. Sprech nie über Geld
3. Höre nie darauf was andere sagen oder schreiben!!!! ( wenns um Geld geht.)
Ja,ich bin mit einer großen Position bei Palatin investiert,allerdings gehört das z.b.
unter Punkt 2.
Normalerweise handel ich gerne gegen den Trend und wie man Dinge normalerweise tut ,
in der Mehrzahl mit Erfolg. Ein sehr großer Fehler z.b. ist große Positionen zu halten von
nur einer Firma. Im Falle Palatin ist es allerdings das erste !!!!!!!!!! mal das ich diese Weisheit
mißachte. Was soll ich übrigens drüben, da bin ich hinterher auch nicht schlauer,oder glaubst
du ,daß Herr Span irgendwelche Geheimnisse verrät,was schließlich als Insiderwissen
hart bestraft würde.Aber deinen Vorschlag habe ich natürlich als lustigen Scherz verstanden!!!
Derjenige ,der Geduld übt, ist in den meisten Fällen der Gewinner. Warte ganz einfach ab oder
geb den Aktienhandel auf.Lass alle anderen reden was sie wollen.Mit kurzfristigen Sachen
kannst du keine großen Gewinne machen auf lange Sicht.Ausnahmen mag es auch hier geben.
Trink ein schönes Bierchen, im Frühjahr gibt es ohnehin dann schon zum Frühstück Champus,
wenn man das möchte.
Antwort auf Beitrag Nr.: 59.133.985 von Schurik am 04.11.18 12:39:24Ich wiederhole mich ansich ungern,aber einen Schwarzmarkt gibt es definitiv nicht,es ist
etwas völlig anderes was da für ein Mist angeboten wird. Es gibt genügend Firmen die von
dem Wirkstoff irgendwas vertreiben. Mit ein bischen Fantasie kannst du das alles rauskriegen,
schreib die Firmen an und frage ob es sich um den gleichen Stoff handelt. Du wirst erstaunt sein
was du für Antworten bekommst.Immer mit dem Hintergrund das du ein sehr interessierter Käufer
bist.Im Übrigen mache ich ja nicht die Arbeit für andere, das muss schon jeder selber machen.
Viele wissen auch gar nicht wo sie die Informationen herbekommen.Aber das ist schließlich die Sache
eines jeden.Intensive Recherche und Geduld ist das Erfolgsrezept!!!!!! das must du schon alles für
dich selber machen und nicht auf das Gewäsch anderer hören.
schönen Wochenbeginn!
etwas völlig anderes was da für ein Mist angeboten wird. Es gibt genügend Firmen die von
dem Wirkstoff irgendwas vertreiben. Mit ein bischen Fantasie kannst du das alles rauskriegen,
schreib die Firmen an und frage ob es sich um den gleichen Stoff handelt. Du wirst erstaunt sein
was du für Antworten bekommst.Immer mit dem Hintergrund das du ein sehr interessierter Käufer
bist.Im Übrigen mache ich ja nicht die Arbeit für andere, das muss schon jeder selber machen.
Viele wissen auch gar nicht wo sie die Informationen herbekommen.Aber das ist schließlich die Sache
eines jeden.Intensive Recherche und Geduld ist das Erfolgsrezept!!!!!! das must du schon alles für
dich selber machen und nicht auf das Gewäsch anderer hören.
schönen Wochenbeginn!
Antwort auf Beitrag Nr.: 59.135.709 von nvidia am 04.11.18 20:20:31Ja nivida igendwie haben wir ähnliche Ideen. Obwohl ich schon Risiken bei Palatin sehe.
Da ich neben der Börse ich noch arbeite und Familie und Kinder habe, bleibt zur tiefen Analyse
nicht so viel Zeit.
Ein Grundsatz von mir ist, immer auch die Motive der Gegenseite zu verstehen.
Ich erkläre mir die mikrige Bewertung von PNT mit den herben Enttäuschungen aus der Vergangenheit. Wenn ich aber solche Sachen lese von
Tien Duy Vo
Growth, research analyst, biotech, healthcare bei Seeking Alpha
dann stimmt mich das Optimistisch. Ich meine bei Palatin ist das Risiko gerechtfertigt.
Da ich neben der Börse ich noch arbeite und Familie und Kinder habe, bleibt zur tiefen Analyse
nicht so viel Zeit.
Ein Grundsatz von mir ist, immer auch die Motive der Gegenseite zu verstehen.
Ich erkläre mir die mikrige Bewertung von PNT mit den herben Enttäuschungen aus der Vergangenheit. Wenn ich aber solche Sachen lese von
Tien Duy Vo
Growth, research analyst, biotech, healthcare bei Seeking Alpha
dann stimmt mich das Optimistisch. Ich meine bei Palatin ist das Risiko gerechtfertigt.
Antwort auf Beitrag Nr.: 59.144.247 von apano am 05.11.18 23:12:18Ist das der Analyst von der Goethe Universität Frankfurt?
OK,jeder hat eine unterschiedliche
Sichtweise.Schau dir aber mal die Vita
der Aufsichtsratmitglieder von Palatin
an.!!!! Und vergesse niemals wer die grossen
Positionen bei Palatin haelt. Vanguard
und Black Rock ,das sagt wohl alles.
Verluste wollen die garantiert keine
machen!!!!!
OK,jeder hat eine unterschiedliche
Sichtweise.Schau dir aber mal die Vita
der Aufsichtsratmitglieder von Palatin
an.!!!! Und vergesse niemals wer die grossen
Positionen bei Palatin haelt. Vanguard
und Black Rock ,das sagt wohl alles.
Verluste wollen die garantiert keine
machen!!!!!
Antwort auf Beitrag Nr.: 59.174.283 von Jack48 am 09.11.18 07:17:17Super News, vielen Dank für den Link
Tja, leider scheint’s den Kurs nicht zu kratzen...😌
Details zum Ergebnisbericht von Palatin Technologies Inc. im ersten Quartal
ERGEBNISÜBERSICHT: Details zum Ergebnisbericht von Palatin Technologies Inc. im ersten QuartalVon RTTNews Staff Writer ✉ | Veröffentlicht: 13.11.2014 07:38 Uhr ET
Nachfolgend sind die Ergebnishighlights für Palatin Technologies Inc. ( PTN ) aufgeführt:
-Ergebnisse: - 5,68 Millionen US-Dollar im ersten Quartal gegenüber 10,60 Millionen US-Dollar im Vorjahreszeitraum.
-EPS: - 0,03 USD im ersten Quartal gegenüber 0,05 USD im Vorjahreszeitraum.
- Umsatz: 0,03 Millionen US-Dollar im ersten Quartal gegenüber 26,94 Millionen US-Dollar im Vorjahreszeitraum.
Zulassung verschiebt sich um 3-6 Monate. Adcommeeting im Januar findet nicht statt.Lest mal den bei der SEC eingereichten Quartalsbericht unter Edgar online. Nicht gut! Irgendwelche Phase1 Daten müssen noch nachgeliefert werden.
Antwort auf Beitrag Nr.: 59.205.469 von Urbi am 13.11.18 14:33:31 Item 7.01. Regulation FD Disclosure.
AMAG Pharmaceuticals, Inc. (“AMAG”), Palatin Technologies, Inc.’s (“Palatin”) exclusive North American licensee of Vyleesi™ (bremelanotide), has been in discussions with the U.S. Food and Drug Administration (the “FDA”) regarding its review of the New Drug Application (“NDA”) submission for Vyleesi. The FDA has requested that additional data be generated from a small Phase 1 study with premenopausal volunteers assessing 24-hour ambulatory blood pressure with short term daily use of Vyleesi. As part of its ongoing review, the FDA has indicated that these data are required to help characterize the impact of frequent dosing, including to help inform the Vyleesi label. Palatin and AMAG believes that this study can be conducted and data submitted prior to March 23, 2019, the currently scheduled Prescription Drug User Fee Act (“PDUFA”) date. The FDA will assess the need for an Advisory Committee meeting after receipt and review of the requested data, and has informed AMAG that the previously communicated January 2019 Advisory Committee meeting will not take place. Although AMAG’s discussions to date with the FDA are preliminary, and AMAG will continue to have further discussions with the FDA on this matter, AMAG believes that this submission of additional data could cause a delay of the potential approval of Vyleesi by three to six months.
AMAG Pharmaceuticals, Inc. (“AMAG”), Palatin Technologies, Inc.’s (“Palatin”) exclusive North American licensee of Vyleesi™ (bremelanotide), has been in discussions with the U.S. Food and Drug Administration (the “FDA”) regarding its review of the New Drug Application (“NDA”) submission for Vyleesi. The FDA has requested that additional data be generated from a small Phase 1 study with premenopausal volunteers assessing 24-hour ambulatory blood pressure with short term daily use of Vyleesi. As part of its ongoing review, the FDA has indicated that these data are required to help characterize the impact of frequent dosing, including to help inform the Vyleesi label. Palatin and AMAG believes that this study can be conducted and data submitted prior to March 23, 2019, the currently scheduled Prescription Drug User Fee Act (“PDUFA”) date. The FDA will assess the need for an Advisory Committee meeting after receipt and review of the requested data, and has informed AMAG that the previously communicated January 2019 Advisory Committee meeting will not take place. Although AMAG’s discussions to date with the FDA are preliminary, and AMAG will continue to have further discussions with the FDA on this matter, AMAG believes that this submission of additional data could cause a delay of the potential approval of Vyleesi by three to six months.
Antwort auf Beitrag Nr.: 59.205.469 von Urbi am 13.11.18 14:33:31Ist doch traurig! Das gleiche Kaspertheater wie bei Trevena. Jetzt müssen noch Phase-1-Daten nachgeliefert werden---das muß ich doch als Pharmaunternehmen wissen, auf was die FDA Wert legt und was nicht so ausschlaggebend ist. Da frage ich mich langsam, ob Kasper "Kleinaktionär" nur für die Finanzierung gekonnt benutzt wird oder ob da wirklich auch ne Substanz hinter dem Unternehmen hängt?
Antwort auf Beitrag Nr.: 59.207.041 von dollilolli am 13.11.18 19:38:45Jetzt geht der Schwachsinn hier auch noch los.........hier werden nur fehlende Daten zu Phase 1 verlangt....nicht mehr und nicht weniger. Meint ihr ... eine Zulassung wird verteilt wie Konfetti,
es ist immer ein langer Weg und manchmal werden halt fehlende Daten benötigt um an eine Zulassung zu bekommen....das ist doch ok. Aber nein....da wird die Aktie wieder übertrieben abgestraft.....weil irgendwelche aktionäre ihre zittrigen Hände nicht in den Griff bekommen.
es ist immer ein langer Weg und manchmal werden halt fehlende Daten benötigt um an eine Zulassung zu bekommen....das ist doch ok. Aber nein....da wird die Aktie wieder übertrieben abgestraft.....weil irgendwelche aktionäre ihre zittrigen Hände nicht in den Griff bekommen.
Antwort auf Beitrag Nr.: 59.207.041 von dollilolli am 13.11.18 19:38:45
Also Kleinaktionär bist du immer Schütze Arsch im letzen Glied. Keine Sau interessiert sich für Kleinaktionäre. Wir können halt nur hoffen, auch ein paar Brotkrumen abzubekommen.
Zitat von dollilolli: Ist doch traurig! Das gleiche Kaspertheater wie bei Trevena. Jetzt müssen noch Phase-1-Daten nachgeliefert werden---das muß ich doch als Pharmaunternehmen wissen, auf was die FDA Wert legt und was nicht so ausschlaggebend ist. Da frage ich mich langsam, ob Kasper "Kleinaktionär" nur für die Finanzierung gekonnt benutzt wird oder ob da wirklich auch ne Substanz hinter dem Unternehmen hängt?
Also Kleinaktionär bist du immer Schütze Arsch im letzen Glied. Keine Sau interessiert sich für Kleinaktionäre. Wir können halt nur hoffen, auch ein paar Brotkrumen abzubekommen.
Hey Sorry, ich bin hier im Frühjahr bei 1,14 Euro rein. Habe bei 0,99 Euro nochmals nachgekauft.
Und vom Verlust hätte ich mir einen neuen Golf kaufen können.
Und sorry, ich glaube ich verliere hier die Nerven.
Ich sehe nicht das sich in naher Zukunft was verbessert. Sorry
Und vom Verlust hätte ich mir einen neuen Golf kaufen können.
Und sorry, ich glaube ich verliere hier die Nerven.
Ich sehe nicht das sich in naher Zukunft was verbessert. Sorry
Das ist biotech. Hier ist geduld und nerven gefragt...
Antwort auf Beitrag Nr.: 59.207.148 von bernstein789 am 13.11.18 20:17:16
Das ganze Prozedere verlängert sich aber um Monate.
Bin hier auch raus, ohne Verlust. Die Aktie wird noch sinken, es ist noch ein langer Weg, es kommen wieder bessere Kurse!
Zitat von bernstein789: Jetzt geht der Schwachsinn hier auch noch los.........hier werden nur fehlende Daten zu Phase 1 verlangt....nicht mehr und nicht weniger. Meint ihr ... eine Zulassung wird verteilt wie Konfetti,
es ist immer ein langer Weg und manchmal werden halt fehlende Daten benötigt um an eine Zulassung zu bekommen....das ist doch ok. Aber nein....da wird die Aktie wieder übertrieben abgestraft.....weil irgendwelche aktionäre ihre zittrigen Hände nicht in den Griff bekommen.
Das ganze Prozedere verlängert sich aber um Monate.
Bin hier auch raus, ohne Verlust. Die Aktie wird noch sinken, es ist noch ein langer Weg, es kommen wieder bessere Kurse!
Ich bleibe drin und kaufe nach. Ich gehe auch von niedrigeren Kursen aus aber wie heisst es so schön... wenn ich eins weiß dann das ich nichts weiß.
Bin bei Trevena drin geblieben und jetzt schwer im minus. Das reicht mir. Daher bin ich hier noch rechtzeitig mit einem guten plus raus. Werde ich weiter beobachten und evtl. zu einem späteren Zeitpunkt in Betracht ziehen.
Wegen so ner 08-15 Nachricht das die zuständige Behörde was angeforgert hat, wollen einige das Handtuch schmeißen. Da könnt ich mein kommpletes Portf.. abstoßen
es liegt vielleicht daran,daß hier ständig von super Aussichten geredet wird und über Riesengewinne spekuliert wird.permanent wird auf news gewartet,die den Kurs in die Höhe schiessen lassen,aber es passiert nichts.so lanvsam scheint das Vertauen in die Aktie dem Zweifel zu weichen
Hier geht in den nächsten Monate nicht mehr viel, (Range 0.83-0.90) seitwärts,
den $165 Mio Market Cap ist schon gut Bewertet was es braucht ist die Zulassung von Vyleesi.
Gestern waren viele Investoren über die Verzögerung enttäuscht.
den $165 Mio Market Cap ist schon gut Bewertet was es braucht ist die Zulassung von Vyleesi.
Gestern waren viele Investoren über die Verzögerung enttäuscht.
Wer zum jetzigem Zeitpunkt noch investiert ist sollte Geduld und Ruhe mitbringen. Bei Panikverkäufen gibt es immer auch Marktteilnehmer die daraus ihren Provit ziehen. Meine Meinung: Palatin ist eine spekulative Aktie wofür man Nerven mitbringen sollte. Allen viel Erfolg
Eben Prinz. Im Grunde ist fast nichts passiert. Vielleicht eine spätere Zulassung. Geduld. Angst haben am Aktienmarkt nichts verloren. Das Medi soll sehr sicher sein und effektiv. Ich bleib dabei bis zum bitteren Ende. Gruß und viel Erfolg
Antwort auf Beitrag Nr.: 59.218.213 von Reinerle am 15.11.18 05:10:56
Zitat von Reinerle: Eben Prinz. Im Grunde ist fast nichts passiert. Vielleicht eine spätere Zulassung. Geduld. Angst hat am Aktienmarkt nichts verloren. Das Medi soll sehr sicher sein und effektiv. Ich bleib dabei bis zum bitteren Ende. Gruß und viel Erfolg. Es handelt sich um eine amerikanische Firma. Da könnt ich mir vorstellen das die Zulassung eher durchflutscht
Wer den Gesamtmarkt im Blick hat erkennt schnell das momentan beinahe egal ist welche Aktie man in den Fokus nimmt, denn überwiegend wird in den letzten Wochen viel Geld aus dem Markt genommen; sehr volatiler Markt zur Zeit. Palatin bleibt davon nicht unberührt und auch ohne Nachrichten hatten wir in den letzten Wochen immer wieder Kursrückgänge. Wer hier als Kleinanleger drin ist sollte meiner Meinung nach Geduld mitbringen um nicht als Spielball der Profis zu enden.
Ich dachte mal zwischen 0.83 bis 0.90 könnte PTN in den nächsten Monaten konsolidieren.
Aber es sieht nicht danach aus ? Meine Einschätzung eher Bearish.
Aber es sieht nicht danach aus ? Meine Einschätzung eher Bearish.
Vor 2 Tagen habe ich meine PTN Aktien verkauft und in CPRX investiert.
Analyse über Catalyst's Upcoming PDUFA Is a Major Catalyst
https://finance.yahoo.com/news/h-c-wainwright-sees-over-2335…
Analyse über Catalyst's Upcoming PDUFA Is a Major Catalyst
https://finance.yahoo.com/news/h-c-wainwright-sees-over-2335…
Ist doch ganz einfach. Das gesamte Kursplus seit letztem Jahr basierte auf pushen der Aktie und der „garantierten“ Zulassung bei der FDA. Niemand hat das bisher ernstlich in Frage gestellt. Wenn jetzt doch noch Daten seitens der FDA benötigt werden und es zu Verzögerungen kommt wird oder vielleicht zu gar keiner Zulassung verlassen die Ratten das womöglich sinkende Schiff. Ich denke das geht noch erheblich runter.
Antwort auf Beitrag Nr.: 59.235.763 von meissner7309 am 16.11.18 18:38:41Ohhhh.........wieder so ein Schwarzmaler Wieviele Aktien besitzt du denn
Wieviele Aktien besitzt du denn

 Wieviele Aktien besitzt du denn
Wieviele Aktien besitzt du denn

3 bis 4 Stück schätze ich Jetzt mal ohne Spass Der nicht mehr will soll raus Ich habe 70.000 drin und ich bleibe
Antwort auf Beitrag Nr.: 59.235.763 von meissner7309 am 16.11.18 18:38:41
Nur weil du dich nicht mit der Materie beschäftigt hast, musst du nicht auf andere schließen
Zitat von meissner7309: Ist doch ganz einfach. Das gesamte Kursplus seit letztem Jahr basierte auf pushen der Aktie und der „garantierten“ Zulassung bei der FDA. Niemand hat das bisher ernstlich in Frage gestellt. Wenn jetzt doch noch Daten seitens der FDA benötigt werden und es zu Verzögerungen kommt wird oder vielleicht zu gar keiner Zulassung verlassen die Ratten das womöglich sinkende Schiff. Ich denke das geht noch erheblich runter.
Nur weil du dich nicht mit der Materie beschäftigt hast, musst du nicht auf andere schließen
Antwort auf Beitrag Nr.: 59.237.068 von Mammut22 am 16.11.18 21:14:32Der Kurs spricht für sich.
Der wo raus will soll raus Ich bleibe. Sie haben Addyi mit wesentlich mehr Nebenwirkungen zu gelassen. Tschüss an alle die gehen
3 bis 6 Monate ist eine lange Zeit bis sich der Horizont wieder aufhellt.
Hier steigen viele aus warum sollten sie das Geld über diesen Zeitraum parkieren.
Es wird noch ausgezeichnete Einstiegs Möglichkeiten geben um wieder dabei zu sein.
Hier steigen viele aus warum sollten sie das Geld über diesen Zeitraum parkieren.
Es wird noch ausgezeichnete Einstiegs Möglichkeiten geben um wieder dabei zu sein.
3-6 Monate Das ist nur eine Vermutung von AMAG ( und da wahrscheinlich von irgend 1-2 Personen). Ich glaube (ja ich glaube nur) das das keine wesentliche Verzögerung ergibt. Warum auch Die haben nur Ergebnisse nachgefordert die schon lange gemacht wurden. Also es wurden keine neuen Tests gefordert. Wieso soll sich es dann verzögern? Klingt für mich nicht plausibel.
Antwort auf Beitrag Nr.: 59.238.226 von Reinerle am 17.11.18 07:15:51Das sagt sich leicht.
Bei mir ist bei dieser Position derzeit ein Minus von 29K.
Natürlich nur wenn ich rausgehe. Schon klar.
Aber nicht aussteigen und ausharren ist echt ne Folter.
Wenn das meine Frau wüßte. Die schlägt hart aber ungenau
Bei mir ist bei dieser Position derzeit ein Minus von 29K.
Natürlich nur wenn ich rausgehe. Schon klar.
Aber nicht aussteigen und ausharren ist echt ne Folter.
Wenn das meine Frau wüßte. Die schlägt hart aber ungenau
Antwort auf Beitrag Nr.: 59.239.180 von fypet am 17.11.18 10:58:09
Genau so ist es!
Zitat von fypet: 3 bis 6 Monate ist eine lange Zeit bis sich der Horizont wieder aufhellt.
Hier steigen viele aus warum sollten sie das Geld über diesen Zeitraum parkieren.
Es wird noch ausgezeichnete Einstiegs Möglichkeiten geben um wieder dabei zu sein.
Genau so ist es!
Das Handelsvolumen nimmt immerhin wieder zu 😂
Antwort auf Beitrag Nr.: 59.240.182 von Reinerle am 17.11.18 15:26:54Doch,die haben eine neue Phase1 Studie zum Verhalten des Blutdrucks bei sehr häufiger Einnahme gefordert.Diese Studie muss erst noch fertiggestellt werden und befriedigende Ergebnisse abliefern.Wie wir alle wissen war hoher Blutdruck schon das Problem als das Mittel noch als Nasenspray herauskommen sollte,was ja dann aufgegeben wurde.
Antwort auf Beitrag Nr.: 59.242.156 von Urbi am 18.11.18 09:25:57
Es ist ein erheblicher Unterschied ob nur Daten nachgefordert werden oder eine Studie Phase 1 komplett neu erstellt werden muss !!
!!--------------------!!
Quellen Angabe BITTE Es ist ein erheblicher Unterschied ob nur Daten nachgefordert werden oder eine Studie Phase 1 komplett neu erstellt werden muss !!
Die Quelle hab ich hier in diesem Thread am 13.11.2018 gepostet, nachdem das Filing von Palatin bei der SEC eingereicht wurde. Bitte bei Interesse zurückblättern oder bei Edgar online das SEC-Filing vom 13.11.2018 einsehen.
Mein Posting war um 14:59 Uhr am 13.11.2018
Ja das mit den Daten aus Studie 1 hat mich doch sehr negativ überrascht. Die hatten doch vor
Jahren mit der FDA schon einmal Probleme mit dem Wirkstoff und Bluthochdruck. Man wusste also das
die FDA in diese Richtung schaut. Sehr uncool von Carl.
Da ich kein Bock auf Gewinnsteuern habe, werde ich das Aussitzen. Unter 0,39 Euro wird es nicht
mehr gehen, hoffe ich.
Im November 2019 sehe ich Palatin bei 3 bis 4 Euro.
Jahren mit der FDA schon einmal Probleme mit dem Wirkstoff und Bluthochdruck. Man wusste also das
die FDA in diese Richtung schaut. Sehr uncool von Carl.
Da ich kein Bock auf Gewinnsteuern habe, werde ich das Aussitzen. Unter 0,39 Euro wird es nicht
mehr gehen, hoffe ich.
Im November 2019 sehe ich Palatin bei 3 bis 4 Euro.
Antwort auf Beitrag Nr.: 59.244.769 von apano am 18.11.18 21:21:19Das sehe ich genauso
Bllutdruck hin Blutdruck her. Aspirin z.B. ist in den USA für Zehntausende Todesfälle jährlich verantwortlich. Bei Viagra sind auch schon einige dran gestorben Diese 2 Medis gibt es immer noch. Die Pharmaindustire (vor allem mit einem Großen in der Hinderhand " AMAG ") hat schon nen großen Einfluß. Sie werdens schon richten. Wir werden um warten nicht drum rum kommen. Alle die keine Geduld haben Viel Glück wo anders
Wenn die das zulassen bin ich auf deiner Seite, wenn nicht, dann werden wir richtig gen Süden abrauschen. Derzeit sehe ich schon ein größeres Problem. Da sich die FDA scheinbar auf den Bluthochdruck eingeschossen hat und das Mittel hier ein Problem zu haben scheint ist es überhaupt keine klare Sache mehr, ob das Medikament eine Zulassung bekommt. Ist halt letztlich eine Abwegubg der einzelnen Kommissionsmitglieder. Da muss sich jeder die Frage stellen ob der Nutzen des Präparats größer ist als die zu befürchteten Nebeneirkungen. Und auch wenn unsereins vielleicht die Ansicht hat, dass das kein Großes Problem sein sollte, weiß man nicht, welche Vögel da in der Kommission und später bei der FDA sitzen. Man muss bedenken. Die USA sind nach außen prüde und haben teilweise ein seltsames Weltbild.
Ja, als prüde sind sie nach außen hin bekannt, die Amis, aber es hat sie nicht daran gehindert, Viagra auf den Weltmarkt zu bringen. Wenn gesteigerter Blutdruck aufgrund einer übermäßigen Einnahme entstehen und zu einer Verweigerung der Marktzulassung führen würde, dürften viele andere Medikamente mit noch größeren Nebenwirkungen gar nicht mehr auf dem Weltmarkt sein.
Also niemand sagt das der Blutdruck hoch geht. Nicht die FDA nicht AMAG nicht Palatin. Es ist nur nicht getestet worden. Und anscheinend nur nicht für übermäßige Einnahme. Also wieso soll der Blutdruck steigen. Das ist doch nur wegen des ehemaligen Mittels. Dies ist doch ein völlig neuen Mittel. Oder liege ich da falsch?? Und wirkt aufs Gehirn. Soweit vorhanden. So what? Vielleicht gibt es auch Warzen an Arsch wenn es in die Nähe gespritzt wird. Wurde wohl nicht getestet. Vielleicht kommt das als nächstest von der FDA. Ich bleib drin denn falls das Mittel zugelassen wird komm ich nicht mehr zu nem vernünftigen Preis rein
Man kann es drehen wie man will aber PTN braucht oder mindestens die Zuversicht der Zulassung.
Hier liegt der Hase und wer den ausführlichen Artikel lesen möchte unten der link:
Dieser Artikel richtet sich an alle, die sich besser mit Preis-Gewinn-Verhältnissen (P / E-Verhältnissen) auseinandersetzen möchten. Wir zeigen, wie Sie das P / E-Verhältnis von Palatin Technologies Inc. (NYSEMKT: PTN) verwenden können, um Ihre Einschätzung der Investitionsmöglichkeiten zu informieren. Palatin Technologies hat ein KGV von 19,58, basierend auf den letzten zwölf Monaten. Mit anderen Worten: Bei den heutigen Preisen zahlen die Anleger 19,58 USD für jeden 1 USD Gewinn des Vorjahres. Wie berechnen Sie ein P / E-Verhältnis?
Die Formel für P / E lautet: Preis-Gewinn-Verhältnis = Aktienkurs ÷ Ergebnis je Aktie (EPS)
oder für Palatin Technologies: P / E von 19,58 = 0,81 ÷ 0,041 USD (Basierend auf dem Jahr bis September 2018.)
https://finance.yahoo.com/news/palatin-technologies-inc-nyse…
Hier liegt der Hase und wer den ausführlichen Artikel lesen möchte unten der link:
Dieser Artikel richtet sich an alle, die sich besser mit Preis-Gewinn-Verhältnissen (P / E-Verhältnissen) auseinandersetzen möchten. Wir zeigen, wie Sie das P / E-Verhältnis von Palatin Technologies Inc. (NYSEMKT: PTN) verwenden können, um Ihre Einschätzung der Investitionsmöglichkeiten zu informieren. Palatin Technologies hat ein KGV von 19,58, basierend auf den letzten zwölf Monaten. Mit anderen Worten: Bei den heutigen Preisen zahlen die Anleger 19,58 USD für jeden 1 USD Gewinn des Vorjahres. Wie berechnen Sie ein P / E-Verhältnis?
Die Formel für P / E lautet: Preis-Gewinn-Verhältnis = Aktienkurs ÷ Ergebnis je Aktie (EPS)
oder für Palatin Technologies: P / E von 19,58 = 0,81 ÷ 0,041 USD (Basierend auf dem Jahr bis September 2018.)
https://finance.yahoo.com/news/palatin-technologies-inc-nyse…
Unerklärlich warum so viele kalte Füsse bekommen. Solche Nachforderungen sind bestimmt nicht selten. Kalte Füsse ist was für den Freund der macht sie wieder warm. Ich bleib drin und kaufe nach Weinn die Zulassung kommt bin ich saniert und wenn niicht dann auch nicht arm. Völlig unserständlich der Kurs.
Antwort auf Beitrag Nr.: 59.246.389 von meissner7309 am 19.11.18 09:32:19So wie ich die Info verstanden habe, geht es bei den geforderten Daten um das Label.
Also zB nicht mehr als 10 x pro Tag. Bei normaler Dosierung gibt es in den Studien keine
Probleme. Die Anforderung der Daten für das Label ist für mich eher ein Indiz das
es mit der Zulassung klappt.
Der Schaden ist "nur" die Verzögerung.
Für viele aber die Chance nochmal günstig reizukommen.
Also zB nicht mehr als 10 x pro Tag. Bei normaler Dosierung gibt es in den Studien keine
Probleme. Die Anforderung der Daten für das Label ist für mich eher ein Indiz das
es mit der Zulassung klappt.
Der Schaden ist "nur" die Verzögerung.
Für viele aber die Chance nochmal günstig reizukommen.
bevor es vergessen wird
es sind noch andere Medikamente in der Pipline
also 0 wird eher unwahscheinlich
https://www.palatin.com/research-focus/clinical-pipeline/
es sind noch andere Medikamente in der Pipline
also 0 wird eher unwahscheinlich
https://www.palatin.com/research-focus/clinical-pipeline/
Antwort auf Beitrag Nr.: 59.250.925 von Reinerle am 19.11.18 17:35:55Naja, es stellt sich hier eher die Frage, warum PTN diese kritischen Blutdruck-Daten nicht direkt mitgeliefert hat?! Schon aufgrund der vorherigen Blutdruckprobelmatik mit der alten Formulierung wäre es angebracht gewesen solche Daten direkt mitzuliefern.
Für mich kann das nur folgendes bedeuten: Die Blutdruck-Daten wurden bewusst nicht eingereicht, weil sie vermutlich eine Erhöhung des Blutdrucks zeigten.
Für mich kann das nur folgendes bedeuten: Die Blutdruck-Daten wurden bewusst nicht eingereicht, weil sie vermutlich eine Erhöhung des Blutdrucks zeigten.
pipeline
unwahrscheinlich
unwahrscheinlich
Antwort auf Beitrag Nr.: 59.251.270 von petermull am 19.11.18 18:05:53Spekulation. Glaube nicht das die sich die Vermarktung sichern und dann anfangen zu zocken.
Die Muschis verlassen das sinkende Schiff
Antwort auf Beitrag Nr.: 59.251.270 von petermull am 19.11.18 18:05:53Ist schon richtig das man in Studien prüft, was passiert, wenn man das medi überdosiert.
Dies trifft aber für alle medis zu.
Das dürfte wohl für jeden klar sein, dass man zB Schlaftabletten nur eine nimmt und nicht
eine ganze Packung.
Die FDA will nun wissen, was passiert mit dem Blutdruck wenn man Vyleesi überdosiert.
Wie man das ganze werten sollte, sieht man schon daran, dass Verlusste bei relativ geringen
Umsätze zu beobachten sind und Instis einsteigen und Kleinanleger raus gehen.
Dies trifft aber für alle medis zu.
Das dürfte wohl für jeden klar sein, dass man zB Schlaftabletten nur eine nimmt und nicht
eine ganze Packung.
Die FDA will nun wissen, was passiert mit dem Blutdruck wenn man Vyleesi überdosiert.
Wie man das ganze werten sollte, sieht man schon daran, dass Verlusste bei relativ geringen
Umsätze zu beobachten sind und Instis einsteigen und Kleinanleger raus gehen.
Ich denke die meisten von uns, hätten sich vor einem Monat einen Kurs zwischen 0.50und 0.60 € gewünscht, um nochmal ordentlich nachzulegen kurz vor einer wahrscheinlich Zulassung. Für alle die an dieses Unternehmen glauben hat sich nichts geändert, nur für die kurzfristigen Spekulanten ist es gerade nicht interessant. Mein jetziger Kaufkurs gefällt mir besser als vor einer Woche!
Palatin Tech +8.8% as CEO, COO/CFO disclose share purchases.
CEO Carl Spana purchased 20,000 shares on Friday at an average price of $0.7883
CFO/COO Stephen Wills also acquired 20,000 shares on Friday
https://seekingalpha.com/news/3411094-palatin-tech-plus-8_8-…
Da haben also diese beiden insgesamt 40.000 Shares gekauft zu ungefähr 0,7883 / Aktie.
Spana hat jetzt jetzt insgesamt 4.348.102 Stk.
Wills hat 3.918.239
Ich denke schon, dass die Herren stark an steigenden Kursen interessiert sind.
CEO Carl Spana purchased 20,000 shares on Friday at an average price of $0.7883
CFO/COO Stephen Wills also acquired 20,000 shares on Friday
https://seekingalpha.com/news/3411094-palatin-tech-plus-8_8-…
Da haben also diese beiden insgesamt 40.000 Shares gekauft zu ungefähr 0,7883 / Aktie.
Spana hat jetzt jetzt insgesamt 4.348.102 Stk.
Wills hat 3.918.239
Ich denke schon, dass die Herren stark an steigenden Kursen interessiert sind.
Antwort auf Beitrag Nr.: 59.254.267 von boersenkeks am 20.11.18 06:33:37Ja glaube ich zwar auch, aber warum kaufen die nur so eine kleine Anzahl Aktien wenn der Kurs doch soooo günstig ist? Haben die nicht mehrauf der hohen Kante 😂
Antwort auf Beitrag Nr.: 59.258.125 von rallyseeker am 20.11.18 13:35:29Kann mir vorstellen das die ein Zeichen setzen wollten.
Ein Zeichen Unglaubwürdigkeit? Kurs rauscht knapp 30% runter und Carl kauft nur 20k shares? Weiß nicht ob es ein gutes Zeichen ist? Oder möchte er somit die verbliebenen nicht noch mehr in Verkaufslaune bringen? Anderseits die Istis haben nachgekauft. Wem ist hier glauben zu schenken, wissen diese evtl. noch etwas mehr als Carl?
Antwort auf Beitrag Nr.: 59.266.534 von Dumounde am 21.11.18 11:04:22Mein Reden mit der Anzahl der nachgekaufen Shares durch Carl, aber was sollen die Instis denn mehr wissen als der CEO der Firma? 🤔
Antwort auf Beitrag Nr.: 59.277.004 von rallyseeker am 22.11.18 13:19:50Paladin steigt ja mal wieder seit 2 Tagen---wie komisch---hat wohl der Chef nen wahnsinns Furz im Chefsessel gelassen, der von den Amis als äußerst positives Zeichen gewertet wird?
Antwort auf Beitrag Nr.: 59.327.714 von dollilolli am 29.11.18 18:03:56Extrem geistreicher Beitrag. Wäre schön, wenn wenigstens der Firmenname beim nächsten Mal richtig wäre.
Antwort auf Beitrag Nr.: 59.328.194 von meissner7309 am 29.11.18 19:03:47
Zitat von meissner7309: Extrem geistreicher Beitrag. Wäre schön, wenn wenigstens der Firmenname beim nächsten Mal richtig wäre.
Antwort auf Beitrag Nr.: 59.328.716 von PrinzStorno am 29.11.18 20:07:42Hervorragendes Niveau heute  Hat jemand was konstruktives? VG
Hat jemand was konstruktives? VG
 Hat jemand was konstruktives? VG
Hat jemand was konstruktives? VG
Antwort auf Beitrag Nr.: 59.328.731 von PrinzStorno am 29.11.18 20:09:44Nee, drum frag ich, warum Palatin---ich hoffe jetzt richtig---die letzten 2 Tage anzieht? 0 verwertbare Nachrichten irgendwo entdeckt.
Antwort auf Beitrag Nr.: 59.328.830 von dollilolli am 29.11.18 20:22:15Neuer Lizenzdeal soll bevorstehen...quelle: diverse US Foren ... Decken sich alle neu ein
Antwort auf Beitrag Nr.: 59.329.397 von Foerderung_ am 29.11.18 21:45:50Danke sehr!
Antwort auf Beitrag Nr.: 59.329.478 von dollilolli am 29.11.18 21:54:46Hab selbe um 8:30 nochmal 2k zu 0.67 nachgeschossen. Denke bis Februar stehen wir wieder locker bei 1€. IMO
Antwort auf Beitrag Nr.: 59.329.529 von Foerderung_ am 29.11.18 22:01:53Hab im Moment leider nichts mehr zum Nachschießen, hänge noch in etlichen anderen Aktien drin, aber im Moment ist wahrscheinlich eine breit gefächerte Korrektur angesagt u.a., meiner Meinung nach, aufgrund der Politik von Trump, was man aber nicht unbedingt auf Biotech-Aktien ummünzen kann, weil da ja andere Kriterien ne Rolle spielen. Hoffe, es wird werden und das Nachgeliefert wird, was die FDA haben bzw. sehen möchte. Bin hier nicht unbedingt die große Leuchte, aber bei manchen Dingen muß man halt nur 1 und 1 zusammen zählen.
Was stehen denn als nächstes für (offizielle) Termine an?
Antwort auf Beitrag Nr.: 59.348.795 von Schlotz68 am 03.12.18 10:47:01Wahrscheinlich gar keine, wenn ich so auf Realtime sehe, wie uns heute der Ami mal wieder anfängt, den Kopf langsam zu waschen!
Bei so wenig Volumem kann man das eher weniger anführen.
Hier tut AMAG im Rahmen einer gestrigen Conference
(https://www.maconferenceforwomen.org/conference/agenda/) schon was hinsichtlich der Vermarktung von VYLEESI mittels Initiierung von digitalen Foren zum Austausch:
11:05 am – 11:25 am: Connecting Through Social Networks to Achieve Better Sexual Health Outcomes
Speaker: Meghan Rivera, vice president, digital engagement and women’s health marketing, AMAG Pharmaceuticals
Sexual health can be uncomfortable for women to talk about—whether it be with her partner, friends or even her healthcare provider – which can lead to women not seeking necessary treatment. Creating a safe and supportive environment in which women can connect with others and learn how to talk about their sexual health is critical and may lead to better health outcomes. Attend this session to learn how digital health communities can help empower women to seek support, tools and information about their sexual health.
(https://www.maconferenceforwomen.org/conference/agenda/) schon was hinsichtlich der Vermarktung von VYLEESI mittels Initiierung von digitalen Foren zum Austausch:
11:05 am – 11:25 am: Connecting Through Social Networks to Achieve Better Sexual Health Outcomes
Speaker: Meghan Rivera, vice president, digital engagement and women’s health marketing, AMAG Pharmaceuticals
Sexual health can be uncomfortable for women to talk about—whether it be with her partner, friends or even her healthcare provider – which can lead to women not seeking necessary treatment. Creating a safe and supportive environment in which women can connect with others and learn how to talk about their sexual health is critical and may lead to better health outcomes. Attend this session to learn how digital health communities can help empower women to seek support, tools and information about their sexual health.
Sorry das ich nach frage aber bin jetzt schon eine Weile nicht mehr hier im Forum gewesen. Steht der Termin im April 2019 noch für die FDA Erlaubnis oder ist das Thema jetzt komplett vom Tisch und hat sich nach hinten verschoben?
Weiß keine Sau Sorry
FDA-Termin mW am 23.03.2019
Augenscheinlich schwindet das Vertrauen in die Zulassung. Warum sollte die Aktie dermaßen auf Tauchstation gehen. Naja Biotech ist reiner Zock. Kann man auch ins Casino gehen
Antwort auf Beitrag Nr.: 59.492.988 von meissner7309 am 21.12.18 20:30:41
NBI am Abkacken. Deswegen sinkt der Kurs.
Zitat von meissner7309: Augenscheinlich schwindet das Vertrauen in die Zulassung. Warum sollte die Aktie dermaßen auf Tauchstation gehen. Naja Biotech ist reiner Zock. Kann man auch ins Casino gehen
NBI am Abkacken. Deswegen sinkt der Kurs.
Jetzt hab ich mal ne blöde Frage
Palatin hat ja Vereinbarungen mit China und Südkorea. Haben diese Länder ein seperates Zulassungsverfahren oder ist es expliziet wichtig das zuerst die FDA Zulassung in USA kommt?
Palatin hat ja Vereinbarungen mit China und Südkorea. Haben diese Länder ein seperates Zulassungsverfahren oder ist es expliziet wichtig das zuerst die FDA Zulassung in USA kommt?
Ich sehe hier reine Vorsichtsmaßnahmen die momentan überall am Aktienmarkt stattfinden. Der Aktienausverkauf geht hier wie auch in anderen Marktsegmenten erstmal weiter.
Nachbörslich + 25
Antwort auf Beitrag Nr.: 59.532.259 von bundi007 am 31.12.18 09:16:35Tatsächlich, Nasdaq nachbörslich Kurs $0,87 (+25,81%) 😃
Mal schauen, wie sich der Kurs die nächsten Wochen und Monate entwickelt.
Mal schauen, wie sich der Kurs die nächsten Wochen und Monate entwickelt.
Volumen ist dabei auch nicht ganz unwichtig...
Bei dem kleinen Volumen. Da tut sich gar nichts
Die Frage die sich stellt ist doch ob die Nachreichung den geplanten Termin im März verzögert. Komisch ich war beim April aber gut März ist auch okay.
Verschiebt sich der Termin oder nicht das wäre wichtig zu wissen. Ich habe nirgendwo was gefunden. Das Produkt wird durchgewunken. Bei allem was berichtet wurde würde es mich massiv wundern. Aber ist nur meine Meinung.
Verschiebt sich der Termin oder nicht das wäre wichtig zu wissen. Ich habe nirgendwo was gefunden. Das Produkt wird durchgewunken. Bei allem was berichtet wurde würde es mich massiv wundern. Aber ist nur meine Meinung.
Antwort auf Beitrag Nr.: 59.542.093 von Geldverbrennung am 02.01.19 14:59:16...massiv wundern wenn es nicht klappen sollte.
Bei amag war zu lesen, dass sich die Zulassung um 3 bis 6 Monate verschieben könnte, wegen den
zusätzlichen Daten bei Überdosierung. (Für mich ein Indiz, dass die Zulassung warscheinlich kommt,
das Label muss aber noch festgelegt werden)
zusätzlichen Daten bei Überdosierung. (Für mich ein Indiz, dass die Zulassung warscheinlich kommt,
das Label muss aber noch festgelegt werden)
Wenn Palatin die geforderte Studie in der Zeit bis März nachreicht glaube ich nicht das sich der Termin verschiebt. Wieso auch
Am Mittwoch wird amag in seinem Bericht sicher auch was zu vyleesi veröffentlichen.
Dann sind hoffentlich die Unsicherheiten weg. Ich rechne mit der Zulassung im September.
Bis dahin werde ich weiter zukaufen.
Kann mir einer mal einen Tipp geben.
Ich bin bei comdirect. Die bieten leider keine call`s zu amag an.
Wie könnte ich an solche Scheine kommen ohne die Bank zu wechseln.
Dann sind hoffentlich die Unsicherheiten weg. Ich rechne mit der Zulassung im September.
Bis dahin werde ich weiter zukaufen.
Kann mir einer mal einen Tipp geben.
Ich bin bei comdirect. Die bieten leider keine call`s zu amag an.
Wie könnte ich an solche Scheine kommen ohne die Bank zu wechseln.
Antwort auf Beitrag Nr.: 59.570.546 von apano am 06.01.19 19:22:40AMAG Pharmaceuticals, Inc. (“AMAG”), Palatin Technologies, Inc.’s (“Palatin”) exclusive North American licensee of Vyleesi™ (bremelanotide), provided an update today on the regulatory development of Vyleesi, including noting that the U.S. Food and Drug Administration (the “FDA”) has extended the Prescription Drug User Fee Act (“PDUFA”) date for by three months to June 23, 2019.
An FDA-requested frequent-dosing study with premenopausal volunteers assessing short term daily use of Vyleesi has been initiated. Study results are anticipated to be submitted to the FDA prior to the updated PDUFA date of June 23, 2019.
https://www.sec.gov/Archives/edgar/data/911216/0001654954190…
An FDA-requested frequent-dosing study with premenopausal volunteers assessing short term daily use of Vyleesi has been initiated. Study results are anticipated to be submitted to the FDA prior to the updated PDUFA date of June 23, 2019.
https://www.sec.gov/Archives/edgar/data/911216/0001654954190…
Antwort auf Beitrag Nr.: 59.532.259 von bundi007 am 31.12.18 09:16:35
Tagestief war bei 0,531 - 20 % auf tradegate

Tief von 2017 erreicht
wieder mal so ein angeblicher Tenbagger bei sharedeals
natürlich nur so lange bis der Fisch verkauft hat
Zitat von bundi007: Nachbörslich + 25
Tagestief war bei 0,531 - 20 % auf tradegate


Tief von 2017 erreicht

wieder mal so ein angeblicher Tenbagger bei sharedeals

natürlich nur so lange bis der Fisch verkauft hat
Antwort auf Beitrag Nr.: 59.575.298 von bastisuperman am 07.01.19 15:08:57hey basti,
ganz cool bleiben.
Bei 0,53 hätte ich gern nochmal nachgekauft.
Wenn sich die Zulassung um 3 Monate verschiebt, ist das doch eine gute Nachricht.
Ich hatte mit 6 Monaten gerechnet.
ganz cool bleiben.
Bei 0,53 hätte ich gern nochmal nachgekauft.
Wenn sich die Zulassung um 3 Monate verschiebt, ist das doch eine gute Nachricht.
Ich hatte mit 6 Monaten gerechnet.
Antwort auf Beitrag Nr.: 59.576.282 von apano am 07.01.19 16:56:00Das sieht für mich eher nach Stop Loss abfischen aus. Einmal kurz runter um Stops auszulösen und dann gleich wieder hoch.
Da werden einige blöd aus der Wäsche gucken,wenn plötzlich die guten Palatin Aktien aus dem Depot gespült wurden
Wir stehen kurz vor einer wichtigen Entscheidung, da verkauft man doch nicht freiwillig. Zukaufen ist da eher die Devise, bei den Aussichten.
Nur meine persönliche Meinung.
Da werden einige blöd aus der Wäsche gucken,wenn plötzlich die guten Palatin Aktien aus dem Depot gespült wurden

Wir stehen kurz vor einer wichtigen Entscheidung, da verkauft man doch nicht freiwillig. Zukaufen ist da eher die Devise, bei den Aussichten.
Nur meine persönliche Meinung.
Schade das durch das Nachreichen sich die Genehmigung ggf. Verzögert. Es wird einen massiven Einbruch geben sollte Ende März noch keine Freigabe der FDA erfolgen.
Allerdings knallt es sobald die Genehmigung kommt...nur wann?!
Allerdings knallt es sobald die Genehmigung kommt...nur wann?!
Antwort auf Beitrag Nr.: 59.576.282 von apano am 07.01.19 16:56:00hi apano, will dir deine laune ja nicht vermiesen, aber wo steht denn bitte dass sich die zulassung um 3 monate verschiebt? Es wurde lediglich eine fristverlängerung der fda um diese 3 monate zur nachreichung der studie seitens amag/palatin gewährt. Die durchschnittliche dauer von einreichung bis freigabe durch fda bei pharmazeutischen wirkstoffen habe ich bei statista.com gefunden. hoffe zwar auch das es schneller von statten geht, aber 3 monate glaube ich kaum!! https://de.statista.com/statistik/daten/studie/591453/umfrag…
Antwort auf Beitrag Nr.: 59.593.064 von rallyseeker am 09.01.19 14:39:56Ich laß mich gern korigieren, nach meinem Erkentnisstand hat amag vor einiger Zeit kommuniziert,
das die FDA das Meeting Anfang Jannuar gestrichen hat und Daten für eine Überdosierung angefordert
hat. Der ursprüngliche Zulassungstermien war Ende März.
Deswegen erwartet amag eine Verspätung von 3-6 Monate beim Zulassungsentscheid.
Wenn jetzt die Zulassung im Juni und nicht erst im September kommt, finde ich das gut.
das die FDA das Meeting Anfang Jannuar gestrichen hat und Daten für eine Überdosierung angefordert
hat. Der ursprüngliche Zulassungstermien war Ende März.
Deswegen erwartet amag eine Verspätung von 3-6 Monate beim Zulassungsentscheid.
Wenn jetzt die Zulassung im Juni und nicht erst im September kommt, finde ich das gut.
Na schön das die Aktie noch nicht ganz vom Markt verschwunden ist.
Und meine Einschätzung vom Oktober, dass wir Kurse um die 70 Cent sehen
müssen bevor ich wieder einsteige muss ich ja wohl deutlich nach unten korrigieren.
Und was musste ich mir alles anhören wie ich nur so was posten könne.
Einige haben den Staffelstab noch in der Hand und müssen wohl schnell noch Käufer finden.
Nach der "tolen" Nachrichtenlage sind wohl eher Kurse um die 44 -46 Cent interessant um wieder
einzusteigen.
Dann werde ich mal eine Kauforder in diesen Regionen platzieren.
Und meine Einschätzung vom Oktober, dass wir Kurse um die 70 Cent sehen
müssen bevor ich wieder einsteige muss ich ja wohl deutlich nach unten korrigieren.
Und was musste ich mir alles anhören wie ich nur so was posten könne.
Einige haben den Staffelstab noch in der Hand und müssen wohl schnell noch Käufer finden.
Nach der "tolen" Nachrichtenlage sind wohl eher Kurse um die 44 -46 Cent interessant um wieder
einzusteigen.
Dann werde ich mal eine Kauforder in diesen Regionen platzieren.
Antwort auf Beitrag Nr.: 59.596.571 von Moneymaker123 am 09.01.19 20:46:09Das du mit deiner Einschätzung völlig richtig gelegen hast beruht auf einem Umstand den niemand vorher erahnen konnte. Weitere Verzögerungen werden den Kurs sehr wahrscheinlich weiter stark beeinflussen. Sollte eine Zulassung kommen erwarte ich hier aber auch kein absolutes Kursfeuerwerk. Das sieht mir eher nach einem Langinvestment aus.
Antwort auf Beitrag Nr.: 59.596.571 von Moneymaker123 am 09.01.19 20:46:09Warum willst einsteigen, wenn du die Vermutung hast, das die Firma vom Markt verschwindet. Den Sinn versteh ich nicht. Letztlich ist es wie bei jeder Biotech Penny Aktie. Je Näher die mögliche Zulassung kommt, wird mehr gezockt, dann wird die Aktie anziehen. Wenn es durchgeht, geht die Wette auf, wenn nicht, wie bei so manch anderer gehts 80 % runter mindestens. Also eine simple Wette. Die große Frage ist, wenn man die FDA Entscheidung nicht abwarten will, wann man für den Zock davor einsteigen kann.....
Punkt 7.01. Verordnung FD-Offenlegung.
AMAG Pharmaceuticals, Inc. („AMAG“), der ausschließliche nordamerikanische Lizenznehmer von Vyleesi ™ (Bremelanotid) von Palatin Technologies, Inc. („Palatin“), hat heute ein Update zur regulatorischen Entwicklung von Vyleesi geliefert, einschließlich der Feststellung der USA Die Food and Drug Administration (die „FDA“) hat den Termin für verschreibungspflichtige Medikamentenkosten („PDUFA“) um drei Monate bis zum 23. Juni 2019 verlängert.
Eine von der FDA geforderte Studie zur häufigen Verabreichung von Probanden mit prämenopausaler Untersuchung, die die kurzfristige tägliche Anwendung von Vyleesi bewertet, wurde eingeleitet. Die Ergebnisse der Studie werden voraussichtlich vor dem aktualisierten PDUFA-Datum vom 23. Juni 2019 bei der FDA eingereicht.
Dieser Bericht enthält zukunftsgerichtete Aussagen im Sinne von Abschnitt 27A des Securities Act von 1933, Abschnitt 21E des Securities Exchange Act von 1934 und wie dieser Begriff in dem Private Securities Litigation Reform Act von 1995 definiert ist Darin werden keine historischen Fakten beschrieben, darunter auch Erwartungen hinsichtlich der Anforderungen der FDA.Überzeugung, dass die zusätzliche Studie vor dem PDUFA-Datum durchgeführt und Daten übermittelt werden können;die Auswirkungen der möglichen Zulassung von Vyleesi auf den Zeitplan; und Erwartungen hinsichtlich weiterer Diskussionen mit der FDA sind zukunftsgerichtete Aussagen, die Risiken und Unsicherheiten beinhalten, die dazu führen können, dass die tatsächlichen Ergebnisse wesentlich von den in diesen zukunftsgerichteten Aussagen erörterten abweichen.
Solche Risiken und Unwägbarkeiten können die Geschäftsergebnisse, die Rentabilität und die Cashflows von Palatin erheblich und nachteilig beeinflussen, was sich wiederum erheblich und negativ auf den Aktienkurs von Palatin auswirken würde. Palatin warnt Sie davor, sich auf zukunftsgerichtete Aussagen zu verlassen, die sich nur auf den Tag beziehen, an dem sie gemacht werden. Palatin lehnt jede Verpflichtung ab, solche Aussagen öffentlich zu aktualisieren oder zu überarbeiten, um etwaige Änderungen der Erwartungen oder Ereignisse, Bedingungen oder Umstände widerzuspiegeln, auf denen solche Aussagen beruhen, oder die die Wahrscheinlichkeit beeinflussen können, dass die tatsächlichen Ergebnisse von den in Ziff die zukunftsgerichteten Aussagen. haben einen erheblichen und nachteiligen Einfluss auf den Aktienkurs von Palatin.Palatin warnt Sie davor, sich auf zukunftsgerichtete Aussagen zu verlassen, die sich nur auf den Tag beziehen, an dem sie gemacht werden. Palatin lehnt jede Verpflichtung ab, solche Aussagen öffentlich zu aktualisieren oder zu überarbeiten, um etwaige Änderungen der Erwartungen oder Ereignisse, Bedingungen oder Umstände widerzuspiegeln, auf denen solche Aussagen beruhen, oder die die Wahrscheinlichkeit beeinflussen können, dass die tatsächlichen Ergebnisse von den in Ziff die zukunftsgerichteten Aussagen. haben einen erheblichen und nachteiligen Einfluss auf den Aktienkurs von Palatin.Palatin warnt Sie davor, sich auf zukunftsgerichtete Aussagen zu verlassen, die sich nur auf den Tag beziehen, an dem sie gemacht werden. Palatin lehnt jede Verpflichtung ab, solche Aussagen öffentlich zu aktualisieren oder zu überarbeiten, um etwaige Änderungen der Erwartungen oder Ereignisse, Bedingungen oder Umstände widerzuspiegeln, auf denen solche Aussagen beruhen, oder die die Wahrscheinlichkeit beeinflussen können, dass die tatsächlichen Ergebnisse von den in Ziff die zukunftsgerichteten Aussagen.
AMAG Pharmaceuticals, Inc. („AMAG“), der ausschließliche nordamerikanische Lizenznehmer von Vyleesi ™ (Bremelanotid) von Palatin Technologies, Inc. („Palatin“), hat heute ein Update zur regulatorischen Entwicklung von Vyleesi geliefert, einschließlich der Feststellung der USA Die Food and Drug Administration (die „FDA“) hat den Termin für verschreibungspflichtige Medikamentenkosten („PDUFA“) um drei Monate bis zum 23. Juni 2019 verlängert.
Eine von der FDA geforderte Studie zur häufigen Verabreichung von Probanden mit prämenopausaler Untersuchung, die die kurzfristige tägliche Anwendung von Vyleesi bewertet, wurde eingeleitet. Die Ergebnisse der Studie werden voraussichtlich vor dem aktualisierten PDUFA-Datum vom 23. Juni 2019 bei der FDA eingereicht.
Dieser Bericht enthält zukunftsgerichtete Aussagen im Sinne von Abschnitt 27A des Securities Act von 1933, Abschnitt 21E des Securities Exchange Act von 1934 und wie dieser Begriff in dem Private Securities Litigation Reform Act von 1995 definiert ist Darin werden keine historischen Fakten beschrieben, darunter auch Erwartungen hinsichtlich der Anforderungen der FDA.Überzeugung, dass die zusätzliche Studie vor dem PDUFA-Datum durchgeführt und Daten übermittelt werden können;die Auswirkungen der möglichen Zulassung von Vyleesi auf den Zeitplan; und Erwartungen hinsichtlich weiterer Diskussionen mit der FDA sind zukunftsgerichtete Aussagen, die Risiken und Unsicherheiten beinhalten, die dazu führen können, dass die tatsächlichen Ergebnisse wesentlich von den in diesen zukunftsgerichteten Aussagen erörterten abweichen.
Solche Risiken und Unwägbarkeiten können die Geschäftsergebnisse, die Rentabilität und die Cashflows von Palatin erheblich und nachteilig beeinflussen, was sich wiederum erheblich und negativ auf den Aktienkurs von Palatin auswirken würde. Palatin warnt Sie davor, sich auf zukunftsgerichtete Aussagen zu verlassen, die sich nur auf den Tag beziehen, an dem sie gemacht werden. Palatin lehnt jede Verpflichtung ab, solche Aussagen öffentlich zu aktualisieren oder zu überarbeiten, um etwaige Änderungen der Erwartungen oder Ereignisse, Bedingungen oder Umstände widerzuspiegeln, auf denen solche Aussagen beruhen, oder die die Wahrscheinlichkeit beeinflussen können, dass die tatsächlichen Ergebnisse von den in Ziff die zukunftsgerichteten Aussagen. haben einen erheblichen und nachteiligen Einfluss auf den Aktienkurs von Palatin.Palatin warnt Sie davor, sich auf zukunftsgerichtete Aussagen zu verlassen, die sich nur auf den Tag beziehen, an dem sie gemacht werden. Palatin lehnt jede Verpflichtung ab, solche Aussagen öffentlich zu aktualisieren oder zu überarbeiten, um etwaige Änderungen der Erwartungen oder Ereignisse, Bedingungen oder Umstände widerzuspiegeln, auf denen solche Aussagen beruhen, oder die die Wahrscheinlichkeit beeinflussen können, dass die tatsächlichen Ergebnisse von den in Ziff die zukunftsgerichteten Aussagen. haben einen erheblichen und nachteiligen Einfluss auf den Aktienkurs von Palatin.Palatin warnt Sie davor, sich auf zukunftsgerichtete Aussagen zu verlassen, die sich nur auf den Tag beziehen, an dem sie gemacht werden. Palatin lehnt jede Verpflichtung ab, solche Aussagen öffentlich zu aktualisieren oder zu überarbeiten, um etwaige Änderungen der Erwartungen oder Ereignisse, Bedingungen oder Umstände widerzuspiegeln, auf denen solche Aussagen beruhen, oder die die Wahrscheinlichkeit beeinflussen können, dass die tatsächlichen Ergebnisse von den in Ziff die zukunftsgerichteten Aussagen.
Der offizielle Termin für die fehlenden Unterlagen ist der 23.06.2019 und nicht wie hier bereits gelesen März. Bereits im Vorfeld ist dieser Zeitraum benannt worden und stellt somit die bereits angenommene Verzögerung dar. Allen unvestierten viel Erfolg
Antwort auf Beitrag Nr.: 59.640.185 von PrinzStorno am 16.01.19 00:28:1523.06.19 klingt doch klasse. Ein strahlender Tag mitten im Sommer und Palatin steht bei 5 USD. Was will man mehr!
Auf einem Sonntag?
Antwort auf Beitrag Nr.: 59.646.188 von Geldverbrennung am 16.01.19 18:19:20Der 23.06. ist ein Sonntag. Wenn Palatin dann eim Produkt hat sieht die Dach über kurz oder lang wahrscheinlich anders auf. Neue Partnerschaften werden vermutlich auch erst dann kommen. Und auch wenn es noch dauern wird, aber die Pipeline von Palatin ist voll mit anderen Projekten.
In anderen Foren kann man zu dieser Aktie im Moment tägliche Aktivitäten feststellten. Kann mir jemand sagen wann Palatin die nächsten Zahlen vorlegen wird. Feb 2019? Konnte nichts finden.
Antwort auf Beitrag Nr.: 59.648.984 von PrinzStorno am 16.01.19 23:46:34Laut Finanznet.de sollen die am 31.3.19 kommen. Wenn die Studie erst im Juni eingereicht wird kann die Genehmigung erst ca. September - Dezember erfolgen. Ist das echt so spät angedacht?
Antwort auf Beitrag Nr.: 59.650.958 von Geldverbrennung am 17.01.19 10:11:01Wie zu lesen war sollen die Ergebnisse noch vor dem 23.06. eingereicht werden. Ich denke das einige im Vorfeld und nach Freigabe durch die FDA zurück einsteigen werden. Auch die üblichen Zocker werden nicht lange auf sich warten lassen.
Antwort auf Beitrag Nr.: 59.651.429 von PrinzStorno am 17.01.19 10:57:56AMAG Pharmaceuticals, Inc. (NASDAQ: AMAG) und Palatin Technologies, Inc. (NYSE: PTN) gaben bekannt, dass der PDUFA-Termin für Vyleesi (Bremelanotid) um drei Monate bis zum 23. Juni 2019 verlängert wurde -Dosierungsstudie mit prämenopausalen Freiwilligen, die die kurzfristige tägliche Anwendung von Vyleesi bewerten, wurde eingeleitet. Die Ergebnisse werden der FDA vor dem aktualisierten PDUFA-Datum vom 23. Juni 2019 übermittelt.
2019 BioPharmCatalyst
2019 BioPharmCatalyst
Antwort auf Beitrag Nr.: 59.665.181 von onkelen am 18.01.19 19:17:18Danke das war sehr verständlich 

Antwort auf Beitrag Nr.: 59.674.779 von Geldverbrennung am 21.01.19 09:59:12Es wird so ablaufen wie bei vielen anderen Biotech Aktien. Wenn die angeforderte Studie eingereicht wird werden höchstwahrscheinlich viele Zocker wieder einsteigen in der Hoffnung dass das Mittel zugelassen wird und spätestens am Tag der Entscheidung beziehungsweise wenn die Empfehlung an die FDA gefällt wird, wird der Kurs in die eine oder andere Richtung weit ausschlagen. Es ist also nichts anderes als ein reiner Zock. Wenn man an eine Zulassung wirklich glaubt, spielen fünf oder zehn Cent Kursunterschied überhaupt keine Rolle, weil man davon ausgehen kann, dass der Kurs nach Zulassung wesentlich höher da stehen wird. Es wird aber auch genug andere geben die versuchen mit dem Zock vorher Geld zu verdienen. Bei denen spielt der Einstiegspunkt jetzt natürlich eine große Rolle. Die versuchen jetzt einen günstigen Einstiegspunkt zu treffen und nehmen dann den zu erwartenden Kursgewinn bei Unterlageneinreichung zum Anlass, um sich zu verabschieden. Wie so etwas aussehen kann sieht man derzeit bei Trevena perfekt. Viel Zock vorher, dann doch ganz knapp keine Zulassung und der jähe Abstieg.
Antwort auf Beitrag Nr.: 59.674.911 von meissner7309 am 21.01.19 10:21:36Ja stimmt allerdings sehe ich die Wahrscheinlichkeit für Palatin die Genehmigung zu erhalten recht groß. Alles spricht für eine Zulassung. Und dann geht's hier richtig rund. Der Entscheidungstag fällt wirklich auf einen Sonntag? Das finde ich sehr komisch. Allerdings genug Zeit zur Not am Montag Morgen einzusteigen. Das wäre zumindest sicher.
Ich frage mich ob vorher noch eine KE stattfindet. Genehmigt ist sie für den Fall der Fälle. Gibt's noch eine HV vorher? Vielleicht steht noch was an. Dann wäre es besser die Finger bis zum Juni erstmal fern zu halten.
Ich frage mich ob vorher noch eine KE stattfindet. Genehmigt ist sie für den Fall der Fälle. Gibt's noch eine HV vorher? Vielleicht steht noch was an. Dann wäre es besser die Finger bis zum Juni erstmal fern zu halten.
Antwort auf Beitrag Nr.: 59.676.045 von Geldverbrennung am 21.01.19 12:49:09Sicher ist gar nichts in meinen Augen. Um nochmal auf Trevena zurückzukommen. Da wurde auch im Vorfeld davon ausgegangen, dass die ihr Mittel durchbekommen. Dann gab es die Abstimmung in der Kommission (die gibt die Empfehlung an die FDA, die muss sich aber nicht daran halten) und die hat mit einer Stimme Mehrheit dagegen gestimmt. Die FDA ist in diesem Fall gefolgt und es kam zum großen Knall. Es kommt echt darauf an, wer in der Kommission sitzt und wie die gegenüber dem Mittel stehen. Wenn du da ein paar Skeptiker hast, die aufgrund des erhöhten Blutdrucks mehr Risiken als Nutzen sehen, dann kann das auch ganz schnell nach hinten losgehe. Da können die Ergebnisse vorher noch so toll sein.
Fakt ist, der erste Zoll wird dann eintreten, wenn bekannt gegeben wird, dass die nachgeartete Studie eingereicht wurde, egal wie die ausgefallen ist und das wird vor dem 23. Juni sein, wenn ich das richtig gelesen habe und nicht erst am letzten tag. Die Frage ist halt für den gemeinen Zucker, wann wird das sein und wie tief geht es vorher oder stützen genug Geier den Kurs jetzt schon, eben weil nicht bekannt ist, wann genau die Studie fertig ist. Keiner will zu spät drin sein. Es ist schon ein heisses Eisen. Kann halt gut gehen und richtig den Bach runter
Fakt ist, der erste Zoll wird dann eintreten, wenn bekannt gegeben wird, dass die nachgeartete Studie eingereicht wurde, egal wie die ausgefallen ist und das wird vor dem 23. Juni sein, wenn ich das richtig gelesen habe und nicht erst am letzten tag. Die Frage ist halt für den gemeinen Zucker, wann wird das sein und wie tief geht es vorher oder stützen genug Geier den Kurs jetzt schon, eben weil nicht bekannt ist, wann genau die Studie fertig ist. Keiner will zu spät drin sein. Es ist schon ein heisses Eisen. Kann halt gut gehen und richtig den Bach runter
Antwort auf Beitrag Nr.: 59.676.996 von meissner7309 am 21.01.19 14:57:42Besser kann man es nicht zusammenfassen.
Experten erwarten, dass Bremelanotid Anhänger finden wird
Ein kürzlich hergestelltes US-Medikament, das Frauen mit hypoaktiver sexueller Luststörung (HSDD) helfen soll, dürfte nach Einschätzung von Experten wahrscheinlich höhere Einnahmegeschwindigkeiten verzeichnen als seine jüngeren Konkurrenten.Die Einnahme von Vyleesi (Bromelanotid), einem von Amag Pharmaceuticals zur Behandlung von Frauen mit HSDD hergestellten Medikament, wird voraussichtlich langsam sein, wenn es zugelassen wird, aber es ist unwahrscheinlich, dass es den gleichen Herausforderungen wie Sprout's Addyi, einem bereits zugelassenen ähnlichen Medikament, begegnet.
HSDD ist eine Erkrankung, bei der Frauen das Interesse an Sex verlieren. Während Experten mit Analysten übereinstimmten, dass die subkutane Verabreichung und das Verträglichkeitsprofil von Bremelanotid als signifikante Markthürden bezeichnet wurden, waren die meisten der Meinung, beide seien nicht unüberwindbar und Bremelanotid werde Nischennutzung finden.
Die Forscher der Phase III-Studie zu bremelanotid sagten, die erfahrungen der Studie zeigten eine besser als erwartete akzeptanz der auto-injektoren und dass Patienten - insbesondere Responder - in der Lage waren, Übelkeit zu antizipieren und zu bewältigen.
Bremelanotide FDA-Zulassung
Zwar ist die subkutane Verabreichung von Brelananotid weniger günstig als Addyi (Flibanserin) - ein zugelassenes orales HSDD-Medikament, das von Sprout Pharmaceuticals mit Sitz in Raleigh, North Carolina, hergestellt wird - Vyleesi wird wahrscheinlich nicht den gleichen sicherheitsbezogenen Herausforderungen gegenüberstehen, die die Aufnahme von Addyi stark beeinträchtigten.
Die Kontraindikation von Alkoholkonsum auf dem Addyi-Label und das damit verbundene Programm zur Risikobewertung und Risikominderung (REMS) waren die größten Hindernisse, aber bei beiden dieser Herausforderungen wird von Bromelanotid nicht erwartet. Ein REMS-Programm stellt sicher, dass die Vorteile eines Arzneimittels oder eines biologischen Produkts die Risiken überwiegen.
Bremelanotide hat ein PDUFA-Datum vom 23. März 2019, an dem die US-amerikanische Behörde für Lebens- und Arzneimittelbehörde (FDA) eine Zulassungsentscheidung treffen muss. Dies wird sich jedoch wahrscheinlich um 3 bis 6 Monate verzögern, da die FDA zusätzliche Daten der Phase I anfordert Ein Amag-Sprecher bewertete die ambulanten Blutdruckänderungen bei Patienten. Es sei unwahrscheinlich, dass diese Anforderung den Genehmigungsprozess erheblich behindere, wurde berichtet.
Amag schätzt, dass Bromelanotid ein Umsatzpotenzial von 1 Milliarde Dollar hat. Laut Schätzungen von GlobalData liegen die Umsatzschätzungen für Bromelanotid im Jahr 2024 bei 810 Millionen US-Dollar. Amag hat eine Marktkapitalisierung von 533,6 Millionen US-Dollar.
Im Januar 2017 hat Palatin Technologies die nordamerikanischen Entwicklungs- und Vermarktungsrechte für Bromelanotid an Amag lizenziert.
Die Aufnahme von Bromelanotid ist anfangs langsam
Die subkutane Verabreichungsmethode wird die Verwendung im Vergleich zu einem oralen oder intranasalen Medikament abschrecken, sagte Dr. Robert Pyke, ehemaliger Direktor der klinischen Forschung bei Boehringer Ingelheim (wo er das Addyi-Programm leitete) und Präsident von Pykonsult (New Fairfield, Connecticut).
Die Aufnahme des Medikaments werde zumindest in den ersten Jahren langsam sein, sagte er und schätzte, dass vielleicht 1% der HSDD-Patienten es verwenden werde. Amag schätzt, dass die Prävalenz von HSDD bei Frauen vor der Menopause 10% beträgt.
Dr. Sheryl Kingsberg, Abteilungsleiter für Verhaltensmedizin des Universitätsklinikums Cleveland Medical Center, sagte, die subkutane Injektion sei schnell und benutzerfreundlich.
Die subkutane Verabreichung erwies sich als weniger abschreckend, als zunächst befürchtet wurde, und es kam zu keinen Aussetzern der Phase-III-Studien aufgrund der Verabreichungsmethode, und die meisten Frauen hatten keine Probleme mit dem Medikament, fügte Dr. Kingsberg hinzu .
Die allgemeine Bevölkerung unterscheidet sich jedoch von motivierten Versuchspersonen, so dass die Verwendung des Autoinjektors für einige eine steile Lernkurve ist und da es sich nicht um ein tägliches Medikament handelt, wird es nicht zu viel Rückstoß von Patienten geben, so Dr. Kingsberg.
Bremelanotid soll 45 Minuten vor der sexuellen Aktivität nach Bedarf verwendet werden. Mehr als 90% der Patienten in den Phase-III-Studien berichteten, dass der selbst injizierbare Stift einfach zu verwenden sei und Frauen die feine Nadel gut vertragen würden, sagte ein Sprecher von Amag.
Übelkeit Nebenwirkungen sind ein Problem mit Bromelanotid
Neben der Art der Verabreichung sind die gemeldeten Übelkeitsraten besorgniserregend, da sie die Akzeptanz des Medikaments beeinflussen, sagte Dr. Pyke.
Das am häufigsten auftretende unerwünschte (Sicherheits-) Ereignis bei den 627 mit Bromelanotid behandelten Patienten in den beiden Phase-III-Studien war Übelkeit (250 Ereignisse, 39,9%). Dies wurde auf einem Poster auf der Konferenz zum Jubiläumskongress „Frauengesundheit“ im April 2017 gezeigt. Das gleiche Poster sagte, dass 18% der Patienten die Studie abgebrochen hatten.
Die Studienabbruchquote insgesamt ist vergleichsweise schlecht, da weniger Patienten aus den Addyi-Studien ausgetreten sind, sagte Dr. Pyke. Dies sei besonders beunruhigend, da sich die Patienten verpflichtet hätten, an der Studie teilzunehmen, nachdem sie einen langwierigen Einwilligungsprozess durchlaufen hatten, fügte er hinzu.
Dr. Kingsberg schien weniger besorgt über die Übelkeitsraten zu sein. Wenn man bedenkt, dass etwa 40% Übelkeit hatten, ist eine Dropout-Rate von 18% insgesamt akzeptabel, da Frauen zu diesem Zeitpunkt eine Entscheidung treffen können, sie nicht zu nehmen. Die Versuchspersonen empfanden die Übelkeit als akzeptabel und es gab nur sehr wenige Ausfälle speziell dafür, sagte Dr. Kingsberg.
Es ist nicht klar, ob die Übelkeit nur bei der ersten Verwendung auftritt oder wenn sie bei fortgesetzter Verwendung abnimmt, fügte Pyke hinzu. Übelkeit scheint sich zu zerstreuen, aber dies kann zu jedem Zeitpunkt während der Behandlung sein, da sie zeitweise verwendet wird, sagte Dr. Kingsberg. Es wird erwartet, dass Patienten, die milde Symptome und robuste Reaktionen haben, an dem Medikament bleiben, fügte er hinzu.
Der Einsatz antiemetischer Medikamente war eine erfolgreiche Strategie zur Bekämpfung von Übelkeit in den Phase-III-Studien, erklärte der Untersuchungsbeauftragte Dr. James Simon, Präsident der Internationalen Gesellschaft zur Erforschung der sexuellen Gesundheit von Frauen, Washington, DC.
Aufgrund seiner Erfahrungen in der Studie sagte er, dass die Übelkeit relativ mild war und sich mit der Zeit nicht verschlimmerte, aber natürlich das Interesse der Patienten am Geschlechtsverkehr beeinträchtigte.
Einige Analysten betrachteten die Übelkeitsraten als besorgniserregend, zumal Brelelanotid möglicherweise täglich verwendet werden könnte, andere Quellen berichteten jedoch, dass Experten nicht erwarteten, dass Brelelanotid so oft verwendet würde.
Insgesamt könnten soziale Medien einen erheblichen Einfluss darauf haben, wie Frauen sich an die Verwendung eines Auto-Injektors anpassen oder wie sie mit Übelkeit umgehen, sagte Dr. Pyke.
Einige Frauen sehen die subkutane Verabreichungsmethode als Nachteil an, sie hängt jedoch davon ab, wie sie eingeführt wird, während die Kosten des Medikaments ein weiterer wichtiger Aspekt sind, sagte ein HSDD-Experte.
Im Gegensatz dazu beeinträchtigte ein Warnhinweis auf dem Addyi-Rezept, Alkohol nicht mit dem Medikament einzunehmen, die Aufnahme des Medikaments erheblich, sagte der Experte.
On-Demand-Charakter von Bromelanotid
Die FDA hat die Verwendung von Addyi mit dem REMS-Programm so stark eingeschränkt, dass es immer noch nicht sehr verbreitet ist, sagte Dr. Pyke.
Demgegenüber erwarten Experten keine größeren Warnungen oder Kontraindikationen mit Bromelanotid. Addyi wurde im August 2015 zur Behandlung von HSDD zugelassen und erzielte im Jahr 2016 einen Umsatz von weniger als 10 Millionen US-Dollar. Damit wurde das vom Unternehmen für Juli 2017 festgelegte Ziel von 1 Milliarde US-Dollar weit übertroffen.
Neben dem REMS-Programm können breitere Probleme mit Valeant Pharma - heute Bausch Health Companies genannt - Sprout erwerben und zwei Jahre später wieder verkaufen, was den Erfolg des Medikaments beeinflussen kann.
Valeant erwarb Sprout im Jahr 2015 für eine Milliarde US-Dollar, verkaufte das Unternehmen jedoch 2017 an einen mit ehemaligen Sprout-Aktionären verbundenen Käufer.
Einige Frauen könnten auch die On-Demand-Natur von Bromelanotid der chronischen täglichen Einnahme von Medikamenten vorziehen, sagte Dr. Kingsberg. Diejenigen, die dazu neigen, sexuelle Aktivitäten auszulösen, möchten möglicherweise mehr Kontrolle über ihr Leben haben und ziehen es vor, dass Bromelanotid eine tägliche Pille einnimmt, sagte Dr. Simon.
von Manasi Vaidya in New York
Manasi Vaidya ist Senior Reporter für das investigative Journalismus-Team der Muttergesellschaft GlobalData für pharmazeutische Technologien. Eine Version dieses Artikels erschien ursprünglich im Insights-Modul des Pharmaceutical Intelligence Center von GlobalData. Um auf weitere Artikel wie diesen zuzugreifen, besuchen Sie GlobalData .
https://www.pharmaceutical-technology.com/comment/bremelanot…
Wird schon werden. Ich bleibe dabei
Antwort auf Beitrag Nr.: 59.685.855 von onkelen am 22.01.19 17:26:30 Hm liest sich aber nicht gut. .....!🤐
Wieso liest sich das nicht gut?? Wegen bissle Übelkeit? Was glaubst was Viagra für Nebenwirkungen hat oder Aspirin. Ich finde das liest sich fantastisch
Antwort auf Beitrag Nr.: 59.686.809 von Reinerle am 22.01.19 19:00:37
Was sind die größten Nebenwirkungen von Viagra?
Migräne bei den Frauen 😂
Sorry Jungs.
Ich bin bei über einem Euro rein.
Mir hilft nur noch Galgenhumor
Zitat von Reinerle: Wieso liest sich das nicht gut?? Wegen bissle Übelkeit? Was glaubst was Viagra für Nebenwirkungen hat oder Aspirin. Ich finde das liest sich fantastisch
Was sind die größten Nebenwirkungen von Viagra?
Migräne bei den Frauen 😂
Sorry Jungs.
Ich bin bei über einem Euro rein.
Mir hilft nur noch Galgenhumor
Antwort auf Beitrag Nr.: 59.687.169 von 11marvin11 am 22.01.19 19:36:10Wenn du ein wenig Geduld mitbringst, gehst du hier mit über 100% Gewinn aus dem Geschäft.
Das ist sicher eine angemessene Entschädigung für die ausgestandene Angst.
Bei dem vom onkel eingestellten Artikel haben die Zweifler sicher mit ihren Argumenten recht.
Aber bestimmt wollen viele das Mittel mal ausprobieren. Vyleesi ist viel wirksammer als Addyi und wirkt auch bei Männern. Das wird eine Lifestyle Droge mit großen Umsätzen.
Amag nimmt nicht von ungfähr millionen Dollar in die Hand um an das Mittel zu kommen.
Für die Lizens von Addyi wurde 1 Milliarde $ ausgegeben.
Das ist sicher eine angemessene Entschädigung für die ausgestandene Angst.
Bei dem vom onkel eingestellten Artikel haben die Zweifler sicher mit ihren Argumenten recht.
Aber bestimmt wollen viele das Mittel mal ausprobieren. Vyleesi ist viel wirksammer als Addyi und wirkt auch bei Männern. Das wird eine Lifestyle Droge mit großen Umsätzen.
Amag nimmt nicht von ungfähr millionen Dollar in die Hand um an das Mittel zu kommen.
Für die Lizens von Addyi wurde 1 Milliarde $ ausgegeben.
Also ich wäre da etwas vorsichtiger mit den Einschätzungen. Sicher kann es so eintreten und das Mittel wird ein Erfolg. Allerdings hege ich stand heute doch erhebliche Zweifel.
Zuerst einmal wäre es nicht der erste und nicht der letzte Flop, wenn das Mittel nicht zugelassen wird. Von daher spielt es überhaupt keine Rolle, ob AMAG dafür Millionen in die Hand nimmt oder nicht Wenn das ein Indikator wäre, wäre es einfach. Es gibt zwei Faktoren, die viel wichtiger sind:
1.) Für die Entscheidung der Kommission für eine positive Einschätzung des Mittels und der Zulassung des Mittels durch die FDA ist es wichtig, dass die Risiken des Mittels geringer einzuschätzen sind, als der zu erwartende Mehrwert dem es den Patienten bringt.
Meine Einschätzung hierzu: Es ist schwierig abzuschätzen, was die geneigten Damen und Herren in der Kommission und der FDA als Ausschlaggebend für ihre Stimme ist. Dafür könnte sprechen, dass die bekannten Nebenwirkungen unter Umständen nicht so gravierend sind. Übelkeit ist zwar nicht schön, aber nicht lebensbedrohlich. Warum das Mittel also nicht zulassen. Außerdem kann es für die Verbraucher/Patienten preislich von Vorteil sind, wenn es verschiedene Produkte am Markt gibt.
Dagegen könnte sprechen, dass der erhöhte Blutdruck doch solche Ausmaße annehmen kann, dass dies für eine größere Patientengruppe eben doch gefährlich sein könnte. In diesem Fall wäre die körperliche Versehrtheit wohl höher zu bewerten als die Lust auf Sex. Außerdem könnten in der Kommission und der FDA eine reihe von Leuten sitzen die z.B. streng katholisch sind und sich daher vom Glauben her schon gegen ein Luststeigerungsmittel stellen (würden sie natürlich nie zugeben, die Begründung wäre eine andere).
Dies ist also der erste Zock vor und bis zur möglichen Zulassung. Ich denke, wie bereits schon einmal geschrieben, dass der Kurs dann zum ersten Mal anspringt, wenn die geforderte Studie eingereicht wird und das egal was da drin steht. Gibt hier genug Zocker, die dann Gas geben werden. Das kann aber dann auch ganz schnell wieder abstürzen, wenn Details an Licht kommen würden, die nicht für eine Zulassung sprechen.
2.) Der zweite Faktor spielt nur eine Rolle bei einer möglichen Zulassung. Nämlich ob das Mittel wirklich ein wirtschaftlicher Erfolg wird. Auch hier habe ich meine Zweifel. Gibt es wirklich so viele Patientinnen, die ein Problem damit haben, das so groß ist, um ein Medikament zu nehmen? Ich bin keine Frau, die Welt ist groß, ich weiss es nicht wirklich. Aber wenn es viele geben sollte, die auch bereit wären ein Medikament dagegen zu nehmen, wären die bereit sich was zu spritzen? Und das geplant 45 Minuten vor dem Sex? Klingt sehr romantisch :-) Das mit dem Spritzen sehe ich schon als großes Problem. Das mach nur jemand der echt verzweifelt ist. Und wenn ich dann schon bereit bin mir das zu spritzen, dann ist nach jetzigem Stand die Möglichkeit sehr groß, dass mir Übel wird. Wow, dann hab ich ja was gewonnen. Ich kriege Lust, muss aber fast kotzen? Und der dritte Faktor ist die unbekannte (zumindest für mich bisher) Sache mit dem Bluthochdruck. Ja, wenn ich Sex haben will geht der Blutdruck eh hoch und bei Viagra ist es natürlich auch ein Nebeneffekt und es ist ein Erfolg, aber sind Frauen auch bereit sich dem Risiko hinzugeben und wie hoch ist das Risiko überhaupt. Aber gut, das würde ja vor der Zulassung von der FDA ja eingeschätzt.
Also zusammenfassend ist hier für mich gar nichts klar. Es wird natürlich beide Positionen geben. Die einen, die vehement davon ausgehen, dass das Mittel an den Markt geht und danach natürlich ein Erfolg wird und die die eben nicht daran glauben. Wobei ich behaupte das alle, aber wirklich alle die hier im Moment die Aktie haben es überhaupt nicht interessiert, ob das Mittel später ein Erfolg wird, sondern nur darauf wetten, dass das Mittel zugelassen wird und allein durch die Zulassung der Kurs nach oben schnellt und sich dann von der Aktie schnell verabschieden. Das nennt man einen reinen Zock bzw. eine Wette. Chancen derzeit 50%-50% aus meiner Sicht.
Letztlich muss das jeder selbst für sich entscheiden, welches Risiko er eingehen will.
Zuerst einmal wäre es nicht der erste und nicht der letzte Flop, wenn das Mittel nicht zugelassen wird. Von daher spielt es überhaupt keine Rolle, ob AMAG dafür Millionen in die Hand nimmt oder nicht Wenn das ein Indikator wäre, wäre es einfach. Es gibt zwei Faktoren, die viel wichtiger sind:
1.) Für die Entscheidung der Kommission für eine positive Einschätzung des Mittels und der Zulassung des Mittels durch die FDA ist es wichtig, dass die Risiken des Mittels geringer einzuschätzen sind, als der zu erwartende Mehrwert dem es den Patienten bringt.
Meine Einschätzung hierzu: Es ist schwierig abzuschätzen, was die geneigten Damen und Herren in der Kommission und der FDA als Ausschlaggebend für ihre Stimme ist. Dafür könnte sprechen, dass die bekannten Nebenwirkungen unter Umständen nicht so gravierend sind. Übelkeit ist zwar nicht schön, aber nicht lebensbedrohlich. Warum das Mittel also nicht zulassen. Außerdem kann es für die Verbraucher/Patienten preislich von Vorteil sind, wenn es verschiedene Produkte am Markt gibt.
Dagegen könnte sprechen, dass der erhöhte Blutdruck doch solche Ausmaße annehmen kann, dass dies für eine größere Patientengruppe eben doch gefährlich sein könnte. In diesem Fall wäre die körperliche Versehrtheit wohl höher zu bewerten als die Lust auf Sex. Außerdem könnten in der Kommission und der FDA eine reihe von Leuten sitzen die z.B. streng katholisch sind und sich daher vom Glauben her schon gegen ein Luststeigerungsmittel stellen (würden sie natürlich nie zugeben, die Begründung wäre eine andere).
Dies ist also der erste Zock vor und bis zur möglichen Zulassung. Ich denke, wie bereits schon einmal geschrieben, dass der Kurs dann zum ersten Mal anspringt, wenn die geforderte Studie eingereicht wird und das egal was da drin steht. Gibt hier genug Zocker, die dann Gas geben werden. Das kann aber dann auch ganz schnell wieder abstürzen, wenn Details an Licht kommen würden, die nicht für eine Zulassung sprechen.
2.) Der zweite Faktor spielt nur eine Rolle bei einer möglichen Zulassung. Nämlich ob das Mittel wirklich ein wirtschaftlicher Erfolg wird. Auch hier habe ich meine Zweifel. Gibt es wirklich so viele Patientinnen, die ein Problem damit haben, das so groß ist, um ein Medikament zu nehmen? Ich bin keine Frau, die Welt ist groß, ich weiss es nicht wirklich. Aber wenn es viele geben sollte, die auch bereit wären ein Medikament dagegen zu nehmen, wären die bereit sich was zu spritzen? Und das geplant 45 Minuten vor dem Sex? Klingt sehr romantisch :-) Das mit dem Spritzen sehe ich schon als großes Problem. Das mach nur jemand der echt verzweifelt ist. Und wenn ich dann schon bereit bin mir das zu spritzen, dann ist nach jetzigem Stand die Möglichkeit sehr groß, dass mir Übel wird. Wow, dann hab ich ja was gewonnen. Ich kriege Lust, muss aber fast kotzen? Und der dritte Faktor ist die unbekannte (zumindest für mich bisher) Sache mit dem Bluthochdruck. Ja, wenn ich Sex haben will geht der Blutdruck eh hoch und bei Viagra ist es natürlich auch ein Nebeneffekt und es ist ein Erfolg, aber sind Frauen auch bereit sich dem Risiko hinzugeben und wie hoch ist das Risiko überhaupt. Aber gut, das würde ja vor der Zulassung von der FDA ja eingeschätzt.
Also zusammenfassend ist hier für mich gar nichts klar. Es wird natürlich beide Positionen geben. Die einen, die vehement davon ausgehen, dass das Mittel an den Markt geht und danach natürlich ein Erfolg wird und die die eben nicht daran glauben. Wobei ich behaupte das alle, aber wirklich alle die hier im Moment die Aktie haben es überhaupt nicht interessiert, ob das Mittel später ein Erfolg wird, sondern nur darauf wetten, dass das Mittel zugelassen wird und allein durch die Zulassung der Kurs nach oben schnellt und sich dann von der Aktie schnell verabschieden. Das nennt man einen reinen Zock bzw. eine Wette. Chancen derzeit 50%-50% aus meiner Sicht.
Letztlich muss das jeder selbst für sich entscheiden, welches Risiko er eingehen will.
Ihr glaubt wirklich an happy end? Ich Zweifel langsam an der aktie. Welche Back up plan hat palatin wenn es nicht klappt?
Die Dinge könnten bei FDA haarig werden, wenn das Herunterfahren weitergeht: Analysten
Die FDA hält es während des längsten Regierungsstillstands in der Geschichte immer noch zusammen, könnte jedoch vor großen Problemen stehen, wenn sie einen weiteren Monat andauert und die Nutzungsgebühren versiegen.Laut zwei von der Jefferies-Analysten zitierten FDA-Experten, die darauf hindeuten, dass die Überprüfungen in wenigen Wochen zum Erliegen kommen könnten, was Dutzende von Medikamentenanwendungen beeinträchtigen und möglicherweise zu einem "wachsenden Rückstand" verzögerter Programme führen könnte.
Bemerkenswerte kurzfristige Marketinganwendungen, die beeinträchtigt werden könnten, wenn die staatliche Sackgasse nicht beseitigt wird, umfassen die postpartale Depressionstherapie von Sage, Brexanolon, Karyopharms Selinexor für das multiple Myelom und Amag Pharmas Brelanotid gegen weibliche sexuelle Erregungsstörung, sagen die Analysten.
https://www.fiercebiotech.com/biotech/things-could-get-hairy…
Antwort auf Beitrag Nr.: 59.699.658 von Schurik am 24.01.19 10:35:07Das Ding ist halt kein Evotec und daher viel eher ein Risiko- bzw. Für manche ein Zockerwert!
Um es mit den Worten von Eminiem zu sagen „You have one shot one opportunity“
Wenn die net klappt....
Um es mit den Worten von Eminiem zu sagen „You have one shot one opportunity“
Wenn die net klappt....
Antwort auf Beitrag Nr.: 59.700.078 von M_Engel am 24.01.19 11:16:52Das Ding ist eine reine Wette.
Antwort auf Beitrag Nr.: 59.709.294 von meissner7309 am 25.01.19 11:03:41
So ein Schwachsinn, was ist hier bitte denn eine Wette bzw. die große Unbekannte?!? Es wurde ein Medikament entwickelt, klinisch in mehreren Stadien geprüft, alle Ergebnisse kann man detailliert nachlesen. Wie alle anderen Medikamente auch gibt es auch hier gewisse Nebenwirkungen, aber ich weiß nicht ob einer von euch mal den Beipackzettel von Aspirin oder anderen weltweit häufigsten Produkten durchgelesen und die Nebenwirkungen dort mal durchgegangen ist. Also was soll die Panikmache hier? Jeder kann alle Ergebnisse für sich durchlesen und entweder glaubt man an den Erfolg bzw die Story oder man lässt es eben sein. Die Leute bei der FDA würfeln doch nicht sondern schauen sich genauso diese Ergebnisse an und entscheiden dann. Niemand sitzt da und würfelt von denen, das wäre nämlich eine Wette.
Zitat von meissner7309: Das Ding ist eine reine Wette.
So ein Schwachsinn, was ist hier bitte denn eine Wette bzw. die große Unbekannte?!? Es wurde ein Medikament entwickelt, klinisch in mehreren Stadien geprüft, alle Ergebnisse kann man detailliert nachlesen. Wie alle anderen Medikamente auch gibt es auch hier gewisse Nebenwirkungen, aber ich weiß nicht ob einer von euch mal den Beipackzettel von Aspirin oder anderen weltweit häufigsten Produkten durchgelesen und die Nebenwirkungen dort mal durchgegangen ist. Also was soll die Panikmache hier? Jeder kann alle Ergebnisse für sich durchlesen und entweder glaubt man an den Erfolg bzw die Story oder man lässt es eben sein. Die Leute bei der FDA würfeln doch nicht sondern schauen sich genauso diese Ergebnisse an und entscheiden dann. Niemand sitzt da und würfelt von denen, das wäre nämlich eine Wette.
Jeder kann sich die Infos zum Unternehmen verschaffen und seine Investmententscheidung treffen.
Ich gehe von einer Zulassung im Sommer aus und erwarte einen Kurs von ~ 3,50 $ im Jan 2020.
Sollten gute Lizensgeschäfte folgen und die anderen Medis zugelassen werden, geht es weiter bis
6 $ und darüber hinaus in 2021 und 2022.
Das wäre dann etwa ein verzehnfacher bei überschaubarem Risiko.
Ich gehe von einer Zulassung im Sommer aus und erwarte einen Kurs von ~ 3,50 $ im Jan 2020.
Sollten gute Lizensgeschäfte folgen und die anderen Medis zugelassen werden, geht es weiter bis
6 $ und darüber hinaus in 2021 und 2022.
Das wäre dann etwa ein verzehnfacher bei überschaubarem Risiko.
Antwort auf Beitrag Nr.: 59.713.905 von Mammut22 am 25.01.19 18:53:14Das sehe ich vollkommen anders. Natürlich ist es eine Wette. Es gibt zwei Möglichkeiten, eine Zulassung oder eben keine Zulassung. Klar kann man sich Infos aus dem Netz ziehen zum Unternehmen. Aber wie die FDA entscheidet kann hier keiner sagen. denn keiner hier kann mit Sicherheit sagen, zu welcher einzelnen Entscheidung die Herren und Damen der FDA kommen werden. Wer etwas anderes behauptet und meint alles sei sicher, der lügt.
Warum steht denn der Kurs bei 0,60 € und nicht schon bei 2 Euro? Weil alles so sicher ist? Es ist ein Mittel mit Nebenwirkungen und ob diese Nebenwirkungen oder Risiken geringer zu bewerten sind als die positiven Effekte, dass ist die grosse Unbekannte. Das hat nichts mit Würfeln zu tun, nur eine Einschätzung die jeder für sich treffen muss und die stehen meiner Meinung nach 50-50. Und diese Unsicherheit sieht man halt auch im Kurs.
Im übrigen ist jedes Investment an der Börse eine Wette. Denn bis auf die paar Leute, die wirklich extrem long investieren und sich mit der Dividende zufrieden geben, wollen alle doch nur eins: Kursgewinne. Ob die kommen, kann keiner voraussehen. Man kann nur aufgrund der eigenen gesammelten Daten zu einem Ergebnis kommen. Und wenn dieses Ergebnis heisst, ich investiere in eine Aktie, dann ist es im Grunde eine Wette auf steigende Kurse, aber sicher ist gar nichts. Weder der gewinn, noch der Verlust, der durch entstehen kann.
Warum steht denn der Kurs bei 0,60 € und nicht schon bei 2 Euro? Weil alles so sicher ist? Es ist ein Mittel mit Nebenwirkungen und ob diese Nebenwirkungen oder Risiken geringer zu bewerten sind als die positiven Effekte, dass ist die grosse Unbekannte. Das hat nichts mit Würfeln zu tun, nur eine Einschätzung die jeder für sich treffen muss und die stehen meiner Meinung nach 50-50. Und diese Unsicherheit sieht man halt auch im Kurs.
Im übrigen ist jedes Investment an der Börse eine Wette. Denn bis auf die paar Leute, die wirklich extrem long investieren und sich mit der Dividende zufrieden geben, wollen alle doch nur eins: Kursgewinne. Ob die kommen, kann keiner voraussehen. Man kann nur aufgrund der eigenen gesammelten Daten zu einem Ergebnis kommen. Und wenn dieses Ergebnis heisst, ich investiere in eine Aktie, dann ist es im Grunde eine Wette auf steigende Kurse, aber sicher ist gar nichts. Weder der gewinn, noch der Verlust, der durch entstehen kann.
Antwort auf Beitrag Nr.: 59.722.125 von meissner7309 am 27.01.19 16:55:24Jeder hat seine Sicht auf die Dinge und das ist auch gut so. Der Kurs steht bei 60 Cent weil die Entscheidung vertagt wurde, ich bin mir sicher dass es kurz vor der FDA Entscheidung bei den 2€ stehen wird, denn je näher die Entscheidung rückt desto höher wird es gehen. Und die Chancen dass es zur Genehmigung kommt, sehe ich weit höher als 50%, das ist aber wie gesagt meine Meinung nachdem ich mich nun über Dreiviertel Jahr damit auseinander gesetzt habe. Und 50:50 steht’s doch bei allen Aktien: entweder es geht hoch oder runter. Ich persönlich glaube an dieses Medikament und denke, dass es relativ klar genehmigt wird. Alles meine Meinung, keine kaufemfehlung
Antwort auf Beitrag Nr.: 59.722.125 von meissner7309 am 27.01.19 16:55:24Dann sind wir uns doch alle einig. Es ist sicher das die Kurse an der Börse nicht sicher sind.
(nicht sicher vorhersehbar sind)
Trotzdem gibt es Indizien die ein Ereignis warscheinlicher machen. Das Markteilnehmer die Indizien anders interpretieren und andere Schlüsse ziehen ist normal. Daraus ergeben sich die Kurse.
Ich interpretiere die Ereignisse um Palatin und anderen Firmen so, dass die Zulassung kommt und
Vyleesi ein Erfolg wird.
(nicht sicher vorhersehbar sind)
Trotzdem gibt es Indizien die ein Ereignis warscheinlicher machen. Das Markteilnehmer die Indizien anders interpretieren und andere Schlüsse ziehen ist normal. Daraus ergeben sich die Kurse.
Ich interpretiere die Ereignisse um Palatin und anderen Firmen so, dass die Zulassung kommt und
Vyleesi ein Erfolg wird.
Auch wenn keiner Interesse an meinen Selbstgesprächen hat, trotz alle dem:
Aus der jüngsten Telefonkonferens von Amag
Julie Krop
Thanks, Bill. As you can see, on the slides are a number of significant milestones throughout 2019 and the first half of 2020 and a lot of work in front of us. I’ll start off with Vyleesi, which is currently under review with the FDA for the treatment of low libido associated with distress. As we recently disclosed, FDA has requested that we conduct a short-duration ambulatory blood pressure monitoring study in a small number of healthy volunteers. We’ve initiated that study and expect to have the results submitted to the agency prior to the PDUFA date of June 23.
We look forward to the FDA’s decision and the potential launch of Vyleesi in the second half of the year.
Wenn Vyleesi wie geplant in der 2. Jahreshälfte am Markt startet, wäre das für Palatin der
Durchbruch weil eine dicke einmalige Zahlung erfolgt und dann beständig Lizenzahlungen folgen.
Und mal ehrlich, Viagra war eines der meistverkauften Medis, weshalb sollte Vyleesi das
wirksammer ist und bei Frau und Mann wirkt, nicht auch zumindest etwas erfolgreich sein.
Aus der jüngsten Telefonkonferens von Amag
Julie Krop
Thanks, Bill. As you can see, on the slides are a number of significant milestones throughout 2019 and the first half of 2020 and a lot of work in front of us. I’ll start off with Vyleesi, which is currently under review with the FDA for the treatment of low libido associated with distress. As we recently disclosed, FDA has requested that we conduct a short-duration ambulatory blood pressure monitoring study in a small number of healthy volunteers. We’ve initiated that study and expect to have the results submitted to the agency prior to the PDUFA date of June 23.
We look forward to the FDA’s decision and the potential launch of Vyleesi in the second half of the year.
Wenn Vyleesi wie geplant in der 2. Jahreshälfte am Markt startet, wäre das für Palatin der
Durchbruch weil eine dicke einmalige Zahlung erfolgt und dann beständig Lizenzahlungen folgen.
Und mal ehrlich, Viagra war eines der meistverkauften Medis, weshalb sollte Vyleesi das
wirksammer ist und bei Frau und Mann wirkt, nicht auch zumindest etwas erfolgreich sein.
Antwort auf Beitrag Nr.: 59.820.585 von apano am 07.02.19 23:14:16
http://filings.irdirect.net/data/911216/000021545719006566/0…
Schaut gut aus, jetzt geht wohl bald die Ralley los!
VG
Blackrock Inc steigt ein!
SEC Alert heute von Palatin:http://filings.irdirect.net/data/911216/000021545719006566/0…
Schaut gut aus, jetzt geht wohl bald die Ralley los!
VG
Antwort auf Beitrag Nr.: 59.823.978 von Foerderung_ am 08.02.19 12:47:05
Blackrock nun über 6 % beteiligt.
https://fintel.io/soh/us/ptn/blackrock
Antwort auf Beitrag Nr.: 59.820.585 von apano am 07.02.19 23:14:16
Danke für die Info
Zitat von apano: Auch wenn keiner Interesse an meinen Selbstgesprächen hat, trotz alle dem:
Aus der jüngsten Telefonkonferens von Amag
Julie Krop
Thanks, Bill. As you can see, on the slides are a number of significant milestones throughout 2019 and the first half of 2020 and a lot of work in front of us. I’ll start off with Vyleesi, which is currently under review with the FDA for the treatment of low libido associated with distress. As we recently disclosed, FDA has requested that we conduct a short-duration ambulatory blood pressure monitoring study in a small number of healthy volunteers. We’ve initiated that study and expect to have the results submitted to the agency prior to the PDUFA date of June 23.
We look forward to the FDA’s decision and the potential launch of Vyleesi in the second half of the year.
Wenn Vyleesi wie geplant in der 2. Jahreshälfte am Markt startet, wäre das für Palatin der
Durchbruch weil eine dicke einmalige Zahlung erfolgt und dann beständig Lizenzahlungen folgen.
Und mal ehrlich, Viagra war eines der meistverkauften Medis, weshalb sollte Vyleesi das
wirksammer ist und bei Frau und Mann wirkt, nicht auch zumindest etwas erfolgreich sein.
Danke für die Info

Antwort auf Beitrag Nr.: 59.824.440 von Foerderung_ am 08.02.19 13:29:54
Kann mir das mal jemand erklären was das genau bedeztet. Danke schön
Zitat von Foerderung_: https://fintel.io/soh/us/ptn/blackrock
Kann mir das mal jemand erklären was das genau bedeztet. Danke schön
Antwort auf Beitrag Nr.: 59.826.084 von PrinzStorno am 08.02.19 16:16:15Blackrock hat seine Anteile an Palatin deutlich aufgestockt...
Google Übersetzung!
7. Februar 2019 - BlackRock Inc. hat bei der Securities and Exchange Commission (SEC) ein SC 13G-Formular eingereicht, das den Besitz von 12.428.014 Aktien von Palatin Technologies, Inc. (AMEX: PTN) angibt. Dies entspricht einem Anteil von 6,1 Prozent am Unternehmen.
7. Februar 2019 - BlackRock Inc. hat bei der Securities and Exchange Commission (SEC) ein SC 13G-Formular eingereicht, das den Besitz von 12.428.014 Aktien von Palatin Technologies, Inc. (AMEX: PTN) angibt. Dies entspricht einem Anteil von 6,1 Prozent am Unternehmen.
Kann mir mal jemand den Handel der letzten Stunden erklären?! 🧐
Solche Mini-Veränderungen im Kurs sieht man oft bei erfolgten Übernahmeangeboten...hab ich was verpasst?! 🤔😜
Btw: hab‘s Blackrock mal nachgemacht und mir wieder ein paar Anteile ergattert. 😉
Hab im Sommer 2017 schonmal gekauft, dann aber alle Anteile zw. 0,80 - 1,20 veräußert. Imho sollten hier die nächsten Monate locker 50% drin sein, ergo mind 1$.
Solche Mini-Veränderungen im Kurs sieht man oft bei erfolgten Übernahmeangeboten...hab ich was verpasst?! 🤔😜
Btw: hab‘s Blackrock mal nachgemacht und mir wieder ein paar Anteile ergattert. 😉
Hab im Sommer 2017 schonmal gekauft, dann aber alle Anteile zw. 0,80 - 1,20 veräußert. Imho sollten hier die nächsten Monate locker 50% drin sein, ergo mind 1$.
Palatin wird auch eine Telefonkonferenz und einen Live-Audio-Webcast abhalten, der am 12. Februar 2019 um 11:00 Uhr (ET) von seiner Geschäftsführung moderiert wird. Die Telefonkonferenz umfasst einen Überblick über die Betriebsergebnisse des Unternehmens und ein Update der in Entwicklung befindlichen Programme.
Zeitplan für die Betriebsergebnisse Pressemitteilung, Telefonkonferenz / Audio-Webcast
Finanzergebnisse für das 2. Quartal des Geschäftsjahres 2019 Pressemitteilung
12.02.2014 um 7:30 Uhr ET
Q2 Geschäftsjahr 2019 Telefonkonferenz-Live
12.02.2014 um 11:00 Uhr ET
US / Kanada-Einwahlnummer:
1-877-260-1479
Internationale Einwahlnummer:
1-334-323-0522
Konferenz ID:
4414047
F2-Telefonkonferenz-Wiederholung für das Geschäftsjahr 2019
2/12 / 2019-2 / 19/2019
US / Kanada-Einwahlnummer:
1-888-203-1112
Internationale Einwahlnummer:
1-719-457-0820
Code wiederholen:
4414047
Audio-Webcast Live- und Wiedergabezugriff
http://www.palatin.com
Auf das Audio-Webcast und die Wiedergabe können Sie zugreifen, indem Sie sich im Bereich "Investors-Webcasts" auf der Palatin-Website unter http://www.palatin.com anmelden.
Über Palatin Technologies, Inc.
Palatin Technologies, Inc. ist ein biopharmazeutisches Unternehmen, das zielgerichtete, rezeptorspezifische Peptidtherapeutika zur Behandlung von Krankheiten mit erheblichem medizinischem Bedarf und kommerziellem Potenzial entwickelt. Palatins Strategie besteht darin, Produkte zu entwickeln und anschließend Marketingkooperationen mit Branchenführern einzugehen, um deren kommerzielles Potenzial zu maximieren. Weitere Informationen finden Sie unter http://www.palatin.com.
Zeitplan für die Betriebsergebnisse Pressemitteilung, Telefonkonferenz / Audio-Webcast
Finanzergebnisse für das 2. Quartal des Geschäftsjahres 2019 Pressemitteilung
12.02.2014 um 7:30 Uhr ET
Q2 Geschäftsjahr 2019 Telefonkonferenz-Live
12.02.2014 um 11:00 Uhr ET
US / Kanada-Einwahlnummer:
1-877-260-1479
Internationale Einwahlnummer:
1-334-323-0522
Konferenz ID:
4414047
F2-Telefonkonferenz-Wiederholung für das Geschäftsjahr 2019
2/12 / 2019-2 / 19/2019
US / Kanada-Einwahlnummer:
1-888-203-1112
Internationale Einwahlnummer:
1-719-457-0820
Code wiederholen:
4414047
Audio-Webcast Live- und Wiedergabezugriff
http://www.palatin.com
Auf das Audio-Webcast und die Wiedergabe können Sie zugreifen, indem Sie sich im Bereich "Investors-Webcasts" auf der Palatin-Website unter http://www.palatin.com anmelden.
Über Palatin Technologies, Inc.
Palatin Technologies, Inc. ist ein biopharmazeutisches Unternehmen, das zielgerichtete, rezeptorspezifische Peptidtherapeutika zur Behandlung von Krankheiten mit erheblichem medizinischem Bedarf und kommerziellem Potenzial entwickelt. Palatins Strategie besteht darin, Produkte zu entwickeln und anschließend Marketingkooperationen mit Branchenführern einzugehen, um deren kommerzielles Potenzial zu maximieren. Weitere Informationen finden Sie unter http://www.palatin.com.
Filing ist da: https://seekingalpha.com/filing/4341780?app=1
10% Minus hier vorbörslich...
Mal gespannt, was im CC später so berichtet wird...
Mal gespannt, was im CC später so berichtet wird...
Antwort auf Beitrag Nr.: 59.850.451 von Stoxtrayder am 12.02.19 11:13:47Man sieht eins. Alles steht und fällt mit der Zulassung. Wenn das nicht klappt geht die Firma ganz schnell ganz runter um nicht zu sagen, dann kreist ganz schnell der Pleitegeier. Wenn es klappt können alle investierten einschließlich aller Mitarbeiter ein Stoßgebet gen Himmel senden. Die Aussicht läßt den einen oder anderen dann doch wohl zweifeln. Das Risiko ist groß, die Gewinn-, aber auch Verlustmöglichkeit ebenso.
The same procedure as... nach der Vorlage jedes Quartalsberichts gehts runter. Die Unterstützung bei 0,68$ sollte aber halten. Zahlen wie erwartet, Studie von AMAG wird ja bis Juni fertig.
Antwort auf Beitrag Nr.: 59.850.451 von Stoxtrayder am 12.02.19 11:13:47Vorbörslich ist ja noch nicht's passiert.... , hier wird unter Pari ohne Grund verkauft.
https://www.nasdaq.com/de/symbol/ptn/premarket
https://www.nasdaq.com/de/symbol/ptn/premarket
Antwort auf Beitrag Nr.: 59.850.607 von bonny1960 am 12.02.19 11:26:11Einige Stop-Loss dürften durch den Panikverkauf (anders kann man es nicht nennen), auch ausgelöst werden.
Ich sehe keinen Grund zu verkaufen.
Gerade wo Blackrock aufgestockt hat.
Das machen die ja nun nicht ohne Grund.
Nur meine persönliche Meinung.
Ich sehe keinen Grund zu verkaufen.
Gerade wo Blackrock aufgestockt hat.
Das machen die ja nun nicht ohne Grund.
Nur meine persönliche Meinung.
Antwort auf Beitrag Nr.: 59.851.015 von stigma68 am 12.02.19 11:58:46
das sehe ich genauso!
Bin schon recht lange investiert, mit einem Durchschnitt von 0,45 EUR.
Habe heute nochmal ein Körbchen aufgestellt und zu 0,59 EUR nachgekauft...
Sehe die richtigung weiter positiv, wobei natürlich alles von der Zulassung abhängt...
Aber:
Wer nicht wagt, der nicht gewinnt
Heute ist ein guter Einstiegszeitpunkt...schön günstig
Zitat von stigma68: Einige Stop-Loss dürften durch den Panikverkauf (anders kann man es nicht nennen), auch ausgelöst werden.
Ich sehe keinen Grund zu verkaufen.
Gerade wo Blackrock aufgestockt hat.
Das machen die ja nun nicht ohne Grund.
Nur meine persönliche Meinung.
das sehe ich genauso!
Bin schon recht lange investiert, mit einem Durchschnitt von 0,45 EUR.
Habe heute nochmal ein Körbchen aufgestellt und zu 0,59 EUR nachgekauft...
Sehe die richtigung weiter positiv, wobei natürlich alles von der Zulassung abhängt...
Aber:
Wer nicht wagt, der nicht gewinnt

Heute ist ein guter Einstiegszeitpunkt...schön günstig

Stimme Euch zu. Und die Verschuldung ist auch nochmal deutlich gesenkt worden. Das sieht alles sehr vielversprechend aus. Da gebe ich kein Stück ab.
Mal sehen was noch passiert heute. Ggf. verbillige ich auch noch etwas.
Mal sehen was noch passiert heute. Ggf. verbillige ich auch noch etwas.
Schönes Intraday-Reversal an der Heimatbörse 👌
Null Mitleid mit den deutschen Honks, die heute unter 0,60 Euro verkauft haben 😛
Null Mitleid mit den deutschen Honks, die heute unter 0,60 Euro verkauft haben 😛
Antwort auf Beitrag Nr.: 59.854.765 von Stoxtrayder am 12.02.19 17:50:02
Palatin sieht keinerlei Probleme und hält erneute Licences und Vertrieb für Q3 realistisch. FDA benötigt bei Einreichung bis 23.06.19 lediglich 1 bis 2 Wochen für approval! Pro Forma Durchschau... )
)
FDA Zulassung nur Formsache
Nachzureichende Daten zu Blutdruck mit höherer Dosis 4-5 x pro Woche (vs 1 x Woche) als vorgesehen sind nur zwecks Labeling / Hinweise für FDA relevant. Also rein pro Forma. Palatin sieht keinerlei Probleme und hält erneute Licences und Vertrieb für Q3 realistisch. FDA benötigt bei Einreichung bis 23.06.19 lediglich 1 bis 2 Wochen für approval! Pro Forma Durchschau...
 )
)
Woher weißt du das. Das steht ja so wohl nicht drin
Antwort auf Beitrag Nr.: 59.855.482 von Reinerle am 12.02.19 18:48:12Hab heut Abend den Webcast mitverfolgt. Da wurden explizit diese Themen in der Fragerunde angesprochen und beantwortet.
Palatin Technologies, Inc. gibt Ergebnisse für das zweite Quartal 2019 bekannt
Palatin Technologies, Inc. gibt Ergebnisse für das zweite Quartal 2019 bekanntDer folgende Auszug stammt aus der SEC-Hinterlegung des Unternehmens .
und bietet Unternehmensupdate
Telefonkonferenz und Webcast finden am 12. Februar 2019 statt
CRANBURY, NJ - 12. Februar 2019 - Palatin Technologies, Inc. (NYSE Amerikanisch: PTN), ein spezialisiertes biopharmazeutisches Unternehmen, das erstklassige Medikamente auf der Basis von Molekülen entwickelt, die die Aktivität der Melanocortin- und natriuretischen Peptidrezeptorsysteme für die Behandlung modulieren Im Zusammenhang mit Krankheiten mit erheblichem ungedecktem medizinischen Bedarf und kommerziellem Potenzial gab heute die Ergebnisse für das zweite Quartal, das am 31. Dezember 2018 endete, bekannt.
Aktuelle Highlights und Programm-Updates
Weibliche sexuelle Funktionsstörung / Vyle esi ™ (Bromelanotid)
Vyleesi, der Markenname für bremelanotide - In Entwicklung für Hypoactive Sexual Desire Disorder ("HSDD"):
Der Termin für das Medikament für verschreibungspflichtige Medikamentenkosten („PDUFA“) für den Abschluss der FDA-Überprüfung des Vyleesi New Drug Application („NDA“) wurde um drei Monate bis zum 23. Juni 2019 verlängert.
Die US-amerikanische Food and Drug Administration („FDA“) beantragte eine Phase-1-Studie mit freiwilligen Probanden vor der Menopause. Diese Studie wird derzeit von Palatin und AMAG Pharmaceuticals, unserem exklusiven Lizenznehmer für Nordamerika, durchgeführt.
Die Studienergebnisse werden voraussichtlich vor dem aktualisierten PDUFA-Datum bei der FDA eingereicht.
Palatin führt derzeit Gespräche mit potenziellen Kooperationspartnern für bestimmte Regionen außerhalb der lizenzierten Gebiete Nordamerika, China und Südkorea.
Entzündungshemmende / Autoimmun-Programme
Melanocortinrezeptor 1 und 1/5 ("MC1r", "MC1 / 5r") Agonisten in der Entwicklung zur Behandlung von entzündlichen und autoimmunen Erkrankungen wie trockenes Auge, Uveitis, diabetischer Retinopathie und entzündlichen Darmerkrankungen:
PL-8177, ein selektiver MC1r-Peptidagonist:
Abgeschlossene subkutane Dosierung von Menschen in einer klinischen Sicherheitsstudie der Phase 1 für einzelne und mehrere aufsteigende Dosen. In einer Pressemitteilung vom 8. November 2018 wurden keine Sicherheits- oder Verträglichkeitsbedenken festgestellt.
Im Quartal, das am 31. Dezember 2018 endete, wurde eine separate klinische Studie mit oraler Dosierung bei Menschen begonnen. Die Daten werden für das erste Quartal des Kalenderjahres 2019 erwartet.
Das Programm befindet sich derzeit in der internen Bewertung für Waisenbezeichnungen.
PL-8331 und PL-9643, duale MC1r- und MC5r-Peptidagonisten:
Fortsetzung der präklinischen Investigational New Drug ("IND") - Aktivierungsaktivitäten.
Das Programm befindet sich derzeit in der internen Bewertung für Waisenbezeichnungen.
Natriuretic Peptide Receptor ("NPR") Systemprogramm
Wir haben potentielle NPR-Wirkstoffkandidaten entwickelt und entwickeln, die für einen oder mehrere verschiedene natriuretische Peptidrezeptoren selektiv sind, einschließlich des natriuretischen Peptidrezeptors A ("NPR-A"), des natriuretischen Peptidrezeptors B ("NPR-B") und des Natriuretikums Peptidrezeptor C ("NPR-C"):
PL-3994, ein NPR-A-Agonist, der potentiell bei der Behandlung einer Anzahl von Herz-Kreislauf-Erkrankungen, einschließlich genetischer und Orphan-Erkrankungen, die aus einem Mangel an endogenem aktivem NPR-A resultieren, geeignet ist.
Akademische Kooperationen mit mehreren Institutionen laufen.
PL-5028, ein dualer NPR-A- und NPR-C-Agonist, der sich derzeit für kardiovaskuläre Erkrankungen entwickelt, einschließlich der Verringerung der Herzhypertrophie und der Fibrose.
Programm für genetische Adipositas
Melanocortin-Rezeptor 4 ("MC4r") -Peptid PL-8905 und oral aktives niedermolekulares PL-9610 zur Behandlung seltener genetischer Stoffwechsel- und Adipositas-Erkrankungen:
Corporate
Verminderte Schulden und damit verbundene Verbindlichkeiten von 7,2 Mio. USD zum 30. Juni 2018 auf 2,8 Mio. USD zum 31. Dezember 2018.
Finanzergebnisse des zweiten Quartals für das Geschäftsjahr 2019
Palatin wies für das Quartal zum 31. Dezember 2018 einen Nettoverlust von (5,0) Mio. USD oder 0,02 USD je Aktie und eine verwässerte Aktie aus, verglichen mit einem Nettogewinn von 3,0 Mio. USD oder 0,02 USD je Aktie und 0,01 USD je verwässerter Aktie. für den gleichen Zeitraum 2017.
Der Unterschied in den Finanzergebnissen zwischen den drei Monaten zum 31. Dezember 2018 und 2017 war im Wesentlichen auf die Verbuchung von Lizenz- und Vertragserlösen in Höhe von 10,6 Mio. USD im Zeitraum 2017 gemäß unserer Lizenzvereinbarung mit der AMAG zurückzuführen.
Einnahmen
Im Quartal zum 31. Dezember 2018 wurden keine Umsätze erzielt.
Für das Quartal, das zum 31. Dezember 2017 endete, standen 100% des Umsatzes, den Palatin ausgewiesen hat, im Zusammenhang mit unserer Lizenzvereinbarung mit der AMAG.
Betriebsaufwand
Die Gesamtbetriebskosten des Quartals zum 31. Dezember 2018 beliefen sich auf USD 5,1 Mio. gegenüber USD 7,7 Mio. im Vergleichsquartal 2017. Der Rückgang der Betriebsaufwendungen ist im Wesentlichen auf den Abschluss des klinischen Phase-3-Programms von Vyleesi und die dazu erforderlichen Zusatzstudien zurückzuführen die NDA in HSDD im März 2018.
Andere Einnahmen / Ausgaben
Die gesamten sonstigen Erträge beliefen sich netto für das Quartal zum 31. Dezember 2018 auf USD 7.871 im Vergleich zu den gesamten sonstigen Aufwendungen, netto (0,3) Mio. USD für das Quartal, das am 31. Dezember 2017 endete Wagnisschuld.
Einkommenssteuer
Im Quartal zum 31. Dezember 2018 wurde kein Ertragsteueraufwand oder -ertrag erfasst.
Gemäß den Lizenzvereinbarungen mit Fosun und Kwangdong wurden 500.000 bzw. 82.500 US-Dollar gemäß den Steuererfordernissen in China bzw. der Republik Korea einbehalten und im Geschäftsjahr zum 30. Juni 2018 als Aufwand verbucht. Für das Quartal, das am 31. Dezember 2017 endete, verbuchte Palatin einen Ertragsteueraufwand in Höhe von 100.880 USD, der sich auf den Quellensteuerbetrag stützte, wobei ein geschätzter effektiver jährlicher Ertragsteuersatz verwendet wurde, der auf das Quartalsergebnis angewandt wurde. Der verbleibende Saldo von 256.365 USD war in den Rechnungsabgrenzungsposten und sonstigen kurzfristigen Vermögenswerten enthalten zum 31. Dezember 2017. Jeder potenzielle Kredit, den Palatin aus den US-Steuererklärungen erhalten kann, wird derzeit durch die Wertberichtigung von Palatin ausgeglichen. Der Ertragsteueraufwand in Höhe von 100.880 USD wurde durch einen Steuervorteil in Höhe von 500.000 USD kompensiert, den Palatin im Quartal zum 31. Dezember 2017 im Zusammenhang mit der Auflösung einer Wertberichtigung für Palatins alternativer Mindeststeuergutschrift aufgrund des unterzeichneten Tax Cuts and Jobs Act erlangte im Dezember 2017. Dementsprechend waren zum 31. Dezember 2017 500.000 USD in den sonstigen langfristigen Vermögenswerten enthalten.
Finanzielle Situation
Die liquiden Mittel und Zahlungsmitteläquivalente von Palatin beliefen sich zum 31. Dezember 2018 auf 24,7 Millionen US-Dollar, verglichen mit Zahlungsmitteln und Zahlungsmitteläquivalenten von 38,0 Millionen US-Dollar zum 30. Juni 2018. Die kurzfristigen Verbindlichkeiten beliefen sich zum 31. Dezember 2018 auf 4,5 Millionen US-Dollar gegenüber 10,8 Millionen US-Dollar im Juni 30, 2018.
Palatin ist der Ansicht, dass die vorhandenen Kapitalmittel ausreichen werden, um unsere geplanten Operationen mindestens bis zum 31. März 2020 zu finanzieren.
Palatin Drug Discovery-Programme
In der Telefonkonferenz und im Webcast wird das Management die nächsten Schritte in Palatins Portfolio an Medikamentenentwicklungsprogrammen aktualisieren und diskutieren. Dazu gehören die MC1r- und MC1 / 5r-Agonistenpeptide von Palatin zur Behandlung von entzündungshemmenden und Autoimmun-Indikationen, MC4r-Peptid und kleinmolekulare Agonisten zur Behandlung von genetischen Fettleibigkeit-Indikationen und natriuretische Peptid-Rezeptor-Agonisten-Verbindungen zur Behandlung von kardiovaskulären und pulmonalen Indikationen.
Telefonkonferenz / Webcast
Palatin wird am 12. Februar 2019 um 11:00 Uhr Eastern Time eine Telefonkonferenz und einen Webcast abhalten, um die Geschäftsergebnisse des Quartals zum 31. Dezember 2018 ausführlicher zu erörtern und aktuelle Informationen über die Unternehmensentwicklung zu geben. Personen, die an der Live-Telefonkonferenz interessiert sind, können die Rufnummer 1-877-260-1479 (USA / Kanada) oder 1-334-323-0522 (international), Konferenz-ID 4414047, wählen. Auf den Webcast und die Wiedergabe kann durch Anmelden zugegriffen werden der Abschnitt "Investor / Webcasts" auf der Palatin-Website unter http://www.palatin.com. Eine Telefon- und Webcast-Wiedergabe wird etwa eine Stunde nach Beendigung des Anrufs verfügbar sein. Um auf die Telefonwiedergabe zuzugreifen, wählen Sie 1-888-203-1112 (USA / Kanada) oder 1-719-457-0820 (international), Kennziffer 4414047. Die Webcast- und Telefonwiedergabe ist bis zum 19. Februar 2019 verfügbar.
Über Palatin Technologies, Inc.
Palatin Technologies, Inc. ist ein spezialisiertes biopharmazeutisches Unternehmen, das erstklassige Arzneimittel entwickelt, die auf Molekülen basieren, die die Aktivität der Melanocortin- und natriuretischen Peptidrezeptorsysteme modulieren, sowie gezielte, rezeptorspezifische Produktkandidaten für die Behandlung von Krankheiten mit erheblichen nicht erfüllten Medikamenten Bedarf und wirtschaftliches Potenzial. Palatins Strategie besteht darin, Produkte zu entwickeln und anschließend Marketingkooperationen mit Branchenführern einzugehen, um deren kommerzielles Potenzial zu maximieren. Weitere Informationen zu Palatin finden Sie auf der Website von Palatin unter www.Palatin.com.
Vorausschauende Aussagen
Aussagen in dieser Pressemitteilung, die keine historischen Fakten sind, einschließlich Aussagen über zukünftige Erwartungen von Palatin Technologies, Inc., wie etwa Aussagen zu Ergebnissen klinischer Studien, mögliche Maßnahmen von Aufsichtsbehörden, einschließlich der FDA, Regulierungspläne, Entwicklungsprogramme, vorgeschlagene Indikationen für das Produkt Kandidaten und Marktpotenzial für Produktkandidaten sind „zukunftsgerichtete Aussagen“ im Sinne von Abschnitt 27A des Securities Act von 1933, Abschnitt 21E des Securities Exchange Act von 1934, und dieser Begriff ist im Private Securities Litigation Reform Act definiert Palatin beabsichtigt, solche zukunftsgerichteten Aussagen den sicheren Häfen zu unterwerfen. Solche zukunftsgerichteten Aussagen beinhalten bekannte und unbekannte Risiken, Ungewissheiten und andere Faktoren, die dazu führen könnten, dass die tatsächlichen Ergebnisse von Palatin wesentlich von den historischen Ergebnissen oder von Ergebnissen abweichen, die durch solche zukunftsgerichteten Aussagen ausgedrückt oder impliziert werden. Die tatsächlichen Ergebnisse von Palatin können erheblich von den in den zukunftsgerichteten Aussagen erörterten Ergebnissen abweichen, unter anderem aufgrund von Ergebnissen klinischer Studien, regulatorischer Maßnahmen der FDA und der Notwendigkeit behördlicher Zulassungen sowie der Fähigkeit Palatins, die Entwicklung seiner Technologie zu fördern klinische Studien durchführen und erfolgreich abschließen, Zeit und Kosten für den Abschluss klinischer Studien und die Einreichung von Zulassungsanträgen, von konkurrierenden pharmazeutischen, biopharmazeutischen und biotechnologischen Unternehmen entwickelte Produkten, die kommerzielle Akzeptanz der Produkte von Palatin und andere in den regelmäßigen Anmeldungen von Palatin diskutierte Faktoren mit der Securities and Exchange Commission. Palatin ist nicht für die Aktualisierung von Ereignissen verantwortlich, die nach dem Datum dieser Pressemitteilung auftreten.
Investorenanfragen:
Medienanfragen:
Stephen T. Wills, CPA, MST
Paul Arndt, MBA, LifeSci-Berater
CFO / COO (
609) 495-2200
Geschäftsführer (646) 597-6992
Info@Palatin.com
Paul@LifeSciAdvisors.com
PALATIN TECHNOLOGIES, INC.
und Tochtergesellschaft
Konzern-Gewinn- und Verlustrechnung
(ungeprüft)
Drei Monate endeten am 31. Dezember
Sechs Monate bis 31. Dezember
ERLÖSE:
Lizenz und Vertrag
10,612,153
34,505
37,553,661
BETRIEBSAUFWAND:
Forschung und Entwicklung
2,961,656
6.045.884
6.584.347
20.208.981
Allgemeine und administrative
2,088,565
1,625,189
4.129.147
3 169 764
Geschäftsaufwand
5,050,221
7.671.073
10.713.494
23,378,745
(Verlust) Ergebnis aus Geschäftstätigkeit
(5,050,221
2,941,080
(10,678,989)
14,174,916
SONSTIGE EINNAHMEN (Aufwand):
Kapitalerträge
100.169
81,356
253,752
133 082
Zinsaufwendungen
(92 298)
(391.363
(299.169
(848.040
Total sonstige Erträge (Aufwendungen), netto
(310.007
(45,417
(714,958
(Verlust) Ergebnis vor Ertragsteuern
(5,042,350)
2,631,073
(10.724.406
13,459,958
Einkommensteuervorteil
399,120
173.865
Netto (Verlust) Einkommen
3,030,193
13,633,823
Nettoergebnis (Verlust) je Stammaktie
Verwässertes Nettoergebnis je Stammaktie
Gewichtete durchschnittliche Anzahl ausstehender Stammaktien, die zur Berechnung des Nettoergebnisses (Verlusts) pro Stammaktie verwendet werden
206,487,984
197,238,056
205,724,321
197,175,316
Gewichtete durchschnittliche Anzahl ausstehender Stammaktien, die zur Berechnung des verwässerten Nettoergebnisses je Stammaktie verwendet wurden
202,711,616
200,430,824
PALATIN TECHNOLOGIES, INC.
Konsolidierte Bilanzen
30. Juni
VERMÖGENSWERTE
Umlaufvermögen:
Zahlungsmittel und Zahlungsmitteläquivalente
24,658,024
38.000.171
Debitorenkonto
Rechnungsabgrenzungsposten und sonstige kurzfristige Vermögenswerte
535,147
513,688
Gesamten Umlaufvermögens
25,193,171
38,513,859
Sachanlagen, netto
136,153
164.035
Sonstige Vermögensgegenstände
338,916
Gesamtvermögen
25,668,240
39.016.810
VERBINDLICHKEITEN UND AKTIONÄRE EIGENKAPITAL
Kurzfristige Verbindlichkeiten:
Abbrechnungsverbindlichkeiten
619.900
2,223,693
Angefallene Aufwendungen
1,101,045
2,103,021
Schuldverschreibungen ohne Abzug
2,321,123
5,948,763
Sonstige kurzfristige Verbindlichkeiten
486,474
487.488
Summe kurzfristige Verbindlichkeiten
4,528,542
10,762,965
332.898
Rechnungsabgrenzungsposten
Andere nicht gegenwärtige Belastungen
456,038
Gesamtverbindlichkeiten
12.051.901
Eigenkapital:
Vorzugsaktien im Wert von 0,01 USD - autorisierte 10.000.000 Aktien:
Serie A Convertible: Am 31. Dezember 2018 und am 30. Juni 2018 wurden 4.030 Aktien ausgegeben und ausstehend
Stammaktien mit einem Nennwert von 0,01 USD - genehmigte 300.000.000 Aktien:
ausgegebene und ausstehende 203.063.429 Aktien zum 31. Dezember 2018 und 200.554.205 Aktien zum 30. Juni 2018
2,030,634
2,005,542
Zusätzliches eingezahltes Kapital
361,379,336
357,005,233
Kumuliertes Defizit
(342,270,312
(332,045,906)
Total Eigenkapital
21,139,698
26.964.909
Gesamtverbindlichkeiten und Eigenkapital
Die oben genannten Informationen wurden in einer Hinterlegung bei der SEC veröffentlicht. Klicken Sie hier, um die Einreichung anzuzeigen.
Melden Sie sich an, um eine kostenlose E-Mail-Benachrichtigung zu erhalten, wenn Palatin Technologies einen ähnlichen Schritt unternimmt.
Andere kürzlich eingereichte Dokumente des Unternehmens umfassen Folgendes:
Palatin Technologies hat gerade seinen Quartalsbericht eingereicht: Nettoeinkommen (Verlust) ... - 11. Februar 2019
Registrierungserklärung gemäß Securities Act vom 1933 - 5. Februar 2019
Automatische Aktualisierung
http://www.conferencecalltranscripts.org/8/summary2/?id=5762…
Geil Wir werden REICH
Webcast vom 12.02.2019:
SA Stock Market News
Seeking Alpha
Palatin Technologies, Inc. (PTN) CEO Carl Spana on Q2 2019 Results - Earnings Call Transcript
Feb. 12, 2019 2:11 PM•PTN
Palatin Technologies, Inc. (NYSEMKT:PTN)
Q2 2019 Earnings Conference Call
February 12, 2019, 11:00 AM ET
Company Participants
Carl Spana - President & CEO
Steve Wills - EVP, CFO & COO
Conference Call Participants
John Newman - Canaccord
Joe Pantginis - H.C. Wainwright
Michael Higgins - Ladenburg Thalmann
Presentation
Operator
Good morning, ladies and gentlemen, and welcome to the Palatin Technologies Second Fiscal Quarter 2019 Operating Results Conference Call. As a reminder, this conference is being recorded.
Before we begin our remarks, I would like to remind you that the statements made by Palatin that are not historical facts may be forward-looking statements. These statements are based on assumptions that may or may not prove to be accurate and actual results could differ materially from those anticipated due to a variety of risks and uncertainties discussed in the company's most recent filings with the Securities and Exchange Commission. Please consider such risks and uncertainties carefully in evaluating these forward-looking statements and Palatin's prospects.
Advertisement
Now I'd like to introduce you to your host for today, Dr. Carl Spana, President and Chief Executive Officer of Palatin Technologies. Please go ahead, sir.
Carl Spana
Thank you. Good morning, and welcome to the Palatin Technologies' second quarter fiscal year 2019 call. I am Dr. Carl Spana, CEO and President of Palatin. With me on the call today is Steve Wills, Palatin's Executive Vice President, Chief Financial Officer and Chief Operating Officer. On today's call, we will provide financial and operating updates.
Now, I'm going to turn the call over to Steve, who'll provide financial updates. Steve?
Steve Wills
Thank you, Carl. And good morning, everyone. Regarding Palatin's quarter ended December 31, 2018, and recent operational and financial highlights, with respect to Vyleesi, which is under development for female hypoactive sexual desire disorder or HSDD, the FDA PDUFA date is June 23, 2019. Of note, if approved Palatin is due to receive a $60 million milestone from AMAG Pharmaceuticals, our North American licensee.
On the Vyleesi business development front, Palatin is in discussions with potential collaboration partners for certain regions outside the licensed territories of North America, China and South Korea. Carl will expand on the Vyleesi program during his portion of the presentation as well as our other programs under development.
Regarding the quarter ended December 31, 2018 financial results, Palatin reported a net loss of $5 million or $0.02 per basic and diluted share for the quarter ended December 31, 2018 compared to net income of $3 million or $0.02 per basic and diluted share for the same period in 2017. The difference in financial results between the three months ended December 31, 2018 and 2017 was mainly due to the recognition of $10.6 million in license and contract revenue during the 2017 period pursuant to our license agreement with AMAG.
Regarding revenue, there were no revenues recorded in the three months ended December 31, 2018. For the three months ended December 31, 2017, 100% of the revenue Palatin recognized was related to our license agreement with AMAG. Regarding operating expenses, total operating expenses for the quarter ended December 31, 2018, were $5.1 million compared to $7.7 million for the comparable quarter in 2017. The decrease in operating expenses reflects the completion of the Vyleesi Phase 3 clinical trial program and related ancillary studies necessary to file the NDA in 2018.
Regarding our cash position and working capital, Palatin's cash and cash equivalents were 24.7 million at December 31, 2018 compared to $32.6 million at September 30, 2018 and $38 million at June 30, 2018 are natural fiscal year. Current liabilities were $4.5 million at December 31, 2018, compared to $8.5 million of September 30, 2018. Palatin has also decreased its debt and related liabilities from $7.2 million at June 30, 2018 to $5.3 million at September 30, 2018 to $2.8 million at December 31, 2018. We believe that existing capital resources will be sufficient to fund our planned operations through at least March 31, 2020. Carl?
Advertisement
Carl Spana
Thank you, Steve. I'll start operational update with Vyleesi, our lead clinical product. Vyleesi is a first in class melanocortin agonist which is the only on-demand drug to complete Phase 3 clinical trial for hypoactive sexual desire disorder. Product's format is a simple single-use subcutaneous autoinjector self-administered by the patient approximately one hour prior to sexual activity.
We've been working with AMAG Pharmaceuticals, our North American licensee partner for Vyleesi to support the Vyleesi new drug application, which AMAG submitted to the FDA in March 2018. The NDA was accepted for review by the FDA in June 2018 and the PDUFA date for Vyleesi NDA is June 23, 2019.
In November 2018, as part of our discussions with the FDA regarding its review of the new drug application submitted for Vyleesi, the FDA requested additional data assessing 24-hour ambulatory blood pressure with short term daily use of Vyleesi. Palatin and AMAG are currently conducting the study and will have the data submitted to the FDA in advance of the Vyleesi June 23, 2019 PDUFA date.
In the two large North American Phase 3 Vyleesi studies subject to Vyleesi approximately three or four times per month or about once per week. However, there was a small subset of subjects that use Vyleesi more frequently. The requested study is designed to provide data on the short term daily dosing of Vyleesi or informed labeling purposes.
Outside of North America, we are working with our Chinese licensee, Fosun Pharma and our South Korean licensee partner Kwangdong Pharmaceuticals to advance Vyleesi development in those territories towards regulatory filings. In addition, the Committee for Medicinal Products for human use of European Medicines Agency has provided advice on the European Union Vyleesi Development Program indicating that only a single Phase 3 study in the European Union is needed to support a licensing application.
Now moving on to Palatin's earlier drug development programs, which include development from melanocortin four receptor agonist. We have developed new families of highly selective melanocortin receptor agonist with potentially broad applications in the treatment of a variety of inflammatory and autoimmune diseases including inflammatory bowel disease, dry eye, uveitis and other retinal diseases.
Our lead development candidate PL 8177 is a highly selective and potent melanocortin one receptor agonist, which we believe will have broad applications in treating inflammatory and autoimmune diseases. We recently announced their results in single ascending and multiple ascending dose study, Phase 1 study of PL-8177 in healthy volunteers. In this study, subcutaneously administered PL-8177 was well tolerated and no potential safety concerns were noted.
We've also completed a Phase 1 pharmacokinetic study of an oral dosing formulation of PL-8177 as a potential treatment for inflammatory bowel disease. The data is expected in the first quarter of 2019. Our next step with PL-8177 is to conduct a clinical study that will evaluate the safety and activity of PL-8177 in a variety of autoimmune diseases. This study is designed to provide the data needed to support larger Phase 2 efficacy studies and is anticipated to start in the first half of 2019.
PL-8331 is our dual Melanocortin receptor-1 and 5 agonist that in preclinical models has demonstrated the potential to treat a variety of ocular autoimmune diseases such as dry eye, uveitis and diabetic retinopathy. We have developed an eye drop formulation of PL-8331 as a potential treatment for dry eye and the IND enabling activities haven't started. Clinical studies in dry eye are anticipated to start in the second half of calendar 2019.
We've also worked to expand our product portfolio by leveraging our expertise in melanocortin biology and chemistry. We have developed an orally active small molecule, that's active against the Melanocortin 4 receptor called PL-9610. PL-9610 has demonstrated efficacy in a number of animal models of rare human genetic obesity and preclinical IND enabling activities to support IND filing and first human studies have started. We also anticipate filing for orphan drug designation for a number of autoimmune and genetic obesity indications for Melanocortin compounds.
Finally a naturally peptide development candidate PL-3994 is scheduled to start a Phase 2 trial sponsored by the American Heart Association in conjunction with major research centers in the first half of 2019. We believe that PL-3994 has a potential as a treatment for heart failure patients with well preserved or reduced ejection fraction.
Our PL-5028 is a dual natural peptide A receptor C agonist for use in cardiovascular and fibrotic diseases; including reduction of cardiac fibrosis. This peptide is in preclinical evaluation as a potential treatment for fibrotic diseases. We'll provide additional information on our programs on our website www.Palatin.com and at this point, I'm going to stop and open the call for questions and answers. Thank you.
Question-and-Answer Session
Operator
[Operator Instructions] Our first question will come from John Newman, Canaccord
John Newman
Hi there. Good morning. And thanks for the update. Thanks also for taking my question. So Carl, you give us an update on the clinical data that the FDA have asked you for and just curious if you could talk to us about why you think the agency is asking for this study at this particular time point? And also just remind us the blood pressure monitoring that was done in clinical studies, I know that you had previous alluded that.
Carl Spana
Sure. I think as I noted in the presentation or the discussion, for the most part, the Vyleesi is used about once a week. That's probably going to be the average use pattern for the product. However, we turned out that there was a small set of patients that clustered their dosing. So they may have taken the drug for four five days in a row versus say once a week.
In our Phase 3 program or in our overall program, we extensively evaluated the effects of Vyleesi on blood pressure using ambulatory blood pressure measurements in a once a week format and I think the agency was very pleased with that data. They accepted it and realized that there was a small 2 to 4 millimeter transient change in blood pressure.
However, we didn’t have the data or we didn’t have comprehensive data on what happened if patients took it every day or say four or five days and naturally what the study is doing. It's really just evaluating the use of Vyleesi over eight consecutive days and measuring and characterizing the blood pressure effect.
I don't anticipate that we were going to see anything different than we saw in the once a week, but I think the agency is doing its job and being careful. There is a non-life-threatening indication and I think that they're dotting the I's and crossing the T's and making sure that they can provide a label to patients and prescribing physicians that really characterize the effects of the drug.
I determined if there are any subsets of patients that you might not want to take the drug or if you have some precaution when taking it. So that's really the nature of this. I don't think this is not an issue, I don't anticipate that we were going to see anything that we haven't already seen or don't really understand but it will be a formal study that will characterize the effect over short term daily use, which will allow the agency to feel comfortable in putting the appropriate label on the product.
John Newman
Great. Thank you.
Operator
Thank you. Our next question will come from Joe Pantginis, H.C. Wainwright.
Joe Pantginis
Carl, since you just mentioned the label curious, if the data come out clean from this blood pressure study, could this lead to a potentially better label for the drug?
Carl Spana
Certainly, compared to not having it yes, in the absence of the data, the agency would have had to put a very cautionary label on because it didn't exist or they weren’t comfortable with the data over there or the extent of it. So I think that we will wind up with a label that is appropriate for the product that that highlights or has all the pertinent information allows the safe use of the product.
Joe Pantginis
And just had a curiosity, did the filing, the NDA filing with the Phase 3 data, did that have the level of granularity for patients enrolled in the reconnect studies that had sort of as you describe it the clustering use and impacts on blood pressure that would sort of act as a supplement to this study.
Carl Spana
So in the Phase 3 program, that's a more general study. So blood pressure there was characterize through blood pressure cuff measurement. We certainly have patient, different types of patient there and pre-menopause, women are relative healthy, premenopausal women that were your control [indiscernible] were in that study.
In general go over up to almost 18 or 24 months of use, there were no signal, there's no change in blood pressure over time with it, but that's not the type of study one that you would use to characterize the potential effect. We did have other Phase 1 data over short term daily use, but not using as extensive ambulatory blood pressure over 24 hours. We use them over the duration of dosing for example 12 hours. We did have 24 hours.
So there was enough data in there to one, indicate that there is not a high probability that there is going to be an effect here, but we didn’t -- we have always characterized the drug as a pure end drug with the subset that this will be taken once or twice per week and I think we came out and when they got to the point of looking at the labeling and looking at the dosing density, there were a subset of patients they did use a daily basis and this is just really a study that is better characterize the blood pressure in those patients.
As I said, I don't anticipate based on what we know, based on previous Phase 1 studies that there is going to be any cumulative effect. We know that there does appear to be at all. It's just that this is really a formal study that poses that question and answers it using up-to-date methodology that wasn't necessarily using the earlier programs, earlier studies.
Joe Pantginis
And then my last question is, I don't know if you can answer this, based on either direct feedback from the regulatory agents or from the FDA in this case or from even body language regards to the need or the desire for them to conduct an adcom at this point assuming the data are clean?
Carl Spana
What I can tell you is there was an Adcom scheduled for January 15 that obviously did not occur and I think based on -- I think if we get a study done in a timely fashion, which we will and submit it to the agency with sufficient time for review, I think if there's no -- if it's a clean study, which I anticipate it will be. I don't think that there will be -- I don't personally think there will be need for an Adcom and they certainly would not be time from when we would submit it to the June 23 date. So I'll leave it at that.
Operator
The next question will come from Michael Higgins, Ladenburg Thalmann.
Michael Higgins
Thanks for taking the questions. Couple on Vyleesi if I could and then on the pipeline. The plan outside you also believe they started to bridge in the first half of '19, if that's still the case and also noted in your PR and your Q, I think all your discussions with partners outside you currently partnered Vyleesi, can you give us some feedback on the timing of those discussions? Great to have those, I am little surprised what's happening there? Are your partners involved with your discussions with European authorities and when you look for next year as it relates to potential [ph].
Carl Spana
Sure, I'll start and then I'll pass over to Steve, what we did, one thing that we wanted to accomplish prior to really finalizing any business development activities with the -- around the year right to [indiscernible] and European market in particular, was really to understand and get feedback from the EMA, the regulatory authorities for the territory as to what would be required for the development of bremelanotide or Vyleesi in that territory.
We had some earlier discussions with them and we wanted to confirm your structure of the trial, what it would look like. We obviously want to conduct the trial that is very similar almost identical to what we did in North America marketplace and we wanted to confirm that a single study would be sufficient in conjunction with the North American studies for a licensing application.
We have just towards the end of last year, got our feedback. We were pleased with the feedback. I think we were able to conduct a trial using endpoints that were identical to what we used in the US and that a single Phase 3 trial would be a sufficient filing.
So that now really opens up the door for us to accelerate or reinstituting the discussion that we were having and I'll turn that over to Steve, since he is leading that activity.
Steve Wills
As Carl mentioned, the AI that we needed was, we needed more specificity, granularity around the specific protocol for approval in Europe. We have that now and as Carl mentioned, we were pleased with the response and the dialogue from IMA/CHMP. So that activity has definitely increased, not just us calling, but also inbound calls. We're actively and aggressively in discussions with all the regions outside of the already licensed territories of North America with AMAG, China with Fosun and South Korea with Kwangdong Pharmaceuticals.
So we and as we get closer to the PDUFA date and the approval I'm very comfortable that these discussions will even advanced greater. We're also working closely with our existing rest of the world partners i.e. Fosun, Pharma and Kwangdong. They are in active discussions with the related regulatory FDI in China and the same equivalent in South Korea on planning their specific regulatory path.
So we're very excited and enthusiastic with the activity and the interest and with the assumption and caveat that were approved in June. We would anticipate that frankly all the regions outside the existing territories would be licensed before the end of calendar 2019.
Michael Higgins
Okay. Congrats. That's great, that's critical, identical to what you've done in the U.S. Last week in the conference call management suggested that the common signal at the experts on the blood pressure signal, is that you're viewing that without the Adcom agencies more bullish on the NDA and early May your time in which we would expect to hear whether or not there be an Adcom ahead of the PDUFA?
Steve Wills
Sure, so just to tell you I think that each product is evaluated by our own merits, risk reward profile. Vyleesi is a PRN medication, the vast majority of patients who are going to have exposures of three to four times per month, there will be a very limited subset of patients that may have a few more times in that. Keep in mind our dosing limitations we really would anticipate approximately six to eight doses being available per month on a prescription basis.
So I think that Vyleesi falls into a category where you're characterizing the blood pressure effect. The clinical risk is low and probably I don't think that they would necessarily have to go out and seek advice from an adcom. I think that the personnel that we've been working with the agency that are coming from the cardio legal group or are quite conversant with the type of study signs we're using and the potential risk of intermittent changes, small change in blood pressure. So I think that we're okay there.
However, with that being said, we will be submitting the data back. The agency has the right to take -- to have additional time to review that data should they choose to do so. I don't think at the moment based on our discussions with them, that they will do that, but we always have to plan for that, that they could.
Michael Higgins
Okay. And then just I think the timing, it's early May, there is the adcom requested that a reasonable timeframe to look for that will signal that wouldn’t be in adcom or think of a discussion.
Carl Spana
Sure, I am not getting into the exact time, we're really submitting sufficiently in advance of the PDUFA date. The agency will make a decision relatively quickly I am sure on whether or not they will be in a major submission and request additional time or not. So I think what I would say is I would anticipate there would be an announcement that we file the data back and then you if you don't hear anything within one to two weeks, you can anticipate that they're moving towards a decision on the June PDUFA date and they won't wait long.
The data is pretty simple, it's pretty straightforward, it's going to be a few grasp. They will make a decision relatively quickly I would think on whether or not they want to maintain the current timeline or they want additional time. And obviously if there is any change in that, we would communicate that.
Michael Higgins
Just as a follow-up to that, any plans in the press release about pressure results from this study?
Carl Spana
That is not, the study is in conjunction with AMAG and the NDA is filed in AMAG's name. So although we are heavily involved in the conduct of the study, AMAG will be submitting the data. So that will be up to them as to what they do. I would guess that they will have some statement of concerning the data when they submit it, but I can't speak for them and we have to be guided by them of when they want to disclose.
Michael Higgins
Couple of questions on the play time if I could 8177, when do you expect to start grower report the sub-queue formulations?
Carl Spana
We're targeting probably second quarter start and the study design that we're anticipating are relatively quick. So I would expect if we start in the second quarter, we will get preliminary data late fourth quarter, early first quarter from those studies. They're not designed to be long-term studies. They're designed to have 28 day treatment periods, So they go quickly.
Michael Higgins
Okay. And based on the point that's really light, next there I think maybe Phase 1 results if you can on that, it will be great.
Carl Spana
I missed, you broke up on
Michael Higgins
Sure 9610, the
Carl Spana
So 9610 right now, sure 9610 is in scale manufacturing for drug product, for the active pharmaceutical ingredient that will be done probably second quarter and then we'll institute the formal phase preclinical studies. So I expect you really talking about first half 2019 first in human studies, that compound.
You will see that we will put out some data on the compound. We have been put this date out on some of the preclinical model and we've done. So we will probably second quarter, we will begin to put out some of that data at some point.
Steve Wills
Just quick correction, Carl said first half of 2019, he meant 2020, sorry for that initiation study.
Michael Higgins
Got you. Sounds good and then one final one here on 8331 dry eye, we plan on Phase 2 back half of '19, is that the oral or is that due?
Carl Spana
So that's for 8331 for dry eye is -- they are eye drops and that is progressing and we would expect to start in the second half of this calendar year, we have that already scaled. We are actually working with Ora Pharmaceuticals out of Boston area and this is all they do.
So they’ll be helping us lead that charge and we feel comfortable with the timelines they put forward.
Michael Higgins
Good. You get a lot of pipeline news coming up over the next year or so, so look forward to that. Appreciate the time. Thanks guys.
Operator
Thank you. Our next question will come from Joe Pantginis, H.C. Wainwright.
Joe Pantginis
Hey guys. Thanks for taking the follow-up, Just had a curiosity and you could say Joe it's too early to ask these questions, but if we get the good news that we're all expecting in June and the drug is approved, maybe this is a question even more for AMAG, but you know what do you think the potential launch timing or turnaround could be number one?
And then number two, can you give some comments about the supply chain of the finished device your support there?
Carl Spana
Just quickly in their public disclosures, they're anticipating a second half calendar 2019 launch. Steve has been working with them very closely on the supply side. So probably I'll turn it to him.
Steve Wills
As Carl stated, AMAG has publicly disclosed that assuming we have that June PDUFA date and approval that they will be launching commercially in the third quarter of calendar 2019. Everything is moving towards that, planning towards success albeit whether it's the education on all the various fronts, AMAG is an excellent partner. Really fits the profile. We're extremely pleased with the relationship and when I say planning for that lines, that does include obviously commercial inventory.
Joe Pantginis
Thanks a lot guys.
Operator
Thank you. At this time, we have no further questions in the queue. So I would like to turn the conference back over to Dr. Spana.
Carl Spana
Well I would like to thank all of you for participating in the Palatin Technologies second fiscal quarter 2019 call. We look forward to updating you next quarter. It's exciting time for the company. We have a lot of great things going on and we're quite excited about the prospects for the company. So have a great day and we'll talk to you soon, bye, bye.
Operator
Thank you very much. Ladies and gentlemen, at this time, this now concludes this morning's conference. You may disconnect your phone lines and have a great rest of the week. Thank you.
0
Recommended for you:
GLOP These 2 Preferred Stocks Are Like Coiled Springs, Waiting To Rip Higher, From Gaslog Partners
4h • Rida Morwa
TSLA Tesla Bears Retreat
53m • ValueAnalyst
5 REITs To Hold 'Forever'
2/4/19 • Brad Thomas
T AT&T: Stephenson Sets The Record Straight
7h • David Alton Clark
SA Stock Market News
Seeking Alpha
Palatin Technologies, Inc. (PTN) CEO Carl Spana on Q2 2019 Results - Earnings Call Transcript
Feb. 12, 2019 2:11 PM•PTN
Palatin Technologies, Inc. (NYSEMKT:PTN)
Q2 2019 Earnings Conference Call
February 12, 2019, 11:00 AM ET
Company Participants
Carl Spana - President & CEO
Steve Wills - EVP, CFO & COO
Conference Call Participants
John Newman - Canaccord
Joe Pantginis - H.C. Wainwright
Michael Higgins - Ladenburg Thalmann
Presentation
Operator
Good morning, ladies and gentlemen, and welcome to the Palatin Technologies Second Fiscal Quarter 2019 Operating Results Conference Call. As a reminder, this conference is being recorded.
Before we begin our remarks, I would like to remind you that the statements made by Palatin that are not historical facts may be forward-looking statements. These statements are based on assumptions that may or may not prove to be accurate and actual results could differ materially from those anticipated due to a variety of risks and uncertainties discussed in the company's most recent filings with the Securities and Exchange Commission. Please consider such risks and uncertainties carefully in evaluating these forward-looking statements and Palatin's prospects.
Advertisement
Now I'd like to introduce you to your host for today, Dr. Carl Spana, President and Chief Executive Officer of Palatin Technologies. Please go ahead, sir.
Carl Spana
Thank you. Good morning, and welcome to the Palatin Technologies' second quarter fiscal year 2019 call. I am Dr. Carl Spana, CEO and President of Palatin. With me on the call today is Steve Wills, Palatin's Executive Vice President, Chief Financial Officer and Chief Operating Officer. On today's call, we will provide financial and operating updates.
Now, I'm going to turn the call over to Steve, who'll provide financial updates. Steve?
Steve Wills
Thank you, Carl. And good morning, everyone. Regarding Palatin's quarter ended December 31, 2018, and recent operational and financial highlights, with respect to Vyleesi, which is under development for female hypoactive sexual desire disorder or HSDD, the FDA PDUFA date is June 23, 2019. Of note, if approved Palatin is due to receive a $60 million milestone from AMAG Pharmaceuticals, our North American licensee.
On the Vyleesi business development front, Palatin is in discussions with potential collaboration partners for certain regions outside the licensed territories of North America, China and South Korea. Carl will expand on the Vyleesi program during his portion of the presentation as well as our other programs under development.
Regarding the quarter ended December 31, 2018 financial results, Palatin reported a net loss of $5 million or $0.02 per basic and diluted share for the quarter ended December 31, 2018 compared to net income of $3 million or $0.02 per basic and diluted share for the same period in 2017. The difference in financial results between the three months ended December 31, 2018 and 2017 was mainly due to the recognition of $10.6 million in license and contract revenue during the 2017 period pursuant to our license agreement with AMAG.
Regarding revenue, there were no revenues recorded in the three months ended December 31, 2018. For the three months ended December 31, 2017, 100% of the revenue Palatin recognized was related to our license agreement with AMAG. Regarding operating expenses, total operating expenses for the quarter ended December 31, 2018, were $5.1 million compared to $7.7 million for the comparable quarter in 2017. The decrease in operating expenses reflects the completion of the Vyleesi Phase 3 clinical trial program and related ancillary studies necessary to file the NDA in 2018.
Regarding our cash position and working capital, Palatin's cash and cash equivalents were 24.7 million at December 31, 2018 compared to $32.6 million at September 30, 2018 and $38 million at June 30, 2018 are natural fiscal year. Current liabilities were $4.5 million at December 31, 2018, compared to $8.5 million of September 30, 2018. Palatin has also decreased its debt and related liabilities from $7.2 million at June 30, 2018 to $5.3 million at September 30, 2018 to $2.8 million at December 31, 2018. We believe that existing capital resources will be sufficient to fund our planned operations through at least March 31, 2020. Carl?
Advertisement
Carl Spana
Thank you, Steve. I'll start operational update with Vyleesi, our lead clinical product. Vyleesi is a first in class melanocortin agonist which is the only on-demand drug to complete Phase 3 clinical trial for hypoactive sexual desire disorder. Product's format is a simple single-use subcutaneous autoinjector self-administered by the patient approximately one hour prior to sexual activity.
We've been working with AMAG Pharmaceuticals, our North American licensee partner for Vyleesi to support the Vyleesi new drug application, which AMAG submitted to the FDA in March 2018. The NDA was accepted for review by the FDA in June 2018 and the PDUFA date for Vyleesi NDA is June 23, 2019.
In November 2018, as part of our discussions with the FDA regarding its review of the new drug application submitted for Vyleesi, the FDA requested additional data assessing 24-hour ambulatory blood pressure with short term daily use of Vyleesi. Palatin and AMAG are currently conducting the study and will have the data submitted to the FDA in advance of the Vyleesi June 23, 2019 PDUFA date.
In the two large North American Phase 3 Vyleesi studies subject to Vyleesi approximately three or four times per month or about once per week. However, there was a small subset of subjects that use Vyleesi more frequently. The requested study is designed to provide data on the short term daily dosing of Vyleesi or informed labeling purposes.
Outside of North America, we are working with our Chinese licensee, Fosun Pharma and our South Korean licensee partner Kwangdong Pharmaceuticals to advance Vyleesi development in those territories towards regulatory filings. In addition, the Committee for Medicinal Products for human use of European Medicines Agency has provided advice on the European Union Vyleesi Development Program indicating that only a single Phase 3 study in the European Union is needed to support a licensing application.
Now moving on to Palatin's earlier drug development programs, which include development from melanocortin four receptor agonist. We have developed new families of highly selective melanocortin receptor agonist with potentially broad applications in the treatment of a variety of inflammatory and autoimmune diseases including inflammatory bowel disease, dry eye, uveitis and other retinal diseases.
Our lead development candidate PL 8177 is a highly selective and potent melanocortin one receptor agonist, which we believe will have broad applications in treating inflammatory and autoimmune diseases. We recently announced their results in single ascending and multiple ascending dose study, Phase 1 study of PL-8177 in healthy volunteers. In this study, subcutaneously administered PL-8177 was well tolerated and no potential safety concerns were noted.
We've also completed a Phase 1 pharmacokinetic study of an oral dosing formulation of PL-8177 as a potential treatment for inflammatory bowel disease. The data is expected in the first quarter of 2019. Our next step with PL-8177 is to conduct a clinical study that will evaluate the safety and activity of PL-8177 in a variety of autoimmune diseases. This study is designed to provide the data needed to support larger Phase 2 efficacy studies and is anticipated to start in the first half of 2019.
PL-8331 is our dual Melanocortin receptor-1 and 5 agonist that in preclinical models has demonstrated the potential to treat a variety of ocular autoimmune diseases such as dry eye, uveitis and diabetic retinopathy. We have developed an eye drop formulation of PL-8331 as a potential treatment for dry eye and the IND enabling activities haven't started. Clinical studies in dry eye are anticipated to start in the second half of calendar 2019.
We've also worked to expand our product portfolio by leveraging our expertise in melanocortin biology and chemistry. We have developed an orally active small molecule, that's active against the Melanocortin 4 receptor called PL-9610. PL-9610 has demonstrated efficacy in a number of animal models of rare human genetic obesity and preclinical IND enabling activities to support IND filing and first human studies have started. We also anticipate filing for orphan drug designation for a number of autoimmune and genetic obesity indications for Melanocortin compounds.
Finally a naturally peptide development candidate PL-3994 is scheduled to start a Phase 2 trial sponsored by the American Heart Association in conjunction with major research centers in the first half of 2019. We believe that PL-3994 has a potential as a treatment for heart failure patients with well preserved or reduced ejection fraction.
Our PL-5028 is a dual natural peptide A receptor C agonist for use in cardiovascular and fibrotic diseases; including reduction of cardiac fibrosis. This peptide is in preclinical evaluation as a potential treatment for fibrotic diseases. We'll provide additional information on our programs on our website www.Palatin.com and at this point, I'm going to stop and open the call for questions and answers. Thank you.
Question-and-Answer Session
Operator
[Operator Instructions] Our first question will come from John Newman, Canaccord
John Newman
Hi there. Good morning. And thanks for the update. Thanks also for taking my question. So Carl, you give us an update on the clinical data that the FDA have asked you for and just curious if you could talk to us about why you think the agency is asking for this study at this particular time point? And also just remind us the blood pressure monitoring that was done in clinical studies, I know that you had previous alluded that.
Carl Spana
Sure. I think as I noted in the presentation or the discussion, for the most part, the Vyleesi is used about once a week. That's probably going to be the average use pattern for the product. However, we turned out that there was a small set of patients that clustered their dosing. So they may have taken the drug for four five days in a row versus say once a week.
In our Phase 3 program or in our overall program, we extensively evaluated the effects of Vyleesi on blood pressure using ambulatory blood pressure measurements in a once a week format and I think the agency was very pleased with that data. They accepted it and realized that there was a small 2 to 4 millimeter transient change in blood pressure.
However, we didn’t have the data or we didn’t have comprehensive data on what happened if patients took it every day or say four or five days and naturally what the study is doing. It's really just evaluating the use of Vyleesi over eight consecutive days and measuring and characterizing the blood pressure effect.
I don't anticipate that we were going to see anything different than we saw in the once a week, but I think the agency is doing its job and being careful. There is a non-life-threatening indication and I think that they're dotting the I's and crossing the T's and making sure that they can provide a label to patients and prescribing physicians that really characterize the effects of the drug.
I determined if there are any subsets of patients that you might not want to take the drug or if you have some precaution when taking it. So that's really the nature of this. I don't think this is not an issue, I don't anticipate that we were going to see anything that we haven't already seen or don't really understand but it will be a formal study that will characterize the effect over short term daily use, which will allow the agency to feel comfortable in putting the appropriate label on the product.
John Newman
Great. Thank you.
Operator
Thank you. Our next question will come from Joe Pantginis, H.C. Wainwright.
Joe Pantginis
Carl, since you just mentioned the label curious, if the data come out clean from this blood pressure study, could this lead to a potentially better label for the drug?
Carl Spana
Certainly, compared to not having it yes, in the absence of the data, the agency would have had to put a very cautionary label on because it didn't exist or they weren’t comfortable with the data over there or the extent of it. So I think that we will wind up with a label that is appropriate for the product that that highlights or has all the pertinent information allows the safe use of the product.
Joe Pantginis
And just had a curiosity, did the filing, the NDA filing with the Phase 3 data, did that have the level of granularity for patients enrolled in the reconnect studies that had sort of as you describe it the clustering use and impacts on blood pressure that would sort of act as a supplement to this study.
Carl Spana
So in the Phase 3 program, that's a more general study. So blood pressure there was characterize through blood pressure cuff measurement. We certainly have patient, different types of patient there and pre-menopause, women are relative healthy, premenopausal women that were your control [indiscernible] were in that study.
In general go over up to almost 18 or 24 months of use, there were no signal, there's no change in blood pressure over time with it, but that's not the type of study one that you would use to characterize the potential effect. We did have other Phase 1 data over short term daily use, but not using as extensive ambulatory blood pressure over 24 hours. We use them over the duration of dosing for example 12 hours. We did have 24 hours.
So there was enough data in there to one, indicate that there is not a high probability that there is going to be an effect here, but we didn’t -- we have always characterized the drug as a pure end drug with the subset that this will be taken once or twice per week and I think we came out and when they got to the point of looking at the labeling and looking at the dosing density, there were a subset of patients they did use a daily basis and this is just really a study that is better characterize the blood pressure in those patients.
As I said, I don't anticipate based on what we know, based on previous Phase 1 studies that there is going to be any cumulative effect. We know that there does appear to be at all. It's just that this is really a formal study that poses that question and answers it using up-to-date methodology that wasn't necessarily using the earlier programs, earlier studies.
Joe Pantginis
And then my last question is, I don't know if you can answer this, based on either direct feedback from the regulatory agents or from the FDA in this case or from even body language regards to the need or the desire for them to conduct an adcom at this point assuming the data are clean?
Carl Spana
What I can tell you is there was an Adcom scheduled for January 15 that obviously did not occur and I think based on -- I think if we get a study done in a timely fashion, which we will and submit it to the agency with sufficient time for review, I think if there's no -- if it's a clean study, which I anticipate it will be. I don't think that there will be -- I don't personally think there will be need for an Adcom and they certainly would not be time from when we would submit it to the June 23 date. So I'll leave it at that.
Operator
The next question will come from Michael Higgins, Ladenburg Thalmann.
Michael Higgins
Thanks for taking the questions. Couple on Vyleesi if I could and then on the pipeline. The plan outside you also believe they started to bridge in the first half of '19, if that's still the case and also noted in your PR and your Q, I think all your discussions with partners outside you currently partnered Vyleesi, can you give us some feedback on the timing of those discussions? Great to have those, I am little surprised what's happening there? Are your partners involved with your discussions with European authorities and when you look for next year as it relates to potential [ph].
Carl Spana
Sure, I'll start and then I'll pass over to Steve, what we did, one thing that we wanted to accomplish prior to really finalizing any business development activities with the -- around the year right to [indiscernible] and European market in particular, was really to understand and get feedback from the EMA, the regulatory authorities for the territory as to what would be required for the development of bremelanotide or Vyleesi in that territory.
We had some earlier discussions with them and we wanted to confirm your structure of the trial, what it would look like. We obviously want to conduct the trial that is very similar almost identical to what we did in North America marketplace and we wanted to confirm that a single study would be sufficient in conjunction with the North American studies for a licensing application.
We have just towards the end of last year, got our feedback. We were pleased with the feedback. I think we were able to conduct a trial using endpoints that were identical to what we used in the US and that a single Phase 3 trial would be a sufficient filing.
So that now really opens up the door for us to accelerate or reinstituting the discussion that we were having and I'll turn that over to Steve, since he is leading that activity.
Steve Wills
As Carl mentioned, the AI that we needed was, we needed more specificity, granularity around the specific protocol for approval in Europe. We have that now and as Carl mentioned, we were pleased with the response and the dialogue from IMA/CHMP. So that activity has definitely increased, not just us calling, but also inbound calls. We're actively and aggressively in discussions with all the regions outside of the already licensed territories of North America with AMAG, China with Fosun and South Korea with Kwangdong Pharmaceuticals.
So we and as we get closer to the PDUFA date and the approval I'm very comfortable that these discussions will even advanced greater. We're also working closely with our existing rest of the world partners i.e. Fosun, Pharma and Kwangdong. They are in active discussions with the related regulatory FDI in China and the same equivalent in South Korea on planning their specific regulatory path.
So we're very excited and enthusiastic with the activity and the interest and with the assumption and caveat that were approved in June. We would anticipate that frankly all the regions outside the existing territories would be licensed before the end of calendar 2019.
Michael Higgins
Okay. Congrats. That's great, that's critical, identical to what you've done in the U.S. Last week in the conference call management suggested that the common signal at the experts on the blood pressure signal, is that you're viewing that without the Adcom agencies more bullish on the NDA and early May your time in which we would expect to hear whether or not there be an Adcom ahead of the PDUFA?
Steve Wills
Sure, so just to tell you I think that each product is evaluated by our own merits, risk reward profile. Vyleesi is a PRN medication, the vast majority of patients who are going to have exposures of three to four times per month, there will be a very limited subset of patients that may have a few more times in that. Keep in mind our dosing limitations we really would anticipate approximately six to eight doses being available per month on a prescription basis.
So I think that Vyleesi falls into a category where you're characterizing the blood pressure effect. The clinical risk is low and probably I don't think that they would necessarily have to go out and seek advice from an adcom. I think that the personnel that we've been working with the agency that are coming from the cardio legal group or are quite conversant with the type of study signs we're using and the potential risk of intermittent changes, small change in blood pressure. So I think that we're okay there.
However, with that being said, we will be submitting the data back. The agency has the right to take -- to have additional time to review that data should they choose to do so. I don't think at the moment based on our discussions with them, that they will do that, but we always have to plan for that, that they could.
Michael Higgins
Okay. And then just I think the timing, it's early May, there is the adcom requested that a reasonable timeframe to look for that will signal that wouldn’t be in adcom or think of a discussion.
Carl Spana
Sure, I am not getting into the exact time, we're really submitting sufficiently in advance of the PDUFA date. The agency will make a decision relatively quickly I am sure on whether or not they will be in a major submission and request additional time or not. So I think what I would say is I would anticipate there would be an announcement that we file the data back and then you if you don't hear anything within one to two weeks, you can anticipate that they're moving towards a decision on the June PDUFA date and they won't wait long.
The data is pretty simple, it's pretty straightforward, it's going to be a few grasp. They will make a decision relatively quickly I would think on whether or not they want to maintain the current timeline or they want additional time. And obviously if there is any change in that, we would communicate that.
Michael Higgins
Just as a follow-up to that, any plans in the press release about pressure results from this study?
Carl Spana
That is not, the study is in conjunction with AMAG and the NDA is filed in AMAG's name. So although we are heavily involved in the conduct of the study, AMAG will be submitting the data. So that will be up to them as to what they do. I would guess that they will have some statement of concerning the data when they submit it, but I can't speak for them and we have to be guided by them of when they want to disclose.
Michael Higgins
Couple of questions on the play time if I could 8177, when do you expect to start grower report the sub-queue formulations?
Carl Spana
We're targeting probably second quarter start and the study design that we're anticipating are relatively quick. So I would expect if we start in the second quarter, we will get preliminary data late fourth quarter, early first quarter from those studies. They're not designed to be long-term studies. They're designed to have 28 day treatment periods, So they go quickly.
Michael Higgins
Okay. And based on the point that's really light, next there I think maybe Phase 1 results if you can on that, it will be great.
Carl Spana
I missed, you broke up on
Michael Higgins
Sure 9610, the
Carl Spana
So 9610 right now, sure 9610 is in scale manufacturing for drug product, for the active pharmaceutical ingredient that will be done probably second quarter and then we'll institute the formal phase preclinical studies. So I expect you really talking about first half 2019 first in human studies, that compound.
You will see that we will put out some data on the compound. We have been put this date out on some of the preclinical model and we've done. So we will probably second quarter, we will begin to put out some of that data at some point.
Steve Wills
Just quick correction, Carl said first half of 2019, he meant 2020, sorry for that initiation study.
Michael Higgins
Got you. Sounds good and then one final one here on 8331 dry eye, we plan on Phase 2 back half of '19, is that the oral or is that due?
Carl Spana
So that's for 8331 for dry eye is -- they are eye drops and that is progressing and we would expect to start in the second half of this calendar year, we have that already scaled. We are actually working with Ora Pharmaceuticals out of Boston area and this is all they do.
So they’ll be helping us lead that charge and we feel comfortable with the timelines they put forward.
Michael Higgins
Good. You get a lot of pipeline news coming up over the next year or so, so look forward to that. Appreciate the time. Thanks guys.
Operator
Thank you. Our next question will come from Joe Pantginis, H.C. Wainwright.
Joe Pantginis
Hey guys. Thanks for taking the follow-up, Just had a curiosity and you could say Joe it's too early to ask these questions, but if we get the good news that we're all expecting in June and the drug is approved, maybe this is a question even more for AMAG, but you know what do you think the potential launch timing or turnaround could be number one?
And then number two, can you give some comments about the supply chain of the finished device your support there?
Carl Spana
Just quickly in their public disclosures, they're anticipating a second half calendar 2019 launch. Steve has been working with them very closely on the supply side. So probably I'll turn it to him.
Steve Wills
As Carl stated, AMAG has publicly disclosed that assuming we have that June PDUFA date and approval that they will be launching commercially in the third quarter of calendar 2019. Everything is moving towards that, planning towards success albeit whether it's the education on all the various fronts, AMAG is an excellent partner. Really fits the profile. We're extremely pleased with the relationship and when I say planning for that lines, that does include obviously commercial inventory.
Joe Pantginis
Thanks a lot guys.
Operator
Thank you. At this time, we have no further questions in the queue. So I would like to turn the conference back over to Dr. Spana.
Carl Spana
Well I would like to thank all of you for participating in the Palatin Technologies second fiscal quarter 2019 call. We look forward to updating you next quarter. It's exciting time for the company. We have a lot of great things going on and we're quite excited about the prospects for the company. So have a great day and we'll talk to you soon, bye, bye.
Operator
Thank you very much. Ladies and gentlemen, at this time, this now concludes this morning's conference. You may disconnect your phone lines and have a great rest of the week. Thank you.
0
Recommended for you:
GLOP These 2 Preferred Stocks Are Like Coiled Springs, Waiting To Rip Higher, From Gaslog Partners
4h • Rida Morwa
TSLA Tesla Bears Retreat
53m • ValueAnalyst
5 REITs To Hold 'Forever'
2/4/19 • Brad Thomas
T AT&T: Stephenson Sets The Record Straight
7h • David Alton Clark
Die wichtigste Frage aus der TK nochmal mit google tl
John Newman
Hallo. Guten Morgen. Und danke für das Update. Danke auch für meine Frage. Also, Carl, geben Sie uns ein Update zu den klinischen Daten, nach denen Sie von der FDA gefragt wurden, und sind Sie nur neugierig, ob Sie mit uns darüber sprechen könnten, warum Sie denken, dass die Agentur zu diesem Zeitpunkt nach dieser Studie fragt? Und erinnern Sie uns auch einfach an die Blutdrucküberwachung, die in klinischen Studien durchgeführt wurde. Ich weiß, dass Sie das vorher angesprochen hatten.
Carl Spana
Sicher. Ich denke, wie ich in der Präsentation oder der Diskussion feststellte, wird das Vyleesi meistens einmal pro Woche verwendet. Dies ist wahrscheinlich das durchschnittliche Nutzungsmuster für das Produkt. Es stellte sich jedoch heraus, dass es eine kleine Gruppe von Patienten gab, die ihre Dosierung in Gruppen bildeten. Vielleicht haben sie das Medikament vier oder fünf Tage hintereinander gegen einmal wöchentlich eingenommen.
In unserem Phase-3-Programm oder in unserem Gesamtprogramm haben wir die Auswirkungen von Vyleesi auf den Blutdruck mithilfe von ambulanten Blutdruckmessungen einmal wöchentlich ausführlich untersucht, und ich bin der Meinung, dass die Agentur mit diesen Daten sehr zufrieden war. Sie akzeptierten es und stellten fest, dass sich der Blutdruck nur um 2 bis 4 Millimeter kurzzeitig ändert.
Wir hatten jedoch keine Daten oder wir hatten keine umfassenden Daten darüber, was passiert ist, wenn Patienten täglich eingenommen oder vier oder fünf Tage gesprochen haben und natürlich, was die Studie macht. Es ist wirklich nur eine Bewertung der Anwendung von Vyleesi an acht aufeinander folgenden Tagen und die Messung und Charakterisierung des Blutdruckeffekts.
Ich rechne nicht damit, dass wir einmal in der Woche etwas anderes sehen würden als in der Woche, aber ich denke, dass die Agentur ihre Arbeit erledigt und vorsichtig ist. Es gibt eine nicht lebensbedrohliche Andeutung, und ich denke, dass sie die I-Punkte punktieren und die T-Werte durchqueren und sicherstellen, dass sie Patienten und verschreibenden Ärzten ein Etikett geben können, das die Wirkungen des Medikaments wirklich charakterisiert.
Ich habe festgestellt, ob es Untermengen von Patienten gibt, bei denen Sie das Medikament möglicherweise nicht einnehmen möchten, oder ob Sie bei der Einnahme Vorsichtsmaßnahmen treffen. Das ist also die Natur. Ich denke nicht, dass dies kein Thema ist, ich erwarte nicht, dass wir etwas sehen werden, das wir nicht bereits gesehen haben oder nicht wirklich verstehen, aber es wird eine formale Studie sein, die den Effekt über kurz prägen wird Begriff der täglichen Nutzung, so dass sich die Agentur wohl fühlen kann, wenn das Produkt mit dem entsprechenden Etikett versehen wird.
John Newman
Hallo. Guten Morgen. Und danke für das Update. Danke auch für meine Frage. Also, Carl, geben Sie uns ein Update zu den klinischen Daten, nach denen Sie von der FDA gefragt wurden, und sind Sie nur neugierig, ob Sie mit uns darüber sprechen könnten, warum Sie denken, dass die Agentur zu diesem Zeitpunkt nach dieser Studie fragt? Und erinnern Sie uns auch einfach an die Blutdrucküberwachung, die in klinischen Studien durchgeführt wurde. Ich weiß, dass Sie das vorher angesprochen hatten.
Carl Spana
Sicher. Ich denke, wie ich in der Präsentation oder der Diskussion feststellte, wird das Vyleesi meistens einmal pro Woche verwendet. Dies ist wahrscheinlich das durchschnittliche Nutzungsmuster für das Produkt. Es stellte sich jedoch heraus, dass es eine kleine Gruppe von Patienten gab, die ihre Dosierung in Gruppen bildeten. Vielleicht haben sie das Medikament vier oder fünf Tage hintereinander gegen einmal wöchentlich eingenommen.
In unserem Phase-3-Programm oder in unserem Gesamtprogramm haben wir die Auswirkungen von Vyleesi auf den Blutdruck mithilfe von ambulanten Blutdruckmessungen einmal wöchentlich ausführlich untersucht, und ich bin der Meinung, dass die Agentur mit diesen Daten sehr zufrieden war. Sie akzeptierten es und stellten fest, dass sich der Blutdruck nur um 2 bis 4 Millimeter kurzzeitig ändert.
Wir hatten jedoch keine Daten oder wir hatten keine umfassenden Daten darüber, was passiert ist, wenn Patienten täglich eingenommen oder vier oder fünf Tage gesprochen haben und natürlich, was die Studie macht. Es ist wirklich nur eine Bewertung der Anwendung von Vyleesi an acht aufeinander folgenden Tagen und die Messung und Charakterisierung des Blutdruckeffekts.
Ich rechne nicht damit, dass wir einmal in der Woche etwas anderes sehen würden als in der Woche, aber ich denke, dass die Agentur ihre Arbeit erledigt und vorsichtig ist. Es gibt eine nicht lebensbedrohliche Andeutung, und ich denke, dass sie die I-Punkte punktieren und die T-Werte durchqueren und sicherstellen, dass sie Patienten und verschreibenden Ärzten ein Etikett geben können, das die Wirkungen des Medikaments wirklich charakterisiert.
Ich habe festgestellt, ob es Untermengen von Patienten gibt, bei denen Sie das Medikament möglicherweise nicht einnehmen möchten, oder ob Sie bei der Einnahme Vorsichtsmaßnahmen treffen. Das ist also die Natur. Ich denke nicht, dass dies kein Thema ist, ich erwarte nicht, dass wir etwas sehen werden, das wir nicht bereits gesehen haben oder nicht wirklich verstehen, aber es wird eine formale Studie sein, die den Effekt über kurz prägen wird Begriff der täglichen Nutzung, so dass sich die Agentur wohl fühlen kann, wenn das Produkt mit dem entsprechenden Etikett versehen wird.
Palatin Technologies, Inc. (NYSEMKT: PTN ) 2. Quartal 2019 Telefonkonferenz zu den Ergebnissen 12. Februar 2019 11:00 Uhr ET
Unternehmensteilnehmer
Carl Spana - Präsident und CEO
Steve Wills - EVP, CFO und COO
Teilnehmer an der Telefonkonferenz
John Newman - Canaccord
Joe Pantginis - HC Wainwright
Michael Higgins - Ladenburg Thalmann
Operator
Guten Morgen, meine Damen und Herren, und herzlich willkommen zur Telefonkonferenz zum zweiten Quartal des Geschäftsjahres 2019 von Palatin Technologies. Zur Erinnerung wird diese Konferenz aufgezeichnet.
Bevor wir mit unseren Ausführungen beginnen, möchte ich Sie daran erinnern, dass die Aussagen von Palatin, die keine historischen Fakten sind, zukunftsgerichtete Aussagen sein können. Diese Aussagen basieren auf Annahmen, die sich als zutreffend erweisen können oder auch nicht, und die tatsächlichen Ergebnisse können aufgrund einer Vielzahl von Risiken und Ungewissheiten, die in den jüngsten Einreichungen des Unternehmens bei der Securities and Exchange Commission erörtert wurden, erheblich von den erwarteten abweichen. Bitte berücksichtigen Sie diese Risiken und Unwägbarkeiten sorgfältig, wenn Sie diese zukunftsgerichteten Aussagen und die Aussichten von Palatin bewerten.
Jetzt möchte ich Sie Ihrem heutigen Gastgeber, Dr. Carl Spana, President und Chief Executive Officer von Palatin Technologies, vorstellen. Bitte fahren Sie fort, Sir.
Carl Spana
Vielen Dank. Guten Morgen und herzlich willkommen zum Aufruf von Palatin Technologies im zweiten Quartal des Geschäftsjahres 2019. Ich bin Dr. Carl Spana, CEO und Präsident von Palatin. Heute ist Steve Wills bei mir, der Executive Vice President, Chief Financial Officer und Chief Operating Officer von Palatin. Bei dem heutigen Anruf werden wir finanzielle und betriebliche Updates bereitstellen.
Jetzt werde ich den Anruf an Steve weiterleiten, der finanzielle Updates bereitstellt. Steve
Steve Wills
Vielen Dank, Carl. Und guten Morgen, alle zusammen. Bezüglich des Quartals von Palatin, das am 31. Dezember 2018 endete, und der jüngsten operativen und finanziellen Höhepunkte in Bezug auf Vyleesi, das sich derzeit für weibliche hypoaktive sexuelle Luststörung oder HSDD entwickelt, ist das Datum der FDA PDUFA der 23. Juni 2019. Bemerkenswert, sofern Palatin zugelassen ist wird einen Meilenstein in Höhe von 60 Millionen US-Dollar von AMAG Pharmaceuticals, unserem nordamerikanischen Lizenznehmer, erhalten.
In Bezug auf die Geschäftsentwicklung von Vyleesi führt Palatin Gespräche mit potenziellen Kooperationspartnern für bestimmte Regionen außerhalb der Lizenzgebiete Nordamerika, China und Südkorea. Carl wird das Vyleesi-Programm während seines Teils der Präsentation sowie unserer anderen in Entwicklung befindlichen Programme erweitern.
In Bezug auf das Finanzergebnis des Quartals zum 31. Dezember 2018 verzeichnete Palatin für das Quartal zum 31. Dezember 2018 einen Nettoverlust von 5 Millionen USD oder 0,02 USD je verwässerter und unverwässerter Aktie, verglichen mit einem Nettogewinn von 3 Millionen USD oder 0,02 USD je verwässerten und verwässerten Aktie für den gleichen Zeitraum im Jahr 2017. Der Unterschied in den Finanzergebnissen zwischen den drei Monaten zum 31. Dezember 2018 und 2017 war im Wesentlichen auf den Einzug von Lizenz- und Vertragserlösen in Höhe von 10,6 Mio. USD im Zeitraum 2017 gemäß unserer Lizenzvereinbarung mit der AMAG zurückzuführen.
Bezüglich der Umsatzerlöse wurden in den drei Monaten zum 31. Dezember 2018 keine Umsatzerlöse erzielt. In den drei Monaten zum 31. Dezember 2017 standen 100% der Umsatzerlöse, die Palatin verbuchte, im Zusammenhang mit unserer Lizenzvereinbarung mit der AMAG. Bezüglich der Betriebsaufwendungen beliefen sich die Betriebsaufwendungen des Quartals zum 31. Dezember 2018 auf USD 5,1 Mio. gegenüber USD 7,7 Mio. im Vergleichsquartal 2017. Der Rückgang der Betriebsaufwendungen spiegelt den Abschluss des klinischen Phase-3-Studienprogramms von Vyleesi und damit verbundene Zusatzstudien wider erforderlich, um die NDA 2018 einzureichen.
Bezüglich unserer Liquidität und des Umlaufvermögens beliefen sich die liquiden Mittel von Palatin zum 31. Dezember 2018 auf 24,7 Mio. US-Dollar im Vergleich zu 32,6 Mio. US-Dollar am 30. September 2018 und 38 Mio. US-Dollar am 30. Juni 2018 als natürliches Geschäftsjahr. Die kurzfristigen Verbindlichkeiten beliefen sich zum 31. Dezember 2018 auf 4,5 Mio. US-Dollar, verglichen mit 8,5 Mio. US-Dollar am 30. September 2018. Palatin reduzierte außerdem seine Schulden und die damit verbundenen Verbindlichkeiten von 7,2 Mio. US-Dollar am 30. Juni 2018 auf 5,3 Mio. US-Dollar am 30. September 2018 auf 2,8 Mio. US-Dollar 31. Dezember 2018. Wir sind der Ansicht, dass die vorhandenen Kapitalressourcen ausreichen werden, um unsere geplanten Operationen mindestens bis zum 31. März 2020 zu finanzieren. Carl?
https://seekingalpha.com/article/4240256-palatin-technologie…
Unternehmensteilnehmer
Carl Spana - Präsident und CEO
Steve Wills - EVP, CFO und COO
Teilnehmer an der Telefonkonferenz
John Newman - Canaccord
Joe Pantginis - HC Wainwright
Michael Higgins - Ladenburg Thalmann
Operator
Guten Morgen, meine Damen und Herren, und herzlich willkommen zur Telefonkonferenz zum zweiten Quartal des Geschäftsjahres 2019 von Palatin Technologies. Zur Erinnerung wird diese Konferenz aufgezeichnet.
Bevor wir mit unseren Ausführungen beginnen, möchte ich Sie daran erinnern, dass die Aussagen von Palatin, die keine historischen Fakten sind, zukunftsgerichtete Aussagen sein können. Diese Aussagen basieren auf Annahmen, die sich als zutreffend erweisen können oder auch nicht, und die tatsächlichen Ergebnisse können aufgrund einer Vielzahl von Risiken und Ungewissheiten, die in den jüngsten Einreichungen des Unternehmens bei der Securities and Exchange Commission erörtert wurden, erheblich von den erwarteten abweichen. Bitte berücksichtigen Sie diese Risiken und Unwägbarkeiten sorgfältig, wenn Sie diese zukunftsgerichteten Aussagen und die Aussichten von Palatin bewerten.
Jetzt möchte ich Sie Ihrem heutigen Gastgeber, Dr. Carl Spana, President und Chief Executive Officer von Palatin Technologies, vorstellen. Bitte fahren Sie fort, Sir.
Carl Spana
Vielen Dank. Guten Morgen und herzlich willkommen zum Aufruf von Palatin Technologies im zweiten Quartal des Geschäftsjahres 2019. Ich bin Dr. Carl Spana, CEO und Präsident von Palatin. Heute ist Steve Wills bei mir, der Executive Vice President, Chief Financial Officer und Chief Operating Officer von Palatin. Bei dem heutigen Anruf werden wir finanzielle und betriebliche Updates bereitstellen.
Jetzt werde ich den Anruf an Steve weiterleiten, der finanzielle Updates bereitstellt. Steve
Steve Wills
Vielen Dank, Carl. Und guten Morgen, alle zusammen. Bezüglich des Quartals von Palatin, das am 31. Dezember 2018 endete, und der jüngsten operativen und finanziellen Höhepunkte in Bezug auf Vyleesi, das sich derzeit für weibliche hypoaktive sexuelle Luststörung oder HSDD entwickelt, ist das Datum der FDA PDUFA der 23. Juni 2019. Bemerkenswert, sofern Palatin zugelassen ist wird einen Meilenstein in Höhe von 60 Millionen US-Dollar von AMAG Pharmaceuticals, unserem nordamerikanischen Lizenznehmer, erhalten.
In Bezug auf die Geschäftsentwicklung von Vyleesi führt Palatin Gespräche mit potenziellen Kooperationspartnern für bestimmte Regionen außerhalb der Lizenzgebiete Nordamerika, China und Südkorea. Carl wird das Vyleesi-Programm während seines Teils der Präsentation sowie unserer anderen in Entwicklung befindlichen Programme erweitern.
In Bezug auf das Finanzergebnis des Quartals zum 31. Dezember 2018 verzeichnete Palatin für das Quartal zum 31. Dezember 2018 einen Nettoverlust von 5 Millionen USD oder 0,02 USD je verwässerter und unverwässerter Aktie, verglichen mit einem Nettogewinn von 3 Millionen USD oder 0,02 USD je verwässerten und verwässerten Aktie für den gleichen Zeitraum im Jahr 2017. Der Unterschied in den Finanzergebnissen zwischen den drei Monaten zum 31. Dezember 2018 und 2017 war im Wesentlichen auf den Einzug von Lizenz- und Vertragserlösen in Höhe von 10,6 Mio. USD im Zeitraum 2017 gemäß unserer Lizenzvereinbarung mit der AMAG zurückzuführen.
Bezüglich der Umsatzerlöse wurden in den drei Monaten zum 31. Dezember 2018 keine Umsatzerlöse erzielt. In den drei Monaten zum 31. Dezember 2017 standen 100% der Umsatzerlöse, die Palatin verbuchte, im Zusammenhang mit unserer Lizenzvereinbarung mit der AMAG. Bezüglich der Betriebsaufwendungen beliefen sich die Betriebsaufwendungen des Quartals zum 31. Dezember 2018 auf USD 5,1 Mio. gegenüber USD 7,7 Mio. im Vergleichsquartal 2017. Der Rückgang der Betriebsaufwendungen spiegelt den Abschluss des klinischen Phase-3-Studienprogramms von Vyleesi und damit verbundene Zusatzstudien wider erforderlich, um die NDA 2018 einzureichen.
Bezüglich unserer Liquidität und des Umlaufvermögens beliefen sich die liquiden Mittel von Palatin zum 31. Dezember 2018 auf 24,7 Mio. US-Dollar im Vergleich zu 32,6 Mio. US-Dollar am 30. September 2018 und 38 Mio. US-Dollar am 30. Juni 2018 als natürliches Geschäftsjahr. Die kurzfristigen Verbindlichkeiten beliefen sich zum 31. Dezember 2018 auf 4,5 Mio. US-Dollar, verglichen mit 8,5 Mio. US-Dollar am 30. September 2018. Palatin reduzierte außerdem seine Schulden und die damit verbundenen Verbindlichkeiten von 7,2 Mio. US-Dollar am 30. Juni 2018 auf 5,3 Mio. US-Dollar am 30. September 2018 auf 2,8 Mio. US-Dollar 31. Dezember 2018. Wir sind der Ansicht, dass die vorhandenen Kapitalressourcen ausreichen werden, um unsere geplanten Operationen mindestens bis zum 31. März 2020 zu finanzieren. Carl?
https://seekingalpha.com/article/4240256-palatin-technologie…
Tolles Faktenboard hier!
Aber vielleicht sollte man auch mal bewerten was da geschrieben steht .
Keine Einnahmen im Oktober/November/Dezember generiert!?
Betriebsausgaben in Höhe von 7,7 Mio zu verarbeiten.
Aber zum Glück hat man ja noch 24 MIO Cash und ist zumindest bis zum 31 März 2020 safe.
Das schreit doch nach Sekt............... oder ?
Prost!
Aber vielleicht sollte man auch mal bewerten was da geschrieben steht .
Keine Einnahmen im Oktober/November/Dezember generiert!?
Betriebsausgaben in Höhe von 7,7 Mio zu verarbeiten.
Aber zum Glück hat man ja noch 24 MIO Cash und ist zumindest bis zum 31 März 2020 safe.
Das schreit doch nach Sekt............... oder ?
Prost!
Wenn die Zulassung von Vyleesi kommt und es sich gut verkauft wird eine Zahlung von AMAG fällig
und dann beginnen die Lizenzzahlungen. In einem Jahr sehe ich Palatin bei ~ 3,50 $.
Langfristig erwarte ich noch mehr. (meine Wertung der Lage)
Andere werten die Fakten anders und sehen Palatin mittelfristig bei 0,0 $.
Der zweite Fall wäre für mich nicht so schön.
und dann beginnen die Lizenzzahlungen. In einem Jahr sehe ich Palatin bei ~ 3,50 $.
Langfristig erwarte ich noch mehr. (meine Wertung der Lage)
Andere werten die Fakten anders und sehen Palatin mittelfristig bei 0,0 $.
Der zweite Fall wäre für mich nicht so schön.
Antwort auf Beitrag Nr.: 59.888.218 von apano am 15.02.19 22:25:54Gehe auch von rd 3$ aus...d.h.Faktor 4,5 

Im Grunde ist es einfach. Schlägt Vyleesi ein werden wir reich, falls nicht war es ein Griff ins Klo und Palatin verschwindet von der Bildfläche. Und die Kohle mit
Antwort auf Beitrag Nr.: 59.892.949 von Reinerle am 17.02.19 05:42:38Bevor es zur Entscheidung kommt, wird es hier abgehen, denn die Zocker werden den Kurs puschen, siehe Trevena. Ich denke dass 2€ also bereits vorher locker drin sind.
Ich bin bei Comdirect. Leider bieten die kein Call für AMAG an.
Kann mir einer eien Tipp geben wie ich an so ein Papier komme?
Kann mir einer eien Tipp geben wie ich an so ein Papier komme?
Antwort auf Beitrag Nr.: 59.913.587 von apano am 19.02.19 20:11:13
Schau mal hier bei WO auf dem Rechner unter Amag rein und da unter Optionsscheinen bzw. Zertifikaten. Ich bin fast immer am Smartphone, kann daher nicht sagen ob es überhaupt irgendwelche gibt
Zitat von apano: Ich bin bei Comdirect. Leider bieten die kein Call für AMAG an.
Kann mir einer eien Tipp geben wie ich an so ein Papier komme?
Schau mal hier bei WO auf dem Rechner unter Amag rein und da unter Optionsscheinen bzw. Zertifikaten. Ich bin fast immer am Smartphone, kann daher nicht sagen ob es überhaupt irgendwelche gibt
Antwort auf Beitrag Nr.: 59.913.683 von Mammut22 am 19.02.19 20:24:49Danke für den Tip. Leider kein Resultat.
Ich spekuliere auf die Zulassung von Vyleesi im Juni und das es ein Bestseller wird.
Mit einem call auf AMAG wäre ein noch größerer Hebel möglich.
Ich spekuliere auf die Zulassung von Vyleesi im Juni und das es ein Bestseller wird.
Mit einem call auf AMAG wäre ein noch größerer Hebel möglich.
Auf die Zulassung von Vyleesi spekulieren ist eine sehr gute Idee. 👍 Bis dahin geht es sicherlich wieder Richtung 1$. Vyleesi hat wohl auch gute Chancen auf eine Zulassung.
Jedoch bezweifle ich, daß das Medi ein Blockbuster werden wird. Ich denke, die wenigsten Frauen werden sich Vyleesi applizieren, um (wieder) ‚Lust auf Sex‘ zu haben...😉
Meine bescheidene Meinung, falls es doch zum Blockbuster werden sollte, gönne ich Palatin & den Aktionären (hier) den Erfolg 🤗
Jedoch bezweifle ich, daß das Medi ein Blockbuster werden wird. Ich denke, die wenigsten Frauen werden sich Vyleesi applizieren, um (wieder) ‚Lust auf Sex‘ zu haben...😉
Meine bescheidene Meinung, falls es doch zum Blockbuster werden sollte, gönne ich Palatin & den Aktionären (hier) den Erfolg 🤗
Könnte mir schon vorstellen das es ein Bestseller wird. Grad im asiatischen Raum. Die probieren doch jeden Scheis zur Potenzsteigerung. Wie gemahlenes Nashorn-Horn. Oder Wal-Penis. usw
...die Männer aber nicht die Frauen 😄😉
1. Na und 2. Ist auch für Männer
Antwort auf Beitrag Nr.: 59.949.353 von Stoxtrayder am 24.02.19 14:06:17Pfizer ist mit Viagra zum größten Pharmakonzern der Welt geworden. Bestimmt nicht mit den paar
Pillen für die, die beim Sex Probleme hatten. Nach dem Medienrummel wollte jeder das Zeug mal
probieren. Ich kann mich erinnern, es gab eine Zeit, da waren die Zeitungen voll damit, dass die
Frauen durch die egoistischen Männer ein unerfülltes Sexleben haben. Durch die voranschreitende
Emanzipation kann ich mir sehr gut vorstellen, das viele Frauen sich über ein Stimulationsmittel
freuen, dessen Wirksamkeit wissenschaftlich nachgewiesen ist.
(Das der Bedarf groß ist, sieht man auch an dem riesigem Angebot der Quacksalber)
Was die Nebenwirkungen betrifft, der Autoinjektor ist Schmerzfrei und es gibt kaum ein Medikament ohne Nebenwirkungen.
Wenn ich abens die Tagesschau sehe, wird mir auch immer Übel.
Da greife ich doch lieber zu Vylessi.
Pillen für die, die beim Sex Probleme hatten. Nach dem Medienrummel wollte jeder das Zeug mal
probieren. Ich kann mich erinnern, es gab eine Zeit, da waren die Zeitungen voll damit, dass die
Frauen durch die egoistischen Männer ein unerfülltes Sexleben haben. Durch die voranschreitende
Emanzipation kann ich mir sehr gut vorstellen, das viele Frauen sich über ein Stimulationsmittel
freuen, dessen Wirksamkeit wissenschaftlich nachgewiesen ist.
(Das der Bedarf groß ist, sieht man auch an dem riesigem Angebot der Quacksalber)
Was die Nebenwirkungen betrifft, der Autoinjektor ist Schmerzfrei und es gibt kaum ein Medikament ohne Nebenwirkungen.
Wenn ich abens die Tagesschau sehe, wird mir auch immer Übel.
Da greife ich doch lieber zu Vylessi.
Antwort auf Beitrag Nr.: 59.952.019 von apano am 24.02.19 22:32:35
Bin ja mit einer Mini Position dabei.
Alles wird gut


Nun mal Butter bei die Fische
Fakt ist! Ein neuer Lover für die Mutter ,und schon braucht sie keine Medikamente mehr um die Beine breit zu machen.Ähnlich wie bei uns Männern die auf Viagra verzichten können sobald sie mal ne fremde Mutter am Start haben.So sieht die Sache leider aus.Bin ja mit einer Mini Position dabei.
Alles wird gut



Antwort auf Beitrag Nr.: 59.958.820 von fitwiefisch am 25.02.19 17:59:04
Ohje, ich hoffe du gibst nicht noch mehr von deinen tollen Ansichten Preis....
Zitat von fitwiefisch: Fakt ist! Ein neuer Lover für die Mutter ,und schon braucht sie keine Medikamente mehr um die Beine breit zu machen.Ähnlich wie bei uns Männern die auf Viagra verzichten können sobald sie mal ne fremde Mutter am Start haben.So sieht die Sache leider aus.
Bin ja mit einer Mini Position dabei.
Alles wird gut
Ohje, ich hoffe du gibst nicht noch mehr von deinen tollen Ansichten Preis....
Antwort auf Beitrag Nr.: 59.959.318 von Mammut22 am 25.02.19 19:00:33
Alles wir gut.
Nicht so ernst
Es ist Faschingszeit,da kann man wohl einen raus hauen.Alles wir gut.

Antwort auf Beitrag Nr.: 59.960.263 von fitwiefisch am 25.02.19 20:26:14
Als Kölner kann ich dem ausnahmsweise zustimmen. 😉
Zitat von fitwiefisch: Es ist Faschingszeit,da kann man wohl einen raus hauen.
Alles wir gut.
Als Kölner kann ich dem ausnahmsweise zustimmen. 😉
Antwort auf Beitrag Nr.: 59.960.263 von fitwiefisch am 25.02.19 20:26:14...und als berliner ebenso.....alaaf und viel glück für den FC und PTN.
Was ist denn hier im Busch? Kann mir einer den heutigen Ausbruch erklären? Habe bishef keine News gefunden... Gott sei Dank bin ich vorgestern wieder mit einer Posi eingestiegen 😀😀
Antwort auf Beitrag Nr.: 59.977.468 von rallyseeker am 27.02.19 15:56:13
Die Amis gehen ab, da gab es auch keine News, soweit ich das sehen kann. Hier ist noch sehr viel Luft nach oben
Zitat von rallyseeker: Was ist denn hier im Busch? Kann mir einer den heutigen Ausbruch erklären? Habe bishef keine News gefunden... Gott sei Dank bin ich vorgestern wieder mit einer Posi eingestiegen 😀😀
Die Amis gehen ab, da gab es auch keine News, soweit ich das sehen kann. Hier ist noch sehr viel Luft nach oben
Antwort auf Beitrag Nr.: 59.977.579 von Mammut22 am 27.02.19 16:04:59Sehr schön!! Wir arbeiten uns auf das Datum zur Nachreichung der erforderlichen Unterlagen und hoffentlichen Zulassung hin 😁
Am Freitag der Euro
Antwort auf Beitrag Nr.: 59.978.644 von rallyseeker am 27.02.19 17:42:29Dafür startet sie aber recht früh.
Gruß aaahhh
Gruß aaahhh
PALATIN TECHNOLOGIES, INC. (PTN) REPORT OVERVIEW
Palatin Technologies' Recent Financial Performance
For the twelve months ended June 30th, 2018 vs June 30th, 2017, Palatin Technologies reported revenue of $67.13MM vs $44.72MM (up 50.11%) and analysts estimated basic earnings per share $0.12 vs -$0.07. Analysts expect earnings to be released on May 21st, 2019. The report will be for the fiscal period ending March 31st, 2019. Reported EPS for the same quarter last year was $0.00. The estimated EPS forecast for the next fiscal year is $0.16 and is expected to report on September 12th, 2019.
To read the full Palatin Technologies, Inc. (PTN) report, download it here: http://Fundamental-Markets.com/register/?so=PTN
Palatin Technologies' Recent Financial Performance
For the twelve months ended June 30th, 2018 vs June 30th, 2017, Palatin Technologies reported revenue of $67.13MM vs $44.72MM (up 50.11%) and analysts estimated basic earnings per share $0.12 vs -$0.07. Analysts expect earnings to be released on May 21st, 2019. The report will be for the fiscal period ending March 31st, 2019. Reported EPS for the same quarter last year was $0.00. The estimated EPS forecast for the next fiscal year is $0.16 and is expected to report on September 12th, 2019.
To read the full Palatin Technologies, Inc. (PTN) report, download it here: http://Fundamental-Markets.com/register/?so=PTN
Von Google die Übersetzung
PALATIN TECHNOLOGIES, INC. (PTN) BERICHTSÜBERSICHT Die jüngste finanzielle Performance von Palatin Technologies In den zwölf Monaten, die am 30. Juni 2018 endeten, verglichen mit dem 30. Juni 2017, erzielte Palatin Technologies einen Umsatz von 67,13 Mio. US-Dollar gegenüber 44,72 Mio. US-Dollar (plus 50,11%) Gewinn pro Aktie 0,12 US-Dollar - 0,07 US-Dollar. Analysten erwarten, dass die Gewinne am 21. Mai 2019 veröffentlicht werden. Der Bericht bezieht sich auf die am 31. März 2019 endende Geschäftsperiode. Das ausgewiesene Ergebnis je Quartal des Vorjahres betrug 0,00 USD. Die geschätzte EPS-Prognose für das nächste Geschäftsjahr liegt bei 0,16 US-Dollar und wird voraussichtlich am 12. September 2019 veröffentlicht. Den vollständigen Bericht von Palatin Technologies, Inc. (PTN) finden Sie hier: http://Fundamental-Markets.com/ register /? so = PTNPalatin Technology / voraussichtliches Marktpotential von 1,3 Mrd $ bis 2020 allein in USA | wallstreet-online.de - Vollständige Diskussion unter:
https://www.wallstreet-online.de/diskussion/1207859-2781-279…
Antwort auf Beitrag Nr.: 59.978.665 von aaahhh am 27.02.19 17:43:55Den letzten beißen die Hunde... Ausserdem ist das Datum ja nicht in Stein gemeisselt, es ist eine Frist!!! Es könnte ja auch deutlich früher eingereicht und bestätigt werden. Alleine die Tatsache, dass die fehlenden Unterlagen nachgereicht wurden könnte nochmal einen Sprung auslösen und dann wird es teuer reinzukommen. N.M.M.
Es wird wieder voller hier im Haus. Unerwartet frühe Kursentwicklung.
Der Handel drüben ist um ein Vielfaches höher als bei uns. Schon seit einigen Tagen
AMAG sucht nach einem Director of Consumer Marketing für Vyleesi:
https://www.linkedin.com/jobs/view/director-of-consumer-mark…
https://www.linkedin.com/jobs/view/director-of-consumer-mark…
Antwort auf Beitrag Nr.: 60.062.275 von Schurik am 10.03.19 12:17:24
Wer lesen kann... sorry hatte deinen Post übersehen
Zitat von Schurik: Was zum lesen: https://www.linkedin.com/jobs/view/director-of-consumer-marketing-vyleesi-at-amag-pharmaceuticals-900513476
Wer lesen kann... sorry hatte deinen Post übersehen
Wenn Annalysten Millardenumsätze nur in den USA erwarten, ist Palatin 3 !/2 Monate
vor der Zulassung moderat bewertet.
Schnell wird sich im Herbst , wie bei Viagra, zeigen, dass Vyleesi weit über die ursprüngliche Zielgruppe hinaus, nachgefragt wird.
Der Höchstkurs von Palatin war mal über 102 $. Das zeigt wie hoch mal die Erwartungen waren.
Die jetzige Zurückhaltung erkläre ich mir damit, das sich an dem Teil einige mächtig die Finger
verbrannt haben.
vor der Zulassung moderat bewertet.
Schnell wird sich im Herbst , wie bei Viagra, zeigen, dass Vyleesi weit über die ursprüngliche Zielgruppe hinaus, nachgefragt wird.
Der Höchstkurs von Palatin war mal über 102 $. Das zeigt wie hoch mal die Erwartungen waren.
Die jetzige Zurückhaltung erkläre ich mir damit, das sich an dem Teil einige mächtig die Finger
verbrannt haben.
Dumme Frage zwischendurch: dachte immer, Vyleesi ‚wirkt’ nur bei Frauen?
Antwort auf Beitrag Nr.: 60.121.006 von Stoxtrayder am 16.03.19 21:10:27Auf you tube schildert ein Kanadier die Wirkung von Bremelanotide die er sich eingepfiffen hat.
( unter anderem ein Dauerständer über merere Tage vermutlich nach einer Überdosierung )
Also Vyleesi wirkt bei Frauen und Männern. Ob es auch bei Ganter wirkt weiß ich nicht.
( unter anderem ein Dauerständer über merere Tage vermutlich nach einer Überdosierung )
Also Vyleesi wirkt bei Frauen und Männern. Ob es auch bei Ganter wirkt weiß ich nicht.
Antwort auf Beitrag Nr.: 60.121.201 von apano am 16.03.19 22:00:15
Wo kommen die 102$ her??
Zitat von apano: Auf you tube schildert ein Kanadier die Wirkung von Bremelanotide die er sich eingepfiffen hat.
( unter anderem ein Dauerständer über merere Tage vermutlich nach einer Überdosierung )
Also Vyleesi wirkt bei Frauen und Männern. Ob es auch bei Ganter wirkt weiß ich nicht.
Wo kommen die 102$ her??
Antwort auf Beitrag Nr.: 60.125.289 von Mammut22 am 17.03.19 21:19:03okay, 1,75$ habe ich unterschlagen.
Bei Comdirect steht exakt als Höchstkurs 103,75.
Bei Comdirect steht exakt als Höchstkurs 103,75.
Palatin Technologies, Inc. ("Palatin") gab heute bekannt, dass auf Antrag der Food and Drug Administration ("FDA") zusätzliche Daten zur Beurteilung des ambulanten 24-Stunden-Blutdrucks mit kurzfristiger täglicher Anwendung von Vyleesi® bei prämenopausalen gesunden Freiwilligen vorliegen wurde bei der FDA eingereicht. Der derzeitige Termin für das Medikament für verschreibungspflichtige Medikamentenkosten ("PDUFA") für den Abschluss der FDA-Überprüfung des Vyleesi New Drug Application ist der 23. Juni 2019.
https://www.sec.gov/Archives/edgar/data/911216/0001654954190…
https://www.sec.gov/Archives/edgar/data/911216/0001654954190…
Habe ich da was verpasst?
Weiß jemand wo der Ansteig herkommt?
Doch was gefunden:
https://www.sec.gov/Archives/edgar/data/911216/0001654954190…
Weiß jemand wo der Ansteig herkommt?
Doch was gefunden:
https://www.sec.gov/Archives/edgar/data/911216/0001654954190…
Palatin Technologies gibt positive Ergebnisse der klinischen Studie von PL-8177 zur Behandlung ...
Palatin Technologies gibt positive Ergebnisse der klinischen Studie von PL-8177 zur Behandlung von Colitis ulcerosa und anderen entzündlichen Darmerkrankungen bekannthttps://www.nasdaq.com/press-release/palatin-technologies-an…
"Studie traf alle primären und sekundären Endpunkte - PL-8177 ist ein Melanocortin-Rezeptor-1-Agonist
Cranbury, New Jersey, 4. April 2019 / PRNewswire / - Palatin Technologies, Inc. (NYSE American: PTN ), ein biopharmazeutisches Unternehmen, das zielgerichtete, rezeptorspezifische Peptidtherapeutika zur Behandlung von Krankheiten mit erheblichem ungedecktem medizinischen Bedarf und kommerziellem Potenzial entwickelt, gab heute positive Ergebnisse einer Mikrodosisstudie mit radioaktiv markiertem PL-8177 unter Verwendung einer oralen Polymerformulierung mit verzögerter Freisetzung bekannt. Die Studie erreichte alle primären und sekundären Endpunkte. PL-8177 ist ein patentierter Melanocortin-Rezeptor-1-Agonist mit potenzieller Anwendung bei der Behandlung von Colitis ulcerosa und anderen entzündlichen Darmerkrankungen."
Antwort auf Beitrag Nr.: 60.276.714 von chris.tian am 04.04.19 13:46:53Da bin ich mal neugierig wie der Kurs reagiert!
Gruß aaahhh
Gruß aaahhh
Antwort auf Beitrag Nr.: 60.276.786 von aaahhh am 04.04.19 13:52:56
Jetzt geht's auf die Zielgrade Richtung FDA Zulassung. Kurs heut tlw bei 1,15$! Geht wohl Richtung 3 $ bei Zulassung von vyleesi
FDA Zulassung nur Formsache, Daten eingereicht!
Palatin geht nun ab.. 
Jetzt geht's auf die Zielgrade Richtung FDA Zulassung. Kurs heut tlw bei 1,15$! Geht wohl Richtung 3 $ bei Zulassung von vyleesi
Ich lasse Palatin ewig liegen Auch nach der Zulassung von Vyleesi. Dann wird erst mal Geld verdient und die Partner kommen
------dem schließe ich mich im vollem umfang an-----
Meine Meinung ist auch liegen lassen über längere Sicht
Läuft hier. Top Aktie
...für mich geht es nur noch darum , ob man bis zum 23. 06. 19 die 2,- dollar-marke erreichen , oder sogar überschreiten sollte . ich kenne das von anderen bio-tech-schmieden die kurz vor der zulassung standen , dass sich der kurs in erheblicher weise in positiver hinsicht entwickeln sollte .
Was ist denn heute mit dem Kurs los? Ich habe überall nach Nachrichten gesucht aber nichts finden können. Das Volumen ist dreimal höher als normalerweise und der Kurs legt zweistellig zu.
Antwort auf Beitrag Nr.: 60.326.317 von Be_eR am 10.04.19 21:16:56
D.h. jeden Moment mit Zulassung zu rechnen
FDA Zulassung
Bloodpressure Daten aus Phase 1 an FDA vor 1 Woche durch AMAG eingereicht.D.h. jeden Moment mit Zulassung zu rechnen

Antwort auf Beitrag Nr.: 60.326.917 von Foerderung_ am 10.04.19 22:29:11
Quelle?!? Das ist glaube ich Quatsch was du erzählst, denn der FDA Termin ist am 23.06
Zitat von Foerderung_: Bloodpressure Daten aus Phase 1 an FDA vor 1 Woche durch AMAG eingereicht.
D.h. jeden Moment mit Zulassung zu rechnen
Quelle?!? Das ist glaube ich Quatsch was du erzählst, denn der FDA Termin ist am 23.06
Antwort auf Beitrag Nr.: 60.326.917 von Foerderung_ am 10.04.19 22:29:11Ja, aber das war vor einer Woche. Das ist doch in Börsenzeiten gesehen Urschnee...!?
Vor Zulassung findet erst noch ein Adcom-Meeting statt und das muss erst noch terminiert werden.
Antwort auf Beitrag Nr.: 60.326.944 von Mammut22 am 10.04.19 22:32:02Häh? Das ist kein Quatsch sondern der 1:1 Wortlaut vom CFO von AMAG. Kannst ja gern den Webcast nochmal anhören, siehe AMAG website. Der CFO hat im Rahmen der Needham Konferenz berichtet, dass AMAG vor einer Woche die BP Data an die FDA übermittelt hat.
Zur Info: 23.06 ist ne Deadline für die Einreichung gewesen. FDA approval kann nun eher kommen.
Zur Info: 23.06 ist ne Deadline für die Einreichung gewesen. FDA approval kann nun eher kommen.
Du hast schon recht, mit dem was AMAG publiziert hat, doch Spana hat in einer Telefonkonferenz vor einigen Quartalen bereits gesagt, dass auf jeden Fall ein Adcom-Meeting stattfindet. Ohne das Meeting auch kein PUF-Date. Adcom-Meeting wird von FDA auf Agenda gesetzt und bisher ist im Terminkalender der FDA noch keines terminiert. Die Terminierung wird der nächste Schritt zur Zulassung sein.
PDUFA nicht PUF
Antwort auf Beitrag Nr.: 60.328.240 von Urbi am 11.04.19 08:35:32Einberufung ADCOM war noch nicht safe oder?
https://www.google.com/amp/s/www.fool.com/amp/knowledge-cent…
https://www.google.com/amp/s/www.fool.com/amp/knowledge-cent…
Antwort auf Beitrag Nr.: 60.328.555 von Foerderung_ am 11.04.19 08:59:24Hier das Zitat von Carl im Feb 19
Carl Spana
What I can tell you is there was an Adcom scheduled for January 15 that obviously did not occur and I think based on -- I think if we get a study done in a timely fashion, which we will and submit it to the agency with sufficient time for review, I think if there's no -- if it's a clean study, which I anticipate it will be. I don't think that there will be -- I don't personally think there will be need for an Adcom and they certainly would not be time from when we would submit it to the June 23 date. So I'll leave it at that.
Carl Spana
What I can tell you is there was an Adcom scheduled for January 15 that obviously did not occur and I think based on -- I think if we get a study done in a timely fashion, which we will and submit it to the agency with sufficient time for review, I think if there's no -- if it's a clean study, which I anticipate it will be. I don't think that there will be -- I don't personally think there will be need for an Adcom and they certainly would not be time from when we would submit it to the June 23 date. So I'll leave it at that.
Geduld zahlt sich aus 
Nun kommt hier Bewegung rein!
Bin gespannt auf die Zulassung und wie sich der Kurs verhält...

Nun kommt hier Bewegung rein!
Bin gespannt auf die Zulassung und wie sich der Kurs verhält...
Warum steigt AMAG nicht, wo doch PTN Vyleesi an AMAG lizenziert hat?
Antwort auf Beitrag Nr.: 60.338.335 von Ulfred am 12.04.19 09:03:25
Letzter Anstieg wegen einer Erfolgsmeldung zu einem anderen Produkt in der Pipeline
"The results of this study support moving forward with development of polymer-bound PL-8177 to deliver drug to the lower gastrointestinal tract to treat ulcerative colitis and other inflammatory bowel diseases," said Dr. Carl Spana, President and Chief Executive Officer of Palatin Technologies. "Importantly, this study demonstrates that our oral, delayed-release polymer formulation of PL-8177 can deliver peptide to the diseased region of the bowel, without systemic uptake. The melanocortin receptor 1 is a novel target for treating ulcerative colitis and other inflammatory diseases, as it is present on the interior wall, or lumen, of the colon and lower gastrointestinal tract."
Ok. Also steigt der Kurs nicht wegen der erwarteten Vyleesi-Zulassung?
Antwort auf Beitrag Nr.: 60.341.662 von Ulfred am 12.04.19 14:33:56
Das geht Hand in Hand
Sowohl als auch. Eine Wette auf Vyleesi mit einem weiteren erfolgsversprechenden Produkt in der Pipeline dürfte weniger riskant sein.
AMAG muss Palatin schließlich erst mal 80 Millionen überweisen und hat erst mal noch nichts rein bekommen. Wieso sollen die steigen??
Hallo, was geht los darein?
Über 10% Minus in den letzten Tagen??
Habe ich was verpaßt???

Über 10% Minus in den letzten Tagen??
Habe ich was verpaßt???

Habe aufgestockt heute zu 0,942
Warum aufgestockt? Weil es gerade mal wieder in den Keller Geht??
Hatte einen Teilgewinn bei 1,05 realisiert. Jetzt wieder aufgestockt.
OK, dann hoffen wir das es bald wieder über die 1 Euro geht!
Aber bei dem regen Interesse hier im Chat .....
Aber bei dem regen Interesse hier im Chat .....
scheinen die meisten ja schon abgesprungen zu sein
scheinen die meisten ja schon abgesprungen zu sein

Die meisten springen maximal eine Woche vor dem 23.6. auf bzw. vor dem Adcom-Meeting falls noch eins angesetzt wird. Bei Trevena war es ähnlich.
Auf oder ab?
Nach meiner Meinung auf. Ich erwarte einen Anstieg auf mindestens 1,50$. Vor einem Jahr nach Abgabe der NDA waren einige Tage mit 5-10 Millionen Aktienumsatz zu Kursen zwischen 1,35-1,50$. Diese Masse wird vor der FDA-Entscheidung nicht mit Verlust raus gehen wollen. Die Frage ist, ob der Widerstand von 1,50$ vor der Zulassung bereits geknackt wird oder erst nach Zulassung. Nach Zulassung dürfte zeitnah der EU-Deal bekannt gegeben werden, müsste ja im Vergleich zum AMAG-Deal auch ne Upfront-Zahlung zwischen 50-100 Mio $ einbringen. Die Kasse von Palatin wird bei einer Zulassung sehr gut gefüllt sein.
Ich kann nur jedem empfehlen das aktuell Earnings Call Transcript vom 12.02.19 durchzulesen bzw. den Webcast anzuhören. Hier stehen wirklich viele interessante Infos drin. Unter anderem, dass Carl Spana davon ausgeht, dass kein Adcom-Meeting stattfinden wird.
https://seekingalpha.com/article/4240256-palatin-technologie…
https://seekingalpha.com/article/4240256-palatin-technologie…
Dann geht es ja hoffentlich nochmal in die richtige Richtung 

Und wer zu Ostern nicht die richtigen Eier gefunden hat, kann sich mit
Palatin noch ein paar (hoffentlich ) goldene ins Nest (Depot) legen
Palatin noch ein paar (hoffentlich ) goldene ins Nest (Depot) legen

Ich bin jedenfalls schon dabei 

......kurs zieht , wie erwartet vor so einer bedeuteten entscheidung , leicht an .....stepp by stepp ......kontinuierlich tag für tag und das bis hin zu dem wichtigsten tage der palatin-story . heute in nur noch 2 MONATEN ist es schon soweit . good luck allen invetierten und für alle die es noch werden sollten....!!!!!
Antwort auf Beitrag Nr.: 60.405.870 von herthafan am 23.04.19 18:01:21hallo hertha 😉 die geduld zahlt sich aus 👍. auf weiterhin grüne kurse.
>10% .... zieht leicht an!?
Dann bin ich aber mal gespannt was da noch kommt
Dann bin ich aber mal gespannt was da noch kommt

Antwort auf Beitrag Nr.: 60.405.975 von walle1fc am 23.04.19 18:14:34Eben, einfach nur etwas Geduld. Ich denke hier werden bis zur Zulassungsentscheidung noch ganz andere Kurse kommen
Wollte eigentlich bei 93 Cent aufstocken 

Antwort auf Beitrag Nr.: 60.406.005 von Mammut22 am 23.04.19 18:18:18
....müsste eigentlich auch mit absoluter sicherheit so erfolgen.......siehe andere div. beispiele dafür von deitschen bzw. us/canadischen bio-tech-schmieden in ähnlichen situationen d.h. wenige tagen / wochen vor endgültigem entscheid der FDA......!!!!!!
Zitat von Mammut22: Eben, einfach nur etwas Geduld. Ich denke hier werden bis zur Zulassungsentscheidung noch ganz andere Kurse kommen
....müsste eigentlich auch mit absoluter sicherheit so erfolgen.......siehe andere div. beispiele dafür von deitschen bzw. us/canadischen bio-tech-schmieden in ähnlichen situationen d.h. wenige tagen / wochen vor endgültigem entscheid der FDA......!!!!!!
Antwort auf Beitrag Nr.: 60.407.457 von herthafan am 23.04.19 21:03:08Ja, bestes Beispiel war für mich Trevena, habe da auch gutes Geld verdient
Antwort auf Beitrag Nr.: 60.407.868 von Mammut22 am 23.04.19 21:42:57...ja und genau darauf ( trevena ) hatte ich grade gewartet......trev. wurde beim 1 . zulassungstermin der FDA sang und klanglos abgewiesen und ein neuer termin liegt in weiter ferne. warum , so frage ich mich , liegt der kurs von trev . bei ca. 1,40 euro und unsere palatin mit kurzziel vor augen ( 23.06.19 ) bei gut einem euro ??? da besteht wohl hoffentlich noch eine riesen menge shares als dringendes nachkauf-signal bereit....!!!!
Sehr schön, hier geht bald die Post ab
Antwort auf Beitrag Nr.: 60.451.175 von Mammut22 am 29.04.19 20:31:31
Starker Tagesverlauf
Der Kursverlauf ist zum genießen. Wäre schön wenn sich das morgen fortsetzt und die Shorts die Hose voll bekommen.
Antwort auf Beitrag Nr.: 60.451.634 von HugoHuskarl am 29.04.19 21:20:37Wie ist eure Kurseinschätzung bei Zulassung? So ungefähr..
Antwort auf Beitrag Nr.: 60.451.667 von Greenlock am 29.04.19 21:24:16Ich rechne mit 5€
Antwort auf Beitrag Nr.: 60.451.667 von Greenlock am 29.04.19 21:24:16Ich finde solche Schätzungen eher unseriös. In amerikanischen Foren geistert häufig die 5 USD umher.
Woher so eine Zahl kommt weiß am Ende keiner aber sie wird weitergetragen (jetzt von mir auch .
.
Seriöse Argumente für einen Kurs der einiges höher liegt als der aktuelle:
- Meilensteinzahlungen
- Profit durch Vermarktung
- Weitere Medikamente in der Pipeline für dessen Entwicklung man jetzt eine Cashcow hat.
Das stimmt mich positiv.
Woher so eine Zahl kommt weiß am Ende keiner aber sie wird weitergetragen (jetzt von mir auch
 .
.Seriöse Argumente für einen Kurs der einiges höher liegt als der aktuelle:
- Meilensteinzahlungen
- Profit durch Vermarktung
- Weitere Medikamente in der Pipeline für dessen Entwicklung man jetzt eine Cashcow hat.
Das stimmt mich positiv.
Antwort auf Beitrag Nr.: 60.451.721 von HugoHuskarl am 29.04.19 21:29:27Ok danke mal für eure Einschätzung lassen wir uns Überraschen..
Heute über 1.5 Mio Stück an der NYSE. Der Zug nimmt langsam Fahrt auf.
Antwort auf Beitrag Nr.: 60.451.676 von Mammut22 am 29.04.19 21:25:41
Palatins Konkurrenzprodukt Addyi wurde für eine Milliarde US Dollar aufgekauft, ist aber viel schlechter.
Wenn man den Wert von Vyleesi auch mit einer Milliarde ansetzt, dann kommt man etwa auf 5 $.
Die anderen Medis sind da noch nicht mit drin.
Ich rechne mit 1,5 - 1,6 Euro bei Zulassung. (die Zulassung ist schon eingepreist) Danach geht es wieder runter. Im Herbst kommt der Lizensvertrag mit einer Firma für Europa mit üppigen Zahlungen.
Dann geht es über 2 Euro. Und richtig ab geht es wenn erste Zahlen von AMAG kommen und
sich das Medi als Erfolg abzeichnet. Dann geht es 2020 über 5 $ und wenn die anderen Medis
von Palatin zum Tragen kommen geht es weiter steil noch oben.
Palatins Konkurrenzprodukt Addyi wurde für eine Milliarde US Dollar aufgekauft, ist aber viel schlechter.
Wenn man den Wert von Vyleesi auch mit einer Milliarde ansetzt, dann kommt man etwa auf 5 $.
Die anderen Medis sind da noch nicht mit drin.
Ich rechne mit 1,5 - 1,6 Euro bei Zulassung. (die Zulassung ist schon eingepreist) Danach geht es wieder runter. Im Herbst kommt der Lizensvertrag mit einer Firma für Europa mit üppigen Zahlungen.
Dann geht es über 2 Euro. Und richtig ab geht es wenn erste Zahlen von AMAG kommen und
sich das Medi als Erfolg abzeichnet. Dann geht es 2020 über 5 $ und wenn die anderen Medis
von Palatin zum Tragen kommen geht es weiter steil noch oben.
Sorry da rechne ich schon mit etwas mehr. Falls die Zulassung wirklich kommt. Könnte mir auch vorstellen das dann relativ schnell Partner gefunden werden
Antwort auf Beitrag Nr.: 60.452.240 von apano am 29.04.19 22:34:45
Top Ausführung von Dir, so ungefähr sehe ich das auch. Allerdings denke ich, dass schon vor PFUDA Entscheidung ähnlich zu Trevena sehr viel gezockt wird und der Kurs ganz schnell auf 2-3$ steigen kann und dann wieder zurück und dann wieder hoch. Es wird denke ich hin und her gehen. Allerdings hoffe ich dass der Ausgang hier besser sein wird als bei Trevena (8 zu 7 Stimmen wurde das Medikament nicht empfohlen)
Zitat von apano: Palatins Konkurrenzprodukt Addyi wurde für eine Milliarde US Dollar aufgekauft, ist aber viel schlechter.
Wenn man den Wert von Vyleesi auch mit einer Milliarde ansetzt, dann kommt man etwa auf 5 $.
Die anderen Medis sind da noch nicht mit drin.
Ich rechne mit 1,5 - 1,6 Euro bei Zulassung. (die Zulassung ist schon eingepreist) Danach geht es wieder runter. Im Herbst kommt der Lizensvertrag mit einer Firma für Europa mit üppigen Zahlungen.
Dann geht es über 2 Euro. Und richtig ab geht es wenn erste Zahlen von AMAG kommen und
sich das Medi als Erfolg abzeichnet. Dann geht es 2020 über 5 $ und wenn die anderen Medis
von Palatin zum Tragen kommen geht es weiter steil noch oben.
Top Ausführung von Dir, so ungefähr sehe ich das auch. Allerdings denke ich, dass schon vor PFUDA Entscheidung ähnlich zu Trevena sehr viel gezockt wird und der Kurs ganz schnell auf 2-3$ steigen kann und dann wieder zurück und dann wieder hoch. Es wird denke ich hin und her gehen. Allerdings hoffe ich dass der Ausgang hier besser sein wird als bei Trevena (8 zu 7 Stimmen wurde das Medikament nicht empfohlen)
....ich persönlich schätze die rechnung von apano auch eher als sehr zurückhaltend ein , vielleicht besser so als umgekehrt . meine meinung ist eher so , als das sich der kurs -----kurz vor der zulassung----- auf knapp unter 2,-dollar einpendeln sollte.....!!!!
Antwort auf Beitrag Nr.: 60.452.240 von apano am 29.04.19 22:34:45Gute Einschätzung, Danke!
Kurs zieht heute an, weiter so!
Kurs zieht heute an, weiter so!
Nochmal nachgekauft. Allen viel Erfolg
AMAG hat eine neue Seite für Vyleesi erstellt:
https://www.unblush.com/
https://www.unblush.com/
Und so präsentiert sich AMAG auf der Messe
https://twitter.com/AMAGPharma/status/1124342967655968773
https://twitter.com/AMAGPharma/status/1124342967655968773
Antwort auf Beitrag Nr.: 60.483.671 von Dumounde am 03.05.19 21:37:49sehr schön, wie der Kurs hier anzieht.
Wie wahrscheinlich haltet ihr die Zulassung?
Wie wahrscheinlich haltet ihr die Zulassung?
Geringes Handelsvolumen
Antwort auf Beitrag Nr.: 60.507.123 von PrinzStorno am 07.05.19 16:47:19 )))
)))
Geht nun Richtung 1,30-1,50 zum ER Release
Potential für 1,80€ bis approval  )))
)))
Seltsamerweise steigt PTN um knapp 10% und AMAG fällt um 10%. Kann mir das jemand erklären?
AMAG muss Palatin bei Zulassung 60 Millionen überweisen
Der Markt ist anders als hier heute ein Schlachtfeld. Muss keine Bedeutung haben mit AMAG
Hier werden heute noch gewinne mitgenommen, aber dieses Jahr wird der Kurs mit Sicherheit an die 2 € gehen meiner Meinung nach
Conference call transcript from $AMAG earnings seekingalpha.com/article/42...
Das hört sich sehr gut an. Zwei Sachen finde ich besonders gut, 1. die Zuversicht bei der Zulassung,
und 2. das AMAG bei den Erwartungen eher tief stapelt und die Erwartung übertreffen will.
Das hört sich sehr gut an. Zwei Sachen finde ich besonders gut, 1. die Zuversicht bei der Zulassung,
und 2. das AMAG bei den Erwartungen eher tief stapelt und die Erwartung übertreffen will.
Der einzige Lichtblick  heute in meinem Depot
heute in meinem Depot 
 heute in meinem Depot
heute in meinem Depot 
Palatin mein Trostpflaster 

Antwort auf Beitrag Nr.: 60.510.951 von mafei am 07.05.19 22:27:54
aber was für ein Trostpflaster!
Wenn erstmal die Zulassung kommt...
hier werden wir die kommenden Wochen noch sehr viel freude haben
Zitat von mafei: Palatin mein Trostpflaster
aber was für ein Trostpflaster!

Wenn erstmal die Zulassung kommt...
hier werden wir die kommenden Wochen noch sehr viel freude haben

Jaaaa, zumal der Countdown läuft 

....ich schrieb bereits , bis zum 23.06. sehen wir mit sicherheit die knapp 2,-euro-marke und bei zulassung fast selbverständlich in richtung 3,-euro aufwärtsstrebend.
Wie genau profitiert PTN eigentlich von der Zulassung? Sie haben es doch an AMAG lizenziert.
Hier gibt es im Moment nur eine Richtung 

Der Handel zieht die letzten Tage deutlich an
.....das müsste eigentlich vor einem zulassungstermin einer bio-tech-schmiede ganz klare sache sein .ich hoffe doch , wir sehen anfang juni 19 noch knapp die 2,-euro-marke , kurz vor dem termin eventuell sogar darüber und bei einer zulassung so ca. richtung 3,- euro.....aber n m M.
Ich sehe hier kurzfristig schon die 2 EUR. Das warten hat sich gelohnt!
Deutlich über 1 Millionen Stücke wurden heute gehandelt
Antwort auf Beitrag Nr.: 60.520.281 von PrinzStorno am 08.05.19 20:12:10Heute kommen die Zahlen.
Und obwohl die Zahlen des letzten Quartals hier völlig wurscht sind, weil andere Themen die Richtung bestimmen müssten, werden wir 10% korrigieren, wie immer...
Und obwohl die Zahlen des letzten Quartals hier völlig wurscht sind, weil andere Themen die Richtung bestimmen müssten, werden wir 10% korrigieren, wie immer...
Geht hier aber die letzten Tage immer schon munter rauf-runter-rauf,
da scheinen einige stoploss abzufischen
da scheinen einige stoploss abzufischen

Aber so lange die Richtung stimmt 

Wo hier die Stopplose wieder gesetzt werden 

...also eigentlich unverständlich und völlig befremdend so kurz vor dem zulassungstermin am 23.06. mit hohen erwartungen (wie immer in der bio-tech-branche) billig zu verkaufen . zumindestens wäre noch zeit zur genüge vorhanden bis kurz vor dem termin , ganz zu schweigen nach einem positivem bescheid der FDA......
Hab nochmal nachgekauft. Bin hier die Ruhe selbst.
Palatin Technologies, Inc. Reports Third Quarter Fiscal Year 2019 Results
https://seekingalpha.com/pr/17506166-palatin-technologies-in…
https://seekingalpha.com/pr/17506166-palatin-technologies-in…
Antwort auf Beitrag Nr.: 60.526.452 von boersenkeks am 09.05.19 13:58:39Nachtrag: Zahlen entsprechen den Erwartungen der Analysten.
EPS of -$0.03
EPS of -$0.03
dreht nach US Eröffnung schon wieder ins Plus....
Gutes Zeichen!!!
Hier ist Druck auf dem Kessel!!!
Gutes Zeichen!!!
Hier ist Druck auf dem Kessel!!!
Weiter gehts nach oben 

Über Amex ist gerade mehr Handel als über Tradegate 

Der kommt dann morgen 😊
nächste Woche 2 Euro
Das geht so wie es aussieht auch schneller nach oben als wir alle denken 😉
aus einem Nachbarforum
traumzone: gelesen und übersetzt...
08.05.19 00:57
#7936
Quelle: seekingalpha.com/article/...nings-call-transcript?part=single
From an alignment perspective, so yeah, so we have a combined sales force now roughly of 125. They're getting after it with OB-GYN, they've been cross trained. And we've got a very strong leadership team that oversees that team. And we're gearing up for a Vyleesi launch that everyone's really, really excited about.
Aus Sicht der Ausrichtung, also ja, so dass wir jetzt über einen gemeinsamen Außendienst von rund 125 Mitarbeitern verfügen. Sie sind mit OB-GYN hinterher, sie sind crosstrainiert. Und wir haben ein sehr starkes Führungsteam, das dieses Team leitet. Und wir bereiten uns auf einen Vyleesi-Launch vor, von dem alle wirklich, wirklich begeistert sind.
ACHTUNG Tony Casciano unterstreicht das Produnkt mit "von dem alle wirklich, wirklich begeister sind" - also wenn das nix wird, dann weis ich auch nicht....
traumzone: gelesen und übersetzt...
08.05.19 00:57
#7936
Quelle: seekingalpha.com/article/...nings-call-transcript?part=single
From an alignment perspective, so yeah, so we have a combined sales force now roughly of 125. They're getting after it with OB-GYN, they've been cross trained. And we've got a very strong leadership team that oversees that team. And we're gearing up for a Vyleesi launch that everyone's really, really excited about.
Aus Sicht der Ausrichtung, also ja, so dass wir jetzt über einen gemeinsamen Außendienst von rund 125 Mitarbeitern verfügen. Sie sind mit OB-GYN hinterher, sie sind crosstrainiert. Und wir haben ein sehr starkes Führungsteam, das dieses Team leitet. Und wir bereiten uns auf einen Vyleesi-Launch vor, von dem alle wirklich, wirklich begeistert sind.
ACHTUNG Tony Casciano unterstreicht das Produnkt mit "von dem alle wirklich, wirklich begeister sind" - also wenn das nix wird, dann weis ich auch nicht....
Jetzt hat sich aber jemand eingedeckt
Heute wie die letzten Tage auch schon um 1 Mio Stücke gehandelt. Hier will jetzt niemand zuspät rein 

......keine bange liselotte , datt wird noch mehr , viel mehr sogar.......trevena ging bis kurz vor dem ziel auf knapp 3,- euro hoch.....muss nicht , aber kann....!!!!
Finde unsere Perle trotz starker Frequenz heute hier im Forum
gar nicht in der Liste der meistgelesenen Hotstocks
gar nicht in der Liste der meistgelesenen Hotstocks

Sorry, doch gefunden. Bei meistdiskutierte, komischerweise aber
nur bei ALLE (nicht bei > 1 € !? ) 🤔
nur bei ALLE (nicht bei > 1 € !? ) 🤔
Habe ich gestern auch schon mal nach geschaut aber das wird sich auch ändern wenn das hier so weiter geht.
Ich bin ja mal sehr froh, bei 35ct zum Zuge gekommen zu sein...das Ding läuft und läuft ... nach all den Aussagen der heutigen HV dürfte es jetzt richtig los gehen ... Meilensteinzahlungen von 60, 7.5 und 2.5Mio sind erst der Anfang.. in n paar Jahren lacht man über 1.40US$
Antwort auf Beitrag Nr.: 60.532.452 von burgkauz am 10.05.19 02:07:55
Was waren das noch für schöne Zeiten Da war sogar SD noch hier aktiv
Da war sogar SD noch hier aktiv
Zitat von burgkauz: Ich bin ja mal sehr froh, bei 35ct zum Zuge gekommen zu sein...das Ding läuft und läuft ... nach all den Aussagen der heutigen HV dürfte es jetzt richtig los gehen ... Meilensteinzahlungen von 60, 7.5 und 2.5Mio sind erst der Anfang.. in n paar Jahren lacht man über 1.40US$
Was waren das noch für schöne Zeiten
 Da war sogar SD noch hier aktiv
Da war sogar SD noch hier aktiv Kursziel erhöht nach Conference Call - von 5 auf 6$
Palatin price target raised to $6 from $5 at H.C. Wainwright H.C. Wainwright analyst Joseph Pantginis raised his price target for Palatin Technologies to $6 from $5 saying the potential Vyleesi label continues to look "attractive and broad reaching." The analyst believes the company provides a "derisked opportunity for investors" and keeps a Buy rating on the shareshttps://thefly.com/landingPageNews.php?id=2907098
Ja, dann mal LOS 🤑
Antwort auf Beitrag Nr.: 60.532.452 von burgkauz am 10.05.19 02:07:55
Bin seit 0,6€ dabei. Im Nachhinein mit zu wenigen Tausend Stücken. Aber später ist man immer schlauer
Zitat von burgkauz: Ich bin ja mal sehr froh, bei 35ct zum Zuge gekommen zu sein...das Ding läuft und läuft ... nach all den Aussagen der heutigen HV dürfte es jetzt richtig los gehen ... Meilensteinzahlungen von 60, 7.5 und 2.5Mio sind erst der Anfang.. in n paar Jahren lacht man über 1.40US$
Bin seit 0,6€ dabei. Im Nachhinein mit zu wenigen Tausend Stücken. Aber später ist man immer schlauer
Das sind aber schon ordentliche Renditen 

Bin auch bei 35 Cent rein. Immer wieder nachgekauft. Schnitt 50 Cent. 90.000 Stück. Sieht gut aus Lasse es aber noch lange liegen
45.000€ in einen Pennystock investiert, ich hoffe dein Mut wird belohnt.
Die Story hat mich fasziniert. Hatte eigentlich 100.000. Hab dann aber gemeint ich müsste für 10.000 einen Palatin Optionsschein kaufen. Ging dann aber als er unter 60 Cent fiel in die Hose. Na ja muss man auch sagen
Trotzdem...... Daumen hoch !!!
Antwort auf Beitrag Nr.: 60.544.710 von Reinerle am 11.05.19 14:35:21
Respekt, nicht jeder schreibt gern über seine Verluste. Drücke dir und uns die Daumen
Zitat von Reinerle: Die Story hat mich fasziniert. Hatte eigentlich 100.000. Hab dann aber gemeint ich müsste für 10.000 einen Palatin Optionsschein kaufen. Ging dann aber als er unter 60 Cent fiel in die Hose. Na ja muss man auch sagen
Respekt, nicht jeder schreibt gern über seine Verluste. Drücke dir und uns die Daumen
Weiter geht's Richtung 1,40
Antwort auf Beitrag Nr.: 60.552.585 von PrinzStorno am 13.05.19 10:53:47
.....aber nur als kurzen zwischenstopp zu bezeichnen . vor dem 23.06.19 sehen wir eventuell noch die 2,- euro , um nach einem positivem bescheid der FDA weiter zu schreiten richtung 5,-/6,- $ (siehe analysten-kursziel ).....aber n m M.
Zitat von PrinzStorno: Weiter geht's Richtung 1,40
.....aber nur als kurzen zwischenstopp zu bezeichnen . vor dem 23.06.19 sehen wir eventuell noch die 2,- euro , um nach einem positivem bescheid der FDA weiter zu schreiten richtung 5,-/6,- $ (siehe analysten-kursziel ).....aber n m M.
Da ist SD direkt zurück 

Jeden Tag ein Stück höher :-) Egal was der Gesamtmarkt macht.
Da ärgert man sich schon das man seine Posi nicht früher verdoppelt hat.
Aber immer noch besser als gar nicht dabei zusein:-)
WB
Da ärgert man sich schon das man seine Posi nicht früher verdoppelt hat.
Aber immer noch besser als gar nicht dabei zusein:-)
WB
richtig. bin erst seit 1,13€ dabei. aber besser kleiner gewinn als verlust
Bin sehr gespannt wie der Kurs sich jetzt weiterentwickelt. Die Aufmerksamkeit steigt nun durch SD erheblich.
Anders als SD, sehe ich bei Palatin ein besseres Chancen/Risiko-Profiel als bei seiner "Aktie des Jahres".
Zwar kann der Kurs stärker steigen aber das Risiko zu floppen ist auch viel größer.
Yyleesi wird ein absoluter Bestseller und Palatin wird davon profitieren. Weitere 100% sind
nicht unrealistisch.
Zwar kann der Kurs stärker steigen aber das Risiko zu floppen ist auch viel größer.
Yyleesi wird ein absoluter Bestseller und Palatin wird davon profitieren. Weitere 100% sind
nicht unrealistisch.
Feierabend auf Allzeithoch
Allzeithoch?! 🧐 in der 1-Jahres-Chart-Ansicht vielleicht...
Leute, mal bisserl auf’m Teppich bleiben, ok?! 😉
Die Kurse werden (zum Glück immernoch) in den USA gemacht, da kann SD pushen wie sie wollen, wird den Kurs nicht beeinflussen. ☝️
Zudem ist die Zulassung für viele (hier) wohl nur noch reine Formsache...ich hab schon Pferde kotzen sehen im Bezug auf Zulassungen bei der FDA. Und wenn die Zulassung kommt, wird der Kurs sicherlich nicht von heute auf morgen auf 5 oder 6$ steigen...dann wäre die Marktkapitalisierung bei über 600 Mio. $ ohne daß das Produkt jemals verkauft wurde (auch wenn natürlich erstmal ‘ne schöne Summe an Meilensteinzahlungen fließt).
Leute, mal bisserl auf’m Teppich bleiben, ok?! 😉
Die Kurse werden (zum Glück immernoch) in den USA gemacht, da kann SD pushen wie sie wollen, wird den Kurs nicht beeinflussen. ☝️
Zudem ist die Zulassung für viele (hier) wohl nur noch reine Formsache...ich hab schon Pferde kotzen sehen im Bezug auf Zulassungen bei der FDA. Und wenn die Zulassung kommt, wird der Kurs sicherlich nicht von heute auf morgen auf 5 oder 6$ steigen...dann wäre die Marktkapitalisierung bei über 600 Mio. $ ohne daß das Produkt jemals verkauft wurde (auch wenn natürlich erstmal ‘ne schöne Summe an Meilensteinzahlungen fließt).
Kleine Korrektur meinerseits: bei 5-6$ wäre die Marktkapitalisierung 1 Milliarde $
Daher erstmal Utopie... 😉
Daher erstmal Utopie... 😉
Antwort auf Beitrag Nr.: 60.559.404 von Stoxtrayder am 13.05.19 22:42:00
Wer hier länger dabei ist weiß das es hier um das letzte Jahr geht
Zitat von Stoxtrayder: Allzeithoch?! 🧐 in der 1-Jahres-Chart-Ansicht vielleicht...
Leute, mal bisserl auf’m Teppich bleiben, ok?! 😉
Die Kurse werden (zum Glück immernoch) in den USA gemacht, da kann SD pushen wie sie wollen, wird den Kurs nicht beeinflussen. ☝️
Zudem ist die Zulassung für viele (hier) wohl nur noch reine Formsache...ich hab schon Pferde kotzen sehen im Bezug auf Zulassungen bei der FDA. Und wenn die Zulassung kommt, wird der Kurs sicherlich nicht von heute auf morgen auf 5 oder 6$ steigen...dann wäre die Marktkapitalisierung bei über 600 Mio. $ ohne daß das Produkt jemals verkauft wurde (auch wenn natürlich erstmal ‘ne schöne Summe an Meilensteinzahlungen fließt).
Wer hier länger dabei ist weiß das es hier um das letzte Jahr geht

Stoxy, ich sehe auch in den letzten 3 Jahren keinen höheren US Schlußkurs als heute
Also im 10-Jahres-Chart sehe ich Höchstkurse von 4 Euro, ihr nicht?! 🧐
Gabz zu schweigen vom historischen Chart...😉
Gabz zu schweigen vom historischen Chart...😉
Antwort auf Beitrag Nr.: 60.559.404 von Stoxtrayder am 13.05.19 22:42:00Besonders die " Zulassungen" die im Vorfeld schon als durch gewunken angesehen werden, gehen meist in die Hose. Nach meiner Erfahrung gehen 4 von 5" sicheren" Zulassungen schief, zumindest werden dann weitere Auflagen fällig oder die Termine nach hinten verschoben. Mal abwarten, bin hier schon sehr lange dabei, aber vor dem Termin geht die Hälft raus, schon zu oft alles oder nichts gespielt und meist das Nachsehen dabei gehabt. Es gibt keine sicheren Sachen an der Börse!!! Muss aber jeder selber wissen.
Gruß aaahhh
Gruß aaahhh
ich sage1mal GUTEN Tag, Hier.
Soso, da hab ich wohl ein paar Fremdgänger entdeckt! Stoxy, Popeye, sofort wieder ins CUV Forum!
Naja, auch andere Mütter haben auch schöne Töchter 😋
....neben meinen Depotschwergewichten Clinuvel & Evotec, die ich bis ins Rentenalter halten werde.
Und da der Post nicht ganz off-topic sein soll: AMAG Pharma vertreibt ja Vyleesi, falls die Zulassung erfolgt. Da ist z.Zt. bewertungstechnisch nicht mehr viel Unterschied zw. Palatin & AMAG. Wenn man an den Erfolg von Vyleesi glaubt, könnte man sich doch fast ein paar AMAG-Anteile ins Depot legen?! Oder was meint ihr?
....neben meinen Depotschwergewichten Clinuvel & Evotec, die ich bis ins Rentenalter halten werde.
Und da der Post nicht ganz off-topic sein soll: AMAG Pharma vertreibt ja Vyleesi, falls die Zulassung erfolgt. Da ist z.Zt. bewertungstechnisch nicht mehr viel Unterschied zw. Palatin & AMAG. Wenn man an den Erfolg von Vyleesi glaubt, könnte man sich doch fast ein paar AMAG-Anteile ins Depot legen?! Oder was meint ihr?
Wir können hier echt nicht meckern
Ich bin so happy hiermit. Hat sich jetzt schon super gelohnt für viele hier. Ich drücke uns die Daumen 

Antwort auf Beitrag Nr.: 60.559.404 von Stoxtrayder am 13.05.19 22:42:00Wer oder was ist eigentlich SD? 🤔
Antwort auf Beitrag Nr.: 60.562.617 von petermull am 14.05.19 11:22:16
ich gehe nun wieder Essen,
nach HAUSE.
Zitat von petermull: Soso, da hab ich wohl ein paar Fremdgänger entdeckt! Stoxy, Popeye, sofort wieder ins CUV Forum!
ich gehe nun wieder Essen,
nach HAUSE.
Antwort auf Beitrag Nr.: 60.567.963 von Wilfried0110 am 14.05.19 19:28:56
www.sharedeals.de
Zitat von Wilfried0110: Wer oder was ist eigentlich SD? 🤔
www.sharedeals.de
Antwort auf Beitrag Nr.: 60.567.963 von Wilfried0110 am 14.05.19 19:28:56
Im PRINZIP kann man Diese Institution als Eine ART "Seedbank" bezeichnen.
Samenbank, also.
Zitat von Wilfried0110: Wer oder was ist eigentlich SD? 🤔
Im PRINZIP kann man Diese Institution als Eine ART "Seedbank" bezeichnen.
Samenbank, also.
Antwort auf Beitrag Nr.: 60.569.379 von Popeye82 am 14.05.19 21:43:59Bin zwar nicht neu hier, aber das habe ich noch nicht gehört 😂🙈
Dann wollen wir mal hoffen, dass es mit unserer Palatin so weiter geht... 👍🏼
Dann wollen wir mal hoffen, dass es mit unserer Palatin so weiter geht... 👍🏼
Antwort auf Beitrag Nr.: 60.569.415 von Wilfried0110 am 14.05.19 21:47:14"Seed" kommt nicht ganz hin.
Ist nochmal Was Anderes.
Aber im Prinzip Eine Art "EARLY MarktLIEBE anSCHIEBER".
GIVE it to Them, When They need the MOST.
Ist nochmal Was Anderes.
Aber im Prinzip Eine Art "EARLY MarktLIEBE anSCHIEBER".
GIVE it to Them, When They need the MOST.
Seit ul wil pop hier im Forum aufgetaucht sind, geht es mit dem Palatinkurs nach unten.
Geht doch ins Epi Forum. Da bekommt ihr eine genaue Anallyse auch was eure Rechtschreibung
und Englischkenntnisse angeht.
Geht doch ins Epi Forum. Da bekommt ihr eine genaue Anallyse auch was eure Rechtschreibung
und Englischkenntnisse angeht.
Bitte?! 😂
Antwort auf Beitrag Nr.: 60.570.060 von apano am 14.05.19 23:10:35Mein Markteinfluss (Heimatbörsen) ist, OFFENsichtlich, LEIDER zu gross.
Die verrückten sind auch wieder zurück 

1,5 Euro bis morgen abend !! Wer hält dagegen?
1,499  Weiter gehts!
Weiter gehts!
 Weiter gehts!
Weiter gehts!
Antwort auf Beitrag Nr.: 60.582.516 von Reinerle am 16.05.19 11:14:33
...ich jedenfalls nicht......vor ein paar wochen wurde ich noch ausgelacht mit meiner prognose , das der kurs kurz vor dem zulassungstermin kräftig anschub bekommen sollte . zum glück sollte ich recht behalten damit , denn ich kenne derartiges prozedere von anderen bio-tech-schmieden in ähnlichen situationen und wenn dann noch die FDA ihre zustimmung geben sollte , beginnt erst einmal der run aud die shares ganz stramm gen norden.....aber nur bei den o.g. abläufen....!!!
Zitat von Reinerle: 1,5 Euro bis morgen abend !! Wer hält dagegen?
...ich jedenfalls nicht......vor ein paar wochen wurde ich noch ausgelacht mit meiner prognose , das der kurs kurz vor dem zulassungstermin kräftig anschub bekommen sollte . zum glück sollte ich recht behalten damit , denn ich kenne derartiges prozedere von anderen bio-tech-schmieden in ähnlichen situationen und wenn dann noch die FDA ihre zustimmung geben sollte , beginnt erst einmal der run aud die shares ganz stramm gen norden.....aber nur bei den o.g. abläufen....!!!
.......im ariva forum schrieb soeben ein user.....nicht am 23.06.19 entscheidet die FDA über die zulassung , sondern bis zum 23.06. !!!!! ich denke mal , das er damit sogar recht behalten sollte....DANKE....also insgesamt sogar noch besser für uns , wenn es dann durchgewunken werden sollte......good luck.....
Grüße Freunde...der Zug rollt langsam, die 1,50 € sind schon mal angerissen.
Antwort auf Beitrag Nr.: 60.583.158 von herthafan am 16.05.19 12:41:19
Das haben wir hier vor einigen Monaten auch kurz besprochen. Der 23.06. ist als spätester Termin zu verstehen. Mit Sicherheit immer noch ein guter Zeitpunkt um einzusteigen. Habe heute morgen nochmal nachgekauft.
Zitat von herthafan: .......im ariva forum schrieb soeben ein user.....nicht am 23.06.19 entscheidet die FDA über die zulassung , sondern bis zum 23.06. !!!!! ich denke mal , das er damit sogar recht behalten sollte....DANKE....also insgesamt sogar noch besser für uns , wenn es dann durchgewunken werden sollte......good luck.....
Das haben wir hier vor einigen Monaten auch kurz besprochen. Der 23.06. ist als spätester Termin zu verstehen. Mit Sicherheit immer noch ein guter Zeitpunkt um einzusteigen. Habe heute morgen nochmal nachgekauft.
Antwort auf Beitrag Nr.: 60.584.743 von Nasgu am 16.05.19 16:36:43
🤑
Zitat von Nasgu: Grüße Freunde...der Zug rollt langsam, die 1,50 € sind schon mal angerissen.
🤑
nicht angerissen Hinter sich gelassen
Antwort auf Beitrag Nr.: 60.585.277 von Reinerle am 16.05.19 17:41:07
1,53 EUR Weiter geht's!
Weiter geht's!
Zitat von Reinerle: nicht angerissen Hinter sich gelassen
1,53 EUR
 Weiter geht's!
Weiter geht's!
Antwort auf Beitrag Nr.: 60.585.175 von PrinzStorno am 16.05.19 17:25:46So wie sich der Kurs verhält kommt da vor dem 23.6 was. Ansonsten ist bei den täglichen Zuschlägen am 23 nichts mehr zu holen, weil das Ziel dann bereits erreicht ist.
Gruß aaahhh
Gruß aaahhh
Fahnenstange. Das wird demnächst ne ordentliche Korrektur geben.
Antwort auf Beitrag Nr.: 60.585.461 von aaahhh am 16.05.19 18:04:44
Wahrscheinlich behältst du Recht. Wiedereinmal.
Zitat von aaahhh: So wie sich der Kurs verhält kommt da vor dem 23.6 was. Ansonsten ist bei den täglichen Zuschlägen am 23 nichts mehr zu holen, weil das Ziel dann bereits erreicht ist.
Gruß aaahhh
Wahrscheinlich behältst du Recht. Wiedereinmal.
Antwort auf Beitrag Nr.: 60.585.609 von Ulfred am 16.05.19 18:24:59
Wenn der Kurs bis dahin weiter so klettert ist das nur logisch.
Zitat von Ulfred: Fahnenstange. Das wird demnächst ne ordentliche Korrektur geben.
Wenn der Kurs bis dahin weiter so klettert ist das nur logisch.
Wir werden sehen wie weit es jetzt noch nach oben geht vor der Zulassung. Das wird auch nicht das letzte Produkt swin
Antwort auf Beitrag Nr.: 60.585.609 von Ulfred am 16.05.19 18:24:59
Die gab es bereits vor paar Monaten von 1,25 auf 0,60€
Zitat von Ulfred: Fahnenstange. Das wird demnächst ne ordentliche Korrektur geben.
Die gab es bereits vor paar Monaten von 1,25 auf 0,60€
Meint ihr als Korrektur so in etwa wie bei axsome im letzten bzw diesen Monat ?! Wenn ja, wäre es auch eine feine Geschichte
Bin schon lang hier investiert. ... habe bis dato nur mitgelesen , aber was jetzt hier gepostet wird zeigt nur wieder dumme GIER........viel Spaß noch.
Antwort auf Beitrag Nr.: 60.586.952 von Weltbummler am 16.05.19 22:08:36
Aktienanzahl
Ich habe mal eine Frage hoffe jemand kann mir die beantworten. Als ich anfang des Jahres palatin beobachtet habe hatte palatin etwas mit 158 Millionen Aktien jetzt wird bei ariva schon über 200 Millionen angegeben. Hab ich was verpasst woher kommt diese Erhöhung und welche aktienanzahl ist jetzt die richtige. Schon mal vielen Dank an die die mir diese Frage beantwortet.
Antwort auf Beitrag Nr.: 60.586.952 von Weltbummler am 16.05.19 22:08:36
Wann bitte ist Wertpapierhandel jemals etwas anderes? Nimm gerne wieder an der Seitenlinie Platz. Ganz egal wo das hier endet. Habe 2 x meinen Einsatz verdoppelt und bin auch jetzt wieder mehr als glücklich dabei zu sein.
Zitat von Weltbummler: Bin schon lang hier investiert. ... habe bis dato nur mitgelesen , aber was jetzt hier gepostet wird zeigt nur wieder dumme GIER........viel Spaß noch.
Wann bitte ist Wertpapierhandel jemals etwas anderes? Nimm gerne wieder an der Seitenlinie Platz. Ganz egal wo das hier endet. Habe 2 x meinen Einsatz verdoppelt und bin auch jetzt wieder mehr als glücklich dabei zu sein.
Antwort auf Beitrag Nr.: 60.586.952 von Weltbummler am 16.05.19 22:08:36...so ist nun einmal börse , alle wünsche der gier gehen nun niemals in erfüllung und niederlagen nimmt man auch in kauf . habe für 0,33 euro gekauft und bin mehr als nur zufrieden , dafür hapert es an anderen stellen mehr als zur genüge .......allen weiterhin viel glück , zumindestens mit diesem titel....!!!!
Antwort auf Beitrag Nr.: 60.588.163 von herthafan am 17.05.19 08:37:26
Dem ist absolut nichts hinzuzufügen.
Zitat von herthafan: ...so ist nun einmal börse , alle wünsche der gier gehen nun niemals in erfüllung und niederlagen nimmt man auch in kauf . habe für 0,33 euro gekauft und bin mehr als nur zufrieden , dafür hapert es an anderen stellen mehr als zur genüge .......allen weiterhin viel glück , zumindestens mit diesem titel....!!!!
Dem ist absolut nichts hinzuzufügen.
Antwort auf Beitrag Nr.: 60.588.415 von PrinzStorno am 17.05.19 09:11:43Ebenso!!!
(Von aktuell 10 Titeln nur 2 im Plus,
alle anderen zum Teil DICK im roten Bereich !
!
Und da ist Palatin schon jetzt ein wirksames
Potenzmittel, hoffentlich bleibt das so!?! )
)
(Von aktuell 10 Titeln nur 2 im Plus,
alle anderen zum Teil DICK im roten Bereich
 !
!Und da ist Palatin schon jetzt ein wirksames
Potenzmittel, hoffentlich bleibt das so!?!
 )
)
Antwort auf Beitrag Nr.: 60.589.229 von mafei am 17.05.19 10:58:18
Wirecard und Palatin sind meine einzigen Sachen die im Moment im Plus sind
Zitat von mafei: Ebenso!!!
(Von aktuell 10 Titeln nur 2 im Plus,
alle anderen zum Teil DICK im roten Bereich!
Und da ist Palatin schon jetzt ein wirksames
Potenzmittel, hoffentlich bleibt das so!?!)
Wirecard und Palatin sind meine einzigen Sachen die im Moment im Plus sind

Antwort auf Beitrag Nr.: 60.589.333 von PrinzStorno am 17.05.19 11:14:16Wenn das deine einzigen Positionen im Depot sind.......
........... dann HERZLICHEN GLÜCKWUNSCH 🤑
........... dann HERZLICHEN GLÜCKWUNSCH 🤑
Warum gibt es hier bei den Smilies nur so wenige ?
(Mir fehlt z.B. des öfteren Daumen hoch/runter)



(Mir fehlt z.B. des öfteren Daumen hoch/runter)



Antwort auf Beitrag Nr.: 60.589.399 von mafei am 17.05.19 11:24:50
Dank Donald sind alle grünen Positionen aus überseh aus meinem Depot rausgeworfen worden
Zitat von mafei: Wenn das deine einzigen Positionen im Depot sind.......
........... dann HERZLICHEN GLÜCKWUNSCH 🤑
Dank Donald sind alle grünen Positionen aus überseh aus meinem Depot rausgeworfen worden

Antwort auf Beitrag Nr.: 60.589.421 von mafei am 17.05.19 11:27:12
Zitat von mafei: Warum gibt es hier bei den Smilies nur so wenige ?
(Mir fehlt z.B. des öfteren Daumen hoch/runter)
......stimmt leider , als ich hier vor einiger zeit mit eingestiegen bin herrschte hier ein tuwabou schlimmsten grades , bzw. kleinkrieg unter investoren . ich habe dann aber versucht hier wieder ruhe rein zu bekommen was mir auch bestens gelungen zu sein scheint , worauf ich heute noch ein wenig stolz darüber sein können zu dürfen ......also daumen hoch , wenn angebracht und weiterhin viel glück bis bzw. mit dem tag der alles für uns entscheiden könnte.....
Mehr smilies braucht das Land ;-)
@herthafan ich weiß das du hier auch schon eine ganze Weile mit dabei bist. Weißt du ob das noch ein aktuelles Thema ist oder ob sich das evtl schon erledigt hat ?!
Mir ist heut Morgen das Thema mit den Warrants in den Kopf geschossen ...war da nicht was von 20-25 Mio. letzten Herbst die Rede ....ich glaube mich daran zu erinnern das der User OnkelEn immer fleißig darüber berichtet hat, das da noch was aussteht.
Vielleicht kannst du oder die anderen User ...was darüber sagen.
Beste Grüße Richtung Norden
@herthafan ich weiß das du hier auch schon eine ganze Weile mit dabei bist. Weißt du ob das noch ein aktuelles Thema ist oder ob sich das evtl schon erledigt hat ?!
Mir ist heut Morgen das Thema mit den Warrants in den Kopf geschossen ...war da nicht was von 20-25 Mio. letzten Herbst die Rede ....ich glaube mich daran zu erinnern das der User OnkelEn immer fleißig darüber berichtet hat, das da noch was aussteht.
Vielleicht kannst du oder die anderen User ...was darüber sagen.
Beste Grüße Richtung Norden
Antwort auf Beitrag Nr.: 60.589.843 von Nasgu am 17.05.19 12:22:16...werter nasgo , habe noch einmal überall nachgeblättert (auch bei SD ) aber leider auch nichts mehr gefunden darüber und möchte auch nichts durcheinander bringen mit anderen us/can. bio-tech"s in ähnlichen situationen......allen ein wunderschönes WE.......
Antwort auf Beitrag Nr.: 60.589.843 von Nasgu am 17.05.19 12:22:16
CFO Steve Wills zu den Pennywarrants:
In den letzten vier Monaten Juni, Juli, August und September haben wir circa 32 Millionen gewandelte Prefunded Warrants erlebt, von denen wir glauben, dass sie alle oder die überwältigende Mehrheit in den Markt verkauft wurden. Allein im Monat September haben wir 16 Millionen Wandlungen bezogen auf die Prefunded Warrants verzeichnet. Am heutigen Tage haben wir noch etwa 11,5 Millionen Prefunded oder Pennywarrants ausstehend und unsere Erwartung ist, dass sie (ihr Bestand, Anm. d. Redaktion) innerhalb der nächsten 30 bis 60 Tage auf Null sinken.
https://www.sharedeals.de/palatin-die-letzten-warrants-der-l…
Zitat von Nasgu: Mehr smilies braucht das Land ;-)
@herthafan ich weiß das du hier auch schon eine ganze Weile mit dabei bist. Weißt du ob das noch ein aktuelles Thema ist oder ob sich das evtl schon erledigt hat ?!
Mir ist heut Morgen das Thema mit den Warrants in den Kopf geschossen ...war da nicht was von 20-25 Mio. letzten Herbst die Rede ....ich glaube mich daran zu erinnern das der User OnkelEn immer fleißig darüber berichtet hat, das da noch was aussteht.
Vielleicht kannst du oder die anderen User ...was darüber sagen.
Beste Grüße Richtung Norden
CFO Steve Wills zu den Pennywarrants:
In den letzten vier Monaten Juni, Juli, August und September haben wir circa 32 Millionen gewandelte Prefunded Warrants erlebt, von denen wir glauben, dass sie alle oder die überwältigende Mehrheit in den Markt verkauft wurden. Allein im Monat September haben wir 16 Millionen Wandlungen bezogen auf die Prefunded Warrants verzeichnet. Am heutigen Tage haben wir noch etwa 11,5 Millionen Prefunded oder Pennywarrants ausstehend und unsere Erwartung ist, dass sie (ihr Bestand, Anm. d. Redaktion) innerhalb der nächsten 30 bis 60 Tage auf Null sinken.
https://www.sharedeals.de/palatin-die-letzten-warrants-der-l…
Vielen Dank für die Info euch beiden!
Antwort auf Beitrag Nr.: 60.590.453 von onkelen am 17.05.19 13:55:26...onkelen...ebenfalls besten dank auch von meiner seite....!!!!
PTN -21% $1.28
WAS GEHT HIER AB ??? !!! 

 !!! ???
!!! ???


 !!! ???
!!! ???
Antwort auf Beitrag Nr.: 60.591.979 von mafei am 17.05.19 17:50:24Da es keine News gibt...shortattacke abfischen?
Jaaaaaa, günstig aufstocken!
Vielleicht kommt meine Order ja doch noch zu 93Cent zum Zuge
Vielleicht kommt meine Order ja doch noch zu 93Cent zum Zuge
Stoplose abgefischt 


(vergessen)
1.5 mio über Tradegate
Ich denke da hat es einige STOPLOSS rausgehauen 

1,5 mio Stück...... so viele hab ich doch garnicht 



Und gleich <100000 Stück wieder eingesammelt 

Also, nicht ich , sondern auf Tradegate nach dieser Verkaufswelle
, sondern auf Tradegate nach dieser Verkaufswelle 
 , sondern auf Tradegate nach dieser Verkaufswelle
, sondern auf Tradegate nach dieser Verkaufswelle 
Wie gesagt: Fahnenstange wird immer abverkauft/stark korrigiert. Mit Glück war's das aber schon. Mit Pech... tja...
In ner Stunde ist der Spuk vorbei und wir stehen wieder mindestens bei 1,4
Bin bei 1,11 wieder rein 

Schaut euch den Handel jetzt auch in Übersee an!
Antwort auf Beitrag Nr.: 60.592.179 von PrinzStorno am 17.05.19 18:24:04Hab auch nochmal bei 1,20 nachgekauft...
Schöner Dip zum billig eindecken... Denke wir schliessen bei 1,45€...
Schöner Dip zum billig eindecken... Denke wir schliessen bei 1,45€...
Dieses Spiel wird jetzt wieder regelmäßige kommen. Man merkt das Mitspieler wie SD zurück sind. Jetzt folgt erstmal wieder eine Push Meldung demnächst und dann wird das zeitnah wiederholt 

Das war ein ALBTRAUM 

Antwort auf Beitrag Nr.: 60.592.307 von mafei am 17.05.19 18:52:01Schlusskurs über 1,50 heute? Würde mich nicht wundern.
Antwort auf Beitrag Nr.: 60.592.313 von Spondon am 17.05.19 18:53:14Mich auch nicht  ! Sag ja, war nur ein Albtraum 😴
! Sag ja, war nur ein Albtraum 😴
 ! Sag ja, war nur ein Albtraum 😴
! Sag ja, war nur ein Albtraum 😴
Krass, heute morgen noch die Hälfte verkauft.
Und ich dachte noch, nimm einfach mal die alten Fangorder um einen Euro raus, weil die Kurse nicht mehr kommen. Gut dass ich so faul war ;-)
Und ich dachte noch, nimm einfach mal die alten Fangorder um einen Euro raus, weil die Kurse nicht mehr kommen. Gut dass ich so faul war ;-)
Aber weiß jemand was los war, konnte bisher nix finden und auch die AMAG Zahlen sind ja jetzt schon ein paar Tage raus und der Analyst Call ist erst am 22.5.
Antwort auf Beitrag Nr.: 60.592.345 von zebion2019 am 17.05.19 18:59:46Wenn mal einer anfängt zu schmeißen ( oder auch SL fishing) wird eben eine Lawine los getreten und bei den Gewinnen der letzten Zeit nimmt man diese auch mal gerne mit vor den langen WE, am Mo hat CAN zu Victoria day! Könnte mir vorstellen, dass es das noch nicht war für heute.
Gruß aaahhh
Gruß aaahhh
Antwort auf Beitrag Nr.: 60.592.335 von zebion2019 am 17.05.19 18:58:50
Ich hab 1/3 50 min vorher umgeschichtet. Man muss auch einfach mal Glück haben!
Zitat von zebion2019: Krass, heute morgen noch die Hälfte verkauft.
Und ich dachte noch, nimm einfach mal die alten Fangorder um einen Euro raus, weil die Kurse nicht mehr kommen. Gut dass ich so faul war ;-)
Ich hab 1/3 50 min vorher umgeschichtet. Man muss auch einfach mal Glück haben!
11 Mio Shares heute getraded
Was ist geschehen?
Antwort auf Beitrag Nr.: 60.592.699 von FRLA am 17.05.19 20:04:56
Sieht nach einer Short Attacke aus.
Zitat von FRLA: Was ist geschehen?
Sieht nach einer Short Attacke aus.
....is wohl WE.....und bargeld lockt halt immer wieder......montag treffen wir uns wieder.....
Beitrag zu dieser Diskussion schreiben
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -3,69 | |
| -4,26 | |
| +0,48 | |
| 0,00 | |
| +1,09 | |
| -3,16 | |
| +1,33 | |
| +0,66 | |
| -4,17 | |
| -6,80 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 240 | ||
| 98 | ||
| 81 | ||
| 78 | ||
| 75 | ||
| 53 | ||
| 41 | ||
| 38 | ||
| 36 | ||
| 33 |





















