MORPHOSYS -Schwellenmitteilungen-Tabelle / Analysten-Tabelle / Charts (Seite 8)
eröffnet am 12.07.13 15:54:43 von
neuester Beitrag 26.08.22 08:51:48 von
neuester Beitrag 26.08.22 08:51:48 von
Beiträge: 1.080
ID: 1.183.757
ID: 1.183.757
Aufrufe heute: 0
Gesamt: 186.476
Gesamt: 186.476
Aktive User: 0
ISIN: DE0006632003 · WKN: 663200 · Symbol: MOR
68,10
EUR
+0,15 %
+0,10 EUR
Letzter Kurs 12:23:39 Lang & Schwarz
Neuigkeiten
| TitelBeiträge |
|---|
| Morphosys Aktien jetzt im kostenlosen Demokonto handeln!Anzeige |
22.05.24 · wO Chartvergleich |
22.05.24 · kapitalerhoehungen.de |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,2300 | +48,01 | |
| 1,0800 | +28,56 | |
| 2,1800 | +27,49 | |
| 1,9900 | +20,61 | |
| 10.777,50 | +19,75 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 46,20 | -16,00 | |
| 0,5701 | -16,77 | |
| 2,5100 | -17,43 | |
| 2,2001 | -20,57 | |
| 0,5884 | -38,71 |
Beitrag zu dieser Diskussion schreiben
Time for Bingo ^^

Nachricht vom 25.01.2021 | 22:00
MorphoSys und I-Mab geben die Dosierung des ersten Patienten in der Phase 1-Studie mit MOR210/TJ210 in den USA bei Patienten mit fortgeschrittenem Krebs bekannt
DGAP-News: MorphoSys AG / Schlagwort(e): Sonstiges
25.01.2021 / 22:00
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber verantwortlich.
Medienmitteilung
MorphoSys und I-Mab geben die Dosierung des ersten Patienten in der Phase 1-Studie mit MOR210/TJ210 in den USA bei Patienten mit fortgeschrittenem Krebs bekannt
PLANEGG/MÜNCHEN, Deutschland und SHANGHAI, China - 25. Januar 2021 - MorphoSys (FSE: MOR; Prime Standard Segment, MDAX & TecDAX; NASDAQ: MOR) und I-Mab (NASDAQ: IMAB) gaben heute bekannt, dass der erste Patient in einer Phase-1-Dosisfindungsstudie zur Untersuchung der Sicherheit, Verträglichkeit, Pharmakokinetik (PK) und Pharmakodynamik (PD) von MOR210/TJ210 als Monotherapie bei Patienten mit rezidivierten oder refraktären fortgeschrittenen soliden Tumoren in den Vereinigten Staaten dosiert wurde.
MOR210/TJ210 ist ein von MorphoSys entwickelter monoklonaler Antikörper, der gegen den Rezeptor des Komplementfaktor C5a (C5aR1) gerichtet ist. Sein Ligand C5a wird im Tumor-Milieu produziert und führt zur chemotaktischen Anlockung von Zellen, wie myeloide Suppressorzellen, M2-Makrophagen und Neutrophile, welche das Tumorwachstum begünstigen. MOR210/TJ210 wurde entwickelt, um die Aktivierung und Migration von C5aR1-exprimierenden myeloiden Zellen zu blockieren und dadurch eine anti-tumoröse Wirkung zu entfalten.
In präklinischen Studien konnte gezeigt werden, dass eine Blockade der C5aR-C5a-Achse in Kombination mit Immun-Checkpoint-Inhibitoren das Tumorwachstum deutlich einschränkt. Im Rahmen von in vitro Experimenten konnte darüber hinaus gezeigt werden, dass auch bei sehr hohen C5a-Konzentrationen der C5a/C5aR-Signalweg blockiert werden konnte, was zu einer lang anhaltenden Wirkung führte. Des weiteren zeigte MOR210/TJ210 ein gutes Sicherheitsprofil ohne das Auftreten von Nebenwirkungen bis zur höchsten in nicht-klinischen Sicherheitsstudien getesteten Dosis.
Die klinische Phase-1-Studie ist eine nicht-verblindete Dosisfindungsstudie mit mehreren Dosisgruppen in verschiedenen Zentren der USA, um die Sicherheit, Verträglichkeit und PK/PD von MOR210/TJ210 bei Patienten mit fortgeschrittenen soliden Tumoren zu untersuchen. Daran anschließend sind weitere klinische Kombinationsstudien von MOR210/TJ210 mit Checkpoint-Inhibitoren geplant.
"Wir sind von den in den präklinischen Studien beobachteten Daten überzeugt und glauben, dass TJ210/MOR210 mit seinen einzigartigen Eigenschaften ein großes Potenzial für die Behandlung von schwer behandelbaren Krebserkrankungen hat", sagte Dr. Joan Shen, CEO von I-Mab. "Die aus dieser Studie gewonnenen Daten liefern wertvolle Informationen über das Sicherheits- und Verträglichkeitsprofil von TJ210/MOR210 und dem potenziellen Nutzen bei Patienten mit fortgeschrittenem Krebs."
"Wir freuen uns darauf, mit I-Mab zusammen das Potenzial von MOR210/TJ210 als neuartige Therapieoption für Patienten mit fortgeschrittenen soliden Tumoren in klinischen Studien zu untersuchen", sagte Dr. Malte Peters, Forschungs- und Entwicklungsvorstand von MorphoSys.
https://www.dgap.de/dgap/News/corporate/morphosys-und-imab-g…
MorphoSys und I-Mab geben die Dosierung des ersten Patienten in der Phase 1-Studie mit MOR210/TJ210 in den USA bei Patienten mit fortgeschrittenem Krebs bekannt
DGAP-News: MorphoSys AG / Schlagwort(e): Sonstiges
25.01.2021 / 22:00
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber verantwortlich.
Medienmitteilung
MorphoSys und I-Mab geben die Dosierung des ersten Patienten in der Phase 1-Studie mit MOR210/TJ210 in den USA bei Patienten mit fortgeschrittenem Krebs bekannt
PLANEGG/MÜNCHEN, Deutschland und SHANGHAI, China - 25. Januar 2021 - MorphoSys (FSE: MOR; Prime Standard Segment, MDAX & TecDAX; NASDAQ: MOR) und I-Mab (NASDAQ: IMAB) gaben heute bekannt, dass der erste Patient in einer Phase-1-Dosisfindungsstudie zur Untersuchung der Sicherheit, Verträglichkeit, Pharmakokinetik (PK) und Pharmakodynamik (PD) von MOR210/TJ210 als Monotherapie bei Patienten mit rezidivierten oder refraktären fortgeschrittenen soliden Tumoren in den Vereinigten Staaten dosiert wurde.
MOR210/TJ210 ist ein von MorphoSys entwickelter monoklonaler Antikörper, der gegen den Rezeptor des Komplementfaktor C5a (C5aR1) gerichtet ist. Sein Ligand C5a wird im Tumor-Milieu produziert und führt zur chemotaktischen Anlockung von Zellen, wie myeloide Suppressorzellen, M2-Makrophagen und Neutrophile, welche das Tumorwachstum begünstigen. MOR210/TJ210 wurde entwickelt, um die Aktivierung und Migration von C5aR1-exprimierenden myeloiden Zellen zu blockieren und dadurch eine anti-tumoröse Wirkung zu entfalten.
In präklinischen Studien konnte gezeigt werden, dass eine Blockade der C5aR-C5a-Achse in Kombination mit Immun-Checkpoint-Inhibitoren das Tumorwachstum deutlich einschränkt. Im Rahmen von in vitro Experimenten konnte darüber hinaus gezeigt werden, dass auch bei sehr hohen C5a-Konzentrationen der C5a/C5aR-Signalweg blockiert werden konnte, was zu einer lang anhaltenden Wirkung führte. Des weiteren zeigte MOR210/TJ210 ein gutes Sicherheitsprofil ohne das Auftreten von Nebenwirkungen bis zur höchsten in nicht-klinischen Sicherheitsstudien getesteten Dosis.
Die klinische Phase-1-Studie ist eine nicht-verblindete Dosisfindungsstudie mit mehreren Dosisgruppen in verschiedenen Zentren der USA, um die Sicherheit, Verträglichkeit und PK/PD von MOR210/TJ210 bei Patienten mit fortgeschrittenen soliden Tumoren zu untersuchen. Daran anschließend sind weitere klinische Kombinationsstudien von MOR210/TJ210 mit Checkpoint-Inhibitoren geplant.
"Wir sind von den in den präklinischen Studien beobachteten Daten überzeugt und glauben, dass TJ210/MOR210 mit seinen einzigartigen Eigenschaften ein großes Potenzial für die Behandlung von schwer behandelbaren Krebserkrankungen hat", sagte Dr. Joan Shen, CEO von I-Mab. "Die aus dieser Studie gewonnenen Daten liefern wertvolle Informationen über das Sicherheits- und Verträglichkeitsprofil von TJ210/MOR210 und dem potenziellen Nutzen bei Patienten mit fortgeschrittenem Krebs."
"Wir freuen uns darauf, mit I-Mab zusammen das Potenzial von MOR210/TJ210 als neuartige Therapieoption für Patienten mit fortgeschrittenen soliden Tumoren in klinischen Studien zu untersuchen", sagte Dr. Malte Peters, Forschungs- und Entwicklungsvorstand von MorphoSys.
https://www.dgap.de/dgap/News/corporate/morphosys-und-imab-g…
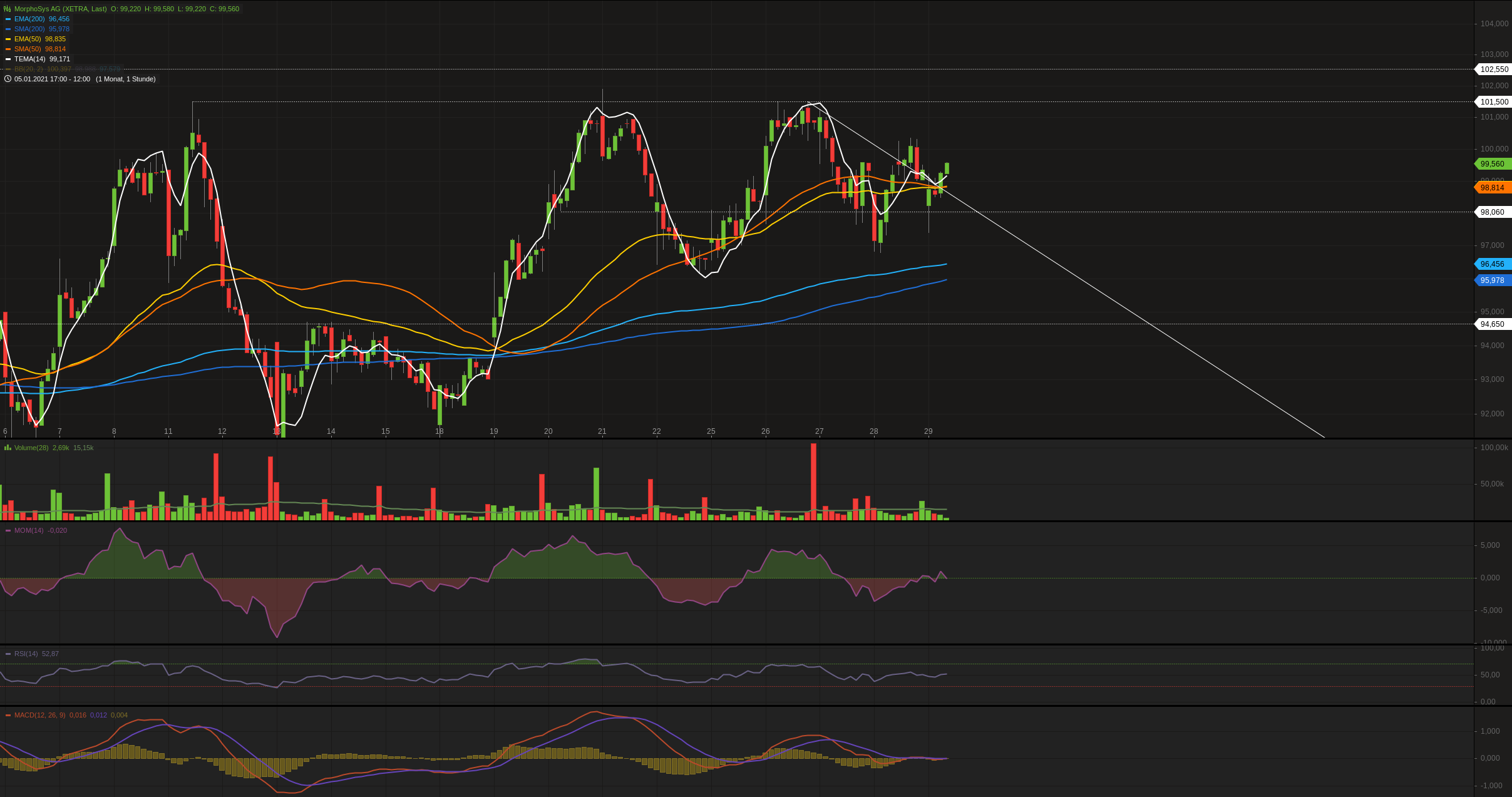
Antwort auf Beitrag Nr.: 66.556.559 von trufo am 22.01.21 09:36:17Wenn das Momentum einen Doppelboden zeichnet bin ich bisschen zuversichtlicher, wenn der Fast Stochastic nördlich kreuzt freut mich das, was mich jedoch optimistisch stimmt ist die Dezember Kerze + TEMA.
Wenn der Kurs über 94,00€ zum Monatsende hin schließt, würde mich das freuen.

Wenn der Kurs über 94,00€ zum Monatsende hin schließt, würde mich das freuen.

Abwarten, ist ja noch nicht vorbei heute, die 98€ sind noch machbar. Volumen ist auch normal und nicht hoch.

science fiction?
gerne.., solange Du mir keinen Diamanten reinmalst
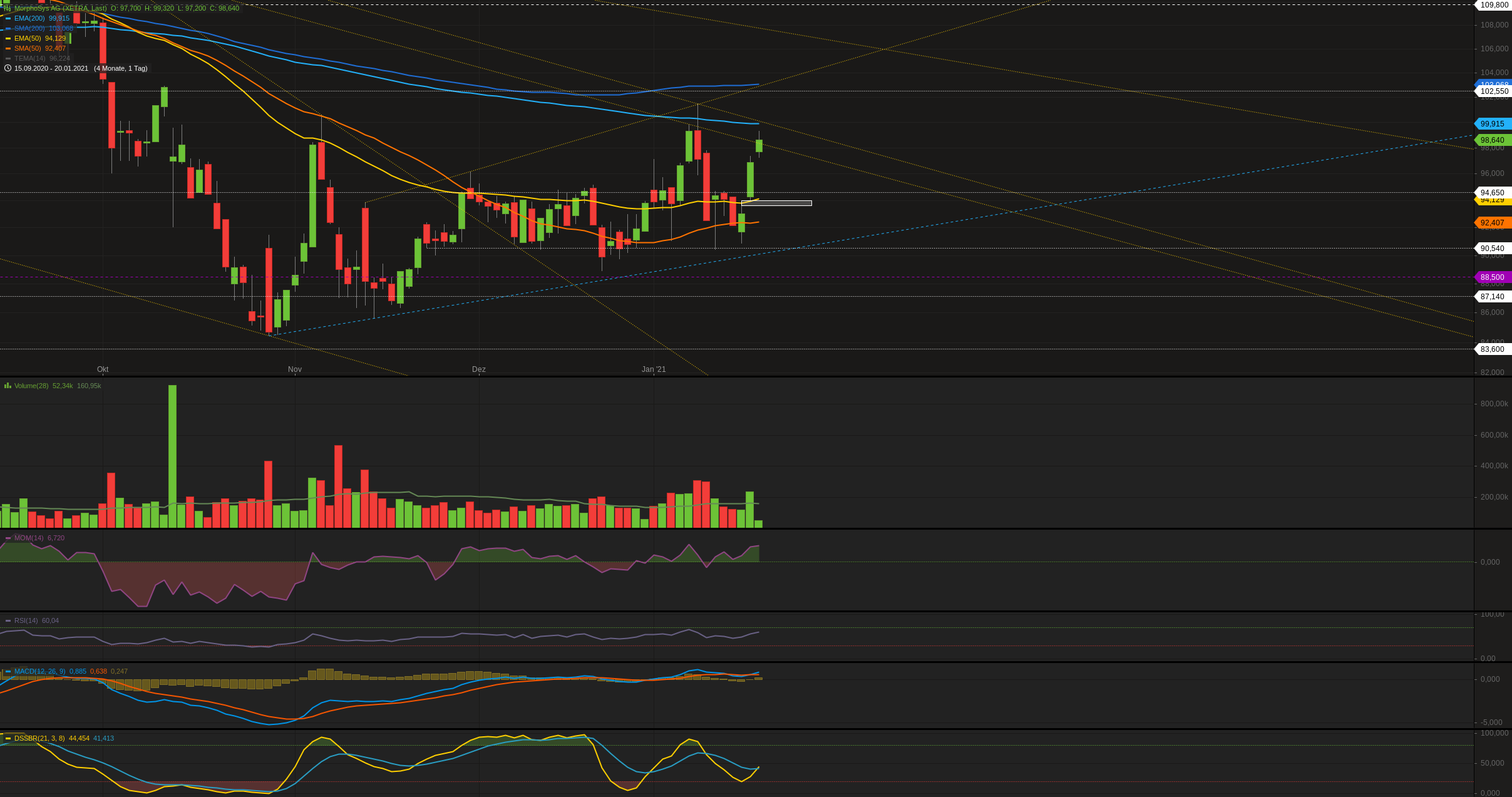
Willst du monthly. 

einfach auf weekly umstellen und beten dass es keiner sieht 😇
Kleiner Schönheitsfehler @ 93,64€.

MorphoSys und Incyte geben die Annahme des Zulassungsantrags für Tafasitamab durch Health Canada bekannt
https://www.dgap.de/dgap/News/corporate/morphosys-und-incyte…
https://www.dgap.de/dgap/News/corporate/morphosys-und-incyte…
22.05.24 · wO Chartvergleich · Deutsche Bank |
22.05.24 · kapitalerhoehungen.de · Morphosys |
20.05.24 · wO Newsflash · Apple |
16.05.24 · wO Newsflash · Advanced Micro Devices |
16.05.24 · dpa-AFX · Morphosys |
30.04.24 · dpa-AFX · Mercedes-Benz Group |
30.04.24 · wO Newsflash · Apple |
30.04.24 · dpa-AFX · Mercedes-Benz Group |
30.04.24 · wallstreetONLINE Redaktion · Morphosys |
| Zeit | Titel |
|---|---|
| 11:37 Uhr | |
| 08:46 Uhr | |
| 16.05.24 | |
| 24.04.24 | |
| 16.01.24 | |
| 05.01.24 | |
| 11.12.23 |





















