Deutsche Biotechwerte Fakten ab 2016 (Seite 12)
eröffnet am 03.01.16 16:22:15 von
neuester Beitrag 11.02.24 11:08:20 von
neuester Beitrag 11.02.24 11:08:20 von
Beiträge: 673
ID: 1.223.874
ID: 1.223.874
Aufrufe heute: 0
Gesamt: 39.446
Gesamt: 39.446
Aktive User: 0
Top-Diskussionen
| Titel | letzter Beitrag | Aufrufe |
|---|---|---|
| heute 18:41 | 1965 | |
| vor 1 Stunde | 1860 | |
| heute 20:29 | 1619 | |
| vor 1 Stunde | 1618 | |
| heute 20:08 | 1610 | |
| vor 52 Minuten | 1403 | |
| gestern 15:24 | 1174 | |
| vor 58 Minuten | 941 |
Meistdiskutierte Wertpapiere
| Platz | vorher | Wertpapier | Kurs | Perf. % | Anzahl | ||
|---|---|---|---|---|---|---|---|
| 1. | 1. | 18.002,02 | -1,44 | 264 | |||
| 2. | 2. | 26,58 | -0,63 | 137 | |||
| 3. | 3. | 178,01 | -2,44 | 77 | |||
| 4. | Neu! | 479,00 | -5,71 | 69 | |||
| 5. | 6. | 0,1855 | -1,85 | 67 | |||
| 6. | 15. | 17,550 | -4,10 | 63 | |||
| 7. | 5. | 131,88 | +1,75 | 48 | |||
| 8. | 18. | 5,2900 | -1,89 | 43 |
Beitrag zu dieser Diskussion schreiben
Antwort auf Beitrag Nr.: 58.323.032 von BICYPAPA am 28.07.18 08:17:37
Zur Lage des NBINasdaq Biotechindex. Seit gut 2,5 Jahren zeichnet er positiven Trend nachdem er vor ca 3 Jahren eine sehr heftigen Einbruch und eine Korrektur von ca 4160 auf 2650 zu verzeichnen hat. Mittlerweile ist er mit kleineren Korrekturen wieder bei etwa 3670 Punkten angelangt. Die Performance in den letzten zwei Jahren etwa 20%.
Der DBI Deutsche Biotechindex in den letzten 4 Wochen. Nach durchweg guten Quartalsberichten und Zahlen pendelt der NBI weiterhin um den Jahresausgangswert. Der anfängliche Jahresgewinn von ca 18% ist wieder ganz aufgezehrt und nur einigen Einzelwerten ist dann diese Stabilität dafür ausschlaggebend, dass es nicht weiter in den Keller ging. Neben Sartorius, der eigentlich gar kein echter Biotechwert ist sorgten vor allem Evotec, Qiagen, MorphoSys und Cytotools für die entscheidenden Pluspunkte.
Zu den Einzelwerten:
Evotec:Einfach glänzende Zahlen und Aussichten. Ich habe versucht die überhitzten Phasen ein wenig zu traden, um so meine Performance ein wenig zu erhöhen. Es ist relativ gut gelungen. Eine noch immer hohe Shortquote und der zu erwartende gute Newsflow sprechen eher für einen weiteren positiven Kursverlauf.
Cytotools:Gerade gestern wurde eine weitere Maßnahme positiv abgeschlossen. Die Gelder sollten zur Entwicklung einiger neuer Wirkstoffkandidaten der Tochter Cytotpharma genutzt werden. Die Europastudie mit Dermapro ist gestartet und erste Ergebnisse werden etwa Q1 19 erwaret. Doch ein weiterer wichtiger Punkt steht nun bald an. Der Schadensersatzprozess gegen den alten Wirkstoffhersteller, der für das ganze Desaster bei Cytotools verantwortlich war. Sollte der Prozess positiv für Cytotools entschieden werden, dürfte dann auch ein beträchtlicher Betrag an Schadensersatz zugesprochen werden. Dies würde dann ein Großteil der jetzigen laufenden Studie finanzieren können. Es ist der finale Prozess, der jetzt zur Entscheidung ansteht. Ein positiver Ausgang dürfte für heftige Kursbewegungen sorgen.
Paion:Paion kommt jetzt mit den Zulassungsmodalitäten in die entscheidenden Phasen. Im Laufe der nächsten Monate wird alleine in 6 verschiedenen Ländern mit diesen Anträgen gerechnet. Die Phase 3 in Europa ist gestartet. Es werden bald die ersten Milestones on den noch 89 Millionen ausstehenden Geldern fließen. Die Finanzierung dürfte damit ausreichen um die weitere Finanzierung zu sichern. Ein wenig Unsicherheit brachte der USA Partner Cosmo durch die Probleme bei der Zulassung von Methylenblau MMX. Dies ist insofern wichtig, da hier eine gemeinsame Vermarktung mit Remimazolam angestrebt wurde. Cosmo hattte noch einen weiteren Termin mit der FDA und man ist jetzt optimistisch eine Einigung zu erzielen.
Heidelberg Pharma:Warten auf Godot. Ganz unauffällig zur Zeit. Doch es stehen entscheidende Nachrichten mit den Geschäftspartnern an. Da sie aber weiterhin im Verlauf und vom Kurs stabil sind werde ich sie im Depot belassen.
Magforce , MologenAuffälligkeiten bei diesen beiden Werten. Bei Magforce konnte ich einen positiven Verlauf durch eine Kapitalmaßnahme mit einem Trade nutzen . Mologen zeigt unerwartet Lebenszeichen. Vielleicht ist hier auch eine Kapitalmaßnahme in Planung.
Zu den Depots.
Tradingdepot:Trotz eines schweren Tradingfehlers (es war sehr heiß) konnte ich meine Performance von gut 23% auf über 27% ausbauen. Damit befindet sich mein Depot etwa auf Rang 33 von etwa 1530 Mitspielern im Ariva Boardspiel. Im Augenblick befindet sich nur Paion und Heidelberg Pharma im Depot. Geplant ist weiter Evotec und unter gewissen Bedingungen Magforce aufzunehmen. Die Cashquote ist im Augenblick auch bedingt durch die Gewinnmitnahmen recht hoch. Weiterhin versuche ich die Sondersituationen in einigen Werten zu nutzen.
Langfristdepot:Auch das Langfristdepot konnte weiter von ca 56% auf ca 59% zulegen. Es wurde aber schon am 12. 11. letzten Jahres gestartet. Es sollte eigentlich mein Biotechwikifolio werden. Doch leider konnte ich etwa die Hälfte meiner gewünschten Werte dort nicht einbuchen. Ich führe es deshalb als öffentliches Depot bei Ariva.
Dies kurz zum letzten Monat und einige Gedanken zu meinen Depotwerten oder Auffälligkeiten. Weiterhin ist bei mir große Vorsicht mit sehr hohen Cashquoten angesagt. In der Tabelle noch die Performance der Deutschen Biotechwerte im letzten Monat. Bleibt mir noch euch viel Glück und Erfolg bei euren Aktionen zu wünschen.
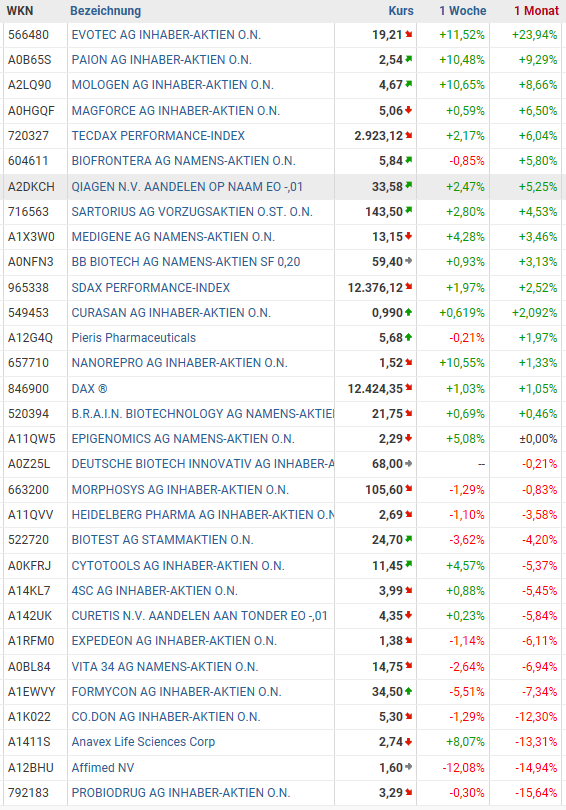
Der letzte Monat
Ein wenig Statistik und einige Gedanken zu den Einzelwerten. Der letzte Monat ist für mich trotz eines schweren Tradingfehlers noch sehr gut gelaufen. Die vorher von mir prognostizierten Werte Paion und Evotec bestimmten die Biotechperformance im letzten Monat. Dazu nutzte ich dann noch eine Tradingchance bei Magforce. Zur Lage des NBINasdaq Biotechindex. Seit gut 2,5 Jahren zeichnet er positiven Trend nachdem er vor ca 3 Jahren eine sehr heftigen Einbruch und eine Korrektur von ca 4160 auf 2650 zu verzeichnen hat. Mittlerweile ist er mit kleineren Korrekturen wieder bei etwa 3670 Punkten angelangt. Die Performance in den letzten zwei Jahren etwa 20%.
Der DBI Deutsche Biotechindex in den letzten 4 Wochen. Nach durchweg guten Quartalsberichten und Zahlen pendelt der NBI weiterhin um den Jahresausgangswert. Der anfängliche Jahresgewinn von ca 18% ist wieder ganz aufgezehrt und nur einigen Einzelwerten ist dann diese Stabilität dafür ausschlaggebend, dass es nicht weiter in den Keller ging. Neben Sartorius, der eigentlich gar kein echter Biotechwert ist sorgten vor allem Evotec, Qiagen, MorphoSys und Cytotools für die entscheidenden Pluspunkte.
Zu den Einzelwerten:
Evotec:Einfach glänzende Zahlen und Aussichten. Ich habe versucht die überhitzten Phasen ein wenig zu traden, um so meine Performance ein wenig zu erhöhen. Es ist relativ gut gelungen. Eine noch immer hohe Shortquote und der zu erwartende gute Newsflow sprechen eher für einen weiteren positiven Kursverlauf.
Cytotools:Gerade gestern wurde eine weitere Maßnahme positiv abgeschlossen. Die Gelder sollten zur Entwicklung einiger neuer Wirkstoffkandidaten der Tochter Cytotpharma genutzt werden. Die Europastudie mit Dermapro ist gestartet und erste Ergebnisse werden etwa Q1 19 erwaret. Doch ein weiterer wichtiger Punkt steht nun bald an. Der Schadensersatzprozess gegen den alten Wirkstoffhersteller, der für das ganze Desaster bei Cytotools verantwortlich war. Sollte der Prozess positiv für Cytotools entschieden werden, dürfte dann auch ein beträchtlicher Betrag an Schadensersatz zugesprochen werden. Dies würde dann ein Großteil der jetzigen laufenden Studie finanzieren können. Es ist der finale Prozess, der jetzt zur Entscheidung ansteht. Ein positiver Ausgang dürfte für heftige Kursbewegungen sorgen.
Paion:Paion kommt jetzt mit den Zulassungsmodalitäten in die entscheidenden Phasen. Im Laufe der nächsten Monate wird alleine in 6 verschiedenen Ländern mit diesen Anträgen gerechnet. Die Phase 3 in Europa ist gestartet. Es werden bald die ersten Milestones on den noch 89 Millionen ausstehenden Geldern fließen. Die Finanzierung dürfte damit ausreichen um die weitere Finanzierung zu sichern. Ein wenig Unsicherheit brachte der USA Partner Cosmo durch die Probleme bei der Zulassung von Methylenblau MMX. Dies ist insofern wichtig, da hier eine gemeinsame Vermarktung mit Remimazolam angestrebt wurde. Cosmo hattte noch einen weiteren Termin mit der FDA und man ist jetzt optimistisch eine Einigung zu erzielen.
Heidelberg Pharma:Warten auf Godot. Ganz unauffällig zur Zeit. Doch es stehen entscheidende Nachrichten mit den Geschäftspartnern an. Da sie aber weiterhin im Verlauf und vom Kurs stabil sind werde ich sie im Depot belassen.
Magforce , MologenAuffälligkeiten bei diesen beiden Werten. Bei Magforce konnte ich einen positiven Verlauf durch eine Kapitalmaßnahme mit einem Trade nutzen . Mologen zeigt unerwartet Lebenszeichen. Vielleicht ist hier auch eine Kapitalmaßnahme in Planung.
Zu den Depots.
Tradingdepot:Trotz eines schweren Tradingfehlers (es war sehr heiß) konnte ich meine Performance von gut 23% auf über 27% ausbauen. Damit befindet sich mein Depot etwa auf Rang 33 von etwa 1530 Mitspielern im Ariva Boardspiel. Im Augenblick befindet sich nur Paion und Heidelberg Pharma im Depot. Geplant ist weiter Evotec und unter gewissen Bedingungen Magforce aufzunehmen. Die Cashquote ist im Augenblick auch bedingt durch die Gewinnmitnahmen recht hoch. Weiterhin versuche ich die Sondersituationen in einigen Werten zu nutzen.
Langfristdepot:Auch das Langfristdepot konnte weiter von ca 56% auf ca 59% zulegen. Es wurde aber schon am 12. 11. letzten Jahres gestartet. Es sollte eigentlich mein Biotechwikifolio werden. Doch leider konnte ich etwa die Hälfte meiner gewünschten Werte dort nicht einbuchen. Ich führe es deshalb als öffentliches Depot bei Ariva.
Dies kurz zum letzten Monat und einige Gedanken zu meinen Depotwerten oder Auffälligkeiten. Weiterhin ist bei mir große Vorsicht mit sehr hohen Cashquoten angesagt. In der Tabelle noch die Performance der Deutschen Biotechwerte im letzten Monat. Bleibt mir noch euch viel Glück und Erfolg bei euren Aktionen zu wünschen.

Antwort auf Beitrag Nr.: 58.323.032 von BICYPAPA am 28.07.18 08:17:37
Quelle: https://www.finanzen.ch/nachrichten/aktien/Cosmo-VRP-Wir-hab…
Optimismus bei Cosmo / Paion Methylenblau MMX
Cosmo zeigt sich nach dem Gespräch bei der FDA optimistisch, dass man zu Methylenblau MMX eine Lösung finden wird. Damit dürfte dann auch für Remimazolam in den USA alles in geordneten Bahnen verlaufen.Quelle: https://www.finanzen.ch/nachrichten/aktien/Cosmo-VRP-Wir-hab…
Antwort auf Beitrag Nr.: 58.304.744 von BICYPAPA am 26.07.18 08:27:37
Evotec scheint ein wenig überhitzt und deswegen habe ich gestern die Gewinne mitgenommen. Es ist gut möglich, dass ich hier falsch liege. Doch einige Tage Korrektur würden der Aktie ganz gut tun. Ich rechne selber damit und plane auch wieder den Einstieg bei passender Gelegenheit. Vielleicht erleben wir noch mal eine Short Attacke.
Paion macht sich langsam auf den Weg. Gestern die Meldung zum Studienstart in Europa. Cosmo hatte vorgestern das Gespräch mit der FDA. Es sind keine Auffälligkeiten im Cosmo Chart. Deshalb gehe ich davon aus, dass eine Einigung gefunden wurde Methylenblau MMX doch zuzulassen. Dies wäre für Paion wichtig, da eine gemeinsame Vermarktung mit Remimazolam angestrebt wurde. Der Zulassungsantrag in den USA wird jetzt wahrscheinlich in Q1 19 gestellt. Auch Pendopharm in Kanada dürfte dann zusammen mit diesem Antrag seine Zulassung in Kanada anstreben. In Russland dürfte der Antrag schon in einigen Monaten gestellt werden. Japan ist ähnlich gelagert. Wir werden jetzt in Kürze einen regen Newsflow erwarten. Weitere Kapitalmaßnahmen sind wahrscheinlich nicht mehr geplant, da jetzt langsam von den ausstehenden 89 Millionen Milestones die ersten Beträge überwiesen werden. Deshalb habe ich Paion im Trading und im Langfristdepot.
Cytotools meldet den Studienstart in Europa und plant eine weitere Maßnahme zur Entwicklung der Cytopharma Tochter Aktivitäten. Auch hier scheinen alle Türen aufzugehen. Der Wert, der in der Vergangenheit so viel Pech hatte. Der Studienaufbau in Europa ist so geplant, dass er für die USA als eine FDA Forderungen gebraucht werden kann. Es würde mich nicht wundern, wenn es bald eine Lizensierung in die USA geben könnte. Dazu jetzt die neuen Indikationen von Cytopharma. Weiterhin wird Sepsis als zusätzliche Indikation für Dermapro angedacht. Hier hab ich einfach zu wenig Ahnung, um dies einschätzen zu können. Ich werde mal Cytotools kontaktieren um hier die Chancen ein wenig auszuloten. Hier gehen sämtliche Türen auf und nach der Maßnahme rechne ich auch hier wieder mit weiter steigenden Kursen. Cytotools ist weiter mit einer sehr hohen Gewichtung im Langfristdepot.
Heidelberg Pharma ist im Augenblick bis auf einen Insiderkauf eher unauffällig. Kaum Bewegung an der Börse. Ich lasse sie trotzdem im Depot, da jederzeit der Studienstart von Telix vermeldet werden kann und noch zwei Optionsentscheidungen von Takeda und Magenta Therapeutics anstehen.
Kurz zu den Depots. Das Tradingdepot befindet sich mit gut 23 % weiter auf dem Weg nach oben und befindet sich im Augenblick auf Rang 33 von etwa 1500 Mitspielern.
Auch das Langfristdepot steht glänzend da. Es sollte am Anfang eigentlich mein Wikifolio werden. Doch da ich ca die Hälfte meiner Werte nicht ordern konnte führe ich es öffentlich als Ariva Depot. Auch hier eine leichte Verbesserung auf ca 56% mit Studienstart am 12.11. letzten Jahres.
Die Cashquote ist in beiden Depots mit über 60% in Erwartung kleinerer Korrekturen recht hoch. Ich versuche weiterhin bis auf die oben angesprochenen Werte nur Sondersituationen zu nutzen.
Das wars diese Woche von den deutschen Biotechwerten. Ich wünsch euch viel Glück mit euren Aktien
Die letzte Woche
Diesmal keine Statistik. Nur kurz einige Gedanken zur letzten Woche. Der NBI Nasdaq Biotechindex korrigiert ein wenig und in der Folge auch einige deutsche Werte.Evotec scheint ein wenig überhitzt und deswegen habe ich gestern die Gewinne mitgenommen. Es ist gut möglich, dass ich hier falsch liege. Doch einige Tage Korrektur würden der Aktie ganz gut tun. Ich rechne selber damit und plane auch wieder den Einstieg bei passender Gelegenheit. Vielleicht erleben wir noch mal eine Short Attacke.
Paion macht sich langsam auf den Weg. Gestern die Meldung zum Studienstart in Europa. Cosmo hatte vorgestern das Gespräch mit der FDA. Es sind keine Auffälligkeiten im Cosmo Chart. Deshalb gehe ich davon aus, dass eine Einigung gefunden wurde Methylenblau MMX doch zuzulassen. Dies wäre für Paion wichtig, da eine gemeinsame Vermarktung mit Remimazolam angestrebt wurde. Der Zulassungsantrag in den USA wird jetzt wahrscheinlich in Q1 19 gestellt. Auch Pendopharm in Kanada dürfte dann zusammen mit diesem Antrag seine Zulassung in Kanada anstreben. In Russland dürfte der Antrag schon in einigen Monaten gestellt werden. Japan ist ähnlich gelagert. Wir werden jetzt in Kürze einen regen Newsflow erwarten. Weitere Kapitalmaßnahmen sind wahrscheinlich nicht mehr geplant, da jetzt langsam von den ausstehenden 89 Millionen Milestones die ersten Beträge überwiesen werden. Deshalb habe ich Paion im Trading und im Langfristdepot.
Cytotools meldet den Studienstart in Europa und plant eine weitere Maßnahme zur Entwicklung der Cytopharma Tochter Aktivitäten. Auch hier scheinen alle Türen aufzugehen. Der Wert, der in der Vergangenheit so viel Pech hatte. Der Studienaufbau in Europa ist so geplant, dass er für die USA als eine FDA Forderungen gebraucht werden kann. Es würde mich nicht wundern, wenn es bald eine Lizensierung in die USA geben könnte. Dazu jetzt die neuen Indikationen von Cytopharma. Weiterhin wird Sepsis als zusätzliche Indikation für Dermapro angedacht. Hier hab ich einfach zu wenig Ahnung, um dies einschätzen zu können. Ich werde mal Cytotools kontaktieren um hier die Chancen ein wenig auszuloten. Hier gehen sämtliche Türen auf und nach der Maßnahme rechne ich auch hier wieder mit weiter steigenden Kursen. Cytotools ist weiter mit einer sehr hohen Gewichtung im Langfristdepot.
Heidelberg Pharma ist im Augenblick bis auf einen Insiderkauf eher unauffällig. Kaum Bewegung an der Börse. Ich lasse sie trotzdem im Depot, da jederzeit der Studienstart von Telix vermeldet werden kann und noch zwei Optionsentscheidungen von Takeda und Magenta Therapeutics anstehen.
Kurz zu den Depots. Das Tradingdepot befindet sich mit gut 23 % weiter auf dem Weg nach oben und befindet sich im Augenblick auf Rang 33 von etwa 1500 Mitspielern.
Auch das Langfristdepot steht glänzend da. Es sollte am Anfang eigentlich mein Wikifolio werden. Doch da ich ca die Hälfte meiner Werte nicht ordern konnte führe ich es öffentlich als Ariva Depot. Auch hier eine leichte Verbesserung auf ca 56% mit Studienstart am 12.11. letzten Jahres.
Die Cashquote ist in beiden Depots mit über 60% in Erwartung kleinerer Korrekturen recht hoch. Ich versuche weiterhin bis auf die oben angesprochenen Werte nur Sondersituationen zu nutzen.
Das wars diese Woche von den deutschen Biotechwerten. Ich wünsch euch viel Glück mit euren Aktien
Antwort auf Beitrag Nr.: 58.305.380 von BICYPAPA am 26.07.18 09:15:05
CytoTools AG meldet erfolgreiche Freigabe der Studienmedikation in Europa und Start der Behandlung der ersten Patienten in der klinischen Studie zur Therapie des diabetischen Fußes.
Qualität der in Indien hergestellten Studienmedikamente durch unabhängiges deutsches Prüflabor bestätigt
Patienten-Rekrutierung läuft
Erste Ergebnisse im Rahmen einer Zwischenauswertung Anfang 2019 erwartet
Darmstadt, den 27.07.2018: Nachdem ein unabhängiges deutsches Prüflabor die Qualität und Übereinstimmung mit den Spezifikationen der in Indien hergestellten Studienmedikamente bestätigt und zur Behandlung am Patienten freigegeben hat, wurde mit der Belieferung der Prüfzentren und Krankenhäuser begonnen. Dementgegen läuft die Auswahl geeigneter Patienten bereits seit einigen Wochen, so dass die Behandlung einer größeren Zahl an Patienten unmittelbar erfolgen kann.
Insgesamt werden in dieser klinischen Studie europaweit 200 Patienten an renommierten Kliniken behandelt, um die optimale Dosis der Behandlung mit DermaPro(R) festzulegen und die Wirksamkeit nachzuweisen. Damit wird unter anderem den Forderungen der amerikanischen Behörden entsprochen, die diese Art der Untersuchung für eine Zulassung im amerikanischen Markt fordern. Erste aussagekräftige Ergebnisse werden im Rahmen einer Zwischenauswertung für das vierte Quartal 2018 bzw. erste Quartal 2019 erwartet.
Chronische und schlecht heilende Wunden an den Beinen und Füßen, wie sie insbesondere in Folge von Diabetes auftreten, stellen weltweit ein immer größeres, sehr ernst zu nehmendes medizinisches Problem dar. Untersuchungen der "International Diabetes Federation" zufolge hat die Gesamtanzahl an Diabetikern im Jahr 2016 weltweit die Marke von 420 Millionen überschritten. Allein in Deutschland leben weit über 5 Millionen Diabetiker. Bis zu 20 % aller Diabetiker entwickeln aufgrund von Durchblutungsstörungen und Gefäßverengungen einen diabetischen Fuß, der nicht selten zu Amputationen führt. In den vorangegangen Studien in Indien und Deutschland hat die Behandlung mit DermaPro(R) außerordentliche Erfolge verzeichnen können und stellt einen Durchbruch bei der Behandlung des diabetischen Fußes dar.
Cytotools Studienstart Europa
Ich poste die Meldungen zu Cytotools hier im DBI Thread. Einfach aus dem Grund, weil die Threads zu Cytotools schon jahrelang durch Trolle und Basher verseucht sind. Der einzige Grund ist Cytotools mit diesen Beiträgen zu diskreditieren. Ich versuche hier ein kleines Gegengewicht zu schaffen und poste die aktuellen Meldungen und Neuigkeiten parallel, damit eine sinnvolle Diskussion stattfinden kann.CytoTools AG meldet erfolgreiche Freigabe der Studienmedikation in Europa und Start der Behandlung der ersten Patienten in der klinischen Studie zur Therapie des diabetischen Fußes.
Qualität der in Indien hergestellten Studienmedikamente durch unabhängiges deutsches Prüflabor bestätigt
Patienten-Rekrutierung läuft
Erste Ergebnisse im Rahmen einer Zwischenauswertung Anfang 2019 erwartet
Darmstadt, den 27.07.2018: Nachdem ein unabhängiges deutsches Prüflabor die Qualität und Übereinstimmung mit den Spezifikationen der in Indien hergestellten Studienmedikamente bestätigt und zur Behandlung am Patienten freigegeben hat, wurde mit der Belieferung der Prüfzentren und Krankenhäuser begonnen. Dementgegen läuft die Auswahl geeigneter Patienten bereits seit einigen Wochen, so dass die Behandlung einer größeren Zahl an Patienten unmittelbar erfolgen kann.
Insgesamt werden in dieser klinischen Studie europaweit 200 Patienten an renommierten Kliniken behandelt, um die optimale Dosis der Behandlung mit DermaPro(R) festzulegen und die Wirksamkeit nachzuweisen. Damit wird unter anderem den Forderungen der amerikanischen Behörden entsprochen, die diese Art der Untersuchung für eine Zulassung im amerikanischen Markt fordern. Erste aussagekräftige Ergebnisse werden im Rahmen einer Zwischenauswertung für das vierte Quartal 2018 bzw. erste Quartal 2019 erwartet.
Chronische und schlecht heilende Wunden an den Beinen und Füßen, wie sie insbesondere in Folge von Diabetes auftreten, stellen weltweit ein immer größeres, sehr ernst zu nehmendes medizinisches Problem dar. Untersuchungen der "International Diabetes Federation" zufolge hat die Gesamtanzahl an Diabetikern im Jahr 2016 weltweit die Marke von 420 Millionen überschritten. Allein in Deutschland leben weit über 5 Millionen Diabetiker. Bis zu 20 % aller Diabetiker entwickeln aufgrund von Durchblutungsstörungen und Gefäßverengungen einen diabetischen Fuß, der nicht selten zu Amputationen führt. In den vorangegangen Studien in Indien und Deutschland hat die Behandlung mit DermaPro(R) außerordentliche Erfolge verzeichnen können und stellt einen Durchbruch bei der Behandlung des diabetischen Fußes dar.
Antwort auf Beitrag Nr.: 58.304.744 von BICYPAPA am 26.07.18 08:27:37
DGAP-News: CytoTools AG / Schlagwort(e): Sonstiges
Die CytoTools AG wird durch gezielte Investitionen in neue Therapiefelder
bald weitere klinische Entwicklungsprogramme starten
25.07.2018 / 11:00
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber verantwortlich.
Die CytoTools AG wird durch gezielte Investitionen in neue Therapiefelder
bald weitere klinische Entwicklungsprogramme starten
Darmstadt, den 25. Juli 2018 - Nachdem die CytoTools AG (WKN: A0KFRJ; ISIN:
DE000A0KFRJ1) gestern die Ausgabe einer weiteren Wandelanleihe im
Gesamtnennbetrag von bis zu EUR 2.500.000,00 angekündigt hat, werden nun
erste Einzelheiten zur Mittelverwendung des erwarteten Emissionserlöses
genannt. Demnach plant der Vorstand gezielte Investitionen, um das
Geschäftsmodell durch weitere Produkte und Anwendungsbereiche zu erweitern.
Sollte diese Kapitalmaßnahme wie erwartet erfolgreich platziert werden,
unterstreicht das zudem ein hohes Vertrauen von Investoren in das
Unternehmen, nachdem zuletzt am 07. Juni die Ausgabe einer Wandelanleihe in
Höhe von nominell 2,1 Mio. EUR realisiert wurde.
Die Investitionen sollen insbesondere die Tochtergesellschaft CytoPharma
GmbH in die Lage versetzen, erste klinische Versuchsreihen durchzuführen.
Der Schwerpunkt der Gesellschaft im Bereich der Forschung & Entwicklung
liegt bislang auf Wirkstoffen zur Therapie von Gefäßverschlusskrankheiten
(Carotis-Stenosen, Ateriosklerose und Restenose) und zum selektiven Abtöten
von Krebszellen. In der Indikation Onkologie werden nach Erfolgen im Labor
noch in diesem Jahr erste Tiermodellversuche gestartet, die eine
Voraussetzung für erste klinische Phasen sind. Weiterhin wurde ein neues
Projekt mit dem bekannten Wirkstoff Dichlorsäure in der Indikation Sepsis
gestartet. Hier wird nach ersten guten Ergebnissen im Herbst eine große
Tiermodelltestreihe initiiert, die bei weiteren Erfolgen im nächsten Jahr in
die klinische Entwicklung übergehen könnte.
Damit wird die CytoTools AG mittelfristig gezielt von einer dermatologisch
geprägten Biotechfirma zu einer Firma im Pharma-Research / Development mit
vielseitigen Indikationen und Wirkstofffeldern weiter entwickelt.
Kapitalmaßnahme Cytotools
Die CytoTools AG wird durch gezielte Investitionen in neue Therapiefelder bald weitere klinische Entwicklungsprogramme startenDGAP-News: CytoTools AG / Schlagwort(e): Sonstiges
Die CytoTools AG wird durch gezielte Investitionen in neue Therapiefelder
bald weitere klinische Entwicklungsprogramme starten
25.07.2018 / 11:00
Für den Inhalt der Mitteilung ist der Emittent / Herausgeber verantwortlich.
Die CytoTools AG wird durch gezielte Investitionen in neue Therapiefelder
bald weitere klinische Entwicklungsprogramme starten
Darmstadt, den 25. Juli 2018 - Nachdem die CytoTools AG (WKN: A0KFRJ; ISIN:
DE000A0KFRJ1) gestern die Ausgabe einer weiteren Wandelanleihe im
Gesamtnennbetrag von bis zu EUR 2.500.000,00 angekündigt hat, werden nun
erste Einzelheiten zur Mittelverwendung des erwarteten Emissionserlöses
genannt. Demnach plant der Vorstand gezielte Investitionen, um das
Geschäftsmodell durch weitere Produkte und Anwendungsbereiche zu erweitern.
Sollte diese Kapitalmaßnahme wie erwartet erfolgreich platziert werden,
unterstreicht das zudem ein hohes Vertrauen von Investoren in das
Unternehmen, nachdem zuletzt am 07. Juni die Ausgabe einer Wandelanleihe in
Höhe von nominell 2,1 Mio. EUR realisiert wurde.
Die Investitionen sollen insbesondere die Tochtergesellschaft CytoPharma
GmbH in die Lage versetzen, erste klinische Versuchsreihen durchzuführen.
Der Schwerpunkt der Gesellschaft im Bereich der Forschung & Entwicklung
liegt bislang auf Wirkstoffen zur Therapie von Gefäßverschlusskrankheiten
(Carotis-Stenosen, Ateriosklerose und Restenose) und zum selektiven Abtöten
von Krebszellen. In der Indikation Onkologie werden nach Erfolgen im Labor
noch in diesem Jahr erste Tiermodellversuche gestartet, die eine
Voraussetzung für erste klinische Phasen sind. Weiterhin wurde ein neues
Projekt mit dem bekannten Wirkstoff Dichlorsäure in der Indikation Sepsis
gestartet. Hier wird nach ersten guten Ergebnissen im Herbst eine große
Tiermodelltestreihe initiiert, die bei weiteren Erfolgen im nächsten Jahr in
die klinische Entwicklung übergehen könnte.
Damit wird die CytoTools AG mittelfristig gezielt von einer dermatologisch
geprägten Biotechfirma zu einer Firma im Pharma-Research / Development mit
vielseitigen Indikationen und Wirkstofffeldern weiter entwickelt.
Antwort auf Beitrag Nr.: 58.285.499 von BICYPAPA am 24.07.18 10:19:07
Vollständiges Antwortschreiben der FDA in Bezug auf Methylene Blue MMX NDA erhalten. Der Zulassungsantrag (NDA) in vorliegender Form wurde nicht gewährt. Ein Type A Treffen mit der FDA fand am 25. Juli 2018 statt, das Ergebnis wird mitgeteilt, sobald es verfügbar ist.
https://www.finanznachrichten.de/nachrichten-2018-07/4437553…
Paion Cosmo
Cosmo hat gestern das Treffen mit der FDA gehabt. Jetzt ist Warten auf den Brief angesagt.Vollständiges Antwortschreiben der FDA in Bezug auf Methylene Blue MMX NDA erhalten. Der Zulassungsantrag (NDA) in vorliegender Form wurde nicht gewährt. Ein Type A Treffen mit der FDA fand am 25. Juli 2018 statt, das Ergebnis wird mitgeteilt, sobald es verfügbar ist.
https://www.finanznachrichten.de/nachrichten-2018-07/4437553…
Antwort auf Beitrag Nr.: 58.279.091 von BICYPAPA am 23.07.18 15:52:36
- Multizentrische, randomisierte und aktiv kontrollierte EU-Phase-III-Studie
mit ungefähr 500 Patienten im Rahmen einer geplanten Operation
- Untersuchung der Wirksamkeit und Sicherheit, inklusive hämodynamischer
Stabilität, von Remimazolam im Vergleich zu Propofol bei Allgemeinanästhesie
- Abschluss der Patientenrekrutierung 2019 erwartet
Aachen, 24. Juli 2018 - Das Specialty-Pharma-Unternehmen PAION AG (ISIN
DE000A0B65S3; Frankfurter Wertpapierbörse, Prime Standard: PA8) gibt heute
den Start einer klinischen Phase-III-Studie in der EU mit dem ultra-
kurzwirksamen Benzodiazepin-Sedativum/-Anästhetikum Remimazolam für die
Einleitung und Aufrechterhaltung einer Allgemeinanästhesie bekannt.
Die randomisierte, einfach-blinde, Propofol-kontrollierte, konfirmatorische
Phase-III-Studie wird ungefähr 500 ASA-III/IV-Patienten (American Society of
Anesthesiologists-Klassifizierung III-IV), die sich keiner Notfalloperation
unterziehen, in mehr als 20 europäischen Studienzentren einschließen. Der
Abschluss der Patientenrekrutierung wird 2019 erwartet.
Das primäre Studienziel besteht darin, zu zeigen, dass Remimazolam in seiner
Wirksamkeit zur Einleitung und Aufrechterhaltung einer Allgemeinanästhesie
während einer geplanten Operation im Vergleich zu Propofol nicht unterlegen
ist ("Non-Inferiority"). Das sekundäre Hauptziel ist es, eine überlegene
hämodynamische Stabilität (Vermeidung intraoperativen Blutdruckabfalls sowie
der Notwendigkeit der Verabreichung blutdrucksteigernder Mittel) von
Remimazolam im Vergleich zu Propofol zu zeigen.
Die Studie wurde in Absprache mit führenden europäischen Meinungsbildnern in
der Allgemeinanästhesie entwickelt. Auf Basis der im Januar 2018 erfolgten
wissenschaftlichen Konsultation mit der europäischen Zulassungsbehörde EMA
(European Medicines Agency) geht PAION davon aus, dass eine positive
Phase-III-Studie zusammen mit den früheren schon in Europa und Japan
durchgeführten klinischen Studien für die Einreichung eines
Zulassungsantrags in der Indikation Allgemeinanästhesie in der EU
ausreichend sein sollte.
Dr. Wolfgang Söhngen, Vorstandsvorsitzender der PAION AG, kommentierte: "Der
Beginn dieser Phase-III-Studie ist ein wichtiger Meilenstein für PAION. Die
alternde Bevölkerung führt zu einer steigenden Anzahl medizinischer
Eingriffe mit erhöhter Komplexität. Es ist inzwischen anerkannt, dass
ausgeprägt niedrige Blutdruckwerte während einer Allgemeinanästhesie häufig
vorkommen und zu bedeutsamen Folgeerkrankungen beitragen. Wenn die
Phase-III-Studie das gute hämodynamische Profil von Remimazolam bestätigt,
könnte es Anästhesisten zukünftig eine sicherere therapeutische Alternative
bieten und die Lebensqualität von Patienten und deren Familien nach einem
Eingriff deutlich verbessern. Dies könnte auch zu einer erheblichen
Kosteneinsparung beitragen."
Über Remimazolam
Remimazolam ist ein ultrakurz wirksames intravenöses Benzodiazepin-Sedativum
und -Anästhetikum, das bereits positive Ergebnisse in klinischen
Phase-III-Studien gezeigt hat. Im menschlichen Körper wird Remimazolam von
Gewebe-Esterasen, einer weit verbreiteten Art von Enzymen, zu einem
inaktiven Metaboliten abgebaut und nicht über cytochromabhängige Abbauwege
in der Leber. Wie bei anderen Benzodiazepinen steht mit Flumazenil ein
Gegenmittel zur Verfügung, um bei Bedarf die Sedierung und Narkose des
Patienten wieder rasch beenden zu können. Wirksamkeit und Sicherheit wurden
in klinischen Studien bei über 1.700 Probanden und Patienten gezeigt. Die
bisherigen Daten deuten darauf hin, dass Remimazolam einen raschen
Wirkeintritt und ein schnelles Abklingen der Wirkung hat und dabei ein
günstiges kardiorespiratorisches Sicherheitsprofil besitzt.
PAION hat die klinische Entwicklung von Remimazolam für Kurzsedierungen in
den USA abgeschlossen. Derzeit läuft eine integrierte Gesamtanalyse aller
klinischen Studien mit Remimazolam in Vorbereitung auf die Einreichung des
Zulassungsantrags durch Cosmo. Nach Abschluss der Entwicklung für
Kurzsedierungen liegen alle weiteren Entwicklungsarbeiten in den USA in der
Verantwortung von Cosmo. Der US-amerikanische Lizenzpartner plant die
Einreichung des Zulassungsantrags in der Indikation Kurzsedierung aktuell im
vierten Quartal 2018/ersten Quartal 2019. In Japan wurde ein vollständiges
klinisches Entwicklungsprogramm in der Allgemeinanästhesie abgeschlossen,
und der dortige Remimazolam-Lizenzpartner Mundipharma beabsichtigt die
Einreichung des Zulassungsantrags für Remimazolam in dieser Indikation in
Japan in 2018. In Europa wurde eine Phase-III-Studie in der
Allgemeinanästhesie im Juli 2018 gestartet, von der nach der bei der EMA im
Januar 2018 erfolgten wissenschaftlichen Konsultation (sog. "Scientific
Advice") erwartet werden kann, dass sie die einzige noch für den
Zulassungsantrag in der EU benötigte Studie sein wird.
Basierend auf den positiven Ergebnissen einer Phase-II-Studie ist die
Sedierung auf der Intensivstation (für mehr als 24 Stunden nach der
Operation) eine weitere mögliche attraktive Indikation für eine
Weiterentwicklung in Europa durch PAION selbst und in den verpartnerten
Territorien durch die Lizenznehmer.
Paion Studienstart Europa
PAION STARTET EU-PHASE-III-STUDIE MIT REMIMAZOLAM IN DER ALLGEMEINANÄSTHESIE- Multizentrische, randomisierte und aktiv kontrollierte EU-Phase-III-Studie
mit ungefähr 500 Patienten im Rahmen einer geplanten Operation
- Untersuchung der Wirksamkeit und Sicherheit, inklusive hämodynamischer
Stabilität, von Remimazolam im Vergleich zu Propofol bei Allgemeinanästhesie
- Abschluss der Patientenrekrutierung 2019 erwartet
Aachen, 24. Juli 2018 - Das Specialty-Pharma-Unternehmen PAION AG (ISIN
DE000A0B65S3; Frankfurter Wertpapierbörse, Prime Standard: PA8) gibt heute
den Start einer klinischen Phase-III-Studie in der EU mit dem ultra-
kurzwirksamen Benzodiazepin-Sedativum/-Anästhetikum Remimazolam für die
Einleitung und Aufrechterhaltung einer Allgemeinanästhesie bekannt.
Die randomisierte, einfach-blinde, Propofol-kontrollierte, konfirmatorische
Phase-III-Studie wird ungefähr 500 ASA-III/IV-Patienten (American Society of
Anesthesiologists-Klassifizierung III-IV), die sich keiner Notfalloperation
unterziehen, in mehr als 20 europäischen Studienzentren einschließen. Der
Abschluss der Patientenrekrutierung wird 2019 erwartet.
Das primäre Studienziel besteht darin, zu zeigen, dass Remimazolam in seiner
Wirksamkeit zur Einleitung und Aufrechterhaltung einer Allgemeinanästhesie
während einer geplanten Operation im Vergleich zu Propofol nicht unterlegen
ist ("Non-Inferiority"). Das sekundäre Hauptziel ist es, eine überlegene
hämodynamische Stabilität (Vermeidung intraoperativen Blutdruckabfalls sowie
der Notwendigkeit der Verabreichung blutdrucksteigernder Mittel) von
Remimazolam im Vergleich zu Propofol zu zeigen.
Die Studie wurde in Absprache mit führenden europäischen Meinungsbildnern in
der Allgemeinanästhesie entwickelt. Auf Basis der im Januar 2018 erfolgten
wissenschaftlichen Konsultation mit der europäischen Zulassungsbehörde EMA
(European Medicines Agency) geht PAION davon aus, dass eine positive
Phase-III-Studie zusammen mit den früheren schon in Europa und Japan
durchgeführten klinischen Studien für die Einreichung eines
Zulassungsantrags in der Indikation Allgemeinanästhesie in der EU
ausreichend sein sollte.
Dr. Wolfgang Söhngen, Vorstandsvorsitzender der PAION AG, kommentierte: "Der
Beginn dieser Phase-III-Studie ist ein wichtiger Meilenstein für PAION. Die
alternde Bevölkerung führt zu einer steigenden Anzahl medizinischer
Eingriffe mit erhöhter Komplexität. Es ist inzwischen anerkannt, dass
ausgeprägt niedrige Blutdruckwerte während einer Allgemeinanästhesie häufig
vorkommen und zu bedeutsamen Folgeerkrankungen beitragen. Wenn die
Phase-III-Studie das gute hämodynamische Profil von Remimazolam bestätigt,
könnte es Anästhesisten zukünftig eine sicherere therapeutische Alternative
bieten und die Lebensqualität von Patienten und deren Familien nach einem
Eingriff deutlich verbessern. Dies könnte auch zu einer erheblichen
Kosteneinsparung beitragen."
Über Remimazolam
Remimazolam ist ein ultrakurz wirksames intravenöses Benzodiazepin-Sedativum
und -Anästhetikum, das bereits positive Ergebnisse in klinischen
Phase-III-Studien gezeigt hat. Im menschlichen Körper wird Remimazolam von
Gewebe-Esterasen, einer weit verbreiteten Art von Enzymen, zu einem
inaktiven Metaboliten abgebaut und nicht über cytochromabhängige Abbauwege
in der Leber. Wie bei anderen Benzodiazepinen steht mit Flumazenil ein
Gegenmittel zur Verfügung, um bei Bedarf die Sedierung und Narkose des
Patienten wieder rasch beenden zu können. Wirksamkeit und Sicherheit wurden
in klinischen Studien bei über 1.700 Probanden und Patienten gezeigt. Die
bisherigen Daten deuten darauf hin, dass Remimazolam einen raschen
Wirkeintritt und ein schnelles Abklingen der Wirkung hat und dabei ein
günstiges kardiorespiratorisches Sicherheitsprofil besitzt.
PAION hat die klinische Entwicklung von Remimazolam für Kurzsedierungen in
den USA abgeschlossen. Derzeit läuft eine integrierte Gesamtanalyse aller
klinischen Studien mit Remimazolam in Vorbereitung auf die Einreichung des
Zulassungsantrags durch Cosmo. Nach Abschluss der Entwicklung für
Kurzsedierungen liegen alle weiteren Entwicklungsarbeiten in den USA in der
Verantwortung von Cosmo. Der US-amerikanische Lizenzpartner plant die
Einreichung des Zulassungsantrags in der Indikation Kurzsedierung aktuell im
vierten Quartal 2018/ersten Quartal 2019. In Japan wurde ein vollständiges
klinisches Entwicklungsprogramm in der Allgemeinanästhesie abgeschlossen,
und der dortige Remimazolam-Lizenzpartner Mundipharma beabsichtigt die
Einreichung des Zulassungsantrags für Remimazolam in dieser Indikation in
Japan in 2018. In Europa wurde eine Phase-III-Studie in der
Allgemeinanästhesie im Juli 2018 gestartet, von der nach der bei der EMA im
Januar 2018 erfolgten wissenschaftlichen Konsultation (sog. "Scientific
Advice") erwartet werden kann, dass sie die einzige noch für den
Zulassungsantrag in der EU benötigte Studie sein wird.
Basierend auf den positiven Ergebnissen einer Phase-II-Studie ist die
Sedierung auf der Intensivstation (für mehr als 24 Stunden nach der
Operation) eine weitere mögliche attraktive Indikation für eine
Weiterentwicklung in Europa durch PAION selbst und in den verpartnerten
Territorien durch die Lizenznehmer.
Antwort auf Beitrag Nr.: 58.265.891 von BICYPAPA am 20.07.18 20:55:57
Dabei ist die Aktie noch mit knapp 4% geshortet. Durch die Dynamik, die im Augenblick vorherrscht und den erwarteten guten Newsflow können wir hier dann wohl von einer Grillfete ausgehen. Charttechnisch sind alle Hürden weggeräumt.
Grillfete bei Evotec
Evotec hat in den letzten ca 3 Wochen drei wichtige Widerstände durchbrochen. Der Grund sind einige gute Nachrichten in Folge und erwartete gute Quartalszahlen. Außerdem wird über eine Notierung im M-DAX spekuliert.Dabei ist die Aktie noch mit knapp 4% geshortet. Durch die Dynamik, die im Augenblick vorherrscht und den erwarteten guten Newsflow können wir hier dann wohl von einer Grillfete ausgehen. Charttechnisch sind alle Hürden weggeräumt.
schau dir die präsi des vorstandes an von der letzten hv
die perspektiven sind da deutlich dargelegt.
zu dem streit
wir haben den vorstand und maruho den japanischen partner in der forschung (hält ca 22% der aktien)
gegenseite ist balaton / zours und die heidelberger clique (zusammen ca 15%)
die gegenseite versucht mit allen mögliche mitteln aktien vom streubesitz zu ergaunern, denen sind alle mittel recht... denn sie wissen um das potential dieser firma.
biofrontera hat in den usa ihren ärgsten konkurenten verklagt auf unlauteren wettbewerb. es gibt aber auch eine gegenklage gegen zwei patente an der lampe (sehe ich nicht so wild)
die klage von biofrontera beanstanded das verkaufssystem von dusa (schlechteres produkt und deutlich teurer aber sehr große rabatte an die ärzte)
sollte diese klage von biofrontera gegen dusa durchkommen, dann ist dusa am arsch aber richtig und biofrontera wäre der neue platzhirsch...
von analysten wird der breakeven für ende 2019 angepeilt... wenn wirklich alles gut geht dann könnte das wirklich klappen vlt sogar schon eher, wenn die klagen fruchten
aktuell läuft auch eine klage in den usa gegen balaton und ihre clique, das wird auch nochmal spannnend.
die perspektiven sind da deutlich dargelegt.
zu dem streit
wir haben den vorstand und maruho den japanischen partner in der forschung (hält ca 22% der aktien)
gegenseite ist balaton / zours und die heidelberger clique (zusammen ca 15%)
die gegenseite versucht mit allen mögliche mitteln aktien vom streubesitz zu ergaunern, denen sind alle mittel recht... denn sie wissen um das potential dieser firma.
biofrontera hat in den usa ihren ärgsten konkurenten verklagt auf unlauteren wettbewerb. es gibt aber auch eine gegenklage gegen zwei patente an der lampe (sehe ich nicht so wild)
die klage von biofrontera beanstanded das verkaufssystem von dusa (schlechteres produkt und deutlich teurer aber sehr große rabatte an die ärzte)
sollte diese klage von biofrontera gegen dusa durchkommen, dann ist dusa am arsch aber richtig und biofrontera wäre der neue platzhirsch...
von analysten wird der breakeven für ende 2019 angepeilt... wenn wirklich alles gut geht dann könnte das wirklich klappen vlt sogar schon eher, wenn die klagen fruchten
aktuell läuft auch eine klage in den usa gegen balaton und ihre clique, das wird auch nochmal spannnend.
Antwort auf Beitrag Nr.: 58.265.921 von walle1fc am 20.07.18 20:57:52
Habe ich leider..
Habe ich leider nicht in der engeren Auswahl. Die Situation mit der Streiterei war für mich nicht durchschaubar. Da hab ich dann die Finger davon gelassen. Wenn du magst, schreib du was dazu. Wahrscheinlich bist du auch besser informiert. 




















