Biotech Depot - verschiede Werte und Strategien - 500 Beiträge pro Seite (Seite 3)
eröffnet am 06.04.12 20:55:15 von
neuester Beitrag 15.12.21 20:44:42 von
neuester Beitrag 15.12.21 20:44:42 von
Beiträge: 2.765
ID: 1.173.523
ID: 1.173.523
Aufrufe heute: 2
Gesamt: 306.559
Gesamt: 306.559
Aktive User: 0
Top-Diskussionen
| Titel | letzter Beitrag | Aufrufe |
|---|---|---|
| vor 5 Minuten | 2145 | |
| heute 14:00 | 1601 | |
| vor 42 Minuten | 1382 | |
| vor 6 Minuten | 1304 | |
| vor 11 Minuten | 1191 | |
| gestern 18:31 | 1019 | |
| vor 18 Minuten | 909 | |
| vor 8 Minuten | 857 |
Meistdiskutierte Wertpapiere
| Platz | vorher | Wertpapier | Kurs | Perf. % | Anzahl | ||
|---|---|---|---|---|---|---|---|
| 1. | 1. | 18.161,01 | +1,36 | 217 | |||
| 2. | 3. | 0,1885 | -0,26 | 90 | |||
| 3. | 2. | 1,1800 | -14,49 | 77 | |||
| 4. | 5. | 9,3500 | +1,14 | 60 | |||
| 5. | 4. | 168,29 | -1,11 | 50 | |||
| 6. | Neu! | 0,4400 | +3,53 | 36 | |||
| 7. | Neu! | 4,7950 | +6,91 | 34 | |||
| 8. | Neu! | 11,905 | +14,97 | 31 |
Antwort auf Beitrag Nr.: 48.453.840 von SLGramann am 30.11.14 11:58:11Sehr wichtig und mir noch recht unklar ist sicher das Verhältnis Entinostat zu Palbociclib.
Die überragenden Daten von Palbo bezogen sich ja auf die first-line-Therapie, während Entinostat wohl in einem späteren Behandlungszeitpunkt eingesetzt wird...
Aber grundsätzlich gefragt: Sind Palbociclib und Entinostat sich ausschließend konkurrierend, sich ergänzend oder vielleicht gar sich kombinierend zu betrachten?
http://www.cancernetwork.com/oncology-journal/postmenopausal…
Die überragenden Daten von Palbo bezogen sich ja auf die first-line-Therapie, während Entinostat wohl in einem späteren Behandlungszeitpunkt eingesetzt wird...
Aber grundsätzlich gefragt: Sind Palbociclib und Entinostat sich ausschließend konkurrierend, sich ergänzend oder vielleicht gar sich kombinierend zu betrachten?
http://www.cancernetwork.com/oncology-journal/postmenopausal…
Hallo SLGramann,
danke für den Hinweis auf Syndax... hört sich interessant an! Ich finde HDAC-Hemmer in Bezug auf IO sehr spannend...
http://www.obroncology.com/blog/2013/04/aacr-2013-post-view-…
...Immunotherapy: When the Body Cures the Body
...Dr. Topalian, the lead author of the 2012 NEJM article, discussed the biology of the PD-1/PD-L1 axis and the differences between it and the CTLA-4 axis, the target of Yervoy. ... What most impressed us, and immediately caused us to crystallize the impact on patients of Dr. Topalian’s data, was the slide she showed on the durability of response of three patients who has ceased treatment with nivolumab. Dr. Topalian provided vignettes of three patients-one with colorectal cancer (CRC), one with renal (kidney) cancer (RCC), and one with melanoma-showing that patients can remain in complete or partial response 4-5 years into their therapy. The patient with CRC remains in complete response just short of four years into follow up after stopping treatment shy of one year. The RCC patient received therapy for approximately six months had a partial response (PR) as best response shortly thereafter, then went on to produce a complete response (CR) at roughly 3.5 years, and at nearly 4.5 years remains in CR. Finally, Dr. Topalian’s example of the melanoma patient was a bit more complicated. The patient achieved a PR just shy of two years on therapy, was diagnosed with a new metastasis just over three years after diagnosis, was retreated to a PR at year four, and was still in PR at roughly 4.5 years...
... Perhaps most exciting was the slide shown by Dr. Topalian that described a patient with squamous non-small cell lung cancer, a tumor type that is widely thought to be non-immunogenic. This particular patient responded to anti-PD-1 antibody therapy after an immediately previous treatment with epigenetic therapy of 5-azacitidine (Vidaza, CELG, MO) and entinostat (Syndax, private, NC), an inhibitor of HDAC 6 (Entinostat ist allerdings ein HDAC1+3-Hemmer!?). Dr. Topalian indicated that this patient has recently completed two years of anti-PD-1 therapy. Moreover, Dr. Topalian indicated that there are five more patients like the one in the example she cited who have achieved durable responses after prior treatment with epigenetic therapy. While the number of patients is small, the 100% response rate in this population is impressive...
...Session on Epigenetics Packs the House
...Peter Laird of the USC Epigenome Center in Los Angeles led the speaker’s roster and provided a fascinating discussion of how the epigenetic signature of cancer cells is vastly different than that of normal cells in terms of both the number of genes silenced as well as turned on (or “de-silenced”). Dr. Laird showed that there is massive (“focal”) hypermethylation at CpG islands (the start sites for gene transcription) across a wide variety of tumor types. These regions of hypermethylation are in areas of gene expression that would normally be associated with genes that would either prevent the outbreak of cancer or provide signals to the cancer cell that would normally tell cancer cells to die... During the same talk, James “Jay” Bradner from the Dana-Farber Cancer Center gave an outstanding talk (though similar to the one we had seen at ASH 2012) about his work on the probe molecule, JQ-1, and its role in the regulation of the MYC gene, one of the most commonly over-expressed genes in all of cancer (behind only p53). JQ-1 (and presumably chemical matter from privately-held Constellation Pharmaceuticals) blocks a key regulator of MYC activation, bromodomain 4 (brd4), a key regulator of MYC gene transcription. Dr. Bradner’s slides showed the pattern of benefit that is now becoming familiar to those of us groupies of epigenetics-that of a flat-line pattern of tumor growth (better yet, death). Dr. Bradner showed some amazing CT scans of a patient with KRAS-mutated lung cancer who experienced a near-total regression of a massive tumor. ... Again, the shape of Dr. Copeland’s Kaplan Meier curves was virtually identical to those of the other speakers-flat-to-downward sloping, rather than right-shifted as has been seen with so many other interventional therapies in oncology. We will be producing a fuller report on the epigenetics space in the near-term.
Early Signs that Epigenetics Holds the Keys to Immunotherapy & Vice Versa
In addition to the separate plenary sessions on immunotherapy and epigenetics, we noted several poster presentations that hinted strongly at the ability to boost anti-tumor immune responses through the epigenetic reprogramming, primarily through the use of hypothmethylating agents. Some of these presentations were in prior notes by us relation to Astex (ASTX, MO) in which tumor specific antigen expression, namely of NY-ESO1 and MAGE-A, in peripheral blood mononuclear cells (PBMCs) was found to increase in response to global gene demethylation in AML/MDS patients treated with SGI-110. In a separate poster, Dacogen induced demethylation in AML cell lines correlated with increased NY-ESO1 and MAGE-A protein expression, further supporting the likelihood that T cell activation plays a role in the mediation of tumor responses by hypomethylating agents (HMAs). Future experiments from Griffiths et al. will measure if tumor antigen specific CD4+/CD8+ T cell responses are in fact elicited by HMA therapy. Meanwhile, a forthcoming prospective study will test the hypothesis in vivo, assessing the combined effect of Dacogen plus the NY-ESO1 vaccine CDX-1401 (CLDX, NC) in patients with AML/MDS. One has to take the good with the bad when it comes to HMA induced gene expression, however. This was evidenced in part in a poster presented by Edward Kadel et al of Genentech (Roche, NC) showing that differential expression of PD-L1 mRNA in NSCLC cell lines was regulated by the level of the promoter by DNA methylation. Induction of PD-L1 expression was most responsive to treatment with Dacogen in cell lines where baseline methylation was high and gene expression low. One initial interpretation of these data might be that DNA demethylation and immune checkpoint activation are antagonistic and that without PD-1/PD-L1 blockade, HMA activity is actually undermined by immnosuppressive mechanisms. Such was the conclusion reached by Garcia-Manero et al in a poster presented at last ASH last December in which the expression of PD-1, PD-L1, PD-L2 and CTLA4 were all induced in the PBMCs of AML/MDS patients treated with low dose Dacogen, or Vidaza in combination with Revlimid (CELG) or vorinostat. On the other hand, it is possible that the induction of PD-L1 expression though HMA exposure acts as primer or homing mechanism for activated T cells. Recall in relation to the plenary talk by Dr. Topalian that tumors responding to nivolumab exhibited relatively higher levels of PD-L1 expression compared with non-responders. Taken together, we believe that future clinical studies of epigenetic therapy used combination with PD-1/PD-L1 antibodies (given perhaps in sequence) will indeed show these regimens to be synergistic in their activities...
***
Soweit ich es verstehe, spielt die Epigenetik bei Krebs eine größere Rolle. U.a. über die Methylisierung der DNA werden Gene abgeschaltet bzw. stumm geschaltet, die den Krebs ansonsten behindern würden... z.B. Gene, die bei entarteten Krebszellen den Zelltod aktivieren würden. Ein echter Gendefekt liegt nicht vor, die fehlerhafte Methylisierung kann wieder rückgängig gemacht werden.
http://www.onclive.com/publications/obtn/2013/April-2013/USC…
... As oncologists practicing in an era of “genomic medicine,” when we consider alterations in gene expression, we generally default to DNA mutation as the primary mechanism. Gene expression can also be regulated by epigenetic changes, such as DNA methylation and histone modification. These changes dysregulate gene function without actually altering the underlying DNA sequence. In principle, these modifications are reversible (restoring gene function) and “druggable.” Epigenetic modifications have been strongly implicated in carcinogenesis and maintenance of a malignant clone by silencing key tumor suppressor genes.
...Preclinical studies suggest that combining inhibitors of DNA methyltransferase, such as 5-azacytidine, with inhibitors of histone deacetylase (HDAC), such as entinostat, synergistically induces re-expression of epigenetically silenced tumor suppressor genes
...Also of great interest is testing the concept of epigenetic “priming” as a strategy to sensitize tumors to subsequent therapy.
Bei der Kombination von IO mit epigenetisch wirkenden Mitteln geht es um das Priming... durch epigenetische Wirkstoffe könnten anschließende IO-Mittel sehr viel wirksamer werden. Bisher kommt es ja nur bei einem kleineren Teil von Krebspatienten zur langanhaltenden IO-Wirkung. U.a. mit HDAC-Hemmern, die die Epigenik verändern, könnte sich dieser Anteil steigern lassen.
Was genau Effekt von Entinostat + IO zustande kommt, müsste ich nochmal genauer schauen...
"Studies Support Ongoing Clinical Strategy of Using Syndax's Entinostat as Epigenetic Priming to Immune Therapy
WALTHAM, Mass., July 30, 2014 /PRNewswire/ -- Syndax Pharmaceuticals, Inc. today announced that newly published results demonstrate that in preclinical studies entinostat significantly improved treatment outcomes in mouse tumor models when combined with anti-PD1 and anti-CTLA4 targeted antibodies. The paper from Kim, et al. at The Sidney Kimmel Comprehensive Cancer Center, Johns Hopkins University School of Medicine, titled "Eradication of metastatic mouse cancers resistant to immune checkpoint blockade by suppression of myeloid derived cells" was published in the journal Proceedings of the National Academy of Sciences (PNAS). The study demonstrated that the combination therapy produced 100 percent inhibition of primary tumors and metastases in aggressive mouse colorectal and breast tumor models. The authors also reported an 80 percent cure rate when epigenetic therapy with entinostat and azacitidine was combined with anti-PD1 and anti-CTLA4 antibodies in an aggressive non-immunogenic metastatic breast cancer mouse model.
The mechanism underlying these results, the authors note, is believed to be entinostat's inhibition of myeloid derived suppressor cells (MDSCs) at concentrations which importantly have only modest effects on CD8+ T cells creating the potential for a large therapeutic window in which MDSCs can be depleted while sparing CD8+ T cells."
Ich meine, dass u.a. CSF1R (z.B. letzte Kooperation FPRX + BMS) auch auf MDSCs und TAMs wirkt.
****
(31.05.2013)
Top Prospects from Pipeline Remain Unclear but Plenty of Options. Despite the enthusiasm generated at Celgene's recent investor day, Celgene have not yet firmly established any particular new pipeline asset (beyond apremilast and Abraxane) in the minds of investors. The presentation and Q&A with CFO Jackie Fouse did not alter this perspective although we were (and are) impressed with the company's ability to identify new variations on their original IMiD platform to advance into clinical trials in a variety of different indications. Management highlighted CC-292 with clinical data expected at ASH in December 2013, as well as plans to accelerate timelines for the study of this BTK inhibitor in combination with Revlimid in CLL and NHL. Ms. Fouse noted she was “pretty excited” with the mTOR kinase inhibitor CC-223, which demonstrated broad activity in pre-clinical models, as well as with the potential for epigenetic priming with Vidaza and CC-486 (oral Vidaza). Recall that these two agents are tested in combination with entinostat, an HDAC inhibitor developed by Syndax, in phase I trials in patients with advanced solid tumor. The combination of epigenetic modulators is thought to enable superior anti-tumor efficacy for chemotherapy and immunotherapy.
****
(07.05.2013)
Epigenetic priming with the oral Vidaza follow-on CC-486 shaping up as a new theme with a Phase Ib trial in solid tumors priming with CC-486 on days 1-14 followed by carboplatin or Abraxane with a CC-486 only control (days 1-21). Part 2 of the Phase Ib calls for expansion cohorts in bladed and ovarian (+carboplatin), NSCLC and pancreatic (+Abraxane) and monotherapy (colorectal). Case study data for CC-486 priming with Abraxane was supportive in pancreatic and endometrial cancers. Longer term, plans call for CC-486 +IMiDs in solid tumors. The CTEP trial in metastatic NSCLC will explore synergy of HDAC inhibition with entinostat and CC-486 epigenetic priming (vs Vidaza + entinostat and vs investigators choice). With BMS and SU2C, Celgene will test epigenetic priming with Vidaza + entinostat or CC-486 monotherapy prior to anti-PD-1 therapy with nivolumab. In the more traditional setting of hematologic malignancies, combination work with R-CHOP in DLBCL and T-cell lymphoma and Phase I iNHL trials are being pursued.
****
(28.08.2013)
Syndax Raises $26.6M to Test Resistance-Reversing Cancer Drug, Entinostat; Plans to Begin Phase III in ER+ mBC
Syndax Pharmaceuticals has raised $26.6 million in equity to pay for a late-stage trial of its drug candidate intended to reverse resistance to therapies used for advanced breast cancer.
CEO Arlene Morris said the company is working on epigenetic therapies – which she said “modifies the software of DNA” - to make drugs to which a patient’s cancer has become resistant effective again.
While Syndax’s lead compound, called entinostat, has wide applications in a variety of both solid and liquid cancers, the company is focusing first on metastatic breast cancer. The reason is partly because of the unmet need in that area and the effectiveness entinostat has shown against that type of cancer. Further, Syndax’s former CEO, Joanna Horobin – who last year left to join Verastem – had a significant background in breast cancer.
In a Phase 2 trial, entinostat helped extend both progression-free survival and overall survival when used with exemestane in postmenopausal women with estrogen receptor-positive (ER+) metastatic breast cancer which had become resistant to a non-steroidal aromatase inhibitor. In other words, Morris explained, the drug candidate helped women who were receiving a type of hormone therapy used in breast cancer that has less severe side effects than chemotherapy but had become resistant to it. She said that’s better for the patient than more advanced therapies because hormone therapy is “much better tolerated.”
The company is now planning a Phase 3 study of entinostat in the same types of patients to be sponsored by the National Cancer Institute (NCI). Morris said the company also plans to conduct a study in a certain subset of lung cancer patients in which the candidate showed effectiveness.
****
(11.09.2013)
Syndax: FDA Grants Breakthrough Designation for Entinostat; Phase III Breast Cancer Study Set to Begin in
Early 2014 Syndax Pharmaceuticals announced that it has received the FDA's breakthrough designation (BTD) for a Phase III-ready breast cancer therapy. The biotech won the BTD for entinostat, an experimental histone deacetylase inhibitor (HDACi) set to begin Phase III testing in early 2014 in combination with exemestane in postmenopausal women with metastatic ERpositive breast cancer who have progressed on hormonal therapy.
"We expect it to have some influence on the pathway," CEO Arlene Morris tells FierceBiotech. "Exactly what, we're not sure yet. But we believe it will help gain a higher level of attention (at the FDA). We're also hoping that it will help us enroll the trial faster."
The BTD delivers another piece of a compelling picture for Syndax. The biotech is already working with the National Cancer Institute on its upcoming study. And the Phase II data provided some solid supporting evidence that the drug could reverse resistance to hormone therapy, giving breast cancer patients a reprieve from chemotherapy--the kind of medical need that helped drive the agency to put it on its special oversight track. The FDA has indicated that it's open to allowing Syndax to use Phase II data to support an application, says Morris. And the latest venture round has provided a firm financial footing.
Grüße
ipollit
danke für den Hinweis auf Syndax... hört sich interessant an! Ich finde HDAC-Hemmer in Bezug auf IO sehr spannend...
http://www.obroncology.com/blog/2013/04/aacr-2013-post-view-…
...Immunotherapy: When the Body Cures the Body
...Dr. Topalian, the lead author of the 2012 NEJM article, discussed the biology of the PD-1/PD-L1 axis and the differences between it and the CTLA-4 axis, the target of Yervoy. ... What most impressed us, and immediately caused us to crystallize the impact on patients of Dr. Topalian’s data, was the slide she showed on the durability of response of three patients who has ceased treatment with nivolumab. Dr. Topalian provided vignettes of three patients-one with colorectal cancer (CRC), one with renal (kidney) cancer (RCC), and one with melanoma-showing that patients can remain in complete or partial response 4-5 years into their therapy. The patient with CRC remains in complete response just short of four years into follow up after stopping treatment shy of one year. The RCC patient received therapy for approximately six months had a partial response (PR) as best response shortly thereafter, then went on to produce a complete response (CR) at roughly 3.5 years, and at nearly 4.5 years remains in CR. Finally, Dr. Topalian’s example of the melanoma patient was a bit more complicated. The patient achieved a PR just shy of two years on therapy, was diagnosed with a new metastasis just over three years after diagnosis, was retreated to a PR at year four, and was still in PR at roughly 4.5 years...
... Perhaps most exciting was the slide shown by Dr. Topalian that described a patient with squamous non-small cell lung cancer, a tumor type that is widely thought to be non-immunogenic. This particular patient responded to anti-PD-1 antibody therapy after an immediately previous treatment with epigenetic therapy of 5-azacitidine (Vidaza, CELG, MO) and entinostat (Syndax, private, NC), an inhibitor of HDAC 6 (Entinostat ist allerdings ein HDAC1+3-Hemmer!?). Dr. Topalian indicated that this patient has recently completed two years of anti-PD-1 therapy. Moreover, Dr. Topalian indicated that there are five more patients like the one in the example she cited who have achieved durable responses after prior treatment with epigenetic therapy. While the number of patients is small, the 100% response rate in this population is impressive...
...Session on Epigenetics Packs the House
...Peter Laird of the USC Epigenome Center in Los Angeles led the speaker’s roster and provided a fascinating discussion of how the epigenetic signature of cancer cells is vastly different than that of normal cells in terms of both the number of genes silenced as well as turned on (or “de-silenced”). Dr. Laird showed that there is massive (“focal”) hypermethylation at CpG islands (the start sites for gene transcription) across a wide variety of tumor types. These regions of hypermethylation are in areas of gene expression that would normally be associated with genes that would either prevent the outbreak of cancer or provide signals to the cancer cell that would normally tell cancer cells to die... During the same talk, James “Jay” Bradner from the Dana-Farber Cancer Center gave an outstanding talk (though similar to the one we had seen at ASH 2012) about his work on the probe molecule, JQ-1, and its role in the regulation of the MYC gene, one of the most commonly over-expressed genes in all of cancer (behind only p53). JQ-1 (and presumably chemical matter from privately-held Constellation Pharmaceuticals) blocks a key regulator of MYC activation, bromodomain 4 (brd4), a key regulator of MYC gene transcription. Dr. Bradner’s slides showed the pattern of benefit that is now becoming familiar to those of us groupies of epigenetics-that of a flat-line pattern of tumor growth (better yet, death). Dr. Bradner showed some amazing CT scans of a patient with KRAS-mutated lung cancer who experienced a near-total regression of a massive tumor. ... Again, the shape of Dr. Copeland’s Kaplan Meier curves was virtually identical to those of the other speakers-flat-to-downward sloping, rather than right-shifted as has been seen with so many other interventional therapies in oncology. We will be producing a fuller report on the epigenetics space in the near-term.
Early Signs that Epigenetics Holds the Keys to Immunotherapy & Vice Versa
In addition to the separate plenary sessions on immunotherapy and epigenetics, we noted several poster presentations that hinted strongly at the ability to boost anti-tumor immune responses through the epigenetic reprogramming, primarily through the use of hypothmethylating agents. Some of these presentations were in prior notes by us relation to Astex (ASTX, MO) in which tumor specific antigen expression, namely of NY-ESO1 and MAGE-A, in peripheral blood mononuclear cells (PBMCs) was found to increase in response to global gene demethylation in AML/MDS patients treated with SGI-110. In a separate poster, Dacogen induced demethylation in AML cell lines correlated with increased NY-ESO1 and MAGE-A protein expression, further supporting the likelihood that T cell activation plays a role in the mediation of tumor responses by hypomethylating agents (HMAs). Future experiments from Griffiths et al. will measure if tumor antigen specific CD4+/CD8+ T cell responses are in fact elicited by HMA therapy. Meanwhile, a forthcoming prospective study will test the hypothesis in vivo, assessing the combined effect of Dacogen plus the NY-ESO1 vaccine CDX-1401 (CLDX, NC) in patients with AML/MDS. One has to take the good with the bad when it comes to HMA induced gene expression, however. This was evidenced in part in a poster presented by Edward Kadel et al of Genentech (Roche, NC) showing that differential expression of PD-L1 mRNA in NSCLC cell lines was regulated by the level of the promoter by DNA methylation. Induction of PD-L1 expression was most responsive to treatment with Dacogen in cell lines where baseline methylation was high and gene expression low. One initial interpretation of these data might be that DNA demethylation and immune checkpoint activation are antagonistic and that without PD-1/PD-L1 blockade, HMA activity is actually undermined by immnosuppressive mechanisms. Such was the conclusion reached by Garcia-Manero et al in a poster presented at last ASH last December in which the expression of PD-1, PD-L1, PD-L2 and CTLA4 were all induced in the PBMCs of AML/MDS patients treated with low dose Dacogen, or Vidaza in combination with Revlimid (CELG) or vorinostat. On the other hand, it is possible that the induction of PD-L1 expression though HMA exposure acts as primer or homing mechanism for activated T cells. Recall in relation to the plenary talk by Dr. Topalian that tumors responding to nivolumab exhibited relatively higher levels of PD-L1 expression compared with non-responders. Taken together, we believe that future clinical studies of epigenetic therapy used combination with PD-1/PD-L1 antibodies (given perhaps in sequence) will indeed show these regimens to be synergistic in their activities...
***
Soweit ich es verstehe, spielt die Epigenetik bei Krebs eine größere Rolle. U.a. über die Methylisierung der DNA werden Gene abgeschaltet bzw. stumm geschaltet, die den Krebs ansonsten behindern würden... z.B. Gene, die bei entarteten Krebszellen den Zelltod aktivieren würden. Ein echter Gendefekt liegt nicht vor, die fehlerhafte Methylisierung kann wieder rückgängig gemacht werden.
http://www.onclive.com/publications/obtn/2013/April-2013/USC…
... As oncologists practicing in an era of “genomic medicine,” when we consider alterations in gene expression, we generally default to DNA mutation as the primary mechanism. Gene expression can also be regulated by epigenetic changes, such as DNA methylation and histone modification. These changes dysregulate gene function without actually altering the underlying DNA sequence. In principle, these modifications are reversible (restoring gene function) and “druggable.” Epigenetic modifications have been strongly implicated in carcinogenesis and maintenance of a malignant clone by silencing key tumor suppressor genes.
...Preclinical studies suggest that combining inhibitors of DNA methyltransferase, such as 5-azacytidine, with inhibitors of histone deacetylase (HDAC), such as entinostat, synergistically induces re-expression of epigenetically silenced tumor suppressor genes
...Also of great interest is testing the concept of epigenetic “priming” as a strategy to sensitize tumors to subsequent therapy.
Bei der Kombination von IO mit epigenetisch wirkenden Mitteln geht es um das Priming... durch epigenetische Wirkstoffe könnten anschließende IO-Mittel sehr viel wirksamer werden. Bisher kommt es ja nur bei einem kleineren Teil von Krebspatienten zur langanhaltenden IO-Wirkung. U.a. mit HDAC-Hemmern, die die Epigenik verändern, könnte sich dieser Anteil steigern lassen.
Was genau Effekt von Entinostat + IO zustande kommt, müsste ich nochmal genauer schauen...
"Studies Support Ongoing Clinical Strategy of Using Syndax's Entinostat as Epigenetic Priming to Immune Therapy
WALTHAM, Mass., July 30, 2014 /PRNewswire/ -- Syndax Pharmaceuticals, Inc. today announced that newly published results demonstrate that in preclinical studies entinostat significantly improved treatment outcomes in mouse tumor models when combined with anti-PD1 and anti-CTLA4 targeted antibodies. The paper from Kim, et al. at The Sidney Kimmel Comprehensive Cancer Center, Johns Hopkins University School of Medicine, titled "Eradication of metastatic mouse cancers resistant to immune checkpoint blockade by suppression of myeloid derived cells" was published in the journal Proceedings of the National Academy of Sciences (PNAS). The study demonstrated that the combination therapy produced 100 percent inhibition of primary tumors and metastases in aggressive mouse colorectal and breast tumor models. The authors also reported an 80 percent cure rate when epigenetic therapy with entinostat and azacitidine was combined with anti-PD1 and anti-CTLA4 antibodies in an aggressive non-immunogenic metastatic breast cancer mouse model.
The mechanism underlying these results, the authors note, is believed to be entinostat's inhibition of myeloid derived suppressor cells (MDSCs) at concentrations which importantly have only modest effects on CD8+ T cells creating the potential for a large therapeutic window in which MDSCs can be depleted while sparing CD8+ T cells."
Ich meine, dass u.a. CSF1R (z.B. letzte Kooperation FPRX + BMS) auch auf MDSCs und TAMs wirkt.
****
(31.05.2013)
Top Prospects from Pipeline Remain Unclear but Plenty of Options. Despite the enthusiasm generated at Celgene's recent investor day, Celgene have not yet firmly established any particular new pipeline asset (beyond apremilast and Abraxane) in the minds of investors. The presentation and Q&A with CFO Jackie Fouse did not alter this perspective although we were (and are) impressed with the company's ability to identify new variations on their original IMiD platform to advance into clinical trials in a variety of different indications. Management highlighted CC-292 with clinical data expected at ASH in December 2013, as well as plans to accelerate timelines for the study of this BTK inhibitor in combination with Revlimid in CLL and NHL. Ms. Fouse noted she was “pretty excited” with the mTOR kinase inhibitor CC-223, which demonstrated broad activity in pre-clinical models, as well as with the potential for epigenetic priming with Vidaza and CC-486 (oral Vidaza). Recall that these two agents are tested in combination with entinostat, an HDAC inhibitor developed by Syndax, in phase I trials in patients with advanced solid tumor. The combination of epigenetic modulators is thought to enable superior anti-tumor efficacy for chemotherapy and immunotherapy.
****
(07.05.2013)
Epigenetic priming with the oral Vidaza follow-on CC-486 shaping up as a new theme with a Phase Ib trial in solid tumors priming with CC-486 on days 1-14 followed by carboplatin or Abraxane with a CC-486 only control (days 1-21). Part 2 of the Phase Ib calls for expansion cohorts in bladed and ovarian (+carboplatin), NSCLC and pancreatic (+Abraxane) and monotherapy (colorectal). Case study data for CC-486 priming with Abraxane was supportive in pancreatic and endometrial cancers. Longer term, plans call for CC-486 +IMiDs in solid tumors. The CTEP trial in metastatic NSCLC will explore synergy of HDAC inhibition with entinostat and CC-486 epigenetic priming (vs Vidaza + entinostat and vs investigators choice). With BMS and SU2C, Celgene will test epigenetic priming with Vidaza + entinostat or CC-486 monotherapy prior to anti-PD-1 therapy with nivolumab. In the more traditional setting of hematologic malignancies, combination work with R-CHOP in DLBCL and T-cell lymphoma and Phase I iNHL trials are being pursued.
****
(28.08.2013)
Syndax Raises $26.6M to Test Resistance-Reversing Cancer Drug, Entinostat; Plans to Begin Phase III in ER+ mBC
Syndax Pharmaceuticals has raised $26.6 million in equity to pay for a late-stage trial of its drug candidate intended to reverse resistance to therapies used for advanced breast cancer.
CEO Arlene Morris said the company is working on epigenetic therapies – which she said “modifies the software of DNA” - to make drugs to which a patient’s cancer has become resistant effective again.
While Syndax’s lead compound, called entinostat, has wide applications in a variety of both solid and liquid cancers, the company is focusing first on metastatic breast cancer. The reason is partly because of the unmet need in that area and the effectiveness entinostat has shown against that type of cancer. Further, Syndax’s former CEO, Joanna Horobin – who last year left to join Verastem – had a significant background in breast cancer.
In a Phase 2 trial, entinostat helped extend both progression-free survival and overall survival when used with exemestane in postmenopausal women with estrogen receptor-positive (ER+) metastatic breast cancer which had become resistant to a non-steroidal aromatase inhibitor. In other words, Morris explained, the drug candidate helped women who were receiving a type of hormone therapy used in breast cancer that has less severe side effects than chemotherapy but had become resistant to it. She said that’s better for the patient than more advanced therapies because hormone therapy is “much better tolerated.”
The company is now planning a Phase 3 study of entinostat in the same types of patients to be sponsored by the National Cancer Institute (NCI). Morris said the company also plans to conduct a study in a certain subset of lung cancer patients in which the candidate showed effectiveness.
****
(11.09.2013)
Syndax: FDA Grants Breakthrough Designation for Entinostat; Phase III Breast Cancer Study Set to Begin in
Early 2014 Syndax Pharmaceuticals announced that it has received the FDA's breakthrough designation (BTD) for a Phase III-ready breast cancer therapy. The biotech won the BTD for entinostat, an experimental histone deacetylase inhibitor (HDACi) set to begin Phase III testing in early 2014 in combination with exemestane in postmenopausal women with metastatic ERpositive breast cancer who have progressed on hormonal therapy.
"We expect it to have some influence on the pathway," CEO Arlene Morris tells FierceBiotech. "Exactly what, we're not sure yet. But we believe it will help gain a higher level of attention (at the FDA). We're also hoping that it will help us enroll the trial faster."
The BTD delivers another piece of a compelling picture for Syndax. The biotech is already working with the National Cancer Institute on its upcoming study. And the Phase II data provided some solid supporting evidence that the drug could reverse resistance to hormone therapy, giving breast cancer patients a reprieve from chemotherapy--the kind of medical need that helped drive the agency to put it on its special oversight track. The FDA has indicated that it's open to allowing Syndax to use Phase II data to support an application, says Morris. And the latest venture round has provided a firm financial footing.
Grüße
ipollit
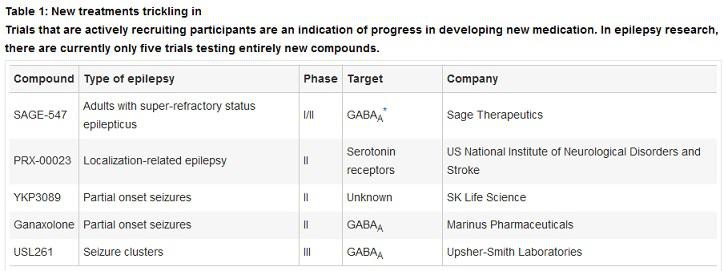
SAGE
Ohad Hammer hat heute geschrieben: "I am actually looking into MRNS these days given the points you bring up (agree to all). The fact their drug is an allopregnanolone drivative similar to SAGE-547 makes it very interesting. Given the huge difference in valuations, I am trying to find the catch…"
MRNS hat mit Ganaxolone auch einen GABA-a Kandidaten gegen Epilepsie in der Pipeline. Allerdings ist Ganaxolone schon recht lange in der Entwicklung... kommt urspünglich von CoCensys, die von Purdue Pharma übernommen wurden. Letztere stellten die Entwicklung von Ganaxolone ein. MRNS hat diesen Kandidaten dann 2004 einlizensiert.
Ich weiß auch nicht, ob Ganaxolone wirklich mit SAGE-547 vergleichbar ist... wird er auch gegen SRSE entwickelt? Ich glaube nicht.
In diesem Zusammenhang fand ich aber den folgenden Artikel ganz interessant:
http://www.nature.com/nature/journal/v511/n7508_supp/full/51…
Drug development: Illuminated targets
Darin wird beschrieben, wie früher bei CNS nur nach Try-And-Error entwickelt wurde... es wurden in Tiermodellen einfach viele potentielle Wirkstoffkandidaten durchgetestet, bis einer zufällig mal eine Wirkung zeigt.
Heute versucht man dagegen die Ursachen zu verstehen und gezielt dagegen vorzugehen. Allerdings haben sich inzwischen die meisten Pharmas aus diesem Bereich zurückgezogen. Sollte Sage Erfolg haben, scheint es nicht viel Konkurrenz zu geben.
Gruß
ipollit
Ohad Hammer hat heute geschrieben: "I am actually looking into MRNS these days given the points you bring up (agree to all). The fact their drug is an allopregnanolone drivative similar to SAGE-547 makes it very interesting. Given the huge difference in valuations, I am trying to find the catch…"
MRNS hat mit Ganaxolone auch einen GABA-a Kandidaten gegen Epilepsie in der Pipeline. Allerdings ist Ganaxolone schon recht lange in der Entwicklung... kommt urspünglich von CoCensys, die von Purdue Pharma übernommen wurden. Letztere stellten die Entwicklung von Ganaxolone ein. MRNS hat diesen Kandidaten dann 2004 einlizensiert.
Ich weiß auch nicht, ob Ganaxolone wirklich mit SAGE-547 vergleichbar ist... wird er auch gegen SRSE entwickelt? Ich glaube nicht.
In diesem Zusammenhang fand ich aber den folgenden Artikel ganz interessant:
http://www.nature.com/nature/journal/v511/n7508_supp/full/51…
Drug development: Illuminated targets
Darin wird beschrieben, wie früher bei CNS nur nach Try-And-Error entwickelt wurde... es wurden in Tiermodellen einfach viele potentielle Wirkstoffkandidaten durchgetestet, bis einer zufällig mal eine Wirkung zeigt.
Heute versucht man dagegen die Ursachen zu verstehen und gezielt dagegen vorzugehen. Allerdings haben sich inzwischen die meisten Pharmas aus diesem Bereich zurückgezogen. Sollte Sage Erfolg haben, scheint es nicht viel Konkurrenz zu geben.

Gruß
ipollit
Antwort auf Beitrag Nr.: 48.457.562 von ipollit am 01.12.14 00:06:51"Letztere stellten die Entwicklung von Ganaxolone ein. MRNS hat diesen Kandidaten dann 2004 einlizensiert."
Wenn ich mich nicht verlesen habe, ist der ursprüngliche IND von 1993...
Das macht es alles etwas suspekt, finde ich. Die Marktkapitalisierung ist in der Tat ein Witz. Derzeit wohl eher bei 70 Mio. als bei 90 Mio. Dollar. Würde man den Cash gegenrechnen, ist das Unternehmen nur 30 Mio. Dollar wert.
Was genau stimmt da nicht?
Wenn ich mich nicht verlesen habe, ist der ursprüngliche IND von 1993...
Das macht es alles etwas suspekt, finde ich. Die Marktkapitalisierung ist in der Tat ein Witz. Derzeit wohl eher bei 70 Mio. als bei 90 Mio. Dollar. Würde man den Cash gegenrechnen, ist das Unternehmen nur 30 Mio. Dollar wert.
Was genau stimmt da nicht?
Antwort auf Beitrag Nr.: 48.453.840 von SLGramann am 30.11.14 11:58:11Hat jemand eine Meinung zu Syndax? Vor allem Kritisches und Negatives ist gefragt!
Sorry SLGramann, hab nichts Negatives beizusteuern.
Im Gegenteil: Das was du und ipollit schreiben hört sich sehr interessant an. Entscheidend wird für mich sein, wie Syndax an der Börse bewertet wird.
Eine Marktkapitalisierung von 300-400 Mio fände ich durchaus vertretbar.
In einem Bericht zum IPO ist sogar von 170 Mio die Rede-zu dem Preis wird man aber wohl kaum zum Zuge kommen:
http://seekingalpha.com/article/2276103-ipo-preview-syndax-p…
SG kmastra
Sorry SLGramann, hab nichts Negatives beizusteuern.

Im Gegenteil: Das was du und ipollit schreiben hört sich sehr interessant an. Entscheidend wird für mich sein, wie Syndax an der Börse bewertet wird.
Eine Marktkapitalisierung von 300-400 Mio fände ich durchaus vertretbar.
In einem Bericht zum IPO ist sogar von 170 Mio die Rede-zu dem Preis wird man aber wohl kaum zum Zuge kommen:
http://seekingalpha.com/article/2276103-ipo-preview-syndax-p…
SG kmastra
Antwort auf Beitrag Nr.: 48.399.590 von SLGramann am 24.11.14 16:13:47ACAD:
Es gibt eine Analyse von Cowen im Netz:
http://www.investorvillage.com/smbd.asp?mb=523&mn=1142&pt=ms…
Das Wesentliche:
Initiating ACAD with Outperform and $46 target
We think Nuplazid has extraordinarily high chances of U.S. approval for Parkinson's Disease
Psychosis.
Our KOL survey strongly suggests broad PDP adoption and we estimate $2B WW peak sales. We also think Nuplazid has potential in other psychoses.
We think Nuplazid will be approved in 2015/2016 WW and become standard of care first line treatment for Parkinson's Disease Psychosis.
There are over 1MM Parkinson’s patients in the US alone and ~33% have PDP but there are currently no approved therapies for the condition.
We conservatively model 50% and 30% retail and US penetration by 2022 for PDP patients and expect peak US sales of $1.1B. is worth $28 to our valuation.
We price the drug conservatively, at $35.20/day, a 10% premium to available branded
antipsychotics ($25-$32/day). We also assume a 300-day-treatment year, because of the long half-life of Nuplazid.
We see peak sales of Nuplazid for PDP reaching $1.1B by 2025 in the US and $2B in the EU. We assume that Acadia will partner for EU sales at what we think would be a ~20% royalty. We assume a 90% chance of success given the positive safety, efficacy,
and breakthrough designation. We conservatively estimate a peak penetration of 50% in retail and 25% in LTC in the US, and 40% and 20% in the EU.
We assume a lower, 20%, chance of success in the ADP trial, with peak US and EU sales reaching $5.48B and $730M respectively, in 2023. We estimate a US 50% and EU 30% peak penetration. We also assume a 60% chance of success for the schizophrenia trial, with global peak sales of $3.3B in 2024.
Our survey of high-prescribing neurologists indicated that 51% of PDP patients are taking antipsychotics and that 35% of PDP patients do not receive antipsychotics because of their undesirable safety profile. Neurologists would prescribe Nuplazid to 53% of this treatment group. They expect about a ~41% uptake in three years.
We see Nuplazid pricing at ~$12,000 annually, which puts the drug at risk for some
payor-pushback, but given the benign safety profile, we do not foresee significant
issues with reimbursement (except for, perhaps, medicare/Medicaid). The U.S. salesforce will likely contain 135-150 representatives, which should cost $250K each annually (or, in total, around $35MM annually).
Es gibt eine Analyse von Cowen im Netz:
http://www.investorvillage.com/smbd.asp?mb=523&mn=1142&pt=ms…
Das Wesentliche:
Initiating ACAD with Outperform and $46 target
We think Nuplazid has extraordinarily high chances of U.S. approval for Parkinson's Disease
Psychosis.
Our KOL survey strongly suggests broad PDP adoption and we estimate $2B WW peak sales. We also think Nuplazid has potential in other psychoses.
We think Nuplazid will be approved in 2015/2016 WW and become standard of care first line treatment for Parkinson's Disease Psychosis.
There are over 1MM Parkinson’s patients in the US alone and ~33% have PDP but there are currently no approved therapies for the condition.
We conservatively model 50% and 30% retail and US penetration by 2022 for PDP patients and expect peak US sales of $1.1B. is worth $28 to our valuation.
We price the drug conservatively, at $35.20/day, a 10% premium to available branded
antipsychotics ($25-$32/day). We also assume a 300-day-treatment year, because of the long half-life of Nuplazid.
We see peak sales of Nuplazid for PDP reaching $1.1B by 2025 in the US and $2B in the EU. We assume that Acadia will partner for EU sales at what we think would be a ~20% royalty. We assume a 90% chance of success given the positive safety, efficacy,
and breakthrough designation. We conservatively estimate a peak penetration of 50% in retail and 25% in LTC in the US, and 40% and 20% in the EU.
We assume a lower, 20%, chance of success in the ADP trial, with peak US and EU sales reaching $5.48B and $730M respectively, in 2023. We estimate a US 50% and EU 30% peak penetration. We also assume a 60% chance of success for the schizophrenia trial, with global peak sales of $3.3B in 2024.
Our survey of high-prescribing neurologists indicated that 51% of PDP patients are taking antipsychotics and that 35% of PDP patients do not receive antipsychotics because of their undesirable safety profile. Neurologists would prescribe Nuplazid to 53% of this treatment group. They expect about a ~41% uptake in three years.
We see Nuplazid pricing at ~$12,000 annually, which puts the drug at risk for some
payor-pushback, but given the benign safety profile, we do not foresee significant
issues with reimbursement (except for, perhaps, medicare/Medicaid). The U.S. salesforce will likely contain 135-150 representatives, which should cost $250K each annually (or, in total, around $35MM annually).
ARRY
jetzt ist das eingetreten, wovon schon viele ausgegangen sind... ARRY erhält Binimetinib von NVS zurück. Jetzt gibt es wieder Planungssicherheit.
ARRY < Array To Regain Worldwide Rights To Binimetinib
- Array to receive up to $85 million upfront payment from Novartis -
- Novartis to conduct and/or substantially fund all ongoing and several planned clinical studies, including COLUMBUS, NEMO and MILO -
- Agreement subject to Novartis-GSK transaction close -
- Conference call to discuss transaction on Thursday, December 4, 2014 at 9:00 a.m. Eastern Time -
BOULDER, Colo., Dec. 3, 2014 /PRNewswire/ -- Array BioPharma Inc. (ARRY) today announced that it has reached a definitive agreement with Novartis International Pharmaceutical Ltd. to regain full worldwide rights to binimetinib, a MEK inhibitor in three Phase 3 trials. This agreement is conditional on the closing of transactions announced by Novartis and GlaxoSmithKline PLC (GSK) on April 22, 2014, which are expected in the first half of 2015, and remain subject to regulatory approval. Array had previously granted Novartis worldwide exclusive rights to develop and commercialize binimetinib under a 2010 License Agreement, which will terminate and be superseded by a new set of agreements between the parties.
Gruß
ipollit
jetzt ist das eingetreten, wovon schon viele ausgegangen sind... ARRY erhält Binimetinib von NVS zurück. Jetzt gibt es wieder Planungssicherheit.
ARRY < Array To Regain Worldwide Rights To Binimetinib
- Array to receive up to $85 million upfront payment from Novartis -
- Novartis to conduct and/or substantially fund all ongoing and several planned clinical studies, including COLUMBUS, NEMO and MILO -
- Agreement subject to Novartis-GSK transaction close -
- Conference call to discuss transaction on Thursday, December 4, 2014 at 9:00 a.m. Eastern Time -
BOULDER, Colo., Dec. 3, 2014 /PRNewswire/ -- Array BioPharma Inc. (ARRY) today announced that it has reached a definitive agreement with Novartis International Pharmaceutical Ltd. to regain full worldwide rights to binimetinib, a MEK inhibitor in three Phase 3 trials. This agreement is conditional on the closing of transactions announced by Novartis and GlaxoSmithKline PLC (GSK) on April 22, 2014, which are expected in the first half of 2015, and remain subject to regulatory approval. Array had previously granted Novartis worldwide exclusive rights to develop and commercialize binimetinib under a 2010 License Agreement, which will terminate and be superseded by a new set of agreements between the parties.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.483.473 von ipollit am 03.12.14 22:08:14Konditionen lesen sich auf den ersten Blick sehr gut!!
Unter anderem:
Novartis will also provide Array continued access to several Novartis pipeline compounds including, but not limited to, LEE011 (CDK 4/6 inhibitor) and BYL719 (α-PI3K inhibitor), for use in currently ongoing combination studies, and possible future studies, including Phase 3 trials, with binimetinib.
Die Cash-Komponente ist ebenfalls sehr, sehr gut!
Bin glücklich heute Abend!
Unter anderem:
Novartis will also provide Array continued access to several Novartis pipeline compounds including, but not limited to, LEE011 (CDK 4/6 inhibitor) and BYL719 (α-PI3K inhibitor), for use in currently ongoing combination studies, and possible future studies, including Phase 3 trials, with binimetinib.
Die Cash-Komponente ist ebenfalls sehr, sehr gut!
Bin glücklich heute Abend!
Man hat sich also quasi außergerichtlich geeinigt! Sehr schön!!
Hinzufügen möchte ich noch, dass der Verweis auf den "future owner of LGX818 (encorafenib)" noch wichtig werden könnte, denn auch hier wird NOV noch evtl. auf Druck des Kartellamts tätig werden müssen.
Ich hoffe das AF hier im letzten Absatz irrt:
http://www.thestreet.com/story/12973807/1/array-biooharma-re…
http://ih.advfn.com/p.php?pid=nmona&article=64659971&xref=ne…
Hinzufügen möchte ich noch, dass der Verweis auf den "future owner of LGX818 (encorafenib)" noch wichtig werden könnte, denn auch hier wird NOV noch evtl. auf Druck des Kartellamts tätig werden müssen.
Ich hoffe das AF hier im letzten Absatz irrt:
http://www.thestreet.com/story/12973807/1/array-biooharma-re…
http://ih.advfn.com/p.php?pid=nmona&article=64659971&xref=ne…
Erste Kurse nach Halt - +31%! Mal sehen was morgen pasiert...
Antwort auf Beitrag Nr.: 48.483.578 von kmastra am 03.12.14 22:27:25erste Kurse sind deutlich im Plus... mal schauen, wie morgen der Markt reagiert
Gruß
ipollit
Gruß
ipollit
Ich denke, heute wird bei Array erst mal heftig gezockt werden. Viele werden auch Gewinne mitnehmen.
Wenn sich der Staub gelegt hat, wird der Markt realisieren, dass Array nun die vollen Rechte an einem aussichtsreichen und weit fortgeschrittenen P III-Asset hat und auch finanziell wieder recht stabil dasteht (ich sehe überhaupt keinen vernünftigen Grund, jetzt die finanziellen Ressourcen durch eine Filanesib-PIII zu strapazieren).
Eine Unternehmensbewertung zwischen 800 Millionen und 1 Mrd. Dollar erscheint mir für 2015 als absolut angemessen.
Man darf auch Selumetinib nicht außen vor lassen. Was wäre bei einem Erfolg in NSCLC? Allein Selumetinib könnte mittelfristig für eine Mrd. Marktkapitalisierung gut sein.
Rückblickend muss man sagen, dass alles was mit Binimetinib gelaufen ist, für Array optimal war. Novartis hat den Wirkstoff mit viel Aufwand weit voran gebracht - und Array erntet die Früchte.
Wer will ausschließen, dass Array Binimetinib neu verpartnert? Nur die Ex-US-Rechte vielleicht? Auf jeden Fall zu besseren Konditionen...
Alles läuft optimal für Array und der Markt ist nach wie vor nicht bereit, das voll einzupreisen.
Alles was heute unter +50% bleibt, ist für mich Marktversagen.
Wenn sich der Staub gelegt hat, wird der Markt realisieren, dass Array nun die vollen Rechte an einem aussichtsreichen und weit fortgeschrittenen P III-Asset hat und auch finanziell wieder recht stabil dasteht (ich sehe überhaupt keinen vernünftigen Grund, jetzt die finanziellen Ressourcen durch eine Filanesib-PIII zu strapazieren).
Eine Unternehmensbewertung zwischen 800 Millionen und 1 Mrd. Dollar erscheint mir für 2015 als absolut angemessen.
Man darf auch Selumetinib nicht außen vor lassen. Was wäre bei einem Erfolg in NSCLC? Allein Selumetinib könnte mittelfristig für eine Mrd. Marktkapitalisierung gut sein.
Rückblickend muss man sagen, dass alles was mit Binimetinib gelaufen ist, für Array optimal war. Novartis hat den Wirkstoff mit viel Aufwand weit voran gebracht - und Array erntet die Früchte.
Wer will ausschließen, dass Array Binimetinib neu verpartnert? Nur die Ex-US-Rechte vielleicht? Auf jeden Fall zu besseren Konditionen...
Alles läuft optimal für Array und der Markt ist nach wie vor nicht bereit, das voll einzupreisen.
Alles was heute unter +50% bleibt, ist für mich Marktversagen.
Antwort auf Beitrag Nr.: 48.484.346 von SLGramann am 04.12.14 07:31:06Der Kursanstieg bildet ziemlich genau den Cash-Zufluss ab.
Der Markt "weiß" also, dass der Wert von Binimetinib selbst bei ziemlich genau 0,0 Dollar liegt. Beeindruckend...
Der Markt "weiß" also, dass der Wert von Binimetinib selbst bei ziemlich genau 0,0 Dollar liegt. Beeindruckend...
Antwort auf Beitrag Nr.: 48.490.898 von SLGramann am 04.12.14 16:25:28Hammer mit einem Artikel zur Rückgabe von Binimetinib:
(er glaubt scheinbar irgendwie, dass der Kandidat einen gewissen Wert haben könnte...)
http://www.orf-blog.com/array-gets-binimetinib-back-phenomen…
(er glaubt scheinbar irgendwie, dass der Kandidat einen gewissen Wert haben könnte...)
http://www.orf-blog.com/array-gets-binimetinib-back-phenomen…
Antwort auf Beitrag Nr.: 48.491.453 von SLGramann am 04.12.14 17:13:37arry:
Die wichtigsten Fakten hier noch mal als Präsentation:
http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9M…
In 2015 wird es vor allem darum gehen, einen neuen Partner ins Boot zu holen. Ich würde mich wundern, wenn es nicht schon erste Sondierungsgespräche gäbe.
-----------
AGIO:
Ich habe heute meine Position halbiert. So großartig ich das Unternehmen auch finde, denke ich doch, dass der Kurs arg viel vorwegnimmt...
Die wichtigsten Fakten hier noch mal als Präsentation:
http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9M…
In 2015 wird es vor allem darum gehen, einen neuen Partner ins Boot zu holen. Ich würde mich wundern, wenn es nicht schon erste Sondierungsgespräche gäbe.
-----------
AGIO:
Ich habe heute meine Position halbiert. So großartig ich das Unternehmen auch finde, denke ich doch, dass der Kurs arg viel vorwegnimmt...
ESPR
Empfehlung von CS... sofort reagiert der Kurs


Gruß
ipollit
Empfehlung von CS... sofort reagiert der Kurs


Gruß
ipollit
Antwort auf Beitrag Nr.: 48.494.159 von ipollit am 04.12.14 22:02:06Schon verrückt, dass die Kursreaktion bei ESPR (es hat sich ja fundamental nix geändert) und ARRY heute fast gleich war.
ONTY:
ipollit hatte hier im Forum mal was zu ont380 geschrieben:
http://www.wallstreet-online.de/diskussion/1173523-791-800/b…
Erste Ergebnisse, der PI Kombistudien sollen nun auf dem San Antonio Breast Cancer Symposium (SABCS) präsentiert werden (9-13 Dezember).
Hier noch eine recht aktuelle Studie:
https://hcwco.bluematrix.com/sellside/EmailDocViewer?encrypt…
Ich habe mir hier eine Tradingposition gekauft, weil ich die Bewertung auch in Bezug auf Puma nicht so ganz nachvollziehen kann. Ich habe auch den Eindruck, dass ONTY noch unter den gescheiterten Stimuvax Studien leidet, was zudem keinen Sinn ergibt.
ONTY:
ipollit hatte hier im Forum mal was zu ont380 geschrieben:
http://www.wallstreet-online.de/diskussion/1173523-791-800/b…
Erste Ergebnisse, der PI Kombistudien sollen nun auf dem San Antonio Breast Cancer Symposium (SABCS) präsentiert werden (9-13 Dezember).
Hier noch eine recht aktuelle Studie:
https://hcwco.bluematrix.com/sellside/EmailDocViewer?encrypt…
Ich habe mir hier eine Tradingposition gekauft, weil ich die Bewertung auch in Bezug auf Puma nicht so ganz nachvollziehen kann. Ich habe auch den Eindruck, dass ONTY noch unter den gescheiterten Stimuvax Studien leidet, was zudem keinen Sinn ergibt.
AMBI
Da es höchstwahrscheinlich einige Mitleser hier betrifft, möchte ich nochmal auf den Kapitalertragsteuerabzug eingehen. Ich habe zwischenzeitlich herausgefunden, daß es flächendeckend und systematisch zu viel zu hohen KESt-Abzügen gekommen ist, und zwar bei sehr vielen Banken. Jeder ehemalige AMBI-Aktionär ist wirklich sehr gut beraten, wenn er den bei ihm vorgenommenen KEST-Abzug genau prüft.
Der Fehler beruht wohl (das muß ich aber noch genauer prüfen) auf Mitteilungen des WM-Datenservice. Die Banken bedienen sich regelmäßig in einem automatisierten Abrufverfahren bei der WM-Datenbank.
WM hat den Banken scheinbar mitgeteilt, daß es sich bei der Übernahme angeblich um eine "Fusion" und zudem um einen "TAUSCH" der Aktien gegen die CVR gehandelt habe. Dies führt nun dazu, daß die Banken die historischen Anschaffungskosten für die Aktien reihenweise schlicht auf die CVR übertragen und den KESt-Abzug auf das volle Brutto-Entgelt berechnen (also nicht nur auf den Gewinn). Dies ist steuerrechtlich ganz gewiß unzutreffend! Die nachteiligen Auswirkungen sind erheblich. Außerdem scheidet dadurch eine Verlustverrechnung mit etwaigen Veräußerungsverlusten aus. Und wenn es ganz schlecht läuft, können die auf die CVR übertragenen historischen Anschaffungskosten der Aktien gänzlich untergehen und verpuffen, je nach Schicksal der CVR.
Also zusammenfassend: Dringend den KESt-Abzug prüfen!
Da es höchstwahrscheinlich einige Mitleser hier betrifft, möchte ich nochmal auf den Kapitalertragsteuerabzug eingehen. Ich habe zwischenzeitlich herausgefunden, daß es flächendeckend und systematisch zu viel zu hohen KESt-Abzügen gekommen ist, und zwar bei sehr vielen Banken. Jeder ehemalige AMBI-Aktionär ist wirklich sehr gut beraten, wenn er den bei ihm vorgenommenen KEST-Abzug genau prüft.
Der Fehler beruht wohl (das muß ich aber noch genauer prüfen) auf Mitteilungen des WM-Datenservice. Die Banken bedienen sich regelmäßig in einem automatisierten Abrufverfahren bei der WM-Datenbank.
WM hat den Banken scheinbar mitgeteilt, daß es sich bei der Übernahme angeblich um eine "Fusion" und zudem um einen "TAUSCH" der Aktien gegen die CVR gehandelt habe. Dies führt nun dazu, daß die Banken die historischen Anschaffungskosten für die Aktien reihenweise schlicht auf die CVR übertragen und den KESt-Abzug auf das volle Brutto-Entgelt berechnen (also nicht nur auf den Gewinn). Dies ist steuerrechtlich ganz gewiß unzutreffend! Die nachteiligen Auswirkungen sind erheblich. Außerdem scheidet dadurch eine Verlustverrechnung mit etwaigen Veräußerungsverlusten aus. Und wenn es ganz schlecht läuft, können die auf die CVR übertragenen historischen Anschaffungskosten der Aktien gänzlich untergehen und verpuffen, je nach Schicksal der CVR.
Also zusammenfassend: Dringend den KESt-Abzug prüfen!
CBST
Merck scheint ernsthaftes Interesse an CBST zu haben... 100 USD (+33% zum aktuellen Kurs) sind im Gespräch. Ich fände einen höheren Preis für angebracht, da schon in Kürze (PDUFA ist der 21.12.) mit Zerbaxa der nächste Antibiotika-Blockbuster von CBST die US-Zulassung erhalten dürfte.
http://dealbook.nytimes.com/2014/12/05/merck-in-talks-to-acq…
Merck & Company, the big drug maker, is in talks to to acquire the biopharmaceuticals company Cubist for more than $7 billion, according to people briefed on the matter...
Merck is expected to pay roughly $100 per share for Cubist, valuing the company in the range of $7.5 billion, these people said. A deal could be announced as early as next week. Merck and Cubist did not reply to requests for comment...
AH zumindest deutlich im Plus...

Gruß
ipollit
Merck scheint ernsthaftes Interesse an CBST zu haben... 100 USD (+33% zum aktuellen Kurs) sind im Gespräch. Ich fände einen höheren Preis für angebracht, da schon in Kürze (PDUFA ist der 21.12.) mit Zerbaxa der nächste Antibiotika-Blockbuster von CBST die US-Zulassung erhalten dürfte.
http://dealbook.nytimes.com/2014/12/05/merck-in-talks-to-acq…
Merck & Company, the big drug maker, is in talks to to acquire the biopharmaceuticals company Cubist for more than $7 billion, according to people briefed on the matter...
Merck is expected to pay roughly $100 per share for Cubist, valuing the company in the range of $7.5 billion, these people said. A deal could be announced as early as next week. Merck and Cubist did not reply to requests for comment...
AH zumindest deutlich im Plus...
Gruß
ipollit
vielleicht ist das für euch etwas
"Omeros Corp.
TICKER: OMER:NASDAQ
Omeros Corp. is a clinical-stage biopharmaceutical company discovering, developing and commercializing small-molecule and protein therapeutics targeting inflammation, coagulopathies and disorders of the central nervous system. Lead drug product Omidria (OMS302) for lens … read more
The information provided below is from analysts, newsletters and other contributors. Please contact the company and visit its website before making an investment decision.
Expert Comments:
The Life Sciences Report Interview with Steve Brozak (11/13/14) "Omeros Corp.'s product, Omidria (phenylephrine + ketorolac), was approved on May 30 of this year. Omidria is a simple combination of two older drugs that have been in the public domain for quite some time. One is a mydriatic or pupil-dilating agent, and the other is an anti-inflammatory and analgesic. The product was designed for use in cataract and intraocular lens replacement surgery, and it results in patients having less post-operative pain. The company will start selling Omidria on Jan. 1, 2015, and just recently, on Oct. 30, the product received pass-through reimbursement approval from the Center for Medicare & Medicaid Services. Now Omidria can be reimbursed by Medicare, Medicaid and many private insurers beyond the cost of the surgical procedure itself. Omeros' reimbursement will be based on the product's wholesale acquisition cost of $465 per single-use vial, which would cover a single procedure. . . .instead of having to use compounded products or homebrews to do lens surgery, the surgeon can now use a product that is FDA-approved, proven sterile and safe, and reimbursable by payers. Physicians should be using it as standard of care. I don't think there is an obstacle to adoption of Omidria at this point." More >
The Life Sciences Report Interview with George Zavoico (11/12/14) "I think Omeros Corp. is on the cusp of an inflection point. At the end of May, the company's Omidria (phenylephrine + ketorolac) irrigation solution for intraocular lens replacement surgery was approved. . .Omidria should have a big effect on this very large market. One of the important issues for investors is that Omeros is likely to be marketing Omidria itself, which is prudent since the company can focus on centers that do a lot of these procedures. It won't need a huge sales force. . .the benefit is that Omeros collects all the revenue, and doesn't have to share the profit. . .recently Omeros got a very favorable decision from the Centers for Medicare and Medicaid Services (CMS) on reimbursement. The company requested, and received, pass-through reimbursement status, effective Jan. 1, 2015, which means that Omidria's cost will not be bundled with the reimbursement for an intraocular replacement surgery procedure. Omeros is guiding to a launch early next year, just as the pass-through status becomes effective. . .we'll be watching the quarterly sales revenue numbers to better gauge market penetration. . .we see a pretty healthy revenue stream coming from Omidria. . ." More >
The Life Sciences Report Biotech Watchlist Update with George Zavoico (11/6/14) "We believe Omeros Corp.'s Omidria will have a successful launch and become widely used by ophthalmic surgeons and that Omeros will become profitable in 2016. . .key catalysts with Omidria will be the success of the launch and growth in sales revenue from quarter to quarter. . .[while Omidria] by itself is enough to keep a company busy and prosperous, we think that Omeros' diverse and promising drug pipeline has even more potential." More >
Jason Kolbert, Maxim Group (11/3/14) "Omeros Corp.'s Omidria has been approved, and we currently assume OMS302 (intraocular lens replacement surgery) will see a full launch in late Q4/14. . .we believe global sales could reach north of $30M by 2017 for OMS302."
Jason Kolbert, Maxim Group (10/22/14) "Omeros Corp. self-imposed a temporary suspension of OMS824 Huntington's disease trial. . .what does this mean? Likely not much, but we are confident that the right call is being made by Omeros to temporarily suspend the current Phase 2 trial to be cautious. Omeros has had communications with the FDA and it agreed that Omeros should sort out the preclinical data." ...
www.thelifesciencesreport.com/pub/co/4364#quote "
"Omeros Corp.
TICKER: OMER:NASDAQ
Omeros Corp. is a clinical-stage biopharmaceutical company discovering, developing and commercializing small-molecule and protein therapeutics targeting inflammation, coagulopathies and disorders of the central nervous system. Lead drug product Omidria (OMS302) for lens … read more
The information provided below is from analysts, newsletters and other contributors. Please contact the company and visit its website before making an investment decision.
Expert Comments:
The Life Sciences Report Interview with Steve Brozak (11/13/14) "Omeros Corp.'s product, Omidria (phenylephrine + ketorolac), was approved on May 30 of this year. Omidria is a simple combination of two older drugs that have been in the public domain for quite some time. One is a mydriatic or pupil-dilating agent, and the other is an anti-inflammatory and analgesic. The product was designed for use in cataract and intraocular lens replacement surgery, and it results in patients having less post-operative pain. The company will start selling Omidria on Jan. 1, 2015, and just recently, on Oct. 30, the product received pass-through reimbursement approval from the Center for Medicare & Medicaid Services. Now Omidria can be reimbursed by Medicare, Medicaid and many private insurers beyond the cost of the surgical procedure itself. Omeros' reimbursement will be based on the product's wholesale acquisition cost of $465 per single-use vial, which would cover a single procedure. . . .instead of having to use compounded products or homebrews to do lens surgery, the surgeon can now use a product that is FDA-approved, proven sterile and safe, and reimbursable by payers. Physicians should be using it as standard of care. I don't think there is an obstacle to adoption of Omidria at this point." More >
The Life Sciences Report Interview with George Zavoico (11/12/14) "I think Omeros Corp. is on the cusp of an inflection point. At the end of May, the company's Omidria (phenylephrine + ketorolac) irrigation solution for intraocular lens replacement surgery was approved. . .Omidria should have a big effect on this very large market. One of the important issues for investors is that Omeros is likely to be marketing Omidria itself, which is prudent since the company can focus on centers that do a lot of these procedures. It won't need a huge sales force. . .the benefit is that Omeros collects all the revenue, and doesn't have to share the profit. . .recently Omeros got a very favorable decision from the Centers for Medicare and Medicaid Services (CMS) on reimbursement. The company requested, and received, pass-through reimbursement status, effective Jan. 1, 2015, which means that Omidria's cost will not be bundled with the reimbursement for an intraocular replacement surgery procedure. Omeros is guiding to a launch early next year, just as the pass-through status becomes effective. . .we'll be watching the quarterly sales revenue numbers to better gauge market penetration. . .we see a pretty healthy revenue stream coming from Omidria. . ." More >
The Life Sciences Report Biotech Watchlist Update with George Zavoico (11/6/14) "We believe Omeros Corp.'s Omidria will have a successful launch and become widely used by ophthalmic surgeons and that Omeros will become profitable in 2016. . .key catalysts with Omidria will be the success of the launch and growth in sales revenue from quarter to quarter. . .[while Omidria] by itself is enough to keep a company busy and prosperous, we think that Omeros' diverse and promising drug pipeline has even more potential." More >
Jason Kolbert, Maxim Group (11/3/14) "Omeros Corp.'s Omidria has been approved, and we currently assume OMS302 (intraocular lens replacement surgery) will see a full launch in late Q4/14. . .we believe global sales could reach north of $30M by 2017 for OMS302."
Jason Kolbert, Maxim Group (10/22/14) "Omeros Corp. self-imposed a temporary suspension of OMS824 Huntington's disease trial. . .what does this mean? Likely not much, but we are confident that the right call is being made by Omeros to temporarily suspend the current Phase 2 trial to be cautious. Omeros has had communications with the FDA and it agreed that Omeros should sort out the preclinical data." ...
www.thelifesciencesreport.com/pub/co/4364#quote "
Antwort auf Beitrag Nr.: 48.504.401 von ipollit am 06.12.14 01:47:41"Merck scheint ernsthaftes Interesse an CBST zu haben... 100 USD (+33% zum aktuellen Kurs) sind im Gespräch."
Wenn es so kommt, herzlichen Glückwunsch ipollit! (auch wenn Du einen höheren Preis berechtigt findest, wäre es ja auch so ein hervorragendes Investment gewesen). Du hast immer an CBST geglaubt. Ich war nie ganz überzeugt wegen des Patentablaufs von Cubicin.
(auch wenn Du einen höheren Preis berechtigt findest, wäre es ja auch so ein hervorragendes Investment gewesen). Du hast immer an CBST geglaubt. Ich war nie ganz überzeugt wegen des Patentablaufs von Cubicin.
Hast dann vielleicht ein ähnliches Problem wie ich zur Zeit seit dem Agio-Teilverkauf. Ein wenig mehr Cash als neue Ideen...
Wenn es so kommt, herzlichen Glückwunsch ipollit!
 (auch wenn Du einen höheren Preis berechtigt findest, wäre es ja auch so ein hervorragendes Investment gewesen). Du hast immer an CBST geglaubt. Ich war nie ganz überzeugt wegen des Patentablaufs von Cubicin.
(auch wenn Du einen höheren Preis berechtigt findest, wäre es ja auch so ein hervorragendes Investment gewesen). Du hast immer an CBST geglaubt. Ich war nie ganz überzeugt wegen des Patentablaufs von Cubicin. Hast dann vielleicht ein ähnliches Problem wie ich zur Zeit seit dem Agio-Teilverkauf. Ein wenig mehr Cash als neue Ideen...

Antwort auf Beitrag Nr.: 48.504.884 von SLGramann am 06.12.14 09:16:04Danke! So schlecht wäre der Kurs ja auch nicht. Es stimmt, dass Cubicin irgendwann Probleme mit Generika bekommen wird, aber momentan produziert es noch fleißig reichlich Cash, dass wieder investiert werden kann. Cubist ist im Bereich der Antibiotika für mich das führende Unternehmen weltweit, da sie sich darauf spezialisiert haben, während die Pharmas aus diesen Bereich ausgestiegen sind. Zuletzt gab es bei den Pharmas aber wohl wieder ein Umdenken, die US-Regierung will die Entwicklung von Antibiotika fördern... schließlich laufen in diesem Markt nicht nur die Patente sondern auch die Wirkung der Antibiotika mit der Zeit ab, es wird ständig Nachschub benötigt.
Durch die Übernahme von Trius und Optimer, sowie vor längerer Zeit Calixa ist Cubist inzwischen viel breiter aufgestellt. Neben Cubicin haben sie nun 2 neue Antibiotika am Markt und in Kürze das dritte, welches sich langfristig besser als Cubicin entwickeln könnte. Ein viertes befindet sich in PIII und mit der Übernahme von Adelor gibt es mit Bevenopran gegen OIC in PIII ein Mittel, das zwar ein hohes Risiko aber auch sehr hohe Chancen bietet. Bisher hat Cubist vieles richtig gemacht.
https://www.youtube.com/watch?v=x1c24imxqig
***
http://www.cnbc.com/id/102245250
Merck in talks to acquire Cubist for over $8 billion: Sources
Drug giant Merck is in talks to acquire antibiotics maker Cubist for about $102 a share in cash, according to people familiar with the matter.
The deal has an equity value of more than $8 billion, and could be announced as soon as Monday, the people said.
The New York Times reported earlier Friday evening a deal was likely to be announced as soon as next week. The plans are not finalized and talks could still break up, the people said.
The move would give Merck access to Cubist's medicines, administered primarily in hospitals. Cubist sells the nearly billion-dollar a year antibiotic Cubicin, as well as a slate of other drugs for bacterial infections and a medicine to aid recovery from bowel surgery.
Cubist is one of few drugmakers with a major focus on antibiotics, a neglected area of drug development in recent years; the company last year acquired smaller antibiotics makers Trius and Optimer.
A decision is expected from the Food and Drug Administration later this month on another antibiotic, Zerbaxa, which RBC Capital Markets analyst Adnan Butt estimates could draw $1 billion in peak annual revenue.
***
Ich habe mich nur auf CBST als den Marktführer konzentriert. Es gibt aber auch noch andere wie z.B. TTPH oder CEMP... die schaue ich mir nochmal näher an.
Gruß
ipollit
Durch die Übernahme von Trius und Optimer, sowie vor längerer Zeit Calixa ist Cubist inzwischen viel breiter aufgestellt. Neben Cubicin haben sie nun 2 neue Antibiotika am Markt und in Kürze das dritte, welches sich langfristig besser als Cubicin entwickeln könnte. Ein viertes befindet sich in PIII und mit der Übernahme von Adelor gibt es mit Bevenopran gegen OIC in PIII ein Mittel, das zwar ein hohes Risiko aber auch sehr hohe Chancen bietet. Bisher hat Cubist vieles richtig gemacht.
https://www.youtube.com/watch?v=x1c24imxqig
***
http://www.cnbc.com/id/102245250
Merck in talks to acquire Cubist for over $8 billion: Sources
Drug giant Merck is in talks to acquire antibiotics maker Cubist for about $102 a share in cash, according to people familiar with the matter.
The deal has an equity value of more than $8 billion, and could be announced as soon as Monday, the people said.
The New York Times reported earlier Friday evening a deal was likely to be announced as soon as next week. The plans are not finalized and talks could still break up, the people said.
The move would give Merck access to Cubist's medicines, administered primarily in hospitals. Cubist sells the nearly billion-dollar a year antibiotic Cubicin, as well as a slate of other drugs for bacterial infections and a medicine to aid recovery from bowel surgery.
Cubist is one of few drugmakers with a major focus on antibiotics, a neglected area of drug development in recent years; the company last year acquired smaller antibiotics makers Trius and Optimer.
A decision is expected from the Food and Drug Administration later this month on another antibiotic, Zerbaxa, which RBC Capital Markets analyst Adnan Butt estimates could draw $1 billion in peak annual revenue.
***
Ich habe mich nur auf CBST als den Marktführer konzentriert. Es gibt aber auch noch andere wie z.B. TTPH oder CEMP... die schaue ich mir nochmal näher an.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.504.884 von SLGramann am 06.12.14 09:16:04"Hast dann vielleicht ein ähnliches Problem wie ich zur Zeit seit dem Agio-Teilverkauf. Ein wenig mehr Cash als neue Ideen..."
nein... Ideen gibt es noch viele! Bei AGIO war ich leider nicht dabei, sehe es aber momentan auch so wie du. Deren IDH-Hemmer scheinen zwar sehr wirksam zu sein, aber dafür ist der Markt nicht so groß oder täusche ich mich da? Ich hätte wohl auch erstmal einen Teil verkauft.
Ideen gibt es noch viele! Bei AGIO war ich leider nicht dabei, sehe es aber momentan auch so wie du. Deren IDH-Hemmer scheinen zwar sehr wirksam zu sein, aber dafür ist der Markt nicht so groß oder täusche ich mich da? Ich hätte wohl auch erstmal einen Teil verkauft.
Du hast ja einiges zu ACAD geschrieben. Seit längerem finde ich die auch interessant. CNS habe ich allerdings immer als zu risikoreich gesehen... z.B. mit TRGT hatte ich nicht viel Glück gehabt. ACAD scheint aber wirklich gut zu sein... ich könnte mir auch eine Position vorstellen. Sollte Pimavanserin wirklich breit zum Einsatz kommen, müsste der Kurs deutlich höher stehen als heute (zweistellige Mrd MC). Vielleicht ist es besser, statt auf die riskanten Kleinen zu setzen die größeren, in ihrem Bereich führenden oder nur die sehr aussichtsreichen zu wählen. Ich habe das Gefühl, dass es im Moment sehr viele gute Unternehmen am Markt gibt. Eine andere Frage ist, wie lange es bei den Biotechs generell noch nach oben geht oder Markt zu überhitzt ist. Normalerweise ist aber zumindest der vor uns liegende Zeitraum (Jahresanfang) für Biotechs nach meinem Gefühl immer der beste gewesen.
Alle hier zuletzt genannten Unternehmen wie FGEN, ZFGN, ZSPH+RLYP und ACAD gehören für mich zu den besseren Unternehmen, die ich mir vorstellen kann.





Ich streue allerdings auch sehr breit... eine Position macht dann nur 1-5% aus.
Mein Schwerpunkt ist aber nachwievor der Krebs-Bereich und da speziell IO.
Grüße
ipollit
nein...
 Ideen gibt es noch viele! Bei AGIO war ich leider nicht dabei, sehe es aber momentan auch so wie du. Deren IDH-Hemmer scheinen zwar sehr wirksam zu sein, aber dafür ist der Markt nicht so groß oder täusche ich mich da? Ich hätte wohl auch erstmal einen Teil verkauft.
Ideen gibt es noch viele! Bei AGIO war ich leider nicht dabei, sehe es aber momentan auch so wie du. Deren IDH-Hemmer scheinen zwar sehr wirksam zu sein, aber dafür ist der Markt nicht so groß oder täusche ich mich da? Ich hätte wohl auch erstmal einen Teil verkauft.Du hast ja einiges zu ACAD geschrieben. Seit längerem finde ich die auch interessant. CNS habe ich allerdings immer als zu risikoreich gesehen... z.B. mit TRGT hatte ich nicht viel Glück gehabt. ACAD scheint aber wirklich gut zu sein... ich könnte mir auch eine Position vorstellen. Sollte Pimavanserin wirklich breit zum Einsatz kommen, müsste der Kurs deutlich höher stehen als heute (zweistellige Mrd MC). Vielleicht ist es besser, statt auf die riskanten Kleinen zu setzen die größeren, in ihrem Bereich führenden oder nur die sehr aussichtsreichen zu wählen. Ich habe das Gefühl, dass es im Moment sehr viele gute Unternehmen am Markt gibt. Eine andere Frage ist, wie lange es bei den Biotechs generell noch nach oben geht oder Markt zu überhitzt ist. Normalerweise ist aber zumindest der vor uns liegende Zeitraum (Jahresanfang) für Biotechs nach meinem Gefühl immer der beste gewesen.
Alle hier zuletzt genannten Unternehmen wie FGEN, ZFGN, ZSPH+RLYP und ACAD gehören für mich zu den besseren Unternehmen, die ich mir vorstellen kann.
Ich streue allerdings auch sehr breit... eine Position macht dann nur 1-5% aus.
Mein Schwerpunkt ist aber nachwievor der Krebs-Bereich und da speziell IO.
Grüße
ipollit
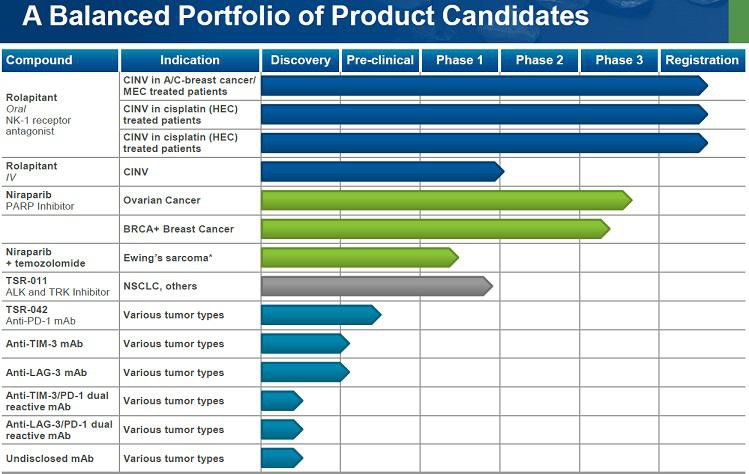
TSRO
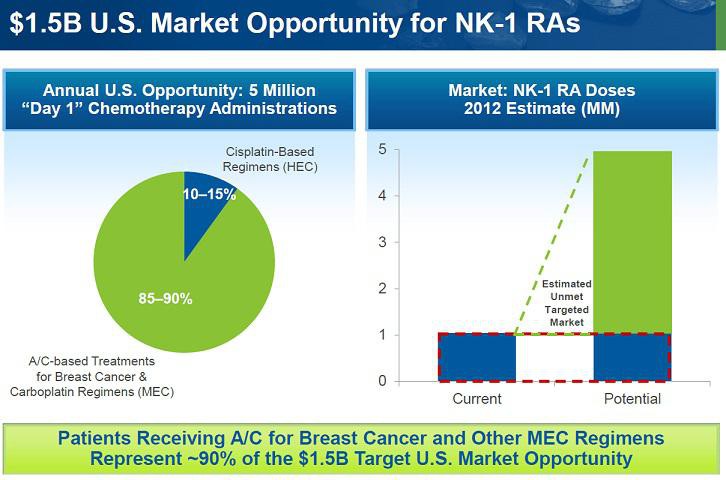
hier (31. Nasdaq Investor Programm) erklärt der CEO Leon O. Moulder meiner Meinung nach ganz gut, worum es bei TSRO geht. Er hat bereits bei MGI einen guten Job gemacht und scheint kompetent zu sein. TSRO hat mit Rolapitant etwas kurz vor der Zulassung, mit dem PARP-Hemmer mittelfristig Potential und mit den IO-AKs eine langfristig interessante Pipeline (möglicherweise den ersten TIM3 in der Klinik und sehr interessante Bi-AKs).
http://www.media-server.com/m/p/auztme6s



Gruß
ipollit
hier (31. Nasdaq Investor Programm) erklärt der CEO Leon O. Moulder meiner Meinung nach ganz gut, worum es bei TSRO geht. Er hat bereits bei MGI einen guten Job gemacht und scheint kompetent zu sein. TSRO hat mit Rolapitant etwas kurz vor der Zulassung, mit dem PARP-Hemmer mittelfristig Potential und mit den IO-AKs eine langfristig interessante Pipeline (möglicherweise den ersten TIM3 in der Klinik und sehr interessante Bi-AKs).
http://www.media-server.com/m/p/auztme6s




Gruß
ipollit
Antwort auf Beitrag Nr.: 48.505.844 von ipollit am 06.12.14 13:10:08Hallo ipollit,
jetzt sind es für Cubist 102 Dollar geworden. Jetzt kannst Du andere Ideen umsetzen.
http://www.fiercebiotech.com/story/merck-splashes-antibiotic…
Ich gebe Dir in Bezug auf die Anlagestrategie doppelt recht. Man sollte sich auf Qualität konzentrieren und eher bei der Bewertung einen Kompromiss machen. Qualität setzt sich am Ende durch und die guten Unternehmen sind fast immer und fast überall hoch bewertet – in aller Regel ist ihre Performance trotzdem besser, als die der scheinbaren Schnäppchen.
Was ich bis vor einiger Zeit noch etwas anders gesehen habe, ist die breite Diversifizierung. Ich habe ja früher eher die Meinung vertreten, dass man stärker konzentrieren soll, sich eben auf die Qualität konzentrieren soll.
Inzwischen denke ich, dass eine so breite Streuung wie bei Dir mehr Vorteile als Nachteile bringt. Natürlich muss man bei 25 bis 30 Werten im Depot aufpassen, dass man die Qualität nicht vernachlässigt und dass man seine eigene Aufmerksamkeitsspanne nicht überstrapaziert. Die Gefahr ist schon vorhanden.
Ich werde wohl kleine Positionen bei Tesaro, ZS Pharma und Relypsa eingehen. Relypsa gewichte ich niedriger als ZS Pharma. Schade, dass man hier zwei Player hat.
Ich bin aber etwas unsicher, was das Marktpotential für Hyperkaliämie betrifft...
jetzt sind es für Cubist 102 Dollar geworden. Jetzt kannst Du andere Ideen umsetzen.
http://www.fiercebiotech.com/story/merck-splashes-antibiotic…
Ich gebe Dir in Bezug auf die Anlagestrategie doppelt recht. Man sollte sich auf Qualität konzentrieren und eher bei der Bewertung einen Kompromiss machen. Qualität setzt sich am Ende durch und die guten Unternehmen sind fast immer und fast überall hoch bewertet – in aller Regel ist ihre Performance trotzdem besser, als die der scheinbaren Schnäppchen.
Was ich bis vor einiger Zeit noch etwas anders gesehen habe, ist die breite Diversifizierung. Ich habe ja früher eher die Meinung vertreten, dass man stärker konzentrieren soll, sich eben auf die Qualität konzentrieren soll.
Inzwischen denke ich, dass eine so breite Streuung wie bei Dir mehr Vorteile als Nachteile bringt. Natürlich muss man bei 25 bis 30 Werten im Depot aufpassen, dass man die Qualität nicht vernachlässigt und dass man seine eigene Aufmerksamkeitsspanne nicht überstrapaziert. Die Gefahr ist schon vorhanden.
Ich werde wohl kleine Positionen bei Tesaro, ZS Pharma und Relypsa eingehen. Relypsa gewichte ich niedriger als ZS Pharma. Schade, dass man hier zwei Player hat.
Ich bin aber etwas unsicher, was das Marktpotential für Hyperkaliämie betrifft...
Alexion Pharma, Celgene, Biogen-Idec, Vertex und ein Bio-ETF - ein Wahnsinn, so etwas habe ich noch nicht erlebt.
Allen wünsche ich ein Frohes Weihnachten 2014 !
Allen wünsche ich ein Frohes Weihnachten 2014 !
Antwort auf Beitrag Nr.: 48.515.519 von SLGramann am 08.12.14 15:17:30"Jetzt kannst Du andere Ideen umsetzen."
...ja, ich habe mich für zwei neue Positionen ACAD und CEMP entschieden. TSRO und IPH.PA stocke ich etwas auf. Mal schauen.
Grüße
ipollit
...ja, ich habe mich für zwei neue Positionen ACAD und CEMP entschieden. TSRO und IPH.PA stocke ich etwas auf. Mal schauen.
Grüße
ipollit
BLUE:
Ist man wirklich auf dem Weg zur ersten funktionierenden Gentherapie zur Heilung einer Erbkrankheit?
Es spricht einiges dafür:
http://www.fiercebiotech.com/story/bluebird-posts-more-promi…
Die Aktie reagiert nachbörslich mit einem deutlichen Sprung. Das ist auch nicht verwunderlich, denn das kommerzielle Potential dieser Technologie könnte sich ggf. als ganz außerordentlich bedeutsam erweisen.
Gentherapie, IO, CAR-T, TCR - sehr, sehr wichtige Entwicklungen. Eine richtungsweisende ASH.
Ist man wirklich auf dem Weg zur ersten funktionierenden Gentherapie zur Heilung einer Erbkrankheit?
Es spricht einiges dafür:
http://www.fiercebiotech.com/story/bluebird-posts-more-promi…
Die Aktie reagiert nachbörslich mit einem deutlichen Sprung. Das ist auch nicht verwunderlich, denn das kommerzielle Potential dieser Technologie könnte sich ggf. als ganz außerordentlich bedeutsam erweisen.
Gentherapie, IO, CAR-T, TCR - sehr, sehr wichtige Entwicklungen. Eine richtungsweisende ASH.
Antwort auf Beitrag Nr.: 48.520.763 von SLGramann am 09.12.14 07:21:36"The most dramatic and durable benefit from LentiGlobin comes from the French HGB-205 study. Last June, the first beta-thalassemia patient was producing 6.6 g/dl of "marked" hemoglobin after 4.5 months. As reported Monday, this patient is now producing 7.7 g/dl of "marked" hemoglobin at 12 months of follow-up. The patient's total hemoglobin is 11 g/dl, essentially normal. No blood transfusions have been required since LentiGlobin treatment.
The second patient in the '205 study has been transfusion free for nine months. At the last assessment done six months following LentiGlobin infusion, the patient was producing 9.6 g/dl of "marked" hemoglobin and total hemoglobin of 13.4 g/dl. Again, this is the hemoglobin level of a healthy adult.
"These results are outstanding," said Bluebird CEO Leschly. "Originally, we thought these patients might start to flatline but they're still improving. We've never seen this before." Bluebird continues to enroll patients in both studies."
So schön das ist - der blutige Laie fragt sich jetzt allerdings, ob hier ein Überschießen bzw. eine Übersteuerung möglich wäre?
Es ist natürlich genau das Ziel, gesunde Werte zu erreichen. Die Werte sind über die Zeit immer weiter angestiegen und sind jetzt normal. Ist es vorstellbar, dass sie weiter steigen? Und welche Konsequenzen hätte dies? Das ist das unheimliche bei der Gentherapie. Du drückst ein mal den Knopf und dann...
The second patient in the '205 study has been transfusion free for nine months. At the last assessment done six months following LentiGlobin infusion, the patient was producing 9.6 g/dl of "marked" hemoglobin and total hemoglobin of 13.4 g/dl. Again, this is the hemoglobin level of a healthy adult.
"These results are outstanding," said Bluebird CEO Leschly. "Originally, we thought these patients might start to flatline but they're still improving. We've never seen this before." Bluebird continues to enroll patients in both studies."
So schön das ist - der blutige Laie fragt sich jetzt allerdings, ob hier ein Überschießen bzw. eine Übersteuerung möglich wäre?
Es ist natürlich genau das Ziel, gesunde Werte zu erreichen. Die Werte sind über die Zeit immer weiter angestiegen und sind jetzt normal. Ist es vorstellbar, dass sie weiter steigen? Und welche Konsequenzen hätte dies? Das ist das unheimliche bei der Gentherapie. Du drückst ein mal den Knopf und dann...
JUNO:
85,4 Mio. Aktien nach IPO.
IPO kommt zu 18 Dollar = 1,5 Mrd. MC, vermutlicher erster Börsenpreis deutlich jenseits der 2 Mrd. Marke.
Da vergehts einem irgendwie etwas...
BLCM:
(Bellicum)
Kommen zu 17 Dollar. 24,8 Mio. Aktien nach IPO = 421 Mio. MC - ein wenig geerdeter...
-------------------
TGTX:
Viel Wind um ihre Ergebnisse. safety wird in den Vordergrund geschoben, da nicht gerade first in class-pipeline, um es vorsichtig zu sagen.
Was ist davon zu halten?
85,4 Mio. Aktien nach IPO.
IPO kommt zu 18 Dollar = 1,5 Mrd. MC, vermutlicher erster Börsenpreis deutlich jenseits der 2 Mrd. Marke.
Da vergehts einem irgendwie etwas...
BLCM:
(Bellicum)
Kommen zu 17 Dollar. 24,8 Mio. Aktien nach IPO = 421 Mio. MC - ein wenig geerdeter...
-------------------
TGTX:
Viel Wind um ihre Ergebnisse. safety wird in den Vordergrund geschoben, da nicht gerade first in class-pipeline, um es vorsichtig zu sagen.
Was ist davon zu halten?
ONTY/ARRY:
Wie sie sehen - sehen sie nichts. Die Ergebnisse sind doch noch sehr früh.


Wie sie sehen - sehen sie nichts. Die Ergebnisse sind doch noch sehr früh.


Antwort auf Beitrag Nr.: 48.515.519 von SLGramann am 08.12.14 15:17:30CBST
"jetzt sind es für Cubist 102 Dollar geworden."
so etwas habe ich auch noch nicht gesehen... wenige Stunden nach der offiziellen Ankündigung der Übernahme kippt ein Gericht einen größeren Teil der Cubicin-Patente, so dass es theoretisch ab 2016 generische Konkurrenz geben könnte. Obwohl Merck 102 USD zahlen will, steht der Kurs nun bei 96 USD... es wird offensichtlich darauf spekuliert, dass die Übernahme noch platzen könnte. Zum Glück habe ich meine Position gestern schon verkauft.

Gruß
ipollit
"jetzt sind es für Cubist 102 Dollar geworden."
so etwas habe ich auch noch nicht gesehen... wenige Stunden nach der offiziellen Ankündigung der Übernahme kippt ein Gericht einen größeren Teil der Cubicin-Patente, so dass es theoretisch ab 2016 generische Konkurrenz geben könnte. Obwohl Merck 102 USD zahlen will, steht der Kurs nun bei 96 USD... es wird offensichtlich darauf spekuliert, dass die Übernahme noch platzen könnte. Zum Glück habe ich meine Position gestern schon verkauft.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.530.147 von ipollit am 09.12.14 21:22:37Da hast du jetzt doppelten Grund zur Freude!!
Man möchte eigentlich meinen, eine Firma wie Merck hat das irgendwie auf dem Schirm
Man möchte eigentlich meinen, eine Firma wie Merck hat das irgendwie auf dem Schirm

Antwort auf Beitrag Nr.: 48.527.705 von SLGramann am 09.12.14 17:29:24JUNO/KITE/BLCM/ALCLS.PA
"Kommen zu 17 Dollar. 24,8 Mio. Aktien nach IPO = 421 Mio. MC - ein wenig geerdeter..."
im Bereich CART/TCR würde ich eher auf Cellectis ALCLS.PA setzen. In der Entwicklung sind sie zwar noch nicht so weit, aber für mich klingen deren CARTs technologisch besser:
- T-Zellen brauchen nicht dem Patienten entnommen und verändert werden, sondern alle Patienten erhalten die gleichen CARTs. Das dürfte schneller und billiger sein.
- CART ist zusätzlich optimiert... z.B. keine Checkpoint-Rezeptoren mehr, so dass man sich einen PD-1 AK für die CARTs sparen kann. Sie sind resistenter gegen Chemo, so dass eine Chemo-Kombi möglich ist
- Schalter-Gen, um die CARTs bei Problemen leicht deaktivieren zu können
- CART und TCR
Partner sind mit Pfizer und Servier auch nicht schlecht. Das ganze für eine MK von ca. 400 Mio USD, wenn ich das richtig sehe. Ist allerdings ein französische Unternehmen, wird aber auch von den Amis beobachtet.

*********
TGTX
"Was ist davon zu halten?" ... so uninteressant finde ich die nicht. GILDs pi3k-delta Idelalisib ist ja bisher eher enttäuschend... angeblich wegen der Nebenwirkungen, insbesondere Kolitis. INFIs pi3k-delta/gamma halte ich wegen gamma für etwas differenzierter... vielleicht ist die Wirkung höher, Nebenwirkungen könnten aber auch hier ein Problem sein. TGR-1202 (delta) könnte von den Nebenwirkungen schon deutlich besser sein. Angeblich hat pi3k-delta wichtige IO-Eigenschaften... bei einer IO-Kombie z.B. mit PD-1 sind meiner Meinung nach geringe Nebenwirkungen wichtig.
Gruß
ipollit
"Kommen zu 17 Dollar. 24,8 Mio. Aktien nach IPO = 421 Mio. MC - ein wenig geerdeter..."
im Bereich CART/TCR würde ich eher auf Cellectis ALCLS.PA setzen. In der Entwicklung sind sie zwar noch nicht so weit, aber für mich klingen deren CARTs technologisch besser:
- T-Zellen brauchen nicht dem Patienten entnommen und verändert werden, sondern alle Patienten erhalten die gleichen CARTs. Das dürfte schneller und billiger sein.
- CART ist zusätzlich optimiert... z.B. keine Checkpoint-Rezeptoren mehr, so dass man sich einen PD-1 AK für die CARTs sparen kann. Sie sind resistenter gegen Chemo, so dass eine Chemo-Kombi möglich ist
- Schalter-Gen, um die CARTs bei Problemen leicht deaktivieren zu können
- CART und TCR
Partner sind mit Pfizer und Servier auch nicht schlecht. Das ganze für eine MK von ca. 400 Mio USD, wenn ich das richtig sehe. Ist allerdings ein französische Unternehmen, wird aber auch von den Amis beobachtet.
*********
TGTX
"Was ist davon zu halten?" ... so uninteressant finde ich die nicht. GILDs pi3k-delta Idelalisib ist ja bisher eher enttäuschend... angeblich wegen der Nebenwirkungen, insbesondere Kolitis. INFIs pi3k-delta/gamma halte ich wegen gamma für etwas differenzierter... vielleicht ist die Wirkung höher, Nebenwirkungen könnten aber auch hier ein Problem sein. TGR-1202 (delta) könnte von den Nebenwirkungen schon deutlich besser sein. Angeblich hat pi3k-delta wichtige IO-Eigenschaften... bei einer IO-Kombie z.B. mit PD-1 sind meiner Meinung nach geringe Nebenwirkungen wichtig.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.520.763 von SLGramann am 09.12.14 07:21:36"Gentherapie, IO, CAR-T, TCR - sehr, sehr wichtige Entwicklungen. Eine richtungsweisende ASH."
schon schön zu sehen, dass es im Biotech/Medizin-Bereich in den letzten Jahren bedeutende Neu-Entwicklungen gibt.
Gen-Therapie ist ja auch ein großes Feld. Wie man an BLUE sieht, hängen Gentherapie und CART eng zusammen, da man für die Konstruktion von CARTs aus den T-Zellen die gleichen Technologien benötigt wie für die Gen-Therapie. CART ist quasi eine Gentherapie außerhalb vom Körper.
Ein weiterer Durchbruch scheint nun auch RNAi zu sein... ich hätte nie gedacht, dass ISIS oder ALNY mal so hohe MKs erreichen. Auch mit RNAi lassen sich Erbkrankheiten behandeln, bei denen bisher nichts geholfen hat. Und gegen Krebs sind nun Targets direkt über RNAi erreichbar... aussichtsreich z.B. ISIS/AZs ISIS-STAT3... ein IO-Target. Oder ISIS-AR, das bei Xtandi-Resistenzen helfen soll.
Gruß
ipollit
schon schön zu sehen, dass es im Biotech/Medizin-Bereich in den letzten Jahren bedeutende Neu-Entwicklungen gibt.
Gen-Therapie ist ja auch ein großes Feld. Wie man an BLUE sieht, hängen Gentherapie und CART eng zusammen, da man für die Konstruktion von CARTs aus den T-Zellen die gleichen Technologien benötigt wie für die Gen-Therapie. CART ist quasi eine Gentherapie außerhalb vom Körper.
Ein weiterer Durchbruch scheint nun auch RNAi zu sein... ich hätte nie gedacht, dass ISIS oder ALNY mal so hohe MKs erreichen. Auch mit RNAi lassen sich Erbkrankheiten behandeln, bei denen bisher nichts geholfen hat. Und gegen Krebs sind nun Targets direkt über RNAi erreichbar... aussichtsreich z.B. ISIS/AZs ISIS-STAT3... ein IO-Target. Oder ISIS-AR, das bei Xtandi-Resistenzen helfen soll.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.530.501 von ipollit am 09.12.14 22:02:14CART... KITE&Co
hier ist ein kritischer Artikel zu CARTs...
http://seekingalpha.com/article/2723935-the-car-t-bubble
Die These darin ist zumindest bedenkenswert: CARTs sind so potent, dass sie selbst Zellen, die das Target in winzigen Mengen expressionieren, bekämpfen können. Das führt aber dazu, dass das Target entweder ganz strikt nur auf Tumorzellen vorkommen darf oder zusätzlich nur auf gesunde Zellen, die sich regenerieren können. Letzteres gilt für CD19-CARTs, bei denen sich die B-Zellen mit CD19 wieder regenerieren. Kritikpunkt ist nun, dass es für CARTs kaum Targets gibt, die das erfüllen, weshalb es kaum andere Targets als CD19 gibt. CART könnte somit ein Hype sein. Der Autor sieht eher TCR als aussichtsreicher.
"My argument is that CD19 could be one of only a few good targets for CAR. So BT for CD19 CAR or a CD19 BiTE is supporting my argument more than it's taking away from it.
You seem to think that CD19 CAR is enough to justify the valuations of Juno, Kite, etc. That's where we disagree. In addition to more established therapies, now there is Blincyto which will be in front of CAR T for CD19 malignancies because of cost. Only patients who fail all other treatments including Blincyto would move on to CAR T. That's not a huge patient population (Blincyto will make it much smaller) and you have at least 4 companies who will be competing for it.
Furthermore, if Cellectis can make the allogenic thing work, they will dominate the CAR T marketplace and Kite and Juno's autologous CD19 CAR will be worthless. Cellectis seems to be leading the field in terms of innovation, yet their valuation is only a fraction of Kite's. The valuation of Cellectis at <$300M is the only one that seems reasonable."
Gruß
ipollit
hier ist ein kritischer Artikel zu CARTs...
http://seekingalpha.com/article/2723935-the-car-t-bubble
Die These darin ist zumindest bedenkenswert: CARTs sind so potent, dass sie selbst Zellen, die das Target in winzigen Mengen expressionieren, bekämpfen können. Das führt aber dazu, dass das Target entweder ganz strikt nur auf Tumorzellen vorkommen darf oder zusätzlich nur auf gesunde Zellen, die sich regenerieren können. Letzteres gilt für CD19-CARTs, bei denen sich die B-Zellen mit CD19 wieder regenerieren. Kritikpunkt ist nun, dass es für CARTs kaum Targets gibt, die das erfüllen, weshalb es kaum andere Targets als CD19 gibt. CART könnte somit ein Hype sein. Der Autor sieht eher TCR als aussichtsreicher.
"My argument is that CD19 could be one of only a few good targets for CAR. So BT for CD19 CAR or a CD19 BiTE is supporting my argument more than it's taking away from it.
You seem to think that CD19 CAR is enough to justify the valuations of Juno, Kite, etc. That's where we disagree. In addition to more established therapies, now there is Blincyto which will be in front of CAR T for CD19 malignancies because of cost. Only patients who fail all other treatments including Blincyto would move on to CAR T. That's not a huge patient population (Blincyto will make it much smaller) and you have at least 4 companies who will be competing for it.
Furthermore, if Cellectis can make the allogenic thing work, they will dominate the CAR T marketplace and Kite and Juno's autologous CD19 CAR will be worthless. Cellectis seems to be leading the field in terms of innovation, yet their valuation is only a fraction of Kite's. The valuation of Cellectis at <$300M is the only one that seems reasonable."
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.531.143 von ipollit am 10.12.14 00:04:31Hallo ipollit,
mal wieder großen Dank dafür, dass du dir hier die Mühe machst, komplexe Themen so zu erklären, dass ich sie (zumindest ansatzweise) nachzuvollziehen kann!!
Welche Möglichkeiten gibt es denn, in TCR zu investieren. Juno, Kite? Ich weiß das Adaptimmune (das ist die Firma, die Medigene verschenkt hat) in diesem Bereich tätig ist. GSK scheint von dem Ansatz zumindest sehr überzeugt zu sein. Ist der Verkauf der Onkologiesparte vielleicht auch vor dem Hintergrund zu sehen, dass GSK da so etwas wie den Resetknopf gedrückt hat, weil sie glauben, dass sich in einigen Jahren die Behandlung eh komplett wandelt?
Wahrscheinlich kennst du die Links schon - ich stelle sie trotzdem mal rein:
http://www.fiercebiotech.com/story/glaxosmithkline-opens-new…
http://www.sugarconebiotech.com/?p=774
http://www.adaptimmune.com/technology/
Eine Diskussion, die sicherlich in nächster Zeit wieder geführt wird ist die nach der Bezahlbarkeit. Die neueren Ergebnisse geben Hoffnung, dass diese Diskussion nicht nur die Krankenkasse betrifft, sondern letztlich auch die Rentenversicherung.
http://www.forbes.com/sites/johnlamattina/2014/12/05/new-can…
Es wird aber sicherlich spannend werden, wie die Bezahlung der Kombinationen praktisch abläuft. Ich hoffe sehr, dass sich die Pharmaunternehmen da verantwortungsvoll verhalten.
Insgesamt finde ich, dass es immer komplexer und unübersichtlicher wird, sich halbwegs auf dem Laufenden zu halten. Zudem werden erfolgsversprechende Ansätze auch immer schneller durch die Klinik gebracht (was ja gut ist). Die Nachhaltigkeit von medizinischen Meilensteinen ist immer begrenzter. Und "Das Bessere ist ja bekanntlich der Feind des Guten"
SG kmastra
mal wieder großen Dank dafür, dass du dir hier die Mühe machst, komplexe Themen so zu erklären, dass ich sie (zumindest ansatzweise) nachzuvollziehen kann!!
Welche Möglichkeiten gibt es denn, in TCR zu investieren. Juno, Kite? Ich weiß das Adaptimmune (das ist die Firma, die Medigene verschenkt hat) in diesem Bereich tätig ist. GSK scheint von dem Ansatz zumindest sehr überzeugt zu sein. Ist der Verkauf der Onkologiesparte vielleicht auch vor dem Hintergrund zu sehen, dass GSK da so etwas wie den Resetknopf gedrückt hat, weil sie glauben, dass sich in einigen Jahren die Behandlung eh komplett wandelt?
Wahrscheinlich kennst du die Links schon - ich stelle sie trotzdem mal rein:
http://www.fiercebiotech.com/story/glaxosmithkline-opens-new…
http://www.sugarconebiotech.com/?p=774
http://www.adaptimmune.com/technology/
Eine Diskussion, die sicherlich in nächster Zeit wieder geführt wird ist die nach der Bezahlbarkeit. Die neueren Ergebnisse geben Hoffnung, dass diese Diskussion nicht nur die Krankenkasse betrifft, sondern letztlich auch die Rentenversicherung.

http://www.forbes.com/sites/johnlamattina/2014/12/05/new-can…
Es wird aber sicherlich spannend werden, wie die Bezahlung der Kombinationen praktisch abläuft. Ich hoffe sehr, dass sich die Pharmaunternehmen da verantwortungsvoll verhalten.
Insgesamt finde ich, dass es immer komplexer und unübersichtlicher wird, sich halbwegs auf dem Laufenden zu halten. Zudem werden erfolgsversprechende Ansätze auch immer schneller durch die Klinik gebracht (was ja gut ist). Die Nachhaltigkeit von medizinischen Meilensteinen ist immer begrenzter. Und "Das Bessere ist ja bekanntlich der Feind des Guten"
SG kmastra
Antwort auf Beitrag Nr.: 48.529.796 von kmastra am 09.12.14 20:38:15Wie sie sehen - sehen sie nichts. Die Ergebnisse sind doch noch sehr früh.
Abstracts sind wohl aber auch 6 Monate alt. So wie ich es verstehe, werden noch neuere Daten präsentiert. ONTY hat neben 380 noch eine Technologie Namens Protocells zu bieten:
The protocell consists of porous nanoparticles that are covered with a protective coating similar to the membranes that surround live cells, plus a protein that allows them to bind specifically with cancer cells.
The goal is to load the nanoparticles with cancer-killing drugs and inject them into the bloodstream, where they then would drift harmlessly until binding with cancer cells to release their cargo.
http://alpinebio.com/technology.html
http://www.abqjournal.com/316517/biz/protocell-therapy-gains…
Was ist davon zu halten? Klingt fast schon altmodisch!?
Abstracts sind wohl aber auch 6 Monate alt. So wie ich es verstehe, werden noch neuere Daten präsentiert. ONTY hat neben 380 noch eine Technologie Namens Protocells zu bieten:
The protocell consists of porous nanoparticles that are covered with a protective coating similar to the membranes that surround live cells, plus a protein that allows them to bind specifically with cancer cells.
The goal is to load the nanoparticles with cancer-killing drugs and inject them into the bloodstream, where they then would drift harmlessly until binding with cancer cells to release their cargo.
http://alpinebio.com/technology.html
http://www.abqjournal.com/316517/biz/protocell-therapy-gains…
Was ist davon zu halten? Klingt fast schon altmodisch!?
Rückblick auf 2014 und Ausblick auf 2015:
http://editiondigital.net/publication/frame.php?i=236495&p&p…
http://www.evaluategroup.com/public/Reports/EPVantage-Pharma…
http://editiondigital.net/publication/frame.php?i=236495&p&p…
http://www.evaluategroup.com/public/Reports/EPVantage-Pharma…
CLDN:
Vermutlich habt ihr auch den Kommentar im Hammer-Blog gelesen:
CLDN in particular looks very interesting – breakthrough designation, Phase II data in April with endpoints easy to achieve: Risk Reduction of 45%, HR 0.55, while they had in Phase I with one year data RR 88%, HR 0.12 at p=0.003.
Based on the BTD and relatively large Ph II trail (250 pts.) they may ask for accelerated approval with the Phase II data.
It is still $370M even after the run in the last several days.
----------
Auf den ersten Blick sieht das wirklich ganz spannend aus. Ich habe das S1 mal überflogen. Ich denke, hier lohnt sich ein zweiter Blick - mindestens.
Hier müsste das S1 als pdf zum download stehen (Achtung: großes File):
http://ir.celladon.com/common/download/sec.cfm?CompanyID=AMD…
Vermutlich habt ihr auch den Kommentar im Hammer-Blog gelesen:
CLDN in particular looks very interesting – breakthrough designation, Phase II data in April with endpoints easy to achieve: Risk Reduction of 45%, HR 0.55, while they had in Phase I with one year data RR 88%, HR 0.12 at p=0.003.
Based on the BTD and relatively large Ph II trail (250 pts.) they may ask for accelerated approval with the Phase II data.
It is still $370M even after the run in the last several days.
----------
Auf den ersten Blick sieht das wirklich ganz spannend aus. Ich habe das S1 mal überflogen. Ich denke, hier lohnt sich ein zweiter Blick - mindestens.
Hier müsste das S1 als pdf zum download stehen (Achtung: großes File):
http://ir.celladon.com/common/download/sec.cfm?CompanyID=AMD…
FGEN:
Analysts at Leerink Swann initiate coverage of FibroGen, Inc (FGEN) with a "outperform" rating.

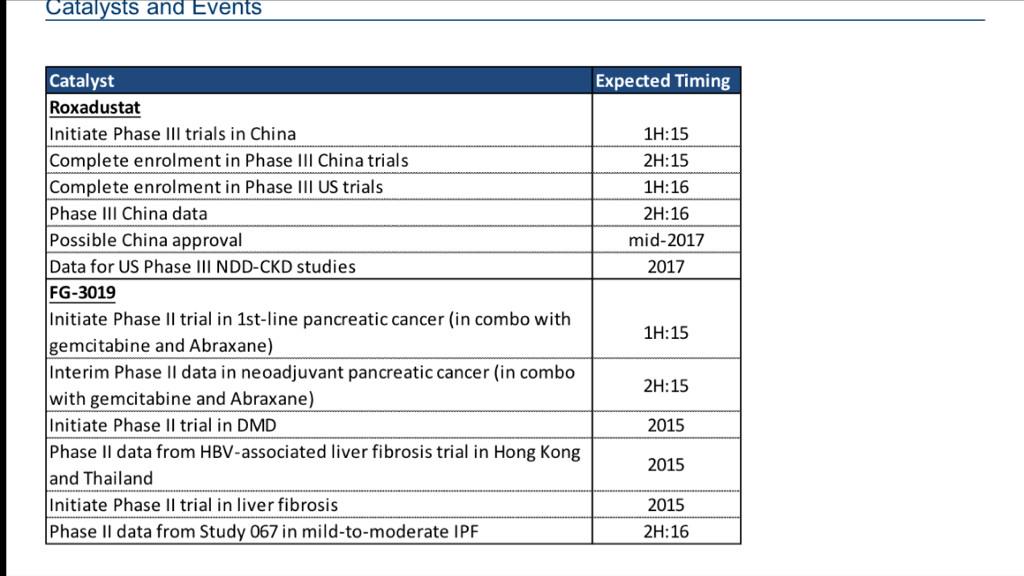
Analysts at Leerink Swann initiate coverage of FibroGen, Inc (FGEN) with a "outperform" rating.


ARRY:
Oncothyreon Announces Exclusive License Agreement With Array BioPharma for ONT-380
http://finance.yahoo.com/news/oncothyreon-announces-exclusiv…
Finde ich vernünftig. Man generiert etwas Cash, reduziert das eigene Engagement, profitiert aber signifikant von eventuellen künftigen Erfolgen.
Der Deal ist offensichtlich Teil der strategischen Entscheidung, sich auf Binimetinib zu konzentrieren.
Oncothyreon Announces Exclusive License Agreement With Array BioPharma for ONT-380
http://finance.yahoo.com/news/oncothyreon-announces-exclusiv…
Finde ich vernünftig. Man generiert etwas Cash, reduziert das eigene Engagement, profitiert aber signifikant von eventuellen künftigen Erfolgen.
Der Deal ist offensichtlich Teil der strategischen Entscheidung, sich auf Binimetinib zu konzentrieren.
CCXI:
Vorbörslich über 100% im Plus wegen:
ChemoCentryx Announces Positive Results in Phase II Diabetic Nephropathy Trial With CCR2 Inhibitor CCX140
http://finance.yahoo.com/news/chemocentryx-announces-positiv…
Leider kann ich den Sachverhalt derzeit nicht recht einordnen.
Vorbörslich über 100% im Plus wegen:
ChemoCentryx Announces Positive Results in Phase II Diabetic Nephropathy Trial With CCR2 Inhibitor CCX140
http://finance.yahoo.com/news/chemocentryx-announces-positiv…
Leider kann ich den Sachverhalt derzeit nicht recht einordnen.
Antwort auf Beitrag Nr.: 48.556.709 von SLGramann am 12.12.14 13:49:08ARRY:
Oncothyreon Announces Presentation of Positive ONT-380 Data at San Antonio Breast Cancer Symposium
http://finance.yahoo.com/news/oncothyreon-announces-presenta…
Sieht vielversprechend aus!
Sollte heute erfreulich werden für Array bzw. die Aktionäre.
Oncothyreon Announces Presentation of Positive ONT-380 Data at San Antonio Breast Cancer Symposium
http://finance.yahoo.com/news/oncothyreon-announces-presenta…
Sieht vielversprechend aus!
Sollte heute erfreulich werden für Array bzw. die Aktionäre.
Antwort auf Beitrag Nr.: 48.556.709 von SLGramann am 12.12.14 13:49:08Ja. Macht Sinn für beide. ARRY hätte ja sonst auch Co-Finanzieren müssen. Etwas enttäuschend finde ich die Royalties "up to doubledigit". Das kann natürlich viel heißen, jedoch hört es sich so an, als ob es im einstelligen Prozentbereich losgeht. Merkwürdig, dass explizit eine mögliche Übernahme von ONTY in den Deal eingearbeitet wurde. Das wäre jetzt zumindest möglich (im Bezug auf ONT380).
Die Ergebnisse selber finde ich eigentlich auch sehr vielversprechend. ONT380 ist auf jeden Fall keine Luftnummer. Wird an der Börse aber irgendwie so bewertet...
http://finance.yahoo.com/news/oncothyreon-announces-presenta…
Die Ergebnisse selber finde ich eigentlich auch sehr vielversprechend. ONT380 ist auf jeden Fall keine Luftnummer. Wird an der Börse aber irgendwie so bewertet...
http://finance.yahoo.com/news/oncothyreon-announces-presenta…
Antwort auf Beitrag Nr.: 48.557.300 von SLGramann am 12.12.14 14:44:25CCXI
Den Kurssprung - falls er sich etabliert - finde ich überraschend. Denn bei der Bekanntgabe von eher schwachen 12-Wochen-Interimsdaten aus dieser Studie im Sep/13 wurde die Aktie nach unten durchgereicht. Nun ist zu lesen, dass der beste ACR-Effekt während der 52-Wochen-Behandlung just nach diesen 12 Wochen gemessen wurde, sich also durch längere Behandlung nicht weiter verbessert hat. Die heutige Kursexplosion verstehe ich daher nicht wirklich. Vielleicht liegt es an den aggressiv formulierten P3-Absichten in der PM.
Mich interessiert CCX140 gegen CCR2 in Diabet. Nephropathie, weil Noxxon Pharma mit NOX-E36 direkter Konkurrent ist, allerdings nicht gegen den Rezeptor, sondern gegen den Liganden CCL2. M.E. sind die 12-Wochen-Daten von NOX-E36 deutlich besser gewesen als die vergleichbaren von CCX140.
Ich werde mir die Tage den CC anhören und auch die genauen Daten der Studie anschauen, sobald sie von CCXI veröffentlicht werden. Vermutlich werde ich irgendwas dazu dann im Noxxon-Thread schreiben, falls es Dich/jemanden interessiert. Wird aber dauern, muss mich erst wieder intensiver einarbeiten.
Grüße - und danke an alle für diesen tollen Thread!
Den Kurssprung - falls er sich etabliert - finde ich überraschend. Denn bei der Bekanntgabe von eher schwachen 12-Wochen-Interimsdaten aus dieser Studie im Sep/13 wurde die Aktie nach unten durchgereicht. Nun ist zu lesen, dass der beste ACR-Effekt während der 52-Wochen-Behandlung just nach diesen 12 Wochen gemessen wurde, sich also durch längere Behandlung nicht weiter verbessert hat. Die heutige Kursexplosion verstehe ich daher nicht wirklich. Vielleicht liegt es an den aggressiv formulierten P3-Absichten in der PM.
Mich interessiert CCX140 gegen CCR2 in Diabet. Nephropathie, weil Noxxon Pharma mit NOX-E36 direkter Konkurrent ist, allerdings nicht gegen den Rezeptor, sondern gegen den Liganden CCL2. M.E. sind die 12-Wochen-Daten von NOX-E36 deutlich besser gewesen als die vergleichbaren von CCX140.
Ich werde mir die Tage den CC anhören und auch die genauen Daten der Studie anschauen, sobald sie von CCXI veröffentlicht werden. Vermutlich werde ich irgendwas dazu dann im Noxxon-Thread schreiben, falls es Dich/jemanden interessiert. Wird aber dauern, muss mich erst wieder intensiver einarbeiten.
Grüße - und danke an alle für diesen tollen Thread!
Antwort auf Beitrag Nr.: 48.557.975 von Saaletaler am 12.12.14 15:47:21"Ich werde mir die Tage den CC anhören und auch die genauen Daten der Studie anschauen, sobald sie von CCXI veröffentlicht werden. Vermutlich werde ich irgendwas dazu dann im Noxxon-Thread schreiben, falls es Dich/jemanden interessiert. Wird aber dauern, muss mich erst wieder intensiver einarbeiten."
Hallo Saaletaler,
wäre sehr schön, dazu etwas von Dir zu lesen. Ich habe Deinen Thread immer mit im Auge.
Gruß
SLG
Hallo Saaletaler,
wäre sehr schön, dazu etwas von Dir zu lesen. Ich habe Deinen Thread immer mit im Auge.
Gruß
SLG
Antwort auf Beitrag Nr.: 48.557.666 von kmastra am 12.12.14 15:25:04"Wird an der Börse aber irgendwie so bewertet..."
Ja, weder bei Array noch bei ONTY eine Reaktion. Ich war aber auch noch nie gut im Kurse vorhersagen. Da sieht man es wieder.
Ja, weder bei Array noch bei ONTY eine Reaktion. Ich war aber auch noch nie gut im Kurse vorhersagen. Da sieht man es wieder.

Antwort auf Beitrag Nr.: 48.500.792 von lawmeetstax am 05.12.14 16:34:59@AMBI
Folgende Antwort habe ich von der ING-Diba bekommen:
Guten Tag Herr XXX,
wir haben eine Anfrage an unseren Dienstleister Wertpapier-Mitteilungen gestellt. Folgende Auskunft haben wir jetzt erhalten:
Die Einbuchung der Contingent Value Rights (CVRs) stellt einen Kapitalertrag in Höhe von 0,00 Euro dar. Das Anschaffungsdatum sowie nicht durch die erste Zahlung aufgebrauchte Anschaffungskosten sind zu übernehmen. Die CVRs gelten zum 26.05.2014 als angeschafft. Die Einbuchung erfolgt mit einem Kurs von 0,00 Euro.
Beispiel:
Usprüngliche Anschaffungskosten: 18 Euro
Veräußerung zu 15 Euro + Zuteilung CVR
Die übrigen 3 Euro werden auf die CVRs übertragen. Sollte es zu einer Nachzahlung über die CVR's kommen, sind diese Zahlungen steuerfrei bis zu 3 Euro.
Sollten die Anschaffungskosten allerdings 15 EUR oder weniger betragen haben, werden auch keine weiteren Anschaffungskosten auf die CVR's übertragen. Somit wären künftige Zahlungen über die CVR's steuerpflichtig.
Die erforderlichen Stornierungen und Neuabrechnungen führen wir heute durch.
Sie haben weitere Fragen? Auf www.ing-diba.de/wertpapiere haben wir alles Wissenswerte für Sie zusammengefasst. Oder senden Sie uns eine E-Mail an info@ing-diba.de.
Mit freundlichen Grüßen
XXX
ING-DiBa AG
60628 Frankfurt am Main
info@ing-diba.de
www.ing-diba.de
Meine zuviel abgezogene Steuer wurde erstattet und die CVRs sind jetzt mit Anschaffungswert 0€ bewertet, so wie sich das gehört. Habe allerdings 2x nachbohren müssen.
Folgende Antwort habe ich von der ING-Diba bekommen:
Guten Tag Herr XXX,
wir haben eine Anfrage an unseren Dienstleister Wertpapier-Mitteilungen gestellt. Folgende Auskunft haben wir jetzt erhalten:
Die Einbuchung der Contingent Value Rights (CVRs) stellt einen Kapitalertrag in Höhe von 0,00 Euro dar. Das Anschaffungsdatum sowie nicht durch die erste Zahlung aufgebrauchte Anschaffungskosten sind zu übernehmen. Die CVRs gelten zum 26.05.2014 als angeschafft. Die Einbuchung erfolgt mit einem Kurs von 0,00 Euro.
Beispiel:
Usprüngliche Anschaffungskosten: 18 Euro
Veräußerung zu 15 Euro + Zuteilung CVR
Die übrigen 3 Euro werden auf die CVRs übertragen. Sollte es zu einer Nachzahlung über die CVR's kommen, sind diese Zahlungen steuerfrei bis zu 3 Euro.
Sollten die Anschaffungskosten allerdings 15 EUR oder weniger betragen haben, werden auch keine weiteren Anschaffungskosten auf die CVR's übertragen. Somit wären künftige Zahlungen über die CVR's steuerpflichtig.
Die erforderlichen Stornierungen und Neuabrechnungen führen wir heute durch.
Sie haben weitere Fragen? Auf www.ing-diba.de/wertpapiere haben wir alles Wissenswerte für Sie zusammengefasst. Oder senden Sie uns eine E-Mail an info@ing-diba.de.
Mit freundlichen Grüßen
XXX
ING-DiBa AG
60628 Frankfurt am Main
info@ing-diba.de
www.ing-diba.de
Meine zuviel abgezogene Steuer wurde erstattet und die CVRs sind jetzt mit Anschaffungswert 0€ bewertet, so wie sich das gehört. Habe allerdings 2x nachbohren müssen.
@Eilzug
Besten Dank für Deine Nachricht! Die neuen Einsichten bei WM sollten den allermeisten weiterhelfen. Ganz richtig ist das freilich immer noch nicht, im Verlustfall stellt WM immer noch die falschen Daten bereit...
Die Deutsche Bank sitzt immer noch auf dem Fall und hat noch nicht berichtigt.
Besten Dank für Deine Nachricht! Die neuen Einsichten bei WM sollten den allermeisten weiterhelfen. Ganz richtig ist das freilich immer noch nicht, im Verlustfall stellt WM immer noch die falschen Daten bereit...
Die Deutsche Bank sitzt immer noch auf dem Fall und hat noch nicht berichtigt.
arry:
Die GSK Aktionäre segnen den GSK/NVS Deal ab. Am 14.1. sollen die europäischen Wettbewerbshüter entscheiden. Das dürfte einer der letzten Bausteine sein, bevor die Rückkehr von MEK162 definitiv wird.
A
Die GSK Aktionäre segnen den GSK/NVS Deal ab. Am 14.1. sollen die europäischen Wettbewerbshüter entscheiden. Das dürfte einer der letzten Bausteine sein, bevor die Rückkehr von MEK162 definitiv wird.
A
ARRY... in den nächsten 2 Jahren anstehende Events
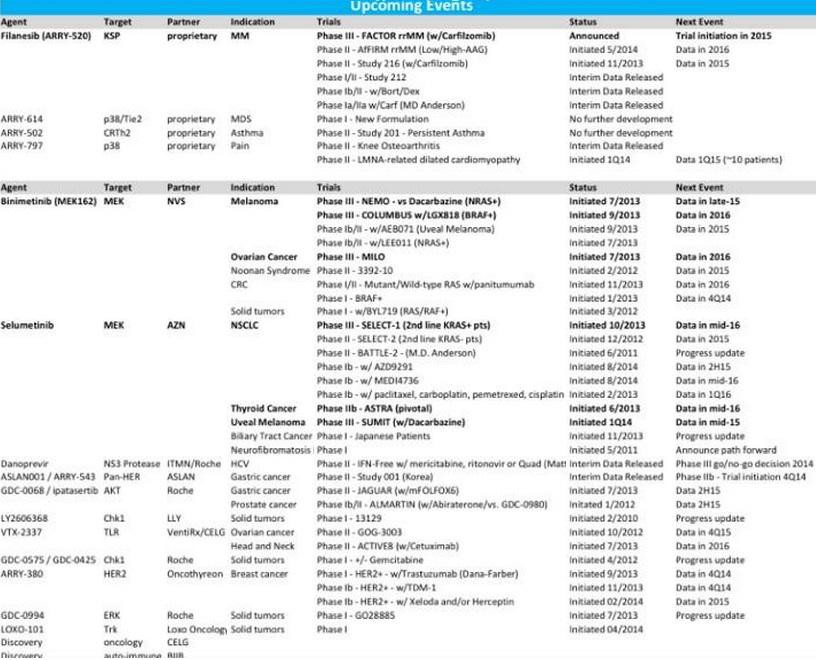
Gruß
ipollit

Gruß
ipollit
MGNX
AMGNs (zuvor Micromets) CD19 x CD3 BITE Blincyto (Blinatumomab) hat vor Kurzen weit vor dem eigentlichen PDFUA-Datum die Zulassung gegen ALL erhalten:
http://www.bioworld.com/content/amgen-takes-%E2%80%98bite%E2…
"The FDA today granted accelerated approval with breakneck speed – more than five months ahead of its May 19, 2015, PDUFA date – to Amgen Inc.’s blinatumomab to treat patients with relapsed or refractory Philadelphia chromosome-negative precursor B-cell acute lymphoblastic leukemia, or B-cell ALL, a rare form of ALL."
Die BITE-Technologie kommt ursprünglich aus Deutschland... Micromet war allerdings nicht in Deutschland sondern direkt in den USA gelistet.
http://www.helmholtz.de/gesundheit/was-ist-dran-am-neuen-ant…
Was ist dran am neuen Anti-Leukämie-Wirkstoff?...
Mit 178.000 USD ist es nun einer der teuersten Krebstherapien. Allerdings gibt es in den USA nur ca. 1000 ALL-Patienten, für die diese Therapie in Frage kommt. Andere IO-Therapien sind auch recht teuer:
http://www.reuters.com/article/2014/12/17/us-amgen-cancer-ex…
"... "The overall price of Blincyto is definitely on the high side for cancer drugs," said Michael Yee, an analyst with RBC Capital Markets. But he said the price was not surprising given the drug's impressive effectiveness and that only about 1,000 Americans who had failed previous therapy would be eligible to take it. Yee estimated Blincyto could reap annual sales of $100 million for ALL, assuming that half of all eligible patients take the medicine. "That would make it a pretty small drug," he said.
... Other costly immuno-oncology drugs, which work by harnessing the immune system, include Bristol-Myers Squibb Co's Yervoy treatment for melanoma, which costs about $120,000 for a complete course of four infusions. Merck & Co's new Keytruda melanoma drug costs $150,000 for a year of treatment..."
Blincyto ist ähnlich wie CD19-CARTs. Mal schauen, wie teuer in Zukunft die CART-Therapien werden. CART wird jedenfalls sehr viel teuerer in der Herstellung sein, da für jeden Patienten individuelle CARTs aus lebenden Zellen erzeugt werden müssen.
https://twitter.com/adamfeuerstein/status/545258823259521024
Is $AMGN Blincyto price a proxy for eventual CAR-T pricing? Although Blincyto isn’t personalized like CAR-Ts, right?
***
No. The CAR-Ts will price above stem cell transplants, which they hope to replace, or $350,000-450,000
***
The CAR-T programs can't make money at $178,000
***
Jimenez has specifically told me that he will not do this, and I think Bishop told me that was too high.
***
results would need to be superior to HCT to be priced above and HCT cures patients
***
David, your price point seems obscene and unjustifiable given relapse rates.
***
COGS high. Don't have good numbers. Margins might be better than $DNDN's. @AlpineBV_Miller, what say you on COGS?
***
COGS are orders of magnitude higher than Provenge.
Ein Nachteil von Blincyto ist die kurze Halbwertzeit, d.h. der Wirkstoff bleibt nur sehr kurz im Blut. Daher muss es mit einer permanenten Infusion über mehrere Wochen verabreicht werden.
MGNXs DART-Technologie ist ein Konkurrent von BITE... beides sind quasi bi-spezifische AKs. Der CD19 x CD3 DART, der demnächst in P1 gehen soll, soll stärker gepackt sein als BITE, wodurch T-Zellen näher an das Target gebunden werden, was die Wirkung erhöht. Außerdem können sie eine Modifikation erhalten, die die Halbwertzeit deutlich verlängern... ähnlich wie AKs können die DARTs dann einmal pro Woche oder weniger verabreicht werden. Langfristig könnten DARTs eine interessante Technologie sein.
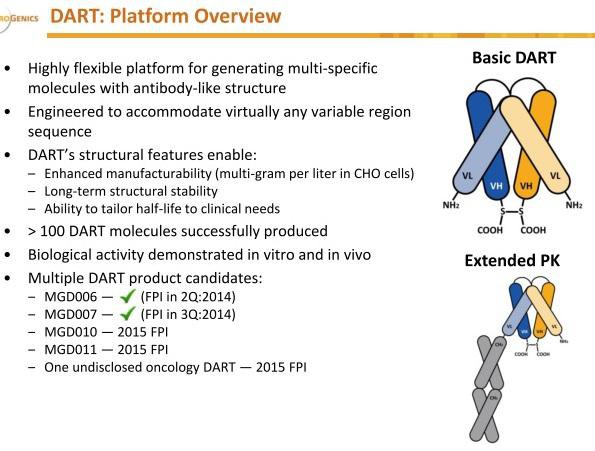
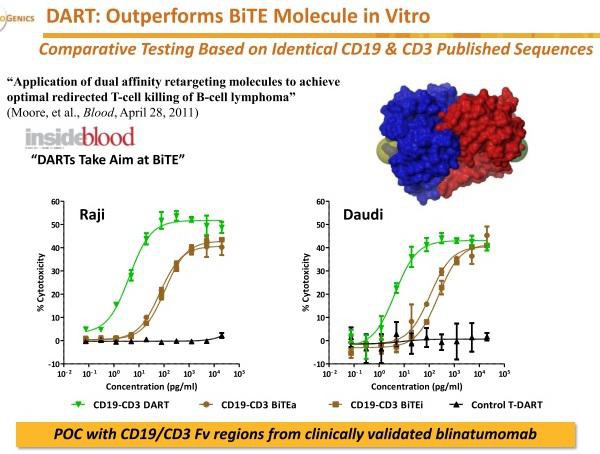
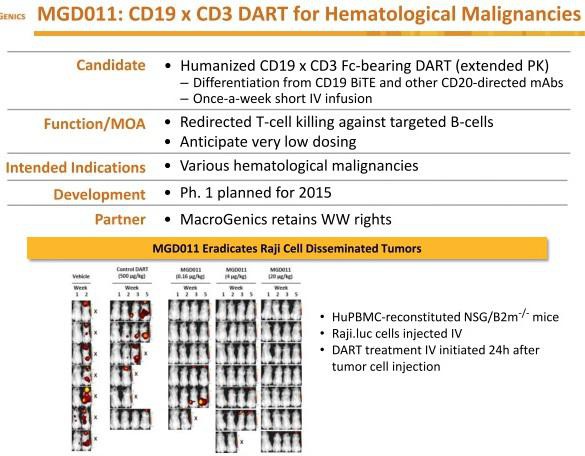
Ohad Hammer hatte mal geschrieben...
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3499297/
"A CD19xCD3 DART was designed for optimal recruitment of T cells for killing CD19-positive cells. Like blinatumomab, it is a bivalent antibody capable of co-engaging a T cell and a target cell simultaneously. Using PBMC as effector cells, CD19xCD3 DART demonstrated potent lysis of CD19-positive cells in a target-specific manner.48 Interestingly, compared with the same Fv sequences incorporated into a BiTE format, CD19XCD3 DART was 16–60 fold more potent."
CD19-Therapien sind eine Alternative zu CD20-AKs wie Rituxan... also sind es im wesentlichen Blutkrebsarten, für die diese Therapien in Frage kommen.

Gruß
ipollit
AMGNs (zuvor Micromets) CD19 x CD3 BITE Blincyto (Blinatumomab) hat vor Kurzen weit vor dem eigentlichen PDFUA-Datum die Zulassung gegen ALL erhalten:
http://www.bioworld.com/content/amgen-takes-%E2%80%98bite%E2…
"The FDA today granted accelerated approval with breakneck speed – more than five months ahead of its May 19, 2015, PDUFA date – to Amgen Inc.’s blinatumomab to treat patients with relapsed or refractory Philadelphia chromosome-negative precursor B-cell acute lymphoblastic leukemia, or B-cell ALL, a rare form of ALL."
Die BITE-Technologie kommt ursprünglich aus Deutschland... Micromet war allerdings nicht in Deutschland sondern direkt in den USA gelistet.
http://www.helmholtz.de/gesundheit/was-ist-dran-am-neuen-ant…
Was ist dran am neuen Anti-Leukämie-Wirkstoff?...
Mit 178.000 USD ist es nun einer der teuersten Krebstherapien. Allerdings gibt es in den USA nur ca. 1000 ALL-Patienten, für die diese Therapie in Frage kommt. Andere IO-Therapien sind auch recht teuer:
http://www.reuters.com/article/2014/12/17/us-amgen-cancer-ex…
"... "The overall price of Blincyto is definitely on the high side for cancer drugs," said Michael Yee, an analyst with RBC Capital Markets. But he said the price was not surprising given the drug's impressive effectiveness and that only about 1,000 Americans who had failed previous therapy would be eligible to take it. Yee estimated Blincyto could reap annual sales of $100 million for ALL, assuming that half of all eligible patients take the medicine. "That would make it a pretty small drug," he said.
... Other costly immuno-oncology drugs, which work by harnessing the immune system, include Bristol-Myers Squibb Co's Yervoy treatment for melanoma, which costs about $120,000 for a complete course of four infusions. Merck & Co's new Keytruda melanoma drug costs $150,000 for a year of treatment..."
Blincyto ist ähnlich wie CD19-CARTs. Mal schauen, wie teuer in Zukunft die CART-Therapien werden. CART wird jedenfalls sehr viel teuerer in der Herstellung sein, da für jeden Patienten individuelle CARTs aus lebenden Zellen erzeugt werden müssen.
https://twitter.com/adamfeuerstein/status/545258823259521024
Is $AMGN Blincyto price a proxy for eventual CAR-T pricing? Although Blincyto isn’t personalized like CAR-Ts, right?
***
No. The CAR-Ts will price above stem cell transplants, which they hope to replace, or $350,000-450,000
***
The CAR-T programs can't make money at $178,000
***
Jimenez has specifically told me that he will not do this, and I think Bishop told me that was too high.
***
results would need to be superior to HCT to be priced above and HCT cures patients
***
David, your price point seems obscene and unjustifiable given relapse rates.
***
COGS high. Don't have good numbers. Margins might be better than $DNDN's. @AlpineBV_Miller, what say you on COGS?
***
COGS are orders of magnitude higher than Provenge.
Ein Nachteil von Blincyto ist die kurze Halbwertzeit, d.h. der Wirkstoff bleibt nur sehr kurz im Blut. Daher muss es mit einer permanenten Infusion über mehrere Wochen verabreicht werden.
MGNXs DART-Technologie ist ein Konkurrent von BITE... beides sind quasi bi-spezifische AKs. Der CD19 x CD3 DART, der demnächst in P1 gehen soll, soll stärker gepackt sein als BITE, wodurch T-Zellen näher an das Target gebunden werden, was die Wirkung erhöht. Außerdem können sie eine Modifikation erhalten, die die Halbwertzeit deutlich verlängern... ähnlich wie AKs können die DARTs dann einmal pro Woche oder weniger verabreicht werden. Langfristig könnten DARTs eine interessante Technologie sein.



Ohad Hammer hatte mal geschrieben...
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3499297/
"A CD19xCD3 DART was designed for optimal recruitment of T cells for killing CD19-positive cells. Like blinatumomab, it is a bivalent antibody capable of co-engaging a T cell and a target cell simultaneously. Using PBMC as effector cells, CD19xCD3 DART demonstrated potent lysis of CD19-positive cells in a target-specific manner.48 Interestingly, compared with the same Fv sequences incorporated into a BiTE format, CD19XCD3 DART was 16–60 fold more potent."
CD19-Therapien sind eine Alternative zu CD20-AKs wie Rituxan... also sind es im wesentlichen Blutkrebsarten, für die diese Therapien in Frage kommen.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.608.051 von ipollit am 18.12.14 18:03:27MGNX, IPH.PA
ein eher kritischer Artikel zu MGNX B7-H3 AK MGA271...
http://seekingalpha.com/article/2755545-b7-h3-and-pdminus-1-…
- B7-H3 sei kein IO-Target wie z.B. PD1... die Funktion sei unklar (kann z.B. hemmend und stimmulierend wirken)
- B7-H3 könnte aber ein gutes Krebs-Target sein: "What does seem to be special about B7-H3 is that it's highly expressed on many solid tumors and not on normal tissue."
- 131I-8H9 ist ein nicht humaner B7-H3 AK, der als ADC mit einem radioaktivem Stoff gekoppelt ist. Dieser lieferte bereits interessante klinische Ergebnisse, was B7-H3 validiert und das Risiko von Nebenwirkungen für B7-H3 AKs senkt
- MGA271 ist ein AK, der auf hohe ADCC optimiert ist... d.h. die Aktivierung von NK-Zellen bei der Bindung an das Target. Kritisch wäre aber, dass laut präklinischen Studien MGA271 gleichzeitg NK-Zellen senken würde.
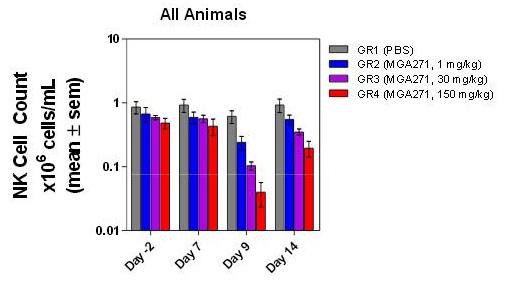
(MGA271 wurde am 8. Tag verabreicht)
Die Senkung von NK-Zellen wäre natürlich ungünstig, wenn MGA271 für seine Wirkung im Wesentlichen NK-Zellen benötigt. Allerdings ist es nicht ganz klar, ob sich dies auch im Menschen so verhält und ob nicht eine Senkung im Blut durch das Wandern der NK-Zellen in den Tumor erklärt werden kann. Es ist zumindest etwas Unsicherheit.
In diesem Zusammenhang ist aber auch interessant, dass NK-Zellen bei der Wirkung von AKs eine wichtige Rolle zu spielen scheinen. So wurde zuletzt bei Untersuchungen festgestellt, dass die Wirkung des bekannten HER2-AK Herceptin nicht direkt von der Bindung des AKs an HER2 abhängt, sondern HER2 durch aktivierte NK-Zellen heruntergeregelt wird. Das Zusammenspielt von Herceptin mit NK-Zellen ist sehr wichtig. Dies wird auch in diesem Artikel erwähnt:
"The importance of NK cells for therapeutic monoclonal antibodies that treat malignancy is well known. For example, this paper nicely demonstrates in a mouse tumor model that the efficacy of 4D5 (the parent for trastuzumab) is entirely dependent on NK cells. The tumor volume in the NK cell depleted, 4D5 treated animals is identical or even slightly larger than the undepleted, PBS treated animals."
Dies finde ich spannend im Bezug auf IPH.PA, da dies eines der wenigen Unternehmen ist, die speziell diesen Teil des Immunsystems untersuchen und Therapien entwickeln, die etwas entsprechends wie PD1 für T-Zellen auch für NK-Zellen sind. So kann z.B. der IPH.PAs KIR-AK, der die Hemmung von NK-Zellen unterbricht, die Wirkung von anderen AKs wie Herceptin erhöhen, insbesondere, wenn diese AKs von NK-Zellen abhängen.
http://innate-pharma.com/en/product-pipeline/lirilumab-first…
"Lirilumab (IPH2102/BMS-986015) is a fully human monoclonal antibody blocking interaction between Killer-cell immunoglobulin-like receptors (KIR) on NK cells with their ligands.
Blocking these receptors facilitates activation of NK cells and, potentially, destruction of tumor cells by the latter.
NK cells (Natural Killer) are non conventional lymphocytes, belonging to the innate immunity compartment. They are able to:
- Directly and selectively kill « stressed » cells (cancerous, infected or over-activated cells);
- Participate in the set up of a global immune reaction against a selected target, notably via the production of cytokines (the communicating agents of the immune system)
- Bind one of the two ends of cytotoxic antibodies, and then kill cells recognized by these antibodies. This property is known as antibody-dependent cellular cytotoxicity (ADCC)
The mechanism behind NK cells activation depends on a balance between activatory and inhibitory signals, ie. signals of abnormality sent by the target:
- Normal cells send “normality” signals and are thus spared by NK cells;
- Cells undergoing a stress (infection, cancerous transformation, over activation) can send normality as well as danger signals at the same time. This can result in the “blinding” of NK cells.
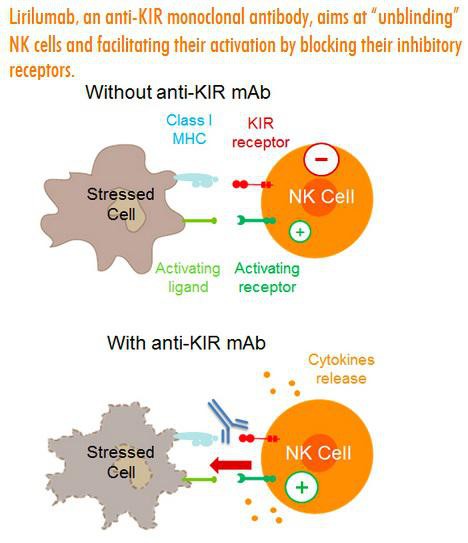

"MGNX to broaden MGA271 monotherapy Phase Ib program in 2H14. In addition to three currently enrolling expansion cohorts in prostate cancer, melanoma, and B7-H3+ all-comers, MGNX will pursue other tumor types in further cohorts 2H14. The specific indications have not been determined yet but will take into consideration the expression profile of B7-H3. B7-H3 is also highly expressed on cancers of the kidney, pancreas, breast, and ovaries. MGNX expects to complete the initial three cohorts in late '14 and the additional cohorts in '15. Servier will initiate two additional tumor types this week.
MGNX to test MGA271 combinations likely including, but not limited to, immuno-oncology (IO) combinations. Potential combinations will take into consideration mechanistic synergies, e.g., with Tx that target the tumor vasculature where B7-H3 is expressed. Potential combos with other checkpoint inhibitors are possibilities. Combination with natural killer (NK)-cell targeted agents such as IPH/BMY's anti-KIR (lirilumab) would also make sense in our view, given that it can enhance antibody-dependent cellular cytotoxicity (ADCC), which is part of MGA271's mechanism. Combos with Tx that are approved or those that are still in development are being considered by mgmt. We like MGNX's broad and rigorous approach in Phase Ib before settling on specific development plans.
***
Lirilumab’s potential beyond current indications may include Rituxan combo in RA/blood cancer, with management citing synergistic impact on ADCC induction in preclinical studies.
Potential highly attractive combinations could include anti- KIR or anti-NKG2A with anti-CD20 (rituximab) or anti-4-1BB (e.g., urelumab). Recently published preclinical data suggest that KIR blockade with NK cell activating antibodies could lead to a more substantial immune-mediated effect. Antigen-specific therapeutic antibodies that stimulate the NK cell activating Fc receptor such as rituximab (Rituxan) or trastuzumab (Herceptin) are significantly more potent in combination with lirilumab. KOLs also suggested that blocking KIR or NKG2A could enhance anti-4-1BB (CD137) activity at a lower dose and thus overcome some of the toxicities associated with this molecule while enhancing both NK cell and T-cell activity against tumors.
***
Bristol-Myers Squibb: Next Focus is Antibody Enhancement Through Immunotherapy; Long-Term Potential of
Triple Combination with Urelumab, Lirilumab and a MAb Intriguing Bristol-Myers (BMY) have demonstrated that it can leverage the potency of passive immunotherapy with antibodies like Roche’s Rituxan through the co-administration of novel antibody based immunotherapies such as urelumab (anti-CD137) and lirilimab (anti-KIR). Both agents are in phase I/II trials with data anticipated in 2015. We anticipate the initiation of phase III trials as early as 2016. Novel immunotherapeutic agents such as urelumab and lirilumab provide significant upside to our long term estimates for BMY immunotherapy franchise. We currently estimate $11bn for BMY’s immunotherapy revenues in 2022. The long term potential of a triple combination with urelumab, lirilumab and a monoclonal is intriguing.
BMY’s antibody-based immunotherapies lirilumab (anti-KIR) and urelumab (anti-CD137) can potentially enhance the activity of any co-administered antibody in both hematologic and solid tumors. Potential indications include CD20 sensitive blood cancers such as NHL, CLL (in combination with Roche’s Rituxan, Gazyva or GSK’s Arzerra) and solid tumors such as Her2+ve breast and gastric cancer (in combination with Roche’s Herceptin, Kadcyla), BMY’s Erbitux (colorectal, lung and head and neck cancer). We anticipate BMY to report first phase Ib data with urelumab as monotherapy and in combination with Rituxan in 2015.
Co-administering antibody enhancing immunotherapy with monoclonal antibodies such as Rituxan may lower rather than increase the adverse event profile of the immunotherapy. We understand that co-administration of Rituxan with urelumab (anti-CD137) allows for significantly lower dosing and significantly lower hepatoxicity (liver toxicity) than seen with urelumab mono-therapy. Clinical experience with lirilumab is more limited but the apparently well tolerated adverse event profile is consistent with the unique expression of KIR on only NK cells.
Liriliumab and urelumab enhance antibody associated ADCC. Monoclonal antibodies such as Rituxan and Herceptin exert their therapeutic activity through antibody dependent cytotoxicity mediated by NK cells (natural killer cells). Lirilumab enhances NK activation by blocking the anti-KIR receptor. The co-stimulatory agent urelumab stimulates natural killer (NK) cells which have been activated by a tumorspecific mAb, resulting in increased ADCC against cancer cells. Potential triple combination would effect a localized, antigen specific NK mediated cytoxicity that could translate into material clinical benefit with tolerable adverse events."
Gruß
ipollit
ein eher kritischer Artikel zu MGNX B7-H3 AK MGA271...
http://seekingalpha.com/article/2755545-b7-h3-and-pdminus-1-…
- B7-H3 sei kein IO-Target wie z.B. PD1... die Funktion sei unklar (kann z.B. hemmend und stimmulierend wirken)
- B7-H3 könnte aber ein gutes Krebs-Target sein: "What does seem to be special about B7-H3 is that it's highly expressed on many solid tumors and not on normal tissue."
- 131I-8H9 ist ein nicht humaner B7-H3 AK, der als ADC mit einem radioaktivem Stoff gekoppelt ist. Dieser lieferte bereits interessante klinische Ergebnisse, was B7-H3 validiert und das Risiko von Nebenwirkungen für B7-H3 AKs senkt
- MGA271 ist ein AK, der auf hohe ADCC optimiert ist... d.h. die Aktivierung von NK-Zellen bei der Bindung an das Target. Kritisch wäre aber, dass laut präklinischen Studien MGA271 gleichzeitg NK-Zellen senken würde.

(MGA271 wurde am 8. Tag verabreicht)
Die Senkung von NK-Zellen wäre natürlich ungünstig, wenn MGA271 für seine Wirkung im Wesentlichen NK-Zellen benötigt. Allerdings ist es nicht ganz klar, ob sich dies auch im Menschen so verhält und ob nicht eine Senkung im Blut durch das Wandern der NK-Zellen in den Tumor erklärt werden kann. Es ist zumindest etwas Unsicherheit.
In diesem Zusammenhang ist aber auch interessant, dass NK-Zellen bei der Wirkung von AKs eine wichtige Rolle zu spielen scheinen. So wurde zuletzt bei Untersuchungen festgestellt, dass die Wirkung des bekannten HER2-AK Herceptin nicht direkt von der Bindung des AKs an HER2 abhängt, sondern HER2 durch aktivierte NK-Zellen heruntergeregelt wird. Das Zusammenspielt von Herceptin mit NK-Zellen ist sehr wichtig. Dies wird auch in diesem Artikel erwähnt:
"The importance of NK cells for therapeutic monoclonal antibodies that treat malignancy is well known. For example, this paper nicely demonstrates in a mouse tumor model that the efficacy of 4D5 (the parent for trastuzumab) is entirely dependent on NK cells. The tumor volume in the NK cell depleted, 4D5 treated animals is identical or even slightly larger than the undepleted, PBS treated animals."
Dies finde ich spannend im Bezug auf IPH.PA, da dies eines der wenigen Unternehmen ist, die speziell diesen Teil des Immunsystems untersuchen und Therapien entwickeln, die etwas entsprechends wie PD1 für T-Zellen auch für NK-Zellen sind. So kann z.B. der IPH.PAs KIR-AK, der die Hemmung von NK-Zellen unterbricht, die Wirkung von anderen AKs wie Herceptin erhöhen, insbesondere, wenn diese AKs von NK-Zellen abhängen.
http://innate-pharma.com/en/product-pipeline/lirilumab-first…
"Lirilumab (IPH2102/BMS-986015) is a fully human monoclonal antibody blocking interaction between Killer-cell immunoglobulin-like receptors (KIR) on NK cells with their ligands.
Blocking these receptors facilitates activation of NK cells and, potentially, destruction of tumor cells by the latter.
NK cells (Natural Killer) are non conventional lymphocytes, belonging to the innate immunity compartment. They are able to:
- Directly and selectively kill « stressed » cells (cancerous, infected or over-activated cells);
- Participate in the set up of a global immune reaction against a selected target, notably via the production of cytokines (the communicating agents of the immune system)
- Bind one of the two ends of cytotoxic antibodies, and then kill cells recognized by these antibodies. This property is known as antibody-dependent cellular cytotoxicity (ADCC)
The mechanism behind NK cells activation depends on a balance between activatory and inhibitory signals, ie. signals of abnormality sent by the target:
- Normal cells send “normality” signals and are thus spared by NK cells;
- Cells undergoing a stress (infection, cancerous transformation, over activation) can send normality as well as danger signals at the same time. This can result in the “blinding” of NK cells.


"MGNX to broaden MGA271 monotherapy Phase Ib program in 2H14. In addition to three currently enrolling expansion cohorts in prostate cancer, melanoma, and B7-H3+ all-comers, MGNX will pursue other tumor types in further cohorts 2H14. The specific indications have not been determined yet but will take into consideration the expression profile of B7-H3. B7-H3 is also highly expressed on cancers of the kidney, pancreas, breast, and ovaries. MGNX expects to complete the initial three cohorts in late '14 and the additional cohorts in '15. Servier will initiate two additional tumor types this week.
MGNX to test MGA271 combinations likely including, but not limited to, immuno-oncology (IO) combinations. Potential combinations will take into consideration mechanistic synergies, e.g., with Tx that target the tumor vasculature where B7-H3 is expressed. Potential combos with other checkpoint inhibitors are possibilities. Combination with natural killer (NK)-cell targeted agents such as IPH/BMY's anti-KIR (lirilumab) would also make sense in our view, given that it can enhance antibody-dependent cellular cytotoxicity (ADCC), which is part of MGA271's mechanism. Combos with Tx that are approved or those that are still in development are being considered by mgmt. We like MGNX's broad and rigorous approach in Phase Ib before settling on specific development plans.
***
Lirilumab’s potential beyond current indications may include Rituxan combo in RA/blood cancer, with management citing synergistic impact on ADCC induction in preclinical studies.
Potential highly attractive combinations could include anti- KIR or anti-NKG2A with anti-CD20 (rituximab) or anti-4-1BB (e.g., urelumab). Recently published preclinical data suggest that KIR blockade with NK cell activating antibodies could lead to a more substantial immune-mediated effect. Antigen-specific therapeutic antibodies that stimulate the NK cell activating Fc receptor such as rituximab (Rituxan) or trastuzumab (Herceptin) are significantly more potent in combination with lirilumab. KOLs also suggested that blocking KIR or NKG2A could enhance anti-4-1BB (CD137) activity at a lower dose and thus overcome some of the toxicities associated with this molecule while enhancing both NK cell and T-cell activity against tumors.
***
Bristol-Myers Squibb: Next Focus is Antibody Enhancement Through Immunotherapy; Long-Term Potential of
Triple Combination with Urelumab, Lirilumab and a MAb Intriguing Bristol-Myers (BMY) have demonstrated that it can leverage the potency of passive immunotherapy with antibodies like Roche’s Rituxan through the co-administration of novel antibody based immunotherapies such as urelumab (anti-CD137) and lirilimab (anti-KIR). Both agents are in phase I/II trials with data anticipated in 2015. We anticipate the initiation of phase III trials as early as 2016. Novel immunotherapeutic agents such as urelumab and lirilumab provide significant upside to our long term estimates for BMY immunotherapy franchise. We currently estimate $11bn for BMY’s immunotherapy revenues in 2022. The long term potential of a triple combination with urelumab, lirilumab and a monoclonal is intriguing.
BMY’s antibody-based immunotherapies lirilumab (anti-KIR) and urelumab (anti-CD137) can potentially enhance the activity of any co-administered antibody in both hematologic and solid tumors. Potential indications include CD20 sensitive blood cancers such as NHL, CLL (in combination with Roche’s Rituxan, Gazyva or GSK’s Arzerra) and solid tumors such as Her2+ve breast and gastric cancer (in combination with Roche’s Herceptin, Kadcyla), BMY’s Erbitux (colorectal, lung and head and neck cancer). We anticipate BMY to report first phase Ib data with urelumab as monotherapy and in combination with Rituxan in 2015.
Co-administering antibody enhancing immunotherapy with monoclonal antibodies such as Rituxan may lower rather than increase the adverse event profile of the immunotherapy. We understand that co-administration of Rituxan with urelumab (anti-CD137) allows for significantly lower dosing and significantly lower hepatoxicity (liver toxicity) than seen with urelumab mono-therapy. Clinical experience with lirilumab is more limited but the apparently well tolerated adverse event profile is consistent with the unique expression of KIR on only NK cells.
Liriliumab and urelumab enhance antibody associated ADCC. Monoclonal antibodies such as Rituxan and Herceptin exert their therapeutic activity through antibody dependent cytotoxicity mediated by NK cells (natural killer cells). Lirilumab enhances NK activation by blocking the anti-KIR receptor. The co-stimulatory agent urelumab stimulates natural killer (NK) cells which have been activated by a tumorspecific mAb, resulting in increased ADCC against cancer cells. Potential triple combination would effect a localized, antigen specific NK mediated cytoxicity that could translate into material clinical benefit with tolerable adverse events."
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.453.840 von SLGramann am 30.11.14 11:58:11"Hat jemand eine Meinung zu Syndax? Vor allem Kritisches und Negatives ist gefragt!"
ein Problem könnte die Patent-Lage von Entinostat sein... ein wichtiges Patent läuft offensichtlich 2017 aus:
http://www.sec.gov/Archives/edgar/data/1395937/0001193125141…
Furthermore, given the amount of time required for the development, testing and regulatory review of new product candidates, patents protecting such candidates might expire before or shortly after such candidates are commercialized. As a result, our owned and licensed patent portfolio may not provide us with sufficient rights to exclude others from commercializing products similar or identical to ours. For example, the composition of matter patent on entinostat will expire in 2017. We expect to seek extensions of patent terms where these are available in any countries where we are prosecuting patents.
... Entinostat composition of matter U.S. Patent RE39,754, which we licensed from Bayer, expires in 2017. Even if we submit the NDA before the expiration of U.S. Patent RE39,754 and are successful in obtaining an extension of the term of U.S. Patent RE39,754 based on FDA regulatory delays, such extension will only extend the term of RE39,754 for a few additional years (up to a maximum of five additional years for patent claims covering a new chemical entity).
Gruß
ipollit
ein Problem könnte die Patent-Lage von Entinostat sein... ein wichtiges Patent läuft offensichtlich 2017 aus:
http://www.sec.gov/Archives/edgar/data/1395937/0001193125141…
Furthermore, given the amount of time required for the development, testing and regulatory review of new product candidates, patents protecting such candidates might expire before or shortly after such candidates are commercialized. As a result, our owned and licensed patent portfolio may not provide us with sufficient rights to exclude others from commercializing products similar or identical to ours. For example, the composition of matter patent on entinostat will expire in 2017. We expect to seek extensions of patent terms where these are available in any countries where we are prosecuting patents.
... Entinostat composition of matter U.S. Patent RE39,754, which we licensed from Bayer, expires in 2017. Even if we submit the NDA before the expiration of U.S. Patent RE39,754 and are successful in obtaining an extension of the term of U.S. Patent RE39,754 based on FDA regulatory delays, such extension will only extend the term of RE39,754 for a few additional years (up to a maximum of five additional years for patent claims covering a new chemical entity).
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.609.317 von ipollit am 18.12.14 20:10:03Danke, ipollit. Die Patentfragen sind ja allgemein kaum zu durchschauen, weil es ja fast immer um ein ganzes Bündel verschiedener Patente geht. Aber hier geht es ja offenbar um den Kern der Sache. Das ist natürlich nicht gut.
Hammer hatte kürzlich mal kritisiert, dass HDAC-Inhibitoren in der Vergangenheit schon so oft enttäuscht hätten, dass man die guten PII-Ergebnisse hier kaum glauben könne.
Das Patentproblem wäre eine Sorge mehr. Unschön.
Hammer hatte kürzlich mal kritisiert, dass HDAC-Inhibitoren in der Vergangenheit schon so oft enttäuscht hätten, dass man die guten PII-Ergebnisse hier kaum glauben könne.
Das Patentproblem wäre eine Sorge mehr. Unschön.
Antwort auf Beitrag Nr.: 48.609.053 von ipollit am 18.12.14 19:36:44IPH.PA
Innate hat heute den Start der ersten PII ihres NKG2A Checkpoint-AK IPH2201 bekannt gegeben.
Hier noch Analysten-Kommentare vom letzten Monat, die die Dominanz von Innate im Bereich von NK-Zellen unterstreichen...

(Citi)

Gruß
ipollit
Innate hat heute den Start der ersten PII ihres NKG2A Checkpoint-AK IPH2201 bekannt gegeben.
Hier noch Analysten-Kommentare vom letzten Monat, die die Dominanz von Innate im Bereich von NK-Zellen unterstreichen...

(Citi)

Gruß
ipollit
was ist denn heute los?
IMGN:
Roche gab heute morgen bekannt, dass die MARIANNE Studie den Endpunkt verfehlt hat. Das ist doch eine ziemliche Überraschung und lässt für IMGN ziemlich viel Spielraum nach Unten.
http://www.roche.com/media/media_releases/med-cor-2014-12-19…
Roche gab zudem bekannt, dass man Gantenerumab (Morphosys) zumindest in Prodromal Alzheimer einstellt. Auch das ziemlich überraschend. Weniger als Ergebnis als vielmehr dass man hier jetzt überhaupt eine Zwischenanalyse durchgeführt hat?!
http://www.morphosys.com/pressrelease/morphosyss-partner-roc…
IMGN:
Roche gab heute morgen bekannt, dass die MARIANNE Studie den Endpunkt verfehlt hat. Das ist doch eine ziemliche Überraschung und lässt für IMGN ziemlich viel Spielraum nach Unten.
http://www.roche.com/media/media_releases/med-cor-2014-12-19…
Roche gab zudem bekannt, dass man Gantenerumab (Morphosys) zumindest in Prodromal Alzheimer einstellt. Auch das ziemlich überraschend. Weniger als Ergebnis als vielmehr dass man hier jetzt überhaupt eine Zwischenanalyse durchgeführt hat?!
http://www.morphosys.com/pressrelease/morphosyss-partner-roc…
Antwort auf Beitrag Nr.: 48.614.630 von kmastra am 19.12.14 12:58:34Ich teile Deine Meinung weitestgehend. Was Gantenerumab angeht, so habe ich der Sache immer nur bestenfalls 20% Erfolgswahrscheinlichkeit zugebilligt, aber dass man da jetzt schon Schluss macht, spricht aus meiner Sicht Bände. Der Amyloid-Beta-Ansatz ist ja schon umstritten und produziert einen Fehlschlag nach dem anderen. Der Prodromal-Ansatz sollte den Ausweg weisen, ist aber wahrscheinlich das Sinnloseste, was man sich ausdenken konnte. Na ja, jetzt hat an halt auch das mal versucht...
IMGN: Das ist ein echter Hammer. Bin total unangenehm überrascht! Ich hätte wirklich nicht gedacht, dass es ausgerechnet bei diesem Trial ein Problem geben könnte, zumal es ja auch einen T-DM1/Perjeta-Arm gab.
IMGN wird nun den cashburn reduzieren und die Pipeline einer Priorisierung unterwerfen müssen. Sie stehen wirklich nicht gut da im Moment. Sehr enttäuschend.
IMGN: Das ist ein echter Hammer. Bin total unangenehm überrascht! Ich hätte wirklich nicht gedacht, dass es ausgerechnet bei diesem Trial ein Problem geben könnte, zumal es ja auch einen T-DM1/Perjeta-Arm gab.
IMGN wird nun den cashburn reduzieren und die Pipeline einer Priorisierung unterwerfen müssen. Sie stehen wirklich nicht gut da im Moment. Sehr enttäuschend.
TSRO, CLVS
Die FDA und die EMA haben soeben den AZN's PARP-Hemmer Lynparza (olaparib) gegen BRCA-mut ovarian cancer vorzeitig zugelassen, wenn ich das richtig sehe. Ich hatte nicht gewusst, dass das nun überhaupt ansteht. Eigentlich hat sich das Panel auch gegen eine vorzeitige Zulassung ausgesprochen: "ODAC Voted 11:2 Against Accelerated Approval"
Hmm... ist das nun gut oder schlecht für die Konkurrenten TSRO und CLVS?
Gruß
ipollit
Die FDA und die EMA haben soeben den AZN's PARP-Hemmer Lynparza (olaparib) gegen BRCA-mut ovarian cancer vorzeitig zugelassen, wenn ich das richtig sehe. Ich hatte nicht gewusst, dass das nun überhaupt ansteht. Eigentlich hat sich das Panel auch gegen eine vorzeitige Zulassung ausgesprochen: "ODAC Voted 11:2 Against Accelerated Approval"
Hmm... ist das nun gut oder schlecht für die Konkurrenten TSRO und CLVS?
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.617.471 von SLGramann am 19.12.14 17:24:27"IMGN: Das ist ein echter Hammer. Bin total unangenehm überrascht! Ich hätte wirklich nicht gedacht, dass es ausgerechnet bei diesem Trial ein Problem geben könnte,"
Das zeigt übrigens auch noch mal exemplarisch auf, was bei Biotech ganz extrem und immer gilt: Du kannst wissen und denken was Du willst - es kann trotzdem immer ganz anders kommen und es kommt sehr, sehr oft wirklich ganz anders.
Das was ipollit hier schon immer vertreten hat - eine sehr breite Diversifikation - ist in diesem Geschäft unabdingbar.
Eine Position sollte nur selten mehr als 5% des Depots ausmachen und 10% sollten wohl besser nie überschritten werden.
Das zeigt übrigens auch noch mal exemplarisch auf, was bei Biotech ganz extrem und immer gilt: Du kannst wissen und denken was Du willst - es kann trotzdem immer ganz anders kommen und es kommt sehr, sehr oft wirklich ganz anders.
Das was ipollit hier schon immer vertreten hat - eine sehr breite Diversifikation - ist in diesem Geschäft unabdingbar.
Eine Position sollte nur selten mehr als 5% des Depots ausmachen und 10% sollten wohl besser nie überschritten werden.
ENTA
Wie ist nach der FDA-Zulassung von ABBV's HepC-Cocktail Viekira Pak ENTA zu bewerten?
Irgendwie finde ich momentan nur unklare oder wiedersprüchliche Kommentare. Der Preis scheint höher zu sein, als erwartet. Ist das gut oder schlecht?
http://www.fiercebiotech.com/story/abbvies-blockbuster-hep-c…
AbbVie ($ABBV) won an expected FDA approval for its next-generation treatment for hepatitis C, kicking off a race with Gilead Sciences ($GILD) for dominance in a blockbuster field.
The agency has signed off on AbbVie's four-agent combo, which combines the new treatments ombitasvir, paritaprevir and dasabuvir with the company's previously approved ritonavir. The multi-pill treatment, which will sell as Viekira Pak, works much like Gilead's competing Harvoni, using a cocktail of antivirals to halt viral replication.
The approval is based on data from 6 Phase III studies in which AbbVie's combo therapy clocked impressive 12-week cure rates, notching a 99% sustained virologic response mark in some hep C populations, including patients with the tough-to-treat genotype 1. Those stellar results came without the need for interferon injections, which often lead to uncomfortable flu-like symptoms.
Analysts expect AbbVie's treatment to bring in more than $3 billion a year at its peak. And while that's enough to spell AbbVie's biggest product since Humira, it's just a fraction of the $10 billion in global sales pegged for Gilead's Harvoni. Despite the two treatments charting similar efficacy across their pivotal trials, Gilead's drug, approved in October, demands patients take just one pill a day while AbbVie's regimen requires at least four, a difference that will likely influence prescription rates.
But AbbVie could shift the balance of power when it comes to pricing. Harvoni's cost--$94,500 for a 12-week regimen--has spurred gripes, protests and threats from payers around the world, giving AbbVie the chance to chip away at Gilead's market share by undercutting the sticker price. The company is yet to disclose Viekira Pak's cost.
No matter which company wins out, the approval of a second next-gen hep C treatment is good news for the roughly 3.2 million Americans who suffer from the virus. Since the launch of Gilead's Sovaldi last year, the standard of care for hep C has forever changed, ushering in a new era of all-oral treatments that leave behind painful injections.
"The new generation of therapeutics for hepatitis C virus is changing the treatment paradigm for Americans living with the disease," Dr. Edward Cox, director of the FDA's Office of Antimicrobial Products, said in a statement. "We continue to see the development of new all-oral treatments with very high virologic response rates and improved safety profiles compared to some of the older interferon-based drug regimens."
Enanta Pharmaceuticals ($ENTA), a Massachusetts biotech, co-developed the cocktail alongside AbbVie and, under a 2006 deal between the two, is guaranteed double-digit royalties on all sales of the combo.
****
Defenitiv nicht korrekt ist der letzte Satz... ENTA erhält 10-20% Royalties für den Paritaprevir-Anteil, der nur 30% der Combi ausmacht. D.h. ENTAs Royalties dürften im 5%-Bereich von den gesamten Viekira Pak Umsätzen liegen.
Twitter:
BMO" $ABBV Viekira Label Worse Than We Expected, Price In Line; We’re Cautious on the Launch,net price AbbVie will book is roughly $73,000"
***
The FDA approved AbbVie's interferon-free hepatitis C treatment Viekira Pak. It'll cost $83,319 for 12 weeks vs. $94,500 for Gilead's blockbuster Harvoni.
Preis gut oder schlecht??? Label gut oder schlecht???
Bisher gibt es z.B. im ihub-Biotech-Forum keine klaren Aussagen. Dort ist meine ich DewDiligence mit über 1 Mio USD in ENTA investiert...
altes Bewertungs-Modell, das aber in Teilen überholt ist (z.B. Anteil 30%, Preis, Marktgröße):
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
aktuelle Kommentare zum Label:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"ABBV/ENTA—FDA PR implies ribavirin use is optional—see third paragraph. This is a pretty big concession by the FDA, and no one I know expected it. Still waiting for the official label.
***
The PR doesn't say optional. It says -" Viekira Pak can be used with or without ribavirin, but it is not recommended for patients whose liver is unable to function properly (decompensated cirrhosis)." Precisely what "with and without" means we will have to wait on.
***
In practice, most GT1b patents probably won't use ribavirin, but most GT1a patients probably will.
***
The Viekira Label doesn't agree with optional:
All 1a and 1b cirrhotics - with
1b non-cirrhotic - without"
https://twitter.com/AndyBiotech/status/546051924051886080/ph…
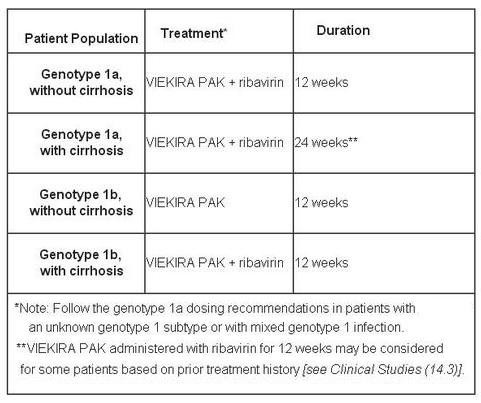
Cirrhotic label 12 wks for cirrhotic (W exceptions) seems better than expected vs Harvoni where TX exp w cirrhosis need 24 wks
***
Der wichtigere Markt für ABBV/ENTA scheint aber Europa zu sein... dort soll zudem HepC 1b verbreiteter sein.
Mal schauen, wie der Markt am Montag reagiert...

Gruß
ipollit
Wie ist nach der FDA-Zulassung von ABBV's HepC-Cocktail Viekira Pak ENTA zu bewerten?
Irgendwie finde ich momentan nur unklare oder wiedersprüchliche Kommentare. Der Preis scheint höher zu sein, als erwartet. Ist das gut oder schlecht?
http://www.fiercebiotech.com/story/abbvies-blockbuster-hep-c…
AbbVie ($ABBV) won an expected FDA approval for its next-generation treatment for hepatitis C, kicking off a race with Gilead Sciences ($GILD) for dominance in a blockbuster field.
The agency has signed off on AbbVie's four-agent combo, which combines the new treatments ombitasvir, paritaprevir and dasabuvir with the company's previously approved ritonavir. The multi-pill treatment, which will sell as Viekira Pak, works much like Gilead's competing Harvoni, using a cocktail of antivirals to halt viral replication.
The approval is based on data from 6 Phase III studies in which AbbVie's combo therapy clocked impressive 12-week cure rates, notching a 99% sustained virologic response mark in some hep C populations, including patients with the tough-to-treat genotype 1. Those stellar results came without the need for interferon injections, which often lead to uncomfortable flu-like symptoms.
Analysts expect AbbVie's treatment to bring in more than $3 billion a year at its peak. And while that's enough to spell AbbVie's biggest product since Humira, it's just a fraction of the $10 billion in global sales pegged for Gilead's Harvoni. Despite the two treatments charting similar efficacy across their pivotal trials, Gilead's drug, approved in October, demands patients take just one pill a day while AbbVie's regimen requires at least four, a difference that will likely influence prescription rates.
But AbbVie could shift the balance of power when it comes to pricing. Harvoni's cost--$94,500 for a 12-week regimen--has spurred gripes, protests and threats from payers around the world, giving AbbVie the chance to chip away at Gilead's market share by undercutting the sticker price. The company is yet to disclose Viekira Pak's cost.
No matter which company wins out, the approval of a second next-gen hep C treatment is good news for the roughly 3.2 million Americans who suffer from the virus. Since the launch of Gilead's Sovaldi last year, the standard of care for hep C has forever changed, ushering in a new era of all-oral treatments that leave behind painful injections.
"The new generation of therapeutics for hepatitis C virus is changing the treatment paradigm for Americans living with the disease," Dr. Edward Cox, director of the FDA's Office of Antimicrobial Products, said in a statement. "We continue to see the development of new all-oral treatments with very high virologic response rates and improved safety profiles compared to some of the older interferon-based drug regimens."
Enanta Pharmaceuticals ($ENTA), a Massachusetts biotech, co-developed the cocktail alongside AbbVie and, under a 2006 deal between the two, is guaranteed double-digit royalties on all sales of the combo.
****
Defenitiv nicht korrekt ist der letzte Satz... ENTA erhält 10-20% Royalties für den Paritaprevir-Anteil, der nur 30% der Combi ausmacht. D.h. ENTAs Royalties dürften im 5%-Bereich von den gesamten Viekira Pak Umsätzen liegen.
Twitter:
BMO" $ABBV Viekira Label Worse Than We Expected, Price In Line; We’re Cautious on the Launch,net price AbbVie will book is roughly $73,000"
***
The FDA approved AbbVie's interferon-free hepatitis C treatment Viekira Pak. It'll cost $83,319 for 12 weeks vs. $94,500 for Gilead's blockbuster Harvoni.
Preis gut oder schlecht??? Label gut oder schlecht???
Bisher gibt es z.B. im ihub-Biotech-Forum keine klaren Aussagen. Dort ist meine ich DewDiligence mit über 1 Mio USD in ENTA investiert...
altes Bewertungs-Modell, das aber in Teilen überholt ist (z.B. Anteil 30%, Preis, Marktgröße):
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
aktuelle Kommentare zum Label:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"ABBV/ENTA—FDA PR implies ribavirin use is optional—see third paragraph. This is a pretty big concession by the FDA, and no one I know expected it. Still waiting for the official label.
***
The PR doesn't say optional. It says -" Viekira Pak can be used with or without ribavirin, but it is not recommended for patients whose liver is unable to function properly (decompensated cirrhosis)." Precisely what "with and without" means we will have to wait on.
***
In practice, most GT1b patents probably won't use ribavirin, but most GT1a patients probably will.
***
The Viekira Label doesn't agree with optional:
All 1a and 1b cirrhotics - with
1b non-cirrhotic - without"
https://twitter.com/AndyBiotech/status/546051924051886080/ph…

Cirrhotic label 12 wks for cirrhotic (W exceptions) seems better than expected vs Harvoni where TX exp w cirrhosis need 24 wks
***
Der wichtigere Markt für ABBV/ENTA scheint aber Europa zu sein... dort soll zudem HepC 1b verbreiteter sein.
Mal schauen, wie der Markt am Montag reagiert...
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.621.728 von ipollit am 20.12.14 13:29:47ENTA
Es sieht so aus, als ob die Zulassung insgesamt neutral zu werten ist...
http://news.investors.com/technology/121914-731574-abbvie-he…
...The AbbVie (NYSE:ABBV) regimen consists of three drugs: ombitasvir, paritaprevir (first developed by Enanta Pharmaceuticals (NASDAQ:ENTA) and dasabuvir. The label advises most patients to take it with ribavirin, a long-established HCV pill that is now generic. The only exceptions are patients with genotype 1b of the virus, without cirrhosis (i.e. scarring) of the liver.
The label also advises taking the regimen for 12 weeks. Patients with genotype 1a with cirrhosis are urged to take it for 24 weeks, though a footnote states that for this group that 12-week run "may be considered for some patients based on prior treatment history." Only genotype 1 patients were on the label, but they make up an estimated 70% of U.S. sufferers.
This is similar to the label for Harvoni, which Gilead launched in October and which was the first interferon-free treatment for most genotype 1 patients. Harvoni combines a novel drug with sofosbuvir, which debuted solo in December 2013 as Sovaldi and has raked in nearly $9 billion since then.
One difference, though, is a footnote on Harvoni's label saying that an eight-week round "can be considered" for non-cirrhotic patients who haven't been treated before. Gilead estimated that as many as 45% of genotype 1 patients may be eligible for this.
Without ribavirin, the Viekira Pak regimen involves three pills in the morning and one at night. Ribavirin adds two more. The Harvoni regimen involves only one pill a day, and both have cure rates upward of 90%. This has led to much speculation about how much the convenience factor — and compliance factor — might affect the adoption rate.
In a Friday note, RBC Capital Markets analyst Michael Yee called the AbbVie label "a little better than Street expectations." The fact that genotype 1b patients weren't required to take ribavirin was "a little positive surprise," since he'd expected all patient groups would have to take it.
"On the flip side, we note there is a section with numerous drugs 'contra-indicated' due to interactions with ritonavir booster, but this seems relatively niche (less than 10-15%) of the population while GILD has no contra-indications," Yee added.
Yee, like many analysts, believes Gilead will retain 80% of the market, which could be good for as much as $15 billion next year. That still leaves around $3 billion for AbbVie.
Most analysts had assumed that AbbVie will gain that share by providing a modest discount to the $94,500 for 12 weeks of Harvoni. AbbVie ultimately will charge 12% less, though 8-week Harvoni patients pay less...
...
Gruß
ipollit
Es sieht so aus, als ob die Zulassung insgesamt neutral zu werten ist...
http://news.investors.com/technology/121914-731574-abbvie-he…
...The AbbVie (NYSE:ABBV) regimen consists of three drugs: ombitasvir, paritaprevir (first developed by Enanta Pharmaceuticals (NASDAQ:ENTA) and dasabuvir. The label advises most patients to take it with ribavirin, a long-established HCV pill that is now generic. The only exceptions are patients with genotype 1b of the virus, without cirrhosis (i.e. scarring) of the liver.
The label also advises taking the regimen for 12 weeks. Patients with genotype 1a with cirrhosis are urged to take it for 24 weeks, though a footnote states that for this group that 12-week run "may be considered for some patients based on prior treatment history." Only genotype 1 patients were on the label, but they make up an estimated 70% of U.S. sufferers.
This is similar to the label for Harvoni, which Gilead launched in October and which was the first interferon-free treatment for most genotype 1 patients. Harvoni combines a novel drug with sofosbuvir, which debuted solo in December 2013 as Sovaldi and has raked in nearly $9 billion since then.
One difference, though, is a footnote on Harvoni's label saying that an eight-week round "can be considered" for non-cirrhotic patients who haven't been treated before. Gilead estimated that as many as 45% of genotype 1 patients may be eligible for this.
Without ribavirin, the Viekira Pak regimen involves three pills in the morning and one at night. Ribavirin adds two more. The Harvoni regimen involves only one pill a day, and both have cure rates upward of 90%. This has led to much speculation about how much the convenience factor — and compliance factor — might affect the adoption rate.
In a Friday note, RBC Capital Markets analyst Michael Yee called the AbbVie label "a little better than Street expectations." The fact that genotype 1b patients weren't required to take ribavirin was "a little positive surprise," since he'd expected all patient groups would have to take it.
"On the flip side, we note there is a section with numerous drugs 'contra-indicated' due to interactions with ritonavir booster, but this seems relatively niche (less than 10-15%) of the population while GILD has no contra-indications," Yee added.
Yee, like many analysts, believes Gilead will retain 80% of the market, which could be good for as much as $15 billion next year. That still leaves around $3 billion for AbbVie.
Most analysts had assumed that AbbVie will gain that share by providing a modest discount to the $94,500 for 12 weeks of Harvoni. AbbVie ultimately will charge 12% less, though 8-week Harvoni patients pay less...
...
Gruß
ipollit
GILD, ENTA, MDVN
Der HepC-Markt soll über die nächsten Jahre einer der umsatz-stärksten im Pharma-Bereich sein.
http://www.biopharmadive.com/news/icymi-the-14-drugs-most-li…
Die geschätzten Top 10 Medikamente 2015...
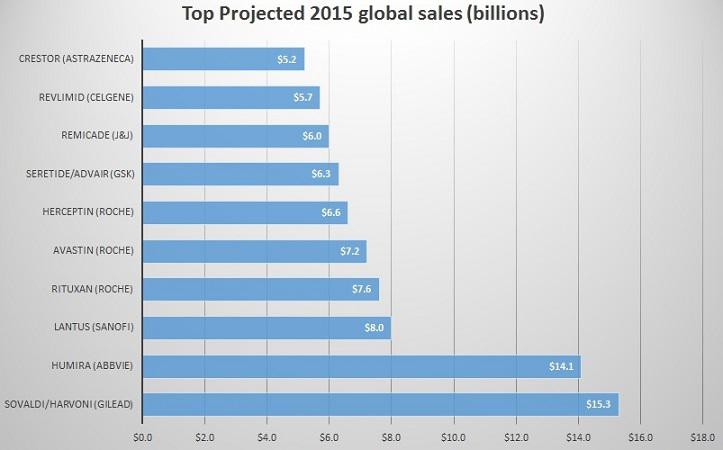
und 2020 (aus heutiger Sicht, was sich im Laufe der Zeit natürlich nochmal deutlich ändern kann)...
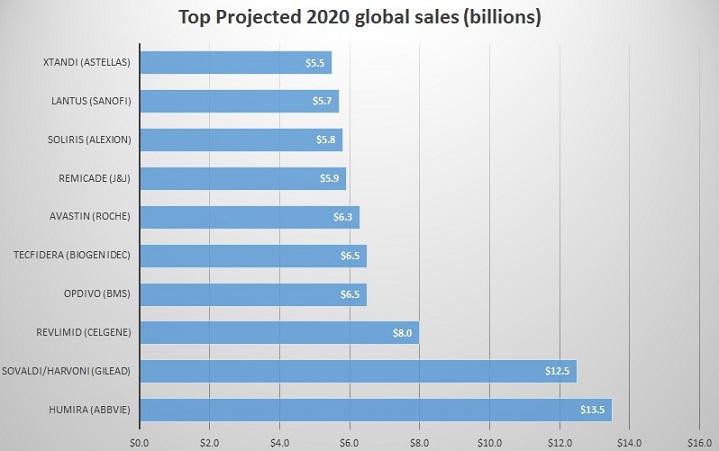
GILD ist mit Harvoni immer vorne mit dabei.
Interessant ist auch, dass die großen Biotechs genauso vertreten sind wie die Pharmas... GILD, CELG, BIIB, ALXN. Die Biotechs haben sich insgesamt in den letzten Jahren sehr gut entwickelt.
MDVNs Xtandi wird hier 2020 auch in den Top 10 gesehen... mal schauen.
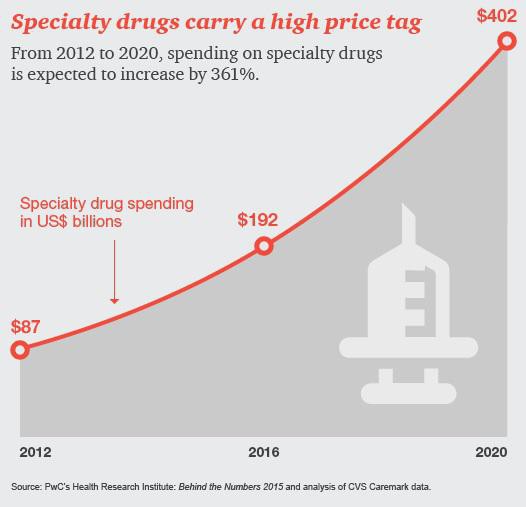
Gruß
ipollit
Der HepC-Markt soll über die nächsten Jahre einer der umsatz-stärksten im Pharma-Bereich sein.
http://www.biopharmadive.com/news/icymi-the-14-drugs-most-li…
Die geschätzten Top 10 Medikamente 2015...

und 2020 (aus heutiger Sicht, was sich im Laufe der Zeit natürlich nochmal deutlich ändern kann)...

GILD ist mit Harvoni immer vorne mit dabei.
Interessant ist auch, dass die großen Biotechs genauso vertreten sind wie die Pharmas... GILD, CELG, BIIB, ALXN. Die Biotechs haben sich insgesamt in den letzten Jahren sehr gut entwickelt.
MDVNs Xtandi wird hier 2020 auch in den Top 10 gesehen... mal schauen.

Gruß
ipollit
Antwort auf Beitrag Nr.: 48.621.911 von ipollit am 20.12.14 14:17:10ENTA
JPMorgan on $ABBV This afternoon, FDA announced that it has approved Viekira Pak, AbbVie’s
HCV combo (ABT-450/267/333). The Viekira Pak label is consistent with our
expectations with 12-week dosing recommended for the majority of patients
and 24-week dosing recommended for some GT1a cirrhotics. In our view, the
label enables AbbVie to be competitive in the market. We continue to expect
AbbVie to take at least 20% market share in what is likely a $15bn+ market,
which translates to our 2015 sales estimate of ~$3bn, with room for upside.
We remain OW ABBV shares.
? Viekira Pak is indicated for 12-week dosing for a majority of patients.
As expected, Viekira Pak is indicated for 12-week dosing for a majority of
patients, including all GT1b patients and all non-cirrhotic GT1a patients.
Ribavirin is recommended for GT1a patients and GT1b cirrhotic patients. In
our view, the Viekira Pak label enables AbbVie to be competitive in the
market.
? Not surprisingly, 24-week dosing is recommended for GT1a patients
with cirrhosis. The FDA is recommending a 24-week treatment duration for
GT1a cirrhotics. We note that the label also states that a 12-week treatment
duration may be considered for some GT1a cirrhotics based on prior
treatment history. As a reminder, phase III TURQUOISE-II data showed a
modest SVR12 rate improvement with 24-week dosing in
treatment-experienced GT1a cirrhotics, while treatment-naïve patients had
similar SVR12 rates with both 12-week and 24-week treatments. Along
these lines, we continue to see most GT1a cirrhotic patients on 12-weeks of
treatment.
? Viekira Pak pricing in line with our expectations. Viekira Pak has a list
price of $83,319 for a 12-week treatment, a 12% discount to a list price for a
12-week treatment of Harvoni ($94,500), but a premium to 8-wk Harvoni
($63,000). We continue to expect fairly rational discounting between
AbbVie and Gilead, and we would not be surprised to see AbbVie offer
select rebates in exchange for enhanced formulary access.
? We continue to forecast $3bn in HCV sales for AbbVie in 2015. AbbVie
is well-positioned to capture share in certain difficult patient populations
(i.e. cirrhotics), in our view, and we see AbbVie also capturing additional
share in select accounts with favorable formulary access. We continue to
expect AbbVie to capture ~20% share in a $15+ billion market, which
translates to $3 billion in 2015 HCV sales (with room for upside) and overall
ABBV EPS of $4.40. We would note that with launch spend already
factored into estimates and high gross margins, we would expect much of
any sales upside to fall to the bottom line. We estimate that an additional
$200 million in 2015 HCV sales would translate to roughly $0.09 of EPS
upside.
****
3 Mrd USD Umsatz 2015 wären wohl ca. 150 Mio USD Royalties, die ENTA nächstes Jahr erhalten würden... dazu käme noch eine Einmalzahlung von 75 Mio USD für die Zulassung.
Gruß
ipollit
JPMorgan on $ABBV This afternoon, FDA announced that it has approved Viekira Pak, AbbVie’s
HCV combo (ABT-450/267/333). The Viekira Pak label is consistent with our
expectations with 12-week dosing recommended for the majority of patients
and 24-week dosing recommended for some GT1a cirrhotics. In our view, the
label enables AbbVie to be competitive in the market. We continue to expect
AbbVie to take at least 20% market share in what is likely a $15bn+ market,
which translates to our 2015 sales estimate of ~$3bn, with room for upside.
We remain OW ABBV shares.
? Viekira Pak is indicated for 12-week dosing for a majority of patients.
As expected, Viekira Pak is indicated for 12-week dosing for a majority of
patients, including all GT1b patients and all non-cirrhotic GT1a patients.
Ribavirin is recommended for GT1a patients and GT1b cirrhotic patients. In
our view, the Viekira Pak label enables AbbVie to be competitive in the
market.
? Not surprisingly, 24-week dosing is recommended for GT1a patients
with cirrhosis. The FDA is recommending a 24-week treatment duration for
GT1a cirrhotics. We note that the label also states that a 12-week treatment
duration may be considered for some GT1a cirrhotics based on prior
treatment history. As a reminder, phase III TURQUOISE-II data showed a
modest SVR12 rate improvement with 24-week dosing in
treatment-experienced GT1a cirrhotics, while treatment-naïve patients had
similar SVR12 rates with both 12-week and 24-week treatments. Along
these lines, we continue to see most GT1a cirrhotic patients on 12-weeks of
treatment.
? Viekira Pak pricing in line with our expectations. Viekira Pak has a list
price of $83,319 for a 12-week treatment, a 12% discount to a list price for a
12-week treatment of Harvoni ($94,500), but a premium to 8-wk Harvoni
($63,000). We continue to expect fairly rational discounting between
AbbVie and Gilead, and we would not be surprised to see AbbVie offer
select rebates in exchange for enhanced formulary access.
? We continue to forecast $3bn in HCV sales for AbbVie in 2015. AbbVie
is well-positioned to capture share in certain difficult patient populations
(i.e. cirrhotics), in our view, and we see AbbVie also capturing additional
share in select accounts with favorable formulary access. We continue to
expect AbbVie to capture ~20% share in a $15+ billion market, which
translates to $3 billion in 2015 HCV sales (with room for upside) and overall
ABBV EPS of $4.40. We would note that with launch spend already
factored into estimates and high gross margins, we would expect much of
any sales upside to fall to the bottom line. We estimate that an additional
$200 million in 2015 HCV sales would translate to roughly $0.09 of EPS
upside.
****
3 Mrd USD Umsatz 2015 wären wohl ca. 150 Mio USD Royalties, die ENTA nächstes Jahr erhalten würden... dazu käme noch eine Einmalzahlung von 75 Mio USD für die Zulassung.
Gruß
ipollit
ich habe mal 2 allgemeine(re) Fragen
wenn Jemand antworten kann/mag, wäre es schön
gibt es irgendwo Seiten/Übersichten wo man mal sehen kann wie groß die einzelnen "Untermärkte"/Indikationen im Bio/medizintechnologischen bereich sind?
jetzt z.B. lung cancer 10bln US, 13bln RoW, Markt 23bln total
sowas
und -können Bio/medtechnologiefirmen eigentlich auch -ich würde mal sagen in einem Umsatz/Gewinnsinne- "erfolgreich" sein, OHNE dass sie die FDA Genehmigung -schon?- bekommen haben?(offengelassen ob sie die noch bekommen werden, oder nicht)
meine Vermutung, letzten Endes, ist: möööglich ist es schon, aber wahrscheinlich nicht gerade?
Gruß
P.
wenn Jemand antworten kann/mag, wäre es schön
gibt es irgendwo Seiten/Übersichten wo man mal sehen kann wie groß die einzelnen "Untermärkte"/Indikationen im Bio/medizintechnologischen bereich sind?
jetzt z.B. lung cancer 10bln US, 13bln RoW, Markt 23bln total
sowas
und -können Bio/medtechnologiefirmen eigentlich auch -ich würde mal sagen in einem Umsatz/Gewinnsinne- "erfolgreich" sein, OHNE dass sie die FDA Genehmigung -schon?- bekommen haben?(offengelassen ob sie die noch bekommen werden, oder nicht)
meine Vermutung, letzten Endes, ist: möööglich ist es schon, aber wahrscheinlich nicht gerade?
Gruß
P.
Antwort auf Beitrag Nr.: 48.621.911 von ipollit am 20.12.14 14:17:10ENTA
CS schätzt 2,1 Mrd USD für Viekira in diesem Jahr... mittelfristig 20-30% vom Markt (der >15 Mrd USD, vielleicht >20 Mrd USD sein soll). 5% Royalties sind für ENTA schon ein signifikanter Betrag.

Ebenfalls scheint nun doch ein Preiskampf zwischen ABBV und GILD zu beginnen. Wie heute gemeldet wurde, hat die erste große Versicherung in den USA angekündigt, nach einem Rabatt von ABBV nur noch Viekira zu bezahlen. Das betrifft schonmal 25 Mio Amerikaner.
http://www.reuters.com/article/2014/12/22/us-express-scripts…
"Express Scripts to cover AbbVie hepatitis C drug, drops Gilead treatment
...AbbVie, whose Viekira Pak drug was approved on Friday by U.S. regulators, has set a significantly lower price, Express Scripts Chief Medical Officer Steve Miller said in an interview.
The pricing agreement covers Express Scripts' National Preferred Formulary, a list of approved and covered drugs that applies to 25 million Americans with its pharmacy insurance...
...Express Scripts declined to say how much it would pay for the AbbVie drug, which it will sell only through its by-mail Accredo specialty pharmacy. It lists for $83,319 for a 12-week treatment and is also indicated for a 24-week treatment for some patients. Drug makers typically discount drugs in the United States by 10 to 20 percent.
Miller said that the AbbVie price was narrowing the gap towards the lower prices that Western European countries have negotiated for their citizens for Sovaldi. They run from $51,373 in France to $66,000 in Germany...
Gruß
ipollit
CS schätzt 2,1 Mrd USD für Viekira in diesem Jahr... mittelfristig 20-30% vom Markt (der >15 Mrd USD, vielleicht >20 Mrd USD sein soll). 5% Royalties sind für ENTA schon ein signifikanter Betrag.

Ebenfalls scheint nun doch ein Preiskampf zwischen ABBV und GILD zu beginnen. Wie heute gemeldet wurde, hat die erste große Versicherung in den USA angekündigt, nach einem Rabatt von ABBV nur noch Viekira zu bezahlen. Das betrifft schonmal 25 Mio Amerikaner.
http://www.reuters.com/article/2014/12/22/us-express-scripts…
"Express Scripts to cover AbbVie hepatitis C drug, drops Gilead treatment
...AbbVie, whose Viekira Pak drug was approved on Friday by U.S. regulators, has set a significantly lower price, Express Scripts Chief Medical Officer Steve Miller said in an interview.
The pricing agreement covers Express Scripts' National Preferred Formulary, a list of approved and covered drugs that applies to 25 million Americans with its pharmacy insurance...
...Express Scripts declined to say how much it would pay for the AbbVie drug, which it will sell only through its by-mail Accredo specialty pharmacy. It lists for $83,319 for a 12-week treatment and is also indicated for a 24-week treatment for some patients. Drug makers typically discount drugs in the United States by 10 to 20 percent.
Miller said that the AbbVie price was narrowing the gap towards the lower prices that Western European countries have negotiated for their citizens for Sovaldi. They run from $51,373 in France to $66,000 in Germany...
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.625.622 von Popeye82 am 21.12.14 13:48:30"gibt es irgendwo Seiten/Übersichten wo man mal sehen kann wie groß die einzelnen "Untermärkte"/Indikationen im Bio/medizintechnologischen bereich sind?"
So eine Übersicht kenne ich nicht... aber mir ist auch nicht klar, was du daraus ablesen willst? Dass ein "Markt" heute so oder so groß ist, heißt ja nicht, dass er das nächstes Jahr auch noch so ist. Wenn in einer Indikation ein Medikament der Standard ist, das demnächst generisch wird, so werden auch die Umsätze um z.B. 80% sinken. Andersherum kann ein neues Medikament den Umsatz in einer Indikation deutlich vergrößern, wenn damit Patienten behandelt werden können, die zuvor nicht behandelt worden sind oder es deutlich besser und teurer ist als die aktuellen Medikamente.
HCV war ein relativ kleiner "Markt"... jetzt ist es ein sehr großer. Wenn die meisten Patienten geheilt sein werden, wird es wieder ein eher kleiner sein.
Gruß
ipollit
So eine Übersicht kenne ich nicht... aber mir ist auch nicht klar, was du daraus ablesen willst? Dass ein "Markt" heute so oder so groß ist, heißt ja nicht, dass er das nächstes Jahr auch noch so ist. Wenn in einer Indikation ein Medikament der Standard ist, das demnächst generisch wird, so werden auch die Umsätze um z.B. 80% sinken. Andersherum kann ein neues Medikament den Umsatz in einer Indikation deutlich vergrößern, wenn damit Patienten behandelt werden können, die zuvor nicht behandelt worden sind oder es deutlich besser und teurer ist als die aktuellen Medikamente.
HCV war ein relativ kleiner "Markt"... jetzt ist es ein sehr großer. Wenn die meisten Patienten geheilt sein werden, wird es wieder ein eher kleiner sein.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.630.065 von ipollit am 22.12.14 11:25:42ENTA
http://www.cnbc.com/id/102287817
...About 3.2 million people in the U.S. have hepatitis C, according to the Centers for Disease Control and Prevention. Three-quarters of those have genotype 1, Express Scripts said. About 3.2 million people in the U.S. have hepatitis C, according to the Centers for Disease Control and Prevention. Three-quarters of those have genotype 1, Express Scripts said. The viral infection affects as many as 150 million people worldwide; it's spread through the blood and can lead to liver failure and liver cancer. As many as 500,000 people worldwide die of hepatitis C-related liver diseases each year, according to the World Health Organization...
Gruß
ipollit
http://www.cnbc.com/id/102287817
...About 3.2 million people in the U.S. have hepatitis C, according to the Centers for Disease Control and Prevention. Three-quarters of those have genotype 1, Express Scripts said. About 3.2 million people in the U.S. have hepatitis C, according to the Centers for Disease Control and Prevention. Three-quarters of those have genotype 1, Express Scripts said. The viral infection affects as many as 150 million people worldwide; it's spread through the blood and can lead to liver failure and liver cancer. As many as 500,000 people worldwide die of hepatitis C-related liver diseases each year, according to the World Health Organization...
Gruß
ipollit
MGNX
huii... eigentlich halte ich CD3-Bites&Co und insbesondere MGNXs DARTs für konkurrenzfähig gegen CARTs. Ich setze darauf, dass sie vor CARTs zum Einsatz kommen.
Der CD3xCD19 DART MGD011 ist gerade erst öffentlich gemacht worden und noch nicht in der PI. Trotzdem übernimmt J&J nun die Entwicklung... 50 Mio USD Upfront + 75 Mio USD Aktien zu 39 USD... 575 Mio USD mögliche Meilensteinzahlungen... double digit Royalties WW und Option auf 50:50 in den USA
Hört sich für mich auf den ersten Blick nicht schlecht an!
http://finance.yahoo.com/news/macrogenics-enters-collaborati…
- MacroGenics licenses MGD011 (CD19 x CD3 DART(R)) to Janssen
- $50 million upfront license fee paid to MacroGenics, and a $75 million equity investment by Johnson & Johnson Innovation - JJDC, Inc.
- MacroGenics may elect to fund a portion of late-stage development costs in exchange for a U.S. and Canada profit share
- MacroGenics may elect to co-promote in the United States
... Janssen will be fully responsible for developing MGD011 following submission of the IND, which is planned for 2015...
J&J besitzt in diesem Bereich bereits sehr wichtige Produkte mit PCYSs Imbruvica und Genmabs Daratumumab.

Gruß
ipollit
huii... eigentlich halte ich CD3-Bites&Co und insbesondere MGNXs DARTs für konkurrenzfähig gegen CARTs. Ich setze darauf, dass sie vor CARTs zum Einsatz kommen.
Der CD3xCD19 DART MGD011 ist gerade erst öffentlich gemacht worden und noch nicht in der PI. Trotzdem übernimmt J&J nun die Entwicklung... 50 Mio USD Upfront + 75 Mio USD Aktien zu 39 USD... 575 Mio USD mögliche Meilensteinzahlungen... double digit Royalties WW und Option auf 50:50 in den USA
Hört sich für mich auf den ersten Blick nicht schlecht an!

http://finance.yahoo.com/news/macrogenics-enters-collaborati…
- MacroGenics licenses MGD011 (CD19 x CD3 DART(R)) to Janssen
- $50 million upfront license fee paid to MacroGenics, and a $75 million equity investment by Johnson & Johnson Innovation - JJDC, Inc.
- MacroGenics may elect to fund a portion of late-stage development costs in exchange for a U.S. and Canada profit share
- MacroGenics may elect to co-promote in the United States
... Janssen will be fully responsible for developing MGD011 following submission of the IND, which is planned for 2015...
J&J besitzt in diesem Bereich bereits sehr wichtige Produkte mit PCYSs Imbruvica und Genmabs Daratumumab.
Gruß
ipollit
ACHN
ein guter Tag für die offensichtlich sehr guten Daten ihrer HCV-Kombi, die anscheinend mit GILD und ABBV konkurrieren können...

Da wäre dieses Jahr ein Verzehnfacher drin gewesen.
Gruß
ipollit
ein guter Tag für die offensichtlich sehr guten Daten ihrer HCV-Kombi, die anscheinend mit GILD und ABBV konkurrieren können...
Da wäre dieses Jahr ein Verzehnfacher drin gewesen.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.630.566 von ipollit am 22.12.14 12:21:12Unglaublich gute Konditionen sind das! Spricht enorm für die Plattform von MGNX. Großes Kino.
Antwort auf Beitrag Nr.: 48.630.806 von SLGramann am 22.12.14 12:56:18Ja... und J&J ist einer der Besten der Branche, ich hoffe, das zahlt sich aus. Allerdings wird die Entwicklung noch Jahre dauern. Ich denke, man wird sehr vorsichtig vorgehen in der PI. Die Kosten und das Risiko trägt aber nun J&J.
Grüße
ipollit
Grüße
ipollit
GILD
Die großen Biotechs waren führend bei den starken Kursanstiegen im Biotech-Bereich. Und GILD war vorne mit dabei. Hoffentlich wirkt sich der Druck auf GILD nicht nun auf den gesamten Sektor aus... mal schauen, wie heute der Tag wird


Gruß
ipollit
Die großen Biotechs waren führend bei den starken Kursanstiegen im Biotech-Bereich. Und GILD war vorne mit dabei. Hoffentlich wirkt sich der Druck auf GILD nicht nun auf den gesamten Sektor aus... mal schauen, wie heute der Tag wird

Gruß
ipollit
Antwort auf Beitrag Nr.: 48.630.719 von ipollit am 22.12.14 12:49:35"ACHN
ein guter Tag für die offensichtlich sehr guten Daten ihrer HCV-Kombi, die anscheinend mit GILD und ABBV konkurrieren können..."
Manche reden jetzt von best-in-class... Zumindest wäre es für einen BigPharma eine aussichtsreiche Methode, noch auf den HCV-Zug zu springen.
Ich frage mich, was von der Marktkapitalisierung zu halten ist. An sich könnte da ja noch ne Menge gehen, wenn sie weiter Top-Daten liefern sollten.
Für Pharmasset wurden damals 11 Milliarden gezahlt, oder? Klar, das kommt nicht wieder, denn jetzt ist der Markt schon hart umkämpft, aber die Frage ist, wie viel ACHN im Erfolgsfall wert sein könnte?
Mehr als 1,5 Milliarden sicher. 4? 5?
ein guter Tag für die offensichtlich sehr guten Daten ihrer HCV-Kombi, die anscheinend mit GILD und ABBV konkurrieren können..."
Manche reden jetzt von best-in-class... Zumindest wäre es für einen BigPharma eine aussichtsreiche Methode, noch auf den HCV-Zug zu springen.
Ich frage mich, was von der Marktkapitalisierung zu halten ist. An sich könnte da ja noch ne Menge gehen, wenn sie weiter Top-Daten liefern sollten.
Für Pharmasset wurden damals 11 Milliarden gezahlt, oder? Klar, das kommt nicht wieder, denn jetzt ist der Markt schon hart umkämpft, aber die Frage ist, wie viel ACHN im Erfolgsfall wert sein könnte?
Mehr als 1,5 Milliarden sicher. 4? 5?
Antwort auf Beitrag Nr.: 48.636.515 von SLGramann am 23.12.14 06:20:13Kritisches zum Thema von AF:
http://www.thestreet.com/story/12993244/1/achillion-pharma-t…
http://www.thestreet.com/story/12993244/1/achillion-pharma-t…
Antwort auf Beitrag Nr.: 48.549.200 von SLGramann am 11.12.14 17:49:47CLDN
"Auf den ersten Blick sieht das wirklich ganz spannend aus. Ich habe das S1 mal überflogen. Ich denke, hier lohnt sich ein zweiter Blick - mindestens."
im Folgenden ist einer, der angeblich mit der Materie vertraut ist und den momentanen Ansatz als nicht ausreichend sieht, um beim Menschen etwas zu bewirken. Bisherige Ergebnisse wären wahrscheinlich nur ein statistischer Zufall. Demnach sollte man bei einer Investition einen Fehlschlag mit einkalkulieren... d.h. nur eine Hochrisiko-Position.
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"I've harped on about this one on twitter, likely to the point of boring readers.
I've worked hands-on with AAV (serotype 9), and I know from first hand experience that the doses CLDN is using in humans are high doses for a rat. These doses are insufficient for a dog heart, let alone a human heart. Dosing does matter, since these AAV are replication defective, so dosing needs to scale with heart size.
Second point is that intracoronary bloodstream administration is not effective in large animals. In the dog, intracoronary does not work whereas in the rat it is highly effective and cardiotropic. Some of it has to do with the tissue tropism of the virus. However, we found that if the virus isn't directly injected into the myocardium, you see no expression. At the near placebo doses that CLDN uses, their wishful delivery method will assure very little transduction.
Their papers also do a very poor job of convincing that large animal models show actual expression. In fact, one of the papers using pigs shows that SERCA protein expression does not increase following AAV administration.
That's just a weak structure upon which to build a clinical program."
und weiter... http://investorshub.advfn.com/boards/replies.aspx?msg=109414…
Honestly, I think it's just one of those fluke results you get in small CV trials. I'm rather confident it's unrelated to their intended mechanism. Expression trumps persistence, and their pig model data demonstrated no meaningful increase in protein expression.
As for the persistence:
They note that they see anywhere from 20 to 365 copies of the AAV in a typical ug of DNA. So let's do the math:
1e-6 g DNA / 660 g per mol of DNA basepairs = 1.52 e-9 mol of DNA basepairs
1.52e-9 mol DNA basepairs x 6.02e23 basepairs per mol = 9.12e13 basepairs of DNA
9.12e13 basepairs of DNA / 3e9 basepairs of DNA per genome = 3.05e5 copies of the genome
So basically, what they're telling you is that they collected a DNA sample that contains 300000 copies of the genome and, therefore, 600000 of the endogenous SERCA gene they're targeting. From that sample, they're telling you that they find up to 365 copies of their AAV. In other words, increasing the SERCA copies from 600000 copies to 600365 provides a meaningful clinical benefit?
To say the least, I'm skeptical.
oder... http://investorshub.advfn.com/boards/replies.aspx?msg=109415…
"Thanks for that. I was wondering about this: "There were some imbalances in baseline patient characteristics across the treatment arms in CUPID 1. In particular, there was a higher percentage of healthier patients in Mydicar arms relative to placebo arms. Post-hoc sensitivity analyses though suggested that the differences in baseline patient characteristics could not completely explain the clinical outcomes observed in CUPID 1."
Gruß
ipollit
"Auf den ersten Blick sieht das wirklich ganz spannend aus. Ich habe das S1 mal überflogen. Ich denke, hier lohnt sich ein zweiter Blick - mindestens."
im Folgenden ist einer, der angeblich mit der Materie vertraut ist und den momentanen Ansatz als nicht ausreichend sieht, um beim Menschen etwas zu bewirken. Bisherige Ergebnisse wären wahrscheinlich nur ein statistischer Zufall. Demnach sollte man bei einer Investition einen Fehlschlag mit einkalkulieren... d.h. nur eine Hochrisiko-Position.
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"I've harped on about this one on twitter, likely to the point of boring readers.
I've worked hands-on with AAV (serotype 9), and I know from first hand experience that the doses CLDN is using in humans are high doses for a rat. These doses are insufficient for a dog heart, let alone a human heart. Dosing does matter, since these AAV are replication defective, so dosing needs to scale with heart size.
Second point is that intracoronary bloodstream administration is not effective in large animals. In the dog, intracoronary does not work whereas in the rat it is highly effective and cardiotropic. Some of it has to do with the tissue tropism of the virus. However, we found that if the virus isn't directly injected into the myocardium, you see no expression. At the near placebo doses that CLDN uses, their wishful delivery method will assure very little transduction.
Their papers also do a very poor job of convincing that large animal models show actual expression. In fact, one of the papers using pigs shows that SERCA protein expression does not increase following AAV administration.
That's just a weak structure upon which to build a clinical program."
und weiter... http://investorshub.advfn.com/boards/replies.aspx?msg=109414…
Honestly, I think it's just one of those fluke results you get in small CV trials. I'm rather confident it's unrelated to their intended mechanism. Expression trumps persistence, and their pig model data demonstrated no meaningful increase in protein expression.
As for the persistence:
They note that they see anywhere from 20 to 365 copies of the AAV in a typical ug of DNA. So let's do the math:
1e-6 g DNA / 660 g per mol of DNA basepairs = 1.52 e-9 mol of DNA basepairs
1.52e-9 mol DNA basepairs x 6.02e23 basepairs per mol = 9.12e13 basepairs of DNA
9.12e13 basepairs of DNA / 3e9 basepairs of DNA per genome = 3.05e5 copies of the genome
So basically, what they're telling you is that they collected a DNA sample that contains 300000 copies of the genome and, therefore, 600000 of the endogenous SERCA gene they're targeting. From that sample, they're telling you that they find up to 365 copies of their AAV. In other words, increasing the SERCA copies from 600000 copies to 600365 provides a meaningful clinical benefit?
To say the least, I'm skeptical.
oder... http://investorshub.advfn.com/boards/replies.aspx?msg=109415…
"Thanks for that. I was wondering about this: "There were some imbalances in baseline patient characteristics across the treatment arms in CUPID 1. In particular, there was a higher percentage of healthier patients in Mydicar arms relative to placebo arms. Post-hoc sensitivity analyses though suggested that the differences in baseline patient characteristics could not completely explain the clinical outcomes observed in CUPID 1."
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.659.852 von ipollit am 29.12.14 14:07:02"d.h. nur eine Hochrisiko-Position."
Das ist hier sicher die richtige Herangehensweise. Ich selbst habe als ich das geschrieben habe eine Position von ca. 1% des Depotwerts eröffnet.
Auf der "Haben-Seite" stehen positive IIa-Ergebnisse und eine BT-Entscheidung der FDA. Wenn die IIa-Ergebnisse im April 2015 bestätigt werden, wird das wohl zur Zulassung führen. Wenn sie sich als statistischer "fluke" erweisen, wird der Kurs komplett zusammenbrechen.
Dieses:
"There were some imbalances in baseline patient characteristics across the treatment arms in CUPID 1. In particular, there was a higher percentage of healthier patients in Mydicar arms relative to placebo arms. Post-hoc sensitivity analyses though suggested that the differences in baseline patient characteristics could not completely explain the clinical outcomes observed in CUPID 1."
hat mir gestern auch nicht gefallen.
Ich bleibe dabei, aber eben nur mit einer sehr kleinen Position.
Gruß
SLG
PS: 2014 war ein gutes Jahr, dass uns inzwischen allerdings teilweise aberwitzige Bewertungen in einem heißgelaufenen Markt eingebracht hat. Auf den 10-Jahreschart des NASDAQ-Biotech-Index darf man besser nicht schauen, wenn man noch ruhig schlafen will. Ich werde morgen mal meine aktuelle Depotzusammenstellung und Gewichtung posten. Was 2015 wohl bringen wird? Kommt der Crash? Oder kommen wir einfach in ruhigeres Fahrwasser?
Das ist hier sicher die richtige Herangehensweise. Ich selbst habe als ich das geschrieben habe eine Position von ca. 1% des Depotwerts eröffnet.
Auf der "Haben-Seite" stehen positive IIa-Ergebnisse und eine BT-Entscheidung der FDA. Wenn die IIa-Ergebnisse im April 2015 bestätigt werden, wird das wohl zur Zulassung führen. Wenn sie sich als statistischer "fluke" erweisen, wird der Kurs komplett zusammenbrechen.
Dieses:
"There were some imbalances in baseline patient characteristics across the treatment arms in CUPID 1. In particular, there was a higher percentage of healthier patients in Mydicar arms relative to placebo arms. Post-hoc sensitivity analyses though suggested that the differences in baseline patient characteristics could not completely explain the clinical outcomes observed in CUPID 1."
hat mir gestern auch nicht gefallen.
Ich bleibe dabei, aber eben nur mit einer sehr kleinen Position.
Gruß
SLG
PS: 2014 war ein gutes Jahr, dass uns inzwischen allerdings teilweise aberwitzige Bewertungen in einem heißgelaufenen Markt eingebracht hat. Auf den 10-Jahreschart des NASDAQ-Biotech-Index darf man besser nicht schauen, wenn man noch ruhig schlafen will. Ich werde morgen mal meine aktuelle Depotzusammenstellung und Gewichtung posten. Was 2015 wohl bringen wird? Kommt der Crash? Oder kommen wir einfach in ruhigeres Fahrwasser?
Antwort auf Beitrag Nr.: 48.662.627 von SLGramann am 29.12.14 20:54:35CLDN:
Einige Szenarien für mögliche Kursentwicklungen...

Ist eines dieser "alles oder nichts"-Dinger.
Einige Szenarien für mögliche Kursentwicklungen...

Ist eines dieser "alles oder nichts"-Dinger.
Moin moin,
habe grade die Chartsammlung aktualisiert:
http://www.wallstreet-online.de/diskussion/1190461-1-10/biot…
IMGN:
Man konnte auch wieder sehen, wie riskant es ist, Biotechaktien bei Events wie PIII oder Zulassungen zu halten. (Es gäbe natürlich auch Beispiele dafür wie chancenreich das Ganze sein kann) Ich persönlich gewichte Aktien durchaus höher als 10% aber bei einem solchen Event würde ich immer vorher das Risiko minimieren.
Noch ein paar Links:
Müsste man weniger hier als vielmehr in vielen anderen Boards posten:
http://www.thestreet.com/story/12725934/1/the-seven-deadly-s…
Eine anschauliche Zusammenfassung zum Thema IO:
http://www.wsj.com/articles/cancers-super-survivors-how-immu…
Von den Besten lernen:
http://www.focus.de/finanzen/money-magazin/archiv/jahrgang_2… Interessante Überlegungen zur Portfoliostruktur. Ich wusste auch gar nicht, dass ich Kostolany so gut finde: Sein Mentor, ein Freund des Börsenmaklers Perquel, lehrte ihn, dass der Kurs davon abhängt, „ob es mehr Dummköpfe als Papiere oder mehr Papiere als Dummköpfe gibt“.
SG kmastra
habe grade die Chartsammlung aktualisiert:
http://www.wallstreet-online.de/diskussion/1190461-1-10/biot…
IMGN:
Man konnte auch wieder sehen, wie riskant es ist, Biotechaktien bei Events wie PIII oder Zulassungen zu halten. (Es gäbe natürlich auch Beispiele dafür wie chancenreich das Ganze sein kann) Ich persönlich gewichte Aktien durchaus höher als 10% aber bei einem solchen Event würde ich immer vorher das Risiko minimieren.
Noch ein paar Links:
Müsste man weniger hier als vielmehr in vielen anderen Boards posten:
http://www.thestreet.com/story/12725934/1/the-seven-deadly-s…
Eine anschauliche Zusammenfassung zum Thema IO:
http://www.wsj.com/articles/cancers-super-survivors-how-immu…
Von den Besten lernen:
http://www.focus.de/finanzen/money-magazin/archiv/jahrgang_2… Interessante Überlegungen zur Portfoliostruktur. Ich wusste auch gar nicht, dass ich Kostolany so gut finde: Sein Mentor, ein Freund des Börsenmaklers Perquel, lehrte ihn, dass der Kurs davon abhängt, „ob es mehr Dummköpfe als Papiere oder mehr Papiere als Dummköpfe gibt“.

SG kmastra
Antwort auf Beitrag Nr.: 48.663.740 von kmastra am 30.12.14 00:10:30
eben!!
etwas was ich ja schon immer sage
nein, ich finde diesen Artikel ganz amüsant geschrieben, möchte aber nur mal anmerken dass es auch Möglichkeiten gibt sich weder auf die eine noch die andere Seite "zu stellen"
etwas was ich teilweise, sehr bewusst, so "praktiziere"
Gruß
P.
Zitat von kmastra/The Street: "You may safely ignore others who are more critical. It is well known these bashers are paid by hedge funds shorting your biotech stock and are only hanging out on the message board to shake your confidence. Once you sell and the stock drops, these hedge funds will swoop in and buy the stock lower. Don't let them do this! Honestly, if someone is not a true believer why would he be hanging out on a biotech stock message board in the first place? It makes no sense. "
www.thestreet.com/story/12725934/1/the-seven-deadly-sins-of-…
eben!!
etwas was ich ja schon immer sage
nein, ich finde diesen Artikel ganz amüsant geschrieben, möchte aber nur mal anmerken dass es auch Möglichkeiten gibt sich weder auf die eine noch die andere Seite "zu stellen"
etwas was ich teilweise, sehr bewusst, so "praktiziere"
Gruß
P.
Antwort auf Beitrag Nr.: 48.662.627 von SLGramann am 29.12.14 20:54:35Depotstruktur zum Jahresende:
Ich habe das Depot im Laufe des Jahres immer mehr in Richtung einer sehr breiten Diversifikation umgebaut (ich denke, dass ipollits Herangehensweise doch die vernünftigere ist).
Manche Positionen habe ich durch Teilverkäufe deutlich geschrumpft. Andere Positionen sind durch eine schlechte Kursentwicklung auf ein winziges Maß gefallen (unter 1%).
Ich werde so auch in das Jahr 2015 gehen, obschon ich mich frage, ob nicht mehr Cash Sinn machen würde.
Wert Gewichtung in Prozent
ACAD 2,82
XLRN 2,58
AERI 2,65
AGIO 5,08
ARQL 0,63
ARRY 5,33
AAVL 1,72
BLCM 1,02
BLUE 6,16
CLDN 1,32
CLDX 6,36
CLVS 7,41
CNAT 1,54
ESPR 2,38
EXEL 0,89
FGEN 3,57
FMI 2,65
Genmab 3,89
IMGN 1,38
INCY 6,53
KITE 2,47
MGNX 3,86
RLYP 1,57
SAGE 4,08
SGEN 3,64
STML 1,99
TSRO 2,45
TGTX 2,12
ZFGN 2,74
ZSPH 1,85
Cash 7,31
Ich habe das Depot im Laufe des Jahres immer mehr in Richtung einer sehr breiten Diversifikation umgebaut (ich denke, dass ipollits Herangehensweise doch die vernünftigere ist).
Manche Positionen habe ich durch Teilverkäufe deutlich geschrumpft. Andere Positionen sind durch eine schlechte Kursentwicklung auf ein winziges Maß gefallen (unter 1%).
Ich werde so auch in das Jahr 2015 gehen, obschon ich mich frage, ob nicht mehr Cash Sinn machen würde.
Antwort auf Beitrag Nr.: 48.668.147 von SLGramann am 30.12.14 16:11:58Hallo SLGramann,
vielen Dank für die Offenlegung. Dein Depot gefällt mir sehr gut. (Überraschung! ) Werde mein Depot auch mal posten. CLVS ist auch bei mir die größte Position - soviel weiß ich aus dem Kopf.
) Werde mein Depot auch mal posten. CLVS ist auch bei mir die größte Position - soviel weiß ich aus dem Kopf.
Was die Strukturierung des Depots angeht, gibt es meines Erachtens viele Möglichkeiten. Wie gesagt hängt es von vielen ganz individuellen Faktoren ab. Dabei merke ich, dass auch die absolute Größe des Depots eine Rolle spielt. (Die Angst vor Verlusten ist ja größer als die Freude am Gewinn)
Die Sorge um eine Korrektur im nächsten Jahr treibt mich auch um. Ich versuche dem zu entgegnen, indem ich Teilverkäufe mache (alles würd ich nie verkaufen) und in andere Assetklassen umschichte. Das sind neben Cash auch Aktien, die eine hohe Dividendenrendite versprechen und möglichst auch Dividendenaristrokaten sind. Logischerweise sind hier die Schwankungen geringer.
Ich habe die Erfahrung gemacht, dass man dann Korrekturen viel entspannter "erträgt", wenn man dann noch Handlungsbereit ist - also z.B. wieder umschichten kann. Aber da bin ich noch sehr am lernen...
SG kmastra
vielen Dank für die Offenlegung. Dein Depot gefällt mir sehr gut. (Überraschung!
 ) Werde mein Depot auch mal posten. CLVS ist auch bei mir die größte Position - soviel weiß ich aus dem Kopf.
) Werde mein Depot auch mal posten. CLVS ist auch bei mir die größte Position - soviel weiß ich aus dem Kopf.Was die Strukturierung des Depots angeht, gibt es meines Erachtens viele Möglichkeiten. Wie gesagt hängt es von vielen ganz individuellen Faktoren ab. Dabei merke ich, dass auch die absolute Größe des Depots eine Rolle spielt. (Die Angst vor Verlusten ist ja größer als die Freude am Gewinn)
Die Sorge um eine Korrektur im nächsten Jahr treibt mich auch um. Ich versuche dem zu entgegnen, indem ich Teilverkäufe mache (alles würd ich nie verkaufen) und in andere Assetklassen umschichte. Das sind neben Cash auch Aktien, die eine hohe Dividendenrendite versprechen und möglichst auch Dividendenaristrokaten sind. Logischerweise sind hier die Schwankungen geringer.
Ich habe die Erfahrung gemacht, dass man dann Korrekturen viel entspannter "erträgt", wenn man dann noch Handlungsbereit ist - also z.B. wieder umschichten kann. Aber da bin ich noch sehr am lernen...
SG kmastra
Antwort auf Beitrag Nr.: 48.668.147 von SLGramann am 30.12.14 16:11:58Hallo SLGramann,
wow... da hast du ja inzwischen genauso viele Positionen wie ich... sieht gut aus!
Mit BLUE, AAVL und CLDN setzt du ein wenig auf die Gentherapie... wird es deiner Meinung nach in diesem Bereich in den nächsten Jahren einen Durchbruch geben? Hier bin ich noch gar nicht dabei, genauso wie bei CAR-T... KITE, BLCM, BLUE. Beide Bereiche sind momentan sehr gefragt. Wie siehst du BLCM im Vergleich zu JUNO oder KITE? Letztere sind ja deutlich höher bewertet.
Viele Positionen sind für mich ein Vorteil, wenn bei einzelnen mal etwas ziemlich schief läuft. Selbst Kurseinbrüche von über 50% sind so gut zu verkraften. Außerdem ist es so für mich leichter, Positionen aufzugeben, wenn sie sich anders entwickelt, als gedacht. Auf der anderen Seite nähert man sich dadurch dem Index an... am Ende könnte man auch direkt z.B. den IBB kaufen.
Mein Depot hat sich dieses Jahr soweit gut entwickelt... ca. +30%. Über 10% davon sind allerdings Währungsgewinne. Und im Vergleich zum NBI bin ich ca. 10% schlechter... also nicht so toll. Das "Problem" sind die großen Biotechs, die in diesem Jahr offensichtlich für Generalisten interessant waren, die auf sicheres Gewinnwachstum und nicht speziell auf Biotechs setzen. Das Verhältnis von KGV zum erwarteten Gewinnwachstum ist bei den großen Biotechs meiner Meinung nach recht attraktiv. Kleinere Biotechs haben weniger profitieren können.
Vielleicht kommt es in absehbarer Zeit auch mal wieder zu einem großen Crash im Biotech-Bereich. Allerdings sehe ich momentan nicht eine vollständige Überhitzung des Bereichs... die Schwergewichte laufen aufgrund des Gewinnwachstums, manche Bereich wie zuletzt z.B. CAR-T wie JUNO sind sehr gefragt, ich habe aber auch mehrere Biotechs, die sich eher schlecht entwickelt haben. Ich würde erwarten, dass in einer vollständigen Hype-Phase alle Biotechs massiv überbewertet sind. Crashs wie im Frühjahr oder Tages-Einbrüche von >4% wie in den letzten Wochen führen bisher nicht zu einem Bruch des langfristigen Aufwärtstrends. Würde eine echte Blase soetwas aushalten?
Ich gehe wohl so ins neue Jahr...
(Depot-Anteil ... Kurssteigerung 2014; MK in Mio USD)
9,3% INCY ... +45%; 12.390
7,7% PCYC ... +16%; 9.285
6,6% CLDX ... -24%; 1.640
5,7% GEN.CO ... +70%; 3.356
5,7% MGNX ... +22%; 928
5,1% MDVN ... +55%; 7.700
5,0% CLVS ... -8%; 1.890
4,8% ISIS ... +55%; 7.315
4,6% ARRY ... -4%; 634
4,4% REGN ... +49%; 41.360
4,2% ENTA ... +89%; 955
4,2% ALNY ... +51%; 7.470
3,5% FPRX ... +57%; 566
3,3% INFI ... +24%; 835
3,0% TSRO ... +31%; 1.330
3,0% IPH.PA ... +60%; 512
2,2% ESPR ... +203%; 645
1,9% XLRN ... -3%; 1.240
1,8% EXEL ... -78%; 264
1,7% CEMP ... +84%; 815
1,6% ACAD ... +27%; 3.170
1,6% SNTA ... -50%; 284
1,5% IMMU ... +2%; 435
1,5% SAGE ... +27%; 981
1,3% SGEN ... -18%; 4.040
1,2% AERI ... +66%; 710
1,2% ARQL ... -47%; 72
1,0% VSTM ... -23%; 228
1,0% STML ... -19%; 206
0,4% KBIO ... -63%; 54
Grüße,
ipollit
wow... da hast du ja inzwischen genauso viele Positionen wie ich... sieht gut aus!
Mit BLUE, AAVL und CLDN setzt du ein wenig auf die Gentherapie... wird es deiner Meinung nach in diesem Bereich in den nächsten Jahren einen Durchbruch geben? Hier bin ich noch gar nicht dabei, genauso wie bei CAR-T... KITE, BLCM, BLUE. Beide Bereiche sind momentan sehr gefragt. Wie siehst du BLCM im Vergleich zu JUNO oder KITE? Letztere sind ja deutlich höher bewertet.
Viele Positionen sind für mich ein Vorteil, wenn bei einzelnen mal etwas ziemlich schief läuft. Selbst Kurseinbrüche von über 50% sind so gut zu verkraften. Außerdem ist es so für mich leichter, Positionen aufzugeben, wenn sie sich anders entwickelt, als gedacht. Auf der anderen Seite nähert man sich dadurch dem Index an... am Ende könnte man auch direkt z.B. den IBB kaufen.
Mein Depot hat sich dieses Jahr soweit gut entwickelt... ca. +30%. Über 10% davon sind allerdings Währungsgewinne. Und im Vergleich zum NBI bin ich ca. 10% schlechter... also nicht so toll. Das "Problem" sind die großen Biotechs, die in diesem Jahr offensichtlich für Generalisten interessant waren, die auf sicheres Gewinnwachstum und nicht speziell auf Biotechs setzen. Das Verhältnis von KGV zum erwarteten Gewinnwachstum ist bei den großen Biotechs meiner Meinung nach recht attraktiv. Kleinere Biotechs haben weniger profitieren können.
Vielleicht kommt es in absehbarer Zeit auch mal wieder zu einem großen Crash im Biotech-Bereich. Allerdings sehe ich momentan nicht eine vollständige Überhitzung des Bereichs... die Schwergewichte laufen aufgrund des Gewinnwachstums, manche Bereich wie zuletzt z.B. CAR-T wie JUNO sind sehr gefragt, ich habe aber auch mehrere Biotechs, die sich eher schlecht entwickelt haben. Ich würde erwarten, dass in einer vollständigen Hype-Phase alle Biotechs massiv überbewertet sind. Crashs wie im Frühjahr oder Tages-Einbrüche von >4% wie in den letzten Wochen führen bisher nicht zu einem Bruch des langfristigen Aufwärtstrends. Würde eine echte Blase soetwas aushalten?
Ich gehe wohl so ins neue Jahr...
(Depot-Anteil ... Kurssteigerung 2014; MK in Mio USD)
9,3% INCY ... +45%; 12.390
7,7% PCYC ... +16%; 9.285
6,6% CLDX ... -24%; 1.640
5,7% GEN.CO ... +70%; 3.356
5,7% MGNX ... +22%; 928
5,1% MDVN ... +55%; 7.700
5,0% CLVS ... -8%; 1.890
4,8% ISIS ... +55%; 7.315
4,6% ARRY ... -4%; 634
4,4% REGN ... +49%; 41.360
4,2% ENTA ... +89%; 955
4,2% ALNY ... +51%; 7.470
3,5% FPRX ... +57%; 566
3,3% INFI ... +24%; 835
3,0% TSRO ... +31%; 1.330
3,0% IPH.PA ... +60%; 512
2,2% ESPR ... +203%; 645
1,9% XLRN ... -3%; 1.240
1,8% EXEL ... -78%; 264
1,7% CEMP ... +84%; 815
1,6% ACAD ... +27%; 3.170
1,6% SNTA ... -50%; 284
1,5% IMMU ... +2%; 435
1,5% SAGE ... +27%; 981
1,3% SGEN ... -18%; 4.040
1,2% AERI ... +66%; 710
1,2% ARQL ... -47%; 72
1,0% VSTM ... -23%; 228
1,0% STML ... -19%; 206
0,4% KBIO ... -63%; 54
Grüße,
ipollit
Antwort auf Beitrag Nr.: 48.669.920 von ipollit am 30.12.14 20:27:43"Mit BLUE, AAVL und CLDN setzt du ein wenig auf die Gentherapie... wird es deiner Meinung nach in diesem Bereich in den nächsten Jahren einen Durchbruch geben? Hier bin ich noch gar nicht dabei, genauso wie bei CAR-T... KITE, BLCM, BLUE. Beide Bereiche sind momentan sehr gefragt. Wie siehst du BLCM im Vergleich zu JUNO oder KITE? Letztere sind ja deutlich höher bewertet."
Hallo ipollit,
tja... schwierig. Ich habe dazu folgende Meinung, was natürlich etwas ganz anderes als Wissen ist:
Ja, bei der Gentherapie hoffe ich auf den Durchbruch. Nach endlosen Jahren scheinbar leerer Versprechen gibt es jetzt doch Hinweise, dass man an der Schwelle zur medizinischen Anwendung steht.
Wichtig ist für mich in diesem Zusammenhang, dass es von allen drei Unternehmen (BLUE, AAVL, CLDN) erste, vorläufige, aber eben ermutigende, klinische Daten gibt.
Das ist für mich wirklich entscheidend. Theorie klingt immer gut, aber hier haben wir klinische Daten. Das ist einfach ein anderes Level.
Die Risiken sind enorm. Dementsprechend sind die Positionen bescheiden. BLUE zum Beispiel haben jetzt zwar 6% am Depot erreicht. Gekauft wurden sie aber zu 20,43 Dollar, so dass der inzwischen eher hohe Depotanteil allein auf die Kursentwicklung zurückzuführen ist.
CAR-T: Hier hatte ich die grundsätzliche Entscheidung getroffen, dabei sein zu wollen. Für unsereins bleibt die Lage unübersichtlich und ich gebe gerne zu, mich hier auf mein Bauchgefühl zu verlassen. KITE halte ich für den besten Wert. Wenn ich mir die handelnden Personen ansehe, habe ich hier das größte Vertrauen. BLCM sehe ich nur in zweiter Linie als CAR-T-Play. In erster Linie gefällt mir ihre "cell-suicide"-Technologie, also dieser Sicherheitsschalter, der natürlich ein Problem adressiert, das gerade bei den CAR-T-Techniken auftaucht. Zunächst mal finde ich aber die Idee, die allogeneic hematopoietic stem cell transplantation (HSCT) sicherer zu machen, attraktiv (BPX-501).
http://www.bellicum.com/product-candidates/bpx-501/
Ähnlich wie bei BLUE sehe ich auch hier CAR-T eher als Zugabe. Durch den "Sicherheitsschalter" hier aber als besonders interessante Zugabe.
JUNO: Sagen wir mal so: Die werden schon was drauf haben... aber, mein Bauchgefühl sagt mir, dass hier mehr Hype als bei allen anderen ist. Wirkt auf mich alles etwas krawallig und von den handelnden Personen her nicht so elitär wie bei KITE (nur mein Eindruck). Nach meinem Bauchgefühl der am wenigsten seriöse, am wenigsten besondere, dafür aber der bei weitem am lauteste und teuerste CAR-T-Play. Ich fand die 1 Milliarde bei KITE schon unverschämt (erster Börsenkurs). Bei Juno (jenseits 4 Milliarden für bis jetzt fast nichts) kann ich nur sagen: Machts euch selbst.
Grüße
SLG
Hallo ipollit,
tja... schwierig. Ich habe dazu folgende Meinung, was natürlich etwas ganz anderes als Wissen ist:
Ja, bei der Gentherapie hoffe ich auf den Durchbruch. Nach endlosen Jahren scheinbar leerer Versprechen gibt es jetzt doch Hinweise, dass man an der Schwelle zur medizinischen Anwendung steht.
Wichtig ist für mich in diesem Zusammenhang, dass es von allen drei Unternehmen (BLUE, AAVL, CLDN) erste, vorläufige, aber eben ermutigende, klinische Daten gibt.
Das ist für mich wirklich entscheidend. Theorie klingt immer gut, aber hier haben wir klinische Daten. Das ist einfach ein anderes Level.
Die Risiken sind enorm. Dementsprechend sind die Positionen bescheiden. BLUE zum Beispiel haben jetzt zwar 6% am Depot erreicht. Gekauft wurden sie aber zu 20,43 Dollar, so dass der inzwischen eher hohe Depotanteil allein auf die Kursentwicklung zurückzuführen ist.
CAR-T: Hier hatte ich die grundsätzliche Entscheidung getroffen, dabei sein zu wollen. Für unsereins bleibt die Lage unübersichtlich und ich gebe gerne zu, mich hier auf mein Bauchgefühl zu verlassen. KITE halte ich für den besten Wert. Wenn ich mir die handelnden Personen ansehe, habe ich hier das größte Vertrauen. BLCM sehe ich nur in zweiter Linie als CAR-T-Play. In erster Linie gefällt mir ihre "cell-suicide"-Technologie, also dieser Sicherheitsschalter, der natürlich ein Problem adressiert, das gerade bei den CAR-T-Techniken auftaucht. Zunächst mal finde ich aber die Idee, die allogeneic hematopoietic stem cell transplantation (HSCT) sicherer zu machen, attraktiv (BPX-501).
http://www.bellicum.com/product-candidates/bpx-501/
Ähnlich wie bei BLUE sehe ich auch hier CAR-T eher als Zugabe. Durch den "Sicherheitsschalter" hier aber als besonders interessante Zugabe.
JUNO: Sagen wir mal so: Die werden schon was drauf haben... aber, mein Bauchgefühl sagt mir, dass hier mehr Hype als bei allen anderen ist. Wirkt auf mich alles etwas krawallig und von den handelnden Personen her nicht so elitär wie bei KITE (nur mein Eindruck). Nach meinem Bauchgefühl der am wenigsten seriöse, am wenigsten besondere, dafür aber der bei weitem am lauteste und teuerste CAR-T-Play. Ich fand die 1 Milliarde bei KITE schon unverschämt (erster Börsenkurs). Bei Juno (jenseits 4 Milliarden für bis jetzt fast nichts) kann ich nur sagen: Machts euch selbst.
Grüße
SLG
könnte mir jemand von den experten eine einschätzing zu Epizyme (EPZM) geben?
Wäre sehr nett
Danke
Wäre sehr nett
Danke
Ohad Hammer mit einer Zusammenfassung von 2014 und Ausblick auf 2015...
http://www.orf-blog.com/biotech-portfolio-update-2014-summar…
Manche Entscheidungen kann ich nicht so ganz nachvollziehen... hat es nicht auch Gründe, dass MRNS deutlich niedriger als SAGE bewertet wird?
Vielleicht fehlt ihm manchmal die Zeit... das eine oder andere ist so nicht korrekt. Z.B. schreibt er einiges zu INCYs JAK1 INCB047986 in RA. Soweit ich weiß hat INCY die Entwicklung dieses Kandidaten vor ein paar Monaten bereits eingestellt aufgrund von Nebenwirkungen.
Gruß
ipollit
http://www.orf-blog.com/biotech-portfolio-update-2014-summar…
Manche Entscheidungen kann ich nicht so ganz nachvollziehen... hat es nicht auch Gründe, dass MRNS deutlich niedriger als SAGE bewertet wird?
Vielleicht fehlt ihm manchmal die Zeit... das eine oder andere ist so nicht korrekt. Z.B. schreibt er einiges zu INCYs JAK1 INCB047986 in RA. Soweit ich weiß hat INCY die Entwicklung dieses Kandidaten vor ein paar Monaten bereits eingestellt aufgrund von Nebenwirkungen.
Gruß
ipollit
CAR-T, TCR...
hier sind ein paar Präsentationen zu diesem Bereich...
https://www.youtube.com/channel/UCvJ7SAK-5kH3MHxuClDCmAA
u.a. eine Präsentation von Prof. Carl June zu CAR-T, der soweit ich weiß zu den bedeutesten Personen in diesem Bereich gehört (http://www.fiercebiotech.com/special-reports/carl-june-unive…)...
https://www.youtube.com/watch?v=D3WmGZi4Xms
"Engineered T-Cells for Cancer in the Era of Synthetic Biology Challenges & Opportunities"
Ein interessanter Aspekt darin, den ich bisher so nicht gesehen habe, ist, dass die modifizieren T-Zellen als lebende Zellen sich zum einen im Körper noch stark vermehren können (spricht die Therapie an, vermehren sie sich... spricht sie nicht an, gibt es keine Vermehrung) und zum anderen sehr lange im Körper aktiv bleiben. Lange heißt u.U. Jahrzehnte.
Letzteres kann ein Vorteil sein, da eine einmalige Gabe von CAR-Ts eine sehr lange Wirkung hat... allerdings wird dadurch auch sehr lange das Target im Körper eliminiert. D.h. im Fall von CD19-CARTs, dass über einen sehr langen Zeitraum sämtliche B-Zellen zerstört werden (CD19 ist noch weitreichender auf B-Zellen vorhanden als CD19). Nach einer CD19 CAR-T Behandlung muss ein Patient alle paar Monate neue B-Zellen erhalten. CARTs und ähnliche Zelltherapien benötigen daher viele Blutspenden, aus denen z.B. B-Zellen oder Serum zur Kultivierung der CARTs gewonnen werden. Zur Begrenzung der B-Zell-Infusionen wäre laut Prof. June z.B. ein Kill-Switch hilfreich... nach z.B. 3 Jahren würde man alle CARTs per Switch zerstören. Kommt der Krebs danach zurück, müsste eine weitere CART-Therapie erfolgen.
Laut Prof June sind Resistenzen gegen CAR-Ts möglich, z.B. wenn das Target nicht mehr expressioniert wird. Dies wäre bei ca. 10% der Patienten... z.B. wenn nach einer CD19-CART Therapie die Krebszellen kein CD19 mehr expressionieren. Eine einfache Lösung sind Kombi-Therapien, also die Verabreichung von mehreren CARTs gegen unterschiedliche Targets... so wie z.B. auch HIV-Therapien üblicherweise Kombi-Therapien sind zur Vermeidung von Resistenzen.
Interessant ist auch das Einführungsbeispiel...

Im Maus-Experiment entsteht in Mäusen, in denen man eine bestimmte Mutation einfügt, Krebs. Diese Mutationen sind "Driver". Behebt man diese Mutation wieder, so bildet sich der Krebs wieder zurück (untere Line). Dies ist der Ansatzpunkt für alle Target-Therapien, die sich gegen bestimmte Driver-Mutationen richten. Interessant ist nun, dass in Mäusen, bei denen man zusätzlich das Immunsystem unterdrückt, die Behebung der Driver-Mutation zwar einige Zeit zu einer Verringerung des Krebs führt... dann bricht der Krebs aber auch ohne die Mutation durch. Daraus folgt, dass das Immunsystem zur Bekämpfung des Krebs sehr wichtig ist. Target-Therapien sind demnach nicht das einzige, was zur Heilung notwendig ist.
Ein weiteres Beispiel von Prof. June zur Bedeutung des Immunsystems: Eine Patientin erhält nach einer Blutkrebs-Erkrankung eine Stammzellspende, die erfolgreich ist... die Patientin scheint geheilt zu sein. Viele Jahre später stirbt sie an etwas anderem... ihre Organe werden danach gespendet. Alle Patienten, die ein Organ erhalten, erkranken daraufhin an diesem Krebs. Ursache ist wohl, dass bei den Patienten das Immunsystem unterdrückt werden muss, damit das neue Organ nicht abgestoßen wird. Im Organ gibt es aber wohl nachwievor Krebszellen, die von einem intakten Immunsystem offensichtlich in Schach gehalten werden können (die Patientin hatte ja kein nachweisbaren Krebs mehr). Als man die Unterdrückung des Immunsystems bei den Patienten mit Spenderorgan wieder aufhob, verschwand der Krebs wieder (das Organ haben sie dabei aber auch wieder verloren).
Prof. June scheint mit NVS zusammen zu arbeiten. NVS nutzt die Technologie von Oxford Biomedica... letztere erhalten dafür kleine Royalties für alle NVS CARTs. Oxford Biomedica sehe ich als europäischen Konkurrent zu BLUE.
Hier sind auch Präsentationen zu TCR-modifizierten T-Zellen von Adaptimmune: CARTs greifen Moleküle an, an die auch Antikörper andocken wie CD19, CD20, HER2 usw... TCRs sind dagegen T-Zell-Rezeptoren, die auch in natürlichen T-Zellen vorkommen, mit denen T-Zellen normalerweise problematische Zellen erkennen. Traurig, dass Medigene u.a. Adaptimmune verschenkt hat.
https://www.youtube.com/watch?v=ChinX6Jug1w
https://www.youtube.com/watch?v=qhVZ3jPYv6A
Da T-Zellen ein Target sehr aggressiv angreifen, sind körpereigene Antigene nur sehr schwach oder garnicht in der Lage, eine T-Zelle zu aktivieren... ansonsten käme es zu schwersten Autoimmunreaktionen. Krebszellen weisen meistens nur körpereigene Antigene auf... das macht es auch sehr schwer, das Immunsysten z.B. durch therapeutische Impfungen gegen den Krebs zu aktivieren. Ist eine Zelle dagegen von einem Virus befallen, so wird eine T-Zelle anhand der Virus-Antigene viel schneller aktiv.
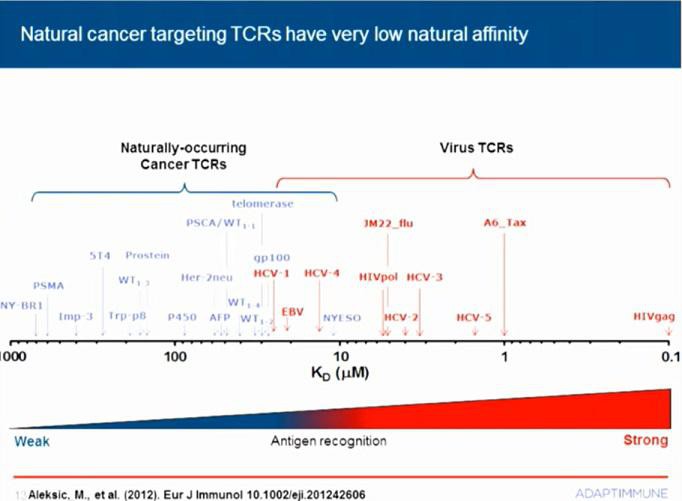
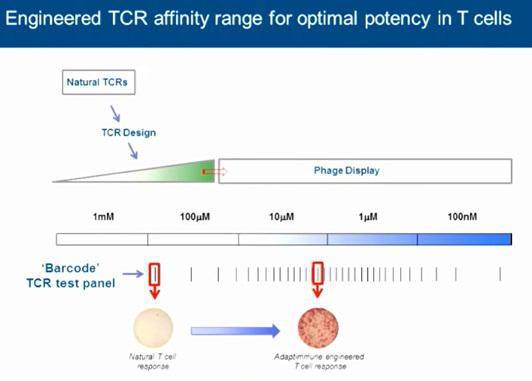
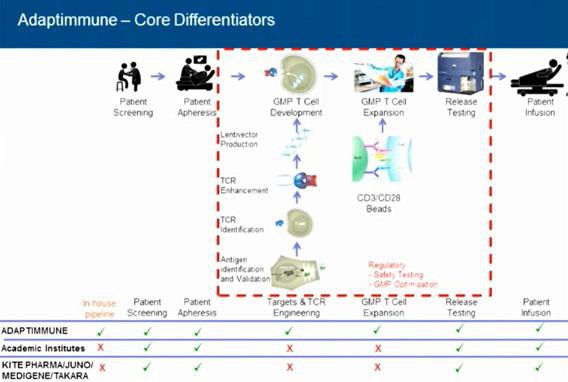
NYESO scheint ein körpereigenes Antigen zu sein, was aber kaum auf normalen Zellen vorkommt und somit besser von T-Zellen erkannt werden kann (CLDX hat dagegen auch eine AK-Vakzine mit CDX-1401). Adaptimmune behauptet, dass nur sie im Gegensatz zu KITE&Co in der Lage wären, die TCRs so zu optimieren, dass sie die T-Zellen ausreichend aktivieren können. Mal abwarten.
Gruß
ipollit
hier sind ein paar Präsentationen zu diesem Bereich...
https://www.youtube.com/channel/UCvJ7SAK-5kH3MHxuClDCmAA
u.a. eine Präsentation von Prof. Carl June zu CAR-T, der soweit ich weiß zu den bedeutesten Personen in diesem Bereich gehört (http://www.fiercebiotech.com/special-reports/carl-june-unive…)...
https://www.youtube.com/watch?v=D3WmGZi4Xms
"Engineered T-Cells for Cancer in the Era of Synthetic Biology Challenges & Opportunities"
Ein interessanter Aspekt darin, den ich bisher so nicht gesehen habe, ist, dass die modifizieren T-Zellen als lebende Zellen sich zum einen im Körper noch stark vermehren können (spricht die Therapie an, vermehren sie sich... spricht sie nicht an, gibt es keine Vermehrung) und zum anderen sehr lange im Körper aktiv bleiben. Lange heißt u.U. Jahrzehnte.
Letzteres kann ein Vorteil sein, da eine einmalige Gabe von CAR-Ts eine sehr lange Wirkung hat... allerdings wird dadurch auch sehr lange das Target im Körper eliminiert. D.h. im Fall von CD19-CARTs, dass über einen sehr langen Zeitraum sämtliche B-Zellen zerstört werden (CD19 ist noch weitreichender auf B-Zellen vorhanden als CD19). Nach einer CD19 CAR-T Behandlung muss ein Patient alle paar Monate neue B-Zellen erhalten. CARTs und ähnliche Zelltherapien benötigen daher viele Blutspenden, aus denen z.B. B-Zellen oder Serum zur Kultivierung der CARTs gewonnen werden. Zur Begrenzung der B-Zell-Infusionen wäre laut Prof. June z.B. ein Kill-Switch hilfreich... nach z.B. 3 Jahren würde man alle CARTs per Switch zerstören. Kommt der Krebs danach zurück, müsste eine weitere CART-Therapie erfolgen.
Laut Prof June sind Resistenzen gegen CAR-Ts möglich, z.B. wenn das Target nicht mehr expressioniert wird. Dies wäre bei ca. 10% der Patienten... z.B. wenn nach einer CD19-CART Therapie die Krebszellen kein CD19 mehr expressionieren. Eine einfache Lösung sind Kombi-Therapien, also die Verabreichung von mehreren CARTs gegen unterschiedliche Targets... so wie z.B. auch HIV-Therapien üblicherweise Kombi-Therapien sind zur Vermeidung von Resistenzen.
Interessant ist auch das Einführungsbeispiel...

Im Maus-Experiment entsteht in Mäusen, in denen man eine bestimmte Mutation einfügt, Krebs. Diese Mutationen sind "Driver". Behebt man diese Mutation wieder, so bildet sich der Krebs wieder zurück (untere Line). Dies ist der Ansatzpunkt für alle Target-Therapien, die sich gegen bestimmte Driver-Mutationen richten. Interessant ist nun, dass in Mäusen, bei denen man zusätzlich das Immunsystem unterdrückt, die Behebung der Driver-Mutation zwar einige Zeit zu einer Verringerung des Krebs führt... dann bricht der Krebs aber auch ohne die Mutation durch. Daraus folgt, dass das Immunsystem zur Bekämpfung des Krebs sehr wichtig ist. Target-Therapien sind demnach nicht das einzige, was zur Heilung notwendig ist.
Ein weiteres Beispiel von Prof. June zur Bedeutung des Immunsystems: Eine Patientin erhält nach einer Blutkrebs-Erkrankung eine Stammzellspende, die erfolgreich ist... die Patientin scheint geheilt zu sein. Viele Jahre später stirbt sie an etwas anderem... ihre Organe werden danach gespendet. Alle Patienten, die ein Organ erhalten, erkranken daraufhin an diesem Krebs. Ursache ist wohl, dass bei den Patienten das Immunsystem unterdrückt werden muss, damit das neue Organ nicht abgestoßen wird. Im Organ gibt es aber wohl nachwievor Krebszellen, die von einem intakten Immunsystem offensichtlich in Schach gehalten werden können (die Patientin hatte ja kein nachweisbaren Krebs mehr). Als man die Unterdrückung des Immunsystems bei den Patienten mit Spenderorgan wieder aufhob, verschwand der Krebs wieder (das Organ haben sie dabei aber auch wieder verloren).
Prof. June scheint mit NVS zusammen zu arbeiten. NVS nutzt die Technologie von Oxford Biomedica... letztere erhalten dafür kleine Royalties für alle NVS CARTs. Oxford Biomedica sehe ich als europäischen Konkurrent zu BLUE.
Hier sind auch Präsentationen zu TCR-modifizierten T-Zellen von Adaptimmune: CARTs greifen Moleküle an, an die auch Antikörper andocken wie CD19, CD20, HER2 usw... TCRs sind dagegen T-Zell-Rezeptoren, die auch in natürlichen T-Zellen vorkommen, mit denen T-Zellen normalerweise problematische Zellen erkennen. Traurig, dass Medigene u.a. Adaptimmune verschenkt hat.
https://www.youtube.com/watch?v=ChinX6Jug1w
https://www.youtube.com/watch?v=qhVZ3jPYv6A
Da T-Zellen ein Target sehr aggressiv angreifen, sind körpereigene Antigene nur sehr schwach oder garnicht in der Lage, eine T-Zelle zu aktivieren... ansonsten käme es zu schwersten Autoimmunreaktionen. Krebszellen weisen meistens nur körpereigene Antigene auf... das macht es auch sehr schwer, das Immunsysten z.B. durch therapeutische Impfungen gegen den Krebs zu aktivieren. Ist eine Zelle dagegen von einem Virus befallen, so wird eine T-Zelle anhand der Virus-Antigene viel schneller aktiv.



NYESO scheint ein körpereigenes Antigen zu sein, was aber kaum auf normalen Zellen vorkommt und somit besser von T-Zellen erkannt werden kann (CLDX hat dagegen auch eine AK-Vakzine mit CDX-1401). Adaptimmune behauptet, dass nur sie im Gegensatz zu KITE&Co in der Lage wären, die TCRs so zu optimieren, dass sie die T-Zellen ausreichend aktivieren können. Mal abwarten.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.681.146 von pickuru am 02.01.15 15:18:44EPZM
leider kann ich es auch nicht gut einschätzen. Eigentlich habe ich gedacht, dass EPZM als ein führendes Unternehmen für epigenetische Therapien interessant ist. Bisherige Ergebnisse scheinen aber nicht so toll zu sein... jedenfalls scheint der Markt EPZM nicht sehr positiv zu sehen, anders als z.B. AGIO. Müsste ich mir nochmal genauer ansehen.

Gruß
ipollit
leider kann ich es auch nicht gut einschätzen. Eigentlich habe ich gedacht, dass EPZM als ein führendes Unternehmen für epigenetische Therapien interessant ist. Bisherige Ergebnisse scheinen aber nicht so toll zu sein... jedenfalls scheint der Markt EPZM nicht sehr positiv zu sehen, anders als z.B. AGIO. Müsste ich mir nochmal genauer ansehen.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.691.052 von ipollit am 04.01.15 16:14:37"Manche Entscheidungen kann ich nicht so ganz nachvollziehen... hat es nicht auch Gründe, dass MRNS deutlich niedriger als SAGE bewertet wird?
Vielleicht fehlt ihm manchmal die Zeit..."
Hallo ipollit,
geht mir wie Dir. Ich glaube, Hammer ist bei den Bewertungen etwas zu streng. Er ist auch insgesamt vorsichtiger geworden, manchmal zu vorsichtig, wie ich finde. 40% Cash im Depot sind schon heftig... Vielleicht ist das auch zum Teil dem Zeitmangel geschuldet. Dafür fehlt andererseits aber bspw. eine MGNX, die er ja ziemlich toll findet, aber immer vor einem Kauf zurückgeschreckt ist. PCYC viel zu früh verkauft, obwohl er genau wusste und geschrieben hat, dass hier ein Mega-Blockbuster in der Mache ist.
Trotzdem natürlich der beste Biotech-Blog ever. Keine Frage.
(toller Beitrag von Dir zu CAR und TCR)
Gruß
SLG
PS: Mache ab morgen erst mal Urlaub und schau Ende Januar mal, was alles passiert ist.
Vielleicht fehlt ihm manchmal die Zeit..."
Hallo ipollit,
geht mir wie Dir. Ich glaube, Hammer ist bei den Bewertungen etwas zu streng. Er ist auch insgesamt vorsichtiger geworden, manchmal zu vorsichtig, wie ich finde. 40% Cash im Depot sind schon heftig... Vielleicht ist das auch zum Teil dem Zeitmangel geschuldet. Dafür fehlt andererseits aber bspw. eine MGNX, die er ja ziemlich toll findet, aber immer vor einem Kauf zurückgeschreckt ist. PCYC viel zu früh verkauft, obwohl er genau wusste und geschrieben hat, dass hier ein Mega-Blockbuster in der Mache ist.
Trotzdem natürlich der beste Biotech-Blog ever. Keine Frage.
(toller Beitrag von Dir zu CAR und TCR)
Gruß
SLG
PS: Mache ab morgen erst mal Urlaub und schau Ende Januar mal, was alles passiert ist.

CEMP
das neue Jahr startet direkt mit positiven PIII-Daten von CEMPs Antibiotikum Solithromycin ...
http://finance.yahoo.com/news/cempra-announces-positive-topl…
"Solithromycin met the primary and secondary objectives of non-inferiority compared to moxifloxacin"
hier ein Analysten-Kommentar von letzter Woche...
"In a report published Wednesday, Stifel analyst Stephen Willey reiterated a Buy rating on Cempra Inc (NASDAQ: CEMP), and raised the price target from $22.00 to $33.00.
In the report, Stifel noted, “Despite recent price appreciation, we continue to like risk/reward ahead of what we believe will be early-1Q15/top-line P3 SOLITAIRE-ORAL data for solithromycin in community acquired bacterial pneumonia (CABP). Updated model changes include a shallower solithromycin launch trajectory, marginally-reduced peak CABP sales, and favorable risk adjustments to what were admittedly overly-conservative inputs driving our valuation methodologies. Target price increases to $33 (previously $22) and we believe recent acquisition multiples in what is proving to be a rapidly-consolidating antibiotic space comfortably support a 2-3x higher valuation. Remains our 2015 Top Pick.”"

...Can you tell us what they say about peak sales for Sol?
U.S./Europe $1.25-1.35B (previously $1.85-1.95B) and Japan $350M (previously $250M)

Gruß
ipollit
das neue Jahr startet direkt mit positiven PIII-Daten von CEMPs Antibiotikum Solithromycin ...

http://finance.yahoo.com/news/cempra-announces-positive-topl…
"Solithromycin met the primary and secondary objectives of non-inferiority compared to moxifloxacin"
hier ein Analysten-Kommentar von letzter Woche...
"In a report published Wednesday, Stifel analyst Stephen Willey reiterated a Buy rating on Cempra Inc (NASDAQ: CEMP), and raised the price target from $22.00 to $33.00.
In the report, Stifel noted, “Despite recent price appreciation, we continue to like risk/reward ahead of what we believe will be early-1Q15/top-line P3 SOLITAIRE-ORAL data for solithromycin in community acquired bacterial pneumonia (CABP). Updated model changes include a shallower solithromycin launch trajectory, marginally-reduced peak CABP sales, and favorable risk adjustments to what were admittedly overly-conservative inputs driving our valuation methodologies. Target price increases to $33 (previously $22) and we believe recent acquisition multiples in what is proving to be a rapidly-consolidating antibiotic space comfortably support a 2-3x higher valuation. Remains our 2015 Top Pick.”"

...Can you tell us what they say about peak sales for Sol?
U.S./Europe $1.25-1.35B (previously $1.85-1.95B) and Japan $350M (previously $250M)
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.692.405 von SLGramann am 04.01.15 20:53:25Hallo SLGramann,
dann eine schöne erholsame Zeit! Bin gespannt, wie es in den nächsten Wochen weiter geht. Nächste Woche (ab dem 12.1.) ist erstmal die JPM Healthcare Conference... die wohl größte derartige Biotech-Konferenz im Laufe eines Jahres. Vielleicht gibt es dort ja die eine oder andere Neuigkeit.
Grüße
ipollit
dann eine schöne erholsame Zeit! Bin gespannt, wie es in den nächsten Wochen weiter geht. Nächste Woche (ab dem 12.1.) ist erstmal die JPM Healthcare Conference... die wohl größte derartige Biotech-Konferenz im Laufe eines Jahres. Vielleicht gibt es dort ja die eine oder andere Neuigkeit.
Grüße
ipollit
Antwort auf Beitrag Nr.: 48.692.873 von ipollit am 04.01.15 23:56:03Wow. Glückwunsch ipollit!!
Das CEMP sich innerhalb von 3 Monaten verdreifacht (und das nicht ohne Grund) spricht definitiv gegen eine Biotechblase. Auf jeden Fall eine unfassbare Performance!
@SLGramann: Ich hoffe es ist noch nicht so weit, dass du deinen Urlaub in San Francisco auf der JPMorgan Konferenz verbringst!?
SG kmastra
Das CEMP sich innerhalb von 3 Monaten verdreifacht (und das nicht ohne Grund) spricht definitiv gegen eine Biotechblase. Auf jeden Fall eine unfassbare Performance!
@SLGramann: Ich hoffe es ist noch nicht so weit, dass du deinen Urlaub in San Francisco auf der JPMorgan Konferenz verbringst!?
SG kmastra
FGEN, KITE, CNAT, ISIS
heute gab es einige größere Kurssprünge (>+10%)... u.a.




Gruß
ipollit
heute gab es einige größere Kurssprünge (>+10%)... u.a.
Gruß
ipollit
ZFGN:
ZFGN weiß heute mit positiven P2 Ergebnissen zu gefallen. Die Studie hatte nur 14 Teilnehmer und war trotzdem signifikant. Es scheint so, als ob Beloranib tatsächlich bei Jedem funktioniert - zumindest über die bisher getesteten Zeiträume. Scheitern kann Beloranib doch eigentlich nur an der Sicherheit!?
Zwar gibt es hier noch keine Anzeichen aber das wäre dann die Vollkatastrophe, denn was wäre ZFGN dann noch Wert, da eigentlich alles von MetAP2 abhängt. Bei der P3 wird nun aber über 6 bzw. 12 Monate getestet. Hopp oder Top!
http://www.fiercebiotech.com/story/zafgens-promising-obesity…
ZFGN weiß heute mit positiven P2 Ergebnissen zu gefallen. Die Studie hatte nur 14 Teilnehmer und war trotzdem signifikant. Es scheint so, als ob Beloranib tatsächlich bei Jedem funktioniert - zumindest über die bisher getesteten Zeiträume. Scheitern kann Beloranib doch eigentlich nur an der Sicherheit!?
Zwar gibt es hier noch keine Anzeichen aber das wäre dann die Vollkatastrophe, denn was wäre ZFGN dann noch Wert, da eigentlich alles von MetAP2 abhängt. Bei der P3 wird nun aber über 6 bzw. 12 Monate getestet. Hopp oder Top!
http://www.fiercebiotech.com/story/zafgens-promising-obesity…
Antwort auf Beitrag Nr.: 48.718.691 von kmastra am 07.01.15 18:01:50Hallo kmastra,
ja... der Markt hat auch sehr positiv reagiert.
ZFGN gehört damit heute ebenfalls zu den Biotechs mit einem Kursplus von >+10%...

der französische CART-Play Cellectis ist nach dem Erhalt eines Patents ebenfalls deutlich im Plus

Beim IO-Biotech Trillium SCTPF / TRIL macht sich das Nasdaq-Listing bemerkbar...

Gruß
ipollit
ja... der Markt hat auch sehr positiv reagiert.
ZFGN gehört damit heute ebenfalls zu den Biotechs mit einem Kursplus von >+10%...
der französische CART-Play Cellectis ist nach dem Erhalt eines Patents ebenfalls deutlich im Plus
Beim IO-Biotech Trillium SCTPF / TRIL macht sich das Nasdaq-Listing bemerkbar...
Gruß
ipollit
Hab gestern dann doch mal mein Depot genauer aufgeschlüsselt.
Ich setzte insbesondere auf Werte, bei denen 2015 große Events (PIII Ergebnisse/ Zulassungsentscheidungen) anstehen - und ich zudem einen Erfolg für wahrscheinlich halte. Wird sicherlich ein spannendes Jahr und ging ja auch schon ganz gut los!
CLVS: 18%
ARRY: 13%
ESPR: 12%
ZFGN: 10%
FMI: 8%
ONTY: 7%
GILD: 5%
ENTA: 4%
ARQL: 4%
ACAD: 4%
Medigene: 3%
AMBI CVRs: 0%
GSK: 5%
NEM: 3%
Cash:4%
SG kmastra
Ich setzte insbesondere auf Werte, bei denen 2015 große Events (PIII Ergebnisse/ Zulassungsentscheidungen) anstehen - und ich zudem einen Erfolg für wahrscheinlich halte. Wird sicherlich ein spannendes Jahr und ging ja auch schon ganz gut los!
CLVS: 18%
ARRY: 13%
ESPR: 12%
ZFGN: 10%
FMI: 8%
ONTY: 7%
GILD: 5%
ENTA: 4%
ARQL: 4%
ACAD: 4%
Medigene: 3%
AMBI CVRs: 0%

GSK: 5%
NEM: 3%
Cash:4%
SG kmastra
KBIO
nachdem der GM-CSF AK KB003 bereits gescheitert ist und Sanofi aus KB001-Programm ausgestiegen ist, gab es nun eindeutig negative PII-Ergebnisse von KB001 in CF und den Abbruch dieses Programms.
Ursprünglich habe ich nur aufgrund des EphA3 AKs KB004 u.a. gegen AML eine Position gekauft und die anderen beiden Kandidaten als zusätzliche Chance gesehen. Nun ist nur noch KB004 übrig. Die MK war schon recht niedrig... trotzdem scheint es für die Bewertung keine Grenze nach unten zu geben. Nach dem Absturz sind es nur noch 16 Mio USD bei Cash von 50 Mio USD und EV von -20 Mio USD. Selbst die Aktien, die aufgrund einer niedrigen Bewertung eigentlich "günstig" aussehen, können trotzdem noch stark fallen.
Letztlich ist nun auch noch der CEO zurückgetreten. So macht das Investment trotz KB004 für mich keinen Sinn mehr.

Gruß
ipollit
nachdem der GM-CSF AK KB003 bereits gescheitert ist und Sanofi aus KB001-Programm ausgestiegen ist, gab es nun eindeutig negative PII-Ergebnisse von KB001 in CF und den Abbruch dieses Programms.
Ursprünglich habe ich nur aufgrund des EphA3 AKs KB004 u.a. gegen AML eine Position gekauft und die anderen beiden Kandidaten als zusätzliche Chance gesehen. Nun ist nur noch KB004 übrig. Die MK war schon recht niedrig... trotzdem scheint es für die Bewertung keine Grenze nach unten zu geben. Nach dem Absturz sind es nur noch 16 Mio USD bei Cash von 50 Mio USD und EV von -20 Mio USD. Selbst die Aktien, die aufgrund einer niedrigen Bewertung eigentlich "günstig" aussehen, können trotzdem noch stark fallen.
Letztlich ist nun auch noch der CEO zurückgetreten. So macht das Investment trotz KB004 für mich keinen Sinn mehr.
Gruß
ipollit
INFI
ein weiteres negatives Ereignis diese Woche war der Fehlschlag von Duvelisib in RA. Infolge dessen beendet INFI die Entwicklung von Duvelisib und anderen pki3-delta/gamma-Hemmern wie IPI-443 gegen Autoimmunerkrankungen wie RA oder Asthma. Eigentlich hatte ich gehofft, dass speziell die delta/gamma Kombination in diesem Bereich wirksam ist.
Trotzdem sehe ich Duvelisib unabhängig davon als sehr aussichtsreich gegen Krebs... z.B. gegen iNHL. Ich setze darauf, dass es u.a. in iNHL besser als GILDs pi3k-delta-Hemmer Zydelig oder PCYCs BTK-Hemmer Imbruvica wirkt. Die Partnerschaft mit ABBV ist sehr gut, da ABBVs BCL2-Hemmer ABT-199 ebenfalls ein möglicher starker Konkurrent u.a. zu Imbruvica sein kann. Soweit ich die bisherigen Ergebnisse sehe, hat ABT-199 eine deutlich höhere CR-Rate, dafür aber das Risiko eines Tumor Lysis Syndroms (TLS), welches zu schweren Nebenwirkungen führen kann. TLS tritt wohl dann auf, wenn ABT-199 die Tumorzellen massiv abtötet, was eigentlich erstmal gut ist, da es eine hohe Wirksamkeit belegt. Die große Menge abgetöteter Zellen führt aber zu starken lebensbedrohlichen Immunreaktionen des Körpers, die sich nur schwer kontrollieren lassen. Selbst wenn ABT-199 wirksamer ist, wird man aufgrund des TLS-Risikos zuerst immer etwas anderes versuchen, da ABT-199 nach einer Verabreichung wohl einer aufwändigen Kontrolle bedarf, um bei TLS möglichst schnell reagieren zu können und es besteht das Risiko, dass Patienten unmittelbar an TLS sterben. Andere Mittel wie Imbruvica haben keine derartigen Risiken. Studien mit ABT-199 wurden aufgrund von TLS bereits angehalten.
Ich bin zwar kein Experte, aber nach dem, was ich dazu gelesen habe, ist eine Strategie zur Reduzierung des TLS-Risikos eine variable Dosierung, bei der man zuerst eine niedrige Dosis gibt, damit nicht zu viele Krebszellen absterben und dann die Dosis langsam zu steigern. Alternativ kann man zuvor andere Medikamente geben, die kein TLS-Risiko besitzen, um die Anzahl der Krebszellen so weit zu reduzieren (Debulking), dass ABT-199 kein TLS mehr auslöst. Hierfür könnte meiner Meinung nach Duvelisib sehr sinnvoll sein, da es offensichtlich (vielleicht durch pi3k-gamma) deutlich schneller wirkt als z.B. Zydelig. Die pi3k- oder BTK-Hemmer brauchen immer einige Zeit, um ihre volle Wirkung zu entfalten. Anfangs werden die Tumorzellen aus den Lymphknoten usw. "ausgeschwemmt" und erst mit der Zeit werden diese abgetötet. Daher gibt es oft bei den Studien die Angaben von "nodal response rate" als Angabe, ob Tumorzellen ausgeschwemmt werden und dann erst die übliche PR/CR-Rate. Anfangs gibt es eine nodal response und erst mit der Zeit wandelt sich diese in PR und später CR um. Duvelisib spricht dabei anscheinend deutlich schneller an. ABBV wird daher wohl an der ABT-199 + Duvelisib Kombination interessiert sein.
[URLL]http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3910377/[/URL]
Toward a cure for chronic lymphocytic leukemia: an attack on multiple fronts
...Kill them in the open
Prior to the emergence of BCL2 inhibitors, other approaches had been used to reduce the peripheral CLL cells. For example, rituximab can reduce the peripheral CLL cell count, but responses are transient. Initially, the introduction of BCL2 inhibitors appeared very promising, but grade 4 tumor lysis syndrome (TLS) was observed in a patient receiving navitoclax as part of a Phase I study [13]. The switch to ABT-199 resulted in additional cases of TLS, thereby halting clinical trials. Moving forward, clinical trials will employ a stepwise dose escalation of ABT-199 to slowly reduce the peripheral cell count. A better strategy might be to initially administer an alternative drug such as rituximab to decrease the peripheral tumor load (or ofatumumab in rituximab-refractory patients) and then to administer full dose ABT-199 which may reduce the potential for drug resistance.
Other drugs might also be effectively used to kill peripheral CLL cells. For example, dinaciclib targets CDK9, inhibits global transcription and induces rapid apoptosis in CLL cells [15]. Vinca alkaloids also induce apoptosis in CLL cells ex vivo, and this effect can be enhanced by combination with dinaciclib, perhaps due to inhibition of MCL1 transcription[16]. Hence many strategies, both established and novel, could be effectively used in combination with BCL2 inhibitors.
Get out of town
In the past decade, several B-cell receptor-targeting agents have shown significant efficacy in CLL patients. Of these, the Bruton tyrosine kinase inhibitor ibrutinib and the PI3-kinase delta inhibitor idelalisib have been most extensively studied in both preclinical and clinic settings [17]. Through disruption of cell homing, these inhibitors force CLL cells to leave the protective microenvironment [18]. Alternatively, egress of the CLL cells into the periphery may be promoted via disruption of the chemokine network, for example, by pharmacologically antagonizing the a-chemokine receptor CXCR4 with plerixafor. Once deprived of the microenvironmental stimuli, CLL cells should be more sensitive to rituximab or the BCL2-targeting agents discussed above. These approaches also reduce the size of the lymph nodes which will further reduce the potential for TLS on administration of ABT199 or navitoclax.
...
Interessant ist demnach auch die Gazyva + Duvelisib Kombination die momentan getestet wird, da Gazyva als optimierter CD20-AK ein wirksameres Rituxan sein kann.


Gruß
ipollit
ein weiteres negatives Ereignis diese Woche war der Fehlschlag von Duvelisib in RA. Infolge dessen beendet INFI die Entwicklung von Duvelisib und anderen pki3-delta/gamma-Hemmern wie IPI-443 gegen Autoimmunerkrankungen wie RA oder Asthma. Eigentlich hatte ich gehofft, dass speziell die delta/gamma Kombination in diesem Bereich wirksam ist.
Trotzdem sehe ich Duvelisib unabhängig davon als sehr aussichtsreich gegen Krebs... z.B. gegen iNHL. Ich setze darauf, dass es u.a. in iNHL besser als GILDs pi3k-delta-Hemmer Zydelig oder PCYCs BTK-Hemmer Imbruvica wirkt. Die Partnerschaft mit ABBV ist sehr gut, da ABBVs BCL2-Hemmer ABT-199 ebenfalls ein möglicher starker Konkurrent u.a. zu Imbruvica sein kann. Soweit ich die bisherigen Ergebnisse sehe, hat ABT-199 eine deutlich höhere CR-Rate, dafür aber das Risiko eines Tumor Lysis Syndroms (TLS), welches zu schweren Nebenwirkungen führen kann. TLS tritt wohl dann auf, wenn ABT-199 die Tumorzellen massiv abtötet, was eigentlich erstmal gut ist, da es eine hohe Wirksamkeit belegt. Die große Menge abgetöteter Zellen führt aber zu starken lebensbedrohlichen Immunreaktionen des Körpers, die sich nur schwer kontrollieren lassen. Selbst wenn ABT-199 wirksamer ist, wird man aufgrund des TLS-Risikos zuerst immer etwas anderes versuchen, da ABT-199 nach einer Verabreichung wohl einer aufwändigen Kontrolle bedarf, um bei TLS möglichst schnell reagieren zu können und es besteht das Risiko, dass Patienten unmittelbar an TLS sterben. Andere Mittel wie Imbruvica haben keine derartigen Risiken. Studien mit ABT-199 wurden aufgrund von TLS bereits angehalten.
Ich bin zwar kein Experte, aber nach dem, was ich dazu gelesen habe, ist eine Strategie zur Reduzierung des TLS-Risikos eine variable Dosierung, bei der man zuerst eine niedrige Dosis gibt, damit nicht zu viele Krebszellen absterben und dann die Dosis langsam zu steigern. Alternativ kann man zuvor andere Medikamente geben, die kein TLS-Risiko besitzen, um die Anzahl der Krebszellen so weit zu reduzieren (Debulking), dass ABT-199 kein TLS mehr auslöst. Hierfür könnte meiner Meinung nach Duvelisib sehr sinnvoll sein, da es offensichtlich (vielleicht durch pi3k-gamma) deutlich schneller wirkt als z.B. Zydelig. Die pi3k- oder BTK-Hemmer brauchen immer einige Zeit, um ihre volle Wirkung zu entfalten. Anfangs werden die Tumorzellen aus den Lymphknoten usw. "ausgeschwemmt" und erst mit der Zeit werden diese abgetötet. Daher gibt es oft bei den Studien die Angaben von "nodal response rate" als Angabe, ob Tumorzellen ausgeschwemmt werden und dann erst die übliche PR/CR-Rate. Anfangs gibt es eine nodal response und erst mit der Zeit wandelt sich diese in PR und später CR um. Duvelisib spricht dabei anscheinend deutlich schneller an. ABBV wird daher wohl an der ABT-199 + Duvelisib Kombination interessiert sein.
[URLL]http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3910377/[/URL]
Toward a cure for chronic lymphocytic leukemia: an attack on multiple fronts
...Kill them in the open
Prior to the emergence of BCL2 inhibitors, other approaches had been used to reduce the peripheral CLL cells. For example, rituximab can reduce the peripheral CLL cell count, but responses are transient. Initially, the introduction of BCL2 inhibitors appeared very promising, but grade 4 tumor lysis syndrome (TLS) was observed in a patient receiving navitoclax as part of a Phase I study [13]. The switch to ABT-199 resulted in additional cases of TLS, thereby halting clinical trials. Moving forward, clinical trials will employ a stepwise dose escalation of ABT-199 to slowly reduce the peripheral cell count. A better strategy might be to initially administer an alternative drug such as rituximab to decrease the peripheral tumor load (or ofatumumab in rituximab-refractory patients) and then to administer full dose ABT-199 which may reduce the potential for drug resistance.
Other drugs might also be effectively used to kill peripheral CLL cells. For example, dinaciclib targets CDK9, inhibits global transcription and induces rapid apoptosis in CLL cells [15]. Vinca alkaloids also induce apoptosis in CLL cells ex vivo, and this effect can be enhanced by combination with dinaciclib, perhaps due to inhibition of MCL1 transcription[16]. Hence many strategies, both established and novel, could be effectively used in combination with BCL2 inhibitors.
Get out of town
In the past decade, several B-cell receptor-targeting agents have shown significant efficacy in CLL patients. Of these, the Bruton tyrosine kinase inhibitor ibrutinib and the PI3-kinase delta inhibitor idelalisib have been most extensively studied in both preclinical and clinic settings [17]. Through disruption of cell homing, these inhibitors force CLL cells to leave the protective microenvironment [18]. Alternatively, egress of the CLL cells into the periphery may be promoted via disruption of the chemokine network, for example, by pharmacologically antagonizing the a-chemokine receptor CXCR4 with plerixafor. Once deprived of the microenvironmental stimuli, CLL cells should be more sensitive to rituximab or the BCL2-targeting agents discussed above. These approaches also reduce the size of the lymph nodes which will further reduce the potential for TLS on administration of ABT199 or navitoclax.
...
Interessant ist demnach auch die Gazyva + Duvelisib Kombination die momentan getestet wird, da Gazyva als optimierter CD20-AK ein wirksameres Rituxan sein kann.

Gruß
ipollit
AGEN, INCY
INCY erweitert den IO-Bereich in der Pipeline mit AGENs Programmen, die AGEN vor einiger Zeit durch die Übernahme der deutschen 4-Antibody erworben hat. Dies umfasst neben den etablierten PD1 und CTLA-4 Targets die neuen hemmenden Targets TIM3 und LAG3 sowie die stimulierenden GITR und OX40.
Die Entwicklung von einem eigenen PD1-AK ist eigentlich nicht notwendig, da die Konkurrenz schon uneinholbar vorne liegt, doch erhält man dadurch mehr Flexibiliät und Unabhängigkeit für die Entwicklung von PD1-Kombinationen, da man sonst von Partnern abhängig wäre bzw. sich den PD1-AK für die Studien auch teuer einkaufen müsste.
Bei CLTA-4 wären noch Verbesserungen möglich, da es bisher nur Yervoy am Markt und wenige Kandidaten in der Entwicklung gibt, anders als bei PD-1.
Am weitesten ist man wohl bei GITR... hier sollen gleich zwei Kandidaten in die klinische Entwicklung gehen. Die Konkurrenz ist meine ich noch überschaubar. OX40 ist angeblich auch interessant. Bei TIM3/LAG3 sehe ich eher z.B. TSRO weiter.
GITR und OX40 entwickelt AGEN und INCY gemeinsam... Gewinne werden später geteilt. Für TIM3 und LAG3 erhält AGEN dagegen nur Royalties im Bereich von 5% - 13%.
Bisher wollte AGEN mit allen Kandidaten Ende 2016 in der Klinik sein. Mit GITR könnte es Ende diesen Jahres schon etwas geben.
Zuletzt hatte AGEN mit dem Adjuvant QS-21 Erfolge erzielt. Dieser dient dazu, die Wirkung von Impfungen zu erhöhen. U.a. GSK verwendet QS-21 wohl bei mehreren Vakzinen in der Entwicklung. GSKs Impfung gegen Gürtelrose war zusammen mit OS-21 erfolgreich... ebenfalls eine Malaria-Impfung. AGEN erhält Royalties... aber wohl nur im niedrigen einstelligen Prozent-Bereich.
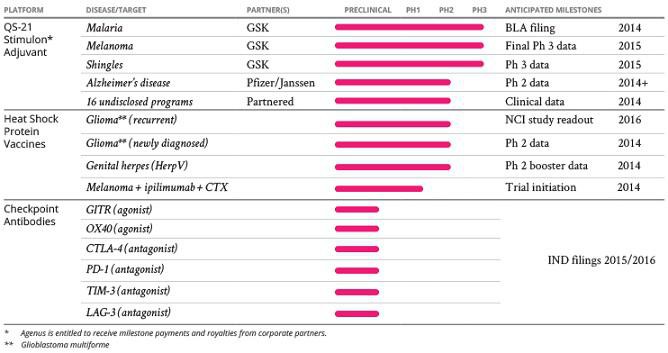
http://www.fiercebiotech.com/story/incyte-agenus-partner-imm…
... In this deal Incyte is paying Lexington, MA-based Agenus $25 million upfront and investing another $35 million in Agenus stock. They plan to split the costs--and profits--on their GITR and OX40 antibody programs, adding milestones for Agenus, while Incyte will cover the costs on TIM-3 and LAG-3 and hand out milestones and royalties on any products. Agenus gets up to $155 million in milestones on each royalty-bearing product and $20 million for the profit-sharing products. ...


Am Montag könnte es weiter nach oben gehen... Jim Cramer hat hier am Freitag noch etwas gepusht.
Gruß
ipollit
INCY erweitert den IO-Bereich in der Pipeline mit AGENs Programmen, die AGEN vor einiger Zeit durch die Übernahme der deutschen 4-Antibody erworben hat. Dies umfasst neben den etablierten PD1 und CTLA-4 Targets die neuen hemmenden Targets TIM3 und LAG3 sowie die stimulierenden GITR und OX40.
Die Entwicklung von einem eigenen PD1-AK ist eigentlich nicht notwendig, da die Konkurrenz schon uneinholbar vorne liegt, doch erhält man dadurch mehr Flexibiliät und Unabhängigkeit für die Entwicklung von PD1-Kombinationen, da man sonst von Partnern abhängig wäre bzw. sich den PD1-AK für die Studien auch teuer einkaufen müsste.
Bei CLTA-4 wären noch Verbesserungen möglich, da es bisher nur Yervoy am Markt und wenige Kandidaten in der Entwicklung gibt, anders als bei PD-1.
Am weitesten ist man wohl bei GITR... hier sollen gleich zwei Kandidaten in die klinische Entwicklung gehen. Die Konkurrenz ist meine ich noch überschaubar. OX40 ist angeblich auch interessant. Bei TIM3/LAG3 sehe ich eher z.B. TSRO weiter.
GITR und OX40 entwickelt AGEN und INCY gemeinsam... Gewinne werden später geteilt. Für TIM3 und LAG3 erhält AGEN dagegen nur Royalties im Bereich von 5% - 13%.
Bisher wollte AGEN mit allen Kandidaten Ende 2016 in der Klinik sein. Mit GITR könnte es Ende diesen Jahres schon etwas geben.
Zuletzt hatte AGEN mit dem Adjuvant QS-21 Erfolge erzielt. Dieser dient dazu, die Wirkung von Impfungen zu erhöhen. U.a. GSK verwendet QS-21 wohl bei mehreren Vakzinen in der Entwicklung. GSKs Impfung gegen Gürtelrose war zusammen mit OS-21 erfolgreich... ebenfalls eine Malaria-Impfung. AGEN erhält Royalties... aber wohl nur im niedrigen einstelligen Prozent-Bereich.

http://www.fiercebiotech.com/story/incyte-agenus-partner-imm…
... In this deal Incyte is paying Lexington, MA-based Agenus $25 million upfront and investing another $35 million in Agenus stock. They plan to split the costs--and profits--on their GITR and OX40 antibody programs, adding milestones for Agenus, while Incyte will cover the costs on TIM-3 and LAG-3 and hand out milestones and royalties on any products. Agenus gets up to $155 million in milestones on each royalty-bearing product and $20 million for the profit-sharing products. ...
Am Montag könnte es weiter nach oben gehen... Jim Cramer hat hier am Freitag noch etwas gepusht.
Gruß
ipollit
STML, KPTI
STML mit einer 60 Mio KE (zu 15,75 USD)... bei einer 200 Mio USD MK schon einiges. Gleichzeitig lizensieren sie aber auch einen XPO1-Hemmer ein, bei dem es dieses Jahr einen IND geben soll...
http://finance.yahoo.com/news/stemline-therapeutics-licenses…
Recent work has demonstrated that XPO1 is a clinically relevant target, and nuclear export inhibitors have emerged as a new approach in cancer treatment with activity in patients across multiple indications. Given that SL-801 is a novel reversible inhibitor of XPO1, we believe it has the potential to offer a broad therapeutic window with dosing and scheduling flexibility. SL-801 has demonstrated preclinical anti-cancer activity, including efficacy and safety in animal models, across a wide array of solid and hematologic cancers. Stemline expects to file an Investigational New Drug (IND) application in 2015.
XPO1 ist auch das Target von KPTIs Selinexor, der meine ich aber nur schwach reversibel ist. Es könnte im Krebs-Bereich eine sehr breite Anwendung haben. KPTI kommt jedenfalls mit der folgenden Pipeline auf eine MK von 1 Mrd USD...
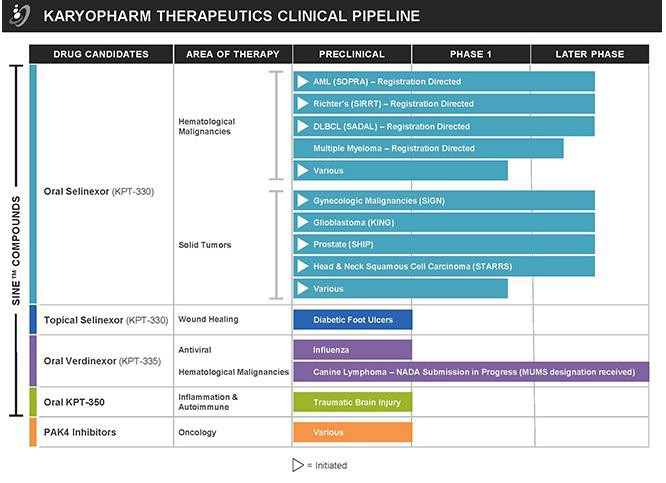
Ohad Hammer sieht die Einlizensierung positiv: "I like this deal very much because the mechanism is validated by KPTI and the drug is very close to IND. This could become a major value driver towards YE2015 if KPTI generates more positive data with their XPO1 inhibitor. The point about a reversible inhibitor having a better therapeutic window is intriguing but needs further validation."




Gruß
ipollit
STML mit einer 60 Mio KE (zu 15,75 USD)... bei einer 200 Mio USD MK schon einiges. Gleichzeitig lizensieren sie aber auch einen XPO1-Hemmer ein, bei dem es dieses Jahr einen IND geben soll...
http://finance.yahoo.com/news/stemline-therapeutics-licenses…
Recent work has demonstrated that XPO1 is a clinically relevant target, and nuclear export inhibitors have emerged as a new approach in cancer treatment with activity in patients across multiple indications. Given that SL-801 is a novel reversible inhibitor of XPO1, we believe it has the potential to offer a broad therapeutic window with dosing and scheduling flexibility. SL-801 has demonstrated preclinical anti-cancer activity, including efficacy and safety in animal models, across a wide array of solid and hematologic cancers. Stemline expects to file an Investigational New Drug (IND) application in 2015.
XPO1 ist auch das Target von KPTIs Selinexor, der meine ich aber nur schwach reversibel ist. Es könnte im Krebs-Bereich eine sehr breite Anwendung haben. KPTI kommt jedenfalls mit der folgenden Pipeline auf eine MK von 1 Mrd USD...

Ohad Hammer sieht die Einlizensierung positiv: "I like this deal very much because the mechanism is validated by KPTI and the drug is very close to IND. This could become a major value driver towards YE2015 if KPTI generates more positive data with their XPO1 inhibitor. The point about a reversible inhibitor having a better therapeutic window is intriguing but needs further validation."


Gruß
ipollit
ein paar IO-Programme in 2015...
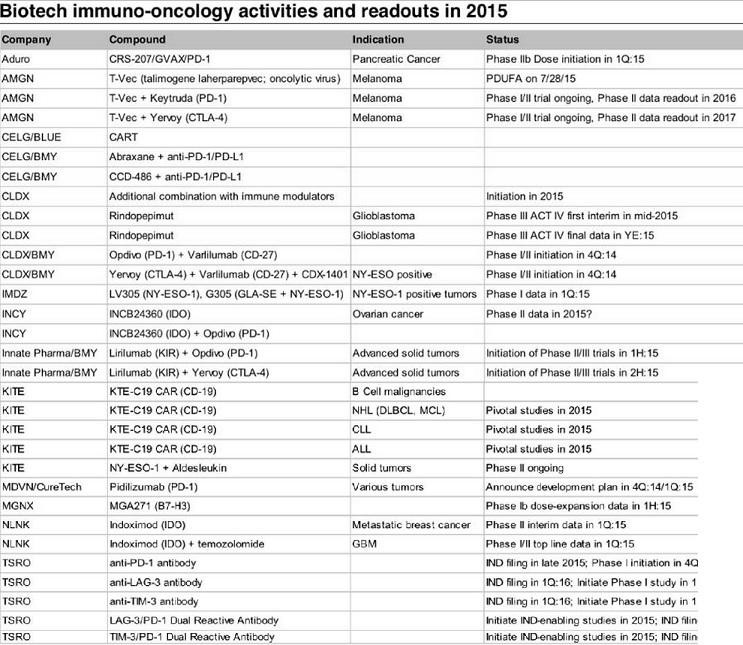
Gruß
ipollit

Gruß
ipollit
IPH.PA
Dieses Jahr müssten einige Daten zum KIR-AK Lirilumab vom Partner BMS kommen... erste Combi-Daten mit PD1 und PII-Mono in AML (EFFIKIR), die theoretisch die Basis für eine vorzeitige Zulassung bilden können.
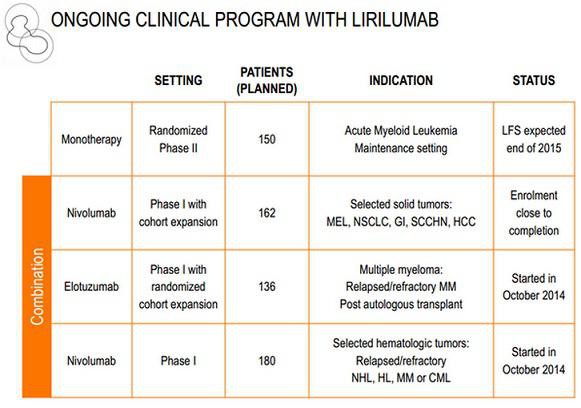
Vielleicht gibt es dieses Jahr auch schon PII-Daten von IPH2201 (NKG2A-AK), obwohl diese Studien erst vor Kurzem oder noch garnicht gestartet sind. Sie laufen zwar bis 2016/2017, aber soweit ich es verstehe sollen auch RR bewertet werden, die früher zur Verfügung stehen und angeblich auch für eine vorzeitige Zulassung verwendet werden können. Mal schauen...

Angeblich soll IPH.PA genauso wie Cellectis (ALCLS.PA) neben Paris ein Zweit-Listing an der Nasdaq anstreben... das wäre ebenfalls sehr positiv.

Gruß
ipollit
Dieses Jahr müssten einige Daten zum KIR-AK Lirilumab vom Partner BMS kommen... erste Combi-Daten mit PD1 und PII-Mono in AML (EFFIKIR), die theoretisch die Basis für eine vorzeitige Zulassung bilden können.

Vielleicht gibt es dieses Jahr auch schon PII-Daten von IPH2201 (NKG2A-AK), obwohl diese Studien erst vor Kurzem oder noch garnicht gestartet sind. Sie laufen zwar bis 2016/2017, aber soweit ich es verstehe sollen auch RR bewertet werden, die früher zur Verfügung stehen und angeblich auch für eine vorzeitige Zulassung verwendet werden können. Mal schauen...

Angeblich soll IPH.PA genauso wie Cellectis (ALCLS.PA) neben Paris ein Zweit-Listing an der Nasdaq anstreben... das wäre ebenfalls sehr positiv.
Gruß
ipollit
NPSP
und wieder eine größere Übernahme... SHPG kauft NPSP für 46 USD bzw. 5,2 Mio USD...zum Start der JPM-Biotech-Konferenz morgen. Während dieser Konferenz gibt es öfters größere Übernahmen.
http://www.fiercebiotech.com/story/shire-nabs-nps-rare-disea…
"Shire nabs NPS's rare disease drug portfolio in $5.2B buyout
The rumors were true. Shire has struck a deal to buy NPS Pharma ($NPSP) and its rare disease drug portfolio for $46 a share, or $5.2 billion, making big headlines for its go-it-alone strategy on the eve of the big JP Morgan conference in San Francisco.
The buyout comes at a hefty premium, beating out the standard markup that usually comes with an acquisition like this. Shire is paying 51% more per share than the December 16 price, as NPS shares started to gyrate upwards after rumors started to proliferate and then Goldman Sachs was brought in to field bids.
Shares of NPS closed at $41.91 on Friday.

Gruß
ipollit
und wieder eine größere Übernahme... SHPG kauft NPSP für 46 USD bzw. 5,2 Mio USD...zum Start der JPM-Biotech-Konferenz morgen. Während dieser Konferenz gibt es öfters größere Übernahmen.
http://www.fiercebiotech.com/story/shire-nabs-nps-rare-disea…
"Shire nabs NPS's rare disease drug portfolio in $5.2B buyout
The rumors were true. Shire has struck a deal to buy NPS Pharma ($NPSP) and its rare disease drug portfolio for $46 a share, or $5.2 billion, making big headlines for its go-it-alone strategy on the eve of the big JP Morgan conference in San Francisco.
The buyout comes at a hefty premium, beating out the standard markup that usually comes with an acquisition like this. Shire is paying 51% more per share than the December 16 price, as NPS shares started to gyrate upwards after rumors started to proliferate and then Goldman Sachs was brought in to field bids.
Shares of NPS closed at $41.91 on Friday.
Gruß
ipollit
MDVN
morgen sollte MDVN auch bekannt geben, was sie mit dem PD1-AK von Curetech vorhaben.
Hier ein paar Unternehmen, die in den nächsten Tagen ihr Unternehmen auf der JPM-Konferenz präsentieren...

Gruß
ipollit
morgen sollte MDVN auch bekannt geben, was sie mit dem PD1-AK von Curetech vorhaben.
Hier ein paar Unternehmen, die in den nächsten Tagen ihr Unternehmen auf der JPM-Konferenz präsentieren...

Gruß
ipollit
FMI
und noch ein großer Deal zur JPM-Konferenz... Roche kauft für 1 Mrd mehr als 50% von FMI zum Kurs von 50 USD. Also keine komplette Übernahme... dafür dürfte der Kurs heute mehr als 100% im Plus liegen, wenn ich es richtig sehe. Nicht schlecht!

Gruß
ipollit
und noch ein großer Deal zur JPM-Konferenz... Roche kauft für 1 Mrd mehr als 50% von FMI zum Kurs von 50 USD. Also keine komplette Übernahme... dafür dürfte der Kurs heute mehr als 100% im Plus liegen, wenn ich es richtig sehe. Nicht schlecht!
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.750.011 von ipollit am 12.01.15 09:04:08Wow! Was für ein großartiger Deal. Damit bleibt/wird FMI langfristig extrem aussichtsreich.
Ohad Hammer hat es so ähnlich ja vorausgesehen, schreibt auch gleich was dazu:
http://www.orf-blog.com/roche-acquires-majority-stake-in-fou…
Ohad Hammer hat es so ähnlich ja vorausgesehen, schreibt auch gleich was dazu:
http://www.orf-blog.com/roche-acquires-majority-stake-in-fou…
Die aktuelle Meldung sollte Seattle Genetics börslich ordentlich Auftrieb verleihen. SGEN und BMY kooperieren, statt zu konkurrieren.
Seattle Genetics, Inc. (SGEN) and Bristol-Myers Squibb Co. (BMY) Monday said they have entered into a clinical trial collaboration agreement to evaluate the investigational combination of Seattle Genetics' antibody-drug conjugate, or ADC, Adcetris (brentuximab vedotin) and Bristol-Myers Squibb's immunotherapy Opdivo (nivolumab) in two planned Phase 1/2 clinical trials. The first trial will evaluate the combination of Adcetris and Opdivo as a potential treatment option for patients with relapsed or refractory Hodgkin lymphoma or HL, and the second trial will focus on patients with relapsed or refractory B-cell and T-cell non-Hodgkin lymphomas, including diffuse large B-cell lymphoma. Adcetris is an ADC directed to CD30, a defining marker of classical HL, which combines the targeting ability of a monoclonal antibody with the potency of a cell-killing agent. Opdivo is a human programmed death receptor-1 blocking antibody that binds to the PD-1 receptor expressed on activated T-cells. The studies are expected to begin in 2015, with Seattle Genetics conducting the HL trial and Bristol-Myers Squibb conducting the NHL trial. Adcetris is approved in relapsed HL and systemic anaplastic large cell lymphoma, but is not currently approved for the treatment of relapsed, transplant eligible HL or for the treatment of other types of NHL. Opdivo is currently not approved for the treatment of lymphoma.
Seattle Genetics, Inc. (SGEN) and Bristol-Myers Squibb Co. (BMY) Monday said they have entered into a clinical trial collaboration agreement to evaluate the investigational combination of Seattle Genetics' antibody-drug conjugate, or ADC, Adcetris (brentuximab vedotin) and Bristol-Myers Squibb's immunotherapy Opdivo (nivolumab) in two planned Phase 1/2 clinical trials. The first trial will evaluate the combination of Adcetris and Opdivo as a potential treatment option for patients with relapsed or refractory Hodgkin lymphoma or HL, and the second trial will focus on patients with relapsed or refractory B-cell and T-cell non-Hodgkin lymphomas, including diffuse large B-cell lymphoma. Adcetris is an ADC directed to CD30, a defining marker of classical HL, which combines the targeting ability of a monoclonal antibody with the potency of a cell-killing agent. Opdivo is a human programmed death receptor-1 blocking antibody that binds to the PD-1 receptor expressed on activated T-cells. The studies are expected to begin in 2015, with Seattle Genetics conducting the HL trial and Bristol-Myers Squibb conducting the NHL trial. Adcetris is approved in relapsed HL and systemic anaplastic large cell lymphoma, but is not currently approved for the treatment of relapsed, transplant eligible HL or for the treatment of other types of NHL. Opdivo is currently not approved for the treatment of lymphoma.
Antwort auf Beitrag Nr.: 48.747.812 von ipollit am 11.01.15 18:10:01hier sind die Präsentationen und Webcasts von der JPM-Biotech-Konferenz... teilweise sind sie recht spät (Zeitdifferenz zu hier sind 9 Stunden):
http://jpmorgan.metameetings.com/confbook/healthcare15/agend…
PCYC mit weiter guten Imbruvica-Zahlen... 2015 werden etwas mehr als 1 Mrd USD Umsatz erwartet.
Gruß
ipollit
http://jpmorgan.metameetings.com/confbook/healthcare15/agend…
PCYC mit weiter guten Imbruvica-Zahlen... 2015 werden etwas mehr als 1 Mrd USD Umsatz erwartet.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.747.509 von ipollit am 11.01.15 17:05:06habe heute mal eine Anfangsposition KPTI gekauft. EPZM könnte ich mir auch vorstellen... mal schauen.
Gruß
ipollit
Gruß
ipollit
PCYC
PCYC ist sehr zufrieden mit der Zusammenarbeit mit JNJ. Imbruvica wird sehr breit entwickelt, PCYC wäre alleine dazu wahrscheinlich nicht in der Lage gewesen. Bis heute wurden mehr als 5000 Patienten in den klinischen Studien behandelt... bei Kosten von 50T bis 100T pro Patienten, ist das auch finanziell eine Menge.
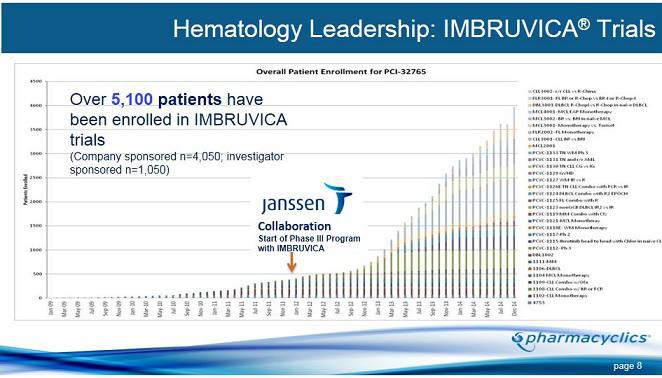
Imbruvica entwickelt sich bisher sehr gut. Zuletzt hatten Analysten eine Plateau-Bildung befürchtet... nach den aktuellen Zahlen ist davon nichts zu sehen. Momentan ist es das umsatzstärkste Mittel gegen Blutkrebs nach 5Q ab Markteinführung in den USA, fast auf dem Niveau von Avastin. Angeblich soll der CEO prognostiziert haben, dass Imbruvica erfolgreicher als CELGs Revlimid wird. Revlimid soll dieses Jahr fast 6 Mrd USD bringen und ist der Hauptgrund dafür, dass CELG heute eine MK von fast 100 Mrd USD hat.
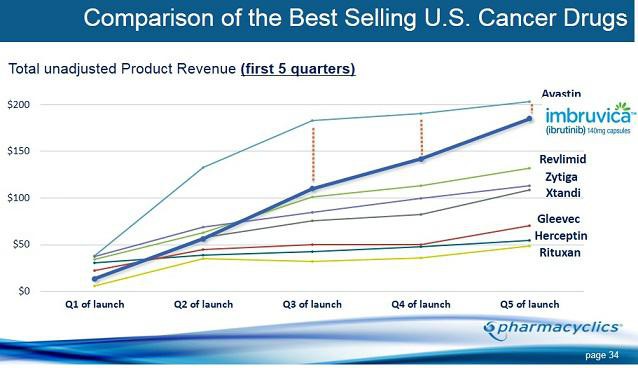
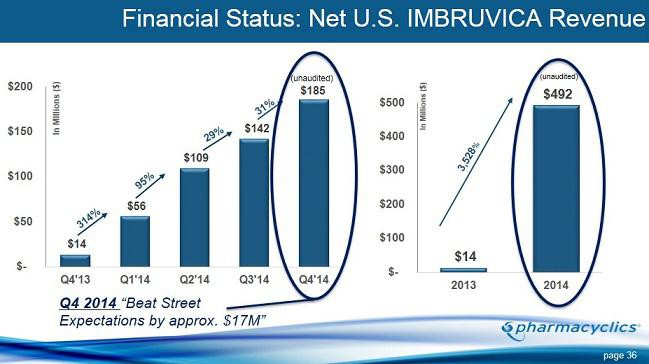
Nächstes Jahr soll Imbruvica alleine in den USA 1 Mrd USD erzielen. JNJ und PCYC teilen sich die weltweiten Gewinne, PCYC verbucht den US-Umsatz.

Wenn ich es richtig sehe, ist dies im Wesentlichen auf der Basis von den beiden bisher zugelassenen Indikationen RR CLL & RR MCL. Offlabel-Anwendung soll bei 10% liegen.
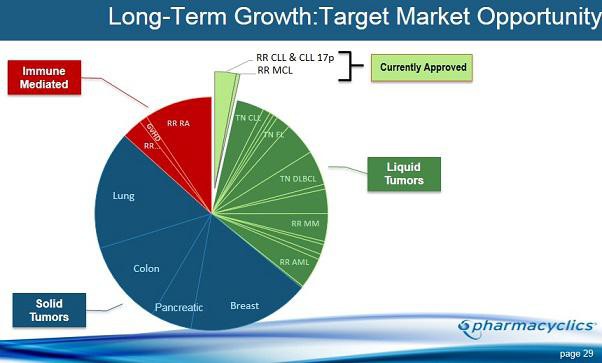
Neben Blutkrebs-Arten könnte Imbruvica auch gegen solide Tumore wie Lungenkrebs wirken. Eine Wirkkomponente ist mit ITK im Bereich IO. In Tierversuchen ist PD1 + Imbruvica deutlich synergetisch:
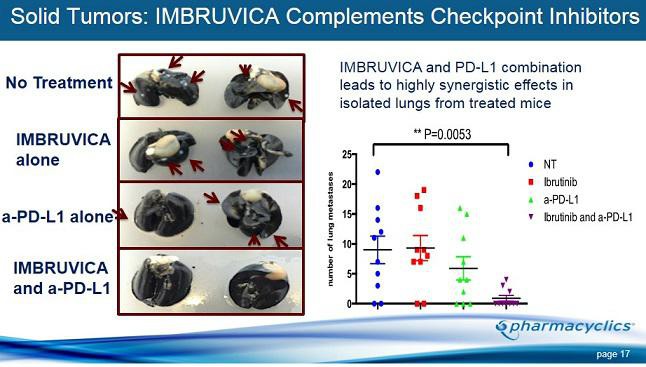
Da Imbruvica auf das Immunsystem (TH1/TH2-Verhältnis) wirkt, scheint es auch bei Abstoßungs-Reaktionen (GVHD) z.B. nach einer Knochenmarks-Spende zu helfen. Mehrere CLL-Patienten sollen das folgende Verhalten gezeigt haben, dass Abstoßungsreaktionen mit Imbruvica anhaltend verschwunden sind.
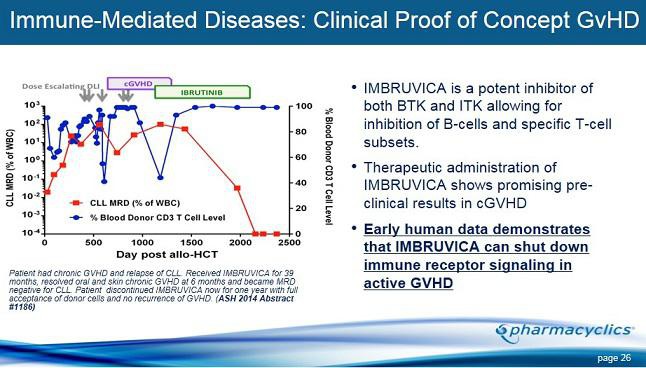
Schon ein etwas älterer Artikel...
http://www.nature.com/bmt/journal/v28/n2/full/1703111a.html
"Chronic graft-versus-host disease (GVHD) is a major cause of morbidity and mortality in long-term survivors of allogeneic stem cell transplantation. The immunopathogenesis of chronic GVHD is, in part, TH-2 mediated, resulting in a syndrome of immunodeficiency and an autoimmune disorder...Chronic graft-versus-host disease (GVHD) occurs in approximately 60-80% of long-term survivors of allogeneic hematopoietic cell transplant (HCT)...In conclusion, chronic GVHD remains one of the most important challenges in allogeneic transplantation...."
Gruß
ipollit
PCYC ist sehr zufrieden mit der Zusammenarbeit mit JNJ. Imbruvica wird sehr breit entwickelt, PCYC wäre alleine dazu wahrscheinlich nicht in der Lage gewesen. Bis heute wurden mehr als 5000 Patienten in den klinischen Studien behandelt... bei Kosten von 50T bis 100T pro Patienten, ist das auch finanziell eine Menge.

Imbruvica entwickelt sich bisher sehr gut. Zuletzt hatten Analysten eine Plateau-Bildung befürchtet... nach den aktuellen Zahlen ist davon nichts zu sehen. Momentan ist es das umsatzstärkste Mittel gegen Blutkrebs nach 5Q ab Markteinführung in den USA, fast auf dem Niveau von Avastin. Angeblich soll der CEO prognostiziert haben, dass Imbruvica erfolgreicher als CELGs Revlimid wird. Revlimid soll dieses Jahr fast 6 Mrd USD bringen und ist der Hauptgrund dafür, dass CELG heute eine MK von fast 100 Mrd USD hat.


Nächstes Jahr soll Imbruvica alleine in den USA 1 Mrd USD erzielen. JNJ und PCYC teilen sich die weltweiten Gewinne, PCYC verbucht den US-Umsatz.

Wenn ich es richtig sehe, ist dies im Wesentlichen auf der Basis von den beiden bisher zugelassenen Indikationen RR CLL & RR MCL. Offlabel-Anwendung soll bei 10% liegen.

Neben Blutkrebs-Arten könnte Imbruvica auch gegen solide Tumore wie Lungenkrebs wirken. Eine Wirkkomponente ist mit ITK im Bereich IO. In Tierversuchen ist PD1 + Imbruvica deutlich synergetisch:

Da Imbruvica auf das Immunsystem (TH1/TH2-Verhältnis) wirkt, scheint es auch bei Abstoßungs-Reaktionen (GVHD) z.B. nach einer Knochenmarks-Spende zu helfen. Mehrere CLL-Patienten sollen das folgende Verhalten gezeigt haben, dass Abstoßungsreaktionen mit Imbruvica anhaltend verschwunden sind.

Schon ein etwas älterer Artikel...
http://www.nature.com/bmt/journal/v28/n2/full/1703111a.html
"Chronic graft-versus-host disease (GVHD) is a major cause of morbidity and mortality in long-term survivors of allogeneic stem cell transplantation. The immunopathogenesis of chronic GVHD is, in part, TH-2 mediated, resulting in a syndrome of immunodeficiency and an autoimmune disorder...Chronic graft-versus-host disease (GVHD) occurs in approximately 60-80% of long-term survivors of allogeneic hematopoietic cell transplant (HCT)...In conclusion, chronic GVHD remains one of the most important challenges in allogeneic transplantation...."
Gruß
ipollit
Die JPMorgan Konferenz haben viele Firmen genzutzt, um einen Ausblick auf 2015 zu gegeben. Zwecks rascher Übersicht habe ich das mal für mein Depot zusammengetragen (ohne Gewähr und sicherlich unvollständig). Grundlage waren zudem Ohad Hammers Ausblick sowie Analystenkommentare.
Habe mich zudem von einem Teil FMI getrennt (Position war mir zu groß) und habe dafür eine Position AERI gekauft.
CLVS: MK: 2,3 Mil - Cash 500 Mio
Q2: ASCO mit Updates zu Roci und Ruca (auch AZ9291)
M: ROCI P II und NDA Filing
Q4: Zulassung Roci
Dezember: PII Ergebnisse Lucitanib
2016 will Clovis die Zulassung von Ruca beantragen (accelerated approval bei singlearm)
ARRY: MK: 600 Mio - Cash ca. 100 Mio

2015: 2 mal PIII (Q4), zudem Rückgabe Bini und Entscheidungen wie/mit welchen Kombinationen es weiter geht
2016: 4 mal PIII Ergebnisse!
ESPR: MK: 700 Mio - Cash ca. 140 Mio
März: Endgültige Ergebnisse der Studie 008 (1002 +/vs. Ezetimibe), PII Ergebnisse 009Studie (1002 + Statin wenn LDL-C Ziel nicht erreicht)
Q2: FDA Entscheidet über Aufhebung des partial clinical hold
Q2: Ergebnisse 014Studie: PII mit Schwerpunkt auf Patienten mit Bluthochdruck
Q3: Zulassung der PCSK9-I. von Amgen bzw. Sanofi (Preis?-diskussion)
Q4: Gespräche FDA und Entscheidung über PIII
PIII Ergebnisse dann 2017
ZFGN: MK: 830 Mio - Cash ca. 120 Mio
Q4: PII Beloranib bei schwerer Adipositas (und Diabetis) -- Ziel könnte hier sein, B. so zu entwickeln, dass B. eine Operation (Magenband) ermöglicht.
Q4: PIII Zwischenergebnisse nach 6 Monaten in PWS (zulassungsrelevant)
Zudem in 2015 IND ZGN839 (NASH) und 2nd generation B. (general Obesity)
2016 ggf. Zulassung in PWS sowie PIII endgültige Ergebnisse zudem ggf. PIII Entscheidungen severe obesity und HIAO
FMI: MK: 1,35 Mil Cash ca. 120 Mio wobei ? nach Rochedeal und letztlich wohl irrelevant
Q1,2,3,4: Verkaufszahlen der Tests
zudem alles zu Ruca von CLVS sowie Agios AG221 u. AG120
Viele ??? z.B. Konkurrenz, weitere Deals, Übernahme der Kosten?
ONTY: MK 150 Mio - Cash ca. 65 Mio
Q2: ASCO Update zur Kombination 380 mit Kadcyla bzw. Herceptin
Q4?: Entscheidung über PII (Herceptin?)
zudem von Interesse Ergebnisse der zahlreichen Kombinationsstudien von PBYIs Neratinib (Nebenwirkungen!)
ARQL: MK: 72 Mio - Cash ca. 60 Mio
Oktober: PI ARQ092 Protheus Syndrome
November: PI ARQ092 zahlreiche Krebsarten (selected population)
YE: interim PIII Tivantib in HCC
zudem Ergebnisse anderer AKT Programme von Roche und AZ z.B. GDC0068 in 2H
ENTA: MK: 930 Mio - Cash ca. 280 Mio

Q1,2,3,4: Ergebnisse ENTA und ABBVIE, Verkaufszahlen
Was macht ENTA mit dem Geld?
GILD: MK: 150 Mil - Cash ca. 8 Mil?

Q1,2,3,4: Verkaufszahlen Harvoni
Was macht GILD mit dem Geld?
AMBI CVR:
Q4?: Interim Quizartinib PIII
ACAD: MK: 3,2 Mil - Cash ca. 310 Mio
Q1: NDA Prima in Psychose bei Parkinson
M: Zulassung?
Q3/4: Antrag EU
YE: Prima bei Psychose bei Alzheimer (Hier wird neben dem Rückgag der Halluzinationen auch der Einfluss auf die Kognitionen (Lotterieticket) überprüft!!)
AERI: MK: 700 Mio - Cash ca. 160 Mio
Q2: erste PIII Rhopressa Daten
M: weitere PIII Daten Rh, Start Roclatan PIII
2016 (Q2/3?) Rhopressa Sicherheitsdaten PIII
M16: Roclatan erste PIII Ergebnisse, Rhopressa Zulassungsantrag
2H17: Rh Vermarktungsstart, Zulassungsantrag Ro
Medigene: MK: 55 Mio EUR - Cash ca 16 Mio?
Lauter ???
Verkaufszahlen Veregen Q1,2,3,4
Startet Syncore dann doch mal die PIII von Endotag bei TNBreastcancer?
Geht die Entwicklung von Rhudex (PII bei Primär biliäre Zirrhose) weiter?
Börsengänge Immunocore und/oder Adaptimmune? (Ist Medigene zumindest mittelbar am Erfolg von A. über I. beteiligt?)
Wie geht es mit den 3 IO-Plattformen weiter? Partner?
Wie geht es mit den durch andere finanzierten und durchgeführten Studien weiter?
SG kmastra
Habe mich zudem von einem Teil FMI getrennt (Position war mir zu groß) und habe dafür eine Position AERI gekauft.
CLVS: MK: 2,3 Mil - Cash 500 Mio
Q2: ASCO mit Updates zu Roci und Ruca (auch AZ9291)
M: ROCI P II und NDA Filing
Q4: Zulassung Roci
Dezember: PII Ergebnisse Lucitanib
2016 will Clovis die Zulassung von Ruca beantragen (accelerated approval bei singlearm)
ARRY: MK: 600 Mio - Cash ca. 100 Mio

2015: 2 mal PIII (Q4), zudem Rückgabe Bini und Entscheidungen wie/mit welchen Kombinationen es weiter geht
2016: 4 mal PIII Ergebnisse!
ESPR: MK: 700 Mio - Cash ca. 140 Mio
März: Endgültige Ergebnisse der Studie 008 (1002 +/vs. Ezetimibe), PII Ergebnisse 009Studie (1002 + Statin wenn LDL-C Ziel nicht erreicht)
Q2: FDA Entscheidet über Aufhebung des partial clinical hold
Q2: Ergebnisse 014Studie: PII mit Schwerpunkt auf Patienten mit Bluthochdruck
Q3: Zulassung der PCSK9-I. von Amgen bzw. Sanofi (Preis?-diskussion)
Q4: Gespräche FDA und Entscheidung über PIII
PIII Ergebnisse dann 2017
ZFGN: MK: 830 Mio - Cash ca. 120 Mio
Q4: PII Beloranib bei schwerer Adipositas (und Diabetis) -- Ziel könnte hier sein, B. so zu entwickeln, dass B. eine Operation (Magenband) ermöglicht.
Q4: PIII Zwischenergebnisse nach 6 Monaten in PWS (zulassungsrelevant)
Zudem in 2015 IND ZGN839 (NASH) und 2nd generation B. (general Obesity)
2016 ggf. Zulassung in PWS sowie PIII endgültige Ergebnisse zudem ggf. PIII Entscheidungen severe obesity und HIAO
FMI: MK: 1,35 Mil Cash ca. 120 Mio wobei ? nach Rochedeal und letztlich wohl irrelevant
Q1,2,3,4: Verkaufszahlen der Tests
zudem alles zu Ruca von CLVS sowie Agios AG221 u. AG120
Viele ??? z.B. Konkurrenz, weitere Deals, Übernahme der Kosten?
ONTY: MK 150 Mio - Cash ca. 65 Mio
Q2: ASCO Update zur Kombination 380 mit Kadcyla bzw. Herceptin
Q4?: Entscheidung über PII (Herceptin?)
zudem von Interesse Ergebnisse der zahlreichen Kombinationsstudien von PBYIs Neratinib (Nebenwirkungen!)
ARQL: MK: 72 Mio - Cash ca. 60 Mio
Oktober: PI ARQ092 Protheus Syndrome
November: PI ARQ092 zahlreiche Krebsarten (selected population)
YE: interim PIII Tivantib in HCC
zudem Ergebnisse anderer AKT Programme von Roche und AZ z.B. GDC0068 in 2H
ENTA: MK: 930 Mio - Cash ca. 280 Mio

Q1,2,3,4: Ergebnisse ENTA und ABBVIE, Verkaufszahlen
Was macht ENTA mit dem Geld?
GILD: MK: 150 Mil - Cash ca. 8 Mil?

Q1,2,3,4: Verkaufszahlen Harvoni
Was macht GILD mit dem Geld?
AMBI CVR:
Q4?: Interim Quizartinib PIII
ACAD: MK: 3,2 Mil - Cash ca. 310 Mio
Q1: NDA Prima in Psychose bei Parkinson
M: Zulassung?
Q3/4: Antrag EU
YE: Prima bei Psychose bei Alzheimer (Hier wird neben dem Rückgag der Halluzinationen auch der Einfluss auf die Kognitionen (Lotterieticket) überprüft!!)
AERI: MK: 700 Mio - Cash ca. 160 Mio
Q2: erste PIII Rhopressa Daten
M: weitere PIII Daten Rh, Start Roclatan PIII
2016 (Q2/3?) Rhopressa Sicherheitsdaten PIII
M16: Roclatan erste PIII Ergebnisse, Rhopressa Zulassungsantrag
2H17: Rh Vermarktungsstart, Zulassungsantrag Ro
Medigene: MK: 55 Mio EUR - Cash ca 16 Mio?
Lauter ???
Verkaufszahlen Veregen Q1,2,3,4
Startet Syncore dann doch mal die PIII von Endotag bei TNBreastcancer?
Geht die Entwicklung von Rhudex (PII bei Primär biliäre Zirrhose) weiter?
Börsengänge Immunocore und/oder Adaptimmune? (Ist Medigene zumindest mittelbar am Erfolg von A. über I. beteiligt?)
Wie geht es mit den 3 IO-Plattformen weiter? Partner?
Wie geht es mit den durch andere finanzierten und durchgeführten Studien weiter?
SG kmastra
Antwort auf Beitrag Nr.: 48.806.516 von kmastra am 17.01.15 13:07:09Hallo kmastra,
danke für die Infos!... war bestimmt einiges an Arbeit.
Grüße
ipollit
danke für die Infos!... war bestimmt einiges an Arbeit.
Grüße
ipollit
ENTA
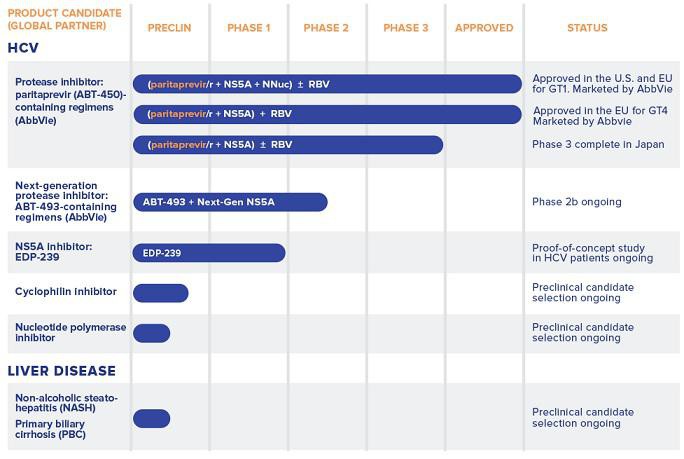
JPM Q&A-Session... http://jpmorgan.metameetings.com/confbook/healthcare15/compa…
Nach meinem Verständnis wurde Folgendes gesagt:
ABT-450 (ENTAs Protease Hemmer als eins von drei Mitteln im kürzlich zugelassenen Viekira Pak):
- bisher gibt es keine Zahlen oder Prognosen zu Umsätzen
- Royalties für ABT-450 sind gestaffelt zwischen "low double digit" und "20%" der weltweiten Net-Sales, wobei der ABT-450 Anteil bei Viekira Pak 30% beträgt
Royalties erhöhen sich bei den nächsten Kombinationen mit ABT-450 oder ABT-493... der Umsatz-Anteil für ABT-450 bzw. ABT-493, auf den die oben genannten Royalties zwischen 10% bis 20% entfallen, ist wie folgt:
- ABT-450 Kombi mit 3 Mitteln (Viekira Pak): 30%
- ABT-450 Kombi mit 2 Mitteln: 45%
- ABT-493 Kombi mit 2 Mitteln: 50%
d.h. es müsste folgende Matrix herauskommen:
/// # 10% | 15% | 20% (Royalties auf Anteil)
####+######+######+######
30% # 3,0% | 4,5% | 6,0% (ABT-450 3Kombi)
45% # 4,5% | 6,8% | 9,0% (ABT-450 2Kombi)
50% # 5,0% | 7,5% | 10,0% (ABT-493 2Kombi)
Bei 3,5 Mrd USD WW Umsatz, die wohl mindestens erreichbar sein sollten, vieleicht schon in diesem Jahr, wären das in Mio USD:
/// # 10% | 15% | 20%
####+#####+#####+#######
30% # 105 # 157 # 210
45% # 157 # 236 # 315
50% # 175 # 262 # 350
ENTA steckt diesen Cash-Flow u.a. in die eigene Pipeline, die aus zwei Teilen besteht: HCV und Leber-Erkrankungen (HCV führt auch zu weiteren Lebererkrankungen wie chronische Leberentzündung).
HCV-Pipeline:
- ENTA besitzt die vollen Rechte
- NS5A Hemmer EPD-239, der von NVS an ENTA zurückgegeben wurde, nachdem sie komplett aus der HCV-Entwicklung ausgestiegen sind: ENTA erhält von NVS bisherige Daten, die ENTA dann für die weitere Entwicklung beurteilen muss
- Cyclophilin Hemmer und NUC: beide befinden sich noch in der Lead-Optimierungs-Phase. Sobald der Entwicklungskandidat(Lead) gefunden ist, dauert es noch 9-12 Monate bis zur P1... also P1 2016, wenn Lead noch dieses Jahr
- NUC-Entwicklung soll insbesondere wegen der Patentlage "sehr schwierig" sein
- Cyclophilin hat bisher wohl nur Debiopharm in der Pipeline, die es vor kurzem ebenfalls von NVS zurückerhalten haben (NVS wollte wohl ENTAs NS5a + Debiopharms Cyclophilin Kombi)
- mögliche zukünftige Kombis (für die ENTA bisher die alleinigen Rechte besitzt) sollen sein: NS5a + NUC, NS5a + Cyclo, Cyclo + NUC
- interessanteste Kombi ist Cyclo + NUC, da beide Komponenten die höchste Barriere gegen Resistenzen haben. Wenn in Zukunft HCV-Viren durch die aktuellen Kombis mit der Zeit resistent werden (wie bei Antibiotika), müssen solche Kombis zur Anwendung kommen. ENTA sollen bisher die einzigen sein, die beides in der Pipeline haben... in der Praxis wurde diese Kombi noch nie getestet.
Leber-Erkrankungen:
- FXR-Hemmer u.a. gegen NASH wie OCA von ICPT oder das Mittel von Phenex, das GILD vor Kurzen für 470 Mio USD gekauft hat http://www.fiercebiotech.com/story/gilead-buys-its-way-block…
- Lead-Optimierungsphase wie präklinische HCS-Kandidaten... also PI 2016 oder 2017.
- Markt soll auch so groß wie der HCV-Markt sein (>10 Mrd USD)
http://www.fiercebiotech.com/story/enanta-plots-future-nash-…
"Enanta bills its move into NASH as a natural outgrowth of its core competency in hep C. The liver disease leads to fibrosis, cirrhosis and hepatic failure--all hallmarks of the virus Enanta has spent the last 10 years dissecting and attacking. "It's the same pathophysiology as HCV," Luly said. "It just happens to be caused by a fatty liver instead of a virus."


Gruß
ipollit

JPM Q&A-Session... http://jpmorgan.metameetings.com/confbook/healthcare15/compa…
Nach meinem Verständnis wurde Folgendes gesagt:
ABT-450 (ENTAs Protease Hemmer als eins von drei Mitteln im kürzlich zugelassenen Viekira Pak):
- bisher gibt es keine Zahlen oder Prognosen zu Umsätzen
- Royalties für ABT-450 sind gestaffelt zwischen "low double digit" und "20%" der weltweiten Net-Sales, wobei der ABT-450 Anteil bei Viekira Pak 30% beträgt
Royalties erhöhen sich bei den nächsten Kombinationen mit ABT-450 oder ABT-493... der Umsatz-Anteil für ABT-450 bzw. ABT-493, auf den die oben genannten Royalties zwischen 10% bis 20% entfallen, ist wie folgt:
- ABT-450 Kombi mit 3 Mitteln (Viekira Pak): 30%
- ABT-450 Kombi mit 2 Mitteln: 45%
- ABT-493 Kombi mit 2 Mitteln: 50%
d.h. es müsste folgende Matrix herauskommen:
/// # 10% | 15% | 20% (Royalties auf Anteil)
####+######+######+######
30% # 3,0% | 4,5% | 6,0% (ABT-450 3Kombi)
45% # 4,5% | 6,8% | 9,0% (ABT-450 2Kombi)
50% # 5,0% | 7,5% | 10,0% (ABT-493 2Kombi)
Bei 3,5 Mrd USD WW Umsatz, die wohl mindestens erreichbar sein sollten, vieleicht schon in diesem Jahr, wären das in Mio USD:
/// # 10% | 15% | 20%
####+#####+#####+#######
30% # 105 # 157 # 210
45% # 157 # 236 # 315
50% # 175 # 262 # 350
ENTA steckt diesen Cash-Flow u.a. in die eigene Pipeline, die aus zwei Teilen besteht: HCV und Leber-Erkrankungen (HCV führt auch zu weiteren Lebererkrankungen wie chronische Leberentzündung).
HCV-Pipeline:
- ENTA besitzt die vollen Rechte
- NS5A Hemmer EPD-239, der von NVS an ENTA zurückgegeben wurde, nachdem sie komplett aus der HCV-Entwicklung ausgestiegen sind: ENTA erhält von NVS bisherige Daten, die ENTA dann für die weitere Entwicklung beurteilen muss
- Cyclophilin Hemmer und NUC: beide befinden sich noch in der Lead-Optimierungs-Phase. Sobald der Entwicklungskandidat(Lead) gefunden ist, dauert es noch 9-12 Monate bis zur P1... also P1 2016, wenn Lead noch dieses Jahr
- NUC-Entwicklung soll insbesondere wegen der Patentlage "sehr schwierig" sein
- Cyclophilin hat bisher wohl nur Debiopharm in der Pipeline, die es vor kurzem ebenfalls von NVS zurückerhalten haben (NVS wollte wohl ENTAs NS5a + Debiopharms Cyclophilin Kombi)
- mögliche zukünftige Kombis (für die ENTA bisher die alleinigen Rechte besitzt) sollen sein: NS5a + NUC, NS5a + Cyclo, Cyclo + NUC
- interessanteste Kombi ist Cyclo + NUC, da beide Komponenten die höchste Barriere gegen Resistenzen haben. Wenn in Zukunft HCV-Viren durch die aktuellen Kombis mit der Zeit resistent werden (wie bei Antibiotika), müssen solche Kombis zur Anwendung kommen. ENTA sollen bisher die einzigen sein, die beides in der Pipeline haben... in der Praxis wurde diese Kombi noch nie getestet.
Leber-Erkrankungen:
- FXR-Hemmer u.a. gegen NASH wie OCA von ICPT oder das Mittel von Phenex, das GILD vor Kurzen für 470 Mio USD gekauft hat http://www.fiercebiotech.com/story/gilead-buys-its-way-block…
- Lead-Optimierungsphase wie präklinische HCS-Kandidaten... also PI 2016 oder 2017.
- Markt soll auch so groß wie der HCV-Markt sein (>10 Mrd USD)
http://www.fiercebiotech.com/story/enanta-plots-future-nash-…
"Enanta bills its move into NASH as a natural outgrowth of its core competency in hep C. The liver disease leads to fibrosis, cirrhosis and hepatic failure--all hallmarks of the virus Enanta has spent the last 10 years dissecting and attacking. "It's the same pathophysiology as HCV," Luly said. "It just happens to be caused by a fatty liver instead of a virus."

Gruß
ipollit
AERI
Erste PIII-Ergebnisse von Rhopressa sollen nun in Q2 kommen. Dass die Studie schneller alle Patienten aufnehmen konnte, ist meiner Meinung nach ein Hinweis, dass Bedarf an neuen Mitteln besteht und Rhopressa als eine aussichtsreiche Option gesehen wird.
http://www.bizjournals.com/triangle/news/2015/01/12/rtp-duke…
"... Aerie (Nasdaq: AERI) says it is ahead of schedule in a 400-patient Phase 3 registration trial of Rhopressa, Aerie's developmental eye drop is being tested for its ability to lower intraocular pressure (IOP) in patients with glaucoma or ocular hypertension. Specifically, Aerie's drug is being tested against the prescription drug timolol, sold under brand names including Betimol and Timoptic. Timolol is the most widely used comparator in registration trials for lowering of IOP. ... "As a result of Rocket 1 enrollment having been completed well ahead of schedule and after thorough review we are accelerating the expected timeline for the reporting of efficacy results from this Rhopressa Phase 3 registration trial," said Vicente Anido, Aerie CEO. "We originally planned to release the efficacy results of both Rocket 1 and Rocket 2 in mid-2015, and now expect to report efficacy results for Rocket 1 in the middle of second-quarter 2015, with Rocket 2 still on schedule for a mid-2015 efficacy read-out."...

Gruß
ipollit
Erste PIII-Ergebnisse von Rhopressa sollen nun in Q2 kommen. Dass die Studie schneller alle Patienten aufnehmen konnte, ist meiner Meinung nach ein Hinweis, dass Bedarf an neuen Mitteln besteht und Rhopressa als eine aussichtsreiche Option gesehen wird.
http://www.bizjournals.com/triangle/news/2015/01/12/rtp-duke…
"... Aerie (Nasdaq: AERI) says it is ahead of schedule in a 400-patient Phase 3 registration trial of Rhopressa, Aerie's developmental eye drop is being tested for its ability to lower intraocular pressure (IOP) in patients with glaucoma or ocular hypertension. Specifically, Aerie's drug is being tested against the prescription drug timolol, sold under brand names including Betimol and Timoptic. Timolol is the most widely used comparator in registration trials for lowering of IOP. ... "As a result of Rocket 1 enrollment having been completed well ahead of schedule and after thorough review we are accelerating the expected timeline for the reporting of efficacy results from this Rhopressa Phase 3 registration trial," said Vicente Anido, Aerie CEO. "We originally planned to release the efficacy results of both Rocket 1 and Rocket 2 in mid-2015, and now expect to report efficacy results for Rocket 1 in the middle of second-quarter 2015, with Rocket 2 still on schedule for a mid-2015 efficacy read-out."...
Gruß
ipollit
INCY
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
http://jpmorgan.metameetings.com/confbook/healthcare15/compa…
Meiner Meinung nach entwickelt sich die Pipeline von INCY sehr positiv... auch für ein 10+ Mrd MK ist das recht ansehlich:
- weltweit führend bei JAK1/2-Hemmern
- weltweit führend bei IDO-Hemern
- mehrere Target-Therapien: pi3k-delta, cMet, BRD4, FGFR
- IO-Kandidaten mit GITR, OX40, TIM3, LAG3
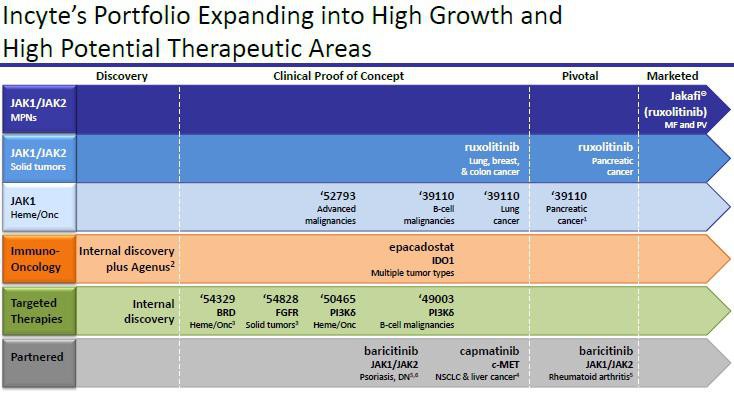
Jakafi entwickelt sich ebenfalls weiter positiv. INCY prognostiziert nun einen US-Umsatz in MF&PV von über 1 Mrd USD... im US-Markt vermarktet INCY Jakafi selber. Dazu kommen Royalties von NVS für Ex-US. Für Jakafi gibt es in MF&PV bisher keine Konkurrenz, da keine anderen entsprechend wirksame Mittel in dieser Indikation vorhanden sind.
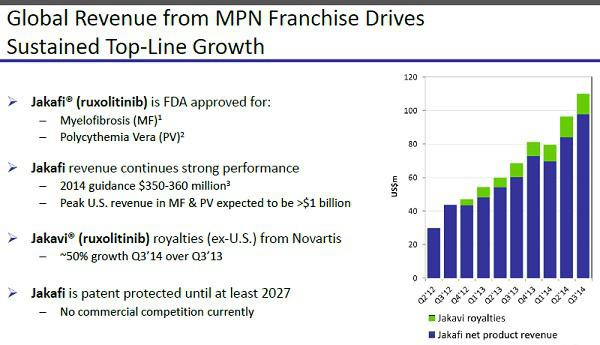
Eine Weiterentwicklung des JAK1/JAK2-Hemmers Jakafi sind die JAK1-Hemmer INCB39110 und INCB52793. Eine Hemmung nur von JAK1 hat den Vorteil, dass die Myelosuppression (Hemmung der Blutbildung im Knochenmark) geringer ist, was in Kombi mit z.B. Chemo wichtig ist, die selber diese Nebenwirkung hat, oder in Indikationen, in denen die Blutbildung bereits beeinträchtigt ist. Die Wirkung soll auch ohne JAK2-Hemmung gleich sein. (Es gibt auch Indikationen wie Nierenprobleme, in denen eine JAK2-Hemmung wichtig ist). 39110 soll dieses Jahr in PIII gegen Bauchspeicheldrüsenkrebs gehen.
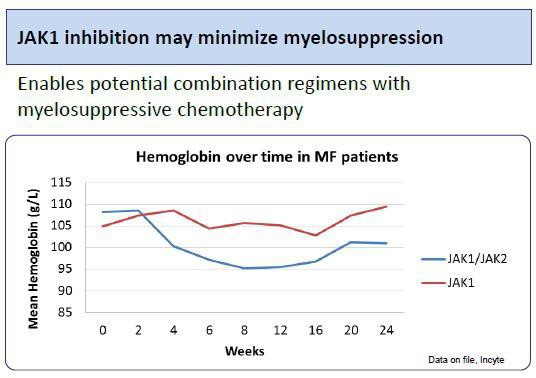
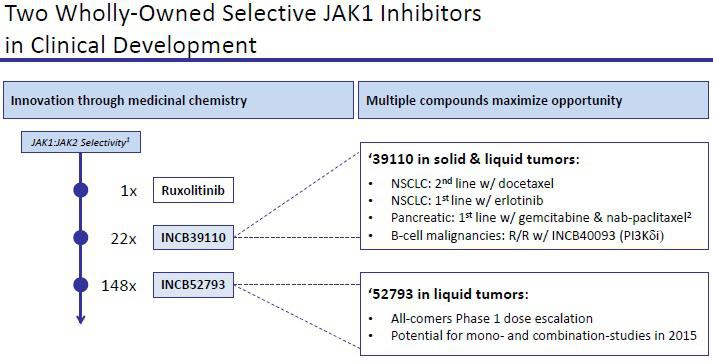
In soliden Tumoren soll die Hemmung von JAK sich über den JAK/STAT-Signalweg positiv auf die entzündliche Umgebung des Tumors auswirken, die den Tumor u.a. über Zytokine fördert. Vielleicht wird daher auch der CRP-Marker zur Prognose eines guten Ansprechens von JAK-Hemmern verwendet, der bei Entzündungen erhöht ist.
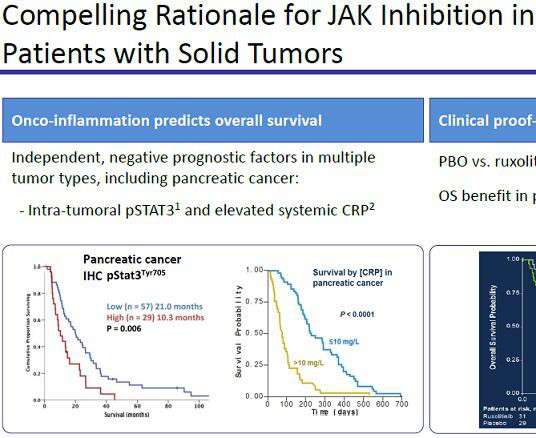
Da Zytokine das Immunsystem beeinflussen, sollen JAK-Hemmer auch IO-Eigenschaften haben: z.B. werden über JAK/STAT immunsystem-unterdrückende Zellen wie Treg und MDSC reduziert. Dies erhöht z.B. T-Zellen, die den Krebs bekämpfen können. Präklinische Studien zeigen z.B. eine Synergie von JAK1 + IDO1.
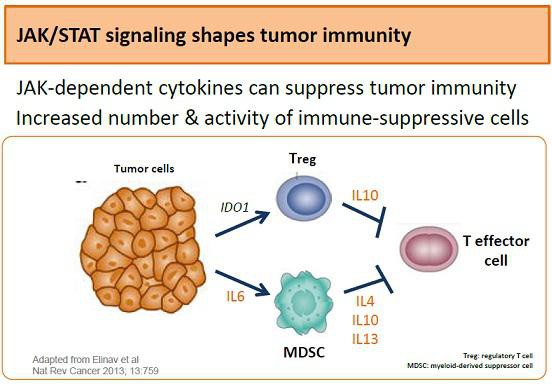
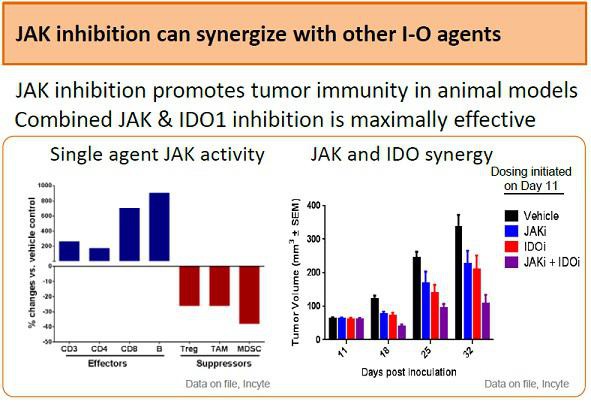
INCY hat auch zwei pi3k-delta Hemmer in der Entwicklung... also wie GILDs Zydelig. Sie versuchen dabei einen besseren Hemmer zu entwickeln, der eine höhere Wirkung und weniger Nebenwirkung hat. Vor einiger Zeit habe ich mal gelesen, dass sich pi3k-delta ebenfalls positiv auf das Immunsystem auswirken kann (Reduzierung von hemmenden Tregs), um den Krebs bekämpfen zu können, unabhängig von der Wirkung bei Blutkrebsarten wie CLL, DLBCL, NHL usw: z.B. http://www.immunotherapyofcancer.org/content/2/S3/O4 "...We found that pharmacologic inhibition of PI3Kd isoform but not PI3Ka or PI3Kß exhibit a selective blockade of PI3K/Akt signaling and the inhibition of proliferation of Tregs... Interestingly, PI3Ka or PI3Kß were unable to compensate for PI3Kd in Tregs, making PI3Kd inhibition a selective Treg-targeting approach. Importantly, we also show that inhibition of PI3Kd and not PI3Ka PI3Kb in tumor-bearing mice significantly decreases the level of Tregs without affecting other T cell subsets. We believe that our findings provide a basis for development of novel cancer immunotherapies based on selective inhibition of Tregs.".
Diese Hemmer sollen auch mit JAK1 synergetisch sein.
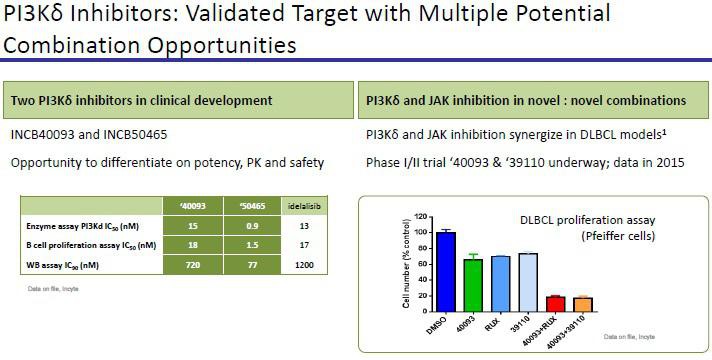
Neu in der Pipeline sind ein FGRR-Hemmer und BRD4 BET-Hemmer. Beiden sollen in den nächsten Monaten in PI gehen. Den BET-Hemmer finde ich auch sehr spannend... dabei handelt es sich um ein epigentisch wirkendes Mittel, dass u.a. Myc hemmen kann. Myc soll angeblich für einige Tumore wichtig sein (Driver) und konnte vor der Erforschung von BET-Hemmern nicht beeinflusst werden.
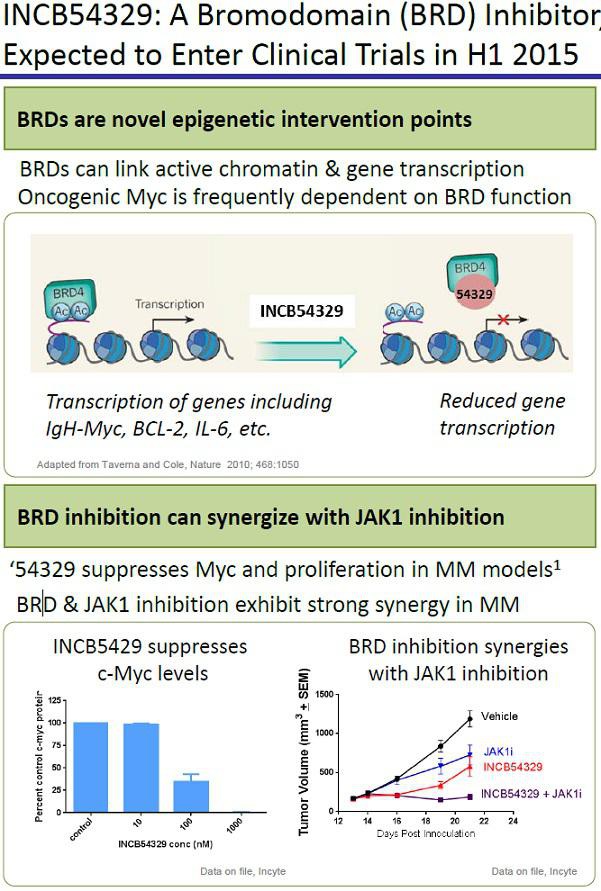
Hier ist z.B. etwas über BET-Hemmer... http://pharmastrategyblog.com/2013/03/bromodomain-inhibitors…

Zu dem JAK1/2 Baricitinib, das von Lilly u.a. gegen RA entwickelt wird, sollen dieses Jahr weitere PIII-Daten kommen. Es besteht die Hoffnung, dass es als ein orales Mittel gegen RA eine Konkurrenz zu den AKs werden kann, die den Markt als IV-Mittel dominieren und alle Multi-Mrd Blockbuster sind. Pfizers zugelassener oraler JAK-Hemmer Xeljanz konnte diese Hoffnung bisher nicht erfüllen. Allerdings hemmt Xeljanz im wesentlichen auch JAK3, was zu problematischen Nebenwirkungen führen kann, die wohl eine breitere Anwendung verhindert haben. INCY bekommt bis zu "high 20%" Royalties, wenn es Baricitinib auf den Markt schafft.
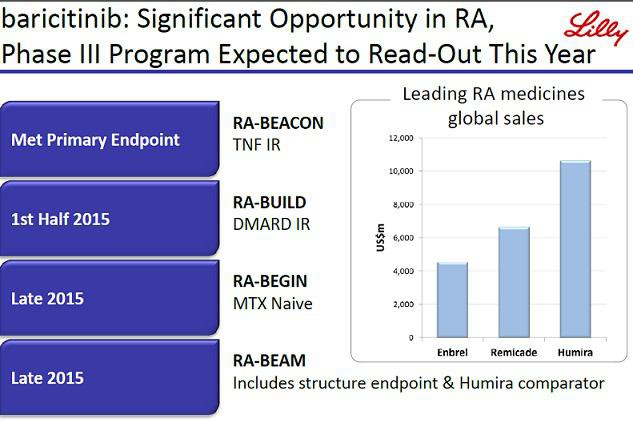


Gruß
ipollit
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
http://jpmorgan.metameetings.com/confbook/healthcare15/compa…
Meiner Meinung nach entwickelt sich die Pipeline von INCY sehr positiv... auch für ein 10+ Mrd MK ist das recht ansehlich:
- weltweit führend bei JAK1/2-Hemmern
- weltweit führend bei IDO-Hemern
- mehrere Target-Therapien: pi3k-delta, cMet, BRD4, FGFR
- IO-Kandidaten mit GITR, OX40, TIM3, LAG3

Jakafi entwickelt sich ebenfalls weiter positiv. INCY prognostiziert nun einen US-Umsatz in MF&PV von über 1 Mrd USD... im US-Markt vermarktet INCY Jakafi selber. Dazu kommen Royalties von NVS für Ex-US. Für Jakafi gibt es in MF&PV bisher keine Konkurrenz, da keine anderen entsprechend wirksame Mittel in dieser Indikation vorhanden sind.

Eine Weiterentwicklung des JAK1/JAK2-Hemmers Jakafi sind die JAK1-Hemmer INCB39110 und INCB52793. Eine Hemmung nur von JAK1 hat den Vorteil, dass die Myelosuppression (Hemmung der Blutbildung im Knochenmark) geringer ist, was in Kombi mit z.B. Chemo wichtig ist, die selber diese Nebenwirkung hat, oder in Indikationen, in denen die Blutbildung bereits beeinträchtigt ist. Die Wirkung soll auch ohne JAK2-Hemmung gleich sein. (Es gibt auch Indikationen wie Nierenprobleme, in denen eine JAK2-Hemmung wichtig ist). 39110 soll dieses Jahr in PIII gegen Bauchspeicheldrüsenkrebs gehen.


In soliden Tumoren soll die Hemmung von JAK sich über den JAK/STAT-Signalweg positiv auf die entzündliche Umgebung des Tumors auswirken, die den Tumor u.a. über Zytokine fördert. Vielleicht wird daher auch der CRP-Marker zur Prognose eines guten Ansprechens von JAK-Hemmern verwendet, der bei Entzündungen erhöht ist.

Da Zytokine das Immunsystem beeinflussen, sollen JAK-Hemmer auch IO-Eigenschaften haben: z.B. werden über JAK/STAT immunsystem-unterdrückende Zellen wie Treg und MDSC reduziert. Dies erhöht z.B. T-Zellen, die den Krebs bekämpfen können. Präklinische Studien zeigen z.B. eine Synergie von JAK1 + IDO1.


INCY hat auch zwei pi3k-delta Hemmer in der Entwicklung... also wie GILDs Zydelig. Sie versuchen dabei einen besseren Hemmer zu entwickeln, der eine höhere Wirkung und weniger Nebenwirkung hat. Vor einiger Zeit habe ich mal gelesen, dass sich pi3k-delta ebenfalls positiv auf das Immunsystem auswirken kann (Reduzierung von hemmenden Tregs), um den Krebs bekämpfen zu können, unabhängig von der Wirkung bei Blutkrebsarten wie CLL, DLBCL, NHL usw: z.B. http://www.immunotherapyofcancer.org/content/2/S3/O4 "...We found that pharmacologic inhibition of PI3Kd isoform but not PI3Ka or PI3Kß exhibit a selective blockade of PI3K/Akt signaling and the inhibition of proliferation of Tregs... Interestingly, PI3Ka or PI3Kß were unable to compensate for PI3Kd in Tregs, making PI3Kd inhibition a selective Treg-targeting approach. Importantly, we also show that inhibition of PI3Kd and not PI3Ka PI3Kb in tumor-bearing mice significantly decreases the level of Tregs without affecting other T cell subsets. We believe that our findings provide a basis for development of novel cancer immunotherapies based on selective inhibition of Tregs.".
Diese Hemmer sollen auch mit JAK1 synergetisch sein.

Neu in der Pipeline sind ein FGRR-Hemmer und BRD4 BET-Hemmer. Beiden sollen in den nächsten Monaten in PI gehen. Den BET-Hemmer finde ich auch sehr spannend... dabei handelt es sich um ein epigentisch wirkendes Mittel, dass u.a. Myc hemmen kann. Myc soll angeblich für einige Tumore wichtig sein (Driver) und konnte vor der Erforschung von BET-Hemmern nicht beeinflusst werden.

Hier ist z.B. etwas über BET-Hemmer... http://pharmastrategyblog.com/2013/03/bromodomain-inhibitors…

Zu dem JAK1/2 Baricitinib, das von Lilly u.a. gegen RA entwickelt wird, sollen dieses Jahr weitere PIII-Daten kommen. Es besteht die Hoffnung, dass es als ein orales Mittel gegen RA eine Konkurrenz zu den AKs werden kann, die den Markt als IV-Mittel dominieren und alle Multi-Mrd Blockbuster sind. Pfizers zugelassener oraler JAK-Hemmer Xeljanz konnte diese Hoffnung bisher nicht erfüllen. Allerdings hemmt Xeljanz im wesentlichen auch JAK3, was zu problematischen Nebenwirkungen führen kann, die wohl eine breitere Anwendung verhindert haben. INCY bekommt bis zu "high 20%" Royalties, wenn es Baricitinib auf den Markt schafft.


Gruß
ipollit
MDVN
Xtandi ist inzwischen auf Blockbuster-Niveau angekommen mit 300 Mio USD WW-Umsatz in 3Q14 (181 Mio USD davon in den USA). Mittel-/Langfristig sehen einige Analysten Umsätze von 6 Mrd USD, womit alleine gegen Prostatakrebs Xtandi eines der umsatzstärksten Krebsmittel werden könnte.
In den USA teilen sich MDVN und Parnter Astellas Umsätze und Gewinne, für ex-US Umsätze erhält MDVN Royalties im Bereich von "low teens to low twenties"... also vielleicht 11% - 21%.
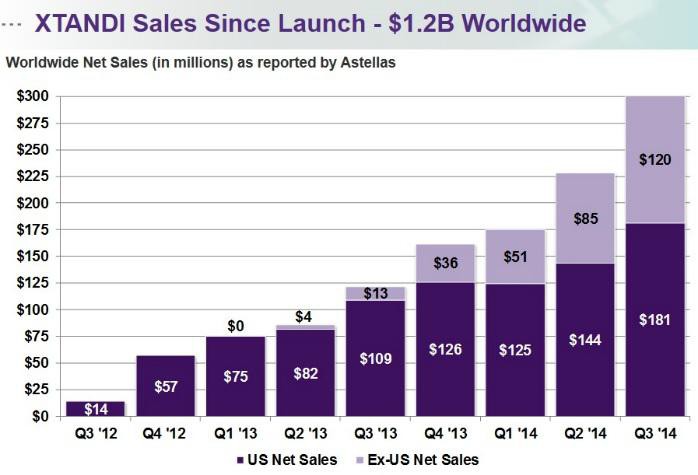
In der Entwicklung bewegt sich Xtandi weiter in Richtung früheren Stadien der Prostatakrebs-Erkrankung... beginnend von Chemo über die Anwendung vor einer möglichen Chemo, den nicht metastatischen hormon-resistenten Prostatakrebs bis zum hormon-sensitiven Prostatakrebs. Damit verbunden ist auch eine Anwendung von Xtandi von Urologen statt Onkologen. Urologen sind eher konservativ und ändern etablierte Medikamente nur langsam, weshalb Xtandi erstmal gegen Casodex überzeugen muss.
Dementsprechnd sind die PIII-Studien angelegt worden... PREVAIL (vor einer Chemo) war sehr erfolgreich... in den nächsten Jahren stehen noch Ergebnisse von PROSPER (nicht metastisierter Krebs) und BCR (hormon-sensitiver Krebs, Xtandi vs Lupron) an.
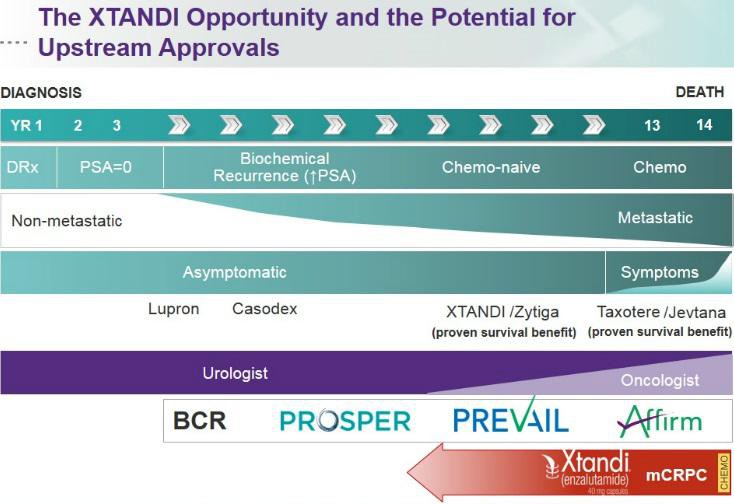
Zunächst kommen aber noch PII-Daten, die insbesondere für Urologen wichtig sind, da es Vergleichsstudien zwischen Xtandi und Casodex (ein Standard-Medikament von Urologen, wie Xtandi ein AR-Hemmer, der aber etwas anders wirkt) sind. In Kürze (Anfang Q1) sollten die TERRAIN-Daten (metastasierter Krebs, EU) kommen und später dann STRIVE (auch nicht metastasierter Krebs, USA).

Neben Prostatakrebs könnte Xtandi auch bei Brustkrebs helfen, wobei die Rolle von AR bei Brustkrebs nicht so ganz klar ist. Es befindet sich in einer PII gegen TBNC (wo bisher nichts hilft, weder Hormon-Hemmer noch HER2-Hemmer). Mir ist nicht ganz klar, ob die bisherigen Ergebnisse aussichtsreich sind... in einer Untergruppe von Patienten mit einem bestimmten Biomarker ist 6M-PFS 45%, was deutlich über einer Chemo liegen soll. Ein PFS-Vorteil ist in TNBC ausreichend für eine Zulassung (anders als in Prostatakrebs, wo erst OS ausreichend ist). Jedenfalls sollen dieses Jahr weitere Daten dazu kommen.

Für den kürzlich von Curetech einlizensierte PD1-AK soll dieses Jahr eine PIII in einer Blutkrebs-Indikation gestartet werden. Basis dafür soll u.a. eine Studie von Pidilizumab + Rituxan in FL sei, bei der selbst Patienten, die zuvor nicht auf Rituxan angesprochen haben, einen CR oder ein langanhaltendes Ansprechen auf die Kombination gezeigt haben. Bisher sind andere PD1-AKs glaube ich noch nicht soweit entwickelt in Blutkrebs (mir fehlt dazu aber etwas der Überblick)... bei der letzten ASH im Dezember war ja z.B. HL ein Thema, während CLL wohl nicht funktioniert. Obwohl viele von Pidilizumab nicht viel halten, nachdem Teva diesen AK an Curetech zurückgegeben hat und er in anderen Indikationen wie Lungenkrebs weit hinter der Konkurrenz zurückliegt, könnte z.B. soetwas wie FL interessant sein, wenn die anderen dort noch nicht so weit sind.
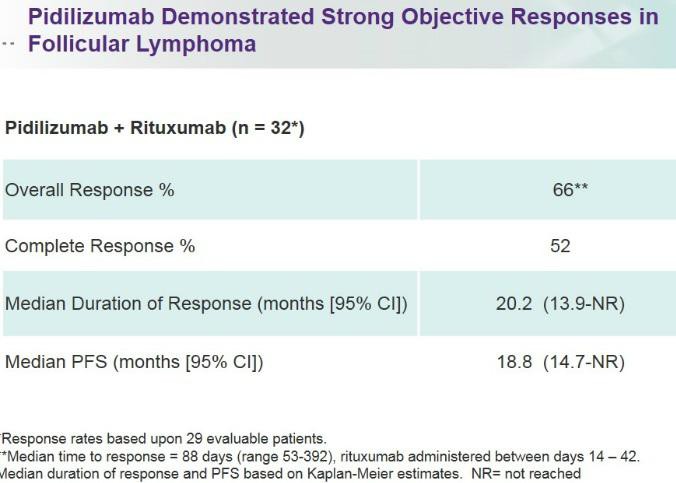
Ein Kommentar zu dieser Studie von 2013:
"What Next – PD-L1 Inhibition in Lymphoma Too! Another of the surprises as the meeting was the first demonstration of activity for an "immune checkpoint inhibitor" cancer immunotherapy in hematological malignancies. Curetech's pidilizumab (formerly CT-011 - humanized antibody to PD-1) was given with Rituxan to patients with low grade follicular lymphoma. The combination appeared to be well tolerated. Of the 29 patients, 66% responded, with 52% having complete responses and 14% partial responses. 86% of patients had some degree of tumor regression. The depth of these responses, including the high rate of complete responses, was impressive, particularly since they were only given 4 cycles of Rituxan. Of the 15 complete responses, 10 remain on treatment, several out beyond 30 months. As in prior studies with this class of drugs, there were significant numbers of "late responders" with some patients converting to responses, or even to complete responses after 10 or more months on study. The median PFS of the entire population is 19.6 months and there appears to be a subpopulation with very durable responses. While we aren't sure what Curetech will do with this drug, this activity fits with comments from the leaders in this field (Bristol-Myers Squibb, Merck, and Roche), that early work suggests activity in blood cancers as well. This presentation suggests that a significant proportion of lymphoma patients could benefit from this class of medicine, particularly given the ubiquity of Rituxan in these diseases."
***
More upside for our anti-PD1 and nivolumab revenue forecast. We estimate that the market potential for anti-PD1 in NSCLC, MEL and mRCC could be $13B globally, with additional $15B upside from all other indications being tested in Phase 1/2 studies. It is estimated that there are ~100K new cases of NHL and ~40K related deaths in major developed markets each year. DLBCL and FL account for ~50% of NHL cases in the U.S. Our back-of-the-envelope calculation shows ~$1B global market potential for anti-PD1 in NHL patients assuming 30% penetration rates."
Von der Theorie her scheint aber HL (was auch den letzten ASH-Ergebnissen entspricht) für PD-1 interessanter zu sein, da HL-Krebszellen wohl PD-1 deutlich expressionieren, so dass es bei dieser Krebsart wichtig sein könnte. Bei FL ist es viel unsicherer, bei CLL eher unwahrscheinlich, dass PD-1 etwas bewirkt:
"Potential in DLBCL and Hodgkin's Lymphoma. The utility of PD1 therapy in untreated NHL is unclear. The PD-L1 opportunity in NHL is likely confined to a subset of diffuse large B-cell lymphomas (DLBCL) with activated B-cell features (24% of primary DLBCL). The administration of anti-PD-L1 blocking antibody boosted the T cell proliferation and IFN-? secretion in DLBCL and ALCL models only, resulting in enhanced secretion of several inflammatory cytokines. The potential role of PD1 therapy in the less common Hodgkin's Lymphoma segment looks much greater given the up regulation in the Hodgkin cells. PD1 blockade in patients restores IFN- ? consistent with T-cell exhaustion being an important target for treatment. We calculate that the addressable PD1 population is $1bn for DLBCL subgroup and Hodgkins combined."
****
Für MDVN ist meiner Meinung nach besonders eine Kombi von PD1 und Xtandi interessant... z.B. in Prostatakrebs, wo Xtandi etabliert ist, oder Brustkrebs wie TNBC, wo sowohl Xtandi als auch PD-1 Ansätze einer Wirkung zeigt.
Laut MDVN hat Xtandi selbst eine immunologische Wirkung, die IOs wie PD1 unterstützen könnten. Konkret wurden zwei Wirkungen genannt, die jeweils aus Untersuchungen/Veröffentlichungen abgeleitet werden:
1.) Xtandi soll auf den Thymus wirken und diesen anregen. Der Thymus ist ein Organ, in dem in jungen Jahren T-Zellen entstehen... im Laufe der Jahre bildet sich der Thymus zurück, es entstehen keine neuen T-Zellen mehr, die bestehenden bleiben aber im Körper aktiv und vermehren sich gegebenfalls selber. Inwieweit eine Anregnung des Thymus Einfluss auf die Aktivierung der Immunabwehr gegen Krebs hat, ist mir nicht ganz klar. Aber es heißt z.B. "Die vollständige Rückbildung des Thymus ist ein wesentlicher Faktor für die Immunoseneszenz (langsame Verschlechterung des Immunsystems bei älteren Menschen)".
Hier ist die Studie zu finden... http://clincancerres.aacrjournals.org/content/19/22/6205.ful…
"Conclusions: These data support the combination of enzalutamide and immunotherapy as a promising treatment strategy for CRPC."
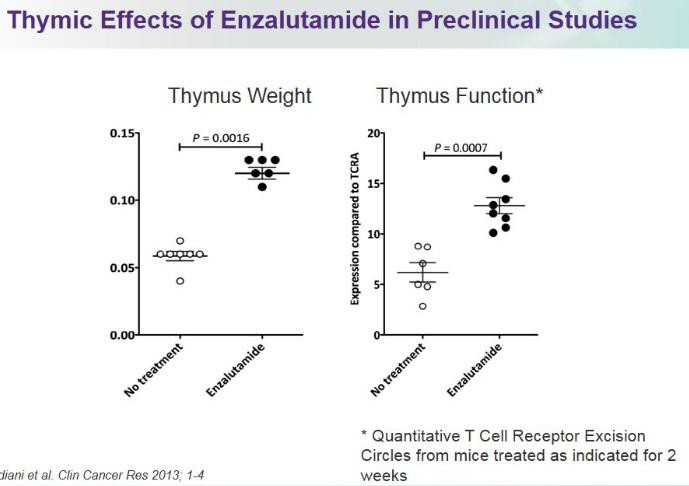
2.) Zudem soll Xtandi Prostata-Zellen sensitiver gegen einen Angriff von T-Zellen machen (T-Zellen können Prostata-Krebszellen effektiver abtöten), wenn sie erst einmal aktiviert sind. Dies soll insbesondere auch für Krebszellen gelten, die gegen Xtandi resistent geworden sind:
http://www.ncbi.nlm.nih.gov/pubmed/25344864
" The immunomodulatory properties of enzalutamide and abiraterone provide a rationale for their use in combination with immunotherapeutic agents in CRPC, especially for patients with minimal response to enzalutamide or abiraterone alone, or for patients who have developed resistance to ADT."
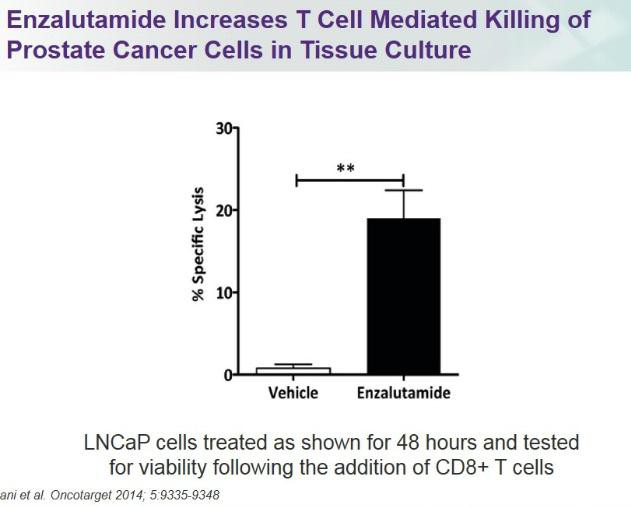
Die IO-Eigenschaften von Xtandi sind aber meiner Meinung nach noch etwas unklar... ob und was wirklich im Menschen hilft, muss sich erst zeigen.

Gruß
ipollit
Xtandi ist inzwischen auf Blockbuster-Niveau angekommen mit 300 Mio USD WW-Umsatz in 3Q14 (181 Mio USD davon in den USA). Mittel-/Langfristig sehen einige Analysten Umsätze von 6 Mrd USD, womit alleine gegen Prostatakrebs Xtandi eines der umsatzstärksten Krebsmittel werden könnte.
In den USA teilen sich MDVN und Parnter Astellas Umsätze und Gewinne, für ex-US Umsätze erhält MDVN Royalties im Bereich von "low teens to low twenties"... also vielleicht 11% - 21%.

In der Entwicklung bewegt sich Xtandi weiter in Richtung früheren Stadien der Prostatakrebs-Erkrankung... beginnend von Chemo über die Anwendung vor einer möglichen Chemo, den nicht metastatischen hormon-resistenten Prostatakrebs bis zum hormon-sensitiven Prostatakrebs. Damit verbunden ist auch eine Anwendung von Xtandi von Urologen statt Onkologen. Urologen sind eher konservativ und ändern etablierte Medikamente nur langsam, weshalb Xtandi erstmal gegen Casodex überzeugen muss.
Dementsprechnd sind die PIII-Studien angelegt worden... PREVAIL (vor einer Chemo) war sehr erfolgreich... in den nächsten Jahren stehen noch Ergebnisse von PROSPER (nicht metastisierter Krebs) und BCR (hormon-sensitiver Krebs, Xtandi vs Lupron) an.

Zunächst kommen aber noch PII-Daten, die insbesondere für Urologen wichtig sind, da es Vergleichsstudien zwischen Xtandi und Casodex (ein Standard-Medikament von Urologen, wie Xtandi ein AR-Hemmer, der aber etwas anders wirkt) sind. In Kürze (Anfang Q1) sollten die TERRAIN-Daten (metastasierter Krebs, EU) kommen und später dann STRIVE (auch nicht metastasierter Krebs, USA).

Neben Prostatakrebs könnte Xtandi auch bei Brustkrebs helfen, wobei die Rolle von AR bei Brustkrebs nicht so ganz klar ist. Es befindet sich in einer PII gegen TBNC (wo bisher nichts hilft, weder Hormon-Hemmer noch HER2-Hemmer). Mir ist nicht ganz klar, ob die bisherigen Ergebnisse aussichtsreich sind... in einer Untergruppe von Patienten mit einem bestimmten Biomarker ist 6M-PFS 45%, was deutlich über einer Chemo liegen soll. Ein PFS-Vorteil ist in TNBC ausreichend für eine Zulassung (anders als in Prostatakrebs, wo erst OS ausreichend ist). Jedenfalls sollen dieses Jahr weitere Daten dazu kommen.

Für den kürzlich von Curetech einlizensierte PD1-AK soll dieses Jahr eine PIII in einer Blutkrebs-Indikation gestartet werden. Basis dafür soll u.a. eine Studie von Pidilizumab + Rituxan in FL sei, bei der selbst Patienten, die zuvor nicht auf Rituxan angesprochen haben, einen CR oder ein langanhaltendes Ansprechen auf die Kombination gezeigt haben. Bisher sind andere PD1-AKs glaube ich noch nicht soweit entwickelt in Blutkrebs (mir fehlt dazu aber etwas der Überblick)... bei der letzten ASH im Dezember war ja z.B. HL ein Thema, während CLL wohl nicht funktioniert. Obwohl viele von Pidilizumab nicht viel halten, nachdem Teva diesen AK an Curetech zurückgegeben hat und er in anderen Indikationen wie Lungenkrebs weit hinter der Konkurrenz zurückliegt, könnte z.B. soetwas wie FL interessant sein, wenn die anderen dort noch nicht so weit sind.

Ein Kommentar zu dieser Studie von 2013:
"What Next – PD-L1 Inhibition in Lymphoma Too! Another of the surprises as the meeting was the first demonstration of activity for an "immune checkpoint inhibitor" cancer immunotherapy in hematological malignancies. Curetech's pidilizumab (formerly CT-011 - humanized antibody to PD-1) was given with Rituxan to patients with low grade follicular lymphoma. The combination appeared to be well tolerated. Of the 29 patients, 66% responded, with 52% having complete responses and 14% partial responses. 86% of patients had some degree of tumor regression. The depth of these responses, including the high rate of complete responses, was impressive, particularly since they were only given 4 cycles of Rituxan. Of the 15 complete responses, 10 remain on treatment, several out beyond 30 months. As in prior studies with this class of drugs, there were significant numbers of "late responders" with some patients converting to responses, or even to complete responses after 10 or more months on study. The median PFS of the entire population is 19.6 months and there appears to be a subpopulation with very durable responses. While we aren't sure what Curetech will do with this drug, this activity fits with comments from the leaders in this field (Bristol-Myers Squibb, Merck, and Roche), that early work suggests activity in blood cancers as well. This presentation suggests that a significant proportion of lymphoma patients could benefit from this class of medicine, particularly given the ubiquity of Rituxan in these diseases."
***
More upside for our anti-PD1 and nivolumab revenue forecast. We estimate that the market potential for anti-PD1 in NSCLC, MEL and mRCC could be $13B globally, with additional $15B upside from all other indications being tested in Phase 1/2 studies. It is estimated that there are ~100K new cases of NHL and ~40K related deaths in major developed markets each year. DLBCL and FL account for ~50% of NHL cases in the U.S. Our back-of-the-envelope calculation shows ~$1B global market potential for anti-PD1 in NHL patients assuming 30% penetration rates."
Von der Theorie her scheint aber HL (was auch den letzten ASH-Ergebnissen entspricht) für PD-1 interessanter zu sein, da HL-Krebszellen wohl PD-1 deutlich expressionieren, so dass es bei dieser Krebsart wichtig sein könnte. Bei FL ist es viel unsicherer, bei CLL eher unwahrscheinlich, dass PD-1 etwas bewirkt:
"Potential in DLBCL and Hodgkin's Lymphoma. The utility of PD1 therapy in untreated NHL is unclear. The PD-L1 opportunity in NHL is likely confined to a subset of diffuse large B-cell lymphomas (DLBCL) with activated B-cell features (24% of primary DLBCL). The administration of anti-PD-L1 blocking antibody boosted the T cell proliferation and IFN-? secretion in DLBCL and ALCL models only, resulting in enhanced secretion of several inflammatory cytokines. The potential role of PD1 therapy in the less common Hodgkin's Lymphoma segment looks much greater given the up regulation in the Hodgkin cells. PD1 blockade in patients restores IFN- ? consistent with T-cell exhaustion being an important target for treatment. We calculate that the addressable PD1 population is $1bn for DLBCL subgroup and Hodgkins combined."
****
Für MDVN ist meiner Meinung nach besonders eine Kombi von PD1 und Xtandi interessant... z.B. in Prostatakrebs, wo Xtandi etabliert ist, oder Brustkrebs wie TNBC, wo sowohl Xtandi als auch PD-1 Ansätze einer Wirkung zeigt.

Laut MDVN hat Xtandi selbst eine immunologische Wirkung, die IOs wie PD1 unterstützen könnten. Konkret wurden zwei Wirkungen genannt, die jeweils aus Untersuchungen/Veröffentlichungen abgeleitet werden:
1.) Xtandi soll auf den Thymus wirken und diesen anregen. Der Thymus ist ein Organ, in dem in jungen Jahren T-Zellen entstehen... im Laufe der Jahre bildet sich der Thymus zurück, es entstehen keine neuen T-Zellen mehr, die bestehenden bleiben aber im Körper aktiv und vermehren sich gegebenfalls selber. Inwieweit eine Anregnung des Thymus Einfluss auf die Aktivierung der Immunabwehr gegen Krebs hat, ist mir nicht ganz klar. Aber es heißt z.B. "Die vollständige Rückbildung des Thymus ist ein wesentlicher Faktor für die Immunoseneszenz (langsame Verschlechterung des Immunsystems bei älteren Menschen)".
Hier ist die Studie zu finden... http://clincancerres.aacrjournals.org/content/19/22/6205.ful…
"Conclusions: These data support the combination of enzalutamide and immunotherapy as a promising treatment strategy for CRPC."

2.) Zudem soll Xtandi Prostata-Zellen sensitiver gegen einen Angriff von T-Zellen machen (T-Zellen können Prostata-Krebszellen effektiver abtöten), wenn sie erst einmal aktiviert sind. Dies soll insbesondere auch für Krebszellen gelten, die gegen Xtandi resistent geworden sind:
http://www.ncbi.nlm.nih.gov/pubmed/25344864
" The immunomodulatory properties of enzalutamide and abiraterone provide a rationale for their use in combination with immunotherapeutic agents in CRPC, especially for patients with minimal response to enzalutamide or abiraterone alone, or for patients who have developed resistance to ADT."

Die IO-Eigenschaften von Xtandi sind aber meiner Meinung nach noch etwas unklar... ob und was wirklich im Menschen hilft, muss sich erst zeigen.
Gruß
ipollit
CLVS
http://jpmorgan.metameetings.com/confbook/healthcare15/compa…
Im Sommer müssten die für eine Zulassung vom EGFR-Hemmer Roci entscheidenden Daten vorliegen, eine Zulassung soll Ende des Jahres möglich sein. Nächstes Jahr soll dann auch schon die Zulassung des PARP-Hemmers Ruca beantragt werden.

Roci ist zunächst erstmal als Hemmer von EGFR mit der Mutation T790m in Lungenkrebs gedacht. Diese Mutation entsteht bei der Behandlung mit einem herkömmlichen EGFR-Hemmer in etwa 50% und führt zur Resistenz gegen diese EGFR-Hemmer. D.h. rund 50% der 1st-line EGFR-Patienten sind irgendwann auf einen EGFR-T790m-Hemmer angewiesen.
Die EGFR-Hemmer der ersten Generation, z.B. Tarceva, haben den Nachteil, dass sie auch normales wt-EGFR hemmen, was zu Nebenwirkungen wie starkem Haut-Ausschlag führt. Roci bindet dagegen kaum an wt-EGFR.
CLVS hat mit AZN einen sehr starken Konkurrenten sowohl beim EGFR-Hemmer Roci als auch beim PARP-Hemmer Ruca. Im letzten Sommer ist der Kurs von CLVS stark gesunken, weil als Nebenwirkung von Roci ein temporärer Diabetes entsteht, während AZNs Kandidat AZD9291 diese Nebenwirkung nicht hat. Ursache hierfür ist ein Zerfallsprodukt (Metabolit), das beim Abbau des EGFR-Hemmers entsteht. Ein Metabolit von Roci ist ein IGF1R-/IR-Hemmer... IGF1R ist der Insulin-like-growth-factor-1-Rezeptor, IR der Insulin-Rezeptor. Ersterer steuert Wachstumsprozesse und soll auch an Krebs beteiligt sein, obwohl IGF1R-Hemmer&AKs in klinischen Studien bisher gescheitert sind. Über den IR-Rezeptor wirkt dagegen das Insulin... die Blockierung führt zu zeitweisem Diabetes. IR und IGF1R sind verwandt und kommunizieren miteinander, so dass normalerweise immer beide beeinflusst werden. Alle IGF1R-Hemmer zeigen diese Nebenwirkung.
Laut CLVS soll der Metabolit von Roci ein besonders starker Hemmer von IGF1R sein (stärker als die bekannten), aber weniger stark zu temporärem Diabetes führen. Angeblich ist keine Gabe von Insulin notwendig, sondern es reicht ein orales Standard-T2-Diabetes-Mittel, um dieser Nebenwirkung zu begegnen.
AZD9291 soll dagegen einen Metaboliten haben, der wt-EGFR und HER2 hemmt. Dadurch hat AZD9291 auch Hautausschlag (Rash) als Nebenwirkung (allerdings weniger als die bekannten EGFR-Hemmer), Roci dagegen nicht.
Im Sommer wurden nur die negativen Seiten der IGF1R-Hemmung durch Roci gesehen. Allerdings gibt es Untersuchungen, dass IGF1R auch ein wichtiger Resistenz-Mechanismus gegen EGFR-Hemmer ist, genauso wie die Mutation T790m. Schließlich gibt es auch viele Patienten (50%), die nicht T790m entwickeln und trotzdem resistent gegen EGFR-Hemmer werden... bei einem Teil soll IGF1R beteiligt sein (wenn ich es richtig verstanden habe, könnten es 30% sein). Demnach kann auch über IGF1R eine Resistenz gegen einen T790m-EGFR-Hemmer entstehen. D.h. theoretisch könnte aufgrund des IGF1R-Metaboliten Roci länger wirken oder auch bei Patienten ohne T790m helfen.
Letzteres scheint nach den bisherigen Daten der Fall zu sein. Auch nach aktualisierten Daten mit zusätzlichen Patienten liegt ein ORR von 50% (mit der höhreren Dosierung) bei T790m- über dem, was man eigentlich bei Patienten erwarten würde, bei denen zuvor die anderen EGFR-Hemmern nicht mehr wirken. Dadurch könnte sich Roci positiv von AZD9291 absetzen, das bei T790m- nicht wirken sollte. CLVS hat nun die Studien um T790m-neg-Arme ergänzt.
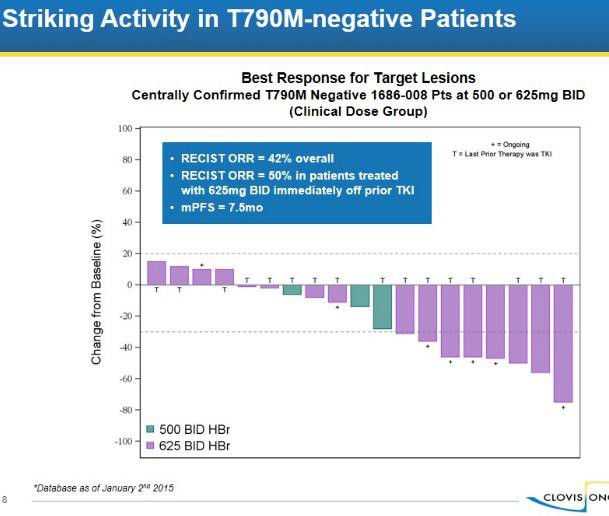
AZN's PARP-Hemmer Lynparza wurde vor Kurzem gegen mBRCA Eierstockkrebs zugelassen... dies ist unten der grüne Anteil. CLVS entwickelt Ruca zusätzlich noch gegen BRCAness (gelber Bereich)... dies sind nochmal deutlich mehr Patienten als mBRCA. Der Marker BRCAess wird speziell für CLVS anhand von einem Test von FMI ermittelt.
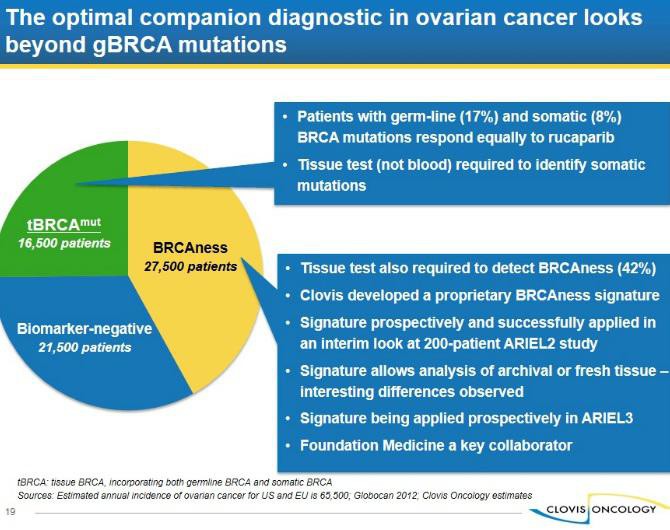
Neben Eierstock-Krebs gibt es auch in anderen Krebsarten die BRCA-Mutation und BRCAness... es könnten in Zukunft also deutlich mehr Patienten von Ruca profitieren, wobei der gelbe Bereich speziell von CLVS und FMI ermittelt wird. P2-Studien sollen dabei von Sponsoren durchgeführt werden und erst wenn deren Ergebnisse positiv sind, führt CLVS die Zulassungsstudien durch.
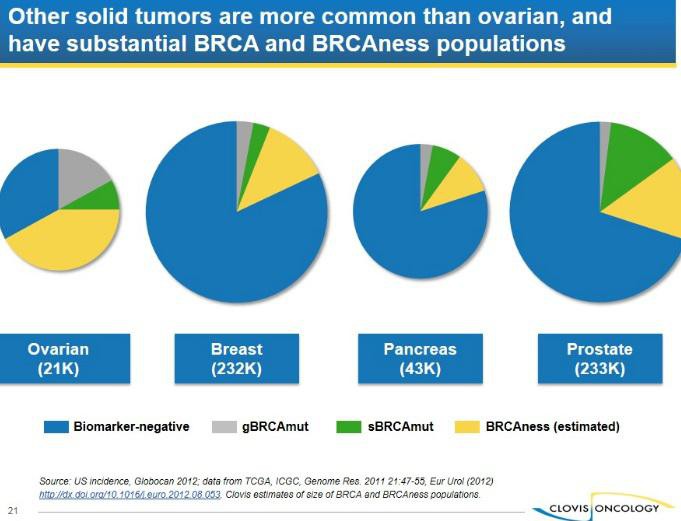
Für den FGFR/VEGFR-Hemmer Lucitanib könnten nächsten Jahr auch PIII-Studien starten, wenn die laufenden PIIs positiv verlaufen. Mit einem FGFR-Hemmer lassen sich theoretisch auch sehr viele Patienten behandeln... in 25% von Brustkrebs und 15% von Lungenkrebs fördert FGFR den Krebs.
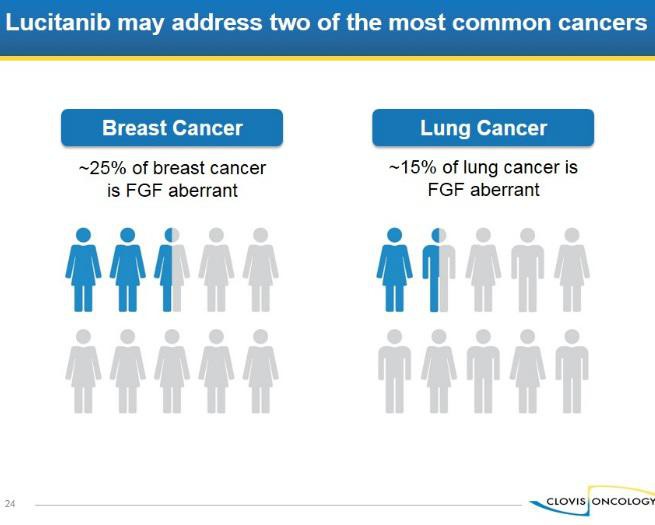
Zum Vergleich... hier sind relevante Targets in Lungenkrebs dargestellt. FGFR ist sogar mit 20% angegeben. Der Patienten-Anteil mit EGFR-Mutation ist auch nur 10-35% groß (in Asien mehr, in Europa/USA weniger) oder ALK 3-7%. Eine weitere wichtige Mutation ist KRAS mit 15-25%, gegen die u.a. ARRYs MEKs entwickelt werden.
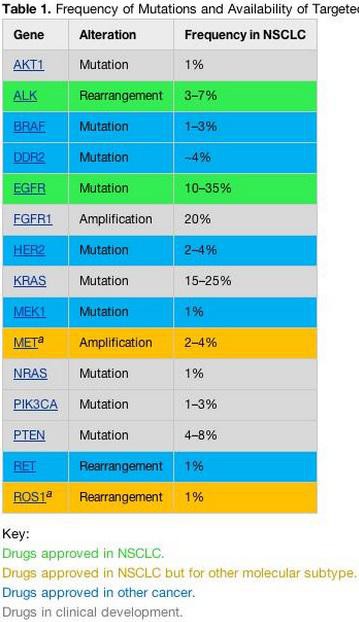


Gruß
ipollit
http://jpmorgan.metameetings.com/confbook/healthcare15/compa…
Im Sommer müssten die für eine Zulassung vom EGFR-Hemmer Roci entscheidenden Daten vorliegen, eine Zulassung soll Ende des Jahres möglich sein. Nächstes Jahr soll dann auch schon die Zulassung des PARP-Hemmers Ruca beantragt werden.

Roci ist zunächst erstmal als Hemmer von EGFR mit der Mutation T790m in Lungenkrebs gedacht. Diese Mutation entsteht bei der Behandlung mit einem herkömmlichen EGFR-Hemmer in etwa 50% und führt zur Resistenz gegen diese EGFR-Hemmer. D.h. rund 50% der 1st-line EGFR-Patienten sind irgendwann auf einen EGFR-T790m-Hemmer angewiesen.
Die EGFR-Hemmer der ersten Generation, z.B. Tarceva, haben den Nachteil, dass sie auch normales wt-EGFR hemmen, was zu Nebenwirkungen wie starkem Haut-Ausschlag führt. Roci bindet dagegen kaum an wt-EGFR.
CLVS hat mit AZN einen sehr starken Konkurrenten sowohl beim EGFR-Hemmer Roci als auch beim PARP-Hemmer Ruca. Im letzten Sommer ist der Kurs von CLVS stark gesunken, weil als Nebenwirkung von Roci ein temporärer Diabetes entsteht, während AZNs Kandidat AZD9291 diese Nebenwirkung nicht hat. Ursache hierfür ist ein Zerfallsprodukt (Metabolit), das beim Abbau des EGFR-Hemmers entsteht. Ein Metabolit von Roci ist ein IGF1R-/IR-Hemmer... IGF1R ist der Insulin-like-growth-factor-1-Rezeptor, IR der Insulin-Rezeptor. Ersterer steuert Wachstumsprozesse und soll auch an Krebs beteiligt sein, obwohl IGF1R-Hemmer&AKs in klinischen Studien bisher gescheitert sind. Über den IR-Rezeptor wirkt dagegen das Insulin... die Blockierung führt zu zeitweisem Diabetes. IR und IGF1R sind verwandt und kommunizieren miteinander, so dass normalerweise immer beide beeinflusst werden. Alle IGF1R-Hemmer zeigen diese Nebenwirkung.
Laut CLVS soll der Metabolit von Roci ein besonders starker Hemmer von IGF1R sein (stärker als die bekannten), aber weniger stark zu temporärem Diabetes führen. Angeblich ist keine Gabe von Insulin notwendig, sondern es reicht ein orales Standard-T2-Diabetes-Mittel, um dieser Nebenwirkung zu begegnen.
AZD9291 soll dagegen einen Metaboliten haben, der wt-EGFR und HER2 hemmt. Dadurch hat AZD9291 auch Hautausschlag (Rash) als Nebenwirkung (allerdings weniger als die bekannten EGFR-Hemmer), Roci dagegen nicht.
Im Sommer wurden nur die negativen Seiten der IGF1R-Hemmung durch Roci gesehen. Allerdings gibt es Untersuchungen, dass IGF1R auch ein wichtiger Resistenz-Mechanismus gegen EGFR-Hemmer ist, genauso wie die Mutation T790m. Schließlich gibt es auch viele Patienten (50%), die nicht T790m entwickeln und trotzdem resistent gegen EGFR-Hemmer werden... bei einem Teil soll IGF1R beteiligt sein (wenn ich es richtig verstanden habe, könnten es 30% sein). Demnach kann auch über IGF1R eine Resistenz gegen einen T790m-EGFR-Hemmer entstehen. D.h. theoretisch könnte aufgrund des IGF1R-Metaboliten Roci länger wirken oder auch bei Patienten ohne T790m helfen.
Letzteres scheint nach den bisherigen Daten der Fall zu sein. Auch nach aktualisierten Daten mit zusätzlichen Patienten liegt ein ORR von 50% (mit der höhreren Dosierung) bei T790m- über dem, was man eigentlich bei Patienten erwarten würde, bei denen zuvor die anderen EGFR-Hemmern nicht mehr wirken. Dadurch könnte sich Roci positiv von AZD9291 absetzen, das bei T790m- nicht wirken sollte. CLVS hat nun die Studien um T790m-neg-Arme ergänzt.

AZN's PARP-Hemmer Lynparza wurde vor Kurzem gegen mBRCA Eierstockkrebs zugelassen... dies ist unten der grüne Anteil. CLVS entwickelt Ruca zusätzlich noch gegen BRCAness (gelber Bereich)... dies sind nochmal deutlich mehr Patienten als mBRCA. Der Marker BRCAess wird speziell für CLVS anhand von einem Test von FMI ermittelt.

Neben Eierstock-Krebs gibt es auch in anderen Krebsarten die BRCA-Mutation und BRCAness... es könnten in Zukunft also deutlich mehr Patienten von Ruca profitieren, wobei der gelbe Bereich speziell von CLVS und FMI ermittelt wird. P2-Studien sollen dabei von Sponsoren durchgeführt werden und erst wenn deren Ergebnisse positiv sind, führt CLVS die Zulassungsstudien durch.

Für den FGFR/VEGFR-Hemmer Lucitanib könnten nächsten Jahr auch PIII-Studien starten, wenn die laufenden PIIs positiv verlaufen. Mit einem FGFR-Hemmer lassen sich theoretisch auch sehr viele Patienten behandeln... in 25% von Brustkrebs und 15% von Lungenkrebs fördert FGFR den Krebs.

Zum Vergleich... hier sind relevante Targets in Lungenkrebs dargestellt. FGFR ist sogar mit 20% angegeben. Der Patienten-Anteil mit EGFR-Mutation ist auch nur 10-35% groß (in Asien mehr, in Europa/USA weniger) oder ALK 3-7%. Eine weitere wichtige Mutation ist KRAS mit 15-25%, gegen die u.a. ARRYs MEKs entwickelt werden.


Gruß
ipollit
Antwort auf Beitrag Nr.: 48.812.948 von ipollit am 18.01.15 18:50:25MDVN
ergänzend noch ein Analysten-Kommentar...

Gruß
ipollit
ergänzend noch ein Analysten-Kommentar...

Gruß
ipollit
Antwort auf Beitrag Nr.: 48.813.890 von ipollit am 18.01.15 21:44:53Hallo ipollit,
mal wieder tolle Zusammenfassungen/Erklärungen von dir!
Ich finde CLVS steht jetzt schon richtig gut da. Die Umsatzmöglichkeiten haben sich doch sowohl für Ruca als auch für Roci deutlich vergrößert. Zudem kristallisiert sich immer mehr heraus, dass sich Roci von AZD9291 eben unterscheidet. So wie ich es auf der JPM verstanden habe, sind zudem die Tests natürlich nicht zu 100% richtig (in Bezug auf T790m+/-). Wenn das wirklich eine Rolle spielt ist da ein weiteres Argument für Roci, da es bei T790m- eben besser funktioniert.
CLVS könnte zudem Ende des Jahres nochmal viel besser und Mitte nächsten Jahres viel viel besser darstehen!
NASH könnte ein großes Thema in 2015 werden. Auch ZFGN will 2015 wohl einen Kandidaten in die Klinik bringen, der auf dem gleichen Ansatz wie B. beruht. Klingt für mich erstmal plausibel, da B. ja direkt in den Fettstoffwechsel eingreift. Zudem könnte ein Vorteil sein, dass sich der Ansatz von denen von ICPT, GILD, ENTA etc. unterscheidet. Man wird sehen...
MDVN habe ich auf meiner engeren Kaufliste (würde ich PCYC vorziehen). Ich finde die Bewertung noch nicht zu hoch, zumal ja noch Wachstumspotenziale da sind.
SG kmastra
mal wieder tolle Zusammenfassungen/Erklärungen von dir!
Ich finde CLVS steht jetzt schon richtig gut da. Die Umsatzmöglichkeiten haben sich doch sowohl für Ruca als auch für Roci deutlich vergrößert. Zudem kristallisiert sich immer mehr heraus, dass sich Roci von AZD9291 eben unterscheidet. So wie ich es auf der JPM verstanden habe, sind zudem die Tests natürlich nicht zu 100% richtig (in Bezug auf T790m+/-). Wenn das wirklich eine Rolle spielt ist da ein weiteres Argument für Roci, da es bei T790m- eben besser funktioniert.
CLVS könnte zudem Ende des Jahres nochmal viel besser und Mitte nächsten Jahres viel viel besser darstehen!
NASH könnte ein großes Thema in 2015 werden. Auch ZFGN will 2015 wohl einen Kandidaten in die Klinik bringen, der auf dem gleichen Ansatz wie B. beruht. Klingt für mich erstmal plausibel, da B. ja direkt in den Fettstoffwechsel eingreift. Zudem könnte ein Vorteil sein, dass sich der Ansatz von denen von ICPT, GILD, ENTA etc. unterscheidet. Man wird sehen...
MDVN habe ich auf meiner engeren Kaufliste (würde ich PCYC vorziehen). Ich finde die Bewertung noch nicht zu hoch, zumal ja noch Wachstumspotenziale da sind.
SG kmastra
Antwort auf Beitrag Nr.: 48.746.951 von ipollit am 11.01.15 15:01:51INFI
Für den pi3k-delta/gamma-Hemmer Duvelisib könnten im zweiten Halbjahr erste Zulassungsdaten der PII in iNHL kommen. Im Erfolgsfall dürfte INFI die vorzeitige Zulassung beantragen.
Die Indikation iNHL hat Priorität und das größte Potential, in CLL hat PCYCs Imbruvica die Nase deutlich vorne. Die PIII in CLL soll dieses Jahr alle Patienten aufgenommen haben (was glaube ich ganz gut wäre, da manche deutliche Verzögerungen aufgrund der Imbruvica-Zulassung erwartet haben)... theoretisch könnte die PIII auch vorzeitig nach Auswertung von Zwischenanalysen abgebrochen werden.

Laut INFI hat pi3k-delta im Wesentlichen einen direkten Einfluss auf die kranken B-Zellen... dies zeigt sich auch in der starken Wirkung von pi3k-delta-Hemmern auf Blutkrebs. Pi3k-gamma wirkt dagegen mehr auf Zellen der Umgebung wie TAMs, die die kranke B-Zelle unterstützen... dadurch sollen delta + gamma Hemmer noch stärker die kranken B-Zellen absterben lassen.
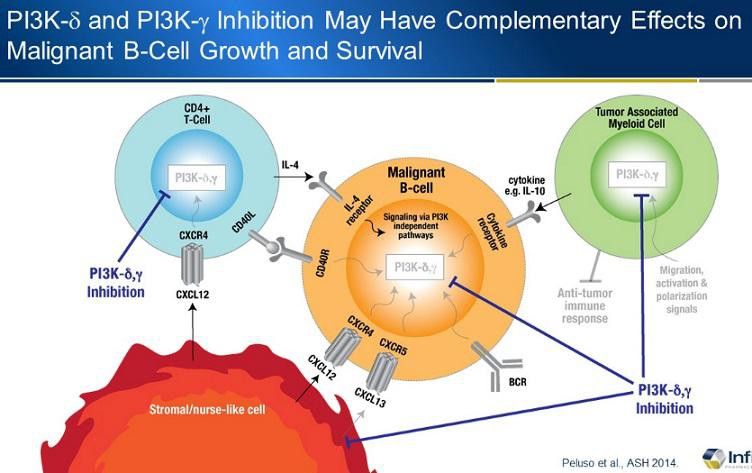
In iNHL möchte man mit Duvelisib zur besten Standard-Therapie werden. Nach einer eventuellen vorzeitigen Zulassung (Daten 2H15) wird versucht mit der Duvelisib + Rituxan PIII die volle Zulassung in 2+ line zu erreichen. Die 1st-line Entwicklung soll dann in der Kombi mit Rituxan oder der neueren CD20-Therapie Gazyva erfolgen. Langfristig ist die Kombi Duvelisib + Venetoclax (BCL2-Hemmer ABT-199) als potentiell beste Therapie geplant... Duvelisib hat eine starke Wirkung auf den Krebs in den Lymphknoten, Venetoclax auf den Bereich außerhalb.
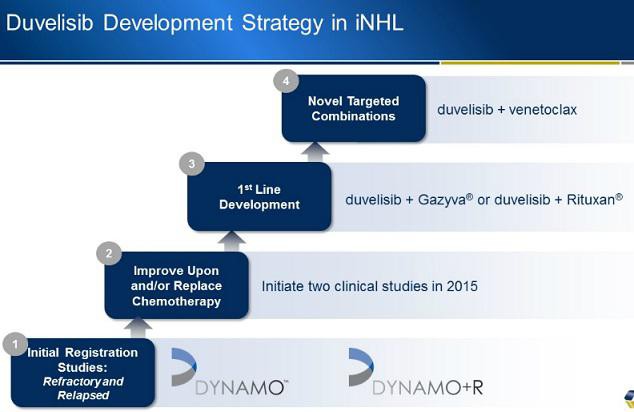
In CLL überlässt man erstmal Imbruvica die Spitze... entwickelt werden soll Duvelisib als beste Therapie gegen CLL nach einer Imbruvica-Behandlung. Die Kombi Duvelisib + Venetoclax könnte langfristig aber auch ein starker Konkurrent zu Imbruvica werden.
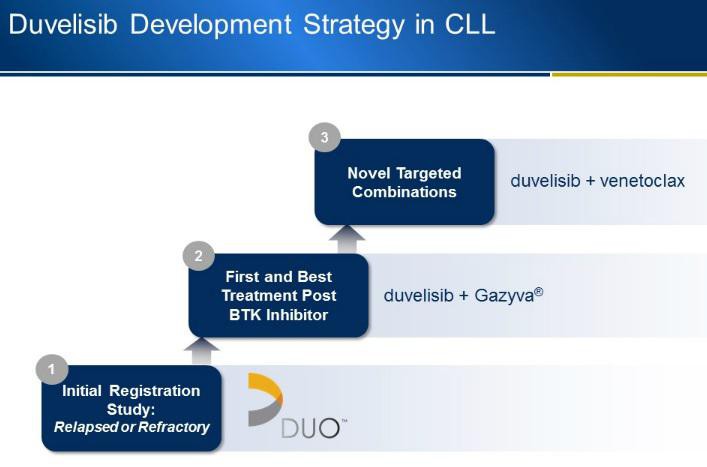
Wenn Imbruvica bei CLL nicht mehr wirkt, ist der Krebs meist in einem sehr agressivem Stadium. In den laufenden Studien gibt es bereits einige wenige Patienten, die bereits mit Imbruvica behandelt worden sind... dort scheint Duvelisib noch zu wirken.
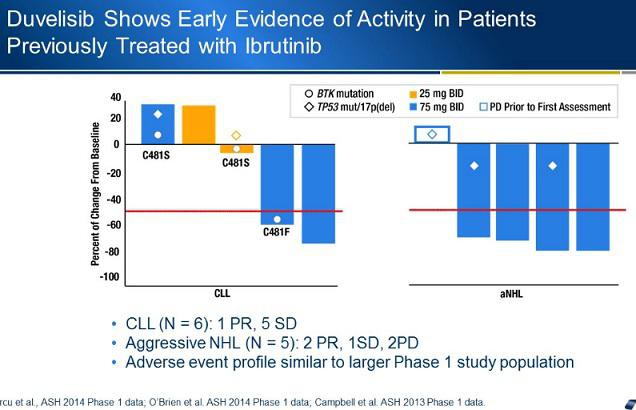
Der Deal mit ABBV sieht ganz gut aus... 50:50 in den USA und ex-US 23,5% bis 30,5% Royalties. Dafür muss INFI allerdings auch einen größeren Teil der Entwicklung zahlen... das Geld dafür erhält INFI aber u.a. bei Erreichen von Meilensteinen.

Interessant für INFI sind auch T-Zell Blutkrebs-Indikationen wie CTCL oder PTCL... Duvelisib wirkt hier wohl wegen pi3k-gamma, während hier Imbruvica oder pi3k-delta-Hemmer bisher keine Wirkung gezeigt haben. Allerdings sind es deutlich kleinere Indikationen als z.B. CLL.
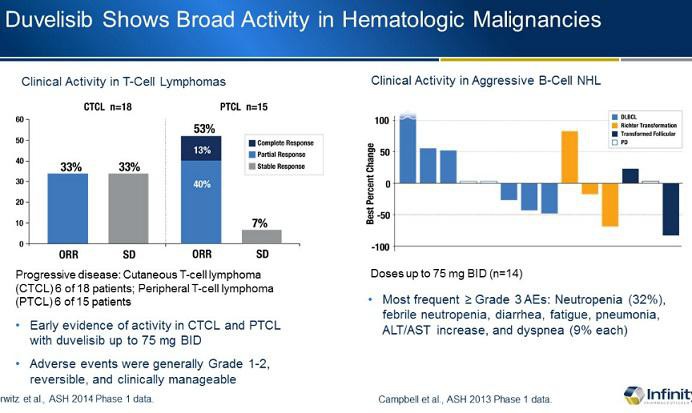
Vergleich von iNHL-Studien inkl. Duvelisib (IPI-145), Imbruvica (Ibrutinib), Zydelig (Idelalisib), Venetoclax (ABT-199) und Gazyva (GA101)
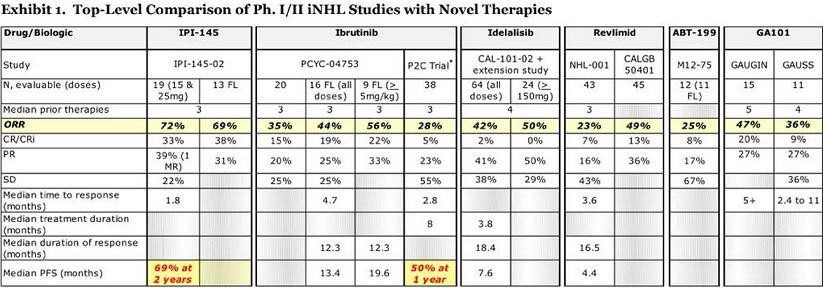
Ansatz für Kombi von pi3k (z.B. Duvelisib) und BCL2 (z.B. Venetoclax)
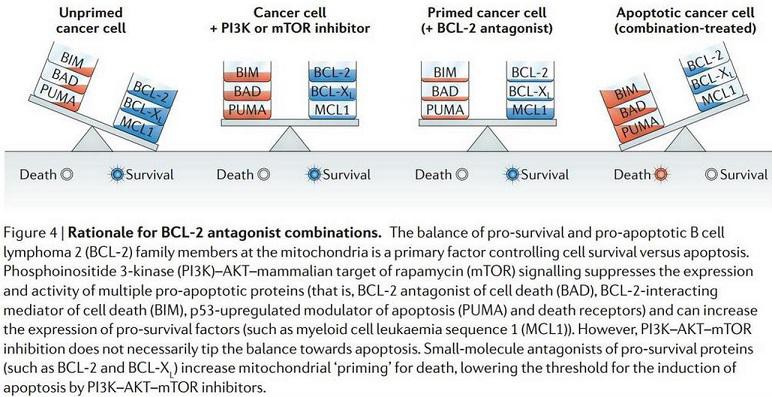


Gruß
ipollit
Für den pi3k-delta/gamma-Hemmer Duvelisib könnten im zweiten Halbjahr erste Zulassungsdaten der PII in iNHL kommen. Im Erfolgsfall dürfte INFI die vorzeitige Zulassung beantragen.
Die Indikation iNHL hat Priorität und das größte Potential, in CLL hat PCYCs Imbruvica die Nase deutlich vorne. Die PIII in CLL soll dieses Jahr alle Patienten aufgenommen haben (was glaube ich ganz gut wäre, da manche deutliche Verzögerungen aufgrund der Imbruvica-Zulassung erwartet haben)... theoretisch könnte die PIII auch vorzeitig nach Auswertung von Zwischenanalysen abgebrochen werden.

Laut INFI hat pi3k-delta im Wesentlichen einen direkten Einfluss auf die kranken B-Zellen... dies zeigt sich auch in der starken Wirkung von pi3k-delta-Hemmern auf Blutkrebs. Pi3k-gamma wirkt dagegen mehr auf Zellen der Umgebung wie TAMs, die die kranke B-Zelle unterstützen... dadurch sollen delta + gamma Hemmer noch stärker die kranken B-Zellen absterben lassen.

In iNHL möchte man mit Duvelisib zur besten Standard-Therapie werden. Nach einer eventuellen vorzeitigen Zulassung (Daten 2H15) wird versucht mit der Duvelisib + Rituxan PIII die volle Zulassung in 2+ line zu erreichen. Die 1st-line Entwicklung soll dann in der Kombi mit Rituxan oder der neueren CD20-Therapie Gazyva erfolgen. Langfristig ist die Kombi Duvelisib + Venetoclax (BCL2-Hemmer ABT-199) als potentiell beste Therapie geplant... Duvelisib hat eine starke Wirkung auf den Krebs in den Lymphknoten, Venetoclax auf den Bereich außerhalb.

In CLL überlässt man erstmal Imbruvica die Spitze... entwickelt werden soll Duvelisib als beste Therapie gegen CLL nach einer Imbruvica-Behandlung. Die Kombi Duvelisib + Venetoclax könnte langfristig aber auch ein starker Konkurrent zu Imbruvica werden.

Wenn Imbruvica bei CLL nicht mehr wirkt, ist der Krebs meist in einem sehr agressivem Stadium. In den laufenden Studien gibt es bereits einige wenige Patienten, die bereits mit Imbruvica behandelt worden sind... dort scheint Duvelisib noch zu wirken.

Der Deal mit ABBV sieht ganz gut aus... 50:50 in den USA und ex-US 23,5% bis 30,5% Royalties. Dafür muss INFI allerdings auch einen größeren Teil der Entwicklung zahlen... das Geld dafür erhält INFI aber u.a. bei Erreichen von Meilensteinen.

Interessant für INFI sind auch T-Zell Blutkrebs-Indikationen wie CTCL oder PTCL... Duvelisib wirkt hier wohl wegen pi3k-gamma, während hier Imbruvica oder pi3k-delta-Hemmer bisher keine Wirkung gezeigt haben. Allerdings sind es deutlich kleinere Indikationen als z.B. CLL.

Vergleich von iNHL-Studien inkl. Duvelisib (IPI-145), Imbruvica (Ibrutinib), Zydelig (Idelalisib), Venetoclax (ABT-199) und Gazyva (GA101)

Ansatz für Kombi von pi3k (z.B. Duvelisib) und BCL2 (z.B. Venetoclax)


Gruß
ipollit
Antwort auf Beitrag Nr.: 48.832.505 von ipollit am 20.01.15 23:28:39He ipollit
Danke für Deine unermüdliche Arbeit hier. Sehr informativ!
Danke für Deine unermüdliche Arbeit hier. Sehr informativ!
Antwort auf Beitrag Nr.: 48.822.368 von ipollit am 19.01.15 22:12:14MDVN
Heute wurden die Ergebnisse der TERRAIN Studie (Xtandi vs. Casodex) veröffentlicht. Trotz beeindruckendem Vorteil im PFS (Median PFS was 15.7 months in the enzalutamide group compared to 5.8 months in the bicalutamide group)
wird die Aktie heute abgestraft, weil es im Xtandi Arm zu mehr schweren Nebenwirkungen kam (Serious adverse events were reported in 31.1% of enzalutamide-treated patients and 23.3% of bicalutamide-treated patients. Grade 3 or higher cardiac adverse events were reported in 5.5% of enzalutamide-treated patients versus 2.1% of bicalutamide-treated patients)
Jedoch waren die Patienten in der Xtandigruppe auch entsprechend länger behandelt (The median time on treatment in TERRAIN was 11.7 months in the enzalutamide group versus 5.8 months in the bicalutamide group.)
Es ist also zu vermuten, dass der negative Effekt bei den AEs dadurch zu erklären ist und nicht durch Xtandi selbst verursacht wurde.
http://www.marketwatch.com/story/enzalutamide-phase-2-terrai…
Ich habe mir heute eine erste Position gekauft, weil ich mir zur Zeit auch lieber größere Biotechs mit bereits am Markt befindlichen und wachsenden Medikamenten ins Depot lege.
Ein Analystenkommentar:

SG kmastra
Heute wurden die Ergebnisse der TERRAIN Studie (Xtandi vs. Casodex) veröffentlicht. Trotz beeindruckendem Vorteil im PFS (Median PFS was 15.7 months in the enzalutamide group compared to 5.8 months in the bicalutamide group)
wird die Aktie heute abgestraft, weil es im Xtandi Arm zu mehr schweren Nebenwirkungen kam (Serious adverse events were reported in 31.1% of enzalutamide-treated patients and 23.3% of bicalutamide-treated patients. Grade 3 or higher cardiac adverse events were reported in 5.5% of enzalutamide-treated patients versus 2.1% of bicalutamide-treated patients)
Jedoch waren die Patienten in der Xtandigruppe auch entsprechend länger behandelt (The median time on treatment in TERRAIN was 11.7 months in the enzalutamide group versus 5.8 months in the bicalutamide group.)
Es ist also zu vermuten, dass der negative Effekt bei den AEs dadurch zu erklären ist und nicht durch Xtandi selbst verursacht wurde.
http://www.marketwatch.com/story/enzalutamide-phase-2-terrai…
Ich habe mir heute eine erste Position gekauft, weil ich mir zur Zeit auch lieber größere Biotechs mit bereits am Markt befindlichen und wachsenden Medikamenten ins Depot lege.
Ein Analystenkommentar:

SG kmastra
Antwort auf Beitrag Nr.: 48.833.360 von straumen am 21.01.15 08:03:39hi ipollit,
mir wird ganz schwindlig, wenn ich all deine Recherchen mitverfolge...und je mehr ich mich damit beschäftige, umso mehr Fragen tauchen auf.
Ich würde gerne in die eine oder andere Firma investieren - allein mir fehlt echt die Übersicht.
Solltest du mal Zeit haben...welche würdest du als besonders hoffnungsvoll in kommenden Jahr erachten ? sagen wir mal 3 - 4 Vorschläge ?
Dieselbe Frage stell ich gerne auch an die anderen user hier.
msfg und vielen dank im voraus
skipper
mir wird ganz schwindlig, wenn ich all deine Recherchen mitverfolge...und je mehr ich mich damit beschäftige, umso mehr Fragen tauchen auf.
Ich würde gerne in die eine oder andere Firma investieren - allein mir fehlt echt die Übersicht.
Solltest du mal Zeit haben...welche würdest du als besonders hoffnungsvoll in kommenden Jahr erachten ? sagen wir mal 3 - 4 Vorschläge ?
Dieselbe Frage stell ich gerne auch an die anderen user hier.
msfg und vielen dank im voraus
skipper
Antwort auf Beitrag Nr.: 48.857.699 von skipper2004 am 22.01.15 21:48:34Hatte so vor ca. einem 3/4 Jahr einige "meine Favoriten" hier gepostet, die da wären (halte ich immer noch):
Flamel FLML (MK heute um 550 Mio $) hier vorgstellt
Cardiome CRME (MK um 175 Mio $), ebenfalls hier vorgestellt
Cytosorbents CTSO (MK um 190 Mio)
Catalyst CPRX (MK um 200 Mio)
Marina MRNA (MK < 20 Mio)
Als besonderns aussichtsreich (mit > 40% Depotanteil)erachte ich: CTSO, Kurs aktuell: um 8,30. Traue dem Wert sich ver-10 bis zu ver-50 zufachen!
--> Sepsis-Therapie, kürzliche Kooperaton mit Fresenius!
www.cytosorbents.com
Grüsse an Euch Alle und auch von mir wieder eine SUPER-Vielen Dank für Eure Mühen (die DREI gemeint),
Gruss,
s.
Flamel FLML (MK heute um 550 Mio $) hier vorgstellt
Cardiome CRME (MK um 175 Mio $), ebenfalls hier vorgestellt
Cytosorbents CTSO (MK um 190 Mio)
Catalyst CPRX (MK um 200 Mio)
Marina MRNA (MK < 20 Mio)
Als besonderns aussichtsreich (mit > 40% Depotanteil)erachte ich: CTSO, Kurs aktuell: um 8,30. Traue dem Wert sich ver-10 bis zu ver-50 zufachen!
--> Sepsis-Therapie, kürzliche Kooperaton mit Fresenius!
www.cytosorbents.com
Grüsse an Euch Alle und auch von mir wieder eine SUPER-Vielen Dank für Eure Mühen (die DREI gemeint),
Gruss,
s.
Antwort auf Beitrag Nr.: 48.858.053 von sufenta am 22.01.15 22:13:09vielen dank für die prompte Antwort 
mfg
skipper

mfg
skipper
ARRY:
Gerade erst aus dem Urlaub zurück und schon überrascht Array mit folgender Nachricht:
Array Announces Agreement To Acquire ENCORAFENIB (LGX818)
- Array to receive global rights from Novartis to innovative BRAF inhibitor -
Und das so wie ich das lese quasi geschenkt!!!
Weil - vermute ich mal...: In order to address competition concerns raised by the European Commission, Array has agreed to obtain an experienced partner for global development and European commercialization of both binimetinib and encorafenib. The European Commission is expected to issue a decision regarding the Novartis-GSK transaction on January 28, 2015.
Ich find das ist ein Oberknaller! Bisher vorbörsliche Reaktion lustigerweise bei Null.
Gerade erst aus dem Urlaub zurück und schon überrascht Array mit folgender Nachricht:
Array Announces Agreement To Acquire ENCORAFENIB (LGX818)
- Array to receive global rights from Novartis to innovative BRAF inhibitor -
Und das so wie ich das lese quasi geschenkt!!!
Weil - vermute ich mal...: In order to address competition concerns raised by the European Commission, Array has agreed to obtain an experienced partner for global development and European commercialization of both binimetinib and encorafenib. The European Commission is expected to issue a decision regarding the Novartis-GSK transaction on January 28, 2015.
Ich find das ist ein Oberknaller! Bisher vorbörsliche Reaktion lustigerweise bei Null.
Antwort auf Beitrag Nr.: 48.865.136 von SLGramann am 23.01.15 14:28:16Die Deal-Konditionen für Binimetinib und LGX818 sind unfassbar gut. Ihr werdet es ja schon gelesen haben.
Erklärbar ist das für mich alles nur mit dem offensichtlichen Druck der europäischen Regulierungs- bzw. Kartellbehörde. Der Deal zwischen GSK und Novartis scheint auf ernsthafte Bedenken zu treffen, so dass Novartis bittere Kröten schlucken muss, um das durchzubekommen.
Array steht jetzt mit einer eigenen PIII-Pipeline da, die hochattraktiv und quasi "wie vom Himmel gefallen" ist.
Rückblickend scheint der Novartis/GSK ein unglaubliches Geschenk für Array zu sein.
Nur der Markt versteht bisher so gut wie nichts.
Dass Array für (deutlich) weniger als eine Milliarde gehandelt wird, ist ein Witz!
Erklärbar ist das für mich alles nur mit dem offensichtlichen Druck der europäischen Regulierungs- bzw. Kartellbehörde. Der Deal zwischen GSK und Novartis scheint auf ernsthafte Bedenken zu treffen, so dass Novartis bittere Kröten schlucken muss, um das durchzubekommen.
Array steht jetzt mit einer eigenen PIII-Pipeline da, die hochattraktiv und quasi "wie vom Himmel gefallen" ist.
Rückblickend scheint der Novartis/GSK ein unglaubliches Geschenk für Array zu sein.
Nur der Markt versteht bisher so gut wie nichts.
Dass Array für (deutlich) weniger als eine Milliarde gehandelt wird, ist ein Witz!
Antwort auf Beitrag Nr.: 48.865.136 von SLGramann am 23.01.15 14:28:16Wow! Das muss ich auch erst mal so richtig verstehen.
Verstehe ich es richtig, dass ARRY quasi jetzt auch den Auftrag hat einen Partner für sowohl Enco als auch Bini zu suchen?
Wenn NOV nicht 2 Mek-I haben kann hatte ich schon drauf spekuliert, dass sie nicht auch 2 BRAF-I haben dürfen. In hatte aber eher damit gerechnet, dass NOV da jetzt einen Partner für sucht und findet. Aber so ist das ja für ARRY genial.
BTW: ARRY ist auch charttechnisch in einer interessanten Situation, weil sie direkt an einem Widerstand befindet. Bin gespannt was der Markt draus macht...

Verstehe ich es richtig, dass ARRY quasi jetzt auch den Auftrag hat einen Partner für sowohl Enco als auch Bini zu suchen?
Wenn NOV nicht 2 Mek-I haben kann hatte ich schon drauf spekuliert, dass sie nicht auch 2 BRAF-I haben dürfen. In hatte aber eher damit gerechnet, dass NOV da jetzt einen Partner für sucht und findet. Aber so ist das ja für ARRY genial.
BTW: ARRY ist auch charttechnisch in einer interessanten Situation, weil sie direkt an einem Widerstand befindet. Bin gespannt was der Markt draus macht...
Antwort auf Beitrag Nr.: 48.865.361 von SLGramann am 23.01.15 14:47:40Offensichtlich hält die Wettbewerbskomission ARRY ja nicht für einen wettbewerbsfähigen Konkurenten. So nach dem Motto: Gute Idee NOV (und wir können das auch nachvollziehen) , aber das ist nicht das was wir unter einem Wettbewerb verstehen!?
Fragen, die mir spontan zudem kommen:
Wie definiert sich ein "competitive Partner"?
Wie lange hat ARRY Zeit diesen zu finden?
Und was passiert dann aus Sicht von ARRY?
Ist die Eigenvermarktung in den USA somit vom Tisch?
Freue mich auf den CC!
Fragen, die mir spontan zudem kommen:
Wie definiert sich ein "competitive Partner"?
Wie lange hat ARRY Zeit diesen zu finden?
Und was passiert dann aus Sicht von ARRY?
Ist die Eigenvermarktung in den USA somit vom Tisch?
Freue mich auf den CC!
Antwort auf Beitrag Nr.: 48.865.736 von kmastra am 23.01.15 15:15:52"Offensichtlich hält die Wettbewerbskomission ARRY ja nicht für einen wettbewerbsfähigen Konkurenten."
Nein, zu recht nicht. Gebraucht wird etwas Großes mit richtig Vertriebspower, um der durch die GSK-Onkologiesparte gestärkten Novartis etwas entgegenzusetzen.
Ich gehe außerdem davon aus (vielleicht mal wieder zu optimistisch), dass man sich über diesen künftigen Partner bereits einige Gedanken gemacht hat und es diesbezüglich schon Gespräche gibt.
Die geplante künftige Struktur scheint mir so auszusehen, dass Array die US-Rechte von Binimetinib und Encorafenib behalten und die europäischen sowie die ROW-Rechte auslizensieren wird - natürlich gegen eine Beteiligung an den weiteren Entwicklungskosten, signifikante Royalties (vielleicht aber auch gegenseitige Royalties?) und Meilensteine. Die Meilensteine sollten dann einen großen Teil der bei Array verbleibenden Entwicklungskosten wieder einspielen.
Die Frage ist nun also, wer dieser europäische Partner werden könnte. Wer könnte Interesse daran haben, einen MEK und einen BRAF-Inhibitor vor allem für Europa + ROW zu kaufen?
In jedem Falle hat sich die Position Arrays sehr deutlich verbessert, weil man nun ein MEK/BRAF-Paket aus einer Hand anbieten kann.
Nein, zu recht nicht. Gebraucht wird etwas Großes mit richtig Vertriebspower, um der durch die GSK-Onkologiesparte gestärkten Novartis etwas entgegenzusetzen.
Ich gehe außerdem davon aus (vielleicht mal wieder zu optimistisch), dass man sich über diesen künftigen Partner bereits einige Gedanken gemacht hat und es diesbezüglich schon Gespräche gibt.
Die geplante künftige Struktur scheint mir so auszusehen, dass Array die US-Rechte von Binimetinib und Encorafenib behalten und die europäischen sowie die ROW-Rechte auslizensieren wird - natürlich gegen eine Beteiligung an den weiteren Entwicklungskosten, signifikante Royalties (vielleicht aber auch gegenseitige Royalties?) und Meilensteine. Die Meilensteine sollten dann einen großen Teil der bei Array verbleibenden Entwicklungskosten wieder einspielen.
Die Frage ist nun also, wer dieser europäische Partner werden könnte. Wer könnte Interesse daran haben, einen MEK und einen BRAF-Inhibitor vor allem für Europa + ROW zu kaufen?
In jedem Falle hat sich die Position Arrays sehr deutlich verbessert, weil man nun ein MEK/BRAF-Paket aus einer Hand anbieten kann.
Antwort auf Beitrag Nr.: 48.870.470 von SLGramann am 23.01.15 21:48:10Spontan würde mir Bristol-Meyer einfallen. Die haben in dem Bereich ein Loch in der Pipeline und wenn es sich bestätigen würde, dass man PD1 und MEK kombinieren kann, dann wäre dieses Loch doppelt ärgerlich.
Allerdings würden die sicher nicht auf die US-Rechte verzichten. Vielleicht bin ich da gerade auch mal wieder zu optimistisch, was die US-Rechte für Array angeht. Vielleicht wäre aber auch eine 50:50-Verpartnerung der US-Rechte + Auslizensierung Europa+ROW denkbar.
Amgen wäre vielleicht auch ein Kandidat. Oder will vielleicht Gilead mal etwas diversifizieren?
Es gibt sicher viele Optionen für Array.
Na ja, genug spekuliert für heute.
Allerdings würden die sicher nicht auf die US-Rechte verzichten. Vielleicht bin ich da gerade auch mal wieder zu optimistisch, was die US-Rechte für Array angeht. Vielleicht wäre aber auch eine 50:50-Verpartnerung der US-Rechte + Auslizensierung Europa+ROW denkbar.
Amgen wäre vielleicht auch ein Kandidat. Oder will vielleicht Gilead mal etwas diversifizieren?
Es gibt sicher viele Optionen für Array.
Na ja, genug spekuliert für heute.
Antwort auf Beitrag Nr.: 48.865.736 von kmastra am 23.01.15 15:15:52Der Link zur Präsentation:
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
Seite 7 sieht so aus, dass der commercialisation partner (nur?) für Europa gesucht wird. Das macht Sinn, weil der ganze Aufstand ja wohl nur auf Veranlassung der europäischen Kartellbehörde gemacht wird. Ob das so umsetzbar ist, ist natürlich noch eine andere Frage.
(Witzbolde bei Twitter haben ja schon GSK als neuen Partner für Array vorgeschlagen...).
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
Seite 7 sieht so aus, dass der commercialisation partner (nur?) für Europa gesucht wird. Das macht Sinn, weil der ganze Aufstand ja wohl nur auf Veranlassung der europäischen Kartellbehörde gemacht wird. Ob das so umsetzbar ist, ist natürlich noch eine andere Frage.
(Witzbolde bei Twitter haben ja schon GSK als neuen Partner für Array vorgeschlagen...).
ARRY
dass ARRY nun auch noch den BRAF-Hemmer LGX818 von Novartis erhält, finde ich nach den bisherigen Aussagen von ARRY schon etwas überraschend. LGX818 musste abgegeben werden, das ist klar, aber ich hatte es so verstanden, dass Novartis bei einem Verauf von LGX818 an einen Dritten auch die Zahlungsverpflichtungen z.B. mit der Binimetinib LGX818 Kombi an den diesen hätte übertragen können. Nun muss anscheinend NVS auch noch für LGX818 zahlen.
Wieviel ist LGX818 wert? Binimetinib würde ich als MEK-Hemmer höher einschätzen. LGX818 ist ein weiterer BRAF-Hemmer hinter Roche's Zelboraf und GSK/NVSs Tafinlar, die beide bereits zugelassen sind. Ursprünglich wurde einem BRAF-Hemmer wie Zelboraf ein Potential von deutlich über 1 Mrd USD zugetraut. Ich weiß nicht, ob das nun auch noch so ist bei der gestiegenen Konkurrenz und der Erfahrung, dass sich gegen BRAF-Hemmer alleine auch schnell Resistenzen bilden können.
BRAF-Hemmer kommen bei BRAF-Mutationen zum Einsatz, die in mehreren Krebsarten vorkommen... unten sind das die grünen Bereiche.
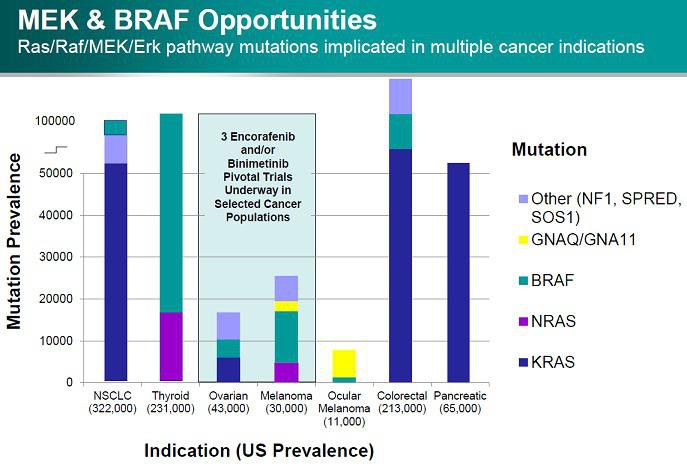
Die bisher mit Abstand wichtigste Anwendung ist Melanoma (Schwarzer Hautkrebs)... die übrigens bisher auch die erste/wichtigste Indikation von PD1&Co ist. Wie unten zu sehen hat ein großer Teil der 30.000 US-Patienten diese Mutation (im speziellen ist das meistens die V600e BRAF-Mutation). Daher hat man den ersten BRAF-Hemmer Zelboraf wie auch alle weiterern zuerst in dieser Indikation entwickelt. Die ersten Ergebnisse sahen sehr gut aus... BRAF-Hemmer führten erstmal zu einem starken Rückgang des Krebs (falls eine BRAF-Mutation vorlag). Aber leider gab es oft einen unerwarteten Rückfall... nach einiger Zeit schien der BRAF-Hemmer nicht mehr zu wirken, der Krebs kam wieder ungehindert zurück.
Was das für Patienten bedeutet, zeigen folgende Bilder sehr eindrücklich... (ACHTUNG: die Bilder sind meiner Meinung nach nicht angenehm zu sehen... Krebs ist eine schlimme Erkrankung!) http://primepresentations.s3.amazonaws.com/2012/paris_melano… Dies ist ein Melanoma-Patient vor und mit einer BRAF-Behandlung (Zelboraf)... es sieht fast wie ein Wunder aus, was der BRAF-Hemmer bewirkt. Umso erschreckender ist dann das dritte Bild, das wieder dem ersten zu gleichen scheint trotz Einnahme des BRAF-Hemmers. Mit der Zeit hat man u.a. bei Roche erkannt, dass der Krebs die BRAF-Hemmung umgehen kann. Es handelt sich um einen dauerhaft aktiven RAS/RAF/MEK/ERK-Signalweg, der den Krebs wachsen lässt. Unter der Hemmung von BRAF kommt es bei Melanoma oft zu einer Umgehung direkt auf MEK. D.h., dass durch BRAF + MEK Hemmung die Wirkung deutlich länger anhält.
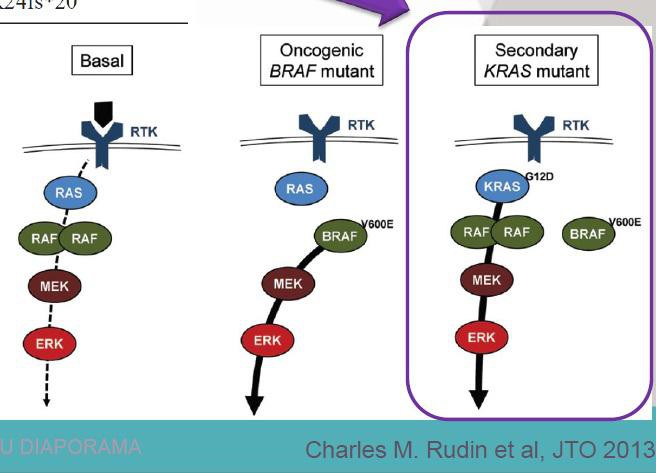
Zuerst besteht aufgrund der V600E BRAF-Mutation ein ständiges Wachstumssignal, dass man mit einem BRAF-Hemmer unterbinden kann. Danach kommt es aber zu weiteren Mutationen (z.B. KRAS), die den Weg wieder aktiveren. Der MEK-Hemmer setzt tiefer an... auch da kann es wieder zu Mutationen kommen. Eine weitere Möglichkeit ist z.B. ein ERK-Hemmer wie ARRY/Roches GDC-0994.
BRAF-Mutationen gibt es aber noch in zahlreichen weiteren Krebsarten, wobei sie dort deutlich seltener sind, als in Melanoma. Wie oben zu sehen ist, ist zwar in Thyroid-Krebs die BRAF-Mutation sehr verbreitet, doch wird dieser Krebs in der Regel durch eine Operation behandelt, so dass Hemmer&Co hier wenig benötigt werden. Daneben gibt es relativ viele Patienten mit BRAF-mutierten Darmkrebs.
Wenn ich es richtig verstehe, so ist BRAF-mut aber selbst auch wieder unterschiedlich. Zelboraf&Co sind zunächst V600E BRAF-Hemmer, da diese Mutation u.a. in Melanoma sehr verbreitet ist. Z.B. in Lungenkrebs (NSCLC) ist offensichtlich aber auch G469A BRAF relevant. Wie gut BRAF-Hemmer wie LGX818 in so Fällen wirken, ist mir nicht klar.
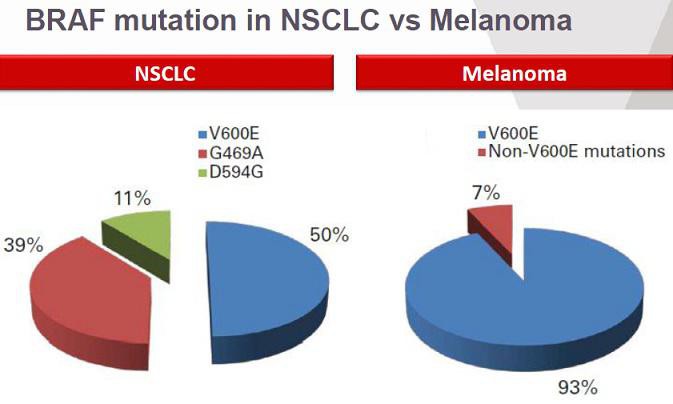
Außerdem sind Resistenz-Bildungen anscheinend unterschiedlich. EGFR scheint in Darmkrebs als Resistenz-Mechanismus relevant zu sein.
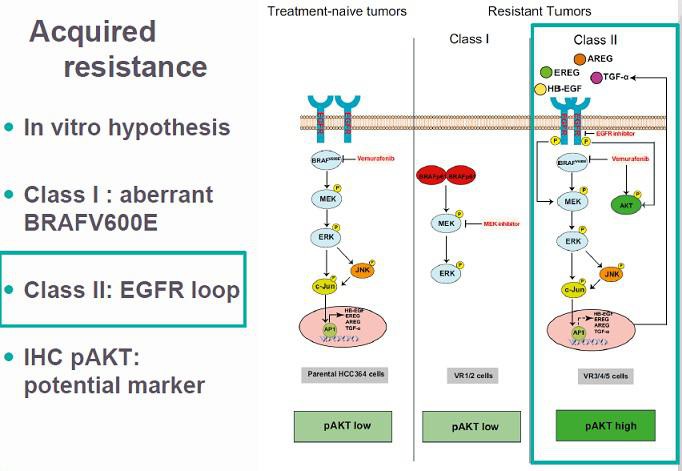
Daher kann in CRC eine BRAF + EGFR Kombi sinnvoll sein.
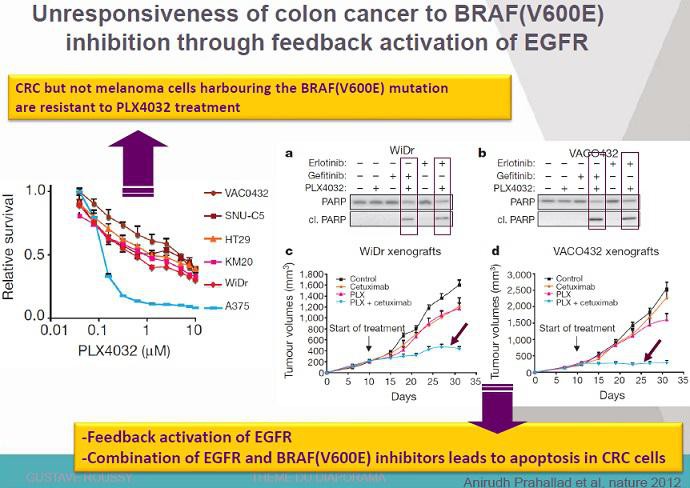
Die PI von LGX818 ("ENC") in Darmkrebs zusammen mit dem EGFR-AK Cetuximab ("CTX", Erbitux) oder dem pi3k-alpha Hemmer BYL719 ("ALP") entspricht dieser Theorie. Letzteres wirkt u.a. wohl auch auf AKT, das ebenfalls oben im Diagramm der Resistenz zu finden ist.

Ich meine ARRY hat auch Brustkrebs als eine interessante Indikation für BRAF-Hemmer genannt... es sind jeweils aber nur kleine Anteile von Patienten, die eine solche Mutation besitzen. In großen Indikationen mit vielen Patienten wie Brustkrebs sind aber auch ein paar Prozent viele Patienten.
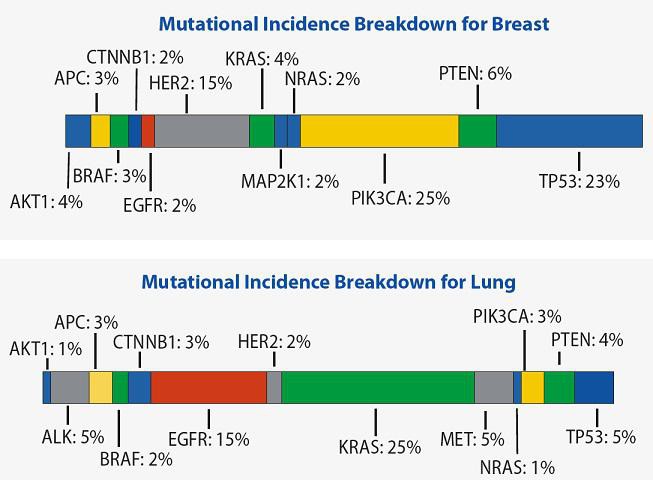
Vielleicht wäre ja die deutsche Merck ein möglicher Interessent für LGX818 und Binimetinib... sie haben bereits einen BRAF- und einen MEK-Hemmer in der Entwicklung, der aber anscheinend noch lange bis zum Markt brauchen würden. Mit Erbitux (Cetuximab) sind sie bereits in Darmkrebs etabliert und mit ihrem PD1-AK sollten sie auch in der Melanoma-Indikation vertreten sein.
Gruß
ipollit
dass ARRY nun auch noch den BRAF-Hemmer LGX818 von Novartis erhält, finde ich nach den bisherigen Aussagen von ARRY schon etwas überraschend. LGX818 musste abgegeben werden, das ist klar, aber ich hatte es so verstanden, dass Novartis bei einem Verauf von LGX818 an einen Dritten auch die Zahlungsverpflichtungen z.B. mit der Binimetinib LGX818 Kombi an den diesen hätte übertragen können. Nun muss anscheinend NVS auch noch für LGX818 zahlen.
Wieviel ist LGX818 wert? Binimetinib würde ich als MEK-Hemmer höher einschätzen. LGX818 ist ein weiterer BRAF-Hemmer hinter Roche's Zelboraf und GSK/NVSs Tafinlar, die beide bereits zugelassen sind. Ursprünglich wurde einem BRAF-Hemmer wie Zelboraf ein Potential von deutlich über 1 Mrd USD zugetraut. Ich weiß nicht, ob das nun auch noch so ist bei der gestiegenen Konkurrenz und der Erfahrung, dass sich gegen BRAF-Hemmer alleine auch schnell Resistenzen bilden können.
BRAF-Hemmer kommen bei BRAF-Mutationen zum Einsatz, die in mehreren Krebsarten vorkommen... unten sind das die grünen Bereiche.

Die bisher mit Abstand wichtigste Anwendung ist Melanoma (Schwarzer Hautkrebs)... die übrigens bisher auch die erste/wichtigste Indikation von PD1&Co ist. Wie unten zu sehen hat ein großer Teil der 30.000 US-Patienten diese Mutation (im speziellen ist das meistens die V600e BRAF-Mutation). Daher hat man den ersten BRAF-Hemmer Zelboraf wie auch alle weiterern zuerst in dieser Indikation entwickelt. Die ersten Ergebnisse sahen sehr gut aus... BRAF-Hemmer führten erstmal zu einem starken Rückgang des Krebs (falls eine BRAF-Mutation vorlag). Aber leider gab es oft einen unerwarteten Rückfall... nach einiger Zeit schien der BRAF-Hemmer nicht mehr zu wirken, der Krebs kam wieder ungehindert zurück.
Was das für Patienten bedeutet, zeigen folgende Bilder sehr eindrücklich... (ACHTUNG: die Bilder sind meiner Meinung nach nicht angenehm zu sehen... Krebs ist eine schlimme Erkrankung!) http://primepresentations.s3.amazonaws.com/2012/paris_melano… Dies ist ein Melanoma-Patient vor und mit einer BRAF-Behandlung (Zelboraf)... es sieht fast wie ein Wunder aus, was der BRAF-Hemmer bewirkt. Umso erschreckender ist dann das dritte Bild, das wieder dem ersten zu gleichen scheint trotz Einnahme des BRAF-Hemmers. Mit der Zeit hat man u.a. bei Roche erkannt, dass der Krebs die BRAF-Hemmung umgehen kann. Es handelt sich um einen dauerhaft aktiven RAS/RAF/MEK/ERK-Signalweg, der den Krebs wachsen lässt. Unter der Hemmung von BRAF kommt es bei Melanoma oft zu einer Umgehung direkt auf MEK. D.h., dass durch BRAF + MEK Hemmung die Wirkung deutlich länger anhält.

Zuerst besteht aufgrund der V600E BRAF-Mutation ein ständiges Wachstumssignal, dass man mit einem BRAF-Hemmer unterbinden kann. Danach kommt es aber zu weiteren Mutationen (z.B. KRAS), die den Weg wieder aktiveren. Der MEK-Hemmer setzt tiefer an... auch da kann es wieder zu Mutationen kommen. Eine weitere Möglichkeit ist z.B. ein ERK-Hemmer wie ARRY/Roches GDC-0994.
BRAF-Mutationen gibt es aber noch in zahlreichen weiteren Krebsarten, wobei sie dort deutlich seltener sind, als in Melanoma. Wie oben zu sehen ist, ist zwar in Thyroid-Krebs die BRAF-Mutation sehr verbreitet, doch wird dieser Krebs in der Regel durch eine Operation behandelt, so dass Hemmer&Co hier wenig benötigt werden. Daneben gibt es relativ viele Patienten mit BRAF-mutierten Darmkrebs.
Wenn ich es richtig verstehe, so ist BRAF-mut aber selbst auch wieder unterschiedlich. Zelboraf&Co sind zunächst V600E BRAF-Hemmer, da diese Mutation u.a. in Melanoma sehr verbreitet ist. Z.B. in Lungenkrebs (NSCLC) ist offensichtlich aber auch G469A BRAF relevant. Wie gut BRAF-Hemmer wie LGX818 in so Fällen wirken, ist mir nicht klar.

Außerdem sind Resistenz-Bildungen anscheinend unterschiedlich. EGFR scheint in Darmkrebs als Resistenz-Mechanismus relevant zu sein.

Daher kann in CRC eine BRAF + EGFR Kombi sinnvoll sein.

Die PI von LGX818 ("ENC") in Darmkrebs zusammen mit dem EGFR-AK Cetuximab ("CTX", Erbitux) oder dem pi3k-alpha Hemmer BYL719 ("ALP") entspricht dieser Theorie. Letzteres wirkt u.a. wohl auch auf AKT, das ebenfalls oben im Diagramm der Resistenz zu finden ist.

Ich meine ARRY hat auch Brustkrebs als eine interessante Indikation für BRAF-Hemmer genannt... es sind jeweils aber nur kleine Anteile von Patienten, die eine solche Mutation besitzen. In großen Indikationen mit vielen Patienten wie Brustkrebs sind aber auch ein paar Prozent viele Patienten.

Vielleicht wäre ja die deutsche Merck ein möglicher Interessent für LGX818 und Binimetinib... sie haben bereits einen BRAF- und einen MEK-Hemmer in der Entwicklung, der aber anscheinend noch lange bis zum Markt brauchen würden. Mit Erbitux (Cetuximab) sind sie bereits in Darmkrebs etabliert und mit ihrem PD1-AK sollten sie auch in der Melanoma-Indikation vertreten sein.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.857.699 von skipper2004 am 22.01.15 21:48:34Hallo Skipper,
3-4 hoffnungsvolle Biotechs? Sorry, ich tue mich schwer damit, dir jetzt konkret einige zu nennen, da ich wahrscheinlich eher daneben liege. Da ich selber nie weiß, welches Unternehmen Erfolg hat und welches sich als Flop erweist, habe ich selber ca. 30 Unternehmen in meinem Depot. Letztes Jahr hätte ich dir vielleicht EXEL als interessant genannt... dies war nach dem Fehlschlag von Carbo aber ein großer Flop mit -76%. In 2013 habe ich ARIA als sicher gesehen, da sie damals gerade das aussichtsreiche Iclusig gegen CML auf den Markt gebracht haben... kurze Zeit später hat die FDA Iclusig vom Markt genommen, da es unerwartete Nebenwirkungen zeigte. Egal wie gut etwas aussieht, es kann jederzeit anders kommen, als man denkt.
Wäre nicht auch ein Index-Fond wie der IBB auf den Nasdaq-Biotech-Index (NBI) interessant? Letztes Jahr war ich mit meinen 30 Werten ca. 10% schlechter, 2013 genau gleich und 2012 20% besser als der NBI. Oder wie wäre BB-Biotech? Damit lassen sich einzelne Flops vermeiden und das Risiko von Ausreißern senken.
Die Biotechs stehen nach den letzten sehr guten Jahren auch recht hoch... es könnte eine kleine Blase sein, die irgendwann auch mal wieder platzt... das ist auch ein Risiko. Letztes Jahr ging es im März schnell stark nach unten... nur die großen Biotechs konnten sich einigermaßen halten. Grundsätzlich sehe ich den Bereich aber positiv, da es meiner Meinung nach viele echte Innovationen gibt und nicht alles nur heiße Luft ist.
Hier gibt es mehrere, die sich theoretisch mit Biotechs auskennen: http://www.siliconinvestor.com/subject.aspx?subjectid=59557 bei den Depots geht es aber auch darum, im Jahr 2015 die beste Performance zu erzielen... das Risiko gehen die in ihrem echten Depot vielleicht nicht ein.
Depots... http://www.siliconinvestor.com/readmsg.aspx?msgid=29882715
Gewählte Werte nach Häufigkeit... http://www.siliconinvestor.com/readmsg.aspx?msgid=29882751
TRIL wurde am meisten genannt... beobachte ich auch: ein CD47 Konkurrent der noch recht günstig ist, bei dem aber auch als Trap statt AK Frage-Zeichen bestehen... kann sich im IO-Hype vervielfachen, aber auch in einem schlechten Biotech-Umfeld wieder deutlich fallen.
Gruß
ipollit
3-4 hoffnungsvolle Biotechs? Sorry, ich tue mich schwer damit, dir jetzt konkret einige zu nennen, da ich wahrscheinlich eher daneben liege. Da ich selber nie weiß, welches Unternehmen Erfolg hat und welches sich als Flop erweist, habe ich selber ca. 30 Unternehmen in meinem Depot. Letztes Jahr hätte ich dir vielleicht EXEL als interessant genannt... dies war nach dem Fehlschlag von Carbo aber ein großer Flop mit -76%. In 2013 habe ich ARIA als sicher gesehen, da sie damals gerade das aussichtsreiche Iclusig gegen CML auf den Markt gebracht haben... kurze Zeit später hat die FDA Iclusig vom Markt genommen, da es unerwartete Nebenwirkungen zeigte. Egal wie gut etwas aussieht, es kann jederzeit anders kommen, als man denkt.
Wäre nicht auch ein Index-Fond wie der IBB auf den Nasdaq-Biotech-Index (NBI) interessant? Letztes Jahr war ich mit meinen 30 Werten ca. 10% schlechter, 2013 genau gleich und 2012 20% besser als der NBI. Oder wie wäre BB-Biotech? Damit lassen sich einzelne Flops vermeiden und das Risiko von Ausreißern senken.
Die Biotechs stehen nach den letzten sehr guten Jahren auch recht hoch... es könnte eine kleine Blase sein, die irgendwann auch mal wieder platzt... das ist auch ein Risiko. Letztes Jahr ging es im März schnell stark nach unten... nur die großen Biotechs konnten sich einigermaßen halten. Grundsätzlich sehe ich den Bereich aber positiv, da es meiner Meinung nach viele echte Innovationen gibt und nicht alles nur heiße Luft ist.
Hier gibt es mehrere, die sich theoretisch mit Biotechs auskennen: http://www.siliconinvestor.com/subject.aspx?subjectid=59557 bei den Depots geht es aber auch darum, im Jahr 2015 die beste Performance zu erzielen... das Risiko gehen die in ihrem echten Depot vielleicht nicht ein.
Depots... http://www.siliconinvestor.com/readmsg.aspx?msgid=29882715
Gewählte Werte nach Häufigkeit... http://www.siliconinvestor.com/readmsg.aspx?msgid=29882751
TRIL wurde am meisten genannt... beobachte ich auch: ein CD47 Konkurrent der noch recht günstig ist, bei dem aber auch als Trap statt AK Frage-Zeichen bestehen... kann sich im IO-Hype vervielfachen, aber auch in einem schlechten Biotech-Umfeld wieder deutlich fallen.
Gruß
ipollit
KPTI
meine erste KPTI-Position habe ich weiter erhöht. Ich denke, dass der XPO1-Hemmer Selinexor eine Menge Potential hat, wenn er in der Weise funktioniert wie gedacht. Interessant finde ich es besonders, weil es ein recht grundsätzlicher Ansatz ist, der sich deutlich von anderen Therapien unterscheidet, wodurch er sich theoretisch sehr breit in vielen Krebsarten anwenden lässt und mit vielen anderen Therapien kombinierbar sein könnte. STML hat zuletzt auch einen XPO1-Hemmer einlizensiert.
Selinexor bezeichnet KPTI als "SINE" (Selective Inhibitor of Nuclear Export). Im folgenden Diagramm sind Krebs-Therapien in verschiedene Klassen eingeteilt. Dazu zählen Chemos, die schnell teilende Zellen beschädigen und damit abtöten (die meisten Krebszellen teilen sich schnell, u.U. aber keine Krebsstammzellen). Der Krebs kann resistent gegen die Chemo werden, indem er z.B. Transporter in der Zelle verstärkt, die die Chemo schnell wieder aus der Zelle pumpen können. Dann gibt es die Target-Therapien, die bestimmte fehlerhafte Signalwege unterdrücken... dazu zählen z.B. die TKIs wie MEK- oder BRAF-Hemmer. Der Krebs benötigt für sein starkes Wachstum sehr viele Nährstoffe und eine gute Blutversorgung... z.B. VEGF-Hemmer sollen den Krebs von der Versorgung abschneiden. Und es gibt Mittel, die sich darauf auswirken, ob ein Krebs Metastasen bildet, sich also unkontrolliert im Körper verteilt.
Selinexor betrifft nun zwei weitere Bereiche: in Krebszellen sind Mechanismen defekt, die normalerweise in beschädigten Zellen zum Zelltod führen. Die Krebszelle wird dadurch praktisch unsterblich. Ein konkretes Beispiel ist hier BCL2, das den Zelltod verhindern kann... BCL2-Hemmer wie ABT-199 (siehe INFI) zeigen sehr gute Ergebnisse. Desweiteren besitzen Zellen Mechanismen die das Verhalten steuern und kontrollieren, z.B. wann sich eine Zelle teilt, wie sie wächst usw. In Krebszellen sind auch diese defekt, so dass die Zelle sich völlig unnatürlich verhalten kann. Selinexor versucht diese beiden Mechanismen wieder herzustellen... quasi die Mechanismen, mit denen der Körper den Krebs normalerweise selber verhindert.
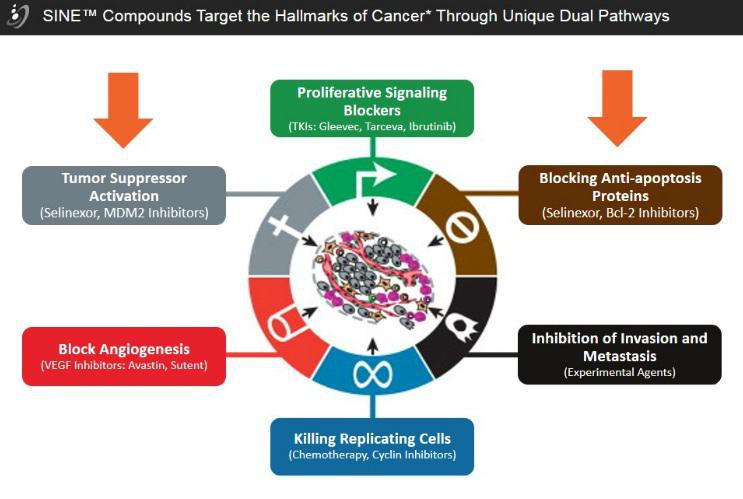
Dabei greift Selinexor nicht ein konkretes Target an, das den Zelltod oder die Zellentwicklung steuert, sondern das Transport-Protein XPO1, das im Zellkern arbeitet. Es gibt mehrere Transporter-Proteine, die z.B. Dinge aus dem Zellkern (der Zellkern enthält die DNA) in die Zelle oder aus der Zelle heraus transportieren. Dabei sind bestimmte Stoffe auf bestimmte Transporter beschränkt. XPO1 transportiert eine große Anzahl an Stoffen aus dem Zellkern, die normalerweise dort die Zellentwicklung steuern und überwachen sollen... wie z.B. p53: "Der humane Tumorsuppressor p53 reguliert als Transkriptionsfaktor nach DNA-Schädigung die Expression von Genen, die an der Kontrolle des Zellzyklus, an der Induktion der Apoptose (des programmierten Zelltods) oder an der DNA-Reparatur beteiligt sind. Aufgrund dieser Eigenschaft wird p53 in der Literatur als „Wächter des Genoms“ bezeichnet. Die besondere medizinische Bedeutung erklärt sich aus dem Befund, dass p53 in 50 % aller menschlichen Tumoren mutiert ist. Der Verlust der p53-Funktion spielt daher eine kritische Rolle bei der Entstehung von Krebs, ist jedoch nicht dessen ursächlicher Auslöser.". Dieser Transport ist ein normaler Vorgang, der auch in gesundern Zellen zu finden ist... Krebszellen steigern aber XPO1, um die kontrollierenden und den Krebs unterdrückenden Stoffe schnell aus dem Zellkern zu befördern, so dass sie in der Krebszelle nicht mehr richtig wirken.
Wird der Transporter nun blockiert, so können diese Stoffe nicht mehr aus dem Zellkern entweichen und regulieren die Zelle, prüfen die DNA, reparieren sie oder leiten einen Zelltod ein. Auf anderem Weg kann die Krebszelle die Stoffe nicht herausbefördern.
Zu den Stoffen gehört auch das elF4E-Protein. Soweit ich es verstehe, ist dieses Protein selber ein Transporter für bestimmte RNA-Stückchen. Solche RNA ist ein Schritt zur Produktion von Proteinen... RNA wird aus der DNA ausgelesen und danach werden die Proteine gebaut. Dies geschieht aber offensichtlich außerhalb des Zellkerns. Transportiert XPO1 elF4E mit der bestimmten RNA nicht aus dem Zellkern, so wird das Protein nicht hergestellt. Zu diesen Proteinen gehört u.a. BCL2 (das den Zelltod verhindert) und cMyc (siehe INCYs BET-Hemmer). Das heißt die Hemmung von XPO1 verringert indirekt auch die Produktion krebsfördernder Proteine.
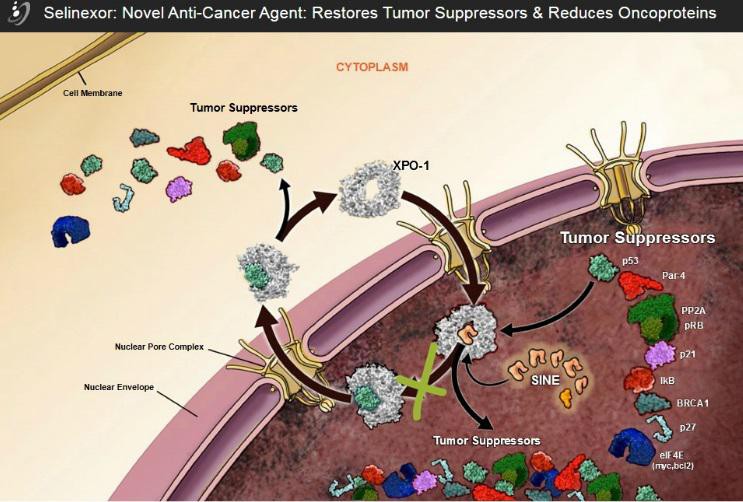
Es gab schonmal einen XPO1-Hemmer in der Entwicklung (nicht bei KPTI)... dieses war aber auch für gesunde Zellen giftig, wahrscheinlich, weil es dauerhaft an XPO1 gebunden hat. Selinexor bleibt aber nicht dauerhaft an XPO1 gebunden... nach mehreren Stunden löst es sich wieder. In dieser Zeit können die Kontroll-Stoffe im Zellkern wirken und die Produktion krebsfördernder Proteine wird gesenkt. Gesunde Zellen sollen dadurch keine Probleme bekommen, die Mechanismen finden dort ja keinen DNA-Schaden usw.. danach arbeiten die XPO1-Transporter wieder eine Zeit normal bis die nächste Dosis erfolgt.
Da es so ein fundamentaler Mechanismus ist, müsste Selinexor eigentlich bei fast allen Krebszellen etwas bewirken. Vielleicht sind Mechanismen wie p53 in der Krebszelle selber defekt (laut oben in 50% mutiert), aber es ist nicht wahrscheinlich, dass alle Mechanismen in einer Krebszelle defekt sind und Selinexor steigert ja alle zusammen. Theoretisch sehe ich auch Synergien mit z.B. Chemos ähnlich wie bei PARP-Hemmern. Die Chemo beschädigt stärker die Krebszellen als gesunde Zellen, da sie bei der Zellteilung eingreift und gesunde Zellen, die sich wenig teilen, auch nicht betroffen sind. Die Krebszelle übersteht die Chemo aber vielleicht trotz der Defekte (was vielleicht auch eine Ursache für weitere Mutationen und damit Resistenzen sein kann), weil die Kontroll-Mechanismen nicht funktionieren oder der Zelltod unterdrückt wird. Selinexor könnte die Krebszellen sensibler für die Chemo machen.
Zum Beispiel gibt sehr interessante Ergebnisse (noch kleines N) im Multiplen Myelom ohne und mit Dex. Es ist eine last-line Studie, das heißt die Patienten haben bereits zahlreiche Therapien hinter sich, die nicht mehr wirken... u.a. alle auch Dex-Kombis. Selinexor Mono wirkt bereits... aber bei Selinexor + Dex sind die Ergebnisse ausgezeichnet mit ORR von 67% und 11% CR... CBR von 89%! Dabei handelt es sich um low dose Dex mit 20mg, das für sich genommen eigentlich zu niedrig dosiert ist, um eine Wirkung zu haben.

Zum Vergleich hier ARRYs Filanesib mit Dex (auch last-line, Dex mit 40mg doppelt so hoch)... hier liegt selbst bei AAG-low CBR nur bei 28% und ORR bei 19%.
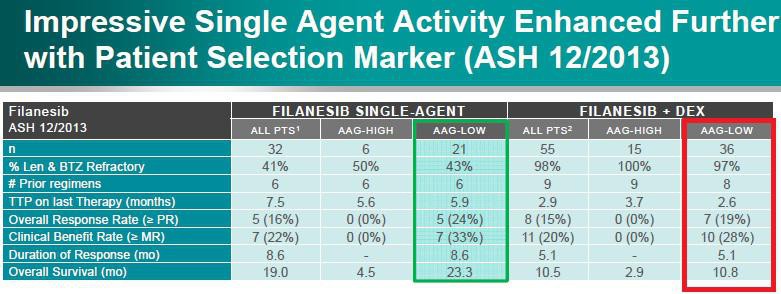
Jetzt sind nicht alle Ergebnisse so gut (bisher in Blutkrebs deutlich besser als in soliden Tumoren), aber ich denke, es braucht Zeit die richtigen Kombis usw zu finden. Selinexor scheint auch in extrem agressiven Blutkrebsarten wie "double hit" DLBCL und Richters eine Wirkung zu haben, die sich bisher kaum behandeln lassen... dadurch sind beschleunigte Zulassungen möglich.
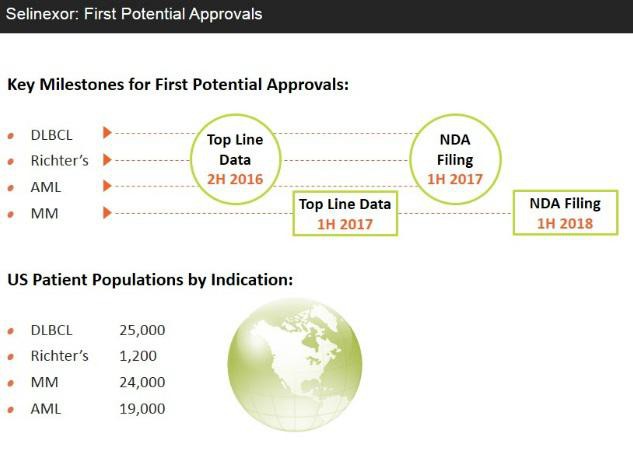
In AML wäre z.B. auch eine Kombi mit AMBIs FLT3-Hemmer Quizartinib, da es über XPO1 u.a. auch FLT3 hemmt... zumindest in der Maus funktioniert es.
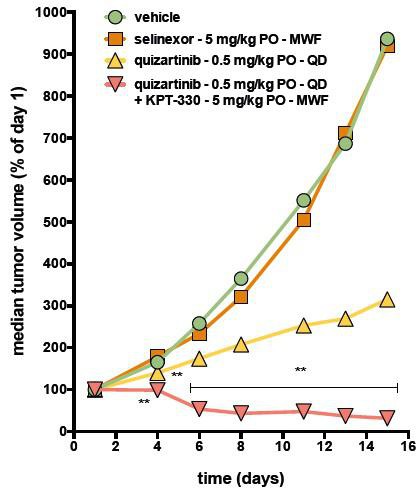
Es gibt auch eine ganze Reihe Studien von Dritten
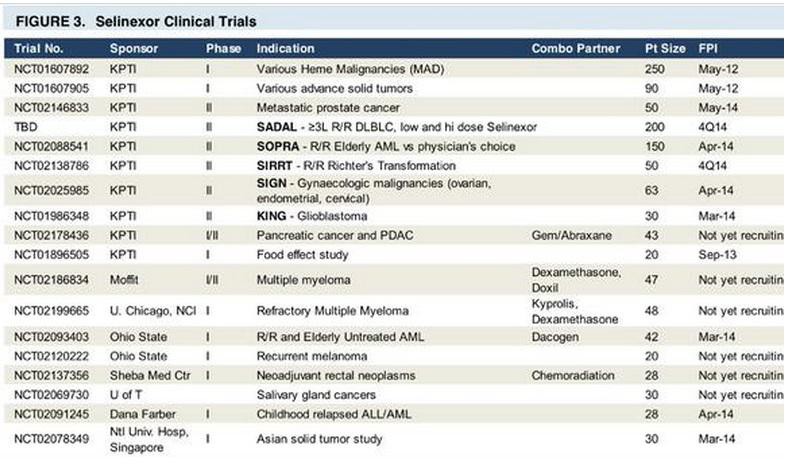
Das klingt für mich alles so, als ob Selinexor sehr breit funktioniert. KPTI hat alle Rechte, Patentschutz bis mindestens 2032 und will es alleine in den USA und Europa auf den Markt bringen.
Einige Umsatzschätzungen sehen auch nach einem Blockbuster aus:
JMP Product Sales and Royalties: Selinexor
US Sales
ROW Sales
Total Product Sales and Royalties
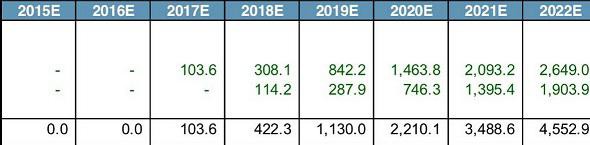



Gruß
ipollit
meine erste KPTI-Position habe ich weiter erhöht. Ich denke, dass der XPO1-Hemmer Selinexor eine Menge Potential hat, wenn er in der Weise funktioniert wie gedacht. Interessant finde ich es besonders, weil es ein recht grundsätzlicher Ansatz ist, der sich deutlich von anderen Therapien unterscheidet, wodurch er sich theoretisch sehr breit in vielen Krebsarten anwenden lässt und mit vielen anderen Therapien kombinierbar sein könnte. STML hat zuletzt auch einen XPO1-Hemmer einlizensiert.
Selinexor bezeichnet KPTI als "SINE" (Selective Inhibitor of Nuclear Export). Im folgenden Diagramm sind Krebs-Therapien in verschiedene Klassen eingeteilt. Dazu zählen Chemos, die schnell teilende Zellen beschädigen und damit abtöten (die meisten Krebszellen teilen sich schnell, u.U. aber keine Krebsstammzellen). Der Krebs kann resistent gegen die Chemo werden, indem er z.B. Transporter in der Zelle verstärkt, die die Chemo schnell wieder aus der Zelle pumpen können. Dann gibt es die Target-Therapien, die bestimmte fehlerhafte Signalwege unterdrücken... dazu zählen z.B. die TKIs wie MEK- oder BRAF-Hemmer. Der Krebs benötigt für sein starkes Wachstum sehr viele Nährstoffe und eine gute Blutversorgung... z.B. VEGF-Hemmer sollen den Krebs von der Versorgung abschneiden. Und es gibt Mittel, die sich darauf auswirken, ob ein Krebs Metastasen bildet, sich also unkontrolliert im Körper verteilt.
Selinexor betrifft nun zwei weitere Bereiche: in Krebszellen sind Mechanismen defekt, die normalerweise in beschädigten Zellen zum Zelltod führen. Die Krebszelle wird dadurch praktisch unsterblich. Ein konkretes Beispiel ist hier BCL2, das den Zelltod verhindern kann... BCL2-Hemmer wie ABT-199 (siehe INFI) zeigen sehr gute Ergebnisse. Desweiteren besitzen Zellen Mechanismen die das Verhalten steuern und kontrollieren, z.B. wann sich eine Zelle teilt, wie sie wächst usw. In Krebszellen sind auch diese defekt, so dass die Zelle sich völlig unnatürlich verhalten kann. Selinexor versucht diese beiden Mechanismen wieder herzustellen... quasi die Mechanismen, mit denen der Körper den Krebs normalerweise selber verhindert.

Dabei greift Selinexor nicht ein konkretes Target an, das den Zelltod oder die Zellentwicklung steuert, sondern das Transport-Protein XPO1, das im Zellkern arbeitet. Es gibt mehrere Transporter-Proteine, die z.B. Dinge aus dem Zellkern (der Zellkern enthält die DNA) in die Zelle oder aus der Zelle heraus transportieren. Dabei sind bestimmte Stoffe auf bestimmte Transporter beschränkt. XPO1 transportiert eine große Anzahl an Stoffen aus dem Zellkern, die normalerweise dort die Zellentwicklung steuern und überwachen sollen... wie z.B. p53: "Der humane Tumorsuppressor p53 reguliert als Transkriptionsfaktor nach DNA-Schädigung die Expression von Genen, die an der Kontrolle des Zellzyklus, an der Induktion der Apoptose (des programmierten Zelltods) oder an der DNA-Reparatur beteiligt sind. Aufgrund dieser Eigenschaft wird p53 in der Literatur als „Wächter des Genoms“ bezeichnet. Die besondere medizinische Bedeutung erklärt sich aus dem Befund, dass p53 in 50 % aller menschlichen Tumoren mutiert ist. Der Verlust der p53-Funktion spielt daher eine kritische Rolle bei der Entstehung von Krebs, ist jedoch nicht dessen ursächlicher Auslöser.". Dieser Transport ist ein normaler Vorgang, der auch in gesundern Zellen zu finden ist... Krebszellen steigern aber XPO1, um die kontrollierenden und den Krebs unterdrückenden Stoffe schnell aus dem Zellkern zu befördern, so dass sie in der Krebszelle nicht mehr richtig wirken.
Wird der Transporter nun blockiert, so können diese Stoffe nicht mehr aus dem Zellkern entweichen und regulieren die Zelle, prüfen die DNA, reparieren sie oder leiten einen Zelltod ein. Auf anderem Weg kann die Krebszelle die Stoffe nicht herausbefördern.
Zu den Stoffen gehört auch das elF4E-Protein. Soweit ich es verstehe, ist dieses Protein selber ein Transporter für bestimmte RNA-Stückchen. Solche RNA ist ein Schritt zur Produktion von Proteinen... RNA wird aus der DNA ausgelesen und danach werden die Proteine gebaut. Dies geschieht aber offensichtlich außerhalb des Zellkerns. Transportiert XPO1 elF4E mit der bestimmten RNA nicht aus dem Zellkern, so wird das Protein nicht hergestellt. Zu diesen Proteinen gehört u.a. BCL2 (das den Zelltod verhindert) und cMyc (siehe INCYs BET-Hemmer). Das heißt die Hemmung von XPO1 verringert indirekt auch die Produktion krebsfördernder Proteine.

Es gab schonmal einen XPO1-Hemmer in der Entwicklung (nicht bei KPTI)... dieses war aber auch für gesunde Zellen giftig, wahrscheinlich, weil es dauerhaft an XPO1 gebunden hat. Selinexor bleibt aber nicht dauerhaft an XPO1 gebunden... nach mehreren Stunden löst es sich wieder. In dieser Zeit können die Kontroll-Stoffe im Zellkern wirken und die Produktion krebsfördernder Proteine wird gesenkt. Gesunde Zellen sollen dadurch keine Probleme bekommen, die Mechanismen finden dort ja keinen DNA-Schaden usw.. danach arbeiten die XPO1-Transporter wieder eine Zeit normal bis die nächste Dosis erfolgt.
Da es so ein fundamentaler Mechanismus ist, müsste Selinexor eigentlich bei fast allen Krebszellen etwas bewirken. Vielleicht sind Mechanismen wie p53 in der Krebszelle selber defekt (laut oben in 50% mutiert), aber es ist nicht wahrscheinlich, dass alle Mechanismen in einer Krebszelle defekt sind und Selinexor steigert ja alle zusammen. Theoretisch sehe ich auch Synergien mit z.B. Chemos ähnlich wie bei PARP-Hemmern. Die Chemo beschädigt stärker die Krebszellen als gesunde Zellen, da sie bei der Zellteilung eingreift und gesunde Zellen, die sich wenig teilen, auch nicht betroffen sind. Die Krebszelle übersteht die Chemo aber vielleicht trotz der Defekte (was vielleicht auch eine Ursache für weitere Mutationen und damit Resistenzen sein kann), weil die Kontroll-Mechanismen nicht funktionieren oder der Zelltod unterdrückt wird. Selinexor könnte die Krebszellen sensibler für die Chemo machen.
Zum Beispiel gibt sehr interessante Ergebnisse (noch kleines N) im Multiplen Myelom ohne und mit Dex. Es ist eine last-line Studie, das heißt die Patienten haben bereits zahlreiche Therapien hinter sich, die nicht mehr wirken... u.a. alle auch Dex-Kombis. Selinexor Mono wirkt bereits... aber bei Selinexor + Dex sind die Ergebnisse ausgezeichnet mit ORR von 67% und 11% CR... CBR von 89%! Dabei handelt es sich um low dose Dex mit 20mg, das für sich genommen eigentlich zu niedrig dosiert ist, um eine Wirkung zu haben.

Zum Vergleich hier ARRYs Filanesib mit Dex (auch last-line, Dex mit 40mg doppelt so hoch)... hier liegt selbst bei AAG-low CBR nur bei 28% und ORR bei 19%.

Jetzt sind nicht alle Ergebnisse so gut (bisher in Blutkrebs deutlich besser als in soliden Tumoren), aber ich denke, es braucht Zeit die richtigen Kombis usw zu finden. Selinexor scheint auch in extrem agressiven Blutkrebsarten wie "double hit" DLBCL und Richters eine Wirkung zu haben, die sich bisher kaum behandeln lassen... dadurch sind beschleunigte Zulassungen möglich.

In AML wäre z.B. auch eine Kombi mit AMBIs FLT3-Hemmer Quizartinib, da es über XPO1 u.a. auch FLT3 hemmt... zumindest in der Maus funktioniert es.

Es gibt auch eine ganze Reihe Studien von Dritten

Das klingt für mich alles so, als ob Selinexor sehr breit funktioniert. KPTI hat alle Rechte, Patentschutz bis mindestens 2032 und will es alleine in den USA und Europa auf den Markt bringen.
Einige Umsatzschätzungen sehen auch nach einem Blockbuster aus:
JMP Product Sales and Royalties: Selinexor
US Sales
ROW Sales
Total Product Sales and Royalties



Gruß
ipollit
EPZM
Da ich immer schon die epigenetischen Therapien interessant fand und EPZM bei HMTs führend ist, habe ich mir nun auch eine kleine Position gekauft. DOT1L sieht bisher leider nicht so vielversprechend aus. EZH2 kann breiter angewendet werden. Dieses Jahr soll auch ein PRMT5-Hemmer in PI gehen.
Vielleicht schafft der Kurs es mal über 20 USD...

Gruß
ipollit
Da ich immer schon die epigenetischen Therapien interessant fand und EPZM bei HMTs führend ist, habe ich mir nun auch eine kleine Position gekauft. DOT1L sieht bisher leider nicht so vielversprechend aus. EZH2 kann breiter angewendet werden. Dieses Jahr soll auch ein PRMT5-Hemmer in PI gehen.
Vielleicht schafft der Kurs es mal über 20 USD...
Gruß
ipollit
ARRY
Die Pharmas treffen anscheinend auch nicht selten große Fehlentscheidungen... hier z.B. Pfizer, die u.a. auch durch Übernahmen einige Blockbuster aus der Hand gegeben haben:
http://www.forbes.com/sites/johnlamattina/2014/08/19/the-neg…
Ich wusste auch garnicht, dass der CDK4/6-Hemmer Palbociclib, den Pfizer jetzt als großen potentiellen Blockbuster feiert, vor Jahren schonmal von ihnen aussortiert worden war... weitsichtig war das nicht.
Hoffentlich lohnt es sich für ARRY!
Gruß
ipollit
Die Pharmas treffen anscheinend auch nicht selten große Fehlentscheidungen... hier z.B. Pfizer, die u.a. auch durch Übernahmen einige Blockbuster aus der Hand gegeben haben:
http://www.forbes.com/sites/johnlamattina/2014/08/19/the-neg…
Ich wusste auch garnicht, dass der CDK4/6-Hemmer Palbociclib, den Pfizer jetzt als großen potentiellen Blockbuster feiert, vor Jahren schonmal von ihnen aussortiert worden war... weitsichtig war das nicht.
Hoffentlich lohnt es sich für ARRY!
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.876.221 von ipollit am 24.01.15 23:56:46Hallo ipollit,
sehr starker Beitrag zu KPTI! Vielen Dank dafür!
Gruß
SLG
sehr starker Beitrag zu KPTI! Vielen Dank dafür!
Gruß
SLG
Antwort auf Beitrag Nr.: 48.875.150 von ipollit am 24.01.15 18:24:38Vielen Dank für die ausführliche Antwort - ich weiß, es ist sehr schwer, manchmal sogar unmöglich, die Biotechs auch nur ansatzweise zu bewerten. Da ist man doch für den einen oder anderen tipp dankbar, wohlwissend, dass der Tippgeber ebenso daneben wie auch richtig liegen kann.
Ich versuche eine Balance zu finden zwischen "Altbewährtes" wie GILEAD, CELGENE, ABBVIE, daneben nicht allzu risikoreiche "Newcomer" wie TEKMIRA und dann letztendlich mit Spielgeld CURIS,EDAP, TELESTA und IDT AUSTRALIA.
Da hätt ich eben noch ein wenig Platz für den einen oder anderen Wert.
Nochmal Dank und viel Erfolg
mfg
skipper
Ich versuche eine Balance zu finden zwischen "Altbewährtes" wie GILEAD, CELGENE, ABBVIE, daneben nicht allzu risikoreiche "Newcomer" wie TEKMIRA und dann letztendlich mit Spielgeld CURIS,EDAP, TELESTA und IDT AUSTRALIA.
Da hätt ich eben noch ein wenig Platz für den einen oder anderen Wert.
Nochmal Dank und viel Erfolg

mfg
skipper
Nachtrag....CYTOSORBENTS wär vielleicht eine Sünde wert.
Interessante Grafik:

Man sieht sehr schön, wie in den letzten Jahren die Zahl der IPOs nach oben geschnellt ist, während die Qualität (gemessen an der Reife der Pipeline) nachlässt. Zuletzt über 40% der IPOs mit ausschließlich vorklinischen Projekten.
Immer mehr Druck im Markt, immer mehr Risiko, immer mehr Hype.
Das wird sich wieder ändern, keine Frage. Irgendwann kommt das Gewitter.

Man sieht sehr schön, wie in den letzten Jahren die Zahl der IPOs nach oben geschnellt ist, während die Qualität (gemessen an der Reife der Pipeline) nachlässt. Zuletzt über 40% der IPOs mit ausschließlich vorklinischen Projekten.
Immer mehr Druck im Markt, immer mehr Risiko, immer mehr Hype.
Das wird sich wieder ändern, keine Frage. Irgendwann kommt das Gewitter.
Antwort auf Beitrag Nr.: 48.878.555 von SLGramann am 25.01.15 17:10:05"Zuletzt über 40% der IPOs mit ausschließlich vorklinischen Projekten."
Sorry: vorklinisch + PI ist korrekt. Der Trend ist dennoch klar.
Sorry: vorklinisch + PI ist korrekt. Der Trend ist dennoch klar.
Antwort auf Beitrag Nr.: 48.878.555 von SLGramann am 25.01.15 17:10:05"...während die Qualität (gemessen an der Reife der Pipeline) nachlässt...
Immer mehr Druck im Markt, immer mehr Risiko, immer mehr Hype."
Naja, dieser Sichtweise kann ich so nicht zustimmen... meinem Gefühl nach waren es zuletzt mehr hoch-qualitative Unternehmen als früher. Die Reife der Pipeline ist für mich dafür kein Maß. Wahrscheinlich stimmt eher, dass die Biotechs, die es in guten Marktphasen nur mit einem deutlich fortgeschrittenen Kandidaten an den Markt schaffen, schwach sind... bzw. schaffen es die aussichtsreichen Unternehmen auch mit einer PI an den Markt. Im letzten Jahr gab es einige, die mit PII oder PIII an den Markt wollten, den IPO aber aufgrund mangelnder Nachfrage wieder absagen mussten. Sind das dann die High-Quality-Unternehmen?
Gemessen an der Pipeline gibt es zahlreiche Low-Quality-Unternehmen... da fällt mir z.B. direkt LOXO, AGIO, FPRX, JUNO, BLCM, CLVS, STML und EPZM usw. ein... alles P0- oder P1-IPOs. BLUE und KITE kann man eigentlich auch dazu zählen.
High-Qualities wie z.B. KBIO oder ONTX sind keine Garantie für steigende Kurse.
Ich denke, es gibt in jeder Pipeline-Phase gute und schlechte Qualität. Insgesamt sind die Bewertungen vielleicht eher hoch und Hypes kann es immer geben. Aber die Betrachtung von P0/1-IPOs halte ich für falsch! Hohe Bewertungen erklären sich auch aus historisch hohen Zulassungszahlen und niedrigen KGVs der großen Biotechs, die den Pharmas den Rang abgelaufen haben.
Grüße
ipollit
Immer mehr Druck im Markt, immer mehr Risiko, immer mehr Hype."
Naja, dieser Sichtweise kann ich so nicht zustimmen... meinem Gefühl nach waren es zuletzt mehr hoch-qualitative Unternehmen als früher. Die Reife der Pipeline ist für mich dafür kein Maß. Wahrscheinlich stimmt eher, dass die Biotechs, die es in guten Marktphasen nur mit einem deutlich fortgeschrittenen Kandidaten an den Markt schaffen, schwach sind... bzw. schaffen es die aussichtsreichen Unternehmen auch mit einer PI an den Markt. Im letzten Jahr gab es einige, die mit PII oder PIII an den Markt wollten, den IPO aber aufgrund mangelnder Nachfrage wieder absagen mussten. Sind das dann die High-Quality-Unternehmen?
Gemessen an der Pipeline gibt es zahlreiche Low-Quality-Unternehmen... da fällt mir z.B. direkt LOXO, AGIO, FPRX, JUNO, BLCM, CLVS, STML und EPZM usw. ein... alles P0- oder P1-IPOs. BLUE und KITE kann man eigentlich auch dazu zählen.
High-Qualities wie z.B. KBIO oder ONTX sind keine Garantie für steigende Kurse.
Ich denke, es gibt in jeder Pipeline-Phase gute und schlechte Qualität. Insgesamt sind die Bewertungen vielleicht eher hoch und Hypes kann es immer geben. Aber die Betrachtung von P0/1-IPOs halte ich für falsch! Hohe Bewertungen erklären sich auch aus historisch hohen Zulassungszahlen und niedrigen KGVs der großen Biotechs, die den Pharmas den Rang abgelaufen haben.
Grüße
ipollit
ARRY
Noch einige Anmerkungen zum CC:
-Grundsätzlich wurde deutlich, dass das Ganze noch ein längerer Prozess werden wird, bei dem aber mehr und mehr auch bekannt gegeben werden kann (vieles ist vertraulich, vor allem so lange der Deal zwischen GSK und NOV noch nicht fix ist)
-das jetzt die EU-Kartellbehörde diese Bedingungen gestellt hat bedeutet nicht, dass nicht auch andere Kartellbehörden (USA) noch ähnliche oder andere Bedingungen stellen können
-Die zur Verfügung stehende Zeit kann nicht kommuniziert werden.
-ARRY muss - nachdem ein Partner gefunden wurde - diesen der Kartellbehörde vorstellen
-ARRY bekäme auch dann Milestones, Royalties etc. , wenn sie es nicht schaffen einen Partner zu finden und eine Kommisson ihn dann sucht und findet.
Was die Suche betrifft ist mein Gefühl, dass ARRY da jetzt nicht die beste Verhandlungsposition hat, weil sie unter Zugzwang stehen. Da kann man nur hoffen, das mindestens 2 passende Partner ein echtes Interesse haben. Die Deutsche Merck macht vielleicht wirklich am meisten Sinn. Merck hat ja kürzlich auch mit Pfizer eine umfassende Kooperation im Bezug auf PD1 geschlossen: http://www.fiercebiotech.com/story/pfizer-forges-285b-immuno…
Von daher ist vielleicht eine Erweiterung sinnvoll. So wie ich es sehe, böte sich eben auch Pfizer als Partner für die USA an. Pfizer hat ja auch noch einen recht vielversprechenden CDK 4/6 I. im Rennen, den man ähnlich wie NOV LEE011 entwickeln könnte...
___
Ich habe einen kleinen Teil ARRY verkauft und mir dafür ein Position LOXO gekauft. Hauptsächlich wegen der chartechnisch doch interessanten Situation. Mal schauen...

SG kmastra
Noch einige Anmerkungen zum CC:
-Grundsätzlich wurde deutlich, dass das Ganze noch ein längerer Prozess werden wird, bei dem aber mehr und mehr auch bekannt gegeben werden kann (vieles ist vertraulich, vor allem so lange der Deal zwischen GSK und NOV noch nicht fix ist)
-das jetzt die EU-Kartellbehörde diese Bedingungen gestellt hat bedeutet nicht, dass nicht auch andere Kartellbehörden (USA) noch ähnliche oder andere Bedingungen stellen können
-Die zur Verfügung stehende Zeit kann nicht kommuniziert werden.
-ARRY muss - nachdem ein Partner gefunden wurde - diesen der Kartellbehörde vorstellen
-ARRY bekäme auch dann Milestones, Royalties etc. , wenn sie es nicht schaffen einen Partner zu finden und eine Kommisson ihn dann sucht und findet.
Was die Suche betrifft ist mein Gefühl, dass ARRY da jetzt nicht die beste Verhandlungsposition hat, weil sie unter Zugzwang stehen. Da kann man nur hoffen, das mindestens 2 passende Partner ein echtes Interesse haben. Die Deutsche Merck macht vielleicht wirklich am meisten Sinn. Merck hat ja kürzlich auch mit Pfizer eine umfassende Kooperation im Bezug auf PD1 geschlossen: http://www.fiercebiotech.com/story/pfizer-forges-285b-immuno…
Von daher ist vielleicht eine Erweiterung sinnvoll. So wie ich es sehe, böte sich eben auch Pfizer als Partner für die USA an. Pfizer hat ja auch noch einen recht vielversprechenden CDK 4/6 I. im Rennen, den man ähnlich wie NOV LEE011 entwickeln könnte...
___
Ich habe einen kleinen Teil ARRY verkauft und mir dafür ein Position LOXO gekauft. Hauptsächlich wegen der chartechnisch doch interessanten Situation. Mal schauen...
SG kmastra
Antwort auf Beitrag Nr.: 48.889.343 von kmastra am 26.01.15 19:37:43ARRY
"Grundsätzlich wurde deutlich, dass das Ganze noch ein längerer Prozess werden wird..." ... ein wichtiger Termin ist sicherlich in den nächsten Tagen die Genehmigung des NVS-GSK-Deals durch die EU.
Merck hatte ich weniger wegen PD1 gedacht (PD1 ist sicherlich auch wichtig, da sowohl PD1 als auch BRAF+MEK in Melanoma Standard sein werden... vielleicht auch eine Kombi aus diesen), mehr wegen Mercks EGFR-AK Erbitux. Erbitux ist in Darmkrebs das, was Herceptin in Brustkrebs ist. Komischerweise funktionieren in EGFR-mutierten Lungenkrebs nur EGFR-TKI-Hemmer, in EGFR-mutierten Darmkrebs dagegen nur EGFR-AKs. Erbitux funktioniert u.a nicht bei einer KRAS-Mutation. Bei KRAS könnte ein MEK oder eine MEK-Kombi hilfreich sein. Bei BRAF-Darmkrebs wiederum scheint eine Kombi mit Erbitux sinnvoll, um eine BRAF-Resistenz über EGFR zu verhindern.
z.B. http://www.reuters.com/article/2013/10/04/us-germany-merck-e…
Germany's Merck sees long-term growth in cancer drug Erbitux
DARMSTADT, Germany Fri Oct 4, 2013 10:27am EDT
...
Erbitux, which accounted for roughly 8 percent of Merck's 10.7 billion euros ($14.6 billion) in sales last year, in June was shown to be more effective at prolonging the lives of colorectal cancer patients than Roche's Avastin.
Only patients whose tumors contain the non-mutated version of a gene called KRAS took part in the trial. Erbitux is only approved in this patient subgroup, which accounts for about 60 percent of colorectal cancer cases.
"We still have room to grow in colorectal cancer due to our personalized KRAS-approach," Belen Garijo, the head of Merck's prescription drugs division, told Reuters.
She said the study results would help her marketing teams argue the case for Erbitux, which unlike Avastin, requires doctors to perform a genetic test on the cancer tissue before starting therapy.
Depending on the country, the testing can delay treatment by anything from a few days to one and a half weeks, making it a priority for Merck to provide support for faster testing and lab procedures, Garijo said.
Merck has the marketing and development rights to Erbitux outside North America, while Bristol-Myers Squibb sells the product in North America with Eli Lilly receiving royalties.
Garijo's projections for long-term growth are at odds with analysts polled by Thomson Reuters Pharma, who on average expect Merck's Erbitux sales to peak at $1.25 billion in 2014, slipping to $1.1 billion by 2018.
...
Both Erbitux and Avastin are approved and are in use as initial treatments of metastatic bowel cancer in combination with chemotherapy.
Merck had 887 million euros ($1.21 billion) in Erbitux sales last year, from head and neck as well as bowel cancer, while Bristol-Myers Squibb generated $702 million in sales from the drug...
***
z.B. laufende PI/II von Binimetinib + dem EGFR-AK Vectibix in KRAS-mCRC: "Phase Ib/II Study of Efficacy and Safety of MEK162 and Panitumumab, in Adult mCRC Patients With Mutant or Wild-type RAS Tumors" ... Vectibix ist das Konkurrenzprodukt von AMGN zu Erbitux.

Gruß
ipollit
"Grundsätzlich wurde deutlich, dass das Ganze noch ein längerer Prozess werden wird..." ... ein wichtiger Termin ist sicherlich in den nächsten Tagen die Genehmigung des NVS-GSK-Deals durch die EU.
Merck hatte ich weniger wegen PD1 gedacht (PD1 ist sicherlich auch wichtig, da sowohl PD1 als auch BRAF+MEK in Melanoma Standard sein werden... vielleicht auch eine Kombi aus diesen), mehr wegen Mercks EGFR-AK Erbitux. Erbitux ist in Darmkrebs das, was Herceptin in Brustkrebs ist. Komischerweise funktionieren in EGFR-mutierten Lungenkrebs nur EGFR-TKI-Hemmer, in EGFR-mutierten Darmkrebs dagegen nur EGFR-AKs. Erbitux funktioniert u.a nicht bei einer KRAS-Mutation. Bei KRAS könnte ein MEK oder eine MEK-Kombi hilfreich sein. Bei BRAF-Darmkrebs wiederum scheint eine Kombi mit Erbitux sinnvoll, um eine BRAF-Resistenz über EGFR zu verhindern.
z.B. http://www.reuters.com/article/2013/10/04/us-germany-merck-e…
Germany's Merck sees long-term growth in cancer drug Erbitux
DARMSTADT, Germany Fri Oct 4, 2013 10:27am EDT
...
Erbitux, which accounted for roughly 8 percent of Merck's 10.7 billion euros ($14.6 billion) in sales last year, in June was shown to be more effective at prolonging the lives of colorectal cancer patients than Roche's Avastin.
Only patients whose tumors contain the non-mutated version of a gene called KRAS took part in the trial. Erbitux is only approved in this patient subgroup, which accounts for about 60 percent of colorectal cancer cases.
"We still have room to grow in colorectal cancer due to our personalized KRAS-approach," Belen Garijo, the head of Merck's prescription drugs division, told Reuters.
She said the study results would help her marketing teams argue the case for Erbitux, which unlike Avastin, requires doctors to perform a genetic test on the cancer tissue before starting therapy.
Depending on the country, the testing can delay treatment by anything from a few days to one and a half weeks, making it a priority for Merck to provide support for faster testing and lab procedures, Garijo said.
Merck has the marketing and development rights to Erbitux outside North America, while Bristol-Myers Squibb sells the product in North America with Eli Lilly receiving royalties.
Garijo's projections for long-term growth are at odds with analysts polled by Thomson Reuters Pharma, who on average expect Merck's Erbitux sales to peak at $1.25 billion in 2014, slipping to $1.1 billion by 2018.
...
Both Erbitux and Avastin are approved and are in use as initial treatments of metastatic bowel cancer in combination with chemotherapy.
Merck had 887 million euros ($1.21 billion) in Erbitux sales last year, from head and neck as well as bowel cancer, while Bristol-Myers Squibb generated $702 million in sales from the drug...
***
z.B. laufende PI/II von Binimetinib + dem EGFR-AK Vectibix in KRAS-mCRC: "Phase Ib/II Study of Efficacy and Safety of MEK162 and Panitumumab, in Adult mCRC Patients With Mutant or Wild-type RAS Tumors" ... Vectibix ist das Konkurrenzprodukt von AMGN zu Erbitux.

Gruß
ipollit
arry:
Wichtiger Schritt in Richtung des definitiven Transfers von Binimetinib und Encorafenib:
http://www.nzz.ch/wirtschaft/newsticker/eu-kommission-genehm…
A
Wichtiger Schritt in Richtung des definitiven Transfers von Binimetinib und Encorafenib:
http://www.nzz.ch/wirtschaft/newsticker/eu-kommission-genehm…
A
Gestern das IPO von Once liegen lassen, weil mein Broker nicht in der Lage war, die Order an die NASDAQ zu routen (angeblich ein Problem des WM-Systems). Man hätte zu 41 oder 42 Dollar kaufen können. Na ja, vielleicht gibts mal einen Rücksetzer.
Denke eh, dass 2015 kein gutes Börsenjahr wird.
Worum es mir eigentlich geht:
EXEL:
Da gab es zuletzt ja etwas wildere Kursbewegungen. Ich stell mir schon länger die Frage, was passieren wird, wenn die Daten der RCC-PIII von Cabozantinib raus kommen. Das soll in Q2 so weit sein, auch wenn bei clinical trials der September eingetragen ist:
https://clinicaltrials.gov/ct2/show/NCT01865747?term=METEOR&…
Es gibt ja eine gewisse Wahrscheinlichkeit, dass der Trial erfolgreich ist. Ich würde diese Wahrscheinlichkeit nicht sehr hoch ansetzen (30%?) und ich würde meine kleine Exelixis-Position auch vor den Daten nicht aufstocken.
Mir geht es vielmehr um die Frage, wie die Situation einzuschätzen wäre, falls der Trial doch erfolgreich abschließt?
Konkreter gefragt: Welches kommerzielle Potential würde durch einen Erfolg bei RCC mittelfristig entstehen?
Welche Marktkapitalisierung wäre dann zu rechtfertigen? Derzeit liegt die Marktkapitalisierung bei ca. 370 Mio. Dollar. Dazu kommen aber gute 400 Mio. Dollar an Verbindlichkeiten, die der Marktkapitalisierung zuzuschlagen sind.
Ich glaube ein mal gelesen zu haben, dass das Marktpotential, dass sich bei einem erfolgreichen METEOR-Trial eröffnen würde, bei ungefähr einer Milliarde Dollar liegen soll.
Hat hier jemand andere, bessere Schätzungen?
Wenn das mit der Milliarde richtig wäre, würde nämlich selbst ein Kurssprung von 100% nach erfolgreichen RCC-Daten noch weiteres Potential erlauben, wenn man seine Position dann aufstocken würde.
Es wäre einfach gut, vorher ein paar Szenarien durchzugehen, wie man handeln würde, falls dies oder jenes geschieht.
Wenn Cabo bei RCC floppt, könnte es das mit EXEL gewesen sein, oder? Die Verbindlichkeiten sind haarsträubend:
http://services.corporate-ir.net/SEC/Document.Service?id=P3V…
Denke eh, dass 2015 kein gutes Börsenjahr wird.
Worum es mir eigentlich geht:
EXEL:
Da gab es zuletzt ja etwas wildere Kursbewegungen. Ich stell mir schon länger die Frage, was passieren wird, wenn die Daten der RCC-PIII von Cabozantinib raus kommen. Das soll in Q2 so weit sein, auch wenn bei clinical trials der September eingetragen ist:
https://clinicaltrials.gov/ct2/show/NCT01865747?term=METEOR&…
Es gibt ja eine gewisse Wahrscheinlichkeit, dass der Trial erfolgreich ist. Ich würde diese Wahrscheinlichkeit nicht sehr hoch ansetzen (30%?) und ich würde meine kleine Exelixis-Position auch vor den Daten nicht aufstocken.
Mir geht es vielmehr um die Frage, wie die Situation einzuschätzen wäre, falls der Trial doch erfolgreich abschließt?
Konkreter gefragt: Welches kommerzielle Potential würde durch einen Erfolg bei RCC mittelfristig entstehen?
Welche Marktkapitalisierung wäre dann zu rechtfertigen? Derzeit liegt die Marktkapitalisierung bei ca. 370 Mio. Dollar. Dazu kommen aber gute 400 Mio. Dollar an Verbindlichkeiten, die der Marktkapitalisierung zuzuschlagen sind.
Ich glaube ein mal gelesen zu haben, dass das Marktpotential, dass sich bei einem erfolgreichen METEOR-Trial eröffnen würde, bei ungefähr einer Milliarde Dollar liegen soll.
Hat hier jemand andere, bessere Schätzungen?
Wenn das mit der Milliarde richtig wäre, würde nämlich selbst ein Kurssprung von 100% nach erfolgreichen RCC-Daten noch weiteres Potential erlauben, wenn man seine Position dann aufstocken würde.
Es wäre einfach gut, vorher ein paar Szenarien durchzugehen, wie man handeln würde, falls dies oder jenes geschieht.
Wenn Cabo bei RCC floppt, könnte es das mit EXEL gewesen sein, oder? Die Verbindlichkeiten sind haarsträubend:
http://services.corporate-ir.net/SEC/Document.Service?id=P3V…
Antwort auf Beitrag Nr.: 48.941.693 von SLGramann am 31.01.15 10:49:09"Ich glaube ein mal gelesen zu haben, dass das Marktpotential, dass sich bei einem erfolgreichen METEOR-Trial eröffnen würde, bei ungefähr einer Milliarde Dollar liegen soll."
Scheint ein sehr optimistisches Szenario zu sein...
Diese Übersicht mahnt zur Vorsicht. Eine Milliarde ist sicher nicht ohne First-Line-Einsatz zu machen und das steht ja wohl erst mal nicht zur Debatte:
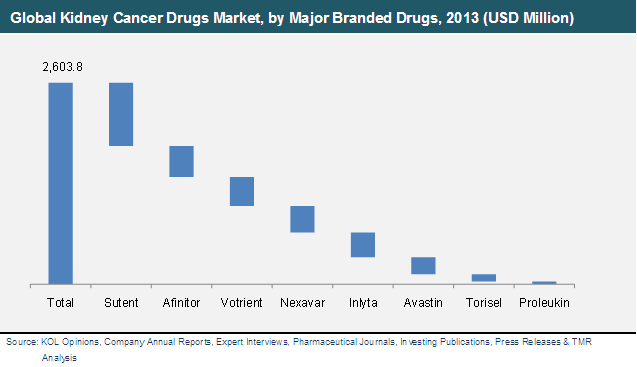
http://www.transparencymarketresearch.com/pressrelease/kidne…
Scheint ein sehr optimistisches Szenario zu sein...
Diese Übersicht mahnt zur Vorsicht. Eine Milliarde ist sicher nicht ohne First-Line-Einsatz zu machen und das steht ja wohl erst mal nicht zur Debatte:

http://www.transparencymarketresearch.com/pressrelease/kidne…
Antwort auf Beitrag Nr.: 48.942.296 von SLGramann am 31.01.15 12:34:57EXEL
Hallo SLGramann,
wenn ich es richtig verstehe, willst du deine EXEL-Position nicht weiter aufstocken? Willst du sie denn verkaufen, weil die Situation zu unsicher ist? Ich behalte meine Position so bei wie sie ist... als High-Risk, bei der ich einen Totalverlust einkalkuliere. Für mich ist es eine 50:50-Sache... wenn bei EXEL etwas funktioniert, dann Carbo in RCC und RET+ NSCLC, allerdings war es rückblickend wohl von EXEL zu gewagt, Carbo massiv gegen Prostatakrebs zu entwickeln auf Grundlage von überraschenden Ergebnissen in der PII, unklarem Wirkmechanismus und ungewissen Auswirkungen auf OS. Daher bin ich bei EXEL vorsichtig, was ihre Entscheidungen betrifft.
Wie kommst du denn auf 30% Erfolgswahrscheinlichkeit? Warum nicht sehr hoch? Sind das nicht reine Spekulationen? Ich sehe in RCC die höchste Wahrscheinlichkeit für Carbo (neben RET+ NSCLC), da...
1) Carbo auf dem bei RCC etablierten Wirkmechanismus VEGFR basiert. Alle Mittel, die bei RCC wirksam sind und dort eingesetzt werden basieren im Wesentlichen auf VEGFR. Soweit ich mich erinnere, ist RCC das Paradebeispiel für die Wirksamkeit von VEGFR-Hemmern... die Wirksamkeit in RCC lässt sich aus der Theorie ableiten
2) Carbo ist zudem ein dualer VEGFR + MET Hemmer. MET ist entsprechend der Theorie und präklinischen Experimenten ein wesentlicher Resistenz-Mechanismus gegen VEGFR (sagen wir soetwas wie z.B. T790M bei EGFR NSCLC oder besser IGF1R bei EGFR). Unter Anwendung von VEGFR soll MET hochgeregelt werden und zu einer Resistenz gegen VEGFR-Hemmer führen
3) In einer PI(!) waren die Ergebnisse bei RCC-Patienten, die gegen mehrere Therapien (darunter sicherlich auch mehrere VEGFRs) resistent waren, sehr gut... PFS (in RCC für eine Zulassung ausreichend?) war so gut oder besser als bei einer Erstbehandlung mit den etablierten VEGFR-Hemmern. Theorie und Praxis passen daher bisher.
4) es gibt einzelne Patienten-Berichte von einer guten Wirkung nach off-label Anwendung (Carbo ist ja bereits in MTC zugelassen)
5) Die PIII konnte schneller die Patienten rekrutieren als geplant... d.h. es gibt hohes Interesse von Ärtzen/Patienten
Ich hatte ja schon einige Male etwas zu METEOR geschrieben...
http://www.wallstreet-online.de/diskussion/1173523-841-850/b…
http://www.wallstreet-online.de/diskussion/1173523-841-850/b…
http://www.wallstreet-online.de/diskussion/1173523-841-850/b…
z.B. theoretischer Ansatz von Carbo in RCC:
http://blog.dana-farber.org/insight/2014/01/new-strategies-i…
PI-Ergebnisse:
http://www.ackc.org/kidney-cancer-information/asco-2012-repo…
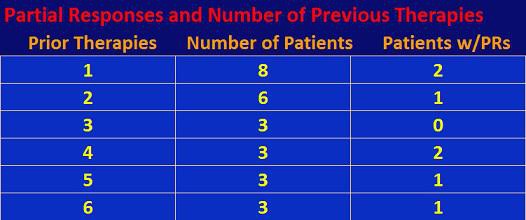
"What stands out in this trial is the response rate, specifically the pfs of 14.7 months and some tumor shrinkage in 19 of the 21 evaluated patients for a patient mix that was heavily pre-treated. For example, of the 7 patients who showed partial tumor response (> 30% shrinkage), 4 of them had four or more prior treatments. The best pfs in current therapies is about a year, and this is mostly for treatment-naïve patients. The axitinib-sorafenib second-line trial (with one prior therapy) yielded a pfs of 6.7 months and 4.7 months for axitinib and sorafenib, respectively. Additionally, the patients on this trial were all in the intermediate and poor risk categories."
Zum Marktpotential in RCC...
"We believe cabo’s mechanism of action makes sense in RCC where VEGF has been established as a key target and MET is a driver in a large percentage of RCC and HCC. We model a $376M and $135M U.S. market opportunity in RCC and HCC, respectively, and assume a 65% probability of success."
Letztlich geht es um 1st-line, das stimmt. Aber kein Mittel wird sofort 1st-line entwickelt, wenn es bereits etablierte ähnliche 1st-line Mittel gibt. Das ginge wahrscheinlich nur head-to-head... dann hast du das Risiko, dass wenn du nicht deutlich besser bist oder riesige Studien durchführst, keine Signifikanz erreichst.
Der Ansatz von Carbo zielt aber auch speziell auf 2+line ab, um mit VEGFR+MET etwas bei VGFR-Resistenz machen zu können.
Hier ist der RCC-Markt aufgeschlüsselt... erstmal geht es bei Carbo um 2nd-line und 3+ line. Von den Patienten her sind es fast do viele wie 1st-line. Allerdings ist oft die Wirkung und damit die Behandlungsdauer 1st-line größer (wobei PFS bei Carbo ja schonmal sehr gut aussah)
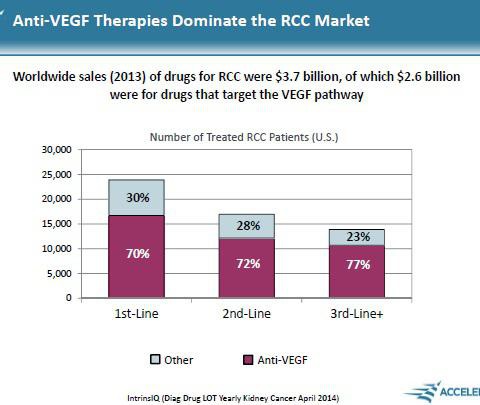
Wie zu sehen ist, dominiert VEGFR den RCC-Markt. Hier wird ein WW-Umsatz 2013 von 2,6 Mrd USD mit VEGFR-Hemmern genannt... so ganz passt das nicht zu deinem Diagramm, da Afinitor und Torisel eigentlich mTor-Hemmer sind. Die anderen sind aber VEGFRs.
Gruß
ipollit
Hallo SLGramann,
wenn ich es richtig verstehe, willst du deine EXEL-Position nicht weiter aufstocken? Willst du sie denn verkaufen, weil die Situation zu unsicher ist? Ich behalte meine Position so bei wie sie ist... als High-Risk, bei der ich einen Totalverlust einkalkuliere. Für mich ist es eine 50:50-Sache... wenn bei EXEL etwas funktioniert, dann Carbo in RCC und RET+ NSCLC, allerdings war es rückblickend wohl von EXEL zu gewagt, Carbo massiv gegen Prostatakrebs zu entwickeln auf Grundlage von überraschenden Ergebnissen in der PII, unklarem Wirkmechanismus und ungewissen Auswirkungen auf OS. Daher bin ich bei EXEL vorsichtig, was ihre Entscheidungen betrifft.
Wie kommst du denn auf 30% Erfolgswahrscheinlichkeit? Warum nicht sehr hoch? Sind das nicht reine Spekulationen? Ich sehe in RCC die höchste Wahrscheinlichkeit für Carbo (neben RET+ NSCLC), da...
1) Carbo auf dem bei RCC etablierten Wirkmechanismus VEGFR basiert. Alle Mittel, die bei RCC wirksam sind und dort eingesetzt werden basieren im Wesentlichen auf VEGFR. Soweit ich mich erinnere, ist RCC das Paradebeispiel für die Wirksamkeit von VEGFR-Hemmern... die Wirksamkeit in RCC lässt sich aus der Theorie ableiten
2) Carbo ist zudem ein dualer VEGFR + MET Hemmer. MET ist entsprechend der Theorie und präklinischen Experimenten ein wesentlicher Resistenz-Mechanismus gegen VEGFR (sagen wir soetwas wie z.B. T790M bei EGFR NSCLC oder besser IGF1R bei EGFR). Unter Anwendung von VEGFR soll MET hochgeregelt werden und zu einer Resistenz gegen VEGFR-Hemmer führen
3) In einer PI(!) waren die Ergebnisse bei RCC-Patienten, die gegen mehrere Therapien (darunter sicherlich auch mehrere VEGFRs) resistent waren, sehr gut... PFS (in RCC für eine Zulassung ausreichend?) war so gut oder besser als bei einer Erstbehandlung mit den etablierten VEGFR-Hemmern. Theorie und Praxis passen daher bisher.
4) es gibt einzelne Patienten-Berichte von einer guten Wirkung nach off-label Anwendung (Carbo ist ja bereits in MTC zugelassen)
5) Die PIII konnte schneller die Patienten rekrutieren als geplant... d.h. es gibt hohes Interesse von Ärtzen/Patienten
Ich hatte ja schon einige Male etwas zu METEOR geschrieben...
http://www.wallstreet-online.de/diskussion/1173523-841-850/b…
http://www.wallstreet-online.de/diskussion/1173523-841-850/b…
http://www.wallstreet-online.de/diskussion/1173523-841-850/b…
z.B. theoretischer Ansatz von Carbo in RCC:
http://blog.dana-farber.org/insight/2014/01/new-strategies-i…
PI-Ergebnisse:
http://www.ackc.org/kidney-cancer-information/asco-2012-repo…

"What stands out in this trial is the response rate, specifically the pfs of 14.7 months and some tumor shrinkage in 19 of the 21 evaluated patients for a patient mix that was heavily pre-treated. For example, of the 7 patients who showed partial tumor response (> 30% shrinkage), 4 of them had four or more prior treatments. The best pfs in current therapies is about a year, and this is mostly for treatment-naïve patients. The axitinib-sorafenib second-line trial (with one prior therapy) yielded a pfs of 6.7 months and 4.7 months for axitinib and sorafenib, respectively. Additionally, the patients on this trial were all in the intermediate and poor risk categories."
Zum Marktpotential in RCC...
"We believe cabo’s mechanism of action makes sense in RCC where VEGF has been established as a key target and MET is a driver in a large percentage of RCC and HCC. We model a $376M and $135M U.S. market opportunity in RCC and HCC, respectively, and assume a 65% probability of success."
Letztlich geht es um 1st-line, das stimmt. Aber kein Mittel wird sofort 1st-line entwickelt, wenn es bereits etablierte ähnliche 1st-line Mittel gibt. Das ginge wahrscheinlich nur head-to-head... dann hast du das Risiko, dass wenn du nicht deutlich besser bist oder riesige Studien durchführst, keine Signifikanz erreichst.
Der Ansatz von Carbo zielt aber auch speziell auf 2+line ab, um mit VEGFR+MET etwas bei VGFR-Resistenz machen zu können.
Hier ist der RCC-Markt aufgeschlüsselt... erstmal geht es bei Carbo um 2nd-line und 3+ line. Von den Patienten her sind es fast do viele wie 1st-line. Allerdings ist oft die Wirkung und damit die Behandlungsdauer 1st-line größer (wobei PFS bei Carbo ja schonmal sehr gut aussah)

Wie zu sehen ist, dominiert VEGFR den RCC-Markt. Hier wird ein WW-Umsatz 2013 von 2,6 Mrd USD mit VEGFR-Hemmern genannt... so ganz passt das nicht zu deinem Diagramm, da Afinitor und Torisel eigentlich mTor-Hemmer sind. Die anderen sind aber VEGFRs.
Gruß
ipollit
Antwort auf Beitrag Nr.: 48.942.824 von ipollit am 31.01.15 14:23:35Hallo ipollit,
ich werde meine Position bis zu den Daten so halten, wie sie derzeit ist.
Ich will nur ein Gefühl dafür bekommen, wie man die Situation nach einem Erfolg des METEOR-Trials einzuschätzen hätte.
Nehmen wir an, sie melden wirklich gute und überzeugende PFS-Daten und nehmen wir an, der Kurs eröffnet mit einem Plus von 100 oder 150%.
Ich hätte einfach gern ein Gefühl dafür, bis zu welchem Punkt ich nach einem solchen Ereignis meine Position vielleicht noch aufstocken würde.
Wenn man - gute Daten vorausgesetzt - für Cabo in RCC längerfristig ein Marktpotential von bspw. zwischen 500 Millionen und 1 Milliarde unterstellt, dann macht ein Nachkaufen wohl auch nach einem Kurssprung von 100 oder sogar 150% noch Sinn.
Geht man eher von 200 bis 400 Millionen aus, dann sieht es schon anders aus.
Die 30% sind ein rein fiktiver Wert, reines Bauchgefühl, in dem sich für mich die schwierige klinische Entwicklungsgeschichte von Cabo ausdrückt.
Gruß
SLG
ich werde meine Position bis zu den Daten so halten, wie sie derzeit ist.
Ich will nur ein Gefühl dafür bekommen, wie man die Situation nach einem Erfolg des METEOR-Trials einzuschätzen hätte.
Nehmen wir an, sie melden wirklich gute und überzeugende PFS-Daten und nehmen wir an, der Kurs eröffnet mit einem Plus von 100 oder 150%.
Ich hätte einfach gern ein Gefühl dafür, bis zu welchem Punkt ich nach einem solchen Ereignis meine Position vielleicht noch aufstocken würde.
Wenn man - gute Daten vorausgesetzt - für Cabo in RCC längerfristig ein Marktpotential von bspw. zwischen 500 Millionen und 1 Milliarde unterstellt, dann macht ein Nachkaufen wohl auch nach einem Kurssprung von 100 oder sogar 150% noch Sinn.
Geht man eher von 200 bis 400 Millionen aus, dann sieht es schon anders aus.
Die 30% sind ein rein fiktiver Wert, reines Bauchgefühl, in dem sich für mich die schwierige klinische Entwicklungsgeschichte von Cabo ausdrückt.
Gruß
SLG
Antwort auf Beitrag Nr.: 48.941.693 von SLGramann am 31.01.15 10:49:09ONCE
Starkes IPO - aus dem Stand jedoch nun schon eine Marketcap. von ca. 1 Mrd. USD...
Das Management gefällt mir sehr gut.
Leider bin ich kein Experte auf dem Gebiet der Augenheilkunde. Hier noch ein etwas "kritischer" bzw. interessanter Bericht zum Produkt welches am weitesten fortgeschritten ist in der Piepline:
Since 2007, clinical researchers have been dipping their toes into gene therapy for congenital forms of retinal degeneration such as LCA. The goal is to use a virus to supply retinal cells with working copies of a gene called RPE65, which is mutated in the form of the disease known as LCA2. The hope is that the working gene will repair malfunctioning cells and keep them alive, preserving and even improving vision. Trials by three different groups have shown not only that the procedure is safe, but also that it boosts vision in most participants — and that most improvements seem to be maintained for up to seven years. The biotechnology company Spark Therapeutics in Philadelphia, Pennsylvania, is now testing gene therapy for LCA2 in an advanced trial, and it hopes to file for regulatory approval in the United States as early as 2016.
But some studies have raised questions about how well the therapy is working. An analysis (Cideciyan, A. V. et al. Proc. Natl Acad. Sci. USA 110, E517–E525 (2013).) of data from one (Hauswirth, W. W. et al. Hum. Gene Ther. 19, 979–990 (2008).) of the three initial trials found that although participants' vision had improved, their photoreceptors were still dying at about the same rate as before the treatment. Artur Cideciyan, a vision scientist at the University of Pennsylvania in Philadelphia and a co-author of the study, says that the improvements probably came from the rescue of only some retinal cells. Gene therapy may not have affected the more dysfunctional photoreceptors, and these were the ones that probably died after treatment.
Researchers have observed that there seems to be a point of no return in some forms of retinal loss. A possible reason is that cell death disrupts the structure of retinal tissue, leading to a domino-like decline. Cideciyan argues that after retinal degeneration has started, even cells improved by gene therapy may eventually die off, at least in LCA2.
Robin Ali, a geneticist at University College London who led one of the early LCA2 trials, is more confident about the promise of these treatments: the careful animal work that preceded human trials showed that gene therapy, if given at the right dose and the right time, can slow degeneration. “We're still at the very start of the optimization process in humans,” he says.
Discovering the best timing for the treatment in humans remains a central challenge. Most researchers agree that the best approach is to replace the faulty gene when patients are young, before the degeneration starts or at least when there are more viable cells to save. That could mean doing retinal surgery in someone with good vision — a difficult decision, says Robert MacLaren, an ophthalmologist at the University of Oxford, UK, who is running a gene-therapy clinical trial for another form of congenital blindness. “That is where the risks are greatest, but so are the gains.” Spark's phase III LCA2 trial was open to children as young as three years old.
Quelle: http://www.nature.com/news/curing-blindness-vision-quest-1.1…

Starkes IPO - aus dem Stand jedoch nun schon eine Marketcap. von ca. 1 Mrd. USD...
Das Management gefällt mir sehr gut.
Leider bin ich kein Experte auf dem Gebiet der Augenheilkunde. Hier noch ein etwas "kritischer" bzw. interessanter Bericht zum Produkt welches am weitesten fortgeschritten ist in der Piepline:
Since 2007, clinical researchers have been dipping their toes into gene therapy for congenital forms of retinal degeneration such as LCA. The goal is to use a virus to supply retinal cells with working copies of a gene called RPE65, which is mutated in the form of the disease known as LCA2. The hope is that the working gene will repair malfunctioning cells and keep them alive, preserving and even improving vision. Trials by three different groups have shown not only that the procedure is safe, but also that it boosts vision in most participants — and that most improvements seem to be maintained for up to seven years. The biotechnology company Spark Therapeutics in Philadelphia, Pennsylvania, is now testing gene therapy for LCA2 in an advanced trial, and it hopes to file for regulatory approval in the United States as early as 2016.
But some studies have raised questions about how well the therapy is working. An analysis (Cideciyan, A. V. et al. Proc. Natl Acad. Sci. USA 110, E517–E525 (2013).) of data from one (Hauswirth, W. W. et al. Hum. Gene Ther. 19, 979–990 (2008).) of the three initial trials found that although participants' vision had improved, their photoreceptors were still dying at about the same rate as before the treatment. Artur Cideciyan, a vision scientist at the University of Pennsylvania in Philadelphia and a co-author of the study, says that the improvements probably came from the rescue of only some retinal cells. Gene therapy may not have affected the more dysfunctional photoreceptors, and these were the ones that probably died after treatment.
Researchers have observed that there seems to be a point of no return in some forms of retinal loss. A possible reason is that cell death disrupts the structure of retinal tissue, leading to a domino-like decline. Cideciyan argues that after retinal degeneration has started, even cells improved by gene therapy may eventually die off, at least in LCA2.
Robin Ali, a geneticist at University College London who led one of the early LCA2 trials, is more confident about the promise of these treatments: the careful animal work that preceded human trials showed that gene therapy, if given at the right dose and the right time, can slow degeneration. “We're still at the very start of the optimization process in humans,” he says.
Discovering the best timing for the treatment in humans remains a central challenge. Most researchers agree that the best approach is to replace the faulty gene when patients are young, before the degeneration starts or at least when there are more viable cells to save. That could mean doing retinal surgery in someone with good vision — a difficult decision, says Robert MacLaren, an ophthalmologist at the University of Oxford, UK, who is running a gene-therapy clinical trial for another form of congenital blindness. “That is where the risks are greatest, but so are the gains.” Spark's phase III LCA2 trial was open to children as young as three years old.
Quelle: http://www.nature.com/news/curing-blindness-vision-quest-1.1…
Antwort auf Beitrag Nr.: 48.807.410 von ipollit am 17.01.15 16:21:47ENTA
ABBV prognostiziert für Ende des Jahres eine jährliche Run-Rate von 3+ Mrd USD mit Viekira... das ist kein Jahresumsatz, sondern (soweit ich es verstehe) ein Umsatz Ende des Jahres z.B. innerhalb eines Monats, der hochgerechnet auf ein Jahr (12x) dann 3+ Mrd USD entspricht. In 2016 sollten die Umsätze damit aber über 3 Mrd USD liegen... die Royalties für ENTA liegen bei etwa 5%. Bei einer aktuellen MK von 880 Mio USD für ENTA (bei vielleicht 250(?) Mio USD Cash) ist das nicht gerade wenig mit z.B. 5% von 3,5 Mrd USD = 175 Mio USD, zumal die Kosten für diese Royalties ja bei 0 liegen.

In Japan ist die 2er-Kombi PIII (GIFT-I) aus Paritaprevir + Ombitasvir erfolgreich gewesen... die Zulassung dieser 2er Kombi in Japan könnte Ende des Jahres erfolgen... Royalties liegen bei etwa 7%.
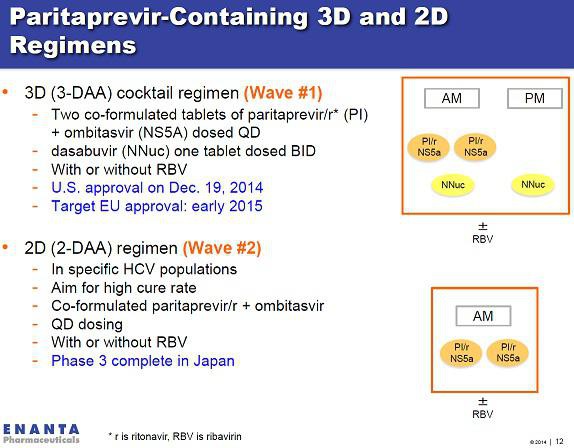
Ein Vorteil der 2er-Kombi gegenüber der in Europa und den USA zugelassen 3er-Kombi Viekira, ist die einmalige Einnahme von 2 Tabletten pro Tag gegenüber zweimaliger Einnahme von insgesamt vier Tabletten bei Viekira...

ABBV sichert sich auf Kosten von deutlichen Preisnachlässen Marktanteile, da das Konkurrenz-Produkt Harvoni von GILD sowohl einen zeitlichen Vorsprung hat als auch eigentlich etwas besser ist (ENTAs Paritaprevir braucht in Viekira zur Verstärkung den Booster Ritonavir, der allerdings u.a. Wechselwirkungen mit machen Essen haben kann)... zumal es sich nur um eine Tablette handelt.

Wie geht es dann weiter? Die 3er-Kombi Viekira soll in den USA/EU mittelfristig durch eine verbesserte 2er-Kombi ersetzt werden... ENTA's ABT-493 (als besseres Paritaprevir) und ABT-530 (besseres Ombitasvir). Damit soll u.a. auf den Booster Ritonavir verzichtet werden können, als auch eine gleichmäßig gute Wirkung gegen verschiedene HSV-Stämme erreicht werden (Viekira ist in den USA gegen GT1a/b zugelassen, womit sich die meisten HSV-Patienten dort behandeln lassen... es gibt aber auch noch GT2, GT3, usw...). Die sehr wichtigen PII-Daten zu dieser Kombi sollen dieses Jahr vorliegen und möglichst auch positiv ausfallen, um in Zukunft bei steigender Konkurrenz mithalten zu können. Diese verbesserte 2er-Kombi könnte dann 2017 oder 2018 am Markt sein. Ein Vorteil für ENTA wäre dann, dass die Royalties gegenüber Viekira deutlich besser sind mit ca. 8% gegenüber 5% jetzt.

Der Knackpunkt von ENTA im Bereich HCV scheint aber dennoch die Frage zu sein, wie konkurrenzfähig man in Zukunft ist... ob die aktuellen Royalties dauerhaft bestehen oder in ein 2-3 Jahren wieder verschwinden. Bisher konnte man gut sehen, dass neue bessere Mittel die alten Therapien schnell verdrängen konnten. GILDs Harvoni (2er-Kombi aus Sovaldi + Ledipasvir) hat z.B. GILDs Sovaldi weitgehend verdrängt
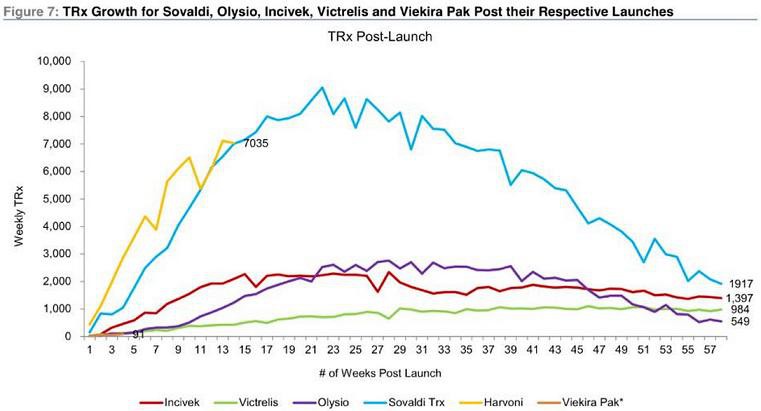
(Viekira wird hier nicht ganz korrekt erfasst... "1,100 US V-Pak scripts have been written through 1/16/15")
Mir ist nicht ganz klar, wie die Konkurrenz-Situation ausssieht. Wahrscheinlich ist deshalb ENTA im Vergleich zu den Royalties recht niedrig bewertet. Bei ENTAs Paritaprevir, ABBVs Ombitasvir oder GILDs Sovaldi handelt es sich um verschiedene Arten von Mitteln gegen HCV. Paritaprevir ist ein PI (NS3/4a), Ombitasvir ein NS5a-Hemmer und Sovaldi ein NUC (NS5b Nuc). NS5b-Hemmer gibt es als Nuc oder Non-Nuc. GILD hat sich damals durch die 11 Mrd USD Übernahme von Pharmasset den NUC Sovaldi gesichert... und wie sich herausgestellt hat, scheinen NUCs das momentan beste gegen HCV zu sein. Aus diesem Grund wurde im letzten Jahr z.B. Idenix für fast 4 Mrd USD von Merck übernommen, da diese mit IDX21437 auch einen NUC in PI/II hatten. ENTAs Paritaprevir ist dagegen ein PI... dies waren die ersten neuen Mittel gegen HCV. VRTX hatte mit Incivek den ersten PI vor vier Jahren auf den Markt gebracht (heute hat HCV für VRTX keine Bedeutung mehr... gegen GILD und ABBV hatten sie keine Chance). Ein PI alleine benötigte aber noch zusätzlich Interferon, das deutliche Nebenwirkungen hervorruft. Nun sind IFN-freie Therapien Standard. Wünschenswert wäre auch noch eine Therapie ohne Zugabe von Ribavirin, das heute meistens noch benötigt wird.
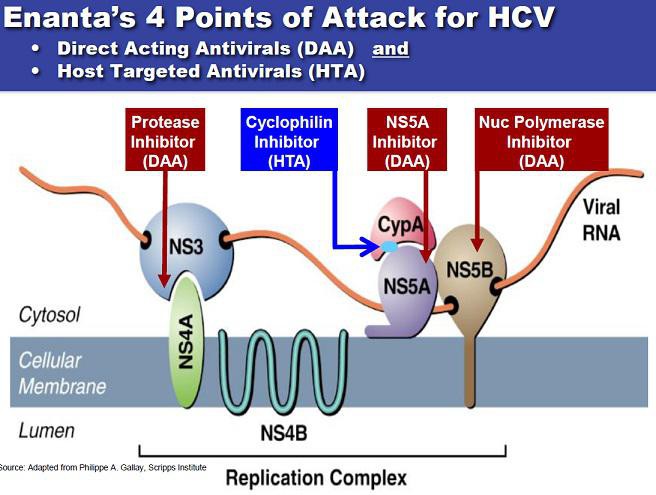
Die Frage ist nun, ob man in Zukunft mindestens einen NUC benötigt und ob PIs vielleicht überflüssig werden. GILDs Marktführer Harvoni ist ein NUC + NS5a. ENTA hat selber einen NS5a. Ob sie aber auch mal einen NUC haben werden, ist meiner Meinung nach nicht klar. Sie wollen zwar einen Kandidaten in die Klinik bringen, haben aber auf der letzten CC gesagt, dass es aus patentrechtlichen Gründen sehr schwierig sein wird. ENTA hat allerdings noch einen Cyclophilin-Hemmer in der Präklink... davon gibt es bisher nicht viele in der Entwicklung. NUCs und Cycs sollen angeblich die höchsten Resistenz-Barrieren haben. Debiopharm hat mit Alisporivir ebenfalls einen Cyc, der allerdings schon viel weiter in PII oder PIII ist. Wenn Cycs sinnvoll sind, dann würde z.B. GILD doch bei Debiopharm nachfragen. Warum ist NVS aus der Cyc + NS5a Kombi ausgestiegen, wenn diese Kombi aussichtsreich wäre?
Konkurrent ACHN hat mit dem PI Sovasprevir (der schonmal von der FDA auf clinical hold gesetzt worden ist) und NS5a-Hemmer ACH-3102 selber etwas, was der 2er-Kombi von ABBV/ENTA entspricht. Außerdem befindet sich ein NUC ACH-3422 in PI... ACH-3422 + ACH-3102 wäre soetwas wie GILDs Harvoni. Ich weiß nicht, wie konkurrenzfähig diese Kandidaten sind. ACHN MK liegt mit 1,5 Mrd USD, also schon deutlich über ENTAs mit 880 Mio USD, aber noch deutlich unter dem Übernahmepreis von IDIX mit 3,85 Mrd USD. Das ist hier das schwierige... wenn ACHNs Kandidaten konkurrenzfähig sind, dann sind sie Milliarden wert... wenn nicht, dann sind sie fast wertlos.
Hier noch ein älterer Überblick über verschiedene Kombis...
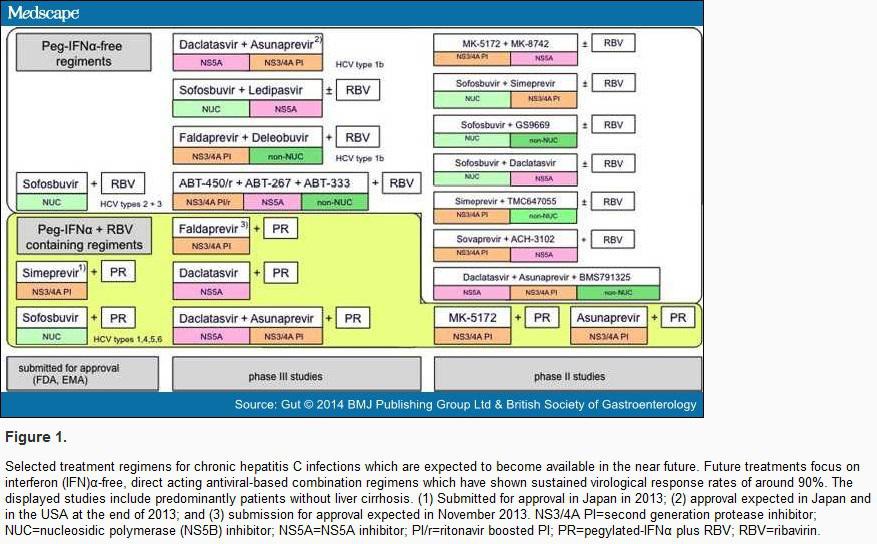
Gruß
ipollit
ABBV prognostiziert für Ende des Jahres eine jährliche Run-Rate von 3+ Mrd USD mit Viekira... das ist kein Jahresumsatz, sondern (soweit ich es verstehe) ein Umsatz Ende des Jahres z.B. innerhalb eines Monats, der hochgerechnet auf ein Jahr (12x) dann 3+ Mrd USD entspricht. In 2016 sollten die Umsätze damit aber über 3 Mrd USD liegen... die Royalties für ENTA liegen bei etwa 5%. Bei einer aktuellen MK von 880 Mio USD für ENTA (bei vielleicht 250(?) Mio USD Cash) ist das nicht gerade wenig mit z.B. 5% von 3,5 Mrd USD = 175 Mio USD, zumal die Kosten für diese Royalties ja bei 0 liegen.

In Japan ist die 2er-Kombi PIII (GIFT-I) aus Paritaprevir + Ombitasvir erfolgreich gewesen... die Zulassung dieser 2er Kombi in Japan könnte Ende des Jahres erfolgen... Royalties liegen bei etwa 7%.

Ein Vorteil der 2er-Kombi gegenüber der in Europa und den USA zugelassen 3er-Kombi Viekira, ist die einmalige Einnahme von 2 Tabletten pro Tag gegenüber zweimaliger Einnahme von insgesamt vier Tabletten bei Viekira...

ABBV sichert sich auf Kosten von deutlichen Preisnachlässen Marktanteile, da das Konkurrenz-Produkt Harvoni von GILD sowohl einen zeitlichen Vorsprung hat als auch eigentlich etwas besser ist (ENTAs Paritaprevir braucht in Viekira zur Verstärkung den Booster Ritonavir, der allerdings u.a. Wechselwirkungen mit machen Essen haben kann)... zumal es sich nur um eine Tablette handelt.

Wie geht es dann weiter? Die 3er-Kombi Viekira soll in den USA/EU mittelfristig durch eine verbesserte 2er-Kombi ersetzt werden... ENTA's ABT-493 (als besseres Paritaprevir) und ABT-530 (besseres Ombitasvir). Damit soll u.a. auf den Booster Ritonavir verzichtet werden können, als auch eine gleichmäßig gute Wirkung gegen verschiedene HSV-Stämme erreicht werden (Viekira ist in den USA gegen GT1a/b zugelassen, womit sich die meisten HSV-Patienten dort behandeln lassen... es gibt aber auch noch GT2, GT3, usw...). Die sehr wichtigen PII-Daten zu dieser Kombi sollen dieses Jahr vorliegen und möglichst auch positiv ausfallen, um in Zukunft bei steigender Konkurrenz mithalten zu können. Diese verbesserte 2er-Kombi könnte dann 2017 oder 2018 am Markt sein. Ein Vorteil für ENTA wäre dann, dass die Royalties gegenüber Viekira deutlich besser sind mit ca. 8% gegenüber 5% jetzt.

Der Knackpunkt von ENTA im Bereich HCV scheint aber dennoch die Frage zu sein, wie konkurrenzfähig man in Zukunft ist... ob die aktuellen Royalties dauerhaft bestehen oder in ein 2-3 Jahren wieder verschwinden. Bisher konnte man gut sehen, dass neue bessere Mittel die alten Therapien schnell verdrängen konnten. GILDs Harvoni (2er-Kombi aus Sovaldi + Ledipasvir) hat z.B. GILDs Sovaldi weitgehend verdrängt

(Viekira wird hier nicht ganz korrekt erfasst... "1,100 US V-Pak scripts have been written through 1/16/15")
Mir ist nicht ganz klar, wie die Konkurrenz-Situation ausssieht. Wahrscheinlich ist deshalb ENTA im Vergleich zu den Royalties recht niedrig bewertet. Bei ENTAs Paritaprevir, ABBVs Ombitasvir oder GILDs Sovaldi handelt es sich um verschiedene Arten von Mitteln gegen HCV. Paritaprevir ist ein PI (NS3/4a), Ombitasvir ein NS5a-Hemmer und Sovaldi ein NUC (NS5b Nuc). NS5b-Hemmer gibt es als Nuc oder Non-Nuc. GILD hat sich damals durch die 11 Mrd USD Übernahme von Pharmasset den NUC Sovaldi gesichert... und wie sich herausgestellt hat, scheinen NUCs das momentan beste gegen HCV zu sein. Aus diesem Grund wurde im letzten Jahr z.B. Idenix für fast 4 Mrd USD von Merck übernommen, da diese mit IDX21437 auch einen NUC in PI/II hatten. ENTAs Paritaprevir ist dagegen ein PI... dies waren die ersten neuen Mittel gegen HCV. VRTX hatte mit Incivek den ersten PI vor vier Jahren auf den Markt gebracht (heute hat HCV für VRTX keine Bedeutung mehr... gegen GILD und ABBV hatten sie keine Chance). Ein PI alleine benötigte aber noch zusätzlich Interferon, das deutliche Nebenwirkungen hervorruft. Nun sind IFN-freie Therapien Standard. Wünschenswert wäre auch noch eine Therapie ohne Zugabe von Ribavirin, das heute meistens noch benötigt wird.

Die Frage ist nun, ob man in Zukunft mindestens einen NUC benötigt und ob PIs vielleicht überflüssig werden. GILDs Marktführer Harvoni ist ein NUC + NS5a. ENTA hat selber einen NS5a. Ob sie aber auch mal einen NUC haben werden, ist meiner Meinung nach nicht klar. Sie wollen zwar einen Kandidaten in die Klinik bringen, haben aber auf der letzten CC gesagt, dass es aus patentrechtlichen Gründen sehr schwierig sein wird. ENTA hat allerdings noch einen Cyclophilin-Hemmer in der Präklink... davon gibt es bisher nicht viele in der Entwicklung. NUCs und Cycs sollen angeblich die höchsten Resistenz-Barrieren haben. Debiopharm hat mit Alisporivir ebenfalls einen Cyc, der allerdings schon viel weiter in PII oder PIII ist. Wenn Cycs sinnvoll sind, dann würde z.B. GILD doch bei Debiopharm nachfragen. Warum ist NVS aus der Cyc + NS5a Kombi ausgestiegen, wenn diese Kombi aussichtsreich wäre?
Konkurrent ACHN hat mit dem PI Sovasprevir (der schonmal von der FDA auf clinical hold gesetzt worden ist) und NS5a-Hemmer ACH-3102 selber etwas, was der 2er-Kombi von ABBV/ENTA entspricht. Außerdem befindet sich ein NUC ACH-3422 in PI... ACH-3422 + ACH-3102 wäre soetwas wie GILDs Harvoni. Ich weiß nicht, wie konkurrenzfähig diese Kandidaten sind. ACHN MK liegt mit 1,5 Mrd USD, also schon deutlich über ENTAs mit 880 Mio USD, aber noch deutlich unter dem Übernahmepreis von IDIX mit 3,85 Mrd USD. Das ist hier das schwierige... wenn ACHNs Kandidaten konkurrenzfähig sind, dann sind sie Milliarden wert... wenn nicht, dann sind sie fast wertlos.
Hier noch ein älterer Überblick über verschiedene Kombis...

Gruß
ipollit
ESPR
Die FDA hat den "partial clinical hold" für 1002 aufgehoben und somit den Weg für die PIII später im Jahr frei gemacht.
http://www.fiercebiotech.com/story/esperion-gets-out-under-f…
In diesem Jahr stehen bei ESPR doch noch einige wichtige Ereignisse an.
ESPR: MK: 700 Mio - Cash ca. 140 Mio
März: Endgültige Ergebnisse der Studie 008 (1002 +/vs. Ezetimibe), PII Ergebnisse 009Studie (1002 + Statin wenn LDL-C Ziel nicht erreicht)
Q2: FDA Entscheidet über Aufhebung des partial clinical hold
Q2: Ergebnisse 014Studie: PII mit Schwerpunkt auf Patienten mit Bluthochdruck
Q3: Zulassung der PCSK9-I. von Amgen bzw. Sanofi (Preis?-diskussion)
Q4: Gespräche FDA und Entscheidung über PIII
PIII Ergebnisse dann 2017
ENTA
ENTA hat heute gut 10% verloren. Man ist scheinbar vom Ausblick ABBVIEs bzgl. Viekira enttäuscht. So ganz kann ich das nicht nachvollziehen. ENTA hat jetzt schon um und bei 280 MIO US$ Cash (Marktkapitalisierung 730 Mio). Im Jahr 2014 hatte man Ausgaben (R&D etc.) von ca. 30 Mio. ENTA ist zudem bemüht die Kosten im Griff zu behalten. So hat man die Option auf Co-Development für ABT493 nicht gezogen, sowie Programme konsequent eingestellt. Ich würde also davon ausgehen, dass ENTA das Geld nicht sinnlos verprasst.
Und von nun an bekommt man ja quartalsweise einen Scheck von ABBVIE, der mit keinerlei eigenen Kosten in Verbindung steht. Bei 2 Milliarden Umsatz wären das 100 Mio. Für die Zulassung in Japan (die zimlich sicher ist) bekommt ENTA auch nochmal 30 Mio. Dazu ggf. steigende Royalties etc. und eine Pipeline einerseits aber natürlich andereseits auch die Frage nach der Nachhaltigkeit der Umsätze (s. Beitrag von ipollit). Ich denke aber insgesamt wird hier zu schwarz gesehen! ABBVIE hat sicherlich einen sehr konservativen Ausblick gegeben.

SG kmastra
Die FDA hat den "partial clinical hold" für 1002 aufgehoben und somit den Weg für die PIII später im Jahr frei gemacht.
http://www.fiercebiotech.com/story/esperion-gets-out-under-f…
In diesem Jahr stehen bei ESPR doch noch einige wichtige Ereignisse an.
ESPR: MK: 700 Mio - Cash ca. 140 Mio
März: Endgültige Ergebnisse der Studie 008 (1002 +/vs. Ezetimibe), PII Ergebnisse 009Studie (1002 + Statin wenn LDL-C Ziel nicht erreicht)
Q2: FDA Entscheidet über Aufhebung des partial clinical hold
Q2: Ergebnisse 014Studie: PII mit Schwerpunkt auf Patienten mit Bluthochdruck
Q3: Zulassung der PCSK9-I. von Amgen bzw. Sanofi (Preis?-diskussion)
Q4: Gespräche FDA und Entscheidung über PIII
PIII Ergebnisse dann 2017
ENTA
ENTA hat heute gut 10% verloren. Man ist scheinbar vom Ausblick ABBVIEs bzgl. Viekira enttäuscht. So ganz kann ich das nicht nachvollziehen. ENTA hat jetzt schon um und bei 280 MIO US$ Cash (Marktkapitalisierung 730 Mio). Im Jahr 2014 hatte man Ausgaben (R&D etc.) von ca. 30 Mio. ENTA ist zudem bemüht die Kosten im Griff zu behalten. So hat man die Option auf Co-Development für ABT493 nicht gezogen, sowie Programme konsequent eingestellt. Ich würde also davon ausgehen, dass ENTA das Geld nicht sinnlos verprasst.
Und von nun an bekommt man ja quartalsweise einen Scheck von ABBVIE, der mit keinerlei eigenen Kosten in Verbindung steht. Bei 2 Milliarden Umsatz wären das 100 Mio. Für die Zulassung in Japan (die zimlich sicher ist) bekommt ENTA auch nochmal 30 Mio. Dazu ggf. steigende Royalties etc. und eine Pipeline einerseits aber natürlich andereseits auch die Frage nach der Nachhaltigkeit der Umsätze (s. Beitrag von ipollit). Ich denke aber insgesamt wird hier zu schwarz gesehen! ABBVIE hat sicherlich einen sehr konservativen Ausblick gegeben.
SG kmastra
Heute und morgen findet die Leerink Healthcare Konferenz statt. Dort präsentieren einige interessante Firmen...
http://leerink.metameetings.com/confbook/healthcare15/agenda…
http://leerink.metameetings.com/confbook/healthcare15/agenda…
EXEL:
Ist Hammer zu langsam?
Er hatte ja in Kommentaren mehrfach angekündigt, vor dem Q2 eventuell wieder eine Position bei Exelixis aufzubauen.
Inzwischen läuft die Spekulation auf den METEOR-Trial aber offensichtlich bereits auf Hochtouren und hat den Kurs seit Weihnachten schon mal um 100% nach oben getrieben:

Bei einem vollen Erfolg von METEOR könnte aber mittelfristig möglicherweise auch ein Kurs von 10 Dollar erreichbar sein.
Ist Hammer zu langsam?
Er hatte ja in Kommentaren mehrfach angekündigt, vor dem Q2 eventuell wieder eine Position bei Exelixis aufzubauen.
Inzwischen läuft die Spekulation auf den METEOR-Trial aber offensichtlich bereits auf Hochtouren und hat den Kurs seit Weihnachten schon mal um 100% nach oben getrieben:
Bei einem vollen Erfolg von METEOR könnte aber mittelfristig möglicherweise auch ein Kurs von 10 Dollar erreichbar sein.
Ihr solltet Werte ins Depot nehmen, die Unternehmen wie BB Biotech oder DWS ins Depot neu aufnehmen.
Schaut Euch an, was mit Novavax passiert ist die letzten Monate, seitdem BB Biotech investiert ist.
Das gleiche könnte nun mit JUNO Therapeutics passieren, weil der DWS Biotech Fonds investiert ist.
Schaut Euch an, was mit Novavax passiert ist die letzten Monate, seitdem BB Biotech investiert ist.
Das gleiche könnte nun mit JUNO Therapeutics passieren, weil der DWS Biotech Fonds investiert ist.
arry:
weiterer Schritt in Richtung Dealabschluß NVS/GSK:
Novartis und GSK erhalten Grünes Licht aus Australien für Portfolio-Deals
Zürich (awp) - Die beiden Pharma-Konzerne Novartis und GlaxoSmithKline (GSK) haben von der australischen Wettbewerbsbehörde die Zustimmung zu der vergangenes Frühjahr vereinbarten Produktportfolio-Transaktion erhalten. Die Australian Competition and Consumer Commission (ACCC) sei von den Vorschlägen von GSK und Novartis zum Verkauf gewisser konkurrenzierender Produkte überzeugt gewesen, heisst es in einer Mitteilung der Behörde vom Freitag. Die Transaktionen dürften den Wettbewerb nicht in bedeutendem Umfang beeinträchtigen.
GSK werde in Australien die Meningokokken-Impfstoffprodukte devestieren und Novartis die Raucherstopp-Palette, heisst es weiter. Weltweit würde Novartis zwei Produktkandidaten zur Behandlung von fortgeschrittenem Melanom verkaufen, wie bereits mit der EU-Kommission vereinbart.
Die EU-Kommission hat die Novartis/GSK-Transaktionen Ende Januar dieses Jahres unter Auflagen genehmigt.
Novartis übernimmt von GSK im Rahmen einer dreiteiligen Transaktion bekanntlich gewisse Onkologie-Produkte. Zudem führen die beiden Konzerne ihre nicht rezeptpflichtigen Gesundheitsprodukte in ein Gemeinschaftsunternehmen über. Und GSK übernimmt das Impfstoff-Geschäft von Novartis.
weiterer Schritt in Richtung Dealabschluß NVS/GSK:
Novartis und GSK erhalten Grünes Licht aus Australien für Portfolio-Deals
Zürich (awp) - Die beiden Pharma-Konzerne Novartis und GlaxoSmithKline (GSK) haben von der australischen Wettbewerbsbehörde die Zustimmung zu der vergangenes Frühjahr vereinbarten Produktportfolio-Transaktion erhalten. Die Australian Competition and Consumer Commission (ACCC) sei von den Vorschlägen von GSK und Novartis zum Verkauf gewisser konkurrenzierender Produkte überzeugt gewesen, heisst es in einer Mitteilung der Behörde vom Freitag. Die Transaktionen dürften den Wettbewerb nicht in bedeutendem Umfang beeinträchtigen.
GSK werde in Australien die Meningokokken-Impfstoffprodukte devestieren und Novartis die Raucherstopp-Palette, heisst es weiter. Weltweit würde Novartis zwei Produktkandidaten zur Behandlung von fortgeschrittenem Melanom verkaufen, wie bereits mit der EU-Kommission vereinbart.
Die EU-Kommission hat die Novartis/GSK-Transaktionen Ende Januar dieses Jahres unter Auflagen genehmigt.
Novartis übernimmt von GSK im Rahmen einer dreiteiligen Transaktion bekanntlich gewisse Onkologie-Produkte. Zudem führen die beiden Konzerne ihre nicht rezeptpflichtigen Gesundheitsprodukte in ein Gemeinschaftsunternehmen über. Und GSK übernimmt das Impfstoff-Geschäft von Novartis.
FGEN
mit einer MK von 1,7 Mrd USD ist FGEN leider nicht gerade günstig, doch sehe ich dennoch eine Menge Potential für Roxadustat. Als besseres EPO könnte es ein Multi-Mrd Blockbuster werden mit Umsätzen von 5+ vielleicht sogar 10+ Mrd USD. FGEN hat durch die Partner keine Kosten und trotzdem sehr gute 20-25% Royalties. PIII-Ergebnisse in Amerika werden nicht vor 2017 vorliegen... nächstes Jahr sollen aber bereits PIII-Daten aus Studien in China kommen, die vielleicht Hinweise liefern.
Daneben befindet sich mit FG-3019 ein zweiter Kandidat in der Pipeline, der interessant werden könnte, wenn man die 8 Mrd USD Übernahme von Intermune durch Roche als Maßstab nimmt. FG-3019 könnte in IPF besser als Intermune's Esbriet sein. Allerdings gibt es wohl noch konkurrierende CTGF-AKs in der Entwicklung.
In der nächsten Zeit werde ich vielleicht eine erste Position kaufen.
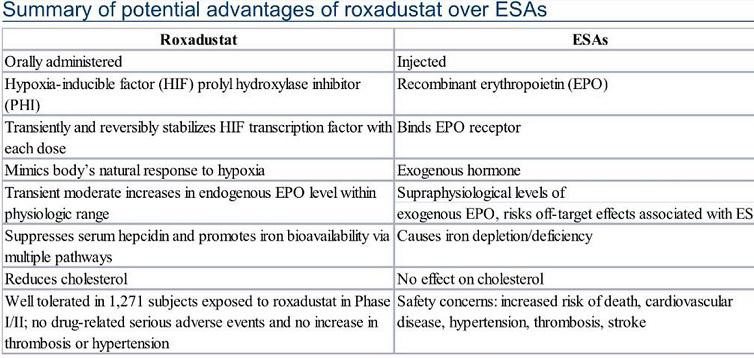
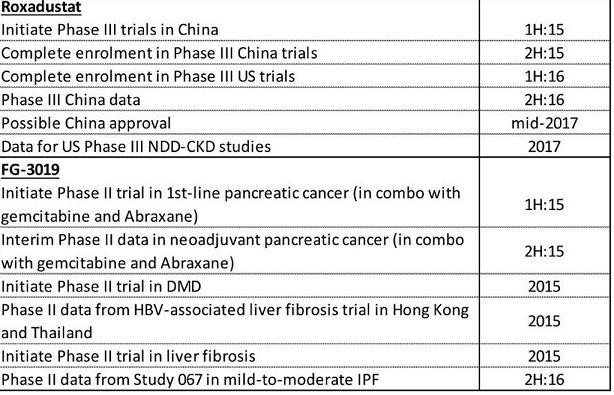
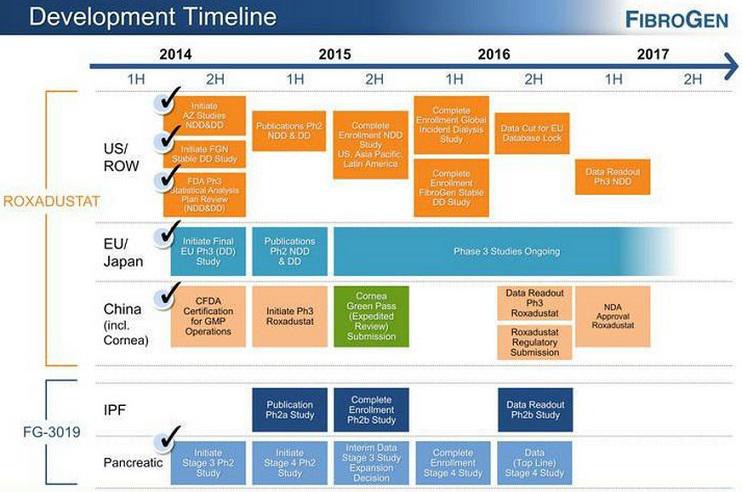

Gruß
ipollit
mit einer MK von 1,7 Mrd USD ist FGEN leider nicht gerade günstig, doch sehe ich dennoch eine Menge Potential für Roxadustat. Als besseres EPO könnte es ein Multi-Mrd Blockbuster werden mit Umsätzen von 5+ vielleicht sogar 10+ Mrd USD. FGEN hat durch die Partner keine Kosten und trotzdem sehr gute 20-25% Royalties. PIII-Ergebnisse in Amerika werden nicht vor 2017 vorliegen... nächstes Jahr sollen aber bereits PIII-Daten aus Studien in China kommen, die vielleicht Hinweise liefern.
Daneben befindet sich mit FG-3019 ein zweiter Kandidat in der Pipeline, der interessant werden könnte, wenn man die 8 Mrd USD Übernahme von Intermune durch Roche als Maßstab nimmt. FG-3019 könnte in IPF besser als Intermune's Esbriet sein. Allerdings gibt es wohl noch konkurrierende CTGF-AKs in der Entwicklung.
In der nächsten Zeit werde ich vielleicht eine erste Position kaufen.



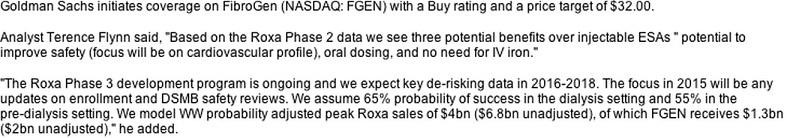
Gruß
ipollit
INCY
Jakafi scheint immer besser angenommen zu werden. In MV und PV gibt es bisher keine Alternative... optimistische peak sales in diesen beiden Indikationen könnten in den USA bei 3 Mrd USD liegen, wo INCY 100% der Rechte hält. Dazu kommen ex-US Royalties von Novartis (wäre INCY für die nicht auch ein interessanter Übernahme-Kandidat?)
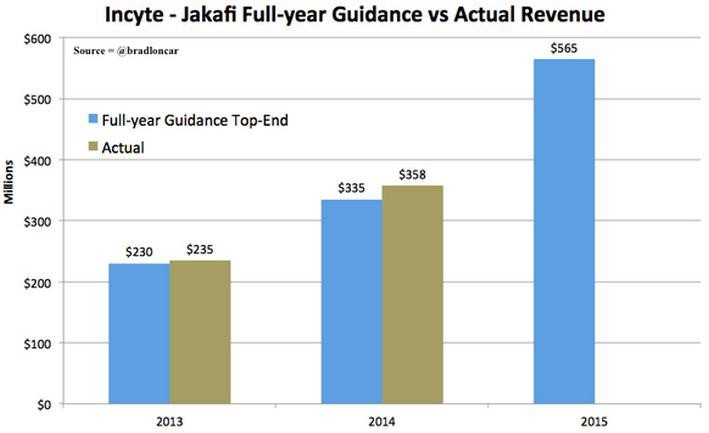


Dazu kommt eine recht breite Pipeline...

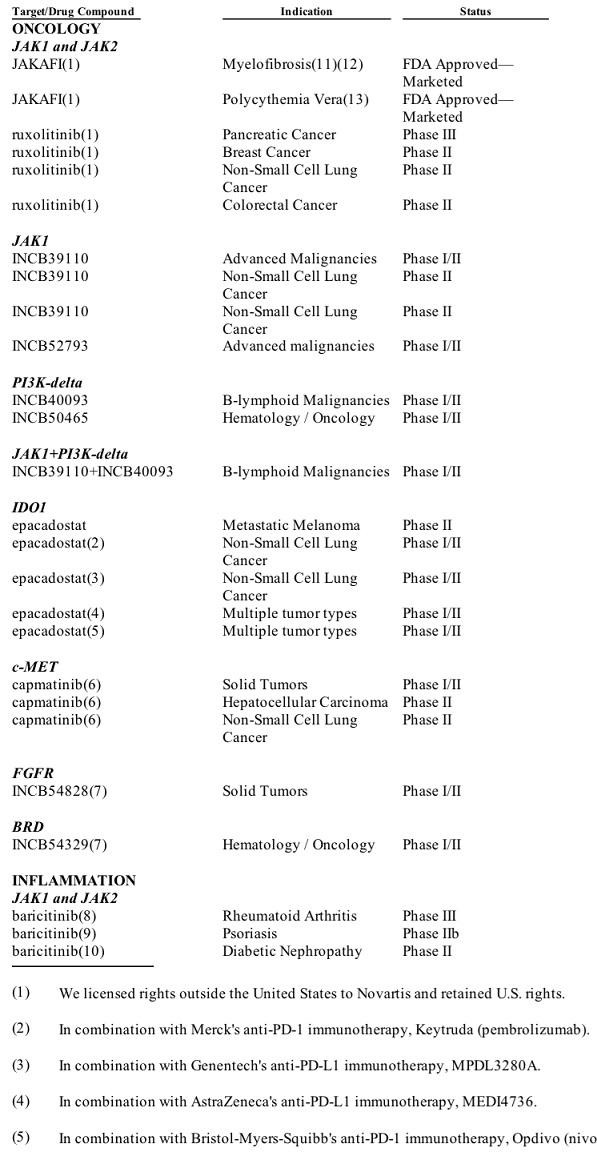

Gruß
ipollit
Jakafi scheint immer besser angenommen zu werden. In MV und PV gibt es bisher keine Alternative... optimistische peak sales in diesen beiden Indikationen könnten in den USA bei 3 Mrd USD liegen, wo INCY 100% der Rechte hält. Dazu kommen ex-US Royalties von Novartis (wäre INCY für die nicht auch ein interessanter Übernahme-Kandidat?)



Dazu kommt eine recht breite Pipeline...


Gruß
ipollit
PCYC
die Imbruvica Umsätze dürften in den nächsten Jahren deutlich wachsen. Analysten schätzen für dieses Jahr >1 Mrd USD und nächstes Jahr >2 Mrd USD. Im Folgenden steht z.B. eine EPS16 Schätzung von 6,39 USD
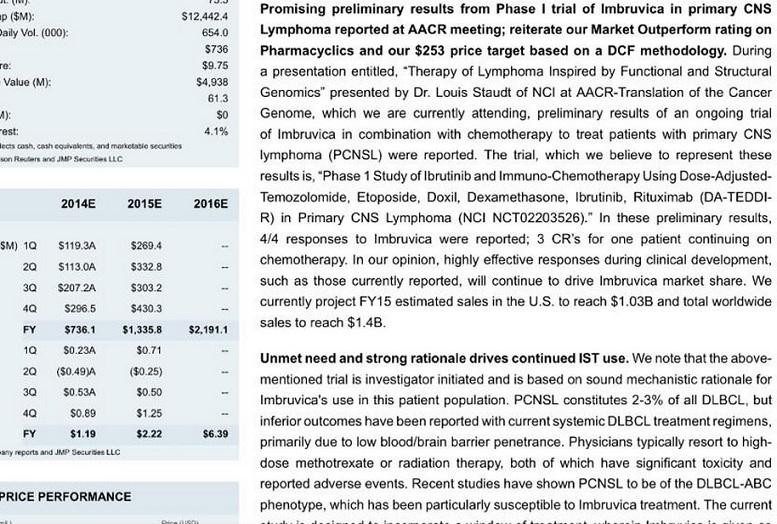
PCYC bucht die US-Umsätze, JNJ die ex-US Umsätze... die Gewinne werden aber jeweils geteilt...
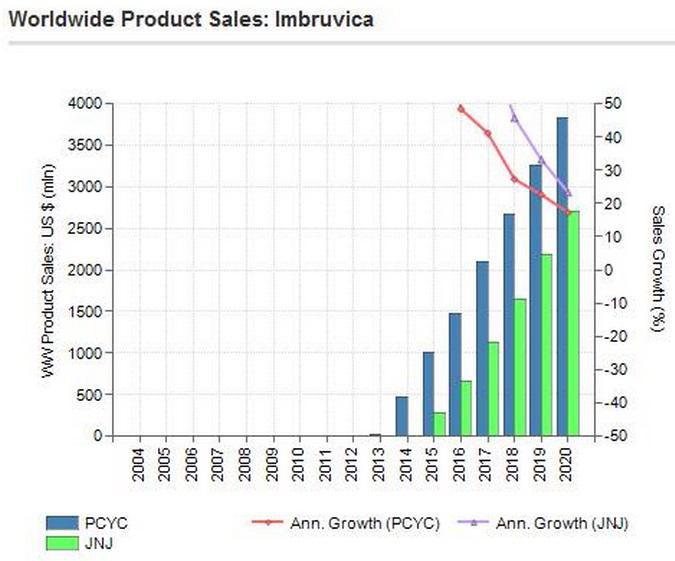
(MDVNs Xtandi gehört auch mit zu den erfolgreichsten Krebsmitteln...)
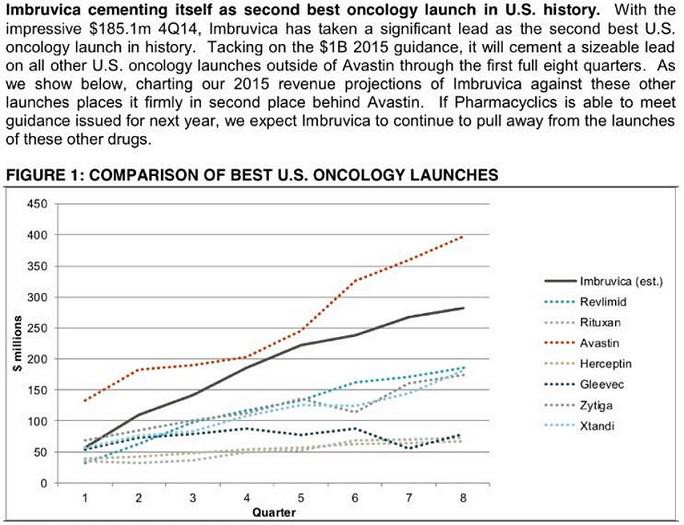


Angeblich gibt es präklinische Hinweise, dass Imbruvica wegen der Wirkung auf ITK ADCC (Aktivierung von z.B. NK-Zellen durch den AK beim Andocken an die Zielzelle) von AKs wie Rituxan senkt. Dadurch wäre Rituxan in der Kombi mit Imruvica nicht so wirksam, wie es normalerweise sein könnte. Ob das im Menschen auch so ist, muss sich erst zeigen. ITK soll aber auch eine positive IO-Wirkung haben... dies ist die Grundlage für die Imbruvica + PD-1 Kombis und könnte zur lang anhaltenden Wirkung von Imbruvica beitragen. Sollte es wirklich ADCC beeinflussen, wäre eine sequentielle Verabreichung vielleicht besser. Könnte dann nicht vielleicht auch eine Arzerra + Imbruvica Kombi besser sein, da Genmabs Arzerra eine größere CDC-Wirkung hat?... CDC ist eine direkt toxische Wirkung des AK gegen die Zielzelle.



Gruß
ipollit
die Imbruvica Umsätze dürften in den nächsten Jahren deutlich wachsen. Analysten schätzen für dieses Jahr >1 Mrd USD und nächstes Jahr >2 Mrd USD. Im Folgenden steht z.B. eine EPS16 Schätzung von 6,39 USD

PCYC bucht die US-Umsätze, JNJ die ex-US Umsätze... die Gewinne werden aber jeweils geteilt...

(MDVNs Xtandi gehört auch mit zu den erfolgreichsten Krebsmitteln...)



Angeblich gibt es präklinische Hinweise, dass Imbruvica wegen der Wirkung auf ITK ADCC (Aktivierung von z.B. NK-Zellen durch den AK beim Andocken an die Zielzelle) von AKs wie Rituxan senkt. Dadurch wäre Rituxan in der Kombi mit Imruvica nicht so wirksam, wie es normalerweise sein könnte. Ob das im Menschen auch so ist, muss sich erst zeigen. ITK soll aber auch eine positive IO-Wirkung haben... dies ist die Grundlage für die Imbruvica + PD-1 Kombis und könnte zur lang anhaltenden Wirkung von Imbruvica beitragen. Sollte es wirklich ADCC beeinflussen, wäre eine sequentielle Verabreichung vielleicht besser. Könnte dann nicht vielleicht auch eine Arzerra + Imbruvica Kombi besser sein, da Genmabs Arzerra eine größere CDC-Wirkung hat?... CDC ist eine direkt toxische Wirkung des AK gegen die Zielzelle.


Gruß
ipollit
ACAD
Zuletzt habe ich meine Position weiter erhöht. Nuplazid besitzt für den CNS-Bereich ein relativ geringes Zulassungs-Risiko (u.a. BTD von der FDA)... das Potential kann aufgrund der relativ geringen Nebenwirkungen im Mrd-Bereich liegen. Bei 100% der Rechte ist das sehr interessant.
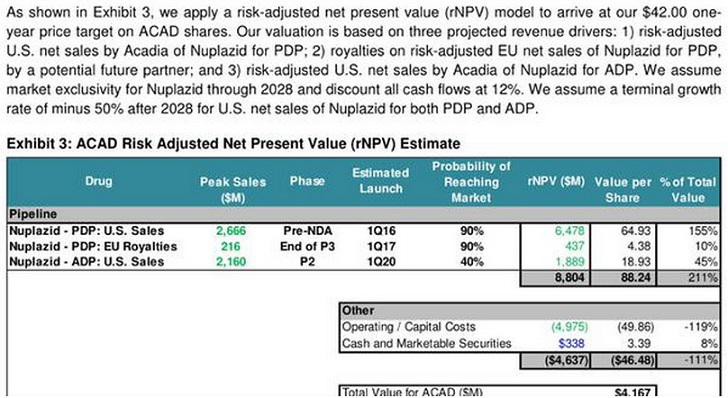
Schätzungen zu Psychosen bei Parkinson... der ersten Indikation.

Später könnte es auch bei Alzheimer-Psychosen zugelassen werden (vorher vielleicht schon off-label)

Dazu könnten noch weitere Indikationen kommen. Hier sind z.B. Schätzungen für US-Umsätze bei fast 8 Mrd USD... das liegt im Bereich von z.B. CELG heute, einem 100 Mrd USD MK Biotech.
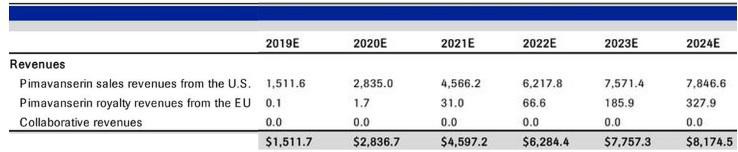


Anders als andere Medikamente dieser Art wirkt Nuplazid im wesentlichen nur auch das gewünschte Zeil-Target 5HT2a
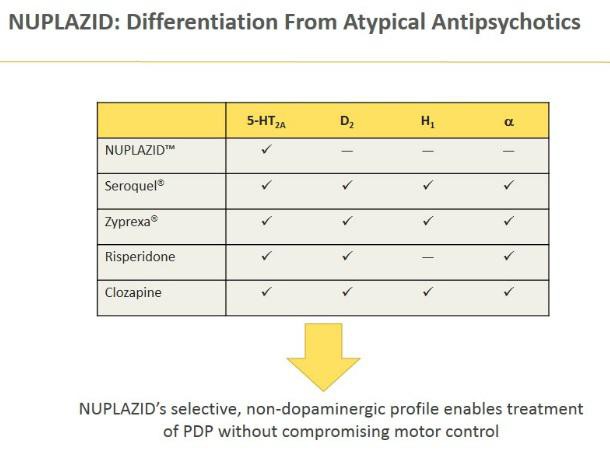

Gruß
ipollit
Zuletzt habe ich meine Position weiter erhöht. Nuplazid besitzt für den CNS-Bereich ein relativ geringes Zulassungs-Risiko (u.a. BTD von der FDA)... das Potential kann aufgrund der relativ geringen Nebenwirkungen im Mrd-Bereich liegen. Bei 100% der Rechte ist das sehr interessant.

Schätzungen zu Psychosen bei Parkinson... der ersten Indikation.

Später könnte es auch bei Alzheimer-Psychosen zugelassen werden (vorher vielleicht schon off-label)

Dazu könnten noch weitere Indikationen kommen. Hier sind z.B. Schätzungen für US-Umsätze bei fast 8 Mrd USD... das liegt im Bereich von z.B. CELG heute, einem 100 Mrd USD MK Biotech.



Anders als andere Medikamente dieser Art wirkt Nuplazid im wesentlichen nur auch das gewünschte Zeil-Target 5HT2a

Gruß
ipollit
IPH.PA
Innate wird im Folgenden als aussichtsreicher möglicher europäischer Übernahmekandidat gesehen...
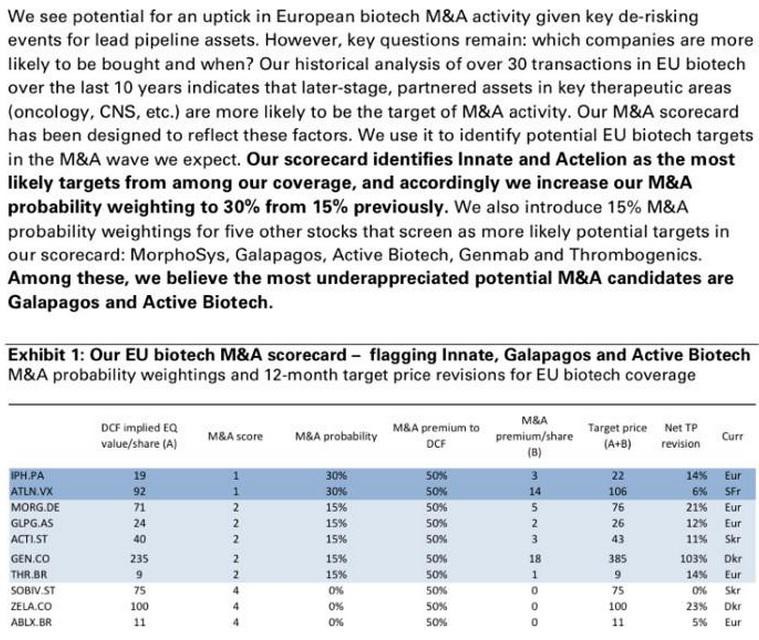
Momentan gibt es drei interessante Entwicklungen:
- Liri-Mono PII-Daten in AML Ende des Jahres (die zu einer Zulassung führen können
- Liri-Kombi-Daten u.a. mit PD-1 (BMS hat zuletzt Liri nachträglich einigen Kombinationen hinzugefügt) in soliden Tumoren (Liri kann u.a. auch interessant in Kombi mit AKs sein, da es ADCC steigern kann)
- erste IPH2201-PII Daten... Innate möchte mit guten RR-Daten eine vorzeitige Zulassung erreichen



Schön wäre auch ein US-Listing... z.B. der französische CART-Biotech Cellectis hat die Tage den US-IPO als CLLS angekündigt.

Gruß
ipollit
Innate wird im Folgenden als aussichtsreicher möglicher europäischer Übernahmekandidat gesehen...

Momentan gibt es drei interessante Entwicklungen:
- Liri-Mono PII-Daten in AML Ende des Jahres (die zu einer Zulassung führen können
- Liri-Kombi-Daten u.a. mit PD-1 (BMS hat zuletzt Liri nachträglich einigen Kombinationen hinzugefügt) in soliden Tumoren (Liri kann u.a. auch interessant in Kombi mit AKs sein, da es ADCC steigern kann)
- erste IPH2201-PII Daten... Innate möchte mit guten RR-Daten eine vorzeitige Zulassung erreichen



Schön wäre auch ein US-Listing... z.B. der französische CART-Biotech Cellectis hat die Tage den US-IPO als CLLS angekündigt.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.139.213 von ipollit am 21.02.15 23:38:39Hallo ipollit,
super Beiträge. Danke dafür! Von ACAD verspreche ich mir auch sehr viel. Ich wundere mich aber, dass der Zulassungsantrag noch immer nicht eingereicht wurde.
Man hatte ja ursprünglich immer das 4. Quartal 2014 anvisiert. Dann wurde der Termin auf das erste Quartal 2015 verschoben. Das hatte zu einem kleinen Kurseinbruch geführt. Es wurde allerdings betont, dass es keine Probleme gäbe, insbesondere brauche man keine neuen Daten, sondern nur "mehr Zeit".
Ich hatte dann eigentlich angenommen, dass sich "mehr Zeit" auf wenige Wochen belaufen würde. Jetzt sind es schon wieder fast zwei Monate.
Nächste Woche am Donnerstag kommen die Zahlen fürs Jahr 2014. Da wird Acadia zum Zulassungsantrag sicher Stellung nehmen.
Die wesentlichen Daten liegen inzwischen seit zwei Jahren vor, auch wenn man noch weitere Daten erheben musste.
Ich überlege, bei Xencor (XNCR) einzusteigen.
Die bispezifischen mabs finde ich spannend, vor allem der CD38/CD3-mab könnte viel Potential haben.
Leider ist das alles noch präklinisch.
Aus der klinischen Pipeline könnte vielleicht XmAb7195 interessant werden, der unter anderem bei Asthma wirksam sein könnte (allerdings auch noch sehr frühes Stadium der Entwicklung).
Die Pipeline ist insgesamt - obschon sehr unreif - doch recht breit und gut verpartnert.
Die Marktkapitalisierung ist für heutige Maßstäbe mit ca. 500 Mio. Dollar nicht zu hoch.
Allerdings ist nur wenig Cash vorhanden. Eine Kapitalmaßnahme - welcher Art auch immer - muss definitiv auf der Tagesordnung stehen.

super Beiträge. Danke dafür! Von ACAD verspreche ich mir auch sehr viel. Ich wundere mich aber, dass der Zulassungsantrag noch immer nicht eingereicht wurde.
Man hatte ja ursprünglich immer das 4. Quartal 2014 anvisiert. Dann wurde der Termin auf das erste Quartal 2015 verschoben. Das hatte zu einem kleinen Kurseinbruch geführt. Es wurde allerdings betont, dass es keine Probleme gäbe, insbesondere brauche man keine neuen Daten, sondern nur "mehr Zeit".
Ich hatte dann eigentlich angenommen, dass sich "mehr Zeit" auf wenige Wochen belaufen würde. Jetzt sind es schon wieder fast zwei Monate.
Nächste Woche am Donnerstag kommen die Zahlen fürs Jahr 2014. Da wird Acadia zum Zulassungsantrag sicher Stellung nehmen.
Die wesentlichen Daten liegen inzwischen seit zwei Jahren vor, auch wenn man noch weitere Daten erheben musste.
Ich überlege, bei Xencor (XNCR) einzusteigen.
Die bispezifischen mabs finde ich spannend, vor allem der CD38/CD3-mab könnte viel Potential haben.
Leider ist das alles noch präklinisch.
Aus der klinischen Pipeline könnte vielleicht XmAb7195 interessant werden, der unter anderem bei Asthma wirksam sein könnte (allerdings auch noch sehr frühes Stadium der Entwicklung).
Die Pipeline ist insgesamt - obschon sehr unreif - doch recht breit und gut verpartnert.
Die Marktkapitalisierung ist für heutige Maßstäbe mit ca. 500 Mio. Dollar nicht zu hoch.
Allerdings ist nur wenig Cash vorhanden. Eine Kapitalmaßnahme - welcher Art auch immer - muss definitiv auf der Tagesordnung stehen.

Antwort auf Beitrag Nr.: 49.140.056 von SLGramann am 22.02.15 10:24:40Hallo SLGramann,
als Biotechs im Bereich der bi-AKs fallen mir Xencor (XNCR), Macrogenics (MGNX), Genmab (GEN.CO) und die deutsche Affimed (AFMD) ein... u.U. haben auch andere entsprechende Technologien, so hat z.B. REGN einen CD20 x CD3 in PI gebracht.
Die Idee, bi-spezifische AKs zu entwickeln, gibt es schon lange... früher war man technologisch aber noch nicht so weit, stabile bi-AKs oder ähnliches zu konstruieren. Micromet war wohl einer der ersten, die hier entscheidende Fortschritte geschafft haben. Inzwischen ist der CD19 x CD3 BITE Blinatumomab zugelassen. Ein Problem dieser ersten BITEs ist aber, dass sie sehr schnell aus dem Blut gefiltert werden. So weit ich es verstehe, handelt es sich bei BITE nur um Stückchen des AKs und zwar die vorderen Bereiche des AKs, die an die Zielzelle andocken (nano-AK). Ein Vorteil von diesen kleinen Fromate ist, dass sie besser in das Gewebe eindringen können als z.B. komplette AKs (bei Blutkrebs ist das irrelevant)... ein großer Nachteil aber eben, dass sie schnell unwirksam werden. Dadurch muss z.B. Blinatumomab per kontinuierlicher Infusion verabreicht werden... man braucht also über Wochen eine permanente Infusionspumpe.
Richtige AKs besitzen dagegen noch den Fc-Bereich, der den AK stabilisiert und für die Wechselwirkungen mit dem Immunsystem wie ADCC verantwortlich ist. Dadurch wird der AK aber größer und kann nicht mehr so gut in das Tumorgewebe eindringen. Dafür kann man solche AKs dann aber z.B. einmal pro Woche per IV oder subkutan verabreichen und auch besser lagern. Das klingt erstmal gut. Für die Anwendung mit T-Zellen, also CD3 + X könnte es nach meinem Verständnis aber auch Nachteile geben. AKs haben immer zwei "Beinchen", die normalerweise das gleiche Target wie z.B. CD20 binden. Bei bi-Aks bindet jedes Bein an ein anderes Target... also eins an CD3 (T-Zelle) und das andere an CD20 (Krebszelle). Ich bin kein Experte, aber dieses natürliche Format klingt für mich nicht sehr kompakt. Nachdem, was ich zu BITE und DART gelesen habe, hat auch der Abstand dieser beiden Bindestellen eine Relevanz. Wenn sie nicht nicht eng aneinander liegen, kann es sein, dass ein solcher bi-AK zwar die T-Zelle an z.B. die CD20-Krebszelle bindet, die T-Zelle aufgrund des Abstands aber nicht richtig aktiviert wird. BITE (oder DART) sind sehr kompakte Strukturen, da es erstmal nur die Beinchen sind, die direkt miteinander verbunden sind. Die T-Zelle bindet sehr eng an die CD20-Krebszelle und erkennt diese daraufhin als Ziel, das zerstört werden soll. Nach meinem Verständnis (ich bin kein Experte) muss sich also erst zeigen, welche Formate bei CD3 + X am wirkungsvollsten sind... und echten klinischen Studien nicht in der Präklinik.
Neben den beiden Beinchen (bi-AKs) kann man auch den fc-Bereich verbessern, um z.B. ADCC zu erhöhen. Der fc-Bereich bindet auch an z.B. NK-Zellen und signalisiert diesen, dass sie z.B. bei Rituxan das CD20-Target eliminieren sollen, sobald der AK an eine CD20-Zelle gebunden hat. Dieser fc-Bereich sendet auch positive und negative Signale an das Immunsystem. Eine fc-Optimierung aktiviert diese ADCC-Reaktion stärker. Angeblich soll z.B. Rituxan oder Herceptin im wesentlichen auf diesem Mechanismus beruhen.
Für mein Verständnis ist XNCR u.a. auf diese fc-Optimierung spezialisiert (z.B. MOR208). XNCRs bi-AKs entsprechen wohl eher den echten AKs...

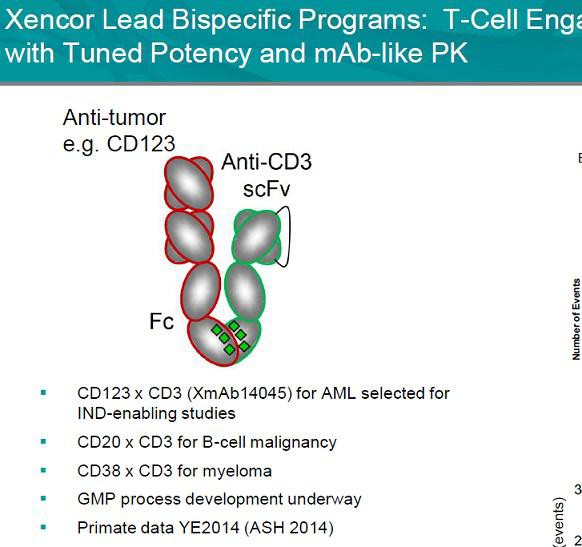
Dieses Format scheint auch Genmab zu haben, wobei diese betonen, sehr nah an natürlichen AKs zu sein... d.h. bi-AKs die im Vergleich zu natürlichen AKs nur sehr wenig modifiziert worden sind (Modifikationen können vielleicht Nebenwirkungen wie auto-AKs oder unerwünschtes Vehalten provozieren???). Genmab ist aber noch nicht in der Klinik und hat bisher wohl auch keine eigene biAK-Pipeline.
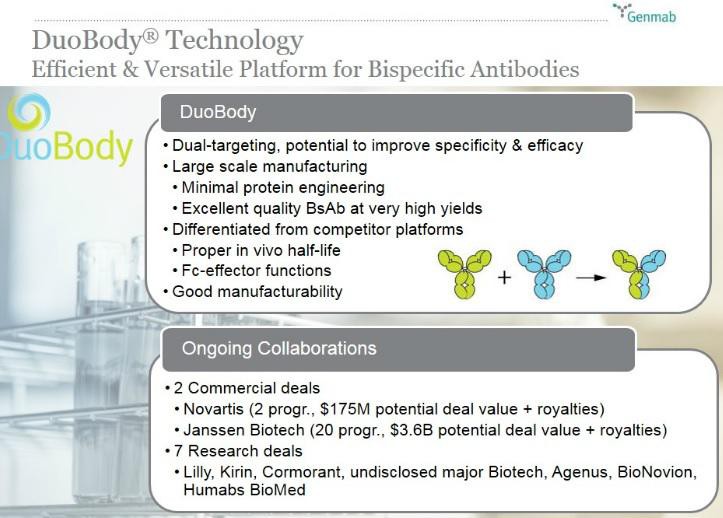
Mein Favorit ist MGNX mit den DARTs. Diese entsprechen den BITEs, sind also erstmal nur die Beinchen. Zuletzt hat MGNX zur Stabilisieurng aber diese Beinchen noch einen fc-Bereich hinzugefügt, so dass sie auch 1x pro Woche oder länger dosieren können. Die zwei Targets binden aber nicht an den beiden Beinchen, sondern direkt an einem in der kompakten Struktur.
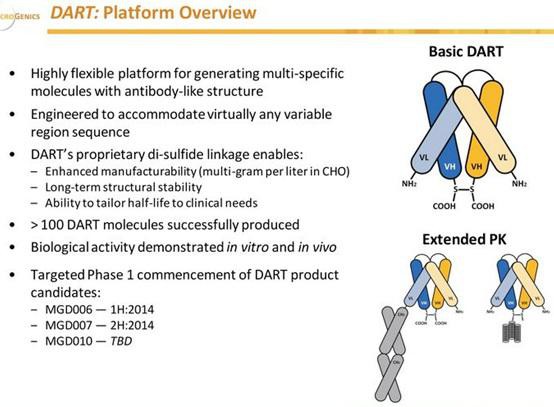
Desweiteren ist MGNX schon in der Klinik. Die Targets sind meiner Meinung nach auch besser... der Klassiker CD19 (wie Blinatumomab) gegen Blutkrebs. Dann noch CD123 (IL-3R) wie STMLs SL-401 auch gegen Blutkrebs... CD123 könnte in AML auch Krebs-Stammmzellen beseitigen (diese überleben oft die Chemo und führen u.U. dazu, dass der Krebs nicht geheilt werden kann). gpA33 ist ein krebsspzifisches Target, das bei Darmkrebs verbreitet ist. MGNX selbst hat noch einen DART, der dieses Jahr in PI gehen sollen, dessen Target aber noch nicht veröffentlicht wurde... er soll ich aber gegen solide Tumore richten (vielleicht EGFRvIII???). Und mit Takeda hat man auch einen Autoimmun-DART CD23B x CD79B. Bei allen diesen DARTs hat man trotz der Pharma-Partner noch nennswerte Rechte (z.B. sind 50% der US-Rechte möglich... mit Servier hat man bereits 100% US-Rechte).
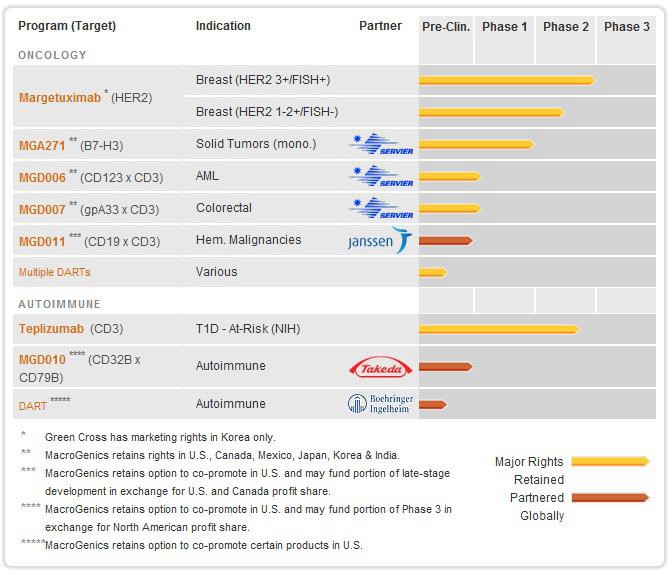
AFMDs bi-AKs entsprechen auch den BITEs. Am weitesten ist AFM13 in PII gegen Blutkrebs. Hierbei handelt es sich aber um keine T-Zell AK, sondern es bindet an NK-Zellen... könnte auch interessant sein. Das Target ist CD30 wie bei SGENs ADCETRIS. Daneben scheint die Pipeline noch recht dünn zu sein.

Anders als BITE sind die AFMD-biAks quasi doppelte BITEs... also 4 Beinchen. Jeweils zwei binden an das Target und 2 an die T-Zelle, wodurch eine höhere T-Zell-Bindung möglich sein soll. Zudem können so auch tri-AKs erzeugt werden... z.B. CD3 + 2 Targets. Vielleicht ist das sicherer, wenn dann Krebszellen bevorzugt werden, die gleichzeitig 2 Krebs-Targets besitzen. Bei diesen Targets ist nämlich stets das Problem, dass sie auch auf gesunden Zellen vorkommen können und somit das Immunsystem sich auch gegen gesunde Zellen richtet (das wäre aufgrund der Stärke des Immunsystems gravierender als bei normalen AKs oder ADCs, bei denen es auch schon zu problematischen Nebenwirkungen führen kann). AFMD-biAks scheinen zwar keine permanente IV zu benötigen (tägliche Dosis), doch sind sie offensichtlich auch nicht speziell mit fc oder ähnlichem versehen.

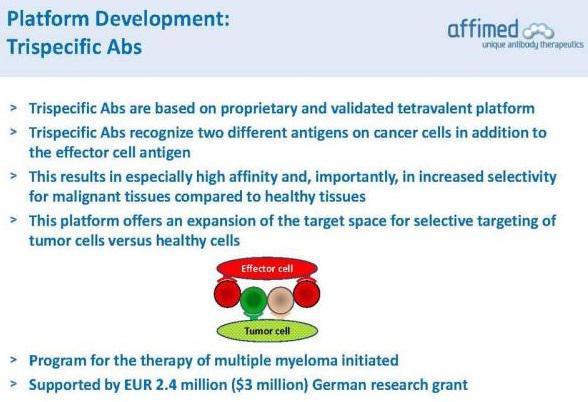

AKs wie auch bi-AKs oder CARTs werden oft gegen Blutkrebsarten entwickelt. Hier besteht der Vorteil, dass man auch gesunde Zellen eleminieren kann, die sich später regenerieren. CD20, CD19 oder CD38 gehören dazu... das sind Target, die auf B-Zellen vorkommen. Ein CD19-BITE beseitigt alle B-Zellen mit CD19, egal ob krank oder gesund. Mit der Zeit werden wieder neue B-Zellen gebildet. Ist hier CD38 ein besseren Target als z.B. CD19? Anders sieht es bei soliden Tumoren aus. Wenn beispielsweise ein EGFR-BITE nicht nur Darmkrebs, sondern auch Hautzellen zerstört, ist dies ein Problem, da diese sich nicht einfach regenerieren. Daher finde ich es interessant, welche Targets man in diesem Bereich auswählt und ob diese dann auch praktikabel sind. AFMD hat mit AFM21 z.B. einen EGFRvIII + CD3 biAK (EGFRvIII ist eine EGFR-Variante, die sich wohl im wesentlichen auf Krebs beschränkt. EGFRvIII ist auch das Target von CLDX Rindopepimut, ein therapeutischer Impfstoff gegen Gehintumore mit EGFRvIII. CLDX meinte kürzlich auf die Frage, wie die Konkurrenz-Situation zu EGFRvIII CART/biAKs sei, dass Rindopepimut als Impfstoff bereits alle EGFRvIII-Zellen beseitigen würde und somit kein Bedarf mehr an weiteren EGFRvIII-Mitteln bestehen würde. Das ist ja auch so eine Frage... mit einem biAK oder CART kann man vielleicht alle Zellen mit dem entsprechenden Target beseitigen... Krebs-Zellen können aber einfach immun werden, wenn sie dieses Target verlieren.

MKs
- MGNX... 997 Mio USD
- XNCR... 473 Mio USD
- AFMD... 130 Mio USD
Grüße
ipollit
als Biotechs im Bereich der bi-AKs fallen mir Xencor (XNCR), Macrogenics (MGNX), Genmab (GEN.CO) und die deutsche Affimed (AFMD) ein... u.U. haben auch andere entsprechende Technologien, so hat z.B. REGN einen CD20 x CD3 in PI gebracht.
Die Idee, bi-spezifische AKs zu entwickeln, gibt es schon lange... früher war man technologisch aber noch nicht so weit, stabile bi-AKs oder ähnliches zu konstruieren. Micromet war wohl einer der ersten, die hier entscheidende Fortschritte geschafft haben. Inzwischen ist der CD19 x CD3 BITE Blinatumomab zugelassen. Ein Problem dieser ersten BITEs ist aber, dass sie sehr schnell aus dem Blut gefiltert werden. So weit ich es verstehe, handelt es sich bei BITE nur um Stückchen des AKs und zwar die vorderen Bereiche des AKs, die an die Zielzelle andocken (nano-AK). Ein Vorteil von diesen kleinen Fromate ist, dass sie besser in das Gewebe eindringen können als z.B. komplette AKs (bei Blutkrebs ist das irrelevant)... ein großer Nachteil aber eben, dass sie schnell unwirksam werden. Dadurch muss z.B. Blinatumomab per kontinuierlicher Infusion verabreicht werden... man braucht also über Wochen eine permanente Infusionspumpe.
Richtige AKs besitzen dagegen noch den Fc-Bereich, der den AK stabilisiert und für die Wechselwirkungen mit dem Immunsystem wie ADCC verantwortlich ist. Dadurch wird der AK aber größer und kann nicht mehr so gut in das Tumorgewebe eindringen. Dafür kann man solche AKs dann aber z.B. einmal pro Woche per IV oder subkutan verabreichen und auch besser lagern. Das klingt erstmal gut. Für die Anwendung mit T-Zellen, also CD3 + X könnte es nach meinem Verständnis aber auch Nachteile geben. AKs haben immer zwei "Beinchen", die normalerweise das gleiche Target wie z.B. CD20 binden. Bei bi-Aks bindet jedes Bein an ein anderes Target... also eins an CD3 (T-Zelle) und das andere an CD20 (Krebszelle). Ich bin kein Experte, aber dieses natürliche Format klingt für mich nicht sehr kompakt. Nachdem, was ich zu BITE und DART gelesen habe, hat auch der Abstand dieser beiden Bindestellen eine Relevanz. Wenn sie nicht nicht eng aneinander liegen, kann es sein, dass ein solcher bi-AK zwar die T-Zelle an z.B. die CD20-Krebszelle bindet, die T-Zelle aufgrund des Abstands aber nicht richtig aktiviert wird. BITE (oder DART) sind sehr kompakte Strukturen, da es erstmal nur die Beinchen sind, die direkt miteinander verbunden sind. Die T-Zelle bindet sehr eng an die CD20-Krebszelle und erkennt diese daraufhin als Ziel, das zerstört werden soll. Nach meinem Verständnis (ich bin kein Experte) muss sich also erst zeigen, welche Formate bei CD3 + X am wirkungsvollsten sind... und echten klinischen Studien nicht in der Präklinik.
Neben den beiden Beinchen (bi-AKs) kann man auch den fc-Bereich verbessern, um z.B. ADCC zu erhöhen. Der fc-Bereich bindet auch an z.B. NK-Zellen und signalisiert diesen, dass sie z.B. bei Rituxan das CD20-Target eliminieren sollen, sobald der AK an eine CD20-Zelle gebunden hat. Dieser fc-Bereich sendet auch positive und negative Signale an das Immunsystem. Eine fc-Optimierung aktiviert diese ADCC-Reaktion stärker. Angeblich soll z.B. Rituxan oder Herceptin im wesentlichen auf diesem Mechanismus beruhen.
Für mein Verständnis ist XNCR u.a. auf diese fc-Optimierung spezialisiert (z.B. MOR208). XNCRs bi-AKs entsprechen wohl eher den echten AKs...


Dieses Format scheint auch Genmab zu haben, wobei diese betonen, sehr nah an natürlichen AKs zu sein... d.h. bi-AKs die im Vergleich zu natürlichen AKs nur sehr wenig modifiziert worden sind (Modifikationen können vielleicht Nebenwirkungen wie auto-AKs oder unerwünschtes Vehalten provozieren???). Genmab ist aber noch nicht in der Klinik und hat bisher wohl auch keine eigene biAK-Pipeline.

Mein Favorit ist MGNX mit den DARTs. Diese entsprechen den BITEs, sind also erstmal nur die Beinchen. Zuletzt hat MGNX zur Stabilisieurng aber diese Beinchen noch einen fc-Bereich hinzugefügt, so dass sie auch 1x pro Woche oder länger dosieren können. Die zwei Targets binden aber nicht an den beiden Beinchen, sondern direkt an einem in der kompakten Struktur.

Desweiteren ist MGNX schon in der Klinik. Die Targets sind meiner Meinung nach auch besser... der Klassiker CD19 (wie Blinatumomab) gegen Blutkrebs. Dann noch CD123 (IL-3R) wie STMLs SL-401 auch gegen Blutkrebs... CD123 könnte in AML auch Krebs-Stammmzellen beseitigen (diese überleben oft die Chemo und führen u.U. dazu, dass der Krebs nicht geheilt werden kann). gpA33 ist ein krebsspzifisches Target, das bei Darmkrebs verbreitet ist. MGNX selbst hat noch einen DART, der dieses Jahr in PI gehen sollen, dessen Target aber noch nicht veröffentlicht wurde... er soll ich aber gegen solide Tumore richten (vielleicht EGFRvIII???). Und mit Takeda hat man auch einen Autoimmun-DART CD23B x CD79B. Bei allen diesen DARTs hat man trotz der Pharma-Partner noch nennswerte Rechte (z.B. sind 50% der US-Rechte möglich... mit Servier hat man bereits 100% US-Rechte).

AFMDs bi-AKs entsprechen auch den BITEs. Am weitesten ist AFM13 in PII gegen Blutkrebs. Hierbei handelt es sich aber um keine T-Zell AK, sondern es bindet an NK-Zellen... könnte auch interessant sein. Das Target ist CD30 wie bei SGENs ADCETRIS. Daneben scheint die Pipeline noch recht dünn zu sein.

Anders als BITE sind die AFMD-biAks quasi doppelte BITEs... also 4 Beinchen. Jeweils zwei binden an das Target und 2 an die T-Zelle, wodurch eine höhere T-Zell-Bindung möglich sein soll. Zudem können so auch tri-AKs erzeugt werden... z.B. CD3 + 2 Targets. Vielleicht ist das sicherer, wenn dann Krebszellen bevorzugt werden, die gleichzeitig 2 Krebs-Targets besitzen. Bei diesen Targets ist nämlich stets das Problem, dass sie auch auf gesunden Zellen vorkommen können und somit das Immunsystem sich auch gegen gesunde Zellen richtet (das wäre aufgrund der Stärke des Immunsystems gravierender als bei normalen AKs oder ADCs, bei denen es auch schon zu problematischen Nebenwirkungen führen kann). AFMD-biAks scheinen zwar keine permanente IV zu benötigen (tägliche Dosis), doch sind sie offensichtlich auch nicht speziell mit fc oder ähnlichem versehen.



AKs wie auch bi-AKs oder CARTs werden oft gegen Blutkrebsarten entwickelt. Hier besteht der Vorteil, dass man auch gesunde Zellen eleminieren kann, die sich später regenerieren. CD20, CD19 oder CD38 gehören dazu... das sind Target, die auf B-Zellen vorkommen. Ein CD19-BITE beseitigt alle B-Zellen mit CD19, egal ob krank oder gesund. Mit der Zeit werden wieder neue B-Zellen gebildet. Ist hier CD38 ein besseren Target als z.B. CD19? Anders sieht es bei soliden Tumoren aus. Wenn beispielsweise ein EGFR-BITE nicht nur Darmkrebs, sondern auch Hautzellen zerstört, ist dies ein Problem, da diese sich nicht einfach regenerieren. Daher finde ich es interessant, welche Targets man in diesem Bereich auswählt und ob diese dann auch praktikabel sind. AFMD hat mit AFM21 z.B. einen EGFRvIII + CD3 biAK (EGFRvIII ist eine EGFR-Variante, die sich wohl im wesentlichen auf Krebs beschränkt. EGFRvIII ist auch das Target von CLDX Rindopepimut, ein therapeutischer Impfstoff gegen Gehintumore mit EGFRvIII. CLDX meinte kürzlich auf die Frage, wie die Konkurrenz-Situation zu EGFRvIII CART/biAKs sei, dass Rindopepimut als Impfstoff bereits alle EGFRvIII-Zellen beseitigen würde und somit kein Bedarf mehr an weiteren EGFRvIII-Mitteln bestehen würde. Das ist ja auch so eine Frage... mit einem biAK oder CART kann man vielleicht alle Zellen mit dem entsprechenden Target beseitigen... Krebs-Zellen können aber einfach immun werden, wenn sie dieses Target verlieren.

MKs
- MGNX... 997 Mio USD
- XNCR... 473 Mio USD
- AFMD... 130 Mio USD
Grüße
ipollit
Antwort auf Beitrag Nr.: 49.141.394 von ipollit am 22.02.15 15:09:56Hallo ipollit,
sehr schöne Übersicht von Dir! Ich favorisiere ebenfalls MGNX. Ist mir nach wie vor unverständlich, warum Hammer die nie ins Depot genommen hat. Bei Micromet war er damals ganz früh dabei und war - zurecht - sehr positiv eingestellt.
Genmab habe ich ja auch im Depot... Und hier sind wir beim Kern meiner Gedanken. Ich frage mich nämlich, ob ich Genmab nicht ganz verkaufen sollte. Sie haben nur einen mäßigen Anteil an Daratumumab und der Rest der Pipeline ist kommerziell fragwürdig oder eben einfach noch sehr, sehr unreif.
Die Marktkapitalisierung beträgt hingegen 4 Milliarden Dollar. Ich will gar nicht sagen, dass das nicht durch Daratumumab gerechtfertigt wäre. Ich denke, es ist gerechtfertigt. Aber wie viel weiteres Potential ist noch da? So mal ganz grob über den Daumen gepeilt würde ich sagen, dass für eine weitere Verdopplung auf dann 8 Mrd. Dollar Daratumumab dann schon Umsätze von 3 Milliarden Dollar ansteuern sollte. Und das ist schon eine Hausnummer.
Ich denke daher verstärkt über alternative Investitionsmöglichkeiten zu Genmab nach.
Auch an unsere etwas verrückte Intercept denke ich wieder. Dass sie einen Breaktrough bekommen haben, hat mich überrascht nach dem Trödel den es damals wegen der Cholesterin-Sache gab. Die FDA scheint das aber nicht als kriegsentscheidend anzusehen.
Gruß
SLG
sehr schöne Übersicht von Dir! Ich favorisiere ebenfalls MGNX. Ist mir nach wie vor unverständlich, warum Hammer die nie ins Depot genommen hat. Bei Micromet war er damals ganz früh dabei und war - zurecht - sehr positiv eingestellt.
Genmab habe ich ja auch im Depot... Und hier sind wir beim Kern meiner Gedanken. Ich frage mich nämlich, ob ich Genmab nicht ganz verkaufen sollte. Sie haben nur einen mäßigen Anteil an Daratumumab und der Rest der Pipeline ist kommerziell fragwürdig oder eben einfach noch sehr, sehr unreif.
Die Marktkapitalisierung beträgt hingegen 4 Milliarden Dollar. Ich will gar nicht sagen, dass das nicht durch Daratumumab gerechtfertigt wäre. Ich denke, es ist gerechtfertigt. Aber wie viel weiteres Potential ist noch da? So mal ganz grob über den Daumen gepeilt würde ich sagen, dass für eine weitere Verdopplung auf dann 8 Mrd. Dollar Daratumumab dann schon Umsätze von 3 Milliarden Dollar ansteuern sollte. Und das ist schon eine Hausnummer.
Ich denke daher verstärkt über alternative Investitionsmöglichkeiten zu Genmab nach.
Auch an unsere etwas verrückte Intercept denke ich wieder. Dass sie einen Breaktrough bekommen haben, hat mich überrascht nach dem Trödel den es damals wegen der Cholesterin-Sache gab. Die FDA scheint das aber nicht als kriegsentscheidend anzusehen.
Gruß
SLG
AERI
"New wave of drugs poised to shake up glaucoma treatment"
http://www.reuters.com/article/2015/02/10/us-health-glaucoma…
Nach wie vor gibt es einen hohen Bedarf an neuen Mitteln gegen Glaucoma: "... We continue to have people who are going blind from glaucoma and that's a problem," said Dr. Wiley Chambers, deputy director of the U.S. Food and Drug Administration’s transplant and ophthalmology products. "We need alternatives."
So far, analysts are betting that Aerie's second drug, Roclatan, will be the most effective at lowering eye pressure. It is a fixed-dose combination product that includes Rhopressa and latanoprost..."
$AERI Phase 3 registration studies, three-month efficacy results are expected in the middle of 2ndQ2015 for Rocket 1 + mid-2015 for Rocket 2
***
Rhopressa könnte ein wirklicher Fortschritt sein:
http://investors.aeriepharma.com/releasedetail.cfm?ReleaseID…
Aerie Pharmaceuticals Announces Potential Breakthroughs with New Preclinical Research
Rhopressa™ Displays Preliminary Evidence of Disease-Modifying Activity in Glaucoma
...This is the first study to show that RhopressaTM, a novel once-daily, triple-action eye drop that lowers IOP in glaucoma patients, has the potential to modify the course of the disease by arresting fibrosis...
***
eine aktuelle Meinung zu AERI:
https://www.youtube.com/watch?v=8ff9rFkakc0&feature=youtu.be

Gruß
ipollit
"New wave of drugs poised to shake up glaucoma treatment"
http://www.reuters.com/article/2015/02/10/us-health-glaucoma…
Nach wie vor gibt es einen hohen Bedarf an neuen Mitteln gegen Glaucoma: "... We continue to have people who are going blind from glaucoma and that's a problem," said Dr. Wiley Chambers, deputy director of the U.S. Food and Drug Administration’s transplant and ophthalmology products. "We need alternatives."
So far, analysts are betting that Aerie's second drug, Roclatan, will be the most effective at lowering eye pressure. It is a fixed-dose combination product that includes Rhopressa and latanoprost..."
$AERI Phase 3 registration studies, three-month efficacy results are expected in the middle of 2ndQ2015 for Rocket 1 + mid-2015 for Rocket 2
***
Rhopressa könnte ein wirklicher Fortschritt sein:
http://investors.aeriepharma.com/releasedetail.cfm?ReleaseID…
Aerie Pharmaceuticals Announces Potential Breakthroughs with New Preclinical Research
Rhopressa™ Displays Preliminary Evidence of Disease-Modifying Activity in Glaucoma
...This is the first study to show that RhopressaTM, a novel once-daily, triple-action eye drop that lowers IOP in glaucoma patients, has the potential to modify the course of the disease by arresting fibrosis...
***
eine aktuelle Meinung zu AERI:
https://www.youtube.com/watch?v=8ff9rFkakc0&feature=youtu.be
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.141.892 von ipollit am 22.02.15 17:19:58Ohad sieht sowhl bei AERI als auch bei ESPR eine Übernahme für wahrscheinlich an in den nächsten Monaten. Für ESPR sieht das die Credit Suisse ähnlich und hatte auf dieser Basis bereits kürzlich das Kursziel auf USD 100 angehoben: http://www.benzinga.com/analyst-ratings/analyst-color/15/02/…
Antwort auf Beitrag Nr.: 49.141.670 von SLGramann am 22.02.15 16:05:48Genmab ... ja, das sehe ich auch so wie du. Zuletzt habe ich meine Position etwas reduziert, da ich für Dara zwar 3 Mrd USD für möglich halte, Genmab davon aber nur Royalties von vielleicht 15% erhält. Die peak sales wird es auch erst längerfristig geben nach einer 1st-line Zulassung.
Andererseits hat der Kurs bisher eigentlich keine Schwäche gezeigt. Und Arzerra könne in den nächsten Jahren bei NVS doch noch 1 Mrd USD Umsatz erreichen... Royalties liegen bei ca. 20%.

Gruß
ipollit
Andererseits hat der Kurs bisher eigentlich keine Schwäche gezeigt. Und Arzerra könne in den nächsten Jahren bei NVS doch noch 1 Mrd USD Umsatz erreichen... Royalties liegen bei ca. 20%.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.141.952 von SpanishEyes am 22.02.15 17:35:21Übernahme... da hätte ich nichts gegen, wäre schön! Mal schauen...
Gruß
ipollit
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.142.000 von ipollit am 22.02.15 17:44:19Kaum schreibe ich es, widmet Ohad wenige Studen später den beiden Werten auch schon einen kompletten neuen Artikel - netter Zufall
http://www.orf-blog.com/esperion-and-aerie-countdown-to-ma/

http://www.orf-blog.com/esperion-and-aerie-countdown-to-ma/
CLDX:
Breakthrough für Rindopepimut!
Sieht es jetzt eventuell gut aus für eine vorzeitige (vorläufige) Zulassung auf Basis der anstehenden ReAct-Daten?
Celldex's Rindopepimut (Rintega(R)) Receives FDA Breakthrough Therapy Designation for the Treatment of Adult Patients with EGFRvIII-positive Glioblastoma
HAMPTON, N.J., Feb. 23, 2015 (GLOBE NEWSWIRE) -- Celldex Therapeutics, Inc. (Nasdaq:CLDX) today announced that the U.S. Food and Drug Administration (FDA) has granted rindopepimut (Rintega®) Breakthrough Therapy Designation for the treatment of adult patients with EGFRvIII-positive glioblastoma (GBM).
Breakthrough für Rindopepimut!
Sieht es jetzt eventuell gut aus für eine vorzeitige (vorläufige) Zulassung auf Basis der anstehenden ReAct-Daten?
Celldex's Rindopepimut (Rintega(R)) Receives FDA Breakthrough Therapy Designation for the Treatment of Adult Patients with EGFRvIII-positive Glioblastoma
HAMPTON, N.J., Feb. 23, 2015 (GLOBE NEWSWIRE) -- Celldex Therapeutics, Inc. (Nasdaq:CLDX) today announced that the U.S. Food and Drug Administration (FDA) has granted rindopepimut (Rintega®) Breakthrough Therapy Designation for the treatment of adult patients with EGFRvIII-positive glioblastoma (GBM).
Antwort auf Beitrag Nr.: 49.148.891 von SLGramann am 23.02.15 15:38:33Wedbush:

Wedbush $CLDX OUTPERFORM : Breakthrough for Rindopepimut Signals FDA's Likely Favorable View of Glioblastoma Data

Wedbush $CLDX OUTPERFORM : Breakthrough for Rindopepimut Signals FDA's Likely Favorable View of Glioblastoma Data
ARRY
Das klingt für mich so, als wäre die Entscheidung Seitens der US-Kartellbehörde nur noch eine Frage der Zeit. Die Kartellbehörden haben sich scheinbar abgestimmt (was natürlich auch Sinn macht)
http://www.in-pharmatechnologist.com/Processing/FTC-requires…
LOXO (ARRY, MRTX, RXDX, TSRO...)
Ein wirklich mal toller Artikel über Seeking Alpha, der u.A. LOXO beinhaltet.
Loxo hat gerade bekannt gegeben, dass sie am 2.3. ein Programmupdate geben werden. Dort könnten erste Ergebnisse der PIa zu 101 präsentiert werden (Unselected, Sicherheitsstudie, evtl. aber "NTRK positive" dabei). Wichtiger wird dann die PIb, die nur NTRK+ Patienten untersuchen soll.
Ebenso könnten nähere Details zum 2. Programm (Target?) bekannt gegeben werden. Loxo hat eine Partnershaft mit ARRY. ARRY wird für die präklinische Arbeit bezahlt und bekäme dann u.A. 5% Royalties. Bei 101 hoffentlich mehr.
http://seekingalpha.com/article/2926906-investing-in-precisi…
Noch etwas Älteres mit Verweis auch auf FMI, die eine wichtige Rolle spielen.
http://www.eurekalert.org/pub_releases/2014-05/uocd-ara05281…
Ansonsten vielen Dank für die tollen Beiträge übers WE. Ich denke neben AERI und ESPR ist auch bei CLVS und ACAD eine Übernahme sehr wahrscheinlich.
Ich denke neben AERI und ESPR ist auch bei CLVS und ACAD eine Übernahme sehr wahrscheinlich.
SG kmastra
Das klingt für mich so, als wäre die Entscheidung Seitens der US-Kartellbehörde nur noch eine Frage der Zeit. Die Kartellbehörden haben sich scheinbar abgestimmt (was natürlich auch Sinn macht)
http://www.in-pharmatechnologist.com/Processing/FTC-requires…
LOXO (ARRY, MRTX, RXDX, TSRO...)
Ein wirklich mal toller Artikel über Seeking Alpha, der u.A. LOXO beinhaltet.
Loxo hat gerade bekannt gegeben, dass sie am 2.3. ein Programmupdate geben werden. Dort könnten erste Ergebnisse der PIa zu 101 präsentiert werden (Unselected, Sicherheitsstudie, evtl. aber "NTRK positive" dabei). Wichtiger wird dann die PIb, die nur NTRK+ Patienten untersuchen soll.
Ebenso könnten nähere Details zum 2. Programm (Target?) bekannt gegeben werden. Loxo hat eine Partnershaft mit ARRY. ARRY wird für die präklinische Arbeit bezahlt und bekäme dann u.A. 5% Royalties. Bei 101 hoffentlich mehr.
http://seekingalpha.com/article/2926906-investing-in-precisi…
Noch etwas Älteres mit Verweis auch auf FMI, die eine wichtige Rolle spielen.
http://www.eurekalert.org/pub_releases/2014-05/uocd-ara05281…
Ansonsten vielen Dank für die tollen Beiträge übers WE.
 Ich denke neben AERI und ESPR ist auch bei CLVS und ACAD eine Übernahme sehr wahrscheinlich.
Ich denke neben AERI und ESPR ist auch bei CLVS und ACAD eine Übernahme sehr wahrscheinlich. SG kmastra
Antwort auf Beitrag Nr.: 49.152.734 von kmastra am 23.02.15 20:37:29Ich bin auch sehr dankbar für diesen tollen, qualitativ hochwertigen Thread, den ich erst seit ca. Mitte letzten Jahres intensiver verfolge. Nicht zuletzt auf dieser Grundlage habe ich mir über die letzten Monate ein kleines aber ich denke feines Biotechdepot zusammengestellt:
KPTI
MGNX
IPH.PA
ESPR
ACAD
ARRY hat mir auch einen schönen Gewinn beschert, habe ich mittlerweile wieder veräussert. Von IMGN und MOR hatte ich mich ebenfalls mit (zumindest Stand heute) ganz gutem Timing noch getrennt gehabt.
-----
Zu KPTI gab es heute noch diese Meldung: http://finance.yahoo.com/news/nature-neuroscience-publishes-…
Schon beeindruckend wie breit KPTI's SINE letztlich zum Einsatz kommen könnte - Umsätze von USD 3 Mrd. scheinen möglich. Auch hier könnte es früher oder später wohl zu einer Übernahme kommen.
KPTI
MGNX
IPH.PA
ESPR
ACAD
ARRY hat mir auch einen schönen Gewinn beschert, habe ich mittlerweile wieder veräussert. Von IMGN und MOR hatte ich mich ebenfalls mit (zumindest Stand heute) ganz gutem Timing noch getrennt gehabt.
-----
Zu KPTI gab es heute noch diese Meldung: http://finance.yahoo.com/news/nature-neuroscience-publishes-…
Schon beeindruckend wie breit KPTI's SINE letztlich zum Einsatz kommen könnte - Umsätze von USD 3 Mrd. scheinen möglich. Auch hier könnte es früher oder später wohl zu einer Übernahme kommen.
MGNX
Von Stifel Research gab es Anfang des Monats noch folgende Übersicht - USD 7 Mrd. Umsatz eines Tages aus Partnerschaften/Meilensteinzahlungen wären eine Hausnummer...

Von Stifel Research gab es Anfang des Monats noch folgende Übersicht - USD 7 Mrd. Umsatz eines Tages aus Partnerschaften/Meilensteinzahlungen wären eine Hausnummer...

TSRO / CLVS
TSRO heute mit einem Sprung nach oben, nachdem Citi die Aktie auf ihre Focus Liste gesetzt haben.
Zusätzlich sehen sie im Bereich der PARP-Hemmer TSRO und CLVS als aussichtsreich.


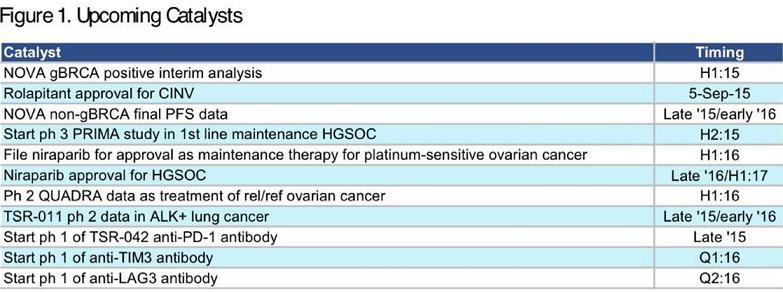
PARP-Hemmer...


Gruß
ipollit
TSRO heute mit einem Sprung nach oben, nachdem Citi die Aktie auf ihre Focus Liste gesetzt haben.
Zusätzlich sehen sie im Bereich der PARP-Hemmer TSRO und CLVS als aussichtsreich.



PARP-Hemmer...

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.153.172 von SpanishEyes am 23.02.15 21:14:15KPTI
hier noch ein Kommentar zur Entwicklung von XPO1 gegen Autoimmunerkrankungen, insbesondere MS


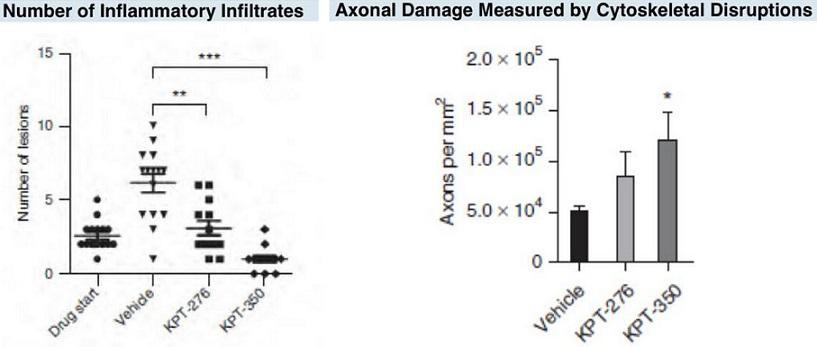
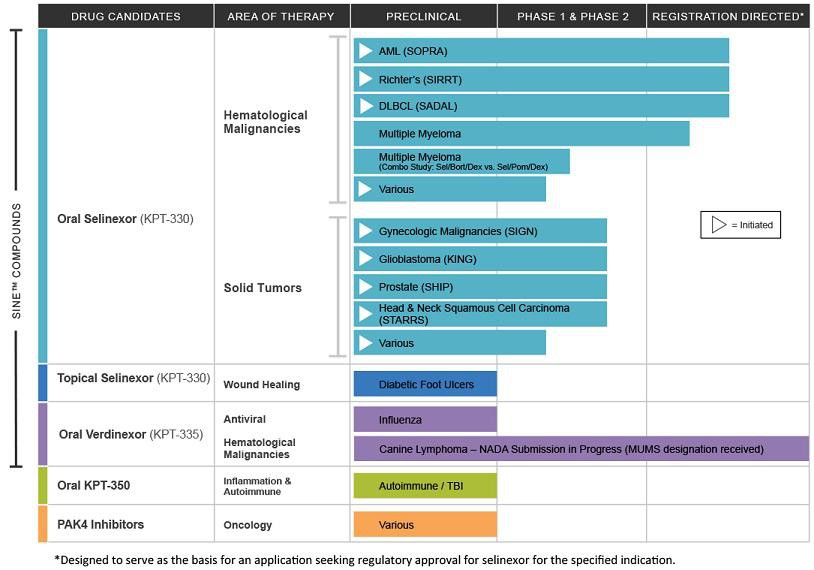

Gruß
ipollit
hier noch ein Kommentar zur Entwicklung von XPO1 gegen Autoimmunerkrankungen, insbesondere MS




Gruß
ipollit
PCYC
Um PCYC gibt es scheinbar Ernst zu nehmende Übernahmespekulationen.
http://www.bloomberg.com/news/articles/2015-02-25/pharmacycl…

SG kmastra
Um PCYC gibt es scheinbar Ernst zu nehmende Übernahmespekulationen.
http://www.bloomberg.com/news/articles/2015-02-25/pharmacycl…
SG kmastra
OTIC
Ich habe hier eine Position gekauft. Ich finde das was Brad Loncar sagt nachvollziehbar.
Die Bewertung liegt bei ca. 800 Mio US$. Sicherlich kein Schnäppchen mehr aber andereseits ist im Erfolgsfall auch noch Luft nach Oben vorhanden. Eine KE wurde gerade erfolgreich abgeschlossen. Heute wurde die Zulassung für Audipro beantragt.

Eine Linksammlung: http://www.twitlonger.com/show/n_1sko182
SG kmastra
Ich habe hier eine Position gekauft. Ich finde das was Brad Loncar sagt nachvollziehbar.
Die Bewertung liegt bei ca. 800 Mio US$. Sicherlich kein Schnäppchen mehr aber andereseits ist im Erfolgsfall auch noch Luft nach Oben vorhanden. Eine KE wurde gerade erfolgreich abgeschlossen. Heute wurde die Zulassung für Audipro beantragt.
Eine Linksammlung: http://www.twitlonger.com/show/n_1sko182
SG kmastra
NVS GSK deal
arry:Novartis-GSK-Transaktion: GSK kündigt Abschluss für nächste Woche an
London/Basel (awp) - Die grosse Portfolio-Transaktion zwischen Novartis und GlaxoSmithKline (GSK) soll früher als erwartet abgeschlossen werden. Aufgrund der guten Fortschritte und der erhaltenen Bewilligungen erwartet GSK einen Abschluss des Deals in der nächsten Woche, wie das Unternehmen am Mittwoch mitteilt.
Novartis übernimmt von GSK im Rahmen der dreiteiligen Transaktion bekanntlich gewisse Onkologie-Produkte. Zudem führen die beiden Konzerne ihre nicht rezeptpflichtigen Gesundheitsprodukte in ein Gemeinschaftsunternehmen über. Und GSK übernimmt das Impfstoff-Geschäft von Novartis.
Bisher war von einem Abschluss der Transaktion im ersten Halbjahr 2015 die Rede.
http://www.finanzen.ch/nachrichten/aktien/Novartis-GSK-Trans…
Antwort auf Beitrag Nr.: 49.196.021 von Axel_Olsson am 27.02.15 14:56:22ARRY:
Geschafft.
Array Announces Completion Of Binimetinib And Encorafenib Transactions
http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
Geschafft.
Array Announces Completion Of Binimetinib And Encorafenib Transactions
http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
AMGN, LGND, (ARRY)
Amgen gab gestern bereits überzeugende Ergebnisse der Endavour-Studie (Kyprolis vs. Velcade) bekannt:
http://www.fiercepharma.com/story/was-onyx-worth-it-amgens-c…
Zwei Analystenkommentare:


Profitieren kann davon auch LGND, die Royalties für Kyprolis bekommen. Diese Klarheit hilft der Aktie heute auf die Sprünge. Zudem herrscht seit heute Klarheit was den GSK NOV Deal betrifft. Promacta ist ein Medikament, dass jetzt von NOV vermarktet wird. Es ist ein bereits zugelassenes Medikament, dass die Bildung von Blutplättchen fördert. Ich bin deshalb heute wieder bei LGND eingestiegen, weil jetzt doch Klarheit herrscht. Werde im Ligand Thread mein Tagebuch wieder aufschlagen...
Ich traue es mich kaum zu sagen, aber die Ergebnisse der Endavour Studie haben natürlich auch eine gewisse Relevanz für ARRY und den Start der PIII von Filanesib. Die Ausichten um Kyprolis haben sich doch merklich verbessert.
SG kmastra
Amgen gab gestern bereits überzeugende Ergebnisse der Endavour-Studie (Kyprolis vs. Velcade) bekannt:
http://www.fiercepharma.com/story/was-onyx-worth-it-amgens-c…
Zwei Analystenkommentare:


Profitieren kann davon auch LGND, die Royalties für Kyprolis bekommen. Diese Klarheit hilft der Aktie heute auf die Sprünge. Zudem herrscht seit heute Klarheit was den GSK NOV Deal betrifft. Promacta ist ein Medikament, dass jetzt von NOV vermarktet wird. Es ist ein bereits zugelassenes Medikament, dass die Bildung von Blutplättchen fördert. Ich bin deshalb heute wieder bei LGND eingestiegen, weil jetzt doch Klarheit herrscht. Werde im Ligand Thread mein Tagebuch wieder aufschlagen...
Ich traue es mich kaum zu sagen, aber die Ergebnisse der Endavour Studie haben natürlich auch eine gewisse Relevanz für ARRY und den Start der PIII von Filanesib. Die Ausichten um Kyprolis haben sich doch merklich verbessert.
SG kmastra
Momentan läuft die Cowen Healthcare Conference mit einigen interessanten Firmen (ARRY, LOXO, ZFGN, OTIC, ONTY, KITE, JUNO, FMI, BLUE, INCY, EXEL...)
http://www.wsw.com/webcast/cowen22/#table1
LOXO
Heute nun das Programmupdate. RET, FGFR und FLT3 wurden als Targets bekannt gegeben. Um dazu was sagen zu können, verstehe ich zu wenig davon. Ich denke bei LOXO wird man viel Geduld benötigen.
Folgende Sicht hört sich sehr optimistisch an, wenn man bedent, dass es noch keine aussagekräftigen Studienergebnisse gibt. Mehr als eine kleine Position wage ich hier nicht. Spannend wird es wohl erst mit den Ergebnissen der PIb.


SG kmastra
http://www.wsw.com/webcast/cowen22/#table1
LOXO
Heute nun das Programmupdate. RET, FGFR und FLT3 wurden als Targets bekannt gegeben. Um dazu was sagen zu können, verstehe ich zu wenig davon. Ich denke bei LOXO wird man viel Geduld benötigen.
Folgende Sicht hört sich sehr optimistisch an, wenn man bedent, dass es noch keine aussagekräftigen Studienergebnisse gibt. Mehr als eine kleine Position wage ich hier nicht. Spannend wird es wohl erst mit den Ergebnissen der PIb.


SG kmastra
möchte mich hiermit als bisher stiller Mitleser zu Erkennen geben!
eines der besten und niveavollsten Threads bei WO, wie ich finde!
1000Dank für eure Beiträge und weiter so
Bin aktuell stark an KPTI dran und werde wohl demnächst einsteigen!
hier meine aktuellen Bio Pos.
Nur, wen es interessiert! in anderen Threads wird man dafür gleich immer blöd angemacht, siehe Juno Thread
IDRA
EXEL
AETS
TST
GALE
Watchlist Faves
KPTI
RNN
INFI
LG S.
eines der besten und niveavollsten Threads bei WO, wie ich finde!
1000Dank für eure Beiträge und weiter so

Bin aktuell stark an KPTI dran und werde wohl demnächst einsteigen!
hier meine aktuellen Bio Pos.
Nur, wen es interessiert! in anderen Threads wird man dafür gleich immer blöd angemacht, siehe Juno Thread

IDRA
EXEL
AETS
TST
GALE
Watchlist Faves
KPTI
RNN
INFI
LG S.
Antwort auf Beitrag Nr.: 49.224.476 von Schaeffi am 03.03.15 11:15:21ersetze
niveavollsten
mit
niveauvollsten
niveavollsten

mit
niveauvollsten
Antwort auf Beitrag Nr.: 49.226.030 von Schaeffi am 03.03.15 13:34:08...schließe mich dem Outing meines Vorgängers an - noch ein bisheriger stiller Mitleser - allerdings schon seit letzter Woche bei KPTI eingestiegen und heute noch ein paar nachgekauft...die Chance zu diesem Preis einfach mal genutzt. 
Für meine Begriffe ein Wert der schon einmal für Furore gesorgt hat und dies wohl wieder tun wird.
Aktuell bei mir Depotneuaufbau nach deutlich gewinnbehaftetem Ausverkauf meiner vorherigen Positionen.
Deshalb aktuell nur eine Position im Warenkorb - andere Zukäufe werde ich posten.
Schöner Schräd hier - allen Akteuren die hierzu beitragen ein Danke und weiter so...
hier - allen Akteuren die hierzu beitragen ein Danke und weiter so...

Für meine Begriffe ein Wert der schon einmal für Furore gesorgt hat und dies wohl wieder tun wird.
Aktuell bei mir Depotneuaufbau nach deutlich gewinnbehaftetem Ausverkauf meiner vorherigen Positionen.
Deshalb aktuell nur eine Position im Warenkorb - andere Zukäufe werde ich posten.
Schöner Schräd
 hier - allen Akteuren die hierzu beitragen ein Danke und weiter so...
hier - allen Akteuren die hierzu beitragen ein Danke und weiter so...
Guten Morgen zusammen,
kann mich den letzten Postings nur anschließen - höchstes Niveau was hier geboten wird, und alles auf sachlicher Ebene, ohne den - bei solchen Werten - üblicherweise unvermeidbaren Hauch von Push. Lese hier schon länger mit, und auch wenn ich generell konservativ unterwegs bin, will man doch ab und zu einen spekulativen Wert dazumischen.
Bevor aber mein Posting als Push rüberkommt; hab extra nachgeschaut. Zum einen wurde der Wert hier schon vor langer Zeit besprochen, zum anderen werden die Kurse sowieso an der Nasdaq gemacht, Umsatz ist drüben um ein XX-faches höher. Wollte also mal Eure Meinung zu Aveo Pharma hören, welche am Freitag ein Conference Call zu Tivozanib haben.
http://www.wallstreet-online.de/nachricht/7418906-aveo-oncol…
Quasi 2. Versuch, 2013 im ersten Anlauf ein Flop, der Kurs ist dementsprechend auch da wo er gerade ist. Immerhin MK zu großen Teilen durch Cash abgesichert und zwei neuere Meldungen haben mich veranlasst, eine Miniposition von 1000 Stk. zu kaufen. Zum einen wurden 2/3 der Belegschaft gekündigt, und dann der CEO ausgewechselt. Der neue - Bailey - war immerhin jahrelang bei ImClone, Genentech, Smithkline usw. Wird da evtl. eine Kooperation oder Übernahme vorbereitet ?? Ersteres wäre mir lieber, bei Biotechs spekuliert man ja generell nicht auf 30% Übernahmeprämie.
Dies zu meinen Kaufhintergründen; die Miniposition halte ich mal durch. Freitag dann hop oder top, also +-50% möglich. Würde mich aber trotzdem interessieren was Ihr von dieser PhaseII haltet bzw. welche Erfolgschancen Ihr der Firma bzw. den 4 Kandidaten einräumt.
Schönen Tag noch
Timburg
kann mich den letzten Postings nur anschließen - höchstes Niveau was hier geboten wird, und alles auf sachlicher Ebene, ohne den - bei solchen Werten - üblicherweise unvermeidbaren Hauch von Push. Lese hier schon länger mit, und auch wenn ich generell konservativ unterwegs bin, will man doch ab und zu einen spekulativen Wert dazumischen.
Bevor aber mein Posting als Push rüberkommt; hab extra nachgeschaut. Zum einen wurde der Wert hier schon vor langer Zeit besprochen, zum anderen werden die Kurse sowieso an der Nasdaq gemacht, Umsatz ist drüben um ein XX-faches höher. Wollte also mal Eure Meinung zu Aveo Pharma hören, welche am Freitag ein Conference Call zu Tivozanib haben.
http://www.wallstreet-online.de/nachricht/7418906-aveo-oncol…
Quasi 2. Versuch, 2013 im ersten Anlauf ein Flop, der Kurs ist dementsprechend auch da wo er gerade ist. Immerhin MK zu großen Teilen durch Cash abgesichert und zwei neuere Meldungen haben mich veranlasst, eine Miniposition von 1000 Stk. zu kaufen. Zum einen wurden 2/3 der Belegschaft gekündigt, und dann der CEO ausgewechselt. Der neue - Bailey - war immerhin jahrelang bei ImClone, Genentech, Smithkline usw. Wird da evtl. eine Kooperation oder Übernahme vorbereitet ?? Ersteres wäre mir lieber, bei Biotechs spekuliert man ja generell nicht auf 30% Übernahmeprämie.
Dies zu meinen Kaufhintergründen; die Miniposition halte ich mal durch. Freitag dann hop oder top, also +-50% möglich. Würde mich aber trotzdem interessieren was Ihr von dieser PhaseII haltet bzw. welche Erfolgschancen Ihr der Firma bzw. den 4 Kandidaten einräumt.
Schönen Tag noch
Timburg
Antwort auf Beitrag Nr.: 49.232.627 von Timburg am 04.03.15 06:56:49Hallo zusammen,
also ich würde mich freuen, wenn sich hier mehr Leute beteilgen. Von daher nur Mut! Ich habe hier schon viel gelernt und denke, dass das Aufschreiben und der Austausch einen nur voran bringen kann...
zu Aveo:
Aveo wurde in der Vergangenheit besprochen. Leider war ich beim ersten Versuch investiert und bin da immer ein wenig nachtragend. Diese war ja vor allem deshalb gescheitert, weil die Studie schlecht geplant war (wenn ich das richtig erinnere)
und bin da immer ein wenig nachtragend. Diese war ja vor allem deshalb gescheitert, weil die Studie schlecht geplant war (wenn ich das richtig erinnere)
Ohad Hammer hatte damals auch viel von Aveo gehalten.
http://www.orf-blog.com/buying-aveo-ahead-of-fda-panel/
Soweit ich das weiß geht es jetzt um die EU Zulassung. Eine kleine Position kann man vielleicht wagen. Man sollte sich des Risikos bewusst sein. Ich lasse da mal schön die Finger von (s.O.)
(s.O.)
SG kmastra
also ich würde mich freuen, wenn sich hier mehr Leute beteilgen. Von daher nur Mut! Ich habe hier schon viel gelernt und denke, dass das Aufschreiben und der Austausch einen nur voran bringen kann...
zu Aveo:
Aveo wurde in der Vergangenheit besprochen. Leider war ich beim ersten Versuch investiert
 und bin da immer ein wenig nachtragend. Diese war ja vor allem deshalb gescheitert, weil die Studie schlecht geplant war (wenn ich das richtig erinnere)
und bin da immer ein wenig nachtragend. Diese war ja vor allem deshalb gescheitert, weil die Studie schlecht geplant war (wenn ich das richtig erinnere) Ohad Hammer hatte damals auch viel von Aveo gehalten.
http://www.orf-blog.com/buying-aveo-ahead-of-fda-panel/
Soweit ich das weiß geht es jetzt um die EU Zulassung. Eine kleine Position kann man vielleicht wagen. Man sollte sich des Risikos bewusst sein. Ich lasse da mal schön die Finger von
 (s.O.)
(s.O.)SG kmastra
Antwort auf Beitrag Nr.: 49.231.955 von Chancenjaeger am 03.03.15 22:47:11hallo Mitstreiter
bin seit gestern auch bei KPTI dabei.
Kurs war zu verlockend für mich, mal sehen wo die Reise hingeht!
Viel Glück allen
Gruss S.

bin seit gestern auch bei KPTI dabei.
Kurs war zu verlockend für mich, mal sehen wo die Reise hingeht!
Viel Glück allen
Gruss S.
PCYC
angeblich könnte Partner JNJ in Kürze eine Übernahme von PCYC fix machen, nachdem es zuletzt entsprechende Gerüchte gab. Der Kurs müsste dem Übernahmekurs inzwischen schon recht nahe gekommen sein... viel mehr wird es jetzt wohl nicht mehr geben. Mal schauen...


Gruß
ipollit
angeblich könnte Partner JNJ in Kürze eine Übernahme von PCYC fix machen, nachdem es zuletzt entsprechende Gerüchte gab. Der Kurs müsste dem Übernahmekurs inzwischen schon recht nahe gekommen sein... viel mehr wird es jetzt wohl nicht mehr geben. Mal schauen...
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.243.289 von ipollit am 04.03.15 23:04:46http://www.bloomberg.com/news/articles/2015-03-04/j-j-said-t…
"(Bloomberg) -- Johnson & Johnson has agreed to acquire cancer-drug maker Pharmacyclics Inc., people with knowledge of the matter said. A deal may be announced as soon as Thursday, the people said, asking not to be identified discussing private information..."
"(Bloomberg) -- Johnson & Johnson has agreed to acquire cancer-drug maker Pharmacyclics Inc., people with knowledge of the matter said. A deal may be announced as soon as Thursday, the people said, asking not to be identified discussing private information..."
Antwort auf Beitrag Nr.: 49.243.502 von ipollit am 04.03.15 23:52:31Abbvie hat JNJ wohl ausgestochen. 261 Dollar pro Aktie, 21 Milliarden für 50% an Ibrutinib.
http://www.reuters.com/article/2015/03/05/us-pharmacyclics-m…
Ich kann nur sagen, dass ich meinn Kritik an Hammer zu früh verkauft zu haben, auch an mich selbst richten muss.
Ich hatte eine Marktkapitalisierung von ca. 8 Milliarden bei PCYC für ausreichend gehalten.
Das hat sich nun als schwerer Irrtum erwiesen.
http://www.reuters.com/article/2015/03/05/us-pharmacyclics-m…
Ich kann nur sagen, dass ich meinn Kritik an Hammer zu früh verkauft zu haben, auch an mich selbst richten muss.
Ich hatte eine Marktkapitalisierung von ca. 8 Milliarden bei PCYC für ausreichend gehalten.
Das hat sich nun als schwerer Irrtum erwiesen.
CLDN:

Celladon ist eine absolute rot/schwarz-Roulette-Spekulation. Wenn ihre Technik tatsächlich wirkt und hilft - was extrem unsicher ist - dann sind die 70 Dollar Kursziel ein Scherz bzw. der Anfang des Anfangs der Kurssteigerung.
Sind allerdings die CUPID2-Daten ein Flop, dürfte die Aktie mehr oder weniger wertlos sein.
Vielleicht eine der derzeit faszinierendsten Möglichkeiten für eine Wette mit einem wirklich absolut extremen Chance/Risiko-Potential.
Ich bin und bleibe mit einer sehr kleinen Position dabei.

Celladon ist eine absolute rot/schwarz-Roulette-Spekulation. Wenn ihre Technik tatsächlich wirkt und hilft - was extrem unsicher ist - dann sind die 70 Dollar Kursziel ein Scherz bzw. der Anfang des Anfangs der Kurssteigerung.
Sind allerdings die CUPID2-Daten ein Flop, dürfte die Aktie mehr oder weniger wertlos sein.
Vielleicht eine der derzeit faszinierendsten Möglichkeiten für eine Wette mit einem wirklich absolut extremen Chance/Risiko-Potential.
Ich bin und bleibe mit einer sehr kleinen Position dabei.
KPTI
hier mal ein Link - von dem ich nun hoffe dass er nun auch so erscheint wie ich mir das vorstelle...
https://clinicaltrials.gov/ct2/results?term=selinexor&recr=O…
Zum besseren Verständnis was KPTI eigentlich so an Versuchsreihen betreibt.
Mit 34 Trials ganz schön umfangreich...
Aus dem heutigen Kursgebastel an der Nasdaq werde ich zwar nicht ganz so schlau - aber ich muss ja auch nicht immer alles verstehen...
Apropos verstehen - lt.Nasdaq sollten gestern doch eigentlich die Quartalszahlen veröffentlicht werden....kamen jedoch nicht. Auch heute keine Zahlen hierzu - auch keine "Vorankündigung" wann diese denn nun veröffentlicht werden....hmmm
hier mal ein Link - von dem ich nun hoffe dass er nun auch so erscheint wie ich mir das vorstelle...

https://clinicaltrials.gov/ct2/results?term=selinexor&recr=O…
Zum besseren Verständnis was KPTI eigentlich so an Versuchsreihen betreibt.
Mit 34 Trials ganz schön umfangreich...

Aus dem heutigen Kursgebastel an der Nasdaq werde ich zwar nicht ganz so schlau - aber ich muss ja auch nicht immer alles verstehen...
Apropos verstehen - lt.Nasdaq sollten gestern doch eigentlich die Quartalszahlen veröffentlicht werden....kamen jedoch nicht. Auch heute keine Zahlen hierzu - auch keine "Vorankündigung" wann diese denn nun veröffentlicht werden....hmmm

ESPR
Gestern hab es "Zahlen". Einige interessante Punkte aus dem CC:
Es gab Äußerungen, die Hinweise auf den Plan der PIII gaben:
I believe that 1002 will help two patient populations. First, patients with high levels of LDL-cholesterol who can't tolerate statins and second, patients with high levels of LDL-cholesterol who are taking statins but are not getting sufficient LDL-cholesterol lowering.
http://seekingalpha.com/article/2978636-esperion-therapeutic…
Zudem plant man neben 1002 als single agent auch zeitgleich eine PIII mit 1002 und Zetia als fixed dose combination also 1 Pille. Möglich wäre auch eine Kombination aus sehr niedrig dosiertem Statin und 1002. Eine Triplekombo wird es laut CC nicht in der PIII geben.
Erfreulich auch, dass man die Kosten im Griff hat und weniger Verlust machte, als erwartet.
Ich finde es absolut nachvollziehbar, dass viele meinen, dass eine Übernahme hier nur eine Frage der Zeit ist.
ESPR: MK: 975 Mio - Cash ca. 140 Mio
März: Endgültige Ergebnisse der Studie 008 (1002 +/vs. Ezetimibe), PII Ergebnisse 009Studie (1002 + Statin wenn LDL-C Ziel nicht erreicht)
Q2: FDA Entscheidet über Aufhebung des partial clinical hold schon im Q1 erfolgt
Q2: Ergebnisse 014Studie: PII mit Schwerpunkt auf Patienten mit Bluthochdruck
Q3: Zulassung der PCSK9-I. von Amgen bzw. Sanofi (Preis?-diskussion)
Q4: Gespräche FDA (wohl schon M 2015) und Entscheidung über PIII
PIII Ergebnisse dann 2017
Mein Plan hier ist es, die Position trotz guter Performance und auch bei Rückschlägen zu halten. Zukaufen würde ich auf aktuellem Niveau aber nicht mehr.

Man darf auch nicht vergessen, dass es sich bei ESPR um ein one-tick-pony handelt (es gibt im Grunde nur ein einziges Medikament). Dazu der CEO: Esperion is effectively a one-trick pony, he said, but that's "not so bad if you're riding Seabiscuit."
Seabiscuit ist wohl ein legendäres Rennpferd. Aber: Wir alle wissen auch was passiert, wenn sich ein Pferd das Bein bricht...
PCYC
Dazu fällt mir eigentlich nicht viel ein außer alle Investierten zu beglückwünschen. Hier im Forum wurde mehrfach auf die Möglichkeiten von Ibru hingewiesen - scheinbar hat man bei ABBVIE mitgelesen. Ich hatte mir aus der "Kategorie" MDVN gekauft, weil ich sie eigentlich chancenreicher/günstiger bewertet fand.
SG kmastra
Gestern hab es "Zahlen". Einige interessante Punkte aus dem CC:
Es gab Äußerungen, die Hinweise auf den Plan der PIII gaben:
I believe that 1002 will help two patient populations. First, patients with high levels of LDL-cholesterol who can't tolerate statins and second, patients with high levels of LDL-cholesterol who are taking statins but are not getting sufficient LDL-cholesterol lowering.
http://seekingalpha.com/article/2978636-esperion-therapeutic…
Zudem plant man neben 1002 als single agent auch zeitgleich eine PIII mit 1002 und Zetia als fixed dose combination also 1 Pille. Möglich wäre auch eine Kombination aus sehr niedrig dosiertem Statin und 1002. Eine Triplekombo wird es laut CC nicht in der PIII geben.
Erfreulich auch, dass man die Kosten im Griff hat und weniger Verlust machte, als erwartet.
Ich finde es absolut nachvollziehbar, dass viele meinen, dass eine Übernahme hier nur eine Frage der Zeit ist.
ESPR: MK: 975 Mio - Cash ca. 140 Mio
März: Endgültige Ergebnisse der Studie 008 (1002 +/vs. Ezetimibe), PII Ergebnisse 009Studie (1002 + Statin wenn LDL-C Ziel nicht erreicht)
Q2: FDA Entscheidet über Aufhebung des partial clinical hold schon im Q1 erfolgt
Q2: Ergebnisse 014Studie: PII mit Schwerpunkt auf Patienten mit Bluthochdruck
Q3: Zulassung der PCSK9-I. von Amgen bzw. Sanofi (Preis?-diskussion)
Q4: Gespräche FDA (wohl schon M 2015) und Entscheidung über PIII
PIII Ergebnisse dann 2017
Mein Plan hier ist es, die Position trotz guter Performance und auch bei Rückschlägen zu halten. Zukaufen würde ich auf aktuellem Niveau aber nicht mehr.
Man darf auch nicht vergessen, dass es sich bei ESPR um ein one-tick-pony handelt (es gibt im Grunde nur ein einziges Medikament). Dazu der CEO: Esperion is effectively a one-trick pony, he said, but that's "not so bad if you're riding Seabiscuit."
Seabiscuit ist wohl ein legendäres Rennpferd. Aber: Wir alle wissen auch was passiert, wenn sich ein Pferd das Bein bricht...
PCYC
Dazu fällt mir eigentlich nicht viel ein außer alle Investierten zu beglückwünschen. Hier im Forum wurde mehrfach auf die Möglichkeiten von Ibru hingewiesen - scheinbar hat man bei ABBVIE mitgelesen. Ich hatte mir aus der "Kategorie" MDVN gekauft, weil ich sie eigentlich chancenreicher/günstiger bewertet fand.
SG kmastra
CNAT:
The company said in a Thursday filing that its Chief Medical Officer Gary C. Burgess resigned.
...
Kurs war zur Börseneröffnung ziemlich unter Druck.
Ich bin ehrlich gesagt auch nicht sonderlich glücklich mit dieser (Mini)Position, mit der ich letztlich "nur" Hammer nachäffe.
Es gibt hier halt noch überhaupt keine vernünftigen Daten, sondern eigentlich nur Theorie. Klar, die Aktie ist spottbillig. Aber, was heißt das schon? Letztlich "nur", dass das Potential nach oben sehr groß sein kann, wenn alles gut geht. Nach unten sinds hingegen immer 100% Risiko (oder realistischer meinethalben 80%), egal, ob das Ding vorher mit 100 Millionen oder 1.000 Millionen bewertet war. Will sagen, eine billige Bewertung reduziert das Risiko für den Investor nicht so wirklich, wenn es sich um ein one-trick-pony handelt.
Ich denke, ich werde mich hier verabschieden...
Hallo kmastra,
ESPR werde ich ebenfalls einfach halten und sehen, was passiert.
Aufstocken würde ich eventuell Aerie, falls die Ergebnisse im Mai wirklich positiv sind. Klar wird dann der Kurs einen ordentlichen Satz machen (+50%???), aber ich denke, dass da dann trotzdem noch einiges mehr an Potential sein könnte.
Die Ergebnisse warte ich aber ab.
VG
SLG
The company said in a Thursday filing that its Chief Medical Officer Gary C. Burgess resigned.
...
Kurs war zur Börseneröffnung ziemlich unter Druck.
Ich bin ehrlich gesagt auch nicht sonderlich glücklich mit dieser (Mini)Position, mit der ich letztlich "nur" Hammer nachäffe.
Es gibt hier halt noch überhaupt keine vernünftigen Daten, sondern eigentlich nur Theorie. Klar, die Aktie ist spottbillig. Aber, was heißt das schon? Letztlich "nur", dass das Potential nach oben sehr groß sein kann, wenn alles gut geht. Nach unten sinds hingegen immer 100% Risiko (oder realistischer meinethalben 80%), egal, ob das Ding vorher mit 100 Millionen oder 1.000 Millionen bewertet war. Will sagen, eine billige Bewertung reduziert das Risiko für den Investor nicht so wirklich, wenn es sich um ein one-trick-pony handelt.
Ich denke, ich werde mich hier verabschieden...
Hallo kmastra,
ESPR werde ich ebenfalls einfach halten und sehen, was passiert.
Aufstocken würde ich eventuell Aerie, falls die Ergebnisse im Mai wirklich positiv sind. Klar wird dann der Kurs einen ordentlichen Satz machen (+50%???), aber ich denke, dass da dann trotzdem noch einiges mehr an Potential sein könnte.
Die Ergebnisse warte ich aber ab.
VG
SLG
Mit der Übernahme von PCYC habe ich mich nun von meiner bisher größten Position getrennt... aufgestockt habe ich dafür ACAD, KPTI, AERI, CEMP, XLRN und SAGE. Dazu kommen neue Positionen in FGEN, ZSPH, EBIO und MRNS... die beiden letzten aber nur als kleine Risiko-Positionen.
Die Kurse sind momentan ja nicht günstig... langfristig lohnen sich die einen oder anderen Biotechs aber hoffentlich noch.

Grüße
ipollit
Die Kurse sind momentan ja nicht günstig... langfristig lohnen sich die einen oder anderen Biotechs aber hoffentlich noch.
Grüße
ipollit
Hier noch eine aktuelle Übersicht welche Titel nach Ansicht der Citibank am aussichtsreichsten / am wenigsten aussichtsreich sind:
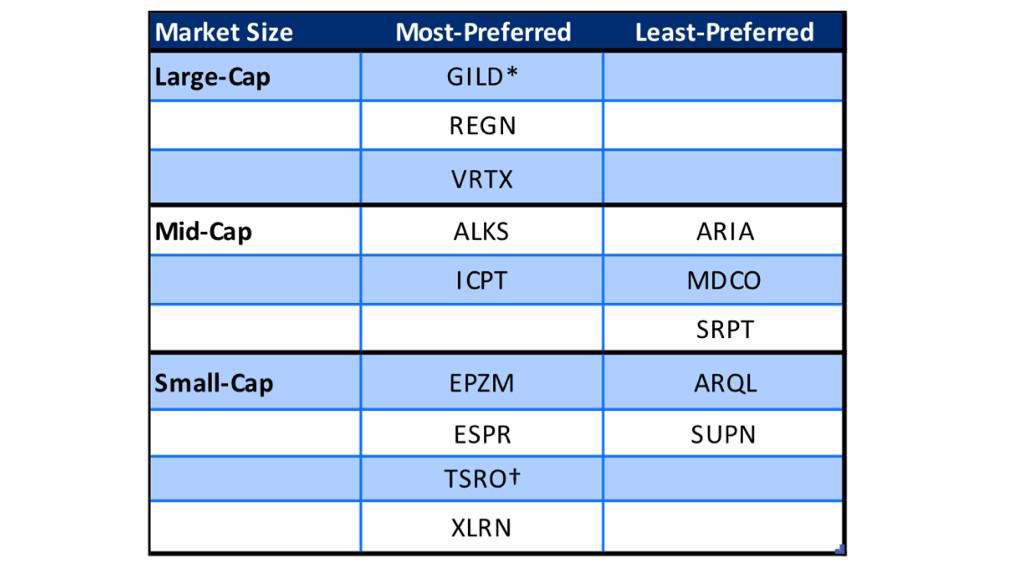

PCYCs Imbruvica war meiner Meinung nach der aussichtsreichste bzw. "sicherste" Blockbuster-Kandidat in meinem Depot. Gibt es nun noch andere interessante Kandidaten?
MDVNs Xtandi ist vielleicht ähnlich gut wie Imbruvica, wobei Imbruvica noch weiteres Potential in IO/soliden Tumoren hat, Xtandi eher nicht so. PCYC erhält auch einen größeren Umsatz-Anteil von JNJ, der für MDVN von Astellas ist etwas kleiner. Trotzdem sehe ich MDVN in einer ähnlichen Kategorie wie PCYC.
Daneben könnte ACAD's Nuplazid sehr aussichtsreich sein... hier halte ich inzwischen eine größere Position. Allerdings gibt es im Moment etwas Unsicherheit, warum sich der NDA immer noch so lange hinzieht.
Hier mal ein Überblick über ein paar meiner Biotechs mit möglichen Blockbustern... jeweils aktuelle Marktkapitalisierung, mögliche recht optimistisch(!!) geschätzte Peak Sales, Royalties/Partner, Entwicklungsstand(BTD=FDA Breakthrough Designation), Indikation und Target.
Die Peak Sales sollte man auf keinen Fall als sicher annehmen und direkt vergleichen... je nach Entwicklungsstand gibt es noch sehr viele Unsicherheiten und wie gesagt, sind sie sehr optimistisch gesehen! Jederzeit sind Fehlschläge möglich oder bessere Konkurrenten können das Potential erheblich reduzieren. Außerdem wird es viele Jahre dauern, bis derartige Umsätze erreichbar wären. Es ist also nur ein sehr grober Anhaltspunkt. Ich übernehme keine Garantie! ;-)
*************
REGN 43.01B
- Eylea: 6B+, 100% US, 50% ex-US (Partner Bayer), market, degenerative Augenerkrankungen (wet AMD, DME), VEGFR
Potential: bestes Mittel gegen AMD&Co, wirkt ein wenig besser als Roche/NVS's Konkurrenz-Produkt Lucentis, muss weniger oft ins Auge gespritzt werden, Risiko: neue vielleicht bessere Mittel in der Entwicklung
- Praluent: 3-4B (nur US), 50% US, 35-45% ex-US (Partner Sanofi), NDA, Cholesterin-Senker (LDL), PCKS9
Potential: PCKS9-AKs sind die stärksten LDL-Senker, deutlich stärker als mit Statinen (10B+ Markt), die allerdings noch weitere positive Effekte haben, Risiko: Konkurrenz-Produkt von Amgen kommt gleichzeitig auf den Markt, unklar ob sich das alle paar Monate zu spritzende Mittel gegen orale Statine in der Breite durchsetzen kann, zumal es deutlich teurer sein wird, möglicher Preiskampf wie in HCV
- Dupilumab: 4,5B+, 50% US, 35-45% ex-US (Partner Sanofi), PIII/BTD, Asthma und Neurodermitis, IL-4/13
Potential: möglicherweise bestes Mittel gegen Asthma und Neurodermitis... bisher gibt in diesen Massen-Indikationen noch nicht viel
- Sarilumab: 2B+, 50% US, 35-45% ex-US (Partner Sanofi), PIII, rheumatoide Arthritis (RA), IL-6R
Potential: Konkurrenz-Produkt zu Actemra, Risiko: zu wenig differenzert zu Actemra, IL-6R-Mittel bieten vielleicht gegenüber Humira&Co keine Vorteile
PCYC 19.35B
- Imbruvica: 6B+, 50% ww (Partner JNJ), market/BTD, Blutkrebs, BTK + ITK
Potential: umsatzstärkstes Blutkrebs-Medikament (ähnlich Rituxan, Revlimid), Upside: Kombi mit IO (PD1&Co) in soliden Tumoren aufgrund von ITK
INCY 15.46B
- Jakafi: 3B+ (nur US), 100% US, 15-25% ex-US (Partner NVS), market, Knochenmarkfibrose(MV) & Polycythemia Vera (PV), JAK1+2
Potential: einziges Mittel gegen MV und PV, Upside: Wirkung gegen solide Tumore (z.B. Bauspeicheldrüsenkrebs PIII), bei denen Entzündungsprozesse bzw. JAK/STAT eine Rolle spielen (PIII, 1-3B+)
- Baricitinib: 3B+, 25-30% ww (Partner Eli Lilly), PIII, rheumatoide Arthritis(RA), JAK1+2
Potential: bisher wird RA von biologischen Mitteln wie Humira (11B+ Umsatz) dominiert, die aber gespritzt werden müssen... Baricitinib könnte das erste orale Mittel sein, das ähnlich gut wirkt, Risiko: Pfizers oraler JAK3-Hemmer Xeljanz hat bisher enttäuscht mit 300M US-Umsätzen in 2015... Ursache könnten Nebenwirkungen von JAK3 sein, die Baricitinib nicht hat, Upside: Wirkung gegen Nierenerkrankungen und/oder andere Autoimmunerkrankungen wie Schuppenflechte
- INCB24360: 2,5B+, 100% ww, PII, Krebs u.a. in Kombi mit PD1, IDO1
Potential: INCB24360 ist der führende IDO1-Hemmer... IO-AKs wie PD1 sollen eine große Zukunft haben mit angeblichen 20B+ Umsatz aufgrund ihrer lang anhaltenden Wirkung gegen Krebs. Allerdings bleibt die Wirkung bisher nur auf einen Teil der Patienten (10-30%) beschränkt... eine IDO-Kombi könnte diesen Anteil deutlich erhöhen. Pharmas haben anscheinend ein großes Interesse an IDO.
MDVN 9.9B
- Xtandi: 6B+, 50% US/15-20% ex-US (Partner Astellas), market, Prostatakrebs, AR
Potential: wichtigstes Mittel gegen Prostatakrebs in allen Stadien, Upside: Brustkrebs, IO-Kombi
GEN.CO 4.5B
- Daratumumab: 3.5B, ca. 15% ww (Partner JNJ), PIII/BTD, Multiple Myeloma (MM), CD38
Potential: erster zielgerichteter AK in MM (wie z.B. Rituxan in DLBCL) könnte zum Standard in MM werden, Upside: andere Blutkrebsarten wie DLBCL
- Arzerra: 1B, 20% ww (Partner NVS), market, B-Zell Blutkrebs (CLL, FL), CD20
Potential: bindet etwas anders an CD20 als der Standard CD20-AK Rituxan (6B+ Umsatz) und wirkt mehr über CDC als ADCC, Upside: Multiple Sklerose (MS), Risiko: bisher sind die Umsätze relativ gering, vielleicht ist der Unterschied zu Rituxan zu gering
ACAD 3.9B
- Nuplazid: 4B-7B+ (nur US), 100% ww, NDA/BTD, Psychosen bei u.a. Parkinson&Alzheimer (PDP&ADP), 5HT2a
Potential: wenig Nebenwirkungen u.a. keine Einschränkung der Beweglichkeit bei Älternen, Risiko: bisher nur in PDP PIII-Daten
CLVS 2.69B
- Rociletinib: 2,5B+, 100% ww, PIII/BTD, EGFR (T790M+/-) Lungenkrebs (NSCLC), EGFR T790M (+IGF1)
Potential: eines der ersten Mittel gegen T790M EGFR (50% EGFR), kein Hautausschlag (rash)... dadurch bessere Kombi mit bisherigen EGFRs, aufgrund von IGFR1 Behandlung von T790M- EGFR Lungenkrebs, bei dem EGFR-Hemmer nicht mehr wirken, Risiko: Konkurrenz von AZNs AZD9291 in T790m+ (aber nicht T790m-), 1st-line unklar aber notwendig für peak sales (möglicherweise ist 1st-line Kombi mit aktuellen EGFR-Hemmern notwendig, da diese vielleicht besser gegen nicht T790m-Mutationen wirken... Vorteil gegenüber AZD9291 aufgrund weniger überlappender Nebenwirkungen wie Rash)
- Rucaparib: 1B+, 100 ww, PIII, Eierstock- und Bauchspeicheldrüsenkrebs, PARP
Potential: in Eierstockkrebs nicht nur auf BRCAmut beschränkt, Upside: andere Krebsarten mit BRCAmut oder HRD+
CLDX 2.63B
- Rintega: 0,5-1B, 100% ww, PIII/BTD, EGFRvIII Gehirntumor (GBM), EGFRvIII Vakzine
Potential: bisher hilft nichts gegen das besonders aggressive EGFRvIII GBM, Rintega könnte als nebenwirkungsarme therapeutische Impfung das Leben deutlich verlängern
TSRO 1.99B
- Rolapitant: 1B (nur US), 100% ww, NDA, Übelkeit bei Chemo (CINV), NK-1
Potential: weniger Wechselwirkungen, optimale Wirkungsdauer, einfache Anwendung, IV+oral, Management mit großer Erfahrung in diesem Markt
- Niraparib: 2B+, 100% ww, PIII, Eierstock- und Brustkrebs, PARP
Potential: in Eierstockkrebs nicht nur auf BRCAmut beschränkt, Upside: andere Krebsarten mit BRCAmut oder HRD+
FGEN 1.69B
- Roxadustat: 7B+, 20-25% ww, 50% China (Astellas, AstraZeneca), PIII, Blutarmut u.a. bei Dialyse, HIF-alpha
Potential: ESAs wie EPO erzielen 8B+ trotz problematischer Nebenwirkungen, Roxadustat bietet eine bessere Wirkung und könnte aufgrund geringerer Nebenwirkungen breiter angewendet werden
- FG-3019: 3B+, 100% ww, PII, Entzündung/Vernarbung der Lunge (IPF), CTGF
Potential: Anders als Esbriet (ITMN wurde vor Marktzulassung von Esbriet für 8 Mrd USD von Roche übernommen) soll FG-3019 den Krankheitsverlauf von IPF nicht nur verlangsamen, sondern umkehren können, Upside: Bauchspeicheldrüsenkrebs, Risiko: konkurrierende CTGF-Hemmer
CEMP 1.46B
- Solithromycin: 2B, 100% ww, PIII, u.a. Lungenentzündung, Makrolide-Antibiotikum
Potential: Antibiotika werden in den USA öffentlich gefördert, weniger Nebenwirkungen, IV + oral (ideal für Krankenhäuser, um nach Infusion auf die Tablettenform zu wechseln zur früheren Entlassung), Makrolide ist mit die größte Antibiotika-Klasse
XLRN 1.32B
- Luspatercept und Sotatercept: 5B+, 20-25% ww (Partner CELG), PII, MDS/beta-Thalassemia/Blutarmut/Nierenerkrankungen, ActRIIA
Potential: Erhöhung roter Blutkörperchen uanabhängig von und weitreichender als ESAs (EPO&Co), Risiko: BLUE entwickelt Genterapie, die beta-Thalassemia theoretisch heilen kann
SAGE 1.1B
- SAGE-547: 1,5B+, 100% ww, PII, extrem lange, lebensbedrohliche epileptische Anfälle (SRSE), GABAa
Potential: bisher gibt es noch nichts, was bei SRSE hilft, könnte sehr hohe Krankenhauskosten reduzieren und so einen hohen Preis rechtfertigen
ZSPH 1.01B
- ZS-9: 1.2B+ (nur US), 100% ww, PIII, hohe Kaliumkonzentration im Blut (Hyperkalemia), Kalium-Binder
Potential: Bisher gibt es nur ein zugelassenes Mittel gegen Hyperkalemia, das aber nicht optimal ist... ZS-9 könnte vor allen Dingen in chronischer Anwendung das Mittel der Wahl werden, da es hier etwas besser zu sein scheint als der Konkurrent Patiromer von RLYP, der wahrscheinlich dieses Jahr ein wenig vor ZS-9 zugelassen wird, Upside: Ein Pharma-Partner könnte das Marktpotential deutlich vergrößern
KPTI 883M
- Selinexor: 4B+, 100% ww, PII/III, Blutkrebs (u.a. Myeloma, Richters, DLBCL), solide Tumore, XPO1
Potential: breiter unabhänger Wirkmechanismus gegen viele Krebsarten, viele Kombis möglich
INFI 760M
- Duvelisib: 2,5B (nur US), 50% US, 23,5-30,5% ex-US (Partner ABBV), PIII, iNHL und Ibruvica resistenter CLL, pi3k-delta+gamma
Potential: möglicherweise bestes Mittel gegen iNHL, Upside: T-Zell-Krebs, Kombi mit ABBVs BCL2-Hemmer ABT-199 könnte in Blutkrebs sehr wirksam sein
AERI 680M
- Rhopressa/Roclatan: 1,5B+, 100% ww, PIII/PII, Grüner Star (glaucoma), ROCK+NET
Potential: Bedarf an neuen Mitteln, erstes Mittel gegen grünen Star (8B ww Markt), das die Krankheitsursache selber behandeln könnte
ENTA 653M
- Viekira Pak: 4B, 5% ww (Partner ABBV), market, HCV genotype 1, Protease-Hemmer (PI)
Potential: bisher einziges Konkurrenz-Produkt zu GILDs 10B+ Harvoni, Risiko: bessere Konkurrenz-Mittel in den nächsten Jahren, weiterer Preiskampf
EXEL 595M
- Cometriq: 1,5B, 100% ww, PIII/market, Nieren- und Schilddrüsenkrebs (RCC, MTC), VEGFR+MET/RET
Potential: bestes Mittel gegen Nierenkrebs über VEGFR+MET, Upside: Leberkrebs (PIII), RET+ Lungenkrebs, Risiko: PIII gegen Prostatakrebs fehlgeschlagen, 2 Pharmas haben Cometriq bereits an EXEL zurückgegeben
- Cobimetinib: 0,5B, 35% ww (Partner Roche), NDA, schwarzer Hautkrebs, MEK
Potential: Kombi mit Roche's BRAF-Hemmer Zelboraf um BRAF-Resistenz zu verhindern, Upside: Roche testet IO-Kombis mit PD-1
Gruß
ipollit
MDVNs Xtandi ist vielleicht ähnlich gut wie Imbruvica, wobei Imbruvica noch weiteres Potential in IO/soliden Tumoren hat, Xtandi eher nicht so. PCYC erhält auch einen größeren Umsatz-Anteil von JNJ, der für MDVN von Astellas ist etwas kleiner. Trotzdem sehe ich MDVN in einer ähnlichen Kategorie wie PCYC.
Daneben könnte ACAD's Nuplazid sehr aussichtsreich sein... hier halte ich inzwischen eine größere Position. Allerdings gibt es im Moment etwas Unsicherheit, warum sich der NDA immer noch so lange hinzieht.
Hier mal ein Überblick über ein paar meiner Biotechs mit möglichen Blockbustern... jeweils aktuelle Marktkapitalisierung, mögliche recht optimistisch(!!) geschätzte Peak Sales, Royalties/Partner, Entwicklungsstand(BTD=FDA Breakthrough Designation), Indikation und Target.
Die Peak Sales sollte man auf keinen Fall als sicher annehmen und direkt vergleichen... je nach Entwicklungsstand gibt es noch sehr viele Unsicherheiten und wie gesagt, sind sie sehr optimistisch gesehen! Jederzeit sind Fehlschläge möglich oder bessere Konkurrenten können das Potential erheblich reduzieren. Außerdem wird es viele Jahre dauern, bis derartige Umsätze erreichbar wären. Es ist also nur ein sehr grober Anhaltspunkt. Ich übernehme keine Garantie! ;-)
*************
REGN 43.01B
- Eylea: 6B+, 100% US, 50% ex-US (Partner Bayer), market, degenerative Augenerkrankungen (wet AMD, DME), VEGFR
Potential: bestes Mittel gegen AMD&Co, wirkt ein wenig besser als Roche/NVS's Konkurrenz-Produkt Lucentis, muss weniger oft ins Auge gespritzt werden, Risiko: neue vielleicht bessere Mittel in der Entwicklung
- Praluent: 3-4B (nur US), 50% US, 35-45% ex-US (Partner Sanofi), NDA, Cholesterin-Senker (LDL), PCKS9
Potential: PCKS9-AKs sind die stärksten LDL-Senker, deutlich stärker als mit Statinen (10B+ Markt), die allerdings noch weitere positive Effekte haben, Risiko: Konkurrenz-Produkt von Amgen kommt gleichzeitig auf den Markt, unklar ob sich das alle paar Monate zu spritzende Mittel gegen orale Statine in der Breite durchsetzen kann, zumal es deutlich teurer sein wird, möglicher Preiskampf wie in HCV
- Dupilumab: 4,5B+, 50% US, 35-45% ex-US (Partner Sanofi), PIII/BTD, Asthma und Neurodermitis, IL-4/13
Potential: möglicherweise bestes Mittel gegen Asthma und Neurodermitis... bisher gibt in diesen Massen-Indikationen noch nicht viel
- Sarilumab: 2B+, 50% US, 35-45% ex-US (Partner Sanofi), PIII, rheumatoide Arthritis (RA), IL-6R
Potential: Konkurrenz-Produkt zu Actemra, Risiko: zu wenig differenzert zu Actemra, IL-6R-Mittel bieten vielleicht gegenüber Humira&Co keine Vorteile
PCYC 19.35B
- Imbruvica: 6B+, 50% ww (Partner JNJ), market/BTD, Blutkrebs, BTK + ITK
Potential: umsatzstärkstes Blutkrebs-Medikament (ähnlich Rituxan, Revlimid), Upside: Kombi mit IO (PD1&Co) in soliden Tumoren aufgrund von ITK
INCY 15.46B
- Jakafi: 3B+ (nur US), 100% US, 15-25% ex-US (Partner NVS), market, Knochenmarkfibrose(MV) & Polycythemia Vera (PV), JAK1+2
Potential: einziges Mittel gegen MV und PV, Upside: Wirkung gegen solide Tumore (z.B. Bauspeicheldrüsenkrebs PIII), bei denen Entzündungsprozesse bzw. JAK/STAT eine Rolle spielen (PIII, 1-3B+)
- Baricitinib: 3B+, 25-30% ww (Partner Eli Lilly), PIII, rheumatoide Arthritis(RA), JAK1+2
Potential: bisher wird RA von biologischen Mitteln wie Humira (11B+ Umsatz) dominiert, die aber gespritzt werden müssen... Baricitinib könnte das erste orale Mittel sein, das ähnlich gut wirkt, Risiko: Pfizers oraler JAK3-Hemmer Xeljanz hat bisher enttäuscht mit 300M US-Umsätzen in 2015... Ursache könnten Nebenwirkungen von JAK3 sein, die Baricitinib nicht hat, Upside: Wirkung gegen Nierenerkrankungen und/oder andere Autoimmunerkrankungen wie Schuppenflechte
- INCB24360: 2,5B+, 100% ww, PII, Krebs u.a. in Kombi mit PD1, IDO1
Potential: INCB24360 ist der führende IDO1-Hemmer... IO-AKs wie PD1 sollen eine große Zukunft haben mit angeblichen 20B+ Umsatz aufgrund ihrer lang anhaltenden Wirkung gegen Krebs. Allerdings bleibt die Wirkung bisher nur auf einen Teil der Patienten (10-30%) beschränkt... eine IDO-Kombi könnte diesen Anteil deutlich erhöhen. Pharmas haben anscheinend ein großes Interesse an IDO.
MDVN 9.9B
- Xtandi: 6B+, 50% US/15-20% ex-US (Partner Astellas), market, Prostatakrebs, AR
Potential: wichtigstes Mittel gegen Prostatakrebs in allen Stadien, Upside: Brustkrebs, IO-Kombi
GEN.CO 4.5B
- Daratumumab: 3.5B, ca. 15% ww (Partner JNJ), PIII/BTD, Multiple Myeloma (MM), CD38
Potential: erster zielgerichteter AK in MM (wie z.B. Rituxan in DLBCL) könnte zum Standard in MM werden, Upside: andere Blutkrebsarten wie DLBCL
- Arzerra: 1B, 20% ww (Partner NVS), market, B-Zell Blutkrebs (CLL, FL), CD20
Potential: bindet etwas anders an CD20 als der Standard CD20-AK Rituxan (6B+ Umsatz) und wirkt mehr über CDC als ADCC, Upside: Multiple Sklerose (MS), Risiko: bisher sind die Umsätze relativ gering, vielleicht ist der Unterschied zu Rituxan zu gering
ACAD 3.9B
- Nuplazid: 4B-7B+ (nur US), 100% ww, NDA/BTD, Psychosen bei u.a. Parkinson&Alzheimer (PDP&ADP), 5HT2a
Potential: wenig Nebenwirkungen u.a. keine Einschränkung der Beweglichkeit bei Älternen, Risiko: bisher nur in PDP PIII-Daten
CLVS 2.69B
- Rociletinib: 2,5B+, 100% ww, PIII/BTD, EGFR (T790M+/-) Lungenkrebs (NSCLC), EGFR T790M (+IGF1)
Potential: eines der ersten Mittel gegen T790M EGFR (50% EGFR), kein Hautausschlag (rash)... dadurch bessere Kombi mit bisherigen EGFRs, aufgrund von IGFR1 Behandlung von T790M- EGFR Lungenkrebs, bei dem EGFR-Hemmer nicht mehr wirken, Risiko: Konkurrenz von AZNs AZD9291 in T790m+ (aber nicht T790m-), 1st-line unklar aber notwendig für peak sales (möglicherweise ist 1st-line Kombi mit aktuellen EGFR-Hemmern notwendig, da diese vielleicht besser gegen nicht T790m-Mutationen wirken... Vorteil gegenüber AZD9291 aufgrund weniger überlappender Nebenwirkungen wie Rash)
- Rucaparib: 1B+, 100 ww, PIII, Eierstock- und Bauchspeicheldrüsenkrebs, PARP
Potential: in Eierstockkrebs nicht nur auf BRCAmut beschränkt, Upside: andere Krebsarten mit BRCAmut oder HRD+
CLDX 2.63B
- Rintega: 0,5-1B, 100% ww, PIII/BTD, EGFRvIII Gehirntumor (GBM), EGFRvIII Vakzine
Potential: bisher hilft nichts gegen das besonders aggressive EGFRvIII GBM, Rintega könnte als nebenwirkungsarme therapeutische Impfung das Leben deutlich verlängern
TSRO 1.99B
- Rolapitant: 1B (nur US), 100% ww, NDA, Übelkeit bei Chemo (CINV), NK-1
Potential: weniger Wechselwirkungen, optimale Wirkungsdauer, einfache Anwendung, IV+oral, Management mit großer Erfahrung in diesem Markt
- Niraparib: 2B+, 100% ww, PIII, Eierstock- und Brustkrebs, PARP
Potential: in Eierstockkrebs nicht nur auf BRCAmut beschränkt, Upside: andere Krebsarten mit BRCAmut oder HRD+
FGEN 1.69B
- Roxadustat: 7B+, 20-25% ww, 50% China (Astellas, AstraZeneca), PIII, Blutarmut u.a. bei Dialyse, HIF-alpha
Potential: ESAs wie EPO erzielen 8B+ trotz problematischer Nebenwirkungen, Roxadustat bietet eine bessere Wirkung und könnte aufgrund geringerer Nebenwirkungen breiter angewendet werden
- FG-3019: 3B+, 100% ww, PII, Entzündung/Vernarbung der Lunge (IPF), CTGF
Potential: Anders als Esbriet (ITMN wurde vor Marktzulassung von Esbriet für 8 Mrd USD von Roche übernommen) soll FG-3019 den Krankheitsverlauf von IPF nicht nur verlangsamen, sondern umkehren können, Upside: Bauchspeicheldrüsenkrebs, Risiko: konkurrierende CTGF-Hemmer
CEMP 1.46B
- Solithromycin: 2B, 100% ww, PIII, u.a. Lungenentzündung, Makrolide-Antibiotikum
Potential: Antibiotika werden in den USA öffentlich gefördert, weniger Nebenwirkungen, IV + oral (ideal für Krankenhäuser, um nach Infusion auf die Tablettenform zu wechseln zur früheren Entlassung), Makrolide ist mit die größte Antibiotika-Klasse
XLRN 1.32B
- Luspatercept und Sotatercept: 5B+, 20-25% ww (Partner CELG), PII, MDS/beta-Thalassemia/Blutarmut/Nierenerkrankungen, ActRIIA
Potential: Erhöhung roter Blutkörperchen uanabhängig von und weitreichender als ESAs (EPO&Co), Risiko: BLUE entwickelt Genterapie, die beta-Thalassemia theoretisch heilen kann
SAGE 1.1B
- SAGE-547: 1,5B+, 100% ww, PII, extrem lange, lebensbedrohliche epileptische Anfälle (SRSE), GABAa
Potential: bisher gibt es noch nichts, was bei SRSE hilft, könnte sehr hohe Krankenhauskosten reduzieren und so einen hohen Preis rechtfertigen
ZSPH 1.01B
- ZS-9: 1.2B+ (nur US), 100% ww, PIII, hohe Kaliumkonzentration im Blut (Hyperkalemia), Kalium-Binder
Potential: Bisher gibt es nur ein zugelassenes Mittel gegen Hyperkalemia, das aber nicht optimal ist... ZS-9 könnte vor allen Dingen in chronischer Anwendung das Mittel der Wahl werden, da es hier etwas besser zu sein scheint als der Konkurrent Patiromer von RLYP, der wahrscheinlich dieses Jahr ein wenig vor ZS-9 zugelassen wird, Upside: Ein Pharma-Partner könnte das Marktpotential deutlich vergrößern
KPTI 883M
- Selinexor: 4B+, 100% ww, PII/III, Blutkrebs (u.a. Myeloma, Richters, DLBCL), solide Tumore, XPO1
Potential: breiter unabhänger Wirkmechanismus gegen viele Krebsarten, viele Kombis möglich
INFI 760M
- Duvelisib: 2,5B (nur US), 50% US, 23,5-30,5% ex-US (Partner ABBV), PIII, iNHL und Ibruvica resistenter CLL, pi3k-delta+gamma
Potential: möglicherweise bestes Mittel gegen iNHL, Upside: T-Zell-Krebs, Kombi mit ABBVs BCL2-Hemmer ABT-199 könnte in Blutkrebs sehr wirksam sein
AERI 680M
- Rhopressa/Roclatan: 1,5B+, 100% ww, PIII/PII, Grüner Star (glaucoma), ROCK+NET
Potential: Bedarf an neuen Mitteln, erstes Mittel gegen grünen Star (8B ww Markt), das die Krankheitsursache selber behandeln könnte
ENTA 653M
- Viekira Pak: 4B, 5% ww (Partner ABBV), market, HCV genotype 1, Protease-Hemmer (PI)
Potential: bisher einziges Konkurrenz-Produkt zu GILDs 10B+ Harvoni, Risiko: bessere Konkurrenz-Mittel in den nächsten Jahren, weiterer Preiskampf
EXEL 595M
- Cometriq: 1,5B, 100% ww, PIII/market, Nieren- und Schilddrüsenkrebs (RCC, MTC), VEGFR+MET/RET
Potential: bestes Mittel gegen Nierenkrebs über VEGFR+MET, Upside: Leberkrebs (PIII), RET+ Lungenkrebs, Risiko: PIII gegen Prostatakrebs fehlgeschlagen, 2 Pharmas haben Cometriq bereits an EXEL zurückgegeben
- Cobimetinib: 0,5B, 35% ww (Partner Roche), NDA, schwarzer Hautkrebs, MEK
Potential: Kombi mit Roche's BRAF-Hemmer Zelboraf um BRAF-Resistenz zu verhindern, Upside: Roche testet IO-Kombis mit PD-1
Gruß
ipollit
ohne PCYC ist nun INCY mein größte Position...
7,9% INCY
7,9% CLDX
6,3% ARRY
5,8% CLVS
5,2% MDVN
5,2% GEN.CO
4,8% MGNX
4,4% ISIS
3,9% ACAD
3,7% ALNY
3,7% TSRO
3,2% EXEL
3,1% REGN
2,9% KPTI
2,8% ESPR
2,8% IPH.PA
2,6% FPRX
2,4% CEMP
2,4% INFI
2,3% ENTA
2,0% XLRN
1,8% ARQL
1,8% SAGE
1,7% AERI
1,4% FGEN
1,2% SNTA
1,2% SGEN
1,1% IMMU
0,9% EPZM
0,8% VSTM
0,8% STML
0,8% ZSPH
0,7% EBIO
0,6% MRNS
Gruß
ipollit
7,9% INCY
7,9% CLDX
6,3% ARRY
5,8% CLVS
5,2% MDVN
5,2% GEN.CO
4,8% MGNX
4,4% ISIS
3,9% ACAD
3,7% ALNY
3,7% TSRO
3,2% EXEL
3,1% REGN
2,9% KPTI
2,8% ESPR
2,8% IPH.PA
2,6% FPRX
2,4% CEMP
2,4% INFI
2,3% ENTA
2,0% XLRN
1,8% ARQL
1,8% SAGE
1,7% AERI
1,4% FGEN
1,2% SNTA
1,2% SGEN
1,1% IMMU
0,9% EPZM
0,8% VSTM
0,8% STML
0,8% ZSPH
0,7% EBIO
0,6% MRNS
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.270.244 von ipollit am 07.03.15 22:01:09"PCYCs Imbruvica war meiner Meinung nach der aussichtsreichste bzw. "sicherste" Blockbuster-Kandidat in meinem Depot. Gibt es nun noch andere interessante Kandidaten?"
Hallo ipollit,
starke Übersicht!
Zu Deiner Frage fällt mir spontan noch Intercepts OCA ein... Tja, das kann man natürlich auch sehr kritisch sehen.
Aber immerhin haben sie eine BTD bekommen. Das hat für mich letztlich den Ausschlag gegeben, mit einer vorsichtigen Positionierung bei 219 Dollar wieder reinzugehen.
ICPT 6,0B
- OCA: 3B+, 100% ww (außer Japan, Korea undChina),PIIb/PIII/BTD, Obeticholic acid, zunächst Primary biliary cirrhosis (PBC), vor allem aber Nonalcoholic steatohepatitis (NASH)
Potential: Sehr großer Markt in NASH, first-in-class, bisher kein zugelassener Wirkstoff in NASH.
Risiken: Konkurrenzentwicklungen, Nebenwirkungsprofil, Vetrieb
Gruß
SLG
Hallo ipollit,
starke Übersicht!
Zu Deiner Frage fällt mir spontan noch Intercepts OCA ein... Tja, das kann man natürlich auch sehr kritisch sehen.
Aber immerhin haben sie eine BTD bekommen. Das hat für mich letztlich den Ausschlag gegeben, mit einer vorsichtigen Positionierung bei 219 Dollar wieder reinzugehen.
ICPT 6,0B
- OCA: 3B+, 100% ww (außer Japan, Korea undChina),PIIb/PIII/BTD, Obeticholic acid, zunächst Primary biliary cirrhosis (PBC), vor allem aber Nonalcoholic steatohepatitis (NASH)
Potential: Sehr großer Markt in NASH, first-in-class, bisher kein zugelassener Wirkstoff in NASH.
Risiken: Konkurrenzentwicklungen, Nebenwirkungsprofil, Vetrieb
Gruß
SLG
Antwort auf Beitrag Nr.: 49.270.244 von ipollit am 07.03.15 22:01:09"INFI 760M
- Duvelisib: 2,5B (nur US), 50% US, 23,5-30,5% ex-US (Partner ABBV), PIII, iNHL und Ibruvica resistenter CLL, pi3k-delta+gamma"
Hallo ipollit,
hast Du für diese Peak-Sales-Schätzung eine Quelle bzw. kannst Du das eventuell herleiten? Soll das nur für iNHL sein?
Oder geht man da doch von einem signifikanten Marktanteil bei CLL aus? (an den ich nicht glaube)
Gruß
SLG
- Duvelisib: 2,5B (nur US), 50% US, 23,5-30,5% ex-US (Partner ABBV), PIII, iNHL und Ibruvica resistenter CLL, pi3k-delta+gamma"
Hallo ipollit,
hast Du für diese Peak-Sales-Schätzung eine Quelle bzw. kannst Du das eventuell herleiten? Soll das nur für iNHL sein?
Oder geht man da doch von einem signifikanten Marktanteil bei CLL aus? (an den ich nicht glaube)
Gruß
SLG
Antwort auf Beitrag Nr.: 49.272.173 von SLGramann am 08.03.15 14:41:15Hallo SLG,
naja, es handelt sich sicherlich um eine optimistische Schätzung, die voraussetzt, dass Duvelisib das beste Mittel gegen iNHL sein wird (nach den bisherigen Studienergebnissen ist das möglich)... im Wesentlichen ist es wohl iNHL. Bezüglich CLL sagt INFI selber, dass sie keine Konkurrenz zu Imbruvica sein können (vielleicht irgendwann mal in Kombi mit ABT-199)... hier möchte man es nur bei Patienten anwenden, bei denen Imbruvica (wohl der zukünftige Standard in CLL) nicht mehr wirkt.
2,5 Mrd USD habe ich von hier übernommen...

Grüße
ipollit
naja, es handelt sich sicherlich um eine optimistische Schätzung, die voraussetzt, dass Duvelisib das beste Mittel gegen iNHL sein wird (nach den bisherigen Studienergebnissen ist das möglich)... im Wesentlichen ist es wohl iNHL. Bezüglich CLL sagt INFI selber, dass sie keine Konkurrenz zu Imbruvica sein können (vielleicht irgendwann mal in Kombi mit ABT-199)... hier möchte man es nur bei Patienten anwenden, bei denen Imbruvica (wohl der zukünftige Standard in CLL) nicht mehr wirkt.
2,5 Mrd USD habe ich von hier übernommen...

Grüße
ipollit
Antwort auf Beitrag Nr.: 49.270.244 von ipollit am 07.03.15 22:01:09Hi ipollit, super hilfreich. Danke!
Ich würde ESPR (1B) noch hinzunehmen.
ETC-1002: 2-4B LDL-Senker bei Statin Intoleranz oder als Zusatz, wenn Ziel nicht durch Statine (und/oder Zetia) erreicht.
Potential: bisher wenig Nebenwirkungen, orale Verbreichung, als Small Molecule billiger als die PCKS9 und in Kombi mit Zetia ähnlich effektiv, könnte von einer Diskussion um die Preise der PCKS9 profitieren, positive Effekte auf andere Parameter, potentiell 1. Option nach den Statinen, Kombipille mit Zetia
Risken: Nebenwirkungen tauchen auf - besonders über längeren Zeitraum noch nicht untersucht, Nachhaltigkeit der Effekte?, Zetia dann generisch und billig, Konkurrenz taucht auf (z.B. CETP funktioniert doch: http://www.fiercebiotech.com/story/lilly-delays-its-high-ris… )
Grundsätzlich hat sich auch mein Depot seit Beginn des Jahres schon sehr verändert. Läuft ja schon wieder beängstigend gut...!
SG kmastra
Ich würde ESPR (1B) noch hinzunehmen.
ETC-1002: 2-4B LDL-Senker bei Statin Intoleranz oder als Zusatz, wenn Ziel nicht durch Statine (und/oder Zetia) erreicht.
Potential: bisher wenig Nebenwirkungen, orale Verbreichung, als Small Molecule billiger als die PCKS9 und in Kombi mit Zetia ähnlich effektiv, könnte von einer Diskussion um die Preise der PCKS9 profitieren, positive Effekte auf andere Parameter, potentiell 1. Option nach den Statinen, Kombipille mit Zetia
Risken: Nebenwirkungen tauchen auf - besonders über längeren Zeitraum noch nicht untersucht, Nachhaltigkeit der Effekte?, Zetia dann generisch und billig, Konkurrenz taucht auf (z.B. CETP funktioniert doch: http://www.fiercebiotech.com/story/lilly-delays-its-high-ris… )
Grundsätzlich hat sich auch mein Depot seit Beginn des Jahres schon sehr verändert. Läuft ja schon wieder beängstigend gut...!
SG kmastra
Antwort auf Beitrag Nr.: 49.272.713 von kmastra am 08.03.15 17:21:12Ein Update zu meinem Depot:
ACAD 4%
AERI 5,5%
ARQL 4,5%
ARRY 9%
BLUE 4%
CLVS 15%
ENTA 7,5%
ESPR 12%
LGND 5%
LOXO 2,5%
Medigene 2%
MDVN 4,5%
ONTY 5,5%
OTIC 4,5%
ZFGN 7,5%
Cash 7%
ACAD 4%
AERI 5,5%
ARQL 4,5%
ARRY 9%
BLUE 4%
CLVS 15%
ENTA 7,5%
ESPR 12%
LGND 5%
LOXO 2,5%
Medigene 2%
MDVN 4,5%
ONTY 5,5%
OTIC 4,5%
ZFGN 7,5%
Cash 7%
Antwort auf Beitrag Nr.: 49.270.277 von ipollit am 07.03.15 22:10:11Ich bin -zufällig- auf Euer Forum gestoßen - leider findet man mit den Abkürzungen nicht immmer
die Aktie dazu - könnte man bitte den Namen der Firma dazu schreiben ?
damit man die auch findet - danke
7,9% INCY
7,9% CLDX
6,3% ARRY
5,8% CLVS
5,2% MDVN
5,2% GEN.CO
4,8% MGNX
4,4% ISIS
3,9% ACAD
3,7% ALNY
3,7% TSRO
3,2% EXEL
3,1% REGN
2,9% KPTI
2,8% ESPR
2,8% IPH.PA
2,6% FPRX
2,4% CEMP
2,4% INFI
2,3% ENTA
2,0% XLRN
1,8% ARQL
1,8% SAGE
1,7% AERI
1,4% FGEN
1,2% SNTA
1,2% SGEN
1,1% IMMU
0,9% EPZM
0,8% VSTM
0,8% STML
0,8% ZSPH
0,7% EBIO
0,6% MRNS
die Aktie dazu - könnte man bitte den Namen der Firma dazu schreiben ?
damit man die auch findet - danke
7,9% INCY
7,9% CLDX
6,3% ARRY
5,8% CLVS
5,2% MDVN
5,2% GEN.CO
4,8% MGNX
4,4% ISIS
3,9% ACAD
3,7% ALNY
3,7% TSRO
3,2% EXEL
3,1% REGN
2,9% KPTI
2,8% ESPR
2,8% IPH.PA
2,6% FPRX
2,4% CEMP
2,4% INFI
2,3% ENTA
2,0% XLRN
1,8% ARQL
1,8% SAGE
1,7% AERI
1,4% FGEN
1,2% SNTA
1,2% SGEN
1,1% IMMU
0,9% EPZM
0,8% VSTM
0,8% STML
0,8% ZSPH
0,7% EBIO
0,6% MRNS
Antwort auf Beitrag Nr.: 49.274.630 von urpferdchen am 09.03.15 07:59:53Hallo, schau mal auf https://finance.yahoo.com/ Dort müssten die Kürzel funktionieren.
SG kmastra
SG kmastra
Antwort auf Beitrag Nr.: 49.275.356 von kmastra am 09.03.15 09:13:38Vielen Dank - die meisten habe ich gefunden, bis auf GEN.co - und EXEL
ich werde mal hier weiter mitlesen
ich werde mal hier weiter mitlesen
Um den Überblich über mein Depot halbwegs zu behalten habe ich die Depotfunktion von ariva.de zu schätzen gelernt. Man kann dort auch einen Kommentar zu den jeweiligen Positionen hinzufügen. Also z.B. Kaufgrund, nächster Event, Stoppkurs, Zielkurs oder was auch immer.
Zudem habe ich auf w:o einen Thread quasi nur für mich eröffnet. Dort poste ich die Charts meiner Positionen von finviz.com. Sicherlich sollte man es mit Charttechnik nicht übertreiben und die automatischen Signale von finviz sind teilweise auch mit Vorsicht zu genießen (Nichts ist so alt wie der Trendkanal von gestern!) - aber für einen schnellen Überblick finde ich das ganz brauchbar.
Hier noch ein Link zur Roth Konferenz mit einigen interessanten Fimen:
http://www.wsw.com/webcast/roth29/#table1
SG kmastra
P.S. Was ist eigentlich mit ENTA los?
Zudem habe ich auf w:o einen Thread quasi nur für mich eröffnet. Dort poste ich die Charts meiner Positionen von finviz.com. Sicherlich sollte man es mit Charttechnik nicht übertreiben und die automatischen Signale von finviz sind teilweise auch mit Vorsicht zu genießen (Nichts ist so alt wie der Trendkanal von gestern!) - aber für einen schnellen Überblick finde ich das ganz brauchbar.
Hier noch ein Link zur Roth Konferenz mit einigen interessanten Fimen:
http://www.wsw.com/webcast/roth29/#table1
SG kmastra
P.S. Was ist eigentlich mit ENTA los?
Antwort auf Beitrag Nr.: 49.276.025 von urpferdchen am 09.03.15 10:34:38hallo urpferdchen hier ein link zu exelhttp://www.wallstreet-online.de/diskussion/1194406-101-110/e…
Antwort auf Beitrag Nr.: 49.281.041 von kmastra am 09.03.15 19:14:28Ein Unternehmen das bei Roth präsentieren wird ist u.a. Cytori Therapeutics (CYTX).
http://www.cytori.com
In der Vergangenheit haben sie sich insbesondere durch schlechtes Management ausgezeichnet, was letztlich zu einer katastrophalen finanziellen Bilanz, beinahe zur Pleite geführt hat. Die Technologie (sie bewegen sich im Bereich von Fettstammzellen) scheint jedoch zu funktionieren und könnte letztlich breit zur Anwendung kommen. Weitere Informationen können u.a. auf dieser Seite gefunden werden:http://www.cytx-investor.com
Das Management wurde mittlerweile, u.a. auf der Position des CEO, neu besetzt (wenngleich dieser aus den eigenen Reihen stammt). Wenn nun noch der finanzielle Turnaround gelingt, könnte dies noch ein interessantes Investment werden. Ich hatte die Aktie vor vielen Jahren schon im Depot, mich aber zwischenzeitlich davon verabschiedet. Kürzlich bin ich mit einer Riskoposition wieder eingestiegen, bei der ich einen möglichen Totalverlust einkalkuliere.
@ipollit: Kennst du diese Firma und kannst ggf. deine Einschätzung dazu geben?

http://www.cytori.com
In der Vergangenheit haben sie sich insbesondere durch schlechtes Management ausgezeichnet, was letztlich zu einer katastrophalen finanziellen Bilanz, beinahe zur Pleite geführt hat. Die Technologie (sie bewegen sich im Bereich von Fettstammzellen) scheint jedoch zu funktionieren und könnte letztlich breit zur Anwendung kommen. Weitere Informationen können u.a. auf dieser Seite gefunden werden:http://www.cytx-investor.com
Das Management wurde mittlerweile, u.a. auf der Position des CEO, neu besetzt (wenngleich dieser aus den eigenen Reihen stammt). Wenn nun noch der finanzielle Turnaround gelingt, könnte dies noch ein interessantes Investment werden. Ich hatte die Aktie vor vielen Jahren schon im Depot, mich aber zwischenzeitlich davon verabschiedet. Kürzlich bin ich mit einer Riskoposition wieder eingestiegen, bei der ich einen möglichen Totalverlust einkalkuliere.
@ipollit: Kennst du diese Firma und kannst ggf. deine Einschätzung dazu geben?
IPH.PA heute mit dieser Meldung: http://finance.yahoo.com/news/innate-pharma-collaborates-nci… auf 52w high, bis zum ATH ist es nun auch nicht mehr weit...

Antwort auf Beitrag Nr.: 49.275.356 von kmastra am 09.03.15 09:13:38sonst auch unter www.de.advfn.com, liest die meisten int. kürzel.
gruß ins board, thums
gruß ins board, thums
Antwort auf Beitrag Nr.: 49.282.178 von Schaeffi am 09.03.15 20:49:36Vielen Dank, werde ich mir mal ansehen
Was würdet Ihr bevorzugen und warum?
KPTI
CLDX
BSLN
POZN
KPTI
CLDX
BSLN
POZN
Ich habe heute sehr massiv verkauft und den Cash-Bestand stark hochgefahren.
Ich poste demnächst mal die neue Depotstruktur.
Cash ist jetzt aber bei ca. 40%!
Ich poste demnächst mal die neue Depotstruktur.
Cash ist jetzt aber bei ca. 40%!
Antwort auf Beitrag Nr.: 49.288.448 von SLGramann am 10.03.15 14:58:26Habe heute auch signifikante Cashbestände aufgebaut. Auch weil ich morgen in den Urlaub fahre und dann keine Lust habe mich zu kümmern bzw. dann auch nichts mehr machen kann. Habe eher Teilverkäufe getätigt. Cash ist jetzt so um 30%. Mal sehen...
SG kmastra
SG kmastra
Hallo ipollit 
im November habe ich eine Watchliste mit Werten von dir zusammengestellt, dabei habe ich auch ein wenig auf den Chart geachtet.
Jedenfalls sind die Aktien alle wahnsinnig gestiegen, 30 % ist das Mindeste.
Tolle Arbeit hier.
Schade, dass ich nichts von den Bios verstehe sondern eigentlich bloss nach dem Chart gehen kann.
Aber immerhin.
Kann man sagen, dass die Bios konjunkturunabhängig sind ?

im November habe ich eine Watchliste mit Werten von dir zusammengestellt, dabei habe ich auch ein wenig auf den Chart geachtet.
Jedenfalls sind die Aktien alle wahnsinnig gestiegen, 30 % ist das Mindeste.
Tolle Arbeit hier.
Schade, dass ich nichts von den Bios verstehe sondern eigentlich bloss nach dem Chart gehen kann.
Aber immerhin.
Kann man sagen, dass die Bios konjunkturunabhängig sind ?
Hier ein Überblick:
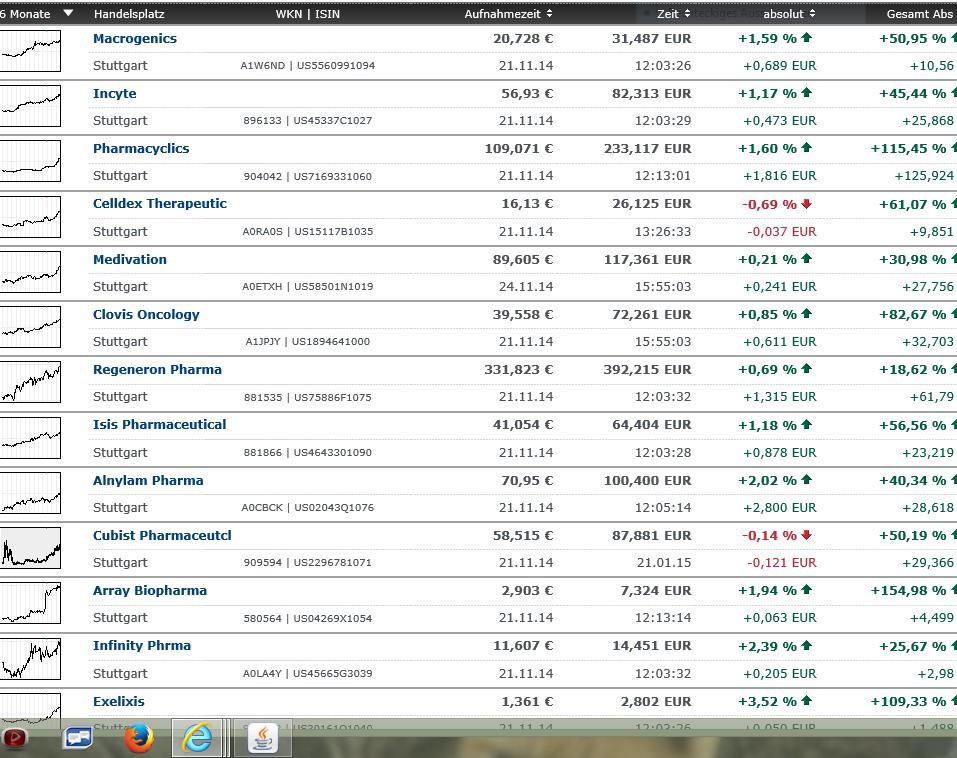

Antwort auf Beitrag Nr.: 49.270.244 von ipollit am 07.03.15 22:01:09Übernahmespekulation nun auch bei ACAD: http://www.bloomberg.com/news/articles/2015-03-10/acadia-sur…
Wenn das so weiter geht ist in kurzer Zeit die Hälfte meines Depots quasi übernommen worden...

Wenn das so weiter geht ist in kurzer Zeit die Hälfte meines Depots quasi übernommen worden...
Antwort auf Beitrag Nr.: 49.293.239 von SpanishEyes am 10.03.15 22:13:41http://www.cnbc.com/id/102497166#.
So viel zum Thema Übernahme... CEO tritt zurück und Zulassungsantrag auf Q2 verschoben.
So viel zum Thema Übernahme... CEO tritt zurück und Zulassungsantrag auf Q2 verschoben.
Antwort auf Beitrag Nr.: 49.305.293 von SpanishEyes am 11.03.15 21:34:13Ein ziemliches Desaster und ein großer Vertrauensschaden. Man muss sich mal reinziehen, dass am 26.02. zur Vorlage der Jahreszahlen 2014 die NDA submission für das Q1/15 nochmals bestätigt worden war.
Natürlich wird jetzt auch in Zweifel gezogen werden, dass es hier wirklich nur um den Produktionsprozess geht.
Am Ende wird wohl "alles gut" werden, denke ich, aber es ist schon ein herber Rückschlag.
Was allgemeines:
Das wird nicht der letzte Rückschlag im Biotechsektor gewesen sein. Es wurde zuletzt sehr viel angeschoben und das Grundgesetz der Branche heißt immer noch, dass das allermeiste schief geht. Ich denke nicht, dass dieses Gesetz aufgehoben ist.
Der Markt scheint mir generell im Hysteriemodus zu sein.
Eine große Korrektur ist überfällig.
Natürlich wird jetzt auch in Zweifel gezogen werden, dass es hier wirklich nur um den Produktionsprozess geht.
Am Ende wird wohl "alles gut" werden, denke ich, aber es ist schon ein herber Rückschlag.
Was allgemeines:
Das wird nicht der letzte Rückschlag im Biotechsektor gewesen sein. Es wurde zuletzt sehr viel angeschoben und das Grundgesetz der Branche heißt immer noch, dass das allermeiste schief geht. Ich denke nicht, dass dieses Gesetz aufgehoben ist.
Der Markt scheint mir generell im Hysteriemodus zu sein.
Eine große Korrektur ist überfällig.
Antwort auf Beitrag Nr.: 49.305.293 von SpanishEyes am 11.03.15 21:34:13"Zulassungsantrag auf Q2 verschoben."
Du meintest sicher H2 und hast Dich verschrieben. Jedenfalls ist die Timeline ziemlich unpräzise und geht jetzt bis Dezember.
Manufactering? Echt?
Du meintest sicher H2 und hast Dich verschrieben. Jedenfalls ist die Timeline ziemlich unpräzise und geht jetzt bis Dezember.
Manufactering? Echt?
Antwort auf Beitrag Nr.: 49.305.575 von SLGramann am 11.03.15 22:02:01Ja richtig, H2... da ist jetzt deutlich vertrauen verloren gegangen.
Die weiteren von dir genannten Punkte sehe ich auch so.
Die weiteren von dir genannten Punkte sehe ich auch so.
Antwort auf Beitrag Nr.: 49.305.413 von SLGramann am 11.03.15 21:45:02Aufgrund des Vertrauensschadens habe ich heute zur Börseneröffnung meine restlichen ACAD verkauft.
Dieses Management hat dermaßen dreist gelogen, dass ich denen keinen Kredit mehr einräume.
Wenn nach Zulassung von Nuplazid die Aktie noch immer Potential bieten sollte, bin ich sicher wieder dabei. Aber ich gehe bei diesem Management nicht mehr in "Vorkasse".
Wer so dreist lügt, der fälscht im Zweifel auch Daten. Damit meine ich nicht, dass ich davon ausgehe, dass die Daten gefälscht sind. Die Wahrscheinlichkeit dafür ist sicher sehr gering. Aber das man denen das jetzt überhaupt zutrauen kann, reicht mir vollkommen für einen konsequenten Abschied.
Dieses Management hat dermaßen dreist gelogen, dass ich denen keinen Kredit mehr einräume.
Wenn nach Zulassung von Nuplazid die Aktie noch immer Potential bieten sollte, bin ich sicher wieder dabei. Aber ich gehe bei diesem Management nicht mehr in "Vorkasse".
Wer so dreist lügt, der fälscht im Zweifel auch Daten. Damit meine ich nicht, dass ich davon ausgehe, dass die Daten gefälscht sind. Die Wahrscheinlichkeit dafür ist sicher sehr gering. Aber das man denen das jetzt überhaupt zutrauen kann, reicht mir vollkommen für einen konsequenten Abschied.
Antwort auf Beitrag Nr.: 49.313.006 von SLGramann am 12.03.15 17:04:28"Aufgrund des Vertrauensschadens habe ich heute zur Börseneröffnung meine restlichen ACAD verkauft."
naja, so kritisch sehe ich die Sache nicht. Eigentlich ist es erstmal nicht zu verstehen, dass man es nach einer erfolgreichen PIII nicht schafft, einen Zulassungsantrag zu stellen. Daher ist die Verschiebung schon ärgerlich.
Ich habe mich mit dem Management von ACAD bisher nicht näher beschäftigt... das Unternehmen habe ich früher aber immer als kleines Biotech-Unternehmen gesehen, das nicht viel zustande bringen kann. Es kann doch sein, dass sie insgesamt eher unerfahren sind und den Zulassungsantrag einfach zu blauäugig angegangen sind. Das klinische ist das eine (und da zählt sicherlich auch einiges an Glück und Zufall dazu und nicht nur erfahrene Leute, um in Studien erfolgreich zu sein)... formale Dinge wie Zulassungen usw aber das andere. Was sollen sie denn machen, wenn sie merken, dass sie damit überfordert sind? Kann doch sein, dass sie bis zum letzten Augenblick nicht zugegeben wollen, dass sie es wieder nicht hinbekommen.
Hat sich nun etwas an der Perspektive von Nuplazid geändert (es sei denn, man zweifelt nun auch an den klinischen Daten)? Im Erfolgsfall geht es um viel Geld... ich hoffe mal, dass im Umfeld von ACAD nun einige Leute sind (Investoren, usw), die dafür Sorgen, dass soetwas nicht nochmal passiert, indem sie jetzt fähigere Personen finden. Der CEO musste gehen... das ist doch schonmal ein Zeichen. Außerdem steht jetzt ACAD unter noch größeren Druck, es diesmal besser zu machen... eventuell auch mit Zugeständnissen, eben erfahreneren Leuten die Sachen zu überlassen oder Pharmas gegenüber offener zu sein.
Dass ist auch ein Vorteil von Deals... PCYC oder Genmab haben zwar einen Teil ihrer Rechte an JNJ abgegeben... dafür bekommen sie aber auch die Unterstützung von in Zulassungsfragen sehr erfahrenen Leuten. So sind diese Dinge einfacher. Ein Pharma-Partner würde auch ACAD gut tun...
Der Kurs ist heute ja nicht völlig kollabiert... ich habe meine Position weiter erhöht... mal schauen.
Apropos Crash... rechnet ihr denn in Kürze mit einem größeren Rücksetzer? Die Zeit jetzt ist eher schwierig (letztes Jahr ging es um die Zeit rum ja auch abwärts)... aber ist es im Fall des Falles dann nur ein temporärer Einbruch oder eine grundsätzliche Trendumkehr? Ich bin mir nicht sicher, dass der Markt schon derart überhitzt ist... Geld ist ja anscheinend noch ausreichend vorhanden, solange der Gesamtmarkt hält.
Grüße
ipollit
naja, so kritisch sehe ich die Sache nicht. Eigentlich ist es erstmal nicht zu verstehen, dass man es nach einer erfolgreichen PIII nicht schafft, einen Zulassungsantrag zu stellen. Daher ist die Verschiebung schon ärgerlich.
Ich habe mich mit dem Management von ACAD bisher nicht näher beschäftigt... das Unternehmen habe ich früher aber immer als kleines Biotech-Unternehmen gesehen, das nicht viel zustande bringen kann. Es kann doch sein, dass sie insgesamt eher unerfahren sind und den Zulassungsantrag einfach zu blauäugig angegangen sind. Das klinische ist das eine (und da zählt sicherlich auch einiges an Glück und Zufall dazu und nicht nur erfahrene Leute, um in Studien erfolgreich zu sein)... formale Dinge wie Zulassungen usw aber das andere. Was sollen sie denn machen, wenn sie merken, dass sie damit überfordert sind? Kann doch sein, dass sie bis zum letzten Augenblick nicht zugegeben wollen, dass sie es wieder nicht hinbekommen.
Hat sich nun etwas an der Perspektive von Nuplazid geändert (es sei denn, man zweifelt nun auch an den klinischen Daten)? Im Erfolgsfall geht es um viel Geld... ich hoffe mal, dass im Umfeld von ACAD nun einige Leute sind (Investoren, usw), die dafür Sorgen, dass soetwas nicht nochmal passiert, indem sie jetzt fähigere Personen finden. Der CEO musste gehen... das ist doch schonmal ein Zeichen. Außerdem steht jetzt ACAD unter noch größeren Druck, es diesmal besser zu machen... eventuell auch mit Zugeständnissen, eben erfahreneren Leuten die Sachen zu überlassen oder Pharmas gegenüber offener zu sein.
Dass ist auch ein Vorteil von Deals... PCYC oder Genmab haben zwar einen Teil ihrer Rechte an JNJ abgegeben... dafür bekommen sie aber auch die Unterstützung von in Zulassungsfragen sehr erfahrenen Leuten. So sind diese Dinge einfacher. Ein Pharma-Partner würde auch ACAD gut tun...
Der Kurs ist heute ja nicht völlig kollabiert... ich habe meine Position weiter erhöht... mal schauen.
Apropos Crash... rechnet ihr denn in Kürze mit einem größeren Rücksetzer? Die Zeit jetzt ist eher schwierig (letztes Jahr ging es um die Zeit rum ja auch abwärts)... aber ist es im Fall des Falles dann nur ein temporärer Einbruch oder eine grundsätzliche Trendumkehr? Ich bin mir nicht sicher, dass der Markt schon derart überhitzt ist... Geld ist ja anscheinend noch ausreichend vorhanden, solange der Gesamtmarkt hält.
Grüße
ipollit
Antwort auf Beitrag Nr.: 49.290.104 von jambam1 am 10.03.15 17:20:10Hallo jambam,
ja, danke!... fairerweise muss man aber auch sagen, dass bei EUR-Kursen der Wechselkurs kräftig mitgeholfen hat.

konjunkturunabhängig... zumindest nicht so konjunkturunabhängig wie andere zyklische Sektoren. Medikamente werden ja nicht mehr oder weniger gekauft, weil die Wirtschaft gut läuft. Ich denke Biotechs sind erfolgreich, wenn sie innovative Mittel auf den Markt bringen, die besser sind als das, was es heute gibt.
Die Konjunktur ist eher der Staat... wenn die Öffentlichkeit sagt, dass zuviel für Medikamente ausgegeben wird, dann sind am Ende die Unternehmen gezwungen die Preise zu senken. Das ist durchaus ein Risiko.
Gruß
ipollit
ja, danke!... fairerweise muss man aber auch sagen, dass bei EUR-Kursen der Wechselkurs kräftig mitgeholfen hat.
konjunkturunabhängig... zumindest nicht so konjunkturunabhängig wie andere zyklische Sektoren. Medikamente werden ja nicht mehr oder weniger gekauft, weil die Wirtschaft gut läuft. Ich denke Biotechs sind erfolgreich, wenn sie innovative Mittel auf den Markt bringen, die besser sind als das, was es heute gibt.
Die Konjunktur ist eher der Staat... wenn die Öffentlichkeit sagt, dass zuviel für Medikamente ausgegeben wird, dann sind am Ende die Unternehmen gezwungen die Preise zu senken. Das ist durchaus ein Risiko.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.315.541 von ipollit am 12.03.15 21:29:51"Es kann doch sein, dass sie insgesamt eher unerfahren sind und den Zulassungsantrag einfach zu blauäugig angegangen sind."
Hallo ipollit,
ich denke, dass es so war und das würde ich ärgerlich, aber letztlich verzeihlich finden.
Was nicht geht ist folgendes:
Aussage am 26.02.2015:
...remain on track to submit our New Drug Application to the FDA in the first quarter of 2015.”
Aussage am 11.03.2015:
ACADIA plans to submit its NUPLAZID NDA for the treatment of Parkinson’s disease psychosis in the second half of 2015.
Ich glaube, niemand wird davon ausgehen, dass man sich am 26.02.2015 einfach im Sachverhalt geirrt hat. Dass man den NDA nun um wohl ca. 6 Monate verschieben muss, spricht für ein etwas größeres Problem und das kann nicht binnen weniger Tage vom Himmel gefallen sein.
De Punkt ist also folgender: Das Management hat die Anleger über einen wichtigen und kursrelevanten Sachverhalt belogen.
Belogen ist das richtige Wort, weil es den Vorsatz beinhaltet. Man wollte lügen und an hat gelogen.
Ich bin der Meinung, dass hier die SEC ermitteln sollte und dass man das Unternehmen auch mit Sammelklagen überziehen wird (auch wenn da vermutlich nichts bei rum kommt).
Das Management bei ACADIA war nicht nur inkompetent (das kann man bis zu einem gewissen Grad verzeihen), es war auch betrügerisch. Das ist ein no go.
Viele Grüße
SLG
Hallo ipollit,
ich denke, dass es so war und das würde ich ärgerlich, aber letztlich verzeihlich finden.
Was nicht geht ist folgendes:
Aussage am 26.02.2015:
...remain on track to submit our New Drug Application to the FDA in the first quarter of 2015.”
Aussage am 11.03.2015:
ACADIA plans to submit its NUPLAZID NDA for the treatment of Parkinson’s disease psychosis in the second half of 2015.
Ich glaube, niemand wird davon ausgehen, dass man sich am 26.02.2015 einfach im Sachverhalt geirrt hat. Dass man den NDA nun um wohl ca. 6 Monate verschieben muss, spricht für ein etwas größeres Problem und das kann nicht binnen weniger Tage vom Himmel gefallen sein.
De Punkt ist also folgender: Das Management hat die Anleger über einen wichtigen und kursrelevanten Sachverhalt belogen.
Belogen ist das richtige Wort, weil es den Vorsatz beinhaltet. Man wollte lügen und an hat gelogen.
Ich bin der Meinung, dass hier die SEC ermitteln sollte und dass man das Unternehmen auch mit Sammelklagen überziehen wird (auch wenn da vermutlich nichts bei rum kommt).
Das Management bei ACADIA war nicht nur inkompetent (das kann man bis zu einem gewissen Grad verzeihen), es war auch betrügerisch. Das ist ein no go.
Viele Grüße
SLG
Antwort auf Beitrag Nr.: 49.315.541 von ipollit am 12.03.15 21:29:51"Apropos Crash... rechnet ihr denn in Kürze mit einem größeren Rücksetzer? Die Zeit jetzt ist eher schwierig (letztes Jahr ging es um die Zeit rum ja auch abwärts)... aber ist es im Fall des Falles dann nur ein temporärer Einbruch oder eine grundsätzliche Trendumkehr? Ich bin mir nicht sicher, dass der Markt schon derart überhitzt ist... Geld ist ja anscheinend noch ausreichend vorhanden, solange der Gesamtmarkt hält."
In Kürze weiß ich nicht, ich habe nur das Gefühl, dass wir in sehr luftigen Höhen sind und dass sehr viel neues Geld in den Biotechsektor geströmt ist. Noch läuft die Party natürlich...
Wenn es knallt, dann rechne ich mit einem temporären Einbruch, der allerdings sehr rabiat sein könnte.
Insgesamt wird der NBI natürlich von Unternehmen getragen, die sich in der Tat auch fundamental sehr stark entwickelt haben.
Die Frage ist dann allerdings immer auch, wie man das alles bewerten muss.
Die Abkopplung des NBI vom allgemeinen Markt ist schon krass:

Die allgemeine Erfahrung sagt, dass solche "Fahnenstangen-Charts" meist nichts Gutes bedeuten.
In Kürze weiß ich nicht, ich habe nur das Gefühl, dass wir in sehr luftigen Höhen sind und dass sehr viel neues Geld in den Biotechsektor geströmt ist. Noch läuft die Party natürlich...
Wenn es knallt, dann rechne ich mit einem temporären Einbruch, der allerdings sehr rabiat sein könnte.
Insgesamt wird der NBI natürlich von Unternehmen getragen, die sich in der Tat auch fundamental sehr stark entwickelt haben.
Die Frage ist dann allerdings immer auch, wie man das alles bewerten muss.
Die Abkopplung des NBI vom allgemeinen Markt ist schon krass:
Die allgemeine Erfahrung sagt, dass solche "Fahnenstangen-Charts" meist nichts Gutes bedeuten.
Hallo Ipollit und Trader,
ich hätte bei den Bios eher damit gerechnet, dass es konjunkturunabhängig weiterläuft, da die Forschungsergebniss nichts mit der Wirtschaft zu tun haben. Bin also jetzt gespannt wie ein Flitzebogen.
Werde demnächst ein weitere Depot anlegen.
Grüsse und vielen Dank.
ich hätte bei den Bios eher damit gerechnet, dass es konjunkturunabhängig weiterläuft, da die Forschungsergebniss nichts mit der Wirtschaft zu tun haben. Bin also jetzt gespannt wie ein Flitzebogen.
Werde demnächst ein weitere Depot anlegen.
Grüsse und vielen Dank.
Antwort auf Beitrag Nr.: 49.320.902 von jambam1 am 13.03.15 13:20:24Der Chef von Regeneron hat letzte Woche gesagt:
Das Schöne an unserer Branche ist, wir brauchen keine Werbung und kein Marketing.
Wir entwickeln ein neues Produkt. Und wenn es besser ist als die existierenden,verkauft es sich von selbst.
Das Schöne an unserer Branche ist, wir brauchen keine Werbung und kein Marketing.
Wir entwickeln ein neues Produkt. Und wenn es besser ist als die existierenden,verkauft es sich von selbst.
Antwort auf Beitrag Nr.: 49.315.634 von ipollit am 12.03.15 21:41:32
das ist auch so ziemlich exaaakt mein (Grund)Verständnis, von diesen Bio/Med(für Erstere mehr)techfirmen
Gruß
P.
Zitat von ipollit: konjunkturunabhängig... zumindest nicht so konjunkturunabhängig wie andere zyklische Sektoren. Medikamente werden ja nicht mehr oder weniger gekauft, weil die Wirtschaft gut läuft.
Ich denke Biotechs sind erfolgreich, wenn sie innovative Mittel auf den Markt bringen, die besser sind als das, was es heute gibt.
Die Konjunktur ist eher der Staat...
das ist auch so ziemlich exaaakt mein (Grund)Verständnis, von diesen Bio/Med(für Erstere mehr)techfirmen
Gruß
P.
Antwort auf Beitrag Nr.: 49.319.522 von SLGramann am 13.03.15 11:26:41"Die allgemeine Erfahrung sagt, dass solche "Fahnenstangen-Charts" meist nichts Gutes bedeuten."
Aber handelt es sich wirklich um eine "Fahnenstange"? Nach meinem Verständnis ist es gerade in den letzten Jahren ein qualitativ hochwertiger, gesunder Trend... im Chart kann man eine schöne Linie einzeichnen, an der sich der Index gleichmäßig nach oben bewegt...
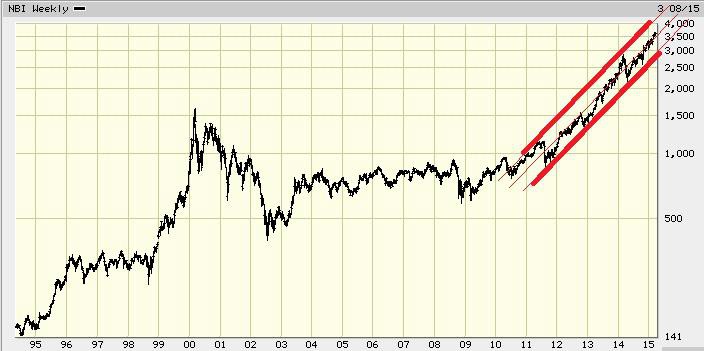
Eine Fahnenstange gibt es dagegen im NBI um 2000 rum.
Gleichmäßige langfristige Trends sind meiner Meinung nach keine exzessive Entwicklung, die durch einen anschließenden Crash korrigiert werden muss.
Der mit 148 Mrd USD von der Marktkapitalisierung größte Biotech Gilead hatte auch solche linearen Trends... einen wirklichen Crash gab es danach nicht
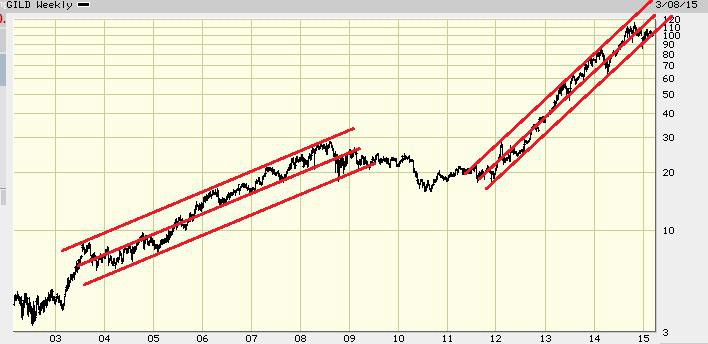
Die Kurse werden ja nicht nur von Zockern oder Investoren getrieben, sondern auch vom Zwang der Pharmas&Co, die Patentverluste kompensieren bzw. in immer neue Medikamente investieren zu müssen, um in Zukunft zu bestehen. Die eigenen Pipelines sind dafür nicht ausreichend... aber gleichzeitig ist viel Geld vorhanden, um entsprechende Medikamente einkaufen zu können.
So soll zuletzt Abbvie bei der 21 Mrd USD Übernahme von PCYC u.a. JNJ, vielleicht auch Novartis ausgestochen haben... angeblich lagen die Gebote dabei nur 4% auseinander. D.h. nicht nur ABBV war bereit mehr als 20 Mrd USD für PCYC auf den Tisch zu legen. Dieses Geld ist nun immer noch vorhanden... statt PCYC wird es nun woanders investiert werden. Das ist Geld, welches dauerhaft in den Sektor fließt... z.B. die 21 Mrd von ABBV werden später nicht wieder eingesammelt.
Hier ist eine Free-Cashflow Auflistung... dies sind die Beträge die die entsprechenden Unternehmen aus dem laufenden Geschäft Jahr für Jahr investieren können. Alleine GILD kommt hier auf 15 Mrd USD pro Jahr... sie könnten damit fast jedes Jahr eine PCYC kaufen.
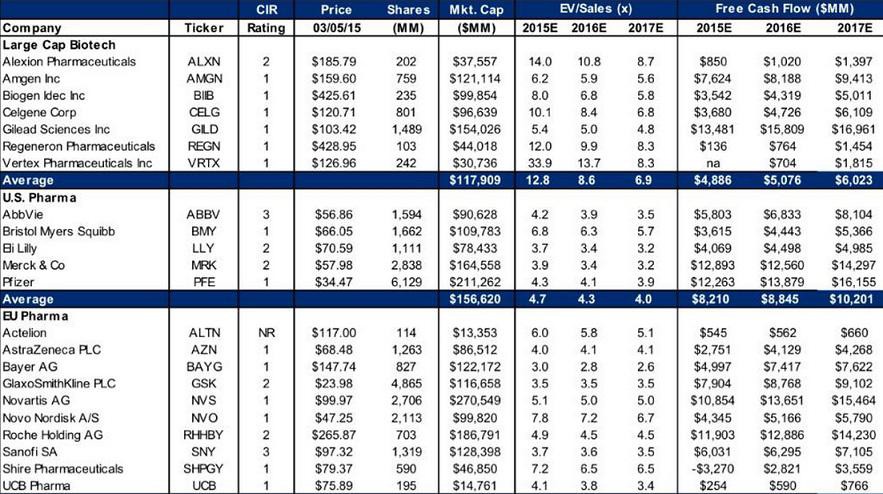
Gruß
ipollit
Aber handelt es sich wirklich um eine "Fahnenstange"? Nach meinem Verständnis ist es gerade in den letzten Jahren ein qualitativ hochwertiger, gesunder Trend... im Chart kann man eine schöne Linie einzeichnen, an der sich der Index gleichmäßig nach oben bewegt...

Eine Fahnenstange gibt es dagegen im NBI um 2000 rum.
Gleichmäßige langfristige Trends sind meiner Meinung nach keine exzessive Entwicklung, die durch einen anschließenden Crash korrigiert werden muss.
Der mit 148 Mrd USD von der Marktkapitalisierung größte Biotech Gilead hatte auch solche linearen Trends... einen wirklichen Crash gab es danach nicht

Die Kurse werden ja nicht nur von Zockern oder Investoren getrieben, sondern auch vom Zwang der Pharmas&Co, die Patentverluste kompensieren bzw. in immer neue Medikamente investieren zu müssen, um in Zukunft zu bestehen. Die eigenen Pipelines sind dafür nicht ausreichend... aber gleichzeitig ist viel Geld vorhanden, um entsprechende Medikamente einkaufen zu können.
So soll zuletzt Abbvie bei der 21 Mrd USD Übernahme von PCYC u.a. JNJ, vielleicht auch Novartis ausgestochen haben... angeblich lagen die Gebote dabei nur 4% auseinander. D.h. nicht nur ABBV war bereit mehr als 20 Mrd USD für PCYC auf den Tisch zu legen. Dieses Geld ist nun immer noch vorhanden... statt PCYC wird es nun woanders investiert werden. Das ist Geld, welches dauerhaft in den Sektor fließt... z.B. die 21 Mrd von ABBV werden später nicht wieder eingesammelt.
Hier ist eine Free-Cashflow Auflistung... dies sind die Beträge die die entsprechenden Unternehmen aus dem laufenden Geschäft Jahr für Jahr investieren können. Alleine GILD kommt hier auf 15 Mrd USD pro Jahr... sie könnten damit fast jedes Jahr eine PCYC kaufen.

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.335.677 von ipollit am 15.03.15 22:01:47"Aber handelt es sich wirklich um eine "Fahnenstange"? Nach meinem Verständnis ist es gerade in den letzten Jahren ein qualitativ hochwertiger, gesunder Trend..."
Hallo ipollit,
das kann natürlich sein, ich bin eh kein Chartdeuter. Ich sehe halt nur, dass es eine sehr, sehr ausgeprägte Aufwärtsbewegung gegeben hat, die historische Maßstäbe sprengt und ich habe das Gefühl, dass der Markt ziemlich heißgelaufen ist.
Ich rechne aber ebenfalls nicht mit einem kompletten Trendbruch, sondern "nur" mit einer scharfen Korrektur.
Ich würde mich daher auch nicht ganz aus dem Markt zurückziehen - bin ja noch zu 60% investiert.
Wie würde es nach Deine Ansicht weitergehen? Dass irgendwann dieser Aufwärtstrend einfach abflacht? Wie bei GILD als Beispiel? Das kann sehr gut sein.
Sondersituationen sind außerdem immer gesondert zu bewerten. Ich denke da bspw. an CLVS.
Nehmen wir an, die Daten zur ASCO entsprechen den positiven Erwartungen voll und ganz.
Sollte CLVS dann nicht binnen 2 bis 3 Jahren bis zu 8 Milliarden Dollar wert werden? Unabhängig von einer Korrektur am Gesamtmarkt.
Wie siehst Du das?
Gruß
SLG
Hallo ipollit,
das kann natürlich sein, ich bin eh kein Chartdeuter. Ich sehe halt nur, dass es eine sehr, sehr ausgeprägte Aufwärtsbewegung gegeben hat, die historische Maßstäbe sprengt und ich habe das Gefühl, dass der Markt ziemlich heißgelaufen ist.
Ich rechne aber ebenfalls nicht mit einem kompletten Trendbruch, sondern "nur" mit einer scharfen Korrektur.
Ich würde mich daher auch nicht ganz aus dem Markt zurückziehen - bin ja noch zu 60% investiert.
Wie würde es nach Deine Ansicht weitergehen? Dass irgendwann dieser Aufwärtstrend einfach abflacht? Wie bei GILD als Beispiel? Das kann sehr gut sein.
Sondersituationen sind außerdem immer gesondert zu bewerten. Ich denke da bspw. an CLVS.
Nehmen wir an, die Daten zur ASCO entsprechen den positiven Erwartungen voll und ganz.
Sollte CLVS dann nicht binnen 2 bis 3 Jahren bis zu 8 Milliarden Dollar wert werden? Unabhängig von einer Korrektur am Gesamtmarkt.
Wie siehst Du das?
Gruß
SLG
Antwort auf Beitrag Nr.: 49.337.744 von SLGramann am 16.03.15 10:02:08
KPTI
...brachte heute seine Zahlen zum 4.Quartal. Das Unternehmen macht ja bekanntermaßen noch keine Gewinne (was jedem Investiertem hier klar sein dürfte...) und das erzielte Ergebnis pro Aktie war mit -0,79$ noch 14 Cent unterhalb der erwarteten -0,65$ Verlustschätzung.
Das Unternehmen gab zudem Freitag nachbörslich bekannt ca. 1,3 Mio Aktien zu veräussern um die Kapitaldecke aufzustocken.
Heute vorbörslich dann eine CC zu den Zahlen - sowie ein Update auf die Pipeline...und die Unternehmensführung weis seinen Anlegern zu gefallen, was am heute massiv anziehenden Kurs unschwer zu erkennen ist. Aktuell zieht der Kurs um gut 10 Prozent an - die Kursziele der Analystenhäuser liegen derzeit zwischen 50 und 60$ - da könnte sich also noch recht ordentlich was beim Kurs nach oben tun.
KPTI
...brachte heute seine Zahlen zum 4.Quartal. Das Unternehmen macht ja bekanntermaßen noch keine Gewinne (was jedem Investiertem hier klar sein dürfte...) und das erzielte Ergebnis pro Aktie war mit -0,79$ noch 14 Cent unterhalb der erwarteten -0,65$ Verlustschätzung.
Das Unternehmen gab zudem Freitag nachbörslich bekannt ca. 1,3 Mio Aktien zu veräussern um die Kapitaldecke aufzustocken.
Heute vorbörslich dann eine CC zu den Zahlen - sowie ein Update auf die Pipeline...und die Unternehmensführung weis seinen Anlegern zu gefallen, was am heute massiv anziehenden Kurs unschwer zu erkennen ist. Aktuell zieht der Kurs um gut 10 Prozent an - die Kursziele der Analystenhäuser liegen derzeit zwischen 50 und 60$ - da könnte sich also noch recht ordentlich was beim Kurs nach oben tun.

ESPR & REGN
es ist noch gar nicht so lange her, dass ESPR unter 20 USD gehandelt wurden... heute waren sie erstmals dreistellig...

Vorgestern gab es detailliertere PII-Ergebnisse bezüglich einem Vergleich von ETC-1002 und Zetia... wie bereits bekannt, ist ETC-1002 deutlich besser. Zudem kann eine Kombi ETC-1002 + Zetia Sinn machen als Alternative zu Statinen oder PCSK9 AKs.

Heute gab es nun PII-Ergebnisse zur ETC-1002 + Statin Kombi... ETC-1002 wirkt sich zusätzlich zum Statin-Effekt positiv aus, was diese Kombination ebenfalls interessant macht.


REGN, AMGN usw können ebenfalls positive Ergebnisse zu ihren PCSK9 AKs bekanntgeben. Diese senken im wesentlichen LDL deutlich... dies scheint sich offensichtlich positiv auch kardiovaskuläre Probleme wie Herzinfarkt auszuwirken. Sowohl REGN als auch AMGN können sie etwa um die Hälfte senken.


Gruß
ipollit
es ist noch gar nicht so lange her, dass ESPR unter 20 USD gehandelt wurden... heute waren sie erstmals dreistellig...
Vorgestern gab es detailliertere PII-Ergebnisse bezüglich einem Vergleich von ETC-1002 und Zetia... wie bereits bekannt, ist ETC-1002 deutlich besser. Zudem kann eine Kombi ETC-1002 + Zetia Sinn machen als Alternative zu Statinen oder PCSK9 AKs.

Heute gab es nun PII-Ergebnisse zur ETC-1002 + Statin Kombi... ETC-1002 wirkt sich zusätzlich zum Statin-Effekt positiv aus, was diese Kombination ebenfalls interessant macht.


REGN, AMGN usw können ebenfalls positive Ergebnisse zu ihren PCSK9 AKs bekanntgeben. Diese senken im wesentlichen LDL deutlich... dies scheint sich offensichtlich positiv auch kardiovaskuläre Probleme wie Herzinfarkt auszuwirken. Sowohl REGN als auch AMGN können sie etwa um die Hälfte senken.

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.356.083 von ipollit am 17.03.15 22:08:58Ja, fantastische Entwicklung bei ESPR.
Sie nutzen das auch für eine KE, um ca. 170 Mio. Dollar einzusammeln. Gute Sache, wie ich finde, denn so etwas stärkt ihre Stellung in möglichen Verpartnerungsverhandlungen:
ANN ARBOR, MI -- (Marketwired) -- 03/17/15 -- Esperion Therapeutics, Inc. (NASDAQ: ESPR), an emerging pharmaceutical company focused on developing and commercializing first-in-class, oral low-density lipoprotein cholesterol (LDL-cholesterol) lowering therapies for the treatment of hypercholesterolemia and other cardiometabolic risk markers, today announced that it intends to offer and sell, subject to market and other conditions, $150 million of its common stock in an underwritten public offering. Esperion expects to grant the underwriters a 30-day option to purchase up to $22.5 million of additional shares of its common stock.
Hammer hat ja mal den für ihn fairen Preis für eine denkbare Übernahme wie folgt berechnet:

Diese Marktkapitalisierung wurde jetzt bereits erreicht.
Man muss sich fragen, wo man an seinen "DCF"-Annahmen drehen will, um weiteres Potential zu begründen.
Ganz sicher nicht bei der Zulassungswahrscheinlichkeit. Die ist mit 80% schon großzügig bemessen. Ebenso die sales multiple von 8.
Bleiben die peak sales und der Abzinsungsfaktor. Letzterer ist zwar sehr fett, aber man muss ja sehen, dass das auch der erwarteten bzw. aus dem Modell erwartbaren Rendite entspricht. Und wer erwartet im Erfolgsfall weniger als 25% Rendite/Jahr in dieser Branche?
Bleiben die peak sales. 2 Milliarden könnten einerseits viel zu vorsichtig geschätzt sein, andererseits bezieht sich das auf 100% der Rechte, die es ja wirklich nur im Fall einer Übernahme bleiben würden, denke ich mal.
Es wäre vielleicht ganz spannend, mal alternative Überlegungen zu den peak sales zu lesen. Ist da wirklich deutlich mehr als 2 Milliarden ww drin?
Wie auch immer, ich werde meine ESPR auch nach diesem Höhenflug halten. Die Bewertungsfrage ist aber auch hier jetzt definitiv ein Thema.
Sie nutzen das auch für eine KE, um ca. 170 Mio. Dollar einzusammeln. Gute Sache, wie ich finde, denn so etwas stärkt ihre Stellung in möglichen Verpartnerungsverhandlungen:
ANN ARBOR, MI -- (Marketwired) -- 03/17/15 -- Esperion Therapeutics, Inc. (NASDAQ: ESPR), an emerging pharmaceutical company focused on developing and commercializing first-in-class, oral low-density lipoprotein cholesterol (LDL-cholesterol) lowering therapies for the treatment of hypercholesterolemia and other cardiometabolic risk markers, today announced that it intends to offer and sell, subject to market and other conditions, $150 million of its common stock in an underwritten public offering. Esperion expects to grant the underwriters a 30-day option to purchase up to $22.5 million of additional shares of its common stock.
Hammer hat ja mal den für ihn fairen Preis für eine denkbare Übernahme wie folgt berechnet:

Diese Marktkapitalisierung wurde jetzt bereits erreicht.
Man muss sich fragen, wo man an seinen "DCF"-Annahmen drehen will, um weiteres Potential zu begründen.
Ganz sicher nicht bei der Zulassungswahrscheinlichkeit. Die ist mit 80% schon großzügig bemessen. Ebenso die sales multiple von 8.
Bleiben die peak sales und der Abzinsungsfaktor. Letzterer ist zwar sehr fett, aber man muss ja sehen, dass das auch der erwarteten bzw. aus dem Modell erwartbaren Rendite entspricht. Und wer erwartet im Erfolgsfall weniger als 25% Rendite/Jahr in dieser Branche?
Bleiben die peak sales. 2 Milliarden könnten einerseits viel zu vorsichtig geschätzt sein, andererseits bezieht sich das auf 100% der Rechte, die es ja wirklich nur im Fall einer Übernahme bleiben würden, denke ich mal.
Es wäre vielleicht ganz spannend, mal alternative Überlegungen zu den peak sales zu lesen. Ist da wirklich deutlich mehr als 2 Milliarden ww drin?
Wie auch immer, ich werde meine ESPR auch nach diesem Höhenflug halten. Die Bewertungsfrage ist aber auch hier jetzt definitiv ein Thema.
Mal wieder eine positive Phase I Studie (Signifikanz ab 3 mg/kg) zu Alzheimer mit dem "bewährten" Ansatz der Plaque-Entfernung. Biogen IDEC geht daraufhin gleich in Phase III.
http://finance.yahoo.com/news/biogen-idec-presents-positive-…
Biogen ist bislang hauptsächlich im Multiple Sklerose Bereich erfolgreich u. hat bei einem Kurs von 433 USD ca. 100 Mrd USD Marktkapitalisierung. Der kommunizierte PI Erfolg hat insgesamt zu ca. 30 USD Kursanstieg (ca. 425 -> 455 USD = Vorbörse) geführt. u. damit 7-8 Mrd USD Marktkapitalisierung.
Biotech in den USA hat m.e. noch den Vorteil von einigen Punkten besonders zu profitieren:
1. für Millionen Neukunden in den USA aufgrund Versicherung u. Kostenübernahme durch Obamacare
2. der besonders lukrative US-Markt wird nicht vom Dollarverfall negativ beeinflusst
3. die Leitzinsen bleiben niedrig u. damit steht Risikokapital zur Verfügung
Insbesondere Biogen ist ein solides Unternehmen im Biotechsektor, aber es erhöhen sich für mich die Anzeichen, dass der Markt überhitzt.
http://finance.yahoo.com/news/biogen-idec-presents-positive-…
Biogen ist bislang hauptsächlich im Multiple Sklerose Bereich erfolgreich u. hat bei einem Kurs von 433 USD ca. 100 Mrd USD Marktkapitalisierung. Der kommunizierte PI Erfolg hat insgesamt zu ca. 30 USD Kursanstieg (ca. 425 -> 455 USD = Vorbörse) geführt. u. damit 7-8 Mrd USD Marktkapitalisierung.
Biotech in den USA hat m.e. noch den Vorteil von einigen Punkten besonders zu profitieren:
1. für Millionen Neukunden in den USA aufgrund Versicherung u. Kostenübernahme durch Obamacare
2. der besonders lukrative US-Markt wird nicht vom Dollarverfall negativ beeinflusst
3. die Leitzinsen bleiben niedrig u. damit steht Risikokapital zur Verfügung
Insbesondere Biogen ist ein solides Unternehmen im Biotechsektor, aber es erhöhen sich für mich die Anzeichen, dass der Markt überhitzt.
Blase oder nicht?
Ich denke schon, dass ein Rücksetzer dem Markt ganz gut täte und kommen wird. Eine Blase sehe ich aber auch nicht, insbesondere nicht, wenn man sich einzelne Werte ansieht. Es gibt eben auch rational nachvollziehbare Gründe für die Bewertungen. Aber auch bzw. vor allem dann, wenn alles gut läuft. Ein Riskopuffer ist teilwiese nicht mehr vorhanden.
Eine schöne Übersicht (Anm: von BBBiotech) zeigt den/einen entscheidenden Unterschied zur Blase aus dem Jahr 2000:

Eine wichtige Rolle beim Boom wird auch der niedrige Zinssatz spielen. Dadurch ist viel Kapital da, dass an die Börsen fließt. Zudem werden ja auch Übernahmen meist über Kredite finanziert. Und da lohnt sich eine große Übernahme (ähnlich wie ein Immobilienkauf) zur Zeit eben eher. Die Raten werden dann von den Umsätzen der Medikamente getragen bzw. können oft ja auch Synergien nutzbar gemacht werden.
Aber ewig wird es so nicht weiter gehen. Der von mir entwickelte Medigene Indikator ist auch angesprungen. Ich denke einen "Plan" für eine Korrektur zu haben kann nicht schaden - nur überraschen sollte einen das nicht...
ist auch angesprungen. Ich denke einen "Plan" für eine Korrektur zu haben kann nicht schaden - nur überraschen sollte einen das nicht...
Ich habe heute dennoch meine ENTA Position ausgebaut. Ich denke, dass dies ein weniger spekulativer Wert ist, als z.B. Juno, da ja bereits jetzt Umsätze erzielt werden. Die Bewertung ist für mich nicht mehr nachvollziehbar. Die bekannt gegebenen Verschreibungen vom Viekira Pack sind doch merklich am wachsen und vor allem ist ja Express Scripts bekanntermaßen bei diesen Zahlen noch gar nicht dabei. Ebenso Europa nicht. Sind einge da von den Zahlen im Vergleich zu Harvoni verunsichert? Ich denke ein Trend lässt sich anhand der bekannten Zahlen aber schon ableiten.
Ende April bzw. spätestens Ende Juli nah den Zahlen von ABBVIE weiß man es genau.


DewDiligence Bewertungsmodell:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
SG kmastra
Ich denke schon, dass ein Rücksetzer dem Markt ganz gut täte und kommen wird. Eine Blase sehe ich aber auch nicht, insbesondere nicht, wenn man sich einzelne Werte ansieht. Es gibt eben auch rational nachvollziehbare Gründe für die Bewertungen. Aber auch bzw. vor allem dann, wenn alles gut läuft. Ein Riskopuffer ist teilwiese nicht mehr vorhanden.
Eine schöne Übersicht (Anm: von BBBiotech) zeigt den/einen entscheidenden Unterschied zur Blase aus dem Jahr 2000:

Eine wichtige Rolle beim Boom wird auch der niedrige Zinssatz spielen. Dadurch ist viel Kapital da, dass an die Börsen fließt. Zudem werden ja auch Übernahmen meist über Kredite finanziert. Und da lohnt sich eine große Übernahme (ähnlich wie ein Immobilienkauf) zur Zeit eben eher. Die Raten werden dann von den Umsätzen der Medikamente getragen bzw. können oft ja auch Synergien nutzbar gemacht werden.
Aber ewig wird es so nicht weiter gehen. Der von mir entwickelte Medigene Indikator
 ist auch angesprungen. Ich denke einen "Plan" für eine Korrektur zu haben kann nicht schaden - nur überraschen sollte einen das nicht...
ist auch angesprungen. Ich denke einen "Plan" für eine Korrektur zu haben kann nicht schaden - nur überraschen sollte einen das nicht... Ich habe heute dennoch meine ENTA Position ausgebaut. Ich denke, dass dies ein weniger spekulativer Wert ist, als z.B. Juno, da ja bereits jetzt Umsätze erzielt werden. Die Bewertung ist für mich nicht mehr nachvollziehbar. Die bekannt gegebenen Verschreibungen vom Viekira Pack sind doch merklich am wachsen und vor allem ist ja Express Scripts bekanntermaßen bei diesen Zahlen noch gar nicht dabei. Ebenso Europa nicht. Sind einge da von den Zahlen im Vergleich zu Harvoni verunsichert? Ich denke ein Trend lässt sich anhand der bekannten Zahlen aber schon ableiten.
Ende April bzw. spätestens Ende Juli nah den Zahlen von ABBVIE weiß man es genau.

DewDiligence Bewertungsmodell:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
SG kmastra
arry:
gut zu lesen, dass die Vorteile von BRAF und MEK Inhibitoren mit denen der Immuntherapien kombinierbar sind - zumindest im Tiermodell.
Bin gespannt auf die Asco-Daten.
Es dürfte dann Merck oder Bristol interessieren, MEK und BRAF Inhibitoren mit ihren Antikörpern zu testen.
Triple Combo Appears Effective in Metastatic Melanoma
Researchers at the University of California, Los Angeles, found that a triple-combination drug therapy appears to be effective at controlling advanced melanoma with increased immune response and fewer adverse events.
About 50% of patients with melanoma have a BRAF mutation, which in most cases enables the cancer to develop resistance to many drug therapies.
The strategy of combining a targeted therapy with an immunotherapy to improve antitumor activity in melanoma has been tried, but there were serious liver toxicity in some patients, making the BRAF and/or MEK inhibitors less effective resulting in reactivated cancer cell growth (N Engl J Med 2013;368:1365-1366; PMID: 23550685).
In this controlled laboratory experiment in with mice, the researchers combined two targeted therapies using the BRAF inhibitor, dabrafenib (Taflinar, GlaxoSmithKine) and the MEK inhibitor, trametinib (Mekinist, GSK) with tumor antigen-specific adoptive cell transfer or anti-PD1 antibody immunotherapy. The three together were shown to be more effective treatments because they sensitize the immune system to enhance immunotherapy and reduce the probability of the melanoma eventually developing resistance, according to lead investigators, Antoni Ribas, MD, PhD, the director of the Tumor Immunology Program Area, and Siwen Hu-Lieskovan, MD, PhD, an instructor of hematology and oncology at the UCLA Jonsson Comprehensive Cancer Center (Sci Transl Med 2015 Mar 18. [Epublished March 18 ahead of print]).
“We are trying to take advantage of the high response rate of the targeted therapy and durability of the immune therapy to induce a response that lasts in the majority of patients,” said Dr. Hu-Lieskovan. Combining the BRAF and MEK inhibitors with immunotherapy appears to do that by increasing the regimen’s killing ability.
“The two two-drug combination of BRAF and MEK inhibitors works synergistically and decreases the side effects of the BRAF inhibitor or normal cells. We reasoned that this combo would allows us to synergize with immunotherapy without increasing toxicities,” said Dr. Ribas, who is also a professor of hematology and oncology at UCLA. “We have made incredible progress in the last three years of treating advanced melanoma, with six new drug therapies approved by the FDA. Half are immunotherapies and the other half are BRAF or MEK inhibitors.”
The next step, he said would be to determine the best way to combine them to “merge their benefits in the clinic."
The researchers have begun two clinical trials to test the effectiveness of the triple combination therapy in metastatic melanoma. The first reported findings will be presented at the American Society of Clinical Oncology annual meeting in May.
Each year, an estimated 70,000 new cases of melanoma are diagnosed in the United States, and more than 8,600 die, according to the American Melanoma Foundation.
http://www.clinicaloncology.com/ViewArticle.aspx?d=Web%2BExc…
gut zu lesen, dass die Vorteile von BRAF und MEK Inhibitoren mit denen der Immuntherapien kombinierbar sind - zumindest im Tiermodell.
Bin gespannt auf die Asco-Daten.
Es dürfte dann Merck oder Bristol interessieren, MEK und BRAF Inhibitoren mit ihren Antikörpern zu testen.
Triple Combo Appears Effective in Metastatic Melanoma
Researchers at the University of California, Los Angeles, found that a triple-combination drug therapy appears to be effective at controlling advanced melanoma with increased immune response and fewer adverse events.
About 50% of patients with melanoma have a BRAF mutation, which in most cases enables the cancer to develop resistance to many drug therapies.
The strategy of combining a targeted therapy with an immunotherapy to improve antitumor activity in melanoma has been tried, but there were serious liver toxicity in some patients, making the BRAF and/or MEK inhibitors less effective resulting in reactivated cancer cell growth (N Engl J Med 2013;368:1365-1366; PMID: 23550685).
In this controlled laboratory experiment in with mice, the researchers combined two targeted therapies using the BRAF inhibitor, dabrafenib (Taflinar, GlaxoSmithKine) and the MEK inhibitor, trametinib (Mekinist, GSK) with tumor antigen-specific adoptive cell transfer or anti-PD1 antibody immunotherapy. The three together were shown to be more effective treatments because they sensitize the immune system to enhance immunotherapy and reduce the probability of the melanoma eventually developing resistance, according to lead investigators, Antoni Ribas, MD, PhD, the director of the Tumor Immunology Program Area, and Siwen Hu-Lieskovan, MD, PhD, an instructor of hematology and oncology at the UCLA Jonsson Comprehensive Cancer Center (Sci Transl Med 2015 Mar 18. [Epublished March 18 ahead of print]).
“We are trying to take advantage of the high response rate of the targeted therapy and durability of the immune therapy to induce a response that lasts in the majority of patients,” said Dr. Hu-Lieskovan. Combining the BRAF and MEK inhibitors with immunotherapy appears to do that by increasing the regimen’s killing ability.
“The two two-drug combination of BRAF and MEK inhibitors works synergistically and decreases the side effects of the BRAF inhibitor or normal cells. We reasoned that this combo would allows us to synergize with immunotherapy without increasing toxicities,” said Dr. Ribas, who is also a professor of hematology and oncology at UCLA. “We have made incredible progress in the last three years of treating advanced melanoma, with six new drug therapies approved by the FDA. Half are immunotherapies and the other half are BRAF or MEK inhibitors.”
The next step, he said would be to determine the best way to combine them to “merge their benefits in the clinic."
The researchers have begun two clinical trials to test the effectiveness of the triple combination therapy in metastatic melanoma. The first reported findings will be presented at the American Society of Clinical Oncology annual meeting in May.
Each year, an estimated 70,000 new cases of melanoma are diagnosed in the United States, and more than 8,600 die, according to the American Melanoma Foundation.
http://www.clinicaloncology.com/ViewArticle.aspx?d=Web%2BExc…
ESPR:
Sehr erfreuliche Entwicklung. Aber irgendwie auch komisch. Sind die Ergebnisse denn so überraschend, dass sie einen solchen Sprung rechtfertigen?
Interessant dürften auch noch die genaueren Zahlen sein.
Wie wirksam war 1002 z.B. bei der niedrigen Dosierung der Statine-auch absolut?
Im CC zum letzen Q kamen schon viele Fragen zu einer 3xFix-dosed-Combination. (1002+Zetia+Statin) als orale Alternative zu den PCSK9s.
Im CC zu den 09 Ergebnissen wird dazu sinngemäß gesagt, dass das eher das Potenzial für einen potenziellen Parner erhöht und man bei der Wahl eines potenziellen Partners (Ex-Us) Wert darauf läge, dass dieser das Potenzial ausschöpft.
Wenn Merck hier nicht zuschlägt versteh ich die Welt nicht mehr. Das passt in so ziemlich jeglicher Hinsicht.
ZFGN:
Auch hier eine erfreuliche Entwicklung. Hier noch komischer, da die PII Daten im Grunde schon im Januar bekannt gegeben wurden. Grundsätzlich finde ich ZFGN aber weiterhin sehr spannend - wobei hier schon viel eingepreist scheint. Fantasie kann eher noch durch eine Labelerweiterung entstehen. B. ist unfassbar effektiv. Man kann von einem Gewichtsverlust von ca. 1KG pro Woche ausgehen und das ohne Diät oder Sport! Es gibt Leute die würden töten für ein solches Medikament!
Auf jeden Fall schön zu sehen, was passiert, wenn die Kontrollgruppe nach 3 Wochen zu B. wechselt.

Auch das NASH Programm ist für mich als Laien viel versprechend. NASH hat ja oft Übergewicht und einen daraus gestörten Fettstoffwechsel/eine Leberverfettung als Ursache. Könnte der Ansatz von ZFGN nicht die Ursache bekämpfen?
ZFGN ist hier aber erst am Anfang und hat noch gar nicht mit Studien begonnen.

An ZFGN gefällt mir definitiv auch das Management, dass bei der Entwicklung sehr bedacht und doch zielgerichtet vorgeht.
http://lifescivc.com/2015/03/rare-diseases-rare-opportunitie…
AERI:
Hier stehen ja bald die ersten PIII Ergebnisse an. Eigentlich war mein Plan hier noch vorher zuzukaufen, da ein Erfolg ja wahrscheinlicher ist, als ein Miserfolg. Da bin ich mir aber jetzt nicht mehr sicher. Es scheint so, dass AERI gewisse Nebenwirkungen heruntergespielt hat (Augenrötung). Ich denke aber, dass man das auch nicht überbewerten sollte. Dagegen gibt es ja auch Augentropfen, wenn es das allein ist. Die Quelle des Bildes ist ein Konkurent, der das vielleicht bzw. ganz bestimmt auch hochspielt. Erstmal geht es ja auch nur um die Wirksamkeit.

Wie seht ihr das?
SG kmastra
Sehr erfreuliche Entwicklung. Aber irgendwie auch komisch. Sind die Ergebnisse denn so überraschend, dass sie einen solchen Sprung rechtfertigen?
Interessant dürften auch noch die genaueren Zahlen sein.
Wie wirksam war 1002 z.B. bei der niedrigen Dosierung der Statine-auch absolut?
Im CC zum letzen Q kamen schon viele Fragen zu einer 3xFix-dosed-Combination. (1002+Zetia+Statin) als orale Alternative zu den PCSK9s.
Im CC zu den 09 Ergebnissen wird dazu sinngemäß gesagt, dass das eher das Potenzial für einen potenziellen Parner erhöht und man bei der Wahl eines potenziellen Partners (Ex-Us) Wert darauf läge, dass dieser das Potenzial ausschöpft.
Wenn Merck hier nicht zuschlägt versteh ich die Welt nicht mehr. Das passt in so ziemlich jeglicher Hinsicht.
ZFGN:
Auch hier eine erfreuliche Entwicklung. Hier noch komischer, da die PII Daten im Grunde schon im Januar bekannt gegeben wurden. Grundsätzlich finde ich ZFGN aber weiterhin sehr spannend - wobei hier schon viel eingepreist scheint. Fantasie kann eher noch durch eine Labelerweiterung entstehen. B. ist unfassbar effektiv. Man kann von einem Gewichtsverlust von ca. 1KG pro Woche ausgehen und das ohne Diät oder Sport! Es gibt Leute die würden töten für ein solches Medikament!
Auf jeden Fall schön zu sehen, was passiert, wenn die Kontrollgruppe nach 3 Wochen zu B. wechselt.

Auch das NASH Programm ist für mich als Laien viel versprechend. NASH hat ja oft Übergewicht und einen daraus gestörten Fettstoffwechsel/eine Leberverfettung als Ursache. Könnte der Ansatz von ZFGN nicht die Ursache bekämpfen?
ZFGN ist hier aber erst am Anfang und hat noch gar nicht mit Studien begonnen.

An ZFGN gefällt mir definitiv auch das Management, dass bei der Entwicklung sehr bedacht und doch zielgerichtet vorgeht.
http://lifescivc.com/2015/03/rare-diseases-rare-opportunitie…
AERI:
Hier stehen ja bald die ersten PIII Ergebnisse an. Eigentlich war mein Plan hier noch vorher zuzukaufen, da ein Erfolg ja wahrscheinlicher ist, als ein Miserfolg. Da bin ich mir aber jetzt nicht mehr sicher. Es scheint so, dass AERI gewisse Nebenwirkungen heruntergespielt hat (Augenrötung). Ich denke aber, dass man das auch nicht überbewerten sollte. Dagegen gibt es ja auch Augentropfen, wenn es das allein ist. Die Quelle des Bildes ist ein Konkurent, der das vielleicht bzw. ganz bestimmt auch hochspielt. Erstmal geht es ja auch nur um die Wirksamkeit.

Wie seht ihr das?
SG kmastra
Antwort auf Beitrag Nr.: 49.241.438 von kmastra am 04.03.15 19:36:27
hallo Timburg,
keiiine Ahnung zu Deinem Unternehmen, aber was ich generell raten würde
ich würde aufpassen nicht "zuuu lehrbuchmässig" zu denken
ist würde ich sagen so ein bisschen deutsches Ding
was meiner Erfahrung nach -nicht immer, aber- oft in die Hose geht
Problem ist: die Wirklichkeit passt da oft(meistens)nicht rein
hallo Kmastra,
dem werde ich voraussichtlich noch sehr gern nachkommen
es ist immer so ein bisschen die Frage wenn schon ein gutes bis sehr gutes Niveau vorhanden ist, wie weit da(nn) quasi niedrige(re)s akzeptiert wird
wenn es nicht stört, dann sehr gern
dann würde es aber voaussichtlich noch einige Zeit dauern, ganz in Ruhe, und dann voraussichtlich nur wenige, vorselektierte Firmen
Gruß
P.
Zitat von Timburg: Guten Morgen zusammen,
kann mich den letzten Postings nur anschließen - höchstes Niveau was hier geboten wird, und alles auf sachlicher Ebene, ohne den - bei solchen Werten - üblicherweise unvermeidbaren Hauch von Push. Lese hier schon länger mit, und auch wenn ich generell konservativ unterwegs bin, will man doch ab und zu einen spekulativen Wert dazumischen.
Bevor aber mein Posting als Push rüberkommt; hab extra nachgeschaut. Zum einen wurde der Wert hier schon vor langer Zeit besprochen, zum anderen werden die Kurse sowieso an der Nasdaq gemacht, Umsatz ist drüben um ein XX-faches höher. Wollte also mal Eure Meinung zu Aveo Pharma hören, welche am Freitag ein Conference Call zu Tivozanib haben.
http://www.wallstreet-online.de/nachricht/7418906-aveo-oncol…
Quasi 2. Versuch, 2013 im ersten Anlauf ein Flop, der Kurs ist dementsprechend auch da wo er gerade ist. Immerhin MK zu großen Teilen durch Cash abgesichert und zwei neuere Meldungen haben mich veranlasst, eine Miniposition von 1000 Stk. zu kaufen. Zum einen wurden 2/3 der Belegschaft gekündigt, und dann der CEO ausgewechselt. Der neue - Bailey - war immerhin jahrelang bei ImClone, Genentech, Smithkline usw. Wird da evtl. eine Kooperation oder Übernahme vorbereitet ?? Ersteres wäre mir lieber, bei Biotechs spekuliert man ja generell nicht auf 30% Übernahmeprämie.
Dies zu meinen Kaufhintergründen; die Miniposition halte ich mal durch. Freitag dann hop oder top, also +-50% möglich. Würde mich aber trotzdem interessieren was Ihr von dieser PhaseII haltet bzw. welche Erfolgschancen Ihr der Firma bzw. den 4 Kandidaten einräumt.
Schönen Tag noch
Timburg
hallo Timburg,
keiiine Ahnung zu Deinem Unternehmen, aber was ich generell raten würde
ich würde aufpassen nicht "zuuu lehrbuchmässig" zu denken
ist würde ich sagen so ein bisschen deutsches Ding
was meiner Erfahrung nach -nicht immer, aber- oft in die Hose geht
Problem ist: die Wirklichkeit passt da oft(meistens)nicht rein
Zitat von kmastra: Hallo zusammen,
also ich würde mich freuen, wenn sich hier mehr Leute beteilgen. Von daher nur Mut! Ich habe hier schon viel gelernt und denke, dass das Aufschreiben und der Austausch einen nur voran bringen kann...
hallo Kmastra,
dem werde ich voraussichtlich noch sehr gern nachkommen
es ist immer so ein bisschen die Frage wenn schon ein gutes bis sehr gutes Niveau vorhanden ist, wie weit da(nn) quasi niedrige(re)s akzeptiert wird
wenn es nicht stört, dann sehr gern
dann würde es aber voaussichtlich noch einige Zeit dauern, ganz in Ruhe, und dann voraussichtlich nur wenige, vorselektierte Firmen
Gruß
P.
Demnächst kommt mit der AACR eine weitere Konferenz mit vielleicht den ein oder anderen interessanten Daten...

Gruß
ipollit

Gruß
ipollit
INCY
Hinter Jakafi bauen sie eine interessante Pipeline auf, die viele Kombinations-Möglichkeiten bietet. Inzwischen kommen sie auch schon auf eine MK von 16,4 Mrd USD und gehören somit zu den Schwergewichten.



Gruß
ipollit
Hinter Jakafi bauen sie eine interessante Pipeline auf, die viele Kombinations-Möglichkeiten bietet. Inzwischen kommen sie auch schon auf eine MK von 16,4 Mrd USD und gehören somit zu den Schwergewichten.


Gruß
ipollit
KPTI
meine KPTI-Position habe ich in den letzten Tagen weiter erhöht, da ich Selinexor nach wie vor sehr interessant finde. Hinzu kommen noch weitere XPO1-Kandiaten u.a. gegen MS oder Infektionskrankheiten, sowie ein neuer PAK4-Hemmer, den Ohad Hammer auch mal als aussichtsreich erwähnt hat.


Da Selinexor einen so fundamentalen Ansatz besitzt, könnte es in vielen Krebsarten hilfreich sein. Dementsprechend groß ist jetzt schon die Pipeline, die zum einem wesentlichen Teil auch von akademischen Institutionen vorangetrieben wird.
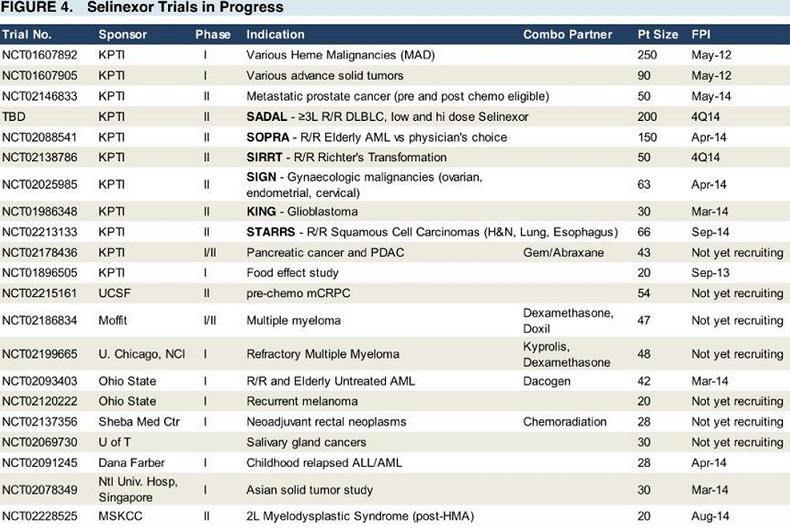
Eine weitere Übersicht über laufende/geplante Selinexor-Studien (rot markiert sind die möglichen Zulassungs-Studien)...
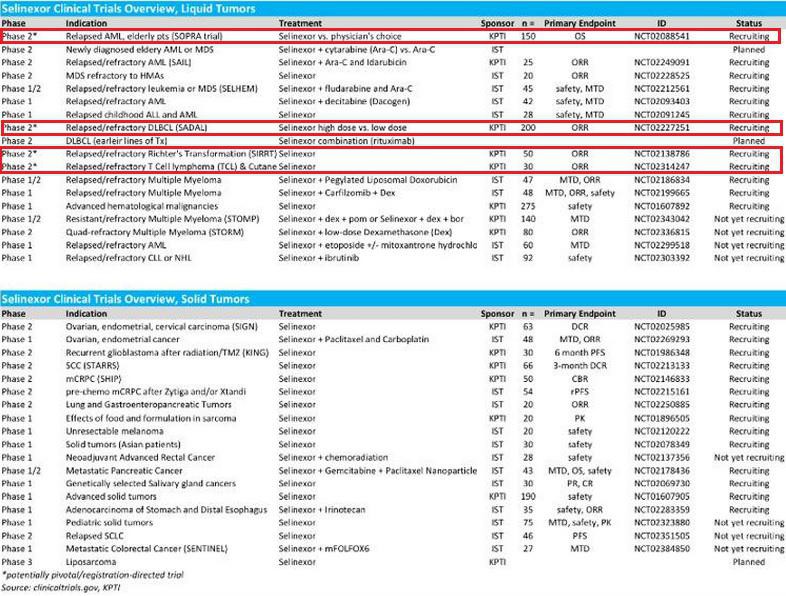
Momentan gibt es bereits 3 oder 4 PII-Studien mit dem Ziel einer vorzeitigen Zulassung in Patientengruppen, bei denen so gut wie nichts anderes mehr hilft: SOPRA in AML bei älteren Patienten, SADAL in mehrfach resistenten DLBLC und SIRRT in Richters Transformation (das z.B. nach einer Verschärfung von CLL auftreten kann). Dieses Jahr könnten weitere zwei solcher Studien gestartet werden: STORM in mehrfach resistenten MM (u.a. auch nach CD38-Resistenz) und gegen Liposarcoma. Langfristig könnte Selinexor vielleicht aber auch generell sehr breit angewendet werden.



Bisher gibt es noch nicht soviele Daten, die die Anwendung von Selinexor in Soliden Tumoren unterstützen. Zur ASCO könnten hierzu aussagekräftigere PI-Daten kommen.

Präklinische Wirkung von Selinexor u.a. gegen Liposarcoma (LPS) und GIST, die anscheinend auf anderen Mechanismen beruhen als die bisher bekannten. Meiner Meinung eignet sich Selinexor daher gut für Kombinationen, da es den Krebs grundsätzlich anders angreift und so vielleicht eine vom kombinierten Mittel unabhängige synergetische Wirkung entsteht.

Selinexor wirkt in AML anscheinend auch gegen Blutkrebs-Stammzellen (LIC), die andere Therapien überstehen und später zu einer Wiederkehr des Krebs führen. Z.B. STML will auch diese Zellen mit SL-401, das als Target IL-3R hat, zerstören. Dadurch könnte in Kombination mit anderen Mitteln, die alle anderen Zellen außer LIC abtöten, der Krebs vielleicht langanhaltend bekämpft werden. Selinexor wird z.B. in AML mit der Standard-Chemo kombiniert.

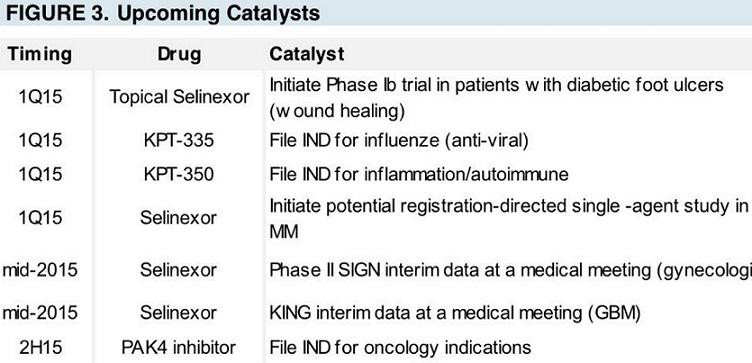

Gruß
ipollit
meine KPTI-Position habe ich in den letzten Tagen weiter erhöht, da ich Selinexor nach wie vor sehr interessant finde. Hinzu kommen noch weitere XPO1-Kandiaten u.a. gegen MS oder Infektionskrankheiten, sowie ein neuer PAK4-Hemmer, den Ohad Hammer auch mal als aussichtsreich erwähnt hat.


Da Selinexor einen so fundamentalen Ansatz besitzt, könnte es in vielen Krebsarten hilfreich sein. Dementsprechend groß ist jetzt schon die Pipeline, die zum einem wesentlichen Teil auch von akademischen Institutionen vorangetrieben wird.

Eine weitere Übersicht über laufende/geplante Selinexor-Studien (rot markiert sind die möglichen Zulassungs-Studien)...

Momentan gibt es bereits 3 oder 4 PII-Studien mit dem Ziel einer vorzeitigen Zulassung in Patientengruppen, bei denen so gut wie nichts anderes mehr hilft: SOPRA in AML bei älteren Patienten, SADAL in mehrfach resistenten DLBLC und SIRRT in Richters Transformation (das z.B. nach einer Verschärfung von CLL auftreten kann). Dieses Jahr könnten weitere zwei solcher Studien gestartet werden: STORM in mehrfach resistenten MM (u.a. auch nach CD38-Resistenz) und gegen Liposarcoma. Langfristig könnte Selinexor vielleicht aber auch generell sehr breit angewendet werden.



Bisher gibt es noch nicht soviele Daten, die die Anwendung von Selinexor in Soliden Tumoren unterstützen. Zur ASCO könnten hierzu aussagekräftigere PI-Daten kommen.

Präklinische Wirkung von Selinexor u.a. gegen Liposarcoma (LPS) und GIST, die anscheinend auf anderen Mechanismen beruhen als die bisher bekannten. Meiner Meinung eignet sich Selinexor daher gut für Kombinationen, da es den Krebs grundsätzlich anders angreift und so vielleicht eine vom kombinierten Mittel unabhängige synergetische Wirkung entsteht.

Selinexor wirkt in AML anscheinend auch gegen Blutkrebs-Stammzellen (LIC), die andere Therapien überstehen und später zu einer Wiederkehr des Krebs führen. Z.B. STML will auch diese Zellen mit SL-401, das als Target IL-3R hat, zerstören. Dadurch könnte in Kombination mit anderen Mitteln, die alle anderen Zellen außer LIC abtöten, der Krebs vielleicht langanhaltend bekämpft werden. Selinexor wird z.B. in AML mit der Standard-Chemo kombiniert.


Gruß
ipollit
KPTI
hier noch etwas zum PAK4-Hemmer, der dieses Jahr in PI gehen soll. Gegenüber anderen PAK4-Hemmern könnte er weniger Nebenwirkungen aufweisen.

PAK4 scheint auch eine zentrale Rolle zu spielen... theoretisch ist der Hemmer sowohl in Blutkrebsarten als auch in soliden Tumoren wirksam
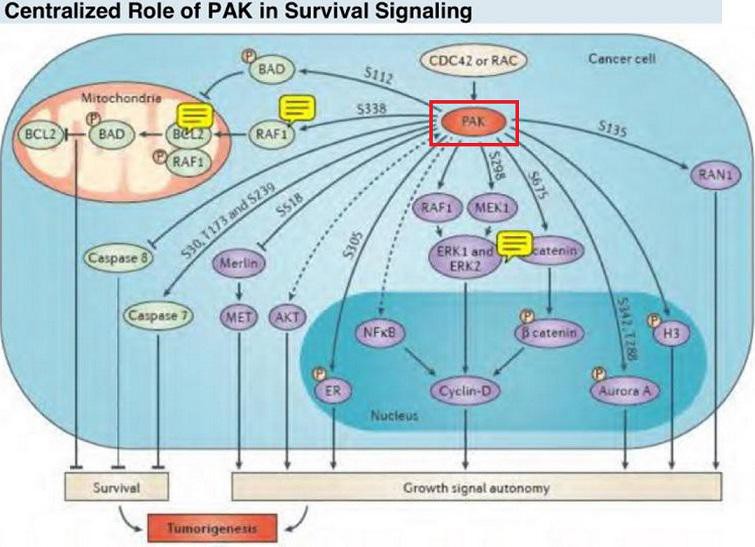
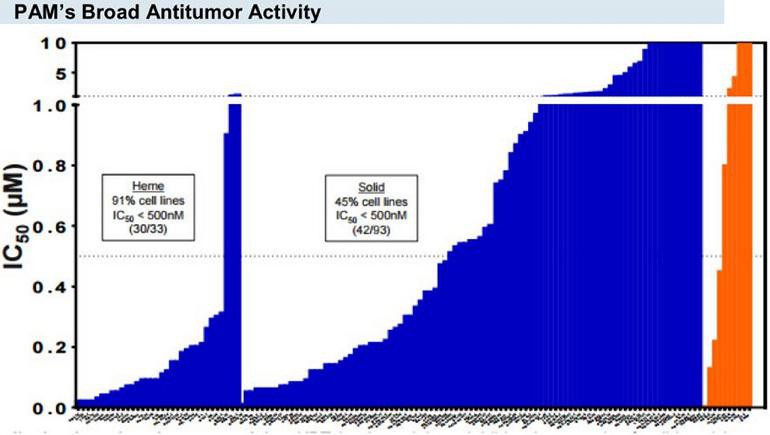
Gruß
ipollit
hier noch etwas zum PAK4-Hemmer, der dieses Jahr in PI gehen soll. Gegenüber anderen PAK4-Hemmern könnte er weniger Nebenwirkungen aufweisen.

PAK4 scheint auch eine zentrale Rolle zu spielen... theoretisch ist der Hemmer sowohl in Blutkrebsarten als auch in soliden Tumoren wirksam


Gruß
ipollit
Antwort auf Beitrag Nr.: 49.390.859 von ipollit am 21.03.15 20:13:42Hallo ipollit,
ich sehe KPTI ebenfalls als besonders aussichtsreich an und habe ebenfalls meine dortige Position erhöht, obschon ich ja generell sehr viel Cash aufgebaut habe.
Ich habe so ein wenig die Hoffnung, dass sich Hammer in seinem heutigen Beitrag vielleicht auch mit KPTI befasst. Mal sehen.
Gruß
SLG
ich sehe KPTI ebenfalls als besonders aussichtsreich an und habe ebenfalls meine dortige Position erhöht, obschon ich ja generell sehr viel Cash aufgebaut habe.
Ich habe so ein wenig die Hoffnung, dass sich Hammer in seinem heutigen Beitrag vielleicht auch mit KPTI befasst. Mal sehen.
Gruß
SLG
MGNX
Die DART-Pipeline füllt sich weiter. Unter den AACR-Abstracts finden sich zwei neue präklinische DARTs. Ein P-Cadherin + CD3 DART wird von Pfizer entwickelt. Anders als bei den meisten CARTs handelt es sich hierbei um ein Target auf soliden Tumoren wie z.B. Brustkrebs. Da die DART-Kooperation mit Pfizer einer der ersten war, sind die Royalties für MGNX wahrscheinlich nur im einstelligen Bereich.


Der zweite DART ist wahrscheinlich aus der eigenen Pipeline von MGNX (dabei handelt es sich nicht um MGD009, dessen Target aus dem Bereich der soliden Tumore bisher nicht bekannt ist). Er zeigt, dass bi-spezifische AKs wie DARTs nicht nur eine Alternative zu z.B. CARTs sind, wenn sie eine Kombination aus Target + CD3 bilden, um T-Zellen zu binden. Es gibt auch eine Vielzahl weiterer neuer Anwendungsmöglichkeiten.
Bei diesem neuen DART handelt es sich um einen DR5 DART, der nach meinem Verständnis doppelt an DR5 bindet, jeweils an unterschiedliche, nicht überlappende Bereiche von DR5.
Vor einigen Jahren galten Antikörper&Co gegen TRAIL oder DR4/DR5 als aussichtsreich. Death Receptors(DR) lösen den Zelltod der Zelle aus, wenn sie entsprechend stimuliert werden. Interessant war dies, weil anscheinend speziell die DR4- und DR5-Rezeptoren hauptsächtlich auf Krebszellen vorkamen. Theoretisch würden AKs, die diese Rezeptoren stimulieren, die Krebszellen unmittelbar abtöten können, während normale gesunde Zellen geschont werden. TRAIL-Liganden, die an TRAIL andocken, stimulieren dabei DR4 und DR5, so dass man alternativ auch diese löslichen TRAIL-Liganden verwenden könnte.
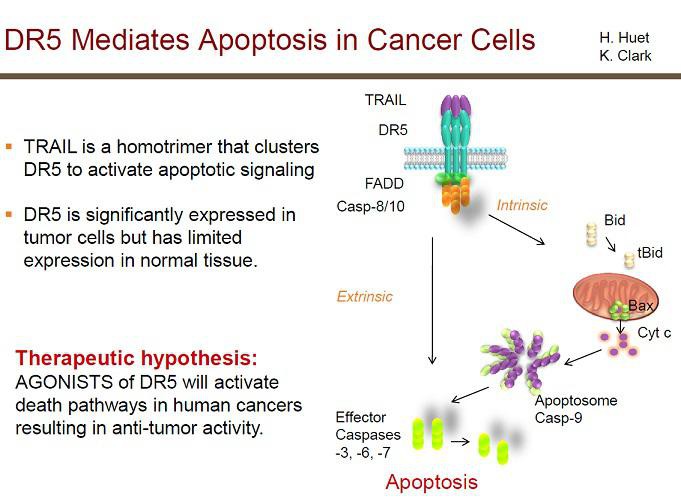
http://www.nature.com/news/small-molecule-drug-drives-cancer…
...“TRAIL is a part of our immune system: all of us with functional immune systems use this molecule to keep tumours from forming or spreading, so boosting this will not be as toxic as chemotherapy,”...
The potential for TRAIL to usher in a new age in cancer therapy was first identified in the mid-1990s. However, although early clinical trials for TRAIL-based therapies showed little toxicity, they were not very successful at treating cancer, ... “All the large clinical trials found no significant survival benefit to adding TRAIL-based therapeutics to standard treatments,” he ads. Many large biomedical research groups have shelved their TRAIL-based drugs.
In der Petrischale oder in Tierexperimenten waren DR4/5-AKs sehr erfolgreich... in klinischen Versuchen war die Wirkung dagegen sehr enttäuschend. Hierfür gibt es wohl mehrere Ursachen: zum einen waren einige Krebszellen resistent, weil diese Rezeptoren mutiert waren. Zum anderen konnte wohl in Tierexperimenten der AK die Rezeptoren leichter aktivieren. Es reicht nicht, dass ein einzelner AK an den Rezeptor andockt... es müssen noch weitere Signale hinzukommen. Bei den AKs in den Studien waren das oft Immun-Zellen, die an den fc-Bereich andocken und dort z.B. ADCC auslösen (was hier garnicht erwünscht ist, da man den Rezeptor ja nur stimulieren will). Diese bestimmten Immunzellen waren aber in der Tumorumgebung nur unzureichend vorhanden, wodurch die Wirkung zu schwach war.
Im Folgenden (Patent von Roche) gibt es z.B. einen Überblick über die DR5-Kandidaten...
"BISPECIFIC ANTIBODIES SPECIFIC FOR FAP AND DR5, ANTIBODIES SPECIFIC FOR DR5 AND METHODS OF USE"
http://patents.justia.com/patent/20140370019
DR5 scheint für eine vollständige Aktivierung offensichtlich auch drei Bindungen zu benötigen... normale AKs binden aber nur an zwei Stellen. Für eine vollständige Aktivierung müssen nach meinem Verständnis mehrere AKs am Rezeptor und aneinander Binden ("secondary cross linking"). TRAIL, das u.a. DR5 aktiviert, scheint selber dreifach bindend zu sein.
Vor ein paar Jahren hatte Ablynx zusammen mit Novartis den Nano-AK TAS266 in der PI, der dieses berücksichtigt. Er bindet dreifach an den Rezeptor:
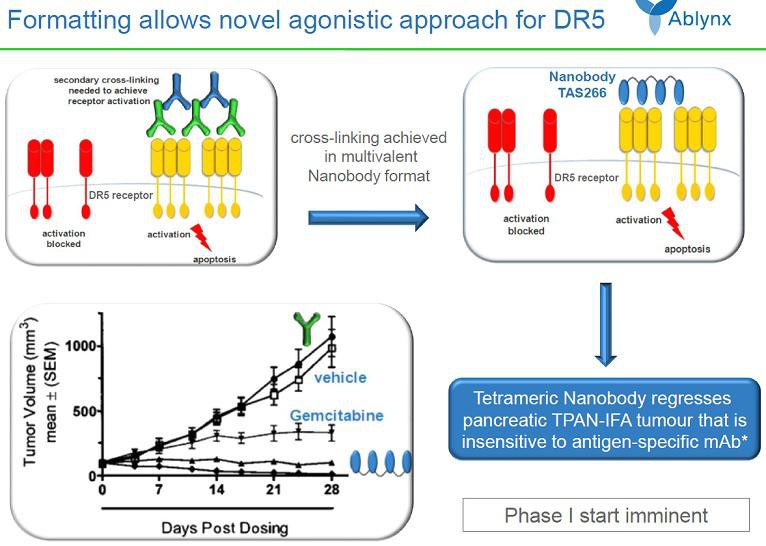
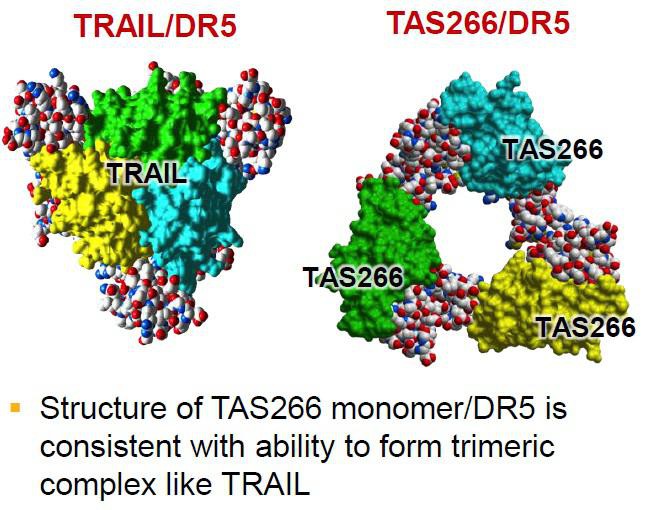
AACR-Abstract von 2012...
http://www.ablynx.com/wp-content/uploads/2012/03/AACR-Annual…
"Preferential induction of apoptosis in cancer cells has been the objective of therapeutic strategies targeting apoptotic pathways. To this end, multiple therapeutic agonists of Death Receptors 4 and 5 (DR4, DR5), have been developed and are under clinical evaluation. Although these agonists, including antibodies and soluble ligand TRAIL, demonstrate significant anti-tumor activity in preclinical models, the clinical efficacy in human cancer patients has been notably disappointing. One possible explanation for the discrepant pre-clinical and clinical results is that DR5 may play a more prominent role in in vitro model systems as opposed to cancers in humans. Alternatively, these results might indicate that the current classes of therapeutic molecules are not sufficiently potent to elicit significant response in patients. In particular, naturally dimeric antibody agonists require secondary cross-linking via Fc? receptors expressed on immune cells present in the tumor microenvironment to achieve optimal clustering of DR5 into a ternary active state. Because immune cell content in the tumor can be heterogeneous, reliance on this secondary mechanism for activity may limit the potency of these antibodies.
In der PI kam es aber zu gravierenden Nebenwirkungen, da TAS266 offensichtlich auch DR5 in der Leber aktiverte und dadurch zu Leberschäden führte: http://www.ncbi.nlm.nih.gov/pubmed/25721064
Der neue DR5-DART von MGNX beruht auf einem ähnlichen Ansatz. Er bindet an verschiedenen Stellen des Rezeptors, soll dadurch diesen wesentlich stärker als TRAIL oder DR5-AKs aktivieren können (ähnlich wie TAS266), aber trotzdem wie DR5-AKs auf Krebszellen beschränkt sein:
http://www.abstractsonline.com/Plan/ViewAbstract.aspx?sKey=9…
"Binding analyses revealed DR5 mAbs recognizing non-overlapping epitopes that do not block the TRAIL-DR5 interaction. Upon secondary cross-linking or when combined, the DR5 mAbs induced apoptosis across multiple cancer cell lines. Further potency enhancement independent of secondary cross-linking was obtained by the engineered multivalent DR5-targeting DARTs. Dose-dependent growth inhibition assay demonstrated that the DR5-targeting DARTs delivered significantly greater potency than TRAIL (=100-fold) across a broad range of cancer cell lines. Furthermore, the DR5-targeting DARTs maintained the exquisite tumor/normal differential reactivity displayed by the parental DR5 mAbs from which they were derived. Combination of an HDAC inhibitor with DR5-targeting DARTs revealed maintenance of synergistic activity and potential to overcome pathway resistance."
Letztlich wird sich erst in der Klinik zeigen, inwieweit dieser DART die Probleme anderer DR5-AKs beseitigen kann. Sollte es funktionieren, wäre dies insgesamt eine neue Art von Krebsmittel, die sich recht breit anwenden ließe, ähnlich wie KPTIs Selinexor. Chemos beschädigen u.a. die DNA von sich schnell teilenden Krebszellen. Dies löst dann den Zelltod aus, wenn die Schäden zu groß sind. Dafür sind u.a. Kontroll-Proteine im Zellkern verantwortlich, die die DNA auf Schäden prüfen und dann den Zelltod einleiten (hier setzt z.B. Selinexor an, indem diese Proteine im Zellkern erhöht werden). Eine sehr häufige Mutation findet sich in Krebszellen in einem dieser Kontrollproteine p53. Ist dieses defekt, wird in der Zelle trotz Schäden von p53 kein Zelltod mehr eingeleitet. Dies macht dann z.B. die Chemo weniger wirksam. DR5 wäre dann ein Ansatz, von außen den Zelltod gezielt einzuleiten.
Roche präsentiert auf der AACR einen eigenen biAk gegen DR5 + FAP: "Induction of avidity-driven hyperclustering of DR5 by a new FAP-DR5 bispecific antibody (RG7386) leads to strong anti-tumor efficacy" http://www.abstractsonline.com/Plan/ViewAbstract.aspx?sKey=d…
Dieser ist allerdings vom zweiten Target FAP abhängig, das eher im den Tumor umgebenen Gewebe vorkommt.
Außerdem hat Genmab letzte Woche einen DR5-AK inlusiv zugehöriger Patente gekauft. Genmab entwickelt ebenfalls bi-AKs. "Antibodies targeting DR5 (TRAIL-R2) and related patents purchased from iDD Biotech" http://ir.genmab.com/releasedetail.cfm?ReleaseID=902278
Hier noch ein wenig mehr über DR5/TRAIL...
http://www.nature.com/cdd/journal/v21/n9/full/cdd201481a.htm…
"Getting TRAIL back on track for cancer therapy
Unlike other members of the TNF superfamily, the TNF-related apoptosis-inducing ligand (TRAIL, also known as Apo2L) possesses the unique capacity to induce apoptosis selectively in cancer cells in vitro and in vivo. This exciting discovery provided the basis for the development of TRAIL-receptor agonists (TRAs), which have demonstrated robust anticancer activity in a number of preclinical studies. Subsequently initiated clinical trials testing TRAs demonstrated, on the one hand, broad tolerability but revealed, on the other, that therapeutic benefit was rather limited...."
Dies zeigt die vielfältigen Möglichkeiten, die bi-AKs bieten.
MGNX hat zusammen mit Takeda ja auch einen DART gegen Autoimmun-Erkrankungen... hierfür sind ebenfalls zwei Targets erforderlich.


Gruß
ipollit
Die DART-Pipeline füllt sich weiter. Unter den AACR-Abstracts finden sich zwei neue präklinische DARTs. Ein P-Cadherin + CD3 DART wird von Pfizer entwickelt. Anders als bei den meisten CARTs handelt es sich hierbei um ein Target auf soliden Tumoren wie z.B. Brustkrebs. Da die DART-Kooperation mit Pfizer einer der ersten war, sind die Royalties für MGNX wahrscheinlich nur im einstelligen Bereich.


Der zweite DART ist wahrscheinlich aus der eigenen Pipeline von MGNX (dabei handelt es sich nicht um MGD009, dessen Target aus dem Bereich der soliden Tumore bisher nicht bekannt ist). Er zeigt, dass bi-spezifische AKs wie DARTs nicht nur eine Alternative zu z.B. CARTs sind, wenn sie eine Kombination aus Target + CD3 bilden, um T-Zellen zu binden. Es gibt auch eine Vielzahl weiterer neuer Anwendungsmöglichkeiten.
Bei diesem neuen DART handelt es sich um einen DR5 DART, der nach meinem Verständnis doppelt an DR5 bindet, jeweils an unterschiedliche, nicht überlappende Bereiche von DR5.
Vor einigen Jahren galten Antikörper&Co gegen TRAIL oder DR4/DR5 als aussichtsreich. Death Receptors(DR) lösen den Zelltod der Zelle aus, wenn sie entsprechend stimuliert werden. Interessant war dies, weil anscheinend speziell die DR4- und DR5-Rezeptoren hauptsächtlich auf Krebszellen vorkamen. Theoretisch würden AKs, die diese Rezeptoren stimulieren, die Krebszellen unmittelbar abtöten können, während normale gesunde Zellen geschont werden. TRAIL-Liganden, die an TRAIL andocken, stimulieren dabei DR4 und DR5, so dass man alternativ auch diese löslichen TRAIL-Liganden verwenden könnte.

http://www.nature.com/news/small-molecule-drug-drives-cancer…
...“TRAIL is a part of our immune system: all of us with functional immune systems use this molecule to keep tumours from forming or spreading, so boosting this will not be as toxic as chemotherapy,”...
The potential for TRAIL to usher in a new age in cancer therapy was first identified in the mid-1990s. However, although early clinical trials for TRAIL-based therapies showed little toxicity, they were not very successful at treating cancer, ... “All the large clinical trials found no significant survival benefit to adding TRAIL-based therapeutics to standard treatments,” he ads. Many large biomedical research groups have shelved their TRAIL-based drugs.
In der Petrischale oder in Tierexperimenten waren DR4/5-AKs sehr erfolgreich... in klinischen Versuchen war die Wirkung dagegen sehr enttäuschend. Hierfür gibt es wohl mehrere Ursachen: zum einen waren einige Krebszellen resistent, weil diese Rezeptoren mutiert waren. Zum anderen konnte wohl in Tierexperimenten der AK die Rezeptoren leichter aktivieren. Es reicht nicht, dass ein einzelner AK an den Rezeptor andockt... es müssen noch weitere Signale hinzukommen. Bei den AKs in den Studien waren das oft Immun-Zellen, die an den fc-Bereich andocken und dort z.B. ADCC auslösen (was hier garnicht erwünscht ist, da man den Rezeptor ja nur stimulieren will). Diese bestimmten Immunzellen waren aber in der Tumorumgebung nur unzureichend vorhanden, wodurch die Wirkung zu schwach war.
Im Folgenden (Patent von Roche) gibt es z.B. einen Überblick über die DR5-Kandidaten...
"BISPECIFIC ANTIBODIES SPECIFIC FOR FAP AND DR5, ANTIBODIES SPECIFIC FOR DR5 AND METHODS OF USE"
http://patents.justia.com/patent/20140370019
DR5 scheint für eine vollständige Aktivierung offensichtlich auch drei Bindungen zu benötigen... normale AKs binden aber nur an zwei Stellen. Für eine vollständige Aktivierung müssen nach meinem Verständnis mehrere AKs am Rezeptor und aneinander Binden ("secondary cross linking"). TRAIL, das u.a. DR5 aktiviert, scheint selber dreifach bindend zu sein.
Vor ein paar Jahren hatte Ablynx zusammen mit Novartis den Nano-AK TAS266 in der PI, der dieses berücksichtigt. Er bindet dreifach an den Rezeptor:


AACR-Abstract von 2012...
http://www.ablynx.com/wp-content/uploads/2012/03/AACR-Annual…
"Preferential induction of apoptosis in cancer cells has been the objective of therapeutic strategies targeting apoptotic pathways. To this end, multiple therapeutic agonists of Death Receptors 4 and 5 (DR4, DR5), have been developed and are under clinical evaluation. Although these agonists, including antibodies and soluble ligand TRAIL, demonstrate significant anti-tumor activity in preclinical models, the clinical efficacy in human cancer patients has been notably disappointing. One possible explanation for the discrepant pre-clinical and clinical results is that DR5 may play a more prominent role in in vitro model systems as opposed to cancers in humans. Alternatively, these results might indicate that the current classes of therapeutic molecules are not sufficiently potent to elicit significant response in patients. In particular, naturally dimeric antibody agonists require secondary cross-linking via Fc? receptors expressed on immune cells present in the tumor microenvironment to achieve optimal clustering of DR5 into a ternary active state. Because immune cell content in the tumor can be heterogeneous, reliance on this secondary mechanism for activity may limit the potency of these antibodies.
In der PI kam es aber zu gravierenden Nebenwirkungen, da TAS266 offensichtlich auch DR5 in der Leber aktiverte und dadurch zu Leberschäden führte: http://www.ncbi.nlm.nih.gov/pubmed/25721064
Der neue DR5-DART von MGNX beruht auf einem ähnlichen Ansatz. Er bindet an verschiedenen Stellen des Rezeptors, soll dadurch diesen wesentlich stärker als TRAIL oder DR5-AKs aktivieren können (ähnlich wie TAS266), aber trotzdem wie DR5-AKs auf Krebszellen beschränkt sein:
http://www.abstractsonline.com/Plan/ViewAbstract.aspx?sKey=9…
"Binding analyses revealed DR5 mAbs recognizing non-overlapping epitopes that do not block the TRAIL-DR5 interaction. Upon secondary cross-linking or when combined, the DR5 mAbs induced apoptosis across multiple cancer cell lines. Further potency enhancement independent of secondary cross-linking was obtained by the engineered multivalent DR5-targeting DARTs. Dose-dependent growth inhibition assay demonstrated that the DR5-targeting DARTs delivered significantly greater potency than TRAIL (=100-fold) across a broad range of cancer cell lines. Furthermore, the DR5-targeting DARTs maintained the exquisite tumor/normal differential reactivity displayed by the parental DR5 mAbs from which they were derived. Combination of an HDAC inhibitor with DR5-targeting DARTs revealed maintenance of synergistic activity and potential to overcome pathway resistance."
Letztlich wird sich erst in der Klinik zeigen, inwieweit dieser DART die Probleme anderer DR5-AKs beseitigen kann. Sollte es funktionieren, wäre dies insgesamt eine neue Art von Krebsmittel, die sich recht breit anwenden ließe, ähnlich wie KPTIs Selinexor. Chemos beschädigen u.a. die DNA von sich schnell teilenden Krebszellen. Dies löst dann den Zelltod aus, wenn die Schäden zu groß sind. Dafür sind u.a. Kontroll-Proteine im Zellkern verantwortlich, die die DNA auf Schäden prüfen und dann den Zelltod einleiten (hier setzt z.B. Selinexor an, indem diese Proteine im Zellkern erhöht werden). Eine sehr häufige Mutation findet sich in Krebszellen in einem dieser Kontrollproteine p53. Ist dieses defekt, wird in der Zelle trotz Schäden von p53 kein Zelltod mehr eingeleitet. Dies macht dann z.B. die Chemo weniger wirksam. DR5 wäre dann ein Ansatz, von außen den Zelltod gezielt einzuleiten.
Roche präsentiert auf der AACR einen eigenen biAk gegen DR5 + FAP: "Induction of avidity-driven hyperclustering of DR5 by a new FAP-DR5 bispecific antibody (RG7386) leads to strong anti-tumor efficacy" http://www.abstractsonline.com/Plan/ViewAbstract.aspx?sKey=d…
Dieser ist allerdings vom zweiten Target FAP abhängig, das eher im den Tumor umgebenen Gewebe vorkommt.
Außerdem hat Genmab letzte Woche einen DR5-AK inlusiv zugehöriger Patente gekauft. Genmab entwickelt ebenfalls bi-AKs. "Antibodies targeting DR5 (TRAIL-R2) and related patents purchased from iDD Biotech" http://ir.genmab.com/releasedetail.cfm?ReleaseID=902278
Hier noch ein wenig mehr über DR5/TRAIL...
http://www.nature.com/cdd/journal/v21/n9/full/cdd201481a.htm…
"Getting TRAIL back on track for cancer therapy
Unlike other members of the TNF superfamily, the TNF-related apoptosis-inducing ligand (TRAIL, also known as Apo2L) possesses the unique capacity to induce apoptosis selectively in cancer cells in vitro and in vivo. This exciting discovery provided the basis for the development of TRAIL-receptor agonists (TRAs), which have demonstrated robust anticancer activity in a number of preclinical studies. Subsequently initiated clinical trials testing TRAs demonstrated, on the one hand, broad tolerability but revealed, on the other, that therapeutic benefit was rather limited...."
Dies zeigt die vielfältigen Möglichkeiten, die bi-AKs bieten.
MGNX hat zusammen mit Takeda ja auch einen DART gegen Autoimmun-Erkrankungen... hierfür sind ebenfalls zwei Targets erforderlich.

Gruß
ipollit
ZFGN:
Hier mal eine peak-sales-Schätzung für das Prader-Willi-Syndrom und HIAO:

Die große Frage wird dann irgendwann werden, ob und wie sie in dem allgemeinen obesity-Markt Fuß fassen können.
Dieser Markt ist zwar theoretisch sehr groß, aber er zumindest bisher ist er nur mit erheblichen Marketing- und Vertriebsanstrengungen zu erschließen und die Preise sind niedrig.
Der Weg über Nischenindikationen ist zunächst mal sehr geschickt gewählt. Aber die ganz großen Umsätze sind dort eben nicht zu machen.
Hier mal eine peak-sales-Schätzung für das Prader-Willi-Syndrom und HIAO:

Die große Frage wird dann irgendwann werden, ob und wie sie in dem allgemeinen obesity-Markt Fuß fassen können.
Dieser Markt ist zwar theoretisch sehr groß, aber er zumindest bisher ist er nur mit erheblichen Marketing- und Vertriebsanstrengungen zu erschließen und die Preise sind niedrig.
Der Weg über Nischenindikationen ist zunächst mal sehr geschickt gewählt. Aber die ganz großen Umsätze sind dort eben nicht zu machen.
ICPT:
Eine Meinung zur Bewertung:

Ich lese jetzt zum zweiten mal, dass sich die jetzige Bewertung angeblich allein durch die Indikation PBC rechtfertigen ließe...
Wenn das richtig wäre, dann hätte ICPT ein wesentlich besseres Chance-/Risikoprofil, als man vielleicht im allgemeinen annimmt.
(Wobei sich das Chance-/Risikoprofil durch die Erteilung des breakthrough in NASH ja ohnehin verbessert hat, denke ich.)
Eine Meinung zur Bewertung:

Ich lese jetzt zum zweiten mal, dass sich die jetzige Bewertung angeblich allein durch die Indikation PBC rechtfertigen ließe...
Wenn das richtig wäre, dann hätte ICPT ein wesentlich besseres Chance-/Risikoprofil, als man vielleicht im allgemeinen annimmt.
(Wobei sich das Chance-/Risikoprofil durch die Erteilung des breakthrough in NASH ja ohnehin verbessert hat, denke ich.)
Mal was ganz anderes:
Bei welchem Broker kauft ihr eure Aktien in den USA?
Ich habe über Consors die Erfahrung gemacht, dass eine Order oft in so viele Kleinstausführungen aufgesplitet wird, dass die Gebühren echt happig sind.
Muss ich das akzeptieren oder gibt es da bessere Broker/andere Möglichkeiten?
SG kmastra
Bei welchem Broker kauft ihr eure Aktien in den USA?
Ich habe über Consors die Erfahrung gemacht, dass eine Order oft in so viele Kleinstausführungen aufgesplitet wird, dass die Gebühren echt happig sind.
Muss ich das akzeptieren oder gibt es da bessere Broker/andere Möglichkeiten?
SG kmastra
Antwort auf Beitrag Nr.: 49.399.892 von kmastra am 23.03.15 17:18:07Hallo kmastra,
das mit den Gebühren pro Teilausführung ist wirklich eine sehr ärgerliche Sache! Momentan bin ich beim sbroker... naja, wohl nicht gerade der günstigste, dafür kann ich fast überall auf der Welt problemlos handeln. In den USA wird die Order meist ohne Zeitverzögerung sofort ausgeführt... das finde ich angenehm.
Letztes Jahr gab es dort auch diese Teilausführungen. Besonders schön, wenn dabei die Kurse sogar noch in Bruchteilen von Cents gestellt werden... D.h. 100 Stück zu ca. 10 USD konnten als 90 Stück zu 10.01 und 10 zu 10.009997 ausgeführt werden. Für beides wurden die Mindestgebühren fällig, weil laut Broker zwei Rechnungen zu schreiben wären... da freut man sich besonders über den 0,0003 Cent besseren Kurs.
Teilausführungen zu gleichen Kursen wurden damals bereits zu einer Rechnung zusammengefasst. Inzwischen sind sie aber so fair geworden, dass die Gebühren des Brokers in allen Fällen so gerechnet werden, als ob die Order voll zu einem Kurs bedient worden wäre... die Gebühren für die Teilausführungen werden dann entsprechend anteilig umgerechnet. D.h. Teilausführungen oder nicht... die Kosten bleiben jetzt bei mir dieselben.
Grüße
ipollit
das mit den Gebühren pro Teilausführung ist wirklich eine sehr ärgerliche Sache! Momentan bin ich beim sbroker... naja, wohl nicht gerade der günstigste, dafür kann ich fast überall auf der Welt problemlos handeln. In den USA wird die Order meist ohne Zeitverzögerung sofort ausgeführt... das finde ich angenehm.
Letztes Jahr gab es dort auch diese Teilausführungen. Besonders schön, wenn dabei die Kurse sogar noch in Bruchteilen von Cents gestellt werden... D.h. 100 Stück zu ca. 10 USD konnten als 90 Stück zu 10.01 und 10 zu 10.009997 ausgeführt werden. Für beides wurden die Mindestgebühren fällig, weil laut Broker zwei Rechnungen zu schreiben wären... da freut man sich besonders über den 0,0003 Cent besseren Kurs.
Teilausführungen zu gleichen Kursen wurden damals bereits zu einer Rechnung zusammengefasst. Inzwischen sind sie aber so fair geworden, dass die Gebühren des Brokers in allen Fällen so gerechnet werden, als ob die Order voll zu einem Kurs bedient worden wäre... die Gebühren für die Teilausführungen werden dann entsprechend anteilig umgerechnet. D.h. Teilausführungen oder nicht... die Kosten bleiben jetzt bei mir dieselben.
Grüße
ipollit
Deutsche Biotechs sind heute teilwiese "durch die Decke" gegangen:
Medigene +50%
Mologen +40% (heute abend gleich schön die KE!)
Paion +20%
Und das mehr oder weniger ohne einen fundamentalen Grund. Ich habe neulich etwas scherzhaft vom Medigene Indikator gesprochen. Wenn Aktien aus der 2. Reihe anspringen könnte das ein Zeichen dafür sein, dass der Markt überhitzt.
Ähem Medigene:
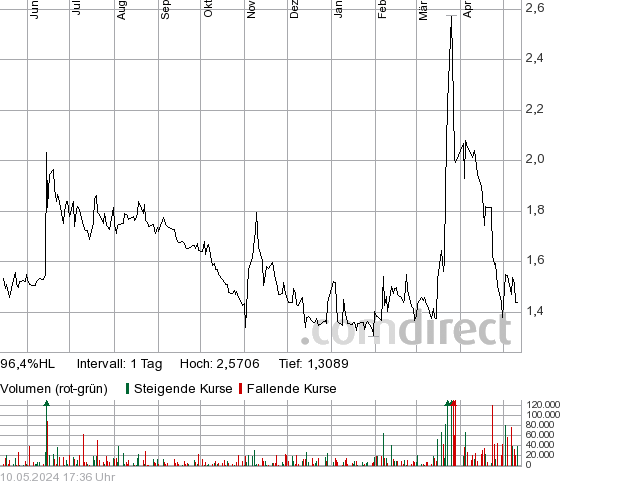
Eine Blase a la 2000 sehe ich wie gesagt noch nicht, es könnte aber eine entstehen (wenn die Kurse irrationaler Weise weiter steigen). Medigene wird jetzt von einigen in einen Topf mit Juno, Kite, Cellectis etc. geworfen. Den Vergleich halte ich für etwas gewagt. Ich habe mich heute von einem Großteil meiner Medigene Aktien getrennt und weiter Cash aufgebaut. Ob das richtig war wird man sehen...
@ipollit: Danke für den Tipp. Werde jetzt mal meine Abrechnung abwarten und dann ggf. meinen Broker wechseln. Es kann doch nicht sein, dass eine Order von 500 Stück in 5 Einzelorder aufgeteilt wird und ich dann 5 mal Gebühren zahlen soll. Eine davon waren 2 Stück!
SG kmastra
Medigene +50%
Mologen +40% (heute abend gleich schön die KE!)
Paion +20%
Und das mehr oder weniger ohne einen fundamentalen Grund. Ich habe neulich etwas scherzhaft vom Medigene Indikator gesprochen. Wenn Aktien aus der 2. Reihe anspringen könnte das ein Zeichen dafür sein, dass der Markt überhitzt.
Ähem Medigene:
Eine Blase a la 2000 sehe ich wie gesagt noch nicht, es könnte aber eine entstehen (wenn die Kurse irrationaler Weise weiter steigen). Medigene wird jetzt von einigen in einen Topf mit Juno, Kite, Cellectis etc. geworfen. Den Vergleich halte ich für etwas gewagt. Ich habe mich heute von einem Großteil meiner Medigene Aktien getrennt und weiter Cash aufgebaut. Ob das richtig war wird man sehen...
@ipollit: Danke für den Tipp. Werde jetzt mal meine Abrechnung abwarten und dann ggf. meinen Broker wechseln. Es kann doch nicht sein, dass eine Order von 500 Stück in 5 Einzelorder aufgeteilt wird und ich dann 5 mal Gebühren zahlen soll. Eine davon waren 2 Stück!
SG kmastra
Antwort auf Beitrag Nr.: 49.413.179 von kmastra am 24.03.15 22:35:14Hat die - überfällige - Korrektur vielleicht heute begonnen?

Wenn ja, wie tief wird sie gehen? 30 bis 40% vom Top wären extrem, aber sind m.E. denkbar.
Wenn ja, wie tief wird sie gehen? 30 bis 40% vom Top wären extrem, aber sind m.E. denkbar.
Antwort auf Beitrag Nr.: 49.399.892 von kmastra am 23.03.15 17:18:07
Das kann ich nicht ganz nachvollziehen. Es werden doch nicht für jede Teilausführung Mindestgebühren abgerechnet. Positiv bei Consors ist zudem der Cap.
Zitat von kmastra: Ich habe über Consors die Erfahrung gemacht, dass eine Order oft in so viele Kleinstausführungen aufgesplitet wird, dass die Gebühren echt happig sind.
Das kann ich nicht ganz nachvollziehen. Es werden doch nicht für jede Teilausführung Mindestgebühren abgerechnet. Positiv bei Consors ist zudem der Cap.
Antwort auf Beitrag Nr.: 49.426.520 von Joschka Schröder am 26.03.15 09:41:53Korrekt. Habe ich gestern auch gesehen. Das wurde anscheinend geändert. Es wurde nur einmal die Gebühr abgezogen und logischerweise jeweils die Provision. Also alles gut bei Consors! In der Vergangenheit hatte ich das mal, dass mit jeder Order die Gebühr fällig wurde.
SG kmastra
SG kmastra
Antwort auf Beitrag Nr.: 49.423.553 von SLGramann am 25.03.15 21:31:28Ich habe meine MGNX-Position heute um ein Drittel aufgestockt. Gut möglich, dass wir noch weit bessere Kurse sehen, aber dann würde ich die Position weiter ausbauen.
Ich denke, dass MGNX mit DART eine der interessantesten Plattformen überhaupt hat. Leider sind die DART-Projekte alle noch in einem sehr frühen Stadium, so dass das wohl ein Langzeitprojekt ist. Vom "Rest" der Plattform muss man vermutlich nicht viel halten...
Ich denke, dass MGNX mit DART eine der interessantesten Plattformen überhaupt hat. Leider sind die DART-Projekte alle noch in einem sehr frühen Stadium, so dass das wohl ein Langzeitprojekt ist. Vom "Rest" der Plattform muss man vermutlich nicht viel halten...
Heute schwere Rückschläge für MorphoSys und Genfit.
MorphoSys verliert Celgene als Partner für ihren CD38-mab. Das kann man sich eigentlich nur so erklären, dass Celgene keine große Chance sieht, sich gegen Dara durchzusetzen.
Genfit hat bei NASH verkackt - und redet Unsinn. Das dürfte dort ganz, ganz bitter werden.
MorphoSys verliert Celgene als Partner für ihren CD38-mab. Das kann man sich eigentlich nur so erklären, dass Celgene keine große Chance sieht, sich gegen Dara durchzusetzen.
Genfit hat bei NASH verkackt - und redet Unsinn. Das dürfte dort ganz, ganz bitter werden.
Auch INNATE PHARMA erlebt einen Rückschlag diese Woche.
Antwort auf Beitrag Nr.: 49.443.059 von Fruehrentner am 27.03.15 19:04:47Dazu vielleicht diese Einschätzung nicht uninteressant:
Shares of the European immuno-oncology company Innate Pharmaceuticals (IPH.PA) dipped late this week with the news that one arm (which treatment group has not been disclosed) in its ongoing EffiKIR trial would be stopped, and that results comparing the remaining arm to placebo have been pushed back to the second quarter of 2016.
EffiKIR is a randomized phase II trial of lirilumab as maintenance treatment in elderly patients with Acute Myeloid Leukemia (AML) who are in first complete remission. The trial includes three arms: single agent lirilumab at 0.1mg/kg every 12 weeks (q12w, or intermittent), 1 mg/kg every 4 weeks (q4w, or continuous), or placebo. Our read-through and the general consensus among investors is that it is likely the low-dose arm that has been stopped. (We confirmed with the company that they remain blinded to the study, including which arm was halted) That shouldn’t be entirely surprising given that this arm includes a dose 90% lower than the alternative and at 1/3 the frequency. Additionally, an ongoing trial of lirilumab in combination with partner Bristol-Myers Squibb’s (BMY) nivolumab utilizes the continuous dosing schedule.
More immediate, perhaps, Investors are selling IPH because there’s now a risk that the company has no major catalysts this year, making IPH.PA a 2016 story and giving investors little reason to tie up capital until later this year. We’re working through some details based on this latest update and will publish a deeper look on the implications of this news in the near-term. Though IPH.PA is likely dead money for now, it’s certainly an intriguing story for biotech investors to track.
https://propthink.com/uh-oh-bubble-talk-is-back-in-biotech/
Shares of the European immuno-oncology company Innate Pharmaceuticals (IPH.PA) dipped late this week with the news that one arm (which treatment group has not been disclosed) in its ongoing EffiKIR trial would be stopped, and that results comparing the remaining arm to placebo have been pushed back to the second quarter of 2016.
EffiKIR is a randomized phase II trial of lirilumab as maintenance treatment in elderly patients with Acute Myeloid Leukemia (AML) who are in first complete remission. The trial includes three arms: single agent lirilumab at 0.1mg/kg every 12 weeks (q12w, or intermittent), 1 mg/kg every 4 weeks (q4w, or continuous), or placebo. Our read-through and the general consensus among investors is that it is likely the low-dose arm that has been stopped. (We confirmed with the company that they remain blinded to the study, including which arm was halted) That shouldn’t be entirely surprising given that this arm includes a dose 90% lower than the alternative and at 1/3 the frequency. Additionally, an ongoing trial of lirilumab in combination with partner Bristol-Myers Squibb’s (BMY) nivolumab utilizes the continuous dosing schedule.
More immediate, perhaps, Investors are selling IPH because there’s now a risk that the company has no major catalysts this year, making IPH.PA a 2016 story and giving investors little reason to tie up capital until later this year. We’re working through some details based on this latest update and will publish a deeper look on the implications of this news in the near-term. Though IPH.PA is likely dead money for now, it’s certainly an intriguing story for biotech investors to track.
https://propthink.com/uh-oh-bubble-talk-is-back-in-biotech/
Antwort auf Beitrag Nr.: 49.446.557 von SLGramann am 28.03.15 14:55:53IPH.PA
Als echten "Rückschlag" sehe ich es auch nicht, da der dritte Arm, der wahrscheinlich gestoppt worden ist, eine deutlich geringere Dosis besitzt, die ansonsten auch nicht verwendet wird. Interessant fand ich KIR auch eher in Kombinationen (BMS hat in den letzten Monaten zu anderne bereits laufenden Kombi-Studien den KIR-AK nachträglich hinzugefügt, was doch eher ein Zeichen von Zuversicht ist). Insbesondere spannend sind Kombis mit AKs wie Rituxan, Herceptin usw, die ADCC nutzen... bisher sind es eher IO-Kombis.



Vom KIR-AK Lirilumab profitiert IPH auch nur zu einem kleinen Teil, da die Royalties nicht so hoch sind. Wichtiger finde ich den NKG2A-AK IPH2201, der alleine IPH gehört. Über HLA-E hemmt der Krebs NK- und T-Zellen... ähnlich wie z.B. PD1.
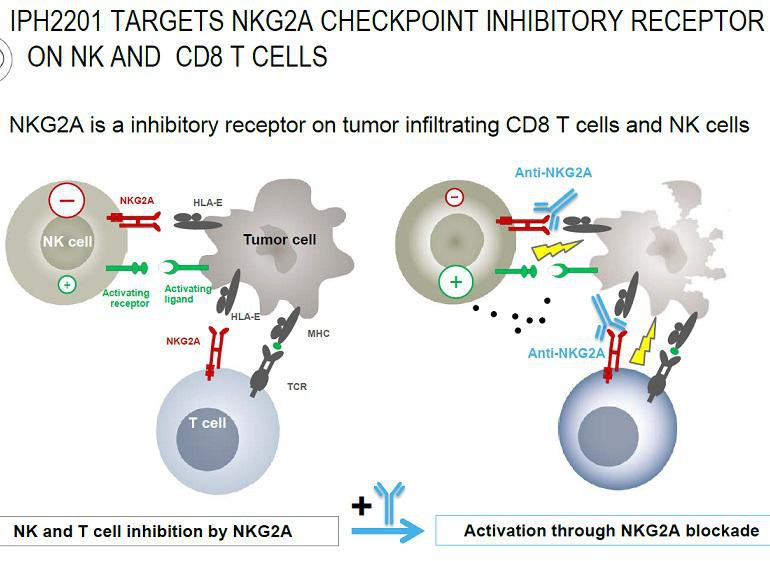
"More immediate, perhaps, Investors are selling IPH because there’s now a risk that the company has no major catalysts this year, making IPH.PA a 2016 story and giving investors little reason to tie up capital until later this year. ... Though IPH.PA is likely dead money for now, it’s certainly an intriguing story for biotech investors to track."
Sollen nicht zur ASCO erste Kombi-Daten zum KIR-AK z.B. mit PD1 kommen? Außerdem sieht das Folgende meiner Meinung nach so aus, als ob bei den IPH2201 PII-Studien viel früher relevante Ergebnisse vorliegen können, als von den meisten erwartet wird. Die vollständigen Ergebnisse kommen erst Ende 2016/2017... aber die für eine mögliche vorzeitige Zulassung relevanten ORR&Co sollen bereis viel früher vorliegen (vielleicht schon dieses Jahr?). In Ovarian soll z.B. laut der Folien nur eine Kombi mit SOC gestartet werden, wenn Mono positiv aussieht. Im Plan ist der SOC-Kombi Start auch deutlich vor Studienende von Mono in 2017.

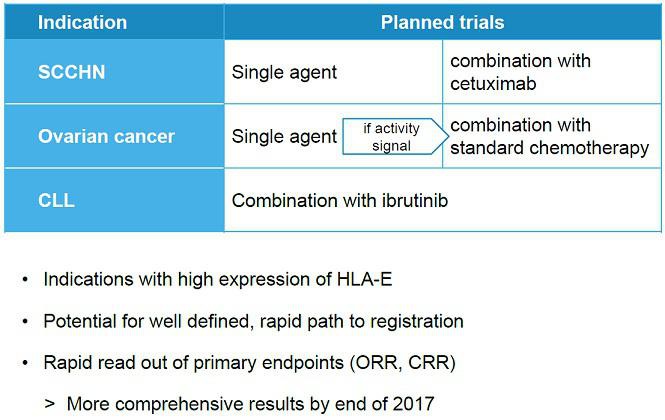
Insgesamt ist IPH meines Wissens nach das führende Biotech-Unternehmen im Bereich der NK-Zellen gegen Krebs... und die sind wahrscheinlich ebenso wichtig wie die T-Zellen (PD1&Co, CARTs usw...). D.h. IPH hat hier ein Monopol und einen erheblich Vorsprung.

Gruß
ipollit
Als echten "Rückschlag" sehe ich es auch nicht, da der dritte Arm, der wahrscheinlich gestoppt worden ist, eine deutlich geringere Dosis besitzt, die ansonsten auch nicht verwendet wird. Interessant fand ich KIR auch eher in Kombinationen (BMS hat in den letzten Monaten zu anderne bereits laufenden Kombi-Studien den KIR-AK nachträglich hinzugefügt, was doch eher ein Zeichen von Zuversicht ist). Insbesondere spannend sind Kombis mit AKs wie Rituxan, Herceptin usw, die ADCC nutzen... bisher sind es eher IO-Kombis.



Vom KIR-AK Lirilumab profitiert IPH auch nur zu einem kleinen Teil, da die Royalties nicht so hoch sind. Wichtiger finde ich den NKG2A-AK IPH2201, der alleine IPH gehört. Über HLA-E hemmt der Krebs NK- und T-Zellen... ähnlich wie z.B. PD1.

"More immediate, perhaps, Investors are selling IPH because there’s now a risk that the company has no major catalysts this year, making IPH.PA a 2016 story and giving investors little reason to tie up capital until later this year. ... Though IPH.PA is likely dead money for now, it’s certainly an intriguing story for biotech investors to track."
Sollen nicht zur ASCO erste Kombi-Daten zum KIR-AK z.B. mit PD1 kommen? Außerdem sieht das Folgende meiner Meinung nach so aus, als ob bei den IPH2201 PII-Studien viel früher relevante Ergebnisse vorliegen können, als von den meisten erwartet wird. Die vollständigen Ergebnisse kommen erst Ende 2016/2017... aber die für eine mögliche vorzeitige Zulassung relevanten ORR&Co sollen bereis viel früher vorliegen (vielleicht schon dieses Jahr?). In Ovarian soll z.B. laut der Folien nur eine Kombi mit SOC gestartet werden, wenn Mono positiv aussieht. Im Plan ist der SOC-Kombi Start auch deutlich vor Studienende von Mono in 2017.


Insgesamt ist IPH meines Wissens nach das führende Biotech-Unternehmen im Bereich der NK-Zellen gegen Krebs... und die sind wahrscheinlich ebenso wichtig wie die T-Zellen (PD1&Co, CARTs usw...). D.h. IPH hat hier ein Monopol und einen erheblich Vorsprung.
Gruß
ipollit
Die Biotech-Performance seit 2000 ist schon ziemlich beeindruckend. Unter den Indizes hat sich der BTK am besten entwickelt, der im Wesentlichen die großen Biotechs beinhaltet... d.h. dieser langjährige Aufschwung wird offensichtlich maßgeblich von den Schwergewichten der Branche getragen.
http://www.bloomberg.com/news/articles/2015-03-27/credit-sui…
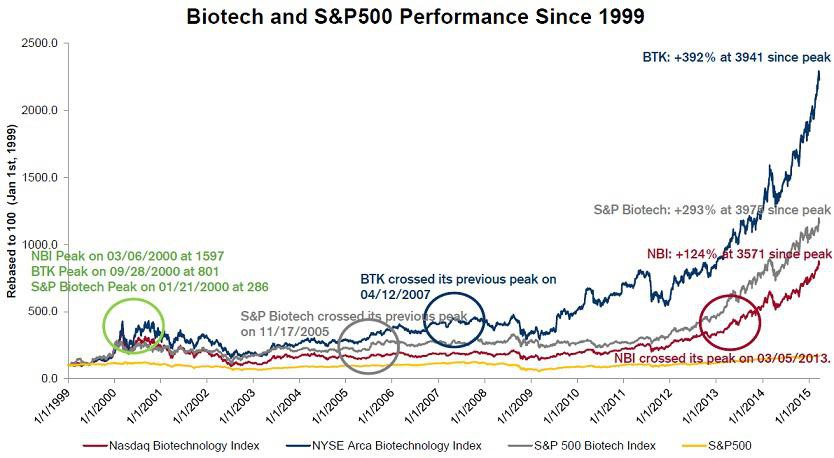
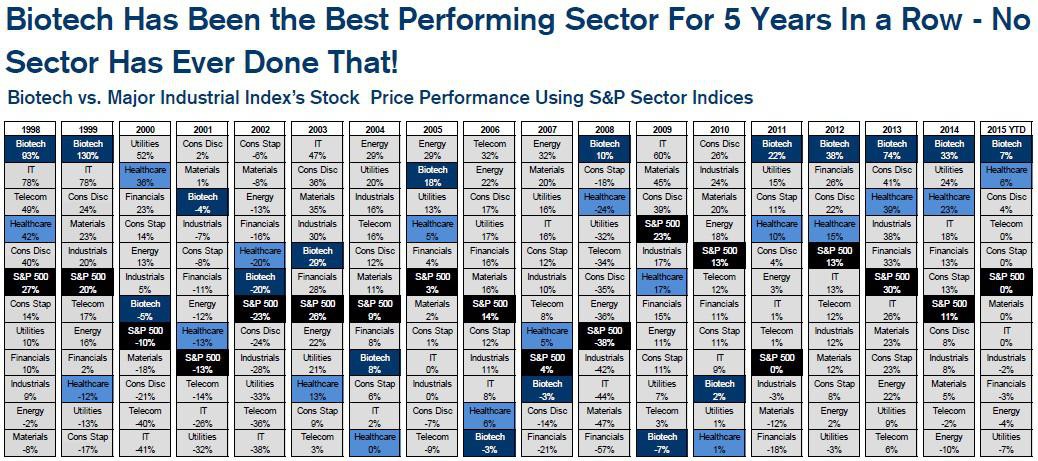
Gruß
ipollit
http://www.bloomberg.com/news/articles/2015-03-27/credit-sui…


Gruß
ipollit
Antwort auf Beitrag Nr.: 49.433.132 von SLGramann am 26.03.15 18:22:31RBC zu ICPT und Genfit:

Ich finde ICPT ja spätestens seit der BT-Entscheidung wieder wirklich spannend und hab sie seit einiger Zeit wieder im Depot.
Es stehen weitere de-risking Ereignisse unmittelbar bevor. Zum einen die Finalisierung des PIII-Protokolls in NASH und zum anderen die Finalisierung des NDA von OCA in der "orphan"-Indikation PBC (wird beides für Q2 erwartet).
Hier noch die aktuelle Unternehmenspräsentation:
http://files.shareholder.com/downloads/AMDA-1AUOV7/400812179…
Wenn OCA der erwartete Mega-Blockbuster werden sollte, wird ICPT sicher ein 20-Milliarden-Dollar+X-Unternehmen werden.

Ich finde ICPT ja spätestens seit der BT-Entscheidung wieder wirklich spannend und hab sie seit einiger Zeit wieder im Depot.
Es stehen weitere de-risking Ereignisse unmittelbar bevor. Zum einen die Finalisierung des PIII-Protokolls in NASH und zum anderen die Finalisierung des NDA von OCA in der "orphan"-Indikation PBC (wird beides für Q2 erwartet).
Hier noch die aktuelle Unternehmenspräsentation:
http://files.shareholder.com/downloads/AMDA-1AUOV7/400812179…
Wenn OCA der erwartete Mega-Blockbuster werden sollte, wird ICPT sicher ein 20-Milliarden-Dollar+X-Unternehmen werden.
INFI & KPTI
Zwar ist Imbruvica von PCYC ein deutlicher Fortschritt und wohl das Maß der Dinge in CLL, doch gibt es nach wie vor hohen Bedarf, falls Imbruvica nicht mehr wirkt.
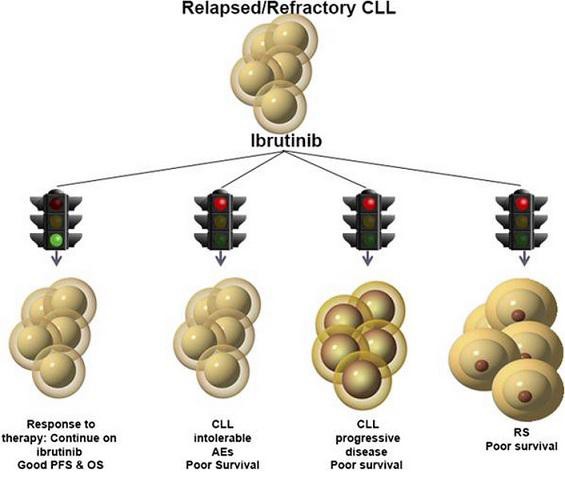
http://www.bloodjournal.org/content/125/13/2013?sso-checked=…
"Definitely, ibrutinib has dramatically changed the landscape of relapsed/refractory CLL treatment and constitutes an important paradigm in the molecularly targeted approach of this disease, with excellent efficacy and tolerability. However, patients who discontinue treatment represent a challenge to the practicing oncologist, and treatment options are very limited. In the near future, early identification of very high-risk patients treated with ibrutinib should be the target of new combinatorial therapies that can improve the outcomes in this population. This report highlights that the road toward a cure (or effective disease control) of CLL has not ended and that, instead, we might be facing a new unmet need in this disease."
Eine Möglichkeit Resistenzen gegen den BTK-Hemmer vorzubeugen, ist vielleicht eine Kombi mit einem IRAK4-Hemmer wie den von TGTX.
In CLL konzentriert sich vor allen INFI auf die Behandlung von Imbruvica resistenten CLL. Duvelisib scheint hier zu wirken. Es befindet sich bereits in der DUO PIII für eine mögliche Zulassung. Zudem besitzt ABBV nach der Übernahme von PCYC sowohl Imbruvica als auch Duvelisib.
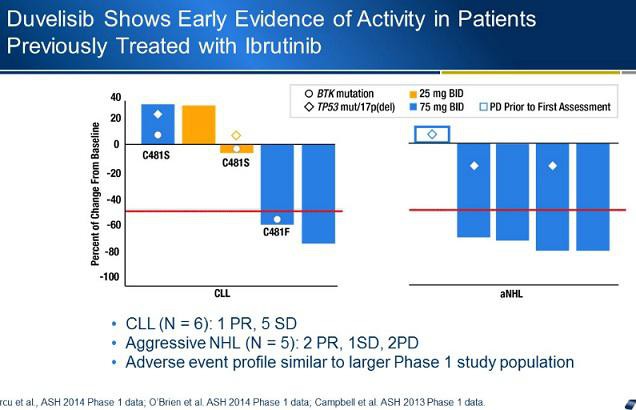
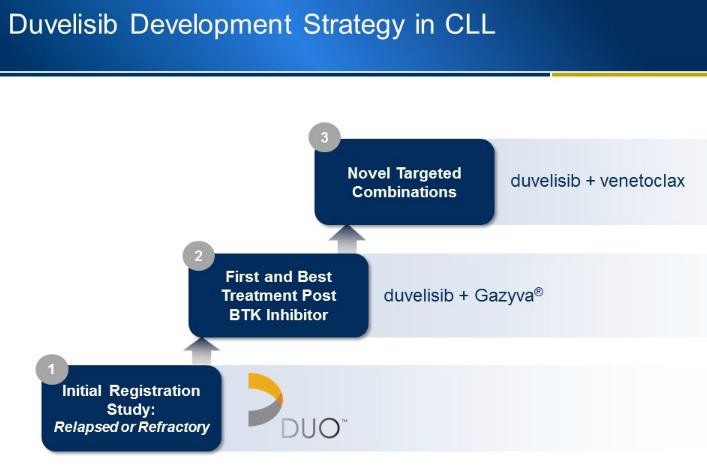
Die entstehenden Resistenzen können sehr aggressiv sein. Eine spezielle Form ist dann die Richters Transformation ("RS"). Gegen Richters ist KPTIs Selinexor ebenfalls in einer Zulassung-Studie SIRRT. Generell kann Selinexor gegen schwer zu behandelnde CLL-Formen eingesetzt werden, bei denen zuvor schon viele Therapien versagt haben, da der Ansatzpunkt ein grundsätzlich anderer ist als die Signalweg-Unterdrückung von z.B. BTK (Imbruvica) oder pi3k (Duvelisib).
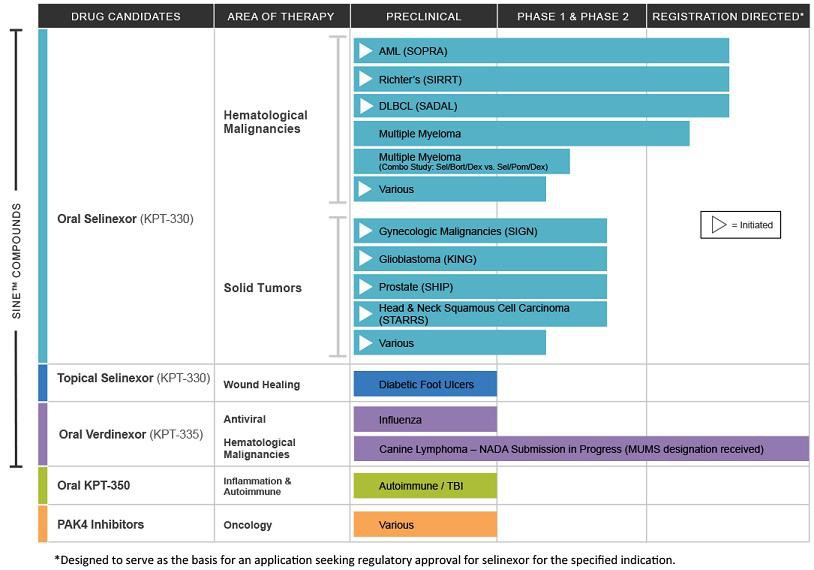
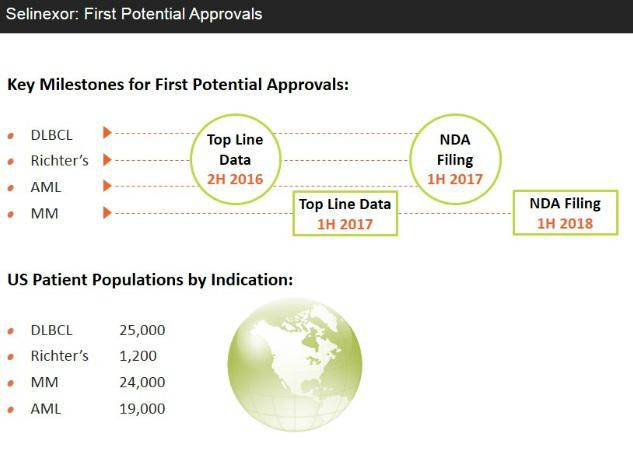
INFI und KPTI sind in CLL also gut aufgestellt, gerade auch wenn Imbruvica das führende Mittel gegen CLL ist.
Gruß
ipollit
Zwar ist Imbruvica von PCYC ein deutlicher Fortschritt und wohl das Maß der Dinge in CLL, doch gibt es nach wie vor hohen Bedarf, falls Imbruvica nicht mehr wirkt.

http://www.bloodjournal.org/content/125/13/2013?sso-checked=…
"Definitely, ibrutinib has dramatically changed the landscape of relapsed/refractory CLL treatment and constitutes an important paradigm in the molecularly targeted approach of this disease, with excellent efficacy and tolerability. However, patients who discontinue treatment represent a challenge to the practicing oncologist, and treatment options are very limited. In the near future, early identification of very high-risk patients treated with ibrutinib should be the target of new combinatorial therapies that can improve the outcomes in this population. This report highlights that the road toward a cure (or effective disease control) of CLL has not ended and that, instead, we might be facing a new unmet need in this disease."
Eine Möglichkeit Resistenzen gegen den BTK-Hemmer vorzubeugen, ist vielleicht eine Kombi mit einem IRAK4-Hemmer wie den von TGTX.
In CLL konzentriert sich vor allen INFI auf die Behandlung von Imbruvica resistenten CLL. Duvelisib scheint hier zu wirken. Es befindet sich bereits in der DUO PIII für eine mögliche Zulassung. Zudem besitzt ABBV nach der Übernahme von PCYC sowohl Imbruvica als auch Duvelisib.


Die entstehenden Resistenzen können sehr aggressiv sein. Eine spezielle Form ist dann die Richters Transformation ("RS"). Gegen Richters ist KPTIs Selinexor ebenfalls in einer Zulassung-Studie SIRRT. Generell kann Selinexor gegen schwer zu behandelnde CLL-Formen eingesetzt werden, bei denen zuvor schon viele Therapien versagt haben, da der Ansatzpunkt ein grundsätzlich anderer ist als die Signalweg-Unterdrückung von z.B. BTK (Imbruvica) oder pi3k (Duvelisib).


INFI und KPTI sind in CLL also gut aufgestellt, gerade auch wenn Imbruvica das führende Mittel gegen CLL ist.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.386.896 von kmastra am 20.03.15 21:35:41AERI
"Es scheint so, dass AERI gewisse Nebenwirkungen heruntergespielt hat (Augenrötung)"
Wie relevant das ist, weiß ich nicht... wenn ich andere richtig verstanden habe, wird Rhopressa&Co vor dem Schlafengehen genommen. Im Schlaf sind dann eventuelle Augenrötungen nicht bedeutsam und am nächsten Morgen ist es dann wahrscheinlich abgeklungen.
Am Grünen Star ist oft ein fehlerhafter Augeninnendruck beteiligt, weil Flüssigkeit nicht richtig abfließen kann. Hauptursache scheint ein spezieller Gewebeteil im Auge zu sein (wenn ich das richtig verstehe)... das sogenannte "trabecular meshwork". Die bisherigen Mittel wirken aber über zwei andere Wege. Rhopressa ist als ROCK-Hemmer wahrscheinlich das erste Mittel, dass direkt auf das trabecular meshwork wirkt. Allerdings hatte man sich dadurch vielleicht einen höheren Effekt versprochen...
http://www.aao.org/publications/eyenet/201310/feature.cfm
Although ROCK inhibition may be a good approach, and a couple of Rho kinase inhibitors have demonstrated effectiveness, Dr. Rhee said that he is “a little disappointed” with the modest effects reported in early trials. “I really thought that this class of drugs would be an absolute knockout.”
Dennoch scheint es ein Fortschritt zu sein. Nach meinem Verständnis wirken die verschiedenen vorhandenen Mittel nicht bei jedem gleich gut... es werden Alternativen benötigt. ROCK-Hemmer sind etwas komplett neues und somit wohl eine gute Alternative zu bestehenen Mitteln. Zudem ist die Kombi Roclatan aus Rhopressa + dem bisher besten Mittel Latanoprost wahrscheinlich dann das effektivste Mittel, was es gibt.
Zuletzt gab es Hinweise, dass Rhopressa weitere positive Effekte haben könnte und sich auf fibrotische Veränderungen beim grünen Star auswirkt. Das wäre dann eine direkte Krankheitsverbesserung über die Änderung des Druckes hinaus. Der Augeninnendruck ist nach meinem Verständnis nur eine Ursache für Grünen Star... die Veränderung der Nerven bis hin zur Erblindung ist aber die eigentliche Erkrankung.
ITEK hat dagegen einen Adenosine Agonist, der ebenfalls wie ROCK-Hemmer auf das trabecular meshwork wirken soll. Allerdings sind ROCK-Hemmer bisher besser erforscht. ITEKs Kandidat kann auch funktionieren... die Unsicherheit ist aber offensichtlich viel größer.
AERI scheint auch etwas gegen AMD in der präklinischen Pipeline zu haben. Das lässt sich zwar bisher so nicht bewerten, aber AMD ist ein sehr großer Markt. Es soll angeblich besser wirken, als REGNs Eylea...



Grüße
ipollit
"Es scheint so, dass AERI gewisse Nebenwirkungen heruntergespielt hat (Augenrötung)"
Wie relevant das ist, weiß ich nicht... wenn ich andere richtig verstanden habe, wird Rhopressa&Co vor dem Schlafengehen genommen. Im Schlaf sind dann eventuelle Augenrötungen nicht bedeutsam und am nächsten Morgen ist es dann wahrscheinlich abgeklungen.
Am Grünen Star ist oft ein fehlerhafter Augeninnendruck beteiligt, weil Flüssigkeit nicht richtig abfließen kann. Hauptursache scheint ein spezieller Gewebeteil im Auge zu sein (wenn ich das richtig verstehe)... das sogenannte "trabecular meshwork". Die bisherigen Mittel wirken aber über zwei andere Wege. Rhopressa ist als ROCK-Hemmer wahrscheinlich das erste Mittel, dass direkt auf das trabecular meshwork wirkt. Allerdings hatte man sich dadurch vielleicht einen höheren Effekt versprochen...
http://www.aao.org/publications/eyenet/201310/feature.cfm
Although ROCK inhibition may be a good approach, and a couple of Rho kinase inhibitors have demonstrated effectiveness, Dr. Rhee said that he is “a little disappointed” with the modest effects reported in early trials. “I really thought that this class of drugs would be an absolute knockout.”
Dennoch scheint es ein Fortschritt zu sein. Nach meinem Verständnis wirken die verschiedenen vorhandenen Mittel nicht bei jedem gleich gut... es werden Alternativen benötigt. ROCK-Hemmer sind etwas komplett neues und somit wohl eine gute Alternative zu bestehenen Mitteln. Zudem ist die Kombi Roclatan aus Rhopressa + dem bisher besten Mittel Latanoprost wahrscheinlich dann das effektivste Mittel, was es gibt.
Zuletzt gab es Hinweise, dass Rhopressa weitere positive Effekte haben könnte und sich auf fibrotische Veränderungen beim grünen Star auswirkt. Das wäre dann eine direkte Krankheitsverbesserung über die Änderung des Druckes hinaus. Der Augeninnendruck ist nach meinem Verständnis nur eine Ursache für Grünen Star... die Veränderung der Nerven bis hin zur Erblindung ist aber die eigentliche Erkrankung.
ITEK hat dagegen einen Adenosine Agonist, der ebenfalls wie ROCK-Hemmer auf das trabecular meshwork wirken soll. Allerdings sind ROCK-Hemmer bisher besser erforscht. ITEKs Kandidat kann auch funktionieren... die Unsicherheit ist aber offensichtlich viel größer.
AERI scheint auch etwas gegen AMD in der präklinischen Pipeline zu haben. Das lässt sich zwar bisher so nicht bewerten, aber AMD ist ein sehr großer Markt. Es soll angeblich besser wirken, als REGNs Eylea...


Grüße
ipollit
Antwort auf Beitrag Nr.: 49.447.424 von ipollit am 28.03.15 19:02:32das gefällt mir ! 

Antwort auf Beitrag Nr.: 49.413.179 von kmastra am 24.03.15 22:35:14das wurde auch mal zeit. leider wird die Morphosys schwer gewichtet sein...
wo kann man den dt. index finden?

wo kann man den dt. index finden?
Antwort auf Beitrag Nr.: 49.449.464 von ipollit am 29.03.15 13:34:08"Dennoch scheint es ein Fortschritt zu sein. Nach meinem Verständnis wirken die verschiedenen vorhandenen Mittel nicht bei jedem gleich gut... es werden Alternativen benötigt. ROCK-Hemmer sind etwas komplett neues und somit wohl eine gute Alternative zu bestehenen Mitteln."
Hallo ipollit,
so habe ich es auch immer verstanden, dass das Hauptargument nicht die Effektivität ist (die sollte gegenüber Latanoprost nur mehr oder weniger non-inferior sein, das wäre schon nicht schlecht), sondern der ganz andere MOA.
Ich erinnere mich dunkel an eine Präsentation (vielleicht von Aerie selbst) wo man Augenärzte befragt hatte, warum sie ggf. Rhopressa verschreiben würden. Sehr viele (20 bis 50%) hatten den anderen MOA als wichtigstes Kriterium angeführt.
Der Punkt ist wohl der, dass alle Mittel über die Zeit - zumindest bei einigen Patienten - in der Wirksamkeit nachlassen. Deshalb ist der Bedarf nach "etwas neuem" sehr groß, ganz unabhängig davon, ob das dann auch deutlich besser als bspw. Latanoprost wirkt.
Ich gehe dann aber auch davon aus, dass Rhopressa Zeit brauchen wird, um sich seinen Marktanteil zu erkämpfen.
Die Umsätze werden ziemlich langsam, aber recht stetig steigen - so stelle ich es mir jedenfalls vor.
Noch etwas anderes:
Wie siehst Du das Verhältnis zwischen ABT-199 und Duvalesib bei Abbvie?
Gruß
SLG
Hallo ipollit,
so habe ich es auch immer verstanden, dass das Hauptargument nicht die Effektivität ist (die sollte gegenüber Latanoprost nur mehr oder weniger non-inferior sein, das wäre schon nicht schlecht), sondern der ganz andere MOA.
Ich erinnere mich dunkel an eine Präsentation (vielleicht von Aerie selbst) wo man Augenärzte befragt hatte, warum sie ggf. Rhopressa verschreiben würden. Sehr viele (20 bis 50%) hatten den anderen MOA als wichtigstes Kriterium angeführt.
Der Punkt ist wohl der, dass alle Mittel über die Zeit - zumindest bei einigen Patienten - in der Wirksamkeit nachlassen. Deshalb ist der Bedarf nach "etwas neuem" sehr groß, ganz unabhängig davon, ob das dann auch deutlich besser als bspw. Latanoprost wirkt.
Ich gehe dann aber auch davon aus, dass Rhopressa Zeit brauchen wird, um sich seinen Marktanteil zu erkämpfen.
Die Umsätze werden ziemlich langsam, aber recht stetig steigen - so stelle ich es mir jedenfalls vor.
Noch etwas anderes:
Wie siehst Du das Verhältnis zwischen ABT-199 und Duvalesib bei Abbvie?
Gruß
SLG
Antwort auf Beitrag Nr.: 49.455.563 von SLGramann am 30.03.15 15:04:28
Hallo,
was die Effektivität (ich beziehe mich da auf die Senkung des Augeninnendrucks) betrifft ist es in der Tat so, dass Rhopressa vergleichbar gut wirkt wie Latanoprost.

Roclatan wirkt signifikant besser, was nicht verwundert, da es eine Kombination aus Beiden ist. Aeri möchte Rhopressa als neue 2. Alternative (nach dem generischen Lataoprost) anstelle von Timonol positionieren, weshalb die PIIIs hier auch logischerweise mit Timonol als Vergleich arbeiten. Bisher gab es diesen direkten Vergleich nicht aber bisher war Timonol in Studien ca. um 1 mmHG schlechter als Latanoprost. Der Effektivitäts Endpunkt ist non inferioty zu Timonol. Rhopressa könnte also sogar schlechter abschneiden als Timonol und könnte trotzdem den Endpunkt erreichen. Aber das scheint ja unwahrscheich, wenn Rhopressa bisher vergleichbar gut wirkte wie Latanoprost. Hinzu kommt der angesprochene medizinische Bedarf nach "etwas Anderem", dass evtl. auch die Wirkung nicht verliert und ggf. sogar die Ursache bekämpft.

Roctalan will man wohl für Patienten mit stark erhöhtem Augeninnedruck und Patienten mit weit fortsgeschrittenem Glaukom entwickeln. Als "biggest gun".
Was die Effektivitätsstudie(n) betrifft denke ich stehen die Chancen sehr gut. Und das steht als Nächstes (Mai?) an. Ich werde meine Position auf jeden Fall halten und bei einem Fehler (den man nie ausschließen kann) gäbe es evtl. die Möglichkeit nachzukaufen und auf positive Roclatan Ergebnisse zu setzen.
Zur Sicherheit:
Ich habe nochmal recherchiert und bin einigermaßen beruhigt.
Die Augenrötung tritt zwar bei 40% auf (Rhopressa) - jedoch ist diese bei 80% mild. Aeri hat dies auch nicht verheimlicht, sondern genau so gesagt.
Auch Latanoprost und Timonol sind natürlich nicht frei von Nebenwirkungen.
Latanoprost:
> 5–15 %: Verschwommene Sicht, brennendes oder stechendes Gefühl, conjunktivale Hyperämie, Fremdkörpergefühl, Jucken, erhöhte Pigmentierung der Iris, die zu Iris-Heterochromie führen kann, Keratitis superficialis punctata
4 %: Erkältung oder Infektion der oberen Atemwege, grippeähnliche Symptome
1–4 %: Trockene Augen, starke Tränenbildung, Augenschmerzen, Verkrustung des Augenlids, Lidödem, Erythema des Lids (Hyperämie), Lidschmerzen, Lichtempfindlichkeit
1–2 %: Schmerzen im Brustkorb, allergische Hautreaktionen, Arthralgie, Rückenschmerzen, Muskelschmerzen, Verdickung der Wimpern
< 1 % (nur wichtige oder lebensbedrohliche): Asthma, Herpes-Keratitis, Iritis, Keratitis, retinale Arterienembolie, Ablösung der Netzhaut, Lyell-Syndrom, Uveitis, Glaskörperblutung durch diabetische Retinopathie
http://de.wikipedia.org/wiki/Latanoprost
Timonol:
In den USA wurden Timolol-Augentropfen zwischen 1978 und 1985 schätzungsweise 40 Millionen Mal verschrieben. In dieser Zeitspanne wurden 450 ernsthafte kardiovaskuläre oder respiratorische Nebenwirkungen sowie 32 Todesfälle registriert, die wahrscheinlich im Zusammenhang mit den Timolol-Augentropfen standen.
http://www.infomed.ch/pk_template.php?pkid=614
SG kmastra
Zitat von SLGramann: "Dennoch scheint es ein Fortschritt zu sein. Nach meinem Verständnis wirken die verschiedenen vorhandenen Mittel nicht bei jedem gleich gut... es werden Alternativen benötigt. ROCK-Hemmer sind etwas komplett neues und somit wohl eine gute Alternative zu bestehenen Mitteln."
Hallo ipollit,
so habe ich es auch immer verstanden, dass das Hauptargument nicht die Effektivität ist (die sollte gegenüber Latanoprost nur mehr oder weniger non-inferior sein, das wäre schon nicht schlecht), sondern der ganz andere MOA.
Ich erinnere mich dunkel an eine Präsentation (vielleicht von Aerie selbst) wo man Augenärzte befragt hatte, warum sie ggf. Rhopressa verschreiben würden. Sehr viele (20 bis 50%) hatten den anderen MOA als wichtigstes Kriterium angeführt.
Der Punkt ist wohl der, dass alle Mittel über die Zeit - zumindest bei einigen Patienten - in der Wirksamkeit nachlassen. Deshalb ist der Bedarf nach "etwas neuem" sehr groß, ganz unabhängig davon, ob das dann auch deutlich besser als bspw. Latanoprost wirkt.
Ich gehe dann aber auch davon aus, dass Rhopressa Zeit brauchen wird, um sich seinen Marktanteil zu erkämpfen.
Die Umsätze werden ziemlich langsam, aber recht stetig steigen - so stelle ich es mir jedenfalls vor.
Noch etwas anderes:
Wie siehst Du das Verhältnis zwischen ABT-199 und Duvalesib bei Abbvie?
Gruß
SLG
Hallo,
was die Effektivität (ich beziehe mich da auf die Senkung des Augeninnendrucks) betrifft ist es in der Tat so, dass Rhopressa vergleichbar gut wirkt wie Latanoprost.
Roclatan wirkt signifikant besser, was nicht verwundert, da es eine Kombination aus Beiden ist. Aeri möchte Rhopressa als neue 2. Alternative (nach dem generischen Lataoprost) anstelle von Timonol positionieren, weshalb die PIIIs hier auch logischerweise mit Timonol als Vergleich arbeiten. Bisher gab es diesen direkten Vergleich nicht aber bisher war Timonol in Studien ca. um 1 mmHG schlechter als Latanoprost. Der Effektivitäts Endpunkt ist non inferioty zu Timonol. Rhopressa könnte also sogar schlechter abschneiden als Timonol und könnte trotzdem den Endpunkt erreichen. Aber das scheint ja unwahrscheich, wenn Rhopressa bisher vergleichbar gut wirkte wie Latanoprost. Hinzu kommt der angesprochene medizinische Bedarf nach "etwas Anderem", dass evtl. auch die Wirkung nicht verliert und ggf. sogar die Ursache bekämpft.
Roctalan will man wohl für Patienten mit stark erhöhtem Augeninnedruck und Patienten mit weit fortsgeschrittenem Glaukom entwickeln. Als "biggest gun".
Was die Effektivitätsstudie(n) betrifft denke ich stehen die Chancen sehr gut. Und das steht als Nächstes (Mai?) an. Ich werde meine Position auf jeden Fall halten und bei einem Fehler (den man nie ausschließen kann) gäbe es evtl. die Möglichkeit nachzukaufen und auf positive Roclatan Ergebnisse zu setzen.
Zur Sicherheit:
Ich habe nochmal recherchiert und bin einigermaßen beruhigt.
Die Augenrötung tritt zwar bei 40% auf (Rhopressa) - jedoch ist diese bei 80% mild. Aeri hat dies auch nicht verheimlicht, sondern genau so gesagt.
Auch Latanoprost und Timonol sind natürlich nicht frei von Nebenwirkungen.
Latanoprost:
> 5–15 %: Verschwommene Sicht, brennendes oder stechendes Gefühl, conjunktivale Hyperämie, Fremdkörpergefühl, Jucken, erhöhte Pigmentierung der Iris, die zu Iris-Heterochromie führen kann, Keratitis superficialis punctata
4 %: Erkältung oder Infektion der oberen Atemwege, grippeähnliche Symptome
1–4 %: Trockene Augen, starke Tränenbildung, Augenschmerzen, Verkrustung des Augenlids, Lidödem, Erythema des Lids (Hyperämie), Lidschmerzen, Lichtempfindlichkeit
1–2 %: Schmerzen im Brustkorb, allergische Hautreaktionen, Arthralgie, Rückenschmerzen, Muskelschmerzen, Verdickung der Wimpern
< 1 % (nur wichtige oder lebensbedrohliche): Asthma, Herpes-Keratitis, Iritis, Keratitis, retinale Arterienembolie, Ablösung der Netzhaut, Lyell-Syndrom, Uveitis, Glaskörperblutung durch diabetische Retinopathie
http://de.wikipedia.org/wiki/Latanoprost
Timonol:
In den USA wurden Timolol-Augentropfen zwischen 1978 und 1985 schätzungsweise 40 Millionen Mal verschrieben. In dieser Zeitspanne wurden 450 ernsthafte kardiovaskuläre oder respiratorische Nebenwirkungen sowie 32 Todesfälle registriert, die wahrscheinlich im Zusammenhang mit den Timolol-Augentropfen standen.
http://www.infomed.ch/pk_template.php?pkid=614
SG kmastra
interessanter Thread...muss ich mal markieren.
arry:
Der CEO bei Fox:
http://finance.yahoo.com/video/latest-drugs-being-tested-fig…
Ron Squarer konnte endlich mal klar Stellung nehmen, warum NVS die Medikamente abgegeben hat.
A
Der CEO bei Fox:
http://finance.yahoo.com/video/latest-drugs-being-tested-fig…
Ron Squarer konnte endlich mal klar Stellung nehmen, warum NVS die Medikamente abgegeben hat.
A
Antwort auf Beitrag Nr.: 49.452.026 von SLGramann am 30.03.15 08:11:26ICTP:
Intercept mit einer erneuten KE.
Nachdem Anfang Februar 191 Mio. Dollar eingenommen wurden (für 1,15 Mio. Aktien = 166 Dollar / Aktie netto), werden nun weitere 390 Mio. Euro eingesammelt (für 1,4 Mio. Aktien = 278 Dollar / Aktie netto).
Damit hat Intercept im Q1 2015 immerhin 469 Mio. Dollar netto am Kapitalmarkt eingesammelt.
Man will OCA in NASH wohl ohne Partner zur Zulassung bekommen und vielleicht sogar allein vermarkten.
Jedenfalls dürfte Intercept zum Jahresende ungefähr noch 800 Millionen Dollar Cash haben, was viele Optionen bietet.
Die bereits sehr hohe Marktkap. macht es leicht, große Beträge einzusammeln.
Intercept mit einer erneuten KE.
Nachdem Anfang Februar 191 Mio. Dollar eingenommen wurden (für 1,15 Mio. Aktien = 166 Dollar / Aktie netto), werden nun weitere 390 Mio. Euro eingesammelt (für 1,4 Mio. Aktien = 278 Dollar / Aktie netto).
Damit hat Intercept im Q1 2015 immerhin 469 Mio. Dollar netto am Kapitalmarkt eingesammelt.
Man will OCA in NASH wohl ohne Partner zur Zulassung bekommen und vielleicht sogar allein vermarkten.
Jedenfalls dürfte Intercept zum Jahresende ungefähr noch 800 Millionen Dollar Cash haben, was viele Optionen bietet.
Die bereits sehr hohe Marktkap. macht es leicht, große Beträge einzusammeln.
INFI:

ABT199, Ibrutinib und Duvelisib laut RBC in trauter Harmonie.
Auch eine Umsatzschätzung zu Duvalesib dabei.
PS: Ich muss mir mal angewöhnen, Intercept korrekt mit ICPT abzukürzen...

ABT199, Ibrutinib und Duvelisib laut RBC in trauter Harmonie.
Auch eine Umsatzschätzung zu Duvalesib dabei.
PS: Ich muss mir mal angewöhnen, Intercept korrekt mit ICPT abzukürzen...

Eine sehr umfangreiche Übersicht zum Thema Immuntherapie von Paul D. Rennert:
http://de.slideshare.net/PaulDRennert/the-immune-checkpoint-…
Man kann sich da 107 Slides anschauen. Enorme Stoffmenge - ist vielleicht was für ipollit.
(Zum Ende hin werden auch NK-Zellen als neuer Ansatz hervorgehoben)
http://de.slideshare.net/PaulDRennert/the-immune-checkpoint-…
Man kann sich da 107 Slides anschauen. Enorme Stoffmenge - ist vielleicht was für ipollit.

(Zum Ende hin werden auch NK-Zellen als neuer Ansatz hervorgehoben)
Antwort auf Beitrag Nr.: 49.447.328 von ipollit am 28.03.15 18:30:28IPH.PA
"...der dritte Arm, der wahrscheinlich gestoppt worden ist, eine deutlich geringere Dosis besitzt, die ansonsten auch nicht verwendet wird. .."
Wenn dies zutrifft, frage ich mich, warum man überhaupt einen Arm mit einer derart niedrigen Dosis in das Studiendesign mit aufgenommen hat.
"...der dritte Arm, der wahrscheinlich gestoppt worden ist, eine deutlich geringere Dosis besitzt, die ansonsten auch nicht verwendet wird. .."
Wenn dies zutrifft, frage ich mich, warum man überhaupt einen Arm mit einer derart niedrigen Dosis in das Studiendesign mit aufgenommen hat.

Antwort auf Beitrag Nr.: 49.493.912 von Fruehrentner am 03.04.15 20:09:38"Wenn dies zutrifft, frage ich mich, warum man überhaupt einen Arm mit einer derart niedrigen Dosis in das Studiendesign mit aufgenommen hat."
Eine Antwort liefert der Analystenkommentar, der darunter steht... demnach gäbe es Tierexperimente, bei denen eine vollständige dauerhafte Blockierung von KIR zur eine Toleranz der NK-Zellen führen würde.
Etwas anders verstehe ich das Paper zur vorausgehenden PI. Die aktuelle in 2012 gestartete EFFIKIR-Studie in AML mit den drei Armen ist eine PII, die eine vorzeitige Zulassung erlaubt. Sie basiert auf der folgenden PI: http://www.bloodjournal.org/content/bloodjournal/120/22/4317… "A phase 1 trial of the anti-inhibitory KIR mAb IPH2101 forAMLin complete remission"
Dort wurden mehrere Dosierungen getestet. Ich denke, da KIR auf das Immunsystem einwirkt, hat man mit sehr niedrigen Dosierungen von 0,0003 mg/kg gestartet... die höchste Dosierung lag bei 3 mg/kg. Eine weitgehende Blockierung von KIR wurde im Bereich bei 0,3 mg/kg, 1 mg/kg und 3 mg/kg erreicht. Bei letzterer Dosierung hielt diese vollständige Blockierung mindestens 4 Wochen an.
Eigentlich ist es nicht das Ziel einer PI, die Wirksamkeit zu prüfen... trotzdem ergab sich in diesen 3 höchsten Studien eine deutlich erhöhte Lebenszeit gegenüber den niedrigeren Dosierungen (29,7 vs. 11,8 Monate).
Der eine Arm in EFFIKIR hat daher eine Dosierung von 1 mg/kg alle 4 Wochen... diese Dosis zeigte in der PI eine Wirksamkeit.
Der zweite Arm besitzt als Dosierung 0,1 mg/kg alle 12 Wochen und hat dadurch keine durchgehende KIR-Hemmung. Dies wurde in der PI nicht getestet und liegt unterhalb der drei höchsten Dosierungsgruppen, die einen Überlebensvorteil zeigten. Dazu heißt es im Paper:

D.h. eine vollständige, dauerhafte KIR-Hemmung könnte auch die Ausbildung/Reifung von NK-Zellen stören, da hierbei KIR ebenfalls eine Rolle spielt. Das wäre eher negativ. In der PI mit wenigen Patienten hat man dies so nicht beobachtet... in der PII dürfte allerdings die Wirksamkeit eine klare Aussage liefern, ob dies relevant ist.
Die Studien werden nicht von Innate durchgeführt, sondern von BMS. BMS hat in allen anderen Studien mit KIR offensichtlich die höhere Dosierung zur vollständigen KIR-Hemung gewählt.
Gruß
ipollt
Eine Antwort liefert der Analystenkommentar, der darunter steht... demnach gäbe es Tierexperimente, bei denen eine vollständige dauerhafte Blockierung von KIR zur eine Toleranz der NK-Zellen führen würde.
Etwas anders verstehe ich das Paper zur vorausgehenden PI. Die aktuelle in 2012 gestartete EFFIKIR-Studie in AML mit den drei Armen ist eine PII, die eine vorzeitige Zulassung erlaubt. Sie basiert auf der folgenden PI: http://www.bloodjournal.org/content/bloodjournal/120/22/4317… "A phase 1 trial of the anti-inhibitory KIR mAb IPH2101 forAMLin complete remission"
Dort wurden mehrere Dosierungen getestet. Ich denke, da KIR auf das Immunsystem einwirkt, hat man mit sehr niedrigen Dosierungen von 0,0003 mg/kg gestartet... die höchste Dosierung lag bei 3 mg/kg. Eine weitgehende Blockierung von KIR wurde im Bereich bei 0,3 mg/kg, 1 mg/kg und 3 mg/kg erreicht. Bei letzterer Dosierung hielt diese vollständige Blockierung mindestens 4 Wochen an.
Eigentlich ist es nicht das Ziel einer PI, die Wirksamkeit zu prüfen... trotzdem ergab sich in diesen 3 höchsten Studien eine deutlich erhöhte Lebenszeit gegenüber den niedrigeren Dosierungen (29,7 vs. 11,8 Monate).
Der eine Arm in EFFIKIR hat daher eine Dosierung von 1 mg/kg alle 4 Wochen... diese Dosis zeigte in der PI eine Wirksamkeit.
Der zweite Arm besitzt als Dosierung 0,1 mg/kg alle 12 Wochen und hat dadurch keine durchgehende KIR-Hemmung. Dies wurde in der PI nicht getestet und liegt unterhalb der drei höchsten Dosierungsgruppen, die einen Überlebensvorteil zeigten. Dazu heißt es im Paper:

D.h. eine vollständige, dauerhafte KIR-Hemmung könnte auch die Ausbildung/Reifung von NK-Zellen stören, da hierbei KIR ebenfalls eine Rolle spielt. Das wäre eher negativ. In der PI mit wenigen Patienten hat man dies so nicht beobachtet... in der PII dürfte allerdings die Wirksamkeit eine klare Aussage liefern, ob dies relevant ist.
Die Studien werden nicht von Innate durchgeführt, sondern von BMS. BMS hat in allen anderen Studien mit KIR offensichtlich die höhere Dosierung zur vollständigen KIR-Hemung gewählt.
Gruß
ipollt
Das erste Quartal ist seit einigen Tagen vorbei und hat an klinischen Daten wenig geboten. Dafür gab es im strategischen Bereich bei FMI und bei Array interessante Entwicklungen.
Das zweite Quartal wird klinisch sicher interessanter.
- Losgehen wird es vermutlich Ende April mit CLDN, welche die CUPID2-Daten vorlegen werden.
Ein absolut binäres Event, dass den Kurs sehr schnell entweder Richtung 1 Dollar oder Richtung 100 Dollar befördern wird.
Die Kritik an Celladon hat zuletzt deutlich zugenommen. Einige Kommentare sind nicht weit davon entfernt, CLDN der Manipulation zu bezichtigen.
- Im Mai dürften dann bei EXEL die METEOR-Daten anstehen. Auch das ist ein make-or-brake-Ereignis, würde ich sagen. Nicht ganz so extrem wie bei CLDN, aber aus meiner Sicht ist METEOR für EXEL letztlich auch existenziell.
Beide Aktienpositionen sind in meinem Depot allerdings meiner "Verkaufsorgie" vom 10.03.2015 komplett zum Opfer gefallen, so dass ich mir die Sache von der Seitenlinie aus ansehe.
Bei überzeugenden Daten bin ich aber ggf. bereit, auf den dann fahrenden Zug wieder aufzuspringen.
- Ebenfalls im Mai dürften bei Aerie die PIII-Daten des Rocket 1-Trials (Rhopressa) anstehen.
- Zur ASCO Ende Mai/Anfang Juni sollte dann CLVS zeigen, mit welchen Daten sie die Zulassung von Rociletinib beantragen wollen. (Für mich persönlich sehr wichtig, da ich hier stark investiert bin).
- Vielleicht noch im Juni wird Avalanche die PII-Daten ihres AMD-Kandidaten vorlegen. Ebenfalls ein binäres Ereignis.
Das ist das, was ich jetzt für Q2 auf dem Schirm habe, was wichtige klinische Studiendaten angeht.
Wer hat noch was?
(Es dürfte jedenfalls eine spannende Zeit werden.)
Das zweite Quartal wird klinisch sicher interessanter.
- Losgehen wird es vermutlich Ende April mit CLDN, welche die CUPID2-Daten vorlegen werden.
Ein absolut binäres Event, dass den Kurs sehr schnell entweder Richtung 1 Dollar oder Richtung 100 Dollar befördern wird.
Die Kritik an Celladon hat zuletzt deutlich zugenommen. Einige Kommentare sind nicht weit davon entfernt, CLDN der Manipulation zu bezichtigen.
- Im Mai dürften dann bei EXEL die METEOR-Daten anstehen. Auch das ist ein make-or-brake-Ereignis, würde ich sagen. Nicht ganz so extrem wie bei CLDN, aber aus meiner Sicht ist METEOR für EXEL letztlich auch existenziell.
Beide Aktienpositionen sind in meinem Depot allerdings meiner "Verkaufsorgie" vom 10.03.2015 komplett zum Opfer gefallen, so dass ich mir die Sache von der Seitenlinie aus ansehe.
Bei überzeugenden Daten bin ich aber ggf. bereit, auf den dann fahrenden Zug wieder aufzuspringen.
- Ebenfalls im Mai dürften bei Aerie die PIII-Daten des Rocket 1-Trials (Rhopressa) anstehen.
- Zur ASCO Ende Mai/Anfang Juni sollte dann CLVS zeigen, mit welchen Daten sie die Zulassung von Rociletinib beantragen wollen. (Für mich persönlich sehr wichtig, da ich hier stark investiert bin).
- Vielleicht noch im Juni wird Avalanche die PII-Daten ihres AMD-Kandidaten vorlegen. Ebenfalls ein binäres Ereignis.
Das ist das, was ich jetzt für Q2 auf dem Schirm habe, was wichtige klinische Studiendaten angeht.
Wer hat noch was?
(Es dürfte jedenfalls eine spannende Zeit werden.)
Antwort auf Beitrag Nr.: 49.497.434 von SLGramann am 05.04.15 08:11:25"... Das ist das, was ich jetzt für Q2 auf dem Schirm habe, was wichtige klinische Studiendaten angeht.
Wer hat noch was?"
ELEVEN BIOTHERAPEUTICS
EBI-005 gegen dry eye disease.
Im November hiess es: We look forward to reporting top-line results of pivotal phase 3 study in the second quarter of 2015.
http://www.elevenbio.com/pipeline/pipeline.html
Allergan verdient sich mit Restasis seit Jahren eine goldene Nase in dieser Indikation. Viele potentielle Nachfolger sind spät. in Phase 3 gescheitert. Ob Eleven den Durchbruch schafft?
Dry Eye Disease ist weitverbreitet und wird weiter zunehmen in den Industrieländern aufgrund zunehmender Überalterung.
Wer hat noch was?"
ELEVEN BIOTHERAPEUTICS
EBI-005 gegen dry eye disease.
Im November hiess es: We look forward to reporting top-line results of pivotal phase 3 study in the second quarter of 2015.
http://www.elevenbio.com/pipeline/pipeline.html
Allergan verdient sich mit Restasis seit Jahren eine goldene Nase in dieser Indikation. Viele potentielle Nachfolger sind spät. in Phase 3 gescheitert. Ob Eleven den Durchbruch schafft?
Dry Eye Disease ist weitverbreitet und wird weiter zunehmen in den Industrieländern aufgrund zunehmender Überalterung.
Interessanter WiWo Artikel zur Gentherapie, einige börsennotierte Firmen werden genannt, z.B. Uniqure, Spark Therapeutics und Celladon:
http://www.wiwo.de/technologie/forschung/gen-therapie-erober…
http://www.wiwo.de/technologie/forschung/gen-therapie-erober…
Antwort auf Beitrag Nr.: 49.499.108 von Fruehrentner am 05.04.15 20:05:40"Ob Eleven den Durchbruch schafft?"
Die Daten sollen jedenfalls in Q2 kommen, da hast Du recht.
Die Marktkapitalisierung ist mit 140 Mio. Dollar recht niedrig, so dass scheinbar zumindest der Markt keine hohen Erwartungen hegt.
Hat jemand eine Meinung zu EBIO?
Was ich auch noch ganz vergessen habe, sind die Rindopepimut-Daten von CLDX (Interim-Analyse der PIII und finale Daten der ReACT-Studie, die eventuell bereits zu einem Zulassungsantrag führen könnten). Die Daten sind für die "Mitte des Jahres" angekündigt, womit sie wahrscheinlich eher in das 3. als in das 2. Quartal fallen werden, aber wer weiß.
Die Daten sollen jedenfalls in Q2 kommen, da hast Du recht.
Die Marktkapitalisierung ist mit 140 Mio. Dollar recht niedrig, so dass scheinbar zumindest der Markt keine hohen Erwartungen hegt.
Hat jemand eine Meinung zu EBIO?
Was ich auch noch ganz vergessen habe, sind die Rindopepimut-Daten von CLDX (Interim-Analyse der PIII und finale Daten der ReACT-Studie, die eventuell bereits zu einem Zulassungsantrag führen könnten). Die Daten sind für die "Mitte des Jahres" angekündigt, womit sie wahrscheinlich eher in das 3. als in das 2. Quartal fallen werden, aber wer weiß.
INCY (und allgemein von Interesse):
Sehr starker Text zu IDO1 (dem derzeit heißest gehandelten Immuno-Target nach PD1):
http://cen.acs.org/articles/93/i14/Using-IDO1-Inhibitors-Com…
Auch für den Laien verständlich und dennoch tiefgründig und einsichtsreich! Lesenswert!
Sehr starker Text zu IDO1 (dem derzeit heißest gehandelten Immuno-Target nach PD1):
http://cen.acs.org/articles/93/i14/Using-IDO1-Inhibitors-Com…
Auch für den Laien verständlich und dennoch tiefgründig und einsichtsreich! Lesenswert!
Antwort auf Beitrag Nr.: 49.499.144 von Fruehrentner am 05.04.15 20:16:28Und heute ein fetter Deal zwischen BMS und uniQure:
http://finance.yahoo.com/news/bristol-myers-squibb-uniqure-e…
uniQure dürften heute stark im Plus starten. Vorbörslich +40%.
http://finance.yahoo.com/news/bristol-myers-squibb-uniqure-e…
uniQure dürften heute stark im Plus starten. Vorbörslich +40%.
Antwort auf Beitrag Nr.: 49.501.475 von SLGramann am 06.04.15 14:03:25

Antwort auf Beitrag Nr.: 49.501.475 von SLGramann am 06.04.15 14:03:25Einstieg mal wieder verpasst 

Antwort auf Beitrag Nr.: 49.502.102 von Fruehrentner am 06.04.15 16:37:27"Einstieg mal wieder verpasst"
Geht mir auch so.
Der Witz ist, dass ich auch heute nicht hätte kaufen können, was ich zur Börseneröffnung vielleicht getan hätte.
Denn beim S-Broker (wie ipollit bin ich - jedenfalls seit der Finanzkrise - tatsächlich bei der Sparkasse... ) werden heute keine US-Orders ausgeführt. Auch keine Online-Orders. Das finde ich mal so richtig scheiße und das war mir bisher auch nicht bewusst.
) werden heute keine US-Orders ausgeführt. Auch keine Online-Orders. Das finde ich mal so richtig scheiße und das war mir bisher auch nicht bewusst.
Kann jemand sagen, wie das bei Consors ist? Oder der comdirect?
Geht mir auch so.
Der Witz ist, dass ich auch heute nicht hätte kaufen können, was ich zur Börseneröffnung vielleicht getan hätte.
Denn beim S-Broker (wie ipollit bin ich - jedenfalls seit der Finanzkrise - tatsächlich bei der Sparkasse...
 ) werden heute keine US-Orders ausgeführt. Auch keine Online-Orders. Das finde ich mal so richtig scheiße und das war mir bisher auch nicht bewusst.
) werden heute keine US-Orders ausgeführt. Auch keine Online-Orders. Das finde ich mal so richtig scheiße und das war mir bisher auch nicht bewusst.Kann jemand sagen, wie das bei Consors ist? Oder der comdirect?
Spark Therapeutics, Inc. focuses on the development of gene therapy products for patients suffering from debilitating genetic diseases.
The company is developing SPK-RPE65, which is in Phase III clinical trial for the treatment of inherited retinal dystrophies, a group of rare blinding conditions caused by non-sex linked, or autosomal recessive, mutations in the RPE65 gene.
It is also developing SPK-CHM for the treatment of choroideremia; and preclinical programs in development for the treatment of hemophilia A and neurodegenerative diseases, as well as a pipeline of product candidates targeting rare blinding conditions.
The company has collaboration agreement with Pfizer, Inc. for the development and commercialization of SPK-FIX product candidates in its gene therapy program for the treatment of hemophilia B. Spark Therapeutics, Inc. was founded in 2013 and is based in Philadelphia, Pennsylvania
http://www.sparktx.com
Nasdaq Symbol: ONCE
The company is developing SPK-RPE65, which is in Phase III clinical trial for the treatment of inherited retinal dystrophies, a group of rare blinding conditions caused by non-sex linked, or autosomal recessive, mutations in the RPE65 gene.
It is also developing SPK-CHM for the treatment of choroideremia; and preclinical programs in development for the treatment of hemophilia A and neurodegenerative diseases, as well as a pipeline of product candidates targeting rare blinding conditions.
The company has collaboration agreement with Pfizer, Inc. for the development and commercialization of SPK-FIX product candidates in its gene therapy program for the treatment of hemophilia B. Spark Therapeutics, Inc. was founded in 2013 and is based in Philadelphia, Pennsylvania
http://www.sparktx.com
Nasdaq Symbol: ONCE
Antwort auf Beitrag Nr.: 49.497.434 von SLGramann am 05.04.15 08:11:25@SLGramann
Könntest Du bitte bei Gelegenheit 1 oder 2 Fundstellen für die von Dir angesprochenen kritischen Stellungnahmen für CLDN hier reinstellen? Das wäre klasse und vielen Dank dafür. Ich bin nämlich noch dabei und muß jetzt bald eine Entscheidung treffen...
Könntest Du bitte bei Gelegenheit 1 oder 2 Fundstellen für die von Dir angesprochenen kritischen Stellungnahmen für CLDN hier reinstellen? Das wäre klasse und vielen Dank dafür. Ich bin nämlich noch dabei und muß jetzt bald eine Entscheidung treffen...
Antwort auf Beitrag Nr.: 49.502.102 von Fruehrentner am 06.04.15 16:37:27
Werte wo man sich im Nachhinein ärgert "oooch verpasst" sind es meistens nicht wert
wenn man sich nicht vorher drauf vorbereiten konnte -Worüber ärgert man sich dann eigentlich genau?
Zitat von Fruehrentner: Einstieg mal wieder verpasst
Werte wo man sich im Nachhinein ärgert "oooch verpasst" sind es meistens nicht wert
wenn man sich nicht vorher drauf vorbereiten konnte -Worüber ärgert man sich dann eigentlich genau?
Antwort auf Beitrag Nr.: 49.502.807 von lawmeetstax am 06.04.15 19:03:07Hi,
ein Beispiel wäre hier:
http://www.ozgurogut.com/thoughts/2015/1/20/gene-therapy-for…
Unschön fand ich auch das hier:

Vergleiche mal die Imbalance zwischen der Placebo-Gruppe und der High-Verum Gruppe (CUPID1).
Bspw. "Ischemic heart Disease, aber auch andere baselines. Da würde ich sagen: Kein großes Wunder, dass die Verum-Gruppe besser abschneidet?
Andererseits haben sie halt den BT-Status - trotz allem.
Sehr schwierig. Sehr, sehr hohes Risiko. Auch sehr, sehr viel Potential nach oben, wenns klappt.
Leute fragen heute zurecht: Warum geht BMS mit QURE und nicht mit CLDN im Kardio-Bereich?
ein Beispiel wäre hier:
http://www.ozgurogut.com/thoughts/2015/1/20/gene-therapy-for…
Unschön fand ich auch das hier:

Vergleiche mal die Imbalance zwischen der Placebo-Gruppe und der High-Verum Gruppe (CUPID1).
Bspw. "Ischemic heart Disease, aber auch andere baselines. Da würde ich sagen: Kein großes Wunder, dass die Verum-Gruppe besser abschneidet?
Andererseits haben sie halt den BT-Status - trotz allem.
Sehr schwierig. Sehr, sehr hohes Risiko. Auch sehr, sehr viel Potential nach oben, wenns klappt.
Leute fragen heute zurecht: Warum geht BMS mit QURE und nicht mit CLDN im Kardio-Bereich?
CLVS:
Clovis Oncology Receives Breakthrough Therapy Designation for Rucaparib for Monotherapy Treatment of Advanced Ovarian Cancer in Patients with BRCA-mutated Tumors
http://finance.yahoo.com/news/clovis-oncology-receives-break…
Eine weitere Breakthrough Designation für Clovis. Und wie sie stolz schreiben: Rucaparib ist der "Only PARP inhibitor to receive Breakthrough Therapy designation".
ADAP:
Adaptimmune bereitet das IPO vor. Ein Unternehmen, das man im Auge behalten sollte.
http://www.sec.gov/Archives/edgar/data/1621227/0001047469150…
Clovis Oncology Receives Breakthrough Therapy Designation for Rucaparib for Monotherapy Treatment of Advanced Ovarian Cancer in Patients with BRCA-mutated Tumors
http://finance.yahoo.com/news/clovis-oncology-receives-break…
Eine weitere Breakthrough Designation für Clovis. Und wie sie stolz schreiben: Rucaparib ist der "Only PARP inhibitor to receive Breakthrough Therapy designation".
ADAP:
Adaptimmune bereitet das IPO vor. Ein Unternehmen, das man im Auge behalten sollte.
http://www.sec.gov/Archives/edgar/data/1621227/0001047469150…
Antwort auf Beitrag Nr.: 49.503.647 von SLGramann am 06.04.15 21:21:56@SLGramann
Besten Dank für Deine schnelle Antwort!
Hinsichtlich BMS habe ich mir die Frage bis jetzt eher einfach beantwortet und halte dies auch weiterhin für richtig: BMS wollte einen Teileinstieg, also einen Fuß in der Tür. Bei CLDN sind aber schon Novartis und Pfizer beteiligt. BMS hätte bei CLDN also schlicht nicht das bekommen, was sie gesucht haben.
Kennst Du den Backround von Ozgur Ogut? Ich konnte dazu nichts finden...
Auf den ersten Blick scheinen seine zahlreichen sehr kritischen Beiträge durchaus fundiert und insbesondere detailverliebt zu sein, was ich grundsätzlich sehr schätze. Allerdings stört mich ein wenig, daß der Eindruck vermittelt wird, viele andere seien nicht in der Lage, offen erkennbare Widersprüche richtig zu deuten. Als Beispiel für diese gewisse Überheblichkeit möchte ich verweisen auf seine Bemerkung, daß der CEO angeblich im CC durch die Blume kundgetan hätte, CLDN könne vorher "entblinden". So unterstellt er dem CEO gewiß eine gehörige Portion Naivität.
Die von Dir aufgezeigten unterschiedlichen Ausgangssituationen der Studienteilnehmer sind auch für mich bemerkenswert! Das erinnert mich ein bißchen an den letzten Herbst bei CLDX, dort hat die FDA aber auch Breakthrough Status gewährt.
Nach allem: ich bleibe weiterhin an Board, die aktuelle Renaissance der Gentherapie und das große Interesse von Pfizer und Novartis sind für mich wichtige Indikatoren.
@ipolli
Du hattest hier Anfang des Jahres mal auf Deine Beobachtung TRIL hingewiesen. Seither deutlich über 100%. Hat sich Deine Einschätzung zu diesem Wert weiter geschärft?
Besten Dank für Deine schnelle Antwort!
Hinsichtlich BMS habe ich mir die Frage bis jetzt eher einfach beantwortet und halte dies auch weiterhin für richtig: BMS wollte einen Teileinstieg, also einen Fuß in der Tür. Bei CLDN sind aber schon Novartis und Pfizer beteiligt. BMS hätte bei CLDN also schlicht nicht das bekommen, was sie gesucht haben.
Kennst Du den Backround von Ozgur Ogut? Ich konnte dazu nichts finden...
Auf den ersten Blick scheinen seine zahlreichen sehr kritischen Beiträge durchaus fundiert und insbesondere detailverliebt zu sein, was ich grundsätzlich sehr schätze. Allerdings stört mich ein wenig, daß der Eindruck vermittelt wird, viele andere seien nicht in der Lage, offen erkennbare Widersprüche richtig zu deuten. Als Beispiel für diese gewisse Überheblichkeit möchte ich verweisen auf seine Bemerkung, daß der CEO angeblich im CC durch die Blume kundgetan hätte, CLDN könne vorher "entblinden". So unterstellt er dem CEO gewiß eine gehörige Portion Naivität.
Die von Dir aufgezeigten unterschiedlichen Ausgangssituationen der Studienteilnehmer sind auch für mich bemerkenswert! Das erinnert mich ein bißchen an den letzten Herbst bei CLDX, dort hat die FDA aber auch Breakthrough Status gewährt.
Nach allem: ich bleibe weiterhin an Board, die aktuelle Renaissance der Gentherapie und das große Interesse von Pfizer und Novartis sind für mich wichtige Indikatoren.
@ipolli
Du hattest hier Anfang des Jahres mal auf Deine Beobachtung TRIL hingewiesen. Seither deutlich über 100%. Hat sich Deine Einschätzung zu diesem Wert weiter geschärft?
ICPT:
Nomura mit einer Meinung (Kursziel sind 440 Dollar):

Den Satz mit dem Upside-Potential zu den 7 Milliarden geschätzten Peak-Sales, falls die Konkurrenz weiter schwächelt, muss man sich mal zu Gemüte führen.
Das klingt alles so extrem, dass man es eigentlich als dummes Zeug abtun möchte, aber vermutlich ist es das nicht...
Nomura mit einer Meinung (Kursziel sind 440 Dollar):

Den Satz mit dem Upside-Potential zu den 7 Milliarden geschätzten Peak-Sales, falls die Konkurrenz weiter schwächelt, muss man sich mal zu Gemüte führen.
Das klingt alles so extrem, dass man es eigentlich als dummes Zeug abtun möchte, aber vermutlich ist es das nicht...
Antwort auf Beitrag Nr.: 49.506.656 von lawmeetstax am 07.04.15 11:38:54"Kennst Du den Backround von Ozgur Ogut?"
hier schreibt er... http://investorshub.advfn.com/boards/read_msg.aspx?message_i… "I've worked hands-on with AAV (serotype 9), and I know from first hand experience that the doses CLDN is using in humans are high doses for a rat...
***
Zu TRIL... leider bin ich nicht dabei. TRIL arbeitet im Bereich CD47... ein "Don't eat me"-Signal der Krebszellen. Ich bin mir immer noch nicht so sicher (habe mich bisher allerdings auch nicht weiter eingelesen), wie ich TRIL bewerten soll. CD47 könnte ein sehr heißes IO-Target werden... u.a. CELG ist hier aktiv: http://www.techinvestingdaily.com/articles/celgenes-nasdaq-c… "Celgene's (NASDAQ: CELG) $500 Million Cancer Bet". Die meisten sind aber CD47-AKs, während TRIL es mit einem SIRPα fusion protein versucht. SIRPα ist das Gegenstück zu CD47, das Fusion Protein ist kein kompletter AK, sondern quasi nur ein Stückchen davon, das ebenfalls CD47 binden und blockieren kann. AKs sollen wohl zielgerichteter sein und damit wirksamer sein. Ein Problem könnten aber Nebenwirkungen werden, wenn das CD47-Mittel auch an gesunden Zellen bindet. Hier behauptet TRIL Vorteile zu besitzen.
Insgesamt ist es ein interessanter Bereich, der aber noch recht früh in der Entwicklung ist (z.B. TRIL ist nicht nicht in PI)und so das Nutzen/Schaden-Profil bisher recht unklar ist.
Gruß
ipollit
hier schreibt er... http://investorshub.advfn.com/boards/read_msg.aspx?message_i… "I've worked hands-on with AAV (serotype 9), and I know from first hand experience that the doses CLDN is using in humans are high doses for a rat...
***
Zu TRIL... leider bin ich nicht dabei. TRIL arbeitet im Bereich CD47... ein "Don't eat me"-Signal der Krebszellen. Ich bin mir immer noch nicht so sicher (habe mich bisher allerdings auch nicht weiter eingelesen), wie ich TRIL bewerten soll. CD47 könnte ein sehr heißes IO-Target werden... u.a. CELG ist hier aktiv: http://www.techinvestingdaily.com/articles/celgenes-nasdaq-c… "Celgene's (NASDAQ: CELG) $500 Million Cancer Bet". Die meisten sind aber CD47-AKs, während TRIL es mit einem SIRPα fusion protein versucht. SIRPα ist das Gegenstück zu CD47, das Fusion Protein ist kein kompletter AK, sondern quasi nur ein Stückchen davon, das ebenfalls CD47 binden und blockieren kann. AKs sollen wohl zielgerichteter sein und damit wirksamer sein. Ein Problem könnten aber Nebenwirkungen werden, wenn das CD47-Mittel auch an gesunden Zellen bindet. Hier behauptet TRIL Vorteile zu besitzen.
Insgesamt ist es ein interessanter Bereich, der aber noch recht früh in der Entwicklung ist (z.B. TRIL ist nicht nicht in PI)und so das Nutzen/Schaden-Profil bisher recht unklar ist.
Gruß
ipollit
arry:
Recht ermutigend für den MEK/BRAF Kombo-Ansatz:
meiner Meinung nach noch nicht hoch eingepreist bei arry.
First Reported Case of Six-Year Survival for Patient With Metastatic Lung Cancer and Rare Genetic Mutation
Results of Targeted, Combination Drug Therapy That Extends Survival
Published in Journal of Cancer Prevention & Current Research
April 07, 2015 10:00 ET | Source: Author Mitchell Gaynor
"Targeting specific genetic mutations with enhanced drug therapy that works on the genetic level is the hope offered by ecogenetic medicine," Dr. Mitchell Gaynor
NEW YORK, April 7, 2015 (GLOBE NEWSWIRE) -- The patient, a 54-year-old male with metastatic lung cancer that had spread to his brain, liver, and bone and a very rare genetic mutation, continues to thrive because of targeted, combination drug therapy that works through epigenetic means and was introduced in his treatment plan three years ago. His case, treated at Gaynor Integrative Oncology in New York, is reported in the current issue of the Journal of Cancer Prevention and Current Research (Vol 2 Issue 3), the first reported clinical case study about the extended survival rate of a patient with this profile.
Dr. Mitchell Gaynor, renowned integrative oncologist and author of the forthcoming book from Viking, The Gene Therapy Plan - Taking Control of Your Genetic Destiny with Diet and Lifestyle (to be released by Viking April 21), is lead author of the paper. Dr. Gaynor is Assistant Clinical Professor Medicine at the College, writes daily for www.genechanger.com, and is a frequent contributor to other publications and media outlets. In the paper, he outlines the targeted epigenetic therapy for this patient who is a non-smoker with Stage 4 lung cancer and a mutation of the BRAF gene which is usually found only in a type of skin cancer called melanoma.
This case is particularly compelling since mortality from metastatic lung cancer is greater than the combined mortality of the next three most common forms of cancer (breast, colon, and pancreatic). Given the high mortality rate and the reported resistance to BRAF inhibition therapy, this case represents a breakthrough analysis of a new drug treatment plan that offers huge potential for extending life for patients with a similar molecular profile.
The patient was originally diagnosed in 2008 and was treated with several chemotherapy regimens but developed progressive disease in the brain, bone, liver and lung. Molecular profiling subsequently confirmed a mutation in BRAF V600E, and he was treated with BRAF inhibitor, Dabrafenib. After initial positive response to Dabrafenib, significant disease progression was indicated by PET/CT and MRI and the patient was determined to have developed resistance to this drug. The patient was subsequently treated with a regimen co-targeting BRAF and MEK with Vemurafenib and Trametinib, drugs also usually used only for melanoma patients.
"Targeting specific genetic mutations with enhanced drug therapy that works on the genetic level is the hope offered by ecogenetic medicine," Dr. Gaynor comments. "Because of medicine's evolution into treatment that targets the functioning of tumor promoting and suppressing genes, there is hope of longer, more vibrant lives for all cancer patients. This case is a stunning example of the efficacy of targeted gene therapy treatment."
The conclusion of this clinical case study highlights the efficacy of targeted therapy in patients with cancer of the lung with BRAF mutations and the importance of molecular profiling in modern oncology. Since there is a high probability that patients will develop resistance to BRAF inhibition therapy, this breakthrough case study suggests the importance of examining new combinations of alternative BRAF inhibitors combined with MEK inhibition for malignancies other than melanoma.
Recht ermutigend für den MEK/BRAF Kombo-Ansatz:
meiner Meinung nach noch nicht hoch eingepreist bei arry.
First Reported Case of Six-Year Survival for Patient With Metastatic Lung Cancer and Rare Genetic Mutation
Results of Targeted, Combination Drug Therapy That Extends Survival
Published in Journal of Cancer Prevention & Current Research
April 07, 2015 10:00 ET | Source: Author Mitchell Gaynor
"Targeting specific genetic mutations with enhanced drug therapy that works on the genetic level is the hope offered by ecogenetic medicine," Dr. Mitchell Gaynor
NEW YORK, April 7, 2015 (GLOBE NEWSWIRE) -- The patient, a 54-year-old male with metastatic lung cancer that had spread to his brain, liver, and bone and a very rare genetic mutation, continues to thrive because of targeted, combination drug therapy that works through epigenetic means and was introduced in his treatment plan three years ago. His case, treated at Gaynor Integrative Oncology in New York, is reported in the current issue of the Journal of Cancer Prevention and Current Research (Vol 2 Issue 3), the first reported clinical case study about the extended survival rate of a patient with this profile.
Dr. Mitchell Gaynor, renowned integrative oncologist and author of the forthcoming book from Viking, The Gene Therapy Plan - Taking Control of Your Genetic Destiny with Diet and Lifestyle (to be released by Viking April 21), is lead author of the paper. Dr. Gaynor is Assistant Clinical Professor Medicine at the College, writes daily for www.genechanger.com, and is a frequent contributor to other publications and media outlets. In the paper, he outlines the targeted epigenetic therapy for this patient who is a non-smoker with Stage 4 lung cancer and a mutation of the BRAF gene which is usually found only in a type of skin cancer called melanoma.
This case is particularly compelling since mortality from metastatic lung cancer is greater than the combined mortality of the next three most common forms of cancer (breast, colon, and pancreatic). Given the high mortality rate and the reported resistance to BRAF inhibition therapy, this case represents a breakthrough analysis of a new drug treatment plan that offers huge potential for extending life for patients with a similar molecular profile.
The patient was originally diagnosed in 2008 and was treated with several chemotherapy regimens but developed progressive disease in the brain, bone, liver and lung. Molecular profiling subsequently confirmed a mutation in BRAF V600E, and he was treated with BRAF inhibitor, Dabrafenib. After initial positive response to Dabrafenib, significant disease progression was indicated by PET/CT and MRI and the patient was determined to have developed resistance to this drug. The patient was subsequently treated with a regimen co-targeting BRAF and MEK with Vemurafenib and Trametinib, drugs also usually used only for melanoma patients.
"Targeting specific genetic mutations with enhanced drug therapy that works on the genetic level is the hope offered by ecogenetic medicine," Dr. Gaynor comments. "Because of medicine's evolution into treatment that targets the functioning of tumor promoting and suppressing genes, there is hope of longer, more vibrant lives for all cancer patients. This case is a stunning example of the efficacy of targeted gene therapy treatment."
The conclusion of this clinical case study highlights the efficacy of targeted therapy in patients with cancer of the lung with BRAF mutations and the importance of molecular profiling in modern oncology. Since there is a high probability that patients will develop resistance to BRAF inhibition therapy, this breakthrough case study suggests the importance of examining new combinations of alternative BRAF inhibitors combined with MEK inhibition for malignancies other than melanoma.
Antwort auf Beitrag Nr.: 49.497.434 von SLGramann am 05.04.15 08:11:25Wer hat noch was?
ENTA: Heute schon einige Studienergebnisse zu HEP C auf der EASL:
http://www.thestreet.com/story/13105130/1/merck-faces-hep-c-…
Es ist zwar kein Studienergebnis aber fast schon ein "binary event", wenn ABBVIE die Quartalszahlen und Umsätze von V-Pak veröffentlicht.
OTIC:
https://pbs.twimg.com/media/CBU-945VAAEeRuc.jpg
BLUE:
Hier werden wohl im Juni erste Ergebnisse zur Sichelzellenanämie kommen. So wie ich es verstehe wären positive Ergebnisse hier eine große Sache.
SG kmastra
ENTA: Heute schon einige Studienergebnisse zu HEP C auf der EASL:
http://www.thestreet.com/story/13105130/1/merck-faces-hep-c-…
Es ist zwar kein Studienergebnis aber fast schon ein "binary event", wenn ABBVIE die Quartalszahlen und Umsätze von V-Pak veröffentlicht.
OTIC:
https://pbs.twimg.com/media/CBU-945VAAEeRuc.jpg
BLUE:
Hier werden wohl im Juni erste Ergebnisse zur Sichelzellenanämie kommen. So wie ich es verstehe wären positive Ergebnisse hier eine große Sache.
SG kmastra
uniQure nutzt die Gunst der Stunde und führt eine KE über ca. 100 Mio. Dollar durch:
Amsterdam, the Netherlands, April 7, 2015 – uniQure N.V. (NASDAQ: QURE), a leader in human gene therapy, today announced that it has commenced a follow-on public offering of 3,000,000 of its ordinary shares. All ordinary shares to be sold in the offering will be offered by uniQure. In addition, uniQure intends to grant the underwriters a 30-day option to purchase up to an additional 450,000 ordinary shares.
Zusammen mit dem BMS-Deal hat uniQure jetzt mal eben 200 Mio. organisiert.
Damit sollte es möglich sein, die Entwicklung der Pipeline zu beschleunigen. Das Unternehmen behauptet ja, eine Art Modulsystem zu haben, mit dem man relativ schnell neue Targets adressieren könne.
Ich habe mich dann auch mal - besser spät als nie? - an QURE beteiligt.
Amsterdam, the Netherlands, April 7, 2015 – uniQure N.V. (NASDAQ: QURE), a leader in human gene therapy, today announced that it has commenced a follow-on public offering of 3,000,000 of its ordinary shares. All ordinary shares to be sold in the offering will be offered by uniQure. In addition, uniQure intends to grant the underwriters a 30-day option to purchase up to an additional 450,000 ordinary shares.
Zusammen mit dem BMS-Deal hat uniQure jetzt mal eben 200 Mio. organisiert.
Damit sollte es möglich sein, die Entwicklung der Pipeline zu beschleunigen. Das Unternehmen behauptet ja, eine Art Modulsystem zu haben, mit dem man relativ schnell neue Targets adressieren könne.
Ich habe mich dann auch mal - besser spät als nie? - an QURE beteiligt.
Antwort auf Beitrag Nr.: 49.506.656 von lawmeetstax am 07.04.15 11:38:54CLDN:
noch etwas zur CUPID-Debatte:

noch etwas zur CUPID-Debatte:

Antwort auf Beitrag Nr.: 49.536.161 von SLGramann am 10.04.15 13:14:03@SLGramann
Sehr informativ, danke! Alles sehr ungewiß...
Nur schade, daß dort der Einfluß des Base Case auf die Kursentwicklung nicht eingeschätzt wird.
Sehr informativ, danke! Alles sehr ungewiß...
Nur schade, daß dort der Einfluß des Base Case auf die Kursentwicklung nicht eingeschätzt wird.
Antwort auf Beitrag Nr.: 49.537.679 von lawmeetstax am 10.04.15 15:30:25
Ich würde die Kursziele aber nicht zu ernst nehmen. Nach oben dürfte m.E. mehr Luft sein - theoretisch...
Vor allem weiß ich aber nicht, ob man eine Wahrscheinlichkeit von 70% für einen positiven Ausgang veranschlagen sollte.
Finde ich persönlich viel zu optimistisch.

Ich würde die Kursziele aber nicht zu ernst nehmen. Nach oben dürfte m.E. mehr Luft sein - theoretisch...

Vor allem weiß ich aber nicht, ob man eine Wahrscheinlichkeit von 70% für einen positiven Ausgang veranschlagen sollte.
Finde ich persönlich viel zu optimistisch.
Sage und Marinus - starker Text von Hammer:
http://www.orf-blog.com/sage-and-marinus-not-the-typical-cns…
http://www.orf-blog.com/sage-and-marinus-not-the-typical-cns…
CLVS:
Goldman Sachs mit neuem Kursziel von 117 Dollar:

Es klingt sicher klugscheißerisch, aber ich kann nicht so recht nachvollziehen, warum Markt und Analysten so langsam waren und eigentlich immer noch sind.
Das Rociletinib wahrscheinlich in einem Jahr zugelassen sein wird und dass es wahrscheinlich Umsätze zwischen 1 und 2 Milliarden Dollar erreichen kann, ist ja nicht neu.
Wir werden sehen, was die ASCO bringt, aber wenn nichts überraschend negatives passiert, bleibt CLVS einfach auf Kurs mit einem künftigen Blockbuster.
Eine Marktkapitalisierung von unter 2 Milliarden Dollar - wie wir sie bspw. im Dezember noch hatten - passt doch da nicht ins Bild.
Wenn mit Rociletinib alles perfekt laufen würde, würde allein dieses Programm CLVS langfristig wohl auf mehr als 10 Mrd. Dollar Marktkap. befördern. Vom ja nicht gerade unattraktiven "Rest" der Pipeline ist dabei noch keine Rede.
Goldman Sachs mit neuem Kursziel von 117 Dollar:

Es klingt sicher klugscheißerisch, aber ich kann nicht so recht nachvollziehen, warum Markt und Analysten so langsam waren und eigentlich immer noch sind.
Das Rociletinib wahrscheinlich in einem Jahr zugelassen sein wird und dass es wahrscheinlich Umsätze zwischen 1 und 2 Milliarden Dollar erreichen kann, ist ja nicht neu.
Wir werden sehen, was die ASCO bringt, aber wenn nichts überraschend negatives passiert, bleibt CLVS einfach auf Kurs mit einem künftigen Blockbuster.
Eine Marktkapitalisierung von unter 2 Milliarden Dollar - wie wir sie bspw. im Dezember noch hatten - passt doch da nicht ins Bild.
Wenn mit Rociletinib alles perfekt laufen würde, würde allein dieses Programm CLVS langfristig wohl auf mehr als 10 Mrd. Dollar Marktkap. befördern. Vom ja nicht gerade unattraktiven "Rest" der Pipeline ist dabei noch keine Rede.
Antwort auf Beitrag Nr.: 49.553.300 von SLGramann am 13.04.15 18:13:43Es klingt sicher klugscheißerisch, aber ich kann nicht so recht nachvollziehen, warum Markt und Analysten so langsam waren und eigentlich immer noch sind.
Ich finde das Timing auch etwas merkwürdig, denn was hat sich bei Roci denn in letzter Zeit geändert? Zudem wird Ruca da jetzt nicht in die Überlegungen mit einbezogen?! Wie kommt man da jetzt also auf ein Kursziel von 117 (von 68!)
Aber ich will mich gar nicht beschweren und denke auch, dass die Analyse noch weiter ging als das was da jetzt über Twitter gepostet wurde. Hier noch ein weiterer Ausschnitt:

Interessant finde ich, dass GS sogar einen Übernahmekurs von 179$ sieht. Eine Übernahme ist doch auch hier sehr wahrscheinlich von daher...
Hier noch was JPM zu CLVS schreibt. Die ASCO wird sicherlich spannend!

Was den Gesamtmarkt betrifft sieht es ja auch wieder ganz gut aus.

Trotzdem noch ein Video zum Thema Blase oder Boom mit einigen vernünftigen Argumenten:
SG kmastra
Ich finde das Timing auch etwas merkwürdig, denn was hat sich bei Roci denn in letzter Zeit geändert? Zudem wird Ruca da jetzt nicht in die Überlegungen mit einbezogen?! Wie kommt man da jetzt also auf ein Kursziel von 117 (von 68!)
Aber ich will mich gar nicht beschweren und denke auch, dass die Analyse noch weiter ging als das was da jetzt über Twitter gepostet wurde. Hier noch ein weiterer Ausschnitt:

Interessant finde ich, dass GS sogar einen Übernahmekurs von 179$ sieht. Eine Übernahme ist doch auch hier sehr wahrscheinlich von daher...
Hier noch was JPM zu CLVS schreibt. Die ASCO wird sicherlich spannend!

Was den Gesamtmarkt betrifft sieht es ja auch wieder ganz gut aus.
Trotzdem noch ein Video zum Thema Blase oder Boom mit einigen vernünftigen Argumenten:
SG kmastra
INCY ist heute ebenfalls deutlich im Plus... langsam werden sie zu einem weiter BigCap unter den Biotechs mit aktuell bereits 17 Mrd USD.

zuletzt habe ich weiter KPTI und ACAD aufgestockt... letztere könnten meiner Meinung nach auch ein 10+ Mrd USD Unternehmen werden, wenn Nuplazid sich so entwickelt wie erhofft. Peak Sales könnten bei 5+ oder 10+ Mrd USD p.a. liegen... nicht schlecht, wenn man die alleinigen Rechte hält.
Bezüglich möglichen Blockbustern in Marktnähe könnten auch RCPT und PTLA interessant sein. Kommentare zu RCPT fand ich früher leider nicht so überzeugend... inzwischen scheint Ozanimod aber doch sehr aussichtsreich zu sein... möglicherweise ebenfalls 5++ Mrd USD peak sales in MS, IBD&Co: http://www.thestreet.com/story/13060528/1/biotech-stock-mail… FXa-Hemmer wie Bayers Xarelto sind ja jetzt bereits Blockbuster... wohl ein zukünftiger 10+ Mrd USD Markt. PTLA hat mit Andexanet alfa das einzige Mittel, das die Blutverdünnung von FXa-Hemmern umkehren kann, um z.B. kurzfristige Operationen durchführen zu können. Zudem besitzt PTLA einen eigenen FXa-Hemmer mit möglicherweisen besseren Wirkprofil für eine breitere Anwendung.


AERI heute auch mit einem schönen Kursplus auf ein neues ATH...

Gruß
ipollit
zuletzt habe ich weiter KPTI und ACAD aufgestockt... letztere könnten meiner Meinung nach auch ein 10+ Mrd USD Unternehmen werden, wenn Nuplazid sich so entwickelt wie erhofft. Peak Sales könnten bei 5+ oder 10+ Mrd USD p.a. liegen... nicht schlecht, wenn man die alleinigen Rechte hält.
Bezüglich möglichen Blockbustern in Marktnähe könnten auch RCPT und PTLA interessant sein. Kommentare zu RCPT fand ich früher leider nicht so überzeugend... inzwischen scheint Ozanimod aber doch sehr aussichtsreich zu sein... möglicherweise ebenfalls 5++ Mrd USD peak sales in MS, IBD&Co: http://www.thestreet.com/story/13060528/1/biotech-stock-mail… FXa-Hemmer wie Bayers Xarelto sind ja jetzt bereits Blockbuster... wohl ein zukünftiger 10+ Mrd USD Markt. PTLA hat mit Andexanet alfa das einzige Mittel, das die Blutverdünnung von FXa-Hemmern umkehren kann, um z.B. kurzfristige Operationen durchführen zu können. Zudem besitzt PTLA einen eigenen FXa-Hemmer mit möglicherweisen besseren Wirkprofil für eine breitere Anwendung.
AERI heute auch mit einem schönen Kursplus auf ein neues ATH...
Gruß
ipollit
Aerie:
RBC mit einem Kursziel von 50$


Rest platzsparend:
https://twitter.com/CashRocket/status/588559205214199809/pho…
https://twitter.com/CashRocket/status/588559277247172608/pho…
https://twitter.com/CashRocket/status/588559538887872513/pho…
https://twitter.com/CashRocket/status/588559832875040768/pho…
https://twitter.com/CashRocket/status/588560046885249024/pho…
https://twitter.com/CashRocket/status/588560269200138240/pho…
https://twitter.com/CashRocket/status/588560441313394688/pho…
https://twitter.com/CashRocket/status/588560606573105152/pho…
Leider ohne M&A Kursziel!
SG kmastra
RBC mit einem Kursziel von 50$


Rest platzsparend:
https://twitter.com/CashRocket/status/588559205214199809/pho…
https://twitter.com/CashRocket/status/588559277247172608/pho…
https://twitter.com/CashRocket/status/588559538887872513/pho…
https://twitter.com/CashRocket/status/588559832875040768/pho…
https://twitter.com/CashRocket/status/588560046885249024/pho…
https://twitter.com/CashRocket/status/588560269200138240/pho…
https://twitter.com/CashRocket/status/588560441313394688/pho…
https://twitter.com/CashRocket/status/588560606573105152/pho…
Leider ohne M&A Kursziel!
SG kmastra
CLVS:
Brutal starke Daten von AstraZenca:
AstraZeneca's ($AZN) in-development lung cancer pill extended survival by more than a year in new Phase II data, a positive sign for a drug the company believes can bring in $3 billion in annual sales at its peak.
The treatment, AZD9291, charted a median progression-free survival of 13.5 months in patients with non-small cell lung cancer and EGFR mutations. The updated data come from AstraZeneca's ongoing Phase II study on nearly 300 patients, besting the 9.6-month PFS rate the company reported last fall. The drug also clocked a 54% overall response rate and a median duration of response of 12.4 months, AstraZeneca said.
http://www.fiercebiotech.com/story/astrazenecas-3b-lung-canc…
Da wird in den nächsten Wochen wohl einiges an Unsicherheit im Markt sein, ob CLVS da mithalten kann...
Brutal starke Daten von AstraZenca:
AstraZeneca's ($AZN) in-development lung cancer pill extended survival by more than a year in new Phase II data, a positive sign for a drug the company believes can bring in $3 billion in annual sales at its peak.
The treatment, AZD9291, charted a median progression-free survival of 13.5 months in patients with non-small cell lung cancer and EGFR mutations. The updated data come from AstraZeneca's ongoing Phase II study on nearly 300 patients, besting the 9.6-month PFS rate the company reported last fall. The drug also clocked a 54% overall response rate and a median duration of response of 12.4 months, AstraZeneca said.
http://www.fiercebiotech.com/story/astrazenecas-3b-lung-canc…
Da wird in den nächsten Wochen wohl einiges an Unsicherheit im Markt sein, ob CLVS da mithalten kann...
Antwort auf Beitrag Nr.: 49.555.274 von ipollit am 13.04.15 22:31:17"Kommentare zu RCPT fand ich früher leider nicht so überzeugend... inzwischen scheint Ozanimod aber doch sehr aussichtsreich zu sein... möglicherweise ebenfalls 5++ Mrd USD peak sales in MS, IBD&Co"
RCPT hatte ich bisher absolut nicht auf dem Schirm. Alles, was ich seit Deinem Beitrag über sie gelesen habe, klingt aber wirklich spannend...
Bspw.:

RCPT hatte ich bisher absolut nicht auf dem Schirm. Alles, was ich seit Deinem Beitrag über sie gelesen habe, klingt aber wirklich spannend...
Bspw.:

arry:
FDA Grants AstraZeneca's Selumetinib Orphan Drug Status for Treatment of Uveal Melanoma --Update
By Dow Jones Business News, April 17, 2015, 06:25:00 AM EDT
By Razak Musah Baba
LONDON--AstraZeneca PLC's (AZN.LN) selumetinib drug has been granted a special status by the U.S. Food and Drug Administration for treatment of Uveal melanoma, a rare eye disease.
The biopharmaceutical firm said Friday the FDA has granted 'Orphan' drug status to selumetinib for the treatment of Uveal melanoma, a rare disease in which cancer cells form in the tissues of the eye.
The 'Orphan' status is granted to drugs and biologics intended for the safe and effective treatment, diagnosis or prevention of rare diseases or disorders that affect fewer than 200,000 people in the U.S.
AstraZeneca acquired exclusive worldwide rights to selumetinib from Array BioPharma Inc in 2003.
Selumetinib, inhibits the MEK pathway -- a chain of communication proteins -- in cancer cells to prevent the tumor from growing.
AstraZeneca also said Friday that data from a phase III study evaluating selumetinib in combination with chemotherapy in patients with first-line metastatic uveal melanoma is expected to be available later this year.
In addition to uveal melanoma, selumetinib is being investigated in Phase III studies in KRAS mutation positive lung cancer and thyroid cancer and in Phase II in children with neurofibromatosis Type 1, the company added.
At 1005 GMT AstraZeneca shares traded up 9 pence, or 0.1% higher, at GBP48.43, valuing the FTSE 100 pharmaceutical company at GBP61.15 billion.
Write to Razak Musah Baba at razak.baba@wsj.com; Twitter: @Raztweet
Subscribe to WSJ: http://online.wsj.com?mod=djnwires
Read more: http://www.nasdaq.com/article/fda-grants-astrazenecas-selume…
FDA Grants AstraZeneca's Selumetinib Orphan Drug Status for Treatment of Uveal Melanoma --Update
By Dow Jones Business News, April 17, 2015, 06:25:00 AM EDT
By Razak Musah Baba
LONDON--AstraZeneca PLC's (AZN.LN) selumetinib drug has been granted a special status by the U.S. Food and Drug Administration for treatment of Uveal melanoma, a rare eye disease.
The biopharmaceutical firm said Friday the FDA has granted 'Orphan' drug status to selumetinib for the treatment of Uveal melanoma, a rare disease in which cancer cells form in the tissues of the eye.
The 'Orphan' status is granted to drugs and biologics intended for the safe and effective treatment, diagnosis or prevention of rare diseases or disorders that affect fewer than 200,000 people in the U.S.
AstraZeneca acquired exclusive worldwide rights to selumetinib from Array BioPharma Inc in 2003.
Selumetinib, inhibits the MEK pathway -- a chain of communication proteins -- in cancer cells to prevent the tumor from growing.
AstraZeneca also said Friday that data from a phase III study evaluating selumetinib in combination with chemotherapy in patients with first-line metastatic uveal melanoma is expected to be available later this year.
In addition to uveal melanoma, selumetinib is being investigated in Phase III studies in KRAS mutation positive lung cancer and thyroid cancer and in Phase II in children with neurofibromatosis Type 1, the company added.
At 1005 GMT AstraZeneca shares traded up 9 pence, or 0.1% higher, at GBP48.43, valuing the FTSE 100 pharmaceutical company at GBP61.15 billion.
Write to Razak Musah Baba at razak.baba@wsj.com; Twitter: @Raztweet
Subscribe to WSJ: http://online.wsj.com?mod=djnwires
Read more: http://www.nasdaq.com/article/fda-grants-astrazenecas-selume…
ACAD
Sind die Peak-Sales Schätzungen der Analysten zu Nuplazid in PDP (Psychosen infolge von Parkinson) nicht sehr konservativ?
Aus den folgenden Kommentaren kann man doch einige Zahlen zu PDP herauslesen:
- 1 Mio Parkinson-Patienten (zumeist ältere Menschen) in den USA
- von Analysten geschätzte 33% mit PDP, Ärzte halten aber auch 40-60% für möglich
- geschätzer Preis nach Zulassung 15T USD... möglich wäre aber auch 18T
- mögliche jährliche Preissteigerung 5%
- Nuplazid wäre das einzige zugelassene Medikament gegen PDP
- Alternativen erhöhen Sterblichkeit (black box warnings) und wirken der Parkinson-Behandlung entgegen
- PDP ist gravierend, mit hohen Kosten verbunden und aktuell schlecht behandelbar => hoher medizinischer Bedarf
D.h...
- es gibt in den USA zwischen 330T und 600T PDP-Patienten
- der Preis liegt in 2021 bei ca. 19T bis 23T USD
Bei hohem Bedarf und ohne echte Alternativen müssten doch auch viele PDP-Patienten mit Nuplazid behandelt werden...
Bei 80% in 2021 wären das dann US-Umsätze zwischen 5 Mrd USD und 11 Mrd USD alleine in PDP.
Die weltweiten Umsätze könnten doppelt so hoch ausfallen.
Desweiteren könnte Nuplazid auch gegen Psychosen infolge von Alzheimer (ADP) zum Einsatz kommen. Hier wäre das Umsatz-Potential noch größer als bei PDP.
Sollten die Nuplazid-Umsätze auch nur annähernd in solche Bereiche kommen, wäre dagegen die aktuelle MK von 3,9 Mrd USD recht bescheiden. Mir ist so auch nicht ganz klar, warum Ohad Hammer ACAD für uninteressant hält.



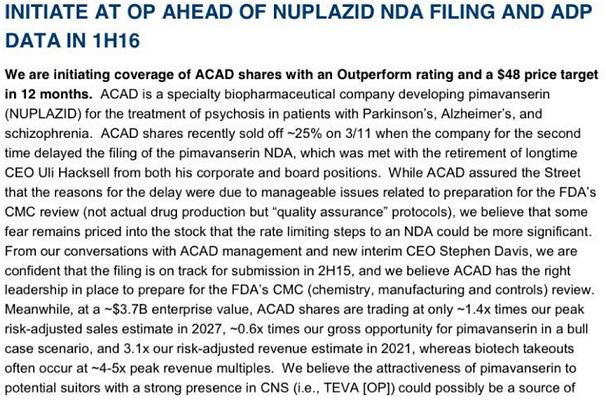


Hier noch etwas zur NDA-Problematik...



Gruß
ipollit
Sind die Peak-Sales Schätzungen der Analysten zu Nuplazid in PDP (Psychosen infolge von Parkinson) nicht sehr konservativ?
Aus den folgenden Kommentaren kann man doch einige Zahlen zu PDP herauslesen:
- 1 Mio Parkinson-Patienten (zumeist ältere Menschen) in den USA
- von Analysten geschätzte 33% mit PDP, Ärzte halten aber auch 40-60% für möglich
- geschätzer Preis nach Zulassung 15T USD... möglich wäre aber auch 18T
- mögliche jährliche Preissteigerung 5%
- Nuplazid wäre das einzige zugelassene Medikament gegen PDP
- Alternativen erhöhen Sterblichkeit (black box warnings) und wirken der Parkinson-Behandlung entgegen
- PDP ist gravierend, mit hohen Kosten verbunden und aktuell schlecht behandelbar => hoher medizinischer Bedarf
D.h...
- es gibt in den USA zwischen 330T und 600T PDP-Patienten
- der Preis liegt in 2021 bei ca. 19T bis 23T USD
Bei hohem Bedarf und ohne echte Alternativen müssten doch auch viele PDP-Patienten mit Nuplazid behandelt werden...
Bei 80% in 2021 wären das dann US-Umsätze zwischen 5 Mrd USD und 11 Mrd USD alleine in PDP.
Die weltweiten Umsätze könnten doppelt so hoch ausfallen.
Desweiteren könnte Nuplazid auch gegen Psychosen infolge von Alzheimer (ADP) zum Einsatz kommen. Hier wäre das Umsatz-Potential noch größer als bei PDP.
Sollten die Nuplazid-Umsätze auch nur annähernd in solche Bereiche kommen, wäre dagegen die aktuelle MK von 3,9 Mrd USD recht bescheiden. Mir ist so auch nicht ganz klar, warum Ohad Hammer ACAD für uninteressant hält.






Hier noch etwas zur NDA-Problematik...


Gruß
ipollit
ESPR
ESPR dürfte langfristig noch einiges an Potential besitzen...


Gruß
ipollit
ESPR dürfte langfristig noch einiges an Potential besitzen...

Gruß
ipollit
CLDX
Präklinische Daten zur Kombination von CLDX Varlilumab mit PD1 sehen nicht schlecht aus... allerdings sind Maus-Modelle nicht immer so aussagekräftig. Mal schauen, wie die ersten P1-Daten ausfallen werden.


Gruß
ipollit
Präklinische Daten zur Kombination von CLDX Varlilumab mit PD1 sehen nicht schlecht aus... allerdings sind Maus-Modelle nicht immer so aussagekräftig. Mal schauen, wie die ersten P1-Daten ausfallen werden.

Gruß
ipollit
ENTA:
ABBVIE heute mit Zahlen. V-Pak hatte im Q1 Umsätze von 238 Mio $. Schätzungen gingen wohl von etwas mehr aus. ABBVIE hat aber die etwas schwammige Vorhersage 3 Milliarden exit runrate bekräftigt. Das wären 750 Mio Umsatz in Q4.
ESPR:
Esperion kann heute von der bereits geposteten Empfehlung profitieren. Ergänzend dazu:

Aeri:
Jemand hat mal die Fakten zu Rhopressa/Rocket 1 zusammengetragen. Lesenswert!
https://docs.google.com/document/d/1YqJwEsCiXGvPULvtXnpiMSnx…
SG kmastra
ABBVIE heute mit Zahlen. V-Pak hatte im Q1 Umsätze von 238 Mio $. Schätzungen gingen wohl von etwas mehr aus. ABBVIE hat aber die etwas schwammige Vorhersage 3 Milliarden exit runrate bekräftigt. Das wären 750 Mio Umsatz in Q4.
ESPR:
Esperion kann heute von der bereits geposteten Empfehlung profitieren. Ergänzend dazu:

Aeri:
Jemand hat mal die Fakten zu Rhopressa/Rocket 1 zusammengetragen. Lesenswert!
https://docs.google.com/document/d/1YqJwEsCiXGvPULvtXnpiMSnx…
SG kmastra
CLDN
Die Spekulationen reißen ja nicht ab in diesen Tagen, der Kurs ist regelrecht zusammengesackt.
Zusätzlich zu all den spannenden gegenläufigen Lesarten der CUPID 1 Ergebnisse hier vielleicht ebenso interessant eine erste positive Aussage eines an CUPID 2 angeblich beteiligten Arztes Dr. Lyon aus England vom 10. Februar 2015
https://perseengage.files.wordpress.com/2015/02/heart-failur…
Der interessanteste Teil kommt ganz am Schluß.
Ob das so nun glaubhaft ist...ich weiß es nicht.
Die Spekulationen reißen ja nicht ab in diesen Tagen, der Kurs ist regelrecht zusammengesackt.
Zusätzlich zu all den spannenden gegenläufigen Lesarten der CUPID 1 Ergebnisse hier vielleicht ebenso interessant eine erste positive Aussage eines an CUPID 2 angeblich beteiligten Arztes Dr. Lyon aus England vom 10. Februar 2015
https://perseengage.files.wordpress.com/2015/02/heart-failur…
Der interessanteste Teil kommt ganz am Schluß.
Ob das so nun glaubhaft ist...ich weiß es nicht.
AERI:
Rocket 1 ist gescheitert!
RhopressaTM did not meet its primary efficacy endpoint of demonstrating non-inferiority of IOP lowering for RhopressaTM compared to twice-daily timolol, based upon IOP measurements at the end of week 2, week 6 and day 90.
http://finance.yahoo.com/news/aerie-pharmaceuticals-reports-…
Sehr übel. Sehr heftiger Rückschlag.
Rocket 1 ist gescheitert!
RhopressaTM did not meet its primary efficacy endpoint of demonstrating non-inferiority of IOP lowering for RhopressaTM compared to twice-daily timolol, based upon IOP measurements at the end of week 2, week 6 and day 90.
http://finance.yahoo.com/news/aerie-pharmaceuticals-reports-…
Sehr übel. Sehr heftiger Rückschlag.
Bitter! Aeri PIII schon heute die Ergebnisse bekannt und die sind denkbar schlecht!
http://finance.yahoo.com/news/aerie-pharmaceuticals-reports-…
http://finance.yahoo.com/news/aerie-pharmaceuticals-reports-…
Antwort auf Beitrag Nr.: 49.632.719 von kmastra am 23.04.15 22:11:57Nachbörslich -70%...
Hier ein Artikel, der die Sache zusammenfasst:
http://www.xconomy.com/new-york/2015/04/23/aerie-craters-as-…
Ich bin mir noch nicht im klaren, wie ich weiter verfahre. Der Verlust ist erst mal da. Aber Rhopressa muss noch nicht vollkommen tot sein. Eine gewisse Wirkung ist da. Ein neuer MOA ist es auch. Und als Kombiwirkstoff Roclatan mag es vielleicht zulassungsfähig/verkäuflich sein. Allerdings wird sich wohl nun auch die Roclactan-Entwicklung verzögern.
Viele offene Fragen...
Hier ein Artikel, der die Sache zusammenfasst:
http://www.xconomy.com/new-york/2015/04/23/aerie-craters-as-…
Ich bin mir noch nicht im klaren, wie ich weiter verfahre. Der Verlust ist erst mal da. Aber Rhopressa muss noch nicht vollkommen tot sein. Eine gewisse Wirkung ist da. Ein neuer MOA ist es auch. Und als Kombiwirkstoff Roclatan mag es vielleicht zulassungsfähig/verkäuflich sein. Allerdings wird sich wohl nun auch die Roclactan-Entwicklung verzögern.
Viele offene Fragen...
IPH.PA
AZN steigt groß bei IPH2201 ein, u.a. als Kombi mit ihrem PD1-AK: 250 Mio Upfront, 1 Mrd USD Milestones, double digit royalties (?), aber immerhin Option auf 50:50 in Europa

Gruß
ipollit
AZN steigt groß bei IPH2201 ein, u.a. als Kombi mit ihrem PD1-AK: 250 Mio Upfront, 1 Mrd USD Milestones, double digit royalties (?), aber immerhin Option auf 50:50 in Europa
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.633.658 von SLGramann am 24.04.15 07:25:51
So ganz klar ist mir auch noch nicht, was ich mache. Es ist kompliziert. Zu Ende scheint auch mir die Entwicklung noch nicht. Viel hängt wohl auch davon ab, wie dringend eine neue Option benötigt wird und wie man sich mit der FDA einig wird. Auf dem derzeitigen Niveau werde ich wohl eher nicht verkaufen und auf eine Erholung setzen. Mit dem Kursziel von 27$ könnte ich natürlich gut leben....

Zitat von SLGramann: Nachbörslich -70%...
Hier ein Artikel, der die Sache zusammenfasst:
http://www.xconomy.com/new-york/2015/04/23/aerie-craters-as-…
Ich bin mir noch nicht im klaren, wie ich weiter verfahre. Der Verlust ist erst mal da. Aber Rhopressa muss noch nicht vollkommen tot sein. Eine gewisse Wirkung ist da. Ein neuer MOA ist es auch. Und als Kombiwirkstoff Roclatan mag es vielleicht zulassungsfähig/verkäuflich sein. Allerdings wird sich wohl nun auch die Roclactan-Entwicklung verzögern.
Viele offene Fragen...
So ganz klar ist mir auch noch nicht, was ich mache. Es ist kompliziert. Zu Ende scheint auch mir die Entwicklung noch nicht. Viel hängt wohl auch davon ab, wie dringend eine neue Option benötigt wird und wie man sich mit der FDA einig wird. Auf dem derzeitigen Niveau werde ich wohl eher nicht verkaufen und auf eine Erholung setzen. Mit dem Kursziel von 27$ könnte ich natürlich gut leben....

Antwort auf Beitrag Nr.: 49.633.898 von ipollit am 24.04.15 08:13:14Hallo ipollit,
du hast ja auch noch eine kleine Position IMMU, wie ich gesehen habe. Die letzten Nachrichten und die Finanzierung klangen ja ganz gut. Irgendwie hatt die niemand auf dem Schirm, trotz dass sie schon lange im Bereich ADC aktiv sind, insbs. IMMU-130 und IMMU-132. Oder übersehe ich irgendetwas
Über ein kurzes Statement würde ich mich freuen. Innate war/ist ja auch ein weitere Top-Empfehlung/Vorstellung von dir, über die ich mich heute sehr gefreut habe. Für die Tolle Arbeit und die echt guten und ausführlichen Berichte zu einzelnen Werten ein großes Danke von mir. Natürlich auch an die anderen fleißigen Schreiber im Board.
PHILADELPHIA, April 20, 2015 (GLOBE NEWSWIRE) -- Immunomedics, Inc., (IMMU) today announced that, in a mid-stage clinical study, a multitude of patients with late stage solid cancers showed significant and durable tumor shrinkage after receiving treatments with sacituzumab govitecan, the Company's lead antibody-directed chemotherapeutic agent in development. These include patients with metastatic triple-negative breast cancer whose cancers after treatment were no longer detected by computed tomography, a test commonly used to find and locate tumors, and to measure a patient's treatment response.
"All of these patients had failed many prior therapies for their cancers and were running out of options before being treated with sacituzumab govitecan," stated Dr. Alexander N. Starodub of the Indiana Health Center for Cancer Care, Goshen, Indiana, one of the Principal Investigators. "In this respect, we are very encouraged with the responses we are reporting at this year's Annual Meeting of the American Association for Cancer Research, especially in light of the fact that this novel agent is given to patients as a monotherapy, and not part of a drug cocktail. I believe sacituzumab govitecan has the potential to become a viable alternative for treating patients with advanced, metastatic solid cancers if these results are confirmed in a late-stage clinical trial," added Dr. Starodub.
At the time of analysis, a total of 184 patients with many different advanced, metastatic cancers were enrolled into the study. Dr. Starodub's oral presentation focused on interim responses from 130 patients having these four major solid cancer types: breast, lung, esophageal, and colorectal.
For patients with triple-negative breast cancer, 26% showed objective response to sacituzumab govitecan, with 2 having a complete disappearance of their tumors, or complete response, and 10 showing a 30% or better tumor reduction, which qualified them as partial responders in accordance with the rules set by the Response Evaluation Criteria In Solid Tumors (RECIST 1.1). Including patients with responses between less than 30% tumor shrinkage and less than 20% tumor increase, which are considered stable disease, the disease control rate was 74%. At present, 21 of these patients are continuing therapy.
Cancer Types (N*) Objective Response** Disease Control
Triple-Negative Breast (46) (2+10) (26%) 34 (74%)
Non-Small Cell Lung (19) 6 (32%) 14 (74%)
Small Cell Lung (20) 6 (30%) 11 (55%)
Esophageal (16) 2 (13%) 9 (56%)
* N represents the number of patients that are evaluable at this time for treatment response.
** Except with triple-negative breast cancer (2 patients with complete response), all objective responses are partial responses.
In lung cancer, the objective response rates were 32% and 30% for non-small-cell and small-cell lung cancers, respectively, and disease control rates were 74% and 55%, respectively. "These results compare very favorably to all other agents used in this disease and setting," commented Dr. Starodub. For the 18 patients with advanced cancer of the esophagus enrolled into the study, 16 were assessable for response, having an objective response rate of 13% and a disease control rate of 44%.
Also reported were results on 29 patients with colorectal cancer in early assessments of survival. The median length of time living without the disease getting worse from the beginning of their sacituzumab govitecan treatments was 3.9 months. The median length of survival from the start of treatment was 18.0 months. "These are very encouraging preliminary results for patients who had a median of 4 prior therapies for metastatic colorectal cancer, some as many as 8," remarked Dr. Starodub.
Commenting on these encouraging results, Ms. Cynthia L. Sullivan, President and Chief Executive Officer stated, "We are in discussion with FDA to formulate a registration pathway for sacituzumab govitecan to advance the agent to a Phase 3 registration trial." "We are completing the enrollment of additional patients with triple-negative breast cancer, non-small and small-cell lung cancers. Our ultimate goal is to develop the full potential of this important and valuable asset for the benefits of cancer patients by advancing it with a corporate partner," Ms. Sullivan concluded.
Sacituzumab govitecan was created by the Company for the therapy of solid cancers by selectively delivering the active anticancer drug, SN-38, to a target called TROP-2 that is produced in high amounts by cancer cells relative to normal tissues. These cancers include breast, lung, esophageal, stomach, colon, rectal, pancreatic, prostate, ovarian, urinary bladder, and uterine cancers.
SN-38 is formed in the body from irinotecan, a drug used in various combinations to treat patients with colorectal and other cancers. However, the process of converting irinotecan to the active SN-38 is inefficient, which lowers the efficacy of irinotecan. By attaching active SN-38 directly to a tumor-targeting antibody, as much as 136-times more SN-38 can be delivered directly to the tumor than when irinotecan is administered, without increasing the toxicity to the body at the same time.
Sacituzumab govitecan is well tolerated by patients. At the optimal doses of 8 and 10 mg/kg, only 7% of patients required having dosing delayed due to adverse reactions, while dose reductions were experienced in only 15-16% of patients. Grades 3 and 4 adverse events occurring in more than 5% of patients include fatigue (5%), neutropenia (24%), and anemia (6%). Irinotecan shows an increased incidence of severe diarrhea (38%), neutropenia (31%), and neutropenic fever (8%). Further, despite repeated injections, no patient produced any antibody against sacituzumab govitecan.
In addition to Dr. Starodub, other clinical investigators participated in this multicenter trial are Drs. Allyson J. Ocean, Linda T. Vahdat, Scott T. Tagawa, and Manish A. Shah, Weill Cornell Medical College, New York, NY; Dr. Aditya Bardia, Massachusetts General Hospital Cancer Center, Harvard Medical School, Boston, MA; Drs. Michael J. Guarino and Gregory A. Masters, Helen F. Graham Cancer Center & Research Institute, Newark, DE; Drs. Wells A. Messersmith and Jennifer S. Diamond, University of Colorado Cancer Center, Aurora, CO; Drs. Jordan Berlin and Ingrid A. Mayer, Vanderbilt-Ingra Cancer Center, Nashville, TN; Dr. Vincent J. Picozzi, Virginia Mason Cancer Center, Seattle, WA; and Drs. Sajeve S. Thomas and Rebecca Moroose, UF Health Cancer Center-Orlando Health, Orlando, FL.
About Immunomedics
Immunomedics is a clinical-stage biopharmaceutical company developing monoclonal antibody-based products for the targeted treatment of cancer, autoimmune disorders and other serious diseases. Immunomedics' advanced proprietary technologies allow the Company to create humanized antibodies that can be used either alone in unlabeled or "naked" form, or conjugated with radioactive isotopes, chemotherapeutics, cytokines or toxins. Using these technologies, Immunomedics has built a pipeline of nine clinical-stage product candidates. Immunomedics has an ongoing collaboration with UCB, S.A. (UCB), to whom the Company licensed epratuzumab for the treatment of all non-cancer indications worldwide. UCB expects Phase 3 data in systemic lupus erythematosus in the first half of 2015. Immunomedics is exploring epratuzumab in oncology in collaboration with independent cancer study groups. Immunomedics' most advanced candidate to which it retains worldwide rights for all indications is 90Y-clivatuzumab tetraxetan. The Company initiated a Phase 3 registration trial in January 2014 in patients with advanced pancreatic cancer and expects topline data in mid-2016. Immunomedics' portfolio of wholly owned product candidates also includes antibody-drug conjugates (ADCs) that are designed to deliver a specific payload of a chemotherapeutic directly to the tumor while reducing overall toxic effects that are usually found with conventional administration of these chemotherapeutic agents. Immunomedics' most advanced ADCs are sacituzumab govitecan (IMMU-132) and labetuzumab govitecan (IMMU-130), which are in Phase 2 trials for a number of solid tumors and metastatic colorectal cancer, respectively. Immunomedics also has a number of other product candidates that target solid tumors and hematologic malignancies, as well as other diseases, in various stages of clinical and pre-clinical development. These include bispecific antibodies targeting cancers and infectious diseases as T-cell redirecting immunotherapies, as well as bispecific antibodies for next-generation cancer and autoimmune disease therapies, created using its patented DOCK-AND-LOCK(R) protein conjugation technology. The Company believes that its portfolio of intellectual property, which includes approximately 267 active patents in the United States and more than 400 foreign patents, protects its product candidates and technologies. Immunomedics' strength in intellectual property has resulted in a top-8 ranking in the Biotechnology industry by the Patent Board for the 2014 fiscal year. For additional information on the Company, please visit its website at www.immunomedics.com. The information on its website does not, however, form a part of this press release.
du hast ja auch noch eine kleine Position IMMU, wie ich gesehen habe. Die letzten Nachrichten und die Finanzierung klangen ja ganz gut. Irgendwie hatt die niemand auf dem Schirm, trotz dass sie schon lange im Bereich ADC aktiv sind, insbs. IMMU-130 und IMMU-132. Oder übersehe ich irgendetwas

Über ein kurzes Statement würde ich mich freuen. Innate war/ist ja auch ein weitere Top-Empfehlung/Vorstellung von dir, über die ich mich heute sehr gefreut habe. Für die Tolle Arbeit und die echt guten und ausführlichen Berichte zu einzelnen Werten ein großes Danke von mir. Natürlich auch an die anderen fleißigen Schreiber im Board.
PHILADELPHIA, April 20, 2015 (GLOBE NEWSWIRE) -- Immunomedics, Inc., (IMMU) today announced that, in a mid-stage clinical study, a multitude of patients with late stage solid cancers showed significant and durable tumor shrinkage after receiving treatments with sacituzumab govitecan, the Company's lead antibody-directed chemotherapeutic agent in development. These include patients with metastatic triple-negative breast cancer whose cancers after treatment were no longer detected by computed tomography, a test commonly used to find and locate tumors, and to measure a patient's treatment response.
"All of these patients had failed many prior therapies for their cancers and were running out of options before being treated with sacituzumab govitecan," stated Dr. Alexander N. Starodub of the Indiana Health Center for Cancer Care, Goshen, Indiana, one of the Principal Investigators. "In this respect, we are very encouraged with the responses we are reporting at this year's Annual Meeting of the American Association for Cancer Research, especially in light of the fact that this novel agent is given to patients as a monotherapy, and not part of a drug cocktail. I believe sacituzumab govitecan has the potential to become a viable alternative for treating patients with advanced, metastatic solid cancers if these results are confirmed in a late-stage clinical trial," added Dr. Starodub.
At the time of analysis, a total of 184 patients with many different advanced, metastatic cancers were enrolled into the study. Dr. Starodub's oral presentation focused on interim responses from 130 patients having these four major solid cancer types: breast, lung, esophageal, and colorectal.
For patients with triple-negative breast cancer, 26% showed objective response to sacituzumab govitecan, with 2 having a complete disappearance of their tumors, or complete response, and 10 showing a 30% or better tumor reduction, which qualified them as partial responders in accordance with the rules set by the Response Evaluation Criteria In Solid Tumors (RECIST 1.1). Including patients with responses between less than 30% tumor shrinkage and less than 20% tumor increase, which are considered stable disease, the disease control rate was 74%. At present, 21 of these patients are continuing therapy.
Cancer Types (N*) Objective Response** Disease Control
Triple-Negative Breast (46) (2+10) (26%) 34 (74%)
Non-Small Cell Lung (19) 6 (32%) 14 (74%)
Small Cell Lung (20) 6 (30%) 11 (55%)
Esophageal (16) 2 (13%) 9 (56%)
* N represents the number of patients that are evaluable at this time for treatment response.
** Except with triple-negative breast cancer (2 patients with complete response), all objective responses are partial responses.
In lung cancer, the objective response rates were 32% and 30% for non-small-cell and small-cell lung cancers, respectively, and disease control rates were 74% and 55%, respectively. "These results compare very favorably to all other agents used in this disease and setting," commented Dr. Starodub. For the 18 patients with advanced cancer of the esophagus enrolled into the study, 16 were assessable for response, having an objective response rate of 13% and a disease control rate of 44%.
Also reported were results on 29 patients with colorectal cancer in early assessments of survival. The median length of time living without the disease getting worse from the beginning of their sacituzumab govitecan treatments was 3.9 months. The median length of survival from the start of treatment was 18.0 months. "These are very encouraging preliminary results for patients who had a median of 4 prior therapies for metastatic colorectal cancer, some as many as 8," remarked Dr. Starodub.
Commenting on these encouraging results, Ms. Cynthia L. Sullivan, President and Chief Executive Officer stated, "We are in discussion with FDA to formulate a registration pathway for sacituzumab govitecan to advance the agent to a Phase 3 registration trial." "We are completing the enrollment of additional patients with triple-negative breast cancer, non-small and small-cell lung cancers. Our ultimate goal is to develop the full potential of this important and valuable asset for the benefits of cancer patients by advancing it with a corporate partner," Ms. Sullivan concluded.
Sacituzumab govitecan was created by the Company for the therapy of solid cancers by selectively delivering the active anticancer drug, SN-38, to a target called TROP-2 that is produced in high amounts by cancer cells relative to normal tissues. These cancers include breast, lung, esophageal, stomach, colon, rectal, pancreatic, prostate, ovarian, urinary bladder, and uterine cancers.
SN-38 is formed in the body from irinotecan, a drug used in various combinations to treat patients with colorectal and other cancers. However, the process of converting irinotecan to the active SN-38 is inefficient, which lowers the efficacy of irinotecan. By attaching active SN-38 directly to a tumor-targeting antibody, as much as 136-times more SN-38 can be delivered directly to the tumor than when irinotecan is administered, without increasing the toxicity to the body at the same time.
Sacituzumab govitecan is well tolerated by patients. At the optimal doses of 8 and 10 mg/kg, only 7% of patients required having dosing delayed due to adverse reactions, while dose reductions were experienced in only 15-16% of patients. Grades 3 and 4 adverse events occurring in more than 5% of patients include fatigue (5%), neutropenia (24%), and anemia (6%). Irinotecan shows an increased incidence of severe diarrhea (38%), neutropenia (31%), and neutropenic fever (8%). Further, despite repeated injections, no patient produced any antibody against sacituzumab govitecan.
In addition to Dr. Starodub, other clinical investigators participated in this multicenter trial are Drs. Allyson J. Ocean, Linda T. Vahdat, Scott T. Tagawa, and Manish A. Shah, Weill Cornell Medical College, New York, NY; Dr. Aditya Bardia, Massachusetts General Hospital Cancer Center, Harvard Medical School, Boston, MA; Drs. Michael J. Guarino and Gregory A. Masters, Helen F. Graham Cancer Center & Research Institute, Newark, DE; Drs. Wells A. Messersmith and Jennifer S. Diamond, University of Colorado Cancer Center, Aurora, CO; Drs. Jordan Berlin and Ingrid A. Mayer, Vanderbilt-Ingra Cancer Center, Nashville, TN; Dr. Vincent J. Picozzi, Virginia Mason Cancer Center, Seattle, WA; and Drs. Sajeve S. Thomas and Rebecca Moroose, UF Health Cancer Center-Orlando Health, Orlando, FL.
About Immunomedics
Immunomedics is a clinical-stage biopharmaceutical company developing monoclonal antibody-based products for the targeted treatment of cancer, autoimmune disorders and other serious diseases. Immunomedics' advanced proprietary technologies allow the Company to create humanized antibodies that can be used either alone in unlabeled or "naked" form, or conjugated with radioactive isotopes, chemotherapeutics, cytokines or toxins. Using these technologies, Immunomedics has built a pipeline of nine clinical-stage product candidates. Immunomedics has an ongoing collaboration with UCB, S.A. (UCB), to whom the Company licensed epratuzumab for the treatment of all non-cancer indications worldwide. UCB expects Phase 3 data in systemic lupus erythematosus in the first half of 2015. Immunomedics is exploring epratuzumab in oncology in collaboration with independent cancer study groups. Immunomedics' most advanced candidate to which it retains worldwide rights for all indications is 90Y-clivatuzumab tetraxetan. The Company initiated a Phase 3 registration trial in January 2014 in patients with advanced pancreatic cancer and expects topline data in mid-2016. Immunomedics' portfolio of wholly owned product candidates also includes antibody-drug conjugates (ADCs) that are designed to deliver a specific payload of a chemotherapeutic directly to the tumor while reducing overall toxic effects that are usually found with conventional administration of these chemotherapeutic agents. Immunomedics' most advanced ADCs are sacituzumab govitecan (IMMU-132) and labetuzumab govitecan (IMMU-130), which are in Phase 2 trials for a number of solid tumors and metastatic colorectal cancer, respectively. Immunomedics also has a number of other product candidates that target solid tumors and hematologic malignancies, as well as other diseases, in various stages of clinical and pre-clinical development. These include bispecific antibodies targeting cancers and infectious diseases as T-cell redirecting immunotherapies, as well as bispecific antibodies for next-generation cancer and autoimmune disease therapies, created using its patented DOCK-AND-LOCK(R) protein conjugation technology. The Company believes that its portfolio of intellectual property, which includes approximately 267 active patents in the United States and more than 400 foreign patents, protects its product candidates and technologies. Immunomedics' strength in intellectual property has resulted in a top-8 ranking in the Biotechnology industry by the Patent Board for the 2014 fiscal year. For additional information on the Company, please visit its website at www.immunomedics.com. The information on its website does not, however, form a part of this press release.
Hallo, ich hab mal ne Frage in die Expertenrunde hier:
Ich habe durch den Kursanstieg von Morphosys inzwischen einen Depotanteil an dem Wert, der mir eigentlich zu viel Risiko ist. Ich würde also gern ein paar Aktien von Morphosys verkaufen und das Risiko streuen. Das einfachste wäre natürlich, in BB Biotech umzuschichten, ich habe aber auch schon Biotec-Fonds...und ein paar kleinere Werte, die ich hier entdeckt habe, mit wenig Geldeinsatz (wie damals auch Morphosys klein angefangen hat).
Interessanter fände ich aber ein großes Unternehmen, etwa Novartis oder Astrazeneca, die so viele Programme begleiten, dass man weniger abhängig von Einzelerfolgen ist. Was würdet Ihr da empfehlen, natürlich ohne Gewähr??
Das Unternehmen muss nicht mehr "billig" sein, sowas findet man wohl derzeit auch gar nicht, sondern wichtiger wäre mir, dass sie im Bereich Biotechnologie an vielen erfolverprechenden Programmen beteiligt sind. Es soll sozusagen das "Gegengewicht" zu Morphosys sein, das nicht so stark schwankt, daher auch keine 100 %-Chance mehr bietet, aber trotzdem noch Perspektive hat.
Ich habe durch den Kursanstieg von Morphosys inzwischen einen Depotanteil an dem Wert, der mir eigentlich zu viel Risiko ist. Ich würde also gern ein paar Aktien von Morphosys verkaufen und das Risiko streuen. Das einfachste wäre natürlich, in BB Biotech umzuschichten, ich habe aber auch schon Biotec-Fonds...und ein paar kleinere Werte, die ich hier entdeckt habe, mit wenig Geldeinsatz (wie damals auch Morphosys klein angefangen hat).
Interessanter fände ich aber ein großes Unternehmen, etwa Novartis oder Astrazeneca, die so viele Programme begleiten, dass man weniger abhängig von Einzelerfolgen ist. Was würdet Ihr da empfehlen, natürlich ohne Gewähr??
Das Unternehmen muss nicht mehr "billig" sein, sowas findet man wohl derzeit auch gar nicht, sondern wichtiger wäre mir, dass sie im Bereich Biotechnologie an vielen erfolverprechenden Programmen beteiligt sind. Es soll sozusagen das "Gegengewicht" zu Morphosys sein, das nicht so stark schwankt, daher auch keine 100 %-Chance mehr bietet, aber trotzdem noch Perspektive hat.
AERIE heute - 61 %
IPH heute +50 %
IPH heute +50 %
Antwort auf Beitrag Nr.: 49.633.658 von SLGramann am 24.04.15 07:25:51AERI
die ROCKET-1 PIII-Daten für Rhopressa sind leider sehr enttäuschend. So hatte z.B. Ohad Hammer für das gesamte PIII-Programm eine Erfolgswahrscheinlichkeit von 80% gesehen und das Vergleichsmittel Timolol (ein generischer Beta-Blocker) als niedrige Hürde bezeichnet, zumal Rhopressa für einen Erfolg der PIII nur vergleichbar wie Timolol wirken musste, nicht besser.
Besonders unschön finde ich den Drift-Effekt bei Rhopressa... der erwünschte Effekt auf den Augeninnendruck nimmt in der PIII mit der Zeit deutlich ab, während er für Timolol recht konstant bleibt. Dies ist sehr problematisch, da Rhopressa ja chronisch über sehr lange Zeit (theoretisch lebenslang) angewendet werden soll. Eine Begründung dafür, dass trotz generischer gut wirkender Mittel noch neue Mittel benötigt würden, ist ja gerade, dass bisherige Mittel nicht dauerhaft wirken. Sollte hier Rhopressa noch schlechter abschneiden?
Gemessen wurde der Augeninnendruck an drei verschiedenen Tagen... nach 2 Wochen, 6 Wochen und 3 Monaten (was ja im Vergleich einer langjährigen Anwendung immer noch nicht viel ist):
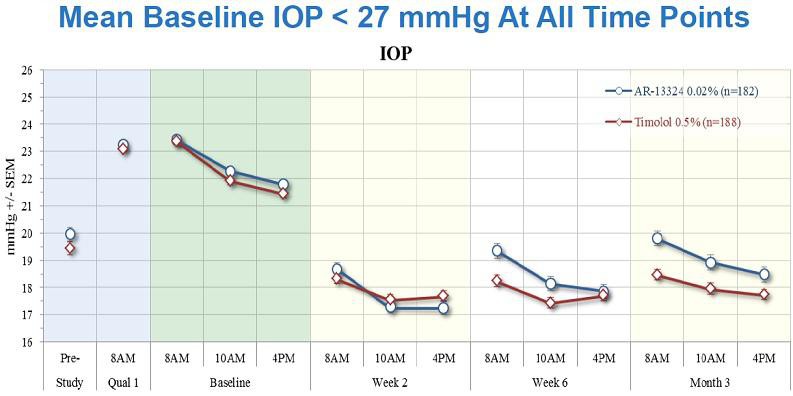
AERI behauptet, dass die Ergebnisse gegenüber Timolol besser und der Drift-Effekt weniger wäre, wenn man nur Patienten betrachtet, deren Druck vor der Behandlung nicht so hoch war, die also weniger gravierend bzw. noch nicht so lange erkrankt sind:
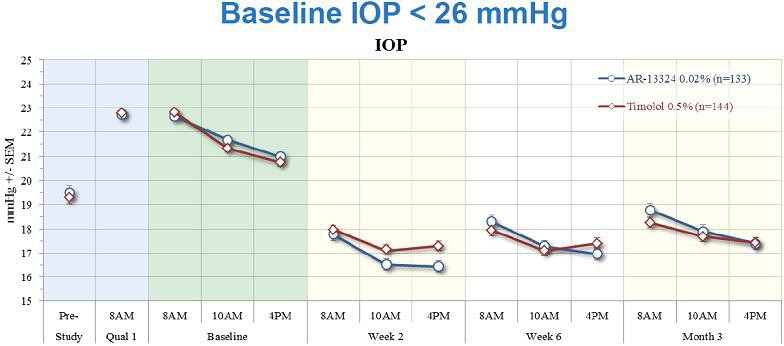
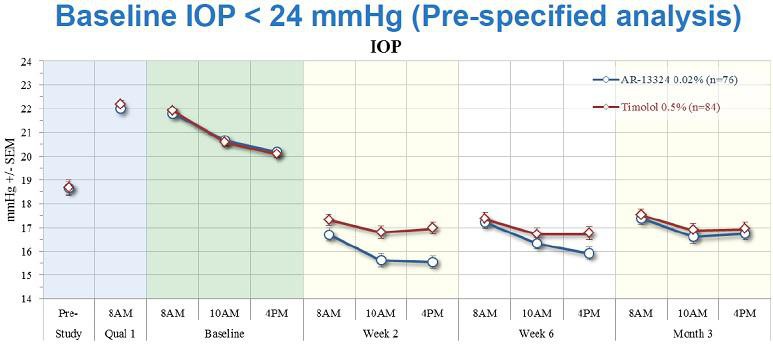
Das mag sein, doch ist der Drift Effekt meiner Meinung nach auch dann noch durchgehend vorhanden:
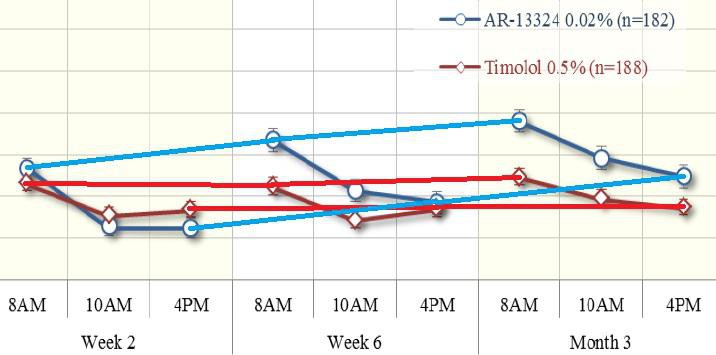
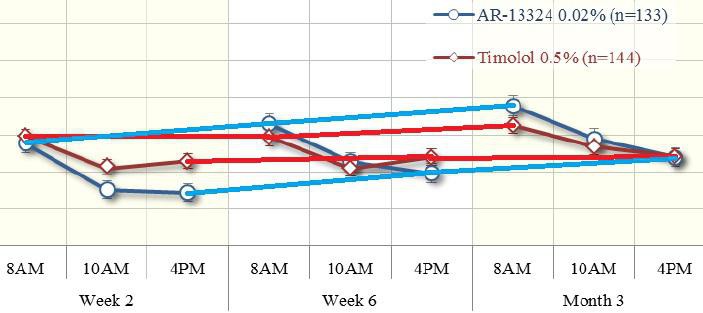
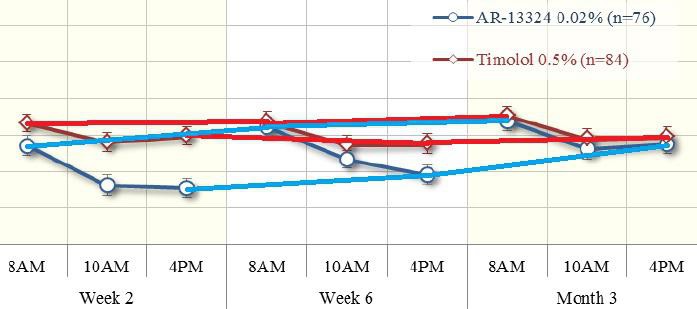

Im CC spricht AERI davon, dass bei einigen Patienten Rhopressa fast vollständig die Wirkung verliert, d.h. der Druck steigt auf Werte an, die vor der Behandlung vorgelegen haben. Die Erklärungen von AERI sind mir leider bisher nicht schlüssig. So könnte ein Ursache sein, dass insbesondere Patienten, die bereits lange krank sind, so schwerwiegende Veränderungen in dem Gewebe haben, auf das Rhopressa hauptsächlich wirkt, dass ein Flüssigkeitsabfluss darüber nicht mehr möglich ist. Dann müsste meiner Meinung nach aber die Wirkung durchgehend nicht vorhanden sein... am Anfang nach den ersten 2 Wochen ist die Wirkung aber im Durchschnitt okay.
AERI führt dann weiter an, dass vielleicht diese Patienten bei der ersten Untersuchung nach 2 Wochen einen so schlechten Augeninnendruck haben, dass sie danach Rhopressa kaum oder garnicht mehr einnehmen, weil sie von der Wirkung nicht mehr überzeugt sind. So könnte der komplette Wirkungsverlust zustande kommen.
Dann frage ich mich aber, warum diese Patienten die Studie nicht ganz abbrechen? Immerhin hat ja ein Teil der Patienten die Studie auch abgebrochen... in 7% aufgrund fehlernder Wirkung. Diese sind in der Augendruck-Bewertung nicht mehr enthalten.

Gruß
ipollit
die ROCKET-1 PIII-Daten für Rhopressa sind leider sehr enttäuschend. So hatte z.B. Ohad Hammer für das gesamte PIII-Programm eine Erfolgswahrscheinlichkeit von 80% gesehen und das Vergleichsmittel Timolol (ein generischer Beta-Blocker) als niedrige Hürde bezeichnet, zumal Rhopressa für einen Erfolg der PIII nur vergleichbar wie Timolol wirken musste, nicht besser.
Besonders unschön finde ich den Drift-Effekt bei Rhopressa... der erwünschte Effekt auf den Augeninnendruck nimmt in der PIII mit der Zeit deutlich ab, während er für Timolol recht konstant bleibt. Dies ist sehr problematisch, da Rhopressa ja chronisch über sehr lange Zeit (theoretisch lebenslang) angewendet werden soll. Eine Begründung dafür, dass trotz generischer gut wirkender Mittel noch neue Mittel benötigt würden, ist ja gerade, dass bisherige Mittel nicht dauerhaft wirken. Sollte hier Rhopressa noch schlechter abschneiden?
Gemessen wurde der Augeninnendruck an drei verschiedenen Tagen... nach 2 Wochen, 6 Wochen und 3 Monaten (was ja im Vergleich einer langjährigen Anwendung immer noch nicht viel ist):

AERI behauptet, dass die Ergebnisse gegenüber Timolol besser und der Drift-Effekt weniger wäre, wenn man nur Patienten betrachtet, deren Druck vor der Behandlung nicht so hoch war, die also weniger gravierend bzw. noch nicht so lange erkrankt sind:


Das mag sein, doch ist der Drift Effekt meiner Meinung nach auch dann noch durchgehend vorhanden:




Im CC spricht AERI davon, dass bei einigen Patienten Rhopressa fast vollständig die Wirkung verliert, d.h. der Druck steigt auf Werte an, die vor der Behandlung vorgelegen haben. Die Erklärungen von AERI sind mir leider bisher nicht schlüssig. So könnte ein Ursache sein, dass insbesondere Patienten, die bereits lange krank sind, so schwerwiegende Veränderungen in dem Gewebe haben, auf das Rhopressa hauptsächlich wirkt, dass ein Flüssigkeitsabfluss darüber nicht mehr möglich ist. Dann müsste meiner Meinung nach aber die Wirkung durchgehend nicht vorhanden sein... am Anfang nach den ersten 2 Wochen ist die Wirkung aber im Durchschnitt okay.
AERI führt dann weiter an, dass vielleicht diese Patienten bei der ersten Untersuchung nach 2 Wochen einen so schlechten Augeninnendruck haben, dass sie danach Rhopressa kaum oder garnicht mehr einnehmen, weil sie von der Wirkung nicht mehr überzeugt sind. So könnte der komplette Wirkungsverlust zustande kommen.
Dann frage ich mich aber, warum diese Patienten die Studie nicht ganz abbrechen? Immerhin hat ja ein Teil der Patienten die Studie auch abgebrochen... in 7% aufgrund fehlernder Wirkung. Diese sind in der Augendruck-Bewertung nicht mehr enthalten.

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.583.258 von kmastra am 16.04.15 21:18:33AERI
leider sieht es meiner Meinung nach noch schlechter aus, als gedacht. Den Punkt, dass die Wirkung von Rhopressa&Co mit der Zeit abnimmt, hatte ich bisher komplett übersehen.
Schon vor der PIII gab es ja offensichtlich bereits entsprechende Hinweise...

...


Ich wusste nicht, dass der ROCK/NET-Hemmer Rhopressa bei AERI bereits einen Vorgänger ROCK-Hemmer AR-12286 hatte, der angeblich genau aus diesen Gründen (mit der Zeit schwindende Wirkung) nicht in PIII gebracht wurde.
Im folgenden S1 kann man das auch nachlesen...
http://www.sec.gov/Archives/edgar/data/1337553/0001193125133…
Several companies have previously pursued ROCK inhibitors for ophthalmic use but to date no ROCK inhibitors have been approved and most of those companies have chosen to discontinue clinical development of their ROCK inhibitors. One of our ROCK inhibitors, AR-12286, was discontinued in the clinical stage of development due to an inability to maintain its effectiveness over time. In a 28-day Phase 2b clinical trial, AR-12286 lowered IOP by 6.7 mmHg on day seven, but lowered IOP by only 5.3 mmHg on day 28. This trend continued in a follow-up three-month study.As a result, in June 2013 we discontinued any further clinical development of AR-12286 and its fixed-dose combination product PG286. AR-13324 showed a 0.1 mmHg change in IOP from day seven to day 28 in our Phase 2b trial, and published clinical data for other ROCK inhibitors similarly have not shown a loss of efficacy over time. However, we have not previously conducted a three-month Phase 2b clinical trial for AR-13324, and therefore there can be no assurance as to the efficacy of AR-13324 beyond 28 days. In addition, our current product candidates remain subject to the risks associated with clinical drug development as indicated above.
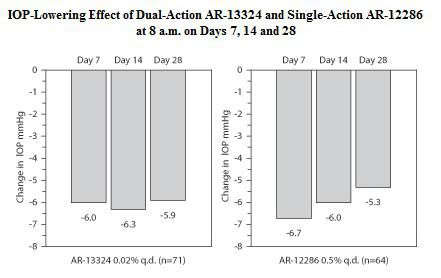
AR-13324 Comparison to AR-12286
We have analyzed our clinical and preclinical data for AR-13324, the lead candidate from our dual-action ROCK/NET inhibitor class, relative to our clinical and preclinical data for AR-12286, our single-action ROCK-selective compound that we were previously evaluating for further clinical development in addition to AR-13324. We conducted similarly designed 28-day Phase 2 clinical trials for each of AR-13324 and AR-12286, the comparative results of which are presented in the chart below. AR-13324 0.02% maintained stable efficacy on day 28 relative to day seven in its 28-day Phase 2 clinical trial. In contrast, AR-12286 0.5% lost 1.4 mmHg of IOP-lowering efficacy from day seven to day 28 in its 28-day Phase 2 clinical trial.
We subsequently completed a three-month Phase 2 clinical trial for AR-12286, for which data were available in June 2013. This trial confirmed the trend observed in the 28-day trial discussed above. In the three-month trial, the efficacy of AR-12286 continued to decline over the trial period such that it failed to meet its primary efficacy endpoint, non-inferiority to timolol.
So wie es jetzt für mich aussieht, scheint sich Rhopressa (AR-13324) aber nun genauso wie AR-12286 zu verhalten. Konsequenterweise müsste AERI nun ebenfalls die Entwicklung von Rhopressa sowie Roclatan einstellen.
Auf in der PII von Roclatan gibt es diesen Trend... Roclatan verliert seine Wirkung ebenso wie die beiden Rhopressa-Arme. Dagegen ist Latanoprost über den Zeitraum gleich wirksam bzw. gewinnt sogar noch leicht an Wirkung.
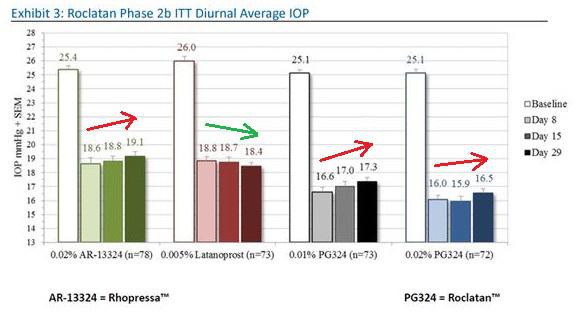
Wie bereits gesagt, müssen diese Mittel nicht 28 Tage oder 3 Monate genommen werden, sondern über viele viele Jahre. AERI muss meiner Meinung nach zuerst belegen, dass seine ROCK-Hemmer nicht dauerhaft an Wirkung verlieren, d.h. auch über deutlich längere Zeiträume als 3 Monate.
In diesem Zusammenhang ist soetwas auch bedenklich...
"Insider Selling: Aerie Pharmaceuticals Director Sells 425K in Stock on 4/15 average price of $33.64, for a total value of ~$14.3M $AERI"
Gruß
ipollit
leider sieht es meiner Meinung nach noch schlechter aus, als gedacht. Den Punkt, dass die Wirkung von Rhopressa&Co mit der Zeit abnimmt, hatte ich bisher komplett übersehen.
Schon vor der PIII gab es ja offensichtlich bereits entsprechende Hinweise...

...


Ich wusste nicht, dass der ROCK/NET-Hemmer Rhopressa bei AERI bereits einen Vorgänger ROCK-Hemmer AR-12286 hatte, der angeblich genau aus diesen Gründen (mit der Zeit schwindende Wirkung) nicht in PIII gebracht wurde.
Im folgenden S1 kann man das auch nachlesen...
http://www.sec.gov/Archives/edgar/data/1337553/0001193125133…
Several companies have previously pursued ROCK inhibitors for ophthalmic use but to date no ROCK inhibitors have been approved and most of those companies have chosen to discontinue clinical development of their ROCK inhibitors. One of our ROCK inhibitors, AR-12286, was discontinued in the clinical stage of development due to an inability to maintain its effectiveness over time. In a 28-day Phase 2b clinical trial, AR-12286 lowered IOP by 6.7 mmHg on day seven, but lowered IOP by only 5.3 mmHg on day 28. This trend continued in a follow-up three-month study.As a result, in June 2013 we discontinued any further clinical development of AR-12286 and its fixed-dose combination product PG286. AR-13324 showed a 0.1 mmHg change in IOP from day seven to day 28 in our Phase 2b trial, and published clinical data for other ROCK inhibitors similarly have not shown a loss of efficacy over time. However, we have not previously conducted a three-month Phase 2b clinical trial for AR-13324, and therefore there can be no assurance as to the efficacy of AR-13324 beyond 28 days. In addition, our current product candidates remain subject to the risks associated with clinical drug development as indicated above.

AR-13324 Comparison to AR-12286
We have analyzed our clinical and preclinical data for AR-13324, the lead candidate from our dual-action ROCK/NET inhibitor class, relative to our clinical and preclinical data for AR-12286, our single-action ROCK-selective compound that we were previously evaluating for further clinical development in addition to AR-13324. We conducted similarly designed 28-day Phase 2 clinical trials for each of AR-13324 and AR-12286, the comparative results of which are presented in the chart below. AR-13324 0.02% maintained stable efficacy on day 28 relative to day seven in its 28-day Phase 2 clinical trial. In contrast, AR-12286 0.5% lost 1.4 mmHg of IOP-lowering efficacy from day seven to day 28 in its 28-day Phase 2 clinical trial.
We subsequently completed a three-month Phase 2 clinical trial for AR-12286, for which data were available in June 2013. This trial confirmed the trend observed in the 28-day trial discussed above. In the three-month trial, the efficacy of AR-12286 continued to decline over the trial period such that it failed to meet its primary efficacy endpoint, non-inferiority to timolol.
So wie es jetzt für mich aussieht, scheint sich Rhopressa (AR-13324) aber nun genauso wie AR-12286 zu verhalten. Konsequenterweise müsste AERI nun ebenfalls die Entwicklung von Rhopressa sowie Roclatan einstellen.
Auf in der PII von Roclatan gibt es diesen Trend... Roclatan verliert seine Wirkung ebenso wie die beiden Rhopressa-Arme. Dagegen ist Latanoprost über den Zeitraum gleich wirksam bzw. gewinnt sogar noch leicht an Wirkung.

Wie bereits gesagt, müssen diese Mittel nicht 28 Tage oder 3 Monate genommen werden, sondern über viele viele Jahre. AERI muss meiner Meinung nach zuerst belegen, dass seine ROCK-Hemmer nicht dauerhaft an Wirkung verlieren, d.h. auch über deutlich längere Zeiträume als 3 Monate.
In diesem Zusammenhang ist soetwas auch bedenklich...
"Insider Selling: Aerie Pharmaceuticals Director Sells 425K in Stock on 4/15 average price of $33.64, for a total value of ~$14.3M $AERI"
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.590.809 von SLGramann am 17.04.15 17:21:05CLVS
"Brutal starke Daten von AstraZenca... Da wird in den nächsten Wochen wohl einiges an Unsicherheit im Markt sein, ob CLVS da mithalten kann"
Ob AZD9291 oder CLVS's Roci besser ist, muss man sehen. Meiner Meinung nach gibt es auch deutliche Unterschiede zwischen beiden Mitteln unabhängig von der Wirkung gegen 2nd-line NSCLC mit T790M.
Die EGFR-Hemmer Tarceva&Co sind ja der 1st-line Standard gegen EGFR-sensitiven NSCLC. Daran ändert Roci oder AZD9291 erstmal nichts. Tarceva hat 1st-line aber nur eine zeitlich begrenzte Wirkung... in ca. 50% kommt es unter der Anwendung der etablierten EGFR-Hemmer zur T790M Mutation bei der die bisherigen Hemmer unwirksam sind. D.h. der 2nd-line T790M-Markt ist auch recht groß. Daneben gibt es aber auch noch 50%, bei denen EGFR-Hemmer unwirksam werden, aber kein T790M vorliegt... T790M- EGFR. Bei T790M- EGFR könnte Roci z.B. über IGF1 wirksam sein... AZD9291 hat diese Wirkung bisher nicht gezeigt.
T790M EGFR NSCLC wird auch irgendwann gegen einen T790M-Hemmer wie Roci resistent. Eine Möglichkeit ist auch hier IGF1, so dass theoretisch Roci auf 2nd-line länger wirken könnte. Die aktuellen AZD9291 Daten sprechen allerdings schonmal für AZD9291... Roci muss hier nun nachlegen.
Ein ganz anderes Thema ist allerdings 1st-line. So Kommentare wie der folgende, dass die guten AZD9291 T790M-Ergebnisse für eine erfolgreiche 1st-line Anwendung sprechen würden, kann ich nicht nachvollziehen...

Roci&AZD9291 wurden speziell gegen diese Mutation entwickelt, die aber 1st-line so gut wie nicht vorkommt, sondern erst unter Anwendung eines "normalen" EGFR-Hemmer auftetetn kann. D.h. eine Wirkung gegen T790M sagt überhaupt nichts über die 1st-line Wirkung aus!
EGFR fördert in veränderter Form (mutiert, erhöht) den Krebs... EGF ist aber als wild-type EGF auch ein ganz normaler Signalstoff in gesunden Zellen. U.a. gibt es wt-EGFR in Hautzellen... eine Hemmung dort führt zu starken Hautrötungen (Rash) wie bei einer Entzündung.
Tarceva&Co hemmen auch wt-EGFR sehr stark, weshalb hier diese Nebenwirkungen auftreten. Roci&AZD9291 vesuchen wt-EGFR auszusparen. Roci macht das allerdings deutlich besser als AZD9291. Aufgrund von IGF1 wirkt Roci aber auch auf den Blutzucker, so dass es als Nebenwirkung zu einer Art Diabetes kommmt. Dagegen helfen normale T2-Diabetes-Mittel in Form von Tabletten. Vielleicht ist so eine Nebenwirkung, von der der Patient nichts merkt, subjektiv besser zu tolerieren als etwas, was man sieht und fühlt.
Hier sind z.B. die theoretschen Wirkungen von Tarceva (Erlotinib), Roci (CO-1686) und AZD9291 gegen verschiedene EGFR-Typen zusammengefasst. Je kleiner die Zahl, um so höher die Wirkung. Die ersten beiden Spalten sind 2nd-line T790M-Mutationen. L858R und Del sind typische 1st-line Mutationen. Daneben finden sich noch 2 WT-Typen... "epidermal" wahrscheinlich der in der Haut.
Wie man sieht, wirkt Tarceva nicht gegen T790M, aber gegen L858R, Del und WT etwa gleich stark... daher kommt es zu den entsprechenden Nebenwirkungen z.B. auf der Haut (Ratio jeweils 1).
Roci&AZD9291 wirken am meisten gegen T790M, weniger gegen L858R, Del und deutlich weniger gegen WT. Wie man sieht, wirkt Roci aber kaum gegen WT (sehr hohe Werte)... das Verhältnis von Wirkung zu EGFR-Nebenwirkung ist daher am besten.
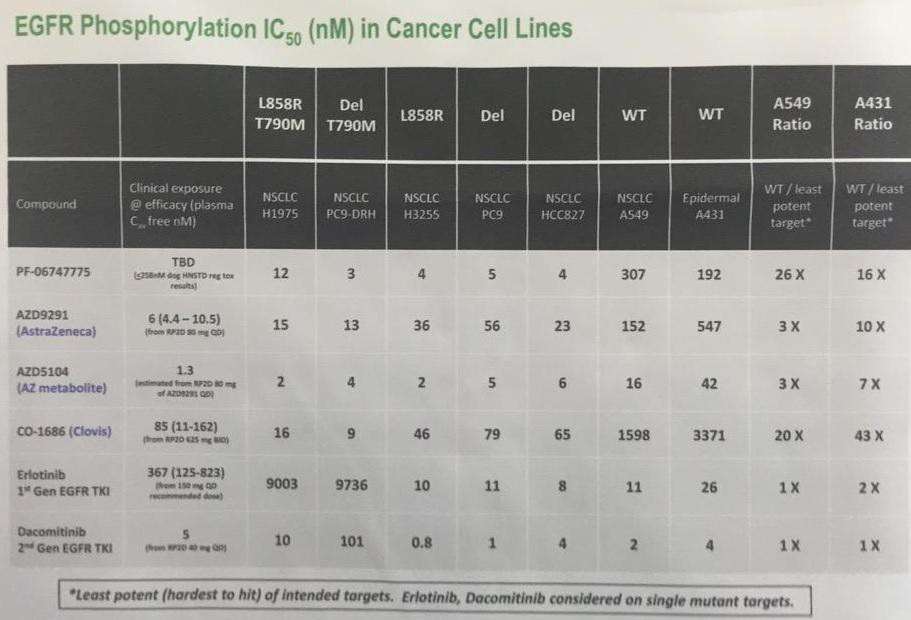
Nach diesen theoretischen(!) Werten kann es aber durchaus sein, dass Roci&AZD9291 zwar gut gegen T790M (2nd-line) wirkt aber nicht ausreichend gut gegen L858R/Del (1st-line)... vielleicht ist hier Tarceva überlegen.
Sollte das so sein, könnte aber Roci wieder die Nase vorne haben... denn dann würde eine Kombi mit Tarceva Sinn machen. Für die Dosierung würde es dann eine Rolle spielen, wie stark Roci bzw. AZD9291 wt-EGFR hemmt, da man bei Tarceva bereits ans Limit geht. AZD9291 könnte dann für eine Kombi zu viel sein und man muss mit der Dosis herunter gehen... Roci könnte man vielleicht aufgrund der geringen wt-EGFR Hemmung mit der vollen Dosis kombinieren.
Naja... das ist die Theorie, die Praxis sieht vielleicht ganz anders aus.
Gruß
ipollit
"Brutal starke Daten von AstraZenca... Da wird in den nächsten Wochen wohl einiges an Unsicherheit im Markt sein, ob CLVS da mithalten kann"
Ob AZD9291 oder CLVS's Roci besser ist, muss man sehen. Meiner Meinung nach gibt es auch deutliche Unterschiede zwischen beiden Mitteln unabhängig von der Wirkung gegen 2nd-line NSCLC mit T790M.
Die EGFR-Hemmer Tarceva&Co sind ja der 1st-line Standard gegen EGFR-sensitiven NSCLC. Daran ändert Roci oder AZD9291 erstmal nichts. Tarceva hat 1st-line aber nur eine zeitlich begrenzte Wirkung... in ca. 50% kommt es unter der Anwendung der etablierten EGFR-Hemmer zur T790M Mutation bei der die bisherigen Hemmer unwirksam sind. D.h. der 2nd-line T790M-Markt ist auch recht groß. Daneben gibt es aber auch noch 50%, bei denen EGFR-Hemmer unwirksam werden, aber kein T790M vorliegt... T790M- EGFR. Bei T790M- EGFR könnte Roci z.B. über IGF1 wirksam sein... AZD9291 hat diese Wirkung bisher nicht gezeigt.
T790M EGFR NSCLC wird auch irgendwann gegen einen T790M-Hemmer wie Roci resistent. Eine Möglichkeit ist auch hier IGF1, so dass theoretisch Roci auf 2nd-line länger wirken könnte. Die aktuellen AZD9291 Daten sprechen allerdings schonmal für AZD9291... Roci muss hier nun nachlegen.
Ein ganz anderes Thema ist allerdings 1st-line. So Kommentare wie der folgende, dass die guten AZD9291 T790M-Ergebnisse für eine erfolgreiche 1st-line Anwendung sprechen würden, kann ich nicht nachvollziehen...

Roci&AZD9291 wurden speziell gegen diese Mutation entwickelt, die aber 1st-line so gut wie nicht vorkommt, sondern erst unter Anwendung eines "normalen" EGFR-Hemmer auftetetn kann. D.h. eine Wirkung gegen T790M sagt überhaupt nichts über die 1st-line Wirkung aus!
EGFR fördert in veränderter Form (mutiert, erhöht) den Krebs... EGF ist aber als wild-type EGF auch ein ganz normaler Signalstoff in gesunden Zellen. U.a. gibt es wt-EGFR in Hautzellen... eine Hemmung dort führt zu starken Hautrötungen (Rash) wie bei einer Entzündung.
Tarceva&Co hemmen auch wt-EGFR sehr stark, weshalb hier diese Nebenwirkungen auftreten. Roci&AZD9291 vesuchen wt-EGFR auszusparen. Roci macht das allerdings deutlich besser als AZD9291. Aufgrund von IGF1 wirkt Roci aber auch auf den Blutzucker, so dass es als Nebenwirkung zu einer Art Diabetes kommmt. Dagegen helfen normale T2-Diabetes-Mittel in Form von Tabletten. Vielleicht ist so eine Nebenwirkung, von der der Patient nichts merkt, subjektiv besser zu tolerieren als etwas, was man sieht und fühlt.
Hier sind z.B. die theoretschen Wirkungen von Tarceva (Erlotinib), Roci (CO-1686) und AZD9291 gegen verschiedene EGFR-Typen zusammengefasst. Je kleiner die Zahl, um so höher die Wirkung. Die ersten beiden Spalten sind 2nd-line T790M-Mutationen. L858R und Del sind typische 1st-line Mutationen. Daneben finden sich noch 2 WT-Typen... "epidermal" wahrscheinlich der in der Haut.
Wie man sieht, wirkt Tarceva nicht gegen T790M, aber gegen L858R, Del und WT etwa gleich stark... daher kommt es zu den entsprechenden Nebenwirkungen z.B. auf der Haut (Ratio jeweils 1).
Roci&AZD9291 wirken am meisten gegen T790M, weniger gegen L858R, Del und deutlich weniger gegen WT. Wie man sieht, wirkt Roci aber kaum gegen WT (sehr hohe Werte)... das Verhältnis von Wirkung zu EGFR-Nebenwirkung ist daher am besten.

Nach diesen theoretischen(!) Werten kann es aber durchaus sein, dass Roci&AZD9291 zwar gut gegen T790M (2nd-line) wirkt aber nicht ausreichend gut gegen L858R/Del (1st-line)... vielleicht ist hier Tarceva überlegen.
Sollte das so sein, könnte aber Roci wieder die Nase vorne haben... denn dann würde eine Kombi mit Tarceva Sinn machen. Für die Dosierung würde es dann eine Rolle spielen, wie stark Roci bzw. AZD9291 wt-EGFR hemmt, da man bei Tarceva bereits ans Limit geht. AZD9291 könnte dann für eine Kombi zu viel sein und man muss mit der Dosis herunter gehen... Roci könnte man vielleicht aufgrund der geringen wt-EGFR Hemmung mit der vollen Dosis kombinieren.
Naja... das ist die Theorie, die Praxis sieht vielleicht ganz anders aus.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.643.231 von ipollit am 25.04.15 17:03:56Hallo ipollit,
dann sieht es wirklich gar nicht gut aus. Ich denke, dass ich die Position mit dem entsprechenden Verlust schließen werde.
Soweit Aeri mit den besseren Ergebnissen von Patienten mit niedrigerem Anfangs-IOP argumentiert, ist das vermutlich auch durch folgendes zu relativieren, das sich im S-1 des Konkurrenten Inotek findet:
The Ocular Hypertension Treatment Study, or the OHTS Study, was a large, randomized academic trial published in 2002 that followed a total of 1,636 participants who initially had no evidence of glaucoma-related damage.
The OHTS Study found that higher IOPs generally indicate a higher risk for progression to glaucoma. An IOP of 10 to 21 mmHg is generally considered in the normal range.
Individuals with IOPs greater than 21 and up to 25 mmHg will often not be prescribed drug therapy unless they have evidence of both structural changes and some vision loss, or some combination of these and other risk factors for future vision loss. In fact, the United Kingdom’s National Institute of Health and Care Excellence Guidelines, or NICE Guidelines, for the treatment of suspected glaucoma (structural changes but without vision loss) plus elevated IOP, does not recommend treatment of eyes with corneal thickness of 555-590 nm and IOP of 25 mmHg or below. Drug treatment is much more common when patients have IOPs greater than 25 mmHg.
http://www.sec.gov/Archives/edgar/data/1281895/0001193125143…
Also dürfte insbesondere die Bezugnahme auf Patienten mit IOP unter 24 in der Praxis nicht die große Relevanz haben.
Inotek (ITEK) hat von Aeris Fehlschlag übrigens profitiert. Sie werden dieses Jahr wohl die P III beginnen und sind laut googlefinance mit nur 90 Mio. Dollar (wirklich?) bewertet.
Insofern könnte es bei Aeri noch deutlich weiter nach unten gehen.
Einmal mehr eine Erinnerung an Diversifizierung. Die Unwägbarkeiten in diesem Business sind einfach extrem groß.
dann sieht es wirklich gar nicht gut aus. Ich denke, dass ich die Position mit dem entsprechenden Verlust schließen werde.
Soweit Aeri mit den besseren Ergebnissen von Patienten mit niedrigerem Anfangs-IOP argumentiert, ist das vermutlich auch durch folgendes zu relativieren, das sich im S-1 des Konkurrenten Inotek findet:
The Ocular Hypertension Treatment Study, or the OHTS Study, was a large, randomized academic trial published in 2002 that followed a total of 1,636 participants who initially had no evidence of glaucoma-related damage.
The OHTS Study found that higher IOPs generally indicate a higher risk for progression to glaucoma. An IOP of 10 to 21 mmHg is generally considered in the normal range.
Individuals with IOPs greater than 21 and up to 25 mmHg will often not be prescribed drug therapy unless they have evidence of both structural changes and some vision loss, or some combination of these and other risk factors for future vision loss. In fact, the United Kingdom’s National Institute of Health and Care Excellence Guidelines, or NICE Guidelines, for the treatment of suspected glaucoma (structural changes but without vision loss) plus elevated IOP, does not recommend treatment of eyes with corneal thickness of 555-590 nm and IOP of 25 mmHg or below. Drug treatment is much more common when patients have IOPs greater than 25 mmHg.
http://www.sec.gov/Archives/edgar/data/1281895/0001193125143…
Also dürfte insbesondere die Bezugnahme auf Patienten mit IOP unter 24 in der Praxis nicht die große Relevanz haben.
Inotek (ITEK) hat von Aeris Fehlschlag übrigens profitiert. Sie werden dieses Jahr wohl die P III beginnen und sind laut googlefinance mit nur 90 Mio. Dollar (wirklich?) bewertet.
Insofern könnte es bei Aeri noch deutlich weiter nach unten gehen.
Einmal mehr eine Erinnerung an Diversifizierung. Die Unwägbarkeiten in diesem Business sind einfach extrem groß.
ich oute mich hiermit als Biotech-Laie.
Welche deutsche börsennotierte Biotech-Firma (Wirkstoffentwickler) hat es geschafft einen Wirkstoff in den Markt zu bringen ?
Welche deutsche börsennotierte Biotech-Firma (Wirkstoffentwickler) hat es geschafft einen Wirkstoff in den Markt zu bringen ?
Antwort auf Beitrag Nr.: 49.643.450 von SmartCap am 25.04.15 18:21:20
Biofrontera
Zitat von SmartCap: ich oute mich hiermit als Biotech-Laie.
Welche deutsche börsennotierte Biotech-Firma (Wirkstoffentwickler) hat es geschafft einen Wirkstoff in den Markt zu bringen ?
Biofrontera
Antwort auf Beitrag Nr.: 49.637.021 von McNay am 24.04.15 13:49:07Hallo McNay,
ja, ich habe eine kleine IMMU-Position. Allerdings verfolge ich sie nicht so regelmäßig. Gekauft habe ich wegen der beiden ADCs, die ja noch in einem eher frühen Entwicklungs-Stadium sind... ich kann aber nicht sagen, ob sie im Moment sehr aussichtsreich sind. Von den Ergebnissen her, sehen sie für mich immer noch gut aus.
IMMU sind irgendwie etwas schwer zu greifen. Sie sind ein sehr altes Biotech-Unternehmen (schon Anfang der 90 an der Börse gewesen)... eine Mischung aus AK&Co-Technologien: normale AKs, radioaktive AKs, ADCs usw. Irgendetwas nennenswertes kam bisher nicht heraus (denke mal dass IMMU daher keinen guten Ruf hat). Sie haben so manches in der Pipeline... aber nur ein Teil davon ist noch aktiv.
Ein wichtiges Event steht wohl in Kürze an, wenn Pharma-Partner UCB PIII-Daten des CD22 AKs Epratuzumab gegen SLE bekannt gibt. Viele sehen den wohl als einzig relevanten Kandidaten in der Pipeline, so dass ein Erfolg oder Scheitern den Kurs stark bewegen sollten. SLE ist meiner Meinung nach eine riskante Indikation und bezüglich Epratuzumab habe ich bisher keine große Begeisterung gehört. Wohl ein Hoch-Risiko-Programm... eine Vorhersage kann man da nicht machen. Im Erfolgsfall dürfte aber IMMU mit hohen Royalties bis 25% beteiligt sein.
Ich dachte, dass die beiden ADC aussichtsreich sind und IMMU im Verhältnis dazu noch niedrig bewertet ist. Laut Ohad Hammer ist das verwendete Toxin SN-38 (ist die aktive Substanz der Chemo Irinotecan) weniger toxisch als die von den meisten anderen ADCs verwendeten Toxine. Ist aber nicht unbedingt ein Nachteil... dadurch sind die Nebenwirkungen vielleicht auch geringer. Im Vergleich von Irinotecan (das im Körper zu SN-38 umgewandelt wird) sind die ADCs zumindest schonmal erheblich verträglicher.
Die letzte Finanzrunde war meiner Meinung nach nicht so toll... der Kurs ist daraufhin regelrecht abgestürzt. Hätte man das nicht besser lösen können? Ein solches Vorgehen ist meiner Meinung nach zumindest kein Zeichen von Stärke.
Für mich ist es erstmal eine Risiko-Position. Erst wenn Epratuzumab erfolgreich ist oder sich insgesamt die Stimmung gegenüber IMMU dreht, würde ich überlegen, die Position zu erhöhen.
Oder wie siehst du IMMU?

Grüße
ipollit
ja, ich habe eine kleine IMMU-Position. Allerdings verfolge ich sie nicht so regelmäßig. Gekauft habe ich wegen der beiden ADCs, die ja noch in einem eher frühen Entwicklungs-Stadium sind... ich kann aber nicht sagen, ob sie im Moment sehr aussichtsreich sind. Von den Ergebnissen her, sehen sie für mich immer noch gut aus.
IMMU sind irgendwie etwas schwer zu greifen. Sie sind ein sehr altes Biotech-Unternehmen (schon Anfang der 90 an der Börse gewesen)... eine Mischung aus AK&Co-Technologien: normale AKs, radioaktive AKs, ADCs usw. Irgendetwas nennenswertes kam bisher nicht heraus (denke mal dass IMMU daher keinen guten Ruf hat). Sie haben so manches in der Pipeline... aber nur ein Teil davon ist noch aktiv.
Ein wichtiges Event steht wohl in Kürze an, wenn Pharma-Partner UCB PIII-Daten des CD22 AKs Epratuzumab gegen SLE bekannt gibt. Viele sehen den wohl als einzig relevanten Kandidaten in der Pipeline, so dass ein Erfolg oder Scheitern den Kurs stark bewegen sollten. SLE ist meiner Meinung nach eine riskante Indikation und bezüglich Epratuzumab habe ich bisher keine große Begeisterung gehört. Wohl ein Hoch-Risiko-Programm... eine Vorhersage kann man da nicht machen. Im Erfolgsfall dürfte aber IMMU mit hohen Royalties bis 25% beteiligt sein.
Ich dachte, dass die beiden ADC aussichtsreich sind und IMMU im Verhältnis dazu noch niedrig bewertet ist. Laut Ohad Hammer ist das verwendete Toxin SN-38 (ist die aktive Substanz der Chemo Irinotecan) weniger toxisch als die von den meisten anderen ADCs verwendeten Toxine. Ist aber nicht unbedingt ein Nachteil... dadurch sind die Nebenwirkungen vielleicht auch geringer. Im Vergleich von Irinotecan (das im Körper zu SN-38 umgewandelt wird) sind die ADCs zumindest schonmal erheblich verträglicher.
Die letzte Finanzrunde war meiner Meinung nach nicht so toll... der Kurs ist daraufhin regelrecht abgestürzt. Hätte man das nicht besser lösen können? Ein solches Vorgehen ist meiner Meinung nach zumindest kein Zeichen von Stärke.
Für mich ist es erstmal eine Risiko-Position. Erst wenn Epratuzumab erfolgreich ist oder sich insgesamt die Stimmung gegenüber IMMU dreht, würde ich überlegen, die Position zu erhöhen.
Oder wie siehst du IMMU?
Grüße
ipollit
AERI:
Analysten geben sich relativ entspannt:

Wie schon geschrieben, bin ich nicht sicher, wie weit dieser "wirkt ja bei niedrigem IOP Ansatz" wirklich trägt.
Außerdem wird der von ipollit hervorragend dargestellte Drift-Effekt hier vernachlässigt.
Wenn sich aber trotzdem so eine relativierende Sichtweise am Markt durchsetzt, dann ist natürlich auch eine deutliche Erholung des Kurses möglich.
Analysten geben sich relativ entspannt:

Wie schon geschrieben, bin ich nicht sicher, wie weit dieser "wirkt ja bei niedrigem IOP Ansatz" wirklich trägt.
Außerdem wird der von ipollit hervorragend dargestellte Drift-Effekt hier vernachlässigt.
Wenn sich aber trotzdem so eine relativierende Sichtweise am Markt durchsetzt, dann ist natürlich auch eine deutliche Erholung des Kurses möglich.
Antwort auf Beitrag Nr.: 49.643.462 von Aurum2010 am 25.04.15 18:33:17Besten Dank Aurum
Waren/sind die Erwartungen nicht höher ?
Im Jan 2015 hatte ich mir das Portfolio von BB Biotech angesehen, und dort keinen einzigen deutschen Wirkstoffentwickler gesehen (falls ich mich nicht verlesen habe). Ich unterstelle, dass dort Biotech-Profis arbeiten.
Waren/sind die Erwartungen nicht höher ?
Im Jan 2015 hatte ich mir das Portfolio von BB Biotech angesehen, und dort keinen einzigen deutschen Wirkstoffentwickler gesehen (falls ich mich nicht verlesen habe). Ich unterstelle, dass dort Biotech-Profis arbeiten.
Antwort auf Beitrag Nr.: 49.643.633 von ipollit am 25.04.15 19:34:45Hallo ipollit,
danke für deine Rückmeldung und wie immer guten Ausführung.
Bei mir ist IMMU aktuell auch nur eine kleine Position. Negativ sehe ich immer noch den Ausstieg von Takeda-Nycomed bei Veltuzumab.
Außer Epratuzumab ist mit UCB auch keine weitere Entwicklung verpartnert.
Das stellt sich mir die Frage nach der Fähigkeit des Managements bzw. Werthaltigkeit der Pipeline.
Wie du ja bereits geschrieben hast, gibt es die Firma schon lange, ohne einen wirklichen Durchbruch bisher geschafft zu haben. Da helfen auch keine Patent Awards, die IMMU ja regelmäßig vermeldet. Wenn es nach der Menge an Patent Awards geht, müsste IMMU in der ersten Liga spielen.
An Hand der Anzahl an Projekten und Pipeline hätte ich auch einen höheren Cash-Verbrauch in den letzten Monaten erwartet und eine schnellere und bessere Finanzierungsrunde. Was ein Indiz dafür sein könnte, dass das eine oder andere Projekt nicht wirklich vorangetrieben wird. Entweder aus Geldmangel oder weil man selbst nicht von den Ergebnissen überzeugt ist.
Dann wäre es besser die Pipeline zu bereinigen und uns Investoren zu informieren.
Das erklärt vielleicht auch den schlechten Ruf.
Auf der positiven Seite stehen für mich IMMU-130 und 132.
Die halte ich auch für sehr interessant.
Ein kleines Lottoticket. Ich bin ebenfalls noch unentschlossen hier aufzustocken. Sollte es nochmal Richtung 3 Dollar ohne News gehen, werde ich wohl nochmal eine kleine Position nachlegen.
AERI ja sehr schade, dass die Ergebnisse so ausgefallen sind. Ich war nicht investiert, fand die Story aber interessant. Ohad hat aktuelle viele neue Firmen im Portfolio, wo ich mich nicht so richtig anfreunden kann, wie SAGE und MRNS, CNAT.
Aktuelle halte ich Ablynx (hoffe auf ein zweites Galapagos), OMED, IPH, BLRX, RDHL, AGEN, IMMU, MRNA, ARWR, BIND.
Bei Cellectis und MGNX warte ich auf Rücksetzer.
danke für deine Rückmeldung und wie immer guten Ausführung.
Bei mir ist IMMU aktuell auch nur eine kleine Position. Negativ sehe ich immer noch den Ausstieg von Takeda-Nycomed bei Veltuzumab.
Außer Epratuzumab ist mit UCB auch keine weitere Entwicklung verpartnert.
Das stellt sich mir die Frage nach der Fähigkeit des Managements bzw. Werthaltigkeit der Pipeline.
Wie du ja bereits geschrieben hast, gibt es die Firma schon lange, ohne einen wirklichen Durchbruch bisher geschafft zu haben. Da helfen auch keine Patent Awards, die IMMU ja regelmäßig vermeldet. Wenn es nach der Menge an Patent Awards geht, müsste IMMU in der ersten Liga spielen.
An Hand der Anzahl an Projekten und Pipeline hätte ich auch einen höheren Cash-Verbrauch in den letzten Monaten erwartet und eine schnellere und bessere Finanzierungsrunde. Was ein Indiz dafür sein könnte, dass das eine oder andere Projekt nicht wirklich vorangetrieben wird. Entweder aus Geldmangel oder weil man selbst nicht von den Ergebnissen überzeugt ist.
Dann wäre es besser die Pipeline zu bereinigen und uns Investoren zu informieren.
Das erklärt vielleicht auch den schlechten Ruf.
Auf der positiven Seite stehen für mich IMMU-130 und 132.
Die halte ich auch für sehr interessant.
Ein kleines Lottoticket. Ich bin ebenfalls noch unentschlossen hier aufzustocken. Sollte es nochmal Richtung 3 Dollar ohne News gehen, werde ich wohl nochmal eine kleine Position nachlegen.
AERI ja sehr schade, dass die Ergebnisse so ausgefallen sind. Ich war nicht investiert, fand die Story aber interessant. Ohad hat aktuelle viele neue Firmen im Portfolio, wo ich mich nicht so richtig anfreunden kann, wie SAGE und MRNS, CNAT.
Aktuelle halte ich Ablynx (hoffe auf ein zweites Galapagos), OMED, IPH, BLRX, RDHL, AGEN, IMMU, MRNA, ARWR, BIND.
Bei Cellectis und MGNX warte ich auf Rücksetzer.
CLDN hat es leider nicht geschafft...Studie CUPID 2 auf ganzer Linie gescheitert. Schade!
Antwort auf Beitrag Nr.: 49.647.455 von lawmeetstax am 26.04.15 22:53:29Kursziel sollte man so bei 1,5 bis 2,5 Dollar veranschlagen. Denke nicht, dass sie sich davon je erholen werden.
Wahrscheinlich werden heute auch andere "Gen-Plays" unter Druck kommen (BLUE, QURE, AAVL), obwohl das objektiv keinen Sinn macht.
Wahrscheinlich werden heute auch andere "Gen-Plays" unter Druck kommen (BLUE, QURE, AAVL), obwohl das objektiv keinen Sinn macht.
Adaptimmune - ADAP:
Das IPO rückt näher.
http://www.sec.gov/Archives/edgar/data/1621227/0001047469150…
Wenn ich es richtig verstehe, soll die IPO-Marktkap. bei ca. 1,2 Mrd. Dollar liegen.
Es werden ca. 10,7 Mio. ADS zu einem Preis von 17 Dollar verkauft werden.
Das IPO rückt näher.
http://www.sec.gov/Archives/edgar/data/1621227/0001047469150…
Wenn ich es richtig verstehe, soll die IPO-Marktkap. bei ca. 1,2 Mrd. Dollar liegen.
Es werden ca. 10,7 Mio. ADS zu einem Preis von 17 Dollar verkauft werden.
Antwort auf Beitrag Nr.: 49.643.231 von ipollit am 25.04.15 17:03:56AERI
Die Ergebnisse waren/sind einfach eine herbe Enttäuschung. Primärer Endpunkt verpasst, Effektivität geht scheinbar verloren und auch bei den Nebenwirkungen waren die Ergebnisse eher schlecht. Es gab doch insgesamt mit 44 von 411 Teilnehmern viele Abbrüche (55% davon wegen Nebenwirkungen-in beiden Armen zusammen). Im Rhopressa Arm waren es fast dreimal so viele Abbrüche wie im Timonol Arm. Da liegt es nahe, dass die Augenrötungen eventuell doch ein Problem darstellen könnten. Auch hier muss man ja sehen, dass die Studie nur 3 Monate lang war.
Was den Drift Effekt betrifft, habe ich es so verstanden, dass ein Teil der Teilnehmer komplett die Wirkung verloren hat und das dann sozusagen den Schnitt versaut hat. Hier wäre mal eine genaue Aufschlüsselung interessant. Gibt es z.B. eine Gruppe von 50% bei denen die Wirkung absolut stabil bleibt?
Und wäre es dann medizinisch möglich und sinnvoll, Rhopressa bei den Patienten, auszuprobieren?
Die Ergebnisse waren/sind einfach eine herbe Enttäuschung. Primärer Endpunkt verpasst, Effektivität geht scheinbar verloren und auch bei den Nebenwirkungen waren die Ergebnisse eher schlecht. Es gab doch insgesamt mit 44 von 411 Teilnehmern viele Abbrüche (55% davon wegen Nebenwirkungen-in beiden Armen zusammen). Im Rhopressa Arm waren es fast dreimal so viele Abbrüche wie im Timonol Arm. Da liegt es nahe, dass die Augenrötungen eventuell doch ein Problem darstellen könnten. Auch hier muss man ja sehen, dass die Studie nur 3 Monate lang war.
Was den Drift Effekt betrifft, habe ich es so verstanden, dass ein Teil der Teilnehmer komplett die Wirkung verloren hat und das dann sozusagen den Schnitt versaut hat. Hier wäre mal eine genaue Aufschlüsselung interessant. Gibt es z.B. eine Gruppe von 50% bei denen die Wirkung absolut stabil bleibt?
Und wäre es dann medizinisch möglich und sinnvoll, Rhopressa bei den Patienten, auszuprobieren?
TTPH
Gute News aber Sell on good News?
https://www.tradingview.com/x/18qZQL3u/
****
Two late-stage studies show encouraging results for Tetraphase's eravacycline
Apr 27 2015, 15:30 ET | About: Tetraphase Pharmaceuti... (TTPH) | By: Douglas W. House, SA News Editor [Contact this editor with comments or a news tip]
Two Phase 3 clinical trials evaluating Tetraphase Pharmaceuticals' (TTPH -5.1%) lead product candidate, eravacycline, show positive results for the treatment of complicated intra-abdominal infections (cIAI) and complicated urinary tract infections (cUTI).
The first study, IGNITE-1, compared eravacycline to Merck's (MRK -1.1%) Invanz (ertapenem) for the treatment of cIAI. It achieved the primary endpoint of statistical non-inferiority (no worse than) of clinical response at the test-of-cure (TOC) visit. In the microbiological intent-to-treat (micro-ITT) population (n=446) 86.8% of patients receiving eravacycline achieved a clinical cure compared to 87.6% of patients receiving ertapenem (FDA criteria). In the clinically evaluable population (n=477) 92.9% of patients receiving eravacycline achieved a clinical cure versus 94.5% of patients receiving ertapenem (EMA criteria). These results were first reported in December.
In the lead-in portion of the second study, IGNITE-2, both IV-to-oral dosing regimens of eravacycline (1.5 mg/kg followed by 200 mg or 250 mg) compared favorably with levofloxacin, a broad spectrum antibiotic, for the treatment of cUTI. The primary endpoint, per the FDA's criteria, was the responder rate (defined as both clinical cure and successful microbiological outcome) in the micro-ITT population. The responder rates for 200 mg (n=24), 250 mg (n=28) and levofloxacin (n=23) were 75.0%, 64.3% and 56.4%, respectively. In the microbiologically evaluable population, the primary endpoint was the microbiological response per the EMA's criteria. The respective responses for levofloxacin isolates (n=24) were: 83.3%, 72.7% and 42.9%. Based on these data, the 200 mg dose will be used for the pivotal portion of the Phase 3 that is currently underway.
The company expects to submit its regulatory applications by the end of the year.
The data were presented at this week's 25th European Congress of Clinical Microbiology and Infectious Diseases in Copenhagen, Denmark.
****
Tetraphase Pharmaceuticals Given a $50.00 Price Target at Brean Capital (TTPH)
http://www.lulegacy.com/2015/04/28/tetraphase-pharmaceutical…
Gruss S.
Gute News aber Sell on good News?
https://www.tradingview.com/x/18qZQL3u/
****
Two late-stage studies show encouraging results for Tetraphase's eravacycline
Apr 27 2015, 15:30 ET | About: Tetraphase Pharmaceuti... (TTPH) | By: Douglas W. House, SA News Editor [Contact this editor with comments or a news tip]
Two Phase 3 clinical trials evaluating Tetraphase Pharmaceuticals' (TTPH -5.1%) lead product candidate, eravacycline, show positive results for the treatment of complicated intra-abdominal infections (cIAI) and complicated urinary tract infections (cUTI).
The first study, IGNITE-1, compared eravacycline to Merck's (MRK -1.1%) Invanz (ertapenem) for the treatment of cIAI. It achieved the primary endpoint of statistical non-inferiority (no worse than) of clinical response at the test-of-cure (TOC) visit. In the microbiological intent-to-treat (micro-ITT) population (n=446) 86.8% of patients receiving eravacycline achieved a clinical cure compared to 87.6% of patients receiving ertapenem (FDA criteria). In the clinically evaluable population (n=477) 92.9% of patients receiving eravacycline achieved a clinical cure versus 94.5% of patients receiving ertapenem (EMA criteria). These results were first reported in December.
In the lead-in portion of the second study, IGNITE-2, both IV-to-oral dosing regimens of eravacycline (1.5 mg/kg followed by 200 mg or 250 mg) compared favorably with levofloxacin, a broad spectrum antibiotic, for the treatment of cUTI. The primary endpoint, per the FDA's criteria, was the responder rate (defined as both clinical cure and successful microbiological outcome) in the micro-ITT population. The responder rates for 200 mg (n=24), 250 mg (n=28) and levofloxacin (n=23) were 75.0%, 64.3% and 56.4%, respectively. In the microbiologically evaluable population, the primary endpoint was the microbiological response per the EMA's criteria. The respective responses for levofloxacin isolates (n=24) were: 83.3%, 72.7% and 42.9%. Based on these data, the 200 mg dose will be used for the pivotal portion of the Phase 3 that is currently underway.
The company expects to submit its regulatory applications by the end of the year.
The data were presented at this week's 25th European Congress of Clinical Microbiology and Infectious Diseases in Copenhagen, Denmark.
****
Tetraphase Pharmaceuticals Given a $50.00 Price Target at Brean Capital (TTPH)
http://www.lulegacy.com/2015/04/28/tetraphase-pharmaceutical…
Gruss S.
Ich stelle diesen Beitrag hier mal eher unvermittelt rein:
http://www.fiercebiotech.com/story/patent-battle-brews-celge…
Ich finde den Artikel jetzt nicht per se entscheidend lesenswert, aber ich glaube, wir haben hier noch nie das Thema CRISPR-Cas9 erwähnt.
Meine vorläufige Meinung dazu: Das ist nicht die neueste Sau, die gerade durchs Dorf getrieben wird.
Es ist, denke ich, DER FUNDAMENTALE DURCHBRUCH überhaupt. Wir können jetzt direkt in Maschinensprache programmieren.
Ich denke, das ändert über die nächsten Jahre und Jahrzehnte fast alles.
http://www.fiercebiotech.com/story/patent-battle-brews-celge…
Ich finde den Artikel jetzt nicht per se entscheidend lesenswert, aber ich glaube, wir haben hier noch nie das Thema CRISPR-Cas9 erwähnt.
Meine vorläufige Meinung dazu: Das ist nicht die neueste Sau, die gerade durchs Dorf getrieben wird.
Es ist, denke ich, DER FUNDAMENTALE DURCHBRUCH überhaupt. Wir können jetzt direkt in Maschinensprache programmieren.
Ich denke, das ändert über die nächsten Jahre und Jahrzehnte fast alles.
ADAP:
Adaptimmune Therapeutics, which is developing cancer immunotherapies based on genetically engineered T-cell receptors, announced terms for its IPO on Monday. The Abingdon, United Kingdom-based company plans to raise $150 million by offering 9.4 million shares at a price range of $15 to $17. At the midpoint of the proposed range, Adaptimmune Therapeutics would command a fully diluted market value of $1.2 billion.
Adaptimmune Therapeutics was founded in 2008 and plans to list on the NASDAQ under the symbol ADAP. BofA Merrill Lynch, Cowen & Company and Leerink Partners are the joint bookrunners on the deal. It is expected to price during the week of May 4, 2015.
Nächste Woche dürfte das IPO von ADAP in die heiße Phase kommen.
Hat jemand schon eine Meinung?
ipollit, Du hast Dich ja schon vor geraumer Zeit positiv zum Thema TCR geäußert - durchaus auch mit kritischem Blick auf den gehypten "Cousin" CAR-T.
Wie siehst Du in dem Zusammenhang ADAP? Sind sie nicht ein sehr guter Ansatz, wenn man die TCR-Karte spielen will?
Ich schaue mir am Wochenende noch mal ihr S1 (oder F1) an, aber meine Grundtendenz ist bisher deutlich positiv
Grüße
SLG
Adaptimmune Therapeutics, which is developing cancer immunotherapies based on genetically engineered T-cell receptors, announced terms for its IPO on Monday. The Abingdon, United Kingdom-based company plans to raise $150 million by offering 9.4 million shares at a price range of $15 to $17. At the midpoint of the proposed range, Adaptimmune Therapeutics would command a fully diluted market value of $1.2 billion.
Adaptimmune Therapeutics was founded in 2008 and plans to list on the NASDAQ under the symbol ADAP. BofA Merrill Lynch, Cowen & Company and Leerink Partners are the joint bookrunners on the deal. It is expected to price during the week of May 4, 2015.
Nächste Woche dürfte das IPO von ADAP in die heiße Phase kommen.
Hat jemand schon eine Meinung?
ipollit, Du hast Dich ja schon vor geraumer Zeit positiv zum Thema TCR geäußert - durchaus auch mit kritischem Blick auf den gehypten "Cousin" CAR-T.
Wie siehst Du in dem Zusammenhang ADAP? Sind sie nicht ein sehr guter Ansatz, wenn man die TCR-Karte spielen will?
Ich schaue mir am Wochenende noch mal ihr S1 (oder F1) an, aber meine Grundtendenz ist bisher deutlich positiv
Grüße
SLG
Antwort auf Beitrag Nr.: 49.679.616 von SLGramann am 30.04.15 09:48:17Als Ergänzung zum Thema, hat jemand eine Meinung zu Cardio3BioSciences?
Insbesondere zu NKG2D.
Ursprünglich kommen die ja aus dem cardiovascular-diseases Bereich und haben hier auch eine Phase3.
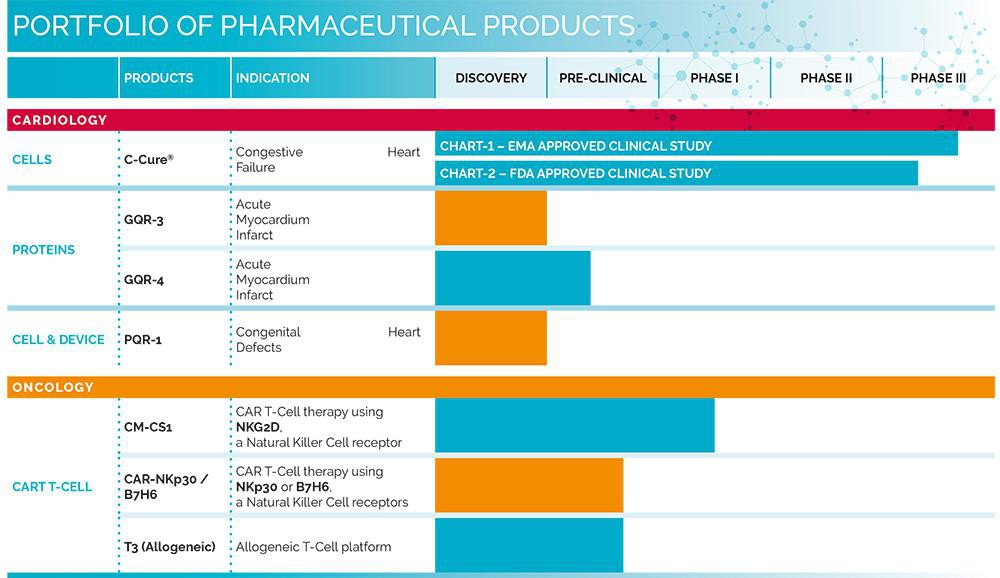
Insbesondere zu NKG2D.
Ursprünglich kommen die ja aus dem cardiovascular-diseases Bereich und haben hier auch eine Phase3.

NBI - NASDAQ Biotechnology Index

Bin kein Charttechniker, aber das sieht nicht gut aus, denke ich.
(Gleichwohl ist eine heftige Korrektur bzw. selbst ein Crash ja gefühlt überfällig.)
Bin kein Charttechniker, aber das sieht nicht gut aus, denke ich.
(Gleichwohl ist eine heftige Korrektur bzw. selbst ein Crash ja gefühlt überfällig.)
Antwort auf Beitrag Nr.: 49.687.626 von SLGramann am 01.05.15 08:10:49Ja. Es ist irgendwie dann doch nicht schön auch wenn man damit gerechnet hat. Die Frage aller Fragen: Wann findet der IBB seinen Boden bzw. wie weit geht die Korrektur?
Das weiß natürlich keiner aber in der Vergangenheit hat der SMA ganz gute Hinweise geliefert.
Die 50 Tageslinie ist naürlich längst nach Unten durchbrochen. Momentan befindet sich der IBB (wieder) knapp über der 100 Tageslinie.
Eine größere Korektur könnte noch bis an die 200 Tageslinie gehen. Ein Crash natürlich auch weit darunter...

XBI (kurz vor Schluss gestern):

Hier nochmal eine andere Sichtweise von gestern:

SG kmastra
Das weiß natürlich keiner aber in der Vergangenheit hat der SMA ganz gute Hinweise geliefert.
Die 50 Tageslinie ist naürlich längst nach Unten durchbrochen. Momentan befindet sich der IBB (wieder) knapp über der 100 Tageslinie.
Eine größere Korektur könnte noch bis an die 200 Tageslinie gehen. Ein Crash natürlich auch weit darunter...
XBI (kurz vor Schluss gestern):

Hier nochmal eine andere Sichtweise von gestern:

SG kmastra
Antwort auf Beitrag Nr.: 49.687.626 von SLGramann am 01.05.15 08:10:49"Gleichwohl ist eine heftige Korrektur bzw. selbst ein Crash ja gefühlt überfällig."
Warum ist ein Crash überfällig sein? Gibt es dafür eine andere Begründung (insbesondere eine fundamentale), als dass die Kurse in den letzten Jahren deutlich gestiegen sind?
Für den Anstieg sehe ich jedenfalls gute Gründe. Z.B. Apple ist auch stark gestiegen, passend zu Umsatz und Gewinn... würdest du auch über Apple sagen, dass ein Crash überfällig ist?

So schlimm sieht es im langfristigen Chart doch noch nicht aus, oder?

Ein Crash wie 2008 im Dow ist meiner Meinung nach die Ausnahme und nicht die Regel... Korrekturen gibt es immer mal wieder, aber es ist unwahrscheinlich, dass der Dow irgendwann wieder bei 2000 steht.

Meiner Meinung nach sind gesunde Aufwärtsbewegungen linear im Log-Chart. Blasen/Übertreibungen zeigen sich dagegen durch parabolische Kursverläufe im Log-Chart... so z.B. 2000 beim Nasdaq...

Es wird ja alle Jahre bei jeder Korrektur gerne von einer Biotech-Blase gesprochen. Fundamental sehe ich dafür aber keine Begründung. Selbst wenn es zu einer ausgedehnten Korrektur oder einem Crash kommt, ist dies für mich bei unveränderter fundamentaler Lage dann eine Übertreibung nach unten, die nach einer gewissen Zeit auch wieder nach oben korrigiert wird.
Wovon wird denn der NBI-Aufschwung getragen? Von völlig übertrieben bewerteten kleinen oder mittleren Biotechs? Ich denke ohne eine deutliche Korrektur der Large-Cap Biotechs wie GILD, CELG&Co wird es nicht gehen, denn diese alleine machen vom Index-Gewicht so weit ich weiß in etwa 50% aus.
Der ibb = nbi im Vergleich zu den großen Biotechs... diese haben sich sogar oft noch besser entwickelt als der Index. Wie soll der Index stark korrigieren ohne eine genauso große oder größere Korrektur dieser großen Biotechs?
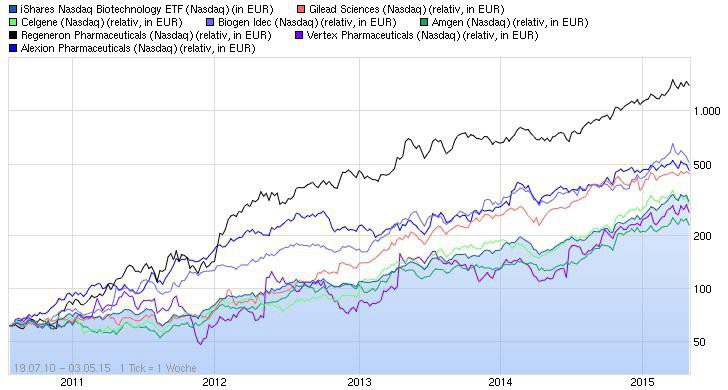
Sind die Large-Caps aber auch fundamental überbewertet und eine erhebliche Korrektur gerechtfertigt? Die KGVs liegen auf Pharma-Niveau. Eine Bayer hat ein KGV von aktuell 17,9 und 2017e von 13,9... eine Novartis aktuell 20,3 und 2017e 15,0... BMS aktuell 34,9 und 2017e 21,8. Der größte Biotech Gilead (mit 149 Mrd USD größerer Börsenwert als z.B. Bayer) hat ein aktuelles KGV von 8,3 und 2017e von 8,9... der zweitgrößte Biotech Amgen (gleicher Wert wie Bayer) aktuell 16,9 und 2017e 13,3... der drittgrößte Celgene aktuell 22,9 und 2017e 14,3. Warum befinden die sich deiner Meinung nach auf Blasen/Crash-Niveau??? Wie gesagt, machen diese schon einen großen Teil vom Index aus.
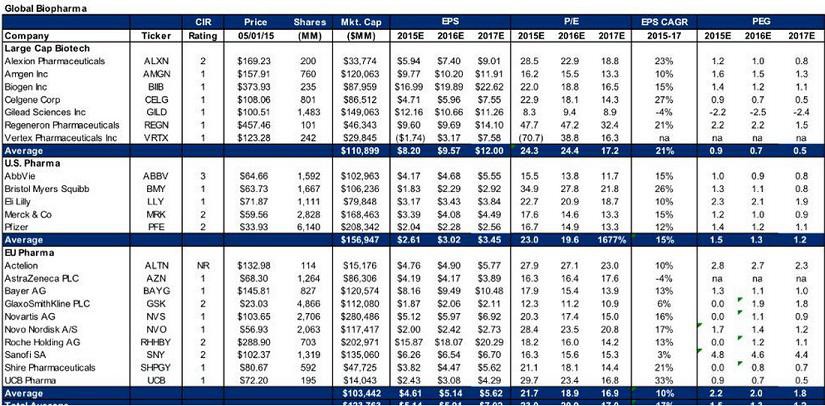
Die großen Biotechs produzieren zudem Jahr für Jahr große Cash-Beträge, die sie in mittlere und kleiner Biotech investieren... alleine bei Gilead sind es jedes Jahr mehr als 15 Mrd USD. Dies gilt ebenfalls für die Pharmas, die ständig ihre Pipelines auffüllen müssen. Übernahmen führen zu hohen Kursen, die sich dann auch im Index widerspiegeln.
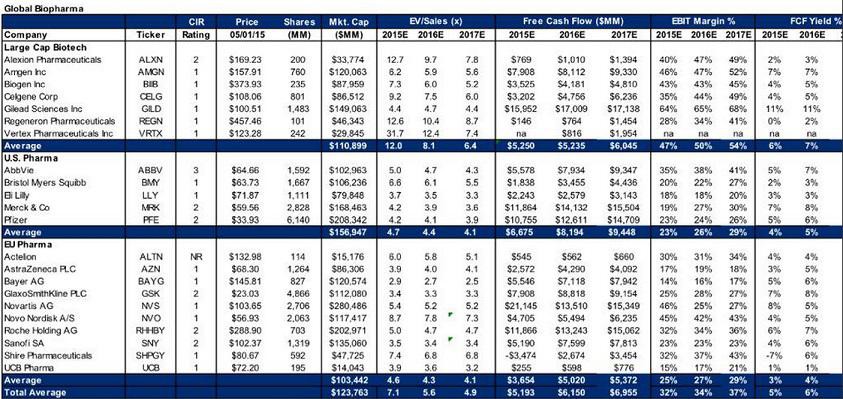
Übernahmen führen aber meiner Meinung nach auch zu Index-Verzerrungen nach oben. Vereinfacht gesagt, wenn der Index nur aus zwei gleich großen Unternehmen mit einem Kurs zu je 100 besteht, so berechnet der Index sich so zu (100 + 100) / 2 = 100. Nun wird ein Unternehmen übernommen zu einem Kurs von 200... der Index ist dann bei (100 + 200) / 2 = 150... als 50% im Plus. Nach der Übernahme verschwindet das Unternehmen und fällt somit aus dem Index, der dann aber trotzdem noch bei 150 als +50% steht. Dann kommt die gefühlte Index-Korrektur dieser Übertreibung von 150 auf einen Index-Kurs von 100. Dazu muss das verbleibende Unternehmen um 33% fallen auf einen Kurs von 67. Durch die Übernahmen steht der Index wieder bei 100 wie anfangs... trotzdem ist das Unternehmen um 33% gefallen. Chart-technisch mag das logisch sein... fundamental ergibt das aber keinen Sinn!
Im NBI gibt es immer wieder Übernahmen... z.B:
Pharmasset 11 Mrd USD
Onyx 10,4 Mrd USD
Idenix 3,8 Mrd USD
InterMune 8,3 Mrd USD
Cubist 9,5 Mrd USD
Salix 14,5 Mrd USD
Pharmacyclics 21 Mrd USD
Mit Mylan, für die Teva aktuell 40 Mrd USD geboten hat, wären das 118 Mrd USD... also etwa der Börsenwert von Bayer oder Amgen. Zu Höchstkursen werden diese Unternehmen aus dem Index genommen, ohne das dieser (übertriebene?) Kurswert korrigiert werden kann.
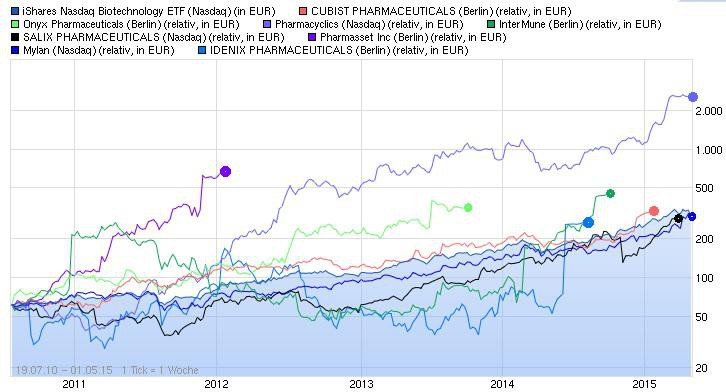
Gibt es vielleicht bei den Small-Caps eine Blase? Die Small-Caps in meinem Depot mit einer MK von 300 Mio oder weniger sehen nicht nach Übertreibung aus... von der aktuellen Korrektur sind sie aber auch betroffen. Aber selbst wenn sie auf 0 fallen, wird das alleine den Index kaum bewegen...
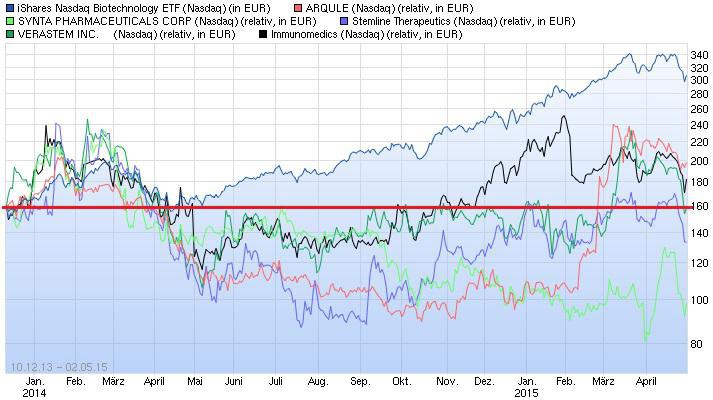
Dann gibt es noch so Unternehmen wie ESPR, ICPT oder RCPT, die stark gestiegen sind und im Mrd USD Bereich liegen. Wenn die LargeCaps nicht deutlich korrigieren, die SmallCaps nicht ausreichen, dann müssen diese stark korrigeren! Aber welchen Korrekturbedarf siehst du hier? -50%... -80%... es muss schon in Richtung letzterem gehen, um den Index deutlich, d.h. z.B. -30% nach unten zu bringen...
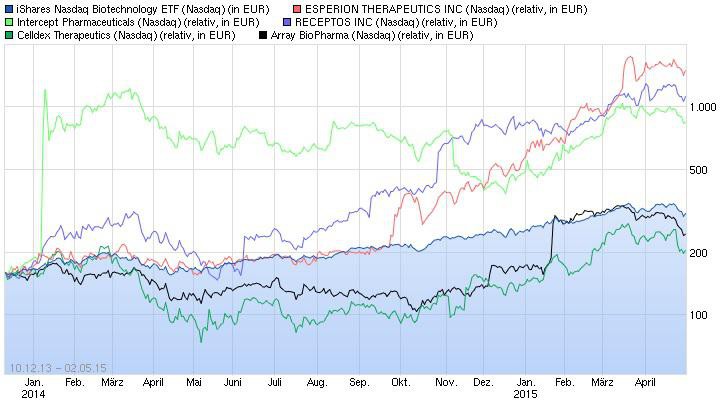
Grüße
ipollit
Warum ist ein Crash überfällig sein? Gibt es dafür eine andere Begründung (insbesondere eine fundamentale), als dass die Kurse in den letzten Jahren deutlich gestiegen sind?
Für den Anstieg sehe ich jedenfalls gute Gründe. Z.B. Apple ist auch stark gestiegen, passend zu Umsatz und Gewinn... würdest du auch über Apple sagen, dass ein Crash überfällig ist?
So schlimm sieht es im langfristigen Chart doch noch nicht aus, oder?
Ein Crash wie 2008 im Dow ist meiner Meinung nach die Ausnahme und nicht die Regel... Korrekturen gibt es immer mal wieder, aber es ist unwahrscheinlich, dass der Dow irgendwann wieder bei 2000 steht.
Meiner Meinung nach sind gesunde Aufwärtsbewegungen linear im Log-Chart. Blasen/Übertreibungen zeigen sich dagegen durch parabolische Kursverläufe im Log-Chart... so z.B. 2000 beim Nasdaq...
Es wird ja alle Jahre bei jeder Korrektur gerne von einer Biotech-Blase gesprochen. Fundamental sehe ich dafür aber keine Begründung. Selbst wenn es zu einer ausgedehnten Korrektur oder einem Crash kommt, ist dies für mich bei unveränderter fundamentaler Lage dann eine Übertreibung nach unten, die nach einer gewissen Zeit auch wieder nach oben korrigiert wird.
Wovon wird denn der NBI-Aufschwung getragen? Von völlig übertrieben bewerteten kleinen oder mittleren Biotechs? Ich denke ohne eine deutliche Korrektur der Large-Cap Biotechs wie GILD, CELG&Co wird es nicht gehen, denn diese alleine machen vom Index-Gewicht so weit ich weiß in etwa 50% aus.
Der ibb = nbi im Vergleich zu den großen Biotechs... diese haben sich sogar oft noch besser entwickelt als der Index. Wie soll der Index stark korrigieren ohne eine genauso große oder größere Korrektur dieser großen Biotechs?

Sind die Large-Caps aber auch fundamental überbewertet und eine erhebliche Korrektur gerechtfertigt? Die KGVs liegen auf Pharma-Niveau. Eine Bayer hat ein KGV von aktuell 17,9 und 2017e von 13,9... eine Novartis aktuell 20,3 und 2017e 15,0... BMS aktuell 34,9 und 2017e 21,8. Der größte Biotech Gilead (mit 149 Mrd USD größerer Börsenwert als z.B. Bayer) hat ein aktuelles KGV von 8,3 und 2017e von 8,9... der zweitgrößte Biotech Amgen (gleicher Wert wie Bayer) aktuell 16,9 und 2017e 13,3... der drittgrößte Celgene aktuell 22,9 und 2017e 14,3. Warum befinden die sich deiner Meinung nach auf Blasen/Crash-Niveau??? Wie gesagt, machen diese schon einen großen Teil vom Index aus.

Die großen Biotechs produzieren zudem Jahr für Jahr große Cash-Beträge, die sie in mittlere und kleiner Biotech investieren... alleine bei Gilead sind es jedes Jahr mehr als 15 Mrd USD. Dies gilt ebenfalls für die Pharmas, die ständig ihre Pipelines auffüllen müssen. Übernahmen führen zu hohen Kursen, die sich dann auch im Index widerspiegeln.

Übernahmen führen aber meiner Meinung nach auch zu Index-Verzerrungen nach oben. Vereinfacht gesagt, wenn der Index nur aus zwei gleich großen Unternehmen mit einem Kurs zu je 100 besteht, so berechnet der Index sich so zu (100 + 100) / 2 = 100. Nun wird ein Unternehmen übernommen zu einem Kurs von 200... der Index ist dann bei (100 + 200) / 2 = 150... als 50% im Plus. Nach der Übernahme verschwindet das Unternehmen und fällt somit aus dem Index, der dann aber trotzdem noch bei 150 als +50% steht. Dann kommt die gefühlte Index-Korrektur dieser Übertreibung von 150 auf einen Index-Kurs von 100. Dazu muss das verbleibende Unternehmen um 33% fallen auf einen Kurs von 67. Durch die Übernahmen steht der Index wieder bei 100 wie anfangs... trotzdem ist das Unternehmen um 33% gefallen. Chart-technisch mag das logisch sein... fundamental ergibt das aber keinen Sinn!
Im NBI gibt es immer wieder Übernahmen... z.B:
Pharmasset 11 Mrd USD
Onyx 10,4 Mrd USD
Idenix 3,8 Mrd USD
InterMune 8,3 Mrd USD
Cubist 9,5 Mrd USD
Salix 14,5 Mrd USD
Pharmacyclics 21 Mrd USD
Mit Mylan, für die Teva aktuell 40 Mrd USD geboten hat, wären das 118 Mrd USD... also etwa der Börsenwert von Bayer oder Amgen. Zu Höchstkursen werden diese Unternehmen aus dem Index genommen, ohne das dieser (übertriebene?) Kurswert korrigiert werden kann.

Gibt es vielleicht bei den Small-Caps eine Blase? Die Small-Caps in meinem Depot mit einer MK von 300 Mio oder weniger sehen nicht nach Übertreibung aus... von der aktuellen Korrektur sind sie aber auch betroffen. Aber selbst wenn sie auf 0 fallen, wird das alleine den Index kaum bewegen...

Dann gibt es noch so Unternehmen wie ESPR, ICPT oder RCPT, die stark gestiegen sind und im Mrd USD Bereich liegen. Wenn die LargeCaps nicht deutlich korrigieren, die SmallCaps nicht ausreichen, dann müssen diese stark korrigeren! Aber welchen Korrekturbedarf siehst du hier? -50%... -80%... es muss schon in Richtung letzterem gehen, um den Index deutlich, d.h. z.B. -30% nach unten zu bringen...

Grüße
ipollit
Antwort auf Beitrag Nr.: 49.694.349 von ipollit am 02.05.15 14:34:47kann man irgendwo sehen wie hoch die kumulierte market cap aller Biotechs/Pharmas ist ?
Antwort auf Beitrag Nr.: 49.694.457 von SmartCap am 02.05.15 15:05:48"aller Biotechs/Pharmas"... was bedeutet alle?
Z.B. im Nasdaq Biotech Index (NBI) gibt es laut yahoo 148 Unternehmen, deren Marktkapitalisierungs in Summe aktuell ca. 1000 Millionen USD (also 1 Billionen USD) beträgt...
GILD + AMGN + CELG + BIIB + REGN + ALXN + VRTX kommen zusammen auf 570 Mrd USD... das sind ca. 59% der NBI-Summe.
Gruß
ipollit
Z.B. im Nasdaq Biotech Index (NBI) gibt es laut yahoo 148 Unternehmen, deren Marktkapitalisierungs in Summe aktuell ca. 1000 Millionen USD (also 1 Billionen USD) beträgt...
AAVL 709 0,07% Avalanche Biotechnologies
ACAD 3.570 0,37% ACADIA Pharmaceuticals Inc.
ACHN 1.070 0,11% Achillion Pharmaceuticals
ACOR 1.250 0,13% Acorda Therapeutics
ACRX 176 0,02% AcelRx Pharmaceuticals
AEGR 674 0,07% Aegerion Pharmaceuticals
AERI 225 0,02% Aerie Pharmaceuticals
AFFX 909 0,09% Affymetrix
AGIO 3.560 0,37% Agios Pharmaceuticals
AKBA 144 0,01% Akebia Therapeutics
AKRX 4.900 0,51% Akorn
ALDR 1.010 0,10% Alder BioPharmaceuticals
ALIM 196 0,02% Alimera Sciences
ALKS 8.750 0,91% Alkermes plc
ALNY 8.950 0,93% Alnylam Pharmaceuticals
ALXN 34.870 3,61% Alexion Pharmaceuticals
AMAG 1.340 0,14% AMAG Pharmaceuticals
AMGN 121.870 12,61% Amgen Inc.
AMPH 651 0,07% Amphastar Pharmaceuticals
AMRI 570 0,06% Albany Molecular Research
ANAC 2.360 0,24% Anacor Pharmaceuticals
ANIP 718 0,07% ANI Pharmaceuticals
ARIA 1.720 0,18% ARIAD Pharmaceuticals
ARNA 1.050 0,11% Arena Pharmaceuticals
ARRY 883 0,09% Array BioPharma Inc.
ASPX 3.210 0,33% Auspex Pharmaceuticals
BCRX 677 0,07% BioCryst Pharmaceuticals
BIIB 90.610 9,38% Biogen Idec Inc.
BLUE 4.520 0,47% bluebird bio
BMRN 18.450 1,91% BioMarin Pharmaceutical Inc.
CARA 240 0,02% Cara Therapeutics
CCXI 309 0,03% ChemoCentryx
CELG 88.510 9,16% Celgene Corporation
CEMP 1.420 0,15% Cempra
CERS 421 0,04% Cerus Corporation
CGEN 329 0,03% Compugen Ltd.
CLDN 62 0,01% Celladon Corporation
CLDX 2.220 0,23% Celldex Therapeutics
CLVS 2.790 0,29% Clovis Oncology
CMRX 1.450 0,15% Chimerix
CNCE 271 0,03% Concert Pharmaceuticals
DEPO 1.420 0,15% Depomed
DYAX 3.410 0,35% Dyax Corp.
ECYT 251 0,03% Endocyte
ENDP 15.100 1,56% Endo International plc
ENTA 656 0,07% Enanta Pharmaceuticals
EPZM 551 0,06% Epizyme
EXEL 554 0,06% Exelixis
FLML 558 0,06% Flamel Technologies S.A.
FMI 1.330 0,14% Foundation Medicine
FOLD 998 0,10% Amicus Therapeutics
FPRX 530 0,05% Five Prime Therapeutics
GERN 620 0,06% Geron Corporation
GEVA 3.650 0,38% Synageva BioPharma Corp.
GHDX 910 0,09% Genomic Health
GILD 156.400 16,19% Gilead Sciences
GRFS 21.780 2,25% Grifols
GWPH 2.150 0,22% GW Pharmaceuticals Plc
HALO 1.970 0,20% Halozyme Therapeutics
HPTX 955 0,10% Hyperion Therapeutics
HZNP 3.660 0,38% Horizon Pharma plc
ICPT 5.770 0,60% Intercept Pharmaceuticals
ILMN 27.490 2,85% Illumina
IMGN 722 0,07% ImmunoGen
IMMU 360 0,04% Immunomedics
INCY 16.880 1,75% Incyte Corporation
INFI 641 0,07% Infinity Pharmaceuticals
INO 511 0,05% Inovio Pharmaceuticals
INSM 1.060 0,11% Insmed
INSY 1.890 0,20% Insys Therapeutics
IPXL 3.200 0,33% Impax Laboratories
IRWD 1.960 0,20% Ironwood Pharmaceuticals
ISIS 6.930 0,72% Isis Pharmaceuticals
JAZZ 10.960 1,13% Jazz Pharmaceuticals plc
KITE 2.190 0,23% Kite Pharma
KPTI 1.040 0,11% Karyopharm Therapeutics Inc.
KYTH 1.030 0,11% Kythera Biopharmaceuticals
LGND 1.560 0,16% Ligand Pharmaceuticals Incorpor
LMNX 680 0,07% Luminex Corporation
LXRX 754 0,08% Lexicon Pharmaceuticals
MACK 1.270 0,13% Merrimack Pharmaceuticals
MDCO 1.760 0,18% The Medicines Company
MDVN 9.810 1,02% Medivation
MGNX 892 0,09% MacroGenics
MNKD 1.660 0,17% MannKind Corporation
MNTA 969 0,10% Momenta Pharmaceuticals
MYGN 2.430 0,25% Myriad Genetics
MYL 27.960 2,89% Mylan Inc.
NBIX 2.740 0,28% Neurocrine Biosciences
NKTR 1.510 0,16% Nektar Therapeutics
NLNK 1.330 0,14% NewLink Genetics Corporation
NVAX 1.900 0,20% Novavax
OMED 711 0,07% OncoMed Pharmaceuticals
OMER 772 0,08% Omeros Corporation
OPHT 1.570 0,16% Ophthotech Corporation
OREX 825 0,09% Orexigen Therapeutics
OSIR 529 0,05% Osiris Therapeutics
PACB 423 0,04% Pacific Biosciences of Californ
PCRX 2.490 0,26% Pacira Pharmaceuticals
PDLI 1.120 0,12% PDL BioPharma
PETX 450 0,05% Aratana Therapeutics
PGNX 365 0,04% Progenics Pharmaceuticals Inc.
POZN 258 0,03% Pozen
PRTA 922 0,10% Prothena Corporation plc
PTCT 1.970 0,20% PTC Therapeutics
PTLA 1.840 0,19% Portola Pharmaceuticals
PTX 256 0,03% Pernix Therapeutics Holdings
QGEN 5.580 0,58% Qiagen N.V.
QLTI 189 0,02% QLT Inc.
RARE 2.130 0,22% Ultragenyx Pharmaceutical Inc.
RCPT 4.930 0,51% Receptos
RDUS 1.380 0,14% Radius Health
REGN 48.000 4,97% Regeneron Pharmaceuticals
RGEN 1.030 0,11% Repligen Corporation
RGLS 680 0,07% Regulus Therapeutics Inc.
RLYP 1.250 0,13% Relypsa
RPTP 667 0,07% Raptor Pharmaceutical Corp.
RTRX 594 0,06% Retrophin
RVNC 484 0,05% Revance Therapeutics
SAGE 1.540 0,16% Sage Therapeutics
SCLN 426 0,04% SciClone Pharmaceuticals
SCMP 819 0,08% Sucampo Pharmaceuticals
SGEN 4.230 0,44% Seattle Genetics
SGMO 886 0,09% Sangamo BioSciences
SGNT 751 0,08% Sagent Pharmaceuticals
SGYP 342 0,04% Synergy Pharmaceuticals
SHPG 47.710 4,94% Shire plc
SNTA 259 0,03% Synta Pharmaceuticals Corp.
SPPI 380 0,04% Spectrum Pharmaceuticals
SQNM 541 0,06% Sequenom
SRPT 526 0,05% Sarepta Therapeutics
SUPN 565 0,06% Supernus Pharmaceuticals
SVA 278 0,03% Sinovac Biotech
TBPH 559 0,06% Theravance Biopharma
TECH 3.590 0,37% Bio-Techne Corp
THRX 1.940 0,20% Theravance
TTPH 1.140 0,12% Tetraphase Pharmaceuticals
UTHR 7.980 0,83% United Therapeutics Corporation
VNDA 394 0,04% Vanda Pharmaceuticals Inc.
VRTX 30.410 3,15% Vertex Pharmaceuticals Incorpor
VSAR 407 0,04% Versartis
VSTM 307 0,03% Verastem
VVUS 240 0,02% VIVUS
XLRN 938 0,10% Acceleron Pharma Inc.
XNPT 382 0,04% XenoPort
XOMA 379 0,04% XOMA Corporation
ZFGN 863 0,09% Zafgen
ZSPH 972 0,10% ZS Pharma
Summe 966.097
GILD + AMGN + CELG + BIIB + REGN + ALXN + VRTX kommen zusammen auf 570 Mrd USD... das sind ca. 59% der NBI-Summe.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.694.601 von ipollit am 02.05.15 15:57:17bzw. nach MK sortiert...
Gruß
ipollit
GILD 156.400 16,19% Gilead Sciences
AMGN 121.870 12,61% Amgen Inc.
BIIB 90.610 9,38% Biogen Idec Inc.
CELG 88.510 9,16% Celgene Corporation
REGN 48.000 4,97% Regeneron Pharmaceuticals
SHPG 47.710 4,94% Shire plc
ALXN 34.870 3,61% Alexion Pharmaceuticals
VRTX 30.410 3,15% Vertex Pharmaceuticals Incorpor
MYL 27.960 2,89% Mylan Inc.
ILMN 27.490 2,85% Illumina
GRFS 21.780 2,25% Grifols
BMRN 18.450 1,91% BioMarin Pharmaceutical Inc.
INCY 16.880 1,75% Incyte Corporation
ENDP 15.100 1,56% Endo International plc
JAZZ 10.960 1,13% Jazz Pharmaceuticals plc
MDVN 9.810 1,02% Medivation
ALNY 8.950 0,93% Alnylam Pharmaceuticals
ALKS 8.750 0,91% Alkermes plc
UTHR 7.980 0,83% United Therapeutics Corporation
ISIS 6.930 0,72% Isis Pharmaceuticals
ICPT 5.770 0,60% Intercept Pharmaceuticals
QGEN 5.580 0,58% Qiagen N.V.
RCPT 4.930 0,51% Receptos
AKRX 4.900 0,51% Akorn
BLUE 4.520 0,47% bluebird bio
SGEN 4.230 0,44% Seattle Genetics
HZNP 3.660 0,38% Horizon Pharma plc
GEVA 3.650 0,38% Synageva BioPharma Corp.
TECH 3.590 0,37% Bio-Techne Corp
ACAD 3.570 0,37% ACADIA Pharmaceuticals Inc.
AGIO 3.560 0,37% Agios Pharmaceuticals
DYAX 3.410 0,35% Dyax Corp.
ASPX 3.210 0,33% Auspex Pharmaceuticals
IPXL 3.200 0,33% Impax Laboratories
CLVS 2.790 0,29% Clovis Oncology
NBIX 2.740 0,28% Neurocrine Biosciences
PCRX 2.490 0,26% Pacira Pharmaceuticals
MYGN 2.430 0,25% Myriad Genetics
ANAC 2.360 0,24% Anacor Pharmaceuticals
CLDX 2.220 0,23% Celldex Therapeutics
KITE 2.190 0,23% Kite Pharma
GWPH 2.150 0,22% GW Pharmaceuticals Plc
RARE 2.130 0,22% Ultragenyx Pharmaceutical Inc.
HALO 1.970 0,20% Halozyme Therapeutics
PTCT 1.970 0,20% PTC Therapeutics
IRWD 1.960 0,20% Ironwood Pharmaceuticals
THRX 1.940 0,20% Theravance
NVAX 1.900 0,20% Novavax
INSY 1.890 0,20% Insys Therapeutics
PTLA 1.840 0,19% Portola Pharmaceuticals
MDCO 1.760 0,18% The Medicines Company
ARIA 1.720 0,18% ARIAD Pharmaceuticals
MNKD 1.660 0,17% MannKind Corporation
OPHT 1.570 0,16% Ophthotech Corporation
LGND 1.560 0,16% Ligand Pharmaceuticals Incorpor
SAGE 1.540 0,16% Sage Therapeutics
NKTR 1.510 0,16% Nektar Therapeutics
CMRX 1.450 0,15% Chimerix
CEMP 1.420 0,15% Cempra
DEPO 1.420 0,15% Depomed
RDUS 1.380 0,14% Radius Health
AMAG 1.340 0,14% AMAG Pharmaceuticals
FMI 1.330 0,14% Foundation Medicine
NLNK 1.330 0,14% NewLink Genetics Corporation
MACK 1.270 0,13% Merrimack Pharmaceuticals
ACOR 1.250 0,13% Acorda Therapeutics
RLYP 1.250 0,13% Relypsa
TTPH 1.140 0,12% Tetraphase Pharmaceuticals
PDLI 1.120 0,12% PDL BioPharma
ACHN 1.070 0,11% Achillion Pharmaceuticals
INSM 1.060 0,11% Insmed
ARNA 1.050 0,11% Arena Pharmaceuticals
KPTI 1.040 0,11% Karyopharm Therapeutics Inc.
KYTH 1.030 0,11% Kythera Biopharmaceuticals
RGEN 1.030 0,11% Repligen Corporation
ALDR 1.010 0,10% Alder BioPharmaceuticals
FOLD 998 0,10% Amicus Therapeutics
ZSPH 972 0,10% ZS Pharma
MNTA 969 0,10% Momenta Pharmaceuticals
HPTX 955 0,10% Hyperion Therapeutics
XLRN 938 0,10% Acceleron Pharma Inc.
PRTA 922 0,10% Prothena Corporation plc
GHDX 910 0,09% Genomic Health
AFFX 909 0,09% Affymetrix
MGNX 892 0,09% MacroGenics
SGMO 886 0,09% Sangamo BioSciences
ARRY 883 0,09% Array BioPharma Inc.
ZFGN 863 0,09% Zafgen
OREX 825 0,09% Orexigen Therapeutics
SCMP 819 0,08% Sucampo Pharmaceuticals
OMER 772 0,08% Omeros Corporation
LXRX 754 0,08% Lexicon Pharmaceuticals
SGNT 751 0,08% Sagent Pharmaceuticals
IMGN 722 0,07% ImmunoGen
ANIP 718 0,07% ANI Pharmaceuticals
OMED 711 0,07% OncoMed Pharmaceuticals
AAVL 709 0,07% Avalanche Biotechnologies
RGLS 680 0,07% Regulus Therapeutics Inc.
LMNX 680 0,07% Luminex Corporation
BCRX 677 0,07% BioCryst Pharmaceuticals
AEGR 674 0,07% Aegerion Pharmaceuticals
RPTP 667 0,07% Raptor Pharmaceutical Corp.
ENTA 656 0,07% Enanta Pharmaceuticals
AMPH 651 0,07% Amphastar Pharmaceuticals
INFI 641 0,07% Infinity Pharmaceuticals
GERN 620 0,06% Geron Corporation
RTRX 594 0,06% Retrophin
AMRI 570 0,06% Albany Molecular Research
SUPN 565 0,06% Supernus Pharmaceuticals
TBPH 559 0,06% Theravance Biopharma
FLML 558 0,06% Flamel Technologies S.A.
EXEL 554 0,06% Exelixis
EPZM 551 0,06% Epizyme
SQNM 541 0,06% Sequenom
FPRX 530 0,05% Five Prime Therapeutics
OSIR 529 0,05% Osiris Therapeutics
SRPT 526 0,05% Sarepta Therapeutics
INO 511 0,05% Inovio Pharmaceuticals
RVNC 484 0,05% Revance Therapeutics
PETX 450 0,05% Aratana Therapeutics
SCLN 426 0,04% SciClone Pharmaceuticals
PACB 423 0,04% Pacific Biosciences of Californ
CERS 421 0,04% Cerus Corporation
VSAR 407 0,04% Versartis
VNDA 394 0,04% Vanda Pharmaceuticals Inc.
XNPT 382 0,04% XenoPort
SPPI 380 0,04% Spectrum Pharmaceuticals
XOMA 379 0,04% XOMA Corporation
PGNX 365 0,04% Progenics Pharmaceuticals Inc.
IMMU 360 0,04% Immunomedics
SGYP 342 0,04% Synergy Pharmaceuticals
CGEN 329 0,03% Compugen Ltd.
CCXI 309 0,03% ChemoCentryx
VSTM 307 0,03% Verastem
SVA 278 0,03% Sinovac Biotech
CNCE 271 0,03% Concert Pharmaceuticals
SNTA 259 0,03% Synta Pharmaceuticals Corp.
POZN 258 0,03% Pozen
PTX 256 0,03% Pernix Therapeutics Holdings
ECYT 251 0,03% Endocyte
CARA 240 0,02% Cara Therapeutics
VVUS 240 0,02% VIVUS
AERI 225 0,02% Aerie Pharmaceuticals
ALIM 196 0,02% Alimera Sciences
QLTI 189 0,02% QLT Inc.
ACRX 176 0,02% AcelRx Pharmaceuticals
AKBA 144 0,01% Akebia Therapeutics
CLDN 62 0,01% Celladon Corporation
Summe NBI 966.097
Gruß
ipollit
vielen Dank ipollit
im grunde alle börsennotierten ...
im grunde alle börsennotierten ...
Noch jemand bei AERI dabei?
Meldung vom 28.04.15:
"Aerie Pharmaceuticals, Inc. (AERI) (the “Company”), announced today that its first quarter 2015 financial results will be released after the market closes on Thursday, May 7, 2015. Following the release, the Company will host a live conference call and webcast at 5:00 p.m. Eastern Time to discuss the Company's financial results and provide a general business and strategic update. Additionally, the Company has been continuing to review the results of its first Phase 3 registration trial (“Rocket 1”) for Rhopressa™ and expects to discuss additional findings from the Rocket 1 study during the live conference call and webcast."
Spekulativer Anstieg vom aktuellen Low möglich.
Meldung vom 28.04.15:
"Aerie Pharmaceuticals, Inc. (AERI) (the “Company”), announced today that its first quarter 2015 financial results will be released after the market closes on Thursday, May 7, 2015. Following the release, the Company will host a live conference call and webcast at 5:00 p.m. Eastern Time to discuss the Company's financial results and provide a general business and strategic update. Additionally, the Company has been continuing to review the results of its first Phase 3 registration trial (“Rocket 1”) for Rhopressa™ and expects to discuss additional findings from the Rocket 1 study during the live conference call and webcast."
Spekulativer Anstieg vom aktuellen Low möglich.
Antwort auf Beitrag Nr.: 49.694.349 von ipollit am 02.05.15 14:34:47"Warum ist ein Crash überfällig sein? Gibt es dafür eine andere Begründung (insbesondere eine fundamentale), als dass die Kurse in den letzten Jahren deutlich gestiegen sind?"
Hallo ipollit, danke für Deinen Beitrag! Es ist natürlich immer entscheidend, die fundamentalen Fakten im Blick zu behalten und ich kann Deinen Argumenten im Grunde allen folgen.
Vielleicht muss man aber kurz die Begriffe "Korrektur" und "Crash" noch definieren. Für mich ist eine Korrektur ein Marktgeschehen, das einen Index um mehr als 10% nach unten treibt. Eine "heftige Korrektur" wäre dann etwas ab -20%.
Von einem "Crash" spreche ich ab -30%.
Die Kurse sind gerade auch im Jahr 2015 bis Ende März mit nochmals gesteigerter Dynamik stark gestiegen. Insofern halte ich zumindest eine Korrektur für geradezu notwendig. Diese Art der Aufwärtsdynamik sollte eher früher als später gebrochen werden. Übertreibungen nach unten sind dabei natürlich immer möglich (das wäre dann der Crash mit -30% oder schlimmer).
Von der fundamentalen Seite her sehe ich durchaus Warnzeichen. Um zu vernünftigen Bewertungen der großen Biotechs zu kommen, muss man auf 2017 schauen. 2016 reicht nicht mehr, weil die KGVs dann schon zu hoch sind. Fundamental wäre eine Korrektur vom jetzigen Niveau aus um weitere 10% sicher nicht unsinnig.
Zur Vorsicht mahnt auch die prächtige IPO-Stimmung. Vielversprechende (oder doch nur viel versprechende?) Unternehmen haben keine Probleme, in einer sehr frühen Entwicklungsphase - teilweise noch vorklinisch - an die Börse zu gehen und erhalten sofort Milliarden-Bewertungen.
Natürlich gibt es gerade derzeit auch echte Fortschritte, teilweise revolutionäre Fortschritte (ich bin ja selbst sehr fasziniert), aber es herrscht schon eine ziemliche Euphorie und Goldgräberstimmung und so etwas war noch nie ein gutes Zeichen.
Gruß
SLG
Hallo ipollit, danke für Deinen Beitrag! Es ist natürlich immer entscheidend, die fundamentalen Fakten im Blick zu behalten und ich kann Deinen Argumenten im Grunde allen folgen.
Vielleicht muss man aber kurz die Begriffe "Korrektur" und "Crash" noch definieren. Für mich ist eine Korrektur ein Marktgeschehen, das einen Index um mehr als 10% nach unten treibt. Eine "heftige Korrektur" wäre dann etwas ab -20%.
Von einem "Crash" spreche ich ab -30%.
Die Kurse sind gerade auch im Jahr 2015 bis Ende März mit nochmals gesteigerter Dynamik stark gestiegen. Insofern halte ich zumindest eine Korrektur für geradezu notwendig. Diese Art der Aufwärtsdynamik sollte eher früher als später gebrochen werden. Übertreibungen nach unten sind dabei natürlich immer möglich (das wäre dann der Crash mit -30% oder schlimmer).
Von der fundamentalen Seite her sehe ich durchaus Warnzeichen. Um zu vernünftigen Bewertungen der großen Biotechs zu kommen, muss man auf 2017 schauen. 2016 reicht nicht mehr, weil die KGVs dann schon zu hoch sind. Fundamental wäre eine Korrektur vom jetzigen Niveau aus um weitere 10% sicher nicht unsinnig.
Zur Vorsicht mahnt auch die prächtige IPO-Stimmung. Vielversprechende (oder doch nur viel versprechende?) Unternehmen haben keine Probleme, in einer sehr frühen Entwicklungsphase - teilweise noch vorklinisch - an die Börse zu gehen und erhalten sofort Milliarden-Bewertungen.
Natürlich gibt es gerade derzeit auch echte Fortschritte, teilweise revolutionäre Fortschritte (ich bin ja selbst sehr fasziniert), aber es herrscht schon eine ziemliche Euphorie und Goldgräberstimmung und so etwas war noch nie ein gutes Zeichen.
Gruß
SLG
Antwort auf Beitrag Nr.: 49.696.593 von SLGramann am 03.05.15 09:57:04Aus fundamentaler Sicht kann ich zur aktuellen Marktbewertung wenig beitragen. Aber zwei Aspekte aus dem NBI-Chart sind möglicherweise hilfreich:
Der steile Aufwärtstrend, den der NBI seit Ende 2011 ausgebildet hat, hat eine Steigung von knapp über 40% pro Jahr. Und die untere Trendbegrenzung verläuft momentan bei etwa 3200 bis 3300 Punkten, was gut mit GD200 im Daily bzw. GD38 im Weekly (s. blaue Linie im Bild) zusammenfällt. Eine Korrektur hätte also noch etwa 10% Luft nach unten, ohne dass dieser steile Trend gebrochen wird. Dass ein Bruch jedoch irgendwann erfolgen muss, ist aufgrund der extremen Steigung sicher. 40% Wachstum p.a. ist auf Dauer nicht durchzuhalten.

Der steile Aufwärtstrend, den der NBI seit Ende 2011 ausgebildet hat, hat eine Steigung von knapp über 40% pro Jahr. Und die untere Trendbegrenzung verläuft momentan bei etwa 3200 bis 3300 Punkten, was gut mit GD200 im Daily bzw. GD38 im Weekly (s. blaue Linie im Bild) zusammenfällt. Eine Korrektur hätte also noch etwa 10% Luft nach unten, ohne dass dieser steile Trend gebrochen wird. Dass ein Bruch jedoch irgendwann erfolgen muss, ist aufgrund der extremen Steigung sicher. 40% Wachstum p.a. ist auf Dauer nicht durchzuhalten.

Zum Thema Bewertung der Biotechs eine Übersicht von Mark Schoenbaum, der anmerkt, dass die Bewertung der großen Biotechs momentan unter dem Schnitt des S&P 500 liegt. (leider nicht lesbar ich denke aber, dass das KGV dargestellt ist) Und das erst zum 2. mal innerhalb der letzten 10 Jahre. Das widerlegt natürlich erstmal die These einer allgemeinen Biotechblase.
Ich denke eigentlich auch, dass die fundamentalen Rahmenbedingungen extrem positiv sind und auch bleiben werden. Einen Crash wird es wohl erst geben, wenn das Geschäftsmodell "hohe Preise für Innovation" ernsthaft in Frage gestelt wird.

Hält die 100 Tageslinie?

http://blogs.barrons.com/stockstowatchtoday/2015/05/01/a-bio…
SG kmastra
Ich denke eigentlich auch, dass die fundamentalen Rahmenbedingungen extrem positiv sind und auch bleiben werden. Einen Crash wird es wohl erst geben, wenn das Geschäftsmodell "hohe Preise für Innovation" ernsthaft in Frage gestelt wird.

Hält die 100 Tageslinie?

http://blogs.barrons.com/stockstowatchtoday/2015/05/01/a-bio…
SG kmastra
Antwort auf Beitrag Nr.: 49.694.976 von Aurum2010 am 02.05.15 18:42:10
10.92 Up 1.55(16.54%)
Aerie Pharma: Was Rocket 1 Really A Failure?
http://seekingalpha.com/article/3136616-aerie-pharma-was-roc…
Zitat von Aurum2010: Noch jemand bei AERI dabei?
Meldung vom 28.04.15:
"Aerie Pharmaceuticals, Inc. (AERI) (the “Company”), announced today that its first quarter 2015 financial results will be released after the market closes on Thursday, May 7, 2015. Following the release, the Company will host a live conference call and webcast at 5:00 p.m. Eastern Time to discuss the Company's financial results and provide a general business and strategic update. Additionally, the Company has been continuing to review the results of its first Phase 3 registration trial (“Rocket 1”) for Rhopressa™ and expects to discuss additional findings from the Rocket 1 study during the live conference call and webcast."
Spekulativer Anstieg vom aktuellen Low möglich.
10.92 Up 1.55(16.54%)
Aerie Pharma: Was Rocket 1 Really A Failure?
http://seekingalpha.com/article/3136616-aerie-pharma-was-roc…
ADAP:
Adaptimmune Therapeutics prices upsized IPO at $17, the high end of the range
5/5/15
Adaptimmune Therapeutics, which is developing cancer immunotherapies using genetically enhanced T-cell receptors, raised $191 million by offering 11.3 million shares at $17, at high end of the $15-$17 range. At its offer price, Adaptimmune Therapeutics will command a fully diluted market cap at $1.3 billion. The company will list on the NASDAQ under the symbol ADAP. BofA Merrill Lynch, Cowen & Company and Leerink Partners acted as lead managers on the deal.
Damit werden mehr Aktien verkauft, als zunächst geplant. Das IPO-Fenster ist also noch immer weit offen, obschon ADAP natürlich auch wirklich Qualität hat.
Bin auf den Eröffnungskurs gespannt. Sicher noch mal deutlich höher als 17 Dollar.
Ob die Leute beachten, dass ihr vielversprechendes Lead-Programm (NY-ESO) zu wirklich miesen Konditionen auslizensiert worden ist? Die Royalties dürften im Schnitt kaum über 8% liegen.
Adaptimmune Therapeutics prices upsized IPO at $17, the high end of the range
5/5/15
Adaptimmune Therapeutics, which is developing cancer immunotherapies using genetically enhanced T-cell receptors, raised $191 million by offering 11.3 million shares at $17, at high end of the $15-$17 range. At its offer price, Adaptimmune Therapeutics will command a fully diluted market cap at $1.3 billion. The company will list on the NASDAQ under the symbol ADAP. BofA Merrill Lynch, Cowen & Company and Leerink Partners acted as lead managers on the deal.
Damit werden mehr Aktien verkauft, als zunächst geplant. Das IPO-Fenster ist also noch immer weit offen, obschon ADAP natürlich auch wirklich Qualität hat.
Bin auf den Eröffnungskurs gespannt. Sicher noch mal deutlich höher als 17 Dollar.
Ob die Leute beachten, dass ihr vielversprechendes Lead-Programm (NY-ESO) zu wirklich miesen Konditionen auslizensiert worden ist? Die Royalties dürften im Schnitt kaum über 8% liegen.
QURE:
Nachdem es zuletzt einige Verwirrung in Bezug auf Glybera gab und generell alles sehr schwarz gesehen wurde, hat sich dieser - ohnehin eher unwichtige - Punkt jetzt zunächst mal entspannt:


Nachdem es zuletzt einige Verwirrung in Bezug auf Glybera gab und generell alles sehr schwarz gesehen wurde, hat sich dieser - ohnehin eher unwichtige - Punkt jetzt zunächst mal entspannt:


Antwort auf Beitrag Nr.: 49.717.623 von SLGramann am 06.05.15 06:38:59ADAP:
Zunächst mal Kurse in der Nähe des IPO-Preises. Sogar kurz drunter.
Jedoch: Laut Auskunft S Broker ist die Aktie zumindest heute noch nicht aus Deutschland handelbar.
Oh man. Ich finde das echt ärgerlich.
Hat jemand anderswo andere Auskünfte bekommen?
PS: Muss man denn echt zu einem US-Broker wechseln, um vernünftig arbeiten zu können?
Ich komme mir manchmal vor, als lebte ich in Kirgisien...
Zunächst mal Kurse in der Nähe des IPO-Preises. Sogar kurz drunter.
Jedoch: Laut Auskunft S Broker ist die Aktie zumindest heute noch nicht aus Deutschland handelbar.
Oh man. Ich finde das echt ärgerlich.
Hat jemand anderswo andere Auskünfte bekommen?
PS: Muss man denn echt zu einem US-Broker wechseln, um vernünftig arbeiten zu können?
Ich komme mir manchmal vor, als lebte ich in Kirgisien...
Antwort auf Beitrag Nr.: 49.710.135 von Aurum2010 am 05.05.15 11:40:16
Präsentation des gestrigen CC's:
http://files.shareholder.com/downloads/AMDA-29CD43/152537223…
Zitat von Aurum2010:Zitat von Aurum2010: Noch jemand bei AERI dabei?
Meldung vom 28.04.15:
"Aerie Pharmaceuticals, Inc. (AERI) (the “Company”), announced today that its first quarter 2015 financial results will be released after the market closes on Thursday, May 7, 2015. Following the release, the Company will host a live conference call and webcast at 5:00 p.m. Eastern Time to discuss the Company's financial results and provide a general business and strategic update. Additionally, the Company has been continuing to review the results of its first Phase 3 registration trial (“Rocket 1”) for Rhopressa™ and expects to discuss additional findings from the Rocket 1 study during the live conference call and webcast."
Spekulativer Anstieg vom aktuellen Low möglich.
10.92 Up 1.55(16.54%)
Aerie Pharma: Was Rocket 1 Really A Failure?
http://seekingalpha.com/article/3136616-aerie-pharma-was-roc…
Präsentation des gestrigen CC's:
http://files.shareholder.com/downloads/AMDA-29CD43/152537223…
Antwort auf Beitrag Nr.: 49.723.956 von SLGramann am 06.05.15 17:30:35Die Langsamkeit des deutschen WM-Systems hat mich ja nun dazu verurteilt, mit dem ADAP-Kauf bis gestern zu warten. Zur Börseneröffnung habe ich dann einen Kurs von 15,75 Dollar bekommen. Da war die deutsche Lahmarschigkeit mal gar nicht so verkehrt... 


Ich sehe ADAP als langfristigen Technologie-Play im TCR-Bereich.
Ihr Lead-Programm haben sie an GSK geradezu verschenkt. Für einen wirklichen Werttreiber - über die ja nicht anspruchslose heutige Börsenbewertung hinaus - wird es auf weitere Erfolge von Kandidaten ankommen, die heute noch in der Vorklinik stecken.
Insofern "lohnt" sich hier ein Investment wohl nur für jemanden, der TCR und ADAP vielversprechend findet.



Ich sehe ADAP als langfristigen Technologie-Play im TCR-Bereich.
Ihr Lead-Programm haben sie an GSK geradezu verschenkt. Für einen wirklichen Werttreiber - über die ja nicht anspruchslose heutige Börsenbewertung hinaus - wird es auf weitere Erfolge von Kandidaten ankommen, die heute noch in der Vorklinik stecken.
Insofern "lohnt" sich hier ein Investment wohl nur für jemanden, der TCR und ADAP vielversprechend findet.
MDVN
Die Q1-Zahlen von Xtandi waren nicht so berauschend... dies hat allerdings saisonale Gründe und zeigt nicht etwa ein generelles Abschwächen der Umsatzzuwächse: US-Umsätze 224 Mio USD (split mit Astellas) und ex-US-Umsätze 133 Mio USD (10-22% Royalties). Im gesamten Jahr sollen die US-Umsätze bei insgesamt etwa 1 - 1,25 Mrd USD liegen... d.h. die weltweiten Umsätze werden wohl nächstes Jahr die 2 Mrd USD übersteigen, langfristig könnten es mehr als 6 Mrd USD sein.
Zur ASCO soll es ein Update von Xtandi in TNBC Brustkrebs geben... bisher waren die Ergebnisse noch nicht so herausragend, also high-risk bzw. mögliches Upside. Im Folgenden ist von einer möglichen Konkurrenz von IO in TNBC die Rede... allerdings sehe ich eine mögliche Synergie mit IO, wenn es darauf ankommt.




Gruß
ipollit
Die Q1-Zahlen von Xtandi waren nicht so berauschend... dies hat allerdings saisonale Gründe und zeigt nicht etwa ein generelles Abschwächen der Umsatzzuwächse: US-Umsätze 224 Mio USD (split mit Astellas) und ex-US-Umsätze 133 Mio USD (10-22% Royalties). Im gesamten Jahr sollen die US-Umsätze bei insgesamt etwa 1 - 1,25 Mrd USD liegen... d.h. die weltweiten Umsätze werden wohl nächstes Jahr die 2 Mrd USD übersteigen, langfristig könnten es mehr als 6 Mrd USD sein.
Zur ASCO soll es ein Update von Xtandi in TNBC Brustkrebs geben... bisher waren die Ergebnisse noch nicht so herausragend, also high-risk bzw. mögliches Upside. Im Folgenden ist von einer möglichen Konkurrenz von IO in TNBC die Rede... allerdings sehe ich eine mögliche Synergie mit IO, wenn es darauf ankommt.



Gruß
ipollit
ACAD
ACAD peilt nach wie vor den US-Zulassungsantrag von Nuplazid in PDP in 2H15 an... sie wollen bewusst keinen konkreteren Zeitraum nennen, um nicht erneut den NDA verschieben zu müssen. Dabei geht es nicht um den eigentlichen Antrag, da dieser bereits fertig ist, sondern um Papiere und Verfahren der industriellen Herstellung, die nicht zum Antrag selber gehören aber trotzdem von der FDA überprüft werden.

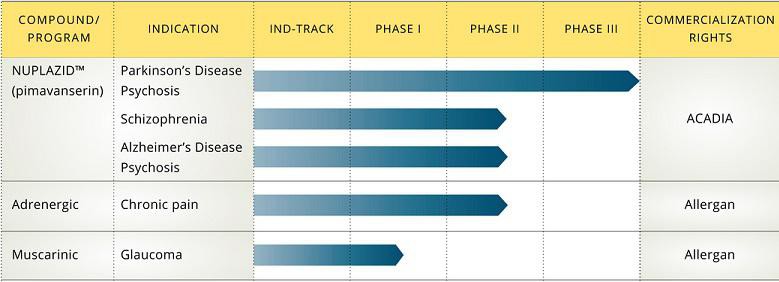
Neben PDP und ADP wird Nuplazid auch bei allgemeiner Schizophrenie getestet in Kombi mit etablierten Mitteln. Ziel ist hierbei eine gleiche Wirkung wie bisherige Mittel zu erreichen bei gleichzeitig deutlich reduzierten Nebenwirkungen... insbesondere für die längere Behandlungsdauer.
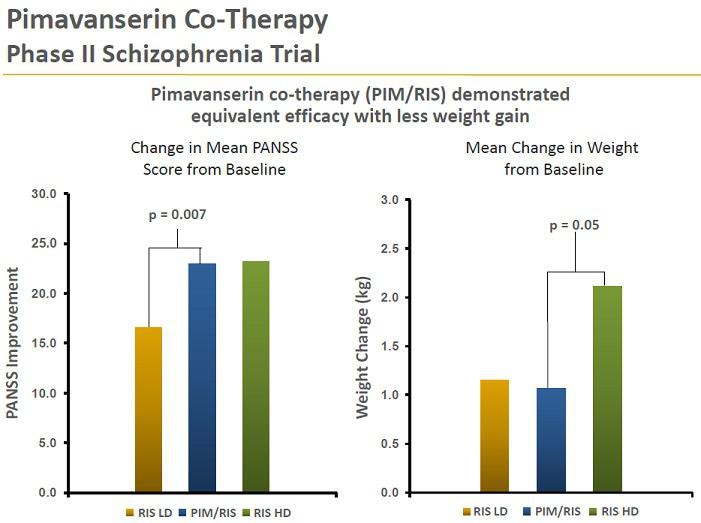
Zusätzlich sind auch Studien bei Schlafstörungen geplant... Nuplazid scheint sich hier auch positiv auszuwirken und ist relativ verträglich.
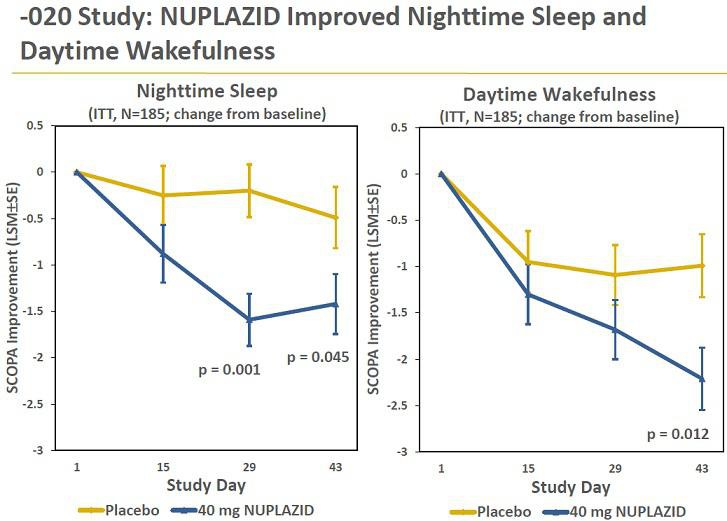

Gruß
ipollit
ACAD peilt nach wie vor den US-Zulassungsantrag von Nuplazid in PDP in 2H15 an... sie wollen bewusst keinen konkreteren Zeitraum nennen, um nicht erneut den NDA verschieben zu müssen. Dabei geht es nicht um den eigentlichen Antrag, da dieser bereits fertig ist, sondern um Papiere und Verfahren der industriellen Herstellung, die nicht zum Antrag selber gehören aber trotzdem von der FDA überprüft werden.


Neben PDP und ADP wird Nuplazid auch bei allgemeiner Schizophrenie getestet in Kombi mit etablierten Mitteln. Ziel ist hierbei eine gleiche Wirkung wie bisherige Mittel zu erreichen bei gleichzeitig deutlich reduzierten Nebenwirkungen... insbesondere für die längere Behandlungsdauer.

Zusätzlich sind auch Studien bei Schlafstörungen geplant... Nuplazid scheint sich hier auch positiv auszuwirken und ist relativ verträglich.

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.747.965 von ipollit am 09.05.15 20:31:39CNS... ACAD, SAGE
Hier ist ein guter Artikel, der deutliche Fortschritte in der Behandlung von CNS-Erkrankungen sieht, indem man mehr und mehr die Ursachen der Krankheiten erkennt. Früher war vieles zufällig ohne wirkliches Verständnis der Ursachen... die bisherigen Medikamente sind daher "unscharf" mit vielen Nebenwirkungen und nur eingeschränkter Wirkung.
http://www.forbes.com/sites/matthewherper/2015/02/11/brain-b…
"... THE HISTORY OF BRAIN DRUGS IS BASED ALMOST entirely on luck. The first antipsychotic, Thorazine, was tried on schizophrenics in the 1950s as a sedative and miraculously stopped their hallucinations. The first antidepressant, imipramine, was an attempt at making a new antipsychotic that failed but turned out to improve mood.
New blockbuster brain drugs of the past few decades–Prozac, Celexa, Zoloft, Zyprexa, Risperdal, Abilify–all mostly plumb the same basic mechanisms as the old ones: boosting neurotransmitters like serotonin for the antidepressants; blocking the dopamine receptor D2 for antipsychotics. They differ somewhat with regard to efficacy and a lot with regard to side effects, but they operate in essentially similar ways. For years drug companies have been trying out new drugs that hit other chemicals without a good understanding of whether, or in whom, they’ll work.
But thanks to the revolution in our understanding of the human genome and other advances, scientists are finally starting to grasp the overwhelming complexity of illnesses that afflict the brain–and how to treat them. “Depression isn’t one disease, it’s many diseases,” says Novartis’ Fishman, who finds the new insights hopeful rather than discouraging. “Like cancer, once you understand the disease you have hope for making drugs,” he says.
Some of the improvements are incremental. Psychiatry clinical trials often fail because placebo groups do better than they should. Part of the problem is that patients can exaggerate their symptoms to get into a study, and developing a relationship with their new doctor actually makes their symptoms seem better.
Acadia Pharmaceuticals watched its Nuplazid, for Parkinson’s psychosis, fail in a clinical trial. In 2013 it ran another study that used videoconferencing, having the same specially trained group of doctors rate the symptoms of all patients. The dramatically positive results have sent the stock up 437% and have shown other companies that psychiatry trials can still succeed. “We expect to become the leading neurology company in the U.S.,” crows Acadia Chief Executive Uli Hacksell.
...
Another way to find drugs that have big effects: develop treatments for rare, terrible diseases, where creating any hope can change people’s lives. That’s the approach taken by Sage Therapeutics, a Cambridge, Mass.-based startup that went public in July, as it attacks a rare form of epilepsy.
Melissa Fishburn, 21, started having seizures at 14. Last November she stiffened like a board and fell to the ground in a seizure that would not end. Doctors put her in a medically induced coma because the only hope for patients with this condition is that after resting the patient can be brought back to consciousness and the seizure will have stopped.
But for Melissa, seizures were detectable on an electroencephalogram (EEG) even when she was fully unconscious. Doctors tried every drug they could think of, and nothing worked. “They were telling us either the seizures or the medication would end her life, one way or another,” says her father, Dale.
Melissa’s sister read about Sage’s experimental drug, Sage-547, on the Internet. It blocks haywire electrical signals from jumping across nerve synapses in the brain and central nervous system. Dale mentioned it to her neurologist. Melissa, still in a coma, was flown from Springfield, Mo. to Wichita, Kans. to be part of a clinical trial.
After 24 hours her EEG readings improved. Six days later doctors started to wean her off of the drugs that kept her in a coma. A few days after that she regained consciousness. Now she loves singing Ed Sheeran songs at karaoke. It’s not perfect: She’s never been on a date and takes 22 pills a day. But because of the Sage treatment, she’s alive.
TREATMENTS LIKE SAGE’S ARE JUST THE START of the changes scientists hope to bring about in the way we battle brain disease ... "
Gruß
ipollit
Hier ist ein guter Artikel, der deutliche Fortschritte in der Behandlung von CNS-Erkrankungen sieht, indem man mehr und mehr die Ursachen der Krankheiten erkennt. Früher war vieles zufällig ohne wirkliches Verständnis der Ursachen... die bisherigen Medikamente sind daher "unscharf" mit vielen Nebenwirkungen und nur eingeschränkter Wirkung.
http://www.forbes.com/sites/matthewherper/2015/02/11/brain-b…
"... THE HISTORY OF BRAIN DRUGS IS BASED ALMOST entirely on luck. The first antipsychotic, Thorazine, was tried on schizophrenics in the 1950s as a sedative and miraculously stopped their hallucinations. The first antidepressant, imipramine, was an attempt at making a new antipsychotic that failed but turned out to improve mood.
New blockbuster brain drugs of the past few decades–Prozac, Celexa, Zoloft, Zyprexa, Risperdal, Abilify–all mostly plumb the same basic mechanisms as the old ones: boosting neurotransmitters like serotonin for the antidepressants; blocking the dopamine receptor D2 for antipsychotics. They differ somewhat with regard to efficacy and a lot with regard to side effects, but they operate in essentially similar ways. For years drug companies have been trying out new drugs that hit other chemicals without a good understanding of whether, or in whom, they’ll work.
But thanks to the revolution in our understanding of the human genome and other advances, scientists are finally starting to grasp the overwhelming complexity of illnesses that afflict the brain–and how to treat them. “Depression isn’t one disease, it’s many diseases,” says Novartis’ Fishman, who finds the new insights hopeful rather than discouraging. “Like cancer, once you understand the disease you have hope for making drugs,” he says.
Some of the improvements are incremental. Psychiatry clinical trials often fail because placebo groups do better than they should. Part of the problem is that patients can exaggerate their symptoms to get into a study, and developing a relationship with their new doctor actually makes their symptoms seem better.
Acadia Pharmaceuticals watched its Nuplazid, for Parkinson’s psychosis, fail in a clinical trial. In 2013 it ran another study that used videoconferencing, having the same specially trained group of doctors rate the symptoms of all patients. The dramatically positive results have sent the stock up 437% and have shown other companies that psychiatry trials can still succeed. “We expect to become the leading neurology company in the U.S.,” crows Acadia Chief Executive Uli Hacksell.
...
Another way to find drugs that have big effects: develop treatments for rare, terrible diseases, where creating any hope can change people’s lives. That’s the approach taken by Sage Therapeutics, a Cambridge, Mass.-based startup that went public in July, as it attacks a rare form of epilepsy.
Melissa Fishburn, 21, started having seizures at 14. Last November she stiffened like a board and fell to the ground in a seizure that would not end. Doctors put her in a medically induced coma because the only hope for patients with this condition is that after resting the patient can be brought back to consciousness and the seizure will have stopped.
But for Melissa, seizures were detectable on an electroencephalogram (EEG) even when she was fully unconscious. Doctors tried every drug they could think of, and nothing worked. “They were telling us either the seizures or the medication would end her life, one way or another,” says her father, Dale.
Melissa’s sister read about Sage’s experimental drug, Sage-547, on the Internet. It blocks haywire electrical signals from jumping across nerve synapses in the brain and central nervous system. Dale mentioned it to her neurologist. Melissa, still in a coma, was flown from Springfield, Mo. to Wichita, Kans. to be part of a clinical trial.
After 24 hours her EEG readings improved. Six days later doctors started to wean her off of the drugs that kept her in a coma. A few days after that she regained consciousness. Now she loves singing Ed Sheeran songs at karaoke. It’s not perfect: She’s never been on a date and takes 22 pills a day. But because of the Sage treatment, she’s alive.
TREATMENTS LIKE SAGE’S ARE JUST THE START of the changes scientists hope to bring about in the way we battle brain disease ... "
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.748.256 von ipollit am 09.05.15 23:05:37ITCI & ACAD
Bei der Parkinson-Erkrankung sterben die dopaminproduzierenden Nervenzellen, wodurch immer weniger Dopamin gebildet wird, welches für die Signalübertragung an die Muskeln notwendig ist. Die Patienten haben Bewegungseinschränkungen bis hin zur völligen Bewegungslosigkeit. Die Krankheit wird daher u.a. behandelt, indem man versucht, den Dopamin-Mangel auszugleichen.
Dopamin ist an vielen Prozessen im Gehirn beteiligt. Parkinson-Patienten können auch psychotische Störungen wie Halluzinationen, Ängste usw bekommen. An Psychosen sind u.a. Dopamin und Serotonin beteiligt. Die meisten Mittel gegen Psychosen wirken auf Serotonin über 5-HT2A und Dopamin über z.B. D2.
Parkinson-Patienten mit Psychosen lassen sich bisher aber nur schlecht behandeln, da die bisherigen Mittel eben auch das Dopamin hemmen, dass bei Parkinson bereits zu gering ist. Außerdem ist es eine Alters-Erkrankung... Antipsychotika sind aber oft unspezifisch, weshalb sie viele Nebenwirkungen haben, z.B. aufs Herz, die im Alter sehr problematisch sind.
Hier setzt ACADs Nuplazid an... es wirkt spezifisch auf 5-HT2A und nicht auf u.a. D2. Bei Parkison ist das von Vorteil, weshalb es gerade bei PDP sehr aussichtsreich ist.
In anderen Erkrankungen wie Schizophrenie kann aber auch die D2-Wirkung hilfreich sein. Daher testet ACAD hier Kombis mit bestehenden Mitteln, um insgesamt die Nebenwirkungen der alten Mittel zu verringern, indem diese nicht mehr so hoch dosiert werden müssen.
Für Schizophrenie usw. könnte aber auch ITCIs ITI-007 interessant sein. Es ist auch spezifischer wie Nuplazid, doch umfasst es neben 5-HT2A noch weitere positive Wirkungen wie z.B. D2 (das bei Parkinson oder Patienten mit Bewegungsproblemen auch negativ sein kann).
Im Artikel vom letzten Posting heißt es... "SCHIZOPHRENIA Outlook: Fair. Interesting drugs in development but not enough of them. Currently: Drugs can be effective at treating hallucinations and paranoia but don’t yet treat cognitive problems and social difficulties caused by the disease. What’s next: Add-on drugs. In 2016 Forum Pharmaceuticals hopes to have results on its encenicline, aimed at helping schizophrenics think more clearly. Acadia Pharmaceuticals is testing its Nuplazid to help existing antipsychotics. Long term: Intra-Cellular Therapies, a new publicly traded company, is testing a pill that, instead of working outside neurons, gets deep inside them. “It could be the most promising advance in antipsychotic pharmacology [in decades],” says Jeffrey Lieberman, psychiatrist in chief at NewYork-Presbyterian Hospital-Columbia University Medical Center."

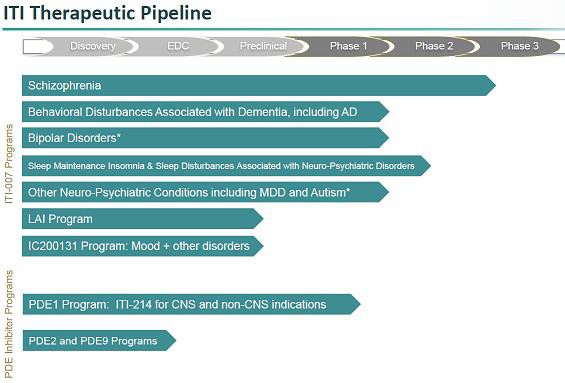

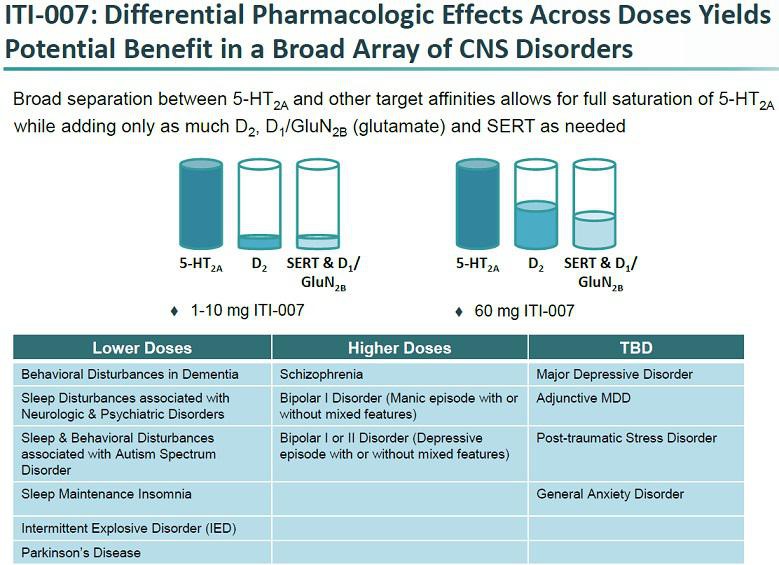
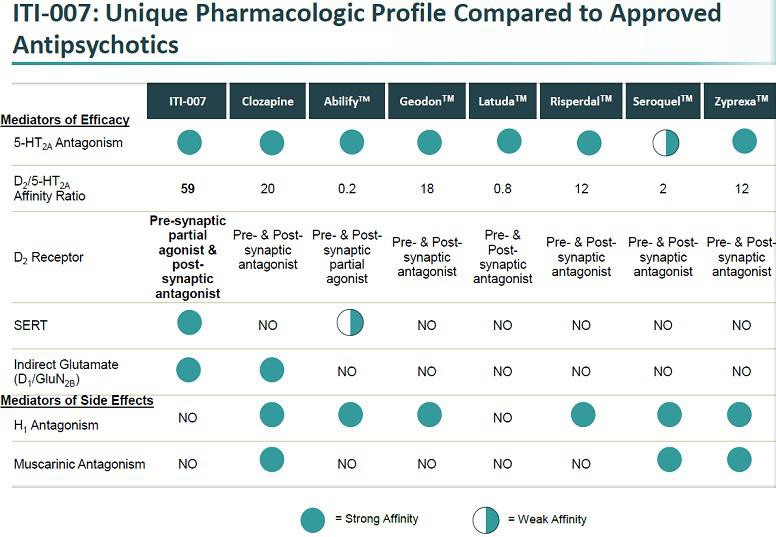
Erste PIII-Daten sollen noch dieses Jahr kommen.



Im Erfolgsfall ist die aktuelle MK von 765 Mio USD noch recht gering... allerdings ist CNS insgesamt riskant, so dass die PIII auch scheitern kann, selbst wenn ITI-007 aussichtsreich aussieht.

Gruß
ipollit
Bei der Parkinson-Erkrankung sterben die dopaminproduzierenden Nervenzellen, wodurch immer weniger Dopamin gebildet wird, welches für die Signalübertragung an die Muskeln notwendig ist. Die Patienten haben Bewegungseinschränkungen bis hin zur völligen Bewegungslosigkeit. Die Krankheit wird daher u.a. behandelt, indem man versucht, den Dopamin-Mangel auszugleichen.
Dopamin ist an vielen Prozessen im Gehirn beteiligt. Parkinson-Patienten können auch psychotische Störungen wie Halluzinationen, Ängste usw bekommen. An Psychosen sind u.a. Dopamin und Serotonin beteiligt. Die meisten Mittel gegen Psychosen wirken auf Serotonin über 5-HT2A und Dopamin über z.B. D2.
Parkinson-Patienten mit Psychosen lassen sich bisher aber nur schlecht behandeln, da die bisherigen Mittel eben auch das Dopamin hemmen, dass bei Parkinson bereits zu gering ist. Außerdem ist es eine Alters-Erkrankung... Antipsychotika sind aber oft unspezifisch, weshalb sie viele Nebenwirkungen haben, z.B. aufs Herz, die im Alter sehr problematisch sind.
Hier setzt ACADs Nuplazid an... es wirkt spezifisch auf 5-HT2A und nicht auf u.a. D2. Bei Parkison ist das von Vorteil, weshalb es gerade bei PDP sehr aussichtsreich ist.
In anderen Erkrankungen wie Schizophrenie kann aber auch die D2-Wirkung hilfreich sein. Daher testet ACAD hier Kombis mit bestehenden Mitteln, um insgesamt die Nebenwirkungen der alten Mittel zu verringern, indem diese nicht mehr so hoch dosiert werden müssen.
Für Schizophrenie usw. könnte aber auch ITCIs ITI-007 interessant sein. Es ist auch spezifischer wie Nuplazid, doch umfasst es neben 5-HT2A noch weitere positive Wirkungen wie z.B. D2 (das bei Parkinson oder Patienten mit Bewegungsproblemen auch negativ sein kann).
Im Artikel vom letzten Posting heißt es... "SCHIZOPHRENIA Outlook: Fair. Interesting drugs in development but not enough of them. Currently: Drugs can be effective at treating hallucinations and paranoia but don’t yet treat cognitive problems and social difficulties caused by the disease. What’s next: Add-on drugs. In 2016 Forum Pharmaceuticals hopes to have results on its encenicline, aimed at helping schizophrenics think more clearly. Acadia Pharmaceuticals is testing its Nuplazid to help existing antipsychotics. Long term: Intra-Cellular Therapies, a new publicly traded company, is testing a pill that, instead of working outside neurons, gets deep inside them. “It could be the most promising advance in antipsychotic pharmacology [in decades],” says Jeffrey Lieberman, psychiatrist in chief at NewYork-Presbyterian Hospital-Columbia University Medical Center."





Erste PIII-Daten sollen noch dieses Jahr kommen.



Im Erfolgsfall ist die aktuelle MK von 765 Mio USD noch recht gering... allerdings ist CNS insgesamt riskant, so dass die PIII auch scheitern kann, selbst wenn ITI-007 aussichtsreich aussieht.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.748.354 von ipollit am 10.05.15 00:16:07Hallo ipollit,
ITCI klingt interessant. Hast Du wieder super ausgearbeitet.
Wenn man sich die Seite 14 der Unternehmenspräsentation ansieht, dann fällt sofort ins Auge, dass sie bei ihrer erfolgreichen PII bei ihrem Endpunkt "Positive and Negative Syndrome Scale (PANSS)" non-inferiority zu Risperidone nur in der 60 mg-Gruppe erreicht haben.
Die höhere 120 mg-Dosis-Gruppe schneidet hingegen kaum besser als die Placebo-Gruppe ab.
Wenn es so ein - sagen wir mal - negativ-dosisabhängiges Wirksamkeitsprofil gibt, ist das ja erst mal ein Warnzeichen.
Klar, bei höherer Dosierung dürfte ITI-007 etwas von seiner 5-HT2A-Spezifik verlieren und auch stärker auf D2 usw. wirken. Aber sollte man davon einen negativen Effekt auf die Wirksamkeit erwarten?
Siehst Du das wie ich? Wie würdest Du das einschätzen?
Gruß
SLG
PS: Nächste Woche - am 13. Mai- werden die ASCO-Abstracts veröffentlicht. Ich liege auf der Lauer, um eventuell meine CLVS-Position deutlich auszubauen.
ITCI klingt interessant. Hast Du wieder super ausgearbeitet.
Wenn man sich die Seite 14 der Unternehmenspräsentation ansieht, dann fällt sofort ins Auge, dass sie bei ihrer erfolgreichen PII bei ihrem Endpunkt "Positive and Negative Syndrome Scale (PANSS)" non-inferiority zu Risperidone nur in der 60 mg-Gruppe erreicht haben.
Die höhere 120 mg-Dosis-Gruppe schneidet hingegen kaum besser als die Placebo-Gruppe ab.
Wenn es so ein - sagen wir mal - negativ-dosisabhängiges Wirksamkeitsprofil gibt, ist das ja erst mal ein Warnzeichen.
Klar, bei höherer Dosierung dürfte ITI-007 etwas von seiner 5-HT2A-Spezifik verlieren und auch stärker auf D2 usw. wirken. Aber sollte man davon einen negativen Effekt auf die Wirksamkeit erwarten?
Siehst Du das wie ich? Wie würdest Du das einschätzen?
Gruß
SLG
PS: Nächste Woche - am 13. Mai- werden die ASCO-Abstracts veröffentlicht. Ich liege auf der Lauer, um eventuell meine CLVS-Position deutlich auszubauen.
AAVL:
Ohad Hammer mit einem Artikel zu Avalanche, verbunden mit einer Erhöhung der Depotposition:
http://www.orf-blog.com/avalanche-biotech-approaching-the-mo…
Ich selbst werde meine Position nicht erhöhen, sondern das Ergebnis abwarten. Im Falle überzeugender Daten werde ich dann bei (von Ohad) vermuteten ca. 90 bis 100 Dollar nachkaufen.
So wie ich die Sache sehe, ist im Erfolgsfall das Potential nämlich auch nach einem 200%-Kurssprung gerade erst angekratzt.
Ohad Hammer mit einem Artikel zu Avalanche, verbunden mit einer Erhöhung der Depotposition:
http://www.orf-blog.com/avalanche-biotech-approaching-the-mo…
Ich selbst werde meine Position nicht erhöhen, sondern das Ergebnis abwarten. Im Falle überzeugender Daten werde ich dann bei (von Ohad) vermuteten ca. 90 bis 100 Dollar nachkaufen.
So wie ich die Sache sehe, ist im Erfolgsfall das Potential nämlich auch nach einem 200%-Kurssprung gerade erst angekratzt.
Antwort auf Beitrag Nr.: 49.749.471 von SLGramann am 10.05.15 13:07:45Ohad hat ja in seinem Artikel diese Tabelle über die P I von AVA-101:

Man sieht, dass die high-dose-Gruppe nur deshalb abfällt, weil Patient R2005 ein sehr schlechtes Ergebnis erzielt hat.
Dazu führen AAVL in ihrem S1 folgendes aus:
"One subject lost six letters from baseline; this subject had significant sub-foveal scarring at baseline, and consequently may not have had the ability to improve. Such subjects will be excluded from future trials designed to evaluate the efficacy of AVA-101."
Jetzt darf man in diese winzige Datenbasis nicht zu viel reininterpretieren, aber das ist eben das, was wir derzeit haben und der Ausreißer in der high-dose-Gruppe ist erklärbar.
Insgesamt habe ich hier schon ein anderes Gefühl als bei CLDN.

Man sieht, dass die high-dose-Gruppe nur deshalb abfällt, weil Patient R2005 ein sehr schlechtes Ergebnis erzielt hat.
Dazu führen AAVL in ihrem S1 folgendes aus:
"One subject lost six letters from baseline; this subject had significant sub-foveal scarring at baseline, and consequently may not have had the ability to improve. Such subjects will be excluded from future trials designed to evaluate the efficacy of AVA-101."
Jetzt darf man in diese winzige Datenbasis nicht zu viel reininterpretieren, aber das ist eben das, was wir derzeit haben und der Ausreißer in der high-dose-Gruppe ist erklärbar.
Insgesamt habe ich hier schon ein anderes Gefühl als bei CLDN.
Antwort auf Beitrag Nr.: 49.748.484 von SLGramann am 10.05.15 07:52:17ITCI
Stimmt... in der PII war nur der 60mg-Arm erfolgreich, während es bei 120mg kaum ein Unterschied zum Placebo gab. Laut ITCI könnte die Ursache die erhöhte Nebenwirkung der Sedierung/Schläfrigkeit in der 120mg-Gruppe sein:
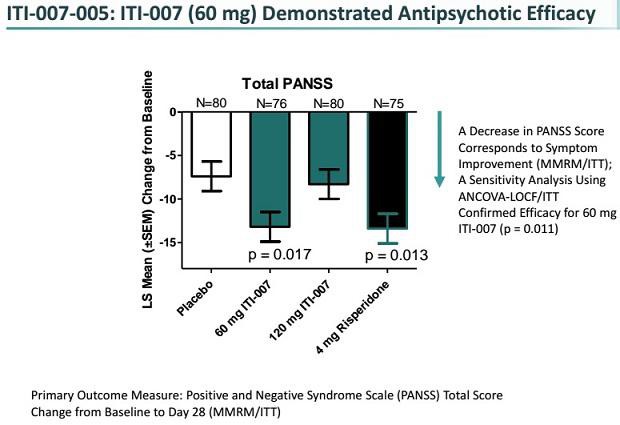
"The improvement in the total PANSS score in the 120 mg dose group did not reach statistical significance. We believe that it is possible that sedation, the most frequent side effect in the 120 mg dose group, interfered with the ability to detect an efficacy signal at this dose administered once daily in the morning. Approximately 32.5% of subjects randomized to 120 mg ITI-007 experienced sedation/somnolence, compared to 21% of subjects randomized to risperidone, 17% of subjects randomized to 60 mg ITI-007, and 13% randomized to placebo. We believe that nighttime administration may be more appropriate for testing the effectiveness of the 120 mg dose of ITI-007 in this patient population. In the trial, the 60 mg dose of ITI-007 was effective when administered once daily in the morning."
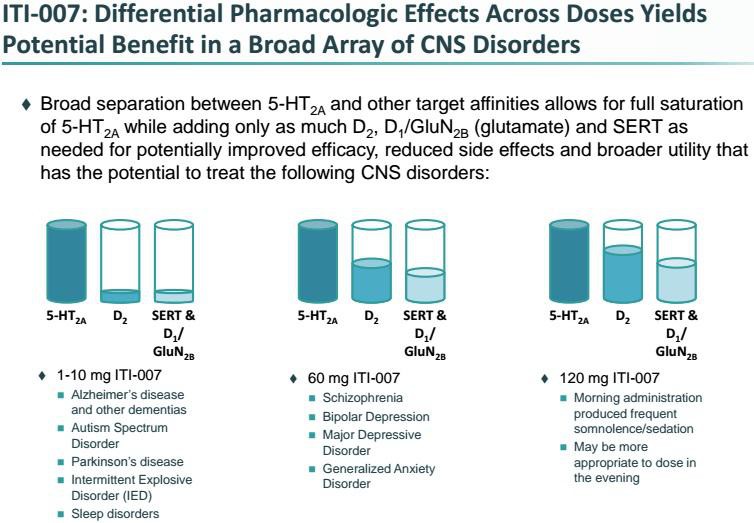
Grundsätzlich sind CNS-Studien riskant, da das subjektive Empfinden noch von anderen Faktoren beeinflusst werden kann. ACADs Nuplazid ist ja auch in einer Studie gescheitert.
Ich verstehe es so, dass sowohl Nuplazid als auch ITI-007 problematische Nebenwirkungen vermeidet. Z.B. ist die Wirkung auf 5-HT2A für Psychosen erwünscht, da dies u.a. mit Halluzinationen z.B. durch LSD in Verbindung gebracht wird. 5-HT2A wirkt aber auch auf viele andere Prozesse, z.B. auf den Kreislauf. Zudem scheinen schnell gleichzeitig andere Rezeptoren aktiviert zu werden: z.B. wird der 5-HT2A-Hemmer Ketanserin gegen Bluthochdruck eingesetzt... der Blutdruck wird über Alpha1 und H1 verändert, zudem können in höheren Konzentrationen Herzrhythmusstörungen auftreten. Es gab mal einen Appetitzügler FenPhen, der über den verwandten Serotonin-Rezeptor 5-HT2B zu Herzschäden führte und für den der Pharma Wyeth Entschädigungen im zweistelligen Mrd-Bereich zahlen musste. D.h. solche Mittel können sehr problematisch sein.
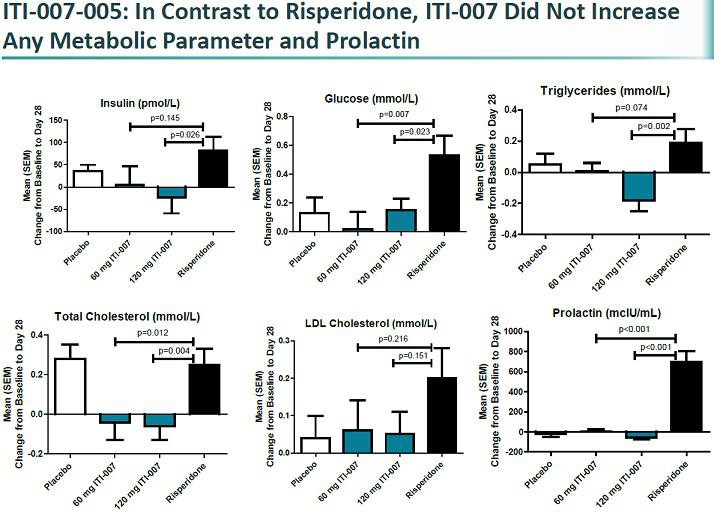
Ebenfalls sind beide Mittel "atypische Antipsychotika"... klassische Antipsychotika wirken auf die Psychose (Halluzinationen, Angstzustände usw) und sind seditativ (Hemmen die Bewegungsfähigkeit ähnlich wie bei Parkinson). Letzteres ist nicht erwünscht und hängt z.B. mit Dopamin wie D2 zusammen. Atypische Mittel wirken deutlich stärker auf die Psychose und vermeiden die Sedierung.
Nuplazid und ITI-007 unterschieden sich, indem Nuplazid hauptsächlich auf 5-HT2A wirken soll... es kann Vorteile bieten, wenn die Bewegung bereits eingeschränkt ist wie bei Parkinson oder älternen Patienten (Alzheimer usw). ITI-007 wirkt dagegen breiter... vielleicht auch dann, wenn Nuplazid nicht wirkt. Dieser breitere Ansatz (der trotzdem problematische Nebenwirkungen vermeidet) könnte sich aber auch negativ auswirken... wie vorher beschrieben, ist der Bereich recht komplex. Vielleicht werden bei höheren Dosierungen Rezeptoren aktiviert/gehemmt, die sich negativ auf die Psychose auswirken. Vielleicht ist es auch die Sedierung, von der ITCI spricht, die Patienten unzufriedener macht. Wie gesagt, ist meiner Meinung nach der CNS-Bereich recht riskant.
Trotzdem basiert ja ITI-007 auf den bekannten Wirkmechanismen. Die bisherigen atypischen Standardmittel wie Risperdal (Risperidone) haben die problematischen Nebenwirkungen. Risperdal hat ein Black-Box-Warning, dass es die Sterblichkeit von älterne Patienten erhört: "According to the FDA, this warning is based on clinical evidence gathered from 17 placebo-controlled trials that enrolled 5,106 elderly individuals who suffered dementia-related behavioral disorders. Data from those trials, collected over a period of 10 weeks, showed a 4.5 percent rate of death in patients treated with Risperdal and other atypical antipsychotic drugs, compared with a 2.6 percent risk in patients taking a placebo. While causes of those deaths varied, the majority were cardiovascular deaths, heart failure or sudden death, or infectious conditions, mostly pneumonia."
Auf der einen Seite nehmen Patienten vielleicht teure Mittel wie z.B. PCSK9-AKs, um das Risiko von Herzinfakt oder Schlaganfall zu halbieren, um es dann mit Antipsychotika wieder zu verdoppeln? Gerade im Bereich Demenz, Alzheimer, Parkinson usw gibt es doch auch Probleme mit Halluzinationen, Ängsten usw. Und auch bei jüngeren Patitienten sehe ich Potential für Mittel mit weniger Nebenwirkungen, zu denen ich Nuplazid und ITI-007 zähle.
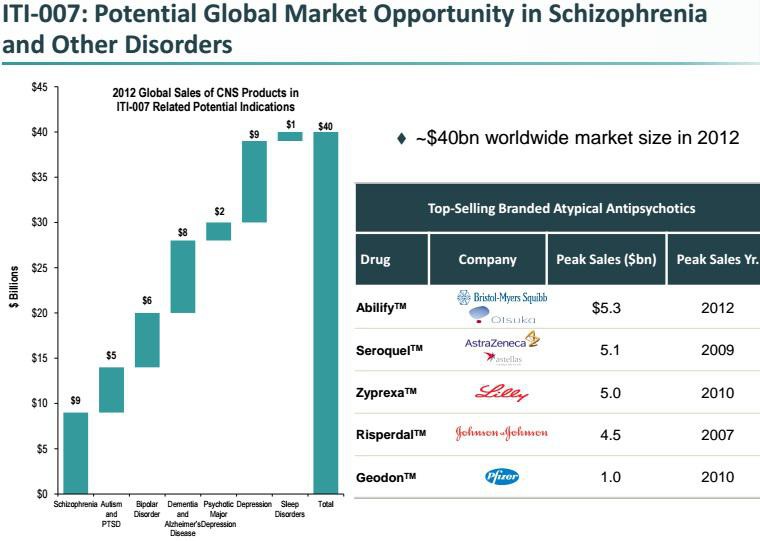
Gruß
ipollit
Stimmt... in der PII war nur der 60mg-Arm erfolgreich, während es bei 120mg kaum ein Unterschied zum Placebo gab. Laut ITCI könnte die Ursache die erhöhte Nebenwirkung der Sedierung/Schläfrigkeit in der 120mg-Gruppe sein:

"The improvement in the total PANSS score in the 120 mg dose group did not reach statistical significance. We believe that it is possible that sedation, the most frequent side effect in the 120 mg dose group, interfered with the ability to detect an efficacy signal at this dose administered once daily in the morning. Approximately 32.5% of subjects randomized to 120 mg ITI-007 experienced sedation/somnolence, compared to 21% of subjects randomized to risperidone, 17% of subjects randomized to 60 mg ITI-007, and 13% randomized to placebo. We believe that nighttime administration may be more appropriate for testing the effectiveness of the 120 mg dose of ITI-007 in this patient population. In the trial, the 60 mg dose of ITI-007 was effective when administered once daily in the morning."

Grundsätzlich sind CNS-Studien riskant, da das subjektive Empfinden noch von anderen Faktoren beeinflusst werden kann. ACADs Nuplazid ist ja auch in einer Studie gescheitert.
Ich verstehe es so, dass sowohl Nuplazid als auch ITI-007 problematische Nebenwirkungen vermeidet. Z.B. ist die Wirkung auf 5-HT2A für Psychosen erwünscht, da dies u.a. mit Halluzinationen z.B. durch LSD in Verbindung gebracht wird. 5-HT2A wirkt aber auch auf viele andere Prozesse, z.B. auf den Kreislauf. Zudem scheinen schnell gleichzeitig andere Rezeptoren aktiviert zu werden: z.B. wird der 5-HT2A-Hemmer Ketanserin gegen Bluthochdruck eingesetzt... der Blutdruck wird über Alpha1 und H1 verändert, zudem können in höheren Konzentrationen Herzrhythmusstörungen auftreten. Es gab mal einen Appetitzügler FenPhen, der über den verwandten Serotonin-Rezeptor 5-HT2B zu Herzschäden führte und für den der Pharma Wyeth Entschädigungen im zweistelligen Mrd-Bereich zahlen musste. D.h. solche Mittel können sehr problematisch sein.

Ebenfalls sind beide Mittel "atypische Antipsychotika"... klassische Antipsychotika wirken auf die Psychose (Halluzinationen, Angstzustände usw) und sind seditativ (Hemmen die Bewegungsfähigkeit ähnlich wie bei Parkinson). Letzteres ist nicht erwünscht und hängt z.B. mit Dopamin wie D2 zusammen. Atypische Mittel wirken deutlich stärker auf die Psychose und vermeiden die Sedierung.
Nuplazid und ITI-007 unterschieden sich, indem Nuplazid hauptsächlich auf 5-HT2A wirken soll... es kann Vorteile bieten, wenn die Bewegung bereits eingeschränkt ist wie bei Parkinson oder älternen Patienten (Alzheimer usw). ITI-007 wirkt dagegen breiter... vielleicht auch dann, wenn Nuplazid nicht wirkt. Dieser breitere Ansatz (der trotzdem problematische Nebenwirkungen vermeidet) könnte sich aber auch negativ auswirken... wie vorher beschrieben, ist der Bereich recht komplex. Vielleicht werden bei höheren Dosierungen Rezeptoren aktiviert/gehemmt, die sich negativ auf die Psychose auswirken. Vielleicht ist es auch die Sedierung, von der ITCI spricht, die Patienten unzufriedener macht. Wie gesagt, ist meiner Meinung nach der CNS-Bereich recht riskant.
Trotzdem basiert ja ITI-007 auf den bekannten Wirkmechanismen. Die bisherigen atypischen Standardmittel wie Risperdal (Risperidone) haben die problematischen Nebenwirkungen. Risperdal hat ein Black-Box-Warning, dass es die Sterblichkeit von älterne Patienten erhört: "According to the FDA, this warning is based on clinical evidence gathered from 17 placebo-controlled trials that enrolled 5,106 elderly individuals who suffered dementia-related behavioral disorders. Data from those trials, collected over a period of 10 weeks, showed a 4.5 percent rate of death in patients treated with Risperdal and other atypical antipsychotic drugs, compared with a 2.6 percent risk in patients taking a placebo. While causes of those deaths varied, the majority were cardiovascular deaths, heart failure or sudden death, or infectious conditions, mostly pneumonia."
Auf der einen Seite nehmen Patienten vielleicht teure Mittel wie z.B. PCSK9-AKs, um das Risiko von Herzinfakt oder Schlaganfall zu halbieren, um es dann mit Antipsychotika wieder zu verdoppeln? Gerade im Bereich Demenz, Alzheimer, Parkinson usw gibt es doch auch Probleme mit Halluzinationen, Ängsten usw. Und auch bei jüngeren Patitienten sehe ich Potential für Mittel mit weniger Nebenwirkungen, zu denen ich Nuplazid und ITI-007 zähle.

Gruß
ipollit
XLRN
Ich werde wohl meine XLRN-Position weiter ausbauen. Die CELG-Kooperation bezügl. Luspatercept/Sotatercept entwickelt sich meiner Meinung nach sehr gut.
Die PII-Ergebnisse in MDS scheinen mit der Zeit besser zu werden.
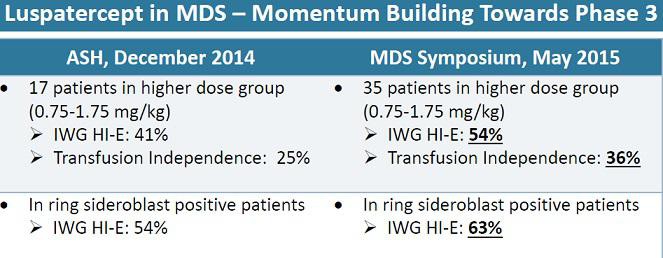
Bei Myelodysplastic Syndromes (MDS) gibt es eine Störung in der Bildung von roten Blutkörperchen, die zu einer Blutarmut führt. Mit der Zeit kann MDS dann auch zu zum Blutkrebs AML werden.
Low-Risk MDS wird zunächst mit EPO und Transfusionen behandelt. Dabei sollen bei MDS übermäßig viele Blutkörperchen gebildet werden, die aber nicht zu echten Zellen reifen. EPO hilft eigentlich bei Blutarmut, indem mehr rote Blutkörperchen gebildet werden. Bei MDS bringt dies aber nicht viel, da auch diese nicht weiter reifen. Luspatercept (ACE-536) greift in den Reifungsprozess ein und soll diesen Normalisieren:
"Patients with MDS have a hypercellular bone marrow with various dysplastic changes of the cells that are also seen in peripheral blood, resulting in cytopenias (low blood cell counts) and an increased risk of progression to acute myeloid leukemia (AML). Nearly all MDS patients suffer from anemia. The anemia in MDS is characterized by increased levels of endogenous erythropoietin (EPO) driving an abundance of early stage red blood cell precursors and an inability of these precursor cells to properly differentiate into healthy, functional red blood cells. Many patients are therefore unresponsive to the administration of erythropoietin to correct the resulting anemia and instead require red blood cell transfusions, which can increase the risk of infection and iron-overload related toxicities.
ACE-536 regulates late-stage erythrocyte (red blood cell) precursor cell differentiation and maturation, distinct from erythropoietin (EPO) which stimulates the proliferation of early-stage erythrocyte precursor cells.
Acceleron’s oral presentation highlighted preclinical data demonstrating that ACE-536 inhibits SMAD 2/3 signaling and consequently increases levels of red blood cells (RBC) and hemoglobin by promoting the differentiation of late stage RBC precursors. ACE-536 also normalized the level of RBC precursors in the bone marrow of MDS mice, further indicating that ACE-536 may correct the ineffective erythropoiesis observed in MDS patients. In MDS patients, overactive signaling by the SMAD 2/3 pathway in the bone marrow may contribute to ineffective erythropoiesis, a defect in which red blood cell precursors in the bone marrow are prevented from maturing into healthy, functional red blood cells."
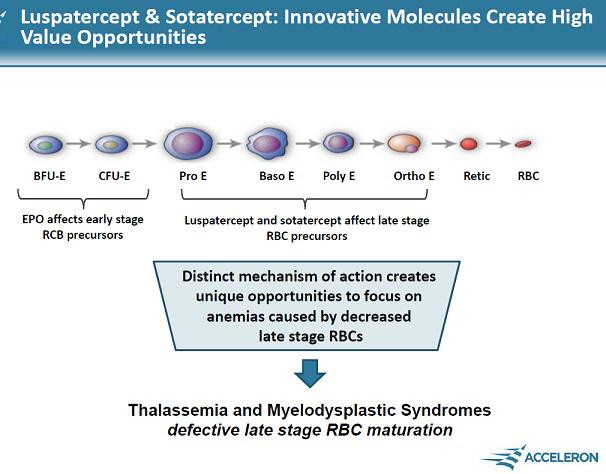
Die Kooperation mit CELG ist besonders positiv, da CELG in diesem Gebiet mit Revlimid, Vidaza, Thalomid usw bereits sehr aktiv und führend ist, die in späteren Verläufen der Krankheit und AML zum Einsatz kommen. D.h. Luspatercept dürfte auch für CELG ein wichtiger Kandidat sein. Sie bezahlen 100% aller Entwicklungs-Kosten... dafür erhält XLRN später gute 20-25% Royalties weltweit.
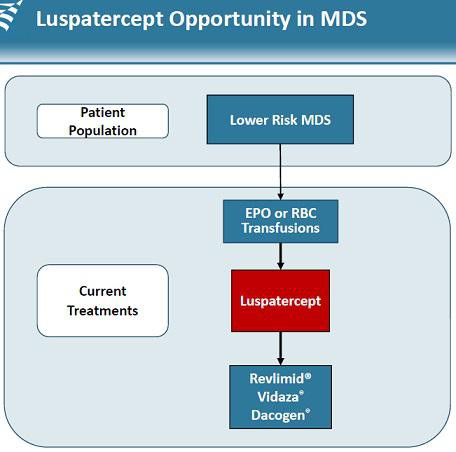





Die weitere Pipeline ist zwar noch sehr früh, XLRNs Spezialgebiet TGF-Beta scheint aber ein interessanter Bereich zu sein, der in vielen großen Indikationen relevant ist.
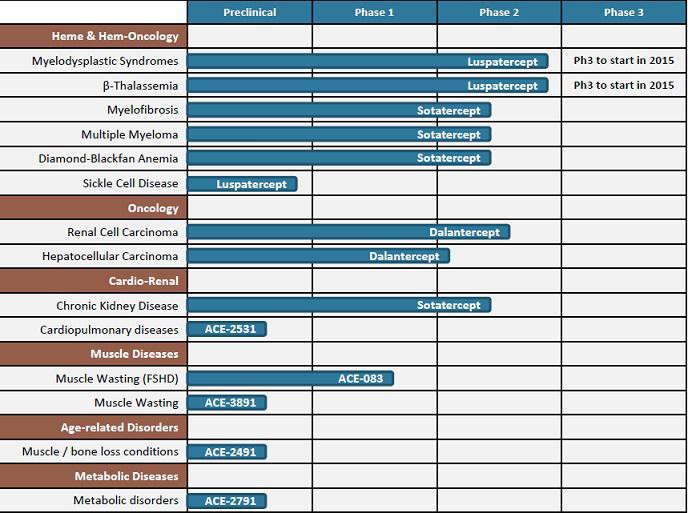
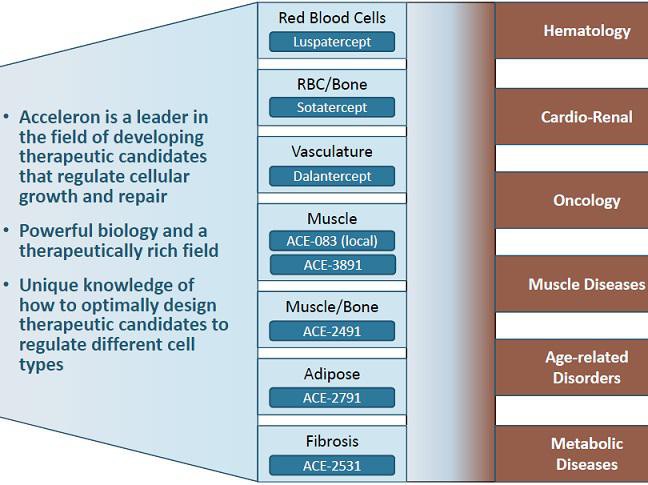


Gruß
ipollit
Ich werde wohl meine XLRN-Position weiter ausbauen. Die CELG-Kooperation bezügl. Luspatercept/Sotatercept entwickelt sich meiner Meinung nach sehr gut.
Die PII-Ergebnisse in MDS scheinen mit der Zeit besser zu werden.

Bei Myelodysplastic Syndromes (MDS) gibt es eine Störung in der Bildung von roten Blutkörperchen, die zu einer Blutarmut führt. Mit der Zeit kann MDS dann auch zu zum Blutkrebs AML werden.
Low-Risk MDS wird zunächst mit EPO und Transfusionen behandelt. Dabei sollen bei MDS übermäßig viele Blutkörperchen gebildet werden, die aber nicht zu echten Zellen reifen. EPO hilft eigentlich bei Blutarmut, indem mehr rote Blutkörperchen gebildet werden. Bei MDS bringt dies aber nicht viel, da auch diese nicht weiter reifen. Luspatercept (ACE-536) greift in den Reifungsprozess ein und soll diesen Normalisieren:
"Patients with MDS have a hypercellular bone marrow with various dysplastic changes of the cells that are also seen in peripheral blood, resulting in cytopenias (low blood cell counts) and an increased risk of progression to acute myeloid leukemia (AML). Nearly all MDS patients suffer from anemia. The anemia in MDS is characterized by increased levels of endogenous erythropoietin (EPO) driving an abundance of early stage red blood cell precursors and an inability of these precursor cells to properly differentiate into healthy, functional red blood cells. Many patients are therefore unresponsive to the administration of erythropoietin to correct the resulting anemia and instead require red blood cell transfusions, which can increase the risk of infection and iron-overload related toxicities.
ACE-536 regulates late-stage erythrocyte (red blood cell) precursor cell differentiation and maturation, distinct from erythropoietin (EPO) which stimulates the proliferation of early-stage erythrocyte precursor cells.
Acceleron’s oral presentation highlighted preclinical data demonstrating that ACE-536 inhibits SMAD 2/3 signaling and consequently increases levels of red blood cells (RBC) and hemoglobin by promoting the differentiation of late stage RBC precursors. ACE-536 also normalized the level of RBC precursors in the bone marrow of MDS mice, further indicating that ACE-536 may correct the ineffective erythropoiesis observed in MDS patients. In MDS patients, overactive signaling by the SMAD 2/3 pathway in the bone marrow may contribute to ineffective erythropoiesis, a defect in which red blood cell precursors in the bone marrow are prevented from maturing into healthy, functional red blood cells."

Die Kooperation mit CELG ist besonders positiv, da CELG in diesem Gebiet mit Revlimid, Vidaza, Thalomid usw bereits sehr aktiv und führend ist, die in späteren Verläufen der Krankheit und AML zum Einsatz kommen. D.h. Luspatercept dürfte auch für CELG ein wichtiger Kandidat sein. Sie bezahlen 100% aller Entwicklungs-Kosten... dafür erhält XLRN später gute 20-25% Royalties weltweit.






Die weitere Pipeline ist zwar noch sehr früh, XLRNs Spezialgebiet TGF-Beta scheint aber ein interessanter Bereich zu sein, der in vielen großen Indikationen relevant ist.



Gruß
ipollit
AUPH
Was ist von AUPH zu halten? Für mich sieht es jedenfalls recht interessant aus...
Im Ohad Hammer Blog wurde auch darauf hingewiesen...
"have you looked at AUPH?
Somehow, there are some similarities with MRNS (be it positive or negative):
- small company (11 FTEs end 2014, lot of experience with the compound and with the disease Lupus Nephritis)
- one-drug company (Voclosporin)
- large safety database (about 2000 patients tread in other indications)
- some proof of concept that calcineurin inhibitors when added to SoC in LN (i.e. Cellcept, with only 9% complete remission) improve outcomes considerably
- rather low valuation (approx. USD 120 mio)
- considerable unmet medical need (LN)
- important read-out of P2b towards end of the year
would be nice to hear your opinion!
questions to me are e.g. whether the other 2 calcineurin inhibitors (which are generic) can be a threat or not; company claims they are not suitable for LN in combination with Cellcept due to adverse event profile respectively interaction with Cellcept.
****
Actually I started tracking them closely a couple of months ago and think it’s a compelling opportunity based on reasonable likelihood of success in a decently powered study, potentially differentiated profile vs. cyclospronie and high unmet need (lupus nephritis).
****
I like AUPH , as conveyed by what Chris posted (thanks). I tend to accept AUPH’s arguments regarding a differentiated profile that should allow them to capture a meaningful market share."
******
Voclosporin ist Mittel zur Unterdrückung des Immunsystems aus der Klasse der Calcineurin-Hemmer (CNI), das u.a. von Roche gegen Abstoßungsreaktionen bei Transplantationen getestet aber letztlich zurückgegeben worden ist:
"Isotechnika says Roche gives up global rights to voclosporin for organ transplants
EDMONTON — Canadian drug developer Isotechnika Inc. says Swiss drug giant Roche has given up its rights to license the Edmonton company's voclosporin drug for solid organ transplants.
Isotechnika said it's disappointed about Roche's different priorities and plans to seek other potential licensing partners for voclosporin for use in transplant and autoimmune system treatment.
The announcement by Isotechnika late Monday came several hours after Roche offered US$43.7 billion for the remaining shares of its U.S. biotech partner Genentech Inc. in a move to boost its stature in the market for drugs to fight cancer and other diseases.
"Adding transplant to the list of available indications will greatly strengthen our position and improve the attractiveness of the opportunity to potential partners," said Dr. Robert Foster, Isotechnika's chairman and CEO.
"While we are disappointed about Roche's different priorities, we feel that this represents the first time since 2002 that we can offer a more comprehensive licensing package including both transplant and autoimmune indications to a focused and strong global partner."
Voclosporin recently completed a Phase 2b North American trial for the prevention of kidney rejection following transplants. The drug is also being tested on other ailments."
Daher gibt es bereits umfangreiche Daten, insbesondere zur Sicherheit von Voclosporin.
AUPH entwickelt es nun gegen Nierenerkrankungen (LN) in Folge von Lupus (Autoimmunerkrankung)...
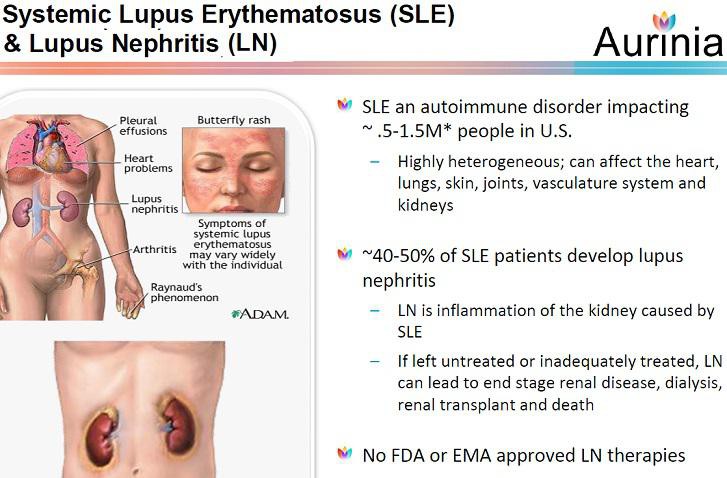
CellCept ist der Standard gegen LN. Allerdings soll es für einen langfristigen Erfolg entscheidend sein, dass man bei der Therapie einen vollständigen Rückgang der Erkrankung erreicht, was aber alleine mit Cellcept nur selten erreicht wird.
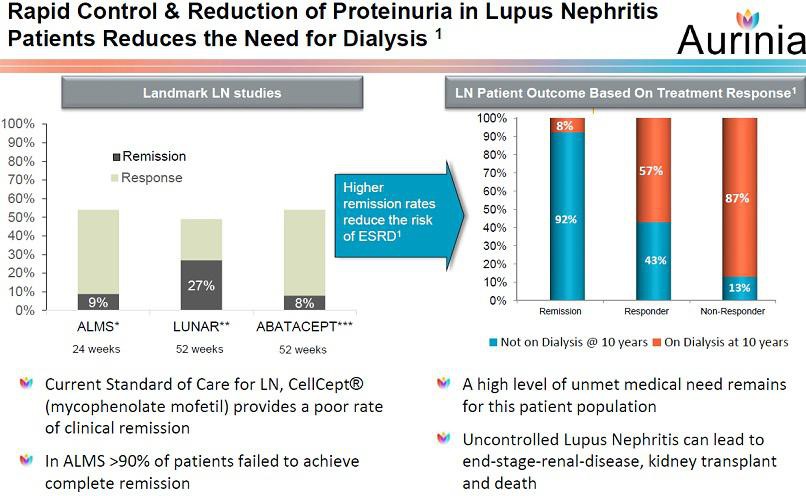
Mit einer CNI-Kombi lassen sich die Ergebnisse deutlich steigern. CellCept + CNI sind bereits bei Organabstoßung der Standard. In Japan ist CNI auch gegen LN zugelassen. Die Erfolgswahrscheinlichkeit ist also sehr groß, mit der Sicherheit sollte es ebenfalls kein Problem geben aufgrund der umfangreichen Daten, die es bereits gibt.
Ein Haken könnte sein, dass CNIs bereits generisch sind. Allerdings sind in den USA keine CNIs gegen LN zugelassen und die generischen CNIs haben laut AUPH deutliche Nebenwirkungen:
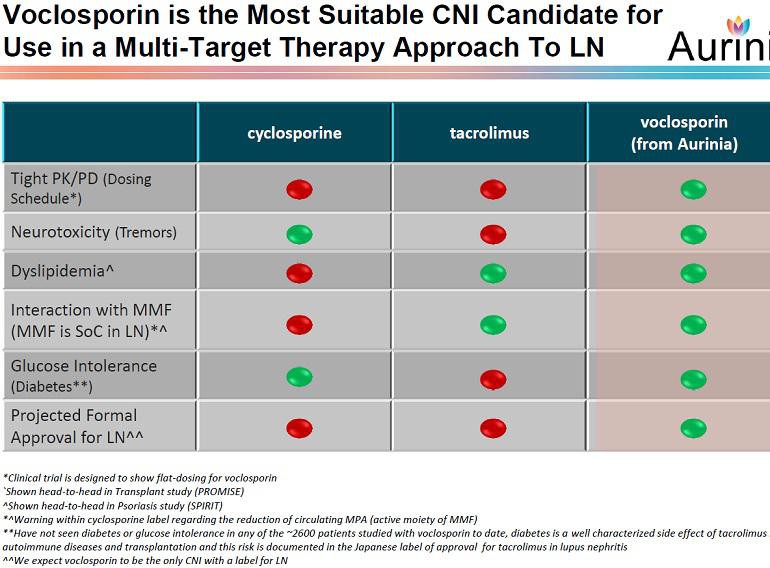
Interessant ist auch die MK von AUPH... mit 126 Mio USD noch sehr gering im Vergleich von einem theoretische 1+ Mrd peak sale Potential.

Hier einige Analysten-Kommentare...








Gruß
ipollit
Was ist von AUPH zu halten? Für mich sieht es jedenfalls recht interessant aus...
Im Ohad Hammer Blog wurde auch darauf hingewiesen...
"have you looked at AUPH?
Somehow, there are some similarities with MRNS (be it positive or negative):
- small company (11 FTEs end 2014, lot of experience with the compound and with the disease Lupus Nephritis)
- one-drug company (Voclosporin)
- large safety database (about 2000 patients tread in other indications)
- some proof of concept that calcineurin inhibitors when added to SoC in LN (i.e. Cellcept, with only 9% complete remission) improve outcomes considerably
- rather low valuation (approx. USD 120 mio)
- considerable unmet medical need (LN)
- important read-out of P2b towards end of the year
would be nice to hear your opinion!
questions to me are e.g. whether the other 2 calcineurin inhibitors (which are generic) can be a threat or not; company claims they are not suitable for LN in combination with Cellcept due to adverse event profile respectively interaction with Cellcept.
****
Actually I started tracking them closely a couple of months ago and think it’s a compelling opportunity based on reasonable likelihood of success in a decently powered study, potentially differentiated profile vs. cyclospronie and high unmet need (lupus nephritis).
****
I like AUPH , as conveyed by what Chris posted (thanks). I tend to accept AUPH’s arguments regarding a differentiated profile that should allow them to capture a meaningful market share."
******
Voclosporin ist Mittel zur Unterdrückung des Immunsystems aus der Klasse der Calcineurin-Hemmer (CNI), das u.a. von Roche gegen Abstoßungsreaktionen bei Transplantationen getestet aber letztlich zurückgegeben worden ist:
"Isotechnika says Roche gives up global rights to voclosporin for organ transplants
EDMONTON — Canadian drug developer Isotechnika Inc. says Swiss drug giant Roche has given up its rights to license the Edmonton company's voclosporin drug for solid organ transplants.
Isotechnika said it's disappointed about Roche's different priorities and plans to seek other potential licensing partners for voclosporin for use in transplant and autoimmune system treatment.
The announcement by Isotechnika late Monday came several hours after Roche offered US$43.7 billion for the remaining shares of its U.S. biotech partner Genentech Inc. in a move to boost its stature in the market for drugs to fight cancer and other diseases.
"Adding transplant to the list of available indications will greatly strengthen our position and improve the attractiveness of the opportunity to potential partners," said Dr. Robert Foster, Isotechnika's chairman and CEO.
"While we are disappointed about Roche's different priorities, we feel that this represents the first time since 2002 that we can offer a more comprehensive licensing package including both transplant and autoimmune indications to a focused and strong global partner."
Voclosporin recently completed a Phase 2b North American trial for the prevention of kidney rejection following transplants. The drug is also being tested on other ailments."
Daher gibt es bereits umfangreiche Daten, insbesondere zur Sicherheit von Voclosporin.
AUPH entwickelt es nun gegen Nierenerkrankungen (LN) in Folge von Lupus (Autoimmunerkrankung)...

CellCept ist der Standard gegen LN. Allerdings soll es für einen langfristigen Erfolg entscheidend sein, dass man bei der Therapie einen vollständigen Rückgang der Erkrankung erreicht, was aber alleine mit Cellcept nur selten erreicht wird.

Mit einer CNI-Kombi lassen sich die Ergebnisse deutlich steigern. CellCept + CNI sind bereits bei Organabstoßung der Standard. In Japan ist CNI auch gegen LN zugelassen. Die Erfolgswahrscheinlichkeit ist also sehr groß, mit der Sicherheit sollte es ebenfalls kein Problem geben aufgrund der umfangreichen Daten, die es bereits gibt.
Ein Haken könnte sein, dass CNIs bereits generisch sind. Allerdings sind in den USA keine CNIs gegen LN zugelassen und die generischen CNIs haben laut AUPH deutliche Nebenwirkungen:

Interessant ist auch die MK von AUPH... mit 126 Mio USD noch sehr gering im Vergleich von einem theoretische 1+ Mrd peak sale Potential.
Hier einige Analysten-Kommentare...








Gruß
ipollit
Antwort auf Beitrag Nr.: 49.747.896 von ipollit am 09.05.15 20:00:02MDVN
Hier auch nochmal die Astellas-Prognose für Xtandi... sie schätzen in den nächsten 12 Monaten US-Umsätze von 1,18 Mio USD und ex-US 790 Mio USD, also in Summe nahe an 2 Mrd USD:

Gruß
ipollit
Hier auch nochmal die Astellas-Prognose für Xtandi... sie schätzen in den nächsten 12 Monaten US-Umsätze von 1,18 Mio USD und ex-US 790 Mio USD, also in Summe nahe an 2 Mrd USD:

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.751.373 von ipollit am 10.05.15 23:54:21AUPH
theoretisch könnte Voclosporin in LN eine Menge Potential besitzen, wenn es sich gegen die generischen CNIs (die keine Zulassung in LN haben) durchsetzen kann. Bin mal mit einer kleineren Position dabei.
Die Leute von AUPH scheinen zumindest keine Anfänger zu sein, da die meisten von Aspreva kommen... Aspreva hat den aktuellen LN-Standard Cellcept zusammen mit Roche entwickelt und wurde von Galenica für fast 1 Mrd USD übernommen. Der CEO von AUPH scheint auch viel Erfahrung von Bayer und ZymoGenetics mitzubringen.

CellCept + CNI ist bereits der Standard bei Organtransplantationen und Studien in LN zeigen, dass die Kombi auch dort klar besser ist, insbesondere bezügl. CR
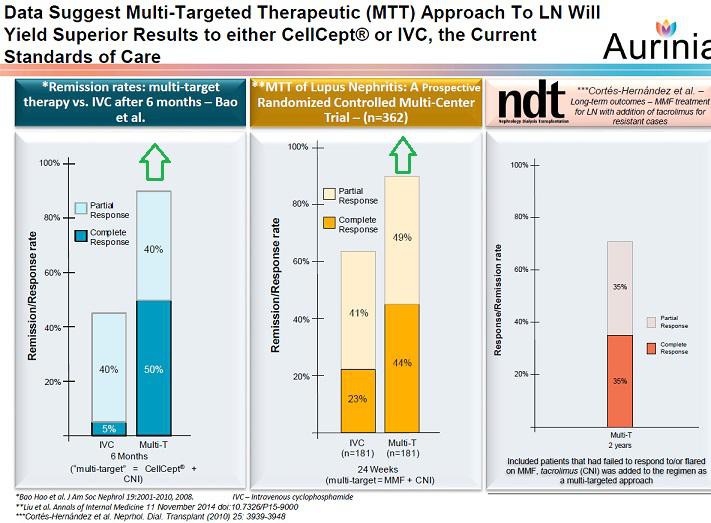
Cellcept ist bereits recht verbreitet und dürfte weitere Marktanteile bei Lupus gewinnen, nachdem es generisch geworden ist. LN ist der Anteil von Lupus, der mit den höchsten Behandlungskosten verbunden ist.
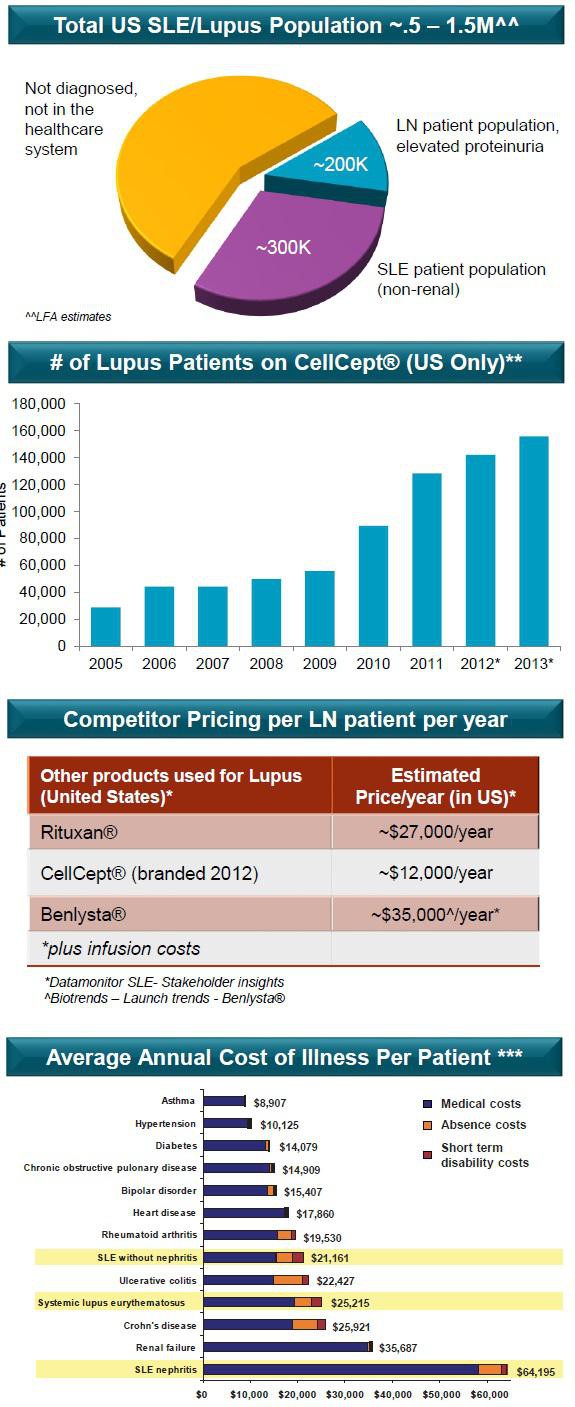
Für Lupus gibt es bisher wenige Alternativen... eine wäre IMMUs Epratuzumab (allerdings nicht speziell LN), für das bald auch PIII-Daten kommen sollten. Für Voclosporin's laufende PII AURA LV sind in 1Q16 Daten geplant, die den wichtigsten Teil für eine mögliche Zulassung bilden.
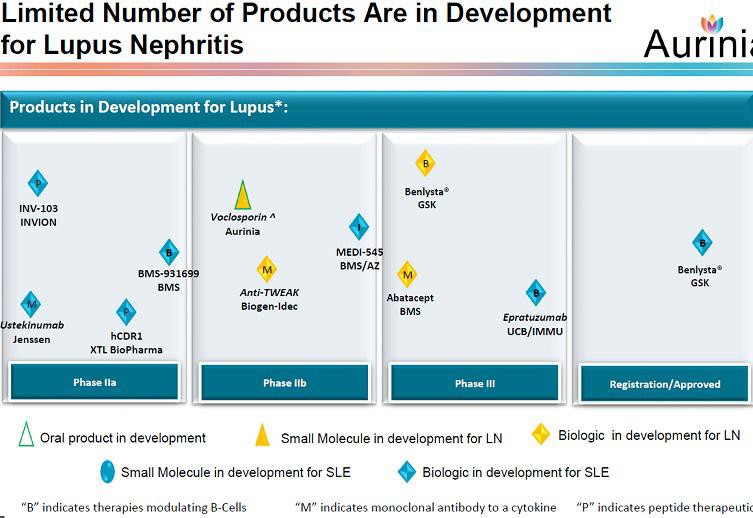

mal schauen...
Gruß
ipollit
theoretisch könnte Voclosporin in LN eine Menge Potential besitzen, wenn es sich gegen die generischen CNIs (die keine Zulassung in LN haben) durchsetzen kann. Bin mal mit einer kleineren Position dabei.
Die Leute von AUPH scheinen zumindest keine Anfänger zu sein, da die meisten von Aspreva kommen... Aspreva hat den aktuellen LN-Standard Cellcept zusammen mit Roche entwickelt und wurde von Galenica für fast 1 Mrd USD übernommen. Der CEO von AUPH scheint auch viel Erfahrung von Bayer und ZymoGenetics mitzubringen.

CellCept + CNI ist bereits der Standard bei Organtransplantationen und Studien in LN zeigen, dass die Kombi auch dort klar besser ist, insbesondere bezügl. CR

Cellcept ist bereits recht verbreitet und dürfte weitere Marktanteile bei Lupus gewinnen, nachdem es generisch geworden ist. LN ist der Anteil von Lupus, der mit den höchsten Behandlungskosten verbunden ist.

Für Lupus gibt es bisher wenige Alternativen... eine wäre IMMUs Epratuzumab (allerdings nicht speziell LN), für das bald auch PIII-Daten kommen sollten. Für Voclosporin's laufende PII AURA LV sind in 1Q16 Daten geplant, die den wichtigsten Teil für eine mögliche Zulassung bilden.


mal schauen...
Gruß
ipollit
Arry/Selumetinib
Die laufende Select1-Studie (Phase III) dreht sich um KRAS NSCLC in der Kombination mit Docetaxel.
In dem untenstehenden Abstract aus dem Februar 2015 steht, daß Selumetinib bei KRAS NSCLC eine response rate von nur 11% hatte und den dortigen primary endpoint verfehlte (rd. 150 Patienten).
Ist das nun besorgniserregend oder sollte der Schwerpunkt auf der Kombi mit Docetaxel liegen, so daß Rückschlüsse auf die laufende Select1-Studie nicht angezeigt sind?
Lt ASCO-Abstract scheint Selumetinib aber jedenfalls mit MK2206 bei PC unwirksam zu sein.
Das Abstract zur TATTON-Studie lese ich für Selumetinib auch eher mit gemischt-negativen Gefühlen, oder lese ich das nur falsch?
Was hat sich für Euch an der Beurteilung von Arry aufgrund der heutigen Abstract-Veröffentlichungen geändert?
http://jco.ascopubs.org/content/early/2015/02/03/JCO.2014.58…
Die laufende Select1-Studie (Phase III) dreht sich um KRAS NSCLC in der Kombination mit Docetaxel.
In dem untenstehenden Abstract aus dem Februar 2015 steht, daß Selumetinib bei KRAS NSCLC eine response rate von nur 11% hatte und den dortigen primary endpoint verfehlte (rd. 150 Patienten).
Ist das nun besorgniserregend oder sollte der Schwerpunkt auf der Kombi mit Docetaxel liegen, so daß Rückschlüsse auf die laufende Select1-Studie nicht angezeigt sind?
Lt ASCO-Abstract scheint Selumetinib aber jedenfalls mit MK2206 bei PC unwirksam zu sein.
Das Abstract zur TATTON-Studie lese ich für Selumetinib auch eher mit gemischt-negativen Gefühlen, oder lese ich das nur falsch?
Was hat sich für Euch an der Beurteilung von Arry aufgrund der heutigen Abstract-Veröffentlichungen geändert?
http://jco.ascopubs.org/content/early/2015/02/03/JCO.2014.58…
Antwort auf Beitrag Nr.: 49.776.090 von lawmeetstax am 14.05.15 00:34:50Durch ein bißchen weitere Recherche könnte ich mir eine meiner Fragen bereits selbst beantworten. Es scheint tatsächlich ganz entscheidend zu sein, ob Selumetinib allein oder in Kombi verabreicht wird. Daß es alleine nicht klappen kann, ist wohl schon länger bekannt und nichts Neues. Gleiches scheint auch Mekinist zu gelten...
Meine übrigen Fragen bleiben vorerst weiterhin offen...
Meine übrigen Fragen bleiben vorerst weiterhin offen...
CLVS:
Das Abstract zu Rociletinib gint noch nicht so viel her, weil die PFS-Daten fehlen:
http://abstracts.asco.org/156/AbstView_156_152181.html
Da müssen wir bis zur ASCO warten.
ORR ergibt ein gemischtes Bild. Nur noch 49% bei T790M+, was m.E. enttäuschend ist. Dafür wurden die >30% bei T790M- bestätigt, was auf lange Sicht noch wichtig werden könnte.
Das Abstract zu Rociletinib gint noch nicht so viel her, weil die PFS-Daten fehlen:
http://abstracts.asco.org/156/AbstView_156_152181.html
Da müssen wir bis zur ASCO warten.
ORR ergibt ein gemischtes Bild. Nur noch 49% bei T790M+, was m.E. enttäuschend ist. Dafür wurden die >30% bei T790M- bestätigt, was auf lange Sicht noch wichtig werden könnte.
Antwort auf Beitrag Nr.: 49.777.056 von SLGramann am 14.05.15 09:47:52Ergänzung zum vorigen Beitrag:
Patienten: "...87% from US sites..."
Das könnte wichtig sein für irgendwelche Quervergleiche zu anderen Studien und relativiert möglicherweise die "schlechte" ORR.
Patienten: "...87% from US sites..."
Das könnte wichtig sein für irgendwelche Quervergleiche zu anderen Studien und relativiert möglicherweise die "schlechte" ORR.
Antwort auf Beitrag Nr.: 49.777.140 von SLGramann am 14.05.15 09:55:47
Man kann wirklich auf die Präsentationen gespannt sein.
Eine Gegenüberstellung:


Was mich verwirrt sind die doch recht guten PFS Daten von Roci im NEJM (habe dort keinen Zugang).
Laut einer Diskussion über Twitter könnte es sich auch um einen Fehler handeln:

PFS=oberes Ende vom Konfidenzintervall? So kann das ja nicht stimmen...
Interessant auch erste? Ergebnisse von Konkurrenten von Roci. Hier wird z.B. deutlich wie viel besser die Ansprechraten in Asien zu sein scheinen (kleine PI).
80%PR in Japan vs. 25% PR in USA!
http://abstracts.asco.org/156/AbstView_156_144377.html
http://abstracts.asco.org/156/AbstView_156_147772.html
CLVS ist und bleibt so oder so in meinem Depot...!
SG kmastra
Zitat von SLGramann: Ergänzung zum vorigen Beitrag:
Patienten: "...87% from US sites..."
Das könnte wichtig sein für irgendwelche Quervergleiche zu anderen Studien und relativiert möglicherweise die "schlechte" ORR.
Man kann wirklich auf die Präsentationen gespannt sein.
Eine Gegenüberstellung:


Was mich verwirrt sind die doch recht guten PFS Daten von Roci im NEJM (habe dort keinen Zugang).
Laut einer Diskussion über Twitter könnte es sich auch um einen Fehler handeln:

PFS=oberes Ende vom Konfidenzintervall? So kann das ja nicht stimmen...
Interessant auch erste? Ergebnisse von Konkurrenten von Roci. Hier wird z.B. deutlich wie viel besser die Ansprechraten in Asien zu sein scheinen (kleine PI).
80%PR in Japan vs. 25% PR in USA!
http://abstracts.asco.org/156/AbstView_156_144377.html
http://abstracts.asco.org/156/AbstView_156_147772.html
CLVS ist und bleibt so oder so in meinem Depot...!
SG kmastra
Antwort auf Beitrag Nr.: 49.778.067 von kmastra am 14.05.15 12:08:46Goldman weist auf noch etwas wichtiges hin beim "fröhlichen" Quervergleichen:
Goldman Sachs CLVS
CLVS (Buy): Roci T790M-negative data still encouraging
Recall that competitor AZN reported data for AZD9291 (80mg) at ELCC
last month of a response rate of 54% by central review (median PFS of 13.5 months) and ORR of 66% per investigator (median PFS of 10.9 months). When we spoke with CLVS last month they confirmed that the investigator and independent response rates for Roci are internally consistent.
In addition the Roci abstract also contained response rate data for T790M negative
patients – 36%/33% (12/33 via tissue and 10/30 via plasma). The abstract notes that the majority of T790M negative responders were on an EGFR TKI immediately before Roci (10/12 tissue and 10/10 plasma), and hence the responses cannot be explained by a retreatment effect. If we only consider the Roci T790M negative responders
immediately off of prior TKI then the response rates are 30% (10/33) and 33% (10/30), which was lower than the January 2015 update of 44% (7/16), but we note this figure only included the 500/625mg doses. In our view Roci’s response rate is still differentiated from AZN’s AZD9291 data (11% response rate in T790M negative patients who were immediately off of prior TKI). We are also encouraged by the consistency of the T790M negative response rate across tissue and plasma, which in our view decreases the potential risk that a sampling bias drove the delta vs. AZN.
Goldman Sachs CLVS
CLVS (Buy): Roci T790M-negative data still encouraging
Recall that competitor AZN reported data for AZD9291 (80mg) at ELCC
last month of a response rate of 54% by central review (median PFS of 13.5 months) and ORR of 66% per investigator (median PFS of 10.9 months). When we spoke with CLVS last month they confirmed that the investigator and independent response rates for Roci are internally consistent.
In addition the Roci abstract also contained response rate data for T790M negative
patients – 36%/33% (12/33 via tissue and 10/30 via plasma). The abstract notes that the majority of T790M negative responders were on an EGFR TKI immediately before Roci (10/12 tissue and 10/10 plasma), and hence the responses cannot be explained by a retreatment effect. If we only consider the Roci T790M negative responders
immediately off of prior TKI then the response rates are 30% (10/33) and 33% (10/30), which was lower than the January 2015 update of 44% (7/16), but we note this figure only included the 500/625mg doses. In our view Roci’s response rate is still differentiated from AZN’s AZD9291 data (11% response rate in T790M negative patients who were immediately off of prior TKI). We are also encouraged by the consistency of the T790M negative response rate across tissue and plasma, which in our view decreases the potential risk that a sampling bias drove the delta vs. AZN.
SAGE:
SAGE Therapeutics Achieves 77 Percent Response Rate in Completed Phase 1/2 Clinical Trial of SAGE-547
Phase 3 STATUS Trial Expected to Initiate by Mid-2015
http://investor.sagerx.com/releasedetail.cfm?ReleaseID=91312…
http://www.fiercebiotech.com/story/sage-steps-pivotal-phiii-…
None of this is likely to take Sage-watchers by surprise, as the results tend to reflect what investigators were seeing at the interim point. Now, with a successful end-of-Phase II meeting behind the company, the 30-person biotech can see how quickly they can recruit about 126 patients for Phase III and how quickly they can pull it off, aiming to be closer to a year than two years for this next big step toward launching their own U.S. commercial operations.
Läuft...
SAGE Therapeutics Achieves 77 Percent Response Rate in Completed Phase 1/2 Clinical Trial of SAGE-547
Phase 3 STATUS Trial Expected to Initiate by Mid-2015
http://investor.sagerx.com/releasedetail.cfm?ReleaseID=91312…
http://www.fiercebiotech.com/story/sage-steps-pivotal-phiii-…
None of this is likely to take Sage-watchers by surprise, as the results tend to reflect what investigators were seeing at the interim point. Now, with a successful end-of-Phase II meeting behind the company, the 30-person biotech can see how quickly they can recruit about 126 patients for Phase III and how quickly they can pull it off, aiming to be closer to a year than two years for this next big step toward launching their own U.S. commercial operations.
Läuft...
Antwort auf Beitrag Nr.: 49.776.090 von lawmeetstax am 14.05.15 00:34:50ARRY:
Cantor:
Data from abstracts are supportive for binimetinib (with encorafenib), which when
combined with modest expectations, could get revalued in the shares, in our view. The larger trials are ongoing, but earlier/smaller trials point to utility. Selumetinib, licensed to AstraZeneca, looks less compelling to us, and may temper enthusiasm. An interesting option for Array is ONT-380, licensed to Oncothyreon, of which Array is eligible for double-digit royalties (or financial consideration if the drug is partnered or Oncothyreon is acquired). We discuss ONT-380
with Oncothyreon below.
Oncothyreon's ONT-380 data has already been presented, and will be updated at ASCO, thus we believe the shares should not be reactive to abstract publications, and
maintain our HOLD rating. Offsetting this is could be data from a drug with a similar mechanism (neratinib/Puma Biotechnology), though the trial published is unlikely to be in a setting that Oncothyreon would pursue. We think that ONT-380 is undervalued but with such dependence on this candidate, we think the shares are likely to continue to struggle until a clear development path
- like a partner or additional capital - is known.
Read more: http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
Cantor:
Data from abstracts are supportive for binimetinib (with encorafenib), which when
combined with modest expectations, could get revalued in the shares, in our view. The larger trials are ongoing, but earlier/smaller trials point to utility. Selumetinib, licensed to AstraZeneca, looks less compelling to us, and may temper enthusiasm. An interesting option for Array is ONT-380, licensed to Oncothyreon, of which Array is eligible for double-digit royalties (or financial consideration if the drug is partnered or Oncothyreon is acquired). We discuss ONT-380
with Oncothyreon below.
Oncothyreon's ONT-380 data has already been presented, and will be updated at ASCO, thus we believe the shares should not be reactive to abstract publications, and
maintain our HOLD rating. Offsetting this is could be data from a drug with a similar mechanism (neratinib/Puma Biotechnology), though the trial published is unlikely to be in a setting that Oncothyreon would pursue. We think that ONT-380 is undervalued but with such dependence on this candidate, we think the shares are likely to continue to struggle until a clear development path
- like a partner or additional capital - is known.
Read more: http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
Antwort auf Beitrag Nr.: 49.778.325 von SLGramann am 14.05.15 12:53:39nochmal ARRY:
Leerink ASCO Abstracts:
• ARRY (OP): Among 4 abstracts, Ph I data of an investigatorsponsored
trial of binimetinib in combination with imatinib looks
intriguing. NVS (OP)/ARRY saw a 33% PR rate in 15 imatinib-refractory
gastrointestinal stromal tumor (GIST) pts in Ph I when bini was added to
imatinib, indicating MEK inhibition may partially overcome resistance to
KIT/PDGFRA Inhibition in GIST. A Ph II trial in previously untreated GIST
pts is enrolling.
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
So etwas erhoffe ich mir in Zukunft öfters- es tauchen aus irgendeinem investigatorsponsored trial interessante Daten auf. Die MEKs werden eben so breit getestet, da wird vieles, vieles nicht gut funktionieren, aber es kann eben auch immer wieder positive Ergebnisse geben.
Leerink ASCO Abstracts:
• ARRY (OP): Among 4 abstracts, Ph I data of an investigatorsponsored
trial of binimetinib in combination with imatinib looks
intriguing. NVS (OP)/ARRY saw a 33% PR rate in 15 imatinib-refractory
gastrointestinal stromal tumor (GIST) pts in Ph I when bini was added to
imatinib, indicating MEK inhibition may partially overcome resistance to
KIT/PDGFRA Inhibition in GIST. A Ph II trial in previously untreated GIST
pts is enrolling.
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
So etwas erhoffe ich mir in Zukunft öfters- es tauchen aus irgendeinem investigatorsponsored trial interessante Daten auf. Die MEKs werden eben so breit getestet, da wird vieles, vieles nicht gut funktionieren, aber es kann eben auch immer wieder positive Ergebnisse geben.
Antwort auf Beitrag Nr.: 49.778.067 von kmastra am 14.05.15 12:08:46CLVS
Huii... ihr habt hier ja schon eine Menge zusammengetragen... prima!
Interessant finde ich immer noch die Frage, inwiefern die AZD9291-Ergebnisse durch einen höheren Anteil Asiatischer Patienten gegenüber CLVS Rociletinib "geschönt" sind. So findet sich z.B. in den ASCO-Abstracts auch PI-Studien von Astellas T790M-EGFR-Hemmer ASP8273, der bei asiatischen Patienten deutlich bessere ORR-Ergebnisse liefert... 80% vs 25%. AZD9291 hat in seiner Studie anscheinend einen Anteil 2:1 von asiatischen Patienten. CLVS hat dagegen fast 90% der Studie in den USA durchgeführt, so dass der Anteil von asiatischen Patienten erheblich niedriger liegen sollte.
Astellas ASP8273
PI in T790M US-Studie
http://abstracts.asco.org/156/AbstView_156_147772.html
- N = 35
- prior erlotinib: 100%
- median prior TX: 2
- T790M+ ORR 25% (N = 12)
PI in T790M Asian-Studie
http://abstracts.asco.org/156/AbstView_156_144377.html
- N = 30
- prior EGFR-TKI: 51% (sind hier zwar nicht 100%, doch sollten die meisten T790M+ nach EGFR-TKI sein, da 1st-line T790M+ sehr gering ist)
- T790M+: 49% (13% T790M-, 39% unknown)
- T790M+ ORR 80% (N = 15)
#################
AZD9291
AURA PI/II... Veröffentlichung April in NEJM
http://www.nejm.org/doi/full/10.1056/NEJMoa1411817?query=fea…
- N = 253
- Asian / Caucasian: 61% / 31%
- T790M+ ORR 61% (N = 127)
A total of 253 patients were treated. ... Among 127 patients with centrally confirmed EGFR T790M who could be evaluated for response, the response rate was 61% (95% CI, 52 to 70). In contrast, among 61 patients without centrally detectable EGFR T790M who could be evaluated for response, the response rate was 21% (95% CI, 12 to 34). The median progression-free survival was 9.6 months (95% CI, 8.3 to not reached) in EGFR T790M–positive patients and 2.8 months (95% CI, 2.1 to 4.3) in EGFR T790M–negative patients.
***
http://www.onclive.com/web-exclusives/AZD9291-Shows-Promisin…
... In the updated analysis of patients with EGFR T790M-positive NSCLC, the median duration of response has not yet been reached, although data are still immature. The longest duration of response was >8 months and the immature median progression-free survival (PFS) was 10.9 months with the 80 mg dose AZD9291, according to investigator-assessed criteria. An independent review of the data for the 80 mg cohort found an objective response rate (ORR) of 54%. The duration of response was 12.4 months and the PFS was 13.5 months
...
Included in the analysis of the ongoing phase I AURA study were 283 patients with EGFR-mutant advanced NSCLC who received treatment with AZD9291 at 5 doses ranging from 20 to 240 mg once daily. T790M-positive tumors were found in 163 of these patients.
Patients included in the study were a median age of 60 years old, and 62% were female; 61% were Asian and 31% were Caucasian. AZD9291 was administered to patients with advanced NSCLC who were experiencing disease progression after treatment with an EGFR inhibitor.
At all dose levels, the ORR was 59% for patients with EGFR T790M-positive tumors. The ORR was 23% in patients with T790M-negative tumors....
***
1st-line EGFR (also KEINE T790M-Studie!!!... T790M ist hier nur in 8%) ASCO 2015
http://abstracts.asco.org/156/AbstView_156_145109.html
- N = 60
- Asian 72%, White 23%
- mutations: exon 19 del 37%, L858R 40%, other EGFR sensitizing mutations 3%, T790M 8%
- ORR 60% (80 mg), 80% (160 mg)
##########
Rociletinib
PI/II T790M+ ASCO 2015
http://abstracts.asco.org/156/AbstView_156_152181.html
- N = 345
- 87% from US sites
- median prior TX: 3
- T70M+ ORR 48% (N = 186+)
Die T790M- Ergebnisse sehen momentan bei CLVS deutlich besser aus.
https://twitter.com/BMTEdny/status/598696154289799168/photo/…
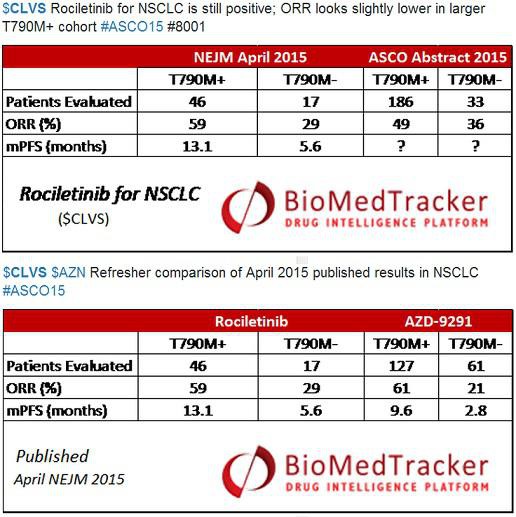
Die entscheidenden Daten von CLVS werden allerdings erst direkt während der ASCO-Präsentation bekannt gegeben!


Gruß
ipollit
Huii... ihr habt hier ja schon eine Menge zusammengetragen... prima!

Interessant finde ich immer noch die Frage, inwiefern die AZD9291-Ergebnisse durch einen höheren Anteil Asiatischer Patienten gegenüber CLVS Rociletinib "geschönt" sind. So findet sich z.B. in den ASCO-Abstracts auch PI-Studien von Astellas T790M-EGFR-Hemmer ASP8273, der bei asiatischen Patienten deutlich bessere ORR-Ergebnisse liefert... 80% vs 25%. AZD9291 hat in seiner Studie anscheinend einen Anteil 2:1 von asiatischen Patienten. CLVS hat dagegen fast 90% der Studie in den USA durchgeführt, so dass der Anteil von asiatischen Patienten erheblich niedriger liegen sollte.
Astellas ASP8273
PI in T790M US-Studie
http://abstracts.asco.org/156/AbstView_156_147772.html
- N = 35
- prior erlotinib: 100%
- median prior TX: 2
- T790M+ ORR 25% (N = 12)
PI in T790M Asian-Studie
http://abstracts.asco.org/156/AbstView_156_144377.html
- N = 30
- prior EGFR-TKI: 51% (sind hier zwar nicht 100%, doch sollten die meisten T790M+ nach EGFR-TKI sein, da 1st-line T790M+ sehr gering ist)
- T790M+: 49% (13% T790M-, 39% unknown)
- T790M+ ORR 80% (N = 15)
#################
AZD9291
AURA PI/II... Veröffentlichung April in NEJM
http://www.nejm.org/doi/full/10.1056/NEJMoa1411817?query=fea…
- N = 253
- Asian / Caucasian: 61% / 31%
- T790M+ ORR 61% (N = 127)
A total of 253 patients were treated. ... Among 127 patients with centrally confirmed EGFR T790M who could be evaluated for response, the response rate was 61% (95% CI, 52 to 70). In contrast, among 61 patients without centrally detectable EGFR T790M who could be evaluated for response, the response rate was 21% (95% CI, 12 to 34). The median progression-free survival was 9.6 months (95% CI, 8.3 to not reached) in EGFR T790M–positive patients and 2.8 months (95% CI, 2.1 to 4.3) in EGFR T790M–negative patients.
***
http://www.onclive.com/web-exclusives/AZD9291-Shows-Promisin…
... In the updated analysis of patients with EGFR T790M-positive NSCLC, the median duration of response has not yet been reached, although data are still immature. The longest duration of response was >8 months and the immature median progression-free survival (PFS) was 10.9 months with the 80 mg dose AZD9291, according to investigator-assessed criteria. An independent review of the data for the 80 mg cohort found an objective response rate (ORR) of 54%. The duration of response was 12.4 months and the PFS was 13.5 months
...
Included in the analysis of the ongoing phase I AURA study were 283 patients with EGFR-mutant advanced NSCLC who received treatment with AZD9291 at 5 doses ranging from 20 to 240 mg once daily. T790M-positive tumors were found in 163 of these patients.
Patients included in the study were a median age of 60 years old, and 62% were female; 61% were Asian and 31% were Caucasian. AZD9291 was administered to patients with advanced NSCLC who were experiencing disease progression after treatment with an EGFR inhibitor.
At all dose levels, the ORR was 59% for patients with EGFR T790M-positive tumors. The ORR was 23% in patients with T790M-negative tumors....
***
1st-line EGFR (also KEINE T790M-Studie!!!... T790M ist hier nur in 8%) ASCO 2015
http://abstracts.asco.org/156/AbstView_156_145109.html
- N = 60
- Asian 72%, White 23%
- mutations: exon 19 del 37%, L858R 40%, other EGFR sensitizing mutations 3%, T790M 8%
- ORR 60% (80 mg), 80% (160 mg)
##########
Rociletinib
PI/II T790M+ ASCO 2015
http://abstracts.asco.org/156/AbstView_156_152181.html
- N = 345
- 87% from US sites
- median prior TX: 3
- T70M+ ORR 48% (N = 186+)
Die T790M- Ergebnisse sehen momentan bei CLVS deutlich besser aus.
https://twitter.com/BMTEdny/status/598696154289799168/photo/…

Die entscheidenden Daten von CLVS werden allerdings erst direkt während der ASCO-Präsentation bekannt gegeben!

Gruß
ipollit
Antwort auf Beitrag Nr.: 49.778.649 von ipollit am 14.05.15 13:42:36"Interessant finde ich immer noch die Frage, inwiefern die AZD9291-Ergebnisse durch einen höheren Anteil Asiatischer Patienten gegenüber CLVS Rociletinib "geschönt" sind."
Definitiv! Zum ersten Mal bin ich damals durch den Beitrag von Dr. Paul DeSantis auf diese Problematik aufmerksam geworden und war... erstaunt...
Deine Zusammenstellung ist beeindruckend! Asiaten oder Kaukasier ist offensichtlich von ziemlicher Bedeutung und das spricht dann eindeutig für Clovis und gegen AstraZeneca.
Inzwischen hat sich die Marktstimmung auch ziemlich gedreht. Nach einem Stark im Minus ist Clovis nun sehr deutlich im Plus.
Fraglich ist vielleicht, welchen Anteil daran Rociletinib und welchen Anteil Rucaparib hat.


Definitiv! Zum ersten Mal bin ich damals durch den Beitrag von Dr. Paul DeSantis auf diese Problematik aufmerksam geworden und war... erstaunt...
Deine Zusammenstellung ist beeindruckend! Asiaten oder Kaukasier ist offensichtlich von ziemlicher Bedeutung und das spricht dann eindeutig für Clovis und gegen AstraZeneca.
Inzwischen hat sich die Marktstimmung auch ziemlich gedreht. Nach einem Stark im Minus ist Clovis nun sehr deutlich im Plus.
Fraglich ist vielleicht, welchen Anteil daran Rociletinib und welchen Anteil Rucaparib hat.


Antwort auf Beitrag Nr.: 49.780.275 von SLGramann am 14.05.15 18:49:10Ähm, mit "definitiv" meinte ich, dass ipollits Frage definitiv berechtigt und interessant ist und nicht, dass sie definitiv beantwortet ist (wobei ich persönlich davon ausgehe, dass die Daten von AstraZeneca tatsächlich positiv "verfälscht" sind).
BLCM:
Kleiner Artikel bei Bloomberg, der erklärt, was an denen so cool ist:
http://www.bloomberg.com/news/articles/2015-05-14/-safety-sw…
BLCM:
Kleiner Artikel bei Bloomberg, der erklärt, was an denen so cool ist:
http://www.bloomberg.com/news/articles/2015-05-14/-safety-sw…
Grund für den KPTI Taucher nach dem ASCO Preview?
Antwort auf Beitrag Nr.: 49.781.103 von Aurum2010 am 14.05.15 21:52:29KPTI
"Grund für den KPTI Taucher nach dem ASCO Preview?"
Ich sehe keinen wirklichen Grund, außer dass es öfters passiert, dass Aktien nach ASCO-Daten erstmal verkauft werden (es sei denn, sie sind unerwartet sensationell, was selten der Fall ist).
Selinexor hat bisher die größte Wirkung bei Blutkrebsarten (flüssige Tumore) gezeigt... hier laufen ja auch die aktuellen Zulassungs-Studien. In soliden Tumoren gibt es dagegen bisher noch nicht so aussagekräftige Daten. In den gestrigen ASCO-Abstracts gibt es erste Hinweise...

Ich kann nicht genau sagen, wie gut oder schlecht diese Daten sind... könnte mir aber vorstellen, dass nicht wenige sie als nicht gut interpretieren, also dass die Wirkung nur marginal ist mit niedrigen ORRs (PRs).
Zuviel sollte man meiner Meinung nach aber nicht erwarten, da es sich um Patienten mit sehr fortgeschrittener Krankheit und einer Selinexor Mono-Therapie handelt. Ich sehe Selinexor eher in der Kombi-Anwendung mit einer Vielzahl anderer Mittel... z.B. war bei Mono-Anwendung in MM (Blutkrebs) PR nur 7%... in Kombi mit Dex über 50%. Wichtig ist auch die DCR-Rate (CR+PR+SD), also inkl. stabilen Zustand (kein Krankheitsfortschritt). Diese kann sich in Kombi vielleicht zu PR steigern lassen. KPTI hat auch öfters hervorgehoben, dass es langanhaltende stabile Zustände geben kann.
Dementsprechend sehe ich in den gestrigen Daten bisher nichts negatives. Solange es keine umfangreicheren Daten gibt, z.B. wie lange die Wirkung anhält oder ob sich durch Kombis die Ansprechraten steigern lassen, kann man wohl das Potential von Selinexor in Soliden Tumoren noch nicht abschätzen. Die Erwartungen des Marktes sind meiner Meinung nach bisher sehr gering.
Ich bin schon relativ hoch investiert... eventuell lege ich bei diesen Kursen aber noch etwas nach.




Gruß
ipollit
"Grund für den KPTI Taucher nach dem ASCO Preview?"
Ich sehe keinen wirklichen Grund, außer dass es öfters passiert, dass Aktien nach ASCO-Daten erstmal verkauft werden (es sei denn, sie sind unerwartet sensationell, was selten der Fall ist).
Selinexor hat bisher die größte Wirkung bei Blutkrebsarten (flüssige Tumore) gezeigt... hier laufen ja auch die aktuellen Zulassungs-Studien. In soliden Tumoren gibt es dagegen bisher noch nicht so aussagekräftige Daten. In den gestrigen ASCO-Abstracts gibt es erste Hinweise...

Ich kann nicht genau sagen, wie gut oder schlecht diese Daten sind... könnte mir aber vorstellen, dass nicht wenige sie als nicht gut interpretieren, also dass die Wirkung nur marginal ist mit niedrigen ORRs (PRs).
Zuviel sollte man meiner Meinung nach aber nicht erwarten, da es sich um Patienten mit sehr fortgeschrittener Krankheit und einer Selinexor Mono-Therapie handelt. Ich sehe Selinexor eher in der Kombi-Anwendung mit einer Vielzahl anderer Mittel... z.B. war bei Mono-Anwendung in MM (Blutkrebs) PR nur 7%... in Kombi mit Dex über 50%. Wichtig ist auch die DCR-Rate (CR+PR+SD), also inkl. stabilen Zustand (kein Krankheitsfortschritt). Diese kann sich in Kombi vielleicht zu PR steigern lassen. KPTI hat auch öfters hervorgehoben, dass es langanhaltende stabile Zustände geben kann.
Dementsprechend sehe ich in den gestrigen Daten bisher nichts negatives. Solange es keine umfangreicheren Daten gibt, z.B. wie lange die Wirkung anhält oder ob sich durch Kombis die Ansprechraten steigern lassen, kann man wohl das Potential von Selinexor in Soliden Tumoren noch nicht abschätzen. Die Erwartungen des Marktes sind meiner Meinung nach bisher sehr gering.
Ich bin schon relativ hoch investiert... eventuell lege ich bei diesen Kursen aber noch etwas nach.



Gruß
ipollit
FGEN
könnte auf dem Niveau auch interessant sein. Wenn ich es richtig verstanden habe, machen gerade einige Kasse, da die Haltefristen nach dem IPO jetzt abgelaufen sind.
"Coincidentally $FGEN lock-up expired yesterday. Affects 82% of outstanding shares"

Gruß
ipollit
könnte auf dem Niveau auch interessant sein. Wenn ich es richtig verstanden habe, machen gerade einige Kasse, da die Haltefristen nach dem IPO jetzt abgelaufen sind.
"Coincidentally $FGEN lock-up expired yesterday. Affects 82% of outstanding shares"
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.781.673 von ipollit am 14.05.15 23:57:33
OK Danke - Habe mir gestern beim Taucher eine erste Pos. zugelegt.
Zitat von ipollit: KPTI
"Grund für den KPTI Taucher nach dem ASCO Preview?"
Ich sehe keinen wirklichen Grund, außer dass es öfters passiert, dass Aktien nach ASCO-Daten erstmal verkauft werden (es sei denn, sie sind unerwartet sensationell, was selten der Fall ist).
Selinexor hat bisher die größte Wirkung bei Blutkrebsarten (flüssige Tumore) gezeigt... hier laufen ja auch die aktuellen Zulassungs-Studien. In soliden Tumoren gibt es dagegen bisher noch nicht so aussagekräftige Daten. In den gestrigen ASCO-Abstracts gibt es erste Hinweise...
Ich kann nicht genau sagen, wie gut oder schlecht diese Daten sind... könnte mir aber vorstellen, dass nicht wenige sie als nicht gut interpretieren, also dass die Wirkung nur marginal ist mit niedrigen ORRs (PRs).
Zuviel sollte man meiner Meinung nach aber nicht erwarten, da es sich um Patienten mit sehr fortgeschrittener Krankheit und einer Selinexor Mono-Therapie handelt. Ich sehe Selinexor eher in der Kombi-Anwendung mit einer Vielzahl anderer Mittel... z.B. war bei Mono-Anwendung in MM (Blutkrebs) PR nur 7%... in Kombi mit Dex über 50%. Wichtig ist auch die DCR-Rate (CR+PR+SD), also inkl. stabilen Zustand (kein Krankheitsfortschritt). Diese kann sich in Kombi vielleicht zu PR steigern lassen. KPTI hat auch öfters hervorgehoben, dass es langanhaltende stabile Zustände geben kann.
Dementsprechend sehe ich in den gestrigen Daten bisher nichts negatives. Solange es keine umfangreicheren Daten gibt, z.B. wie lange die Wirkung anhält oder ob sich durch Kombis die Ansprechraten steigern lassen, kann man wohl das Potential von Selinexor in Soliden Tumoren noch nicht abschätzen. Die Erwartungen des Marktes sind meiner Meinung nach bisher sehr gering.
Ich bin schon relativ hoch investiert... eventuell lege ich bei diesen Kursen aber noch etwas nach.
Gruß
ipollit
OK Danke - Habe mir gestern beim Taucher eine erste Pos. zugelegt.
MDVN
mal schauen, wo Xtandi irgendwann auch in Brustkrebs eine Option wird. Die Rolle von AR ist in dieser Indikation anders als in Prostatakrebs eher unklar. Ursprünglich habe ich es als high risk gesehen. MDVN argumentiert, dass es z.B. in TNBC (Brustkrebs, bei dem keine der drei bekannten Klassen Estrogen Receptor (ER), Progesterone Receptor (PR) und HER2 wirkt) auch etwas geben muss, das den Krebs antreibt... eine Möglichkeit wäre der Androgen receptor (AR).
In TNBC wird auch PD1&Co getestet... ich fände daher eine Kombi aus Xtandi + z.B. MDVNs PD1 Pidilizumab interessant. MDVN will Pidilizumab neben der Zulassungsstudie in DLBCL Blutkrebs auch in Prostata- und Brustkrebs entwickeln, soweit ich es verstanden habe.
Xtandi wird aber auch noch über TNBC hinaus in Brustkrebs getestet.
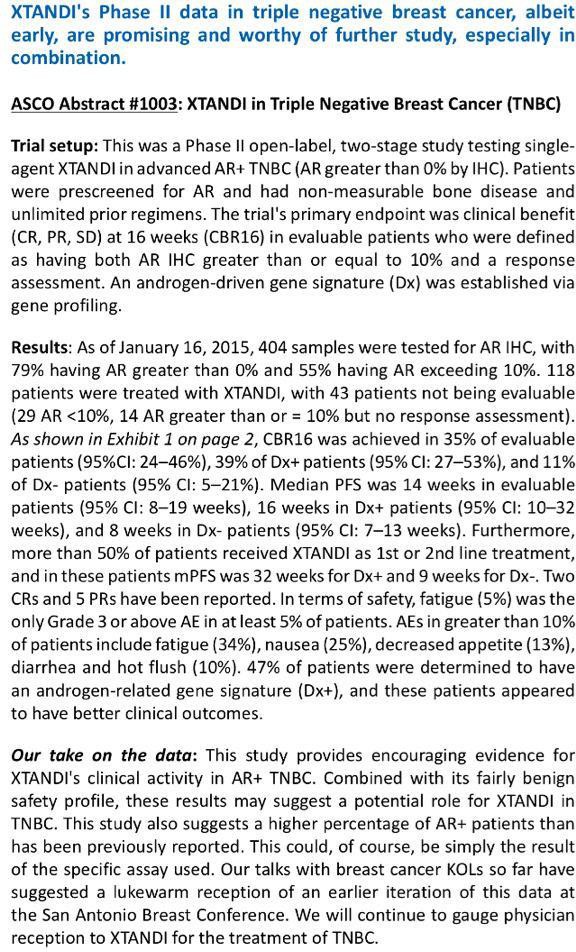
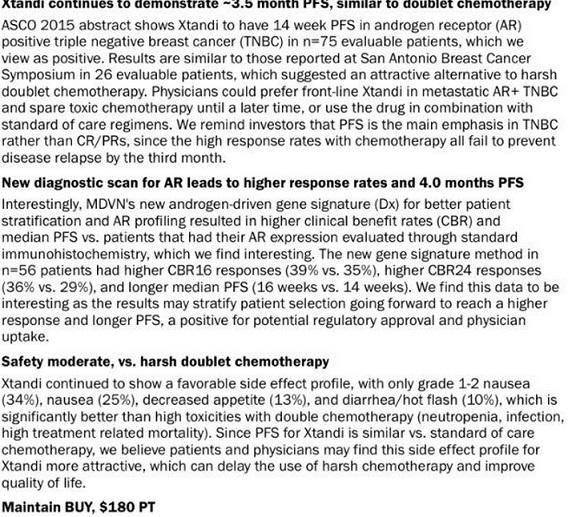

Gruß
ipollit
mal schauen, wo Xtandi irgendwann auch in Brustkrebs eine Option wird. Die Rolle von AR ist in dieser Indikation anders als in Prostatakrebs eher unklar. Ursprünglich habe ich es als high risk gesehen. MDVN argumentiert, dass es z.B. in TNBC (Brustkrebs, bei dem keine der drei bekannten Klassen Estrogen Receptor (ER), Progesterone Receptor (PR) und HER2 wirkt) auch etwas geben muss, das den Krebs antreibt... eine Möglichkeit wäre der Androgen receptor (AR).
In TNBC wird auch PD1&Co getestet... ich fände daher eine Kombi aus Xtandi + z.B. MDVNs PD1 Pidilizumab interessant. MDVN will Pidilizumab neben der Zulassungsstudie in DLBCL Blutkrebs auch in Prostata- und Brustkrebs entwickeln, soweit ich es verstanden habe.
Xtandi wird aber auch noch über TNBC hinaus in Brustkrebs getestet.


Gruß
ipollit
INCY
die ersten Daten von INCYs pi3k-delta mit/ohne JAK1 sehen meiner Meinung nach ganz gut aus... INCY will hier als nächstes Zulassungsstudien starten.


Gruß
ipollit
die ersten Daten von INCYs pi3k-delta mit/ohne JAK1 sehen meiner Meinung nach ganz gut aus... INCY will hier als nächstes Zulassungsstudien starten.


Gruß
ipollit
CLVS:
Nach dem Kurssprung gestern sieht Piper die Bewertung als vorerst ausgereizt an, verweist aber auf die Möglichkeit einer Übernahme, bei der sicher immer noch eine ordentliche Prämie draufgelegt werden würde.
Ich denke, wenn die endgültigen Daten auf der ASCO wirklich den Erwartungen entsprechen, dann ist eine Übernahme nicht unwahrscheinlich. Clovis hat ja wirklich etwas zu bieten!

Nach dem Kurssprung gestern sieht Piper die Bewertung als vorerst ausgereizt an, verweist aber auf die Möglichkeit einer Übernahme, bei der sicher immer noch eine ordentliche Prämie draufgelegt werden würde.
Ich denke, wenn die endgültigen Daten auf der ASCO wirklich den Erwartungen entsprechen, dann ist eine Übernahme nicht unwahrscheinlich. Clovis hat ja wirklich etwas zu bieten!

ZFGN
Zafgen ist ein weiterer Wert, der vom Hoch ein ganzes Stück zurück gekommen ist. Man muss aber auch die KE beachten. Momentan wird ZFGN mit 850 Mio $ bewertet.

Im Bereich von 30$ könnte sich eine Unterstützung gebildet haben.
Für den Rückgang gibt es m.E. aber durchaus Gründe, die insebsondere mit der PIII in PWS zu tun haben.
- erst Verzögerung der ersten Ergebnisse von Q4/15 auf Q2/16 (mitlerweile wieder early Q1/16)
- Ganz schön viele Veränderungen in der Studie (s. Anaystenkommentare)
Ich habe hier nochmal zugekauft in der Hoffnung dass die 30$ Marke hält. Zudem ist durch die Verschiebung der PIII in PWS jetzt erstmal eine PII bei übergewichtigen Menschen mit Diabetes das nächste größere Ereignis.
Zudem soll dieses Jahr noch Neues zum NASH Programm kommen.
Einige Analystenkommentare:




Hier noch ein Video, dass neben PWS auch noch einen Fall in HIAO aufgreift. Das sind die beiden Orpha Indikationen, in denen B. entwickelt wird. So wie ich es verstehe ist der Erfolg mit einem Magenband aber eher die Ausnahme und zudem sehr riskant.
Ist ZFGN nicht auch ein Klasse Übernahmeziel? Ein großer Partner könnte die Pipeline viel konsequenter in Richtung Massenmarkt entwickeln. Wenn man sieht was gerade für Orphanmedikamenten bezahlt wurde ist ZFGN ja noch sehr günstig. Andereseits ist der Erfolg in PWS bestimmt keine sichere Sache, obwohl B. ja erstaunlich effektiv ist.
SG kmastra
Zafgen ist ein weiterer Wert, der vom Hoch ein ganzes Stück zurück gekommen ist. Man muss aber auch die KE beachten. Momentan wird ZFGN mit 850 Mio $ bewertet.
Im Bereich von 30$ könnte sich eine Unterstützung gebildet haben.
Für den Rückgang gibt es m.E. aber durchaus Gründe, die insebsondere mit der PIII in PWS zu tun haben.
- erst Verzögerung der ersten Ergebnisse von Q4/15 auf Q2/16 (mitlerweile wieder early Q1/16)
- Ganz schön viele Veränderungen in der Studie (s. Anaystenkommentare)
Ich habe hier nochmal zugekauft in der Hoffnung dass die 30$ Marke hält. Zudem ist durch die Verschiebung der PIII in PWS jetzt erstmal eine PII bei übergewichtigen Menschen mit Diabetes das nächste größere Ereignis.
Zudem soll dieses Jahr noch Neues zum NASH Programm kommen.
Einige Analystenkommentare:




Hier noch ein Video, dass neben PWS auch noch einen Fall in HIAO aufgreift. Das sind die beiden Orpha Indikationen, in denen B. entwickelt wird. So wie ich es verstehe ist der Erfolg mit einem Magenband aber eher die Ausnahme und zudem sehr riskant.
Ist ZFGN nicht auch ein Klasse Übernahmeziel? Ein großer Partner könnte die Pipeline viel konsequenter in Richtung Massenmarkt entwickeln. Wenn man sieht was gerade für Orphanmedikamenten bezahlt wurde ist ZFGN ja noch sehr günstig. Andereseits ist der Erfolg in PWS bestimmt keine sichere Sache, obwohl B. ja erstaunlich effektiv ist.
SG kmastra
Antwort auf Beitrag Nr.: 49.784.919 von kmastra am 15.05.15 14:02:09"Zafgen ist ein weiterer Wert, der vom Hoch ein ganzes Stück zurück gekommen ist."
Ich bin überrascht über den Niedergang des Wertes und über die Dynamik der Abwärtsbewegung. Ich halte viel von Zafgen und werde meine Position jetzt wahrscheinlich ausbauen.
Zwar weiß ich nicht, wann und wo der Niedergang endet, aber ich denke nicht, dass die Aktie zu teuer ist.
Das größte Risiko sehe ich darin, dass der Effekt von Beloranib vielleicht nicht dauerhaft sein könnte.
Ich bin überrascht über den Niedergang des Wertes und über die Dynamik der Abwärtsbewegung. Ich halte viel von Zafgen und werde meine Position jetzt wahrscheinlich ausbauen.
Zwar weiß ich nicht, wann und wo der Niedergang endet, aber ich denke nicht, dass die Aktie zu teuer ist.
Das größte Risiko sehe ich darin, dass der Effekt von Beloranib vielleicht nicht dauerhaft sein könnte.
Antwort auf Beitrag Nr.: 49.783.158 von ipollit am 15.05.15 10:25:48In diesem Zusammenhang ist TOKAI PHARMACEUTICALS Galeteron interessant:
http://www.tokaipharmaceuticals.com/programs.php
http://247wallst.com/healthcare-business/2015/05/12/could-th…
http://www.tokaipharmaceuticals.com/programs.php
http://247wallst.com/healthcare-business/2015/05/12/could-th…
Antwort auf Beitrag Nr.: 49.637.021 von McNay am 24.04.15 13:49:07IMMU
IMMU-132 hat nun in TNBC, SCLC und NSCLC Fast-Track von der FDA.
Die Ergebnisse sehen schon recht vielversprechend aus. Z.B. im Vergleich mit CLDXs ADC Glembatumumab scheint IMMU-132 deutlich besser zu sein (so wie es auch unten steht). MDVNs Xtandi ist bisher in TNBC von den Zahlen auch eher hinter IMMU-132... allerdings könnte Xtandi eine Option am Anfang oder in Kombi sein, da die Nebenwirkungen recht gering sind.
Laut CC will IMMU für die Zulassungsstudie unbedingt einen größeren Partner mit im Boot haben, um die Entwicklung schnell und breit voranzutreiben. Der Partner müsste in diesem Fall in der nächsten Zeit bekannt gegeben werden, wenn die Studie noch dieses Jahr beginnen soll.
http://www.immunomedics.com/pdfs/company-presentation.pdf

CBR 6 Monate von 50% müsste eigentlich gleichbedeutend mit einem medianen PFS von 6 Monaten sein...
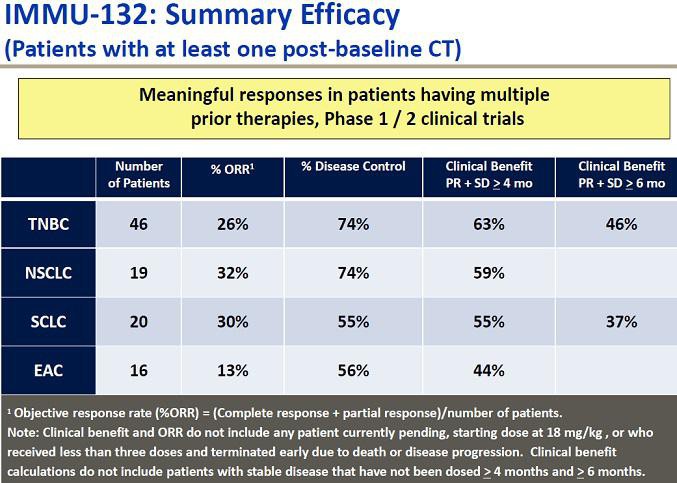
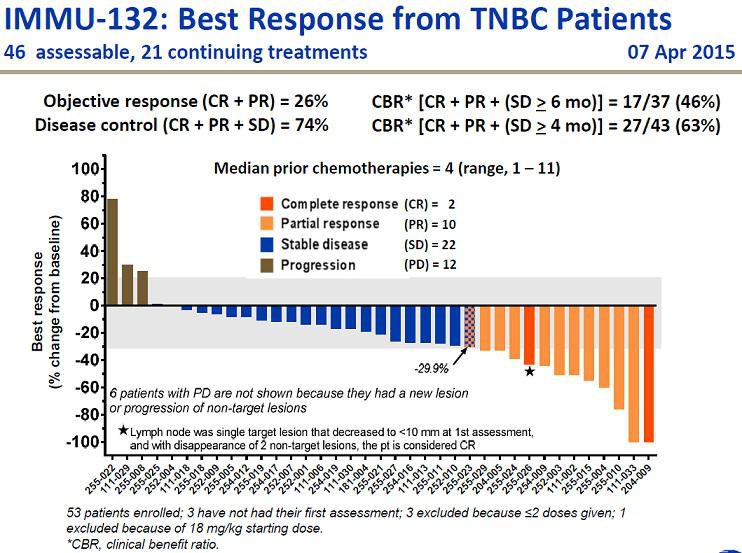
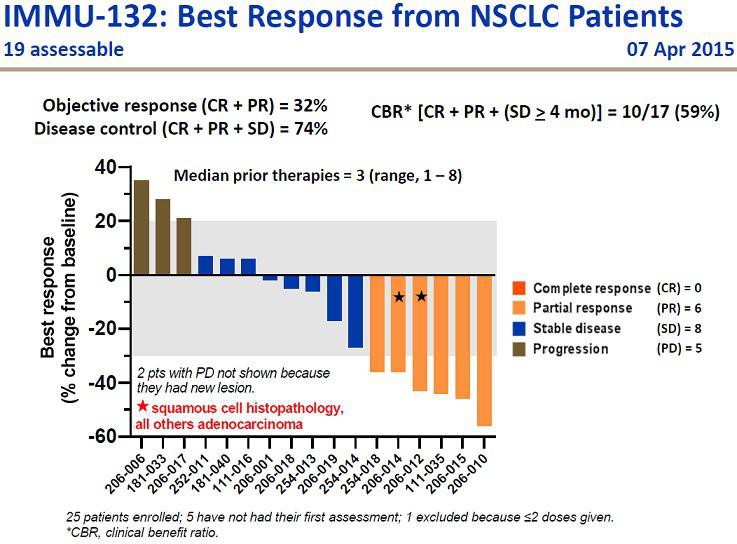
Nebenwirkungen sind relativ mild... insbesondere im Vergleich mit der Irinotecan-Chemo, die den gleichen aktiven Wirkstoff SN-38 besitzt, nur dass IMMU-132 diesen im Tumor viel stärker anreichert.
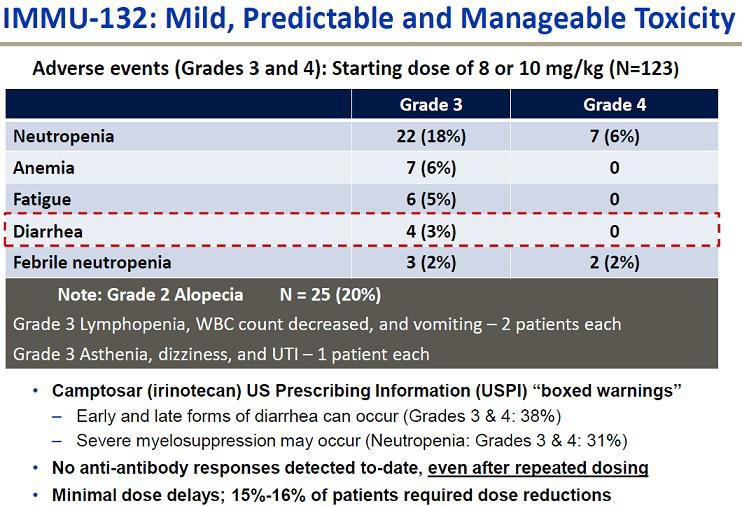
In der nächsten Zeit sollten auch PIII-Daten zum CD22-AK Epratuzumab in Lupus vom Partner UCB kommen... aus meiner Sicht ein HighRisk-Event.
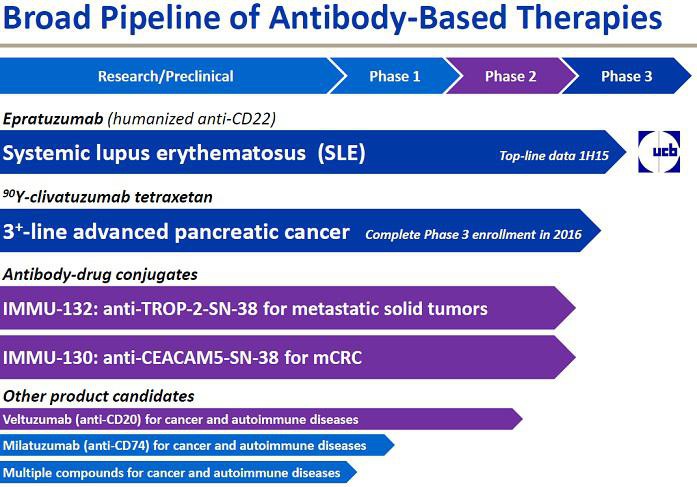
****
IMMU: IMMU-132 Analysis Points To A Promising Oncology Asset Triple-negative Breast Cancer To Anchor A Global License Mid-15?
• Summary: While investors eagerly await the Phase III EMBODY-1 & 2 pooled, top-line results for epratuzumab in lupus by the end of Q2 2015E (the key inflection point for IMMU shares in 2015), a key near-term and under- appreciated event for shares potentially prior to the EMBODY data is the announcement of a global partnership with a major pharmaceutical company for sacituzumab govitecan (SG; formerly IMMU-132), IMMU's lead antibody drug conjugate (ADC) in solid tumors. Following last week's Phase I/II update at the American Association for Cancer Research (AACR) Meeting we completed a deeper dive on SG's overall profile with a key focus on lead indication, triple- negative breast cancer (TNBC). Our conclusion: While TNBC has historically been a very challenging disease to treat we believe SG could have a best-in-class profile, and importantly early efficacy results in non-small cell lung cancer (NSCLC) are in the vicinity of Merck and Bristol-Myers' promising programmed- death ligand 1 antibodies (PD-L1/PD-1) Keytruda and Opdivo, offering an attractive 2nd shot on goal for future development by a partner. Thus we believe enthusiasm around SG is justified and the asset could indeed warrant strong licensing interest due to its overall profile (responses in six tumor types and good tolerability), quicker to market indications (TNBC and small-cell lung cancer [SCLC]), larger (but more competitive) markets (NSCLC), and potential to move into earlier lines of therapy longer-term as monotherapy and in combinations.
• TNBC data suggests a potential best-in-class efficacy profile. SG's largest data set is in TNBC (n=46 assessable) with a 26% Objective Response Rate (ORR), 2 Complete Responses [CR] have been observed with one previously being a Partial Response [PR], 74% Disease Control Rate (DCR), 46% of patients have achieved stable disease [SD] or better for 6+ months, and maturing median progression-free survival (PFS) of 6 months (at the 10mg/kg dose). The PFS results are generally in-line with what will likely be needed to demonstrate a statistically significant difference over chemotherapy in a Ph. III program. Overall SG compares favorably, in our view, to other mid/late stage competitors. Consider, Merck's Keytruda and Roche's MPDL3280A PD-L1 19% ORR and 24- 27% 6-month PFS; Celldex's glembatumumab's 33% ORR but only 3.0 month PFS in glycoprotein NMB (GPNMB) protein high expressers; BMRN's BMN673 has generated Key Opinion Leader enthusiasm with 22% ORR as a single agent, but is primarily being developed for germline Breast Cancer 1/2 early onset (BRCA1/2) mutant patients; and Medivation's enzalutamide targets androgen receptor positive (AR+) TNBC but has reported a lower 8% ORR (see Exhibit 4 for more details). Celldex is currently running the Ph. III METRIC study, Merck plans to initiate a Ph. II in 2015, enzalutamide's Ph. I/II data will continue to mature during 2015, and Roche plans to pursue a Ph. III program in 1st-Line TNBC in combination with nab-paclitaxel.
Valuation Range: $7.00 to $7.50
2015 could be a transformative year and we see upside potential from current levels with positive Ph. III epratuzumab data and an IMMU-132 partnership.
• SG's Next steps. (1) Management has guided to End-of-Ph. II FDA/EMA meetings to discuss current data and a Ph. III protocol by early Q2 (we expect an update on this during the Fiscal Q3 2015 earnings call next week). (2) At the 2015 ASCO Meeting there will be a poster in TNBC (Saturday May 30, #1016) and an oral presentation in NSCLC (Tuesday June 2, 9:00-9:12 am CT, #2504). (3) Announcement of a licensing agreement during Q2 or Q3. (4) The prospective partner is to commence the Ph. III study in relapsed/refractory TNBC by the end of 2015 (a key “must have” for IMMU as part of a licensing agreement based on recent IMMU management comments). We assume a Q2 licensing deal is announced ahead of the EMBODY data with a $65 million upfront payment, up to $190 million in clinical/regulatory milestones related to TNBC, and a 20% flat global royalty. At this time we only model TNBC revenues (at 50% probability of success) with US and European Union launches in 2022. If a Ph. III TNBC program is initiated by the end of 2015 (instead of a randomized Ph. II study followed by a subsequent Ph. III), this could accelerate development timelines by roughly two years, and may offer upside to our current estimates.
• 2015 AACR Update on ORR and safety… steady as she goes. As with previous updates during 2014 at multiple medical meetings (with fewer assessable patients and shorter duration of dosing and response), efficacy and safety data reported at the 2015 AACR Meeting are generally consistent for the overall patient population (n=162 assessable for efficacy and n=123 for safety). ORR and DCR were 17% and 64% with broad clinical activity as PRs have been observed in 6 tumor types to date. ORR and DCR for updates in November 2014 and February 2015 were 18%/62% and 19%/67%, respectively. Please refer to Exhibit 1 for more details. Safety remains unremarkable, in our view, as Grade 3/4 neutropenia was 24%, febrile neutropenia was 4%, and diarrhea was 3%. Please refer to Exhibit 3 for more details. These rates – while in different tumors types and fewer patients – are numerically lower than those observed with irinotecan (per the Camptosar label).
• Data suggest SG may have a broader market opportunity (in 2nd-Line+ TNBC) than other mid/late stage TNBC competitors. Based on data to date, it appears SG is potentially effective in all unselected TNBC patients (as the ADC targets tumors that over-express human trophoblast cell surface antigen ) whereas Keytruda (PD-L1+ high-expressers), MPDL3280A (PD-L1+ expressers), enzalutamide (AR+ high expressers), and glembatumumab vedotin (GPNMB high expressers) can only target sub-populations (based on biomarkers) and appear more effective in TNBC that over-express the specific proteins. The proportion of patients that express these various proteins varies from roughly 33% to 70%. Please refer to Exhibit 5 for more details. Clearly this is an important consideration for partnering discussions as it potentially would enable treatment of all the roughly 35,000+ U.S. and 56,000+ European Union TNBC patients (in all lines) with SG compared to somewhat narrower market opportunities for the other drugs/antibodies.
• While early and with a smaller “N”, SG’s NSCLC data are encouraging and suggest SG is on the right track and not that dissimilar from Merck’s Keytruda and Bristol’s Opdivo in 2nd/3rd-Line NSCLC. Behind TNBC we believe NSCLC offers a 2nd tumor type that could be attractive to potential licensing suitors due to the large market opportunity and unmet medical need, albeit with significantly more competition than TNBC. At the AACR Meeting IMMU reported 32% ORR (with 6 PR’s), 32% DCR, and 59% CBR (SD/PR/CR for 4+ months), respectively, in NSCLC patients who failed a median of 3 prior therapies. Overall Survival (OS) data are too immature to assess but PFS for the 18 patients dosed at 8 or 10mg/kg, was 5.4 months. By comparison, at the 2012 ASCO Meeting, Bristol-Myers’ reported 28% ORR for Opdivo 3mg/kg (the go-forward Ph. III monotherapy dose in NSCLC) in 18 patients in the Ph. I(b) -003 Study. SG compares similarly well to Merck’s Keytruda as last week’s NEJM online paper indicates that ORR was 44% in high expressers of PD-L1 with a median PFS of 6.1 months. While we don’t want to over-interpret early data compared to two broad Ph. III programs for Merck and Bristol-Myers, these initial results suggest SG is a highly active ADC. Ultimately duration of response, maturing PFS, and initial OS (potentially at the 2015 ASCO or European Society for Medical Oncology Scientific Sessions) will help determine what role SG could play in this tumor type.
Most promising activity appears to be in TNBC, NSCLC, and SCLC. During 2014 IMMU provided periodic updates on the Ph. I/II study (ASCO, World Antibody Drug Conjugate Summit, and San Antonio Breast Cancer Symposium [SABCS]). The update at last week’s AACR Meeting was numerically similar for ORR for all assessable patients and by specific tumor type. Patients had very advanced disease at baseline with an average of 2.5 to 4 prior therapies (depending on tumor type) and some with 11 priors (in the TNBC population). As noted in the prior exhibit, TNBC, NSCLC, and SCLC ORR and CBR rates were 26%/74%, 32%/74%, and 30%/55%, respectively. Roughly 50% of TNBC patients were able to achieve stable disease or better for at least six months (as represented by CBR >6), suggesting a good tolerability profile combined with meaningful clinical benefit. Interestingly one TNBC patient has had their prior PR convert to a CR, potentially suggesting a deepening of response may occur the longer a patient can stay on therapy. This phenomenon has been broadly observed with many novel oral therapies for blood cancers (e.g., Revlimid, Imbruvica, Zydelig). Maturing PFS data were provided for TNBC (3.7 months at 8mg/kg and 6.0 months at 10mg/kg), for NSCLC (5.4 months), SCLC (2.4 months), esophageal (4.1 months), and colorectal (3.9 months). OS data are too immature for TNBC, NSCLC, and SCLC, while a median has not been reached for esophageal.
Minimal severe/life-threatening adverse events have been observed to date. As of the 2015 AACR Meeting, fatigue (5% Grade 3), diarrhea (3% Grade 3), alopecia (18 % overall, 0% Grade 3/4), and vomiting (2% Grade 3) were the most common non-hematologic adverse events. Neutropenia (18% Grade 3, and 6% Grade 4) was the most common hematologic AE, as would be expected due to SG’s similarity to irinotecan, and febrile neutropenia was limited (2% Grade 3 and 2% Grade 4). In patients where neutropenia was observed, the SG dose was reduced or delayed and/or the physician administered growth factor support, when appropriate. SG’s AE profile has generally been consistent in terms of numerical rates compared with updates at the 2014 ASCO Meeting, World ADC Summit in October, and SABCS in December. Importantly, to date no antibodies against SG or SN-38 have been detected and dose reductions at the 8 (n=76) and 10mg/kg (n=33) groups have been limited with a total of 17 patients requiring a dose reduction (~15-16% of patients in both dosing arms).
Comparison to irinotecan suggests much lower toxicities, which may allow for a more tolerable regimen, ability to dose longer, and lead to improved outcomes. While it is challenging to compare single-arm Ph. I/II results for SG to Ph. III data for irinotecan (in a different indication), results to date suggest SG has a more tolerable profile, based on rates of key AEs. As noted in Exhibit 3 above, irinotecan has Grade 3/ 4 rates of neutropenia, diarrhea, and febrile neutropenia of 31%, 38%, and 8% compared to SG’s 24%, 3% and 4%, respectively.
Broader market opportunity than other mid/late stage programs? As noted in Exhibit 5, SG is likely to have a broader market opportunity compared to other programs in development for TNBC since SG does not target selected sub-populations based on a biomarker. Merck’s Keytruda and Roche’s MPDL3280A may only be applicable in PD-L1+ TNBC patients, but what proportion of patients are truly PD-L1+ may be driven by both companies’ immunohistochemistry assays and their respective definitions. In addition, it is currently unclear based on data to date for both programs, if they will target high expressers or all PD-L1+ TNBC. In NSCLC, we note low expressers of PD-L1 have poorer outcomes with Keytruda than those identified as high expressers. Thus Merck may opt to target high expressers in its upcoming Ph. II study. Roche has already announced plans to move into a Ph. III combination study with nab-paclitaxel in 1st-Line TNBC, and may forego 2nd-Line+ patients. The Ph. III EMBRACA study for talazoparib is targeting locally advanced and/or metastatic breast cancer with germline BRCA1/2 mutations. Research suggests roughly 25% of TNBC patients have the BRCA1 mutation. Thus, talazoparib may only be approved for use in this subset of TNBC (or not at all depending on how large a proportion of the Ph. III study is TNBC). For Medivation’s enzalutamide, a key question is what proportion of TNBC are truly androgen receptor positive and high expressers, as well. We identified an abstract presented at the 2014 SABCS which suggested roughly 1/3 of TNBC are AR+. Medivation believes up to 80% of TNBC express some level of AR+ while 55% express high levels. Finally, Celldex is targeting high GPNMB expressers, which the company believes could represent upwards of roughly 35% of TNBC.

Gruß
ipollit
IMMU-132 hat nun in TNBC, SCLC und NSCLC Fast-Track von der FDA.
Die Ergebnisse sehen schon recht vielversprechend aus. Z.B. im Vergleich mit CLDXs ADC Glembatumumab scheint IMMU-132 deutlich besser zu sein (so wie es auch unten steht). MDVNs Xtandi ist bisher in TNBC von den Zahlen auch eher hinter IMMU-132... allerdings könnte Xtandi eine Option am Anfang oder in Kombi sein, da die Nebenwirkungen recht gering sind.
Laut CC will IMMU für die Zulassungsstudie unbedingt einen größeren Partner mit im Boot haben, um die Entwicklung schnell und breit voranzutreiben. Der Partner müsste in diesem Fall in der nächsten Zeit bekannt gegeben werden, wenn die Studie noch dieses Jahr beginnen soll.
http://www.immunomedics.com/pdfs/company-presentation.pdf

CBR 6 Monate von 50% müsste eigentlich gleichbedeutend mit einem medianen PFS von 6 Monaten sein...



Nebenwirkungen sind relativ mild... insbesondere im Vergleich mit der Irinotecan-Chemo, die den gleichen aktiven Wirkstoff SN-38 besitzt, nur dass IMMU-132 diesen im Tumor viel stärker anreichert.

In der nächsten Zeit sollten auch PIII-Daten zum CD22-AK Epratuzumab in Lupus vom Partner UCB kommen... aus meiner Sicht ein HighRisk-Event.

****
IMMU: IMMU-132 Analysis Points To A Promising Oncology Asset Triple-negative Breast Cancer To Anchor A Global License Mid-15?
• Summary: While investors eagerly await the Phase III EMBODY-1 & 2 pooled, top-line results for epratuzumab in lupus by the end of Q2 2015E (the key inflection point for IMMU shares in 2015), a key near-term and under- appreciated event for shares potentially prior to the EMBODY data is the announcement of a global partnership with a major pharmaceutical company for sacituzumab govitecan (SG; formerly IMMU-132), IMMU's lead antibody drug conjugate (ADC) in solid tumors. Following last week's Phase I/II update at the American Association for Cancer Research (AACR) Meeting we completed a deeper dive on SG's overall profile with a key focus on lead indication, triple- negative breast cancer (TNBC). Our conclusion: While TNBC has historically been a very challenging disease to treat we believe SG could have a best-in-class profile, and importantly early efficacy results in non-small cell lung cancer (NSCLC) are in the vicinity of Merck and Bristol-Myers' promising programmed- death ligand 1 antibodies (PD-L1/PD-1) Keytruda and Opdivo, offering an attractive 2nd shot on goal for future development by a partner. Thus we believe enthusiasm around SG is justified and the asset could indeed warrant strong licensing interest due to its overall profile (responses in six tumor types and good tolerability), quicker to market indications (TNBC and small-cell lung cancer [SCLC]), larger (but more competitive) markets (NSCLC), and potential to move into earlier lines of therapy longer-term as monotherapy and in combinations.
• TNBC data suggests a potential best-in-class efficacy profile. SG's largest data set is in TNBC (n=46 assessable) with a 26% Objective Response Rate (ORR), 2 Complete Responses [CR] have been observed with one previously being a Partial Response [PR], 74% Disease Control Rate (DCR), 46% of patients have achieved stable disease [SD] or better for 6+ months, and maturing median progression-free survival (PFS) of 6 months (at the 10mg/kg dose). The PFS results are generally in-line with what will likely be needed to demonstrate a statistically significant difference over chemotherapy in a Ph. III program. Overall SG compares favorably, in our view, to other mid/late stage competitors. Consider, Merck's Keytruda and Roche's MPDL3280A PD-L1 19% ORR and 24- 27% 6-month PFS; Celldex's glembatumumab's 33% ORR but only 3.0 month PFS in glycoprotein NMB (GPNMB) protein high expressers; BMRN's BMN673 has generated Key Opinion Leader enthusiasm with 22% ORR as a single agent, but is primarily being developed for germline Breast Cancer 1/2 early onset (BRCA1/2) mutant patients; and Medivation's enzalutamide targets androgen receptor positive (AR+) TNBC but has reported a lower 8% ORR (see Exhibit 4 for more details). Celldex is currently running the Ph. III METRIC study, Merck plans to initiate a Ph. II in 2015, enzalutamide's Ph. I/II data will continue to mature during 2015, and Roche plans to pursue a Ph. III program in 1st-Line TNBC in combination with nab-paclitaxel.
Valuation Range: $7.00 to $7.50
2015 could be a transformative year and we see upside potential from current levels with positive Ph. III epratuzumab data and an IMMU-132 partnership.
• SG's Next steps. (1) Management has guided to End-of-Ph. II FDA/EMA meetings to discuss current data and a Ph. III protocol by early Q2 (we expect an update on this during the Fiscal Q3 2015 earnings call next week). (2) At the 2015 ASCO Meeting there will be a poster in TNBC (Saturday May 30, #1016) and an oral presentation in NSCLC (Tuesday June 2, 9:00-9:12 am CT, #2504). (3) Announcement of a licensing agreement during Q2 or Q3. (4) The prospective partner is to commence the Ph. III study in relapsed/refractory TNBC by the end of 2015 (a key “must have” for IMMU as part of a licensing agreement based on recent IMMU management comments). We assume a Q2 licensing deal is announced ahead of the EMBODY data with a $65 million upfront payment, up to $190 million in clinical/regulatory milestones related to TNBC, and a 20% flat global royalty. At this time we only model TNBC revenues (at 50% probability of success) with US and European Union launches in 2022. If a Ph. III TNBC program is initiated by the end of 2015 (instead of a randomized Ph. II study followed by a subsequent Ph. III), this could accelerate development timelines by roughly two years, and may offer upside to our current estimates.
• 2015 AACR Update on ORR and safety… steady as she goes. As with previous updates during 2014 at multiple medical meetings (with fewer assessable patients and shorter duration of dosing and response), efficacy and safety data reported at the 2015 AACR Meeting are generally consistent for the overall patient population (n=162 assessable for efficacy and n=123 for safety). ORR and DCR were 17% and 64% with broad clinical activity as PRs have been observed in 6 tumor types to date. ORR and DCR for updates in November 2014 and February 2015 were 18%/62% and 19%/67%, respectively. Please refer to Exhibit 1 for more details. Safety remains unremarkable, in our view, as Grade 3/4 neutropenia was 24%, febrile neutropenia was 4%, and diarrhea was 3%. Please refer to Exhibit 3 for more details. These rates – while in different tumors types and fewer patients – are numerically lower than those observed with irinotecan (per the Camptosar label).
• Data suggest SG may have a broader market opportunity (in 2nd-Line+ TNBC) than other mid/late stage TNBC competitors. Based on data to date, it appears SG is potentially effective in all unselected TNBC patients (as the ADC targets tumors that over-express human trophoblast cell surface antigen ) whereas Keytruda (PD-L1+ high-expressers), MPDL3280A (PD-L1+ expressers), enzalutamide (AR+ high expressers), and glembatumumab vedotin (GPNMB high expressers) can only target sub-populations (based on biomarkers) and appear more effective in TNBC that over-express the specific proteins. The proportion of patients that express these various proteins varies from roughly 33% to 70%. Please refer to Exhibit 5 for more details. Clearly this is an important consideration for partnering discussions as it potentially would enable treatment of all the roughly 35,000+ U.S. and 56,000+ European Union TNBC patients (in all lines) with SG compared to somewhat narrower market opportunities for the other drugs/antibodies.
• While early and with a smaller “N”, SG’s NSCLC data are encouraging and suggest SG is on the right track and not that dissimilar from Merck’s Keytruda and Bristol’s Opdivo in 2nd/3rd-Line NSCLC. Behind TNBC we believe NSCLC offers a 2nd tumor type that could be attractive to potential licensing suitors due to the large market opportunity and unmet medical need, albeit with significantly more competition than TNBC. At the AACR Meeting IMMU reported 32% ORR (with 6 PR’s), 32% DCR, and 59% CBR (SD/PR/CR for 4+ months), respectively, in NSCLC patients who failed a median of 3 prior therapies. Overall Survival (OS) data are too immature to assess but PFS for the 18 patients dosed at 8 or 10mg/kg, was 5.4 months. By comparison, at the 2012 ASCO Meeting, Bristol-Myers’ reported 28% ORR for Opdivo 3mg/kg (the go-forward Ph. III monotherapy dose in NSCLC) in 18 patients in the Ph. I(b) -003 Study. SG compares similarly well to Merck’s Keytruda as last week’s NEJM online paper indicates that ORR was 44% in high expressers of PD-L1 with a median PFS of 6.1 months. While we don’t want to over-interpret early data compared to two broad Ph. III programs for Merck and Bristol-Myers, these initial results suggest SG is a highly active ADC. Ultimately duration of response, maturing PFS, and initial OS (potentially at the 2015 ASCO or European Society for Medical Oncology Scientific Sessions) will help determine what role SG could play in this tumor type.
Most promising activity appears to be in TNBC, NSCLC, and SCLC. During 2014 IMMU provided periodic updates on the Ph. I/II study (ASCO, World Antibody Drug Conjugate Summit, and San Antonio Breast Cancer Symposium [SABCS]). The update at last week’s AACR Meeting was numerically similar for ORR for all assessable patients and by specific tumor type. Patients had very advanced disease at baseline with an average of 2.5 to 4 prior therapies (depending on tumor type) and some with 11 priors (in the TNBC population). As noted in the prior exhibit, TNBC, NSCLC, and SCLC ORR and CBR rates were 26%/74%, 32%/74%, and 30%/55%, respectively. Roughly 50% of TNBC patients were able to achieve stable disease or better for at least six months (as represented by CBR >6), suggesting a good tolerability profile combined with meaningful clinical benefit. Interestingly one TNBC patient has had their prior PR convert to a CR, potentially suggesting a deepening of response may occur the longer a patient can stay on therapy. This phenomenon has been broadly observed with many novel oral therapies for blood cancers (e.g., Revlimid, Imbruvica, Zydelig). Maturing PFS data were provided for TNBC (3.7 months at 8mg/kg and 6.0 months at 10mg/kg), for NSCLC (5.4 months), SCLC (2.4 months), esophageal (4.1 months), and colorectal (3.9 months). OS data are too immature for TNBC, NSCLC, and SCLC, while a median has not been reached for esophageal.
Minimal severe/life-threatening adverse events have been observed to date. As of the 2015 AACR Meeting, fatigue (5% Grade 3), diarrhea (3% Grade 3), alopecia (18 % overall, 0% Grade 3/4), and vomiting (2% Grade 3) were the most common non-hematologic adverse events. Neutropenia (18% Grade 3, and 6% Grade 4) was the most common hematologic AE, as would be expected due to SG’s similarity to irinotecan, and febrile neutropenia was limited (2% Grade 3 and 2% Grade 4). In patients where neutropenia was observed, the SG dose was reduced or delayed and/or the physician administered growth factor support, when appropriate. SG’s AE profile has generally been consistent in terms of numerical rates compared with updates at the 2014 ASCO Meeting, World ADC Summit in October, and SABCS in December. Importantly, to date no antibodies against SG or SN-38 have been detected and dose reductions at the 8 (n=76) and 10mg/kg (n=33) groups have been limited with a total of 17 patients requiring a dose reduction (~15-16% of patients in both dosing arms).
Comparison to irinotecan suggests much lower toxicities, which may allow for a more tolerable regimen, ability to dose longer, and lead to improved outcomes. While it is challenging to compare single-arm Ph. I/II results for SG to Ph. III data for irinotecan (in a different indication), results to date suggest SG has a more tolerable profile, based on rates of key AEs. As noted in Exhibit 3 above, irinotecan has Grade 3/ 4 rates of neutropenia, diarrhea, and febrile neutropenia of 31%, 38%, and 8% compared to SG’s 24%, 3% and 4%, respectively.
Broader market opportunity than other mid/late stage programs? As noted in Exhibit 5, SG is likely to have a broader market opportunity compared to other programs in development for TNBC since SG does not target selected sub-populations based on a biomarker. Merck’s Keytruda and Roche’s MPDL3280A may only be applicable in PD-L1+ TNBC patients, but what proportion of patients are truly PD-L1+ may be driven by both companies’ immunohistochemistry assays and their respective definitions. In addition, it is currently unclear based on data to date for both programs, if they will target high expressers or all PD-L1+ TNBC. In NSCLC, we note low expressers of PD-L1 have poorer outcomes with Keytruda than those identified as high expressers. Thus Merck may opt to target high expressers in its upcoming Ph. II study. Roche has already announced plans to move into a Ph. III combination study with nab-paclitaxel in 1st-Line TNBC, and may forego 2nd-Line+ patients. The Ph. III EMBRACA study for talazoparib is targeting locally advanced and/or metastatic breast cancer with germline BRCA1/2 mutations. Research suggests roughly 25% of TNBC patients have the BRCA1 mutation. Thus, talazoparib may only be approved for use in this subset of TNBC (or not at all depending on how large a proportion of the Ph. III study is TNBC). For Medivation’s enzalutamide, a key question is what proportion of TNBC are truly androgen receptor positive and high expressers, as well. We identified an abstract presented at the 2014 SABCS which suggested roughly 1/3 of TNBC are AR+. Medivation believes up to 80% of TNBC express some level of AR+ while 55% express high levels. Finally, Celldex is targeting high GPNMB expressers, which the company believes could represent upwards of roughly 35% of TNBC.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.790.496 von ipollit am 16.05.15 16:57:05Hallo ipollit,
die Daten bei IMMU-132 sehen gut aus. Mit Partner wäre mir auch am liebsten, IMMU hat ja trotz Finanzierungsrunde nicht wirklich viel an Cash-Bestand.
Ich bin jetzt auch bei Fibrogen eingestiegen, auch auf Grund deines Beitrags. Jedoch etwas oberhalb des Schlusskurses vom Freitag . Hätte nicht gedacht, dass ein auslaufen der Haltefristen zu einem so starken Abverkauf führt.
. Hätte nicht gedacht, dass ein auslaufen der Haltefristen zu einem so starken Abverkauf führt.
Ich überlege mir gerade bei Cerenis einzusteigen.
CER002 wird auch in NASH getestet.
CER001 sehe ich allerdings kritisch, die Ergebnisse Anfang 2014 waren nicht gerade überzeugend.
http://www.cerenis.com/pipeline.asp
die Daten bei IMMU-132 sehen gut aus. Mit Partner wäre mir auch am liebsten, IMMU hat ja trotz Finanzierungsrunde nicht wirklich viel an Cash-Bestand.
Ich bin jetzt auch bei Fibrogen eingestiegen, auch auf Grund deines Beitrags. Jedoch etwas oberhalb des Schlusskurses vom Freitag
 . Hätte nicht gedacht, dass ein auslaufen der Haltefristen zu einem so starken Abverkauf führt.
. Hätte nicht gedacht, dass ein auslaufen der Haltefristen zu einem so starken Abverkauf führt. Ich überlege mir gerade bei Cerenis einzusteigen.
CER002 wird auch in NASH getestet.
CER001 sehe ich allerdings kritisch, die Ergebnisse Anfang 2014 waren nicht gerade überzeugend.
http://www.cerenis.com/pipeline.asp
Antwort auf Beitrag Nr.: 49.781.673 von ipollit am 14.05.15 23:57:33KPTI:
Die Kursverluste sind schon harsch, aber so wie ipollit sehe ich auch keinen wirklichen Grund dafür. Der Markt ist offensichtlich enttäuscht von den schwachen ORR-Daten, die in den ASCO-Abstracts präsentiert worden sind.
Ich schließe mich aber ipollits Meinung an, dass man bei soliden Tumoren eher auf Kombitherapien mit Selinexor setzen muss.
Aber der Markt ist eben stimmungsgetrieben.
Wichtig ist natürlich, dass KPTI einen schnellen Weg zum Markt findet und schnell heißt Monotherapie oder im Fall MM Selinexor + Dex.
Dies ist in den Indikationen AML, DLBCL und Richters ja auch der Fall und auf diesen Indikationen und eben auch auf den MM-Daten muss das Augenmerk liegen.
Leider wird es aber auch in diesen Indikationen noch ca. 12 bis 18 Monate dauern, bis da wesentliche neue Daten vorliegen, die dann aber eventuell bereits zulassungsrelevant sein könnten.
Die Frage der Wirksamkeit als Kombitherapie bei soliden Tumoren muss erst deutlich später gestellt werden und sollte zunächst auch keinen entscheidenden Einfluss auf die Bewertung haben.
Ich sehe keinen Grund, meine positive Meinung zu KPTI zu revidieren.
Die Kursverluste sind schon harsch, aber so wie ipollit sehe ich auch keinen wirklichen Grund dafür. Der Markt ist offensichtlich enttäuscht von den schwachen ORR-Daten, die in den ASCO-Abstracts präsentiert worden sind.
Ich schließe mich aber ipollits Meinung an, dass man bei soliden Tumoren eher auf Kombitherapien mit Selinexor setzen muss.
Aber der Markt ist eben stimmungsgetrieben.
Wichtig ist natürlich, dass KPTI einen schnellen Weg zum Markt findet und schnell heißt Monotherapie oder im Fall MM Selinexor + Dex.
Dies ist in den Indikationen AML, DLBCL und Richters ja auch der Fall und auf diesen Indikationen und eben auch auf den MM-Daten muss das Augenmerk liegen.
Leider wird es aber auch in diesen Indikationen noch ca. 12 bis 18 Monate dauern, bis da wesentliche neue Daten vorliegen, die dann aber eventuell bereits zulassungsrelevant sein könnten.
Die Frage der Wirksamkeit als Kombitherapie bei soliden Tumoren muss erst deutlich später gestellt werden und sollte zunächst auch keinen entscheidenden Einfluss auf die Bewertung haben.
Ich sehe keinen Grund, meine positive Meinung zu KPTI zu revidieren.
PTLA
Bayers Blutverdünner Xarelto scheint sich recht gut zu entwickeln... Es dürfte das umsatzstärkste Produkt von Bayer werden: "Estimated peak annual sales potential for Xarelto has been increased from more than 2 billion euros to 3.5 billion euros"
Xarelto gehört zu einer neuen Klasse von Blutverdünnern z.B. zur Vermeidung von Trombosen nach OPs, die zu Schlaganfällen oder Herzinfakten führen können... die Faktor Xa-Hemmer. Bisher wird in Amerika meistens Warfarin (das auch als Rattengift bekannt ist) eingesetzt, in Europa meines Wissens nach mehr Heparin. Zwar verhindern Blutverdünner Trombosen, doch kann ein zu dünnes Blut wieder zu gefährlichen Blutungen z.b. im Gehirn führen. Die Dosierung von ältere Mitteln ist von vielen Faktoren abhängig... eventuell müssen Patienten genau überwacht werden, damit die Blutverdünnung im gewünschten Bereich bleibt.
Xa-Hemmer sollen einfacher zu dosieren sein, wobei auch bei diesen noch ein Blutungsrisiko besteht. Ein Fortschritt könnte hier vielleicht ISIS Factor XI Antisense ISIS-FXI in PII bringen, das angeblich das Blut ohne erhöhtes Blutungsrisiko verdünnen kann, und bei dem Bayer vor Kurzen mit eingestiegen ist: http://www.fiercebiotech.com/story/bayer-fronting-155m-promi…
Jedenfalls gibt es momentan einen stark wachsenden FXa-Hemmer Markt mit Xarelto, Eliquis, usw... viele große Pharmas sind dabei. Momentan besteht aber das Problem, dass die blutverdünnende Wirkung von FXa-Hemmern nicht aufgehoben werden kann, wenn es zu einer Blutung kommt oder man kurzfristig erneut operieren muss.
PTLA hat nun mit Andexanet Alfa das erste und vielleicht einzige Mittel kurz vor der Zulassung, dass die Wirkung von FXa-Hemmern innerhalb von Minuten über einen beliebig langen Zeitraum aufheben kann, so dass gefährliche Blutungen gestoppt oder OPs mit geringerem Blutungsrisiko durchgeführt werden können. Aus meiner Sicht besteht ein hoher Bedarf (die FDA hat Andexanet den Breakthrough-Status gegeben) und PTLA kooperiert mit allen großen Pharmas wie Bayer, J&J, Pfizer, BMS, Daiichi, die FXa-Hemmer entwickeln. Ich denke, PTLA wird von diesen umfangreich unterstützt werden, da sie so auch ihre Hemmer sicherer machen und besser vermarkten können.
PTLA schätzt das Potential für Andexanet auf über 1+ Mrd USD.
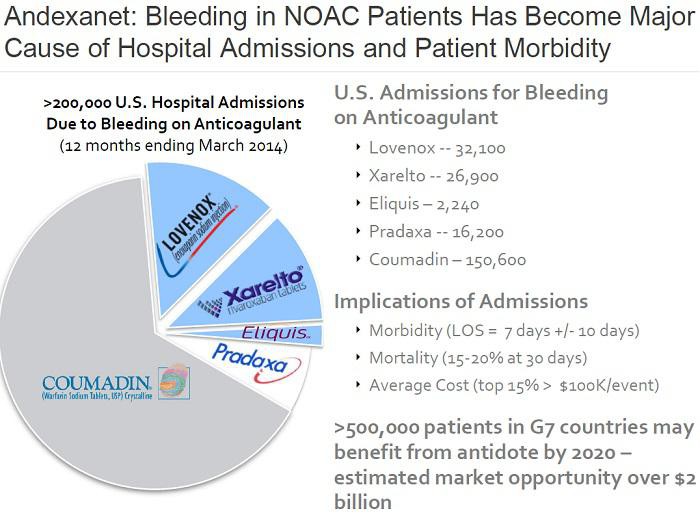

Daneben haben sie auch einen eigenen FXa-Hemmer Betrixaban in der Entwicklung, zu dem Anfang nächstes Jahres die PIII-Daten kommen sollen. Nach meinem Verständnis konkurriert PTLA nicht direkt mit Mitteln wie Xarelto, die z.B. direkt nach einer OP im Krankenhaus gegeben werden. PTLA will stattdessen Betrixaban in der Akut-medizin zum Einsatz bringen, bei der ein erhöhtes Trombose-Risiko besteht wie Herzprobleme, Schlaganfall, Infektionen usw. Laut PTLA bekommen mehr als 1 Mio von 22 Mio Patienten Trombosen, woran 150.000 Menschen sterben.

Bisher werden diese Patienten z.B. in den USA im Krankenhaus mit Heparin behandelt... ein FXa-Hemmer ist bisher für diese Anwendung nicht zugelassen. Heparin muss allerdings gespritzt werden (Betrixaban ist eine Tablette), ist auch als Generika teurer als Betrixaban und wird zuhause nicht mehr genommen.
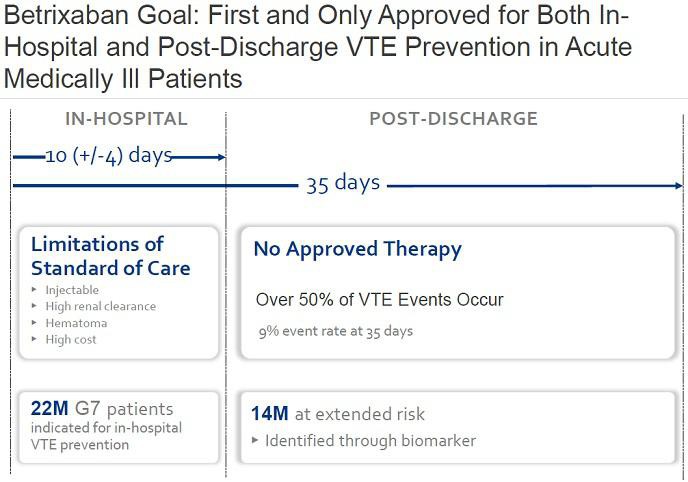
Betrixaban wird daher in der PIII gegen Heparin getestet.
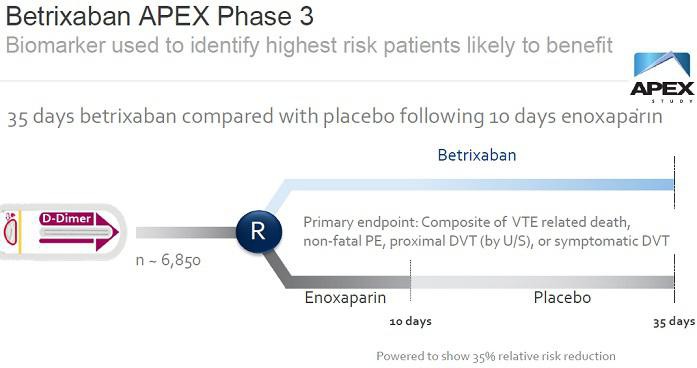
Betrixaban soll hierfür besser geeignet sein, da es geringere Schwankungen aufweisen soll (wird nur langsam abgebaut, unabhänger von einer besseren oder schlechteren Niere, keine Wechselwirkungen mit Lebensmitteln oder anderen Medikamenten).
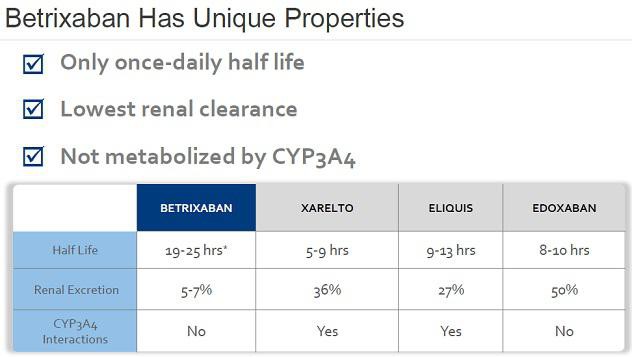
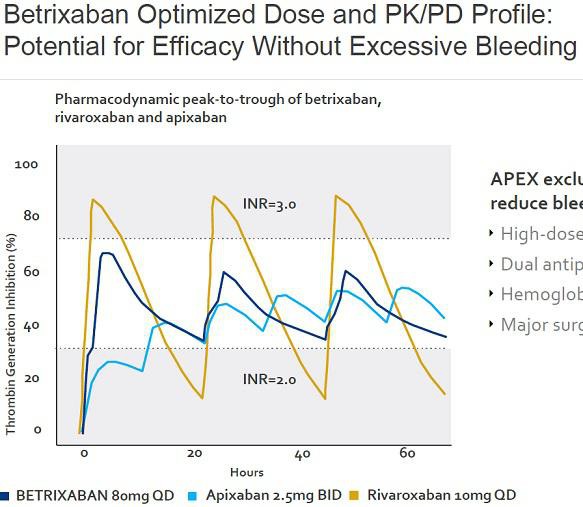
Dieses Mittel könnte ebenfalls Blockbuster-Potential haben.
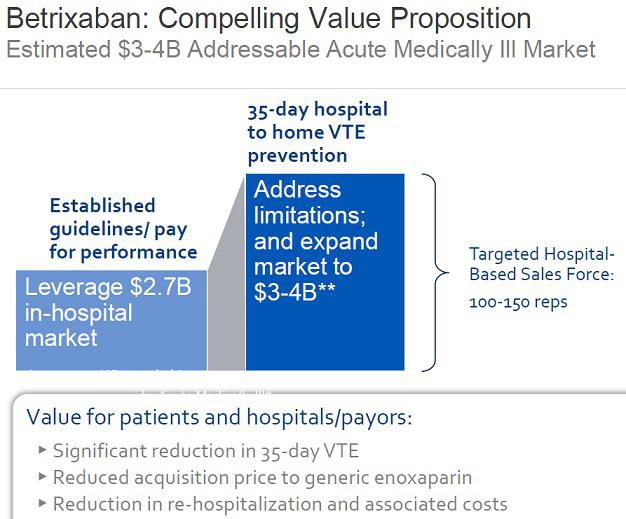
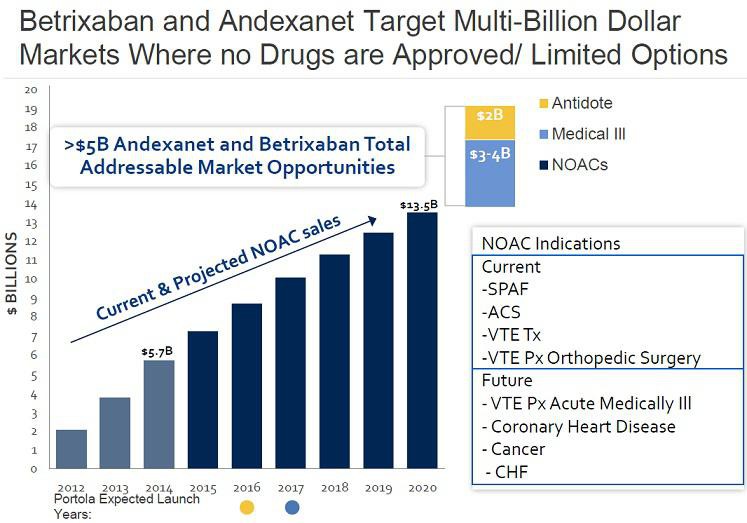

Da beide Mittel in nicht allzuferner Zukunft zugelassen werden könnten und zumindest Andexanet konkurrenzlos ist und hierfür hoher Bearf besteht, sehe ich die aktuelle MK von 1,94 Mrd USD noch als moderat an und habe mit eine Position zugelegt.

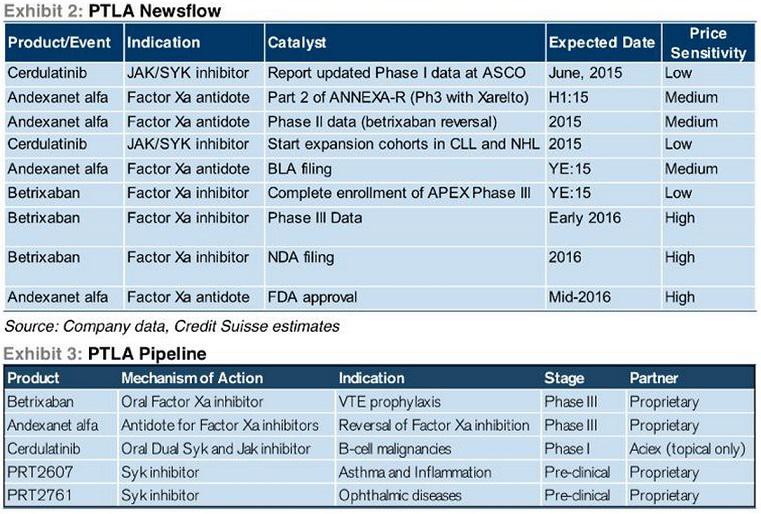

Gruß
ipollit
Bayers Blutverdünner Xarelto scheint sich recht gut zu entwickeln... Es dürfte das umsatzstärkste Produkt von Bayer werden: "Estimated peak annual sales potential for Xarelto has been increased from more than 2 billion euros to 3.5 billion euros"
Xarelto gehört zu einer neuen Klasse von Blutverdünnern z.B. zur Vermeidung von Trombosen nach OPs, die zu Schlaganfällen oder Herzinfakten führen können... die Faktor Xa-Hemmer. Bisher wird in Amerika meistens Warfarin (das auch als Rattengift bekannt ist) eingesetzt, in Europa meines Wissens nach mehr Heparin. Zwar verhindern Blutverdünner Trombosen, doch kann ein zu dünnes Blut wieder zu gefährlichen Blutungen z.b. im Gehirn führen. Die Dosierung von ältere Mitteln ist von vielen Faktoren abhängig... eventuell müssen Patienten genau überwacht werden, damit die Blutverdünnung im gewünschten Bereich bleibt.
Xa-Hemmer sollen einfacher zu dosieren sein, wobei auch bei diesen noch ein Blutungsrisiko besteht. Ein Fortschritt könnte hier vielleicht ISIS Factor XI Antisense ISIS-FXI in PII bringen, das angeblich das Blut ohne erhöhtes Blutungsrisiko verdünnen kann, und bei dem Bayer vor Kurzen mit eingestiegen ist: http://www.fiercebiotech.com/story/bayer-fronting-155m-promi…
Jedenfalls gibt es momentan einen stark wachsenden FXa-Hemmer Markt mit Xarelto, Eliquis, usw... viele große Pharmas sind dabei. Momentan besteht aber das Problem, dass die blutverdünnende Wirkung von FXa-Hemmern nicht aufgehoben werden kann, wenn es zu einer Blutung kommt oder man kurzfristig erneut operieren muss.
PTLA hat nun mit Andexanet Alfa das erste und vielleicht einzige Mittel kurz vor der Zulassung, dass die Wirkung von FXa-Hemmern innerhalb von Minuten über einen beliebig langen Zeitraum aufheben kann, so dass gefährliche Blutungen gestoppt oder OPs mit geringerem Blutungsrisiko durchgeführt werden können. Aus meiner Sicht besteht ein hoher Bedarf (die FDA hat Andexanet den Breakthrough-Status gegeben) und PTLA kooperiert mit allen großen Pharmas wie Bayer, J&J, Pfizer, BMS, Daiichi, die FXa-Hemmer entwickeln. Ich denke, PTLA wird von diesen umfangreich unterstützt werden, da sie so auch ihre Hemmer sicherer machen und besser vermarkten können.
PTLA schätzt das Potential für Andexanet auf über 1+ Mrd USD.


Daneben haben sie auch einen eigenen FXa-Hemmer Betrixaban in der Entwicklung, zu dem Anfang nächstes Jahres die PIII-Daten kommen sollen. Nach meinem Verständnis konkurriert PTLA nicht direkt mit Mitteln wie Xarelto, die z.B. direkt nach einer OP im Krankenhaus gegeben werden. PTLA will stattdessen Betrixaban in der Akut-medizin zum Einsatz bringen, bei der ein erhöhtes Trombose-Risiko besteht wie Herzprobleme, Schlaganfall, Infektionen usw. Laut PTLA bekommen mehr als 1 Mio von 22 Mio Patienten Trombosen, woran 150.000 Menschen sterben.

Bisher werden diese Patienten z.B. in den USA im Krankenhaus mit Heparin behandelt... ein FXa-Hemmer ist bisher für diese Anwendung nicht zugelassen. Heparin muss allerdings gespritzt werden (Betrixaban ist eine Tablette), ist auch als Generika teurer als Betrixaban und wird zuhause nicht mehr genommen.

Betrixaban wird daher in der PIII gegen Heparin getestet.

Betrixaban soll hierfür besser geeignet sein, da es geringere Schwankungen aufweisen soll (wird nur langsam abgebaut, unabhänger von einer besseren oder schlechteren Niere, keine Wechselwirkungen mit Lebensmitteln oder anderen Medikamenten).


Dieses Mittel könnte ebenfalls Blockbuster-Potential haben.



Da beide Mittel in nicht allzuferner Zukunft zugelassen werden könnten und zumindest Andexanet konkurrenzlos ist und hierfür hoher Bearf besteht, sehe ich die aktuelle MK von 1,94 Mrd USD noch als moderat an und habe mit eine Position zugelegt.


Gruß
ipollit
Antwort auf Beitrag Nr.: 49.793.391 von ipollit am 17.05.15 17:21:54Hallo ipollit,
schön, dass Du dieses Thema aufgreifst. Ich erinnere mich noch, dass ich mich - als die PD1-Story mit Nivolumab gerade ins Rollen kam - für BMS begeistert habe. Eben wegen Nivolumab aber auch wegen Eliquis. Es gibt irgendwo einen alten Thread von mir dazu...
Jedenfalls habe ich keine Zweifel am Marktpotential der FXa-Hemmer. Die Antidote-Problematik lag natürlich damals schon auf dem Tisch und dass die Lösung wohl über Portola kommen würde war auch schon ziemlich klar. Wenn ich mich recht erinnere, war Portola damals noch nicht börsennotiert.
Ich hab damals das langfristige Marktpotential der FXa-Hemmer bei deutlich mehr als 10 Milliarden Dollar gesehen und allein Eliquis bei so um die 5 Mrd. oder so (hab vermutlich Eliquis überschätzt und die Konkurrenz unterschätzt).
Na ja, lange Rede, wenig Sinn... der Punkt ist der, dass ich - so großzügig ich mir den FXa-Markt auch vorstelle früher nicht im entferntesten vorstellen konnte, dass der Antidote ebenfalls ein Blockbuster werden soll?!
Ehrlich gesagt fällt mir diese Vorstellung auch jetzt etwas schwer. Aber wenn man die Masse an künftig möglichen Fällen bedenkt und ein hohen, aber nicht unrealistischen Preis unterstellt, dann haut das vielleicht tatsächlich hin.
Am grundsätzlichen BEDARF habe ich nicht den geringsten Zweifel. Am Umsatzpotential schon eher, aber da kann ich meine Zweifel nicht gut begründen muss ich zugeben...
Gruß
SLG
schön, dass Du dieses Thema aufgreifst. Ich erinnere mich noch, dass ich mich - als die PD1-Story mit Nivolumab gerade ins Rollen kam - für BMS begeistert habe. Eben wegen Nivolumab aber auch wegen Eliquis. Es gibt irgendwo einen alten Thread von mir dazu...
Jedenfalls habe ich keine Zweifel am Marktpotential der FXa-Hemmer. Die Antidote-Problematik lag natürlich damals schon auf dem Tisch und dass die Lösung wohl über Portola kommen würde war auch schon ziemlich klar. Wenn ich mich recht erinnere, war Portola damals noch nicht börsennotiert.
Ich hab damals das langfristige Marktpotential der FXa-Hemmer bei deutlich mehr als 10 Milliarden Dollar gesehen und allein Eliquis bei so um die 5 Mrd. oder so (hab vermutlich Eliquis überschätzt und die Konkurrenz unterschätzt).
Na ja, lange Rede, wenig Sinn... der Punkt ist der, dass ich - so großzügig ich mir den FXa-Markt auch vorstelle früher nicht im entferntesten vorstellen konnte, dass der Antidote ebenfalls ein Blockbuster werden soll?!
Ehrlich gesagt fällt mir diese Vorstellung auch jetzt etwas schwer. Aber wenn man die Masse an künftig möglichen Fällen bedenkt und ein hohen, aber nicht unrealistischen Preis unterstellt, dann haut das vielleicht tatsächlich hin.
Am grundsätzlichen BEDARF habe ich nicht den geringsten Zweifel. Am Umsatzpotential schon eher, aber da kann ich meine Zweifel nicht gut begründen muss ich zugeben...
Gruß
SLG
Antwort auf Beitrag Nr.: 49.793.697 von SLGramann am 17.05.15 18:51:56Konkurrenz?
Es scheint von Boehringer einen konkurrierenden Antidote speziell für Pradaxa zu geben:
http://www.fiercebiotech.com/story/boehringer-takes-pole-pos…
Das müsste man mal näher beleuchten. Warum behauptet Portola, es gäbe keine Konkurrenz?
Es scheint von Boehringer einen konkurrierenden Antidote speziell für Pradaxa zu geben:
http://www.fiercebiotech.com/story/boehringer-takes-pole-pos…
Das müsste man mal näher beleuchten. Warum behauptet Portola, es gäbe keine Konkurrenz?
Antwort auf Beitrag Nr.: 49.793.697 von SLGramann am 17.05.15 18:51:56Hallo SLG...
"dass der Antidote ebenfalls ein Blockbuster werden soll"
Das hängt davon ab, welche Zahlen man ansetzt. Laut PTLA-Präsentation gab es 2013 in den USA über 200.000 Blutungen infolge von Blutverdünnern. Die meisten (150.600) gehen dabei auf Warfarin... etwas über 60.000 auf die FXa-Hemmer Xarelto und Eliquis sowie Heparin (Heparin, also kein FXa-Hemmer). Pradaxa ist dagegen ein direkter Thrombin-Hemmer... da wirkt anscheinend Andexanet gar nicht? Andexanet kann bei allen FXa-Hemmern und Heparin angewendet werden, soweit ich das verstehe: "The company also conducted a study on the drug’s effect on enoxaparin (ended 2Q2014). It was found to rapidly reduce the effect of enoxaparin, showing full reversal within 2 minutes and sustaining the effect for two hours, which is consistent with Xarelto and Eliquis results. This is significant because it shows that Andexanet Alfa can effectively mitigate the effect of both types (direct and indirect) and all major brands of anticoagulation medication withing two minutes of administration."
PTLA setzt 2020 weltweit (G7-Staaten... USA, Japan, 5 EU-Staaten) 23 bis 36 Mio Patienten an, die mit FXa-Hemmern behandelt werden. Das Blutungsrisiko sehen sie bei 1-4% sowie 1% Not-OPs... das wären zwischen 460.000 und 1,8 Mio, die ein Antidote benötigen.
"A Phase III study conducted by BMS and Pfizer showed that between 1% and 4% of people taking Factor Xa Inhibitors on a chronic basis experience a major bleed. The acute medically ill population taking Factor Xa Inhibitors is likely to have a comparable risk of bleeding. The average cost of treating a direct, uncontrolled bleed can be between about $15,000 and $50,000, with a massively uncontrolled bleed costing between $50,000 and 4100,000."
***
"Millions of patients at risk for blood clots are currently being treated with a new class of novel oral anticoagulants, known as Factor Xa inhibitors. While Factor Xa inhibitors represent a significant improvement in safety and efficacy over the the previous standard of care (warfarin and low molecular weight heparins), they are still associated with a potentially life-threatening side effect: severe bleeding, including in the brain and gastrointestinal tract. Each year, between 1 and 4 percent of patients treated with Factor Xa inhibitors may experience major bleeding and an additional 1 percent of patients may need to reverse the activity of their anticoagulant because they require emergency surgery. We estimate that by the year 2020, with the increase in adoption of these novel anticoagulants along with the use of injectable Factor Xa inhibitors, more than 500,000 patients in the United States, Spain, Japan, France, Italy, Germany, and the United Kingdom may benefit from an antidote."
PTLA hat in der Präsenation >500.000 angesetzt. Wenn es 2013 in den USA 60.000 sind, sind es weltweit vielleicht doppelt so viele oder mehr. Bei mehr als einer Verdreifachung des FXa-Marktes von 2013 bis 2020 sind 500.000 weltweit im Jahre 2020 ja nicht so unplausibel, zumal ja noch die Not-OPs hinzukommen.
Zum Vergleich gibt es in einer PTLA-Präsentation Zahlen zu Warfarin in den USA... 4+ Mio Patienten, 200.000+ Vitamin K Dosen (Warfarin-Reversal) und 130.000 Plasma-Dosen... das sind mehr als 8% im Verhältnis von behandelten Patienten zur Mitteln, die die Wirkung von Warfarin aufheben. 500.000 zu 23+ Mio Patienten sind nur 2%.
Bei 500.000+ Patienten sieht PTLA Umsätze von über 2 Mrd USD... grob gerechnet sind das 4000 USD pro Patient, wenn man 100% Marktanteil ansetzt.
Eine konkrete Zahl für die Kosten einer Andexanet-Behandlung kenne ich nicht... billig wird diese aber bestimmt nicht sein. Hier steht z.B. http://www.fiercebiotech.com/story/portola-says-its-ready-fi…
"Bernstein's Geoffrey Porges has counted himself among the analysts confident that Portola is on the right track with the Phase III program. He's far less happy with some manufacturing snafus that appear to be setting the stage for limited supplies postapproval. In a recent note to investors he related that manufacturing problems will likely drive up costs to $20,000 per "bleed"--at least initially."
Im unrealistischen Extremfall könnte man also auch rechnen... (4%+1%) von 36 Mio Patienten x 100% Martkanteil x 20.000 USD... das wären 36 Mrd USD ww Umsatz! Naja, 1+ Mrd USD könnten es aber schon sein.
Naja, 1+ Mrd USD könnten es aber schon sein.
Grüße
ipollit
"dass der Antidote ebenfalls ein Blockbuster werden soll"
Das hängt davon ab, welche Zahlen man ansetzt. Laut PTLA-Präsentation gab es 2013 in den USA über 200.000 Blutungen infolge von Blutverdünnern. Die meisten (150.600) gehen dabei auf Warfarin... etwas über 60.000 auf die FXa-Hemmer Xarelto und Eliquis sowie Heparin (Heparin, also kein FXa-Hemmer). Pradaxa ist dagegen ein direkter Thrombin-Hemmer... da wirkt anscheinend Andexanet gar nicht? Andexanet kann bei allen FXa-Hemmern und Heparin angewendet werden, soweit ich das verstehe: "The company also conducted a study on the drug’s effect on enoxaparin (ended 2Q2014). It was found to rapidly reduce the effect of enoxaparin, showing full reversal within 2 minutes and sustaining the effect for two hours, which is consistent with Xarelto and Eliquis results. This is significant because it shows that Andexanet Alfa can effectively mitigate the effect of both types (direct and indirect) and all major brands of anticoagulation medication withing two minutes of administration."
PTLA setzt 2020 weltweit (G7-Staaten... USA, Japan, 5 EU-Staaten) 23 bis 36 Mio Patienten an, die mit FXa-Hemmern behandelt werden. Das Blutungsrisiko sehen sie bei 1-4% sowie 1% Not-OPs... das wären zwischen 460.000 und 1,8 Mio, die ein Antidote benötigen.
"A Phase III study conducted by BMS and Pfizer showed that between 1% and 4% of people taking Factor Xa Inhibitors on a chronic basis experience a major bleed. The acute medically ill population taking Factor Xa Inhibitors is likely to have a comparable risk of bleeding. The average cost of treating a direct, uncontrolled bleed can be between about $15,000 and $50,000, with a massively uncontrolled bleed costing between $50,000 and 4100,000."
***
"Millions of patients at risk for blood clots are currently being treated with a new class of novel oral anticoagulants, known as Factor Xa inhibitors. While Factor Xa inhibitors represent a significant improvement in safety and efficacy over the the previous standard of care (warfarin and low molecular weight heparins), they are still associated with a potentially life-threatening side effect: severe bleeding, including in the brain and gastrointestinal tract. Each year, between 1 and 4 percent of patients treated with Factor Xa inhibitors may experience major bleeding and an additional 1 percent of patients may need to reverse the activity of their anticoagulant because they require emergency surgery. We estimate that by the year 2020, with the increase in adoption of these novel anticoagulants along with the use of injectable Factor Xa inhibitors, more than 500,000 patients in the United States, Spain, Japan, France, Italy, Germany, and the United Kingdom may benefit from an antidote."
PTLA hat in der Präsenation >500.000 angesetzt. Wenn es 2013 in den USA 60.000 sind, sind es weltweit vielleicht doppelt so viele oder mehr. Bei mehr als einer Verdreifachung des FXa-Marktes von 2013 bis 2020 sind 500.000 weltweit im Jahre 2020 ja nicht so unplausibel, zumal ja noch die Not-OPs hinzukommen.
Zum Vergleich gibt es in einer PTLA-Präsentation Zahlen zu Warfarin in den USA... 4+ Mio Patienten, 200.000+ Vitamin K Dosen (Warfarin-Reversal) und 130.000 Plasma-Dosen... das sind mehr als 8% im Verhältnis von behandelten Patienten zur Mitteln, die die Wirkung von Warfarin aufheben. 500.000 zu 23+ Mio Patienten sind nur 2%.
Bei 500.000+ Patienten sieht PTLA Umsätze von über 2 Mrd USD... grob gerechnet sind das 4000 USD pro Patient, wenn man 100% Marktanteil ansetzt.
Eine konkrete Zahl für die Kosten einer Andexanet-Behandlung kenne ich nicht... billig wird diese aber bestimmt nicht sein. Hier steht z.B. http://www.fiercebiotech.com/story/portola-says-its-ready-fi…
"Bernstein's Geoffrey Porges has counted himself among the analysts confident that Portola is on the right track with the Phase III program. He's far less happy with some manufacturing snafus that appear to be setting the stage for limited supplies postapproval. In a recent note to investors he related that manufacturing problems will likely drive up costs to $20,000 per "bleed"--at least initially."
Im unrealistischen Extremfall könnte man also auch rechnen... (4%+1%) von 36 Mio Patienten x 100% Martkanteil x 20.000 USD... das wären 36 Mrd USD ww Umsatz!
 Naja, 1+ Mrd USD könnten es aber schon sein.
Naja, 1+ Mrd USD könnten es aber schon sein.Grüße
ipollit
RCPT:

Interessante Einschätzung des künftigen IBD-Marktes... kann man ja mal gelesen haben, ohne das gleich 1:1 zu kaufen.
Heiß ist das alles auf jeden Fall!

Interessante Einschätzung des künftigen IBD-Marktes... kann man ja mal gelesen haben, ohne das gleich 1:1 zu kaufen.
Heiß ist das alles auf jeden Fall!
EBIO
huii... das war wohl nix! Naja, war bei mir zum Glück nur eine kleine Risiko-Position.
"Eleven Biotherapeutics Announces Top-Line Results from Pivotal Phase 3 Study of EBI-005 in Patients with Moderate to Severe Dry Eye Disease
- Study Did Not Achieve Primary Endpoints; No Statistical Difference between EBI-005 and Vehicle Control
- EBI-005 Program to Focus on Allergic Conjunctivitis with Pivotal Phase 3 Study to Initiate in Second Half of 2015"
--> -70%
Da die Allergie-Indikation bereits einmal fehlgeschlagen ist, sollte man das Programm meiner Meinung nach mit Null ansetzen. So sehe ich momentan keinen Sinn, investiert zu sein.

Gruß
ipollit
huii... das war wohl nix! Naja, war bei mir zum Glück nur eine kleine Risiko-Position.
"Eleven Biotherapeutics Announces Top-Line Results from Pivotal Phase 3 Study of EBI-005 in Patients with Moderate to Severe Dry Eye Disease
- Study Did Not Achieve Primary Endpoints; No Statistical Difference between EBI-005 and Vehicle Control
- EBI-005 Program to Focus on Allergic Conjunctivitis with Pivotal Phase 3 Study to Initiate in Second Half of 2015"
--> -70%

Da die Allergie-Indikation bereits einmal fehlgeschlagen ist, sollte man das Programm meiner Meinung nach mit Null ansetzen. So sehe ich momentan keinen Sinn, investiert zu sein.
Gruß
ipollit
BLUE:
Der regulatorische Pfad zur Zulassung ist nun grunsätzlich klar:
http://investor.bluebirdbio.com/phoenix.zhtml?c=251820&p=iro…

Der regulatorische Pfad zur Zulassung ist nun grunsätzlich klar:
http://investor.bluebirdbio.com/phoenix.zhtml?c=251820&p=iro…

Antwort auf Beitrag Nr.: 49.805.943 von SLGramann am 19.05.15 14:39:00BLUE
weitere Analysteneinschätzungen:
BofA zur Timeline:

Piper mit der Meinung, dass auch der Beta thalassemia-Markt finanziell bedeutsam ist (das scheint ja nicht so Konsens zu sein, hatte ich zuletzt den Eindruck):

weitere Analysteneinschätzungen:
BofA zur Timeline:

Piper mit der Meinung, dass auch der Beta thalassemia-Markt finanziell bedeutsam ist (das scheint ja nicht so Konsens zu sein, hatte ich zuletzt den Eindruck):

ICPT:
Intercept Pharmaceuticals Announces Pivotal Phase 3 Clinical Trial of Obeticholic Acid in NASH
http://ir.interceptpharma.com/releasedetail.cfm?ReleaseID=91…
Intercept hat jetzt die PIII-Planung in NASH finalisiert.
Der Trial wird sehr groß und wird relativ viel Zeit benötigen, was aber eigentlich klar war.
Der Markt reagiert darauf jetzt erst mal mit einem Einbruch von den zuletzt erreichten Höhen.

Letztendlich ist aber eigentlich alles in bester Ordnung, finde ich.

Intercept Pharmaceuticals Announces Pivotal Phase 3 Clinical Trial of Obeticholic Acid in NASH
http://ir.interceptpharma.com/releasedetail.cfm?ReleaseID=91…
Intercept hat jetzt die PIII-Planung in NASH finalisiert.
Der Trial wird sehr groß und wird relativ viel Zeit benötigen, was aber eigentlich klar war.
Der Markt reagiert darauf jetzt erst mal mit einem Einbruch von den zuletzt erreichten Höhen.
Letztendlich ist aber eigentlich alles in bester Ordnung, finde ich.

BLUE:
Heute gab es ein sehr positives abstract der anstehenden EHA. Es macht den Anschein, als könnte man auch in der Indikation SCD (sickle cell disease) einen Durchbruch erzielen:
http://investor.bluebirdbio.com/phoenix.zhtml?c=251820&p=iro…
http://www.fiercebiotech.com/story/bluebird-offers-promising…
Ich finde den derzeitigen Kurs gerechtfertigt und bei weiter positiven Daten ist noch sehr viel Potential nach oben.
Es handelt sich um Milliarden-Märkte, die hier adressiert werden und zwar mit einem Verfahren, dass eine quasi-Heilung möglich machen könnte.



Heute gab es ein sehr positives abstract der anstehenden EHA. Es macht den Anschein, als könnte man auch in der Indikation SCD (sickle cell disease) einen Durchbruch erzielen:
http://investor.bluebirdbio.com/phoenix.zhtml?c=251820&p=iro…
http://www.fiercebiotech.com/story/bluebird-offers-promising…
Ich finde den derzeitigen Kurs gerechtfertigt und bei weiter positiven Daten ist noch sehr viel Potential nach oben.
Es handelt sich um Milliarden-Märkte, die hier adressiert werden und zwar mit einem Verfahren, dass eine quasi-Heilung möglich machen könnte.


Antwort auf Beitrag Nr.: 49.825.875 von SLGramann am 21.05.15 16:48:18Ich finde den derzeitigen Kurs gerechtfertigt und bei weiter positiven Daten ist noch sehr viel Potential nach oben.
Es handelt sich um Milliarden-Märkte, die hier adressiert werden und zwar mit einem Verfahren, dass eine quasi-Heilung möglich machen könnte.
Mir gefällt Bluebird von allen "spektakulären" Werten am besten. Leider habe ich meine Position zu früh verkauft, auch weil ich das Risiko heute nicht eingehen wollte. Überlege aber wieder einzusteigen. Was mir zudem gefällt ist, dass BLUE in mehreren zukunftsträchtigen Bereichen tätig ist, und natürlich eben auch schon gute Ergebnisse geliefert hat.

Es handelt sich um Milliarden-Märkte, die hier adressiert werden und zwar mit einem Verfahren, dass eine quasi-Heilung möglich machen könnte.
Mir gefällt Bluebird von allen "spektakulären" Werten am besten. Leider habe ich meine Position zu früh verkauft, auch weil ich das Risiko heute nicht eingehen wollte. Überlege aber wieder einzusteigen. Was mir zudem gefällt ist, dass BLUE in mehreren zukunftsträchtigen Bereichen tätig ist, und natürlich eben auch schon gute Ergebnisse geliefert hat.

Antwort auf Beitrag Nr.: 49.827.315 von kmastra am 21.05.15 19:44:50"Mir gefällt Bluebird von allen "spektakulären" Werten am besten. Leider habe ich meine Position zu früh verkauft,"
Geht mir ähnlich. Ich hatte meine ohnehin nicht so sehr große Position im März halbiert, so dass ich trotz des gewaltigen Kursanstiegs nicht darüber nachdenken muss, ob die Gewichtung zu groß wird.
Eine ähnliche Entwicklung - allerdings von einem bereits höheren Startniveau aus - könnten theoretisch AAVL nehmen.
Auch dort geht es um einen Multi-Milliarden-Markt, den man ziemlich durcheinander wirbeln könnte.
Hammer hat in seinem letzten Beitrag dazu ja alles wichtige geschrieben. Auch die weiteren Kommentare sind sehr interessant gewesen.
Wir werden es in den nächsten Wochen erfahren. Meine AAVL-Position beläuft sich zur Zeit aber wiederum auf lediglich ca. 2% des Depotvolumens. Das Risiko ist eben auch enorm. Man muss immer sehen, dass im Fall des Scheiterns 80 bis 90% des investierten Kapitals verloren sind.
Geht mir ähnlich. Ich hatte meine ohnehin nicht so sehr große Position im März halbiert, so dass ich trotz des gewaltigen Kursanstiegs nicht darüber nachdenken muss, ob die Gewichtung zu groß wird.
Eine ähnliche Entwicklung - allerdings von einem bereits höheren Startniveau aus - könnten theoretisch AAVL nehmen.
Auch dort geht es um einen Multi-Milliarden-Markt, den man ziemlich durcheinander wirbeln könnte.
Hammer hat in seinem letzten Beitrag dazu ja alles wichtige geschrieben. Auch die weiteren Kommentare sind sehr interessant gewesen.
Wir werden es in den nächsten Wochen erfahren. Meine AAVL-Position beläuft sich zur Zeit aber wiederum auf lediglich ca. 2% des Depotvolumens. Das Risiko ist eben auch enorm. Man muss immer sehen, dass im Fall des Scheiterns 80 bis 90% des investierten Kapitals verloren sind.
Hallo,
ich habe mir heute eine Startposition XENE gekauft. Mir war der Wert bis vor kurzem noch völlig unbekannt, ist aber in Ohad Hammers Blog erwähnt worden.
Für mich ist das eine Position aus der Kategorie "under the radar". Die Marktkapitalisierung beträgt 175 Mio US$, wobei noch fast 75 Mio an Cash da sind.
Xenon hat eine erstaunlich breite (verpartnerte) Pipeline, wenngleich vieles noch sehr früh ist.
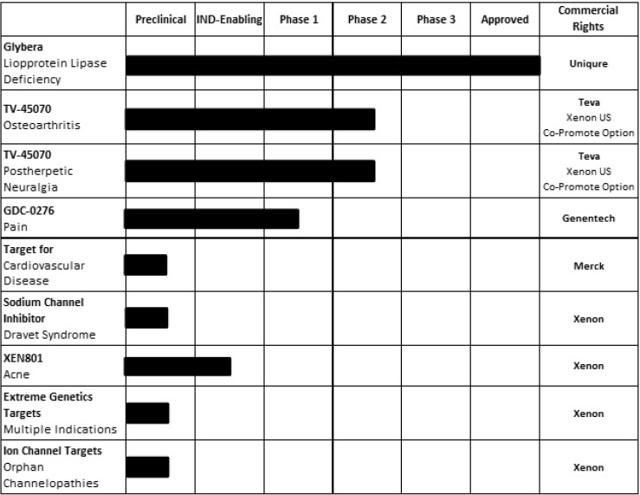
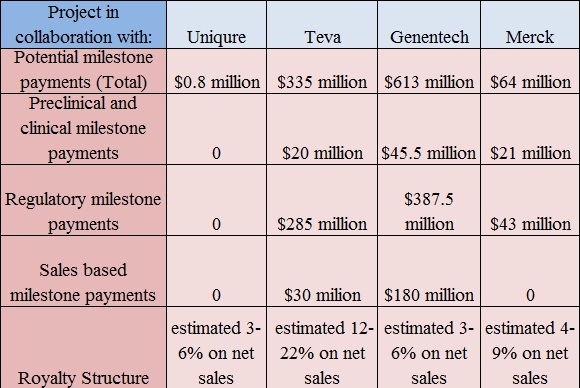
Quelle Seekingalpha - von daher mit Vorsicht zu genießen.
Besonders die Kooperation mit Genentech scheint Potenzial zu haben. Ohad sieht hier wohl das Größte Potenzial und findet vor allem das target gut. Genentech hat sogar ein hübsches Video dazu gemacht:
Xenon verfügt über eine eigene Plattform, die "extreme genetics" heißt. Wenn ich es richtig verstehe, werden Familien, die bestimmte Symptome/Fähigkeiten haben auf Genveränderungen untersucht, um daraus dann Targets zu finden. Das finde ich einen spannenden Ansatz, obwohl ich mir nicht so ganz vorstellen kann, wie das geht. Zudem ist das Finden neuer Targets ja ein ziemlich heißer und wichtiger Bereich, so dass durchaus noch weitere Impulse/Partnerschaften darasu entsehen könnten.
Bei Xene ist wie bei FGEN die Lockup Periode (Anfang Mai) ausgelaufen, so dass scheinbar zusätzlicher Verkaufsdruck aufkam. Im Bereich von 12$ könnte sich ein Boden bilden.

Dieses Jahr steht noch einiges an:
Key 2015 Anticipated Milestones in Xenon's Partnered Programs
Xenon's partner Teva Pharmaceutical Industries Ltd. (NYSE:TEVA) is currently conducting a double-blind, placebo-controlled Phase 2b clinical trial for TV-45070 in osteoarthritis in which 300 patients will be randomized. Data from the trial is expected in the third quarter of 2015. Teva also plans to initiate a Phase 2b clinical trial for TV-45070 in postherpetic neuralgia in the first half of 2015. TV-45070 is a topically applied small-molecule inhibitor of the sodium channel Nav1.7 and other sodium channels, including those that are expressed in the pain-sensing peripheral nervous system.
Xenon's partner Genentech, a member of the Roche Group (SIX:RO) (SIX:ROG) (OTCQX:RHHBY), is currently conducting a Phase 1 clinical trial for GDC-0276, which is expected to be completed by mid-2015. GDC-0276 is a selective, oral Nav1.7 small-molecule inhibitor being developed for the treatment of pain.
Xenon and Genentech formed a second collaboration in 2014 focused on pain genetics and rare phenotypes where individuals have an inability to perceive pain or where individuals have non-precipitated spontaneous severe pain. A key goal of this collaboration is to identify new pain targets for drug discovery in 2015.
Based on guidance from its licensee uniQure Biopharma B.V. (Nasdaq:QURE), Xenon expects that Glybera® will be launched in Europe in the first quarter of 2015. Glybera is the first gene therapy product approved in the European Union for the treatment of the orphan disorder lipoprotein lipase deficiency, and is the first product whose active ingredient was derived from Xenon's platform to receive commercial approval. Glybera is being commercialized by uniQure's partner, Chiesi Farmaceutici S.p.A. and Xenon is eligible to receive a royalty on commercial sales.
Key 2015 Anticipated Milestones in Xenon's Proprietary Programs
Xenon's Extreme Genetics discovery platform has enabled development of a broad pipeline, including one approved product, two clinical-stage product candidates and additional preclinical programs. A key corporate goal for 2015 is continued development of the company's lead proprietary product candidates.
XEN801, is a stearoyl Co-A desaturase or SCD1 inhibitor, for the treatment of acne. Xenon expects to file an investigational new drug, or IND, or IND equivalent application to initiate a Phase 1 clinical trial in the first half of 2015. If supported by positive data from the Phase 1 trial, Xenon plans to initiate a proof-of-concept Phase 2 clinical trial in the second half of 2015. It is estimated that in the United States there are approximately 11 million people with moderate acne and 1.2 million people with severe acne. SCD1 is an enzyme involved in lipid synthesis that is expressed in sebaceous glands in the skin. By inhibiting SCD1, XEN801 represents a novel approach to treat acne with a dual mechanism of action expected to reduce both sebum production and the size and number of sebaceous glands.
Xenon's development of a Nav1.6 sodium channel inhibitor for the treatment of the orphan disorder Dravet Syndrome continues to progress and Xenon expects to file an IND application in 2016. Dravet Syndrome is an orphan disease of severe childhood epilepsy, and represents a high unmet medical need, affecting 7,500-15,000 patients in the U.S. Xenon's approach to treating Dravet Syndrome is to develop selective and potent inhibitors of Nav1.6 which have demonstrated efficacy for seizures in a preclinical animal model.
Xenon also anticipates selecting its next target in 2015 by leveraging its Extreme Genetics discovery platform and expertise in ion channel chemistry and biology.
Hat sich jemand mal eingehender mit Xene beschäftigt?
Grundsätzlich versuche ich ja die Indikation Schmerz zu vermeiden....aber hier vielleicht ja doch "no pain no gain"?
SG kmastra
ich habe mir heute eine Startposition XENE gekauft. Mir war der Wert bis vor kurzem noch völlig unbekannt, ist aber in Ohad Hammers Blog erwähnt worden.
Für mich ist das eine Position aus der Kategorie "under the radar". Die Marktkapitalisierung beträgt 175 Mio US$, wobei noch fast 75 Mio an Cash da sind.
Xenon hat eine erstaunlich breite (verpartnerte) Pipeline, wenngleich vieles noch sehr früh ist.


Quelle Seekingalpha - von daher mit Vorsicht zu genießen.
Besonders die Kooperation mit Genentech scheint Potenzial zu haben. Ohad sieht hier wohl das Größte Potenzial und findet vor allem das target gut. Genentech hat sogar ein hübsches Video dazu gemacht:
Xenon verfügt über eine eigene Plattform, die "extreme genetics" heißt. Wenn ich es richtig verstehe, werden Familien, die bestimmte Symptome/Fähigkeiten haben auf Genveränderungen untersucht, um daraus dann Targets zu finden. Das finde ich einen spannenden Ansatz, obwohl ich mir nicht so ganz vorstellen kann, wie das geht. Zudem ist das Finden neuer Targets ja ein ziemlich heißer und wichtiger Bereich, so dass durchaus noch weitere Impulse/Partnerschaften darasu entsehen könnten.
Bei Xene ist wie bei FGEN die Lockup Periode (Anfang Mai) ausgelaufen, so dass scheinbar zusätzlicher Verkaufsdruck aufkam. Im Bereich von 12$ könnte sich ein Boden bilden.
Dieses Jahr steht noch einiges an:
Key 2015 Anticipated Milestones in Xenon's Partnered Programs
Xenon's partner Teva Pharmaceutical Industries Ltd. (NYSE:TEVA) is currently conducting a double-blind, placebo-controlled Phase 2b clinical trial for TV-45070 in osteoarthritis in which 300 patients will be randomized. Data from the trial is expected in the third quarter of 2015. Teva also plans to initiate a Phase 2b clinical trial for TV-45070 in postherpetic neuralgia in the first half of 2015. TV-45070 is a topically applied small-molecule inhibitor of the sodium channel Nav1.7 and other sodium channels, including those that are expressed in the pain-sensing peripheral nervous system.
Xenon's partner Genentech, a member of the Roche Group (SIX:RO) (SIX:ROG) (OTCQX:RHHBY), is currently conducting a Phase 1 clinical trial for GDC-0276, which is expected to be completed by mid-2015. GDC-0276 is a selective, oral Nav1.7 small-molecule inhibitor being developed for the treatment of pain.
Xenon and Genentech formed a second collaboration in 2014 focused on pain genetics and rare phenotypes where individuals have an inability to perceive pain or where individuals have non-precipitated spontaneous severe pain. A key goal of this collaboration is to identify new pain targets for drug discovery in 2015.
Based on guidance from its licensee uniQure Biopharma B.V. (Nasdaq:QURE), Xenon expects that Glybera® will be launched in Europe in the first quarter of 2015. Glybera is the first gene therapy product approved in the European Union for the treatment of the orphan disorder lipoprotein lipase deficiency, and is the first product whose active ingredient was derived from Xenon's platform to receive commercial approval. Glybera is being commercialized by uniQure's partner, Chiesi Farmaceutici S.p.A. and Xenon is eligible to receive a royalty on commercial sales.
Key 2015 Anticipated Milestones in Xenon's Proprietary Programs
Xenon's Extreme Genetics discovery platform has enabled development of a broad pipeline, including one approved product, two clinical-stage product candidates and additional preclinical programs. A key corporate goal for 2015 is continued development of the company's lead proprietary product candidates.
XEN801, is a stearoyl Co-A desaturase or SCD1 inhibitor, for the treatment of acne. Xenon expects to file an investigational new drug, or IND, or IND equivalent application to initiate a Phase 1 clinical trial in the first half of 2015. If supported by positive data from the Phase 1 trial, Xenon plans to initiate a proof-of-concept Phase 2 clinical trial in the second half of 2015. It is estimated that in the United States there are approximately 11 million people with moderate acne and 1.2 million people with severe acne. SCD1 is an enzyme involved in lipid synthesis that is expressed in sebaceous glands in the skin. By inhibiting SCD1, XEN801 represents a novel approach to treat acne with a dual mechanism of action expected to reduce both sebum production and the size and number of sebaceous glands.
Xenon's development of a Nav1.6 sodium channel inhibitor for the treatment of the orphan disorder Dravet Syndrome continues to progress and Xenon expects to file an IND application in 2016. Dravet Syndrome is an orphan disease of severe childhood epilepsy, and represents a high unmet medical need, affecting 7,500-15,000 patients in the U.S. Xenon's approach to treating Dravet Syndrome is to develop selective and potent inhibitors of Nav1.6 which have demonstrated efficacy for seizures in a preclinical animal model.
Xenon also anticipates selecting its next target in 2015 by leveraging its Extreme Genetics discovery platform and expertise in ion channel chemistry and biology.
Hat sich jemand mal eingehender mit Xene beschäftigt?
Grundsätzlich versuche ich ja die Indikation Schmerz zu vermeiden....aber hier vielleicht ja doch "no pain no gain"?
SG kmastra
Antwort auf Beitrag Nr.: 49.860.295 von kmastra am 27.05.15 20:54:52Hallo kmastra
Es ist schon witzig, bei mir war es genau der gleiche Ablauf - hatte vor paar Wochen erstmals die Erwähnung in Ohad's Blog gelesen und etwas recherchiert, fand es dann aber fast irgendwie zu "mühsam/langweilig" nur copy&paste von Ohad's Blog zu übernehmen (nicht vom Inhalt, da ja noch nicht viel dort dazu geschrieben wurde - sondern rein von der Idee, da ich davon ausgehe, dass wahrscheinlich alle hier ebenfalls Ohad's Blog lesen). Bin dir für deinen Effort nun aber umso dankbarer.
Das Video fand ich auch echt "hübsch" gemacht ;-)
Es ist wirklich schade, dass es - diesen Thread hier ausgenommen - so wenig hochwertige deutschsprachige Infos im Biotechbereich gibt.
Habe noch keine Position bei XENE, habe aber vor dies bald zu ändern. AUPH finde ich ebenfalls sehr spannend, aber auch noch keine Position.
AAVL habe ich mir dafür mal eine Position aufgebaut, nachdem ich mich intensiver damit beschäftigt habe und eine interessante Konversation in Ohad's Blog führen konnte.
Es ist schon witzig, bei mir war es genau der gleiche Ablauf - hatte vor paar Wochen erstmals die Erwähnung in Ohad's Blog gelesen und etwas recherchiert, fand es dann aber fast irgendwie zu "mühsam/langweilig" nur copy&paste von Ohad's Blog zu übernehmen (nicht vom Inhalt, da ja noch nicht viel dort dazu geschrieben wurde - sondern rein von der Idee, da ich davon ausgehe, dass wahrscheinlich alle hier ebenfalls Ohad's Blog lesen). Bin dir für deinen Effort nun aber umso dankbarer.
Das Video fand ich auch echt "hübsch" gemacht ;-)
Es ist wirklich schade, dass es - diesen Thread hier ausgenommen - so wenig hochwertige deutschsprachige Infos im Biotechbereich gibt.
Habe noch keine Position bei XENE, habe aber vor dies bald zu ändern. AUPH finde ich ebenfalls sehr spannend, aber auch noch keine Position.
AAVL habe ich mir dafür mal eine Position aufgebaut, nachdem ich mich intensiver damit beschäftigt habe und eine interessante Konversation in Ohad's Blog führen konnte.
Antwort auf Beitrag Nr.: 49.860.445 von SpanishEyes am 27.05.15 21:10:28Hallo Spanisheyes,
ja Ohad Hammers Blog, dieser Thread sowie die Meinung einiger Twitter User (und am Ende auch meine bescheidene Meinung/ob ich das nachvollziehen kann) sind für mich die Grundlage im Grunde aller Investitionsentscheidungen. Ich bin wirklich sehr dankbar dafür! Neulich war mal wieder eine Titelgeschichte im Aktionär zum Thema Biotech und über einen Freund konnte ich mal reinschauen. Da musste ich wirklich schmunzeln, weil das Niveau so niedrig war, dass ich damit im Grunde gar nichts anfangen konnte. Es gibt bei w:o sicherlich wenig qualitative Treads aber schon noch ein paar mehr. Warum allerdings gerade die schlechtesten Aktien oft am meisten Beachtung finden ist mir ein Rätsel?!
Mir persönlich gefallen neben qulitativ hochwertigen Werten mit 1a Produkten (ESPR, CLVS, BLUE, ...) auch Werte, die aus irgendeinem Grund noch unentdeckt sind und deshalb ein angemessenes Chance-Risiko Verhältnis haben. Manchmal braucht man da zwar etwas Geduld aber langfristig habe ich da gute Erfahrungen mit gemacht. So habe ich gerade die Hälfte meiner ONTY Position verkauft. Und habe bereits/werde das Geld in andere Werte aus der Kategorie "unterm Radar" investieren. Neben XENE habe ich diesbezüglich insbesondere MRNS(aufstocken), AUPH, LOXO und auch ARNI auf der Liste.
Zu MRNS hat Ohad Hammer ja neulich einen Beitrag geschrieben.
Unterschätzt er dabei vielleicht sogar das Potenzial bei PCDH19 FEMALE PEDIATRIC EPILEPSY? So wie ich es verstehe gibt es hier ein großen Bedarf und auch eine vorhandene Chance auf einen Erfolg. Zudem ist das der nächste Event. Ein positives Signal dürfte am Markt gut ankommen. Finanziell dürfte der Markt doch auch lukrativ sein, da es als Orphan-Indication sehr teuer zu vermarkten wäre?
Es scheint zumindest in einem Fall gute Effekte zu haben.
https://www.pcdh19info.org/
http://philadelphia.cbslocal.com/2015/03/26/health-purple-da…
SG kmastra
ja Ohad Hammers Blog, dieser Thread sowie die Meinung einiger Twitter User (und am Ende auch meine bescheidene Meinung/ob ich das nachvollziehen kann) sind für mich die Grundlage im Grunde aller Investitionsentscheidungen. Ich bin wirklich sehr dankbar dafür! Neulich war mal wieder eine Titelgeschichte im Aktionär zum Thema Biotech und über einen Freund konnte ich mal reinschauen. Da musste ich wirklich schmunzeln, weil das Niveau so niedrig war, dass ich damit im Grunde gar nichts anfangen konnte. Es gibt bei w:o sicherlich wenig qualitative Treads aber schon noch ein paar mehr. Warum allerdings gerade die schlechtesten Aktien oft am meisten Beachtung finden ist mir ein Rätsel?!
Mir persönlich gefallen neben qulitativ hochwertigen Werten mit 1a Produkten (ESPR, CLVS, BLUE, ...) auch Werte, die aus irgendeinem Grund noch unentdeckt sind und deshalb ein angemessenes Chance-Risiko Verhältnis haben. Manchmal braucht man da zwar etwas Geduld aber langfristig habe ich da gute Erfahrungen mit gemacht. So habe ich gerade die Hälfte meiner ONTY Position verkauft. Und habe bereits/werde das Geld in andere Werte aus der Kategorie "unterm Radar" investieren. Neben XENE habe ich diesbezüglich insbesondere MRNS(aufstocken), AUPH, LOXO und auch ARNI auf der Liste.
Zu MRNS hat Ohad Hammer ja neulich einen Beitrag geschrieben.
Unterschätzt er dabei vielleicht sogar das Potenzial bei PCDH19 FEMALE PEDIATRIC EPILEPSY? So wie ich es verstehe gibt es hier ein großen Bedarf und auch eine vorhandene Chance auf einen Erfolg. Zudem ist das der nächste Event. Ein positives Signal dürfte am Markt gut ankommen. Finanziell dürfte der Markt doch auch lukrativ sein, da es als Orphan-Indication sehr teuer zu vermarkten wäre?
Es scheint zumindest in einem Fall gute Effekte zu haben.
https://www.pcdh19info.org/
http://philadelphia.cbslocal.com/2015/03/26/health-purple-da…
SG kmastra
Antwort auf Beitrag Nr.: 49.868.980 von kmastra am 28.05.15 19:24:29Sehr guter Thread hier!
Bin seit ein paar Wochen in BLUE drin, erscheint mir jetzt aber doch etwas überhitzt. Überlege in ESPR oder CLVS zu investieren, gefallen mir beide charttechnisch sehr gut, CLVS gefällt mir noch etwas besser als ESPR. Welchen Wert würdet ihr empfehlen bzw. gibt es bei den beiden Werten noch was zu wissen? Bin leider in der Materie nicht so tief drin.
Vielen Dank schon mal vorab für die Info.
Bin seit ein paar Wochen in BLUE drin, erscheint mir jetzt aber doch etwas überhitzt. Überlege in ESPR oder CLVS zu investieren, gefallen mir beide charttechnisch sehr gut, CLVS gefällt mir noch etwas besser als ESPR. Welchen Wert würdet ihr empfehlen bzw. gibt es bei den beiden Werten noch was zu wissen? Bin leider in der Materie nicht so tief drin.
Vielen Dank schon mal vorab für die Info.
Antwort auf Beitrag Nr.: 49.860.295 von kmastra am 27.05.15 20:54:52"ist aber in Ohad Hammers Blog erwähnt worden."
Hallo kmastra,
ja, das war mir auch aufgefallen.
Es wurden zuletzt einige Werte als interessant besprochen, auch ohne, dass das zu einer unmittelbaren Depotaufnahme geführt hat (ich denke, dass Hammer bei Bewertungsfragen sehr (zu?) streng ist).
Das gilt - wenn ich alles richtig erinnere - für:
- AUPH
- BLCM
- KPTI
- LIFE
- LOXO
- MGNX
- OCAT
- ONCE
- XENE
- ZFGN
Sehr viel. Zu viel. Zunehmende Überforderung...
Zuletzt bin ich über die Anmerkung zu LIFE gestolpert ("Phenomenal science but I prefer to wait for a better entry point.")
Ich habe mir darauf hin ihr S1 mal zu Gemüte geführt und dabei eigentlich nur festgestellt, dass ich mich immer mehr von der Masse an völlig neuen Ansätzen überfordert fühle.
LIFE ist das Kürzel für aTyr Pharma. http://www.atyrpharma.com/
Ich muss ehrlich sagen, dass ich hier zunächst mal nicht mehr mitkommen. ADCs konnte ich konzeptionell noch in meinen Laienverstand transformieren. "Physiocrine" (und manch anderes) nicht mehr wirklich.
Haben wir einen Ansatz, der vielleicht auf lange Sicht das ganze Feld der Autoimmunerkrankungen beeinflussen könnte? Keine Ahnung...
(es gibt hier bei W einen User (Tregs), der damit vielleicht etwas anfangen könnte. Leider schreibt der nicht in diesem Thread.)
einen User (Tregs), der damit vielleicht etwas anfangen könnte. Leider schreibt der nicht in diesem Thread.)
Bei Fierce ist mir folgendes anstehende IPO aufgefallen:
Seres:
http://www.fiercebiotech.com/story/pioneering-microbiome-ups…
Das ist besser zu verstehen (für mich) und ich bin erst mal ziemlich fasziniert.
Aber das ist schon wieder ein komplett neues Feld!
Die Überforderung ist bei mir definitiv da. Man tanzt mit viel Gottvertrauen und sehr wenig Ahnung durch ein Minenfeld... so kommt mir das vor.
Na ja, jetzt erst mal ASCO. Zumindest die anstehenden CLVS-Daten werde ich einordnen können - dazu reichts dann doch noch...
Gruß
SLG
Hallo kmastra,
ja, das war mir auch aufgefallen.
Es wurden zuletzt einige Werte als interessant besprochen, auch ohne, dass das zu einer unmittelbaren Depotaufnahme geführt hat (ich denke, dass Hammer bei Bewertungsfragen sehr (zu?) streng ist).
Das gilt - wenn ich alles richtig erinnere - für:
- AUPH
- BLCM
- KPTI
- LIFE
- LOXO
- MGNX
- OCAT
- ONCE
- XENE
- ZFGN
Sehr viel. Zu viel. Zunehmende Überforderung...
Zuletzt bin ich über die Anmerkung zu LIFE gestolpert ("Phenomenal science but I prefer to wait for a better entry point.")
Ich habe mir darauf hin ihr S1 mal zu Gemüte geführt und dabei eigentlich nur festgestellt, dass ich mich immer mehr von der Masse an völlig neuen Ansätzen überfordert fühle.
LIFE ist das Kürzel für aTyr Pharma. http://www.atyrpharma.com/
Ich muss ehrlich sagen, dass ich hier zunächst mal nicht mehr mitkommen. ADCs konnte ich konzeptionell noch in meinen Laienverstand transformieren. "Physiocrine" (und manch anderes) nicht mehr wirklich.
Haben wir einen Ansatz, der vielleicht auf lange Sicht das ganze Feld der Autoimmunerkrankungen beeinflussen könnte? Keine Ahnung...
(es gibt hier bei W
 einen User (Tregs), der damit vielleicht etwas anfangen könnte. Leider schreibt der nicht in diesem Thread.)
einen User (Tregs), der damit vielleicht etwas anfangen könnte. Leider schreibt der nicht in diesem Thread.)Bei Fierce ist mir folgendes anstehende IPO aufgefallen:
Seres:
http://www.fiercebiotech.com/story/pioneering-microbiome-ups…
Das ist besser zu verstehen (für mich) und ich bin erst mal ziemlich fasziniert.
Aber das ist schon wieder ein komplett neues Feld!
Die Überforderung ist bei mir definitiv da. Man tanzt mit viel Gottvertrauen und sehr wenig Ahnung durch ein Minenfeld... so kommt mir das vor.
Na ja, jetzt erst mal ASCO. Zumindest die anstehenden CLVS-Daten werde ich einordnen können - dazu reichts dann doch noch...

Gruß
SLG
Antwort auf Beitrag Nr.: 49.879.546 von SLGramann am 30.05.15 10:30:57Hallo SLGramann,
"Die Überforderung ist bei mir definitiv da. Man tanzt mit viel Gottvertrauen und sehr wenig Ahnung durch ein Minenfeld... so kommt mir das vor."
Andersherum können selbst die besten Experten auf ihrem Feld nicht sagen, ob letztlich etwas funktionert oder nicht.
Vielleicht ist es daher gar kein Nachteil, sich mit vielen Dingen zu beschäftigen, von denen man nur recht wenig Ahnung hat, statt sich auf etwas zu konzentrieren und jedes Detail zu bewerten. Im ersten Fall erwischt man nach dem Gießkannenprinzip wahrscheinlich eher etwas erfolgreiches, während man im zweiten Fall am Ende so überzeugt von sich ist, dass man in gewisser Weise auch blind wird (die ganze Recherchearbeit und das viele Wissen müssen sich ja rentieren) und verkennt, dass vieles doch zufällig ist.
Allerdings hast du natürlich recht, dass viele Dinge schwer zu verstehen sind und man ohne jedes Verständnis eigentlich auch keine Investment eingehen sollte. Ich denke ein hilfreicher Indikator für eine Investition ist die Meinung möglichst vieler anderer "Experten" in Summe... also von so Leuten wie Ohad Hammer oder anderen auf z.B. Twitter. Zweitens sollte man sehr vorsichtig sein, zuviel auf ein Unternehmen zu setzen, da der Zufall jederzeit zuschlagen kann. Und man sollte unter diesen Experten auch immer Ausschau nach eventuellen Risiken halten. Vielleicht wäre ich bei AERI vorsichtiger gewesen, wenn ich von einem möglichen Drift-Problem bereits vorher gehört hätte.
Letztlich ist vielleicht der Erfolgs-Unterschied zwischen einem eigenen Investment in zig Einzelwerte mit entsprechener Arbeit und einem Fonds oder ähnlichem gar nicht so groß. Viele Werte steigen ja auch deswegen, weil Biotechs angesagt sind und nicht weil spezielle Erfolge in der Pipeline vorhanden sind. Die Beobachtung von Einzelwerten und dem, was dahinter steht macht mir persönlich allerdings mehr Spaß. Mich fazinieren die Fortschritte in der Medizin, bei einem Fonds wüsste ich aber garnicht, was eigentlich dahinter steckt... dafür spart man sich die Arbeit.
***
ASCO-Zeit... mal schauen, wie es mit CLDX und CLVS die nächsten Tage läuft. Nicht selten kommt es ja zum ASCO-Blues, d.h. die Kurse geben nach, egal ob es positive oder negative Nachrichten gibt. Bei beiden Unternehmen besteht ein höheres Risiko zu enttäuschen, da die Erwartungen nach meinem Gefühl in den letzten Monaten deutlich gestiegen sind. Andererseits können sie auch auf einer Erfolgswelle weiter nach oben laufen... wie gesagt vieles ist auch Zufall. Meine Erwartungen bezüglich steigender Kurse sind nach den Erfahrungen der vergangenen Jahre recht niedrig. Allerdings können die Daten sehr wichtig sein und die Kurse mittelfristig bestimmen, egal wie es in den nächsten Tagen läuft.
BMY ist gestern ja schonmal deutlich unter die Räder gekommen aufgrund der Checkmate PD-1 Daten... was wurde da erwartet?

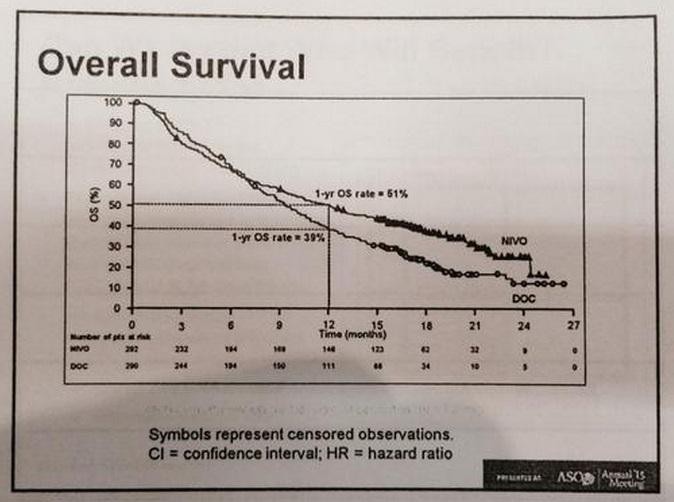
Hat es etwas mit den PD-L1 Daten zutun, dass OS offensichtlich doch von PD-L1 abhängig ist (PD-L1 das Gegenstück zu PD1)?... die Frage war immer, ob PD-L1 ein Biomarker sein kann. Es gibt PD1 AKs und PD-L1 AKs.
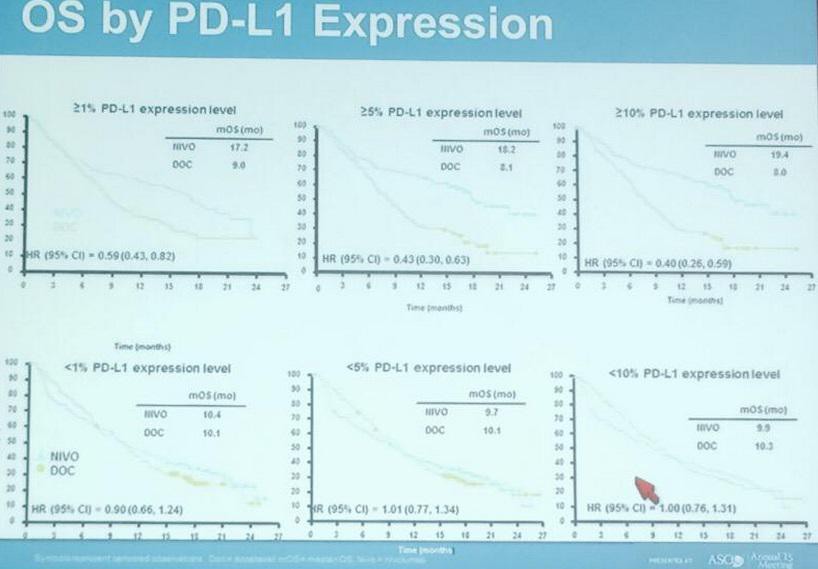
Die Erwartungen an PD1&Co sind zumindest nicht gerade gering... BMY ist vorne dabei. Bei Checkmate geht es um NSCLC als um den grünen Anteil... PD1 vs. Standard-Chemo. Ein weitere Standard in NSCLC sind die EGFR-Hemmer... AZN hat hier vor ein paar Tagen bereits eine PIII PD1 + AZD9291 (CLVS T790M-Konkurrent) gestartet"$AZN opens 9291+MEDI4736 vs 9291 P3 in T790+ NSCLC before 9291 is approved..." https://clinicaltrials.gov/ct2/show/NCT02454933
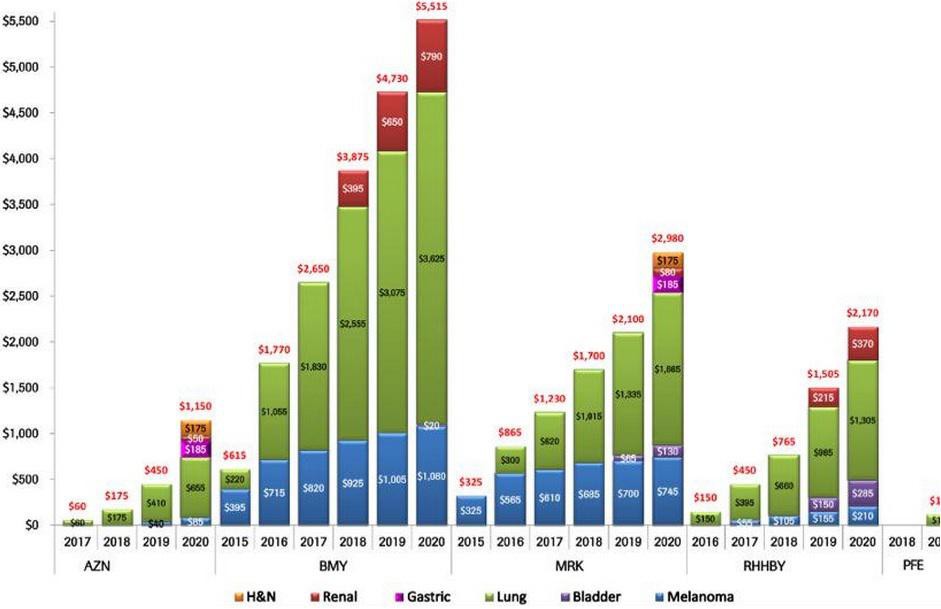
Grüße
ipollit
"Die Überforderung ist bei mir definitiv da. Man tanzt mit viel Gottvertrauen und sehr wenig Ahnung durch ein Minenfeld... so kommt mir das vor."
Andersherum können selbst die besten Experten auf ihrem Feld nicht sagen, ob letztlich etwas funktionert oder nicht.
Vielleicht ist es daher gar kein Nachteil, sich mit vielen Dingen zu beschäftigen, von denen man nur recht wenig Ahnung hat, statt sich auf etwas zu konzentrieren und jedes Detail zu bewerten. Im ersten Fall erwischt man nach dem Gießkannenprinzip wahrscheinlich eher etwas erfolgreiches, während man im zweiten Fall am Ende so überzeugt von sich ist, dass man in gewisser Weise auch blind wird (die ganze Recherchearbeit und das viele Wissen müssen sich ja rentieren) und verkennt, dass vieles doch zufällig ist.
Allerdings hast du natürlich recht, dass viele Dinge schwer zu verstehen sind und man ohne jedes Verständnis eigentlich auch keine Investment eingehen sollte. Ich denke ein hilfreicher Indikator für eine Investition ist die Meinung möglichst vieler anderer "Experten" in Summe... also von so Leuten wie Ohad Hammer oder anderen auf z.B. Twitter. Zweitens sollte man sehr vorsichtig sein, zuviel auf ein Unternehmen zu setzen, da der Zufall jederzeit zuschlagen kann. Und man sollte unter diesen Experten auch immer Ausschau nach eventuellen Risiken halten. Vielleicht wäre ich bei AERI vorsichtiger gewesen, wenn ich von einem möglichen Drift-Problem bereits vorher gehört hätte.
Letztlich ist vielleicht der Erfolgs-Unterschied zwischen einem eigenen Investment in zig Einzelwerte mit entsprechener Arbeit und einem Fonds oder ähnlichem gar nicht so groß. Viele Werte steigen ja auch deswegen, weil Biotechs angesagt sind und nicht weil spezielle Erfolge in der Pipeline vorhanden sind. Die Beobachtung von Einzelwerten und dem, was dahinter steht macht mir persönlich allerdings mehr Spaß. Mich fazinieren die Fortschritte in der Medizin, bei einem Fonds wüsste ich aber garnicht, was eigentlich dahinter steckt... dafür spart man sich die Arbeit.
***
ASCO-Zeit... mal schauen, wie es mit CLDX und CLVS die nächsten Tage läuft. Nicht selten kommt es ja zum ASCO-Blues, d.h. die Kurse geben nach, egal ob es positive oder negative Nachrichten gibt. Bei beiden Unternehmen besteht ein höheres Risiko zu enttäuschen, da die Erwartungen nach meinem Gefühl in den letzten Monaten deutlich gestiegen sind. Andererseits können sie auch auf einer Erfolgswelle weiter nach oben laufen... wie gesagt vieles ist auch Zufall. Meine Erwartungen bezüglich steigender Kurse sind nach den Erfahrungen der vergangenen Jahre recht niedrig. Allerdings können die Daten sehr wichtig sein und die Kurse mittelfristig bestimmen, egal wie es in den nächsten Tagen läuft.
BMY ist gestern ja schonmal deutlich unter die Räder gekommen aufgrund der Checkmate PD-1 Daten... was wurde da erwartet?

Hat es etwas mit den PD-L1 Daten zutun, dass OS offensichtlich doch von PD-L1 abhängig ist (PD-L1 das Gegenstück zu PD1)?... die Frage war immer, ob PD-L1 ein Biomarker sein kann. Es gibt PD1 AKs und PD-L1 AKs.

Die Erwartungen an PD1&Co sind zumindest nicht gerade gering... BMY ist vorne dabei. Bei Checkmate geht es um NSCLC als um den grünen Anteil... PD1 vs. Standard-Chemo. Ein weitere Standard in NSCLC sind die EGFR-Hemmer... AZN hat hier vor ein paar Tagen bereits eine PIII PD1 + AZD9291 (CLVS T790M-Konkurrent) gestartet"$AZN opens 9291+MEDI4736 vs 9291 P3 in T790+ NSCLC before 9291 is approved..." https://clinicaltrials.gov/ct2/show/NCT02454933

Grüße
ipollit
ONTY (ARRY):
Die ASCO-Daten von ONT-380 werden sehr positiv kommentiert:
http://ir.oncothyreon.com/releasedetail.cfm?ReleaseID=915576
Natürlich denken die Leute an Puma mit ihren 6 Milliarden Marketcap...
Die ASCO-Daten von ONT-380 werden sehr positiv kommentiert:
http://ir.oncothyreon.com/releasedetail.cfm?ReleaseID=915576
Natürlich denken die Leute an Puma mit ihren 6 Milliarden Marketcap...
Hallo SLGramann und ipollit,
kurz einige Gedanken zu dem was ihr geschrieben habt. Pünktlich zur ASCO befindet sich der IBB in einer charttechnisch interessanten Konstellation. Charttechnik hin oder her - Zufall ist das wohl eher nicht. Gute (besser als erwartet) fundamentale Entwicklungen könnten für einen Ausbruch sorgen, während der Rückwärtsgang (ASCO-Blues) ein durchaus wahrscheinliches Szenario ist.

Habt ihr gesehen, dass es über Twitter/Periscope sogar erste Videoübertragungen von der ASCO gibt? Unglaublich!
Das ist natürlich schön aber zeigt auch, wie rasant die mediale Entwicklung ist. Im Grunde ja ein gesellschatliches Problem. Man kann sich derart gut informieren, dass es auch zu viel werden kann. In der Biotechnologie wird das noch dadurch potenziert, dass die Entwicklungen immer schneller und mehr werden und es ja auch immer mehr Aktien gibt. Wie soll man da den Überblick behalten? Unmöglich! Wieviele Biotechaktien gab es vor 20 Jahren?
Wie man damit umgeht - da muss wohl jeder seinen Weg finden. Ich persönlich versuche mich zu beschränken, nicht überall dabei sein zu wollen und nehme mir auch mal regelrecht Auszeiten vom www. Aber nicht dieses WE
ONTY/ARRY
Heute wurden die ASCO Poster veröffentlicht. Ich finde das klingt wirklich gut. Hat jemand eine Meinung dazu?
http://finance.yahoo.com/news/oncothyreon-announces-presenta…
Brain mets data looking great even w/ bigger N: 1CR + 4PR + 9SD in ALL 14 evaluable pts
ONT-380 + Xeloda and/or Herceptin combo data also much better than abstract
2CR+12PR+9SD in 27 pts: 52% ORR; 85% DCR
SG kmastra
kurz einige Gedanken zu dem was ihr geschrieben habt. Pünktlich zur ASCO befindet sich der IBB in einer charttechnisch interessanten Konstellation. Charttechnik hin oder her - Zufall ist das wohl eher nicht. Gute (besser als erwartet) fundamentale Entwicklungen könnten für einen Ausbruch sorgen, während der Rückwärtsgang (ASCO-Blues) ein durchaus wahrscheinliches Szenario ist.
Habt ihr gesehen, dass es über Twitter/Periscope sogar erste Videoübertragungen von der ASCO gibt? Unglaublich!
Das ist natürlich schön aber zeigt auch, wie rasant die mediale Entwicklung ist. Im Grunde ja ein gesellschatliches Problem. Man kann sich derart gut informieren, dass es auch zu viel werden kann. In der Biotechnologie wird das noch dadurch potenziert, dass die Entwicklungen immer schneller und mehr werden und es ja auch immer mehr Aktien gibt. Wie soll man da den Überblick behalten? Unmöglich! Wieviele Biotechaktien gab es vor 20 Jahren?
Wie man damit umgeht - da muss wohl jeder seinen Weg finden. Ich persönlich versuche mich zu beschränken, nicht überall dabei sein zu wollen und nehme mir auch mal regelrecht Auszeiten vom www. Aber nicht dieses WE

ONTY/ARRY
Heute wurden die ASCO Poster veröffentlicht. Ich finde das klingt wirklich gut. Hat jemand eine Meinung dazu?
http://finance.yahoo.com/news/oncothyreon-announces-presenta…
Brain mets data looking great even w/ bigger N: 1CR + 4PR + 9SD in ALL 14 evaluable pts
ONT-380 + Xeloda and/or Herceptin combo data also much better than abstract
2CR+12PR+9SD in 27 pts: 52% ORR; 85% DCR
SG kmastra
IMGN:
http://investor.immunogen.com/releasedetail.cfm?ReleaseID=91…
Die Daten von IMGN853 sehen jetzt im Vergleich zum abstract noch mal deutlich besser aus:
Seventeen of the 22 patients were included in the efficacy analysis; the other five patients were still on study and had not yet reached their first assessment.
Nine of these 17 patients had an objective response (8 partial responses, 1 complete response) to treatment, for an ORR of 53%.
The responses in six of these nine patients were ongoing at the time of data cutoff, with five of these six patients on treatment for more than 15 weeks.
Eine ORR von 50% ist sicher am oberen Ende der Erwartungen, die man haben konnte.
Möglicherweise hat IMGN hier wirklich das Asset, das sie für eine signifikante Steigerung des Unternehmenswertes so dringend brauchen?
http://investor.immunogen.com/releasedetail.cfm?ReleaseID=91…
Die Daten von IMGN853 sehen jetzt im Vergleich zum abstract noch mal deutlich besser aus:
Seventeen of the 22 patients were included in the efficacy analysis; the other five patients were still on study and had not yet reached their first assessment.
Nine of these 17 patients had an objective response (8 partial responses, 1 complete response) to treatment, for an ORR of 53%.
The responses in six of these nine patients were ongoing at the time of data cutoff, with five of these six patients on treatment for more than 15 weeks.
Eine ORR von 50% ist sicher am oberen Ende der Erwartungen, die man haben konnte.
Möglicherweise hat IMGN hier wirklich das Asset, das sie für eine signifikante Steigerung des Unternehmenswertes so dringend brauchen?
@arry
Wenñ ich das richtig verstanden habe, dann sollte AstraZeneca mit seinem Medi4736 (PD-L1) in Kombi mit BRAF/MEK-Inhibitoren in einer Phase I in BRAF+ Melanoma (26 Patienten) nach meinem Verständnis tolle Ergebnisse erzielt haben: PR 69%, DCR 100%. Nach 7,1 Monaten Follow-up hatten immer noch 89% der PR eine response (ASCO-Abstract 3003).
Sollte dies nicht die Übernahmephantasie für Array eigentlich weiter anheizen müssen, denn es gibt doch einige sehr große Player mit PD-1 oder PD-L1, die eine zusätzliche BRAF/MEK Kombi nun gut gebrauchen können...
Was meine die Experten dazu?
Wenñ ich das richtig verstanden habe, dann sollte AstraZeneca mit seinem Medi4736 (PD-L1) in Kombi mit BRAF/MEK-Inhibitoren in einer Phase I in BRAF+ Melanoma (26 Patienten) nach meinem Verständnis tolle Ergebnisse erzielt haben: PR 69%, DCR 100%. Nach 7,1 Monaten Follow-up hatten immer noch 89% der PR eine response (ASCO-Abstract 3003).
Sollte dies nicht die Übernahmephantasie für Array eigentlich weiter anheizen müssen, denn es gibt doch einige sehr große Player mit PD-1 oder PD-L1, die eine zusätzliche BRAF/MEK Kombi nun gut gebrauchen können...
Was meine die Experten dazu?
Arry
Die Ergebnisse zu BINI und ENCO sind da:
http://meeting.ascopubs.org/cgi/content/short/33/15_suppl/90…
Klingt doch gut! Allerdings wundert mich die Formulierung "well tolerated".
Die Ergebnisse zu BINI und ENCO sind da:
http://meeting.ascopubs.org/cgi/content/short/33/15_suppl/90…
Klingt doch gut! Allerdings wundert mich die Formulierung "well tolerated".
ASCO 2015
ein paar Analysten-Kommentare...
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
leerink
Immuno-oncology: Our Pre-ASCO Series Takeaways
• Bottom Line: The seventh key opinion leader (KOL) discussion in our Pre-ASCO Series focused on the current state and future prospects of immuno-oncology (IO). The breadth of confirmatory and new data supports broad use of PD1/PD-L1 agents, with emphasis on emerging evidence of activity in DNA mismatch repair (MMR) tumors. PD-L1 biomarkers likely will be important for prioritization, but not patient selection. Among combinations, the KOL believes data at ASCO 2015 are too early to draw conclusions on for chemo/PD1 or PD1/CTLA-4 combos, but questioned the utility of each, viewing ASCO 2016 as the year when novel combinations with broader utility would emerge. Among novel checkpoint targets, LAG3 and IDO were called out while CD137/41BB was highlighted as the leading T-cell agonist. In addition, evidence for cancer vaccines is considered to be strongest currently among approaches other than checkpoint inhibitors, but the evidence for targeting suppressive immune cells is expected to grow significantly over the next 5 years.
• MRK's data in MMR cancer subtypes could apply to 3-5% of all solid tumors. Among new data included in the late breakers on 5/30, MRK's (MP) data in microsatellite instability (MSI; aka mismatch repair) was cited as the most novel and interesting. Initially characterized in colorectal cancer, MMR is now being identified in many cancer types such as gastric, endometrial, and prostate cancer and could represent up to ~5% of all solid malignancies. Interestingly, immuno-histochemistry tests to MMR are available and may help to identify more PD1/PD-L1 responders over time. Due to high PD-L1 staining overlap in MMR tumors, this discovery was viewed as more incremental, but important to building evidence that mutational burden is an important marker for PD1/PD-L1 responders.
• PD-L1 biomarkers useful for prioritization; FDA engaging companies to harmonize test. Two principles are expected to be reiterated as ASCO: (1) Despite a higher probability of responding to PD1/ PD-L1 agents, biomarkers should not be used to exclude pts since PDL1 negative pts also respond; and (2) PD-L1 biomarkers are useful for treatment prioritization. Interestingly, the KOL noted that the agency has engaged the leading PD1/PD-L1 companies with biomarkers in an attempt to harmonize the PD-L1 test.
• Data for PD1/PD-L1 + chemo combos are too early to draw definitive conclusions on. While the first chemo/Opdivo (BMY [OP]) combo study in lung cancer did not demonstrate clear additive or synergistic effect, the KOL believes response rate data for chemo/ PD1 (MRK) or PD-L1 (Roche) are encouraging. However, giving immunotherapy -- which expands T-cells -- simultaneous with a chemo regimen (the "traditional" approach to drug development) that is toxic to proliferating T-cells is likely to be problematic. A more reasonable approach could be sequencing chemo followed by an anti-PD1/PD-L1.
• Checkpoint/checkpoint combos: Toxicity remains a barrier to PD1/ CTLA-4 adoption; LAG3 and IDO highlighted as more interesting with PD1. The KOL expects the big question emerging from BMY's CHECKMATE-067 study on Sunday, May 31, to be the breadth of PD1/ CTLA-4 combo adoption. In the KOL's view, "You are essentially trading an extra 10-20% ORR for 3-4 fold higher frequency of grade 3 or 4 toxicity”. While it is less of a problem in academic centers, it could impact uptake in community practices. AZN's (MP) data on the tremelimumab/ MEDI4736 combo "validated it has activity" but it is still too early to determine if it is differentiated from other combinations. Interestingly, AZN recently listed a new study of the combo in first-line non-small cell lung cancer (NSCLC) called MYSTIC. Among novel checkpoint targets, the KOL highlighted LAG3 and IDO as “very interesting” clinical efforts, while TIM3 and TIGIT were cited as interesting compounds approaching the clinic.
• The finding of the association of neoantigens and response to checkpoint inhibitors highlighted, but how to best utilize these results scientifically and therapeutically remains to be seen. The recent data from Memorial Sloan Kettering Cancer Center (Rizvi et al., Science 2015; Snyder et al., NEJM 2014) demonstrating that the response to Opdivo or Yervoy in melanoma and lung cancer patients, respectively, is associated with the presence of neoantigens, suggest that mutations may be a driver for immune response. These data appear to have generated a lot of interest and were also highlighted by the KOL. However, the KOL does not see mutational density used as a biomarker for therapy, and PDL1 status may already be a reflection of the mutational load. Therapeutically, the KOL noted that he is not in favor of the approach by a start-up company of identifying neoantigens by exome sequencing and preparing peptides as individualized cancer vaccine. He believes that there are a number of technical issues with this approach, which the KOL believes will not be competitive with other approaches.
• Among T-cell agonists, antibodies targeting CD137/4-1BB are viewed as the most interesting and most well-developed based on Rituxan combination data at ASCO. The KOL expressed particular excitement about an abstract at the upcoming ASCO meeting (#3004), which has data from an ongoing Phase I study of PF-05082566 (PFE [MP]) in combination with rituximab in CD20-positive non-Hodgkin's lymphoma (NHL). The abstract reported a response rate of 21% (6/28) and 4 objective responses in 14 rituximab-refractory patients for an objective response rate of 29%, including 2 CRs lasting at least 2 years. We note that the proposed mechanism for CD137 antibody/Rituxan combination has been the stimulatory effect on natural killer (NK) cells through CD137 agonism, which in turn enhances antibody-dependent cellular cytotoxicity mediated by Rituxan. The abstract reported increases in memory T-cells and activated NK cells. Beyond the combination with Rituxan, both PF-05082566 and BMY’s urelumab (both CD137 agonist antibodies) are in combination studies with anti-PD1 antibodies, but no clinical data are available yet. The KOL also saw a number of additional Tcell targets as interesting, highlighting OX40, GITR and CD27, but noted that drugs directed against these targets have only recently entered the clinic or initiated combination studies. It was noted that CDX-1127 (CLDX [OP]) appeared interesting in that it has both direct anti-tumor cell activity and also acts as an immuno-stimulatory agent.
• Antigen-specific T-cell responses will be important to evaluable in early clinical data for cancer vaccines but their correlation with clinical endpoints is unknown. Although the KOL believes that it is important to look at the induction of T-cell responses against the vaccinated antigen in all of these trials, he views these immune analyses as being exploratory. He notes that we cannot be sure that what is measured in peripheral blood by conventional assays will ultimately be predictive of patient benefit. As such, the endpoints for future trials will have to be similar to those for other cancer therapies, namely response rates or, in the case of randomized studies, progression-free survival (PFS) or overall survival (OS).
• Tumor microenvironment (TME) and myeloid derived cell targets highly attractive, but still an under-explored area; CSF1R represents currently the most interesting target. FPRX (OP) and RHHBY have anti-CSF1R antibodies in the clinic (FPA008 and RG7155, respectively). Phase I single-agent data for RG7155 presented at ASCO 2014 has confirmed the mechanism (update at ASCO 2015) and either agent is now being evaluated in combination with PD1/PDL1 inhibitors (Opdivo and MPDL3280A, respectively). FPRX/BMY's trial is expected to initiate in mid-2015 and investigate 6 different tumor types initially. RHHBY's anti-CSF1R anti-PDL1 combination trial launched in 1Q15. Chemokine receptors also represent an interesting emerging area, according to the KOL. CXCR4 block, for example, has enhanced PD1 inhibition in animal models. The challenge ultimately will be to determine the exact effects of various chemokines on various cells in the TME, according to the KOL.
• Evidence for cancer vaccines is considered to be strongest currently, but the evidence supporting targeting Treg and MDSC/TAM is expected to grow significantly over the next 5 years. Benchmarked to the current level of scientific evidence for PD1/PD-L1 agents (score of 10), among novel treatment approaches, the KOL cited cancer vaccines as the most interesting (7 out of 10) near term, followed by T-cell agonists and Tregs (both at 6). Myeloid derived suppressor cells (MDSC) and tumor-associated macrophages (TAM) currently have the lowest evidence level, in his view. However, the KOL predicted that MDSC/TAM and Treg could reach the highest evidence level (at 9) among these therapeutic approaches within the next 5 years.
Gruß
ipollit
ein paar Analysten-Kommentare...
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
leerink
Immuno-oncology: Our Pre-ASCO Series Takeaways
• Bottom Line: The seventh key opinion leader (KOL) discussion in our Pre-ASCO Series focused on the current state and future prospects of immuno-oncology (IO). The breadth of confirmatory and new data supports broad use of PD1/PD-L1 agents, with emphasis on emerging evidence of activity in DNA mismatch repair (MMR) tumors. PD-L1 biomarkers likely will be important for prioritization, but not patient selection. Among combinations, the KOL believes data at ASCO 2015 are too early to draw conclusions on for chemo/PD1 or PD1/CTLA-4 combos, but questioned the utility of each, viewing ASCO 2016 as the year when novel combinations with broader utility would emerge. Among novel checkpoint targets, LAG3 and IDO were called out while CD137/41BB was highlighted as the leading T-cell agonist. In addition, evidence for cancer vaccines is considered to be strongest currently among approaches other than checkpoint inhibitors, but the evidence for targeting suppressive immune cells is expected to grow significantly over the next 5 years.
• MRK's data in MMR cancer subtypes could apply to 3-5% of all solid tumors. Among new data included in the late breakers on 5/30, MRK's (MP) data in microsatellite instability (MSI; aka mismatch repair) was cited as the most novel and interesting. Initially characterized in colorectal cancer, MMR is now being identified in many cancer types such as gastric, endometrial, and prostate cancer and could represent up to ~5% of all solid malignancies. Interestingly, immuno-histochemistry tests to MMR are available and may help to identify more PD1/PD-L1 responders over time. Due to high PD-L1 staining overlap in MMR tumors, this discovery was viewed as more incremental, but important to building evidence that mutational burden is an important marker for PD1/PD-L1 responders.
• PD-L1 biomarkers useful for prioritization; FDA engaging companies to harmonize test. Two principles are expected to be reiterated as ASCO: (1) Despite a higher probability of responding to PD1/ PD-L1 agents, biomarkers should not be used to exclude pts since PDL1 negative pts also respond; and (2) PD-L1 biomarkers are useful for treatment prioritization. Interestingly, the KOL noted that the agency has engaged the leading PD1/PD-L1 companies with biomarkers in an attempt to harmonize the PD-L1 test.
• Data for PD1/PD-L1 + chemo combos are too early to draw definitive conclusions on. While the first chemo/Opdivo (BMY [OP]) combo study in lung cancer did not demonstrate clear additive or synergistic effect, the KOL believes response rate data for chemo/ PD1 (MRK) or PD-L1 (Roche) are encouraging. However, giving immunotherapy -- which expands T-cells -- simultaneous with a chemo regimen (the "traditional" approach to drug development) that is toxic to proliferating T-cells is likely to be problematic. A more reasonable approach could be sequencing chemo followed by an anti-PD1/PD-L1.
• Checkpoint/checkpoint combos: Toxicity remains a barrier to PD1/ CTLA-4 adoption; LAG3 and IDO highlighted as more interesting with PD1. The KOL expects the big question emerging from BMY's CHECKMATE-067 study on Sunday, May 31, to be the breadth of PD1/ CTLA-4 combo adoption. In the KOL's view, "You are essentially trading an extra 10-20% ORR for 3-4 fold higher frequency of grade 3 or 4 toxicity”. While it is less of a problem in academic centers, it could impact uptake in community practices. AZN's (MP) data on the tremelimumab/ MEDI4736 combo "validated it has activity" but it is still too early to determine if it is differentiated from other combinations. Interestingly, AZN recently listed a new study of the combo in first-line non-small cell lung cancer (NSCLC) called MYSTIC. Among novel checkpoint targets, the KOL highlighted LAG3 and IDO as “very interesting” clinical efforts, while TIM3 and TIGIT were cited as interesting compounds approaching the clinic.
• The finding of the association of neoantigens and response to checkpoint inhibitors highlighted, but how to best utilize these results scientifically and therapeutically remains to be seen. The recent data from Memorial Sloan Kettering Cancer Center (Rizvi et al., Science 2015; Snyder et al., NEJM 2014) demonstrating that the response to Opdivo or Yervoy in melanoma and lung cancer patients, respectively, is associated with the presence of neoantigens, suggest that mutations may be a driver for immune response. These data appear to have generated a lot of interest and were also highlighted by the KOL. However, the KOL does not see mutational density used as a biomarker for therapy, and PDL1 status may already be a reflection of the mutational load. Therapeutically, the KOL noted that he is not in favor of the approach by a start-up company of identifying neoantigens by exome sequencing and preparing peptides as individualized cancer vaccine. He believes that there are a number of technical issues with this approach, which the KOL believes will not be competitive with other approaches.
• Among T-cell agonists, antibodies targeting CD137/4-1BB are viewed as the most interesting and most well-developed based on Rituxan combination data at ASCO. The KOL expressed particular excitement about an abstract at the upcoming ASCO meeting (#3004), which has data from an ongoing Phase I study of PF-05082566 (PFE [MP]) in combination with rituximab in CD20-positive non-Hodgkin's lymphoma (NHL). The abstract reported a response rate of 21% (6/28) and 4 objective responses in 14 rituximab-refractory patients for an objective response rate of 29%, including 2 CRs lasting at least 2 years. We note that the proposed mechanism for CD137 antibody/Rituxan combination has been the stimulatory effect on natural killer (NK) cells through CD137 agonism, which in turn enhances antibody-dependent cellular cytotoxicity mediated by Rituxan. The abstract reported increases in memory T-cells and activated NK cells. Beyond the combination with Rituxan, both PF-05082566 and BMY’s urelumab (both CD137 agonist antibodies) are in combination studies with anti-PD1 antibodies, but no clinical data are available yet. The KOL also saw a number of additional Tcell targets as interesting, highlighting OX40, GITR and CD27, but noted that drugs directed against these targets have only recently entered the clinic or initiated combination studies. It was noted that CDX-1127 (CLDX [OP]) appeared interesting in that it has both direct anti-tumor cell activity and also acts as an immuno-stimulatory agent.
• Antigen-specific T-cell responses will be important to evaluable in early clinical data for cancer vaccines but their correlation with clinical endpoints is unknown. Although the KOL believes that it is important to look at the induction of T-cell responses against the vaccinated antigen in all of these trials, he views these immune analyses as being exploratory. He notes that we cannot be sure that what is measured in peripheral blood by conventional assays will ultimately be predictive of patient benefit. As such, the endpoints for future trials will have to be similar to those for other cancer therapies, namely response rates or, in the case of randomized studies, progression-free survival (PFS) or overall survival (OS).
• Tumor microenvironment (TME) and myeloid derived cell targets highly attractive, but still an under-explored area; CSF1R represents currently the most interesting target. FPRX (OP) and RHHBY have anti-CSF1R antibodies in the clinic (FPA008 and RG7155, respectively). Phase I single-agent data for RG7155 presented at ASCO 2014 has confirmed the mechanism (update at ASCO 2015) and either agent is now being evaluated in combination with PD1/PDL1 inhibitors (Opdivo and MPDL3280A, respectively). FPRX/BMY's trial is expected to initiate in mid-2015 and investigate 6 different tumor types initially. RHHBY's anti-CSF1R anti-PDL1 combination trial launched in 1Q15. Chemokine receptors also represent an interesting emerging area, according to the KOL. CXCR4 block, for example, has enhanced PD1 inhibition in animal models. The challenge ultimately will be to determine the exact effects of various chemokines on various cells in the TME, according to the KOL.
• Evidence for cancer vaccines is considered to be strongest currently, but the evidence supporting targeting Treg and MDSC/TAM is expected to grow significantly over the next 5 years. Benchmarked to the current level of scientific evidence for PD1/PD-L1 agents (score of 10), among novel treatment approaches, the KOL cited cancer vaccines as the most interesting (7 out of 10) near term, followed by T-cell agonists and Tregs (both at 6). Myeloid derived suppressor cells (MDSC) and tumor-associated macrophages (TAM) currently have the lowest evidence level, in his view. However, the KOL predicted that MDSC/TAM and Treg could reach the highest evidence level (at 9) among these therapeutic approaches within the next 5 years.
Gruß
ipollit
ASCO 2015... BMY
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
JPmorgan:
$BMY Despite Controversies, Opdivo -057 Presentation/ Discussant Suggest Broad Usage Likely
This morning, CheckMate-057 (Opdivo in 2L non-squam NSCLC) was presented at ASCO, which confirmed extremely durable responses for Opdivo as well as enhanced efficacy in PD-L1 positive patients. In addition, the discussant for the study (Dr. Roy Herbst) had a very favorable view on the data, suggesting Opdivo represents a new SOC in advanced NSCLC and suggesting still the potential for broad usage of the product regardless of PD-L1 status (at least in the US). While we anticipate lingering controversies around the role of PD-L1 status on NSCLC, we see today updates as very favorable (particularly following yesterday’s 6% sell-off) and we continue to see Bristol as a clear leader in the NSCLC space. Reiterate OW.
• -057 discussant suggests Opdivo represents new SOC in advanced NSCLC, not limited by PD-L1 status. While Dr. Herbst (Chief of Medical Oncology at Yale) acknowledged a higher OS benefit in PD-L1+ patients and the need for more work on the topic, he nonetheless suggested broad usage of the drug regardless of PD-L1 status. This view was based on the strong overall efficacy seen with Opdivo (particularly the durable responses seen with the product), lingering questions about the utility of PD-L1 as a biomarker as well as the lack of harm seen in the PD-L1 negative population.
• Opdivo shows distinct OS benefit in 2L non-sq NSCLC, but this signal appears driven by PD-L1+ patients. These data demonstrate superior overall efficacy and a significant OS benefit compared to the docetaxel arm (HR of 0.73 p=0.0015). Responses to Opdivo were highly durable with a median response of 17.2 months in the Opdivo arm compared to 5.6 months in the docetaxel arm.
• On PD-L1 status, data from Checkmate-057 suggest clear improvement in survival benefit for PD-L1 positive patients. Today’s full presentation highlighted the significant improvement in survival for PD-L1 patients with >1% expression (~50% of total patients, 17.2 months vs 9 months for docetaxel). In contrast, patients less than 1% PD-L1 expression showed a similar benefit on Opdivo compared to docetaxel. However on the PD-L1 negative patients, Opdivo showed a clearly improved safety profile compared to docetaxel and it remains to be seen if Opdivo’s survival in the PD-L1 negatives will also separate from docetaxel over time due to the durable responses seen with PD-1s.
• The validity of PD-L1 as a predictive biomarker remains a main point of controversy. PD-L1 is a highly dynamic marker and its expression can turn on and off in response to changes in the tumor microenvironment, making the classification on the basis of PD-L1 status extremely difficult. Further, the field is yet to identify the appropriate cells to use for the diagnostic assays (tumor cells vs. TILs) and standardize methods to quantify PD-L1 expression, making cross trial comparisons challenging.
• Key questions for the weekend. We see the role and reliability of PD-L1 as a biomarker to represent a key ongoing controversy in the NSCLC setting and we will be closely watching Roche’s POPLAR data in 2L non-sq as well as further KOL commentary on the subject. In addition, Phase I frontline chemo studies from Roche and Merck and the durability of responses seen in this setting as well as PD-1/L1+ CTLA4 combo data in lung from Merck and Astra represent key additional updates for the weekend.
Gruß
ipollit
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
JPmorgan:
$BMY Despite Controversies, Opdivo -057 Presentation/ Discussant Suggest Broad Usage Likely
This morning, CheckMate-057 (Opdivo in 2L non-squam NSCLC) was presented at ASCO, which confirmed extremely durable responses for Opdivo as well as enhanced efficacy in PD-L1 positive patients. In addition, the discussant for the study (Dr. Roy Herbst) had a very favorable view on the data, suggesting Opdivo represents a new SOC in advanced NSCLC and suggesting still the potential for broad usage of the product regardless of PD-L1 status (at least in the US). While we anticipate lingering controversies around the role of PD-L1 status on NSCLC, we see today updates as very favorable (particularly following yesterday’s 6% sell-off) and we continue to see Bristol as a clear leader in the NSCLC space. Reiterate OW.
• -057 discussant suggests Opdivo represents new SOC in advanced NSCLC, not limited by PD-L1 status. While Dr. Herbst (Chief of Medical Oncology at Yale) acknowledged a higher OS benefit in PD-L1+ patients and the need for more work on the topic, he nonetheless suggested broad usage of the drug regardless of PD-L1 status. This view was based on the strong overall efficacy seen with Opdivo (particularly the durable responses seen with the product), lingering questions about the utility of PD-L1 as a biomarker as well as the lack of harm seen in the PD-L1 negative population.
• Opdivo shows distinct OS benefit in 2L non-sq NSCLC, but this signal appears driven by PD-L1+ patients. These data demonstrate superior overall efficacy and a significant OS benefit compared to the docetaxel arm (HR of 0.73 p=0.0015). Responses to Opdivo were highly durable with a median response of 17.2 months in the Opdivo arm compared to 5.6 months in the docetaxel arm.
• On PD-L1 status, data from Checkmate-057 suggest clear improvement in survival benefit for PD-L1 positive patients. Today’s full presentation highlighted the significant improvement in survival for PD-L1 patients with >1% expression (~50% of total patients, 17.2 months vs 9 months for docetaxel). In contrast, patients less than 1% PD-L1 expression showed a similar benefit on Opdivo compared to docetaxel. However on the PD-L1 negative patients, Opdivo showed a clearly improved safety profile compared to docetaxel and it remains to be seen if Opdivo’s survival in the PD-L1 negatives will also separate from docetaxel over time due to the durable responses seen with PD-1s.
• The validity of PD-L1 as a predictive biomarker remains a main point of controversy. PD-L1 is a highly dynamic marker and its expression can turn on and off in response to changes in the tumor microenvironment, making the classification on the basis of PD-L1 status extremely difficult. Further, the field is yet to identify the appropriate cells to use for the diagnostic assays (tumor cells vs. TILs) and standardize methods to quantify PD-L1 expression, making cross trial comparisons challenging.
• Key questions for the weekend. We see the role and reliability of PD-L1 as a biomarker to represent a key ongoing controversy in the NSCLC setting and we will be closely watching Roche’s POPLAR data in 2L non-sq as well as further KOL commentary on the subject. In addition, Phase I frontline chemo studies from Roche and Merck and the durability of responses seen in this setting as well as PD-1/L1+ CTLA4 combo data in lung from Merck and Astra represent key additional updates for the weekend.
Gruß
ipollit
ASCO 2015... AFMD, IMGN, MGNX, MRTX
Darin wird auch erwähnt, dass eine EGFR-T790M + MET Kombi sinnvoll sein könnte, um Resistenzen zu verhindern. CLVS hat dies auch erkannt... http://clovisoncology.com/files/Haringsma_Resistance_AACR_20…
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
Leerink
ASCO Day 1 Takeaways for our Coverage: AFMD, IMGN, MGNX, MRTX
• Bottom Line: ASCO Day 1 presentation takeaways for our coverage companies include: (1) Addl. intriguing preclinical data for AFM13 (CD30/ CD16A bispecific) in Hodgkin's Lymphoma (HL) models provides strong basis for PD1 combo trials in early '16, (2) 53% response rate for IMGN's (MP) FRa targeted ADC impresses in Phase Ib, (3) Phase I margetuximab (anti-HER2) single agent activity compares favorably to historic Herceptin data; bodes well for Phase III, and (4) MRTX (OP) saw initial MGCD265 activity in 3 NSCLC patients with genetic MET alterations; trial accrual slower than expected.
• AFMD (OP): AFM13 (anti-CD30/CD16A) highly synergistic in combination with anti-PD1 in patient-derived Hodgkin's Lymphoma (HL) tumor graft models; basis for combination trials in early '16. Results from the Stanford preclinical study indicated strong AFM13 synergies with immune checkpoint inhibitors (anti-PD1 and anti-CTLA-4) and a costimulatory agent (anti-CD137). Strongest synergy was seen with anti-PD1 where reduction of tumor size was seen in all four independent patient-derived tumors. Importantly, AFM13 induced substantial tumorinfiltration of natural killer (NK) cells as single agent, and this effect was enhanced in combination with either agent. An increased number of tumor-infiltrating cytotoxic T-cells was also observed in combination of AFM-13 with anti-PD1 and anti-CTLA-4. Results were consistent across 4 different studies, representing tumors from 4 different newly diagnosed CD30+ HL patients. We view AFM13’s mechanism of action as an important differentiator vs. Adcetris (anti-CD30 ADC) since AFM13’s immune aggregating mechanism should theoretically be more synergistic in combination with PD1 inhibitors. AFMD plans to launch a new Phase Ib clinical trial early next year, evaluating AFM13 in combination w/ anti- PD1/PDL1, which we think could potentially form the basis of a future partnership/collaboration between AFMD and a company owning anti- PD1/L1 assets.
• IMGN: Impressive IMGN853 (FR-alpha ADC) Ph Ib single agent activity in platinum-resistant ovarian cancer. IMGN853 data presented at ASCO improved upon data previously disclosed in the ASCO abstract, with a 53% objective response rate (ORR) presented (vs. 40% in abstract), and 1 CR and 8 PRs in 17 evaluable patients (vs. 0 CRs and 4 PRs in 10 evaluable patients previously). Based on our prior discussions with KOLs (see ASCO pre-call) we believe the response rate is impressive. Off-target side-effects still appear to be a concern, even with the adjusted ideal body weight dosing schedule. IMGN saw dose delays in 7 patients, dose reductions in 6 patients, and discontinuation in 1 patient, with majority of dose modifications stemming from ocular toxicities (although none were Grade 3 or higher). IMGN is planning to initiate a single agent Phase II trial in late 2015 which could be used for registration in FRa-positive platinum-resistant ovarian cancer. IMGN is also planning to evaluate IMGN853 in combination regimens in ovarian cancer as well as in other types of FRa-positive solid tumors.
• MGNX (OP): Phase I margetuximab (anti-HER2) single agent activity compares favorably to historic Herceptin + chemo data. Updated results from the dose-escalation trial in heavily pretreated pts included data on 60 Her2+ patients (23 breast cancer, 37 other cancers). Pts were dosed once weekly or once every 3 weeks. Among the 23 Her2+ breast cancer patients, 19 were evaluable and tumor reductions were seen in 13/19 evaluable patients, including 4/19 patients with confirmed partial responses (21% ORR) . PFS was 5.5 months which compares favorably to Herceptin + chemotherapy based on results of the Th3resa trial in similar patients (PFS: 3.2 months, ORR: 8.6%).
• We believe the margetuximab single agent data presented bodes well for the planned Phase III SOPHIA trial which MGNX will start enrolling in 3Q. This pivotal study will evaluate margetuximab (15mg/ kg every 3 weeks) plus chemotherapy compared to Herceptin plus chemotherapy in 530 third-line HER2+ metastatic breast cancer patients. We believe 3rd line, margetuximab could address a ~$100-200M US opp'ty in pts refractory to 2nd line Kadcyla. We spoke w/ mgmt., who believe if successful in third line, evaluation of margetuximab also in an earlier line metastatic setting or in the adjuvant and neoadjuvant settings could be considered. Margetuximab checkpoint inhibitor combination studies in gastric cancer are expected to initiate in 4Q15.
• MRTX: MGCD265 Ph Ib extension data in 3 NSCLC patients with genetic MET alterations early, but promising. MRTX' poster presentation highlighted 3 patients with non-small cell lung cancer (NSCLC) who achieved significant tumor regression as well as improvement in clinical symptoms. Although the 3 patients did not meet RECIST criteria and we had hoped for data on more patients, we view this early data as encouraging. Two of the patients had MET exon 14 deletion mutations, one had gene copy number gain. Of interest, the third patient was EFFR+ and refractory to EGFR inhibitor therapy.
• MRTX ramping up efforts to increase identification rate of pts w/ genetic MET alterations. We met w/ mgmt who said it continues to add MET+ patients to the trial with the next data update expected towards year-end. Since initiation of the Ph Ib portion of the trial last Dec. MRTX has added more trial sites and now has 20 sites open on a global basis (from 4 initially). In addition to driving forward the patient screening effort at trial sites, MRTX is now working with Foundation Medicine to source MET+ patients who have been identified with FMI's (MP) test which according to mgmt is particularly helpful in identifying patients with exon 14 deletions.
• Pivotal single agent Phase II trial planned; EGFR combination in the works. MRTX expects to initiate a single arm Phase II registrationenabling study in NSCLC by the end of the year. In addition, we believe there is a strong scientific rationale for the combination of MET inhibitors with a third-generation EGFR inhibitor. MRTX is exploring opportunities to start a combination study in patients with acquired EGFR resistance. Other companies conducting MET inhibitor combination trials with EGFR T790M inhibitors to our knowledge include AZN (MP) (AZD9291 + savolitinib), and NVS(OP)/INCY(OP) (EGF816 + INC280), further validating this approach.
Gruß
ipollit
Darin wird auch erwähnt, dass eine EGFR-T790M + MET Kombi sinnvoll sein könnte, um Resistenzen zu verhindern. CLVS hat dies auch erkannt... http://clovisoncology.com/files/Haringsma_Resistance_AACR_20…
http://bridgetunnelinvestor.freeforums.net/thread/1099/asco1…
Leerink
ASCO Day 1 Takeaways for our Coverage: AFMD, IMGN, MGNX, MRTX
• Bottom Line: ASCO Day 1 presentation takeaways for our coverage companies include: (1) Addl. intriguing preclinical data for AFM13 (CD30/ CD16A bispecific) in Hodgkin's Lymphoma (HL) models provides strong basis for PD1 combo trials in early '16, (2) 53% response rate for IMGN's (MP) FRa targeted ADC impresses in Phase Ib, (3) Phase I margetuximab (anti-HER2) single agent activity compares favorably to historic Herceptin data; bodes well for Phase III, and (4) MRTX (OP) saw initial MGCD265 activity in 3 NSCLC patients with genetic MET alterations; trial accrual slower than expected.
• AFMD (OP): AFM13 (anti-CD30/CD16A) highly synergistic in combination with anti-PD1 in patient-derived Hodgkin's Lymphoma (HL) tumor graft models; basis for combination trials in early '16. Results from the Stanford preclinical study indicated strong AFM13 synergies with immune checkpoint inhibitors (anti-PD1 and anti-CTLA-4) and a costimulatory agent (anti-CD137). Strongest synergy was seen with anti-PD1 where reduction of tumor size was seen in all four independent patient-derived tumors. Importantly, AFM13 induced substantial tumorinfiltration of natural killer (NK) cells as single agent, and this effect was enhanced in combination with either agent. An increased number of tumor-infiltrating cytotoxic T-cells was also observed in combination of AFM-13 with anti-PD1 and anti-CTLA-4. Results were consistent across 4 different studies, representing tumors from 4 different newly diagnosed CD30+ HL patients. We view AFM13’s mechanism of action as an important differentiator vs. Adcetris (anti-CD30 ADC) since AFM13’s immune aggregating mechanism should theoretically be more synergistic in combination with PD1 inhibitors. AFMD plans to launch a new Phase Ib clinical trial early next year, evaluating AFM13 in combination w/ anti- PD1/PDL1, which we think could potentially form the basis of a future partnership/collaboration between AFMD and a company owning anti- PD1/L1 assets.
• IMGN: Impressive IMGN853 (FR-alpha ADC) Ph Ib single agent activity in platinum-resistant ovarian cancer. IMGN853 data presented at ASCO improved upon data previously disclosed in the ASCO abstract, with a 53% objective response rate (ORR) presented (vs. 40% in abstract), and 1 CR and 8 PRs in 17 evaluable patients (vs. 0 CRs and 4 PRs in 10 evaluable patients previously). Based on our prior discussions with KOLs (see ASCO pre-call) we believe the response rate is impressive. Off-target side-effects still appear to be a concern, even with the adjusted ideal body weight dosing schedule. IMGN saw dose delays in 7 patients, dose reductions in 6 patients, and discontinuation in 1 patient, with majority of dose modifications stemming from ocular toxicities (although none were Grade 3 or higher). IMGN is planning to initiate a single agent Phase II trial in late 2015 which could be used for registration in FRa-positive platinum-resistant ovarian cancer. IMGN is also planning to evaluate IMGN853 in combination regimens in ovarian cancer as well as in other types of FRa-positive solid tumors.
• MGNX (OP): Phase I margetuximab (anti-HER2) single agent activity compares favorably to historic Herceptin + chemo data. Updated results from the dose-escalation trial in heavily pretreated pts included data on 60 Her2+ patients (23 breast cancer, 37 other cancers). Pts were dosed once weekly or once every 3 weeks. Among the 23 Her2+ breast cancer patients, 19 were evaluable and tumor reductions were seen in 13/19 evaluable patients, including 4/19 patients with confirmed partial responses (21% ORR) . PFS was 5.5 months which compares favorably to Herceptin + chemotherapy based on results of the Th3resa trial in similar patients (PFS: 3.2 months, ORR: 8.6%).
• We believe the margetuximab single agent data presented bodes well for the planned Phase III SOPHIA trial which MGNX will start enrolling in 3Q. This pivotal study will evaluate margetuximab (15mg/ kg every 3 weeks) plus chemotherapy compared to Herceptin plus chemotherapy in 530 third-line HER2+ metastatic breast cancer patients. We believe 3rd line, margetuximab could address a ~$100-200M US opp'ty in pts refractory to 2nd line Kadcyla. We spoke w/ mgmt., who believe if successful in third line, evaluation of margetuximab also in an earlier line metastatic setting or in the adjuvant and neoadjuvant settings could be considered. Margetuximab checkpoint inhibitor combination studies in gastric cancer are expected to initiate in 4Q15.
• MRTX: MGCD265 Ph Ib extension data in 3 NSCLC patients with genetic MET alterations early, but promising. MRTX' poster presentation highlighted 3 patients with non-small cell lung cancer (NSCLC) who achieved significant tumor regression as well as improvement in clinical symptoms. Although the 3 patients did not meet RECIST criteria and we had hoped for data on more patients, we view this early data as encouraging. Two of the patients had MET exon 14 deletion mutations, one had gene copy number gain. Of interest, the third patient was EFFR+ and refractory to EGFR inhibitor therapy.
• MRTX ramping up efforts to increase identification rate of pts w/ genetic MET alterations. We met w/ mgmt who said it continues to add MET+ patients to the trial with the next data update expected towards year-end. Since initiation of the Ph Ib portion of the trial last Dec. MRTX has added more trial sites and now has 20 sites open on a global basis (from 4 initially). In addition to driving forward the patient screening effort at trial sites, MRTX is now working with Foundation Medicine to source MET+ patients who have been identified with FMI's (MP) test which according to mgmt is particularly helpful in identifying patients with exon 14 deletions.
• Pivotal single agent Phase II trial planned; EGFR combination in the works. MRTX expects to initiate a single arm Phase II registrationenabling study in NSCLC by the end of the year. In addition, we believe there is a strong scientific rationale for the combination of MET inhibitors with a third-generation EGFR inhibitor. MRTX is exploring opportunities to start a combination study in patients with acquired EGFR resistance. Other companies conducting MET inhibitor combination trials with EGFR T790M inhibitors to our knowledge include AZN (MP) (AZD9291 + savolitinib), and NVS(OP)/INCY(OP) (EGF816 + INC280), further validating this approach.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.881.913 von lawmeetstax am 30.05.15 22:02:01arry:
BRAF/MEK + PD-L1
die Studie von AZN ist in der Tat auch in meinen Augen interessant, denn sie ist möglicherweise wegweisend für die weiteren Kombinationen bei Hautkrebs.
AZN hat dazu mal Daten gezeugt, dass PD-L1 auf den Tumorzellen nach BRAF/MEK Behandlung hochreguliert wird. Der Tumor ist dann "geschwächt" und schützt sich offenbar mit PD-L1 gegen das Aufräumkommando, denn gleichzeitig wandern mehr T-Zellen in den Tumor ein. Wenn man dann also die PD-L1/PD-1 Achse inhibiert, kann es durchaus zu Synergien kommen. Wissenschaftlich einleuchtend, aber es kam auf die Verträglichkeit der Kombi an. Daher war ich auf diese AZN Studie mit MEK/BRAF + anti-PD-L1 gespannt.
A
BRAF/MEK + PD-L1
die Studie von AZN ist in der Tat auch in meinen Augen interessant, denn sie ist möglicherweise wegweisend für die weiteren Kombinationen bei Hautkrebs.
AZN hat dazu mal Daten gezeugt, dass PD-L1 auf den Tumorzellen nach BRAF/MEK Behandlung hochreguliert wird. Der Tumor ist dann "geschwächt" und schützt sich offenbar mit PD-L1 gegen das Aufräumkommando, denn gleichzeitig wandern mehr T-Zellen in den Tumor ein. Wenn man dann also die PD-L1/PD-1 Achse inhibiert, kann es durchaus zu Synergien kommen. Wissenschaftlich einleuchtend, aber es kam auf die Verträglichkeit der Kombi an. Daher war ich auf diese AZN Studie mit MEK/BRAF + anti-PD-L1 gespannt.
A
Onkologie allgemein:
Der Zusammenhang zwischen der Anzahl der Mutationen im Tumor und dem Ansprechen auf PD-1/PD-L1/CTLA-4 wird klarer. Es sieht danach aus, dass mehr Mutationen zu einer stärkeren Antwort auf die Immuntherapeutika führen.
Vereinfacht gesagt: Entweder man hat wenige, definierte Mutationen. Dann dürften spezifische Inhibitoren der betroffenen Signalwege wirken. Oder man hat sehr viele Mutationen, so dass der Tumor den spezifischen Inhibitoren ausweichen kann, sich aber dem Immunsystem zu erkennen gibt.
A
Cancer immunotherapy takes aim at mutation-riddled tumors
By Jocelyn Kaiser 29 May 2015 2:30 pm 0 Comments
New immune system-boosting cancer drugs have in clinical trials saved the lives of many people with seemingly untreatable melanoma or lung cancer, but the drugs seem useless against colon cancer. One exception—a man with colon cancer whose metastatic tumors vanished for several years after he was treated in 2007—piqued researchers' interest. They suspected his recovery might have to do with the large number of mutations in his tumors. Now, a small clinical trial suggests that even cancer patients with types of tumors that were thought to be impervious to the new drugs could benefit if those malignancies have the right error-riddled DNA signature, a result that could help 3% to 4% of cancer patients.
The drug tested is an antibody that blocks a receptor called PD-1 on the surface of the immune system’s T cells. Tumor cells can hide from T cells by activating the PD-1 receptor; when this immune “checkpoint” is blocked by a PD-1 inhibitor, however, the T cells see the tumor cells and can attack them. Such drugs are among two new types of immune system–harnessing cancer treatments that have generated tremendous excitement, because in some patients with advanced cancer, they keep tumors at bay for years. One hypothesis about why melanoma and lung cancer respond best to PD-1 inhibitors is that these two cancer types tend to have more mutations than other cancers. Some of these mutations may alter genes so that they code for small stretches of abnormal proteins that the immune system sees as foreign proteins, or antigens. The more mutations, the more of these “neoantigens” that can trigger an attack from T cells that have been unleashed by a PD-1 inhibitor.
When researchers at Johns Hopkins University in Baltimore, Maryland, examined tumor tissue from the original man with colon cancer who responded to a PD-1 inhibitor, they found a clue: His tumor had mutations in “mismatch repair” genes, so-called because their encoded proteins fix errors in DNA bases when cells replicate their DNA. When these genes don’t work properly, they can lead to cancer-promoting mutations and result in a colon tumor riddled with 1000 or more mutations, 10 to 100 times the usual number. The Hopkins group wondered if patients with many cancer types who had tumors with errors in mismatch repair genes would respond to PD-1 inhibitors.
To explore this idea, Hopkins oncologists Dung Le, Luis Diaz, and others looked for mismatch repair mutations in tumor samples from patients with advanced colon cancer and other cancer types whose tumors had stopped responding to other treatments. They divided 48 patients into two groups, those with and without these mutations in their tumors. Then they gave all of them a PD-1 inhibitor called pembrolizumab (Keytruda) every 2 weeks.
The difference in the results was dramatic. Those with mismatch repair mutations were far more likely to respond—of 13 with colorectal cancer, eight saw their tumors shrink, four remained stable, and only one got worse. By contrast, not a single one of 25 colorectal patients lacking mutations in mismatch repair genes responded. Some of the patients who responded are still alive after a year or more, whereas the nonresponders lived on average only 7.6 months. Of 10 patients with other types of cancer—including pancreatic, prostate, and uterine—who had mismatch repair mutations, in seven their tumors shrank or remained stable; the other three progressed. The study will appear tomorrow in The New England Journal of Medicine, and Le will present updated results at the annual meeting of the American Society of Clinical Oncology in Chicago tomorrow.
The results suggest that the 3% to 4% of all cancer patients with mismatch repair defects in their tumors could benefit from PD-1 inhibitors, Diaz says. “It’s a slice. It’s not all cancer,” he says. Still, that could add up to 30,000 to 40,000 advanced cancer patients a year in the United States, he says.
The study also supports the idea that tumors with more mutations—whether from mismatch repair defects or for other reasons—are more likely to respond to PD-1 inhibitors and similar drugs, says immunotherapy cancer researcher Jedd Wolchok of the Memorial Sloan Kettering Cancer Center in New York City. His team has recently reported that melanoma and lung cancer patients with more neoantigen-coding tumor mutations are more likely to respond to immune checkpoint blockers. The Hopkins study “gives us very good confidence that what we’ve seen before is important,” he says. One implication is cancer patients with few mutations in their tumors might respond better to PD-1 inhibitors if they first receive radiation or chemotherapy, because these treatments can create new mutations in tumors. Although some patients in PD-1 inhibitor trials have had such prior treatments, without a trial designed to address the question, “it’s hard to draw conclusions,” Diaz says.
Der Zusammenhang zwischen der Anzahl der Mutationen im Tumor und dem Ansprechen auf PD-1/PD-L1/CTLA-4 wird klarer. Es sieht danach aus, dass mehr Mutationen zu einer stärkeren Antwort auf die Immuntherapeutika führen.
Vereinfacht gesagt: Entweder man hat wenige, definierte Mutationen. Dann dürften spezifische Inhibitoren der betroffenen Signalwege wirken. Oder man hat sehr viele Mutationen, so dass der Tumor den spezifischen Inhibitoren ausweichen kann, sich aber dem Immunsystem zu erkennen gibt.
A
Cancer immunotherapy takes aim at mutation-riddled tumors
By Jocelyn Kaiser 29 May 2015 2:30 pm 0 Comments
New immune system-boosting cancer drugs have in clinical trials saved the lives of many people with seemingly untreatable melanoma or lung cancer, but the drugs seem useless against colon cancer. One exception—a man with colon cancer whose metastatic tumors vanished for several years after he was treated in 2007—piqued researchers' interest. They suspected his recovery might have to do with the large number of mutations in his tumors. Now, a small clinical trial suggests that even cancer patients with types of tumors that were thought to be impervious to the new drugs could benefit if those malignancies have the right error-riddled DNA signature, a result that could help 3% to 4% of cancer patients.
The drug tested is an antibody that blocks a receptor called PD-1 on the surface of the immune system’s T cells. Tumor cells can hide from T cells by activating the PD-1 receptor; when this immune “checkpoint” is blocked by a PD-1 inhibitor, however, the T cells see the tumor cells and can attack them. Such drugs are among two new types of immune system–harnessing cancer treatments that have generated tremendous excitement, because in some patients with advanced cancer, they keep tumors at bay for years. One hypothesis about why melanoma and lung cancer respond best to PD-1 inhibitors is that these two cancer types tend to have more mutations than other cancers. Some of these mutations may alter genes so that they code for small stretches of abnormal proteins that the immune system sees as foreign proteins, or antigens. The more mutations, the more of these “neoantigens” that can trigger an attack from T cells that have been unleashed by a PD-1 inhibitor.
When researchers at Johns Hopkins University in Baltimore, Maryland, examined tumor tissue from the original man with colon cancer who responded to a PD-1 inhibitor, they found a clue: His tumor had mutations in “mismatch repair” genes, so-called because their encoded proteins fix errors in DNA bases when cells replicate their DNA. When these genes don’t work properly, they can lead to cancer-promoting mutations and result in a colon tumor riddled with 1000 or more mutations, 10 to 100 times the usual number. The Hopkins group wondered if patients with many cancer types who had tumors with errors in mismatch repair genes would respond to PD-1 inhibitors.
To explore this idea, Hopkins oncologists Dung Le, Luis Diaz, and others looked for mismatch repair mutations in tumor samples from patients with advanced colon cancer and other cancer types whose tumors had stopped responding to other treatments. They divided 48 patients into two groups, those with and without these mutations in their tumors. Then they gave all of them a PD-1 inhibitor called pembrolizumab (Keytruda) every 2 weeks.
The difference in the results was dramatic. Those with mismatch repair mutations were far more likely to respond—of 13 with colorectal cancer, eight saw their tumors shrink, four remained stable, and only one got worse. By contrast, not a single one of 25 colorectal patients lacking mutations in mismatch repair genes responded. Some of the patients who responded are still alive after a year or more, whereas the nonresponders lived on average only 7.6 months. Of 10 patients with other types of cancer—including pancreatic, prostate, and uterine—who had mismatch repair mutations, in seven their tumors shrank or remained stable; the other three progressed. The study will appear tomorrow in The New England Journal of Medicine, and Le will present updated results at the annual meeting of the American Society of Clinical Oncology in Chicago tomorrow.
The results suggest that the 3% to 4% of all cancer patients with mismatch repair defects in their tumors could benefit from PD-1 inhibitors, Diaz says. “It’s a slice. It’s not all cancer,” he says. Still, that could add up to 30,000 to 40,000 advanced cancer patients a year in the United States, he says.
The study also supports the idea that tumors with more mutations—whether from mismatch repair defects or for other reasons—are more likely to respond to PD-1 inhibitors and similar drugs, says immunotherapy cancer researcher Jedd Wolchok of the Memorial Sloan Kettering Cancer Center in New York City. His team has recently reported that melanoma and lung cancer patients with more neoantigen-coding tumor mutations are more likely to respond to immune checkpoint blockers. The Hopkins study “gives us very good confidence that what we’ve seen before is important,” he says. One implication is cancer patients with few mutations in their tumors might respond better to PD-1 inhibitors if they first receive radiation or chemotherapy, because these treatments can create new mutations in tumors. Although some patients in PD-1 inhibitor trials have had such prior treatments, without a trial designed to address the question, “it’s hard to draw conclusions,” Diaz says.
Antwort auf Beitrag Nr.: 49.883.515 von Axel_Olsson am 31.05.15 13:26:01TSRO / CLVS
"His tumor had mutations in “mismatch repair” genes, so-called because their encoded proteins fix errors in DNA bases when cells replicate their DNA. When these genes don’t work properly, they can lead to cancer-promoting mutations and result in a colon tumor riddled with 1000 or more mutations, 10 to 100 times the usual number.
His team has recently reported that melanoma and lung cancer patients with more neoantigen-coding tumor mutations are more likely to respond to immune checkpoint blockers.
One implication is cancer patients with few mutations in their tumors might respond better to PD-1 inhibitors if they first receive radiation or chemotherapy, because these treatments can create new mutations in tumors."
Eine Möglichkeit, Tumore dazu zu bringen, mehr Antigene wie Neoantigens zu expessionieren, könnten PARP-Hemmer sein. Diese blockieren einen wesentlichen Reparatur-Mechanismus von DNA-Schäden, so das die Fehler, die z.B. durch Chemo oder Bestrahlung entstehen im Tumor erhalten bleiben...
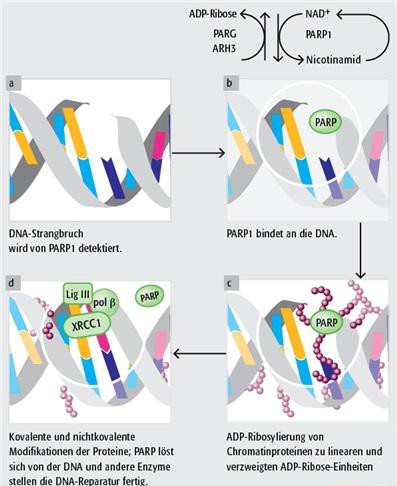

TSRO hat gestern bekannt gegeben, dass sie mit Merck zusammenarbeiten wollen, um die PD1 + PARP Kombi zu testen.

TSRO besitzt auch eine eigene IO-Pipeline... PD1, TIM3 und LAG3 könnten nächstes Jahr in P1 gehen.
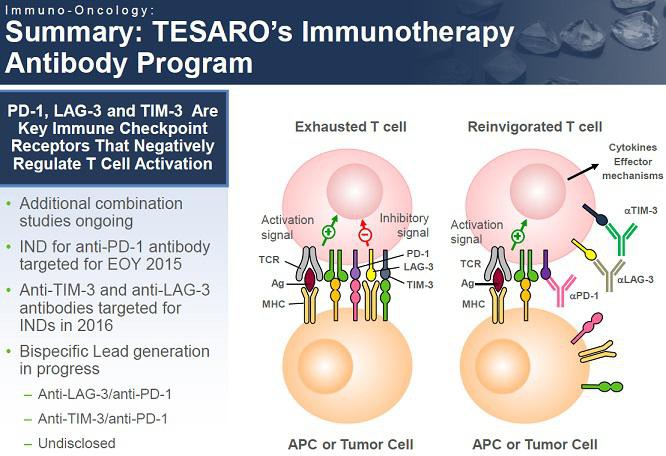
Grüße
ipollit
"His tumor had mutations in “mismatch repair” genes, so-called because their encoded proteins fix errors in DNA bases when cells replicate their DNA. When these genes don’t work properly, they can lead to cancer-promoting mutations and result in a colon tumor riddled with 1000 or more mutations, 10 to 100 times the usual number.
His team has recently reported that melanoma and lung cancer patients with more neoantigen-coding tumor mutations are more likely to respond to immune checkpoint blockers.
One implication is cancer patients with few mutations in their tumors might respond better to PD-1 inhibitors if they first receive radiation or chemotherapy, because these treatments can create new mutations in tumors."
Eine Möglichkeit, Tumore dazu zu bringen, mehr Antigene wie Neoantigens zu expessionieren, könnten PARP-Hemmer sein. Diese blockieren einen wesentlichen Reparatur-Mechanismus von DNA-Schäden, so das die Fehler, die z.B. durch Chemo oder Bestrahlung entstehen im Tumor erhalten bleiben...


TSRO hat gestern bekannt gegeben, dass sie mit Merck zusammenarbeiten wollen, um die PD1 + PARP Kombi zu testen.

TSRO besitzt auch eine eigene IO-Pipeline... PD1, TIM3 und LAG3 könnten nächstes Jahr in P1 gehen.

Grüße
ipollit
CLVS:
Roci:

Das sieht erst mal nicht gut aus...
Roci:

Das sieht erst mal nicht gut aus...
Antwort auf Beitrag Nr.: 49.883.908 von SLGramann am 31.05.15 15:33:19Was Hoffnung macht, ist die doch höhere ORR:
At the recommended dose of 500mg, a 60 percent ORR and a 90 percent DCR was observed
...
A total of 147 evaluable plasma T790M-positive patients were treated with rociletinib; in those treated with 500mg, a 57 percent ORR and an 80 percent DCR has been observed to date
Ebenfalls positiv das Ansprechen bei T790-negativen Patienten:
Rociletinib activity was also observed in 35 evaluable T790M-negative patients treated at all doses. A 37 percent ORR has been observed, in a range of 32 to 39 percent across doses studied.
Das Nebenwirkungsprofil sieht auch recht gut aus.
Ich denke, der Markt wird das alles in allem erst mal deutlich negativ aufnehmen und sich dann wieder beruhigen.
Letztlich ist das alles ganz in Ordnung, denke ich.
http://finance.yahoo.com/news/clovis-oncology-rociletinib-co…
At the recommended dose of 500mg, a 60 percent ORR and a 90 percent DCR was observed
...
A total of 147 evaluable plasma T790M-positive patients were treated with rociletinib; in those treated with 500mg, a 57 percent ORR and an 80 percent DCR has been observed to date
Ebenfalls positiv das Ansprechen bei T790-negativen Patienten:
Rociletinib activity was also observed in 35 evaluable T790M-negative patients treated at all doses. A 37 percent ORR has been observed, in a range of 32 to 39 percent across doses studied.
Das Nebenwirkungsprofil sieht auch recht gut aus.
Ich denke, der Markt wird das alles in allem erst mal deutlich negativ aufnehmen und sich dann wieder beruhigen.
Letztlich ist das alles ganz in Ordnung, denke ich.
http://finance.yahoo.com/news/clovis-oncology-rociletinib-co…
Antwort auf Beitrag Nr.: 49.883.980 von SLGramann am 31.05.15 16:04:06CLDX
tja, sowohl die Daten von CLVS als auch von CLDX sind nicht eindeutig positiv bzw. könnten als etwas unter den Erwartungen interpretiert werden.
CLDX erhöht signifikant OS in der rrGBM PII mit Avastin. Allerdings ist der OS-Vorteil ein wenig geschrumpft. Ich hoffe mal, dass CLDX aufgrund dieser Daten und BTD die vorzeitige Zulassung erhält.

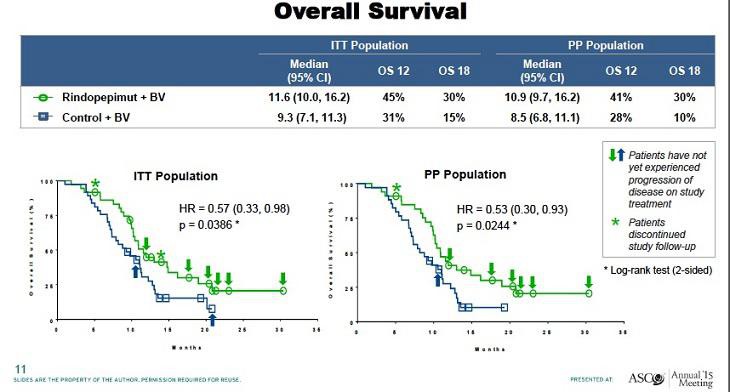
Gruß
ipollit
tja, sowohl die Daten von CLVS als auch von CLDX sind nicht eindeutig positiv bzw. könnten als etwas unter den Erwartungen interpretiert werden.
CLDX erhöht signifikant OS in der rrGBM PII mit Avastin. Allerdings ist der OS-Vorteil ein wenig geschrumpft. Ich hoffe mal, dass CLDX aufgrund dieser Daten und BTD die vorzeitige Zulassung erhält.


Gruß
ipollit
Antwort auf Beitrag Nr.: 49.883.980 von SLGramann am 31.05.15 16:04:06CLVS
ein wesentlicher Vorteil von Rociletinib ist immer noch, dass es 2nd-line auch ohne T790M wirkt. Über 1st-line sagt das allerdings erstmal nichts aus.

Am meisten würden mich Daten von AZD9291 bezüglich regionaler Unterschiede interessieren. Fair wäre nur ein Vergleich entweder mit rein asiatischen Patienten oder ganz ohne diese. Diese Daten müsste AZN auch irgendwann mal liefern... dann steht AZD9291 vielleicht nicht mehr so gut da.
Gruß
ipollit
ein wesentlicher Vorteil von Rociletinib ist immer noch, dass es 2nd-line auch ohne T790M wirkt. Über 1st-line sagt das allerdings erstmal nichts aus.

Am meisten würden mich Daten von AZD9291 bezüglich regionaler Unterschiede interessieren. Fair wäre nur ein Vergleich entweder mit rein asiatischen Patienten oder ganz ohne diese. Diese Daten müsste AZN auch irgendwann mal liefern... dann steht AZD9291 vielleicht nicht mehr so gut da.
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.884.040 von ipollit am 31.05.15 16:29:08"Am meisten würden mich Daten von AZD9291 bezüglich regionaler Unterschiede interessieren. Fair wäre nur ein Vergleich entweder mit rein asiatischen Patienten oder ganz ohne diese. Diese Daten müsste AZN auch irgendwann mal liefern... dann steht AZD9291 vielleicht nicht mehr so gut da."
Direkt nach der Zulassung von AZD9291 sollte Clovis eine Vergleichsstudie mit kaukasischen Patienten durchführen. Ich denke nicht, dass sie vor dem Ergebnis Angst haben müssten!
Direkt nach der Zulassung von AZD9291 sollte Clovis eine Vergleichsstudie mit kaukasischen Patienten durchführen. Ich denke nicht, dass sie vor dem Ergebnis Angst haben müssten!
CLDX
Randomized Phase 2 ReACT Study of RINTEGA(R) in Recurrent Bevacizumab-naive Glioblastoma Demonstrates Statistically Significant Overall Survival and Emergence of Long-term Survival Benefit; Primary Endpoint of PFS6 Met
http://ir.celldex.com/releasedetail.cfm?ReleaseID=915592
"Celldex said it is in discussions with regulators on finding a pathway to approval. "We certainly think the data is good enough to justify accelerated approval," said Celldex Chief Medical Officer Thomas Davis."
Randomized Phase 2 ReACT Study of RINTEGA(R) in Recurrent Bevacizumab-naive Glioblastoma Demonstrates Statistically Significant Overall Survival and Emergence of Long-term Survival Benefit; Primary Endpoint of PFS6 Met
http://ir.celldex.com/releasedetail.cfm?ReleaseID=915592
"Celldex said it is in discussions with regulators on finding a pathway to approval. "We certainly think the data is good enough to justify accelerated approval," said Celldex Chief Medical Officer Thomas Davis."
CLVS:
Der Markt reagiert ohne Hysterie auf die "schlechten" Rociletinib-Daten:

Analysten weisen inzwischen nachdrücklich auf die besonderen Schwierigkeiten bei Cross-trial comparisons zwischen AZ9291 und Rociletinib hin:

Eines Tages werden wir auch Daten besser vergleichbarer Patientenkollektive haben und erst dann wird man in etwa sagen können, ob das eine Produkt dem anderen überlegen ist.
Schade, dass CLVS erst jetzt in Japan in die PII kommt. Diese Daten werden definitiv spannend werden:
"In addition, a Phase 1 study of rociletinib in Japan has completed enrollment and a Phase 2 study in Japanese patients, agreed upon with Japanese regulatory authorities, is expected to initiate in the second half of 2015."
Feuerstein weist außerdem auf die hervorragenden Rucaparib-Daten hin:
http://www.thestreet.com/story/13169113/1/clovis-wins-one-as…
Ich gebe zu, dass ich mich um CLVS PARP-Inhibitor bisher eher wenig geschert habe. Vielleicht sollte man das aber besser mal tun.
Der Markt reagiert ohne Hysterie auf die "schlechten" Rociletinib-Daten:
Analysten weisen inzwischen nachdrücklich auf die besonderen Schwierigkeiten bei Cross-trial comparisons zwischen AZ9291 und Rociletinib hin:

Eines Tages werden wir auch Daten besser vergleichbarer Patientenkollektive haben und erst dann wird man in etwa sagen können, ob das eine Produkt dem anderen überlegen ist.
Schade, dass CLVS erst jetzt in Japan in die PII kommt. Diese Daten werden definitiv spannend werden:
"In addition, a Phase 1 study of rociletinib in Japan has completed enrollment and a Phase 2 study in Japanese patients, agreed upon with Japanese regulatory authorities, is expected to initiate in the second half of 2015."
Feuerstein weist außerdem auf die hervorragenden Rucaparib-Daten hin:
http://www.thestreet.com/story/13169113/1/clovis-wins-one-as…
Ich gebe zu, dass ich mich um CLVS PARP-Inhibitor bisher eher wenig geschert habe. Vielleicht sollte man das aber besser mal tun.
Puh! Ganz schön was los heute nach dem ASCO WE. Und man lernt doch nie aus was wie den Kurs beeinflusst.
CLVS: Hier hätte ich mit höheren Verlusten gerechnet - aber offensichtlich hat "der Markt" dann doch eingesehen, dass es 2 Produkte (bald hoffentlich 3) gibt. Bei Roci bleibts ja beim Quervergleich...
IMGN: 60% scheinen mit doch sehr übertrieben. KP
ONTY: +30-15 Hier werden die Gewinne abverkauft, da der Kurs ja vorher schon gut gelaufen ist. Schade! Habe hier trotzdem weitere Gewinne mitgenommen.
Ich habe mir heute eine Position LOXO gekauft, nachdem RXDX gute Ergebnisse gleiefert hat.

RXDX:

Momentan läuft eine PIb und Loxo hat neulich schon mitgeteilt, dass sie 1 (!) Patienten mit TRK in die Studie aufgenommen haben. Von dem 1 Patienten hängt jetzt kurzfristig erst mal viel ab. Interessanter wird es, wenn LOXO eine ausgewählte Gruppe in der PII mit TRK untersucht. Wer sich für LOXO interessiert sollte auf jeden Fall dies gelesen haben:
http://seekingalpha.com/article/2926906-investing-in-precisi…
Mal sehen, ob jetzt Schwung in die Aktie kommt. Bei 11 und 10$ könnte der Kurs sonst Unterstützung finden.

SG kmastra
CLVS: Hier hätte ich mit höheren Verlusten gerechnet - aber offensichtlich hat "der Markt" dann doch eingesehen, dass es 2 Produkte (bald hoffentlich 3) gibt. Bei Roci bleibts ja beim Quervergleich...
IMGN: 60% scheinen mit doch sehr übertrieben. KP
ONTY: +30-15 Hier werden die Gewinne abverkauft, da der Kurs ja vorher schon gut gelaufen ist. Schade! Habe hier trotzdem weitere Gewinne mitgenommen.
Ich habe mir heute eine Position LOXO gekauft, nachdem RXDX gute Ergebnisse gleiefert hat.

RXDX:

Momentan läuft eine PIb und Loxo hat neulich schon mitgeteilt, dass sie 1 (!) Patienten mit TRK in die Studie aufgenommen haben. Von dem 1 Patienten hängt jetzt kurzfristig erst mal viel ab. Interessanter wird es, wenn LOXO eine ausgewählte Gruppe in der PII mit TRK untersucht. Wer sich für LOXO interessiert sollte auf jeden Fall dies gelesen haben:
http://seekingalpha.com/article/2926906-investing-in-precisi…
Mal sehen, ob jetzt Schwung in die Aktie kommt. Bei 11 und 10$ könnte der Kurs sonst Unterstützung finden.
SG kmastra
Das finde ich eine richtig gute Idee, zumal ich im IO Bereich im Grunde nichts habe. Mal sehen wie die genauen Konditionen sind aber ich denke da werde ich zuschlagen. Gerade als ETF eine super Sache!
http://www.loncarindex.com/#!cancer-immunotherapy-etf-partne…
Momentan im Index:
Novartis
Merck
Amgen
Bristol Myers
Celgene
AstraZeneca
Incyte
Juno Therapeutics
bluebird bio
Kite Pharma
Celldex Therapeutics
TESARO
NewLink Genetics
ZIOPHARM
Cellectis
MacroGenics
Bellicum
Five Prime Therapeutics
Atara Biotherapeutics
Sorrento Therapeutics
Agenus
Northwest Biotherapeutics
Lion Biotechnologies
Inovio Pharma
Advaxis
http://www.loncarindex.com/#!cancer-immunotherapy-etf-partne…
Momentan im Index:
Novartis
Merck
Amgen
Bristol Myers
Celgene
AstraZeneca
Incyte
Juno Therapeutics
bluebird bio
Kite Pharma
Celldex Therapeutics
TESARO
NewLink Genetics
ZIOPHARM
Cellectis
MacroGenics
Bellicum
Five Prime Therapeutics
Atara Biotherapeutics
Sorrento Therapeutics
Agenus
Northwest Biotherapeutics
Lion Biotechnologies
Inovio Pharma
Advaxis
Hallo zusammen
Ich bin gerade auf folgenden interessanten Blog gestossen, den ich bislang noch nicht kannte: http://rnaitherapeutics.blogspot.ch
Kennt einer der Threadteilnehmer hier den Blog oder den Autor und kann daher bereits etwas über seine Qualität sagen, sprich ob es sich lohnt diesen auch regelmässig zu verfolgen?
Auszug über den Autor:
Trained in RNAi molecular biology at the universities of Edinburgh (BSc Hons 2000-2002), Oxford (DPhil 2002-2005), and Stanford (post-doctoral research) and still a scientist at heart, it is my strong belief that sound science is the basis for any successful technology company and investment. My consultancy and blog therefore take a bottom-up approach to the development of RNAi Therapeutics.
Ich bin gerade auf folgenden interessanten Blog gestossen, den ich bislang noch nicht kannte: http://rnaitherapeutics.blogspot.ch
Kennt einer der Threadteilnehmer hier den Blog oder den Autor und kann daher bereits etwas über seine Qualität sagen, sprich ob es sich lohnt diesen auch regelmässig zu verfolgen?
Auszug über den Autor:
Trained in RNAi molecular biology at the universities of Edinburgh (BSc Hons 2000-2002), Oxford (DPhil 2002-2005), and Stanford (post-doctoral research) and still a scientist at heart, it is my strong belief that sound science is the basis for any successful technology company and investment. My consultancy and blog therefore take a bottom-up approach to the development of RNAi Therapeutics.
Antwort auf Beitrag Nr.: 49.907.833 von SpanishEyes am 03.06.15 21:30:10Interessanter Artikel zum Thema allgemein:
http://www.the-scientist.com/?articles.view/articleNo/40871/…
http://www.the-scientist.com/?articles.view/articleNo/40871/…
SAGE, MRNS
zurzeit läuft SAGE ja sehr gut... MRNS bewegt sich dagegen kaum. MK ist aktuell 2,23 Mrd USD vs 119 Mio USD
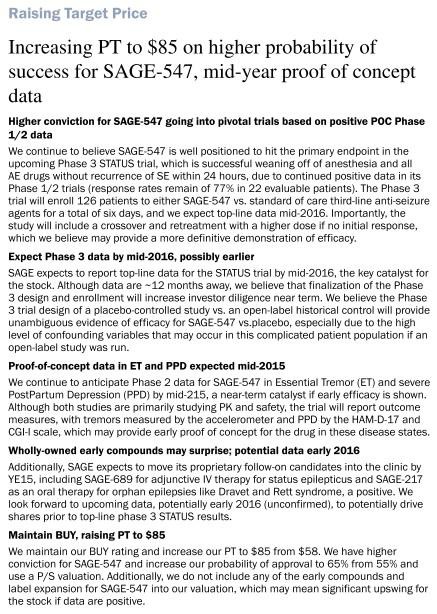
****

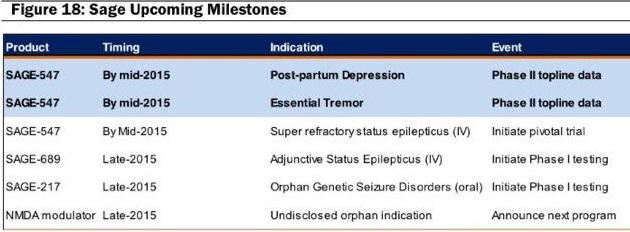


Gruß
ipollit
zurzeit läuft SAGE ja sehr gut... MRNS bewegt sich dagegen kaum. MK ist aktuell 2,23 Mrd USD vs 119 Mio USD

****


Gruß
ipollit
ZSPH
ZSPH hat bei der FDA die die US-Zulassung von ZS-9 beantragt... die Zulassung könnte somit nächstes Jahr erfolgen


Gruß
ipollit
ZSPH hat bei der FDA die die US-Zulassung von ZS-9 beantragt... die Zulassung könnte somit nächstes Jahr erfolgen

Gruß
ipollit
SGYP (Synergy Pharmaceuticals):
Das Unternehmen ist mir kürzlich durch die Erwähnung im Blog von Ozgur Ogut aufgefallen, den ich verfolge, seit er das Scheitern von CLDN auf seriöse und analytische Weise prognostiziert hat.
http://www.ozgurogut.com/thoughts/
Die Marktkapitalisierung beträgt ca. 500 Mio. Dollar. Sie haben außerdem 200 Millionen "Senior Convertible Debentures" in der Bilanz, die mit 7,5% auch straff verzinst sind (außerdem gibts natürlich noch ein Wandlungsrecht in Aktien zum Kurs von 3,11 Dollar).
Der "Enterprise Value" ist also mit ungefähr 700 Mio. Dollar zu veranschlagen.

Wesentlicher Wertreiber ist PLECANATIDE, ein Mittel, das gegen Verstopfung helfen soll (genauer gesagt in den Indikationen "chronic idiopathic constipation (CIC)" und "irritable bowel syndrome with constipation (IBS-C)")
Man ist derzeit in der P III. Ein NDA für CIC wird Ende 2015 und für IBS-C Ende 2016 angestrebt.
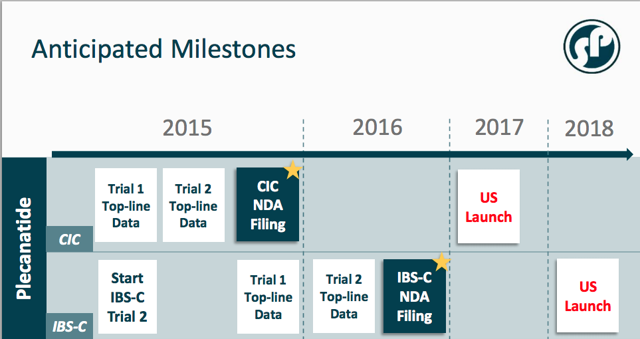
"Verstopfung" klingt vielleicht etwas drollig, aber es ist ein weitverbreitetes Problem (angeblich 45 Millionen Amerikaner betroffen) und es gibt schwere Fälle, in denen eine Behandlung angezeigt ist.
Es gibt zwei zugelassene Konkurrenzpräparate, nämlich Linzess (von Ironwood / Actavis) und Amitiza (von Takeda).
Während Amitiza zu stagnieren scheint, steigen die Umsätze von Linzess schnell an.
Die Umsätze liegen bei ca. 120 bzw. 260 Mio. USD/Jahr. Der Gesamtmarkt wird künftig auf 1,5 Milliarden Dollar geschätzt (ist sicher hinterfragbar, allerdings ist auch nur für Linzess schon von einem 2-Milliarden-Potential die Rede gewesen).
Die bisherigen Daten (P II) waren offenbar gut:
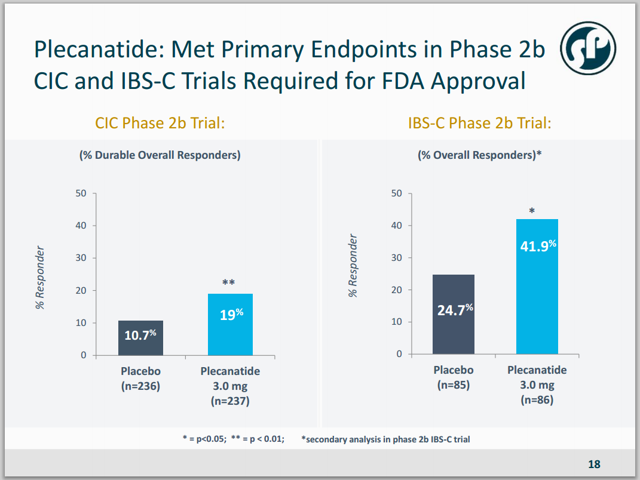
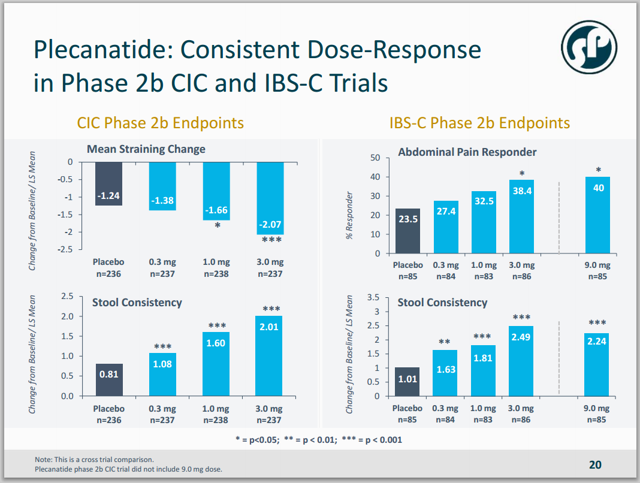
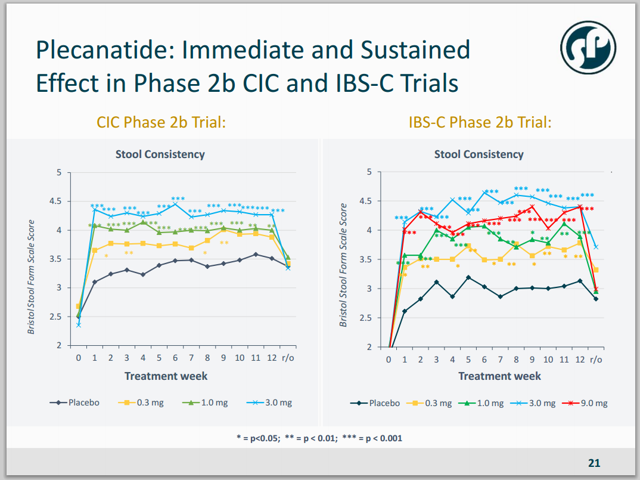
Plecanatide soll vom Konkurrenten Linzess vor allem über ein besseres Nebenwirkungsprofil abgesetzt werden.
Offenbar gibt es bei Linzess ziemliche Probleme mit Durchfällen. Es ist von bis zu 20% der Patienten die Rede, während Plecanatide scheinbar unter 10% bleibt:
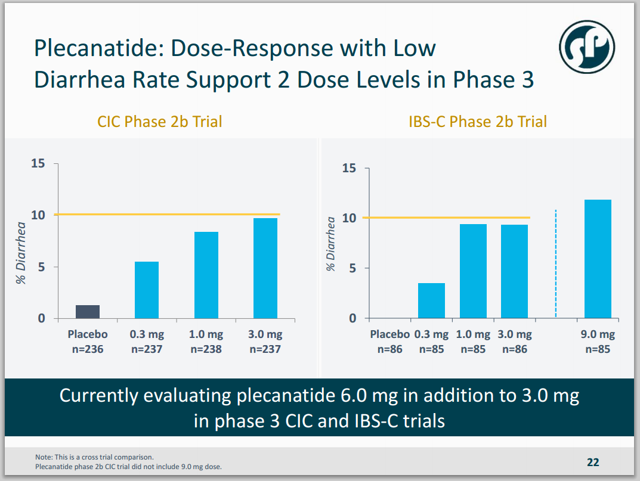
Die Unternehmenspräsentation:
http://content.stockpr.com/synergypharma/media/76808ee80e490…
Ein Artikel bei Seeking Alpha:
http://seekingalpha.com/article/3210856-the-paulson-tug-push…
Eine Analystenmeinung:

Ich habe mir eine 1%-Position zu 4,60 Dollar zugelegt.
Das Unternehmen ist mir kürzlich durch die Erwähnung im Blog von Ozgur Ogut aufgefallen, den ich verfolge, seit er das Scheitern von CLDN auf seriöse und analytische Weise prognostiziert hat.
http://www.ozgurogut.com/thoughts/
Die Marktkapitalisierung beträgt ca. 500 Mio. Dollar. Sie haben außerdem 200 Millionen "Senior Convertible Debentures" in der Bilanz, die mit 7,5% auch straff verzinst sind (außerdem gibts natürlich noch ein Wandlungsrecht in Aktien zum Kurs von 3,11 Dollar).
Der "Enterprise Value" ist also mit ungefähr 700 Mio. Dollar zu veranschlagen.
Wesentlicher Wertreiber ist PLECANATIDE, ein Mittel, das gegen Verstopfung helfen soll (genauer gesagt in den Indikationen "chronic idiopathic constipation (CIC)" und "irritable bowel syndrome with constipation (IBS-C)")
Man ist derzeit in der P III. Ein NDA für CIC wird Ende 2015 und für IBS-C Ende 2016 angestrebt.

"Verstopfung" klingt vielleicht etwas drollig, aber es ist ein weitverbreitetes Problem (angeblich 45 Millionen Amerikaner betroffen) und es gibt schwere Fälle, in denen eine Behandlung angezeigt ist.
Es gibt zwei zugelassene Konkurrenzpräparate, nämlich Linzess (von Ironwood / Actavis) und Amitiza (von Takeda).
Während Amitiza zu stagnieren scheint, steigen die Umsätze von Linzess schnell an.
Die Umsätze liegen bei ca. 120 bzw. 260 Mio. USD/Jahr. Der Gesamtmarkt wird künftig auf 1,5 Milliarden Dollar geschätzt (ist sicher hinterfragbar, allerdings ist auch nur für Linzess schon von einem 2-Milliarden-Potential die Rede gewesen).
Die bisherigen Daten (P II) waren offenbar gut:



Plecanatide soll vom Konkurrenten Linzess vor allem über ein besseres Nebenwirkungsprofil abgesetzt werden.
Offenbar gibt es bei Linzess ziemliche Probleme mit Durchfällen. Es ist von bis zu 20% der Patienten die Rede, während Plecanatide scheinbar unter 10% bleibt:

Die Unternehmenspräsentation:
http://content.stockpr.com/synergypharma/media/76808ee80e490…
Ein Artikel bei Seeking Alpha:
http://seekingalpha.com/article/3210856-the-paulson-tug-push…
Eine Analystenmeinung:

Ich habe mir eine 1%-Position zu 4,60 Dollar zugelegt.
hallo,
mal eine frage in die runde
hat eigentlich jemand -abseits vom frontrunner teva pharmaceuticals- israelische (bio)technologiefirmen, oder sich schonmal damit beschäftigt?
man kann ja in einigen dingen viel gutes über sie hören
ich habe OPK schon länger mit auf der beobachtungsliste, sie aber nie gekauft
Gruß
P.
mal eine frage in die runde
hat eigentlich jemand -abseits vom frontrunner teva pharmaceuticals- israelische (bio)technologiefirmen, oder sich schonmal damit beschäftigt?
man kann ja in einigen dingen viel gutes über sie hören
ich habe OPK schon länger mit auf der beobachtungsliste, sie aber nie gekauft
Gruß
P.
Antwort auf Beitrag Nr.: 49.926.756 von Popeye82 am 07.06.15 13:12:38Ich hab eine kleine Posi RedHill Biopharma LTD, ebefalls aus Israel. Wer sich mal damit beschäftigen möchte:
http://www.redhillbio.com/
http://www.redhillbio.com/RedHill/Templates/showpage.asp?DBI…
http://www.redhillbio.com/
http://www.redhillbio.com/RedHill/Templates/showpage.asp?DBI…
arry:
Selumetinib/MEK Inhibitor
Promising Results in Tumor Shrinkage Study Announced at Neurofibromatosis Conference
Over half of patients treated with selumetinib in phase I trial see reduction in plexiform neurofibromas
New York, NY (PRWEB) June 08, 2015
As hundreds of the world's leading NF experts convene in Monterey, California for the Children's Tumor Foundation NF Conference, the largest gathering dedicated to neurofibromatosis (NF), it was announced today that for the first time in the history of the treatment of plexiform neurofibromas (PNs), over 50% of patients saw decreased volume in these inoperable tumors. In a presentation titled "The Promise of MEK: Therapeutics for NF1", Brigitte C. Widemann, MD, of the National Cancer Institute (NCI), reported that response data in a phase I trial for children and young adults is showing decreases in tumor volume. Anecdotal improvement in function, and reduction in PN related pain and disfigurement has also been observed.
Plexiform neurofibromas exhibit the most rapid growth in young children, and therefore early intervention in children with growing PNs may result in the greatest clinical benefit. Consistent volume decreases of large PNs has not been reported in the past, and today's announcement indicates a promising future for the development of effective medical therapies for NF1 related PNs.
This highly successful clinical study is the result of a major investment of the Children's Tumor Foundation NF Preclinical Consortium (funded since 2008). Nancy Ratner, PhD and Wade Clapp, MD demonstrated that MEK inhibitors (MEKi) have a massive result on PN tumor volume in mice.
"Today, this very robust effect of MEK inhibitors in mice with neurofibromas demonstrates the utility of the Ratner and Clapp NF animal models to select agents for clinical trials," said Annette Bakker, PhD, President and Chief Scientific Officer of the Children's Tumor Foundation. A registration trial of selumetinib for inoperable PN has been developed and will commence enrollment soon.
Neurofibromatosis, or NF, is a genetic disorder that can cause tumors to grow on nerves throughout the body, and may lead to a number of health issues, including deafness, blindness, learning disabilities, bone abnormalities, disabling pain, and sometimes cancer. Neurofibromatosis appears in three possible forms – NF1, NF2, and schwannomatosis – each with its own indications. Today's announcement is most relevant for NF1, which appears in one in 3,000 people. There currently is no cure for NF, but the Foundation's innovative research work is accelerating the path to treatments, as highlighted at its annual NF Conference, the premier gathering of NF experts and leading specialists in related disciplines such as neuroscience and oncology.
In her presentation, Dr. Widemann highlighted that the RAS/RAF/MAPK pathway is activated in NF1 related PNs, and that 16 of 24 patients treated with the MEK inhibitor selumetinib (AZD6244 hydrogen sulfate) saw a tumor volume decrease of ≥ 20% and clinical improvement. This result shows that NF research has made progress not only in the identification of active agents in the preclinical model, but also in the clinic as well.
Additional preclinical and clinical work will be ongoing to direct the future development of agents for NF1 PNs, and a phase II registration trial is in development which will include evaluation of patient reported outcome measures and functional measures, in addition to volumetric MRI analysis to evaluate if PN volume decreases can result in clinical improvement.
"It's very exciting to be able to report this significant clinical progress in the development of effective treatment for NF1," said Dr. Widemann. "NF patients are waiting for results, and through this trial of selumetinib, and the work of Nancy Ratner and Wade Clapp, who highlighted the utility of this model through their work with MEK inhibitors, we're hopeful for the future. I'm especially grateful to the Children's Tumor Foundation, Astra Zeneca, CTEP, the NCI and of course the participating patients for their support and/or funding of NF research, which is resulting in positive results for all patients with NF."
"The success reported today by Dr. Widemann gives us hope", said Annette Bakker, PhD, President and Chief Scientific Officer of the Children's Tumor Foundation. "Our driving focus is on accelerating NF research through innovative collaborations, and Dr. Widemann's incredible work with plexiform neurofibromas is a great example of this model, along with the investments in the preclinical consortia and the partnership with the REiNS Initiative (Response Evaluation in Neurofibromatosis and Schwannomatosis). REiNS provided selection of appropriate patient reported outcomes as well as the functional evaluations of this study. On behalf of the NF community of patients, we give big thanks and congratulations to Dr. Widemann for her success."
Dr. Bakker added, "Today's news is a big step on the path to what we all want – more clinical trials for patients, so they can lead better lives."
To learn more about NF Conference, which runs through Tuesday, June 9, 2015, please visit ctf.org/nfconference.
About Children's Tumor Foundation
The Children's Tumor Foundation is a 501(c)(3) not-for-profit organization dedicated to finding effective treatments for the millions of people worldwide living with neurofibromatosis (NF), a term for three distinct disorders: NF1, NF2, and schwannomatosis. NF can cause tumors to grow on nerves throughout the body and may lead to blindness, bone abnormalities, cancer, deafness, disfigurement, learning disabilities, and excruciating and disabling pain. NF affects one in every 3,000 people, more than cystic fibrosis, Duchenne muscular dystrophy, and Huntington's disease combined. The Children's Tumor Foundation funds critical research into neurofibromatosis. In addition to benefiting those who live with NF, this research is shedding new light on several forms of cancer, brain tumors, bone abnormalities, and learning disabilities, ultimately benefiting the broader community. For more information, please visit http://www.ctf.org.
CONTACT:
Children's Tumor Foundation
Simon Vukelj, VP, Communications
svukelj(at)ctf(dot)org 212-344-7568
For the original version on PRWeb visit: http://www.prweb.com/releases/2015/06/prweb12774808.htm
.
Read more: http://www.benzinga.com/pressreleases/15/06/p5577587/promisi…
Selumetinib/MEK Inhibitor
Promising Results in Tumor Shrinkage Study Announced at Neurofibromatosis Conference
Over half of patients treated with selumetinib in phase I trial see reduction in plexiform neurofibromas
New York, NY (PRWEB) June 08, 2015
As hundreds of the world's leading NF experts convene in Monterey, California for the Children's Tumor Foundation NF Conference, the largest gathering dedicated to neurofibromatosis (NF), it was announced today that for the first time in the history of the treatment of plexiform neurofibromas (PNs), over 50% of patients saw decreased volume in these inoperable tumors. In a presentation titled "The Promise of MEK: Therapeutics for NF1", Brigitte C. Widemann, MD, of the National Cancer Institute (NCI), reported that response data in a phase I trial for children and young adults is showing decreases in tumor volume. Anecdotal improvement in function, and reduction in PN related pain and disfigurement has also been observed.
Plexiform neurofibromas exhibit the most rapid growth in young children, and therefore early intervention in children with growing PNs may result in the greatest clinical benefit. Consistent volume decreases of large PNs has not been reported in the past, and today's announcement indicates a promising future for the development of effective medical therapies for NF1 related PNs.
This highly successful clinical study is the result of a major investment of the Children's Tumor Foundation NF Preclinical Consortium (funded since 2008). Nancy Ratner, PhD and Wade Clapp, MD demonstrated that MEK inhibitors (MEKi) have a massive result on PN tumor volume in mice.
"Today, this very robust effect of MEK inhibitors in mice with neurofibromas demonstrates the utility of the Ratner and Clapp NF animal models to select agents for clinical trials," said Annette Bakker, PhD, President and Chief Scientific Officer of the Children's Tumor Foundation. A registration trial of selumetinib for inoperable PN has been developed and will commence enrollment soon.
Neurofibromatosis, or NF, is a genetic disorder that can cause tumors to grow on nerves throughout the body, and may lead to a number of health issues, including deafness, blindness, learning disabilities, bone abnormalities, disabling pain, and sometimes cancer. Neurofibromatosis appears in three possible forms – NF1, NF2, and schwannomatosis – each with its own indications. Today's announcement is most relevant for NF1, which appears in one in 3,000 people. There currently is no cure for NF, but the Foundation's innovative research work is accelerating the path to treatments, as highlighted at its annual NF Conference, the premier gathering of NF experts and leading specialists in related disciplines such as neuroscience and oncology.
In her presentation, Dr. Widemann highlighted that the RAS/RAF/MAPK pathway is activated in NF1 related PNs, and that 16 of 24 patients treated with the MEK inhibitor selumetinib (AZD6244 hydrogen sulfate) saw a tumor volume decrease of ≥ 20% and clinical improvement. This result shows that NF research has made progress not only in the identification of active agents in the preclinical model, but also in the clinic as well.
Additional preclinical and clinical work will be ongoing to direct the future development of agents for NF1 PNs, and a phase II registration trial is in development which will include evaluation of patient reported outcome measures and functional measures, in addition to volumetric MRI analysis to evaluate if PN volume decreases can result in clinical improvement.
"It's very exciting to be able to report this significant clinical progress in the development of effective treatment for NF1," said Dr. Widemann. "NF patients are waiting for results, and through this trial of selumetinib, and the work of Nancy Ratner and Wade Clapp, who highlighted the utility of this model through their work with MEK inhibitors, we're hopeful for the future. I'm especially grateful to the Children's Tumor Foundation, Astra Zeneca, CTEP, the NCI and of course the participating patients for their support and/or funding of NF research, which is resulting in positive results for all patients with NF."
"The success reported today by Dr. Widemann gives us hope", said Annette Bakker, PhD, President and Chief Scientific Officer of the Children's Tumor Foundation. "Our driving focus is on accelerating NF research through innovative collaborations, and Dr. Widemann's incredible work with plexiform neurofibromas is a great example of this model, along with the investments in the preclinical consortia and the partnership with the REiNS Initiative (Response Evaluation in Neurofibromatosis and Schwannomatosis). REiNS provided selection of appropriate patient reported outcomes as well as the functional evaluations of this study. On behalf of the NF community of patients, we give big thanks and congratulations to Dr. Widemann for her success."
Dr. Bakker added, "Today's news is a big step on the path to what we all want – more clinical trials for patients, so they can lead better lives."
To learn more about NF Conference, which runs through Tuesday, June 9, 2015, please visit ctf.org/nfconference.
About Children's Tumor Foundation
The Children's Tumor Foundation is a 501(c)(3) not-for-profit organization dedicated to finding effective treatments for the millions of people worldwide living with neurofibromatosis (NF), a term for three distinct disorders: NF1, NF2, and schwannomatosis. NF can cause tumors to grow on nerves throughout the body and may lead to blindness, bone abnormalities, cancer, deafness, disfigurement, learning disabilities, and excruciating and disabling pain. NF affects one in every 3,000 people, more than cystic fibrosis, Duchenne muscular dystrophy, and Huntington's disease combined. The Children's Tumor Foundation funds critical research into neurofibromatosis. In addition to benefiting those who live with NF, this research is shedding new light on several forms of cancer, brain tumors, bone abnormalities, and learning disabilities, ultimately benefiting the broader community. For more information, please visit http://www.ctf.org.
CONTACT:
Children's Tumor Foundation
Simon Vukelj, VP, Communications
svukelj(at)ctf(dot)org 212-344-7568
For the original version on PRWeb visit: http://www.prweb.com/releases/2015/06/prweb12774808.htm
.
Read more: http://www.benzinga.com/pressreleases/15/06/p5577587/promisi…
SAGE / MRNS:
Sage hat heute für SAGE-547 überraschende und gute Daten in einem Trial gemeldet, in dem der Wirkstoff bei Patientinnen eingesetzt wurde, die unter einer postpartalen Depression (Wochenbettdepression) litten.
http://de.wikipedia.org/wiki/Postpartale_Stimmungskrisen
In dem Trial wurden vier Patientinnen mit schwerer Depression behandelt. In allen 4 Fällen verschwand die Symptomatik binnen 60 Stunden vollständig.
Hier ein durchaus kritischer Artikel dazu von fierce:
http://www.fiercebiotech.com/story/sage-gets-peek-success-tr…
Für mich ist der Punkt der, dass SAGE-547 einen weiteren - sehr dünnen - Datenpunkt für seine außerordentliche Wirksamkeit geliefert hat und vor allem, dass es nun etwas wahrscheinlicher erscheint, dass man mehr als "nur" Epilepsie adressieren kann.
Der Kurs reagiert deutlich positiv:
5-Tage-Chart:

Zum ersten Mal wird nun scheinbar auch MRNS im Zusammenhang mit SAGE vom Markt wahrgenommen:

Sage hat heute für SAGE-547 überraschende und gute Daten in einem Trial gemeldet, in dem der Wirkstoff bei Patientinnen eingesetzt wurde, die unter einer postpartalen Depression (Wochenbettdepression) litten.
http://de.wikipedia.org/wiki/Postpartale_Stimmungskrisen
In dem Trial wurden vier Patientinnen mit schwerer Depression behandelt. In allen 4 Fällen verschwand die Symptomatik binnen 60 Stunden vollständig.
Hier ein durchaus kritischer Artikel dazu von fierce:
http://www.fiercebiotech.com/story/sage-gets-peek-success-tr…
Für mich ist der Punkt der, dass SAGE-547 einen weiteren - sehr dünnen - Datenpunkt für seine außerordentliche Wirksamkeit geliefert hat und vor allem, dass es nun etwas wahrscheinlicher erscheint, dass man mehr als "nur" Epilepsie adressieren kann.
Der Kurs reagiert deutlich positiv:
5-Tage-Chart:
Zum ersten Mal wird nun scheinbar auch MRNS im Zusammenhang mit SAGE vom Markt wahrgenommen:
Antwort auf Beitrag Nr.: 49.942.260 von SLGramann am 09.06.15 19:38:52Ergänzend noch ein Analystenkommentar:

Von den 4 Millionen Geburten sollte man sich dabei nicht "beeindrucken" lassen. Zum Glück dürften sehr schwere Fälle doch sehr selten sein. Wenn man dann noch Marktanteile usw. berücksichtigt, dann sind wohl kaum mehr als 10.000 bis 20.000 Patientinnen denkbar.
Das wäre aber natürlich dennoch relevant.

Von den 4 Millionen Geburten sollte man sich dabei nicht "beeindrucken" lassen. Zum Glück dürften sehr schwere Fälle doch sehr selten sein. Wenn man dann noch Marktanteile usw. berücksichtigt, dann sind wohl kaum mehr als 10.000 bis 20.000 Patientinnen denkbar.
Das wäre aber natürlich dennoch relevant.
Hallo zusammen,
heute kam eine für mich überraschende Nachricht von SAGE. Ich bin bei SAGE (leider) nicht investiert, habe aber MRNS im Depot.

Ohad Hammer dazu:
SAGE/MRNS, today’s results are very encouraging, only 4 patients but the change is so striking. If I were MRNS I would try to leapfrog SAGE by pursuing this indication with oral ganaxolone. SAGE intends to develop an oral drug for this indication eventually.
Ich finde die Kursreaktionen obgleich man die Ergebnisse natürlich auch als sehr vorläufig betrachten sollte (v.a. keine Placebokontrolle) durchaus nachvollziehbar.
Wäre nicht sogar auch ein Übertrag auf andere Formen der Depression denkbar?
Ich denke das könnte noch ein größeres Thema für SAGE und auch MRNS werden...
Weitere Links zum Thema:
http://www.forbes.com/sites/matthewherper/2015/06/09/promisi…
http://www.fiercebiotech.com/story/sage-gets-peek-success-tr…
Anderes Thema: Letzte Woche war eine Konferenz von Jeffries mit vielen interessante Firmen. Ich stell den Link einfach mal so rein:
http://wsw.com/webcast/jeff88/#table1
SG kmastra
heute kam eine für mich überraschende Nachricht von SAGE. Ich bin bei SAGE (leider) nicht investiert, habe aber MRNS im Depot.

Ohad Hammer dazu:
SAGE/MRNS, today’s results are very encouraging, only 4 patients but the change is so striking. If I were MRNS I would try to leapfrog SAGE by pursuing this indication with oral ganaxolone. SAGE intends to develop an oral drug for this indication eventually.
Ich finde die Kursreaktionen obgleich man die Ergebnisse natürlich auch als sehr vorläufig betrachten sollte (v.a. keine Placebokontrolle) durchaus nachvollziehbar.
Wäre nicht sogar auch ein Übertrag auf andere Formen der Depression denkbar?
Ich denke das könnte noch ein größeres Thema für SAGE und auch MRNS werden...
Weitere Links zum Thema:
http://www.forbes.com/sites/matthewherper/2015/06/09/promisi…
http://www.fiercebiotech.com/story/sage-gets-peek-success-tr…
Anderes Thema: Letzte Woche war eine Konferenz von Jeffries mit vielen interessante Firmen. Ich stell den Link einfach mal so rein:
http://wsw.com/webcast/jeff88/#table1
SG kmastra
REGN
gerade berät die Expertenrunde über eine mögliche FDA-Zulassung von REGNs PCSK9-AK Praluent... offensichtlich haben sie sich für eine Zulassung ausgesprochen (das ist nur eine Empfehlung):
"FDA panel votes 13 to 3 in favor of Praluent $Regn #PCSK9 inhibitor in one or more populations"
Die genaue Auslegung ist aber wohl noch nicht ganz klar... für welche Indikationen ist die Zulassung möglich, z.B. nur high risk Patienten?
Das positive Voting ist zumindest wichtig, als dass so eine Zulassung schon auf Basis der LDL-Senkung vor den Ergebnissen riesiger Langzeitstudien (zum Belegen eines längeren Lebens) möglich ist.
Mal schauen, ob ESPR darauf morgen auch reagiert.
(der REGN-Handel ist ist über den heutigen Tag angehalten)


Gruß
ipollit
gerade berät die Expertenrunde über eine mögliche FDA-Zulassung von REGNs PCSK9-AK Praluent... offensichtlich haben sie sich für eine Zulassung ausgesprochen (das ist nur eine Empfehlung):
"FDA panel votes 13 to 3 in favor of Praluent $Regn #PCSK9 inhibitor in one or more populations"
Die genaue Auslegung ist aber wohl noch nicht ganz klar... für welche Indikationen ist die Zulassung möglich, z.B. nur high risk Patienten?
Das positive Voting ist zumindest wichtig, als dass so eine Zulassung schon auf Basis der LDL-Senkung vor den Ergebnissen riesiger Langzeitstudien (zum Belegen eines längeren Lebens) möglich ist.
Mal schauen, ob ESPR darauf morgen auch reagiert.
(der REGN-Handel ist ist über den heutigen Tag angehalten)
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.942.260 von SLGramann am 09.06.15 19:38:52SAGE / MRNS
Sehr schön! In einer weiteren Indikation Essentieller Tremor sollen ebenfalls in Kürze Daten kommen. Laut Analysten könnten positive Ergebnisse zu einem weiteren Kursschub so wie heute führen.


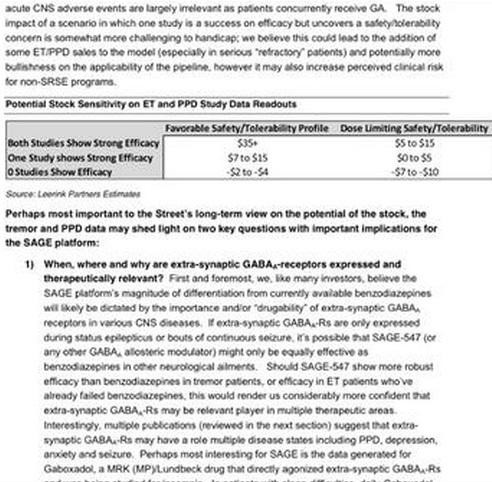
Wie oben steht, hat SAGE-547 aber alleine in der PIII-Indikation SRSE ein Potential von 1,3 Mrd USD in den USA bzw 2 Mrd USD weltweit bei einem geschätzten Marktanteil von 70% in SRSE und 5% in RSE.
Grundsätzlich können die SAGE-Mittel ja auch bei weniger schweren Epilepsie-Fällen zum Einsatz kommen.
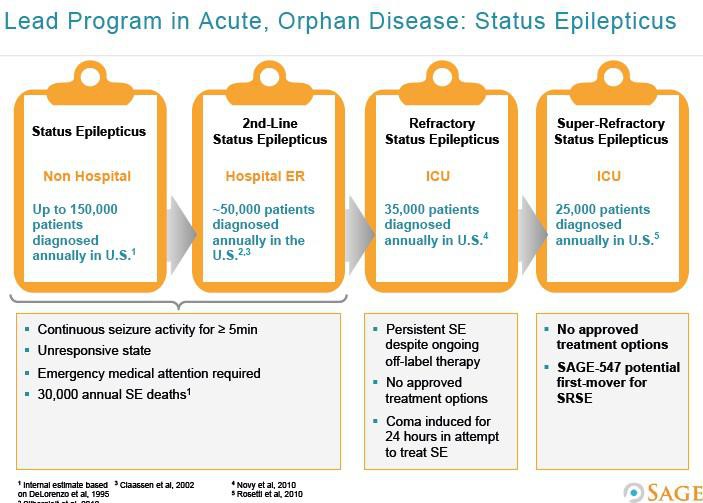
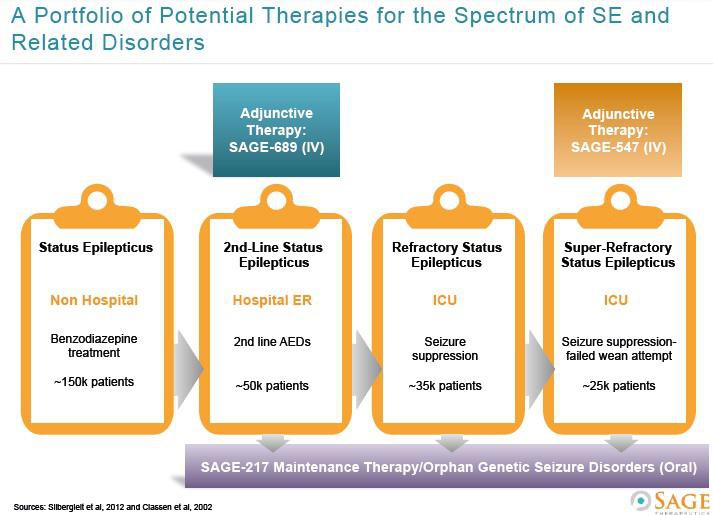

MRNS wird jetzt vielleicht auch interessant aufgrund der niedrigen MK und der oralen Verabreichung...

Gruß
ipollit
Sehr schön! In einer weiteren Indikation Essentieller Tremor sollen ebenfalls in Kürze Daten kommen. Laut Analysten könnten positive Ergebnisse zu einem weiteren Kursschub so wie heute führen.



Wie oben steht, hat SAGE-547 aber alleine in der PIII-Indikation SRSE ein Potential von 1,3 Mrd USD in den USA bzw 2 Mrd USD weltweit bei einem geschätzten Marktanteil von 70% in SRSE und 5% in RSE.
Grundsätzlich können die SAGE-Mittel ja auch bei weniger schweren Epilepsie-Fällen zum Einsatz kommen.


MRNS wird jetzt vielleicht auch interessant aufgrund der niedrigen MK und der oralen Verabreichung...
Gruß
ipollit
Antwort auf Beitrag Nr.: 49.951.554 von kmastra am 10.06.15 21:27:03Hallo kmastra,
ist das Dein aktuelles Depot oder Deine Watchlist?
GLPG haben wir hier ja komplett verpasst. Hab zu dem Wert sogar mal nen Thread eröffnet (vor Jahren). Aber als es dann spannend wurde, war ich nicht mehr dabei...
Gruß
SLG
ist das Dein aktuelles Depot oder Deine Watchlist?
GLPG haben wir hier ja komplett verpasst. Hab zu dem Wert sogar mal nen Thread eröffnet (vor Jahren). Aber als es dann spannend wurde, war ich nicht mehr dabei...

Gruß
SLG
Antwort auf Beitrag Nr.: 49.951.881 von SLGramann am 10.06.15 22:00:59Hallo SLGramann,
nein Sorry hab ich einfach falsch gepostet. Bin wohl mit den Tabs durcheinandergekommen...
Sollte hier hin:
http://www.wallstreet-online.de/diskussion/1190461-1-10/biot…
SG kmastra
P.S. Irgendwie geht es da jetzt nicht mehr zu posten. Schon zweimal versucht!?
nein Sorry hab ich einfach falsch gepostet. Bin wohl mit den Tabs durcheinandergekommen...

Sollte hier hin:
http://www.wallstreet-online.de/diskussion/1190461-1-10/biot…
SG kmastra
P.S. Irgendwie geht es da jetzt nicht mehr zu posten. Schon zweimal versucht!?
BLUE:
Ein Update zur EHA:
http://investor.bluebirdbio.com/phoenix.zhtml?c=251820&p=iro…
Das Entscheidende:
Sickle Cell Disease:
The proportion of anti-sickling hemoglobin being produced by the first-ever patient with severe SCD treated with gene therapy (Subject 1204) is rising steadily and accounted for 45% of all hemoglobin production (40% HbAT87Q + 5% HbF) at the patient’s six-month visit post-drug product infusion; this is above the 30% threshold expected to potentially achieve a disease-modifying clinical effect.
As of May 2015, Subject 1204 had been free of transfusions for more than three months without complications or hospitalizations for SCD-related events post-transplant, and with improvement in hemolysis markers.
Zur Einordnung:
http://www.biotechr.com/search?updated-min=2015-01-01T00:00:…
Wer daran Spaß hat, kann über die 40% HbAT87Q nörgeln. In Wahrheit ist es meiner Meinung nach ein Durchbruch.
Ein Update zur EHA:
http://investor.bluebirdbio.com/phoenix.zhtml?c=251820&p=iro…
Das Entscheidende:
Sickle Cell Disease:
The proportion of anti-sickling hemoglobin being produced by the first-ever patient with severe SCD treated with gene therapy (Subject 1204) is rising steadily and accounted for 45% of all hemoglobin production (40% HbAT87Q + 5% HbF) at the patient’s six-month visit post-drug product infusion; this is above the 30% threshold expected to potentially achieve a disease-modifying clinical effect.
As of May 2015, Subject 1204 had been free of transfusions for more than three months without complications or hospitalizations for SCD-related events post-transplant, and with improvement in hemolysis markers.
Zur Einordnung:
http://www.biotechr.com/search?updated-min=2015-01-01T00:00:…
Wer daran Spaß hat, kann über die 40% HbAT87Q nörgeln. In Wahrheit ist es meiner Meinung nach ein Durchbruch.
Antwort auf Beitrag Nr.: 49.969.032 von SLGramann am 13.06.15 13:49:09Hier die entsprechenden Artikel von The Street und fierce:
http://www.thestreet.com/story/13183966/1/bluebird-sickle-ce…
http://www.fiercebiotech.com/story/bluebird-bio-builds-its-c…
Es macht einfach auch Spaß, wenn man an solchen hoffnungsvollen Fortschritten in gewisser Weise beteiligt ist. Das geht über den finanziellen Aspekt hinaus. Die Sichelzellenanämie ist eine sehr belastende Erbkrankheit, die alle möglichen ständigen Behandlungen erforderlich macht und die Lebenserwartung der Patienten allgemein deutlich verkürzt.
Und hier reden wir jetzt von einer Behandlung, die kurativ oder zumindest quasi-kurativ zu sein scheint.
Natürlich brauchen wir mehr Daten und es ist ja nur ein einziger Patient usw. usf. Aber die Sichelzellenanämie heilt eben nicht einfach mal spontan von selbst. No way. Ich habe deshalb wenig Zweifel daran, dass hier für viele Betroffene, vielleicht für die ganz große Mehrheit, ein Durchbruch erreicht wurde.
Das ist einfach wundervoll!
http://www.thestreet.com/story/13183966/1/bluebird-sickle-ce…
http://www.fiercebiotech.com/story/bluebird-bio-builds-its-c…
Es macht einfach auch Spaß, wenn man an solchen hoffnungsvollen Fortschritten in gewisser Weise beteiligt ist. Das geht über den finanziellen Aspekt hinaus. Die Sichelzellenanämie ist eine sehr belastende Erbkrankheit, die alle möglichen ständigen Behandlungen erforderlich macht und die Lebenserwartung der Patienten allgemein deutlich verkürzt.
Und hier reden wir jetzt von einer Behandlung, die kurativ oder zumindest quasi-kurativ zu sein scheint.
Natürlich brauchen wir mehr Daten und es ist ja nur ein einziger Patient usw. usf. Aber die Sichelzellenanämie heilt eben nicht einfach mal spontan von selbst. No way. Ich habe deshalb wenig Zweifel daran, dass hier für viele Betroffene, vielleicht für die ganz große Mehrheit, ein Durchbruch erreicht wurde.
Das ist einfach wundervoll!
Ohad Hammer mit einigen Änderungen in seinem Depot:
Verkauf von Genmab und MorphoSys
Kauf von XENE, TRVN und OCAT
Ansonsten ist SAGE Thema und sehr interessante Sätze zu IMGN:
http://www.orf-blog.com/biotech-portfolio-update-sage-marinu…
Verkauf von Genmab und MorphoSys
Kauf von XENE, TRVN und OCAT
Ansonsten ist SAGE Thema und sehr interessante Sätze zu IMGN:
http://www.orf-blog.com/biotech-portfolio-update-sage-marinu…
Antwort auf Beitrag Nr.: 49.972.260 von SLGramann am 14.06.15 19:53:39
Die Depotänderungen finde ich absolut nachvollziehbar. Schade finde ich, dass Ohad nicht mehr zu den Neuaufnahmen schreibt. (aber wir sind ja auch nicht bei wünsch dir was )
)
Ich hab mich schon ein wenig mit den Werten beschäftigt, da Ohad sie bereits positive erwähnt hatte, von daher poste hier einfach mal die wenigen gesammelten Infos und Links.
Zu XENE:
Bei Xene stehen in Kürze wichtige Daten von TV-45070 an (Juni/Juli). Von daher ist das erstmal das wichtigeste Ereignis. XENE bekäme Royalties im Bereich niedrige 10-20%. Die kürzlich von mir gepostete Übersicht von SA scheint insgesamt glaubwürdig. Zudem gäbe es für die USA eine Co-Vermarktungsoption (30% der Gewinne). Es handelt sich dabei um eine Salbe, die also lokal wirkt und laut Xenon auch in großer Konzentration in den Körper gelangt. In der Studie wird die Wirksamkeit bei Patienten mit Kniearthrose untersucht.
Bisher gab es mehrere kleinere Studien, die einen positiven Trend aufgezeigt haben aber keine statistische Signifikanz erreicht haben. Jetzt wurden aber 300 Patienten in die Studie aufgenommen...
Hab meine Position hier weiter ausgebaut. Ist sicher nicht ohne Risiko. In Kürze bin ich schlauer!
http://www.sec.gov/Archives/edgar/data/1582313/0001193125143…
https://clinicaltrials.gov/ct2/show/NCT02068599?term=tv-4507…

TRVN:
Auch TRVN ist im Bereich Schmerzen unterwegs und hat vor allem einen Kandidaten, der bei Operationen Morphium ersetzen könnte. Er soll Vorteile in der Wirkung aber auch in den Nebenwirkungen haben. In Q3 stehen auch hier PII Ergebnisse an. Zudem gibt es auch orale Kandidaten, die dann für Schmerzen bzw. Migräne entwickelt werden sollen.

OCAT:
Ist im Bereich Stammzellen aktiv. Eigentlich ein Bereich den ich bisher ausgeklammert habe. Beim Schauen des Vortrags wurde ich aber dann doch positiv überrascht, da es durchaus positive Studienergebnisse gibt. Der CEO scheint mir aber auch ein wenig zu optimistisch, denn es klingt ja fast so als könne er demnächst alles heilen. Kursziel Dausend! Wenn nicht Zweidausend!!

SG kmastra
Zitat von SLGramann: Ohad Hammer mit einigen Änderungen in seinem Depot:
Verkauf von Genmab und MorphoSys
Kauf von XENE, TRVN und OCAT
Ansonsten ist SAGE Thema und sehr interessante Sätze zu IMGN:
http://www.orf-blog.com/biotech-portfolio-update-sage-marinu…
Die Depotänderungen finde ich absolut nachvollziehbar. Schade finde ich, dass Ohad nicht mehr zu den Neuaufnahmen schreibt. (aber wir sind ja auch nicht bei wünsch dir was
 )
) Ich hab mich schon ein wenig mit den Werten beschäftigt, da Ohad sie bereits positive erwähnt hatte, von daher poste hier einfach mal die wenigen gesammelten Infos und Links.
Zu XENE:
Bei Xene stehen in Kürze wichtige Daten von TV-45070 an (Juni/Juli). Von daher ist das erstmal das wichtigeste Ereignis. XENE bekäme Royalties im Bereich niedrige 10-20%. Die kürzlich von mir gepostete Übersicht von SA scheint insgesamt glaubwürdig. Zudem gäbe es für die USA eine Co-Vermarktungsoption (30% der Gewinne). Es handelt sich dabei um eine Salbe, die also lokal wirkt und laut Xenon auch in großer Konzentration in den Körper gelangt. In der Studie wird die Wirksamkeit bei Patienten mit Kniearthrose untersucht.
Bisher gab es mehrere kleinere Studien, die einen positiven Trend aufgezeigt haben aber keine statistische Signifikanz erreicht haben. Jetzt wurden aber 300 Patienten in die Studie aufgenommen...
Hab meine Position hier weiter ausgebaut. Ist sicher nicht ohne Risiko. In Kürze bin ich schlauer!
http://www.sec.gov/Archives/edgar/data/1582313/0001193125143…
https://clinicaltrials.gov/ct2/show/NCT02068599?term=tv-4507…
TRVN:
Auch TRVN ist im Bereich Schmerzen unterwegs und hat vor allem einen Kandidaten, der bei Operationen Morphium ersetzen könnte. Er soll Vorteile in der Wirkung aber auch in den Nebenwirkungen haben. In Q3 stehen auch hier PII Ergebnisse an. Zudem gibt es auch orale Kandidaten, die dann für Schmerzen bzw. Migräne entwickelt werden sollen.
OCAT:
Ist im Bereich Stammzellen aktiv. Eigentlich ein Bereich den ich bisher ausgeklammert habe. Beim Schauen des Vortrags wurde ich aber dann doch positiv überrascht, da es durchaus positive Studienergebnisse gibt. Der CEO scheint mir aber auch ein wenig zu optimistisch, denn es klingt ja fast so als könne er demnächst alles heilen. Kursziel Dausend! Wenn nicht Zweidausend!!
SG kmastra
Habe letzte Woche vor der Entscheidung zwischen XENE oder TRVN gestanden. Habe mich
letztlich für TRVN entschieden. Hier steht in den nächsten 12 Monaten eine wichtige
Entscheidung bezüglich TRV027 an. Actavis könnte sich per Option nach vollendeter
Phase IIb für 65m Dollar die weltweiten Rechte sichern.
letztlich für TRVN entschieden. Hier steht in den nächsten 12 Monaten eine wichtige
Entscheidung bezüglich TRV027 an. Actavis könnte sich per Option nach vollendeter
Phase IIb für 65m Dollar die weltweiten Rechte sichern.
Wow. Das hatte ich so auch noch nie.  Habe mir heute aufgrund eines sehr guten/positiven Berichtes von Alfredo Fontanini dann doch noch eine kleine Position AAVL gekauft. War da nach dem AERI Desaster vorsichtig.
Habe mir heute aufgrund eines sehr guten/positiven Berichtes von Alfredo Fontanini dann doch noch eine kleine Position AAVL gekauft. War da nach dem AERI Desaster vorsichtig.
http://www.thestreet.com/story/13182199/1/avalanche-bio-gene…
Grad kam die Meldung - denke das sieht ganz gut aus.
http://finance.yahoo.com/news/avalanche-biotechnologies-inc-…
Und irgendwie schließt sich der Kreis, da auch Aeri mit einer guten Nachricht zu gefallen weiß und die laufende Studie anpassen darf:
http://finance.yahoo.com/news/aerie-pharmaceuticals-receives…
 Habe mir heute aufgrund eines sehr guten/positiven Berichtes von Alfredo Fontanini dann doch noch eine kleine Position AAVL gekauft. War da nach dem AERI Desaster vorsichtig.
Habe mir heute aufgrund eines sehr guten/positiven Berichtes von Alfredo Fontanini dann doch noch eine kleine Position AAVL gekauft. War da nach dem AERI Desaster vorsichtig.http://www.thestreet.com/story/13182199/1/avalanche-bio-gene…
Grad kam die Meldung - denke das sieht ganz gut aus.
http://finance.yahoo.com/news/avalanche-biotechnologies-inc-…
Und irgendwie schließt sich der Kreis, da auch Aeri mit einer guten Nachricht zu gefallen weiß und die laufende Studie anpassen darf:
http://finance.yahoo.com/news/aerie-pharmaceuticals-receives…
Antwort auf Beitrag Nr.: 49.979.331 von kmastra am 15.06.15 22:22:0950% Reduction bei den Rescue Injections... das ist ok, aber leider nicht berauschend... Ohad meinte wenn ich mich korrekt erinnere 60% wäre er enttäuscht, was die Erwartung von Jeffries war... nachbörslich sehr volatil, aber leider rot... was nicht sehr überraschend ist bei diesen wie es scheint insgesamt durchwachsenen Daten.
Tja man lernt nie aus. AAVL verliert nachbörslich sogar deutlich. Von daher möchte ich die Farbe des Smileys im Vorpost in rot umändern. Mir ist ehrlich gesagt nicht so ganz klar, warum der Markt nachbörslich so reagiert. Was stimmt denn an den Ergebnissen nicht? Mal sehen wie das morgen ausschaut...
Antwort auf Beitrag Nr.: 49.979.391 von kmastra am 15.06.15 22:32:46Zusätzlich ist die Netzhautdicke in der Kontrollgruppe sogar geringer geworden, während sie in der AVA 101 Gruppe sogar zunahm... zu erwarten wäre das Gegenteil... sehr seltsam... war die Kontrollgruppe so "schlecht" dran?
Naja, das entscheidende bleibt denke ich, dass die Reduktion von 4 auf 2 Rescue Injections einfach schon etwas untern den Erwartungen liegt... von 4 auf 1 wäre super gewesen.
Naja, das entscheidende bleibt denke ich, dass die Reduktion von 4 auf 2 Rescue Injections einfach schon etwas untern den Erwartungen liegt... von 4 auf 1 wäre super gewesen.
Antwort auf Beitrag Nr.: 49.979.448 von SpanishEyes am 15.06.15 22:41:03Wenn ich das Ergebnis richtig deute, dann gab es im Kontrollarm eine einzige Person (von den 11), die aus irgendwelchen Gründen bombig abgeschnitten hat (=9,1%). Nach dieser Person scheint im Kontrollarm lange nichts mehr zu kommen. Ohne diese eine Person wären die ausgewiesenen prozentualen Unterschiede sehr viel imposanter gewesen...der Median von immerhin 2 rescues bleibt natürlich leider...
AAVL:
Tja, die Daten sind wirklich schwach und unklar. Was man positiv sagen kann, ist, dass da wohl doch ein Signal ist.
Mein Bauchgefühl ist, dass AVA-101 bei bestimmten Patienten besser wirkt, als bei anderen. Es gibt die guten P Ib-Daten und auch in der doch recht misslungenen PIIa gibt es ja einige Patienten, bei denen sich eine signifikante Verringerung der rescue injections ergeben hat (Specifically, 23.8 percent (treated) vs. 9.1 percent (control) maintained stable vision with ≤1 rescue injections).
Vielleicht wird es in Zukunft darauf ankommen herauszufinden, ob AVA-101 bei bestimmten Patienten besser wirkt als bei anderen und warum dies ggf. so ist. Man könnte dann entsprechend sinnvoll selektieren.
Es gibt nun jedenfalls jede Menge offener Fragen und viele Probleme mit diesem Projekt.
Den Kursrückgang um 50% halte ich für angemessen.
Ich selbst verkaufe meine Position jetzt nicht.
Tja, die Daten sind wirklich schwach und unklar. Was man positiv sagen kann, ist, dass da wohl doch ein Signal ist.
Mein Bauchgefühl ist, dass AVA-101 bei bestimmten Patienten besser wirkt, als bei anderen. Es gibt die guten P Ib-Daten und auch in der doch recht misslungenen PIIa gibt es ja einige Patienten, bei denen sich eine signifikante Verringerung der rescue injections ergeben hat (Specifically, 23.8 percent (treated) vs. 9.1 percent (control) maintained stable vision with ≤1 rescue injections).
Vielleicht wird es in Zukunft darauf ankommen herauszufinden, ob AVA-101 bei bestimmten Patienten besser wirkt als bei anderen und warum dies ggf. so ist. Man könnte dann entsprechend sinnvoll selektieren.
Es gibt nun jedenfalls jede Menge offener Fragen und viele Probleme mit diesem Projekt.
Den Kursrückgang um 50% halte ich für angemessen.
Ich selbst verkaufe meine Position jetzt nicht.
Antwort auf Beitrag Nr.: 49.986.126 von SLGramann am 16.06.15 19:08:36Lohnt da deiner Meinung nach ein Einstig bei AAVL auf diesem Niveau?
RCPT
bisher bin ich noch nicht dabei... anscheinend steht RCPT aber bei vielen Pharmas auf der Liste, so dass ich überlege, vielleicht doch noch einzusteigen trotz einer bereits beachtlichen MK von fast 6 Mrd USD.
Wie realistisch sind solche Zahlen?


Gruß
ipollit
bisher bin ich noch nicht dabei... anscheinend steht RCPT aber bei vielen Pharmas auf der Liste, so dass ich überlege, vielleicht doch noch einzusteigen trotz einer bereits beachtlichen MK von fast 6 Mrd USD.
Wie realistisch sind solche Zahlen?

Gruß
ipollit
AAVL:
Wer investiert ist hat vielleicht gestern auch den CC bzw das Ganze über Twitter etc. verfolgt. Neben den Daten dürfte auch der wirklich gruselige CC den Kurs nochmal nach Unten bewegt haben.
Bedenklich fand ich, dass die Herren die Fragen oft nicht einmal mehr frei beantworten konnten. Das sollte doch möglich sein!
Es wurde keine PPPräsentation etc. oder gar aufbearbeitete Daten, Erklärungen geboten.
Es gab keine Erklärung für die Frage nach der Netzhautdicke. Eigentlich scheint die Antwort bei dem Unterschied auch ziemlich offensichtlich und ist beunruhigend.
Was mich schon öfter gestört hat und auch hier wieder der Fall war: Einige Nachrichtenagenturen haben die Ergebnisse schon vorher bekommen (warum ist das eigentlich gängige Praxis? Ist es zu viel verlangt, dass die Medien dann darüber berichten, wenn etwas passiert?) Der Kurs hatte unter erhöhtem Volumen schon vorher um 6% nachgegeben. Zufall? Sicher nicht!
Insgesamt: Über 50% Minus in weniger als 24 Stunden. Es war natürlich aber klar, dass das Risiko hoch war und von daher hatte ich anders als bei AERI eine kleine Position.
AERI:
Ich habe heute meine Position in Gänze verkauft. Bin hier nochmal mit einem blauen Auge davon gekommen, weil ich nochmal nachgekauft hatte. Grundsätzliche Probleme sind trotz der Anpassungen natürlich geblieben.
Ich denke das größte Plus ist aber der große Bedarf und die doch eher geringe Konkurrenz. Von daher würde ich ggf. auch wieder einsteigen...aber wenn überhaupt nur mit einer Miniposition in die Präsentation gehen!



SG kmastra
Wer investiert ist hat vielleicht gestern auch den CC bzw das Ganze über Twitter etc. verfolgt. Neben den Daten dürfte auch der wirklich gruselige CC den Kurs nochmal nach Unten bewegt haben.
Bedenklich fand ich, dass die Herren die Fragen oft nicht einmal mehr frei beantworten konnten. Das sollte doch möglich sein!
Es wurde keine PPPräsentation etc. oder gar aufbearbeitete Daten, Erklärungen geboten.
Es gab keine Erklärung für die Frage nach der Netzhautdicke. Eigentlich scheint die Antwort bei dem Unterschied auch ziemlich offensichtlich und ist beunruhigend.
Was mich schon öfter gestört hat und auch hier wieder der Fall war: Einige Nachrichtenagenturen haben die Ergebnisse schon vorher bekommen (warum ist das eigentlich gängige Praxis? Ist es zu viel verlangt, dass die Medien dann darüber berichten, wenn etwas passiert?) Der Kurs hatte unter erhöhtem Volumen schon vorher um 6% nachgegeben. Zufall? Sicher nicht!
Insgesamt: Über 50% Minus in weniger als 24 Stunden. Es war natürlich aber klar, dass das Risiko hoch war und von daher hatte ich anders als bei AERI eine kleine Position.
AERI:
Ich habe heute meine Position in Gänze verkauft. Bin hier nochmal mit einem blauen Auge davon gekommen, weil ich nochmal nachgekauft hatte. Grundsätzliche Probleme sind trotz der Anpassungen natürlich geblieben.
Ich denke das größte Plus ist aber der große Bedarf und die doch eher geringe Konkurrenz. Von daher würde ich ggf. auch wieder einsteigen...aber wenn überhaupt nur mit einer Miniposition in die Präsentation gehen!



SG kmastra
Antwort auf Beitrag Nr.: 49.986.621 von fisch29 am 16.06.15 20:02:48"Lohnt da deiner Meinung nach ein Einstig bei AAVL auf diesem Niveau?"
Gemeine Frage...
Die Logik gebietet, dass, wer eine Aktie auf einem bestimmten Niveau hält, sie auf diesem Niveau auch als kaufenswert ansehen muss. Die Aussage: "Halten kann man sie, aber kaufen würde ich sie auf dem Niveau nicht" ist letztlich ziemlich sinnfrei. Trotzdem ist genau das meine persönliche Antwort. Ich halte die Aktie weiterhin. Aber, nein, ich würde sie jetzt nicht neu kaufen.
Womit bewiesen ist, dass ich kein logisch handelnder Mensch bin.
Gemeine Frage...

Die Logik gebietet, dass, wer eine Aktie auf einem bestimmten Niveau hält, sie auf diesem Niveau auch als kaufenswert ansehen muss. Die Aussage: "Halten kann man sie, aber kaufen würde ich sie auf dem Niveau nicht" ist letztlich ziemlich sinnfrei. Trotzdem ist genau das meine persönliche Antwort. Ich halte die Aktie weiterhin. Aber, nein, ich würde sie jetzt nicht neu kaufen.
Womit bewiesen ist, dass ich kein logisch handelnder Mensch bin.

Antwort auf Beitrag Nr.: 49.987.329 von SLGramann am 16.06.15 21:25:30nun, es kann durchaus logisch sein, zu halten und vom Kauf abzuraten, jedenfalls wenn man im Gewinn ist, denn es gibt ja Gebühren und Steuern.
Wenn ich also davon ausgehe, dass die Aktie vielleicht noch etwas fällt, würde ich (noch) nicht kaufen. Wenn ich sie schon habe und den Gewinn versteuern muss und noch Gebühren anfallen für den Handel, müsste sie ja nicht nur "etwas fallen", damit ich sie wirklich billiger bekomme als zum jetzigen Verkauf.
Bei einer Aktie im Verlust kann es sich dagegen durchaus lohnen, sie mal zwischendurch zu verkaufen, weil man dadurch die Verluste mit Gewinnen andersow verrechnen kann.
Wenn ich also davon ausgehe, dass die Aktie vielleicht noch etwas fällt, würde ich (noch) nicht kaufen. Wenn ich sie schon habe und den Gewinn versteuern muss und noch Gebühren anfallen für den Handel, müsste sie ja nicht nur "etwas fallen", damit ich sie wirklich billiger bekomme als zum jetzigen Verkauf.
Bei einer Aktie im Verlust kann es sich dagegen durchaus lohnen, sie mal zwischendurch zu verkaufen, weil man dadurch die Verluste mit Gewinnen andersow verrechnen kann.
SGYP:
Die erste PIII in der Indikation CIC war ein voller Erfolg.
Vor allem sieht das NW-Profil noch besser aus, als in der PII.
http://ir.synergypharma.com/press-releases/detail/1788/syner…
Cantor:

Kurs ist deutlich im Plus:

Ich denke nicht, dass die Aktie jetzt zu teuer ist. Man kann sich wahrscheinlich über ein deutlich besseres NW-Profil vom Konkurrenten Linzess absetzen.
In Zukunft wird die Frage einer Verpartnerung zu klären sein - es sei denn, es kommt gleich zu einer Übernahme.
Die erste PIII in der Indikation CIC war ein voller Erfolg.
Vor allem sieht das NW-Profil noch besser aus, als in der PII.
http://ir.synergypharma.com/press-releases/detail/1788/syner…
Cantor:

Kurs ist deutlich im Plus:
Ich denke nicht, dass die Aktie jetzt zu teuer ist. Man kann sich wahrscheinlich über ein deutlich besseres NW-Profil vom Konkurrenten Linzess absetzen.
In Zukunft wird die Frage einer Verpartnerung zu klären sein - es sei denn, es kommt gleich zu einer Übernahme.
NBI & XBI heute mit neuem Allzeithoch... der Aufwärtstrend scheint noch etwas Bestand zu haben


Gruß
ipollit
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.004.933 von ipollit am 18.06.15 20:36:49gleiches gilt für den Nasdaq, auch ein neues Allzeithoch... mehr als 15 Jahre hat es gedauert

Gruß
ipollit
Gruß
ipollit
guten abend,
nochmal eine weitere frage an die bio- oder medizintechnologie erfahrenen
wenn eine biotechnologiefirma ihr medikament -was immer es sein mag- an den markt bringt -lässt es sich mit statistischen/erfahrungswerten uuungefähr sagen wie lange es dauert bis sie quasi zu den "peak sales" oder einem, rückwirkend betrachtet, repräsentativen durchschnittsninveau kommen?
also was ich weiss das ist ja teilweise schon sehr, sehr kompliziert, kann sich lange hinziehen, und of nicht ganz so einfach wie in den "schönen presentationen"
darüberhinaus, was ich bisher mitbekommen habe, scheint die logistik -(auch)wenn das medikament schon zugelassen ist, für sich folgend ergebende aufgaben- ja einer DER "make or break" gründe zu sein(in der Folge bei mir auch eine hohe gewichtung, ("einfach")zulassung ist nicht alles)
wenn dazu jemand was sagen könnte wäre sehr nett, weil das bei mir schon eine nicht ganz kleine relevanz annehmen dürfte
muss nichts exaktes sein
schönen abend
P.
nochmal eine weitere frage an die bio- oder medizintechnologie erfahrenen
wenn eine biotechnologiefirma ihr medikament -was immer es sein mag- an den markt bringt -lässt es sich mit statistischen/erfahrungswerten uuungefähr sagen wie lange es dauert bis sie quasi zu den "peak sales" oder einem, rückwirkend betrachtet, repräsentativen durchschnittsninveau kommen?
also was ich weiss das ist ja teilweise schon sehr, sehr kompliziert, kann sich lange hinziehen, und of nicht ganz so einfach wie in den "schönen presentationen"
darüberhinaus, was ich bisher mitbekommen habe, scheint die logistik -(auch)wenn das medikament schon zugelassen ist, für sich folgend ergebende aufgaben- ja einer DER "make or break" gründe zu sein(in der Folge bei mir auch eine hohe gewichtung, ("einfach")zulassung ist nicht alles)
wenn dazu jemand was sagen könnte wäre sehr nett, weil das bei mir schon eine nicht ganz kleine relevanz annehmen dürfte
muss nichts exaktes sein
schönen abend
P.
Antwort auf Beitrag Nr.: 50.017.182 von Popeye82 am 20.06.15 22:26:41"wie lange es dauert bis sie quasi zu den "peak sales" oder einem, rückwirkend betrachtet, repräsentativen durchschnittsninveau kommen?"
Meiner Meinung nach kann man das nicht sinnvoll beantworten. Einen Durchschnittswert könnte man sicher berechnen, wenn man genug Daten hat, aber der würde für konkrete Fälle nichts aussagen.
Die Antwort wäre immer: Es kommt darauf an.
Wie dringend ist der medizinische Bedarf? (gibt es alternative, bereits etablierte Wirkstoffe?) Wie schwer ist der Krankheitsverlauf? (absehbar tödlich oder nur chronisch?) Wie gut ist die Wirkung des Wirkstoffs? Wie stark sind die Nebenwirkungen? Aus all dem folgt die Frage: Wie überzeugt ist die Ärzteschaft von dem Sinn und Nutzen des Präparats?
Wenn es ein Produkt ist, dass in bereits behandelbaren und eher chronischen Indikationen entwickelt wird, dann kommt es auch auf die Vermarktungspower an (Ärzte werden dann von den Mitarbeitern des Pharmakonzerns entsprechend bearbeitet -> "Pharmareferenten" in Deutschland).
Dann ist die Frage wichtig, wann die Zulassungen in welchen Märkten erfolgen. Ein in den USA zugelassenes Medikament darf noch lange nicht in Europa, Japan oder sonstwo verkauft werden. Also muss man auch die dortigen Zulassungsprozeduren durchlaufen.
Entscheidend kann auch die Frage sein, ob ein Wirkstoff erst in einer Indikation zugelassen wird und dann in weiteren, anderen Indikationen ebenfalls wirkt und zugelassen wird (oft der Fall im Onkologiebereich oder bei Autoimmunerkrankungen).
Im Ergebnis: Das Peaksale-Niveau erreicht man vermutlich im Zeitraum zwischen 6 Monaten und 15 Jahren nach Zulassung - je nach dem...
Meiner Meinung nach kann man das nicht sinnvoll beantworten. Einen Durchschnittswert könnte man sicher berechnen, wenn man genug Daten hat, aber der würde für konkrete Fälle nichts aussagen.
Die Antwort wäre immer: Es kommt darauf an.
Wie dringend ist der medizinische Bedarf? (gibt es alternative, bereits etablierte Wirkstoffe?) Wie schwer ist der Krankheitsverlauf? (absehbar tödlich oder nur chronisch?) Wie gut ist die Wirkung des Wirkstoffs? Wie stark sind die Nebenwirkungen? Aus all dem folgt die Frage: Wie überzeugt ist die Ärzteschaft von dem Sinn und Nutzen des Präparats?
Wenn es ein Produkt ist, dass in bereits behandelbaren und eher chronischen Indikationen entwickelt wird, dann kommt es auch auf die Vermarktungspower an (Ärzte werden dann von den Mitarbeitern des Pharmakonzerns entsprechend bearbeitet -> "Pharmareferenten" in Deutschland).
Dann ist die Frage wichtig, wann die Zulassungen in welchen Märkten erfolgen. Ein in den USA zugelassenes Medikament darf noch lange nicht in Europa, Japan oder sonstwo verkauft werden. Also muss man auch die dortigen Zulassungsprozeduren durchlaufen.
Entscheidend kann auch die Frage sein, ob ein Wirkstoff erst in einer Indikation zugelassen wird und dann in weiteren, anderen Indikationen ebenfalls wirkt und zugelassen wird (oft der Fall im Onkologiebereich oder bei Autoimmunerkrankungen).
Im Ergebnis: Das Peaksale-Niveau erreicht man vermutlich im Zeitraum zwischen 6 Monaten und 15 Jahren nach Zulassung - je nach dem...

MCRB:
Nächste Woche wird es wohl den IPO von Seres Therapeutics geben.
Derzeit zeichnet sich eine Marktkapitalisierung von ca. 650 Millionen Dollar ab.
IPO-Preis derzeit bei 17 Dollar vorgesehen
37,591,002 shares if the underwriters exercise their option to purchase additional shares in full
Ich gehe davon aus, dass der Preis noch angehoben werden wird. Dieser IPO gilt als heiß und ich finde, zu recht.
Unternehmen:
http://serestherapeutics.com/about/about_seres_therapeutics/
S1-File:
http://www.sec.gov/Archives/edgar/data/1609809/0001193125152…
Roadshow:
http://www.retailroadshow.com/sys/launch.asp?k=911749342
Das ist hier Grundthema:
We are a microbiome therapeutics platform company developing a novel class of biological drugs, which we refer to as Ecobiotic microbiome therapeutics. The human microbiome is an ecology of microorganisms, including bacteria, fungi and viruses, that, when unhealthy, or dysbiotic, can leave the body more susceptible to infections, metabolic disorders, allergies, autoimmune disease, inflammation and other conditions.
Auszüge aus dem S1:
Clostridium difficile Infection, or CDI
The CDC has identified C. difficile as one of the top three most urgent antibiotic-resistant bacterial threats in the United States. It is the most common cause of hospital acquired infection in the United States, having overtaken MRSA. CDI is responsible for the deaths of approximately 29,000 Americans each year.
we estimate that the addressable population of patients in the United States with recurrent CDI, defined as patients who have experienced at least three occurrences of CDI in the past nine months, is between 85,000 and 110,000 patients per year.
SER-109
SER-109 is a bacterial spore ecology consisting of an average of 50 bacterial species derived from healthy donors’ fecal matter that is designed to prevent further recurrences of CDI in patients suffering from recurrent CDI by restoring a dysbiotic microbiome to a state of health.
Phase 1b/2 clinical study results - Efficacy.
Twenty-six of 30 patients, or 87% of patients, in the Phase 1b/2 clinical study achieved the primary efficacy endpoint of experiencing no recurrence of CDI during the eight weeks post-treatment.
-------
Das ganze Konzept ist also verwandt mit dem Thema "Fäkaltransplantation".
Klingt für den einen oder anderen vielleicht komisch oder "witzig". Aber erstens gibt es in unserer Branche überhaupt nichts witziges und zweitens hat das tatsächlich schon Menschen geholfen:
https://de.wikipedia.org/wiki/Stuhltransplantation
Natürlich ist es ganz offensichtlich, warum es Sinn macht, das zu standardisieren und in eine Tabletten bzw. Kapselform zu überführen.
Auch die FDA hält das alles wohl keineswegs für einen "Witz":
Cam, Massachusetts — June 12, 2015
Cambridge, Mass., June 12, 2015 – Seres Therapeutics, Inc., a leading microbiome therapeutics platform company, today announced that SER-109 (Firmacute Eubacterial Spores, Purified Suspension, Encapsulated), its lead product candidate under investigation for the prevention of recurrent Clostridium difficile infection (CDI) in adults, has been granted breakthrough therapy designation by the U.S. Food and Drug Administration (FDA).
----------
Das Gegenteil ist der Fall - abgesehen vom Thema CDI droht sogar das "microbiome-Ding" zum nächsten Hype zu werden, weil es ein völlig neuer Ansatz ist, mit dem man alle möglichen Erkrankungen angehen könnte.
-----------
Ich werde mich auf jeden Fall beteiligen, solange die Marktkapitalisierung unter 1 Mrd. bleibt.
Nächste Woche wird es wohl den IPO von Seres Therapeutics geben.
Derzeit zeichnet sich eine Marktkapitalisierung von ca. 650 Millionen Dollar ab.
IPO-Preis derzeit bei 17 Dollar vorgesehen
37,591,002 shares if the underwriters exercise their option to purchase additional shares in full
Ich gehe davon aus, dass der Preis noch angehoben werden wird. Dieser IPO gilt als heiß und ich finde, zu recht.
Unternehmen:
http://serestherapeutics.com/about/about_seres_therapeutics/
S1-File:
http://www.sec.gov/Archives/edgar/data/1609809/0001193125152…
Roadshow:
http://www.retailroadshow.com/sys/launch.asp?k=911749342
Das ist hier Grundthema:
We are a microbiome therapeutics platform company developing a novel class of biological drugs, which we refer to as Ecobiotic microbiome therapeutics. The human microbiome is an ecology of microorganisms, including bacteria, fungi and viruses, that, when unhealthy, or dysbiotic, can leave the body more susceptible to infections, metabolic disorders, allergies, autoimmune disease, inflammation and other conditions.
Auszüge aus dem S1:
Clostridium difficile Infection, or CDI
The CDC has identified C. difficile as one of the top three most urgent antibiotic-resistant bacterial threats in the United States. It is the most common cause of hospital acquired infection in the United States, having overtaken MRSA. CDI is responsible for the deaths of approximately 29,000 Americans each year.
we estimate that the addressable population of patients in the United States with recurrent CDI, defined as patients who have experienced at least three occurrences of CDI in the past nine months, is between 85,000 and 110,000 patients per year.
SER-109
SER-109 is a bacterial spore ecology consisting of an average of 50 bacterial species derived from healthy donors’ fecal matter that is designed to prevent further recurrences of CDI in patients suffering from recurrent CDI by restoring a dysbiotic microbiome to a state of health.
Phase 1b/2 clinical study results - Efficacy.
Twenty-six of 30 patients, or 87% of patients, in the Phase 1b/2 clinical study achieved the primary efficacy endpoint of experiencing no recurrence of CDI during the eight weeks post-treatment.
-------
Das ganze Konzept ist also verwandt mit dem Thema "Fäkaltransplantation".
Klingt für den einen oder anderen vielleicht komisch oder "witzig". Aber erstens gibt es in unserer Branche überhaupt nichts witziges und zweitens hat das tatsächlich schon Menschen geholfen:
https://de.wikipedia.org/wiki/Stuhltransplantation
Natürlich ist es ganz offensichtlich, warum es Sinn macht, das zu standardisieren und in eine Tabletten bzw. Kapselform zu überführen.
Auch die FDA hält das alles wohl keineswegs für einen "Witz":
Cam, Massachusetts — June 12, 2015
Cambridge, Mass., June 12, 2015 – Seres Therapeutics, Inc., a leading microbiome therapeutics platform company, today announced that SER-109 (Firmacute Eubacterial Spores, Purified Suspension, Encapsulated), its lead product candidate under investigation for the prevention of recurrent Clostridium difficile infection (CDI) in adults, has been granted breakthrough therapy designation by the U.S. Food and Drug Administration (FDA).
----------
Das Gegenteil ist der Fall - abgesehen vom Thema CDI droht sogar das "microbiome-Ding" zum nächsten Hype zu werden, weil es ein völlig neuer Ansatz ist, mit dem man alle möglichen Erkrankungen angehen könnte.
-----------
Ich werde mich auf jeden Fall beteiligen, solange die Marktkapitalisierung unter 1 Mrd. bleibt.
EPZM:
Epizyme hat auf der ICML in Lugano reifere Daten ihres EZH2-inhibitors tazemetostat (EPZ-6438) präsentiert.
Diese sehen für mich sehr ordentlich aus und werden im Netz bisher wohl auch positiv besprochen.
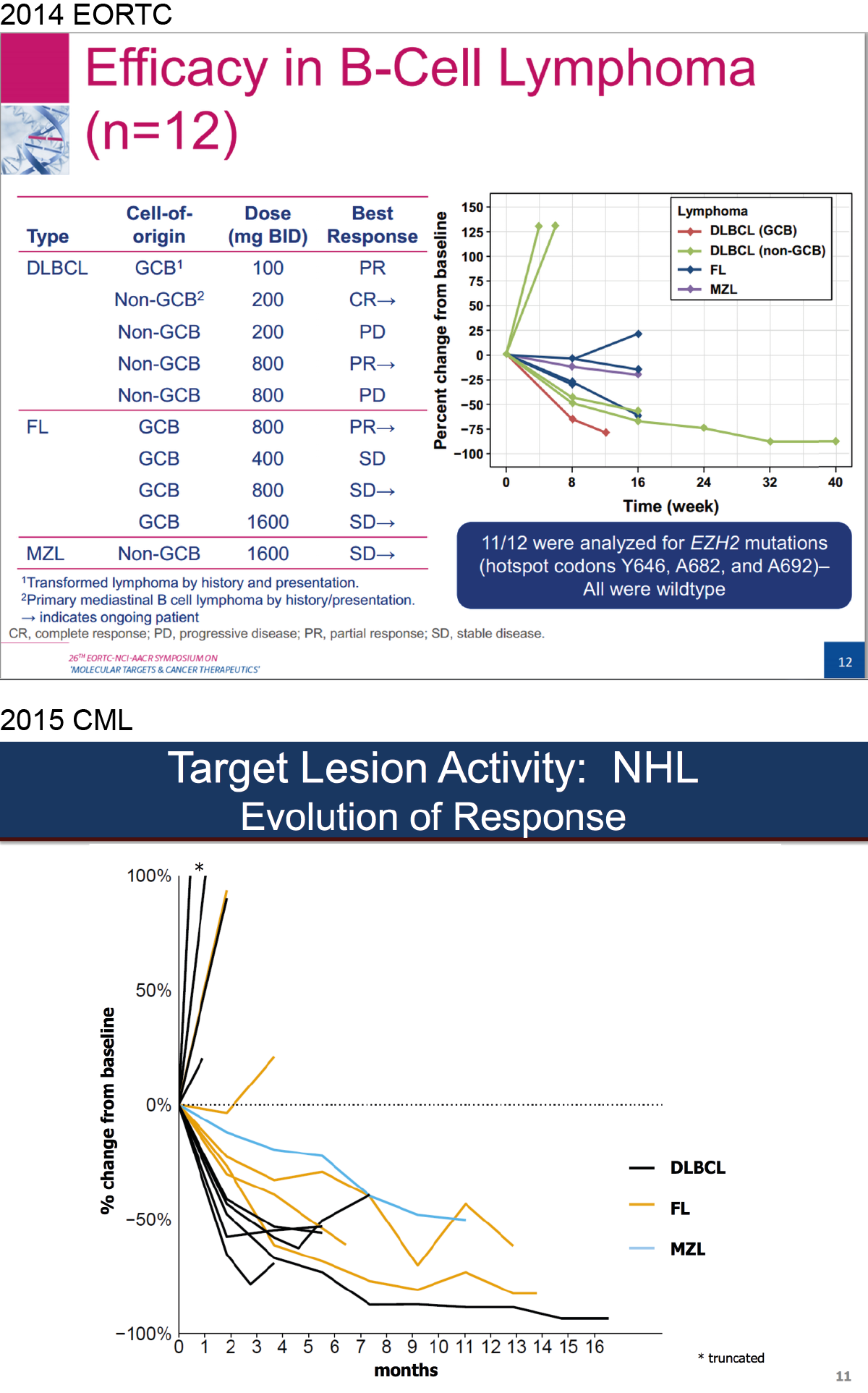
The NHL patients enrolled on study were heavily pre-treated, with 85 percent of patients having received three or more prior therapies and 37 percent of patients having received more than five or more prior therapies. Thirty-seven percent of patients were refractory to their last prior regimen and 26 percent of patients had received a prior autologous hematopoietic stem cell transplant.
Pressemeldung:
http://www.epizyme.com/wp-content/uploads/2015/06/EPZM_News_…
Hier die Präsentation:
http://www.epizyme.com/wp-content/uploads/2015/06/ICML-Slide…
Blog von Garrett Rhyasen:
http://oncologydiscovery.com/2015/06/20/epizyme-provides-upd…
Was ist davon zu halten?
ipollit, kannst Du das näher einschätzen?
Gruß
SLG
Epizyme hat auf der ICML in Lugano reifere Daten ihres EZH2-inhibitors tazemetostat (EPZ-6438) präsentiert.
Diese sehen für mich sehr ordentlich aus und werden im Netz bisher wohl auch positiv besprochen.

The NHL patients enrolled on study were heavily pre-treated, with 85 percent of patients having received three or more prior therapies and 37 percent of patients having received more than five or more prior therapies. Thirty-seven percent of patients were refractory to their last prior regimen and 26 percent of patients had received a prior autologous hematopoietic stem cell transplant.
Pressemeldung:
http://www.epizyme.com/wp-content/uploads/2015/06/EPZM_News_…
Hier die Präsentation:
http://www.epizyme.com/wp-content/uploads/2015/06/ICML-Slide…
Blog von Garrett Rhyasen:
http://oncologydiscovery.com/2015/06/20/epizyme-provides-upd…
Was ist davon zu halten?
ipollit, kannst Du das näher einschätzen?
Gruß
SLG
Antwort auf Beitrag Nr.: 50.017.458 von SLGramann am 21.06.15 07:49:53
Danke
auf so eine Antwort hatte ich gehofft

gruß
P.
Danke
Zitat von SLGramann: Im Ergebnis: Das Peaksale-Niveau erreicht man vermutlich im Zeitraum zwischen 6 Monaten und 15 Jahren nach Zulassung - je nach dem...
auf so eine Antwort hatte ich gehofft


gruß
P.
Ohad Hammer mit allgemeinen Betrachtungen zum Biotech-Markt.
In der Konsequenz hedgt er sein Depot erstmals mit einer short-Position:
http://www.orf-blog.com/are-biotech-valuations-sustainable/
(Ich finde, dass er mit vielem Recht hat, vor allem was die Übernahmeprämien und die ständigen Preiserhöhungen angeht. Die Frage ist, wann sich gegen Letzteres mal substanzieller Widerstand in den USA formiert. Über lange Zeit kann das so sicher nicht weitergehen.)
In der Konsequenz hedgt er sein Depot erstmals mit einer short-Position:
http://www.orf-blog.com/are-biotech-valuations-sustainable/
(Ich finde, dass er mit vielem Recht hat, vor allem was die Übernahmeprämien und die ständigen Preiserhöhungen angeht. Die Frage ist, wann sich gegen Letzteres mal substanzieller Widerstand in den USA formiert. Über lange Zeit kann das so sicher nicht weitergehen.)
Antwort auf Beitrag Nr.: 50.018.739 von SLGramann am 21.06.15 15:56:24"Was ist davon zu halten?"
EPZ-6438

5 aus 9.
Selinexor is active in MYC+ DLBCL (including double hit)

6 aus 14.
Das ist sicher nicht 1:1 vergleichbar, aber das ist es, was wir jetzt haben.
EPZ-6438

5 aus 9.
Selinexor is active in MYC+ DLBCL (including double hit)

6 aus 14.
Das ist sicher nicht 1:1 vergleichbar, aber das ist es, was wir jetzt haben.
Antwort auf Beitrag Nr.: 50.018.739 von SLGramann am 21.06.15 15:56:24EPZM
Hallo SLGramann,
naja, ein Experte bin ich ja auch nicht. Wie schreibt Garrett auf Twitter... "@cancerdocNYC mentioned yday that >50% ORR and PFS >6mos are the targets to shoot for in DLBCL". In Blutkrebsarten wie DLBCL sind hohe ORR-Raten üblicher als in festen Krebsarten... das liegt wohl daran, dass zum einen die betroffenen Zellen wie B-Zellen "nachwachsen" und man zeitweise auch ohne auskommt, so dass man z.B. per AK wie Rituxan einfach alle diese Zellen ob krank oder nicht beseitigen kann... zum anderen kommen die Wirkstoffe viel einfacher an die Zellen dran.
Aber auch Blutkrebs kann sehr resistent werden und damit schwer zu behandeln... z.B. Double-Hit DLBCL (MYC + BCLC2/6 Mutation). KPTI testet Selinexor in den Zulassungsstudien gegen diese schwer zu behandelnden Formen, um eine frühzeitige Zulassung zu erreichen. Ich glaube nicht, dass EPZM Tazemetostat (EPZ6438) speziell gegen diese schwer zu behandelnden Formen untersucht wird.
Selinexor ist als XPO1-Hemmer etwas komplett neues. Genauso dürfte EPZ6438 als epigenetischer Wirkstoff sich anderes verhalten, als übliche Krebsmittel. Die Epigenik moduliert ja die Aktivität der Gene. EPZ6438 richtet sich gegen EZH2. Zunächst hat man erwartet, dass es nur bei einer Mutation in EZH2 wirkt. Überraschenderweise hat es aber auch einen Effekt bei normaler EZH2-Aktivität. Das ganze ist aber wohl ziemlich komplex und schwer vorherzusagen... erst mit laufenden und zukünftigen Studien kann man die Effekte genauer beurteilen.
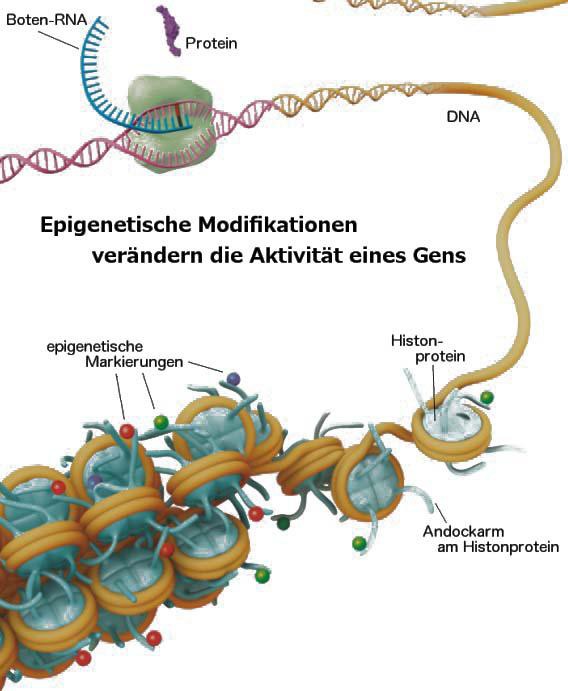
Ich habe seit einiger Zeit eine etwas größere Risiko-Position in EPZM. Grundsätzlich finde ich epigentische Wirkstoffe interessant (allerdings sind viele eher skeptisch). Besonders spannend finde ich bei EPZ6438 die Hinweise in Garrett's Blog... z.B. der Verweis auf AGIO und die "neomorphic oncogenes". AGIOs IDH2-Hemmer soll mit IDH2 auch ein neomorphic Target haben... diese sollen besonders gut wirken, wenn das Target im Krebs relevant ist und man es trifft. Ich hoffe, dass man spezielle Veränderungen findet, bei denen z.B. EPZ6438 eine starke Wirkung hat. EPZM testet z.B. auch gegen feste Krebsarten. Im sehr seltenen Rhabdoid Tumor gab es einen PR, bei dem SMARCB1 eine Rolle spielt. Garrett und zuletzt auch EPZM verweisen auf den SWI/SNF-Komplex, auf den EPZ6438 einwirkt. Das könnte zu einer Wirkung bei einer Vielzahl von Mutationen führen, der für sich genommen zwar selten sind, in Summe aber vielleicht 20% des Krebs in allen Krebsarten beeinflusst.
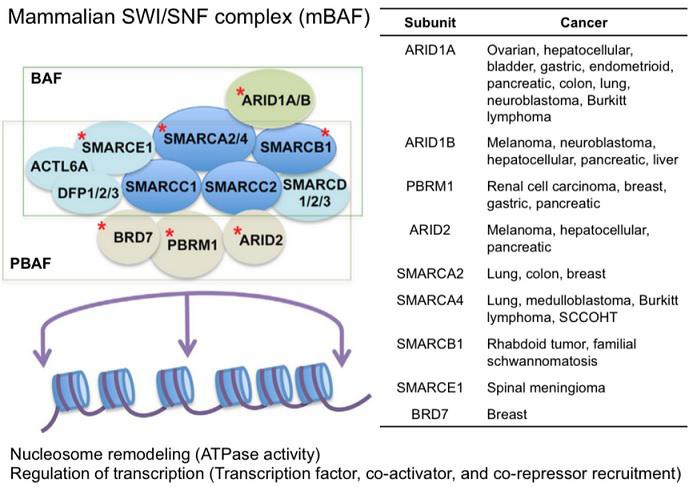
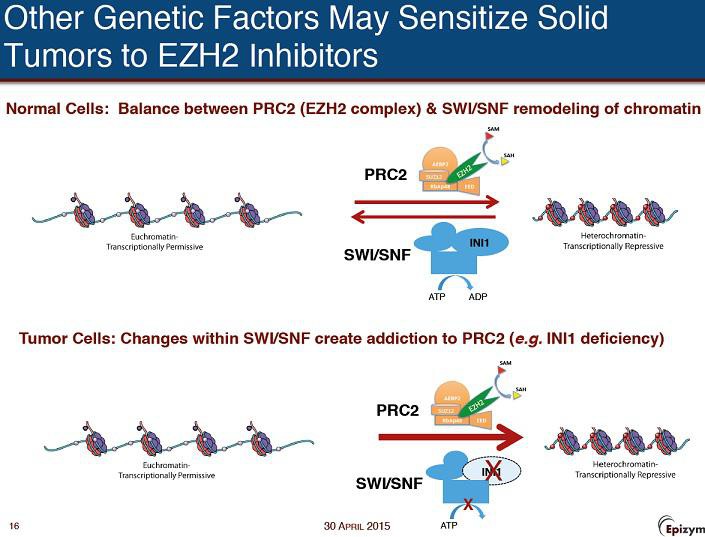
z.B. gibt es hier auch die Mutation von ARID1A. Es gibt Hinweise, dass ARID1A z.B. in dem sehr schwer zu behandelnden Ovarian Clear Cell Krebs eine große Rolle spielt und ARID1A auch mit EZH2 beeinflusst werden kann:
http://www.medicalnewstoday.com/articles/289534.php
"Recent studies have shown that ARID1A is mutated in over half of patients with ovarian clear cell carcinoma; in fact, the gene has one of the highest mutation rates among all types of cancer.
... "Our data indicate that pharmacological inhibition of EZH2 represents a novel treatment strategy for cancers involving ARID1A mutations."
Aber vieles ist noch unklar... daher nur eine Risiko-Position.

Grüße
ipollit
Hallo SLGramann,
naja, ein Experte bin ich ja auch nicht. Wie schreibt Garrett auf Twitter... "@cancerdocNYC mentioned yday that >50% ORR and PFS >6mos are the targets to shoot for in DLBCL". In Blutkrebsarten wie DLBCL sind hohe ORR-Raten üblicher als in festen Krebsarten... das liegt wohl daran, dass zum einen die betroffenen Zellen wie B-Zellen "nachwachsen" und man zeitweise auch ohne auskommt, so dass man z.B. per AK wie Rituxan einfach alle diese Zellen ob krank oder nicht beseitigen kann... zum anderen kommen die Wirkstoffe viel einfacher an die Zellen dran.
Aber auch Blutkrebs kann sehr resistent werden und damit schwer zu behandeln... z.B. Double-Hit DLBCL (MYC + BCLC2/6 Mutation). KPTI testet Selinexor in den Zulassungsstudien gegen diese schwer zu behandelnden Formen, um eine frühzeitige Zulassung zu erreichen. Ich glaube nicht, dass EPZM Tazemetostat (EPZ6438) speziell gegen diese schwer zu behandelnden Formen untersucht wird.
Selinexor ist als XPO1-Hemmer etwas komplett neues. Genauso dürfte EPZ6438 als epigenetischer Wirkstoff sich anderes verhalten, als übliche Krebsmittel. Die Epigenik moduliert ja die Aktivität der Gene. EPZ6438 richtet sich gegen EZH2. Zunächst hat man erwartet, dass es nur bei einer Mutation in EZH2 wirkt. Überraschenderweise hat es aber auch einen Effekt bei normaler EZH2-Aktivität. Das ganze ist aber wohl ziemlich komplex und schwer vorherzusagen... erst mit laufenden und zukünftigen Studien kann man die Effekte genauer beurteilen.

Ich habe seit einiger Zeit eine etwas größere Risiko-Position in EPZM. Grundsätzlich finde ich epigentische Wirkstoffe interessant (allerdings sind viele eher skeptisch). Besonders spannend finde ich bei EPZ6438 die Hinweise in Garrett's Blog... z.B. der Verweis auf AGIO und die "neomorphic oncogenes". AGIOs IDH2-Hemmer soll mit IDH2 auch ein neomorphic Target haben... diese sollen besonders gut wirken, wenn das Target im Krebs relevant ist und man es trifft. Ich hoffe, dass man spezielle Veränderungen findet, bei denen z.B. EPZ6438 eine starke Wirkung hat. EPZM testet z.B. auch gegen feste Krebsarten. Im sehr seltenen Rhabdoid Tumor gab es einen PR, bei dem SMARCB1 eine Rolle spielt. Garrett und zuletzt auch EPZM verweisen auf den SWI/SNF-Komplex, auf den EPZ6438 einwirkt. Das könnte zu einer Wirkung bei einer Vielzahl von Mutationen führen, der für sich genommen zwar selten sind, in Summe aber vielleicht 20% des Krebs in allen Krebsarten beeinflusst.


z.B. gibt es hier auch die Mutation von ARID1A. Es gibt Hinweise, dass ARID1A z.B. in dem sehr schwer zu behandelnden Ovarian Clear Cell Krebs eine große Rolle spielt und ARID1A auch mit EZH2 beeinflusst werden kann:
http://www.medicalnewstoday.com/articles/289534.php
"Recent studies have shown that ARID1A is mutated in over half of patients with ovarian clear cell carcinoma; in fact, the gene has one of the highest mutation rates among all types of cancer.
... "Our data indicate that pharmacological inhibition of EZH2 represents a novel treatment strategy for cancers involving ARID1A mutations."
Aber vieles ist noch unklar... daher nur eine Risiko-Position.
Grüße
ipollit
EURO/Dollar
Eventuell macht es Sinn sich gegen drohende Währungsverluste abzusichern. Hat jemand so was schonmal gemacht?
Charttechnisch wäre ein Übersteigen von 1,15 EUR als Kaufsgnal zu werten und könnte steigende Kurse nach sich ziehen. Es wäre doch total doof, wenn Kursgewinne von Währungsverlusten aufgefressen werden.

Ohad Hammers Kauf von Shortzertifikaten (x2) des IBB kann ich sicherlich nachvollziehen aber ich würde das so nicht machen. Grundsätzlich finde ich eine gewisse Vorsicht zwar richtig. Ich halte aber mehr davon in andere Assetklassen bzw. Cash umzuschichten, Stopkurse zu setzen etc. als "gegen die eigenen Aktien" zu wetten. Da kann man nie so richtig gewinnen.
Eventuell macht es Sinn sich gegen drohende Währungsverluste abzusichern. Hat jemand so was schonmal gemacht?
Charttechnisch wäre ein Übersteigen von 1,15 EUR als Kaufsgnal zu werten und könnte steigende Kurse nach sich ziehen. Es wäre doch total doof, wenn Kursgewinne von Währungsverlusten aufgefressen werden.

Ohad Hammers Kauf von Shortzertifikaten (x2) des IBB kann ich sicherlich nachvollziehen aber ich würde das so nicht machen. Grundsätzlich finde ich eine gewisse Vorsicht zwar richtig. Ich halte aber mehr davon in andere Assetklassen bzw. Cash umzuschichten, Stopkurse zu setzen etc. als "gegen die eigenen Aktien" zu wetten. Da kann man nie so richtig gewinnen.
Portola heute mit guten News zur Phase 3 ANNEXA-A(TM).
"This second part of the study achieved all primary and pre-specified secondary endpoints with high statistical significance. Andexanet alfa produced rapid reversal of the anticoagulant effect of Eliquis, as measured by anti-Factor Xa activity, which was sustained for the duration of the infusion. Andexanet alfa significantly reduced the level of free unbound Eliquis in the plasma and restored thrombin generation to normal. Andexanet alfa was well tolerated, with no serious adverse events, thrombotic events, or antibodies to Factor X or Xa reported. Mild infusion reactions were reported in six subjects: four in the andexanet arm and two in the placebo arm. No subjects discontinued the study due to an adverse event. The full data set was presented today in a Late-Breaking Clinical Trial oral session at the International Society on Thrombosis and Haemostasis (ISTH) 2015 Congress in Toronto."
"This second part of the study achieved all primary and pre-specified secondary endpoints with high statistical significance. Andexanet alfa produced rapid reversal of the anticoagulant effect of Eliquis, as measured by anti-Factor Xa activity, which was sustained for the duration of the infusion. Andexanet alfa significantly reduced the level of free unbound Eliquis in the plasma and restored thrombin generation to normal. Andexanet alfa was well tolerated, with no serious adverse events, thrombotic events, or antibodies to Factor X or Xa reported. Mild infusion reactions were reported in six subjects: four in the andexanet arm and two in the placebo arm. No subjects discontinued the study due to an adverse event. The full data set was presented today in a Late-Breaking Clinical Trial oral session at the International Society on Thrombosis and Haemostasis (ISTH) 2015 Congress in Toronto."
Antwort auf Beitrag Nr.: 50.019.012 von SLGramann am 21.06.15 17:31:03"Ohad Hammer mit allgemeinen Betrachtungen zum Biotech-Markt. In der Konsequenz hedgt er sein Depot erstmals mit einer short-Position."
Den Zeitpunkt finde ich schon merkwürdig. Ich glaube zwar nicht an die Charttechnik, doch wenn wir momentan massiv überbewertet wären, müssten Index-Rückschläge meiner Meinung nach viel gravierender ausfallen, als es zuletzt der Fall war. Im NBI gab es zwei Anläufe einer Korrektur, ein Doppeltop... und trotzdem fängt der Kurs sich und läuft wieder gleichmäßig nach oben auf ein neues Allzeithoch.
Am gleichen Tag bricht der Nasdaq nach oben aus und übertrifft ein 15-Jahreshoch. Warum shortet Ohad Hammer ausgerechnet beim Ausbruch den Index? Im März hätte ich das ja verstehen können, aber jetzt?
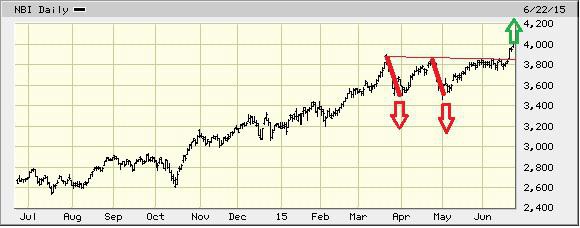
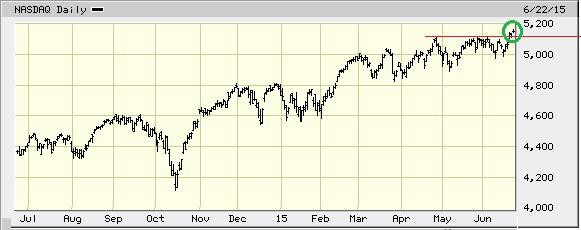
Gruß
ipollit
Den Zeitpunkt finde ich schon merkwürdig. Ich glaube zwar nicht an die Charttechnik, doch wenn wir momentan massiv überbewertet wären, müssten Index-Rückschläge meiner Meinung nach viel gravierender ausfallen, als es zuletzt der Fall war. Im NBI gab es zwei Anläufe einer Korrektur, ein Doppeltop... und trotzdem fängt der Kurs sich und läuft wieder gleichmäßig nach oben auf ein neues Allzeithoch.
Am gleichen Tag bricht der Nasdaq nach oben aus und übertrifft ein 15-Jahreshoch. Warum shortet Ohad Hammer ausgerechnet beim Ausbruch den Index? Im März hätte ich das ja verstehen können, aber jetzt?


Gruß
ipollit
Arry
Hat jemand eine Ahnung (vielleicht aus Erfahrung), wann AZN wohl mit den Topline-Daten zu Selumetinib/SUMIT/uveal melanoma an die Öffentlichkeit gehen wird? Auf clinicaltrial.gov steht hierzu Folgendes zu lesen:
Estimated Primary Completion Date: May 2015 (Final data collection date for primary outcome measure).
Darf man annehmen, daß es jetzt täglich soweit sein könnte oder spricht etwas gegen diese Erwartung?
Hat jemand eine Ahnung (vielleicht aus Erfahrung), wann AZN wohl mit den Topline-Daten zu Selumetinib/SUMIT/uveal melanoma an die Öffentlichkeit gehen wird? Auf clinicaltrial.gov steht hierzu Folgendes zu lesen:
Estimated Primary Completion Date: May 2015 (Final data collection date for primary outcome measure).
Darf man annehmen, daß es jetzt täglich soweit sein könnte oder spricht etwas gegen diese Erwartung?
Antwort auf Beitrag Nr.: 50.034.318 von lawmeetstax am 23.06.15 17:54:35Hallo lawmeetstax,
anbei eine Übersicht von Array selber nach der es so aussieht als ob die Daten im Q3 kommen.

Interessant fand ich an der letzten Präsentation, dass 520 überhaupt nicht mehr auftauchte. Schwerpunkt waren die MEK / BRAF Programme und 797, dass ja in einer Orphan Indikation getestet wird. Da bin ich sehr gespannt, ob da demnächst auch mal Ergebnisse präsentiert werden können. Array scheint mir zumindest einigermaßen optimistsich...
SG kmastra
anbei eine Übersicht von Array selber nach der es so aussieht als ob die Daten im Q3 kommen.

Interessant fand ich an der letzten Präsentation, dass 520 überhaupt nicht mehr auftauchte. Schwerpunkt waren die MEK / BRAF Programme und 797, dass ja in einer Orphan Indikation getestet wird. Da bin ich sehr gespannt, ob da demnächst auch mal Ergebnisse präsentiert werden können. Array scheint mir zumindest einigermaßen optimistsich...
SG kmastra
Antwort auf Beitrag Nr.: 50.017.482 von SLGramann am 21.06.15 08:14:47MRCB:
Heute dann also das IPO. Der Preis wurde auf 18 Dollar angehoben und bleibt damit meiner Meinung nach maßvoll.
Fraglich ist natürlich, wie der Markt dann preist.
http://ir.serestherapeutics.com/phoenix.zhtml?c=254006&p=iro…
Ich gehe fest davon aus, dass ein Handel über deutsche Broker heute mal wieder nicht möglich sein wird.
Mal schauen, wie das heute so läuft.
Heute dann also das IPO. Der Preis wurde auf 18 Dollar angehoben und bleibt damit meiner Meinung nach maßvoll.
Fraglich ist natürlich, wie der Markt dann preist.
http://ir.serestherapeutics.com/phoenix.zhtml?c=254006&p=iro…
Ich gehe fest davon aus, dass ein Handel über deutsche Broker heute mal wieder nicht möglich sein wird.
Mal schauen, wie das heute so läuft.
Antwort auf Beitrag Nr.: 50.053.953 von SLGramann am 26.06.15 07:41:02
MCRB, na ja 51,40 EUR - hypt ganz schön
Zitat von SLGramann: MRCB:
Heute dann also das IPO. Der Preis wurde auf 18 Dollar angehoben und bleibt damit meiner Meinung nach maßvoll.
Fraglich ist natürlich, wie der Markt dann preist.
http://ir.serestherapeutics.com/phoenix.zhtml?c=254006&p=iro…
Ich gehe fest davon aus, dass ein Handel über deutsche Broker heute mal wieder nicht möglich sein wird.
Mal schauen, wie das heute so läuft.
MCRB, na ja 51,40 EUR - hypt ganz schön
Antwort auf Beitrag Nr.: 50.060.649 von riverstar_de am 26.06.15 23:40:25"MCRB, na ja 51,40 EUR - hypt ganz schön"
Ja, ist wahnsinn. Bin etwas frustriert, weil zu diesen Preisen für mich ein Kauf nicht in Betracht kommt.
Ein Aufschlag auf den IPO-Preis von 185%.
Du hast recht mit dem Tickerkürzel: Es heißt MCRB und nicht wie von mir geschrieben MRCB...
(Preis allerdings in Dollar nicht in Euro)
Ich bezweifle, dass es in nächster Zeit zu einem erheblichen Rücksetzer kommen wird. Für unter oder um eine Mrd. Marktkap. würde ich eine Position kaufen, leider ist das derzeit nicht absehbar. Denn dafür müsste sich der Kurs halbieren! Unglaublich...
Ja, ist wahnsinn. Bin etwas frustriert, weil zu diesen Preisen für mich ein Kauf nicht in Betracht kommt.
Ein Aufschlag auf den IPO-Preis von 185%.
Du hast recht mit dem Tickerkürzel: Es heißt MCRB und nicht wie von mir geschrieben MRCB...
(Preis allerdings in Dollar nicht in Euro)
Ich bezweifle, dass es in nächster Zeit zu einem erheblichen Rücksetzer kommen wird. Für unter oder um eine Mrd. Marktkap. würde ich eine Position kaufen, leider ist das derzeit nicht absehbar. Denn dafür müsste sich der Kurs halbieren! Unglaublich...
Antwort auf Beitrag Nr.: 50.017.458 von SLGramann am 21.06.15 07:49:53
diskutiert ihr hier auch medizintech firmen?
weil da hätte ich eine die ich hier gern mal einbringen würde
die ist wahrscheinlich -unter 1,2,3gesichtspunkten zumindest- nicht nach euren vorstellungen/"präferenzen", aber da würde mich mal eure meinung interessieren
gruß
P.
diskutiert ihr hier auch medizintech firmen?
weil da hätte ich eine die ich hier gern mal einbringen würde
die ist wahrscheinlich -unter 1,2,3gesichtspunkten zumindest- nicht nach euren vorstellungen/"präferenzen", aber da würde mich mal eure meinung interessieren
gruß
P.
Angst vor Biotech-Absturz
27.06.2015 | 18:58 | (Die Presse)
Investoren sichern sich mit Optionen gegen einen Absturz von Biotech-Aktien in einem Ausmaß ab, wie lange nicht mehr. In sechs Jahren haben sich deren Kurse mehr als versechsfacht.
Die Rallye der Biotech-Aktien wird manchen Investoren zu heiß. Zu oft schon haben sie sich in den vergangenen sechs Jahren die Finger verbrannt– auch wenn sich die Kurse immer wieder erholt haben.
Die Nachfrage nach Optionen zur Absicherung gegen einen Kursrutsch von Biotechnologie-Aktien im Vergleich zu Optionen auf steigende Kurse ist so hoch wie seit drei Jahren nicht mehr, wie aus Daten von Bloomberg hervorgeht. Der Nasdaq Biotechnology Index ist seit März 2009 um 549 Prozent nach oben geklettert. Vor einem Jahr hatten schon viele von einer Blase gesprochen, doch seitdem hat der Index um weitere 45 Prozent zugelegt, seit Jahresbeginn beläuft sich das Plus auf 23 Prozent.
Das Interesse an den Optionen zur Absicherung gegen Verluste hatte bereits im vergangenen Jahr deutlich zugenommen, nachdem die Vorsitzende der US-Notenbank, Janet Yellen, bei zwei Gelegenheiten gewarnt hatte, der Sektor sei überbewertet.
Die Biotechnologie- und Pharmaunternehmen platzieren Aktien in einem Tempo, das es seit einem Jahrzehnt nicht mehr gab. Im ersten Quartal beschafften die Firmen über 93 Zweitplatzierungen 18,7 Milliarden Dollar– das ist dreimal mehr als 2014, zeigen Daten von Bloomberg.
Eine der Sorgen der Investoren ist, dass der Geldstrom abreißen könnte. „Der Sektor ist von Kapital abhängig, und das könnte beim ersten Anzeichen von Schwäche wegbleiben“, schrieben die Derivate-Strategen Katherine Fogertey und John Marshall von Goldman Sachs in einer Einschätzung für Kunden. „Die jüngsten Rückschläge bei der Medikamenten-Pipeline haben die Besorgnis in dieser Richtung verstärkt.“
Die Aktien im Nasdaq Biotech Index werden Bloomberg-Daten zufolge zum 53-Fachen der von Analysten erwarteten Unternehmensgewinne gehandelt. Zum Vergleich: Die entsprechende Bewertung im breit gefassten US-Aktienindex Standard & Poor's 500, der die Wertentwicklung aller Branchen widerspiegelt, liegt beim 18-Fachen. Zum Teil ist die hohe Bewertung der Biotech-Aktien mit den stärkeren Wachstumserwartungen zu erklären. Gemessen an den für 2016 erwarteten Gewinnen beträgt das Kurs-Gewinn-Verhältnis „nur“ noch 37.
Merkmale einer Blase. „Biotech-Aktien werden seit geraumer Zeit von einem spekulativen Schub getrieben“, sagte Todd Lowenstein, Vermögensverwalter bei High Mark Capital Management in Los Angeles. „Unter allen Marktsegmenten weist dieses zweifellos die meisten Merkmale einer Blase auf.“ Der Nasdaq Biotech Index verzeichnete im vergangenen Jahr mehr als fünf Rücksetzer von jeweils mehr als 6,6 Prozent. Doch konnte der Verlust jedes Mal innerhalb rund eines Monats wieder wettgemacht werden.
Nun haben die Pessimisten Überhand. Die Differenz von Kosten zur Absicherung gegen ein Abrutschen von zehn Prozent im iShares Nasdaq Biotechnology ETF (einem börsengehandelten Fonds) waren am 10. Juni um so viel höher als die Kosten für Kontrakte auf einen Anstieg von zehn Prozent, wie seit August 2012 nicht mehr, zeigen Bloomberg-Daten. (Bloomberg/red.)
27.06.2015 | 18:58 | (Die Presse)
Investoren sichern sich mit Optionen gegen einen Absturz von Biotech-Aktien in einem Ausmaß ab, wie lange nicht mehr. In sechs Jahren haben sich deren Kurse mehr als versechsfacht.
Die Rallye der Biotech-Aktien wird manchen Investoren zu heiß. Zu oft schon haben sie sich in den vergangenen sechs Jahren die Finger verbrannt– auch wenn sich die Kurse immer wieder erholt haben.
Die Nachfrage nach Optionen zur Absicherung gegen einen Kursrutsch von Biotechnologie-Aktien im Vergleich zu Optionen auf steigende Kurse ist so hoch wie seit drei Jahren nicht mehr, wie aus Daten von Bloomberg hervorgeht. Der Nasdaq Biotechnology Index ist seit März 2009 um 549 Prozent nach oben geklettert. Vor einem Jahr hatten schon viele von einer Blase gesprochen, doch seitdem hat der Index um weitere 45 Prozent zugelegt, seit Jahresbeginn beläuft sich das Plus auf 23 Prozent.
Das Interesse an den Optionen zur Absicherung gegen Verluste hatte bereits im vergangenen Jahr deutlich zugenommen, nachdem die Vorsitzende der US-Notenbank, Janet Yellen, bei zwei Gelegenheiten gewarnt hatte, der Sektor sei überbewertet.
Die Biotechnologie- und Pharmaunternehmen platzieren Aktien in einem Tempo, das es seit einem Jahrzehnt nicht mehr gab. Im ersten Quartal beschafften die Firmen über 93 Zweitplatzierungen 18,7 Milliarden Dollar– das ist dreimal mehr als 2014, zeigen Daten von Bloomberg.
Eine der Sorgen der Investoren ist, dass der Geldstrom abreißen könnte. „Der Sektor ist von Kapital abhängig, und das könnte beim ersten Anzeichen von Schwäche wegbleiben“, schrieben die Derivate-Strategen Katherine Fogertey und John Marshall von Goldman Sachs in einer Einschätzung für Kunden. „Die jüngsten Rückschläge bei der Medikamenten-Pipeline haben die Besorgnis in dieser Richtung verstärkt.“
Die Aktien im Nasdaq Biotech Index werden Bloomberg-Daten zufolge zum 53-Fachen der von Analysten erwarteten Unternehmensgewinne gehandelt. Zum Vergleich: Die entsprechende Bewertung im breit gefassten US-Aktienindex Standard & Poor's 500, der die Wertentwicklung aller Branchen widerspiegelt, liegt beim 18-Fachen. Zum Teil ist die hohe Bewertung der Biotech-Aktien mit den stärkeren Wachstumserwartungen zu erklären. Gemessen an den für 2016 erwarteten Gewinnen beträgt das Kurs-Gewinn-Verhältnis „nur“ noch 37.
Merkmale einer Blase. „Biotech-Aktien werden seit geraumer Zeit von einem spekulativen Schub getrieben“, sagte Todd Lowenstein, Vermögensverwalter bei High Mark Capital Management in Los Angeles. „Unter allen Marktsegmenten weist dieses zweifellos die meisten Merkmale einer Blase auf.“ Der Nasdaq Biotech Index verzeichnete im vergangenen Jahr mehr als fünf Rücksetzer von jeweils mehr als 6,6 Prozent. Doch konnte der Verlust jedes Mal innerhalb rund eines Monats wieder wettgemacht werden.
Nun haben die Pessimisten Überhand. Die Differenz von Kosten zur Absicherung gegen ein Abrutschen von zehn Prozent im iShares Nasdaq Biotechnology ETF (einem börsengehandelten Fonds) waren am 10. Juni um so viel höher als die Kosten für Kontrakte auf einen Anstieg von zehn Prozent, wie seit August 2012 nicht mehr, zeigen Bloomberg-Daten. (Bloomberg/red.)
rein methodisch, prinzipiell, finde ich das mal eine ganz interessante geschichte
40% Return In ~4 Months With Our IP Selected Healthcare Companies Since SA Publication
http://seekingalpha.com/article/3293925-40-percent-return-in…
40% Return In ~4 Months With Our IP Selected Healthcare Companies Since SA Publication
http://seekingalpha.com/article/3293925-40-percent-return-in…
Antwort auf Beitrag Nr.: 50.065.584 von Avokado am 28.06.15 11:40:51
Nehmen wir mal eine Aktie die in der Entwicklung mit ca 50 Millionen € bewertet wird und dann kurz vor der Zulassung mit einem Blockbusterwirkstoff steht. Da ist noch enormes Potential was eingepreist werden muss.
Genau das ist ja Börse. Die unterbewerteten Schätze auszugraben.
Andererseits gilt es die jetzt schon überbewerteten Titel mit hohem Risiko zu meiden.
Es gibt jede Menge Titel mit enormen Potential. Aber es gibt auch jede Menge Titel die übebewertet sind.Der Index spiegelt dir nur die Summe alle dieser Fakten wieder.
Selbst eine allgemeine Korrektur macht die Sache ja nicht "gerechter". Allenfalls wird etwas Luft aus den überbewerteten Titeln genommen. Die unterbewerteten Aktien entwickeln da einfach noch mehr Potential für die Zukunft. Sie sind ja jetzt schon unterbewertet.
Die Bewertungsmodelle bei Biotechaktien sind einfach nicht gut. Dies muss ein Biotechinvestor mit seiner Erfahrung dann selbst in die Hand nehmen. Das ist dann halt eben so. Vor der Zulassung hat man noch einen Umsatz von ca 20 Millionen €. Nach der Zulassung dann halt von mehreren hundert Millionen €.
Deshalb halte ich nicht viel davon wenn man sagt der "Index" sei überbewertet wenn die Zukunftsaussichten noch nicht mal eingepreist sind. Die einzelne Aktie ist unter- oder überbewertet. Dies gilt es zu erkennen und umzusetzen. Natürlich werden diese "Schätze" erst in der Zukunft gehoben. Deshalb ist es auch Quatsch einen Biotechwert nach den Umsätzen in der Entwicklungsphase mit in so ein Bewertungsmodell mit einzubeziehen. Die großen Gewinne werden halt erst nach der Zulassung mit enormen Potential gemacht. Deshalb müssen solche Bewertungsmodelle auch immer in die "Zukunft" gemacht werden. Eine Betrachtung zum Istzustand ist für mich nicht hilfreich und hat keinerlei Aussagekraft.
Letztendlich ist es immer
Letztendlich ist es immer eine Einzelaktiebetrachtung. Der Index spiegelt das Gesamtergebnis dann natürlich wieder.Nehmen wir mal eine Aktie die in der Entwicklung mit ca 50 Millionen € bewertet wird und dann kurz vor der Zulassung mit einem Blockbusterwirkstoff steht. Da ist noch enormes Potential was eingepreist werden muss.
Genau das ist ja Börse. Die unterbewerteten Schätze auszugraben.
Andererseits gilt es die jetzt schon überbewerteten Titel mit hohem Risiko zu meiden.
Es gibt jede Menge Titel mit enormen Potential. Aber es gibt auch jede Menge Titel die übebewertet sind.Der Index spiegelt dir nur die Summe alle dieser Fakten wieder.
Selbst eine allgemeine Korrektur macht die Sache ja nicht "gerechter". Allenfalls wird etwas Luft aus den überbewerteten Titeln genommen. Die unterbewerteten Aktien entwickeln da einfach noch mehr Potential für die Zukunft. Sie sind ja jetzt schon unterbewertet.
Die Bewertungsmodelle bei Biotechaktien sind einfach nicht gut. Dies muss ein Biotechinvestor mit seiner Erfahrung dann selbst in die Hand nehmen. Das ist dann halt eben so. Vor der Zulassung hat man noch einen Umsatz von ca 20 Millionen €. Nach der Zulassung dann halt von mehreren hundert Millionen €.
Deshalb halte ich nicht viel davon wenn man sagt der "Index" sei überbewertet wenn die Zukunftsaussichten noch nicht mal eingepreist sind. Die einzelne Aktie ist unter- oder überbewertet. Dies gilt es zu erkennen und umzusetzen. Natürlich werden diese "Schätze" erst in der Zukunft gehoben. Deshalb ist es auch Quatsch einen Biotechwert nach den Umsätzen in der Entwicklungsphase mit in so ein Bewertungsmodell mit einzubeziehen. Die großen Gewinne werden halt erst nach der Zulassung mit enormen Potential gemacht. Deshalb müssen solche Bewertungsmodelle auch immer in die "Zukunft" gemacht werden. Eine Betrachtung zum Istzustand ist für mich nicht hilfreich und hat keinerlei Aussagekraft.
Antwort auf Beitrag Nr.: 49.972.767 von kmastra am 14.06.15 22:02:31XENE
leider ist die PII in Osteoarthritis fehlgeschlagen..."Xenon's Teva-partnered pain drug flunks a test in osteoarthritis" http://www.fiercebiotech.com/story/xenons-teva-partnered-pai…
Meine Position ist zum Glück nur klein. Die Genentech-Kooperation scheint bedeutsamer zu sein, auch wenn die Royalties hier nicht so hoch sind wie die von TEVA. Aktien mit niedriger MK scheinen generell ein höheres Risiko zu beinhalten... insofern halte ich Ohad Hammers Strategie, sich auf solche zu konzentrieren, weil sie so "billig" sind, für nicht unriskant.

Gruß
ipollit
leider ist die PII in Osteoarthritis fehlgeschlagen..."Xenon's Teva-partnered pain drug flunks a test in osteoarthritis" http://www.fiercebiotech.com/story/xenons-teva-partnered-pai…
Meine Position ist zum Glück nur klein. Die Genentech-Kooperation scheint bedeutsamer zu sein, auch wenn die Royalties hier nicht so hoch sind wie die von TEVA. Aktien mit niedriger MK scheinen generell ein höheres Risiko zu beinhalten... insofern halte ich Ohad Hammers Strategie, sich auf solche zu konzentrieren, weil sie so "billig" sind, für nicht unriskant.
Gruß
ipollit
Hat jemand eine Idee, wie es mit KPTI weitergeht? Nähert sich ja 52 Wochen Tief.
Encorafenib and colon cancer
arry:Encorafenib and colon cancer: Combination with Erbitux
Encorafenib-Based Regimens Show Promising Clinical Activity In BRAF-Mutant Colorectal Cancer Patients
-Data encouraging when compared to currently available and investigational therapies in BRAF CRC-
BOULDER, Colo., July 6, 2015 /PRNewswire/ -- Array BioPharma's (NASDAQ: ARRY) wholly-owned RAF inhibitor, encorafenib, was showcased this past weekend at the 2015 ESMO World Congress of Gastrointestinal Cancer during an oral presentation. At the meeting, data were shared from a Phase 1b trial and preliminary data from a 100-patient randomized Phase 2 expansion of that trial testing the combination of encorafenib and cetuximab, an EGFR inhibitor, with or without the addition of alpelisib (BYL719) 1, an investigational PI3K inhibitor in patients with BRAF-mutant colorectal cancer (BRAFmut CRC). Results from the study indicate that these combinations can be administered with good tolerability and show promising clinical activity in this patient population with high unmet medical needs. Patient enrollment is now complete in the Phase 2 study.
The preliminary Phase 2 results show an objective response rate (complete or partial response) and disease control rate (complete or partial response or stable disease) of 29% and 81%, respectively, for patients receiving the combination of encorafenib and cetuximab (encorafenib doublet), and 35% and 79%, respectively, for patients receiving the combination of encorafenib, cetuximab and alpelisib (encorafenib triplet).
Across both the encorafenib doublet and triplet treatment groups, most treatment related adverse events were grade 1 or 2 with few grade 3 or 4 adverse events. The most frequent treatment related adverse events across all grades for the encorafenib doublet were fatigue (36%), nausea (31%), lipase increased (24%), diarrhea (21%) and decreased appetite (21%), while for the encorafenib triplet they were diarrhea (39%), nausea (37%), fatigue (33%) and hyperglycemia (31%).
These results are consistent with the Phase 1b portion of the trial and are encouraging when compared to currently available therapies for BRAFmut CRC patients, as well as with other recently published investigational approaches in this population. Historically, response rates are very low for either single-agent EGFR or RAF inhibitor therapy in patients with BRAFmut CRC, which suggests a synergistic effect for the combination of encorafenib and cetuximab in this population.
"The combination of encorafenib and cetuximab demonstrated promising activity in this hard-to-treat subset of colorectal cancer patients," said Josep Tabernero, M.D., Head of the Medical Oncology Department at the Vall d'Hebron University Hospital and the Director of the Vall d'Hebron Institute of Oncology. "It is critical to identify new, effective treatments for BRAF mutant colorectal cancer patients, and I look forward to rapid development of this combination in a subsequent clinical trial."
1 alpelisib (BYL719) is an investigational Novartis Pharmaceuticals compound.
@Arry
Ich habe mir eben den webcast von der heutigen Präsentation angehört. Ron Squarer sagte mindestens drei interessante Sachen:
Wenn Selumetinib in lung cancer nächstes Jahr erfolgreich sein sollte, dann würden allein die von AZ zu erwartenden Royalties für diese Indikation aus seiner Sicht die jetzige Börsenbewertung rechtfertigen! Etwas ähnliches hatte SLGramann hier mal vor einem dreiviertel Jahr oder so bereits geschrieben. Das ist deshalb so bemerkenswert, weil BINI und ENCO als eigene Produkte noch viel mehr wert sein sollten, die anderen Assets auch noch außen vorgelassen.
Zum Zeitplan für die Verpartnerung EU sprach er davon, daß dies wohl bis zum Ende des Jahres geschehen soll. Für mich der erste wichtige Hinweis, daß die zeitlichen Vorgaben der Kartellbehörden zumindest nicht kurzfristig enden.
Kapitalmaßnahmen hält RS auf nähere Sicht nicht für erforderlich.
Insgesamt wieder sehr interessant, für mich auch sehr ermutigend.
Ich habe mir eben den webcast von der heutigen Präsentation angehört. Ron Squarer sagte mindestens drei interessante Sachen:
Wenn Selumetinib in lung cancer nächstes Jahr erfolgreich sein sollte, dann würden allein die von AZ zu erwartenden Royalties für diese Indikation aus seiner Sicht die jetzige Börsenbewertung rechtfertigen! Etwas ähnliches hatte SLGramann hier mal vor einem dreiviertel Jahr oder so bereits geschrieben. Das ist deshalb so bemerkenswert, weil BINI und ENCO als eigene Produkte noch viel mehr wert sein sollten, die anderen Assets auch noch außen vorgelassen.
Zum Zeitplan für die Verpartnerung EU sprach er davon, daß dies wohl bis zum Ende des Jahres geschehen soll. Für mich der erste wichtige Hinweis, daß die zeitlichen Vorgaben der Kartellbehörden zumindest nicht kurzfristig enden.
Kapitalmaßnahmen hält RS auf nähere Sicht nicht für erforderlich.
Insgesamt wieder sehr interessant, für mich auch sehr ermutigend.
Antwort auf Beitrag Nr.: 50.143.989 von lawmeetstax am 08.07.15 21:13:37Hallo lawmeetstax,
danke, sehr interessant. Ich habe heute massiv Aktien verkauft, aber Array ist eine der wenigen Positionen, die im Depot verblieben sind.
Derzeit habe ich im Depot nur noch:
XLRN
ARRY
BLUE
CLVS
ICPT
KITE
RCPT
SGYP (werde ich aber ebenfalls verkaufen)
QURE
Cash liegt jetzt bei ca. 75%.
danke, sehr interessant. Ich habe heute massiv Aktien verkauft, aber Array ist eine der wenigen Positionen, die im Depot verblieben sind.
Derzeit habe ich im Depot nur noch:
XLRN
ARRY
BLUE
CLVS
ICPT
KITE
RCPT
SGYP (werde ich aber ebenfalls verkaufen)
QURE
Cash liegt jetzt bei ca. 75%.
Antwort auf Beitrag Nr.: 50.152.491 von SLGramann am 09.07.15 19:24:45wieso so viel Cash.
Ich habe den Eindruck, dass jedenfalls Griechenland kein Grund sein sollte, derzeit zu verkaufen. Auch das "Sommertief" ist dieses Jahr ggf. sehr spät dran, also "sell in May"....
Ich habe zuletzt im Biotech-Bereich eher gekauft als verkauft, allerdings hauptsächlich, weil ich "zu viele" Morphosys-Aktien hatte durch den starke Anstieg und das Risiko besser verteilen wollte.
Trotzdem finde ich 75 % Cash sehr viel, wobei ich nicht glaube, klüger zu sein.
Zur Auswahl würde mich auch interessieren, wieso ausgerechnet QURE und CLVS im Depot bleiben, wenn so viel verkauft wird. Beide haben ja zuletzt keine Bäume ausgerissen.
Wenn es steuerliche Gründe sind o.ä., interessiert es mich natürlich nicht, aber wenn es firmenbezogen Gründe sind, würde ich schon gern wissen, warum diese beiden "besser" sein sollen.
Ich habe den Eindruck, dass jedenfalls Griechenland kein Grund sein sollte, derzeit zu verkaufen. Auch das "Sommertief" ist dieses Jahr ggf. sehr spät dran, also "sell in May"....
Ich habe zuletzt im Biotech-Bereich eher gekauft als verkauft, allerdings hauptsächlich, weil ich "zu viele" Morphosys-Aktien hatte durch den starke Anstieg und das Risiko besser verteilen wollte.
Trotzdem finde ich 75 % Cash sehr viel, wobei ich nicht glaube, klüger zu sein.
Zur Auswahl würde mich auch interessieren, wieso ausgerechnet QURE und CLVS im Depot bleiben, wenn so viel verkauft wird. Beide haben ja zuletzt keine Bäume ausgerissen.
Wenn es steuerliche Gründe sind o.ä., interessiert es mich natürlich nicht, aber wenn es firmenbezogen Gründe sind, würde ich schon gern wissen, warum diese beiden "besser" sein sollen.
Antwort auf Beitrag Nr.: 50.152.941 von xylophon am 09.07.15 20:16:32"Trotzdem finde ich 75 % Cash sehr viel, wobei ich nicht glaube, klüger zu sein."
Das ist definitiv sehr, sehr viel und ich bin auch nicht klüger. Eigentlich war mein Timing an der Börse immer ziemlich beschissen und ich mach das schon so ein paar Jährchen. Es ist also ziemlich wahrscheinlich, dass ich mal wieder falsch liege.
Ich habe derzeit einfach ein ganz schlechtes Bauchgefühl. Die Indizes sind so ziemlich am Allzeit-Top, während die Welt doch ziemlich aus den Fugen ist. Griechenland (oder besser, unseren Umgang mit dem Problem, finde ich ziemlich schrecklich und ich denke schon, dass das Potential für einen ziemlichen Knall hat. Aber das ist es nicht allein, aber das führt alles zu weit jetzt.
CLVS - von denen halte ich ganz viel. Ich sehe sie als Übernahmekandidaten. Wahrscheinlich haben sie gleich drei künftige Blockbuster in der Pipeline.
QURE - sind durchaus fragwürdig. Muss man nicht haben, es sei denn, man steht auf Gentherapie...
Bei allen genannten Werten halte ich entweder eine Übernahme für wahrscheinlich oder bin auch - mehr oder weniger guten Gründen - irgendwie von der Technologie fasziniert.
Das ist definitiv sehr, sehr viel und ich bin auch nicht klüger. Eigentlich war mein Timing an der Börse immer ziemlich beschissen und ich mach das schon so ein paar Jährchen. Es ist also ziemlich wahrscheinlich, dass ich mal wieder falsch liege.

Ich habe derzeit einfach ein ganz schlechtes Bauchgefühl. Die Indizes sind so ziemlich am Allzeit-Top, während die Welt doch ziemlich aus den Fugen ist. Griechenland (oder besser, unseren Umgang mit dem Problem, finde ich ziemlich schrecklich und ich denke schon, dass das Potential für einen ziemlichen Knall hat. Aber das ist es nicht allein, aber das führt alles zu weit jetzt.
CLVS - von denen halte ich ganz viel. Ich sehe sie als Übernahmekandidaten. Wahrscheinlich haben sie gleich drei künftige Blockbuster in der Pipeline.
QURE - sind durchaus fragwürdig. Muss man nicht haben, es sei denn, man steht auf Gentherapie...
Bei allen genannten Werten halte ich entweder eine Übernahme für wahrscheinlich oder bin auch - mehr oder weniger guten Gründen - irgendwie von der Technologie fasziniert.
danke für die schnelle Antwort. Was Griechenland betrifft sehe ich allerdings kaum Gefahren. Es wurde zuletzt sehr deutlich kommuniziert, dass man bereit ist, das Risiko einzugehen und es könnte für alle Beteiligten das Beste sein. Könnte, ich will das also nicht vertiefen. Aber die Gefahr, dass andere Länder "infiziert" werden, ist doch eher gering.
Problematischer sehe ich da schon Russland/Ukraine.
Aber: eigentlich sollten Bio-tech-Aktien eher ein Faktor der Stabilität sein, weil sie eben relativ konjunkturunabhängig sind.
Naja, in ein paar Monten wissen wir mehr.
Problematischer sehe ich da schon Russland/Ukraine.
Aber: eigentlich sollten Bio-tech-Aktien eher ein Faktor der Stabilität sein, weil sie eben relativ konjunkturunabhängig sind.
Naja, in ein paar Monten wissen wir mehr.
Antwort auf Beitrag Nr.: 50.152.491 von SLGramann am 09.07.15 19:24:45Hallo SLGramann,
danke fürs Update! Tja eine Kristallkugel bräuchte man.
Ich habe meine Cashosition aber auch wieder erhöht. Sie liegt bei 35%.
Meine Positionen der Größe nach:
CLVS
ESPR
ZFGN
MRNS
XENE
AUPH
ARQL
FGEN
ONTY
ARRY
KPTI
TRVN
AAVL
Was den Gesamtmarkt betrifft bin ich gar nicht so skeptisch. Wohin soll das viele billige Geld auch? Interessant dürfte der Fortgang der Griechenland-Krise vor allem für den EURO werden. Ich habe da den Eindruck, dass der Finanzmarkt einen Grexit sogar begrüßen würde (wenn andere Länder nicht angesteckt werden).
Für die Biotechbranche bleibe ich optimistisch, vor allem was Einzelwerte betrifft. Als Gefahr sehe ist aber, dass sich die hohen Preise nicht langfristig durchsetzen lassen bzw. da wieder Diskussionen aufkommen. Das wäre fatal!
Momentan befindet sich der IBB knapp über der 50 Tageslinie, die 2 mal als Unterstützung gedient hat. Meine Cashposition würde ich spätestens beim Erreichen der 200 Tageslinie wieder komplett abbauen.

SG kmastra
danke fürs Update! Tja eine Kristallkugel bräuchte man.
Ich habe meine Cashosition aber auch wieder erhöht. Sie liegt bei 35%.
Meine Positionen der Größe nach:
CLVS
ESPR
ZFGN
MRNS
XENE
AUPH
ARQL
FGEN
ONTY
ARRY
KPTI
TRVN
AAVL
Was den Gesamtmarkt betrifft bin ich gar nicht so skeptisch. Wohin soll das viele billige Geld auch? Interessant dürfte der Fortgang der Griechenland-Krise vor allem für den EURO werden. Ich habe da den Eindruck, dass der Finanzmarkt einen Grexit sogar begrüßen würde (wenn andere Länder nicht angesteckt werden).
Für die Biotechbranche bleibe ich optimistisch, vor allem was Einzelwerte betrifft. Als Gefahr sehe ist aber, dass sich die hohen Preise nicht langfristig durchsetzen lassen bzw. da wieder Diskussionen aufkommen. Das wäre fatal!
Momentan befindet sich der IBB knapp über der 50 Tageslinie, die 2 mal als Unterstützung gedient hat. Meine Cashposition würde ich spätestens beim Erreichen der 200 Tageslinie wieder komplett abbauen.
SG kmastra
Antwort auf Beitrag Nr.: 50.154.105 von kmastra am 09.07.15 22:31:34Rein charttechnisch sieht es doch gar nicht so schlecht aus, oder? Eine deutliche Schwäche sehe ich noch nicht. Und fudamental sind wir vielleicht im oberen Bereich bewertet, aber kann man dies wirklich schon als Blase bezeichnen? Der Index hat sich zwar in den letzten Jahren vervielfacht, aber die Gewinne doch auch. Würde der Index um 50% fallen, müssten dann nicht auch die großen Biotechs, die fast 50% vom Index ausmachen, ebenfalls deutlich fallen? Die KGVs für nächstes Jahr liegen im Bereich der Pharmas... hoch, aber meiner Meinung nach noch keine Blase, oder?
GILD 10,3
AMGN 14,3
BIIB 20,6
CELG 19,0
REGN 37,8
ALXN 31,5
Zum Vergleich einige Pharmas...
BAY 16,0
NVS 18,3
Roche 17,0
BMY 29,6
AZN 15,8
Ich bin daher noch immer voll investiert...
8,4% INCY
5,7% CLVS
5,7% ACAD
5,2% MGNX
5,0% CLDX
4,3% MDVN
3,8% KPTI
3,8% TSRO
3,8% IPH.PA
3,7% REGN
3,7% ESPR
3,6% ARRY
3,3% EXEL
3,2% ISIS
3,1% ALNY
3,0% SAGE
2,7% FPRX
2,6% GEN.CO
2,6% CEMP
2,4% FGEN
2,3% ENTA
2,0% XLRN
1,7% ZSPH
1,7% EPZM
1,6% RCPT
1,5% SGEN
1,5% INFI
1,5% PTLA
1,3% ARQL
1,1% IMMU
1,0% SNTA
0,9% AUPH
0,7% MRNS
0,7% VSTM
0,6% XENE
0,6% STML
Naja, wenn es zu Rückschlägen kommt, ist Cash natürlich King, dann hat man viele Möglichkeiten... die Frage ist nur, wann es zu einem größeren Rückschlag kommt. Der Markt hätte in den letzten Monaten doch schon Chancen zu einer größeren Korrektur gehabt, warum soll sie jetzt kommen?
Gruß
ipollit
GILD 10,3
AMGN 14,3
BIIB 20,6
CELG 19,0
REGN 37,8
ALXN 31,5
Zum Vergleich einige Pharmas...
BAY 16,0
NVS 18,3
Roche 17,0
BMY 29,6
AZN 15,8
Ich bin daher noch immer voll investiert...
8,4% INCY
5,7% CLVS
5,7% ACAD
5,2% MGNX
5,0% CLDX
4,3% MDVN
3,8% KPTI
3,8% TSRO
3,8% IPH.PA
3,7% REGN
3,7% ESPR
3,6% ARRY
3,3% EXEL
3,2% ISIS
3,1% ALNY
3,0% SAGE
2,7% FPRX
2,6% GEN.CO
2,6% CEMP
2,4% FGEN
2,3% ENTA
2,0% XLRN
1,7% ZSPH
1,7% EPZM
1,6% RCPT
1,5% SGEN
1,5% INFI
1,5% PTLA
1,3% ARQL
1,1% IMMU
1,0% SNTA
0,9% AUPH
0,7% MRNS
0,7% VSTM
0,6% XENE
0,6% STML
Naja, wenn es zu Rückschlägen kommt, ist Cash natürlich King, dann hat man viele Möglichkeiten... die Frage ist nur, wann es zu einem größeren Rückschlag kommt. Der Markt hätte in den letzten Monaten doch schon Chancen zu einer größeren Korrektur gehabt, warum soll sie jetzt kommen?
Gruß
ipollit
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 61 | ||
| 60 | ||
| 46 | ||
| 34 | ||
| 33 | ||
| 32 | ||
| 15 | ||
| 9 | ||
| 8 | ||
| 8 |