Biotech Depot - verschiede Werte und Strategien - 500 Beiträge pro Seite (Seite 4)
eröffnet am 06.04.12 20:55:15 von
neuester Beitrag 15.12.21 20:44:42 von
neuester Beitrag 15.12.21 20:44:42 von
Beiträge: 2.765
ID: 1.173.523
ID: 1.173.523
Aufrufe heute: 1
Gesamt: 306.557
Gesamt: 306.557
Aktive User: 0
Top-Diskussionen
| Titel | letzter Beitrag | Aufrufe |
|---|---|---|
| heute 20:07 | 2870 | |
| heute 11:20 | 1877 | |
| heute 18:31 | 1852 | |
| heute 19:39 | 1706 | |
| vor 1 Stunde | 1432 | |
| heute 15:11 | 1318 | |
| heute 09:52 | 1223 | |
| heute 19:29 | 977 |
Meistdiskutierte Wertpapiere
| Platz | vorher | Wertpapier | Kurs | Perf. % | Anzahl | ||
|---|---|---|---|---|---|---|---|
| 1. | 1. | 18.161,01 | +1,36 | 217 | |||
| 2. | 3. | 0,1935 | 0,00 | 90 | |||
| 3. | 2. | 1,1800 | -14,49 | 77 | |||
| 4. | 5. | 9,3500 | +1,14 | 60 | |||
| 5. | 4. | 158,18 | +0,23 | 50 | |||
| 6. | Neu! | 0,3050 | 0,00 | 36 | |||
| 7. | Neu! | 4,7950 | +6,91 | 34 | |||
| 8. | Neu! | 11,905 | +14,97 | 31 |
Antwort auf Beitrag Nr.: 50.165.070 von ipollit am 11.07.15 13:23:54
ich sehe das ähnlich wie BICYPAPA das hier -@Beitrag Nr. 1.490- geschrieben hat
ich denke in den bewertungsdiskussionen muss man in ein paar, mindestens 3, "fenstern/ebenen" unterscheiden
dann ist das auch in ein vernünftiges bildreinzukriegen
gruß
P.
ich sehe das ähnlich wie BICYPAPA das hier -@Beitrag Nr. 1.490- geschrieben hat
ich denke in den bewertungsdiskussionen muss man in ein paar, mindestens 3, "fenstern/ebenen" unterscheiden
dann ist das auch in ein vernünftiges bildreinzukriegen
gruß
P.
Was haltet Ihr von Pieris Pharmaceuticals?
Letzte Woche mit Nasdaq-Listing, bereits im Dezember über einen Börsenmantel an die OTC gegangen.
Technik sind Anticaline - Antikörper-ähnliche Moleküle
Lipocaline sind die Transporter im Organismus. Als Bestandteil von Blut und Tränenflüssigkeit binden die kelchförmigen Eiweiße empfindliche Hormone, schwerlösliche Vitamine oder Eisenmoleküle, die für Organismen und Krankheitserreger gleichermaßen lebenswichtig sind. Weil sich die modifizierten Lipocaline wie Antikörper verhalten, werden sie auch als „Anticaline“ bezeichnet. Allerdings sind sie achtmal kleiner, passen daher besser in Gewebezwischenräume und ihre Herstellung ist einfacher. Vor allem aber lassen sich Anticaline gut mit anderen Eiweißen zusammenfügen und können diese so mit zusätzlichen biochemischen Funktionen ausstatten.
Flagship ist aktuell PRS-080 Phase 1 - Behandlung von Anämie und funktionellem Eisenmangel.
Es gibt diverse Kooperationen mit u.a. mit Allergan, Sanofi und Daiichi-Sankyo, jedoch sind die zu erwarteten Meilensteine sehr niedrig, auch die zukünftige Umsatzbeteiligung.
Nicht zu verschweigen ist auch, dass das bisherige Aushängeschild PRS-050 gefloppt ist und man sich gerade auch noch in einer rechtlichen Auseinandersetzung mit der TU-München befindet, welche an der Entwicklung der Anticaline maßgeblich beteiligt war.
MarketCap ca. 130 Mio$.
http://www.pieris.com/pipeline/overview
Letzte Woche mit Nasdaq-Listing, bereits im Dezember über einen Börsenmantel an die OTC gegangen.
Technik sind Anticaline - Antikörper-ähnliche Moleküle
Lipocaline sind die Transporter im Organismus. Als Bestandteil von Blut und Tränenflüssigkeit binden die kelchförmigen Eiweiße empfindliche Hormone, schwerlösliche Vitamine oder Eisenmoleküle, die für Organismen und Krankheitserreger gleichermaßen lebenswichtig sind. Weil sich die modifizierten Lipocaline wie Antikörper verhalten, werden sie auch als „Anticaline“ bezeichnet. Allerdings sind sie achtmal kleiner, passen daher besser in Gewebezwischenräume und ihre Herstellung ist einfacher. Vor allem aber lassen sich Anticaline gut mit anderen Eiweißen zusammenfügen und können diese so mit zusätzlichen biochemischen Funktionen ausstatten.
Flagship ist aktuell PRS-080 Phase 1 - Behandlung von Anämie und funktionellem Eisenmangel.
Es gibt diverse Kooperationen mit u.a. mit Allergan, Sanofi und Daiichi-Sankyo, jedoch sind die zu erwarteten Meilensteine sehr niedrig, auch die zukünftige Umsatzbeteiligung.
Nicht zu verschweigen ist auch, dass das bisherige Aushängeschild PRS-050 gefloppt ist und man sich gerade auch noch in einer rechtlichen Auseinandersetzung mit der TU-München befindet, welche an der Entwicklung der Anticaline maßgeblich beteiligt war.
MarketCap ca. 130 Mio$.
http://www.pieris.com/pipeline/overview
Antwort auf Beitrag Nr.: 50.165.070 von ipollit am 11.07.15 13:23:54Hallo ipollit,
ja charttechnisch ist alles im grünen Bereich. Meine hohe Cashquote erklärt sich auch dadurch, dass ich einen Teil meines Depots in andere Assetklassen umschichten möchte. Leider ist es jetzt wohl zu spät Dax ETFs als 2. Assetklasse zu kaufen von daher muss ich jetzt mal sehen was ich mache.
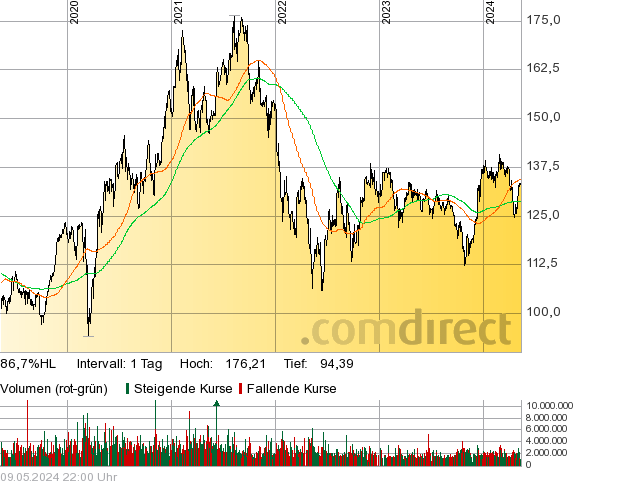
rot:100 - grün 200 Tageslinie
"Gefühlt" wäre eine Korrektur bis an die 200 Tageslinie mal wieder fällig. Aber ob bzw. wann es so kommt? Zudem sieht man im Chart auch ganz gut, dass die 200 Tageslinie auch stark steigt. Von daher könnte eine Korrektur in einigen Monaten immer noch an höheren Kursen als heute enden. Mein Plan ist aber erstmal die traditionell schwachen Sommermonate abzuwarten. Zudem könnte die Einführung der PCSK9 Antikörper Schwierigkeiten mit sich bringen.
SG kmastra
ja charttechnisch ist alles im grünen Bereich. Meine hohe Cashquote erklärt sich auch dadurch, dass ich einen Teil meines Depots in andere Assetklassen umschichten möchte. Leider ist es jetzt wohl zu spät Dax ETFs als 2. Assetklasse zu kaufen von daher muss ich jetzt mal sehen was ich mache.
rot:100 - grün 200 Tageslinie
"Gefühlt" wäre eine Korrektur bis an die 200 Tageslinie mal wieder fällig. Aber ob bzw. wann es so kommt? Zudem sieht man im Chart auch ganz gut, dass die 200 Tageslinie auch stark steigt. Von daher könnte eine Korrektur in einigen Monaten immer noch an höheren Kursen als heute enden. Mein Plan ist aber erstmal die traditionell schwachen Sommermonate abzuwarten. Zudem könnte die Einführung der PCSK9 Antikörper Schwierigkeiten mit sich bringen.
SG kmastra
Antwort auf Beitrag Nr.: 50.173.836 von kmastra am 13.07.15 11:43:48Hallo kmastra,
noch scheint es ja etwas weiter aufwärts zu gehen... IBB(NBI) und XBI heute mit neuem Allzeithoch. Mal schauen wie es die nächsten Wochen weiter geht...
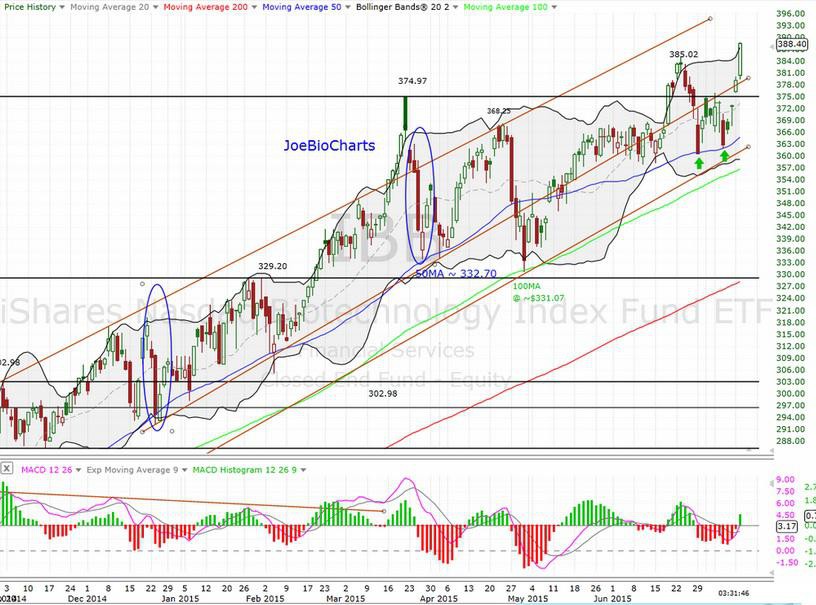
Gruß
ipollit
noch scheint es ja etwas weiter aufwärts zu gehen... IBB(NBI) und XBI heute mit neuem Allzeithoch. Mal schauen wie es die nächsten Wochen weiter geht...

Gruß
ipollit
CEMP
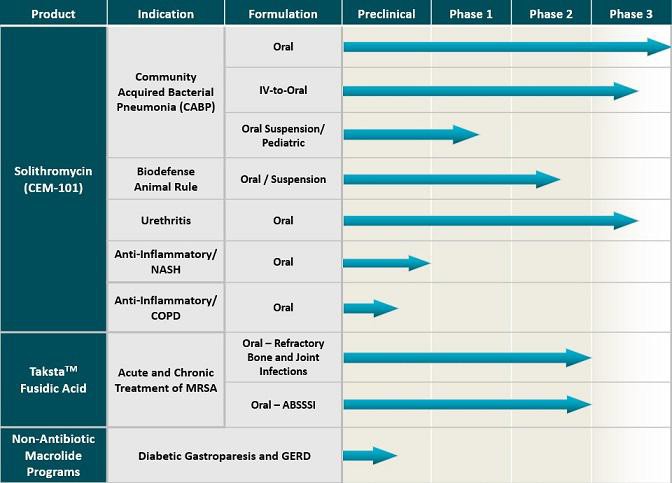
Meiner Meinung nach ist das Antibiotikum Solithromycin insbesondere gegen Lungenentzündung (CABP) sehr aussichtsreich. Solithromycin gehört zu etablierten Antibiotika-Klasse der Makrolide. So ist z.B. das generische Azithromycin mit 51 Mio Verschreibungen in den USA das führende Makrolide-Antibiotikum.
Makrolide-Antibiotika sind zwar sehr verbreitet und relativ verträglich, doch können leicht Resistenzen auftreten, die die Erkrankung schwerer behandelbar machen. Makrolide binden meist nur an einer Stelle an die Bakterien, so dass diese durch Modifikation dieser Stelle resistent werden können. Ketolides sind eine Makrolide-Variante, die über zwei oder mehr Stellen bindet, wodurch die Bakterien es sehr viel schwerer haben, Resistenzen zu bilden. Leider haben diese deutliche Nebenwirkungen... zugelassen mit entsprechenden Einschränkungen ist bisher nur Ketek. Solithromycin scheint nun das erste Ketolides-Antibiotika zu sein, das dreifach bindet und damit ein deutlich geringeres Resistenz-Risiko aufweist, gleichzeitig aber auch sehr verträglich ist.
Ein weiterer großer Vorteil von Solithromycin ist, dass es sowohl als Tablette, als auch intravenös verabreicht werden kann. Anders als mit anderen Makrolide-Antibiotika kann somit flexibel zwischen einer IV-Therapie im Krankenhaus und einer oralen Therapie zuhause gewechselt werden. Dadurch kann eine Behandlung im Krankenhaus verkürzt und Kosten gespart werden.
In der Indikation CABP war die erste PIII Anfang des Jahres bereits erfolgreich, Daten einer weiteren PIII sollen in Q4 folgen... mögliche Zulassung ist 2017. Neue Antibiotika, die helfen, Resistenzen zu überwinden, werden auch speziell vom amerikanischen Staat gefördert.
Solithromycin könnte desweiteren in der Lungenerkrankung CORD eine gute Option sein. Makrolide sind auch entzündungshemmend und kommen als Langzeit-Therapie in CORD zum Einsatz: "Darüber hinaus haben Makrolid-Antibiotika einen entzündungshemmenden und immun-modulierenden Effekt. Studien zeigten insbesondere bei einer Exazerbation einer chronisch obstruktiven Lungenerkrankung eine verminderte Zytokin-Produktion in den Lungen nach Gabe eines Makrolidantibiotikums."






Gruß
ipollit
Meiner Meinung nach ist das Antibiotikum Solithromycin insbesondere gegen Lungenentzündung (CABP) sehr aussichtsreich. Solithromycin gehört zu etablierten Antibiotika-Klasse der Makrolide. So ist z.B. das generische Azithromycin mit 51 Mio Verschreibungen in den USA das führende Makrolide-Antibiotikum.
Makrolide-Antibiotika sind zwar sehr verbreitet und relativ verträglich, doch können leicht Resistenzen auftreten, die die Erkrankung schwerer behandelbar machen. Makrolide binden meist nur an einer Stelle an die Bakterien, so dass diese durch Modifikation dieser Stelle resistent werden können. Ketolides sind eine Makrolide-Variante, die über zwei oder mehr Stellen bindet, wodurch die Bakterien es sehr viel schwerer haben, Resistenzen zu bilden. Leider haben diese deutliche Nebenwirkungen... zugelassen mit entsprechenden Einschränkungen ist bisher nur Ketek. Solithromycin scheint nun das erste Ketolides-Antibiotika zu sein, das dreifach bindet und damit ein deutlich geringeres Resistenz-Risiko aufweist, gleichzeitig aber auch sehr verträglich ist.
Ein weiterer großer Vorteil von Solithromycin ist, dass es sowohl als Tablette, als auch intravenös verabreicht werden kann. Anders als mit anderen Makrolide-Antibiotika kann somit flexibel zwischen einer IV-Therapie im Krankenhaus und einer oralen Therapie zuhause gewechselt werden. Dadurch kann eine Behandlung im Krankenhaus verkürzt und Kosten gespart werden.
In der Indikation CABP war die erste PIII Anfang des Jahres bereits erfolgreich, Daten einer weiteren PIII sollen in Q4 folgen... mögliche Zulassung ist 2017. Neue Antibiotika, die helfen, Resistenzen zu überwinden, werden auch speziell vom amerikanischen Staat gefördert.
Solithromycin könnte desweiteren in der Lungenerkrankung CORD eine gute Option sein. Makrolide sind auch entzündungshemmend und kommen als Langzeit-Therapie in CORD zum Einsatz: "Darüber hinaus haben Makrolid-Antibiotika einen entzündungshemmenden und immun-modulierenden Effekt. Studien zeigten insbesondere bei einer Exazerbation einer chronisch obstruktiven Lungenerkrankung eine verminderte Zytokin-Produktion in den Lungen nach Gabe eines Makrolidantibiotikums."






Gruß
ipollit
RCPT... Handel angehalten... vielleicht Übernahme? 
Gruß
ipollit

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.188.098 von ipollit am 14.07.15 22:49:12RCPT
tja... das ging schnell. CELG hat für 232 USD zugeschlagen. Mmm... hatte gehofft, es wird ein wenig mehr, aber okay!

Gruß
ipollit
tja... das ging schnell. CELG hat für 232 USD zugeschlagen. Mmm... hatte gehofft, es wird ein wenig mehr, aber okay!
Gruß
ipollit
tja, ein Wert weniger zu beobachten.
Und einer der Werte, die noch im Depot von SLGraham waren, was ihn für den Ausstieg aus anderen Werten zum m.E. nicht guten Zeitpunkt etwas entschädigen könnte.
Ich gehe davon aus, dass die kleinen guten Werte morgen wieder steigen, weil viele nach Übernahmen suchen, wer der nächste sein könnte. Ein paar "Lose" hab ich ja auch im Topf.
Und einer der Werte, die noch im Depot von SLGraham waren, was ihn für den Ausstieg aus anderen Werten zum m.E. nicht guten Zeitpunkt etwas entschädigen könnte.
Ich gehe davon aus, dass die kleinen guten Werte morgen wieder steigen, weil viele nach Übernahmen suchen, wer der nächste sein könnte. Ein paar "Lose" hab ich ja auch im Topf.
Antwort auf Beitrag Nr.: 50.188.224 von xylophon am 14.07.15 23:24:16In der Tat... noch ein Wert weniger... Eine Übernahme von RCPT war ja nicht ganz unwahrscheinlich, was auch ein Grund war, an dem Wert festzuhalten.
Indes ist es durchaus interessant hier zu beobachten, dass eine wirklich große Prämie hier nicht mehr drin war. Im Biotechbereich hat es ja oft Übernahmeprämien zwischen 30% bis zu mehr als 100% gegeben.
Das spricht eben auch dafür, dass die Börsenbewertungen doch viele Spielräume langsam ausgereizt haben.
PS: Auf RCPT hatte hier im Thread zuerst (vor einigen Monaten) ipollit aufmerksam gemacht. An mir war der Wert bis dahin komplett vorbei gegangen. Wie so oft habe ich ipollit hier sehr viel zu verdanken.
Indes ist es durchaus interessant hier zu beobachten, dass eine wirklich große Prämie hier nicht mehr drin war. Im Biotechbereich hat es ja oft Übernahmeprämien zwischen 30% bis zu mehr als 100% gegeben.
Das spricht eben auch dafür, dass die Börsenbewertungen doch viele Spielräume langsam ausgereizt haben.
PS: Auf RCPT hatte hier im Thread zuerst (vor einigen Monaten) ipollit aufmerksam gemacht. An mir war der Wert bis dahin komplett vorbei gegangen. Wie so oft habe ich ipollit hier sehr viel zu verdanken.
RLYP /(ZSPH)
meine ZSPH Position werde ich wohl noch um RLYP ergänzen. Beide Mittel (RLYPs Patiromer und ZSPHs ZS-9) haben ihre Vor- und Nachteile... einen klaren Gewinner gibt es bisher nicht. Patiromer wird wahrscheinlich zuerst die Zulassung erhalten... PDFUA ist der 21.10. Der Börsenwert von RLYP liegt mit 1,34 Mrd USD etwas unter dem von ZSPH mit 1,56 Mrd USD.
Hier scheint sich jemand auf Twitter in dem Bereich auszukennen und beide positiv zu sehen: https://twitter.com/Sharma1981N/with_replies




Gruß
ipollit
meine ZSPH Position werde ich wohl noch um RLYP ergänzen. Beide Mittel (RLYPs Patiromer und ZSPHs ZS-9) haben ihre Vor- und Nachteile... einen klaren Gewinner gibt es bisher nicht. Patiromer wird wahrscheinlich zuerst die Zulassung erhalten... PDFUA ist der 21.10. Der Börsenwert von RLYP liegt mit 1,34 Mrd USD etwas unter dem von ZSPH mit 1,56 Mrd USD.
Hier scheint sich jemand auf Twitter in dem Bereich auszukennen und beide positiv zu sehen: https://twitter.com/Sharma1981N/with_replies


Gruß
ipollit
Antwort auf Beitrag Nr.: 50.188.809 von SLGramann am 15.07.15 07:28:18Hallo SLGramann,
"An mir war der Wert bis dahin komplett vorbei gegangen."... naja, lange Zeit habe ich ihn auch nicht gesehen und ich bin auch erst seit Kurzem dabei, fast schon zu spät. Bei dir kann ich mich z.B. für ACAD bedanken, die du hier vorgestellt hast! Ist inzwischen meine zweitgrößte Position. Danke!
Viele Grüße
ipollit
"An mir war der Wert bis dahin komplett vorbei gegangen."... naja, lange Zeit habe ich ihn auch nicht gesehen und ich bin auch erst seit Kurzem dabei, fast schon zu spät. Bei dir kann ich mich z.B. für ACAD bedanken, die du hier vorgestellt hast! Ist inzwischen meine zweitgrößte Position. Danke!
Viele Grüße
ipollit
ja, was ihr hier schreibt, ist bares Geld wert. Ich habe zwar von den medizinischen Fragen keine Ahnung, man merkt aber schon, wessen Beiträge Substanz haben und davon gibt es hier eine Menge.
Antwort auf Beitrag Nr.: 50.191.719 von ipollit am 15.07.15 13:28:38http://www.aerzteblatt.de/nachrichten/63487/Patiromer-Polyme…
Patiromer kling in der Tat sehr vielversprechend und die Zulassung wird offenbar mit viel Power vorangetrieben!
Patiromer kling in der Tat sehr vielversprechend und die Zulassung wird offenbar mit viel Power vorangetrieben!
zu europäischer biotechnologie gibt es hier einige dinge zu lesen, aber da sind die weideflächen ja glaube ich nicht sooo groß, und saftig 
The state of healthcare biotech in Europe
http://biotechaddress.europabio.org/the-state-of-healthcare-…
A European Biotech Stock Basket For 2015 - An Update
http://seekingalpha.com/article/3332095-a-european-biotech-s…
gruß
P.

The state of healthcare biotech in Europe
http://biotechaddress.europabio.org/the-state-of-healthcare-…
A European Biotech Stock Basket For 2015 - An Update
http://seekingalpha.com/article/3332095-a-european-biotech-s…
gruß
P.
NBI
Bezüglich einer möglichen Überbewertung der Biotechs: Im PEG Verhältnis von KGV zum Gewinnwachstum sieht es bei den großen Biotechs eigentlich besser aus als bei den Pharmas (je kleiner, umso besser... PEG von 1 ist gut)
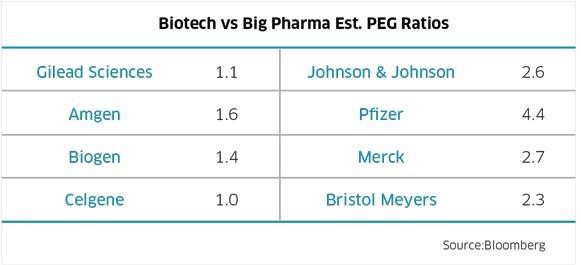
Ausblick auf die Q2-Zahlen...


Gruß
ipollit
Bezüglich einer möglichen Überbewertung der Biotechs: Im PEG Verhältnis von KGV zum Gewinnwachstum sieht es bei den großen Biotechs eigentlich besser aus als bei den Pharmas (je kleiner, umso besser... PEG von 1 ist gut)

Ausblick auf die Q2-Zahlen...

Gruß
ipollit
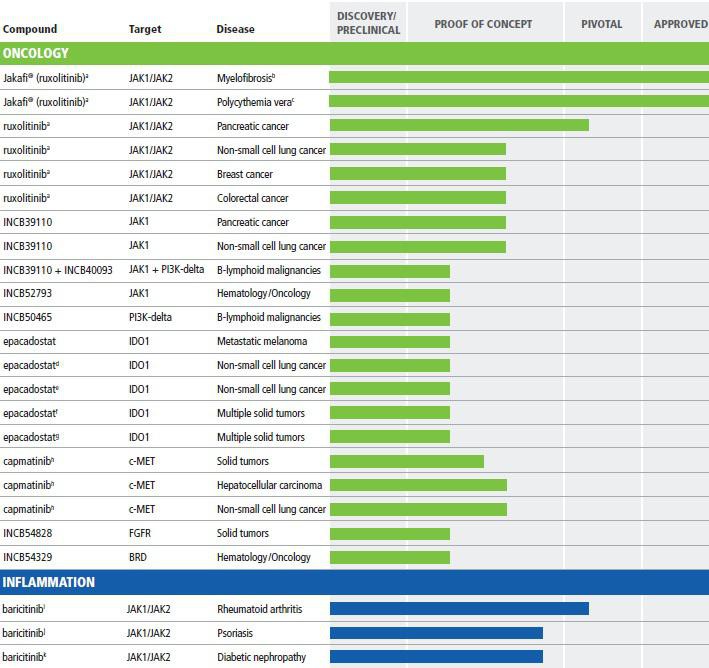
INCY
ist mit einer Marktkapitalisierung von 21 Mrd USD zwar nicht billig, könnte aber mittel-/langfristig zur nächsten CELG werden, falls es nicht vorher zu einer Übernahme kommt (z.B. wurde INCY zuletzt als möglicher Übernahmekandidat von GILD gehandelt).
Der Jak-Hemmer Jakafi entwickelt sich in MF/PV offensichtlich sehr gut. Alleine in den USA könnten bis zu 3 Mrd USD in diesen beiden Indikationen möglich sein... hier besitzt INCY 100% der Rechte. Außerhalb von Amerika ist der Markt vielleicht ähnlich groß... hier erhält INCY vom Partner NVS nochmal 17-25% Royalties. Jakafi könnte als JAK-Hemmer aber auch größeres Potential in mehreren Krebs-Indikationen haben.
Größere Umsätze könnte im Erfolgsfall auch der JAK-Hemmer Baricitinib gegen RA einbringen, der zusammen Lilly entwickelt wird und für den INCY bis zu 30% Royalties erhält.
Ein hohes Potential könnte auch INCY's IDO-Hemmer besitzen, der sich erst in der früheren klinischen Phase befindet. IDO-Hemmer sollen gut mit PD1-AKs gegen Krebs kombinierbar sein. Während es viele konkurrierende PD1-AKs bei den Pharmas gibt, hätte INCY einen großen Vorteil mit dem führenden IDO-Hemmer.
Insgesamt ist INCY im Krebsbereich sehr gut aufgestellt als führendes Unternehmen im JAK- und IDO-Bereich + mehrerer weiterer Target, die diese ergänzen.





Gruß
ipollit
ist mit einer Marktkapitalisierung von 21 Mrd USD zwar nicht billig, könnte aber mittel-/langfristig zur nächsten CELG werden, falls es nicht vorher zu einer Übernahme kommt (z.B. wurde INCY zuletzt als möglicher Übernahmekandidat von GILD gehandelt).
Der Jak-Hemmer Jakafi entwickelt sich in MF/PV offensichtlich sehr gut. Alleine in den USA könnten bis zu 3 Mrd USD in diesen beiden Indikationen möglich sein... hier besitzt INCY 100% der Rechte. Außerhalb von Amerika ist der Markt vielleicht ähnlich groß... hier erhält INCY vom Partner NVS nochmal 17-25% Royalties. Jakafi könnte als JAK-Hemmer aber auch größeres Potential in mehreren Krebs-Indikationen haben.
Größere Umsätze könnte im Erfolgsfall auch der JAK-Hemmer Baricitinib gegen RA einbringen, der zusammen Lilly entwickelt wird und für den INCY bis zu 30% Royalties erhält.
Ein hohes Potential könnte auch INCY's IDO-Hemmer besitzen, der sich erst in der früheren klinischen Phase befindet. IDO-Hemmer sollen gut mit PD1-AKs gegen Krebs kombinierbar sein. Während es viele konkurrierende PD1-AKs bei den Pharmas gibt, hätte INCY einen großen Vorteil mit dem führenden IDO-Hemmer.
Insgesamt ist INCY im Krebsbereich sehr gut aufgestellt als führendes Unternehmen im JAK- und IDO-Bereich + mehrerer weiterer Target, die diese ergänzen.





Gruß
ipollit
FPRX
FPRX hat den GITR-AK INBRX-110 von Inhibrx einlizensiert (CELGs CD47-AK kommt ebenfalls von Inhibrx). AGEN und INCY entwickeln zusammen auch mehrere GITR-AKs, die in den nächsten 12 Monaten in PI gehen könnten. Insgesamt scheint FPRX bei der Entwicklung neuer IO-Targets sehr aktiv zu sein.




Gruß
ipollit
FPRX hat den GITR-AK INBRX-110 von Inhibrx einlizensiert (CELGs CD47-AK kommt ebenfalls von Inhibrx). AGEN und INCY entwickeln zusammen auch mehrere GITR-AKs, die in den nächsten 12 Monaten in PI gehen könnten. Insgesamt scheint FPRX bei der Entwicklung neuer IO-Targets sehr aktiv zu sein.



Gruß
ipollit
Antwort auf Beitrag Nr.: 50.219.361 von ipollit am 19.07.15 19:15:01"ist mit einer Marktkapitalisierung von 21 Mrd USD zwar nicht billig, könnte aber mittel-/langfristig zur nächsten CELG werden, falls es nicht vorher zu einer Übernahme kommt (z.B. wurde INCY zuletzt als möglicher Übernahmekandidat von GILD gehandelt)."
Hallo ipollit,
wie Du vielleicht schon gesehen hast, hat Hammer heute INCY verkauft, weil ihm die Bewertung zu hoch geworden ist.
http://www.orf-blog.com/trevena-late-stage-innovation-flying…
Ich teile grundsätzlich Deine Einschätzung. Insbesondere teile ich Deine Kritik an Hammers Ansatz, offenbar eine niedrige (billige) Börsenbewertung höher zu schätzen, als teurere, aber klar erkennbare Qualität.
Nach meiner Erfahrung ist es besser, für überragende Qualität auch mal mehr zu bezahlen, als nach vermeintlichen Schnäppchen zu jagen.
Dessen ungeachtet finde ich die Bewertungen zum Teil schon abenteuerlich und auch im Falle INCY einfach zu hoch.
An einem bestimmten Punkt lassen sich Preise auch nicht mehr durch ein Mehr an Qualität rechtfertigen.
Für mich ist dieser Punkt in weiten Teilen des Biotech-Marktes erreicht.
Hammer ist jetzt bei 40%-Cashquote - auch schon recht extrem.
Bin wirklich gespannt, wie es weitergeht.
(Der Trevena-Artikel reißt mich auch nicht gerade vom Hocker. Wenn ich an die Zeiten denke, als ein INCY in Hammers Depot auftauchte zu einem Preis von wenigen hundert Millionen, aber schon damals mit klarer Perspektive für eine Zulassung und fette Umsätze... so etwas überzeugendes habe ich bei ihm schon lange nicht mehr gefunden. Seit er sich vom Onkologie-Bereich weg bewegt, finde ich den Blog schwächer.)
Hallo ipollit,
wie Du vielleicht schon gesehen hast, hat Hammer heute INCY verkauft, weil ihm die Bewertung zu hoch geworden ist.
http://www.orf-blog.com/trevena-late-stage-innovation-flying…
Ich teile grundsätzlich Deine Einschätzung. Insbesondere teile ich Deine Kritik an Hammers Ansatz, offenbar eine niedrige (billige) Börsenbewertung höher zu schätzen, als teurere, aber klar erkennbare Qualität.
Nach meiner Erfahrung ist es besser, für überragende Qualität auch mal mehr zu bezahlen, als nach vermeintlichen Schnäppchen zu jagen.
Dessen ungeachtet finde ich die Bewertungen zum Teil schon abenteuerlich und auch im Falle INCY einfach zu hoch.
An einem bestimmten Punkt lassen sich Preise auch nicht mehr durch ein Mehr an Qualität rechtfertigen.
Für mich ist dieser Punkt in weiten Teilen des Biotech-Marktes erreicht.
Hammer ist jetzt bei 40%-Cashquote - auch schon recht extrem.
Bin wirklich gespannt, wie es weitergeht.
(Der Trevena-Artikel reißt mich auch nicht gerade vom Hocker. Wenn ich an die Zeiten denke, als ein INCY in Hammers Depot auftauchte zu einem Preis von wenigen hundert Millionen, aber schon damals mit klarer Perspektive für eine Zulassung und fette Umsätze... so etwas überzeugendes habe ich bei ihm schon lange nicht mehr gefunden. Seit er sich vom Onkologie-Bereich weg bewegt, finde ich den Blog schwächer.)
EXEL
schön, dass METEOR erfolgreich war! Prima ist, dass auch OS positiv ausfallen könnte... damit wäre Cabo klar besser als alle 2nd-line RCC Mittel, die keinen OS-Vorteil besitzen

Interessant, dass neben VEGF und MET hier auch mal AXL als Target von Cabo genannt wird. Ohad Hammer hat AXL mal als interessantes Target bezeichnet.
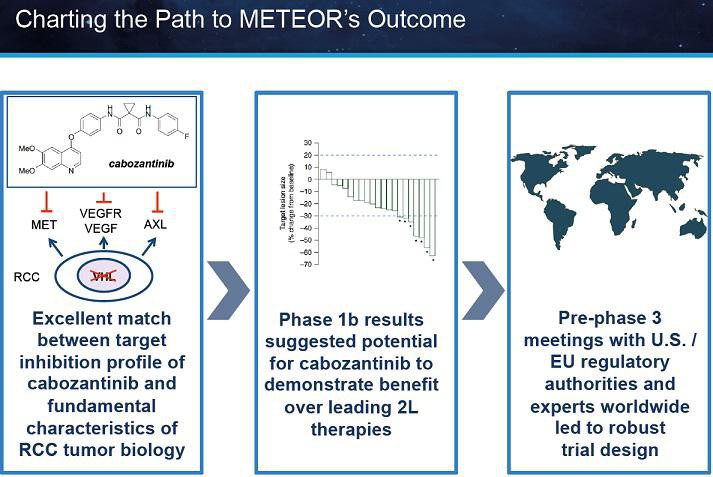
1st-line P2-Daten gegen den Standard Sutent könnten nächstes Jahr folgen... außerdem werden IO-Kombis mit Nivo und Ipi getestet.

US- und EU-Zulassung in RCC dürfte Anfang 2016 beantragt werden. Ein Fast-Track könnte den Prozess beschleunigen. ex-US wird zudem ein Vermarktungs-Partner gesucht.
Im Oktober steht zudem die Zulassung von Cobi an, für das man eventuelle Gewinne in den USA mit Roche teilt.

Gruß
ipollit
schön, dass METEOR erfolgreich war! Prima ist, dass auch OS positiv ausfallen könnte... damit wäre Cabo klar besser als alle 2nd-line RCC Mittel, die keinen OS-Vorteil besitzen

Interessant, dass neben VEGF und MET hier auch mal AXL als Target von Cabo genannt wird. Ohad Hammer hat AXL mal als interessantes Target bezeichnet.

1st-line P2-Daten gegen den Standard Sutent könnten nächstes Jahr folgen... außerdem werden IO-Kombis mit Nivo und Ipi getestet.

US- und EU-Zulassung in RCC dürfte Anfang 2016 beantragt werden. Ein Fast-Track könnte den Prozess beschleunigen. ex-US wird zudem ein Vermarktungs-Partner gesucht.
Im Oktober steht zudem die Zulassung von Cobi an, für das man eventuelle Gewinne in den USA mit Roche teilt.
Gruß
ipollit
ist jemand hier bei sernova dabei? was haltet ihr von diesem biotech-unternehmen?
Antwort auf Beitrag Nr.: 50.219.619 von SLGramann am 19.07.15 20:29:55Hallo SLGramann,
ich finde es nicht leicht zu sagen, was eine angemessene Bewertung ist. Sicherlich sind die Biotechs nicht mehr billig, das stimmt. Soll aber nun eine INCY besser 10 oder 20 Mrd wert sein? 10 Mrd USD finde ich auch bereits viel. Sicherlich würde ich jetzt gerne auch eine solche Aktie bei einer Bewertung von unter 1 Mrd USD kaufen, aber wäre sie momentan soviel Wert, würde wahrscheinlich auch etwas nicht stimmen... dann wären z.B. die Peak Sales für Jakafi wenig realistisch. Ich denke auch nicht, dass INCY sich in der nächsten Zeit nochmals verdoppelt. Es ist meine größte Position, trotzdem habe ich sie zuletzt auch immer etwas mehr reduziert und z.B. in XLRN oder ITCI umgeschichtet.
Andererseits solange die Aktie läuft, lasse ich sie nun auch laufen. Eine REGN habe ich jahrelang verkauft. Eine MK von 5 Mrd fand ich für REGN viel und habe einen Teil verkauft... 10 Mrd USD waren noch unrealistischer... wieder reduziert. Nach zahlreichen weiteren Verkäufen habe ich zuletzt bei einem Kurs von 400 USD deutlich reduziert. Jetzt steht REGN bei über 550 USD und einer MK von fast 60 Mrd USD. Immer noch sehr teuer!

Gleiches gilt z.B. für ALNY... bei 17 USD reduziert, weil zu teuer... bei 24 USD, weil viel zu teuer. Nun steht der Kurs bei über 130 USD und einer MK von über 11 Mrd USD. Zuletzt habe ich wieder reduziert... allerdings verkaufe ich immer nur Teile. Wenn es nach einer angemessenen Bewertung geht, hätte ich wahrscheinlich schon alles zu 17 verkauft.

Bezügl. INCY kann ich mich sehr bei Ohad Hammer bedanken... die habe ich glücklicherweise aufgrund seiner Empfehlung zum Tief bei 3 USD gekauft. Allerdings war es meine ich nicht so klar wie du schreibst "aber schon damals mit klarer Perspektive für eine Zulassung und fette Umsätze". Damals war INCY sehr stark verschuldet... hätte es mit Jakafi nur geringe Probleme gegeben, hätte INCY das wohl nicht überlebt.

Grüße
ipollit
ich finde es nicht leicht zu sagen, was eine angemessene Bewertung ist. Sicherlich sind die Biotechs nicht mehr billig, das stimmt. Soll aber nun eine INCY besser 10 oder 20 Mrd wert sein? 10 Mrd USD finde ich auch bereits viel. Sicherlich würde ich jetzt gerne auch eine solche Aktie bei einer Bewertung von unter 1 Mrd USD kaufen, aber wäre sie momentan soviel Wert, würde wahrscheinlich auch etwas nicht stimmen... dann wären z.B. die Peak Sales für Jakafi wenig realistisch. Ich denke auch nicht, dass INCY sich in der nächsten Zeit nochmals verdoppelt. Es ist meine größte Position, trotzdem habe ich sie zuletzt auch immer etwas mehr reduziert und z.B. in XLRN oder ITCI umgeschichtet.
Andererseits solange die Aktie läuft, lasse ich sie nun auch laufen. Eine REGN habe ich jahrelang verkauft. Eine MK von 5 Mrd fand ich für REGN viel und habe einen Teil verkauft... 10 Mrd USD waren noch unrealistischer... wieder reduziert. Nach zahlreichen weiteren Verkäufen habe ich zuletzt bei einem Kurs von 400 USD deutlich reduziert. Jetzt steht REGN bei über 550 USD und einer MK von fast 60 Mrd USD. Immer noch sehr teuer!
Gleiches gilt z.B. für ALNY... bei 17 USD reduziert, weil zu teuer... bei 24 USD, weil viel zu teuer. Nun steht der Kurs bei über 130 USD und einer MK von über 11 Mrd USD. Zuletzt habe ich wieder reduziert... allerdings verkaufe ich immer nur Teile. Wenn es nach einer angemessenen Bewertung geht, hätte ich wahrscheinlich schon alles zu 17 verkauft.
Bezügl. INCY kann ich mich sehr bei Ohad Hammer bedanken... die habe ich glücklicherweise aufgrund seiner Empfehlung zum Tief bei 3 USD gekauft. Allerdings war es meine ich nicht so klar wie du schreibst "aber schon damals mit klarer Perspektive für eine Zulassung und fette Umsätze". Damals war INCY sehr stark verschuldet... hätte es mit Jakafi nur geringe Probleme gegeben, hätte INCY das wohl nicht überlebt.
Grüße
ipollit
FGEN
hier habe ich in der letzten Zeit auch hinzugekauft... wahrscheinlich gab es aufgrund des Auslaufens von Haltefristen diesen Sell-Off.

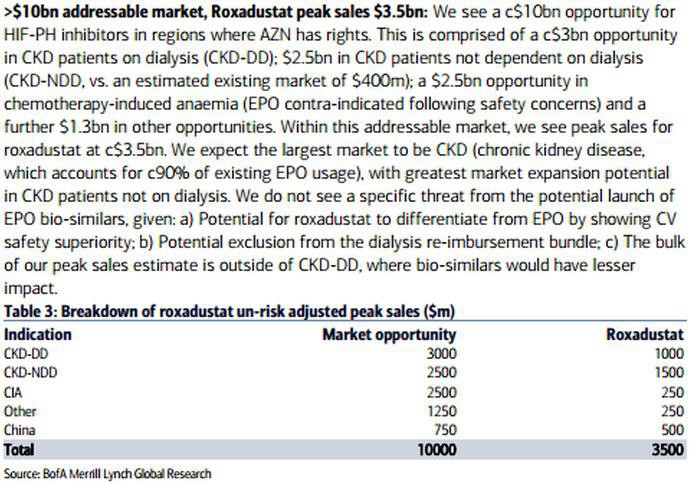
Alleine für AZN (US-Markt + China) werden Roxa Umsätze von 3,4 Mrd geschätzt... FGEN erhält hiervon Royalties zwischen 20% und 25%, in China werden die Umsätze mit AZN geteilt.
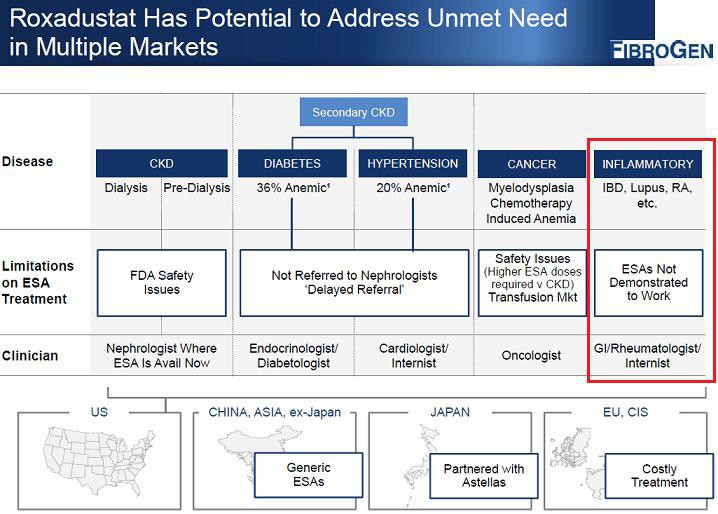
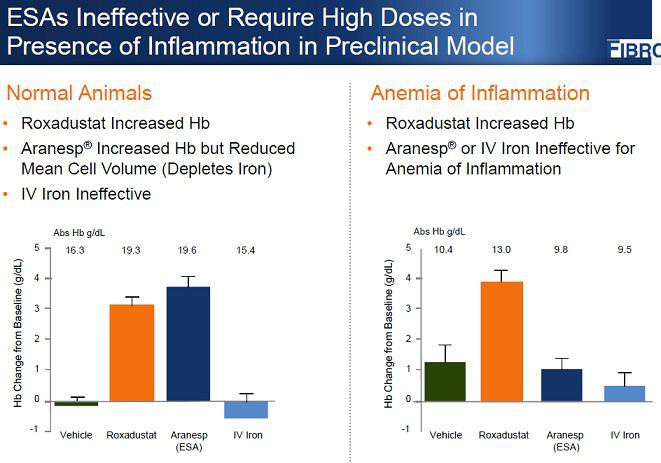
Blutarmut könnte auch eine Folge von chronischen Entzündungen wie RA usw sein, wenn ich das Folgende richtig verstehe. In diesem Fall helfen ESAs nichts... Roxa zeigt aber eine Wirkung:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"Doing a bit of digging here, it seems hepcidin is typically somewhat low in CHF patients, consistent with chronic HIF upregulation. Of course you would expect HIF to be upregulated in any chronic hypoxic condition.
I don't think the Street has fully appreciated the hepcidin data yet. For example, around half of RA patients have upregulated hepcidin and (likely as a result) chronic anemia. So right there is a massive potential market that nobody has discussed much."

Gruß
ipollit
hier habe ich in der letzten Zeit auch hinzugekauft... wahrscheinlich gab es aufgrund des Auslaufens von Haltefristen diesen Sell-Off.

Alleine für AZN (US-Markt + China) werden Roxa Umsätze von 3,4 Mrd geschätzt... FGEN erhält hiervon Royalties zwischen 20% und 25%, in China werden die Umsätze mit AZN geteilt.

Blutarmut könnte auch eine Folge von chronischen Entzündungen wie RA usw sein, wenn ich das Folgende richtig verstehe. In diesem Fall helfen ESAs nichts... Roxa zeigt aber eine Wirkung:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"Doing a bit of digging here, it seems hepcidin is typically somewhat low in CHF patients, consistent with chronic HIF upregulation. Of course you would expect HIF to be upregulated in any chronic hypoxic condition.
I don't think the Street has fully appreciated the hepcidin data yet. For example, around half of RA patients have upregulated hepcidin and (likely as a result) chronic anemia. So right there is a massive potential market that nobody has discussed much."


Gruß
ipollit
CEMP
hier noch ein wenig zum Potential in der Lungenkrankheit CORD...




Gruß
ipollit
hier noch ein wenig zum Potential in der Lungenkrankheit CORD...



Gruß
ipollit
Antwort auf Beitrag Nr.: 50.228.055 von ipollit am 20.07.15 22:21:37Hallo ipollit,
was die Definition einer gerechten Bewertung angeht, habe ich ähnliche Erfahrungen gemacht. Eine ISIS habe ich zu 8$ gekauft und für 16$ und 24$ verkauft. Eine MOR habe ich bei 30 € geschmissen. Die Bewertung sind aktuell teilweise schon Recht hoch.
Ich finde eine ALNY im Gegensatz zu einer ARWR krass überbewertet. Auch RGLS ist auf über 20$ gelaufen und jetzt um die Hälfte eingebrochen, nachdem das halbe Management sich verflüchtigt hat.
Es gibt im Markt aktuell zu viel Geld. Ich glaube für alle die Lange dabei sind, eine ungewohnte Situation weil wir jahrelange sehr niedrige Bewertungen im Sektor gesehen haben. Das triftt auch auf Technologie- und Softwarebranche zu. Da werden auch Mondpreise für das Internet der Dinge bezahlt.
Ich glaube aber auch das es noch echte Schnäppchen gibt, gerade weil diese Aktien gerade nicht im Fokus stehen oder wie bei FGEN Haltefristen ausgelaufen sind. Ich nehme da gerne auch eine OMED die echt geile Partnerschaften und eine recht breite Pipeline hat (wenn auch eine frühe) und trotzdem eine Recht bescheidene Bewertung aufweist.
Ich hatte OMED immer gegenüber MGNX favourisiert, jedoch ist letztere weit aus besser gelaufen.
Oder eine Bellicum, Hälfte der Bewertung ist Cash und wenn ich mir die Mitbewerber so anschaue, kann ich dies auch nicht nachvollziehen.
Gut dann kommen dann wieder Begriffe wie Technologische Führerschaft, First to Market etc. aber die anderen müssen auch erst liefern. Siehe AAVL, viele gute Kommentare im Vorfeld.
Galapagos vs. Ablynx kann ich noch nennen, beide einen Deal mit Abbvie. Wieso Galapagos mit dem 5 fachen von Ablynx bewertet wird erschließt sich mir auch nicht, zu mal beide Rückschläge in der Pipeline hinnehmen mussten.
Ich bin allerdings auch zu 100% investiert, kein Cash. So lange die Angst uns immer noch begleitet, die Zinsen niedrig sind (geschissen auf die vielleicht Anhebung der FED im September, die ich eh nur als symbolische Geste betrachte) wird der Markt weiter nach oben gehen. Und von den Blasen der Dot.com-Ära und Japans Anfang der 90iger sind wir noch weit entfernt. Ich glaube das wir noch eine extreme Überhitzung sehen, bevor der Markt sich bereinigt.
was die Definition einer gerechten Bewertung angeht, habe ich ähnliche Erfahrungen gemacht. Eine ISIS habe ich zu 8$ gekauft und für 16$ und 24$ verkauft. Eine MOR habe ich bei 30 € geschmissen. Die Bewertung sind aktuell teilweise schon Recht hoch.
Ich finde eine ALNY im Gegensatz zu einer ARWR krass überbewertet. Auch RGLS ist auf über 20$ gelaufen und jetzt um die Hälfte eingebrochen, nachdem das halbe Management sich verflüchtigt hat.
Es gibt im Markt aktuell zu viel Geld. Ich glaube für alle die Lange dabei sind, eine ungewohnte Situation weil wir jahrelange sehr niedrige Bewertungen im Sektor gesehen haben. Das triftt auch auf Technologie- und Softwarebranche zu. Da werden auch Mondpreise für das Internet der Dinge bezahlt.
Ich glaube aber auch das es noch echte Schnäppchen gibt, gerade weil diese Aktien gerade nicht im Fokus stehen oder wie bei FGEN Haltefristen ausgelaufen sind. Ich nehme da gerne auch eine OMED die echt geile Partnerschaften und eine recht breite Pipeline hat (wenn auch eine frühe) und trotzdem eine Recht bescheidene Bewertung aufweist.
Ich hatte OMED immer gegenüber MGNX favourisiert, jedoch ist letztere weit aus besser gelaufen.
Oder eine Bellicum, Hälfte der Bewertung ist Cash und wenn ich mir die Mitbewerber so anschaue, kann ich dies auch nicht nachvollziehen.
Gut dann kommen dann wieder Begriffe wie Technologische Führerschaft, First to Market etc. aber die anderen müssen auch erst liefern. Siehe AAVL, viele gute Kommentare im Vorfeld.
Galapagos vs. Ablynx kann ich noch nennen, beide einen Deal mit Abbvie. Wieso Galapagos mit dem 5 fachen von Ablynx bewertet wird erschließt sich mir auch nicht, zu mal beide Rückschläge in der Pipeline hinnehmen mussten.
Ich bin allerdings auch zu 100% investiert, kein Cash. So lange die Angst uns immer noch begleitet, die Zinsen niedrig sind (geschissen auf die vielleicht Anhebung der FED im September, die ich eh nur als symbolische Geste betrachte) wird der Markt weiter nach oben gehen. Und von den Blasen der Dot.com-Ära und Japans Anfang der 90iger sind wir noch weit entfernt. Ich glaube das wir noch eine extreme Überhitzung sehen, bevor der Markt sich bereinigt.
ESPR
Diesen Monat kommen wohl noch weitere Daten zu ETC-1002. Bis September soll dann Klarheit bezügl. der durchzuführenden PIII bestehen. Wie unten beschrieben, gab es zuletzt Unsicherheiten, ob nicht ganz so große PIII-Studien auf Basis von LDL-Reduktion ausreichen oder ob die FDA verlangt umfangreiche und sehr lange PIII-Studien verlangt, die einen positiven Effekt auf die Sterblichkeit nachweisen müssen.
Heute wurde AMGNs PCSK9-AK Repatha in Europa zugelassen mit einem guten Label, das auch große Statin-intolerante Patientengruppen einschließt. Dies stützt die LDL-Hypothese, da Repatha bisher auch nur eine LDL-Reduktion nachgewiesen hat.
Zudem gibt es auch einen Hinweis der FDA, dass sie LDL als ein Problem ansieht und somit bereits eine Reduktion positiv wäre: Sie verbietet schlechte Fette in Lebensmitteln ab 2018 und begründet das u.a. mit den Risiken von LDL.
Dies alles ist prinzipiell positiv für ESPR.





Gruß
ipollit
Diesen Monat kommen wohl noch weitere Daten zu ETC-1002. Bis September soll dann Klarheit bezügl. der durchzuführenden PIII bestehen. Wie unten beschrieben, gab es zuletzt Unsicherheiten, ob nicht ganz so große PIII-Studien auf Basis von LDL-Reduktion ausreichen oder ob die FDA verlangt umfangreiche und sehr lange PIII-Studien verlangt, die einen positiven Effekt auf die Sterblichkeit nachweisen müssen.
Heute wurde AMGNs PCSK9-AK Repatha in Europa zugelassen mit einem guten Label, das auch große Statin-intolerante Patientengruppen einschließt. Dies stützt die LDL-Hypothese, da Repatha bisher auch nur eine LDL-Reduktion nachgewiesen hat.
Zudem gibt es auch einen Hinweis der FDA, dass sie LDL als ein Problem ansieht und somit bereits eine Reduktion positiv wäre: Sie verbietet schlechte Fette in Lebensmitteln ab 2018 und begründet das u.a. mit den Risiken von LDL.
Dies alles ist prinzipiell positiv für ESPR.




Gruß
ipollit
ARRY:
unerwartet und bitter:
BOULDER, Colo., July 22, 2015 /PRNewswire/ -- AstraZeneca today announced that the Phase 3 SUMIT study of selumetinib in combination with dacarbazine for the treatment of patients with metastatic uveal melanoma did not meet its primary endpoint of progression free survival. This combination therapy showed an adverse event profile generally consistent with current knowledge of the safety profiles of dacarbazine and selumetinib. A full evaluation of the data is ongoing. - See more at:
unerwartet und bitter:
BOULDER, Colo., July 22, 2015 /PRNewswire/ -- AstraZeneca today announced that the Phase 3 SUMIT study of selumetinib in combination with dacarbazine for the treatment of patients with metastatic uveal melanoma did not meet its primary endpoint of progression free survival. This combination therapy showed an adverse event profile generally consistent with current knowledge of the safety profiles of dacarbazine and selumetinib. A full evaluation of the data is ongoing. - See more at:
Antwort auf Beitrag Nr.: 50.238.291 von SLGramann am 22.07.15 08:57:21Oje! Ich war da eigentlich recht optimistisch. Die P2 sah ja ganz gut aus.
http://www.fiercebiotech.com/story/astrazenecas-selumetinib-…
Mal sehen was der Markt da heute draus macht. Einerseits wäre das ja eine sehr kleine kommerzielle Chance gewesen. Adererseits wird man eventuell jetzt automatisch die Chancen auf einen Erfolg in anderen Indikationen pessimistischer sehen. Eventuell ja auch eine Chance zum Nachkauf?
http://www.fiercebiotech.com/story/astrazenecas-selumetinib-…
Mal sehen was der Markt da heute draus macht. Einerseits wäre das ja eine sehr kleine kommerzielle Chance gewesen. Adererseits wird man eventuell jetzt automatisch die Chancen auf einen Erfolg in anderen Indikationen pessimistischer sehen. Eventuell ja auch eine Chance zum Nachkauf?
ich kann ja relativ wenig beitragen, aber diesen Artikel fand ich ganz interessant, gerade auch für Laien verständlich.
http://www.faz.net/aktuell/wissen/alzheimer-therapie-es-ist-…
http://www.faz.net/aktuell/wissen/alzheimer-therapie-es-ist-…
Antwort auf Beitrag Nr.: 50.229.831 von McNay am 21.07.15 09:08:37Hallo McNay,
danke für deinen Hinweis auf OMED. Diese hatte ich früher für interessant gehalten, aber dann nicht weiter verfolgt, weil ich es merkwürdig gefunden habe, dass man am DLL4-AK festhält, obwohl viele andere dieses Target aufgrund der Herzprobleme aufgegeben haben. Bisher scheinen sie aber das Problem noch im Griff zu haben, oder? Ich werde mir das Unternehmen nochmal genauer ansehen.
Wie ich vor ein paar Tagen geschrieben habe, hat FPRX ja einen GITR-AK einlizensiert. Hierbei wurde die fc-Problematik erwähnt. Offensichtlich scheint OMED diesbezüglich auch eine Lösung gefunden zu haben. Ist mittelfristig auch ein IND geplant?
Grüße
ipollit
danke für deinen Hinweis auf OMED. Diese hatte ich früher für interessant gehalten, aber dann nicht weiter verfolgt, weil ich es merkwürdig gefunden habe, dass man am DLL4-AK festhält, obwohl viele andere dieses Target aufgrund der Herzprobleme aufgegeben haben. Bisher scheinen sie aber das Problem noch im Griff zu haben, oder? Ich werde mir das Unternehmen nochmal genauer ansehen.
Wie ich vor ein paar Tagen geschrieben habe, hat FPRX ja einen GITR-AK einlizensiert. Hierbei wurde die fc-Problematik erwähnt. Offensichtlich scheint OMED diesbezüglich auch eine Lösung gefunden zu haben. Ist mittelfristig auch ein IND geplant?
Grüße
ipollit
Antwort auf Beitrag Nr.: 50.254.104 von ipollit am 23.07.15 23:16:59Hallo ipollit,
lt. der PH1a scheint OMED die Herzprobleme bei Demcizumab gut im Griff zu haben. Interessant ist sicherlich auch der bispezifische OMP-305B83 (Anti-DLL4/VEGF), hier könnte es aber die selben Nebenwirkungen geben. Aktuell noch in PH1. Jedoch ist nicht auszuschließen, dass beide Entwicklungen noch daran scheitern könnten.
Ich hatte in der Vergangenheit einige kritische Kommentare zu Demcizumab gelesen.
Zu GITR konnte ich nirgends einen Zeitplan finden, hier wird es vermutlich nicht so schnell eine IND geben.
anti-RSPO3 (OMP-131R10) kommt ja jetzt in die Klinik, mal sehen.
Die breite Pipeline verpartnert mit Celgene, Bayer und GSK sichert OMED bei Fehlschlägen aber einigermaßen gut ab.
lt. der PH1a scheint OMED die Herzprobleme bei Demcizumab gut im Griff zu haben. Interessant ist sicherlich auch der bispezifische OMP-305B83 (Anti-DLL4/VEGF), hier könnte es aber die selben Nebenwirkungen geben. Aktuell noch in PH1. Jedoch ist nicht auszuschließen, dass beide Entwicklungen noch daran scheitern könnten.
Ich hatte in der Vergangenheit einige kritische Kommentare zu Demcizumab gelesen.
Zu GITR konnte ich nirgends einen Zeitplan finden, hier wird es vermutlich nicht so schnell eine IND geben.
anti-RSPO3 (OMP-131R10) kommt ja jetzt in die Klinik, mal sehen.
Die breite Pipeline verpartnert mit Celgene, Bayer und GSK sichert OMED bei Fehlschlägen aber einigermaßen gut ab.
REGN & ESPR
REGNs PCSK9-AK ist nun sowohl in Europa (noch nicht offiziell, aber so gut wie) und in den USA zugelassen.
Merkwürdigerweise hat dies mit -20% zu einem erheblichen Einbruch von ESPR geführt. Meiner Meinung nach ist dies auf eine offensichtliche Fehlinterpretation der Analysten zurückzuführen... d.h. der Einbruch ist aus meiner Sicht und soweit man es bisher beurteilen kann ungerechtfertigt und müsste wieder korrigiert werden.
Die Frage ist, ob Studien auf Basis von LDL für eine Zulassung in Indikationen ausreichen, in denen Statine verwendet werden, aber nicht vertragen werden oder alleine ausreichend wirksam sind. Dies wären Indikationen, die für ESPRs Medikament geeignet sind. Analysten interpretieren das US-Label von Praluent wohl so, dass es nur für Patienten mit krankheitsbedingten sehr hohen LDL-Blutfettwerten ist. Da PCSK9-AKs LDL sehr viel stärker senken als das Mittel von ESPR, hat ESPR hier wohl keine Chance. Für ein weiteres Label (z.B. Statin-Intolleranz) müsste ESPR dann sehr aufwändige, lange und teuere PIII Outcome-Studien durchführen, wozu ESPR selber wohl nicht in der Lage ist.
Dies scheint aber ein Interpretationsfehler zu sein... vielleicht ist es genau andersherum: Das EU-Label von Praluent (auf Basis von LDL-Studien) könnte noch über das erhoffte statin-intolerant hinausgehen. Das US-Label scheint die Statin-intoleranz zu beinhalten, auch wenn dies nicht so explizit ausgedrückt ist. D.h. ESPR hat gute Chancen, mit LDL-Studien eine aussichtsreiche Zulassung zu erreichen.
Twitter-Kommentare...
"$REGN IR confirms my reading of the Praluent label: It allows 100% statin intolerant patients. $ESPR
$REGN approval confirms FDA will approve on LDL only, in statin-intolerant pts, and in $ESPR preferred secondary prevention population. Win.
@Miljenkoz @redacre Some $ESPR investors must have been expecting Praluent labels(plural) 2b more severely restricted.EMA label =wide open.
@DewDiligence If you're talking to me, the EU and FDA labels are functionally the same population. Different ways to word it.
@AlpineBV_Miller You know better than that. Even Len Schleifer admitted (by accident) that EMA label=much broader. Read the CC transcript."




Gruß
ipollit
REGNs PCSK9-AK ist nun sowohl in Europa (noch nicht offiziell, aber so gut wie) und in den USA zugelassen.
Merkwürdigerweise hat dies mit -20% zu einem erheblichen Einbruch von ESPR geführt. Meiner Meinung nach ist dies auf eine offensichtliche Fehlinterpretation der Analysten zurückzuführen... d.h. der Einbruch ist aus meiner Sicht und soweit man es bisher beurteilen kann ungerechtfertigt und müsste wieder korrigiert werden.
Die Frage ist, ob Studien auf Basis von LDL für eine Zulassung in Indikationen ausreichen, in denen Statine verwendet werden, aber nicht vertragen werden oder alleine ausreichend wirksam sind. Dies wären Indikationen, die für ESPRs Medikament geeignet sind. Analysten interpretieren das US-Label von Praluent wohl so, dass es nur für Patienten mit krankheitsbedingten sehr hohen LDL-Blutfettwerten ist. Da PCSK9-AKs LDL sehr viel stärker senken als das Mittel von ESPR, hat ESPR hier wohl keine Chance. Für ein weiteres Label (z.B. Statin-Intolleranz) müsste ESPR dann sehr aufwändige, lange und teuere PIII Outcome-Studien durchführen, wozu ESPR selber wohl nicht in der Lage ist.
Dies scheint aber ein Interpretationsfehler zu sein... vielleicht ist es genau andersherum: Das EU-Label von Praluent (auf Basis von LDL-Studien) könnte noch über das erhoffte statin-intolerant hinausgehen. Das US-Label scheint die Statin-intoleranz zu beinhalten, auch wenn dies nicht so explizit ausgedrückt ist. D.h. ESPR hat gute Chancen, mit LDL-Studien eine aussichtsreiche Zulassung zu erreichen.
Twitter-Kommentare...
"$REGN IR confirms my reading of the Praluent label: It allows 100% statin intolerant patients. $ESPR

$REGN approval confirms FDA will approve on LDL only, in statin-intolerant pts, and in $ESPR preferred secondary prevention population. Win.
@Miljenkoz @redacre Some $ESPR investors must have been expecting Praluent labels(plural) 2b more severely restricted.EMA label =wide open.
@DewDiligence If you're talking to me, the EU and FDA labels are functionally the same population. Different ways to word it.
@AlpineBV_Miller You know better than that. Even Len Schleifer admitted (by accident) that EMA label=much broader. Read the CC transcript."


Gruß
ipollit
Als stiller Mitleser bedanke ich mich zunächst für die zahlreichen sehr informativen und interessanten Beiträge.
Ohad Hammer schreibt in seinem Blog bzgl. ESPR, dass hier wohl von einer Überreaktion des Marktes auszugehen ist. Diese Einschätzung teile ich auch, so dass die Korrektur von -20% wohl schnell wieder aufgeholt werden wird.
Zudem möchte ich auf KPTI thematisieren:
Ich habe gesehen, dass hier einige von Euch investiert sind.
Die aktuelle Bewertung von KPTI erscheint mir in Anbetracht von Selinexor doch recht billig. Hat jemand hierzu irgendwelche Infos oder wieso findet dieser Ausverkauf statt? Ich überlege gerade, ob ich hier eine Position aufbauen soll.
Viele Grüße
biopadawan
Ohad Hammer schreibt in seinem Blog bzgl. ESPR, dass hier wohl von einer Überreaktion des Marktes auszugehen ist. Diese Einschätzung teile ich auch, so dass die Korrektur von -20% wohl schnell wieder aufgeholt werden wird.
Zudem möchte ich auf KPTI thematisieren:
Ich habe gesehen, dass hier einige von Euch investiert sind.
Die aktuelle Bewertung von KPTI erscheint mir in Anbetracht von Selinexor doch recht billig. Hat jemand hierzu irgendwelche Infos oder wieso findet dieser Ausverkauf statt? Ich überlege gerade, ob ich hier eine Position aufbauen soll.
Viele Grüße
biopadawan
Antwort auf Beitrag Nr.: 50.264.655 von ipollit am 25.07.15 14:04:25Die Analystengemeinde interpretiert das Label offensichtlich wirklich negativ. Hammer letztlich auch.
Sollte hier wirklich einfach nur ein Missverständnis vorliegen? Ich kann das fast nicht glauben.
Auf der anderen Seite muss man aber auch fragen, ob der Absturz am Freitag nicht in jedem Fall übertrieben ist.
Hier Citi mit einer negativen Interpretation und einem gleichzeitig doch recht hohen Kursziel:


Es scheint mir derzeit eine ziemliche Verwirrung zu herrschen.
Sollte hier wirklich einfach nur ein Missverständnis vorliegen? Ich kann das fast nicht glauben.
Auf der anderen Seite muss man aber auch fragen, ob der Absturz am Freitag nicht in jedem Fall übertrieben ist.
Hier Citi mit einer negativen Interpretation und einem gleichzeitig doch recht hohen Kursziel:


Es scheint mir derzeit eine ziemliche Verwirrung zu herrschen.
Antwort auf Beitrag Nr.: 50.264.655 von ipollit am 25.07.15 14:04:25Hallo ipollit,
wie befürchtet, Fehlschlag bei IMMU in SLE:
UCB today announced that the two EMBODY™ Phase 3 clinical studies for epratuzumab in Systemic Lupus Erythematosus (SLE) did not meet their primary clinical efficacy endpoints in either dose in both studies. Treatment response in patients who received epratuzumab in addition to standard therapy was not statistically significantly higher than those who received placebo in addition to standard therapy. 1
http://www.ucb.com/presscenter/News/article/UCB-announces-Ph…
wie befürchtet, Fehlschlag bei IMMU in SLE:
UCB today announced that the two EMBODY™ Phase 3 clinical studies for epratuzumab in Systemic Lupus Erythematosus (SLE) did not meet their primary clinical efficacy endpoints in either dose in both studies. Treatment response in patients who received epratuzumab in addition to standard therapy was not statistically significantly higher than those who received placebo in addition to standard therapy. 1
http://www.ucb.com/presscenter/News/article/UCB-announces-Ph…
KPTI (Karyopharm Therapeutics)
Was habe ich hier verpasst, das der Titel auf 52w Low ist? Ich konnte keinen negativen News finden!
Was habe ich hier verpasst, das der Titel auf 52w Low ist? Ich konnte keinen negativen News finden!
Arry
Ich weiß, daß Diskussionen über Aktienkurse hier mit guten Gründen eigentlich nicht stattfinden. Aber diese kurze Frage an die Gemeinde sei erlaubt: Array steht gerade bei US$ 5,80 bei sehr hohen Umsätzen...
Welche Gründe könnten hierfür ausschlaggebend sein:
- allgemeines Umfeld? M.E. ist der Einbruch dafür zu hoch...
- Short-Attacke? Die Shortquote war vorher schon extremst hoch...immerhin 25%
- Ist etwas durchgesickert zu NRAS Melanoma? Sollte dafür eigentlich zu früh sein...
- Angst, daß es zu keiner Verpartnerung mehr kommt und die Rechte durch den Treuhänder verscherbelt werden? Wenn RS nicht gelogen hat, hätte er mindestens noch bis Ende des Jahres Zeit...
- Nachwehen vom Scheitern Selu/Uveal Melanoma? Dafür sollte die Indikation zu klein gewesen sein, es sei denn, es wären Rückschlüsse auf die grundsätzlichen Fähigkeiten von Selu erlaubt...
Die jetzige Bewertung scheint jenseits von positiven und negativen Ausreißern derart niedrig, daß man fast vermuten könnte, Array hat nur Smarties entwickelt...
Meine eigene Vermutung ist eine Mischung aus sehr großer Short-Attacke und durchgesickerten schlechten Nachrichten...ich werde langsam etwas nervös...
Ich weiß, daß Diskussionen über Aktienkurse hier mit guten Gründen eigentlich nicht stattfinden. Aber diese kurze Frage an die Gemeinde sei erlaubt: Array steht gerade bei US$ 5,80 bei sehr hohen Umsätzen...
Welche Gründe könnten hierfür ausschlaggebend sein:
- allgemeines Umfeld? M.E. ist der Einbruch dafür zu hoch...
- Short-Attacke? Die Shortquote war vorher schon extremst hoch...immerhin 25%
- Ist etwas durchgesickert zu NRAS Melanoma? Sollte dafür eigentlich zu früh sein...
- Angst, daß es zu keiner Verpartnerung mehr kommt und die Rechte durch den Treuhänder verscherbelt werden? Wenn RS nicht gelogen hat, hätte er mindestens noch bis Ende des Jahres Zeit...
- Nachwehen vom Scheitern Selu/Uveal Melanoma? Dafür sollte die Indikation zu klein gewesen sein, es sei denn, es wären Rückschlüsse auf die grundsätzlichen Fähigkeiten von Selu erlaubt...
Die jetzige Bewertung scheint jenseits von positiven und negativen Ausreißern derart niedrig, daß man fast vermuten könnte, Array hat nur Smarties entwickelt...
Meine eigene Vermutung ist eine Mischung aus sehr großer Short-Attacke und durchgesickerten schlechten Nachrichten...ich werde langsam etwas nervös...
Antwort auf Beitrag Nr.: 50.283.144 von lawmeetstax am 28.07.15 16:17:25Hallo lawmeetstax,
die Punkte 2 und 5 von Deiner Auflistung treffen aus meiner Sicht am meisten zu. Das Short-Interesse war seit Januar bei arry sehr hoch. Eine gute Nachricht hätte ein short squeeze bewirkt. Umgekehrt warten die Shorts schonmal eine Weile, dass ihre Gelegenheit kommt. Das war mit der Augenhautkrebsstudie dann der Fall. Gemessen an der Gesamtsituation des Unternehmens kein großes Ereignis, aber eben negative Psychologie in einem nervösen Markt. So etwas wird ausgenutzt.
Jetzt kommt es darauf an, dass in den Kernbereichen geliefert wird (Verpartnerung, NEMO Studie, COLUMBUS-Studie, arry 797 (lange nichts davon gehört, übrigens)).
A
die Punkte 2 und 5 von Deiner Auflistung treffen aus meiner Sicht am meisten zu. Das Short-Interesse war seit Januar bei arry sehr hoch. Eine gute Nachricht hätte ein short squeeze bewirkt. Umgekehrt warten die Shorts schonmal eine Weile, dass ihre Gelegenheit kommt. Das war mit der Augenhautkrebsstudie dann der Fall. Gemessen an der Gesamtsituation des Unternehmens kein großes Ereignis, aber eben negative Psychologie in einem nervösen Markt. So etwas wird ausgenutzt.
Jetzt kommt es darauf an, dass in den Kernbereichen geliefert wird (Verpartnerung, NEMO Studie, COLUMBUS-Studie, arry 797 (lange nichts davon gehört, übrigens)).
A
Antwort auf Beitrag Nr.: 50.283.144 von lawmeetstax am 28.07.15 16:17:25Hallo lawmeetstax,
die doch recht moderate Bewertung von ARRY ist ja im Grunde zunächst fast schon eine Tradition. Es ist natürlich irgendwie schwer die Gründe für den aktuellen Kursverlauf zu wissen. Ich denke du hast schon einige mögliche Gründe dafür genannt (wobei ich immer nicht so ganz weiß, was eigentlich eine short Attacke ist?)
Was den Kurs momentan drückt ist m.E. vor allem die Unsicherheit über die nächsten größeren Ereignisse nämlich die Verpartnerung von Bini und die Ergebnisse der nächsten PIII in NRAS Melanoma. Die PII Ergebnisse haben einen ja nicht so wirklich vom Hocker gehauen von daher ist ein Erfolg hier keinsesfalls sicher. http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
Auch was die Verpartnerung betrifft "droht" ja so etwas wie eine Zwangsverpartnerung. Natürlich wären die Konditionen dann wohl signifikant schlechter. Keiner weiß momentan welchen Zeitrahmen ARRY dafür hat. Hat überhaupt jemand oder besser mindestens zwei Interesse? Unsicherheit ist halt immer schlecht. Zudem stürzt sich der Markt immer sehr auf das nächste Event auch wenn es langfristig gar nicht so entscheidend ist. Dabei stimmt m.E. die langfristige Perspektive. Im nächsten Jahr stehen erst die wichtigen Ergebnisse an. Zudem wird die verpartnerte Pipeline unterschätzt. Loxo hat z.B. grad bestätigt, dass der eine Patient mit TRK zumindest eine PR (sieht aber fast aus wie eine CR) gezeigt hat:

http://cancerdiscovery.aacrjournals.org/content/early/2015/0…
SG kmastra
die doch recht moderate Bewertung von ARRY ist ja im Grunde zunächst fast schon eine Tradition. Es ist natürlich irgendwie schwer die Gründe für den aktuellen Kursverlauf zu wissen. Ich denke du hast schon einige mögliche Gründe dafür genannt (wobei ich immer nicht so ganz weiß, was eigentlich eine short Attacke ist?)
Was den Kurs momentan drückt ist m.E. vor allem die Unsicherheit über die nächsten größeren Ereignisse nämlich die Verpartnerung von Bini und die Ergebnisse der nächsten PIII in NRAS Melanoma. Die PII Ergebnisse haben einen ja nicht so wirklich vom Hocker gehauen von daher ist ein Erfolg hier keinsesfalls sicher. http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
Auch was die Verpartnerung betrifft "droht" ja so etwas wie eine Zwangsverpartnerung. Natürlich wären die Konditionen dann wohl signifikant schlechter. Keiner weiß momentan welchen Zeitrahmen ARRY dafür hat. Hat überhaupt jemand oder besser mindestens zwei Interesse? Unsicherheit ist halt immer schlecht. Zudem stürzt sich der Markt immer sehr auf das nächste Event auch wenn es langfristig gar nicht so entscheidend ist. Dabei stimmt m.E. die langfristige Perspektive. Im nächsten Jahr stehen erst die wichtigen Ergebnisse an. Zudem wird die verpartnerte Pipeline unterschätzt. Loxo hat z.B. grad bestätigt, dass der eine Patient mit TRK zumindest eine PR (sieht aber fast aus wie eine CR) gezeigt hat:

http://cancerdiscovery.aacrjournals.org/content/early/2015/0…
SG kmastra
Antwort auf Beitrag Nr.: 50.265.120 von SLGramann am 25.07.15 16:06:15Hallo ipollit und SLGramann,
heute kamen ja noch die Ergebnisse der 014 Studie. Für mich war das zumindest nicht die erhoffte positive Überraschung, da der Blutdruck bei dieser Patientengruppe nicht gesenkt wurde (in früheren Studien war ja ein moderater Effekt zu sehen). Anderseits gab es aber auch hier keine negative Überraschung. Von daher eher neural zu werten?
The six-week study met its primary endpoint of greater LDL-cholesterol lowering from baseline with ETC-1002 as compared to placebo. Patients treated with 180 mg of ETC-1002 achieved a 21 percent reduction in LDL-cholesterol from baseline (p < 0.0001), and a 24 percent reduction as compared to placebo (p < 0.0001), which increased by three percent. The reduction occurred within the first two weeks of initiating therapy and continued throughout the treatment period. The LDL-cholesterol lowering effect of ETC-1002 was statistically significant and clinically meaningful.
Consistent with prior studies, ETC-1002 demonstrated statistically significant and clinically meaningful reductions of 25 percent from baseline, 44 percent vs placebo (p < 0.0001), in high-sensitivity C-reactive protein (hsCRP), an important marker of inflammation in coronary disease.
Die Diskussion der letzten Tage über die Implikationen des Praluent Labels kann ich nicht so ganz nachvollziehen. Ich habe deshalb heute moderat nachgekauft.
So wie ich das (sehr oberflächlich) verfolgt habe, geht es der FDA doch vor allem darum, dass es den Ärzten/Patienten nicht zu leicht gemacht wird von Statinen (deren Wirkung auf Herzkreislaufkrankheiten ja belegt ist) auf Praluent (dessen Wirkung langfristig nicht belegt ist) zu wechseln. Das finde ich medizinisch (und auch finanziell) sinnvoll und nachvollziehbar. Auch ETC1002 soll ja erst nach Statinen eingesetzt werden. Von daher soll/wird ETC1002 ja sogar helfen, dass die Patienten Statine nehmen können und trotzdem ihr Cholesterin Ziel erreichen.
Das man von ETC1002 nun als erstes Medikament vor der Zulassung eine Wirksamkeitsstudie in Bezug auf Herzkreislauferkrankungen verlangt würde ich nicht im Ansatz erwarten. Man muss doch sehen, dass Herzkreislauferkrankungen immer noch Todesursache Nummer 1 sind. Und nach Improve-It soll die FDA plötzlich härtere Maßstäbe anlegen?

Charttechnisch hat ESPR erstmal Halt an der 200 Tageslinie gefunden. Ob die hält wird man sehen. Mal sehen, wie der Investorday verläuft und dann hängt mittelfristig erstmal viel von den Gesprächen mit der FDA ab.
Was ist von CETP zu halten. Bisher dachte ich immer, dass die Sicherheitsbedenken da zu groß wären. Ist das eine Gefahr?
SG kmastra
heute kamen ja noch die Ergebnisse der 014 Studie. Für mich war das zumindest nicht die erhoffte positive Überraschung, da der Blutdruck bei dieser Patientengruppe nicht gesenkt wurde (in früheren Studien war ja ein moderater Effekt zu sehen). Anderseits gab es aber auch hier keine negative Überraschung. Von daher eher neural zu werten?
The six-week study met its primary endpoint of greater LDL-cholesterol lowering from baseline with ETC-1002 as compared to placebo. Patients treated with 180 mg of ETC-1002 achieved a 21 percent reduction in LDL-cholesterol from baseline (p < 0.0001), and a 24 percent reduction as compared to placebo (p < 0.0001), which increased by three percent. The reduction occurred within the first two weeks of initiating therapy and continued throughout the treatment period. The LDL-cholesterol lowering effect of ETC-1002 was statistically significant and clinically meaningful.
Consistent with prior studies, ETC-1002 demonstrated statistically significant and clinically meaningful reductions of 25 percent from baseline, 44 percent vs placebo (p < 0.0001), in high-sensitivity C-reactive protein (hsCRP), an important marker of inflammation in coronary disease.
Die Diskussion der letzten Tage über die Implikationen des Praluent Labels kann ich nicht so ganz nachvollziehen. Ich habe deshalb heute moderat nachgekauft.
So wie ich das (sehr oberflächlich) verfolgt habe, geht es der FDA doch vor allem darum, dass es den Ärzten/Patienten nicht zu leicht gemacht wird von Statinen (deren Wirkung auf Herzkreislaufkrankheiten ja belegt ist) auf Praluent (dessen Wirkung langfristig nicht belegt ist) zu wechseln. Das finde ich medizinisch (und auch finanziell) sinnvoll und nachvollziehbar. Auch ETC1002 soll ja erst nach Statinen eingesetzt werden. Von daher soll/wird ETC1002 ja sogar helfen, dass die Patienten Statine nehmen können und trotzdem ihr Cholesterin Ziel erreichen.
Das man von ETC1002 nun als erstes Medikament vor der Zulassung eine Wirksamkeitsstudie in Bezug auf Herzkreislauferkrankungen verlangt würde ich nicht im Ansatz erwarten. Man muss doch sehen, dass Herzkreislauferkrankungen immer noch Todesursache Nummer 1 sind. Und nach Improve-It soll die FDA plötzlich härtere Maßstäbe anlegen?
Charttechnisch hat ESPR erstmal Halt an der 200 Tageslinie gefunden. Ob die hält wird man sehen. Mal sehen, wie der Investorday verläuft und dann hängt mittelfristig erstmal viel von den Gesprächen mit der FDA ab.
Was ist von CETP zu halten. Bisher dachte ich immer, dass die Sicherheitsbedenken da zu groß wären. Ist das eine Gefahr?
SG kmastra
Antwort auf Beitrag Nr.: 50.284.989 von kmastra am 28.07.15 20:19:50"heute kamen ja noch die Ergebnisse der 014 Studie. Für mich war das zumindest nicht die erhoffte positive Überraschung, da der Blutdruck bei dieser Patientengruppe nicht gesenkt wurde (in früheren Studien war ja ein moderater Effekt zu sehen)."
Hallo kmastra,
vielleicht war da doch ein gewisser Effekt (nicht stat. signifikant), auch wenn das in der PM gar nicht thematisiert wurde?
Siehe dazu hier (Absatz 2):

Letztlich ist natürlich entscheidend, dass die Daten insgesamt gut aussehen und kaum Raum zur Kritik lassen.
Es mag schon sein, dass das Praluent-Label nicht optimal ist, aber der Abverkauf ist höchst wahrscheinlich ziemlich übertrieben.
Vieles ist eben stimmungsgetrieben - was derzeit sicher auch auf Array zutrifft. Selbst kleinere Rückschläge führen in diesen Märkten zu hysterischen Reaktionen - andersrum funktioniert das aber auch, wie man derzeit bei ITEK und LOXO beobachten kann.
Bei ESPR wäre ich jedenfalls auf der Käuferseite, weil der Kursverfall meiner Meinung nach zu weit gegangen ist.
Gruß
SLG
Hallo kmastra,
vielleicht war da doch ein gewisser Effekt (nicht stat. signifikant), auch wenn das in der PM gar nicht thematisiert wurde?
Siehe dazu hier (Absatz 2):

Letztlich ist natürlich entscheidend, dass die Daten insgesamt gut aussehen und kaum Raum zur Kritik lassen.
Es mag schon sein, dass das Praluent-Label nicht optimal ist, aber der Abverkauf ist höchst wahrscheinlich ziemlich übertrieben.
Vieles ist eben stimmungsgetrieben - was derzeit sicher auch auf Array zutrifft. Selbst kleinere Rückschläge führen in diesen Märkten zu hysterischen Reaktionen - andersrum funktioniert das aber auch, wie man derzeit bei ITEK und LOXO beobachten kann.
Bei ESPR wäre ich jedenfalls auf der Käuferseite, weil der Kursverfall meiner Meinung nach zu weit gegangen ist.
Gruß
SLG
Biota Pharmaceuticals' direct-acting antivirals target the root cause, of viral conditions
www.stockhouse.com/opinion/independent-reports/2015/07/15/bi…
www.stockhouse.com/opinion/independent-reports/2015/07/15/bi…
Antwort auf Beitrag Nr.: 50.286.480 von SLGramann am 29.07.15 07:34:21ESPR:
Schon "witzig": Die Aktie notiert gegenüber ihrem Topniveau ungefähr 50% im Minus. Auslöser war nur wenig mehr, als ein Hauch von Nichts.
So ist Biotech - absolut stimmungsgetrieben.

Ob wohl ein Charttechniker so im Bereich 45 bis 50 Dollar eine "Unterstützungszone" ausmachen würde? Ich hab ja keine Ahnung von dem Kram, aber es juckt einem natürlich in den Fingern, hier mal zuzugreifen.
Schon "witzig": Die Aktie notiert gegenüber ihrem Topniveau ungefähr 50% im Minus. Auslöser war nur wenig mehr, als ein Hauch von Nichts.
So ist Biotech - absolut stimmungsgetrieben.
Ob wohl ein Charttechniker so im Bereich 45 bis 50 Dollar eine "Unterstützungszone" ausmachen würde? Ich hab ja keine Ahnung von dem Kram, aber es juckt einem natürlich in den Fingern, hier mal zuzugreifen.
Arry
Hat jemand den Mut, hier kräftig nachzukaufen, oder fällt das Messer noch weiter? Ich muß zugeben, ich schwanke zwischen totaler Schockstarre und einem Arry-Einkaufswahn. Bin gespannt, was sich bei mir am Ende durchsetzt...derzeit sagt mir mein siebenter (Un-)Sinn, daß etwas Negatives durchgesickert ist, zB ein abgesprungener Interessent oder Studien-Schwierigkeiten oder etwas zu Ipatasertib, da müßten doch jederzeit die Ergebnisse von Roche/Genentech kommen...
Kennt jemand die aktuellen Verkaufszahlen zu Mekinist und Dabrafenib?
Hat jemand den Mut, hier kräftig nachzukaufen, oder fällt das Messer noch weiter? Ich muß zugeben, ich schwanke zwischen totaler Schockstarre und einem Arry-Einkaufswahn. Bin gespannt, was sich bei mir am Ende durchsetzt...derzeit sagt mir mein siebenter (Un-)Sinn, daß etwas Negatives durchgesickert ist, zB ein abgesprungener Interessent oder Studien-Schwierigkeiten oder etwas zu Ipatasertib, da müßten doch jederzeit die Ergebnisse von Roche/Genentech kommen...
Kennt jemand die aktuellen Verkaufszahlen zu Mekinist und Dabrafenib?
Antwort auf Beitrag Nr.: 50.301.891 von lawmeetstax am 30.07.15 18:25:41arry:
Ich sehe keinen kurzfristigen Kurstreiber, nachdem die SUMIT Studie gescheitert ist. Aber ich lasse mich gerne positiv überraschen.
Die nächsten Events sind NEMO und die Verpartnerung, vielleicht arry-797. Zeitfenster etwa Ende des Jahres?
Bis dahin werden die Bären erstmal dran sein. Das kann auch eine Übertreibung nach unten geben. So etwas sieht man häufiger.
A
Ich sehe keinen kurzfristigen Kurstreiber, nachdem die SUMIT Studie gescheitert ist. Aber ich lasse mich gerne positiv überraschen.
Die nächsten Events sind NEMO und die Verpartnerung, vielleicht arry-797. Zeitfenster etwa Ende des Jahres?
Bis dahin werden die Bären erstmal dran sein. Das kann auch eine Übertreibung nach unten geben. So etwas sieht man häufiger.
A
ESPR:
Also die 200 Tageslinie hat mal sowas von nicht gehalten. Charttechnisch wäre auch eine kleinere Unterstützung im Bereich 60$ (Zwischentief vom März) denkbar.
Fundamental finde ich den Absturz übertrieben. Hier wird scheinbar von einem Katastrophenszenario ausgegangen (bzw. hat man Angst davor), was aber eben nicht wahrscheinlich ist.
Ich gehe davon aus, dass ESPR die CVOT Studien begleitend durchführen darf und eine Zulassung vorher erfolgen kann.
Zudem gehe ich davon aus, dass die PIII auch eine fix dosed Kombination aus Statin und ETC1002 (evtl. sogar zusätzlich Ezetimibe) beinhaltet. Da erscheint es mir einleuchtend, dass ein Label auch entsprechend breit ausfallen dürfte.
Ein weiteres Argument ist für mich, dass Esperion von einer Preisdiskussion profitieren könnte, weil sie ja viel günstiger sind als z.B. Praluent.
ARRY:
Ja die Bewertung ist schon komisch. Mal Pi mal Daumen: Loxo und ONTY kommen zusammen auf ca. 700 Mio. - ARRY alleine auf 800 Mio., hat natürlich weniger Anteil an den Medikamenten bekäme aber signifikante Royalties. Dazu noch die MEKs, Enco und und und...die Technologie, aktive Partnerschaften, Knowhow...
Charttechnisch ist ARRY im Niemansland - Unterstützung böte sich im Bereich 5$. Aber das wäre ja fundamentaler Wahnsinn, weil das Kursregionen vor der Rückgabe von Bini und dem Geschenk Enco sind.
Novartis hat mit Mekinist/Tafinlar im letzten Q 130 Mio umgesetzt.
Das etwas durchgesickert ist glaub ich nicht. Wie gesagt: Die nächsten Ereignisse sind aber eh unsicher.
Also die 200 Tageslinie hat mal sowas von nicht gehalten. Charttechnisch wäre auch eine kleinere Unterstützung im Bereich 60$ (Zwischentief vom März) denkbar.
Fundamental finde ich den Absturz übertrieben. Hier wird scheinbar von einem Katastrophenszenario ausgegangen (bzw. hat man Angst davor), was aber eben nicht wahrscheinlich ist.
Ich gehe davon aus, dass ESPR die CVOT Studien begleitend durchführen darf und eine Zulassung vorher erfolgen kann.
Zudem gehe ich davon aus, dass die PIII auch eine fix dosed Kombination aus Statin und ETC1002 (evtl. sogar zusätzlich Ezetimibe) beinhaltet. Da erscheint es mir einleuchtend, dass ein Label auch entsprechend breit ausfallen dürfte.
Ein weiteres Argument ist für mich, dass Esperion von einer Preisdiskussion profitieren könnte, weil sie ja viel günstiger sind als z.B. Praluent.
ARRY:
Ja die Bewertung ist schon komisch. Mal Pi mal Daumen: Loxo und ONTY kommen zusammen auf ca. 700 Mio. - ARRY alleine auf 800 Mio., hat natürlich weniger Anteil an den Medikamenten bekäme aber signifikante Royalties. Dazu noch die MEKs, Enco und und und...die Technologie, aktive Partnerschaften, Knowhow...
Charttechnisch ist ARRY im Niemansland - Unterstützung böte sich im Bereich 5$. Aber das wäre ja fundamentaler Wahnsinn, weil das Kursregionen vor der Rückgabe von Bini und dem Geschenk Enco sind.
Novartis hat mit Mekinist/Tafinlar im letzten Q 130 Mio umgesetzt.
Das etwas durchgesickert ist glaub ich nicht. Wie gesagt: Die nächsten Ereignisse sind aber eh unsicher.
Antwort auf Beitrag Nr.: 50.303.070 von kmastra am 30.07.15 21:11:37"Fundamental finde ich den Absturz übertrieben. Hier wird scheinbar von einem Katastrophenszenario ausgegangen (bzw. hat man Angst davor), was aber eben nicht wahrscheinlich ist.
Ich gehe davon aus, dass ESPR die CVOT Studien begleitend durchführen darf und eine Zulassung vorher erfolgen kann.
Zudem gehe ich davon aus, dass die PIII auch eine fix dosed Kombination aus Statin und ETC1002 (evtl. sogar zusätzlich Ezetimibe) beinhaltet. Da erscheint es mir einleuchtend, dass ein Label auch entsprechend breit ausfallen dürfte.
Ein weiteres Argument ist für mich, dass Esperion von einer Preisdiskussion profitieren könnte, weil sie ja viel günstiger sind als z.B. Praluent."
Ich denke, dass Deine Einschätzung vollkommen zutrifft. Die Analystengemeinde sieht die Dinge ja auch so:


Ich kann mir gut vorstellen, dass wir im Spätsommer/Herbst wieder bei 100 Dollar sind, wenn das P III-Design ungefähr so aussieht, wie man es jetzt erwartet und vor allem die FDA dabei mitspielt, den Abschluss des CVO-Trial nicht zur Zulassungsvoraussetzung zu machen (wofür die Chancen ja gut stehen).
Ich gehe davon aus, dass ESPR die CVOT Studien begleitend durchführen darf und eine Zulassung vorher erfolgen kann.
Zudem gehe ich davon aus, dass die PIII auch eine fix dosed Kombination aus Statin und ETC1002 (evtl. sogar zusätzlich Ezetimibe) beinhaltet. Da erscheint es mir einleuchtend, dass ein Label auch entsprechend breit ausfallen dürfte.
Ein weiteres Argument ist für mich, dass Esperion von einer Preisdiskussion profitieren könnte, weil sie ja viel günstiger sind als z.B. Praluent."
Ich denke, dass Deine Einschätzung vollkommen zutrifft. Die Analystengemeinde sieht die Dinge ja auch so:


Ich kann mir gut vorstellen, dass wir im Spätsommer/Herbst wieder bei 100 Dollar sind, wenn das P III-Design ungefähr so aussieht, wie man es jetzt erwartet und vor allem die FDA dabei mitspielt, den Abschluss des CVO-Trial nicht zur Zulassungsvoraussetzung zu machen (wofür die Chancen ja gut stehen).
ARRY
Ich denke dass ARRY immer noch ein sehr gutes Longtime-Investment darstellt. Zudem erscheint ein M&A Szenario bei der momentanen Bewertung durch zB GILD durchaus wahrscheinlich.
Bin daher auf der BULLEN-Seite und werde zukaufen!
Grüße
Biopadawan
Ich denke dass ARRY immer noch ein sehr gutes Longtime-Investment darstellt. Zudem erscheint ein M&A Szenario bei der momentanen Bewertung durch zB GILD durchaus wahrscheinlich.
Bin daher auf der BULLEN-Seite und werde zukaufen!
Grüße
Biopadawan
Antwort auf Beitrag Nr.: 50.312.169 von biopadawan am 01.08.15 11:14:15Mal eine Frage abseits von Biotech - Stocks:
Wo kauft ihr Eure US Aktien? Aufgrund der Gebührenlage habe ich diese bisher bei deutschen Börsen (Frankfurt etc) erworben, da ich nicht sehr hohe Beträge investiere.
Zusätzlich profitiert man hier von Abwertungen des EUR gegenüber dem US Dollar.
Wie handhabt ihr das?
Viele Grüße
biopadawan
Wo kauft ihr Eure US Aktien? Aufgrund der Gebührenlage habe ich diese bisher bei deutschen Börsen (Frankfurt etc) erworben, da ich nicht sehr hohe Beträge investiere.
Zusätzlich profitiert man hier von Abwertungen des EUR gegenüber dem US Dollar.
Wie handhabt ihr das?
Viele Grüße
biopadawan
Antwort auf Beitrag Nr.: 50.312.691 von biopadawan am 01.08.15 14:02:12Hallo biopadawan,
na von der Abwertung profitierst du auch, wenn du direkt in den USA kaufst. Bis jetzt hat der Euro-Verfall Vorteile für uns Anleger in US-Aktien, zumindest wenn du bereits welche besitzt. So was kann sich immer drehen.
Man kann das auch umgekehrt sehen, für deinen sauer verdienten Euro bekommst, du jetzt deutlicher weniger an Anteil an US-Firmen.
Aus meiner Sicht ist der Spread in Frankfurt und Stuttgart viel zu hoch. Wenn du nicht gerade für 500 € Aktien kaufst, kommst du bei fast jeden Broker besser weg, wenn du direkt in NY handelst. Zu mal die US-Aktien auch viel liquider dort sind, falls man schnell wieder raus will/muss.
Im Schnitt kostet das bei den meisten Broker nicht mehr als 20-40€ bei Ordergrößen zwischen 2000-5000€. z.B. bei der DIBA bei knapp 20, Onvista, DAB, Consorsbank und comdirekt liegen alle ähnlich. Alle haben Online ein Preisverzeichnis. Es gibt noch verschiedene Modelle für Trader etc. Dann gibt es noch ausländische Anbieter, wie Degiro. Hat den Vorteil/Nachteil du bezahlst nicht gleich Abgeltungssteuer, sondern erst in deiner pers. Steuererklärung. Nachteil deswegen, ne Menge bürokratischer Aufwand.
Muss halt jeder selbst sehen, was am besten für einen passt.
na von der Abwertung profitierst du auch, wenn du direkt in den USA kaufst. Bis jetzt hat der Euro-Verfall Vorteile für uns Anleger in US-Aktien, zumindest wenn du bereits welche besitzt. So was kann sich immer drehen.
Man kann das auch umgekehrt sehen, für deinen sauer verdienten Euro bekommst, du jetzt deutlicher weniger an Anteil an US-Firmen.
Aus meiner Sicht ist der Spread in Frankfurt und Stuttgart viel zu hoch. Wenn du nicht gerade für 500 € Aktien kaufst, kommst du bei fast jeden Broker besser weg, wenn du direkt in NY handelst. Zu mal die US-Aktien auch viel liquider dort sind, falls man schnell wieder raus will/muss.
Im Schnitt kostet das bei den meisten Broker nicht mehr als 20-40€ bei Ordergrößen zwischen 2000-5000€. z.B. bei der DIBA bei knapp 20, Onvista, DAB, Consorsbank und comdirekt liegen alle ähnlich. Alle haben Online ein Preisverzeichnis. Es gibt noch verschiedene Modelle für Trader etc. Dann gibt es noch ausländische Anbieter, wie Degiro. Hat den Vorteil/Nachteil du bezahlst nicht gleich Abgeltungssteuer, sondern erst in deiner pers. Steuererklärung. Nachteil deswegen, ne Menge bürokratischer Aufwand.
Muss halt jeder selbst sehen, was am besten für einen passt.
ARRY
Ganz so optimistisch bin ich bezüglich ARRY nicht. Sie scheinen sich sehr auf ihren MEK-Hemmer Bini und den BRAF-Hemmer Enco zu fokussieren. Das Problem ist, dass es für MEK-Hemmer nicht leicht ist, gute Indikationen oder Kombi-Therapien zu entwickeln... bisher sind sie nur in BRAF+ Melanoma erfolgreich, alle anderen Indikationen sind wohl noch sehr unsicher und damit auch entsprechend riskant.
Das zweite Problem ist, dass man insbesondere in BRAF+ Melanoma direkt gegen Novartis und Roche antritt... beides führende Unternehmen im Bereich der Onkologie und TK-Hemmern. Roche waren mit dem BRAF-Hemmer Zelboraf in BRAF+ Melanoma die ersten am Markt... die MEK+BRAF Kombi sollte in den nächsten Monaten zugelassen werden. Novartis haben mit Tafinlar + Mekinist bereits die erste MEK+BRAF Kombi am Markt. D.h. die beiden starken Konkurrenten haben etablierte Mittel in BRAF+ Melanoma mit einem deutlichen zeitlichen Vorsprung. Ich halte es für unwahrscheinlich, dass ARRYs Bini + Enco in BRAF+ Melanoma relevante Vorteile gegen die anderen beiden Kombis hat (oder?). D.h. ARRY ist hier nur die Nr 3 am Markt. BRAF+ Melanoma ist zudem keine große Indikation... optimistisch sind es wohl nur maximal 1-2 Mrd USD, die sich diese drei teilen müssen.
Bini hat wohl in NRAS+ Melanoma die Nase vorne, oder? Anders als die Wirkung eines BRAF-Hemmers in BRAF+ Melanoma ist die eines MEK-Hemmers in NRAS+ nicht sicher... es sieht bisher gut aus, aber erst die kommenden PIII-Ergebnisse werden Klarheit schaffen. NRAS+ ist aber wohl nur 1/3 so groß wie die BRAF+ Melanoma Indikation.
MEK-Hemmer sind wie gesagt schwierig zu entwickeln, da sich der Einfluss auf den RAS-Signalweg und die Relevanz im Tumor nur schwer vorhersagen lässt... wie man an der letzen gescheiterten PIII sieht. MEK-Hemmer funktionieren vielleicht besser in Kombis wie z.B. in BRAF+ Melanoma, wo der Krebs gegen einen BRAF-Hemmer alleine schnell resistent wird über Aktivierung von RAS ("after a relatively short period of disease control, most patients develop resistance because of reactivation of the RAF-ERK pathway, mediated in many cases by mutations in RAS").
Zwischen ARRY/AZNs MEK-Hemmer Selumetinib und z.B. Bini scheint es größere Unterschiede zu geben. So wird Selumetinib z.B. nicht gegen Melanoma entwickelt. Selumetinib scheint ein schwächerer MEK-Hemmer zu sein. Allerdings sind andere MEK-Hemmer unverträglich in der Kombination mit einer Chemo (wie sieht es hier mit Bini aus?)... Selumetinib lässt sich dagegen bei maximaler Dosierung mit einer Chemo anwenden. Daher wird Selumetinib momentan hauptsächlich gegen Lungenkrebs entwickelt, weil zum einen die Chemo das einzige wirksame Mittel gegen Lungenkrebs ist und zum anderen ein größerer Teil von Lungenkrebs Mutationen im RAS-Signalweg KRAS aufweist. Trotzdem ist es aber alles andere als sicher, dass eine MEK + Chemo in KRAS+ Lungenkrebs funktioniert. Im Erfolgsfall wäre der Markt sehr groß... KRAS ist z.B. deutlich häufiger als EGFR und bei KRAS+ wirkt bisher nur die Chemo. Das Risiko eines Fehlschlags ist meiner Meinung aber auch sehr hoch und Selumetinib könnte damit komplett scheitern, da fast die gesamte Entwicklung auf diese Indikation ausgelegt ist.
D.h. die MEK-Hemmer, auf die sich ARRY fokussiert, besitzen ein hohes Entwicklungsrisiko... und selbst mit Einzelerfolgen ist aufgrund der starken Konkurrenz ein wirtschaftlicher Erfolg keinesfalls sicher.
Somit gewichte ich ARRY nicht so hoch... Chancen sind natürlich da, zumal es auch eine große Partner-Pipeline gibt. Aber wäre es bei den bestehenden Risiken auch realistisch, dass ARRY mittelfristig mit z.B. Richtung 2 Mrd USD bewertet sein wird (d.h. Kursverdoppelung)? Ich bin mir da nicht so sicher. Selumetinib könnte komplett scheitern, Bini+Enco in Melanoma zwar funktionieren, aber gegen die starke Konkurrenz nur dritte Wahl bleiben... und die weitere Entwicklung, die wohl sehr breit erfolgen muss, wird umso teurer, je mehr sich Novartis daraus zurückzieht (was ja absehbar ist). Sollte es zu Erfolgen kommen z.B. in KRAS+ NSCLC, so sieht die Sache natürlich wieder anders aus.
Gruß
ipollit
Ganz so optimistisch bin ich bezüglich ARRY nicht. Sie scheinen sich sehr auf ihren MEK-Hemmer Bini und den BRAF-Hemmer Enco zu fokussieren. Das Problem ist, dass es für MEK-Hemmer nicht leicht ist, gute Indikationen oder Kombi-Therapien zu entwickeln... bisher sind sie nur in BRAF+ Melanoma erfolgreich, alle anderen Indikationen sind wohl noch sehr unsicher und damit auch entsprechend riskant.
Das zweite Problem ist, dass man insbesondere in BRAF+ Melanoma direkt gegen Novartis und Roche antritt... beides führende Unternehmen im Bereich der Onkologie und TK-Hemmern. Roche waren mit dem BRAF-Hemmer Zelboraf in BRAF+ Melanoma die ersten am Markt... die MEK+BRAF Kombi sollte in den nächsten Monaten zugelassen werden. Novartis haben mit Tafinlar + Mekinist bereits die erste MEK+BRAF Kombi am Markt. D.h. die beiden starken Konkurrenten haben etablierte Mittel in BRAF+ Melanoma mit einem deutlichen zeitlichen Vorsprung. Ich halte es für unwahrscheinlich, dass ARRYs Bini + Enco in BRAF+ Melanoma relevante Vorteile gegen die anderen beiden Kombis hat (oder?). D.h. ARRY ist hier nur die Nr 3 am Markt. BRAF+ Melanoma ist zudem keine große Indikation... optimistisch sind es wohl nur maximal 1-2 Mrd USD, die sich diese drei teilen müssen.
Bini hat wohl in NRAS+ Melanoma die Nase vorne, oder? Anders als die Wirkung eines BRAF-Hemmers in BRAF+ Melanoma ist die eines MEK-Hemmers in NRAS+ nicht sicher... es sieht bisher gut aus, aber erst die kommenden PIII-Ergebnisse werden Klarheit schaffen. NRAS+ ist aber wohl nur 1/3 so groß wie die BRAF+ Melanoma Indikation.
MEK-Hemmer sind wie gesagt schwierig zu entwickeln, da sich der Einfluss auf den RAS-Signalweg und die Relevanz im Tumor nur schwer vorhersagen lässt... wie man an der letzen gescheiterten PIII sieht. MEK-Hemmer funktionieren vielleicht besser in Kombis wie z.B. in BRAF+ Melanoma, wo der Krebs gegen einen BRAF-Hemmer alleine schnell resistent wird über Aktivierung von RAS ("after a relatively short period of disease control, most patients develop resistance because of reactivation of the RAF-ERK pathway, mediated in many cases by mutations in RAS").
Zwischen ARRY/AZNs MEK-Hemmer Selumetinib und z.B. Bini scheint es größere Unterschiede zu geben. So wird Selumetinib z.B. nicht gegen Melanoma entwickelt. Selumetinib scheint ein schwächerer MEK-Hemmer zu sein. Allerdings sind andere MEK-Hemmer unverträglich in der Kombination mit einer Chemo (wie sieht es hier mit Bini aus?)... Selumetinib lässt sich dagegen bei maximaler Dosierung mit einer Chemo anwenden. Daher wird Selumetinib momentan hauptsächlich gegen Lungenkrebs entwickelt, weil zum einen die Chemo das einzige wirksame Mittel gegen Lungenkrebs ist und zum anderen ein größerer Teil von Lungenkrebs Mutationen im RAS-Signalweg KRAS aufweist. Trotzdem ist es aber alles andere als sicher, dass eine MEK + Chemo in KRAS+ Lungenkrebs funktioniert. Im Erfolgsfall wäre der Markt sehr groß... KRAS ist z.B. deutlich häufiger als EGFR und bei KRAS+ wirkt bisher nur die Chemo. Das Risiko eines Fehlschlags ist meiner Meinung aber auch sehr hoch und Selumetinib könnte damit komplett scheitern, da fast die gesamte Entwicklung auf diese Indikation ausgelegt ist.
D.h. die MEK-Hemmer, auf die sich ARRY fokussiert, besitzen ein hohes Entwicklungsrisiko... und selbst mit Einzelerfolgen ist aufgrund der starken Konkurrenz ein wirtschaftlicher Erfolg keinesfalls sicher.
Somit gewichte ich ARRY nicht so hoch... Chancen sind natürlich da, zumal es auch eine große Partner-Pipeline gibt. Aber wäre es bei den bestehenden Risiken auch realistisch, dass ARRY mittelfristig mit z.B. Richtung 2 Mrd USD bewertet sein wird (d.h. Kursverdoppelung)? Ich bin mir da nicht so sicher. Selumetinib könnte komplett scheitern, Bini+Enco in Melanoma zwar funktionieren, aber gegen die starke Konkurrenz nur dritte Wahl bleiben... und die weitere Entwicklung, die wohl sehr breit erfolgen muss, wird umso teurer, je mehr sich Novartis daraus zurückzieht (was ja absehbar ist). Sollte es zu Erfolgen kommen z.B. in KRAS+ NSCLC, so sieht die Sache natürlich wieder anders aus.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.313.462 von ipollit am 01.08.15 19:07:05"Das Risiko eines Fehlschlags ist meiner Meinung aber auch sehr hoch und Selumetinib könnte damit komplett scheitern, da fast die gesamte Entwicklung auf diese Indikation ausgelegt ist."
Hallo ipollit,
insgesamt ein sehr ausgewogener und guter Text, den ich weitgehend teile, auch wenn ich insgesamt die Situation doch etwas positiver sehe.
Ich frage mich zum Beispiel, ob es für AZN nicht vielleicht Sinn machen könnte, Array aufzukaufen, gerade um die Entwicklung von Selumetinib mit Bini "zu hedgen". Letztlich steht auch AZN ziemlich unter Druck, irgendetwas auf die Kette zu bekommen, nachdem man ja zu stolz war, um mit Pfizer zusammen zu gehen und den Aktionären die ganz großen eigenen Erfolge versprochen hat.
Für Bini+Enco braucht es jedenfalls einen starken Pharma als Entwicklungspartner und ich favorisiere inzwischen ein Übernahme von Array.
Gruß
SLG
Hallo ipollit,
insgesamt ein sehr ausgewogener und guter Text, den ich weitgehend teile, auch wenn ich insgesamt die Situation doch etwas positiver sehe.
Ich frage mich zum Beispiel, ob es für AZN nicht vielleicht Sinn machen könnte, Array aufzukaufen, gerade um die Entwicklung von Selumetinib mit Bini "zu hedgen". Letztlich steht auch AZN ziemlich unter Druck, irgendetwas auf die Kette zu bekommen, nachdem man ja zu stolz war, um mit Pfizer zusammen zu gehen und den Aktionären die ganz großen eigenen Erfolge versprochen hat.
Für Bini+Enco braucht es jedenfalls einen starken Pharma als Entwicklungspartner und ich favorisiere inzwischen ein Übernahme von Array.
Gruß
SLG
Antwort auf Beitrag Nr.: 50.313.462 von ipollit am 01.08.15 19:07:05Arry
Moin Ipollit,
Array setzt bei Bini/Enco auf das Nebenwirkungsprofil und sie wollen dadurch best-in-Classic werden. Wer das Medikament über ein Jahr nehmen muß, wird sehr auf die Nebenwirkungen bei gleicher Wirksamkeit achten, so jedenfalls Array. Jetzige Daten stützen das bessere Nebenwirkungsprofil, sie sind aber leider nur in insoweit noch sehr kleinen Studien angefallen.
Zur Anwendbarkeit zusätzlich zu BRAF-V600 Melanoma: Hier bin ich eigentlich zu versichtlich. So hat zB NOV für Mekinist/Tafinlar erst im Juli FDA-Breakthrough für BRAF-V600 lung bekommen. Auch scheinen nach meiner Lesart verschiedene Veröffentlichungen die Euphorie zu stützen, daß MEK/RAF zusammen mit einem weiteren Agent noch wirksamer und breiter eingesetzt werden können zB mit PD-L1. Bei derart großen Combos wird aber bereits die Kostenfrage hörbar aufgeworfen.
In diesem Zusammenhang sollte die LOGIC-2 Studie, die noch von NOV angeschoben wurde, mit Spannung erwartet werden. Hier werden für 140 Patienten verschiedene 3. Agenten ausprobiert, allerdings zugegebenermaßen erstmal nur für BRAF-Melanoma. Ergebnisse sollen in diesem Jahr bekannt gemacht werden.
NRAS-Melanoma/NEMO habe ich wegen der PII-Daten auch ein abwartendes Gefühl...
Umsatz Mekinist/Tanfinlar: Danke Kmastra für Deine Info! Die 130mio/Q waren wohl vorerst nur US, da in Eu und ROW noch keine Zulassung der Combo (und auch in US noch keine Vollzulassung). Da diese Combo zudem erst am Anfang steht, bin ich hinsichtlich des Umsatzpotenzials zuversichtlich.
Man merkt wohl: Ich bin ein Fan von Array (und deshalb vielleicht etwas verblendet...)
Moin Ipollit,
Array setzt bei Bini/Enco auf das Nebenwirkungsprofil und sie wollen dadurch best-in-Classic werden. Wer das Medikament über ein Jahr nehmen muß, wird sehr auf die Nebenwirkungen bei gleicher Wirksamkeit achten, so jedenfalls Array. Jetzige Daten stützen das bessere Nebenwirkungsprofil, sie sind aber leider nur in insoweit noch sehr kleinen Studien angefallen.
Zur Anwendbarkeit zusätzlich zu BRAF-V600 Melanoma: Hier bin ich eigentlich zu versichtlich. So hat zB NOV für Mekinist/Tafinlar erst im Juli FDA-Breakthrough für BRAF-V600 lung bekommen. Auch scheinen nach meiner Lesart verschiedene Veröffentlichungen die Euphorie zu stützen, daß MEK/RAF zusammen mit einem weiteren Agent noch wirksamer und breiter eingesetzt werden können zB mit PD-L1. Bei derart großen Combos wird aber bereits die Kostenfrage hörbar aufgeworfen.
In diesem Zusammenhang sollte die LOGIC-2 Studie, die noch von NOV angeschoben wurde, mit Spannung erwartet werden. Hier werden für 140 Patienten verschiedene 3. Agenten ausprobiert, allerdings zugegebenermaßen erstmal nur für BRAF-Melanoma. Ergebnisse sollen in diesem Jahr bekannt gemacht werden.
NRAS-Melanoma/NEMO habe ich wegen der PII-Daten auch ein abwartendes Gefühl...
Umsatz Mekinist/Tanfinlar: Danke Kmastra für Deine Info! Die 130mio/Q waren wohl vorerst nur US, da in Eu und ROW noch keine Zulassung der Combo (und auch in US noch keine Vollzulassung). Da diese Combo zudem erst am Anfang steht, bin ich hinsichtlich des Umsatzpotenzials zuversichtlich.
Man merkt wohl: Ich bin ein Fan von Array (und deshalb vielleicht etwas verblendet...)
Antwort auf Beitrag Nr.: 50.314.146 von SLGramann am 02.08.15 08:04:37arry
Hallo SLGramann,
das ist ein interessanter Gedanke. In der Tat kann man sich Übernahmespekulationen von arry durch verschiedene Pharma/Biotechs herleiten:
Beispiele:
MRK und BMY: Wegen der Kombination von BRAF/MEK mit den Checkpoint-Inhibitoren (hier sind auch Partnerschaften denkbar).
PFE: Wegen der Kombination ihres CDK4/6 Inhibitors mit MEK. PFE hat MEK/BRAF komplett verschlafen und hat (wie immer) Handlungsbedarf für Zukäufe.
Lilly: Wegen der Kombination von Erbitux mit BRAF bei Colon-Cancer. In dem Zusammenhang kann man auch die deutsche Merck ins Spiel bringen, z.B. als Europa-Partner.
Die aufstrebenden, zahlungsstarken Biotechs Celgene und Gilead: Wegen der Stärkung ihrer Onkologie-Portfolios.
Das Interessante ist, dass arry zurzeit abwarten kann, da ja die Studien nicht selbst finanziert werden müssen. Selbst wenn am Ende nur die BRAF/MEK Kombination (das ist zu erwarten) ein Erfolg wird, haben sie es quasi geschenkt bekommen und sind dann ein Player in dem Bereich.
MEK/BRAF ist noch lange nicht ausgereizt. Es werden zurzeit große Studien gestartet, um Tumore konsequent wegen der detektierten Mutationen mit entsprechenden Inhibitoren zu behandeln, nicht wegen ihrer Ursprungsorgane. Voll mit dabei: MEK und BRAF Inhibitoren.
A
Hallo SLGramann,
das ist ein interessanter Gedanke. In der Tat kann man sich Übernahmespekulationen von arry durch verschiedene Pharma/Biotechs herleiten:
Beispiele:
MRK und BMY: Wegen der Kombination von BRAF/MEK mit den Checkpoint-Inhibitoren (hier sind auch Partnerschaften denkbar).
PFE: Wegen der Kombination ihres CDK4/6 Inhibitors mit MEK. PFE hat MEK/BRAF komplett verschlafen und hat (wie immer) Handlungsbedarf für Zukäufe.
Lilly: Wegen der Kombination von Erbitux mit BRAF bei Colon-Cancer. In dem Zusammenhang kann man auch die deutsche Merck ins Spiel bringen, z.B. als Europa-Partner.
Die aufstrebenden, zahlungsstarken Biotechs Celgene und Gilead: Wegen der Stärkung ihrer Onkologie-Portfolios.
Das Interessante ist, dass arry zurzeit abwarten kann, da ja die Studien nicht selbst finanziert werden müssen. Selbst wenn am Ende nur die BRAF/MEK Kombination (das ist zu erwarten) ein Erfolg wird, haben sie es quasi geschenkt bekommen und sind dann ein Player in dem Bereich.
MEK/BRAF ist noch lange nicht ausgereizt. Es werden zurzeit große Studien gestartet, um Tumore konsequent wegen der detektierten Mutationen mit entsprechenden Inhibitoren zu behandeln, nicht wegen ihrer Ursprungsorgane. Voll mit dabei: MEK und BRAF Inhibitoren.
A
Medivation - Split - mögliche Steuerproblematik
Medivation hat Xtandi-Quartalszahlen gemeldet und plant einen 2:1-Aktiensplit durchzuführen: http://investors.medivation.com/secfiling.cfm?filingID=11931…Stichtag Bezugsrecht neue Aktien = 13.08.2015 (ex-Tag = 14.08.2015)
Handelsaufnahme neue Aktien = 15.09.2015
Durchführung als "Stock-Dividend"
Für Aktionäre mit deutschen Depots wird dieser Split evtl. steuerschädlich, da es bei uns fälschlicherweise als Dividenden- / Sachausschüttung in Aktienform gewertet wird.
Mögliche steuerlichen Folgen in D:
- US-(Quellen)-Steuer fällt nicht an
- der Anschaffungskurs des Altbestandes (bzgl. Abgeltungssteuer) bleibt bestehen, obwohl sich der Aktienkurs in etwa halbieren wird.
- die "Sachausschüttung" (alle neuen Splitaktien mit Kurs bei Handelsaufnahme) wird zu 100% sofort besteuert.
- Altbestände vor Abgeltungssteuer (vor 2009) werden damit "halbiert".
Somit wird ungefähr der halbe Aktienbestand mit Kapitalertragssteuer belegt. Diese Steuern sind übrigens (wie Dividende) nicht mit Verlusten aus Aktiengeschäften verrechenbar, wenn z.B. der Altbestand verkauft würde.
O.g. Sachverhalt hängt von der Einstufung u. Meldung von WM-Daten an die Depotführenden Banken ab.
das ist wirklich ärgerlich, wobei ich nicht betroffen bin. Habe das aber gerade bei ebay-paypal erlebt,wo die Abspaltung der Paypal-Aktie zunächst von den dt. Behörden als steuerpflichtige Sachdividende bewertet wurde. Ähnlich war es wohl mal bei google, wobei dort die steuerliche Bewertung später korrigiert wurde.
Im Endeffekt hilft eigentlich nur vor dem Split verkaufen, wenn man nicht völlig absurde Steuern bezahlen will für einen Split.
Im Endeffekt hilft eigentlich nur vor dem Split verkaufen, wenn man nicht völlig absurde Steuern bezahlen will für einen Split.
Antwort auf Beitrag Nr.: 50.330.679 von xylophon am 04.08.15 18:41:31Nur kurz zum Steuerthema:
Ob etwas steuerpflichtig ist oder nicht entscheidet Gott sei Dank allein das Gesetz, nicht aber die Bank und schon gar nicht WM Datenservice als privater kommerzieller Dienstleister. Das Problem liegt darin, daß die Banken den Kapitalertragsteuerabzug vollkommen automatisiert durchführen und dabei stumpf auf die gemeldeten Daten von WM zurückgreifen. Die Wahrscheinlichkeit, daß überhaupt irgendjemand in der automatisierten Kette sich Gedanken macht oder steuerliches Wissen mitbringt, ist nicht groß. Fehler beim Steuereinbehalt sind häufig.
Zwei Möglichkeiten: WM Datenservice über die Hausbank auf die fehlerhafte Meldung hinweisen (kann mühsam sein) oder besser kurz mit dem Finanzamt im Rahmen der Steuererklärung reden und Steuern zurück erhalten.
Ob etwas steuerpflichtig ist oder nicht entscheidet Gott sei Dank allein das Gesetz, nicht aber die Bank und schon gar nicht WM Datenservice als privater kommerzieller Dienstleister. Das Problem liegt darin, daß die Banken den Kapitalertragsteuerabzug vollkommen automatisiert durchführen und dabei stumpf auf die gemeldeten Daten von WM zurückgreifen. Die Wahrscheinlichkeit, daß überhaupt irgendjemand in der automatisierten Kette sich Gedanken macht oder steuerliches Wissen mitbringt, ist nicht groß. Fehler beim Steuereinbehalt sind häufig.
Zwei Möglichkeiten: WM Datenservice über die Hausbank auf die fehlerhafte Meldung hinweisen (kann mühsam sein) oder besser kurz mit dem Finanzamt im Rahmen der Steuererklärung reden und Steuern zurück erhalten.
Antwort auf Beitrag Nr.: 50.330.877 von lawmeetstax am 04.08.15 19:04:28alles richtig, aber Recht haben und Recht bekommen ist nicht immer das selbe. Bei ebay haben wir bei der Bank widersprochen, die wird das weiterleiten. ABER:
bei Google hat es über 1 Jahr gedauert, bis das Ministerium eine Anweisung gab, wie die Gratis-Akien richtig zu bewerten sind. Ich hab das gerade im Zusammenhang mit ebay-paypal alles nachgelesen. M.E. war die Rechtslage ziemlich klar, aber das hat wenig bewirkt....
bei Google hat es über 1 Jahr gedauert, bis das Ministerium eine Anweisung gab, wie die Gratis-Akien richtig zu bewerten sind. Ich hab das gerade im Zusammenhang mit ebay-paypal alles nachgelesen. M.E. war die Rechtslage ziemlich klar, aber das hat wenig bewirkt....
Antwort auf Beitrag Nr.: 50.330.877 von lawmeetstax am 04.08.15 19:04:28
... ich wollte hier nur vorwarnen ;-)
Es liegt m.e. kein Fehler von WM-Daten vor, wenn diese den Vorgang steuerpflichtig auflisten, da aus den USA als Stock-Dividend gemeldet (lt. Gesetz in D steuerpflichtig). WM-Daten ist nicht verpflichtet zu prüfen, ob tatsächlich eine Sachausschüttung in Aktienform vorliegt.
Die depotführende Bank ist ebenso nicht verpflichtet die Mitteilungen auf Richtigkeit zu prüfen, haftet jedoch dafür, die Steuern korrekt abzuführen. Daher wird diese wahrscheinlich bei ungeklärtem Sachverhalt nicht ins Risiko / Vorleistung gehen und eine Erstattung oder Nichtabzug vornehmen.
Der "kleine" Mitarbeiter des Heimatfinanzamts wird normalerweise diesen Sachverhalt genauso wenig klären u. entscheiden können (im nächsten Jahr).
Das BMF nimmt sich dieser Fälle nur an, wenn entsprechendes öffentliches Interesse (wie z.B. bei Google) gegeben ist. Eine Entscheidung dauert auch hier locker ein Jahr. Diese wird nur fallbezogen und nicht allgemeingültig getroffen (siehe http://www.bundesfinanzministerium.de/Content/DE/Downloads/B…).
Das könnte nur der Gesetzgeber ... und der bleibt hier, wie bei der ungerechten Besteuerung von Unternehmensabspaltungen ausländischer Gesellschaften, untätig.
Und da schließt sich der Kreis.
Bleibt für die Aktionäre, welche keine Altbestände vor Abgeltungssteuer haben u. nicht zu stark im plus sind, der Verkauf vor Split, bzw. Umschichtung in Optionen, falls möglich ... wie von Xylophon empfohlen.
Damit sollte das Thema im Biotech-Bereich erledigt sein - es gibt sicher einen Steuer-Thread dafür.
Zitat von lawmeetstax: Nur kurz zum Steuerthema:
...
Zwei Möglichkeiten: WM Datenservice über die Hausbank auf die fehlerhafte Meldung hinweisen (kann mühsam sein) oder besser kurz mit dem Finanzamt im Rahmen der Steuererklärung reden und Steuern zurück erhalten.
... ich wollte hier nur vorwarnen ;-)
Es liegt m.e. kein Fehler von WM-Daten vor, wenn diese den Vorgang steuerpflichtig auflisten, da aus den USA als Stock-Dividend gemeldet (lt. Gesetz in D steuerpflichtig). WM-Daten ist nicht verpflichtet zu prüfen, ob tatsächlich eine Sachausschüttung in Aktienform vorliegt.
Die depotführende Bank ist ebenso nicht verpflichtet die Mitteilungen auf Richtigkeit zu prüfen, haftet jedoch dafür, die Steuern korrekt abzuführen. Daher wird diese wahrscheinlich bei ungeklärtem Sachverhalt nicht ins Risiko / Vorleistung gehen und eine Erstattung oder Nichtabzug vornehmen.
Der "kleine" Mitarbeiter des Heimatfinanzamts wird normalerweise diesen Sachverhalt genauso wenig klären u. entscheiden können (im nächsten Jahr).
Das BMF nimmt sich dieser Fälle nur an, wenn entsprechendes öffentliches Interesse (wie z.B. bei Google) gegeben ist. Eine Entscheidung dauert auch hier locker ein Jahr. Diese wird nur fallbezogen und nicht allgemeingültig getroffen (siehe http://www.bundesfinanzministerium.de/Content/DE/Downloads/B…).
Das könnte nur der Gesetzgeber ... und der bleibt hier, wie bei der ungerechten Besteuerung von Unternehmensabspaltungen ausländischer Gesellschaften, untätig.
Und da schließt sich der Kreis.
Bleibt für die Aktionäre, welche keine Altbestände vor Abgeltungssteuer haben u. nicht zu stark im plus sind, der Verkauf vor Split, bzw. Umschichtung in Optionen, falls möglich ... wie von Xylophon empfohlen.
Damit sollte das Thema im Biotech-Bereich erledigt sein - es gibt sicher einen Steuer-Thread dafür.
Antwort auf Beitrag Nr.: 50.331.600 von Nase_weis_nix am 04.08.15 20:36:55EXEL
Gibt es hier Meinungen zu Exelixis? Das Ding steigt momentan ja recht gut, Ohad Hammer hat es kürzlich auch wieder in sein Portfolio aufgenommen. Bin gespannt wie weit die Reise geht.
Grüße
Gibt es hier Meinungen zu Exelixis? Das Ding steigt momentan ja recht gut, Ohad Hammer hat es kürzlich auch wieder in sein Portfolio aufgenommen. Bin gespannt wie weit die Reise geht.
Grüße
das war aber ein harter Tag heute....Bluebird und QURE mit je 12 % Verlust, um nur die schlimmsten Verlierer zu nennen, aber der ganze Sektor hat bei mir roten Zeichen (die meisten anderen Aktien auchm, aber nicht so extrem).
"das war aber ein harter Tag heute..."
Ja, das war er.
Wenn man auf den NBI schaut, sieht man aber, dass (noch?) so gut wie nichts passiert ist:
NBI - 5 Jahre:

NBI - 2 Jahre:

Vor allem ipollit hat des öfteren - und meiner Meinung nach grundsätzlich zu recht - darauf hingewiesen, dass dieser exorbitante Anstieg des NBI von wissenschaftlichen Durchbrüchen und massiv steigenden Gewinnen der Biotech-Schwergewichte fundamental unterfüttert wird, so dass es sich nicht um eine klassische Blase handeln dürfte.
Dennoch bin ich persönlich der Meinung, dass 1.) die Bewertungen den Fundamentaldaten zum Teil doch etwas davon gelaufen sind, dass 2.) Unternehmen, die noch keine Wirkstoffe am Markt haben teilweise blasenhaft überbewertet sind und dass 3.) ganz grundsätzlich der Anstiegspfad des NBI flacher werden muss, selbst wenn man keine grundsätzlichen fundamentalen Probleme unterstellt.
zu 1.) ein Beispiel ist CELG. Dort würde ich einen heutigen Kurs von ca. 110 Dollar für vertretbarer halten, als bspw. 130 Dollar.
Bei den 110 Dollar sind ja die Gewinne des Jahres 2017 schon im Hinterkopf.
Die Bewertung von REGN ist meiner Meinung nach verrückt. Ein phantastisches Unternehmen natürlich, aber auch dort wachsen die Bäume nicht in den Himmel und der Kurs kann das auch nicht ewig tun.
zu 2.) Bewertungen von Unternehmen, die nur aus PII-Pipelines bestehen oder noch unreifer sind, erreichen inzwischen regelmäßig Multimilliardenwerte. Dabei wird von den Risiken - und seien das bspw. nur Konkurrenzprodukte - freizügig abgesehen.
zu 3.) Wachstum wird ab einem bestimmten Niveau schwieriger. Die Biotech-Branche hat echte Durchbrüche erzielt, aber inzwischen ist eben vieles eingepreist.
Man sieht das auch gut am Einzelwert GILD. Eine der größten Erfolgsgeschichten, aber künftige Verdopplungen des Unternehmenswertes stoßen langsam an Grenzen des auf dieser Erde möglichen.
Alles in allem vermute ich, dass sich im NBI ein flacherer Trend ergeben wird oder sogar eine Art Plateaubildung bevorsteht.
Das könnte mit allerlei verrückten Kursbewegungen und kurzfristigen Übertreibungen - auch nach unten - einhergehen.
Wir sollten auf alles mögliche gefasst sein.
Ja, das war er.
Wenn man auf den NBI schaut, sieht man aber, dass (noch?) so gut wie nichts passiert ist:
NBI - 5 Jahre:
NBI - 2 Jahre:
Vor allem ipollit hat des öfteren - und meiner Meinung nach grundsätzlich zu recht - darauf hingewiesen, dass dieser exorbitante Anstieg des NBI von wissenschaftlichen Durchbrüchen und massiv steigenden Gewinnen der Biotech-Schwergewichte fundamental unterfüttert wird, so dass es sich nicht um eine klassische Blase handeln dürfte.
Dennoch bin ich persönlich der Meinung, dass 1.) die Bewertungen den Fundamentaldaten zum Teil doch etwas davon gelaufen sind, dass 2.) Unternehmen, die noch keine Wirkstoffe am Markt haben teilweise blasenhaft überbewertet sind und dass 3.) ganz grundsätzlich der Anstiegspfad des NBI flacher werden muss, selbst wenn man keine grundsätzlichen fundamentalen Probleme unterstellt.
zu 1.) ein Beispiel ist CELG. Dort würde ich einen heutigen Kurs von ca. 110 Dollar für vertretbarer halten, als bspw. 130 Dollar.
Bei den 110 Dollar sind ja die Gewinne des Jahres 2017 schon im Hinterkopf.
Die Bewertung von REGN ist meiner Meinung nach verrückt. Ein phantastisches Unternehmen natürlich, aber auch dort wachsen die Bäume nicht in den Himmel und der Kurs kann das auch nicht ewig tun.
zu 2.) Bewertungen von Unternehmen, die nur aus PII-Pipelines bestehen oder noch unreifer sind, erreichen inzwischen regelmäßig Multimilliardenwerte. Dabei wird von den Risiken - und seien das bspw. nur Konkurrenzprodukte - freizügig abgesehen.
zu 3.) Wachstum wird ab einem bestimmten Niveau schwieriger. Die Biotech-Branche hat echte Durchbrüche erzielt, aber inzwischen ist eben vieles eingepreist.
Man sieht das auch gut am Einzelwert GILD. Eine der größten Erfolgsgeschichten, aber künftige Verdopplungen des Unternehmenswertes stoßen langsam an Grenzen des auf dieser Erde möglichen.
Alles in allem vermute ich, dass sich im NBI ein flacherer Trend ergeben wird oder sogar eine Art Plateaubildung bevorsteht.
Das könnte mit allerlei verrückten Kursbewegungen und kurzfristigen Übertreibungen - auch nach unten - einhergehen.
Wir sollten auf alles mögliche gefasst sein.
danke für die Einschätzung...
Ich erkläre mir die Bewertungen der kleineren Werte so, dass jeder auf das "große Los" hofft, also ein marktreifes Medikament oder die Übenahme mit gutem Aufschlag. Damit werden die Aktien sicher höher bewertet, als der realistische jetzige Wert ist, aber bei einem gewissen Prozentsatz ist eben die Chance da, dass sie noch extrem steigen, dafür wird der Rest vielleicht auch mehr oder weniger wertlos enden....
Solche Situationen gibt es m.e. in diesem Sektor sehr viel extremer als in der "normalen" Wirtschaft, weil eben die erfolgreiche Entwicklung von Medikamenten für Laien kaum vorhersehbar ist und für Experten auch nicht besonders sicher...
Ich habe selbst ein paar solcher "Hoffnungswerte" im Depot, jeweils mit wenig "Einsatz", einer davon ist gerade deutlich zurückgefallen nach einer schwachen Studie (Immunomedics), andere waren bis Freitag deutlich im Plus und sind jetzt noch leicht im Plus bzw. leicht im Minus, aber ich habe keinen Verkaufsdruck....wie ich auch bei solchen Werten nicht nachkaufe, es sei denn, ich höre sehr deutlich, warum der Markt ein Ergebnis falsch bewertet (gab es neulich hier).
Ich erkläre mir die Bewertungen der kleineren Werte so, dass jeder auf das "große Los" hofft, also ein marktreifes Medikament oder die Übenahme mit gutem Aufschlag. Damit werden die Aktien sicher höher bewertet, als der realistische jetzige Wert ist, aber bei einem gewissen Prozentsatz ist eben die Chance da, dass sie noch extrem steigen, dafür wird der Rest vielleicht auch mehr oder weniger wertlos enden....
Solche Situationen gibt es m.e. in diesem Sektor sehr viel extremer als in der "normalen" Wirtschaft, weil eben die erfolgreiche Entwicklung von Medikamenten für Laien kaum vorhersehbar ist und für Experten auch nicht besonders sicher...
Ich habe selbst ein paar solcher "Hoffnungswerte" im Depot, jeweils mit wenig "Einsatz", einer davon ist gerade deutlich zurückgefallen nach einer schwachen Studie (Immunomedics), andere waren bis Freitag deutlich im Plus und sind jetzt noch leicht im Plus bzw. leicht im Minus, aber ich habe keinen Verkaufsdruck....wie ich auch bei solchen Werten nicht nachkaufe, es sei denn, ich höre sehr deutlich, warum der Markt ein Ergebnis falsch bewertet (gab es neulich hier).
@kpti
Mehrere Sepsis-Fälle, daher Dosisreduzierung! Steigt Ihr aus? Ich werde wohl aussteigen, aber Eure Meinung würde ich vorher gern hören.
@aqxp
dieser Wert wurde hier nur sehr selten angesprochen, Hammer war auch skeptisch. Jetzt sollte dieser Wert aber eine Legende geworden sein: Erst 80% Minus, weil primärer Endpunkt nicht erreicht. Freitag dann Bekanntgabe positiver secondary endpoints. Seit Freitag zwischenzeitlich 2000% (in Worten: zweitausend) im Plus. Ich Blödmann habe nach dem Niedergang zwar nicht verkauft, dann aber bei 200% plus (das war ursprünglich mein Einstieg) verkauft. Nach meinem Ausstieg hat sich der Wert kurz danach zeitweise verzehnfacht innerhalb eines Tages!!
Mehrere Sepsis-Fälle, daher Dosisreduzierung! Steigt Ihr aus? Ich werde wohl aussteigen, aber Eure Meinung würde ich vorher gern hören.
@aqxp
dieser Wert wurde hier nur sehr selten angesprochen, Hammer war auch skeptisch. Jetzt sollte dieser Wert aber eine Legende geworden sein: Erst 80% Minus, weil primärer Endpunkt nicht erreicht. Freitag dann Bekanntgabe positiver secondary endpoints. Seit Freitag zwischenzeitlich 2000% (in Worten: zweitausend) im Plus. Ich Blödmann habe nach dem Niedergang zwar nicht verkauft, dann aber bei 200% plus (das war ursprünglich mein Einstieg) verkauft. Nach meinem Ausstieg hat sich der Wert kurz danach zeitweise verzehnfacht innerhalb eines Tages!!
Antwort auf Beitrag Nr.: 50.369.427 von lawmeetstax am 10.08.15 19:06:43
kpti: ich finde bedenklich, das die Fälle Ende Juli schon bekannt waren, aber jetzt erst öffentlich was gesagt wurde. Glaubwürdigkeit sieht anders aus.
Zitat von lawmeetstax: @kpti
Mehrere Sepsis-Fälle, daher Dosisreduzierung! Steigt Ihr aus? Ich werde wohl aussteigen, aber Eure Meinung würde ich vorher gern hören.
@aqxp
dieser Wert wurde hier nur sehr selten angesprochen, Hammer war auch skeptisch. Jetzt sollte dieser Wert aber eine Legende geworden sein: Erst 80% Minus, weil primärer Endpunkt nicht erreicht. Freitag dann Bekanntgabe positiver secondary endpoints. Seit Freitag zwischenzeitlich 2000% (in Worten: zweitausend) im Plus. Ich Blödmann habe nach dem Niedergang zwar nicht verkauft, dann aber bei 200% plus (das war ursprünglich mein Einstieg) verkauft. Nach meinem Ausstieg hat sich der Wert kurz danach zeitweise verzehnfacht innerhalb eines Tages!!
kpti: ich finde bedenklich, das die Fälle Ende Juli schon bekannt waren, aber jetzt erst öffentlich was gesagt wurde. Glaubwürdigkeit sieht anders aus.
Antwort auf Beitrag Nr.: 50.369.427 von lawmeetstax am 10.08.15 19:06:43"Steigt Ihr aus? Ich werde wohl aussteigen, aber Eure Meinung würde ich vorher gern hören."
Da möchte ich lieber keinen Rat geben...
Zumindest steige ich zur Zeit nicht ein - trotz des stark verbilligten Kurses. Ich finde die Situation zu unübersichtlich.
Ich beurteile die zu Tage getretene Nebenwirkung als schwerwiegend. Kommt man der Sache mit einer Dosisreduzierung bei? Und wie wirkt diese sich auf die Effektivität des Wirkstoffs aus?
Im Moment hängt KPTI in der Luft und ich denke nicht, dass man heute schon einschätzen kann, wie es weitergeht.
Sehr schade dieser Tag heute. Leider durchaus üblich für die Branche. ipollit hatte immer recht mit seiner Methodik, für jeden Wert nur sehr kleine Gewichtungen (KPTI bei 4% des Depots?) zuzulassen.
Das ist einfach Pflicht im Biotech-Bereich.
Da möchte ich lieber keinen Rat geben...

Zumindest steige ich zur Zeit nicht ein - trotz des stark verbilligten Kurses. Ich finde die Situation zu unübersichtlich.
Ich beurteile die zu Tage getretene Nebenwirkung als schwerwiegend. Kommt man der Sache mit einer Dosisreduzierung bei? Und wie wirkt diese sich auf die Effektivität des Wirkstoffs aus?
Im Moment hängt KPTI in der Luft und ich denke nicht, dass man heute schon einschätzen kann, wie es weitergeht.
Sehr schade dieser Tag heute. Leider durchaus üblich für die Branche. ipollit hatte immer recht mit seiner Methodik, für jeden Wert nur sehr kleine Gewichtungen (KPTI bei 4% des Depots?) zuzulassen.
Das ist einfach Pflicht im Biotech-Bereich.
Antwort auf Beitrag Nr.: 50.369.427 von lawmeetstax am 10.08.15 19:06:43KPTI
ich warte erstmal ab... für mich ist es bisher kein Grund auszusteigen, eher werde ich noch etwas hinzukaufen. Allerdings kann es gut sein, dass der Kurs vorerst schwach bleibt.
Soweit ich es verstehe (z.B. CC Transkript... http://seekingalpha.com/article/3423476-karyopharm-therapeut…), betrifft die Dosisreduzierung nur AML. Sepsis ("Blutvergiftung"... massive Ausbreitung von Krankheitserregern im ganzen Körper) ist natürlich ein gravierendes Problem. Allerdings ist die Immunabwehr bei fortgeschrittenen AML bereits von der Erkrankung massiv gestört... prophylaktisch werden sie mit Antibiotika&Co behandelt. In der Kontrollgruppe ohne Selinexor gab es zwei Sepsis Fälle... in der Selinexor-Gruppe 8 Fälle. Wenn Selinexor keinen Einfluss hätte, hätte theoretisch das Verhältnis 2 zu 4 oder 4 zu 8 sein müssen, da der Kontrollarm nur halb soviele Patienten hat. Wenn bei den wenigen Patienten nur eine Sepsis mehr in der Kontrollgruppe und eine weniger in der Selinexor-Gruppe aufgetreten wäre, wäre das Verhältnis mit 3 zu 7 wieder unauffällig. Aber KPTI muss natürlich zur Sicherheit reagieren und kann nicht auf einen Zufall hoffen.
Gleichzeitig sind ähnliche Erkrankungen, die aufgrund eines schwachen Immunsystems und wie Sepsis auch bei AML auftreten können, z.B. Lungenentzündung, nicht erhöht. Also ganz schlüssig ist das Bild nicht, dass sich Selinexor negativ auswirkt.
Laut KPTI ist in anderen Studien außerhalb von AML keine erhöhte Sepsis aufgetreten. Wohl ca. 1000 Patienten haben Selinexor bereits (in niedrigerer oder höherer Dosierung) erhalten.
Die Dosis in AML wird nur um ca 1/3 reduziert. Diese Reduktion soll laut KPTI keinen Einfluss auf die Wirkung haben... unter dieser Dosisierung gab es in AML auch CRs. In anderen Studien gibt es keine Reduktion, soweit ich es verstehe.
Gruß
ipollit
ich warte erstmal ab... für mich ist es bisher kein Grund auszusteigen, eher werde ich noch etwas hinzukaufen. Allerdings kann es gut sein, dass der Kurs vorerst schwach bleibt.
Soweit ich es verstehe (z.B. CC Transkript... http://seekingalpha.com/article/3423476-karyopharm-therapeut…), betrifft die Dosisreduzierung nur AML. Sepsis ("Blutvergiftung"... massive Ausbreitung von Krankheitserregern im ganzen Körper) ist natürlich ein gravierendes Problem. Allerdings ist die Immunabwehr bei fortgeschrittenen AML bereits von der Erkrankung massiv gestört... prophylaktisch werden sie mit Antibiotika&Co behandelt. In der Kontrollgruppe ohne Selinexor gab es zwei Sepsis Fälle... in der Selinexor-Gruppe 8 Fälle. Wenn Selinexor keinen Einfluss hätte, hätte theoretisch das Verhältnis 2 zu 4 oder 4 zu 8 sein müssen, da der Kontrollarm nur halb soviele Patienten hat. Wenn bei den wenigen Patienten nur eine Sepsis mehr in der Kontrollgruppe und eine weniger in der Selinexor-Gruppe aufgetreten wäre, wäre das Verhältnis mit 3 zu 7 wieder unauffällig. Aber KPTI muss natürlich zur Sicherheit reagieren und kann nicht auf einen Zufall hoffen.
Gleichzeitig sind ähnliche Erkrankungen, die aufgrund eines schwachen Immunsystems und wie Sepsis auch bei AML auftreten können, z.B. Lungenentzündung, nicht erhöht. Also ganz schlüssig ist das Bild nicht, dass sich Selinexor negativ auswirkt.
Laut KPTI ist in anderen Studien außerhalb von AML keine erhöhte Sepsis aufgetreten. Wohl ca. 1000 Patienten haben Selinexor bereits (in niedrigerer oder höherer Dosierung) erhalten.
Die Dosis in AML wird nur um ca 1/3 reduziert. Diese Reduktion soll laut KPTI keinen Einfluss auf die Wirkung haben... unter dieser Dosisierung gab es in AML auch CRs. In anderen Studien gibt es keine Reduktion, soweit ich es verstehe.
Gruß
ipollit
CLDX
leider gibt es zurzeit die eine oder andere Enttäuschung ... bei CLDX scheint ein AA für Rintega laut FDA-Feedback auf 0 gesunken zu sein... d.h. sehr wahrscheinlich keine Zulassungschance vor 2017 (also nur nach Erfolg der laufenden 1st-line PIII)! Die guten 2nd-line PII-Daten scheinen relativ irrelevant zu sein.
... bei CLDX scheint ein AA für Rintega laut FDA-Feedback auf 0 gesunken zu sein... d.h. sehr wahrscheinlich keine Zulassungschance vor 2017 (also nur nach Erfolg der laufenden 1st-line PIII)! Die guten 2nd-line PII-Daten scheinen relativ irrelevant zu sein.
Der Kurs wird wohl mehr oder weniger implodieren...

Gruß
ipollit
leider gibt es zurzeit die eine oder andere Enttäuschung
 ... bei CLDX scheint ein AA für Rintega laut FDA-Feedback auf 0 gesunken zu sein... d.h. sehr wahrscheinlich keine Zulassungschance vor 2017 (also nur nach Erfolg der laufenden 1st-line PIII)! Die guten 2nd-line PII-Daten scheinen relativ irrelevant zu sein.
... bei CLDX scheint ein AA für Rintega laut FDA-Feedback auf 0 gesunken zu sein... d.h. sehr wahrscheinlich keine Zulassungschance vor 2017 (also nur nach Erfolg der laufenden 1st-line PIII)! Die guten 2nd-line PII-Daten scheinen relativ irrelevant zu sein.Der Kurs wird wohl mehr oder weniger implodieren...
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.370.657 von ipollit am 10.08.15 22:27:52danke, wieder mal ein gut verständlicher interessanter Beitrag.
Antwort auf Beitrag Nr.: 50.370.876 von ipollit am 10.08.15 23:04:38CLDX
für ReACT gab es von der FDA ein BTD... das hat sich ja gelohnt!
Eine wesentliche Begründung für die Nicht-Genehmigung des AA der FDA zumindest laut CLDX... ein AA (vorzeitige Zulassung auf Basis einer PII) ist nur eine vorläufige Zulassung, die später durch eine PIII-Studie bestätigt werden muss mit einem echten Endpunkt wie OS. Der Endpunkt für AA kann damit nicht OS sein, da dieser erst in der PIII getestet werden soll. Für einen AA zählen nur Endpunkte wie RR, die auf einen möglichen spätere positiven OS in der PIII hindeuten. Ein positiver OS bereits in der PII ist somit wertlos! ... so so, alles klar!
Gruß
ipollit
für ReACT gab es von der FDA ein BTD... das hat sich ja gelohnt!
Eine wesentliche Begründung für die Nicht-Genehmigung des AA der FDA zumindest laut CLDX... ein AA (vorzeitige Zulassung auf Basis einer PII) ist nur eine vorläufige Zulassung, die später durch eine PIII-Studie bestätigt werden muss mit einem echten Endpunkt wie OS. Der Endpunkt für AA kann damit nicht OS sein, da dieser erst in der PIII getestet werden soll. Für einen AA zählen nur Endpunkte wie RR, die auf einen möglichen spätere positiven OS in der PIII hindeuten. Ein positiver OS bereits in der PII ist somit wertlos! ... so so, alles klar!

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.370.657 von ipollit am 10.08.15 22:27:52http://www.bizjournals.com/boston/blog/bioflash/2015/08/kayopharm-shares-hit-new-low-after-cancer-drug.html?ana=yahoo
http://www.bizjournals.com/boston/blog/bioflash/2015/08/kayo…
Du bleibts drin?
http://www.bizjournals.com/boston/blog/bioflash/2015/08/kayo…
Du bleibts drin?

Antwort auf Beitrag Nr.: 50.371.026 von ipollit am 10.08.15 23:50:48
mal ne dumme Frage: Was ist ein BTD?
Zitat von ipollit: CLDX
für ReACT gab es von der FDA ein BTD... das hat sich ja gelohnt!
Eine wesentliche Begründung für die Nicht-Genehmigung des AA der FDA zumindest laut CLDX... ein AA (vorzeitige Zulassung auf Basis einer PII) ist nur eine vorläufige Zulassung, die später durch eine PIII-Studie bestätigt werden muss mit einem echten Endpunkt wie OS. Der Endpunkt für AA kann damit nicht OS sein, da dieser erst in der PIII getestet werden soll. Für einen AA zählen nur Endpunkte wie RR, die auf einen möglichen spätere positiven OS in der PIII hindeuten. Ein positiver OS bereits in der PII ist somit wertlos! ... so so, alles klar!
Gruß
ipollit
mal ne dumme Frage: Was ist ein BTD?
Antwort auf Beitrag Nr.: 50.371.677 von riverstar_de am 11.08.15 08:19:59
Breakthrough Therapy Designation (BTD)
Zitat von riverstar_de:Zitat von ipollit: CLDX
für ReACT gab es von der FDA ein BTD... das hat sich ja gelohnt!
Eine wesentliche Begründung für die Nicht-Genehmigung des AA der FDA zumindest laut CLDX... ein AA (vorzeitige Zulassung auf Basis einer PII) ist nur eine vorläufige Zulassung, die später durch eine PIII-Studie bestätigt werden muss mit einem echten Endpunkt wie OS. Der Endpunkt für AA kann damit nicht OS sein, da dieser erst in der PIII getestet werden soll. Für einen AA zählen nur Endpunkte wie RR, die auf einen möglichen spätere positiven OS in der PIII hindeuten. Ein positiver OS bereits in der PII ist somit wertlos! ... so so, alles klar!
Gruß
ipollit
mal ne dumme Frage: Was ist ein BTD?
Breakthrough Therapy Designation (BTD)
Antwort auf Beitrag Nr.: 50.370.876 von ipollit am 10.08.15 23:04:38
Warum meinst Du das CLDX implodiert? Wie der Kursverlauf scheint, wussten mal wieder einige mehr und so ist es nun klar warum der Kurs seit Tagen / Wochen gesunken ist. RSI ist unter 30, ich denke der heutige Absturz ist überschaubar zumal Rintega ja nicht gefloppt ist.
Zitat von ipollit: CLDX
leider gibt es zurzeit die eine oder andere Enttäuschung... bei CLDX scheint ein AA für Rintega laut FDA-Feedback auf 0 gesunken zu sein... d.h. sehr wahrscheinlich keine Zulassungschance vor 2017 (also nur nach Erfolg der laufenden 1st-line PIII)! Die guten 2nd-line PII-Daten scheinen relativ irrelevant zu sein.
Der Kurs wird wohl mehr oder weniger implodieren...
[IMG]http://bigcharts.marketwatch.com/kaavio.Webhost/charts/big.chart?nosettings=1&symb=cldx&uf=0&type=2&size=2&sid=3374433&style=320&freq=1&entitlementtoken=0c33378313484ba9b46b8e24ded87dd6&time=8&rand=116370097&compidx=&ma=0&maval=9&lf=1&lf2=0&lf3=0&height=335&width=579&mocktick=1[/IMG]
Gruß
ipollit
Warum meinst Du das CLDX implodiert? Wie der Kursverlauf scheint, wussten mal wieder einige mehr und so ist es nun klar warum der Kurs seit Tagen / Wochen gesunken ist. RSI ist unter 30, ich denke der heutige Absturz ist überschaubar zumal Rintega ja nicht gefloppt ist.
Clovis collaboration
http://www.wallstreet-online.de/nachricht/7870074-clovis-onc…
Antwort auf Beitrag Nr.: 50.376.042 von question-mark am 11.08.15 14:50:01ich dachte, die Nachricht wird positiv aufgenommen, scheint den Markt aber nicht zu interessieren.
Antwort auf Beitrag Nr.: 50.371.026 von ipollit am 10.08.15 23:50:48
Lt. CLDX Quartalsinformation war die ReAct PII-Studie nicht für eine beschleunigte Zulassung ausgelegt (warum auch immer).
Nach meinem Verständnis der Frage- u. Antwortrunde hatte die ReAct PII-Studie trotz signifikantem PFS u. OS-Vorteil zu wenige Teilnehmer für eine beschleunigte Zulassung. Sollte die FDA aufgrund der PFS u. OS PII-Ergebnisse zulassen, könnte sie wohl keine PIII-Studie mehr fordern.
Daher sollte für eine beschleunigte Zulassung ein Ersatzendpunkt (z.B. Ansprechrate) herangezogen werden. In einer darauf folgenden PIII-Studie wären dann PFS- u. OS-Vorteile nachzuweisen.
Die ReRCT PII-Studie war wohl ebenso nicht für einen akzeptablen Nachweis der Ansprechrate ausgelegt.
Könnte das ganze ein Problem der evtl. in diesem Fall unsinnigen FDA-Regularien sein?
Zulassung könnte in dem Fall, und wie von CLDX kommuniziert, nur mittels erfolgreicher Act IV - PII-Studie erfolgen - dann wohl für ein größeres potenzielles Patientenkollektiv.
Hoffentlich ist es nur die "spezielle" FDA u. nicht ein Mangel an anderer Stelle. Die FDA würde auch bei fehlerhafter Berichterstattung durch CLDX den Sachverhalt nicht klarstellen o. kommentieren.
Zitat von ipollit: CLDX
... Für einen AA zählen nur Endpunkte wie RR, die auf einen möglichen spätere positiven OS in der PIII hindeuten. Ein positiver OS bereits in der PII ist somit wertlos! ... so so, alles klar!
Lt. CLDX Quartalsinformation war die ReAct PII-Studie nicht für eine beschleunigte Zulassung ausgelegt (warum auch immer).
Nach meinem Verständnis der Frage- u. Antwortrunde hatte die ReAct PII-Studie trotz signifikantem PFS u. OS-Vorteil zu wenige Teilnehmer für eine beschleunigte Zulassung. Sollte die FDA aufgrund der PFS u. OS PII-Ergebnisse zulassen, könnte sie wohl keine PIII-Studie mehr fordern.
Daher sollte für eine beschleunigte Zulassung ein Ersatzendpunkt (z.B. Ansprechrate) herangezogen werden. In einer darauf folgenden PIII-Studie wären dann PFS- u. OS-Vorteile nachzuweisen.
Die ReRCT PII-Studie war wohl ebenso nicht für einen akzeptablen Nachweis der Ansprechrate ausgelegt.
Könnte das ganze ein Problem der evtl. in diesem Fall unsinnigen FDA-Regularien sein?
Zulassung könnte in dem Fall, und wie von CLDX kommuniziert, nur mittels erfolgreicher Act IV - PII-Studie erfolgen - dann wohl für ein größeres potenzielles Patientenkollektiv.
Hoffentlich ist es nur die "spezielle" FDA u. nicht ein Mangel an anderer Stelle. Die FDA würde auch bei fehlerhafter Berichterstattung durch CLDX den Sachverhalt nicht klarstellen o. kommentieren.
Antwort auf Beitrag Nr.: 50.379.507 von Nase_weis_nix am 11.08.15 21:49:04Charts bei vielen Biotechs stark angeknackst. Kommt jetzt die große Korrektur?
Antwort auf Beitrag Nr.: 50.379.636 von fisch29 am 11.08.15 22:12:02Hier habe ich mal die Charts (2 Jahre) aller im NBI enthaltenen Werte aufgelistet... vielleicht lässt sich so der konkrete Korrekturbedarf bei jedem einzelen Wert ein wenig besser abschätzen:
http://www.wallstreet-online.de/diskussion/1217022-1-10/nasd…
Grüße
ipollit
http://www.wallstreet-online.de/diskussion/1217022-1-10/nasd…
Grüße
ipollit
Antwort auf Beitrag Nr.: 50.329.509 von Nase_weis_nix am 04.08.15 16:46:02MDVN
Hallo NaseWeisNix,
danke für den Hinweis zum MDVN-Split! Für mein Verständnis ist nicht der 13.8. relevant... ein Steuerproblem wird wenn dann erst am 15.9. auftreten, wenn die Zuteilung erfolgt, korrekt?
Analog z.B. der Erklärung hier... http://investor.mastercard.com/files/doc_downloads/stock_spl…
Grüße
ipollit
Hallo NaseWeisNix,
danke für den Hinweis zum MDVN-Split! Für mein Verständnis ist nicht der 13.8. relevant... ein Steuerproblem wird wenn dann erst am 15.9. auftreten, wenn die Zuteilung erfolgt, korrekt?
Analog z.B. der Erklärung hier... http://investor.mastercard.com/files/doc_downloads/stock_spl…
Grüße
ipollit
Antwort auf Beitrag Nr.: 50.379.897 von ipollit am 11.08.15 22:56:45"Hier habe ich mal die Charts (2 Jahre) aller im NBI enthaltenen Werte aufgelistet..."
Hallo ipollit,
danke für diese hilfreiche Zusammenstellung. Das war ne Menge Arbeit, denke ich mal.
Gruß
SLG
PS: Habe bei CLVS nachgelegt. Bei ZSPH juckte es mir auch in den Fingern, aber ich konnte mich gestern nicht durchringen.
CLDX: Bin sehr enttäuscht über den Formalismus der FDA. Wie damals die Zurückweisung von T-DM1 für die last-line. Das sind so Sachen, die letztlich auch Patienten ohne guten Grund schaden.
Ansonsten hat sich für CLDX fundamental eigentlich nicht viel geändert.
Hallo ipollit,
danke für diese hilfreiche Zusammenstellung. Das war ne Menge Arbeit, denke ich mal.
Gruß
SLG
PS: Habe bei CLVS nachgelegt. Bei ZSPH juckte es mir auch in den Fingern, aber ich konnte mich gestern nicht durchringen.
CLDX: Bin sehr enttäuscht über den Formalismus der FDA. Wie damals die Zurückweisung von T-DM1 für die last-line. Das sind so Sachen, die letztlich auch Patienten ohne guten Grund schaden.
Ansonsten hat sich für CLDX fundamental eigentlich nicht viel geändert.
Hallo ipollit,
vielen Dank für die Übersicht. Du hattest das vor langer Zeit schonmal gemacht und es war sehr hilfreich. Hatte ich oft reingeschaut!
Jetzt ist die Korrektur dann doch da! Die 50Tageslinie ist gebrochen und momentan findet ein "Kampf" um die 100 Tageslinie statt. Momentan wurde sie nach einem deutlichen Unterschreiten zurückerobert. Persönlich denke ich aber, dass eine Korrektur bis an die 200 Tageslinie führen wird. Die ist momentan bei 240. Aber das ist wirklich nur eine Vermutung. (was auch sonst?) Ich habe heute aber trotzdem bei CLVS und AUPH nachgekauft. Man weiß ja nie, ob die 100 Tageslinie nicht doch hält...

SG kmastra
vielen Dank für die Übersicht. Du hattest das vor langer Zeit schonmal gemacht und es war sehr hilfreich. Hatte ich oft reingeschaut!
Jetzt ist die Korrektur dann doch da! Die 50Tageslinie ist gebrochen und momentan findet ein "Kampf" um die 100 Tageslinie statt. Momentan wurde sie nach einem deutlichen Unterschreiten zurückerobert. Persönlich denke ich aber, dass eine Korrektur bis an die 200 Tageslinie führen wird. Die ist momentan bei 240. Aber das ist wirklich nur eine Vermutung. (was auch sonst?) Ich habe heute aber trotzdem bei CLVS und AUPH nachgekauft. Man weiß ja nie, ob die 100 Tageslinie nicht doch hält...

SG kmastra
Antwort auf Beitrag Nr.: 50.388.096 von ipollit am 12.08.15 19:39:10
Es könnte tatsächlich so sein, wie Du schreibst, bleibt für mich aber letztlich unsicher. Auf der MDVN-Seite sind keine weiteren Details zum Verfahren zu finden. War es bei Mastercard auch eine Stock-Dividende oder nur ein Split?
Der Record-Termin ist bei MDVN der 13.08. - also wird danach / am Folgetag das Anrecht auf die Stock-Dividende abgetrennt. Ab diesem Termin, bis zum Share Distribution Termin am 15.09, existieren zwei Teile - Altaktie, sowie Anrecht auf Splitaktien (Stock-Dividende).
Ob die Anrechte beim Kauf / Verkauf in diesem Zeitraum mit übertragen werden, ist mir unklar. Mit Übertrag wäre der 15.09. für die Steuer relevant; ohne wäre es der 13.08. mit Steuerabzug am 15.09.
Wenn MDVN morgen im US-Handel noch gleich hoch notiert, ist wie bei Mastercard der Share Distribution Termin entscheidend. Da ich es nicht weiß und unklare steuerliche Effekte bei unseren Depotbanken gepaart mit unserer Gesetzgebung / Finanzamt aus leidlicher Erfahrung fürchte, habe ich bereits verkauft.
Muss PIII-Studie lauten.
Bei Act IV sind zwei Zwischenauswertungen (Signifikanz / HR) vorgesehen. Die erste bei 50% war nicht erfolgreich. Die zweite bei 75% soll Ende 2015 / Anfang 2016 erreicht u. durchgeführt werden.
siehe ... The statistics around the study are based essentially on P values for the interim analyses. So the first interim analysis which is based on 50% of events, would have required the data to have a P value of 0.003 or better in order to be kicked out for efficacy. Now that translates to a range in hazard values but essentially it has a value of 0.5 to 0.55 would have had a high likelihood of achieving that P value.
For the second interim analysis, the required P value would be 0.018, which relates again to a range in hazard ratios with something approximately 0.65 would be adequate. For the final analysis, essentially a P value of 0.044, or a hazard ratio of up to 0.79 would be adequate for positive outcome therein.
Quelle http://finance.yahoo.com/news/edited-transcript-cldx-earning…
Wagt jemand anhand bisheriger Studienergebnisse (Activate, Act II u. III) eine Prognose?
Die Endauswertung soll erst Ende 2016 stattfinden. Für Erstellung der einzureichenden Unterlagen u. FDA-Entscheidung wird ca. 1 Jahr bis Entscheidung Zulassung veranschlagt.
Zitat von ipollit: MDVN-Split! Für mein Verständnis ist nicht der 13.8. relevant... ein Steuerproblem wird wenn dann erst am 15.9. auftreten, wenn die Zuteilung erfolgt, korrekt?
Es könnte tatsächlich so sein, wie Du schreibst, bleibt für mich aber letztlich unsicher. Auf der MDVN-Seite sind keine weiteren Details zum Verfahren zu finden. War es bei Mastercard auch eine Stock-Dividende oder nur ein Split?
Der Record-Termin ist bei MDVN der 13.08. - also wird danach / am Folgetag das Anrecht auf die Stock-Dividende abgetrennt. Ab diesem Termin, bis zum Share Distribution Termin am 15.09, existieren zwei Teile - Altaktie, sowie Anrecht auf Splitaktien (Stock-Dividende).
Ob die Anrechte beim Kauf / Verkauf in diesem Zeitraum mit übertragen werden, ist mir unklar. Mit Übertrag wäre der 15.09. für die Steuer relevant; ohne wäre es der 13.08. mit Steuerabzug am 15.09.
Wenn MDVN morgen im US-Handel noch gleich hoch notiert, ist wie bei Mastercard der Share Distribution Termin entscheidend. Da ich es nicht weiß und unklare steuerliche Effekte bei unseren Depotbanken gepaart mit unserer Gesetzgebung / Finanzamt aus leidlicher Erfahrung fürchte, habe ich bereits verkauft.
Zitat von Nase_weis_nix: Zulassung könnte in dem Fall, und wie von CLDX kommuniziert, nur mittels erfolgreicher Act IV - PII-Studie erfolgen - dann wohl für ein größeres potenzielles Patientenkollektiv.
Muss PIII-Studie lauten.
Bei Act IV sind zwei Zwischenauswertungen (Signifikanz / HR) vorgesehen. Die erste bei 50% war nicht erfolgreich. Die zweite bei 75% soll Ende 2015 / Anfang 2016 erreicht u. durchgeführt werden.
siehe ... The statistics around the study are based essentially on P values for the interim analyses. So the first interim analysis which is based on 50% of events, would have required the data to have a P value of 0.003 or better in order to be kicked out for efficacy. Now that translates to a range in hazard values but essentially it has a value of 0.5 to 0.55 would have had a high likelihood of achieving that P value.
For the second interim analysis, the required P value would be 0.018, which relates again to a range in hazard ratios with something approximately 0.65 would be adequate. For the final analysis, essentially a P value of 0.044, or a hazard ratio of up to 0.79 would be adequate for positive outcome therein.
Quelle http://finance.yahoo.com/news/edited-transcript-cldx-earning…
Wagt jemand anhand bisheriger Studienergebnisse (Activate, Act II u. III) eine Prognose?
Die Endauswertung soll erst Ende 2016 stattfinden. Für Erstellung der einzureichenden Unterlagen u. FDA-Entscheidung wird ca. 1 Jahr bis Entscheidung Zulassung veranschlagt.
FGEN
http://investor.fibrogen.com/phoenix.zhtml?c=253783&p=irol-n…
PHASE 2 DATA OF INVESTIGATIONAL ORALLY ACTIVE HIF-PHI ROXADUSTAT (FG-4592) SHOWS IMPROVED HEMOGLOBIN LEVELS IN NON-DIALYSIS CKD SUBJECTS WITH ANEMIA
Zudem wurden die Quartalszahlen veröffentlich. Heute wohl ein guter Tag für FGEN.
http://investor.fibrogen.com/phoenix.zhtml?c=253783&p=irol-n…
PHASE 2 DATA OF INVESTIGATIONAL ORALLY ACTIVE HIF-PHI ROXADUSTAT (FG-4592) SHOWS IMPROVED HEMOGLOBIN LEVELS IN NON-DIALYSIS CKD SUBJECTS WITH ANEMIA
Zudem wurden die Quartalszahlen veröffentlich. Heute wohl ein guter Tag für FGEN.
Antwort auf Beitrag Nr.: 50.359.800 von SLGramann am 08.08.15 20:16:47Auch wenn dies mancher Börsianer oder Fondsmanager nicht gerne hört, befinden wir uns im Biotechsektor zweifellos schon längere Zeit im Blasenmodus. Diejenigen, die einen besseren Branchenüberblick haben (wie z.B. Lechleiter/Lilly und Schwan/Roche) haben dies zuletzt immer wieder betont.
Es gibt eine ungeheure Vielfalt an neuen therapeutischen Ansätzen und Parallelentwicklungen, dazu kommen - jetzt auch in den USA - zunehmend Einwände gegen die Preisgestaltung ... bis man wieder guten Gewissens im Biotechsektor investieren kann (von wenigen Sondersituationen einmal abgesehen), bedarf es eines kräftigen Kursrückgangs des NBI ... und "kräftig" bedeutet nicht 10 % oder 20 %.
Es gibt eine ungeheure Vielfalt an neuen therapeutischen Ansätzen und Parallelentwicklungen, dazu kommen - jetzt auch in den USA - zunehmend Einwände gegen die Preisgestaltung ... bis man wieder guten Gewissens im Biotechsektor investieren kann (von wenigen Sondersituationen einmal abgesehen), bedarf es eines kräftigen Kursrückgangs des NBI ... und "kräftig" bedeutet nicht 10 % oder 20 %.
Antwort auf Beitrag Nr.: 50.405.874 von Joschka Schröder am 14.08.15 20:09:41zunehmend Einwände gegen die Preisgestaltung
... da bieten sich Biosimilars an, aber selbst die sind recht teuer momentan und Geld wird erst in Jahren verdient.
... da bieten sich Biosimilars an, aber selbst die sind recht teuer momentan und Geld wird erst in Jahren verdient.
ESPR
Das ging jetzt doch recht schnell:
- The FDA confirmed that LDL-C remains an acceptable clinical surrogate endpoint
- Based on feedback from the FDA, approval of ETC-1002 in the HeFH and ASCVD patient populations will not require the completion of a cardiovascular outcomes trial (CVOT).
http://finance.yahoo.com/news/esperion-therapeutics-provides…
Nachbörslich schon wieder deutlich über 80...
Das ging jetzt doch recht schnell:
- The FDA confirmed that LDL-C remains an acceptable clinical surrogate endpoint
- Based on feedback from the FDA, approval of ETC-1002 in the HeFH and ASCVD patient populations will not require the completion of a cardiovascular outcomes trial (CVOT).
http://finance.yahoo.com/news/esperion-therapeutics-provides…
Nachbörslich schon wieder deutlich über 80...
ESPR
Heute mit gutem Volumen wieder über die 200 Tage Linine. War wohl vorab schon was durchgesickert:http://finance.yahoo.com/news/esperion-therapeutics-provides…
Auszug:
The FDA confirmed that LDL-C remains an acceptable clinical surrogate endpoint for the approval of an LDL-C lowering therapy such as ETC-1002 in patient populations who have a high unmet medical need, including patients with heterozygous familial hypercholesterolemia (HeFH), or clinical atherosclerotic cardiovascular disease (ASCVD), who are already taking maximally tolerated statins yet require additional LDL-C reduction and where there is a positive benefit/risk ratio. Based on feedback from the FDA, approval of ETC-1002 in the HeFH and ASCVD patient populations will not require the completion of a cardiovascular outcomes trial (CVOT). The Company continues to plan and initiate a CVOT prior to NDA filing to pursue broader label indications related to cardiovascular disease risk reduction.
Antwort auf Beitrag Nr.: 50.420.643 von kmastra am 17.08.15 22:16:00Da warst du einen Tick schneller 
Rückblickend muss man wohl sagen viel Lärm um nichts, aber ist ja auch schön wenn der Markt solche Opportunitäten bietet

Rückblickend muss man wohl sagen viel Lärm um nichts, aber ist ja auch schön wenn der Markt solche Opportunitäten bietet

Antwort auf Beitrag Nr.: 50.376.042 von question-mark am 11.08.15 14:50:01INCY, CLVS
angeblich sehen die ersten Daten der Kombi von PD1 + INCYs IDO1-Hemmer ganz gut aus...

Die geplanten Kombis von INCYs EGFR-Hemmer Roci mit PD1 besitzen wahrscheinlich zwar keine IO-Synergie wie PD1 + IDO, doch sind sie insofern interessant, als dass EGFR-Hemmer in EGFR+ Lungenkrebs sehr wirksam sind und PD1-AKs bei einem Teil von Lungenkrebs-Patienten ebenfalls wirken. Der Krebs würde dann sowohl per Target-Therapie als auch über das Immunsystem bekämpft.
Ein Vorteil von Roci (z.B. gegenüber AZNs 9291) dürfte sein, dass Roci nur sehr geringe Nebenwirkungen wie Hauptrötungen/Entzündungen (Rash) zeigt, da es Wildtype-EGFR ausspart, das u.a. in der Haut vorhanden ist. Diese Nebenwirkungen können die Therapie mit PD1 begrenzen (z.B. Rash Grad 3 in der PD1 + IDO1 Kombi oben)...
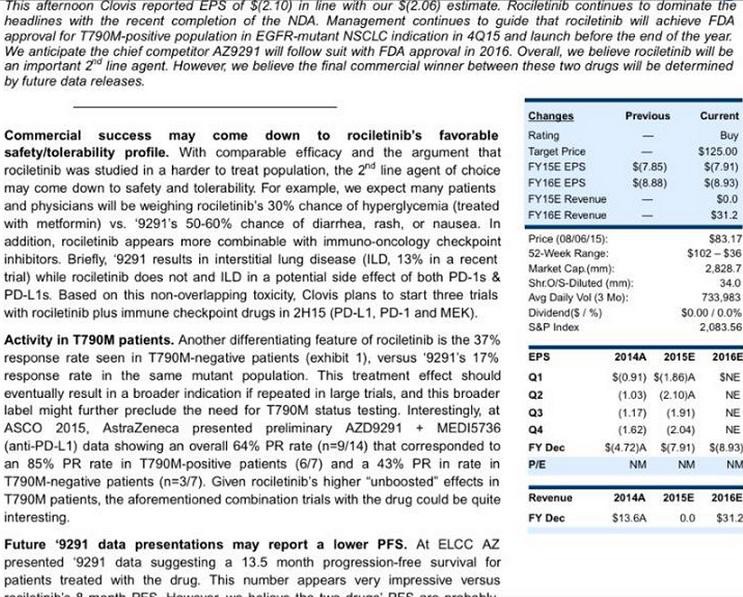
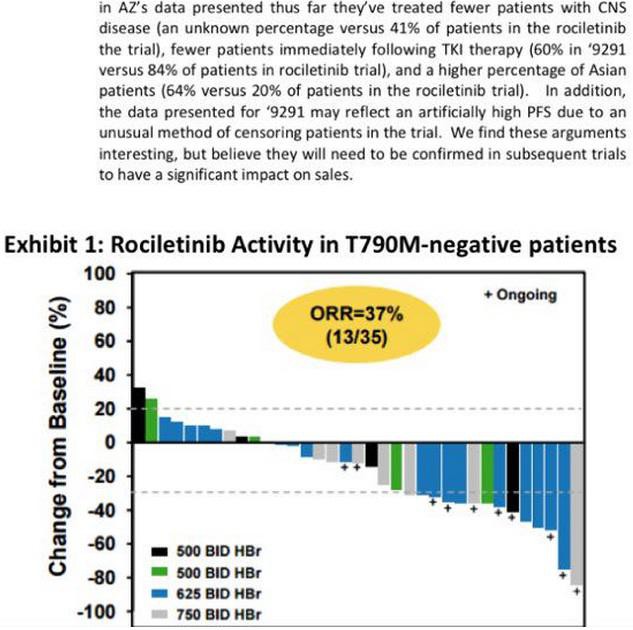


Gruß
ipollit
angeblich sehen die ersten Daten der Kombi von PD1 + INCYs IDO1-Hemmer ganz gut aus...

Die geplanten Kombis von INCYs EGFR-Hemmer Roci mit PD1 besitzen wahrscheinlich zwar keine IO-Synergie wie PD1 + IDO, doch sind sie insofern interessant, als dass EGFR-Hemmer in EGFR+ Lungenkrebs sehr wirksam sind und PD1-AKs bei einem Teil von Lungenkrebs-Patienten ebenfalls wirken. Der Krebs würde dann sowohl per Target-Therapie als auch über das Immunsystem bekämpft.
Ein Vorteil von Roci (z.B. gegenüber AZNs 9291) dürfte sein, dass Roci nur sehr geringe Nebenwirkungen wie Hauptrötungen/Entzündungen (Rash) zeigt, da es Wildtype-EGFR ausspart, das u.a. in der Haut vorhanden ist. Diese Nebenwirkungen können die Therapie mit PD1 begrenzen (z.B. Rash Grad 3 in der PD1 + IDO1 Kombi oben)...


Gruß
ipollit
Antwort auf Beitrag Nr.: 50.420.751 von SpanishEyes am 17.08.15 22:27:23ESPR
Ja... sehr schön! Mal gute Neuigkeiten!
"Esperion remains on track to initiate the ETC-1002 Phase 3 development program by the end of 2015. The program will support a proposed label indication for the use of ETC-1002, an oral, once-daily LDL-C lowering therapy, "as an adjunct to diet and maximally tolerated statin therapy for the treatment of adults with heterozygous familial hypercholesterolemia (HeFH), or atherosclerotic cardiovascular disease (ASCVD), who require additional lowering of LDL-C." Approximately nine million patients in the U.S. fall into these two combined categories.
The ETC-1002 Phase 3 development program will include clinical studies in patients with ASCVD and HeFH. The study designs will be finalized once minutes from the FDA meeting are received. The Company plans to continue to evaluate ETC-1002 as an add-on to statins, including at all doses."
Gruß
ipollit
Ja... sehr schön! Mal gute Neuigkeiten!

"Esperion remains on track to initiate the ETC-1002 Phase 3 development program by the end of 2015. The program will support a proposed label indication for the use of ETC-1002, an oral, once-daily LDL-C lowering therapy, "as an adjunct to diet and maximally tolerated statin therapy for the treatment of adults with heterozygous familial hypercholesterolemia (HeFH), or atherosclerotic cardiovascular disease (ASCVD), who require additional lowering of LDL-C." Approximately nine million patients in the U.S. fall into these two combined categories.
The ETC-1002 Phase 3 development program will include clinical studies in patients with ASCVD and HeFH. The study designs will be finalized once minutes from the FDA meeting are received. The Company plans to continue to evaluate ETC-1002 as an add-on to statins, including at all doses."
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.404.368 von biopadawan am 14.08.15 16:37:45FGEN
FGEN 2Q15 CC notes:
1. FGEN has patents on roxadustat through 2033 and beyond.
2. FGEN completed two separate two-year carcinogenicity studies on roxa in mouse and rat with no concerns.
3. FGEN recently updated their public disclosures given their belief that it is now likely that roxa will be reimbursed outside the dialysis bundle. This appears to be due at least in part to the unmet need in the inflammation/hypo-responder patient settings.
4. The DSMB has been involved with roxa since 2009 and, per the CEO, the DSMB thinks roxa is "well tolerated."
5. Regarding FG-3019, FGEN has patents around blocking CTGF to treat fibrosis.
6. In the open-label 48-week P2 trial of 3019 in IPF patients, 35% of patients had either improved or stable fibrosis after 48 weeks of treatment. FGEN believes they are the only company to show improvement of fibrosis in IPF patients in a clinical trial. (FGEN previously disclosed that 24% of patients specifically had improvement of fibrosis after 48 weeks: http://investor.fibrogen.com/phoenix.zhtml?c=253783&p=irol-n… ).
7. FGEN believes 3019 will be additive, not synergistic, with pirfenidone and nintedanib given different MoAs. FGEN is planning to test 3019 in combo with at least one of these and as front-line single agent ahead of them.
8. Beyond IPF, 3019 has the potential to treat all DMD patients and not just a sub-set like competing drugs. FGEN believes CTGF may be responsible for turning muscle into fat in DMD patients and given 3019's ability to block CTGF, the drug could be disease modifying.
***
Also I heard the CEO mentioned that they had a chance at pirfenidone way back when but gave it a pass after comparing it to their own in house molecule.


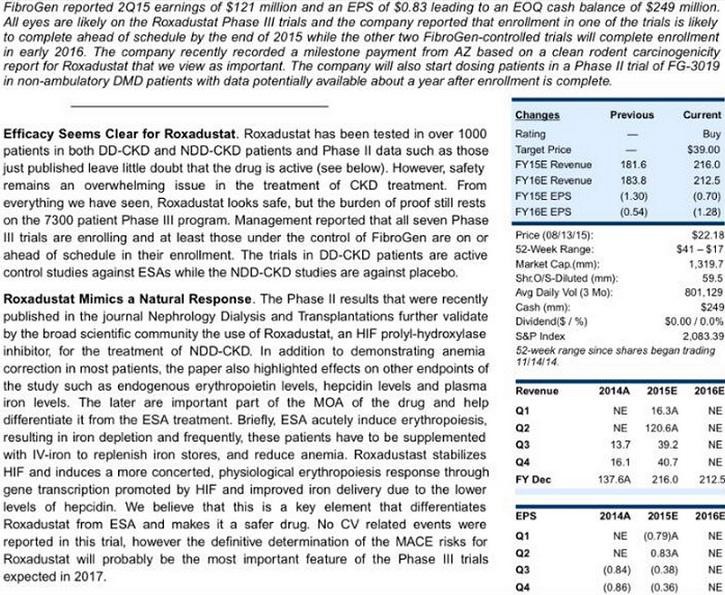


Gruß
ipollit
FGEN 2Q15 CC notes:
1. FGEN has patents on roxadustat through 2033 and beyond.
2. FGEN completed two separate two-year carcinogenicity studies on roxa in mouse and rat with no concerns.
3. FGEN recently updated their public disclosures given their belief that it is now likely that roxa will be reimbursed outside the dialysis bundle. This appears to be due at least in part to the unmet need in the inflammation/hypo-responder patient settings.
4. The DSMB has been involved with roxa since 2009 and, per the CEO, the DSMB thinks roxa is "well tolerated."
5. Regarding FG-3019, FGEN has patents around blocking CTGF to treat fibrosis.
6. In the open-label 48-week P2 trial of 3019 in IPF patients, 35% of patients had either improved or stable fibrosis after 48 weeks of treatment. FGEN believes they are the only company to show improvement of fibrosis in IPF patients in a clinical trial. (FGEN previously disclosed that 24% of patients specifically had improvement of fibrosis after 48 weeks: http://investor.fibrogen.com/phoenix.zhtml?c=253783&p=irol-n… ).
7. FGEN believes 3019 will be additive, not synergistic, with pirfenidone and nintedanib given different MoAs. FGEN is planning to test 3019 in combo with at least one of these and as front-line single agent ahead of them.
8. Beyond IPF, 3019 has the potential to treat all DMD patients and not just a sub-set like competing drugs. FGEN believes CTGF may be responsible for turning muscle into fat in DMD patients and given 3019's ability to block CTGF, the drug could be disease modifying.
***
Also I heard the CEO mentioned that they had a chance at pirfenidone way back when but gave it a pass after comparing it to their own in house molecule.




Gruß
ipollit
Antwort auf Beitrag Nr.: 50.420.994 von ipollit am 17.08.15 23:10:44FGEN
Danke für den Beitrag ipollit, sehr informativ !!
Wie ich im Blog gesehen habe ist Ohad Hammer von FGEN auch sehr angetan und wird wohl irgendwann demnächst einsteigen. Die beiden Produktkandidaten Roxadustat und FG-3019
Die einzige Frage ist der richtige Einstiegspunkt, wobei ich mir nicht vorstellen kann, dass bei einer momentanen Bewertung von ca. 24-25 $ nochmal ein signifikanter Einbruch kommt. (außer evlt. makroökonomischer Natur)
Dies auch in Anbetracht der Tatsache dass keine near term catalysts mehr folgen werden
Was sehr Ihr die Sache?
NLNK
Ist jemand von euch investiert? Wurde der Wert hier schon diskutiert?
NLNK hat auch eine frühe collaboration mit Genentech s.
http://newlinkgenetics.com/development-pipeline bzgl. dem IDO Inhibitor.
Sieht für mich auch sehr vielversprechend aus die ganze Sache. Probleme sehe ich eher bei der aktuellen Bewertung.
Viele Grüße
biopadawan
Danke für den Beitrag ipollit, sehr informativ !!
Wie ich im Blog gesehen habe ist Ohad Hammer von FGEN auch sehr angetan und wird wohl irgendwann demnächst einsteigen. Die beiden Produktkandidaten Roxadustat und FG-3019
Die einzige Frage ist der richtige Einstiegspunkt, wobei ich mir nicht vorstellen kann, dass bei einer momentanen Bewertung von ca. 24-25 $ nochmal ein signifikanter Einbruch kommt. (außer evlt. makroökonomischer Natur)
Dies auch in Anbetracht der Tatsache dass keine near term catalysts mehr folgen werden
Was sehr Ihr die Sache?
NLNK
Ist jemand von euch investiert? Wurde der Wert hier schon diskutiert?
NLNK hat auch eine frühe collaboration mit Genentech s.
http://newlinkgenetics.com/development-pipeline bzgl. dem IDO Inhibitor.
Sieht für mich auch sehr vielversprechend aus die ganze Sache. Probleme sehe ich eher bei der aktuellen Bewertung.
Viele Grüße
biopadawan
Antwort auf Beitrag Nr.: 50.420.853 von ipollit am 17.08.15 22:42:22Ich hatte heute ganz klar mit steigenden oder mindestens stabilen Kursen bei ESPR gerechnet - so ein starker Rückgang bei hohem Volumen ist für mich nicht nachvollziehbar. Durch die letzten Nachkäufe ist ESPR bereits eine sehr grosse Position bei mir, aber die grössten Unsicherheitsfaktoren sind seit gestern beseitigt...und somit eigentlich Kaufkurse. Wurde etwas übersehen?!
Antwort auf Beitrag Nr.: 50.430.270 von SpanishEyes am 18.08.15 23:09:40
Das ging mir ähnlich. Die Analystenkommentare über Twitter ergeben auch kein einheitliches Bild. Zusammengefasst sind die Argumente gegen ESPR wohl:
-Bisher gibt es keine Studiendaten für Patienten mit maximaler Statindosis. Ein Analyst geht hier sogar soweit, dass er da keinen Zusatzeffekt von 1002 sieht. Wie kommt er denn darauf?
-Das Label wird zudem erstmal nur Patienten beinhalten, die schon einmal eine Herzkreislauferkrankung hatten und nicht solche, bei denen um es um eine Erst-Prävention geht.
-Zudem werden jetzt (wenn man schonmal dabei ist) auch Grundsatzthemen wie Sicherheit hervorgekramt. Besonders die Kombination mit Statinen wird kritisch und als riskant angesehen.
Für ESPR sprechen:
-Selbt ein erstmal schmales Label garantiert nahezu Umsätze, die die derzeitige Bewertung rechtfertigen.
-Es wird Offlabel auch zur Prävention eingestzt werden.
-Die Kombination mit Statinen ist kein Sicherheitsproblem.
Hier mal einige Stimmen:












Persönlich halte ich es eher mit den Optimisten. Ohne Risiko ist wohl kein Invest im Bereich Biotech zu haben....
Zitat von SpanishEyes: Ich hatte heute ganz klar mit steigenden oder mindestens stabilen Kursen bei ESPR gerechnet - so ein starker Rückgang bei hohem Volumen ist für mich nicht nachvollziehbar. Durch die letzten Nachkäufe ist ESPR bereits eine sehr grosse Position bei mir, aber die grössten Unsicherheitsfaktoren sind seit gestern beseitigt...und somit eigentlich Kaufkurse. Wurde etwas übersehen?!
Das ging mir ähnlich. Die Analystenkommentare über Twitter ergeben auch kein einheitliches Bild. Zusammengefasst sind die Argumente gegen ESPR wohl:
-Bisher gibt es keine Studiendaten für Patienten mit maximaler Statindosis. Ein Analyst geht hier sogar soweit, dass er da keinen Zusatzeffekt von 1002 sieht. Wie kommt er denn darauf?
-Das Label wird zudem erstmal nur Patienten beinhalten, die schon einmal eine Herzkreislauferkrankung hatten und nicht solche, bei denen um es um eine Erst-Prävention geht.
-Zudem werden jetzt (wenn man schonmal dabei ist) auch Grundsatzthemen wie Sicherheit hervorgekramt. Besonders die Kombination mit Statinen wird kritisch und als riskant angesehen.
Für ESPR sprechen:
-Selbt ein erstmal schmales Label garantiert nahezu Umsätze, die die derzeitige Bewertung rechtfertigen.
-Es wird Offlabel auch zur Prävention eingestzt werden.
-Die Kombination mit Statinen ist kein Sicherheitsproblem.
Hier mal einige Stimmen:












Persönlich halte ich es eher mit den Optimisten. Ohne Risiko ist wohl kein Invest im Bereich Biotech zu haben....
Antwort auf Beitrag Nr.: 50.435.355 von kmastra am 19.08.15 15:01:12Nach dem was ich alles so gelesen habe, inkl. Ohad, rechne ich letztlich mit einer Übernahme - und diese dürfte dann zu deutlich höheren Kursen als heute erfolgen (da ist dann die 200 Tage Linie auch nicht mehr so relevant  ) Klar kann die M&A Aktivität allgemein etwas nachlassen bei steigenden Zinsen, aber momentan werden hier praktisch fast nur die Negativaspekte gesehen. Den Analystenkommentar von Needham fand ich irgendwie amüsant, sinngemäss: weil die Aktie jetzt etwas höher notiert als letzte Woche und wir unser Kursziel aufgrund der angepassten Ertragserwartungen von 130 USD auf 115 USD gesenkt haben, ist sie nur noch ein "buy" und kein "strong buy" mehr... (ausser sie haben eine interne policy, dass für ein strong buy das Potential über 100% liegen muss, was zum Zeitpunkt der Veröffentlichung nicht der Fall war)
) Klar kann die M&A Aktivität allgemein etwas nachlassen bei steigenden Zinsen, aber momentan werden hier praktisch fast nur die Negativaspekte gesehen. Den Analystenkommentar von Needham fand ich irgendwie amüsant, sinngemäss: weil die Aktie jetzt etwas höher notiert als letzte Woche und wir unser Kursziel aufgrund der angepassten Ertragserwartungen von 130 USD auf 115 USD gesenkt haben, ist sie nur noch ein "buy" und kein "strong buy" mehr... (ausser sie haben eine interne policy, dass für ein strong buy das Potential über 100% liegen muss, was zum Zeitpunkt der Veröffentlichung nicht der Fall war)
 ) Klar kann die M&A Aktivität allgemein etwas nachlassen bei steigenden Zinsen, aber momentan werden hier praktisch fast nur die Negativaspekte gesehen. Den Analystenkommentar von Needham fand ich irgendwie amüsant, sinngemäss: weil die Aktie jetzt etwas höher notiert als letzte Woche und wir unser Kursziel aufgrund der angepassten Ertragserwartungen von 130 USD auf 115 USD gesenkt haben, ist sie nur noch ein "buy" und kein "strong buy" mehr... (ausser sie haben eine interne policy, dass für ein strong buy das Potential über 100% liegen muss, was zum Zeitpunkt der Veröffentlichung nicht der Fall war)
) Klar kann die M&A Aktivität allgemein etwas nachlassen bei steigenden Zinsen, aber momentan werden hier praktisch fast nur die Negativaspekte gesehen. Den Analystenkommentar von Needham fand ich irgendwie amüsant, sinngemäss: weil die Aktie jetzt etwas höher notiert als letzte Woche und wir unser Kursziel aufgrund der angepassten Ertragserwartungen von 130 USD auf 115 USD gesenkt haben, ist sie nur noch ein "buy" und kein "strong buy" mehr... (ausser sie haben eine interne policy, dass für ein strong buy das Potential über 100% liegen muss, was zum Zeitpunkt der Veröffentlichung nicht der Fall war)
Antwort auf Beitrag Nr.: 50.435.355 von kmastra am 19.08.15 15:01:12Hallo kmastra,
schöne Zusammenfassung zu ESPR. Ich habe heute bei ESPR und CLVS gekauft. EXEL hatte ich letztens schon gekauft und denke an eine Aufstockung.
ZSPH, PTLA, AGIO, XLRN, KITE und LOXO finde ich ebenfalls attraktiv und denke an Käufe bzw. Nachkäufe.
Nach meiner Erfahrung kommt es zum Ende von Korrekturphasen mitunter zu einem "sell off" bzw. einer Kapitulation der Long-Seite.
Das ist bisher natürlich überhaupt noch nicht passiert und so fürchte ich, dass Käufe einfach noch zu früh kommen.
Aber da man es eh nie wissen kann, komme ich jetzt eben wohl langsam und Stück für Stück wieder auf die Käuferseite.
schöne Zusammenfassung zu ESPR. Ich habe heute bei ESPR und CLVS gekauft. EXEL hatte ich letztens schon gekauft und denke an eine Aufstockung.
ZSPH, PTLA, AGIO, XLRN, KITE und LOXO finde ich ebenfalls attraktiv und denke an Käufe bzw. Nachkäufe.
Nach meiner Erfahrung kommt es zum Ende von Korrekturphasen mitunter zu einem "sell off" bzw. einer Kapitulation der Long-Seite.
Das ist bisher natürlich überhaupt noch nicht passiert und so fürchte ich, dass Käufe einfach noch zu früh kommen.
Aber da man es eh nie wissen kann, komme ich jetzt eben wohl langsam und Stück für Stück wieder auf die Käuferseite.
BRAF Inhibition
arry:Nachtrag zu einer kürzlichen Diskussion:
http://www.cancernetwork.com/news/basket-trial-finds-new-tum…
Basket Trial Finds New Tumor Types That Respond to BRAF Inhibition
August 19, 2015
By Anna Azvolinsky, PhD
A basket trial of patients with various non-melanoma BRAF-mutated cancers has shown that additional tumor types may also be responsive to vemurafenib, a drug used in BRAF-mutated metastatic melanoma patients. Patients with non–small-cell lung cancer (NSCLC), as well as Erdheim–Chester disease and Langerhans’-cell histiocytosis, showed relatively high response rates. Basket trials are a relatively new clinical trial design, in which targeted agents are tested among a variety of different tumors that express the corresponding biomarkers. The goals of these tumor histology-independent trials are to speed up drug testing and to understand whether targeting a mutation or biomarker can effectively block tumor growth.This trial, led by David M. Hyman, MD, of Memorial Sloan Kettering Cancer Center in New York, enrolled 122 patients divided into six cohorts of prespecified tumor types—NSCLC, ovarian cancer, colorectal cancer, breast cancer, cholangiocarcinoma, and multiple myeloma, as well as an additional cohort that included all other tumor types with BRAF mutation–positive disease. Because vemurafenib alone had insufficient activity in colorectal cancer patients, the study protocol was amended to study the combination of the BRAF inhibitor plus cetuximab in these patients. The results of the study were published in the New England Journal of Medicine.The response rate among the NSCLC patients on study was 42% and the median progression-free survival was 7.3 months. The vast majority of these patients had already received platinum-based chemotherapy in the first-line setting. Of the patients with either Erdheim–Chester disease or Langerhans’-cell histiocytosis, the response rate was 43%—one complete response and five partial responses.There were also anecdotal responses among other BRAF-mutated cancers, including ovarian, salivary duct, and anaplastic thyroid cancer, as well as cholangiocarcinoma, pleomorphic xanthoastrocytoma, and clear-cell sarcoma. One of 27 colorectal cancer patients treated with vemurafenib plus cetuximab had a partial response and 18 patients had stable disease. Adverse events were similar to what has previously been seen with metastatic melanoma patients treated with vemurafenib.BRAF V600 mutations, which are associated with aggressive disease and shorter overall survival, have been identified in many non-melanoma cancers but their incidence is typically low—below 5%. Treatment with BRAF inhibitors has largely not been tested outside of melanoma.“The BRAF V600 mutation is a targetable oncogene in some, but not all, cancer types,” concluded the authors. They also noted that it can be challenging to interpret results from basket trials that enroll small patient cohorts.
Antwort auf Beitrag Nr.: 50.447.421 von SLGramann am 20.08.15 18:13:14Hallo SLGramann,
bei CLVS hat heute auch mein (weiteres) Limit gegriffen (200 Tageslinie). CLVS ist jetzt mit Abstand meine größte Position.
Ich habe noch Kauflimits für ARQL, AUPH, MRNS, ZFGN, ARRY gesetzt. Mal sehen, ob die noch greifen. Meine Grundannahme ist weiterhin eine Korrektur des Gesamtmarkts bis mindestens an die 200 Tageslinie. An einen Crash/Blase glaube ich nicht.
Man muss ja auch jeden Wert für sich betrachten. Und da sieht man doch einige Werte, die schon sehr stark gefallen sind.
Der NBI/IBB ist doch auch von pharmaähnlichen Werten dominiert und noch ein gutes Stück von der 200 Tageslinie entfernt.

Eine tolle Übersicht von Brad Loncar gibt einen guten überblick über die bisherige Korrektur:
https://docs.google.com/spreadsheets/d/1nV75wNxajpqb3SbND5D2…
Schaut man sich den XBI (kleinere Werte) an - ist die 200 Tageslinie nicht mehr weit. Es kann/wird aber auch noch richtig übel werden bzw. sich so anfühlen.

Grundsätzlich sollte man es mit der Charttechnik (selbst da gibt es ja auch viele verschiedene Ansätze) sicherlich nicht übertreiben. Ich denke/hoffe aber das man dadurch evtl. Einstiegspunkte und auch Ausstiegspunke optimieren kann.
SG kmastra
bei CLVS hat heute auch mein (weiteres) Limit gegriffen (200 Tageslinie). CLVS ist jetzt mit Abstand meine größte Position.
Ich habe noch Kauflimits für ARQL, AUPH, MRNS, ZFGN, ARRY gesetzt. Mal sehen, ob die noch greifen. Meine Grundannahme ist weiterhin eine Korrektur des Gesamtmarkts bis mindestens an die 200 Tageslinie. An einen Crash/Blase glaube ich nicht.
Man muss ja auch jeden Wert für sich betrachten. Und da sieht man doch einige Werte, die schon sehr stark gefallen sind.
Der NBI/IBB ist doch auch von pharmaähnlichen Werten dominiert und noch ein gutes Stück von der 200 Tageslinie entfernt.
Eine tolle Übersicht von Brad Loncar gibt einen guten überblick über die bisherige Korrektur:
https://docs.google.com/spreadsheets/d/1nV75wNxajpqb3SbND5D2…
Schaut man sich den XBI (kleinere Werte) an - ist die 200 Tageslinie nicht mehr weit. Es kann/wird aber auch noch richtig übel werden bzw. sich so anfühlen.
Grundsätzlich sollte man es mit der Charttechnik (selbst da gibt es ja auch viele verschiedene Ansätze) sicherlich nicht übertreiben. Ich denke/hoffe aber das man dadurch evtl. Einstiegspunkte und auch Ausstiegspunke optimieren kann.
SG kmastra
mal ein kleiner Depot-Check nach Jahren des Biotech-Booms... 
ALNY - seit Jan 2014... 1,5 Jahre: Gewinn: 9%
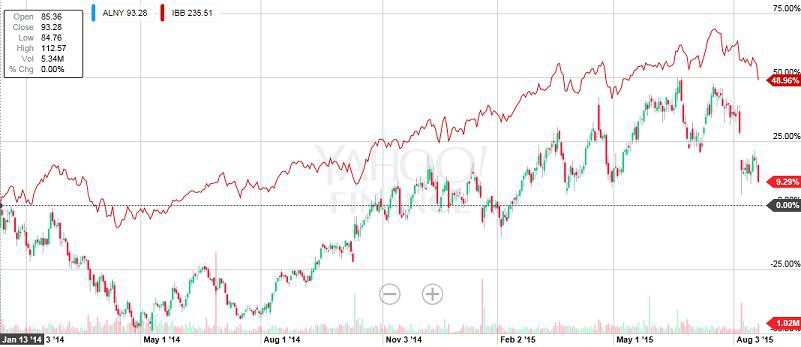
ARQL - seit Mär 2003... 12,5 Jahre: Gewinn: -22%
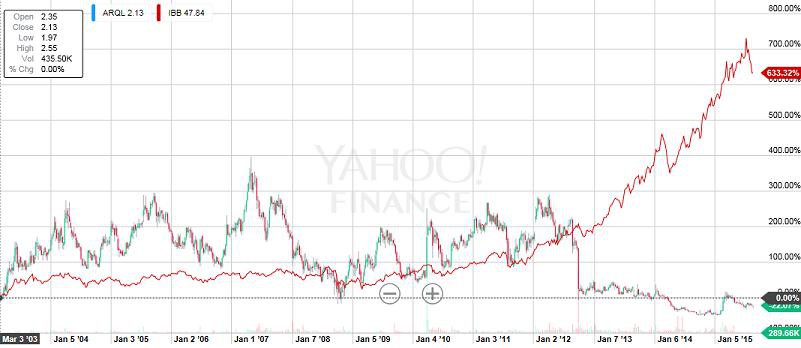
ARRY - seit Feb 2001... 14,5 Jahre: Gewinn: -20%
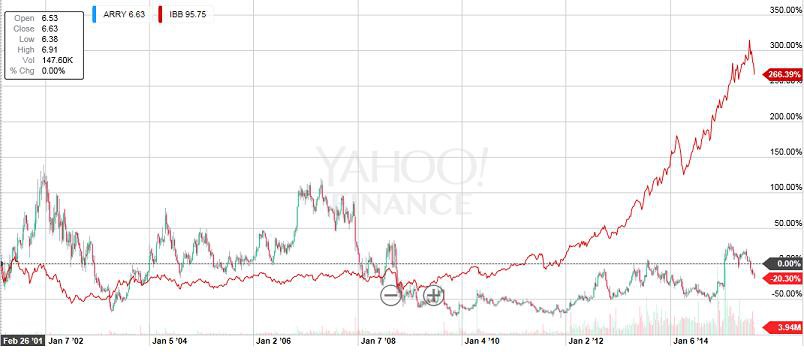
CLDX - seit Apr 2013... 2,5 Jahre: Gewinn: 0%
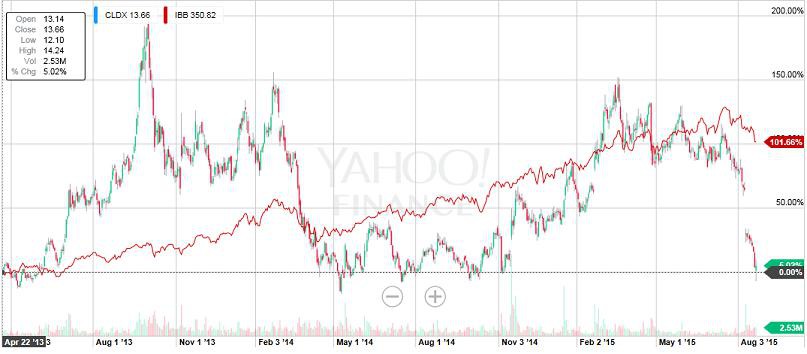
CLVS - seit Jun 2013... 2,0 Jahre: Gewinn: 0%
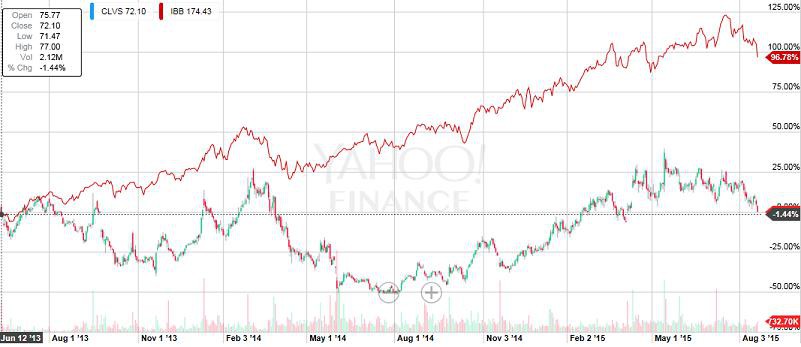
ENTA - seit Feb 2014... 1,5 Jahre: Gewinn: 0%
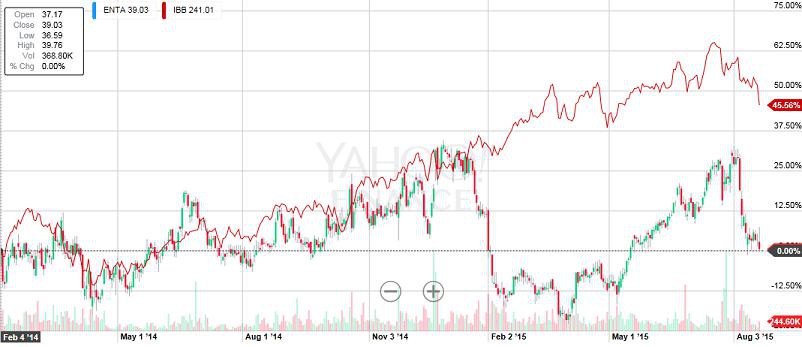
EPZM - seit Mai 2013... 2,5 Jahre: Gewinn: -31%
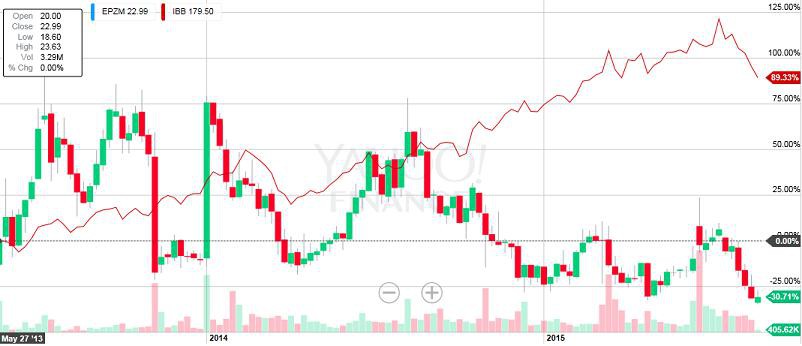
ESPR - seit Feb 2015... 0,5 Jahre: Gewinn: 0%
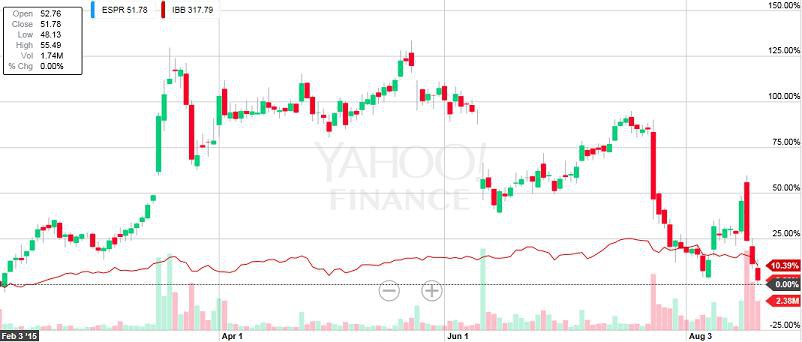
EXEL - seit Feb 2003... 12,5 Jahre: Gewinn 0%
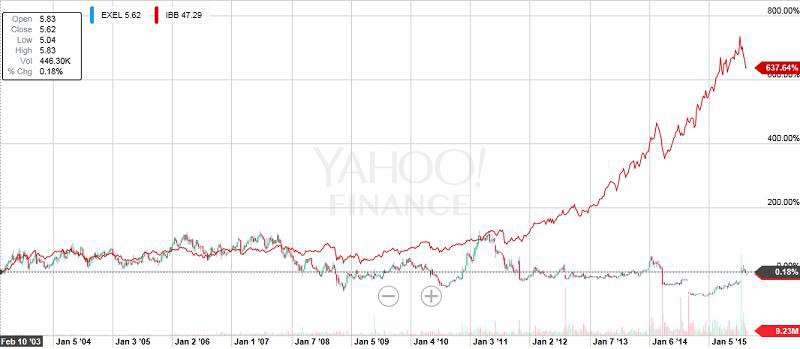
FGEN - seit Aug 2014... 1,0 Jahre: Gewinn 0%
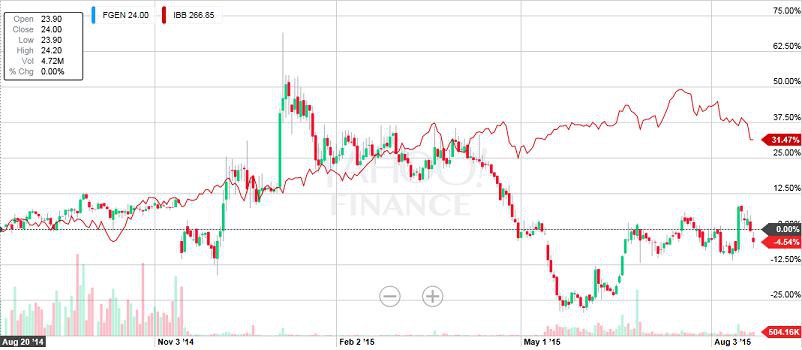
FPRX - seit Jan 2014... 1,5 Jahre: Gewinn 0%
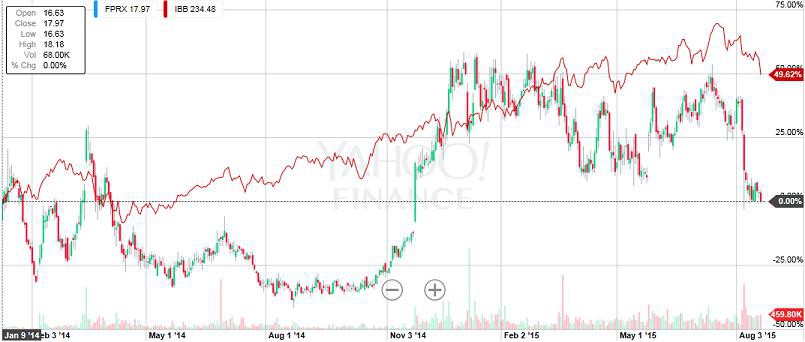
IMMU - seit Jun 2005... 10 Jahre: Gewinn 0%
INFI - seit Jan 2003... 12,5 Jahre: Gewinn 0%
IPH - seit Feb 2014... 1,5 Jahre: Gewinn: 6%
ISIS - seit Jan 2014... 1,5 Jahre: Gewinn: 0%
KPTI - seit Nov 2013... 2,0 Jahre: Gewinn: -18%
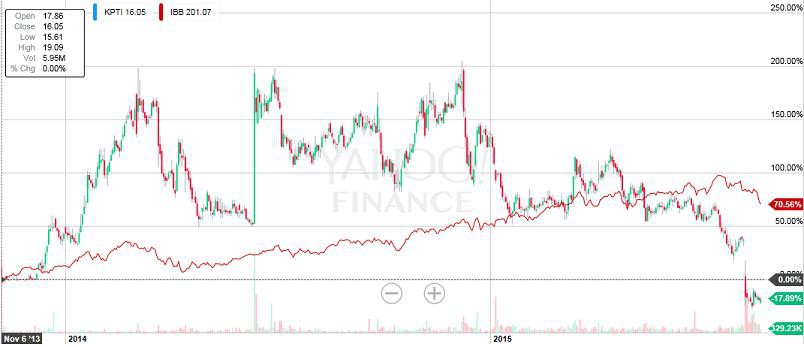
MDVN - seit Aug 2014... 1,0 Jahre: Gewinn: 0%
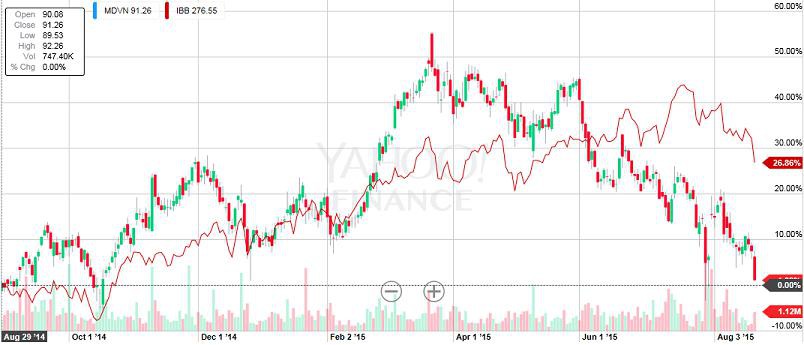
MGNX - seit Okt 2013... 2,0 Jahre: Gewinn: 0%
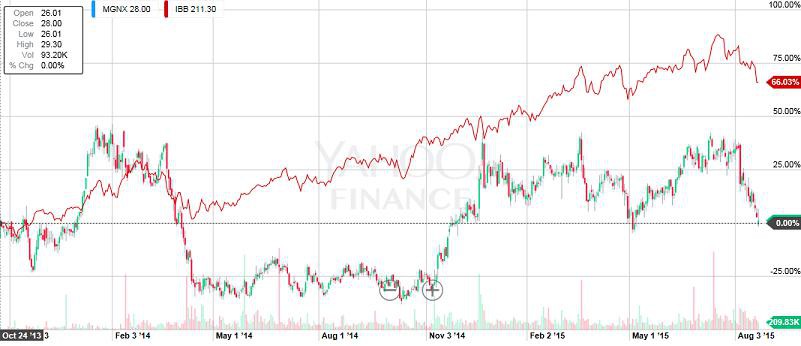
OMED - seit Jul 2013... 2,0 Jahre: Gewinn: 0%
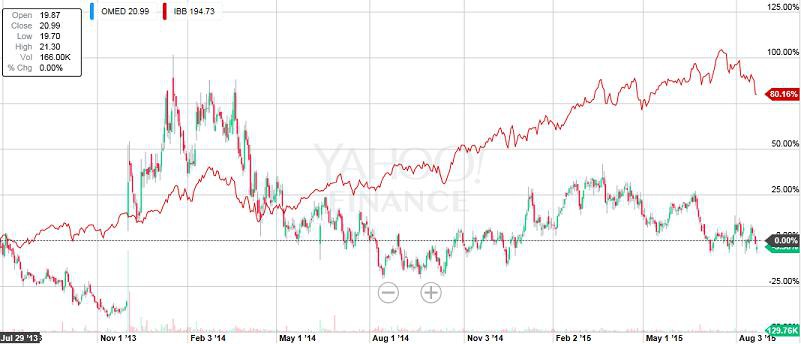
RLYP - seit Dez 2013... 2,0 Jahre: Gewinn: 0%
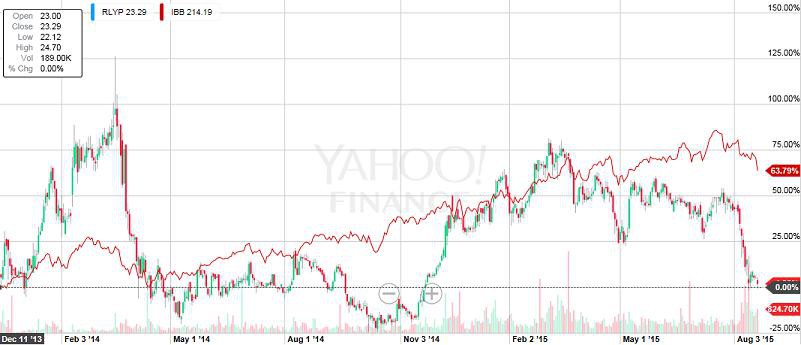
SGEN - seit Aug 2013... 2,0 Jahre: Gewinn: 0%
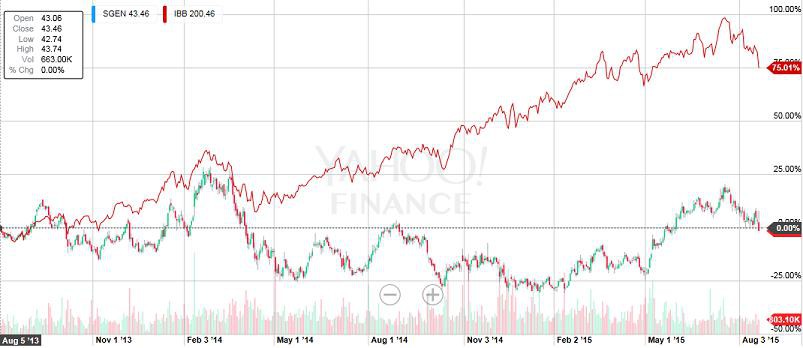
STML - seit Jan 2013... 2,5 Jahre: Gewinn: -15%
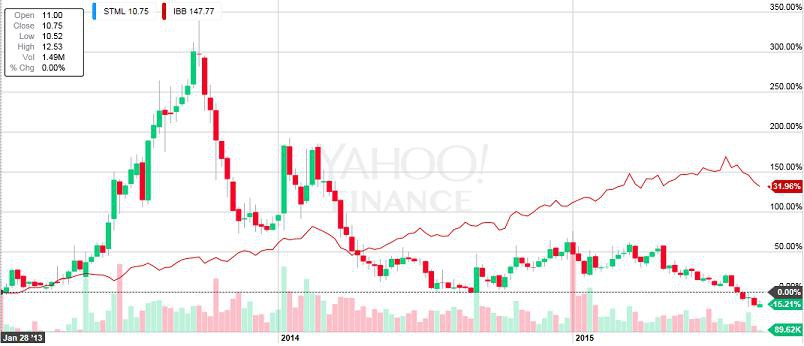
SNTA - seit Mär 2009... 6,5 Jahre: Gewinn: 0%
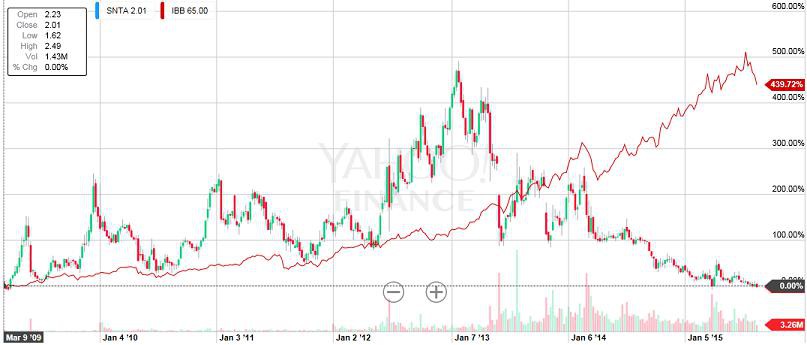
TSRO - seit Sep 2013... 2,0 Jahre: Gewinn: 0%
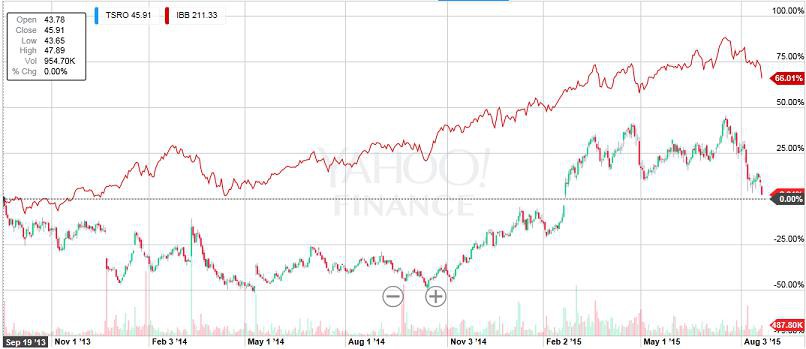
VSTM - seit Dez 2012... 3,0 Jahre: Gewinn: 0%
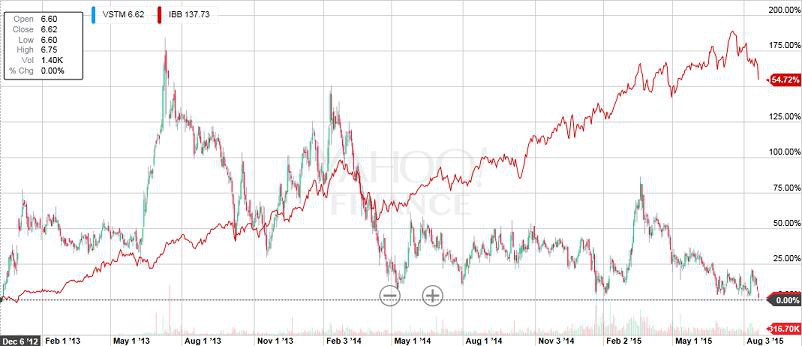
XLRN - seit Dez 2013... 2,0 Jahre: Gewinn: 0%
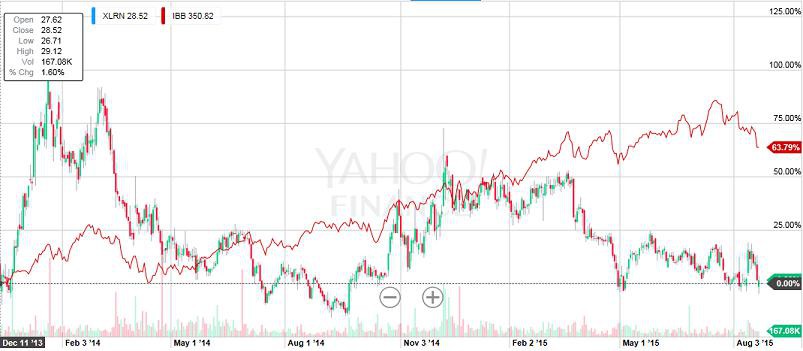
ZSPH - seit Dez 2014... 1,0 Jahre: Gewinn: 0%
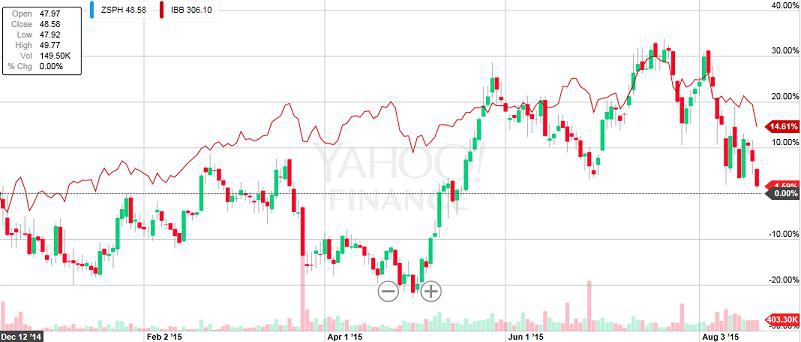
Naja... nicht ganz erst gemeint! Der NBI suggeriert nur immer leicht, dass Biotechs per se gestiegen sind. Die Einzelaktien in meinem Depot geben da aber eher ein differenzierteres Bild. Viele haben immer wieder deutlich korrigiert... wie auch jetzt wieder.
Gruß
ipollit

ALNY - seit Jan 2014... 1,5 Jahre: Gewinn: 9%

ARQL - seit Mär 2003... 12,5 Jahre: Gewinn: -22%

ARRY - seit Feb 2001... 14,5 Jahre: Gewinn: -20%

CLDX - seit Apr 2013... 2,5 Jahre: Gewinn: 0%

CLVS - seit Jun 2013... 2,0 Jahre: Gewinn: 0%

ENTA - seit Feb 2014... 1,5 Jahre: Gewinn: 0%

EPZM - seit Mai 2013... 2,5 Jahre: Gewinn: -31%

ESPR - seit Feb 2015... 0,5 Jahre: Gewinn: 0%

EXEL - seit Feb 2003... 12,5 Jahre: Gewinn 0%

FGEN - seit Aug 2014... 1,0 Jahre: Gewinn 0%

FPRX - seit Jan 2014... 1,5 Jahre: Gewinn 0%

IMMU - seit Jun 2005... 10 Jahre: Gewinn 0%

INFI - seit Jan 2003... 12,5 Jahre: Gewinn 0%

IPH - seit Feb 2014... 1,5 Jahre: Gewinn: 6%

ISIS - seit Jan 2014... 1,5 Jahre: Gewinn: 0%

KPTI - seit Nov 2013... 2,0 Jahre: Gewinn: -18%

MDVN - seit Aug 2014... 1,0 Jahre: Gewinn: 0%

MGNX - seit Okt 2013... 2,0 Jahre: Gewinn: 0%

OMED - seit Jul 2013... 2,0 Jahre: Gewinn: 0%

RLYP - seit Dez 2013... 2,0 Jahre: Gewinn: 0%

SGEN - seit Aug 2013... 2,0 Jahre: Gewinn: 0%

STML - seit Jan 2013... 2,5 Jahre: Gewinn: -15%

SNTA - seit Mär 2009... 6,5 Jahre: Gewinn: 0%

TSRO - seit Sep 2013... 2,0 Jahre: Gewinn: 0%

VSTM - seit Dez 2012... 3,0 Jahre: Gewinn: 0%

XLRN - seit Dez 2013... 2,0 Jahre: Gewinn: 0%

ZSPH - seit Dez 2014... 1,0 Jahre: Gewinn: 0%

Naja... nicht ganz erst gemeint! Der NBI suggeriert nur immer leicht, dass Biotechs per se gestiegen sind. Die Einzelaktien in meinem Depot geben da aber eher ein differenzierteres Bild. Viele haben immer wieder deutlich korrigiert... wie auch jetzt wieder.
Gruß
ipollit
Hammer mit einem Update:
http://www.orf-blog.com/biotech-portfolio-updates-thoughts-o…
Teilverkauf SGEN.
Er enthüllt nebenbei mal seine grundsätzlichen Erwartungen. Er geht davon aus, dass die derzeitige Korrektur noch lange brauchen wird (2016) und noch deutlich weiter gehen wird (weitere -25%).
Klar, mit so etwas kann man immer mächtig schief liegen, aber ein unvernünftiges Szenario ist das sicher nicht.
Ich werde weiterhin vorsichtig auf die Käuferseite zurückkehren, auch wenn es dafür vielleicht noch zu früh sein mag.
http://www.orf-blog.com/biotech-portfolio-updates-thoughts-o…
Teilverkauf SGEN.
Er enthüllt nebenbei mal seine grundsätzlichen Erwartungen. Er geht davon aus, dass die derzeitige Korrektur noch lange brauchen wird (2016) und noch deutlich weiter gehen wird (weitere -25%).
Klar, mit so etwas kann man immer mächtig schief liegen, aber ein unvernünftiges Szenario ist das sicher nicht.
Ich werde weiterhin vorsichtig auf die Käuferseite zurückkehren, auch wenn es dafür vielleicht noch zu früh sein mag.
Was kaufst Du denn ? CLVS, ESPR, EXEL?
CLVS
Persönlich finde ich CLVS auf diesem Level ($ 72,68) ja schon sehr interessant in Anbetracht der noch kommenden Catalysts in diesem Jahr. Zudem ist CLVS m.E. sowieso schon seit jeher unterbewertet, wenn man sich die 3 Produktkandidaten mal genauer ansieht, und auch in welchem Stadium sie sich befinden. Zudem wird CLVS als Übernahmekandidat gehandelt (kein Wunder bei der aktuellen Bewertung). Habe leider noch keine Position in CLVS aber tendiere stark dazu, dies zu ändern. Zumal ich nicht glaube, dass es hier noch sehr weit runtergehen wird da die 200er - Linie schon überschritten wurde. Was meint Ihr ? Wo seht ihr CLVS in der Zukunft?
XENE
Sehr interessant (langfristig) finde ich auch XENE. Ohad Hammer hat dort ja auch kürzlich eine Position aufgebaut.
Abzuwarten bleibt hier was für Umsätze Glybera generieren wird.
Aber die Pipeline und die potentiellen Meilenstein-Zahlungen (insgesamt ca. $1billion) sind schon beeindruckend be einer aktuellen Bewertung von 146 Millionen.
Insbesondere die Kooperation mit Genentech allein ca. $613 milion bzgl. GDC-0276. Hier werden im zweiten Halbjahr 2015 auch noch die Ergebnisse erwartet (aktuell noch P1)
CLVS
Persönlich finde ich CLVS auf diesem Level ($ 72,68) ja schon sehr interessant in Anbetracht der noch kommenden Catalysts in diesem Jahr. Zudem ist CLVS m.E. sowieso schon seit jeher unterbewertet, wenn man sich die 3 Produktkandidaten mal genauer ansieht, und auch in welchem Stadium sie sich befinden. Zudem wird CLVS als Übernahmekandidat gehandelt (kein Wunder bei der aktuellen Bewertung). Habe leider noch keine Position in CLVS aber tendiere stark dazu, dies zu ändern. Zumal ich nicht glaube, dass es hier noch sehr weit runtergehen wird da die 200er - Linie schon überschritten wurde. Was meint Ihr ? Wo seht ihr CLVS in der Zukunft?
XENE
Sehr interessant (langfristig) finde ich auch XENE. Ohad Hammer hat dort ja auch kürzlich eine Position aufgebaut.
Abzuwarten bleibt hier was für Umsätze Glybera generieren wird.
Aber die Pipeline und die potentiellen Meilenstein-Zahlungen (insgesamt ca. $1billion) sind schon beeindruckend be einer aktuellen Bewertung von 146 Millionen.
Insbesondere die Kooperation mit Genentech allein ca. $613 milion bzgl. GDC-0276. Hier werden im zweiten Halbjahr 2015 auch noch die Ergebnisse erwartet (aktuell noch P1)
Hier mal eine Auflistung der bishrigen Korrektur des NBI und der enthaltenen Aktien von ihren jeweiligen Hochs. Der NBI hat bisher 15% verloren... die enthaltenen Aktien im Schnitt 33%.
Hinter dem Symbol ist jeweils die aktuelle Börsenbewertung in Mio USD angegeben, sowie in Klammern die Gewichtung im IBB, falls sie über 1% liegt. Die Summe der angegebenen Gewichtungen ist ca. 75% des IBB. D.h. würden alle anderen Werte (ohne Gewichtungsangabe) auf 0 fallen, würde der IBB (bzw. NBI) nur um weitere 25% sinken.
Interessant ist, dass neben den beiden Übernahmen RCPT und KYTH, die dauerhaft auf ihrem Höchstkurs (Übernahmekurs) notieren der beste Wert die deutsche Qiagen ist.

Grüße
ipollit
Hinter dem Symbol ist jeweils die aktuelle Börsenbewertung in Mio USD angegeben, sowie in Klammern die Gewichtung im IBB, falls sie über 1% liegt. Die Summe der angegebenen Gewichtungen ist ca. 75% des IBB. D.h. würden alle anderen Werte (ohne Gewichtungsangabe) auf 0 fallen, würde der IBB (bzw. NBI) nur um weitere 25% sinken.
Interessant ist, dass neben den beiden Übernahmen RCPT und KYTH, die dauerhaft auf ihrem Höchstkurs (Übernahmekurs) notieren der beste Wert die deutsche Qiagen ist.
0% RCPT 7.320 (1,1%) - Übernahme, Kurs ist fix
-2% KYTH 1.960 - Übernahme, Kurs ist fix
-8% QGEN 6.110
-8% SRPT 1.410
-8% SVA 308
-8% SCMP 1.120
-11% MDCO 2.040
-11% CARA 571
-11% TECH 3.770
-13% VRTX 30.700 (4,2%)
-13% JAZZ 10.450 (1,6%)
-13% REGN 54.240 (7,9%)
-14% INCY 18.830 (2,9%)
-14% RVNC 733
-15% GILD 154.580 (8,2%)
-15% AMGN 117.670 (8,5%)
-15% DEPO 1.730
-15% LMNX 795
-15% NBI
-15% INSM 1.500
-15% CELG 94.110 (9,0%)
-16% PETX 608
-16% PTLA 2.380
-16% MYGN 2.290
-17% IPXL 3.020
-17% ALXN 39.310 (5,1%)
-17% BMRN 20.330 (3,1%)
-17% ANAC 5.720
-18% ILMN 28.930 (4,0%)
-18% CNCE 337
-18% AMRI 635
-18% SHPG 43.840 (1,7%)
-18% SPPI 458
-18% UTHR 7.090 (1,1%)
-18% LXRX 1.170
-19% NVAX 3.260
-19% FLML 850
-20% NLNK 1.360
-20% ALKS 9.020 (1,4%)
-20% CMRX 2.140
-21% ENDP 15.950 (2,5%)
-21% RGEN 1.110
-21% PRTA 1.740
-21% SGEN 5.160
-22% RPTP 1.030
-22% MNTA 1.350
-22% GWPH 2.180
-22% NBIX 3.760
-22% TTPH 1.500
-23% AMAG 1.850
-23% EXEL 1.180
-24% ENTA 753
-24% ZSPH 1.240
-24% CEMP 1.560
-25% AMPH 625
-25% LGND 1.680
-25% RARE 3.980
-25% GRFS 20.710
-25% FOLD 1.670
-25% RDUS 2.700
-26% OSIR 606
-26% VNDA 485
-26% DYAX 3.300
-27% HZNP 4.620
-27% RTRX 964
-28% SUPN 811
-28% AFFX 750
-29% ALNY 8.440 (1,3%)
-29% BCRX 878
-29% CLVS 2.780
-29% AKRX 4.590
-30% MGNX 962
-30% CCXI 294
-30% INSY 2.340
-31% MACK 1.070
-31% OMER 794
-31% SGYP 788
-31% SCLN 405
-31% HALO 2.190
-31% ACAD 3.590
-32% PGNX 531
-32% OMED 610
-33% CERS 458
-33% IMGN 1.140
-33% GHDX 824
-33% MYL 25.320 (3,0%)
-33% ANIP 565
-33% ARIA 1.250
-33% ALDR 1.590
-33% POZN 276
-34% GERN 487
-34% ACOR 1.280
-35% MDVN 7.470 (1,1%)
-36% XNPT 390
-36% FPRX 471
-36% IRWD 1.560
-37% ARRY 769
-37% ZFGN 947
-37% BLUE 4.490
-38% OPHT 1.570
-38% AGIO 3.210
-38% BIIB 69.530 (6,4%)
-39% SAGE 1.560
-39% ICPT 4.620
-40% SGNT 659
-40% ISIS 5.600
-41% NKTR 1.360
-42% XLRN 938
-43% THRX 1.590
-44% KITE 2.200
-44% RLYP 988
-44% ECYT 218
-45% VSTM 252
-45% VSAR 389
-46% INO 507
-46% PDLI 908
-48% PACB 345
-48% INFI 464
-49% QLTI 182
-49% CGEN 260
-50% AEGR 523
-51% PCRX 2.200
-52% MNKD 1.530
-52% ALIM 139
-53% ARNA 719
-53% SNTA 259
-53% ACHN 1.070
-55% PTCT 1.190
-56% AERI 409
-56% TBPH 445
-57% ACRX 180
-57% EPZM 658
-58% SQNM 239
-59% CLDX 1.330
-60% SGMO 539
-60% FMI 743
-64% PTX 280
-66% IMMU 177
-67% OREX 384
-69% RGLS 408
-72% AKBA 122
-73% KPTI 471
-78% VVUS 108
-83% AAVL 227
-87% XOMA 93
-96% CLDN 25
Grüße
ipollit
Ein denkwürdiger Tag heute an den Börsen - speziell auch was Biotech betrifft. Es sind wohl einige institutionelle Anleger im Urlaub. An eine solche Tageskerze des IBB kann ich mich nicht erinnern. Panik in beide Richtungen. Mal sehen wie das weitergeht...

CELG z.B. hat heute mit -21% eröffnet! Das es jetzt auch die Großen trifft ist m.E. aber auch ein gutes Zeichen, denn ohne eine Korrektur bei den GILDs und Celgs wird es nicht gehen.
Leider ist auch die Entwicklung am Devisenmarkt ungünstig.

CELG z.B. hat heute mit -21% eröffnet! Das es jetzt auch die Großen trifft ist m.E. aber auch ein gutes Zeichen, denn ohne eine Korrektur bei den GILDs und Celgs wird es nicht gehen.
Leider ist auch die Entwicklung am Devisenmarkt ungünstig.
Antwort auf Beitrag Nr.: 50.474.148 von kmastra am 24.08.15 17:19:09"Das es jetzt auch die Großen trifft ist m.E. aber auch ein gutes Zeichen, denn ohne eine Korrektur bei den GILDs und Celgs wird es nicht gehen."
Das ist definitiv ein gutes Zeichen. Heute hatten wir in den ersten Handelsminuten tatsächlich Panik und sell off.
Ich glaube, ich hab vor kurzem mal geschrieben, dass größere Korrekturen kaum ohne solche Ereignisse abgehen.
Von daher ist es gut, dass das jetzt passiert ist.
Allerdings sind dann schnell wieder Käufer im Markt gewesen. Von Verzweiflung und Kapitulation kann noch keine Rede sein (muss aber auch nicht zwingend so weit kommen).
Ich habe jedenfalls die Chance heute leider verpasst.
Eine XLRN für 20, eine BPMC für 20 oder durchaus auch eine CELG für 92 wären - neben vielen anderen Gelegenheiten - für mich klare Käufe gewesen.
Die Gesamtsituation bleibt aber schwierig und undurchsichtig. Mag sein, dass noch mehrere solcher Tage wie heute kommen und sich nochmals Gelegenheiten ergeben.
Das ist definitiv ein gutes Zeichen. Heute hatten wir in den ersten Handelsminuten tatsächlich Panik und sell off.
Ich glaube, ich hab vor kurzem mal geschrieben, dass größere Korrekturen kaum ohne solche Ereignisse abgehen.
Von daher ist es gut, dass das jetzt passiert ist.
Allerdings sind dann schnell wieder Käufer im Markt gewesen. Von Verzweiflung und Kapitulation kann noch keine Rede sein (muss aber auch nicht zwingend so weit kommen).
Ich habe jedenfalls die Chance heute leider verpasst.
Eine XLRN für 20, eine BPMC für 20 oder durchaus auch eine CELG für 92 wären - neben vielen anderen Gelegenheiten - für mich klare Käufe gewesen.
Die Gesamtsituation bleibt aber schwierig und undurchsichtig. Mag sein, dass noch mehrere solcher Tage wie heute kommen und sich nochmals Gelegenheiten ergeben.
CLVS
Clovis gibt heute ja noch mehr ab als der Gesamtmarkt. Zwei Gedanken hierzu könnte man diskutieren:
Der PARP-Verkauf von Biomarin an Medivation läßt aufgrund des erzielten Preises die Schlußfolgerung zu, daß Ruca dann auch nicht viel Wert sein kann (nicht meine Behauptung, sondern Gedanke von Feuerstein...)
Oder
Die heute veröffentlichten abstracts zur World Lung Conference werden negativ beurteilt, z.B. dies hier
https://content.webges.com/library/wclc/browse/search/7g8#2y…
Ob die Daten tatsächlich gut oder schlecht sind, müssten die Experten beurteilen, wäre jedenfalls toll.
Clovis gibt heute ja noch mehr ab als der Gesamtmarkt. Zwei Gedanken hierzu könnte man diskutieren:
Der PARP-Verkauf von Biomarin an Medivation läßt aufgrund des erzielten Preises die Schlußfolgerung zu, daß Ruca dann auch nicht viel Wert sein kann (nicht meine Behauptung, sondern Gedanke von Feuerstein...)
Oder
Die heute veröffentlichten abstracts zur World Lung Conference werden negativ beurteilt, z.B. dies hier
https://content.webges.com/library/wclc/browse/search/7g8#2y…
Ob die Daten tatsächlich gut oder schlecht sind, müssten die Experten beurteilen, wäre jedenfalls toll.
Antwort auf Beitrag Nr.: 50.477.550 von lawmeetstax am 24.08.15 22:07:39Hallo lawmeetstax.
Ich würde das besonders an einem solchen Tag wie gestern nicht überbewerten.
Goldmansachs sehen die Abstracts eher neutral.


Stifel hat neulich einige gute Punkte zusammengefasst. Grundsätzlich zeigen sich doch deutliche Unterschiede zwischen Roci und 9291. Ich gehe davon aus, dass deshalb beide ihren Anteil haben werden. Roci scheint eher überlegen, aber evtl. muss man das in einem Direktvergleich in einer Studie nachweisen.


SG kmastra
Ich würde das besonders an einem solchen Tag wie gestern nicht überbewerten.
Goldmansachs sehen die Abstracts eher neutral.


Stifel hat neulich einige gute Punkte zusammengefasst. Grundsätzlich zeigen sich doch deutliche Unterschiede zwischen Roci und 9291. Ich gehe davon aus, dass deshalb beide ihren Anteil haben werden. Roci scheint eher überlegen, aber evtl. muss man das in einem Direktvergleich in einer Studie nachweisen.


SG kmastra
Antwort auf Beitrag Nr.: 50.484.669 von kmastra am 25.08.15 16:23:26Rebound bei den Biotechaktien allgemein schwach, insbesondere aber auch wieder CLVS, gestern überdurchschnittlich nach unten und heute unterdurchschnittlich nach oben ... so was nennt man dann Underperformer!
Antwort auf Beitrag Nr.: 50.420.796 von ipollit am 17.08.15 22:33:00INCY, PD1&Co, BMY
obwohl ich von INCY sehr überzeugt bin, überrascht es mich doch ein wenig, wie gut sie sich in der Korrektur halten. Inzwischen stehen sie kurz vor einem neuem Allzeithoch trotz einer eigentlich sehr ambitionierten Bewertung von aktuell über 21 Mrd USD. Wie kann das sein?

Eine Erklärung wäre aus meiner Sicht das mögliche Potential des IDO-Hemmers. Der folgende sehr bullische Analysten-Kommentar verweist u.a. auch darauf und sieht INCY insgesamt auf dem Weg zum nächsten 100 Mrd USD Biotech... also zur nächsten CELG.



Ein hohes Rekrutierungs-Interesse in die PD1 + IDO Kombistudien ist schonmal ein positives Anzeichen für eine gute Wirksamkeit... wenn Ärzte und Patienten ein Mittel positiv beurteilen und dann auch in der Studie gute Erfahrungen machen, ist die Rekrutierung meistens besser. Eine schleppende Rekrutierung kann dagegen ein Hinweis sein, dass es schlechter als bereits verfügbare Alternativen ist.
Offensichtlich ist es auch möglich, dass INCY bereits PIII-Studien vor Bekanntgabe der PII-Daten startet:

Warum wäre eine IDO + PD1 Kombi für INCY so wertvoll? Vielleicht sind die folgenden Zahlen zu PD1 mit einem weltweiten Potential von 51 Mrd USD etwas zu optimistisch, aber so oder so wird PD1 als eine oder die wichtigste Medikamenten-Klasse gegen Krebs gesehen.


Viele große Pharmas sind in der PD1-Entwicklung vertreten, während die Biotech hier eher außen vor sind.
- Pfizer steigt auch groß in IO ein?
- PDL1 könnte bezüglich Kombis einen Vorteil zu PD1 bieten?

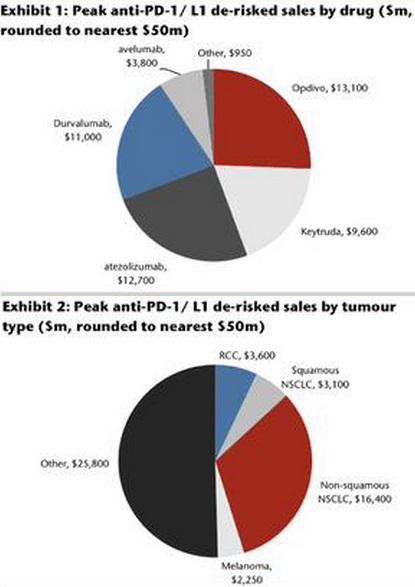

PD1-Therapien werden in Zukunft die Grundlage von vielen Krebs-Therapien bilden, weil anders als z.B. bei einer Chemo die Wirkung (sofern diese eintritt) sehr langanhaltend ist... sogar eine Heilung ist möglich. Gegen Chemo, Target-Therapien usw. bilden sich meistens nach einiger Zeit Resistenzen. Bei IO-Mitteln bleibt bei einen Teil der Patienten die Wirkung aber sehr lange erhalten... die OS-Kurven fallen nicht auf 0, sondern bilden einen Boden >0 aus.
Typisch für IO-Therapien ist es aber auch, dass nur ein relativ kleiner Teil anspricht. Und hier liegt das Potential für Mittel wie IDO usw, die synergetisch mit PD1 wirken können. Ein Ziel muss es in Zukunft sein, den Anteil der Patienten zu vergrößern, bei denen die Therapie eine dauerhafte Wirkung zeigt... und IDO ist hier offensichtlich ein aussichtsreicher Kandidat.
Z.B. in Eierstock-Krebs sind die Ansprechraten von PD1 mit um die 10% relativ gering. U.a. ist hierfür die direkt Umgebung des Tumors (TME) verantwortlich, die das Immunsystem unterdrückt. Paul Rennert sieht hier u.a. IDO als eine relevante Größe.
http://www.sugarconebiotech.com/?p=942



Sollte IDO + PD1 wirklich eine gute IO-Kombi sein, so wäre dies sehr positiv für INCY, da sie den führenden IDO-Hemmer besitzen, der bereits mit allen PD1-AKs getestet wird (INCY hält die vollen Rechte). Auf der einen Seite könnten PD1 einen riesigen Markt bilden (oben wird z.B. von 51 Mrd USD gesprochen)... auf der anderen Seite wäre PD1 auf gute Kombis angewiesen und INCY hat bei IDO fast ein kleines Monopol.
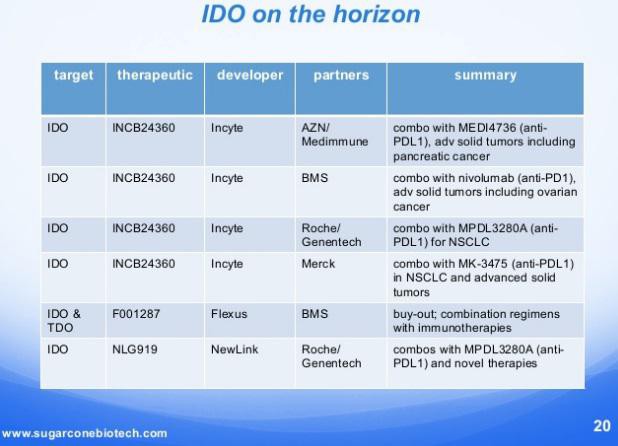
Die letzten PD1 + CTLA4 Kombi-Ergebnisse wurden in Twitter eher negativ gesehen... niedrige Ansprechraten bei hohen Nebenwirkungen. Eine PD1 + IDO Kombi könnte überlegen sein.

Gruß
ipollit
obwohl ich von INCY sehr überzeugt bin, überrascht es mich doch ein wenig, wie gut sie sich in der Korrektur halten. Inzwischen stehen sie kurz vor einem neuem Allzeithoch trotz einer eigentlich sehr ambitionierten Bewertung von aktuell über 21 Mrd USD. Wie kann das sein?
Eine Erklärung wäre aus meiner Sicht das mögliche Potential des IDO-Hemmers. Der folgende sehr bullische Analysten-Kommentar verweist u.a. auch darauf und sieht INCY insgesamt auf dem Weg zum nächsten 100 Mrd USD Biotech... also zur nächsten CELG.



Ein hohes Rekrutierungs-Interesse in die PD1 + IDO Kombistudien ist schonmal ein positives Anzeichen für eine gute Wirksamkeit... wenn Ärzte und Patienten ein Mittel positiv beurteilen und dann auch in der Studie gute Erfahrungen machen, ist die Rekrutierung meistens besser. Eine schleppende Rekrutierung kann dagegen ein Hinweis sein, dass es schlechter als bereits verfügbare Alternativen ist.
Offensichtlich ist es auch möglich, dass INCY bereits PIII-Studien vor Bekanntgabe der PII-Daten startet:

Warum wäre eine IDO + PD1 Kombi für INCY so wertvoll? Vielleicht sind die folgenden Zahlen zu PD1 mit einem weltweiten Potential von 51 Mrd USD etwas zu optimistisch, aber so oder so wird PD1 als eine oder die wichtigste Medikamenten-Klasse gegen Krebs gesehen.


Viele große Pharmas sind in der PD1-Entwicklung vertreten, während die Biotech hier eher außen vor sind.
- Pfizer steigt auch groß in IO ein?
- PDL1 könnte bezüglich Kombis einen Vorteil zu PD1 bieten?



PD1-Therapien werden in Zukunft die Grundlage von vielen Krebs-Therapien bilden, weil anders als z.B. bei einer Chemo die Wirkung (sofern diese eintritt) sehr langanhaltend ist... sogar eine Heilung ist möglich. Gegen Chemo, Target-Therapien usw. bilden sich meistens nach einiger Zeit Resistenzen. Bei IO-Mitteln bleibt bei einen Teil der Patienten die Wirkung aber sehr lange erhalten... die OS-Kurven fallen nicht auf 0, sondern bilden einen Boden >0 aus.
Typisch für IO-Therapien ist es aber auch, dass nur ein relativ kleiner Teil anspricht. Und hier liegt das Potential für Mittel wie IDO usw, die synergetisch mit PD1 wirken können. Ein Ziel muss es in Zukunft sein, den Anteil der Patienten zu vergrößern, bei denen die Therapie eine dauerhafte Wirkung zeigt... und IDO ist hier offensichtlich ein aussichtsreicher Kandidat.
Z.B. in Eierstock-Krebs sind die Ansprechraten von PD1 mit um die 10% relativ gering. U.a. ist hierfür die direkt Umgebung des Tumors (TME) verantwortlich, die das Immunsystem unterdrückt. Paul Rennert sieht hier u.a. IDO als eine relevante Größe.
http://www.sugarconebiotech.com/?p=942



Sollte IDO + PD1 wirklich eine gute IO-Kombi sein, so wäre dies sehr positiv für INCY, da sie den führenden IDO-Hemmer besitzen, der bereits mit allen PD1-AKs getestet wird (INCY hält die vollen Rechte). Auf der einen Seite könnten PD1 einen riesigen Markt bilden (oben wird z.B. von 51 Mrd USD gesprochen)... auf der anderen Seite wäre PD1 auf gute Kombis angewiesen und INCY hat bei IDO fast ein kleines Monopol.

Die letzten PD1 + CTLA4 Kombi-Ergebnisse wurden in Twitter eher negativ gesehen... niedrige Ansprechraten bei hohen Nebenwirkungen. Eine PD1 + IDO Kombi könnte überlegen sein.

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.516.853 von ipollit am 29.08.15 14:31:46INCY
PD1 ist ein wichtiger Signalweg, über den das Immunsystem (z.B. T-Zellen) gedämpft wird. Krebszellen können sich so mittels PD1 vor dem Immunsystem schützen, indem sie selber PD1 expressionieren und die andockenden T-Zellen deaktivieren.
Neben diesen direkten Weg können Krebszellen aber auch indirekt das Immunsystem dämpfen, indem sie spezielle Immunzellen anlocken und aktiveren, die ihrerseits das Immunsystem herunterregeln... dies können TAMs, MDSCs oder Tregs sein. Hierbei scheint der STAT-Weg und damit Entzündungsreaktionen eine Rolle zu spielen. In der entzündlichen Umgebung des Tumors sammeln sich so z.B. TAMs, die auch PD1 bzw. PDL1 expressionieren und die T-Zellen daran hindern, die Krebszellen anzugreifen.
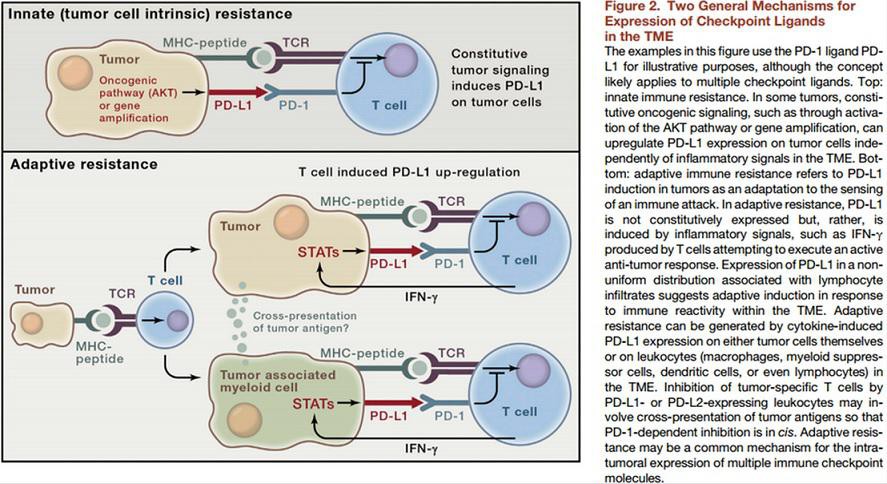
Daraus leitet sich INCYs Ansatz ab, mit JAK-Hemmern den STAT-Signalweg zu blockieren... dadurch werden auch diese immununterdrückenden Mechanismen gedämpft. Neben der Reduzierung von PD1 können dies auch andere Checkpoints sein, die man vielleicht noch gar nicht kennt (die Wirkung ist also breiter als nur die PD1-Blockierung mittels PD1-AKs). Demnach würden auch IO-Kombis mit JAK einen Sinn ergeben. Präklinisch sind so z.B. JAK und IDO synergetisch.
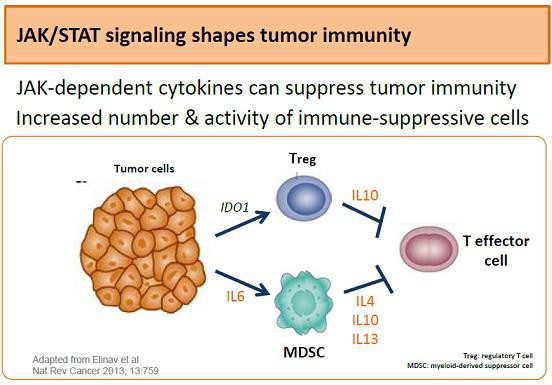
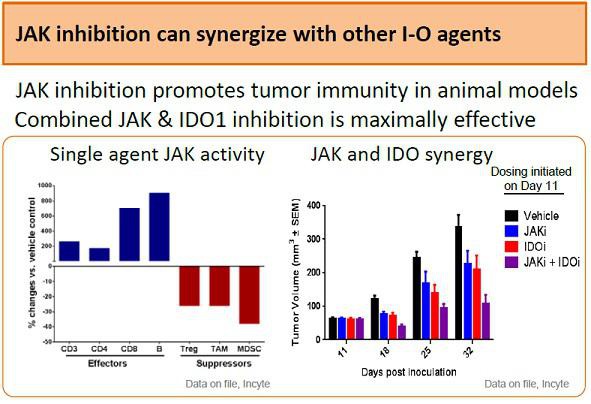
Gruß
ipollit
PD1 ist ein wichtiger Signalweg, über den das Immunsystem (z.B. T-Zellen) gedämpft wird. Krebszellen können sich so mittels PD1 vor dem Immunsystem schützen, indem sie selber PD1 expressionieren und die andockenden T-Zellen deaktivieren.
Neben diesen direkten Weg können Krebszellen aber auch indirekt das Immunsystem dämpfen, indem sie spezielle Immunzellen anlocken und aktiveren, die ihrerseits das Immunsystem herunterregeln... dies können TAMs, MDSCs oder Tregs sein. Hierbei scheint der STAT-Weg und damit Entzündungsreaktionen eine Rolle zu spielen. In der entzündlichen Umgebung des Tumors sammeln sich so z.B. TAMs, die auch PD1 bzw. PDL1 expressionieren und die T-Zellen daran hindern, die Krebszellen anzugreifen.

Daraus leitet sich INCYs Ansatz ab, mit JAK-Hemmern den STAT-Signalweg zu blockieren... dadurch werden auch diese immununterdrückenden Mechanismen gedämpft. Neben der Reduzierung von PD1 können dies auch andere Checkpoints sein, die man vielleicht noch gar nicht kennt (die Wirkung ist also breiter als nur die PD1-Blockierung mittels PD1-AKs). Demnach würden auch IO-Kombis mit JAK einen Sinn ergeben. Präklinisch sind so z.B. JAK und IDO synergetisch.


Gruß
ipollit
FPRX
Wie in den letzten beiden Postings zu sehen, trägt die Umgebung des Tumors dazu bei, dass sich der Tumor vor dem Immunsystem schützen kann. Paul Rennert zeigt hier zwei IO-Arten:
http://www.sugarconebiotech.com/?page_id=37
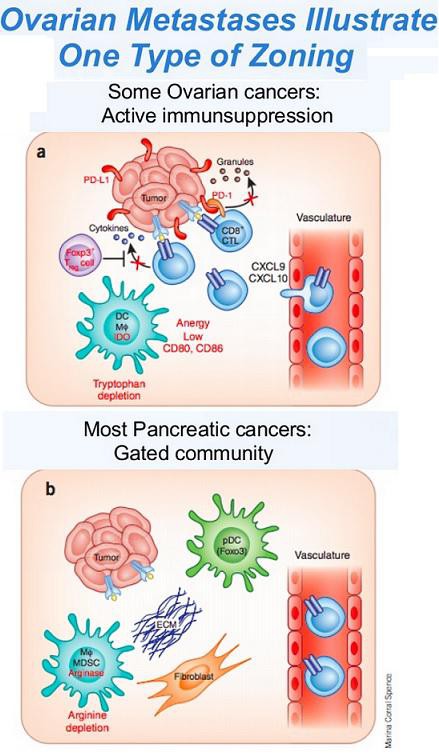
In (a) ist drinnen Immunzellen wie T-Zellen in den Tumor ein, werden dort aber über PD1, IDO usw gehemmt. Dieser Tumor spricht z.B. auf PD1-Therapien. Dann kann es aber auch wie in (b) sein, dass der Tumor nicht selber das Immunsystem unterdrückt, sondern es um den Tumor herum Bereiche gibt, die den Tumor vom Immunsystem abschotten.
Eine Zellart, die daran beteiligt ist, sind TAM. Hier sind z.B. CD163+ TAMs braun eingefärbt zu sehen, die den Tumor umgeben. In diesen Bereichen wird auch PD1 u.a. von den TAMs expressioniert. Neben PD1 können dies aber auch andere Dinge sein, die das Immunsystem unterdrücken.
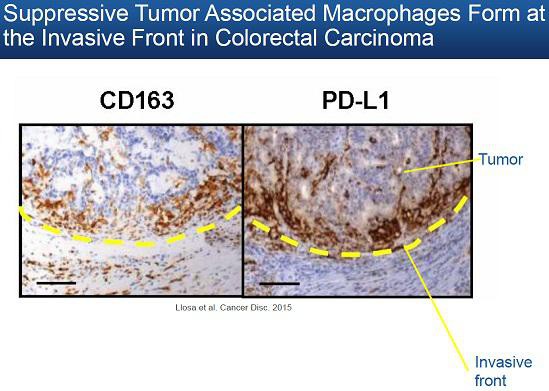
D.h. neben dem Tumor selber schützen auch andere Zellarten den Krebs. Tregs (regulatorische T-Zellen) werden u.a. von IDO stimuliert, so dass gegen diese IDO-Hemmer helfen. TAMs können dagegen über die Hemmung von CSF1R vermindert werden.
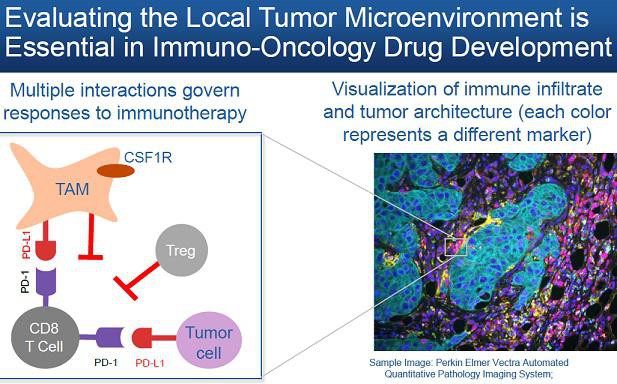
Tumore, bei denen TAMs aktiv sind, besitzen eine deutlich schlechtere Überlebensrate.
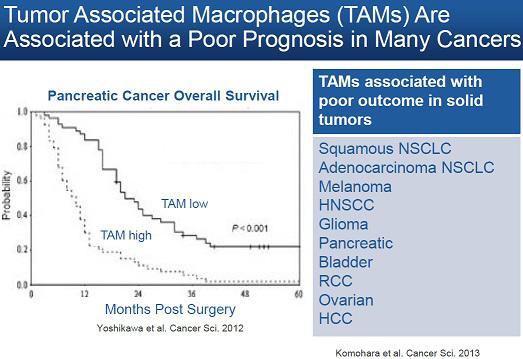
FPRX hat hier mit FPA008 einen guten Kandidaten, der zur Zeit zusammen mit BMYs PD1-AK Nivo getestet wird (BMY bezahlt die Studien-Kosten, FPRX besitzt noch alle Rechte). Roche hat einen eigenen CSF1R-AK in der Entwicklung. Vielleicht wird CSF1R ja ähnlich interessant wie IDO.
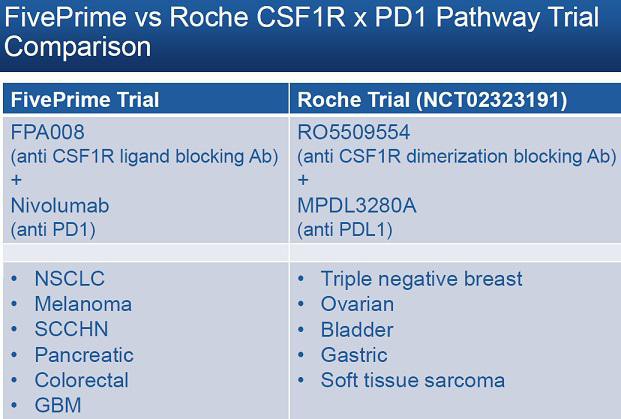
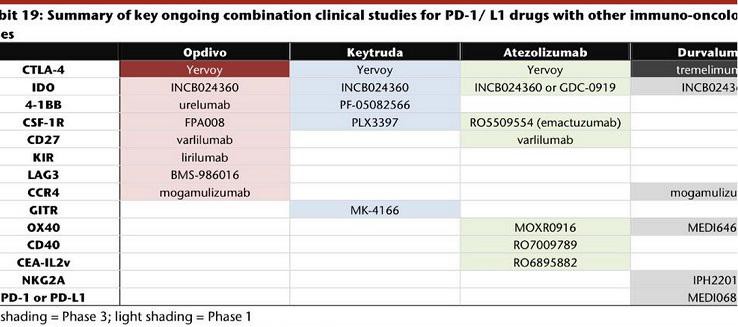
Bisher gibt es noch wenige Daten zu einer solchen Kombi.
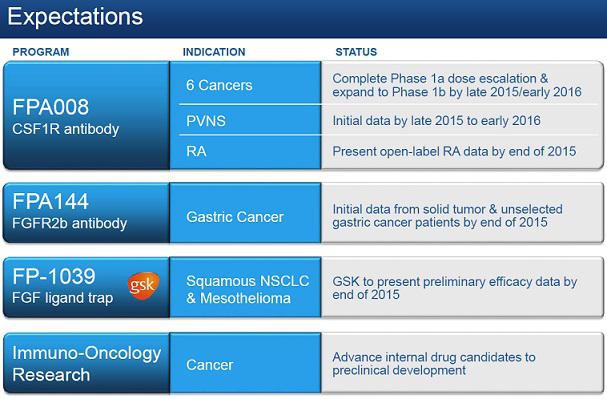
Dies ist ein Grund, warum ich FPRX bei der aktuellen MK von 500 Mio USD interessant finde.

Gruß
ipollit
Wie in den letzten beiden Postings zu sehen, trägt die Umgebung des Tumors dazu bei, dass sich der Tumor vor dem Immunsystem schützen kann. Paul Rennert zeigt hier zwei IO-Arten:
http://www.sugarconebiotech.com/?page_id=37

In (a) ist drinnen Immunzellen wie T-Zellen in den Tumor ein, werden dort aber über PD1, IDO usw gehemmt. Dieser Tumor spricht z.B. auf PD1-Therapien. Dann kann es aber auch wie in (b) sein, dass der Tumor nicht selber das Immunsystem unterdrückt, sondern es um den Tumor herum Bereiche gibt, die den Tumor vom Immunsystem abschotten.
Eine Zellart, die daran beteiligt ist, sind TAM. Hier sind z.B. CD163+ TAMs braun eingefärbt zu sehen, die den Tumor umgeben. In diesen Bereichen wird auch PD1 u.a. von den TAMs expressioniert. Neben PD1 können dies aber auch andere Dinge sein, die das Immunsystem unterdrücken.

D.h. neben dem Tumor selber schützen auch andere Zellarten den Krebs. Tregs (regulatorische T-Zellen) werden u.a. von IDO stimuliert, so dass gegen diese IDO-Hemmer helfen. TAMs können dagegen über die Hemmung von CSF1R vermindert werden.

Tumore, bei denen TAMs aktiv sind, besitzen eine deutlich schlechtere Überlebensrate.

FPRX hat hier mit FPA008 einen guten Kandidaten, der zur Zeit zusammen mit BMYs PD1-AK Nivo getestet wird (BMY bezahlt die Studien-Kosten, FPRX besitzt noch alle Rechte). Roche hat einen eigenen CSF1R-AK in der Entwicklung. Vielleicht wird CSF1R ja ähnlich interessant wie IDO.


Bisher gibt es noch wenige Daten zu einer solchen Kombi.

Dies ist ein Grund, warum ich FPRX bei der aktuellen MK von 500 Mio USD interessant finde.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.517.993 von ipollit am 29.08.15 22:47:12CLVS
Würde gerne CLVS kaufen, habe leider bisher noch keine Position aufgebaut.
Als die Aktie bei $68 stand, wollte ich zukaufen, hatte aber leider das Kapital noch nicht. Jetzt ist sie wieder auf $80 gestiegen. Das ist wohl nicht der beste Einstiegskurs im Moment.
Was meint ihr, wird CLVS nochmal deutlich runtergehen in nächster Zeit? Zum Jahresende hin gibt es ja einige Catalysts, die den Kurs wohl eher hochdrucken sollten (hoffentlich) ;-)
Wie ist eure Einschätzung?
Viele Grüße
biopadawan
Würde gerne CLVS kaufen, habe leider bisher noch keine Position aufgebaut.
Als die Aktie bei $68 stand, wollte ich zukaufen, hatte aber leider das Kapital noch nicht. Jetzt ist sie wieder auf $80 gestiegen. Das ist wohl nicht der beste Einstiegskurs im Moment.
Was meint ihr, wird CLVS nochmal deutlich runtergehen in nächster Zeit? Zum Jahresende hin gibt es ja einige Catalysts, die den Kurs wohl eher hochdrucken sollten (hoffentlich) ;-)
Wie ist eure Einschätzung?
Viele Grüße
biopadawan
ganz allgemein kann ich antworten, dass dies auch vom Gesamtmarkt abhängen wird. Ist die Korrektur nur eine heftige Welle in der üblichen Sommerkrise gewesen, können wir schon die Tiefstkurse gesehen haben. Dafür sprechen die hier wiederholt angebrachten Bewertungsvergleiche.
War die Korrektur dagegen nur der Anfang einer längeren Abwärtsbewerung, bestünde ohnehin derzeit kein drigender Handlungsbedarf. Das muss jeder selbst einschätzen.
Allgemein kann man aber sagen, dass es immer ein positives Zeichen ist, wenn Werte nach einer Korrektur relativ schnell wieder steigen, weil viele Investoren die Chance nutzen, die Aktie zu Kursen zu kaufen, die sie nicht mehr erwartet hätten. Die schlechten Aktien erholen sich dagegen erst deutlich später und langsamer.
War die Korrektur dagegen nur der Anfang einer längeren Abwärtsbewerung, bestünde ohnehin derzeit kein drigender Handlungsbedarf. Das muss jeder selbst einschätzen.
Allgemein kann man aber sagen, dass es immer ein positives Zeichen ist, wenn Werte nach einer Korrektur relativ schnell wieder steigen, weil viele Investoren die Chance nutzen, die Aktie zu Kursen zu kaufen, die sie nicht mehr erwartet hätten. Die schlechten Aktien erholen sich dagegen erst deutlich später und langsamer.
Arry
NEMO-Trail
Gestern wurde auf clinicaltrials.gov upgedated. Primary outcome data von Oktober 2015 auf September 2015 vorgezogen. Wohl nicht weiter wichtig. ABER: Completion Date wurde von März 2017 ebenfalls auf September 2015 vorgezogen, also um 1,5 Jahre!
Nur ein Fehler? Grund zur Sorge, da Abbruch? Grund zur Freude, da schnelle Beendigung?
Was soll man davon halten?
NEMO-Trail
Gestern wurde auf clinicaltrials.gov upgedated. Primary outcome data von Oktober 2015 auf September 2015 vorgezogen. Wohl nicht weiter wichtig. ABER: Completion Date wurde von März 2017 ebenfalls auf September 2015 vorgezogen, also um 1,5 Jahre!
Nur ein Fehler? Grund zur Sorge, da Abbruch? Grund zur Freude, da schnelle Beendigung?
Was soll man davon halten?
Antwort auf Beitrag Nr.: 50.526.717 von xylophon am 31.08.15 19:41:36Danke für die Einschätzung xylophon!!
TRVN
http://seekingalpha.com/news/2754186-trevenas-iv-pain-med-su…
Results from a Phase 2b clinical trial show that Travena's (NASDAQ:TRVN) lead pain medication candidate, TRV130, was successful in demonstrating a statistically significant reduction in pain over 24 hours compared to placebo in patients with moderate-to-severe pain following abdominoplasty surgery. TRV130 was also superior to morphine in pre-specified secondary measures, showing significantly reduced nausea, vomiting and hypoventilation events while providing comparable pain relief.
Sehr gute News!
TRVN
http://seekingalpha.com/news/2754186-trevenas-iv-pain-med-su…
Results from a Phase 2b clinical trial show that Travena's (NASDAQ:TRVN) lead pain medication candidate, TRV130, was successful in demonstrating a statistically significant reduction in pain over 24 hours compared to placebo in patients with moderate-to-severe pain following abdominoplasty surgery. TRV130 was also superior to morphine in pre-specified secondary measures, showing significantly reduced nausea, vomiting and hypoventilation events while providing comparable pain relief.
Sehr gute News!
Antwort auf Beitrag Nr.: 50.526.723 von lawmeetstax am 31.08.15 19:41:59Arry
Eigene Antwort
Ich habe mal geschaut, in den vergangenen zwei Jahren sind beide Daten wild hin und her gesprungen, häufig waren beide Zeitpunkte auch gleich. Meine Schlußfolgerung daher: unwichtig
Eigene Antwort
Ich habe mal geschaut, in den vergangenen zwei Jahren sind beide Daten wild hin und her gesprungen, häufig waren beide Zeitpunkte auch gleich. Meine Schlußfolgerung daher: unwichtig
Hallo zusammen,
ich habe meine Cashposition jetzt nach und nach aufgelöst. Wahrscheinlich zu früh aber das hätte eine gewisse Tradition. Ich sehe eigentlich bei allen Werten auf Sicht von 2 Jahren Verdopplungspotenzial (wenn es fundamental gut läuft). Eventuelle Gewinne im Biotech Depot würde ich zum Teil auch in die konservativere Assetklasse stecken. Sollten andererseits die Biotechkurse massiv einbrechen würde ich die zweite Assetklasse reduzieren bzw. auflösen...
CLVS 16%
AUPH 12%
MRNS 9%
ESPR 8%
ZFGN 6%
ARQl 5%
TRVN 5%
ARRY 5%
XENE 4%
FGEN 4%
ONTY 3%
OCAT 3%
KPTI 3%
AAVL 1%
Zweite Assetklassen 18% (Bauspar, Dax ETF, Hamborner Reit)
Prozentangaben sind natürlich gerundet...
SG kmastra
ich habe meine Cashposition jetzt nach und nach aufgelöst. Wahrscheinlich zu früh aber das hätte eine gewisse Tradition. Ich sehe eigentlich bei allen Werten auf Sicht von 2 Jahren Verdopplungspotenzial (wenn es fundamental gut läuft). Eventuelle Gewinne im Biotech Depot würde ich zum Teil auch in die konservativere Assetklasse stecken. Sollten andererseits die Biotechkurse massiv einbrechen würde ich die zweite Assetklasse reduzieren bzw. auflösen...
CLVS 16%
AUPH 12%
MRNS 9%
ESPR 8%
ZFGN 6%
ARQl 5%
TRVN 5%
ARRY 5%
XENE 4%
FGEN 4%
ONTY 3%
OCAT 3%
KPTI 3%
AAVL 1%
Zweite Assetklassen 18% (Bauspar, Dax ETF, Hamborner Reit)
Prozentangaben sind natürlich gerundet...
SG kmastra
Antwort auf Beitrag Nr.: 50.544.032 von kmastra am 02.09.15 18:23:01Hi kmastra,
welchen Grund hat es warum du AUPH derart hoch gewichtest? Ist ja absoluter Smallcap-Stock (high risk), wenn auch mit guten Ansätzen.
Auch würde ich gerne deine Meinung zu ZFGN hören, habe mich noch nicht so damit beschäftigt.
Ansonsten schönes Depot und Glückwunsch zu TRVN. Das Ding geht durch die Decke und ist mit aktuell 400 Mio. immer noch nicht teuer bewertet. XENE finde ich auch sehr erfolgsversprechend.
Viele Grüße,
biopadawan
welchen Grund hat es warum du AUPH derart hoch gewichtest? Ist ja absoluter Smallcap-Stock (high risk), wenn auch mit guten Ansätzen.
Auch würde ich gerne deine Meinung zu ZFGN hören, habe mich noch nicht so damit beschäftigt.
Ansonsten schönes Depot und Glückwunsch zu TRVN. Das Ding geht durch die Decke und ist mit aktuell 400 Mio. immer noch nicht teuer bewertet. XENE finde ich auch sehr erfolgsversprechend.
Viele Grüße,
biopadawan
Antwort auf Beitrag Nr.: 50.546.798 von biopadawan am 03.09.15 07:39:56Hallo biopadawan,
ich habe AUPH (und auch MRNS und CLVS) mit Sicherheit irrational hoch gewichtet. Mir gefällt hier das Chance-Risikoverhältnis einfach sehr gut. Zudem bin ich bei AUPH mit meinem Limit bei 3$ zum Zuge gekommen. Natürlich kann es noch tiefer gehen, aber charttechnisch befindet sich hier eine Unterstützung.

Ipollit hatte den Wert hier mal vorgestellt und die Chancen aber auch Risken sehr gut herasugearbeitet:
http://www.wallstreet-online.de/diskussion/1173523-1361-1370…
Die hohe Gewichtung ist natürlich ein großes Risiko. Keinesfalls zur Nachahmung empfohlen, denn hier hängt ja zudem viel an einem Produkt. Ich werde bei der Position aber auch ggf. Gewinne recht schnell mitnehmen. Keinesfalls würde ich mit dieser Größe in den Event (Ergebnisse wohl Ende Q2 16) gehen.
ZFGN gefällt mir sehr gut. Ich hatte schon ein paar mal was dazu geschrieben. Musst du mal googeln. Kurz gesagt haben die ein erstaunlich wiksames Medikament gegen Übergewicht. Da es aber stark in den Stoffwechsel eingreift ist das Risiko unerwünschter Nebenwirkungen nicht zu verachten auch wenn bisher nichts in die Richtung deutet.


Hier ein recht neuer Analystenkommentar:


Zudem ist ZFGN sowas wie ein Charttechnischer Musterschüler!

SG kmastra
ich habe AUPH (und auch MRNS und CLVS) mit Sicherheit irrational hoch gewichtet. Mir gefällt hier das Chance-Risikoverhältnis einfach sehr gut. Zudem bin ich bei AUPH mit meinem Limit bei 3$ zum Zuge gekommen. Natürlich kann es noch tiefer gehen, aber charttechnisch befindet sich hier eine Unterstützung.
Ipollit hatte den Wert hier mal vorgestellt und die Chancen aber auch Risken sehr gut herasugearbeitet:
http://www.wallstreet-online.de/diskussion/1173523-1361-1370…
Die hohe Gewichtung ist natürlich ein großes Risiko. Keinesfalls zur Nachahmung empfohlen, denn hier hängt ja zudem viel an einem Produkt. Ich werde bei der Position aber auch ggf. Gewinne recht schnell mitnehmen. Keinesfalls würde ich mit dieser Größe in den Event (Ergebnisse wohl Ende Q2 16) gehen.
ZFGN gefällt mir sehr gut. Ich hatte schon ein paar mal was dazu geschrieben. Musst du mal googeln. Kurz gesagt haben die ein erstaunlich wiksames Medikament gegen Übergewicht. Da es aber stark in den Stoffwechsel eingreift ist das Risiko unerwünschter Nebenwirkungen nicht zu verachten auch wenn bisher nichts in die Richtung deutet.


Hier ein recht neuer Analystenkommentar:


Zudem ist ZFGN sowas wie ein Charttechnischer Musterschüler!
SG kmastra
Alk und MEK Kombination
arry:Ein interessanter Artikel zur prophylaktischen Gabe von MEK Inhibitoren zusammen mit Alk-Inhibitoren.
Da man weiss, dass der Lungen-Tumor nach Behandlung mit Alk-Inhibitoren oft über Modifikation des RAS/MEK Signalweges ausweicht, hat man erfolgreich versucht, von vornherein MEK mitzublocken.
Interessant ist, dass Novartis einen MEK Inhibitor für ihren Alk-Inhibitoren hätte, Pfizer aber nicht...
http://www.nature.com/nm/journal/vaop/ncurrent/full/nm.3930.…
RAS-MAPK dependence underlies a rational polytherapy strategy in EML4-ALK–positive lung cancer
One strategy for combating cancer-drug resistance is to deploy rational polytherapy up front that suppresses the survival and emergence of resistant tumor cells. Here we demonstrate in models of lung adenocarcinoma harboring the oncogenic fusion of ALK and EML4 that the GTPase RAS–mitogen-activated protein kinase (MAPK) pathway, but not other known ALK effectors, is required for tumor-cell survival. EML4-ALK activated RAS-MAPK signaling by engaging all three major RAS isoforms through the HELP domain of EML4. Reactivation of the MAPK pathway via either a gain in the number of copies of the gene encoding wild-type K-RAS (KRASWT) or decreased expression of the MAPK phosphatase DUSP6 promoted resistance to ALK inhibitors in vitro, and each was associated with resistance to ALK inhibitors in individuals with EML4-ALK–positive lung adenocarcinoma. Upfront inhibition of both ALK and the kinase MEK enhanced both the magnitude and duration of the initial response in preclinical models of EML4-ALK lung adenocarcinoma. Our findings identify RAS-MAPK dependence as a hallmark of EML4-ALK lung adenocarcinoma and provide a rationale for the upfront inhibition of both ALK and MEK to forestall resistance and improve patient outcomes.
Hier ein sehr informatives Interview mit dem Chef von Ohad Hammer bei Pontifax, Nussbaum:
http://www.thelifesciencesreport.com/pub/na/16756
Die dort diskutierten Biotechs und Sichtweisen sind wirklich sehr interessant, aber die auffälligen Übereinstimmungen mit Hammers Blog lassen auch ein bißchen die Schlufolgerung zu, daß es beim Blog nicht nur um rein private Interessen geht...
http://www.thelifesciencesreport.com/pub/na/16756
Die dort diskutierten Biotechs und Sichtweisen sind wirklich sehr interessant, aber die auffälligen Übereinstimmungen mit Hammers Blog lassen auch ein bißchen die Schlufolgerung zu, daß es beim Blog nicht nur um rein private Interessen geht...
Antwort auf Beitrag Nr.: 50.562.143 von lawmeetstax am 04.09.15 22:05:42Sehr schöner Fund!
(Was den Blog angeht sehe ich es so, dass sich hier berufliche und private Interessen insofern verbinden, als Hammer durch den Beruf vertiefte Einblicke bekommt und dass sich das dann zum Teil in seinem Blog widerspiegelt. Den Versuch eines "front runnings" sehe ich aber nicht. Ich bin manchmal sogar frustriert, dass er bestimmte Themen nicht behandelt, wenn Pontifax in solchen Unternehmen investiert ist. Durch das KITE-Investment von Pontifax ist ja bspw. das gesamte Themengebiet CAR-T/TCR im Blog tot und tabu - was wirklich einfach nur unendlich schade ist.
btw - mir scheint Nussbaum aggressiver zu sein, als Hammer, oder?)
(Was den Blog angeht sehe ich es so, dass sich hier berufliche und private Interessen insofern verbinden, als Hammer durch den Beruf vertiefte Einblicke bekommt und dass sich das dann zum Teil in seinem Blog widerspiegelt. Den Versuch eines "front runnings" sehe ich aber nicht. Ich bin manchmal sogar frustriert, dass er bestimmte Themen nicht behandelt, wenn Pontifax in solchen Unternehmen investiert ist. Durch das KITE-Investment von Pontifax ist ja bspw. das gesamte Themengebiet CAR-T/TCR im Blog tot und tabu - was wirklich einfach nur unendlich schade ist.
btw - mir scheint Nussbaum aggressiver zu sein, als Hammer, oder?)
Antwort auf Beitrag Nr.: 50.562.143 von lawmeetstax am 04.09.15 22:05:42Hallo lawmeetstax,
ich möchte dir da ganz entschieden widersprechen. Eine gewisse kritische Distanz ist natürlich immer gut.
Hier gehst du mit deiner Schlussfolgerung aber m. E. zu weit!
Früher hat auch Ohad Hammer bei Sekking-Alpha geschrieben. Im ersten Artikel zum Depot steht:
In order to put this approach to the test, I asked Pontifax’s Ran Nussbaum for his help in building a virtual portfolio of promising biotech stocks. This portfolio is not intended for short term trading, but for long term investment of at least several years. Although we do not expect active trading in this portfolio, from time to time there may be changes as additional stocks will be added and existing holdings may be sold. Any future changes can be made only when markets are closed. On a more cautionary note, regardless of the attractiveness of all of these companies, all the inherent risks associated with biotech remain, including long time to market and statistically low success rates.
http://seekingalpha.com/article/99363-when-theres-blood-in-t…
Von daher lassen sich die Übereinstimmungen leicht erklären. Auch die Formulierung "when there is blood on the streets buy biotech stocks" findet sich da wieder. Ich geh davon aus, dass die beiden das Depot immer noch zusammen managen, während Ohad die Artikel schreibt und auch die Fragen beantwortet.
"We are selling one of two positions in Seattle Genetics"...
Zudem ist es ja so, dass Ohad Hammer auf einige Fragen gar nicht erst antwortet, damit er eben in keinen Interessenkonflikt kommt (ARNI, das Thema CART, israelische Firmen). Ran Nussbaum sieht es da wohl nicht so eng...
Pontifax ist, so wie ich es verstehe auch kein Aktienfonds sondern eine Beratungsfirma, die sich insbesondere auf Start Ups spezialisiert hat, die oft noch gar nicht an der Börse sind.
Ohad Hammer hat wohl aber ein privates Depot. Es ist davon auszugehen, dass sich die Werte darin wiederfinden. Für mich gibt es überhaupt keinen Anlass Ohad Hammers Motive irgendwie in Frage zu stellen...
Es gab schon 2 weitere Interviews mit Ran Nussbaum:
http://www.thelifesciencesreport.com/pub/htdocs/expert.html?…
SG kmastra
ich möchte dir da ganz entschieden widersprechen. Eine gewisse kritische Distanz ist natürlich immer gut.
Hier gehst du mit deiner Schlussfolgerung aber m. E. zu weit!
Früher hat auch Ohad Hammer bei Sekking-Alpha geschrieben. Im ersten Artikel zum Depot steht:
In order to put this approach to the test, I asked Pontifax’s Ran Nussbaum for his help in building a virtual portfolio of promising biotech stocks. This portfolio is not intended for short term trading, but for long term investment of at least several years. Although we do not expect active trading in this portfolio, from time to time there may be changes as additional stocks will be added and existing holdings may be sold. Any future changes can be made only when markets are closed. On a more cautionary note, regardless of the attractiveness of all of these companies, all the inherent risks associated with biotech remain, including long time to market and statistically low success rates.
http://seekingalpha.com/article/99363-when-theres-blood-in-t…
Von daher lassen sich die Übereinstimmungen leicht erklären. Auch die Formulierung "when there is blood on the streets buy biotech stocks" findet sich da wieder. Ich geh davon aus, dass die beiden das Depot immer noch zusammen managen, während Ohad die Artikel schreibt und auch die Fragen beantwortet.
"We are selling one of two positions in Seattle Genetics"...
Zudem ist es ja so, dass Ohad Hammer auf einige Fragen gar nicht erst antwortet, damit er eben in keinen Interessenkonflikt kommt (ARNI, das Thema CART, israelische Firmen). Ran Nussbaum sieht es da wohl nicht so eng...
Pontifax ist, so wie ich es verstehe auch kein Aktienfonds sondern eine Beratungsfirma, die sich insbesondere auf Start Ups spezialisiert hat, die oft noch gar nicht an der Börse sind.
Ohad Hammer hat wohl aber ein privates Depot. Es ist davon auszugehen, dass sich die Werte darin wiederfinden. Für mich gibt es überhaupt keinen Anlass Ohad Hammers Motive irgendwie in Frage zu stellen...
Es gab schon 2 weitere Interviews mit Ran Nussbaum:
http://www.thelifesciencesreport.com/pub/htdocs/expert.html?…
SG kmastra
Antwort auf Beitrag Nr.: 50.563.415 von kmastra am 05.09.15 10:39:18Hallo Leute,
wie seht ihr diese Sache mit Arno?
Abgesehen davon, dass sie ein OTC-Pennystock sind, hatten sie am 30.06.2015 noch 2,3 Mio. USD Cash.
Der Cashverbrauch im ersten Halbjahr lag bei 5,5 Mio. USD, als etwas mehr als 2 Mio. pro Quartal.
http://www.sec.gov/Archives/edgar/data/1195116/0001144204150…
Ich kann nicht erkennen, dass seitdem irgendwie neues Geld aufgetrieben wurde. Wenn dies nicht in kürzester Zeit passiert, sind sie insolvent.
Wenn sie bankrott gehen, wer wird dann die Rechte an ihren Wirkstoffkandidaten erhalten? Wahrscheinlich doch die Fremdkapitalgeber, oder?
Kommt mir sehr suspekt vor...
wie seht ihr diese Sache mit Arno?
Abgesehen davon, dass sie ein OTC-Pennystock sind, hatten sie am 30.06.2015 noch 2,3 Mio. USD Cash.
Der Cashverbrauch im ersten Halbjahr lag bei 5,5 Mio. USD, als etwas mehr als 2 Mio. pro Quartal.
http://www.sec.gov/Archives/edgar/data/1195116/0001144204150…
Ich kann nicht erkennen, dass seitdem irgendwie neues Geld aufgetrieben wurde. Wenn dies nicht in kürzester Zeit passiert, sind sie insolvent.
Wenn sie bankrott gehen, wer wird dann die Rechte an ihren Wirkstoffkandidaten erhalten? Wahrscheinlich doch die Fremdkapitalgeber, oder?
Kommt mir sehr suspekt vor...
Antwort auf Beitrag Nr.: 50.563.985 von SLGramann am 05.09.15 13:31:47Hallo SLGramann,
ARNI ist auf jeden Fall extrem spekulativ. Ich hatte mich mal vor gut zwei Jahren ein wenig mit der Aktie beschäftigt (weil Ran Nussbum sie damals schon empfohlen hatte). Man darf auf keinen Fall den Fehler machen, die Angabe der Marktkapitalisierung z.B. auf yahoo zu glauben. ANRI hatte 2013 eine Kapitalmaßnahme gemacht und den Kurs über warrants im Grunde stark verwässert. So richtig hab ich das Prinzip nicht verstanden aber es sind wohl so Art Otionsscheine.
Ob Substanz vorhanden ist kann ich nicht beurteilen. Die Ergebnisse fand ich bisher eher nicht besonders berauschend. Für die Aktie spricht sicherlich am ehesten, dass eine Menge Experten scheinbar viel davon halten (CEO Opko, CEO Kite, Pontifax)
Ohad Hammer hat ja immer jeglichen Kommentar verweigert. Auffällig finde ich in der Tat, dass Informationen zu der Aktie vor allem über die Seite lifesciencereport zu finden sind.
http://www.thelifesciencesreport.com/pub/na/three-new-picks-…
http://www.thelifesciencesreport.com/pub/na/venture-capitali…
http://www.thelifesciencesreport.com/pub/na/arno-therapeutic…
http://www.thelifesciencesreport.com/pub/na/buy-biotech-when…
http://www.thelifesciencesreport.com/pub/na/bring-on-the-orp…
http://www.thelifesciencesreport.com/pub/na/do-the-math-ram-…
Was bei einer Pleite passiert weiß ich auch nicht. Die Gefahr ist sicherlich da. Ich persönlich fühle mich in der Risikoregion mit z.B. ARQL oder AUPH wohler...
SG kmastra
ARNI ist auf jeden Fall extrem spekulativ. Ich hatte mich mal vor gut zwei Jahren ein wenig mit der Aktie beschäftigt (weil Ran Nussbum sie damals schon empfohlen hatte). Man darf auf keinen Fall den Fehler machen, die Angabe der Marktkapitalisierung z.B. auf yahoo zu glauben. ANRI hatte 2013 eine Kapitalmaßnahme gemacht und den Kurs über warrants im Grunde stark verwässert. So richtig hab ich das Prinzip nicht verstanden aber es sind wohl so Art Otionsscheine.
Ob Substanz vorhanden ist kann ich nicht beurteilen. Die Ergebnisse fand ich bisher eher nicht besonders berauschend. Für die Aktie spricht sicherlich am ehesten, dass eine Menge Experten scheinbar viel davon halten (CEO Opko, CEO Kite, Pontifax)
Ohad Hammer hat ja immer jeglichen Kommentar verweigert. Auffällig finde ich in der Tat, dass Informationen zu der Aktie vor allem über die Seite lifesciencereport zu finden sind.
http://www.thelifesciencesreport.com/pub/na/three-new-picks-…
http://www.thelifesciencesreport.com/pub/na/venture-capitali…
http://www.thelifesciencesreport.com/pub/na/arno-therapeutic…
http://www.thelifesciencesreport.com/pub/na/buy-biotech-when…
http://www.thelifesciencesreport.com/pub/na/bring-on-the-orp…
http://www.thelifesciencesreport.com/pub/na/do-the-math-ram-…
Was bei einer Pleite passiert weiß ich auch nicht. Die Gefahr ist sicherlich da. Ich persönlich fühle mich in der Risikoregion mit z.B. ARQL oder AUPH wohler...
SG kmastra
Clovis
was ist denn da heute los, keine Nachrichten und ordentlicher Anstieg bei hohem Volumen.Ist das eine Präsentation auf dem Kongress, die da für Kauflaune sorgt?
Antwort auf Beitrag Nr.: 50.589.863 von question-mark am 09.09.15 17:12:36Doch, es gibt "indirekte" Nachrichten von der Konkurrenz:
Data on two AURA Phase II studies (AURA extension and AURA2) in previously treated patients with EGFR T790M mutation were also presented. While still preliminary, these studies showed an efficacy and tolerability profile for AZD9291 consistent with previously reported data. In AURA extension (n=201), ORR was 61% (95% CI 54% to 68%); median DoR and median PFS were not calculable (NC). Consistent results were observed in AURA2 (n=210), ORR was 71% (95% CI 64% to 77%); median DoR was 7.8 months (95% CI 7.1 months to NC) and median PFS was 8.6 months (95% CI 8.3 months to 9.7 months).
http://www.businesswire.com/news/home/20150908006803/en/Astr…
Das Gedröhne von AZN hinsichtlich einer angeblichen Überlegenheit ihres Kandidaten gegenüber Clovis Roci löst sich mehr und mehr in Luft auf.
Nachdem sich schon das angeblich so viel bessere NW-Profil als haltlose PR-Behauptung erwiesen hat, ist man jetzt auch bei PFS offenbar nicht mehr besser als Roci - und das trotz eines fragwürdigen und tendenziell positiv verfälschenden Studiendesigns.
Mich würde es nicht wundern, wenn der Markt in der nächsten Zeit sein Szenario komplett drehen wird. Nicht CLVS hat das Nischenprodukt, sondern AZN.
Data on two AURA Phase II studies (AURA extension and AURA2) in previously treated patients with EGFR T790M mutation were also presented. While still preliminary, these studies showed an efficacy and tolerability profile for AZD9291 consistent with previously reported data. In AURA extension (n=201), ORR was 61% (95% CI 54% to 68%); median DoR and median PFS were not calculable (NC). Consistent results were observed in AURA2 (n=210), ORR was 71% (95% CI 64% to 77%); median DoR was 7.8 months (95% CI 7.1 months to NC) and median PFS was 8.6 months (95% CI 8.3 months to 9.7 months).
http://www.businesswire.com/news/home/20150908006803/en/Astr…
Das Gedröhne von AZN hinsichtlich einer angeblichen Überlegenheit ihres Kandidaten gegenüber Clovis Roci löst sich mehr und mehr in Luft auf.
Nachdem sich schon das angeblich so viel bessere NW-Profil als haltlose PR-Behauptung erwiesen hat, ist man jetzt auch bei PFS offenbar nicht mehr besser als Roci - und das trotz eines fragwürdigen und tendenziell positiv verfälschenden Studiendesigns.
Mich würde es nicht wundern, wenn der Markt in der nächsten Zeit sein Szenario komplett drehen wird. Nicht CLVS hat das Nischenprodukt, sondern AZN.
Antwort auf Beitrag Nr.: 50.590.190 von SLGramann am 09.09.15 17:41:14CLVS
Stimmt, der angebliche Wirksamkeits-Vorteil von AZD9291 schwindet. Dies noch vor dem Hintergrund, dass AZN seine Studien hauptsächlich im asiatischen Raum durchgeführt hat und dort ohnehin die Ansprechraten höher ausfallen sollten.


Gab es nicht auch noch ein paar neue Details von CLVS selber?... z.B. ein Update der T790m- Daten?
http://finance.yahoo.com/mbview/threadview/?&bn=e626e6c2-694…
"windsor thanks for pointing that out. rociletinib continues to demonstrate strong activity against T790 negative disease ORR ~ 40%. they have identified combination therapy to extend use of rociletinib in those whom have developed resistance. development of roci is progressing nicely. windsor, what are your thoughts?
***
In 64 plasma T790M negative patients a 35% or greater shrinkage in the tumor from baseline (ORR) occurred in 29(45%) of patients. This is the new data. The 37 tissue T790M negative patients have been reported before (except for two) and an ORR occurred in 14 (38%). What is significant in this group is that their lesions continue to shrink beyond that previously reported. This is evident in comparing the waterfall charts.
The plasma T790M positive results reported at ASCO had 147 patients with an ORR of 53%.
The disease control rate (DCR) throughout the plasma T790M positive and negative patient population was 82% to 83%, respectively.
It would appear that Clovis Oncology's rociletinib can be used to treat patients with nsclc regardless of the patient's T790M status and is singular in its effect..
These data are both compelling and remarkable.
Hier sind die entsprechenden Folien zu finden...
http://clovisoncology.com/products-companion-diagnostics/sci…
ORR bei T790M- scheint weiter zu steigen, zumindest wenn man sich die Plasma-Daten ansieht. Plasma-Tests sind vielleicht noch brauchbarer als Gewebe-Tests und zudem wohl leichter durchzuführen.
Grundsätzlich nähert sich die T790m- Wirkung der T790m+ Wirkung. Daher stellt sich die Frage, wofür man überhaupt auf T790m testen sollte. Das macht nur Sinn, wenn man AZD9291 als Option sieht, das wohl nur bei T790+ wirkt. Stattdessen könnte man sich die Zeit und Kosten für den Test sparen und generell Roci nach einem 1st-line EGFR anwenden unabhängig von T790m+/-. Ob nach Roci AZD9291 noch etwas bewirkt, ist unklar, da der Krebs nach einer Resistenz gegen Roci auch T790m- ist.
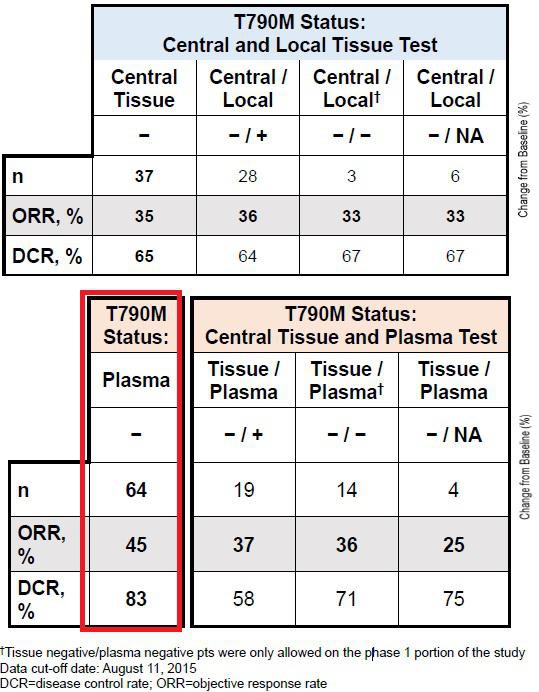

Nicht gerade neu, aber trotzdem nochmal... Roci + MET-Hemmer oder Roci + MEK-Hemmer könnten weiteren Resistenzen vorbeugen.
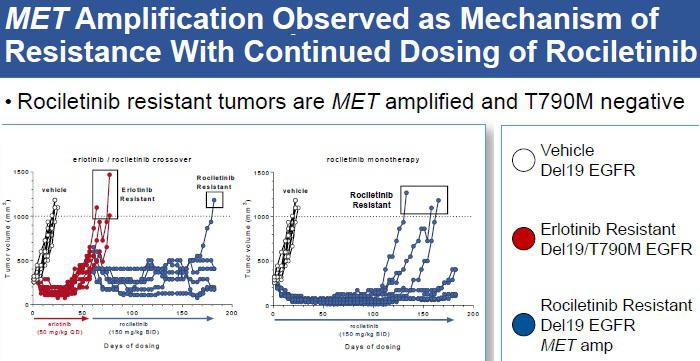
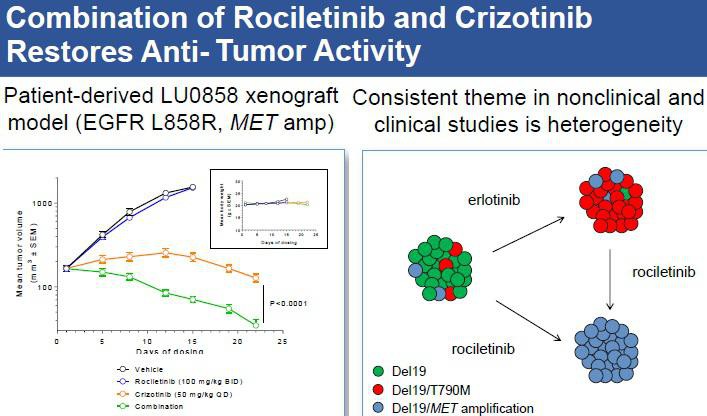
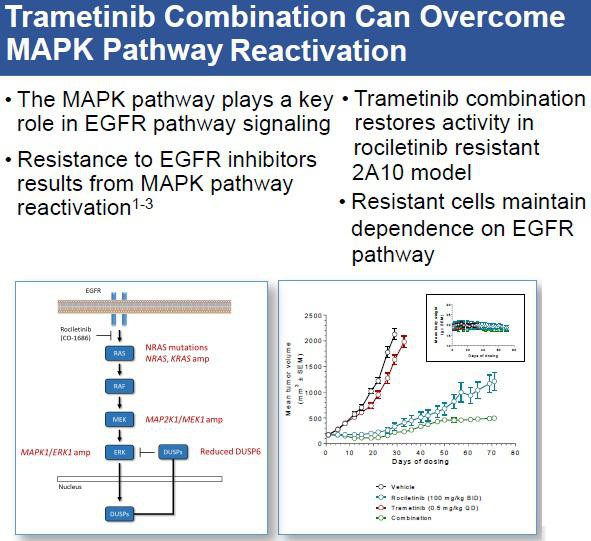

Gruß
ipollit
Stimmt, der angebliche Wirksamkeits-Vorteil von AZD9291 schwindet. Dies noch vor dem Hintergrund, dass AZN seine Studien hauptsächlich im asiatischen Raum durchgeführt hat und dort ohnehin die Ansprechraten höher ausfallen sollten.


Gab es nicht auch noch ein paar neue Details von CLVS selber?... z.B. ein Update der T790m- Daten?
http://finance.yahoo.com/mbview/threadview/?&bn=e626e6c2-694…
"windsor thanks for pointing that out. rociletinib continues to demonstrate strong activity against T790 negative disease ORR ~ 40%. they have identified combination therapy to extend use of rociletinib in those whom have developed resistance. development of roci is progressing nicely. windsor, what are your thoughts?
***
In 64 plasma T790M negative patients a 35% or greater shrinkage in the tumor from baseline (ORR) occurred in 29(45%) of patients. This is the new data. The 37 tissue T790M negative patients have been reported before (except for two) and an ORR occurred in 14 (38%). What is significant in this group is that their lesions continue to shrink beyond that previously reported. This is evident in comparing the waterfall charts.
The plasma T790M positive results reported at ASCO had 147 patients with an ORR of 53%.
The disease control rate (DCR) throughout the plasma T790M positive and negative patient population was 82% to 83%, respectively.
It would appear that Clovis Oncology's rociletinib can be used to treat patients with nsclc regardless of the patient's T790M status and is singular in its effect..
These data are both compelling and remarkable.
Hier sind die entsprechenden Folien zu finden...
http://clovisoncology.com/products-companion-diagnostics/sci…
ORR bei T790M- scheint weiter zu steigen, zumindest wenn man sich die Plasma-Daten ansieht. Plasma-Tests sind vielleicht noch brauchbarer als Gewebe-Tests und zudem wohl leichter durchzuführen.
Grundsätzlich nähert sich die T790m- Wirkung der T790m+ Wirkung. Daher stellt sich die Frage, wofür man überhaupt auf T790m testen sollte. Das macht nur Sinn, wenn man AZD9291 als Option sieht, das wohl nur bei T790+ wirkt. Stattdessen könnte man sich die Zeit und Kosten für den Test sparen und generell Roci nach einem 1st-line EGFR anwenden unabhängig von T790m+/-. Ob nach Roci AZD9291 noch etwas bewirkt, ist unklar, da der Krebs nach einer Resistenz gegen Roci auch T790m- ist.


Nicht gerade neu, aber trotzdem nochmal... Roci + MET-Hemmer oder Roci + MEK-Hemmer könnten weiteren Resistenzen vorbeugen.




Gruß
ipollit
ZSPH, RLYP
Actelion soll angeblich Interesse an ZSPH haben... 2,5 Mrd USD könnten 100 USD sein, wenn nicht weitere Dinge eingerechnet werden.
http://www.bloomberg.com/news/articles/2015-09-10/actelion-s…
Actelion Ltd. Chief Executive Officer Jean-Paul Clozel made a preliminary offer last month to buy ZS Pharma Inc. in a deal that would value the U.S. company at about $2.5 billion, people with knowledge of the matter said.
It is unclear how ZS responded or if there have been discussions between the two companies, said one of the people, who asked not to be identified because the information is private. Actelion is assessing a number of potential acquisitions and is not wedded to any particular deal, another person said.
ZSPH hat im Mai die Zulassung von ZS-9 bei der FDA beantragt.
Vielleicht könnte auch noch Novartis Interesse haben... "$ZSPH I still would not be surprised to see $NVS enter the fray. Perfect pairing with Entresto where >10% will stop due to hyperkalemia." Entresto ist das neue Herzmittel von NVS... soll ein Blockbuster mit 5+ Mrd USD werden.
Für PLYP's Konkurrenzprodukt Patiromer steht bald die FDA-Zulassung an... PDFUA ist der 21.10. Sie haben in den USA einen Deal mit Sanofi, die beim Vertrieb von Patiromer unterstützen. RLYP besitzt aber noch alle Rechte in den USA. In Europa haben sie einen Deal mit Fresenius und erhalten Royalties. Beide Partner sind in den entsprechenden Märkten führend.


Gruß
ipollit
Actelion soll angeblich Interesse an ZSPH haben... 2,5 Mrd USD könnten 100 USD sein, wenn nicht weitere Dinge eingerechnet werden.
http://www.bloomberg.com/news/articles/2015-09-10/actelion-s…
Actelion Ltd. Chief Executive Officer Jean-Paul Clozel made a preliminary offer last month to buy ZS Pharma Inc. in a deal that would value the U.S. company at about $2.5 billion, people with knowledge of the matter said.
It is unclear how ZS responded or if there have been discussions between the two companies, said one of the people, who asked not to be identified because the information is private. Actelion is assessing a number of potential acquisitions and is not wedded to any particular deal, another person said.
ZSPH hat im Mai die Zulassung von ZS-9 bei der FDA beantragt.
Vielleicht könnte auch noch Novartis Interesse haben... "$ZSPH I still would not be surprised to see $NVS enter the fray. Perfect pairing with Entresto where >10% will stop due to hyperkalemia." Entresto ist das neue Herzmittel von NVS... soll ein Blockbuster mit 5+ Mrd USD werden.
Für PLYP's Konkurrenzprodukt Patiromer steht bald die FDA-Zulassung an... PDFUA ist der 21.10. Sie haben in den USA einen Deal mit Sanofi, die beim Vertrieb von Patiromer unterstützen. RLYP besitzt aber noch alle Rechte in den USA. In Europa haben sie einen Deal mit Fresenius und erhalten Royalties. Beide Partner sind in den entsprechenden Märkten führend.
Gruß
ipollit
AKBA, FGEN
Ergänzend zu FGEN habe ich mir nun auch eine Position AKBA zugelegt. HIFs könnten ein großes Marktpotential besitzen (im 5-10 Mrd USD Bereich). FGEN hat zwar einen größeren zeitlichen Vorsprung und sehr gute Partner, doch ist die MK von AKBA noch recht gering mit 280 Mio USD bei gleichzeitig 100% der Rechte. Meine Position ist allerdings deutlich kleiner als die von FGEN, da AKBA größeres Risiko beinhaltet und FGEN zudem mit dem CTGF-AK FG-3019 einen weiteren interessanten Kandidaten in der Pipeline hat (btw... FG-3019 könnte nach letzten Daten auch gegen die schwerwiegende Muskelerkrankung DMD wirksam sein).
"Brean Capital analyst Jonathan Aschoff reiterated a Buy rating and boosted his price target on Akebia Therapeutics (NASDAQ: AKBA) to $26.00 (from $18.00) after vadadustat proved potent and safe in dialysis setting.
Aschoff commented, "Akebia released positive top-line data from its open-label Phase 2 trial of vadadustat in anemia related to CKD in patients undergoing dialysis. We are raising our target price to $26 from $18 to reflect our reduction in risk assessed to vadadustat development. In addition to the clear potency demonstrated at all three dosing regimens in patients switched from ESA therapy, the clean safety profile goes a long way, in our view, toward reversing CV concerns from the Phase 2 trial in anemia related to CKD in predialysis patients. In our view, the current dialysis setting’s composition of sicker patients than a predialysis setting should be a better arena for safety concerns to surface, but the absence of adverse event data in support of these concerns underscores our view that preexisting patient conditions in the predialysis trial drove any observed imbalance in death and MACE. In the dialysis trial, there were no drug-related SAEs despite the SAEs reported in 13 of the 94 patients (well within the expected range), and TEAEs were well balanced across all dosing cohorts. This outcome increases our confidence in Phase 3 success, where we expect hemoglobin maintenance as a primary efficacy endpoint and MACE as a primary safety endpoint."
Hier sind ein paar Details zu AKBA...
http://seekingalpha.com/article/3490866-addressing-6-misconc…
Addressing 6 Misconceptions About Akebia, A Highly Undervalued Biotech


Gruß
ipollit
Ergänzend zu FGEN habe ich mir nun auch eine Position AKBA zugelegt. HIFs könnten ein großes Marktpotential besitzen (im 5-10 Mrd USD Bereich). FGEN hat zwar einen größeren zeitlichen Vorsprung und sehr gute Partner, doch ist die MK von AKBA noch recht gering mit 280 Mio USD bei gleichzeitig 100% der Rechte. Meine Position ist allerdings deutlich kleiner als die von FGEN, da AKBA größeres Risiko beinhaltet und FGEN zudem mit dem CTGF-AK FG-3019 einen weiteren interessanten Kandidaten in der Pipeline hat (btw... FG-3019 könnte nach letzten Daten auch gegen die schwerwiegende Muskelerkrankung DMD wirksam sein).
"Brean Capital analyst Jonathan Aschoff reiterated a Buy rating and boosted his price target on Akebia Therapeutics (NASDAQ: AKBA) to $26.00 (from $18.00) after vadadustat proved potent and safe in dialysis setting.
Aschoff commented, "Akebia released positive top-line data from its open-label Phase 2 trial of vadadustat in anemia related to CKD in patients undergoing dialysis. We are raising our target price to $26 from $18 to reflect our reduction in risk assessed to vadadustat development. In addition to the clear potency demonstrated at all three dosing regimens in patients switched from ESA therapy, the clean safety profile goes a long way, in our view, toward reversing CV concerns from the Phase 2 trial in anemia related to CKD in predialysis patients. In our view, the current dialysis setting’s composition of sicker patients than a predialysis setting should be a better arena for safety concerns to surface, but the absence of adverse event data in support of these concerns underscores our view that preexisting patient conditions in the predialysis trial drove any observed imbalance in death and MACE. In the dialysis trial, there were no drug-related SAEs despite the SAEs reported in 13 of the 94 patients (well within the expected range), and TEAEs were well balanced across all dosing cohorts. This outcome increases our confidence in Phase 3 success, where we expect hemoglobin maintenance as a primary efficacy endpoint and MACE as a primary safety endpoint."
Hier sind ein paar Details zu AKBA...
http://seekingalpha.com/article/3490866-addressing-6-misconc…
Addressing 6 Misconceptions About Akebia, A Highly Undervalued Biotech
Gruß
ipollit
auch schön... CLVS und INCY heute jeweils mit neuen Allzeithochs


Gruß
ipollit
Gruß
ipollit
ZSPH wurde angehalten... mmm, ist an den Gerüchten nun etwas dran oder nicht? 

Antwort auf Beitrag Nr.: 50.600.516 von ipollit am 10.09.15 22:44:11Actelion hat die Gerüchte bestätigt insofern, dass Gespräche für eine Übernahme von ZSPH laufen... also noch nichts definitives.
Gruß
ipollit
Gruß
ipollit
GILD
hier könnte es auch spannend werden. Anscheinend nimmt GILD gerade 10 Mrd USD Cash auf und das, obwohl sie bereits über hohe Reserven verfügen (müssten aufgrund der hohen Gewinne im 2-stelligen Mrd Bereich aktuell locker über 10 Mrd USD sein). Es wird ja schon länger darüber spekuliert, ob der größte Biotech nicht auch mal wieder im M&A Bereich aktiv werden müsste. Vielleicht kommt es ja demnächst zu einer großen Übernahme.
http://www.fiercebiotech.com/story/gilead-banks-10b-stirring…
Gilead banks $10B, stirring fresh buzz about a blockbuster buyout
...Gilead's last quarterly call with analysts was highlighted by CEO John Martin's flirtatious remark that the company is "taking suggestions" about what it should buy. And with no hard hit list to contemplate, analysts have suggested the likes of Vertex ($VRTX), Incyte ($INCY), BioMarin ($BMRN), Medivation ($MDVN) and Alexion ($ALXN).
President John Milligan, though, essentially said that everything is on the table...
Gruß
ipollit
hier könnte es auch spannend werden. Anscheinend nimmt GILD gerade 10 Mrd USD Cash auf und das, obwohl sie bereits über hohe Reserven verfügen (müssten aufgrund der hohen Gewinne im 2-stelligen Mrd Bereich aktuell locker über 10 Mrd USD sein). Es wird ja schon länger darüber spekuliert, ob der größte Biotech nicht auch mal wieder im M&A Bereich aktiv werden müsste. Vielleicht kommt es ja demnächst zu einer großen Übernahme.
http://www.fiercebiotech.com/story/gilead-banks-10b-stirring…
Gilead banks $10B, stirring fresh buzz about a blockbuster buyout
...Gilead's last quarterly call with analysts was highlighted by CEO John Martin's flirtatious remark that the company is "taking suggestions" about what it should buy. And with no hard hit list to contemplate, analysts have suggested the likes of Vertex ($VRTX), Incyte ($INCY), BioMarin ($BMRN), Medivation ($MDVN) and Alexion ($ALXN).
President John Milligan, though, essentially said that everything is on the table...
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.600.411 von ipollit am 10.09.15 22:35:29Hallo ipollit,
habe mir auch eine Position AKBA zugelegt. Wie schätzt du hier die kurzfristigen Chancen ein? Könnte sein, dass AKBA wegen einer Kapitalerhöhung (selbiges sieht man ja bei TRVN) und auch der Suche nach einem Partner etwas in straucheln gerät. Der Abverkauf über 14-15% auf 9,8 hat mich schon etwas überrascht. Single Digits war etwas woran, ich eigentlich nicht mehr geglaubt habe. Hätte ich noch Kapital zur Verfügung, würde ich nochmals zukaufen.
Die Aktie stand früher schon bei $20-30 (ohne diese sensationellen News). Einziger Grund des Abverkaufs über die letzte Zeit war meiner Meinung nach, dass der Kurs wegen der möglichen "Safety Issues" gedrückt wurde. Diese Zweifel wurden aber vollumfänglich ausgeräumt, die Daten sind absolut top.
Das Produkt selber ist sicherlich mit dem von FGEN vergleichbar, so dass wir eine Bewertung von $1600m zu $280m haben. Schon ein krasser Gap, der sicherlich nicht gerechtfertigt ist, nur weil FGEN 12-18 Monate mit dem Produkt voran ist. Wie siehst du das?
Ansonsten geht zur Zeit ja ziemlich die Post ab, bin gespannt wenn GILD kauft.
Viele Grüße
habe mir auch eine Position AKBA zugelegt. Wie schätzt du hier die kurzfristigen Chancen ein? Könnte sein, dass AKBA wegen einer Kapitalerhöhung (selbiges sieht man ja bei TRVN) und auch der Suche nach einem Partner etwas in straucheln gerät. Der Abverkauf über 14-15% auf 9,8 hat mich schon etwas überrascht. Single Digits war etwas woran, ich eigentlich nicht mehr geglaubt habe. Hätte ich noch Kapital zur Verfügung, würde ich nochmals zukaufen.
Die Aktie stand früher schon bei $20-30 (ohne diese sensationellen News). Einziger Grund des Abverkaufs über die letzte Zeit war meiner Meinung nach, dass der Kurs wegen der möglichen "Safety Issues" gedrückt wurde. Diese Zweifel wurden aber vollumfänglich ausgeräumt, die Daten sind absolut top.
Das Produkt selber ist sicherlich mit dem von FGEN vergleichbar, so dass wir eine Bewertung von $1600m zu $280m haben. Schon ein krasser Gap, der sicherlich nicht gerechtfertigt ist, nur weil FGEN 12-18 Monate mit dem Produkt voran ist. Wie siehst du das?
Ansonsten geht zur Zeit ja ziemlich die Post ab, bin gespannt wenn GILD kauft.
Viele Grüße
Antwort auf Beitrag Nr.: 50.600.927 von ipollit am 10.09.15 23:35:43"Es wird ja schon länger darüber spekuliert, ob der größte Biotech nicht auch mal wieder im M&A Bereich aktiv werden müsste."
Ich denke schon, dass das klug wäre. Sie müssen ihre Pipeline diversifizieren und langfristiges Umsatzwachstum sichern.
Wer könnte das Ziel sein?
GILD hatten zum 30.06.2015 mehr als 14 Milliarden Dollar Cash in der Bilanz. Bis zum Jahresende sind es vermutlich 18 Milliarden (mindestens!).
Dazu jetzt Bonds über 10 Milliarden.
Die Kriegskasse ist demnach sicher ungefähr 30 Mrd. schwer - ohne weitere Kapitalmaßnahmen, die natürlich immer möglich sind.
Für wahrscheinlich halte ich aber eigentlich nur ein Ziel, dass zwischen 10 und 20 Milliarden kosten würde.
Natürlich kommen einem schnell die "üblichen Verdächtigen" in den Sinn, wenn man ein Übernahmeziel denkt.
Ich wäre aber nicht überrascht, wenn uns GILD mit etwas Unerwartetem überrascht. Bei der Pharmasset-Übernahme haben sie bewiesen, dass sie "verrückte" Preise zu zahlen bereit sind, was sich dann doch als ein riesen Deal für GILD entpuppte.
Bei der Pharmasset-Übernahme haben sie bewiesen, dass sie "verrückte" Preise zu zahlen bereit sind, was sich dann doch als ein riesen Deal für GILD entpuppte.
Ich denke, dass ein Übernahmeziel aus der Sicht von GILD eine sehr hohe Wahrscheinlichkeit aufweisen muss, in absehbarer Zukunft viele Milliarden Umsatz einzuspielen und/oder einen bestimmten technologischen Bereich dominieren muss (was auch bedeutet, dass sie 100% der Rechte an ihrer Technologie und ihren Produkten halten müssen).
Falls GILD zu der Überzeugung kommen würde, dass bspw. BLUE eine echte Breakthrough-Technologie in den Händen halten würde (was ich für möglich halte, es aber natürlich nicht wirklich einschätzen kann), dann wäre das aus meiner Sicht beispielsweise ein guter Übernahmekandidat.
Aber vielleicht überraschen sie uns alle komplett.
Ich denke schon, dass das klug wäre. Sie müssen ihre Pipeline diversifizieren und langfristiges Umsatzwachstum sichern.
Wer könnte das Ziel sein?
GILD hatten zum 30.06.2015 mehr als 14 Milliarden Dollar Cash in der Bilanz. Bis zum Jahresende sind es vermutlich 18 Milliarden (mindestens!).
Dazu jetzt Bonds über 10 Milliarden.
Die Kriegskasse ist demnach sicher ungefähr 30 Mrd. schwer - ohne weitere Kapitalmaßnahmen, die natürlich immer möglich sind.
Für wahrscheinlich halte ich aber eigentlich nur ein Ziel, dass zwischen 10 und 20 Milliarden kosten würde.
Natürlich kommen einem schnell die "üblichen Verdächtigen" in den Sinn, wenn man ein Übernahmeziel denkt.
Ich wäre aber nicht überrascht, wenn uns GILD mit etwas Unerwartetem überrascht.
 Bei der Pharmasset-Übernahme haben sie bewiesen, dass sie "verrückte" Preise zu zahlen bereit sind, was sich dann doch als ein riesen Deal für GILD entpuppte.
Bei der Pharmasset-Übernahme haben sie bewiesen, dass sie "verrückte" Preise zu zahlen bereit sind, was sich dann doch als ein riesen Deal für GILD entpuppte.Ich denke, dass ein Übernahmeziel aus der Sicht von GILD eine sehr hohe Wahrscheinlichkeit aufweisen muss, in absehbarer Zukunft viele Milliarden Umsatz einzuspielen und/oder einen bestimmten technologischen Bereich dominieren muss (was auch bedeutet, dass sie 100% der Rechte an ihrer Technologie und ihren Produkten halten müssen).
Falls GILD zu der Überzeugung kommen würde, dass bspw. BLUE eine echte Breakthrough-Technologie in den Händen halten würde (was ich für möglich halte, es aber natürlich nicht wirklich einschätzen kann), dann wäre das aus meiner Sicht beispielsweise ein guter Übernahmekandidat.
Aber vielleicht überraschen sie uns alle komplett.
Antwort auf Beitrag Nr.: 50.600.411 von ipollit am 10.09.15 22:35:29"Hier sind ein paar Details zu AKBA...
http://seekingalpha.com/article/3490866-addressing-6-misconc…
Addressing 6 Misconceptions About Akebia, A Highly Undervalued Biotech"
Hallo ipollit,
"ein paar Details" dürfte die Untertreibung des Jahres sein.
Es passiert ja nicht alle Tage, dass man wirklich hilfreiches bei seekingalpha findet, aber dieser Artikel gehört zum Besten, was ich je gelesen habe. Aus meiner Sicht auf Augenhöhe (mindestens!) mit Hammer oder Dr. DeSantis.
Ganz stark.
Gruß
SLG
http://seekingalpha.com/article/3490866-addressing-6-misconc…
Addressing 6 Misconceptions About Akebia, A Highly Undervalued Biotech"
Hallo ipollit,
"ein paar Details" dürfte die Untertreibung des Jahres sein.

Es passiert ja nicht alle Tage, dass man wirklich hilfreiches bei seekingalpha findet, aber dieser Artikel gehört zum Besten, was ich je gelesen habe. Aus meiner Sicht auf Augenhöhe (mindestens!) mit Hammer oder Dr. DeSantis.
Ganz stark.
Gruß
SLG
Antwort auf Beitrag Nr.: 50.607.914 von SLGramann am 11.09.15 20:35:53Hallo SLGramann,
bei der Größe von GILD wäre es ja auch möglich, dass sie einen Pharma schlucken wie z.B. BMY.
Bei der Übernahme von Pharmasset waren sie noch deutlich kleiner. GILD ist mit der Behandlung von HIV groß geworden, dort sind sie Marktführer. Die Ergänzung mit HCV war damals recht passend, da es beides gravierende Virus-Erkrankungen sind. HCV ist zusätzlich eine Lebererkrankung... in diesem Breich wäre z.B. soetwas wie NASH sehr passend. Wenn sie nicht Anfang des Jahres einen PII FXR der deutschen Phenex gekauft hätten, hätte ich auf ICPT als wahrscheinlichster Übernahmekandidat getippt.
Vielleicht wäre als Ergänzung auch etwas gegen HBV gut, falls es hier auch ein größeres Potential gibt. HBV kann man prinzipiell behandeln, anders als es bis vor einigen Jahren bei HCV der Fall war. Allerdings kann HBV auch chronisch werden, wobei es deutlich mehr HBV als HCV gibt. Insofern könnte ich mir auch etwas im RNAi-Bereich vorstellen... vielleicht eine ALNY. Wenn ich es richtig verstehe, wirken wichtige RNAi-Technologien über die Leber, wodurch sie prinzipiell auch gut für Lebererkrankungen geeignet sind.
GILD hat ein Standbein im Bereich von Blutkrebs... pi3k-Hemmer auf dem Markt sowie Jak-, Syk- Btk- und BET-Hemmer in der Entwicklung. Daher würde für mich eine Übernahme von INCY Sinn ergeben, da diese in JAK das Maß der Dinge sind. Zudem könnten sie mit IDO eine führende Position im wichtigen IO-Bereich einnehmen.
Oder eben noch eine Nummer größer durch Übernahme eines Pharmas oder eines großen Biotech-Konkurrenten.
Grüße
ipollit
bei der Größe von GILD wäre es ja auch möglich, dass sie einen Pharma schlucken wie z.B. BMY.
Bei der Übernahme von Pharmasset waren sie noch deutlich kleiner. GILD ist mit der Behandlung von HIV groß geworden, dort sind sie Marktführer. Die Ergänzung mit HCV war damals recht passend, da es beides gravierende Virus-Erkrankungen sind. HCV ist zusätzlich eine Lebererkrankung... in diesem Breich wäre z.B. soetwas wie NASH sehr passend. Wenn sie nicht Anfang des Jahres einen PII FXR der deutschen Phenex gekauft hätten, hätte ich auf ICPT als wahrscheinlichster Übernahmekandidat getippt.
Vielleicht wäre als Ergänzung auch etwas gegen HBV gut, falls es hier auch ein größeres Potential gibt. HBV kann man prinzipiell behandeln, anders als es bis vor einigen Jahren bei HCV der Fall war. Allerdings kann HBV auch chronisch werden, wobei es deutlich mehr HBV als HCV gibt. Insofern könnte ich mir auch etwas im RNAi-Bereich vorstellen... vielleicht eine ALNY. Wenn ich es richtig verstehe, wirken wichtige RNAi-Technologien über die Leber, wodurch sie prinzipiell auch gut für Lebererkrankungen geeignet sind.
GILD hat ein Standbein im Bereich von Blutkrebs... pi3k-Hemmer auf dem Markt sowie Jak-, Syk- Btk- und BET-Hemmer in der Entwicklung. Daher würde für mich eine Übernahme von INCY Sinn ergeben, da diese in JAK das Maß der Dinge sind. Zudem könnten sie mit IDO eine führende Position im wichtigen IO-Bereich einnehmen.
Oder eben noch eine Nummer größer durch Übernahme eines Pharmas oder eines großen Biotech-Konkurrenten.
Grüße
ipollit
Antwort auf Beitrag Nr.: 50.610.863 von ipollit am 12.09.15 12:46:09Hallo ipollit,
ja, BMY und INCY wären technologisch gesehen wundervolle Ziele. Ich halte diese nur aus Bewertungsgründen für eher unwahrscheinlich. Andererseits: Roche hat vor Jahren die fehlende Hälfte von Genentech auch weitgehend mit Fremdkapital gekauft. Obwohl die Zinsen da noch viel höher waren, bezahlte sich die Übernahme quasi von selbst, weil der gesamt Cashstrom von Genentech zur Verfügung stand, um die Kredite wieder zu tilgen.
Aus dieser Sicht wäre BMY - mit reichlich Cashfluss und Synergieeffekten - sicher geeigneter als INCY, die aber technologisch vielleicht noch attraktiver sind.
INCY wäre jedenfalls aus meiner Sicht ein sehr aggressiver Schachzug. Man müsste dann doch sicher 30 bis 35 Milliarden Dollar bieten, oder? Und noch macht INCY ja kaum eigenen Umsatz.
Wenn aber GILD von IDO voll überzeugt ist, dann würden sie möglicherweise auch diesen Preis bezahlen...
Ich bin jedenfalls super gespannt, ob das Übernahme-Karussell im Biotechbereich - trotz recht hoher Bewertungen - demnächst tatsächlich Fahrt aufnimmt.
Gruß
SLG
ja, BMY und INCY wären technologisch gesehen wundervolle Ziele. Ich halte diese nur aus Bewertungsgründen für eher unwahrscheinlich. Andererseits: Roche hat vor Jahren die fehlende Hälfte von Genentech auch weitgehend mit Fremdkapital gekauft. Obwohl die Zinsen da noch viel höher waren, bezahlte sich die Übernahme quasi von selbst, weil der gesamt Cashstrom von Genentech zur Verfügung stand, um die Kredite wieder zu tilgen.
Aus dieser Sicht wäre BMY - mit reichlich Cashfluss und Synergieeffekten - sicher geeigneter als INCY, die aber technologisch vielleicht noch attraktiver sind.
INCY wäre jedenfalls aus meiner Sicht ein sehr aggressiver Schachzug. Man müsste dann doch sicher 30 bis 35 Milliarden Dollar bieten, oder? Und noch macht INCY ja kaum eigenen Umsatz.
Wenn aber GILD von IDO voll überzeugt ist, dann würden sie möglicherweise auch diesen Preis bezahlen...
Ich bin jedenfalls super gespannt, ob das Übernahme-Karussell im Biotechbereich - trotz recht hoher Bewertungen - demnächst tatsächlich Fahrt aufnimmt.
Gruß
SLG
Antwort auf Beitrag Nr.: 50.601.671 von biopadawan am 11.09.15 08:29:08AKBA, FGEN
Hallo Biopadawan,
sowohl AKBA als auch FGEN könnten niedrig bewertet sein. Dabei setzt AKBA voll auf HIF und steht momentan ohne Parnter da, während FGEN risikoärmer aufgestellt ist durch eine breitere Pipeline (insbesondere den CTGF-AK) und Partnern, die einen großen Teil der HIF-Entwicklungskosten tragen und zusätzlich permantent Cash an FGEN überweisen (z.B. diesen Sommer 120 Mio USD von AZN).
Angeblich soll HIF ein sehr großer Markt werden. Bisher gibt es ESAs wie Epo, die gespritzt werden müssen (HIFs wie AKB-6548 sind Tabletten) und die Umsätze von 10 Mrd USD hatten, bevor sich problemtische Nebenwirkungen zeigten. Trotz dieser Nebenwirkungen sind es immer noch Mrd-Umsätze. HIFs könnten folgende Vorteile bieten:
- oral statt gespritzt
- durch den HIF-Ansatz bleibt das Hormon Epo innerhalb natürlicher Grenzen, während es bei ESAs unnatürlich erhöht ist
- über HIF wird ein breiterer, natürlicher Mechanismus zur besseren Sauerstoff-Versorgung angesprochen, bei dem Epo nur ein Teil ist
- ESAs führen zu Eisenmangel, der mit weiteren Mittel behandelt werden muss
- ESAs können aufgrund des unnatürlichen Prozesses gravierende Nebenwirkungen haben wie z.B. Schlaganfall oder Herzinfakte
- bei allen entzündlichen Erkrankungen wie z.B. RA kann es zu Blutarmut kommen, bei der ESAs nicht wirksam sind, HIFs schon
- ESAs sind als Hormone aufwendiger zu produzieren
Allerdings gibt es auch Risiken. HIF greift wie gesagt in einen natürlichen Prozess ein, so wie der Körper auf Sauerstoff-Mangel reagieren würde. Dazu kann auch eine vermehrte Bildung von Blutgefäßen gehören. Solche Prozesse spielen auch bei der Entstehung von Krebs eine Rolle. HIFs können theoretisch z.B. VEGF erhöhen (das hängt davon ab, wie spezifisch die HIF-Mittel sind)... dies kann Krebs fördern. Z.B. hemmt EXELs Cabo VEGF+MET in RCC oder Avastin ist ein VEGF-AK, der bei vielen Krebsarten eingesetzt wird. VEGF&Co spielt auch bei Augenerkrankungen eine Rolle... REGNs Eylea ist ein VEGF-Trap. Sollte ein HIF-Mittel z.B. VEGF erhöhen, dann dürfte vermehrt Krebs auftreten... das dürfte dann ein erhebliches Problem für eine Zulassung werden. Diese Probleme wird man wahrscheinlich erst dann wirklich beurteilen können, wenn PIII-Daten von sehr vielen Patienten vorliegen. Es besteht also bis zum Schluss das Risiko, dass HIF keine Zulassung erhalten kann und damit wertlos wird. Bisher sieht allerdings alles gut aus.
AKBA hatte meine ich Patent-Streitigkeiten mit FGEN (FGEN will AKBA teilweise blocken)... bisher hatte FGEN hier aber keinen Erfolg. FGEN ist bereits in P3, während AKBA gerade erst die P2 abgeschlossen hat. In den ersten P2-Daten gab es im AKB-6548 Arm eine höhere Sterblichkeit als im Placebo-Arm... das könnte auf ein gravierendes Risiko hinweisen. Dies hat erheblich auf dem Kurs gelastet. In den P2-Daten von letzter Woche, war das nicht mehr zu beobachten. Alles handelt es sich aber nur um eine P2 mit wenigen Patienten, so dass man nichts mit Sicherheit sagen kann. Vielleicht könnte am Ende AKB-6548 auch sicherer als FGENs Roxa sein, wenn Roxa z.B. VEGF erhöht. Roxa hatte ein Problem, wenn man es täglich verabreicht hat... dann ließ die Wirkung irgendwann nach. FGEN hat dann eine Tablette jeden zweiten Tag getestet. Bei dieser Dosierung gibt es kein Problem. Diese Dosierung finde ich aber nicht so vorteilhaft: bei Dialyse-Patienten ist das kein Problem, da man die Tablette immer zusammen mit der Dialyse geben kann. Aber alleine zuhause wäre es einfacher, wenn man die Tablette täglich einnehmen könnte, als sich die Tage merken zu müssen, wann man die Tablette nehmen muss. AKB-6548 wird in beiden Dosierungen getestet... täglich und jeden zweiten Tag. Beides scheint zu gehen, wenn auch die PIII-Dosierung auch jeden zweiten Tag sein soll. Vielleicht hat in Zukunft AKBA hier aber einen Vorteil. Bisher sind sie noch ohne (Pharma-)Partner... mit den letzten Daten könnten sich aber Interessenten finden, da im Erfolgsfall der Markt sehr groß ist (Amgen und Genentech sind mit ESAs groß geworden).
FGEN hat mit dem CTGF-AK noch ein weiteres sehr interessantes Standbein. FG-3019 könnte deutlich besser gegen IPF wirken als ITMNs Esbriet... die Wirkung scheint höher zu sein und die Studien können bisher sehr erfolgreich Patienten gewinnen, obwohl Esbriet bereits zugelassen ist. Roche hat für ITMN bzw. Esbriet 8 Mrd USD gezahlt. CTGF könnte bei vielen entzündlichen, fibrotischen Prozessen eine Rolle spielen. FGEN testet es neben IPF (Lungen-Fibrose) auch bei Leber-Fibrose (z.B. infolge von HBV/HCV) oder NASH. Außerdem könnte es bei entzündlichen Krebsarten wie Bauchspeicheldrüsenkrebs helfen. Und zuletzt hat FGEN gesagt, dass CTGF auch eine große Rolle bei der seltenen aber sehr schweren Muskelerkrankung DMD eine bedeutende Rolle spielt... dies ist der Bereich von SRPT (1,5 Mrd USD MK), wobei SRPT nur auf bestimmte genetische Veränderungen abzielt. Z.B. hat SRPT die Zulassung von Eteplirsen gegen Exon51-DMD beantragt, das nur bei 13% von DMD auftritt. Alleine in den USA wird für diesen DMD-Teil ein Umsatzpotential von 700 Mio USD gesehen. Sollte FG-3019 gegen DMD unabhängig von genetischen Veränderungen wirken, wäre das Potential wohl im Mult-Mrd USD Bereich.
Insgesamt habe ich daher FGEN höher als AKBA gewichtet. Sollte die Skepsis gegenüber Nebenwirkungen bei AKB-6548 bestehen bleiben, so wird sich AKBA wohl eher schwach entwickeln. Sollten sie dagegen einen Partner finden, haben sie viel Potential.
Gruß
ipollit
Hallo Biopadawan,
sowohl AKBA als auch FGEN könnten niedrig bewertet sein. Dabei setzt AKBA voll auf HIF und steht momentan ohne Parnter da, während FGEN risikoärmer aufgestellt ist durch eine breitere Pipeline (insbesondere den CTGF-AK) und Partnern, die einen großen Teil der HIF-Entwicklungskosten tragen und zusätzlich permantent Cash an FGEN überweisen (z.B. diesen Sommer 120 Mio USD von AZN).
Angeblich soll HIF ein sehr großer Markt werden. Bisher gibt es ESAs wie Epo, die gespritzt werden müssen (HIFs wie AKB-6548 sind Tabletten) und die Umsätze von 10 Mrd USD hatten, bevor sich problemtische Nebenwirkungen zeigten. Trotz dieser Nebenwirkungen sind es immer noch Mrd-Umsätze. HIFs könnten folgende Vorteile bieten:
- oral statt gespritzt
- durch den HIF-Ansatz bleibt das Hormon Epo innerhalb natürlicher Grenzen, während es bei ESAs unnatürlich erhöht ist
- über HIF wird ein breiterer, natürlicher Mechanismus zur besseren Sauerstoff-Versorgung angesprochen, bei dem Epo nur ein Teil ist
- ESAs führen zu Eisenmangel, der mit weiteren Mittel behandelt werden muss
- ESAs können aufgrund des unnatürlichen Prozesses gravierende Nebenwirkungen haben wie z.B. Schlaganfall oder Herzinfakte
- bei allen entzündlichen Erkrankungen wie z.B. RA kann es zu Blutarmut kommen, bei der ESAs nicht wirksam sind, HIFs schon
- ESAs sind als Hormone aufwendiger zu produzieren
Allerdings gibt es auch Risiken. HIF greift wie gesagt in einen natürlichen Prozess ein, so wie der Körper auf Sauerstoff-Mangel reagieren würde. Dazu kann auch eine vermehrte Bildung von Blutgefäßen gehören. Solche Prozesse spielen auch bei der Entstehung von Krebs eine Rolle. HIFs können theoretisch z.B. VEGF erhöhen (das hängt davon ab, wie spezifisch die HIF-Mittel sind)... dies kann Krebs fördern. Z.B. hemmt EXELs Cabo VEGF+MET in RCC oder Avastin ist ein VEGF-AK, der bei vielen Krebsarten eingesetzt wird. VEGF&Co spielt auch bei Augenerkrankungen eine Rolle... REGNs Eylea ist ein VEGF-Trap. Sollte ein HIF-Mittel z.B. VEGF erhöhen, dann dürfte vermehrt Krebs auftreten... das dürfte dann ein erhebliches Problem für eine Zulassung werden. Diese Probleme wird man wahrscheinlich erst dann wirklich beurteilen können, wenn PIII-Daten von sehr vielen Patienten vorliegen. Es besteht also bis zum Schluss das Risiko, dass HIF keine Zulassung erhalten kann und damit wertlos wird. Bisher sieht allerdings alles gut aus.
AKBA hatte meine ich Patent-Streitigkeiten mit FGEN (FGEN will AKBA teilweise blocken)... bisher hatte FGEN hier aber keinen Erfolg. FGEN ist bereits in P3, während AKBA gerade erst die P2 abgeschlossen hat. In den ersten P2-Daten gab es im AKB-6548 Arm eine höhere Sterblichkeit als im Placebo-Arm... das könnte auf ein gravierendes Risiko hinweisen. Dies hat erheblich auf dem Kurs gelastet. In den P2-Daten von letzter Woche, war das nicht mehr zu beobachten. Alles handelt es sich aber nur um eine P2 mit wenigen Patienten, so dass man nichts mit Sicherheit sagen kann. Vielleicht könnte am Ende AKB-6548 auch sicherer als FGENs Roxa sein, wenn Roxa z.B. VEGF erhöht. Roxa hatte ein Problem, wenn man es täglich verabreicht hat... dann ließ die Wirkung irgendwann nach. FGEN hat dann eine Tablette jeden zweiten Tag getestet. Bei dieser Dosierung gibt es kein Problem. Diese Dosierung finde ich aber nicht so vorteilhaft: bei Dialyse-Patienten ist das kein Problem, da man die Tablette immer zusammen mit der Dialyse geben kann. Aber alleine zuhause wäre es einfacher, wenn man die Tablette täglich einnehmen könnte, als sich die Tage merken zu müssen, wann man die Tablette nehmen muss. AKB-6548 wird in beiden Dosierungen getestet... täglich und jeden zweiten Tag. Beides scheint zu gehen, wenn auch die PIII-Dosierung auch jeden zweiten Tag sein soll. Vielleicht hat in Zukunft AKBA hier aber einen Vorteil. Bisher sind sie noch ohne (Pharma-)Partner... mit den letzten Daten könnten sich aber Interessenten finden, da im Erfolgsfall der Markt sehr groß ist (Amgen und Genentech sind mit ESAs groß geworden).
FGEN hat mit dem CTGF-AK noch ein weiteres sehr interessantes Standbein. FG-3019 könnte deutlich besser gegen IPF wirken als ITMNs Esbriet... die Wirkung scheint höher zu sein und die Studien können bisher sehr erfolgreich Patienten gewinnen, obwohl Esbriet bereits zugelassen ist. Roche hat für ITMN bzw. Esbriet 8 Mrd USD gezahlt. CTGF könnte bei vielen entzündlichen, fibrotischen Prozessen eine Rolle spielen. FGEN testet es neben IPF (Lungen-Fibrose) auch bei Leber-Fibrose (z.B. infolge von HBV/HCV) oder NASH. Außerdem könnte es bei entzündlichen Krebsarten wie Bauchspeicheldrüsenkrebs helfen. Und zuletzt hat FGEN gesagt, dass CTGF auch eine große Rolle bei der seltenen aber sehr schweren Muskelerkrankung DMD eine bedeutende Rolle spielt... dies ist der Bereich von SRPT (1,5 Mrd USD MK), wobei SRPT nur auf bestimmte genetische Veränderungen abzielt. Z.B. hat SRPT die Zulassung von Eteplirsen gegen Exon51-DMD beantragt, das nur bei 13% von DMD auftritt. Alleine in den USA wird für diesen DMD-Teil ein Umsatzpotential von 700 Mio USD gesehen. Sollte FG-3019 gegen DMD unabhängig von genetischen Veränderungen wirken, wäre das Potential wohl im Mult-Mrd USD Bereich.
Insgesamt habe ich daher FGEN höher als AKBA gewichtet. Sollte die Skepsis gegenüber Nebenwirkungen bei AKB-6548 bestehen bleiben, so wird sich AKBA wohl eher schwach entwickeln. Sollten sie dagegen einen Partner finden, haben sie viel Potential.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.614.520 von ipollit am 13.09.15 14:13:32AKBA
noch ein paar ältere Analysten-Kommentare...



und hier der Einfluss von HIF auf die Produktion roter Blutkörperchen...
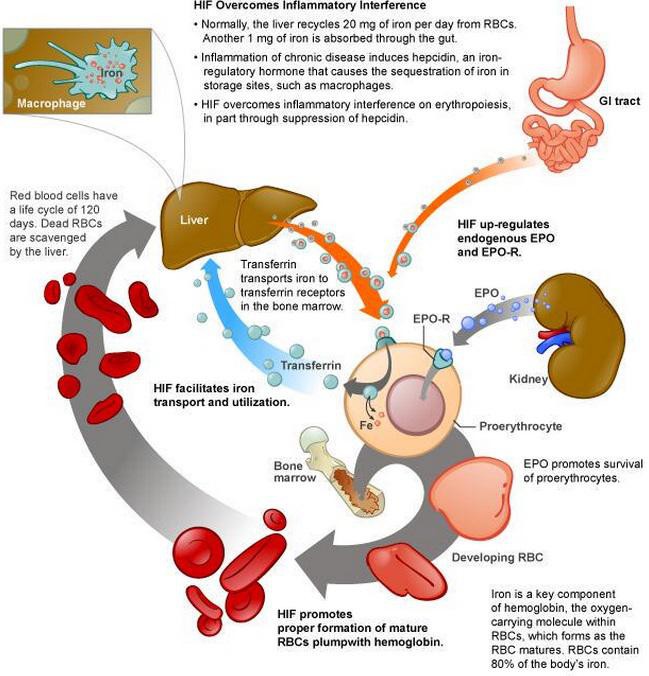
Gruß
ipollit
noch ein paar ältere Analysten-Kommentare...



und hier der Einfluss von HIF auf die Produktion roter Blutkörperchen...

Gruß
ipollit
RLYP, ZSPH
Aufgrund der Übernahme-Phantasie ist ZSPH's Bewertung auf ca. 2 Mrd USD gestiegen. RLYP liegt dagegen momentan bei ca. 1 Mrd USD. Daher habe ich einen Teil ZSPH in RLYP umgeschichtet. Eigentlich sollten die Bewertungen ähnlich sein, da sowohl Patiromer als auch ZS-9 vergleichbar sind.
ZS-9 hat den Vorteil, dass es deutlich schneller wirkt als Patiromer, um gefährlich hohe Kalium-Werte im Blut zu reduzieren. Im akuten Fall dürfte damit ZS-9 die bessere Wahl sein. Ein Nachteil von ZS-9 ist meiner Meinung nach dagegen, dass es ein erhöhtes Risiko von Schwellungen und Wasseransammlungen gibt, zusammen mit der höheren Wassermenge, die zur Einnahme benötigt wird. Für Menschen mit Herzproblemen könnte das ein Problem sein, da ein schwaches Herz generell zu Wasseransammlungen führt und eine zusätzliche Erhöhung das Herz zusätzlich belasten kann. D.h. in der Langzeit-Therapie könnte vielleicht Patiromer die Nase vorne haben.
Ein Vergleich von Patiromer (rot) mit ZS-9 (blau)...
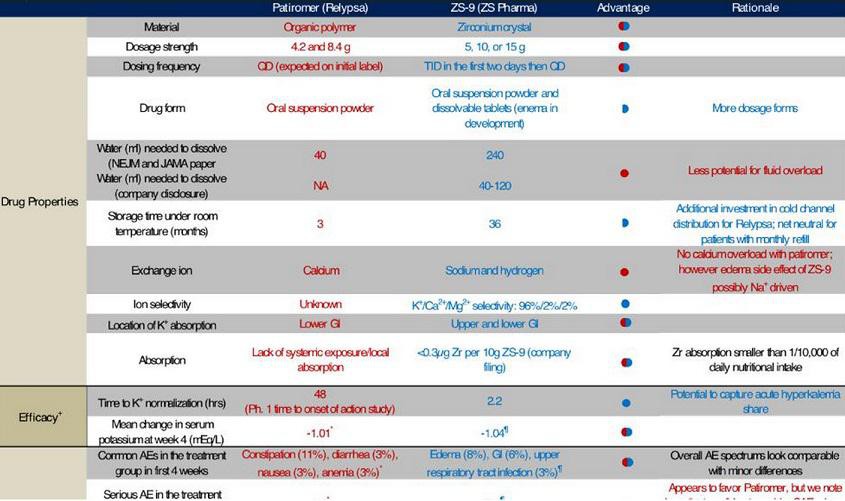
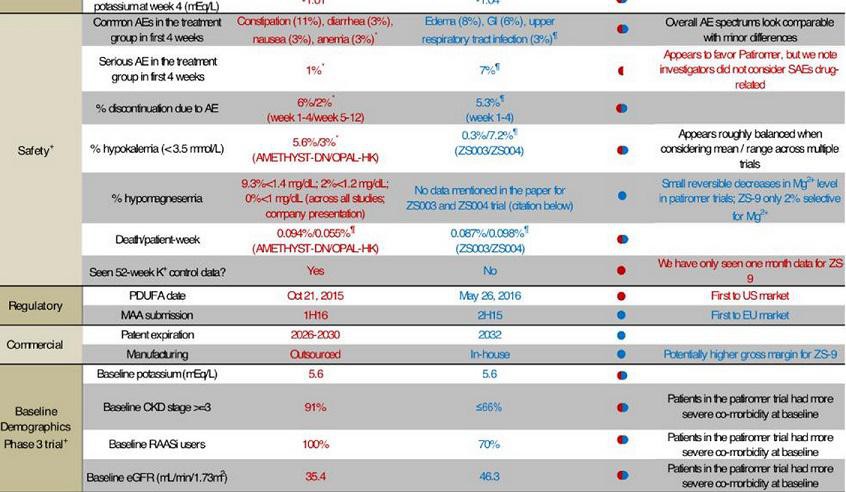
Der WSW-Webcast erklärt ganz gut die Kalium-Problematik gegen die diese beiden Mittel helfen sollen.
http://www.wsw.com/webcast/biocentury/rlyp/
Kalium wird über die Nahrung aufgenommen und über die Nieren wieder ausgeschieden. Durch chronische Nierenprobleme (CKD) kann der Kalium-Wert im Blut deutlich ansteigen. Dies wird noch verstärkt, wenn gleichzeiteig eine Behandlung der Nieren- oder von Herzproblemen mit RAASi-Medikamenten erfolgt
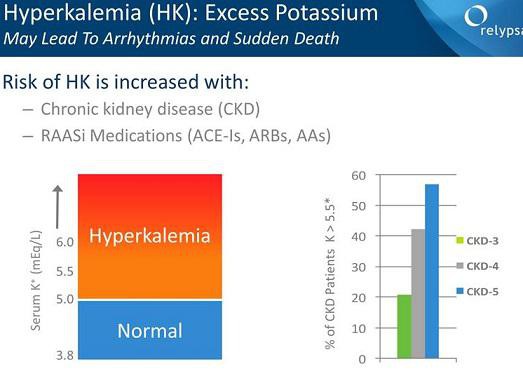

Steigt der Kalium-Wert über 5,5 kann es lebensgefährlich werden...

Bisher gibt es nur wenig Möglichkeiten... meistens bleibt nur, die RAASi-Behandlung zu reduzieren oder einzustellen. Angeblich können so nur 25% der CKD mit der optimalen RAASI-Dosierung behandelt werden, 33% garnicht...

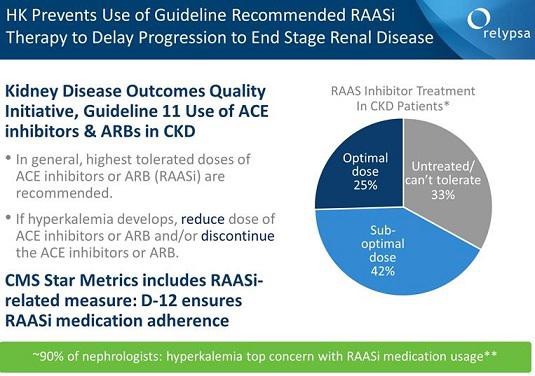
Patiromer und ZS-9 binden Kalium. Es ist ein Pulver, welches in Flüssigkeit aufgelöst täglich eingenommen werden muss und über den Darm Kalim aufnimmt, so dass der Blutwert wieder auf ein Normalmaß sinkt
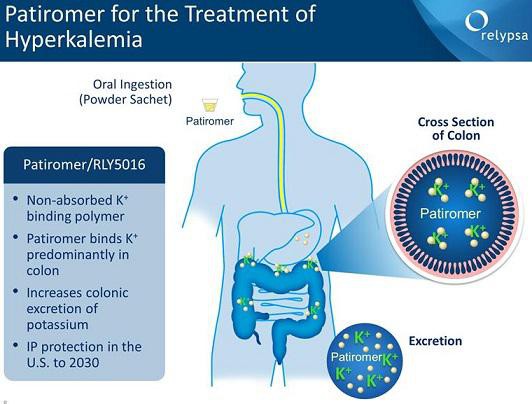
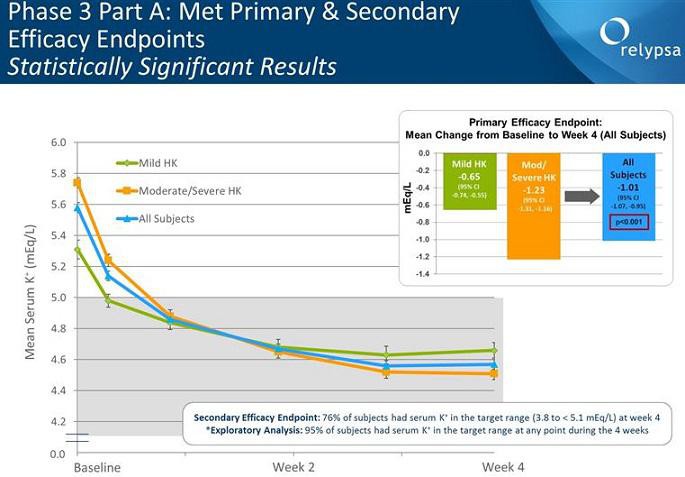
Gefährlich hohe Werte kann im aktuten Fall von Patiromer erst nach 48 Stunden gesenkt... ZS-9 ist hier deutlich schneller. Dafür gibt es zu Patiromer schon Langzeitdaten, die die Sicherheit bei Anwendung über ein Jahr belegen.
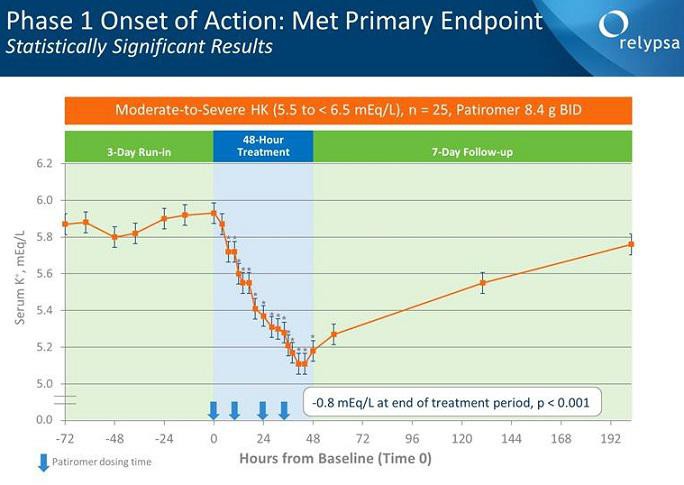
Das Marktpotential ergibt sich aus den CKD-Patienten mit hohen Kalium-Werten zusammen mit Herzpatienten ohne CKD, die mit RAASI behandelt werden.
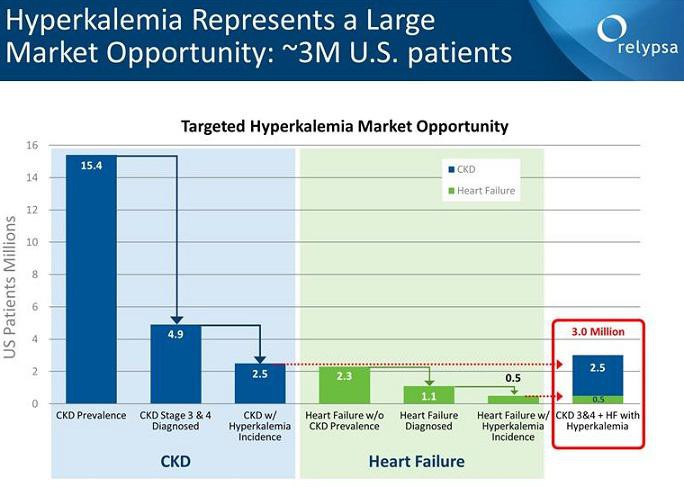
In den USA wird Patiromer von Sanofi promotet...

In Europa erfolgt der Vertrieb über Fresenius mit Royalties zwischen 10% und 22%

Wenn alles gut läuft, könnte Patiromer in den USA nächste oder übernächste Woche zugelassen werden.

Gruß
ipollit
Aufgrund der Übernahme-Phantasie ist ZSPH's Bewertung auf ca. 2 Mrd USD gestiegen. RLYP liegt dagegen momentan bei ca. 1 Mrd USD. Daher habe ich einen Teil ZSPH in RLYP umgeschichtet. Eigentlich sollten die Bewertungen ähnlich sein, da sowohl Patiromer als auch ZS-9 vergleichbar sind.
ZS-9 hat den Vorteil, dass es deutlich schneller wirkt als Patiromer, um gefährlich hohe Kalium-Werte im Blut zu reduzieren. Im akuten Fall dürfte damit ZS-9 die bessere Wahl sein. Ein Nachteil von ZS-9 ist meiner Meinung nach dagegen, dass es ein erhöhtes Risiko von Schwellungen und Wasseransammlungen gibt, zusammen mit der höheren Wassermenge, die zur Einnahme benötigt wird. Für Menschen mit Herzproblemen könnte das ein Problem sein, da ein schwaches Herz generell zu Wasseransammlungen führt und eine zusätzliche Erhöhung das Herz zusätzlich belasten kann. D.h. in der Langzeit-Therapie könnte vielleicht Patiromer die Nase vorne haben.
Ein Vergleich von Patiromer (rot) mit ZS-9 (blau)...


Der WSW-Webcast erklärt ganz gut die Kalium-Problematik gegen die diese beiden Mittel helfen sollen.
http://www.wsw.com/webcast/biocentury/rlyp/
Kalium wird über die Nahrung aufgenommen und über die Nieren wieder ausgeschieden. Durch chronische Nierenprobleme (CKD) kann der Kalium-Wert im Blut deutlich ansteigen. Dies wird noch verstärkt, wenn gleichzeiteig eine Behandlung der Nieren- oder von Herzproblemen mit RAASi-Medikamenten erfolgt


Steigt der Kalium-Wert über 5,5 kann es lebensgefährlich werden...

Bisher gibt es nur wenig Möglichkeiten... meistens bleibt nur, die RAASi-Behandlung zu reduzieren oder einzustellen. Angeblich können so nur 25% der CKD mit der optimalen RAASI-Dosierung behandelt werden, 33% garnicht...


Patiromer und ZS-9 binden Kalium. Es ist ein Pulver, welches in Flüssigkeit aufgelöst täglich eingenommen werden muss und über den Darm Kalim aufnimmt, so dass der Blutwert wieder auf ein Normalmaß sinkt


Gefährlich hohe Werte kann im aktuten Fall von Patiromer erst nach 48 Stunden gesenkt... ZS-9 ist hier deutlich schneller. Dafür gibt es zu Patiromer schon Langzeitdaten, die die Sicherheit bei Anwendung über ein Jahr belegen.

Das Marktpotential ergibt sich aus den CKD-Patienten mit hohen Kalium-Werten zusammen mit Herzpatienten ohne CKD, die mit RAASI behandelt werden.

In den USA wird Patiromer von Sanofi promotet...

In Europa erfolgt der Vertrieb über Fresenius mit Royalties zwischen 10% und 22%

Wenn alles gut läuft, könnte Patiromer in den USA nächste oder übernächste Woche zugelassen werden.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.615.306 von ipollit am 13.09.15 17:21:56und noch ein paar Analysten-Kommentare...

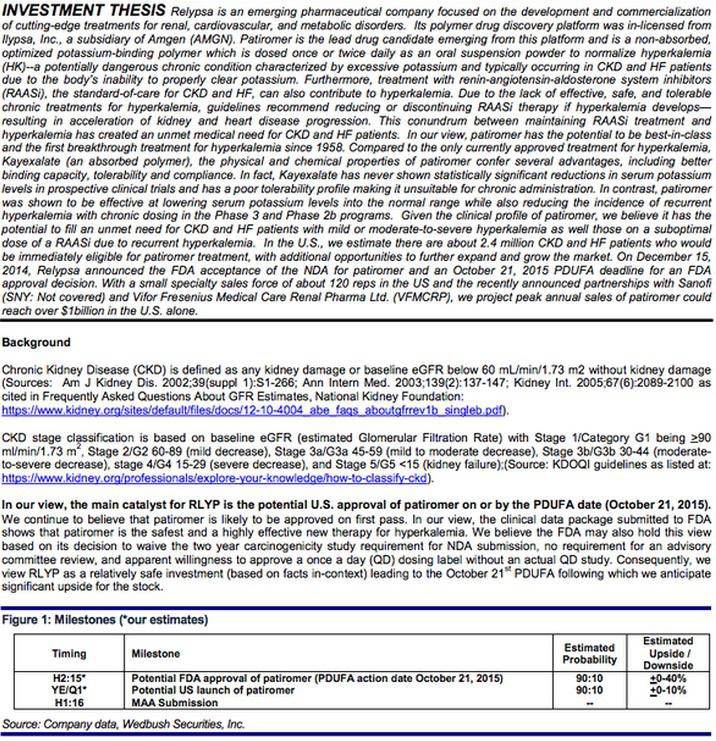

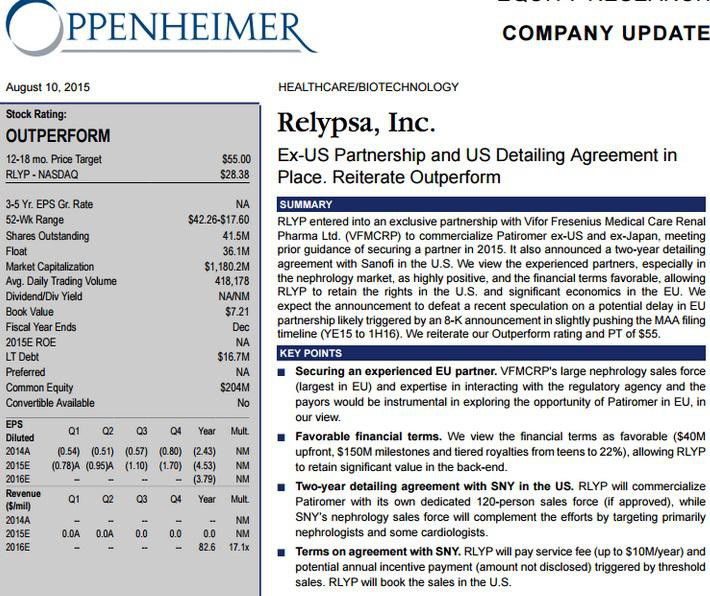

Gruß
ipollit





Gruß
ipollit
Antwort auf Beitrag Nr.: 50.615.306 von ipollit am 13.09.15 17:21:56"Wenn alles gut läuft, könnte Patiromer in den USA nächste oder übernächste Woche zugelassen werden."
Das ist falsch... natürlich erst im Oktober... PDUFA ist der 21.10.!
Gruß
ipollit
Das ist falsch... natürlich erst im Oktober... PDUFA ist der 21.10.!
Gruß
ipollit
Hallo,
ich habe noch eine Frag zu Clovis. Ich möchte eigentlich mittelfristig meine Position weiter aufbauen, der momentane Anstieg lässt mich allerdings überlegen, einen Teil wieder zu verkaufen, da ich irgendwann eine Konsolidierung erwarte.
Seht ihr das auch so bzw. wie würdet ihr vorgehen?
Gleichzeitig möchte ich mich für die extrem fundierten Beiträge hier bedanken, eine Freude hier mitzulesen !!!
ich habe noch eine Frag zu Clovis. Ich möchte eigentlich mittelfristig meine Position weiter aufbauen, der momentane Anstieg lässt mich allerdings überlegen, einen Teil wieder zu verkaufen, da ich irgendwann eine Konsolidierung erwarte.
Seht ihr das auch so bzw. wie würdet ihr vorgehen?
Gleichzeitig möchte ich mich für die extrem fundierten Beiträge hier bedanken, eine Freude hier mitzulesen !!!
ich bin eh nicht der große Biotech-Experte, lese hier aber gern mit.
Allgemein kann ich zu der Frage aber sagen: den richtigen Ausstieg zu finden, ist eigentlich immer schwerer als der Einstieg. Von daher verkaufe ich und kaufe ich in der Regel eher zum Teil...
Bei Biotec-Werten finde ich es aber fast unmöglich, weil so viele Faktoren eine Rolle spielen, die man von außen kaum erkennen kann. Wird eine Testphase vorzeitig abgebrochen, weil es Komplikationen gab, gibt es ein Übernahmeangebot? Auf einmal steigt oder fällt der Kurs um 30 %.
Die einzige Antwort die ich daher hier geben kann: gerade im Biotec-Bereich muss man sich von dem Gedanken lösen, man könne alles richtig machen. Also nicht ärgern, wenn man zu früh oder zu spät ge- oder verkauft hat. Sondern die längerfristige Entwicklung beobachten und danach handeln, wie man selbst den Wert mit fachkundiger Hilfe (hier) einschätzt. Mehr geht m.E. nicht.
Also eher eine Frage des Kopfes und des Anspruchs an den eigenen Erfolg.
Allgemein kann ich zu der Frage aber sagen: den richtigen Ausstieg zu finden, ist eigentlich immer schwerer als der Einstieg. Von daher verkaufe ich und kaufe ich in der Regel eher zum Teil...
Bei Biotec-Werten finde ich es aber fast unmöglich, weil so viele Faktoren eine Rolle spielen, die man von außen kaum erkennen kann. Wird eine Testphase vorzeitig abgebrochen, weil es Komplikationen gab, gibt es ein Übernahmeangebot? Auf einmal steigt oder fällt der Kurs um 30 %.
Die einzige Antwort die ich daher hier geben kann: gerade im Biotec-Bereich muss man sich von dem Gedanken lösen, man könne alles richtig machen. Also nicht ärgern, wenn man zu früh oder zu spät ge- oder verkauft hat. Sondern die längerfristige Entwicklung beobachten und danach handeln, wie man selbst den Wert mit fachkundiger Hilfe (hier) einschätzt. Mehr geht m.E. nicht.
Also eher eine Frage des Kopfes und des Anspruchs an den eigenen Erfolg.
Ich denke sich selber seine Unwissenheit einzugestehen ist der einzig mögliche Weg. Wenn man mal in anderen Foren querliest ist das doch der größte Fehler, dass Leute meinen sie sind die Experten und hätten "alles im Griff". Schuld am miesen Kurs sind dann immer die anderen, die Shorts, Experten die anderer Meinung sind (!), Kursmanipulatoren, FDA...die haben ja alle keine Ahnung!
Was den Aufbau/die Verwaltung seines Depots angeht habe ich ganz gute Erfahrungen damit gemacht Teilkäufe/verkäufe zu tätigen, wenn ich mir nicht sicher bin. Besonders bei Werten wie CLVS halte ich auch viel davon eine Kernposition zu halten, da eine Übernahme doch sehr wahrscheinlich ist.
Momentan läuft es ja bei vielen der hier vorgestelleten Werte (und überhaupt) ja wieder erstaunlich gut.
Bei AERI und ITCI reicht ein Blick auf den Chart, um zu erraten, wie die Studienergebnisse ausgefallen sind - Glückwunsch allen Investierten!



Bei ZFGN ist endlich der Ausbruch gelungen. Fast schon ein charttechnischer Streber (50/200 Tageslinie).
Was steht dieses Jahr noch an?
ASH: KPTI, JUNO, BLUE...
SABCS: CLVS (!), ONTY...
SG kmastra
Was den Aufbau/die Verwaltung seines Depots angeht habe ich ganz gute Erfahrungen damit gemacht Teilkäufe/verkäufe zu tätigen, wenn ich mir nicht sicher bin. Besonders bei Werten wie CLVS halte ich auch viel davon eine Kernposition zu halten, da eine Übernahme doch sehr wahrscheinlich ist.
Momentan läuft es ja bei vielen der hier vorgestelleten Werte (und überhaupt) ja wieder erstaunlich gut.
Bei AERI und ITCI reicht ein Blick auf den Chart, um zu erraten, wie die Studienergebnisse ausgefallen sind - Glückwunsch allen Investierten!
Bei ZFGN ist endlich der Ausbruch gelungen. Fast schon ein charttechnischer Streber (50/200 Tageslinie).
Was steht dieses Jahr noch an?
ASH: KPTI, JUNO, BLUE...
SABCS: CLVS (!), ONTY...
SG kmastra
BRAF Inhibition Leukemia
arry:Potenzieller Anwendungsbereich Encorafenib (möglicherweise plus MEK Inhibitor):
BRAF Inhibition Effective for Hairy-Cell Leukemia
Treatment with a short course of vemurafenib, a BRAF inhibitor, was effective and rapid in patients with relapsed or refractory hairy-cell leukemia, resulting in overall response rates of greater than 95%, according to the results of two phase II studies. “In these two trials involving patients with hairy-cell leukemia, an oral course of vemurafenib (at a dose of 960 mg twice daily for 16 to 18 weeks) was rapidly and highly effective, with response rates of 96% in the Italian study and 100% in the US study and with low-grade toxic effects in patients who not only were heavily pretreated but often had disease that was refractory to their last therapy,” wrote Brunangelo Falini, MD, of the University of Perugia, and colleagues in the New England Journal of Medicine.Falini and colleagues conducted phase II single-group studies of vemurafenib 960 mg in the United States and in Italy. Therapy was given for a median of 16 weeks in the Italian study and 18 weeks in the US study. The primary endpoints were complete response rate (Italian trial) and overall response rate (US trial).“Rather than administering vemurafenib for an indefinite duration, as is done in patients with metastatic melanoma, we limited the initial vemurafenib treatment to a few months (even if this perhaps reduced the type or duration of response) owing to concern about vemurafenib induced secondary tumors,” the researchers explained.In the Italian study, the overall response rate was 96% after a median of 8 weeks with a complete response rate of 35%. At a median follow-up of 23 months, the median relapse-free survival was 19 months among those patients with a complete response. Among patients with a partial response, median relapse-free survival was 6 months. Median treatment-free survival was 25 months and 18 months among these two groups respectively.In the US trial, the overall response rate was 100% after a median of 12 weeks and the complete response rate was 42%. At 1 year, the progression-free survival rate was 73% with an overall survival rate of 91%.“A longer duration of treatment did not appear to improve the type or duration of the response,” the researchers wrote. “Retreatment with vemurafenib at the time of relapse was effective in the two trials, although to a lesser extent in the patients who had a relapse after a partial response than in those who had a relapse after a complete response in the Italian study.”According to the study, the most common adverse events, typically grade 1 or 2, were toxic events of the skin, arthralgia or arthritis, pyrexia, and elevated bilirubin level. Seven of 50 patients developed secondary cutaneous tumors.To evaluate the use of vemurafenib further in this patient population, Felini and colleagues recommended a study of BRAF inhibitors in combination with anti-CD20 monoclonal antibodies or with MEK inhibitors.
- See more at: http://www.cancernetwork.com/hematologic-malignancies/braf-i…
Antwort auf Beitrag Nr.: 50.649.708 von kmastra am 17.09.15 21:30:54AERI
"Bei AERI und ITCI reicht ein Blick auf den Chart, um zu erraten, wie die Studienergebnisse ausgefallen sind"
AERI hatte ich ja nach der negativen Rocket1 verkauft. Zwar war die Rocket2 anders als die Rocket1 nun erfolgreich, aber trotzdem sehe ich immer noch Probleme.
Rhopressa ist in Rocket2 statistisch nicht schlechter als Timolol... dies gilt allerdings nur für IOPs<25 mmHg, also für einen nur gering erhöhten Augeninnendruck. Für höhere Drücke scheint dagegen Rhopressa schlechter als Timolol zu sein... zumindest ist Rocket2 in diesem sekundären Endpunkt fehlgeschlagen. Laut Ohad Hammer war Timolol nur eine kleine Hürde, da es nur eine geringe Effektivität aufweist... z.B. PGAs sind viel wirksamer, insbesondere bei hohen Drücken.

Der meiner Meinung nach sehr problematische Drift (die Wirkung geht von Rhopressa geht mit der Zeit verloren) ist in Rocket2 nicht mehr so ausgeprägt. Trotzdem kann man ihn in BID (zweimalige Einnahme pro Tag) beobachten.
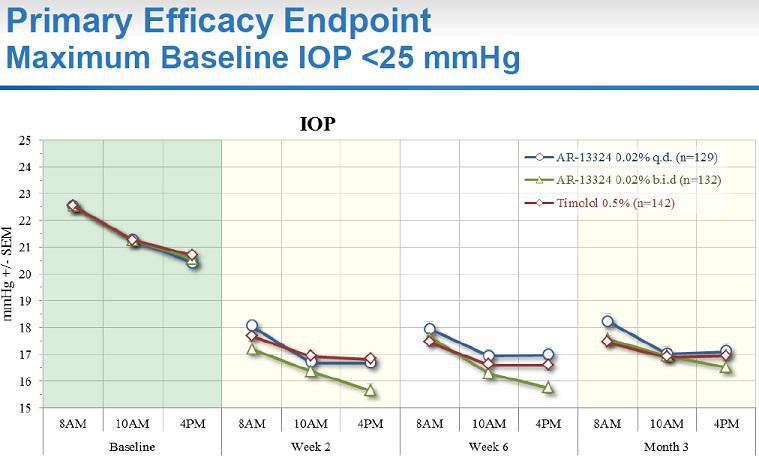
Die Ursache für den Drift ist unklar. Vor ein paar Monaten hat AERI einen Zusammenhang zwischen Drift und PGA-Einnahme vor Studien-Beginn gezeigt. Patienten, die vor Beginn der Studie PGAs eingenommen haben, zeigten eine höhere Wirkung von Rhopressa, die mit der Zeit verschwand. Ohne PGAs gab es dagegen nur einen kleinen Drift... die Drucksenkung nach 3 Monaten war ähnlich wie nach 2 Wochen. In Rocket2 soll es mehr naive Patienten gegeben haben... also Patienten, die zuvor nicht behandelt worden sind. Vielleicht ist deshalb der Drift geringer!?
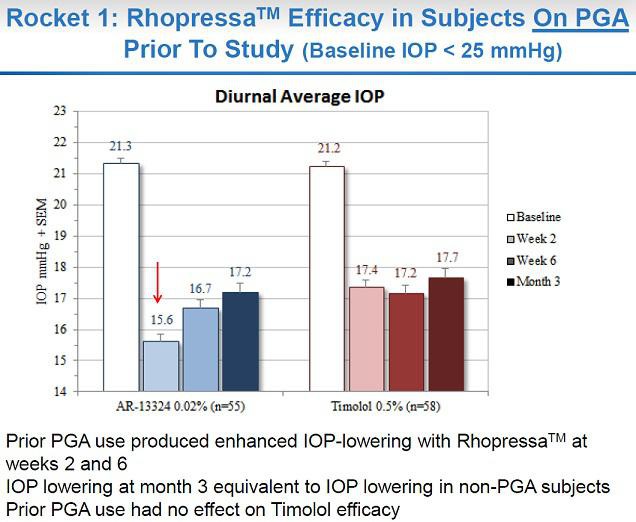
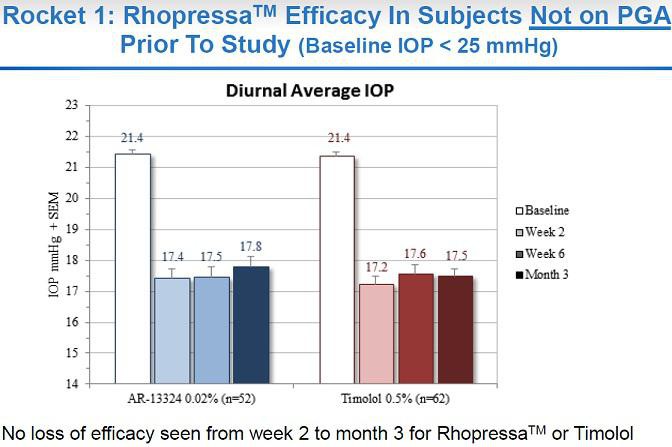
Ein größeres Problem für Rhopressa kann aber auch sein, dass anscheinend Nebenwirkungen so gravierend sind, dass deutlich mehr Patienten die Einnahme von Rhopressa abbrechen als bei Timolol.

Unterm Strich könnte also AERI vielleicht eine Zulassung von Rhopressa aufgrund der Rocket2-Ergebnisse erhalten. Allerdings ist es nur bei gering erhöhtem Augeninnendruck vergleichbar wirksam wie das wenig wirksame und generische Timolol. Dafür besitzt Rhopressa aber deutlich mehr Nebenwirkungen. Für mich klingt das eher danach, dass Rhopressa nur dann zum Einsatz kommt, wenn nichts anderes mehr hilft. Wird zu einem späteren Zeitpunkt (wenn nichts anderes mehr wirkt) der Augeninnendruck aber nicht eher höher liegen und zudem starken Drift aufweisen, da PGAs immer die erste Wahl sein werden? Dann ist die Anwendung von Rhopressa auch fraglich, da es bei hohem Druck wohl nur schlecht oder garnicht wirkt.
Vielleicht bringt ja die Rhopressa + PGA Kombi etwas... das Risiko ist aber auch hier recht hoch.
Gruß
ipollit
"Bei AERI und ITCI reicht ein Blick auf den Chart, um zu erraten, wie die Studienergebnisse ausgefallen sind"
AERI hatte ich ja nach der negativen Rocket1 verkauft. Zwar war die Rocket2 anders als die Rocket1 nun erfolgreich, aber trotzdem sehe ich immer noch Probleme.
Rhopressa ist in Rocket2 statistisch nicht schlechter als Timolol... dies gilt allerdings nur für IOPs<25 mmHg, also für einen nur gering erhöhten Augeninnendruck. Für höhere Drücke scheint dagegen Rhopressa schlechter als Timolol zu sein... zumindest ist Rocket2 in diesem sekundären Endpunkt fehlgeschlagen. Laut Ohad Hammer war Timolol nur eine kleine Hürde, da es nur eine geringe Effektivität aufweist... z.B. PGAs sind viel wirksamer, insbesondere bei hohen Drücken.

Der meiner Meinung nach sehr problematische Drift (die Wirkung geht von Rhopressa geht mit der Zeit verloren) ist in Rocket2 nicht mehr so ausgeprägt. Trotzdem kann man ihn in BID (zweimalige Einnahme pro Tag) beobachten.

Die Ursache für den Drift ist unklar. Vor ein paar Monaten hat AERI einen Zusammenhang zwischen Drift und PGA-Einnahme vor Studien-Beginn gezeigt. Patienten, die vor Beginn der Studie PGAs eingenommen haben, zeigten eine höhere Wirkung von Rhopressa, die mit der Zeit verschwand. Ohne PGAs gab es dagegen nur einen kleinen Drift... die Drucksenkung nach 3 Monaten war ähnlich wie nach 2 Wochen. In Rocket2 soll es mehr naive Patienten gegeben haben... also Patienten, die zuvor nicht behandelt worden sind. Vielleicht ist deshalb der Drift geringer!?


Ein größeres Problem für Rhopressa kann aber auch sein, dass anscheinend Nebenwirkungen so gravierend sind, dass deutlich mehr Patienten die Einnahme von Rhopressa abbrechen als bei Timolol.

Unterm Strich könnte also AERI vielleicht eine Zulassung von Rhopressa aufgrund der Rocket2-Ergebnisse erhalten. Allerdings ist es nur bei gering erhöhtem Augeninnendruck vergleichbar wirksam wie das wenig wirksame und generische Timolol. Dafür besitzt Rhopressa aber deutlich mehr Nebenwirkungen. Für mich klingt das eher danach, dass Rhopressa nur dann zum Einsatz kommt, wenn nichts anderes mehr hilft. Wird zu einem späteren Zeitpunkt (wenn nichts anderes mehr wirkt) der Augeninnendruck aber nicht eher höher liegen und zudem starken Drift aufweisen, da PGAs immer die erste Wahl sein werden? Dann ist die Anwendung von Rhopressa auch fraglich, da es bei hohem Druck wohl nur schlecht oder garnicht wirkt.
Vielleicht bringt ja die Rhopressa + PGA Kombi etwas... das Risiko ist aber auch hier recht hoch.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.649.708 von kmastra am 17.09.15 21:30:54ITCI
Meine ITCI-Risikoposition habe ich nun verkauft (in MDVN und RLYP umgeschichtet), da offensichtlich immer noch deutliche Risiken bestehen bei einer nun nicht mehr so geringen MK von ca. 2 Mrd USD. In diesem Bereich bleibe ich lieber bei ACAD.
In Twitter wurden die Ergebnisse eher kritisch gesehen. Die Wirkung von ITI-007 ist zwar statistisch signifikant besser als die Placebo-Wirkung, doch in dieser P3 ist der Unterschied eher gering: -14,5 für 60mg ITI-007 vs. -10,3 für Placebo. Das etablierte Risperidone zeigt normalerweise eine höhere Wirkung. In der nächsten PIII, deren Ergebnisse in einem Jahr vorliegen sollten, ist neben dem Placebo-Arm auch ein Risperidone-Arm enthalten. Es könnte sein, dass die Ergebnisse für ITI-007 nicht signifikant besser sind als die des Placebos, wenn die Wirkung nicht so groß ist... CNS-Studien lassen sich nicht immer so leicht bewerten, da ja subjektive Eindrücke eine Rolle spielen. Somit kann der Abstand zwischen Placebo und ITI-007 schnell auch mal so klein werden, dass die Signifikanz nicht mehr gegeben ist. Auch ACADs Nuplazid hatte negative Studien. Außerdem könnte in der nächsten PIII Risperidone deutlich wirksamer als ITI-007 sein, was das Marktpotential schmälern würde.
Ideal wäre es, wenn ITI-007 so wirksam wie Risperidone wäre, aber weniger Nebenwirkungen aufweist. Anders als z.B. ACADs Nuplazid ist ITI-007 aber nicht sehr selektiv. Das kann positiv sein, wenn dies die Wirkung erhöht, es können sich aber auch mehr Nebenwirkungen zeigen. Gegenüber Risperidone scheint es nach den bisherigen Ergebnissen schon besser zu sein... trotzdem ist hier noch Unsicherheit. Falls ITI-007 klar weniger wirksam als Risperidone ist, kommt es auf die Nebenwirkungen an.
Die Analysten-Kursziele sind deutlich angehoben worden... 70-90 USD. ITI-007 könnte im Erfolgsfall ein Multi-Mrd USD Medikament werden. Bei einer aktuellen MK von 2 Mrd USD ist aber wohl schon ein wenig Erfolg eingepreist... die nächsten Ergebnisse in einem Jahr können auch schnell enttäuschen.
http://www.thestreet.com/story/13290846/1/intra-cellular-sur…
... The most common side effects attributable to ITI-007 were drowsiness, fatigue and mild sedation. Some currently approved antipsychotics used to treat schizophrenia can cause weight gain or high cholesterol. Intra-Cellular said there was no difference in weight gain or metabolic measures between ITI-007 and placebo observed in the study.
"Today's data does not suggest ITI-007 will be a strong drug. Nevertheless, the p value suggests this effect is consistent and real, as do the secondary efficacy endpoints," Cowen analyst Ritu Baral wrote in a research note Wednesday. She continued, "Overall, today's data set supports the promising profile our key opinion leader consultants suspected this drug would have.... ITI-007 might be a less strong anti-psychotic that could be best for use in disease control maintenance, especially because of its weight/metabolic neutrality."
Intra-Cellular is running a second phase III study in schizophrenia comparing ITI-007 to placebo and risperidone, a currently approved antipsychotic. The primary efficacy endpoint of the ongoing study, like the first, compares ITI-007 against placebo. From a commercial perspective, seeing how the efficacy and safety of ITI-007 compares against risperidone will be equally important.
Schizophrenia patients tend to cycle through multiple drugs, so even inferior products, like Pfizer's Geodon, can generate substantial sales. However, Vanda Pharmaceuticals' schizophrenia drug Fanapt is not seen as different enough from cheaper alternatives and has struggled commercially.

Gruß
ipollit
Meine ITCI-Risikoposition habe ich nun verkauft (in MDVN und RLYP umgeschichtet), da offensichtlich immer noch deutliche Risiken bestehen bei einer nun nicht mehr so geringen MK von ca. 2 Mrd USD. In diesem Bereich bleibe ich lieber bei ACAD.
In Twitter wurden die Ergebnisse eher kritisch gesehen. Die Wirkung von ITI-007 ist zwar statistisch signifikant besser als die Placebo-Wirkung, doch in dieser P3 ist der Unterschied eher gering: -14,5 für 60mg ITI-007 vs. -10,3 für Placebo. Das etablierte Risperidone zeigt normalerweise eine höhere Wirkung. In der nächsten PIII, deren Ergebnisse in einem Jahr vorliegen sollten, ist neben dem Placebo-Arm auch ein Risperidone-Arm enthalten. Es könnte sein, dass die Ergebnisse für ITI-007 nicht signifikant besser sind als die des Placebos, wenn die Wirkung nicht so groß ist... CNS-Studien lassen sich nicht immer so leicht bewerten, da ja subjektive Eindrücke eine Rolle spielen. Somit kann der Abstand zwischen Placebo und ITI-007 schnell auch mal so klein werden, dass die Signifikanz nicht mehr gegeben ist. Auch ACADs Nuplazid hatte negative Studien. Außerdem könnte in der nächsten PIII Risperidone deutlich wirksamer als ITI-007 sein, was das Marktpotential schmälern würde.
Ideal wäre es, wenn ITI-007 so wirksam wie Risperidone wäre, aber weniger Nebenwirkungen aufweist. Anders als z.B. ACADs Nuplazid ist ITI-007 aber nicht sehr selektiv. Das kann positiv sein, wenn dies die Wirkung erhöht, es können sich aber auch mehr Nebenwirkungen zeigen. Gegenüber Risperidone scheint es nach den bisherigen Ergebnissen schon besser zu sein... trotzdem ist hier noch Unsicherheit. Falls ITI-007 klar weniger wirksam als Risperidone ist, kommt es auf die Nebenwirkungen an.
Die Analysten-Kursziele sind deutlich angehoben worden... 70-90 USD. ITI-007 könnte im Erfolgsfall ein Multi-Mrd USD Medikament werden. Bei einer aktuellen MK von 2 Mrd USD ist aber wohl schon ein wenig Erfolg eingepreist... die nächsten Ergebnisse in einem Jahr können auch schnell enttäuschen.
http://www.thestreet.com/story/13290846/1/intra-cellular-sur…
... The most common side effects attributable to ITI-007 were drowsiness, fatigue and mild sedation. Some currently approved antipsychotics used to treat schizophrenia can cause weight gain or high cholesterol. Intra-Cellular said there was no difference in weight gain or metabolic measures between ITI-007 and placebo observed in the study.
"Today's data does not suggest ITI-007 will be a strong drug. Nevertheless, the p value suggests this effect is consistent and real, as do the secondary efficacy endpoints," Cowen analyst Ritu Baral wrote in a research note Wednesday. She continued, "Overall, today's data set supports the promising profile our key opinion leader consultants suspected this drug would have.... ITI-007 might be a less strong anti-psychotic that could be best for use in disease control maintenance, especially because of its weight/metabolic neutrality."
Intra-Cellular is running a second phase III study in schizophrenia comparing ITI-007 to placebo and risperidone, a currently approved antipsychotic. The primary efficacy endpoint of the ongoing study, like the first, compares ITI-007 against placebo. From a commercial perspective, seeing how the efficacy and safety of ITI-007 compares against risperidone will be equally important.
Schizophrenia patients tend to cycle through multiple drugs, so even inferior products, like Pfizer's Geodon, can generate substantial sales. However, Vanda Pharmaceuticals' schizophrenia drug Fanapt is not seen as different enough from cheaper alternatives and has struggled commercially.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.477.550 von lawmeetstax am 24.08.15 22:07:39MDVN (TSRO, CLVS)
"Der PARP-Verkauf von Biomarin an Medivation läßt aufgrund des erzielten Preises die Schlußfolgerung zu, daß Ruca dann auch nicht viel Wert sein kann (nicht meine Behauptung, sondern Gedanke von Feuerstein...)"
Eigentlich sehe ich 4 relevante PARP-Hemmer: AZNs Olaparib, TSROs Niraparib, CLVS Rucaparib und BMRN/MDVNs Talazoparib. Dabei kommt Niraparib ursprünglich von Merck und Rucaparib von Pfizer.
Nicht alle PARP-Hemmer sind gleich... prinzipiell sehen sie in der Wirkung noch ähnlich aus, obwohl sie jeweils etwas anders und unterschiedlich stark auf PARP wirken. Ich meine Talazoparib soll am selektivsten und stärksten gegen PARP1/2 wirken.
Sie unterscheiden sich aber in der Entwicklung: Olaparib ist bereits zugelassen in Eierstockkrebs... allerdings nur in BCRA-mut und nicht in der längeren Maintenance-Therapie, d.h. Olaparib kann offiziell nur bei wenigen Patienten eingesetzt werden. Bei größeren Patientengruppen liegen Niraparib und Rucaparib meine ich in der Entwicklung inzwischen vorne. Zu Niraparib sollen wohl Ende des Jahres PIII_Daten in der 2nd-line Maintenance-Therapie kommen und zudem in den drei Gruppen BCRA-mut, HRD+ und HRD- Platin-sensitive. Wenn alles klappt, wäre dies das umfangreichste Label. Rucaparib könnten vielleicht nächsten Sommer Zulassungsdaten zu 2nd-line Maintenance-Therapie in BCRA-mut und HRD+ haben... HRD- Platin-sensitive wird meine ich nicht getestet. D.h. die aktuelle Zulassung von Olaparib gilt nur für den dunkel-blauen Bereich unter Treatment, Niraparib könnte demnächst im kompletten Bereich 2L-Maintenance (oder nur in Teilen) Zulassungsdaten haben, Rucaparib in 2L-Maintenance dunkel-blau und grün.
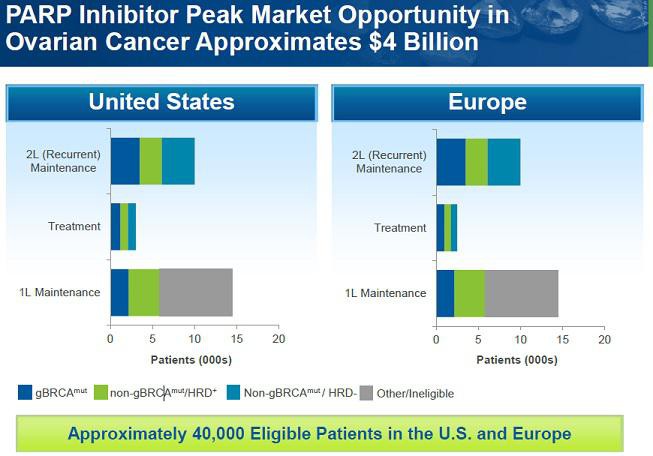
Rucaparib hat in Maintenance z.B. BTD, Olaparib nicht...

Talazoparib wird dagegen prinzipiell nicht gegen Eierstockkrebs entwickelt, vielleicht weil der Vorsprung der anderen zu groß war. Allerdings gibt es in Eierstockkrebs eine Studie, die Talazoparib testet, nachdem andere PARP-Hemmer keine Wirkung mehr zeigen. Der Ansatz hierfür ist wohl, dass Talazoparib theoretisch potenter ist (dies muss in der Praxis aber nicht unbedingt relevant sein, da bei PARP für die Wirkung nicht nur die Potenz zählt).
Statt in Eierstockkrebs befindet sich Talazoparib in BCRA-mut Brustkrebs in der PIII... wohl nächstes Jahr sollen diese vorliegen. Dagegen entwickelt z.B. CLVS Rucaparib bisher nicht, wohl aber Niraparib mit einer PIII. Ich denke, dass Talazoparib in Brustkrebs mit führend ist... BCRA-mut ist aber nur ein kleiner Teil der Brustkrebs-Patienten. Hier gibt es auch noch HRD+ (="BRCAness")
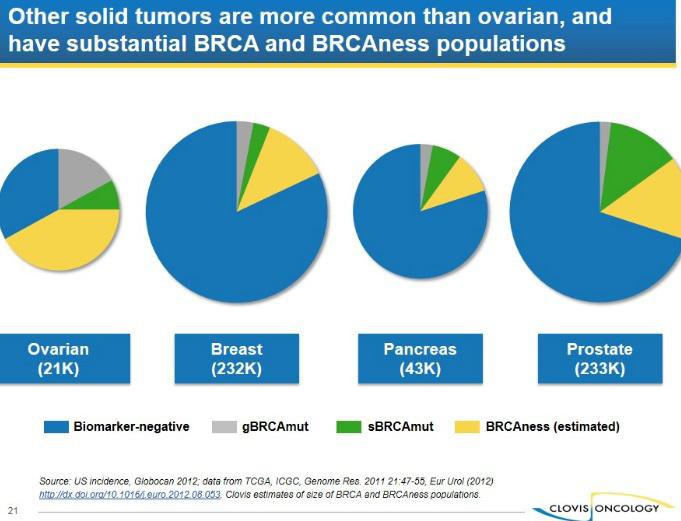
Auch in anderen Krebsarten könnten PARPs helfen. Ich hatte gedacht, dass MDVN insbesondere an Prostatakrebs Interesse hat.
PARP-Hemmer unterbrechen den Reparatur-Mechanismus von DNA-Einzelstrang-Brüchen. Krebszellen weisen zahlreiche Defekte auf. Wenn sie einen Defekt im Reparatur-Mechanismus von DNA-Doppelstrang-Brüchen wie BCRAmut besitzen, benötigen sie PARP, um sich teilen zu können. Solche Krebszellen sterben durch die Mono-Therapie mit PARP. Das ist der Ansatz für all das oben.
Ein anderer Einsatz wäre aber die Kombi mit Chemo-/Radiotherapien. Hierbei wird mit Absicht die DNA bei der Zellteilung beschädigt (jedenfalls wenn es sich um eine DNA-schädigende Chemo wie z.B. Cisplatin handelt). Krebszellen teilen sich sehr oft... wenn die Chemo dort genügend DNA-Schäden anrichtet, sterben die Krebszellen. Die sich nicht teilenden gesunden Zellen überleben. PARP kann als Reparatur-Mechanismus aber die geschädigten Krebszellen weiter am Leben halten. Theoretisch macht die PARP-Hemmung die Chemo deutlich wirksamer.
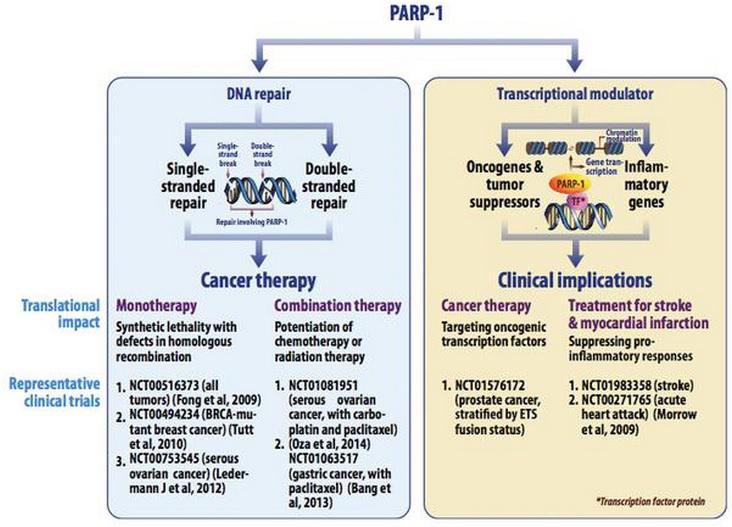
PARP-Hemmer + Chemo scheinen aber oft zu toxisch zu sein. Mit Talazoparib gibt es aber schon Studien für eine solche Kombi. Wenn ich MDVN in der CC bei MS vor ein paar Tagen richtig verstehe, sehen sie hier eine wesentliche Zukunft von Talazoparib. Der Chemo/Strahlentherapie-Markt wäre riesig.
Ein weiterer Einsatz von PARP könnte die IO-Kombi z.B. mit PD1 sein. Das Immunsystem kann erst aktiv werden, wenn Krebszellen Fehler aufweisen, die sie von gesunden Zellen unterschieden. PARP-Hemmer könnten Reparaturen von Fehlern verhindern und somit Krebszellen für das Immunsystem sichtbar machen.
Z.B. hier http://oncologydiscovery.com/2015/08/08/strategies-to-enhanc…
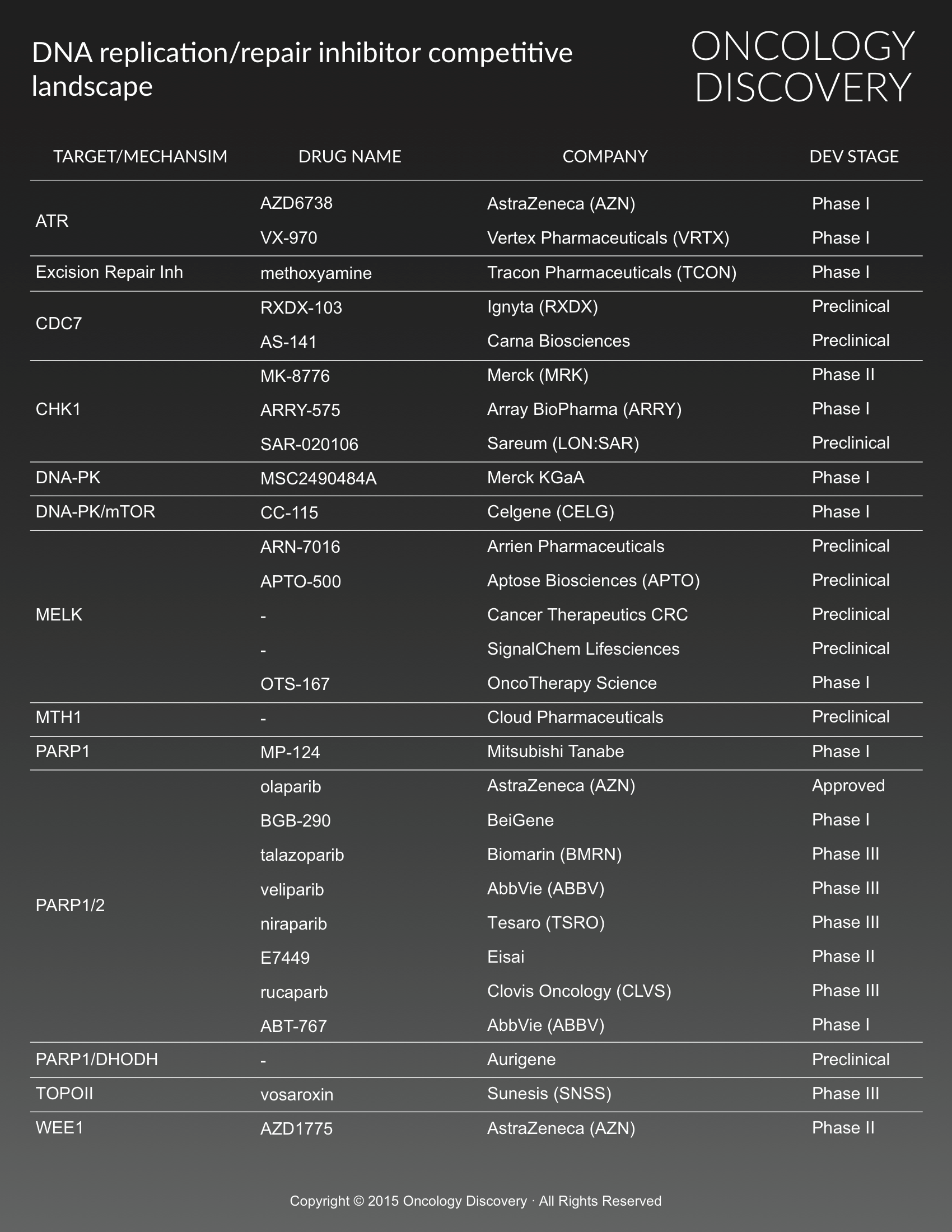
"...Our current understanding of checkpoint inhibitors suggests that highly mutated tumors can be seen by the immune system through neoantigen presentation. As a result, these cancers are primed for a checkpoint inhibitor-induced immune response. Unfortunately, not all tumors are highly mutated. A rational approach would seek to generate DNA alterations in tumors which have intrinsically low mutational burdens to induce increased neoantigen presentation. This could be achieved through the use of DNA replication/repair pathway inhibitors. For example, there are a number of approved and clinical-stage small molecule inhibitors of this pathway including inhibitors of PARP, DNA-PK, ATR, and WEE1 (see Figure 3 for a complete view on the competitive landscape). Deploying DNA damage pathway inhibitors as a means to induce neoantigen presentation makes good sense based on our current biological understanding of immuno-oncology..."
MDVN hat ja selber einen PD1 in der PIII. Diesen könnten sie mit Talazoparib kombinieren, u.U. zusammen mit Xtandi in Prostatakrebs oder in TNBC-Brustkrebs.
(PT vor Split)


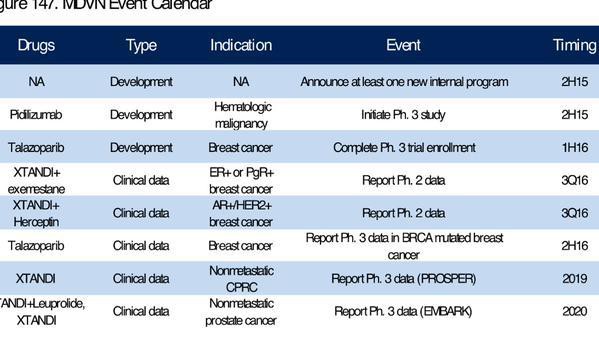

Gruß
ipollit
"Der PARP-Verkauf von Biomarin an Medivation läßt aufgrund des erzielten Preises die Schlußfolgerung zu, daß Ruca dann auch nicht viel Wert sein kann (nicht meine Behauptung, sondern Gedanke von Feuerstein...)"
Eigentlich sehe ich 4 relevante PARP-Hemmer: AZNs Olaparib, TSROs Niraparib, CLVS Rucaparib und BMRN/MDVNs Talazoparib. Dabei kommt Niraparib ursprünglich von Merck und Rucaparib von Pfizer.
Nicht alle PARP-Hemmer sind gleich... prinzipiell sehen sie in der Wirkung noch ähnlich aus, obwohl sie jeweils etwas anders und unterschiedlich stark auf PARP wirken. Ich meine Talazoparib soll am selektivsten und stärksten gegen PARP1/2 wirken.
Sie unterscheiden sich aber in der Entwicklung: Olaparib ist bereits zugelassen in Eierstockkrebs... allerdings nur in BCRA-mut und nicht in der längeren Maintenance-Therapie, d.h. Olaparib kann offiziell nur bei wenigen Patienten eingesetzt werden. Bei größeren Patientengruppen liegen Niraparib und Rucaparib meine ich in der Entwicklung inzwischen vorne. Zu Niraparib sollen wohl Ende des Jahres PIII_Daten in der 2nd-line Maintenance-Therapie kommen und zudem in den drei Gruppen BCRA-mut, HRD+ und HRD- Platin-sensitive. Wenn alles klappt, wäre dies das umfangreichste Label. Rucaparib könnten vielleicht nächsten Sommer Zulassungsdaten zu 2nd-line Maintenance-Therapie in BCRA-mut und HRD+ haben... HRD- Platin-sensitive wird meine ich nicht getestet. D.h. die aktuelle Zulassung von Olaparib gilt nur für den dunkel-blauen Bereich unter Treatment, Niraparib könnte demnächst im kompletten Bereich 2L-Maintenance (oder nur in Teilen) Zulassungsdaten haben, Rucaparib in 2L-Maintenance dunkel-blau und grün.

Rucaparib hat in Maintenance z.B. BTD, Olaparib nicht...

Talazoparib wird dagegen prinzipiell nicht gegen Eierstockkrebs entwickelt, vielleicht weil der Vorsprung der anderen zu groß war. Allerdings gibt es in Eierstockkrebs eine Studie, die Talazoparib testet, nachdem andere PARP-Hemmer keine Wirkung mehr zeigen. Der Ansatz hierfür ist wohl, dass Talazoparib theoretisch potenter ist (dies muss in der Praxis aber nicht unbedingt relevant sein, da bei PARP für die Wirkung nicht nur die Potenz zählt).
Statt in Eierstockkrebs befindet sich Talazoparib in BCRA-mut Brustkrebs in der PIII... wohl nächstes Jahr sollen diese vorliegen. Dagegen entwickelt z.B. CLVS Rucaparib bisher nicht, wohl aber Niraparib mit einer PIII. Ich denke, dass Talazoparib in Brustkrebs mit führend ist... BCRA-mut ist aber nur ein kleiner Teil der Brustkrebs-Patienten. Hier gibt es auch noch HRD+ (="BRCAness")

Auch in anderen Krebsarten könnten PARPs helfen. Ich hatte gedacht, dass MDVN insbesondere an Prostatakrebs Interesse hat.
PARP-Hemmer unterbrechen den Reparatur-Mechanismus von DNA-Einzelstrang-Brüchen. Krebszellen weisen zahlreiche Defekte auf. Wenn sie einen Defekt im Reparatur-Mechanismus von DNA-Doppelstrang-Brüchen wie BCRAmut besitzen, benötigen sie PARP, um sich teilen zu können. Solche Krebszellen sterben durch die Mono-Therapie mit PARP. Das ist der Ansatz für all das oben.
Ein anderer Einsatz wäre aber die Kombi mit Chemo-/Radiotherapien. Hierbei wird mit Absicht die DNA bei der Zellteilung beschädigt (jedenfalls wenn es sich um eine DNA-schädigende Chemo wie z.B. Cisplatin handelt). Krebszellen teilen sich sehr oft... wenn die Chemo dort genügend DNA-Schäden anrichtet, sterben die Krebszellen. Die sich nicht teilenden gesunden Zellen überleben. PARP kann als Reparatur-Mechanismus aber die geschädigten Krebszellen weiter am Leben halten. Theoretisch macht die PARP-Hemmung die Chemo deutlich wirksamer.

PARP-Hemmer + Chemo scheinen aber oft zu toxisch zu sein. Mit Talazoparib gibt es aber schon Studien für eine solche Kombi. Wenn ich MDVN in der CC bei MS vor ein paar Tagen richtig verstehe, sehen sie hier eine wesentliche Zukunft von Talazoparib. Der Chemo/Strahlentherapie-Markt wäre riesig.
Ein weiterer Einsatz von PARP könnte die IO-Kombi z.B. mit PD1 sein. Das Immunsystem kann erst aktiv werden, wenn Krebszellen Fehler aufweisen, die sie von gesunden Zellen unterschieden. PARP-Hemmer könnten Reparaturen von Fehlern verhindern und somit Krebszellen für das Immunsystem sichtbar machen.
Z.B. hier http://oncologydiscovery.com/2015/08/08/strategies-to-enhanc…

"...Our current understanding of checkpoint inhibitors suggests that highly mutated tumors can be seen by the immune system through neoantigen presentation. As a result, these cancers are primed for a checkpoint inhibitor-induced immune response. Unfortunately, not all tumors are highly mutated. A rational approach would seek to generate DNA alterations in tumors which have intrinsically low mutational burdens to induce increased neoantigen presentation. This could be achieved through the use of DNA replication/repair pathway inhibitors. For example, there are a number of approved and clinical-stage small molecule inhibitors of this pathway including inhibitors of PARP, DNA-PK, ATR, and WEE1 (see Figure 3 for a complete view on the competitive landscape). Deploying DNA damage pathway inhibitors as a means to induce neoantigen presentation makes good sense based on our current biological understanding of immuno-oncology..."
MDVN hat ja selber einen PD1 in der PIII. Diesen könnten sie mit Talazoparib kombinieren, u.U. zusammen mit Xtandi in Prostatakrebs oder in TNBC-Brustkrebs.
(PT vor Split)



Gruß
ipollit
Es war ja klar, dass die hohen Medikamentenpreise Thema im US-Wahlkampf werden.
Aktuell sorgt ein Tweet von Hillary Clinton dafür, dass der NBI regelrecht abschmiert.
"Price gouging like this in the specialty drug market is outrageous. Tomorrow I'll lay out a plan to take it on. -H "
Hintergrund ist ein Artikel über die von einem Hedge-Fonds Manager geleitete Firma Turing. Ein in meinen Augen völlig fehlgeleiteter und gänzlich unsympatischer Typ. Die Kritik finde ich also absolut berechtigt:
http://www.nytimes.com/2015/09/21/business/a-huge-overnight-…
oder: http://www.fiercebiotech.com/story/why-would-martin-shkreli-…
Schade nur, dass jetzt viele Firmen in Sippenhaft genommen werden. Mal schauen wie der Plan von Hillary morgen aussieht. Schön wäre es ja auch gewesen, den Plan gleich zu präsentieren und nicht so eine vage Ankündigung zu tweeten. Da kommt jetzt natürlich schön Panik auf. Und der Tag ist noch lang...
Aber im Wahlkampf werden vielleicht ja dann auch Pläne und Versprechungen gemacht, die sich dann später nicht umsetzen lassen. An eine Einführung der Planwirtschaft in den USA glaube ich nicht. Aber das man für ein Medikament verlangen kann was man will halte ich auch nicht für praktikabel. Einerseits kann im Wahlkampf auch eine populistische Idee kommen aber anderesits kann man jetzt auch nichts präsentieren, dass die Industrie zu sehr schwächt. Das wird sicherlich spannend morgen...
Aktuell sorgt ein Tweet von Hillary Clinton dafür, dass der NBI regelrecht abschmiert.
"Price gouging like this in the specialty drug market is outrageous. Tomorrow I'll lay out a plan to take it on. -H "
Hintergrund ist ein Artikel über die von einem Hedge-Fonds Manager geleitete Firma Turing. Ein in meinen Augen völlig fehlgeleiteter und gänzlich unsympatischer Typ. Die Kritik finde ich also absolut berechtigt:
http://www.nytimes.com/2015/09/21/business/a-huge-overnight-…
oder: http://www.fiercebiotech.com/story/why-would-martin-shkreli-…
Schade nur, dass jetzt viele Firmen in Sippenhaft genommen werden. Mal schauen wie der Plan von Hillary morgen aussieht. Schön wäre es ja auch gewesen, den Plan gleich zu präsentieren und nicht so eine vage Ankündigung zu tweeten. Da kommt jetzt natürlich schön Panik auf. Und der Tag ist noch lang...
Aber im Wahlkampf werden vielleicht ja dann auch Pläne und Versprechungen gemacht, die sich dann später nicht umsetzen lassen. An eine Einführung der Planwirtschaft in den USA glaube ich nicht. Aber das man für ein Medikament verlangen kann was man will halte ich auch nicht für praktikabel. Einerseits kann im Wahlkampf auch eine populistische Idee kommen aber anderesits kann man jetzt auch nichts präsentieren, dass die Industrie zu sehr schwächt. Das wird sicherlich spannend morgen...
Antwort auf Beitrag Nr.: 50.673.309 von kmastra am 21.09.15 18:23:44Das Thema Turing hat es bis in die Blödzeitung geschafft. Das lässt für den Biotechsektor hoffen - ist ja schon öfter ein Wendepunkt gewesen.
http://www.bild.de/ratgeber/gesundheit/gesundheit/ex-banker-…
Ansonsten wurden die Vorschläge von Clinton so wie ich es lese recht gelassen/neutral aufgenommen. Das Thema könnte im Wahlkampf aber weiter brodeln, da man damit sicherlich Stimmen gewinnen kann. Und das Thema auch angegangen werden muss. Ob und was dann umgesetz wird/ werden kann ist eine andere Sache...
http://www.thestreet.com/story/13296240/1/clinton-drug-plan-…
Im Grunde sollte die Pharma/Biotechbranche selber ein großes Interesse haben, das Thema anzugehen, bevor es ohne sie geregelt wird.
Ich gehe aber davon aus, dass gute, innovative Medikamente auch weiterhin einen hohen Preis rechtfertigen werden. Das ist vielleicht ja sogar gut für gute Biotechunternehmen (Übernahmen werden noch lukrativer). Es gibt zudem ja auch Medikamente, die langfrsitig die Gesundheitskasse entlasten. ACAD, ESPR, ENTA, eine Firma die das Problem Übergewicht "löst" könnte ZFGN werden...
Skeptisch bin ich eher bei Kombinationspräperaten in der Krebstherapie. Wie soll das bezahlt werden?
SG kmastra
http://www.bild.de/ratgeber/gesundheit/gesundheit/ex-banker-…
Ansonsten wurden die Vorschläge von Clinton so wie ich es lese recht gelassen/neutral aufgenommen. Das Thema könnte im Wahlkampf aber weiter brodeln, da man damit sicherlich Stimmen gewinnen kann. Und das Thema auch angegangen werden muss. Ob und was dann umgesetz wird/ werden kann ist eine andere Sache...
http://www.thestreet.com/story/13296240/1/clinton-drug-plan-…
Im Grunde sollte die Pharma/Biotechbranche selber ein großes Interesse haben, das Thema anzugehen, bevor es ohne sie geregelt wird.
Ich gehe aber davon aus, dass gute, innovative Medikamente auch weiterhin einen hohen Preis rechtfertigen werden. Das ist vielleicht ja sogar gut für gute Biotechunternehmen (Übernahmen werden noch lukrativer). Es gibt zudem ja auch Medikamente, die langfrsitig die Gesundheitskasse entlasten. ACAD, ESPR, ENTA, eine Firma die das Problem Übergewicht "löst" könnte ZFGN werden...
Skeptisch bin ich eher bei Kombinationspräperaten in der Krebstherapie. Wie soll das bezahlt werden?
SG kmastra
Panic selling . denke der Boden wird bald erreicht sein.
Antwort auf Beitrag Nr.: 50.728.068 von biopadawan am 28.09.15 19:33:47Was denkst du wo, 2900?
Antwort auf Beitrag Nr.: 50.728.068 von biopadawan am 28.09.15 19:33:47"Panic selling . denke der Boden wird bald erreicht sein."
Ich stimme zu, dass heute richtig Panik herrscht.
Schauen wir und die letzten 5 Jahre mal an:

Als ich diesen Chart vor einigen Wochen (Monaten) so gepostet habe, habe ich kommentiert: "Noch ist nicht viel passiert."
Das ist jetzt anders. Es ist eine ausgewachsene Korrektur, die nicht mehr weit weg ist, die Bezeichnung Crash zu verdienen.
Dennoch sieht man auch, dass wir immer noch auf fetten Gewinnen aus den letzten Jahren sitzen (theoretisch...).
Ich bin kein Charttechniker, aber mir scheint der Bereich zwischen 2.200 und 2.800 Punkte im NBI eine Zone zu sein, in der eine Beruhigung stattfinden könnte.
Aber wer weiß so etwas schon...
Fakt ist aber auch, dass die massive Korrektur ja auch die Schwergewichte wie AMGN, BIIB, CELG oder auch REGN, MDVN usw. trifft und wir dort auch nach meiner Meinung jetzt wieder vernünftige Bewertungsniveaus erreichen.
Ich bin heute jedenfalls mal wieder auf der Käuferseite (unter anderem bei QURE und REGN und bei vielen Werten aus dem Hammer-Depot).
Wo der Boden ist, weiß kein Mensch. Aber die Panik und die wieder vernünftigeren Bewertungen der Schwergewichte machen mir durchaus Hoffnung.
Der Knall war überfällig. Und jetzt ist er halt da. Im Grunde ist das gut so.
Ich stimme zu, dass heute richtig Panik herrscht.
Schauen wir und die letzten 5 Jahre mal an:
Als ich diesen Chart vor einigen Wochen (Monaten) so gepostet habe, habe ich kommentiert: "Noch ist nicht viel passiert."
Das ist jetzt anders. Es ist eine ausgewachsene Korrektur, die nicht mehr weit weg ist, die Bezeichnung Crash zu verdienen.
Dennoch sieht man auch, dass wir immer noch auf fetten Gewinnen aus den letzten Jahren sitzen (theoretisch...).
Ich bin kein Charttechniker, aber mir scheint der Bereich zwischen 2.200 und 2.800 Punkte im NBI eine Zone zu sein, in der eine Beruhigung stattfinden könnte.
Aber wer weiß so etwas schon...
Fakt ist aber auch, dass die massive Korrektur ja auch die Schwergewichte wie AMGN, BIIB, CELG oder auch REGN, MDVN usw. trifft und wir dort auch nach meiner Meinung jetzt wieder vernünftige Bewertungsniveaus erreichen.
Ich bin heute jedenfalls mal wieder auf der Käuferseite (unter anderem bei QURE und REGN und bei vielen Werten aus dem Hammer-Depot).
Wo der Boden ist, weiß kein Mensch. Aber die Panik und die wieder vernünftigeren Bewertungen der Schwergewichte machen mir durchaus Hoffnung.
Der Knall war überfällig. Und jetzt ist er halt da. Im Grunde ist das gut so.
ich finde die Korrektur schon sehr heftig. Man weiß ja oft gar nicht, ob es eine Meldung gegeben hat oder der Kurs einfach nur "normal" unter die Räder gekommen ist.
Ich haber hier zB viel Positives über Bluebird gelesen, die haben jetzt vom Hoch fast die Hälfte verloren....
Krass finde ich auch, dass es vor kurzem noch so aussah, als wäre die Korrektur im Wesentlichen vorbei, stattdessen ging es nochmal deutlichst nach unten....
Ich haber hier zB viel Positives über Bluebird gelesen, die haben jetzt vom Hoch fast die Hälfte verloren....
Krass finde ich auch, dass es vor kurzem noch so aussah, als wäre die Korrektur im Wesentlichen vorbei, stattdessen ging es nochmal deutlichst nach unten....
Antwort auf Beitrag Nr.: 50.728.716 von SLGramann am 28.09.15 20:44:08Hallo SLGramann,
bist du immer noch 90% Cash? Ich bin immer noch dabei und versuche die Sache möglichst entspannt anzugehen...

Wahrscheinlich wird im Moment auch viel von Leuten bewegt, die Biotechs beigemischt haben, ohne dass sie auf diesen Bereich beschränkt wären... die Generalisten. Momentum-Trader haben bestimmt auch ihren Spaß.
Es geht ja durch die Bank... siehst du eine MRNS nun auch wieder vernünftiger bewertet? -30% heute ohne News, soweit ich sehe. Oder eine VSTM... Studie angehalten, was natürlich nicht schön ist. Das wird in einem solchen Markt gleich mit -70% quittiert... macht eine MK von 66 Mio USD bei 132 Mio USD Cash, das ist momentan für den Markt fair.

Dagegen eine CELG... hat sich hier wirklich viel getan?

Grüße
ipollit
bist du immer noch 90% Cash? Ich bin immer noch dabei und versuche die Sache möglichst entspannt anzugehen...


Wahrscheinlich wird im Moment auch viel von Leuten bewegt, die Biotechs beigemischt haben, ohne dass sie auf diesen Bereich beschränkt wären... die Generalisten. Momentum-Trader haben bestimmt auch ihren Spaß.
Es geht ja durch die Bank... siehst du eine MRNS nun auch wieder vernünftiger bewertet? -30% heute ohne News, soweit ich sehe. Oder eine VSTM... Studie angehalten, was natürlich nicht schön ist. Das wird in einem solchen Markt gleich mit -70% quittiert... macht eine MK von 66 Mio USD bei 132 Mio USD Cash, das ist momentan für den Markt fair.
Dagegen eine CELG... hat sich hier wirklich viel getan?
Grüße
ipollit
Antwort auf Beitrag Nr.: 50.729.268 von xylophon am 28.09.15 21:53:33"als wäre die Korrektur im Wesentlichen vorbei, stattdessen ging es nochmal deutlichst nach unten...."
ja... das haben wir diesem netten Herrn hier zu verdanken. Unfassbar, dass man so jemanden noch frei herumlaufen lässt!

Diskussionen um Preise sind Gift in diesem Markt... wenn die Gefahr besteht, dass Patente entzogen werden und somit bisher einkalkulierte Gewinne dahinschmelzen, ergreifen Generalisten die Flucht.
Gruß
ipollit
ja... das haben wir diesem netten Herrn hier zu verdanken. Unfassbar, dass man so jemanden noch frei herumlaufen lässt!


Diskussionen um Preise sind Gift in diesem Markt... wenn die Gefahr besteht, dass Patente entzogen werden und somit bisher einkalkulierte Gewinne dahinschmelzen, ergreifen Generalisten die Flucht.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.729.325 von ipollit am 28.09.15 22:00:21Hallo ipollit,
nein, ich bin wieder mit fast 60% drin und werde vermutlich weiter aufstocken. Hammer geht ja davon aus, dass wir noch ein Jahr Baisse im Biotechbereich vor uns haben könnten... na ja, wer weiß.
MRNS ist ein gutes Beispiel. Heute -30% im Tagesverlauf - einfach mal so. Waren sie vorher viel zu teuer? Eigentlich nicht unbedingt.
Oder EXEL - die Cabo-Daten sind doch wohl werthaltig, doch auch die Aktie fällt.
Solche Beispiele bringen mich zu der Aussage, dass wir heute Panik gesehen haben. Möglicherweise zum Teil auch die emotionslose Panik irgendwelcher Trading-Algos.
Was CELG (und andere Schwergewichte) angeht: Nein, da hat sich (noch?) nicht so schrecklich viel getan. Aber nehmen wir an, die Aktie fällt auf 90 Dollar und in drei Monaten schauen wir auf die Gewinne des Jahres 2017 voraus.
Dann haben wir unter KGV- und Wachstums-Aspekten doch wirklich eine hoch attraktive Aktie vor uns. Bei den Schwergewichten ist es ja so, dass die Gewinne deutlich wachsen und die so über die Zeit selbst bei einer einigermaßen maßvollen Korrektur von bspw 20% vom Top irgendwann wieder spannend werden.
Obschon wir sicher eine Überhitzung (und meiner Meinung nach ein Blase) im Biotechsektor hatten, sollte man nicht vergessen, dass so manches auch fundamental getragen wird. Es gab viele reale wissenschaftliche Fortschritte und es werden reale Umsätze und Gewinne gemacht - und das wird sich auch nicht durch eine eventuelle vernünftigere Regulierung der Preise grundsätzlich ändern.
PS - mit "Wort zum Sonntag":
"Der Markt" kann eben nur Hysterie. Entweder manisch oder depressiv, egal, jedenfalls immer hysterisch. Wie wir seit den 80er Jahren auf die Idee kommen konnten, der Markt habe immer recht und man sollte dem Markt die Steuerung der menschlichen Gesellschaft überlassen, ist mir heute (seit 2007/2008) ein großes Rätsel. Der "Neoliberalismus" ist der ideologische Irrweg meines Lebens gewesen. Heute - wo dieses Konzept alternativlos realisiert worden ist - kann ich darüber nur noch traurig lachen.)
nein, ich bin wieder mit fast 60% drin und werde vermutlich weiter aufstocken. Hammer geht ja davon aus, dass wir noch ein Jahr Baisse im Biotechbereich vor uns haben könnten... na ja, wer weiß.
MRNS ist ein gutes Beispiel. Heute -30% im Tagesverlauf - einfach mal so. Waren sie vorher viel zu teuer? Eigentlich nicht unbedingt.
Oder EXEL - die Cabo-Daten sind doch wohl werthaltig, doch auch die Aktie fällt.
Solche Beispiele bringen mich zu der Aussage, dass wir heute Panik gesehen haben. Möglicherweise zum Teil auch die emotionslose Panik irgendwelcher Trading-Algos.
Was CELG (und andere Schwergewichte) angeht: Nein, da hat sich (noch?) nicht so schrecklich viel getan. Aber nehmen wir an, die Aktie fällt auf 90 Dollar und in drei Monaten schauen wir auf die Gewinne des Jahres 2017 voraus.
Dann haben wir unter KGV- und Wachstums-Aspekten doch wirklich eine hoch attraktive Aktie vor uns. Bei den Schwergewichten ist es ja so, dass die Gewinne deutlich wachsen und die so über die Zeit selbst bei einer einigermaßen maßvollen Korrektur von bspw 20% vom Top irgendwann wieder spannend werden.
Obschon wir sicher eine Überhitzung (und meiner Meinung nach ein Blase) im Biotechsektor hatten, sollte man nicht vergessen, dass so manches auch fundamental getragen wird. Es gab viele reale wissenschaftliche Fortschritte und es werden reale Umsätze und Gewinne gemacht - und das wird sich auch nicht durch eine eventuelle vernünftigere Regulierung der Preise grundsätzlich ändern.
PS - mit "Wort zum Sonntag":
"Der Markt" kann eben nur Hysterie. Entweder manisch oder depressiv, egal, jedenfalls immer hysterisch. Wie wir seit den 80er Jahren auf die Idee kommen konnten, der Markt habe immer recht und man sollte dem Markt die Steuerung der menschlichen Gesellschaft überlassen, ist mir heute (seit 2007/2008) ein großes Rätsel. Der "Neoliberalismus" ist der ideologische Irrweg meines Lebens gewesen. Heute - wo dieses Konzept alternativlos realisiert worden ist - kann ich darüber nur noch traurig lachen.)
Antwort auf Beitrag Nr.: 50.729.490 von ipollit am 28.09.15 22:20:42ah, danke. Ich hatte nur von dem Clinton-Vorschlag gelesen, aber nicht woher er kam. Das erklärt natürlich manches...
Es zeigt sich mal wieder, dass zu viel Gier am Ende nach hinten losgehen kann. Ein guter Geschäftmann presst nicht den letzten Cent aus seinen Kunden/Lieferanten, sondern denkt in größeren Dimensionen. Man will ja länger zusammenarbeiten.
Es zeigt sich mal wieder, dass zu viel Gier am Ende nach hinten losgehen kann. Ein guter Geschäftmann presst nicht den letzten Cent aus seinen Kunden/Lieferanten, sondern denkt in größeren Dimensionen. Man will ja länger zusammenarbeiten.
Hallo BioTech-Freunde,
hat sich jemand von Euch mit dem heutigen 35%-Absturz von RXDX, Ignyta beschäftigt und kann einschätzen woran es lag?
Ignyta hat auf dem ECC am Wochenende Phase1-Zwischenergebnisse seines ALK-Inhibitors entrectinib vorgestellt, und ich kann die Ergebnisse nicht als schlecht erkennen. Was geht hier ab?
(Bin glücklicherweise bei 14.30 erstmal raus, wollte aber wieder einsteigen, gut, dass erstmal nicht. Heute SK 8.72.)
Irgendwelche Meinungen?
Gruß
TwoPack
hat sich jemand von Euch mit dem heutigen 35%-Absturz von RXDX, Ignyta beschäftigt und kann einschätzen woran es lag?
Ignyta hat auf dem ECC am Wochenende Phase1-Zwischenergebnisse seines ALK-Inhibitors entrectinib vorgestellt, und ich kann die Ergebnisse nicht als schlecht erkennen. Was geht hier ab?
(Bin glücklicherweise bei 14.30 erstmal raus, wollte aber wieder einsteigen, gut, dass erstmal nicht. Heute SK 8.72.)
Irgendwelche Meinungen?
Gruß
TwoPack
Antwort auf Beitrag Nr.: 50.730.090 von TwoPack am 29.09.15 00:31:30"hat sich jemand von Euch mit dem heutigen 35%-Absturz von RXDX, Ignyta beschäftigt und kann einschätzen woran es lag?"
Man sollte nicht versuchen, irgendeine Logik in den Kursbewegungen zu sehen. RXDX hat gestern eine AdHoc-Meldung herausgebracht... das ist ausreichend Grund, der Inhalt ist irrelevant. EPZMs Daten waren auch eher gut... aber aufgrund der AdHoc-Meldung ging es gleichfalls 30% nach unten. Am besten man verhält sich in diesen Zeiten unauffällig... irgendetwas bekannt zu geben ist generell schlecht!
Theoretisch wird es ESPR heute zerreißen... ihre AdHoc heute enthält eher leicht negatives. Das kommt also noch zu den obligatorischen -30% für die News hinzu. War ESPR nicht ein großer Favorit von Hammer? 120 USD -> 30 USD...
Gruß
ipollit
Man sollte nicht versuchen, irgendeine Logik in den Kursbewegungen zu sehen. RXDX hat gestern eine AdHoc-Meldung herausgebracht... das ist ausreichend Grund, der Inhalt ist irrelevant. EPZMs Daten waren auch eher gut... aber aufgrund der AdHoc-Meldung ging es gleichfalls 30% nach unten. Am besten man verhält sich in diesen Zeiten unauffällig... irgendetwas bekannt zu geben ist generell schlecht!
Theoretisch wird es ESPR heute zerreißen... ihre AdHoc heute enthält eher leicht negatives. Das kommt also noch zu den obligatorischen -30% für die News hinzu. War ESPR nicht ein großer Favorit von Hammer? 120 USD -> 30 USD...

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.729.904 von xylophon am 28.09.15 23:21:58"Ein guter Geschäftmann..."
sieht so ein guter Geschäftsmann aus?...
der Typ ist ein ehemaliger Hedge-Fond-"Manager", der durch aggressives Shorten u.a. von Biotechs aufgefallen ist. Er wird momentan von seiner letzten Firma Retrophin, bei der er auch einfach alte Medikamente aufkaufte, diese gegen Generikas abschirmte und Wucher-Preise einführte, auf 65 Mio USD Schadensersatz verklagt... http://www.fiercebiotech.com/story/retrophin-comes-after-shk… Der macht eher den Eindruck eines jugendlichen Rüpels... ich glaube nicht, dass der eine Firma leiten kann und von Medikamentenentwicklung hat der erst recht keine Ahnung... kann ich mir zumindest nur äußerst schwer vorstellen!
https://www.youtube.com/watch?v=vx6Ct8kG0iU
Gruß
ipollit
sieht so ein guter Geschäftsmann aus?...

der Typ ist ein ehemaliger Hedge-Fond-"Manager", der durch aggressives Shorten u.a. von Biotechs aufgefallen ist. Er wird momentan von seiner letzten Firma Retrophin, bei der er auch einfach alte Medikamente aufkaufte, diese gegen Generikas abschirmte und Wucher-Preise einführte, auf 65 Mio USD Schadensersatz verklagt... http://www.fiercebiotech.com/story/retrophin-comes-after-shk… Der macht eher den Eindruck eines jugendlichen Rüpels... ich glaube nicht, dass der eine Firma leiten kann und von Medikamentenentwicklung hat der erst recht keine Ahnung... kann ich mir zumindest nur äußerst schwer vorstellen!
https://www.youtube.com/watch?v=vx6Ct8kG0iU

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.730.519 von ipollit am 29.09.15 07:59:44"Theoretisch wird es ESPR heute zerreißen... ihre AdHoc heute enthält eher leicht negatives. Das kommt also noch zu den obligatorischen -30% für die News hinzu."
So wird es wahrscheinlich sein. Und an solchen Dingen sieht man, dass Irrationalität auch nach unten möglich ist.
Wir kommen jetzt in die Phase, wo nur noch das Negative und die Risiken gesehen werden und niemand mehr viel darauf gibt, in welchem Verhältnis die Marktkapitalisierung zu den künftigen Chancen steht.
Wie gesagt, der Markt kann nur eindimensional und hysterisch sein - egal, welche Richtung.
So wird es wahrscheinlich sein. Und an solchen Dingen sieht man, dass Irrationalität auch nach unten möglich ist.
Wir kommen jetzt in die Phase, wo nur noch das Negative und die Risiken gesehen werden und niemand mehr viel darauf gibt, in welchem Verhältnis die Marktkapitalisierung zu den künftigen Chancen steht.
Wie gesagt, der Markt kann nur eindimensional und hysterisch sein - egal, welche Richtung.
Antwort auf Beitrag Nr.: 50.730.657 von SLGramann am 29.09.15 08:24:13Bin auch der Ansicht, dass ESPR gut in den 20er Bereich gehen wird. Daran wird bei diesem Marke kein Weg dran vorbei führen. Das Management hat sich als "etwas" unfähig erwiesen IMO. Premarket bereits -10 %
Wie ist Eure Taktik während einer solchen Crash-Phase? Kaufen, Verkaufen, Halten?
Für einen Verkauf scheint es mir fast schon spät zu sein ;-)
Eine Erholung des Marktes wird diesmal sicherlich längere Zeit in Anspruch nehmen, so wie es hier einige Kandidaten zerfetzt hat bzw. noch zerfetzen wird.
Aber an sich auch keine schlechte Sache, dass von nun an wieder vernünftigere Bewertungen herrschen (sicherlich kann man bei einigen Titeln darüber streiten). Aber letztendlich trennt sich die Spreu vom Weizen und wir werden in Zukunft mit unseren guten Titeln dennoch Erfolg haben.
Diese Woche wird aber noch grausig... ;-)
Wie ist Eure Taktik während einer solchen Crash-Phase? Kaufen, Verkaufen, Halten?
Für einen Verkauf scheint es mir fast schon spät zu sein ;-)
Eine Erholung des Marktes wird diesmal sicherlich längere Zeit in Anspruch nehmen, so wie es hier einige Kandidaten zerfetzt hat bzw. noch zerfetzen wird.
Aber an sich auch keine schlechte Sache, dass von nun an wieder vernünftigere Bewertungen herrschen (sicherlich kann man bei einigen Titeln darüber streiten). Aber letztendlich trennt sich die Spreu vom Weizen und wir werden in Zukunft mit unseren guten Titeln dennoch Erfolg haben.
Diese Woche wird aber noch grausig... ;-)
Antwort auf Beitrag Nr.: 50.730.600 von ipollit am 29.09.15 08:18:16Man merkt doch wieder das Menschen Fluchttiere sind. Hinter dem kleinsten Knacken im Unterholz wird die größtmögliche Katastrophe vermutet. Einer rationalen Überprüfung halten solche Szenarien aber nicht stand...
Martin Shkreli eignet sich natürlich ganz hervorragend als Hassobjekt und wird/wurde von den Medien auch entsprechend ausgeschlachtet. Der Typ ist in meinen Augen ein Psychopath. Das soll es ja in den Chefetagen recht häufig geben:
http://www.spiegel.de/karriere/berufsleben/fuehrungskraefte-…
Ein gutes Beispiel wie wenig der Herr als CEO geeignet ist:
http://www.thefrisky.com/2015-09-22/martin-shkreli-harassmen…
Die Demokraten haben jetzt auch Valeant im Visier:
http://www.streetinsider.com/Corporate+News/Democratics+Lett…
Auch das ist ein Geschäftsmodell das man durchaus an den Pranger stellen darf und sollte. Immer nur teuer kaufen und das dann an die Patienten weiterreichen ist kein nachhaltiges Geschäftsmodell. Selber forschen - zu riskant?!
Bisher bezieht sich allerdings die Kritik ja gar nicht auf die hohen Preise innovativer Produkte. Und ich bin mir ziemlich sicher, dass sich in den USA weiterhin höhere Preise als in z.B. der EU rechtfertigen lassen.
ESPR:
Das nun ein CVOT vor der Zulassung notweng sein könnte, ist vor dem Hintergrund der Kommunikation von Esperion selber, enttäuschend. Aus Sicht der FDA macht es natürlich Sinn den Ball flach zu halten. Könnte ist natürlich keine Formulierung, die an der Börse gut ankommt. Die Frage ist, ob das nicht im Grunde schon eingepreist war?
Martin Shkreli eignet sich natürlich ganz hervorragend als Hassobjekt und wird/wurde von den Medien auch entsprechend ausgeschlachtet. Der Typ ist in meinen Augen ein Psychopath. Das soll es ja in den Chefetagen recht häufig geben:
http://www.spiegel.de/karriere/berufsleben/fuehrungskraefte-…
Ein gutes Beispiel wie wenig der Herr als CEO geeignet ist:
http://www.thefrisky.com/2015-09-22/martin-shkreli-harassmen…
Die Demokraten haben jetzt auch Valeant im Visier:
http://www.streetinsider.com/Corporate+News/Democratics+Lett…
Auch das ist ein Geschäftsmodell das man durchaus an den Pranger stellen darf und sollte. Immer nur teuer kaufen und das dann an die Patienten weiterreichen ist kein nachhaltiges Geschäftsmodell. Selber forschen - zu riskant?!
Bisher bezieht sich allerdings die Kritik ja gar nicht auf die hohen Preise innovativer Produkte. Und ich bin mir ziemlich sicher, dass sich in den USA weiterhin höhere Preise als in z.B. der EU rechtfertigen lassen.
ESPR:
Das nun ein CVOT vor der Zulassung notweng sein könnte, ist vor dem Hintergrund der Kommunikation von Esperion selber, enttäuschend. Aus Sicht der FDA macht es natürlich Sinn den Ball flach zu halten. Könnte ist natürlich keine Formulierung, die an der Börse gut ankommt. Die Frage ist, ob das nicht im Grunde schon eingepreist war?
Antwort auf Beitrag Nr.: 50.730.786 von biopadawan am 29.09.15 08:37:19
so in der Art sehe ich das auch
m.E.n. sind noch genug Möglichkeiten vorhanden,
aber die werden, auch, selektiver werden
gruß
P.
Zitat von biopadawan: Eine Erholung des Marktes wird diesmal sicherlich längere Zeit in Anspruch nehmen, so wie es hier einige Kandidaten zerfetzt hat bzw. noch zerfetzen wird.
Aber an sich auch keine schlechte Sache, dass von nun an wieder vernünftigere Bewertungen herrschen (sicherlich kann man bei einigen Titeln darüber streiten). Aber letztendlich trennt sich die Spreu vom Weizen und wir werden in Zukunft mit unseren guten Titeln dennoch Erfolg haben.
Diese Woche wird aber noch grausig... ;-)
so in der Art sehe ich das auch
m.E.n. sind noch genug Möglichkeiten vorhanden,
aber die werden, auch, selektiver werden
gruß
P.
Antwort auf Beitrag Nr.: 50.731.149 von kmastra am 29.09.15 09:14:53ESPR
Premarket -26,82% (25.68$)
spätestens jetzt dürfte klar sein in welchem Zustand der Markt zur Zeit ist ;-)
Wer hier für unter 30 das Ding raushaut ist auf jeden Fall nicht mehr zu rationalen Gedanken fähig!
Heute wirds spannend. In diesem Sinne.
Premarket -26,82% (25.68$)
spätestens jetzt dürfte klar sein in welchem Zustand der Markt zur Zeit ist ;-)
Wer hier für unter 30 das Ding raushaut ist auf jeden Fall nicht mehr zu rationalen Gedanken fähig!
Heute wirds spannend. In diesem Sinne.
Antwort auf Beitrag Nr.: 50.734.500 von biopadawan am 29.09.15 15:16:34
Wenn sie jedoch bei 14 angekommen sein sollte, war es im Nachhinein gesehen die goldrichtige Entscheidung und sehr vernünftig
Zitat von biopadawan: ESPR
Wer hier für unter 30 das Ding raushaut ist auf jeden Fall nicht mehr zu rationalen Gedanken fähig!
Wenn sie jedoch bei 14 angekommen sein sollte, war es im Nachhinein gesehen die goldrichtige Entscheidung und sehr vernünftig

Die Frage ist, ob das nicht im Grunde schon eingepreist war?
O.k. war es nicht! Wobei: Was wäre denn heute passiert, wenn ESPR noch bei 100 $ gestanden hätte? Ein Kursverlust von 75%? Am Medikament hat sich ja nichts geändert - es gibt zugegeben jetzt mehr Unsicherheitsfaktoren:
-Wie verläuft die P2 mit hochdosierten Statinen? (Sicherheit und Effektivität)
-Ergebnisse der CVOT von CETP und PCSK9?
-Ergebnisse der CVOT von 1002?
Ich habe einen Teil meiner 2. Assetklasse aufgelöst und bei ESPR zugekauft. ESPR wird momentan mit 500 Mio$ bewertet. Cashbestand sind um die 300 Mio. (Geld wird aber voll für die Entwicklung von 1002 draufgehen). Mit einer schnellen Kurserholung rechne ich nicht unbedingt, ebenso klang es im CC so, als würde man das eher alleine durchziehen wollen. Eine Übernahme im dreistelligen Bereich ist wohl momentan auch eher auszuschließen...
O.k. war es nicht! Wobei: Was wäre denn heute passiert, wenn ESPR noch bei 100 $ gestanden hätte? Ein Kursverlust von 75%? Am Medikament hat sich ja nichts geändert - es gibt zugegeben jetzt mehr Unsicherheitsfaktoren:
-Wie verläuft die P2 mit hochdosierten Statinen? (Sicherheit und Effektivität)
-Ergebnisse der CVOT von CETP und PCSK9?
-Ergebnisse der CVOT von 1002?
Ich habe einen Teil meiner 2. Assetklasse aufgelöst und bei ESPR zugekauft. ESPR wird momentan mit 500 Mio$ bewertet. Cashbestand sind um die 300 Mio. (Geld wird aber voll für die Entwicklung von 1002 draufgehen). Mit einer schnellen Kurserholung rechne ich nicht unbedingt, ebenso klang es im CC so, als würde man das eher alleine durchziehen wollen. Eine Übernahme im dreistelligen Bereich ist wohl momentan auch eher auszuschließen...
Antwort auf Beitrag Nr.: 50.736.708 von kmastra am 29.09.15 18:20:43"ESPR wird momentan mit 500 Mio$ bewertet. Cashbestand sind um die 300 Mio. (Geld wird aber voll für die Entwicklung von 1002 draufgehen)."
Wenn der Kurs auf den gegenwärtigen Cashbestand fällt, sind das die von TwoPack ins Spiel gebrachten 14 Dollar.
Wer weiß, vielleicht sind für "Pipeline-Biotechs" erst die Cashbestände die Auffanglinie für die Kurse.
Der Markt kann jetzt ja ruhig mal sämtliche Pipelineprojekte mit Null bewerten, nachdem man bis vor wenigen Monaten alles mit Milliarden bewertet hat. Macht alles irre viel Sinn...
Macht alles irre viel Sinn...
MCRB: Ich habe heute eine erste Position bei Seres gekauft. Die fand ich ja schon beim IPO ziemlich toll, aber bisher immer arg teuer (kommen von über 50 Dollar).
Aber vermutlich gilt auch hier: In ein paar Tagen/Wochen bekomme ich sie für 15 Dollar.
Wenn der Kurs auf den gegenwärtigen Cashbestand fällt, sind das die von TwoPack ins Spiel gebrachten 14 Dollar.
Wer weiß, vielleicht sind für "Pipeline-Biotechs" erst die Cashbestände die Auffanglinie für die Kurse.
Der Markt kann jetzt ja ruhig mal sämtliche Pipelineprojekte mit Null bewerten, nachdem man bis vor wenigen Monaten alles mit Milliarden bewertet hat.
 Macht alles irre viel Sinn...
Macht alles irre viel Sinn...MCRB: Ich habe heute eine erste Position bei Seres gekauft. Die fand ich ja schon beim IPO ziemlich toll, aber bisher immer arg teuer (kommen von über 50 Dollar).
Aber vermutlich gilt auch hier: In ein paar Tagen/Wochen bekomme ich sie für 15 Dollar.

IBB, XBI
Bisher gibt es einen kleinen Boden in der Abwärtsbewegung... mal schauen, wie es weiter geht. Saisonal ist es für Biotechs zum Jahreswechsel/Frühjahr meistens eine eher bessere Zeit gewesen.
IBB
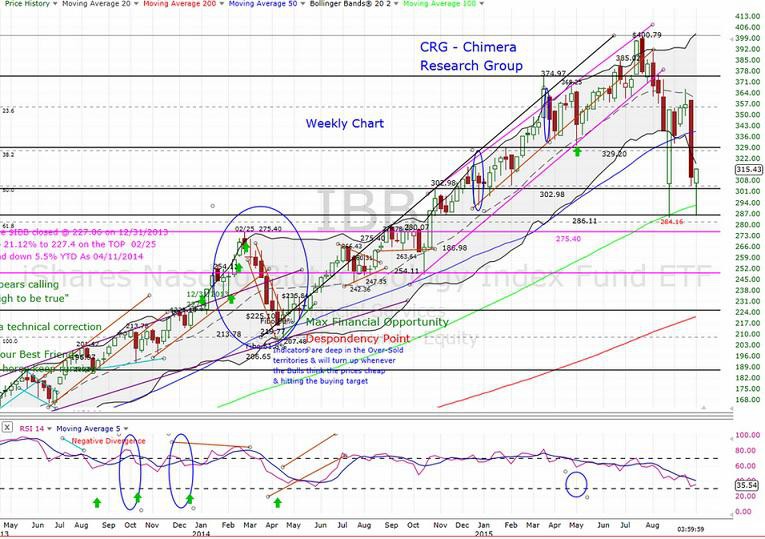
XBI (enthält mehr kleinere Biotechs)
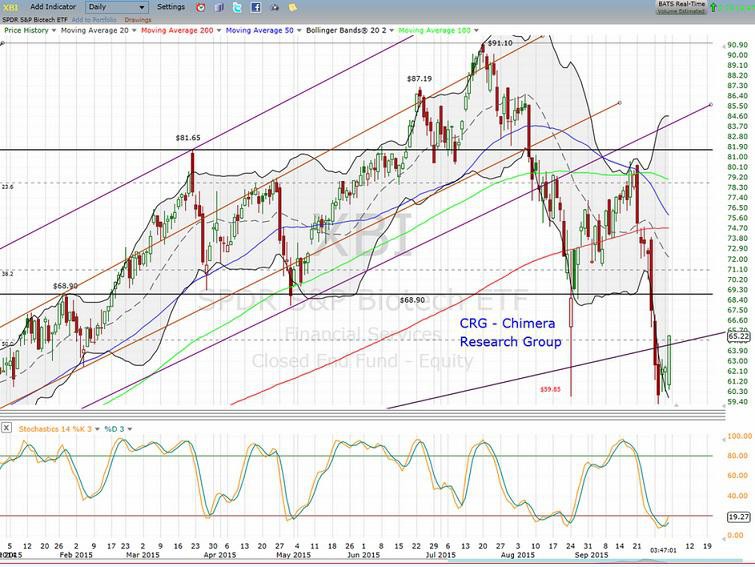
Gruß
ipollit
Bisher gibt es einen kleinen Boden in der Abwärtsbewegung... mal schauen, wie es weiter geht. Saisonal ist es für Biotechs zum Jahreswechsel/Frühjahr meistens eine eher bessere Zeit gewesen.
IBB

XBI (enthält mehr kleinere Biotechs)

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.737.770 von SLGramann am 29.09.15 20:45:37



eine frage
weil ihr hier immer wieder welche einstellt,
aber nur teile -habt ihr broker/recherchezugänge?
gruß
P.
Zitat von SLGramann: Der Markt kann jetzt ja ruhig mal sämtliche Pipelineprojekte mit Null bewerten, nachdem man bis vor wenigen Monaten alles mit Milliarden bewertet hat.Macht alles irre viel Sinn...



eine frage
weil ihr hier immer wieder welche einstellt,
aber nur teile -habt ihr broker/recherchezugänge?
gruß
P.
Arry
Es wurde ja im Markt von einigen in Zweifel gezogen, ob Bini und Enco tatsächlich konkurrenzfähig sein können, denn warum sonst hätte Novartis sie seinerzeit abgeben sollen...? Auf dieser Annahme beruht wahrscheinlich auch die sehr starke Erhöhung der Shortquote.
Vorgestern ist in der Financial Times ein lobender Artikel über die Qualität der Arbeit der damals beteiligten Anwälte erschienen. Ausweislich dieses Artikels waren die Forderungen der EU-Kartellbehörden nicht nur kartellrechtliches Neuland, sondern kamen für Novartis auch überraschend. Offenbar hatte Novartis zu Beginn gar nicht damit gerechnet, beide Assets abgeben zu müssen. Erst die am Ende entstandene Hektik im Verfahren hat zu dieser Entscheidung geführt. Man mußte sehr schnell eine Lösung erarbeiten, um nicht noch höhere Kostennachteile zu riskieren.
Ich hatte Ähnliches zwar schon vermutet, aber dies ist eine nette Bestätigung. Für die Shorts eine ungünstige Wendung.
http://www.ft.com/intl/cms/s/2/c3158492-5ac4-11e5-9846-de406…
Es wurde ja im Markt von einigen in Zweifel gezogen, ob Bini und Enco tatsächlich konkurrenzfähig sein können, denn warum sonst hätte Novartis sie seinerzeit abgeben sollen...? Auf dieser Annahme beruht wahrscheinlich auch die sehr starke Erhöhung der Shortquote.
Vorgestern ist in der Financial Times ein lobender Artikel über die Qualität der Arbeit der damals beteiligten Anwälte erschienen. Ausweislich dieses Artikels waren die Forderungen der EU-Kartellbehörden nicht nur kartellrechtliches Neuland, sondern kamen für Novartis auch überraschend. Offenbar hatte Novartis zu Beginn gar nicht damit gerechnet, beide Assets abgeben zu müssen. Erst die am Ende entstandene Hektik im Verfahren hat zu dieser Entscheidung geführt. Man mußte sehr schnell eine Lösung erarbeiten, um nicht noch höhere Kostennachteile zu riskieren.
Ich hatte Ähnliches zwar schon vermutet, aber dies ist eine nette Bestätigung. Für die Shorts eine ungünstige Wendung.
http://www.ft.com/intl/cms/s/2/c3158492-5ac4-11e5-9846-de406…
ONCE (Spark Therapeutics):
Positives Ergebnis der PIII ihrer Gentherapie für Erblindungen aufgrund eines RPE65-Gendefekts:
PHILADELPHIA, Oct. 05, 2015 (GLOBE NEWSWIRE) -- Spark Therapeutics (NASDAQ:ONCE) today announced positive top-line results from the Phase 3 pivotal trial of its lead gene therapy product candidate, SPK-RPE65, for the treatment of RPE65-mediated inherited retinal dystrophies (IRDs).
The pivotal trial met its primary endpoint (p = 0.001), demonstrating improvement of functional vision in the intervention group compared to the control group, as measured by the change in bilateral mobility testing between baseline and one year.
http://ir.sparktx.com/phoenix.zhtml?c=253900&p=irol-newsArti…
Kurs steigt heute maßvoll um derzeit 22%, was mich zum Rückkauf meiner vor einiger Zeit verkauften Position veranlasst hat.
Zulassung soll 2016 beantragt werden. Gentherapie ist natürlich in Sachen Zulassung und Abrechnung ziemliches Neuland, so dass es da noch holprig werden könnte.
Umsatzpotential wird auf mehrere 100 Mio. Dollar weltweit geschätzt (600 Mio. von J.P. Morgan, zitiert nach Brad Loncar). Fraglich ist aber, ob dann nicht die Mehrheit der Patienten (zumindest für längere Zeit) "geheilt" sein wird - was natürlich medizinisch Sinn der Sache ist.
Langfristig könnte das jetzt aber auch erst mal nur der erste Schritt gewesen sein.
Hier noch etwas Hintergrund von Piper Jaffray:
http://online.liebertpub.com/doi/pdf/10.1089/humc.2015.29001…
Positives Ergebnis der PIII ihrer Gentherapie für Erblindungen aufgrund eines RPE65-Gendefekts:
PHILADELPHIA, Oct. 05, 2015 (GLOBE NEWSWIRE) -- Spark Therapeutics (NASDAQ:ONCE) today announced positive top-line results from the Phase 3 pivotal trial of its lead gene therapy product candidate, SPK-RPE65, for the treatment of RPE65-mediated inherited retinal dystrophies (IRDs).
The pivotal trial met its primary endpoint (p = 0.001), demonstrating improvement of functional vision in the intervention group compared to the control group, as measured by the change in bilateral mobility testing between baseline and one year.
http://ir.sparktx.com/phoenix.zhtml?c=253900&p=irol-newsArti…
Kurs steigt heute maßvoll um derzeit 22%, was mich zum Rückkauf meiner vor einiger Zeit verkauften Position veranlasst hat.
Zulassung soll 2016 beantragt werden. Gentherapie ist natürlich in Sachen Zulassung und Abrechnung ziemliches Neuland, so dass es da noch holprig werden könnte.
Umsatzpotential wird auf mehrere 100 Mio. Dollar weltweit geschätzt (600 Mio. von J.P. Morgan, zitiert nach Brad Loncar). Fraglich ist aber, ob dann nicht die Mehrheit der Patienten (zumindest für längere Zeit) "geheilt" sein wird - was natürlich medizinisch Sinn der Sache ist.
Langfristig könnte das jetzt aber auch erst mal nur der erste Schritt gewesen sein.
Hier noch etwas Hintergrund von Piper Jaffray:
http://online.liebertpub.com/doi/pdf/10.1089/humc.2015.29001…
CLVS scheinbar gibt es Probleme bei AZD9291
http://seekingalpha.com/news/2820436-astrazeneca-halts-lung-…
http://seekingalpha.com/news/2820436-astrazeneca-halts-lung-…
Antwort auf Beitrag Nr.: 50.810.784 von hati682000 am 09.10.15 10:51:48Interessant!
Es gab schon früher (vereinzelte) "Grad 5-Probleme" mit ILD bei AZD9291. Auf deutsch, es sind Patienten an den Nebenwirkungen verstorben.
Dennoch wurde in der Vergangenheit immer das NW-Profil von AZD9291 als sehr viel besser als das von Rociletinib dargestellt.
Wie schon beim Wirkungsprofil scheint es sich auch beim NW-Profil immer mehr herauszustellen, dass es sich weniger um ein reales Plus, sondern eher um die Propaganda eines Pharamakonzerns handelt, der gewaltig unter Druck steht.
Es gab schon früher (vereinzelte) "Grad 5-Probleme" mit ILD bei AZD9291. Auf deutsch, es sind Patienten an den Nebenwirkungen verstorben.
Dennoch wurde in der Vergangenheit immer das NW-Profil von AZD9291 als sehr viel besser als das von Rociletinib dargestellt.
Wie schon beim Wirkungsprofil scheint es sich auch beim NW-Profil immer mehr herauszustellen, dass es sich weniger um ein reales Plus, sondern eher um die Propaganda eines Pharamakonzerns handelt, der gewaltig unter Druck steht.
Antwort auf Beitrag Nr.: 50.812.230 von SLGramann am 09.10.15 12:37:04CLVS
insbesondere ist es interessant, dass es sich bei den gestoppten Studien um Kombi-Studien mit PD1 handelt!
http://www.fiercebiotech.com/story/astrazeneca-halts-pair-lu…
"The company is testing a combination of AZD9291 and durvalumab, formerly MEDI4736, in two studies involving patients with non-small cell lung cancer. Late last month, AstraZeneca hit the brakes on enrollment in both trials due to an increase in reports of interstitial lung disease, which can lead to dangerous scarring and impaired pulmonary function."
Auf dieses Risiko hatte ich ja früher schonmal hingewiesen. Nach meinem Verständnis schützt PD1 die Lungen davor, dass diese aufgrund des direkten ständigen Kontaktes mit Stoffen aus der Umwelt (über die Atemluft) permanent entzündet sind. D.h., dass Immunsystem wird an dieser Kontaktfläche etwas gedämpft. Die Hemmung von PD1 führt zwar dazu, dass Krebszellen für das Immunsystem sichtbar werden und somit bekämpft werden können, allerdings kann dies auch zu Problemen mit den Lungen führen.
EGFR-Hemmer hemmen mutierte Formen von EGFR, die den Krebs fördern. EGFR-Hemmer der ersten Generation wie Tarceva hemmen aber gleichzeitig natürliche Formen von EGFR... das wildtype-EGFR. Dieses befindet sich u.a. in der Haut, so dass EGFR-Hemmer oft zu einem starken schmerzhaften Hautausschlag (Rash) führen. Dies kann auch die Lungen betreffen.
ILD und ähnliche Lungenprobleme sind schwerwiegend und können aufgrund einer Hemmung von PD1 oder auch von wildtype-EGFR auftreten. Überlappende toxische Nebenwirkungen können sich leicht verstärken, so dass man meistens versucht, Kombinationen ohne Überlappungen zu finden.
AZD9291 hemmt weniger wildtype-EGFR als z.B. Tarceva... allerdings wird wildtype-EGFR nicht ausgespart, d.h. auch mit AZD9291 kommt es zu Rash oder ILD.
CLVSs Roci ist dagegen ein EGFR-Hemmer, der wildtype-EGFR wenig oder garnicht hemmt. D.h. es gibt keine direkte Überlappung von Nebenwirkungen mit PD1-AKs.
PD1-AKs sollen bald eine wesentliche Standardanwendung bei NSCLC werden. EGFR-Hemmer sind es bereits. Daher spricht viel für eine Kombi dieser beiden Klassen. In diesem Fall dürfte Roci die Nase weit vorne haben... d.h. nicht nur bezügl. T790m pos oder neg, sondern auch aufgrund des Aussparens von wt-EGFR. Theoretisch könnte es das Mittel der Wahl sein vor allen anderen EGFR-Hemmern.
Ich hoffe, dass ich das soweit richtig verstanden und hier keinen Unsinn erzählt habe.

Gruß
ipollit
insbesondere ist es interessant, dass es sich bei den gestoppten Studien um Kombi-Studien mit PD1 handelt!
http://www.fiercebiotech.com/story/astrazeneca-halts-pair-lu…
"The company is testing a combination of AZD9291 and durvalumab, formerly MEDI4736, in two studies involving patients with non-small cell lung cancer. Late last month, AstraZeneca hit the brakes on enrollment in both trials due to an increase in reports of interstitial lung disease, which can lead to dangerous scarring and impaired pulmonary function."
Auf dieses Risiko hatte ich ja früher schonmal hingewiesen. Nach meinem Verständnis schützt PD1 die Lungen davor, dass diese aufgrund des direkten ständigen Kontaktes mit Stoffen aus der Umwelt (über die Atemluft) permanent entzündet sind. D.h., dass Immunsystem wird an dieser Kontaktfläche etwas gedämpft. Die Hemmung von PD1 führt zwar dazu, dass Krebszellen für das Immunsystem sichtbar werden und somit bekämpft werden können, allerdings kann dies auch zu Problemen mit den Lungen führen.
EGFR-Hemmer hemmen mutierte Formen von EGFR, die den Krebs fördern. EGFR-Hemmer der ersten Generation wie Tarceva hemmen aber gleichzeitig natürliche Formen von EGFR... das wildtype-EGFR. Dieses befindet sich u.a. in der Haut, so dass EGFR-Hemmer oft zu einem starken schmerzhaften Hautausschlag (Rash) führen. Dies kann auch die Lungen betreffen.
ILD und ähnliche Lungenprobleme sind schwerwiegend und können aufgrund einer Hemmung von PD1 oder auch von wildtype-EGFR auftreten. Überlappende toxische Nebenwirkungen können sich leicht verstärken, so dass man meistens versucht, Kombinationen ohne Überlappungen zu finden.
AZD9291 hemmt weniger wildtype-EGFR als z.B. Tarceva... allerdings wird wildtype-EGFR nicht ausgespart, d.h. auch mit AZD9291 kommt es zu Rash oder ILD.
CLVSs Roci ist dagegen ein EGFR-Hemmer, der wildtype-EGFR wenig oder garnicht hemmt. D.h. es gibt keine direkte Überlappung von Nebenwirkungen mit PD1-AKs.
PD1-AKs sollen bald eine wesentliche Standardanwendung bei NSCLC werden. EGFR-Hemmer sind es bereits. Daher spricht viel für eine Kombi dieser beiden Klassen. In diesem Fall dürfte Roci die Nase weit vorne haben... d.h. nicht nur bezügl. T790m pos oder neg, sondern auch aufgrund des Aussparens von wt-EGFR. Theoretisch könnte es das Mittel der Wahl sein vor allen anderen EGFR-Hemmern.
Ich hoffe, dass ich das soweit richtig verstanden und hier keinen Unsinn erzählt habe.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.780.502 von SLGramann am 05.10.15 21:06:28ONCE mit weiteren Daten:
http://ir.sparktx.com/phoenix.zhtml?c=253900&p=irol-newsArti…
Die bereits nachgewiesene Wirkung SPK-RPE65 hat sich nun auch als lang andauernd herausgestellt.
Das dürfte "den Markt" auf dem falschen Fuß erwischen, der ja nach den bereits gemeldeten positiven Daten nach einem kurzen Kurssprung zu einem hysterischen sell off übergegangen war. Frei nach dem Motto: "Es kann im Biotechsektor keine guten Nachrichten geben. Es ist immer alles schlecht."
Hier noch ein einordnender Artikel:
http://www.bloomberg.com/news/articles/2015-10-10/-holy-grai…
PS: Mit dem "falschen Fuß" ist es natürlich relativ. Der Markt kann am Montag ja auch das Spiel spielen: "Wer weiß, wie Regulierung und Preisgestaltung einer Gentherapie aussehen sollen? Das ist ja Neuland! Um Gottes willen. Verkaufen. Alles. Sofort. Ohne Limit. Und dann Leerverkaufen."
http://ir.sparktx.com/phoenix.zhtml?c=253900&p=irol-newsArti…
Die bereits nachgewiesene Wirkung SPK-RPE65 hat sich nun auch als lang andauernd herausgestellt.
Das dürfte "den Markt" auf dem falschen Fuß erwischen, der ja nach den bereits gemeldeten positiven Daten nach einem kurzen Kurssprung zu einem hysterischen sell off übergegangen war. Frei nach dem Motto: "Es kann im Biotechsektor keine guten Nachrichten geben. Es ist immer alles schlecht."

Hier noch ein einordnender Artikel:
http://www.bloomberg.com/news/articles/2015-10-10/-holy-grai…
PS: Mit dem "falschen Fuß" ist es natürlich relativ. Der Markt kann am Montag ja auch das Spiel spielen: "Wer weiß, wie Regulierung und Preisgestaltung einer Gentherapie aussehen sollen? Das ist ja Neuland! Um Gottes willen. Verkaufen. Alles. Sofort. Ohne Limit. Und dann Leerverkaufen."

Antwort auf Beitrag Nr.: 50.819.280 von SLGramann am 10.10.15 14:44:30Hallo SLGramann,
da hast du den Nagel auf den Kopf getroffen. Es gibt keine guten Nachrichten mehr. Gar nicht! Alles ist immer gleich schlecht!
ONCE verliert dann heute auch 4%...?
ESPR
Nach anfänglichen Gewinnen verliert die Aktie. Dabei gab es indirekt gute Nachrichten, weil Evacetrapib von Lilly (CETP) wohl endgültig tot ist. http://www.thestreet.com/story/13319800/1.html
Eine gute Übersicht zur Konkurrenzsituation:
http://alanhobbes.blogspot.de/2015/10/esperion-therapeutics-…
ZFGN
Heute ein Tagesverlust von 35% ohne wirkliche news. Allerdings hat ZFGN eine Teilnahme an einer Investorenkonferenz abgesagt. Was vor einigen Monaten noch als Zeichen einer bevorstehende Übernahme interpretiert worden wäre, ist heute die Vollkatastrophe...Ich hoffe mal, dass ZFGN selber da morgen Stellung bezieht.
http://www.thestreet.com/story/13320690/1/zafgen-cancels-mee…
SG kmastra
da hast du den Nagel auf den Kopf getroffen. Es gibt keine guten Nachrichten mehr. Gar nicht! Alles ist immer gleich schlecht!
ONCE verliert dann heute auch 4%...?
ESPR
Nach anfänglichen Gewinnen verliert die Aktie. Dabei gab es indirekt gute Nachrichten, weil Evacetrapib von Lilly (CETP) wohl endgültig tot ist. http://www.thestreet.com/story/13319800/1.html
Eine gute Übersicht zur Konkurrenzsituation:
http://alanhobbes.blogspot.de/2015/10/esperion-therapeutics-…
ZFGN
Heute ein Tagesverlust von 35% ohne wirkliche news. Allerdings hat ZFGN eine Teilnahme an einer Investorenkonferenz abgesagt. Was vor einigen Monaten noch als Zeichen einer bevorstehende Übernahme interpretiert worden wäre, ist heute die Vollkatastrophe...Ich hoffe mal, dass ZFGN selber da morgen Stellung bezieht.
http://www.thestreet.com/story/13320690/1/zafgen-cancels-mee…
SG kmastra
Antwort auf Beitrag Nr.: 50.833.017 von kmastra am 12.10.15 23:17:02
Bei Zafgen ZFGN sind die Investoren sehr vorsichtig, da die Firma nur einen von Chong Kun Dang (CKD) Pharmaceuticals einlizenzierten Wirkstoff (ZGN-433 = beloranib) in klinischen Studien hat. Des weiteren versteht selbst ZFGN die Wirkungsweise nicht wirklich - siehe letzten Link. Es gibt auch kritische Anmerkungen zur Struktur des Moleküls (auf den Link "The Tail´s ..." klicken) http://cenblog.org/the-haystack?s=zafgen
In bisherigen Studien wurde der Wirkstoff m.e. nicht längerfristig verabreicht. Daher können langfristig auftretende Nebenwirkungen nicht ausgeschlossen werden. Bislang sind hauptsächlich Schlaflosigkeit /-unterbrechungen dosisabhängig aufgetreten.
http://www.zafgen.com/docs/default-source/press-releases/zaf…
Sollte heute keine negative Meldung von ZFGN kommen, würde ich auf dem heute nochmals ermäßigtem Kursniveau kaufen. Sonst macht sich die Firma in den USA haftbar / angreifbar, was natürlich auch nicht komplett auszuschließen ist.
Nase
PS
Während des Schreibens habe ich meine erste kleine Position gekauft.
Mal sehen!
Zitat von kmastra: ZFGN
Heute ein Tagesverlust von 35% ohne wirkliche news. Allerdings hat ZFGN eine Teilnahme an einer Investorenkonferenz abgesagt. Was vor einigen Monaten noch als Zeichen einer bevorstehende Übernahme interpretiert worden wäre, ist heute die Vollkatastrophe...Ich hoffe mal, dass ZFGN selber da morgen Stellung bezieht.
http://www.thestreet.com/story/13320690/1/zafgen-cancels-mee…
Bei Zafgen ZFGN sind die Investoren sehr vorsichtig, da die Firma nur einen von Chong Kun Dang (CKD) Pharmaceuticals einlizenzierten Wirkstoff (ZGN-433 = beloranib) in klinischen Studien hat. Des weiteren versteht selbst ZFGN die Wirkungsweise nicht wirklich - siehe letzten Link. Es gibt auch kritische Anmerkungen zur Struktur des Moleküls (auf den Link "The Tail´s ..." klicken) http://cenblog.org/the-haystack?s=zafgen
In bisherigen Studien wurde der Wirkstoff m.e. nicht längerfristig verabreicht. Daher können langfristig auftretende Nebenwirkungen nicht ausgeschlossen werden. Bislang sind hauptsächlich Schlaflosigkeit /-unterbrechungen dosisabhängig aufgetreten.
http://www.zafgen.com/docs/default-source/press-releases/zaf…
Sollte heute keine negative Meldung von ZFGN kommen, würde ich auf dem heute nochmals ermäßigtem Kursniveau kaufen. Sonst macht sich die Firma in den USA haftbar / angreifbar, was natürlich auch nicht komplett auszuschließen ist.
Nase
PS
Während des Schreibens habe ich meine erste kleine Position gekauft.
Mal sehen!
ZFGN:
Ich glaube nicht, dass ich schon mal einen so massiven Kursverfall ohne harte Fakten in so kurzer Zeit gesehen habe.

Es gibt nun - natürlich - auch immer mehr Gerüchte, dass bad news anstehen (safety):
Zafgen shares continue to slide on market fears
October 13, 2015 | By John Carroll
With investors spooked at the sudden cancellation of an RBC Capital roadshow appearance slated for today, Zafgen's ($ZFGN) shares plunged 35% on Monday and another 7% on Tuesday morning. Rumors about potential trouble with the biotech's lead drug, beloranib, provided all the dry tinder needed to heat up speculation. A turbulent market has blasted a variety of biotech stocks, and investors seem ready to flee a stock at any sign of trouble--real or imagined. Zafgen did not immediately respond to a query from FierceBiotech--or anyone else--this morning. RBC's Simos Simeonidis doesn't like the careful silence. "We believe the reason that management hasn't been able to communicate with investors is that they're in possession of material information and they're in the process of getting ready to inform investors," notes the analyst. Beloranib is in Phase III for Prader-Willi syndrome, in which patients suffer from an uncontrolled appetite and severe obesity. It's also in two other Phase II studies.
Dass sich ZFGN dermaßen tot stellt ist aber in der Tat kein gutes Zeichen, glaube ich.
Ich glaube nicht, dass ich schon mal einen so massiven Kursverfall ohne harte Fakten in so kurzer Zeit gesehen habe.
Es gibt nun - natürlich - auch immer mehr Gerüchte, dass bad news anstehen (safety):
Zafgen shares continue to slide on market fears
October 13, 2015 | By John Carroll
With investors spooked at the sudden cancellation of an RBC Capital roadshow appearance slated for today, Zafgen's ($ZFGN) shares plunged 35% on Monday and another 7% on Tuesday morning. Rumors about potential trouble with the biotech's lead drug, beloranib, provided all the dry tinder needed to heat up speculation. A turbulent market has blasted a variety of biotech stocks, and investors seem ready to flee a stock at any sign of trouble--real or imagined. Zafgen did not immediately respond to a query from FierceBiotech--or anyone else--this morning. RBC's Simos Simeonidis doesn't like the careful silence. "We believe the reason that management hasn't been able to communicate with investors is that they're in possession of material information and they're in the process of getting ready to inform investors," notes the analyst. Beloranib is in Phase III for Prader-Willi syndrome, in which patients suffer from an uncontrolled appetite and severe obesity. It's also in two other Phase II studies.
Dass sich ZFGN dermaßen tot stellt ist aber in der Tat kein gutes Zeichen, glaube ich.
Antwort auf Beitrag Nr.: 50.841.381 von SLGramann am 13.10.15 20:46:42ZFGN
Ich bin einigermaßen sprachlos! Nachdem gestern noch ein halber Feiertag war, hatte ich eigentlich heute vor Börsenstart schon mit einer Mitteilung (was auch immer) gerechnet. Aber selbst nach dem weiteren massiven Abverkauf kommt von ZFGN selber - Nichts!
Ich bin mittlerweile extrem pessimistisch was das Ganze betrifft. Meine Position habe ich aber (leider) gehalten. Nachkaufen würde ich ohne Klarheit nicht.
Ich bin einigermaßen sprachlos! Nachdem gestern noch ein halber Feiertag war, hatte ich eigentlich heute vor Börsenstart schon mit einer Mitteilung (was auch immer) gerechnet. Aber selbst nach dem weiteren massiven Abverkauf kommt von ZFGN selber - Nichts!
Ich bin mittlerweile extrem pessimistisch was das Ganze betrifft. Meine Position habe ich aber (leider) gehalten. Nachkaufen würde ich ohne Klarheit nicht.
Antwort auf Beitrag Nr.: 50.842.152 von kmastra am 13.10.15 22:28:32
Ich setze hier nur "Spielgeld" ein. Worst case sehe ich in diesem Marktumfeld einen massiven Kursrückgang auf den Netto-Cashbestand abzüglich ein Quartal Cashverbrauch. Das wären (222 Mio USD Cash - 17 Mio USD Verbindlichkeiten - 20 Mio USD Quartalscashverbrauch) / 27,12 Mio Aktien = ca 6,8 USD pro Aktie.
Falls ich bereits investiert wäre, würde ich auch nicht mehr verkaufen, sondern abwarten. Die aktuelle Situation - positiv, wie negativ - ist ohne neue Information nicht einschätzbar.
Die gestrige Email von ZFGN an ausgewählte Personen bringt auch kein Licht ins Dunkel, da sie Null Informationsgehalt hat.
On Tuesday night, Zafgen CFO Patty Allen sent the following email to analysts, some shareholders and reporters:
We have received a number of inquiries from the investment community. As you are aware, we do not comment on share price movement or market speculation. We appreciate the concerns of our stakeholders. Zafgen remains committed to developing novel therapies to improve the health and well-being of patients affected by obesity and complex metabolic disorders.
http://www.thestreet.com/story/13323265/1/zafgen-finally-spe…
Zitat von kmastra: ZFGN
Ich bin einigermaßen sprachlos! Nachdem gestern noch ein halber Feiertag war, hatte ich eigentlich heute vor Börsenstart schon mit einer Mitteilung (was auch immer) gerechnet. Aber selbst nach dem weiteren massiven Abverkauf kommt von ZFGN selber - Nichts
...
Ich setze hier nur "Spielgeld" ein. Worst case sehe ich in diesem Marktumfeld einen massiven Kursrückgang auf den Netto-Cashbestand abzüglich ein Quartal Cashverbrauch. Das wären (222 Mio USD Cash - 17 Mio USD Verbindlichkeiten - 20 Mio USD Quartalscashverbrauch) / 27,12 Mio Aktien = ca 6,8 USD pro Aktie.
Falls ich bereits investiert wäre, würde ich auch nicht mehr verkaufen, sondern abwarten. Die aktuelle Situation - positiv, wie negativ - ist ohne neue Information nicht einschätzbar.
Die gestrige Email von ZFGN an ausgewählte Personen bringt auch kein Licht ins Dunkel, da sie Null Informationsgehalt hat.
On Tuesday night, Zafgen CFO Patty Allen sent the following email to analysts, some shareholders and reporters:
We have received a number of inquiries from the investment community. As you are aware, we do not comment on share price movement or market speculation. We appreciate the concerns of our stakeholders. Zafgen remains committed to developing novel therapies to improve the health and well-being of patients affected by obesity and complex metabolic disorders.
http://www.thestreet.com/story/13323265/1/zafgen-finally-spe…
Antwort auf Beitrag Nr.: 50.846.499 von Nase_weis_nix am 14.10.15 13:55:02
so eine mail rausschicken finde ich aber eine ganz schöne frechheit?
dann liiieber gar nichts, antworten,
oder
"we are not aware of any reason ..."
gruß
P.
Zitat von Nase_weis_nix: Die gestrige Email von ZFGN an ausgewählte Personen bringt auch kein Licht ins Dunkel, da sie Null Informationsgehalt hat.
On Tuesday night, Zafgen CFO Patty Allen sent the following email to analysts, some shareholders and reporters:
We have received a number of inquiries from the investment community. As you are aware, we do not comment on share price movement or market speculation. We appreciate the concerns of our stakeholders. Zafgen remains committed to developing novel therapies to improve the health and well-being of patients affected by obesity and complex metabolic disorders.
http://www.thestreet.com/story/13323265/1/zafgen-finally-spe…
so eine mail rausschicken finde ich aber eine ganz schöne frechheit?
dann liiieber gar nichts, antworten,
oder
"we are not aware of any reason ..."
gruß
P.
Antwort auf Beitrag Nr.: 50.846.499 von Nase_weis_nix am 14.10.15 13:55:02Die aktuelle Situation - positiv, wie negativ - ist ohne neue Information nicht einschätzbar.
Absolut. Aber wäre es nicht Aufgabe einer IR Abteilung da für Klarheit zu sorgen?
Scheinbar kann/will man das momentan aber noch nicht. Für mich erhöht sich dadurch die Wahrscheinlichkeit, dass es etwas Negatives ist. Bei allem was man so über Twitter liest, könnten es in der Tat zu schweren Nebenwirkungen (Thrombose oder Herzinfarkt/Schlaganfall) gekommen sein.
Bei etwas Positivem oder wenn gar nichts los wäre, hätte man m.E. schon sehr klar mitgeteilt, dass alles auf dem Weg ist. Mir fehlt in der PR auch irgendwie das Wort Beloranib. Zufall? Und warum antwortet eigentlich der CFO?
Wie tief kann es gehen?
Das hängt natürlich von der Nachricht ab. Bei schweren Nebenwirkungen könnte der Kurs auch weit unter die Cashgrenze fallen, weil alle Projekte auf dem gleichen Ansatz beruhen.
Auch die Analysten sind nicht schlauer (zumidest nach Außen )
)


@Nase_weiß_nix: Weißt du in welchem zeitlichen Rahmen negative Ereignisse mitgeteilt werden müssen? Auf Twitter hatte ich 48 Std. gelesen...
SG kmastra
Absolut. Aber wäre es nicht Aufgabe einer IR Abteilung da für Klarheit zu sorgen?
Scheinbar kann/will man das momentan aber noch nicht. Für mich erhöht sich dadurch die Wahrscheinlichkeit, dass es etwas Negatives ist. Bei allem was man so über Twitter liest, könnten es in der Tat zu schweren Nebenwirkungen (Thrombose oder Herzinfarkt/Schlaganfall) gekommen sein.
Bei etwas Positivem oder wenn gar nichts los wäre, hätte man m.E. schon sehr klar mitgeteilt, dass alles auf dem Weg ist. Mir fehlt in der PR auch irgendwie das Wort Beloranib. Zufall? Und warum antwortet eigentlich der CFO?
Wie tief kann es gehen?
Das hängt natürlich von der Nachricht ab. Bei schweren Nebenwirkungen könnte der Kurs auch weit unter die Cashgrenze fallen, weil alle Projekte auf dem gleichen Ansatz beruhen.
Auch die Analysten sind nicht schlauer (zumidest nach Außen
 )
) 

@Nase_weiß_nix: Weißt du in welchem zeitlichen Rahmen negative Ereignisse mitgeteilt werden müssen? Auf Twitter hatte ich 48 Std. gelesen...
SG kmastra
Antwort auf Beitrag Nr.: 50.847.522 von kmastra am 14.10.15 15:31:13Jetzt ist es raus. Ein Patient ist verstorben. Allerdings ist der Grund unbekannt.
Handel ist angehalten.
Solange man über den Grund nichts näheres weiß, kann man immer noch nichts sagen. Dass ein PWS-Patient stirbt ist leider nicht ganz außergewöhnlich.
Handel ist angehalten.
Solange man über den Grund nichts näheres weiß, kann man immer noch nichts sagen. Dass ein PWS-Patient stirbt ist leider nicht ganz außergewöhnlich.
Antwort auf Beitrag Nr.: 50.849.034 von SLGramann am 14.10.15 18:09:32Das hätte man doch genau so auch schon am Montag mitteilen können!?
So bleibt für mich ein "Geschmäckle" - eher ein ganz penetranter und übler Geschmack - muss ich sagen.
Letztlich ist es ja tatsächlich so, dass das passieren kann. Jetzt ist aber der PR-Supergau da.
So bleibt für mich ein "Geschmäckle" - eher ein ganz penetranter und übler Geschmack - muss ich sagen.
Letztlich ist es ja tatsächlich so, dass das passieren kann. Jetzt ist aber der PR-Supergau da.
Antwort auf Beitrag Nr.: 50.849.034 von SLGramann am 14.10.15 18:09:32
Hier die Mitteilung im Wortlaut von der Firmenwebseite:
"Zafgen recently learned of a patient death which occurred in the Company's ongoing double-blind, randomized, placebo-controlled Phase 3 bestPWS study of beloranib in Prader-Willi Syndrome, a rare genetic disorder with a high rate of mortality linked to obesity and its co-morbidities. The cause of death remains unknown at this time. According to normal practice, the event was reported to the U.S. Food and Drug Administration, at which point the Agency initiated a discussion with the Company. The Company is working with the Agency to expedite a review and understanding of this event, and to determine implications of the event on the conduct of the trial, and anticipates providing an update as its discussions with the Agency progress. The thoughts of the Company are with the family of the patient at this time. Zafgen remains committed to ensuring the safety of all patients enrolled in its studies."
http://ir.zafgen.com/releasedetail.cfm?ReleaseID=936610
Hier die Mitteilung im Wortlaut von der Firmenwebseite:
"Zafgen recently learned of a patient death which occurred in the Company's ongoing double-blind, randomized, placebo-controlled Phase 3 bestPWS study of beloranib in Prader-Willi Syndrome, a rare genetic disorder with a high rate of mortality linked to obesity and its co-morbidities. The cause of death remains unknown at this time. According to normal practice, the event was reported to the U.S. Food and Drug Administration, at which point the Agency initiated a discussion with the Company. The Company is working with the Agency to expedite a review and understanding of this event, and to determine implications of the event on the conduct of the trial, and anticipates providing an update as its discussions with the Agency progress. The thoughts of the Company are with the family of the patient at this time. Zafgen remains committed to ensuring the safety of all patients enrolled in its studies."
http://ir.zafgen.com/releasedetail.cfm?ReleaseID=936610
Antwort auf Beitrag Nr.: 50.849.109 von kmastra am 14.10.15 18:17:20Handelseinstellung u. Meldung hätten eigentlich gleich am Montag nach Absage der Investorenkonferenzen kommen müssen - da hat ZFGN sehr unprofessionell gearbeitet.
Substantielle Mitteilungen müssen im Form 8k innerhalb 4 Werktagen veröffentlicht werden. Ob die neuen Erkenntnisse der klinischen Studie darunter fallen ist streitbar. z.B. suche 2. Ergebnis von "day" in folgendem Link:http://www.sec.gov/info/smallbus/qasbsec.htm
Wichtiger sind hier die Fair Disclosure u. Insider Trading Regeln.
http://www.sec.gov/answers/regfd.htm
http://www.sec.gov/answers/insider.htm
Diese können m.e. nun von Anwälten herangezogen u. ZFGN verklagt werden, da Insiderhandel (auch Personen ausserhalb ZFGN mit Kenntnissen des Sachverhaltes) nicht ausgeschlossen werden kann. Das werden wir wohl als nächstes erleben.
Und wieder bewahrheitet sich der Spruch, im Zweifel nicht schlauer als der Markt sein zu wollen. Gleich nochmals dick in mein Investorentagebuch hineinschreiben und den bereits vorhandenen das x-te mal mit Textmarker überstreichen!
Substantielle Mitteilungen müssen im Form 8k innerhalb 4 Werktagen veröffentlicht werden. Ob die neuen Erkenntnisse der klinischen Studie darunter fallen ist streitbar. z.B. suche 2. Ergebnis von "day" in folgendem Link:http://www.sec.gov/info/smallbus/qasbsec.htm
Wichtiger sind hier die Fair Disclosure u. Insider Trading Regeln.
http://www.sec.gov/answers/regfd.htm
http://www.sec.gov/answers/insider.htm
Diese können m.e. nun von Anwälten herangezogen u. ZFGN verklagt werden, da Insiderhandel (auch Personen ausserhalb ZFGN mit Kenntnissen des Sachverhaltes) nicht ausgeschlossen werden kann. Das werden wir wohl als nächstes erleben.
Und wieder bewahrheitet sich der Spruch, im Zweifel nicht schlauer als der Markt sein zu wollen. Gleich nochmals dick in mein Investorentagebuch hineinschreiben und den bereits vorhandenen das x-te mal mit Textmarker überstreichen!
Antwort auf Beitrag Nr.: 50.849.313 von Nase_weis_nix am 14.10.15 18:45:02Danke. Ich denke da wird so oder so jetzt eine Klagewelle auf ZFGN zurollen. Das da so gar nichts nach Außen gedrungen ist - hmmm!? Sorry wir müssen das Investorenfrühstück leider absagen, aber vielleicht solltet ihr auch eher kleine Brötchen backen...
Aber wichtiger ist natürlich wie es mit Beloranib weitergeht.
Ist der verstorbene Patient in der Beloranib oder Placebogruppe?!
Woran genau ist er gestorben? - Ist eine Verbindung zu Beloranib gegeben?
Welche Dosis?
Wird die/werden die laufenden Studien angehalten?
Das sind jetzt alles offene Fragen, die mir spontan einfallen. Man stelle sich mal vor, der Patient war in der Placebogruppe!
Man wird jetzt erstmal abwarten müssen. Wahrscheinlich wollte Zafgen erst dann an die Öffentlichkeit gehen, wenn das alles klarer ist. Sollten die Studien angehalten werden, wäre das wohl ziemlich übel, weil dann ggf. nochmal von Vorne begonnen werden müsste und wer nimmt dann noch Teil? Wer will das verantworten? In dem Fall können das die Patienten ja nicht selber entscheiden sondern werden einen gesetzlichen Betreuer haben...
Aber wichtiger ist natürlich wie es mit Beloranib weitergeht.
Ist der verstorbene Patient in der Beloranib oder Placebogruppe?!
Woran genau ist er gestorben? - Ist eine Verbindung zu Beloranib gegeben?
Welche Dosis?
Wird die/werden die laufenden Studien angehalten?
Das sind jetzt alles offene Fragen, die mir spontan einfallen. Man stelle sich mal vor, der Patient war in der Placebogruppe!
Man wird jetzt erstmal abwarten müssen. Wahrscheinlich wollte Zafgen erst dann an die Öffentlichkeit gehen, wenn das alles klarer ist. Sollten die Studien angehalten werden, wäre das wohl ziemlich übel, weil dann ggf. nochmal von Vorne begonnen werden müsste und wer nimmt dann noch Teil? Wer will das verantworten? In dem Fall können das die Patienten ja nicht selber entscheiden sondern werden einen gesetzlichen Betreuer haben...
Antwort auf Beitrag Nr.: 50.849.634 von kmastra am 14.10.15 19:26:18
Kann es sein, dass noch nicht bekannt ist, welchen der 3 Studienarme der verstorbene Patient in der PWS-Studie zugeordnet war? Kann, bzw. muss der Patient bei einem Todesfall nicht sofort entblindet werden? In Europa wird m.e. der Patient bei schweren, nicht zu erwartenden Nebenwirkungen einzeln entblindet u. an die Behörde, bzw. Überwachungsstellen gemeldet.
Ich dachte, es geht nur noch darum, die Todesursache u. einen möglichen Zusammenhang mit der Gabe von Beloranib zu klären.
In der amerikanischen PWS PIII Studie sind 102 Patienten (12-65 Jahre) aufgenommen. Start Sept 2014.
1 - Placebo Comparator: Placebo for Injectable Suspension
2 - Experimental: ZGN-440 Injectable Suspension (1.8 mg)
3 - Experimental: ZGN-440 Injectable Suspension (2.4 mg)
aus https://www.clinicaltrials.gov/ct2/show?term=beloranib&rank=…
In der australischen Diabetes PII Studie sind 152 Patienten (18-65 Jahre) aufgenommen. Start Dez 2014.
1 - Experimental: ZGN-440 Injectable Suspension (1.2mg)
2 - Experimental: ZGN-440 Injectable Suspension (1.8mg)
3 - Placebo Comparator: Placebo for Injectable Suspension
aus https://www.clinicaltrials.gov/ct2/show?term=beloranib&rank=…
Die für mich erkennbaren Unterschiede sind Dosishöhe (warum eigentlich 2.4 mg, obwohl mehrere Abbrüche wg. dosisabhängigen Schlafstörungen in PWS PII?), Mindestalter, 3-Monate früherer Startzeitpunkt der PWS-Studie, sowie stärkere Vorschädigung / Begleiterkrankungen bei PWS.
Worst case wäre Abbruch aller Beloranib-Studien. Best case, dass hinreichend ausgeschlossen werden kann, dass der Todesfall im Zusammenhang mit der Beloranib-Verabreichung steht.
Ich werde mein Spielgeld die nächsten Tage trotzdem wieder vom Tisch nehmen, da mir die Kommunikation zu unprofessionell erscheint. Das widerspricht der angeblichen Professionalität u. Erfahrung, die viele Analysten ZFGN zuerkannten.
Kann es sein, dass noch nicht bekannt ist, welchen der 3 Studienarme der verstorbene Patient in der PWS-Studie zugeordnet war? Kann, bzw. muss der Patient bei einem Todesfall nicht sofort entblindet werden? In Europa wird m.e. der Patient bei schweren, nicht zu erwartenden Nebenwirkungen einzeln entblindet u. an die Behörde, bzw. Überwachungsstellen gemeldet.
Ich dachte, es geht nur noch darum, die Todesursache u. einen möglichen Zusammenhang mit der Gabe von Beloranib zu klären.
In der amerikanischen PWS PIII Studie sind 102 Patienten (12-65 Jahre) aufgenommen. Start Sept 2014.
1 - Placebo Comparator: Placebo for Injectable Suspension
2 - Experimental: ZGN-440 Injectable Suspension (1.8 mg)
3 - Experimental: ZGN-440 Injectable Suspension (2.4 mg)
aus https://www.clinicaltrials.gov/ct2/show?term=beloranib&rank=…
In der australischen Diabetes PII Studie sind 152 Patienten (18-65 Jahre) aufgenommen. Start Dez 2014.
1 - Experimental: ZGN-440 Injectable Suspension (1.2mg)
2 - Experimental: ZGN-440 Injectable Suspension (1.8mg)
3 - Placebo Comparator: Placebo for Injectable Suspension
aus https://www.clinicaltrials.gov/ct2/show?term=beloranib&rank=…
Die für mich erkennbaren Unterschiede sind Dosishöhe (warum eigentlich 2.4 mg, obwohl mehrere Abbrüche wg. dosisabhängigen Schlafstörungen in PWS PII?), Mindestalter, 3-Monate früherer Startzeitpunkt der PWS-Studie, sowie stärkere Vorschädigung / Begleiterkrankungen bei PWS.
Worst case wäre Abbruch aller Beloranib-Studien. Best case, dass hinreichend ausgeschlossen werden kann, dass der Todesfall im Zusammenhang mit der Beloranib-Verabreichung steht.
Ich werde mein Spielgeld die nächsten Tage trotzdem wieder vom Tisch nehmen, da mir die Kommunikation zu unprofessionell erscheint. Das widerspricht der angeblichen Professionalität u. Erfahrung, die viele Analysten ZFGN zuerkannten.
Antwort auf Beitrag Nr.: 50.849.976 von Nase_weis_nix am 14.10.15 20:17:37Tja. Das ist eine berechtigte Frage. ZFGN selber sagt wohl, dass noch nicht entblindet wurde:
Zafgen patient could have been on placebo, says RBC Capital
RBC Capital analyst Simos Simeonidis says there is a 33% chance that the patient who died in Zafgen's Phase 3 study was on the placebo arm. Management told the analyst that they are still blinded to which trial arm the patient who passed away was on. Zafgen avoided the worst case of the trial receiving a clinical hold, Simeonidis tells investors in an intraday research note. He points out the company has $8 per share in cash. The analyst has an Outperform rating on the name. After declining over 30% today, shares of Zafgen are now up $3.08 to $18.83.
http://www.thefly.com/landingPageNews.php?id=2266530&headlin…
Andere User zitieren die FDA in deinem Sinn, dass im Rahmen der Meldung an die FDA entblindet werden muss:

Insgesamt unfassbar, was da heute (und die letzten Tage) passiert. Erst der weitere Absturz, dann die Meldung, dann weiterer Absturz und dann der starke Anstieg. Eine große Rolle spielen wohl auch die shorts, die jetzt ihre Gewinne sichern bzw. von dem Anstieg überrascht wurden. Das Volumen ist heute ja nochmal deutlich angezogen:

Ich werde mich auch zumindest von einem Teil trennen (hab schon angefangen), weil mir die kurzfristigen Risiken da doch zu groß werden. Ein Halt der Studie ist ja nicht vom Tisch. Ganz werde ich mich aber auch nicht verabschieden...
Zafgen patient could have been on placebo, says RBC Capital
RBC Capital analyst Simos Simeonidis says there is a 33% chance that the patient who died in Zafgen's Phase 3 study was on the placebo arm. Management told the analyst that they are still blinded to which trial arm the patient who passed away was on. Zafgen avoided the worst case of the trial receiving a clinical hold, Simeonidis tells investors in an intraday research note. He points out the company has $8 per share in cash. The analyst has an Outperform rating on the name. After declining over 30% today, shares of Zafgen are now up $3.08 to $18.83.
http://www.thefly.com/landingPageNews.php?id=2266530&headlin…
Andere User zitieren die FDA in deinem Sinn, dass im Rahmen der Meldung an die FDA entblindet werden muss:

Insgesamt unfassbar, was da heute (und die letzten Tage) passiert. Erst der weitere Absturz, dann die Meldung, dann weiterer Absturz und dann der starke Anstieg. Eine große Rolle spielen wohl auch die shorts, die jetzt ihre Gewinne sichern bzw. von dem Anstieg überrascht wurden. Das Volumen ist heute ja nochmal deutlich angezogen:

Ich werde mich auch zumindest von einem Teil trennen (hab schon angefangen), weil mir die kurzfristigen Risiken da doch zu groß werden. Ein Halt der Studie ist ja nicht vom Tisch. Ganz werde ich mich aber auch nicht verabschieden...
FPRX
BMY-Deal... wow... 350 Mio USD Upfront bei einer aktuellen MK von 440 Mio USD! Das hört sich schonmal nicht schlecht an
IO scheint für die Pharmas immer noch eine hohe Priorität zu haben und FPRXs CFS1R-AK FPA008 scheint hier gut aufgestellt zu sein. Soweit ich mit erinnere, hat Roche gemeint, dass PD1 im Zusammenhang mit Krebs weit mehr von Immunzellen expressioniert wird als vom Tumor selber... so z.B. von TAMs, die vom Tumor wiederum gefördert werden. CFS1R stoppt TAMs, wirkt also auch die Umgebung des Tumors. FPA008 ist als AK spezifischer als konkurrierende Small Molecules... zudem wurde bei der ursprünglich ersten Entwicklung gegen RA auch auf die Sicherheit Wert gelegt.
1,74 Mrd USD Deal für einen P1-Kandidaten... double digit Royalties sind noch etwas unklar, können aber durch eine Co-Promotion in den USA gesteigert werden. BMY kooperierte bereits mit FPRX in CFS1R + PD1 Kombi-Studien, Vielleicht sind die bisherigen Ergebnisse ja interessant.
"Bristol-Myers Squibb will be responsible for global commercialization, and Five Prime will retain rights to a U.S. co-promotion option. In addition to the upfront payment, Five Prime will be eligible to receive up to $1.05 billion in development and regulatory milestone payments per anti-CSF1R product for oncology indications (including combinations with Opdivo and any other agent), and up to $340 million in development and regulatory milestone payments per anti-CSF1R product for non-oncology indications, as well as double digit royalties, such royalties to be enhanced in the U.S. in the event that Five Prime exercises its co-promotion option."
FPRX ist präklinisch sehr aktiv in IO und untersuchen neue Ansätze. U.a. haben sie auch einen GITR-AK einlizensiert, der vielleicht auch einmal einiges einbringen wird.
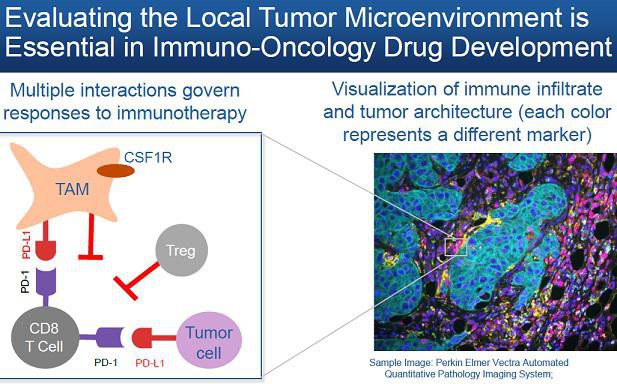
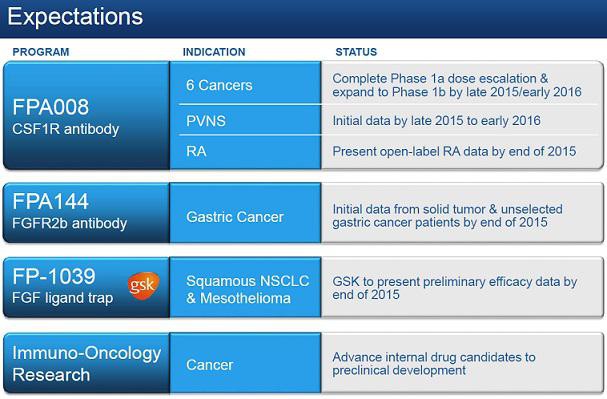

Gruß
ipollit
BMY-Deal... wow... 350 Mio USD Upfront bei einer aktuellen MK von 440 Mio USD! Das hört sich schonmal nicht schlecht an

IO scheint für die Pharmas immer noch eine hohe Priorität zu haben und FPRXs CFS1R-AK FPA008 scheint hier gut aufgestellt zu sein. Soweit ich mit erinnere, hat Roche gemeint, dass PD1 im Zusammenhang mit Krebs weit mehr von Immunzellen expressioniert wird als vom Tumor selber... so z.B. von TAMs, die vom Tumor wiederum gefördert werden. CFS1R stoppt TAMs, wirkt also auch die Umgebung des Tumors. FPA008 ist als AK spezifischer als konkurrierende Small Molecules... zudem wurde bei der ursprünglich ersten Entwicklung gegen RA auch auf die Sicherheit Wert gelegt.
1,74 Mrd USD Deal für einen P1-Kandidaten... double digit Royalties sind noch etwas unklar, können aber durch eine Co-Promotion in den USA gesteigert werden. BMY kooperierte bereits mit FPRX in CFS1R + PD1 Kombi-Studien, Vielleicht sind die bisherigen Ergebnisse ja interessant.
"Bristol-Myers Squibb will be responsible for global commercialization, and Five Prime will retain rights to a U.S. co-promotion option. In addition to the upfront payment, Five Prime will be eligible to receive up to $1.05 billion in development and regulatory milestone payments per anti-CSF1R product for oncology indications (including combinations with Opdivo and any other agent), and up to $340 million in development and regulatory milestone payments per anti-CSF1R product for non-oncology indications, as well as double digit royalties, such royalties to be enhanced in the U.S. in the event that Five Prime exercises its co-promotion option."
FPRX ist präklinisch sehr aktiv in IO und untersuchen neue Ansätze. U.a. haben sie auch einen GITR-AK einlizensiert, der vielleicht auch einmal einiges einbringen wird.


Gruß
ipollit
440 Mio MK bei 200 Mio USD Cash... d.h. mit diesem Deal dürfte der Cash bereits bei über 500 Mio USD liegen. Hier sollte es heute ordentlich nach oben gehen... obwohl in diesem Markt weiß man ja nie, was passiert 
Gruß
ipollit

Gruß
ipollit
INCY
ähnlich wie CSF1R wirkt IDO auf die Umgebung des Tumors. Inzwischen sind die Erwartungen an IDO wohl ziemlich hoch... insbesondere an INCYs IDO-Hemmer Epacadostat. INCY kooperiert bereits mit allen wichtigen PD1-Kandidaten. Nun werden sie bereits vor entsprechenden PII-Ergebnissen eine IDO + PD1 PIII in schwarzen Hautkrebs mit Merck starten. INCY baut damit seinen Führung in IDO aus... sie besitzen noch sämtliche Rechte.
Interessant an der PIII ist, dass diese nun alle anderen PD1-Kandidaten in 1st-line Melanoma mit Epacadostat für 2 Jahre blockt.
"...Phase 3 study evaluating the combination of epacadostat, Incyte’s investigational selective IDO1 inhibitor, with Keytruda® (pembrolizumab), Merck’s anti-PD-1 therapy, as first-line treatment for patients with advanced or metastatic melanoma. The Phase 3 study, which is expected to begin in the first half of 2016, will be co-funded by Incyte and Merck.
...
Under the terms of the agreement Incyte and Merck have also agreed, for a period of two years, not to initiate new pivotal studies of an IDO1 inhibitor in combination with a PD-1/PD-L1 antagonist as first-line therapy in advanced or metastatic melanoma with any third party. During this time, the companies will each offer the other the opportunity to collaborate on any new pivotal study involving an IDO1 inhibitor in combination with a PD-1/PD-L1 antagonist for types of melanoma and lines of therapy outside of the current collaboration agreement."
****
http://investorshub.advfn.com/boards/replies.aspx?msg=117681…
The exclusivity term in this likely serves a few purposes:
1) Discourage MRK from playing off other IDO inhibitors against epacadostat. Likely a way of INCY protecting their turf.
2) Helps MRK compete against BMY in the PD-1 / PD-L1 space.
3) I'm speculating that INCY wants to move a bunch of these epacadostat combos rapidly into phase 3. This type of exclusivity deal may spur some of the pharmas currently in non-binding collaborations with INCY to act quickly. This is likely a secondary effect, but has clear financial benefits for INCY and could offer competitive benefits for pharmas with PD-1 / PD-L1 drugs.
****
Außerdem war eine weitere PIII des JAK1/2 Baricitinib in RA erfolgreich, das zusammen mit LLY entwickelt wird. In dieser RA-BEAM Studie gab es auch einen Vergleich mit dem 12 Mrd USD TNF-AK Humira. Nach den Ergebnissen ist Baricitinib Humira teilweise überlegen:
"The study met its primary objective of demonstrating superiority compared to placebo after 12 weeks of treatment based on ACR20 response - a standard clinical measure that represents at least a 20 percent improvement in RA disease activity. Baricitinib was also superior to adalimumab on key secondary objectives of ACR20 response and improvement in DAS28-hsCRP score after 12 weeks of treatment. Following 24 weeks of treatment, baricitinib was superior to placebo in preventing progressive radiographic structural joint damage. These treatment benefits with baricitinib observed at 12 and 24 weeks were maintained through 52 weeks of therapy."
Anderes als Humira kann Baricitinib oral verabreicht werden. Baricitinib Konkurrent ist aber erstmal Pfizers JAK3 Xeljanz, das bisher kommerziell enttäuscht hat. Im Moment sieht es aus, als ob Baricitinib insbesondere von den Nebenwirkungen her besser als Xeljanz ist.
$LLY $INCY LLY plans to file barcitinib with the FDA by year end peak sales of >$4B INCY to receive peak royalties of nearly $1.2B from LLY
LR $8/sh baricitinib NPV contribution $INCY conservative. Recall, INCY receive 20-29% royalty on WW baricitinib launch 2017
Gruß
ipollit
ähnlich wie CSF1R wirkt IDO auf die Umgebung des Tumors. Inzwischen sind die Erwartungen an IDO wohl ziemlich hoch... insbesondere an INCYs IDO-Hemmer Epacadostat. INCY kooperiert bereits mit allen wichtigen PD1-Kandidaten. Nun werden sie bereits vor entsprechenden PII-Ergebnissen eine IDO + PD1 PIII in schwarzen Hautkrebs mit Merck starten. INCY baut damit seinen Führung in IDO aus... sie besitzen noch sämtliche Rechte.
Interessant an der PIII ist, dass diese nun alle anderen PD1-Kandidaten in 1st-line Melanoma mit Epacadostat für 2 Jahre blockt.
"...Phase 3 study evaluating the combination of epacadostat, Incyte’s investigational selective IDO1 inhibitor, with Keytruda® (pembrolizumab), Merck’s anti-PD-1 therapy, as first-line treatment for patients with advanced or metastatic melanoma. The Phase 3 study, which is expected to begin in the first half of 2016, will be co-funded by Incyte and Merck.
...
Under the terms of the agreement Incyte and Merck have also agreed, for a period of two years, not to initiate new pivotal studies of an IDO1 inhibitor in combination with a PD-1/PD-L1 antagonist as first-line therapy in advanced or metastatic melanoma with any third party. During this time, the companies will each offer the other the opportunity to collaborate on any new pivotal study involving an IDO1 inhibitor in combination with a PD-1/PD-L1 antagonist for types of melanoma and lines of therapy outside of the current collaboration agreement."
****
http://investorshub.advfn.com/boards/replies.aspx?msg=117681…
The exclusivity term in this likely serves a few purposes:
1) Discourage MRK from playing off other IDO inhibitors against epacadostat. Likely a way of INCY protecting their turf.
2) Helps MRK compete against BMY in the PD-1 / PD-L1 space.
3) I'm speculating that INCY wants to move a bunch of these epacadostat combos rapidly into phase 3. This type of exclusivity deal may spur some of the pharmas currently in non-binding collaborations with INCY to act quickly. This is likely a secondary effect, but has clear financial benefits for INCY and could offer competitive benefits for pharmas with PD-1 / PD-L1 drugs.
****
Außerdem war eine weitere PIII des JAK1/2 Baricitinib in RA erfolgreich, das zusammen mit LLY entwickelt wird. In dieser RA-BEAM Studie gab es auch einen Vergleich mit dem 12 Mrd USD TNF-AK Humira. Nach den Ergebnissen ist Baricitinib Humira teilweise überlegen:
"The study met its primary objective of demonstrating superiority compared to placebo after 12 weeks of treatment based on ACR20 response - a standard clinical measure that represents at least a 20 percent improvement in RA disease activity. Baricitinib was also superior to adalimumab on key secondary objectives of ACR20 response and improvement in DAS28-hsCRP score after 12 weeks of treatment. Following 24 weeks of treatment, baricitinib was superior to placebo in preventing progressive radiographic structural joint damage. These treatment benefits with baricitinib observed at 12 and 24 weeks were maintained through 52 weeks of therapy."
Anderes als Humira kann Baricitinib oral verabreicht werden. Baricitinib Konkurrent ist aber erstmal Pfizers JAK3 Xeljanz, das bisher kommerziell enttäuscht hat. Im Moment sieht es aus, als ob Baricitinib insbesondere von den Nebenwirkungen her besser als Xeljanz ist.
$LLY $INCY LLY plans to file barcitinib with the FDA by year end peak sales of >$4B INCY to receive peak royalties of nearly $1.2B from LLY
LR $8/sh baricitinib NPV contribution $INCY conservative. Recall, INCY receive 20-29% royalty on WW baricitinib launch 2017
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.853.576 von ipollit am 15.10.15 11:15:31FPRX:
In der Tat: Wow! Tolle Konditionen für einen P1 Kandidaten.
Was ich mich als Laie immer frag: Warum kaufen die den Laden nicht gleich?
Zum Thema IO:
Seit gestern ist der Loncarindex als ETF handelbar. Eine jährliche Gebühr von 0,79% finde ich akzeptabel.
http://www.exchangetradedconcepts.com/Data/Sites/22/docs/CNC…
ZFGN
Ein aktueller, etwas längerer Analystenkommentar.
http://www.twitlonger.com/show/n_1snlh3f
Letztlich fischen alle im trüben. Man kann nur spekulieren. Ich spekuliere zumindest darauf, dass die Studie nicht abgebrochen wird, wenn keine weiteren Todesfälle hinzukommen.
So wie ich es verstehe, dürfte es sehr schwer werden festzustellen, ob z.B. ein Herzinfarkt in Zusammenhang mit dem Medikament steht oder nicht, weil solche Ereignisse bei Menschen mit PWS auch sehr häufig vorkommen und auch eng mit dem Übergewicht zusammenhängen (was ja durch B. gesenkt werden soll):
whereas death in adults was associated with obesity and its complications, including cardiovascular problems, diabetes mellitus, sleep apnea, and hypertension.
....The pattern of death in those with Prader-Willi syndrome suggests that obesityrelated disease is a likely major risk factor. Management of caloric intake is truly a life-and-death issue for people with this syndrome.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2422866/#!po=56.…
Das die Entblindung so lange dauert finde ich sehr merkwürdig.
In der Tat: Wow! Tolle Konditionen für einen P1 Kandidaten.
Was ich mich als Laie immer frag: Warum kaufen die den Laden nicht gleich?
Zum Thema IO:
Seit gestern ist der Loncarindex als ETF handelbar. Eine jährliche Gebühr von 0,79% finde ich akzeptabel.
http://www.exchangetradedconcepts.com/Data/Sites/22/docs/CNC…
ZFGN
Ein aktueller, etwas längerer Analystenkommentar.
http://www.twitlonger.com/show/n_1snlh3f
Letztlich fischen alle im trüben. Man kann nur spekulieren. Ich spekuliere zumindest darauf, dass die Studie nicht abgebrochen wird, wenn keine weiteren Todesfälle hinzukommen.
So wie ich es verstehe, dürfte es sehr schwer werden festzustellen, ob z.B. ein Herzinfarkt in Zusammenhang mit dem Medikament steht oder nicht, weil solche Ereignisse bei Menschen mit PWS auch sehr häufig vorkommen und auch eng mit dem Übergewicht zusammenhängen (was ja durch B. gesenkt werden soll):
whereas death in adults was associated with obesity and its complications, including cardiovascular problems, diabetes mellitus, sleep apnea, and hypertension.
....The pattern of death in those with Prader-Willi syndrome suggests that obesityrelated disease is a likely major risk factor. Management of caloric intake is truly a life-and-death issue for people with this syndrome.
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2422866/#!po=56.…
Das die Entblindung so lange dauert finde ich sehr merkwürdig.
MGNX
diese Woche war der R&D-Tag von MGNX, bei dem sie ausführlicher über neue Entwicklungen informiert haben... http://files.shareholder.com/downloads/AMDA-278VRP/673334835…
U.a. wurde das Target des CD3-DARTs MGD009 öffentlich gemacht, der sich nun bereits in PI befindet. Anhand der Patente konnte man bereits vermuten, dass es sich dabei um B7H3 handelt. Ich bin sehr gespannt wie dieser Kandidat sich in der Klinik schlägt, MGNX hält noch 100% der Rechte.
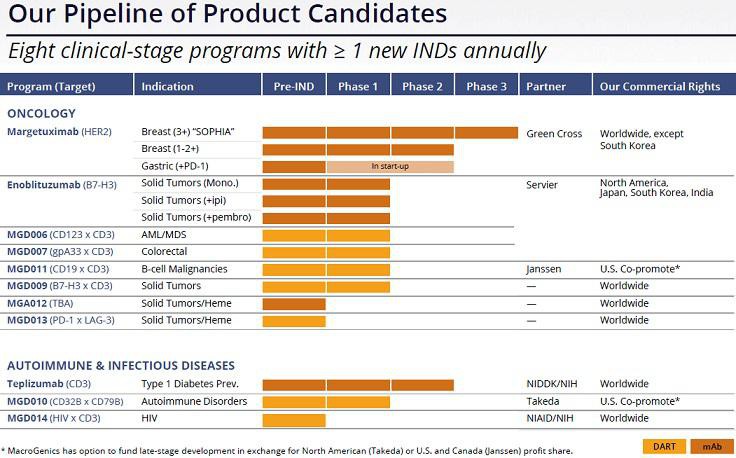
MGNX bezeichnet B7H3 als IO-Target. Mit Enoblituzumab haben sie bereits einen B7H3-AK in der Klinik, der aktuell auch in Kombi mit PD1 getestet wird. Allerdings ist Enoblituzumab ein AK mit extra hohem ADCC, d.h. er zielt darauf ab, das Target zu elemenieren und nicht nur zu blockieren. PD1-AKs blockieren eher nur den Signalweg. ADCC benötigt zudem ein intaktes Immunsystem... u.a sind NK-Zellen und Makrophagen an ADCC beteiligt. Hierüber wirkt auch Rituxan oder Herceptin, wobei diese nicht speziell ADCC-optimiert sind. Prinzipiell kann man den Unterschied zwischen diesem Ansatz und dem bei PD1-AKs aber erklären, weil PD1 auch von gesunden Zellen, u.a. von T-Zellen expressioniert wird. Man möchte mit PD1 nur verhindern, dass der Tumor die T-Zellen deaktiviert, aber nicht die T-Zellen selber zerstören. B7H3 ist dagegen kaum auf gesunden Zellen vorhanden. Im Gegensatz zu PD1 (B7H1) ist die Rolle von B7H3 bei der Immunabwehr aber weniger klar.
http://www.medicographia.com/2014/11/targeting-b7-h3-in-canc…
Hier wird der ADCC-Ansatz von Enoblituzumab eher kritisch gesehen, da angeblich dieser AK auch NK-Zellen usw reduziert, so dass er am Ende als ADCC-AK nicht richtig wirken kann:
http://seekingalpha.com/article/2755545-b7-h3-and-pdminus-1-…

Demnach sollte aber der neue B7H3xCD3 DART sehr vielversprechend sein. biAKs wie DART oder BITE sind eine Alternative zu CARTs. Zuletzt hörten sich die Ergebnisse von AMGNs zugelassenen CD19xCD3 BITE Blincyto recht gut an. Ein großes Problem von Blincyto ist noch, dass es nicht sehr lange im Blut bleibt und somit mit permanenter Infusion verabrecht werden muss, d.h. man trägt ständig eine Infusionspumpe bei sich. Aufgrund der kompakteren Konstruktion sollen DARTs wirksamer sein (T-Zellen werden mit CD3 näher am Target gebunden) und zudem besitzen viele DARTs einen Fc-Teil, damit sie wie AKs bis zu mehreren Wochen im Blut bleiben. J&J hat sich bereits die Rechte an dem Blincyto Konkurrenten CD19xC3 DART MGD011 gesichert.
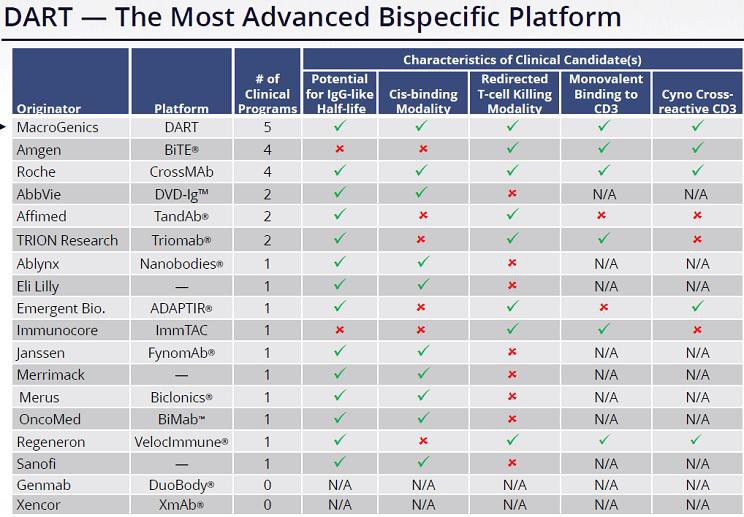
CD19 ist das typische CART-Target. Hierbei werden alle CD19 Blutzellen zerstört, bei Blutkrebs damit auch die Krebszellen. Da Blutzellen ständig nachwachsen, ist dies kein Problem. Bei soliden Tumoren sieht dies anders aus. Hier dürfen nur die Krebszellen abgetötet werden, aber keine gesunden Zellen, wie z.B. Hautzellen, da diese sich nicht so einfach reproduzieren. Bisher gibt es wohl wenig entsprechende Targets.
Und genau hier könnte B7H3 interessant werden, da es offensichtlich kaum auf gesunden Zellen vorhanden ist, wohl aber oft auf Krebszellen zu finden ist. Theoretisch könnte MGD009 damit sehr erfolgreich sein. Zudem will MGNX auch einen B7H3-ADC entwickeln und testet dafür zahlreiche Linker.
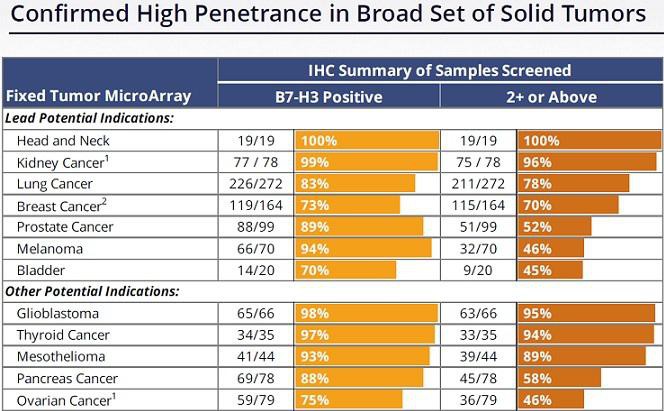
Zudem entwickelt man nun auch einen IO-DART MGD013 mit PD1 x LAG3. MGA012 ist ein neuer normaler AK... dieser könnte vielleicht ein entsprechender LAG3-AK sein? INDs sind für 2017 bzw nächstes Jahr geplant. Ein Konkurrent ist hier TSRO mit ähnlichen biAKs.
Ebenfalls neu ist ein HIV-DART, der gegen HIV helfen soll.

Neu ist zudem eine Ergänzung der DART-Technologie um eine Tri-AK-Technologie Trident. Damit soll entweder die Aktivierung von T-Zellen feiner geregelt werden können, indem z.B. nur bestimmte T-Zellen aktiviert werden oder das Target kann selektiver angegriffen werden, indem nur Zellen mit zwei definierten Targets zusammen gebunden werden.
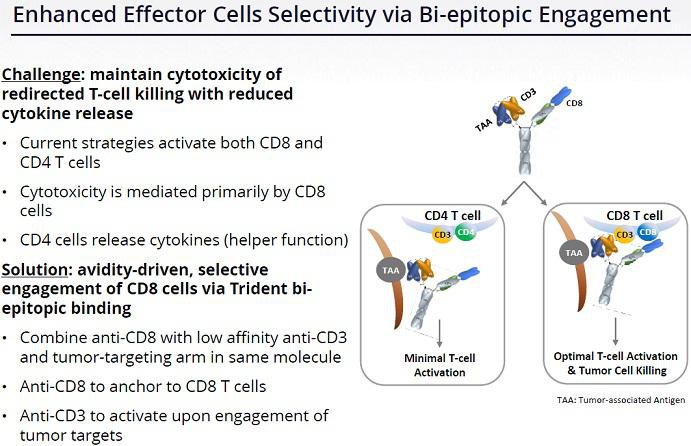
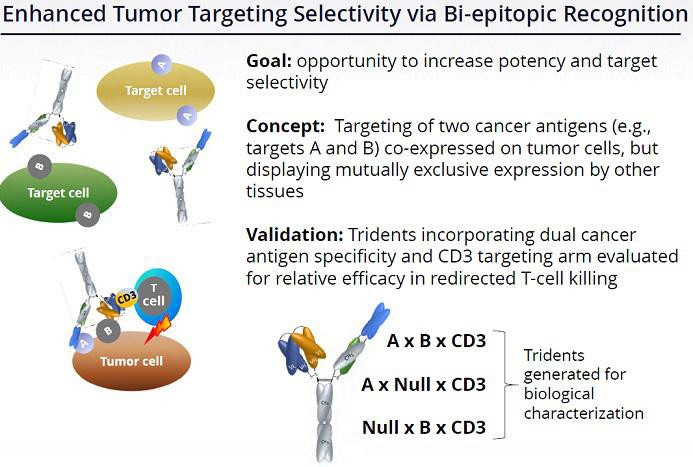
Insgesamt gute Entwicklungen, finde ich.

Gruß
ipollit
diese Woche war der R&D-Tag von MGNX, bei dem sie ausführlicher über neue Entwicklungen informiert haben... http://files.shareholder.com/downloads/AMDA-278VRP/673334835…
U.a. wurde das Target des CD3-DARTs MGD009 öffentlich gemacht, der sich nun bereits in PI befindet. Anhand der Patente konnte man bereits vermuten, dass es sich dabei um B7H3 handelt. Ich bin sehr gespannt wie dieser Kandidat sich in der Klinik schlägt, MGNX hält noch 100% der Rechte.

MGNX bezeichnet B7H3 als IO-Target. Mit Enoblituzumab haben sie bereits einen B7H3-AK in der Klinik, der aktuell auch in Kombi mit PD1 getestet wird. Allerdings ist Enoblituzumab ein AK mit extra hohem ADCC, d.h. er zielt darauf ab, das Target zu elemenieren und nicht nur zu blockieren. PD1-AKs blockieren eher nur den Signalweg. ADCC benötigt zudem ein intaktes Immunsystem... u.a sind NK-Zellen und Makrophagen an ADCC beteiligt. Hierüber wirkt auch Rituxan oder Herceptin, wobei diese nicht speziell ADCC-optimiert sind. Prinzipiell kann man den Unterschied zwischen diesem Ansatz und dem bei PD1-AKs aber erklären, weil PD1 auch von gesunden Zellen, u.a. von T-Zellen expressioniert wird. Man möchte mit PD1 nur verhindern, dass der Tumor die T-Zellen deaktiviert, aber nicht die T-Zellen selber zerstören. B7H3 ist dagegen kaum auf gesunden Zellen vorhanden. Im Gegensatz zu PD1 (B7H1) ist die Rolle von B7H3 bei der Immunabwehr aber weniger klar.
http://www.medicographia.com/2014/11/targeting-b7-h3-in-canc…
Hier wird der ADCC-Ansatz von Enoblituzumab eher kritisch gesehen, da angeblich dieser AK auch NK-Zellen usw reduziert, so dass er am Ende als ADCC-AK nicht richtig wirken kann:
http://seekingalpha.com/article/2755545-b7-h3-and-pdminus-1-…

Demnach sollte aber der neue B7H3xCD3 DART sehr vielversprechend sein. biAKs wie DART oder BITE sind eine Alternative zu CARTs. Zuletzt hörten sich die Ergebnisse von AMGNs zugelassenen CD19xCD3 BITE Blincyto recht gut an. Ein großes Problem von Blincyto ist noch, dass es nicht sehr lange im Blut bleibt und somit mit permanenter Infusion verabrecht werden muss, d.h. man trägt ständig eine Infusionspumpe bei sich. Aufgrund der kompakteren Konstruktion sollen DARTs wirksamer sein (T-Zellen werden mit CD3 näher am Target gebunden) und zudem besitzen viele DARTs einen Fc-Teil, damit sie wie AKs bis zu mehreren Wochen im Blut bleiben. J&J hat sich bereits die Rechte an dem Blincyto Konkurrenten CD19xC3 DART MGD011 gesichert.

CD19 ist das typische CART-Target. Hierbei werden alle CD19 Blutzellen zerstört, bei Blutkrebs damit auch die Krebszellen. Da Blutzellen ständig nachwachsen, ist dies kein Problem. Bei soliden Tumoren sieht dies anders aus. Hier dürfen nur die Krebszellen abgetötet werden, aber keine gesunden Zellen, wie z.B. Hautzellen, da diese sich nicht so einfach reproduzieren. Bisher gibt es wohl wenig entsprechende Targets.
Und genau hier könnte B7H3 interessant werden, da es offensichtlich kaum auf gesunden Zellen vorhanden ist, wohl aber oft auf Krebszellen zu finden ist. Theoretisch könnte MGD009 damit sehr erfolgreich sein. Zudem will MGNX auch einen B7H3-ADC entwickeln und testet dafür zahlreiche Linker.

Zudem entwickelt man nun auch einen IO-DART MGD013 mit PD1 x LAG3. MGA012 ist ein neuer normaler AK... dieser könnte vielleicht ein entsprechender LAG3-AK sein? INDs sind für 2017 bzw nächstes Jahr geplant. Ein Konkurrent ist hier TSRO mit ähnlichen biAKs.
Ebenfalls neu ist ein HIV-DART, der gegen HIV helfen soll.

Neu ist zudem eine Ergänzung der DART-Technologie um eine Tri-AK-Technologie Trident. Damit soll entweder die Aktivierung von T-Zellen feiner geregelt werden können, indem z.B. nur bestimmte T-Zellen aktiviert werden oder das Target kann selektiver angegriffen werden, indem nur Zellen mit zwei definierten Targets zusammen gebunden werden.


Insgesamt gute Entwicklungen, finde ich.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.850.129 von kmastra am 14.10.15 20:40:07ZFGN:
"Ein Halt der Studie ist ja nicht vom Tisch."
Dies hat sich nun erst mal bestätigt:
Zafgen hammered (again) as FDA clamps partial hold on PhIII obesity drug
http://www.fiercebiotech.com/story/zafgen-hammered-again-fda…
Vorbörslich -30%.
Sehr schade. Dieses eigentlich sehr hoffnungsvolle Programm ist jetzt wirklich beschädigt. Zumindest eine Anwendung im Massenmarkt (außerhalb PWS) steht jetzt sehr in Frage.
"Ein Halt der Studie ist ja nicht vom Tisch."
Dies hat sich nun erst mal bestätigt:
Zafgen hammered (again) as FDA clamps partial hold on PhIII obesity drug
http://www.fiercebiotech.com/story/zafgen-hammered-again-fda…
Vorbörslich -30%.
Sehr schade. Dieses eigentlich sehr hoffnungsvolle Programm ist jetzt wirklich beschädigt. Zumindest eine Anwendung im Massenmarkt (außerhalb PWS) steht jetzt sehr in Frage.
Antwort auf Beitrag Nr.: 50.864.163 von SLGramann am 16.10.15 14:15:04In der Tat sehr Schade. Das man da jetzt auf Nummer sicher geht und erst mal alle Patienten in Ruhe screent finde ich vernünftig. Ich habe keine Erfahrung mit einem "clinical hold". Aber ich denke jetzt geht es halt darum, festzustellen, ob es Blutgerinsel im B.-Arm gibt oder nicht. Ein kompetter Abbruch ist somit ja durchaus nicht
Interessant wäre es nochmal festzustellen, ob es vorher schon ähnliche Ereignisse ohne Todesfolge gab. Auffällig ist nämlich, dass viele im Vorstand sich Mitte September von ihren Aktienpaketen getrennt haben. Wieder mal ein Beispiel, wie schnell das alles geht bei Biotech von hero zu zero...Was die Effektivität betriff waren beide Studien ja relativ sichere Sachen.
Interessant wäre es nochmal festzustellen, ob es vorher schon ähnliche Ereignisse ohne Todesfolge gab. Auffällig ist nämlich, dass viele im Vorstand sich Mitte September von ihren Aktienpaketen getrennt haben. Wieder mal ein Beispiel, wie schnell das alles geht bei Biotech von hero zu zero...Was die Effektivität betriff waren beide Studien ja relativ sichere Sachen.
CEMP:
Ebenfalls eine interessante Entwicklung heute. Eigentlich ein Trial-Erfolg:
Cempra Announces Positive Topline Phase 3 Clinical Results for Intravenous Solithromycin in the Treatment of Community-Acquired Bacterial Pneumonia
http://investor.cempra.com/releasedetail.cfm?ReleaseID=93699…
Der Kurs reagiert mit einem Minus von derzeit 34%...
Offenbar ist man doch nicht so ganz zufrieden mit den Daten (unter anderem safety):


Dennoch wird allgemein davon ausgegangen, dass das Produkt zulassungsfähig ist und einen Markt hat.
Ich habe heute jedenfalls gekauft. Allerdings zu früh (für 20 Dollar), wie sich jetzt schon zeigt.
Ebenfalls eine interessante Entwicklung heute. Eigentlich ein Trial-Erfolg:
Cempra Announces Positive Topline Phase 3 Clinical Results for Intravenous Solithromycin in the Treatment of Community-Acquired Bacterial Pneumonia
http://investor.cempra.com/releasedetail.cfm?ReleaseID=93699…
Der Kurs reagiert mit einem Minus von derzeit 34%...
Offenbar ist man doch nicht so ganz zufrieden mit den Daten (unter anderem safety):


Dennoch wird allgemein davon ausgegangen, dass das Produkt zulassungsfähig ist und einen Markt hat.
Ich habe heute jedenfalls gekauft. Allerdings zu früh (für 20 Dollar), wie sich jetzt schon zeigt.
Antwort auf Beitrag Nr.: 50.865.621 von SLGramann am 16.10.15 16:29:03CEMP
Hallo SLGramann,
wie siehst du denn die Daten? Ich finde es schwer, ein klares Bild zu erhalten. Für den Kursverfall werden ja mehrere Gründe genannt, so dass man sich offensichtlich auch allgemein nicht sicher ist über die Gründe.
Solithromycin hatte ja Anfang des Jahres die erfolgreiche PIII in der oralen Studie gegen Moxifloxacin. Moxifloxacin wird als ein sehr wirksames Antibiotikum gesehen, so dass Non-Inferiority bereits ein großer Erfolg wäre. In der oralen Studie wurde dies erreicht, wobei Solithromycin über einen kürzeren Zeitraum verabreicht wurde, so dass es prinzipiell gegenüber Moxifloxacin überlegen ist. Die orale Studie soll bei Antibiotika die höhere Hürde als die IV Studie sein, was man z.B. an TTPH sehen kann, wo die orale Studie nach erfolgreicher IV Studie fehlgeschlagen ist. Der große Erfolg in der oralen Studie hat wohl die Erwartungen bei der IV angeheizt.
In der IV Studie wurden nun Solithromycin und Moxifloxacin über den gleichen Zeitraum dosiert (konkret war es eine IV Studie mit möglichen Switch auf oral). Wieder wurde Non-Inferiority erreicht. Vielleicht hat man hier mehr erwartet, z.B. zahlenmäßig bessere Ergebnisse von Solithromycin, da es nun länger verabreicht wurde. Außerdem soll Moxifloxacin schlechter bei älteren Patienten wirken... dazu gibt es bisher keine Zahlen?
Ein möglicher Knackpunkt ist der primäre Endpunkt in CE-SFU mit Port 3/4, der für eine EU-Zulassung benötigt wird. Offensichtlich gab es Probleme mit der Verfügbarkeit von Solithromycin, so dass ein paar Patienten nicht über den vollen Zeitraum die Therapie erhielten, wodurch die Ergebnisse dieser Patienten schlechter sind. Mit diesen Patienten zusammen konnte keine Non-Inferiority belegt werden... CEMP will diese zensieren, dann wird Non-Inferiority erreicht, aber wird sich die EMA darauf einlassen? Für die US-Zulassung spielt dies keine Rolle.
Von der Wirkung her sieht es also prinzipiell okay aus, auch wenn man vielleicht auf klarere Ergebnisse gehofft hat.
Ein weiteres Problem sind die Nebenwirkungen. Anders als in der oralen Studie besitzt Solithromycin mit 34% deutlich mehr Nebenwirkungen als Moxifloxacin mit 13%. Dies relativiert sich aber, da die meisten Nebenwirkungen von Solithromycin Schmerzen bei der Infusion sind. Dies soll typisch für Makrolide sein, zu denen Solithromycin gehört... Moxifloxacin gehört nicht dieser Klasse an.
Bis hierhin sehe ich also kein gravierendes Problem. Das Folgende ist mir aber unklar... vielleicht stellt es ein gewisses Risiko dar: Solithromycin erhöht genauso wie Moxifloxacin die Leberwerte. ALT Grad 3 war bereits bei der oralen Studie unter Solithromycin mehr erhöht als unter Moxifloxacin. Grad 4 war bei oral sehr gering, nun bei IV vergleichbar mit Moxifloxacin.
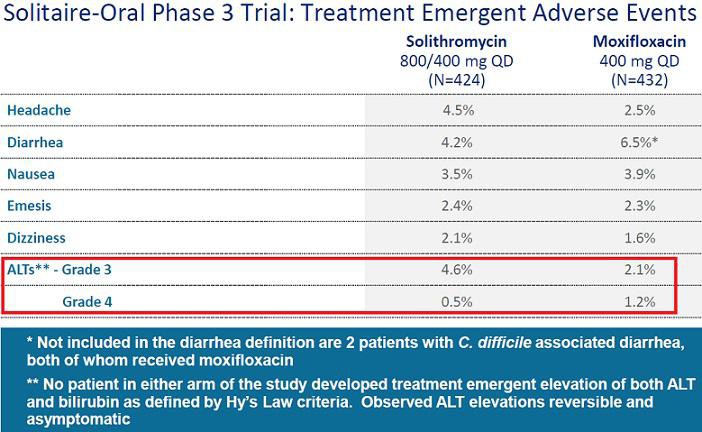
"Alanine transaminase (ALT) elevation was observed in both treatment arms. Grade 3 ALT elevations ( > 3-8×ULN) occurred in 8.2% of solithromycin patients and 3.4% of moxifloxacin patients and Grade 4 ALT elevations ( > 8×ULN) occurred in 0.7% of solithromycin patients and 0.5% of moxifloxacin patients. Treatment emergent ALT elevations were generally asymptomatic, reversible, and not associated with increased bilirubin. No solithromycin patient met Hy's Law criteria of concurrent ALT and bilirubin elevations post-baseline."
Leberwerte können angeblich erhöht sein, wenn man recht hohe Dosen eines Medikaments verabreicht bekommt, was z.B. bei Antibiotika der Fall ist. Solange die Werte nur erhöht sind und nach der Verabreichung wieder fallen, ist dies kein Problem. Erhöhte Leberwerte sind aber auch ein Hinweis auf Leberschäden. Ein Leberschaden bis hin zum Versagen ist sehr gravierend! Bei Antibiotika gibt es dieses Risiko unterschiedlich stark:
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3112029/
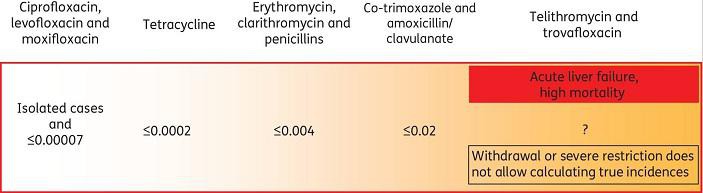
CEMP behauptet, dass Makrolide IV typischerweise auch zu einer Erhöhung von ALT führen. Moxifloxacin ist allerdings kein Makrolide. In Europa ist die Verabreichung von oralen Moxifloxacin aufgrund möglicher Leberschäden eingeschränkt. Im Diagramm oben besitzt es allerdings nur ein geringes Risiko. Ein hohes Risiko hat dort dagegen Telithromycin, das unter dem Namen Ketek vermarktet wird: "Telithromycin ist bisher (2006) das einzige für den klinischen Einsatz am Menschen verfügbare Ketolid. Es ist eine abgewandelte Form des Makrolids Erythromycin."
Ketek hat große Probleme gemacht: https://en.wikipedia.org/wiki/Telithromycin
"After significant controversy regarding safety and research fraud, the US Food and Drug Administration sharply curtailed the approved uses of the drug in 2007... In the United States the FDA's Office of Epidemiology and Surveillance identified 12 cases of acute liver failure, resulting in four deaths, and an additional 23 cases of acute, serious liver injury in among 3.3 million patients taking telithromycin up to April 2006."
Neben Ketek gibt es zwei weitere Ketolide, die bisher nicht zugelassen sind: Cethromycin und Solithromycin. Solithromycin zeigt vergleichbare oder höhere Leberwerte als Moxifloxacin, das z.B. in Europa Probleme mit Leberschäden hat. Außerdem ist es eine Variante von Ketek, das ein großes Risiko von u.a. Leberschäden besitzt. Das sind keine so guten Voraussetzungen.
Im Wiki heißt es weiter... "In 2010, a published report described the likely mechanism of action underlying not only the cases of liver failure but also cases of visual disturbances and exacerbations of myasthenia gravis. The study showed that a pyridine moiety that is part of the telithromycin molecule acts as an antagonist on cholinergic receptors located in the neuromuscular junction, the ciliary ganglion of the eye and the vagus nerve innervating the liver. Other macrolides, such as azithromycin and clarithromycin and the fluoroketolide, solithromycin, do not contain the pyridine moiety and do not antagonize these cholinergic receptors significantly." Dies klingt positiver. Andererseits behauptet z.B. einer auf Twitter, dass die Leberschäden auch anders verursacht werden:
https://twitter.com/JohnTuckerPhD/with_replies
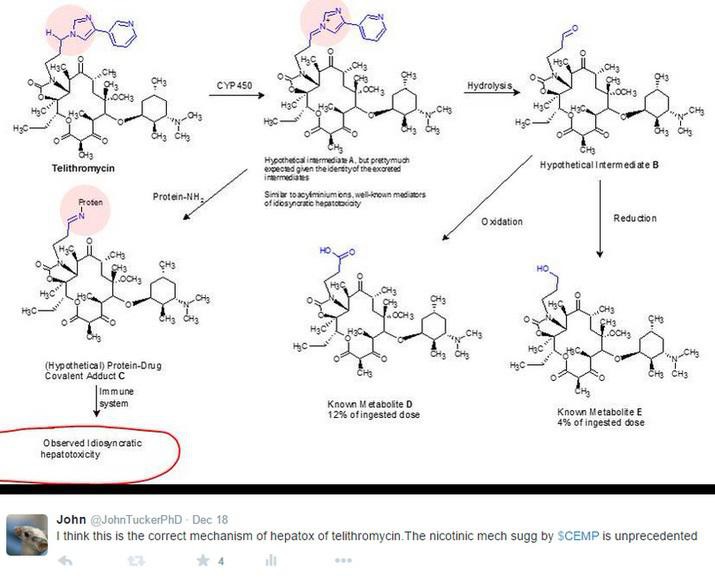
Einige Punkte sprechen auch für CEMP: das zweite Ketolid Cethromycin wurde vor einigen Jahren nicht zugelassen aufgrund zu geringer Effektivität, während die Sicherheit laut FDA okay war. Laut FDA gab es in einer P1 von Cethromycin einen Fall der das Hy's Law Kriterium erfüllt hat. In den PIII-Studien von Cethromycin scheint ALT aber deutlich weniger erhöht zu sein als bei Solithromycin:
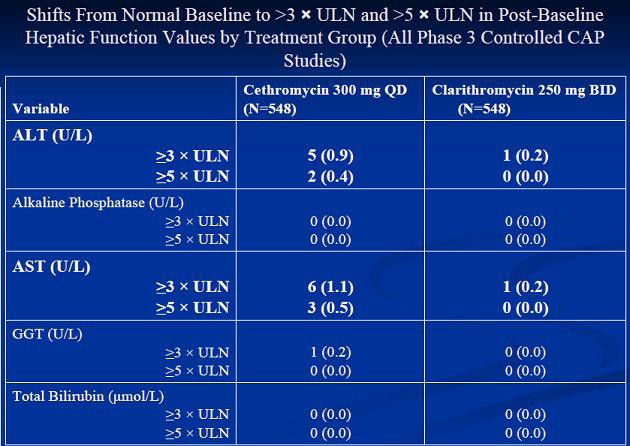
Außerdem erlauben die Behörden, Solithromycin über längere Zeiträume auch an Kindern zu testen, was laut CEMP nicht möglich wäre, wenn die Behörden Zweifel an der Sicherheit hätten. Und es merkwürdig, dass die Leberwerte bei IV höher sind als bei oraler Verabreichung, da oral mehr auf die Leber wirken müsste: "everything dosed orally goes thru liver first, which is why EMA restricted oral not IV moxi."
Trotzdem scheint das Risiko zu bestehen, dass man Solithromycin aufgrund der Verbindung zu Ketek bei den Zulassungsbehörden kritischer betrachtet. Und die seltenen schweren Leberschäden könnten erst nach einer Zulassung auftreten, wenn mehr Patienten als in der PIII behandelt werden.
Der Ansatz für Solithromycin in Lungenentzündung ist, dass bei den schweren Fällen, die im Krankenhaus behandelt werden müssen, das Standard-Makrolid Azithromycin alleine nicht mehr ausreicht. Es muss zusammen mit z.B. Ceftriaxone verabreicht werden, das nur IV gegeben werden kann... insgesamt also eine längere Krankenhausbehandlung. Eine Alternative wäre z.B. Moxifloxacin, das aber deutlich mehr Nebenwirkungen aufweist.
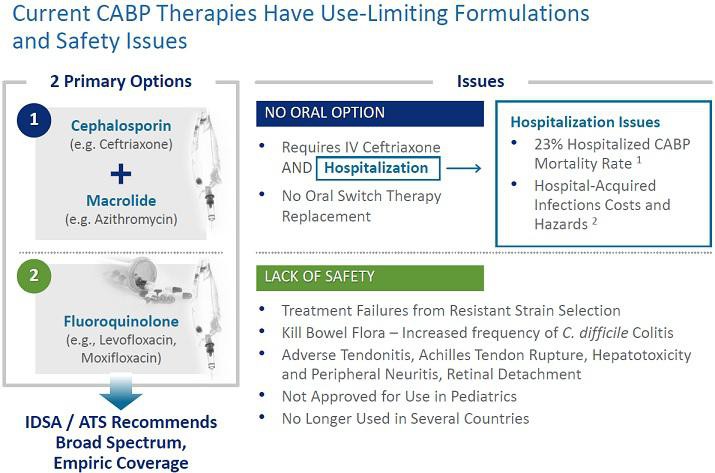

Gegen Makrolide bestehen bereits deutliche Resistenzen... Solithromycin soll quasi ein stärkeres Makrolid sein.
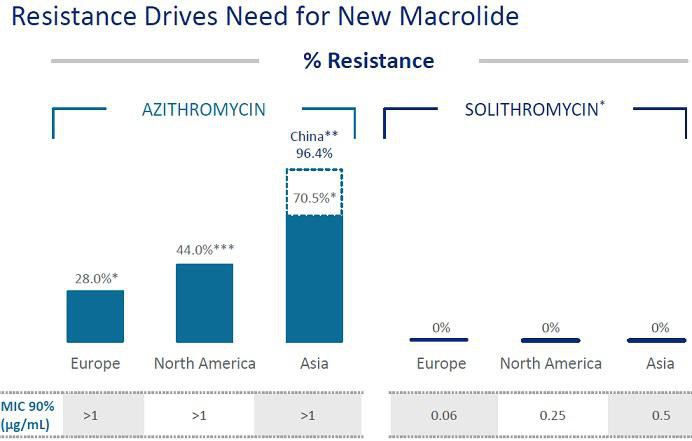
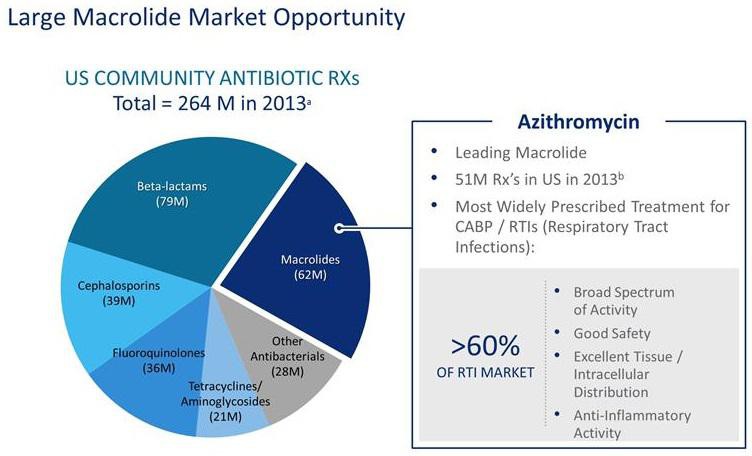
62 Mio Makrolide Rx wären bei 5 Tagen pro Rx und 50 USD pro Pille theoretisch ein 15 Mrd USD Markt in den USA. Solithromycin könnte irgendwann einen kleineren Teil davon haben.


Gruß
ipollit
Hallo SLGramann,
wie siehst du denn die Daten? Ich finde es schwer, ein klares Bild zu erhalten. Für den Kursverfall werden ja mehrere Gründe genannt, so dass man sich offensichtlich auch allgemein nicht sicher ist über die Gründe.
Solithromycin hatte ja Anfang des Jahres die erfolgreiche PIII in der oralen Studie gegen Moxifloxacin. Moxifloxacin wird als ein sehr wirksames Antibiotikum gesehen, so dass Non-Inferiority bereits ein großer Erfolg wäre. In der oralen Studie wurde dies erreicht, wobei Solithromycin über einen kürzeren Zeitraum verabreicht wurde, so dass es prinzipiell gegenüber Moxifloxacin überlegen ist. Die orale Studie soll bei Antibiotika die höhere Hürde als die IV Studie sein, was man z.B. an TTPH sehen kann, wo die orale Studie nach erfolgreicher IV Studie fehlgeschlagen ist. Der große Erfolg in der oralen Studie hat wohl die Erwartungen bei der IV angeheizt.
In der IV Studie wurden nun Solithromycin und Moxifloxacin über den gleichen Zeitraum dosiert (konkret war es eine IV Studie mit möglichen Switch auf oral). Wieder wurde Non-Inferiority erreicht. Vielleicht hat man hier mehr erwartet, z.B. zahlenmäßig bessere Ergebnisse von Solithromycin, da es nun länger verabreicht wurde. Außerdem soll Moxifloxacin schlechter bei älteren Patienten wirken... dazu gibt es bisher keine Zahlen?
Ein möglicher Knackpunkt ist der primäre Endpunkt in CE-SFU mit Port 3/4, der für eine EU-Zulassung benötigt wird. Offensichtlich gab es Probleme mit der Verfügbarkeit von Solithromycin, so dass ein paar Patienten nicht über den vollen Zeitraum die Therapie erhielten, wodurch die Ergebnisse dieser Patienten schlechter sind. Mit diesen Patienten zusammen konnte keine Non-Inferiority belegt werden... CEMP will diese zensieren, dann wird Non-Inferiority erreicht, aber wird sich die EMA darauf einlassen? Für die US-Zulassung spielt dies keine Rolle.
Von der Wirkung her sieht es also prinzipiell okay aus, auch wenn man vielleicht auf klarere Ergebnisse gehofft hat.
Ein weiteres Problem sind die Nebenwirkungen. Anders als in der oralen Studie besitzt Solithromycin mit 34% deutlich mehr Nebenwirkungen als Moxifloxacin mit 13%. Dies relativiert sich aber, da die meisten Nebenwirkungen von Solithromycin Schmerzen bei der Infusion sind. Dies soll typisch für Makrolide sein, zu denen Solithromycin gehört... Moxifloxacin gehört nicht dieser Klasse an.
Bis hierhin sehe ich also kein gravierendes Problem. Das Folgende ist mir aber unklar... vielleicht stellt es ein gewisses Risiko dar: Solithromycin erhöht genauso wie Moxifloxacin die Leberwerte. ALT Grad 3 war bereits bei der oralen Studie unter Solithromycin mehr erhöht als unter Moxifloxacin. Grad 4 war bei oral sehr gering, nun bei IV vergleichbar mit Moxifloxacin.

"Alanine transaminase (ALT) elevation was observed in both treatment arms. Grade 3 ALT elevations ( > 3-8×ULN) occurred in 8.2% of solithromycin patients and 3.4% of moxifloxacin patients and Grade 4 ALT elevations ( > 8×ULN) occurred in 0.7% of solithromycin patients and 0.5% of moxifloxacin patients. Treatment emergent ALT elevations were generally asymptomatic, reversible, and not associated with increased bilirubin. No solithromycin patient met Hy's Law criteria of concurrent ALT and bilirubin elevations post-baseline."
Leberwerte können angeblich erhöht sein, wenn man recht hohe Dosen eines Medikaments verabreicht bekommt, was z.B. bei Antibiotika der Fall ist. Solange die Werte nur erhöht sind und nach der Verabreichung wieder fallen, ist dies kein Problem. Erhöhte Leberwerte sind aber auch ein Hinweis auf Leberschäden. Ein Leberschaden bis hin zum Versagen ist sehr gravierend! Bei Antibiotika gibt es dieses Risiko unterschiedlich stark:
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3112029/

CEMP behauptet, dass Makrolide IV typischerweise auch zu einer Erhöhung von ALT führen. Moxifloxacin ist allerdings kein Makrolide. In Europa ist die Verabreichung von oralen Moxifloxacin aufgrund möglicher Leberschäden eingeschränkt. Im Diagramm oben besitzt es allerdings nur ein geringes Risiko. Ein hohes Risiko hat dort dagegen Telithromycin, das unter dem Namen Ketek vermarktet wird: "Telithromycin ist bisher (2006) das einzige für den klinischen Einsatz am Menschen verfügbare Ketolid. Es ist eine abgewandelte Form des Makrolids Erythromycin."
Ketek hat große Probleme gemacht: https://en.wikipedia.org/wiki/Telithromycin
"After significant controversy regarding safety and research fraud, the US Food and Drug Administration sharply curtailed the approved uses of the drug in 2007... In the United States the FDA's Office of Epidemiology and Surveillance identified 12 cases of acute liver failure, resulting in four deaths, and an additional 23 cases of acute, serious liver injury in among 3.3 million patients taking telithromycin up to April 2006."
Neben Ketek gibt es zwei weitere Ketolide, die bisher nicht zugelassen sind: Cethromycin und Solithromycin. Solithromycin zeigt vergleichbare oder höhere Leberwerte als Moxifloxacin, das z.B. in Europa Probleme mit Leberschäden hat. Außerdem ist es eine Variante von Ketek, das ein großes Risiko von u.a. Leberschäden besitzt. Das sind keine so guten Voraussetzungen.
Im Wiki heißt es weiter... "In 2010, a published report described the likely mechanism of action underlying not only the cases of liver failure but also cases of visual disturbances and exacerbations of myasthenia gravis. The study showed that a pyridine moiety that is part of the telithromycin molecule acts as an antagonist on cholinergic receptors located in the neuromuscular junction, the ciliary ganglion of the eye and the vagus nerve innervating the liver. Other macrolides, such as azithromycin and clarithromycin and the fluoroketolide, solithromycin, do not contain the pyridine moiety and do not antagonize these cholinergic receptors significantly." Dies klingt positiver. Andererseits behauptet z.B. einer auf Twitter, dass die Leberschäden auch anders verursacht werden:
https://twitter.com/JohnTuckerPhD/with_replies

Einige Punkte sprechen auch für CEMP: das zweite Ketolid Cethromycin wurde vor einigen Jahren nicht zugelassen aufgrund zu geringer Effektivität, während die Sicherheit laut FDA okay war. Laut FDA gab es in einer P1 von Cethromycin einen Fall der das Hy's Law Kriterium erfüllt hat. In den PIII-Studien von Cethromycin scheint ALT aber deutlich weniger erhöht zu sein als bei Solithromycin:

Außerdem erlauben die Behörden, Solithromycin über längere Zeiträume auch an Kindern zu testen, was laut CEMP nicht möglich wäre, wenn die Behörden Zweifel an der Sicherheit hätten. Und es merkwürdig, dass die Leberwerte bei IV höher sind als bei oraler Verabreichung, da oral mehr auf die Leber wirken müsste: "everything dosed orally goes thru liver first, which is why EMA restricted oral not IV moxi."
Trotzdem scheint das Risiko zu bestehen, dass man Solithromycin aufgrund der Verbindung zu Ketek bei den Zulassungsbehörden kritischer betrachtet. Und die seltenen schweren Leberschäden könnten erst nach einer Zulassung auftreten, wenn mehr Patienten als in der PIII behandelt werden.
Der Ansatz für Solithromycin in Lungenentzündung ist, dass bei den schweren Fällen, die im Krankenhaus behandelt werden müssen, das Standard-Makrolid Azithromycin alleine nicht mehr ausreicht. Es muss zusammen mit z.B. Ceftriaxone verabreicht werden, das nur IV gegeben werden kann... insgesamt also eine längere Krankenhausbehandlung. Eine Alternative wäre z.B. Moxifloxacin, das aber deutlich mehr Nebenwirkungen aufweist.


Gegen Makrolide bestehen bereits deutliche Resistenzen... Solithromycin soll quasi ein stärkeres Makrolid sein.


62 Mio Makrolide Rx wären bei 5 Tagen pro Rx und 50 USD pro Pille theoretisch ein 15 Mrd USD Markt in den USA. Solithromycin könnte irgendwann einen kleineren Teil davon haben.

Gruß
ipollit
Antwort auf Beitrag Nr.: 50.875.002 von ipollit am 18.10.15 17:41:09Hallo ipollit,
was hälst du von AKAO - Achaogen plazomicin ist zwar aminoglycoside, mit einer MCAP von ca. 100 Mio $ und 60 Mio $ in Cash, allerdings Recht günstig.
Der Bedarf scheint auch gegeben:
The need for new antibiotics to treat CRE is particularly acute, as CRE are one of the top global threats in infectious disease. In 2013, the CDC labeled CRE as “nightmare bacteria” and indicated that CRE pose a public health threat requiring “urgent and aggressive action.” These bacteria are commonly MDR, exhibiting resistance to not only carbapenems, but also to nearly all antibiotics commonly used to treat gram-negative infections, including cephalosporins, beta-lactam/beta-lactamase inhibitor combinations, fluoroquinolones, and currently marketed aminoglycosides. Resistance to carbapenems, which we define as non-susceptibility to a carbapenem antibiotic, has been highlighted because these drugs are one of the last lines of defense against resistant gram-negative infections. Most CRE express enzymes called carbapenemases which break down the carbapenem antibiotic molecule before it can kill the bacteria. Due to the lack of effective therapies, CRE infections are associated with significant mortality, with up to 50% mortality observed in patients with bloodstream infections.
http://www.achaogen.com/plazomicin/
was hälst du von AKAO - Achaogen plazomicin ist zwar aminoglycoside, mit einer MCAP von ca. 100 Mio $ und 60 Mio $ in Cash, allerdings Recht günstig.
Der Bedarf scheint auch gegeben:
The need for new antibiotics to treat CRE is particularly acute, as CRE are one of the top global threats in infectious disease. In 2013, the CDC labeled CRE as “nightmare bacteria” and indicated that CRE pose a public health threat requiring “urgent and aggressive action.” These bacteria are commonly MDR, exhibiting resistance to not only carbapenems, but also to nearly all antibiotics commonly used to treat gram-negative infections, including cephalosporins, beta-lactam/beta-lactamase inhibitor combinations, fluoroquinolones, and currently marketed aminoglycosides. Resistance to carbapenems, which we define as non-susceptibility to a carbapenem antibiotic, has been highlighted because these drugs are one of the last lines of defense against resistant gram-negative infections. Most CRE express enzymes called carbapenemases which break down the carbapenem antibiotic molecule before it can kill the bacteria. Due to the lack of effective therapies, CRE infections are associated with significant mortality, with up to 50% mortality observed in patients with bloodstream infections.
http://www.achaogen.com/plazomicin/
Antwort auf Beitrag Nr.: 50.864.163 von SLGramann am 16.10.15 14:15:04Sehr schade. Dieses eigentlich sehr hoffnungsvolle Programm ist jetzt wirklich beschädigt. Zumindest eine Anwendung im Massenmarkt (außerhalb PWS) steht jetzt sehr in Frage.
ZFGN
Wieder mal ein Wert bei dem ich "Lehrgeld" zahlen musste. Leider hat sich die Vermutung bestätigt, dass es schon vorher zumindest zu Komplikationen mit Thrombose gekommen ist. Wenn ich das über Twitter richtig verfolgt habe, gab es laut CC jetzt 4 solcher Vorfälle in der PIII (alle im B.-Arm) und insgesamt 6 in allen Studien zusammen. Das wird dann wohl auch der Grund gewesen sein, warum CEO und Co ab September ihre Aktienpakete verkauft haben. "Fairerweise" muss man sagen, dass sie sich sicherlich an geltene Bestimmungen gehalten haben. Trotzdem bleibt ein übler Geschmack, dass - was die Informationsfluss betrifft - eine 3 Klassengesellschaft herrscht. Wie es mit B. weitergeht - darüber kann man nur spekulieren. Eventuell wird die Studie unter verschärften Sicherheitsbestimmungen (regelmäßige Scans) zumindest bei PWS fortgesetzt. Traurig wie es ist, wurde durch den Todesfall auch der große medizinische Bedarf vor Augen geführt. Der/die Verstorbene hatte einen BMI von 55. Für den Massenmarkt sehe ich es wie SLG..., hinzu kommt, dass im Grunde alle Projekte (also auch Nash) auf dem gleichen Wirkprinzip beruhen, das jetzt doch sehr in Frage steht.
BBBiotech
Hier ist ein neuer Quartalsbericht veröffentlicht.
http://www.bbbiotech.ch/index.php?eID=tx_nawsecuredl&u=5&g=2…
Oder
Sie sehen die aktuelle Phase wohl als Chance und haben ihre Cashposition komplett (und mehr) abgebaut. Unter anderem ESPR aufgenommen...

SG kmastra
ZFGN
Wieder mal ein Wert bei dem ich "Lehrgeld" zahlen musste. Leider hat sich die Vermutung bestätigt, dass es schon vorher zumindest zu Komplikationen mit Thrombose gekommen ist. Wenn ich das über Twitter richtig verfolgt habe, gab es laut CC jetzt 4 solcher Vorfälle in der PIII (alle im B.-Arm) und insgesamt 6 in allen Studien zusammen. Das wird dann wohl auch der Grund gewesen sein, warum CEO und Co ab September ihre Aktienpakete verkauft haben. "Fairerweise" muss man sagen, dass sie sich sicherlich an geltene Bestimmungen gehalten haben. Trotzdem bleibt ein übler Geschmack, dass - was die Informationsfluss betrifft - eine 3 Klassengesellschaft herrscht. Wie es mit B. weitergeht - darüber kann man nur spekulieren. Eventuell wird die Studie unter verschärften Sicherheitsbestimmungen (regelmäßige Scans) zumindest bei PWS fortgesetzt. Traurig wie es ist, wurde durch den Todesfall auch der große medizinische Bedarf vor Augen geführt. Der/die Verstorbene hatte einen BMI von 55. Für den Massenmarkt sehe ich es wie SLG..., hinzu kommt, dass im Grunde alle Projekte (also auch Nash) auf dem gleichen Wirkprinzip beruhen, das jetzt doch sehr in Frage steht.
BBBiotech
Hier ist ein neuer Quartalsbericht veröffentlicht.
http://www.bbbiotech.ch/index.php?eID=tx_nawsecuredl&u=5&g=2…
Oder
Sie sehen die aktuelle Phase wohl als Chance und haben ihre Cashposition komplett (und mehr) abgebaut. Unter anderem ESPR aufgenommen...
SG kmastra
Antwort auf Beitrag Nr.: 50.876.193 von kmastra am 18.10.15 21:31:17Danke kmastra. Ich hatte vergangene Woche bei ESPR nochmal nachgekauft, daher freut es mich zu sehen, dass die Manager von BB Biotech auch positiv gestimmt sind, nach meinem laienhaften Verständnis wird dort (BB Biotech) solide Arbeit geleistet.
Antwort auf Beitrag Nr.: 50.875.002 von ipollit am 18.10.15 17:41:09Hallo ipollit,
Du hast die Daten und Fragen zu CEMP besser aufbereitet, als ich es könnte, insofern kann ich Deine diesbezügliche Frage nicht wirklich beantworten.
Wie Du wohl auch sehe ich die Leberwerte als entscheidend für den Kursverfall an. Ich sehe darin auch durchaus ein ernstes Warnzeichen. Allerdings gehe ich eben davon aus, dass eine Zulassung immer noch überwiegend wahrscheinlich ist. Die Marktkapitalisierung beträgt jetzt nur noch 850 Mio. USD und an dem Punkt scheint mir die Chance doch größer als das Risiko zu sein.
Wie immer sollte man natürlich eine eventuelle Position klein halten. Meine beträgt ca. 2% des Depotvolumens.
PS: Heute ein ziemlich lächerlicher Abverkauf bei BLUE. Wenn ich da nicht eh schon zu viele von hätte, hätte ich mich heute über diese Dummheit des Marktes gefreut.
Du hast die Daten und Fragen zu CEMP besser aufbereitet, als ich es könnte, insofern kann ich Deine diesbezügliche Frage nicht wirklich beantworten.
Wie Du wohl auch sehe ich die Leberwerte als entscheidend für den Kursverfall an. Ich sehe darin auch durchaus ein ernstes Warnzeichen. Allerdings gehe ich eben davon aus, dass eine Zulassung immer noch überwiegend wahrscheinlich ist. Die Marktkapitalisierung beträgt jetzt nur noch 850 Mio. USD und an dem Punkt scheint mir die Chance doch größer als das Risiko zu sein.
Wie immer sollte man natürlich eine eventuelle Position klein halten. Meine beträgt ca. 2% des Depotvolumens.
PS: Heute ein ziemlich lächerlicher Abverkauf bei BLUE. Wenn ich da nicht eh schon zu viele von hätte, hätte ich mich heute über diese Dummheit des Marktes gefreut.
Antwort auf Beitrag Nr.: 50.883.672 von SLGramann am 19.10.15 21:39:56was ist denn bei BLUE eigentich los, die haben ca 50 % eingebüßt, fast ohne wirkliche Erholung. Andere Werte haben sich doch schon wieder ganz gut erholt, etwa Karyopharm, Esperion oder Intercept.
Nur Blue fällt und fällt....
Hab ich eine Meldung verpasst?
Nur Blue fällt und fällt....
Hab ich eine Meldung verpasst?
RLYP
ich verstehe die Kursschwäche von RLYP in der letzten Zeit nicht? Was stimmt da nicht?
Übermorgen ist der offizielle PDFUA Tag, d.h. die FDA müsste sich bald zur möglichen Zulassung von Patiromer äußern. Aktuelle MK liegt bei 750 Mio USD bei ca. 300 Mio USD Cash... zum Vergleich ist die MK vom Konkurrent ZSPH mit 1,6 Mrd USD mehr als doppelt so hoch. Angeblich ist Actelion bereit 2,5 Mrd USD für ZSPH zu zahlen. ZS-9 steht aber erst nächstes Jahr zur Zulassung an.
Ist ZS-9 besser als Patiromer? In der akuten Anwendung kann dies sein, da laut Studien ZS-9 schneller wirkt. Aber der größere Markt ist die chronische Anwendung... hier sehe ich persönlich Vorteile für Patiromer, da es mit weniger Flüssigkeit eingenommen werden muss und das Risiko von Schwellungen geringer ist. Für Patienten mit Herzproblemen dürften Schwellungen und große Flüssigkeitsmengen wohl ein Problem sein. Der Markt spiegelt das bisher aber nicht wieder.
Hyperkaliämie, d.h. hohe Kaliumwerte im Blut, können dazu führen, dass Patienten mit Herz- oder Nierenproblemen nur unzureichend behandelt werden.
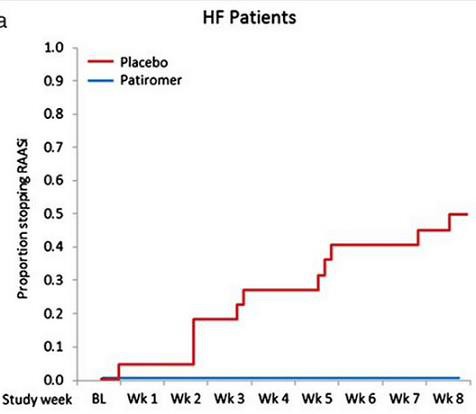

Alleine in den USA dürften 3 Mio CDK- und HF- unter hohen Kaliumwerten leiden. Theoretisch ist dies z.B. bei 2000 USD für Patiromer oder ZS-9 pro Jahr ein 6 Mrd USD Markt... natürlich wird davon nur ein Teil mit diesen Medikamenten behandelt werden, sollten sie zugelassen werden.
Mal sehen, wie die FDA Patiromer sieht. Ich habe jedenfalls meine Position weiter erhöht, ebenso wie OMED... bei KPTI werde ich wohl auch nachkaufen.


Gruß
ipollit
ich verstehe die Kursschwäche von RLYP in der letzten Zeit nicht? Was stimmt da nicht?
Übermorgen ist der offizielle PDFUA Tag, d.h. die FDA müsste sich bald zur möglichen Zulassung von Patiromer äußern. Aktuelle MK liegt bei 750 Mio USD bei ca. 300 Mio USD Cash... zum Vergleich ist die MK vom Konkurrent ZSPH mit 1,6 Mrd USD mehr als doppelt so hoch. Angeblich ist Actelion bereit 2,5 Mrd USD für ZSPH zu zahlen. ZS-9 steht aber erst nächstes Jahr zur Zulassung an.
Ist ZS-9 besser als Patiromer? In der akuten Anwendung kann dies sein, da laut Studien ZS-9 schneller wirkt. Aber der größere Markt ist die chronische Anwendung... hier sehe ich persönlich Vorteile für Patiromer, da es mit weniger Flüssigkeit eingenommen werden muss und das Risiko von Schwellungen geringer ist. Für Patienten mit Herzproblemen dürften Schwellungen und große Flüssigkeitsmengen wohl ein Problem sein. Der Markt spiegelt das bisher aber nicht wieder.
Hyperkaliämie, d.h. hohe Kaliumwerte im Blut, können dazu führen, dass Patienten mit Herz- oder Nierenproblemen nur unzureichend behandelt werden.


Alleine in den USA dürften 3 Mio CDK- und HF- unter hohen Kaliumwerten leiden. Theoretisch ist dies z.B. bei 2000 USD für Patiromer oder ZS-9 pro Jahr ein 6 Mrd USD Markt... natürlich wird davon nur ein Teil mit diesen Medikamenten behandelt werden, sollten sie zugelassen werden.
Mal sehen, wie die FDA Patiromer sieht. Ich habe jedenfalls meine Position weiter erhöht, ebenso wie OMED... bei KPTI werde ich wohl auch nachkaufen.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.875.407 von McNay am 18.10.15 19:01:04Hallo McNay,
mit AKAO kenne ich mich nicht so aus, aber danke für den Hinweis, müsste ich mir mal genauer anschauen. Die PIII wird noch ein wenig laufen... wenn ich es richtig sehe, ist erst in 2 Jahren mit Ergebnissen zu rechnen, richtig?
Gruß
ipollit
mit AKAO kenne ich mich nicht so aus, aber danke für den Hinweis, müsste ich mir mal genauer anschauen. Die PIII wird noch ein wenig laufen... wenn ich es richtig sehe, ist erst in 2 Jahren mit Ergebnissen zu rechnen, richtig?
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.876.193 von kmastra am 18.10.15 21:31:17"ZFGN
Wieder mal ein Wert bei dem ich "Lehrgeld" zahlen musste."
Hallo kmastra,
den Wert im Depot gehabt zu haben, ist jedenfalls nicht vorwerfbar. Die Geschichte war extrem spannend und erschien sehr aussichtsreich. Es gab sehr gute Gründe, in ZFGN investiert zu sein.
Das Einzige, was man hieraus mitnehmen kann, ist (wieder mal), dass keine Depotposition eine bestimmte Größe überschreiten sollte. Bei einem Wert wie ZFGN sollten das vermutlich keinesfalls mehr als 5% sein - eher 3.
Viele Grüße
SLG
Wieder mal ein Wert bei dem ich "Lehrgeld" zahlen musste."
Hallo kmastra,
den Wert im Depot gehabt zu haben, ist jedenfalls nicht vorwerfbar. Die Geschichte war extrem spannend und erschien sehr aussichtsreich. Es gab sehr gute Gründe, in ZFGN investiert zu sein.
Das Einzige, was man hieraus mitnehmen kann, ist (wieder mal), dass keine Depotposition eine bestimmte Größe überschreiten sollte. Bei einem Wert wie ZFGN sollten das vermutlich keinesfalls mehr als 5% sein - eher 3.
Viele Grüße
SLG
RLYP
so ein Markt kann doch nicht gesund sein!? Schon zwei Volatilitäts-Halts ohne News... wird etwas geleakt oder wer tobt sich da gerade aus?
Mal schauen, ob die FDA heute wirklich den Daumen senkt...
Gruß
ipollit
so ein Markt kann doch nicht gesund sein!? Schon zwei Volatilitäts-Halts ohne News... wird etwas geleakt oder wer tobt sich da gerade aus?

Mal schauen, ob die FDA heute wirklich den Daumen senkt...
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.901.309 von ipollit am 21.10.15 19:52:14Schon Krass ich hab den "Plumser" genutzt mal sehen wie es kommt.
SNTA
wenigstens hier ist die Sache eindeutig... eine längere Geschichte geht zuende, leider ist es kein gutes Ende! Der Hsp90-Hemmer Ganetespib ist in der GALAXY2 Lungenkrebs PIII vorzeitig gescheitert.
http://www.fiercebiotech.com/story/synta-gets-decimated-afte…


Gruß
ipollit
wenigstens hier ist die Sache eindeutig... eine längere Geschichte geht zuende, leider ist es kein gutes Ende! Der Hsp90-Hemmer Ganetespib ist in der GALAXY2 Lungenkrebs PIII vorzeitig gescheitert.
http://www.fiercebiotech.com/story/synta-gets-decimated-afte…
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.901.408 von schnappi am 21.10.15 20:00:14Die Zulassungswahrscheinlichkeit soll angeblich ziemlich hoch sein... Unklarheiten betreffen eher das Label.
Konkurrent ZSPH macht es heute nicht besser... auch dick im Minus. Sollte RLYP scheitern, müsste das eigentlich gut für ZSPH sein.
Gruß
ipollit
Konkurrent ZSPH macht es heute nicht besser... auch dick im Minus. Sollte RLYP scheitern, müsste das eigentlich gut für ZSPH sein.
Gruß
ipollit
Antwort auf Beitrag Nr.: 50.901.606 von ipollit am 21.10.15 20:18:43Ich wurde auf RLYP durch das mitlesen hier aufmerksam und konnte vorhin keine News finden.
Da habe ich mich schnell entschlossen mal etwas Money zu riskieren.
Da habe ich mich schnell entschlossen mal etwas Money zu riskieren.
Antwort auf Beitrag Nr.: 50.901.672 von schnappi am 21.10.15 20:27:03Das die FDA Entscheidung geleaked ist kann ja eigentlich nicht sein!?
Das zeigt wohl eher, wie nervös der Markt ist. Daytraders Paradise momentan!
Ich drück die Daumen! Der Markt kann ein Erfolgserlebnis ganz gut brauchen...
Das zeigt wohl eher, wie nervös der Markt ist. Daytraders Paradise momentan!
Ich drück die Daumen! Der Markt kann ein Erfolgserlebnis ganz gut brauchen...
Antwort auf Beitrag Nr.: 50.901.945 von kmastra am 21.10.15 20:52:42Der Nasi Bio macht heute auch wieder zick-zack bei knapp 3100 gab es wieder verstärkt kaufinteresse.
Antwort auf Beitrag Nr.: 50.901.945 von kmastra am 21.10.15 20:52:42RLYP
Der FDA-Daumen zeigt nach oben! Veltassa ist zugelassen... Label soll gut sein. Mal schauen.
Veltassa ist zugelassen... Label soll gut sein. Mal schauen.
Gruß
ipollit
Der FDA-Daumen zeigt nach oben!
 Veltassa ist zugelassen... Label soll gut sein. Mal schauen.
Veltassa ist zugelassen... Label soll gut sein. Mal schauen.Gruß
ipollit
Antwort auf Beitrag Nr.: 50.903.010 von ipollit am 21.10.15 23:25:50Sehr schön bin gespannt zu welchem Kurs der Markt dies einpreist.
Antwort auf Beitrag Nr.: 50.903.376 von schnappi am 22.10.15 00:46:47
ich glaube Biotech ist aktuell so etwas von out.
RLYP: Mit Zulassung vorbörslich massiv im Minus in den USA.
Zitat von schnappi: Sehr schön bin gespannt zu welchem Kurs der Markt dies einpreist.
ich glaube Biotech ist aktuell so etwas von out.
RLYP: Mit Zulassung vorbörslich massiv im Minus in den USA.
RLYP:
(nur mal so)
At ~12 $RLYP enterprise value will be ~150M. $ZSPH @ 55 will have EV of 1.1B
2:43 PM - 22 Oct 2015
Ich denke, der Markt ist aus drei Gründen verstimmt:
1.) Es gab eine News. (In der derzeitigen Stimmungslage führt jede News unabhängig vom Inhalt erst mal zu einem pauschalen Bewertungsabschlag von 30%...)
2.) Es gibt (erst ein mal) ein "box warning":
Adam Feuerstein ✔ @adamfeuerstein
$RLYP Box warning spooking folks. Worries 6-hr dose separation recommendation will pinch sales. $ZSPH bulls piling on. Show me launch story.

3.) Der Markt muss für diese Art von Medikament ganz neu erschlossen werden. Das könnte mühsam werden. Manche Analysten hinterfragen ganz grundsätzlich das Potential. Die Peak Sales-Schätzungen gehen zwar bis "über eine Milliarde", aber andere Analysten halten 200 Millionen für realistischer.
-----------------------
Die Frage ist allerdings, wie niedrig man den RLYP bewerten will. Bei allen Risiken und Unsicherheiten ist ein EV von 150 Millionen Dollar schon... etwas befremdlich.
(nur mal so)
At ~12 $RLYP enterprise value will be ~150M. $ZSPH @ 55 will have EV of 1.1B
2:43 PM - 22 Oct 2015
Ich denke, der Markt ist aus drei Gründen verstimmt:
1.) Es gab eine News. (In der derzeitigen Stimmungslage führt jede News unabhängig vom Inhalt erst mal zu einem pauschalen Bewertungsabschlag von 30%...)

2.) Es gibt (erst ein mal) ein "box warning":
Adam Feuerstein ✔ @adamfeuerstein
$RLYP Box warning spooking folks. Worries 6-hr dose separation recommendation will pinch sales. $ZSPH bulls piling on. Show me launch story.

3.) Der Markt muss für diese Art von Medikament ganz neu erschlossen werden. Das könnte mühsam werden. Manche Analysten hinterfragen ganz grundsätzlich das Potential. Die Peak Sales-Schätzungen gehen zwar bis "über eine Milliarde", aber andere Analysten halten 200 Millionen für realistischer.
-----------------------
Die Frage ist allerdings, wie niedrig man den RLYP bewerten will. Bei allen Risiken und Unsicherheiten ist ein EV von 150 Millionen Dollar schon... etwas befremdlich.
Antwort auf Beitrag Nr.: 50.907.522 von SLGramann am 22.10.15 14:57:47Hier wird die Warnung relativiert:

Das ist sicher eine vernünftige Ansicht, nur wird der Markt wohl erst mal vermuten, dass das alles ZSPH einen bedeutenden Marketingsvorsprung verschaffen wird. Das kann man aber heute sicher so gar nicht verlässlich wissen.
(Insofern aber logisch, dass ZSPH vorbörslich im Plus notiert)

Das ist sicher eine vernünftige Ansicht, nur wird der Markt wohl erst mal vermuten, dass das alles ZSPH einen bedeutenden Marketingsvorsprung verschaffen wird. Das kann man aber heute sicher so gar nicht verlässlich wissen.
(Insofern aber logisch, dass ZSPH vorbörslich im Plus notiert)
Antwort auf Beitrag Nr.: 50.884.260 von ipollit am 19.10.15 23:27:29Hallo ipollit,
Rlyp kann ich den Kursverfall nicht nachvollziehen, zu mal ZSPHs ZS-9 auch noch nicht zugelassen ist.
AKAO, ja Richtig Phase 3 cUTI trial: top-line data and NDA 2H 2017.
Es gibt natürlich auch einiges an Wettbewerbern, wie man in der Präsi sieht. Die Ph 3 dürfte aber finanziert sein.
Die Frage ist sicherlich, ob man sich am Markt durchsetzen kann, gegen die großen Player ohne Partner und ob es gelingt einen guten Preis zu erzielen.
Generika-Konkurenz ist ja außerdem nicht zu unterschätzen.
Ich denke man kann hier vielleicht noch warten mit einem Einstieg.
Gruß
McNay
Rlyp kann ich den Kursverfall nicht nachvollziehen, zu mal ZSPHs ZS-9 auch noch nicht zugelassen ist.
AKAO, ja Richtig Phase 3 cUTI trial: top-line data and NDA 2H 2017.
Es gibt natürlich auch einiges an Wettbewerbern, wie man in der Präsi sieht. Die Ph 3 dürfte aber finanziert sein.
Die Frage ist sicherlich, ob man sich am Markt durchsetzen kann, gegen die großen Player ohne Partner und ob es gelingt einen guten Preis zu erzielen.
Generika-Konkurenz ist ja außerdem nicht zu unterschätzen.
Ich denke man kann hier vielleicht noch warten mit einem Einstieg.
Gruß
McNay
Antwort auf Beitrag Nr.: 50.907.522 von SLGramann am 22.10.15 14:57:47Danke für deine Erläuterung.
Von Ohad Hammer gab es ein Update zu Esperion.
http://www.orf-blog.com/esperion-seeing-the-glass-half-full/
http://www.orf-blog.com/esperion-seeing-the-glass-half-full/
Antwort auf Beitrag Nr.: 50.979.495 von schnappi am 01.11.15 13:59:37Wenn man bedenkt, welchen Aufwand Ohad betreibt und seine zweifelsohne große Expertise, ist es ihm trotzdem nicht gelungen (zumindest momentan gerade nicht) den I-Shares Nasdaq Biotech Index Fund zu schlagen. In Anbetracht der niedrigen Gebühren (0,48%), stellt sich schon die Frage, ob man mit einem ETF auf lange Sicht nicht besser fährt und die volatilen Phasen zu Zukäufen nutzt? Zumindest zur Depotmischung macht es vielleicht Sinn. Analog gibt es ja Aktien, wie BB Biotech die ebenfalls ein breites Spektrum abbilden, aber eigentlich auch analog zum Index laufen.
Antwort auf Beitrag Nr.: 50.979.834 von McNay am 01.11.15 16:26:55Ich muss allerdings anmerken, dass ich selbst in diesem Zeitraum nicht annähernd auf eine ähnliche Perfomance komme.
In meinen Fall ist die Thematik ganz klar, Verluste begrenzen. Ohad lässt seine Verluste aktuell auch recht laufen, was allerdings auch schwer zu vermeiden ist, bei der aktuellen Volatilität. Bei ESPR um die 50$ habe ich auch nicht damit gerechnet, dass es noch so viel tiefer geht. Er hat sich zwar mit dem Ultrashort gesichert. Jedoch greift diese Strategie auch nicht, wenn seine relativ risikoreichen Einzeltitel mit 40% im Minus liegen und der Index nicht ganz so hoch verliert bzw. auch wieder zulegt.
In meinen Fall ist die Thematik ganz klar, Verluste begrenzen. Ohad lässt seine Verluste aktuell auch recht laufen, was allerdings auch schwer zu vermeiden ist, bei der aktuellen Volatilität. Bei ESPR um die 50$ habe ich auch nicht damit gerechnet, dass es noch so viel tiefer geht. Er hat sich zwar mit dem Ultrashort gesichert. Jedoch greift diese Strategie auch nicht, wenn seine relativ risikoreichen Einzeltitel mit 40% im Minus liegen und der Index nicht ganz so hoch verliert bzw. auch wieder zulegt.
INCY
Insgesamt sehen die Baricitinib Ergebnisse gegenüber Humira doch sehr erfreulich aus! Tendenziell sind sie durchgehend besser. Immerhin ist Baricitinib als orales Mittel einfacher zu verabreichen und billiger herzustellen als der AK Humira. ABBV möchte mit Humira 2020 stolze 18 Mrd USD Umsatz erzielen.
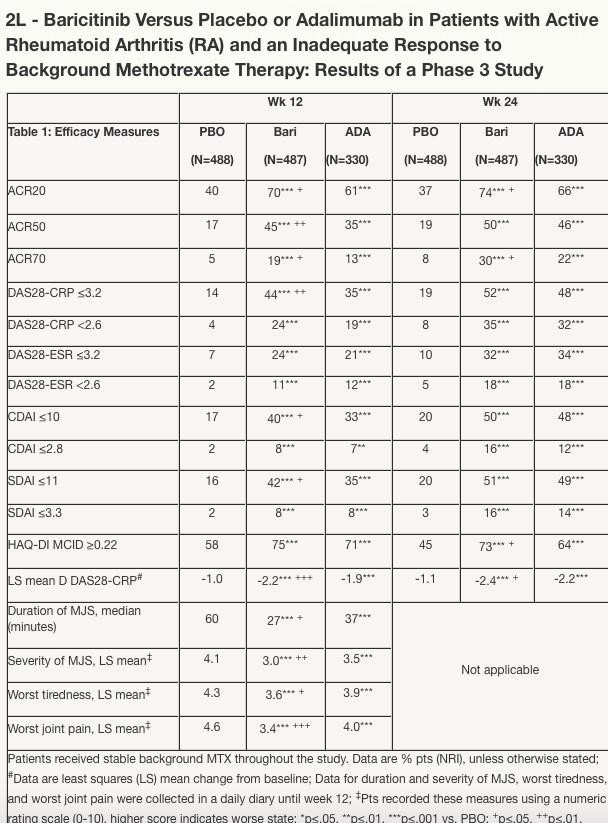

Gruß
ipollit
Insgesamt sehen die Baricitinib Ergebnisse gegenüber Humira doch sehr erfreulich aus! Tendenziell sind sie durchgehend besser. Immerhin ist Baricitinib als orales Mittel einfacher zu verabreichen und billiger herzustellen als der AK Humira. ABBV möchte mit Humira 2020 stolze 18 Mrd USD Umsatz erzielen.

Gruß
ipollit
ACAD
Nuplazid erhält als BTD heute auch PR von der FDA... PDUFA-Tag ist der 01.05.2016.
******
einige Zulassungsentscheidungen der FDA von meinen aktuellen Investitionen...
Erfolgte Zulassungsentscheidungen:
24.07.2015 REGN Praluent HeFH, Atherosclerosis (BLA ? acc 26.01.2015 PR) -> 24.07.2015 OK
04.09.2015 TSRO Rolapitant CINV (BLA 08.09.2014) -> 02.09.2015 OK
21.10.2015 RLYP Patiromer Hyperkalemia (BLA 28.10.2014, acc 15.12.2014) -> 21.10.2015 OK
Anstehende Zulassungsentscheidungen:
11.11.2015 EXEL Cobimetinib Melanoma (acc 19.02.2015 PR, delayed 11.08.2015)
09.03.2016 Gen Daratumumab Myeloma (BLA 09.07.2015 (rol), acc 04.09.2015 PR, BTD)
30.03.2016 CLVS Rociletinib NSCLC (BLA 03.08.2015 (rol), BTD, acc 29.09.2015)
01.05.2016 ACAD Nuplazid PDP (BLA 03.09.2015, acc 02.11.2015 PR, BTD)
26.05.2016 ZSPH ZS-9 Hyperkalemia (BLA 26.05.2015, acc 29.07.2015)
Geschätzte Zulassungsentscheidungen
3Q16e PTLA Andexanet Alfa Factor Xa Anticoagulant Antidote (BTD)... BLA YE15
3Q16e EXEL Cabozantinib RCC (BTD)... BLA YE15
YE16e INCY/LLY Baricitinib RA... BLA YE15
1Q17e CEMP Solithromycin CAPB (FT)... BLA 1H16

Gruß
ipollit
Nuplazid erhält als BTD heute auch PR von der FDA... PDUFA-Tag ist der 01.05.2016.
******
einige Zulassungsentscheidungen der FDA von meinen aktuellen Investitionen...
Erfolgte Zulassungsentscheidungen:
24.07.2015 REGN Praluent HeFH, Atherosclerosis (BLA ? acc 26.01.2015 PR) -> 24.07.2015 OK
04.09.2015 TSRO Rolapitant CINV (BLA 08.09.2014) -> 02.09.2015 OK
21.10.2015 RLYP Patiromer Hyperkalemia (BLA 28.10.2014, acc 15.12.2014) -> 21.10.2015 OK
Anstehende Zulassungsentscheidungen:
11.11.2015 EXEL Cobimetinib Melanoma (acc 19.02.2015 PR, delayed 11.08.2015)
09.03.2016 Gen Daratumumab Myeloma (BLA 09.07.2015 (rol), acc 04.09.2015 PR, BTD)
30.03.2016 CLVS Rociletinib NSCLC (BLA 03.08.2015 (rol), BTD, acc 29.09.2015)
01.05.2016 ACAD Nuplazid PDP (BLA 03.09.2015, acc 02.11.2015 PR, BTD)
26.05.2016 ZSPH ZS-9 Hyperkalemia (BLA 26.05.2015, acc 29.07.2015)
Geschätzte Zulassungsentscheidungen
3Q16e PTLA Andexanet Alfa Factor Xa Anticoagulant Antidote (BTD)... BLA YE15
3Q16e EXEL Cabozantinib RCC (BTD)... BLA YE15
YE16e INCY/LLY Baricitinib RA... BLA YE15
1Q17e CEMP Solithromycin CAPB (FT)... BLA 1H16
Gruß
ipollit
NVAX
kennt sich jemand mit NVAX aus? Ein Impfstoff-Unternehmen mit ca. 2 Mrd USD MK.
NVAX entwickelt neuartige Nanopartikel-Impfstoffe, die spezielle Merkmale von Krankheitserregern dem Immunsystem zugänglich machen, die bei herkömmlichen Impfungen verborgen sind.
http://novavax.com/presentation.show


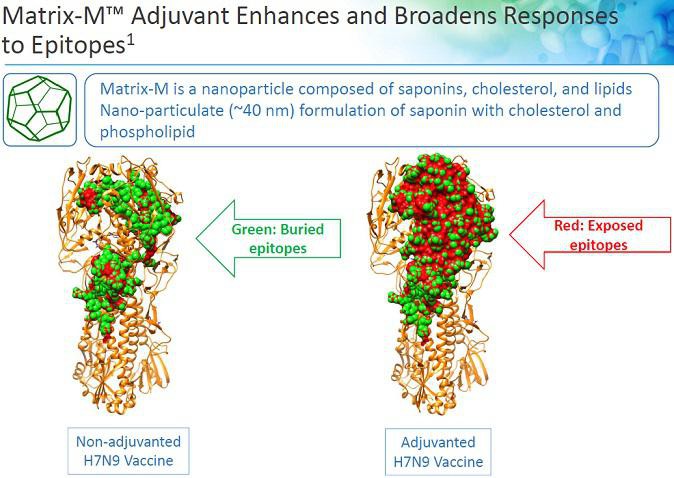
Die zwei fortgeschrittensten Pipeline-Kandidaten richtet sich gegen das RSV-Virus und gegen Grippe-Viren. So wie CEMP ein gutes Antibiotika gegen Lungenkrebs entwickelt, könnte NVAX gegen RSV und Grippe führend sein. RSV ist ein sehr großer Markt... ein klassischer Blockbuster ist z.B. Medimmunes Synagis. Mehrere Medimmune-Mitarbeiter sind nun bei NVAX tätig.
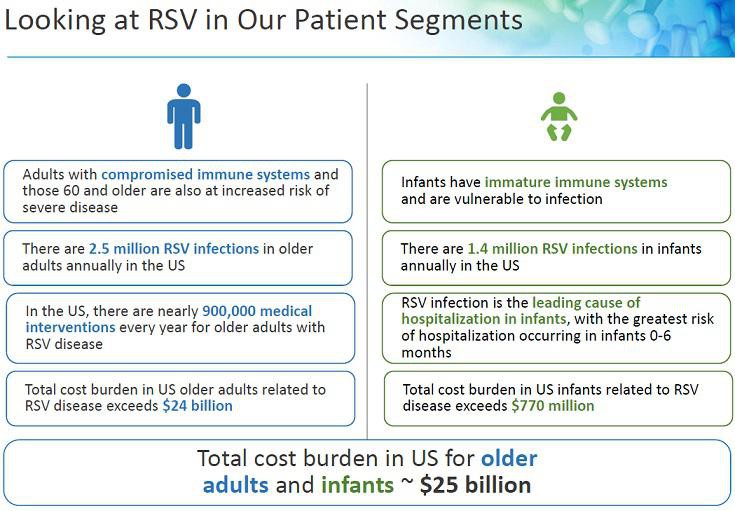

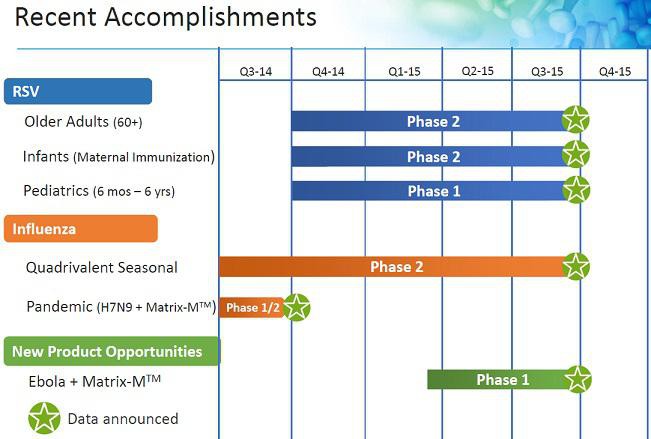
So entwickelt NVAX auch einen Impfstoff gegen Ebola... er soll deutlich stärker als die Konkurrenz sein. Prinzipiell eignet sich die Technologie aber auch zur Impfung gegen viele andere Krankheiten.


Gruß
ipollit
kennt sich jemand mit NVAX aus? Ein Impfstoff-Unternehmen mit ca. 2 Mrd USD MK.
NVAX entwickelt neuartige Nanopartikel-Impfstoffe, die spezielle Merkmale von Krankheitserregern dem Immunsystem zugänglich machen, die bei herkömmlichen Impfungen verborgen sind.
http://novavax.com/presentation.show



Die zwei fortgeschrittensten Pipeline-Kandidaten richtet sich gegen das RSV-Virus und gegen Grippe-Viren. So wie CEMP ein gutes Antibiotika gegen Lungenkrebs entwickelt, könnte NVAX gegen RSV und Grippe führend sein. RSV ist ein sehr großer Markt... ein klassischer Blockbuster ist z.B. Medimmunes Synagis. Mehrere Medimmune-Mitarbeiter sind nun bei NVAX tätig.



So entwickelt NVAX auch einen Impfstoff gegen Ebola... er soll deutlich stärker als die Konkurrenz sein. Prinzipiell eignet sich die Technologie aber auch zur Impfung gegen viele andere Krankheiten.

Gruß
ipollit
CEMP
CEMP scheint überzeugt zu sein, dass die erhöhten ALT-Werte nur temporär und kein Hinweis auch schwerwiegende Leberschäden sind. Der Kurs hat sich zuletzt wieder ein gutes Stück erholt.



Gruß
ipollit
CEMP scheint überzeugt zu sein, dass die erhöhten ALT-Werte nur temporär und kein Hinweis auch schwerwiegende Leberschäden sind. Der Kurs hat sich zuletzt wieder ein gutes Stück erholt.


Gruß
ipollit
NVAX, CEMP
Relevanz von RSV, Grippe und Lungenentzündung in den USA...
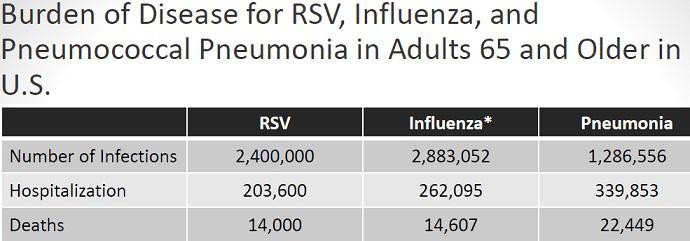
Gruß
ipollit
Relevanz von RSV, Grippe und Lungenentzündung in den USA...

Gruß
ipollit
XLRN, EXEL
Der ALK1 Trap Dalantercept ist eine Ergänzung u.a. der VEGF TKIs. ALK1 spielt wie VEGF bei der Bildung von Blutgefäßen eine Rolle, wobei VEGF eher an der Neubildung und ALK1 bei der Reifung der neuen Blutgefäße beteiligt ist. Theoretisch ist ALK1 also synergetisch mit VEGF.
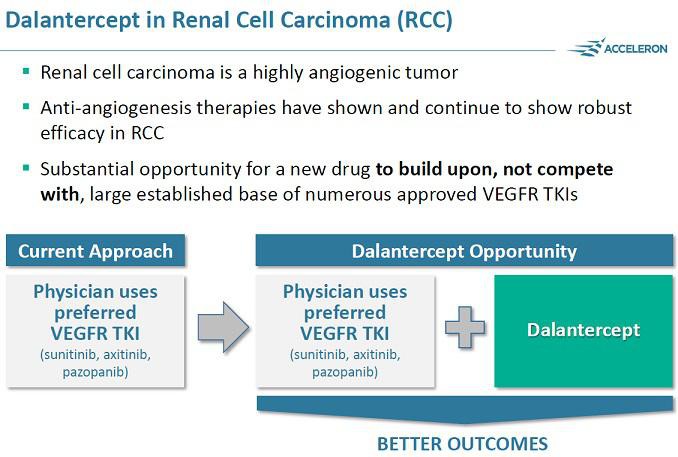
In RCC sehen die ersten PII-Daten des Dalantercept in Kombi mit dem VEGF-Hemmer Axitinib besser aus als EXELs METEOR PIII-Daten von Cabo (wobei PII-Daten natürlich tendenziell besser ausfallen als PIII-Daten)
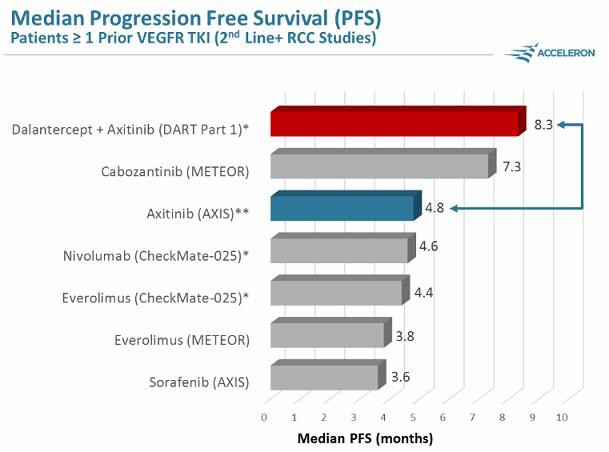
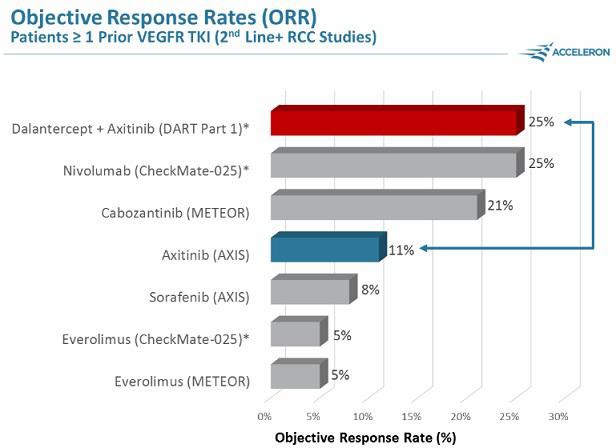
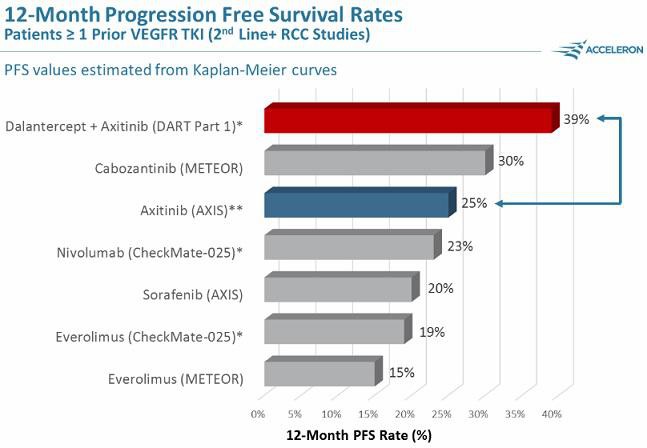
XLRN sagt, dass ALK1 ein anderes Nebenwirkungsprofil hat... vielleicht könnte das interessant sein z.B. bei einer Kombi mit PD1. Dalantercept hat von der FDA Fast Track erhalten.

Gruß
ipollit
Der ALK1 Trap Dalantercept ist eine Ergänzung u.a. der VEGF TKIs. ALK1 spielt wie VEGF bei der Bildung von Blutgefäßen eine Rolle, wobei VEGF eher an der Neubildung und ALK1 bei der Reifung der neuen Blutgefäße beteiligt ist. Theoretisch ist ALK1 also synergetisch mit VEGF.

In RCC sehen die ersten PII-Daten des Dalantercept in Kombi mit dem VEGF-Hemmer Axitinib besser aus als EXELs METEOR PIII-Daten von Cabo (wobei PII-Daten natürlich tendenziell besser ausfallen als PIII-Daten)



XLRN sagt, dass ALK1 ein anderes Nebenwirkungsprofil hat... vielleicht könnte das interessant sein z.B. bei einer Kombi mit PD1. Dalantercept hat von der FDA Fast Track erhalten.

Gruß
ipollit
http://finance.yahoo.com/news/bluebird-bio-present-lentiglob…
BLUE heute mit Kurssturz nachdem gemeldet wurde, dass Beta-Thalassämie Patienten mit der Ausprägung beta0-beta0 weiter Bluttransfusionen benötigen (wenn auch weniger). Diese Ausprägung macht wohl etwa 1/3 des Marktes in dieser Indikation aus. Nachdem ich lange an der Seitenlinie stand bei dem Titel, habe ich heute mal bei 68 USD eine erste kleine Position riskiert... mal schauen. Gem. Chart ist wohl nicht ausgeschlossen, dass es auf 50 oder gar mal noch 40 USD runter geht, da gibt es zumindest ein recht grosses Gap...

BLUE heute mit Kurssturz nachdem gemeldet wurde, dass Beta-Thalassämie Patienten mit der Ausprägung beta0-beta0 weiter Bluttransfusionen benötigen (wenn auch weniger). Diese Ausprägung macht wohl etwa 1/3 des Marktes in dieser Indikation aus. Nachdem ich lange an der Seitenlinie stand bei dem Titel, habe ich heute mal bei 68 USD eine erste kleine Position riskiert... mal schauen. Gem. Chart ist wohl nicht ausgeschlossen, dass es auf 50 oder gar mal noch 40 USD runter geht, da gibt es zumindest ein recht grosses Gap...
FPRX, INCY, MGNX, OMED, XLRN
Hier eine interessante Folie von Roche zu PD1-Kombis in Abhängigkeit von bestimmten Tumor-Eigenschaften.
Speziell werden hier CSF1R, IDO, Angiogenese und CD3-biAKs genannt. Bei IDO ist wohl INCY führend, bei CSF1R ist FPRX vorne mit dabei, bei den CD3-biAKs ist meiner Meinung nach MGNX führend und neben den Standard VEGFRs könnten die Angiogenese-Hemmer DLL4 (mono und +VEGF-biAK) von OMED und ALK1 von XLRN interessant sein.
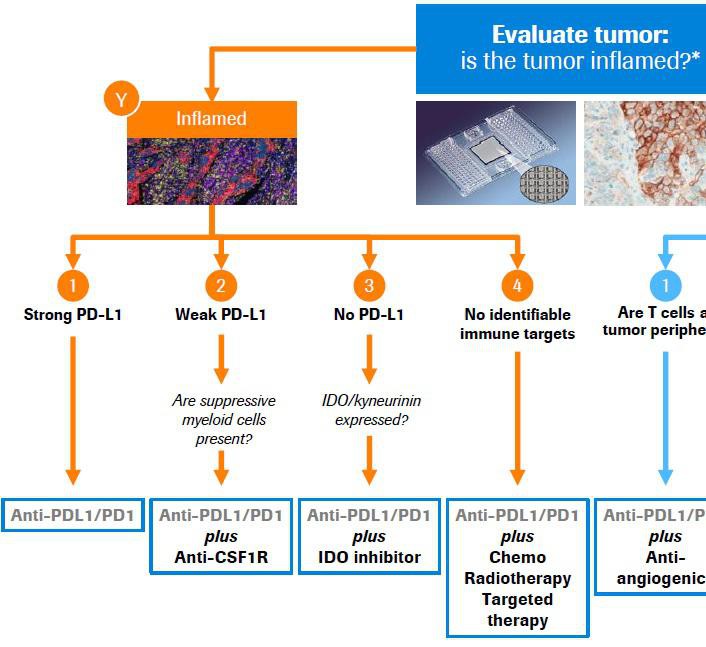
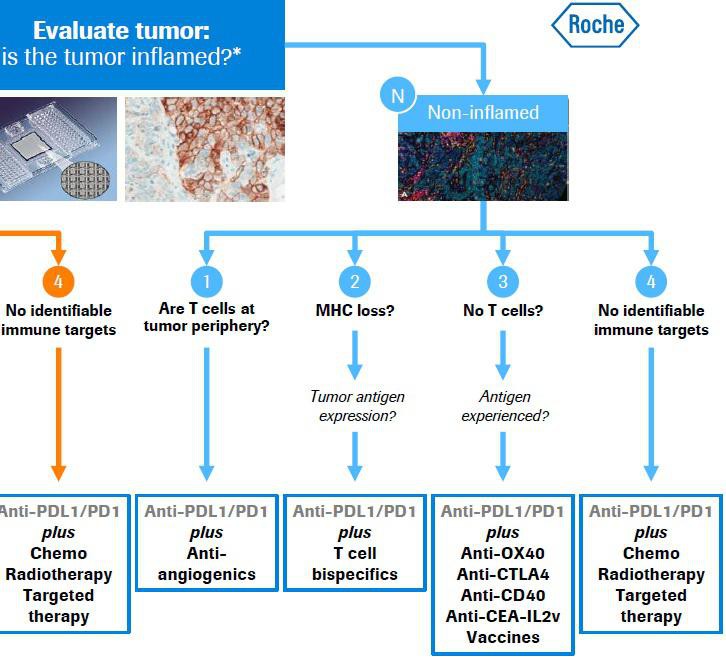
Gruß
ipollit
Hier eine interessante Folie von Roche zu PD1-Kombis in Abhängigkeit von bestimmten Tumor-Eigenschaften.
Speziell werden hier CSF1R, IDO, Angiogenese und CD3-biAKs genannt. Bei IDO ist wohl INCY führend, bei CSF1R ist FPRX vorne mit dabei, bei den CD3-biAKs ist meiner Meinung nach MGNX führend und neben den Standard VEGFRs könnten die Angiogenese-Hemmer DLL4 (mono und +VEGF-biAK) von OMED und ALK1 von XLRN interessant sein.


Gruß
ipollit
ZSPH, RLYP
Vor einigen Wochen wurde bekannt, dass die schweizerische Actelion Interesse hätte ZSPH für 2,5 Mrd USD zu übernehmen. Offensichtlich gab es noch andere Interesssenten... nun geht ZSPH für 2,7 Mrd USD an AZN!
Sowohl ZSPH als auch der Konkurrent RLYP haben nur ein Produkt kurz vor oder nach der Zulassung... einen Kalium-Binder, der Kalium dem Blut entziehen soll, da hohe Kalium-Werte (Hyperkaliämie) schnell zu schweren und tödlichen Herzrhythmus-Störungen führen kann. Hohe Kalium-Werte können u.a. infolge von Nieren-Problemen (CKD) auftreten oder aufgrund von Nieren- oder Herzmedikamenten RAASI.

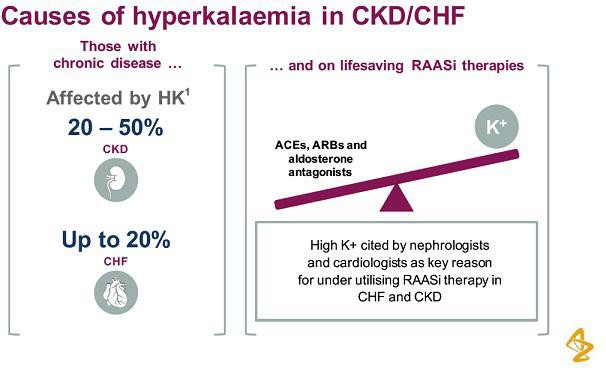
RLYPs Veltassa wurde vor Kurzem von der FDA in den USA zugelassen, die US-Zulassung von ZSPHs ZS-9 steht Ende Mai nächsten Jahres an. Trotz Zulassung ist RLYPs Kurs eingebrochen, wahrscheinlich weil Veltassa eine Black-Box Warnung erhalten hat, dass es nicht nur Kalium sondern auch einige Medikamente bindet, so dass es nur im Abstand von 6 Stunden zu anderen Medikamenten eingenommen werden darf (Veltassa und ZS-9 sind Pulver, die in Flüssigkeit aufgelösst eingenommen werden müssen).
Interessant ist nun der große Bewertungs-Unterschied zwischen RLYP mit einer MK von 787 Mio USD und ZSPH mit 2,7 Mrd USD. RLYP erhält in Europa Royalties von einem Fresenius-Unternehmen, das führend bei Herz- und Nierenmedikamenten ist. In den USA hält RLYP die vollen Rechte und wird von Sanofi bei der Vermarktung unterstützt.
ZS-9 wirkt schneller als Veltassa. Dafür hat es meiner Meinung nach einen größeren Nachteil bei chronischer Anwendung (und die dürfte den größten Teil des zukünftigen Marktes bilden). ZS-9 ist ein Salz, dass mit relativ viel Wasser eingenommen werden muss und zu Schwellungen führen kann. Die Zielgruppe der Nieren- und Herzpatienten hat aber so schon Probleme mit Schwellungen, die sich an Organen bilden können und so z.B eine Herzschwäche noch verstärken. Zudem versucht man die Salz- und Wasserzufuhr zu reduzieren.

Es gibt sogar Hinweise, dass die Bindung von Veltassa, das selbst kein Salz ist, dem Körper weiteres Salz entzieht und somit z.B. den Blutdruck senken kann. Dies wäre ein positiver Effekt, der über die gewünschte Kalium-Reduktion hinausgeht.

Vielleicht könnte Veltassa den chronischen Markt dominieren. RLYP wäre dann massiv unterbewertet.
Heute kamen weitere Daten zu ZS-9, die auf die Probleme mit Schwellungen und die Erhöhung de Blutdrucks hinweisen und somit die Position von Veltassa weiter verbessern.


Gruß
ipollit
Vor einigen Wochen wurde bekannt, dass die schweizerische Actelion Interesse hätte ZSPH für 2,5 Mrd USD zu übernehmen. Offensichtlich gab es noch andere Interesssenten... nun geht ZSPH für 2,7 Mrd USD an AZN!

Sowohl ZSPH als auch der Konkurrent RLYP haben nur ein Produkt kurz vor oder nach der Zulassung... einen Kalium-Binder, der Kalium dem Blut entziehen soll, da hohe Kalium-Werte (Hyperkaliämie) schnell zu schweren und tödlichen Herzrhythmus-Störungen führen kann. Hohe Kalium-Werte können u.a. infolge von Nieren-Problemen (CKD) auftreten oder aufgrund von Nieren- oder Herzmedikamenten RAASI.



RLYPs Veltassa wurde vor Kurzem von der FDA in den USA zugelassen, die US-Zulassung von ZSPHs ZS-9 steht Ende Mai nächsten Jahres an. Trotz Zulassung ist RLYPs Kurs eingebrochen, wahrscheinlich weil Veltassa eine Black-Box Warnung erhalten hat, dass es nicht nur Kalium sondern auch einige Medikamente bindet, so dass es nur im Abstand von 6 Stunden zu anderen Medikamenten eingenommen werden darf (Veltassa und ZS-9 sind Pulver, die in Flüssigkeit aufgelösst eingenommen werden müssen).
Interessant ist nun der große Bewertungs-Unterschied zwischen RLYP mit einer MK von 787 Mio USD und ZSPH mit 2,7 Mrd USD. RLYP erhält in Europa Royalties von einem Fresenius-Unternehmen, das führend bei Herz- und Nierenmedikamenten ist. In den USA hält RLYP die vollen Rechte und wird von Sanofi bei der Vermarktung unterstützt.
ZS-9 wirkt schneller als Veltassa. Dafür hat es meiner Meinung nach einen größeren Nachteil bei chronischer Anwendung (und die dürfte den größten Teil des zukünftigen Marktes bilden). ZS-9 ist ein Salz, dass mit relativ viel Wasser eingenommen werden muss und zu Schwellungen führen kann. Die Zielgruppe der Nieren- und Herzpatienten hat aber so schon Probleme mit Schwellungen, die sich an Organen bilden können und so z.B eine Herzschwäche noch verstärken. Zudem versucht man die Salz- und Wasserzufuhr zu reduzieren.

Es gibt sogar Hinweise, dass die Bindung von Veltassa, das selbst kein Salz ist, dem Körper weiteres Salz entzieht und somit z.B. den Blutdruck senken kann. Dies wäre ein positiver Effekt, der über die gewünschte Kalium-Reduktion hinausgeht.

Vielleicht könnte Veltassa den chronischen Markt dominieren. RLYP wäre dann massiv unterbewertet.
Heute kamen weitere Daten zu ZS-9, die auf die Probleme mit Schwellungen und die Erhöhung de Blutdrucks hinweisen und somit die Position von Veltassa weiter verbessern.
Gruß
ipollit
Momentan sieht es so in meinem Depot aus... ZSPH verkauft, dafür nun bei NVAX dabei und CEMP erhöht. KPTI werde ich zukaufen. HALO und ADRO beobachte ich.
7,8% INCY
7,8% CLVS
6,2% EXEL
5,2% ACAD
4,7% MGNX
4,1% IPH.PA
4,1% FPRX
3,7% ISIS
3,7% XLRN
3,4% MDVN
3,3% TSRO
3,2% REGN
3,2% GEN.CO
3,0% CLDX
2,9% ARRY
2,9% FGEN
2,9% ALNY
2,9% RLYP
2,8% CEMP
2,6% KPTI
2,4% SAGE
2,3% ARQL
2,2% OMED
1,8% PTLA
1,7% NVAX
1,5% INFI
1,3% EPZM
1,3% ESPR
1,1% SGEN
1,1% AKBA
0,9% IMMU
0,8% AUPH
0,5% XENE
0,5% STML
0,3% MRNS
Gruß
ipollit
7,8% INCY
7,8% CLVS
6,2% EXEL
5,2% ACAD
4,7% MGNX
4,1% IPH.PA
4,1% FPRX
3,7% ISIS
3,7% XLRN
3,4% MDVN
3,3% TSRO
3,2% REGN
3,2% GEN.CO
3,0% CLDX
2,9% ARRY
2,9% FGEN
2,9% ALNY
2,9% RLYP
2,8% CEMP
2,6% KPTI
2,4% SAGE
2,3% ARQL
2,2% OMED
1,8% PTLA
1,7% NVAX
1,5% INFI
1,3% EPZM
1,3% ESPR
1,1% SGEN
1,1% AKBA
0,9% IMMU
0,8% AUPH
0,5% XENE
0,5% STML
0,3% MRNS
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.033.126 von ipollit am 08.11.15 01:49:14RLYP
noch ein Kommentar zu den neuen Daten vom Wochenende... darin auch, dass der blutdrucksenkende Effekt von Veltassa durchaus relevant sein kann, zumal der Blutdruck für CKD- und HF-Patienten besonders bedeutsam ist

Gruß
ipollit
noch ein Kommentar zu den neuen Daten vom Wochenende... darin auch, dass der blutdrucksenkende Effekt von Veltassa durchaus relevant sein kann, zumal der Blutdruck für CKD- und HF-Patienten besonders bedeutsam ist

Gruß
ipollit
OACT
huii... und wieder hat es einen erwischt. Astellas kauft OCAT zu 8,5 USD... letzter Kurs waren 4,46 USD. Im Kursverlauf war bis dahin nichts von einer Ünernahme zu sehen. OCAT ist auch eine Position von Ohad Hammer, ich war bisher leider nicht dabei. Schade, technologisch fand ich OCAT (Stammzell-Therapien) interessant, hoffentlich bringt Astellas die Sache gut voran.

Gruß
ipollit
huii... und wieder hat es einen erwischt. Astellas kauft OCAT zu 8,5 USD... letzter Kurs waren 4,46 USD. Im Kursverlauf war bis dahin nichts von einer Ünernahme zu sehen. OCAT ist auch eine Position von Ohad Hammer, ich war bisher leider nicht dabei. Schade, technologisch fand ich OCAT (Stammzell-Therapien) interessant, hoffentlich bringt Astellas die Sache gut voran.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.048.234 von ipollit am 10.11.15 08:40:00$OCAT
War leider auch nicht dabei - aber da sieht man mal wieder wie schnell es gehen kann. Die Japaner sind wohl verrückt nach Cell Therapy.
Ipollit, findest du CLVS mittlerweile angemessen bewertet oder besser gesagt: wieviel Spielraum nach oben siehst du noch? Habe immer noch keine Position, da mir $100 nicht mehr billig erscheinen.
Im Übrigen habe ich eine Position in STML eröffnet, bin gespannt wie sich der Chart bis/nach ASH im Dezember entwickeln wird.
Viele Grüße
War leider auch nicht dabei - aber da sieht man mal wieder wie schnell es gehen kann. Die Japaner sind wohl verrückt nach Cell Therapy.
Ipollit, findest du CLVS mittlerweile angemessen bewertet oder besser gesagt: wieviel Spielraum nach oben siehst du noch? Habe immer noch keine Position, da mir $100 nicht mehr billig erscheinen.
Im Übrigen habe ich eine Position in STML eröffnet, bin gespannt wie sich der Chart bis/nach ASH im Dezember entwickeln wird.
Viele Grüße
Angeblich ist AMGN auf der Suche nach einem größeren Biotech-Übernahmekandiat im Bereich von 10 Mrd USD. GILD und BIIB haben vor einiger Zeit ihrerseits auch größere Geldbeträge aufgenommen, die für Übernahmen zur Verfügung stehen. Wahrscheinlich werden wir also neben OCAT noch weitere Übernahmen sehen.

Gruß
ipollit

Gruß
ipollit
Antwort auf Beitrag Nr.: 51.048.234 von ipollit am 10.11.15 08:40:00Da hatte ich eine Limit- Order laufen schade das sie nicht bedient wurde 
Neu habe ich seit paar Tagen
http://www.bellicum.com/
und
http://www.affimed.com/index.php

Neu habe ich seit paar Tagen
http://www.bellicum.com/
und
http://www.affimed.com/index.php
Ich war mit einer kleinen Position bei OCAT dabei. Auf eine Übernahme hatte ich gar nicht spekuliert. Aber das nehme ich natürlich gerne mit! Langfristig könnten sich die 400 Mio durchaus rentieren. Ich hätte hier gerne einen CVR bei Zulassung eines Prduktes gehabt. 
Ansonsten habe ich mein Depot diversiviziert, weil es m.E. einige gute "derisked" Werte gibt. Habe mir deshalb ACAD und auch EXEL gekauft, ESPR vergrößert. Zudem bei ZFGN den Einstiegspreis verringert.
SG kmastra

Ansonsten habe ich mein Depot diversiviziert, weil es m.E. einige gute "derisked" Werte gibt. Habe mir deshalb ACAD und auch EXEL gekauft, ESPR vergrößert. Zudem bei ZFGN den Einstiegspreis verringert.
SG kmastra
Antwort auf Beitrag Nr.: 51.063.225 von kmastra am 11.11.15 15:24:57Wie lautet denn deine Meinung zu ACAD? Wieviel Spielraum nach oben?
Grüße
Grüße
Antwort auf Beitrag Nr.: 51.062.412 von schnappi am 11.11.15 14:12:10Hi Schnappi,
kannst du etwas dazu sagen, warum du Affimed jetzt gekauft hast?
kannst du etwas dazu sagen, warum du Affimed jetzt gekauft hast?
Antwort auf Beitrag Nr.: 51.063.285 von biopadawan am 11.11.15 15:31:30Hallo biopadawan,
also meine Überlegungen enden eigentlich nie mit einem konkreten Kursziel. Aber natürlich finde ich ACAD gut. Ich habe jetzt (wieder) gekauft, weil die Zulassung für Pimavanserin bei Parkinson Psychose eingereicht und akzeptiert wurde (da gab es vorher ja Probleme).
Pimavanserin hat Blockbusterpotenzial in der ersten Indikation (hat hier auch die BTD der FDA). Zudem gibt es eine realistische Chance auf eine deutliche Labelerweiterung - und auch den Einsatz "off label"(Alzheimer Psychose und Psychose).
http://www.medscapemedizin.de/artikel/4901630
Insgesamt ist ACAD auch ein heiß gehandelter Übernahmekandidat. Auf der anderen Seite gibt es mehr oder weniger nur das eine Mittel und ACAD ist damit sehr riskant.
SG kmastra
also meine Überlegungen enden eigentlich nie mit einem konkreten Kursziel. Aber natürlich finde ich ACAD gut. Ich habe jetzt (wieder) gekauft, weil die Zulassung für Pimavanserin bei Parkinson Psychose eingereicht und akzeptiert wurde (da gab es vorher ja Probleme).
Pimavanserin hat Blockbusterpotenzial in der ersten Indikation (hat hier auch die BTD der FDA). Zudem gibt es eine realistische Chance auf eine deutliche Labelerweiterung - und auch den Einsatz "off label"(Alzheimer Psychose und Psychose).
http://www.medscapemedizin.de/artikel/4901630
Insgesamt ist ACAD auch ein heiß gehandelter Übernahmekandidat. Auf der anderen Seite gibt es mehr oder weniger nur das eine Mittel und ACAD ist damit sehr riskant.
SG kmastra
Antwort auf Beitrag Nr.: 51.063.291 von question-mark am 11.11.15 15:31:49Hatte die schon etwas länger beobachtet und fand den Kurs nun Okay.
Medizinische Angaben dazu überlass ich denen die sich damit auskennen.
Medizinische Angaben dazu überlass ich denen die sich damit auskennen.
CLVS
die Konkurrenz ist einen Schritt schneller gewesen... AZNs AZD9291/osimertinib bekommt als Tagrisso heute die FDA-Zulassung weit vor dem eigentlich PDFUA-Tag.
Weiß jemand, wann AZN AZD9291 beantragt oder wann die FDA AZD9291 Priority Review gegeben hat? Am 4.9. spricht AZN von "recently" bezüglich PR von der FDA. Wenn die FDA den Antrag mit Priority Review akzeptiert, ist der PDFUA meist ca. 6 Monate später. Falls PR Anfang September war, so hat die Entscheidung nichtmal 3 Monate gedauert... extrem schnell.
Roci hat am 29.9. PR erhalten... PDUFA ist der 30.03.2016. Wie AZD9291 hat Roci BTD, PD und FT. Zudem war es ein rolling BLA. Wenn die FDA beide Mittel gleich behandelt, so müsste die Zulassungsentscheidung für Roci noch im Dezember kommen... vielleicht in 4 Wochen.
Gruß
ipollit
die Konkurrenz ist einen Schritt schneller gewesen... AZNs AZD9291/osimertinib bekommt als Tagrisso heute die FDA-Zulassung weit vor dem eigentlich PDFUA-Tag.
Weiß jemand, wann AZN AZD9291 beantragt oder wann die FDA AZD9291 Priority Review gegeben hat? Am 4.9. spricht AZN von "recently" bezüglich PR von der FDA. Wenn die FDA den Antrag mit Priority Review akzeptiert, ist der PDFUA meist ca. 6 Monate später. Falls PR Anfang September war, so hat die Entscheidung nichtmal 3 Monate gedauert... extrem schnell.
Roci hat am 29.9. PR erhalten... PDUFA ist der 30.03.2016. Wie AZD9291 hat Roci BTD, PD und FT. Zudem war es ein rolling BLA. Wenn die FDA beide Mittel gleich behandelt, so müsste die Zulassungsentscheidung für Roci noch im Dezember kommen... vielleicht in 4 Wochen.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.086.223 von ipollit am 13.11.15 21:39:41Hallo ipollit,
da könntest du Recht haben.
Andy Biotech schrieb vorhin:
$AZN -- FDA approves Tagrisso (aka AZD9291) ~3mo before PDUFA http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/uc… … $CLVS CO-1686 up next, PDUFA 3/30/16
Das war wirklich schnell. Ich denke jetzt wird zurecht erwartet, dass auch Ruca vergleichbar schnell zugelassen wird. Tick Tack...
Gespannt warte ich bei CLVS auf die PII Ergebnisse von Lucatinib, die ja für das SABCS Anfang Dezember erwartet werden...
SG kmastra
da könntest du Recht haben.
Andy Biotech schrieb vorhin:
$AZN -- FDA approves Tagrisso (aka AZD9291) ~3mo before PDUFA http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/uc… … $CLVS CO-1686 up next, PDUFA 3/30/16
Das war wirklich schnell. Ich denke jetzt wird zurecht erwartet, dass auch Ruca vergleichbar schnell zugelassen wird. Tick Tack...
Gespannt warte ich bei CLVS auf die PII Ergebnisse von Lucatinib, die ja für das SABCS Anfang Dezember erwartet werden...
SG kmastra
Antwort auf Beitrag Nr.: 51.086.853 von kmastra am 13.11.15 23:23:34CLVS: Mit der schnellen Zulassung wird es nichts 
http://finance.yahoo.com/news/clovis-oncology-announces-regu…
Schlimmer noch - es gibt auch ein "Update" zur Wirksamkeit!
As the efficacy data have matured, the number of patients with an unconfirmed response who converted to a confirmed response was lower than expected.
Oje!

http://finance.yahoo.com/news/clovis-oncology-announces-regu…
Schlimmer noch - es gibt auch ein "Update" zur Wirksamkeit!
As the efficacy data have matured, the number of patients with an unconfirmed response who converted to a confirmed response was lower than expected.
Oje!
Antwort auf Beitrag Nr.: 51.099.909 von kmastra am 16.11.15 14:15:20Roci steht jetzt weitaus schlechter da als AZD9291:
28% ORR bei 500mg sieht im Vergleich jetzt ziemlich schwach aus.
AZD9291:

Wirklich übel! Aktie verliert vorbörslich über 60%!
28% ORR bei 500mg sieht im Vergleich jetzt ziemlich schwach aus.
AZD9291:

Wirklich übel! Aktie verliert vorbörslich über 60%!
ist der Abschlag gerechtfertigt? Oder vorbörsliche Hysterie?
Wahnsinn. Musste zweimal hinsehen: vorbörslich - 70%
Ob das gerechtfertigt ist, bleibt fraglich. M.E. auf jeden Fall ordentlich Hysterie dabei.
Ob das gerechtfertigt ist, bleibt fraglich. M.E. auf jeden Fall ordentlich Hysterie dabei.
sieht nicht nach schneller Erholung aus bei Clovis, Mist.
aber das ist Biotech ...
aber das ist Biotech ...
Antwort auf Beitrag Nr.: 51.101.265 von question-mark am 16.11.15 16:33:12Abstufung ist doch arg übertrieben, oder? Wieviele Produkte in P1, P2 und P3-Phase hat CLVS denn?
arry MEK BRAF Deal Europa
Arry macht Europa-Deal mit .... Pierre Fabremeine erste Reaktion war ungläubiges Entsetzen - offenbar sieht es der Markt auch so. Man musste schon lange suchen, um ein Europa-Unternehmen zu finden, das ich bisher gar nicht bemerkt habe. Das muss bedeuten, dass ALLE Großen abgewunken haben müssen. Jetzt ist die weitere Entwicklung und Kommerzialisierung fraglich, holprig und teuer. Eine schnelle Übernahme dürfte auch vom Tisch sein. Wenn das jemand verfolgt hätte, hätte er versucht, einen Fuß in die Tür zu bekommen. Fraglich auch, ob das den europäischen Wettbewerbshütern überhaupt reicht.
Wenn jetzt NEMO scheitert, gibt es ein Desaster. Wo sind die Dealmaker um Snitman hin?
Meinungen dazu?
VG
A
Array BioPharma And Pierre Fabre Announce Development And Commercialization Collaboration For Two Novel Oncology Products, Binimetinib And Encorafenib
- Array to receive a $30 million up-front payment and up to $425 million in additional development and commercialization milestones, as well as robust double-digit royalties on future sales -
- Array retains full commercialization rights to binimetinib and encorafenib in United States, Canada, Japan and Korea -
-NEMO Phase 3 trial remains on-track for top-line results by end of 2015 -
- Array to host conference call November 16, 2015 at 9:00 am Eastern Time -
BOULDER, Colo., Nov. 16, 2015 /PRNewswire/ -- Array BioPharma Inc. (Nasdaq: ARRY) and Pierre Fabre today announced a collaboration to globally develop and commercialize Array's late-stage novel oncology products, binimetinib and encorafenib. Binimetinib, a MEK inhibitor, and encorafenib, a BRAF inhibitor, are currently advancing in three, global Phase 3 trials for melanoma and ovarian cancer. Top-line results from NEMO, a Phase 3 study of binimetinib in patients with NRAS-mutant melanoma, are anticipated before the end of 2015. Array plans to host a conference call on November 16, 2015 at 9:00 am ET to discuss the collaboration.
Under the terms of the agreement, Array will receive an upfront payment of $30 million and retains exclusive commercialization rights for binimetinib and encorafenib in the United States, Canada, Japan, Korea and Israel. Pierre Fabre will have exclusive rights to commercialize both products in all other countries, including Europe, Asia and Latin America. Array is entitled to receive up to $425 million if certain development and commercialization milestones are achieved, and is eligible for robust, tiered double-digit royalties. Array and Pierre Fabre have agreed to split future development costs on a 60:40 basis (Array:Pierre Fabre) with initial funding committed for new clinical trials in colorectal cancer and melanoma. All ongoing binimetinib and encorafenib clinical trials remain substantially funded through completion by Novartis.
Pierre Fabre Oncology, a business unit of the global 10,000-employee Pierre Fabre company, is supported by over 1,000 employees with a strong focus on European markets. In 2014, worldwide annual sales of Pierre Fabre Oncology products surpassed $200 million on the strength of the Oral Navelbine, Javlor and Busilvex brands. In addition, Pierre Fabre has a significant commitment and track record in pharmaceutical R&D, developing products for patients afflicted with lung, breast and other solid tumors and hematological cancers.
"In Pierre Fabre we selected a partner with a European and emerging market focus in oncology to develop and commercialize binimetinib and encorafenib in these geographies," said Ron Squarer, Chief Executive Officer, Array BioPharma. "With Phase 3 trials approaching data readouts, and over 30 additional Phase 1/2 trials underway, we are confident that binimetinib and encorafenib are well positioned for near-term regulatory submissions and significant commercial value."
"Pierre Fabre is strongly committed to develop and commercialize oncology products," said Frederic Duchesne, Chief Executive Officer, Pierre Fabre Pharmaceuticals. "This partnership with Array is aligned with our growth strategy in Pharmaceuticals, our geographic footprint, and our corporate mission to bring to the market novel oncology products which address unmet patient needs. Binimetinib and encorafenib will fit perfectly with our broad expertise in oncology and dermatology, and will strengthen our current portfolio and international presence."
The agreement remains subject to European Commission on Competition review and approval.
und wie toll was CLVS noch vor kurzem und welche Überlegenheit gegenüber AZN. Tja, da nützt eben das ganze Wissen nichts.
Antwort auf Beitrag Nr.: 51.101.964 von Axel_Olsson am 16.11.15 17:36:02@arry
Ich bin enttäuscht, sehr enttäuscht sogar! Die Franzosen drehen bisher gerade mal 200Mio. in Oncology. Da ist überhaupt keine SalesForce vorhanden. Und ich befürchte, daß die gar nicht die finanziellen Möglichkeiten haben, in die Erweiterung der SalesForce zu investieren. Es darf nicht vergessen werden, daß die Konkurrenten keine geringeren sind als Novartis und Roche. Man muß davon ausgehen, daß Arry an die Wand gedrückt wird.So gut können die Daten gar nicht sein, als daß der Marktmachtnachteil ausgeglichen werden könnte.
Axel_Olsson stellt völlig zurecht die Frage, warum scheinbar alle Großen abgewunken haben. Da bin ich ehrlich gesagt schon fast geschockt, wie falsch ich da gelegen habe. Für mich enttäuschend. Und weiter: das haben einige schon vorher gewußt, sonst wäre der Kurs in den letzten zwei Handelstagen nicht plötzlich nach unten gegangen...ich höre mir gleich mal den CC an.
Bei CLVS bin ich übrigens auch dabei, so daß es für mich ein rabenschwarzer Börsentag ist. Echt traurig, das Ganze.
Ich bin enttäuscht, sehr enttäuscht sogar! Die Franzosen drehen bisher gerade mal 200Mio. in Oncology. Da ist überhaupt keine SalesForce vorhanden. Und ich befürchte, daß die gar nicht die finanziellen Möglichkeiten haben, in die Erweiterung der SalesForce zu investieren. Es darf nicht vergessen werden, daß die Konkurrenten keine geringeren sind als Novartis und Roche. Man muß davon ausgehen, daß Arry an die Wand gedrückt wird.So gut können die Daten gar nicht sein, als daß der Marktmachtnachteil ausgeglichen werden könnte.
Axel_Olsson stellt völlig zurecht die Frage, warum scheinbar alle Großen abgewunken haben. Da bin ich ehrlich gesagt schon fast geschockt, wie falsch ich da gelegen habe. Für mich enttäuschend. Und weiter: das haben einige schon vorher gewußt, sonst wäre der Kurs in den letzten zwei Handelstagen nicht plötzlich nach unten gegangen...ich höre mir gleich mal den CC an.
Bei CLVS bin ich übrigens auch dabei, so daß es für mich ein rabenschwarzer Börsentag ist. Echt traurig, das Ganze.
CLVS
puh, CLVS war meine zweitgrößte Positon... mit soetwas habe ich nicht gerechnet. Wie sich hier ein weiteres Mal zeigt, ist nichts sicher, auch wenn es noch so gut aussieht.
Auf dem Papier sieht AZNs Tagrisso natürlich jetzt besser aus, dazu kommt noch ein klarer zeitlicher Vorsprung. Leider gab es nie eine Debatte, inwiefern der große Anteil asiatischer Patienten, die Ergebnisse von Tagrisso positiv beeinflusst hat. Ich kann mich auch an mehrere Zulassungsanträge erinnern, bei denen die FDA es kritisiert hat, dass die Patienten nicht aussagekräftig für Amerika wären. Hier hätte man auch mal darüber diskutieren können. Mit mehr asiatischen Patienten sähen die Ergebnisse von CLVS wahrscheinlich auch deutlich besser aus.
Sollte Roci nicht sowohl bei T790M+ als auch bei T790M- angewendet werden können?... 2nd-line müsste ca. 50:50 sein, d.h. auch T790M- ist ein relevanter Markt. Tagrisso soll bei T790M- nur wenig Wirkung haben... ist das für Roci nun auch nicht mehr relevant? Ich würde es zudem für einen großen Vorteil halten, wenn Roci mit PD1 kombiniert werden kann... Tagrisso hatte zuletzt auch hier Probleme.
T790M+ ist aber der wesentliche Markt, auf den die Zulassung abzielt... hier sieht Roci nun nicht mehr so gut aus, obwohl ich im direkten Vergleich es auch für nicht unwahrscheinlich halten würde, dass beide Mittel ähnlich sind.
Beim PARP-Hemmer Ruca sah es zuletzt eher besser aus. Wenn ich es richtig verstanden habe, könnte Ruca TSROs Niraparib zeitlich noch überholen, nachdem es bei letzterem Verzögerungen gibt.
Das ganze ist aber schon ziemlich bitter!

Grüße
ipollit
puh, CLVS war meine zweitgrößte Positon... mit soetwas habe ich nicht gerechnet. Wie sich hier ein weiteres Mal zeigt, ist nichts sicher, auch wenn es noch so gut aussieht.
Auf dem Papier sieht AZNs Tagrisso natürlich jetzt besser aus, dazu kommt noch ein klarer zeitlicher Vorsprung. Leider gab es nie eine Debatte, inwiefern der große Anteil asiatischer Patienten, die Ergebnisse von Tagrisso positiv beeinflusst hat. Ich kann mich auch an mehrere Zulassungsanträge erinnern, bei denen die FDA es kritisiert hat, dass die Patienten nicht aussagekräftig für Amerika wären. Hier hätte man auch mal darüber diskutieren können. Mit mehr asiatischen Patienten sähen die Ergebnisse von CLVS wahrscheinlich auch deutlich besser aus.
Sollte Roci nicht sowohl bei T790M+ als auch bei T790M- angewendet werden können?... 2nd-line müsste ca. 50:50 sein, d.h. auch T790M- ist ein relevanter Markt. Tagrisso soll bei T790M- nur wenig Wirkung haben... ist das für Roci nun auch nicht mehr relevant? Ich würde es zudem für einen großen Vorteil halten, wenn Roci mit PD1 kombiniert werden kann... Tagrisso hatte zuletzt auch hier Probleme.
T790M+ ist aber der wesentliche Markt, auf den die Zulassung abzielt... hier sieht Roci nun nicht mehr so gut aus, obwohl ich im direkten Vergleich es auch für nicht unwahrscheinlich halten würde, dass beide Mittel ähnlich sind.
Beim PARP-Hemmer Ruca sah es zuletzt eher besser aus. Wenn ich es richtig verstanden habe, könnte Ruca TSROs Niraparib zeitlich noch überholen, nachdem es bei letzterem Verzögerungen gibt.
Das ganze ist aber schon ziemlich bitter!
Grüße
ipollit
Genmab
besser sieht es mit Genmab aus... ein guter Partner wie J&J ist sicherlich vorteilhaft.
Daratumumab wurde von der FDA als Darzalex zugelassen... fast 4 Monate vor dem PDFUA-Tag am 9.3. nächsten Jahres.
Genmab hat aktuell eine MK von 6,4 Mrd USD... ganz schön teuer wie ich finde. Trotzdem steigt und steigt der Kurs.

Gruß
ipollit
besser sieht es mit Genmab aus... ein guter Partner wie J&J ist sicherlich vorteilhaft.
Daratumumab wurde von der FDA als Darzalex zugelassen... fast 4 Monate vor dem PDFUA-Tag am 9.3. nächsten Jahres.
Genmab hat aktuell eine MK von 6,4 Mrd USD... ganz schön teuer wie ich finde. Trotzdem steigt und steigt der Kurs.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.102.573 von riverstar_de am 16.11.15 18:34:00
Da nützt das Wissen nichts, wenn sich die Hälfte der Ansprechrate als Luftnummer erweist. Das finde ich fast schon Betrug! Wann wollte man bei CLVS denn die eigenen Aktionäre darüber informieren? Oder hat man geglaubt, die FDA gibt sich mit Wischiwaschi Daten zufrieden und niemand merkt das?
Mal sehen wie das jetzt mit der FDA weiter geht. Ich würde nicht ausschließen, dass die BTD verloren geht (weil es jetzt ja auch keinen so großen ungedeckten Bedarf mehr gibt und auch die Effektivität schlechter ist) und sich insgesamt die Zulassung hinzieht.
Bei Roci ist die Lage jetzt derart unübersichtlich, dass im Grunde nur ein Direktvergleich mit AZD9291 für Klarheit sorgen kann. Ist der Unterschied noch durch die schwerer zu behandelnden Patienten (mehr mit CNS Metastasen) und die Region der Studien (weniger Asiaten) erklärbar?
Natürlich strahlen die Ereignisse um Roci auch irgendwie (ob berechtigt oder nicht) auf Ruca ab. Wie glaubhaft sind denn da die Ergebnisse? Ist ein Filing im nächsten Jahr wirklich realistisch?
Einzig die (potenziell guten) Ergebnisse von Lucitanib geben mir momentan Hoffnung. Die Kursreaktion finde ich aber schon sehr heftig. Auspreisen kann man Roci sicherlich nicht...
ARRY
Ergänzend: ARRY bekommt 20-35% Royalties. Aber ich teile die Einschätzung, dass der Partner eine Enttäuschung ist, zumal jetzt eine Übernahme unwahrscheinlich ist. Die NEMO Ergebnisse sind wohl nicht ganz so wichtig, weil das Marktpotenzial hier nicht so groß ist.
SG kmastra
Zitat von riverstar_de: und wie toll was CLVS noch vor kurzem und welche Überlegenheit gegenüber AZN. Tja, da nützt eben das ganze Wissen nichts.
Da nützt das Wissen nichts, wenn sich die Hälfte der Ansprechrate als Luftnummer erweist. Das finde ich fast schon Betrug! Wann wollte man bei CLVS denn die eigenen Aktionäre darüber informieren? Oder hat man geglaubt, die FDA gibt sich mit Wischiwaschi Daten zufrieden und niemand merkt das?
Mal sehen wie das jetzt mit der FDA weiter geht. Ich würde nicht ausschließen, dass die BTD verloren geht (weil es jetzt ja auch keinen so großen ungedeckten Bedarf mehr gibt und auch die Effektivität schlechter ist) und sich insgesamt die Zulassung hinzieht.
Bei Roci ist die Lage jetzt derart unübersichtlich, dass im Grunde nur ein Direktvergleich mit AZD9291 für Klarheit sorgen kann. Ist der Unterschied noch durch die schwerer zu behandelnden Patienten (mehr mit CNS Metastasen) und die Region der Studien (weniger Asiaten) erklärbar?
Natürlich strahlen die Ereignisse um Roci auch irgendwie (ob berechtigt oder nicht) auf Ruca ab. Wie glaubhaft sind denn da die Ergebnisse? Ist ein Filing im nächsten Jahr wirklich realistisch?
Einzig die (potenziell guten) Ergebnisse von Lucitanib geben mir momentan Hoffnung. Die Kursreaktion finde ich aber schon sehr heftig. Auspreisen kann man Roci sicherlich nicht...
ARRY
Ergänzend: ARRY bekommt 20-35% Royalties. Aber ich teile die Einschätzung, dass der Partner eine Enttäuschung ist, zumal jetzt eine Übernahme unwahrscheinlich ist. Die NEMO Ergebnisse sind wohl nicht ganz so wichtig, weil das Marktpotenzial hier nicht so groß ist.
SG kmastra
Antwort auf Beitrag Nr.: 51.104.541 von kmastra am 16.11.15 23:02:22
Wenn ich nicht falsch liege, dann gab es ziemlich voeleinsiderverkäufe in der letzten zeit - es ist halt wie immer, auf die zeichen hören
Zitat von kmastra:Zitat von riverstar_de: und wie toll was CLVS noch vor kurzem und welche Überlegenheit gegenüber AZN. Tja, da nützt eben das ganze Wissen nichts.
Da nützt das Wissen nichts, wenn sich die Hälfte der Ansprechrate als Luftnummer erweist. Das finde ich fast schon Betrug! Wann wollte man bei CLVS denn die eigenen Aktionäre darüber informieren? Oder hat man geglaubt, die FDA gibt sich mit Wischiwaschi Daten zufrieden und niemand merkt das?
Mal sehen wie das jetzt mit der FDA weiter geht. Ich würde nicht ausschließen, dass die BTD verloren geht (weil es jetzt ja auch keinen so großen ungedeckten Bedarf mehr gibt und auch die Effektivität schlechter ist) und sich insgesamt die Zulassung hinzieht.
Bei Roci ist die Lage jetzt derart unübersichtlich, dass im Grunde nur ein Direktvergleich mit AZD9291 für Klarheit sorgen kann. Ist der Unterschied noch durch die schwerer zu behandelnden Patienten (mehr mit CNS Metastasen) und die Region der Studien (weniger Asiaten) erklärbar?
Natürlich strahlen die Ereignisse um Roci auch irgendwie (ob berechtigt oder nicht) auf Ruca ab. Wie glaubhaft sind denn da die Ergebnisse? Ist ein Filing im nächsten Jahr wirklich realistisch?
Einzig die (potenziell guten) Ergebnisse von Lucitanib geben mir momentan Hoffnung. Die Kursreaktion finde ich aber schon sehr heftig. Auspreisen kann man Roci sicherlich nicht...
ARRY
Ergänzend: ARRY bekommt 20-35% Royalties. Aber ich teile die Einschätzung, dass der Partner eine Enttäuschung ist, zumal jetzt eine Übernahme unwahrscheinlich ist. Die NEMO Ergebnisse sind wohl nicht ganz so wichtig, weil das Marktpotenzial hier nicht so groß ist.
SG kmastra
Wenn ich nicht falsch liege, dann gab es ziemlich voeleinsiderverkäufe in der letzten zeit - es ist halt wie immer, auf die zeichen hören
es gibt wohl eine Klage gegen CLVS möglich. Hat jemand Erfahrungen? Vielleicht sollte man denen mal folgen, oder?
in den USA sind Klagen gegen das Unternehmen relativ leicht möglich. Allerdings halte ich mehr von der dt. Variante, weil letztlich die Kläger dem Unternehmen den Rest geben. Geschädigt sind alle Aktionäre gleichermaßen.
Sinnvoller sind Klagen gegen die Vorstände, die ggf. getäuscht haben. Ich schreibe das aber völlig unabhängig von Clovis, wo man mal abwarten muss, wie sich dies alles weiter entwickelt.
Sinnvoller sind Klagen gegen die Vorstände, die ggf. getäuscht haben. Ich schreibe das aber völlig unabhängig von Clovis, wo man mal abwarten muss, wie sich dies alles weiter entwickelt.
Antwort auf Beitrag Nr.: 51.112.059 von xylophon am 17.11.15 19:55:13Arry
Behaltet ihr eure Positionen oder verkauft ihr? Seh ordentlich down risk , auch wenn nemo failed, was meint ihr?
Behaltet ihr eure Positionen oder verkauft ihr? Seh ordentlich down risk , auch wenn nemo failed, was meint ihr?
CLVS
Ich hatte Kontakt mit der IR:
Das Update zu Lucitanib wird erst zur ASCO 2016 erwartet. (Mal sehen, ob/was schon auf dem SABCS im Dez. präsentiert wird)
Die Ansprechraten bei Ruca sind überwiegend bestätigte.
Ich werde meine Aktien jetzt aber halten. Roci ist jetzt schwer bis gar nicht zu bewerten. Hier wird man wohl abwarten müssen. Ob die Ansprechraten z.B. bei T790- jetzt tatsächlich noch besser sind als bei Tagrisso?
ARRY
Auch ARRY halte ich, weil sich die Werte m.E. aufsummieren. So wie ich es sehe ist vor allem die SELECT Studie nächstes Jahr wichtig.

Das Management hat insgesamt leider zu oft auf das falsche Pferd gesetzt. Ein Beispiel ist LOXO. LOXO ist jetzt genausoviel Wert wie ARRY. Man hätte 101 wohl besser selber zumindest durch die PI gebracht. Zudem hatte man im Zuge des Deals 1,6 Mio Aktien von LOXO bekommen, die man wohl aber schon verkauft hat. Die Aktien wären jetzt ca. 50 Mio Wert. Ähnlich verhält es sich bei ONTY...
SG kmastra
Ich hatte Kontakt mit der IR:
Das Update zu Lucitanib wird erst zur ASCO 2016 erwartet. (Mal sehen, ob/was schon auf dem SABCS im Dez. präsentiert wird)
Die Ansprechraten bei Ruca sind überwiegend bestätigte.
Ich werde meine Aktien jetzt aber halten. Roci ist jetzt schwer bis gar nicht zu bewerten. Hier wird man wohl abwarten müssen. Ob die Ansprechraten z.B. bei T790- jetzt tatsächlich noch besser sind als bei Tagrisso?
ARRY
Auch ARRY halte ich, weil sich die Werte m.E. aufsummieren. So wie ich es sehe ist vor allem die SELECT Studie nächstes Jahr wichtig.

Das Management hat insgesamt leider zu oft auf das falsche Pferd gesetzt. Ein Beispiel ist LOXO. LOXO ist jetzt genausoviel Wert wie ARRY. Man hätte 101 wohl besser selber zumindest durch die PI gebracht. Zudem hatte man im Zuge des Deals 1,6 Mio Aktien von LOXO bekommen, die man wohl aber schon verkauft hat. Die Aktien wären jetzt ca. 50 Mio Wert. Ähnlich verhält es sich bei ONTY...
SG kmastra
Hammer Short squeeze
http://www.nasdaq.com/de/symbol/kbio/after-hours
http://www.nasdaq.com/de/symbol/kbio/after-hours
Antwort auf Beitrag Nr.: 51.124.830 von schnappi am 18.11.15 23:41:07Das ist der Grund
http://www.marketwatch.com/story/kalobios-soars-800-after-ma…
http://www.marketwatch.com/story/kalobios-soars-800-after-ma…
Antwort auf Beitrag Nr.: 51.134.748 von Popeye82 am 20.11.15 05:00:12AUPH
Warum findet hier so ein ausverkauf statt?
Viele Grüße
Warum findet hier so ein ausverkauf statt?
Viele Grüße
CLDX: Kein überragenden Daten, aber für jeden Glioblastombetroffenen vielleicht doch ein wenig Hoffnung
Antwort auf Beitrag Nr.: 51.144.342 von riverstar_de am 21.11.15 10:19:30CLDX
"Kein überragenden Daten, aber für jeden Glioblastombetroffenen vielleicht doch ein wenig Hoffnung"
Nicht überragend hört sich eher negativ an, oder? Dabei sind die Daten doch ausgezeichnet oder worauf beziehst du deine Einschätzung? Das Problem bei diesen ReACT-Daten ist ja nicht, dass sie nicht gut wären, sondern dass sie laut Aussage der FDA aus quasi "technischen" Gründen nicht für eine Zulassung genutzt werden können. ReACT ist eine PII... eine Zulassung aufgrund von PII ist eine vorzeitige Zulassung und damit nur aufgrund von Surrogat-Parametern für einen Überlebensvorteil wie z.B. Ansprechraten möglich. Paradoxerweise ist ein statistisch signifikanter Überlebensvorteil, wie er in ReACT vorliegt, kein Surrogat-Parameter für einen Überlebensvorteil. Das einzige, was aus meiner Sicht gegen eine vorzeitige Zulassung sprechen könnte, ist eine eventuelle Unausgewogenheit der beiden Studienarme. Der Rindo-Arm enthält mehr Patienten, die eine etwas bessere Prognose haben. Aber das ist wohl trotzdem nicht ausreichend, um die Unterschiede im Überleben zu erklären.
Die nun aktualisierten Daten sagen, dass nach 2 Jahren im Rindo+Avastin Arm noch 25% leben, während im Avastin-Arm niemand mehr am leben ist. Vielleicht findest du 25% nicht ausreichend, um das als überragend zu bezeichnen.
Allerdings muss man auch berücksichtigen, dass GBM insgesamt eine schlechte Prognose hat und die Prognose von EGFRvIII+ GBM ist nochmal deutlich schlechter als von EGFRvIII- GBM: Median OS 1st-line EGFRvIII+ ist 14,3 Monate gegenüber EGFRvIII- mit 18,2 Monaten.
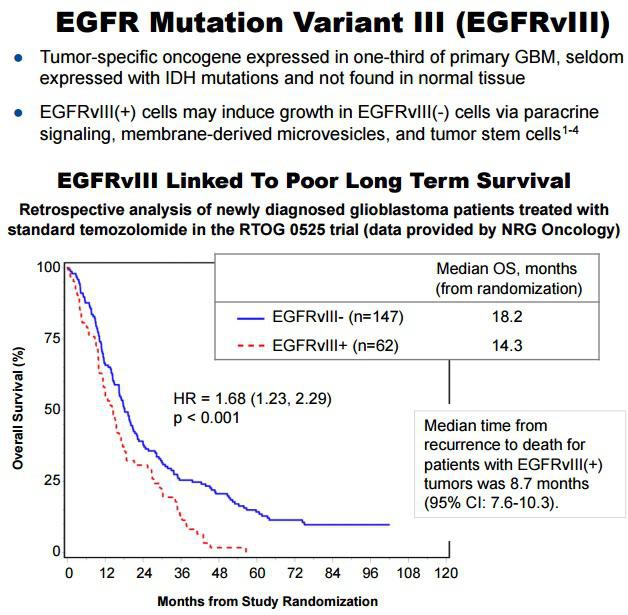
ReACT ist eine Studie in EGFRvIII+ GBM-Patienten, die bereits behandelt worden sind und bei denen diese Behandlungen nicht mehr ansprechen. D.h. Patienten mit schlechter Prognose, bei denen nichts anderes mehr wirksam ist. Oben wird Median OS bei EGFRvIII+ nach Rückfall mit 8,7 Monate angegeben. Avastin alleine zeigt bei GBM nach Rückfall einen Median OS vom 9,2 Monaten... das dürfte allerdings unabhängig von EGFRvIII sein.

Median OS von Rindo+Avastin bei ReACT ist nun 11,3 Monate... also schon einiges besser als ca. 9 Monate.
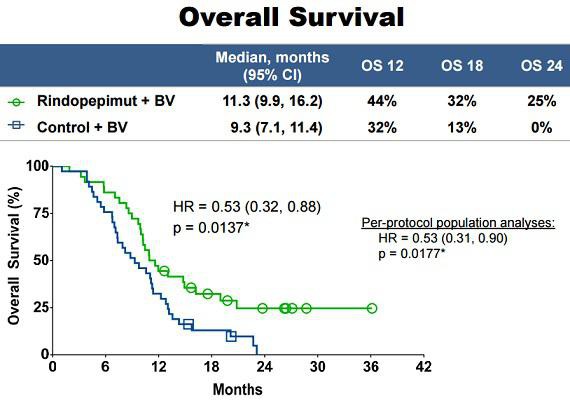
Rindo wirkt dabei über das Immunsystem. Typisch für IO ist, dass nur ein Teil der Patienten davon profitiert, dieser Teil aber oft ein erhebliche Lebensverlängerung aufweist. In ReACT sieht es momentan so aus, als ob die Überlebenskurve bei ca 25% deutlich abflacht. Selbst wenn die 2 Monate mehr im Median nicht viel sind, so können doch einige Patienten viele Monate länger leben, wenn Rindo sich wirklich positiv auswirkt.
Das ist ja das besondere an so Mitteln wie Ipi oder PD1... es gibt Langzeitüberlebende. Sollte das mit Rindo auch so sein, wäre das doch schon ein erheblicher Fortschritt, oder?
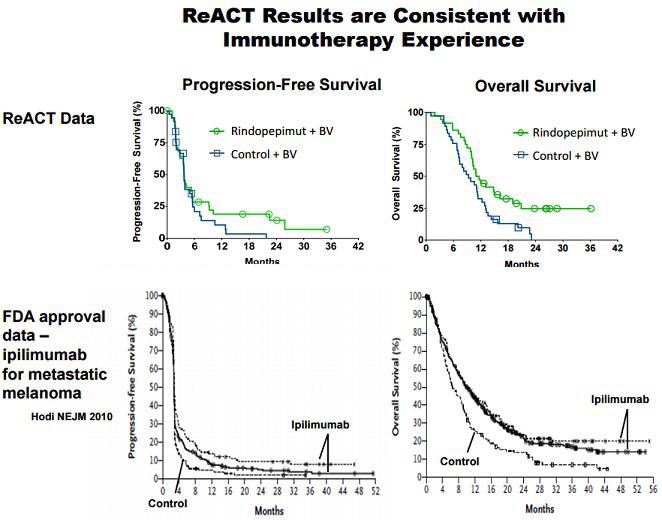
Rindo wirkt gegen EGFRvIII. Nur ein Teil von GBM ist EGFRvIII+. Laut CLDX expressionieren nach der Rindo-Behandlung die Krebszellen kein EGFRvIII mehr, d.h. also nicht, dass der Krebs völlig zerstört werden kann, nur dass er nicht mehr diese sehr agressive Form ausbildet. Rindo wäre vergleichbar mit z.B. EGFRvIII-CARTs, nur dass Rindo als Immpfstoff relativ milde Nebenwirkungen zeigt.
In ReACT gibt es einen Zusammenhang zwischen der Anzahl der EGFRvIII-AKs, die der Körper als Immunantwort auf Rindo bildet, und der längeren Überlebenszeit. Zumindest scheinen hier die Daten konsistent bezüglich des Wirkmechanismus zu sein.
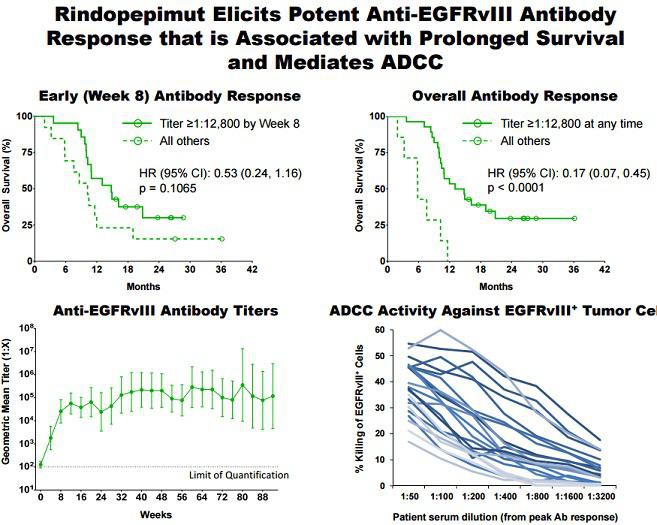

Gruß
ipollit
"Kein überragenden Daten, aber für jeden Glioblastombetroffenen vielleicht doch ein wenig Hoffnung"
Nicht überragend hört sich eher negativ an, oder? Dabei sind die Daten doch ausgezeichnet oder worauf beziehst du deine Einschätzung? Das Problem bei diesen ReACT-Daten ist ja nicht, dass sie nicht gut wären, sondern dass sie laut Aussage der FDA aus quasi "technischen" Gründen nicht für eine Zulassung genutzt werden können. ReACT ist eine PII... eine Zulassung aufgrund von PII ist eine vorzeitige Zulassung und damit nur aufgrund von Surrogat-Parametern für einen Überlebensvorteil wie z.B. Ansprechraten möglich. Paradoxerweise ist ein statistisch signifikanter Überlebensvorteil, wie er in ReACT vorliegt, kein Surrogat-Parameter für einen Überlebensvorteil. Das einzige, was aus meiner Sicht gegen eine vorzeitige Zulassung sprechen könnte, ist eine eventuelle Unausgewogenheit der beiden Studienarme. Der Rindo-Arm enthält mehr Patienten, die eine etwas bessere Prognose haben. Aber das ist wohl trotzdem nicht ausreichend, um die Unterschiede im Überleben zu erklären.
Die nun aktualisierten Daten sagen, dass nach 2 Jahren im Rindo+Avastin Arm noch 25% leben, während im Avastin-Arm niemand mehr am leben ist. Vielleicht findest du 25% nicht ausreichend, um das als überragend zu bezeichnen.
Allerdings muss man auch berücksichtigen, dass GBM insgesamt eine schlechte Prognose hat und die Prognose von EGFRvIII+ GBM ist nochmal deutlich schlechter als von EGFRvIII- GBM: Median OS 1st-line EGFRvIII+ ist 14,3 Monate gegenüber EGFRvIII- mit 18,2 Monaten.

ReACT ist eine Studie in EGFRvIII+ GBM-Patienten, die bereits behandelt worden sind und bei denen diese Behandlungen nicht mehr ansprechen. D.h. Patienten mit schlechter Prognose, bei denen nichts anderes mehr wirksam ist. Oben wird Median OS bei EGFRvIII+ nach Rückfall mit 8,7 Monate angegeben. Avastin alleine zeigt bei GBM nach Rückfall einen Median OS vom 9,2 Monaten... das dürfte allerdings unabhängig von EGFRvIII sein.

Median OS von Rindo+Avastin bei ReACT ist nun 11,3 Monate... also schon einiges besser als ca. 9 Monate.

Rindo wirkt dabei über das Immunsystem. Typisch für IO ist, dass nur ein Teil der Patienten davon profitiert, dieser Teil aber oft ein erhebliche Lebensverlängerung aufweist. In ReACT sieht es momentan so aus, als ob die Überlebenskurve bei ca 25% deutlich abflacht. Selbst wenn die 2 Monate mehr im Median nicht viel sind, so können doch einige Patienten viele Monate länger leben, wenn Rindo sich wirklich positiv auswirkt.
Das ist ja das besondere an so Mitteln wie Ipi oder PD1... es gibt Langzeitüberlebende. Sollte das mit Rindo auch so sein, wäre das doch schon ein erheblicher Fortschritt, oder?

Rindo wirkt gegen EGFRvIII. Nur ein Teil von GBM ist EGFRvIII+. Laut CLDX expressionieren nach der Rindo-Behandlung die Krebszellen kein EGFRvIII mehr, d.h. also nicht, dass der Krebs völlig zerstört werden kann, nur dass er nicht mehr diese sehr agressive Form ausbildet. Rindo wäre vergleichbar mit z.B. EGFRvIII-CARTs, nur dass Rindo als Immpfstoff relativ milde Nebenwirkungen zeigt.
In ReACT gibt es einen Zusammenhang zwischen der Anzahl der EGFRvIII-AKs, die der Körper als Immunantwort auf Rindo bildet, und der längeren Überlebenszeit. Zumindest scheinen hier die Daten konsistent bezüglich des Wirkmechanismus zu sein.

Gruß
ipollit
Antwort auf Beitrag Nr.: 51.146.592 von ipollit am 21.11.15 19:38:01
Oh doch ich finde das sehr gut, was cldx abgeliefert hat, aber eben nichts, was für eine vorzeitige zulassung reicht, leider.
Ich bin für jede forschung auf diesem gebiet sehr dankbar. Avastin hilft leider nicht so oft, jdenfalls nicht lange.
Wenn du mal bei mc600.de guckst und liest, dann weißt du warum. Manche haben glück und leben sogar noch recht lange, aber im allgemeinen sieht es eben ganz schlecht aus.
Zitat von ipollit: CLDX
"Kein überragenden Daten, aber für jeden Glioblastombetroffenen vielleicht doch ein wenig Hoffnung"
Nicht überragend hört sich eher negativ an, oder? Dabei sind die Daten doch ausgezeichnet oder worauf beziehst du deine Einschätzung? Das Problem bei diesen ReACT-Daten ist ja nicht, dass sie nicht gut wären, sondern dass sie laut Aussage der FDA aus quasi "technischen" Gründen nicht für eine Zulassung genutzt werden können. ReACT ist eine PII... eine Zulassung aufgrund von PII ist eine vorzeitige Zulassung und damit nur aufgrund von Surrogat-Parametern für einen Überlebensvorteil wie z.B. Ansprechraten möglich. Paradoxerweise ist ein statistisch signifikanter Überlebensvorteil, wie er in ReACT vorliegt, kein Surrogat-Parameter für einen Überlebensvorteil. Das einzige, was aus meiner Sicht gegen eine vorzeitige Zulassung sprechen könnte, ist eine eventuelle Unausgewogenheit der beiden Studienarme. Der Rindo-Arm enthält mehr Patienten, die eine etwas bessere Prognose haben. Aber das ist wohl trotzdem nicht ausreichend, um die Unterschiede im Überleben zu erklären.
Die nun aktualisierten Daten sagen, dass nach 2 Jahren im Rindo+Avastin Arm noch 25% leben, während im Avastin-Arm niemand mehr am leben ist. Vielleicht findest du 25% nicht ausreichend, um das als überragend zu bezeichnen.
Allerdings muss man auch berücksichtigen, dass GBM insgesamt eine schlechte Prognose hat und die Prognose von EGFRvIII+ GBM ist nochmal deutlich schlechter als von EGFRvIII- GBM: Median OS 1st-line EGFRvIII+ ist 14,3 Monate gegenüber EGFRvIII- mit 18,2 Monaten.
ReACT ist eine Studie in EGFRvIII+ GBM-Patienten, die bereits behandelt worden sind und bei denen diese Behandlungen nicht mehr ansprechen. D.h. Patienten mit schlechter Prognose, bei denen nichts anderes mehr wirksam ist. Oben wird Median OS bei EGFRvIII+ nach Rückfall mit 8,7 Monate angegeben. Avastin alleine zeigt bei GBM nach Rückfall einen Median OS vom 9,2 Monaten... das dürfte allerdings unabhängig von EGFRvIII sein.
Median OS von Rindo+Avastin bei ReACT ist nun 11,3 Monate... also schon einiges besser als ca. 9 Monate.
Rindo wirkt dabei über das Immunsystem. Typisch für IO ist, dass nur ein Teil der Patienten davon profitiert, dieser Teil aber oft ein erhebliche Lebensverlängerung aufweist. In ReACT sieht es momentan so aus, als ob die Überlebenskurve bei ca 25% deutlich abflacht. Selbst wenn die 2 Monate mehr im Median nicht viel sind, so können doch einige Patienten viele Monate länger leben, wenn Rindo sich wirklich positiv auswirkt.
Das ist ja das besondere an so Mitteln wie Ipi oder PD1... es gibt Langzeitüberlebende. Sollte das mit Rindo auch so sein, wäre das doch schon ein erheblicher Fortschritt, oder?
Rindo wirkt gegen EGFRvIII. Nur ein Teil von GBM ist EGFRvIII+. Laut CLDX expressionieren nach der Rindo-Behandlung die Krebszellen kein EGFRvIII mehr, d.h. also nicht, dass der Krebs völlig zerstört werden kann, nur dass er nicht mehr diese sehr agressive Form ausbildet. Rindo wäre vergleichbar mit z.B. EGFRvIII-CARTs, nur dass Rindo als Immpfstoff relativ milde Nebenwirkungen zeigt.
In ReACT gibt es einen Zusammenhang zwischen der Anzahl der EGFRvIII-AKs, die der Körper als Immunantwort auf Rindo bildet, und der längeren Überlebenszeit. Zumindest scheinen hier die Daten konsistent bezüglich des Wirkmechanismus zu sein.
[IMG]http://bigcharts.marketwatch.com/kaavio.Webhost/charts/big.chart?nosettings=1&symb=cldx&uf=0&type=2&size=2&sid=3374433&style=320&freq=1&entitlementtoken=0c33378313484ba9b46b8e24ded87dd6&time=8&rand=1457043386&compidx=&ma=0&maval=9&lf=1&lf2=0&lf3=0&height=335&width=579&mocktick=1[/IMG]
Gruß
ipollit
Oh doch ich finde das sehr gut, was cldx abgeliefert hat, aber eben nichts, was für eine vorzeitige zulassung reicht, leider.
Ich bin für jede forschung auf diesem gebiet sehr dankbar. Avastin hilft leider nicht so oft, jdenfalls nicht lange.
Wenn du mal bei mc600.de guckst und liest, dann weißt du warum. Manche haben glück und leben sogar noch recht lange, aber im allgemeinen sieht es eben ganz schlecht aus.
MDVN
Zwar steht Xtandi im Mittelpunkt (laut Homepage besteht die Pipeline nur aus Xtandi), doch baut MDVN im Hintergrund fleißig an einer breiteren Pipeline.
Da ist zum einen der PD1-AK Pidilizumab. Zwar sind hier andere PD1-AKs wie Nivo viel weiter und Pidi wird nur als schwacher PD1-AK gesehen, doch soll sich Pidi laut MDVN auch deutlich von anderen AKs unterscheiden, da alle anderen AKs gegen das PD1-Protein entwickelt wurden, während Pidi direkt gegen Zelllinien optimiert wurde. Dadurch soll es breiter wirken als nur gegen PD1, z.B. auch NK-Zellen aktivieren: "And there is some published data showing that pidilizumab appears to activate natural killer cells and increase NK migration. So, again, a profile that may be somewhat different from other PD-1 molecules." Zulassungsstudien sollen die Blutkrebsarten gestartet werden, in denen andere PD1-AKs noch wenig vertreten sind (typisch für PD1 sind Melanoma, NSCLC oder RCC) wie DLBCL: "We remain on track to take pidilizumab into a pivotal study in diffuse large B-cell lymphoma this year... We're also considering the initiation of clinical trials for pidilizumab in other hematological malignancies, such as multiple myeloma." Pidi wurde z.B. auch in Kombi mit Rituxan getestet. Falls Pidi wirklich NK-Zellen aktiviert, könnte sich das positiv auf solche Kombinationen auswirken, da AKs wie Rituxan oder Herceptin sehr stark über ADCC wirken, das von der Aktivität von NK-Zellen abhängt.
MDVN hat den PARP-Hemmer Talazoparib von BRMN einlizensiert. Wie die PARP-Hemmer von AZN, TSRO oder CLVS wirkt auch Tala bei Tumoren, die einen Defekt der DNA-Reparatur aufweisen wie BRCA-Mutationen. Talazoparib soll aber erheblich stärker sein, insbesondere bis zu 1000mal stärker im PARP trapping. Letzteres soll sich positiv auf Kombinationen mit Chemos oder Strahlentherapien auswirken, die die DNA schädigen, um Krebszellen zu zerstören... ein sehr großer Markt. "Talazoparib is the most potent PARP inhibitor in development. Perhaps even more importantly, in head-to-head preclinical studies, talazoparib has been shown to be superior to other PARP inhibitors in a phenomenon known as PARP trapping, an effect that Yves Pommier at the National Cancer Institute has correlated with a superior ability to kill cancer cells... in 2014, in the U.S. alone, approximately 500,000 patients received DNA damaging radiation therapy, while more than 500,000 patients received DNA damaging chemotherapy. We believe that the PARP trapping ability of talazoparib may differentiate talazoparib from other PARP inhibitors, particularly in combination with DNA damaging therapies"
Mit Xtandi hat MDVN eines der wichtigsten Therapien gegen Prostatakrebs. PARP-Hemmer scheinen ebenfalls gegen Prostatakrebs zu helfen. So hat AZNs Olaparib in einer PII eine RR von sehr guten 88% in Prostatakrebs-Patienten, die HRD positiv waren (d.h. die Reparaturschäden aufwiesen wie BRCA... das ist nur bei einem Teil der Patienten der Fall, hier waren es 16 von 49). http://www.ascopost.com/ViewNews.aspx?nid=34024&utm_medium=E… Dies ist sehr ungewöhnlich, da die Patienten sehr stark vorbehandelt waren mit u.a. Taxotere und Xtandi, die nicht mehr wirkten. Bei vielen waren nach Olaparib-Behandlung keine Krebszellen mehr im Blut nachweisebar (CTC decline 100%)... CTC ist in Prostatakrebs ein Surrogat-Parameter für das Überleben, besser noch als PSA. Ich denke, dass MDVN Tala auch in Prostatakrebs entwickeln wird (momentan ist es am weitesten in Brustkrebs mit PIII-Zulassungsstudien), wahrscheinlich auch in Kombi mit Xtandi, da Tala auch eine Wirkung auf AR haben soll: "Talazoparib obviously affects DNA repair. But as it turns out, that appears to have also real effects on AR expression as an example."
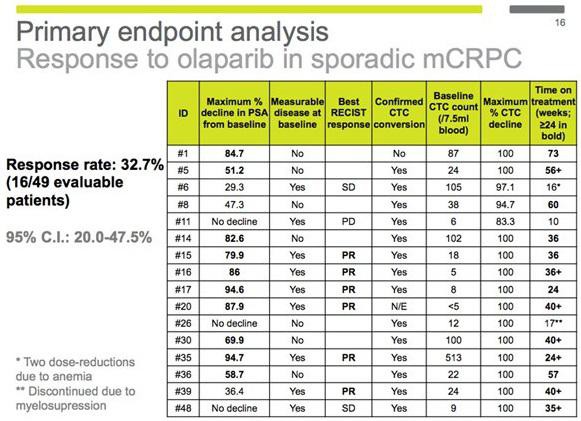
Zudem hat MDVN mit MDV4463 einen neuartigen SREBP-Hemmer in PI. SREBP könnte in einer Vielzahl von Anwendungen relevant sein wie Herz-Kreislauferkrankungen, NASH oder Krebs: "Finally, we're very pleased to announce that we are currently in a Phase 1 trial in healthy volunteers with a novel small molecule inhibitor of the SREBP pathway. This molecule was developed internally at Medivation. SREBP, or sterol regulatory element-binding proteins, are master regulators of cholesterol and lipid biosynthesis. SREBP modulates the expression of multiple metabolic proteins, including, but not limited to, PCSK9, a target of Regeneron's recently approved antibody, alirocumab, for hypercholesterolemia and atherosclerotic cardiovascular disease, and HNG-CoA reductase, the target of all statins. In some preclinical studies, we demonstrated that our SREBP pathway inhibitor, which is codenamed MDV4463, lowered triglycerides, cholesterol, glucose, insulin and weight in animals. MDV4463 also reduced fat in the liver in animal models of non-alcoholic hepatic steatosis or NASH."
Der Kurs ist leider zuletzt sehr schwach... MDVN bekommt von einigen Analysten immer wieder negative Kommentare, dass Xtandi nicht weiter wachsen würde. Mal schauen...

Gruß
ipollit
Zwar steht Xtandi im Mittelpunkt (laut Homepage besteht die Pipeline nur aus Xtandi), doch baut MDVN im Hintergrund fleißig an einer breiteren Pipeline.
Da ist zum einen der PD1-AK Pidilizumab. Zwar sind hier andere PD1-AKs wie Nivo viel weiter und Pidi wird nur als schwacher PD1-AK gesehen, doch soll sich Pidi laut MDVN auch deutlich von anderen AKs unterscheiden, da alle anderen AKs gegen das PD1-Protein entwickelt wurden, während Pidi direkt gegen Zelllinien optimiert wurde. Dadurch soll es breiter wirken als nur gegen PD1, z.B. auch NK-Zellen aktivieren: "And there is some published data showing that pidilizumab appears to activate natural killer cells and increase NK migration. So, again, a profile that may be somewhat different from other PD-1 molecules." Zulassungsstudien sollen die Blutkrebsarten gestartet werden, in denen andere PD1-AKs noch wenig vertreten sind (typisch für PD1 sind Melanoma, NSCLC oder RCC) wie DLBCL: "We remain on track to take pidilizumab into a pivotal study in diffuse large B-cell lymphoma this year... We're also considering the initiation of clinical trials for pidilizumab in other hematological malignancies, such as multiple myeloma." Pidi wurde z.B. auch in Kombi mit Rituxan getestet. Falls Pidi wirklich NK-Zellen aktiviert, könnte sich das positiv auf solche Kombinationen auswirken, da AKs wie Rituxan oder Herceptin sehr stark über ADCC wirken, das von der Aktivität von NK-Zellen abhängt.
MDVN hat den PARP-Hemmer Talazoparib von BRMN einlizensiert. Wie die PARP-Hemmer von AZN, TSRO oder CLVS wirkt auch Tala bei Tumoren, die einen Defekt der DNA-Reparatur aufweisen wie BRCA-Mutationen. Talazoparib soll aber erheblich stärker sein, insbesondere bis zu 1000mal stärker im PARP trapping. Letzteres soll sich positiv auf Kombinationen mit Chemos oder Strahlentherapien auswirken, die die DNA schädigen, um Krebszellen zu zerstören... ein sehr großer Markt. "Talazoparib is the most potent PARP inhibitor in development. Perhaps even more importantly, in head-to-head preclinical studies, talazoparib has been shown to be superior to other PARP inhibitors in a phenomenon known as PARP trapping, an effect that Yves Pommier at the National Cancer Institute has correlated with a superior ability to kill cancer cells... in 2014, in the U.S. alone, approximately 500,000 patients received DNA damaging radiation therapy, while more than 500,000 patients received DNA damaging chemotherapy. We believe that the PARP trapping ability of talazoparib may differentiate talazoparib from other PARP inhibitors, particularly in combination with DNA damaging therapies"
Mit Xtandi hat MDVN eines der wichtigsten Therapien gegen Prostatakrebs. PARP-Hemmer scheinen ebenfalls gegen Prostatakrebs zu helfen. So hat AZNs Olaparib in einer PII eine RR von sehr guten 88% in Prostatakrebs-Patienten, die HRD positiv waren (d.h. die Reparaturschäden aufwiesen wie BRCA... das ist nur bei einem Teil der Patienten der Fall, hier waren es 16 von 49). http://www.ascopost.com/ViewNews.aspx?nid=34024&utm_medium=E… Dies ist sehr ungewöhnlich, da die Patienten sehr stark vorbehandelt waren mit u.a. Taxotere und Xtandi, die nicht mehr wirkten. Bei vielen waren nach Olaparib-Behandlung keine Krebszellen mehr im Blut nachweisebar (CTC decline 100%)... CTC ist in Prostatakrebs ein Surrogat-Parameter für das Überleben, besser noch als PSA. Ich denke, dass MDVN Tala auch in Prostatakrebs entwickeln wird (momentan ist es am weitesten in Brustkrebs mit PIII-Zulassungsstudien), wahrscheinlich auch in Kombi mit Xtandi, da Tala auch eine Wirkung auf AR haben soll: "Talazoparib obviously affects DNA repair. But as it turns out, that appears to have also real effects on AR expression as an example."

Zudem hat MDVN mit MDV4463 einen neuartigen SREBP-Hemmer in PI. SREBP könnte in einer Vielzahl von Anwendungen relevant sein wie Herz-Kreislauferkrankungen, NASH oder Krebs: "Finally, we're very pleased to announce that we are currently in a Phase 1 trial in healthy volunteers with a novel small molecule inhibitor of the SREBP pathway. This molecule was developed internally at Medivation. SREBP, or sterol regulatory element-binding proteins, are master regulators of cholesterol and lipid biosynthesis. SREBP modulates the expression of multiple metabolic proteins, including, but not limited to, PCSK9, a target of Regeneron's recently approved antibody, alirocumab, for hypercholesterolemia and atherosclerotic cardiovascular disease, and HNG-CoA reductase, the target of all statins. In some preclinical studies, we demonstrated that our SREBP pathway inhibitor, which is codenamed MDV4463, lowered triglycerides, cholesterol, glucose, insulin and weight in animals. MDV4463 also reduced fat in the liver in animal models of non-alcoholic hepatic steatosis or NASH."
Der Kurs ist leider zuletzt sehr schwach... MDVN bekommt von einigen Analysten immer wieder negative Kommentare, dass Xtandi nicht weiter wachsen würde. Mal schauen...
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.124.710 von kmastra am 18.11.15 23:12:43ARRY
die MEK-Pipeline von ARRY sieht eigentlich recht beeindruckend aus... nächstes Jahr stehen mehrere PIII-Daten an, die im Erfolgsfall zu gleich mehreren Zulassungen führen können. Allerdings ist die Frage, ob sich ARRY gegen die großen Pharmas am Markt überhaupt behaupten kann... das wird wahrscheinlich schwierig.
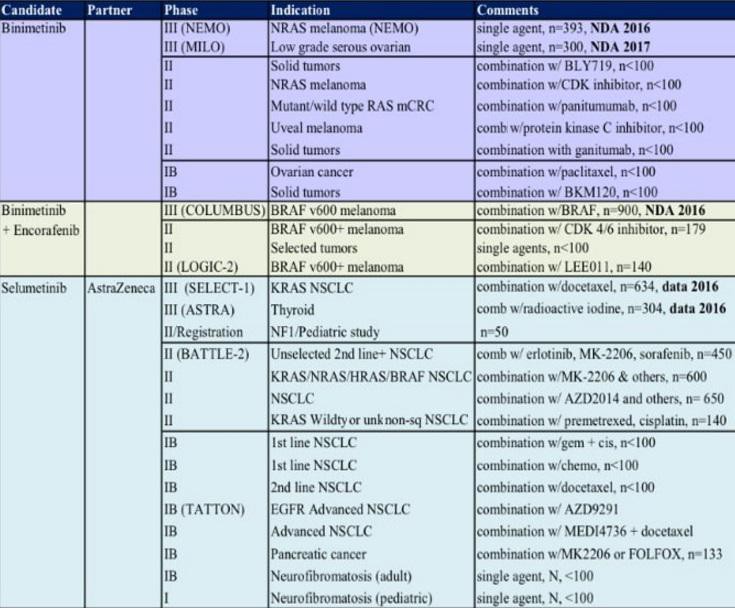
Trotzdem ist der Deal mit Pierre Fabre nicht das, was man erwartet hat. Wenn ich es richtig verstehe, muss ARRY 60% der Entwicklungskosten zahlen, um die double-digit Royalties zu erhalten (Fabry wird wohl auch für Teile der US-Entwicklung seine 40% zahlen, denke ich, obwohl sie dort keine Rechte besitzen... das hängt wohl davon ab, ob die Daten auch für die EU relevant sind). Das einzige, was positiv sein könnte, wäre vielleicht ein höherers Engagement von Fabre, da Bini&Enco nicht ein kleines Produkt unter vielen ist, wie es bei den großen Pharmas der Fall wäre, sondern ein wichtiger Teil der Pipeline.




Gruß
ipollit
die MEK-Pipeline von ARRY sieht eigentlich recht beeindruckend aus... nächstes Jahr stehen mehrere PIII-Daten an, die im Erfolgsfall zu gleich mehreren Zulassungen führen können. Allerdings ist die Frage, ob sich ARRY gegen die großen Pharmas am Markt überhaupt behaupten kann... das wird wahrscheinlich schwierig.

Trotzdem ist der Deal mit Pierre Fabre nicht das, was man erwartet hat. Wenn ich es richtig verstehe, muss ARRY 60% der Entwicklungskosten zahlen, um die double-digit Royalties zu erhalten (Fabry wird wohl auch für Teile der US-Entwicklung seine 40% zahlen, denke ich, obwohl sie dort keine Rechte besitzen... das hängt wohl davon ab, ob die Daten auch für die EU relevant sind). Das einzige, was positiv sein könnte, wäre vielleicht ein höherers Engagement von Fabre, da Bini&Enco nicht ein kleines Produkt unter vielen ist, wie es bei den großen Pharmas der Fall wäre, sondern ein wichtiger Teil der Pipeline.



Gruß
ipollit
Antwort auf Beitrag Nr.: 51.148.365 von ipollit am 22.11.15 13:23:49Hallo ipollit,
vielen Dank mal wieder für deine tollen Beiträge!
ARRY
Bzgl. Array ist auch das 8-K sehr aufschlussreich was die Umsatzaussichten/erwartungen betrifft:
Array is also entitled to receive up to $425 million in milestone payments from Pierre Fabre if certain development and commercialization goals are achieved, and Array is eligible for tiered double-digit royalties on combined annual net sales of binimetinib and encorafenib in the Pierre Fabre territory, starting at 20%, and moving through multiple tiers, including a maximum of 35% on annual combined net sales of binimetinib and encorafenib which exceed €100 million.
Man hat also mehrere Royaltystufen zwischen 0 und 100 Mio festgelegt. Das hätte man wohl kaum getan, wenn man hier von einem signifikant höherem Umsatzpotenzial ausgeht.
Was die Kosten der weiteren Entwicklung betrifft heiß es:
All ongoing clinical trials involving binimetinib and encorafenib, including the NEMO, COLUMBUS and MILO trails and other ongoing Novartis sponsored and investigator sponsored clinical studies, will continue to be conducted pursuant to the terms of the Novartis Agreements. Further worldwide development activities will be governed by a Global Development Plan (GDP). Pierre Fabre and Array will jointly fund worldwide development costs under the GDP, with Array covering 60% and Pierre Fabre covering 40% of such costs. The initial GDP includes multiple trials, and Pierre Fabre and Array have agreed to commit at least €100 million in combined funds for these studies in colorectal cancer and melanoma.
Also:
-Novartis ist natürlich weiterhin in der Pflicht einen Teil der Studien weiter zu finanzieren.
-Darüber hinaus gibt es einen Entwicklungsplan, der eine 60/40 Teilung der Kosten vorsieht.
-Dafür sind erstmal 100 Mio vorgesehen (also kommen 60 Mio von ARRY)
http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
CLVS
Seit dem "Schock" vom Montag ist nun fast eine Woche vergangen aber ich bin eigentlich immer noch einigermaßen fassungslos. Ich hatte mir kurz zuvor den CC zum Quartalsergebnis angehört. Dort hat man beispielsweise betont, dass das Verkaufsteam bereits am arbeiten ist, um auf jeden Fall nach der Zulassung gleich loslegen zu können. Laut CC vom Montag hat man da aber bereits von der niedrigeren Ansprechrate Nach RECIST gewusst!? Jetzt hat (und bezahlt) man also ein Verkaufsteam und wann die Zulassung kommt steht in den Sternen...
Ich würde mir von CLVS jetzt wünschen, dass man reinen Tisch macht und den aktuellen Stand der Studien ganz offen kommuniziert. (z.B. auch T790M- aber gerne auch nochmal ein aktuelles Update zu Ruca)
ZFGN hat das neulich ganz geschickt gemacht. Man hat alle Erkenntnisse zur Sicherheit offen gelegt.



Somit war alles Negative auf dem Tisch und eingepreist. Zudem hat man einen Plan zur Wiederaufnahme der Studien verkündet und man wird tatsächlich die Teilnehmer regelmäßig screenen, um Thrombosen etc. rechzeitig zu entdecken. Denkbar wären auch zusätzliche präventive Maßnahmen z.B. Blutverdünner, Physiotherapie etc.
Grundsätzlich ist ZFGN aber weiterhin extrem riskant, denn wenn jetzt trotz Screening nochmal was passiert...!
SG kmastra
vielen Dank mal wieder für deine tollen Beiträge!
ARRY
Bzgl. Array ist auch das 8-K sehr aufschlussreich was die Umsatzaussichten/erwartungen betrifft:
Array is also entitled to receive up to $425 million in milestone payments from Pierre Fabre if certain development and commercialization goals are achieved, and Array is eligible for tiered double-digit royalties on combined annual net sales of binimetinib and encorafenib in the Pierre Fabre territory, starting at 20%, and moving through multiple tiers, including a maximum of 35% on annual combined net sales of binimetinib and encorafenib which exceed €100 million.
Man hat also mehrere Royaltystufen zwischen 0 und 100 Mio festgelegt. Das hätte man wohl kaum getan, wenn man hier von einem signifikant höherem Umsatzpotenzial ausgeht.
Was die Kosten der weiteren Entwicklung betrifft heiß es:
All ongoing clinical trials involving binimetinib and encorafenib, including the NEMO, COLUMBUS and MILO trails and other ongoing Novartis sponsored and investigator sponsored clinical studies, will continue to be conducted pursuant to the terms of the Novartis Agreements. Further worldwide development activities will be governed by a Global Development Plan (GDP). Pierre Fabre and Array will jointly fund worldwide development costs under the GDP, with Array covering 60% and Pierre Fabre covering 40% of such costs. The initial GDP includes multiple trials, and Pierre Fabre and Array have agreed to commit at least €100 million in combined funds for these studies in colorectal cancer and melanoma.
Also:
-Novartis ist natürlich weiterhin in der Pflicht einen Teil der Studien weiter zu finanzieren.
-Darüber hinaus gibt es einen Entwicklungsplan, der eine 60/40 Teilung der Kosten vorsieht.
-Dafür sind erstmal 100 Mio vorgesehen (also kommen 60 Mio von ARRY)
http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
CLVS
Seit dem "Schock" vom Montag ist nun fast eine Woche vergangen aber ich bin eigentlich immer noch einigermaßen fassungslos. Ich hatte mir kurz zuvor den CC zum Quartalsergebnis angehört. Dort hat man beispielsweise betont, dass das Verkaufsteam bereits am arbeiten ist, um auf jeden Fall nach der Zulassung gleich loslegen zu können. Laut CC vom Montag hat man da aber bereits von der niedrigeren Ansprechrate Nach RECIST gewusst!? Jetzt hat (und bezahlt) man also ein Verkaufsteam und wann die Zulassung kommt steht in den Sternen...
Ich würde mir von CLVS jetzt wünschen, dass man reinen Tisch macht und den aktuellen Stand der Studien ganz offen kommuniziert. (z.B. auch T790M- aber gerne auch nochmal ein aktuelles Update zu Ruca)
ZFGN hat das neulich ganz geschickt gemacht. Man hat alle Erkenntnisse zur Sicherheit offen gelegt.



Somit war alles Negative auf dem Tisch und eingepreist. Zudem hat man einen Plan zur Wiederaufnahme der Studien verkündet und man wird tatsächlich die Teilnehmer regelmäßig screenen, um Thrombosen etc. rechzeitig zu entdecken. Denkbar wären auch zusätzliche präventive Maßnahmen z.B. Blutverdünner, Physiotherapie etc.
Grundsätzlich ist ZFGN aber weiterhin extrem riskant, denn wenn jetzt trotz Screening nochmal was passiert...!
SG kmastra
FGEN
momentan ist DMD ein Thema... BMRN, SRPT und PTCT versuchen eine Zulassung von der FDA zu erhalten, wobei alle drei Mittel ihre Probleme haben

DMD ist eine seltene, sehr schwerwiegende Muskelerkrankung (eine From von Muskelschwund), die im Kindesalter auftritt und dazu führt, dass nach und nach alle Muskeln zerfallen... d.h. irgendwann ist auch die Atmung und das Herz betroffen. Es gibt unterschiedliche genetische Ursachen: in 13% ist es Exon-51. Die oben genannten Mittel versuchen genau diese Genveränderung zu behandeln, z.B. indem das fehlerhafte Gen übersprungen wird.
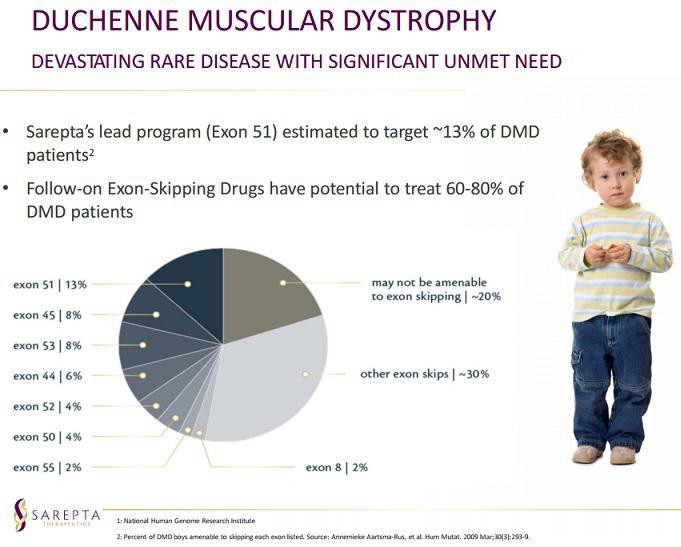
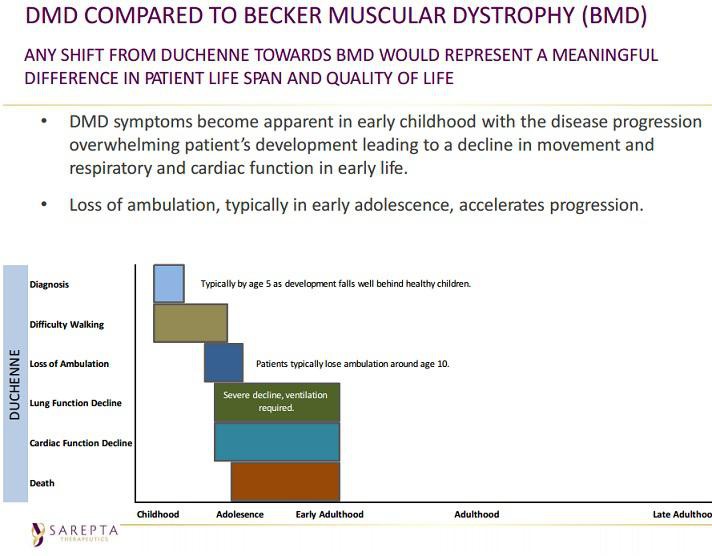
D.h. BMRN und SPRT können erstmal nur maximal 13% der DMD behandeln, falls diese Mittel zugelassen werden. Trotzdem soll eine Zulassung sich sehr deutlich auf den Kurs dieser Unternehmen auswirken: BMRN ist ein 16 Mrd USD Unternehmen, SPRT hat aktuell eine MK von 1,5 Mrd USD (zum Vergleich hat FGEN aktuell eine MK von 1,7 Mrd USD)
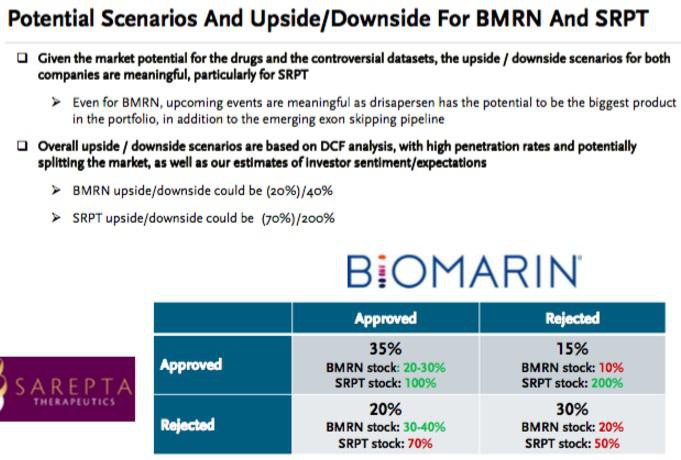
Bei DMD werden Muskelfasern durch anderes Fett- und Bindegewebe ersetzt... es ist ein fibrotischer Prozess. "Als Fibrose wird eine krankhafte Vermehrung des Bindegewebes in menschlichen und tierischen Geweben und Organen bezeichnet, dessen Hauptbestandteil Kollagenfasern sind. Dabei wird das Gewebe des betroffenen Organes verhärtet. Es entstehen narbige Veränderungen, die im fortgeschrittenen Stadium zur Einschränkung der jeweiligen Organfunktion führen."
Laut FGEN spielt bei DMD auch CTGF eine wesentliche Rolle, das grundsätzlich auch bei anderen fibrotischen Prozessen eine Rolle spielt, wie z.B. NASH oder IPF.

Daher wird FG-3019 nun auch in einer PII gegen DMD getestet. Anders als die oben genannten Mittel könnte FG-3019 nicht nur einzelnen DMD-Patienten mit einer bestimmten genetischen Veränderung helfen, sondern allen DMD-Patienten. Es steht auch nicht in Konkurrenz zu den anderen Mitteln, sondern würde in Kombination eingesetzt werden. Bisher kann man diesen Kindern nicht helfen... es wäre schön, wenn man in Zukunft mehrere Optionen hätte, mit denen man diese schwere Krankheit bekämpfen kann.
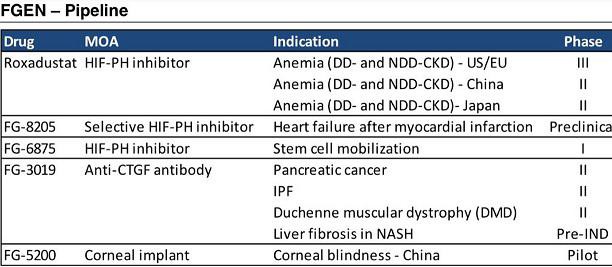

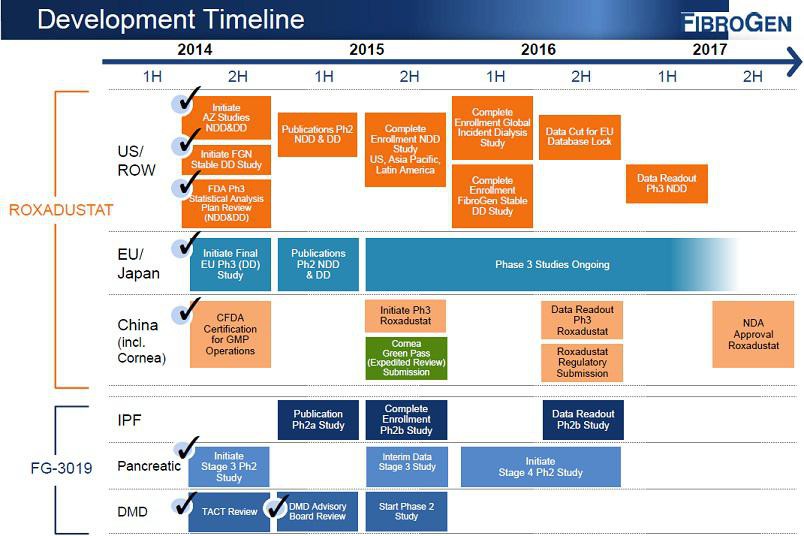

Gruß
ipollit
momentan ist DMD ein Thema... BMRN, SRPT und PTCT versuchen eine Zulassung von der FDA zu erhalten, wobei alle drei Mittel ihre Probleme haben

DMD ist eine seltene, sehr schwerwiegende Muskelerkrankung (eine From von Muskelschwund), die im Kindesalter auftritt und dazu führt, dass nach und nach alle Muskeln zerfallen... d.h. irgendwann ist auch die Atmung und das Herz betroffen. Es gibt unterschiedliche genetische Ursachen: in 13% ist es Exon-51. Die oben genannten Mittel versuchen genau diese Genveränderung zu behandeln, z.B. indem das fehlerhafte Gen übersprungen wird.


D.h. BMRN und SPRT können erstmal nur maximal 13% der DMD behandeln, falls diese Mittel zugelassen werden. Trotzdem soll eine Zulassung sich sehr deutlich auf den Kurs dieser Unternehmen auswirken: BMRN ist ein 16 Mrd USD Unternehmen, SPRT hat aktuell eine MK von 1,5 Mrd USD (zum Vergleich hat FGEN aktuell eine MK von 1,7 Mrd USD)

Bei DMD werden Muskelfasern durch anderes Fett- und Bindegewebe ersetzt... es ist ein fibrotischer Prozess. "Als Fibrose wird eine krankhafte Vermehrung des Bindegewebes in menschlichen und tierischen Geweben und Organen bezeichnet, dessen Hauptbestandteil Kollagenfasern sind. Dabei wird das Gewebe des betroffenen Organes verhärtet. Es entstehen narbige Veränderungen, die im fortgeschrittenen Stadium zur Einschränkung der jeweiligen Organfunktion führen."
Laut FGEN spielt bei DMD auch CTGF eine wesentliche Rolle, das grundsätzlich auch bei anderen fibrotischen Prozessen eine Rolle spielt, wie z.B. NASH oder IPF.

Daher wird FG-3019 nun auch in einer PII gegen DMD getestet. Anders als die oben genannten Mittel könnte FG-3019 nicht nur einzelnen DMD-Patienten mit einer bestimmten genetischen Veränderung helfen, sondern allen DMD-Patienten. Es steht auch nicht in Konkurrenz zu den anderen Mitteln, sondern würde in Kombination eingesetzt werden. Bisher kann man diesen Kindern nicht helfen... es wäre schön, wenn man in Zukunft mehrere Optionen hätte, mit denen man diese schwere Krankheit bekämpfen kann.



Gruß
ipollit
Hallo zusammen,
Ich wollte gerne einmal Fragen, ob sich jemand hier schon einmal mit Opexa Therapeutics und ihrem MS-Wirkstoff befasst hat? Wie ist eure Meinung dazu?
Gruss
Ich wollte gerne einmal Fragen, ob sich jemand hier schon einmal mit Opexa Therapeutics und ihrem MS-Wirkstoff befasst hat? Wie ist eure Meinung dazu?
Gruss
Ohad Hammer mit einem Update zu CLVS, ARRY und IMGN:
http://www.orf-blog.com/biotech-portfolio-update-clovis-arra…
Er hat CLVS jetzt verkauft und ist vom Verhalten des Managements zurecht enttäuscht. Aber hatte er CLVS nicht vor allem wegen Lucitanib gekauft?
http://www.orf-blog.com/biotech-portfolio-update-clovis-arra…
Er hat CLVS jetzt verkauft und ist vom Verhalten des Managements zurecht enttäuscht. Aber hatte er CLVS nicht vor allem wegen Lucitanib gekauft?
ISIS
Inzwischen steht der Name leider auch für sehr negative Dinge (ISIS überlegt schon sich umzubenennen)... doch das Unternehmen entwickelt sich sehr positiv. Man ist führend in der Antisense-Technologie. Selbst für ein 7 Mrd USD Unternehmen ist die Pipeline beachtlich: 38 Kandidaten aktuelle in der Entwicklung mit 3 bis 5 neuen Kandidaten pro Jahr in der Klinik.
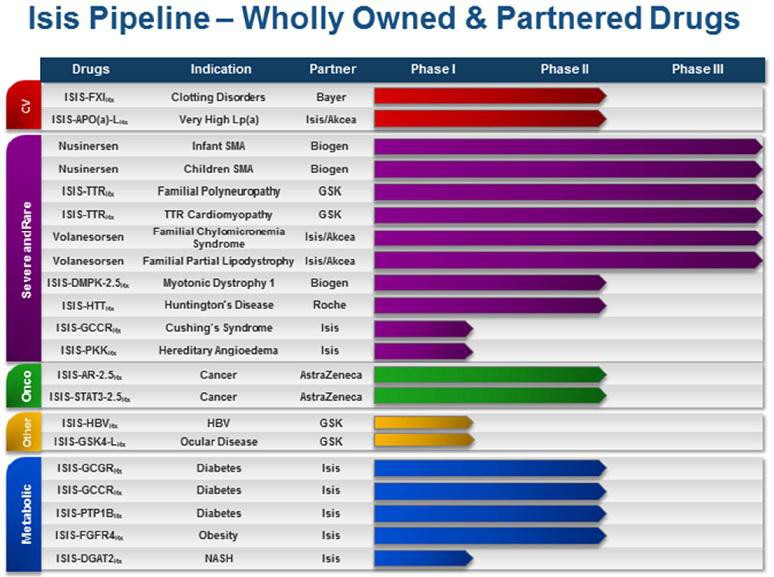


Antisense-Medikamente binden an die mRNA bevor daraus Proteine gebaut werden, so dass man damit genetische Defekte behandeln kann, bei denen Fehler in der DNA falsche, zuviele oder zuwenige Proteine erzeugen. Es ist damit keine Gentherapie, die die Gene direkt verändert, aber eine Medikamentenklasse, die auf DNA-Ebene wirkt.
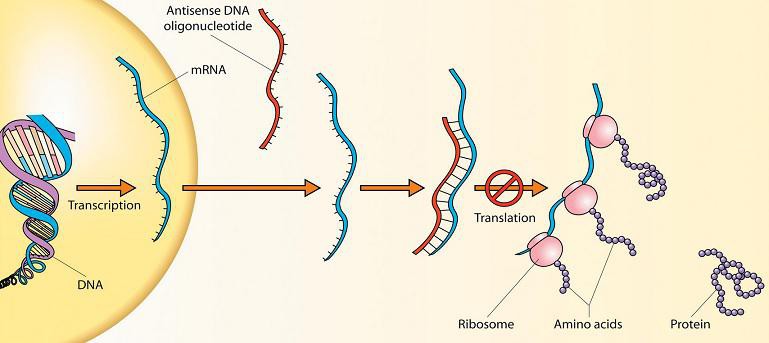
Neben DMD gibt es noch weitere seltene schwere Muskelerkrankungen. ISIS hat zusammen mit Partner BIIB eNusinersen gegen SMA in der PIII. SMA ist eine weitere Form von Muskelschwund in Kindern... bisher gibt es nichts, was bei SMA hilft. Anders als bei DMD, wo die Muskelfaser fibrotisch abgebaut werden, ist SMA ein neurologisches Problem, bei dem die Muskeln nicht mehr aktiviert werden. Ursache ist ein Fehler im SMN1 Gen, so dass das SMN Protein nicht mehr funktionsfähig ist.



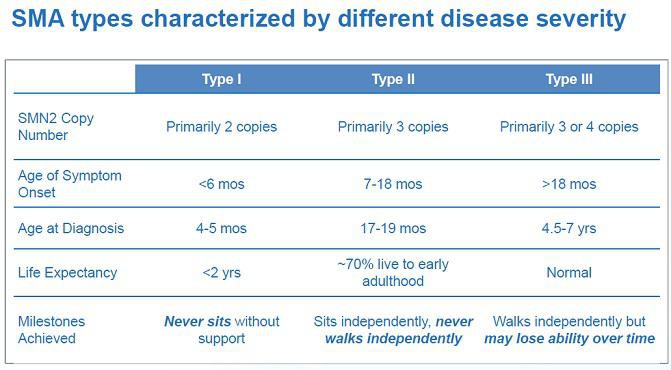
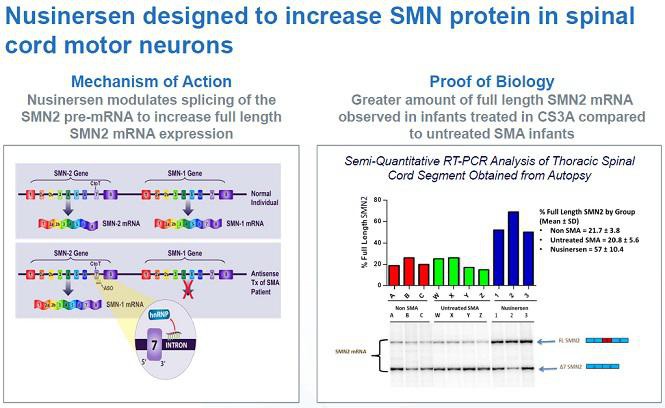
Nusinersen könnte großes Potential bieten gegen diese schwere Erkrankung.
ISIS hat noch weitere bedeutende Mittel in der Pipeline... z.B. ISIS-FXI, das zusammen mit Bayer entwickelt wird. Dieses soll ähnlich wie die Blutverdünner Xarelto&Co wirken, nur dass das Blutungsrisko nicht erhöht wird.
Die neue LICA-Technologie macht die Mittel erheblich potenter, wodurch die Verabreichung deutlich erleichtert wird (kleinere Menge, monatlich oder seltener verabreicht)



Gruß
ipollit
Inzwischen steht der Name leider auch für sehr negative Dinge (ISIS überlegt schon sich umzubenennen)... doch das Unternehmen entwickelt sich sehr positiv. Man ist führend in der Antisense-Technologie. Selbst für ein 7 Mrd USD Unternehmen ist die Pipeline beachtlich: 38 Kandidaten aktuelle in der Entwicklung mit 3 bis 5 neuen Kandidaten pro Jahr in der Klinik.



Antisense-Medikamente binden an die mRNA bevor daraus Proteine gebaut werden, so dass man damit genetische Defekte behandeln kann, bei denen Fehler in der DNA falsche, zuviele oder zuwenige Proteine erzeugen. Es ist damit keine Gentherapie, die die Gene direkt verändert, aber eine Medikamentenklasse, die auf DNA-Ebene wirkt.

Neben DMD gibt es noch weitere seltene schwere Muskelerkrankungen. ISIS hat zusammen mit Partner BIIB eNusinersen gegen SMA in der PIII. SMA ist eine weitere Form von Muskelschwund in Kindern... bisher gibt es nichts, was bei SMA hilft. Anders als bei DMD, wo die Muskelfaser fibrotisch abgebaut werden, ist SMA ein neurologisches Problem, bei dem die Muskeln nicht mehr aktiviert werden. Ursache ist ein Fehler im SMN1 Gen, so dass das SMN Protein nicht mehr funktionsfähig ist.





Nusinersen könnte großes Potential bieten gegen diese schwere Erkrankung.
ISIS hat noch weitere bedeutende Mittel in der Pipeline... z.B. ISIS-FXI, das zusammen mit Bayer entwickelt wird. Dieses soll ähnlich wie die Blutverdünner Xarelto&Co wirken, nur dass das Blutungsrisko nicht erhöht wird.
Die neue LICA-Technologie macht die Mittel erheblich potenter, wodurch die Verabreichung deutlich erleichtert wird (kleinere Menge, monatlich oder seltener verabreicht)


Gruß
ipollit
XLRN
Mit Muskelerkrankungen haben XLRN einige Erfahrung, so dass sie in Zukunft in diesem Bereich eine größere Rolle spielen könnten. XLRN's Spezialgebiet ist TGF-beta... das sind Proteine, die u.a. das Wachstum von Gewebe wie Muskeln regulieren.

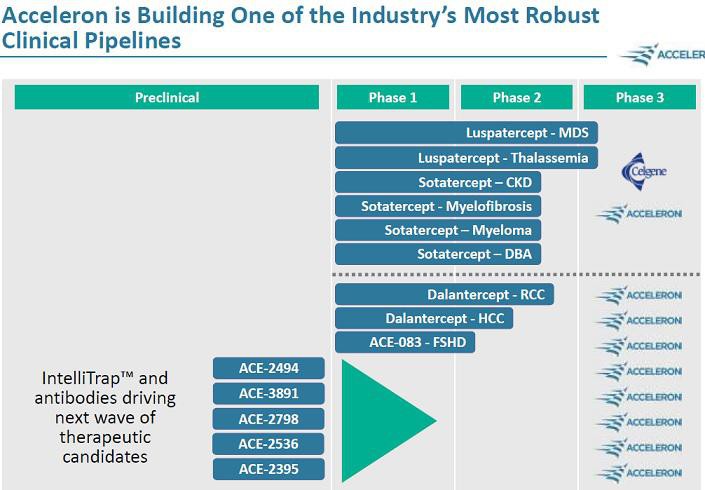
Neben DMD und SMA gibt es noch viele weitere seltene Muskelerkrankungen. Manche Erkrankungen betreffen alle Muskeln, andere nur bestimmte Muskelpartien. Demnach entwickelt XLRN Mittel, die lokal angewendet werden können wie ACE-083 oder Mittel, die sich systemisch auf alle Muskeln auswirken wie ACE-2494.

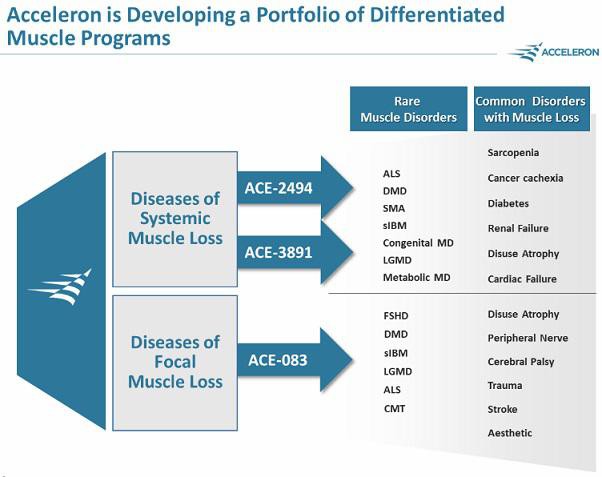
Am weitesten ist ACE-083, das u.a. gegen FSHD entwickelt wird. ACE-083 erhöht lokal die Muskelmasse, in die es verabreicht wird.
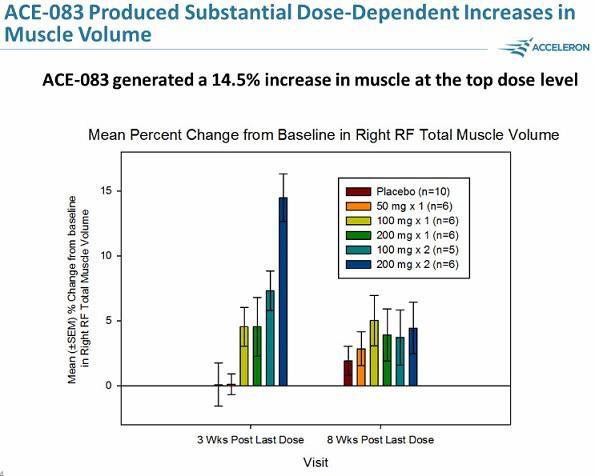
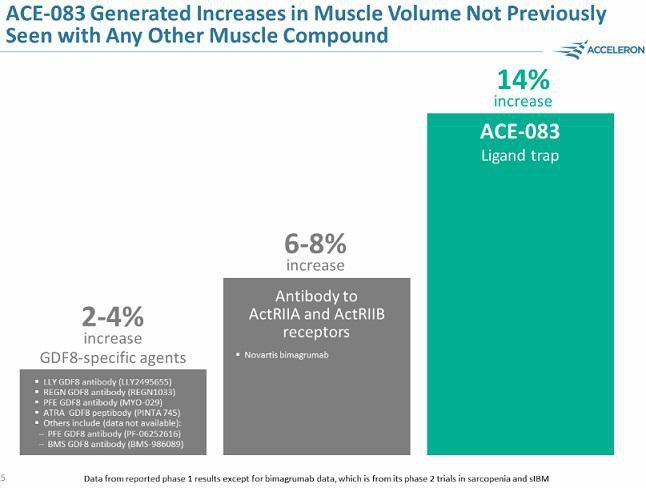
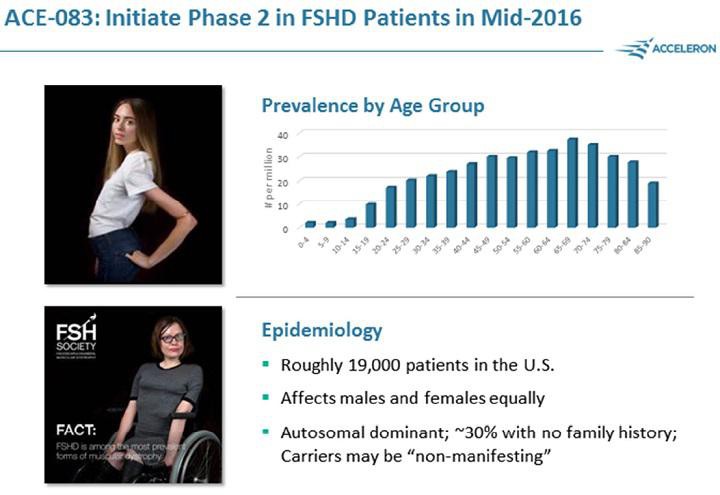
Zum Vergleich: Eine Erhöhung der Muskelmasse um 14% ist dabei deutlich höher als z.B. durch Bimagrumab mit nur 5%, das von NVS und Morphosys entwickelt wird. Bimagrumab hat BTD und befindet sich u.a. in einer PIII gegen sIBM (eine Form von Inclusion Body Myositis). Es soll aber auch bei diversen anderen Arten von Muskelschwund eingesetzt werden z.B. nach OPs oder infolge von Krebs. Solche Mittel sollen ein großes Umsatzpotential besitzen. So sagt NVS über Bimagrumab: "Novartis AG’s muscle-building drug bimagrumab may reach as much as $4 billion in peak sales, according to the medicine’s co-developer. The forecast is for the use of the treatment, known as BYM338, in all indications... The drug is currently being tested to treat other illnesses, and the largest share of sales will probably be from ailments such as cachexia, the weight and muscle loss that’s often found in patients with illnesses such as cancer and chronic obstructive pulmonary disease."
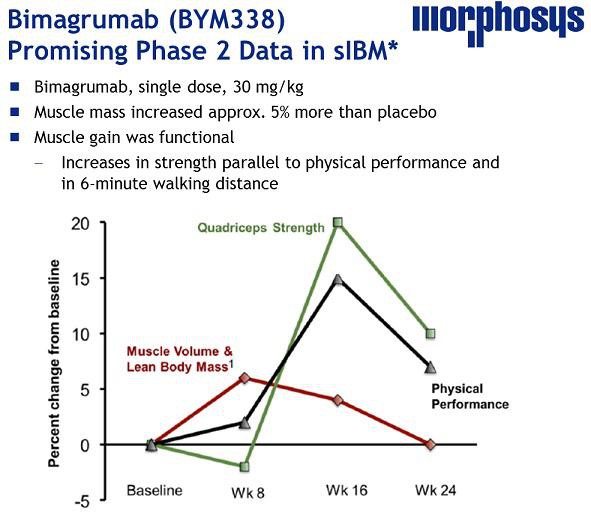
XLRN nutzt als Technologie eine Trap-Plattform... IntelliTrap. Traps binden ähnlich wie AKs das Target, nur dass es sich bei Traps um lösliche Rezeptoren handelt (wenn ich das richtig verstehe). U.a. wurde damit auch ACE-2494 optimiert, das im Gegensatz zu ACE-083 systemisch angewendet werden kann. Die vorklinischen Ergebnisse sind vielversprechend.

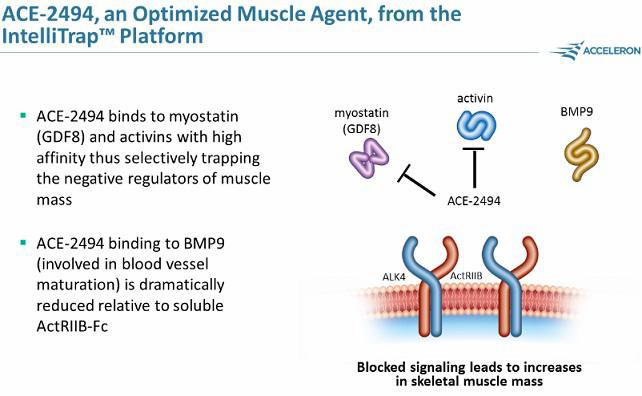
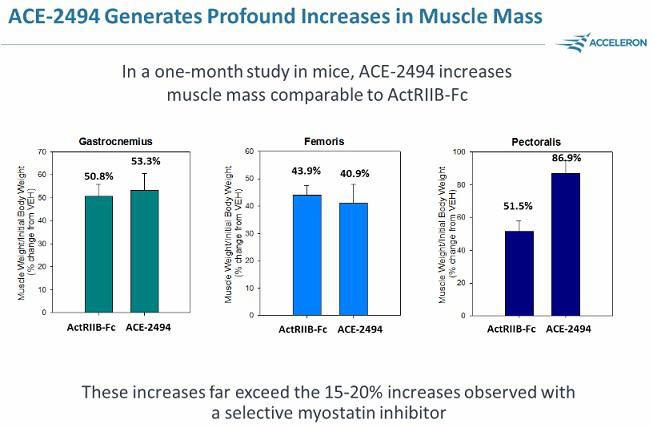
Allerdings sollte man auch erwähnen, dass XLRN mit ACE-031 bereits einmal ein ähnliches Mittel in der Pipeline hatte, das dann aufgrund von Nebenwirkungen in der PII eingestellt wurde. Risiken bestehen immer.


Gruß
ipollit
Mit Muskelerkrankungen haben XLRN einige Erfahrung, so dass sie in Zukunft in diesem Bereich eine größere Rolle spielen könnten. XLRN's Spezialgebiet ist TGF-beta... das sind Proteine, die u.a. das Wachstum von Gewebe wie Muskeln regulieren.


Neben DMD und SMA gibt es noch viele weitere seltene Muskelerkrankungen. Manche Erkrankungen betreffen alle Muskeln, andere nur bestimmte Muskelpartien. Demnach entwickelt XLRN Mittel, die lokal angewendet werden können wie ACE-083 oder Mittel, die sich systemisch auf alle Muskeln auswirken wie ACE-2494.


Am weitesten ist ACE-083, das u.a. gegen FSHD entwickelt wird. ACE-083 erhöht lokal die Muskelmasse, in die es verabreicht wird.



Zum Vergleich: Eine Erhöhung der Muskelmasse um 14% ist dabei deutlich höher als z.B. durch Bimagrumab mit nur 5%, das von NVS und Morphosys entwickelt wird. Bimagrumab hat BTD und befindet sich u.a. in einer PIII gegen sIBM (eine Form von Inclusion Body Myositis). Es soll aber auch bei diversen anderen Arten von Muskelschwund eingesetzt werden z.B. nach OPs oder infolge von Krebs. Solche Mittel sollen ein großes Umsatzpotential besitzen. So sagt NVS über Bimagrumab: "Novartis AG’s muscle-building drug bimagrumab may reach as much as $4 billion in peak sales, according to the medicine’s co-developer. The forecast is for the use of the treatment, known as BYM338, in all indications... The drug is currently being tested to treat other illnesses, and the largest share of sales will probably be from ailments such as cachexia, the weight and muscle loss that’s often found in patients with illnesses such as cancer and chronic obstructive pulmonary disease."

XLRN nutzt als Technologie eine Trap-Plattform... IntelliTrap. Traps binden ähnlich wie AKs das Target, nur dass es sich bei Traps um lösliche Rezeptoren handelt (wenn ich das richtig verstehe). U.a. wurde damit auch ACE-2494 optimiert, das im Gegensatz zu ACE-083 systemisch angewendet werden kann. Die vorklinischen Ergebnisse sind vielversprechend.



Allerdings sollte man auch erwähnen, dass XLRN mit ACE-031 bereits einmal ein ähnliches Mittel in der Pipeline hatte, das dann aufgrund von Nebenwirkungen in der PII eingestellt wurde. Risiken bestehen immer.

Gruß
ipollit
Antwort auf Beitrag Nr.: 51.148.878 von ipollit am 22.11.15 15:49:08
Hallo Ipollit,
ich bin immer wieder erstaunt, dass bei DMD in den USA kaum einer über Santhera spricht. Santhera hat für Raxone eine abgeschlossene positive PIII für DMD und plant aktuell nach zusätzlichen Auswertungen einen Antrag im 1 HJ 16 einzureichen. In Europa ist eine Zulassung in DMD über einen Erweiterungsantrag für die bereits zugelassene Indikation LHON im 1 HJ 2016 vorgesehen.
Santhera reported positive results from the double-blind, randomized, placebo-controlled Phase III study (DELOS) in 65 Duchenne boys aged between 10 and 18 years who were not using concomitant corticosteroids. The outcomes provide clear evidence of a clinical benefit for Catena®/Raxone® in delaying the loss of respiratory function in patients with DMD compared to placebo.
The DELOS trial met the primary endpoint, the difference between Catena®/Raxone® and placebo in the change from baseline to week 52 in Peak Expiratory Flow (PEF as percent predicted, PEF%p). Peak Expiratory Flow is a measure of respiratory muscle strength, the decline of which is a major contributing factor to morbidity and mortality in DMD. Hospital-based spirometry assessments demonstrated that Catena®/Raxone® significantly reduced the annual decline in PEF%p by 66% compared to patients taking placebo.
http://www.santhera.com/index.php?mid=19&vid=&lang=en
Momentan können damit 40 % der DMD-Patienten behandelt werden, unabhängig vom Mutationsstatus, für die 60 % Patienten, die mit Corticosteroiden behandelt werden, soll eine weitere PIII durchgeführt werden.
Marktkapitalisierung ist aktuell bei ca. 550 Mio. CHF.
Overview
Santhera Pharmaceuticals (SIX: SANN) is a Swiss specialty pharmaceutical company focusing on the development and marketing of innovative pharmaceutical products for the treatment of mitochondrial and neuromuscular diseases. This area of high unmet medical need includes many orphan and niche indications with no current therapy.
Santhera strategically focuses on Raxone®/Catena® (INN: idebenone). Raxone has received European Marketing Authorization for the treatment of visual impairment in adolescent and adult patients with Leber's Hereditary Optic Neuropathy (LHON).
In addition, Raxone/Catena is currently being developed in Duchenne Muscular Dystrophy (submissions for marketing application in the USA and Europe pending) and primary progressive Multiple Sclerosis (ppMS) (in Phase II).
The second compound in the clinical pipeline is omigapil for the treatment of Congenital Muscular Dystrophies.
Fipamezole is available for partnering after successfully completed Phase II development for treatment of levodopa-induced Dyskinesia in Parkinson's Disease.
http://www.santhera.com/index.php?mid=47&vid=&lang=en
Eine aktuelle Präsentation mit Pipeline findet man u.a. hier;
http://www.santhera.com/downloads/CS_Healthcare_Conference_2…
Insgesamt scheint mir DMD derzeit eine "Modeindikation" zu sein, da hier viele kleinere Pharmas zuletzt Forschungsabsichten hierzu bekannt gegeben haben, z.B:
Tarix Orphan's TXA127 Fast Track'd for DMD
Marathon Pharma begins NDA process for Duchenne candidate
FibroGen to proceed with mid-stage study of FG-3019 in DMD
Akashi Therapeutics' Duchenne MD candidate shows encouraging results in early stage study
Catabasis Pharma initiates Phase 1/2 study of DMD candidate
Capricor Therapeutics jumps on FDA OK for DMD study
http://seekingalpha.com/symbol/SPHDF
Interessant finde ich im Bereich Seltene Muskelerkrankungen auch noch die israelische BioBlast

http://bioblast-pharma.com/wp-content/uploads/2015/10/bbchar…
Noch alles im relativ frühen Stadium, aber mit interessanten Entwicklungen.
BioBlast Announces Positive Interim Results From HOPEMD Phase 2 Clinical Study of Cabaletta(R) in Oculopharyngeal Muscular Dystrophy (OPMD) Conference Call and Webcast, 8:30 a.m. Eastern Time NEW HAVEN, Conn. and TEL AVIV, Israel, Oct. 27, 2015 (GLOBE NEWSWIRE)
http://bioblast-pharma.com/bioblast-announces-positive-inter…
Markkapitalisierung liegt bei etwa 60 Mio US$.
Gruß Oberländler
Zitat von ipollit: FGEN
momentan ist DMD ein Thema... BMRN, SRPT und PTCT versuchen eine Zulassung von der FDA zu erhalten, wobei alle drei Mittel ihre Probleme haben ...
... D.h. BMRN und SPRT können erstmal nur maximal 13% der DMD behandeln, falls diese Mittel zugelassen werden. Trotzdem soll eine Zulassung sich sehr deutlich auf den Kurs dieser Unternehmen auswirken: BMRN ist ein 16 Mrd USD Unternehmen, SPRT hat aktuell eine MK von 1,5 Mrd USD (zum Vergleich hat FGEN aktuell eine MK von 1,7 Mrd USD)
Hallo Ipollit,
ich bin immer wieder erstaunt, dass bei DMD in den USA kaum einer über Santhera spricht. Santhera hat für Raxone eine abgeschlossene positive PIII für DMD und plant aktuell nach zusätzlichen Auswertungen einen Antrag im 1 HJ 16 einzureichen. In Europa ist eine Zulassung in DMD über einen Erweiterungsantrag für die bereits zugelassene Indikation LHON im 1 HJ 2016 vorgesehen.
Santhera reported positive results from the double-blind, randomized, placebo-controlled Phase III study (DELOS) in 65 Duchenne boys aged between 10 and 18 years who were not using concomitant corticosteroids. The outcomes provide clear evidence of a clinical benefit for Catena®/Raxone® in delaying the loss of respiratory function in patients with DMD compared to placebo.
The DELOS trial met the primary endpoint, the difference between Catena®/Raxone® and placebo in the change from baseline to week 52 in Peak Expiratory Flow (PEF as percent predicted, PEF%p). Peak Expiratory Flow is a measure of respiratory muscle strength, the decline of which is a major contributing factor to morbidity and mortality in DMD. Hospital-based spirometry assessments demonstrated that Catena®/Raxone® significantly reduced the annual decline in PEF%p by 66% compared to patients taking placebo.
http://www.santhera.com/index.php?mid=19&vid=&lang=en
Momentan können damit 40 % der DMD-Patienten behandelt werden, unabhängig vom Mutationsstatus, für die 60 % Patienten, die mit Corticosteroiden behandelt werden, soll eine weitere PIII durchgeführt werden.
Marktkapitalisierung ist aktuell bei ca. 550 Mio. CHF.
Overview
Santhera Pharmaceuticals (SIX: SANN) is a Swiss specialty pharmaceutical company focusing on the development and marketing of innovative pharmaceutical products for the treatment of mitochondrial and neuromuscular diseases. This area of high unmet medical need includes many orphan and niche indications with no current therapy.
Santhera strategically focuses on Raxone®/Catena® (INN: idebenone). Raxone has received European Marketing Authorization for the treatment of visual impairment in adolescent and adult patients with Leber's Hereditary Optic Neuropathy (LHON).
In addition, Raxone/Catena is currently being developed in Duchenne Muscular Dystrophy (submissions for marketing application in the USA and Europe pending) and primary progressive Multiple Sclerosis (ppMS) (in Phase II).
The second compound in the clinical pipeline is omigapil for the treatment of Congenital Muscular Dystrophies.
Fipamezole is available for partnering after successfully completed Phase II development for treatment of levodopa-induced Dyskinesia in Parkinson's Disease.
http://www.santhera.com/index.php?mid=47&vid=&lang=en
Eine aktuelle Präsentation mit Pipeline findet man u.a. hier;
http://www.santhera.com/downloads/CS_Healthcare_Conference_2…
Insgesamt scheint mir DMD derzeit eine "Modeindikation" zu sein, da hier viele kleinere Pharmas zuletzt Forschungsabsichten hierzu bekannt gegeben haben, z.B:
Tarix Orphan's TXA127 Fast Track'd for DMD
Marathon Pharma begins NDA process for Duchenne candidate
FibroGen to proceed with mid-stage study of FG-3019 in DMD
Akashi Therapeutics' Duchenne MD candidate shows encouraging results in early stage study
Catabasis Pharma initiates Phase 1/2 study of DMD candidate
Capricor Therapeutics jumps on FDA OK for DMD study
http://seekingalpha.com/symbol/SPHDF
Interessant finde ich im Bereich Seltene Muskelerkrankungen auch noch die israelische BioBlast

http://bioblast-pharma.com/wp-content/uploads/2015/10/bbchar…
Noch alles im relativ frühen Stadium, aber mit interessanten Entwicklungen.
BioBlast Announces Positive Interim Results From HOPEMD Phase 2 Clinical Study of Cabaletta(R) in Oculopharyngeal Muscular Dystrophy (OPMD) Conference Call and Webcast, 8:30 a.m. Eastern Time NEW HAVEN, Conn. and TEL AVIV, Israel, Oct. 27, 2015 (GLOBE NEWSWIRE)
http://bioblast-pharma.com/bioblast-announces-positive-inter…
Markkapitalisierung liegt bei etwa 60 Mio US$.
Gruß Oberländler
Das waren mal wieder einige interessante Beiträge!
Was ich nicht so nachvollziehen kann das Ohad immer noch die Shorts laufen hat.
Was ich nicht so nachvollziehen kann das Ohad immer noch die Shorts laufen hat.
KBIO


+10.000% in etwa einer Woche... für ein bankrottes Unternehmen... seriös ist anders

Gruß
ipollit


+10.000% in etwa einer Woche... für ein bankrottes Unternehmen... seriös ist anders
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.158.517 von ipollit am 23.11.15 22:58:13"Devastated" Trader Crushed By Soaring Biotech, Starts Online Begging Campaign To Fund $106,000 Margin Call
http://www.zerohedge.com/news/2015-11-19/devastated-trader-c…
http://www.zerohedge.com/news/2015-11-19/devastated-trader-c…
KPTI
Die Aktie arbeitet sich langsam wieder nach oben... aktuelle MK 678 Mio USD bei 195 Mio USD Cash.
Im August war die Aktie ja deutlich gefallen, weil bei der AML-Studie einige Sepsis-Fälle aufgetreten sind, worauf KPTI die Dosis in der laufenden Studie reduziert hat. Wenn ich es richtig verstehe, war dies aber nur eine Vorsichtsmaßnahme des Managements, da die niedrigere Dosis verträglicher ist und trotzdem eine ähnliche Wirkung zeigt. Laut KPTI ist Sepsis bei AML nicht unüblich und der Unterschied zwischen dem Selinexor und Placebo-Arm kann auch durch eine inhomogene Patientengruppe erklärt werden.




Derweil macht die Selinexor-Pipeline Fortschritte... zur ASH-Konferenz nächstes Wochenende sollten neue Daten kommen.


Die Anzahl der laufenden Studien mit Selinexor spricht für sich. Wahrscheinlich wird es auch Fehlschläge geben, trotzdem kann man hoffen, dass das eine oder andere funktioniert. Ein Schwerpunkt bilden wohl Kombi-Therapien in MM.
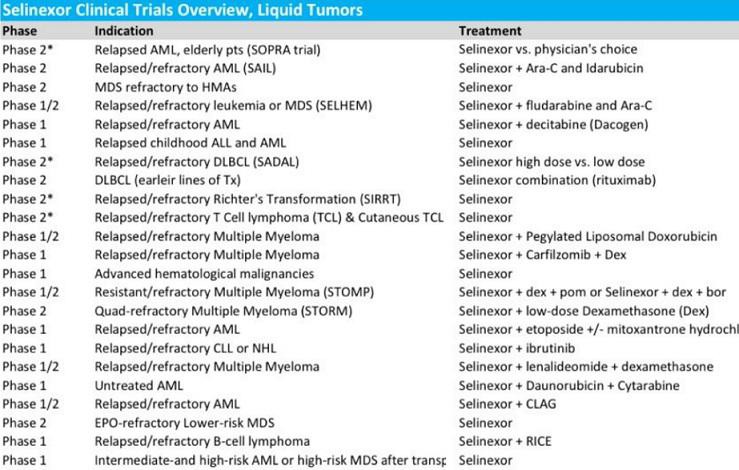
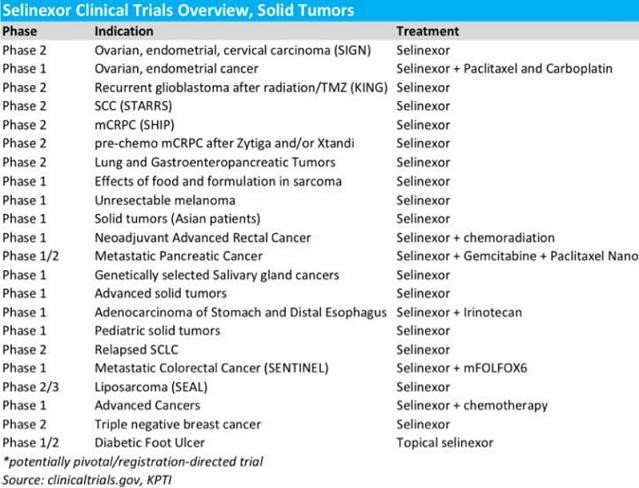
Demnächst wird KPTI auch den PAK4-Hemmer in die Klinik bringen, den Ohad Hammer einmal positiv hervorgehoben hat. Zudem wird es mit KPT-8602 ein Backup zu Selinexor geben, der mehr reversibel an XPO1 bindet (STML hat wohl auch so etwas in der Pipeline) und weniger ins Gehirn gelangt, was eine bessere Dosierung mit höherer Wirkung und weniger Nebenwirkungen erlaubt.


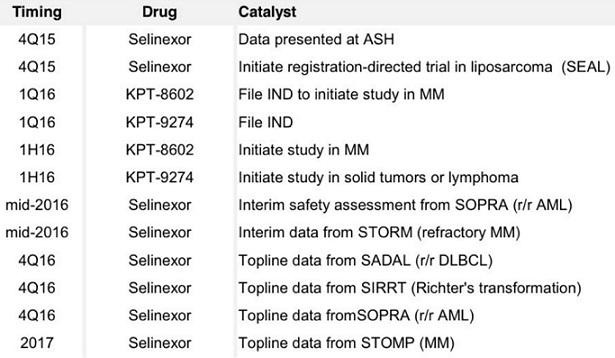

Gruß
ipollit
Die Aktie arbeitet sich langsam wieder nach oben... aktuelle MK 678 Mio USD bei 195 Mio USD Cash.
Im August war die Aktie ja deutlich gefallen, weil bei der AML-Studie einige Sepsis-Fälle aufgetreten sind, worauf KPTI die Dosis in der laufenden Studie reduziert hat. Wenn ich es richtig verstehe, war dies aber nur eine Vorsichtsmaßnahme des Managements, da die niedrigere Dosis verträglicher ist und trotzdem eine ähnliche Wirkung zeigt. Laut KPTI ist Sepsis bei AML nicht unüblich und der Unterschied zwischen dem Selinexor und Placebo-Arm kann auch durch eine inhomogene Patientengruppe erklärt werden.




Derweil macht die Selinexor-Pipeline Fortschritte... zur ASH-Konferenz nächstes Wochenende sollten neue Daten kommen.


Die Anzahl der laufenden Studien mit Selinexor spricht für sich. Wahrscheinlich wird es auch Fehlschläge geben, trotzdem kann man hoffen, dass das eine oder andere funktioniert. Ein Schwerpunkt bilden wohl Kombi-Therapien in MM.


Demnächst wird KPTI auch den PAK4-Hemmer in die Klinik bringen, den Ohad Hammer einmal positiv hervorgehoben hat. Zudem wird es mit KPT-8602 ein Backup zu Selinexor geben, der mehr reversibel an XPO1 bindet (STML hat wohl auch so etwas in der Pipeline) und weniger ins Gehirn gelangt, was eine bessere Dosierung mit höherer Wirkung und weniger Nebenwirkungen erlaubt.



Gruß
ipollit
danke für die Info, das ist übrigens zur Zeit meine erfolgreichste Biotech-Aktie, durch die ich durch dieses Forum aufmerksam geworden bin.
Antwort auf Beitrag Nr.: 51.196.230 von ipollit am 28.11.15 12:44:05Hallo ipollit,
bei KPTI habe ich leider versäumt nachzukaufen. Mal sehen was da auf der ASH jetzt noch kommt. Völlig untergegangen sind die ersten (?) Ergebnisse der PII von Filanesib + Kyprolis. Tja, das Geld hätte ARRY wohl besser mal in andere Programme gesteckt...
https://ash.confex.com/ash/2015/webprogram/Paper86432.html
Hier noch ein paar Links - wahrscheinlich den meisten schon bekannt aber trotzdem:
CLVS
Bullthese
https://www.hvst.com/posts/54724-clovis-oncology-crisis-crea…
Bärthese
https://www.hvst.com/posts/54808-clovis-oncology-clvs-execut…
Ich denke beide haben ihre Berechtigung und würde mich da irgendwo in der Mitte einsortieren, weil Stand jetzt beides möglich erscheint.
ZFGN
http://www.xconomy.com/boston/2015/11/23/after-a-clinical-tr…
So sieht gutes Krisenmanagemant aus. Wenngleich ich es für unwahrscheinlich halte, dass die Herz-Kreislaufevents nichts mit B. zu tun haben.
IBB

Ich betreibe ja nur "Charttechnik für Dummies". Vor allem die 50 und 200 Tageslinie sind da von Bedeutung. Wie man sieht hat der IBB auch mehrfach an der 50 Tageslinie gedreht. Mal sehen, ob jetzt die 200 Tageslinie gleich im ersten Anlauf genommen werden kann?
SG kmastra
bei KPTI habe ich leider versäumt nachzukaufen. Mal sehen was da auf der ASH jetzt noch kommt. Völlig untergegangen sind die ersten (?) Ergebnisse der PII von Filanesib + Kyprolis. Tja, das Geld hätte ARRY wohl besser mal in andere Programme gesteckt...
https://ash.confex.com/ash/2015/webprogram/Paper86432.html
Hier noch ein paar Links - wahrscheinlich den meisten schon bekannt aber trotzdem:
CLVS
Bullthese
https://www.hvst.com/posts/54724-clovis-oncology-crisis-crea…
Bärthese
https://www.hvst.com/posts/54808-clovis-oncology-clvs-execut…
Ich denke beide haben ihre Berechtigung und würde mich da irgendwo in der Mitte einsortieren, weil Stand jetzt beides möglich erscheint.
ZFGN
http://www.xconomy.com/boston/2015/11/23/after-a-clinical-tr…
So sieht gutes Krisenmanagemant aus. Wenngleich ich es für unwahrscheinlich halte, dass die Herz-Kreislaufevents nichts mit B. zu tun haben.
IBB
Ich betreibe ja nur "Charttechnik für Dummies". Vor allem die 50 und 200 Tageslinie sind da von Bedeutung. Wie man sieht hat der IBB auch mehrfach an der 50 Tageslinie gedreht. Mal sehen, ob jetzt die 200 Tageslinie gleich im ersten Anlauf genommen werden kann?
SG kmastra
RLYP
Nachdem der Kurs von RLYP mit der Zulassung von Veltassa abgestürzt ist und ZSPH für 2,7 Mrd USD von AZN übernommen wurde, scheint sich nun die Stimmung etwas zu Gunsten von RLYP zu drehen. RLYP kommt aktuell auf etwa 1 Mrd USD MK bei 287 Mio USD Cash.
Offensichtlich gab es 6 Interessenten an ZSPH... davon waren wohl 2 bereit ernstere Gebote abzugeben, neben AZN wahrscheinlich Actelion. D.h. nicht nur AZN ist an diesem Markt interessiert.

Veltassa's Konkurrent ZS-9 könnte Probleme mit Schwellungen und Bluthochdruck bekommen, beides Nebenwirkungen, die schlecht für Nieren- und Herz-Patienten sind, der eigentliche Markt für Kalium-Senker. Wassersammlungen an Organen und ein höherer Blutdruck verschlechtern die Nieren- und Herzfunktionen zusätzlich. Ursache ist wahrscheinlich, dass ZS-9 ein Salz ist, das vom Körper aufgenommen wird. Dagegen gibt es Indizien, dass Veltassa neben der Kalium-Senkung auch den Blutdruck senkt... das wäre ein großer Vorteil.


Offensichtlich hat ZSPH in der Zulassungsstudie die Grenze für Bluthochdruck ungewöhnlich hoch angesetzt. Mit niedrigeren Grenzen dürfte diese Nebenwirkung höher sein, als bisher von ZSPH veröffentlicht. Auch der Anteil an Schwellungen wird bei längeren Studien wahrscheinlich zunehmen. Gleichzeitig dürfte die BlackBox-Warnung von Veltassa mit der Zeit abgemildert werden, wenn die Wechselwirkungs-Studien vorliegen. Die Zeit spielt also für RLYP.

Heutzutage führen hohe Kalium-Werte dazu, dass die Dosis der Nieren- und Herz-Medikamenten reduziert werden muss. Dies könnte man mit einem Kalium-Senker verhindern.

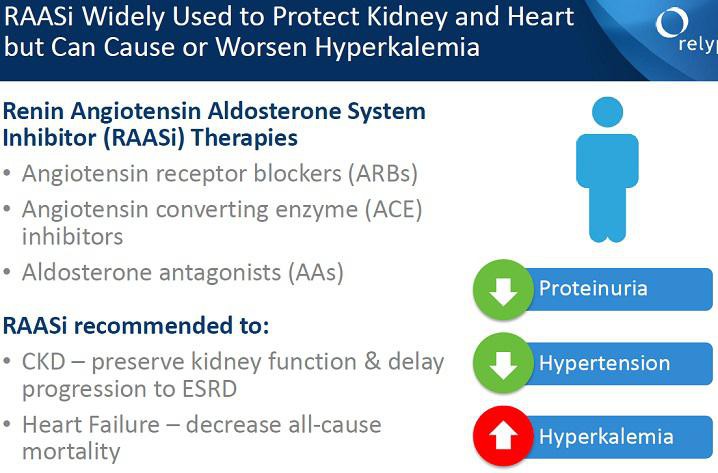
Alleine in den USA haben 3 Mio Nieren- und Herzpatienten dauerhaft Probleme mit hohen Kalium-Werten. In Zukunft werden es eher mehr als weniger Patienten sein.
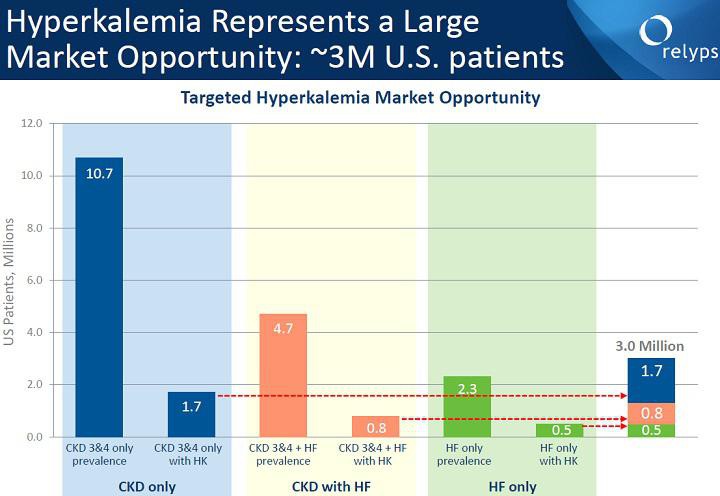
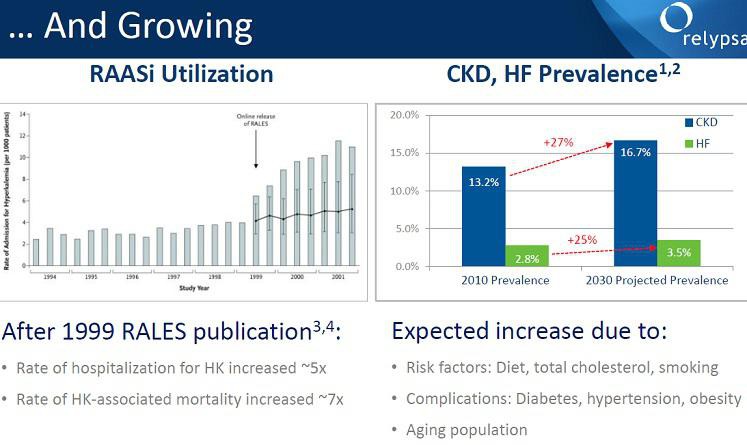
3 Mio Patienten... bei 595 USD pro Monat, d.h. mehr als 7000 USD pro Jahr wäre dies theoretisch ein 21 Mrd USD Markt alleine in den USA. Natürlich werden nicht alle Patienten mit Veltassa behandelt, doch dürfte Veltassa alleine in den USA schon Blockbuster-Potential (> 1 Mrd USD) besitzen.

"Relypsa hopes to launch sales of once-a-day Veltassa, which will cost $595 for a 30-day supply of single-use packets, by the first week of January."

Gruß
ipollit
Nachdem der Kurs von RLYP mit der Zulassung von Veltassa abgestürzt ist und ZSPH für 2,7 Mrd USD von AZN übernommen wurde, scheint sich nun die Stimmung etwas zu Gunsten von RLYP zu drehen. RLYP kommt aktuell auf etwa 1 Mrd USD MK bei 287 Mio USD Cash.
Offensichtlich gab es 6 Interessenten an ZSPH... davon waren wohl 2 bereit ernstere Gebote abzugeben, neben AZN wahrscheinlich Actelion. D.h. nicht nur AZN ist an diesem Markt interessiert.

Veltassa's Konkurrent ZS-9 könnte Probleme mit Schwellungen und Bluthochdruck bekommen, beides Nebenwirkungen, die schlecht für Nieren- und Herz-Patienten sind, der eigentliche Markt für Kalium-Senker. Wassersammlungen an Organen und ein höherer Blutdruck verschlechtern die Nieren- und Herzfunktionen zusätzlich. Ursache ist wahrscheinlich, dass ZS-9 ein Salz ist, das vom Körper aufgenommen wird. Dagegen gibt es Indizien, dass Veltassa neben der Kalium-Senkung auch den Blutdruck senkt... das wäre ein großer Vorteil.


Offensichtlich hat ZSPH in der Zulassungsstudie die Grenze für Bluthochdruck ungewöhnlich hoch angesetzt. Mit niedrigeren Grenzen dürfte diese Nebenwirkung höher sein, als bisher von ZSPH veröffentlicht. Auch der Anteil an Schwellungen wird bei längeren Studien wahrscheinlich zunehmen. Gleichzeitig dürfte die BlackBox-Warnung von Veltassa mit der Zeit abgemildert werden, wenn die Wechselwirkungs-Studien vorliegen. Die Zeit spielt also für RLYP.

Heutzutage führen hohe Kalium-Werte dazu, dass die Dosis der Nieren- und Herz-Medikamenten reduziert werden muss. Dies könnte man mit einem Kalium-Senker verhindern.


Alleine in den USA haben 3 Mio Nieren- und Herzpatienten dauerhaft Probleme mit hohen Kalium-Werten. In Zukunft werden es eher mehr als weniger Patienten sein.


3 Mio Patienten... bei 595 USD pro Monat, d.h. mehr als 7000 USD pro Jahr wäre dies theoretisch ein 21 Mrd USD Markt alleine in den USA. Natürlich werden nicht alle Patienten mit Veltassa behandelt, doch dürfte Veltassa alleine in den USA schon Blockbuster-Potential (> 1 Mrd USD) besitzen.

"Relypsa hopes to launch sales of once-a-day Veltassa, which will cost $595 for a 30-day supply of single-use packets, by the first week of January."
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.197.925 von kmastra am 28.11.15 21:25:27@CLVS
Morgen soll die FDA ja was zum weiteren Verfahren sagen...habt Ihr nach dem Kursdesaster verkauft oder wartet Ihr zumindest das morgige Ergebnis noch ab?
Morgen soll die FDA ja was zum weiteren Verfahren sagen...habt Ihr nach dem Kursdesaster verkauft oder wartet Ihr zumindest das morgige Ergebnis noch ab?
Antwort auf Beitrag Nr.: 51.201.318 von lawmeetstax am 29.11.15 23:14:30CLVS... bisher habe ich meine Position nicht reduziert, ich warte erstmal ab. Tendenziell würde ich persönlich aus heutiger Sicht eher zukaufen als verkaufen, wobei meine Position momentan nur 2,5% meines Depots ausmacht. Muss aber letztlich jeder selber wissen, wie man z.B. das Verhalten des Management beurteilt.
Gruß
ipollit
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.201.318 von lawmeetstax am 29.11.15 23:14:30Ich hatte bei CLVS zugekauft und habe jetzt aber auch schon wieder entsprechend verkauft, weil mir das Risiko heute einfach zu groß ist. Zudem hat das auch steuerliche Gründe. Nach dem firts in first out Prinzip konnte ich so zumindest kurzfristig einen Teil der Verluste vom Vater Staat zurückholen.
Meine Kernposition halte ich auf jeden Fall bis zur ASCO. Bei schlechten Nachrichten und starken Kursverlusten würde ich meine Position wieder vergrößern. Das muss natürlich aber jeder für sich entscheiden... SG kmastra
Meine Kernposition halte ich auf jeden Fall bis zur ASCO. Bei schlechten Nachrichten und starken Kursverlusten würde ich meine Position wieder vergrößern. Das muss natürlich aber jeder für sich entscheiden... SG kmastra
Antwort auf Beitrag Nr.: 51.148.854 von kmastra am 22.11.15 15:46:18Somit war alles Negative auf dem Tisch und eingepreist. Zudem hat man einen Plan zur Wiederaufnahme der Studien verkündet und man wird tatsächlich die Teilnehmer regelmäßig screenen, um Thrombosen etc. rechzeitig zu entdecken. Denkbar wären auch zusätzliche präventive Maßnahmen z.B. Blutverdünner, Physiotherapie etc.
Grundsätzlich ist ZFGN aber weiterhin extrem riskant, denn wenn jetzt trotz Screening nochmal was passiert...!
Leider ist es passiert. Es ist erneut ein Teilehmer der Studie verstorben. Ich denke das war es dann wohl mit B. Man sollte die Studie abbrechen. Wirklich Schade!
http://finance.yahoo.com/news/zafgen-provides-clinical-belor…
Grundsätzlich ist ZFGN aber weiterhin extrem riskant, denn wenn jetzt trotz Screening nochmal was passiert...!
Leider ist es passiert. Es ist erneut ein Teilehmer der Studie verstorben. Ich denke das war es dann wohl mit B. Man sollte die Studie abbrechen. Wirklich Schade!
http://finance.yahoo.com/news/zafgen-provides-clinical-belor…
Antwort auf Beitrag Nr.: 51.221.835 von kmastra am 02.12.15 12:41:18Ich bin raus mit knapp -50% und hier
http://bioblast-pharma.com/
rein
http://bioblast-pharma.com/
rein
Antwort auf Beitrag Nr.: 51.198.258 von ipollit am 29.11.15 00:53:47gerade durch den Ticker
Kreise: Relypsa erwägt einen Verkauf.

Kreise: Relypsa erwägt einen Verkauf.

FGEN
die mögliche US/EU-Zulassung von Roxadustat wird zwar noch einige Zeit dauern, doch der Antrag in China soll schon nächstes Jahr gestellt werden... d.h. erste PIII-Daten müssten etwa Mitte nächsten Jahres vorliegen. AZN hat Roxa bereits auf seiner Liste...

FG-3019 ist der zweite spannende Pipeline-Kandidat... er könnte gleich ein mehrfacher Blockbuster werden.


Gruß
ipollit
die mögliche US/EU-Zulassung von Roxadustat wird zwar noch einige Zeit dauern, doch der Antrag in China soll schon nächstes Jahr gestellt werden... d.h. erste PIII-Daten müssten etwa Mitte nächsten Jahres vorliegen. AZN hat Roxa bereits auf seiner Liste...

FG-3019 ist der zweite spannende Pipeline-Kandidat... er könnte gleich ein mehrfacher Blockbuster werden.

Gruß
ipollit
Verkauf an wen?
Gibt es irgendein Angebot?
Gibt es irgendein Angebot?
Antwort auf Beitrag Nr.: 51.228.237 von xylophon am 02.12.15 23:17:06RLYP: Heute kommen wieder Gerüchte auf. Angeblich ist Merck interessiert.
http://www.streetinsider.com/Hot+M+and+A/Merck+%28MRK%29+Sai…
Der Markt scheint daran zu glauben.
Zudem gab es eine Umfrage unter Ärzten, die das Marktpotenzial von Veltassa gegenüber ZS-9 recht positiv erscheinen lässt.

Hab zwar keine Position, aber das könnte der Markt grad ganz gut gebrauchen...
SG kmastra
http://www.streetinsider.com/Hot+M+and+A/Merck+%28MRK%29+Sai…
Der Markt scheint daran zu glauben.
Zudem gab es eine Umfrage unter Ärzten, die das Marktpotenzial von Veltassa gegenüber ZS-9 recht positiv erscheinen lässt.

Hab zwar keine Position, aber das könnte der Markt grad ganz gut gebrauchen...
SG kmastra
Antwort auf Beitrag Nr.: 51.244.506 von kmastra am 04.12.15 18:10:43
ich hab 'ne Position und ich könnte das grad auch ganz gut gebrauchen.
Zitat von kmastra: RLYP: Heute kommen wieder Gerüchte auf. Angeblich ist Merck interessiert.
http://www.streetinsider.com/Hot+M+and+A/Merck+%28MRK%29+Sai…
Der Markt scheint daran zu glauben.
Zudem gab es eine Umfrage unter Ärzten, die das Marktpotenzial von Veltassa gegenüber ZS-9 recht positiv erscheinen lässt.
![]()
Hab zwar keine Position, aber das könnte der Markt grad ganz gut gebrauchen...
SG kmastra
ich hab 'ne Position und ich könnte das grad auch ganz gut gebrauchen.
RLYP
eine Übernahme zu diesem Zeitpunkt kann ich mir nicht so recht vorstellen. Meiner Meinung nach ist RLYP doch ganz gut aufgestellt. Europa ist auslizensiert, in den USA hat man einen ziemlich guten Vermarktungspartner, die Vertriebsmannschaft ist bereits aktiv... warum sollen sie gerade jetzt verkaufen? Vielleicht, wenn ein sehr gutes Angebot kommt, aber ansonsten gewinnen sie doch nichts. Ob z.B. Sanofi oder Merck Veltassa vertreibt, spielt keine Rolle... vielleicht ist Sanofi in diesem Fall noch besser. In der nächsten Zeit bestehen eher Risiken für den Konkurrent ZS-9 und Chancen für ein besseres Label und Zusatznutzen für Veltassa... mit der Zeit sollte also der Preis für eine Übernahme eher steigen.

Zum Vergleich der aktuelle US-Partner:
- größte Vertriebsmannschaft gegen Herz- und Nierenerkrankungen (der Zielmarkt) in den USA
- vermarktet Kayexalate, das vor Veltassa einzige Mittel gegen Hyperkalemia
- vermarktet erfolgreich den führenden Posphat-Binder Renagal (Veltassa ist als Kalium-Binder ähnlich)
- RLYP besitzt noch 100% der US-Rechte


Gruß
ipollit
eine Übernahme zu diesem Zeitpunkt kann ich mir nicht so recht vorstellen. Meiner Meinung nach ist RLYP doch ganz gut aufgestellt. Europa ist auslizensiert, in den USA hat man einen ziemlich guten Vermarktungspartner, die Vertriebsmannschaft ist bereits aktiv... warum sollen sie gerade jetzt verkaufen? Vielleicht, wenn ein sehr gutes Angebot kommt, aber ansonsten gewinnen sie doch nichts. Ob z.B. Sanofi oder Merck Veltassa vertreibt, spielt keine Rolle... vielleicht ist Sanofi in diesem Fall noch besser. In der nächsten Zeit bestehen eher Risiken für den Konkurrent ZS-9 und Chancen für ein besseres Label und Zusatznutzen für Veltassa... mit der Zeit sollte also der Preis für eine Übernahme eher steigen.

Zum Vergleich der aktuelle US-Partner:
- größte Vertriebsmannschaft gegen Herz- und Nierenerkrankungen (der Zielmarkt) in den USA
- vermarktet Kayexalate, das vor Veltassa einzige Mittel gegen Hyperkalemia
- vermarktet erfolgreich den führenden Posphat-Binder Renagal (Veltassa ist als Kalium-Binder ähnlich)
- RLYP besitzt noch 100% der US-Rechte


Gruß
ipollit
RLYP
Hier auch noch ein ausführlicher Kommentar eines Investierten zu RLYP:




Gruß
ipollit
Hier auch noch ein ausführlicher Kommentar eines Investierten zu RLYP:




Gruß
ipollit
XENE
Unter Ohad Hammers Kommentaren findet sich ein Hinweis, dass Nav1.7-Hemmer vielleicht nicht so wirken, wie gedacht: http://www.nature.com/ncomms/2015/151204/ncomms9967/full/nco…
Menschen, die aufgrund einer Mutation kein Nav1.7 bilden, können keine Schmerzen spüren. Daraus hat man abgeleitet, dass die Hemmung von Nav1.7 das Schmerzempfinden hemmt. Soweit ich es verstehe, zeigen aber nun Experimente, dass das Fehlen von Nav1.7 nur dazu führt, dass mehr natürliche Opiate im Körper vorhanden sind. So führte ein Opiat-Blocker bei einer Person, die aufgrund von Nav1.7 ein Leben lang keine Schmerzen empfinden konnte, dazu, dass sie wieder Schmerzen empfinden konnte. D.h., es kommt auf auf die Kombi von Nav1.7 mit Opiaten an.
http://www.heilpraxisnet.de/naturheilpraxis/nie-mehr-ruecken…
"... Schmerzen werden an das Gehirn als elektrische Signale, entlang der Nervenzellenmembranen übertragen. Diese bezeichnen Wissenschaftler auch als Kanäle. Die UCL Forscher fanden heraus, dass Menschen ohne Nav1.7 mehr Opioidpeptide produzieren. Nach den Studien, an genetisch veränderten Mäusen, gaben die Mediziner einer 39 Jahre alten Frau Naloxon. Die Testperson war an der seltenen genetischen Mutation erkrankt. Das eingesetzte Medikament sei ein Opioid-Blocker und nach der Einnahme, konnte die Frau zum ersten Mal in ihrem Leben Schmerzen fühlen, erklärten die Mediziner vom UCL.
Die letzten zehn Jahre seien die Arzneimittelstudien zu diesem Thema eher enttäuschend gewesen. Die aktuellen Untersuchungen hätten jetzt bestätigt, dass Nav1.7 wirklich ein Schlüsselelement für den menschlichen Schmerz sei, erklärte der Forscher Professor John Wood. Die fehlende Zutat für ein „Super-Schmerzmittel“ seien gute altmodische Opioidpeptide gewesen. Die Wissenschaftler hätten nun ein Patent für die Kombination von einer niedrigen Dosis Opioide mit einem Nav1.7 Blocker, fügte der Mediziner hinzu. Durch diese Kombination soll die Schmerzlosigkeit von Menschen mit der seltenen Mutation repliziert werden. Der Ansatz sei in Versuchen mit nicht modifizierten Mäusen bereits erfolgreich getestet worden, sagte Professor Wood. ...
In der Partnerschaft von XENE mit TEVA gab es bereits einen Fehlschlag von TV-45070 gegen Schmerzen bei Knie-Arthrose. TV-45070 wird dabei nur lokal als Salbe verabreicht. Könnte es sein, dass die Patienten in deiser Studie keine Opiate erhalten haben? Eine Kombi mit anderen Schmerzmitteln macht die Beurteilung der Ergebnisse ja eher schwieriger, so dass man wahrscheinlich darauf verzichtet hat. Vielleicht würde eine eine Kombi von TV-45070 mit einem sehr niedrig dosierten Opiat dagegen sehr wirksam sein?

TV-45070 wird nun noch in PHN getestet. Laut XENE soll Nav1.7 in PHN (Nervenschäden infolge einer Gürtelrose) erhöht sein. Vielleicht hemmt das ja die natürlichen Opiate und somit könnte u.U. ein Nav1.7-Hemmer auch in Mono-Therapie wirken?
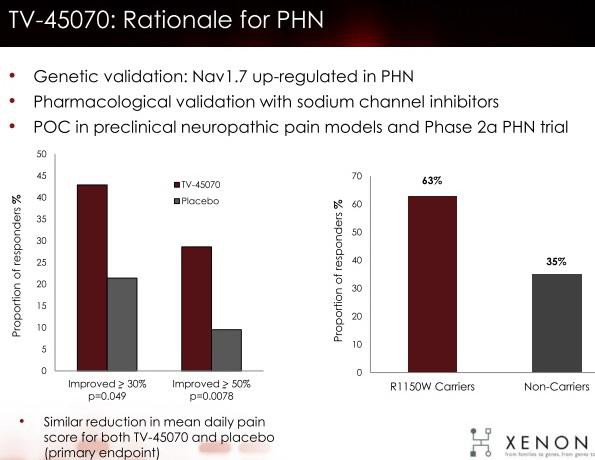

Eine systemische Verabreichung von Nav1.7-Hemmern wird zusammen mit Roche entwickelt. Hier müsste wahrscheinlich mittelfristig eine Kombi mit Opiaten getestet werden, um überhaupt erfolgreich sein zu können.

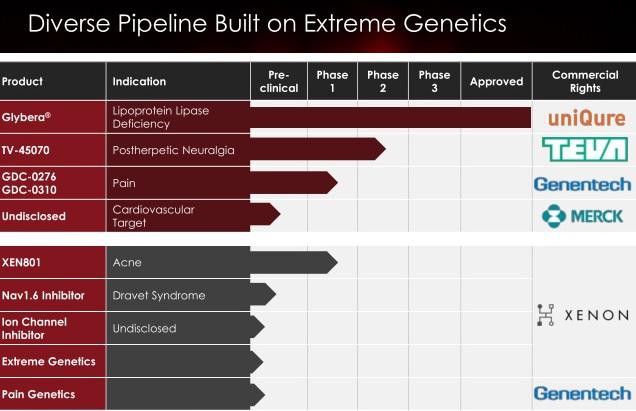

Gruß
ipollit
Unter Ohad Hammers Kommentaren findet sich ein Hinweis, dass Nav1.7-Hemmer vielleicht nicht so wirken, wie gedacht: http://www.nature.com/ncomms/2015/151204/ncomms9967/full/nco…
Menschen, die aufgrund einer Mutation kein Nav1.7 bilden, können keine Schmerzen spüren. Daraus hat man abgeleitet, dass die Hemmung von Nav1.7 das Schmerzempfinden hemmt. Soweit ich es verstehe, zeigen aber nun Experimente, dass das Fehlen von Nav1.7 nur dazu führt, dass mehr natürliche Opiate im Körper vorhanden sind. So führte ein Opiat-Blocker bei einer Person, die aufgrund von Nav1.7 ein Leben lang keine Schmerzen empfinden konnte, dazu, dass sie wieder Schmerzen empfinden konnte. D.h., es kommt auf auf die Kombi von Nav1.7 mit Opiaten an.
http://www.heilpraxisnet.de/naturheilpraxis/nie-mehr-ruecken…
"... Schmerzen werden an das Gehirn als elektrische Signale, entlang der Nervenzellenmembranen übertragen. Diese bezeichnen Wissenschaftler auch als Kanäle. Die UCL Forscher fanden heraus, dass Menschen ohne Nav1.7 mehr Opioidpeptide produzieren. Nach den Studien, an genetisch veränderten Mäusen, gaben die Mediziner einer 39 Jahre alten Frau Naloxon. Die Testperson war an der seltenen genetischen Mutation erkrankt. Das eingesetzte Medikament sei ein Opioid-Blocker und nach der Einnahme, konnte die Frau zum ersten Mal in ihrem Leben Schmerzen fühlen, erklärten die Mediziner vom UCL.
Die letzten zehn Jahre seien die Arzneimittelstudien zu diesem Thema eher enttäuschend gewesen. Die aktuellen Untersuchungen hätten jetzt bestätigt, dass Nav1.7 wirklich ein Schlüsselelement für den menschlichen Schmerz sei, erklärte der Forscher Professor John Wood. Die fehlende Zutat für ein „Super-Schmerzmittel“ seien gute altmodische Opioidpeptide gewesen. Die Wissenschaftler hätten nun ein Patent für die Kombination von einer niedrigen Dosis Opioide mit einem Nav1.7 Blocker, fügte der Mediziner hinzu. Durch diese Kombination soll die Schmerzlosigkeit von Menschen mit der seltenen Mutation repliziert werden. Der Ansatz sei in Versuchen mit nicht modifizierten Mäusen bereits erfolgreich getestet worden, sagte Professor Wood. ...
In der Partnerschaft von XENE mit TEVA gab es bereits einen Fehlschlag von TV-45070 gegen Schmerzen bei Knie-Arthrose. TV-45070 wird dabei nur lokal als Salbe verabreicht. Könnte es sein, dass die Patienten in deiser Studie keine Opiate erhalten haben? Eine Kombi mit anderen Schmerzmitteln macht die Beurteilung der Ergebnisse ja eher schwieriger, so dass man wahrscheinlich darauf verzichtet hat. Vielleicht würde eine eine Kombi von TV-45070 mit einem sehr niedrig dosierten Opiat dagegen sehr wirksam sein?

TV-45070 wird nun noch in PHN getestet. Laut XENE soll Nav1.7 in PHN (Nervenschäden infolge einer Gürtelrose) erhöht sein. Vielleicht hemmt das ja die natürlichen Opiate und somit könnte u.U. ein Nav1.7-Hemmer auch in Mono-Therapie wirken?


Eine systemische Verabreichung von Nav1.7-Hemmern wird zusammen mit Roche entwickelt. Hier müsste wahrscheinlich mittelfristig eine Kombi mit Opiaten getestet werden, um überhaupt erfolgreich sein zu können.


Gruß
ipollit
RLYP
Angeblich sollen mehrere Unternehmen an RLYP Interesse haben...
http://www.bidnessetc.com/58734-who-will-acquire-relypsa-mer…
"Relypsa Inc. soared more than 30% in trade yesterday after rumors emerged that the small biotech might soon court an acquirer. Some time before noon, the Street Insider reported from a source “claiming to have direct knowledge of the situation”, that Merck & Co., Inc. (NYSE:MRK) was planning to extend a non-binding takeover offer to the company.
Soon after, the Financial Times ran a slightly different story. Reporting from sources, it said Relypsa was itself preparing for a sale, and drug-makers like GlaxoSmithKline plc (ADR) (NYSE:GSK), Sanofi SA and Switzerland’s Galenica might be possible bidders. ...
http://www.benzinga.com/analyst-ratings/analyst-color/15/12/…
"RLYP shares are up more than 16 percent on Friday afternoon after unconfirmed reports that Merck & Co., Inc. could make a bid for the $1.07 billion bio therapeutic company. A source familiar with the matter told Benzinga Merck is not involved with a bid, but that three to four companies are evaluating Relypsa.
The evaluation process is in its early stages and no developments are expected until at least 2016, according to the source.
Relypsa investor relations and a Merck spokesperson have declined comment on the market rumors.
Sanofi Seen As 'Natural Buyer'
In a conversation with Benzinga, Wedbush analyst Liana Moussatos said Sanofi SA (ADR) is a "natural buyer" of Relypsa. In August of this year, Relypsa entered into a two-year detailing and distribution agreement with Sanofi for its hyperkalemia treatment, Veltassa, which received FDA approval in late October.
Veltassa is expected to be available to doctors and patients in January 2016 and is the first new treatment for Hyperkalemia in over 50 years.
Billion-Dollar Potential
In a note published shortly after the drug gained FDA approval, Moussatos said she expected Veltassa to have a successful launch to start the New Year, eventually resulting in peak annual sales of more than $1 billion in the US alone. The analyst projected MAA submission would be made in the first half of 2016, followed by a potential launch in the European Union by the middle of 2017.
Moussatos' projections show the drug could reach more than 3 million U.S. patients facing moderate to severe hyperkalemia and over 13 million suffering from a milder case of the condition.
Moussatos holds a $75 12-month price target on Relypsa. Shares currently trade near the $26 mark.
Amid Friday's market gyrations, Stifel released an intra-day note discussing Relypsa's potential takeout value. Analysts there project peak Veltassa U.S. sales of $1.1 billion, translating to a "ZSPH-like" $3.3 billion valuation -- approximately $75 per share."
***
Bei 3 Mio Patienten alleine in den USA plus 13 Mio mit einer milderen Form sind 1+ Mrd USD Peak Sales doch eher moderat. Immerhin kostet die Behandlung pro Jahr etwa 7000 USD, oder?
Gruß
ipollit
Angeblich sollen mehrere Unternehmen an RLYP Interesse haben...
http://www.bidnessetc.com/58734-who-will-acquire-relypsa-mer…
"Relypsa Inc. soared more than 30% in trade yesterday after rumors emerged that the small biotech might soon court an acquirer. Some time before noon, the Street Insider reported from a source “claiming to have direct knowledge of the situation”, that Merck & Co., Inc. (NYSE:MRK) was planning to extend a non-binding takeover offer to the company.
Soon after, the Financial Times ran a slightly different story. Reporting from sources, it said Relypsa was itself preparing for a sale, and drug-makers like GlaxoSmithKline plc (ADR) (NYSE:GSK), Sanofi SA and Switzerland’s Galenica might be possible bidders. ...
http://www.benzinga.com/analyst-ratings/analyst-color/15/12/…
"RLYP shares are up more than 16 percent on Friday afternoon after unconfirmed reports that Merck & Co., Inc. could make a bid for the $1.07 billion bio therapeutic company. A source familiar with the matter told Benzinga Merck is not involved with a bid, but that three to four companies are evaluating Relypsa.
The evaluation process is in its early stages and no developments are expected until at least 2016, according to the source.
Relypsa investor relations and a Merck spokesperson have declined comment on the market rumors.
Sanofi Seen As 'Natural Buyer'
In a conversation with Benzinga, Wedbush analyst Liana Moussatos said Sanofi SA (ADR) is a "natural buyer" of Relypsa. In August of this year, Relypsa entered into a two-year detailing and distribution agreement with Sanofi for its hyperkalemia treatment, Veltassa, which received FDA approval in late October.
Veltassa is expected to be available to doctors and patients in January 2016 and is the first new treatment for Hyperkalemia in over 50 years.
Billion-Dollar Potential
In a note published shortly after the drug gained FDA approval, Moussatos said she expected Veltassa to have a successful launch to start the New Year, eventually resulting in peak annual sales of more than $1 billion in the US alone. The analyst projected MAA submission would be made in the first half of 2016, followed by a potential launch in the European Union by the middle of 2017.
Moussatos' projections show the drug could reach more than 3 million U.S. patients facing moderate to severe hyperkalemia and over 13 million suffering from a milder case of the condition.
Moussatos holds a $75 12-month price target on Relypsa. Shares currently trade near the $26 mark.
Amid Friday's market gyrations, Stifel released an intra-day note discussing Relypsa's potential takeout value. Analysts there project peak Veltassa U.S. sales of $1.1 billion, translating to a "ZSPH-like" $3.3 billion valuation -- approximately $75 per share."
***
Bei 3 Mio Patienten alleine in den USA plus 13 Mio mit einer milderen Form sind 1+ Mrd USD Peak Sales doch eher moderat. Immerhin kostet die Behandlung pro Jahr etwa 7000 USD, oder?
Gruß
ipollit
XLRN
Partner CELG hat auf der ASH gute Ergebnisse für Luspatercept in MDS präsentiert. Luspatercept wird gegen Blutarmut eingesetzt. Anders als EPO&Co, die die frühe Entwicklung von roten Blutkörperchen fördern, stimuliert Luspatercept die spätere Reifung der Blutkörperchen. Bei MDS ist genau diese spätere Entwicklungsstufe der Blutkörperchen gestört, so dass ESAs wie EPO nur sehr bedingt helfen. MDS Patienten müssen somit regelmäßig Bluttransfusionen erhalten.
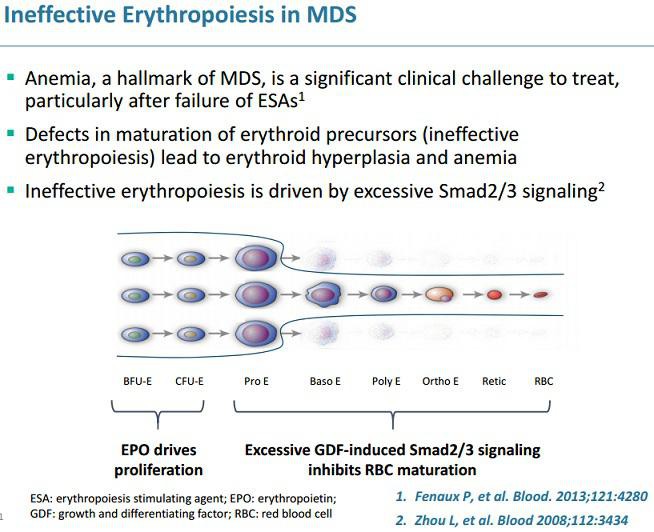
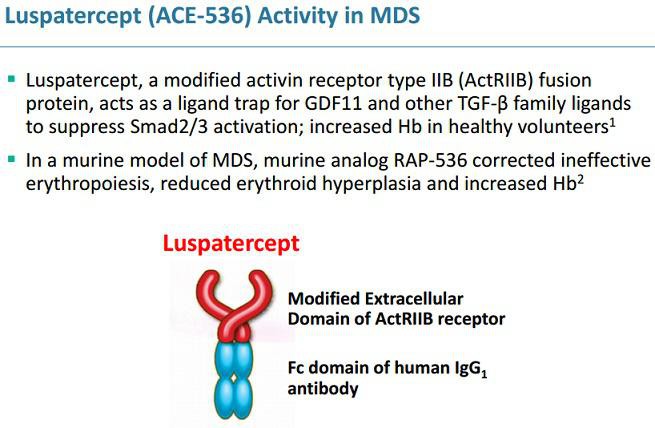
Die heutigen ASH-Ergebnisse scheinen positiv zu sein. Es gibt eine deutliche Reduzierung der Bluttransfusionen... 42% der Patienten mit regelmäßigen Transfusionen kommen nun ohne aus.
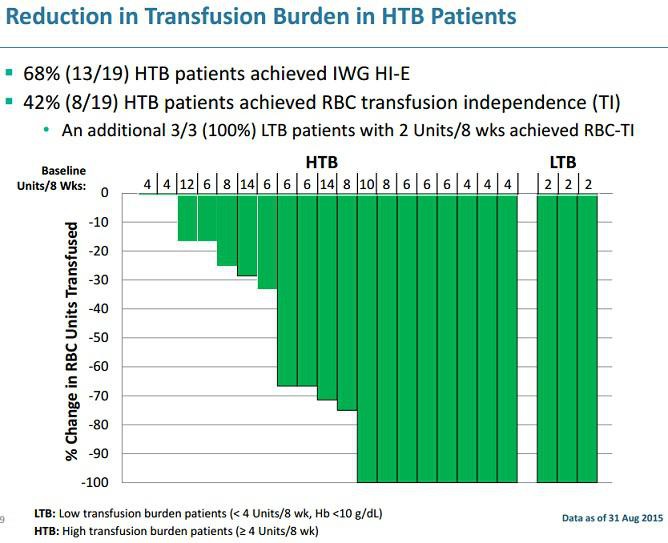
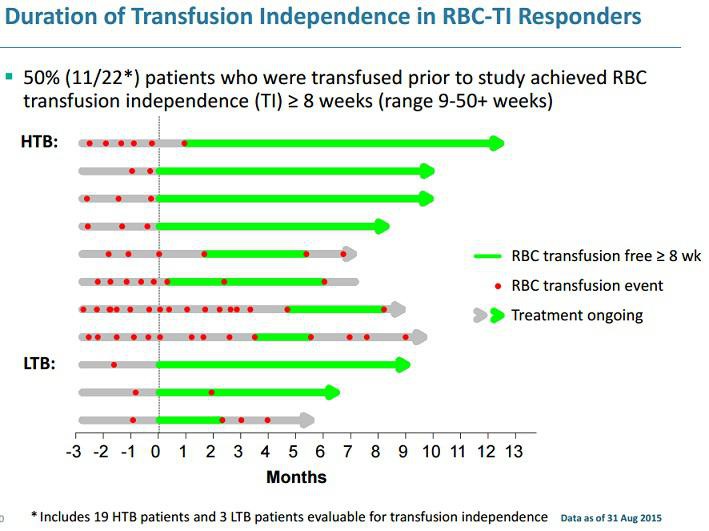
In Beta-Thalassemia besitzt Luspatercept den gleichen Wirkmechanismus. Hier gibt es als Konkurrent u.a. BLUE mit einer Gentherapie. Zumindest die heutigen Daten von BLUE in Sichelzellenanämie sollen etwas enttäuscht haben, so dass die Gentherpaie vielleicht nicht in jedem Fall funktioniert und Luspatercept auch in dieser Indikation seinen Markt findet.
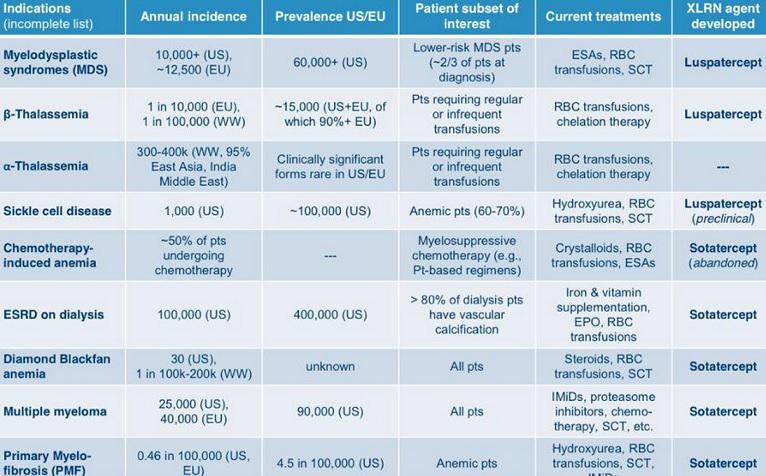


Gruß
ipollit
Partner CELG hat auf der ASH gute Ergebnisse für Luspatercept in MDS präsentiert. Luspatercept wird gegen Blutarmut eingesetzt. Anders als EPO&Co, die die frühe Entwicklung von roten Blutkörperchen fördern, stimuliert Luspatercept die spätere Reifung der Blutkörperchen. Bei MDS ist genau diese spätere Entwicklungsstufe der Blutkörperchen gestört, so dass ESAs wie EPO nur sehr bedingt helfen. MDS Patienten müssen somit regelmäßig Bluttransfusionen erhalten.


Die heutigen ASH-Ergebnisse scheinen positiv zu sein. Es gibt eine deutliche Reduzierung der Bluttransfusionen... 42% der Patienten mit regelmäßigen Transfusionen kommen nun ohne aus.


In Beta-Thalassemia besitzt Luspatercept den gleichen Wirkmechanismus. Hier gibt es als Konkurrent u.a. BLUE mit einer Gentherapie. Zumindest die heutigen Daten von BLUE in Sichelzellenanämie sollen etwas enttäuscht haben, so dass die Gentherpaie vielleicht nicht in jedem Fall funktioniert und Luspatercept auch in dieser Indikation seinen Markt findet.


Gruß
ipollit
die Ergebnisse von Bluebirg kamen wohl nicht so gut an....
http://www.wallstreet-online.de/nachricht/8182023-bluebird-b…
Kursverlust 30 %
http://www.wallstreet-online.de/nachricht/8182023-bluebird-b…
Kursverlust 30 %
Antwort auf Beitrag Nr.: 51.250.593 von ipollit am 06.12.15 13:02:58D.h., es kommt auf auf die Kombi von Nav1.7 mit Opiaten an.
Sehr interessant! Momentan bin ich im Bereich Schmerzmedikamente mit XENE, TRVN und DEPO dabei.
Opiate stehen ja schon länger in der Kritik, weil sie abhängig machen und auch starke Nebenwirkungen haben. Ein funktionierendes Medikament gegen Schmerzen ohne diese unerwünschten Nebenwirkungen wird gemeinhin als "heiliger Grahl" betrachtet. Wenn ich den Beitrag von ipollit richtig nachvollziehe, wäre es evtl. möglich Opiate in Kombination mit Nav1.7 so gering zu dosieren, dass dann die Nebenwirkungen entsprechend geringer ausfallen dürften. Auch im bereich der Opiate gibt es ja Entwicklungen, wenngleich keine Entwicklungssprünge. Meist sind die Medikamente dann länger wirksam, weniger leicht zum Drogenkonsum zu missbrauchen und/oder haben geringere Nebenwirkungen. Ohad Hammer bringt ja bereits als möglichen Kandidaten zur Kombination TRVN ins Spiel...
Aber auch Depomed finde ich als "Story" insgesamt recht gut.
DEPO hat bereits 5 Produkte auf dem Markt und ist somit eher ein kleines Pharmaunternehmen. Besonders mit der Aquisition von Nucynta von Janssen hat man einen großen Ergebnissprung gemacht.

Man hat seitdem das Verkaufsteam vergrößert und anders als Janssen genießt Nucynta bei Depomed höchste Priorität. Seit der Übernahme konnten die Verschreibungen deutlich ausgebaut werden. Zudem hat Depomed den Preis um 44% erhöht (das finde ich nicht so toll aber im Rahmen)

Insgesamt scheint mir die Bewertung bei den Wachstumsraten recht günstig. Momentan wird Depomed mit ca. 1 Milliarde bewertet, wobei man Cash (175 Mio) und Schulden (800 Mio) berücksichtigen muss.
Depomed hat zuletzt die Guidance erhöht und vorher auch übertroffen. Man geht nun z.B. davon aus, dass man mit Nucynta bereits 2018 500 Mio umsetzen wird (vorher 2020)!
http://www.prnewswire.com/news-releases/depomed-reports-reco…
http://www.bionapcfa.com/2015/11/depomed-is-cheap-by-almost-…
SG kmastra
Sehr interessant! Momentan bin ich im Bereich Schmerzmedikamente mit XENE, TRVN und DEPO dabei.
Opiate stehen ja schon länger in der Kritik, weil sie abhängig machen und auch starke Nebenwirkungen haben. Ein funktionierendes Medikament gegen Schmerzen ohne diese unerwünschten Nebenwirkungen wird gemeinhin als "heiliger Grahl" betrachtet. Wenn ich den Beitrag von ipollit richtig nachvollziehe, wäre es evtl. möglich Opiate in Kombination mit Nav1.7 so gering zu dosieren, dass dann die Nebenwirkungen entsprechend geringer ausfallen dürften. Auch im bereich der Opiate gibt es ja Entwicklungen, wenngleich keine Entwicklungssprünge. Meist sind die Medikamente dann länger wirksam, weniger leicht zum Drogenkonsum zu missbrauchen und/oder haben geringere Nebenwirkungen. Ohad Hammer bringt ja bereits als möglichen Kandidaten zur Kombination TRVN ins Spiel...
Aber auch Depomed finde ich als "Story" insgesamt recht gut.
DEPO hat bereits 5 Produkte auf dem Markt und ist somit eher ein kleines Pharmaunternehmen. Besonders mit der Aquisition von Nucynta von Janssen hat man einen großen Ergebnissprung gemacht.

Man hat seitdem das Verkaufsteam vergrößert und anders als Janssen genießt Nucynta bei Depomed höchste Priorität. Seit der Übernahme konnten die Verschreibungen deutlich ausgebaut werden. Zudem hat Depomed den Preis um 44% erhöht (das finde ich nicht so toll aber im Rahmen)


Insgesamt scheint mir die Bewertung bei den Wachstumsraten recht günstig. Momentan wird Depomed mit ca. 1 Milliarde bewertet, wobei man Cash (175 Mio) und Schulden (800 Mio) berücksichtigen muss.
Depomed hat zuletzt die Guidance erhöht und vorher auch übertroffen. Man geht nun z.B. davon aus, dass man mit Nucynta bereits 2018 500 Mio umsetzen wird (vorher 2020)!
http://www.prnewswire.com/news-releases/depomed-reports-reco…
http://www.bionapcfa.com/2015/11/depomed-is-cheap-by-almost-…
SG kmastra
ONTY
ONTY gab gerade ein Update zu ONT380:
http://finance.yahoo.com/news/oncothyreon-announces-data-ont…
Ich hab das jetzt mehrmals gelesen und verstehe es immer noch nicht so ganz. Der Markt versteht es auch nicht und reagiert mit Panik und verkaufen. Die Erwartungen waren da jetzt wohl sehr hoch. Aktuell fällt ONTY über 30%!
Insgesamt erinnert mich das an ein schlecht vorbereitetes Referat. Warum hat man überhaupt jetzt eine PR mit CC gegeben, wenn man die Poster erst am Fr. zeigen wird?
Es hat auch einen Grund, dass die Daten dort (hoffentlich) aufgearbeitet dargestellt werden. Mit Grafiken und Tabellen und so. Ich denke es ist keine gute Idee da einen Fließtext draus zu machen.
Insgesamt ist weniger manchmal auch mehr. Warum hat man z.B. den Schwerpunkt nicht mehr auf die patienten gelegt, die mit Herceptin und Xeloda +380 behandelt wurden (was die PII werden soll).
Was mich enttäuscht ist zudem, dass überhaupt keine Angaben dazu gemacht wurden, wie nachhaltig das Ansprechen denn ist. Und das ist doch das worauf man jetzt wartet (und was auch angekündigt war-meine ich!?). Auf Nachfrage verweist man dann im CC auf die Poster am Freitag...
Hat jemand eine Meinung dazu?
Momentan denke ich eigentlich, dass die Marktreaktion übertrieben ist, weil die Ansprechraten im Grunde ähnlich sind wie vorher und die Daten dann hoffentlich in der Posterpräsentation auch nachvollziehbarer werden. Zudem scheint man sich sehr bemüht zu haben, die Ansprechraten nach RECIST darzustellen, was aber in dem Fall auch sehr verwirrend ist:
Best responses were measured using RECIST 1.1 criteria in 48 evaluable patients. In 34 patients with measurable disease, a best response of a confirmed partial response (cPR) was seen in 14 (41%), stable disease (SD) in 15 (44%) and progressive disease (PD) in 5 (15%). Fourteen patients had non-target lesions, primarily bone metastases, none of whom had a best response of PD (all were non-CR/non-PD by RECIST 1.1). The CBR, defined as patients with a complete response (CR), a cPR, or either SD or non-CR/non-PD for at least 6 months, was 59% (23/39). Patients active on study at the time of the analysis with SD for less than six months were excluded from the calculation of CBR.

Verstehe ich das jetzt richtig, dass die 14 Patienten zwar eine PR hatten aber neue Metastasen woanders hinzu kamen und deshalb quasi rausfallen?
Abschlussworte des CEO im CC: "we realize that we have presented you a lot of numers and a complicated dataset today but we emphasize that we are encouraged...."
Kurze Umfrage über Twitter:

Verwirrte Grüße kmastra
ONTY gab gerade ein Update zu ONT380:
http://finance.yahoo.com/news/oncothyreon-announces-data-ont…
Ich hab das jetzt mehrmals gelesen und verstehe es immer noch nicht so ganz. Der Markt versteht es auch nicht und reagiert mit Panik und verkaufen. Die Erwartungen waren da jetzt wohl sehr hoch. Aktuell fällt ONTY über 30%!
Insgesamt erinnert mich das an ein schlecht vorbereitetes Referat. Warum hat man überhaupt jetzt eine PR mit CC gegeben, wenn man die Poster erst am Fr. zeigen wird?
Es hat auch einen Grund, dass die Daten dort (hoffentlich) aufgearbeitet dargestellt werden. Mit Grafiken und Tabellen und so. Ich denke es ist keine gute Idee da einen Fließtext draus zu machen.
Insgesamt ist weniger manchmal auch mehr. Warum hat man z.B. den Schwerpunkt nicht mehr auf die patienten gelegt, die mit Herceptin und Xeloda +380 behandelt wurden (was die PII werden soll).
Was mich enttäuscht ist zudem, dass überhaupt keine Angaben dazu gemacht wurden, wie nachhaltig das Ansprechen denn ist. Und das ist doch das worauf man jetzt wartet (und was auch angekündigt war-meine ich!?). Auf Nachfrage verweist man dann im CC auf die Poster am Freitag...

Hat jemand eine Meinung dazu?
Momentan denke ich eigentlich, dass die Marktreaktion übertrieben ist, weil die Ansprechraten im Grunde ähnlich sind wie vorher und die Daten dann hoffentlich in der Posterpräsentation auch nachvollziehbarer werden. Zudem scheint man sich sehr bemüht zu haben, die Ansprechraten nach RECIST darzustellen, was aber in dem Fall auch sehr verwirrend ist:
Best responses were measured using RECIST 1.1 criteria in 48 evaluable patients. In 34 patients with measurable disease, a best response of a confirmed partial response (cPR) was seen in 14 (41%), stable disease (SD) in 15 (44%) and progressive disease (PD) in 5 (15%). Fourteen patients had non-target lesions, primarily bone metastases, none of whom had a best response of PD (all were non-CR/non-PD by RECIST 1.1). The CBR, defined as patients with a complete response (CR), a cPR, or either SD or non-CR/non-PD for at least 6 months, was 59% (23/39). Patients active on study at the time of the analysis with SD for less than six months were excluded from the calculation of CBR.

Verstehe ich das jetzt richtig, dass die 14 Patienten zwar eine PR hatten aber neue Metastasen woanders hinzu kamen und deshalb quasi rausfallen?
Abschlussworte des CEO im CC: "we realize that we have presented you a lot of numers and a complicated dataset today but we emphasize that we are encouraged...."
Kurze Umfrage über Twitter:

Verwirrte Grüße kmastra
Antwort auf Beitrag Nr.: 51.267.582 von kmastra am 09.12.15 00:14:57ONTY
Man hat Schadensbegrenzung betrieben und später noch die Poster hochgeladen. Das ist dann gleich verständlicher und man kann auch Ansätze davon sehen, wie lange Patienten ansprechen.
http://www.oncothyreon.com/pdfs/ont-380/ONT-380-004_SABCS_Fi…
http://www.oncothyreon.com/pdfs/ont-380/ONT-380-CNS_SABCS_Fi…
Zudem melden sich heute einige Analysten:
Jefferies analyst Biren Amin reiterated a Buy rating and $5 price target on Oncothyreon (NASDAQ: ONTY), which is down 21% following a confusing call and press release.
Amin commented, "ONTY issued a press release and held a conference that confused many investors regarding the data but ultimately clarified the situation by providing full ONT-380 data to be presented Friday at SABCS. ONTY presented updated data in 12 evaluable pts with metastatic breast cancer and CNS metastasis and reported a 33% ORR in combination w/ Kadcyla. ONTY also plans to initiate a PIIb combo trial with Herceptin and Xeloda and will initiate by YE '15."
http://www.streetinsider.com/Analyst+Comments/Oncothyreon+%2…
Fazit: Schlechtes Management/PR - gute Ergebnisse.
Besser als umgekehrt...
SG kmastra
Man hat Schadensbegrenzung betrieben und später noch die Poster hochgeladen. Das ist dann gleich verständlicher und man kann auch Ansätze davon sehen, wie lange Patienten ansprechen.
http://www.oncothyreon.com/pdfs/ont-380/ONT-380-004_SABCS_Fi…
http://www.oncothyreon.com/pdfs/ont-380/ONT-380-CNS_SABCS_Fi…
Zudem melden sich heute einige Analysten:
Jefferies analyst Biren Amin reiterated a Buy rating and $5 price target on Oncothyreon (NASDAQ: ONTY), which is down 21% following a confusing call and press release.
Amin commented, "ONTY issued a press release and held a conference that confused many investors regarding the data but ultimately clarified the situation by providing full ONT-380 data to be presented Friday at SABCS. ONTY presented updated data in 12 evaluable pts with metastatic breast cancer and CNS metastasis and reported a 33% ORR in combination w/ Kadcyla. ONTY also plans to initiate a PIIb combo trial with Herceptin and Xeloda and will initiate by YE '15."
http://www.streetinsider.com/Analyst+Comments/Oncothyreon+%2…
Fazit: Schlechtes Management/PR - gute Ergebnisse.
Besser als umgekehrt...
SG kmastra
FPRX, OMED
Sowohl FPRX als auch OMED finde ich im IO-Bereich interessant. FPRX besitzt eine umfangreiche Protein-Bibliothek mit Screening-Technologien, die es erlauben, neue IO-Kandidaten zu finden.
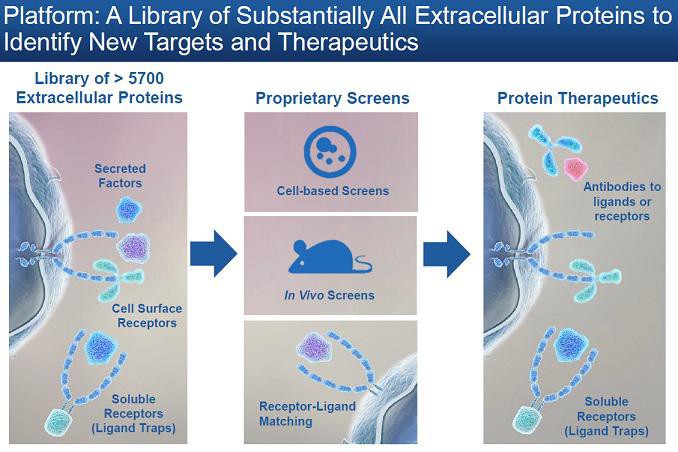
Mögliche IO-Proteine werden bewertet, in wie weit sie Krebs fördern oder unterdrücken. Proteine, die Krebs fördern, sind Checkpoint-Hemmer Kandidaten wie z.B. PD1. Die Proteine, die Krebs hemmen, sind Kandidaten zur Stimmulation des Immunsystems. Laut FPRX befindet sich in der linken Box der aktiviernden Proteine auch GITR.
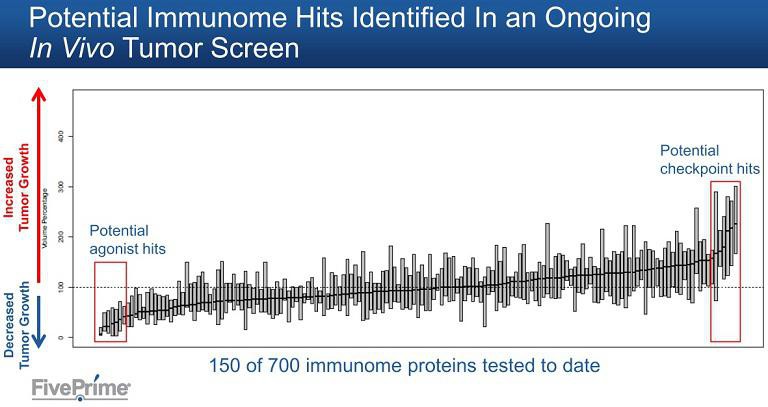
Dies hat FPRX veranlasst, einen GITR-Kandidaten von Inhibrx einzulizensieren. Wichtig ist hierbei der Hinweis, dass es sich um einen multivalenten AK handelt, der mehrfach an GITR binden kann. Wenn ich es richtig verstehe, wird der IND aber erst 2017 sein.

OMED hat seinerseits auch erkannt, dass GITR interessant ist und für eine gute Stimulation der T-Zellen mehrfach gebunden werden muss. Bei normalen AKs funktioniert das nur, wenn nicht nur einzelne AKs binden, sondern noch der fc-Teil der AKs von weiteren AKs gebunden wird, d.h. durch Clustern von AKs. OMED vewendet statt eines normalen AKs einen GITR-Ligand, der natürlicherweise dreifach an GITR bindet. Laut OMED und FPRX sind die aktivierenden IO-Rezeptoren Trimere, die immer dreifach aktiviert werden müssen, um ein starkes Signal zu erzeugen.
Der Ligand wird mit einem stabilisierenden Fc-Teil verbunden. Diese Konstruktion stimuliert deutlich stärker als normale GITR-AKs, die bei Konkurrenten in der Entwicklung sind. Ich weiß z.B. nicht, ob der INCY/AGEN GITR-AK in der Präklinik ebenfalls clustert... falls nicht, wäre er demnach nur ein schwacher Stimulator.
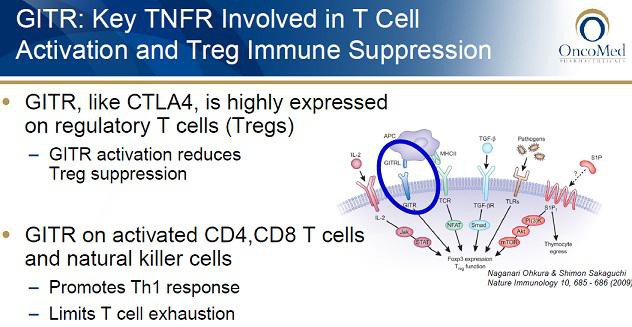
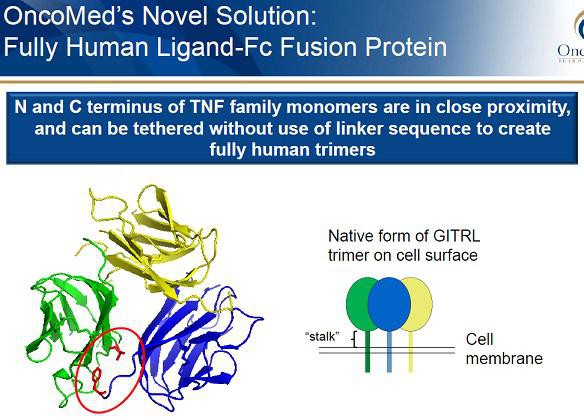
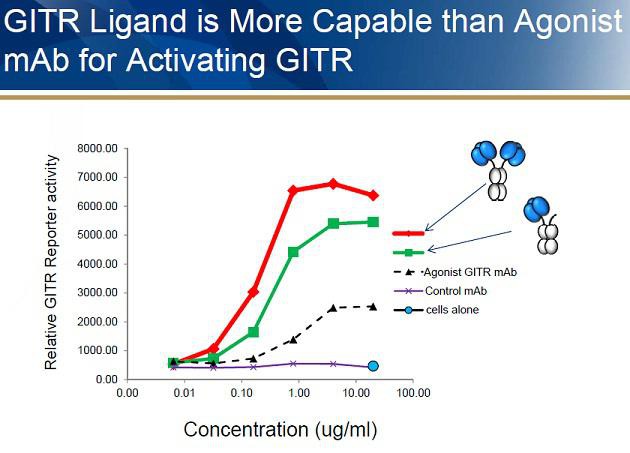
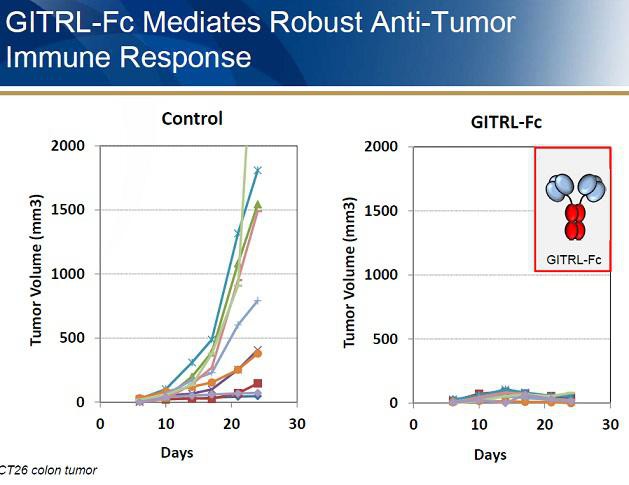
Der IND soll bereits im kommenden Jahr sein:
"Presented new data for GITRL-Fc showing potent single-agent anti-tumor activity and activity in combination with checkpoint inhibitors at the Inaugural International Cancer Immunotherapy Conference in September. OncoMed is advancing GITRL-Fc into IND-enabling studies with the goal of ultimately filing an Investigational New Drug (IND) application with the U.S. Food and Drug Administration.
Advanced preclinical testing of an immuno-oncology antibody under the collaboration with Celgene with goal of achieving formal designation as a clinical development candidate in the collaboration by the end of 2015 followed by an IND filing in 2016.
OncoMed is actively advancing GITRL-Fc with a goal of filing an Investigational New Drug (IND) application in 2016."
OMED hat auch weitere IO-Kandidaten, u.a. mit CELG. Oben ist von einem weiteren IND nächstes Jahr die Rede... dies könnte vielleicht ein Target sein, das auch intensiv von DNA entwickelt wird:
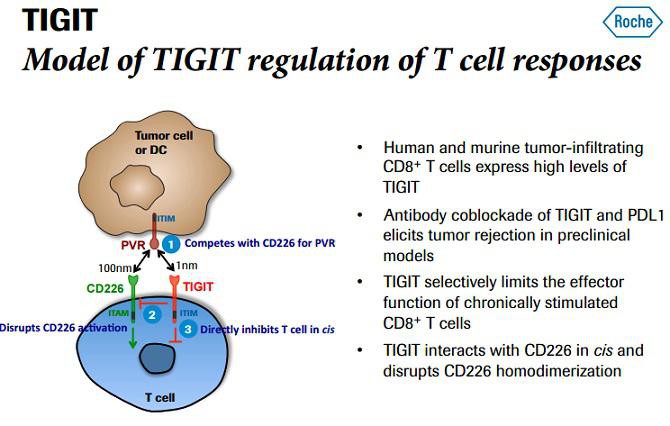
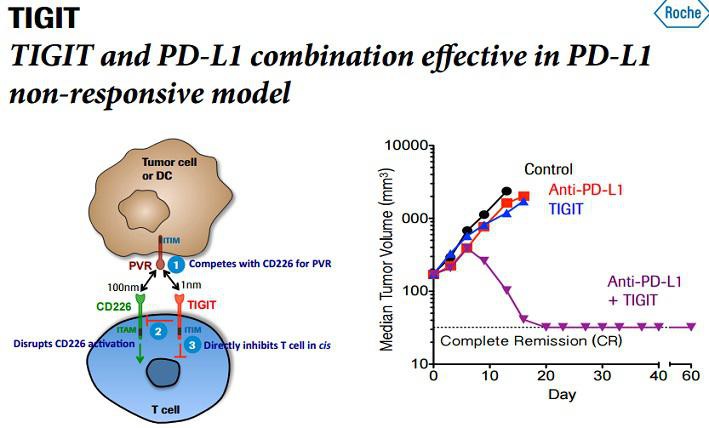
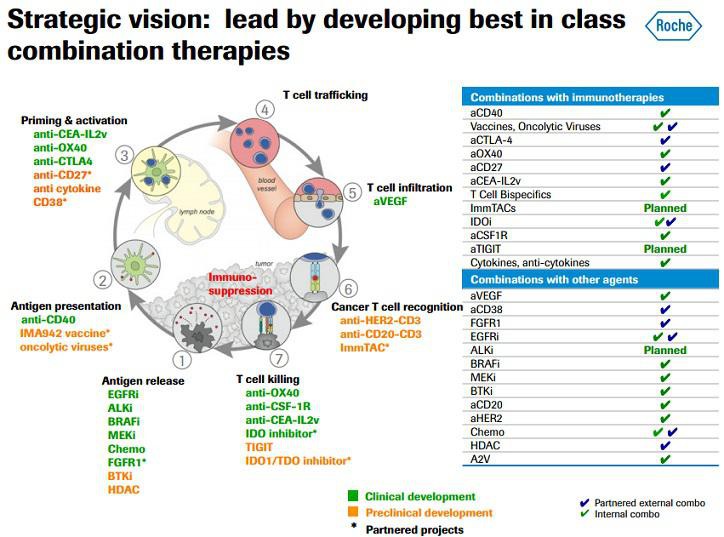
Theoretisch könnte OMED demnach nächstes Jahr zwei spannende IO-Kandidaten in der klinischen Entwicklung haben.


Gruß
ipollit
Sowohl FPRX als auch OMED finde ich im IO-Bereich interessant. FPRX besitzt eine umfangreiche Protein-Bibliothek mit Screening-Technologien, die es erlauben, neue IO-Kandidaten zu finden.

Mögliche IO-Proteine werden bewertet, in wie weit sie Krebs fördern oder unterdrücken. Proteine, die Krebs fördern, sind Checkpoint-Hemmer Kandidaten wie z.B. PD1. Die Proteine, die Krebs hemmen, sind Kandidaten zur Stimmulation des Immunsystems. Laut FPRX befindet sich in der linken Box der aktiviernden Proteine auch GITR.

Dies hat FPRX veranlasst, einen GITR-Kandidaten von Inhibrx einzulizensieren. Wichtig ist hierbei der Hinweis, dass es sich um einen multivalenten AK handelt, der mehrfach an GITR binden kann. Wenn ich es richtig verstehe, wird der IND aber erst 2017 sein.

OMED hat seinerseits auch erkannt, dass GITR interessant ist und für eine gute Stimulation der T-Zellen mehrfach gebunden werden muss. Bei normalen AKs funktioniert das nur, wenn nicht nur einzelne AKs binden, sondern noch der fc-Teil der AKs von weiteren AKs gebunden wird, d.h. durch Clustern von AKs. OMED vewendet statt eines normalen AKs einen GITR-Ligand, der natürlicherweise dreifach an GITR bindet. Laut OMED und FPRX sind die aktivierenden IO-Rezeptoren Trimere, die immer dreifach aktiviert werden müssen, um ein starkes Signal zu erzeugen.
Der Ligand wird mit einem stabilisierenden Fc-Teil verbunden. Diese Konstruktion stimuliert deutlich stärker als normale GITR-AKs, die bei Konkurrenten in der Entwicklung sind. Ich weiß z.B. nicht, ob der INCY/AGEN GITR-AK in der Präklinik ebenfalls clustert... falls nicht, wäre er demnach nur ein schwacher Stimulator.




Der IND soll bereits im kommenden Jahr sein:
"Presented new data for GITRL-Fc showing potent single-agent anti-tumor activity and activity in combination with checkpoint inhibitors at the Inaugural International Cancer Immunotherapy Conference in September. OncoMed is advancing GITRL-Fc into IND-enabling studies with the goal of ultimately filing an Investigational New Drug (IND) application with the U.S. Food and Drug Administration.
Advanced preclinical testing of an immuno-oncology antibody under the collaboration with Celgene with goal of achieving formal designation as a clinical development candidate in the collaboration by the end of 2015 followed by an IND filing in 2016.
OncoMed is actively advancing GITRL-Fc with a goal of filing an Investigational New Drug (IND) application in 2016."
OMED hat auch weitere IO-Kandidaten, u.a. mit CELG. Oben ist von einem weiteren IND nächstes Jahr die Rede... dies könnte vielleicht ein Target sein, das auch intensiv von DNA entwickelt wird:



Theoretisch könnte OMED demnach nächstes Jahr zwei spannende IO-Kandidaten in der klinischen Entwicklung haben.
Gruß
ipollit
TSRO, MGNX
Weitere IO-Programme, die in absehbarer Zeit in die Klinik gehen, kommen von TSRO und MGNX.
Für TSRO's TIM3-AK TSR-022 ist ein IND in 2Q16 geplant. Damit sind sie bei diesem Target wahrscheinlich mit führend. Der LAG3-AK soll Ende 2016 den IND haben. Letztlich ist es aber das Ziel von TSRO biAKs zu entwickeln, d.h. PD1xTIM3 oder PD1xLAG3... diese könnten 2017 in die Klinik gehen.
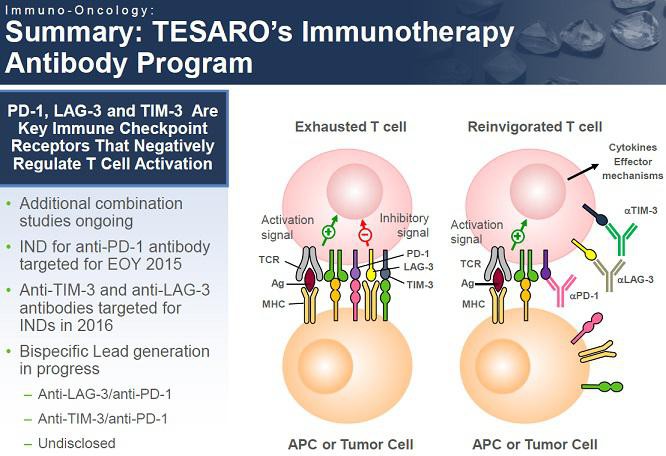
Gegen LAG3 entwickelt MGNX nun auch DARTs. MDG013 ist ein PD1xLAG3 DART, der 1H17 seinen IND haben soll.

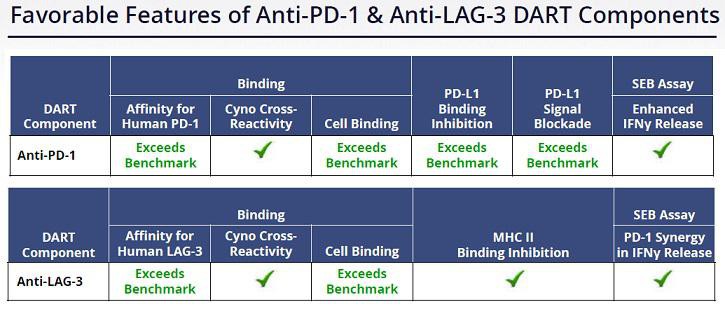
Der DART soll wirksamer sein als eine AK-Kombi PD1 + LAG3 aus zwei einzelnen AKs wie Nivo + BMS25F7.
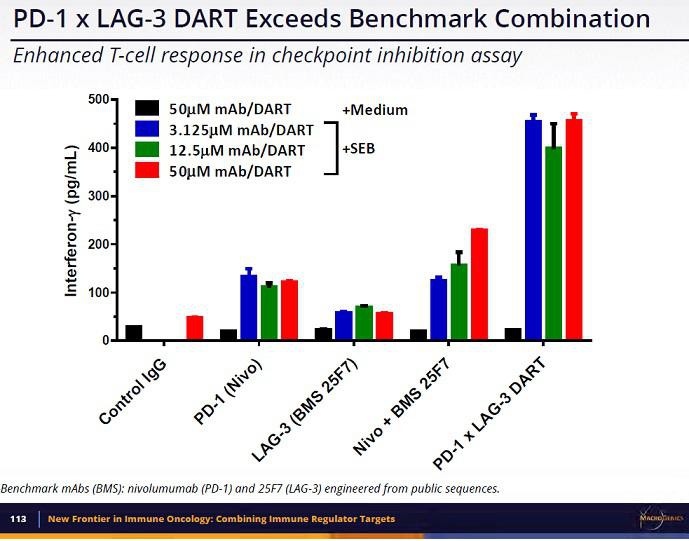
Zudem hat MGNX einen normalen AK MGA012 in der Entwicklung, dessen Target nicht bekannt ist und der in 2H16 den IND haben soll. Ich tippe mal, dass MAG012 ein LAG3-AK ist, da sie für den DART ja bereits mit diesem Target arbeiten.
Wie zuvor bei GITR zu sehen, kann es für IO-Targets relevant sein, dass sie mehrfach gebunden werden. MGNX hat so ja auch einen trimeren DART gegen DR5 in der Entwicklung.
Der PD1xLAG3 DART scheint somit erst der Anfang zu sein. Denkbar sind weitere Kombis aus 2 oder mehr Checkpoint-Hemmern. Oder die Verbindung von PD1&Co mit tumorspezifischen Targets, um z.B. den PD1-Hemmer speziell im Tumor anzureichern. So tritt PD1 auch natürlich an vielen Stellen im Körper auf, so dass die unspezifische Hemmung wie bei Nivo auch zu unerwünschten Nebenwirkungen führt.
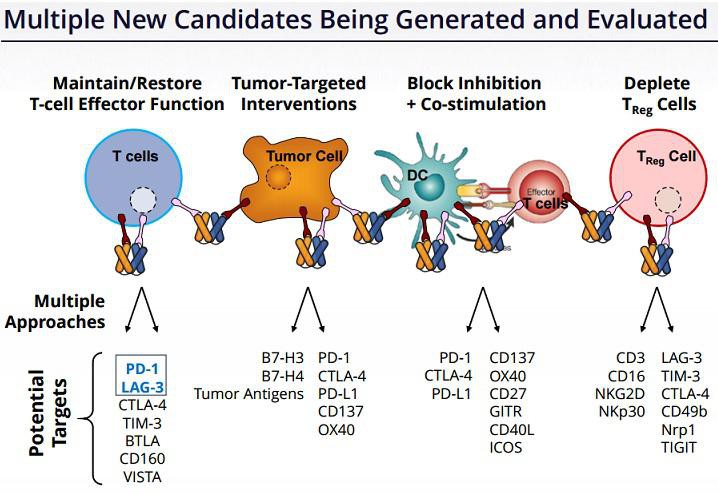
B7H3 wird wie B7H4 als tumorspezifisches Target aufgeführt. MGNX's MGD009-DART B7H3xCD3 basiert darauf, indem T-Zellen über B7H3 die Tumorzellen zerstören sollen.
Vielleicht ist B7H3 oder B7H4 auch das Target, welches FPRX an BLUE für die Entwicklung von CARTs auslizensiert hat, denn FPRX soll diese beiden Target ebenfalls in der Entwicklung haben.



Gruß
ipollit
Weitere IO-Programme, die in absehbarer Zeit in die Klinik gehen, kommen von TSRO und MGNX.
Für TSRO's TIM3-AK TSR-022 ist ein IND in 2Q16 geplant. Damit sind sie bei diesem Target wahrscheinlich mit führend. Der LAG3-AK soll Ende 2016 den IND haben. Letztlich ist es aber das Ziel von TSRO biAKs zu entwickeln, d.h. PD1xTIM3 oder PD1xLAG3... diese könnten 2017 in die Klinik gehen.

Gegen LAG3 entwickelt MGNX nun auch DARTs. MDG013 ist ein PD1xLAG3 DART, der 1H17 seinen IND haben soll.


Der DART soll wirksamer sein als eine AK-Kombi PD1 + LAG3 aus zwei einzelnen AKs wie Nivo + BMS25F7.

Zudem hat MGNX einen normalen AK MGA012 in der Entwicklung, dessen Target nicht bekannt ist und der in 2H16 den IND haben soll. Ich tippe mal, dass MAG012 ein LAG3-AK ist, da sie für den DART ja bereits mit diesem Target arbeiten.
Wie zuvor bei GITR zu sehen, kann es für IO-Targets relevant sein, dass sie mehrfach gebunden werden. MGNX hat so ja auch einen trimeren DART gegen DR5 in der Entwicklung.
Der PD1xLAG3 DART scheint somit erst der Anfang zu sein. Denkbar sind weitere Kombis aus 2 oder mehr Checkpoint-Hemmern. Oder die Verbindung von PD1&Co mit tumorspezifischen Targets, um z.B. den PD1-Hemmer speziell im Tumor anzureichern. So tritt PD1 auch natürlich an vielen Stellen im Körper auf, so dass die unspezifische Hemmung wie bei Nivo auch zu unerwünschten Nebenwirkungen führt.

B7H3 wird wie B7H4 als tumorspezifisches Target aufgeführt. MGNX's MGD009-DART B7H3xCD3 basiert darauf, indem T-Zellen über B7H3 die Tumorzellen zerstören sollen.
Vielleicht ist B7H3 oder B7H4 auch das Target, welches FPRX an BLUE für die Entwicklung von CARTs auslizensiert hat, denn FPRX soll diese beiden Target ebenfalls in der Entwicklung haben.

Gruß
ipollit
AKBA
AKBA möchte Vadadustat als Konkurrent zu FGENs Roxadustat in den USA alleine durch die PIII bringen. Dazu haben sie sich nun weiter Cash gesichert, indem sie die Asien-Rechte an Mitsubishi Tanabe auslizensiert haben: 40 Mio Upfront + 60 Mio für die weltweite Entwicklung von Vadadustat. Dazu kommen 250 Mio USD potentielle Meilensteinzahlungen und 10-20% Royalties.
Für Europa sucht AKBA ebenfalls noch nach einem Partner.
Aktuelle MK ist 298 Mio USD bei 157 Mio USD Cash ohne die 100 Mio USD, die der heutige Deal nun eingebracht hat.

Gruß
ipollit
AKBA möchte Vadadustat als Konkurrent zu FGENs Roxadustat in den USA alleine durch die PIII bringen. Dazu haben sie sich nun weiter Cash gesichert, indem sie die Asien-Rechte an Mitsubishi Tanabe auslizensiert haben: 40 Mio Upfront + 60 Mio für die weltweite Entwicklung von Vadadustat. Dazu kommen 250 Mio USD potentielle Meilensteinzahlungen und 10-20% Royalties.
Für Europa sucht AKBA ebenfalls noch nach einem Partner.
Aktuelle MK ist 298 Mio USD bei 157 Mio USD Cash ohne die 100 Mio USD, die der heutige Deal nun eingebracht hat.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.300.228 von ipollit am 14.12.15 13:39:09AKBA
Sie planen, den US-Markt zu behalten... dafür wird noch ein EU-Partner mit entsprechendem Geld für die Entwicklung benötigt:
AKBA CC Notes:
. Deal covers 2 dozen countries.
. Negotiation was competive.
. Expect to launch non-dialises P3 (PROTECT) in next few weeks.
. Do not think they will need a separate Japan based trial for PROTECT (but not certain).
. Deal provides sufficient cash to fund PROTECT
. Will finalize dialysis (INOVATE) in early(?) 16.
. Will be negotiating an EU deal. That cash is needed to fund INOVATE, though the trial will launch w/o partner if need be.
. Still plan to keep the entire US market.
Der Deal mit Mitsubishi Tanabe schließt übrigend China aus. Konkurrent FGEN hat insgesamt einen deutlichen zeitlichen Vorsprung. Für China sollen bereits nächstes Jahr die ersten PIII-Daten vorliegen.


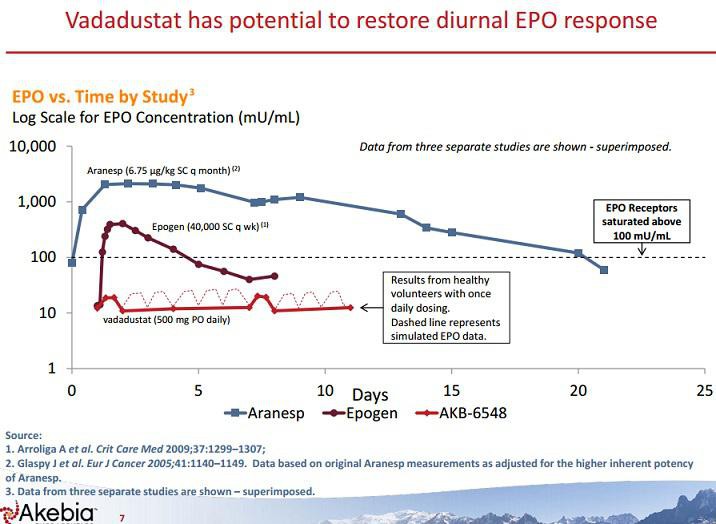

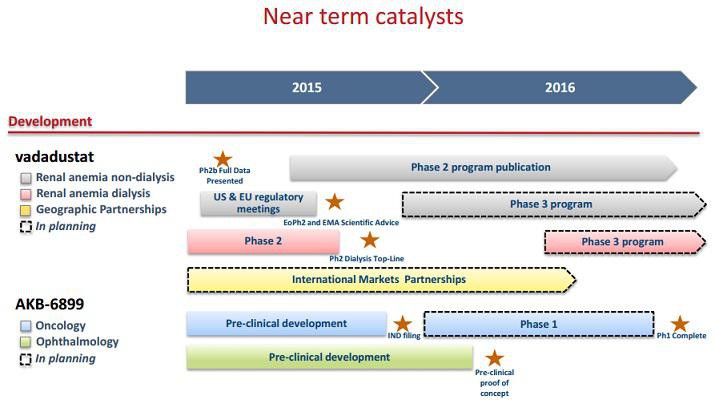
Gruß
ipollit
Sie planen, den US-Markt zu behalten... dafür wird noch ein EU-Partner mit entsprechendem Geld für die Entwicklung benötigt:
AKBA CC Notes:
. Deal covers 2 dozen countries.
. Negotiation was competive.
. Expect to launch non-dialises P3 (PROTECT) in next few weeks.
. Do not think they will need a separate Japan based trial for PROTECT (but not certain).
. Deal provides sufficient cash to fund PROTECT
. Will finalize dialysis (INOVATE) in early(?) 16.
. Will be negotiating an EU deal. That cash is needed to fund INOVATE, though the trial will launch w/o partner if need be.
. Still plan to keep the entire US market.
Der Deal mit Mitsubishi Tanabe schließt übrigend China aus. Konkurrent FGEN hat insgesamt einen deutlichen zeitlichen Vorsprung. Für China sollen bereits nächstes Jahr die ersten PIII-Daten vorliegen.





Gruß
ipollit
ESPR
Ein FDA Experten-Gremium hat sich dagegen ausgesprochen, dass Zetia (Ezetimibe) aufgrund der großen IMPROVE-IT Studie die Label-Erweiterung der Reduzierung von CV-Events bekommen soll.
http://www.fiercepharma.com/story/merck-poised-win-bigger-ma…
Merck & Co.'s ($MRK) cholesterol drug Zetia had another day in the spotlight on Monday. An FDA advisory panel is debating results from an outcomes trial, Improve-It, and whether they're strong enough to give Zetia a bigger role in cholesterol-fighting treatment.
That would include a new indication as an add-on to a variety of statin meds. It could be a needed boost for Zetia, which is also part of Merck's combo cholesterol pill Vytorin. The latter pairs Zetia with the now-off-patent statin Zocor (simvastatin), and the sister products have delivered lackluster sales in recent years, as more blockbuster statin meds fell off patent and questions arose about the utility of Zetia as an add-on.
Improve-It appears to have put those questions to rest. The long-term cardiovascular outcomes trial showed that adding Zetia to simvastatin not only cut levels of "bad" LDL cholesterol, but significantly cut the number of heart attacks, strokes, and other CV "events" that together made up its primary goal.
FDA reviewers laid out the Improve-It results--among 18,144 patients with acute coronary syndrome, CV events in the simvastatin arm ran to 30.2% of patients, while 28.4% of patients in the Zetia-plus-simvastatin suffered from one or more. They also noted that 50 people would need to take Zetia as a simvastatin add-on for 7 years to prevent one of the CV events included in the primary endpoint, CardioBrief notes.
And as CardioBrief reports, the FDA panel debate is likely to center on a couple of issues--data that's missing from the calculations, and analyses of subgroups of patients, which could affect how the agency styles any new use for the drug.
The overall label for both Zetia and Vytorin could get a boost with language saying that they're approved to reduce cardiovascular events--including heart attack, stroke and cardiovascular death--in patients with heart disease. Right now, as CardioBrief notes, statins are the only cholesterol meds labeled this way.
Merck is also asking for a new indication on Zetia allowing it as an add-on to statin meds aside of simvastatin. That would allow the company to market Zetia more broadly, because millions of patients on statins use other meds such as the Pfizer ($PFE) giant Lipitor, which is now available as a generic.
But as CardioBrief notes, the beneficial effects of Zetia in the Improve-It trial "occurred almost exclusively in trial patients who had diabetes." Patients 75 years and older were also big beneficiaries compared with other age groups.
At least one panelist at today's meeting--Dr. Sanjay Kaul, the outspoken cardiologist--has said that a new Zetia use might be limited. "Given these results, it would be difficult to support its use in non-diabetics," Kaul said at the European Society of Cardiology meeting earlier this year (as quoted by CardioBrief). And an FDA reviewer made a point of noting "no effect seen among the under 75, non-diabetic subgroup, which were a majority of the study population."
We'll know soon how the panel votes, and after that, it will be up to the FDA to determine whether--and how--to revamp Zetia's target market. Analysts tend to think Merck will get a broader label out of the data. They also think that the Improve-It results help support the case for PCSK9 drugs recently launched by Sanofi and Regeneron (Praluent) and Amgen (Repatha). Those meds, approved as add-ons to statin therapy, have proven they can cut LDL dramatically, but their outcomes trials won't wrap up for more than a year.
The PCSK9 meds also offer another kind of help to Zetia. Some payers are requiring patients to try the Merck med before moving on to the much-more-expensive PCSK9s, which carry list prices of more than $14,000 per year.
***********
Zetia ist von Relevanz für ESPRs ETC-1002, da beides orale Mittel sind, die LDL senken. PCSK9-AKs senken ebenfalls LDL, allerdings sehr viel deutlicher als z.B. Zetia. Die große Frage war immer, ob eine LDL-Senkung alleine auch CV-Events senkt wie z.B. Herzinfakt oder Schlaganfall. Eine Studie, die die Senkung von LDL untersucht, ist sehr viel einfacher, günstiger und schneller als eine CV-Outcome Studie.
Das Mittel der Wahl sind Statine, die aber eine breitere Wirkung haben außer der LDL-Senkung. PCSK9-AKs wurden nun auch zugelassen aufgrund der starken LDL-Senkung und einigen Anzeichen, dass sie ebenfalls CV-Events senken.
Über Zetia, das bald auch generisch wird, muss die FDA nun über die Labelerweiterung entscheiden.
Hier sind die positiven Ergebnisse der IMPROVE-IT Studie:
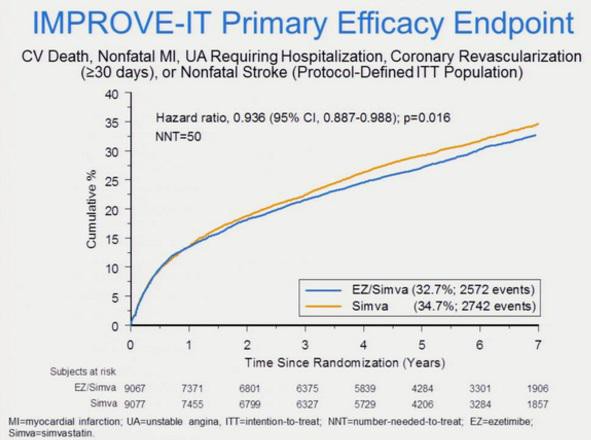
ESPRs ETC-1002 ist vom Wirkmechanismus eher den Statinen ähnlich.
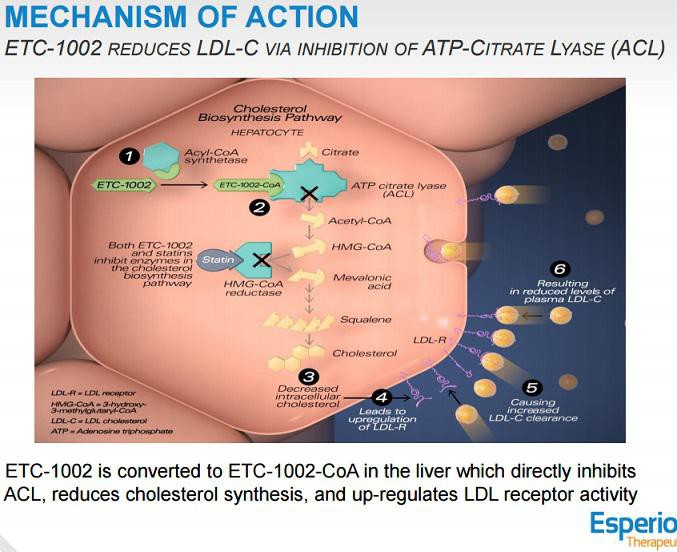
Ein Vergleich von Statinen, Zetia (Ezetimibe), PCSK9-AKs, CETP-Hemmern und ESPR's ETC-1002:
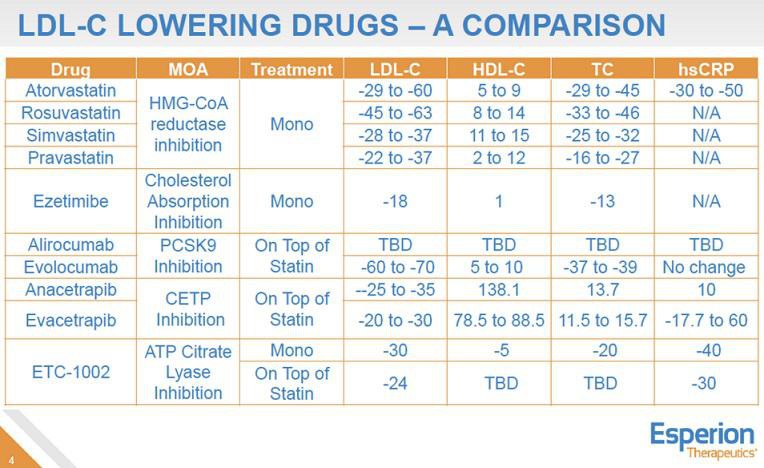
Dass das ganze nicht so einfach ist, zeigen CETP-Hemmer, deren Ergebnisse auf dem Papier gut aussehen, in der Praxis aber nicht funktionieren. Eine mögliche Erklärung findet sich hier:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"Increases in HDL are only clinically meaningful when they increase reverse lipid transport (RLT). CETP inhibition blocks four of five ways HDL offloads collected fats, leaving only one of the more inefficient methods.
If you think of HDL as a garbage bag for bad lipids, CETP inhibitors cause the body to create lots of full garbage bags but make it so there are few places to empty them. Eventually the garbage bags degrade and the lipids are returned to the system.
So despite significant increases in HDL particles, you get no clinical efficacy. Avant, Japan Tobacco, and now Pfizer have all failed with this class of drug.
The only hope torcetrapib had is if Pfizer threaded a narrow pharmacokinetic needle. CETP-inhibition causes the body to create high numbers of HDL molecules, probably in reaction to the low amount of fat being offloaded. Once this is accomplished, however, you have to cease the CETP-inhibition so all the full garbage bags have someplace to offload.
The trick is to inhibit just long enough for an HDL boost but not too long to hamper RLT. I've always believed this PK needle was too small to thread in broad Phase III trials. There simply is too much inter-patient variance in compliance, fat intake, body chemistry, etc."
*****
Ohad Hammer sagt zur Entscheidung des Experten-Gremiums (das nicht identisch mit der späteren FDA-Entscheidung sein muss):
"This is obviously very bad news in the short run but I am still bullish on ESPR as they have a drug that works like a statin clinically (LDL, hsCRP) and mechanistically (cholesterol biosynthesis pathway) without the most troubling side effect of statins. As the only agent with such a profile (plus it’s oral) I believe it has a high likelihood of demonstrating a CV outcome benefit which should make it an attractive acquisition target."
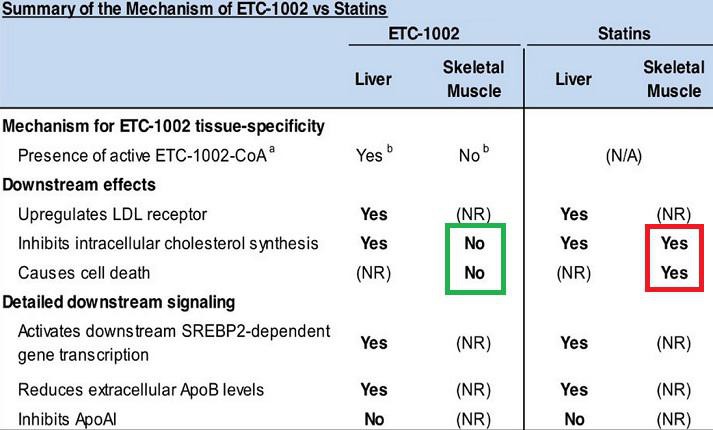
Eine Möglichkeit für ETC-1002 ist auch noch eine Kombi mit Zetia:

Und einige Analysten-Kommentare vor und nach dem Panel:





Gruß
ipollit
Ein FDA Experten-Gremium hat sich dagegen ausgesprochen, dass Zetia (Ezetimibe) aufgrund der großen IMPROVE-IT Studie die Label-Erweiterung der Reduzierung von CV-Events bekommen soll.
http://www.fiercepharma.com/story/merck-poised-win-bigger-ma…
Merck & Co.'s ($MRK) cholesterol drug Zetia had another day in the spotlight on Monday. An FDA advisory panel is debating results from an outcomes trial, Improve-It, and whether they're strong enough to give Zetia a bigger role in cholesterol-fighting treatment.
That would include a new indication as an add-on to a variety of statin meds. It could be a needed boost for Zetia, which is also part of Merck's combo cholesterol pill Vytorin. The latter pairs Zetia with the now-off-patent statin Zocor (simvastatin), and the sister products have delivered lackluster sales in recent years, as more blockbuster statin meds fell off patent and questions arose about the utility of Zetia as an add-on.
Improve-It appears to have put those questions to rest. The long-term cardiovascular outcomes trial showed that adding Zetia to simvastatin not only cut levels of "bad" LDL cholesterol, but significantly cut the number of heart attacks, strokes, and other CV "events" that together made up its primary goal.
FDA reviewers laid out the Improve-It results--among 18,144 patients with acute coronary syndrome, CV events in the simvastatin arm ran to 30.2% of patients, while 28.4% of patients in the Zetia-plus-simvastatin suffered from one or more. They also noted that 50 people would need to take Zetia as a simvastatin add-on for 7 years to prevent one of the CV events included in the primary endpoint, CardioBrief notes.
And as CardioBrief reports, the FDA panel debate is likely to center on a couple of issues--data that's missing from the calculations, and analyses of subgroups of patients, which could affect how the agency styles any new use for the drug.
The overall label for both Zetia and Vytorin could get a boost with language saying that they're approved to reduce cardiovascular events--including heart attack, stroke and cardiovascular death--in patients with heart disease. Right now, as CardioBrief notes, statins are the only cholesterol meds labeled this way.
Merck is also asking for a new indication on Zetia allowing it as an add-on to statin meds aside of simvastatin. That would allow the company to market Zetia more broadly, because millions of patients on statins use other meds such as the Pfizer ($PFE) giant Lipitor, which is now available as a generic.
But as CardioBrief notes, the beneficial effects of Zetia in the Improve-It trial "occurred almost exclusively in trial patients who had diabetes." Patients 75 years and older were also big beneficiaries compared with other age groups.
At least one panelist at today's meeting--Dr. Sanjay Kaul, the outspoken cardiologist--has said that a new Zetia use might be limited. "Given these results, it would be difficult to support its use in non-diabetics," Kaul said at the European Society of Cardiology meeting earlier this year (as quoted by CardioBrief). And an FDA reviewer made a point of noting "no effect seen among the under 75, non-diabetic subgroup, which were a majority of the study population."
We'll know soon how the panel votes, and after that, it will be up to the FDA to determine whether--and how--to revamp Zetia's target market. Analysts tend to think Merck will get a broader label out of the data. They also think that the Improve-It results help support the case for PCSK9 drugs recently launched by Sanofi and Regeneron (Praluent) and Amgen (Repatha). Those meds, approved as add-ons to statin therapy, have proven they can cut LDL dramatically, but their outcomes trials won't wrap up for more than a year.
The PCSK9 meds also offer another kind of help to Zetia. Some payers are requiring patients to try the Merck med before moving on to the much-more-expensive PCSK9s, which carry list prices of more than $14,000 per year.
***********
Zetia ist von Relevanz für ESPRs ETC-1002, da beides orale Mittel sind, die LDL senken. PCSK9-AKs senken ebenfalls LDL, allerdings sehr viel deutlicher als z.B. Zetia. Die große Frage war immer, ob eine LDL-Senkung alleine auch CV-Events senkt wie z.B. Herzinfakt oder Schlaganfall. Eine Studie, die die Senkung von LDL untersucht, ist sehr viel einfacher, günstiger und schneller als eine CV-Outcome Studie.
Das Mittel der Wahl sind Statine, die aber eine breitere Wirkung haben außer der LDL-Senkung. PCSK9-AKs wurden nun auch zugelassen aufgrund der starken LDL-Senkung und einigen Anzeichen, dass sie ebenfalls CV-Events senken.
Über Zetia, das bald auch generisch wird, muss die FDA nun über die Labelerweiterung entscheiden.
Hier sind die positiven Ergebnisse der IMPROVE-IT Studie:

ESPRs ETC-1002 ist vom Wirkmechanismus eher den Statinen ähnlich.

Ein Vergleich von Statinen, Zetia (Ezetimibe), PCSK9-AKs, CETP-Hemmern und ESPR's ETC-1002:

Dass das ganze nicht so einfach ist, zeigen CETP-Hemmer, deren Ergebnisse auf dem Papier gut aussehen, in der Praxis aber nicht funktionieren. Eine mögliche Erklärung findet sich hier:
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"Increases in HDL are only clinically meaningful when they increase reverse lipid transport (RLT). CETP inhibition blocks four of five ways HDL offloads collected fats, leaving only one of the more inefficient methods.
If you think of HDL as a garbage bag for bad lipids, CETP inhibitors cause the body to create lots of full garbage bags but make it so there are few places to empty them. Eventually the garbage bags degrade and the lipids are returned to the system.
So despite significant increases in HDL particles, you get no clinical efficacy. Avant, Japan Tobacco, and now Pfizer have all failed with this class of drug.
The only hope torcetrapib had is if Pfizer threaded a narrow pharmacokinetic needle. CETP-inhibition causes the body to create high numbers of HDL molecules, probably in reaction to the low amount of fat being offloaded. Once this is accomplished, however, you have to cease the CETP-inhibition so all the full garbage bags have someplace to offload.
The trick is to inhibit just long enough for an HDL boost but not too long to hamper RLT. I've always believed this PK needle was too small to thread in broad Phase III trials. There simply is too much inter-patient variance in compliance, fat intake, body chemistry, etc."
*****
Ohad Hammer sagt zur Entscheidung des Experten-Gremiums (das nicht identisch mit der späteren FDA-Entscheidung sein muss):
"This is obviously very bad news in the short run but I am still bullish on ESPR as they have a drug that works like a statin clinically (LDL, hsCRP) and mechanistically (cholesterol biosynthesis pathway) without the most troubling side effect of statins. As the only agent with such a profile (plus it’s oral) I believe it has a high likelihood of demonstrating a CV outcome benefit which should make it an attractive acquisition target."

Eine Möglichkeit für ETC-1002 ist auch noch eine Kombi mit Zetia:

Und einige Analysten-Kommentare vor und nach dem Panel:




Gruß
ipollit
Kreise: Celgene bietet für Juno Therapeutics. Unbestätigt.
vor 4 Min (heute 19:47) via Jandaya.de
vor 4 Min (heute 19:47) via Jandaya.de
Antwort auf Beitrag Nr.: 51.311.694 von schnappi am 15.12.15 19:52:34am Kurs lässt sich aber nichts derartiges ablesen... aus momentaner Sicht wohl eher unwahrscheinlich

Gruß
ipollit
Gruß
ipollit
Stimmt, aber Celgene könnte hier irgendwann zugreifen.
OMED
OMED gefallen mir ganz gut. Eigentlich gilt es als ein Unternehmen, das speziell Therapien gegen Krebs-Stammzellen (CSC) entwickelt. Das sind sich langsam teilende, aber krankhaft Zellen, die neue Krebszellen produzieren. Einer (unbewiesenen) Theorie zufolge führt das dazu, dass der Krebs z.B. nach einer Chemo, bei der die meisten Krebszellen abgetötet worden sind, nach einiger Zeit trotzdem wieder auftritt. CSC-Medikamente sind alleine vielleicht nur wenig wirksam, da sie sich nur auf die CSC-Zellen auswirken aber nicht auf andere Krebszellen, erst in der Kombi bringen sie etwas.
CSC-Zellen können sich unendlich Teilen. Die dabei entstehenden Zellen können sehr unterschiedliche Krebszellen sein (dadurch kann ein Krebs resistent gegenüber bestimmten Target-Therapien werden). Transplatiert man diese CSC-Zellen z.B. in Mäuse, entstehen neue Tumore.
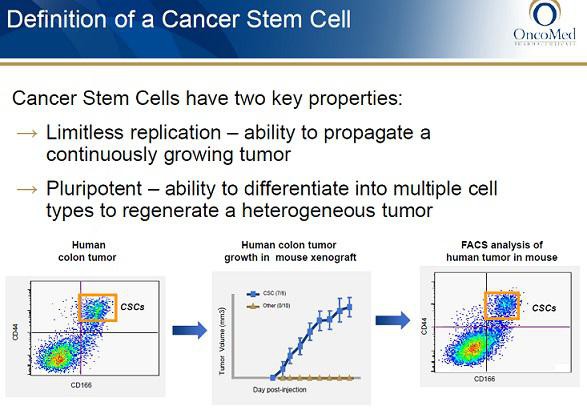
Ziel ist es, entweder die Teilung der CSC-Zellen zu stoppen oder sie so zu verändern, dass keine Krebszellen mehr aus ihnen entstehen.
OMED entwickelt mehrere verschiedene Klassen von Medikamenten, die auf unterschiedliche Signalwege abzielen, die bei CSC-Zellen eine Rolle spielen.
Allerdings zeigt sich, dass diese Signalwege nicht nur bei CSC-Zellen relevant sind. Z.B. haben Notch-Hemmer wie z.B. DLL4 auch Eigenschaften wie Avastin, die die Blutversorgung regulieren oder immunmoduliernde Eigenschaften.
Die Pipeline ist schon jetzt recht breit für ein 600 Mio USD Unternhemen mit 7 Mitteln in der klinischen Entwicklung... im nächsten Jahr sollen weitere folgen.
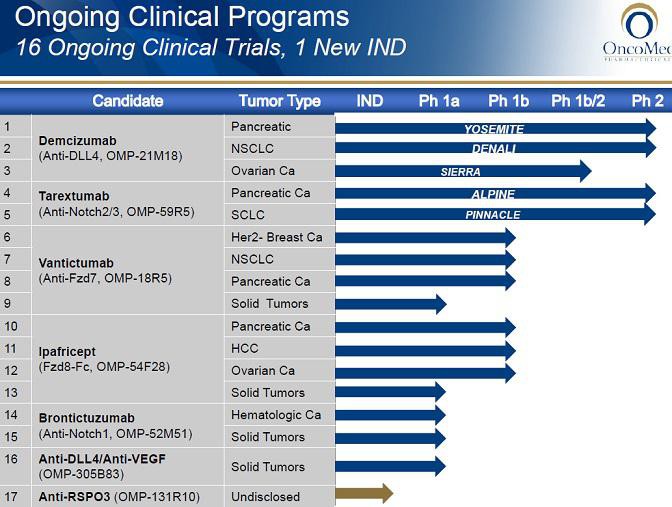
OMED hat für die Entwicklung mehrere Partnerschaften... die wichtigste wohl mit CELG, bei der sie für 30% der Entwicklungskosten 50% vom US-Markt bekommen können. Auch sonst gibt es relevante Royalties bis zu 20%.
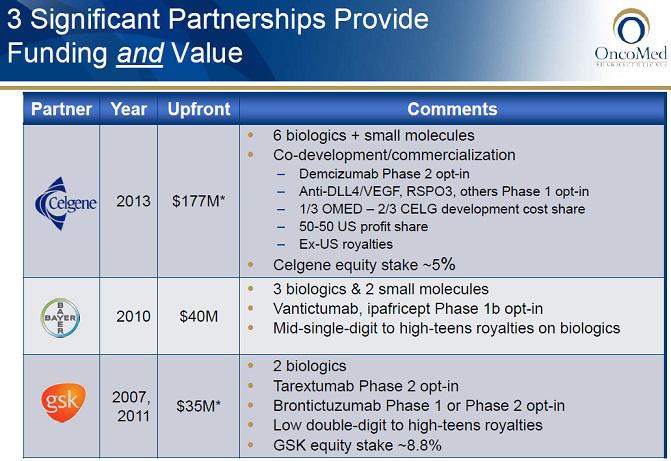
Meilensteinzahlungen bringen permanent neuen Cash... z.B. könnten es in den nächsten 6 Monaten bis zu 150 Mio USD sein.
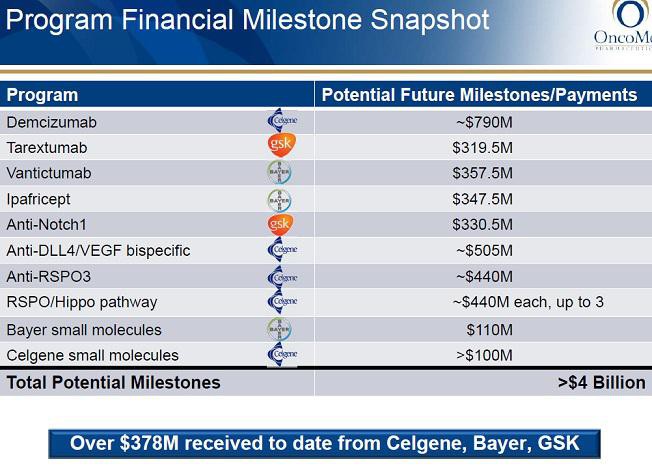


Gruß
ipollit
OMED gefallen mir ganz gut. Eigentlich gilt es als ein Unternehmen, das speziell Therapien gegen Krebs-Stammzellen (CSC) entwickelt. Das sind sich langsam teilende, aber krankhaft Zellen, die neue Krebszellen produzieren. Einer (unbewiesenen) Theorie zufolge führt das dazu, dass der Krebs z.B. nach einer Chemo, bei der die meisten Krebszellen abgetötet worden sind, nach einiger Zeit trotzdem wieder auftritt. CSC-Medikamente sind alleine vielleicht nur wenig wirksam, da sie sich nur auf die CSC-Zellen auswirken aber nicht auf andere Krebszellen, erst in der Kombi bringen sie etwas.
CSC-Zellen können sich unendlich Teilen. Die dabei entstehenden Zellen können sehr unterschiedliche Krebszellen sein (dadurch kann ein Krebs resistent gegenüber bestimmten Target-Therapien werden). Transplatiert man diese CSC-Zellen z.B. in Mäuse, entstehen neue Tumore.

Ziel ist es, entweder die Teilung der CSC-Zellen zu stoppen oder sie so zu verändern, dass keine Krebszellen mehr aus ihnen entstehen.

OMED entwickelt mehrere verschiedene Klassen von Medikamenten, die auf unterschiedliche Signalwege abzielen, die bei CSC-Zellen eine Rolle spielen.

Allerdings zeigt sich, dass diese Signalwege nicht nur bei CSC-Zellen relevant sind. Z.B. haben Notch-Hemmer wie z.B. DLL4 auch Eigenschaften wie Avastin, die die Blutversorgung regulieren oder immunmoduliernde Eigenschaften.
Die Pipeline ist schon jetzt recht breit für ein 600 Mio USD Unternhemen mit 7 Mitteln in der klinischen Entwicklung... im nächsten Jahr sollen weitere folgen.

OMED hat für die Entwicklung mehrere Partnerschaften... die wichtigste wohl mit CELG, bei der sie für 30% der Entwicklungskosten 50% vom US-Markt bekommen können. Auch sonst gibt es relevante Royalties bis zu 20%.

Meilensteinzahlungen bringen permanent neuen Cash... z.B. könnten es in den nächsten 6 Monaten bis zu 150 Mio USD sein.


Gruß
ipollit
ARRY:
Array BioPharma Announces Phase 3 Binimetinib Trial Meets Primary Endpoint For NRAS-Mutant Melanoma
BOULDER, Colo., Dec. 16, 2015 /PRNewswire/ -- Array BioPharma (Nasdaq: ARRY) today reported top-line results from the ongoing Phase 3 clinical trial of binimetinib in patients with advanced NRAS-mutant melanoma, known as the NEMO trial. The study met its primary endpoint of improving progression-free survival (PFS) compared with dacarbazine treatment. The median PFS on the binimetinib arm was 2.8 months versus 1.5 months on the dacarbazine arm; hazard ratio (HR) 0.62, [95% CI 0.47-0.80], p < 0.001.
http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
Man ist ja mittlerweile schon fast überrascht, wenn es mal irgendwo leidlich positive Nachrichten gibt...
Array BioPharma Announces Phase 3 Binimetinib Trial Meets Primary Endpoint For NRAS-Mutant Melanoma
BOULDER, Colo., Dec. 16, 2015 /PRNewswire/ -- Array BioPharma (Nasdaq: ARRY) today reported top-line results from the ongoing Phase 3 clinical trial of binimetinib in patients with advanced NRAS-mutant melanoma, known as the NEMO trial. The study met its primary endpoint of improving progression-free survival (PFS) compared with dacarbazine treatment. The median PFS on the binimetinib arm was 2.8 months versus 1.5 months on the dacarbazine arm; hazard ratio (HR) 0.62, [95% CI 0.47-0.80], p < 0.001.
http://investor.arraybiopharma.com/phoenix.zhtml?c=123810&p=…
Man ist ja mittlerweile schon fast überrascht, wenn es mal irgendwo leidlich positive Nachrichten gibt...
Antwort auf Beitrag Nr.: 51.316.110 von SLGramann am 16.12.15 12:38:35Unabhängig von dem konkreten Umsatzpotential in NRAS-Melanoma (das als nicht sehr bedeutend eingeschätzt wird), dürfte das die Stimmungslage in Bezug auf Array und insbesondere Binimetinib aufhellen und vielleicht grundsätzlich ins Positive drehen.
Antwort auf Beitrag Nr.: 51.315.831 von ipollit am 16.12.15 12:09:04Schöner Beitrag ich habe OMED auch schon länger im Depot wurde über Morphosys auf sie damals aufmerksam:
Die aktive Zusammenarbeit mit dem in den USA ansässigen biopharmazeutischen Unternehmen OncoMed Pharmaceuticals wurde in 2010 eingestellt. Dennoch können therapeutische Programme, die während der laufenden Kollaboration initiiert wurden, weiterentwickelt werden und dadurch in Zukunft zu Meilensteinzahlungen und Tantiemen auf Produktverkäufe führen. OncoMed erforscht derzeit einen HuCAL-basierten Krebsantikörper, Tarextumab (OMP-59R5), in klinischen Studien der Phase 2. Ein zweiter HuCAL-Antikörper, Vantictumab (OMP-18R5), der ein Zielmolekül innerhalb des Wnt-Signalwegs bindet, wird in einer klinischen Studie der Phase 1 an Patienten mit fortgeschrittenen soliden Tumoren geprüft.
Habe im Oktober zugekauft finde die Market Cap im vergleich zu manch anderen sehr klein.
Die aktive Zusammenarbeit mit dem in den USA ansässigen biopharmazeutischen Unternehmen OncoMed Pharmaceuticals wurde in 2010 eingestellt. Dennoch können therapeutische Programme, die während der laufenden Kollaboration initiiert wurden, weiterentwickelt werden und dadurch in Zukunft zu Meilensteinzahlungen und Tantiemen auf Produktverkäufe führen. OncoMed erforscht derzeit einen HuCAL-basierten Krebsantikörper, Tarextumab (OMP-59R5), in klinischen Studien der Phase 2. Ein zweiter HuCAL-Antikörper, Vantictumab (OMP-18R5), der ein Zielmolekül innerhalb des Wnt-Signalwegs bindet, wird in einer klinischen Studie der Phase 1 an Patienten mit fortgeschrittenen soliden Tumoren geprüft.
Habe im Oktober zugekauft finde die Market Cap im vergleich zu manch anderen sehr klein.
AKBA / FGEN:
Hier ein kleiner Artikel zu den jeweiligen HIF-PH inhibitoren. Interessant auch der Hinweis auf weitere Konkurrenzentwicklungen.
http://www.epvantage.com/Universal/View.aspx?type=Story&id=6…
Der safety-Aspekt wird in Bezug auf Akebias vadadustat immer wieder negativ betont. Ob das gerechtfertigt ist, wird aber eben auch bezweifelt.
Ich verweise dazu nochmals auf diesen Artikel, der für mich eines der seltenen highlights bei seeking alpha ist:
http://seekingalpha.com/article/3490866-addressing-6-misconc…
Insgesamt halte ich die Bewertung von Akebia für günstig, allerdings muss man hier sehr viel Zeit mitbringen, wenn man investieren will.
Hier ein kleiner Artikel zu den jeweiligen HIF-PH inhibitoren. Interessant auch der Hinweis auf weitere Konkurrenzentwicklungen.
http://www.epvantage.com/Universal/View.aspx?type=Story&id=6…
Der safety-Aspekt wird in Bezug auf Akebias vadadustat immer wieder negativ betont. Ob das gerechtfertigt ist, wird aber eben auch bezweifelt.
Ich verweise dazu nochmals auf diesen Artikel, der für mich eines der seltenen highlights bei seeking alpha ist:
http://seekingalpha.com/article/3490866-addressing-6-misconc…
Insgesamt halte ich die Bewertung von Akebia für günstig, allerdings muss man hier sehr viel Zeit mitbringen, wenn man investieren will.
CLVS:
Die FDA hat den Zeitpunkt der Entscheidung über eine Zulassung von Rociletinib um drei Monate hinausgeschoben:
BOULDER, Colo.--(BUSINESS WIRE)--Clovis Oncology, Inc. (NASDAQ: CLVS) announced today that the U.S. Food and Drug Administration (FDA) has extended the Prescription Drug User Fee Act (PDUFA) date for Clovis’ New Drug Application (NDA) for rociletinib by the standard extension period of three months with the new goal date of June 28, 2016. Rociletinib is an investigational therapy for the treatment of patients with mutant epidermal growth factor receptor (EGFR) non-small cell lung cancer (NSCLC) who have been previously treated with an EGFR-targeted therapy and have the EGFR T790M mutation.
Clovis submitted a Major Amendment on November 16, 2015 in response to the FDA’s request for additional clinical data for both the 500mg and 625mg BID dose patient groups for rociletinib. As expected, the FDA extended the PDUFA goal date to allow additional time for review of the new information requested by the Agency.
Da man auch befürchten musste, CLVS würde sich gleich einen complete response letter fangen, ist das so weit erst mal ziemlich okay.
Allerdings glaube ich nicht, dass die Gefahr eines complete response letter bereits vom Tisch ist. Wie da die genauen Verfahrensweisen der FDA sind, weiß ich aber nicht.
Die FDA hat den Zeitpunkt der Entscheidung über eine Zulassung von Rociletinib um drei Monate hinausgeschoben:
BOULDER, Colo.--(BUSINESS WIRE)--Clovis Oncology, Inc. (NASDAQ: CLVS) announced today that the U.S. Food and Drug Administration (FDA) has extended the Prescription Drug User Fee Act (PDUFA) date for Clovis’ New Drug Application (NDA) for rociletinib by the standard extension period of three months with the new goal date of June 28, 2016. Rociletinib is an investigational therapy for the treatment of patients with mutant epidermal growth factor receptor (EGFR) non-small cell lung cancer (NSCLC) who have been previously treated with an EGFR-targeted therapy and have the EGFR T790M mutation.
Clovis submitted a Major Amendment on November 16, 2015 in response to the FDA’s request for additional clinical data for both the 500mg and 625mg BID dose patient groups for rociletinib. As expected, the FDA extended the PDUFA goal date to allow additional time for review of the new information requested by the Agency.
Da man auch befürchten musste, CLVS würde sich gleich einen complete response letter fangen, ist das so weit erst mal ziemlich okay.
Allerdings glaube ich nicht, dass die Gefahr eines complete response letter bereits vom Tisch ist. Wie da die genauen Verfahrensweisen der FDA sind, weiß ich aber nicht.
GLPG / GILD:
Ein Hammer-Deal für Galapagos!
Filgotinib ist neu verpartnert - und zwar mit Gilead und das zu ganz ausgezeichneten Konditionen.
Verständlich, dass der Markt heftig negativ reagiert hatte, nachdem ABBV aus dem Projekt ausgestiegen war, weil man einen eigenen Kandidaten favorisiert.
Letztlich war die Reaktion des Marktes aber einfach nur vollkommen falsch - wie so oft!
MECHELEN, Belgium & FOSTER CITY, Calif.--(BUSINESS WIRE)--Dec. 17, 2015-- Galapagos NV (Euronext & NASDAQ:GLPG) and Gilead Sciences, Inc. (NASDAQ:GILD) today announced that the companies have entered into a global partnership for the development and commercialization of the JAK1-selective inhibitor filgotinib for inflammatory disease indications. Galapagos will receive an upfront payment of $725 million consisting of a license fee of $300 million and a $425 million equity investment in Galapagos. In addition, Galapagos is eligible for payments up to $1.35 billion in milestones, with tiered royalties starting at 20% and a profit split in co-promotion territories.
http://investors.gilead.com/phoenix.zhtml?c=69964&p=irol-new…
Ein Hammer-Deal für Galapagos!
Filgotinib ist neu verpartnert - und zwar mit Gilead und das zu ganz ausgezeichneten Konditionen.
Verständlich, dass der Markt heftig negativ reagiert hatte, nachdem ABBV aus dem Projekt ausgestiegen war, weil man einen eigenen Kandidaten favorisiert.
Letztlich war die Reaktion des Marktes aber einfach nur vollkommen falsch - wie so oft!
MECHELEN, Belgium & FOSTER CITY, Calif.--(BUSINESS WIRE)--Dec. 17, 2015-- Galapagos NV (Euronext & NASDAQ:GLPG) and Gilead Sciences, Inc. (NASDAQ:GILD) today announced that the companies have entered into a global partnership for the development and commercialization of the JAK1-selective inhibitor filgotinib for inflammatory disease indications. Galapagos will receive an upfront payment of $725 million consisting of a license fee of $300 million and a $425 million equity investment in Galapagos. In addition, Galapagos is eligible for payments up to $1.35 billion in milestones, with tiered royalties starting at 20% and a profit split in co-promotion territories.
http://investors.gilead.com/phoenix.zhtml?c=69964&p=irol-new…
Antwort auf Beitrag Nr.: 51.322.323 von SLGramann am 17.12.15 07:25:39Der Filgotinib-Deal sieht wirklich sehr gut aus! Der JAK1-Hemmer wird ja speziell nur in Autoimmunerkrankungen entwickelt und nicht z.B. gegen Krebs. Konkurrent INCY hat momentan keinen JAK1 mehr gegen RA in der fortgeschrittenen klinischen Entwicklung... ihr Kandidat hatte Probleme mit Nebenwirkungen. INCY's Bari ist ein JAK1/2... die bisherigen PIII-Ergebnisse sehen gut aus. Die Konditionen des GILD-Deals sehen besser noch aus als die von INCY mit LLY. Galapagos hat mit Crohn zudem eine zweite Indikation neben RA. Prima!
Gruß
ipollit
Gruß
ipollit
SAGE, MRNS
beide werden nächstes Jahr PIII-Daten vorliegen haben... SAGE's PIII könnte zu einer Zulassung fühen.
SAGE-547 mit Orphan Drug, FT und SPA... PIII-Daten sollen in 2H16 vorliegen, vielleicht ja auch noch schneller.
Top-Line Data Expected in Second Half of 2016 for SAGE’s Global Phase 3 Trial in Super-Refractory Status Epilepticus...
“We are pleased to revise our timeline forward for the Phase 3 STATUS Trial top-line results based on current enrollment trends and our team’s continued execution in opening sites. We are excited about the interest in our trial to date,”...
“2016 will be an important and milestone-rich year for SAGE. In the first half of 2016, we expect data readouts from our placebo-controlled Phase 2 trial of SAGE-547 in severe postpartum depression and from the SAGE-217 Phase 1 clinical program. In the second half of the year, in addition to the SAGE-547 Phase 3 data, we expect to launch multiple Phase 2 trials evaluating SAGE-217 in essential tremor, orphan epilepsies and potentially postpartum depression, assuming successful replication of earlier stage work. We also expect to initiate the SAGE-689 Phase 1 development program in the second half of 2016. Along with these clinical milestones, SAGE is also committed to continuing its groundbreaking work studying the NMDA neurotransmitter system and its impact on CNS diseases, and we plan to present additional scientific data on this work in 2016,” added Dr. Jonas.

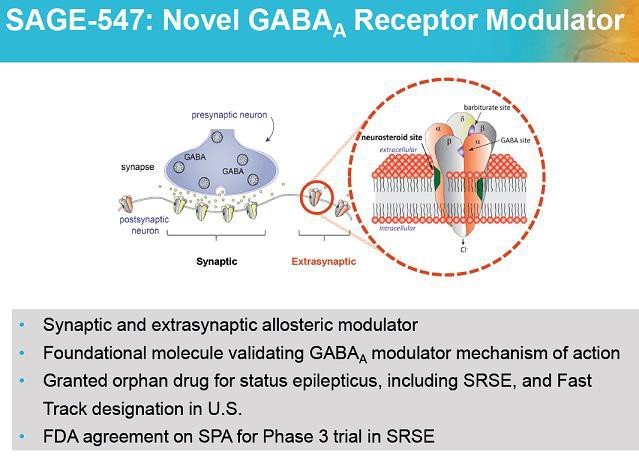

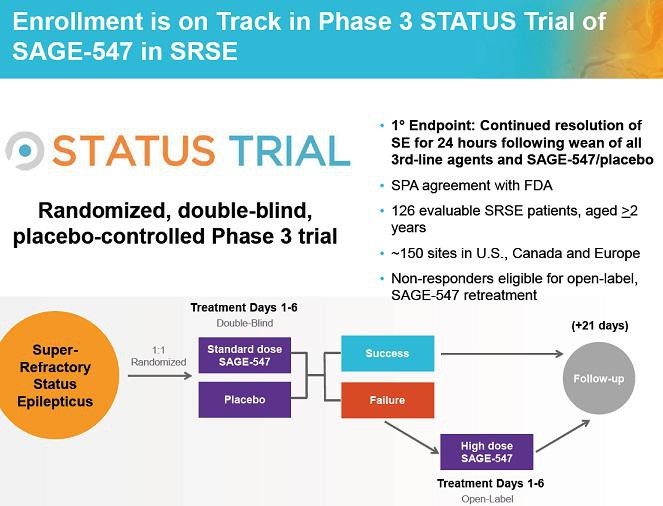

****
MRNS entwickelt Ganaxolone zunächst nicht für die schwersten Fälle, die im Krankenhaus behandelt werden, sondern für eine Behandlung von einer weniger schwerer Form von Epilepsie zuhause. Daher ist Ganaxolone oral und nicht IV wie SAGE-547. Erste PIII-Daten sollen Mitte des Jahres kommen. Es wird allerdings noch eine zweite PIII benötigt, die erst danach gestartet wird.
Marinus Pharmaceuticals, Inc. (MRNS), a biopharmaceutical company dedicated to the development of innovative therapeutics to treat epilepsy and neuropsychiatric disorders, announced that it has completed patient recruitment for the Phase 3 clinical trial of ganaxolone, a CNS-selective GABAA modulator, in adults with drug-resistant focal onset seizures. Sites participating in this global study have completed screening patients. After establishing eight weeks of baseline seizure frequency, patients randomized in the study undergo a two-week titration period followed by a twelve-week maintenance period. The Company anticipates announcing top-line results from the study in mid-2016."

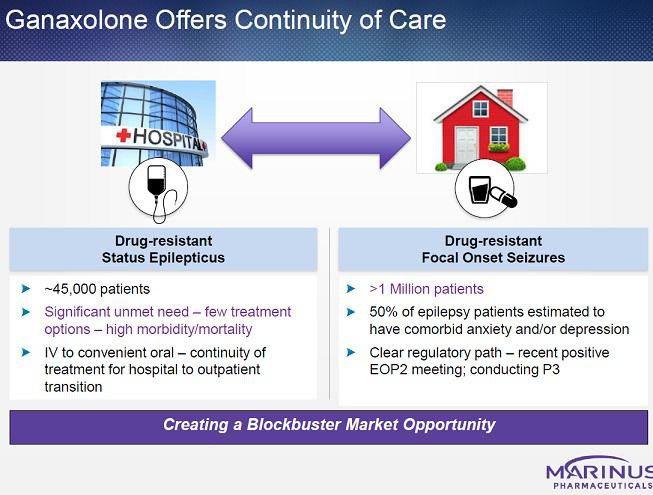




Gruß
ipollit
beide werden nächstes Jahr PIII-Daten vorliegen haben... SAGE's PIII könnte zu einer Zulassung fühen.
SAGE-547 mit Orphan Drug, FT und SPA... PIII-Daten sollen in 2H16 vorliegen, vielleicht ja auch noch schneller.
Top-Line Data Expected in Second Half of 2016 for SAGE’s Global Phase 3 Trial in Super-Refractory Status Epilepticus...
“We are pleased to revise our timeline forward for the Phase 3 STATUS Trial top-line results based on current enrollment trends and our team’s continued execution in opening sites. We are excited about the interest in our trial to date,”...
“2016 will be an important and milestone-rich year for SAGE. In the first half of 2016, we expect data readouts from our placebo-controlled Phase 2 trial of SAGE-547 in severe postpartum depression and from the SAGE-217 Phase 1 clinical program. In the second half of the year, in addition to the SAGE-547 Phase 3 data, we expect to launch multiple Phase 2 trials evaluating SAGE-217 in essential tremor, orphan epilepsies and potentially postpartum depression, assuming successful replication of earlier stage work. We also expect to initiate the SAGE-689 Phase 1 development program in the second half of 2016. Along with these clinical milestones, SAGE is also committed to continuing its groundbreaking work studying the NMDA neurotransmitter system and its impact on CNS diseases, and we plan to present additional scientific data on this work in 2016,” added Dr. Jonas.





****
MRNS entwickelt Ganaxolone zunächst nicht für die schwersten Fälle, die im Krankenhaus behandelt werden, sondern für eine Behandlung von einer weniger schwerer Form von Epilepsie zuhause. Daher ist Ganaxolone oral und nicht IV wie SAGE-547. Erste PIII-Daten sollen Mitte des Jahres kommen. Es wird allerdings noch eine zweite PIII benötigt, die erst danach gestartet wird.
Marinus Pharmaceuticals, Inc. (MRNS), a biopharmaceutical company dedicated to the development of innovative therapeutics to treat epilepsy and neuropsychiatric disorders, announced that it has completed patient recruitment for the Phase 3 clinical trial of ganaxolone, a CNS-selective GABAA modulator, in adults with drug-resistant focal onset seizures. Sites participating in this global study have completed screening patients. After establishing eight weeks of baseline seizure frequency, patients randomized in the study undergo a two-week titration period followed by a twelve-week maintenance period. The Company anticipates announcing top-line results from the study in mid-2016."




Gruß
ipollit
Auch ein krasser Deal... AZN erwirbt für 4 Mrd USD 55% des privaten Biotechs Acerta aufgrund von PII-Daten des BTK-Hemmers Acalabrutinib. Acalabrutinib ist ein möglicher Konkurrent zu Imbruvica von J&J sowie ABBV (vorher PCYC) und aktuell in PIII... angeblich sollen in 2H16 erste PIII-Daten vorliegen.
Gruß
ipollit
Gruß
ipollit
Martin Shkreli ist endlich aus dem Verkehr gezogen worden... sehr schön!
"Pharma CEO Martin Shkreli arrested on charges of securities fraud"
Gruß
ipollit
"Pharma CEO Martin Shkreli arrested on charges of securities fraud"
Gruß
ipollit
OMED
Ich finde OMED aber nicht nur aufgrund der breiten Pipeline interessant, sondern speziell auch aufgrund der IO-Kandidaten.
Am weitesten in der Entwicklung ist der DLL4-AK Demcizumab, der zusammen mit CELG entwickelt wird. DLL4 ist ein Notch-Ligand, so dass Demcizumab über die Hemmung des Notch-Signalweg wirkt.
In den letzten Jahren hat man für Demcizumab immer zwei Wirkweisen gesehen: die Hemmung von Krebsstammzellen (CSC) und eine Hemmung der Blutversorgung ähnlich wie mit Avastin. DLL4-AKs wurden auch von anderen Unternehmen wie z.B. REGN entwickelt. Notch ist allerdings kein unproblematisches Target... so soll gemäß Tierexperimenten die Hemmung u.U. auch Krebs fördern und in klinischen Studien waren diese Mittel toxisch für das Herz.
http://www.nature.com/scibx/journal/v4/n6/full/scibx.2011.15…
"... Although some academics say the entire class of therapeutics should be abandoned, at least one company—OncoMed Pharmaceuticals Inc.—thinks it's still business as usual because the gene knockout data that underpin the new study do not agree with the company's preclinical results. Indeed, whether the mouse model used by the Washington University team has any bearing on the preclinical Notch 1 (NOTCH1) mAbs at Genentech and Aveo is a point of debate.
The Notch pathway emerged in the 1990s as an attractive target for eliminating the stem cell–like tumor progenitor cells thought to drive many endothelial and lymphatic cancers. Starting with a 1997 licensing deal on Notch targets between Exelixis Inc. and Yale University, companies have been trying to inhibit various components of the pathway in hopes of blocking both tumor growth and vascularization.
One of the most promising targets was delta-like ligand 4 (DLL4), an extracellular ligand that activates all four mammalian Notch receptors. However, a Genentech team last year reported that antibodies against DLL4 induced liver and vascular endothelial cell proliferation in mice, rats and monkeys.
...
“We have shown mechanism-based toxicity,” said Kopan. “It's enough to remove just one receptor—NOTCH1—and you have toxicity. This says that the therapeutic window for drugs that target NOTCH1 is extremely small.”
...
“Notch signaling is one of those pathways that are exceedingly dosage dependent,” said Artavanis-Tsakonas. “If you lose Notch signaling, you change the fate of cells. There's absolutely no doubt that if you start fiddling with Notch signaling there will be consequences.”
Artavanis-Tsakonas, who cloned the fly homolog of NOTCH1 in the 1980s, is a cofounder of Exelixis. That biotech licensed patents on Artavanis-Tsakonas' Notch pathway discoveries and subsequently completed a three-year collaboration with Genentech to develop agents against targets in the pathway.
“When you make a genetic knockout, what you get is not necessarily reflective of what you get with partial inhibition with a drug for a brief period of time,” said Max Wicha, professor of oncology at the University of Michigan Medical School and director of the University of Michigan Comprehensive Cancer Center.
Wicha is a cofounder of OncoMed and a principal investigator on the Phase Ib solid tumor trial of the company's OMP-21M18, a DLL4-targeting mAb that is partnered with GlaxoSmithKline plc.
...
“In a chronic setting, inhibiting NOTCH1 would be a problem,” said Kopan. “Anybody on these drugs for a year should be watched closely.”
Wicha agreed. “The strategy for Notch inhibitors is to combine them with chemotherapy intermittently and not continuously,” he said. “I'd be very worried about long-term chronic therapy... ”
Die meisten Unternehmen wie REGN haben damals die Entwicklung eingestellt, nur OMED nicht, weshalb ich sie lange Zeit kritisch gesehen habe. Aber offensichtlich haben sie die Probleme in den Griff bekommen, indem sie Demcizumab mit zeitlichen Pausen verabreichen. Zudem versucht man über Biomarker mögliche Herzschäden bereits in einem sehr frühen Statium zu erkennen.
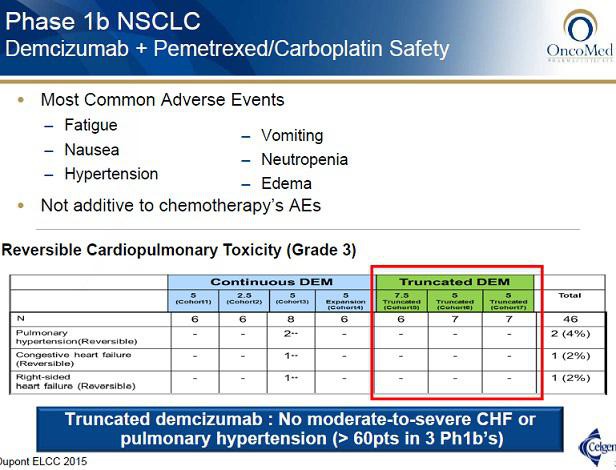
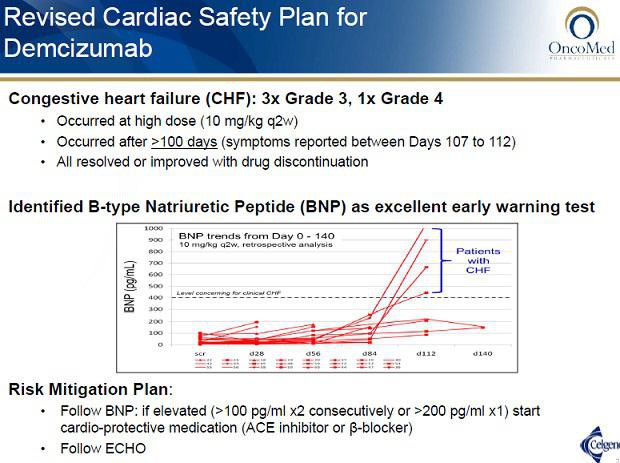
CELG ist eingestiegen, als die Probleme alle bereits bekannt waren. Eine größere Hürde steht noch in 1Q16 an, wenn die Sicherheitsdaten der P2 vorliegen... wenn es keine Bedenken gibt, erhält OMED einen weiteren 70 Mio USD Meilenstein.
Das sind die Risiken... auf der anderen Seite stehen meiner Meinung nach interessante Ergebnisse aus den bisherigen Studien.
Z.B. OS in der NSCLC PI... hier sieht es bei beiden Dosierungsformen (durchgehend und mit Unterbrechnungen) so aus, als ob sich ein "long tail" bildet... also wie bei IOs PD1&Co Langzeitüberlebende.
Es sind zwar nur kleine Studien, doch soll laut OMED die Wahrscheinlichkeit hoch sein, dass dieser Effekt nur rein zufällig aufgetreten ist.
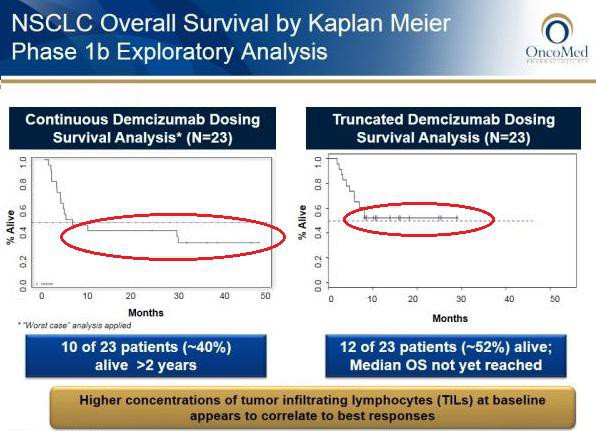
Zum Vergleich die Standard-Chemo, die heute zur Anwendung kommt
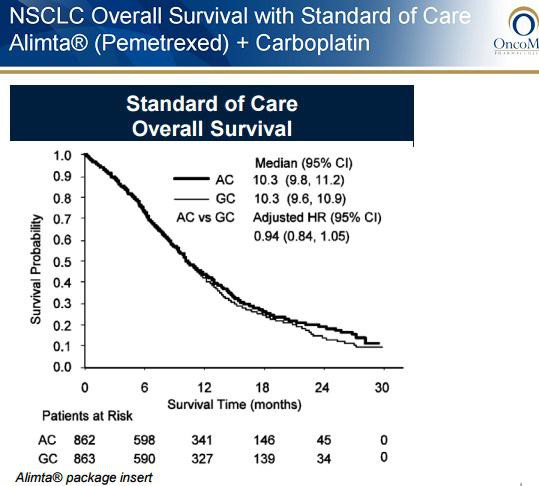
Dieser Effekt scheint abhängig vom Immunsystem zu sein... je mehr Immunzellen (TILs) sich im Tumor befinden, umso stärker ist der Effekt
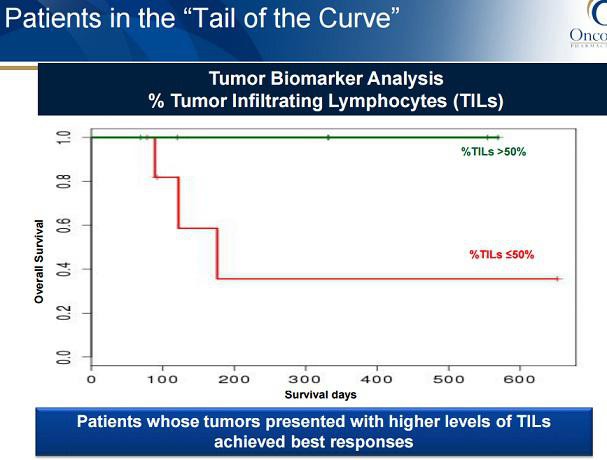
D.h. zu den ersten Effekten scheint noch ein dritter IO-Effekt zu kommen.
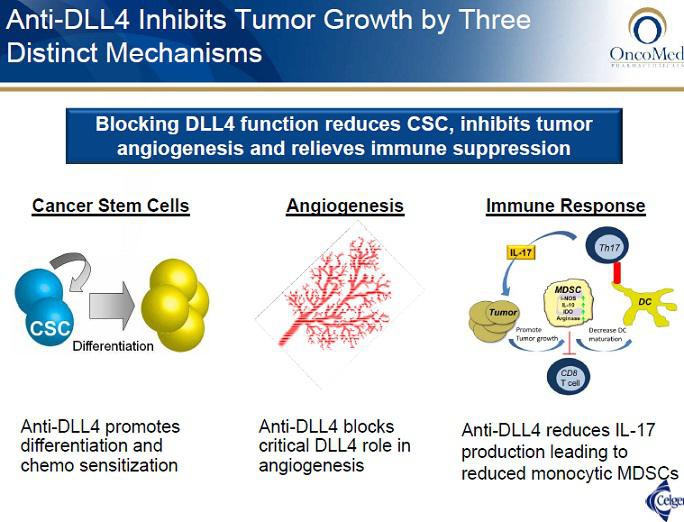
Erklärt wird dies dadurch, dass die Hemmung von DLL4 deutlich einen Teil der Immunzellen, nämlich M-MDSC, reduziert. Diese MDSC-Zellen werden vom Tumor gefördert und schützen ihn vor dem Immunsystem. Dies ist ähnlich wie z.B. FPRXs CSF1R-AK, der TAMs reduziert. Laut INCY wirkt sich auch die Hemmung von JAK oder pi3k-delta auf MDSC-Zellen aus.
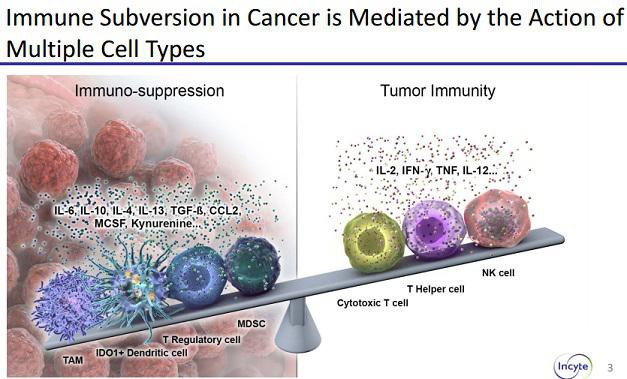
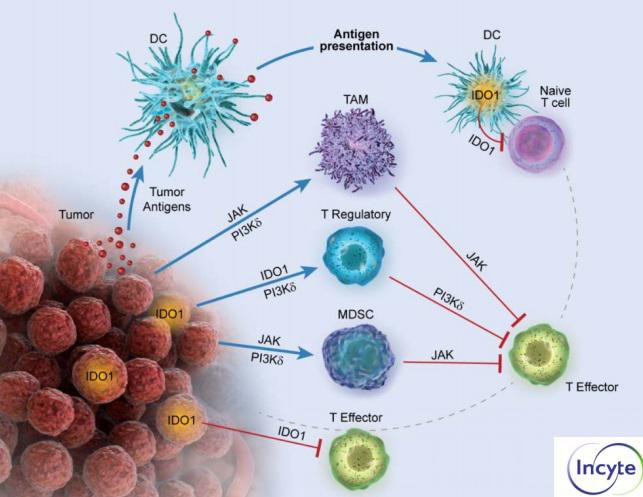
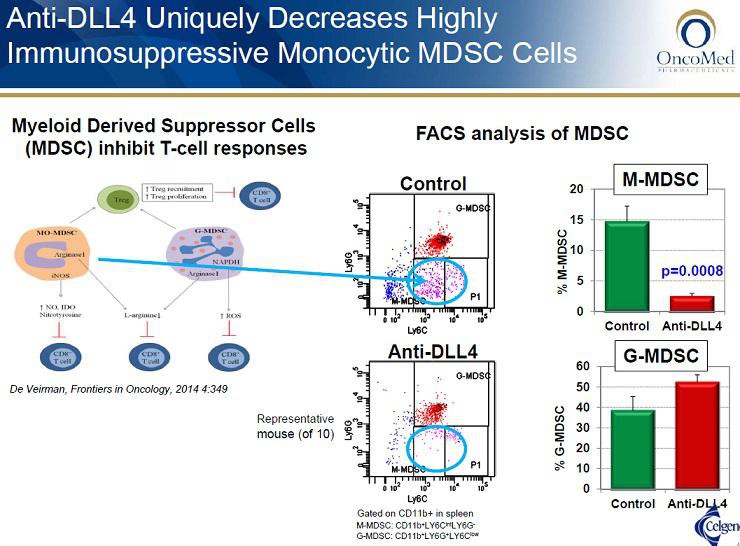
In Tierexperiementen ist eine PD1 + DLL4 Kombi aussichtsreich... Mäuse, die einmal mit dieser Kombi behandelt worden sind, erkranken nicht wieder an Krebs, wenn man erneut Krebszellen in diese Mäuse überträgt. D.h. das Immunsystem bietet einen langfristigen Schutz.
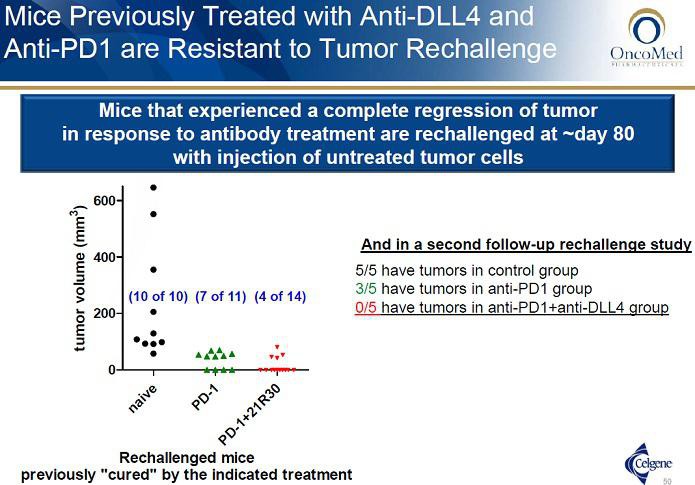
Eine weitere Verbesserung ist OMEDs DLL4+VEGF biAK. Die Hemmung von DLL4 erhöht die Produktion von VEGF, das seinerseits zu Nebenwirkungen führt und Krebs auslösen kann. Die gleichzeitige Hemmung von DLL4 + VEGF kann diese Probleme reduzieren. Außerdem sind die Wirkungen synergetisch.
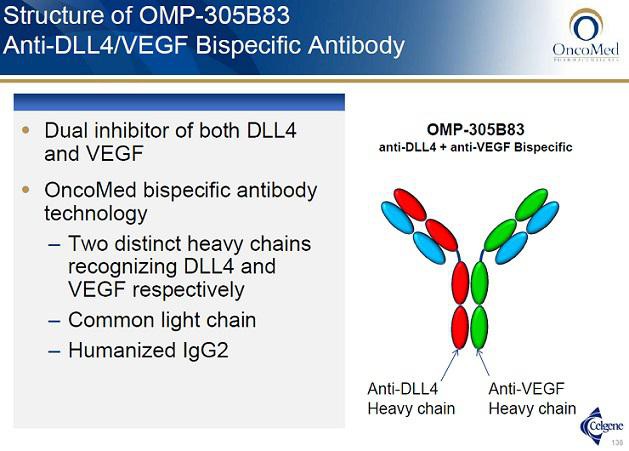
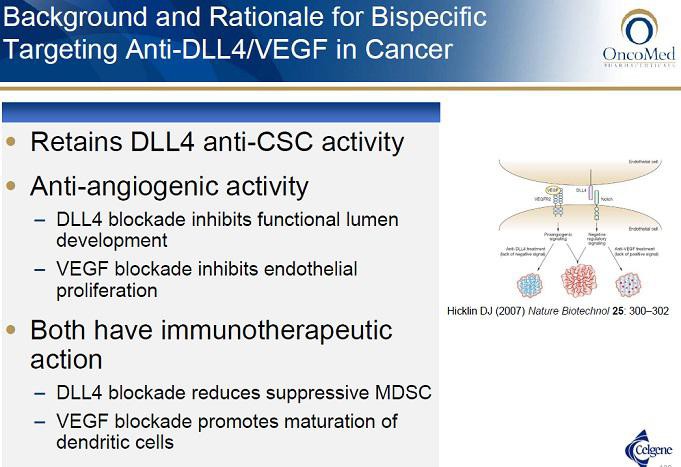
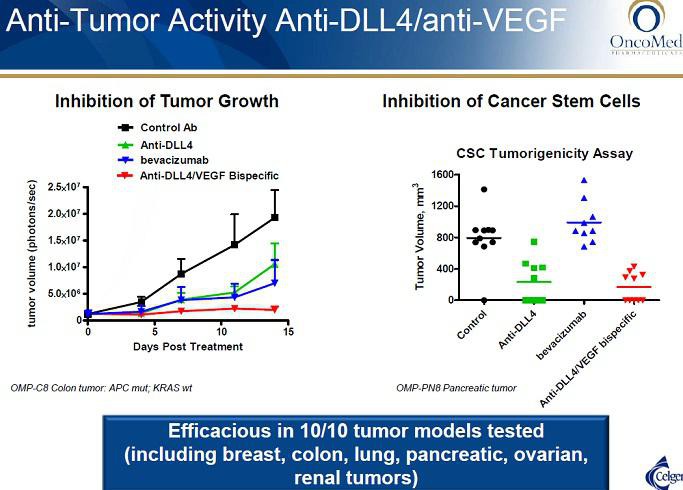
Offensichtlich ist auch CELG von Demcizumab und dem biAK überzeugt... man versucht die Entwicklung zu beschleunigen

Gruß
ipollit
Ich finde OMED aber nicht nur aufgrund der breiten Pipeline interessant, sondern speziell auch aufgrund der IO-Kandidaten.
Am weitesten in der Entwicklung ist der DLL4-AK Demcizumab, der zusammen mit CELG entwickelt wird. DLL4 ist ein Notch-Ligand, so dass Demcizumab über die Hemmung des Notch-Signalweg wirkt.
In den letzten Jahren hat man für Demcizumab immer zwei Wirkweisen gesehen: die Hemmung von Krebsstammzellen (CSC) und eine Hemmung der Blutversorgung ähnlich wie mit Avastin. DLL4-AKs wurden auch von anderen Unternehmen wie z.B. REGN entwickelt. Notch ist allerdings kein unproblematisches Target... so soll gemäß Tierexperimenten die Hemmung u.U. auch Krebs fördern und in klinischen Studien waren diese Mittel toxisch für das Herz.
http://www.nature.com/scibx/journal/v4/n6/full/scibx.2011.15…
"... Although some academics say the entire class of therapeutics should be abandoned, at least one company—OncoMed Pharmaceuticals Inc.—thinks it's still business as usual because the gene knockout data that underpin the new study do not agree with the company's preclinical results. Indeed, whether the mouse model used by the Washington University team has any bearing on the preclinical Notch 1 (NOTCH1) mAbs at Genentech and Aveo is a point of debate.
The Notch pathway emerged in the 1990s as an attractive target for eliminating the stem cell–like tumor progenitor cells thought to drive many endothelial and lymphatic cancers. Starting with a 1997 licensing deal on Notch targets between Exelixis Inc. and Yale University, companies have been trying to inhibit various components of the pathway in hopes of blocking both tumor growth and vascularization.
One of the most promising targets was delta-like ligand 4 (DLL4), an extracellular ligand that activates all four mammalian Notch receptors. However, a Genentech team last year reported that antibodies against DLL4 induced liver and vascular endothelial cell proliferation in mice, rats and monkeys.
...
“We have shown mechanism-based toxicity,” said Kopan. “It's enough to remove just one receptor—NOTCH1—and you have toxicity. This says that the therapeutic window for drugs that target NOTCH1 is extremely small.”
...
“Notch signaling is one of those pathways that are exceedingly dosage dependent,” said Artavanis-Tsakonas. “If you lose Notch signaling, you change the fate of cells. There's absolutely no doubt that if you start fiddling with Notch signaling there will be consequences.”
Artavanis-Tsakonas, who cloned the fly homolog of NOTCH1 in the 1980s, is a cofounder of Exelixis. That biotech licensed patents on Artavanis-Tsakonas' Notch pathway discoveries and subsequently completed a three-year collaboration with Genentech to develop agents against targets in the pathway.
“When you make a genetic knockout, what you get is not necessarily reflective of what you get with partial inhibition with a drug for a brief period of time,” said Max Wicha, professor of oncology at the University of Michigan Medical School and director of the University of Michigan Comprehensive Cancer Center.
Wicha is a cofounder of OncoMed and a principal investigator on the Phase Ib solid tumor trial of the company's OMP-21M18, a DLL4-targeting mAb that is partnered with GlaxoSmithKline plc.
...
“In a chronic setting, inhibiting NOTCH1 would be a problem,” said Kopan. “Anybody on these drugs for a year should be watched closely.”
Wicha agreed. “The strategy for Notch inhibitors is to combine them with chemotherapy intermittently and not continuously,” he said. “I'd be very worried about long-term chronic therapy... ”
Die meisten Unternehmen wie REGN haben damals die Entwicklung eingestellt, nur OMED nicht, weshalb ich sie lange Zeit kritisch gesehen habe. Aber offensichtlich haben sie die Probleme in den Griff bekommen, indem sie Demcizumab mit zeitlichen Pausen verabreichen. Zudem versucht man über Biomarker mögliche Herzschäden bereits in einem sehr frühen Statium zu erkennen.


CELG ist eingestiegen, als die Probleme alle bereits bekannt waren. Eine größere Hürde steht noch in 1Q16 an, wenn die Sicherheitsdaten der P2 vorliegen... wenn es keine Bedenken gibt, erhält OMED einen weiteren 70 Mio USD Meilenstein.
Das sind die Risiken... auf der anderen Seite stehen meiner Meinung nach interessante Ergebnisse aus den bisherigen Studien.
Z.B. OS in der NSCLC PI... hier sieht es bei beiden Dosierungsformen (durchgehend und mit Unterbrechnungen) so aus, als ob sich ein "long tail" bildet... also wie bei IOs PD1&Co Langzeitüberlebende.
Es sind zwar nur kleine Studien, doch soll laut OMED die Wahrscheinlichkeit hoch sein, dass dieser Effekt nur rein zufällig aufgetreten ist.

Zum Vergleich die Standard-Chemo, die heute zur Anwendung kommt

Dieser Effekt scheint abhängig vom Immunsystem zu sein... je mehr Immunzellen (TILs) sich im Tumor befinden, umso stärker ist der Effekt

D.h. zu den ersten Effekten scheint noch ein dritter IO-Effekt zu kommen.

Erklärt wird dies dadurch, dass die Hemmung von DLL4 deutlich einen Teil der Immunzellen, nämlich M-MDSC, reduziert. Diese MDSC-Zellen werden vom Tumor gefördert und schützen ihn vor dem Immunsystem. Dies ist ähnlich wie z.B. FPRXs CSF1R-AK, der TAMs reduziert. Laut INCY wirkt sich auch die Hemmung von JAK oder pi3k-delta auf MDSC-Zellen aus.



In Tierexperiementen ist eine PD1 + DLL4 Kombi aussichtsreich... Mäuse, die einmal mit dieser Kombi behandelt worden sind, erkranken nicht wieder an Krebs, wenn man erneut Krebszellen in diese Mäuse überträgt. D.h. das Immunsystem bietet einen langfristigen Schutz.

Eine weitere Verbesserung ist OMEDs DLL4+VEGF biAK. Die Hemmung von DLL4 erhöht die Produktion von VEGF, das seinerseits zu Nebenwirkungen führt und Krebs auslösen kann. Die gleichzeitige Hemmung von DLL4 + VEGF kann diese Probleme reduzieren. Außerdem sind die Wirkungen synergetisch.



Offensichtlich ist auch CELG von Demcizumab und dem biAK überzeugt... man versucht die Entwicklung zu beschleunigen

Gruß
ipollit
Puh! Ganz schön was los!
CLVS
Ich finde die Verlängerung sehr gut, denn Anfang Juni ist bereits die ASCO. Updates zu Ruca, Roci und Luci (?) könnten also vor der Entscheidung zur Zulassung kommen. Natürlich könnte ein CRL auch vorher kommen, meist kamen die aber nicht so viel früher als nach PDUFA-date vorgesehen. Oder?
Martin Shkreli
Ich bin sonst nicht so gehässig, aber ich habe mich darüber gefreut.

Jetzt noch ein ähnliches Bild mit Sepp Blatter...
GLPG
Warum ist die Aktie bitteschön im Minus? Häh!?
CLVS
Ich finde die Verlängerung sehr gut, denn Anfang Juni ist bereits die ASCO. Updates zu Ruca, Roci und Luci (?) könnten also vor der Entscheidung zur Zulassung kommen. Natürlich könnte ein CRL auch vorher kommen, meist kamen die aber nicht so viel früher als nach PDUFA-date vorgesehen. Oder?
Martin Shkreli
Ich bin sonst nicht so gehässig, aber ich habe mich darüber gefreut.

Jetzt noch ein ähnliches Bild mit Sepp Blatter...
GLPG
Warum ist die Aktie bitteschön im Minus? Häh!?

Antwort auf Beitrag Nr.: 51.324.417 von ipollit am 17.12.15 11:23:59GLPG, INCY
GLPG ist nun trotz des guten GILD-Deals im Minus... vielleicht weil nun erstmal eine Zeit lang nichts mehr ansteht? Eine mögliche Zulassung wird jedenfalls noch Jahre dauern. Trotzdem besitzt GLPG nun über 1 Mrd USD Cash bei einem Börsenwert von 2,2 Mrd USD.
Hat eigentlich dieser Deal Auswirkungen auf mögliche weitere Übernahmekandidaten von GILD? Immerhin haben sie noch deutlich über 20 Mrd USD und müssten eigentlich auch mal eine größere Übernahme tätigen, um langfristig das Wachstum zu sichern.
Oft genannte Kandidaten waren INCY und VRTX. Nun ist INCY aber stark im JAK-Bereich vertreten... Bari ist ein direkter Konkurrent von Filgotinib in RA. Macht es Sinn, in gleich zwei konkurrierende Unternehmen einzusteigen? Ähnlich sieht es mit VRTX aus... das zweite Standbein von GLPG ist CF. Damit ist VRTX ein direkter Konkurrent von GLPG und mit einer Übernahme von VRTX würde der aktuelle Partner GILD gleichzeitig auch zum Konkurrenten. Dieser umfangreiche Deal mit GLPG ist also auch bezügl. INCY und VRTX interessant... eine Übernahme dieser beiden fände ich nun eher merkwürdig.

Gruß
ipollit
GLPG ist nun trotz des guten GILD-Deals im Minus... vielleicht weil nun erstmal eine Zeit lang nichts mehr ansteht? Eine mögliche Zulassung wird jedenfalls noch Jahre dauern. Trotzdem besitzt GLPG nun über 1 Mrd USD Cash bei einem Börsenwert von 2,2 Mrd USD.
Hat eigentlich dieser Deal Auswirkungen auf mögliche weitere Übernahmekandidaten von GILD? Immerhin haben sie noch deutlich über 20 Mrd USD und müssten eigentlich auch mal eine größere Übernahme tätigen, um langfristig das Wachstum zu sichern.
Oft genannte Kandidaten waren INCY und VRTX. Nun ist INCY aber stark im JAK-Bereich vertreten... Bari ist ein direkter Konkurrent von Filgotinib in RA. Macht es Sinn, in gleich zwei konkurrierende Unternehmen einzusteigen? Ähnlich sieht es mit VRTX aus... das zweite Standbein von GLPG ist CF. Damit ist VRTX ein direkter Konkurrent von GLPG und mit einer Übernahme von VRTX würde der aktuelle Partner GILD gleichzeitig auch zum Konkurrenten. Dieser umfangreiche Deal mit GLPG ist also auch bezügl. INCY und VRTX interessant... eine Übernahme dieser beiden fände ich nun eher merkwürdig.
Gruß
ipollit
ich habe mir einige deut. Medtech/Biotechs angesehen - u.a. Biotest, Morphosys. Hat mich alles nicht überzeugt.
Frage an echte Biotechkenner/Mediziner: lohnt es sich Epigenomics anzusehen ?
Frage an echte Biotechkenner/Mediziner: lohnt es sich Epigenomics anzusehen ?
ISIS -> IONS
Isis benennt sich um in Ionis... d.h. ISIS wird zu IONS. Leider ist das wohl nicht anders zu machen, wenn der Name so belastet wird.
Gruß
ipollit
Isis benennt sich um in Ionis... d.h. ISIS wird zu IONS. Leider ist das wohl nicht anders zu machen, wenn der Name so belastet wird.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.332.040 von SmartCap am 18.12.15 11:31:27Hallo SmartCap,
ich finde deutsche Biotechs leider auch nicht so interessant, zumindest ist die Auswahl in den USA zig-fach größer. Morphosys sind wohl die besten.
Ist Epigenomics nicht eher ein MedTech oder Dienstleister? Spannender sind für mich die echten Medikamenten-Entwickler, so dass ich mich im MedTech-Bereich nicht so auskenne. Wäre da nicht eher eine Qiagen interessant? Die sind auch weltweit mit führend.
Gruß
ipollit
ich finde deutsche Biotechs leider auch nicht so interessant, zumindest ist die Auswahl in den USA zig-fach größer. Morphosys sind wohl die besten.
Ist Epigenomics nicht eher ein MedTech oder Dienstleister? Spannender sind für mich die echten Medikamenten-Entwickler, so dass ich mich im MedTech-Bereich nicht so auskenne. Wäre da nicht eher eine Qiagen interessant? Die sind auch weltweit mit führend.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.334.473 von ipollit am 18.12.15 16:01:13danke ipolit: epigenomics = medtech würde ich sagen ...
qiagen ist sicher ein top-Unternehmen, aber vermutlich fair gepreist ...
qiagen ist sicher ein top-Unternehmen, aber vermutlich fair gepreist ...
arry: Pierre Fabre agreement
Array Announces Closing Of Pierre Fabre Transaction
BOULDER, Colo., Dec. 21, 2015 /PRNewswire/ -- Array BioPharma Inc. (NASDAQ: ARRY) today announced the closing of its definitive agreement with Pierre Fabre following approval of the agreement by the European Commission on Competition (ECC). The definitive agreement, announced on November 16, 2015, relates to globally developing and commercializing Array's late-stage novel oncology products, binimetinib and encorafenib. Binimetinib, a MEK inhibitor, and encorafenib, a BRAF inhibitor, are currently advancing in three, global Phase 3 trials for melanoma and ovarian cancer.
About the Array / Pierre Fabre Agreement
Under the terms of the agreement, Array will receive an upfront payment of $30 million and retains exclusive commercialization rights for binimetinib and encorafenib in the United States, Canada, Japan, Korea and Israel. Pierre Fabre will have exclusive rights to commercialize both products in all other countries, including Europe, Asia and Latin America. Array is entitled to receive up to $425 million if certain development and commercialization milestones are achieved, and is eligible for robust, tiered double-digit royalties. Array and Pierre Fabre have agreed to split future development costs on a 60:40 basis (Array:Pierre Fabre) with initial funding committed for new clinical trials in colorectal cancer and melanoma. All ongoing binimetinib and encorafenib clinical trials remain substantially funded through completion by Novartis.
Es würde mich interessieren, ob in den 425 mio auch Meilensteinzahlungen nach erfolgreichen Phase III Studien enthalten sind. Das bleibt wohl offen, bis wir die Q4 Zahlen sehen.
VG
A
MDVN
MDVN hat nun mit dem PD1-AK Pidi eine PII in rr DLBCL gestartet, die theoretisch eine Zulassung aufgrund von ResponseRates ermöglicht.
"...international Phase 2 clinical trial that will evaluate the safety and efficacy of MDV9300 (pidilizumab) in patients with relapsed or refractory diffuse large B-cell lymphoma (DLBCL). In light of the unmet medical need in this area, a positive outcome in this trial has the potential to support registration for this indication in the U.S. and European Union utilizing available expedited pathways... The international, open-label, Phase 2 trial of MDV9300 is expected to enroll approximately 180 patients with an incomplete response following salvage therapy or autologous stem cell transplantation for relapsed or refractory CD20+ diffuse large B-cell lymphoma, transformed indolent lymphoma or primary mediastinal B-cell lymphoma... The primary endpoint of the trial is best overall response rate."

Wie weit das funktioniert, muss man sehen... Pidi soll etwas anders wirken als andere PD1-AKs... viele (die ich nicht für Experten halte) sagen schlechter. Gute Ergebnisse gab es in Kombi mit Rituxan, u.U. aufgrund einer Aktivierung von NK-Zellen. Dies kommt in dieser PII allerdings offensichtlich nicht zum tragen.
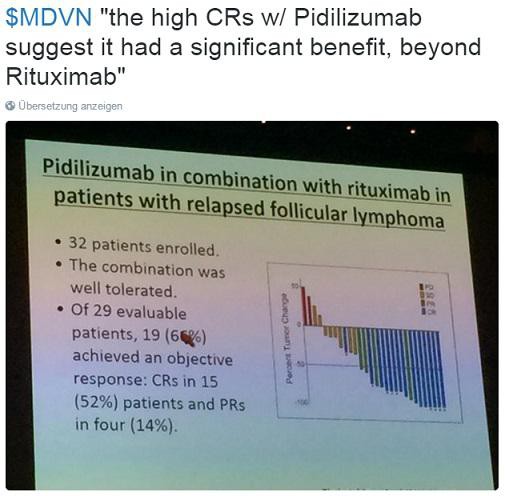
Ende nächsten Jahres oder erst 2017 sollten auf PIII-Daten des PARP-Hemmers Talazoparib in Brustkrebs vorliegen. Es gibt alle auch Zulassungsstudien unabhängig von Xtandi.

Gruß
ipollit
MDVN hat nun mit dem PD1-AK Pidi eine PII in rr DLBCL gestartet, die theoretisch eine Zulassung aufgrund von ResponseRates ermöglicht.
"...international Phase 2 clinical trial that will evaluate the safety and efficacy of MDV9300 (pidilizumab) in patients with relapsed or refractory diffuse large B-cell lymphoma (DLBCL). In light of the unmet medical need in this area, a positive outcome in this trial has the potential to support registration for this indication in the U.S. and European Union utilizing available expedited pathways... The international, open-label, Phase 2 trial of MDV9300 is expected to enroll approximately 180 patients with an incomplete response following salvage therapy or autologous stem cell transplantation for relapsed or refractory CD20+ diffuse large B-cell lymphoma, transformed indolent lymphoma or primary mediastinal B-cell lymphoma... The primary endpoint of the trial is best overall response rate."

Wie weit das funktioniert, muss man sehen... Pidi soll etwas anders wirken als andere PD1-AKs... viele (die ich nicht für Experten halte) sagen schlechter. Gute Ergebnisse gab es in Kombi mit Rituxan, u.U. aufgrund einer Aktivierung von NK-Zellen. Dies kommt in dieser PII allerdings offensichtlich nicht zum tragen.

Ende nächsten Jahres oder erst 2017 sollten auf PIII-Daten des PARP-Hemmers Talazoparib in Brustkrebs vorliegen. Es gibt alle auch Zulassungsstudien unabhängig von Xtandi.
Gruß
ipollit
CMRX
Bald sollten die PIII-Daten zu Brincidofovir gegen CMV in HCT kommen.
Brincidofovir ist ein Breitband-Virostatikum, also so eine Art Antibiotikum gegen Viren. Konkret wirkt es gegen DNA-Viren wie Herpes, aber nicht RNA-Viren wie z.B. Ebola.
In der Regel benötigt man nicht derart potente Mittel, da ein gesunder Körper die meisten Viren abwehren kann. Anders sieht es aus, wenn das Immunsystem geschwächt ist. Dies ist z.B. nach einer Stammzelltransplantation (HCT) der Fall, bei der die komplette Körperabwehr für einige Zeit fehlt oder bei Organtransplantationen (SOT), bei denen das Immunsystem unterdrückt wird, damit es das fremde Organ nicht direkt wieder abstößt.
Cytomegalovirus (CMV) ist normalerweise ein eher harmloses Herpesvirus. Allerdings bleibt es nach einer Infektion ein Leben lang im Körper. Bei einem unterdrücktem Immunsystem wird es wieder aktiv und kann bei Transplantationen u.a. zu einer Abstoßung des Organs führen. Eventuell werden auch weitere Viren wieder aktiv, die ebenfalls gravierende Folgen haben können. In solchen Fällen wird ein Virostatikum benötigt.

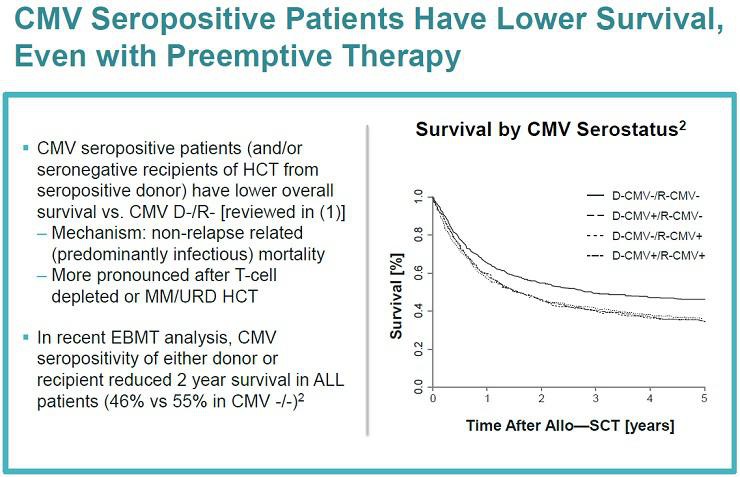
Brincidofovir ist ein sehr wirksames Virostatikum.
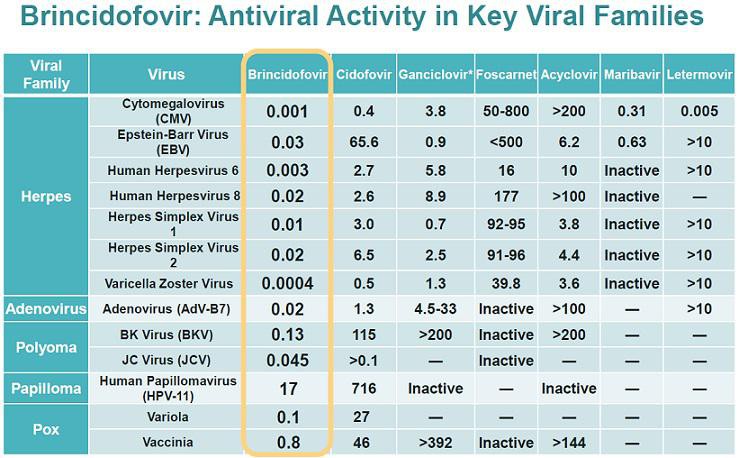
In einer PII konnte Brincidofovir erfolgreich CMV in HCT verhindern.
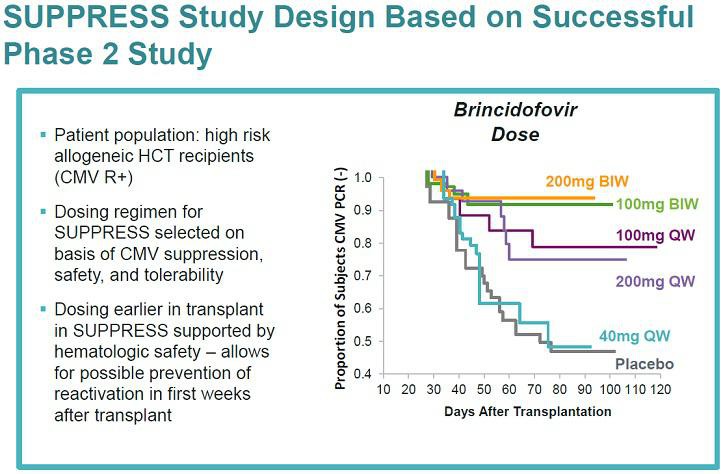
Neben CMV können auch weitere Viren das Überleben reduzieren. Auch hier soll Brincidofovir helfen

Bisher werden Virostatika wenig prophylaktisch gegeben, da sie teilweise erhebliche Nebenwirkungen haben. So kann Ganciclovir zu einer starken Verminderung der weißen Blutkörperchen (neutropenia) führen, also eine weitere starke Schwächung des Immunsystems. Dadurch verschlechtert sich sogar insgesamt das Überleben.
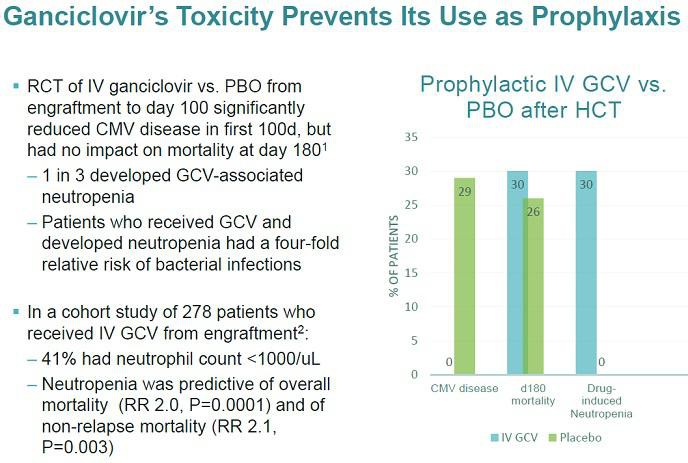
Bei Nierentransplantationen kann neben CMV auch BKV gravierende Folgen haben, da eine Reaktivierung des BKV-Virus die Spenderniere dauerhaft schädigen kann.
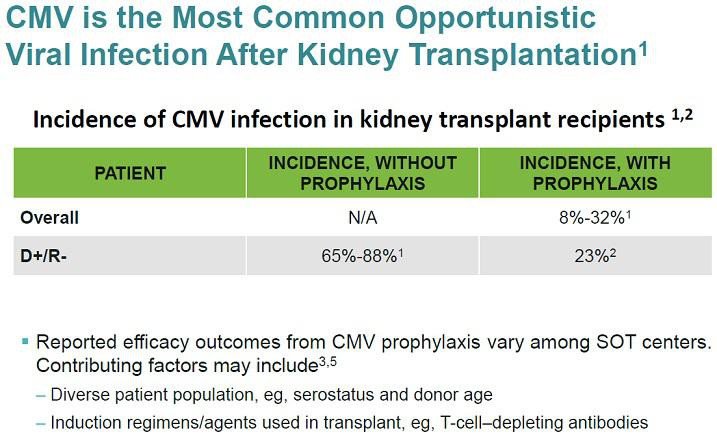
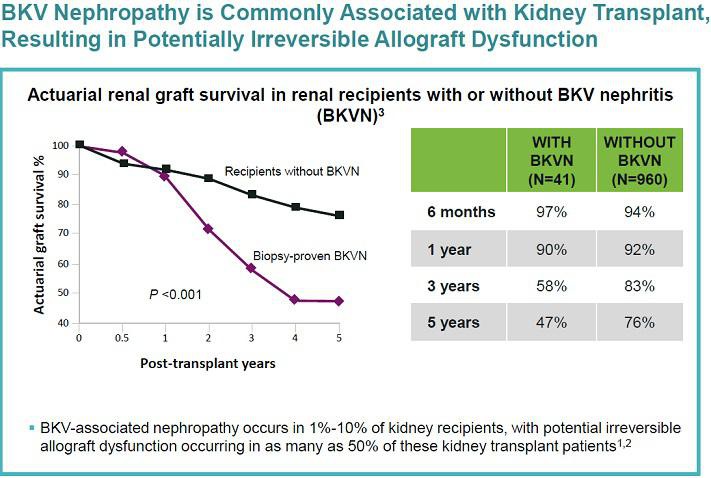
Eine Behandlung mit Brincidofovir könnte die Nierenfunktion der Spenderniere deutlich verbessern.
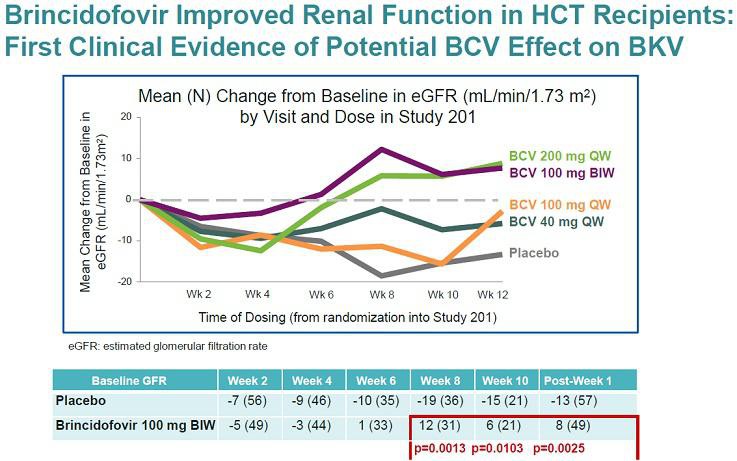
Für Transplantationen müssen passende Spender gefunden werden und die Kosten einer Transplantation können 1 Mio USD erreichen, so dass es nicht nur im Interesse der Patienten ist, dass die Transplantation erfolgreich ist, sondern auch aus Kostengründen das Beste für den Erfolg getan werden sollte. Brincidofovir könnte einen deutlichen Fortschritt bringen.
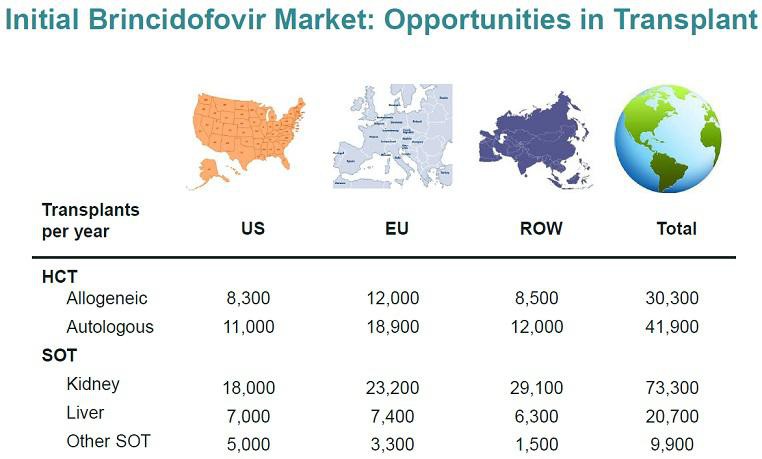
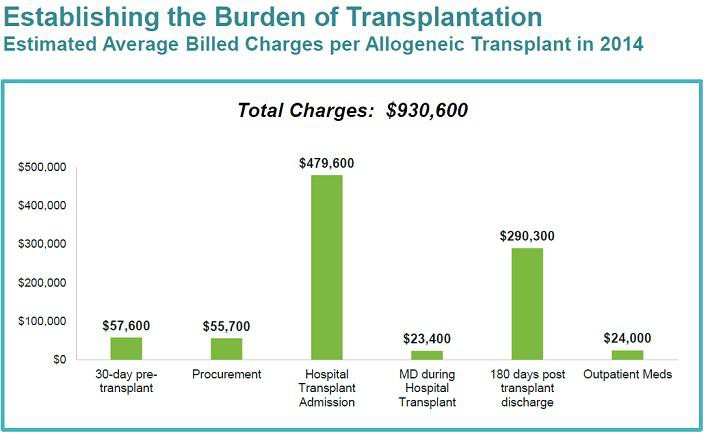
Die SUPPRESS PIII-Daten gegen CMV in HCT sollen Anfang des Jahres kommen. Daneben gibt es noch PIII-Studien in SOT. Brincidofovir hilft auch gegen Pocken-Viren, so dass es einen Auftrag der US-Regierung gibt... nach den Tierstudien könnte eine Brincidofovir-Reserve aufgebaut werden gegen eventuelle biologische Angriffe mit Pocken-Viren.
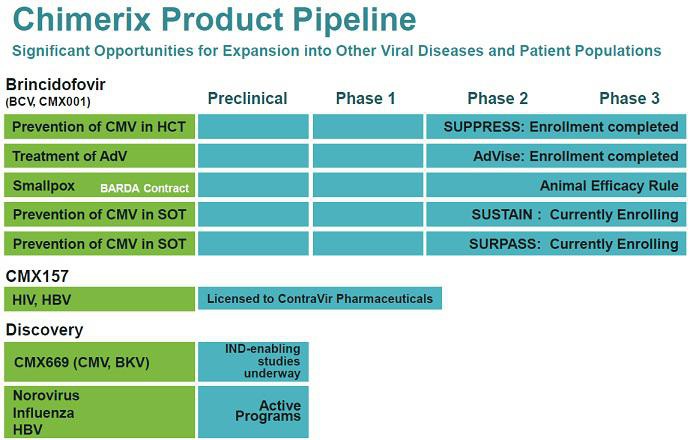

Hier wird z.B. von möglichen 2 Mrd USD Peak Sales gesprochen:
http://www.newsobserver.com/news/business/article10219937.ht…
"Chimerix’s patent for antiviral extended until 2034
...An analyst at William Blair & Co. issued a research note saying the patent increases the total peak sales of the Chimerix drug from $2 billion to $2.4 billion."
CMRX hat aktuell eine MK von 1,68 Mrd USD und besitzt 100% der Rechte an Brincidofovir. Ob solche Umsätze erreichbar sind, hängt vom Erfolg der PIII ab, denn den Kosten für Brincidofovir muss auch ein entsprechender Nutzen gegenüberstehen. Ich habe mir jedenfalls eine erste Position zugelegt.

Gruß
ipollit
Bald sollten die PIII-Daten zu Brincidofovir gegen CMV in HCT kommen.
Brincidofovir ist ein Breitband-Virostatikum, also so eine Art Antibiotikum gegen Viren. Konkret wirkt es gegen DNA-Viren wie Herpes, aber nicht RNA-Viren wie z.B. Ebola.
In der Regel benötigt man nicht derart potente Mittel, da ein gesunder Körper die meisten Viren abwehren kann. Anders sieht es aus, wenn das Immunsystem geschwächt ist. Dies ist z.B. nach einer Stammzelltransplantation (HCT) der Fall, bei der die komplette Körperabwehr für einige Zeit fehlt oder bei Organtransplantationen (SOT), bei denen das Immunsystem unterdrückt wird, damit es das fremde Organ nicht direkt wieder abstößt.
Cytomegalovirus (CMV) ist normalerweise ein eher harmloses Herpesvirus. Allerdings bleibt es nach einer Infektion ein Leben lang im Körper. Bei einem unterdrücktem Immunsystem wird es wieder aktiv und kann bei Transplantationen u.a. zu einer Abstoßung des Organs führen. Eventuell werden auch weitere Viren wieder aktiv, die ebenfalls gravierende Folgen haben können. In solchen Fällen wird ein Virostatikum benötigt.


Brincidofovir ist ein sehr wirksames Virostatikum.

In einer PII konnte Brincidofovir erfolgreich CMV in HCT verhindern.

Neben CMV können auch weitere Viren das Überleben reduzieren. Auch hier soll Brincidofovir helfen

Bisher werden Virostatika wenig prophylaktisch gegeben, da sie teilweise erhebliche Nebenwirkungen haben. So kann Ganciclovir zu einer starken Verminderung der weißen Blutkörperchen (neutropenia) führen, also eine weitere starke Schwächung des Immunsystems. Dadurch verschlechtert sich sogar insgesamt das Überleben.

Bei Nierentransplantationen kann neben CMV auch BKV gravierende Folgen haben, da eine Reaktivierung des BKV-Virus die Spenderniere dauerhaft schädigen kann.


Eine Behandlung mit Brincidofovir könnte die Nierenfunktion der Spenderniere deutlich verbessern.

Für Transplantationen müssen passende Spender gefunden werden und die Kosten einer Transplantation können 1 Mio USD erreichen, so dass es nicht nur im Interesse der Patienten ist, dass die Transplantation erfolgreich ist, sondern auch aus Kostengründen das Beste für den Erfolg getan werden sollte. Brincidofovir könnte einen deutlichen Fortschritt bringen.


Die SUPPRESS PIII-Daten gegen CMV in HCT sollen Anfang des Jahres kommen. Daneben gibt es noch PIII-Studien in SOT. Brincidofovir hilft auch gegen Pocken-Viren, so dass es einen Auftrag der US-Regierung gibt... nach den Tierstudien könnte eine Brincidofovir-Reserve aufgebaut werden gegen eventuelle biologische Angriffe mit Pocken-Viren.


Hier wird z.B. von möglichen 2 Mrd USD Peak Sales gesprochen:
http://www.newsobserver.com/news/business/article10219937.ht…
"Chimerix’s patent for antiviral extended until 2034
...An analyst at William Blair & Co. issued a research note saying the patent increases the total peak sales of the Chimerix drug from $2 billion to $2.4 billion."
CMRX hat aktuell eine MK von 1,68 Mrd USD und besitzt 100% der Rechte an Brincidofovir. Ob solche Umsätze erreichbar sind, hängt vom Erfolg der PIII ab, denn den Kosten für Brincidofovir muss auch ein entsprechender Nutzen gegenüberstehen. Ich habe mir jedenfalls eine erste Position zugelegt.
Gruß
ipollit
AGEN
Zwischenzeitlich hatte ich AGEN verkauft, nun aber wieder eine neue Position. Bis 1Q16 soll es 3 INDs für IO-Kandidaten geben, die zusammen mit INCY oder alleine entwickelt werden: Mit INCY in einer 50:50-Partnerschaft werden das GITR- und OX40-AKs sein. Als erstes möchte AGEN einen eigenen CTLA4-AK in die P1 bringen.
Die IO-Pipeline umfasst 7 veröffentlichte und 8 weitere IO-Targets...

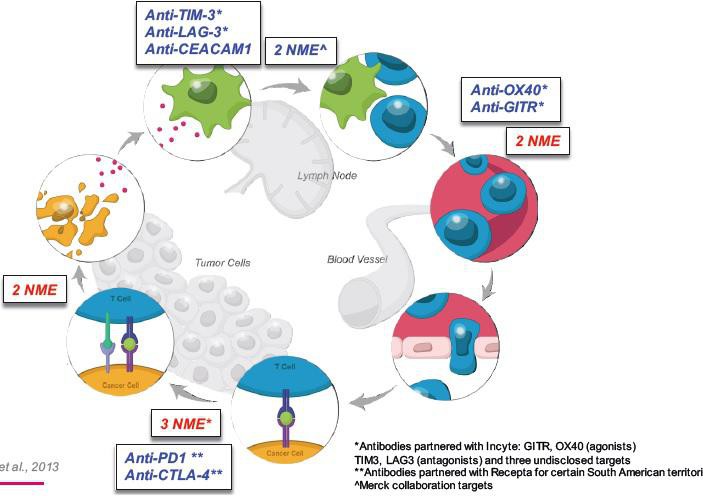
GITR und OX40 werden zu gleichen Teilen zusammen mit INCY entwickelt

CTLA4 ist auch das Target von Yervoy und Tremelimumab. AGEN entwickelt gleich mehrere CTLA4-AKs, die unterschiedliche Wirkweisen haben sollen.
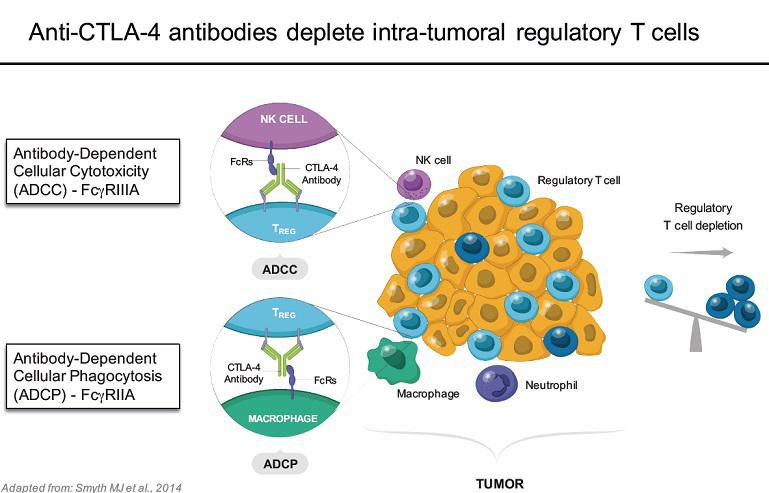
Wichtig für die Wirkung soll der Fc-Teil des Antikörpers sein... z.B. ob der AK aktivierend oder hemmend wirkt. AGEN versucht u.a. über die Optimierung des fc-Teils die IO-AKs weiter zu verbessern.
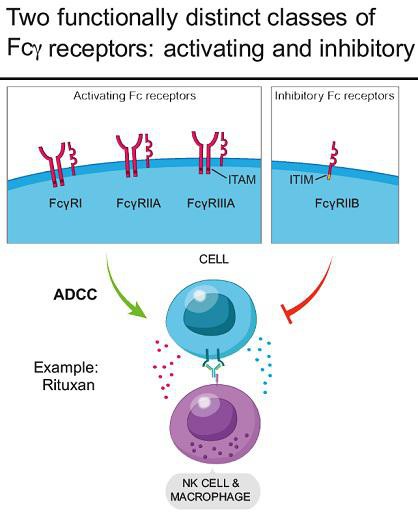
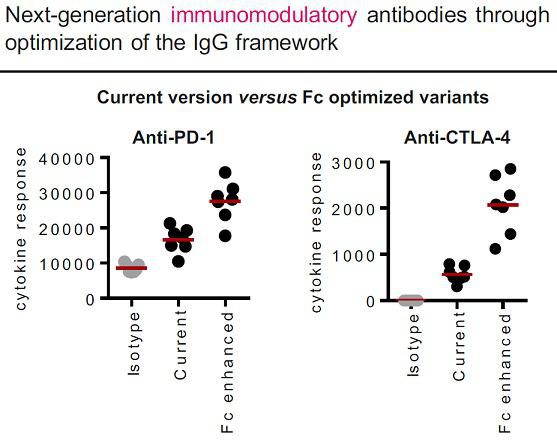
AGEN will CTLA4-AKs auch mit eigenen Vakzinen kombinieren... die Kombis sind theoretisch synergetisch.
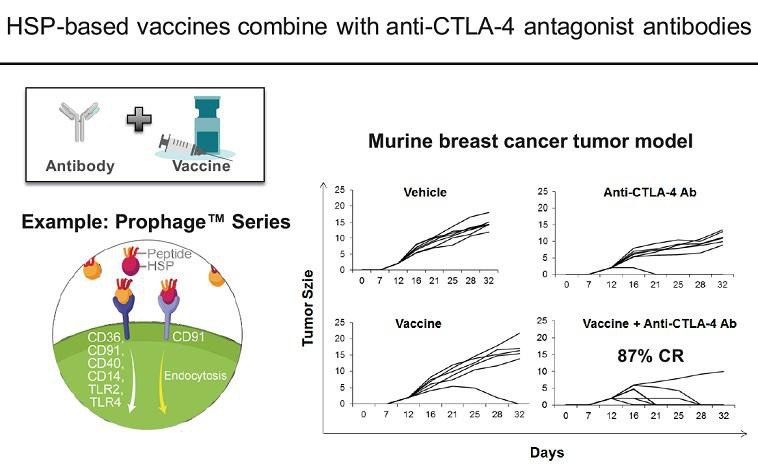
Ein Vorteil der vielen eigenen IO-Kandidaten ist, dass AGEN ohne dritte selber vieles kombinieren kann. Im Sommer hat man z.B. einen CEACAM1-AK einlizensiert. Dieser könnte mit PD1 oder mit TIM3 kombinierbar sein... über beide verfügt AGEN
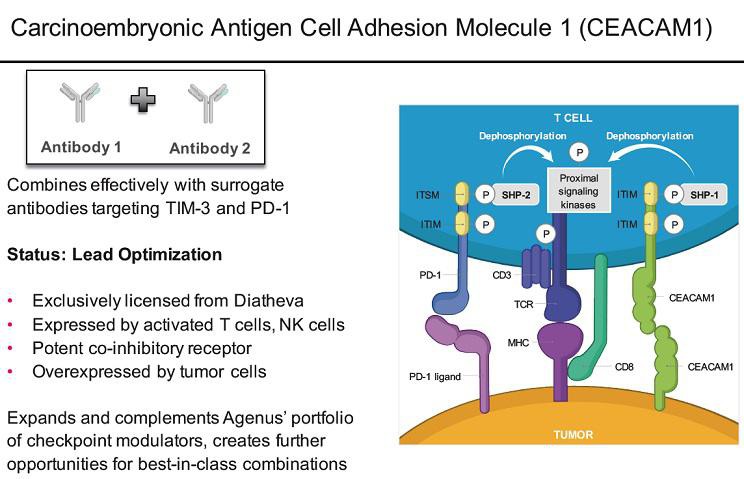
Merck hat im Sommer ebenfalls das Unternehmen cCAM mit einem CEACAM1-AK in P1 für 95 Mio USD + 510 Mio USD Meilensteinen übernommen. Vielleicht wird CEACAM1 auch mal ein interessantes Target sein.

Weiter in der Pipeline gibt es ein Adjuvant für Impfstoffe und eine spezielle Krebs-Vakzine.
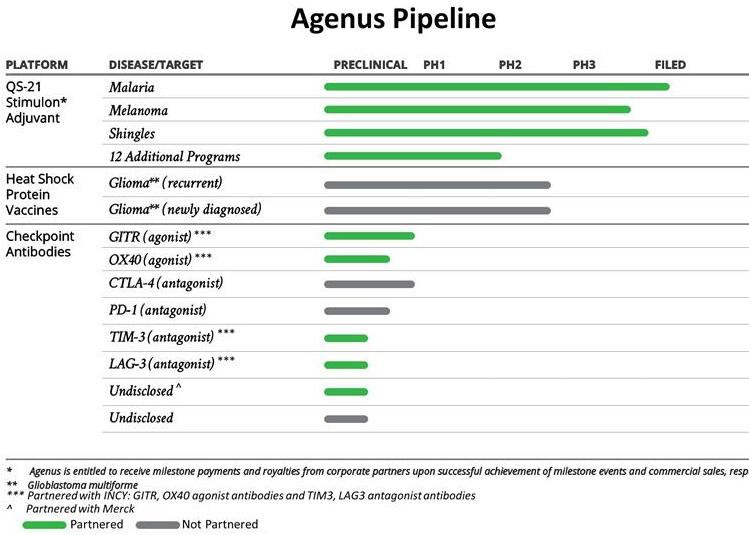
Der Adjuvant QS-21 wird anscheinend von Partnern bei vielen neuen Vakzinen verwendet. Ein Malaria- oder Herpes-Impfstoff kann Mrd einbringen... AGEN erhält davon kleine Royalties von ca. 2%.

Der Krebs-Impfstoff Provenge ist ein sehr spezieller Impfstoff. Er wird für jeden einzelnen Patienten einzeln hergestellt, indem typische Antigene des Tumors über die HSP-Proteine gesammelt werden. HSP transportiert ständig Antigene aus den Zellen, um sie dem Immunsystem zu präsentieren. Die APC-Zellen leiten dann die Immunantwort ein.
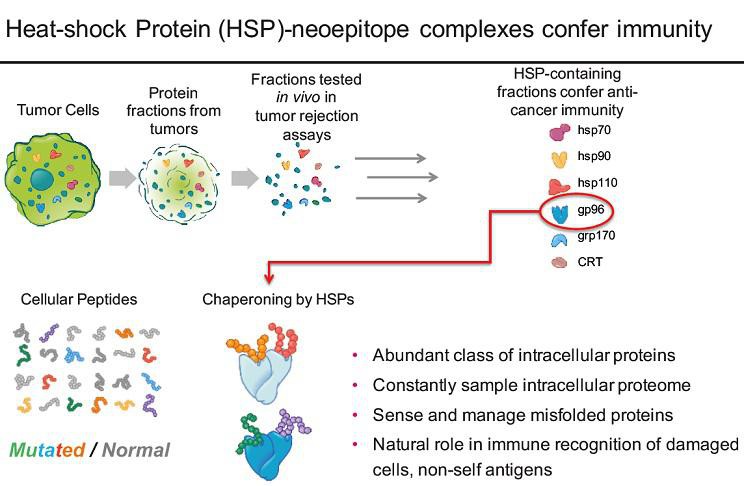
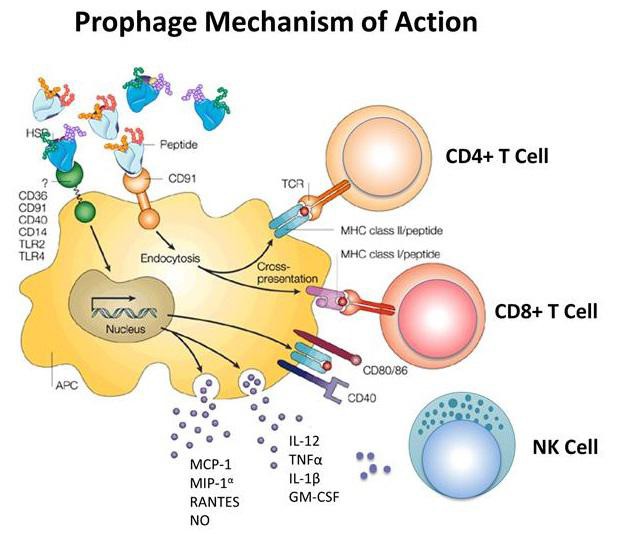
AGEN versucht diesen Ansatz mit AutoSynVax zu optimieren. Der Tumor soll vollständig genetisch analysiert, aus den Daten relevante Neo-Antigene (das sind die Antigene, die eher körperfremd sind und auf die das Immunsystem ansprechen sollte) extrahiert und daraus eine HSP-Vakzine erstellt werden, die dann mit Adjuvanten wie QS-21 und IO-Kandidaten wie CTLA4 dem Patienten verabreicht wird.
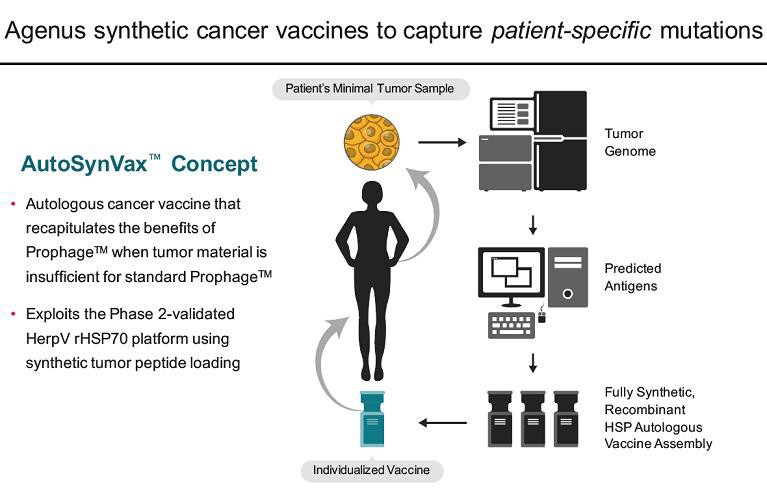
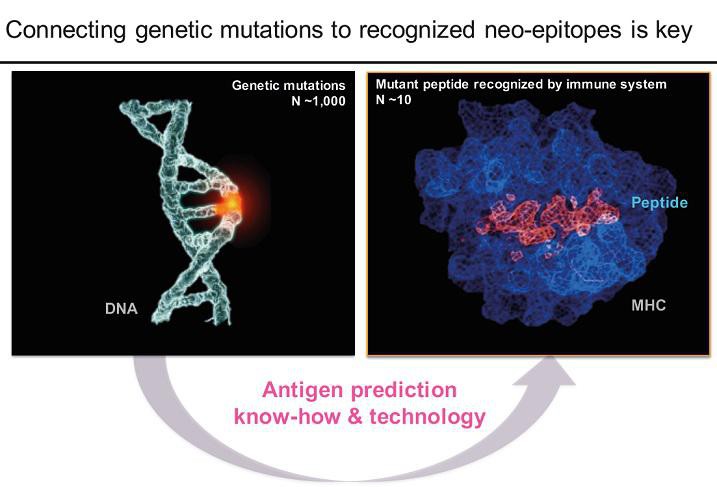
Mal schauen... sehe ich als Ergänzung zu meinen anderen IO-Unternehmen.

Gruß
ipollit
Zwischenzeitlich hatte ich AGEN verkauft, nun aber wieder eine neue Position. Bis 1Q16 soll es 3 INDs für IO-Kandidaten geben, die zusammen mit INCY oder alleine entwickelt werden: Mit INCY in einer 50:50-Partnerschaft werden das GITR- und OX40-AKs sein. Als erstes möchte AGEN einen eigenen CTLA4-AK in die P1 bringen.
Die IO-Pipeline umfasst 7 veröffentlichte und 8 weitere IO-Targets...


GITR und OX40 werden zu gleichen Teilen zusammen mit INCY entwickelt

CTLA4 ist auch das Target von Yervoy und Tremelimumab. AGEN entwickelt gleich mehrere CTLA4-AKs, die unterschiedliche Wirkweisen haben sollen.

Wichtig für die Wirkung soll der Fc-Teil des Antikörpers sein... z.B. ob der AK aktivierend oder hemmend wirkt. AGEN versucht u.a. über die Optimierung des fc-Teils die IO-AKs weiter zu verbessern.


AGEN will CTLA4-AKs auch mit eigenen Vakzinen kombinieren... die Kombis sind theoretisch synergetisch.

Ein Vorteil der vielen eigenen IO-Kandidaten ist, dass AGEN ohne dritte selber vieles kombinieren kann. Im Sommer hat man z.B. einen CEACAM1-AK einlizensiert. Dieser könnte mit PD1 oder mit TIM3 kombinierbar sein... über beide verfügt AGEN

Merck hat im Sommer ebenfalls das Unternehmen cCAM mit einem CEACAM1-AK in P1 für 95 Mio USD + 510 Mio USD Meilensteinen übernommen. Vielleicht wird CEACAM1 auch mal ein interessantes Target sein.

Weiter in der Pipeline gibt es ein Adjuvant für Impfstoffe und eine spezielle Krebs-Vakzine.

Der Adjuvant QS-21 wird anscheinend von Partnern bei vielen neuen Vakzinen verwendet. Ein Malaria- oder Herpes-Impfstoff kann Mrd einbringen... AGEN erhält davon kleine Royalties von ca. 2%.

Der Krebs-Impfstoff Provenge ist ein sehr spezieller Impfstoff. Er wird für jeden einzelnen Patienten einzeln hergestellt, indem typische Antigene des Tumors über die HSP-Proteine gesammelt werden. HSP transportiert ständig Antigene aus den Zellen, um sie dem Immunsystem zu präsentieren. Die APC-Zellen leiten dann die Immunantwort ein.


AGEN versucht diesen Ansatz mit AutoSynVax zu optimieren. Der Tumor soll vollständig genetisch analysiert, aus den Daten relevante Neo-Antigene (das sind die Antigene, die eher körperfremd sind und auf die das Immunsystem ansprechen sollte) extrahiert und daraus eine HSP-Vakzine erstellt werden, die dann mit Adjuvanten wie QS-21 und IO-Kandidaten wie CTLA4 dem Patienten verabreicht wird.


Mal schauen... sehe ich als Ergänzung zu meinen anderen IO-Unternehmen.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.355.581 von ipollit am 22.12.15 20:06:31Hallo ipollit,
AGEN hatte ich auch auf der Liste, sind ganz schön zurückgekommen vom Jahreshoch.
Bei unter 4 $ hatte ich überlegt einzusteigen, habe mich aber für PIRS entschieden.
Der Deal mit Roche war ausschlaggebend:
"Under the terms of the agreement, Pieris will discover, characterize and optimize Anticalin®-based drug candidates against an undisclosed target. Roche and Pieris will evaluate different drug formats against this target and advance them through preclinical development, with Roche being responsible for IND-enabling activities, clinical development and worldwide marketing of any resulting products. Pieris will receive an upfront payment of CHF 6.5 million (~$6.4 million USD) and committed research funding, and may receive development and regulatory-based milestone payments, sales-based milestone payments as well as mid single-digit to low double-digit royalties on any future product sales. If all milestones and other conditions are met, the total payments to Pieris could surpass CHF 415 million (~$409.3 million USD), excluding royalties."
Zudem verläuft die Entwicklung bei PIRS recht erfreulich, Meilensteine aus den Partnerschaften mit Sanofi und Daiichi Sankyo. Und auch eine Klärung mit Münchens TUM.
PIRS würde auch gut zu deiner "Sammlung" an IO-Unternehmen passen und noch recht billig zu haben.
AGEN ist natürlich zu diesen Kursen auch sehr reizvoll, stehen ganz oben auf meiner Einkaufsliste.
AGEN hatte ich auch auf der Liste, sind ganz schön zurückgekommen vom Jahreshoch.
Bei unter 4 $ hatte ich überlegt einzusteigen, habe mich aber für PIRS entschieden.
Der Deal mit Roche war ausschlaggebend:
"Under the terms of the agreement, Pieris will discover, characterize and optimize Anticalin®-based drug candidates against an undisclosed target. Roche and Pieris will evaluate different drug formats against this target and advance them through preclinical development, with Roche being responsible for IND-enabling activities, clinical development and worldwide marketing of any resulting products. Pieris will receive an upfront payment of CHF 6.5 million (~$6.4 million USD) and committed research funding, and may receive development and regulatory-based milestone payments, sales-based milestone payments as well as mid single-digit to low double-digit royalties on any future product sales. If all milestones and other conditions are met, the total payments to Pieris could surpass CHF 415 million (~$409.3 million USD), excluding royalties."
Zudem verläuft die Entwicklung bei PIRS recht erfreulich, Meilensteine aus den Partnerschaften mit Sanofi und Daiichi Sankyo. Und auch eine Klärung mit Münchens TUM.
PIRS würde auch gut zu deiner "Sammlung" an IO-Unternehmen passen und noch recht billig zu haben.
AGEN ist natürlich zu diesen Kursen auch sehr reizvoll, stehen ganz oben auf meiner Einkaufsliste.
Antwort auf Beitrag Nr.: 51.355.581 von ipollit am 22.12.15 20:06:31
nur mal eine ganz platte, teil(weil es ja offensichtlich nicht so ist)rhetorische frage
ist soetwas nicht vielvielviel zu aufwendig, um damit eine sich rechnende behandlung anzubieten?
Zitat von ipollit: Der Krebs-Impfstoff Provenge ist ein sehr spezieller Impfstoff. Er wird für jeden einzelnen Patienten einzeln hergestellt, indem typische Antigene des Tumors über die HSP-Proteine gesammelt werden. HSP transportiert ständig Antigene aus den Zellen, um sie dem Immunsystem zu präsentieren. Die APC-Zellen leiten dann die Immunantwort ein.
...
AGEN versucht diesen Ansatz mit AutoSynVax zu optimieren. Der Tumor soll vollständig genetisch analysiert, aus den Daten relevante Neo-Antigene (das sind die Antigene, die eher körperfremd sind und auf die das Immunsystem ansprechen sollte) extrahiert und daraus eine HSP-Vakzine erstellt werden, die dann mit Adjuvanten wie QS-21 und IO-Kandidaten wie CTLA4 dem Patienten verabreicht wird
nur mal eine ganz platte, teil(weil es ja offensichtlich nicht so ist)rhetorische frage
ist soetwas nicht vielvielviel zu aufwendig, um damit eine sich rechnende behandlung anzubieten?
EXEL:
Hammer hat kürzlich folgenden Kommentar geschrieben:
"With BTD and several years on the market cabo should be approved within ~3 months."
Ich finde das spannend, weil ich persönlich von 6 Monaten ausgegangen bin. Wenn Hammer recht behält (was ich schon vermute), dann könnte die RCC-Zulassung zum Ende des Q1/2016 erfolgen.
Geht damit alles glatt, halte ich EXEL für deutlich unterbewertet. Ich werde meine Position etwas aufstocken.

Die letzten 5 Jahre... Werden nun bald die Früchte geerntet? Die Chancen stehen recht gut, denke ich.
Hammer hat kürzlich folgenden Kommentar geschrieben:
"With BTD and several years on the market cabo should be approved within ~3 months."
Ich finde das spannend, weil ich persönlich von 6 Monaten ausgegangen bin. Wenn Hammer recht behält (was ich schon vermute), dann könnte die RCC-Zulassung zum Ende des Q1/2016 erfolgen.
Geht damit alles glatt, halte ich EXEL für deutlich unterbewertet. Ich werde meine Position etwas aufstocken.
Die letzten 5 Jahre... Werden nun bald die Früchte geerntet? Die Chancen stehen recht gut, denke ich.
Antwort auf Beitrag Nr.: 51.358.746 von McNay am 23.12.15 10:39:13Hallo McNay,
PIRS hatte ich mir auch angesehen, da sie recht niedrig bewertet sind (91 Mio USD). Wenn ich es richtig sehe, gehen die ersten IO-Kandidaten aber frühestens 2017 in die Klinik... daher warte ich erstmal ab, wie sie sich weiter entwickeln.
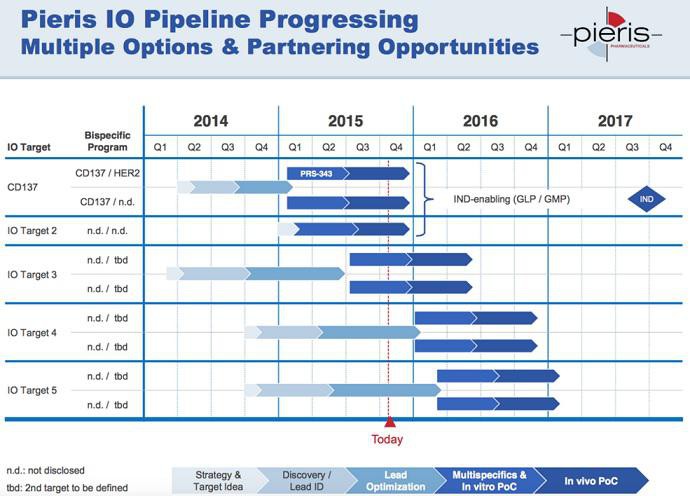
Ihre Anticaline sind quasi wie biAKs, oder? Zudem lassen sich bekannte AKs wie z.B. Rituxan einfach durch Anfügen von Anticalinen noch selektiver auf das Target abzustimmen. Anticaline sollen soetwas ähnliches wie AKs sein, nur kleiner und mehr Targets als nur Proteine binden können.
Im IO-Bereich kann man damit das Immunsystem speziell in der Tumorumgebung verändern, um Nebenwirkungen in gesundem Gewebe zu reduzieren. So soll ein normaler CD137-AK keine T-Zellen stimulieren können ohne problematische Nebenwirkungen zu haben (BMY hat mit Urelumab einen CD137-AK in der Klinik). PRS-343 als CD137 x HER2 reichert den AK speziell an HER2+ Zellen an... das sind z.B. Tumorzellen bei HER2+ Brustkrebs, so dass hier eine Konzentration erreicht werden kann, bei denen auch T-Zellen aktiv werden.
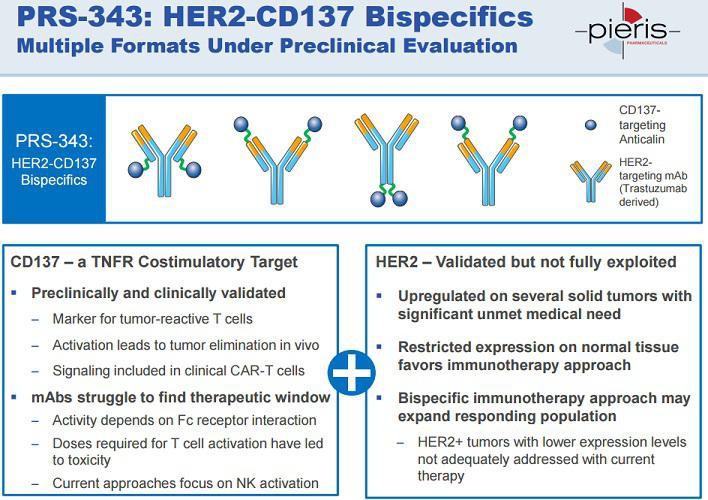
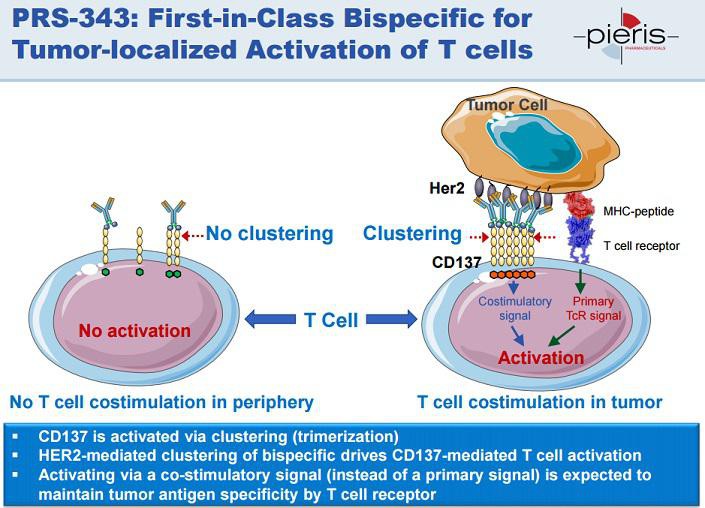
Bei den biAKs favorisiere ich momentan noch MGNX. Ist ein CD137xHER2 nicht so etwas wie ein CD3xHER2... wird es dann nicht sinnvoller sein, die T-Zellen direkt über CD3 zu aktivieren, statt sie nur mit CD137 zu stimulieren? HER2 ist glaube ich auch nicht nut auf Krebszellen beschränkt, oder? Besser könnte hier z.B. soetwas wie B7H3 sein.
Allerdings kann ich bisher nicht abschätzen, ob sich Anticaline und DARTs eher ähnlich sind bzw. welche Vor- und Nachteile die einzelnen Technologien haben. Welche Halbwertszeit haben Anticaline ohne AKs im Blut? Sie sollen deutlich keiner als AKs sein... dann werden sie aber wahrscheinlich auch sehr schnell abgebaut. Ein Nachteil des zugelassenen CD3xCD19 BITE-AKs Blincyto ist es, dass er mit einer kontinuierlichen Infusion verabreicht werden muss, während normale AKs ja teilweise nur alle paar Monate gegeben werden müssen. MGNXs DARTs werden daher mit einem fc-Teil der AKs versehen. Ist das mit Anticalinen ähnlich?
Aber vielleicht bieten Anticaline auch Vorteile, wenn sie mehr binden können als normale AKs... u.U. auch mehrere Targets gleichzeitig (multivalent). Oder ist es ein Nachteil, weil sie so auch unselektiv sein können? Vielleicht könnte auch die Geometrie besser sein? MGNX sagt, dass ihre DARTs besser als BITEs wirken, weil sie kompakter sind und so die T-Zellen sehr nah an das Target gebunden werden.
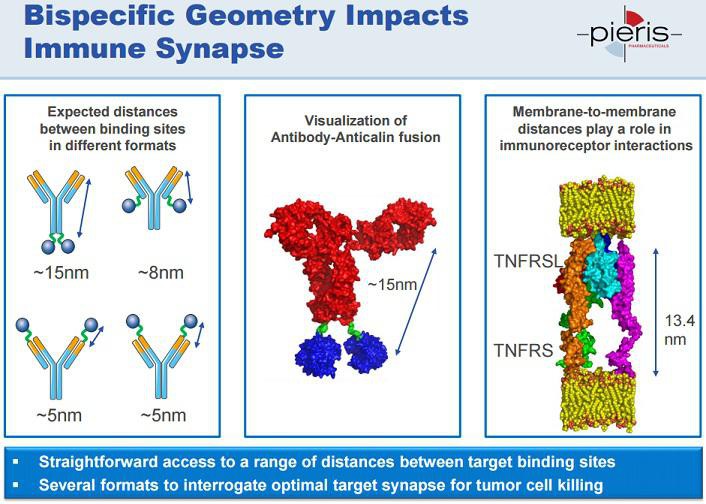
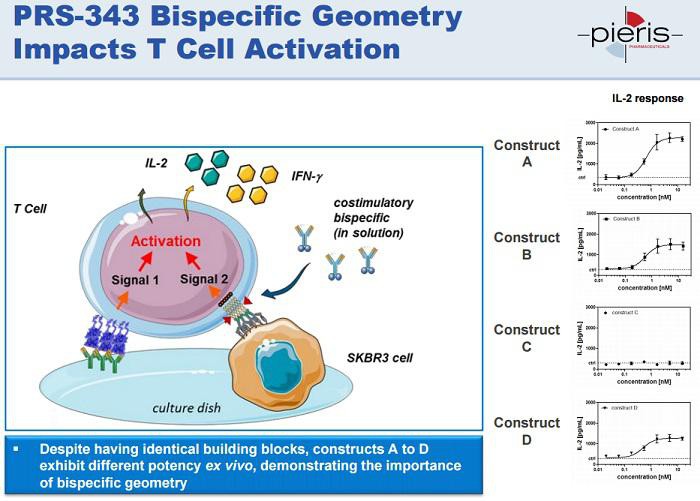
PRS-080 könnte ein Konkurrent für HIFs wie Roxa von FGEN sein.
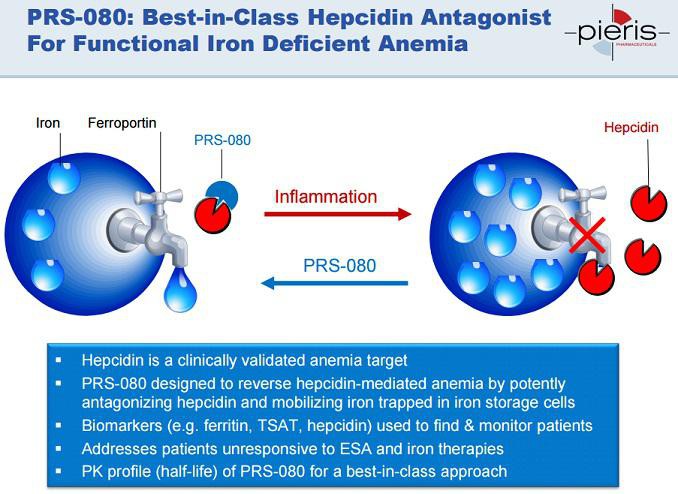
Z.B. hier wird über Hepcidin-Senker diskutiert. Für mich sieht es momentan noch so aus, als ob PRS-080 nur dann breit eingesetzt werden können, wenn HIFs aufgrund von Nebenwirkungen scheitern.
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"Doing a bit of digging here, it seems hepcidin is typically somewhat low in CHF patients, consistent with chronic HIF upregulation. Of course you would expect HIF to be upregulated in any chronic hypoxic condition. I don't think the Street has fully appreciated the hepcidin data yet. For example, around half of RA patients have upregulated hepcidin and (likely as a result) chronic anemia. So right there is a massive potential market that nobody has discussed much.
***
I'm sure this is not new to you but there are competitors looking at lowering hepcidin directly in inflammatory conditions and EPO hyporesponsive pts.
***
Yes, if the FGEN drug flames out for any reason, these hepcidin-lowering drugs would be very interesting. But given they would pretty much always be given in the context of anemia, hard for me to see them getting traction if the HIF-drugs work out."
"http://investorshub.advfn.com/boards/read_msg.aspx?message_…
"If the rationale is that reducing hepcidin (from unphysiologic levels) might increase infections because of increased iron availability, remember that the roxa arm requires significantly less supplemental iron. IV iron for extended periods does seem to pose some infection risk.
***
With Roxadustat we have shown that we down regulated the factor Hepcidin to normal levels..."
Möglicherweise könnte es auch interessant sein, wenn Anticaline ähnlich spezifisch wie AKs wirken, aber z.B. inhalierbar sind. REGN sieht den IL4Ra-AK Dupilumab in PIII als Multi-Mrd Blockbuster (5B+) u.a. gegen Athma. PRS-060 könnte somit ein inhalierbares Dupilumab sein, was sich erstmal nicht schlecht anhört. Allerdings ist die PI erst für 2017 geplant, das ganze also noch in einer recht frühen Entwicklung.
Ich werde PIRS auf jeden Fall weiter beobachten, danke!

Grüße
ipollit
PIRS hatte ich mir auch angesehen, da sie recht niedrig bewertet sind (91 Mio USD). Wenn ich es richtig sehe, gehen die ersten IO-Kandidaten aber frühestens 2017 in die Klinik... daher warte ich erstmal ab, wie sie sich weiter entwickeln.

Ihre Anticaline sind quasi wie biAKs, oder? Zudem lassen sich bekannte AKs wie z.B. Rituxan einfach durch Anfügen von Anticalinen noch selektiver auf das Target abzustimmen. Anticaline sollen soetwas ähnliches wie AKs sein, nur kleiner und mehr Targets als nur Proteine binden können.
Im IO-Bereich kann man damit das Immunsystem speziell in der Tumorumgebung verändern, um Nebenwirkungen in gesundem Gewebe zu reduzieren. So soll ein normaler CD137-AK keine T-Zellen stimulieren können ohne problematische Nebenwirkungen zu haben (BMY hat mit Urelumab einen CD137-AK in der Klinik). PRS-343 als CD137 x HER2 reichert den AK speziell an HER2+ Zellen an... das sind z.B. Tumorzellen bei HER2+ Brustkrebs, so dass hier eine Konzentration erreicht werden kann, bei denen auch T-Zellen aktiv werden.


Bei den biAKs favorisiere ich momentan noch MGNX. Ist ein CD137xHER2 nicht so etwas wie ein CD3xHER2... wird es dann nicht sinnvoller sein, die T-Zellen direkt über CD3 zu aktivieren, statt sie nur mit CD137 zu stimulieren? HER2 ist glaube ich auch nicht nut auf Krebszellen beschränkt, oder? Besser könnte hier z.B. soetwas wie B7H3 sein.
Allerdings kann ich bisher nicht abschätzen, ob sich Anticaline und DARTs eher ähnlich sind bzw. welche Vor- und Nachteile die einzelnen Technologien haben. Welche Halbwertszeit haben Anticaline ohne AKs im Blut? Sie sollen deutlich keiner als AKs sein... dann werden sie aber wahrscheinlich auch sehr schnell abgebaut. Ein Nachteil des zugelassenen CD3xCD19 BITE-AKs Blincyto ist es, dass er mit einer kontinuierlichen Infusion verabreicht werden muss, während normale AKs ja teilweise nur alle paar Monate gegeben werden müssen. MGNXs DARTs werden daher mit einem fc-Teil der AKs versehen. Ist das mit Anticalinen ähnlich?
Aber vielleicht bieten Anticaline auch Vorteile, wenn sie mehr binden können als normale AKs... u.U. auch mehrere Targets gleichzeitig (multivalent). Oder ist es ein Nachteil, weil sie so auch unselektiv sein können? Vielleicht könnte auch die Geometrie besser sein? MGNX sagt, dass ihre DARTs besser als BITEs wirken, weil sie kompakter sind und so die T-Zellen sehr nah an das Target gebunden werden.


PRS-080 könnte ein Konkurrent für HIFs wie Roxa von FGEN sein.

Z.B. hier wird über Hepcidin-Senker diskutiert. Für mich sieht es momentan noch so aus, als ob PRS-080 nur dann breit eingesetzt werden können, wenn HIFs aufgrund von Nebenwirkungen scheitern.
http://investorshub.advfn.com/boards/read_msg.aspx?message_i…
"Doing a bit of digging here, it seems hepcidin is typically somewhat low in CHF patients, consistent with chronic HIF upregulation. Of course you would expect HIF to be upregulated in any chronic hypoxic condition. I don't think the Street has fully appreciated the hepcidin data yet. For example, around half of RA patients have upregulated hepcidin and (likely as a result) chronic anemia. So right there is a massive potential market that nobody has discussed much.
***
I'm sure this is not new to you but there are competitors looking at lowering hepcidin directly in inflammatory conditions and EPO hyporesponsive pts.
***
Yes, if the FGEN drug flames out for any reason, these hepcidin-lowering drugs would be very interesting. But given they would pretty much always be given in the context of anemia, hard for me to see them getting traction if the HIF-drugs work out."
"http://investorshub.advfn.com/boards/read_msg.aspx?message_…
"If the rationale is that reducing hepcidin (from unphysiologic levels) might increase infections because of increased iron availability, remember that the roxa arm requires significantly less supplemental iron. IV iron for extended periods does seem to pose some infection risk.
***
With Roxadustat we have shown that we down regulated the factor Hepcidin to normal levels..."
Möglicherweise könnte es auch interessant sein, wenn Anticaline ähnlich spezifisch wie AKs wirken, aber z.B. inhalierbar sind. REGN sieht den IL4Ra-AK Dupilumab in PIII als Multi-Mrd Blockbuster (5B+) u.a. gegen Athma. PRS-060 könnte somit ein inhalierbares Dupilumab sein, was sich erstmal nicht schlecht anhört. Allerdings ist die PI erst für 2017 geplant, das ganze also noch in einer recht frühen Entwicklung.
Ich werde PIRS auf jeden Fall weiter beobachten, danke!
Grüße
ipollit
Antwort auf Beitrag Nr.: 51.373.404 von SLGramann am 28.12.15 11:38:07Hallo SLGramann,
als Vergleich könnte man ja Daratumumab mit BTD nehmen, das selbst im Vergleich zu anderen BTDs extrem schnell zugelassen worden ist:
09.07.2015 - BLA/NDA
04.09.2015 - angenommen mit PR (beschleunigte Prüfung von 6 Monaten... PDFUA 09.03.2016)
16.11.2015 - Zulassung
D.h. etwas mehr als 4 Monate nach dem Zulassungsantrag. Hochgerechnet auf EXEL wäre das mit dem NDA am 23.12. eine mögliche Zulassung etwa Ende April.
Zwar ist Cabo bereits zugelassen, allerdings wurde der Antrag von der kleinen EXEL gestellt und nicht von J&J mit einem riesigen Entwicklungsprogramm für Daratumumab. Wenn ich es richtig sehe, hat sich auch die Form geändert von der bereits zugelassenen Kapselform hin zu noch nicht zugelassenen Tabletten. Das sieht für mich dann nicht nach einer erweiterten Zulassung (sNDA) sondern einem komplett neuen Zulassungsantrag (NDA) aus, oder?
"Cabozantinib is currently marketed in capsule form under the brand name COMETRIQ® in the United States for the treatment of progressive, metastatic medullary thyroid cancer (MTC), and in the European Union for the treatment of adult patients with progressive, unresectable locally advanced or metastatic MTC. COMETRIQ is not indicated for patients with RCC. In the METEOR trial, and all other cancer trials currently underway, Exelixis is investigating a tablet formulation of cabozantinib distinct from the COMETRIQ capsule form. The tablet formulation of cabozantinib is the subject of the NDA for advanced RCC."
Grüße
ipollit
als Vergleich könnte man ja Daratumumab mit BTD nehmen, das selbst im Vergleich zu anderen BTDs extrem schnell zugelassen worden ist:
09.07.2015 - BLA/NDA
04.09.2015 - angenommen mit PR (beschleunigte Prüfung von 6 Monaten... PDFUA 09.03.2016)
16.11.2015 - Zulassung
D.h. etwas mehr als 4 Monate nach dem Zulassungsantrag. Hochgerechnet auf EXEL wäre das mit dem NDA am 23.12. eine mögliche Zulassung etwa Ende April.
Zwar ist Cabo bereits zugelassen, allerdings wurde der Antrag von der kleinen EXEL gestellt und nicht von J&J mit einem riesigen Entwicklungsprogramm für Daratumumab. Wenn ich es richtig sehe, hat sich auch die Form geändert von der bereits zugelassenen Kapselform hin zu noch nicht zugelassenen Tabletten. Das sieht für mich dann nicht nach einer erweiterten Zulassung (sNDA) sondern einem komplett neuen Zulassungsantrag (NDA) aus, oder?
"Cabozantinib is currently marketed in capsule form under the brand name COMETRIQ® in the United States for the treatment of progressive, metastatic medullary thyroid cancer (MTC), and in the European Union for the treatment of adult patients with progressive, unresectable locally advanced or metastatic MTC. COMETRIQ is not indicated for patients with RCC. In the METEOR trial, and all other cancer trials currently underway, Exelixis is investigating a tablet formulation of cabozantinib distinct from the COMETRIQ capsule form. The tablet formulation of cabozantinib is the subject of the NDA for advanced RCC."
Grüße
ipollit
Antwort auf Beitrag Nr.: 51.359.475 von Popeye82 am 23.12.15 12:44:23Hallo Popeye,
natürlich ist es aufwendiger als ein Mittel, welches man allen Patienten gleich geben kann. Biologische Produkte wie AKs, die von lebenden Organismen erzeugt werden müssen, sind ja auch aufwendiger als Small Molecules wie z.B. EXELs Cabozantinib, die einfach chemisch erzeugt werden. Trotzdem sind sie weit verbreitet.
Ich denke, es hängt immer von der Wirkung ab... wenn es allen Standard-Medikamenten deutlich überlegen ist, wird man es wohl herstellen.
die populären CARTs wie von JUNO oder KITE sind doch auch sehr kompliziert zu erzeugen. Dazu müssen dem Patienten T-Zellen (wohl Blut) entnommen werden, diese individuellen T-Zellen müssen extrahiert, kultiviert und anschließend gentechnisch verändert werden. Die veränderten (lebenden) T-Zellen werden anschließend wieder dem Patienten verabreicht. Wenn man Pech hat, sterben diese T-Zellen schnell wieder und der ganze Aufwand war umsonst. Falls nicht, greifen sie das Target an, für das sie gentechnisch verändert worden sind... z.B. CD19. Die CD19-CARTs zerstören dann im Optimalfall alle CD19-Zellen, Krebszellen wie auch gesunde Zellen.
Wenn der Krebs aber nicht auf CD19 angewiesen ist, werden einige Krebszellen ohne CD19 übrig bleiben... der Krebs kommt zurück und ist gegen die CD19-CARTs resistent. Dann benötigt man weitere CARTs gegen weitere Targets, die wieder neue Nebenwirkungen mit sich bringen. Jedes Target, welches auch auf gesunden Zellen auftritt, besitzt Nebenwirkungen, da auch diese Zellen vom Immunsysten angegriffen werden. Bei Blutkrebs ist das noch akzeptabel, da sich Blutzellen ständig regenerieren. Bei soliden Tumoren wie Lungenkrebs ist das sehr viel schwieriger... wenn z.B. ein EGFR-CART nicht nur EGFR+ Krebszellen in der Lunge zerstört, sondern auch noch viele gesunde Hautzellen, werden die Haut oder andere Organe dauerhaft schwer geschädigt. Man muss also nach Möglichkeit Targets finden, die nur auf Krebszellen vorhanden sind.
CARTs haben offensichtlich schon ihre Probleme... auch mit der Herstellung. NVS hat eine Produktions-Fabrik von Dendreon übernommen. Dendreon hat eine der ersten personalisierten Krebs-Vakzine auf den Markt gebracht, ist aber aufgrund der aufwendigen Herstellung Pleite gegangen... insofern hast du Recht, dass man auch den Aufwand der Herstellung berücksichtigen muss.
http://seekingalpha.com/article/3742046-ash-car-t-struggles-…
"ASH- CAR-T Struggles To Travel Beyond Leukaemia
Then there is manufacturing. A particularly worrying revelation by the University of Pennsylvania’s Dr Stephen Schuster came from a study of the most advanced CAR-T player, Novartis’s CTL019, in a study in patients with relapsed/refractory B-cell lymphomas.
Of 43 patients enrolled, 13 could not be infused– six owing to production failure. Followers of a project that apparently is to be filed for regulatory approval next year could find this alarming...
... Another possible worry is duration of response. In the CTL019 study two partial remissions turned to progressive disease in six to 12 months, while in Kite’s seven-patient Zuma-1 trial of KTE-C19 one complete remission relapsed in three months, there was a grade 4 cytokine storm and a death unrelated to treatment...
...The Swiss firm claims that this is the largest clinical study of a CAR-T therapy, and has been expanded beyond the US to the EU and Asia. The group already has a manufacturing plant bought from Dendreon, while Juno and Kite are constructing facilities, the latter’s for strategic reasons adjacent to Los Angeles airport."
****
Aus meiner Sicht geht der Ansatz von AGEN in die Richtung, möglichst einfach ein sehr spezielles Mittel (in diesem Fall einen Impfstoff... das könnte ein großer Haken sein, da Impfstoffe bisher nicht gut wirken) zu erzeugen, das viele charakteristischen Merkmale der Krebszellen aufweist. Ausgangspunkt wird Tumormaterial (Gewebe oder Blut) sein, das komplett genetisch analysiert wird. In der einen oder anderen Form wird dies aber irgendwann immer gemacht werden... das ist ja die Basis von so Unternehmen wie FMI, die Gewebe- oder Blutproben untersuchen, um festzustellen, welche Medikamente wirken können. Heute testet man ja auch bereits auf HER2, ob z.B. der HER2-AK Herceptin wirkt. Dann könnte man doch direkt eine komplette Gen-Analyse machen... früher war diese sehr teuer, heute gibt es sie für einige tausende Dollar.
Der komplizierte Schritt ist dann, aus diesem riesigen Datenberg die Eigenschaften des Tumors herauszufiltern. Der Tumor besitzt viele Mutationen... benötigt werden aber nur ganz spezielle und zwar Neo-Antigene. Das sind Targets, die normalerweise nicht auf gesunden Zellen vorhanden sind. Wenn das Immunsystem kranke Zellen erkennen soll, dann sind wohl diese Neo-Antigene entscheident. Diesen Schritt übernehmen aber Rechner... je schneller die Rechner und je besser die Programme, umso besser das Ergebnis.
Die gefundene Neo-Antigene sind speziell für den Patienten. Da es pro Patienten mehrere Neo-Antigene sind, werden gleichzeitig mehrere Targets gleichzeitig angegriffen, die zudem nur auf den Krebszellen vorhanden sind. Bei vielen Targets hat der Krebs es schwer, gleichzeitig gegen alle resistent zu werden.
Theoretisch könnte man nun CARTs gegen diese Neo-Antigene erzeugen. AGEN verfügt dagegen über die Vakzine-Technologie. Aus den gewonnenen Daten werden künstliche Peptide dieser Neo-Antigene erzeugt und Standard-HSP-Proteinen dem Patienten verabreicht. Diese HSPs transportieren dann diese Neo-Antigene zu den Immunzellen.
Vielleicht funktioniert das ganze am Ende auch nicht. Doch die Suche nach individuellen Neo-Antigenen ist aus meiner Sicht der richtige Schritt... ob man am Ende daraus CARTs, Vakzine oder was auch immer erzeugt, muss man sehen.
AGEN baut diesen Bereich offensichtlich weiter aus... letzte Woche haben sie PhosImmune übernommen:
"“PhosImmune’s groundbreaking neoantigen assets significantly expand Agenus’ current efforts, and present exciting near-term opportunities for new products and partnerships,” said Dr. Garo H. Armen, Chairman and Chief Executive Officer of Agenus. “This acquisition expands our immuno-oncology pipeline and strengthens our neoantigen capabilities to enable the development of best-in-class cancer vaccines and other novel therapies.”
PhosImmune’s neoantigens have unique advantages in cancer immunotherapy. The company’s phosphopeptide tumor targets (PTTs) are fragments of proteins expressed in cancer cells. These fragments are phosphorylated due to signal dysregulation involved in the development of cancers and, as a result, appear as foreign to the immune system. The approach is synergistic with Agenus’ AutoSynVax™ vaccine program for targeting patient-specific tumor neoantigens. PTTs can expand AutoSynVax and other immunotherapeutic approaches to include patients with lower levels of mutations that may not have enough neoantigens to activate the immune system effectively. PTTs can also be shared by patients with specific cancers, providing the potential for “off-the-shelf” vaccines."
Letzterer Satz lässt auch die Möglichkeit offen, für spezielle Krebsarten Standard-Vakzine zu entwickeln, die auf für diese Krebsarten typische Neo-Antigene basieren.
Ohad Hammer findet ja auch GNCA mit Atlas-Technolgie interessant. Die suchen ja u.a. auch nach Neo-Antigenen:
"GNCA – I really like the new neo-antigen initiative as (like everybody else) I am very excited about this field but it is hard to assign a lot of value given early stage of development."
"Unique mutations identified by sequencing each cancer patient’s tumor will be expressed in ATLAS and screened with T cells from the same patient, collected both before and after treatment with checkpoint inhibitors. In this way, each subject’s own unique neoantigen T cell response profile will be identified, along with their signatures of T cell response to CPI therapy.
Genocea is collaborating with Timothy A. Chan, M.D., Ph.D., Vice Chair, Department of Radiation Oncology, and Jedd D. Wolchok, M.D., Ph.D., Chief of Melanoma and Immunotherapeutics Service at the Memorial Sloan Kettering Cancer Center to screen the T cell responses of melanoma and non-small cell lung cancer patients treated with checkpoint inhibitors against cancer neoantigens."
AGEN arbeit ebenfalls mit Dr. Wolchok:
"Agenus has six preclinical programs that aim to produce monoclonal antibodies that block or activate specific checkpoint target receptors (GITR, OX40, PD-1, CTLA-4, TIM-3, and LAG-3). 4-Antibody has been working on these targets for more than three years, in collaboration with one of the world’s most prestigious and powerful academic groups focused on the interactions between cancer and the immune system, Ludwig Cancer Research and in particular with the leader of the Ludwig collaborative laboratory at Memorial Sloan Kettering Cancer Center, Jedd Wolchok, MD, PhD. Dr. Wolchok is recognized as one the true leaders in the emerging field of immuno-oncology."
AGEN kann gegenüber GNCA den Vorteil haben, Expertise/Technologien für Neo-Antigene und gleichzeitig ein großes Sortiment an IO-Kandidaten sowie Vakzine-Technologien zu besitzen.
***
Neo-Antigene und Checkpoint-Hemmer...
http://oncologydiscovery.com/2015/08/08/strategies-to-enhanc…
"Our current understanding of checkpoint inhibitors suggests that highly mutated tumors can be seen by the immune system through neoantigen presentation. As a result, these cancers are primed for a checkpoint inhibitor-induced immune response."
Gruß
ipollit
natürlich ist es aufwendiger als ein Mittel, welches man allen Patienten gleich geben kann. Biologische Produkte wie AKs, die von lebenden Organismen erzeugt werden müssen, sind ja auch aufwendiger als Small Molecules wie z.B. EXELs Cabozantinib, die einfach chemisch erzeugt werden. Trotzdem sind sie weit verbreitet.
Ich denke, es hängt immer von der Wirkung ab... wenn es allen Standard-Medikamenten deutlich überlegen ist, wird man es wohl herstellen.
die populären CARTs wie von JUNO oder KITE sind doch auch sehr kompliziert zu erzeugen. Dazu müssen dem Patienten T-Zellen (wohl Blut) entnommen werden, diese individuellen T-Zellen müssen extrahiert, kultiviert und anschließend gentechnisch verändert werden. Die veränderten (lebenden) T-Zellen werden anschließend wieder dem Patienten verabreicht. Wenn man Pech hat, sterben diese T-Zellen schnell wieder und der ganze Aufwand war umsonst. Falls nicht, greifen sie das Target an, für das sie gentechnisch verändert worden sind... z.B. CD19. Die CD19-CARTs zerstören dann im Optimalfall alle CD19-Zellen, Krebszellen wie auch gesunde Zellen.
Wenn der Krebs aber nicht auf CD19 angewiesen ist, werden einige Krebszellen ohne CD19 übrig bleiben... der Krebs kommt zurück und ist gegen die CD19-CARTs resistent. Dann benötigt man weitere CARTs gegen weitere Targets, die wieder neue Nebenwirkungen mit sich bringen. Jedes Target, welches auch auf gesunden Zellen auftritt, besitzt Nebenwirkungen, da auch diese Zellen vom Immunsysten angegriffen werden. Bei Blutkrebs ist das noch akzeptabel, da sich Blutzellen ständig regenerieren. Bei soliden Tumoren wie Lungenkrebs ist das sehr viel schwieriger... wenn z.B. ein EGFR-CART nicht nur EGFR+ Krebszellen in der Lunge zerstört, sondern auch noch viele gesunde Hautzellen, werden die Haut oder andere Organe dauerhaft schwer geschädigt. Man muss also nach Möglichkeit Targets finden, die nur auf Krebszellen vorhanden sind.
CARTs haben offensichtlich schon ihre Probleme... auch mit der Herstellung. NVS hat eine Produktions-Fabrik von Dendreon übernommen. Dendreon hat eine der ersten personalisierten Krebs-Vakzine auf den Markt gebracht, ist aber aufgrund der aufwendigen Herstellung Pleite gegangen... insofern hast du Recht, dass man auch den Aufwand der Herstellung berücksichtigen muss.
http://seekingalpha.com/article/3742046-ash-car-t-struggles-…
"ASH- CAR-T Struggles To Travel Beyond Leukaemia
Then there is manufacturing. A particularly worrying revelation by the University of Pennsylvania’s Dr Stephen Schuster came from a study of the most advanced CAR-T player, Novartis’s CTL019, in a study in patients with relapsed/refractory B-cell lymphomas.
Of 43 patients enrolled, 13 could not be infused– six owing to production failure. Followers of a project that apparently is to be filed for regulatory approval next year could find this alarming...
... Another possible worry is duration of response. In the CTL019 study two partial remissions turned to progressive disease in six to 12 months, while in Kite’s seven-patient Zuma-1 trial of KTE-C19 one complete remission relapsed in three months, there was a grade 4 cytokine storm and a death unrelated to treatment...
...The Swiss firm claims that this is the largest clinical study of a CAR-T therapy, and has been expanded beyond the US to the EU and Asia. The group already has a manufacturing plant bought from Dendreon, while Juno and Kite are constructing facilities, the latter’s for strategic reasons adjacent to Los Angeles airport."
****
Aus meiner Sicht geht der Ansatz von AGEN in die Richtung, möglichst einfach ein sehr spezielles Mittel (in diesem Fall einen Impfstoff... das könnte ein großer Haken sein, da Impfstoffe bisher nicht gut wirken) zu erzeugen, das viele charakteristischen Merkmale der Krebszellen aufweist. Ausgangspunkt wird Tumormaterial (Gewebe oder Blut) sein, das komplett genetisch analysiert wird. In der einen oder anderen Form wird dies aber irgendwann immer gemacht werden... das ist ja die Basis von so Unternehmen wie FMI, die Gewebe- oder Blutproben untersuchen, um festzustellen, welche Medikamente wirken können. Heute testet man ja auch bereits auf HER2, ob z.B. der HER2-AK Herceptin wirkt. Dann könnte man doch direkt eine komplette Gen-Analyse machen... früher war diese sehr teuer, heute gibt es sie für einige tausende Dollar.
Der komplizierte Schritt ist dann, aus diesem riesigen Datenberg die Eigenschaften des Tumors herauszufiltern. Der Tumor besitzt viele Mutationen... benötigt werden aber nur ganz spezielle und zwar Neo-Antigene. Das sind Targets, die normalerweise nicht auf gesunden Zellen vorhanden sind. Wenn das Immunsystem kranke Zellen erkennen soll, dann sind wohl diese Neo-Antigene entscheident. Diesen Schritt übernehmen aber Rechner... je schneller die Rechner und je besser die Programme, umso besser das Ergebnis.
Die gefundene Neo-Antigene sind speziell für den Patienten. Da es pro Patienten mehrere Neo-Antigene sind, werden gleichzeitig mehrere Targets gleichzeitig angegriffen, die zudem nur auf den Krebszellen vorhanden sind. Bei vielen Targets hat der Krebs es schwer, gleichzeitig gegen alle resistent zu werden.
Theoretisch könnte man nun CARTs gegen diese Neo-Antigene erzeugen. AGEN verfügt dagegen über die Vakzine-Technologie. Aus den gewonnenen Daten werden künstliche Peptide dieser Neo-Antigene erzeugt und Standard-HSP-Proteinen dem Patienten verabreicht. Diese HSPs transportieren dann diese Neo-Antigene zu den Immunzellen.
Vielleicht funktioniert das ganze am Ende auch nicht. Doch die Suche nach individuellen Neo-Antigenen ist aus meiner Sicht der richtige Schritt... ob man am Ende daraus CARTs, Vakzine oder was auch immer erzeugt, muss man sehen.
AGEN baut diesen Bereich offensichtlich weiter aus... letzte Woche haben sie PhosImmune übernommen:
"“PhosImmune’s groundbreaking neoantigen assets significantly expand Agenus’ current efforts, and present exciting near-term opportunities for new products and partnerships,” said Dr. Garo H. Armen, Chairman and Chief Executive Officer of Agenus. “This acquisition expands our immuno-oncology pipeline and strengthens our neoantigen capabilities to enable the development of best-in-class cancer vaccines and other novel therapies.”
PhosImmune’s neoantigens have unique advantages in cancer immunotherapy. The company’s phosphopeptide tumor targets (PTTs) are fragments of proteins expressed in cancer cells. These fragments are phosphorylated due to signal dysregulation involved in the development of cancers and, as a result, appear as foreign to the immune system. The approach is synergistic with Agenus’ AutoSynVax™ vaccine program for targeting patient-specific tumor neoantigens. PTTs can expand AutoSynVax and other immunotherapeutic approaches to include patients with lower levels of mutations that may not have enough neoantigens to activate the immune system effectively. PTTs can also be shared by patients with specific cancers, providing the potential for “off-the-shelf” vaccines."
Letzterer Satz lässt auch die Möglichkeit offen, für spezielle Krebsarten Standard-Vakzine zu entwickeln, die auf für diese Krebsarten typische Neo-Antigene basieren.
Ohad Hammer findet ja auch GNCA mit Atlas-Technolgie interessant. Die suchen ja u.a. auch nach Neo-Antigenen:
"GNCA – I really like the new neo-antigen initiative as (like everybody else) I am very excited about this field but it is hard to assign a lot of value given early stage of development."
"Unique mutations identified by sequencing each cancer patient’s tumor will be expressed in ATLAS and screened with T cells from the same patient, collected both before and after treatment with checkpoint inhibitors. In this way, each subject’s own unique neoantigen T cell response profile will be identified, along with their signatures of T cell response to CPI therapy.
Genocea is collaborating with Timothy A. Chan, M.D., Ph.D., Vice Chair, Department of Radiation Oncology, and Jedd D. Wolchok, M.D., Ph.D., Chief of Melanoma and Immunotherapeutics Service at the Memorial Sloan Kettering Cancer Center to screen the T cell responses of melanoma and non-small cell lung cancer patients treated with checkpoint inhibitors against cancer neoantigens."
AGEN arbeit ebenfalls mit Dr. Wolchok:
"Agenus has six preclinical programs that aim to produce monoclonal antibodies that block or activate specific checkpoint target receptors (GITR, OX40, PD-1, CTLA-4, TIM-3, and LAG-3). 4-Antibody has been working on these targets for more than three years, in collaboration with one of the world’s most prestigious and powerful academic groups focused on the interactions between cancer and the immune system, Ludwig Cancer Research and in particular with the leader of the Ludwig collaborative laboratory at Memorial Sloan Kettering Cancer Center, Jedd Wolchok, MD, PhD. Dr. Wolchok is recognized as one the true leaders in the emerging field of immuno-oncology."
AGEN kann gegenüber GNCA den Vorteil haben, Expertise/Technologien für Neo-Antigene und gleichzeitig ein großes Sortiment an IO-Kandidaten sowie Vakzine-Technologien zu besitzen.
***
Neo-Antigene und Checkpoint-Hemmer...
http://oncologydiscovery.com/2015/08/08/strategies-to-enhanc…
"Our current understanding of checkpoint inhibitors suggests that highly mutated tumors can be seen by the immune system through neoantigen presentation. As a result, these cancers are primed for a checkpoint inhibitor-induced immune response."
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.351.549 von ipollit am 22.12.15 11:24:03CMRX
huii... das ist leider ziemlich unglücklich und überraschend... Brincidofovir ist auf ganzer Linie gescheitert!
Damit dürfte CMRX höchstens noch Cash-Wert besitzen... vorbörslich -77%

Gruß
ipollit
huii... das ist leider ziemlich unglücklich und überraschend... Brincidofovir ist auf ganzer Linie gescheitert!

Damit dürfte CMRX höchstens noch Cash-Wert besitzen... vorbörslich -77%
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.374.565 von ipollit am 28.12.15 14:54:54CMRX
Die PIII-Studie von Brinci gegen CMV nach einer Stammzelltransplantation ist gescheitert. Am Ende der Studie gab es keinen signifikanten Unterschied an CMV-Infektionen zwischen Brinci und dem Placebo-Arm. Zudem wies der Brinci-Arm einen Trend zu höherer Sterblichkeit auf.
Wie kann das sein? Genauere Daten sollen im Februar kommen. Bisher scheint nur festzustehen, dass Brinci CMV gegenüber dem Placebo-Arm besser unterdrücken konnte, solange es verabreicht wurde. Nach der Behandlung gab es noch einen Zeitraum ohne Behandlung, in dem eigentlich das Riskio von CMV nicht mehr so hoch ist. Hier trat nun aber im Brinci-Arm verstärkt CMV auf, so dass am Ende keinen Unterschied mehr zwischen den Armen bestand.
Bei einer Stammzelltransplantation wird das Immunsystem des Patienten zerstört und fremde blutbildende Stammzellen transplantiert. Diese Zellen bauen ein neues Immunsystem auf. Allerdings funktioniert das nur, wenn dieses neue Immunsystem den Körper des Patienten nicht als fremd erkennt. Passen Spender und Empfänger nicht perfekt zusammen, so kann das neue Immunsystem Zellen des Patienten angreifen... es kommt zu GvHD, z.B. an Organen oder der Haut: "Am häufigsten äußern sich Symptome der GvHD an der Haut, der Leber, am Darm und am Auge". Um den Körper zu schützen werden dann immununterdrückende Mittel wie Steroide gegeben.
Aus irgendeinem Grund ist im Brinci-Arm verstärkt GvHD aufgetreten, das wiederum zur Gabe von immununterdrückende Mitteln geführt hat. Diese erhöhen wieder das Risiko von CMV.
"Preliminary analysis suggests that the primary endpoint failures in both the prevention of CMV infections and mortality in the brincidofovir arm were driven by confirmed cases of graft-versus-host-disease (GVHD), which resulted in a significantly higher use of corticosteroids than in the control arm. Both GVHD and use of corticosteroids are risk factors for “late” CMV infection that occurs after discontinuation of the antiviral in HCT recipients."
Ähnliches scheint bereits in der PII aufgetreten zu sein, nur dass sich dies nicht derart gravierend auf das Endergebnis ausgewirkt hat. In der PII soll CMRX das verstärkte Auftreten von GvHD mit einer Fehldiagnose von Nebenwirkungen von Brinci im Darm (GI) begründet haben. Theoretisch ist es vielleicht möglich, dass ein Arzt Beschwerden im Darm als ein Zeichen von GvHD interpretiert und daher zusätzliche immununterdrückende Mittel verabreicht, die nach dem Absetzen von Brinci zu einem höhere CMV-Risiko führen. Genaueres wird man hoffentlich im Februar sagen können.
Die GvHD-Problematik spielt aber nur bei Stammzelltransplantationen eine Rolle, nicht bei Organtransplantationen, da hier nur das eigene Immunsystem das Organ abstoßen kann. Zumindest eine Fehldiagnose von GI-Nebenwirkungen oder ähnliches ist in diesen Studien nicht möglich. Dennoch hat CMRX selber diese Studien vorerst angehalten bis man das Problem mit Brinci besser einschätzen kann.


Gruß
ipollit
Die PIII-Studie von Brinci gegen CMV nach einer Stammzelltransplantation ist gescheitert. Am Ende der Studie gab es keinen signifikanten Unterschied an CMV-Infektionen zwischen Brinci und dem Placebo-Arm. Zudem wies der Brinci-Arm einen Trend zu höherer Sterblichkeit auf.
Wie kann das sein? Genauere Daten sollen im Februar kommen. Bisher scheint nur festzustehen, dass Brinci CMV gegenüber dem Placebo-Arm besser unterdrücken konnte, solange es verabreicht wurde. Nach der Behandlung gab es noch einen Zeitraum ohne Behandlung, in dem eigentlich das Riskio von CMV nicht mehr so hoch ist. Hier trat nun aber im Brinci-Arm verstärkt CMV auf, so dass am Ende keinen Unterschied mehr zwischen den Armen bestand.
Bei einer Stammzelltransplantation wird das Immunsystem des Patienten zerstört und fremde blutbildende Stammzellen transplantiert. Diese Zellen bauen ein neues Immunsystem auf. Allerdings funktioniert das nur, wenn dieses neue Immunsystem den Körper des Patienten nicht als fremd erkennt. Passen Spender und Empfänger nicht perfekt zusammen, so kann das neue Immunsystem Zellen des Patienten angreifen... es kommt zu GvHD, z.B. an Organen oder der Haut: "Am häufigsten äußern sich Symptome der GvHD an der Haut, der Leber, am Darm und am Auge". Um den Körper zu schützen werden dann immununterdrückende Mittel wie Steroide gegeben.
Aus irgendeinem Grund ist im Brinci-Arm verstärkt GvHD aufgetreten, das wiederum zur Gabe von immununterdrückende Mitteln geführt hat. Diese erhöhen wieder das Risiko von CMV.
"Preliminary analysis suggests that the primary endpoint failures in both the prevention of CMV infections and mortality in the brincidofovir arm were driven by confirmed cases of graft-versus-host-disease (GVHD), which resulted in a significantly higher use of corticosteroids than in the control arm. Both GVHD and use of corticosteroids are risk factors for “late” CMV infection that occurs after discontinuation of the antiviral in HCT recipients."
Ähnliches scheint bereits in der PII aufgetreten zu sein, nur dass sich dies nicht derart gravierend auf das Endergebnis ausgewirkt hat. In der PII soll CMRX das verstärkte Auftreten von GvHD mit einer Fehldiagnose von Nebenwirkungen von Brinci im Darm (GI) begründet haben. Theoretisch ist es vielleicht möglich, dass ein Arzt Beschwerden im Darm als ein Zeichen von GvHD interpretiert und daher zusätzliche immununterdrückende Mittel verabreicht, die nach dem Absetzen von Brinci zu einem höhere CMV-Risiko führen. Genaueres wird man hoffentlich im Februar sagen können.
Die GvHD-Problematik spielt aber nur bei Stammzelltransplantationen eine Rolle, nicht bei Organtransplantationen, da hier nur das eigene Immunsystem das Organ abstoßen kann. Zumindest eine Fehldiagnose von GI-Nebenwirkungen oder ähnliches ist in diesen Studien nicht möglich. Dennoch hat CMRX selber diese Studien vorerst angehalten bis man das Problem mit Brinci besser einschätzen kann.

Gruß
ipollit
Antwort auf Beitrag Nr.: 51.373.632 von ipollit am 28.12.15 12:15:53Hallo ipollit,
schade mit CMRX, klang viel versprechend.
Danke für die informative Analyse zu PIRS. Dass die Anticaline evtl. eine schnellere Abbauzeit im Körper haben, daran hatte ich noch gar nicht gedacht. Klingt aber schlüssig.
Trotz dass die Urspünge von Pieris ja in Deutschland liegen, ich glaube auch Wacker Chemie hatten ihre Hände da auch mal mit drin, ist relativ wenig publiziert.
Ich bin über eine Präsi von Ablynx auf Pieris vor ca. 2 Jahren gestoßen, die hatten dort mal Vergleiche zu direkten Wettbwerbern gezogen u.a. auch zu MGNX, BITE, AFMD.
Der Börsengang war ja zu 2,75 $, wurde auch nicht gerade so viel Cash eingesammelt. Sicherlich wird die Finanzierung der Pipeline bei der geringen Größe eine Herausforderung darstellen oder es gelingen noch weitere Deals. Das halbe Management ist ja Ex-MOR, das kann gut sein oder auch nicht. Zumindest der Newsflow in den letzten Monaten passt erstmal, auch wenn die Entwicklung noch ein paar Jahre dauern wird.
Ich schaue mir gerade auch Probiodrug an. In Alzheimer sind ja bisher alle gescheitert, im Sommer ja Evotec mit Roche. Eine kleine Startposition sind die mir trotzdem Wert. Immerhin Probiodrug erhielt 2015 European Mediscience Award for Best Technology, u.a. wurden in der selben Veranstaltung auch Cellectis mit dem "company of the year" Award ausgezeichnet. Und BB Biotech, TVM und Biogen Idec sind mit ein paar Prozenten beteiligt. Allerdings ist die Pipeline nicht gerade breit und nur Phase I für knapp über 100 Mill. MC.
Gruß
McNay
schade mit CMRX, klang viel versprechend.
Danke für die informative Analyse zu PIRS. Dass die Anticaline evtl. eine schnellere Abbauzeit im Körper haben, daran hatte ich noch gar nicht gedacht. Klingt aber schlüssig.
Trotz dass die Urspünge von Pieris ja in Deutschland liegen, ich glaube auch Wacker Chemie hatten ihre Hände da auch mal mit drin, ist relativ wenig publiziert.
Ich bin über eine Präsi von Ablynx auf Pieris vor ca. 2 Jahren gestoßen, die hatten dort mal Vergleiche zu direkten Wettbwerbern gezogen u.a. auch zu MGNX, BITE, AFMD.
Der Börsengang war ja zu 2,75 $, wurde auch nicht gerade so viel Cash eingesammelt. Sicherlich wird die Finanzierung der Pipeline bei der geringen Größe eine Herausforderung darstellen oder es gelingen noch weitere Deals. Das halbe Management ist ja Ex-MOR, das kann gut sein oder auch nicht. Zumindest der Newsflow in den letzten Monaten passt erstmal, auch wenn die Entwicklung noch ein paar Jahre dauern wird.
Ich schaue mir gerade auch Probiodrug an. In Alzheimer sind ja bisher alle gescheitert, im Sommer ja Evotec mit Roche. Eine kleine Startposition sind die mir trotzdem Wert. Immerhin Probiodrug erhielt 2015 European Mediscience Award for Best Technology, u.a. wurden in der selben Veranstaltung auch Cellectis mit dem "company of the year" Award ausgezeichnet. Und BB Biotech, TVM und Biogen Idec sind mit ein paar Prozenten beteiligt. Allerdings ist die Pipeline nicht gerade breit und nur Phase I für knapp über 100 Mill. MC.
Gruß
McNay
Antwort auf Beitrag Nr.: 51.374.376 von ipollit am 28.12.15 14:14:04Hallo ipollit,
interessant das du FMI ansprichst.
Bisher verbrennen alle Firmen wie FMI, Nanosphere, Nanostring etc. mit ihren Tests wahnsinnig viel Geld. Für jeden verdienten Dollar, geben die locker das 1,5 fache wieder aus. Trotz dass die Zukunftsprognosen sehr gut sind und personalisierte Medizin und Früherkennung nicht nur bei Krebs, sondern auch bei Infektionen, ohne Zweifel die Zukunft sein werden. Jedoch ist fraglich, wer hier das Rennen gewinnt. Dazu kommen noch die Platzhirsche wie Illumina oder auch Qiagen etc... Vielleicht kommt auch von Google oder den Pharmariesen noch Konkurenz. Ich persönliche finde die Thematik sehr, sehr spannend, ich war auch mal in Nanosphere und Nanostring investiert, schaue aber jetzt lieber von der Seite zu. Ohad Hammer hat mit FMI auf Jahressicht auch ein kräftiges "Auf und Ab" erlebt.
Die letzten Q-Zahlen sahen aus meiner Sicht bei FMI auch nicht so super aus. Wen es aber interessiert, die Präsi auf der Website von FMI kann ich nur empfehlen.
Gruß
McNay
interessant das du FMI ansprichst.
Bisher verbrennen alle Firmen wie FMI, Nanosphere, Nanostring etc. mit ihren Tests wahnsinnig viel Geld. Für jeden verdienten Dollar, geben die locker das 1,5 fache wieder aus. Trotz dass die Zukunftsprognosen sehr gut sind und personalisierte Medizin und Früherkennung nicht nur bei Krebs, sondern auch bei Infektionen, ohne Zweifel die Zukunft sein werden. Jedoch ist fraglich, wer hier das Rennen gewinnt. Dazu kommen noch die Platzhirsche wie Illumina oder auch Qiagen etc... Vielleicht kommt auch von Google oder den Pharmariesen noch Konkurenz. Ich persönliche finde die Thematik sehr, sehr spannend, ich war auch mal in Nanosphere und Nanostring investiert, schaue aber jetzt lieber von der Seite zu. Ohad Hammer hat mit FMI auf Jahressicht auch ein kräftiges "Auf und Ab" erlebt.
Die letzten Q-Zahlen sahen aus meiner Sicht bei FMI auch nicht so super aus. Wen es aber interessiert, die Präsi auf der Website von FMI kann ich nur empfehlen.
Gruß
McNay
In Zukunft wird es im IO-Bereich wahrscheinlich auch viele Kombis geben... hier sind einige bereits laufende Kombi-Studien aufgelistet:
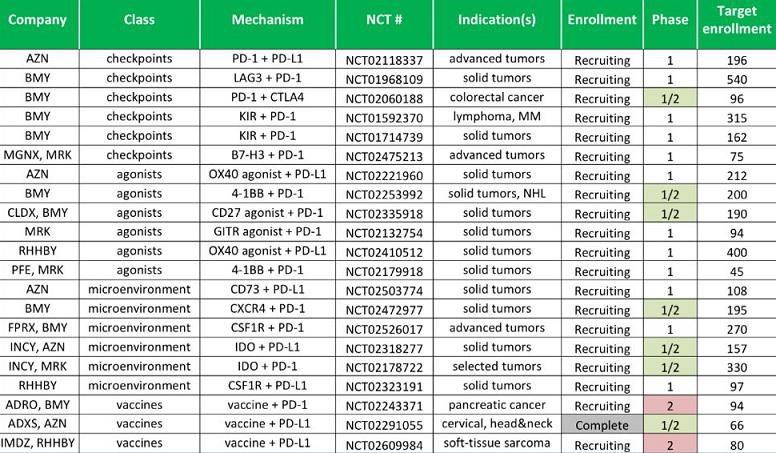
Werte mit IO-Kandiaten, die ich aktuell im Depot habe sind AGEN, CLDX, INCY, IPH, FPRX, MGNX, MDVN, OMED, SGEN, TSRO. Im nächsten Jahr könnte deren klinische Pipeline vielleicht so aussehen. Ich hoffe, dass sie damit auch für die Pharmas interessant werden...
- PD1 (3-4 Kandidaten)
- CTLA4 (1-2)
- TIM3 (2)
- LAG3 (2-3)
- GITR (1-3)
- OX40 (1)
- B7H3 (2)
- CD27 (1)
- CD40 (1)
- TIGIT (1)
- KIR (1)
- NKG2A (1)
- IDO1 (1)
- CSF1R (1)
- DLL4 (1)
Gruß
ipollit

Werte mit IO-Kandiaten, die ich aktuell im Depot habe sind AGEN, CLDX, INCY, IPH, FPRX, MGNX, MDVN, OMED, SGEN, TSRO. Im nächsten Jahr könnte deren klinische Pipeline vielleicht so aussehen. Ich hoffe, dass sie damit auch für die Pharmas interessant werden...
- PD1 (3-4 Kandidaten)
- CTLA4 (1-2)
- TIM3 (2)
- LAG3 (2-3)
- GITR (1-3)
- OX40 (1)
- B7H3 (2)
- CD27 (1)
- CD40 (1)
- TIGIT (1)
- KIR (1)
- NKG2A (1)
- IDO1 (1)
- CSF1R (1)
- DLL4 (1)
Gruß
ipollit
FGEN, XLRN, AKBA
Der Markt für Blutarmut ist ziemlich groß... zuletzt ist er nur geschrumpft, weil ESAs zuviele Nebenwirkungen aufweisen, um sie breiter nutzen zu können. Außerdem sind ESAs nicht überall wirksam... z.B. nicht im Zusammenhang mit Autoimmunerkrankungen wie RA.

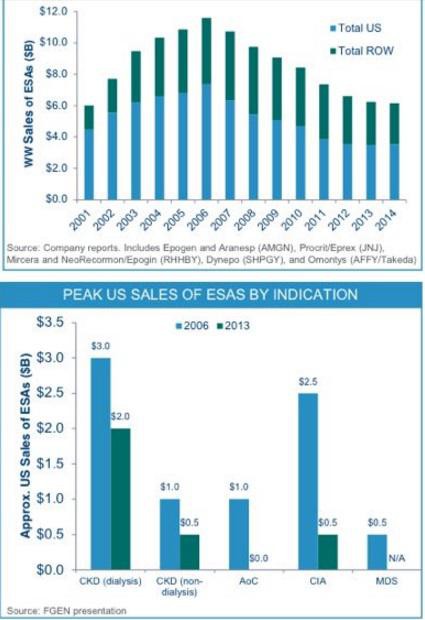




Gruß
ipollit
Der Markt für Blutarmut ist ziemlich groß... zuletzt ist er nur geschrumpft, weil ESAs zuviele Nebenwirkungen aufweisen, um sie breiter nutzen zu können. Außerdem sind ESAs nicht überall wirksam... z.B. nicht im Zusammenhang mit Autoimmunerkrankungen wie RA.



Gruß
ipollit
RLYP
Hyperkalemia ist von den Zahlen her ebenfalls ein großer Markt. Peak Sales von 1 Mrd USD im US-Markt basieren auf einer nur geringen Nutzung bei den betroffenen Patienten.
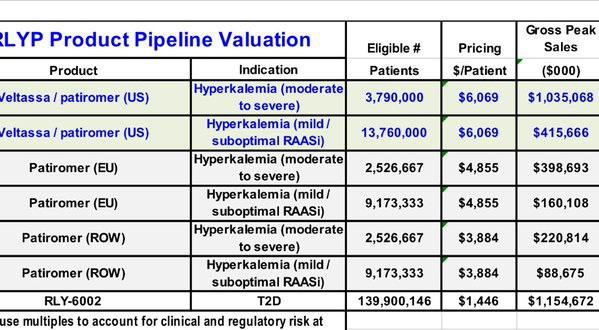
Im nächsten Jahr muss man sehen, ob sich das Label von Veltassa verbessert und ob ZS-9 ohne gravierende Warnungen zugelassen wird. Von Letzterem gehe ich momentan nicht aus.


Gruß
ipollit
Hyperkalemia ist von den Zahlen her ebenfalls ein großer Markt. Peak Sales von 1 Mrd USD im US-Markt basieren auf einer nur geringen Nutzung bei den betroffenen Patienten.

Im nächsten Jahr muss man sehen, ob sich das Label von Veltassa verbessert und ob ZS-9 ohne gravierende Warnungen zugelassen wird. Von Letzterem gehe ich momentan nicht aus.

Gruß
ipollit
IBB
Der IBB/NBI sieht momentan nicht schlecht aus, wie ich finde... vielleicht gelingt ja der Ausbruch, zumal der Januar bevorsteht, der traditionell zu den stärksten Monaten zählt.
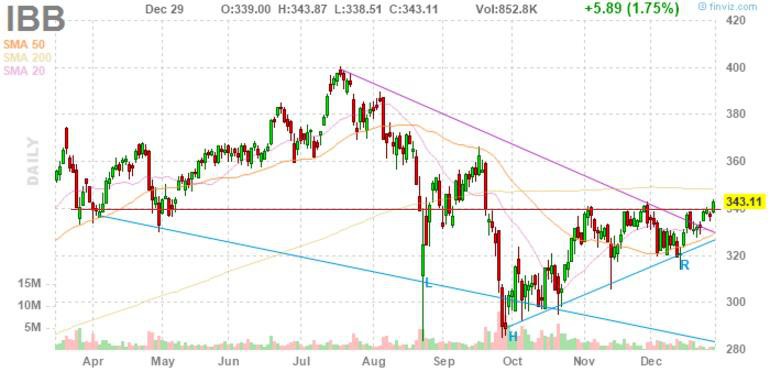
Gruß
ipollit
Der IBB/NBI sieht momentan nicht schlecht aus, wie ich finde... vielleicht gelingt ja der Ausbruch, zumal der Januar bevorsteht, der traditionell zu den stärksten Monaten zählt.

Gruß
ipollit
CEMP
Zwar soll die Hauptanwendung von Solithromycin die Lungenentzündung CABP sein, doch könnte der dringendere Bedarf bei Gonorrhoe (Tripper) bestehen, da diese Bakterien zunehmend resistent gegen alle verfügbaren Antibiotika werden:
http://www.cbsnews.com/news/uk-health-leaders-warn-of-untrea…
"Drug-resistant "super-gonorrhea" could be untreatable, doctors warn
Gonorrhea could become untreatable in the U.K., England's top health official warns. There's concern in the U.S., too... "
Daher wird CEMP bei seien Gonorrhoe-Studien von öffentlicher Seite unterstützt. Die aktuelle PIII wurde zudem ausgeweitet für eine breitere Zulassung... die Daten sollten Mitte 2016 kommen. Neben CABP könnte das dann die zweite Zulassungs-Indikation werden.


Der Bedarf von neuen Makroliden wie Solithromycin u.a. in CABP ergibt sich dadurch, dass die Erreger zunehmend resistent gegen die aktuellen Standard-Makrolide werden und andere wirksame Mittel ein größeres Spektrum besitzen. Das Spektrum von Makroliden passt sehr gut zu den CABP-Erregern, d.h. dass das Antibiotikum im wesentliche diese abtötet, während andere Bakterien unbeeinflusst bleiben. Wären dagegen alle Bakterien betroffen, wie es z.B. bei Breitband-Antibiotika der Fall ist, so wird u.a. auch die "gute" Darm-Flora zerstört. Dies kann wiederum zu gravierenden Erkrankungen wie CDI führen (eine Behandlung wären dann die Mikroorganismen von MCRB).

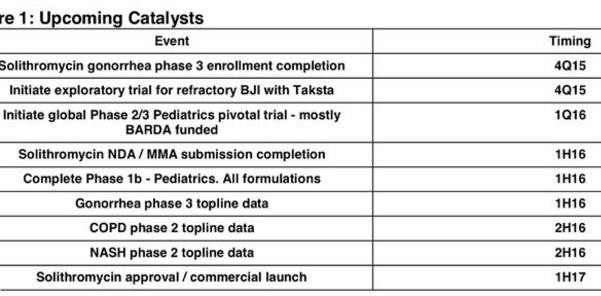

Gruß
ipollit
Zwar soll die Hauptanwendung von Solithromycin die Lungenentzündung CABP sein, doch könnte der dringendere Bedarf bei Gonorrhoe (Tripper) bestehen, da diese Bakterien zunehmend resistent gegen alle verfügbaren Antibiotika werden:
http://www.cbsnews.com/news/uk-health-leaders-warn-of-untrea…
"Drug-resistant "super-gonorrhea" could be untreatable, doctors warn
Gonorrhea could become untreatable in the U.K., England's top health official warns. There's concern in the U.S., too... "
Daher wird CEMP bei seien Gonorrhoe-Studien von öffentlicher Seite unterstützt. Die aktuelle PIII wurde zudem ausgeweitet für eine breitere Zulassung... die Daten sollten Mitte 2016 kommen. Neben CABP könnte das dann die zweite Zulassungs-Indikation werden.


Der Bedarf von neuen Makroliden wie Solithromycin u.a. in CABP ergibt sich dadurch, dass die Erreger zunehmend resistent gegen die aktuellen Standard-Makrolide werden und andere wirksame Mittel ein größeres Spektrum besitzen. Das Spektrum von Makroliden passt sehr gut zu den CABP-Erregern, d.h. dass das Antibiotikum im wesentliche diese abtötet, während andere Bakterien unbeeinflusst bleiben. Wären dagegen alle Bakterien betroffen, wie es z.B. bei Breitband-Antibiotika der Fall ist, so wird u.a. auch die "gute" Darm-Flora zerstört. Dies kann wiederum zu gravierenden Erkrankungen wie CDI führen (eine Behandlung wären dann die Mikroorganismen von MCRB).


Gruß
ipollit
Allen einen guten Rutsch und ein gesundes, frohes und erfolgreiches 2016!
Apropos "Rutsch":
Beim persönlichen Rückblick auf dieses Jahr und generell die Vergangenheit bleiben meine Gedanken unter anderem kurz bei Stemline stehen.
Hier mal die Kursentwicklung seit Oktober 2013:

Der Kursverfall von annährend 90% (!) ist ohne eine einzige signifikante negative Nachricht zustande gekommen.
Im Großen und Ganzen ist STML im Plan (zeitlich gibt es Verzögerungen, was aber nicht ungewöhnlich ist). Nur die Sichtweise des Marktes hat sich radikal verändert. Auf dem Höhepunkt der Blase wurden Risiken systematisch aus den Bewertungen ausgeblendet. Das hat zu ganz verrückten Kursen geführt. Vielleicht werden aber inzwischen hier und da die Chancen zu wenig gesehen?
Hier mal ein Link zur aktuellen Unternehmenspräsentation (teilweise relativ "harte" Krankheitsbilder enthalten):
http://files.shareholder.com/downloads/AMDA-145M5E/107984478…
Im kommenden Jahr wird sich wohl entscheiden, ob der Wirkstoff SL-401 zumindest in der Indikation Blastic Plasmacytoid Dendritic Cell Neoplasm (BPDCN) in Richtung Zulassung geht oder nicht. Nach der Feuerstein-Ratain Rule sieht es für den laufenden pivotal Trial bis jetzt wirklich schlecht aus, aber noch ist sicher ein halbes Jahr Zeit, bis diese Regel wirklich greift. Man darf jedenfalls gespannt sein.
Apropos "Rutsch":
Beim persönlichen Rückblick auf dieses Jahr und generell die Vergangenheit bleiben meine Gedanken unter anderem kurz bei Stemline stehen.
Hier mal die Kursentwicklung seit Oktober 2013:
Der Kursverfall von annährend 90% (!) ist ohne eine einzige signifikante negative Nachricht zustande gekommen.
Im Großen und Ganzen ist STML im Plan (zeitlich gibt es Verzögerungen, was aber nicht ungewöhnlich ist). Nur die Sichtweise des Marktes hat sich radikal verändert. Auf dem Höhepunkt der Blase wurden Risiken systematisch aus den Bewertungen ausgeblendet. Das hat zu ganz verrückten Kursen geführt. Vielleicht werden aber inzwischen hier und da die Chancen zu wenig gesehen?
Hier mal ein Link zur aktuellen Unternehmenspräsentation (teilweise relativ "harte" Krankheitsbilder enthalten):
http://files.shareholder.com/downloads/AMDA-145M5E/107984478…
Im kommenden Jahr wird sich wohl entscheiden, ob der Wirkstoff SL-401 zumindest in der Indikation Blastic Plasmacytoid Dendritic Cell Neoplasm (BPDCN) in Richtung Zulassung geht oder nicht. Nach der Feuerstein-Ratain Rule sieht es für den laufenden pivotal Trial bis jetzt wirklich schlecht aus, aber noch ist sicher ein halbes Jahr Zeit, bis diese Regel wirklich greift. Man darf jedenfalls gespannt sein.
hallo,
ich wünsche auch allen ein frohes neues jahr
hier ein papier wo ich nicht weiss ob es hier reinpasst, etwas bringt
beim googeln zufällig gesehen
Deutscher Biotechnologie-Report 2014
www.biodeutschland.org/tl_files/content/dokumente/biothek/20…
Gruß
P.
ich wünsche auch allen ein frohes neues jahr
hier ein papier wo ich nicht weiss ob es hier reinpasst, etwas bringt
beim googeln zufällig gesehen
Deutscher Biotechnologie-Report 2014
www.biodeutschland.org/tl_files/content/dokumente/biothek/20…
Gruß
P.
Wünsche auch allen ein frohes, erfolgreiches neues Jahr!
Die Indizes sind in 2015 ja eher holprig mehr oder weniger seitwärts gelaufen. Der S&P lag am Ende leicht im Minus, der Nasdaq dagegen etwas im Plus.
Nach dem Top im Sommer mit anschließendem deutlichen Einbruch haben sich die Biotechs am Ende doch noch gut geschlagen, auch wenn sie aktuell klar unter ihren Hochs notieren.

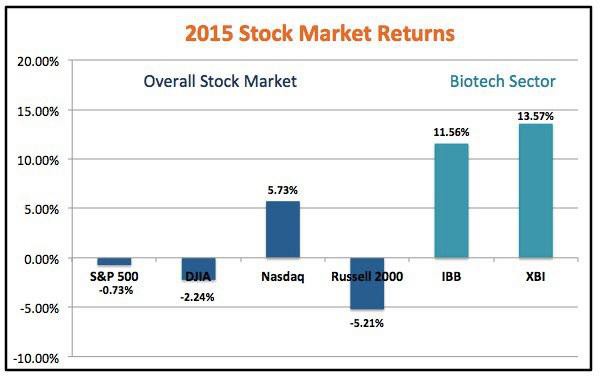
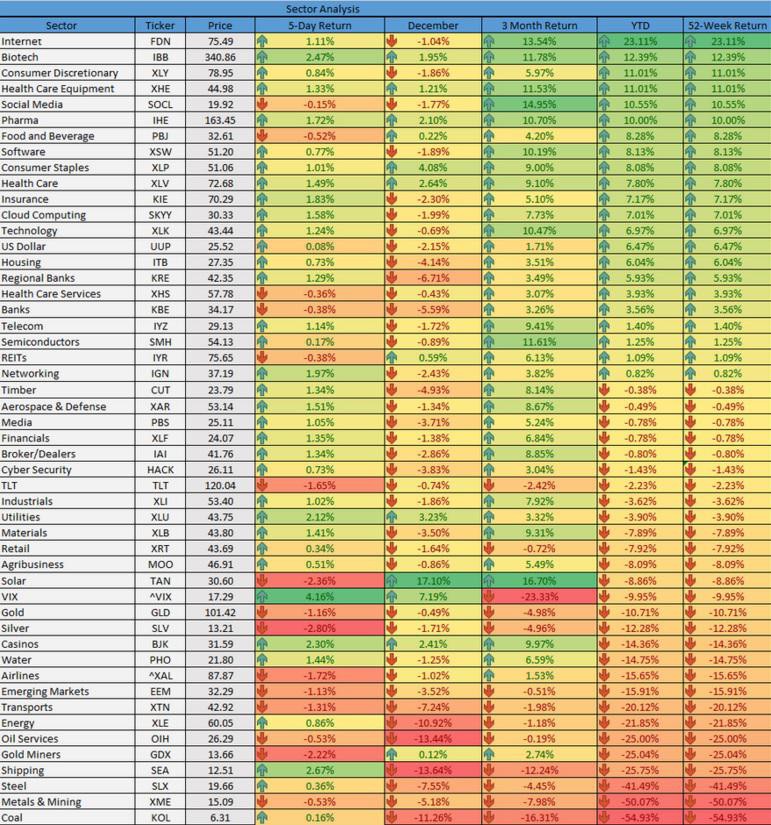
Auch im Vergleich zu anderen Jahren kann sich die Performance des NBI/IBB immer noch sehen lassen...
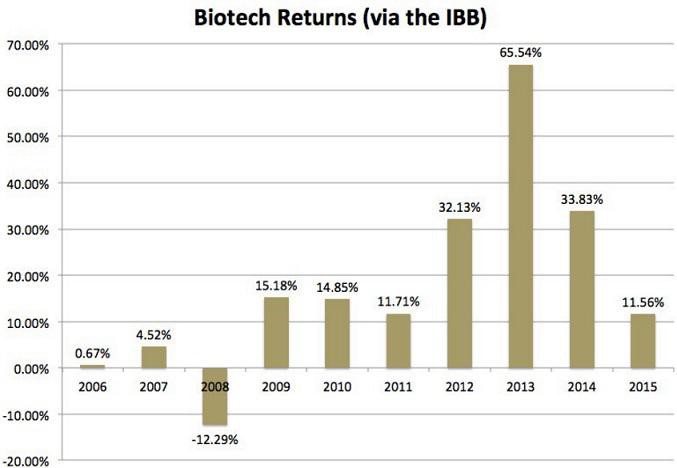
Übernächste Woche wird es auch direkt wieder spannend... dann werden die meisten Biotechs ihren aktuellen Stand auf der J.P. Morgan Annual Healthcare Conference präsentieren, der größten Investoren-Konferenz des Jahres:
http://jpmorgan.metameetings.com/confbook/healthcare16/login…
Öfters kommt es im Zeitraum dieser Konferenz zu neues Deals. Zumindest wird man sehen, wie die Stimmung in der Branche ist, ob die Euphorie der letzten Jahre etwas verflogen ist oder nach wie vor hohes Interesse besteht.
Viele Grüße
ipollit
Die Indizes sind in 2015 ja eher holprig mehr oder weniger seitwärts gelaufen. Der S&P lag am Ende leicht im Minus, der Nasdaq dagegen etwas im Plus.
Nach dem Top im Sommer mit anschließendem deutlichen Einbruch haben sich die Biotechs am Ende doch noch gut geschlagen, auch wenn sie aktuell klar unter ihren Hochs notieren.


Auch im Vergleich zu anderen Jahren kann sich die Performance des NBI/IBB immer noch sehen lassen...

Übernächste Woche wird es auch direkt wieder spannend... dann werden die meisten Biotechs ihren aktuellen Stand auf der J.P. Morgan Annual Healthcare Conference präsentieren, der größten Investoren-Konferenz des Jahres:
http://jpmorgan.metameetings.com/confbook/healthcare16/login…
Öfters kommt es im Zeitraum dieser Konferenz zu neues Deals. Zumindest wird man sehen, wie die Stimmung in der Branche ist, ob die Euphorie der letzten Jahre etwas verflogen ist oder nach wie vor hohes Interesse besteht.
Viele Grüße
ipollit
Da ich viele Werte in meinem Depot habe, um ein etwas gegen Crashs wie zuletzt bei CMRX geschützt zu sein, bewegt sich die Performance auch eher im Bereich des Durchschnitts. Bei einer Anlage in US-Werte konnte man in 2015 auch erheblich vom stärkeren Dollar profitieren, was alleine ca. 10% Gewinn gebracht hat...
NBI +11,4%
USD/EUR +11,4%
Zum Vergleich ist die Entwicklung des Dax mit +9,6% auch sehr ordentlich. Mit deutschen Nebenwerten oder dem TecDax hat man nochmal deutlich besser als mit dem Dax abgeschnitten... der TecDax ist z.B. ca. 34% im Plus.
Mit meinem Depot liege ich am Ende nach Aufs und Abs auch ein wenig besser als der NBI... ca. +33%, wobei wie gesagt alleine der USD über 11% dazu beigetragen hat.
Damit starte ich 2016 mit folgenden Werten... (jeweils mit aktuellem Gewicht und Gewinn oder Verlust des Aktienkurses im Jahr 2015)
6,5% INCY (+ 48,3%)
5,6% EXEL (+ 291,7%)
5,1% ACAD (+ 12,3%)
4,7% FPRX (+ 53,7%)
4,6% MGNX (- 11,7%)
4,5% XLRN (+ 25,2%)
4,3% RLYP (- 8,0%)
4,2% IONS (+ 0,3%)
4,1% MDVN (- 2,9%)
3,9% IPH.PA (+ 71,4%)
3,7% TSRO (+ 40,7%)
3,5% FGEN (+ 11,4%)
3,5% CLDX (- 14,1%)
3,1% CEMP (+ 32,4%)
2,9% OMED (+ 3,6%)
2,8% CLVS (- 37,5%)
2,7% REGN (+ 32,3%)
2,7% ALNY (- 2,9%)
2,7% GEN.CO (+ 154,6%)
2,7% SAGE (+ 59,3%)
2,7% KPTI (- 64,6%)
2,5% NVAX (+ 41,5%)
2,5% ARRY (- 10,8%)
2,0% ARQL (+ 77,9%)
1,8% PTLA (+ 81,7%)
1,4% AKBA (+ 11,0%)
1,3% AGEN (+ 14,4%)
1,3% INFI (- 53,5%)
1,3% EPZM (- 15,1%)
1,2% SGEN (+ 39,7%)
1,0% ESPR (- 45,0%)
0,9% IMMU (- 36,0%)
0,7% AUPH (- 32,1%)
0,5% XENE (- 59,3%)
0,4% MRNS (- 27,7%)
0,4% CMRX (- 77,8%)
0,3% STML (- 63,0%)
Entwicklung von weiteren Werten, die ich 2015 in meinem Depot hatte...
ITCI (+ 204,8%)
ZSPH (+ 116,5%)
PCYC (+ 110,3%)
RCPT (+ 89,3%)
AERI (- 16,6%)
ENTA (- 35,1%)
EBIO (- 74,7%)
VSTM (- 79,6%)
SNTA (- 86,7%)
KBIO (- 100,0%)
Gruß
ipollit
NBI +11,4%
USD/EUR +11,4%
Zum Vergleich ist die Entwicklung des Dax mit +9,6% auch sehr ordentlich. Mit deutschen Nebenwerten oder dem TecDax hat man nochmal deutlich besser als mit dem Dax abgeschnitten... der TecDax ist z.B. ca. 34% im Plus.
Mit meinem Depot liege ich am Ende nach Aufs und Abs auch ein wenig besser als der NBI... ca. +33%, wobei wie gesagt alleine der USD über 11% dazu beigetragen hat.
Damit starte ich 2016 mit folgenden Werten... (jeweils mit aktuellem Gewicht und Gewinn oder Verlust des Aktienkurses im Jahr 2015)
6,5% INCY (+ 48,3%)
5,6% EXEL (+ 291,7%)
5,1% ACAD (+ 12,3%)
4,7% FPRX (+ 53,7%)
4,6% MGNX (- 11,7%)
4,5% XLRN (+ 25,2%)
4,3% RLYP (- 8,0%)
4,2% IONS (+ 0,3%)
4,1% MDVN (- 2,9%)
3,9% IPH.PA (+ 71,4%)
3,7% TSRO (+ 40,7%)
3,5% FGEN (+ 11,4%)
3,5% CLDX (- 14,1%)
3,1% CEMP (+ 32,4%)
2,9% OMED (+ 3,6%)
2,8% CLVS (- 37,5%)
2,7% REGN (+ 32,3%)
2,7% ALNY (- 2,9%)
2,7% GEN.CO (+ 154,6%)
2,7% SAGE (+ 59,3%)
2,7% KPTI (- 64,6%)
2,5% NVAX (+ 41,5%)
2,5% ARRY (- 10,8%)
2,0% ARQL (+ 77,9%)
1,8% PTLA (+ 81,7%)
1,4% AKBA (+ 11,0%)
1,3% AGEN (+ 14,4%)
1,3% INFI (- 53,5%)
1,3% EPZM (- 15,1%)
1,2% SGEN (+ 39,7%)
1,0% ESPR (- 45,0%)
0,9% IMMU (- 36,0%)
0,7% AUPH (- 32,1%)
0,5% XENE (- 59,3%)
0,4% MRNS (- 27,7%)
0,4% CMRX (- 77,8%)
0,3% STML (- 63,0%)
Entwicklung von weiteren Werten, die ich 2015 in meinem Depot hatte...
ITCI (+ 204,8%)
ZSPH (+ 116,5%)
PCYC (+ 110,3%)
RCPT (+ 89,3%)
AERI (- 16,6%)
ENTA (- 35,1%)
EBIO (- 74,7%)
VSTM (- 79,6%)
SNTA (- 86,7%)
KBIO (- 100,0%)
Gruß
ipollit
was aus 100.000 Euro in 2015 geworden wäre...
http://www.faz.net/aktuell/finanzen/meine-finanzen/sparen-un…
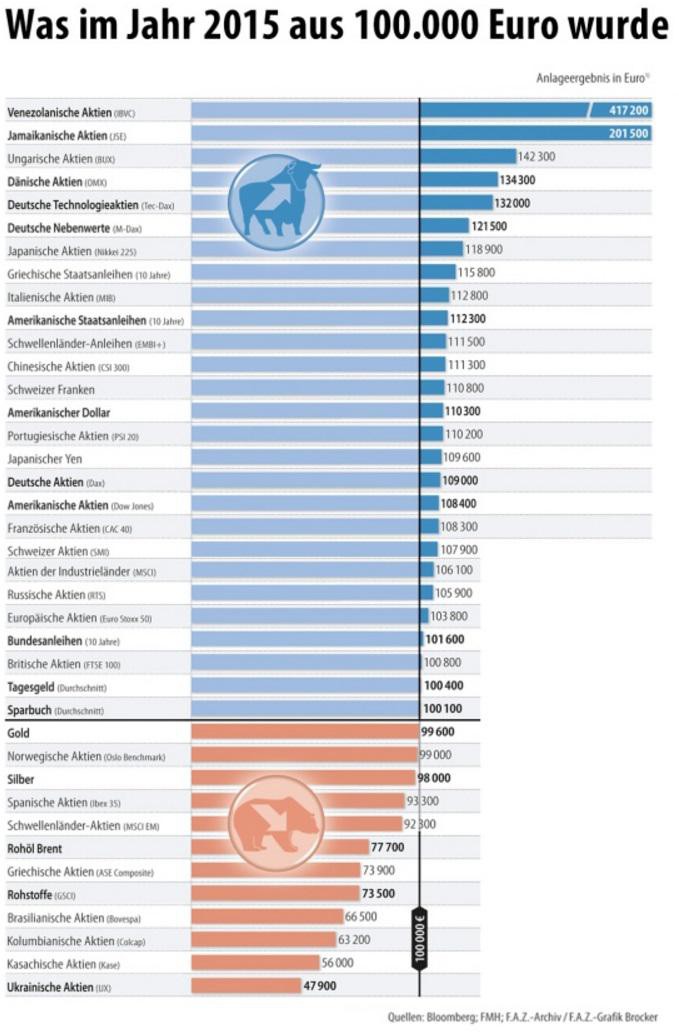
Gruß
ipollit
http://www.faz.net/aktuell/finanzen/meine-finanzen/sparen-un…

Gruß
ipollit
Tja, andere müssen den Aktienbestand verwässern, um an Cash zu kommen...

Brad Loncar @bradloncar
Tonight’s offerings.
Schon extrem für einen einzigen Abend. Da bringen sich wohl einige schon mal für das Jahr 2016 auf die sichere Seite, bevor an den Märkten was passieren kann?

Brad Loncar @bradloncar
Tonight’s offerings.
Schon extrem für einen einzigen Abend. Da bringen sich wohl einige schon mal für das Jahr 2016 auf die sichere Seite, bevor an den Märkten was passieren kann?
Antwort auf Beitrag Nr.: 51.419.301 von SLGramann am 05.01.16 22:28:55Und da kann man AKBA noch hinzuzählen, auch wenn das schon gestern war und heute für -14% gesorgt hat:
http://ir.akebia.com/releasedetail.cfm?ReleaseID=948625
http://ir.akebia.com/releasedetail.cfm?ReleaseID=948625
Antwort auf Beitrag Nr.: 51.419.337 von SLGramann am 05.01.16 22:32:53Neben AKBA war dies gestern auch XLRN...
AKBA 75 Mio USD -> -14,17%
XLRN 150 Mio USD -> -10,34%
Die Kandidaten von heute stehen nach der Ankündigung ähnlich im Minus. Ein wenig ärgerlich ist es, dass dies mit einem sehr schwachen Gesamtmarkt (also nicht nur die Biotechs) zusammenfällt.
Ich glaube allerdings nicht, dass die Kapitalmaßnahmen aus Furcht vor einem Kollaps des Gesamtmarktes jetzt abrupt durchgeführt werden. Ist nicht im Januar die Stimmung öfters eher positiv gewesen?... da plant man vielleicht eher eine Kapitalerhöhung als in traditionell schwierigen Zeiten.
Auffällig ist auch, dass AKBA, PRTA, SAGE, CEMP und ACAD mögliche Blockbuster in PIII oder in der Zulassungsprüfung haben, für die sie jeweils nahezu 100% der Rechte halten. Sie wollen diese zum großen Teil selber vermarkten. Mit ausreichend Kapital macht man sich von unabhängig von Partnern.
EPZM hat die Rechte an Tazemetostat von Eisai zurückgekauft, was auch eher ungewöhnlich ist. Andere entwickeln mit Partnern, so dass der Kapitalbedarf sehr viel geringer ist.
Gruß
ipollit
AKBA 75 Mio USD -> -14,17%
XLRN 150 Mio USD -> -10,34%
Die Kandidaten von heute stehen nach der Ankündigung ähnlich im Minus. Ein wenig ärgerlich ist es, dass dies mit einem sehr schwachen Gesamtmarkt (also nicht nur die Biotechs) zusammenfällt.
Ich glaube allerdings nicht, dass die Kapitalmaßnahmen aus Furcht vor einem Kollaps des Gesamtmarktes jetzt abrupt durchgeführt werden. Ist nicht im Januar die Stimmung öfters eher positiv gewesen?... da plant man vielleicht eher eine Kapitalerhöhung als in traditionell schwierigen Zeiten.
Auffällig ist auch, dass AKBA, PRTA, SAGE, CEMP und ACAD mögliche Blockbuster in PIII oder in der Zulassungsprüfung haben, für die sie jeweils nahezu 100% der Rechte halten. Sie wollen diese zum großen Teil selber vermarkten. Mit ausreichend Kapital macht man sich von unabhängig von Partnern.
EPZM hat die Rechte an Tazemetostat von Eisai zurückgekauft, was auch eher ungewöhnlich ist. Andere entwickeln mit Partnern, so dass der Kapitalbedarf sehr viel geringer ist.
Gruß
ipollit
Antwort auf Beitrag Nr.: 51.420.027 von ipollit am 06.01.16 00:30:56letztes Jahr gab es im Januar auch zahlreiche KEs
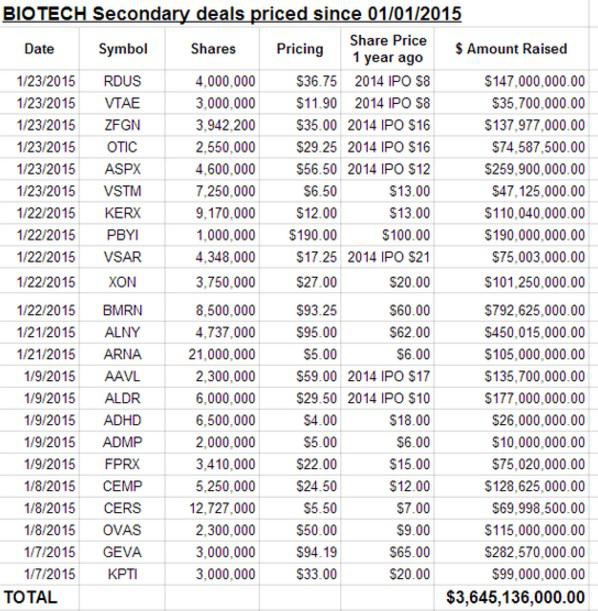
im Vergleich zu anderen Jahren war es im Januar 2015 aber erheblich mehr Geld
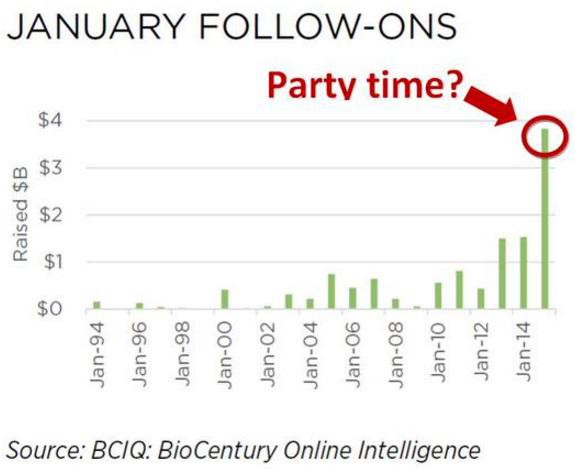
Gruß
ipollit

im Vergleich zu anderen Jahren war es im Januar 2015 aber erheblich mehr Geld

Gruß
ipollit
Relypsa wird immer günstiger für eine Übernahme finde ich verrückt die Kursentwicklung

Heute hab ich wenigstens mal 3 grüne Bios im Depot,
aber Tag ist noch nicht vorbei
Heute hab ich wenigstens mal 3 grüne Bios im Depot,
aber Tag ist noch nicht vorbei

Heute knallts ja mal wieder ganz schön...
Ich bin jetzt wieder bei ADAP dabei. Ich will ganz grundsätzlich im TCR-Bereich engagiert sein und habe jetzt meine KITE-Position wieder mit ADAP ergänzt.
Erste frühe Daten ihres NY-ESO-Programms bei synovial sarcoma sehen gut aus. Das Programm ist zwar im Prinzip an GSK "verschenkt", aber es geht dabei eher um den Nachweis, dass die Technologie funktioniert.
Insgesamt halte ich den TCR-Ansatz für wesentlich vielversprechender als CAR-T.
----
PS: Vielversprechende Daten kommen heute von QURE, die zwar im Plus sind, aber in den letzten Monaten nur noch verprügelt wurden und nicht mehr teuer sind (Marktkapitalisierung 330 Mio. oder so).


Ist auch so ein "Grundsatzding". Wer sich im Gentechnikbereich engagieren will, landet eben vermutlich bei BLUE, QURE (und vielleicht auch ONCE). Wobei ich mich bisher zu einer Neuaufnahme von QURE nicht durchringen kann. Wahrscheinlich werden auch die heutigen Gewinne wieder abverkauft werden. Der Markt ist einfach ziemlich kaputt.
Ich bin jetzt wieder bei ADAP dabei. Ich will ganz grundsätzlich im TCR-Bereich engagiert sein und habe jetzt meine KITE-Position wieder mit ADAP ergänzt.
Erste frühe Daten ihres NY-ESO-Programms bei synovial sarcoma sehen gut aus. Das Programm ist zwar im Prinzip an GSK "verschenkt", aber es geht dabei eher um den Nachweis, dass die Technologie funktioniert.
Insgesamt halte ich den TCR-Ansatz für wesentlich vielversprechender als CAR-T.
----
PS: Vielversprechende Daten kommen heute von QURE, die zwar im Plus sind, aber in den letzten Monaten nur noch verprügelt wurden und nicht mehr teuer sind (Marktkapitalisierung 330 Mio. oder so).


Ist auch so ein "Grundsatzding". Wer sich im Gentechnikbereich engagieren will, landet eben vermutlich bei BLUE, QURE (und vielleicht auch ONCE). Wobei ich mich bisher zu einer Neuaufnahme von QURE nicht durchringen kann. Wahrscheinlich werden auch die heutigen Gewinne wieder abverkauft werden. Der Markt ist einfach ziemlich kaputt.
Antwort auf Beitrag Nr.: 51.439.008 von SLGramann am 07.01.16 21:03:02na ja QURE ist z. B. teurer als KPTI. Das gibt mir schon zu denken.
Antwort auf Beitrag Nr.: 51.444.396 von riverstar_de am 08.01.16 12:51:02QURE Kurs 17.28$ hat ca. 235$ Cash das wären 9.79$ pro Aktie
KITE Kurs 54.63$ hat ca. 369$ Cash das wären 8.35$ pro Aktie
so teuer finde ich sie nicht
KITE Kurs 54.63$ hat ca. 369$ Cash das wären 8.35$ pro Aktie
so teuer finde ich sie nicht
Antwort auf Beitrag Nr.: 51.444.396 von riverstar_de am 08.01.16 12:51:02oh sorry seh gerade hast KPTI gemeint da hab ich mich versehen
Karyopharm Therapeutics, Inc. (KPTI) -NasdaqGS
9.72 Down 0.23(2.31%) 1:30PM EST - Nasdaq Real Time Price
Market Cap (intraday)5: 347.32M
Balance Sheet
Total Cash (mrq): 195.24M
Total Cash Per Share (mrq): 5.46
Total Debt (mrq): 0.00
Total Debt/Equity (mrq): N/A
Current Ratio (mrq): 13.74
Book Value Per Share (mrq): 6.18
9.72 Down 0.23(2.31%) 1:30PM EST - Nasdaq Real Time Price
Market Cap (intraday)5: 347.32M
Balance Sheet
Total Cash (mrq): 195.24M
Total Cash Per Share (mrq): 5.46
Total Debt (mrq): 0.00
Total Debt/Equity (mrq): N/A
Current Ratio (mrq): 13.74
Book Value Per Share (mrq): 6.18
Wow, was für ein Schlachtfest! Ich muss ehrlich zugeben, dass mich das auf dem falschen Fuß erwischt hat und ich entsprechend voll investiert bin. Die zur Zeit laufende JPM Konferenz hat bisher definitiv nicht die Wende gebracht. Im Gegenteil!
Was gibt Hoffnung? Vielleicht, dass man mittlerweile keine Hoffnung mehr hat?
Charttechnisch ist der NBI (größere Biotechs)noch in einer Unterstützungszone, die hat der XBI (kleinere Biotechs) aber schon nach unten durchbrochen.


Dabei gibt es doch nun wirklich günstige Investments (die natürlich trotzdem heute unter die Räder kommen). ESPR, GNCA, KPTI, XENE...sind im Grunde fast auf Cashniveau
Falls momentan überhaupt jemand Lust hat, sich mit Biotech zu beschäftigen:
http://jpmorgan.metameetings.com/confbook/healthcare16/speci…
Hab das bisher aber nur übeflogen - keine Lust momentan
SG kmastra
Was gibt Hoffnung? Vielleicht, dass man mittlerweile keine Hoffnung mehr hat?

Charttechnisch ist der NBI (größere Biotechs)noch in einer Unterstützungszone, die hat der XBI (kleinere Biotechs) aber schon nach unten durchbrochen.
Dabei gibt es doch nun wirklich günstige Investments (die natürlich trotzdem heute unter die Räder kommen). ESPR, GNCA, KPTI, XENE...sind im Grunde fast auf Cashniveau

Falls momentan überhaupt jemand Lust hat, sich mit Biotech zu beschäftigen:
http://jpmorgan.metameetings.com/confbook/healthcare16/speci…
Hab das bisher aber nur übeflogen - keine Lust momentan

SG kmastra
Antwort auf Beitrag Nr.: 51.465.666 von kmastra am 11.01.16 19:16:10Ja da gibt es mächtig auf die Ohren 
Nachkauf:
OMED, RLYP, BLCM, KPTI, ESPR, AFMD, CTRV

Nachkauf:
OMED, RLYP, BLCM, KPTI, ESPR, AFMD, CTRV
So einen schmerzhaften Arschvoll habe ich zuletzt von meinen Eltern bekommen, als ich mit 7 Jahren Bratäpfel auf offenem Feuer in einem Holzhaus gemacht habe...Naja, man soll investieren, wenn richtig Blut fließt, also eigentlich jetzt...Hat jemand von Euch den Mut oder wartet Ihr weiter ab? Und für welche Aktien sollte man sich entscheiden? Die folgenden halte ich für sehr billig, aber der sichere Boden ist bei jeder Aktie bekanntlich erst bei Null erreicht.
STML: 20% unter Cash, sagenhafte Ansprechrate, aber Ansprechdauer fraglich und vorerst nur Nischenindikation. Morgen JPM interessant.
KPTI: nur noch 20% über Cash, runter geprügelt wie kaum eine andere Aktie, unzählige Studien, als Mono wohl nur bedingt geeignet, Kombis aber interessant. Wenn's klappt Alleinstellungsmerkmal
ESPR: wenn man twitter und Hammer vertraut, derjenige Wert, der derzeit wohl die größte Fehleinschätzung erfahren soll.
ARRY: Sehr nah am Markt, viele PIII, aber Konkurrenzsituation ungewiß. Management wirkt sehr träge. Für mich nach allem aber der beste Wert von den genannten vier für 2016.
Und dann die weiter bevorstehende Preisdiskussion in Amerika...Nachkaufen und den Helden spielen??
STML: 20% unter Cash, sagenhafte Ansprechrate, aber Ansprechdauer fraglich und vorerst nur Nischenindikation. Morgen JPM interessant.
KPTI: nur noch 20% über Cash, runter geprügelt wie kaum eine andere Aktie, unzählige Studien, als Mono wohl nur bedingt geeignet, Kombis aber interessant. Wenn's klappt Alleinstellungsmerkmal
ESPR: wenn man twitter und Hammer vertraut, derjenige Wert, der derzeit wohl die größte Fehleinschätzung erfahren soll.
ARRY: Sehr nah am Markt, viele PIII, aber Konkurrenzsituation ungewiß. Management wirkt sehr träge. Für mich nach allem aber der beste Wert von den genannten vier für 2016.
Und dann die weiter bevorstehende Preisdiskussion in Amerika...Nachkaufen und den Helden spielen??
XBIT - Innert 6 Tradingtagen den Börsenwert ohne negative News zu halbieren das ist selbst in einem kritschen Markt fast unmöglich... Tja fast... XBIT hat es geschafft.
Zudem auf RSI Level 15 weitere 12% zu verlieren sucht auch seines gleichen...
Zudem auf RSI Level 15 weitere 12% zu verlieren sucht auch seines gleichen...
Sorry nicht XBIT sondern KPTI
FDA cleared 45 new meds in 2015, 2nd highest on record - Jan 12, 2016
- The FDA approved 45 new drugs in 2015, second only to 1996's 53. 16 (36%) were first-in-class treatments and 21 (47%) were for rare diseases.
- Among the new molecular entities cleared last year were Novartis' Cosentyx (secukinumab) for psoriasis, Farydak (panobinostat) for multiple myeloma and Entresto (sacubitril/valsartan) for heart failure, Pfizer's Ibrance (palbociclib) for breast cancer, Sanofi/Regeneron's Praluent and Amgen's Repatha for lowering cholesterol and Eli Lilly's Portrazza (necitumumab) for lung cancer.
- 2016 should be another strong year for drug approvals, stoked by the FDA's accelerated review designations: Fast Track, Breakthrough Therapy and Priority Review.
http://seekingalpha.com/news/3026366-fda-cleared-45-new-meds…
- The FDA approved 45 new drugs in 2015, second only to 1996's 53. 16 (36%) were first-in-class treatments and 21 (47%) were for rare diseases.
- Among the new molecular entities cleared last year were Novartis' Cosentyx (secukinumab) for psoriasis, Farydak (panobinostat) for multiple myeloma and Entresto (sacubitril/valsartan) for heart failure, Pfizer's Ibrance (palbociclib) for breast cancer, Sanofi/Regeneron's Praluent and Amgen's Repatha for lowering cholesterol and Eli Lilly's Portrazza (necitumumab) for lung cancer.
- 2016 should be another strong year for drug approvals, stoked by the FDA's accelerated review designations: Fast Track, Breakthrough Therapy and Priority Review.
http://seekingalpha.com/news/3026366-fda-cleared-45-new-meds…
Antwort auf Beitrag Nr.: 51.484.542 von lawmeetstax am 13.01.16 20:23:58
1. SECOMBIT Studie
Kombinationsansatz MEK/BRAF mit BMY's Immuntherapeutika (a-PD-1, a-CTLA-4). Hier lässt es aufhorchen, dass die beteiligten europäischen Meinungsbildner (z.B Dummer, Zürich, etc) sich für diese durch eine Stiftung gesponsorte Studie für Enco/Bini entschieden haben, obwohl es bereits zugelassene Alternativen gibt. Das lässt die Spekulation zu, dass diese Experten vielleicht schon wissen, dass Bini/Enco Vorteile bei der Verträglichkeit haben, da sie wie z.B. R. Dummer schon an COLUMBUS gearbeitet haben. Verträglichkeit dürfte hier eine große Rolle spielen, da a-CTLA-4 + Vemurafenib kürzlich zu Leberprobleme geführt hatte.
Insgesamt auch ermutigend, da arry damit den Zug der nächsten Kombinationen nicht verpasst.
2. arry 797
Hier gab es tatsächlich erste Daten aus der laufenden Herzschwäche-Studie. Danach sind also Hinweise auf Wirksamkeit gesehen worden. Ausführliche Daten sollen auf einer Konferenz gezeigt werden.
3. Präklinisches Programm für "small molecule"-check point Inhibitoren
Das kam völlig überraschend und wäre eine Pressemitteilung wert gewesen, da sie dafür mit zwei angesehenen Forschungsinstituten zusammenarbeiten.
4. Start Phase III in colon cancer (BRAF) Enco+a-EGFR für 2016 geplant.
A
arry JPM conference
auf der kürzlichen JPM Konferenz gab es einiges Interessantes zu arry:1. SECOMBIT Studie
Kombinationsansatz MEK/BRAF mit BMY's Immuntherapeutika (a-PD-1, a-CTLA-4). Hier lässt es aufhorchen, dass die beteiligten europäischen Meinungsbildner (z.B Dummer, Zürich, etc) sich für diese durch eine Stiftung gesponsorte Studie für Enco/Bini entschieden haben, obwohl es bereits zugelassene Alternativen gibt. Das lässt die Spekulation zu, dass diese Experten vielleicht schon wissen, dass Bini/Enco Vorteile bei der Verträglichkeit haben, da sie wie z.B. R. Dummer schon an COLUMBUS gearbeitet haben. Verträglichkeit dürfte hier eine große Rolle spielen, da a-CTLA-4 + Vemurafenib kürzlich zu Leberprobleme geführt hatte.
Insgesamt auch ermutigend, da arry damit den Zug der nächsten Kombinationen nicht verpasst.
2. arry 797
Hier gab es tatsächlich erste Daten aus der laufenden Herzschwäche-Studie. Danach sind also Hinweise auf Wirksamkeit gesehen worden. Ausführliche Daten sollen auf einer Konferenz gezeigt werden.
3. Präklinisches Programm für "small molecule"-check point Inhibitoren
Das kam völlig überraschend und wäre eine Pressemitteilung wert gewesen, da sie dafür mit zwei angesehenen Forschungsinstituten zusammenarbeiten.
4. Start Phase III in colon cancer (BRAF) Enco+a-EGFR für 2016 geplant.
A
Antwort auf Beitrag Nr.: 51.501.225 von Axel_Olsson am 15.01.16 14:49:47@arry
Deine positive Einschätzung der JPM-Präsentation aufgrund der genannten Punkte teile ich und hatte gestern nochmal um 20% aufgestockt.
Hinsichtlich der neuen Studie SECOMBIT habe ich aber folgenden kritischen Gedanken: Ich hätte mir gewünscht, daß Arry endlich mal eine echte Kombi mit checkpoint inhibitoren anfängt. Nach meiner Lesart geht es bei SECOMBIT nur um die Reihenfolge (erst BINI und ENCO, danach dann checkpoint Inhibitoren, oder genau andersherum, oder im Wechsel...?). Gleichzeitig leider nicht. Daher dauert die Studie auch sehr lang, nämlich noch 4,5 Jahre bis Herbst 2020.
Die neue Forschungskooperation für small molecules im Bereich der Immunonkologie hat mich auch aufhorchen lassen. Interessant! Zur gleichen Thematik hat übrigens die deutsche Evotec vor kurzem mit Sanofi eine Kooperation geschlossen.
Es klingt ein bißchen nach Substanz.
Deine positive Einschätzung der JPM-Präsentation aufgrund der genannten Punkte teile ich und hatte gestern nochmal um 20% aufgestockt.
Hinsichtlich der neuen Studie SECOMBIT habe ich aber folgenden kritischen Gedanken: Ich hätte mir gewünscht, daß Arry endlich mal eine echte Kombi mit checkpoint inhibitoren anfängt. Nach meiner Lesart geht es bei SECOMBIT nur um die Reihenfolge (erst BINI und ENCO, danach dann checkpoint Inhibitoren, oder genau andersherum, oder im Wechsel...?). Gleichzeitig leider nicht. Daher dauert die Studie auch sehr lang, nämlich noch 4,5 Jahre bis Herbst 2020.
Die neue Forschungskooperation für small molecules im Bereich der Immunonkologie hat mich auch aufhorchen lassen. Interessant! Zur gleichen Thematik hat übrigens die deutsche Evotec vor kurzem mit Sanofi eine Kooperation geschlossen.
Es klingt ein bißchen nach Substanz.
Antwort auf Beitrag Nr.: 51.501.828 von lawmeetstax am 15.01.16 15:30:16Link zur JPM16 mit allen Präsentationen in alphabetischer Reihenfolge:
http://jpmorgan.metameetings.com/confbook/healthcare16/ondem…
Kann sich noch Jemand an die Zeit erinnern, als Pharmawerte als krisensichere, konjunkturunabhängige Investements betrachtet wurden? Was genau hat sich eigentlich seit dem geändert?
http://jpmorgan.metameetings.com/confbook/healthcare16/ondem…
Kann sich noch Jemand an die Zeit erinnern, als Pharmawerte als krisensichere, konjunkturunabhängige Investements betrachtet wurden? Was genau hat sich eigentlich seit dem geändert?
Eine schöne und nützliche Übersicht - jetzt mit neuer Funktion:
http://www.biotechduediligence.com/valuation.html
The real-time Biotech Valuation Tracker is consistently one of the most popular features here at BiotechDueDiligence. In response to suggestions from readers, I have added some addition information to the table. First, you will find the 52-week low and high prices for each stock. In addition, I have generated a "SENTIMENT" score for each stock on the list. This column simply provided a percentile score between 0-100%, based on where the current stock price is in comparison to the 52-week low (0%) or 52-week high (100%).
Needless to say, there are a good many single-digit sentiment scores at the moment. In case you are wondering, the highest scores on the list - and still well off their highs - are Galapagos $GLPG and Ligand $LGND (had to edit this post to delete $SRPT from this list).
http://www.biotechduediligence.com/valuation.html
The real-time Biotech Valuation Tracker is consistently one of the most popular features here at BiotechDueDiligence. In response to suggestions from readers, I have added some addition information to the table. First, you will find the 52-week low and high prices for each stock. In addition, I have generated a "SENTIMENT" score for each stock on the list. This column simply provided a percentile score between 0-100%, based on where the current stock price is in comparison to the 52-week low (0%) or 52-week high (100%).
Needless to say, there are a good many single-digit sentiment scores at the moment. In case you are wondering, the highest scores on the list - and still well off their highs - are Galapagos $GLPG and Ligand $LGND (had to edit this post to delete $SRPT from this list).
Antwort auf Beitrag Nr.: 51.334.473 von ipollit am 18.12.15 16:01:13
morphosys
Morphosys gibt es seit weit über 20 Jahren, bisher hat es jedoch kein Wirkstoff in die Zulassung geschafft. Warum ? Gerade weil das Unternehmen vom Kapitalmarkt seit dem IPO so hoch eingeschätzt wird, stelle ich mir die Frage ob deren Wirkstoff-Ansatz nicht grundsätzlich überschätzt wird.
Hammer geht davon aus, dass die Korrektur/der Crash im Biotech-Sektor weitergehen wird:
http://www.orf-blog.com/biotech-selloff-leaves-wall-street-d…
Er findet die Bewertungen noch immer hoch.
"Biotech valuations are still rich and factor-in limited risk (e.g. clinical failures, longer timelines, biosimilars, drug pricing etc.)."
Ich kann dem nicht mehr so wirklich folgen. Ich finde, dass es so einige Unternehmen gibt, die schreiend billig sind. Die Schwergewichte (CELG, ABBV, GILD, BIIB, AMGN usw.) erscheinen mir als mindestens fair bewertet.
Dann gibt es Unternehmen, die zwar relativ hoch bewertet sind, die aber nach langen Jahren der Pipeline-Entwicklung auch relativ kurz vor möglichen Zulassungen stehen. Nehmen wir CLDX als Beispiel. Die sind 1 Milliarde wert. Aber ist das viel, falls Rindopepimut weiterhin gute Daten liefert? Doch eher nicht.
Wie teuer sind ACAD, PTLA, CEMP, RLYP, TSRO und selbst CLVS, die alle vor möglichen Zulassungen innerhalb der nächsten 12 Monate stehen? Ist SAGE wirklich so kacke, wie es der Kurs aussagt? Wirklich?
Oder überschätzen wir einfach überall das kommerzielle Potential ihrer Wirkstoffe? Darüber denke ich wirklich viel nach...
Ich fand die ganze Entwicklung auch seit geraumer Zeit ungesund und mich hat der "Fahnenstangen-Chart" des NBI (der vielleicht gar keiner war) gestört.
So konnte es wirklich nicht weitergehen.
Aber wer jetzt verlangt, dass der NBI den NASDAQ oder den S&P nicht outperformen durfte, trotz der absolut bahnbrechenden Erfolge in der Wirkstoffentwicklung, hat auch so einiges nicht verstanden.
http://www.orf-blog.com/biotech-selloff-leaves-wall-street-d…
Er findet die Bewertungen noch immer hoch.
"Biotech valuations are still rich and factor-in limited risk (e.g. clinical failures, longer timelines, biosimilars, drug pricing etc.)."
Ich kann dem nicht mehr so wirklich folgen. Ich finde, dass es so einige Unternehmen gibt, die schreiend billig sind. Die Schwergewichte (CELG, ABBV, GILD, BIIB, AMGN usw.) erscheinen mir als mindestens fair bewertet.
Dann gibt es Unternehmen, die zwar relativ hoch bewertet sind, die aber nach langen Jahren der Pipeline-Entwicklung auch relativ kurz vor möglichen Zulassungen stehen. Nehmen wir CLDX als Beispiel. Die sind 1 Milliarde wert. Aber ist das viel, falls Rindopepimut weiterhin gute Daten liefert? Doch eher nicht.
Wie teuer sind ACAD, PTLA, CEMP, RLYP, TSRO und selbst CLVS, die alle vor möglichen Zulassungen innerhalb der nächsten 12 Monate stehen? Ist SAGE wirklich so kacke, wie es der Kurs aussagt? Wirklich?
Oder überschätzen wir einfach überall das kommerzielle Potential ihrer Wirkstoffe? Darüber denke ich wirklich viel nach...
Ich fand die ganze Entwicklung auch seit geraumer Zeit ungesund und mich hat der "Fahnenstangen-Chart" des NBI (der vielleicht gar keiner war) gestört.
So konnte es wirklich nicht weitergehen.
Aber wer jetzt verlangt, dass der NBI den NASDAQ oder den S&P nicht outperformen durfte, trotz der absolut bahnbrechenden Erfolge in der Wirkstoffentwicklung, hat auch so einiges nicht verstanden.
Antwort auf Beitrag Nr.: 51.509.088 von kmastra am 16.01.16 15:11:23Recht ruhig geworden hier, wenig überraschend... Ohad's Beurteilung finde ich wohltuend emotionslos und pragmatisch: http://www.orf-blog.com/biotech-selloff-leaves-wall-street-d…
Antwort auf Beitrag Nr.: 51.522.912 von SpanishEyes am 18.01.16 20:58:18Was kann man momentan auch tun?
Ich habe zumindest mal den ein oder anderen Wert verkauft und umgetauscht (langfristig sind viele Werte interessant geworden).
Zudem habe ich mir vom Vater Staat Geld zurück geholt, indem ich Verluste realisiert habe und gleich danach wieder gekauft habe. Das kann sich bei dem ein oder anderem Investment wirklich lohnen. Beispielrechnung ESPR: Wer hierbei bei einem Kurs von 100 EUR gekauft hat, der hat jetzt noch 13 EUR übrig. Die verrechenbaren Kursverluste liegen bei dieser Beispielrechnung bei 21 EUR, also deutlich mehr als der eigentliche Wert der Aktie!
Hier bietet es sich also an, zu verkaufen und dann enstprechend mit dem Geld ESPR zurück zu kaufen. Das zusätzliche Geld könnte man dann z.B. in einen anderen Wert stecken.
Voraussetzung ist natürlich, dass man entsprechende Gewinne vorher realisiert hatte. Auch die "First in first out" Regel muss man bedenken. Ebenso sollte auch klar sein, dass wenn rein theoretisch ESPR dann wieder auf 100 EUR steigt man auch entsprechend wieder Steuer auf die Gewinne zahlen muss...
Ich denke grunsätzlich mittlerweile leider aber auch, dass es noch weiter bergab gehen könnte. (Vielleicht ein gutes Zeichen ) Aber nicht wegen der hohen Bewertungen, sondern weil der Markt das so will. Wenn halt kaum einer kauft werden die Kurse nicht steigen. Und Biotech wird sich nicht vom allgemeinen Marktgeschehen abkoppeln können.
) Aber nicht wegen der hohen Bewertungen, sondern weil der Markt das so will. Wenn halt kaum einer kauft werden die Kurse nicht steigen. Und Biotech wird sich nicht vom allgemeinen Marktgeschehen abkoppeln können.
Die Bewertungen sind doch nun aber wirklich nicht mehr hoch. Wie hoch ist das KGV von GILD? ABBV hat eine Dividendenrendite von über 4% und das als zuverlässiger Dividendenzahler. Kurzum: langfristig sehe ich viele Kurse als extrem attraktiv an aber kurzfristig könnte es durchaus noch weiter bergab gehen... SG kmastra
Ich habe zumindest mal den ein oder anderen Wert verkauft und umgetauscht (langfristig sind viele Werte interessant geworden).
Zudem habe ich mir vom Vater Staat Geld zurück geholt, indem ich Verluste realisiert habe und gleich danach wieder gekauft habe. Das kann sich bei dem ein oder anderem Investment wirklich lohnen. Beispielrechnung ESPR: Wer hierbei bei einem Kurs von 100 EUR gekauft hat, der hat jetzt noch 13 EUR übrig. Die verrechenbaren Kursverluste liegen bei dieser Beispielrechnung bei 21 EUR, also deutlich mehr als der eigentliche Wert der Aktie!

Hier bietet es sich also an, zu verkaufen und dann enstprechend mit dem Geld ESPR zurück zu kaufen. Das zusätzliche Geld könnte man dann z.B. in einen anderen Wert stecken.
Voraussetzung ist natürlich, dass man entsprechende Gewinne vorher realisiert hatte. Auch die "First in first out" Regel muss man bedenken. Ebenso sollte auch klar sein, dass wenn rein theoretisch ESPR dann wieder auf 100 EUR steigt man auch entsprechend wieder Steuer auf die Gewinne zahlen muss...
Ich denke grunsätzlich mittlerweile leider aber auch, dass es noch weiter bergab gehen könnte. (Vielleicht ein gutes Zeichen
 ) Aber nicht wegen der hohen Bewertungen, sondern weil der Markt das so will. Wenn halt kaum einer kauft werden die Kurse nicht steigen. Und Biotech wird sich nicht vom allgemeinen Marktgeschehen abkoppeln können.
) Aber nicht wegen der hohen Bewertungen, sondern weil der Markt das so will. Wenn halt kaum einer kauft werden die Kurse nicht steigen. Und Biotech wird sich nicht vom allgemeinen Marktgeschehen abkoppeln können.Die Bewertungen sind doch nun aber wirklich nicht mehr hoch. Wie hoch ist das KGV von GILD? ABBV hat eine Dividendenrendite von über 4% und das als zuverlässiger Dividendenzahler. Kurzum: langfristig sehe ich viele Kurse als extrem attraktiv an aber kurzfristig könnte es durchaus noch weiter bergab gehen... SG kmastra
Antwort auf Beitrag Nr.: 51.512.514 von SmartCap am 17.01.16 13:37:23naja, es dauert doch wohl auch, bis ein derart junges Unternehmen einen eigenen Wirkstoff entwickelt durch alle Phasen. Inzwischen sind doch einige recht weit, näheres gibt es ja im eigenen Thread.
Kurs ist aber auch inzwischen deutlich unter die Räder gekommen, dass man noch mal auf - heute - unter 42 Euro fällt, hätte vor ein paar Wochen wohl auch keiner gedacht, wo der "Boden" bei 60 lag und die Aktie zwischen 62 und 68 schwankte.
Kurs ist aber auch inzwischen deutlich unter die Räder gekommen, dass man noch mal auf - heute - unter 42 Euro fällt, hätte vor ein paar Wochen wohl auch keiner gedacht, wo der "Boden" bei 60 lag und die Aktie zwischen 62 und 68 schwankte.
Antwort auf Beitrag Nr.: 51.523.245 von kmastra am 18.01.16 21:47:46Ja, sehe ich ähnlich... ich halte den Sektor an sich auch langfristig nach wie vor für attraktiv, schon allein wegen der demographischen Entwicklung und dass z.B. in China auch immer mehr Menschen Zugang zu "innovativer" medizinischer Versorgung erhalten werden bei gleichzeitig ungesünderem/westlichen Lebenswandel usw.
Für mich bin ich jedoch zum Schluss gekommen, dass ich trotz relativ hohem zeitlichen Aufwands verschiedene Biotech Benchmarks nicht schlagen konnte und habe mich daher entschieden das Kapital in BB Biotech umzuschichten und diese Position dauerhaft weiter auszubauen. Mir gefällt deren Ansatz in vielerlei Hinsicht ausgesprochen gut.
Für mich bin ich jedoch zum Schluss gekommen, dass ich trotz relativ hohem zeitlichen Aufwands verschiedene Biotech Benchmarks nicht schlagen konnte und habe mich daher entschieden das Kapital in BB Biotech umzuschichten und diese Position dauerhaft weiter auszubauen. Mir gefällt deren Ansatz in vielerlei Hinsicht ausgesprochen gut.
GILD bei 90 Dollar mit einem KGV von ca. 7.
Schlimm, diese Überbewertung im Biotechbereich...
Ernsthaft gefragt: Wann wird so was wie GILD zum Übernahme- bzw. Fusionsziel?
Schlimm, diese Überbewertung im Biotechbereich...
Ernsthaft gefragt: Wann wird so was wie GILD zum Übernahme- bzw. Fusionsziel?
Antwort auf Beitrag Nr.: 51.523.320 von xylophon am 18.01.16 22:04:13Gründung war 1992, damit ist Morphosys wohl eher ein Dinosaurier
Antwort überzeugt mich nicht
Antwort überzeugt mich nicht
ZFGN
Leider nur das Teelicht neben dem Osterfeuer, aber trotzdem schön - die Aktie steigt um 100%:
http://finance.yahoo.com/news/zafgens-pivotal-phase-3-trial-…
Die Effektivität finde ich sogar besser als erwartet. Ich hatte hier nur noch eine kleine Zockerposition, weil es für mich an der Wirksamkeit nie Zweifel gab. Trotzdem habe ich diese jetzt verkauft, weil B. doch ziemlich angeschlagen scheint. Im besten Fall kann man mit der FDA eine neue PIII vereinbaren, bei der evtl. eine niedrigere Dosis verwendet wird und zudem Medikamente zur Prävention von Blutgerinseln gegeben werden. Insgesamt ist das Marktpotenzial aber viel kleiner als zuvor. Da gibt es jetzt einfach aussichtsreichere Werte recht günstig zu kaufen!
SG kmastra
Leider nur das Teelicht neben dem Osterfeuer, aber trotzdem schön - die Aktie steigt um 100%:
http://finance.yahoo.com/news/zafgens-pivotal-phase-3-trial-…
Die Effektivität finde ich sogar besser als erwartet. Ich hatte hier nur noch eine kleine Zockerposition, weil es für mich an der Wirksamkeit nie Zweifel gab. Trotzdem habe ich diese jetzt verkauft, weil B. doch ziemlich angeschlagen scheint. Im besten Fall kann man mit der FDA eine neue PIII vereinbaren, bei der evtl. eine niedrigere Dosis verwendet wird und zudem Medikamente zur Prävention von Blutgerinseln gegeben werden. Insgesamt ist das Marktpotenzial aber viel kleiner als zuvor. Da gibt es jetzt einfach aussichtsreichere Werte recht günstig zu kaufen!
SG kmastra
was heute los ist, ist dann auch wieder irgendwo krank....
ESPR zur Zeit 27 % im Plus, AGEN sogar 32 %.....
Die Rückschläge der letzten Tage waren ebenso heftig, da ist schon viel Panik auf beiden Seiten.
Wer cool ist und Geld frei hat, für den sind das spannende Tage.
ESPR zur Zeit 27 % im Plus, AGEN sogar 32 %.....
Die Rückschläge der letzten Tage waren ebenso heftig, da ist schon viel Panik auf beiden Seiten.
Wer cool ist und Geld frei hat, für den sind das spannende Tage.
Antwort auf Beitrag Nr.: 51.550.260 von xylophon am 21.01.16 17:34:17Tja die Shortis werden wohl kalte Füße bei verschiedenen Werten bekommen und ich glaube das wir bei verschieden Werten die Tiefstkurse wohl gesehen haben.
Antwort auf Beitrag Nr.: 51.550.587 von schnappi am 21.01.16 18:03:53
leider hast Du Dich da wohl geirrt. Biotech ist Megaout.
Zitat von schnappi: Tja die Shortis werden wohl kalte Füße bei verschiedenen Werten bekommen und ich glaube das wir bei verschieden Werten die Tiefstkurse wohl gesehen haben.
leider hast Du Dich da wohl geirrt. Biotech ist Megaout.
Antwort auf Beitrag Nr.: 51.602.677 von riverstar_de am 28.01.16 16:42:38Ja vielleicht fällt es doch noch etwas aber manches ist schon ziemlich weit unten finde ich.
Megaout glaube ich auch nicht
http://www.investors.com/politics/on-the-right/sally-pipes-d…
Megaout glaube ich auch nicht
http://www.investors.com/politics/on-the-right/sally-pipes-d…
Also, ich bin wirklich kein Charttechniker, aber vielleicht beruhigt sich das Ganze ja im Bereich von 2.600 Indexpunkten?
Oder muss es bis auf 2.200 runter? Das wäre schon noch ein langer Weg nach unten.

Das "Sentiment" ist jedenfalls komplett im Eimer. Der blasenhaften Entwicklung ist mehr als die Spitze abgebrochen worden.
Allerdings sind viele Aktien meiner Meinung nach inzwischen fundamental höchst interessant. Das gilt sowohl für die Schwergewichte, wie auch für die Kleinen und ganz Kleinen.
Viele kleine Biotechs haben ja interessante Projekte in der Pipeline und notieren teilweise in der Nähe des Cash-Wertes oder darunter.
In den nächsten Wochen gibt es ja wieder jede Menge Zahlen - da kann man sich das dann ja mal im Detail anschauen.
Oder muss es bis auf 2.200 runter? Das wäre schon noch ein langer Weg nach unten.
Das "Sentiment" ist jedenfalls komplett im Eimer. Der blasenhaften Entwicklung ist mehr als die Spitze abgebrochen worden.
Allerdings sind viele Aktien meiner Meinung nach inzwischen fundamental höchst interessant. Das gilt sowohl für die Schwergewichte, wie auch für die Kleinen und ganz Kleinen.
Viele kleine Biotechs haben ja interessante Projekte in der Pipeline und notieren teilweise in der Nähe des Cash-Wertes oder darunter.
In den nächsten Wochen gibt es ja wieder jede Menge Zahlen - da kann man sich das dann ja mal im Detail anschauen.
Like big pharma, biotech is toxic:
http://finance.yahoo.com/video/big-pharma-biotech-toxic-trad…
- 35% gesunken seit 52w high
- 21% YTD
- Schlechtester Monat seit März 2001
Wie SLGramann sagt jedoch viele Titel nähe des Cash-Wertes oder darunter = Pipeline kostenlos im Kurs.
Panik und nicht rationals Handeln an der Biotech Front.
http://finance.yahoo.com/video/big-pharma-biotech-toxic-trad…
- 35% gesunken seit 52w high
- 21% YTD
- Schlechtester Monat seit März 2001
Wie SLGramann sagt jedoch viele Titel nähe des Cash-Wertes oder darunter = Pipeline kostenlos im Kurs.
Panik und nicht rationals Handeln an der Biotech Front.
Eine Graphik, die von Dr. DeSantis gepostet wurde und die wohl von Cowan stammt.

Wenn man das mal mit dem Anstieg des NBI seit 2012 vergleicht, dann sieht man schon, dass eine Verdopplung des NBI bis 2016 (also auf ca. 2.600 bis 2.800 Punkte) so ganz grob durch die steigenden Produktumsätze der Unternehmen unterlegt ist.
Das ist auch kein überraschender Befund, wenn man sich die KGVs der Index-Schwergewichte ansieht, die ja nicht absurd hoch, sondern teilweise richtig attraktiv sind.
Nach wie vor steckt viel in den Pipelines und die Umsatz- und Gewinnentwicklung ist überwiegend sehr positiv.
Das alles spricht dafür, dass der Markt aus fundamentalen Aspekten das Schlimmste hinter sich haben könnte.
Natürlich ist das Sentiment komplett im Eimer und der Markt ist immer bereit, auch in der Abwärtsbewegung das Maß zu verlieren, aber: Selbst Öl ist nicht auf Null gefallen, denn irgendwann setzten sich die Fundamentals eben doch durch.

Wenn man das mal mit dem Anstieg des NBI seit 2012 vergleicht, dann sieht man schon, dass eine Verdopplung des NBI bis 2016 (also auf ca. 2.600 bis 2.800 Punkte) so ganz grob durch die steigenden Produktumsätze der Unternehmen unterlegt ist.
Das ist auch kein überraschender Befund, wenn man sich die KGVs der Index-Schwergewichte ansieht, die ja nicht absurd hoch, sondern teilweise richtig attraktiv sind.
Nach wie vor steckt viel in den Pipelines und die Umsatz- und Gewinnentwicklung ist überwiegend sehr positiv.
Das alles spricht dafür, dass der Markt aus fundamentalen Aspekten das Schlimmste hinter sich haben könnte.
Natürlich ist das Sentiment komplett im Eimer und der Markt ist immer bereit, auch in der Abwärtsbewegung das Maß zu verlieren, aber: Selbst Öl ist nicht auf Null gefallen, denn irgendwann setzten sich die Fundamentals eben doch durch.
Antwort auf Beitrag Nr.: 51.620.143 von SLGramann am 31.01.16 10:17:42Auch interessant:
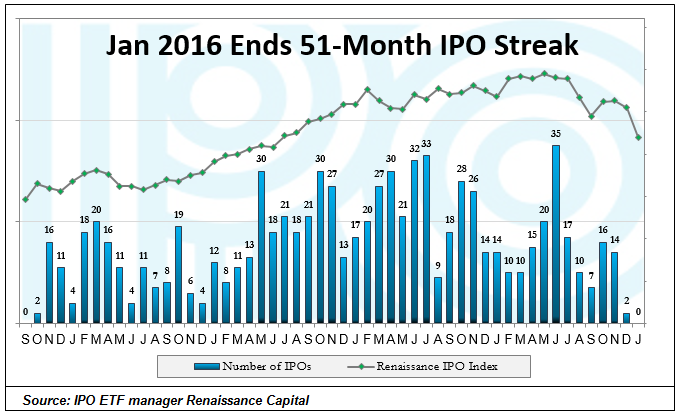
Der IPO-Markt über 4 Jahre.
Im Moment ist er tot. Gut so. Die Hausse stirbt im Überschwang und der Bär stirbt, wenn alle sich nur noch im Elend sielen wollen.
Ein überbordender IPO-Markt ist eigentlich immer ein Signal, dass man in einem Blasenmodus steckt. Ein mausetoter IPO-Markt kann ein Zeichen sein, dass die Verzweiflung auf dem Höhepunkt ist.

Der IPO-Markt über 4 Jahre.
Im Moment ist er tot. Gut so. Die Hausse stirbt im Überschwang und der Bär stirbt, wenn alle sich nur noch im Elend sielen wollen.
Ein überbordender IPO-Markt ist eigentlich immer ein Signal, dass man in einem Blasenmodus steckt. Ein mausetoter IPO-Markt kann ein Zeichen sein, dass die Verzweiflung auf dem Höhepunkt ist.
Antwort auf Beitrag Nr.: 51.621.736 von SLGramann am 31.01.16 16:36:36Wie weit die "Korrektur" schon ging in einem Bild (von Brad Loncar):

Bzgl. Sentiment:
http://boerse.ard.de/anlagestrategie/boersenpsychologie/sag-…
Insgesamt scheint mir der Markt, wie im Artikel beschrieben, von einer großen Angst getrieben, die auch mit einer globalen recht unsicheren Lage (Ölpreis, Eurokrise (war da mal was?), Flüchtlingsproblematik, Russland vs. Türkei, IS,...) zusammenhängen mag. Denn die wirtschaftlichen harten Fakten sind doch eigentlich recht gut, oder?
Bzgl. Biotech exisitiert zudem die Angst vor weiteren negativen Impulsen durch Preisdiskussionen.
Insgesamt glaube ich aber, dass das Chance/Riskoverhältnis bei vielen Biotechs schon jetzt so attraktiv ist wie seit Jahren vielen nicht mehr. Ich bin gespannt, wo die Kurse in einem Jahr stehen. Gier ist ja nicht nur zu unrealistisch hohen Kursen verkaufen zu wollen, sondern auch zu unrealistisch niedrigen Kursen kaufen (bzw. Shortpositionen glatt zu stellen) zu wollen. Kurzfristig mag es noch weiter runtergehen (vor allem wenn mit den Medikamentenpreisen Wahlkampf gemacht wird), aber langfristig finde ich sehr viele Kurse zu billig...

Bzgl. Sentiment:
http://boerse.ard.de/anlagestrategie/boersenpsychologie/sag-…
Insgesamt scheint mir der Markt, wie im Artikel beschrieben, von einer großen Angst getrieben, die auch mit einer globalen recht unsicheren Lage (Ölpreis, Eurokrise (war da mal was?), Flüchtlingsproblematik, Russland vs. Türkei, IS,...) zusammenhängen mag. Denn die wirtschaftlichen harten Fakten sind doch eigentlich recht gut, oder?
Bzgl. Biotech exisitiert zudem die Angst vor weiteren negativen Impulsen durch Preisdiskussionen.
Insgesamt glaube ich aber, dass das Chance/Riskoverhältnis bei vielen Biotechs schon jetzt so attraktiv ist wie seit Jahren vielen nicht mehr. Ich bin gespannt, wo die Kurse in einem Jahr stehen. Gier ist ja nicht nur zu unrealistisch hohen Kursen verkaufen zu wollen, sondern auch zu unrealistisch niedrigen Kursen kaufen (bzw. Shortpositionen glatt zu stellen) zu wollen. Kurzfristig mag es noch weiter runtergehen (vor allem wenn mit den Medikamentenpreisen Wahlkampf gemacht wird), aber langfristig finde ich sehr viele Kurse zu billig...
zu den Preisen gibts nich mal Übernahmen ist wohl zu billig 
ab heute noch mehr ADAP im Depot
@7,50$


vom Boden sprechen wir lieber mal net

ab heute noch mehr ADAP im Depot
@7,50$
vom Boden sprechen wir lieber mal net

Antwort auf Beitrag Nr.: 51.641.620 von schnappi am 02.02.16 21:33:59Zu den Preisen gibts nich mal Übernahmen ist wohl zu billig
Da ist definitiv was dran. Weder Käufer werden sich die "Blöße" eines hohen Aufschlags geben wollen noch werden Verkäufer jetzt zu Preisen verkaufen wollen, die vor Kurzem noch an der Börse gezahlt wurden bzw. sogar darunter lägen.
Momentan sieht man aber viele Übernahmen von Privatfirmen, was wohl auch mit dem schlechteren Zugang zum Kapitalmarkt (IPO oder Kapital) zusammenhängt. Oft mit Aktien bezahlt, was langfristig extrem sinnvoll sein könnte...
Da ist definitiv was dran. Weder Käufer werden sich die "Blöße" eines hohen Aufschlags geben wollen noch werden Verkäufer jetzt zu Preisen verkaufen wollen, die vor Kurzem noch an der Börse gezahlt wurden bzw. sogar darunter lägen.
Momentan sieht man aber viele Übernahmen von Privatfirmen, was wohl auch mit dem schlechteren Zugang zum Kapitalmarkt (IPO oder Kapital) zusammenhängt. Oft mit Aktien bezahlt, was langfristig extrem sinnvoll sein könnte...
Antwort auf Beitrag Nr.: 51.642.010 von kmastra am 02.02.16 22:19:35wenn man sich mal überlegt was Celgene hier Geld rausgehauen hat ob die darüber so Glücklich sind 


Ohad Hammer mit einem sehr schönen Beitrag zu EXEL:
http://www.orf-blog.com/buying-more-exelixis-following-posit…
Er erhöht seine EXEL-Depotposition, sieht aber generell für die Biotechs weiter schwarz.
http://www.orf-blog.com/buying-more-exelixis-following-posit…
Er erhöht seine EXEL-Depotposition, sieht aber generell für die Biotechs weiter schwarz.
Antwort auf Beitrag Nr.: 51.642.316 von schnappi am 02.02.16 22:58:14Die läuft nun paar Tage schon gegen den Trend habe ein paar nachgekauft 


Mal zwei langfristige Charts des NBI.
Hier im 10-Jahreschart sind man gut, wie der NBI Ende 2011 nachhaltig über die 1.000-Punkte-Marke gestiegen ist und einen unglaublichen Anstieg bis auf 4.200 Indexpunkte hingelegt hat:

In diesem ganz langfristigen Chart sieht man auch schön den "Jahr-2000-Crash" als die große Aktienblase platzte:

Damals ist der NBI um gute 70% gefallen. Wollte man das auf heute übertragen, müsste der Index bis auf 1.200 Punkte fallen.
Damit hätte er dann fast seine gesamten Gewinne seit seinem Ausbruch im Jahre 2011 wieder eingebüßt.
Fundamental macht so ein Szenario aber einfach keinen Sinn (anders als in den Jahren 2000 bis 2003).
Allerdings dürften derzeit fundamentale Überlegungen kaum noch eine Rolle spielen. Die Baisse ist in vollem Gange und nährt sich selbst.
Hier im 10-Jahreschart sind man gut, wie der NBI Ende 2011 nachhaltig über die 1.000-Punkte-Marke gestiegen ist und einen unglaublichen Anstieg bis auf 4.200 Indexpunkte hingelegt hat:
In diesem ganz langfristigen Chart sieht man auch schön den "Jahr-2000-Crash" als die große Aktienblase platzte:
Damals ist der NBI um gute 70% gefallen. Wollte man das auf heute übertragen, müsste der Index bis auf 1.200 Punkte fallen.
Damit hätte er dann fast seine gesamten Gewinne seit seinem Ausbruch im Jahre 2011 wieder eingebüßt.
Fundamental macht so ein Szenario aber einfach keinen Sinn (anders als in den Jahren 2000 bis 2003).
Allerdings dürften derzeit fundamentale Überlegungen kaum noch eine Rolle spielen. Die Baisse ist in vollem Gange und nährt sich selbst.
Antwort auf Beitrag Nr.: 51.690.550 von SLGramann am 08.02.16 20:53:04Hallo SLG,
einen ersten Hoffnungsschimmer beim NBI kann man aus GD200 im Wochenchart (rote Linie) ziehen. Man beachte, welche Bedeutung dieser Durchschnitt über den gesamten dargestellten Zeitraum hatte und der zudem beim Absturz 2001 gleich zweimal Startpunkt für einen kräftigen Rebound war.
Prinzipiell stellt sich die Frage, welche Wachstumsrate für den Biotech-Sektor mittel-/langfristig realistisch ist. Dass 40% jährlich nicht haltbar sind, war klar. Aber kann man 16% ansetzen oder eher 6 bis 7% (s. diverse Trendgeraden)? Übrigens sind die beiden gelben Geraden tatsächlich Parallelen - das ist schon krasse Charttechnik!
Hoffen wir also vorerst auf GD200 - eine rote Linie sollte man schließlich nicht so einfach überschreiten!
Schöne Grüße an alle!

einen ersten Hoffnungsschimmer beim NBI kann man aus GD200 im Wochenchart (rote Linie) ziehen. Man beachte, welche Bedeutung dieser Durchschnitt über den gesamten dargestellten Zeitraum hatte und der zudem beim Absturz 2001 gleich zweimal Startpunkt für einen kräftigen Rebound war.
Prinzipiell stellt sich die Frage, welche Wachstumsrate für den Biotech-Sektor mittel-/langfristig realistisch ist. Dass 40% jährlich nicht haltbar sind, war klar. Aber kann man 16% ansetzen oder eher 6 bis 7% (s. diverse Trendgeraden)? Übrigens sind die beiden gelben Geraden tatsächlich Parallelen - das ist schon krasse Charttechnik!
Hoffen wir also vorerst auf GD200 - eine rote Linie sollte man schließlich nicht so einfach überschreiten!

Schöne Grüße an alle!

Antwort auf Beitrag Nr.: 51.700.582 von Saaletaler am 09.02.16 19:03:19Hallo Saaletaler,
welcher Trendkanal nachhaltig sein würde, ist sicher sehr schwer zu beurteilen. Da der Index am Ende doch auch ziemlich an seinen Schwergewichten hängt, würde ich schon sagen, dass ein Wachstum von etwas über 10%/Jahr möglich sein müsste.
In der Zeit zwischen 2010 und sagen wir mal 2020 ist das Umsatz- und Gewinnwachstum der tragenden Unternehmen aber wirklich viel höher als nur 10%/Jahr, so dass der Index eigentlich in jedem Fall einen ziemlichen Anstieg hinlegen musste, um das abzubilden.
Hier noch eine interessante Darstellung:

Dr. Paul DeSantis @DrPaulyDeSantis
$IBB $XBI Multiples for Biotech Revenue are at or Approaching 10 Year Lows
Gruß
SLG
welcher Trendkanal nachhaltig sein würde, ist sicher sehr schwer zu beurteilen. Da der Index am Ende doch auch ziemlich an seinen Schwergewichten hängt, würde ich schon sagen, dass ein Wachstum von etwas über 10%/Jahr möglich sein müsste.
In der Zeit zwischen 2010 und sagen wir mal 2020 ist das Umsatz- und Gewinnwachstum der tragenden Unternehmen aber wirklich viel höher als nur 10%/Jahr, so dass der Index eigentlich in jedem Fall einen ziemlichen Anstieg hinlegen musste, um das abzubilden.
Hier noch eine interessante Darstellung:

Dr. Paul DeSantis @DrPaulyDeSantis
$IBB $XBI Multiples for Biotech Revenue are at or Approaching 10 Year Lows
Gruß
SLG
INCY:
Sind kürzlich stark zurückgekommen. Die Frage ist, ob das allgemein dem Crash geschuldet war oder ob einige wussten/ahnten, dass Jakafi bei soliden Tumoren nun als weitgehend gescheitert angesehen werden muss und zahlreiche laufende Trials beendet werden.
Das war die Meldung von gestern:
Incyte Announces Decision to Discontinue JANUS Studies of Ruxolitinib plus Capecitabine in Patients with Advanced or Metastatic Pancreatic Cancer
http://www.incyte.com/ir/investor-overview/press-releases/
Und hier der Chart:

Es gibt gute Gründe, INCY gerade nach diesem Absturz wieder spannend zu finden:

Jakafi wird auf jeden Fall ein Blockbuster und die Zulassung von Baricitinib ist sehr wahrscheinlich und wird einiges an Royalties abwerfen.
Ich würde sagen, dass der "Rest" der Pipeline nunmehr fast ausgepreist ist und man die "IDO-Plattform" derzeit mehr oder weniger geschenkt bekommt.
Das ist schon recht interessant.
Sind kürzlich stark zurückgekommen. Die Frage ist, ob das allgemein dem Crash geschuldet war oder ob einige wussten/ahnten, dass Jakafi bei soliden Tumoren nun als weitgehend gescheitert angesehen werden muss und zahlreiche laufende Trials beendet werden.
Das war die Meldung von gestern:
Incyte Announces Decision to Discontinue JANUS Studies of Ruxolitinib plus Capecitabine in Patients with Advanced or Metastatic Pancreatic Cancer
http://www.incyte.com/ir/investor-overview/press-releases/
Und hier der Chart:
Es gibt gute Gründe, INCY gerade nach diesem Absturz wieder spannend zu finden:

Jakafi wird auf jeden Fall ein Blockbuster und die Zulassung von Baricitinib ist sehr wahrscheinlich und wird einiges an Royalties abwerfen.
Ich würde sagen, dass der "Rest" der Pipeline nunmehr fast ausgepreist ist und man die "IDO-Plattform" derzeit mehr oder weniger geschenkt bekommt.
Das ist schon recht interessant.
GNCA:
Genocea Biosciences
Ein weiteres Opfer des Biotech-Crashs:

Ohad Hammer hatte sie ins Depot aufgenommen und seitdem hat die Aktie fast 80%(!!) ihres Wertes verloren.
Und das - nebenbei - ohne schlechte Daten. Im Gegenteil.
Jetzt haben sie die Zahlen zum letzten Quartal berichtet, aus denen sich unter anderem folgendes ergibt:
Cash Position: Cash, cash equivalents and investments as of December 31, 2015 were $106.4 compared to $112.5 million as of September 30, 2015.
Diese gut 100 Millionen Cash stehen einer Marktkapitalisierung von ca. 115 Millionen Dollar gegenüber - allerdings steigt die Aktie heute um ca. 25%.
Leicht übertrieben kann man sagen, dass es das Unternehmen derzeit quasi geschenkt gibt.
Noch in diesem Quartal wird es ein Update zu ihrem Hauptprojekt GEN-003 (genital herpes) geben:
Later in the first quarter of 2016, the Company expects to report 12-month durability data from the ongoing Phase 2 dose optimization trial. Positive results, if achieved, would represent an improvement to the already-attractive 6-month durability of effect which was confirmed in the fourth quarter of 2015. This data is also expected to provide guidance on the frequency of administration of maintenance therapy with GEN-003.

Das ist sicher ein high-risk-Investment und man braucht einen langen Atem. Der Preis der Aktie ist dennoch ein Witz imho.
Genocea Biosciences
Ein weiteres Opfer des Biotech-Crashs:
Ohad Hammer hatte sie ins Depot aufgenommen und seitdem hat die Aktie fast 80%(!!) ihres Wertes verloren.
Und das - nebenbei - ohne schlechte Daten. Im Gegenteil.
Jetzt haben sie die Zahlen zum letzten Quartal berichtet, aus denen sich unter anderem folgendes ergibt:
Cash Position: Cash, cash equivalents and investments as of December 31, 2015 were $106.4 compared to $112.5 million as of September 30, 2015.
Diese gut 100 Millionen Cash stehen einer Marktkapitalisierung von ca. 115 Millionen Dollar gegenüber - allerdings steigt die Aktie heute um ca. 25%.
Leicht übertrieben kann man sagen, dass es das Unternehmen derzeit quasi geschenkt gibt.
Noch in diesem Quartal wird es ein Update zu ihrem Hauptprojekt GEN-003 (genital herpes) geben:
Later in the first quarter of 2016, the Company expects to report 12-month durability data from the ongoing Phase 2 dose optimization trial. Positive results, if achieved, would represent an improvement to the already-attractive 6-month durability of effect which was confirmed in the fourth quarter of 2015. This data is also expected to provide guidance on the frequency of administration of maintenance therapy with GEN-003.

Das ist sicher ein high-risk-Investment und man braucht einen langen Atem. Der Preis der Aktie ist dennoch ein Witz imho.
Array ist auch ganz schön zurück gekommen

Antwort auf Beitrag Nr.: 51.740.290 von schnappi am 13.02.16 21:33:48Ja, ARRY ist ziemlich unter die Räder gekommen.
Neben dem sicher letztlich enttäuschenden Deal mit Pierre Fabre zeigt sich nun auch schwarz auf weiß, wie teuer all die Entwicklungsarbeit bei Array ist.
Mich wundert das etwas, weil es immer heißt, dass die laufenden Trials mit Binimetinib und Encorafenib weitgehend noch von Novartis bezahlt werden müssen und mit Fabre kann ja noch nicht viel am laufen sein.
Jedenfalls sind ausweislich der Q10-Files von Array im letzten Quartal 40 Millionen Dollar Cash aus dem Unternehmen abgeflossen.
Das ist eine Hausnummer! Ich bin da schon etwas erschrocken.
Array verfügt zwar gegenwärtig noch über ca. 185 Millionen Cash in der Bilanz und hat Aussicht auf erhebliche Milestones, dennoch ist der Cashburn bedenklich.
Das Jahr 2016 wird jedenfalls entscheidend. Für Binimetinib und Selumetinib kommen die wesentlichen Daten. Im Sommer wird sich klären, welchen Weg Array in Zukunft gehen wird.
Neben dem sicher letztlich enttäuschenden Deal mit Pierre Fabre zeigt sich nun auch schwarz auf weiß, wie teuer all die Entwicklungsarbeit bei Array ist.
Mich wundert das etwas, weil es immer heißt, dass die laufenden Trials mit Binimetinib und Encorafenib weitgehend noch von Novartis bezahlt werden müssen und mit Fabre kann ja noch nicht viel am laufen sein.
Jedenfalls sind ausweislich der Q10-Files von Array im letzten Quartal 40 Millionen Dollar Cash aus dem Unternehmen abgeflossen.
Das ist eine Hausnummer! Ich bin da schon etwas erschrocken.
Array verfügt zwar gegenwärtig noch über ca. 185 Millionen Cash in der Bilanz und hat Aussicht auf erhebliche Milestones, dennoch ist der Cashburn bedenklich.
Das Jahr 2016 wird jedenfalls entscheidend. Für Binimetinib und Selumetinib kommen die wesentlichen Daten. Im Sommer wird sich klären, welchen Weg Array in Zukunft gehen wird.
RLYP:
Hier ist nach wie vor die Frage, wie groß der Markt wirklich ist, wie schnell er sich erschließen lässt und wie man gegen das Konkurrenzprodukt ZS-9 bestehen wird.
Bei Twitter hat jemand eine sehr negative Schätzung künftiger Veltassa-Umsätze gepostet, die von Morgan Stanley kommt:
2016: 9,3 Mio.
2017: 22,2 Mio.
2018: 36 Mio.
Demnach bleibt Veltassa ein Nischenprodukt und hat keine Chance gegen ZS-9. Soweit ich das sehe, ist das aber eine Minderheitenmeinung.
Der Analystenkonsens für die Veltassa-Umsatzentwicklung sieht wohl derzeit so aus:
2016: 33,7 Mio.
2017: 124,2 Mio.
2018: 263 Mio.
Wer hat recht? Oder liegt die Wahrheit in der Mitte? Jedenfalls ist eben die Unsicherheit über das wirkliche künftige Umsatzpotential von Veltassa ziemlich hoch.
Hier ist nach wie vor die Frage, wie groß der Markt wirklich ist, wie schnell er sich erschließen lässt und wie man gegen das Konkurrenzprodukt ZS-9 bestehen wird.
Bei Twitter hat jemand eine sehr negative Schätzung künftiger Veltassa-Umsätze gepostet, die von Morgan Stanley kommt:
2016: 9,3 Mio.
2017: 22,2 Mio.
2018: 36 Mio.
Demnach bleibt Veltassa ein Nischenprodukt und hat keine Chance gegen ZS-9. Soweit ich das sehe, ist das aber eine Minderheitenmeinung.
Der Analystenkonsens für die Veltassa-Umsatzentwicklung sieht wohl derzeit so aus:
2016: 33,7 Mio.
2017: 124,2 Mio.
2018: 263 Mio.
Wer hat recht? Oder liegt die Wahrheit in der Mitte? Jedenfalls ist eben die Unsicherheit über das wirkliche künftige Umsatzpotential von Veltassa ziemlich hoch.
Antwort auf Beitrag Nr.: 51.741.202 von SLGramann am 14.02.16 08:15:26Danke für die Zusammenfassung !
Antwort auf Beitrag Nr.: 51.741.601 von SLGramann am 14.02.16 10:07:43Morgan Stanley scheinen aber die einzigsten zu sein die hier sehr negativ eingestellt sind.
http://ophirgottlieb.tumblr.com/post/139128293489/morgan-sta…
http://ophirgottlieb.tumblr.com/post/139128293489/morgan-sta…
Antwort auf Beitrag Nr.: 51.741.202 von SLGramann am 14.02.16 08:15:26
laut der letzte Telefonkonferenz liegt arry zurzeit bei ca. 18 mio cash burn pro Quartal. Die Zahlen für das letzte Quartal enthielten noch nicht die 30 mio Zahlung von Pierre Fabre. Die kam offenbar erst im Januar. Die Bilanz sieht merkwürdig aus, weil arry die Kosten für laufenden Studien mehr und mehr auslegt und NVS dann die Beträge erstattet. Es bleibt dabei: Bei Bini und Encora zahlt NVS alles. "You have to look into the details to see how positive the terms are." Zitat CEO arry bei der letzten Investorenkonferenz.
VG
A
cash burn arry
Hallo SLGramann,laut der letzte Telefonkonferenz liegt arry zurzeit bei ca. 18 mio cash burn pro Quartal. Die Zahlen für das letzte Quartal enthielten noch nicht die 30 mio Zahlung von Pierre Fabre. Die kam offenbar erst im Januar. Die Bilanz sieht merkwürdig aus, weil arry die Kosten für laufenden Studien mehr und mehr auslegt und NVS dann die Beträge erstattet. Es bleibt dabei: Bei Bini und Encora zahlt NVS alles. "You have to look into the details to see how positive the terms are." Zitat CEO arry bei der letzten Investorenkonferenz.
VG
A
Antwort auf Beitrag Nr.: 51.741.202 von SLGramann am 14.02.16 08:15:26@arry (40 Mil Cashburn)
ich habe das zwar nicht selbst nachgerechnet, aber im cc wurde von einem Cashburn in Q2 (Okt bis Dez) von US$ 22 Mil berichtet, bereinigt um einige Sondereffekte wären es lt Arry US$ 18 Mil gewesen. Entscheidend wird wohl sein, ob Arrays Einschätzung, daß die zukünftig definitiv steigenden Aufwendungen für PIII BRAF Colorectal tatsächlich aufgefangen werden können durch Einsparungen bei nicht fortgeführten Programmen, zutreffend ist. Mir fällt derzeit nur Filanesib ein, vielleicht noch was anderes kleines in der Pipeline, aber ob das reicht...?.
Beruht der Absturz wirklich nur auf der allgemeinen negativen Biotech-Stimmung oder könnte es vielmehr so sein, daß targeted therapy im Markt jetzt schon keine Chance mehr gegenüber Immunoncology eingeräumt wird? Wäre das nicht aber eine sehr einseitige Betrachtung? Immerhin laufen zumindest bei Melanoma mehrere größere Studien, die die Reihenfolge von Checkpoint-Inhibitoren und MEK/BRAF zum Gegenstand haben.
Kurzer Schwenk: NCI-Match Studie
Wenn ich die kürzlichen Verlautbarungen richtig verstanden habe, dann konnte von bisher 700 Teilnehmern nur für 1 Patienten ein Match festgestellt werden. Zwar waren freilich noch nicht alle Patienten ausgewertet und bei einer Vielzahl war eine Analyse aufgrund untauglicher Gewebeentnahmen gar nicht erst möglich und es sind auch noch nicht alle Arme geöffnet, aber trotzdem kann ich diese sehr geringe Zahl nicht ganz glauben. Ich muß etwas übersehen oder falsch verstanden haben...aber was?
ich habe das zwar nicht selbst nachgerechnet, aber im cc wurde von einem Cashburn in Q2 (Okt bis Dez) von US$ 22 Mil berichtet, bereinigt um einige Sondereffekte wären es lt Arry US$ 18 Mil gewesen. Entscheidend wird wohl sein, ob Arrays Einschätzung, daß die zukünftig definitiv steigenden Aufwendungen für PIII BRAF Colorectal tatsächlich aufgefangen werden können durch Einsparungen bei nicht fortgeführten Programmen, zutreffend ist. Mir fällt derzeit nur Filanesib ein, vielleicht noch was anderes kleines in der Pipeline, aber ob das reicht...?.
Beruht der Absturz wirklich nur auf der allgemeinen negativen Biotech-Stimmung oder könnte es vielmehr so sein, daß targeted therapy im Markt jetzt schon keine Chance mehr gegenüber Immunoncology eingeräumt wird? Wäre das nicht aber eine sehr einseitige Betrachtung? Immerhin laufen zumindest bei Melanoma mehrere größere Studien, die die Reihenfolge von Checkpoint-Inhibitoren und MEK/BRAF zum Gegenstand haben.
Kurzer Schwenk: NCI-Match Studie
Wenn ich die kürzlichen Verlautbarungen richtig verstanden habe, dann konnte von bisher 700 Teilnehmern nur für 1 Patienten ein Match festgestellt werden. Zwar waren freilich noch nicht alle Patienten ausgewertet und bei einer Vielzahl war eine Analyse aufgrund untauglicher Gewebeentnahmen gar nicht erst möglich und es sind auch noch nicht alle Arme geöffnet, aber trotzdem kann ich diese sehr geringe Zahl nicht ganz glauben. Ich muß etwas übersehen oder falsch verstanden haben...aber was?
Hallo Axel und law,
Hammer führt den Absturz von Array auch in erster Linie auf die Zweifel am Marktpotenzial beim Melanom zurück und schreibt heute:
"(ARRY) – Yes, I think people are concerned about IO making MEK/BRAF inhibitors irrelevant, at least in melanoma. I still think MEK inhibitors may have a lot of value beyond melanoma including in combination with PD-1 antibodies. ARRY is definitely on my watch list for 2016 after things stabilize."
Ich kann das nicht wirklich beurteilen, die Erfahrung sagt aber, dass bei Krebs meist verschiedene "modes of action" sequentiell oder in Kombination eine Berechtigung haben.
Zum cash-burn:
Array hat zum 30.09.2015 einen operativen cash-Verbrauch in Höhe von 19,2 Millionen für ihr erstes Finanzquartal berichtet (Seite 6 des Q10).
Für die 6 Monate zum 31.12.2015 waren es dann 61,4 Millionen im operativen Bereich.
Das ist natürlich eine vereinfachte Rechnung, weil ich "investing" und "financing" außen vor lasse, aber mir gehts ja um den operativen Teil.
Die 30 Millionen von PF sind im Januar gekommen, das ist richtig:
In December 2015, the Company closed the PF Agreement following approval of the agreement by the European Commission on Competition. In connection with the closing, the Company recorded a $30.0 million receivable from PFM and $30.0 million in deferred revenue related to a nonrefundable,
upfront license payment, which the Company received in January 2016.
Da das für sich eine Einmalzahlung ist, würde ich sie nicht gern gegen den operativen cashflow verrechnen.
Grüße
SLG
Hammer führt den Absturz von Array auch in erster Linie auf die Zweifel am Marktpotenzial beim Melanom zurück und schreibt heute:
"(ARRY) – Yes, I think people are concerned about IO making MEK/BRAF inhibitors irrelevant, at least in melanoma. I still think MEK inhibitors may have a lot of value beyond melanoma including in combination with PD-1 antibodies. ARRY is definitely on my watch list for 2016 after things stabilize."
Ich kann das nicht wirklich beurteilen, die Erfahrung sagt aber, dass bei Krebs meist verschiedene "modes of action" sequentiell oder in Kombination eine Berechtigung haben.
Zum cash-burn:
Array hat zum 30.09.2015 einen operativen cash-Verbrauch in Höhe von 19,2 Millionen für ihr erstes Finanzquartal berichtet (Seite 6 des Q10).
Für die 6 Monate zum 31.12.2015 waren es dann 61,4 Millionen im operativen Bereich.
Das ist natürlich eine vereinfachte Rechnung, weil ich "investing" und "financing" außen vor lasse, aber mir gehts ja um den operativen Teil.
Die 30 Millionen von PF sind im Januar gekommen, das ist richtig:
In December 2015, the Company closed the PF Agreement following approval of the agreement by the European Commission on Competition. In connection with the closing, the Company recorded a $30.0 million receivable from PFM and $30.0 million in deferred revenue related to a nonrefundable,
upfront license payment, which the Company received in January 2016.
Da das für sich eine Einmalzahlung ist, würde ich sie nicht gern gegen den operativen cashflow verrechnen.
Grüße
SLG
Antwort auf Beitrag Nr.: 51.742.942 von SLGramann am 14.02.16 14:59:00Nur kurz, weil es wohl nur wenige interessieren wird:
Der negative operative Cash-Flow in Höhe 61 Mio beruht teilweise darauf, daß die Kostenerstattung von Novartis in Höhe von über 20 Mio bis zum 31. Dezember noch nicht geflossen war (receivables). Da diese Kostenerstattung aber werthaltig ist, sollte sie in den tatsächlichen Cashburn nicht mit einbezogen werden, es handelt sich vielmehr um eine reine Verauslagung von Kosten (Buchung bei Arry: Umsatz und Aufwand).
Die Zahlung von Pierre Fabre wurde bei der Herleitung der Zahlen durch Arry zu Recht nicht bemüht.
Zum Potenzial von MEK/BRAF: Die Novartis-Kombo hat im abgelaufenen Quartal immerhin eine Umsatzsteigerung in Höhe von 40% zum unmittelbaren Vor-Quartal geschafft, nämlich auf US$ 188Mio/Quartal. Und das bei vorerst nur einer Indikation (Melanoma). Mal sehen, ab wann der Einfluß von IO spürbar wird. Hoffentlich finden beide ihren Markt.
Der negative operative Cash-Flow in Höhe 61 Mio beruht teilweise darauf, daß die Kostenerstattung von Novartis in Höhe von über 20 Mio bis zum 31. Dezember noch nicht geflossen war (receivables). Da diese Kostenerstattung aber werthaltig ist, sollte sie in den tatsächlichen Cashburn nicht mit einbezogen werden, es handelt sich vielmehr um eine reine Verauslagung von Kosten (Buchung bei Arry: Umsatz und Aufwand).
Die Zahlung von Pierre Fabre wurde bei der Herleitung der Zahlen durch Arry zu Recht nicht bemüht.
Zum Potenzial von MEK/BRAF: Die Novartis-Kombo hat im abgelaufenen Quartal immerhin eine Umsatzsteigerung in Höhe von 40% zum unmittelbaren Vor-Quartal geschafft, nämlich auf US$ 188Mio/Quartal. Und das bei vorerst nur einer Indikation (Melanoma). Mal sehen, ab wann der Einfluß von IO spürbar wird. Hoffentlich finden beide ihren Markt.
Antwort auf Beitrag Nr.: 51.743.017 von lawmeetstax am 14.02.16 15:24:17"Da diese Kostenerstattung aber werthaltig ist, sollte sie in den tatsächlichen Cashburn nicht mit einbezogen werden,"
Okay, wenn es das war, dann ist es besser, als es auf den ersten Blick aussieht, denn das sehe ich wie Du, dass man ausstehende Erstattungen von Novartis aus dem Cash-burn rausrechnen muss.
In dem Fall müsste sich der cash burn im laufenden Quartal dann relativieren.
Danke für die Aufklärung dieses Punktes!
Okay, wenn es das war, dann ist es besser, als es auf den ersten Blick aussieht, denn das sehe ich wie Du, dass man ausstehende Erstattungen von Novartis aus dem Cash-burn rausrechnen muss.
In dem Fall müsste sich der cash burn im laufenden Quartal dann relativieren.
Danke für die Aufklärung dieses Punktes!
Hallo in die Runde!
ARRY:
Die Bewertung gibt schon einige Rätsel auf. Ich denke, dass viele auch nicht allzuviel von den MEK Ergebnissen erwarten. Leider habe ich bei ARRY schon seit Jahren den Eindruck, dass mit dem über KE reingeholtem Geld keine Werte geschaffen wurden. Beispiele sind die Entwicklung von 614 und vor allem 520, obwohl die vorherigen Ergebnisse alles andere als toll waren. Alles war immer "encouriging" und wurde dann klammheimlich eingestellt...
Auf der positiven Seite bekommt man aber ein sehr breit aufgestelltes Unternehmen für wirklich wenig Geld. Jetzt muss im Sommer aber bei den MEKs auch geliefert werden.
Auf der Leerink Konferenz gab es jetzt meines Wissens erstmals detailliertere Ergebnisse von 797 in LMNA-DCM. Aber da scheint mir der Weg zur Zulassung doch noch recht lang und ungewiss.

Grundsätzlich gibt es aber zur Zeit auch viele chancenreiche Investmentmöglichkeiten.
Auf der Leerink Konferenz waren einige ganz gute Präsentationen: (ARRY, EXEL, ACAD, SAGE, AUPH, ARQL...)
http://wsw.com/webcast/leerink26/
AUPH
Die Ergebnisse von AUPH der Aurion Studie fand ich eigentlich auch ganz gut. Natürlich sollte man das nicht überbewerten aber ich denke man kann es auch nicht ganz ignorieren, zumal es die ersten Ergebnisse in der Indikation sind.


Im Sommer stehen dann die Ergebnisse der PIIb an. Hier ist CR (unter 0,5mg; s. gestrichelte Linie)nach 24 Wochen der primäre Endpunkt. AUPH scheint mir nicht ganz zu Unrecht optimistisch zu sein, dass man hier Erfolg hat. In der PIIb gibt es zudem auch einen Arm mit höherer Dosis als jetzt in der kleinen Studie.
https://www.veracast.com/webcasts/bio/ceoinvestor2016/612255…
https://www.veracast.com/bio/ceoinvestor2016/main/events/225…
SG kmastra
ARRY:
Die Bewertung gibt schon einige Rätsel auf. Ich denke, dass viele auch nicht allzuviel von den MEK Ergebnissen erwarten. Leider habe ich bei ARRY schon seit Jahren den Eindruck, dass mit dem über KE reingeholtem Geld keine Werte geschaffen wurden. Beispiele sind die Entwicklung von 614 und vor allem 520, obwohl die vorherigen Ergebnisse alles andere als toll waren. Alles war immer "encouriging" und wurde dann klammheimlich eingestellt...
Auf der positiven Seite bekommt man aber ein sehr breit aufgestelltes Unternehmen für wirklich wenig Geld. Jetzt muss im Sommer aber bei den MEKs auch geliefert werden.
Auf der Leerink Konferenz gab es jetzt meines Wissens erstmals detailliertere Ergebnisse von 797 in LMNA-DCM. Aber da scheint mir der Weg zur Zulassung doch noch recht lang und ungewiss.
Grundsätzlich gibt es aber zur Zeit auch viele chancenreiche Investmentmöglichkeiten.
Auf der Leerink Konferenz waren einige ganz gute Präsentationen: (ARRY, EXEL, ACAD, SAGE, AUPH, ARQL...)
http://wsw.com/webcast/leerink26/
AUPH
Die Ergebnisse von AUPH der Aurion Studie fand ich eigentlich auch ganz gut. Natürlich sollte man das nicht überbewerten aber ich denke man kann es auch nicht ganz ignorieren, zumal es die ersten Ergebnisse in der Indikation sind.


Im Sommer stehen dann die Ergebnisse der PIIb an. Hier ist CR (unter 0,5mg; s. gestrichelte Linie)nach 24 Wochen der primäre Endpunkt. AUPH scheint mir nicht ganz zu Unrecht optimistisch zu sein, dass man hier Erfolg hat. In der PIIb gibt es zudem auch einen Arm mit höherer Dosis als jetzt in der kleinen Studie.
https://www.veracast.com/webcasts/bio/ceoinvestor2016/612255…
https://www.veracast.com/bio/ceoinvestor2016/main/events/225…
SG kmastra
....erlaube mir mal als neuer Teilnehmer hier das Unternehmen Fate Therapeutics (FATE) einzustellen. Die werden aktuell unter Cash-Niveau gehandelt - haben aber ziemlich gute Technologie im Background, die es derzeit quasi gratis als Zugabe gibt. Cash-Level dürfte bei 2,30-2,50 $ pro Anteil liegen - gehandelt werden die Stücke derzeit in der Gegend um 1,75$. Sprigt der Biosektor wieder an - und das wird er - sollte die Unterbewertung bald Geschichte sein.
Einige Funds haben da zugekauft - FATE hat sich auch zuletzt bei Leerink recht gut präsentiert.
...aber jeder recherchiert und handelt ja für sich selbst.... Bei Interesse versuche ich demnächst mal mehr zum Thema einzustellen...
Einige Funds haben da zugekauft - FATE hat sich auch zuletzt bei Leerink recht gut präsentiert.
...aber jeder recherchiert und handelt ja für sich selbst.... Bei Interesse versuche ich demnächst mal mehr zum Thema einzustellen...
Antwort auf Beitrag Nr.: 51.688.972 von schnappi am 08.02.16 18:47:47Wer kauft denn da fleißig 

News von Celldex zu CDX-301
http://ir.celldex.com/releasedetail.cfm?ReleaseID=955951
Poster
http://celldex.com/docs/ASBMT-2016-Poster-CDX-301.pdf
vielleicht kann ja wer der mediz. Ahnung hat was dazu schreiben Danke!
http://ir.celldex.com/releasedetail.cfm?ReleaseID=955951
Poster
http://celldex.com/docs/ASBMT-2016-Poster-CDX-301.pdf
vielleicht kann ja wer der mediz. Ahnung hat was dazu schreiben Danke!
Momentan muss man sich auch als Biotechinvestor vor allem mit dem Ölpreis rumschlagen! Irgendwie crazy! Tatsächlich habe ich mir aber ein paar Shell B Aktien gekauft, weil ich beruflich viel fahre und so quasi meine momentan erfreulich Tankrechnung über die Dividendenrendite absicher...
Zu Biotech im engeren Sinne:
TRVN
Ohad Hammer hatte vor den tollen IIb Resultaten und er BTD mal was zu TRVN geschrieben :
http://www.orf-blog.com/trevena-late-stage-innovation-flying…
TRVN konnte mit der Nachricht einer BTD vor wenigen Tagen doch ziemlich überraschen. Ich denke das man nach den jüngsten Ereignissen eine BTD auch nicht überbewerten sollte; in dem Fall finde ich die Nachricht aber ganz hervoragend, weil die FDA scheinbar einen Bedarf sieht. TRVN 130 würde im KKH-Setting sehr wahrscheinlich ein Blockbuster werden.
TRVN hat 2 PII Studien abgeschlossen. Die PIII ist schon gestartet und soll ein Filing Ende 2017 ermöglichen. Eine Bewertung von 450 Mio bei Cash von 160 Mio scheint mir günstig, zumal es weitere Projekte gibt.
Die PII Ergebnisse haben gezeigt, dass TRVN im Vergleich zu Morphine schneller wirkt und dabei weniger Nebenwirkungen hat. Ich kann mich z.B. daran erinnern, dass es mir nach meiner letzten OP ziemlich übel ging - gek*%$t hab ich auch!
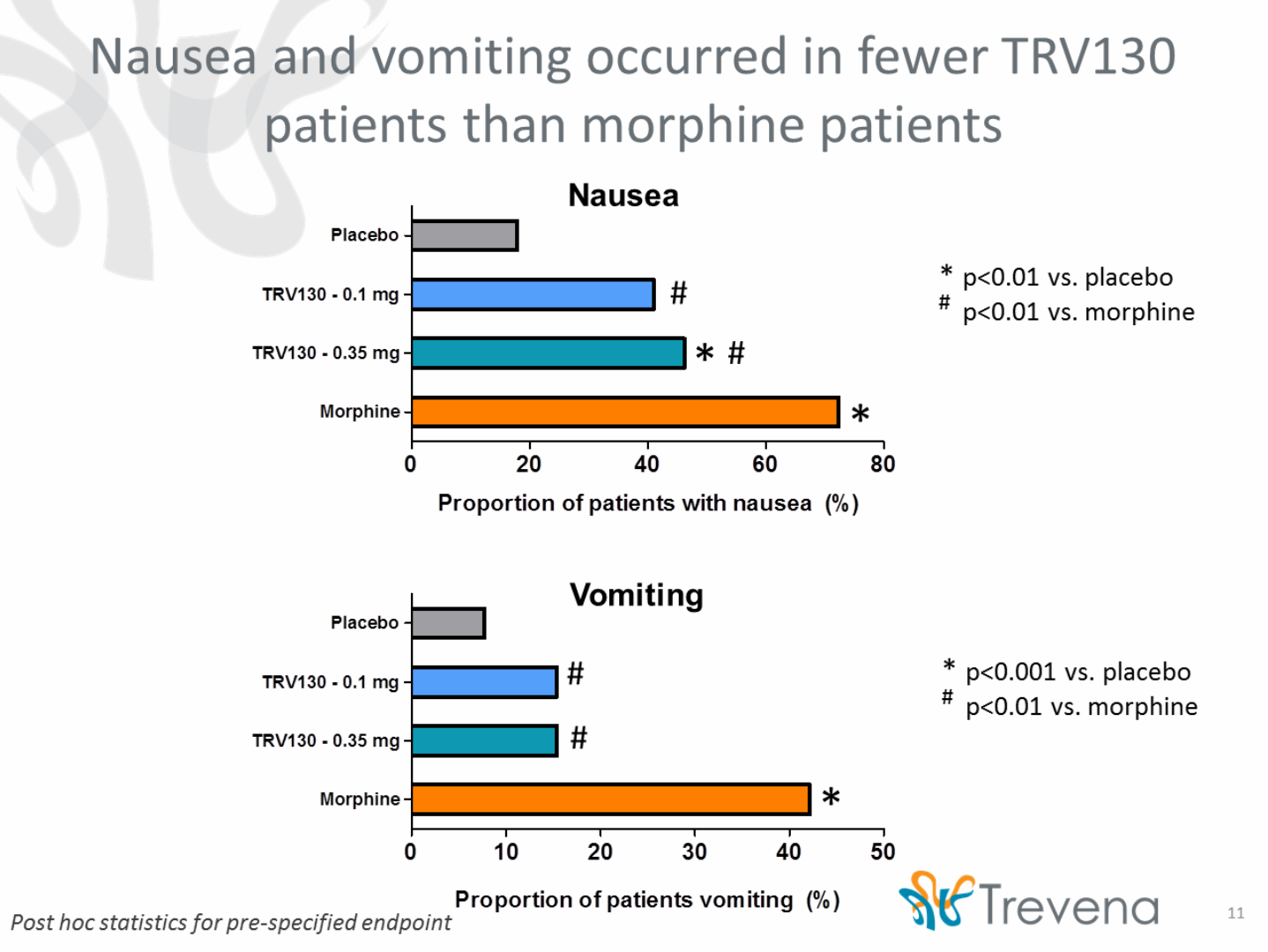
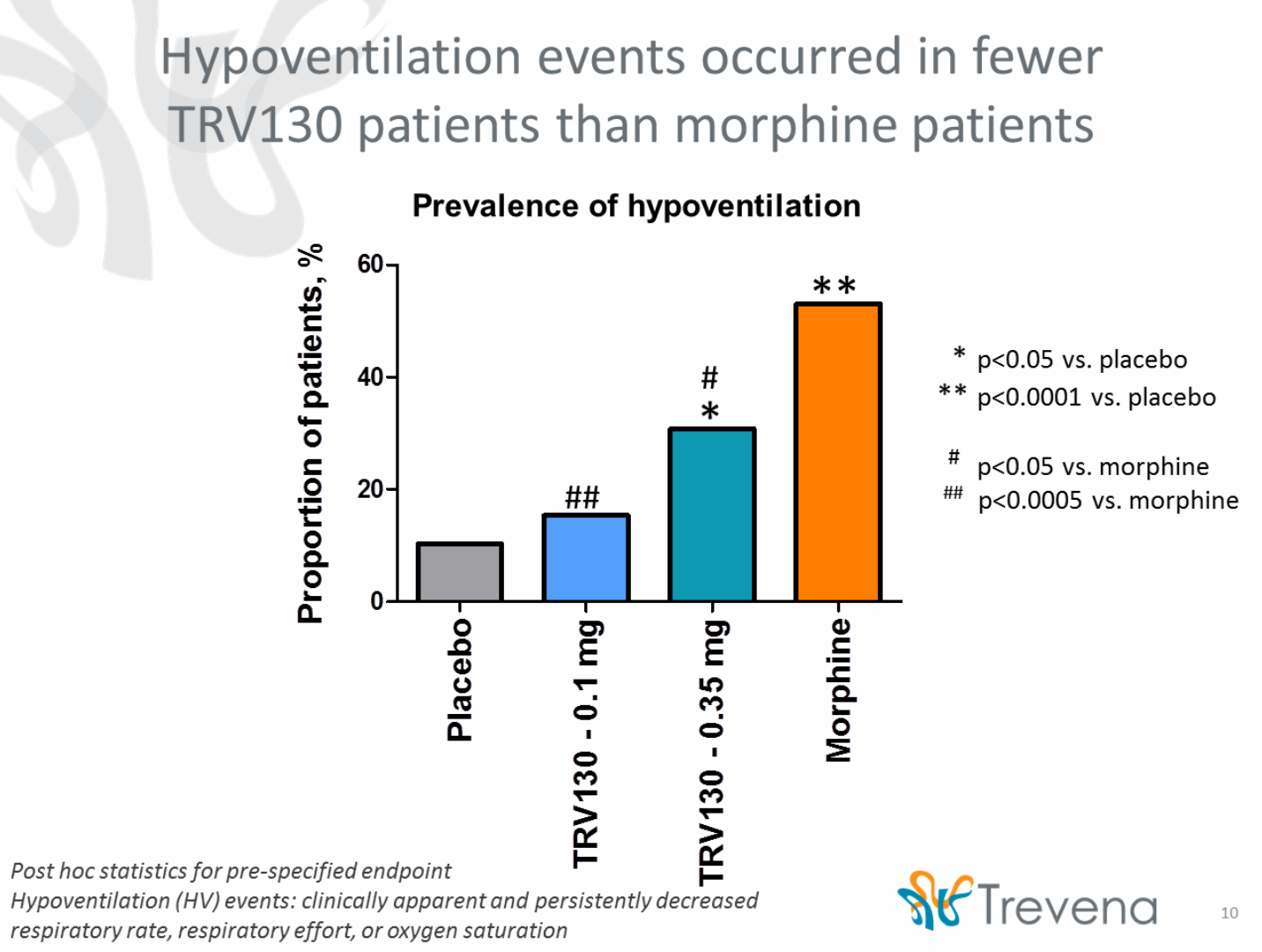
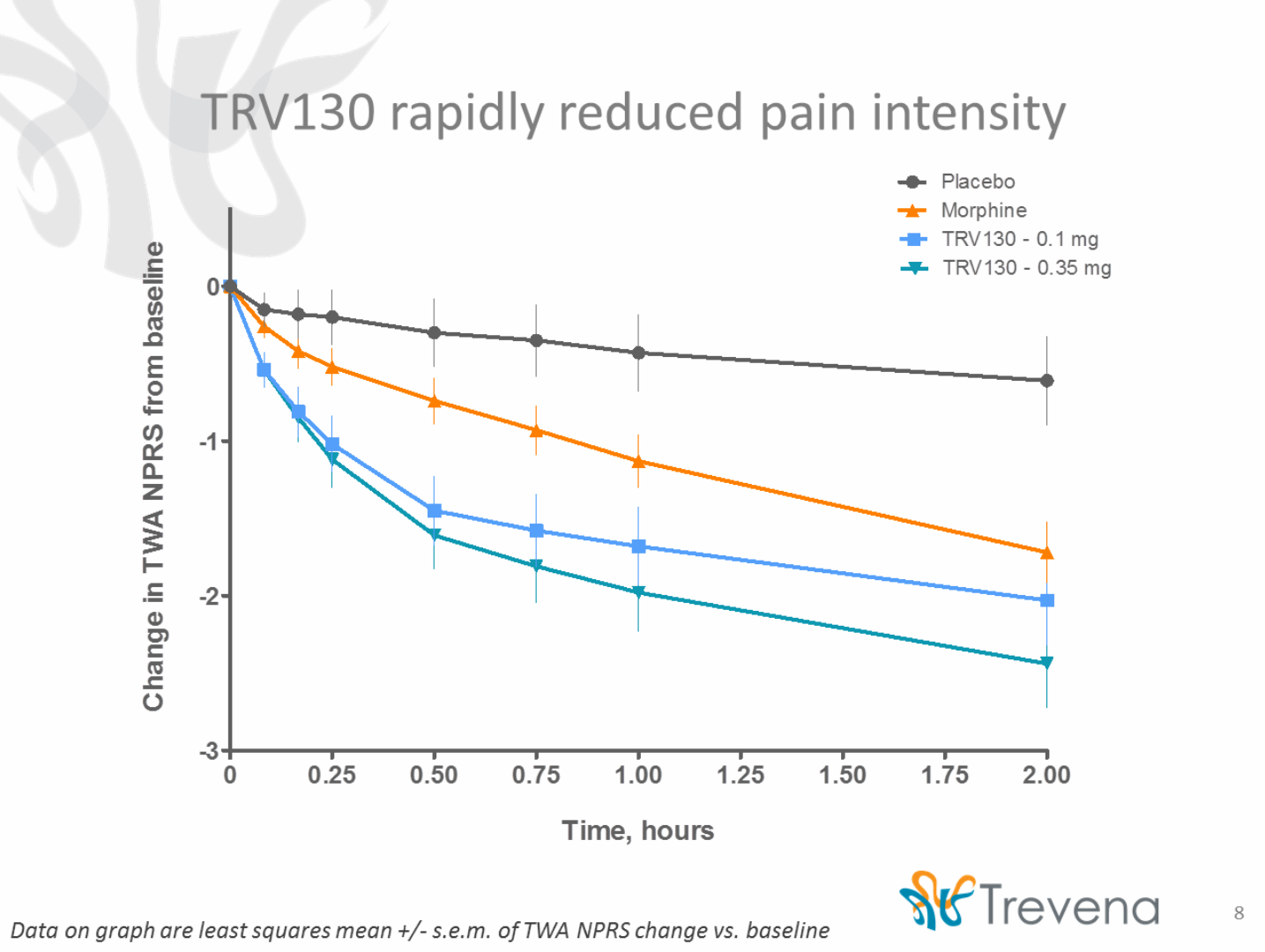
In der PIIa Studie wurden feste Dosen verwand, während sich in der IIb Studie die Patienten über eine Apperatur alle 3 Minuten ggf. selber medikamentieren konnten.
Interessanterweise gab es in der IIa Studie kaum Vorteile im Bereich der Nebenwirkungen. Platt gesagt ging es den Teilnehmern hier genauso übel wie im Morphine Arm.
Wie ist der Unterschied zwischen den Studien zu erklären?
Es wird wohl mit der Verabreichung zu tun haben. Eventuell haben die Patienten bei VTV130 eher ein Gefühl von Kontrolle, da die Schmerzlinderung recht schnell erfolgt. Aufkommender Schmerz kann zügig, per Knopfdruck gelindert werden, während es bei Morphine länger dauert und die Patienten sich präventiv eher zu viel als zu wenig Schmerzmittel verabreichen. Ist aber nur eine Theorie
Zumindest hat es nichts damit zu tun, dass die Patienten im TRV030 Arm eher schlafen. Das habe ich mit der IR geklärt. Die Patienten wurden zur Einschätzung des Schmerzempfindens regelmäßig aufgeweckt!!!

SG kmastra
Zu Biotech im engeren Sinne:
TRVN
Ohad Hammer hatte vor den tollen IIb Resultaten und er BTD mal was zu TRVN geschrieben :
http://www.orf-blog.com/trevena-late-stage-innovation-flying…
TRVN konnte mit der Nachricht einer BTD vor wenigen Tagen doch ziemlich überraschen. Ich denke das man nach den jüngsten Ereignissen eine BTD auch nicht überbewerten sollte; in dem Fall finde ich die Nachricht aber ganz hervoragend, weil die FDA scheinbar einen Bedarf sieht. TRVN 130 würde im KKH-Setting sehr wahrscheinlich ein Blockbuster werden.
TRVN hat 2 PII Studien abgeschlossen. Die PIII ist schon gestartet und soll ein Filing Ende 2017 ermöglichen. Eine Bewertung von 450 Mio bei Cash von 160 Mio scheint mir günstig, zumal es weitere Projekte gibt.
Die PII Ergebnisse haben gezeigt, dass TRVN im Vergleich zu Morphine schneller wirkt und dabei weniger Nebenwirkungen hat. Ich kann mich z.B. daran erinnern, dass es mir nach meiner letzten OP ziemlich übel ging - gek*%$t hab ich auch!



In der PIIa Studie wurden feste Dosen verwand, während sich in der IIb Studie die Patienten über eine Apperatur alle 3 Minuten ggf. selber medikamentieren konnten.
Interessanterweise gab es in der IIa Studie kaum Vorteile im Bereich der Nebenwirkungen. Platt gesagt ging es den Teilnehmern hier genauso übel wie im Morphine Arm.
Wie ist der Unterschied zwischen den Studien zu erklären?
Es wird wohl mit der Verabreichung zu tun haben. Eventuell haben die Patienten bei VTV130 eher ein Gefühl von Kontrolle, da die Schmerzlinderung recht schnell erfolgt. Aufkommender Schmerz kann zügig, per Knopfdruck gelindert werden, während es bei Morphine länger dauert und die Patienten sich präventiv eher zu viel als zu wenig Schmerzmittel verabreichen. Ist aber nur eine Theorie

Zumindest hat es nichts damit zu tun, dass die Patienten im TRV030 Arm eher schlafen. Das habe ich mit der IR geklärt. Die Patienten wurden zur Einschätzung des Schmerzempfindens regelmäßig aufgeweckt!!!
SG kmastra
CLDX:
Das waren die letzten 4 Jahre:

Die zwischenzeitlichen hohen Kursgewinne wurden fast vollständig ausradiert.
Die Frage ist natürlich: zu recht?
Der Cash-Bestand zum 31.12.2015 betrug 290 Mio. USD.
Die gegenwärtige Marktkapitalisierung beläuft sich auf ca. 700 Mio. USD. Ex-Cash ist das Unternehmen heute als gerade mal 400 Mio. USD wert.
Hauptwerttreiber ist und bleibt für mich Ridopepimut.
Hier wird es im März Interim-Daten aus dem ACT IV-Trial geben, die wahrscheinlich den Kurs stark bewegen werden.
Das wahrscheinlichste Ergebnis ist für mich, dass das Data Safety and Monitoring Board (DSMB) eine Fortsetzung des Trials empfehlen wird.
Der Markt würde das wahrscheinlich als negativ interpretieren und den Kurs nochmals deutlich nach unten schicken.
Das wäre für mich aber ein Grund, meine Position, die ich gestern schon zu 6,90 Dollar aufgestockt habe, nochmals deutlich zu vergrößern.
Der Markt wünscht sich vermutlich einen Abbruch des Trials wegen "superiority". Ein dermaßen positives Ergebnis erscheint mit aber relativ unwahrscheinlich.
Geradezu dumm erscheint es mir hingegen, dann im Umkehrschluss eine Fortsetzung des Trials als negativ zu bewerten.
Rindopepimut hat nach allen Daten die wir bisher kennen (ACT II, ACT III, ReACT) einen "long tail"-Effekt, wie er für Immuntherapien geradezu typisch ist.
Die Erwartungshaltung sollte also eher die sein, dass sich nach zwei oder drei Jahren ein Vorteil bei der Gesamtüberlebensrate zeigt.
Beispiel:
Mature OS data continue to show a marked benefit with a long-term survival benefit clearly seen in the RINTEGA arm of the study. At two years, the survival rate is 25% for patients in the RINTEGA arm versus 0% for patients in the control arm.
Einiges zu den bisherigen Daten findet man hier:
http://www.celldex.com/pipeline/rindopepimut.php
Feuerstein hat dazu kürzlich diesen brauchbaren Artikel geschrieben:
http://www.thestreet.com/story/13438923/1/celldex-nears-pivo…
I also spoke with Celldex management this week. Their point -- and it's a good one -- is that longer follow-up is required for some cancer immunotherapies like Rintega to demonstrate a meaningful survival benefit. That's because it takes time for the patient's immune system to mount a response against the cancer. Celldex won't view a decision by data monitors to continue the ACT IV study to be a negative. They believe the final analysis, if the study goes that far, still carries a good shot at a positive outcome.
Do you believe Celldex's argument supports Rintega? You have been bullish on the company and the drug in the past.
Celldex has Rintega data to back up their point. In the "REACT" study involving patients with recurrent GBM, the survival benefit demonstrated by Rintega increased in statistical significance with longer follow-up. Celldex presented that data at two medical meetings last year. The REACT study supports the theory of a "long tail" of survival favoring Rintega.
If the same trend holds up in the ACT IV study, it's entirely possible the final analysis could return with a statistically significant and clinically meaningful survival benefit for Rintega.
usw.
Mein persönliches Szenario ist also, dass ACT IV fortgesetzt werden muss, was der Markt als "fail" ansehen wird.
Ich denke aber dass die Wahrscheinlichkeit nicht so klein ist, dass Rindopepimut am Ende zugelassen werden kann und einen Umsatz von 500 Mio. bis eine Milliarde USD generieren wird.
Im für mich unwahrscheinlichen Fall des vorzeitigen Abbruchs wegen eines frühen signifikanten OS-Vorteils rechne ich mit einem gewaltigen Kurssprung (100%?).
Im ebenfalls nicht sehr wahrscheinlichen Fall eines totalen Scheiterns von ACT IV wird die Aktie natürlich nochmals dramatisch an Wert verlieren.
@schnappi,
zu CDX-301 kann ich nichts konstruktives sagen. Tut mir leid.
ipollit hätte da sicher helfen können, nur ist er leider seit Anfang Januar nicht mehr online.
Hoffentlich hat der Thread nicht seinen besten und kompetentesten Schreiber verloren (ohne jemandem zu nahe treten zu wollen)...
Das waren die letzten 4 Jahre:
Die zwischenzeitlichen hohen Kursgewinne wurden fast vollständig ausradiert.
Die Frage ist natürlich: zu recht?
Der Cash-Bestand zum 31.12.2015 betrug 290 Mio. USD.
Die gegenwärtige Marktkapitalisierung beläuft sich auf ca. 700 Mio. USD. Ex-Cash ist das Unternehmen heute als gerade mal 400 Mio. USD wert.
Hauptwerttreiber ist und bleibt für mich Ridopepimut.
Hier wird es im März Interim-Daten aus dem ACT IV-Trial geben, die wahrscheinlich den Kurs stark bewegen werden.
Das wahrscheinlichste Ergebnis ist für mich, dass das Data Safety and Monitoring Board (DSMB) eine Fortsetzung des Trials empfehlen wird.
Der Markt würde das wahrscheinlich als negativ interpretieren und den Kurs nochmals deutlich nach unten schicken.
Das wäre für mich aber ein Grund, meine Position, die ich gestern schon zu 6,90 Dollar aufgestockt habe, nochmals deutlich zu vergrößern.
Der Markt wünscht sich vermutlich einen Abbruch des Trials wegen "superiority". Ein dermaßen positives Ergebnis erscheint mit aber relativ unwahrscheinlich.
Geradezu dumm erscheint es mir hingegen, dann im Umkehrschluss eine Fortsetzung des Trials als negativ zu bewerten.
Rindopepimut hat nach allen Daten die wir bisher kennen (ACT II, ACT III, ReACT) einen "long tail"-Effekt, wie er für Immuntherapien geradezu typisch ist.
Die Erwartungshaltung sollte also eher die sein, dass sich nach zwei oder drei Jahren ein Vorteil bei der Gesamtüberlebensrate zeigt.
Beispiel:
Mature OS data continue to show a marked benefit with a long-term survival benefit clearly seen in the RINTEGA arm of the study. At two years, the survival rate is 25% for patients in the RINTEGA arm versus 0% for patients in the control arm.
Einiges zu den bisherigen Daten findet man hier:
http://www.celldex.com/pipeline/rindopepimut.php
Feuerstein hat dazu kürzlich diesen brauchbaren Artikel geschrieben:
http://www.thestreet.com/story/13438923/1/celldex-nears-pivo…
I also spoke with Celldex management this week. Their point -- and it's a good one -- is that longer follow-up is required for some cancer immunotherapies like Rintega to demonstrate a meaningful survival benefit. That's because it takes time for the patient's immune system to mount a response against the cancer. Celldex won't view a decision by data monitors to continue the ACT IV study to be a negative. They believe the final analysis, if the study goes that far, still carries a good shot at a positive outcome.
Do you believe Celldex's argument supports Rintega? You have been bullish on the company and the drug in the past.
Celldex has Rintega data to back up their point. In the "REACT" study involving patients with recurrent GBM, the survival benefit demonstrated by Rintega increased in statistical significance with longer follow-up. Celldex presented that data at two medical meetings last year. The REACT study supports the theory of a "long tail" of survival favoring Rintega.
If the same trend holds up in the ACT IV study, it's entirely possible the final analysis could return with a statistically significant and clinically meaningful survival benefit for Rintega.
usw.
Mein persönliches Szenario ist also, dass ACT IV fortgesetzt werden muss, was der Markt als "fail" ansehen wird.
Ich denke aber dass die Wahrscheinlichkeit nicht so klein ist, dass Rindopepimut am Ende zugelassen werden kann und einen Umsatz von 500 Mio. bis eine Milliarde USD generieren wird.
Im für mich unwahrscheinlichen Fall des vorzeitigen Abbruchs wegen eines frühen signifikanten OS-Vorteils rechne ich mit einem gewaltigen Kurssprung (100%?).
Im ebenfalls nicht sehr wahrscheinlichen Fall eines totalen Scheiterns von ACT IV wird die Aktie natürlich nochmals dramatisch an Wert verlieren.
@schnappi,
zu CDX-301 kann ich nichts konstruktives sagen. Tut mir leid.
ipollit hätte da sicher helfen können, nur ist er leider seit Anfang Januar nicht mehr online.
Hoffentlich hat der Thread nicht seinen besten und kompetentesten Schreiber verloren (ohne jemandem zu nahe treten zu wollen)...

Nur mal ne kleine Bemerkung am Rande:
MRNS (Marinus Pharmaceuticals) wird vom Markt nach wie vor absolut gar nichts zugetraut.
Die Marktkapitalisierung liegt bei ca. 80 Mio. Dollar.
Den gegenwärtigen Cashbestand würde ich auf ca. 45 Mio. Dollar schätzen.
Ex-Cash ist das Unternehmen als mit ca. 35 Millionen Dollar bewertet.
Mitte des Jahres werden die P III-Daten von Ganaxolone kommen.
http://ir.marinuspharma.com/releasedetail.cfm?ReleaseID=9472…
Klar können die auch negativ ausfallen und dann ist das Unternehmen eben gar nichts wert.
Es besteht aber eine nicht so kleine Wahrscheinlichkeit eines Erfolges (über die Ähnlichkeiten zu SAGEs Kandidat wurde hier ja schon umfassend geschrieben).
Was macht der Markt denn im Erfolgsfall? Würde auch lustig werden, dass das einzupreisen.
Na ja, warten wirs mal ab.
(SAGE wird sich dieses Jahr ja auch entscheiden)
MRNS (Marinus Pharmaceuticals) wird vom Markt nach wie vor absolut gar nichts zugetraut.
Die Marktkapitalisierung liegt bei ca. 80 Mio. Dollar.
Den gegenwärtigen Cashbestand würde ich auf ca. 45 Mio. Dollar schätzen.
Ex-Cash ist das Unternehmen als mit ca. 35 Millionen Dollar bewertet.
Mitte des Jahres werden die P III-Daten von Ganaxolone kommen.
http://ir.marinuspharma.com/releasedetail.cfm?ReleaseID=9472…
Klar können die auch negativ ausfallen und dann ist das Unternehmen eben gar nichts wert.
Es besteht aber eine nicht so kleine Wahrscheinlichkeit eines Erfolges (über die Ähnlichkeiten zu SAGEs Kandidat wurde hier ja schon umfassend geschrieben).
Was macht der Markt denn im Erfolgsfall? Würde auch lustig werden, dass das einzupreisen.
Na ja, warten wirs mal ab.
(SAGE wird sich dieses Jahr ja auch entscheiden)
Antwort auf Beitrag Nr.: 51.851.800 von SLGramann am 27.02.16 11:21:31Hallo SLGramann,
ich gebe dir in Bezug auf MRNS zu 100% Recht. Mir scheint es fast so, als würde der Markt momentan jegliche Aussicht auf Erfolg auspreisen. Laut Ohad Hammer wäre eine Wiederholung der P2 Ergebnisse ein Erfolg. Ich finde die Grundthese, dass der Markt für Epilepsie groß ist, und die Nebenwirkungen eine wichtige Rolle spielen, einleuchtend.
http://www.orf-blog.com/sage-and-marinus-not-the-typical-cns…
http://www.orf-blog.com/biotech-portfolio-update-sage-marinu…
Ich denke aber, dass MRNS noch mehr zu bieten hat, als nur die PIII in Epilepsie.
Im März kommen auch noch Ergebnisse in Fragil-X Syndrom, wo allerdings gemeinhin ein Misserfolg erwartet und (hoffentlich) eingepreist ist.

Ergänzen würde ich noch, dass MRNS den Vorteil hat, dass SAGE sehr aktiv ist und Erfolge dort auch MRNS beeinflussen sollten. Hier meine ich natürlich vor allem die placebo kontrollierte Studie in Postnataler Depression. Hier hätte MRNS den Vorteil, eine orale Version weit fortgeschritten zu haben. Ein Erfolg von SAGE könnte hier für MRNS die Lage drastisch verändern.


Momentan sieht mein Depot von groß nach klein so aus:
AUPH
ESPR
TRVN
MRNS
GNCA
CLVS
SAGE
ACAD
EXEL
ARQL
XENE
ARRY
ONTY
STML
QURE
SG kmastra
ich gebe dir in Bezug auf MRNS zu 100% Recht. Mir scheint es fast so, als würde der Markt momentan jegliche Aussicht auf Erfolg auspreisen. Laut Ohad Hammer wäre eine Wiederholung der P2 Ergebnisse ein Erfolg. Ich finde die Grundthese, dass der Markt für Epilepsie groß ist, und die Nebenwirkungen eine wichtige Rolle spielen, einleuchtend.
http://www.orf-blog.com/sage-and-marinus-not-the-typical-cns…
http://www.orf-blog.com/biotech-portfolio-update-sage-marinu…
Ich denke aber, dass MRNS noch mehr zu bieten hat, als nur die PIII in Epilepsie.
Im März kommen auch noch Ergebnisse in Fragil-X Syndrom, wo allerdings gemeinhin ein Misserfolg erwartet und (hoffentlich) eingepreist ist.

Ergänzen würde ich noch, dass MRNS den Vorteil hat, dass SAGE sehr aktiv ist und Erfolge dort auch MRNS beeinflussen sollten. Hier meine ich natürlich vor allem die placebo kontrollierte Studie in Postnataler Depression. Hier hätte MRNS den Vorteil, eine orale Version weit fortgeschritten zu haben. Ein Erfolg von SAGE könnte hier für MRNS die Lage drastisch verändern.


Momentan sieht mein Depot von groß nach klein so aus:
AUPH
ESPR
TRVN
MRNS
GNCA
CLVS
SAGE
ACAD
EXEL
ARQL
XENE
ARRY
ONTY
STML
QURE
SG kmastra
Antwort auf Beitrag Nr.: 51.850.888 von SLGramann am 27.02.16 08:25:04Sehr schöner Beitrag und schade das ipollit nicht mehr on ist.
Antwort auf Beitrag Nr.: 51.866.260 von schnappi am 29.02.16 20:21:52In der Tat. Ich denke ipollit hat am meisten Ahnung von allen w:o usern. Das sieht man vor allem daran, dass er die doch recht komplizierten Zusammenhänge so erklären kann, dass selbst ich sie (meist) verstehe!
Grundsätzlich kann ich es aber auch sehr gut verstehen, wenn man sich momentan mit anderen Dingen beschäftigt... macht ja auch heute wieder eher wenig Spaß
Grundsätzlich kann ich es aber auch sehr gut verstehen, wenn man sich momentan mit anderen Dingen beschäftigt... macht ja auch heute wieder eher wenig Spaß

EXEL
Und der Partner ist.... Ipsen!
-200 mio upfront
-bis zu 545 mio milestones
-gestaffelte royalties bis zu 26%
Ohad Hammer hatte folgende Erwartungen:
For a standard ex-US deal (similar to INCY/NVS, SGEN/Takeda), at minimum I would expect a $~150M upfront, $600M in milestones and ~15% royalties on ex-US sales.
Denke das passt! Wäre schön, wenn man näheres zu den Royalties weiß. Ipsen ist vielleicht kein ganz großer Name aber ich denke für Europa gar nicht schlecht...zudem kann Japan auch noch verpartnert werden.
Und der Partner ist.... Ipsen!
-200 mio upfront
-bis zu 545 mio milestones
-gestaffelte royalties bis zu 26%
Ohad Hammer hatte folgende Erwartungen:
For a standard ex-US deal (similar to INCY/NVS, SGEN/Takeda), at minimum I would expect a $~150M upfront, $600M in milestones and ~15% royalties on ex-US sales.
Denke das passt! Wäre schön, wenn man näheres zu den Royalties weiß. Ipsen ist vielleicht kein ganz großer Name aber ich denke für Europa gar nicht schlecht...zudem kann Japan auch noch verpartnert werden.
Antwort auf Beitrag Nr.: 51.867.223 von kmastra am 29.02.16 22:23:22IM CC grad noch einige infos zum Deal mit Ipsen:
Milestones:
60 Mio Meilenstein bei Zulassung EU in RCC
50 Mio Meilenstein insgesamt bei Filing und Zulassung in HCC (PIII Ergebnisse 2017)
zudem bis zu 545 Mio bei Erreichen komerzieller Meilensteine
Bei den Royalties haben sie sich was einfallen lassen:
Zunächst während der ersten Phase der Einführung nur 2-12% Royalties (wenn ich das richtig verstehe gilt das bis 150 Mio umgesetzt wurden)
Danach dann aber 22-26% Royalties!
Interessanter Deal, der mir fair erscheint.
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
Milestones:
60 Mio Meilenstein bei Zulassung EU in RCC
50 Mio Meilenstein insgesamt bei Filing und Zulassung in HCC (PIII Ergebnisse 2017)
zudem bis zu 545 Mio bei Erreichen komerzieller Meilensteine
Bei den Royalties haben sie sich was einfallen lassen:
Zunächst während der ersten Phase der Einführung nur 2-12% Royalties (wenn ich das richtig verstehe gilt das bis 150 Mio umgesetzt wurden)
Danach dann aber 22-26% Royalties!
Interessanter Deal, der mir fair erscheint.
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
arry MEK BRAF vs Immunotherapy
interessantes Interview zur MEK/BRAF/Immuntherapie-Thematik bei Hautkrebs. Danach spricht einiges für first-line mit MEK/BRAF. Weber Compares BRAF/MEK, Immunotherapy Combos in Melanoma Laura Panjwani @OncEditorLaura Published Online: Tuesday, March 1, 2016
Jeffrey S. Weber, MD, PhD
With 2 different BRAF/MEK combination regimens approved by the FDA, as well as an immunotherapy combination, treatment and sequencing decisions for metastatic BRAF-mutated melanoma can be difficult, says Jeffrey S. Weber, MD, PhD, deputy director of the Laura and Isaac Perlmutter Cancer Center, codirector of the Melanoma Program, and head of Experimental Therapeutics at NYU Langone Medical Center.It is still unclear whether BRAF/MEK combinations, such as dabrafenib (Tafinlar) plus trametinib (Mekinist) or vemurafenib (Zelboraf) plus cobimetinib (Cotellic), or immunotherapy combinations, such as the recently approved nivolumab (Opdivo) and ipilimumab (Yervoy) regimen, should be the standard first-line treatment for BRAF-mutated patients, says Weber.“I am not taking bets; there are arguments for both sides,” he explains. “But, I do think all of these combinations are not only going to delay progression with these agents, but we are going to cure some of these patients.“In an interview with OncLive, Weber discusses recent long-term follow-up data of dabrafenib and trametinib that may shed some light on sequencing questions for BRAF-mutated patients. He also discusses an ongoing randomized trial of a head-to-head comparison of BRAF/MEK inhibitors and immunotherapy as first-line treatment. OncLive: How has the role of combination therapies in melanoma evolved in recent years? Weber: There have been 2 combination therapies approved by the FDA recently for melanoma: dabrafenib plus trametinib and vemurafenib plus cobimetinib, which was approved in 2015.Back in 2011, there was a revolution that adding a MEK inhibitor to a BRAF inhibitor in patients with metastatic disease not only augmented the efficacy of the treatment, but also clearly decreased the toxicities, particularly with skin toxicities. Over the next several years, combination MEK plus BRAF therapy has become the standard of care for treating patients with BRAF-mutated melanoma.However, for patients who do not have the BRAF mutation in the tumor, it is inappropriate to use these BRAF drugs. For patients who have the mutation, which occurs in about 40% to 50% of all melanomas, the combination of the BRAF and the MEK drugs can be very effective, with high response rates and long survival. I recently presented data on the long-term follow-up of the original phase II and phase III trials looking at the combination of a MEK inhibitor with a BRAF inhibitor. What were the most significant findings from the long-term follow-up? The follow-up research suggests a couple of things. First, dabrafenib and trametinib have been tested over a longer period of time, so we have longer follow-up. Second, there appears to be a plateau on the curve as you get out in time—in terms of survival follow-up—for dabrafenib and trametinib.The “urban legend” was that the BRAF and MEK inhibitors had a high response rate, but almost all of the patients would progress quickly, progression-free survival would be less than 1 year, and most patients would have to go on another therapy or would die of their disease.That’s not exactly true. There does appear to be a plateau in the curve at about 30% for the patients who receive dabrafenib and trametinib. I am sure it will be virtually identical for vemurafenib and cobimetinib, which have a very similar median survival and 1-year survival track record as dabrafenib and trametinib.We now have mature follow-up data from both dabrafenib and trametinib and vemurafenib and cobimetinib showing that we have about a 25-month median survival in patients treated upfront with metastatic melanoma that is BRAF-mutated who receive these drugs. That is very impressive.The interesting data from the longer follow-up of dabrafenib and trametinib showed that there is an obvious association between having a high tumor burden, poor performance status, a high LDH, and not doing well with these drugs.This means that patients who do best with the combination of BRAF/MEK inhibitors have low disease burden with a normal LDH, few symptoms, etc.This is very interesting, and not exactly like what we have seen with combination immunotherapies. With the combination of ipilimumab and nivolumab, there was not a strong association between LDH—which is a surrogate for tumor burden—and outcome. Patients did very well whether they had a high tumor burden or not. With targeted therapy, that is not the case. Do these findings make it any easier for oncologists to determine frontline treatment for BRAF-mutated patients with melanoma? These findings suggest that oncologists probably want to intervene with BRAF and MEK drugs earlier rather than later.
If the BRAF and MEK drugs only work in patients with low disease burden, but the immunotherapy drugs can work with either a low or high disease burden, the argument would be in a mutated patient to first give BRAF/MEK and then immunotherapy if the patient progressed or failed.The targeted therapy will not work as well if patients are receiving immunotherapy first, then they progress, have high LDH, and high disease burden. The association of patients doing well with targeted therapy with low disease burden bodes well for starting with targeted therapy and using immunotherapy in the second-line setting.This goes against the current “urban legend” that patients should have immunotherapy upfront whether they are BRAF-mutated or BRAF wild-type because those are the patients who are going to get the long tail on the curve in terms of survival. That may not be true. Are there trials exploring sequencing of targeted therapies and immunotherapy agents for BRAF-mutated patients? There is an ongoing randomized phase III trial examining this. One group of patients will get upfront immunotherapy with ipilimumab and nivolumab, and at progression, they will receive BRAF/MEK inhibitors. Other patients in the study will receive upfront dabrafenib and trametinib, and then ipilimumab and nivolumab at progression.The endpoint there is either second-progression or survival; that is going to take a long time. They are both very effective regimens. Each one of them has at least a 2-year median survival and over a 50% response rate. The implication here is we are going to have to wait a long time to see a difference.
http://global.onclive.com/web-exclusives/weber-compares-braf…
@arry
Axel_Olsson hatte ja schon gestern sehr Interessantes von onclive.com hier eingestellt. Hier ergänzend dazu noch etwas:
http://global.onclive.com/web-exclusives/beyond-braf-emergin…
Kurz gesagt geht es um Therapiemöglichkeiten für BRAF negative. Es wird im Interview immer wieder auf MEK-Inhibitoren abgestellt (deckt sich im Groben mit der Erwartung von Ohad Hammer, nach dessen Ansicht MEK-Inhibitoren in Zukunft einen großen Anwendungsbereich haben sollen). Die NEMO-Studie wird ausdrücklich erwähnt verbunden mit der Erwartung, daß MEK-Inhibitoren voraussichtlich nun SOC bei NRAS-Melanoma werden. Da wäre BINI dann natürlich vorne weg.
Insgesamt für Arry-Interessierte lesenswert, zumal Luke zumindest für mich bisher mehr ein Anhänger von Immuntherapien ist. Mithin ein weiteres Argument für ein Nebeneinander.
Axel_Olsson hatte ja schon gestern sehr Interessantes von onclive.com hier eingestellt. Hier ergänzend dazu noch etwas:
http://global.onclive.com/web-exclusives/beyond-braf-emergin…
Kurz gesagt geht es um Therapiemöglichkeiten für BRAF negative. Es wird im Interview immer wieder auf MEK-Inhibitoren abgestellt (deckt sich im Groben mit der Erwartung von Ohad Hammer, nach dessen Ansicht MEK-Inhibitoren in Zukunft einen großen Anwendungsbereich haben sollen). Die NEMO-Studie wird ausdrücklich erwähnt verbunden mit der Erwartung, daß MEK-Inhibitoren voraussichtlich nun SOC bei NRAS-Melanoma werden. Da wäre BINI dann natürlich vorne weg.
Insgesamt für Arry-Interessierte lesenswert, zumal Luke zumindest für mich bisher mehr ein Anhänger von Immuntherapien ist. Mithin ein weiteres Argument für ein Nebeneinander.
Antwort auf Beitrag Nr.: 51.866.500 von kmastra am 29.02.16 20:46:16
Aber die Tage schaut es wieder deutlich besser aus in meinem Depot
Zitat von kmastra: ... macht ja auch heute wieder eher wenig Spaß
Aber die Tage schaut es wieder deutlich besser aus in meinem Depot

Antwort auf Beitrag Nr.: 51.688.972 von schnappi am 08.02.16 18:47:47Mal Gewinne mitgenommen und in QURE nachgelegt.
Ach ja, die Lügenpresse.
Es ist schon witzig: Die Pharmaindustrie ist immer scheiße - egal, was sie tut oder lässt.
Meist sind sich unsere komplett inkompetenten - aber dafür rotzfrechen - Journalisten ja darin einig, dass die Pharmaindustrie eh nur Müll produziert, der die Leute erst recht krank macht und dass man besser auf Bachblüten, Homöopathie oder am allerbesten auf irgend ein obskures "fernöstliches Weisheitswissen" setzen solle.
Normalerweise wird Regulierung und Überwachung der Industrie als viel zu lasch angeprangert. Die Studien mit ihren paar Teilnehmern seien viel zu klein und daher nicht repräsentativ. Die Studiendauer sei immer viel zu kurz, so dass man Langzeitfolgen eh nicht überschauen könne usw. usf.
Jetzt genau umgekehrt:
http://www.sueddeutsche.de/gesundheit/medikamente-darf-eine-…
Hier wird von der schwachsinnigen Journalistin Berndt die Tatsache, dass man ein (noch?) nicht zugelassenes Medikament (noch) nicht in den Vertrieb gibt, zu unterlassenen Hilfeleistung umgedeutet.
Aha.
Gegen die Studie von Biomarin mit BMN 190 lassen sich mit gewissem Recht alle Kritikpunkte auffahren, die sonst gegen Biotech/Pharma gerne ins Feld geführt werden. Die Studie war klein, kurz, hatte keinen (Placebo)Kontrollarm und hat keinen zweiten Trial, der einer Bestätigung oder Falsifikation des Ergebnisses dienen könnte.
Aber in diesem Fall besteht ja die Unverschämtheit und Kriminalität des Entwicklers mal darin, das Produkt bei den Behörden zur Genehmigung einzureichen.
Man "argumentiert" halt, wie man es gerade braucht, um sein vorgefertigtes Feindbild zu bedienen.
Ich wünsche Frau Berndt jedenfalls alles Schlechte.
Hier mal ein Artikel, der sich auf angemessene Weise mit BMN-190 beschäftigt:
http://alanhobbes.blogspot.de/2016/03/biomarin-pharmaceutica…
BMRN ist aus meiner Sicht übrigens ein Kauf, wenn man an einen Erfolg auch bei Pegvaliase glaubt (entscheidet sich wohl noch in diesem Monat).
Auch andere Programme wie BMN-270 und BMN-701 sind sehr spannend.
BMRN gilt nicht umsonst als ein möglicher Übernahmekandidat.
Ich habe eine kleine Position über einen CFD im Depot.
Es ist schon witzig: Die Pharmaindustrie ist immer scheiße - egal, was sie tut oder lässt.
Meist sind sich unsere komplett inkompetenten - aber dafür rotzfrechen - Journalisten ja darin einig, dass die Pharmaindustrie eh nur Müll produziert, der die Leute erst recht krank macht und dass man besser auf Bachblüten, Homöopathie oder am allerbesten auf irgend ein obskures "fernöstliches Weisheitswissen" setzen solle.
Normalerweise wird Regulierung und Überwachung der Industrie als viel zu lasch angeprangert. Die Studien mit ihren paar Teilnehmern seien viel zu klein und daher nicht repräsentativ. Die Studiendauer sei immer viel zu kurz, so dass man Langzeitfolgen eh nicht überschauen könne usw. usf.
Jetzt genau umgekehrt:
http://www.sueddeutsche.de/gesundheit/medikamente-darf-eine-…
Hier wird von der schwachsinnigen Journalistin Berndt die Tatsache, dass man ein (noch?) nicht zugelassenes Medikament (noch) nicht in den Vertrieb gibt, zu unterlassenen Hilfeleistung umgedeutet.
Aha.
Gegen die Studie von Biomarin mit BMN 190 lassen sich mit gewissem Recht alle Kritikpunkte auffahren, die sonst gegen Biotech/Pharma gerne ins Feld geführt werden. Die Studie war klein, kurz, hatte keinen (Placebo)Kontrollarm und hat keinen zweiten Trial, der einer Bestätigung oder Falsifikation des Ergebnisses dienen könnte.
Aber in diesem Fall besteht ja die Unverschämtheit und Kriminalität des Entwicklers mal darin, das Produkt bei den Behörden zur Genehmigung einzureichen.
Man "argumentiert" halt, wie man es gerade braucht, um sein vorgefertigtes Feindbild zu bedienen.
Ich wünsche Frau Berndt jedenfalls alles Schlechte.
Hier mal ein Artikel, der sich auf angemessene Weise mit BMN-190 beschäftigt:
http://alanhobbes.blogspot.de/2016/03/biomarin-pharmaceutica…
BMRN ist aus meiner Sicht übrigens ein Kauf, wenn man an einen Erfolg auch bei Pegvaliase glaubt (entscheidet sich wohl noch in diesem Monat).
Auch andere Programme wie BMN-270 und BMN-701 sind sehr spannend.
BMRN gilt nicht umsonst als ein möglicher Übernahmekandidat.
Ich habe eine kleine Position über einen CFD im Depot.
stimmt, der Artikel ist wirklich abgrundtief schlecht. Ich will die Kritik an der Presse aber nicht vertiefen, weil es sonst vom Thema wegführen würde. Dass ein Lernprozess einsetzt, sieht man aber an einem längeren Artikel, den Giovanni di Lorenzo diese Wochen im Berliner Tagesspiegel veröffentlicht hat über den Vertrauensverlust.
Seriöse Berichterstattung ergreift nicht Partei, wenn man allein diese kleine Grundtugend mal beherzigen würde.
Der Artikel klingt allerdings, als wäre die Firma wirklich ganz interessant mit so einem tollen Medikament (auch wenn die Krankheit selten ist). Wie ernst man die Infos von so einer Person nehmen kann, weiß ich aber natürlich nicht, daher danke für den weiterführenden Link.
Seriöse Berichterstattung ergreift nicht Partei, wenn man allein diese kleine Grundtugend mal beherzigen würde.
Der Artikel klingt allerdings, als wäre die Firma wirklich ganz interessant mit so einem tollen Medikament (auch wenn die Krankheit selten ist). Wie ernst man die Infos von so einer Person nehmen kann, weiß ich aber natürlich nicht, daher danke für den weiterführenden Link.
Antwort auf Beitrag Nr.: 51.909.837 von xylophon am 05.03.16 10:42:45"danke für den weiterführenden Link."
Feuerstein hat die positiven Ergebnisse des Trials ebenfalls aufgegriffen:
http://www.thestreet.com/story/13481136/1/biomarin-drug-prov…
Warum mich der Artikel in der Süddeutschen so in Wut versetzt, ist nicht nur durch Inkompetenz der Autorin begründet. Mich kotzt die ganze Herangehensweise an.
Es wäre nämlich mal angezeigt gewesen, positiv hervorzuheben, dass hier der Wirkstoffentwicklung überhaupt ein kleiner Erfolg gelungen zu sein scheint.
Statt dessen wird auf die Leute, die BMN 190 entwickelt haben, auch noch sinnfrei eingeschlagen.
Übrigens ist Biomarin mit einem anderen Kandidaten für kürzlich in der Zulassung gescheitert und zwar mit Drisapersen bei DMD (Duchenne-Muskeldystrophie).
DMD ist ebenfalls ein sehr seltene und katastrophale Erkrankung bei kleinen Kindern, die diese irgendwann in den Rollstuhl zwingt und meist im jungen Erwachsenenalter tötet:
https://de.wikipedia.org/wiki/Muskeldystrophie_Duchenne
Die Abweisung der Zulassung durch die FDA war sicher berechtigt, auch wenn Drisapersen in Einzelfällen eine gewisse Symptomverbesserung gezeigt haben soll.
Insgesamt war aber das Wirkungs-/Nebenwirkunsprofil einfach mies.
http://www.medscape.com/viewarticle/857406
Nach der Logik dieser Journalistin hätte Biomarin aber wohl auch Drisapersen einfach schon mal ohne Zulassung an die Patienten verteilen sollen...
Oder hätte sie dann geschrieben: "Pharma-Mafia vergiftet aus Profitgier todkranke Kinder mit nicht zugelassenem Wirkstoff!"?
Übrigens gibt es Analysten, die an einer Zulassung von BMN 190 zweifeln, weil eben der Kontrollarm fehlt:
"Coming just after the FDA's resounding rejection of drisapersen, though, BioMarin is facing some skepticism over whether it has the data needed for an approval. Barclays' Geoff Meacham says that the 36-week abstract that BioMarin posted yesterday was "encouraging" but possibly insufficient to warrant an OK at this point.
"While a stat. sig p-value, we question if these data will be sufficient for regulatory approval--especially in light of recent setbacks in DMD (Kyndrisa, eteplirsen, and atalauren)," Meacham noted. "We believe that FDA could require some sort of a placebo-controlled trial to approve cerliponase alfa."
Safety data will also be carefully scrutinized."
http://www.fiercebiotech.com/story/still-licking-duchenne-wo…
(Ich bin da aber einigermaßen optimistisch, es gibt hier schon Unterschiede zum Fall Drisapersen).
Feuerstein hat die positiven Ergebnisse des Trials ebenfalls aufgegriffen:
http://www.thestreet.com/story/13481136/1/biomarin-drug-prov…
Warum mich der Artikel in der Süddeutschen so in Wut versetzt, ist nicht nur durch Inkompetenz der Autorin begründet. Mich kotzt die ganze Herangehensweise an.
Es wäre nämlich mal angezeigt gewesen, positiv hervorzuheben, dass hier der Wirkstoffentwicklung überhaupt ein kleiner Erfolg gelungen zu sein scheint.
Statt dessen wird auf die Leute, die BMN 190 entwickelt haben, auch noch sinnfrei eingeschlagen.
Übrigens ist Biomarin mit einem anderen Kandidaten für kürzlich in der Zulassung gescheitert und zwar mit Drisapersen bei DMD (Duchenne-Muskeldystrophie).
DMD ist ebenfalls ein sehr seltene und katastrophale Erkrankung bei kleinen Kindern, die diese irgendwann in den Rollstuhl zwingt und meist im jungen Erwachsenenalter tötet:
https://de.wikipedia.org/wiki/Muskeldystrophie_Duchenne
Die Abweisung der Zulassung durch die FDA war sicher berechtigt, auch wenn Drisapersen in Einzelfällen eine gewisse Symptomverbesserung gezeigt haben soll.
Insgesamt war aber das Wirkungs-/Nebenwirkunsprofil einfach mies.
http://www.medscape.com/viewarticle/857406
Nach der Logik dieser Journalistin hätte Biomarin aber wohl auch Drisapersen einfach schon mal ohne Zulassung an die Patienten verteilen sollen...
Oder hätte sie dann geschrieben: "Pharma-Mafia vergiftet aus Profitgier todkranke Kinder mit nicht zugelassenem Wirkstoff!"?
Übrigens gibt es Analysten, die an einer Zulassung von BMN 190 zweifeln, weil eben der Kontrollarm fehlt:
"Coming just after the FDA's resounding rejection of drisapersen, though, BioMarin is facing some skepticism over whether it has the data needed for an approval. Barclays' Geoff Meacham says that the 36-week abstract that BioMarin posted yesterday was "encouraging" but possibly insufficient to warrant an OK at this point.
"While a stat. sig p-value, we question if these data will be sufficient for regulatory approval--especially in light of recent setbacks in DMD (Kyndrisa, eteplirsen, and atalauren)," Meacham noted. "We believe that FDA could require some sort of a placebo-controlled trial to approve cerliponase alfa."
Safety data will also be carefully scrutinized."
http://www.fiercebiotech.com/story/still-licking-duchenne-wo…
(Ich bin da aber einigermaßen optimistisch, es gibt hier schon Unterschiede zum Fall Drisapersen).
Antwort auf Beitrag Nr.: 51.867.223 von kmastra am 29.02.16 22:23:22"EXEL
Und der Partner ist.... Ipsen!"
Hallo kmastra,
im ersten Moment war ich enttäuscht. Ich habe gefragt: Ipsen wer? Ipsen was?
Aber inzwischen sehe ich den Deal absolut positiv.
Die upfront-Zahlung dürfte den Kapitalbedarf von EXEL für dieses Jahr weitgehend decken. Das ist ein sehr wichtiger Punkt.
Läuft alles wie erwartet/erhofft, wird EXEL nächstes Jahr bereits signifikante Umsätze erzielen, so dass die Notwendigkeit neues Kapital aufzutreiben, deutlich weniger drängend werden wird.
Ipsen scheint mir ansonsten auch ein vernünftig geführtes und fokussiertes Unternehmen zu sein.
Hier ihre Präsentation zum Geschäftsjahr 2015 (pdf), in der auch der Deal mit EXEL dargestellt wird:
https://www.ipsen.com/wp-content/uploads/2016/03/01-03-2016-…
Im Hammer-Blog hat jemand zu recht darauf hingewiesen, dass Cabo für Ipsen ein ganz wichtiger Teil ihres Portfolios sein wird und die deswegen dem Vertrieb in Europa die maximale Aufmerksamkeit widmen werden.
Gute OS-Daten vorausgesetzt, wird die Nachfrage nach Cabo als Drittlinientherapie hoch sein (auch ohne Sales-Force-Terror) und Ipsen ist groß genug, das dann organisatorisch zu beherrschen, aber nicht so groß, dass das mehr oder weniger nur nebenbei laufen wird, weil 100, 200 oder 300 Mio. Euro Umsatz mehr oder weniger nicht so ausmachen. Bei Ipsen macht das ne Menge aus!
EXEL hat außerdem sehr gute Konditionen bekommen, die so bei einem großen Partner vielleicht nicht zu haben gewesen wären.
Als nächstes steht dann ja wohl die Zulassung von Cabo bei RCC an. Offizieller PDUFA-Tag ist der 22.06.
Hammer kann sich ja eine Vorstellung schon im März vorstellen...
Interessanterweise meldet EXEL ja auch folgendes: "As regulators continue to review our submitted applications, we are on track to be commercially ready in the United States by April 1, should we receive a regulatory decision in advance of the June 22 PDUFA date."
Ich bin gespannt, ob man wirklich schon so viel eher grünes Licht von der FDA bekommen wird.
Und der Partner ist.... Ipsen!"
Hallo kmastra,
im ersten Moment war ich enttäuscht. Ich habe gefragt: Ipsen wer? Ipsen was?
Aber inzwischen sehe ich den Deal absolut positiv.
Die upfront-Zahlung dürfte den Kapitalbedarf von EXEL für dieses Jahr weitgehend decken. Das ist ein sehr wichtiger Punkt.
Läuft alles wie erwartet/erhofft, wird EXEL nächstes Jahr bereits signifikante Umsätze erzielen, so dass die Notwendigkeit neues Kapital aufzutreiben, deutlich weniger drängend werden wird.
Ipsen scheint mir ansonsten auch ein vernünftig geführtes und fokussiertes Unternehmen zu sein.
Hier ihre Präsentation zum Geschäftsjahr 2015 (pdf), in der auch der Deal mit EXEL dargestellt wird:
https://www.ipsen.com/wp-content/uploads/2016/03/01-03-2016-…
Im Hammer-Blog hat jemand zu recht darauf hingewiesen, dass Cabo für Ipsen ein ganz wichtiger Teil ihres Portfolios sein wird und die deswegen dem Vertrieb in Europa die maximale Aufmerksamkeit widmen werden.
Gute OS-Daten vorausgesetzt, wird die Nachfrage nach Cabo als Drittlinientherapie hoch sein (auch ohne Sales-Force-Terror) und Ipsen ist groß genug, das dann organisatorisch zu beherrschen, aber nicht so groß, dass das mehr oder weniger nur nebenbei laufen wird, weil 100, 200 oder 300 Mio. Euro Umsatz mehr oder weniger nicht so ausmachen. Bei Ipsen macht das ne Menge aus!
EXEL hat außerdem sehr gute Konditionen bekommen, die so bei einem großen Partner vielleicht nicht zu haben gewesen wären.
Als nächstes steht dann ja wohl die Zulassung von Cabo bei RCC an. Offizieller PDUFA-Tag ist der 22.06.
Hammer kann sich ja eine Vorstellung schon im März vorstellen...
Interessanterweise meldet EXEL ja auch folgendes: "As regulators continue to review our submitted applications, we are on track to be commercially ready in the United States by April 1, should we receive a regulatory decision in advance of the June 22 PDUFA date."
Ich bin gespannt, ob man wirklich schon so viel eher grünes Licht von der FDA bekommen wird.
Antwort auf Beitrag Nr.: 51.909.588 von SLGramann am 05.03.16 09:52:26@SGL Gramann
Ich möchte Dir da widersprechen. Zwar kann ich Deine grundsätzliche Kritik an der häufigen Widersprüchlichkeit und der damit einhergehenden Qualitätsarmut im Journalismus bestens nachvollziehen (in meinem beruflichen Tätigkeitsfeld ist die journalistische Berichterstattung gefühlt noch viel schlechter).
Aber hier darf nicht unberücksichtigt bleiben, warum BRMN die Herausgabe verweigert. Es handelt sich ganz gewiß nicht um anerkennenswerte wissenschaftliche Motive (nach dem Motto: zu ungewiß, zu risikoreich, nicht verantwortbar), sondern allein darum, die kommerzielle Zulassung nicht durch etwaige unliebsame Überraschungen auf der Zielgeraden zu gefährden. Das ist aus meiner Sicht schäbig und nicht Sinn der gesetzlich zu Recht vorgeschriebenen hohen Zulassungshürden.
Es geht hier (und ganz konkret bei BMRN leider auch in weiteren Fällen) um Leben und Tod! Für mich ist BMRN daher seit Längerem unten durch (nicht zuletzt auch, weil die Ergebnisse zu Drisa im Hinblick auf Kommerz absichtlich positiv verzerrt dargestellt wurden).
Ich möchte Dir da widersprechen. Zwar kann ich Deine grundsätzliche Kritik an der häufigen Widersprüchlichkeit und der damit einhergehenden Qualitätsarmut im Journalismus bestens nachvollziehen (in meinem beruflichen Tätigkeitsfeld ist die journalistische Berichterstattung gefühlt noch viel schlechter).
Aber hier darf nicht unberücksichtigt bleiben, warum BRMN die Herausgabe verweigert. Es handelt sich ganz gewiß nicht um anerkennenswerte wissenschaftliche Motive (nach dem Motto: zu ungewiß, zu risikoreich, nicht verantwortbar), sondern allein darum, die kommerzielle Zulassung nicht durch etwaige unliebsame Überraschungen auf der Zielgeraden zu gefährden. Das ist aus meiner Sicht schäbig und nicht Sinn der gesetzlich zu Recht vorgeschriebenen hohen Zulassungshürden.
Es geht hier (und ganz konkret bei BMRN leider auch in weiteren Fällen) um Leben und Tod! Für mich ist BMRN daher seit Längerem unten durch (nicht zuletzt auch, weil die Ergebnisse zu Drisa im Hinblick auf Kommerz absichtlich positiv verzerrt dargestellt wurden).
Antwort auf Beitrag Nr.: 51.911.991 von lawmeetstax am 05.03.16 18:52:24was sollen das denn für unliebsame Überraschungen sein? Das hätte ich dann schon gern erklärt.
Ein Unternehmen freut sich doch normalerweise, je früher es ein Medikament verkaufen darf.
Aus meiner Sicht ist es durchaus verantwortungsvoll, "die Zulassung nicht zu gefährden", dann kriegt das Medikament ja keiner. Sondern den Antrag zu stellen, wenn die Zulassungvoraussetzungen erfüllt sind.
Das Medikament haben die ja nicht in der Lotterie gewonnen, wenn es erst in 1 Jahr oder 5 Jahren entwickelt worden wäre, hätte sich auch niemand beschweren können.
Ich kenne selbst Leute, die sehr krank sind und hoffen, dass die Forschung etwas für sie findet. Aber natürlich kann es dafür keine Garantie geben und man kann es einem Unternehmen doch nicht vorwerfen, dass es zu langsam ist. Sondern man sollte froh sein, dass es etwas entwickelt. Ist natürlich bitter, wenn es knapp zu spät ist für einen selbst.
Unlauter wäre es, mit der Zulassung zu warten, um den Preis zu manipulieren o.ä....aber ich wüsste nicht, wie das gehen soll. Sonst bleibe ich dabei. Je früher ein Medikament verkauft werden kann, desto mehr freuen sich die Leute doch über Einnahmen.
Ein Unternehmen freut sich doch normalerweise, je früher es ein Medikament verkaufen darf.
Aus meiner Sicht ist es durchaus verantwortungsvoll, "die Zulassung nicht zu gefährden", dann kriegt das Medikament ja keiner. Sondern den Antrag zu stellen, wenn die Zulassungvoraussetzungen erfüllt sind.
Das Medikament haben die ja nicht in der Lotterie gewonnen, wenn es erst in 1 Jahr oder 5 Jahren entwickelt worden wäre, hätte sich auch niemand beschweren können.
Ich kenne selbst Leute, die sehr krank sind und hoffen, dass die Forschung etwas für sie findet. Aber natürlich kann es dafür keine Garantie geben und man kann es einem Unternehmen doch nicht vorwerfen, dass es zu langsam ist. Sondern man sollte froh sein, dass es etwas entwickelt. Ist natürlich bitter, wenn es knapp zu spät ist für einen selbst.
Unlauter wäre es, mit der Zulassung zu warten, um den Preis zu manipulieren o.ä....aber ich wüsste nicht, wie das gehen soll. Sonst bleibe ich dabei. Je früher ein Medikament verkauft werden kann, desto mehr freuen sich die Leute doch über Einnahmen.
Antwort auf Beitrag Nr.: 51.912.696 von xylophon am 05.03.16 22:10:29@xylophon
Ich möchte dieses Thema hier nur ungern vertiefen, aber auch nicht vor der Antwort auf Deine Frage weglaufen. Daher der Kompromiß im Verweis auf untenstehenden Artikel aus der "Welt", der zum gleichen Fall bereits im Sommer des letzten Jahres erschien:
http://www.welt.de/vermischtes/article141398533/Hannahs-Tode…
Mein Argument wird dort ausführlich dargestellt. Ebenso die Herleitung, daß eine Zurverfügungstellung juristisch möglich wäre und Konkurrenzunternehmen dies auch durchaus tun.
Ich halte daran fest, daß Biomarin ein ethisch-moralisch vertretbares Verhalten leider vermissen läßt. Auch wenn ein gewinnorientiertes Unternehmen immer ein solches bleiben muß, werden hier mE Grenzen überschritten.
Ich möchte dieses Thema hier nur ungern vertiefen, aber auch nicht vor der Antwort auf Deine Frage weglaufen. Daher der Kompromiß im Verweis auf untenstehenden Artikel aus der "Welt", der zum gleichen Fall bereits im Sommer des letzten Jahres erschien:
http://www.welt.de/vermischtes/article141398533/Hannahs-Tode…
Mein Argument wird dort ausführlich dargestellt. Ebenso die Herleitung, daß eine Zurverfügungstellung juristisch möglich wäre und Konkurrenzunternehmen dies auch durchaus tun.
Ich halte daran fest, daß Biomarin ein ethisch-moralisch vertretbares Verhalten leider vermissen läßt. Auch wenn ein gewinnorientiertes Unternehmen immer ein solches bleiben muß, werden hier mE Grenzen überschritten.
Antwort auf Beitrag Nr.: 51.914.103 von lawmeetstax am 06.03.16 13:05:52Ich finde, dass man das ruhig etwas vertiefen darf, weil es eigentich eine typische Situation ist.
Zunächst: auch die WELT schreibt nicht, was genau der Grund ist, das Medikament zu verweigern. Sie lassen aber anklingen, dass das betroffene Mädchen eventuell gar nicht genau in die Zielgruppe passt, wenn von einer "Erweiterung" die Rede ist. Letztlich kann ich es verstehen, wenn eine Firma ein Medikament, das vielen mit einer konkreten Problematik helfen kann, nicht herausgibt an andere, denen es "vielleicht" auch helfen kann. Auch wenn es für die Eltern bitter ist.
Für die Entwickler ist es wichtig, dass das Medikament auf den Markt kommt und damit sehr vielen Menschen in den kommenden Jahren helfen kann. Dies will man nicht gefährden. Ich weiß zu wenig über die konkrete Indikaion und die Risiken, aber eins ist klar: man kann nicht für 1 Menschen die Chancen von sehr vielen anderen Menschen schmälern, auch wenn dieser eine Mensch - das ist jetzt etwas böse - Möglichkeiten hat, die Presse auf seine Seite zu bringen.
Es gibt viele andere, deren Fall nicht in der Zeitung steht, die auch hoffen. Und die haben ein Recht, dass die Zulassung nicht gefährdet wird, weil man 1 Menschen mit "Einfluss" helfen will und scheitert.
Letztlich hat man vor einigen Jahren immer gelesen, wie zynisch die Pharma-Firmen sind, dass sie nur in Richtung "großer" Krankheiten forschen und seltene Krankheiten nicht lohnen würden. Jetzt hat man ein Unternehmen, das sich tatsächlich auch um seltene Krankheiten kümmert, das ist erst mal positiv zu würdigen. Und dass sie nicht ein Risiko eingehen, die Zulassung eines Medikaments zu gefährden, das einer bestimmten Zielgruppe offenbar helfen kann, finde ich explizit richtig. Solange es einen "wissenschaftlichen" Grund gibt, dass diese Mädchen ein Risiko darstellen kann, weil es eben nicht in den eigentlichen Zielbereich fällt, ist es völlig richtig, wie die Firma handelt.
Man kann nicht für ein Schickal mit ungewissem Ausgang die Chancen der vielen gefährden, für die das Mittel hilfreich wäre. Geht man davon aus, bei dem Mädchen aus dem Artikel gibt es Komplikationen und keine Verbesserung, weil sie nicht genau auf die Indikation passt - werden sehr viele andere länger warten müssen.
Beide Artikel sind zu den Gründen sehr ungenau, ich selbst kenne mich nicht so gut aus, aber die Andeutung, "Wir möchten die Entwicklung von Cerliponase alfa nicht gefährden", da "Hunderte Patienten und deren Familien profitieren" könnten. Biomarin stellt klar: "Zum jetzigen Zeitpunkt wäre es voreilig, den Anwendungsbereich noch weiter auszuweiten. deutet darauf hin, dass hier falsche Hoffnungen genährt werden.
Der Artikel ist im übrigen auch sehr emotional, es wird das Leid des Kindes geschildert und mehr oder weniger behauptet, das Medikament würde helfen. Genau davon geht das Unternehmen aber wohl nicht aus.
Es kann doch kein Kriterium sein, dass eine Familie sich an die Presse wendet und die "hunderten anderen" werden eventuell keine Chance haben, weil sich bei dem Mächen Probleme zeigen, die die Zulassung verzögern, so dass die eigentliche Zielgruppe vor der Zulassung stirbt?
Ich habe jedenfalls Verständnis für Biormarin. Wenn sie wüssten, dass das Mittel dem Mädchen hilft und keine Probleme auftauchen, wären sie ja dumm, sich den Umsatz und den Erfolg nicht auf die Fahnen zu schreiben. Aber offenbar gehen sie nicht davon aus, dass HIER ein Erfolg eintreten wird. Der Artikel unterstellt das einfach, aus Sicht der Eltern, die sich an jeden Strohalm klammern, verständlich.
Zunächst: auch die WELT schreibt nicht, was genau der Grund ist, das Medikament zu verweigern. Sie lassen aber anklingen, dass das betroffene Mädchen eventuell gar nicht genau in die Zielgruppe passt, wenn von einer "Erweiterung" die Rede ist. Letztlich kann ich es verstehen, wenn eine Firma ein Medikament, das vielen mit einer konkreten Problematik helfen kann, nicht herausgibt an andere, denen es "vielleicht" auch helfen kann. Auch wenn es für die Eltern bitter ist.
Für die Entwickler ist es wichtig, dass das Medikament auf den Markt kommt und damit sehr vielen Menschen in den kommenden Jahren helfen kann. Dies will man nicht gefährden. Ich weiß zu wenig über die konkrete Indikaion und die Risiken, aber eins ist klar: man kann nicht für 1 Menschen die Chancen von sehr vielen anderen Menschen schmälern, auch wenn dieser eine Mensch - das ist jetzt etwas böse - Möglichkeiten hat, die Presse auf seine Seite zu bringen.
Es gibt viele andere, deren Fall nicht in der Zeitung steht, die auch hoffen. Und die haben ein Recht, dass die Zulassung nicht gefährdet wird, weil man 1 Menschen mit "Einfluss" helfen will und scheitert.
Letztlich hat man vor einigen Jahren immer gelesen, wie zynisch die Pharma-Firmen sind, dass sie nur in Richtung "großer" Krankheiten forschen und seltene Krankheiten nicht lohnen würden. Jetzt hat man ein Unternehmen, das sich tatsächlich auch um seltene Krankheiten kümmert, das ist erst mal positiv zu würdigen. Und dass sie nicht ein Risiko eingehen, die Zulassung eines Medikaments zu gefährden, das einer bestimmten Zielgruppe offenbar helfen kann, finde ich explizit richtig. Solange es einen "wissenschaftlichen" Grund gibt, dass diese Mädchen ein Risiko darstellen kann, weil es eben nicht in den eigentlichen Zielbereich fällt, ist es völlig richtig, wie die Firma handelt.
Man kann nicht für ein Schickal mit ungewissem Ausgang die Chancen der vielen gefährden, für die das Mittel hilfreich wäre. Geht man davon aus, bei dem Mädchen aus dem Artikel gibt es Komplikationen und keine Verbesserung, weil sie nicht genau auf die Indikation passt - werden sehr viele andere länger warten müssen.
Beide Artikel sind zu den Gründen sehr ungenau, ich selbst kenne mich nicht so gut aus, aber die Andeutung, "Wir möchten die Entwicklung von Cerliponase alfa nicht gefährden", da "Hunderte Patienten und deren Familien profitieren" könnten. Biomarin stellt klar: "Zum jetzigen Zeitpunkt wäre es voreilig, den Anwendungsbereich noch weiter auszuweiten. deutet darauf hin, dass hier falsche Hoffnungen genährt werden.
Der Artikel ist im übrigen auch sehr emotional, es wird das Leid des Kindes geschildert und mehr oder weniger behauptet, das Medikament würde helfen. Genau davon geht das Unternehmen aber wohl nicht aus.
Es kann doch kein Kriterium sein, dass eine Familie sich an die Presse wendet und die "hunderten anderen" werden eventuell keine Chance haben, weil sich bei dem Mächen Probleme zeigen, die die Zulassung verzögern, so dass die eigentliche Zielgruppe vor der Zulassung stirbt?
Ich habe jedenfalls Verständnis für Biormarin. Wenn sie wüssten, dass das Mittel dem Mädchen hilft und keine Probleme auftauchen, wären sie ja dumm, sich den Umsatz und den Erfolg nicht auf die Fahnen zu schreiben. Aber offenbar gehen sie nicht davon aus, dass HIER ein Erfolg eintreten wird. Der Artikel unterstellt das einfach, aus Sicht der Eltern, die sich an jeden Strohalm klammern, verständlich.
Antwort auf Beitrag Nr.: 51.916.806 von xylophon am 07.03.16 00:25:14
Ich finde Dein Schreiben gut,
sehe das ähnlich.
Ich finde Dein Schreiben gut,
sehe das ähnlich.
Antwort auf Beitrag Nr.: 51.850.888 von SLGramann am 27.02.16 08:25:04"Im ebenfalls nicht sehr wahrscheinlichen Fall eines totalen Scheiterns von ACT IV wird die Aktie natürlich nochmals dramatisch an Wert verlieren."
CLDX:
Leider ist genau der worst case eingetreten.
ACT IV wurde wegen "futility" abgebrochen.
Ich bin extrem enttäuscht. Der Vergleichsarm der Studie hat unerwartet gut abgeschnitten, so dass die verum-Gruppe nicht besser als die Kontrollgruppe liegt:

Ob ich CLDX weiter halte, habe ich noch nicht entschieden. Ein Nachkauf scheidet jedenfalls aus.
CLDX:
Leider ist genau der worst case eingetreten.
ACT IV wurde wegen "futility" abgebrochen.
Ich bin extrem enttäuscht. Der Vergleichsarm der Studie hat unerwartet gut abgeschnitten, so dass die verum-Gruppe nicht besser als die Kontrollgruppe liegt:

Ob ich CLDX weiter halte, habe ich noch nicht entschieden. Ein Nachkauf scheidet jedenfalls aus.
Antwort auf Beitrag Nr.: 51.923.271 von SLGramann am 07.03.16 18:25:30Ja schade zum Glück machen andere Werte heute den Verlust wett, ich halte meine Position mal weiter.
Antwort auf Beitrag Nr.: 51.923.439 von schnappi am 07.03.16 18:39:41"zum Glück machen andere Werte heute den Verlust wett,"
Wieder mal ein Tag, an dem man das Gebot der Diversifikation betonen muss!
Das ist überlebenswichtig. ipollit hat immer Positionsgrößen von normalerweise 1 bis 3% des Depots gehabt und damit hatte er recht!
Ich habe früher größere Positionen gehalten, teilweise über 20%. Seit langem habe ich mich aber an ipollits Vorgabe stark angepasst und das war unglaublich wichtig und wertvoll.
Wieder mal ein Tag, an dem man das Gebot der Diversifikation betonen muss!
Das ist überlebenswichtig. ipollit hat immer Positionsgrößen von normalerweise 1 bis 3% des Depots gehabt und damit hatte er recht!
Ich habe früher größere Positionen gehalten, teilweise über 20%. Seit langem habe ich mich aber an ipollits Vorgabe stark angepasst und das war unglaublich wichtig und wertvoll.
Antwort auf Beitrag Nr.: 51.923.730 von SLGramann am 07.03.16 19:05:53So halte ich es auch in etwa,
zum Glück hatte ich den Mut viele Werte in den letzten Wochen nahe an den tiefs nachzukaufen
zB.: CTRV,IMUC,MRNS,ADAP,OMED die geben heute Gas
zum Glück hatte ich den Mut viele Werte in den letzten Wochen nahe an den tiefs nachzukaufen

zB.: CTRV,IMUC,MRNS,ADAP,OMED die geben heute Gas

Das tummelt sich zur Zeit bei mir im Lager:
Morphosys
CTRV
MRNS
OMED
ADAP
IMUC
QURE
AFMD
ESPR
BLCM
RLYP
CEMP
PGNX
KPTI
ACRX
XNCR
RXII
ONTY
BLUE
ORPN
STML
XENE
JUNO
PIRS
CLDX
Beobachtung ist:
http://www.cidara.com/
Morphosys
CTRV
MRNS
OMED
ADAP
IMUC
QURE
AFMD
ESPR
BLCM
RLYP
CEMP
PGNX
KPTI
ACRX
XNCR
RXII
ONTY
BLUE
ORPN
STML
XENE
JUNO
PIRS
CLDX
Beobachtung ist:
http://www.cidara.com/
Antwort auf Beitrag Nr.: 51.923.730 von SLGramann am 07.03.16 19:05:53dazu mal ne Frage: ich hatte eigentlich auch nie besonders viel Geld in Einzelwerten. Allerdings war im letzten Jahr Morphosys so weit im Plus, dass sie über 10 % meines Depots ausgemacht haben, ich habe dann vorsichtig ein paar verkauft, was im Nachhinein natürlich gut war. Allerdings waren die Käufe auch nicht viel besser als hätte ich alle Morphosys behalten.
Der Punkt ist aber der: wie haltet Ihr es, wenn eine Aktie durch die Kursentwicklung einen viel größeren Depot-Anteil hat als eigentlich gewünscht?
Man will ja auch nicht bei 200 % verkaufen, wenn es ein paar 1000 Prozent geben kann (siehe Amazon, Pro7 und ein paar andere Werte, die sich vervielfacht haben....nicht dass ich sie alle hätte, aber das ist ja eigentlich der Traum, dass man mit einer Aktie richtig viel Geld macht, weil man tief genug dabei war).
Der Punkt ist aber der: wie haltet Ihr es, wenn eine Aktie durch die Kursentwicklung einen viel größeren Depot-Anteil hat als eigentlich gewünscht?
Man will ja auch nicht bei 200 % verkaufen, wenn es ein paar 1000 Prozent geben kann (siehe Amazon, Pro7 und ein paar andere Werte, die sich vervielfacht haben....nicht dass ich sie alle hätte, aber das ist ja eigentlich der Traum, dass man mit einer Aktie richtig viel Geld macht, weil man tief genug dabei war).
Antwort auf Beitrag Nr.: 51.925.863 von xylophon am 07.03.16 23:18:08"dazu mal ne Frage:"
Hallo, die Frage ist gut. Mir ging das vor einiger Zeit so mit PCYC und mit Genmab, die sehr gut gelaufen waren, so dass die Depotpositionen dann relativ schwer geworden sind.
Damals habe ich darauf nicht wirklich reagiert, sondern die Werte dann irgendwann mal verkauft (beide immer noch zu früh, wie sich herausgestellt hat).
Heute würde ich so vorgehen:
Kauf einer Position mit bspw. 2% Depotgewicht.
Sobald die Position wegen extremer Outperformance 10% des Depots ausmacht, würde ich sie auf 5% Depotgewicht herunter nehmen und dann weiter beobachten. Sie bliebe also weiter tendenziell etwas übergewichtet, aber eben nicht sehr stark.
Das ist aber nur meine ganz persönliche Herangehensweise, die ich nicht als allgemeine Empfehlung verstanden haben will.
Die einzige allgemeine Empfehlung ist und bleibt, dass eine Position beim Kauf zwischen 1 und maximal 3% des Depots ausmachen sollte.
Hallo, die Frage ist gut. Mir ging das vor einiger Zeit so mit PCYC und mit Genmab, die sehr gut gelaufen waren, so dass die Depotpositionen dann relativ schwer geworden sind.
Damals habe ich darauf nicht wirklich reagiert, sondern die Werte dann irgendwann mal verkauft (beide immer noch zu früh, wie sich herausgestellt hat).
Heute würde ich so vorgehen:
Kauf einer Position mit bspw. 2% Depotgewicht.
Sobald die Position wegen extremer Outperformance 10% des Depots ausmacht, würde ich sie auf 5% Depotgewicht herunter nehmen und dann weiter beobachten. Sie bliebe also weiter tendenziell etwas übergewichtet, aber eben nicht sehr stark.
Das ist aber nur meine ganz persönliche Herangehensweise, die ich nicht als allgemeine Empfehlung verstanden haben will.
Die einzige allgemeine Empfehlung ist und bleibt, dass eine Position beim Kauf zwischen 1 und maximal 3% des Depots ausmachen sollte.
Antwort auf Beitrag Nr.: 51.925.863 von xylophon am 07.03.16 23:18:08Hallo xylophon,
da sprichst du definitiv einen guten Punkt an. Wahrscheinlich ist ein gutes Depotmanagement wichtiger als die Auswahl der einzelnen Werte. Ein Patentrezept gibt es da aber glaube ich nicht.
Ich denke mittlerweile auch, dass einzelne Werte eine Höchstgrenze haben sollten. Zwar habe ich mit einer deutlichen Übergewichtung auch schon gute Erfahrungen gemacht, aber besonders die Ereignisse um AERI, CLVS und ZFGN haben bei mir Spuren hinterlassen. Ich habe für mich da aber absolute und keine prozentualen Grenzen. (Irgendwann tut es halt weh!)
Mehr als 15 Positionen sind für mich persönlich unpraktikabel, weil ich mich ganz gerne auch auf dem Laufenden halte. Zudem kann man sich dann irgendwann auch einen Fonds oder ETF kaufen.
Grundsätzlich reduziere ich Positionen auch vor "Binary-Events" was ich für ganz wichtig halte. Je nach subjektiver Erfolgsaussicht mal mehr mal weniger. Aber auch hier habe ich schon gute Erfahrungen und schlechte Erfahrungen gemacht. Ich habe auch durchaus schon 2/3 verkauft und dann einen 140% Move verpast. Vor Ereignissen wie bei CLVS oder ZFGN kann einen das aber nicht schützen. Aktuell habe ich meine Position bei ARQL verringert, weil hier eine interim Analyse der PIII von Tivantenib ansteht. Und da bin ich mir gar nicht sicher...
Wenn man Gewinne mitnimmt halte ich es je nach Marktlage (momentan muss man das sicher nicht unbedingt) für unverzichtbar zumindest einen Teil davon in andere Assetklassen umzuschichten. Denn du schilderst es ja ganz gut. Was nützt es einem, wenn man in andere Werte umschichtet, die dann genauso wenn nicht sogr noch mehr an Wert verlieren.
Andere Assetklassen von Interesse sind bei mir:
Konsum - sich auch mal was gönnen Zudem behalten Sachgüter ja auch einen gewissen Wert.
Zudem behalten Sachgüter ja auch einen gewissen Wert.
DAX ETFs, die ich streng nach dem Gebert Indikator verkaufe und kaufe. http://www.gebert-börsenindikator.de/
Dividendentitel wie Shell, Münchener Rück, Hamborner Reit etc. Hier versuche ich mir auch ein passives Einkommen zu generieren. Da muss man aber auch aufpassen was man kauft. Es gibt auch Dividenden Etfs, die das Risiko minimieren. Da gibt es einige ganz brauchbare Blogs zu. http://finanziell-umdenken.blogspot.de/
Und ganz wichtig: Cash
Das ist eigentlich die größte Erkenntnis für mich: "Cash is a position!" Man muss nicht immer voll investiert sein. Denn wenn der Gesamtmarkt runtergeht nützen einem andere Assetklassen auch nicht viel. Wenngleich sie dann natürlich meist weniger verlieren.
Ich bin da aber immer noch am tüfteln. Momentan habe ich für alle meine Werte Verkaufsordern für einen Teilbestand eingegeben und versuche zwischen Kern und Tradingposition zu unterscheiden...
Mein Plan:
10% bei 25%
15% bei 50%
25% bei 100%
Rest bei 1000%
SG kmastra
da sprichst du definitiv einen guten Punkt an. Wahrscheinlich ist ein gutes Depotmanagement wichtiger als die Auswahl der einzelnen Werte. Ein Patentrezept gibt es da aber glaube ich nicht.
Ich denke mittlerweile auch, dass einzelne Werte eine Höchstgrenze haben sollten. Zwar habe ich mit einer deutlichen Übergewichtung auch schon gute Erfahrungen gemacht, aber besonders die Ereignisse um AERI, CLVS und ZFGN haben bei mir Spuren hinterlassen. Ich habe für mich da aber absolute und keine prozentualen Grenzen. (Irgendwann tut es halt weh!)
Mehr als 15 Positionen sind für mich persönlich unpraktikabel, weil ich mich ganz gerne auch auf dem Laufenden halte. Zudem kann man sich dann irgendwann auch einen Fonds oder ETF kaufen.
Grundsätzlich reduziere ich Positionen auch vor "Binary-Events" was ich für ganz wichtig halte. Je nach subjektiver Erfolgsaussicht mal mehr mal weniger. Aber auch hier habe ich schon gute Erfahrungen und schlechte Erfahrungen gemacht. Ich habe auch durchaus schon 2/3 verkauft und dann einen 140% Move verpast. Vor Ereignissen wie bei CLVS oder ZFGN kann einen das aber nicht schützen. Aktuell habe ich meine Position bei ARQL verringert, weil hier eine interim Analyse der PIII von Tivantenib ansteht. Und da bin ich mir gar nicht sicher...
Wenn man Gewinne mitnimmt halte ich es je nach Marktlage (momentan muss man das sicher nicht unbedingt) für unverzichtbar zumindest einen Teil davon in andere Assetklassen umzuschichten. Denn du schilderst es ja ganz gut. Was nützt es einem, wenn man in andere Werte umschichtet, die dann genauso wenn nicht sogr noch mehr an Wert verlieren.
Andere Assetklassen von Interesse sind bei mir:
Konsum - sich auch mal was gönnen
 Zudem behalten Sachgüter ja auch einen gewissen Wert.
Zudem behalten Sachgüter ja auch einen gewissen Wert. DAX ETFs, die ich streng nach dem Gebert Indikator verkaufe und kaufe. http://www.gebert-börsenindikator.de/
Dividendentitel wie Shell, Münchener Rück, Hamborner Reit etc. Hier versuche ich mir auch ein passives Einkommen zu generieren. Da muss man aber auch aufpassen was man kauft. Es gibt auch Dividenden Etfs, die das Risiko minimieren. Da gibt es einige ganz brauchbare Blogs zu. http://finanziell-umdenken.blogspot.de/
Und ganz wichtig: Cash
Das ist eigentlich die größte Erkenntnis für mich: "Cash is a position!" Man muss nicht immer voll investiert sein. Denn wenn der Gesamtmarkt runtergeht nützen einem andere Assetklassen auch nicht viel. Wenngleich sie dann natürlich meist weniger verlieren.
Ich bin da aber immer noch am tüfteln. Momentan habe ich für alle meine Werte Verkaufsordern für einen Teilbestand eingegeben und versuche zwischen Kern und Tradingposition zu unterscheiden...
Mein Plan:
10% bei 25%
15% bei 50%
25% bei 100%
Rest bei 1000%

SG kmastra
danke für die beiden Antworten. Ich habe das Problem jetzt nicht mehr im Biotec-Bereich, aber eine Position macht immerhin fast 1/4 des Depots aus, dies allein durch Kursgewinn. Utd. Internet - ist aber ein relativ solider Wert, der jedes Jahr so viel Dividende zahlt, dass ich schon aus dieser den damaligen Kaufkurs mehrfach raus habe. So tue ich mich schwer, hier zu reduzieren, zumal der Gewinn auch steuerfrei ist. Eher hoffe ich, dass die anderen Werte durch Kursgewinne den prozentualen Anteil steigern können.
Sollte ich irgendwann mal verkaufen, sicher nicht, um zurückzukaufen. Und ich würde es auch nur tun, wenn sich ein deutlicher Abwärtstrend zeigt.
Andere Werte habe ich entsprechend der von Euch genannten Strategie "teilverkauft", bei AMZN habe ich mich geärgert, manchmal war es auch richtig.
Am einfachsten ist es, wenn ein Wert übernommen wird, dann hat man keine Wahl....
Danke für die Antworten, haben mir geholfen.
Sollte ich irgendwann mal verkaufen, sicher nicht, um zurückzukaufen. Und ich würde es auch nur tun, wenn sich ein deutlicher Abwärtstrend zeigt.
Andere Werte habe ich entsprechend der von Euch genannten Strategie "teilverkauft", bei AMZN habe ich mich geärgert, manchmal war es auch richtig.
Am einfachsten ist es, wenn ein Wert übernommen wird, dann hat man keine Wahl....
Danke für die Antworten, haben mir geholfen.
Meinungen zu CLDX nachdem die ACT IV von RINTEGA gefloppt ist?
MK ca. 350 Mio
Firmen / Pipelinewert abzüglich Cash noch ca. 60 Mio
MK ca. 350 Mio
Firmen / Pipelinewert abzüglich Cash noch ca. 60 Mio
Da wurde heute ja wieder Querbeet runter geprügelt,
bin am überlegen ob ich bei Qure,RLYP und BLCM nochmal nachkaufen soll.
bin am überlegen ob ich bei Qure,RLYP und BLCM nochmal nachkaufen soll.
Antwort auf Beitrag Nr.: 51.153.123 von Oberlaendler am 23.11.15 12:54:30http://finance.yahoo.com/news/bioblast-pharma-announces-posi…
gestern dürfte ja Valeant der Auslöser gewesen sein. Schon heftig, wie die eingegangen sind, seit letztem Sommer. Selbst solche Schwergewichte hat es also zerlegt.
Ich kaufe nichts, bis sich ein Boden bei Biotech abzeichnet - ich sehe keinen. Aber bin ja auch nur Laie.
Ich kaufe nichts, bis sich ein Boden bei Biotech abzeichnet - ich sehe keinen. Aber bin ja auch nur Laie.
Antwort auf Beitrag Nr.: 51.992.246 von schnappi am 16.03.16 13:37:56Das tut mal gut mal sehen wo wir um 21 Uhr stehen 
Da hau ich aber mal paar raus vorher

Da hau ich aber mal paar raus vorher
Antwort auf Beitrag Nr.: 51.993.086 von schnappi am 16.03.16 14:59:46
118 % für Phase 2 resultate?
Zitat von schnappi: Das tut mal gut mal sehen wo wir um 21 Uhr stehen
![]()
Da hau ich aber mal paar raus vorher
118 % für Phase 2 resultate?
Antwort auf Beitrag Nr.: 51.992.246 von schnappi am 16.03.16 13:37:56
Schöne Entwicklung heute, wobei ich so eine heftige Reaktion nicht erwartet habe. Mal sehen ob das bis Börsenschluß hält.
Es geht aber noch besser, siehe gestern Celator +432% (sorry kann keinen Chart einfügen) auf diese Nachricht:
http://seekingalpha.com/news/3167284-celator-pharma-big-posi…
Gruß Oberländler
Zitat von schnappi: http://finance.yahoo.com/news/bioblast-pharma-announces-posi…
Schöne Entwicklung heute, wobei ich so eine heftige Reaktion nicht erwartet habe. Mal sehen ob das bis Börsenschluß hält.
Es geht aber noch besser, siehe gestern Celator +432% (sorry kann keinen Chart einfügen) auf diese Nachricht:
http://seekingalpha.com/news/3167284-celator-pharma-big-posi…
Gruß Oberländler
Antwort auf Beitrag Nr.: 51.993.086 von schnappi am 16.03.16 14:59:46Glückwunsch Schnappi!
In der jetzigen Marktphase sind solche Bewegungen doppelt wertvoll!
Ob so eine Bewegung nun bei einem P2 Ergebnis berechtigt ist oder nicht sei mal dahingestellt. Aber ich würde meinen, dass momentan positive Ergebnisse eben nicht eingepreist sind und von daher dann eingepresit werden müssen, wenn sie Fakt sind.
Was den Gesamtmarkt betrifft fand ich neulich die Meinung von Alan Leong sehr gut:
http://alanhobbes.blogspot.de/2016/02/the-sky-is-falling-our…
Natürlich kann es weiter runter gehen. Aber fundamental (und mit einem längeren Anlagehorizont) sind viele Biotechs attraktiv bewertet!
Dass jetzt Valeant in Schwierigkeiten ist hat doch nichts mit z.B. EXEL zu tun. Die haben halt ständig Firmen gekauft (auf Pump) und dann die Preise erhöht. Jetzt wo sich herausstellt, dass dieses "Geschäftsmodell" nicht nachhaltig ist, könnten denen die Schulden das Genick brechen. Das erinnert schon ein wenig an die Subprimekrise. Aber Valeant ist doch sehr speziell und nicht die Regel!
In der jetzigen Marktphase sind solche Bewegungen doppelt wertvoll!
Ob so eine Bewegung nun bei einem P2 Ergebnis berechtigt ist oder nicht sei mal dahingestellt. Aber ich würde meinen, dass momentan positive Ergebnisse eben nicht eingepreist sind und von daher dann eingepresit werden müssen, wenn sie Fakt sind.
Was den Gesamtmarkt betrifft fand ich neulich die Meinung von Alan Leong sehr gut:
http://alanhobbes.blogspot.de/2016/02/the-sky-is-falling-our…
Natürlich kann es weiter runter gehen. Aber fundamental (und mit einem längeren Anlagehorizont) sind viele Biotechs attraktiv bewertet!
Dass jetzt Valeant in Schwierigkeiten ist hat doch nichts mit z.B. EXEL zu tun. Die haben halt ständig Firmen gekauft (auf Pump) und dann die Preise erhöht. Jetzt wo sich herausstellt, dass dieses "Geschäftsmodell" nicht nachhaltig ist, könnten denen die Schulden das Genick brechen. Das erinnert schon ein wenig an die Subprimekrise. Aber Valeant ist doch sehr speziell und nicht die Regel!
Antwort auf Beitrag Nr.: 51.995.210 von kmastra am 16.03.16 18:17:25Danke!
Ja die Bewegung in der ersten Stunde war extrem, aber das bringt die momentane Marktphase mit sich.
Bei RLYP+ BLCM habe ich die Gewinne reininvestiert mal sehen wie es weitergeht.
Heute wurde bei ORPN schon die Hälfte der Aktien gehandelt
Gesamt:14,230,480
Ja die Bewegung in der ersten Stunde war extrem, aber das bringt die momentane Marktphase mit sich.
Bei RLYP+ BLCM habe ich die Gewinne reininvestiert mal sehen wie es weitergeht.
Heute wurde bei ORPN schon die Hälfte der Aktien gehandelt
Gesamt:14,230,480
Heute Kapitalerhöhung was ein hoch und runter unter 3$ werde ich evt. nachkaufen.
GNCA:
Heute mit guten Ergebnissen von 003 bei Genitalherpes. Nachdem letztes Jahr schon gute 6 Monatsdaten veröffentlicht wurden, können heute auch die 12 Monatsdaten überzeugen.

So wie es aussieht ist eine jährliche Impfung (wie Grippe) möglich. Ich fand eigentlich schon die 6 Monatsdaten so gut (dann wäre halt 2 mal im Jahr geimpft worden), dass ich die Bewertung nicht so ganz nachvollziehen konnte. Aber so sieht es nochmal besser aus.
GNCA hat nach dem heutigen Kursplus eine Marktkapitalisierung von 160 Mio. -steigend
So wie ich es verstehe hat 003 eine realistische Chance zum neuen SOC zu werden. Bis dahin ist es aber noch ein langer (und teurer) Weg. Es müssen wohl mehrere PIII Studien gemacht werden. Dabei scheinen Kombinationen mit dem aktuellen SOC aussichtsreich. Man könnte dann z.B. eine Kombination mit Virustatika wählen, die nur in akuten Phasen genommen werden. Laut Analysten ist ein Umsatzpotenzial von 700 Mio möglich.
Zudem ist GNCA aber auch im Bereich IO tätig. Da ihre Plattform über die Beeinflussung der T funktioniert ist das ja naheliegend. Wie aussichtsreich das Ganze ist kann ich nicht beurteilen. Da fehlt jetzt ipollit!
Endlich mal wieder gute Nachrichten zur Zeit!
SG kmastra
Heute mit guten Ergebnissen von 003 bei Genitalherpes. Nachdem letztes Jahr schon gute 6 Monatsdaten veröffentlicht wurden, können heute auch die 12 Monatsdaten überzeugen.

So wie es aussieht ist eine jährliche Impfung (wie Grippe) möglich. Ich fand eigentlich schon die 6 Monatsdaten so gut (dann wäre halt 2 mal im Jahr geimpft worden), dass ich die Bewertung nicht so ganz nachvollziehen konnte. Aber so sieht es nochmal besser aus.
GNCA hat nach dem heutigen Kursplus eine Marktkapitalisierung von 160 Mio. -steigend

So wie ich es verstehe hat 003 eine realistische Chance zum neuen SOC zu werden. Bis dahin ist es aber noch ein langer (und teurer) Weg. Es müssen wohl mehrere PIII Studien gemacht werden. Dabei scheinen Kombinationen mit dem aktuellen SOC aussichtsreich. Man könnte dann z.B. eine Kombination mit Virustatika wählen, die nur in akuten Phasen genommen werden. Laut Analysten ist ein Umsatzpotenzial von 700 Mio möglich.
Zudem ist GNCA aber auch im Bereich IO tätig. Da ihre Plattform über die Beeinflussung der T funktioniert ist das ja naheliegend. Wie aussichtsreich das Ganze ist kann ich nicht beurteilen. Da fehlt jetzt ipollit!
Endlich mal wieder gute Nachrichten zur Zeit!
SG kmastra
Antwort auf Beitrag Nr.: 52.094.891 von kmastra am 31.03.16 21:29:21http://www.goodrx.com/blog/is-there-a-herpes-vaccine/
@arry
Da hier offenbar keiner mehr schreibt, darf ich ruhig zum wiederholten Male Arry pushen...besser als gar nichts ist es ja hoffentlich...
Der folgende link ist ein ganz aktuelles Video von Dr. Sullivan vom MGH in Boston (7. April 2016), in dem die aktuellen Melanoma-Entwicklungen jenseits von BRAF dargestellt werden. Überspitzt gesagt ist das ein Werbevideo für Arry. Zwar wird Arry nicht an einer Stelle namentlich genannt, aber dafür die Produktkandidaten. Lediglich bei NF1 liegt er mE nicht ganz richtig: Zwar hat er hier die vielversprechende Wirksamkeit von MEK-Inhibitoren angesprochen, erwähnt aber nur Trametinib. Dabei sollte Selumetinib bisher noch bessere Ergebnisse geliefert haben. Aber dann wäre es wohl tatsächlich ein echtes Werbevideo geworden...
http://www.healio.com/hematology-oncology/melanoma-skin-canc…
Da hier offenbar keiner mehr schreibt, darf ich ruhig zum wiederholten Male Arry pushen...besser als gar nichts ist es ja hoffentlich...
Der folgende link ist ein ganz aktuelles Video von Dr. Sullivan vom MGH in Boston (7. April 2016), in dem die aktuellen Melanoma-Entwicklungen jenseits von BRAF dargestellt werden. Überspitzt gesagt ist das ein Werbevideo für Arry. Zwar wird Arry nicht an einer Stelle namentlich genannt, aber dafür die Produktkandidaten. Lediglich bei NF1 liegt er mE nicht ganz richtig: Zwar hat er hier die vielversprechende Wirksamkeit von MEK-Inhibitoren angesprochen, erwähnt aber nur Trametinib. Dabei sollte Selumetinib bisher noch bessere Ergebnisse geliefert haben. Aber dann wäre es wohl tatsächlich ein echtes Werbevideo geworden...
http://www.healio.com/hematology-oncology/melanoma-skin-canc…
Antwort auf Beitrag Nr.: 52.162.045 von lawmeetstax am 11.04.16 15:25:06Hi,
da hier wirklich etwas "Diskussions-Ebbe" herrscht, wollte ich kurz anfragen, ob sich von den hier versammelten schon mal einer mit RedHill Biopharma auseinander gesetzt hat!? Die Firma ist in Israel ansässig, an der Nasdaq gelistet, hat eine MC von ca. 150 Mio $, Cash am 31.12.2015 ca. 58 Mio$ und eine meiner Meinung nach beeindruckende Pipeline:
http://www.redhillbio.com/products
News und Infos erfolgen in regelmäßigen Abständen. Arbeiten u.a. an Wirkstoffen gegen
- Multiple Sklerose/MorbusCrohn:
http://finance.yahoo.com/news/redhill-biopharma-announces-in…
- H.pylori:
http://www.wallstreet-online.de/nachricht/8409411-redhill-bi…
- Gastritis/IBS-D:
http://www.wallstreet-online.de/nachricht/8500480-redhill-bi…
da hier wirklich etwas "Diskussions-Ebbe" herrscht, wollte ich kurz anfragen, ob sich von den hier versammelten schon mal einer mit RedHill Biopharma auseinander gesetzt hat!? Die Firma ist in Israel ansässig, an der Nasdaq gelistet, hat eine MC von ca. 150 Mio $, Cash am 31.12.2015 ca. 58 Mio$ und eine meiner Meinung nach beeindruckende Pipeline:
http://www.redhillbio.com/products
News und Infos erfolgen in regelmäßigen Abständen. Arbeiten u.a. an Wirkstoffen gegen
- Multiple Sklerose/MorbusCrohn:
http://finance.yahoo.com/news/redhill-biopharma-announces-in…
- H.pylori:
http://www.wallstreet-online.de/nachricht/8409411-redhill-bi…
- Gastritis/IBS-D:
http://www.wallstreet-online.de/nachricht/8500480-redhill-bi…
Hat hier Jemand eine Meinung zu XON?
Frage ich mal als Amateur
Ein Artikel, für Euch vielleicht noch was zum lesen,
eine meiner Beobachtungslistenfirmen
http://seekingalpha.com/article/3963062-cocrystal-can-open-d…
Frage ich mal als Amateur

Ein Artikel, für Euch vielleicht noch was zum lesen,
eine meiner Beobachtungslistenfirmen
http://seekingalpha.com/article/3963062-cocrystal-can-open-d…
Antwort auf Beitrag Nr.: 52.094.891 von kmastra am 31.03.16 21:29:21GNCA:
Eine durchaus interessante Firma, die gerade sehr kontrovers diskutiert wird. Vor Kurzem wurden erste Ergebnisse der 12 Monats Studie von 003 veröffentlicht. GEN 003 soll gegen Genitalherpes (HSV2) helfen. Dabei sollen nicht die Viren bekämpft (wie beim derzeitigen SOC) sondern das Imunsystem gestärkt werden.
Genitalherpes ist wie auch das bekanntere Lippenherpes (HSV1) eine Krankheit, die sich nicht die ganze Zeit bemerkbar macht, sondern in Schüben auftritt. Dabei spielen Faktoren wie Stress, Ernährung, Zustand des Imunsystems etc. eine Rolle. Die Krankheit ist ansteckend, unangenehm, psychisch belastend (Z.B. Depression bei Patienten verdoppelt) und kann für Neugeborene sogar tödlich sein.
Auf den ersten Blick waren die Ergebnisse ganz hervorragend. Nach 12 Monaten war die "Viral shedding rate" um 64% gesenkt und ebenso war das Vorkommen von Genital lesions um ca. 65% gesenkt.
Tolle Ergebnisse. Die Aktie stieg um 100%. Doch dann ging es nachbörslich deutlich runter.
Grund war vor allem ein Tweet von Adam Feuerstein. Den meisten dürfte er bekannt sein.

Im Grunde zweifelt er einen positiven Effekt von 003 an, weil nach 28 Tagen die Placebogruppe in den aktiven Arm gewechselt ist. Es gab also keinen Placebovergleich sondern nur einen Vergleich zur Baseline.
Feuerstein hat in der Präsentation nun gesehen, dass es keinen Unterschied zwischen Placebogruppe und aktivem Arm gab was die Anzahl der genital lesions betrifft. Das ist auch richtig, wie die Graphik zeigt.

Also alles nur ein Fake?
Zunächst war das nichts Neues. Die Graphik stammt von einer vorherigen Präsentation und dort wurde ausgiebig darüber gesprochen. Es wurde also nicht versteckt.
GNCA selber ist auch erstaunt darüber und erklärt es mit der kurzen Dauer (28 Tage) und der geringen Anzahl der Placebogruppe (1 zu 8). Zudem muss man bedenken, dass es sich um eine Krankheit handelt, die in Schüben auftritt. Das mal 1 Monat Ruhe ist, ist also nicht ungewöhnlich.
Ein weiterer Punkt ist, dass es sich hier um eine subjektive Einschätzung der Patienten handelt und nicht etwa um harte Fakten, die gar von einem Arzt ermitelt werden.
In der Tat gibt es auch keinen logischen Grund dafür, dass langfristig ein Placeboeffekt einen so hohen Effekt haben könnte. Genitalherpes ist momentan unheilbar und es handelte sich um klar diagnosizierte Fälle. Ein Vergleich mit Placebo ist von daher auch unlogisch. Vielmehr geht es m.E. darum Veränderungen bei einzelnen Patienten aufzuzeigen.
Was Feuerstein leider nicht erwähnt ist zudem, dass es beim Endpunkt viral shedding rate einen sehr großen Unterschied zwischen Placebogruppe und aktiven Armen gibt.

So wie ich es verstehe gibt es aber einen hohen Zusammenhang zwische viral shedding und dem auftreten von Genital lesions. Ohne viral shedding keine genital lesions ließe sich das Ganze zusammenfassen. Zudem handelt es sich hier um harte Fakten.
Die Zukunft wird zeigen wer Recht hat. Ich denke in dem Fall liegt Feuerstein daneben.
Bei allem was ich als Laie über Herpes weiß ist zudem das Stärken des Immunsystems ein vielversprechender Ansatz.
P.S. zu den genannten Firmen kann ich nichts sagen.
SG kmastra
Eine durchaus interessante Firma, die gerade sehr kontrovers diskutiert wird. Vor Kurzem wurden erste Ergebnisse der 12 Monats Studie von 003 veröffentlicht. GEN 003 soll gegen Genitalherpes (HSV2) helfen. Dabei sollen nicht die Viren bekämpft (wie beim derzeitigen SOC) sondern das Imunsystem gestärkt werden.
Genitalherpes ist wie auch das bekanntere Lippenherpes (HSV1) eine Krankheit, die sich nicht die ganze Zeit bemerkbar macht, sondern in Schüben auftritt. Dabei spielen Faktoren wie Stress, Ernährung, Zustand des Imunsystems etc. eine Rolle. Die Krankheit ist ansteckend, unangenehm, psychisch belastend (Z.B. Depression bei Patienten verdoppelt) und kann für Neugeborene sogar tödlich sein.
Auf den ersten Blick waren die Ergebnisse ganz hervorragend. Nach 12 Monaten war die "Viral shedding rate" um 64% gesenkt und ebenso war das Vorkommen von Genital lesions um ca. 65% gesenkt.
Tolle Ergebnisse. Die Aktie stieg um 100%. Doch dann ging es nachbörslich deutlich runter.
Grund war vor allem ein Tweet von Adam Feuerstein. Den meisten dürfte er bekannt sein.

Im Grunde zweifelt er einen positiven Effekt von 003 an, weil nach 28 Tagen die Placebogruppe in den aktiven Arm gewechselt ist. Es gab also keinen Placebovergleich sondern nur einen Vergleich zur Baseline.
Feuerstein hat in der Präsentation nun gesehen, dass es keinen Unterschied zwischen Placebogruppe und aktivem Arm gab was die Anzahl der genital lesions betrifft. Das ist auch richtig, wie die Graphik zeigt.
Also alles nur ein Fake?
Zunächst war das nichts Neues. Die Graphik stammt von einer vorherigen Präsentation und dort wurde ausgiebig darüber gesprochen. Es wurde also nicht versteckt.
GNCA selber ist auch erstaunt darüber und erklärt es mit der kurzen Dauer (28 Tage) und der geringen Anzahl der Placebogruppe (1 zu 8). Zudem muss man bedenken, dass es sich um eine Krankheit handelt, die in Schüben auftritt. Das mal 1 Monat Ruhe ist, ist also nicht ungewöhnlich.
Ein weiterer Punkt ist, dass es sich hier um eine subjektive Einschätzung der Patienten handelt und nicht etwa um harte Fakten, die gar von einem Arzt ermitelt werden.
In der Tat gibt es auch keinen logischen Grund dafür, dass langfristig ein Placeboeffekt einen so hohen Effekt haben könnte. Genitalherpes ist momentan unheilbar und es handelte sich um klar diagnosizierte Fälle. Ein Vergleich mit Placebo ist von daher auch unlogisch. Vielmehr geht es m.E. darum Veränderungen bei einzelnen Patienten aufzuzeigen.
Was Feuerstein leider nicht erwähnt ist zudem, dass es beim Endpunkt viral shedding rate einen sehr großen Unterschied zwischen Placebogruppe und aktiven Armen gibt.
So wie ich es verstehe gibt es aber einen hohen Zusammenhang zwische viral shedding und dem auftreten von Genital lesions. Ohne viral shedding keine genital lesions ließe sich das Ganze zusammenfassen. Zudem handelt es sich hier um harte Fakten.
Die Zukunft wird zeigen wer Recht hat. Ich denke in dem Fall liegt Feuerstein daneben.
Bei allem was ich als Laie über Herpes weiß ist zudem das Stärken des Immunsystems ein vielversprechender Ansatz.
P.S. zu den genannten Firmen kann ich nichts sagen.
SG kmastra
ONTY
Oncothyreon ist eine weitere Firma über die man geteilter Meinung sein kann. ONTY hat mit ONT-380 ein Produkt in der Entwicklung, dass in Kombination mit Herceptin oder Kadcyla bei Her+ Brustkrebs Einsatz finden soll. Die klinische Entwicklung befindet sich noch in den Anfängen. Es sind gerade mal erste PI Ergebisse bekannt. Grundsätzlich werden zwei Wege eingeschlagen:
-Kombination mit wohl Herceptin und Xeloda als 3d line Therapie
-Kombination mit Herceptin oder Kadcyla bei Her+ Brustkrebs mit Gehirn/ZNS Metastasen (2nd line)
ONT380 hat theoretisch zwei Vorteile:
1. Es überwindet die Blut-Hirn-Schranke.
2. Es ist vom Nebenwirkungsprofil recht sauber was wohl daran liegt, dass es Her2 nicht aber Her1/EGFR unterdrückt. Andere Kandidaten wie Tykerb oder Neratinib zielen auf beide ab und haben wohl auch deshalb viel stärkere Nebenwirkungen, was den Einsatz in der Kombination erschwert.
Theoretisch machen die Kombinationen Sinn. Es ist z.B. bekannt, dass Herceptin (überwindet BH-Schranke nicht) mit der Entstehung von HER2+ Gehirnmetastasen in Verbindung steht.
http://www.medscape.com/viewarticle/780802
Da scheint es für mich als Laie eine Kombination mit einem HER2+ Inhibitor, der auch die Blut-Hirn-Schranke passiert erstmal logisch.
Schaut man sich die bisherigen Ergebnisse an, sieht man durchaus einen positiven Effekt. Bisher kann nur die Ansprechrate als Hinweis dienen. Auf der ASCO im Mai/Juni gibt es nun erstmals Daten zum progressionsfreien Überleben (PFS) und zur Dauer des Ansprechens (DOR). Aber auch das sind nicht Plazebo kontrollierte Studienergebnisse.
Schut man sich die Richtlinien an, wird auch der Bedarf deutlich:
http://www.breastcancer.org/research-news/new-guidelines-to-…
Der Bearcase soll nicht verschwiegen werden:
Als Singleagent zeigt ONT380 kaum Wirksamkeit.
Bisher gibt es nur Singlearmtrials (also nicht Plazebo kontrolliert) und die Interpretation ist deshalb, besonders weil es sich um Kombinationen handelt, nicht möglich.
Die positiven Effekte gehen nicht auf ONT380 sondern auf die bereits bekannt wirksamen Kombinationspartner zurück. In Studien konnte auch ein Ansprechen bei CNS festgestellt werden.
Wer soll das eigentlich bezahlen, wenn drei Medikamente beteiligt sind?
ONTY braucht dringend Geld und wird in Kürze eine KE machen.
Aussichten zur ASCO von einem Analysten:


Am Chart sieht man, dass ONTY ziemlich Federn hat lassen müssen. Dafür war neben der allgemeinen Marktlage auch eine total verwirrende PR im Dezember verantwortlich. Die Daten waren aber im Endeffekt nicht schlechter als die zur ASCO2015. Zudem musste der alte CEO gehen, was ich als positiv werte.
Momentan ist ONTY mit 110 Mio$ bewertet. Das finde ich günstig und habe mir deshalb zu meiner Kernposition heute eine Tradingposition hinzu gekauft.
18.5. ASCO Release der Abstracts
3-7.6, ASCO
SG kmastra
Oncothyreon ist eine weitere Firma über die man geteilter Meinung sein kann. ONTY hat mit ONT-380 ein Produkt in der Entwicklung, dass in Kombination mit Herceptin oder Kadcyla bei Her+ Brustkrebs Einsatz finden soll. Die klinische Entwicklung befindet sich noch in den Anfängen. Es sind gerade mal erste PI Ergebisse bekannt. Grundsätzlich werden zwei Wege eingeschlagen:
-Kombination mit wohl Herceptin und Xeloda als 3d line Therapie
-Kombination mit Herceptin oder Kadcyla bei Her+ Brustkrebs mit Gehirn/ZNS Metastasen (2nd line)
ONT380 hat theoretisch zwei Vorteile:
1. Es überwindet die Blut-Hirn-Schranke.
2. Es ist vom Nebenwirkungsprofil recht sauber was wohl daran liegt, dass es Her2 nicht aber Her1/EGFR unterdrückt. Andere Kandidaten wie Tykerb oder Neratinib zielen auf beide ab und haben wohl auch deshalb viel stärkere Nebenwirkungen, was den Einsatz in der Kombination erschwert.
Theoretisch machen die Kombinationen Sinn. Es ist z.B. bekannt, dass Herceptin (überwindet BH-Schranke nicht) mit der Entstehung von HER2+ Gehirnmetastasen in Verbindung steht.
http://www.medscape.com/viewarticle/780802
Da scheint es für mich als Laie eine Kombination mit einem HER2+ Inhibitor, der auch die Blut-Hirn-Schranke passiert erstmal logisch.
Schaut man sich die bisherigen Ergebnisse an, sieht man durchaus einen positiven Effekt. Bisher kann nur die Ansprechrate als Hinweis dienen. Auf der ASCO im Mai/Juni gibt es nun erstmals Daten zum progressionsfreien Überleben (PFS) und zur Dauer des Ansprechens (DOR). Aber auch das sind nicht Plazebo kontrollierte Studienergebnisse.
Schut man sich die Richtlinien an, wird auch der Bedarf deutlich:
http://www.breastcancer.org/research-news/new-guidelines-to-…
Der Bearcase soll nicht verschwiegen werden:
Als Singleagent zeigt ONT380 kaum Wirksamkeit.
Bisher gibt es nur Singlearmtrials (also nicht Plazebo kontrolliert) und die Interpretation ist deshalb, besonders weil es sich um Kombinationen handelt, nicht möglich.
Die positiven Effekte gehen nicht auf ONT380 sondern auf die bereits bekannt wirksamen Kombinationspartner zurück. In Studien konnte auch ein Ansprechen bei CNS festgestellt werden.
Wer soll das eigentlich bezahlen, wenn drei Medikamente beteiligt sind?
ONTY braucht dringend Geld und wird in Kürze eine KE machen.
Aussichten zur ASCO von einem Analysten:

Am Chart sieht man, dass ONTY ziemlich Federn hat lassen müssen. Dafür war neben der allgemeinen Marktlage auch eine total verwirrende PR im Dezember verantwortlich. Die Daten waren aber im Endeffekt nicht schlechter als die zur ASCO2015. Zudem musste der alte CEO gehen, was ich als positiv werte.
Momentan ist ONTY mit 110 Mio$ bewertet. Das finde ich günstig und habe mir deshalb zu meiner Kernposition heute eine Tradingposition hinzu gekauft.
18.5. ASCO Release der Abstracts
3-7.6, ASCO
SG kmastra
Antwort auf Beitrag Nr.: 52.239.838 von kmastra am 21.04.16 00:44:05Hochriskant kmasta!
Das Ding hängt an einem Molekül.
Man kann jetzt eventuell damit rechnen, dass die beiden Combi Trials auch bald in P II gehen werden, und dass das etwas auftrieb gibt, aber letztlich ist das eine binäre Sache.
Das Ding ist ja nichtmal Ihr eigenes - haben es von Array reingeholt.
Wenigstens reicht das Cash noch für 2 Jahre.
Aber das sieht wie eine Casinowette aus.
Das Ding hängt an einem Molekül.
Man kann jetzt eventuell damit rechnen, dass die beiden Combi Trials auch bald in P II gehen werden, und dass das etwas auftrieb gibt, aber letztlich ist das eine binäre Sache.
Das Ding ist ja nichtmal Ihr eigenes - haben es von Array reingeholt.
Wenigstens reicht das Cash noch für 2 Jahre.
Aber das sieht wie eine Casinowette aus.
Antwort auf Beitrag Nr.: 52.261.447 von Troy1989 am 23.04.16 19:12:16Natürlich ist ein Invest in ONTY riskant. Ich denke ich habe das halbwegs differenziert dargestellt. Leider habe ich keine Kristallkugel. Mir gefällt das Chance/Risikoverhältnis trotzdem. Grundsätzlich sollte man eh ein Portfolio an Werten haben.
Siehst du ein Problem darin, dass das Molekül von ARRY entwickelt wurde?
Die erste PII ist übrigens bereits gestartet. Geld reicht m.E. vor diesem Hintergrund nicht mal mehr 2 Jahre...
Siehst du ein Problem darin, dass das Molekül von ARRY entwickelt wurde?
Die erste PII ist übrigens bereits gestartet. Geld reicht m.E. vor diesem Hintergrund nicht mal mehr 2 Jahre...
Antwort auf Beitrag Nr.: 52.261.861 von kmastra am 23.04.16 21:29:44Dann sehen wir uns mal die Perspektive von Array zu besagtem Molekül an:
"ONT-380 is an orally active, reversible and selective small-molecule HER2 inhibitor invented by Array and licensed to Oncothyreon for development, manufacturing and commercialization. The License Agreement replaces the prior Development and Collaboration Agreement under which Oncothyreon and Array were jointly developing ONT-380. As part of the License Agreement, Oncothyreon paid Array $20 million as an up-front fee. In addition, Oncothyreon will pay Array a significant portion of any payments received from sublicensing ONT-380 rights. If Oncothyreon is acquired within three years of the effective date of the current agreement, Array will be eligible for up to $280 million in commercial milestone payments. Array is also entitled to receive up to a double-digit royalty based on net sales of ONT-380."
http://www.arraybiopharma.com/product-pipeline/other-compoun…
Für Array ist das ganze eine Lapalie, für Oncothyreon ist es alles oder nichts.
Oben sind nur die Grundzüge des Agreements angeführt, und die sehen recht gut aus für Array. (zur Info: ich bin weder in Array, noch in Oncoythyreon, habe also kein Interesse hier etwas zu Pushen oder zu Bashen)
Wäre jetzt als Aktionär interessant zu wissen, was da genau drinsteht für ONTY und was sie bekommen, wenn es den klappt.
Markt.Kap ONTY liegt bei 113M
Array liegt bei 467M (bei einer Pipeline die sich gewaschen hat)
Wenn du von dem Molekül so begeistert bist, wieso muste es dann ONTY sein, und nicht Array, mit massenhaft Backups?
"ONT-380 is an orally active, reversible and selective small-molecule HER2 inhibitor invented by Array and licensed to Oncothyreon for development, manufacturing and commercialization. The License Agreement replaces the prior Development and Collaboration Agreement under which Oncothyreon and Array were jointly developing ONT-380. As part of the License Agreement, Oncothyreon paid Array $20 million as an up-front fee. In addition, Oncothyreon will pay Array a significant portion of any payments received from sublicensing ONT-380 rights. If Oncothyreon is acquired within three years of the effective date of the current agreement, Array will be eligible for up to $280 million in commercial milestone payments. Array is also entitled to receive up to a double-digit royalty based on net sales of ONT-380."
http://www.arraybiopharma.com/product-pipeline/other-compoun…
Für Array ist das ganze eine Lapalie, für Oncothyreon ist es alles oder nichts.
Oben sind nur die Grundzüge des Agreements angeführt, und die sehen recht gut aus für Array. (zur Info: ich bin weder in Array, noch in Oncoythyreon, habe also kein Interesse hier etwas zu Pushen oder zu Bashen)
Wäre jetzt als Aktionär interessant zu wissen, was da genau drinsteht für ONTY und was sie bekommen, wenn es den klappt.
Markt.Kap ONTY liegt bei 113M
Array liegt bei 467M (bei einer Pipeline die sich gewaschen hat)
Wenn du von dem Molekül so begeistert bist, wieso muste es dann ONTY sein, und nicht Array, mit massenhaft Backups?
Antwort auf Beitrag Nr.: 52.262.191 von Troy1989 am 24.04.16 01:11:49Ich habe überhaupt kein Problem damit, dass du anderer Meinung bist als ich, ganz im Gegenteil!
Abschließend:
Ich bin auch in ARRY investiert.
Ich sehe bei ONTY lediglich ein attraktives Chane/Risikoverhältnis und habe dieses dargestellt - Begeisterung hat an der Börse nichts zu suchen.
Abschließend:
Ich bin auch in ARRY investiert.
Ich sehe bei ONTY lediglich ein attraktives Chane/Risikoverhältnis und habe dieses dargestellt - Begeisterung hat an der Börse nichts zu suchen.
Exelixis
CABO hat US-Zulassung von der FDA erhalten u. heißt in der Verabreichungsform CABOMETYX.http://www.exelixis.com/investors-media/press-releases?cpurl…
Interessant sind die nun veröffentlichten OS-Daten:
As announced in February 2016, CABOMETYX also demonstrated a statistically significant and clinically meaningful increase in overall survival in the METEOR trial. Compared with everolimus, CABOMETYX was associated with a 34 percent reduction in the rate of death. Median overall survival was 21.4 months for patients receiving CABOMETYX versus 16.5 months for those receiving everolimus (HR=0.66, 95% CI 0.53-0.83, P=0.0003).
Opdivo hat m.e. OS von 5.4 Mon., HR=0.73 bei 25.0 Mon gegen 19.6 Vergleichsgruppe.
Studienübergreifend kann man schlecht vergleichen. Evtl. war bei CABO das Patientenkollektiv anspruchsvoller.
arry AZN Selumetinib
AstraZeneca's selumetinib an Orphan Drug for thyroid cancer http://seekingalpha.com/news/3182598-astrazenecas-selumetini…
array NEMO post IO
arry heute mit positiver Überraschung, dass sich das PFS durch Bini in NRAS Melanom in Patienten nach Immuntherapie deutlich verbessert. Eine interessante Wendung für die Abstimmung zwischen Immuntherapie und zielgerichteter Therapie.Gute Daten auch in der Phase II in BRAF+ Colon Cancer.
http://abstract.asco.org/176/IndexView_176.html
Abstract 9500 und 3544
Gute Performance, Gratuliere !
Den meisten Biotech-Fonds überlegen.
Den meisten Biotech-Fonds überlegen.

Antwort auf Beitrag Nr.: 51.923.973 von schnappi am 07.03.16 19:30:16Noch wer da 
Cidara habe ich nun auch im Depot.
Scheint so als hätten verschiedene Werte ein Boden gefunden vielleicht auch nur ein eindecken vor der ASCO.
STML hat gut zugelegt seid der Datenankündigung zur ASCO
CEMP kürzlich auch mit guten Nachrichten
RLYP profitiert nun hoffentlich auch mal Kursmäßig vom ersten scheitern von ZS-9

Cidara habe ich nun auch im Depot.
Scheint so als hätten verschiedene Werte ein Boden gefunden vielleicht auch nur ein eindecken vor der ASCO.
STML hat gut zugelegt seid der Datenankündigung zur ASCO
CEMP kürzlich auch mit guten Nachrichten
RLYP profitiert nun hoffentlich auch mal Kursmäßig vom ersten scheitern von ZS-9
Antwort auf Beitrag Nr.: 52.497.544 von schnappi am 29.05.16 15:23:10CDTX
In letzter Zeit einige Insider-Buys:
http://www.wkrb13.com/markets/1412376/insider-buying-cidara-…
Die Position der BB Biotech AG wurde auch Anfang des Jahres nochmals aufgestockt. Überlege auch, hier eine kleine Position zu eröffnen.
Viele Grüße
In letzter Zeit einige Insider-Buys:
http://www.wkrb13.com/markets/1412376/insider-buying-cidara-…
Die Position der BB Biotech AG wurde auch Anfang des Jahres nochmals aufgestockt. Überlege auch, hier eine kleine Position zu eröffnen.
Viele Grüße
Arry Phase III Colon Cancer
Array BioPharma, Pierre Fabre and Merck KGaA, Darmstadt, Germany Announce Phase 3 BEACON CRC Trialhttp://finance.yahoo.com/news/array-biopharma-pierre-fabre-m…
Konsequenter Schach-Zug bei den Phase II Daten.
A
arry Phase II Daten Colon Cancer BRAF+
Encorafenib-based Regimens Provide Improved PFS and OS in Difficult-to-Treat BRAF-Mutant Colorectal Cancer Compared to Historical Benchmarkshttp://finance.yahoo.com/news/encorafenib-based-regimens-imp…
"Data from this study suggest that median overall survival (OS) for these patients may exceed one year which is more than double historical published benchmarks for this population."
Das sollte den einen oder anderen überzeugen, dass es ein spektakulärer Deal war, Encorafenib (fast) geschenkt zu bekommen.
A
Schade Marinus (MRNS) P3 failed.
Marinus Pharmaceuticals announces ganaxolone did not meet the primary endpoint of demonstrating a statistically significant difference from placebo (shares halted) (MRNS) :
Co announced top-line results from its Phase 3 clinical trial in adults with drug-resistant focal onset seizures.
In this trial, ganaxolone did not meet the primary endpoint of demonstrating a statistically significant difference from placebo. Consistent with previously conducted studies, ganaxolone was generally safe and well tolerated.
Marinus plans to discontinue its program in adult focal onset seizures and focus its efforts on advancing ganaxolone in status epilepticus and pediatric orphan indications.
The study missed its primary endpoint of percent change in the 28-day seizure frequency from baseline (p=0.1537). The median percent reduction of focal onset seizures in the ganaxolone group was 21.28% compared to 10.25% with placebo during the titration and the 12-week treatment period.
Marinus will host a conference call today at 8:00 a.m. Eastern time.
Marinus Pharmaceuticals announces ganaxolone did not meet the primary endpoint of demonstrating a statistically significant difference from placebo (shares halted) (MRNS) :
Co announced top-line results from its Phase 3 clinical trial in adults with drug-resistant focal onset seizures.
In this trial, ganaxolone did not meet the primary endpoint of demonstrating a statistically significant difference from placebo. Consistent with previously conducted studies, ganaxolone was generally safe and well tolerated.
Marinus plans to discontinue its program in adult focal onset seizures and focus its efforts on advancing ganaxolone in status epilepticus and pediatric orphan indications.
The study missed its primary endpoint of percent change in the 28-day seizure frequency from baseline (p=0.1537). The median percent reduction of focal onset seizures in the ganaxolone group was 21.28% compared to 10.25% with placebo during the titration and the 12-week treatment period.
Marinus will host a conference call today at 8:00 a.m. Eastern time.
Antwort auf Beitrag Nr.: 52.607.249 von McNay am 13.06.16 20:39:42Ja das waren leider eine nicht so schöne Nachricht.
Habe seid gestern neu PRTK nach den guten Studienergebnissen sollte hier das Risiko überschaubar sein.
http://paratekpharma.com/
Schade das der Thread hier nicht mehr so genutzt wird mir fehlen die guten Beiträge von den Membern die Ahnung von der Materie haben.
Habe seid gestern neu PRTK nach den guten Studienergebnissen sollte hier das Risiko überschaubar sein.
http://paratekpharma.com/
Schade das der Thread hier nicht mehr so genutzt wird mir fehlen die guten Beiträge von den Membern die Ahnung von der Materie haben.

Gedanken in die Runde
hallo zusammen,wollte mal meine Gedanken in die Runde schmeissen.
hab grad so den Eindruck bzw. mich beschleicht das Gefühl, das viele Biotechs bald auf dem Ausrangierbahnhof stehen könnten in den nächsten paar Jahren.
Zumindest die, die sich nicht in die Richtung Immunotherapie und Gentherapie spezialisiert haben!
Hab die Vermutung, das einige Jetzt in der Entwicklungsphasen befindlichen Moleküle völlig überflüssig
werden durch ganz neue Ansätze und einen Paradigmen-Wechsel.
Liege ich hier völlig falsch???
Den evtl. Negativen Einfluss bei Wahl von Hilary in US mal aussen vor gelassen.
Das Sentiment hat sich um 180° gedreht, so empfinde ich es zumindest.
Bin selbst in einigen dick drinnen.
Was meint die Comunity dazu.
Gruss S.
Das lässt die Kurse im Moment steigen
MEDICARE `IPAB' COST PANEL NOT TRIGGERED THIS YEAR, U.S. SAYS
MEDICARE `IPAB' COST PANEL NOT TRIGGERED THIS YEAR, U.S. SAYS
Antwort auf Beitrag Nr.: 52.649.891 von Schaeffi am 19.06.16 19:30:39
Ich stelle mir die gleiche Frage. Man sieht ja schon an einigen Firmen, das selbst die Zulassung kein Garant ist, das der Kurs sich halbwegs positiv entwickelt.
Antworten wird es hier kaum noch geben - die Experten (ipollit, SLGraman) sind ja nicht mehr online.
Zitat von Schaeffi: hallo zusammen,
wollte mal meine Gedanken in die Runde schmeissen.
hab grad so den Eindruck bzw. mich beschleicht das Gefühl, das viele Biotechs bald auf dem Ausrangierbahnhof stehen könnten in den nächsten paar Jahren.
Zumindest die, die sich nicht in die Richtung Immunotherapie und Gentherapie spezialisiert haben!
Hab die Vermutung, das einige Jetzt in der Entwicklungsphasen befindlichen Moleküle völlig überflüssig
werden durch ganz neue Ansätze und einen Paradigmen-Wechsel.
Liege ich hier völlig falsch???
Den evtl. Negativen Einfluss bei Wahl von Hilary in US mal aussen vor gelassen.
Das Sentiment hat sich um 180° gedreht, so empfinde ich es zumindest.
Bin selbst in einigen dick drinnen.
Was meint die Comunity dazu.
Gruss S.
Ich stelle mir die gleiche Frage. Man sieht ja schon an einigen Firmen, das selbst die Zulassung kein Garant ist, das der Kurs sich halbwegs positiv entwickelt.
Antworten wird es hier kaum noch geben - die Experten (ipollit, SLGraman) sind ja nicht mehr online.
Ja. Leider ist momentan/in diesem Jahr mit einem reinen Biotech Depot (kaufen und liegen lassen) kein Geld zu verdienen.
Der BREXIT hat jetzt zusätzlich dazu geführt, dass der Nasdaq Biotech Index seinen zarten Aufwärtstrend gebrochen hat. Wichtig wäre nun, dass die Marke um 240 hält, ansonsten drohen weitere Kursverluste.

@Schaeffi: Da ist sicher was Wahres dran. Die Innovationszyklen werden immer kürzer. Das ist wohl die Schattenseite des Booms.
Ein weiterer Aspekt ist, dass viele Unternehmen sich auf die gleichen Indikationen und Ansätze spezialisiert haben, die zudem oft in Relation recht klein sind. Aber der Kuchen kann halt nur einmal verteilt werden.
http://www.forbes.com/sites/brucebooth/2016/06/22/immuno-onc…
Aber man darf natürlich nicht alle Unternehmen über einen Kamm scheren. Sind nicht viele Biotechs vom Chance Risiko Verhältnis momentan günstig? Nur müssen sie eben auch liefern. Und da gab leider eben auch viele Enttäuschungen in den letzten Wochen und Monaten (MRNS, CLVS, ZFGN...).
Haben alle Kandidaten viel Konkurrenz? Ich meine auch hier muss man differenzieren.
Ich bleibe deshalb bei Werten wie GNCA, ESPR, AUPH, ARRY dabei... SG kmastra
Der BREXIT hat jetzt zusätzlich dazu geführt, dass der Nasdaq Biotech Index seinen zarten Aufwärtstrend gebrochen hat. Wichtig wäre nun, dass die Marke um 240 hält, ansonsten drohen weitere Kursverluste.
@Schaeffi: Da ist sicher was Wahres dran. Die Innovationszyklen werden immer kürzer. Das ist wohl die Schattenseite des Booms.
Ein weiterer Aspekt ist, dass viele Unternehmen sich auf die gleichen Indikationen und Ansätze spezialisiert haben, die zudem oft in Relation recht klein sind. Aber der Kuchen kann halt nur einmal verteilt werden.
http://www.forbes.com/sites/brucebooth/2016/06/22/immuno-onc…
Aber man darf natürlich nicht alle Unternehmen über einen Kamm scheren. Sind nicht viele Biotechs vom Chance Risiko Verhältnis momentan günstig? Nur müssen sie eben auch liefern. Und da gab leider eben auch viele Enttäuschungen in den letzten Wochen und Monaten (MRNS, CLVS, ZFGN...).
Haben alle Kandidaten viel Konkurrenz? Ich meine auch hier muss man differenzieren.
Ich bleibe deshalb bei Werten wie GNCA, ESPR, AUPH, ARRY dabei... SG kmastra
ESPR habe ich heute mit 40% Verlust verkauft die haben zwar noch reichlich Geld aber zu ungewiss was weiter passiert.
Qure habe ich auch die Tage verkauft neu habe ich BB Biotech, REGN, und INCY
XNCR mach zum Glück mal Laune .
Qure habe ich auch die Tage verkauft neu habe ich BB Biotech, REGN, und INCY
XNCR mach zum Glück mal Laune .
Hatte hier wer TESARO dann mal Glückwunsch 

Antwort auf Beitrag Nr.: 52.724.944 von schnappi am 29.06.16 18:49:53Wieso ist Esperion so eingebrochen? Finde bei WO keine Nachricht dazu.
Antwort auf Beitrag Nr.: 52.735.450 von equinox10 am 30.06.16 20:11:22Eine "gute" Zusammenfassung dazu:
http://alanhobbes.blogspot.de/2016/06/on-june-28-2016-esperi…
Bitter! Das zeigt einmal mehr, wie komplex ein Investment in Biotech Aktien ist, denn bis dato gibt es keinerlei schlechte Studienergebnisse.
http://alanhobbes.blogspot.de/2016/06/on-june-28-2016-esperi…
Bitter! Das zeigt einmal mehr, wie komplex ein Investment in Biotech Aktien ist, denn bis dato gibt es keinerlei schlechte Studienergebnisse.
KPTI (Karyopharm Therapeutics)
- 52w Range: 4.83 - 27.68, aktuell 6.71 (RSI 30)
- Im Juni ohne negative News, auch infolge Brexit Panik um satte 30% gefallen und nicht wie die Märkte und der NBI in den letzten Tagen korrigiert
- Insider CHIONE LTD hat Mai und Juni 450'000 Aktien oder rund 5% des Pakets abgebaut
- Auch hat das Management bisher wesentlich mehr Aktien (zu Höchstkursen) verkauft als gekauft
Demgegenüber stehen einiges an Datenpaketen bis Ende Jahr und Kursziele welche wesentlich höher (USD 10.00 bis USD 20.00 im Schnitt)
Pump and Dump? Meinungen zu KPTI?
- 52w Range: 4.83 - 27.68, aktuell 6.71 (RSI 30)
- Im Juni ohne negative News, auch infolge Brexit Panik um satte 30% gefallen und nicht wie die Märkte und der NBI in den letzten Tagen korrigiert
- Insider CHIONE LTD hat Mai und Juni 450'000 Aktien oder rund 5% des Pakets abgebaut
- Auch hat das Management bisher wesentlich mehr Aktien (zu Höchstkursen) verkauft als gekauft
Demgegenüber stehen einiges an Datenpaketen bis Ende Jahr und Kursziele welche wesentlich höher (USD 10.00 bis USD 20.00 im Schnitt)
Pump and Dump? Meinungen zu KPTI?
Neben GNCA finde ich eigentlich AUPH mit am interessantesten. Beide sind sicherlich hoch riskant aber dafür auch attraktiv bewertet, wenn die Studienergebnisse in diesem Jahr gut sind.
Bei AUPH ist ein Investment sicherlich besonders riskant, weil es nur einen Kandidaten gibt und zudem das Geld fast alle ist (bei einer Bewertung von 100 Mio$). Im August sollen nun die "Sekt-oder-Selter" Ergebnisse der PIIb (AURA) bekannt gegeben werden. Parallel läuft eine kleinere Studie mit 10 Patienten (AURION). Das Update nach 24 Wochen fand ich jetzt nicht so richtig berauschend, weil zwar alle Patienten die bereits nach 8 Wochen als CR einzuschätzen waren weiterhin ansprachen, aber bei denjenigen, die nur als PR einzustufen waren kein zusätzlicher Effekt über die Zeit erkennbar war.
Hierzu ein guter Artikel:
http://seekingalpha.com/article/3986241-aurinia-pharmaceutic…
50% könnten in der AURION Studie ansprechen(10 Teilnehmer!). Die AURA Studie ist so ausgelegt, dass sie bei 41% ansprechen (bei 20% als Annahme im Placeboarm) signifikant wäre. Puh!
Mal sehen, ob eine high risk Studie auch mal wieder erfolgreich sein wird...
SG kmastra
Bei AUPH ist ein Investment sicherlich besonders riskant, weil es nur einen Kandidaten gibt und zudem das Geld fast alle ist (bei einer Bewertung von 100 Mio$). Im August sollen nun die "Sekt-oder-Selter" Ergebnisse der PIIb (AURA) bekannt gegeben werden. Parallel läuft eine kleinere Studie mit 10 Patienten (AURION). Das Update nach 24 Wochen fand ich jetzt nicht so richtig berauschend, weil zwar alle Patienten die bereits nach 8 Wochen als CR einzuschätzen waren weiterhin ansprachen, aber bei denjenigen, die nur als PR einzustufen waren kein zusätzlicher Effekt über die Zeit erkennbar war.
Hierzu ein guter Artikel:
http://seekingalpha.com/article/3986241-aurinia-pharmaceutic…
50% könnten in der AURION Studie ansprechen(10 Teilnehmer!). Die AURA Studie ist so ausgelegt, dass sie bei 41% ansprechen (bei 20% als Annahme im Placeboarm) signifikant wäre. Puh!
Mal sehen, ob eine high risk Studie auch mal wieder erfolgreich sein wird...
SG kmastra
Der Yahoo biotech Index wurde gestern geändert und es werden jetzt nicht mehr alle Companies angezeigt. Weiß einer von Euch eine ähnliche englischsprachige Seite. Die deutschen haben meist keine aktuellen News. Danke
Zafgen, Inc. $3.22* 3.53 -52.3%
Zafgen shuts down development of obesity drug, cuts staff | July 20, 2016 und wiedermal bitter für Aktionäre.
Die Misserfolge nehmen eher zu, oder ist das nur meine subjektive Sichtweise???
Zuletzt GALE
 heute Zafgen.
heute Zafgen.Zeigt mir, dass ich mit meiner Einschätzung auf dem richtigen Pfad bin.
Biotech wird immer schwieriger zu investieren.
habe aktuell nur noch:
IDRA
GILD
und dicke ONVO als Heilsbringer für die Pharmas/Biotechs

S.
Antwort auf Beitrag Nr.: 52.877.524 von Schaeffi am 20.07.16 21:09:53Ganz klares Jein!
Zum Ja:
Nachdem es gefühlt Jahre eigentlich in meinem Depot nur Erfolge gab, hat sich das Ganze seit einem Jahr gewendet. Da gab es doch einige Rückschläge bei Werten wie:
CLVS
ZFGN
ESPR
AERI
MRNS
...
Doch ich denke man darf nicht zu sehr verallgemeinern (Mensch neigt dazu) und sollte sich jeden Fall für sich anschauen.
Zum Nein:
Ich würde zunächst GALE nicht mit ZFGN in einen Topf werfen wollen. Zwar habe ich mich mit GALE nicht beschäftigt, aber das auch aus dem Grund, dass so ziemlich alle "Experten" vor dem Wert gewarnt haben.
ZFGN ist ein Wert von dem einige Experten sehr überzeugt waren und trotzdem ist der "Schuss nach Hinten losgegangen". Zwar war Beloratinib erstaunlich effektiv, jedoch hatte es schwere Nebenwirkungen, die letztlich zu dem Tod von zwei Menschen geführt haben. Das solche Nebenwirkungen auftauchen ist leider Teil des Riskos, auch wenn man bei ZFGN m.E. die Risken heruntergespielt und auch schlecht gemanagt hat. Ich finde es wenig erstaunlich, dass man die Entwicklung von B. jetzt eingestellt hat. Jetzt will man einen Wirkstoff auf gleichem Wirkprinzip weiter entwickeln! Für mich ist die Firma im Grunde wertlos, Cash hin oder her.
Zudem gibt es selbst im Biotech Bereich einige wenige aktuelle Erfolgsstorys wie EXEL, LGND. Und es wird auch in der Zukunft welche geben.
Insgesamt scheint der IBB momentan in einer Range von 240-290 seitwärts zu laufen. Mal sehen ob, wann und in welche Richtung diese verlassen wird. Ich persönlich denke mittlerweile, dass es bis in den Herbst hinein zumindest kein Überwinden nach Oben geben wird...

Die neue yahoo Seite scheint mir noch in einer Art Beta Version zu sein. Um sich zu informieren nutze ich seit längerem Twitter. Dort kann man sich über die wichtigsten News gut auf dem laufenden halten.
SG kmastra
Zum Ja:
Nachdem es gefühlt Jahre eigentlich in meinem Depot nur Erfolge gab, hat sich das Ganze seit einem Jahr gewendet. Da gab es doch einige Rückschläge bei Werten wie:
CLVS
ZFGN
ESPR
AERI
MRNS
...
Doch ich denke man darf nicht zu sehr verallgemeinern (Mensch neigt dazu) und sollte sich jeden Fall für sich anschauen.
Zum Nein:
Ich würde zunächst GALE nicht mit ZFGN in einen Topf werfen wollen. Zwar habe ich mich mit GALE nicht beschäftigt, aber das auch aus dem Grund, dass so ziemlich alle "Experten" vor dem Wert gewarnt haben.
ZFGN ist ein Wert von dem einige Experten sehr überzeugt waren und trotzdem ist der "Schuss nach Hinten losgegangen". Zwar war Beloratinib erstaunlich effektiv, jedoch hatte es schwere Nebenwirkungen, die letztlich zu dem Tod von zwei Menschen geführt haben. Das solche Nebenwirkungen auftauchen ist leider Teil des Riskos, auch wenn man bei ZFGN m.E. die Risken heruntergespielt und auch schlecht gemanagt hat. Ich finde es wenig erstaunlich, dass man die Entwicklung von B. jetzt eingestellt hat. Jetzt will man einen Wirkstoff auf gleichem Wirkprinzip weiter entwickeln! Für mich ist die Firma im Grunde wertlos, Cash hin oder her.
Zudem gibt es selbst im Biotech Bereich einige wenige aktuelle Erfolgsstorys wie EXEL, LGND. Und es wird auch in der Zukunft welche geben.
Insgesamt scheint der IBB momentan in einer Range von 240-290 seitwärts zu laufen. Mal sehen ob, wann und in welche Richtung diese verlassen wird. Ich persönlich denke mittlerweile, dass es bis in den Herbst hinein zumindest kein Überwinden nach Oben geben wird...
Die neue yahoo Seite scheint mir noch in einer Art Beta Version zu sein. Um sich zu informieren nutze ich seit längerem Twitter. Dort kann man sich über die wichtigsten News gut auf dem laufenden halten.
SG kmastra
Habe heute meine RLYP verkauft und einen Teil des Gewinns investiert,
IMGN
AFMD
ADAP
PRTK
ORPN
aufgestockt neu ist CTMX
IMGN
AFMD
ADAP
PRTK
ORPN
aufgestockt neu ist CTMX
Beitrag zu dieser Diskussion schreiben
Zu dieser Diskussion können keine Beiträge mehr verfasst werden, da der letzte Beitrag vor mehr als zwei Jahren verfasst wurde und die Diskussion daraufhin archiviert wurde.
Bitte wenden Sie sich an feedback@wallstreet-online.de und erfragen Sie die Reaktivierung der Diskussion oder starten Sie eine neue Diskussion.
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 55 | ||
| 52 | ||
| 47 | ||
| 44 | ||
| 34 | ||
| 16 | ||
| 12 | ||
| 11 | ||
| 10 | ||
| 10 |
| Wertpapier | Beiträge | |
|---|---|---|
| 10 | ||
| 10 | ||
| 10 | ||
| 10 | ||
| 9 | ||
| 9 | ||
| 8 | ||
| 8 | ||
| 8 | ||
| 8 |























