CytomX - ein bahnbrechender Ansatz in der Tumortherapie - 500 Beiträge pro Seite
eröffnet am 01.07.16 16:03:16 von
neuester Beitrag 27.01.24 11:32:06 von
neuester Beitrag 27.01.24 11:32:06 von
Beiträge: 1.459
ID: 1.234.534
ID: 1.234.534
Aufrufe heute: 0
Gesamt: 163.656
Gesamt: 163.656
Aktive User: 0
ISIN: US23284F1057 · WKN: A14158 · Symbol: 6C1
1,5320
EUR
+1,06 %
+0,0160 EUR
Letzter Kurs 30.04.24 Tradegate
Neuigkeiten
08.04.24 · globenewswire |
03.04.24 · globenewswire |
21.03.24 · globenewswire |
18.03.24 · globenewswire |
12.03.24 · wO Chartvergleich |
Werte aus der Branche Biotechnologie
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 0,5888 | +476,69 | |
| 1,8650 | +40,23 | |
| 1,7900 | +35,61 | |
| 3,9000 | +21,12 | |
| 7,9000 | +20,61 |
| Wertpapier | Kurs | Perf. % |
|---|---|---|
| 1,9600 | -19,67 | |
| 25,81 | -22,12 | |
| 5,1700 | -23,97 | |
| 3,5000 | -26,24 | |
| 0,5103 | -40,66 |
Ich hatte neulich in einem anderen Thread ein (bislang ungenanntes) Unternehmen erwähnt, dessen therapeutischer Ansatz möglicherweise das Potential hat, die Tumortherapie entscheidend voranzubringen. Mein Vorhaben, das Unternehmen gelegentlich ausführlicher vorzustellen, habe ich bislang jedoch wegen Zeitmangels leider nicht umsetzen können. Da sich ein Investment wirklich lohnen könnte und nicht abzusehen ist, wann es mir möglich sein wird, detailliertere Informationen ins Netz zu stellen, möchte ich wenigstens den Unternehmensnamen nennen, damit sich interessierte Forumsteilnehmer ggf. selbst vorab informieren können: Es handelt sich um CytomX, ein US-Biotech-Unternehmen, das sich darauf spezialisiert hat, therapeutische Antikörper und ADC´s so zu maskieren, dass sie im Idealfall - nach Abtrennung maskierender Peptidketten durch tumorspezifische Proteasen - nur im Tumorgewebe wirksam werden können, an gesundes Gewebe infolge ihrer Maskierung jedoch nicht binden. Präklinisch hat sich das Konzept bereits bewährt, die erste klinische Studie müsste in Kürze starten. Kooperationspartner, die gemeinsam mit CytomX entsprechende "Probodys" entwickeln möchten, gibt es auch bereits, darunter AbbVie, Bristol-Myers Squibb, ImmunoGen und Pfizer. Die Börsenkapitalisierung beträgt derzeit 368 Mio. USD, der Unternehmenswert angesichts der NetCash-Position (182 Mio. USD) gerade mal 187 Mio. USD. Die Aktie notiert aktuell unter Ausgabewert (Börsengang war im November 2015), aus meiner Sicht bietet dies eine interessante Einstiegsgelegenheit. Handel an der Nasdaq (ob in Deutschland möglich, weiß ich nicht), wegen der relativen Marktenge sollte man nicht ohne Limits arbeiten.
Antwort auf Beitrag Nr.: 52.743.319 von Joschka Schröder am 01.07.16 16:03:16Sorry, NetCash natürlich 181 Mio. USD, dieser Betrag sollte in jedem Fall bis Ende 2018 ausreichen, um die umfangreichen F&E-Aktivitäten vollumfänglich zu finanzieren.
In der Pipeline befinden sich u.a. ein maskierter PD-L1 checkpoint-Inhibitor und ein maskiertes anti-CD166-Immunkonjugat (CD166 kann mit konventionellen ADC´s nicht angesteuert werden, weil CD166 in größerem Umfang auch von gesundem Gewebe exprimiert wird).
Grundsätzlich kann die Probody-Technik zur Maskierung therapeutischer Antikörper (konventionell, bi- oder trispezifisch), Antikörper-Toxin-Konjugate und CAR-Therapeutika eingesetzt werden kann. Eigentlich sollte die Probody-Technik in der Lage sein, das Wirkungs-/Nebenwirkungsprofil eines jeden in der Onkologie eingesetzten Biotherapeutikums entscheidend zu verbessern.
Entscheidend ist nun, dass das Probody-Konzept in der Klinik das erfüllt, was es gemäß Theorie und Präklinik verspricht.
In Investorenkreisen ist CytomX weitgehend unbekannt, in Internetforen wird man dazu vermutlich kaum etwas finden. Nach Beginn der klinischen Studien (Start in Q3 2016) dürfte sich dies jedoch ändern.
In der Pipeline befinden sich u.a. ein maskierter PD-L1 checkpoint-Inhibitor und ein maskiertes anti-CD166-Immunkonjugat (CD166 kann mit konventionellen ADC´s nicht angesteuert werden, weil CD166 in größerem Umfang auch von gesundem Gewebe exprimiert wird).
Grundsätzlich kann die Probody-Technik zur Maskierung therapeutischer Antikörper (konventionell, bi- oder trispezifisch), Antikörper-Toxin-Konjugate und CAR-Therapeutika eingesetzt werden kann. Eigentlich sollte die Probody-Technik in der Lage sein, das Wirkungs-/Nebenwirkungsprofil eines jeden in der Onkologie eingesetzten Biotherapeutikums entscheidend zu verbessern.
Entscheidend ist nun, dass das Probody-Konzept in der Klinik das erfüllt, was es gemäß Theorie und Präklinik verspricht.
In Investorenkreisen ist CytomX weitgehend unbekannt, in Internetforen wird man dazu vermutlich kaum etwas finden. Nach Beginn der klinischen Studien (Start in Q3 2016) dürfte sich dies jedoch ändern.
Handel in Deutschland nur Frankfurt wie ich gesehen habe.
Habe veranlasst dass die WKN an den Thread angehängt wird. Dürfte im Laufe des Tages erledigt werden.
Werde einmal mitlesen sollten sich andere User zu Wort melden.
Habe veranlasst dass die WKN an den Thread angehängt wird. Dürfte im Laufe des Tages erledigt werden.
Werde einmal mitlesen sollten sich andere User zu Wort melden.
Nach den jüngsten nebenwirkungsbedingen Todesfällen in Junos ROCKET-Leukämiestudie, die in der vergangenen Woche von der FDA gestoppt worden ist, gerät nun die gesamte chimeric antigen receptor T cell (CAR-T)-Therapie unter Druck und wird von der FDA eingehend analysiert.
Einen Ausweg könnte auch hier die Probody-Technologie der CytomX Therapeutics bieten, die für eine Maskierung des chimären Antigen-Rezeptors in gesundem Gewebe konzipiert worden ist (die Demaskierung erfolgt erst im Tumorgewebe mit Hilfe Tumorspezifischer Enzyme). CytomX kooperiert auf diesem Gebiet mit dem MD Anderson Cancer Center.
"NK cells are cytotoxic lymphocytes in the innate immune system that play a key role in defending the body. When these cells are coupled with CARs to target proteins found on cancer cells, they create a powerful therapy and an attractive alternative to CAR T-cell therapies. By combining the promise of CAR-NK cell therapies with the added safety of the Probody technology, CytomX looks to create safer and more effective therapies that realize the full potential of the therapeutic class. CytomX is collaborating with MD Anderson Cancer Center in research around this promising field, leveraging the institution’s expertise in creating durable NK cell therapies."
Einen Ausweg könnte auch hier die Probody-Technologie der CytomX Therapeutics bieten, die für eine Maskierung des chimären Antigen-Rezeptors in gesundem Gewebe konzipiert worden ist (die Demaskierung erfolgt erst im Tumorgewebe mit Hilfe Tumorspezifischer Enzyme). CytomX kooperiert auf diesem Gebiet mit dem MD Anderson Cancer Center.
"NK cells are cytotoxic lymphocytes in the innate immune system that play a key role in defending the body. When these cells are coupled with CARs to target proteins found on cancer cells, they create a powerful therapy and an attractive alternative to CAR T-cell therapies. By combining the promise of CAR-NK cell therapies with the added safety of the Probody technology, CytomX looks to create safer and more effective therapies that realize the full potential of the therapeutic class. CytomX is collaborating with MD Anderson Cancer Center in research around this promising field, leveraging the institution’s expertise in creating durable NK cell therapies."
Die Zahlen bin mit kleiner Posi hier auch dabei
http://seekingalpha.com/pr/16568166-cytomx-announces-second-…
http://seekingalpha.com/pr/16568166-cytomx-announces-second-…
!
Dieser Beitrag wurde von CloudMOD moderiert. Grund: auf eigenen Wunsch des Users
Antwort auf Beitrag Nr.: 52.985.593 von Joschka Schröder am 04.08.16 01:35:29Den letzten Beitrag habe ich versehentlich zu früh abgeschickt, deshalb noch einmal in vernünftiger Form:
Erfreuliche Entwicklungen bei CytomX. Ausbau der NetCash-Position durch Upfront- und Meilensteinzahlungen von 185,7 Mio. USD zum 31.12.15 auf 195,8 Mio. USD zum 30.6.16. Die Produktentwicklungen schreiten mit gutem Tempo voran. Der anti-PD-L1-Probody CX-072 steht unmittelbar vor dem Eintritt in die klinische Studienphase und soll gleich in Kombinationstherapien mit Yervoy (ipilimumab)/BMS or Zelboraf (vemurafenib)/Roche getestet werden. Konventionelle anti-PD1-Antikörper wie nivolumab und pembrolizumab oder anti-PD-L1-Antikörper wie atezolizumab und durvalumab lassen sich nur schwerlich in Kombination mit ipilimumab und vemurafenib verabreichen, weil das Nebenwirkungsprofil zu schaurig ist. Dieses Problem könnte durch die Maskierung der FAB-Region des CX-072 behoben werden.
Die Entwicklung des maskierten anti-CD166-ADC´s liegt ebenfalls voll im Plan. Außerdem wird es 2017 und 2018 mehrere klinische Studieneintritte aus Kooperationen mit großen Pharmakonzernen wie BMS, AbbVie und Pfizer geben.
Bis 2017 sollte der Börsenkurs deutlich anziehen, weil ab 2017 mit ersten klinischen Studiendaten zu rechnen ist.
Erfreuliche Entwicklungen bei CytomX. Ausbau der NetCash-Position durch Upfront- und Meilensteinzahlungen von 185,7 Mio. USD zum 31.12.15 auf 195,8 Mio. USD zum 30.6.16. Die Produktentwicklungen schreiten mit gutem Tempo voran. Der anti-PD-L1-Probody CX-072 steht unmittelbar vor dem Eintritt in die klinische Studienphase und soll gleich in Kombinationstherapien mit Yervoy (ipilimumab)/BMS or Zelboraf (vemurafenib)/Roche getestet werden. Konventionelle anti-PD1-Antikörper wie nivolumab und pembrolizumab oder anti-PD-L1-Antikörper wie atezolizumab und durvalumab lassen sich nur schwerlich in Kombination mit ipilimumab und vemurafenib verabreichen, weil das Nebenwirkungsprofil zu schaurig ist. Dieses Problem könnte durch die Maskierung der FAB-Region des CX-072 behoben werden.
Die Entwicklung des maskierten anti-CD166-ADC´s liegt ebenfalls voll im Plan. Außerdem wird es 2017 und 2018 mehrere klinische Studieneintritte aus Kooperationen mit großen Pharmakonzernen wie BMS, AbbVie und Pfizer geben.
Bis 2017 sollte der Börsenkurs deutlich anziehen, weil ab 2017 mit ersten klinischen Studiendaten zu rechnen ist.
Heute gab es schon mal eine erste kleine Aufwärtsbewegung des Aktienkurses um 7,5 % auf 11,37 USD. Dabei dürfte der Studienflopp des anti-PD1-Antikörpers nivolumab (BMS) in der Lungen-CA-Studie (Indikation "advanced non-small cell lung cancer") von wesentlicher Bedeutung gewesen sein. BMS setzt nun vorerst ersatzweise alle Hoffnung in eine Kombinationstherapie mit nivolumab und dem anti-CTLA-4-Antikörper ipilimumab.
Ich denke schon, dass eine derartige Kombinationsbehandlung wirksam sein wird, NUR ... das Nebenwirkungsprofil wird aller Wahrscheinlichkeit nach nicht akzeptabel sein. In früheren Kombistudien mit nivolumab und ipilimumab, die in der Indikation "malignes Melanom" durchgeführt worden sind, sind bei 55 % aller Patienten Nebenwirkungen der Grade 3 und 4 aufgetreten, bei 36 % der Patienten mußten die Studien wegen der Nebenwirkungen sogar abgebrochen werden.
Derartige Probleme ließen sich vermutlich durch die Maskierung der FAB-Segmente der threapeutischen Antikörper mittels der Probody-Technologie umgehen (im Tierversuch hat das bereits prima funktioniert). CytomX wird deshalb in Kürze seinen maskierten anti-PD-L1-Antikörper CX-072 in die Klinik bringen. Gleichzeitig arbeitet BMS - ebenfalls mit CytomX´s Probody-Technologie - an der Maskierung eines eigenen anti-CTLA-4-Antikörpers. Mit der Kombination derartiger Probodys sollte eine gleich wirksame Tumortherapie möglich sein, ohne dass jedoch die gefürchteten Nebenwirkungen konventioneller Immuntherapeutika auftreten.
Hinsichtlich meines CytomX-Investments bin ich weiterhin hoffnungsvoll.
Ich denke schon, dass eine derartige Kombinationsbehandlung wirksam sein wird, NUR ... das Nebenwirkungsprofil wird aller Wahrscheinlichkeit nach nicht akzeptabel sein. In früheren Kombistudien mit nivolumab und ipilimumab, die in der Indikation "malignes Melanom" durchgeführt worden sind, sind bei 55 % aller Patienten Nebenwirkungen der Grade 3 und 4 aufgetreten, bei 36 % der Patienten mußten die Studien wegen der Nebenwirkungen sogar abgebrochen werden.
Derartige Probleme ließen sich vermutlich durch die Maskierung der FAB-Segmente der threapeutischen Antikörper mittels der Probody-Technologie umgehen (im Tierversuch hat das bereits prima funktioniert). CytomX wird deshalb in Kürze seinen maskierten anti-PD-L1-Antikörper CX-072 in die Klinik bringen. Gleichzeitig arbeitet BMS - ebenfalls mit CytomX´s Probody-Technologie - an der Maskierung eines eigenen anti-CTLA-4-Antikörpers. Mit der Kombination derartiger Probodys sollte eine gleich wirksame Tumortherapie möglich sein, ohne dass jedoch die gefürchteten Nebenwirkungen konventioneller Immuntherapeutika auftreten.
Hinsichtlich meines CytomX-Investments bin ich weiterhin hoffnungsvoll.
Gestern Abend habe ich mich mit einigen aktuellen Entwicklungsarbeiten von CytomX beschäftigt, darunter folgendes interessantes Projekt: Es handelt sich um einen maskierten Antikörper gegen löslichen IL-6-Rezeptor. Je nach Linker kann der Antikörper bei Tumorerkrankungen oder bei entzündlichen Erkrankungen (wie z.B. der rheumatoiden Arthritis) eingesetzt werden. Kurz zur Erklärung: Der Linker stellt das Verbindungsteil zwischen dem Antikörper und dessen Maskierung (= Polypeptidkette, die die FAB-Fragmente, also die spezifischen Bindungsstellen des Antikörpers, verdeckt ... um den Sachverhalt leicht verständlich darzustellen). Dieser Linker wird am gewünschten Zielort (Tumor, entzündliche Synovia o.ä.) durch spezifische Enzyme gespalten, so dass die Bindungsstellen des Antikörpers freigelegt werden und der Antkörper am gewünschten Ort mit dem Zielmolekül eine Verbindung eingehen kann. Im gesunden Gewebe bleibt der Antikörper hingegen maskiert, so dass etwaige Nebenwirkungen minimiert werden. Für die Tumorindikation nimmt man einen Linker, der speziell durch tumorspezifische Peptidasen gespalten wird, bei Autoimmunerkrankungen z.B. einen Linker, der durch bestimmte Enzyme gespalten wird, die sich hochkonzentriert in entzündlichem Milieu finden. Die CytmoX´s Maskierungstechnologie ist konzeptionell so einfach wie genial. Der erste Klinikgang steht nun unmittelbar bevor, auf die Ergebnisse der klinschen Studien bin ich gespannt.
Mit dem Eintritt in die Klinik sollte auch der Bekanntheitsgrad des Unternehmens deutlich zunehmen ... vielleicht bin ich dann irgendwann auch nicht mehr ein Alleinunterhalter.
Mit dem Eintritt in die Klinik sollte auch der Bekanntheitsgrad des Unternehmens deutlich zunehmen ... vielleicht bin ich dann irgendwann auch nicht mehr ein Alleinunterhalter.
Antwort auf Beitrag Nr.: 53.125.233 von Joschka Schröder am 24.08.16 10:58:02Unternehmen ohne laufende Studie und ohne deren Ergebnisse (zunächst ja P1) wird aktuell einfach nicht viel an Wert zugestanden, Notierungen um den Cashbestand oder darunter sind da ja häufig, von daher ist in dieser Hinsicht der Titel gar nicht so günstig, relativ gesehen... In der Theorie und vom wissenschaftlichen Ansatz sieht zB Ohad Hammer den du sicher auch kennst/liest eine LIFE (atyr Pharma) als extrem aussichtsreich (und riskant, da noch dehr wenige Daten vorliegen) an, die notieren auch um den Cashbestand... in so frühen Phasen brauchen die Firmen halt in Zukunft auch noch viel Geld, was idR Verwässerung bedeutet, somit relativiert sich die vermeintlich günstige Bewertung auch... lese aber sehr gerne deine Beiträge, vielen Dank für den immer interessanten und fundierten Input
Antwort auf Beitrag Nr.: 53.125.233 von Joschka Schröder am 24.08.16 10:58:02ich schließe mich SpanishEyes an
Deine Beiträge lese ich auch sehr gerne und vielleicht besser weniger Beiträge aber dafür fachliche gute.
@ Joschka hast du dir schon einmal http://www.regenxbio.com/index.htm angesehen was ich so als Laie gelesen habe fand ich interessant.
Deine Beiträge lese ich auch sehr gerne und vielleicht besser weniger Beiträge aber dafür fachliche gute.
@ Joschka hast du dir schon einmal http://www.regenxbio.com/index.htm angesehen was ich so als Laie gelesen habe fand ich interessant.
Antwort auf Beitrag Nr.: 53.126.823 von schnappi am 24.08.16 13:48:02@schnappi
Gentherapien, ein interessantes Thema ... da überblick ich aber nicht den Markt. Insoweit kann ich zu REGENXBIO leider nichts Fundiertes schreiben.
Gentherapien, ein interessantes Thema ... da überblick ich aber nicht den Markt. Insoweit kann ich zu REGENXBIO leider nichts Fundiertes schreiben.
Antwort auf Beitrag Nr.: 53.126.016 von SpanishEyes am 24.08.16 12:22:28
Wenn die Börsenbewertung in etwa dem (Netto-)Cashbestand entspricht, bedeutet das ja nichts anderes, als dass dem Unternehmen zu diesem Zeitpunkt - stichtags- und substanzbezogen - ein Unternehmenswert Null zugestanden wird. Wenn es sich um ein aussichtsreiches wissenschaftliches Konzept handelt, wäre das eine exzellente Einstiegsmöglichkeit. Man könnte quasi umsonst Teilhaber der gesamten intellektuellen und experimentellen Vorarbeiten werden.
Da ein Kleinaktionär dem Unternehmen dessen liquide Mittel nicht entziehen kann, besteht das einzige Risiko darin, dass man sich mit dem Aktienkauf quasi verpflichtet, den Gegenwert des investierten Kapitals in künftige F&E zu stecken. Was bislang an F&E gelaufen ist, bekommt man aber gleichsam geschenkt.
Zitat von SpanishEyes: Unternehmen ohne laufende Studie und ohne deren Ergebnisse (zunächst ja P1) wird aktuell einfach nicht viel an Wert zugestanden, Notierungen um den Cashbestand oder darunter sind da ja häufig, von daher ist in dieser Hinsicht der Titel gar nicht so günstig, relativ gesehen... In der Theorie und vom wissenschaftlichen Ansatz sieht zB Ohad Hammer den du sicher auch kennst/liest eine LIFE (atyr Pharma) als extrem aussichtsreich (und riskant, da noch dehr wenige Daten vorliegen) an, die notieren auch um den Cashbestand... in so frühen Phasen brauchen die Firmen halt in Zukunft auch noch viel Geld, was idR Verwässerung bedeutet, somit relativiert sich die vermeintlich günstige Bewertung auch... lese aber sehr gerne deine Beiträge, vielen Dank für den immer interessanten und fundierten Input
Wenn die Börsenbewertung in etwa dem (Netto-)Cashbestand entspricht, bedeutet das ja nichts anderes, als dass dem Unternehmen zu diesem Zeitpunkt - stichtags- und substanzbezogen - ein Unternehmenswert Null zugestanden wird. Wenn es sich um ein aussichtsreiches wissenschaftliches Konzept handelt, wäre das eine exzellente Einstiegsmöglichkeit. Man könnte quasi umsonst Teilhaber der gesamten intellektuellen und experimentellen Vorarbeiten werden.
Da ein Kleinaktionär dem Unternehmen dessen liquide Mittel nicht entziehen kann, besteht das einzige Risiko darin, dass man sich mit dem Aktienkauf quasi verpflichtet, den Gegenwert des investierten Kapitals in künftige F&E zu stecken. Was bislang an F&E gelaufen ist, bekommt man aber gleichsam geschenkt.
Hillary Clinton hat mit ihrem gestrigen Twitter-Beitrag ( -> https://twitter.com/HillaryClinton/status/768508732623970304 ) den gesamten Pharma-/Biotech-Markt auf Talfahrt geschickt.
Inhaltlich hat sie mit ihrer Kritik absolut recht, 600 USD für eine EpiPen-Doppelpackung sind ein wahnwitziger Preis, zumal der Wirkstoff nicht patentgeschützt ist. Andererseits hat Clintons Kritiik nichts mit der Preisfestsetzung innovativer Biotherapeutika zu tun.
(Auch dort muss man sich natürlich fragen, wie die Gesellschaft den medizinischen Fortschritt weiter finanzieren möchte und was sie z.B. für die Verlängerung des progressionsfreien Überlebens eines 80jährigen um wenige Monate zu zahlen bereit ist. Diesen wenig angenehmen Fragen wird man auf Dauer nicht ausweichen können. Für wirkliche Innovationen werden jedoch auch in Zukunft angemessene Preise bezahlt werden, weil man den Pharmabetrieb andernfalls stillllegen könnte.)
Insoweit erscheint die aktuelle Börsenreaktion, bei der alle im Pharmasektor tätigen Unternehmen über einen Kamm geschoren werden, - wie vieles an der Börse - deutlich zu undifferenziert. Man sollte schon noch unterscheiden, ob ein Unternehmen z.B. Generika oder rezeptfreie Medikamente o.ä. produziert oder ob es sich um ein hochinnovatives Technologieunternehmen handelt. Na ja, die hysterischen Märkte werden sich schon wieder beruhigen.
Inhaltlich hat sie mit ihrer Kritik absolut recht, 600 USD für eine EpiPen-Doppelpackung sind ein wahnwitziger Preis, zumal der Wirkstoff nicht patentgeschützt ist. Andererseits hat Clintons Kritiik nichts mit der Preisfestsetzung innovativer Biotherapeutika zu tun.
(Auch dort muss man sich natürlich fragen, wie die Gesellschaft den medizinischen Fortschritt weiter finanzieren möchte und was sie z.B. für die Verlängerung des progressionsfreien Überlebens eines 80jährigen um wenige Monate zu zahlen bereit ist. Diesen wenig angenehmen Fragen wird man auf Dauer nicht ausweichen können. Für wirkliche Innovationen werden jedoch auch in Zukunft angemessene Preise bezahlt werden, weil man den Pharmabetrieb andernfalls stillllegen könnte.)
Insoweit erscheint die aktuelle Börsenreaktion, bei der alle im Pharmasektor tätigen Unternehmen über einen Kamm geschoren werden, - wie vieles an der Börse - deutlich zu undifferenziert. Man sollte schon noch unterscheiden, ob ein Unternehmen z.B. Generika oder rezeptfreie Medikamente o.ä. produziert oder ob es sich um ein hochinnovatives Technologieunternehmen handelt. Na ja, die hysterischen Märkte werden sich schon wieder beruhigen.
Danke Joschka für den Thread.
Bis zu den ersten Hinweisen und dem PoC ist es ja leider noch eine Weile hin.
Der Ansatz von CTMX selbst klingt too good to be true, wenn das funktioniert, dann KABOOM.
Bin seit Juni dabei...
Bis zu den ersten Hinweisen und dem PoC ist es ja leider noch eine Weile hin.
Der Ansatz von CTMX selbst klingt too good to be true, wenn das funktioniert, dann KABOOM.
Bin seit Juni dabei...
Antwort auf Beitrag Nr.: 53.161.455 von Ville7 am 29.08.16 20:18:14Guter Zeitpunkt Juni,
da hast du ja die tiefs gekauft!
da hast du ja die tiefs gekauft!
Auch von mir herzlichen Dank für den Thread.
Auf der Homepage wurde inzwischen eine neue Unternehmenspräsentation (Stand August 2016) eingestellt.
Im Vergleich zur Vorgängerversion (ich glaube aus Mai 2016) hat diese meiner Meinung nach qualitativ und quantitativ massiv hinzugewonnen, wenngleich auch in der Zwischenzeit keine "big news" veröffentlicht wurden.
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-irhome
Auf der Homepage wurde inzwischen eine neue Unternehmenspräsentation (Stand August 2016) eingestellt.
Im Vergleich zur Vorgängerversion (ich glaube aus Mai 2016) hat diese meiner Meinung nach qualitativ und quantitativ massiv hinzugewonnen, wenngleich auch in der Zwischenzeit keine "big news" veröffentlicht wurden.
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-irhome
Antwort auf Beitrag Nr.: 53.161.875 von schnappi am 29.08.16 21:19:09Mit der Ansage eines Tiefs bin ich immer sehr vorsichtig....

Schöne Kursentwicklung bei meinem Biotech-Favoriten CytomX. Aktuell +10 % auf 13,29 USD. Gegenüber meinem Einstandskurs ist das ein Plus von über 30 %. Wenn die Sache wie gewünscht ausgeht, könnte sich der Aktienkurs insgesamt verhundertfachen (ich weiß, das klingt bescheuert). Das Prinzip der Antikörpermaskierung ist so simpel wie genial, die Umsetzung aber keineswegs trivial. CytomX könnte sie gelungen sein. Die Präklinik spricht dafür. Während ich diese Zeilen geschrieben habe, ist der Kurs auf weiter auf 13,43 USD gestiegen.
Die Gewinne konnten nicht ganz gehalten werden. Bin auch sehr zufrieden über den bisherigen Kursverlauf.
Irgendwo zwischen Verzehn- bis Verhundertfachung könnte drin sein, aber nur, wenn alles wirklich "as planned" auch im Menschen funktioniert.
Chance extrem gut, aber Risiko ist natürlich auch sehr hoch, da man zwar die sehr guten präklinischen Daten gezeigt bekam (bzw. was die Firma dazu veröffentlichen wollte), aber zwischen Präklinik und Klinik es noch entscheidende Unterschiede und Stolpersteine geben kann, die dann leider auch nicht allzu selten eintreten.
Daher bin ich extrem gespannt auf dann erste Wirksamkeitshinweise im Menschen, die es hoffentlich ab 2017 geben sollte (aber zunächst mal muss der erste AK übnerhaupt in die Klinik!). Sollte sich da abzeichnen, dass die "Maskierung" einen positiven Effekt auf die Sicherheit hat ohne dass die Wirksamkeit (zu sehr) beschnitten wird wird das Teil in einer ersten Raketenstufe abgehen wie Schnitzel.
Irgendwo zwischen Verzehn- bis Verhundertfachung könnte drin sein, aber nur, wenn alles wirklich "as planned" auch im Menschen funktioniert.
Chance extrem gut, aber Risiko ist natürlich auch sehr hoch, da man zwar die sehr guten präklinischen Daten gezeigt bekam (bzw. was die Firma dazu veröffentlichen wollte), aber zwischen Präklinik und Klinik es noch entscheidende Unterschiede und Stolpersteine geben kann, die dann leider auch nicht allzu selten eintreten.
Daher bin ich extrem gespannt auf dann erste Wirksamkeitshinweise im Menschen, die es hoffentlich ab 2017 geben sollte (aber zunächst mal muss der erste AK übnerhaupt in die Klinik!). Sollte sich da abzeichnen, dass die "Maskierung" einen positiven Effekt auf die Sicherheit hat ohne dass die Wirksamkeit (zu sehr) beschnitten wird wird das Teil in einer ersten Raketenstufe abgehen wie Schnitzel.
Antwort auf Beitrag Nr.: 53.221.779 von Ville7 am 07.09.16 00:04:09Ich sehe das ähnlich. Kurz vor Publikation der ersten Studienergebnisse wird es eine besondere Herausforderung sein, sich auf einen "angemessenen" Depotanteil festzulegen, insbesondere wenn bis dahin der Kurs stark gestiegen und die allgemeine Erwartungshaltung entsprechend hoch sein sollten. Derzeit befindet sich das Unternehmen noch außerhalb des Radars der großen Anlegergemeinde, so dass das Investment keine Nerven kostet und eigentlich schon aus markttechnischen Gründen weitere Kursanstiege zu erwarten sind. Schwieriger wird´s im nächsten Jahr: Man kann noch so viele Patente lesen und mit den Verantwortlichen Detailfragen diskutieren, Unwägbarkeiten gibt es immer, wenn ein Präparat am Menschen angewandt wird. Ich versuche schon jetzt, mich mental auf die bevorstehenden Situationen vorzubereiten ... soweit dies überhaupt möglich ist.
Antwort auf Beitrag Nr.: 53.221.998 von Joschka Schröder am 07.09.16 02:01:41Ja, da hast du Recht. Falls das hier wirklich was wird werde ich dir ewig dankbar für deinen Tipp sein.
Ich habe die Hoffnung, dass wir mit unserem Einstiegszeitpunkt in einer komfortablen Situation sind und auch im totalen Rückschlagsfalle derart aus der Geschichte rauskommen, dass wir keinen Totalverlust erleiden. Denn ich hoffe dass der Kurs sich bis zu den ersten Studiendaten noch verzwei/dreifacht. Wenn es dann schlechte Daten gibt wäre ein 50-80% Haircut auf 5-10 USD denkbar. Dann darf man dann nicht lange fackeln und muss sehr schnell rausgehen, wenn man für sich analysiert hat, dass es an der Technologie liegt und ein generelles Problem vorliegt, das die Technologie zum Scheitern verurteilt.
Ich habe die Hoffnung, dass wir mit unserem Einstiegszeitpunkt in einer komfortablen Situation sind und auch im totalen Rückschlagsfalle derart aus der Geschichte rauskommen, dass wir keinen Totalverlust erleiden. Denn ich hoffe dass der Kurs sich bis zu den ersten Studiendaten noch verzwei/dreifacht. Wenn es dann schlechte Daten gibt wäre ein 50-80% Haircut auf 5-10 USD denkbar. Dann darf man dann nicht lange fackeln und muss sehr schnell rausgehen, wenn man für sich analysiert hat, dass es an der Technologie liegt und ein generelles Problem vorliegt, das die Technologie zum Scheitern verurteilt.
Läuft ja sehr schön! Hatte eine erste Position bei knapp 13usd genommen (nachdem ich als interessierter Laie besser verstanden habe wo hier das Potential liegt) und gehofft nochmal bei um die 10 zum zug zu kommen... bislang ist der gesamtmarkt und die aktie im speziellen aber offenbar noch nicht bereit zu einer korrektur...
Nach dem Verfallstag am Freitag kann die Richtung eventuell neu bestimmt werden.
Allerdings gehe ich davon aus, dass bei einem IND eines Cytomx PD-(L)1, der noch dieses Jahr anstehen soll, der Kurs durch die mediale Aufmerksamkeit wieder bei USD 20 steht...aber reine Spekulation.
Allerdings gehe ich davon aus, dass bei einem IND eines Cytomx PD-(L)1, der noch dieses Jahr anstehen soll, der Kurs durch die mediale Aufmerksamkeit wieder bei USD 20 steht...aber reine Spekulation.
Der Kurs kennt im Moment nur eine Richtung schon etwas unheimlich 
Hier mal noch eine September Präsentation
http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9N…

Hier mal noch eine September Präsentation
http://phx.corporate-ir.net/External.File?item=UGFyZW50SUQ9N…
Antwort auf Beitrag Nr.: 53.314.773 von schnappi am 20.09.16 21:32:30Die Präsentation ist wirklich gelungen, sie bringt die wesentlichen Dinge auf den Punkt.
Auf der Suche nach Investitionsmöglichkeiten begegnet man nur alle zig Jahre Unternehmen, denen zuzutrauen ist, einen Lebensbereich oder Wirtschaftszweig grundlegend zu verändern. Entsprechend groß ist - bei allen Risiken - das Kurspotential.
Nachdem der Kurs während der vergangenen drei Monate um über 70 % gestiegen ist (aktuell
17,19 USD), würde mich eine Konsolidierung nicht überraschen. Sollten die klinischen Studien die Ergebnisse der Präklinik annähernd bestätigen, müßte sich der Kurs auf längere Sicht aber vervielfachen (Enterprise Value dann z.B. 42,6 Mrd USD statt aktuell 426 Mio. USD).
Auf der Suche nach Investitionsmöglichkeiten begegnet man nur alle zig Jahre Unternehmen, denen zuzutrauen ist, einen Lebensbereich oder Wirtschaftszweig grundlegend zu verändern. Entsprechend groß ist - bei allen Risiken - das Kurspotential.
Nachdem der Kurs während der vergangenen drei Monate um über 70 % gestiegen ist (aktuell
17,19 USD), würde mich eine Konsolidierung nicht überraschen. Sollten die klinischen Studien die Ergebnisse der Präklinik annähernd bestätigen, müßte sich der Kurs auf längere Sicht aber vervielfachen (Enterprise Value dann z.B. 42,6 Mrd USD statt aktuell 426 Mio. USD).
Antwort auf Beitrag Nr.: 53.224.755 von Ville7 am 07.09.16 11:24:19
Deinen strategischen Überlegungen kann ich voll zustimmen.
In meinem individuellen Fall ist es so, dass ich zunächst eine für meine Verhältnisse relativ betrachtet zu große Depotposition aufgebaut habe. Ich hatte/habe geplant, die Position nach einem ersten größeren Kursanstieg (im Bereich zwischen 17 USD und 22 USD) auf die eigentlich geplante Stückzahl abzuschmelzen. Es wird dann immer noch mein mit Abstand größtes Biotech-Investment sein. Diese zwischenzeitliche Realisation eines größeren Zwischengewinns, so jedenfalls die Hoffnung, könnte mir psychologisch das erforderliche Rückgrat verleihen, um mit dem Kerninvestment die ganze Geschichte bis zum - hoffentlich erfolgreichen - Ende durchzuziehen. So müße sich letztlich auch im ungünstigen Fall nach dem von Dir beschriebenen Szenario ein Gewinn ergeben.
Die Vorstellung, einen riesigen Buchgewinn zu generieren und am Ende das Investment möglicherweise plusminus Null oder etwa mit einem Verlust zu beenden, wäre zu viel für meine Nerven. Mit der beschriebenen Strategie wird es mir hoffentlich gelingen, auf dem weiteren Weg dem natürlichen Bedürfnis, Gewinne zu sichern, zu widerstehen.
PS: Vielen Dank für die netten Worte!
Zitat von Ville7: Ja, da hast du Recht. Falls das hier wirklich was wird werde ich dir ewig dankbar für deinen Tipp sein.
Ich habe die Hoffnung, dass wir mit unserem Einstiegszeitpunkt in einer komfortablen Situation sind und auch im totalen Rückschlagsfalle derart aus der Geschichte rauskommen, dass wir keinen Totalverlust erleiden. Denn ich hoffe dass der Kurs sich bis zu den ersten Studiendaten noch verzwei/dreifacht. Wenn es dann schlechte Daten gibt wäre ein 50-80% Haircut auf 5-10 USD denkbar. Dann darf man dann nicht lange fackeln und muss sehr schnell rausgehen, wenn man für sich analysiert hat, dass es an der Technologie liegt und ein generelles Problem vorliegt, das die Technologie zum Scheitern verurteilt.
Deinen strategischen Überlegungen kann ich voll zustimmen.
In meinem individuellen Fall ist es so, dass ich zunächst eine für meine Verhältnisse relativ betrachtet zu große Depotposition aufgebaut habe. Ich hatte/habe geplant, die Position nach einem ersten größeren Kursanstieg (im Bereich zwischen 17 USD und 22 USD) auf die eigentlich geplante Stückzahl abzuschmelzen. Es wird dann immer noch mein mit Abstand größtes Biotech-Investment sein. Diese zwischenzeitliche Realisation eines größeren Zwischengewinns, so jedenfalls die Hoffnung, könnte mir psychologisch das erforderliche Rückgrat verleihen, um mit dem Kerninvestment die ganze Geschichte bis zum - hoffentlich erfolgreichen - Ende durchzuziehen. So müße sich letztlich auch im ungünstigen Fall nach dem von Dir beschriebenen Szenario ein Gewinn ergeben.
Die Vorstellung, einen riesigen Buchgewinn zu generieren und am Ende das Investment möglicherweise plusminus Null oder etwa mit einem Verlust zu beenden, wäre zu viel für meine Nerven. Mit der beschriebenen Strategie wird es mir hoffentlich gelingen, auf dem weiteren Weg dem natürlichen Bedürfnis, Gewinne zu sichern, zu widerstehen.
PS: Vielen Dank für die netten Worte!
Hi Joschka, hatte ich mir auch so gedacht, aber inzwischen habe ich ne Planänderung.
Aus folgendem Grund: Zu Jahresbeginn hatte ich meinen schon recht hochgewichteten Anteil EXEL massiv aufgestockt. Davon habe ich nun 81% verkauft und mit diesen Gewinnen (EK der verkauften Position im Schnitt USD 3,58 -> VK USD 16,20) habe ich die seit April gekauften Stücke CTMX, SGEN, IMGN (jüngst wieder dabei), Biotest und Morphosys, die ich seither gekauft habe (und sogar nach Steuer) komplett for free und zusätzlich noch ne fünfstellige Summe Cash obendrauf ausgelöst, wobei CTMX davon bei den dieses Jahr gekauften Stücken meine mit Abstand größte Position ist.
Also ich schau mir das ohne Reduktion der Position bis zu den ersten Daten an und entscheide dann..
Aus folgendem Grund: Zu Jahresbeginn hatte ich meinen schon recht hochgewichteten Anteil EXEL massiv aufgestockt. Davon habe ich nun 81% verkauft und mit diesen Gewinnen (EK der verkauften Position im Schnitt USD 3,58 -> VK USD 16,20) habe ich die seit April gekauften Stücke CTMX, SGEN, IMGN (jüngst wieder dabei), Biotest und Morphosys, die ich seither gekauft habe (und sogar nach Steuer) komplett for free und zusätzlich noch ne fünfstellige Summe Cash obendrauf ausgelöst, wobei CTMX davon bei den dieses Jahr gekauften Stücken meine mit Abstand größte Position ist.
Also ich schau mir das ohne Reduktion der Position bis zu den ersten Daten an und entscheide dann..
Antwort auf Beitrag Nr.: 53.318.511 von Ville7 am 21.09.16 13:14:54Hallo Joschka Schröder,
das timing für Deinen Thread war schon extrem gut... Gratulation (und Dankeschön).
Da ich dafür Prinzipien über Bord geworfen habe (keine Biotechs, keine Sachen, von denen man nichts versteht), bin ich nur mit einer bescheidenen Position und wahrscheinlich nicht mehr allzulange mit an Bord.
Viele Grüße!
das timing für Deinen Thread war schon extrem gut... Gratulation (und Dankeschön).
Da ich dafür Prinzipien über Bord geworfen habe (keine Biotechs, keine Sachen, von denen man nichts versteht), bin ich nur mit einer bescheidenen Position und wahrscheinlich nicht mehr allzulange mit an Bord.
Viele Grüße!
Antwort auf Beitrag Nr.: 53.315.439 von Joschka Schröder am 21.09.16 00:52:23Hi Joschka, würde mich sehr interessieren wie du konkret auf solch einen Unternehmenswert kommst? Hast du da ein Excelfile erstellt? Was sind die Prämissen/Inputs und Zeiträume für dieses Ergebnis? Aufgrund der aktuellen Partnerschaften allein ist das ja (noch) nicht möglich, im positiven Fall ist natürlich davon auszugehen dass "alle" Antikörper etc. in der Onkologie die CytomX "Haube" übergezogen bekommen - da fände ich es sehr interessant wie deine Kalkulationen aussehen. Besten Dank in jedem Fall!
Antwort auf Beitrag Nr.: 53.323.689 von SpanishEyes am 22.09.16 00:26:10Ich vermute, dass Du auf die 42,6 Mrd. USD anspielst. Auch wenn ich jede Menge Unternehmens-Excel-Dateien führe, in denen alles mögliche dokumentiert und berechnet wird, so handelt es sich bei o.g. Betrag nur um eine "Hausnummer" (aktueller Enterprise Value x Faktor 100). Es könnte auch ein anderer Faktor sein, es ging mir nur um eine erste Größenordnung (Groborientierung an anderen größeren Pharmakonzernen), die CytomX in jedem Fall erreichen sollte, wenn die präklinischen Daten in der klinischen Studienphase bestätigt würden, das Konzept der Antikörpermaskierung also aufginge.
CytomX ist ein Kleines Unternehmen mit einer hochinteressanten möglichen Schlüsseltechnologie, starken Kooperationspartnern, teilweise exzellenten, erfahrenen Managern (Rachel Humphrey), vielen Patenten, welches das IP absichern...... und ca. 60 Mitarbeitern.
Antwort auf Beitrag Nr.: 53.332.044 von Joschka Schröder am 23.09.16 00:30:48Die dahinterliegende Rechung ist recht einfach erklärt am Beispiel anti-PD-1 / anti-PD-L1, die "zufällig" auch die Leadprogramme von CTMX sind. Den derzeit in Entwicklung befindlichen konvenrionellen anti-PD-(L)1 Antikörpern werden Spitzenumsätzen von 5-10 Mrd USD bis 2020 / 2025 zugetraut. Sollte CTMX hier eine wirksamere Variante bei gleicher Sicherheit auf den Markt bringen können, wird der CTMX Antikörper hier das Rennen machen und die schnell anderen verdrängen und dabei das Sales-Potential von anti-PD-(L)1 sogar noch erhöhen können, da noch breiter und länger (da lebensverlängernd) einsetzbar. Bei 10Mrd USD Sales mit einer Umsatzmultiple von 4 ist man alleine hier in der zugegeben extrem vereinfachenden Rechnung bei 40Mrd USD Firmenbewertung und somit in der genannten Range. Und das ohne dezidiert die anderen AKs in der Pipeline auch nur ansatzweise zu bewerten, die bei Erfolg der Technologie sofort in den Fokus rücken würden. Man kann bei Nachweis des PoC auch davon ausgehen, dass die Aktie abhebt wie eine Rakete. Im Falle, das das alles in vivo nicht funktioniert wird sie natürlich implodieren.
Ville, Joschka - danke euch, nachvollziehbar und bin wirklich gespannt wie die ersten Ergebnisse dann sein werden!
@ville
Ob Cytomx eine vergleichbare Wirksamkeit mit seinem nackten PDL-1- mab, wie die besten im Moment in der Entwicklung befindlichen, oder zugelassenen PDL-1-Hemmer erzielen kann, weiss ich nicht. Dass das prodrug des von Cytomx entwickelten mab jedoch eine erhöhte Sicherheit auch in vivo aufweisen könnte, hoffe ich, und erscheint nachvollziehbar.
Die erhöhte Sicherheit (therapeutic window) kann im Umkehrschluss natürlich zu einer höheren Dosierung, und damit stärkerer Wirkung führen.
Dennoch wird es für unterschiedliche Tumorarten auch verschiedene gute PDL-1-Hemmer, und PD-Hemmer geben. Dass der kurz vor der klinischen Phase stehende PDL-1-Hemmer von Cytomx das Kombi-Mittel der Wahl sein wird (Backbone), vor allen anderen Checkpoint-Inhibitoren, kann ich noch nicht nachvollziehen.
BMS hat ja auch 3 Onkologika mit Probody-Technology mit Cytomx in Entwicklung, wahrscheinlich auch opdivo als probody, der dem Cytomx-Probody Konkurrenz machen wird.
Deswegen kann ich aufgrund der vorhandenen Informationen nicht ad hoc 10 Mrd Dollar Jahresumsatz für den
Cytomx-PDL-1 Probody annehmen/erhoffen.
CD166 ist sicher auch nicht wertlos, da seine weitere Entwicklung mit der vorhandenen Liquidität bis inclusive. Phase 1 abgesichert ist. Alle anderen, spannenden eigenen Projekte müssen aber in der Klinischen Entwicklung durch zukünftige Einnahmen/Milestones finanziert werden.
Ich frage mich jedoch, wie diese kleine manpower auf den vielen Hochzeiten gleichzeitig tanzen kann.
Das geht nur, wenn, die Kooperationspartner bei den Fremdprojekten den größten Teil der Entwicklungsarbeit leisten.
Ob Cytomx eine vergleichbare Wirksamkeit mit seinem nackten PDL-1- mab, wie die besten im Moment in der Entwicklung befindlichen, oder zugelassenen PDL-1-Hemmer erzielen kann, weiss ich nicht. Dass das prodrug des von Cytomx entwickelten mab jedoch eine erhöhte Sicherheit auch in vivo aufweisen könnte, hoffe ich, und erscheint nachvollziehbar.
Die erhöhte Sicherheit (therapeutic window) kann im Umkehrschluss natürlich zu einer höheren Dosierung, und damit stärkerer Wirkung führen.
Dennoch wird es für unterschiedliche Tumorarten auch verschiedene gute PDL-1-Hemmer, und PD-Hemmer geben. Dass der kurz vor der klinischen Phase stehende PDL-1-Hemmer von Cytomx das Kombi-Mittel der Wahl sein wird (Backbone), vor allen anderen Checkpoint-Inhibitoren, kann ich noch nicht nachvollziehen.
BMS hat ja auch 3 Onkologika mit Probody-Technology mit Cytomx in Entwicklung, wahrscheinlich auch opdivo als probody, der dem Cytomx-Probody Konkurrenz machen wird.
Deswegen kann ich aufgrund der vorhandenen Informationen nicht ad hoc 10 Mrd Dollar Jahresumsatz für den
Cytomx-PDL-1 Probody annehmen/erhoffen.
CD166 ist sicher auch nicht wertlos, da seine weitere Entwicklung mit der vorhandenen Liquidität bis inclusive. Phase 1 abgesichert ist. Alle anderen, spannenden eigenen Projekte müssen aber in der Klinischen Entwicklung durch zukünftige Einnahmen/Milestones finanziert werden.
Ich frage mich jedoch, wie diese kleine manpower auf den vielen Hochzeiten gleichzeitig tanzen kann.
Das geht nur, wenn, die Kooperationspartner bei den Fremdprojekten den größten Teil der Entwicklungsarbeit leisten.
Antwort auf Beitrag Nr.: 53.339.277 von StefanR am 23.09.16 22:43:07@Ville und StefanR
Eure intelligenten Beiträge Nr.33 und Nr.35 verdeutlichen noch einmal, wieso man zum jetzigen Zeitpunkt lieber auf scheingenaue Berechnungen verzichten und sich besser auf eine vage Grobabschätzung des künftigen Wertsteigerungspotentials beschränken sollte.
Zunächst geht es für CytomX darum, die Maskierungstechnik klinisch zu validieren. Sollte dies gelingen, werden vermutlich alle wesentlichen Player versuchen, die Probody-Technik zu lizensieren. Dadurch müßte CytomX auch dann auskömmlich vom Erfolg der Lizenznehmer partizipieren, wenn CytomX für ein bestimmtes Target kein gleichwertiges eigenes Präparat im Programm haben sollte.
Weil StefanR den Fall BMS ansprach: BMS hat bislang vier Lizenzen von CytomX gezogen, im Gegenzug wurden CytomX neben hohen Upfront-Zahlungen noch Meilensteinzahlungen von bis zu 1,192 Mrd USD eingeräumt, außerdem eine Beteiligung im mittleren einstelligen bis niedrigen zweistelligen Prozentbereich an künftigen Verkaufserlösen. Unter diesen Bedingungen sollte es für CytomX zu verschmerzen sein, gegen bestimmte Zielmoleküle kein eigenes Präparat ins Rennen zu schicken.
PS: Ville, CTMX wird wohl eher anstreben, gleich wirkame Varianten mit besserer Sicherheit (nicht umgekehrt) auf den Markt zu bringen, weil so Kombinationsbehandlungen möglich würden, die heutzutage wegen übler Nebenwirkungsprofils tabu sind.
PS: Wie erwartet konsolidiert der Kurs erst einmal, nachdem die 17 USD überschritten worden sind.
Eure intelligenten Beiträge Nr.33 und Nr.35 verdeutlichen noch einmal, wieso man zum jetzigen Zeitpunkt lieber auf scheingenaue Berechnungen verzichten und sich besser auf eine vage Grobabschätzung des künftigen Wertsteigerungspotentials beschränken sollte.
Zunächst geht es für CytomX darum, die Maskierungstechnik klinisch zu validieren. Sollte dies gelingen, werden vermutlich alle wesentlichen Player versuchen, die Probody-Technik zu lizensieren. Dadurch müßte CytomX auch dann auskömmlich vom Erfolg der Lizenznehmer partizipieren, wenn CytomX für ein bestimmtes Target kein gleichwertiges eigenes Präparat im Programm haben sollte.
Weil StefanR den Fall BMS ansprach: BMS hat bislang vier Lizenzen von CytomX gezogen, im Gegenzug wurden CytomX neben hohen Upfront-Zahlungen noch Meilensteinzahlungen von bis zu 1,192 Mrd USD eingeräumt, außerdem eine Beteiligung im mittleren einstelligen bis niedrigen zweistelligen Prozentbereich an künftigen Verkaufserlösen. Unter diesen Bedingungen sollte es für CytomX zu verschmerzen sein, gegen bestimmte Zielmoleküle kein eigenes Präparat ins Rennen zu schicken.
PS: Ville, CTMX wird wohl eher anstreben, gleich wirkame Varianten mit besserer Sicherheit (nicht umgekehrt) auf den Markt zu bringen, weil so Kombinationsbehandlungen möglich würden, die heutzutage wegen übler Nebenwirkungsprofils tabu sind.
PS: Wie erwartet konsolidiert der Kurs erst einmal, nachdem die 17 USD überschritten worden sind.
Heute ging es 8% runter auf 13,16 usd. Gibt es Neuigkeiten, die ich nicht finde? Die ganzen letzten tage is die Aktie schon sehr schwach.
Antwort auf Beitrag Nr.: 53.466.147 von hinz12 am 13.10.16 03:44:51Neuigkeiten gibt´s keine. Mit einer Konsolidierung war zu rechnen (s. Beitrag 26), dass sie derart stark ausfallen würde, war allerdings nicht unbedingt zu erwarten. Nachdem ich meine Depotposition bei Kursen über 17 USD auf die langfristig beabsichtigte Aktienzahl abgeschmolzen hatte (s. Beitrag 27), kaufe ich aktuell wieder zu (-> quasi das selbe Spiel von vorne).
Die Volatilität im Biotech-Bereich ist besonders groß, weil die meisten Marktteilnehmer keine feste Meinung haben, da die Materie kompliziert ist. Derartige Kursschwankungen lassen sich aber durchaus in die eigene Anlagestrategie integrieren.
Die Volatilität im Biotech-Bereich ist besonders groß, weil die meisten Marktteilnehmer keine feste Meinung haben, da die Materie kompliziert ist. Derartige Kursschwankungen lassen sich aber durchaus in die eigene Anlagestrategie integrieren.
Antwort auf Beitrag Nr.: 53.475.882 von Joschka Schröder am 14.10.16 09:06:32Ich vermute das war perfektes Timing von dir!
Der Aktienmarkt ist in vielen Indizes an kritischen Punkten angelangt. Entweder es dreht hier wieder nach oben (mein Primärszenario) oder es knallt heftigst ein bis zwei Etagen tiefer. Primärszenario auch deswegen, weil ich nicht denke, dass ein Absturz der Finanzmärkte den USA kurz vor den Wahlen genehm ist. Würde es doch der Wallstreet-Wunsch-Kandidatin Clinton in Not bringen und mehr Wähler würden eine Wahl von Trump in Betracht ziehen. Unsere amerikanische "Finanzmafia" wird das m.E. zu verhindern versuchen.
Tiefs bilden sich zudem gerne ein paar Tage oder eine Woche vor Verfallsterminen von Optionen, dieser Verfallstermin steht nächste Woche Freitag wieder an.
Von daher denke ich auch, dass die Korrektur bei den meisten Biotechs erst mal beendet sein könnte, speziell auch CTMX.
Der Aktienmarkt ist in vielen Indizes an kritischen Punkten angelangt. Entweder es dreht hier wieder nach oben (mein Primärszenario) oder es knallt heftigst ein bis zwei Etagen tiefer. Primärszenario auch deswegen, weil ich nicht denke, dass ein Absturz der Finanzmärkte den USA kurz vor den Wahlen genehm ist. Würde es doch der Wallstreet-Wunsch-Kandidatin Clinton in Not bringen und mehr Wähler würden eine Wahl von Trump in Betracht ziehen. Unsere amerikanische "Finanzmafia" wird das m.E. zu verhindern versuchen.
Tiefs bilden sich zudem gerne ein paar Tage oder eine Woche vor Verfallsterminen von Optionen, dieser Verfallstermin steht nächste Woche Freitag wieder an.
Von daher denke ich auch, dass die Korrektur bei den meisten Biotechs erst mal beendet sein könnte, speziell auch CTMX.
Antwort auf Beitrag Nr.: 53.477.073 von Ville7 am 14.10.16 10:58:40Na ja, falls das Timing halbwegs perfekt gelingen sollte, wäre sicherlich viel Glück dabei. Angesichts der Kursturbulenzen im Biotech-Sektor braucht man derzeit gute Nerven ... wenigstens kann man bei CytomX davon ausgehen, dass während der klinischen Studien keine Patienten verstorben sind o.ä. ... , da der Studienstart erst in Kürze erfolgen wird. 
PS: Zu IMGN werde ich versuchen, am WE etwas mehr zu schreiben. Die dortige Kursentwicklung ist faszinierend.

PS: Zu IMGN werde ich versuchen, am WE etwas mehr zu schreiben. Die dortige Kursentwicklung ist faszinierend.
Antwort auf Beitrag Nr.: 53.480.610 von Joschka Schröder am 14.10.16 17:25:19Dann hoffe ich mal, dass das hier fliegt.
@joschka: Du wolltest noch auf meine Pn antworten.
@joschka: Du wolltest noch auf meine Pn antworten.
CytomX Therapeutics Announces Third Quarter 2016 Financial Results and Provides Pipeline Update
SOUTH SAN FRANCISCO, Calif., Nov. 03, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today reported third quarter 2016 financial results.
“This quarter was marked by a number of significant milestones in our Probody pipeline, most notably the filing of our Investigational New Drug (IND) application for CX-072, our PD-L1-targeting Probody therapeutic for the treatment of cancer patients,” said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. “We have also made strong technical progress in our alliance with Bristol Myers Squibb on anti-CTLA-4 Probody therapeutics and look forward to presentations of preclinical proof-of-concept data at the European Society for Medical Oncology Symposium on Immuno-Oncology and the Society for Immunotherapy in Cancer 31st Annual Meeting & Associated Programs.”
As of September 30, 2016, CytomX had cash and cash equivalents and investments of $180.5 million. The Company continues to expect full year net cash utilization of $20.0 to $25.0 million in 2016. Based upon its current operating plan, the Company expects its existing capital resources will be sufficient to fund operations through 2018.
Business Highlights and Recent Developments
PROCLAIM-072 (PD-L1 Probody) Program
IND application filed with the U.S. FDA for PROCLAIM-072 clinical study of CX-072, a PD-L1-targeting Probody therapeutic for the treatment of cancer patients.
Pending ongoing discussions with the FDA regarding clinical protocol finalization, initial clinical sites are expected to be open by year end to support first patient enrollment.
Clinical data is expected to begin to emerge in the second half of 2017, and throughout 2018.
CX-2009 (CD166 Probody Drug Conjugate) Program
The IND for CX-2009, a first-in-class Probody drug conjugate targeting the highly expressed tumor antigen CD166, remains on track to be filed during the first half of 2017.
Clinical data is expected to begin to emerge in the second half of 2017, and throughout 2018.
Other Pipeline Updates
Pursuant to CytomX’s partnership with AbbVie, AbbVie exercised a licensing option with Seattle Genetics for the clinically and commercially validated payload, MMAE, for conjugation to the CD71 Probody Drug Conjugate that is being advanced in preclinical studies.
Upcoming Presentations
CytomX and partner Bristol-Myers Squibb will present updates on their respective Probody programs at the upcoming European Society for Medical Oncology (ESMO) Symposium on Immuno-Oncology, held November 4-5, 2016, in Lausanne, Switzerland, and the Society for Immunotherapy in Cancer (SITC) 31st Annual Meeting & Associated Programs, held November 9-13, 2016, in National Harbor, MD.
ESMO
Title: Next Generation Anti-CTLA-4 Antibodies
Presenter: Alan J. Korman, Ph.D., vice president, immuno-oncology, Bristol-Myers Squibb Company
Date: Saturday, November 5, 2016
Time: 8:00-8:20 a.m. CET
Session: Beyond PD-1/PD-L1 Axis Blockade: Combinations or New Molecules
SITC
Title: CD3-EGFR Probody T Cell-Engaging Bispecific Induces Tumor Regressions and Substantially Increases Safety Window in Preclinical Studies
Presenter: Bryan A. Irving, Ph.D., vice president, immunology, CytomX Therapeutics
Date: Wednesday, November 9, 2016
Time: 11:45-11:50 a.m. EST
Sub-Session II: Pre-Clinical New Agents in Development
Title: Probody Therapeutic Targeting PD-1 Provides Preclinical Anti-tumor Efficacy While Minimizing Induction of Autoimmunity as a Single Agent and in Combination with CTLA-4 Blockade
Presenter: Kimberly A. Tipton, senior scientist, CytomX Therapeutics
Date: Friday, November 11, 2016
Time: 12:15-1:30 p.m. and 6:15-7:30 p.m. EST
Session: Poster
Title: Next Generation Anti-CTLA-4 Antibodies
Presenter: Alan J. Korman, Ph.D., vice president, immuno-oncology, Bristol-Myers Squibb Company
Date: Saturday, November 12, 2016
Time: 9:10-9:35 a.m. EST
Session: Beyond Single-Agents: The Future of Combination Immunotherapy
Third Quarter Financial Results
Cash, cash equivalents and investments totaled $180.5 million as of September 30, 2016, compared to $186.7 million as of December 31, 2015. The decrease reflects cash used in operations, partially offset by a $30.0 million upfront payment received from AbbVie in connection with the collaboration agreements entered in April 2016, and a $10.0 million milestone payment received from Bristol-Myers Squibb in connection with its third target selection in January 2016.
Research and development expenses were $13.3 million for the third quarter of 2016, compared to $9.2 million for the third quarter of 2015. The increase was primarily attributable to $1.7 million in manufacturing costs for the CX-072 and CX-2009 programs, $1.2 million to advance CX-072 into Phase 1 clinical development, $0.9 million in personnel-related expenses due to an increase in headcount and $0.7 million in non-cash stock-based compensation due to higher stock valuation.
General and administrative expenses were $5.0 million for the third quarter of 2016, compared to $4.1 million for the third quarter of 2015. The increase was predominantly due to $0.6 million in non-cash stock based compensation due to higher stock valuation, $0.2 million in personnel-related expenses due to an increase in headcount and $0.2 million in additional consulting and professional service expenses associated with operating as a public company.
About PROCLAIM
CytomX is launching the PROCLAIM (Probody Clinical Assessment In Man), a first-of its-kind clinical trial program that enables clinical study sites and physicians to access CytomX’s wholly-owned Probody therapeutics under one international umbrella. The first module within the PROCLAIM program is an open-label, dose-finding Phase 1/2 study evaluating CX-072 as monotherapy and in combination with Yervoy® (ipilimumab) or Zelboraf® (vemurafenib) in anti-PD-(L)1 inhibitor naïve patients with certain cancers. CX-072 is a PD-L1-targeting Probody therapeutic for the treatment of cancer patients. CytomX aims to achieve three goals as part of the PROCLAIM-072 clinical trial:
Safety: Demonstrate that CX-072 is well tolerated in patients, and potentially improves safety, particularly in the combination setting.
Anti-cancer activity: Demonstrate initial evidence of CX-072’s anti-cancer activity as monotherapy and in combination.
Translational program and Probody platform proof-of-concept: Explore mechanistic aspects of Probody activity in patients as observed in preclinical studies.
Clinical data is expected to begin to emerge in the second half of 2017, and throughout 2018. The IND application for CX-072 is currently under review with FDA.
SOUTH SAN FRANCISCO, Calif., Nov. 03, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today reported third quarter 2016 financial results.
“This quarter was marked by a number of significant milestones in our Probody pipeline, most notably the filing of our Investigational New Drug (IND) application for CX-072, our PD-L1-targeting Probody therapeutic for the treatment of cancer patients,” said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. “We have also made strong technical progress in our alliance with Bristol Myers Squibb on anti-CTLA-4 Probody therapeutics and look forward to presentations of preclinical proof-of-concept data at the European Society for Medical Oncology Symposium on Immuno-Oncology and the Society for Immunotherapy in Cancer 31st Annual Meeting & Associated Programs.”
As of September 30, 2016, CytomX had cash and cash equivalents and investments of $180.5 million. The Company continues to expect full year net cash utilization of $20.0 to $25.0 million in 2016. Based upon its current operating plan, the Company expects its existing capital resources will be sufficient to fund operations through 2018.
Business Highlights and Recent Developments
PROCLAIM-072 (PD-L1 Probody) Program
IND application filed with the U.S. FDA for PROCLAIM-072 clinical study of CX-072, a PD-L1-targeting Probody therapeutic for the treatment of cancer patients.
Pending ongoing discussions with the FDA regarding clinical protocol finalization, initial clinical sites are expected to be open by year end to support first patient enrollment.
Clinical data is expected to begin to emerge in the second half of 2017, and throughout 2018.
CX-2009 (CD166 Probody Drug Conjugate) Program
The IND for CX-2009, a first-in-class Probody drug conjugate targeting the highly expressed tumor antigen CD166, remains on track to be filed during the first half of 2017.
Clinical data is expected to begin to emerge in the second half of 2017, and throughout 2018.
Other Pipeline Updates
Pursuant to CytomX’s partnership with AbbVie, AbbVie exercised a licensing option with Seattle Genetics for the clinically and commercially validated payload, MMAE, for conjugation to the CD71 Probody Drug Conjugate that is being advanced in preclinical studies.
Upcoming Presentations
CytomX and partner Bristol-Myers Squibb will present updates on their respective Probody programs at the upcoming European Society for Medical Oncology (ESMO) Symposium on Immuno-Oncology, held November 4-5, 2016, in Lausanne, Switzerland, and the Society for Immunotherapy in Cancer (SITC) 31st Annual Meeting & Associated Programs, held November 9-13, 2016, in National Harbor, MD.
ESMO
Title: Next Generation Anti-CTLA-4 Antibodies
Presenter: Alan J. Korman, Ph.D., vice president, immuno-oncology, Bristol-Myers Squibb Company
Date: Saturday, November 5, 2016
Time: 8:00-8:20 a.m. CET
Session: Beyond PD-1/PD-L1 Axis Blockade: Combinations or New Molecules
SITC
Title: CD3-EGFR Probody T Cell-Engaging Bispecific Induces Tumor Regressions and Substantially Increases Safety Window in Preclinical Studies
Presenter: Bryan A. Irving, Ph.D., vice president, immunology, CytomX Therapeutics
Date: Wednesday, November 9, 2016
Time: 11:45-11:50 a.m. EST
Sub-Session II: Pre-Clinical New Agents in Development
Title: Probody Therapeutic Targeting PD-1 Provides Preclinical Anti-tumor Efficacy While Minimizing Induction of Autoimmunity as a Single Agent and in Combination with CTLA-4 Blockade
Presenter: Kimberly A. Tipton, senior scientist, CytomX Therapeutics
Date: Friday, November 11, 2016
Time: 12:15-1:30 p.m. and 6:15-7:30 p.m. EST
Session: Poster
Title: Next Generation Anti-CTLA-4 Antibodies
Presenter: Alan J. Korman, Ph.D., vice president, immuno-oncology, Bristol-Myers Squibb Company
Date: Saturday, November 12, 2016
Time: 9:10-9:35 a.m. EST
Session: Beyond Single-Agents: The Future of Combination Immunotherapy
Third Quarter Financial Results
Cash, cash equivalents and investments totaled $180.5 million as of September 30, 2016, compared to $186.7 million as of December 31, 2015. The decrease reflects cash used in operations, partially offset by a $30.0 million upfront payment received from AbbVie in connection with the collaboration agreements entered in April 2016, and a $10.0 million milestone payment received from Bristol-Myers Squibb in connection with its third target selection in January 2016.
Research and development expenses were $13.3 million for the third quarter of 2016, compared to $9.2 million for the third quarter of 2015. The increase was primarily attributable to $1.7 million in manufacturing costs for the CX-072 and CX-2009 programs, $1.2 million to advance CX-072 into Phase 1 clinical development, $0.9 million in personnel-related expenses due to an increase in headcount and $0.7 million in non-cash stock-based compensation due to higher stock valuation.
General and administrative expenses were $5.0 million for the third quarter of 2016, compared to $4.1 million for the third quarter of 2015. The increase was predominantly due to $0.6 million in non-cash stock based compensation due to higher stock valuation, $0.2 million in personnel-related expenses due to an increase in headcount and $0.2 million in additional consulting and professional service expenses associated with operating as a public company.
About PROCLAIM
CytomX is launching the PROCLAIM (Probody Clinical Assessment In Man), a first-of its-kind clinical trial program that enables clinical study sites and physicians to access CytomX’s wholly-owned Probody therapeutics under one international umbrella. The first module within the PROCLAIM program is an open-label, dose-finding Phase 1/2 study evaluating CX-072 as monotherapy and in combination with Yervoy® (ipilimumab) or Zelboraf® (vemurafenib) in anti-PD-(L)1 inhibitor naïve patients with certain cancers. CX-072 is a PD-L1-targeting Probody therapeutic for the treatment of cancer patients. CytomX aims to achieve three goals as part of the PROCLAIM-072 clinical trial:
Safety: Demonstrate that CX-072 is well tolerated in patients, and potentially improves safety, particularly in the combination setting.
Anti-cancer activity: Demonstrate initial evidence of CX-072’s anti-cancer activity as monotherapy and in combination.
Translational program and Probody platform proof-of-concept: Explore mechanistic aspects of Probody activity in patients as observed in preclinical studies.
Clinical data is expected to begin to emerge in the second half of 2017, and throughout 2018. The IND application for CX-072 is currently under review with FDA.
Was sagst dazu Joschka?
Antwort auf Beitrag Nr.: 53.616.462 von hinz12 am 03.11.16 21:36:40Die operative Entwicklung läuft wunschgemäß nach Plan.
Dass die (in dieser Phase der Unternehmensentwicklung) alberne Analysten-Guidance beim Ergebnis je Aktie um 5 Cent und bei den Umsätzen um 1,6 Mio. USD verfehlt worden ist, hat für mich keine Relevanz.
Die Kursentwicklung ist natürlich weniger begeisternd. Die US-Wahl/Schlammschlacht mit ihren ungewöhnlichen Kandidaten läßt grüßen. Ich gehe aber davon aus, dass die Menschheit auch nach der US-Wahl auf forschende Pharmaunternehmen angewiesen sein wird und nicht vollständig zur Nturheilkunde zurückkehren möchte. Insoweit werden außergewöhnlich gute Präparateentwicklungen auch künftig lukrative Verdienstmöglichkeiten eröffnen. Und dass in Teilen der Pharmabranche der Rotstrich angesetzt werden soll, ist im Grundsatz zu begrüßen. Den einhundertvierzigsten TNF-Antagonisten benötigt niemand, ebenso wenig verständlich ist es, wenn Generikapreise Jahr für Jahr um zweistellige Prozentsätze steigen.
Dass die (in dieser Phase der Unternehmensentwicklung) alberne Analysten-Guidance beim Ergebnis je Aktie um 5 Cent und bei den Umsätzen um 1,6 Mio. USD verfehlt worden ist, hat für mich keine Relevanz.
Die Kursentwicklung ist natürlich weniger begeisternd. Die US-Wahl/Schlammschlacht mit ihren ungewöhnlichen Kandidaten läßt grüßen. Ich gehe aber davon aus, dass die Menschheit auch nach der US-Wahl auf forschende Pharmaunternehmen angewiesen sein wird und nicht vollständig zur Nturheilkunde zurückkehren möchte. Insoweit werden außergewöhnlich gute Präparateentwicklungen auch künftig lukrative Verdienstmöglichkeiten eröffnen. Und dass in Teilen der Pharmabranche der Rotstrich angesetzt werden soll, ist im Grundsatz zu begrüßen. Den einhundertvierzigsten TNF-Antagonisten benötigt niemand, ebenso wenig verständlich ist es, wenn Generikapreise Jahr für Jahr um zweistellige Prozentsätze steigen.
Hat jemand Informationen zum BMS-Vortrag auf der ESMO letztes Wochenende?
Heute tolle Zukauf- bzw. Einstiegsmöglichkeit bei Kursen um bzw. unter 10 USD. Derzeit ist offensichtlich viel Nervosität wegen der ins Auge gefaßten Kapitalerhöhung im Markt.
Antwort auf Beitrag Nr.: 53.646.345 von Joschka Schröder am 08.11.16 18:40:16
Klingt für mich erstmal nach einem Vorratsbeschluss, auch wenn die Gesamtsumme in Höhe von 250 Mio. US$ "substantiell" erscheint.
Angesichts der Cashposition erscheint mir eine (umfangreiche) KE zur Zeit unnötig, es sei denn, man plant eine Übernahme oder ähnliches, was ich angesichts des Alleinstellungsmerkmals der Technologie wiederum auch nicht verstehen könnte.
Ich hoffe, dass der PoC vor etwaigem Kapitalbedarf gelingt, dann würde die Verwässerung glimpflich ausfallen bzw. sich aufgrund des folgenden, massiven Interesses aus der Industrie möglicherweise sogar vollkommen erübrigen (Auslizensierungen zu Höchstpreisen).
Zitat von Joschka Schröder: Derzeit ist offensichtlich viel Nervosität wegen der ins Auge gefaßten Kapitalerhöhung im Markt.
Klingt für mich erstmal nach einem Vorratsbeschluss, auch wenn die Gesamtsumme in Höhe von 250 Mio. US$ "substantiell" erscheint.
Angesichts der Cashposition erscheint mir eine (umfangreiche) KE zur Zeit unnötig, es sei denn, man plant eine Übernahme oder ähnliches, was ich angesichts des Alleinstellungsmerkmals der Technologie wiederum auch nicht verstehen könnte.
Ich hoffe, dass der PoC vor etwaigem Kapitalbedarf gelingt, dann würde die Verwässerung glimpflich ausfallen bzw. sich aufgrund des folgenden, massiven Interesses aus der Industrie möglicherweise sogar vollkommen erübrigen (Auslizensierungen zu Höchstpreisen).
No bounce today . wohl wirklich derzeit viel skepsis bzgl der möglichen kapitalerhöhung am start
Antwort auf Beitrag Nr.: 53.652.405 von BReal am 09.11.16 11:03:50Für die ersten 50 Mio. gibt es mit Jefferies bereits eine vertragliche Regelung. Vermutlich wird der Aktienkurs nicht richtig vorankommen, bis Jefferies die Aktien platziert hat.
Antwort auf Beitrag Nr.: 53.663.682 von Joschka Schröder am 10.11.16 12:28:18Marktpsychologisch hast Du vermutlich vollkommen recht. Es muss aber gar nicht sein, dass demnächst wirklich schon etwas passiert, siehe die Hervorhebungen von mir im Text unten. Ich finde die ganze Aktion insgesamt etwas unglücklich, da ich aktuell keinen akuten Kapitalbedarf erkennen kann. Der Kursverlauf dürfte aber, wie Du schriebst, nun vorläufig im Eimer sein.
We have entered into a Controlled Equity OfferingSM sales agreement with Cantor Fitzgerald & Co., or Cantor Fitzgerald, relating to shares of our common stock offered by this prospectus. In accordance with the terms of the sales agreement, we may offer and sell shares of our common stock having an aggregate offering price of up to $50,000,000 from time to time through Cantor acting as our agent. Sales of our common stock, if any, under this prospectus may be made in sales deemed to be “at-the-market” equity offerings as defined in Rule 415 promulgated under the Securities Act of 1933, as amended, or the Securities Act, including sales made directly on or through The NASDAQ Global Select Market, the existing trading market for our common stock, sales made to or through a market maker other than on an exchange or otherwise, in negotiated transactions at market prices prevailing at the time of sale or at prices related to such prevailing market prices, and/or any other method permitted by law, including in privately negotiated transactions. Cantor Fitzgerald will act as sales agent on a best efforts basis and will use commercially reasonable efforts to sell on our behalf all of the shares of common stock requested to be sold by us, consistent with its normal trading and sales practices, on mutually agreed terms between Cantor Fitzgerald and us. There is no arrangement for funds to be received in any escrow, trust or similar arrangement.
We have entered into a Controlled Equity OfferingSM sales agreement with Cantor Fitzgerald & Co., or Cantor Fitzgerald, relating to shares of our common stock offered by this prospectus. In accordance with the terms of the sales agreement, we may offer and sell shares of our common stock having an aggregate offering price of up to $50,000,000 from time to time through Cantor acting as our agent. Sales of our common stock, if any, under this prospectus may be made in sales deemed to be “at-the-market” equity offerings as defined in Rule 415 promulgated under the Securities Act of 1933, as amended, or the Securities Act, including sales made directly on or through The NASDAQ Global Select Market, the existing trading market for our common stock, sales made to or through a market maker other than on an exchange or otherwise, in negotiated transactions at market prices prevailing at the time of sale or at prices related to such prevailing market prices, and/or any other method permitted by law, including in privately negotiated transactions. Cantor Fitzgerald will act as sales agent on a best efforts basis and will use commercially reasonable efforts to sell on our behalf all of the shares of common stock requested to be sold by us, consistent with its normal trading and sales practices, on mutually agreed terms between Cantor Fitzgerald and us. There is no arrangement for funds to be received in any escrow, trust or similar arrangement.
Antwort auf Beitrag Nr.: 53.663.793 von BReal am 10.11.16 12:40:24Gut, dass Du das Zitat ins Netz gestellt hast. Die Vereinbarung wurde mit Cantor Fitzgerald getroffen, nicht mit Jefferies. Das hatte ich falsch in Erinnerung.
Bin seit heute auch mit einer kleinen Position dabei. Wegen der Marktenge direkt an der Nasdaq gekauft. Hochspekulativ isses allemal, aber natürlich auch wahnsinnig spannend. Wie hat ville geschrieben "to good to be true". Werden sehen... Auf jeden Fall ist der Wert noch völlig abseits der Aufmerksamkeit, und grundsätzlich ist möglicherweise kein schlechter Zeitpunkt, um in Biotech zu investieren.
off topic
https://www.sitcancer.org/support/forwardfund/house-of-blues…
Rachel Humphrey rocks the stage!
SITC 2016- the checkpoints are coming.
https://www.sitcancer.org/support/forwardfund/house-of-blues…
Rachel Humphrey rocks the stage!

SITC 2016- the checkpoints are coming.
Antwort auf Beitrag Nr.: 53.643.759 von BReal am 08.11.16 13:02:42
Wen es interessiert: In der neuen November-Präsentation von CytomX wird auf Seite 19 nun vom präklinischen PoC des CTLA-4-Projekts von BMS berichtet.
Zitat von BReal: Hat jemand Informationen zum BMS-Vortrag auf der ESMO letztes Wochenende?
Wen es interessiert: In der neuen November-Präsentation von CytomX wird auf Seite 19 nun vom präklinischen PoC des CTLA-4-Projekts von BMS berichtet.
Antwort auf Beitrag Nr.: 53.714.070 von BReal am 17.11.16 11:27:42Danke. Die präklinischen Daten des anti-CTLA4 sehen hervorragend aus! Ich bin gespannt wie Flitzebogen auf die klinischen Ergebnisse (des PD-L1) dann in 2017 oder 2018.
Hier ein Link von einer aktuellen Präsentation
http://seekingalpha.com/article/4024598-cytomx-therapeutics-…
http://seekingalpha.com/article/4024598-cytomx-therapeutics-…
Antwort auf Beitrag Nr.: 53.728.467 von schnappi am 18.11.16 21:47:57Heavy insider sells
Antwort auf Beitrag Nr.: 53.759.574 von biopadawan am 23.11.16 21:33:50Ja, Canaan / Tim Shannon (http://www.canaan.com/people/tim-shannon/), Shannon ist im board (~Aufsichtsrat) von CTMX, verkaufen wie schon im April und Mai. Der Bestand wird weiter kontinuierlich abgebaut, schon seit IPO, von je 4,9 Mio Aktien auf derzeit je 3,7 Mio Aktien.
Wahrscheinlich verkaufen sie aus Diversifikationsgründen, denn auch mit 10-12 USD werden sie durch den IPO einen fetten Reibach gemacht haben.
Ein schlechtes Gefühl bleibt natürlich bei solchen Verkäufen, die bei dem aktuell täglichen Volumen natürlich auch die Kurse unten halten.
Wahrscheinlich verkaufen sie aus Diversifikationsgründen, denn auch mit 10-12 USD werden sie durch den IPO einen fetten Reibach gemacht haben.
Ein schlechtes Gefühl bleibt natürlich bei solchen Verkäufen, die bei dem aktuell täglichen Volumen natürlich auch die Kurse unten halten.
Antwort auf Beitrag Nr.: 53.761.131 von Ville7 am 24.11.16 08:12:04Seh ich auch so. Die Verkäufe gehen aktuell weiter. So wird das nichts mit dem Kursanstieg.
Antwort auf Beitrag Nr.: 53.774.163 von biopadawan am 25.11.16 20:01:13Stark irritierend wäre, wenn viele Altaktionäre verkaufen würden. Die Verkäufe beschränken sich jedoch singulär auf die Caanan-Gruppe, deren finanzielle Strukturen wir nicht kennen (Verschuldungsgrad etc.). Die Verkäufe der Caanan-Gruppe drücken derzeit sicherlich den Kurs, sind letztlich aber nicht von Belang. Entscheidend wird sein, ob das Probody-Konzept in den bevorstehenden klinischen Studien das hält, was Theorie und Präklinik versprechen.
S3 Filing: CTMX bereitet sich vor neues Kapital von bis zu 250Mio USD am Kapitalmarkt zu beschaffen...
Antwort auf Beitrag Nr.: 53.775.849 von Ville7 am 26.11.16 09:47:47Dann könnten sich möglicherweise nochmals chancen zum "Average down" ergeben ;-)
Antwort auf Beitrag Nr.: 53.774.601 von Joschka Schröder am 25.11.16 21:27:17ungefähr wann könnte es spannend werden?
Weiterer Meilenstein in der kooperation mit BMS
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-newsArtic…
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-newsArtic…
Antwort auf Beitrag Nr.: 53.830.213 von schnappi am 05.12.16 14:30:08Nach den etwas unverständlichen Canaan-Verkäufen mal wieder eine richtig gute Meldung.
15 Mio. USD für eine Target-Selektion sind schon eine Hausnummer.
@LeoF: Spannend wird es ab 2017, insbesondere zum ASCO-Meeting und danach.
15 Mio. USD für eine Target-Selektion sind schon eine Hausnummer.
@LeoF: Spannend wird es ab 2017, insbesondere zum ASCO-Meeting und danach.
Antwort auf Beitrag Nr.: 53.830.293 von Joschka Schröder am 05.12.16 14:47:56ASCO 2017 wird für klinische Ergebnisse noch viel zu früh sein. Mehr als präklinische Daten wird es bis dahin wohl nicht zu veröffentlichen geben. Oder schätzt du das anders ein?
Falls Cytomx Ansatz Erfolg verspricht könnte ASCO 2018 deren Show werden.
Falls Cytomx Ansatz Erfolg verspricht könnte ASCO 2018 deren Show werden.
Antwort auf Beitrag Nr.: 53.832.037 von Ville7 am 05.12.16 20:00:32cytomx hat in seinen Zeitplänen von ersten klinischen Daten ab dem 2.HJ 2017 gesprochen. Vielleicht veröffentlichen sie bis dahin Daten einer Interimsanalyse ihres PD-L-1 IND`s?
Darüber hinaus ist es bemerkenswert, daß BMS nun schon das 4.Produkt mit cytomx eingeht, dafür 15 mio upfront zahlt (wie im Rahmenvertrag vereinbart und zugegeben bekannt), und, wie bei den anderen 3 Projekten die gesamten Entwicklungskosten trägt, zusätzlich milestones über 298mio pro Projekt im Erfolgsfall berappt.
Hierdurch wird die starke Präklinik und das schlüssige, theoretische Konzept von cytomx geadelt.
Das 4. Projekt wurde kurz nach Veröffentlichung der guten Daten des yervoy-CTLA-4-prodrug abgeschlossen.
Man hielt auf BMS-Seite die Daten offensichtlich für so gut, daß man zügig die gemeinsamen checkpoint-Projekte weiterentwickeln möchte.
Auch die Tatsache, dass Alan J. Korman, als vice president immunotherapy, BMS, das gemeinsame Projekt auf der ESMO vorgestellt hat, unterstreicht die Bedeutung der Kooperation.
Darüber hinaus ist es bemerkenswert, daß BMS nun schon das 4.Produkt mit cytomx eingeht, dafür 15 mio upfront zahlt (wie im Rahmenvertrag vereinbart und zugegeben bekannt), und, wie bei den anderen 3 Projekten die gesamten Entwicklungskosten trägt, zusätzlich milestones über 298mio pro Projekt im Erfolgsfall berappt.
Hierdurch wird die starke Präklinik und das schlüssige, theoretische Konzept von cytomx geadelt.
Das 4. Projekt wurde kurz nach Veröffentlichung der guten Daten des yervoy-CTLA-4-prodrug abgeschlossen.
Man hielt auf BMS-Seite die Daten offensichtlich für so gut, daß man zügig die gemeinsamen checkpoint-Projekte weiterentwickeln möchte.
Auch die Tatsache, dass Alan J. Korman, als vice president immunotherapy, BMS, das gemeinsame Projekt auf der ESMO vorgestellt hat, unterstreicht die Bedeutung der Kooperation.
Antwort auf Beitrag Nr.: 53.832.249 von Probody am 05.12.16 20:59:48Bist du so überzeugt Joschka, dass du direkt deinen Usernamen umbenannt hast? ;-)
Antwort auf Beitrag Nr.: 53.832.545 von SpanishEyes am 05.12.16 22:27:49Stimmt nicht.
Antwort auf Beitrag Nr.: 53.832.249 von Probody am 05.12.16 20:59:48
Wo ist für dich der Unterschied zwischen "ersten klinischen Daten" und "Daten einer Interimsanalyse"?
Zitat von Probody: cytomx hat in seinen Zeitplänen von ersten klinischen Daten ab dem 2.HJ 2017 gesprochen. Vielleicht veröffentlichen sie bis dahin Daten einer Interimsanalyse ihres PD-L-1 IND`s? ...
Wo ist für dich der Unterschied zwischen "ersten klinischen Daten" und "Daten einer Interimsanalyse"?
Hallo, bin hier auch mit einer –noch recht kleinen – Position dabei. Man fragt sich natürlich, was die Verkäufe von Canaan Partners bedeuten und wie lange sie andauern könnten.
Geht man auf die HP von Canaan, dann sieht man, dass die etwa 3 Mrd US$ unter Verwaltung haben (und zusätzlich vielleicht noch 1 Mrd als Fremdkapital aufgenommen haben) und in über 260 verschiedenen Unternehmen engagiert sind. Das ergäbe – eine einigermaßen gleiche Verteilung unterstellt – eine durchschnittliche Positionsgröße von ungefähr 15 Mio US$ pro Unternehmen (wenn sie denn so gleichmässig ist). Die wäre in Bezug auf CytomX dann erreicht, wenn sie etwa die Hälfte ihres Bestandes von derzeit noch ca. 3,2 Mio Stück abgebaut haben. Schaut man sich die Form 4 an, dann könnte man davon ausgehen, dass von Canaan pro Handelstag im Schnitt 10 k veräußert werden um schliesslich eine `durchschnittliche´ Positionsgröße zu erreichen. Damit würden sie dann den Markt für ca.6-9 Monate mit ihren Verkäufen zu belasten. Gutes Geld verdient haben sie ohnehin schon.
Man kann wohl mit ziemlicher Sicherheit davon ausgehen, dass Canaan´s Verkäufe nicht mit der Technologie zusammenhängen sonst hätte BMS sein Engagement aktuell nicht erhöht.
Zum dem Zeitpunkt, an dem vielleicht erste Zwischenergebnisse aus der Klinik erwartet werden könnten, würde dann auch der Verkaufsdruck nachlassen. Das könnte der Zeitpunkt sein, an dem der Kurs anspringt und das Unternehmen die genehmigte Ausgabe von neuen Aktien vornehmen könnte. Sie oder der beauftragte Market Maker werden die Ausgabe der 250 Mio US$ nicht zu 10 US$ pro Stück vornehmen wollen sondern hoffen vielleicht auf 25 US$, also 10 Mio Stück neu zu emittieren.
Dies könnte bedeuten, dass der Kurs möglicherweise noch längere Zeit markttechnisch unter Druck steht. Es sei denn, die klinischen Ergebnisse sind so herausragend, dass alle Welt auf das bislang eher unbekannte Unternehmen springt.
Andererseits bedeuted diese anhaltende Kursbelastung, dass man jetzt ohne Eile zu günstigen Kursen einsteigen kann.
Zugegeben, viel „ hätte“, „könnte“ und „würde“, aber immer noch besser man entwickelt einen `educated guess´, als gar keine Vorstellung.
Anyone?
Geht man auf die HP von Canaan, dann sieht man, dass die etwa 3 Mrd US$ unter Verwaltung haben (und zusätzlich vielleicht noch 1 Mrd als Fremdkapital aufgenommen haben) und in über 260 verschiedenen Unternehmen engagiert sind. Das ergäbe – eine einigermaßen gleiche Verteilung unterstellt – eine durchschnittliche Positionsgröße von ungefähr 15 Mio US$ pro Unternehmen (wenn sie denn so gleichmässig ist). Die wäre in Bezug auf CytomX dann erreicht, wenn sie etwa die Hälfte ihres Bestandes von derzeit noch ca. 3,2 Mio Stück abgebaut haben. Schaut man sich die Form 4 an, dann könnte man davon ausgehen, dass von Canaan pro Handelstag im Schnitt 10 k veräußert werden um schliesslich eine `durchschnittliche´ Positionsgröße zu erreichen. Damit würden sie dann den Markt für ca.6-9 Monate mit ihren Verkäufen zu belasten. Gutes Geld verdient haben sie ohnehin schon.
Man kann wohl mit ziemlicher Sicherheit davon ausgehen, dass Canaan´s Verkäufe nicht mit der Technologie zusammenhängen sonst hätte BMS sein Engagement aktuell nicht erhöht.
Zum dem Zeitpunkt, an dem vielleicht erste Zwischenergebnisse aus der Klinik erwartet werden könnten, würde dann auch der Verkaufsdruck nachlassen. Das könnte der Zeitpunkt sein, an dem der Kurs anspringt und das Unternehmen die genehmigte Ausgabe von neuen Aktien vornehmen könnte. Sie oder der beauftragte Market Maker werden die Ausgabe der 250 Mio US$ nicht zu 10 US$ pro Stück vornehmen wollen sondern hoffen vielleicht auf 25 US$, also 10 Mio Stück neu zu emittieren.
Dies könnte bedeuten, dass der Kurs möglicherweise noch längere Zeit markttechnisch unter Druck steht. Es sei denn, die klinischen Ergebnisse sind so herausragend, dass alle Welt auf das bislang eher unbekannte Unternehmen springt.
Andererseits bedeuted diese anhaltende Kursbelastung, dass man jetzt ohne Eile zu günstigen Kursen einsteigen kann.
Zugegeben, viel „ hätte“, „könnte“ und „würde“, aber immer noch besser man entwickelt einen `educated guess´, als gar keine Vorstellung.
Anyone?
Antwort auf Beitrag Nr.: 53.832.785 von Ville7 am 05.12.16 23:31:22@ville erste klinische Daten ist der exaktere Begriff.
Zu beachten am Geschäftsmodell von Cytomx ist, dass sie
a) neue Targets mit neuen Prodrugs (pro neu und drug neu, vgl cd166ADC)
b) alte Targets mit neuem pro und altem drug (yervoy-prodrug)
entwickeln.
Ersteres hat gewöhnlich 2 Klippen: Wirkung und Nebenwirkung
Bei b) könnte man jedoch durch eine zu stabile Maskierungsbindung wegen folgender mäßiger Aufkonzentrierung im Tumor microenvironment die Wirkung abschwächen. Die Technologie könnte sich durch gegenseitige Effekte also nivellieren (höhere, verträglichere Wirkstoffdosis bei geringerer Wirkung)
Das Nebenwirkungsprofil sollte im wesentlichen dem Unmaskierten Drug entsprechen.
Somit hätte man vereinfacht nur eine Klippe.
Ausschlusskriterien der Technologie: alle Lebensabschnitte, wo mmp im Körper physiologisch hochreguliert sind, wie Wachstumsphase bei Kindern, Heilungsprozesse nach Op oder Knochenbrüchen.
Kritisch wäre es für die Technologie im allgemeinen, wenn andere, hochregulierte mmp Orte im Körper vorhanden wären, an denen auch eine Drug-Aufkonzentrierung erfolgt.
Spekulation: alle Stellen mit starker Zellteilung, wie Haut und Schleimhaut.
Zu beachten am Geschäftsmodell von Cytomx ist, dass sie
a) neue Targets mit neuen Prodrugs (pro neu und drug neu, vgl cd166ADC)
b) alte Targets mit neuem pro und altem drug (yervoy-prodrug)
entwickeln.
Ersteres hat gewöhnlich 2 Klippen: Wirkung und Nebenwirkung
Bei b) könnte man jedoch durch eine zu stabile Maskierungsbindung wegen folgender mäßiger Aufkonzentrierung im Tumor microenvironment die Wirkung abschwächen. Die Technologie könnte sich durch gegenseitige Effekte also nivellieren (höhere, verträglichere Wirkstoffdosis bei geringerer Wirkung)
Das Nebenwirkungsprofil sollte im wesentlichen dem Unmaskierten Drug entsprechen.
Somit hätte man vereinfacht nur eine Klippe.
Ausschlusskriterien der Technologie: alle Lebensabschnitte, wo mmp im Körper physiologisch hochreguliert sind, wie Wachstumsphase bei Kindern, Heilungsprozesse nach Op oder Knochenbrüchen.
Kritisch wäre es für die Technologie im allgemeinen, wenn andere, hochregulierte mmp Orte im Körper vorhanden wären, an denen auch eine Drug-Aufkonzentrierung erfolgt.
Spekulation: alle Stellen mit starker Zellteilung, wie Haut und Schleimhaut.
Antwort auf Beitrag Nr.: 53.834.075 von Probody am 06.12.16 09:48:22Hi prodrug,
meine Rückfrage war gemein. Wenn Cytomx von ersten klinischen Daten in HJ2 2017 spricht kann es per se keine Daten einer Interimsanalyse (d.h. erste klinische Daten) vorher geben.
Zu deinen anderen Punkten: Die präklinischen Daten lassen bereits darauf schließen, dass die Maskierung ein kleines Stück Wirksamkeit kostet. Sollte es aber wirklich zu den präklinisch beobachteten Effekten einer x fach besseren Sicherheit, auch nur im Bruchteil kommen, dann gibt es einen Erfolg.
Das von dir angesprochene Risiko aus Punkt "Bei b)" sehe ich zwar auch, aber mit einer leicht anderen Befürchtung/Begründung. Es könnte m.E. das Risiko bestehen, dass die Maskierung im Tumor Enviroment (wenn die Proteasen aktiv sind) zwar entfernt wird, der demaskierte Anitikörper dann aber (demaskiert) nicht (nur) im Tumor bindet, sondern größere Anteile wieder an heathy tissue diffundieren und dort binden.
Den anderen von dir angesprochenen Punkt kann ich nicht einschätzen, da ich kein Biologe/Mediziner bin: So wie ich Cytomx verstanden habe werden bestimmte zu Demaskierung geeignete Proteasen nur in Tumoren gebildet und nicht in gesundem Gewebe. D.h. auch nicht in den von dir benannten Prozessen. Diese Proteasen sollten dann nicht demaskierend wirken, wenn Cytomx diese richtig designet hat und deren Annahmen korrekt sind...
meine Rückfrage war gemein. Wenn Cytomx von ersten klinischen Daten in HJ2 2017 spricht kann es per se keine Daten einer Interimsanalyse (d.h. erste klinische Daten) vorher geben.
Zu deinen anderen Punkten: Die präklinischen Daten lassen bereits darauf schließen, dass die Maskierung ein kleines Stück Wirksamkeit kostet. Sollte es aber wirklich zu den präklinisch beobachteten Effekten einer x fach besseren Sicherheit, auch nur im Bruchteil kommen, dann gibt es einen Erfolg.
Das von dir angesprochene Risiko aus Punkt "Bei b)" sehe ich zwar auch, aber mit einer leicht anderen Befürchtung/Begründung. Es könnte m.E. das Risiko bestehen, dass die Maskierung im Tumor Enviroment (wenn die Proteasen aktiv sind) zwar entfernt wird, der demaskierte Anitikörper dann aber (demaskiert) nicht (nur) im Tumor bindet, sondern größere Anteile wieder an heathy tissue diffundieren und dort binden.
Den anderen von dir angesprochenen Punkt kann ich nicht einschätzen, da ich kein Biologe/Mediziner bin: So wie ich Cytomx verstanden habe werden bestimmte zu Demaskierung geeignete Proteasen nur in Tumoren gebildet und nicht in gesundem Gewebe. D.h. auch nicht in den von dir benannten Prozessen. Diese Proteasen sollten dann nicht demaskierend wirken, wenn Cytomx diese richtig designet hat und deren Annahmen korrekt sind...
Antwort auf Beitrag Nr.: 53.834.333 von Ville7 am 06.12.16 10:19:26Hi ville,
"...demaskiert wird... und größere Anteile in healthy tissue binden...."
aus meiner Sicht beruhigt die Veröffentlichung von Daten über den cd166-pdc, siehe publications auf der cytomx-Seite.
Wenn die Diffundierung des demaskierten cd-166 ein K.O.-Kriterium für die Technologie wäre, hätte das cynomolgus- oder xenograft-Modell durch jeweilige Toxizitätsmarker (vgl. S.29 Präsentation) reagiert.
Die Theorie der Aufkonzentrierung in Tumornähe und der folgenden ausreichend hohen Internalisierung zur Auslösung einer zytotoxischen Wirkung funktioniert.
Diese Wirkung ist ja durch die schnelle Zellteilung der Krebszelle noch potenziert, da deren Spindelapparat gehemmt wird.
Es gibt wahrscheinlich um ein vielfaches mehr Bindungsstellen cd166 in gesundem Gewebe, aber damit wird für die einzelne Zelle zumeist nicht die Toxizitätsschwelle erreicht.
"...demaskiert wird... und größere Anteile in healthy tissue binden...."
aus meiner Sicht beruhigt die Veröffentlichung von Daten über den cd166-pdc, siehe publications auf der cytomx-Seite.
Wenn die Diffundierung des demaskierten cd-166 ein K.O.-Kriterium für die Technologie wäre, hätte das cynomolgus- oder xenograft-Modell durch jeweilige Toxizitätsmarker (vgl. S.29 Präsentation) reagiert.
Die Theorie der Aufkonzentrierung in Tumornähe und der folgenden ausreichend hohen Internalisierung zur Auslösung einer zytotoxischen Wirkung funktioniert.
Diese Wirkung ist ja durch die schnelle Zellteilung der Krebszelle noch potenziert, da deren Spindelapparat gehemmt wird.
Es gibt wahrscheinlich um ein vielfaches mehr Bindungsstellen cd166 in gesundem Gewebe, aber damit wird für die einzelne Zelle zumeist nicht die Toxizitätsschwelle erreicht.
Antwort auf Beitrag Nr.: 53.834.333 von Ville7 am 06.12.16 10:19:26
Für die Präklinik zutreffend. Für den Menschen wird man das letztlich erst im Rahmen der klinischen Studien beurteilen können, weil es auf das jeweilige CD-Muster ankommt, das zwischen Mensch und Tier meistens stärker differiert (im Tiermodell weist nur das Tumorgewebe ein humanes CD-Muster auf).
Zustimmung
Angesichts der hohen Affinität zwischen Tumorantigen und therapeutischem Antikörper dürfte diesbezüglich kein Anlaß zur Sorge bestehen.
Richtig.
PS: Canaan verkauft nach einem etwas eigenwilligen Schema. Im Mai/Juni wurde zu Kursen um 10 USD verkauft, anschließend, als der Kurs auf über 17 USD anstieg, keine Verkäufe, im November wurde dann wieder bei Kursen um 11 USD verkauft. Diese unter wirtschaftlichen Aspekten eher unsinnige Verkaufsstrategie kann eigentlich nur CytomX-fremde Gründe haben.
PPS: Mit User "Probody" habe ich nichts zu tun. Ich beschränke meine Aktivitäten auch nicht auf ein Unternehmen/eine Technik.
Zitat von Ville7: Die präklinischen Daten lassen bereits darauf schließen, dass die Maskierung ein kleines Stück Wirksamkeit kostet.
Für die Präklinik zutreffend. Für den Menschen wird man das letztlich erst im Rahmen der klinischen Studien beurteilen können, weil es auf das jeweilige CD-Muster ankommt, das zwischen Mensch und Tier meistens stärker differiert (im Tiermodell weist nur das Tumorgewebe ein humanes CD-Muster auf).
Zitat von Ville7: Sollte es aber wirklich zu den präklinisch beobachteten Effekten einer x fach besseren Sicherheit, auch nur im Bruchteil kommen, dann gibt es einen Erfolg.
Zustimmung
Zitat von Ville7: Das von dir angesprochene Risiko aus Punkt "Bei b)" sehe ich zwar auch, aber mit einer leicht anderen Befürchtung/Begründung. Es könnte m.E. das Risiko bestehen, dass die Maskierung im Tumor Enviroment (wenn die Proteasen aktiv sind) zwar entfernt wird, der demaskierte Anitikörper dann aber (demaskiert) nicht (nur) im Tumor bindet, sondern größere Anteile wieder an heathy tissue diffundieren und dort binden.
Angesichts der hohen Affinität zwischen Tumorantigen und therapeutischem Antikörper dürfte diesbezüglich kein Anlaß zur Sorge bestehen.
Zitat von Ville7: Den anderen von dir angesprochenen Punkt kann ich nicht einschätzen, da ich kein Biologe/Mediziner bin: So wie ich Cytomx verstanden habe werden bestimmte zu Demaskierung geeignete Proteasen nur in Tumoren gebildet und nicht in gesundem Gewebe. D.h. auch nicht in den von dir benannten Prozessen. Diese Proteasen sollten dann nicht demaskierend wirken, wenn Cytomx diese richtig designet hat und deren Annahmen korrekt sind...
Richtig.
PS: Canaan verkauft nach einem etwas eigenwilligen Schema. Im Mai/Juni wurde zu Kursen um 10 USD verkauft, anschließend, als der Kurs auf über 17 USD anstieg, keine Verkäufe, im November wurde dann wieder bei Kursen um 11 USD verkauft. Diese unter wirtschaftlichen Aspekten eher unsinnige Verkaufsstrategie kann eigentlich nur CytomX-fremde Gründe haben.
PPS: Mit User "Probody" habe ich nichts zu tun. Ich beschränke meine Aktivitäten auch nicht auf ein Unternehmen/eine Technik.
Lesezeichen !
Antwort auf Beitrag Nr.: 53.835.941 von Joschka Schröder am 06.12.16 14:07:32Ok, Stil und Inhalt erinnerte mich an dich... wer dann auch immer user Probody ist
Immune System, Unleashed by Cancer Therapies, Can Attack Organs - NY Times 3.12.2016
http://www.nytimes.com/2016/12/03/health/immunotherapy-cance…
http://www.nytimes.com/2016/12/03/health/immunotherapy-cance…
Nütze die heutige "Schwäche" mal für eine kleine Position in Cymtox.
Antwort auf Beitrag Nr.: 53.877.627 von Trapos am 12.12.16 18:19:34
solch einen `toxischen´Namen würde sich ein Pharmaunternehmen niemals geben; das Gegenteil ist der Fall, sie wollen die Toxizität hemmen
Zitat von Trapos: Nütze die heutige "Schwäche" mal für eine kleine Position in Cymtox.
solch einen `toxischen´Namen würde sich ein Pharmaunternehmen niemals geben; das Gegenteil ist der Fall, sie wollen die Toxizität hemmen
Antwort auf Beitrag Nr.: 53.877.951 von infomi am 12.12.16 19:16:45Okay, kleiner Tipfehler.

CytomX Announces Selection by Bristol-Myers Squibb of First Clinical Candidate Probody From Collaboration
CTLA-4 Probody Moves to IND-Enabling Studies
SOUTH SAN FRANCISCO, Calif., Dec. 13, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that Bristol-Myers Squibb Company has selected a clinical candidate for its CTLA-4 Probody program under the strategic oncology collaboration established in May 2014. Achieving this milestone results in a $2 million payment to CytomX.
“Selecting a candidate for the CTLA-4 Probody program is a pivotal development in our partnership with CytomX Therapeutics and builds on our I.O. leadership,” said Carl Decicco, Ph. D., Head of Discovery at Bristol-Myers Squibb. “We are studying the CTLA-4 Probody for its potential to deliver a next-generation anti-CTLA-4 therapy as we continue to explore transformational immuno-oncology medicines.”
CTLA-4, a clinically validated inhibitory immune checkpoint protein, is the most advanced target from the companies’ collaboration, which now also includes three additional, unnamed targets in discovery.
“Advancing our CTLA-4 Probody program to clinical candidate stage with Bristol-Myers Squibb underscores the potential of the Probody platform to transform the field of immuno-oncology by delivering safer, more effective therapies,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX. “This partnership milestone, taken together with CytomX’s recently filed Investigational New Drug application for CX-072, a wholly owned PD-L1-directed Probody therapeutic, highlights the potential of our innovative platform to deliver a new generation of anti-cancer treatments.”
About the Collaboration Agreement
Under the terms of the May 2014 agreement, CytomX granted Bristol-Myers Squibb exclusive worldwide rights to discover, develop and commercialize Probody therapeutics for up to four oncology targets. Bristol-Myers Squibb made an upfront payment of $50 million to CytomX in 2014, and is providing research funding over the course of the research term. Upon the selection of the third and fourth targets, Bristol-Myers Squibb paid CytomX selection payments. CytomX is also eligible to receive additional preclinical payments and up to $298 million in development, regulatory and sales milestone payments for each collaboration target, as well as tiered royalties rising from mid-single digit to low double digits on net sales of each product commercialized by Bristol-Myers Squibb.
About CytomX Therapeutics
CytomX is an oncology-focused biopharmaceutical company pioneering a novel class of investigational antibody therapeutics based on its Probody technology platform. The Company uses the platform to create proprietary cancer immunotherapies against clinically-validated targets, as well as to develop first-in-class investigational cancer therapeutics against novel targets. CytomX believes that its Probody platform has the potential to improve the combined efficacy and safety profile of monoclonal antibody modalities, including cancer immunotherapies, antibody drug conjugates and T-cell-recruiting bispecific antibodies. Probody therapeutics are designed to take advantage of unique conditions in the tumor microenvironment to enhance the tumor-targeting features of an antibody and reduce drug activity in healthy tissues. The Company’s investigational Probody therapeutics address clinically-validated cancer targets in immuno-oncology, such as PD-L1, against which the clinical candidate CX-072 is directed, as well as novel targets, such as CD-166, that are difficult to drug without causing damage to healthy tissues. In addition to its proprietary programs, CytomX is collaborating with strategic partners including AbbVie, Bristol-Myers Squibb Company, Pfizer Inc., MD Anderson Cancer Center and ImmunoGen, Inc. For more information, visit www.cytomx.com.
CTLA-4 Probody Moves to IND-Enabling Studies
SOUTH SAN FRANCISCO, Calif., Dec. 13, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that Bristol-Myers Squibb Company has selected a clinical candidate for its CTLA-4 Probody program under the strategic oncology collaboration established in May 2014. Achieving this milestone results in a $2 million payment to CytomX.
“Selecting a candidate for the CTLA-4 Probody program is a pivotal development in our partnership with CytomX Therapeutics and builds on our I.O. leadership,” said Carl Decicco, Ph. D., Head of Discovery at Bristol-Myers Squibb. “We are studying the CTLA-4 Probody for its potential to deliver a next-generation anti-CTLA-4 therapy as we continue to explore transformational immuno-oncology medicines.”
CTLA-4, a clinically validated inhibitory immune checkpoint protein, is the most advanced target from the companies’ collaboration, which now also includes three additional, unnamed targets in discovery.
“Advancing our CTLA-4 Probody program to clinical candidate stage with Bristol-Myers Squibb underscores the potential of the Probody platform to transform the field of immuno-oncology by delivering safer, more effective therapies,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX. “This partnership milestone, taken together with CytomX’s recently filed Investigational New Drug application for CX-072, a wholly owned PD-L1-directed Probody therapeutic, highlights the potential of our innovative platform to deliver a new generation of anti-cancer treatments.”
About the Collaboration Agreement
Under the terms of the May 2014 agreement, CytomX granted Bristol-Myers Squibb exclusive worldwide rights to discover, develop and commercialize Probody therapeutics for up to four oncology targets. Bristol-Myers Squibb made an upfront payment of $50 million to CytomX in 2014, and is providing research funding over the course of the research term. Upon the selection of the third and fourth targets, Bristol-Myers Squibb paid CytomX selection payments. CytomX is also eligible to receive additional preclinical payments and up to $298 million in development, regulatory and sales milestone payments for each collaboration target, as well as tiered royalties rising from mid-single digit to low double digits on net sales of each product commercialized by Bristol-Myers Squibb.
About CytomX Therapeutics
CytomX is an oncology-focused biopharmaceutical company pioneering a novel class of investigational antibody therapeutics based on its Probody technology platform. The Company uses the platform to create proprietary cancer immunotherapies against clinically-validated targets, as well as to develop first-in-class investigational cancer therapeutics against novel targets. CytomX believes that its Probody platform has the potential to improve the combined efficacy and safety profile of monoclonal antibody modalities, including cancer immunotherapies, antibody drug conjugates and T-cell-recruiting bispecific antibodies. Probody therapeutics are designed to take advantage of unique conditions in the tumor microenvironment to enhance the tumor-targeting features of an antibody and reduce drug activity in healthy tissues. The Company’s investigational Probody therapeutics address clinically-validated cancer targets in immuno-oncology, such as PD-L1, against which the clinical candidate CX-072 is directed, as well as novel targets, such as CD-166, that are difficult to drug without causing damage to healthy tissues. In addition to its proprietary programs, CytomX is collaborating with strategic partners including AbbVie, Bristol-Myers Squibb Company, Pfizer Inc., MD Anderson Cancer Center and ImmunoGen, Inc. For more information, visit www.cytomx.com.
FDA OKs CytomX's IND for lead product candidate
Dec. 14, 2016 12:23 PM ET
The FDA approves CytomX Therapeutics' (CTMX -1.9%) Investigational New Drug (IND) application for lead product candidate CX-072, a PD-L1-targeting Probody therapeutic for the treatment of cancer.
The company intends to promptly initiate a Phase 1/2 study, PROCLAIM-072, an open-label, dose-finding trial assessing CX-072 as monotherapy and in combination with Bristol-Myers Sqibb's (BMY +1.5%) Yervoy (ipilimumab) or Roche's (OTCQX:RHHBY) Zelboraf (vemurafenib) in patients with metastatic or locally advanced unresectable solid tumors or lymphomas.
Top-line data are expected in late 2017 and throughout 2018.
Dec. 14, 2016 12:23 PM ET
The FDA approves CytomX Therapeutics' (CTMX -1.9%) Investigational New Drug (IND) application for lead product candidate CX-072, a PD-L1-targeting Probody therapeutic for the treatment of cancer.
The company intends to promptly initiate a Phase 1/2 study, PROCLAIM-072, an open-label, dose-finding trial assessing CX-072 as monotherapy and in combination with Bristol-Myers Sqibb's (BMY +1.5%) Yervoy (ipilimumab) or Roche's (OTCQX:RHHBY) Zelboraf (vemurafenib) in patients with metastatic or locally advanced unresectable solid tumors or lymphomas.
Top-line data are expected in late 2017 and throughout 2018.
bin seit ca 3 monaten in diesem wert dabei. bin alles andere als ein biotech experte, lese gerne in diesem forum.
Antwort auf Beitrag Nr.: 53.835.941 von Joschka Schröder am 06.12.16 14:07:32Auf Twitter gab es nun etwas Aufmerksamkeit vom user C. McCatface, PhD (@Biotech_cat) für CytomX:
I find this whole idea that there are proteases which are tumor specific and universal across patients a little hard to swallow $CTMX
@JohnShaffer3 probably but I think proving equivalency may be tough. Every subject will have different exposure to active Ab. Messy
@JohnShaffer3 it's just such an unknown. Have they ever shared data on what proteases are relevant & expression across a group of patients?
@JohnShaffer3 looks like they've published a decent amount of stuff, I'll have to dig further.
@JasonHolman5 So best case they have best in class PDL1, worst case proteases don't cleave sufficiently & Ab does nothing.
@JasonHolman5 I think most likely outcome is immunotox is mitigated but efficacy also takes a hit. Then what? Super interesting though...
Ich kann diese Punkte nur sehr grob einschätzen als Laie. Der User scheint jedoch ein Fachmann zu sein - er hat einen Artikel zur Firma Cellectar Biosciences, Inc. verfasst, die mit ihrer PDC (phospholipid drug conjugates) Platform dem ADC Ansatz überlegen sein soll und auch wieder das Potential haben soll die Krebstherapie entscheidend zu beeinflussen, da die Therapien effektiver, zielgerichteter und mit geringerer Toxizität durchgeführt werden können:
https://www.scribd.com/mobile/document/333479494/clrb-one-pa…
Die Firma ist winzig, hier der Link zur Plattform:
http://cellectar.com/pdc-platform/
Ausserdem hält der user noch für möglich/wahrscheinlich, dass die Biotest AG die Firma ADMA Biologics übernehmen wird. Finde seine Beiträge alle recht interessant und lesenswert.
I find this whole idea that there are proteases which are tumor specific and universal across patients a little hard to swallow $CTMX
@JohnShaffer3 probably but I think proving equivalency may be tough. Every subject will have different exposure to active Ab. Messy
@JohnShaffer3 it's just such an unknown. Have they ever shared data on what proteases are relevant & expression across a group of patients?
@JohnShaffer3 looks like they've published a decent amount of stuff, I'll have to dig further.
@JasonHolman5 So best case they have best in class PDL1, worst case proteases don't cleave sufficiently & Ab does nothing.
@JasonHolman5 I think most likely outcome is immunotox is mitigated but efficacy also takes a hit. Then what? Super interesting though...
Ich kann diese Punkte nur sehr grob einschätzen als Laie. Der User scheint jedoch ein Fachmann zu sein - er hat einen Artikel zur Firma Cellectar Biosciences, Inc. verfasst, die mit ihrer PDC (phospholipid drug conjugates) Platform dem ADC Ansatz überlegen sein soll und auch wieder das Potential haben soll die Krebstherapie entscheidend zu beeinflussen, da die Therapien effektiver, zielgerichteter und mit geringerer Toxizität durchgeführt werden können:
https://www.scribd.com/mobile/document/333479494/clrb-one-pa…
Die Firma ist winzig, hier der Link zur Plattform:
http://cellectar.com/pdc-platform/
Ausserdem hält der user noch für möglich/wahrscheinlich, dass die Biotest AG die Firma ADMA Biologics übernehmen wird. Finde seine Beiträge alle recht interessant und lesenswert.
Antwort auf Beitrag Nr.: 54.037.288 von SpanishEyes am 08.01.17 23:50:12Noch ein paar Vergleiche zwischen CTMX und CLRB vom user C. McCatface, PhD (@Biotech_cat) auf Twitter:
$CLRB only $12M while being much more advanced clinically. $CTMX hasn't even dosed a patient in p1, CLRB about to embark on p2 for lead.
Difference is 1) partners 2) $$$. $CTMX sitting on $180M, partnered with $BMY $ABBV etc. $CLRB poor, only partnered with Pierre Fabre.
Yet $CLRB has at least as much potential as $CTMX. They need a few more deals & they will also be sporting a $400M cap.
Klingt sehr verlockend, too good to be true?
$CLRB only $12M while being much more advanced clinically. $CTMX hasn't even dosed a patient in p1, CLRB about to embark on p2 for lead.
Difference is 1) partners 2) $$$. $CTMX sitting on $180M, partnered with $BMY $ABBV etc. $CLRB poor, only partnered with Pierre Fabre.
Yet $CLRB has at least as much potential as $CTMX. They need a few more deals & they will also be sporting a $400M cap.
Klingt sehr verlockend, too good to be true?
Antwort auf Beitrag Nr.: 54.038.302 von SpanishEyes am 09.01.17 09:07:17Ich denke schon, dass es nachvollziehbare Gründe gibt, wieso Cellectra an der Börse quasi nichts wert ist:
1) Die verwendeten Alkylphosphocholine binden viel zu unspezifisch an Tumorzellmembranen (in Cellectras Basisarbeiten ist im Vergeich zu gesundem Gewebe von einem Faktor (ca.) 3 die Rede. Ich würde meinen Körper nicht freiwillig auf diese Weise einer kombinierten Beta-/Gammerstrahlung aussetzen.
2) In der Unternehmensführung sucht man vergeblich nach Leuten mit wissenschaftlicher Expertise.
3) Der Trackrekord des Unternehmens ist genauso schauerlich wie die Entwicklung des Aktienkurses während der letzten zehn Jahre.
Da die Aktie aktuell von einigen Seiten kräftig gepusht wird, können Zocker möglicherweise in überschaubarem Zeitraum einige hundert Prozent Gewinn einfahren. Dem steht allerdings die Gefahr eines Totalverlustes gegenüber. Es kommt vermutlich darauf an, an welcher Position man sich in der Verwertungskette befindet.
Vielleicht stöbere ich in den nächsten Tagen noch ein wenig in den wissenschaftlichen Publikationen der Gesellschaft herum.
1) Die verwendeten Alkylphosphocholine binden viel zu unspezifisch an Tumorzellmembranen (in Cellectras Basisarbeiten ist im Vergeich zu gesundem Gewebe von einem Faktor (ca.) 3 die Rede. Ich würde meinen Körper nicht freiwillig auf diese Weise einer kombinierten Beta-/Gammerstrahlung aussetzen.
2) In der Unternehmensführung sucht man vergeblich nach Leuten mit wissenschaftlicher Expertise.
3) Der Trackrekord des Unternehmens ist genauso schauerlich wie die Entwicklung des Aktienkurses während der letzten zehn Jahre.
Da die Aktie aktuell von einigen Seiten kräftig gepusht wird, können Zocker möglicherweise in überschaubarem Zeitraum einige hundert Prozent Gewinn einfahren. Dem steht allerdings die Gefahr eines Totalverlustes gegenüber. Es kommt vermutlich darauf an, an welcher Position man sich in der Verwertungskette befindet.
Vielleicht stöbere ich in den nächsten Tagen noch ein wenig in den wissenschaftlichen Publikationen der Gesellschaft herum.
Antwort auf Beitrag Nr.: 54.050.689 von Joschka Schröder am 10.01.17 16:27:56Muss natürlich heißen "Beta-/Gammastrahlung"
Antwort auf Beitrag Nr.: 54.050.689 von Joschka Schröder am 10.01.17 16:27:56"Verwertungskette" gefällt mir 

Antwort auf Beitrag Nr.: 54.050.689 von Joschka Schröder am 10.01.17 16:27:56Vielen Dank für deine Einschätzung Joschka. Bin immernoch dabei zu lernen im Biotech Bereich... Punkt 2 war mir auch aufgefallen.
Punkt 3 und das mit den Pusher Briefen hat der o.g. Twitter User selbst "kritisiert". Es habe sich seit dem neuen CEO 2015 die Firma zum positiven verändert...
Ich denke am Ende entscheidend ist die wissenschaftliche Grundlage, die kann ich leider nicht beurteilen... als Laie fand ich die Ausführungen des Users diesbzgl. nachvollziehbar und dem Anschein nach kompetent, insbesondere seine 2 Artikel auf scribd.com (der Link scheint oben nicht zu funktionieren, aus Twitter heraus funktioniert er)... eine andere Userin auf Twitter die ich grdstzl als kompetent und seriös einstufe hatte sich auch grdstzl positv über CLRB geäussert... falls du Zeit und Gelegenheit hast würde mich das Ergebnis deiner allfällig tiefer gehenden Analyse sehr interessieren.
In jedem Fall bereits jetzt besten Dank, dass du dir Zeit genommen hast einen Blick auf CLRB zu werfen
Punkt 3 und das mit den Pusher Briefen hat der o.g. Twitter User selbst "kritisiert". Es habe sich seit dem neuen CEO 2015 die Firma zum positiven verändert...
Ich denke am Ende entscheidend ist die wissenschaftliche Grundlage, die kann ich leider nicht beurteilen... als Laie fand ich die Ausführungen des Users diesbzgl. nachvollziehbar und dem Anschein nach kompetent, insbesondere seine 2 Artikel auf scribd.com (der Link scheint oben nicht zu funktionieren, aus Twitter heraus funktioniert er)... eine andere Userin auf Twitter die ich grdstzl als kompetent und seriös einstufe hatte sich auch grdstzl positv über CLRB geäussert... falls du Zeit und Gelegenheit hast würde mich das Ergebnis deiner allfällig tiefer gehenden Analyse sehr interessieren.
In jedem Fall bereits jetzt besten Dank, dass du dir Zeit genommen hast einen Blick auf CLRB zu werfen
Die Präsentation von der JP Morgan Healthcare-Conference ist abrufbar.
Beeindruckend ist die geringe cash burn rate (5 mio$) in 2016, bei dennoch planmäßiger Entwicklung der breiten pipeline.
Cytomx ist jetzt bis ins Jahr 2019 hinein durchfinanziert.
Neue Allianzen sind 2017 denkbar.
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-EventDeta…
Beeindruckend ist die geringe cash burn rate (5 mio$) in 2016, bei dennoch planmäßiger Entwicklung der breiten pipeline.
Cytomx ist jetzt bis ins Jahr 2019 hinein durchfinanziert.
Neue Allianzen sind 2017 denkbar.
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-EventDeta…
Antwort auf Beitrag Nr.: 54.054.187 von SpanishEyes am 10.01.17 23:46:17* immer noch
Antwort auf Beitrag Nr.: 54.071.444 von infomi am 12.01.17 19:20:51Tempting to open a small position in CLRB .
Maybe chance of a lifetime?
Maybe chance of a lifetime?
Applied BioMath, LLC and CytomX Therapeutics, Inc. announce a collaboration to develop a Quantitative Systems Pharmacology Probody platform model for use in lmmuno-Oncology
http://www.prnewswire.com/news-releases/applied-biomath-llc-…
http://www.prnewswire.com/news-releases/applied-biomath-llc-…
CytomX Announces the First Patient Treated in Phase 1/2 PROCLAIM-072 Trial
SOUTH SAN FRANCISCO, Calif., February 2, 2016 (GLOBE NEWSWIRE) — CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced the treatment of the first patient in the PROCLAIM (Probody Clinical Assessment In Man) CX-072 study, a Phase 1/2 clinical trial evaluating CX-072, a PD-L1-targeting Probody therapeutic, as monotherapy and in combination with Yervoy® (ipilimumab) or Zelboraf®(vemurafenib) in patients with all types of cancers
Nach dem von der FDA abgesegneten Studiendesign ist die erste Behandlung eines Patienten gestartet.
Bei klinischen Studien sind immer die ersten Patienten die zeitverzögernde Phase.
Wenn bei denen sich keine allergischen Reaktionen ergeben haben, beschleunigt sich die Rekrutierung der auf 2 Jahre angesetzten klinischen Studie mit 150 Patienten.
Das Ergebnis dieser Studie wird schon eine bedeutende Aussagefähigkeit für die schlüssige Prodrug-Theorie des cytomx-business-Modells sein.
SOUTH SAN FRANCISCO, Calif., February 2, 2016 (GLOBE NEWSWIRE) — CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced the treatment of the first patient in the PROCLAIM (Probody Clinical Assessment In Man) CX-072 study, a Phase 1/2 clinical trial evaluating CX-072, a PD-L1-targeting Probody therapeutic, as monotherapy and in combination with Yervoy® (ipilimumab) or Zelboraf®(vemurafenib) in patients with all types of cancers
Nach dem von der FDA abgesegneten Studiendesign ist die erste Behandlung eines Patienten gestartet.
Bei klinischen Studien sind immer die ersten Patienten die zeitverzögernde Phase.
Wenn bei denen sich keine allergischen Reaktionen ergeben haben, beschleunigt sich die Rekrutierung der auf 2 Jahre angesetzten klinischen Studie mit 150 Patienten.
Das Ergebnis dieser Studie wird schon eine bedeutende Aussagefähigkeit für die schlüssige Prodrug-Theorie des cytomx-business-Modells sein.
CytomX to Present at Upcoming Investor Conferences
SOUTH SAN FRANCISCO, Calif., Feb. 02, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that the company’s management will participate in two upcoming investor conferences.
Bob Goeltz, chief financial officer, will participate in a company fireside chat at the 6th Annual LEERINK Partners Global Healthcare Conference on Thursday, February 16, 2017, at 1:00 p.m. ET.
Sean McCarthy, D. Phil., president and chief executive officer, will participate in a company fireside chat at the RBC Capital Markets 2017 Global Healthcare Conference on Thursday, February 23, 2017, at 1:35 p.m. ET.
A live audio webcast for each event will be available through the Investors and News section of CytomX's website. An archived replay will be available for 90 days following the event.
SOUTH SAN FRANCISCO, Calif., Feb. 02, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that the company’s management will participate in two upcoming investor conferences.
Bob Goeltz, chief financial officer, will participate in a company fireside chat at the 6th Annual LEERINK Partners Global Healthcare Conference on Thursday, February 16, 2017, at 1:00 p.m. ET.
Sean McCarthy, D. Phil., president and chief executive officer, will participate in a company fireside chat at the RBC Capital Markets 2017 Global Healthcare Conference on Thursday, February 23, 2017, at 1:35 p.m. ET.
A live audio webcast for each event will be available through the Investors and News section of CytomX's website. An archived replay will be available for 90 days following the event.
Bin jetzt auch in die Aktie eingestiegen.
Mich überzeugt das Potenzial der Maskierungstechnologie. Hoffe der Ansatz kann das halten was die Präklink verspricht - und findet dann eine möglichst breite Anwendung.
DANKE an alle, für die tollen Informationen, welche hier schon eingestellt sind.
Mich überzeugt das Potenzial der Maskierungstechnologie. Hoffe der Ansatz kann das halten was die Präklink verspricht - und findet dann eine möglichst breite Anwendung.
DANKE an alle, für die tollen Informationen, welche hier schon eingestellt sind.
Ich möchte auch einsteigen, warte aber noch auf Eingriffe ins Gesundheitswesen von Donald.
Antwort auf Beitrag Nr.: 54.278.543 von gunar_s am 09.02.17 10:48:30Der kurs ist nach wie vor unverändert, moglw. die Ruhe vor dem Sturm
Lesezeichen
Wurde die Aktie endlich von der Leine gelassen?
Wo steckt eigentlich Joschka Schröder ?
Hoffe mal das bei ihm alles klar ist!
Ich vermisse seine sehr guten Beiträge hier bei WO.
Hoffentlich hat er sich nicht wie einige andere Mitglieder
von den verschiedene dummpraddlern vertreiben lassen.
Hoffe mal das bei ihm alles klar ist!
Ich vermisse seine sehr guten Beiträge hier bei WO.
Hoffentlich hat er sich nicht wie einige andere Mitglieder
von den verschiedene dummpraddlern vertreiben lassen.
denke ich nicht :-)
Die guten Beiträge von Joschka vermisse ich auch dafür läuft die Aktie....
Bisher läuft alles nach Plan. Entscheidend werden die Ergebnisse der ersten zwei AKs sein. Die ersten Ergebnisse sind weiterhin auf Ende 2017/Anfang 2018 angekündigt.
mir scheint, der CEO nutzt den stark angestiegenen Kurs um ein paar seiner Optionen zu Geld zu machen:
http://ih.advfn.com/p.php?pid=nmona&article=74013515#DOC1_HT…
sei´s ihm gegönnt, fundamental dürfte das ohne Bedeutung sein
http://ih.advfn.com/p.php?pid=nmona&article=74013515#DOC1_HT…
sei´s ihm gegönnt, fundamental dürfte das ohne Bedeutung sein
Heute ganz schön zerrissen. Viel von Anstieg gleich in einen Tag wieder weg.
Hoffe das dies nur momentan Zockerei ist und keine fundamentalen Gründe hat.
Hoffe das dies nur momentan Zockerei ist und keine fundamentalen Gründe hat.
Antwort auf Beitrag Nr.: 54.476.319 von infomi am 06.03.17 16:10:10aktienoptionen haben meines erachtens in diesem stadium einer unternehmensentwicklung nichts verloren, da sie meistens verwirrung stiften. biotechs sind über weite strecken von phase 1-3 sehr nachrichtenarm und umso größer ist der einfluß solcher entlohnungsinstrumente.
THIRD ROCK VENTURES LP reduziert deren Anteil an CytomX: http://insideri.com/1578976_000089924317007785_0000899243-17…
Morgen ein spontanes Update!? Das ist ja selten was Gutes. Hoffe natürlich, dass ich mich irre...
http://www.nasdaq.com/press-release/cytomx-therapeutics-anno…
http://www.nasdaq.com/press-release/cytomx-therapeutics-anno…
Antwort auf Beitrag Nr.: 54.567.810 von kmastra am 20.03.17 00:20:59Jep, der Einschätzung kann ich nur zustimmen... und das alles angesetzt ohne bisher eine Pressemitteilung vorab. Da schießen die Spekulationen wild ins Kraut.
Natürlich denkt man da zuerst und vor allem an negative Nachrichten, da fällt einem natürlich sofort der maskierte anti-PD-L1 Antikörper ein, der seit Januar in der Klinik ist und vielleicht zeigt dieser in der Klinik unerwartete Nebenwirkungen an Menschen. Das ist es an was ich als erstes gedacht habe. Das Timing dazu könnte absolut passen.
Wahrscheinlichkeit für mich: mittel bis hoch
Recht fishy wäre das natürlich in Verbindung mit der Nachricht von vor weniger als 10 Tagen: "Cytomx Therapeutics announces proposed resale of up to 10.9 mln shares by selling stockholders" und dass ein anderer Insider (letztes Jahr) schon länger regelmäßig verkauft.
Wenn man sich selbst Hoffnung machen möchte käme auch noch folgendes in Frage: Ein vorliegendes (feindliches) Übernahmeangebot (z.B. von BMS), welches die Firma publik machen muss / möchte.
Wahrscheinlichkeit für mich: mittel
Oder eine neue Kooperation.
Wahrscheinlichkeit für mich: gering
Es ist aber wie kmastra sagt recht unüblich für Biotechs diese positiven Infos nicht weit vor einem Call rauszuhauen. Zumal die Börse ja geschlossen hat.
Also ich mach mich auch schon mal aufs Schlimmste gefasst...
Natürlich denkt man da zuerst und vor allem an negative Nachrichten, da fällt einem natürlich sofort der maskierte anti-PD-L1 Antikörper ein, der seit Januar in der Klinik ist und vielleicht zeigt dieser in der Klinik unerwartete Nebenwirkungen an Menschen. Das ist es an was ich als erstes gedacht habe. Das Timing dazu könnte absolut passen.
Wahrscheinlichkeit für mich: mittel bis hoch
Recht fishy wäre das natürlich in Verbindung mit der Nachricht von vor weniger als 10 Tagen: "Cytomx Therapeutics announces proposed resale of up to 10.9 mln shares by selling stockholders" und dass ein anderer Insider (letztes Jahr) schon länger regelmäßig verkauft.
Wenn man sich selbst Hoffnung machen möchte käme auch noch folgendes in Frage: Ein vorliegendes (feindliches) Übernahmeangebot (z.B. von BMS), welches die Firma publik machen muss / möchte.
Wahrscheinlichkeit für mich: mittel
Oder eine neue Kooperation.
Wahrscheinlichkeit für mich: gering
Es ist aber wie kmastra sagt recht unüblich für Biotechs diese positiven Infos nicht weit vor einem Call rauszuhauen. Zumal die Börse ja geschlossen hat.
Also ich mach mich auch schon mal aufs Schlimmste gefasst...
Letztes Update der PROCLAIM-072 Studie war am 2.3. bzw. 5.3. auf Clinicaltrials.gov. Studie steht dort auf "This study is currently recruiting participants.".
Antwort auf Beitrag Nr.: 54.552.100 von SpanishEyes am 16.03.17 23:20:25
Ja, auch das würde passen. Third Rock Ventures hat am 15.3. alles abgestoßen. 4 Tage vor Ankündigung des ungeplanten Calls.
Also entweder wussten die schon, dass es in der Klinik gerappelt hat und hatten es deswegen sehr eilig oder sie haben ihr Pakete in die Hände eines interessierten Übernehmers gelegt...
Am 15.3. wurden über die Börse 468 Tsd. Stücke gehandelt. Third Rock hat 850 Tsd an diesem Tag laut SEC Filing verkauft. D.h. der Verkauf ging definitiv nicht über die Börse. Ein anderer hat dieses Paket abgenommen.
Zitat von SpanishEyes: THIRD ROCK VENTURES LP reduziert deren Anteil an CytomX: http://insideri.com/1578976_000089924317007785_0000899243-17…
Ja, auch das würde passen. Third Rock Ventures hat am 15.3. alles abgestoßen. 4 Tage vor Ankündigung des ungeplanten Calls.
Also entweder wussten die schon, dass es in der Klinik gerappelt hat und hatten es deswegen sehr eilig oder sie haben ihr Pakete in die Hände eines interessierten Übernehmers gelegt...
Am 15.3. wurden über die Börse 468 Tsd. Stücke gehandelt. Third Rock hat 850 Tsd an diesem Tag laut SEC Filing verkauft. D.h. der Verkauf ging definitiv nicht über die Börse. Ein anderer hat dieses Paket abgenommen.
Habe meine Gewinne vorsichtshalber einmal mitgenommen. Schaue mir in Ruhe an, was heute Abend berichtet wird. ;-)
Wenn's hoffentlich positive Nachrichten sind, muss ich meine Stücke halt teurer wieder einkaufen.
Wenn's hoffentlich positive Nachrichten sind, muss ich meine Stücke halt teurer wieder einkaufen.
Antwort auf Beitrag Nr.: 54.568.677 von gunar_s am 20.03.17 09:09:30Ich muss mich gedulden bis die Nasdag aufsperrt. Da dort gekauft läßt mich der Brocker ohne Aufpreis nur dort verkaufen.
Und so viele Stücke sind es auch nicht.
Und so viele Stücke sind es auch nicht.

Ja sehr schön!
Antwort auf Beitrag Nr.: 54.568.194 von Ville7 am 20.03.17 07:47:37Super News!
Die erweiterte Kooperation mit BMS im Überblick:
* bis zu 8 zusätzliche Targets
* $200 Mio Upfront
* bis zu $448 Mio Meilensteine
* Royalties: ca. 5% bis 12% auf künftige Produktverkäufe hieraus
Cytomix sollte durch das zusätzliche Cash bis 2020 nicht mehr an den Kapitalmarkt müssen und kann bestehende Projekte beschleunigen und weitere Eigen-Projekte anschieben.
* bis zu 8 zusätzliche Targets
* $200 Mio Upfront
* bis zu $448 Mio Meilensteine
* Royalties: ca. 5% bis 12% auf künftige Produktverkäufe hieraus
Cytomix sollte durch das zusätzliche Cash bis 2020 nicht mehr an den Kapitalmarkt müssen und kann bestehende Projekte beschleunigen und weitere Eigen-Projekte anschieben.
,..freude....die Ankündigung dieser News nebst dem Verkauf hat mich nunmehr etliche tausende gekostet...super..
Das ist ein gutes Beispiel für den (Un-)Sinn, den Markt timen zu wollen. Dieses Investment sollte doch auf die generelle Wirksamkeit der Technologie angelegt sein, langfristig ist es völlig wurscht, ob man nun für 3 oder 4$ günstiger investieren konnte.
Antwort auf Beitrag Nr.: 54.568.896 von Trapos am 20.03.17 09:43:57
Manchmal ist es auch gut das man nicht immer aus ersten "Reflexen" handeln kann.
Zitat von Trapos: Ich muss mich gedulden bis die Nasdag aufsperrt. Da dort gekauft läßt mich der Brocker ohne Aufpreis nur dort verkaufen.
Und so viele Stücke sind es auch nicht.
Manchmal ist es auch gut das man nicht immer aus ersten "Reflexen" handeln kann.

Antwort auf Beitrag Nr.: 54.568.896 von Trapos am 20.03.17 09:43:57Nanu überall die gleichen Leute  klingt so als gehe das in Richtung Evotec oder?
klingt so als gehe das in Richtung Evotec oder?
 klingt so als gehe das in Richtung Evotec oder?
klingt so als gehe das in Richtung Evotec oder?
in ist, wer drinn ist . immer die selben - biotech typen
. immer die selben - biotech typen
 . immer die selben - biotech typen
. immer die selben - biotech typen
Antwort auf Beitrag Nr.: 54.572.052 von pegasusorion am 20.03.17 16:57:29Ja immer die gleichen "Zocker" eh sorry Biotech Anleger.
Gut 24% mehr bei Evotec wäre der Wahnsinn für mein Depot.
Hier ist es eine kleine "Beimischung" zu Mor und Evotec was heute ein kleines Plus bringt.
Aber bei Cytomx habe ich noch weniger Ahnung wie von Evotec, daher nur mit geringer Summe dabei.

Gut 24% mehr bei Evotec wäre der Wahnsinn für mein Depot.

Hier ist es eine kleine "Beimischung" zu Mor und Evotec was heute ein kleines Plus bringt.
Aber bei Cytomx habe ich noch weniger Ahnung wie von Evotec, daher nur mit geringer Summe dabei.

Super Deal. Damit hat Cytomx zurzeit 380 Mio Dollar Cash bei einer Marktkapitalisierung von knapp 700 Mio Dollar.
Ich frage mich, wieso Bristol nicht gleich die ganze Firma gekauft hat. Das hätte sie vielleicht 600 Mio kostet. Gibt es Meinungen hierzu?
Ich hab mir gerade die Telefonkonferenz angehört. Hier mal ein paar Stichpunkte.
Ich weiß auch nicht, ob das schon alle verstanden haben, aber die möglichen Meilensteine liegen nicht bei insgesamt 448 Mio Dollar, sondern bei 448 Mio pro Target! Das heißt, bei acht möglichen Targets reden wir hier über fast 3,4 Billionen Dollar (+200 Mio Upfront)!
285 - 305 Mio Dollar Cash sollen Ende 2017 noch vorhanden sein. Das Geld soll bis über das Jahr 2019 hinaus reichen.
BMS hat keine Rechte an den anderen Programmen gekauft.
Die Tatsache, dass auch zwei Nicht-Onkologie-Targets Teil des Deals sind, zeigt, dass die Technologie auch für andere Krankheiten interessant ist. Cytomx selber möchte sich zunächst nur auf Onkologie konzentrieren und andere Targets über neue Allianzen abdecken. Hier können also weitere Deals dieser Art folgen. Diese Aussage wurde in einer Art getätigt, dass ich glaube, dass da dieses Jahr noch was kommt.
Die zwei am weitesten fortschgeschrittenen eigenen Programme sollen weiter voran getrieben werden. Das Geld soll auch zum Teil für "expanision cohorts" dieser Programme ausgegeben werden. Die T-Cell-Forschung soll stärker vorangetrieben werden. Die Daten hier waren wohl sehr gut. Aber auch andere Programme sollen jetzt stärker vorangetrieben werden. Der Fokus für die Verwendung des neuen Geldes ist insgesamt ein wenig mehr auf einer Ausweitung der Programme als auf einer Beschleunigung.
Bei der ASCO soll der klinische Start des zweiten Programmes CX-2009 näher vorgestellt werden.
Ich frage mich, wieso Bristol nicht gleich die ganze Firma gekauft hat. Das hätte sie vielleicht 600 Mio kostet. Gibt es Meinungen hierzu?
Ich hab mir gerade die Telefonkonferenz angehört. Hier mal ein paar Stichpunkte.
Ich weiß auch nicht, ob das schon alle verstanden haben, aber die möglichen Meilensteine liegen nicht bei insgesamt 448 Mio Dollar, sondern bei 448 Mio pro Target! Das heißt, bei acht möglichen Targets reden wir hier über fast 3,4 Billionen Dollar (+200 Mio Upfront)!
285 - 305 Mio Dollar Cash sollen Ende 2017 noch vorhanden sein. Das Geld soll bis über das Jahr 2019 hinaus reichen.
BMS hat keine Rechte an den anderen Programmen gekauft.
Die Tatsache, dass auch zwei Nicht-Onkologie-Targets Teil des Deals sind, zeigt, dass die Technologie auch für andere Krankheiten interessant ist. Cytomx selber möchte sich zunächst nur auf Onkologie konzentrieren und andere Targets über neue Allianzen abdecken. Hier können also weitere Deals dieser Art folgen. Diese Aussage wurde in einer Art getätigt, dass ich glaube, dass da dieses Jahr noch was kommt.
Die zwei am weitesten fortschgeschrittenen eigenen Programme sollen weiter voran getrieben werden. Das Geld soll auch zum Teil für "expanision cohorts" dieser Programme ausgegeben werden. Die T-Cell-Forschung soll stärker vorangetrieben werden. Die Daten hier waren wohl sehr gut. Aber auch andere Programme sollen jetzt stärker vorangetrieben werden. Der Fokus für die Verwendung des neuen Geldes ist insgesamt ein wenig mehr auf einer Ausweitung der Programme als auf einer Beschleunigung.
Bei der ASCO soll der klinische Start des zweiten Programmes CX-2009 näher vorgestellt werden.
@Joschka danke für die gute Idee hier hoffe wir lesen Dich bald wieder
Antwort auf Beitrag Nr.: 54.573.984 von Huusmeister am 20.03.17 20:15:44100% Zustimmung 

Joschka auch danke von mir. Hier bleib ich länger an Bord wie seinerzeit bei Bavarian Biotech.
Antwort auf Beitrag Nr.: 54.574.191 von Boomaktie am 20.03.17 20:45:22Bavarian Nordic heißt das Ding. Seinerzeit (Mitte bis Ende 2011) eine der wenigen Chancen wie man sie nicht oft erwischt. Hättest du gehalten wäre das jetzt nahezu ein Tenbagger. Der Kooperationspartner bei deren PROSTVAC Vaccine ist hier übrigens auch BMS, die auch hier versuchen einen ergänzenden Fit für ihre Immuntherapien zu finden.
Cytomx hat ohne Frage ein ähnliches, wenn nicht sogar größeres, Potential. Wenn alles wie geplant läuft, hat derjenige, der bei 10-12 USD eingestiegen ist m.E. zu ASCO 2018 einen 5- bis 10-bagger in der Hand.
Wir werden sehen. Ohne PoC in der Klinik wird die Technologie keine echte Einpreisung erfahren. Mit gescheiterten PoCs droht hier immer noch Totalverlust.
Im Übrigen gehe ich davon aus, dass die Chancen von CX-072 weit höher sind als die von CX-2009. Wenn beide AKs nen PoC liefern geht es ab wie Schnitzel.
Cytomx hat ohne Frage ein ähnliches, wenn nicht sogar größeres, Potential. Wenn alles wie geplant läuft, hat derjenige, der bei 10-12 USD eingestiegen ist m.E. zu ASCO 2018 einen 5- bis 10-bagger in der Hand.
Wir werden sehen. Ohne PoC in der Klinik wird die Technologie keine echte Einpreisung erfahren. Mit gescheiterten PoCs droht hier immer noch Totalverlust.
Im Übrigen gehe ich davon aus, dass die Chancen von CX-072 weit höher sind als die von CX-2009. Wenn beide AKs nen PoC liefern geht es ab wie Schnitzel.
Nordic heissen die, genau, wie immer hast Du damit recht.
Schauen wir mal etwas in die Zukunft und spinnen optimistisch herum. Konzentrieren wir uns dabei nur auf den PD-(L)1 Checkpoint-Inhibitor von Cytomx (CTMX).
Angenommen CTMX entwickelt den (viel) besseren, weil (viel) verträglicheren Anti-PD1 bzw. Anti-PDL1 Antikörper. Wer würde dann die aktuell entwickelten PD-1 /PD-L1 Antikörper mit den massiven Nebenwirkungen noch einsetzen? Kaum einer. Diese würden in ein Nischen-Dasein verdrängt.
Schauen wir uns mal Schätzungen an zu den bedeutendsten PD-(L)1 Antikörpern von big pharma:
"Bernstein’s own estimates put Tecentriq at $4.9 billion by 2021. It is forecasting Opdivo at $8.1 billion and Keytruda at $6.5 billion, with AstraZeneca’s yet-to-be-approved PD-L1 checkpoint inhibitor running a distant fourth, but still a blockbuster, at $1.8 billion."
Quelle: http://www.fiercepharma.com/pharma/roche-s-tecentriq-wins-fd…
Der Analyst schätzt mehr als 20 Milliarden USD Umsatz / Jahr für diese Umsatzstars bis 2021.
Gehen wir davon aus, dass die beiden (oder einer der) CTMX Antikörper das Potential haben bis 2025 90% dieser Umsätze an sich zu reißen, dann reden wir hier von 20 Milliarden Umsatz.
Annahme:
1. CTMX vermarktet weltweit selbst
2. Sollten die Ergebnisse so disruptive wie der Ansatz sein, dann reden wir hier von einer Serie von breakthrough's für den CTMX Antikörper und einem extrem schnellen Weg zum Markt, den zudem die bisherigen Immunoonkologie-Produkte geebnet haben.
Gehen wir dann davon aus, dass (optimistisch gedacht) CTMX nur noch um 50% der bisherigen Aktienanzahl (36.6 Mio auf 55 Mio Aktien) verwässern muss und (konservativ gedacht) dass 50% des Umsatzes als Gewinn bei CTMX verbleibt: Gewinn 10 Mrd USD vor Steuer. Gehen wir noch von 35% Unternehmenssteuer aus, dann wären das: Gewinn 6.5 Mrd USD nach Steuern.
Das würde zu einem EPS von 118 USD / Aktie führen. Veranschlagen wir ein KGV von 15, dann wären wir bei einen Kurs von ca. 1750 USD je Aktie. Oder im absoluten best-case-szenario einer Ver-100-Fachung ab hier.
Ich wage aber zu behaupten, dass es nie so weit kommen würde, da CTMX dann zuvor übernommen würde. Ein Bieterwettkampf der Platzhirsche könnte den Preis erheblich früher in hohe Sphären treiben.
Man darf träumen, wenn man zudem ganz fest im Hinterkopf behält, dass alles suboptimaler laufen kann, wenn die Technologie nicht oder nicht ansatzweise ihr Versprechen hält.
Dann droht der Aktie im worst case Szenario sogar Totalverlust.
Angenommen CTMX entwickelt den (viel) besseren, weil (viel) verträglicheren Anti-PD1 bzw. Anti-PDL1 Antikörper. Wer würde dann die aktuell entwickelten PD-1 /PD-L1 Antikörper mit den massiven Nebenwirkungen noch einsetzen? Kaum einer. Diese würden in ein Nischen-Dasein verdrängt.
Schauen wir uns mal Schätzungen an zu den bedeutendsten PD-(L)1 Antikörpern von big pharma:
"Bernstein’s own estimates put Tecentriq at $4.9 billion by 2021. It is forecasting Opdivo at $8.1 billion and Keytruda at $6.5 billion, with AstraZeneca’s yet-to-be-approved PD-L1 checkpoint inhibitor running a distant fourth, but still a blockbuster, at $1.8 billion."
Quelle: http://www.fiercepharma.com/pharma/roche-s-tecentriq-wins-fd…
Der Analyst schätzt mehr als 20 Milliarden USD Umsatz / Jahr für diese Umsatzstars bis 2021.
Gehen wir davon aus, dass die beiden (oder einer der) CTMX Antikörper das Potential haben bis 2025 90% dieser Umsätze an sich zu reißen, dann reden wir hier von 20 Milliarden Umsatz.
Annahme:
1. CTMX vermarktet weltweit selbst
2. Sollten die Ergebnisse so disruptive wie der Ansatz sein, dann reden wir hier von einer Serie von breakthrough's für den CTMX Antikörper und einem extrem schnellen Weg zum Markt, den zudem die bisherigen Immunoonkologie-Produkte geebnet haben.
Gehen wir dann davon aus, dass (optimistisch gedacht) CTMX nur noch um 50% der bisherigen Aktienanzahl (36.6 Mio auf 55 Mio Aktien) verwässern muss und (konservativ gedacht) dass 50% des Umsatzes als Gewinn bei CTMX verbleibt: Gewinn 10 Mrd USD vor Steuer. Gehen wir noch von 35% Unternehmenssteuer aus, dann wären das: Gewinn 6.5 Mrd USD nach Steuern.
Das würde zu einem EPS von 118 USD / Aktie führen. Veranschlagen wir ein KGV von 15, dann wären wir bei einen Kurs von ca. 1750 USD je Aktie. Oder im absoluten best-case-szenario einer Ver-100-Fachung ab hier.
Ich wage aber zu behaupten, dass es nie so weit kommen würde, da CTMX dann zuvor übernommen würde. Ein Bieterwettkampf der Platzhirsche könnte den Preis erheblich früher in hohe Sphären treiben.
Man darf träumen, wenn man zudem ganz fest im Hinterkopf behält, dass alles suboptimaler laufen kann, wenn die Technologie nicht oder nicht ansatzweise ihr Versprechen hält.
Dann droht der Aktie im worst case Szenario sogar Totalverlust.
Antwort auf Beitrag Nr.: 54.586.506 von Ville7 am 22.03.17 09:06:32Hier nochmal der wichtige Hinweis, dass der Proof of Concept in der Klinik noch nicht erbracht wurde.
Daher ist das Risiko weiterhin als sehr hoch einzustufen, dass die präklinischen Versprechungen sich gar nicht erfüllen, z.B. weil
a) die Maskierung sich nicht löst
b) der lokale Ansatz keine genügende Immunreaktion auslöst
c) unerwartete Toxizitäten auftreten oder
d) etwas ganz anders unerwartetes ...
Anlage- oder Trading-Investitionen sind daher m.E. mit höchster Vorsicht vorzunehmen und sollten nur geschehen, wenn auch ein Totalverlust hingenommen werden kann.
Daher ist das Risiko weiterhin als sehr hoch einzustufen, dass die präklinischen Versprechungen sich gar nicht erfüllen, z.B. weil
a) die Maskierung sich nicht löst
b) der lokale Ansatz keine genügende Immunreaktion auslöst
c) unerwartete Toxizitäten auftreten oder
d) etwas ganz anders unerwartetes ...
Anlage- oder Trading-Investitionen sind daher m.E. mit höchster Vorsicht vorzunehmen und sollten nur geschehen, wenn auch ein Totalverlust hingenommen werden kann.
Antwort auf Beitrag Nr.: 54.586.722 von Ville7 am 22.03.17 09:26:20Danke für die Info und Ausführungen.
Daher bei mir nur eine Position wo ich auch 50 bis 70 Prozent Verlust verkraften könnte.
Und sollte es sich wirklich sehr positiv Entwickeln wird es auch noch Gelegenheiten geben aufzustocken.
Lieber nicht Gierig und Risiko so weit wie möglich bei Biotech in Grenzen halten.
Wichtig ist das man dabei ist, das Unternehmen und die Aktie unter "Beobachtung" hat.
Daher bei mir nur eine Position wo ich auch 50 bis 70 Prozent Verlust verkraften könnte.
Und sollte es sich wirklich sehr positiv Entwickeln wird es auch noch Gelegenheiten geben aufzustocken.
Lieber nicht Gierig und Risiko so weit wie möglich bei Biotech in Grenzen halten.
Wichtig ist das man dabei ist, das Unternehmen und die Aktie unter "Beobachtung" hat.

@ ville: danke für die info und einschätzung
@ville
Auch von mir danke, für das (vereinfachte) Abstecken der Torpfosten.
Einen großen Dank auch an den Meister der Unterwelt (Joschka), auf daß er ab und an mal wieder auftaucht !
!
In Bezug auf die Verträglichkeiten der existierenden PD(L)-1 Varianten möchte ich hinzufügen, daß diese im Vergleich zu Standardtherapien schon sehr verträglich sind.
Ich kenne Patienten, die opdivo/nivolumab sehr gut vertragen, und die, trotz schicksalhafter Vorgeschichte (OP, Bestrahlung, Metastasen, Chemo), momentan ganz normal am Alltagsleben teilnehmen.
Die Verträglichkeit leidet jedoch erheblich durch die Kombination von jeweils neuen IO-Onkologika oder IO mit Kinasehemmstoffen.
In der Kombitherapie könnte der Probody-Antikörper sein ganzes Potential ausspielen.
Die zunehmenden Kombi-Therapien sind auf der anderen Seite wiederum so abartig teuer, daß CytomX im Erfolgsfall hier Gegenwind verspüren dürfte.
Dennoch ist der BMS-Deal eine wichtige Vorstufe des PoC, sozusagen ein Proof of value bzw. ein Adelstitel vom IO-König (BMS).
Auch von mir danke, für das (vereinfachte) Abstecken der Torpfosten.
Einen großen Dank auch an den Meister der Unterwelt (Joschka), auf daß er ab und an mal wieder auftaucht
 !
!In Bezug auf die Verträglichkeiten der existierenden PD(L)-1 Varianten möchte ich hinzufügen, daß diese im Vergleich zu Standardtherapien schon sehr verträglich sind.
Ich kenne Patienten, die opdivo/nivolumab sehr gut vertragen, und die, trotz schicksalhafter Vorgeschichte (OP, Bestrahlung, Metastasen, Chemo), momentan ganz normal am Alltagsleben teilnehmen.
Die Verträglichkeit leidet jedoch erheblich durch die Kombination von jeweils neuen IO-Onkologika oder IO mit Kinasehemmstoffen.
In der Kombitherapie könnte der Probody-Antikörper sein ganzes Potential ausspielen.
Die zunehmenden Kombi-Therapien sind auf der anderen Seite wiederum so abartig teuer, daß CytomX im Erfolgsfall hier Gegenwind verspüren dürfte.
Dennoch ist der BMS-Deal eine wichtige Vorstufe des PoC, sozusagen ein Proof of value bzw. ein Adelstitel vom IO-König (BMS).
kam was..oder sl-fishing?


der CFO hat mal gut 300 k$ aus einem stock option plan eingetütet:
http://ih.advfn.com/p.php?pid=nmona&article=74150116#DOC1_HT…
http://ih.advfn.com/p.php?pid=nmona&article=74150116#DOC1_HT…
Antwort auf Beitrag Nr.: 54.600.750 von infomi am 23.03.17 20:17:02So ne radde...
Zur Dokumentation, Ausschnitt präklinischer Daten zum anti-CTLA-4 Probody von BMS/Cytomx, welche BMS so begeistern:
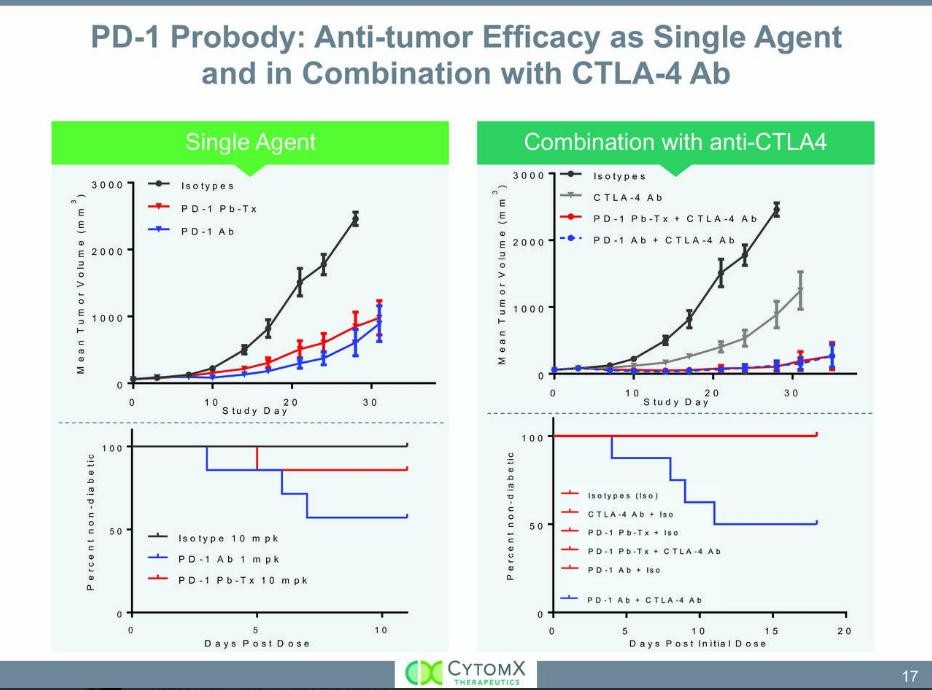
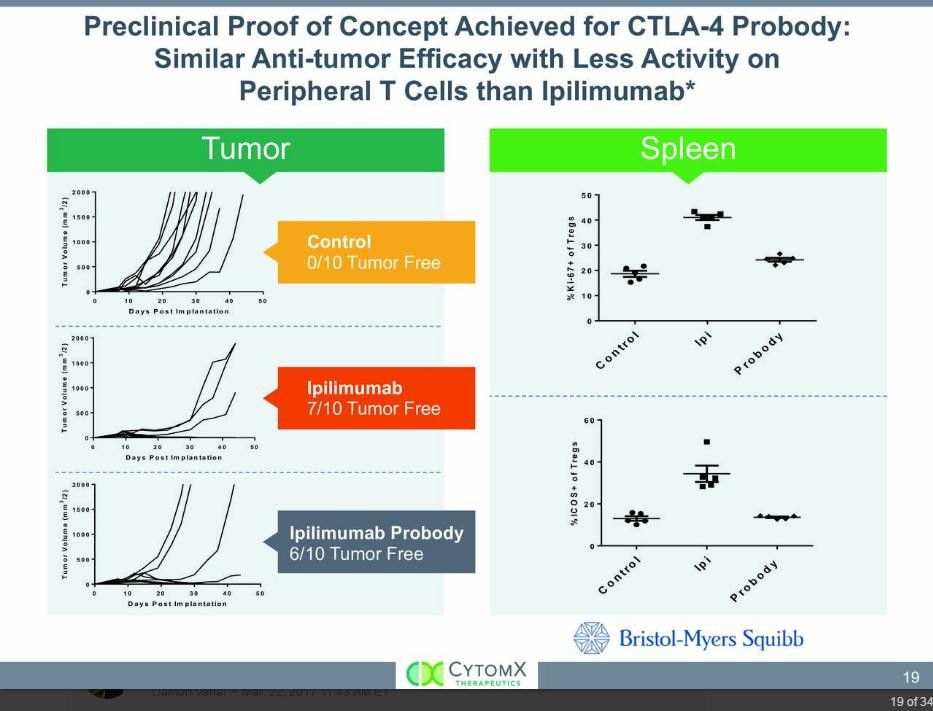


Was mich beim Potential von CTMX erstaunt ist, dass Insider nicht mehr Aktien halten und Ihre Optionen (klar mit sattem Gewinn) umgehend verkaufen.
Sofern die Daten der Nasdaq Seite stimmen, hält der CEO aktuell z.B nur 1,979 Aktien.
http://www.nasdaq.com/quotes/insiders/mccarthy-sean-a-976725
Sofern die Daten der Nasdaq Seite stimmen, hält der CEO aktuell z.B nur 1,979 Aktien.
http://www.nasdaq.com/quotes/insiders/mccarthy-sean-a-976725
Antwort auf Beitrag Nr.: 54.602.550 von Ville7 am 24.03.17 07:55:03Wow, Effektivität praktisch gleich und safety auf control level! Let's hope dass es in der Klinik ähnlich aussieht
das irritierende bei CytomX ist, das den sehr vielversprechenden vor-Poc-Daten die etwas verstörenden Verkäufe des CEO+CFO+Hauptaktionäre entgegenstehen.
Sicher, es gibt eine Reihe möglicher Gründe für einen Verkauf die nicht notwendigerweise den Poc in Frage stellen müssen - und man kann man davon ausgehen, dass auch BMS genau weiss, was sie tun.
Diejenigen die verkaufen, wissen aber schon, was sie damit bewirken.
Sicher, es gibt eine Reihe möglicher Gründe für einen Verkauf die nicht notwendigerweise den Poc in Frage stellen müssen - und man kann man davon ausgehen, dass auch BMS genau weiss, was sie tun.
Diejenigen die verkaufen, wissen aber schon, was sie damit bewirken.
Antwort auf Beitrag Nr.: 54.603.621 von infomi am 24.03.17 09:44:41..das hält mich auch davon ab hier wieder zu investieren..
Muss nicht immer negativ sein. ich hab mich vor jahren von einem beträchtlichen teil meiner aktien getrennt, um ein haus zu bauen. ein fesches :-).
bereu´ es keine tag, auch wenn manche aktie jetzt höher steht.
aktien sind nicht alles, kurse auch nicht.
bereu´ es keine tag, auch wenn manche aktie jetzt höher steht.
aktien sind nicht alles, kurse auch nicht.
(Auch) Bei Biotech-Investments sollte man sich immer auf sein eigenes Urteil verlassen.
Zum konkreten Fall: Risikokapitalgeber und Großaktionär Canaan hat zwischen dem 19.5.2016 und dem 30.11.2016 1,585 Mio. CytomX-Aktien zu Kursen zwischen 10,00 USD und 11,84 USD über die Börse verkauft und zusätzlich 0,7 Mio. CytomX-Aktien an verbundene Unternehmen transferiert. Wäre es ratsam gewesen, sich bei seinem eigenen Anlageverhalten an Canaan zu orientieren?
Ebenso irrelevant ist, dass einzelne Mitglieder der Unternehmensführung Aktienoptionen ausgeübt und die in diesem Zusammenhang bezogenen Aktien über die Börse verkauft haben ... es kommt immer auf die Gesamumstände/Relationen an ... schließlich waren zum 31.12.2016 insgesamt knapp 6,16 Mio. Optionen mit einem mittleren Ausübungspreis von 5,932 USD ausgegeben. Als Betroffener würde ich auch immer mal wieder Optionen ausüben und nicht mit der Ausübung aller Optionen bis zu einem fiktiven Tag X warten. Angesichts des Umfangs der Optionsrechte verwundert auch nicht, dass der CEO nur wenige Aktien hält.
Ich halte CytomX nach wie vor für das interessanteste Unternehmen im Biotech-Universum.
Zum konkreten Fall: Risikokapitalgeber und Großaktionär Canaan hat zwischen dem 19.5.2016 und dem 30.11.2016 1,585 Mio. CytomX-Aktien zu Kursen zwischen 10,00 USD und 11,84 USD über die Börse verkauft und zusätzlich 0,7 Mio. CytomX-Aktien an verbundene Unternehmen transferiert. Wäre es ratsam gewesen, sich bei seinem eigenen Anlageverhalten an Canaan zu orientieren?
Ebenso irrelevant ist, dass einzelne Mitglieder der Unternehmensführung Aktienoptionen ausgeübt und die in diesem Zusammenhang bezogenen Aktien über die Börse verkauft haben ... es kommt immer auf die Gesamumstände/Relationen an ... schließlich waren zum 31.12.2016 insgesamt knapp 6,16 Mio. Optionen mit einem mittleren Ausübungspreis von 5,932 USD ausgegeben. Als Betroffener würde ich auch immer mal wieder Optionen ausüben und nicht mit der Ausübung aller Optionen bis zu einem fiktiven Tag X warten. Angesichts des Umfangs der Optionsrechte verwundert auch nicht, dass der CEO nur wenige Aktien hält.
Ich halte CytomX nach wie vor für das interessanteste Unternehmen im Biotech-Universum.
Hallo Joschka schön mal wieder was von dir zu hören.
Nette Vola.....
"CytomX Therapeutics Appoints Marion McCourt to Board of Directors
SOUTH SAN FRANCISCO, Calif., March 30, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced the appointment of Marion McCourt to its Board of Directors. Ms. McCourt has more than two decades of operational and commercial leadership experience at several of the world's most innovative biopharmaceutical companies. The company also announced that Tim Shannon, M.D., General Partner at Canaan Partners, will leave the Board after more than four years of service.
“Marion’s joining our board comes at an important time for CytomX as our first two wholly-owned programs, CX-072 and CX-2009, enter Phase 1/2 clinical trials,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX Therapeutics. “Her deep commercial expertise makes her an ideal fit as we build our clinical development capabilities and ultimately plan for commercialization of our innovative pipeline of novel Probody cancer therapeutics. We also would like to thank Tim for his many contributions to the Board and for the instrumental role he and the Canaan Partners team have played in our success to date.”
Ms. McCourt most recently served as Chief Operating Officer at Medivation until the company’s acquisition by Pfizer in September 2016. Prior to joining Medivation in February 2016, Ms. McCourt served as Vice President of U.S. Commercial Operations at Amgen Inc. Prior to that, she also served as Vice President and General Manager of Amgen's Bone Health & Primary Care Business Unit. Before joining Amgen, Ms. McCourt held numerous positions of increasing responsibility over a twelve-year career at AstraZeneca. There, she most recently served as Chief Operating Officer of AstraZeneca U.S., where she was responsible for all U.S. commercial functions, including medical affairs, business development, finance, human resources, legal, operations and corporate affairs. Ms. McCourt holds a B.S. degree in Biology from Lafayette College."
Möglicherweise kündigt sich hier der neu COO von cytomX an.
Auch Rachel Humphrey war zuerst einige Monate im Board of Directors, bevor sie CSO wurde.
Die Vita von Frau McCourt ist beeindruckend.
Wenn cytomX die nächste Entwicklungsstufe von Präklinik/Phase1 zu größeren klinischen Studien erklimmt, ist ein erfahrener COO (derzeit vakant) vorteilhaft.
LG
StefanR
SOUTH SAN FRANCISCO, Calif., March 30, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced the appointment of Marion McCourt to its Board of Directors. Ms. McCourt has more than two decades of operational and commercial leadership experience at several of the world's most innovative biopharmaceutical companies. The company also announced that Tim Shannon, M.D., General Partner at Canaan Partners, will leave the Board after more than four years of service.
“Marion’s joining our board comes at an important time for CytomX as our first two wholly-owned programs, CX-072 and CX-2009, enter Phase 1/2 clinical trials,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX Therapeutics. “Her deep commercial expertise makes her an ideal fit as we build our clinical development capabilities and ultimately plan for commercialization of our innovative pipeline of novel Probody cancer therapeutics. We also would like to thank Tim for his many contributions to the Board and for the instrumental role he and the Canaan Partners team have played in our success to date.”
Ms. McCourt most recently served as Chief Operating Officer at Medivation until the company’s acquisition by Pfizer in September 2016. Prior to joining Medivation in February 2016, Ms. McCourt served as Vice President of U.S. Commercial Operations at Amgen Inc. Prior to that, she also served as Vice President and General Manager of Amgen's Bone Health & Primary Care Business Unit. Before joining Amgen, Ms. McCourt held numerous positions of increasing responsibility over a twelve-year career at AstraZeneca. There, she most recently served as Chief Operating Officer of AstraZeneca U.S., where she was responsible for all U.S. commercial functions, including medical affairs, business development, finance, human resources, legal, operations and corporate affairs. Ms. McCourt holds a B.S. degree in Biology from Lafayette College."
Möglicherweise kündigt sich hier der neu COO von cytomX an.
Auch Rachel Humphrey war zuerst einige Monate im Board of Directors, bevor sie CSO wurde.
Die Vita von Frau McCourt ist beeindruckend.
Wenn cytomX die nächste Entwicklungsstufe von Präklinik/Phase1 zu größeren klinischen Studien erklimmt, ist ein erfahrener COO (derzeit vakant) vorteilhaft.
LG
StefanR
Korrektur
Rachel Humphrey ist chief medical officer von cytomx
Rachel Humphrey ist chief medical officer von cytomx
Ist da was dran an diesem Tweet?
"It looks like the CAR-NK deal b/w CytoMx and @MDAndersonNews has been expanded to CAR-T. "
https://twitter.com/i/web/status/849281337370583040
Dass das Textfeld in der Präsentation erweitert wurde, fiel mir auch schon auf. Habe jedoch keine konkrete Meldung hierzu in Erinnerung.
"It looks like the CAR-NK deal b/w CytoMx and @MDAndersonNews has been expanded to CAR-T. "
https://twitter.com/i/web/status/849281337370583040
Dass das Textfeld in der Präsentation erweitert wurde, fiel mir auch schon auf. Habe jedoch keine konkrete Meldung hierzu in Erinnerung.
Antwort auf Beitrag Nr.: 54.685.265 von BReal am 05.04.17 21:55:02Mir ist nicht klar woraus genau das geschlossen werden soll, die verlinkte Präsentation ist ja von 2016?! Sehe auch gerade keine weiteren Infos dazu in der aktuellen Präsi
Antwort auf Beitrag Nr.: 54.686.456 von SpanishEyes am 06.04.17 07:54:15Bis Ende 2017 scheinen ja keine Catalysts mehr in Sicht zu sein. Wie schätzt Ihr den Kursverlauf ein?
Aufgrund des kürzlich abgeschlossenen Deals mit BMY (mit 200 Mio Upfront P.) erscheint mit die derzeitige Bewertung nicht zu hoch zu sein. Evtl. Gibts aber trotzdem ein Sommerloch und ab Sept. dann eine Rally? Meinungen?
Denke ich lege mir mal wieder ein paar Dinger ins Depot
Aufgrund des kürzlich abgeschlossenen Deals mit BMY (mit 200 Mio Upfront P.) erscheint mit die derzeitige Bewertung nicht zu hoch zu sein. Evtl. Gibts aber trotzdem ein Sommerloch und ab Sept. dann eine Rally? Meinungen?
Denke ich lege mir mal wieder ein paar Dinger ins Depot
Antwort auf Beitrag Nr.: 54.749.707 von biopadawan am 18.04.17 08:37:49Habe heute aufgestockt, vereinfacht gesprochen stehen wir jetzt bei 10 USD pre-recent-BMY-deal
Antwort auf Beitrag Nr.: 54.762.190 von SpanishEyes am 19.04.17 20:43:17@spanisheyes
Und durch den Deal kann cytomx in der frühen Phase seiner eigenen Produkte mit diesem Liquiditätspolster richtig Gas geben.
Darüber hinaus gibt es 8 neue Lose, komplett finanziert durch BMS mit der Chance auf Hauptgewinne.
Schon das allein wäre ein Bewertungszuschlag über den Liquiditätszufluß hinaus wert.
Und durch den Deal kann cytomx in der frühen Phase seiner eigenen Produkte mit diesem Liquiditätspolster richtig Gas geben.
Darüber hinaus gibt es 8 neue Lose, komplett finanziert durch BMS mit der Chance auf Hauptgewinne.
Schon das allein wäre ein Bewertungszuschlag über den Liquiditätszufluß hinaus wert.
Man munkelt, dass es sich hier um ein Projekt aus der Kolaboration mit CTMX handelt:
https://clinicaltrials.gov/ct2/show/NCT03110107?spons=bristo…
Ist nicht bestätigt würde mich aber nicht wundern. Ziemlich große Studie mit 531 Teilnehmern!
https://clinicaltrials.gov/ct2/show/NCT03110107?spons=bristo…
Ist nicht bestätigt würde mich aber nicht wundern. Ziemlich große Studie mit 531 Teilnehmern!
Heute geht es ja mal wieder rauf in den USa
Antwort auf Beitrag Nr.: 54.767.473 von kmastra am 20.04.17 16:06:58Das ist eine absolut massive Phase-1. Die Ergebnisse des Phase-2a-Arms dürften von ihrer Aussagekraft statistisch durchaus relevant sein. Hier will es jemand sehr früh bereits sehr genau wissen. Bleibt nur zu hoffen, dass es sich bei dem Antikörper tatsächlich um das CTLA-4-Projekt von CytomX handelt.
**********************************
Is Bristol-Myers Prepping To Outdo Itself In Immuno-Oncology?
Bristol-Myers Squibb (BMY) and Cytomx (CTMX) could be working on a less potent version of Yervoy and have data as early as 2018, an analyst said Thursday — a month after the two announced a deeper tie.
Though neither has commented specifically on which types of cancer they'll target in their deepened partnership, Bristol-Myers recently filed its plan to begin a three-year study of 531 patients with melanoma.
Evercore analyst Umer Raffat called the filing with ClinicalTrials.gov "intriguing." The trial will be a head-to-head comparison of a new immuno-oncology drug vs. Yervoy and look at a combination with Opdivo.
Although the filing doesn't identify whether the new immuno-oncology drug is Cytomx's, the pairing would make sense considering Bristol and Cytomx announced a deeper tie on March 20 to explore up to eight additional targets in oncology.
Their goal, Raffat says, is likely to find a less potent version of Yervoy, an immuno-oncology drug. Yervoy belongs to a class of drugs called CTLA-4 antibodies, which work to help the immune system identify cancer cells hiding behind CTLA-4 proteins.
Yervoy is effective, but it's also toxic. Its label includes warnings of "severe and fatal immune-mediated adverse reactions" including inflammation of the small intestine and colon, hepatitis, skin disorders, nerve damage and endocrine gland damage.
Cytomx is working on what is calls "probody" technology. These therapeutics are activated by certain conditions in the tumor environment. The goal is to limit the toxicity to the affected tissue and improve or create a therapeutic window.
"In simpler words, the intention is to develop a safer anti-CTLA-4 which delivers its effect at the tumor site and avoids the systemic tax elsewhere (which we see a ton of with Yervoy)," Raffat said in a note to clients.
Bristol's main goal of the trial is to reduce the incidence of adverse/serious events. The firm hopes its drug will operate as a more effective monotherapy vs. Yervoy in improving objective response rate, median duration of response and progression-free survival.
It will also combine the new CTLA-4 with Opdivo. Opdivo works similarly to Yervoy, but instead works to block the interaction between the immune system and the PD-1 proteins a tumor cell uses to hide. Opdivo rivals Merck's Keytruda.
Raffat expects to see early results in 2018.
"(The) focus will clearly be on whether the (toxicity) profile is materially better than Yervoy," he said. "In addition, it will also be interesting to see if there is an improvement."
Bristol-Myers stock closed up 0.45% at 53.44 on the stock market today, and Cytomx stock jumped 5.8% to 16.14.
http://www.investors.com/news/technology/is-bristol-myers-pr…
**********************************
Is Bristol-Myers Prepping To Outdo Itself In Immuno-Oncology?
Bristol-Myers Squibb (BMY) and Cytomx (CTMX) could be working on a less potent version of Yervoy and have data as early as 2018, an analyst said Thursday — a month after the two announced a deeper tie.
Though neither has commented specifically on which types of cancer they'll target in their deepened partnership, Bristol-Myers recently filed its plan to begin a three-year study of 531 patients with melanoma.
Evercore analyst Umer Raffat called the filing with ClinicalTrials.gov "intriguing." The trial will be a head-to-head comparison of a new immuno-oncology drug vs. Yervoy and look at a combination with Opdivo.
Although the filing doesn't identify whether the new immuno-oncology drug is Cytomx's, the pairing would make sense considering Bristol and Cytomx announced a deeper tie on March 20 to explore up to eight additional targets in oncology.
Their goal, Raffat says, is likely to find a less potent version of Yervoy, an immuno-oncology drug. Yervoy belongs to a class of drugs called CTLA-4 antibodies, which work to help the immune system identify cancer cells hiding behind CTLA-4 proteins.
Yervoy is effective, but it's also toxic. Its label includes warnings of "severe and fatal immune-mediated adverse reactions" including inflammation of the small intestine and colon, hepatitis, skin disorders, nerve damage and endocrine gland damage.
Cytomx is working on what is calls "probody" technology. These therapeutics are activated by certain conditions in the tumor environment. The goal is to limit the toxicity to the affected tissue and improve or create a therapeutic window.
"In simpler words, the intention is to develop a safer anti-CTLA-4 which delivers its effect at the tumor site and avoids the systemic tax elsewhere (which we see a ton of with Yervoy)," Raffat said in a note to clients.
Bristol's main goal of the trial is to reduce the incidence of adverse/serious events. The firm hopes its drug will operate as a more effective monotherapy vs. Yervoy in improving objective response rate, median duration of response and progression-free survival.
It will also combine the new CTLA-4 with Opdivo. Opdivo works similarly to Yervoy, but instead works to block the interaction between the immune system and the PD-1 proteins a tumor cell uses to hide. Opdivo rivals Merck's Keytruda.
Raffat expects to see early results in 2018.
"(The) focus will clearly be on whether the (toxicity) profile is materially better than Yervoy," he said. "In addition, it will also be interesting to see if there is an improvement."
Bristol-Myers stock closed up 0.45% at 53.44 on the stock market today, and Cytomx stock jumped 5.8% to 16.14.
http://www.investors.com/news/technology/is-bristol-myers-pr…
Antwort auf Beitrag Nr.: 54.772.804 von BReal am 21.04.17 09:49:44
"less potent" ist eigentlich der falsche Begriff. Durch die gezielte Wirkung sollen unerwünschte Nebeneffekte minimiert werden, ohne dass die Wirkung negativ berührt wird (andernfalls könnte man Yervoy einfach niedriger dosieren).
Die Konzeption der Studie ist eindrucksvoll, da setzt jemand früh alles auf eine Karte. Auch wenn sich zu BMS-986218 in den üblichen Datenbanken bislang keine weiteren Angaben finden, müßte es sich um den CTLA-4 Probody Tx handeln.
Zitat von BReal: Bristol-Myers Squibb (BMY) and Cytomx (CTMX) could be working on a less potent version of Yervoy
"less potent" ist eigentlich der falsche Begriff. Durch die gezielte Wirkung sollen unerwünschte Nebeneffekte minimiert werden, ohne dass die Wirkung negativ berührt wird (andernfalls könnte man Yervoy einfach niedriger dosieren).
Die Konzeption der Studie ist eindrucksvoll, da setzt jemand früh alles auf eine Karte. Auch wenn sich zu BMS-986218 in den üblichen Datenbanken bislang keine weiteren Angaben finden, müßte es sich um den CTLA-4 Probody Tx handeln.
Antwort auf Beitrag Nr.: 54.774.220 von Joschka Schröder am 21.04.17 12:35:21Entsprechend sollte es demnächst eine Meilensteinzahlung an CytomX geben. Der CTLA-4 Probody stammt aus der ersten Kooperationsvereinbarung vom Januar 2014 (4 Targets mit Meilensteinzahlungen von bis zu 1,198 Mrd. USD ... da sollten für den ersten Klinikstart schon ein paar Millionen herausspringen).
kleine Korrektur: 1,192 Mrd. USD
Hier noch eine journalistische Zusammenfassung inkl. Konkurrenzsituation:
http://epvantage.com/Universal/View.aspx?type=Story&id=70214…
http://epvantage.com/Universal/View.aspx?type=Story&id=70214…
Antwort auf Beitrag Nr.: 54.774.220 von Joschka Schröder am 21.04.17 12:35:21Ja, fand das wording auch etwas irreführend... anyways, bin sehr gespannt auf die weitere Firmenentwicklung und versuche nicht zu nervös zu sein bis zu den ersten klinischen Daten 

Die 531 Patientenstudie ist der andere inhouse BMS anti-ctla 4 mab
https://twitter.com/AndyBiotech/status/855574588796829696
Antwort auf Beitrag Nr.: 54.779.191 von Ville7 am 22.04.17 02:18:25Vielen Dank für den Twitter-Link. Es wäre interessant zu wissen, woher Umer Raffat seine Informationen hat (BMS äußert sich dazu bislang öffentlich nicht). In anderen Quellen wird Raffat übrigens (noch?) mit der gegenteiligen Meinung zitiert. Hier eine leicht verdauliche Zusammenfassung des CTLA4-Themas -> http://www.epvantage.com/Universal/View.aspx?type=Story&id=7….
Letztendlich wird BMS beide Antikörper (maskiert und modifiziert/afucosylated) in die Klinik bringen, die Frage wird nur sein, ob BMS tatsächlich zwei derartige Mamut-P1-Studien plant. Wäre jedenfalls ein sehr ungewöhnlicher Aufwand.
Am Wochenende werde ich erst einmal das Patent des modifizierten Mab´s lesen, in dem dessen Präklinik beschrieben sein dürfte.
Spannend bleibt das Thema in jedem Fall.
Letztendlich wird BMS beide Antikörper (maskiert und modifiziert/afucosylated) in die Klinik bringen, die Frage wird nur sein, ob BMS tatsächlich zwei derartige Mamut-P1-Studien plant. Wäre jedenfalls ein sehr ungewöhnlicher Aufwand.
Am Wochenende werde ich erst einmal das Patent des modifizierten Mab´s lesen, in dem dessen Präklinik beschrieben sein dürfte.
Spannend bleibt das Thema in jedem Fall.
Antwort auf Beitrag Nr.: 54.780.274 von Joschka Schröder am 22.04.17 11:46:42Zwischenzeitlich habe ich das Patent WO2014/089113A1 in weiten Teilen gelesen. Wirklich empfehlenswert, es gleicht einem gut verständlichen Lehrbuch der Immunonkologie. Darin wird u.a. auch anschaulich beschrieben, auf welchem Weg Medikamentenkandidaten ausgewählt und optimiert werden. Eine sehr aufwendige Angelegenheit, die z.B. Politikern, die über Kosten im Gesundheitssystem sinnieren, wenigstens in Grundzügen bekannt sein sollte.
Zum anti-CTLA-4-Mab der neuen Generation: Durch die Entfukosylierung des Fc-Anteils ist im Wesentlichen die Affinität zu entsprechenden FcRezeptoren und damit die Wirksamkeit des Antikörpers (-> Depletion regulatorischer T-Zellen insbesondere im Tumorgewebe bei gleichzeitiger Stimulation von T-Effektorzellen) gesteigert worden. Eine vergleichbare Technik verwendet Roche´s Schlierener Tochter Gkycart im Rahmen ihrer GycoMAb-Technologie. Da anti-CTLA-Mabs auch gesundes Gewebe binden, dürften gleichzeitig jedoch auch die (autoimmunologischen) Nebenwirkungen zunehmen (-> besonders nachteilig bei Kombitherapien), so dass der tatsächliche Nutzen der Defucosylierung (sieht man einmal von der niedrigeren therapeutischen Antikörperdosis ab) zunächst unklar bleibt. Es ist allerdings zu vermuten, dass BMS den neuen anti-CTLA-4-Mab gegenüber ipilimumab auch in anderer Hinsicht optimiert hat. Einige Optimierungsmöglichkeiten werden in der Patentschrift aufgezeigt.
Was bedeutet das für den anti-CTLA-4-Probody? Eigentlich überhaupt nichts, da durch die Maskierung mittels CytomX´s Probody-Technologie das therapeutische Fenster sämtlicher anti-CTLA-4-Antikörper deutlich erweitert werden sollte. Soweit jedenfalls die Theorie. Außerdem ist davon auszugehen, dass BMS in ihrem anti-CTLA-4-Probody die neueste/wirksamste Antikörpervariante verwendet, da der Probody erst im Anschluss an die neueste anti-CTLA-4-Mab-Generation entwickelt worden ist.
Zum anti-CTLA-4-Mab der neuen Generation: Durch die Entfukosylierung des Fc-Anteils ist im Wesentlichen die Affinität zu entsprechenden FcRezeptoren und damit die Wirksamkeit des Antikörpers (-> Depletion regulatorischer T-Zellen insbesondere im Tumorgewebe bei gleichzeitiger Stimulation von T-Effektorzellen) gesteigert worden. Eine vergleichbare Technik verwendet Roche´s Schlierener Tochter Gkycart im Rahmen ihrer GycoMAb-Technologie. Da anti-CTLA-Mabs auch gesundes Gewebe binden, dürften gleichzeitig jedoch auch die (autoimmunologischen) Nebenwirkungen zunehmen (-> besonders nachteilig bei Kombitherapien), so dass der tatsächliche Nutzen der Defucosylierung (sieht man einmal von der niedrigeren therapeutischen Antikörperdosis ab) zunächst unklar bleibt. Es ist allerdings zu vermuten, dass BMS den neuen anti-CTLA-4-Mab gegenüber ipilimumab auch in anderer Hinsicht optimiert hat. Einige Optimierungsmöglichkeiten werden in der Patentschrift aufgezeigt.
Was bedeutet das für den anti-CTLA-4-Probody? Eigentlich überhaupt nichts, da durch die Maskierung mittels CytomX´s Probody-Technologie das therapeutische Fenster sämtlicher anti-CTLA-4-Antikörper deutlich erweitert werden sollte. Soweit jedenfalls die Theorie. Außerdem ist davon auszugehen, dass BMS in ihrem anti-CTLA-4-Probody die neueste/wirksamste Antikörpervariante verwendet, da der Probody erst im Anschluss an die neueste anti-CTLA-4-Mab-Generation entwickelt worden ist.
"Außerdem ist davon auszugehen, dass BMS in ihrem anti-CTLA-4-Probody die neueste/wirksamste Antikörpervariante verwendet, da der Probody erst im Anschluss an die neueste anti-CTLA-4-Mab-Generation entwickelt worden...."
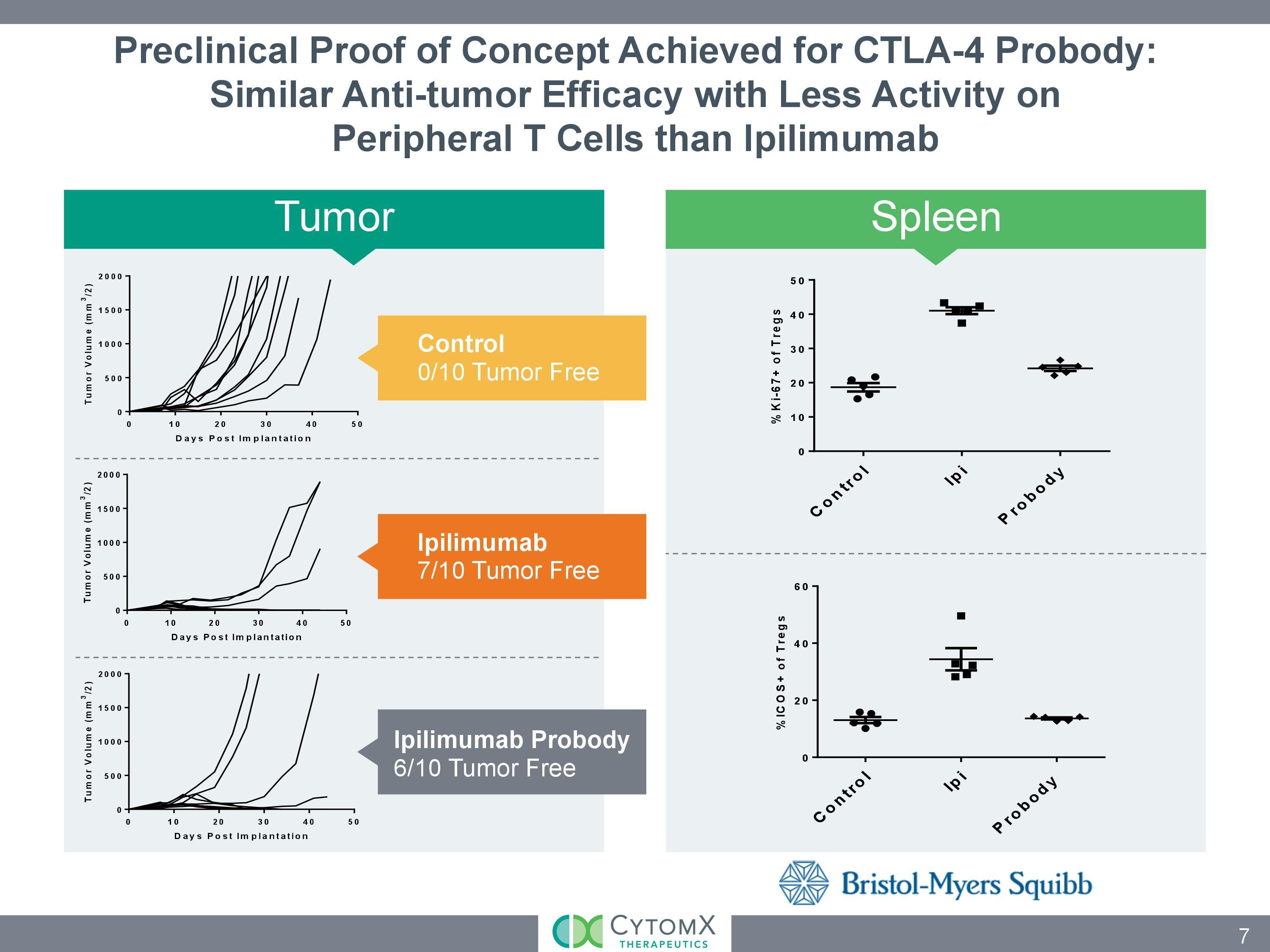
In den letzten Firmenpräsentationen ist vom Ipilimumab-anti-ctl4-probody die Rede.
Insofern bin ich schon davon ausgegangen, daß das laut pipeline-Übersicht (cytomx) kurz vor der klinischen Phase befindliche BMS-cytomx-Produkt auf der weniger wirksamen yervoy/ipilimumab-Basis beruht.
Dieses Produkt hatte ja Ende 2016 die 15 Millionen upfront aufgrund der Festlegung auf den klinischen Kandidaten bedingt.
Vielleicht sind zukünfitge, weniger entwickelte Pipeline-Projekte mit BMS als afucosylierte AB vorgesehen ?
Wie siehst du das, Joschka?
LG
StefanR

In den letzten Firmenpräsentationen ist vom Ipilimumab-anti-ctl4-probody die Rede.
Insofern bin ich schon davon ausgegangen, daß das laut pipeline-Übersicht (cytomx) kurz vor der klinischen Phase befindliche BMS-cytomx-Produkt auf der weniger wirksamen yervoy/ipilimumab-Basis beruht.
Dieses Produkt hatte ja Ende 2016 die 15 Millionen upfront aufgrund der Festlegung auf den klinischen Kandidaten bedingt.
Vielleicht sind zukünfitge, weniger entwickelte Pipeline-Projekte mit BMS als afucosylierte AB vorgesehen ?
Wie siehst du das, Joschka?
LG
StefanR
"CytomX Announces Selection by Bristol-Myers Squibb of First Clinical Candidate Probody From Collaboration
CTLA-4 Probody Moves to IND-Enabling Studies
SOUTH SAN FRANCISCO, Calif., Dec. 13, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that Bristol-Myers Squibb Company has selected a clinical candidate for its CTLA-4 Probody program under the strategic oncology collaboration established in May 2014. Achieving this milestone results in a $2 million payment to CytomX.
“Selecting a candidate for the CTLA-4 Probody program is a pivotal development in our partnership with CytomX Therapeutics and builds on our I.O. leadership,” said Carl Decicco, Ph. D., Head of Discovery at Bristol-Myers Squibb. “We are studying the CTLA-4 Probody for its potential to deliver a next-generation anti-CTLA-4 therapy as we continue to explore transformational immuno-oncology medicines.”
CTLA-4, a clinically validated inhibitory immune checkpoint protein, is the most advanced target from the companies’ collaboration, which now also includes three additional, unnamed targets in discovery.
“Advancing our CTLA-4 Probody program to clinical candidate stage with Bristol-Myers Squibb underscores the potential of the Probody platform to transform the field of immuno-oncology by delivering safer, more effective therapies,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX. “This partnership milestone, taken together with CytomX’s recently filed Investigational New Drug application for CX-072, a wholly owned PD-L1-directed Probody therapeutic, highlights the potential of our innovative platform to deliver a new generation of anti-cancer treatments."
Korrektur: 2mio Dollar upfront
CTLA-4 Probody Moves to IND-Enabling Studies
SOUTH SAN FRANCISCO, Calif., Dec. 13, 2016 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced that Bristol-Myers Squibb Company has selected a clinical candidate for its CTLA-4 Probody program under the strategic oncology collaboration established in May 2014. Achieving this milestone results in a $2 million payment to CytomX.
“Selecting a candidate for the CTLA-4 Probody program is a pivotal development in our partnership with CytomX Therapeutics and builds on our I.O. leadership,” said Carl Decicco, Ph. D., Head of Discovery at Bristol-Myers Squibb. “We are studying the CTLA-4 Probody for its potential to deliver a next-generation anti-CTLA-4 therapy as we continue to explore transformational immuno-oncology medicines.”
CTLA-4, a clinically validated inhibitory immune checkpoint protein, is the most advanced target from the companies’ collaboration, which now also includes three additional, unnamed targets in discovery.
“Advancing our CTLA-4 Probody program to clinical candidate stage with Bristol-Myers Squibb underscores the potential of the Probody platform to transform the field of immuno-oncology by delivering safer, more effective therapies,” said Sean McCarthy, D.Phil., President and Chief Executive Officer of CytomX. “This partnership milestone, taken together with CytomX’s recently filed Investigational New Drug application for CX-072, a wholly owned PD-L1-directed Probody therapeutic, highlights the potential of our innovative platform to deliver a new generation of anti-cancer treatments."
Korrektur: 2mio Dollar upfront
Antwort auf Beitrag Nr.: 54.792.514 von StefanR am 24.04.17 17:20:24Ich bin zwar nicht Joschka, aber genau so denke ich das auch. BMS hat ja noch einige Optionen auf AKs, wieso nicht einen zweiten anti-ctla-4-AK, wenn es Sinn macht... Wirksamer (afucosylated) und sicherer (Probody)... wieso nicht?
Antwort auf Beitrag Nr.: 54.792.514 von StefanR am 24.04.17 17:20:24
Du hast schon recht, die Bezeichnung "Ipilimumab Probody"sieht eindeutig aus.
Den Wahrheitsgehalt der zitierten Twitter-Botschaft vorausgesetzt, wäre nur sehr verwunderlich, wenn BMS zunächst eine Mamutstudie mit einem defucosylierten Antikörper startet, bald darauf eine weitere Studie mit einem Ipilimumab-basierten Probody und später ggf. noch eine zusätzliche Studie mit einem defucosylierten anti-CTLA-4-Probody. Klar, ein Großkonzern wie BMS besitzt erhebliche Ressourcen, aber das wäre dann doch etwas zu viel des Guten für ein targetspezifisches Entwicklungsprogramm.
Am meisten Sinn würde es wohl machen, direkt bei BMS nachzufragen.
Zitat von StefanR: In den letzten Firmenpräsentationen ist vom Ipilimumab-anti-ctl4-probody die Rede.
Insofern bin ich schon davon ausgegangen, daß das laut pipeline-Übersicht (cytomx) kurz vor der klinischen Phase befindliche BMS-cytomx-Produkt auf der weniger wirksamen yervoy/ipilimumab-Basis beruht.
Dieses Produkt hatte ja Ende 2016 die 15 Millionen upfront aufgrund der Festlegung auf den klinischen Kandidaten bedingt.
Vielleicht sind zukünfitge, weniger entwickelte Pipeline-Projekte mit BMS als afucosylierte AB vorgesehen ?
Wie siehst du das, Joschka?
Du hast schon recht, die Bezeichnung "Ipilimumab Probody"sieht eindeutig aus.
Den Wahrheitsgehalt der zitierten Twitter-Botschaft vorausgesetzt, wäre nur sehr verwunderlich, wenn BMS zunächst eine Mamutstudie mit einem defucosylierten Antikörper startet, bald darauf eine weitere Studie mit einem Ipilimumab-basierten Probody und später ggf. noch eine zusätzliche Studie mit einem defucosylierten anti-CTLA-4-Probody. Klar, ein Großkonzern wie BMS besitzt erhebliche Ressourcen, aber das wäre dann doch etwas zu viel des Guten für ein targetspezifisches Entwicklungsprogramm.
Am meisten Sinn würde es wohl machen, direkt bei BMS nachzufragen.
Ten Questions with CytomX Therapeutics
Quelle: http://www.loncarfunds.com/ten-questions-with-cytomx/APRIL 28, 2017
CytomX Therapeutics provides background on their approach to antibody development and cancer immunotherapy.
The Cancer Immunotherapy ETF (Nasdaq: CNCR) is designed to invest both in companies that have immunotherapy drugs on the market today, and also ones that are trying to improve on them by developing second and third generation immunotherapies. The goal of this second group is to help more patients respond to treatments and to move into more types of cancers.
One such company is South San Francisco based CytomX Therapeutics (Nasdaq: CTMX). Through a technology they are developing called Probody therapeutics, CytomX is trying to lower the impact some immunotherapies have on parts of the body other than where tumors are located. By trying to make drugs more active in the tumor microenvironment, while also lowering any collateral damage to healthy tissue, CytomX aims to make immunotherapy more targeted and effective.
To help visitors learn more about the company, we posed ten questions to CytomX’s CFO, Bob Goeltz. Mr. Goeltz provided written answers that we hope will help visitors better understand the rationale behind CytomX’s technology, why this might have advantages compared to existing immunotherapies on the market, and what the company’s plans are for the years ahead.
01
What are Probody therapeutics and what potential advantages does this technology have over standard checkpoint inhibitors and other antibodies?
Promising classes of antibodies, including checkpoint inhibitors and antibody drug conjugates, have shown meaningful improvements for the treatment of cancer, resulting in dramatic anti-cancer activity in certain patients. Yet, most patients do not respond, have responses of limited duration or face a number of adverse events when the antibody binds to healthy tissue and not just to cancer cells. Emergence of these toxicities limits the use of treatments across a range of cancers and targets, leaving some of most compelling cancer targets unaddressed and many available treatments not used to their full potential.
Probody therapeutics are localized to the tumor by leveraging enzymes called proteases that are active in the tumor microenvironment. Designed to remain inactive until they are activated by proteases in the tumor, Probody therapeutics preferentially bind target in tumors and minimize binding in healthy tissue, resulting in reduced toxicity and potentially safer, more effective therapies.
02
Using immunotherapies in combination with other drugs is a big theme in cancer research right how. How do Probody therapeutics fit into that picture?
First-generation checkpoint inhibitors combined with other immunomodulatory antibodies have substantially improved the prognosis for patients with advanced melanoma and a number of other cancers. Despite important benefits, one of the challenges with combination therapy is that certain combinations result not only in a more potent effect, but also in greater toxicities. By activating the immune system, these drugs can set off the equivalent of a five-alarm fire throughout the patient’s body, causing a unique spectrum of autoimmune and inflammatory side effects. In a number of cases, development of promising therapies has been stopped due to severe side effects. By containing the drug’s activity in the tumor, we believe Probody therapeutics have the potential to prevent overactivation of immune system outside of the tumor while retaining the potent effect of combination therapy.
We believe our wholly-owned lead program, CX-072, a PD-L1-targeting Probody therapeutic, has the potential to become the centerpiece of combination therapy in immuno-oncology.
03
In March, CytomX expanded an existing relationship with Bristol-Myers Squibb. Can you tell us more about that?
CytomX and Bristol-Myers Squibb (BMS) have made substantial progress in advancing Probody therapeutics toward the clinic as part of an initial four-target collaboration formed in 2014. The lead target in the collaboration is CTLA-4. CTLA-4 is the target of Yervoy (ipilimumab), a BMS-marketed checkpoint inhibitor. Yervoy has shown promising anti-cancer effects, but can cause serious side effects that can limit its utility. So, it is a logical candidate for the Probody technology. BMS recently nominated a clinical candidate for the CTLA-4 program, which is advancing to IND-enabling studies. All four targets in the original collaboration have been selected, and to date, CytomX has received $77 million in upfront and milestone payments from BMS.
Building on this success, CytomX granted BMS rights to develop and commercialize products directed at up to eight additional targets using the Probody Platform, including six oncology targets and two targets in non-oncology therapeutic areas. BMS will make an upfront payment of $200 million to CytomX, and CytomX is eligible for up to $3.6 billion in additional development and commercialization milestones, or $448 million for each collaboration target. We are also eligible for tiered royalties ranging from the mid-single digits to low-double digits on net sales of each product commercialized by BMS. Between the upfront payment and potential downstream milestones, this represents one of the largest preclinical platform deals in recent history with proceeds enabling CytomX to strategically invest in advancing our wholly-owned pipeline while extending the reach of our technology.
Importantly, existing Probody programs that CytomX has in discovery, preclinical research or clinical development are not eligible for selection under the collaboration, and BMS gains no rights to CytomX’s currently wholly owned lead programs, CX-072, CX-2009 and CX-188.
This alliance expansion firmly underscores the conviction that BMS has in our technology and the promise of the Probody platform to deliver next-generation therapies that may transform the current treatment landscape in cancer.
04
What are some other noteworthy partnerships CytomX has?
In 2016, CytomX entered into a strategic collaboration with AbbVie to co-develop and co-commercialize Probody Drug Conjugates (PDCs). The initial focus of our collaboration is to advance CX-2029, a CD-71-targeting PDC, that is currently advancing through IND-enabling studies. CD71 is the transferrin receptor that is highly expressed on a number of solid and hematologic tumors, as well as many normal tissues, making it an ideal target for the Probody platform.
Under the terms of the agreement, CytomX and AbbVie will co-develop CX-2029 with CytomX leading pre-clinical and early clinical development. AbbVie will then lead later development and commercialization with global late-stage development costs shared between the two companies. AbbVie will lead global commercial activities with CytomX eligible to receive a profit share in the U.S. and tiered double-digit royalties on net product sales outside of the U.S. CytomX retains an option to co-promote in the U.S. AbbVie also receives exclusive worldwide rights to develop and commercialize PDCs against up to two additional, undisclosed oncology targets. CytomX received an upfront payment of $30 million and is eligible to receive up to $470 million in development, regulatory and commercial milestones, pending the achievement of pre-determined outcomes.
We also have partnerships with ImmunoGen and Pfizer to develop multiple PDCs for the treatment of cancer and the University of Texas MD Anderson Cancer Center to research Probody-enabled chimeric antigen receptor natural killer (ProCAR-NK) cell therapies.
05
What clinical trials do you currently have open?
CytomX is currently evaluating CX-072 as monotherapy and in combination with Yervoy (ipilimumab) or Zelboraf (vemurafenib) in a Phase 1/2 clinical trial. Our goal is to demonstrate improved tolerability and anti-cancer activity as monotherapy and in combination, while also exploring translational aspects of Probody mechanistic activity in patients including intra-tumoral Probody activation by tumor-associated proteases.
06
Are any other trials scheduled to start this year?
We plan to submit the IND for CX-2009 during the first half of this year and commence the Phase 1 program in the middle of 2017. CX-2009 is a first-in-class PDC targeting the highly expressed tumor antigen, CD-166 and has the potential for broad utility against a number of different solid tumors.
07
What are your company’s main goals over the next couple of years?
We expect data to emerge for both CX-072 and CX-2009 throughout 2018. We believe both of these programs have the potential to demonstrate proof-of-concept for our Probody technology. Behind our two lead programs, we have three additional programs in IND-enabling studies, including one wholly-owned program (CX-188, a PD-1 targeting Probody), CX-2029 partnered with AbbVie and the CTLA-4 Probody partnered with BMS. Thus, we expect the next few years to be very data rich with the potential to point the way to future registration studies. We are also investing in many additional research programs to form the next wave of innovation in our pipeline. Our strong cash position gives the necessary runway to strategically invest in our pipeline beyond 2019.
08
Where do you see the future of cancer care headed?
While we have made great progress over the last decade, we have a long way to go to achieve durable treatments for the majority of cancer patients. Our work at CytomX supports the industry’s goal of developing next-generation immunotherapies and cell-based therapies to reduce toxicities, improve efficacy and help a greater number of patients benefit from these treatments. And although we are not focused on it per se, we believe that dramatic improvements in early diagnosis will be seen over the next decade causing us to rethink how we bring therapy to patients sooner.
09
CytomX has been listed since October of 2015, but your company has been around for a much longer time. Can you tell us a little more about the company’s history?
CytomX LLC was founded in in 2006, based on the technology developed at University of California Santa Barbara – eCPX to discover high affinity masking peptides and CLiPS to discover highly specific protease substrates. In 2007, CytomX was renamed CytomX Therapeutics to focus on the development of first-in-class, site-directed protein therapeutics, eventually named Probody therapeutics, with the goal of creating safer and more effective therapies. Having been angel-funded to this point, in 2010 we secured our first venture financing from Third Rock Ventures and the Roche Venture Fund, which allowed us to generate robust preclinical proof of concept data over the 2011-2013 timeframe and put our first programs into development. We have been advancing our innovative pipeline ever since, while forming strategic partnerships with leading biopharmaceutical companies and research institutions along the way.
10
What has it been like being a public company and what does support from investors mean to you?
Goeltz: During 2015, we raised approximately $160 million in equity financing from a ‘crossover’ round led by Fidelity and our IPO. At the time, CytomX was still more than a year from launching our first human clinical trial, so investors have been very focused on the preclinical evidence that Probody therapeutics might work in humans. We believe that the innovation inherent in our platform and our robust preclinical data has been the driving force behind why we have attracted a number of top-tier biotech investors. As we have transitioned to a clinical-stage company, much of the investor focus has shifted to our clinical strategy and execution. The CytomX team has focused intently on execution since our IPO and, in fact, we have achieved all of the key milestones we laid out when we went public in 2015. We take great pride in this track record and remain intensely focused on continuing to execute.
Der Kurs will runter....
Aufgrund der Cashposition in Höhe von ca. $ 382m derzeit mit einem EV von ca. $ 130m bewertet.
Der Kurs befindet sich auf einem Pre-200m-Cashdeal (BMY) von ca. 9 $, obwohl, wie von StefanR bereits dargestellt, neue "Lose" in die Entwicklungspipeline von CTMX gekommen sind und der Deal auch die Zuversicht von BMY in die Projekte dokumentiert.
M.E. nicht die schlechteste Nachkaufmöglichkeit.
Der Kurs befindet sich auf einem Pre-200m-Cashdeal (BMY) von ca. 9 $, obwohl, wie von StefanR bereits dargestellt, neue "Lose" in die Entwicklungspipeline von CTMX gekommen sind und der Deal auch die Zuversicht von BMY in die Projekte dokumentiert.
M.E. nicht die schlechteste Nachkaufmöglichkeit.
ctmx
$14.64
-0.24
-1.6%
CytomX beats by $0.28, beats on revenue
May 5, 2017 8:06 AM ET|About: CytomX Therapeutics (CTMX)|By: Gaurav Batavia, SA News Editor
CytomX (NASDAQ:CTMX): Q1 EPS of -$0.23 beats by $0.28.
Revenue of $11.7M (+427.0% Y/Y) beats by $7.7M.
Press Release
Now read: TG Therapeutics misses by $0.14, revenue in-line »
$14.64
-0.24
-1.6%
CytomX beats by $0.28, beats on revenue
May 5, 2017 8:06 AM ET|About: CytomX Therapeutics (CTMX)|By: Gaurav Batavia, SA News Editor
CytomX (NASDAQ:CTMX): Q1 EPS of -$0.23 beats by $0.28.
Revenue of $11.7M (+427.0% Y/Y) beats by $7.7M.
Press Release
Now read: TG Therapeutics misses by $0.14, revenue in-line »
Antwort auf Beitrag Nr.: 54.873.955 von 007coolinvestor am 05.05.17 14:30:04Wenn die technologie aufgeht ist 14.x bald nicht mehr denkbar..
In 400 Tagen (zu/nach ASCO 2018) ist CTMX entweder bei 3-5 USD oder bei über 50 USD.
Trittbrettfahrer in die ein oder andere Richtung: Willkommen! 

Antwort auf Beitrag Nr.: 54.879.724 von Ville7 am 06.05.17 09:04:02
völlig richtig - und bis dahin wird es wohl stark schwanken, weil die Einen dies und die Anderen jenes erwarten.
Zitat von Ville7: In 400 Tagen (zu/nach ASCO 2018) ist CTMX entweder bei 3-5 USD oder bei über 50 USD.
völlig richtig - und bis dahin wird es wohl stark schwanken, weil die Einen dies und die Anderen jenes erwarten.
Antwort auf Beitrag Nr.: 54.880.315 von infomi am 06.05.17 11:28:44Deshalb habe ich ein Abstauberlimit gesetzt. Gehe ohnehin von schwächerer Börse in USA im Verhätnis zum Rest der Welt aus.
Kann mir jemand als Leihe sagen, wie erfolgsversprechend der Therapieansatz zu werten ist. Meine Überlegung als Leihe: Wenn mit 300 Mio. die Forschung durch einen Konzern sichergestellt wird, gehe ich davon aus, dass da eine ganze Menge wissenschaftlicher Substanz da ist, so das am Ende des Tages ein neuer Behandlungsansatz besteht. Deshalb möchte ich auch da meinen Ring grundsätzlich reinwerfen.
Kann mir jemand als Leihe sagen, wie erfolgsversprechend der Therapieansatz zu werten ist. Meine Überlegung als Leihe: Wenn mit 300 Mio. die Forschung durch einen Konzern sichergestellt wird, gehe ich davon aus, dass da eine ganze Menge wissenschaftlicher Substanz da ist, so das am Ende des Tages ein neuer Behandlungsansatz besteht. Deshalb möchte ich auch da meinen Ring grundsätzlich reinwerfen.
Antwort auf Beitrag Nr.: 54.884.662 von 007coolinvestor am 07.05.17 13:56:52Deshalb habe ich ein Abstauberlimit gesetzt. Gehe ohnehin von schwächerer Börse in USA im Verhätnis zum Rest der Welt aus
die Tendenz des Gesamtmarktes dürfte in diesem Fall kaum einen Einfluss auf den Kurs haben; bei einem PoC geht der durch die Decke, egal wo sich der Gesamtmarkt gerade befindet.
In Bezug auf die Schwankungsbreite schrammt der Kurs wohl schon jetzt eher am unteren Ende.
die Tendenz des Gesamtmarktes dürfte in diesem Fall kaum einen Einfluss auf den Kurs haben; bei einem PoC geht der durch die Decke, egal wo sich der Gesamtmarkt gerade befindet.
In Bezug auf die Schwankungsbreite schrammt der Kurs wohl schon jetzt eher am unteren Ende.
Einer der beteilgten Autoren hat mir heute ein informatives Paper zugeschickt, das am Wochenende in Nature Medicine erschienen ist. Es trägt den Titel "Is autoimmunity the Achilles´s heel of cancer immunotherapy?" und ist für alle Investoren, die sich mit CytomX beschäftigen, lesenswert. Die Arbeit beschreibt Ursachen und Folgen von Autoimmun-Mechanismen unter Therapie mit Checkpoint-Inhibitoren (Schwerpunkt CTLA-4, PD-1, PD-L-1) und unter CAR-T-Zelltherapie. Im Grunde genommen werden genau diejenigen Themengebiete diskutiert, die von CytomX mit dem Probody-Ansatz adressiert werden.
Antwort auf Beitrag Nr.: 54.895.844 von Joschka Schröder am 08.05.17 23:57:08Das hört sich nach einem sehr erfolgsversprechenden Therapieansatz an.
Vielen Dank für den Hinweis.
Vielen Dank für den Hinweis.
Antwort auf Beitrag Nr.: 54.896.432 von 007coolinvestor am 09.05.17 07:49:19Die Arbeit gibt kein Urteil über CytomX´s Therapieansatz ab.
Antwort auf Beitrag Nr.: 54.899.444 von Joschka Schröder am 09.05.17 12:54:38Danke. Ich habe das so verstanden, dass die Entwicklung bei dem Problem ansetzt.
Antwort auf Beitrag Nr.: 54.899.573 von 007coolinvestor am 09.05.17 13:11:45Das ist natürlich richtig.
Antwort auf Beitrag Nr.: 54.899.627 von Joschka Schröder am 09.05.17 13:20:11Dann scheint die Entwicklung überdurchschnittlich erfolgsversprechend zu sein, oder ?
der CFO verlässt das Unternehmen:
https://seekingalpha.com/news/3267431-cytomx-cfo-resigns
Er hatte in der Vergangenheit schon verschiedenlich Optionen ausgeübt. Der Kurs steigt, das dürfte keine Auswirkungen auf das Unternehmen haben.
https://seekingalpha.com/news/3267431-cytomx-cfo-resigns
Er hatte in der Vergangenheit schon verschiedenlich Optionen ausgeübt. Der Kurs steigt, das dürfte keine Auswirkungen auf das Unternehmen haben.
Antwort auf Beitrag Nr.: 54.950.306 von infomi am 16.05.17 06:48:27Wenn man sich die Abfindungsregelungen anschaut, drängt sich der Eindruck auf, dass es nicht unbedingt ein freiwilliger Abgang war. Das Abkommen mit BMY ist wohl bereits unter der Federführung seines Nachfolgers ausgehandelt worden.
Antwort auf Beitrag Nr.: 54.895.844 von Joschka Schröder am 08.05.17 23:57:08
In der heutigen CytomX-Meldung heißt es wörtlich: "The occurrence of immune-related adverse events is emerging as the Achilles’ heel of cancer immunotherapy," said Rachel W. Humphrey, M.D., chief medical officer of CytomX Therapeutics.

CytomX wird beim bevorstehenden ASCO-Meeting ein Poster zur Proclaim-001-Studie präsentieren. In der Meldung heißt es dazu "Our recently initiated Phase 1/2 clinical trial, part of our umbrella PROCLAIM program, is investigating the potential of our differentiated, anti-PD-L1 Probody therapeutic, CX-072, to reduce overactivation of the immune system outside of the tumor, while remaining active as a single-agent and in combination therapy. This poster presentation at ASCO will review the design and objectives of this ongoing study.”
Title: PROCLAIM-001: A first-in-human trial to assess tolerability of the protease-activatable anti-PD-L1 Probody CX-072 in solid tumors and lymphomas
Author: Alexander I. Spira, M.D., Ph.D., F.A.C.P., Medical Oncologist and Director, Virginia Cancer Specialists Research Institute and Oncology Research
Session: Developmental Therapeutics—Immunotherapy
Date: Monday, June 5, 2017
Time: 8:00 a.m. - 11:30 a.m.
Location: Hall A
Abstract: TPS3107
Zitat von Joschka Schröder: Einer der beteilgten Autoren hat mir heute ein informatives Paper zugeschickt, das am Wochenende in Nature Medicine erschienen ist. Es trägt den Titel "Is autoimmunity the Achilles´s heel of cancer immunotherapy?" und ist für alle Investoren, die sich mit CytomX beschäftigen, lesenswert. Die Arbeit beschreibt Ursachen und Folgen von Autoimmun-Mechanismen unter Therapie mit Checkpoint-Inhibitoren (Schwerpunkt CTLA-4, PD-1, PD-L-1) und unter CAR-T-Zelltherapie. Im Grunde genommen werden genau diejenigen Themengebiete diskutiert, die von CytomX mit dem Probody-Ansatz adressiert werden.
In der heutigen CytomX-Meldung heißt es wörtlich: "The occurrence of immune-related adverse events is emerging as the Achilles’ heel of cancer immunotherapy," said Rachel W. Humphrey, M.D., chief medical officer of CytomX Therapeutics.

CytomX wird beim bevorstehenden ASCO-Meeting ein Poster zur Proclaim-001-Studie präsentieren. In der Meldung heißt es dazu "Our recently initiated Phase 1/2 clinical trial, part of our umbrella PROCLAIM program, is investigating the potential of our differentiated, anti-PD-L1 Probody therapeutic, CX-072, to reduce overactivation of the immune system outside of the tumor, while remaining active as a single-agent and in combination therapy. This poster presentation at ASCO will review the design and objectives of this ongoing study.”
Title: PROCLAIM-001: A first-in-human trial to assess tolerability of the protease-activatable anti-PD-L1 Probody CX-072 in solid tumors and lymphomas
Author: Alexander I. Spira, M.D., Ph.D., F.A.C.P., Medical Oncologist and Director, Virginia Cancer Specialists Research Institute and Oncology Research
Session: Developmental Therapeutics—Immunotherapy
Date: Monday, June 5, 2017
Time: 8:00 a.m. - 11:30 a.m.
Location: Hall A
Abstract: TPS3107
@ Joschkan Schröder
danke für deine beiträge.
danke für deine beiträge.
Antwort auf Beitrag Nr.: 54.963.281 von ciel34 am 17.05.17 14:36:29Das ist aber nett, vielen Dank!
Die jüngste Kursentwicklung scheint kaum nachvollziehbar. Bald notiert die Aktie wieder in Nähe des Emissionskurses (12 USD) aus dem Jahr 2015, obwohl es in der Zwischenzeit eine Menge positiver Nachrichten gegeben hat.
Auf Basis des aktuellen Kurses (14,30 USD) weist CytomX einen Unternehmenswert (EV) von gerade mal 120 Mio. UD auf. Zur Erinnerung: Allein der letzte Deal mit BMY hat 200 Mio. USD Upfront die Kasse gespült (obendrauf gab es noch die Option auf Meilensteinzahlungen in Milliardenhöhe und Tantiemen auf spätere Umsätze).
Ich kaufe weiter zu.
Auf Basis des aktuellen Kurses (14,30 USD) weist CytomX einen Unternehmenswert (EV) von gerade mal 120 Mio. UD auf. Zur Erinnerung: Allein der letzte Deal mit BMY hat 200 Mio. USD Upfront die Kasse gespült (obendrauf gab es noch die Option auf Meilensteinzahlungen in Milliardenhöhe und Tantiemen auf spätere Umsätze).
Ich kaufe weiter zu.
Antwort auf Beitrag Nr.: 55.042.858 von Joschka Schröder am 30.05.17 16:09:45Habe die letzten Wochen auch zugekauft, bislang war praktisch jeder neue Kauf (abgesehen von der Anfangsposition) günstiger als der vorangegangene, permanentes average down finde ich eigtl. nicht sehr schlau und geht etwas gegen mein Prinzip... andererseits "dümpelt" der Kurs mE etwas vor sich hin nachdem aktuell noch keine Studienergebnisse anstehen, die gehandelten Volumina sind auch unterdurchschnittlich... sobald ein neues partnership agreement o.ä. kommt, geht es auch schnell wieder aufwärts... generell ist Biotech im Vergleich zu anderen Segmenten resp. Assetklassen relativ gesehen fast schon "günstig" und immer noch nicht wieder richtig sexy, somit könnte man aus contrarian Sicht fast darauf setzen dass sich das auch mal wieder ändern könnte bei der Suche nach attraktiven Investmentmöglichkeiten... aktuell ist meine Strategie die volle Position bis in die Ergebnisse hinein zu halten und im Spätherbst vor den ersten Ergebnissen zu beginnen meine Position mit Put-Optionen abzusichern...
Die Frage ist ja wenn Ihr alle kauft wer verkauft dann immer wieder brav........
Ich denke der Markt hat immer Recht und gerade will die Aktie nicht Hoch ich hoffe dies ändert sich
Ich denke der Markt hat immer Recht und gerade will die Aktie nicht Hoch ich hoffe dies ändert sich
Antwort auf Beitrag Nr.: 55.043.989 von SpanishEyes am 30.05.17 18:25:28Gestern wurden einige Supportlevels bei Biotechindizes gebrochen, ausserdem ist seit 2001 im Schnitt Juni der schlechteste Monat für Biotech... könnte also noch weiter runter gehen
Antwort auf Beitrag Nr.: 55.048.834 von SpanishEyes am 31.05.17 12:09:37jo..gestern der Nasdaq Biotech-Index unter die 3000 gefallen..


Zitat von SpanishEyes: Gestern wurden einige Supportlevels bei Biotechindizes gebrochen, ausserdem ist seit 2001 im Schnitt Juni der schlechteste Monat für Biotech... könnte also noch weiter runter gehen
Antwort auf Beitrag Nr.: 55.049.284 von HK12 am 31.05.17 12:56:12Ich habe abstauberlimmit für erste position gesetzt. Bin für USA eher skeptisch. EU positiv bis Frühjahr 2018. Dann dürfte sich die verschlechterte Lage in den USA und höherer US$ auswirken.
Antwort auf Beitrag Nr.: 55.049.284 von HK12 am 31.05.17 12:56:12Das stimmt! Man könnte noch Hoffnung daraus beziehen, dass beim IBB die 200 Tageslinie gehalten hat.

Antwort auf Beitrag Nr.: 55.042.858 von Joschka Schröder am 30.05.17 16:09:45
2015 war auch der Peak des Biotech-Hypes. Aktuell ist die Branche auch aufgrund regulatorischer Anstrengungen ziemlich unter Druck. Das sieht man daran, dass der Volatilitätsindex auf niedrigstem Niveau ist (= Risk on!), aber Biotech da nicht mitgehen kann, ja sogar abgibt. Und das sogar kurz vor ASCO.
CTMX Marktkapitalisierung aktuell 504 Mio USD. Cash zuletzt nördlich von 350 Mio USD.
Joschka, darf man fragen, wie hoch du CTMX inzwischen prozentual in deinem Portfolio gewichtest?
Zitat von Joschka Schröder: Die jüngste Kursentwicklung scheint kaum nachvollziehbar. Bald notiert die Aktie wieder in Nähe des Emissionskurses (12 USD) aus dem Jahr 2015, obwohl es in der Zwischenzeit eine Menge positiver Nachrichten gegeben hat.
Auf Basis des aktuellen Kurses (14,30 USD) weist CytomX einen Unternehmenswert (EV) von gerade mal 120 Mio. UD auf. Zur Erinnerung: Allein der letzte Deal mit BMY hat 200 Mio. USD Upfront die Kasse gespült (obendrauf gab es noch die Option auf Meilensteinzahlungen in Milliardenhöhe und Tantiemen auf spätere Umsätze).
Ich kaufe weiter zu.
2015 war auch der Peak des Biotech-Hypes. Aktuell ist die Branche auch aufgrund regulatorischer Anstrengungen ziemlich unter Druck. Das sieht man daran, dass der Volatilitätsindex auf niedrigstem Niveau ist (= Risk on!), aber Biotech da nicht mitgehen kann, ja sogar abgibt. Und das sogar kurz vor ASCO.
CTMX Marktkapitalisierung aktuell 504 Mio USD. Cash zuletzt nördlich von 350 Mio USD.
Joschka, darf man fragen, wie hoch du CTMX inzwischen prozentual in deinem Portfolio gewichtest?
Mal wieder etwas mehr zu fundamentalen Daten:
https://www.clinicaltrials.gov/ct2/show/NCT03013491?term=CX-…
14 von 15 Locations rekrutieren nun für PROCLAIM-CX-072
https://www.clinicaltrials.gov/ct2/show/NCT03013491?term=CX-…
14 von 15 Locations rekrutieren nun für PROCLAIM-CX-072
Einmal mehr äußerst unschöne Nebenwirkungen der Yervoy-Therapie -> https://news.bms.com/press-release/asco17/new%C2%A0data-eval…
Mittels der von CytomX emtwickelten Probody-(Maskierungs-)Technologie werden sich derartige NW-Probleme immunonkologischer Therapeutika möglicherweise bzw. hoffentlich lösen lassen.
Sollte dem so sein, könnte sich der CytomX-Unternehmenswert auf Sicht mehrerer Jahre verhundertfachen ... dies ist weiterhin die finanzielle Zielsetzung aus Investorensicht, auch wenn die Kursentwicklung (infolge geringer PR-Aktivitäten und mangels klinischer Studienergebnisse) bislang ziemlich träge war.
Mittels der von CytomX emtwickelten Probody-(Maskierungs-)Technologie werden sich derartige NW-Probleme immunonkologischer Therapeutika möglicherweise bzw. hoffentlich lösen lassen.
Sollte dem so sein, könnte sich der CytomX-Unternehmenswert auf Sicht mehrerer Jahre verhundertfachen ... dies ist weiterhin die finanzielle Zielsetzung aus Investorensicht, auch wenn die Kursentwicklung (infolge geringer PR-Aktivitäten und mangels klinischer Studienergebnisse) bislang ziemlich träge war.
Antwort auf Beitrag Nr.: 55.079.377 von Joschka Schröder am 05.06.17 00:50:15In der CheckMate-204-Studie (Kombi nivolumab + ipilimumab) dasselbe Bild: Gute Wirksamkeit, geichzeitig jedoch verheerende Nebenwirkungen (u.a. therapiebedingt mehrere tote Patienten)! https://news.bms.com/press-release/asco17/first-presentation…
Einmal mehr ein wilder intraday-Kursverlauf. Start mit 5 % plus auf 15 USD, danach 8 % runter auf 13,80 USD, nachdem realisiert worden ist, dass es in der gegenwärtigen ASCO-Sitzung keine ersten Zwischenergebnisse der P1-Studie mit CX-072 gibt, sondern nur das Studienkonzept präsentiert wird. Anderes war auch nicht zu erwarten. Insgesamt ist die Kursentwicklung der letzten Wochen sehr enttäuschend.
Antwort auf Beitrag Nr.: 55.082.539 von Joschka Schröder am 05.06.17 17:38:29
ich verstehe Deine Ungeduld nicht. Es passiert doch datenmäßig im Moment gar nichts. Der Vertrag mit BMY hat ja einiges Potenzial, aber warum soll man die Aktie jetzt kaufen, kann man doch mal die ersten Ergebnisse abwarten. Ggf. muss man dann teurer kaufen, aber der Zug ist doch noch nicht abgefahren, sondern steht noch im Bahnhof.
Zitat von Joschka Schröder: Einmal mehr ein wilder intraday-Kursverlauf. Start mit 5 % plus auf 15 USD, danach 8 % runter auf 13,80 USD, nachdem realisiert worden ist, dass es in der gegenwärtigen ASCO-Sitzung keine ersten Zwischenergebnisse der P1-Studie mit CX-072 gibt, sondern nur das Studienkonzept präsentiert wird. Anderes war auch nicht zu erwarten. Insgesamt ist die Kursentwicklung der letzten Wochen sehr enttäuschend.
ich verstehe Deine Ungeduld nicht. Es passiert doch datenmäßig im Moment gar nichts. Der Vertrag mit BMY hat ja einiges Potenzial, aber warum soll man die Aktie jetzt kaufen, kann man doch mal die ersten Ergebnisse abwarten. Ggf. muss man dann teurer kaufen, aber der Zug ist doch noch nicht abgefahren, sondern steht noch im Bahnhof.
ie die neue Immuntherapie helfen könnte
Die zweite Welle gegen Krebs
von:
Siegfried Hofmann HABDELSBLATT
Datum:
06.06.2017 10:57 Uhr
PremiumPharmakonzerne wie BMS, Merck, Roche und Astra Zeneca bauen die Forschung auf dem Gebiet der Immuntherapie gegen Krebs massiv aus. Die Sparte wird zum Wachstumstreiber. Es beginnt ein komplizierter Kampf um die Marktanteile.
In die Erforschung von Immuntherapien gegen Krebs fließen Milliardenbeträge. Quelle: obs
Krebszellen
Kein anderes Thema hat die Pharmaforschung in den letzten Jahren so stark elektrisiert und beflügelt wie die Immuntherapie gegen Krebs. Denn die Idee ist so verheißungsvoll wie einfach: Der Körper soll und kann sich selbst wirkungsvoll gegen Krebszellen wehren, wenn er diese als gefährlich erkennt. Das soll die Immuntherapie bewirken und damit die heute etablierte Chemo ablösen. Bei der Chemotherapie wird der Krebs mit injiziertem Zellgift von außen bekämpft, die Nebenwirkungen sind hoch. Bei der Immuntherapie hilft sich der Körper aus eigener Kraft.
Doch der Weg zu einem breiten und wirkungsvollen Einsatz von Immuntherapie-Mitteln ist lang. Die anfängliche Euphorie verpuffte mit Blick auf einige Rückschläge in größeren klinischen Studien. Doch nun gibt es bereits erste Zulassungen, in die Forschung fließen Milliardenbeträge.
An der Faszination und der Zuversicht hat sich wenig geändert. Das zeigte sich am Wochenende auf dem diesjährigen Kongress der Amerikanischen Gesellschaft für klinische Onkologie (ASCO), dem wichtigsten Treffen der Krebsforscher. 30 000 Mediziner kamen in Chicago zusammen und kürten „Immuntherapie 2.0“ zum Fortschritt des Jahres.
Grund für die Zuversicht der Krebsforscher ist die Fülle an neuen Forschungsergebnissen, die Potenzial und Grenzen des Konzepts beleuchten. In Chicago wurden Hunderte neue Studien präsentiert. Zudem wächst die Zahl an zugelassenen Mitteln. Die Immuntherapie gegen Krebs könnte in den nächsten Jahren zum Wachstumstreiber für die gesamte Pharmaindustrie werden. Schon jetzt zeichnet sich ein intensiver Kampf um Marktanteile ab.
Bisher wird das Geschäft noch weitgehend von den amerikanischen Pharmakonzernen Bristol-Myers Squibb (BMS) und Merck & Co. beherrscht, die mit ihren Medikamenten Pionierarbeit leisteten. Doch in den letzten zwölf Monaten sind die Konkurrenten Roche, Astra-Zeneca und die Merck KGaA mit einer zweiten Welle an Krebsimmun-Mitteln angetreten.
Die deutsche Merck-Gruppe erhielt in den vergangenen Wochen für ihr Medikament Bavencio erste, noch vorläufige Zulassungen in den USA zur Behandlung einer seltenen Form von Hautkrebs sowie für den Einsatz gegen Blasenkrebs. Der Darmstädter Konzern, der nichts mit seinem Namensvetter Merck & Co. zu tun hat, ist damit das erste deutsche Unternehmen, das auf dem Feld Flagge zeigen kann. Eine ganze Reihe weiterer Substanzen befindet sich in frühen Phasen der klinischen Forschung. Sie könnten gegen Ende des Jahrzehnts die Marktreife erlangen und Merck zusätzlichen Auftrieb verleihen.
Die meisten Analysten gehen davon aus, dass BMS und Merck & Co. ihre Vormachtstellung vorerst verteidigen können. Doch den Nachzüglern mangelt es nicht an Ambitionen. „Wir haben die Chance, ein führendes Unternehmen in der Behandlung von Lungenkrebs zu werden“, sagt Pascal Soriot, der Chef der britischen Astra-Zeneca.
Die Darmstädter Merck-Gruppe und ihr US-Partner Pfizer testen Bavencio inzwischen an 5 200 Patienten in 15 verschiedenen Tumorarten, darunter auch häufige Krebsarten wie Lungen- und Nierenkrebs. Sie wollen das klinische Studienprogramm für die Substanz weiter ausbauen. Am Wochenende erweiterte Merck zudem seine Kooperation mit der britischen Biotechfirma F-Star. Die Allianz soll den Ausbau der Pipeline im Bereich Immuntherapien beschleunigen. Der Schweizer Pharmariese Roche, der seit Jahren Marktführer im Onkologiegeschäft ist, geht davon aus, dass sein Wirkstoff Tecentriq zum Rückgrat für eine ganze Palette an Kombinations-Medikamenten gegen diverse Krebserkrankungen werden kann.
Eine alte Idee der Medizin
Die Idee, das körpereigene Immunsystem gegen Krebszellen zu aktivieren, geistert schon seit mehr als 100 Jahren durch die Medizin. Und schon seit längerem wird einigen etablierten Krebsmedikamenten, so etwa Bestsellern wie den Blutkrebsmedikamenten Revlimid und Rituxan, ein gewisser Effekt auf das Immunsystem zugeschrieben.
Er steuert aus den USA die weltweite Pharmaforschung der Merck KGaA.
Wirklich Schub erhielt der Ansatz aber erst, nachdem Forscher im letzten Jahrzehnt genauer aufklärten, auf welche Weise sich Tumorzellen gegen das Immunsystem schützen: Sie produzieren spezielle Signalstoffe, sogenannte „Checkpoints“, die Immunzellen quasi stumm schalten. Diese Signalstoffe sollen durch neue Mittel blockiert werden. Die ersten dieser Checkpoint-Inhibitoren, die ab 2011 auf den Markt kamen, zeigten erstaunlich gute Wirkung bei Krebsarten, die als schwer behandelbar galten, etwa beim schwarzen Hautkrebs.
Die Branche hat ihre Krebsforschung seitdem massiv in Richtung Immuntherapie umdirigiert. Inzwischen wird auch das kommerzielle Gewicht der neuen Substanzklasse deutlich. 2016 hat sich der Umsatz mit den drei bereits zugelassenen Medikamenten der Gruppe (Yervoy, Keytruda, Opdivo) von 2,8 auf 6,2 Milliarden Dollar mehr als verdoppelt. Sie sind damit bereits wesentlicher Wachstumstreiber für das wichtigste Produktsegment der Pharmabranche.
Insgesamt haben die 15 führenden Anbieter von Krebsmitteln ihre Erlöse 2016 um gut zwölf Prozent auf 89 Milliarden Dollar gesteigert. Dies scheint sich ungebremst fortzusetzen: Im ersten Quartal 2017 legten die führenden Akteure ebenfalls um etwa zwölf Prozent zu, wobei die Krebsimmun-Wirkstoffe knapp 80 Prozent Umsatzwachstum verbuchten. Sie dürften damit im laufenden Jahr auf zehn Milliarden Dollar Umsatz zusteuern und könnten nach Einschätzung von Analysten schon Anfang des nächsten Jahrzehnts auf 30 Milliarden Dollar wachsen. „Von vielen Immun-Onkologie-Produkten werden eindrucksvolle Fortschritte erwartet“, heißt es in einem Ausblick des Analyse-Unternehmens Evaluate Pharma.
Allerdings ist das Arbeitsfeld keineswegs vor Fehlschlägen gefeit. Am heftigsten bekam das im vergangenen Oktober der Marktführer BMS zu spüren, als sein Wirkstoff Opdivo zur Überraschung vieler Beobachter in einer großen Studie gegen Lungenkrebs scheiterte. Der Rückschlag kostete den US-Konzern auf einen Schlag rund 20 Milliarden Dollar an Börsenwert und stärkt nach Einschätzung von Analysten die Perspektiven für das Konkurrenzprodukt Keytruda von Merck & Co. Der Wirkstoff Tecentriq von Roche zeigte jüngst in einer Studie gegen Blasenkrebs keine Vorteile gegenüber der Standardtherapie. Das wiederum könnte die vorläufige Zulassung für das Mittel bei Blasenkrebs wieder infrage stellen.
Rudern gegen Krebs
Solche Fehlschläge und zahlreiche weitere Studien beleuchten die Chancen und Herausforderungen der neuen Wirkstoffe: Die Immunmedikamente, so zeigt sich, sind keine Allheilmittel. Wirklich gut wirken sie nur bei 20 bis 30 Prozent der Patienten. Ihre Wirksamkeit hängt stark davon ab, ob genügend Immunzellen in das Tumorgewebe eingewandert sind und in welchem Maße Krebszellen tatsächlich Signalmoleküle produzieren.
Um das zu klären, wird eine möglichst präzise Diagnostik nötig sein. Auch auf diesem Feld tut sich viel: So vereinbarte der deutsche Diagnostik- und Biotechkonzern Qiagen am Wochenende eine Allianz mit dem US-Pharmahersteller BMS zur Entwicklung neuer Begleit-Tests für immun-onkologische Therapien. Qiagen will dazu seine eigene neue Gen-Analyse-Technik einsetzen. Zugleich erwarb der Hildener Konzern Lizenzen von der John Hopkins University für Biomarker, die in der Immun-Onkologie eine Rolle spielen.
Wie wichtig die genetische Diagnostik geworden ist, zeigt etwa die jüngste Zulassung für den Wirkstoff Keytruda von Merck & Co. Er wurde von der FDA für alle Krebsarten mit einer bestimmten genetischen Modifikation zugelassen, die zu einer hohen Produktion eines bestimmten Signalstoffs führt.
Die Tricks der Krebszellen
Neben Signalstoffen verwenden Krebszellen allerdings auch noch andere Abwehrmechanismen gegen die Immunzellen. Um die Erfolgsquoten des Therapiekonzepts zu erhöhen, wird man daher noch andere Checkpoint-Inhibitoren benötigen. Zudem deutet sich an, dass die besten Erfolge in Kombination mit etablierten Medikamenten oder Chemotherapien zu erzielen sind.
Damit zeichnet sich für die Pharmafirmen eine sehr komplizierte Lage ab, was die Gestaltung von klinischen Studien mit den neuen Wirkstoffen angeht. Zulassungen und Marktpotenziale hängen sehr stark davon ab, die richtigen Kombinationen und die richtigen Patientengruppen auszuwählen.
Der US-Konzern BMS etwa scheiterte mit seinem Mittel Opdivo bei Lungenkrebs offenbar deshalb, weil er das Einsatzfeld zu breit ausgelegt hatte. Unter anderem in Reaktion auf den Rückschlag des Konkurrenten haben Merck und Pfizer ihre klinische Studie mit dem Mittel Bavencio im Bereich Lungenkrebs modifiziert und erweitert. Sie differenzieren nun stärker nach Subgruppen von Patienten und wollen auch die Gesamtüberlebensraten messen. Das wird die Studie verteuern und verlängern, soll aber auch die Erfolgschancen erhöhen.
Insgesamt laufen in der Branche inzwischen mehr als 1 500 klinische Studien mit immuntherapeutischen Wirkstoffkandidaten in Dutzenden von Kombinationen, davon allein rund 500 mit Keytruda, dem Spitzenprodukt von Merck & Co., sowie mehr als 400 mit dem BMS-Produkt Opdivo. Die Zahl der Kombinationsstudien hat sich dabei nach Daten von Evaluate Pharma innerhalb von 18 Monaten mehr als verdreifacht.
In den kommenden Jahren dürfte das Arbeitsgebiet daher für einige Überraschungen gut sein und noch erheblichen Spielraum für neue Wirkstoffe und Konzepte bieten. Die Chancen stehen insofern gut, dass in absehbarer Zukunft die „Immuntherapie 3.0“ als Innovation des Jahres gekürt wird.
Die zweite Welle gegen Krebs
von:
Siegfried Hofmann HABDELSBLATT
Datum:
06.06.2017 10:57 Uhr
PremiumPharmakonzerne wie BMS, Merck, Roche und Astra Zeneca bauen die Forschung auf dem Gebiet der Immuntherapie gegen Krebs massiv aus. Die Sparte wird zum Wachstumstreiber. Es beginnt ein komplizierter Kampf um die Marktanteile.
In die Erforschung von Immuntherapien gegen Krebs fließen Milliardenbeträge. Quelle: obs
Krebszellen
Kein anderes Thema hat die Pharmaforschung in den letzten Jahren so stark elektrisiert und beflügelt wie die Immuntherapie gegen Krebs. Denn die Idee ist so verheißungsvoll wie einfach: Der Körper soll und kann sich selbst wirkungsvoll gegen Krebszellen wehren, wenn er diese als gefährlich erkennt. Das soll die Immuntherapie bewirken und damit die heute etablierte Chemo ablösen. Bei der Chemotherapie wird der Krebs mit injiziertem Zellgift von außen bekämpft, die Nebenwirkungen sind hoch. Bei der Immuntherapie hilft sich der Körper aus eigener Kraft.
Doch der Weg zu einem breiten und wirkungsvollen Einsatz von Immuntherapie-Mitteln ist lang. Die anfängliche Euphorie verpuffte mit Blick auf einige Rückschläge in größeren klinischen Studien. Doch nun gibt es bereits erste Zulassungen, in die Forschung fließen Milliardenbeträge.
An der Faszination und der Zuversicht hat sich wenig geändert. Das zeigte sich am Wochenende auf dem diesjährigen Kongress der Amerikanischen Gesellschaft für klinische Onkologie (ASCO), dem wichtigsten Treffen der Krebsforscher. 30 000 Mediziner kamen in Chicago zusammen und kürten „Immuntherapie 2.0“ zum Fortschritt des Jahres.
Grund für die Zuversicht der Krebsforscher ist die Fülle an neuen Forschungsergebnissen, die Potenzial und Grenzen des Konzepts beleuchten. In Chicago wurden Hunderte neue Studien präsentiert. Zudem wächst die Zahl an zugelassenen Mitteln. Die Immuntherapie gegen Krebs könnte in den nächsten Jahren zum Wachstumstreiber für die gesamte Pharmaindustrie werden. Schon jetzt zeichnet sich ein intensiver Kampf um Marktanteile ab.
Bisher wird das Geschäft noch weitgehend von den amerikanischen Pharmakonzernen Bristol-Myers Squibb (BMS) und Merck & Co. beherrscht, die mit ihren Medikamenten Pionierarbeit leisteten. Doch in den letzten zwölf Monaten sind die Konkurrenten Roche, Astra-Zeneca und die Merck KGaA mit einer zweiten Welle an Krebsimmun-Mitteln angetreten.
Die deutsche Merck-Gruppe erhielt in den vergangenen Wochen für ihr Medikament Bavencio erste, noch vorläufige Zulassungen in den USA zur Behandlung einer seltenen Form von Hautkrebs sowie für den Einsatz gegen Blasenkrebs. Der Darmstädter Konzern, der nichts mit seinem Namensvetter Merck & Co. zu tun hat, ist damit das erste deutsche Unternehmen, das auf dem Feld Flagge zeigen kann. Eine ganze Reihe weiterer Substanzen befindet sich in frühen Phasen der klinischen Forschung. Sie könnten gegen Ende des Jahrzehnts die Marktreife erlangen und Merck zusätzlichen Auftrieb verleihen.
Die meisten Analysten gehen davon aus, dass BMS und Merck & Co. ihre Vormachtstellung vorerst verteidigen können. Doch den Nachzüglern mangelt es nicht an Ambitionen. „Wir haben die Chance, ein führendes Unternehmen in der Behandlung von Lungenkrebs zu werden“, sagt Pascal Soriot, der Chef der britischen Astra-Zeneca.
Die Darmstädter Merck-Gruppe und ihr US-Partner Pfizer testen Bavencio inzwischen an 5 200 Patienten in 15 verschiedenen Tumorarten, darunter auch häufige Krebsarten wie Lungen- und Nierenkrebs. Sie wollen das klinische Studienprogramm für die Substanz weiter ausbauen. Am Wochenende erweiterte Merck zudem seine Kooperation mit der britischen Biotechfirma F-Star. Die Allianz soll den Ausbau der Pipeline im Bereich Immuntherapien beschleunigen. Der Schweizer Pharmariese Roche, der seit Jahren Marktführer im Onkologiegeschäft ist, geht davon aus, dass sein Wirkstoff Tecentriq zum Rückgrat für eine ganze Palette an Kombinations-Medikamenten gegen diverse Krebserkrankungen werden kann.
Eine alte Idee der Medizin
Die Idee, das körpereigene Immunsystem gegen Krebszellen zu aktivieren, geistert schon seit mehr als 100 Jahren durch die Medizin. Und schon seit längerem wird einigen etablierten Krebsmedikamenten, so etwa Bestsellern wie den Blutkrebsmedikamenten Revlimid und Rituxan, ein gewisser Effekt auf das Immunsystem zugeschrieben.
Er steuert aus den USA die weltweite Pharmaforschung der Merck KGaA.
Wirklich Schub erhielt der Ansatz aber erst, nachdem Forscher im letzten Jahrzehnt genauer aufklärten, auf welche Weise sich Tumorzellen gegen das Immunsystem schützen: Sie produzieren spezielle Signalstoffe, sogenannte „Checkpoints“, die Immunzellen quasi stumm schalten. Diese Signalstoffe sollen durch neue Mittel blockiert werden. Die ersten dieser Checkpoint-Inhibitoren, die ab 2011 auf den Markt kamen, zeigten erstaunlich gute Wirkung bei Krebsarten, die als schwer behandelbar galten, etwa beim schwarzen Hautkrebs.
Die Branche hat ihre Krebsforschung seitdem massiv in Richtung Immuntherapie umdirigiert. Inzwischen wird auch das kommerzielle Gewicht der neuen Substanzklasse deutlich. 2016 hat sich der Umsatz mit den drei bereits zugelassenen Medikamenten der Gruppe (Yervoy, Keytruda, Opdivo) von 2,8 auf 6,2 Milliarden Dollar mehr als verdoppelt. Sie sind damit bereits wesentlicher Wachstumstreiber für das wichtigste Produktsegment der Pharmabranche.
Insgesamt haben die 15 führenden Anbieter von Krebsmitteln ihre Erlöse 2016 um gut zwölf Prozent auf 89 Milliarden Dollar gesteigert. Dies scheint sich ungebremst fortzusetzen: Im ersten Quartal 2017 legten die führenden Akteure ebenfalls um etwa zwölf Prozent zu, wobei die Krebsimmun-Wirkstoffe knapp 80 Prozent Umsatzwachstum verbuchten. Sie dürften damit im laufenden Jahr auf zehn Milliarden Dollar Umsatz zusteuern und könnten nach Einschätzung von Analysten schon Anfang des nächsten Jahrzehnts auf 30 Milliarden Dollar wachsen. „Von vielen Immun-Onkologie-Produkten werden eindrucksvolle Fortschritte erwartet“, heißt es in einem Ausblick des Analyse-Unternehmens Evaluate Pharma.
Allerdings ist das Arbeitsfeld keineswegs vor Fehlschlägen gefeit. Am heftigsten bekam das im vergangenen Oktober der Marktführer BMS zu spüren, als sein Wirkstoff Opdivo zur Überraschung vieler Beobachter in einer großen Studie gegen Lungenkrebs scheiterte. Der Rückschlag kostete den US-Konzern auf einen Schlag rund 20 Milliarden Dollar an Börsenwert und stärkt nach Einschätzung von Analysten die Perspektiven für das Konkurrenzprodukt Keytruda von Merck & Co. Der Wirkstoff Tecentriq von Roche zeigte jüngst in einer Studie gegen Blasenkrebs keine Vorteile gegenüber der Standardtherapie. Das wiederum könnte die vorläufige Zulassung für das Mittel bei Blasenkrebs wieder infrage stellen.
Rudern gegen Krebs
Solche Fehlschläge und zahlreiche weitere Studien beleuchten die Chancen und Herausforderungen der neuen Wirkstoffe: Die Immunmedikamente, so zeigt sich, sind keine Allheilmittel. Wirklich gut wirken sie nur bei 20 bis 30 Prozent der Patienten. Ihre Wirksamkeit hängt stark davon ab, ob genügend Immunzellen in das Tumorgewebe eingewandert sind und in welchem Maße Krebszellen tatsächlich Signalmoleküle produzieren.
Um das zu klären, wird eine möglichst präzise Diagnostik nötig sein. Auch auf diesem Feld tut sich viel: So vereinbarte der deutsche Diagnostik- und Biotechkonzern Qiagen am Wochenende eine Allianz mit dem US-Pharmahersteller BMS zur Entwicklung neuer Begleit-Tests für immun-onkologische Therapien. Qiagen will dazu seine eigene neue Gen-Analyse-Technik einsetzen. Zugleich erwarb der Hildener Konzern Lizenzen von der John Hopkins University für Biomarker, die in der Immun-Onkologie eine Rolle spielen.
Wie wichtig die genetische Diagnostik geworden ist, zeigt etwa die jüngste Zulassung für den Wirkstoff Keytruda von Merck & Co. Er wurde von der FDA für alle Krebsarten mit einer bestimmten genetischen Modifikation zugelassen, die zu einer hohen Produktion eines bestimmten Signalstoffs führt.
Die Tricks der Krebszellen
Neben Signalstoffen verwenden Krebszellen allerdings auch noch andere Abwehrmechanismen gegen die Immunzellen. Um die Erfolgsquoten des Therapiekonzepts zu erhöhen, wird man daher noch andere Checkpoint-Inhibitoren benötigen. Zudem deutet sich an, dass die besten Erfolge in Kombination mit etablierten Medikamenten oder Chemotherapien zu erzielen sind.
Damit zeichnet sich für die Pharmafirmen eine sehr komplizierte Lage ab, was die Gestaltung von klinischen Studien mit den neuen Wirkstoffen angeht. Zulassungen und Marktpotenziale hängen sehr stark davon ab, die richtigen Kombinationen und die richtigen Patientengruppen auszuwählen.
Der US-Konzern BMS etwa scheiterte mit seinem Mittel Opdivo bei Lungenkrebs offenbar deshalb, weil er das Einsatzfeld zu breit ausgelegt hatte. Unter anderem in Reaktion auf den Rückschlag des Konkurrenten haben Merck und Pfizer ihre klinische Studie mit dem Mittel Bavencio im Bereich Lungenkrebs modifiziert und erweitert. Sie differenzieren nun stärker nach Subgruppen von Patienten und wollen auch die Gesamtüberlebensraten messen. Das wird die Studie verteuern und verlängern, soll aber auch die Erfolgschancen erhöhen.
Insgesamt laufen in der Branche inzwischen mehr als 1 500 klinische Studien mit immuntherapeutischen Wirkstoffkandidaten in Dutzenden von Kombinationen, davon allein rund 500 mit Keytruda, dem Spitzenprodukt von Merck & Co., sowie mehr als 400 mit dem BMS-Produkt Opdivo. Die Zahl der Kombinationsstudien hat sich dabei nach Daten von Evaluate Pharma innerhalb von 18 Monaten mehr als verdreifacht.
In den kommenden Jahren dürfte das Arbeitsgebiet daher für einige Überraschungen gut sein und noch erheblichen Spielraum für neue Wirkstoffe und Konzepte bieten. Die Chancen stehen insofern gut, dass in absehbarer Zukunft die „Immuntherapie 3.0“ als Innovation des Jahres gekürt wird.
Antwort auf Beitrag Nr.: 55.054.294 von SpanishEyes am 31.05.17 22:44:38Nun rekrutieren 16 von 17 Locations für PROCLAIM-CX-072.
Ausserdem hat nun auch die Rekrutierung für PROCLAIM-CX-2009 begonnen, ebenfalls 150 Teilnehmer avisiert: https://clinicaltrials.gov/ct2/show/NCT03149549?term=cytomx&…
CytomX versucht aber auch wirklich jegliche Aufmerksamkeit durch PRs o.ä. zu vermeiden Auf gewisse Art jedoch wohltuend.
Auf gewisse Art jedoch wohltuend.
Wenn die klinischen Daten in ca. 6 Monaten gut sind wird es eh egal sein - wenn sie nicht gut sind, dann auch...
Ausserdem hat nun auch die Rekrutierung für PROCLAIM-CX-2009 begonnen, ebenfalls 150 Teilnehmer avisiert: https://clinicaltrials.gov/ct2/show/NCT03149549?term=cytomx&…
CytomX versucht aber auch wirklich jegliche Aufmerksamkeit durch PRs o.ä. zu vermeiden
 Auf gewisse Art jedoch wohltuend.
Auf gewisse Art jedoch wohltuend. Wenn die klinischen Daten in ca. 6 Monaten gut sind wird es eh egal sein - wenn sie nicht gut sind, dann auch...
Kurs geht stetig bergab. Hoffentlich ist bei den initiierten trials nichts schiefgelaufen, schlechtes omen jedenfalls.
Antwort auf Beitrag Nr.: 55.115.056 von biopadawan am 09.06.17 23:01:52Da mache ich mir keine Sorgen, das hätte man schon mitbekommen.
Börsenkapitalisierung abzgl. NetCash aktuell 122 Mio. USD. Das bedeutet, dass die Erwartungen "des Marktes" an die Probody-Technologie sehr gering sind bzw. CytomX überhaupt nicht wahrgenommen wird.
Börsenkapitalisierung abzgl. NetCash aktuell 122 Mio. USD. Das bedeutet, dass die Erwartungen "des Marktes" an die Probody-Technologie sehr gering sind bzw. CytomX überhaupt nicht wahrgenommen wird.
Antwort auf Beitrag Nr.: 55.115.407 von Joschka Schröder am 10.06.17 01:06:03Die Frage ist, warum der Markt in der Vergangenheit ohne die lukrativen Deals mit Abbvie (milestones bis zu 480mio) , BMS (bekannt) etc. bereits zu einer Bewertung von 200-300mio EV kam.
Seit dem 200Mio Deal mit BMS findet ein ständiger Abverkauf statt.
Letztlich muss man wohl BMS eher Vertrauen als dem irrationalen Markt, jedoch finde ich den Abverkauf in diesen Ausmaß schon irritierend.
Hoffen wir mal, dass es sich gerade um absolute Schnäppchenkurse handelt.
Seit dem 200Mio Deal mit BMS findet ein ständiger Abverkauf statt.
Letztlich muss man wohl BMS eher Vertrauen als dem irrationalen Markt, jedoch finde ich den Abverkauf in diesen Ausmaß schon irritierend.
Hoffen wir mal, dass es sich gerade um absolute Schnäppchenkurse handelt.
Antwort auf Beitrag Nr.: 55.115.779 von biopadawan am 10.06.17 08:08:25Bei den potentiellen (!) Meilensteinen aus besagtem Deal mußt Du noch eine Null dranhängen.
Eine Upfrontzahlung in Höhe von 200 Mio. USD ist aber bereits geflossen ... dennoch notiert der Kurs auf niedrigerem Niveau als zuvor. Natürlich ist das irrational und, wenn man bereits stärker investiert ist, nicht besonders schön mit anzusehen.
Auch vor dem Deal hatte es schon - jeweils ohne News - wilde Kursschwankungen gegeben.
Eine Upfrontzahlung in Höhe von 200 Mio. USD ist aber bereits geflossen ... dennoch notiert der Kurs auf niedrigerem Niveau als zuvor. Natürlich ist das irrational und, wenn man bereits stärker investiert ist, nicht besonders schön mit anzusehen.
Auch vor dem Deal hatte es schon - jeweils ohne News - wilde Kursschwankungen gegeben.
Antwort auf Beitrag Nr.: 55.116.784 von Joschka Schröder am 10.06.17 12:09:51Ich bin nicht vom Fach. Deswegen kann ich die auf dem Prüfstand stehende Technologie nicht beurteilen, außer dass im Bereich Krebsforschung und Immunsystem wol derzeit generell viel Forschungsgelder fließen, weil dort die größten Heilungschancen wohl liegen.
Ob die Aktie billig ist weis man erste wenn man erste Ergebnisse hat und die Technologie besser in der Praxis ein geschätzt werden kann.
Ich habe Abstauberlimits gesetzt, weil die Technologie gut durchfinanziert ist und mit BMS ein auf diesem Bereich stark in der Forschung investiert und nicht ohne Not eine solche Vorfinanzierung in die technologie macht; die erwarten da wohl auch positive Ergebnisse. - Ja insoweit wird man die Aktie vom Chancen Risiko Verhältnis als günstig bezeichnen müssen.
Im Handelsblatt konnte ich in letzter Zeit lesen, das im Bereich Immunsystemaktivierung zur Krebsbekämpfung stark investiert wird und verschiedene Ansätzte entwicket werden.
Kann mir jemand verständlich die konkreten Risiken und Chancen bei der Entwicklung in kurzen Worten erklären ? Würde das gerne grob verstehen, wenn ich da investieren.
Ob die Aktie billig ist weis man erste wenn man erste Ergebnisse hat und die Technologie besser in der Praxis ein geschätzt werden kann.
Ich habe Abstauberlimits gesetzt, weil die Technologie gut durchfinanziert ist und mit BMS ein auf diesem Bereich stark in der Forschung investiert und nicht ohne Not eine solche Vorfinanzierung in die technologie macht; die erwarten da wohl auch positive Ergebnisse. - Ja insoweit wird man die Aktie vom Chancen Risiko Verhältnis als günstig bezeichnen müssen.
Im Handelsblatt konnte ich in letzter Zeit lesen, das im Bereich Immunsystemaktivierung zur Krebsbekämpfung stark investiert wird und verschiedene Ansätzte entwicket werden.
Kann mir jemand verständlich die konkreten Risiken und Chancen bei der Entwicklung in kurzen Worten erklären ? Würde das gerne grob verstehen, wenn ich da investieren.
vielleicht ist die derzeitige Kursentwicklung etwas irritierend, aber auch für BMS sind 200 mio$ + kein Pappenstiel, den sie so einfach mal verplempern. Ich sehe den Kurs z.Zt. Ohne Richtung vor sich her dümpeln.
Auch ohne hartem Poc wird bei dem Engagement von BMS zumindest die Hoffnung auf ein Poc zu irgendeinem Zeitpunkt mal aufkommen. Dies alleine hätte dann das Potential für eine Verdoppelung.
Aber BMS' Engagement lässt berechtigt auf mehr schließen als nur Hoffnung.
Auch ohne hartem Poc wird bei dem Engagement von BMS zumindest die Hoffnung auf ein Poc zu irgendeinem Zeitpunkt mal aufkommen. Dies alleine hätte dann das Potential für eine Verdoppelung.
Aber BMS' Engagement lässt berechtigt auf mehr schließen als nur Hoffnung.
Aktualisierte Firmenpräsentation - keine klinischen Daten mehr dieses Jahr:
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
http://phx.corporate-ir.net/External.File?t=1&item=VHlwZT0yf…
Antwort auf Beitrag Nr.: 55.121.837 von SpanishEyes am 12.06.17 00:04:06An der Präsentation ist mir ein Bild aufgefallen.
S.14 ist ein PET-Imaging of tumor des Chx 072.
Hier handelt es sich um ein diagnostisches Bild eines Menschen mit offensichtlicher Anhäufung des chx 072 im Tumor in vivo.
Da wäre schon mal ein Fingerzeig auf einen zukünftigen proof of concept.
Ist meine Interpretation schlüssig?
LG
StefanR
S.14 ist ein PET-Imaging of tumor des Chx 072.
Hier handelt es sich um ein diagnostisches Bild eines Menschen mit offensichtlicher Anhäufung des chx 072 im Tumor in vivo.
Da wäre schon mal ein Fingerzeig auf einen zukünftigen proof of concept.
Ist meine Interpretation schlüssig?
LG
StefanR
Antwort auf Beitrag Nr.: 55.122.563 von StefanR am 12.06.17 09:24:53
Das Bild ist in der Tat ein Beleg dafür, dass die proteolytische Abspaltung der Maskierung nicht nur im Tiermodell, sondern auch beim Menschen funktioniert.
Zitat von StefanR: Hier handelt es sich um ein diagnostisches Bild eines Menschen mit offensichtlicher Anhäufung des chx 072 im Tumor in vivo.
Da wäre schon mal ein Fingerzeig auf einen zukünftigen proof of concept.
Ist meine Interpretation schlüssig?
Das Bild ist in der Tat ein Beleg dafür, dass die proteolytische Abspaltung der Maskierung nicht nur im Tiermodell, sondern auch beim Menschen funktioniert.
Antwort auf Beitrag Nr.: 55.123.988 von Joschka Schröder am 12.06.17 12:48:48Woran macht ihr fest, dass es sich bei dem PET scan Bild um einen Menschen handelt und nicht um einen Affen?
Antwort auf Beitrag Nr.: 55.123.988 von Joschka Schröder am 12.06.17 12:48:48Was bedeutet das für den thematisch nicht sachkundigen Anleger das für die konkrete Risikoeinschätzung ? Wäre prima wenn ich / wir von Eurem Wissen profitieren könnten.
Antwort auf Beitrag Nr.: 55.123.988 von Joschka Schröder am 12.06.17 12:48:48Zudem stelle ich mir die Frage, ob ich nicht EIB aehnliches Bild bei einem nicht- probody AK erhalten würde. M.E. wird der meiste Teil auch dort in Tumorgewebe gebunden werden, einfach aufgrund Exprimierung...
Des weiteren stelle ich mir die Frage was 89zr bedeutet? Wurde hier eine radioaktive Variante des CX072 verwendet? Diese würde ja bei der PROCLAIM072 Studie ja m.W. nicht eingesetzt.
Also doch ein Affe oder wie ist das erklärbar?
Des weiteren stelle ich mir die Frage was 89zr bedeutet? Wurde hier eine radioaktive Variante des CX072 verwendet? Diese würde ja bei der PROCLAIM072 Studie ja m.W. nicht eingesetzt.
Also doch ein Affe oder wie ist das erklärbar?
Antwort auf Beitrag Nr.: 55.124.261 von Ville7 am 12.06.17 13:28:38Dieses Röntgenbild existiert seit der März-2017-Unternehmenspräsentation.
Der erste Patient wurde ab Januar/Februar behandelt.
ZR 89 wird gern zur Diagnostik bei mab-Therapien am Menschen verwendet, da relativ unschädlich und geeignete HWZ (3-4 Tage) für pharmakokinetische Verteilungsprozesse.
Für Tiermodelle könnte man übliche Biopsien und andere radiologisch (schädlichere) Substanzen verwenden.
Anhand der Umrisse schließe ich auf homo sapiens
Der erste Patient wurde ab Januar/Februar behandelt.
ZR 89 wird gern zur Diagnostik bei mab-Therapien am Menschen verwendet, da relativ unschädlich und geeignete HWZ (3-4 Tage) für pharmakokinetische Verteilungsprozesse.
Für Tiermodelle könnte man übliche Biopsien und andere radiologisch (schädlichere) Substanzen verwenden.
Anhand der Umrisse schließe ich auf homo sapiens

Antwort auf Beitrag Nr.: 55.124.261 von Ville7 am 12.06.17 13:28:38@Ville
Entscheidend für das gesamte Therapiekonzept ist, dass die proteolytische Demaskierung funktioniert. Und das tut sie offensichtlich, weil es andernfalls nicht zur Anhäufung des (demaskierten) Probodys im Tumor käme (-> Bindung der freigelegten Fab-Fragmente an das Target). Dieser Nachweis ist Sinn und Zwecks der Untersuchungen.
Da der gesamte Probody radioaktiv markiert ist, werden natürlich auch stark durchblutete Gewebe (Herz, Leber, Gefäßsystem) dargestellt. (In der Leber wird zudem der Probody/Mab abgebaut.)
Affe und Mensch unterscheiden sich - wenigstens - radiologisch schon, die Abbildung ist eindeutig.
Entscheidend für das gesamte Therapiekonzept ist, dass die proteolytische Demaskierung funktioniert. Und das tut sie offensichtlich, weil es andernfalls nicht zur Anhäufung des (demaskierten) Probodys im Tumor käme (-> Bindung der freigelegten Fab-Fragmente an das Target). Dieser Nachweis ist Sinn und Zwecks der Untersuchungen.
Da der gesamte Probody radioaktiv markiert ist, werden natürlich auch stark durchblutete Gewebe (Herz, Leber, Gefäßsystem) dargestellt. (In der Leber wird zudem der Probody/Mab abgebaut.)
Affe und Mensch unterscheiden sich - wenigstens - radiologisch schon, die Abbildung ist eindeutig.
Antwort auf Beitrag Nr.: 55.124.714 von Joschka Schröder am 12.06.17 14:28:17@Stefan: Danke für die Erläuterungen, hatte bezüglich zr89 keine Zeit auf die Schnelle zu recherchieren...
@Joschka: Okay, ich verstehe. Wenn die Proteasen die Masken nicht abspalten würden, würde man am Tumor keine Konzentration (schwarz) feststellen. Danke für die Klarstellung. Wollen wir hoffen, dass die Abspaltungsprozesse wirklich nur weitgehend am Tumor stattfinden...
Und danke an Euch beide für Eure Einschätzung, dass es sich wohl eindeutig um einen Menschen handelt.
In der Risikobewertung sollte das somit ein kleines Stückchen der weiterhin bestehenden Unsicherheit genommen haben.
@Joschka: Okay, ich verstehe. Wenn die Proteasen die Masken nicht abspalten würden, würde man am Tumor keine Konzentration (schwarz) feststellen. Danke für die Klarstellung. Wollen wir hoffen, dass die Abspaltungsprozesse wirklich nur weitgehend am Tumor stattfinden...
Und danke an Euch beide für Eure Einschätzung, dass es sich wohl eindeutig um einen Menschen handelt.
In der Risikobewertung sollte das somit ein kleines Stückchen der weiterhin bestehenden Unsicherheit genommen haben.
PS: Positiv ist weiterhin, dass das Maskierungspeptid offensichtlich nicht an gesundes Gewebe bindet, was theoretisch ja auch vorstellbar wäre.
Zum Nachweis der Stabilität des Probodys außerhalb des Tumors wäre im Fall von Targets wie PD-L1 wohl am besten eine vergleichende Untersuchung mit einem entsprechenden, radioaktiv markierten Antikörper geeignet. Bei Targets wie CD166, die von multiplen Geweben stark exprimiert werden, würde hingegen bereits eine einzige Aufnahme nach Injektion des markierten Probodys ausreichen.
Zum Nachweis der Stabilität des Probodys außerhalb des Tumors wäre im Fall von Targets wie PD-L1 wohl am besten eine vergleichende Untersuchung mit einem entsprechenden, radioaktiv markierten Antikörper geeignet. Bei Targets wie CD166, die von multiplen Geweben stark exprimiert werden, würde hingegen bereits eine einzige Aufnahme nach Injektion des markierten Probodys ausreichen.
Antwort auf Beitrag Nr.: 55.125.152 von Joschka Schröder am 12.06.17 15:17:45Soweit ich Eure Diskussion verstehe, gibt es erste konkrete Hinweise darauf, dass die zentrale Technologie gezielt den Wirkstoff in das Tumorgewebe zu transportieren wohl auch beim Menschen funktioniert. habe ich das so richtig verstanden ?
Das würde sich auch mit die Zahlung von 225 Mio vom BMS sich decken.
Das würde sich auch mit die Zahlung von 225 Mio vom BMS sich decken.
Antwort auf Beitrag Nr.: 55.125.152 von Joschka Schröder am 12.06.17 15:17:45Aus meiner Sicht ist das Röntgenbild, unkommentiert in die Präsentation(en) geworfen, schon eine kleine Sensation !
Wichtig wäre es, daß beim Metabolismus des Prodrug cx-072 die "Denaturierung" schnell und der Reihenfolge nach geschieht.
Hoffentlich wird nicht zuerst die Maskierung in der Leber proteolytisch entfernt, und danach erst erfolgt die Inaktivierung des cx-072.
Sonst könnte es zu starken immunologischen Reaktionen in der Leber kommen, weil ein "scharf geschalteter PD-L1-Antibody dann T-Zellen am Metabolisierungsort Leber aktivieren würde.
Wichtig wäre es, daß beim Metabolismus des Prodrug cx-072 die "Denaturierung" schnell und der Reihenfolge nach geschieht.
Hoffentlich wird nicht zuerst die Maskierung in der Leber proteolytisch entfernt, und danach erst erfolgt die Inaktivierung des cx-072.
Sonst könnte es zu starken immunologischen Reaktionen in der Leber kommen, weil ein "scharf geschalteter PD-L1-Antibody dann T-Zellen am Metabolisierungsort Leber aktivieren würde.
Antwort auf Beitrag Nr.: 55.125.560 von StefanR am 12.06.17 16:14:55Hinsichtlich der Elimination erwarte ich keine Probleme. Ablauf wie bei konventionellen monoklonalen Antikörpern via Phagozytose durch das retikuloendotheliales System. Wie der Probody dort lysosomal zerlegt wird, sollte ohne Belang sein.
Antwort auf Beitrag Nr.: 55.125.560 von StefanR am 12.06.17 16:14:55
Die kommen halt von der wissenschaftlichen Seite und sind keine PR-Leute. Haben noch nicht einmal den Klinikstart des CX-2009 gemeldet. Telefonkonferenzen finden nur in seltenen Ausnahmefällen statt, wenn es wirklich wichtige Neuigkeiten zu berichten/diskutieren gibt (z.B. BMY-Kooperation). Im Grunde genommen so, wie man es sich von einem seriösen Unternehmen wünscht. Nachteil ist halt die eher bescheidene Kursentwicklung. Wenn das Konzept wie gewünscht aufgeht, spielt das später aber keine Rolle mehr, dann wird sich der Kurs den Fakten zügig anpassen.
Zitat von StefanR: Aus meiner Sicht ist das Röntgenbild, unkommentiert in die Präsentation(en) geworfen, schon eine kleine Sensation !
Die kommen halt von der wissenschaftlichen Seite und sind keine PR-Leute. Haben noch nicht einmal den Klinikstart des CX-2009 gemeldet. Telefonkonferenzen finden nur in seltenen Ausnahmefällen statt, wenn es wirklich wichtige Neuigkeiten zu berichten/diskutieren gibt (z.B. BMY-Kooperation). Im Grunde genommen so, wie man es sich von einem seriösen Unternehmen wünscht. Nachteil ist halt die eher bescheidene Kursentwicklung. Wenn das Konzept wie gewünscht aufgeht, spielt das später aber keine Rolle mehr, dann wird sich der Kurs den Fakten zügig anpassen.
Unerwartete Todesfälle (zumindest) in einer Keytruda (= anti-PD-1)-Kombistudie
https://endpts.com/merck-halts-enrollment-on-two-phiii-keytr…
Der von CytomX entwickelte anti-PD-1-Probody CX-188 befindet sich noch nicht in der Klinik, steht allerdings kurz davor.
https://endpts.com/merck-halts-enrollment-on-two-phiii-keytr…
Der von CytomX entwickelte anti-PD-1-Probody CX-188 befindet sich noch nicht in der Klinik, steht allerdings kurz davor.
Antwort auf Beitrag Nr.: 55.132.703 von Joschka Schröder am 13.06.17 17:20:29Das ist eines der größten Zukunftsthemen des nächsten Jahrzehnts: Wie erhöhe ich den therapeutischen Index, damit ich mehr Wirkung bei weniger Nebenwirkung/Toxizität hinbekomme. Weniger systemisch, noch mehr zielgerichtet. Weniger gesundes Gewebe betreffend, noch mehr nur Wirkung nur direkt am Tumor.
Und das betrifft nicht nur Immuntherapien.
Joschka, sind dir hier inzwischen andere Ansätze bekannt, die ansatzweise ähnliches ( oder zumindest gewisses) Potential versprechen wie eine Maskierung?
Gerne auch Antwort von anderen Usern.
Wenn es da etwas Vielversprechendes gäbe und jemand eine Technologie/Plattform anzubieten hätte wäre das interessant sich anzuschauen.
Und das betrifft nicht nur Immuntherapien.
Joschka, sind dir hier inzwischen andere Ansätze bekannt, die ansatzweise ähnliches ( oder zumindest gewisses) Potential versprechen wie eine Maskierung?
Gerne auch Antwort von anderen Usern.
Wenn es da etwas Vielversprechendes gäbe und jemand eine Technologie/Plattform anzubieten hätte wäre das interessant sich anzuschauen.
So könnte es hier weitergehen
Der Test der 200er Durchschnittslinie wie in den letzten Tagen geschehen könnte ausreichend sein für einen Dreh oder eine Seitwärtskonsolidierung bis zu einem Dreh. Diese Drehs passieren auch meist zu oder kurz vor Options-Expiration (am nächsten Freitag), da große Player die Aktie über den Optionsmarkt bewegen. Dann erwarte ich - selbst wenn der Gesamtmarkt, v.a. auch die Technologiewerte, einbrechen sollte, im Primärszenario einen gewissen Erwartungs-Anstieg bis zu den ersten POC Daten (Kreis orange). Mit dem POC wird dann die Richtung entschieden, entweder "up to the sky" oder "down to hell".

Grafik war zu groß, daher nochmal ein Versuch:
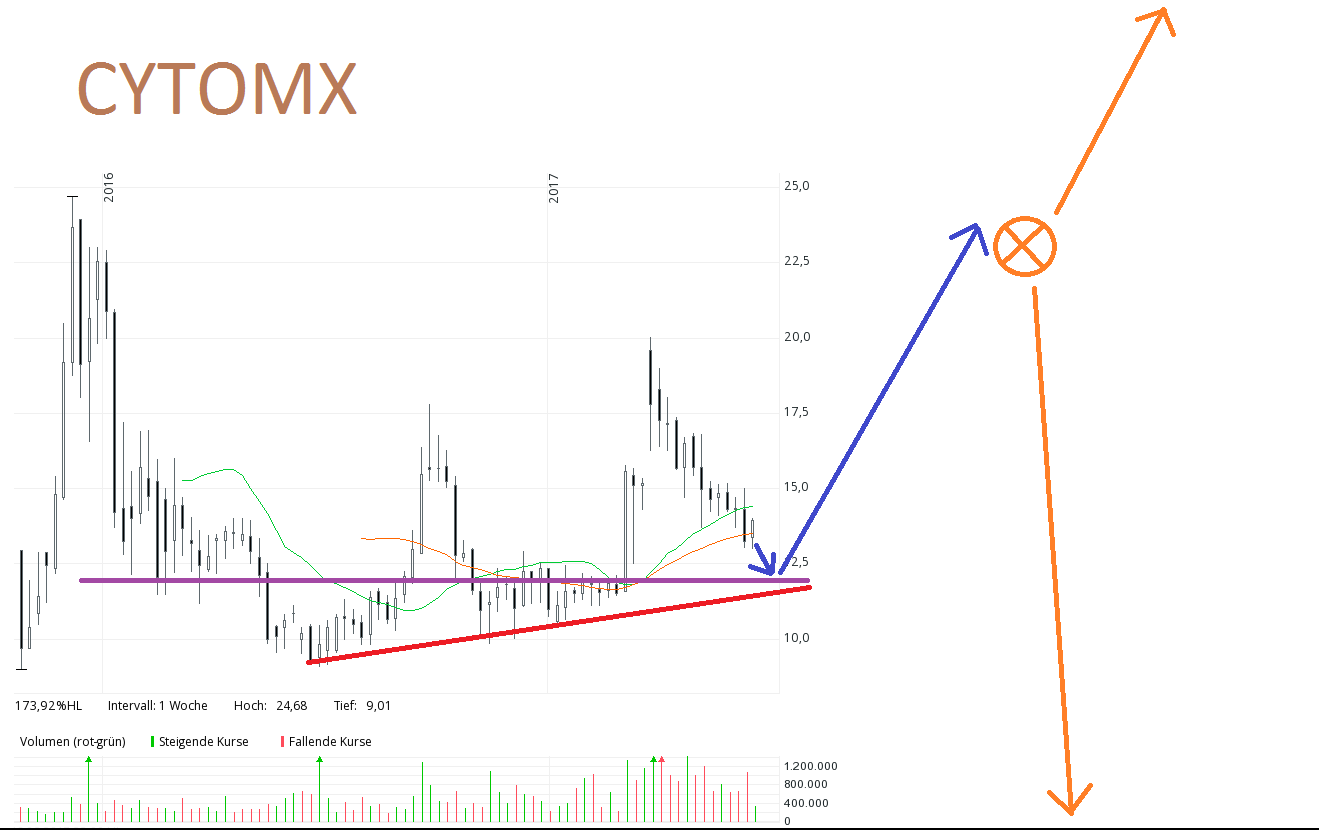

Ergänzung
Ich sehe ein gewisses Risiko, dass CX-2009 nicht funktioniert, da das Wirken des Antikörpers in gesundem Gewebe trotz Maskierung weiterhin zu stark ist und daher die Studie frühzeitig abgebrochen werden muss, noch bevor eine therapeutische Dosis erreicht werden kann. Das würde den Kurs kurzfristig ziemlich belasten, aber das wäre noch kein Beinbruch für die Technologie. Es könnte daher auch eine heftige Achterbahnfahrt werden.Wie sind Eure Einschätzungen für die nächsten 12 Monate?
Antwort auf Beitrag Nr.: 55.132.703 von Joschka Schröder am 13.06.17 17:20:29Sind die Probleme bei Merck gut für Cytomx, weil ein Wettbewerber Probleme hat oder schlecht da bei anti-PD-1 ein Problem aufgetaucht ist?
hinz12, die Probleme bei Merck zeigen nur auf, dass Nebenwirkungen (bis hin zu fatalen Verläufen) ein massives Problem bei Checkpoint-Inhibitor-Kombis sind. Cytomx hat dafür eine potentielle Lösung. Von dem konkreten Halt der beiden Studien profitiert Cytomx aber nicht. Nur vom möglichen Umdenken und der Suche nach Lösungen wie sie Cytomx anbietet....
Antwort auf Beitrag Nr.: 55.135.889 von Ville7 am 14.06.17 08:31:44Danke Ville! Ich hatte mir das schon so gedacht, wollte aber noch eine Bestätigung von Experten. In meiner Sprache war das mit positiv gemeint. Wohlwissend das cytomx nicht direkt profitiert.
Antwort auf Beitrag Nr.: 55.135.523 von Ville7 am 14.06.17 07:30:04
@Ville
Kannst du dein Statement bzgl des Risikos untermauern, oder ist das ein Gut-Feeling?
Bin vor kurzem bei CTMX eingestiegen, weil mich die Story (Deals, Team, ausreichend Cash um sinnvolle Entwicklung zu betreiben) und Technologie beeindruckt.
Die Frage weshalb die Börsenbewertung relativ niedrig ist, im Gegensatz zu den Bewertungen der Pharmadeals würde ich so beantworten: Liquidität. Davon hat BMS genug und kauft sich Optionen für zuküftige Cash Flows. Ein Aktionär hingegen kommt an den Cash von CMTX nicht heran. Im Gegenteil kann der Aktionär davon ausgehen, dass der Cash der heute in CTMX liegt "verbrannt" wird. Insofern ist die Betrachtung EV vielleicht nicht relevant. Ob die Technologie klinisch wirksam sein wird, ist bis heute nicht gezeigt.
Zitat von Ville7: Ich sehe ein gewisses Risiko, dass CX-2009 nicht funktioniert, da das Wirken des Antikörpers in gesundem Gewebe trotz Maskierung weiterhin zu stark ist und daher die Studie frühzeitig abgebrochen werden muss, noch bevor eine therapeutische Dosis erreicht werden kann.
@Ville
Kannst du dein Statement bzgl des Risikos untermauern, oder ist das ein Gut-Feeling?
Bin vor kurzem bei CTMX eingestiegen, weil mich die Story (Deals, Team, ausreichend Cash um sinnvolle Entwicklung zu betreiben) und Technologie beeindruckt.
Die Frage weshalb die Börsenbewertung relativ niedrig ist, im Gegensatz zu den Bewertungen der Pharmadeals würde ich so beantworten: Liquidität. Davon hat BMS genug und kauft sich Optionen für zuküftige Cash Flows. Ein Aktionär hingegen kommt an den Cash von CMTX nicht heran. Im Gegenteil kann der Aktionär davon ausgehen, dass der Cash der heute in CTMX liegt "verbrannt" wird. Insofern ist die Betrachtung EV vielleicht nicht relevant. Ob die Technologie klinisch wirksam sein wird, ist bis heute nicht gezeigt.
Antwort auf Beitrag Nr.: 55.135.523 von Ville7 am 14.06.17 07:30:04@Ville
1. CX-2009: Sehe ich ähnlich. Man hat sich gleich eines der anspruchsvollsten Targets vorgenommen. Falls es funktioniert, hieße dies, dass der PDC-Technik wohl kaum Grenzen gesetzt sind. Falls nicht, könnte dies mehrere Gründe haben: Zu extremes Target, ungenügende Antikörperselektion oder - im ungünstigsten Fall - Mängel der PDC-Technik.
2. Eine ähnlich erfolgversprechend Technik kenne ich nicht. Falls die Maskierung/Demaskierung funktioniert, müßten auf längere Sicht alle Biotherapeutika-Player mit Probodys arbeiten, um konkurrenzfähig zu bleiben. Dies macht den Investmentfall so interessant.
3. Zum Kursverlauf: Konkrete Erwartungen für einen Einjahreszeitraum habe ich mittlerweile nicht mehr. Langfristig hoffe ich natürlich auf eine Vervielfachung des investierten Kapitals und keine zu schnelle Übernahme durch einen Pharmariesen.
1. CX-2009: Sehe ich ähnlich. Man hat sich gleich eines der anspruchsvollsten Targets vorgenommen. Falls es funktioniert, hieße dies, dass der PDC-Technik wohl kaum Grenzen gesetzt sind. Falls nicht, könnte dies mehrere Gründe haben: Zu extremes Target, ungenügende Antikörperselektion oder - im ungünstigsten Fall - Mängel der PDC-Technik.
2. Eine ähnlich erfolgversprechend Technik kenne ich nicht. Falls die Maskierung/Demaskierung funktioniert, müßten auf längere Sicht alle Biotherapeutika-Player mit Probodys arbeiten, um konkurrenzfähig zu bleiben. Dies macht den Investmentfall so interessant.
3. Zum Kursverlauf: Konkrete Erwartungen für einen Einjahreszeitraum habe ich mittlerweile nicht mehr. Langfristig hoffe ich natürlich auf eine Vervielfachung des investierten Kapitals und keine zu schnelle Übernahme durch einen Pharmariesen.
Antwort auf Beitrag Nr.: 55.136.441 von JOWCOL am 14.06.17 09:57:56Das Target ist an heathy tissue ja sehr viel stärker ausgeprägt als z.B. bei HER2 oder bei PD-L1, daher besteht hier zusätzlich das Risiko, dass es hier trotz Maskierung kein genügendes Fenster gibt. Die Realität wird dann die Klinik zeigen, kann ich nicht einschätzen. Riskanter als PD-L1 ist CX-2009 allemal.
Bezüglich EV und "Geld verbrannt" sehe ich das wie du. Im Falle eines negativen PoC kann man solche Firmen teilweise auch below cash einsammeln, (wenn man will).
Bezüglich EV und "Geld verbrannt" sehe ich das wie du. Im Falle eines negativen PoC kann man solche Firmen teilweise auch below cash einsammeln, (wenn man will).
Antwort auf Beitrag Nr.: 55.136.570 von Joschka Schröder am 14.06.17 10:14:15Hi Joschka,
zu deinem Punkt 2:
Ich hatte unlängst Morphosys gebeten sich Cytomx und deren Probody Technologie anzuschauen und sich strategisch vorzubereiten, falls die Technologie erfolgreich ist, denn auch ich bin der Meinung, dass dies auf einen Schlag den Markt verändern und Marktzugänge verhindern wird. Habe versucht das ausführlich und logisch darzulegen.
Alles was zurück kam war, dass man mir nach "Rücksprache mit unseren Forschungs- und Technologiescoutingabteilungen versichern kann, dass sie diese und vergleichbare Technologien sehr eng verfolgen" und "auch in der Lage" seien, sich "bei Bedarf den Zugang zu den jeweiligen Technologien zu sichern". Aus "wettbewerbssensiblen Gründen" würden sie allerdings "nicht bekanntgeben" mit welchen "Unternehmen und Technologien" sie hier "etwa über Kooperationen" zusammenarbeiten.
Also entweder haben sie die Tragweite eines Erfolgs der Technologie nicht verstanden, meine Anfrage nur als lästig empfunden und mir geschrieben was sie denken was ich hören wollte und somit ohne Prüfung abgebügelt oder es gibt noch andere Technologieanbieter mit vergleichbaren Konzepten (was ich nicht glaube....
zu deinem Punkt 2:
Ich hatte unlängst Morphosys gebeten sich Cytomx und deren Probody Technologie anzuschauen und sich strategisch vorzubereiten, falls die Technologie erfolgreich ist, denn auch ich bin der Meinung, dass dies auf einen Schlag den Markt verändern und Marktzugänge verhindern wird. Habe versucht das ausführlich und logisch darzulegen.
Alles was zurück kam war, dass man mir nach "Rücksprache mit unseren Forschungs- und Technologiescoutingabteilungen versichern kann, dass sie diese und vergleichbare Technologien sehr eng verfolgen" und "auch in der Lage" seien, sich "bei Bedarf den Zugang zu den jeweiligen Technologien zu sichern". Aus "wettbewerbssensiblen Gründen" würden sie allerdings "nicht bekanntgeben" mit welchen "Unternehmen und Technologien" sie hier "etwa über Kooperationen" zusammenarbeiten.
Also entweder haben sie die Tragweite eines Erfolgs der Technologie nicht verstanden, meine Anfrage nur als lästig empfunden und mir geschrieben was sie denken was ich hören wollte und somit ohne Prüfung abgebügelt oder es gibt noch andere Technologieanbieter mit vergleichbaren Konzepten (was ich nicht glaube....
Antwort auf Beitrag Nr.: 55.136.993 von Ville7 am 14.06.17 11:19:51
Da würde ich an Deiner Stelle sofort um ein konkretes Beispiel für eine "vergleichbare Technologie" bitten.
Zitat von Ville7: "Rücksprache mit unseren Forschungs- und Technologiescoutingabteilungen versichern kann, dass sie diese und vergleichbare Technologien sehr eng verfolgen"
Da würde ich an Deiner Stelle sofort um ein konkretes Beispiel für eine "vergleichbare Technologie" bitten.
Antwort auf Beitrag Nr.: 55.137.020 von Joschka Schröder am 14.06.17 11:27:18Antwort dazu: siehe Boardmail.
Antwort auf Beitrag Nr.: 55.136.681 von Ville7 am 14.06.17 10:29:37Bei cx2009 kommt es auf eine besonders stabile Linkerverbindung in Bezug auf die Maskierung an.
Interessant wäre es, ob die Peptidlinker so ausdifferenziert sind, daß sie bei verschiedenen Tumorarten mit möglicherweise unterschiedlichen microenvironment-Proteasen entwickelt wurden.
Bei funktionierendem therapeutischen Fenster sollte eine mögliche Höherdosierung des Prodrug Maytansinoid ADC kein Problem sein, da der in der Leber auf 5 bis 50 fach schwächere Toxizität metabolisiert wird.
PBD payloads wären hierfür wohl weniger geeignet.
Falls die cytomx-Technologie erste klinische Erfolge vorweisen kann, dürfte der Leidensdruck bei Hoffmann La Roche zu für cytomx interessanten Deal-Strukturen führen.
Interessant wäre es, ob die Peptidlinker so ausdifferenziert sind, daß sie bei verschiedenen Tumorarten mit möglicherweise unterschiedlichen microenvironment-Proteasen entwickelt wurden.
Bei funktionierendem therapeutischen Fenster sollte eine mögliche Höherdosierung des Prodrug Maytansinoid ADC kein Problem sein, da der in der Leber auf 5 bis 50 fach schwächere Toxizität metabolisiert wird.
PBD payloads wären hierfür wohl weniger geeignet.
Falls die cytomx-Technologie erste klinische Erfolge vorweisen kann, dürfte der Leidensdruck bei Hoffmann La Roche zu für cytomx interessanten Deal-Strukturen führen.
Antwort auf Beitrag Nr.: 55.143.431 von StefanR am 15.06.17 10:21:32Ich meinte : unterschiedliche Peptidlinker bei unterschiedlichen Tumoren
Antwort auf Beitrag Nr.: 55.143.443 von StefanR am 15.06.17 10:23:19
Natürlich ist das der Fall. Nachzulesen in diversen Patentschriften. CytomX verwendet eine Vielzahl tumorspezifischer Linker, deren Spaltung durch unterschiedliche Proteasen erfolgt.
Patentiert ist auch ein recht allgemeingültiges Verfahren, den spezifischen Proteasengehalt diverser Tumoren zu bestimmen. Auch das sollte die CytomX-Technik vor etwaigen Nachahmungen schützen. Z.B. beschäftigt sich in der Schweiz eine universitäre Arbeitsgruppe mit der Maskierung therapeutischer Moleküle (insbes. therapeutisch genutzer Endotoxinverbindungen) mit Hilfe von Polyethylenglycolpolymeren, die ebenfalls im Tumorgewebe proteolytisch abgespalten werden sollen. Die Arbeiten befinden sich noch in einem frühen Stadium, patentiert ist aber offensichtlich nichts, dürfte in weiten Teilen auch nicht gehen, weil dadurch CytomX-Patente verletzt würden.
Zitat von StefanR: Ich meinte : unterschiedliche Peptidlinker bei unterschiedlichen Tumoren
Natürlich ist das der Fall. Nachzulesen in diversen Patentschriften. CytomX verwendet eine Vielzahl tumorspezifischer Linker, deren Spaltung durch unterschiedliche Proteasen erfolgt.
Patentiert ist auch ein recht allgemeingültiges Verfahren, den spezifischen Proteasengehalt diverser Tumoren zu bestimmen. Auch das sollte die CytomX-Technik vor etwaigen Nachahmungen schützen. Z.B. beschäftigt sich in der Schweiz eine universitäre Arbeitsgruppe mit der Maskierung therapeutischer Moleküle (insbes. therapeutisch genutzer Endotoxinverbindungen) mit Hilfe von Polyethylenglycolpolymeren, die ebenfalls im Tumorgewebe proteolytisch abgespalten werden sollen. Die Arbeiten befinden sich noch in einem frühen Stadium, patentiert ist aber offensichtlich nichts, dürfte in weiten Teilen auch nicht gehen, weil dadurch CytomX-Patente verletzt würden.
Antwort auf Beitrag Nr.: 55.143.698 von Joschka Schröder am 15.06.17 10:53:36Danke für den Hinweis!
In der Folge wirkt dann jedoch der cd166-Probody mit einem fest definierten Peptidlinker für potentiell verschiedenste Krebsarten für die einzelne Krebsart "suboptimal".
Aber das kann dann gegebenfalls durch die höhere Dosierungsfähigkeit oder Kombinationsmöglichkeiten mit anderen Konzepten mehr als ausgeglichen werden.
In der Folge wirkt dann jedoch der cd166-Probody mit einem fest definierten Peptidlinker für potentiell verschiedenste Krebsarten für die einzelne Krebsart "suboptimal".
Aber das kann dann gegebenfalls durch die höhere Dosierungsfähigkeit oder Kombinationsmöglichkeiten mit anderen Konzepten mehr als ausgeglichen werden.
Antwort auf Beitrag Nr.: 55.143.698 von Joschka Schröder am 15.06.17 10:53:36
Zitat von Joschka Schröder:Zitat von StefanR: Endotoxinverbindungen
Hab mich vertippt, muss heißen "Biotoxinverbindungen"
$mrsn
Mersana.com - engineer acds with payloads
Konnte das Unternehmen noch nicht begutachten, stelle es mal zur Diskussion.
Vielleicht ein interessanter therapeutischer Ansatz?
Mersana.com - engineer acds with payloads
Konnte das Unternehmen noch nicht begutachten, stelle es mal zur Diskussion.
Vielleicht ein interessanter therapeutischer Ansatz?
Antwort auf Beitrag Nr.: 55.167.119 von biopadawan am 19.06.17 21:47:47Wäre es nicht zielführender, andere Unternehmen in gesonderten Threads vorzustellen? Dieser Diskussionszweig sollte sich auschließlich mit CytomX beschäftigen!
habe aufgestockt. ziel: langfristige wertsteigerung. schau ma mal, ob die rechnung aufgeht.
Gebe Dir recht, wollte deinen Thread nicht missbrauchen, sorry Joschka.
Zur Sache:
CTMX trial update; CX-2009 PDC PHI trial increased recruiting sites from 1 of 1 to 2 of 2.
Zur Sache:
CTMX trial update; CX-2009 PDC PHI trial increased recruiting sites from 1 of 1 to 2 of 2.
Es scheint so als habe auch die CX-072 Studie die Anzahl rekrutierender Sites erhöht. Von 14 von 15 auf 20 von 21 gelisteten Sites.
Olle Kammellen aus YouTube:
https://www.youtube.com/watch?v=gTPSn3xNlOQ
https://www.youtube.com/watch?v=XcyDDawQs8I
(und einer bereits aus 2009 - als die Firma noch aus nur 7 Personen bestand)
https://www.youtube.com/watch?v=zYHmu4SiRdc
https://www.youtube.com/watch?v=gTPSn3xNlOQ
https://www.youtube.com/watch?v=XcyDDawQs8I
(und einer bereits aus 2009 - als die Firma noch aus nur 7 Personen bestand)
https://www.youtube.com/watch?v=zYHmu4SiRdc
CytomX Announces the First Patient Treated in Phase 1/2 PROCLAIM-CX-2009 Trial
SOUTH SAN FRANCISCO, Calif., June 28, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, today announced the treatment of the first patient in the PROCLAIM-CX-2009 study (Probody Clinical Assessment In Man), a Phase 1/2 clinical trial evaluating CX-2009 as monotherapy in patients with select advanced solid tumors. CX-2009 is a Probody drug conjugate (PDC) that targets CD-166, an antigen that is broadly and highly expressed in many types of cancers and is the first PDC to enter the clinic.“The unique targeting ability of our Probody platform allows us to pursue targets not accessible to conventional antibody drug conjugates. With CX-2009, we are leveraging the high levels of CD-166 on many types of cancer cells despite its presence on normal tissue,” said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. “By targeting CD-166 and localizing the activity of the CX-2009 Probody therapeutic to the tumor, we could potentially treat a number of cancers for which few, if any, treatment options exist.”
About CX-2009 and the PROCLAIM-CX-2009 Trial
CX-2009, a PDC that targets cell surface protein CD-166, is being developed for the treatment of solid tumors. CD-166 is highly and homogeneously expressed on multiple tumor types, such as breast cancer, endometrial cancer and prostate cancer. CytomX has demonstrated that CD-166 effectively internalizes antibody-drug conjugates resulting in potent cell killing in-vitro. CX-2009 is designed to target CD-166 specifically in the tumor microenvironment and deliver the tubulin-destabilizing maytansine payload, DM4, to cancer cells. In 2014, CytomX entered into a license agreement with ImmunoGen, Inc. to develop PDCs against a defined number of targets, bringing together CytomX's proprietary antibody masking technology and tumor-selective protease substrates with ImmunoGen's highly potent antibody drug conjugate cell-killing agents and engineered linkers. CX-2009 is wholly owned by CytomX.
CX-2009 is being studied within PROCLAIM, CytomX’s international modular umbrella clinical trial program that encompasses the Phase 1/2 development of multiple Probody therapeutics. PROCLAIM-CX-2009 is a dose-finding Phase 1/2 study evaluating CX-2009 as monotherapy in patients with select cancer types, including non-small cell lung cancer, breast cancer, ovarian cancer, endometrial cancer, cholangiocarcinoma (bile duct cancer), head and neck cancer and castration-resistant prostate cancer. The objectives of the study are to establish the safety, tolerability, pharmacokinetics, pharmacodynamics and preliminary antitumor activity of CX-2009.
More information about the trial is available at ClinicalTrials.gov.
Ein Bruch der 15 bis 15.50 Zone sollte die Aktie mittelfristig wieder an die bzw. über die 20 USD Marke führen. Der Boden sieht bereits tragfähig aus.
CytomX Achieves Development Milestone in Strategic Oncology Collaboration with AbbVie for CD71-Targeting Probody Drug Conjugate
http://www.marketwatch.com/story/cytomx-achieves-development…
http://www.marketwatch.com/story/cytomx-achieves-development…
Antwort auf Beitrag Nr.: 55.229.327 von longitudinalwelle am 29.06.17 14:37:06"Upon commencement of the GLP toxicology study, CytomX will receive a $15 million milestone payment from AbbVie as part of the 2016 strategic oncology collaboration between the companies."
Eine Meilensteinzahlung in Höhe von 15 Mio. USD allein für den Eintritt in eine präklinische GLP-conforme Toxikologiestudie ... so etwas liest man selten. Für CX-2029 hat CytomX Meilenzahlungen bis zu 470 Mio. USD ausgehandelt.
An kein anderes Investment habe ich so hohe Erwartungen wie an CytomX. Hoffentlich geht der Plan auf.
Eine Meilensteinzahlung in Höhe von 15 Mio. USD allein für den Eintritt in eine präklinische GLP-conforme Toxikologiestudie ... so etwas liest man selten. Für CX-2029 hat CytomX Meilenzahlungen bis zu 470 Mio. USD ausgehandelt.
An kein anderes Investment habe ich so hohe Erwartungen wie an CytomX. Hoffentlich geht der Plan auf.
Biotechnology Value Fund L P mit Ownership von 5.50%. Keine Ahnung, ob das neu ist....
Antwort auf Beitrag Nr.: 55.232.075 von Joschka Schröder am 29.06.17 18:50:3715 Mio. sind wirklich viel für das Stadium. Morphosys bekommt insgesamt knapp mehr als 10 Mio, wenn ein Medikament auf den Markt kommt. Für alle Meilensteine zusammen.
Wenn man davon ausgeht, dass die Zahulngen steigen, macht der Phase 1 Start schon richtig Spaß. Bin mal gespannt. Ob die Konditionen mit Bristol genau so gut sind?
Wenn man davon ausgeht, dass die Zahulngen steigen, macht der Phase 1 Start schon richtig Spaß. Bin mal gespannt. Ob die Konditionen mit Bristol genau so gut sind?
Antwort auf Beitrag Nr.: 55.241.900 von hinz12 am 30.06.17 21:10:23
In der aktuellen Vereinbarung mit Bristol-Myers sind es Meilensteinzahlungen in Höhe von 448 Mio. USD je Target.
In den Konditionen der Vereinbarungen spiegelt sich das Alleinstellungsmerkmal der Probody-Technik wider. Insoweit kommen nur die wirklich großen Player als Kooperationspartner in Frage, weil sich kleinere Gesellschaften derartige Zahlungen überhaupt nicht leisten können.
Zitat von hinz12: 15 Mio. sind wirklich viel für das Stadium. Morphosys bekommt insgesamt knapp mehr als 10 Mio, wenn ein Medikament auf den Markt kommt. Für alle Meilensteine zusammen.
Wenn man davon ausgeht, dass die Zahulngen steigen, macht der Phase 1 Start schon richtig Spaß. Bin mal gespannt. Ob die Konditionen mit Bristol genau so gut sind?
In der aktuellen Vereinbarung mit Bristol-Myers sind es Meilensteinzahlungen in Höhe von 448 Mio. USD je Target.
In den Konditionen der Vereinbarungen spiegelt sich das Alleinstellungsmerkmal der Probody-Technik wider. Insoweit kommen nur die wirklich großen Player als Kooperationspartner in Frage, weil sich kleinere Gesellschaften derartige Zahlungen überhaupt nicht leisten können.
Antwort auf Beitrag Nr.: 55.242.371 von Joschka Schröder am 30.06.17 22:30:41
Ich hab mal die Kooperationen von Cytomx zusammengestellt. Fehlen tun die mit ImmunoGen und MD Anderson Cancer Center, weil ich die nicht so richtig verstehe. Vielleicht kann der wer anders mal helfen.
Aber die drei großen Kooperationen sind folgendermaßen aufgestellt und bis jetzt gelaufen.
Kooperation Bristol
1. Kooperation Bristol (27.05.2014)
4 Oncology Targets auswählbar (2 austauschbar). Jeweils exklusiv weltweite Entwicklung und Vermarktung alleine durch Bristol.
298 Mio Milestones pro Target + Tired mid single digits bis low double digit royalty on net sales
50 Mio Upfront
3. Target ausgewählt am 20.01.2016 - 10 Mio. Milestone
4. Target ausgewählt am 05.12.2016 - 15 Mio. Milestone
Erster klinischer Kandidat ausgewählt (CTLA-4 Probody) am 13.12.2016 - 2 Mio. Milestone
Leider finde ich hier nichts zu den ersten beiden Targets. Weiß jemand, wie da die Milestone Zahlungen waren?
2. Kooperation Bristol (20.03.2017)
6 Oncology Targets + 2 Nicht-Onkology Targets auswählbar. Jeweils exklusiv weltweite Entwicklung und Vermarktung alleine durch Bristol
448 Mio. pro Target + Tired mid single digits bis low double digit royalty on net sales
200 Mio. Upfront
Kooperation AbbVie (21.04.2016)
Co-Development und Co-Commeracialization von CD 71 - Cytomx leads pre-clinical und early clinical development. AbbVie leads later clinical development and commercialization. Global late stage (Phase 3) development costs werden geteilt.
AbbVie leads global commerical activities - Cytomx eligible für profit share in USA and abgestufte double digit royalty on net sales für den Rest der Welt. Cytomx hat eine Option für Co-Promotion in der USA
470 Mio. Milestones für das CD 71 Target
30 Mio. Upfront
Erreichen der GLP Toxicology studies für CX-2029 (CD 71 Target) - wichtiger Schritt vor IND 2018, also Start der Phase 1 - am 29.07.2017 - 15 Mio. Milestone
2 weitere Targets auswählbar. Dafür jeweils exklusiv weltweite Entwicklung und Vermarktung alleine durch AbbVie. Dafür dann weitere nicht benannte Milestone und Royalty payments
Kooperation Pfizer (06.06.2013)
Nicht genannte Anzahl von PDCs wählbar. Exklusive Rechte. Cytomx und Pfizer arbeiten im preclinical research zusammen. Pfizer ist verantwortlich für klinische Phasen und Commeracialisation.
610 Mio. (pro Target?) an regulatory and sales Milestones + Tired royalty reaching double digit royalty on net sales
25 Mio. Upfront, research reimbursement and preclinical milestones
Die Kooperation mit Pfizer ist sehr ruhig. Geht es da vorwärts? So richtig verstehe ich auch nicht, ob die 610 Mio. für ein Target sind? Weiß da wer mehr?
-----------------------------------------------------------------------------------
Welche Zahlungspunkte für Milestones wird es geben? Ich tippe auf
Auswahl Target
vielleicht Erreichen GLP Toxicology studies (wie wir gelernt haben)
Start Phase 1
Start Phase 2
Start Phase 3
Filing
Approved
Start Vermarktung?
Wie seht ihr die Punkte? Kommen die hin?
Was meint ihr, wie sich 470 Mio. (CD 71), 298 Mio. (Bristol 1. Kooperation) und 448 Mio. (Bristol 2. Kooperation) Milestones pro Target auf die einzelnen Punkte verteilen?
Meine Tipps:
Wenn CTLA-4 in die Klinik startet, tippe ich schon auf einen 10 Mio. Milestone. Sonst kommen die ja nie auf die 298 Mio. insgesamt für das Target.
Und beim Start von CX-2029 sollten es dann eher 20 Mio. sein. Immerhin gibt es hier insgesamt 470 Mio. insgesamt.
Zitat von Joschka Schröder:Zitat von hinz12: 15 Mio. sind wirklich viel für das Stadium. Morphosys bekommt insgesamt knapp mehr als 10 Mio, wenn ein Medikament auf den Markt kommt. Für alle Meilensteine zusammen.
Wenn man davon ausgeht, dass die Zahulngen steigen, macht der Phase 1 Start schon richtig Spaß. Bin mal gespannt. Ob die Konditionen mit Bristol genau so gut sind?
In der aktuellen Vereinbarung mit Bristol-Myers sind es Meilensteinzahlungen in Höhe von 448 Mio. USD je Target.
In den Konditionen der Vereinbarungen spiegelt sich das Alleinstellungsmerkmal der Probody-Technik wider. Insoweit kommen nur die wirklich großen Player als Kooperationspartner in Frage, weil sich kleinere Gesellschaften derartige Zahlungen überhaupt nicht leisten können.
Ich hab mal die Kooperationen von Cytomx zusammengestellt. Fehlen tun die mit ImmunoGen und MD Anderson Cancer Center, weil ich die nicht so richtig verstehe. Vielleicht kann der wer anders mal helfen.
Aber die drei großen Kooperationen sind folgendermaßen aufgestellt und bis jetzt gelaufen.
Kooperation Bristol
1. Kooperation Bristol (27.05.2014)
4 Oncology Targets auswählbar (2 austauschbar). Jeweils exklusiv weltweite Entwicklung und Vermarktung alleine durch Bristol.
298 Mio Milestones pro Target + Tired mid single digits bis low double digit royalty on net sales
50 Mio Upfront
3. Target ausgewählt am 20.01.2016 - 10 Mio. Milestone
4. Target ausgewählt am 05.12.2016 - 15 Mio. Milestone
Erster klinischer Kandidat ausgewählt (CTLA-4 Probody) am 13.12.2016 - 2 Mio. Milestone
Leider finde ich hier nichts zu den ersten beiden Targets. Weiß jemand, wie da die Milestone Zahlungen waren?
2. Kooperation Bristol (20.03.2017)
6 Oncology Targets + 2 Nicht-Onkology Targets auswählbar. Jeweils exklusiv weltweite Entwicklung und Vermarktung alleine durch Bristol
448 Mio. pro Target + Tired mid single digits bis low double digit royalty on net sales
200 Mio. Upfront
Kooperation AbbVie (21.04.2016)
Co-Development und Co-Commeracialization von CD 71 - Cytomx leads pre-clinical und early clinical development. AbbVie leads later clinical development and commercialization. Global late stage (Phase 3) development costs werden geteilt.
AbbVie leads global commerical activities - Cytomx eligible für profit share in USA and abgestufte double digit royalty on net sales für den Rest der Welt. Cytomx hat eine Option für Co-Promotion in der USA
470 Mio. Milestones für das CD 71 Target
30 Mio. Upfront
Erreichen der GLP Toxicology studies für CX-2029 (CD 71 Target) - wichtiger Schritt vor IND 2018, also Start der Phase 1 - am 29.07.2017 - 15 Mio. Milestone
2 weitere Targets auswählbar. Dafür jeweils exklusiv weltweite Entwicklung und Vermarktung alleine durch AbbVie. Dafür dann weitere nicht benannte Milestone und Royalty payments
Kooperation Pfizer (06.06.2013)
Nicht genannte Anzahl von PDCs wählbar. Exklusive Rechte. Cytomx und Pfizer arbeiten im preclinical research zusammen. Pfizer ist verantwortlich für klinische Phasen und Commeracialisation.
610 Mio. (pro Target?) an regulatory and sales Milestones + Tired royalty reaching double digit royalty on net sales
25 Mio. Upfront, research reimbursement and preclinical milestones
Die Kooperation mit Pfizer ist sehr ruhig. Geht es da vorwärts? So richtig verstehe ich auch nicht, ob die 610 Mio. für ein Target sind? Weiß da wer mehr?
-----------------------------------------------------------------------------------
Welche Zahlungspunkte für Milestones wird es geben? Ich tippe auf
Auswahl Target
vielleicht Erreichen GLP Toxicology studies (wie wir gelernt haben)
Start Phase 1
Start Phase 2
Start Phase 3
Filing
Approved
Start Vermarktung?
Wie seht ihr die Punkte? Kommen die hin?
Was meint ihr, wie sich 470 Mio. (CD 71), 298 Mio. (Bristol 1. Kooperation) und 448 Mio. (Bristol 2. Kooperation) Milestones pro Target auf die einzelnen Punkte verteilen?
Meine Tipps:
Wenn CTLA-4 in die Klinik startet, tippe ich schon auf einen 10 Mio. Milestone. Sonst kommen die ja nie auf die 298 Mio. insgesamt für das Target.
Und beim Start von CX-2029 sollten es dann eher 20 Mio. sein. Immerhin gibt es hier insgesamt 470 Mio. insgesamt.
Eine Sache wundert mich.
Wieso ist die Cytomx Aktie noch nicht auf dem Radar von solchen Blättern wie "Der Aktionär"? Die sind doch sonst immer auf der Suche nach Vervielfachungskandidaten mit denen man reich werden kann.
Cytomx hat das Potential ein Game Changer zu sein und "Der Aktionär" ist ruhig? Komisch oder? Steckt hier zu viel Substanz hinter? :-)
Vielleicht doch eher eine Aktie für "Börse Online"? :-) Aber die haben sie auch noch nicht entdeckt.
Wieso ist die Cytomx Aktie noch nicht auf dem Radar von solchen Blättern wie "Der Aktionär"? Die sind doch sonst immer auf der Suche nach Vervielfachungskandidaten mit denen man reich werden kann.
Cytomx hat das Potential ein Game Changer zu sein und "Der Aktionär" ist ruhig? Komisch oder? Steckt hier zu viel Substanz hinter? :-)
Vielleicht doch eher eine Aktie für "Börse Online"? :-) Aber die haben sie auch noch nicht entdeckt.
Antwort auf Beitrag Nr.: 55.243.955 von hinz12 am 01.07.17 12:04:41
Der größere Teil der Zahlungen ist an Verkaufsbeginn und spezifische Verkaufszielen gebunden. Details findet man teils in den SEC-Meldungen zu den Kooperationsvereinbarungen. Wenn ich das richtig sehe, ist das z.B. bei BMS auch noch auf unterschiedliche Therapiemethoden zu einem Target aufgeteilt. Also selbst wenn ein Target Erfolg hat und alle Verkaufsziele erreicht, müssen dafür nicht zwangsläufig alle möglichen Meilensteinziele erreicht werden.
Zitat von hinz12: Welche Zahlungspunkte für Milestones wird es geben? Ich tippe auf
Auswahl Target
vielleicht Erreichen GLP Toxicology studies (wie wir gelernt haben)
Start Phase 1
Start Phase 2
Start Phase 3
Filing
Approved
Start Vermarktung?
Wie seht ihr die Punkte? Kommen die hin?
Der größere Teil der Zahlungen ist an Verkaufsbeginn und spezifische Verkaufszielen gebunden. Details findet man teils in den SEC-Meldungen zu den Kooperationsvereinbarungen. Wenn ich das richtig sehe, ist das z.B. bei BMS auch noch auf unterschiedliche Therapiemethoden zu einem Target aufgeteilt. Also selbst wenn ein Target Erfolg hat und alle Verkaufsziele erreicht, müssen dafür nicht zwangsläufig alle möglichen Meilensteinziele erreicht werden.
Antwort auf Beitrag Nr.: 55.244.204 von fme_wo am 01.07.17 13:23:41
Ich finde nicht die SEC-Dokumente zu dem Pfizer-Deal und dem ersten Bristol-Deals aus dem Jahre 2014. Die sind in der Edgar-Datenbank zu finden. Da ist eine Lücke zwischen 2012 und 2015. Komisch.
Wenn ich das SEC-Filing für die zweite Bristol-Vereinbarung von März 2017 lese, dann gibs auch nur für die ersten beiden Product Modality Meilensteine für ein Target Geld. Was genau sind denn diese Product Modality für ein Target?
Zitat von fme_wo:Zitat von hinz12: Welche Zahlungspunkte für Milestones wird es geben? Ich tippe auf
Auswahl Target
vielleicht Erreichen GLP Toxicology studies (wie wir gelernt haben)
Start Phase 1
Start Phase 2
Start Phase 3
Filing
Approved
Start Vermarktung?
Wie seht ihr die Punkte? Kommen die hin?
Der größere Teil der Zahlungen ist an Verkaufsbeginn und spezifische Verkaufszielen gebunden. Details findet man teils in den SEC-Meldungen zu den Kooperationsvereinbarungen. Wenn ich das richtig sehe, ist das z.B. bei BMS auch noch auf unterschiedliche Therapiemethoden zu einem Target aufgeteilt. Also selbst wenn ein Target Erfolg hat und alle Verkaufsziele erreicht, müssen dafür nicht zwangsläufig alle möglichen Meilensteinziele erreicht werden.
Ich finde nicht die SEC-Dokumente zu dem Pfizer-Deal und dem ersten Bristol-Deals aus dem Jahre 2014. Die sind in der Edgar-Datenbank zu finden. Da ist eine Lücke zwischen 2012 und 2015. Komisch.
Wenn ich das SEC-Filing für die zweite Bristol-Vereinbarung von März 2017 lese, dann gibs auch nur für die ersten beiden Product Modality Meilensteine für ein Target Geld. Was genau sind denn diese Product Modality für ein Target?
Antwort auf Beitrag Nr.: 55.244.360 von hinz12 am 01.07.17 14:06:01
Damals war CytomX wohl noch nicht verpflichtet zu den SEC-Dokumenten, das dürfte erst mit dem Börsengang 2015 der Fall sein. Im initialen SEC-Filing dazu von 2015 finden sich ein paar Details zu den beiden Deals:
BMS
In May 2014, we entered into a research collaboration and license agreement with BMS pursuant to which we agreed to collaborate to discover and conduct preclinical development of Probody therapeutics directed against four immune-oncology targets. BMS selected the first two targets upon the signing of the agreement, one of which is CTLA-4, and made a $50 million signing payment to us. BMS may select an additional two targets prior to May 23, 2019 by written notification so long as the target is not an excluded target as defined in the agreement and by paying $10 million to us for the first such target and by paying $15 million to us for the second such target. BMS will provide a specified amount of research funding to us to perform the research by funding certain full-time employee expenses. BMS has the responsibility for and control of all development, manufacture and commercialization of any products resulting from the research collaboration. BMS agreed to use commercially reasonable efforts to develop and obtain regulatory approval for and commercialize at least one product for each target.
We granted BMS exclusive worldwide rights to develop and commercialize the Probody therapeutics we discover. The terms of the agreement provide that BMS will make a total of up to $2 million in preclinical milestone payments for each target, a total of up to $112 million in development and regulatory milestone payments for up to three indications for each target, a total of up to $124 million in milestone payments for the first commercial sale in various territories for up to three indications, and sales milestone payments of up to $60 million for each product.
Pfizer
In May 2013, we entered into a research collaboration, option and license agreement with Pfizer pursuant to which we granted Pfizer an option to select four targets on which to collaborate with us on the preclinical research of PDCs using our Probody technology and Pfizer’s ADC technology. Pfizer will
provide a specified amount of research funding to us to perform the research by funding certain full-time employee expenses. Pfizer has selected its first three targets. The selection of the third target triggered a payment of $1.5 million to us, and, if Pfizer selects a fourth target to include in the collaboration, Pfizer will pay us an additional $1.5 million. Pfizer can exercise the option to obtain a commercial license for each target within three to five years after the target is selected upon making a payment of $2 million to $5 million to us, depending on the target. Pfizer has the responsibility for and control of all development, manufacture and commercialization of any product candidates resulting from the research collaboration.
The commercial license will be a worldwide, exclusive, sublicensable license for development and commercialization of product candidates directed against the selected target. The terms of the license include a total for all targets of approximately $80 million in regulatory milestone payments and $530 million in sales milestone payments as well as tiered royalties ranging from mid-single digits to low-teens on potential future sales
Zitat von hinz12: Ich finde nicht die SEC-Dokumente zu dem Pfizer-Deal und dem ersten Bristol-Deals aus dem Jahre 2014. Die sind in der Edgar-Datenbank zu finden. Da ist eine Lücke zwischen 2012 und 2015. Komisch.
Damals war CytomX wohl noch nicht verpflichtet zu den SEC-Dokumenten, das dürfte erst mit dem Börsengang 2015 der Fall sein. Im initialen SEC-Filing dazu von 2015 finden sich ein paar Details zu den beiden Deals:
BMS
In May 2014, we entered into a research collaboration and license agreement with BMS pursuant to which we agreed to collaborate to discover and conduct preclinical development of Probody therapeutics directed against four immune-oncology targets. BMS selected the first two targets upon the signing of the agreement, one of which is CTLA-4, and made a $50 million signing payment to us. BMS may select an additional two targets prior to May 23, 2019 by written notification so long as the target is not an excluded target as defined in the agreement and by paying $10 million to us for the first such target and by paying $15 million to us for the second such target. BMS will provide a specified amount of research funding to us to perform the research by funding certain full-time employee expenses. BMS has the responsibility for and control of all development, manufacture and commercialization of any products resulting from the research collaboration. BMS agreed to use commercially reasonable efforts to develop and obtain regulatory approval for and commercialize at least one product for each target.
We granted BMS exclusive worldwide rights to develop and commercialize the Probody therapeutics we discover. The terms of the agreement provide that BMS will make a total of up to $2 million in preclinical milestone payments for each target, a total of up to $112 million in development and regulatory milestone payments for up to three indications for each target, a total of up to $124 million in milestone payments for the first commercial sale in various territories for up to three indications, and sales milestone payments of up to $60 million for each product.
Pfizer
In May 2013, we entered into a research collaboration, option and license agreement with Pfizer pursuant to which we granted Pfizer an option to select four targets on which to collaborate with us on the preclinical research of PDCs using our Probody technology and Pfizer’s ADC technology. Pfizer will
provide a specified amount of research funding to us to perform the research by funding certain full-time employee expenses. Pfizer has selected its first three targets. The selection of the third target triggered a payment of $1.5 million to us, and, if Pfizer selects a fourth target to include in the collaboration, Pfizer will pay us an additional $1.5 million. Pfizer can exercise the option to obtain a commercial license for each target within three to five years after the target is selected upon making a payment of $2 million to $5 million to us, depending on the target. Pfizer has the responsibility for and control of all development, manufacture and commercialization of any product candidates resulting from the research collaboration.
The commercial license will be a worldwide, exclusive, sublicensable license for development and commercialization of product candidates directed against the selected target. The terms of the license include a total for all targets of approximately $80 million in regulatory milestone payments and $530 million in sales milestone payments as well as tiered royalties ranging from mid-single digits to low-teens on potential future sales
Antwort auf Beitrag Nr.: 55.244.705 von fme_wo am 01.07.17 15:48:46Danke!
Also hat Pfizer schon drei von vier möglichen Targets ausgewählt. Leider haben sie anscheinend für keines der drei schon die kommerzielle Lizenz erworben. Da sie für das Ziehen der kommerziellen Lizenz nur drei bis fünf Jahre Zeit haben nach Auswahl des Targets müssten sie langsam mal in die Strümpfe kommen. Drei Jahre sind schon fast rum. Überhaupt ist es um Pfizer sehr still. Wäre schade, wenn Pfizer die Option nicht zieht. Der Pfizer Deal scheint auch der schlechteste zu sein, was sicher damit zu tun hat, dass er der älteste ist.
Also hat Pfizer schon drei von vier möglichen Targets ausgewählt. Leider haben sie anscheinend für keines der drei schon die kommerzielle Lizenz erworben. Da sie für das Ziehen der kommerziellen Lizenz nur drei bis fünf Jahre Zeit haben nach Auswahl des Targets müssten sie langsam mal in die Strümpfe kommen. Drei Jahre sind schon fast rum. Überhaupt ist es um Pfizer sehr still. Wäre schade, wenn Pfizer die Option nicht zieht. Der Pfizer Deal scheint auch der schlechteste zu sein, was sicher damit zu tun hat, dass er der älteste ist.
Antwort auf Beitrag Nr.: 55.245.011 von hinz12 am 01.07.17 17:40:27In der Präsentation vom Nov. 2016 waren 2 Projekte von Pfizer in Discovery und eines in lead optimization zu sehen. Auf den seitherigen Präsentationen ist von Pfizer kaum mehr was zu sehen. Das spricht nicht dafür hier groß was zu erwarten.
Bezüglich Aktionär verwundert mich das nicht. Wenn noch nicht mal amerikanische Investoren Potential zusprechen, was soll es dann ein drittklassiges deutsches Börsenblättchen?
Cytomx fliegt weiter unter dem Radar oder wird zurecht kein Potential zugeschrieben (sodass wir uns hier irren in unserer Spekulation). Sollten sie aber einen PoC liefern ( und wir richtig spekulieren) dann wird das schlagartig alle aufwecken. Die Börsentüren sind dann besonders eng, wenn alle plötzlich auf einmal rein wollen - was in diesem Falle der Fall wäre.
Daher wird die entscheidende Kurs-Schlacht vielleicht schon mit den ersten Daten geschlagen (ASCO 2018?), wenn nicht zuvor noch eine der Studien floppt (besonderes Risiko in CX2009... ) ...
Bezüglich Aktionär verwundert mich das nicht. Wenn noch nicht mal amerikanische Investoren Potential zusprechen, was soll es dann ein drittklassiges deutsches Börsenblättchen?
Cytomx fliegt weiter unter dem Radar oder wird zurecht kein Potential zugeschrieben (sodass wir uns hier irren in unserer Spekulation). Sollten sie aber einen PoC liefern ( und wir richtig spekulieren) dann wird das schlagartig alle aufwecken. Die Börsentüren sind dann besonders eng, wenn alle plötzlich auf einmal rein wollen - was in diesem Falle der Fall wäre.
Daher wird die entscheidende Kurs-Schlacht vielleicht schon mit den ersten Daten geschlagen (ASCO 2018?), wenn nicht zuvor noch eine der Studien floppt (besonderes Risiko in CX2009... ) ...
Antwort auf Beitrag Nr.: 55.245.581 von Ville7 am 01.07.17 20:30:25Aber wieso sollten die Dinge mit Pfizer nicht laufen umd der Rest schon? Das wundert mich. Ist das nicht die gleiche Sache?
Du hast recht, dass die amerikanischen Investoren die Aktie irgendwie nicht auf dem Schirm haben. Aber wieso investiert Bristol 200 Mio. Upfront? Das zeigt doch großes Vertrauen. Wieso folgen Investoren da nicht den Spezialisten?
Meinst du, wenn CX-2009 scheitert, dann ist alles andere praktisch auch gescheitert?
Du hast recht, dass die amerikanischen Investoren die Aktie irgendwie nicht auf dem Schirm haben. Aber wieso investiert Bristol 200 Mio. Upfront? Das zeigt doch großes Vertrauen. Wieso folgen Investoren da nicht den Spezialisten?
Meinst du, wenn CX-2009 scheitert, dann ist alles andere praktisch auch gescheitert?
Antwort auf Beitrag Nr.: 55.245.581 von Ville7 am 01.07.17 20:30:25....CytomX gegenwärtig keinen Wert zuzuschreiben, wäre anhand der Faktenlage falsch. Auch Geldfluß erzeugende Verpartnerungsoptionen, wie im März BMS und jetzt als milestone abbvie, stellen einen greifbaren Wert dar.
Wenn man sich das jahrelange schwache Verpartnerungsprocedere bei immunogen anschaut, dann kann man über die von cytomx aufgerufenen Summen nur staunen.
Cytomx hat gerade mal 2 klinische Phase 1 Projekte gestartet, und erfährt in der Pharmawelt schon so eine Beachtung.
Ein scheitern des cd166-adc wäre sehr schlecht, jedoch noch kein Weltuntergang.
Die potentielle Toxizitätslage bei cd166 und cd 71 ist einfach dramatisch. Wenn hier kein im Organismus sehr stabiler Linker gefunden wurde, wäre das Thema probody-adc schwer beschädigt.
Dennoch scheint abbvie ein so hohes Vertrauen zu haben, dass sie nicht noch 3 Monate zuwarten wollen, und mögliche Nebenwirkungen bei cd166 abwarten.
Wenn man sich das jahrelange schwache Verpartnerungsprocedere bei immunogen anschaut, dann kann man über die von cytomx aufgerufenen Summen nur staunen.
Cytomx hat gerade mal 2 klinische Phase 1 Projekte gestartet, und erfährt in der Pharmawelt schon so eine Beachtung.
Ein scheitern des cd166-adc wäre sehr schlecht, jedoch noch kein Weltuntergang.
Die potentielle Toxizitätslage bei cd166 und cd 71 ist einfach dramatisch. Wenn hier kein im Organismus sehr stabiler Linker gefunden wurde, wäre das Thema probody-adc schwer beschädigt.
Dennoch scheint abbvie ein so hohes Vertrauen zu haben, dass sie nicht noch 3 Monate zuwarten wollen, und mögliche Nebenwirkungen bei cd166 abwarten.
Antwort auf Beitrag Nr.: 55.245.680 von StefanR am 01.07.17 20:54:21Soll es in drei Monaten Daten zu CX-2009 geben? Ich dachte im Dezember sind die dran. Wenn die positiv ausfallen, könnte es einen Schub gen 20 oder 30 Dollar geben.
Antwort auf Beitrag Nr.: 55.247.971 von hinz12 am 02.07.17 15:57:24@hinz12
Ich gehe davon aus, daß an cytomx von den klinischen Zentren engmaschig Daten weitergeleitet werden. Abbvie als wichtiger Partner würde bei " Aus dem Ruder laufen" der cd166 Studie, sowie auch im positiven Fall, daß es keine nennenswerten,unerwünschten, systemischen proteolytischen Abspaltungen der masking moiety gibt, in Kenntnis gesetzt werden. Aktionäre können nur indirekte Daten für sich interpretieren.
Ich gehe davon aus, daß an cytomx von den klinischen Zentren engmaschig Daten weitergeleitet werden. Abbvie als wichtiger Partner würde bei " Aus dem Ruder laufen" der cd166 Studie, sowie auch im positiven Fall, daß es keine nennenswerten,unerwünschten, systemischen proteolytischen Abspaltungen der masking moiety gibt, in Kenntnis gesetzt werden. Aktionäre können nur indirekte Daten für sich interpretieren.
Antwort auf Beitrag Nr.: 55.248.088 von StefanR am 02.07.17 16:41:02Du gehst also davon aus, dass AbbVie weiß, dass die CD166 Studie positiv ausfällt?
Antwort auf Beitrag Nr.: 55.249.033 von hinz12 am 02.07.17 21:34:46AbbVie kann zum jetzigen Zeitpunkt noch gar nichts von klinischen ersten Hinweisen der cd166 Studie wissen - also klares nein!!
AbbVie kennt jedoch präklinische Daten seines cd71-Projektes, und ist gegebenfalls über die cx072-Studie vorinformiert, so daß AbbVie Schnelligkeit vor Sicherheit geht.
Bei der gesamten Technologie von cytomx gibt es zum gegenwärtigen Zeitpunkt nur sachte, indirekte Hinweise auf Bestätigung der umfassenden Präklinik.
AbbVie kennt jedoch präklinische Daten seines cd71-Projektes, und ist gegebenfalls über die cx072-Studie vorinformiert, so daß AbbVie Schnelligkeit vor Sicherheit geht.
Bei der gesamten Technologie von cytomx gibt es zum gegenwärtigen Zeitpunkt nur sachte, indirekte Hinweise auf Bestätigung der umfassenden Präklinik.
Mal eine Frage in die Runde:
Wie hoch gewichtet ihr CTMX prozentual in eurem Depot?
Klar, CTMX ist eine einmalige Gelegenheit und sicher wert ein gewisses Risiko zu fahren (Chance/Risk-Reward). Zumal gibt es bereits ein paar (wenige) Indizien, dass ein PoC gelingen "könnte". Mangels PoC kann die Kohle jedoch auch komplett verbrannt werden.
Mit welcher Quote löst ihr den Konflikt? Würde mich sehr interessieren.
Grüße
biopadawan
Wie hoch gewichtet ihr CTMX prozentual in eurem Depot?
Klar, CTMX ist eine einmalige Gelegenheit und sicher wert ein gewisses Risiko zu fahren (Chance/Risk-Reward). Zumal gibt es bereits ein paar (wenige) Indizien, dass ein PoC gelingen "könnte". Mangels PoC kann die Kohle jedoch auch komplett verbrannt werden.
Mit welcher Quote löst ihr den Konflikt? Würde mich sehr interessieren.
Grüße
biopadawan
prozentuelle gewichtung einer einzelnen aktie is ned wirklich soo ausschlaggebend, denk ich.
warum? ich denk das gesamtbild seines materiellen vermögens machts aus. wie viel prozent bin ich bereit in wertpapiere oder anders formuliert: nicht in sachwerte anzulegen.
ich hab beispielsweise ca. 30% in cytomx investiert. ich betrachte aber das gesamte aktiendepot von mir, auch wenns komisch klingt, letzten endes als spielgeld. aktien kann zerbröseln und im schlimsten fall steht man mit 0 Euros da.
(gutes) haus, grund, boden von mir aus gold und silber in kleinen einheiten sind wesentlich sicherer und besser und lassen einen ruhiger schlafen. einfach formuliert: sachwerte sind die pflicht, wertpapiere die kür.
is aba natürlich meine meinung - soll jeder machen, wie er denkt.
warum? ich denk das gesamtbild seines materiellen vermögens machts aus. wie viel prozent bin ich bereit in wertpapiere oder anders formuliert: nicht in sachwerte anzulegen.
ich hab beispielsweise ca. 30% in cytomx investiert. ich betrachte aber das gesamte aktiendepot von mir, auch wenns komisch klingt, letzten endes als spielgeld. aktien kann zerbröseln und im schlimsten fall steht man mit 0 Euros da.
(gutes) haus, grund, boden von mir aus gold und silber in kleinen einheiten sind wesentlich sicherer und besser und lassen einen ruhiger schlafen. einfach formuliert: sachwerte sind die pflicht, wertpapiere die kür.
is aba natürlich meine meinung - soll jeder machen, wie er denkt.
Antwort auf Beitrag Nr.: 55.268.260 von ciel34 am 05.07.17 16:28:17Danke für deine Stellungnahme. Letztlich bezog sich die Frage der Gewichtung genau auf den prozentualen Anteil im Aktiendepot
ja, ich weiß. der liegt eben bei 30% bei mir.
wichtig ist mir eben immer darauf hinzuweisen, dass man nicht sein gesamtes glück in aktien suchen soll.. ich muss das dazuschreiben, sonst zerreißts mich :-)
wichtig ist mir eben immer darauf hinzuweisen, dass man nicht sein gesamtes glück in aktien suchen soll.. ich muss das dazuschreiben, sonst zerreißts mich :-)
Antwort auf Beitrag Nr.: 55.267.831 von biopadawan am 05.07.17 15:41:39Jeder Tag, an dem kein Abbruch der klinischen Studie mit CX-2009 gemeldet wird, ist ein guter Tag. Je mehr solcher guten Tage ins Land gehen, desto größer wird die Wahrscheinlichkeit, dass CytomX in der Lage ist, unfallfrei Targets anzusteuern, die in größeren Ausmaß auch von gesundem Gewebe exprimiert werden (wie dies bei CD166 der Fall ist). Medizinisch wäre das eine kleine Sensation. Da ich die Risiken sehr wohl nicht ausblende, vom Probody-Ansatz nach Durchsicht der einschlägigen Patente und präklinischen Daten aber überzeugt bin, hoffe ich unverändert, dass CytomX in einigen Jahren - weitgehend unabhängig vom Ausgangswert - 90 % oder mehr Depotanteil haben wird. 
PS: 30 % Depotanteil als Ausgangswert finde ich wirklich äußerst mutig.

PS: 30 % Depotanteil als Ausgangswert finde ich wirklich äußerst mutig.
Paar insider sales die letzten Tage. Denke vom Volumen her noch nicht weltbewegend CFO (2500) und Robert Tepper (15000). Wird wohl nicht mit den Studien im Zudammenhang stehen (hoffentlich).
Antwort auf Beitrag Nr.: 55.276.336 von biopadawan am 06.07.17 18:02:37Da würde ich mir keine Sorgen machen. Die besitzen so viele Aktienoptionen, dass man aus gelegentlichen Aktienverkäufen nichts ableiten kann.
Antwort auf Beitrag Nr.: 55.276.420 von Joschka Schröder am 06.07.17 18:15:15Die Aussage zu den Optionen bezieht sich auf Debanjan und McCarthy.
Tepper gehört zu Third Rock Ventures, die als Risikokapitalgeber früh investiert waren und bekanntlich ihre Position reduzieren.
Ist alles per Saldo irrelevant.
Tepper gehört zu Third Rock Ventures, die als Risikokapitalgeber früh investiert waren und bekanntlich ihre Position reduzieren.
Ist alles per Saldo irrelevant.
Zwei weitere interessante Targets, die CytomX mit Hilfe von Probodys/PDC´s bearbeitet, ohne dass dies dem Kapitalmarkt bislang bekannt sein dürfte:
1. urokinase-type plasminogen activator (uPA)
2. jagged 1/jagged 2 (-> Notch signaling pathway)
1. urokinase-type plasminogen activator (uPA)
2. jagged 1/jagged 2 (-> Notch signaling pathway)
Antwort auf Beitrag Nr.: 55.279.384 von Joschka Schröder am 07.07.17 09:08:29Weißt Du, ob es sich um firmeneigene oder um Partner-Programme handelt?
Antwort auf Beitrag Nr.: 55.279.414 von BReal am 07.07.17 09:12:32Das sind eigene F&E-Programme.
Details dazu kann man in Patentdatenbanken nachlesen. Es handelt sich um aktuelle Eintragungen.
Antwort auf Beitrag Nr.: 55.279.486 von Joschka Schröder am 07.07.17 09:20:06Vielen Dank!
Die Firma Mersana (http://www.mersana.com/) scheint einen ähnlichen Ansatz wie CytomX zu verfolgen (Reduzierung Nebenwirkungen -> Möglichkeit zur Erhöhung der Dosis -> bessere Wirksamkeit; Anwendbarkeit auf unterschiedliche Targets). Die Pipeline und die Kooperationen wirken auf den ersten Blick nicht ganz so umfangreich wie bei CytomX. Vielleicht kann hier jemand die Ansätze vergleichen?
(Bin über Twitter darauf aufmerksam geworden (https://twitter.com/MauriceOnTW/status/876864057948680194))
(Bin über Twitter darauf aufmerksam geworden (https://twitter.com/MauriceOnTW/status/876864057948680194))
Antwort auf Beitrag Nr.: 55.280.311 von fme_wo am 07.07.17 11:54:28Der Ansatz von CTMX ist m.E. potentiell "disruptive", der von Mersana m.E. nicht.
Daher würde ich bei der derzeitigen Bewertung (CTMX doppelte Marktkapitalisierung von Mersana) eindeutig das riskantere, aber im Erfolgsfall weit weit aussichtsreichere CTMX bevorzugen.
Daher würde ich bei der derzeitigen Bewertung (CTMX doppelte Marktkapitalisierung von Mersana) eindeutig das riskantere, aber im Erfolgsfall weit weit aussichtsreichere CTMX bevorzugen.
Targeted Cancer Therapy - alter Hut ?
An alle Experten Auf der Suche nach den Gründen für die Diskrepanz der Bewertung von CTMX - Börsenbewertung vs Big Pharma Deals, habe ich einen erfahrenen Pharmaprofesional angeschrieben und er hat mir folgendes geantwortet:
"Prinzipiell interessant und ein innovativer Approach, der allerdings vom Prinzip her (Reduktion systemischer Tox durch tumor-spezifische Aktivierung) ein ziemlich alter Hut ist und meines Wissens bisher nicht funktioniert hat, obwohl er in verschiedensten Variationen ausprobiert wurde. Mein Fazit: neue Variation eines alten Themas."
Ich kenne die Firmen-Beispiele, die mit solch einem Targeted Approach gescheitert sind, nicht. Aber könnte das vielleicht die Vorsicht der Börse begründen?
Hier ein paar Artikel zu diesem Thema:
Prodrug Applications for Targeted Cancer Therapy
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4147050/
‘Targeted’ Cancer Therapies Bring Hope and Failure
http://www.nytimes.com/2010/06/15/health/15canc.html
Targeted Cancer Therapies Doomed to Fail?
http://www.medpagetoday.com/hematologyoncology/coloncancer/3…
Hypoxia-activated prodrugs: paths forward in the era of personalised medicine
http://www.nature.com/bjc/journal/v114/n10/full/bjc201679a.h…
Antwort auf Beitrag Nr.: 55.280.849 von JOWCOL am 07.07.17 14:00:47Da wird offensichtlich einiges durcheinander geworfen.
1) Natürlich ist die "Targeted Cancer Therapy" ein "alter Hut", sie umfaßt neben monoklonalen Antikörpern u.a. auch Antikörper-Drug-Konjugate, Verbindungen aus small molecules und Toxinen, Trägersubstanzen, an die radioaktiven Effektoren gekoppelt sind, usw. usw.
2) Bei dem in Deinem verlinkten NY Times-Bericht besprochenen Präparat PLX4032 handelt es um Zelboraf, einen small-molecule B-Raf inhibitor.
3) Hypoxie-aktivierte Prodrugs kann man vergessen, viel zu unspezifisch und gefährlich.
Mit CytomX und dessen Maskierungstechnik hat all dies nichts zu tun.
Richtig ist, dass Mersana Therapeutics - auschließlich für ADC´s - eine Maskierungsplattform entwickelt hat, die sich aber ganz wesentlich von CytomX´s universal verwendbaren Probody-Ansatz unterscheidet. Gleiches gilt für den von Plückthun in Zürich experimentell untersuchten Ansatz, der ebenfalls mit Polymeren arbeitet. Eine selektive Blockade der Fab-Bindungsstellen beinhalten diese Techniken nicht. Zu Mersana werde ich mich später noch ausführlicher äußern, wenn mehr Zeit ist.
1) Natürlich ist die "Targeted Cancer Therapy" ein "alter Hut", sie umfaßt neben monoklonalen Antikörpern u.a. auch Antikörper-Drug-Konjugate, Verbindungen aus small molecules und Toxinen, Trägersubstanzen, an die radioaktiven Effektoren gekoppelt sind, usw. usw.
2) Bei dem in Deinem verlinkten NY Times-Bericht besprochenen Präparat PLX4032 handelt es um Zelboraf, einen small-molecule B-Raf inhibitor.
3) Hypoxie-aktivierte Prodrugs kann man vergessen, viel zu unspezifisch und gefährlich.
Mit CytomX und dessen Maskierungstechnik hat all dies nichts zu tun.
Richtig ist, dass Mersana Therapeutics - auschließlich für ADC´s - eine Maskierungsplattform entwickelt hat, die sich aber ganz wesentlich von CytomX´s universal verwendbaren Probody-Ansatz unterscheidet. Gleiches gilt für den von Plückthun in Zürich experimentell untersuchten Ansatz, der ebenfalls mit Polymeren arbeitet. Eine selektive Blockade der Fab-Bindungsstellen beinhalten diese Techniken nicht. Zu Mersana werde ich mich später noch ausführlicher äußern, wenn mehr Zeit ist.
Risikokapitalgeber Canaan hat mittlerweile - wie angekündigt - seine Position (grob 5 Mio. Aktien) voollständig abgebaut (s. heutige SEC-Mitteilung). Wenn jetzt noch eine Meldung kommt, dass der Bestand des anderen Risikokapitalgebers ThirdRockVentures auf Null reduziert ist, fällt der Kursdeckel weg.
Antwort auf Beitrag Nr.: 55.281.029 von Joschka Schröder am 07.07.17 14:46:51Deine Einschätzung zum Ansatz von Mersana würde mich in der Tat sehr interessieren. Vielen Dank schon mal im Voraus für deine Mühe...
Antwort auf Beitrag Nr.: 55.281.273 von Joschka Schröder am 07.07.17 15:36:45Der Ausstieg von Canaan könnte im Nachhinein eine Erklärung sein, dass die Aktie nach dem mega-BMS Deal wieder auf Kurse vor diesem Deal zurückgefallen ist. Die Meldung ist vom 7.6., 5 Tage später gab es das lokale Tief um 13 USD herum. Hoffen wir mal, dass der Verkaufsdruck nun weg ist und nun langsam steigende Kurse weitere Neugier und vor allem Gier wecken...
Antwort auf Beitrag Nr.: 55.281.029 von Joschka Schröder am 07.07.17 14:46:51
Nur insofern dass eine zusätzliche Technologie (bei CTMX die Maskierung und deren enzymatische Demaskierung am Tumor) zum eigentlichen Wirkmechanismus hinzugefügt wird, die unabhängig vom Wirkmechanismsu ein weiteres Erfolgs- bzw. Perfomancerisiko beinhaltet.
- Was passiert wenn nicht die komplette Maske enzymatisch verarbeitet wird,
- gibt es das Enzym auch an anderen Gewebsorten,
- ist der Ort der Demaskierung überhaupt so relevant oder wandert das demaskierte Antikörper nicht auf Abwege
Übereinander gegelegte Risiken erhöhen das Gesamtrisiko signifikant. Und das ist vielleicht die Erfahrung die die Börse hier zugrundelegt?
Zitat von Joschka Schröder: Da wird offensichtlich einiges durcheinander geworfen.
Mit CytomX und dessen Maskierungstechnik hat all dies nichts zu tun.
Nur insofern dass eine zusätzliche Technologie (bei CTMX die Maskierung und deren enzymatische Demaskierung am Tumor) zum eigentlichen Wirkmechanismus hinzugefügt wird, die unabhängig vom Wirkmechanismsu ein weiteres Erfolgs- bzw. Perfomancerisiko beinhaltet.
- Was passiert wenn nicht die komplette Maske enzymatisch verarbeitet wird,
- gibt es das Enzym auch an anderen Gewebsorten,
- ist der Ort der Demaskierung überhaupt so relevant oder wandert das demaskierte Antikörper nicht auf Abwege
Übereinander gegelegte Risiken erhöhen das Gesamtrisiko signifikant. Und das ist vielleicht die Erfahrung die die Börse hier zugrundelegt?
Antwort auf Beitrag Nr.: 55.281.381 von Ville7 am 07.07.17 15:53:42ThirdRockVentures wird vermutlich noch eine Menge Aktien im Bestand haben, am 27.3.2017 waren es noch 5,17 Mio.
Antwort auf Beitrag Nr.: 55.282.141 von JOWCOL am 07.07.17 18:05:28Alles richtige Fragen. Es bestehen nicht gerade kleine Risiken, dass das nicht so im Menschen funktioniert wie im Reagenzglas oder in Affen/Mäusen. Die Chancen falls es aber funktioniert sind erheblich. Daher muss jeder selbst einschätzen wie er das CRV bewertet und ob und wieviel seines Geldes er hier rein spekuliert. Wie es sich ausgeht werden wir entweder in den nächsten Wochen und/oder spätestens in HJ 1 2018 sehen.
Antwort auf Beitrag Nr.: 55.282.455 von Ville7 am 07.07.17 19:06:43Alles richtige Fragen. Es bestehen nicht gerade kleine Risiken, dass das nicht so im Menschen funktioniert wie im Reagenzglas oder in Affen/Mäusen.
Frage an die Profis/Biometriker: wie groß ist denn die Wahrscheinlichkeit, dass die Ergebnisse im Tiermodell bei solchen Anwendungen gleichermaßen auf das Menschenmodell projeziert werden können? Da gibts doch sicher Statistiken.
Frage an die Profis/Biometriker: wie groß ist denn die Wahrscheinlichkeit, dass die Ergebnisse im Tiermodell bei solchen Anwendungen gleichermaßen auf das Menschenmodell projeziert werden können? Da gibts doch sicher Statistiken.
Antwort auf Beitrag Nr.: 55.285.168 von infomi am 08.07.17 12:43:05Sorry. Du wirst Wahrscheinlichkeitsstatistiken finden mit der Aussage wie viele präklinische Projekte es zur Zulassung schaffen. Hauptgrund für das Scheitern ist in den meisten Fällen das Target.
Das hilft dir aber nicht bei der Abschätzung des Risikos bei Cytomx, da es hier darum geht, ob die Technologie funktioniert. Die präklinischen Daten sind gut, aber man weiss eben nie wie sich das im Menschen dann wirklich ausgeht...
Das hilft dir aber nicht bei der Abschätzung des Risikos bei Cytomx, da es hier darum geht, ob die Technologie funktioniert. Die präklinischen Daten sind gut, aber man weiss eben nie wie sich das im Menschen dann wirklich ausgeht...
Weiß jemand, was da los ist heute? Geht aktuell 6 Prozent runter, nachdem es die Tage vorher ganz gut lief. Ich finde keine News. Weder gute noch schlechte.
Antwort auf Beitrag Nr.: 55.319.158 von hinz12 am 13.07.17 16:33:47Markttechnik. Es gibt keine News.
Antwort auf Beitrag Nr.: 55.319.236 von Joschka Schröder am 13.07.17 16:41:15
Ich hoffe, du hast wie so oft recht. In USA wie auch bei uns ist das Volumen recht hoch. Nicht, dass da Leute mehr wissen.
Zitat von Joschka Schröder: Markttechnik. Es gibt keine News.
Ich hoffe, du hast wie so oft recht. In USA wie auch bei uns ist das Volumen recht hoch. Nicht, dass da Leute mehr wissen.
Antwort auf Beitrag Nr.: 55.319.371 von hinz12 am 13.07.17 16:55:04
Gewinnmitnahmen / Überkauft. CTMX hat von 13 einen guten lauf bis über 17 hinter sich.
Zitat von hinz12:Zitat von Joschka Schröder: Markttechnik. Es gibt keine News.
Ich hoffe, du hast wie so oft recht. In USA wie auch bei uns ist das Volumen recht hoch. Nicht, dass da Leute mehr wissen.
Gewinnmitnahmen / Überkauft. CTMX hat von 13 einen guten lauf bis über 17 hinter sich.
Ich würde ja eher vermuten, dass das höhere Volumen gestern mit Abgabe der Aktien von Third Rock Ventures zu tun hat. Es wurden offensichtlich 850000 an die Partner abgegeben, die besitzen zusammen aber nur rund 225000 Stück. Also müssen doch mindestens 625000 verkauft worden sein.
Findet Ihr nicht etwas bedenklich, dass das Management kaum Aktion hält?
https://finance.yahoo.com/quote/CTMX/holders?p=CTMX
Und Insiderverkäufe deutlich den Käufen überwiegen?
http://www.nasdaq.com/de/symbol/ctmx/ownership-summary
Geht nicht ganz auf wenn man die lukrativen Partnerschaften / das Potential bedenkt..
https://finance.yahoo.com/quote/CTMX/holders?p=CTMX
Und Insiderverkäufe deutlich den Käufen überwiegen?
http://www.nasdaq.com/de/symbol/ctmx/ownership-summary
Geht nicht ganz auf wenn man die lukrativen Partnerschaften / das Potential bedenkt..
Antwort auf Beitrag Nr.: 55.325.332 von Aurum2010 am 14.07.17 13:27:10Vorwiegend steigen und stiegen die Venture Capital Geber aus. Das haben sie auch schon massiv vor dem zweiten BMS Deal gemacht. Das hat somit m.E. weniger damit zu tun, ob sie an den Erfolg glauben, sondern hängt mit deren Investionsfokus zusammen. Solche Geldgeber konzentrieren sich auf Firmen in einem viel früheren Stadium und sind in einem solchen Stadium, wie es Cytomx gerade ist (in der Klinik), eigentlich schon längst wieder ausgestiegen.
Antwort auf Beitrag Nr.: 55.325.611 von Ville7 am 14.07.17 14:07:23Nette preise zum eindecken. Irgendwer drückt hier den kurs enorm.
Man kann nur spekulieren, weil man keine Infos hat. Eine Ursache könnte ein technischer Test der 200er Linie bei 13.6 sein. Sollte dies so sein, sollte der Kurs hier hart nach oben zurückprallen. Alles unter der 200er ist technisch erst mal bearish.
13,48 also weiter fallens und nun unter der 200er daily. Entscheidend für ein technische Signal wird dann der Schlusskurs sein. Am Freitag ist Verfallstag...
Antwort auf Beitrag Nr.: 55.357.424 von biopadawan am 19.07.17 20:03:18Laut Form 4 hat Third Rock bis 13.7. 850.000 Aktien verkauft. Sie sitzen weiterhin auf 4,5 Mio Stück. Wahrscheinlich kommt der Verkaufsdruck von denen...
Antwort auf Beitrag Nr.: 55.357.901 von Ville7 am 19.07.17 21:07:52Ich habe noch was nachgekauft bin weiterhin noch plus mit der Position.
Da fragt man sich wenn es so gut ist warum verkauft wer....
Antwort auf Beitrag Nr.: 55.358.522 von Huusmeister am 19.07.17 22:40:02Bei solchen extremen Kursverlusten schießen natürlich Befürchtungen ins Kraut. Vor allem wenn der Kurs durch alle Unterstützungen wie ein warmes Messer durch die Butter geht. Es gibt keine neuen oeffentlichen Infos. Daher kann natürlich alles sein.. zB. der Spuk in ein paar Tagen wieder vorbei ... oder eine noch ausgedehntere grundlose Korrektur. Oder eben negative Infos die wir noch nicht haben, aber andere... Keiner von uns kann das wissen. Die Science sieht in der Theorie hervorragend aus. Gewichtige Partner scheinen sich was davon zu versprechen. Aber ob das wirklich was wird steht derzeit für uns noch in den Sternen....also entweder Augen zu und durch und sich nicht rausschuetteln lassen oder raus hier wegen hohem Risiko bzw. erst gar nicht einsteigen.
Die aktuelle Kursentwicklung ist wirklich nicht schön anzuschauen, sie irritiert mich aber auch nicht weiter. Bei innovativen Biotechs, zu denen sich die breite Investorenschaft schon mangels Fachwissens im Normalfall keine fundierte Meinung bilden kann (entsprechend heftig sind die Schwankungen zwischen Gier und Angst), sind derartige Kursschwankungen nicht ungewöhnlich. Wesentliche News wären meldepflichtig. Etwas mehr Konstanz wird vermutlich erst dann einkehren, wenn Third Rock Ventures völlig ausgestiegen sind. Im Übrigen teile ich Villes Ansicht.
@Ville Das Thema "Mersana" ist nicht vergessen. Werde dazu gelegentlich noch etwas schreiben. Marsana steht in keinerlei Konkurrenz zu CytomX, im Gegenteil, die Bindungsstellen der Mersana-ADCs ließen sich durchaus mit Hilfe der Probody-Technik maskieren. Im Vergleich zu den von SGEN- und IMGN entwickelten ADCs lassen sich Mersana-ADCs mit deutlich mehr Toxinen beladen.
@Ville Das Thema "Mersana" ist nicht vergessen. Werde dazu gelegentlich noch etwas schreiben. Marsana steht in keinerlei Konkurrenz zu CytomX, im Gegenteil, die Bindungsstellen der Mersana-ADCs ließen sich durchaus mit Hilfe der Probody-Technik maskieren. Im Vergleich zu den von SGEN- und IMGN entwickelten ADCs lassen sich Mersana-ADCs mit deutlich mehr Toxinen beladen.
5 satte Verlusttage in folge:
http://www.v-charts.com/stocks/quotes.asp?s=CTMX
Technisch jedoch noch nicht Überverkauft, werde mir dennoch eine Pos. holen.
http://www.v-charts.com/stocks/quotes.asp?s=CTMX
Technisch jedoch noch nicht Überverkauft, werde mir dennoch eine Pos. holen.
Antwort auf Beitrag Nr.: 55.360.175 von Aurum2010 am 20.07.17 09:34:38Sofern der Kurs in dieser Geschwindigkeit weiterfällt kommen wir bald schon an eine reine Cash-Bewertung heran.
Hier stellt sich mir die spekulative Frage, inwieweit der Kurs von diesem Niveau aus tatsächlich weiterfallen würde, wenn die Studie zu CX-2009 tatsächlich vorzeitig abgebrochen werden müsste.
In Bezug auf die Studie läuft ja momentan und die nächsten Monate die "heiße Phase".
Haltet Ihr in diesem Fall Bewertungen von z.B. 1/2 Cash für möglich? Das würde einem Kurs von ca. $ 5 entsprechen.
Ansonsten finde ich das derzeitige Bewertungsniveau sehr interessant, jedoch von der Bewertung des o.g. downside-potenzials abhängig.
In einigen Monaten sollte sich die Lage - auch wegen vollzogenen Albverkäufen von institutionellen Anlegern - hoffentlich beruhigt haben.
Hier stellt sich mir die spekulative Frage, inwieweit der Kurs von diesem Niveau aus tatsächlich weiterfallen würde, wenn die Studie zu CX-2009 tatsächlich vorzeitig abgebrochen werden müsste.
In Bezug auf die Studie läuft ja momentan und die nächsten Monate die "heiße Phase".
Haltet Ihr in diesem Fall Bewertungen von z.B. 1/2 Cash für möglich? Das würde einem Kurs von ca. $ 5 entsprechen.
Ansonsten finde ich das derzeitige Bewertungsniveau sehr interessant, jedoch von der Bewertung des o.g. downside-potenzials abhängig.
In einigen Monaten sollte sich die Lage - auch wegen vollzogenen Albverkäufen von institutionellen Anlegern - hoffentlich beruhigt haben.
Bin nun auch mit einer kleinen Pos. dabei. CTMX bereits wieder über USD 14.00 ging schneller als gedacht.
Antwort auf Beitrag Nr.: 55.363.667 von Aurum2010 am 20.07.17 16:07:33Bisher nur ne begrenzte technische Gegenreaktion. Kampf um die 200 Tagelinie ist heute wieder auf dem Programm. Verläuft aktuell bei 13.59....
Hallo Joschka, hast du bei deinen Recherchen zufällig herausfinden können was aus dem EGF-R Probody, der ungef. 2010 bis 2013 als quasi POC und dann als spätestens 2015 in der Klinik angepriesen wurde geworden ist?? 2013 kam ja dann Pfizer und hat als eines der Targets EGFR gewählt. Hat die Firma irgendwas verlautbaren lassen? Wieso hat Pfizer nicht den Cytomx probody übernommen? Oder haben sie? Was ist dann mit dem Pfizer EGFR probody geschehen? Hast du da Infos? Mir kommt das alles ziemlich spanisch vor, wenn ich alte PMs oder Publikationen sehe, denn einige Zeit lang, vor den big pharma deals, war dieser Cytomx EGFR-probody deren absolutes Vorzeigeprojekt...
Antwort auf Beitrag Nr.: 55.377.752 von Ville7 am 22.07.17 20:10:04Bist Du Dir sicher, dass EGFR eines der drei von Pfizer selektierten Targets ist? Ich kann mich nicht erinnerin, dass die drei Targets jemals bekannt gegeben worden sind.
Irgendwie paßt dazu auch nicht, dass am 19.6.2017 ein Patent der CytomX veröffentlicht worden ist, das sich auf EGFR bezieht.
Wieso die Pfizer-Kooperation ansonsten nicht so recht voran kommt, entzieht sich meiner Kenntnis.
Irgendwie paßt dazu auch nicht, dass am 19.6.2017 ein Patent der CytomX veröffentlicht worden ist, das sich auf EGFR bezieht.
Wieso die Pfizer-Kooperation ansonsten nicht so recht voran kommt, entzieht sich meiner Kenntnis.
Antwort auf Beitrag Nr.: 55.378.229 von Joschka Schröder am 22.07.17 23:48:42Ja im Annual Report 2015 wird explizit EGFR als von Pfizer selektiert es Target benannt:
"In May 2013, we entered into a research collaboration, option and license agreement with Pfizer pursuant to which we granted Pfizer an option to
select four targets on which to collaborate with us on the preclinical research of PDCs using our Probody technology and Pfizer’s ADC technology. Pfizer will
provide a specified amount of research funding to us to perform the research by funding certain full-time employee expenses. Pfizer has selected its first three
targets, the first of which is EGFR. The selection of the third target triggered a payment of $1.5 million to us, and, if Pfizer selects a fourth target to include in
the collaboration, Pfizer will pay us an additional $1.5 million. Pfizer can exercise the option to obtain a commercial license for each target within three to
five years after the target is selected upon making a payment of $2 million to $5 million to us, depending on the target. Pfizer has the responsibility for and
control of all development, manufacture and commercialization of any product candidates resulting from the research collaboration."
"In May 2013, we entered into a research collaboration, option and license agreement with Pfizer pursuant to which we granted Pfizer an option to
select four targets on which to collaborate with us on the preclinical research of PDCs using our Probody technology and Pfizer’s ADC technology. Pfizer will
provide a specified amount of research funding to us to perform the research by funding certain full-time employee expenses. Pfizer has selected its first three
targets, the first of which is EGFR. The selection of the third target triggered a payment of $1.5 million to us, and, if Pfizer selects a fourth target to include in
the collaboration, Pfizer will pay us an additional $1.5 million. Pfizer can exercise the option to obtain a commercial license for each target within three to
five years after the target is selected upon making a payment of $2 million to $5 million to us, depending on the target. Pfizer has the responsibility for and
control of all development, manufacture and commercialization of any product candidates resulting from the research collaboration."
Antwort auf Beitrag Nr.: 55.378.577 von Ville7 am 23.07.17 09:19:00Vielen Dank für die Quellenangabe. Das ist interessant und so lässt sich das Rätsel lösen.
Aus den Angaben in den Geschäftsberichten für 2015 und 2016 und in den gängigen Patentdatenbanken ergibt sich:
1) Pfizer hat sich von CytomX drei Targets für PDC´s gesichert
2) Das erste Target war EGFR
3) Für das erste Target (EGFR) besitzt Pfizer Probody-Rechte ausschließlich für PDC´s (GB 2016, S. 29)
4) CytomX entwickelt schon seit langem einen eigenen bispezifischen anti-EGFR/CD3-Probody. Das entsprechende Patent ist am 13.7.2017 veröffentlicht worden, Prioritätsdatum war bereits der 27.4.2012. Präklinische Daten finden sich auf der Unternehmenshomepage.
5) Pfizer hat zu EGFR nichts patentiert.
6) Pfizer verfolgt derzeit nur noch zwei Probody-Projekte (GB 2016, S.10)
Schlussfolgerung: Pfizer hat das anti-EGFR-PDC-Projekt eingestellt, weil der von CytomX entwickelte bispezifische anti-EGFR/CD3-Probody zu besseren präklinischen Daten geführt hat. Wegen des eigenen Entwicklungsprojekts hat CytomX von Anfang an Lizenzrechte für EGFR an Pfizer nur im Hinblick auf PDC´s vergeben, während für die anderen Targets umfassende Probody-Rechte gewährt wurden.
So ist es stimmig und macht Sinn!
Aus den Angaben in den Geschäftsberichten für 2015 und 2016 und in den gängigen Patentdatenbanken ergibt sich:
1) Pfizer hat sich von CytomX drei Targets für PDC´s gesichert
2) Das erste Target war EGFR
3) Für das erste Target (EGFR) besitzt Pfizer Probody-Rechte ausschließlich für PDC´s (GB 2016, S. 29)
4) CytomX entwickelt schon seit langem einen eigenen bispezifischen anti-EGFR/CD3-Probody. Das entsprechende Patent ist am 13.7.2017 veröffentlicht worden, Prioritätsdatum war bereits der 27.4.2012. Präklinische Daten finden sich auf der Unternehmenshomepage.
5) Pfizer hat zu EGFR nichts patentiert.
6) Pfizer verfolgt derzeit nur noch zwei Probody-Projekte (GB 2016, S.10)
Schlussfolgerung: Pfizer hat das anti-EGFR-PDC-Projekt eingestellt, weil der von CytomX entwickelte bispezifische anti-EGFR/CD3-Probody zu besseren präklinischen Daten geführt hat. Wegen des eigenen Entwicklungsprojekts hat CytomX von Anfang an Lizenzrechte für EGFR an Pfizer nur im Hinblick auf PDC´s vergeben, während für die anderen Targets umfassende Probody-Rechte gewährt wurden.
So ist es stimmig und macht Sinn!
Antwort auf Beitrag Nr.: 55.379.498 von Joschka Schröder am 23.07.17 13:57:13
"hatte" statt "hat"
Jedes Mal, wenn ich alte Beiträge lese, ärgere ich mich über das grammatikalische Durcheinander, das sich einstellt, wenn ich schnell Beiträge eintippe und sofort absende. Ich nehme mir dann vor, künftig sorgfältiger zu formulieren, kann diesen Vorsatz aber mangels Zeit schon mit dem nächsten Beitrag nicht mehr einhalten. Sorry!
Zitat von Joschka Schröder: Wegen des eigenen Entwicklungsprojekts hat CytomX von Anfang an Lizenzrechte für EGFR an Pfizer nur im Hinblick auf PDC´s vergeben
"hatte" statt "hat"
Jedes Mal, wenn ich alte Beiträge lese, ärgere ich mich über das grammatikalische Durcheinander, das sich einstellt, wenn ich schnell Beiträge eintippe und sofort absende. Ich nehme mir dann vor, künftig sorgfältiger zu formulieren, kann diesen Vorsatz aber mangels Zeit schon mit dem nächsten Beitrag nicht mehr einhalten. Sorry!
CytomX Therapeutics to Announce Second Quarter 2017 Financial Results and Provide Mid-Year Update
Teleconference Scheduled for August 7, 2017, at 5:00 p.m. ETSOUTH SAN FRANCISCO, Calif., July 27, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, will announce financial results for the second quarter ended June 30, 2017 and provide a mid-year update on August 7, 2017, after the NASDAQ market closing.
Conference Call/Webcast Information
Interested parties may access the live audio webcast of the teleconference at 5:00 p.m. ET through the Investor and News page of CytomX's website at http://ir.cytomx.com or by dialing 1-877-809-6037 and using the passcode 61956517. A replay will be available on the CytomX website or by dialing 1-855-859-2056 and using the passcode 61956517. The replay will be available from August 7, 2017, until August 14, 2017.
Antwort auf Beitrag Nr.: 55.404.647 von Ville7 am 27.07.17 14:15:11Spannung steigt 

Antwort auf Beitrag Nr.: 55.404.914 von biopadawan am 27.07.17 14:41:02Täusche ich mich oder ist das das erste Mal (seit IPO), dass sie eine Telefonkonferenz zum Quartalsbericht durchführen?
Proclaim Trial update
Proclaim CX 2009: Anzahl rekrutierender Sites von 1 auf 5 erhöhtProclaim CX 072: Anzahl rekrutierender Sites von 21 auf 23 erhöht
Antwort auf Beitrag Nr.: 55.379.498 von Joschka Schröder am 23.07.17 13:57:13Danke für deine im ersten Augenblick logisch erscheinende Gedankenkette. Ob das Cytomx Projekt wirklich noch aktiv ist, wissen wir aber nicht. Ich bin dabei sehr skeptisch, dass das Projekt überhaupt noch lebt, da es seit Jahren nicht erwähnt wurde und zudem in der Pipeline-Darstellung eigentlich auftauchen müsste. Die Patentanmeldung stammt zudem aus einer Zeit in der das Projekt noch sehr aktiv und das Wichtigste für CTMX war. Ich meine es ist nicht ungewöhnlich, wenn das Patent erst 5 Jahre später zugeteilt wird und zeugt nicht davon, dass das Projekt noch lebt oder wichtig für CTMX ist. Von daher bleibt das für mich spanisch und lässt mich die ansonsten bisher gut aussehende Fassade hinterfragen.
Selbiges gilt für die weitere seltsame Leiche aus ungefähr derselben Zeit (2013/2014): CTX-033 und der damit verbundenen CTX-1003 (notch pathway) Projekt (anti-jagged) gelesen, für den ein präklinischer PoC reklamiert wurde. Auch das ist irgendwie sang- und klanglos von der Bildfläche verschwunden, ohne dass ich auf irgendeine Erklärung gestoßen bin. Kein Wort auch in den Geschäftsberichten von 2015 und 2016.
Dabei gab es am 26.März 2014 noch Pläne, das in die Klinik zu bringen, auch vom derzeitigen CEO McCarthy:
" ... Preclinical data on CTX-1003, a PDC targeting Jagged 1 and 2, shows potent anti-tumor activity and support a Probody drug conjugate approach to this highly expressed target in a number of cancer types.
“These data demonstrate the ability of our Probody platform to produce first in class, highly differentiated therapies for the treatment of cancer,” said Sean McCarthy, D.Phil., chief executive officer of CytomX. “We have made rapid progress in the advancement of our proprietary pipeline and we look forward to further advancing the Jagged program toward clinical testing.” "
http://cytomx.com/cytomx-therapeutics-to-present-data-from-a…
Man könnte jetzt sagen, es war eine strategische Entscheidung und man wollte sich auf Immuntherapien konzentrieren. Aber die Targets (zumindest EGFR) erscheinen mit im Vergleich zu den nun ausgewählten first in class Targets nicht schlecht, v.a. wenn man bereits kurz vor der Klinik stand und 2 Jahre früher clinical testing hätte beginnen können. Da muss etwas anderes mit diesen Projekten gewesen sein. Man weiß nicht, ob es targetbezogen war oder mit der bis dato unausgereiften probody Technologie zu tun hatte? Und genau sowas lässt einen dann auch hinterfragen, denn diese weichen Fakten/Dinge sind die einzigen Dinge, die man neben den logischerweise ultrapositiven Aussagen der Firma selbst und deren wissenschaftlichen Veröffentlichungen besitzt (und wie man weiß kann Wissenschaft auch manchmal unwissenschaftlich betrieben oder beschrieben werden....).
Hier ein bisschen mehr Klarheit reinzubekommen wäre mir schon wichtig.
Ich habe die Firma diesbezüglich angeschrieben. Das hatte ich wegen etwas anderem schon vor drei Wochen und keine Antwort bekommen. Nun habe ich es über die Contactform auf der Homepage versucht. Ich finde es auch immer recht fishy, wenn Investoren Kontaktmöglichkeiten bereitgestellt werden (und versprochen werden, wie nach Absenden der Frage) , dann aber keine Antwort von der Firma kommt.
Hast du (oder jemand anderer hier im Board) diesbezüglich eine andere Beobachtung gemacht und die Firma auf deine (eure) Fragen geantwortet?
Selbiges gilt für die weitere seltsame Leiche aus ungefähr derselben Zeit (2013/2014): CTX-033 und der damit verbundenen CTX-1003 (notch pathway) Projekt (anti-jagged) gelesen, für den ein präklinischer PoC reklamiert wurde. Auch das ist irgendwie sang- und klanglos von der Bildfläche verschwunden, ohne dass ich auf irgendeine Erklärung gestoßen bin. Kein Wort auch in den Geschäftsberichten von 2015 und 2016.
Dabei gab es am 26.März 2014 noch Pläne, das in die Klinik zu bringen, auch vom derzeitigen CEO McCarthy:
" ... Preclinical data on CTX-1003, a PDC targeting Jagged 1 and 2, shows potent anti-tumor activity and support a Probody drug conjugate approach to this highly expressed target in a number of cancer types.
“These data demonstrate the ability of our Probody platform to produce first in class, highly differentiated therapies for the treatment of cancer,” said Sean McCarthy, D.Phil., chief executive officer of CytomX. “We have made rapid progress in the advancement of our proprietary pipeline and we look forward to further advancing the Jagged program toward clinical testing.” "
http://cytomx.com/cytomx-therapeutics-to-present-data-from-a…
Man könnte jetzt sagen, es war eine strategische Entscheidung und man wollte sich auf Immuntherapien konzentrieren. Aber die Targets (zumindest EGFR) erscheinen mit im Vergleich zu den nun ausgewählten first in class Targets nicht schlecht, v.a. wenn man bereits kurz vor der Klinik stand und 2 Jahre früher clinical testing hätte beginnen können. Da muss etwas anderes mit diesen Projekten gewesen sein. Man weiß nicht, ob es targetbezogen war oder mit der bis dato unausgereiften probody Technologie zu tun hatte? Und genau sowas lässt einen dann auch hinterfragen, denn diese weichen Fakten/Dinge sind die einzigen Dinge, die man neben den logischerweise ultrapositiven Aussagen der Firma selbst und deren wissenschaftlichen Veröffentlichungen besitzt (und wie man weiß kann Wissenschaft auch manchmal unwissenschaftlich betrieben oder beschrieben werden....).
Hier ein bisschen mehr Klarheit reinzubekommen wäre mir schon wichtig.
Ich habe die Firma diesbezüglich angeschrieben. Das hatte ich wegen etwas anderem schon vor drei Wochen und keine Antwort bekommen. Nun habe ich es über die Contactform auf der Homepage versucht. Ich finde es auch immer recht fishy, wenn Investoren Kontaktmöglichkeiten bereitgestellt werden (und versprochen werden, wie nach Absenden der Frage) , dann aber keine Antwort von der Firma kommt.
Hast du (oder jemand anderer hier im Board) diesbezüglich eine andere Beobachtung gemacht und die Firma auf deine (eure) Fragen geantwortet?
Antwort auf Beitrag Nr.: 55.420.262 von Ville7 am 30.07.17 00:40:25Hallo Ville,
ich hatte cytomx wegen einer möglichen Kapitalerhöhungsfrage vor ca 9 Monaten angeschrieben, die Antwort (Vorratsbeschluss) kam 5 Monate später.
Interessant, dass du älteren Projekten nachrecherchierst.
Das ist recht aufwändig.
Neuere Signale, wie die Entwicklungsschritte bei den Kooperationsprojekten mit abbvie und bms, sind für mich (wichtigere) Fingerzeige.
BMS hatte bisher in seinen Quartals-Telefonkonferenzen cytomx nicht besonders erwähnt. Im second quarter haben sie beim Thema ctla-4, einem Thema mit hoher Relevanz für bms, den afucosylierten AB und den cytomx-Probody als aussichtsreiche Projekte genannt.
LG StefanR
ich hatte cytomx wegen einer möglichen Kapitalerhöhungsfrage vor ca 9 Monaten angeschrieben, die Antwort (Vorratsbeschluss) kam 5 Monate später.
Interessant, dass du älteren Projekten nachrecherchierst.
Das ist recht aufwändig.
Neuere Signale, wie die Entwicklungsschritte bei den Kooperationsprojekten mit abbvie und bms, sind für mich (wichtigere) Fingerzeige.
BMS hatte bisher in seinen Quartals-Telefonkonferenzen cytomx nicht besonders erwähnt. Im second quarter haben sie beim Thema ctla-4, einem Thema mit hoher Relevanz für bms, den afucosylierten AB und den cytomx-Probody als aussichtsreiche Projekte genannt.
LG StefanR
Antwort auf Beitrag Nr.: 55.420.757 von Ville7 am 30.07.17 10:15:53Zunächst einmal finde ich sehr gut, dass versuchst, Du den Dingen auf den Grund zu gehen. Eine skeptische Grundeinstellung ist an der Börse immer wichtig, wenn man Kapitalverluste vermeiden möchte.
Was das interessante Target EGFR betrifft, so sehe ich keinen Anlass zur Sorge. CytomX ist auf diesem Gebiet noch aktiv, letztens sind im November 2016 präklinische Daten vor der SITC präsentiert worden (Folien sind auf der CytomX-Homepage abrufbar). Ich könnte mir vorstellen, dass im nächsten Jahr der Klinikgang erfolgen wird (man darf nicht vergessen, dass CytomX ein kleines Unternehmen ist, das nicht die Ressourcen besitzt, eine Vielzahl an Präparaten gleichzeitig in die Klinik zu bringen). Insoweit hat sich an meiner Interpretation (Beitrag 323) nichts geändert.
Was aus dem Notch-Projekt geworden ist, weiß ich nicht. Ehrlich gesagt, fand ich das nie besonders interessant, zumal sich am Notch-Signalweg bereits einige Unternehmen erfolglos abgearbeitet haben (Studienendpunkte nicht erreicht, zuletzt Oncomeds Tarextumab). Insoweit dürfte es in jedem Fall Sinn machen, sich auf aussichtsreichere Targets zu konzentrieren. Bzgl. CTX-1003 ist vielleicht noch erwähnenswert, dass dieser PDC ein Immunkonjugat enthält, das auf Basis der von Seattle Genetics patentierten ADC-Technik entwickelt worden ist. Später hat sich CytomX bekanntlich für ImmunoGens ADC-Technik entschieden.
Mit der IR von CytomX habe ich noch keine Erfahrungen gemacht, ich bin mir nicht einmal sicher, ob das Unternehmen überhaupt einen IR-Manager hat. Bislang ist das Unternehmen sehr forschungsaffin, die Kapitalmarktkommunikation läuft allenfalls nebenher.
Was das interessante Target EGFR betrifft, so sehe ich keinen Anlass zur Sorge. CytomX ist auf diesem Gebiet noch aktiv, letztens sind im November 2016 präklinische Daten vor der SITC präsentiert worden (Folien sind auf der CytomX-Homepage abrufbar). Ich könnte mir vorstellen, dass im nächsten Jahr der Klinikgang erfolgen wird (man darf nicht vergessen, dass CytomX ein kleines Unternehmen ist, das nicht die Ressourcen besitzt, eine Vielzahl an Präparaten gleichzeitig in die Klinik zu bringen). Insoweit hat sich an meiner Interpretation (Beitrag 323) nichts geändert.
Was aus dem Notch-Projekt geworden ist, weiß ich nicht. Ehrlich gesagt, fand ich das nie besonders interessant, zumal sich am Notch-Signalweg bereits einige Unternehmen erfolglos abgearbeitet haben (Studienendpunkte nicht erreicht, zuletzt Oncomeds Tarextumab). Insoweit dürfte es in jedem Fall Sinn machen, sich auf aussichtsreichere Targets zu konzentrieren. Bzgl. CTX-1003 ist vielleicht noch erwähnenswert, dass dieser PDC ein Immunkonjugat enthält, das auf Basis der von Seattle Genetics patentierten ADC-Technik entwickelt worden ist. Später hat sich CytomX bekanntlich für ImmunoGens ADC-Technik entschieden.
Mit der IR von CytomX habe ich noch keine Erfahrungen gemacht, ich bin mir nicht einmal sicher, ob das Unternehmen überhaupt einen IR-Manager hat. Bislang ist das Unternehmen sehr forschungsaffin, die Kapitalmarktkommunikation läuft allenfalls nebenher.
Antwort auf Beitrag Nr.: 55.420.757 von Ville7 am 30.07.17 10:15:53Bietet sich da nicht morgen abend MEZ eine optimale Plattform, um diese Fragen im Call zu stellen als Alternative zu 5 Monaten Wartezeit? 

Antwort auf Beitrag Nr.: 55.421.928 von longitudinalwelle am 30.07.17 16:35:06Sorry, Montag in 1 Woche natürlich ...
Antwort auf Beitrag Nr.: 55.421.961 von longitudinalwelle am 30.07.17 16:40:18Ich hatte bislang einen IR-Kontakt, die Antwort kam am nächsten Tag. Allerdings mutmaßlich von einer New Yorker IR-Agentur.
Antwort auf Beitrag Nr.: 55.421.571 von Joschka Schröder am 30.07.17 14:01:54Entschuldigung für meine Börsenparanoia, aber ich möchte auch wenig Sichtbares nicht übersehen. Die SITC Präsentation kenne ich sogar, harte sie nur verdrängt|vergessen...das EGFR Projekt scheint noch am Leben zu sein...
Antwort auf Beitrag Nr.: 55.422.951 von Ville7 am 30.07.17 20:43:42
Kritisches Hinterfragen ist immer nützlich und gut.
Zitat von Ville7: Entschuldigung für meine Börsenparanoia, aber ich möchte auch wenig Sichtbares nicht übersehen. Die SITC Präsentation kenne ich sogar, harte sie nur verdrängt|vergessen...das EGFR Projekt scheint noch am Leben zu sein...
Kritisches Hinterfragen ist immer nützlich und gut.
Antwort auf Beitrag Nr.: 55.423.278 von Joschka Schröder am 30.07.17 22:38:16
Eine Frage:
Mögen Sie vielleicht mal ein paar Sätze zum Eigenen Hintergrund schreiben?
Sind Sie Mediziner, oder Etwas Ähnliches?
Wenn nicht, evt unangenehm, kein Problem.
(p.S. zu Emissionsreduktion können Sie sich evt auch die kanadische DynaCert ansehen
(Ich spiele das mit Anderen Dingen, bin an Umwelt/Tech/Energiethemen aber auch sehr, sehr interessier(Was interessiert Sie da in der Richtung?)
p.p.S. WENN das möglich ist finde ich Etwas Gutes tun/unterstützen, und auf Rendite nicht verzichten zu müssen am Allerschönsten))
Ich werde Hier jetzt ab- und an mitlesen
Eine Frage:
Mögen Sie vielleicht mal ein paar Sätze zum Eigenen Hintergrund schreiben?
Sind Sie Mediziner, oder Etwas Ähnliches?
Wenn nicht, evt unangenehm, kein Problem.
(p.S. zu Emissionsreduktion können Sie sich evt auch die kanadische DynaCert ansehen
(Ich spiele das mit Anderen Dingen, bin an Umwelt/Tech/Energiethemen aber auch sehr, sehr interessier(Was interessiert Sie da in der Richtung?)
p.p.S. WENN das möglich ist finde ich Etwas Gutes tun/unterstützen, und auf Rendite nicht verzichten zu müssen am Allerschönsten))
Ich werde Hier jetzt ab- und an mitlesen
Antwort auf Beitrag Nr.: 55.424.448 von Popeye82 am 31.07.17 09:23:31Ich habe kurz per Boardmail geantwortet.
Anscheinend will CTMX zum midyear update call seine bispezifische Plattform vorstellen und die weiteren klinischen Entwicklungspläne. Sollte das der Fall sein hören wir wahrscheinlich etwas vom eigenen EGFR Projekt.
Die Kursentwicklung bei CTMX ist unbefriedigend. Auch das technische Bild ist nicht eindeutig. Es bräuchte einen Katalysten um einen Aufwärtstrend zu etablieren. Vielleicht durch positive Kommentare beim midyear update oder durch die Vermeldung des Beginns der Kombistudie in CX072?
Das liest sich schon mal nicht schlecht, mal schauen was der Call bringt.
---------------------
Aug 07, 2017 (GLOBE NEWSWIRE via COMTEX) --
Strong Pipeline Momentum Continues
Initiated Combination Arms in Phase 1/2 PROCLAIM-CX-072 Study
Initiated Phase 1/2 PROCLAIM-CX-2009 Study
SOUTH SAN FRANCISCO, Calif., Aug. 07, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. CTMX, +0.22% a biopharmaceutical company developing investigational Probody(TM) therapeutics for the treatment of cancer, today reported second quarter 2017 financial results.
As of June 30, 2017, CytomX had cash, cash equivalents and short-term investments of $335.9 million. Based upon its current operating plan, the Company expects its existing capital resources will be sufficient to fund operations into 2020.
"During the second quarter, our pipeline of innovative Probody therapeutics continued to advance. We now have two wholly owned product candidates in clinical studies - CX-072, a PD-L1-targeting Probody therapeutic, and CX-2009, a Probody drug conjugate that targets the novel, highly expressed tumor antigen, CD-166," said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. "We remain on track to disclose data from these initial Probody clinical trials in 2018, and also expect clinical trial initiation for two partnered programs during this timeframe."
...
http://www.marketwatch.com/story/cytomx-announces-second-qua…
---------------------
Aug 07, 2017 (GLOBE NEWSWIRE via COMTEX) --
Strong Pipeline Momentum Continues
Initiated Combination Arms in Phase 1/2 PROCLAIM-CX-072 Study
Initiated Phase 1/2 PROCLAIM-CX-2009 Study
SOUTH SAN FRANCISCO, Calif., Aug. 07, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. CTMX, +0.22% a biopharmaceutical company developing investigational Probody(TM) therapeutics for the treatment of cancer, today reported second quarter 2017 financial results.
As of June 30, 2017, CytomX had cash, cash equivalents and short-term investments of $335.9 million. Based upon its current operating plan, the Company expects its existing capital resources will be sufficient to fund operations into 2020.
"During the second quarter, our pipeline of innovative Probody therapeutics continued to advance. We now have two wholly owned product candidates in clinical studies - CX-072, a PD-L1-targeting Probody therapeutic, and CX-2009, a Probody drug conjugate that targets the novel, highly expressed tumor antigen, CD-166," said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. "We remain on track to disclose data from these initial Probody clinical trials in 2018, and also expect clinical trial initiation for two partnered programs during this timeframe."
...
http://www.marketwatch.com/story/cytomx-announces-second-qua…
Eine positive Überraschung ist das schnelle Voranschreiten der PROCLAIM-CX-072-Studie, in denen bereits die Kombitherapien mit ipilimumab und vemurafenib durchgeführt werden.
15 Mio. $ Milestone für cx-2029 wird in Q3 fällig, d.h. Netcash von 350 Mio. $ vs. Market Cap 500 Mio. $ aktuell 

Die Auswahl des fünften Targets von BMS hatte ich auch noch nicht mitbekommen. Das ist eine neue Nachricht oder? Sehr positiv!
Ich verstehe zwar fachlich gefühlt maximal 10 Prozent von der Materie, aber zwei Aussagen im Call zur CX-072 monotherapy:
1) excellent progress
2) schnelles Hochfahren der Dosis möglich da bis dato keine "negative side effects" zu beobachten
Weitere Punkte:
- Kooperation mit Pfizer wurde im gleichen Atemzug mit Abbvie und BMS genannt
- "cooperation with BMS is going extraordinary well"
- Die beiden neuen Targets, die im nächsten Jahr starten sind von Abbvie und BMS (Frage kam von Bank of America)
- Die Fragen von Nomura Sec und Jefferies hab ich nicht verstanden (evtl. auch dem chinglish = chinese english der Analysten geschuldet), die teils sehr kurzen Antworten ebenfalls nicht, außer dass es natürlich alles "great questions" waren
Hoffe ich hab da keinen Mist übermittelt, aber ich denke ich bin hier nicht der Einzige, der sich den Call angehört hat oder noch anhören wird
1) excellent progress
2) schnelles Hochfahren der Dosis möglich da bis dato keine "negative side effects" zu beobachten
Weitere Punkte:
- Kooperation mit Pfizer wurde im gleichen Atemzug mit Abbvie und BMS genannt
- "cooperation with BMS is going extraordinary well"
- Die beiden neuen Targets, die im nächsten Jahr starten sind von Abbvie und BMS (Frage kam von Bank of America)
- Die Fragen von Nomura Sec und Jefferies hab ich nicht verstanden (evtl. auch dem chinglish = chinese english der Analysten geschuldet), die teils sehr kurzen Antworten ebenfalls nicht, außer dass es natürlich alles "great questions" waren

Hoffe ich hab da keinen Mist übermittelt, aber ich denke ich bin hier nicht der Einzige, der sich den Call angehört hat oder noch anhören wird

Antwort auf Beitrag Nr.: 55.476.249 von Joschka Schröder am 07.08.17 22:42:31CX-072 wird mittlerweile mit 10 mg/kg dosiert, ohne dass bisher dosislimitirende Toxizitäten aufgetreten sind. Startdosis war 0,03 mg/kg. Mithin arbeitet man bereits mit der 333fachen Ausgangsdosis.
Antwort auf Beitrag Nr.: 55.477.800 von Joschka Schröder am 08.08.17 09:55:02Sicherlich ein deutliches Indiz, dass es derzeit keine Safety Issues gibt und erstmal alles so läuft, wie wir uns das wünschen. Möglicherweise sogar ein Zeitpunkt zum Nachkaufen, weil das sehr hohe Risiko zumindest in kleinem Umfang gesunken ist?
Lässt sich im Übrigen aus der Vorgehensweise von CTMS, also dem schnellen Hochfahren der Dosierungen, noch weiteres ableiten?
Möglicherweise auch Rückschlüsse auf eine nicht vorhandene oder sehr geringe Wirksamkeit?
Lässt sich im Übrigen aus der Vorgehensweise von CTMS, also dem schnellen Hochfahren der Dosierungen, noch weiteres ableiten?
Möglicherweise auch Rückschlüsse auf eine nicht vorhandene oder sehr geringe Wirksamkeit?
Antwort auf Beitrag Nr.: 55.477.800 von Joschka Schröder am 08.08.17 09:55:02Die schnelle Hochdosierung des CX072 von 0,03 auf 10mg ist ein Hinweis auf eine stabile Maskierung des Antikörpers.
In der Proclaim-Studie sind Maximaldosierungen von bis zu 30mg/kg in der Monotherapie vorgesehen.
Zugelassene PD-L1-Inhibitoren werden folgendermaßen dosiert:
-Tecentriq von Roche wird mit 1200mg alle 21 Tage dosiert (17-20mg/kg)
-Bavencio von MerckSerono wird mit 10mg/kg alle 14 Tage dosiert
Die Affinität von CX072 an den PD-L1-Rezeptor in Relation zu den o.g. zugelassenen Antikörpern ist jedoch nicht bekannt. Ich nehme vereinfachend mal an, daß die Affinitäten "ähnlich" sind.
Grob vereinfacht sind weiterhin die mg-Mengen der einzelnen kompletten Antikörper in Korrelation stehend zu der Anzahl der Moleküle (da ca. 150 kDalton Molekulargewicht bei allen kompletten Antikörpern ).
Aus den Dosierungen von Tecentriq und Bavencio heraus kann man annehmen, daß trotz nicht erreichter Maximaldosierung des CX072 wir uns bei der erreichten 10mg/kg Dosierung in der Nähe des therapeutischen Bereichs befinden, damit ist die Aussage, daß es zu keinen dosislimitierenden Toxizitäten gekommen ist, bedeutend.
Die Tatsache, daß cytomx, wie geplant, eine Kombi-Studie mit vemurafenib gestartet hat, bei bekannter schwerer Nebenswirkungsrate vemurafenib mit tecentriq von 69%, ist mutig.
Auch der Start der CX2009-cd166-Studie weist auf das hohe Vertrauen von cytomx in die Stabilität seiner probodies in der Peripherie hin.
Aus meiner Sicht sind die gemeldeten Daten und der Projektfortschritt in der Konsequenz ein starkes Signal!
Ich bin gespannt, wie der Markt in den USA auf die Datenlage reagiert.
In der Proclaim-Studie sind Maximaldosierungen von bis zu 30mg/kg in der Monotherapie vorgesehen.
Zugelassene PD-L1-Inhibitoren werden folgendermaßen dosiert:
-Tecentriq von Roche wird mit 1200mg alle 21 Tage dosiert (17-20mg/kg)
-Bavencio von MerckSerono wird mit 10mg/kg alle 14 Tage dosiert
Die Affinität von CX072 an den PD-L1-Rezeptor in Relation zu den o.g. zugelassenen Antikörpern ist jedoch nicht bekannt. Ich nehme vereinfachend mal an, daß die Affinitäten "ähnlich" sind.
Grob vereinfacht sind weiterhin die mg-Mengen der einzelnen kompletten Antikörper in Korrelation stehend zu der Anzahl der Moleküle (da ca. 150 kDalton Molekulargewicht bei allen kompletten Antikörpern ).
Aus den Dosierungen von Tecentriq und Bavencio heraus kann man annehmen, daß trotz nicht erreichter Maximaldosierung des CX072 wir uns bei der erreichten 10mg/kg Dosierung in der Nähe des therapeutischen Bereichs befinden, damit ist die Aussage, daß es zu keinen dosislimitierenden Toxizitäten gekommen ist, bedeutend.
Die Tatsache, daß cytomx, wie geplant, eine Kombi-Studie mit vemurafenib gestartet hat, bei bekannter schwerer Nebenswirkungsrate vemurafenib mit tecentriq von 69%, ist mutig.
Auch der Start der CX2009-cd166-Studie weist auf das hohe Vertrauen von cytomx in die Stabilität seiner probodies in der Peripherie hin.
Aus meiner Sicht sind die gemeldeten Daten und der Projektfortschritt in der Konsequenz ein starkes Signal!
Ich bin gespannt, wie der Markt in den USA auf die Datenlage reagiert.
Antwort auf Beitrag Nr.: 55.476.186 von longitudinalwelle am 07.08.17 22:32:33
Tja, das sieht der Markt wohl anders. Aktie gerade ordentlich im Minus.
CytomX Therapeutics reports 2Q loss
Associated Press Associated Press8 August 2017
SOUTH SAN FRANCISCO, Calif. (AP) _ CytomX Therapeutics Inc. (CTMX) on Monday reported a loss of $25.2 million in its second quarter.
The South San Francisco, California-based company said it had a loss of 69 cents per share.
The results fell short of Wall Street expectations. The average estimate of three analysts surveyed by Zacks Investment Research was for a loss of 39 cents per share.
The biopharmaceutical company posted revenue of $8.8 million in the period.
Zitat von longitudinalwelle: Das liest sich schon mal nicht schlecht, mal schauen was der Call bringt.
---------------------
Aug 07, 2017 (GLOBE NEWSWIRE via COMTEX) --
Strong Pipeline Momentum Continues
Initiated Combination Arms in Phase 1/2 PROCLAIM-CX-072 Study
Initiated Phase 1/2 PROCLAIM-CX-2009 Study
SOUTH SAN FRANCISCO, Calif., Aug. 07, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. CTMX, +0.22% a biopharmaceutical company developing investigational Probody(TM) therapeutics for the treatment of cancer, today reported second quarter 2017 financial results.
As of June 30, 2017, CytomX had cash, cash equivalents and short-term investments of $335.9 million. Based upon its current operating plan, the Company expects its existing capital resources will be sufficient to fund operations into 2020.
"During the second quarter, our pipeline of innovative Probody therapeutics continued to advance. We now have two wholly owned product candidates in clinical studies - CX-072, a PD-L1-targeting Probody therapeutic, and CX-2009, a Probody drug conjugate that targets the novel, highly expressed tumor antigen, CD-166," said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. "We remain on track to disclose data from these initial Probody clinical trials in 2018, and also expect clinical trial initiation for two partnered programs during this timeframe."
...
http://www.marketwatch.com/story/cytomx-announces-second-qua…
Tja, das sieht der Markt wohl anders. Aktie gerade ordentlich im Minus.
CytomX Therapeutics reports 2Q loss
Associated Press Associated Press8 August 2017
SOUTH SAN FRANCISCO, Calif. (AP) _ CytomX Therapeutics Inc. (CTMX) on Monday reported a loss of $25.2 million in its second quarter.
The South San Francisco, California-based company said it had a loss of 69 cents per share.
The results fell short of Wall Street expectations. The average estimate of three analysts surveyed by Zacks Investment Research was for a loss of 39 cents per share.
The biopharmaceutical company posted revenue of $8.8 million in the period.
das Earnings-Call Transcript ist jetzt online auf Seeking Alpha - ist aber eher was für die Fachleute
Antwort auf Beitrag Nr.: 55.480.695 von Pitschnass am 08.08.17 15:59:37Was der Markt hier sieht oder nicht sollte in diesem Unternehmens-Stadium eigentlich von allergeringstem Interesse sein. Hätten die Analysten ihre Hausaufgaben gemacht und aus den 200 Mio. von BMS die 10 Mio. berücksichtigt, die cytomx durchrouten muss an Unterlizensierungsgebühren, dann wären vielleicht auch nicht solche realitätsfremden (aber zugleich völlig belanglosen) Schätzungen zustande gekommen 
Genauso lächerlich ist in diesem Zusammenhang übrigens das Price Target von 32 USD von Instinet (Nomura).

Genauso lächerlich ist in diesem Zusammenhang übrigens das Price Target von 32 USD von Instinet (Nomura).
Antwort auf Beitrag Nr.: 55.480.695 von Pitschnass am 08.08.17 15:59:37Ist doch schön, dass "der Markt" gelegentlich so deppert ist. Ich habe heute während der Kursrutsches jedenfalls kräftig zugekauft, obwohl ich auch so schon stark investiert war.
Die Analysten haben bei ihren Gewinnschätzungen offenbar übersehen, dass CytomX für gewisse Anlässe Meilensteinzahlungen an die UCSB zahlen muss (später auch Royalties im niedrigen einstelligen Prozentbereich für Produktverkäufe). Dies hat dazu geführt, dass in Q2 eine Zahlung i.H. von 10 Mio. USD an die UCSB fällig geworden ist (aus dem BMY-Kontrakt), die voll umfänglich in die GuV eingeflossen ist. Die 200 Mio. Upfrontzahlung, die CytomX wiederum von BMY erhalten hat und die Anlass der 10 Mio.-Zahlung an die UCSB war, wird demgegenüber über einen längeren Zeitraum abgegrenzt und ist nur zu einem kleinen Teil in Q2 umsatz- und gewinnwirksam geworden. Per Saldo hat die BMY-Upfrontzahlung in der GuV zu einem Verlust geführt! Ein Non-Event! So sind die Analystenschätzungen verfehlt worden.
Operativ läuft es bislang besser als erhofft. Was auch immer Analysten schreiben ... ich bin sehr zufrieden.
Die Analysten haben bei ihren Gewinnschätzungen offenbar übersehen, dass CytomX für gewisse Anlässe Meilensteinzahlungen an die UCSB zahlen muss (später auch Royalties im niedrigen einstelligen Prozentbereich für Produktverkäufe). Dies hat dazu geführt, dass in Q2 eine Zahlung i.H. von 10 Mio. USD an die UCSB fällig geworden ist (aus dem BMY-Kontrakt), die voll umfänglich in die GuV eingeflossen ist. Die 200 Mio. Upfrontzahlung, die CytomX wiederum von BMY erhalten hat und die Anlass der 10 Mio.-Zahlung an die UCSB war, wird demgegenüber über einen längeren Zeitraum abgegrenzt und ist nur zu einem kleinen Teil in Q2 umsatz- und gewinnwirksam geworden. Per Saldo hat die BMY-Upfrontzahlung in der GuV zu einem Verlust geführt! Ein Non-Event! So sind die Analystenschätzungen verfehlt worden.
Operativ läuft es bislang besser als erhofft. Was auch immer Analysten schreiben ... ich bin sehr zufrieden.
Antwort auf Beitrag Nr.: 55.481.214 von longitudinalwelle am 08.08.17 16:44:46
Du bringst hier Markt und Analysten durcheinander. Der Markt sind die Verkäufer und Käufer. Deren Verhalten sehe ich 1:1 in meinem Depot. Die Analysten haben darauf mit dem Blödsinn den sie verzapfen vielleicht Einfluß, der Markt sind sie aber nicht. Aber was rede ich. Vor einer Stunde fast -4%, jetzt über 4% im Plus. Der Markt hat immer recht...
Zitat von longitudinalwelle: Was der Markt hier sieht oder nicht sollte in diesem Unternehmens-Stadium eigentlich von allergeringstem Interesse sein. Hätten die Analysten ihre Hausaufgaben gemacht und aus den 200 Mio. von BMS die 10 Mio. berücksichtigt, die cytomx durchrouten muss an Unterlizensierungsgebühren, dann wären vielleicht auch nicht solche realitätsfremden (aber zugleich völlig belanglosen) Schätzungen zustande gekommen
Genauso lächerlich ist in diesem Zusammenhang übrigens das Price Target von 32 USD von Instinet (Nomura).
Du bringst hier Markt und Analysten durcheinander. Der Markt sind die Verkäufer und Käufer. Deren Verhalten sehe ich 1:1 in meinem Depot. Die Analysten haben darauf mit dem Blödsinn den sie verzapfen vielleicht Einfluß, der Markt sind sie aber nicht. Aber was rede ich. Vor einer Stunde fast -4%, jetzt über 4% im Plus. Der Markt hat immer recht...
Antwort auf Beitrag Nr.: 55.481.214 von longitudinalwelle am 08.08.17 16:44:46
Wieso? Auf Sicht eines Jahres sollte das bei positivem Studienverlauf auf jeden Fall drin sein.
Zitat von longitudinalwelle: Genauso lächerlich ist in diesem Zusammenhang übrigens das Price Target von 32 USD von Instinet (Nomura).
Wieso? Auf Sicht eines Jahres sollte das bei positivem Studienverlauf auf jeden Fall drin sein.
Antwort auf Beitrag Nr.: 55.481.319 von Pitschnass am 08.08.17 16:53:34So so, der Markt hat immer Recht?  Auf den Märkten herrscht folglich Informationseffizienz?
Auf den Märkten herrscht folglich Informationseffizienz?  Das wäre mir neu ...
Das wäre mir neu ...
@ Joschka: die 32 Dollar dürften in diesem Fall voraussichtlich überboten werden (--> Pitschnass: vom Markt! ). Mir ging es eher darum, dass man sich in so einer Ausgangssituation mit konkreten Kurszielen unglaubwürdig macht.
). Mir ging es eher darum, dass man sich in so einer Ausgangssituation mit konkreten Kurszielen unglaubwürdig macht.
 Auf den Märkten herrscht folglich Informationseffizienz?
Auf den Märkten herrscht folglich Informationseffizienz?  Das wäre mir neu ...
Das wäre mir neu ...@ Joschka: die 32 Dollar dürften in diesem Fall voraussichtlich überboten werden (--> Pitschnass: vom Markt!
 ). Mir ging es eher darum, dass man sich in so einer Ausgangssituation mit konkreten Kurszielen unglaubwürdig macht.
). Mir ging es eher darum, dass man sich in so einer Ausgangssituation mit konkreten Kurszielen unglaubwürdig macht.
Antwort auf Beitrag Nr.: 55.479.828 von StefanR am 08.08.17 14:13:15Der schnelle Fortschritt bedeutet nicht, dass man bereits Erfolg proklamieren kann. Es könnte auch sein, dass sich die Masken im Körper nicht, bei nur sehr wenigen Patienten oder ungenügend stark abspalten. Auch das würde zu einem hervorragenden Sicherheitsprofil führen.
Ich sehe schon den positiven Grundton, nur suche ich an der Börse immer zuerst das Haar in der Suppe. Und da frage ich mich, wieso sie die Guidance auf erste Daten von Ende 2017 auf 2018 korrigiert haben? Sollte man mit aktuell rapidem Fortschritt in der Höherdosierung nicht erste Daten bereits in 2017 vorstellen können? Oder sind die Daten doch nicht so eindeutig positiv, dass man sich erst mal sortieren muss?
Ich sehe schon den positiven Grundton, nur suche ich an der Börse immer zuerst das Haar in der Suppe. Und da frage ich mich, wieso sie die Guidance auf erste Daten von Ende 2017 auf 2018 korrigiert haben? Sollte man mit aktuell rapidem Fortschritt in der Höherdosierung nicht erste Daten bereits in 2017 vorstellen können? Oder sind die Daten doch nicht so eindeutig positiv, dass man sich erst mal sortieren muss?
Selten so ein miserables Transcript gelesen.
Beispiel: "The payload for this product candidate is that they tansinoid VM4 under license from Nguyen. "
Beispiel: "The payload for this product candidate is that they tansinoid VM4 under license from Nguyen. "
Antwort auf Beitrag Nr.: 55.482.354 von Ville7 am 08.08.17 18:52:07Es wird nicht ausgeschlossen, noch 2017 Daten zu veröffentlichen (siehe Q&A --> Bank of America).
Wir sollten nun an der orangenen Linie sein:
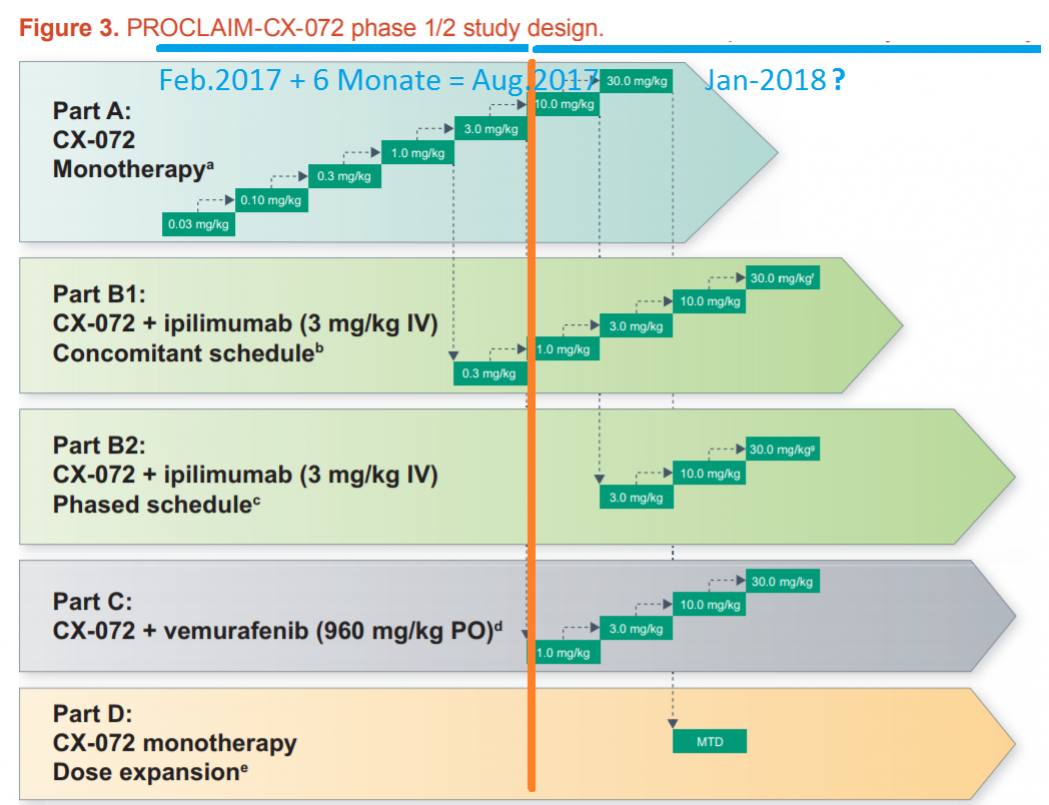
@Joschka, es ist doch üblich die Anzahl der Patienten in den höheren Dosis-Gruppen zu erhöhen, oder? Wenn ich linear hochrechne wären wir mit multipler Dosierung frühestens sogar im Januar 2018 fertig bis zur höchsten Dosis in allen Gruppen - ohne expansion cohort Part D. Erste Daten zu ASCO 2018 sollten somit m.E. drin sein.

@Joschka, es ist doch üblich die Anzahl der Patienten in den höheren Dosis-Gruppen zu erhöhen, oder? Wenn ich linear hochrechne wären wir mit multipler Dosierung frühestens sogar im Januar 2018 fertig bis zur höchsten Dosis in allen Gruppen - ohne expansion cohort Part D. Erste Daten zu ASCO 2018 sollten somit m.E. drin sein.
Antwort auf Beitrag Nr.: 55.483.176 von longitudinalwelle am 08.08.17 20:10:50
Wenn dann aber nur aus dem "translational program", nicht aus PROCLAIM-CX072. Laut Firma aber trotzdem recht unwahrscheinlich. Geguidet wird klar auf 2018.
Zitat von longitudinalwelle: Es wird nicht ausgeschlossen, noch 2017 Daten zu veröffentlichen (siehe Q&A --> Bank of America).
Wenn dann aber nur aus dem "translational program", nicht aus PROCLAIM-CX072. Laut Firma aber trotzdem recht unwahrscheinlich. Geguidet wird klar auf 2018.
Pharma giant Bristol-Myers Squibb just made another big bet on cancer immunotherapy
Business Insider Lydia Ramsey
Business InsiderAugust 3, 2017
(A tray containing cancer cells sits on an optical microscope in the Nanomedicine Lab at UCL's School of Pharmacy in London.REUTERS/Suzanne Plunkett)
Bristol-Myers Squibb, a company known for its cancer immunotherapy drugs, just acquired immunotherapy startup IFM Therapeutics.
The deal is worth $300 million upfront, and if IFM's two drug programs hit certain development milestones, Bristol-Myers could pay an additional $1.01 billion for each, adding up to a total of $2.32 billion.
IFM has two preclinical programs, which work to enhance the immune system's response to cancer cells.
Bristol-Myers has two drugs, Opdivo and Yervoy, that are a part of a new class of cancer treatments called cancer immunotherapy that harness the body's immune system to go after cancer. Unlike chemotherapy, which involves administering powerful drugs that kill both cancerous and healthy cells (most healthy cells can repair themselves), immunotherapies harness the power of the immune system to help it identify and knock out just the cancerous cells.
The drugmaker has made other immunotherapy deals in the past. In March, it partnered with CytomX in a deal that could be worth $3.8 billion. CytomX is trying to do is activate the drug only when it's by diseased tissue, using something called "Probodies." That way, it might be possible to reduce some of the side effects that current cancer immunotherapy treatments have.
Source: https://finance.yahoo.com/news/pharma-giant-bristol-myers-sq…
Antwort auf Beitrag Nr.: 55.483.245 von Ville7 am 08.08.17 20:21:46@ville
Das Prinzip der prodrug-Metabolismus-drug Reihenfolge kennt man in der Arzneimitteltherapie relativ häufig.
Oft ist der Metabilisierungsort die Leber, und zumeist handelt es sich um small molecules, welche im Körper scharf geschaltet werden, oder eben durch Glucoronidierung hydrophil umgewandelt werden und einer Nierenclearance interliegen, oder über Gallensäuren mit dem faeces ausgeschieden werden.
Bei alll diesen kleinen Molekülen ist die Halbwertszeit oft relativ kurz.
Im Gegensatz dazu haben so große Moleküle, wie monoklonale Antikörper eine HWZ von 14-21 Tagen.
Das hat für die Prodrug- Metabolisierung den Vorteil, daß z.b. die in der tumor microenvironment aktivierten membranständigen Metallomercaptasen auch mehr Zeit für den Metabolismus zum Drug haben.
Insofern flutet der PD-L1-Prodrug CX072 nicht so schnell am Rezeptor an, kann aber durch das verlängerte Zeitintervall dann schlußendlich doch mit einer für die Therapie ausreichenden Rate aktiviert werden.
Cytomx hat durch Tumorprobenentnahmen bei über 90 Prozent der menschlichen Gewebskulturen eine Abspaltung der Maskierung feststellen können.Du darfst mit dem Totalausstieg aus cytomX gerne noch etwas warten😎
Dennoch finde ich gut, wenn du Verschiebungen von Veröffentlichungszeitpunkten hinterfragst.
CytomX hat im übrigen in einigen Wochen ( Esmo?) eine Veröffentlichung des Studiendesigns (cx2009) angekündigt.
Viellleicht bringt uns das wieder ein wenig weiter.
Das Prinzip der prodrug-Metabolismus-drug Reihenfolge kennt man in der Arzneimitteltherapie relativ häufig.
Oft ist der Metabilisierungsort die Leber, und zumeist handelt es sich um small molecules, welche im Körper scharf geschaltet werden, oder eben durch Glucoronidierung hydrophil umgewandelt werden und einer Nierenclearance interliegen, oder über Gallensäuren mit dem faeces ausgeschieden werden.
Bei alll diesen kleinen Molekülen ist die Halbwertszeit oft relativ kurz.
Im Gegensatz dazu haben so große Moleküle, wie monoklonale Antikörper eine HWZ von 14-21 Tagen.
Das hat für die Prodrug- Metabolisierung den Vorteil, daß z.b. die in der tumor microenvironment aktivierten membranständigen Metallomercaptasen auch mehr Zeit für den Metabolismus zum Drug haben.
Insofern flutet der PD-L1-Prodrug CX072 nicht so schnell am Rezeptor an, kann aber durch das verlängerte Zeitintervall dann schlußendlich doch mit einer für die Therapie ausreichenden Rate aktiviert werden.
Cytomx hat durch Tumorprobenentnahmen bei über 90 Prozent der menschlichen Gewebskulturen eine Abspaltung der Maskierung feststellen können.Du darfst mit dem Totalausstieg aus cytomX gerne noch etwas warten😎
Dennoch finde ich gut, wenn du Verschiebungen von Veröffentlichungszeitpunkten hinterfragst.
CytomX hat im übrigen in einigen Wochen ( Esmo?) eine Veröffentlichung des Studiendesigns (cx2009) angekündigt.
Viellleicht bringt uns das wieder ein wenig weiter.
Antwort auf Beitrag Nr.: 55.483.440 von StefanR am 08.08.17 20:45:04Keine Sorge. Ich bleibe noch ne Weile erhalten.
Die >90% sind mir bekannt. Frage ist nur, ob diese Quote im Menschen anders ( viel geringer) ist ..
Die >90% sind mir bekannt. Frage ist nur, ob diese Quote im Menschen anders ( viel geringer) ist ..
@StefanR
Es macht Spaß, Deine Beiträge zu lesen. Man merkt, dass der Begriff Pharmakologie für Dich kein Fremdwort ist.
@Ville
Natürlich ließe sich die schnelle Dosisprogression bei guter Verträglichkeit auch anders interpretieren, beispielsweise könnte der im Probody enthaltene anti-PD-L1-Antikörper falsch selektiert und damit wirkungslos sein. Aufgrund der präklinischen Daten, die zwar im Tiermodell, aber an menschlichen Tumoren gewonnen worden sind, darf man jedoch von einer akzeptablen Wirkung des nackten Antinkörpers ausgehen, ebenso davon, dass auch in situ (-> klinische Studie) die Abspaltung der Maskierung im Tumorgewebe grundsätzlich funktioniert.
Eine kritischer Punkt, die sich auch nicht vorab durch Tierversuche klären ließ, war, wie stabil der Masken-Linker (außerhalb des Tumorgewebes) im menschlichen Organismus sein würde. Hier geben die gestrigen Daten eine wichtige Antwort: Der Probody wurde bislang gut vertragen, bis zur aktuellen Dosis von 10 mg/kg sind keine DLT aufgetreten. Der Linker scheint also stabil. Dies war für mich der Anlass, CTMX-Aktien zuzukaufen.
Die Übernahme von IFM durch BMY ist eigentlich ein Thema, das mit CytomX wenig zu tun hat. IFM ist auf dem Gebiet der angeworbenen Immunabwehr tätig, konkret ging es bei dem Deal um einen STING- und einen NLRP3-Agonisten. Ebenfalls auf dem Gebiet der angeborenen Immunabwehr (allerdings mit einem gänzlich anderen Ansatz, der hauptsächlich auf die selektive Aktivierung natürlicher Killerzellen abzielt) ist die in Heidelberg beheimatete Affimed, die ich mir seit einigen Tagen ansehe, zu der ich mir aber noch kein Urteil gebildet habe. Affimed notiert ebenfalls an der Nasdaq.
Noch zur Frage der Patientenzahl: Eigentlich ist davon auszugehen, dass die Patientenzahl in den höheren (klinisch relevanten) Dosisgruppen zunehmen wird. Desweiteren vermute ich, dass man in den beiden Kombi-Armen kein so hohes Tempo gehen wird, weil hier das Nebenwirkungsrisiko deutlich größer ist als bei Monotherapie.
Es macht Spaß, Deine Beiträge zu lesen. Man merkt, dass der Begriff Pharmakologie für Dich kein Fremdwort ist.
@Ville
Natürlich ließe sich die schnelle Dosisprogression bei guter Verträglichkeit auch anders interpretieren, beispielsweise könnte der im Probody enthaltene anti-PD-L1-Antikörper falsch selektiert und damit wirkungslos sein. Aufgrund der präklinischen Daten, die zwar im Tiermodell, aber an menschlichen Tumoren gewonnen worden sind, darf man jedoch von einer akzeptablen Wirkung des nackten Antinkörpers ausgehen, ebenso davon, dass auch in situ (-> klinische Studie) die Abspaltung der Maskierung im Tumorgewebe grundsätzlich funktioniert.
Eine kritischer Punkt, die sich auch nicht vorab durch Tierversuche klären ließ, war, wie stabil der Masken-Linker (außerhalb des Tumorgewebes) im menschlichen Organismus sein würde. Hier geben die gestrigen Daten eine wichtige Antwort: Der Probody wurde bislang gut vertragen, bis zur aktuellen Dosis von 10 mg/kg sind keine DLT aufgetreten. Der Linker scheint also stabil. Dies war für mich der Anlass, CTMX-Aktien zuzukaufen.
Die Übernahme von IFM durch BMY ist eigentlich ein Thema, das mit CytomX wenig zu tun hat. IFM ist auf dem Gebiet der angeworbenen Immunabwehr tätig, konkret ging es bei dem Deal um einen STING- und einen NLRP3-Agonisten. Ebenfalls auf dem Gebiet der angeborenen Immunabwehr (allerdings mit einem gänzlich anderen Ansatz, der hauptsächlich auf die selektive Aktivierung natürlicher Killerzellen abzielt) ist die in Heidelberg beheimatete Affimed, die ich mir seit einigen Tagen ansehe, zu der ich mir aber noch kein Urteil gebildet habe. Affimed notiert ebenfalls an der Nasdaq.
Noch zur Frage der Patientenzahl: Eigentlich ist davon auszugehen, dass die Patientenzahl in den höheren (klinisch relevanten) Dosisgruppen zunehmen wird. Desweiteren vermute ich, dass man in den beiden Kombi-Armen kein so hohes Tempo gehen wird, weil hier das Nebenwirkungsrisiko deutlich größer ist als bei Monotherapie.
Antwort auf Beitrag Nr.: 55.476.486 von longitudinalwelle am 07.08.17 23:46:45
Ich verstehe zwar fachlich gefühlt maximal 10 Prozent von der Materie, aber........
_____________________________________________________________
Ich schliesse mich an
(evt Etwas mehr),
und bedanke mich(umso mehr) für All Die Einschätzungen -Der Fachkundige(re)n-hier!!
Einiges an, geschilderten, Grundkonzepten verstehe ich schon, eine Menge an fachlichen Details aber nicht.
Aber, es macht da(nn) auch wirklich Spass in Einem Umfeld von, tlw, Fachkundigen zu lernen.
Immer wieder Einen, kleinen, weiteren, Schritt, auf Ein 1.000km entferntes Ziel.

DANKE,
Gruss
Ich verstehe zwar fachlich gefühlt maximal 10 Prozent von der Materie, aber........
_____________________________________________________________
Ich schliesse mich an
(evt Etwas mehr),
und bedanke mich(umso mehr) für All Die Einschätzungen -Der Fachkundige(re)n-hier!!
Einiges an, geschilderten, Grundkonzepten verstehe ich schon, eine Menge an fachlichen Details aber nicht.
Aber, es macht da(nn) auch wirklich Spass in Einem Umfeld von, tlw, Fachkundigen zu lernen.
Immer wieder Einen, kleinen, weiteren, Schritt, auf Ein 1.000km entferntes Ziel.


DANKE,
Gruss
Mich persönlich würden auch etwaige Einschätzungen der Experten bzgl. MRNS und AFMD sehr interessieren.
Beide Unternehmen verfolgen interessante Ansätze / Technologien.
Ggf. dann unter Eröffnung eigene Threads, da dieser CTMX vorbehalten bleiben sollte.
Im Übrigen präsentiert CTMX am 10.08.2017 unter anderem bei:
SOUTH SAN FRANCISCO, Calif., Aug. 10, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, will present at the 2017 Wedbush PacGrow Healthcare Conference. Debanjan Ray, chief financial officer and head of corporate development will deliver a corporate overview on August 16, 2017, at 2:30 p.m. ET.
A live audio webcast of the presentation will be available through the Investors and News section of CytomX's website. An archived replay will be available for 90 days following the event.
Weitere Erkenntnisse werden sich dort wohl nicht gewinnen lassen und bleiben der ESMO 2017 vorbehalten.
Beide Unternehmen verfolgen interessante Ansätze / Technologien.
Ggf. dann unter Eröffnung eigene Threads, da dieser CTMX vorbehalten bleiben sollte.
Im Übrigen präsentiert CTMX am 10.08.2017 unter anderem bei:
SOUTH SAN FRANCISCO, Calif., Aug. 10, 2017 (GLOBE NEWSWIRE) -- CytomX Therapeutics, Inc. (Nasdaq:CTMX), a biopharmaceutical company developing investigational Probody™ therapeutics for the treatment of cancer, will present at the 2017 Wedbush PacGrow Healthcare Conference. Debanjan Ray, chief financial officer and head of corporate development will deliver a corporate overview on August 16, 2017, at 2:30 p.m. ET.
A live audio webcast of the presentation will be available through the Investors and News section of CytomX's website. An archived replay will be available for 90 days following the event.
Weitere Erkenntnisse werden sich dort wohl nicht gewinnen lassen und bleiben der ESMO 2017 vorbehalten.
Antwort auf Beitrag Nr.: 55.484.463 von Joschka Schröder am 08.08.17 23:33:02@Joschka: Ich hatte den Artikel nur gepostet um zu zeigen, dass BMS auch in andere bisher un-
bzw. kaum validierte Ansätze immense Summen reinsteckt und nicht nur CTMX solche Deals von BMS bekommt. Das relativiert die Euphorie um diesen Partner etwas.
Was mich generell auch etwas verunsichert ist, dass sowohl Debanjan Ray als auch Sean McCarthy weiter ihre Verkaufspläne unbeeindruckt ausführen. Speziell Debanjan Ray, den ich als finanziell sehr bedacht und für clever halte; dieser scheint nicht bereit zu sein größere mengen von CTMX-Aktien halten zu wollen; seine aktuell noch gehaltene Aktienzahl ist sehr gering - geradezu lächerlich gering für einen Vorstand.
Ich weiß, dass das manchmal gar nichts aussagt, allerdings manchmal schon. CTMX sollte inzwischen ein Bild haben, ob der Ansatz funktionieren kann bzw. wird und in diesem Falle würde ich von rationalen Menschen wie Ray erwarten, dass die regelmäßigen Verkaufsprogramme eingestellt werden.
bzw. kaum validierte Ansätze immense Summen reinsteckt und nicht nur CTMX solche Deals von BMS bekommt. Das relativiert die Euphorie um diesen Partner etwas.
Was mich generell auch etwas verunsichert ist, dass sowohl Debanjan Ray als auch Sean McCarthy weiter ihre Verkaufspläne unbeeindruckt ausführen. Speziell Debanjan Ray, den ich als finanziell sehr bedacht und für clever halte; dieser scheint nicht bereit zu sein größere mengen von CTMX-Aktien halten zu wollen; seine aktuell noch gehaltene Aktienzahl ist sehr gering - geradezu lächerlich gering für einen Vorstand.
Ich weiß, dass das manchmal gar nichts aussagt, allerdings manchmal schon. CTMX sollte inzwischen ein Bild haben, ob der Ansatz funktionieren kann bzw. wird und in diesem Falle würde ich von rationalen Menschen wie Ray erwarten, dass die regelmäßigen Verkaufsprogramme eingestellt werden.
Antwort auf Beitrag Nr.: 55.521.648 von biopadawan am 14.08.17 16:41:33Gut, dass Ray mal am Mittwoch präsentiert... vielleicht ist es dabei möglich ein paar weiche Fakten zwischen den Zeilen zu ergattern...
Antwort auf Beitrag Nr.: 55.526.211 von Ville7 am 15.08.17 11:08:18@Joschka
Herzlichen Dank für deine Wertschätzung!!
@Ville
Ich erwarte von der Präsentation morgen nicht allzu viel.
Viel wichtiger könnte das im telefoncall des second quarter angekündigte update der proclaim-Sudien sein.
Am 8.9. ist ja die ESMO in Spanien, hier der cytomx-Präsentationsausschnitt:
"13:15 - 13:15 422TiP - PROCLAIM-CX-2009: A First-in-Human Trial to Evaluate CX-2009 in Adults With Metastatic or
Locally Advanced Unresectable Solid Tumors
J. Garcia-Corbacho1, A. Spira2, V. Boni3, J. Feliu3, M. Middleton4, H. Burris5, A. Yang Weaver6, M. Will
6, J. Harding7, F. Meric-Bernstam8, V. Heinemann9; 1Barcelona, ES, 2Fairfax, US, 3Madrid, ES, 4
Oxford, GB, 5Nashville, US, 6South San Francisco, US, 7New York, US, 8Houston, US, 9Munich, DE
13:15 - 13:15 423TiP - The First-in-Human, Dose-Finding PROCLAIM-CX-072 Trial to Assess the Antitumor Activity
and Tolerability of the Probody Therapeutic CX-072 as Monotherapy and in Combination With Ipilimumab
or Vemurafenib in Solid Advanced Tumors and Lymphomas
V. Boni1, J. Garcia-Corbacho2, J. Feliu1, J. Wydmanski3, Z. Horvath4, I. Bondarenko5, B. Irving6, M.
Will6, E.G.E. de Vries7, F. Thistlethwaite8; 1Madrid, ES, 2Barcelona, ES, 3Katowice, PL, 4Debrecen,
HU, 5Dnepropetrovsk, UA, 6South San Francisco, US, 7Cluj-Napoca, RO, 8Manchester, GB"
Herzlichen Dank für deine Wertschätzung!!
@Ville
Ich erwarte von der Präsentation morgen nicht allzu viel.
Viel wichtiger könnte das im telefoncall des second quarter angekündigte update der proclaim-Sudien sein.
Am 8.9. ist ja die ESMO in Spanien, hier der cytomx-Präsentationsausschnitt:
"13:15 - 13:15 422TiP - PROCLAIM-CX-2009: A First-in-Human Trial to Evaluate CX-2009 in Adults With Metastatic or
Locally Advanced Unresectable Solid Tumors
J. Garcia-Corbacho1, A. Spira2, V. Boni3, J. Feliu3, M. Middleton4, H. Burris5, A. Yang Weaver6, M. Will
6, J. Harding7, F. Meric-Bernstam8, V. Heinemann9; 1Barcelona, ES, 2Fairfax, US, 3Madrid, ES, 4
Oxford, GB, 5Nashville, US, 6South San Francisco, US, 7New York, US, 8Houston, US, 9Munich, DE
13:15 - 13:15 423TiP - The First-in-Human, Dose-Finding PROCLAIM-CX-072 Trial to Assess the Antitumor Activity
and Tolerability of the Probody Therapeutic CX-072 as Monotherapy and in Combination With Ipilimumab
or Vemurafenib in Solid Advanced Tumors and Lymphomas
V. Boni1, J. Garcia-Corbacho2, J. Feliu1, J. Wydmanski3, Z. Horvath4, I. Bondarenko5, B. Irving6, M.
Will6, E.G.E. de Vries7, F. Thistlethwaite8; 1Madrid, ES, 2Barcelona, ES, 3Katowice, PL, 4Debrecen,
HU, 5Dnepropetrovsk, UA, 6South San Francisco, US, 7Cluj-Napoca, RO, 8Manchester, GB"
Antwort auf Beitrag Nr.: 55.526.181 von Ville7 am 15.08.17 11:05:15Deine Überlegungen sind natürlich verständlich. Da eine nicht unwesentliche Gehaltskomponente aus Aktienoptionen besteht, halte ich es aber für normal, dass seitens der Vorstände regelmäßig Aktien verkauft werden. Dass ich kein Freund von großen Aktienoptionsprogrammen bin, steht auf einem anderen Blatt.
Antwort auf Beitrag Nr.: 55.528.758 von Joschka Schröder am 15.08.17 15:40:10Der Kursverlauf ist wirklich alles andere als schön.
In Anbetracht der relativ erfreulichen Nachrichtenlage (kein Studienabbruch , schnelles hochfahren der Dosierungen, weiterer bms-Deal, neue Targets) schon irritierend.
In Anbetracht der relativ erfreulichen Nachrichtenlage (kein Studienabbruch , schnelles hochfahren der Dosierungen, weiterer bms-Deal, neue Targets) schon irritierend.
Antwort auf Beitrag Nr.: 55.531.155 von biopadawan am 15.08.17 21:51:09Natürlich ist die Kursentwicklung unbefriedigend, zumal auch von Analystenseite kein Gegenwind zu erkennen ist (z.B. Kursziel der Bank of Amerika aktuell von 28 USD auf 30 USD angehoben). Andererseits verunsichert mich der Kursverauf auch nicht, da sich die Kurse kleiner Biotechs in den ersten Jahren (bis handfeste klinische Daten vorliegen) oft erratisch entwickeln. Fakt ist, dass im Biotech-Sektor unter Investoren starke Zurückhaltung herrscht, was markttechnisch nicht ungünstig ist.
Was soll man nun tun? Sorgfältig die Geschäftsentwicklung beobachten (Fortschreiten der Studien, Studienabbrüche, Kooperationen usw.) und auf Studienergebnisse warten. Im Fall positiver Studienergebnisse wird deren Interpretation einfach sein, im Fall negativer Wirksamkeitsdaten (CX-072) oder unerwünschter Nebenwirkungen (CX-2009) wird die Deutung schon schwieriger, weil in diesem Fall noch kein Urteil über die Probody-Technologie möglich ist. Ursache mangelnder Wirkung von CX-072 oder zu großer Nebenwirkungen von CX-2009 könnten auch schlechte Antikörperselektion (CX-072) bzw. zu extremes Target (CD166) sein.
Für Unterhaltung wird in jedem Fall gesorgt sein.
Ich hoffe weiterhin, dass sich das Investement langfristig voll auszahlen wird.
Was soll man nun tun? Sorgfältig die Geschäftsentwicklung beobachten (Fortschreiten der Studien, Studienabbrüche, Kooperationen usw.) und auf Studienergebnisse warten. Im Fall positiver Studienergebnisse wird deren Interpretation einfach sein, im Fall negativer Wirksamkeitsdaten (CX-072) oder unerwünschter Nebenwirkungen (CX-2009) wird die Deutung schon schwieriger, weil in diesem Fall noch kein Urteil über die Probody-Technologie möglich ist. Ursache mangelnder Wirkung von CX-072 oder zu großer Nebenwirkungen von CX-2009 könnten auch schlechte Antikörperselektion (CX-072) bzw. zu extremes Target (CD166) sein.
Für Unterhaltung wird in jedem Fall gesorgt sein.
Ich hoffe weiterhin, dass sich das Investement langfristig voll auszahlen wird.
Enttäuschende Daten aus der CheckMate-214-Studie! Eine weitere Dosiserhöhung des Checkpointinhibitors Opdivo oder des anti-CTLA-4-Antikörpers Yervoy wäre wegen der starken Nebenwirkungen der Präparate (s. Ende der Meldung) nicht möglich. Hier könnte und sollte CytomX´s Probody-Technologie Abhilfe schaffen. Als Alternative für die besagte Opdivo/Yervoy-Kombi böte sich eine Kombinationstherapie z.B. aus CX-072 (CytomX) und dem anti-CTLA-4-Probody (CytomX/BMY) an. Hier sollte man - zumindest in der Therorie - deutlich höher dosieren können, ohne dass unakzeptable Nebenwirkungen auftreten.
Tuesday, August 15, 2017 4:30 pm EDT
PRINCETON, N.J.--(BUSINESS WIRE)--Bristol-Myers Squibb Company (NYSE: BMY) announced topline results today from the CheckMate -214 trial investigating Opdivo (nivolumab) in combination with Yervoy (ipilimumab) versus sunitinib in intermediate and poor-risk patients previously untreated advanced or metastatic renal cell carcinoma. The combination met the co-primary endpoint of objective response rate (ORR) and achieved a 41.6% ORR versus 26.5% for sunitinib. Median duration of response was not reached for the combination of Opdivo and Yervoy and was 18.17 months for sunitinib. While there was an improvement in progression-free survival (PFS) (HR=0.82, [95% CI 0.64 – 1.05]; stratified 2-sided p=0.03), it did not reach statistical significance. The median PFS was 11.56 months (95% CI 8.71 – 15.51) for the Opdivo and Yervoy combination versus 8.38 months (95% CI 7.03-10.81) for sunitinib, The study will continue as planned to allow the third co-primary endpoint of overall survival to mature. The tolerability profile observed in CheckMate-214 was consistent with that observed in previously reported studies of this dosing schedule.
“We are encouraged by the totality of the CheckMate-214 data. The overall response rate and durability of response favored the combination of Opdivo and Yervoy, and the trend for PFS supports the potential of the combination in intermediate and poor-risk advanced renal cell carcinoma, the most common type of kidney cancer. This is an important study in first-line renal cancer as these patients need new options,” said Vicki Goodman, M.D., development lead, Melanoma and Genitourinary Cancers, Bristol-Myers Squibb. “We look forward to presenting the full results from this study at an upcoming medical meeting.”
“Opdivo is now well established as standard of care in the treatment of second-line renal cell carcinoma,” said Goodman. “The company plans to share these important first-line data with regulatory authorities and we look forward to reporting overall survival when these data mature.”
About CheckMate -214
CheckMate -214 is a phase 3, randomized, open-label study evaluating the combination of Opdivo plus Yervoy versus sunitinib in patients with previously untreated advanced or metastatic renal cell carcinoma. Patients in the combination group received Opdivo 3 mg/kg plus Yervoy 1 mg/kg every 3 weeks for 4 doses followed by Opdivo 3 mg/kg every 2 weeks. Patients in the comparator group received sunitinib 50 mg once daily for 4 weeks, followed by 2 weeks off before continuation of treatment. Patients were treated until progression or unacceptable toxic effects. The primary endpoints of the trial are progression-free survival, overall survival and objective response rate in an intermediate to poor-risk patient population (approximately 75 percent of patients). The majority of alpha was allocated to overall survival. Safety is a secondary endpoint.
...
IMPORTANT SAFETY INFORMATION
WARNING: IMMUNE-MEDIATED ADVERSE REACTIONS
YERVOY can result in severe and fatal immune-mediated adverse reactions. These immune-mediated reactions may involve any organ system; however, the most common severe immune-mediated adverse reactions are enterocolitis, hepatitis, dermatitis (including toxic epidermal necrolysis), neuropathy, and endocrinopathy. The majority of these immune-mediated reactions initially manifested during treatment; however, a minority occurred weeks to months after discontinuation of YERVOY.
Assess patients for signs and symptoms of enterocolitis, dermatitis, neuropathy, and endocrinopathy and evaluate clinical chemistries including liver function tests (LFTs), adrenocorticotropic hormone (ACTH) level, and thyroid function tests at baseline and before each dose.
Permanently discontinue YERVOY and initiate systemic high-dose corticosteroid therapy for severe immune-mediated reactions.
Immune-Mediated Pneumonitis
OPDIVO can cause immune-mediated pneumonitis. Fatal cases have been reported. Monitor patients for signs with radiographic imaging and for symptoms of pneumonitis. Administer corticosteroids for Grade 2 or more severe pneumonitis. Permanently discontinue for Grade 3 or 4 and withhold until resolution for Grade 2. In patients receiving OPDIVO monotherapy, fatal cases of immune-mediated pneumonitis have occurred. Immune-mediated pneumonitis occurred in 3.1% (61/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated pneumonitis occurred in 6% (25/407) of patients.
In Checkmate 205 and 039, pneumonitis, including interstitial lung disease, occurred in 6.0% (16/266) of patients receiving OPDIVO. Immune-mediated pneumonitis occurred in 4.9% (13/266) of patients receiving OPDIVO: Grade 3 (n=1) and Grade 2 (n=12).
Immune-Mediated Colitis
OPDIVO can cause immune-mediated colitis. Monitor patients for signs and symptoms of colitis. Administer corticosteroids for Grade 2 (of more than 5 days duration), 3, or 4 colitis. Withhold OPDIVO monotherapy for Grade 2 or 3 and permanently discontinue for Grade 4 or recurrent colitis upon re-initiation of OPDIVO. When administered with YERVOY, withhold OPDIVO and YERVOY for Grade 2 and permanently discontinue for Grade 3 or 4 or recurrent colitis. In patients receiving OPDIVO monotherapy, immune-mediated colitis occurred in 2.9% (58/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated colitis occurred in 26% (107/407) of patients including three fatal cases.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe, life-threatening, or fatal (diarrhea of ≥7 stools above baseline, fever, ileus, peritoneal signs; Grade 3-5) immune-mediated enterocolitis occurred in 34 (7%) patients. Across all YERVOY-treated patients in that study (n=511), 5 (1%) developed intestinal perforation, 4 (0.8%) died as a result of complications, and 26 (5%) were hospitalized for severe enterocolitis.
Immune-Mediated Hepatitis
OPDIVO can cause immune-mediated hepatitis. Monitor patients for abnormal liver tests prior to and periodically during treatment. Administer corticosteroids for Grade 2 or greater transaminase elevations. Withhold for Grade 2 and permanently discontinue for Grade 3 or 4 immune-mediated hepatitis. In patients receiving OPDIVO monotherapy, immune-mediated hepatitis occurred in 1.8% (35/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated hepatitis occurred in 13% (51/407) of patients.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe, life-threatening, or fatal hepatotoxicity (AST or ALT elevations >5x the ULN or total bilirubin elevations >3x the ULN; Grade 3-5) occurred in 8 (2%) patients, with fatal hepatic failure in 0.2% and hospitalization in 0.4%.
Immune-Mediated Neuropathies
In a separate Phase 3 study of YERVOY 3 mg/kg, 1 case of fatal Guillain-Barré syndrome and 1 case of severe (Grade 3) peripheral motor neuropathy were reported.
Immune-Mediated Endocrinopathies
OPDIVO can cause immune-mediated hypophysitis, immune-mediated adrenal insufficiency, autoimmune thyroid disorders, and Type 1 diabetes mellitus. Monitor patients for signs and symptoms of hypophysitis, signs and symptoms of adrenal insufficiency, thyroid function prior to and periodically during treatment, and hyperglycemia. Administer hormone replacement as clinically indicated and corticosteroids for Grade 2 or greater hypophysitis. Withhold for Grade 2 or 3 and permanently discontinue for Grade 4 hypophysitis. Administer corticosteroids for Grade 3 or 4 adrenal insufficiency. Withhold for Grade 2 and permanently discontinue for Grade 3 or 4 adrenal insufficiency. Administer hormone-replacement therapy for hypothyroidism. Initiate medical management for control of hyperthyroidism. Withhold OPDIVO for Grade 3 and permanently discontinue for Grade 4 hyperglycemia.
In patients receiving OPDIVO monotherapy, hypophysitis occurred in 0.6% (12/1994) of patients. In patients receiving OPDIVO with YERVOY, hypophysitis occurred in 9% (36/407) of patients. In patients receiving OPDIVO monotherapy, adrenal insufficiency occurred in 1% (20/1994) of patients. In patients receiving OPDIVO with YERVOY, adrenal insufficiency occurred in 5% (21/407) of patients. In patients receiving OPDIVO monotherapy, hypothyroidism or thyroiditis resulting in hypothyroidism occurred in 9% (171/1994) of patients. Hyperthyroidism occurred in 2.7% (54/1994) of patients receiving OPDIVO monotherapy. In patients receiving OPDIVO with YERVOY, hypothyroidism or thyroiditis resulting in hypothyroidism occurred in 22% (89/407) of patients. Hyperthyroidism occurred in 8% (34/407) of patients receiving OPDIVO with YERVOY. In patients receiving OPDIVO monotherapy, diabetes occurred in 0.9% (17/1994) of patients. In patients receiving OPDIVO with YERVOY, diabetes occurred in 1.5% (6/407) of patients.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe to life-threatening immune-mediated endocrinopathies (requiring hospitalization, urgent medical intervention, or interfering with activities of daily living; Grade 3-4) occurred in 9 (1.8%) patients. All 9 patients had hypopituitarism, and some had additional concomitant endocrinopathies such as adrenal insufficiency, hypogonadism, and hypothyroidism. 6 of the 9 patients were hospitalized for severe endocrinopathies.
Immune-Mediated Nephritis and Renal Dysfunction
OPDIVO can cause immune-mediated nephritis. Monitor patients for elevated serum creatinine prior to and periodically during treatment. Administer corticosteroids for Grades 2-4 increased serum creatinine. Withhold OPDIVO for Grade 2 or 3 and permanently discontinue for Grade 4 increased serum creatinine. In patients receiving OPDIVO monotherapy, immune-mediated nephritis and renal dysfunction occurred in 1.2% (23/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated nephritis and renal dysfunction occurred in 2.2% (9/407) of patients.
Immune-Mediated Skin Adverse Reactions and Dermatitis
OPDIVO can cause immune-mediated rash, including Stevens-Johnson syndrome (SJS) and toxic epidermal necrolysis (TEN), some cases with fatal outcome. Administer corticosteroids for Grade 3 or 4 rash. Withhold for Grade 3 and permanently discontinue for Grade 4 rash. For symptoms or signs of SJS or TEN, withhold OPDIVO and refer the patient for specialized care for assessment and treatment; if confirmed, permanently discontinue. In patients receiving OPDIVO monotherapy, immune-mediated rash occurred in 9% (171/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated rash occurred in 22.6% (92/407) of patients.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe, life-threatening, or fatal immune-mediated dermatitis (eg, Stevens-Johnson syndrome, toxic epidermal necrolysis, or rash complicated by full thickness dermal ulceration, or necrotic, bullous, or hemorrhagic manifestations; Grade 3-5) occurred in 13 (2.5%) patients. 1 (0.2%) patient died as a result of toxic epidermal necrolysis. 1 additional patient required hospitalization for severe dermatitis.
Immune-Mediated Encephalitis
OPDIVO can cause immune-mediated encephalitis. Evaluation of patients with neurologic symptoms may include, but not be limited to, consultation with a neurologist, brain MRI, and lumbar puncture. Withhold OPDIVO in patients with new-onset moderate to severe neurologic signs or symptoms and evaluate to rule out other causes. If other etiologies are ruled out, administer corticosteroids and permanently discontinue OPDIVO for immune-mediated encephalitis. In patients receiving OPDIVO monotherapy, encephalitis occurred in 0.2% (3/1994) of patients. Fatal limbic encephalitis occurred in one patient after 7.2 months of exposure despite discontinuation of OPDIVO and administration of corticosteroids. Encephalitis occurred in one patient receiving OPDIVO with YERVOY (0.2%) after 1.7 months of exposure.
Other Immune-Mediated Adverse Reactions
Based on the severity of adverse reaction, permanently discontinue or withhold treatment, administer high-dose corticosteroids, and, if appropriate, initiate hormone-replacement therapy. Across clinical trials of OPDIVO the following clinically significant immune-mediated adverse reactions occurred in <1.0% of patients receiving OPDIVO: uveitis, iritis, pancreatitis, facial and abducens nerve paresis, demyelination, polymyalgia rheumatica, autoimmune neuropathy, Guillain-Barré syndrome, hypopituitarism, systemic inflammatory response syndrome, gastritis, duodenitis, sarcoidosis, histiocytic necrotizing lymphadenitis (Kikuchi lymphadenitis), myositis, myocarditis, rhabdomyolysis, motor dysfunction, vasculitis, and myasthenic syndrome.
Infusion Reactions
OPDIVO can cause severe infusion reactions, which have been reported in <1.0% of patients in clinical trials. Discontinue OPDIVO in patients with Grade 3 or 4 infusion reactions. Interrupt or slow the rate of infusion in patients with Grade 1 or 2. In patients receiving OPDIVO monotherapy, infusion-related reactions occurred in 6.4% (127/1994) of patients. In patients receiving OPDIVO with YERVOY, infusion-related reactions occurred in 2.5% (10/407) of patients.
Complications of Allogeneic HSCT after OPDIVO
Complications, including fatal events, occurred in patients who received allogeneic HSCT after OPDIVO. Outcomes were evaluated in 17 patients from Checkmate 205 and 039, who underwent allogeneic HSCT after discontinuing OPDIVO (15 with reduced-intensity conditioning, 2 with myeloablative conditioning). Thirty-five percent (6/17) of patients died from complications of allogeneic HSCT after OPDIVO. Five deaths occurred in the setting of severe or refractory GVHD. Grade 3 or higher acute GVHD was reported in 29% (5/17) of patients. Hyperacute GVHD was reported in 20% (n=2) of patients. A steroid-requiring febrile syndrome, without an identified infectious cause, was reported in 35% (n=6) of patients. Two cases of encephalitis were reported: Grade 3 (n=1) lymphocytic encephalitis without an identified infectious cause, and Grade 3 (n=1) suspected viral encephalitis. Hepatic veno-occlusive disease (VOD) occurred in one patient, who received reduced-intensity conditioned allogeneic HSCT and died of GVHD and multi-organ failure. Other cases of hepatic VOD after reduced-intensity conditioned allogeneic HSCT have also been reported in patients with lymphoma who received a PD-1 receptor blocking antibody before transplantation. Cases of fatal hyperacute GVHD have also been reported. These complications may occur despite intervening therapy between PD-1 blockade and allogeneic HSCT.
Follow patients closely for early evidence of transplant-related complications such as hyperacute GVHD, severe (Grade 3 to 4) acute GVHD, steroid-requiring febrile syndrome, hepatic VOD, and other immune-mediated adverse reactions, and intervene promptly.
Embryo-Fetal Toxicity
Based on their mechanisms of action, OPDIVO and YERVOY can cause fetal harm when administered to a pregnant woman. Advise pregnant women of the potential risk to a fetus. Advise females of reproductive potential to use effective contraception during treatment with an OPDIVO- or YERVOY- containing regimen and for at least 5 months after the last dose of OPDIVO.
Lactation
It is not known whether OPDIVO or YERVOY is present in human milk. Because many drugs, including antibodies, are excreted in human milk and because of the potential for serious adverse reactions in nursing infants from an OPDIVO-containing regimen, advise women to discontinue breastfeeding during treatment. Advise women to discontinue nursing during treatment with YERVOY and for 3 months following the final dose.
Serious Adverse Reactions
In Checkmate 037, serious adverse reactions occurred in 41% of patients receiving OPDIVO (n=268). Grade 3 and 4 adverse reactions occurred in 42% of patients receiving OPDIVO . The most frequent Grade 3 and 4 adverse drug reactions reported in 2% to <5% of patients receiving OPDIVO were abdominal pain, hyponatremia, increased aspartate aminotransferase, and increased lipase. In Checkmate 066, serious adverse reactions occurred in 36% of patients receiving OPDIVO (n=206). Grade 3 and 4 adverse reactions occurred in 41% of patients receiving OPDIVO. The most frequent Grade 3 and 4 adverse reactions reported in ≥2% of patients receiving OPDIVO were gamma-glutamyltransferase increase (3.9%) and diarrhea (3.4%). In Checkmate 067, serious adverse reactions (73% and 37%), adverse reactions leading to permanent discontinuation (43% and 14%) or to dosing delays (55% and 28%), and Grade 3 or 4 adverse reactions (72% and 44%) all occurred more frequently in the OPDIVO plus YERVOY arm (n=313) relative to the OPDIVO arm (n=313). The most frequent (≥10%) serious adverse reactions in the OPDIVO plus YERVOY arm and the OPDIVO arm, respectively, were diarrhea (13% and 2.6%), colitis (10% and 1.6%), and pyrexia (10% and 0.6%). In Checkmate 017 and 057, serious adverse reactions occurred in 46% of patients receiving OPDIVO (n=418). The most frequent serious adverse reactions reported in at least 2% of patients receiving OPDIVO were pneumonia, pulmonary embolism, dyspnea, pyrexia, pleural effusion, pneumonitis, and respiratory failure. In Checkmate 025, serious adverse reactions occurred in 47% of patients receiving OPDIVO (n=406). The most frequent serious adverse reactions reported in ≥2% of patients were acute kidney injury, pleural effusion, pneumonia, diarrhea, and hypercalcemia. In Checkmate 205 and 039, adverse reactions leading to discontinuation occurred in 7% and dose delays due to adverse reactions occurred in 34% of patients (n=266). Serious adverse reactions occurred in 26% of patients. The most frequent serious adverse reactions reported in ≥1% of patients were pneumonia, infusion-related reaction, pyrexia, colitis or diarrhea, pleural effusion, pneumonitis, and rash. Eleven patients died from causes other than disease progression: 3 from adverse reactions within 30 days of the last OPDIVO dose, 2 from infection 8 to 9 months after completing OPDIVO, and 6 from complications of allogeneic HSCT. In Checkmate 141, serious adverse reactions occurred in 49% of patients receiving OPDIVO. The most frequent serious adverse reactions reported in at least 2% of patients receiving OPDIVO were pneumonia, dyspnea, respiratory failure, respiratory tract infection, and sepsis. In Checkmate 275, serious adverse reactions occurred in 54% of patients receiving OPDIVO (n=270). The most frequent serious adverse reactions reported in at least 2% of patients receiving OPDIVO were urinary tract infection, sepsis, diarrhea, small intestine obstruction, and general physical health deterioration.
Common Adverse Reactions
In Checkmate 037, the most common adverse reaction (≥20%) reported with OPDIVO (n=268) was rash (21%). In Checkmate 066, the most common adverse reactions (≥20%) reported with OPDIVO (n=206) vs dacarbazine (n=205) were fatigue (49% vs 39%), musculoskeletal pain (32% vs 25%), rash (28% vs 12%), and pruritus (23% vs 12%). In Checkmate 067, the most common (≥20%) adverse reactions in the OPDIVO plus YERVOY arm (n=313) were fatigue (59%), rash (53%), diarrhea (52%), nausea (40%), pyrexia (37%), vomiting (28%), and dyspnea (20%). The most common (≥20%) adverse reactions in the OPDIVO (n=313) arm were fatigue (53%), rash (40%), diarrhea (31%), and nausea (28%). In Checkmate 017 and 057, the most common adverse reactions (≥20%) in patients receiving OPDIVO (n=418) were fatigue, musculoskeletal pain, cough, dyspnea, and decreased appetite. In Checkmate 025, the most common adverse reactions (≥20%) reported in patients receiving OPDIVO (n=406) vs everolimus (n=397) were asthenic conditions (56% vs 57%), cough (34% vs 38%), nausea (28% vs 29%), rash (28% vs 36%), dyspnea (27% vs 31%), diarrhea (25% vs 32%), constipation (23% vs 18%), decreased appetite (23% vs 30%), back pain (21% vs 16%), and arthralgia (20% vs 14%). In Checkmate 205 and 039, the most common adverse reactions (≥20%) reported in patients receiving OPDIVO (n=266) were upper respiratory tract infection (44%), fatigue (39%), cough (36%), diarrhea (33%), pyrexia (29%), musculoskeletal pain (26%), rash (24%), nausea (20%) and pruritus (20%). In Checkmate 141, the most common adverse reactions (≥10%) in patients receiving OPDIVO were cough and dyspnea at a higher incidence than investigator’s choice. In Checkmate 275, the most common adverse reactions (≥ 20%) reported in patients receiving OPDIVO (n=270) were fatigue (46%), musculoskeletal pain (30%), nausea (22%), and decreased appetite (22%).. The most common adverse reactions (≥20%) in patients who received OPDIVO as a single agent were fatigue, rash, musculoskeletal pain, pruritus, diarrhea, nausea, asthenia, cough, dyspnea, constipation, decreased appetite, back pain, arthralgia, upper respiratory tract infection, pyrexia.
In a separate Phase 3 study of YERVOY 3 mg/kg, the most common adverse reactions (≥5%) in patients who received YERVOY at 3 mg/kg were fatigue (41%), diarrhea (32%), pruritus (31%), rash (29%), and colitis (8%).
Tuesday, August 15, 2017 4:30 pm EDT
PRINCETON, N.J.--(BUSINESS WIRE)--Bristol-Myers Squibb Company (NYSE: BMY) announced topline results today from the CheckMate -214 trial investigating Opdivo (nivolumab) in combination with Yervoy (ipilimumab) versus sunitinib in intermediate and poor-risk patients previously untreated advanced or metastatic renal cell carcinoma. The combination met the co-primary endpoint of objective response rate (ORR) and achieved a 41.6% ORR versus 26.5% for sunitinib. Median duration of response was not reached for the combination of Opdivo and Yervoy and was 18.17 months for sunitinib. While there was an improvement in progression-free survival (PFS) (HR=0.82, [95% CI 0.64 – 1.05]; stratified 2-sided p=0.03), it did not reach statistical significance. The median PFS was 11.56 months (95% CI 8.71 – 15.51) for the Opdivo and Yervoy combination versus 8.38 months (95% CI 7.03-10.81) for sunitinib, The study will continue as planned to allow the third co-primary endpoint of overall survival to mature. The tolerability profile observed in CheckMate-214 was consistent with that observed in previously reported studies of this dosing schedule.
“We are encouraged by the totality of the CheckMate-214 data. The overall response rate and durability of response favored the combination of Opdivo and Yervoy, and the trend for PFS supports the potential of the combination in intermediate and poor-risk advanced renal cell carcinoma, the most common type of kidney cancer. This is an important study in first-line renal cancer as these patients need new options,” said Vicki Goodman, M.D., development lead, Melanoma and Genitourinary Cancers, Bristol-Myers Squibb. “We look forward to presenting the full results from this study at an upcoming medical meeting.”
“Opdivo is now well established as standard of care in the treatment of second-line renal cell carcinoma,” said Goodman. “The company plans to share these important first-line data with regulatory authorities and we look forward to reporting overall survival when these data mature.”
About CheckMate -214
CheckMate -214 is a phase 3, randomized, open-label study evaluating the combination of Opdivo plus Yervoy versus sunitinib in patients with previously untreated advanced or metastatic renal cell carcinoma. Patients in the combination group received Opdivo 3 mg/kg plus Yervoy 1 mg/kg every 3 weeks for 4 doses followed by Opdivo 3 mg/kg every 2 weeks. Patients in the comparator group received sunitinib 50 mg once daily for 4 weeks, followed by 2 weeks off before continuation of treatment. Patients were treated until progression or unacceptable toxic effects. The primary endpoints of the trial are progression-free survival, overall survival and objective response rate in an intermediate to poor-risk patient population (approximately 75 percent of patients). The majority of alpha was allocated to overall survival. Safety is a secondary endpoint.
...
IMPORTANT SAFETY INFORMATION
WARNING: IMMUNE-MEDIATED ADVERSE REACTIONS
YERVOY can result in severe and fatal immune-mediated adverse reactions. These immune-mediated reactions may involve any organ system; however, the most common severe immune-mediated adverse reactions are enterocolitis, hepatitis, dermatitis (including toxic epidermal necrolysis), neuropathy, and endocrinopathy. The majority of these immune-mediated reactions initially manifested during treatment; however, a minority occurred weeks to months after discontinuation of YERVOY.
Assess patients for signs and symptoms of enterocolitis, dermatitis, neuropathy, and endocrinopathy and evaluate clinical chemistries including liver function tests (LFTs), adrenocorticotropic hormone (ACTH) level, and thyroid function tests at baseline and before each dose.
Permanently discontinue YERVOY and initiate systemic high-dose corticosteroid therapy for severe immune-mediated reactions.
Immune-Mediated Pneumonitis
OPDIVO can cause immune-mediated pneumonitis. Fatal cases have been reported. Monitor patients for signs with radiographic imaging and for symptoms of pneumonitis. Administer corticosteroids for Grade 2 or more severe pneumonitis. Permanently discontinue for Grade 3 or 4 and withhold until resolution for Grade 2. In patients receiving OPDIVO monotherapy, fatal cases of immune-mediated pneumonitis have occurred. Immune-mediated pneumonitis occurred in 3.1% (61/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated pneumonitis occurred in 6% (25/407) of patients.
In Checkmate 205 and 039, pneumonitis, including interstitial lung disease, occurred in 6.0% (16/266) of patients receiving OPDIVO. Immune-mediated pneumonitis occurred in 4.9% (13/266) of patients receiving OPDIVO: Grade 3 (n=1) and Grade 2 (n=12).
Immune-Mediated Colitis
OPDIVO can cause immune-mediated colitis. Monitor patients for signs and symptoms of colitis. Administer corticosteroids for Grade 2 (of more than 5 days duration), 3, or 4 colitis. Withhold OPDIVO monotherapy for Grade 2 or 3 and permanently discontinue for Grade 4 or recurrent colitis upon re-initiation of OPDIVO. When administered with YERVOY, withhold OPDIVO and YERVOY for Grade 2 and permanently discontinue for Grade 3 or 4 or recurrent colitis. In patients receiving OPDIVO monotherapy, immune-mediated colitis occurred in 2.9% (58/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated colitis occurred in 26% (107/407) of patients including three fatal cases.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe, life-threatening, or fatal (diarrhea of ≥7 stools above baseline, fever, ileus, peritoneal signs; Grade 3-5) immune-mediated enterocolitis occurred in 34 (7%) patients. Across all YERVOY-treated patients in that study (n=511), 5 (1%) developed intestinal perforation, 4 (0.8%) died as a result of complications, and 26 (5%) were hospitalized for severe enterocolitis.
Immune-Mediated Hepatitis
OPDIVO can cause immune-mediated hepatitis. Monitor patients for abnormal liver tests prior to and periodically during treatment. Administer corticosteroids for Grade 2 or greater transaminase elevations. Withhold for Grade 2 and permanently discontinue for Grade 3 or 4 immune-mediated hepatitis. In patients receiving OPDIVO monotherapy, immune-mediated hepatitis occurred in 1.8% (35/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated hepatitis occurred in 13% (51/407) of patients.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe, life-threatening, or fatal hepatotoxicity (AST or ALT elevations >5x the ULN or total bilirubin elevations >3x the ULN; Grade 3-5) occurred in 8 (2%) patients, with fatal hepatic failure in 0.2% and hospitalization in 0.4%.
Immune-Mediated Neuropathies
In a separate Phase 3 study of YERVOY 3 mg/kg, 1 case of fatal Guillain-Barré syndrome and 1 case of severe (Grade 3) peripheral motor neuropathy were reported.
Immune-Mediated Endocrinopathies
OPDIVO can cause immune-mediated hypophysitis, immune-mediated adrenal insufficiency, autoimmune thyroid disorders, and Type 1 diabetes mellitus. Monitor patients for signs and symptoms of hypophysitis, signs and symptoms of adrenal insufficiency, thyroid function prior to and periodically during treatment, and hyperglycemia. Administer hormone replacement as clinically indicated and corticosteroids for Grade 2 or greater hypophysitis. Withhold for Grade 2 or 3 and permanently discontinue for Grade 4 hypophysitis. Administer corticosteroids for Grade 3 or 4 adrenal insufficiency. Withhold for Grade 2 and permanently discontinue for Grade 3 or 4 adrenal insufficiency. Administer hormone-replacement therapy for hypothyroidism. Initiate medical management for control of hyperthyroidism. Withhold OPDIVO for Grade 3 and permanently discontinue for Grade 4 hyperglycemia.
In patients receiving OPDIVO monotherapy, hypophysitis occurred in 0.6% (12/1994) of patients. In patients receiving OPDIVO with YERVOY, hypophysitis occurred in 9% (36/407) of patients. In patients receiving OPDIVO monotherapy, adrenal insufficiency occurred in 1% (20/1994) of patients. In patients receiving OPDIVO with YERVOY, adrenal insufficiency occurred in 5% (21/407) of patients. In patients receiving OPDIVO monotherapy, hypothyroidism or thyroiditis resulting in hypothyroidism occurred in 9% (171/1994) of patients. Hyperthyroidism occurred in 2.7% (54/1994) of patients receiving OPDIVO monotherapy. In patients receiving OPDIVO with YERVOY, hypothyroidism or thyroiditis resulting in hypothyroidism occurred in 22% (89/407) of patients. Hyperthyroidism occurred in 8% (34/407) of patients receiving OPDIVO with YERVOY. In patients receiving OPDIVO monotherapy, diabetes occurred in 0.9% (17/1994) of patients. In patients receiving OPDIVO with YERVOY, diabetes occurred in 1.5% (6/407) of patients.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe to life-threatening immune-mediated endocrinopathies (requiring hospitalization, urgent medical intervention, or interfering with activities of daily living; Grade 3-4) occurred in 9 (1.8%) patients. All 9 patients had hypopituitarism, and some had additional concomitant endocrinopathies such as adrenal insufficiency, hypogonadism, and hypothyroidism. 6 of the 9 patients were hospitalized for severe endocrinopathies.
Immune-Mediated Nephritis and Renal Dysfunction
OPDIVO can cause immune-mediated nephritis. Monitor patients for elevated serum creatinine prior to and periodically during treatment. Administer corticosteroids for Grades 2-4 increased serum creatinine. Withhold OPDIVO for Grade 2 or 3 and permanently discontinue for Grade 4 increased serum creatinine. In patients receiving OPDIVO monotherapy, immune-mediated nephritis and renal dysfunction occurred in 1.2% (23/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated nephritis and renal dysfunction occurred in 2.2% (9/407) of patients.
Immune-Mediated Skin Adverse Reactions and Dermatitis
OPDIVO can cause immune-mediated rash, including Stevens-Johnson syndrome (SJS) and toxic epidermal necrolysis (TEN), some cases with fatal outcome. Administer corticosteroids for Grade 3 or 4 rash. Withhold for Grade 3 and permanently discontinue for Grade 4 rash. For symptoms or signs of SJS or TEN, withhold OPDIVO and refer the patient for specialized care for assessment and treatment; if confirmed, permanently discontinue. In patients receiving OPDIVO monotherapy, immune-mediated rash occurred in 9% (171/1994) of patients. In patients receiving OPDIVO with YERVOY, immune-mediated rash occurred in 22.6% (92/407) of patients.
In a separate Phase 3 study of YERVOY 3 mg/kg, severe, life-threatening, or fatal immune-mediated dermatitis (eg, Stevens-Johnson syndrome, toxic epidermal necrolysis, or rash complicated by full thickness dermal ulceration, or necrotic, bullous, or hemorrhagic manifestations; Grade 3-5) occurred in 13 (2.5%) patients. 1 (0.2%) patient died as a result of toxic epidermal necrolysis. 1 additional patient required hospitalization for severe dermatitis.
Immune-Mediated Encephalitis
OPDIVO can cause immune-mediated encephalitis. Evaluation of patients with neurologic symptoms may include, but not be limited to, consultation with a neurologist, brain MRI, and lumbar puncture. Withhold OPDIVO in patients with new-onset moderate to severe neurologic signs or symptoms and evaluate to rule out other causes. If other etiologies are ruled out, administer corticosteroids and permanently discontinue OPDIVO for immune-mediated encephalitis. In patients receiving OPDIVO monotherapy, encephalitis occurred in 0.2% (3/1994) of patients. Fatal limbic encephalitis occurred in one patient after 7.2 months of exposure despite discontinuation of OPDIVO and administration of corticosteroids. Encephalitis occurred in one patient receiving OPDIVO with YERVOY (0.2%) after 1.7 months of exposure.
Other Immune-Mediated Adverse Reactions
Based on the severity of adverse reaction, permanently discontinue or withhold treatment, administer high-dose corticosteroids, and, if appropriate, initiate hormone-replacement therapy. Across clinical trials of OPDIVO the following clinically significant immune-mediated adverse reactions occurred in <1.0% of patients receiving OPDIVO: uveitis, iritis, pancreatitis, facial and abducens nerve paresis, demyelination, polymyalgia rheumatica, autoimmune neuropathy, Guillain-Barré syndrome, hypopituitarism, systemic inflammatory response syndrome, gastritis, duodenitis, sarcoidosis, histiocytic necrotizing lymphadenitis (Kikuchi lymphadenitis), myositis, myocarditis, rhabdomyolysis, motor dysfunction, vasculitis, and myasthenic syndrome.
Infusion Reactions
OPDIVO can cause severe infusion reactions, which have been reported in <1.0% of patients in clinical trials. Discontinue OPDIVO in patients with Grade 3 or 4 infusion reactions. Interrupt or slow the rate of infusion in patients with Grade 1 or 2. In patients receiving OPDIVO monotherapy, infusion-related reactions occurred in 6.4% (127/1994) of patients. In patients receiving OPDIVO with YERVOY, infusion-related reactions occurred in 2.5% (10/407) of patients.
Complications of Allogeneic HSCT after OPDIVO
Complications, including fatal events, occurred in patients who received allogeneic HSCT after OPDIVO. Outcomes were evaluated in 17 patients from Checkmate 205 and 039, who underwent allogeneic HSCT after discontinuing OPDIVO (15 with reduced-intensity conditioning, 2 with myeloablative conditioning). Thirty-five percent (6/17) of patients died from complications of allogeneic HSCT after OPDIVO. Five deaths occurred in the setting of severe or refractory GVHD. Grade 3 or higher acute GVHD was reported in 29% (5/17) of patients. Hyperacute GVHD was reported in 20% (n=2) of patients. A steroid-requiring febrile syndrome, without an identified infectious cause, was reported in 35% (n=6) of patients. Two cases of encephalitis were reported: Grade 3 (n=1) lymphocytic encephalitis without an identified infectious cause, and Grade 3 (n=1) suspected viral encephalitis. Hepatic veno-occlusive disease (VOD) occurred in one patient, who received reduced-intensity conditioned allogeneic HSCT and died of GVHD and multi-organ failure. Other cases of hepatic VOD after reduced-intensity conditioned allogeneic HSCT have also been reported in patients with lymphoma who received a PD-1 receptor blocking antibody before transplantation. Cases of fatal hyperacute GVHD have also been reported. These complications may occur despite intervening therapy between PD-1 blockade and allogeneic HSCT.
Follow patients closely for early evidence of transplant-related complications such as hyperacute GVHD, severe (Grade 3 to 4) acute GVHD, steroid-requiring febrile syndrome, hepatic VOD, and other immune-mediated adverse reactions, and intervene promptly.
Embryo-Fetal Toxicity
Based on their mechanisms of action, OPDIVO and YERVOY can cause fetal harm when administered to a pregnant woman. Advise pregnant women of the potential risk to a fetus. Advise females of reproductive potential to use effective contraception during treatment with an OPDIVO- or YERVOY- containing regimen and for at least 5 months after the last dose of OPDIVO.
Lactation
It is not known whether OPDIVO or YERVOY is present in human milk. Because many drugs, including antibodies, are excreted in human milk and because of the potential for serious adverse reactions in nursing infants from an OPDIVO-containing regimen, advise women to discontinue breastfeeding during treatment. Advise women to discontinue nursing during treatment with YERVOY and for 3 months following the final dose.
Serious Adverse Reactions
In Checkmate 037, serious adverse reactions occurred in 41% of patients receiving OPDIVO (n=268). Grade 3 and 4 adverse reactions occurred in 42% of patients receiving OPDIVO . The most frequent Grade 3 and 4 adverse drug reactions reported in 2% to <5% of patients receiving OPDIVO were abdominal pain, hyponatremia, increased aspartate aminotransferase, and increased lipase. In Checkmate 066, serious adverse reactions occurred in 36% of patients receiving OPDIVO (n=206). Grade 3 and 4 adverse reactions occurred in 41% of patients receiving OPDIVO. The most frequent Grade 3 and 4 adverse reactions reported in ≥2% of patients receiving OPDIVO were gamma-glutamyltransferase increase (3.9%) and diarrhea (3.4%). In Checkmate 067, serious adverse reactions (73% and 37%), adverse reactions leading to permanent discontinuation (43% and 14%) or to dosing delays (55% and 28%), and Grade 3 or 4 adverse reactions (72% and 44%) all occurred more frequently in the OPDIVO plus YERVOY arm (n=313) relative to the OPDIVO arm (n=313). The most frequent (≥10%) serious adverse reactions in the OPDIVO plus YERVOY arm and the OPDIVO arm, respectively, were diarrhea (13% and 2.6%), colitis (10% and 1.6%), and pyrexia (10% and 0.6%). In Checkmate 017 and 057, serious adverse reactions occurred in 46% of patients receiving OPDIVO (n=418). The most frequent serious adverse reactions reported in at least 2% of patients receiving OPDIVO were pneumonia, pulmonary embolism, dyspnea, pyrexia, pleural effusion, pneumonitis, and respiratory failure. In Checkmate 025, serious adverse reactions occurred in 47% of patients receiving OPDIVO (n=406). The most frequent serious adverse reactions reported in ≥2% of patients were acute kidney injury, pleural effusion, pneumonia, diarrhea, and hypercalcemia. In Checkmate 205 and 039, adverse reactions leading to discontinuation occurred in 7% and dose delays due to adverse reactions occurred in 34% of patients (n=266). Serious adverse reactions occurred in 26% of patients. The most frequent serious adverse reactions reported in ≥1% of patients were pneumonia, infusion-related reaction, pyrexia, colitis or diarrhea, pleural effusion, pneumonitis, and rash. Eleven patients died from causes other than disease progression: 3 from adverse reactions within 30 days of the last OPDIVO dose, 2 from infection 8 to 9 months after completing OPDIVO, and 6 from complications of allogeneic HSCT. In Checkmate 141, serious adverse reactions occurred in 49% of patients receiving OPDIVO. The most frequent serious adverse reactions reported in at least 2% of patients receiving OPDIVO were pneumonia, dyspnea, respiratory failure, respiratory tract infection, and sepsis. In Checkmate 275, serious adverse reactions occurred in 54% of patients receiving OPDIVO (n=270). The most frequent serious adverse reactions reported in at least 2% of patients receiving OPDIVO were urinary tract infection, sepsis, diarrhea, small intestine obstruction, and general physical health deterioration.
Common Adverse Reactions
In Checkmate 037, the most common adverse reaction (≥20%) reported with OPDIVO (n=268) was rash (21%). In Checkmate 066, the most common adverse reactions (≥20%) reported with OPDIVO (n=206) vs dacarbazine (n=205) were fatigue (49% vs 39%), musculoskeletal pain (32% vs 25%), rash (28% vs 12%), and pruritus (23% vs 12%). In Checkmate 067, the most common (≥20%) adverse reactions in the OPDIVO plus YERVOY arm (n=313) were fatigue (59%), rash (53%), diarrhea (52%), nausea (40%), pyrexia (37%), vomiting (28%), and dyspnea (20%). The most common (≥20%) adverse reactions in the OPDIVO (n=313) arm were fatigue (53%), rash (40%), diarrhea (31%), and nausea (28%). In Checkmate 017 and 057, the most common adverse reactions (≥20%) in patients receiving OPDIVO (n=418) were fatigue, musculoskeletal pain, cough, dyspnea, and decreased appetite. In Checkmate 025, the most common adverse reactions (≥20%) reported in patients receiving OPDIVO (n=406) vs everolimus (n=397) were asthenic conditions (56% vs 57%), cough (34% vs 38%), nausea (28% vs 29%), rash (28% vs 36%), dyspnea (27% vs 31%), diarrhea (25% vs 32%), constipation (23% vs 18%), decreased appetite (23% vs 30%), back pain (21% vs 16%), and arthralgia (20% vs 14%). In Checkmate 205 and 039, the most common adverse reactions (≥20%) reported in patients receiving OPDIVO (n=266) were upper respiratory tract infection (44%), fatigue (39%), cough (36%), diarrhea (33%), pyrexia (29%), musculoskeletal pain (26%), rash (24%), nausea (20%) and pruritus (20%). In Checkmate 141, the most common adverse reactions (≥10%) in patients receiving OPDIVO were cough and dyspnea at a higher incidence than investigator’s choice. In Checkmate 275, the most common adverse reactions (≥ 20%) reported in patients receiving OPDIVO (n=270) were fatigue (46%), musculoskeletal pain (30%), nausea (22%), and decreased appetite (22%).. The most common adverse reactions (≥20%) in patients who received OPDIVO as a single agent were fatigue, rash, musculoskeletal pain, pruritus, diarrhea, nausea, asthenia, cough, dyspnea, constipation, decreased appetite, back pain, arthralgia, upper respiratory tract infection, pyrexia.
In a separate Phase 3 study of YERVOY 3 mg/kg, the most common adverse reactions (≥5%) in patients who received YERVOY at 3 mg/kg were fatigue (41%), diarrhea (32%), pruritus (31%), rash (29%), and colitis (8%).
Antwort auf Beitrag Nr.: 55.531.719 von Joschka Schröder am 16.08.17 00:19:48Wobei ich einen Endpunkt "progressionsfreies Überleben" bei einer Immuntherapie(-Kombi) immer noch als falsch gewählt ansehe.
Zu meinen Medarex-Investor-Zeiten (mir kommt immer noch die Galle hoch, dass ich damals so billig von Pien und BMS enteignet wurde, denn sonst könnte ich schon finanziell unabhängig sein) war bereits klar ersichtlich, dass ipilimumab keine statistisch signifikanten PFS Vorteile erzeugen konnte, aber das Gesamtüberleben sehr sehr positiv beeinflusst wurde. Etwas, was die Zulassungsbehörden damals noch nicht wirklich verstanden haben...
Ich könnte mir vorstellen, dass ähnliche Effekte bei einer Kombi wirken. anti-PD(L1) scheint ja mehr PFS Vorteile zu bedingen als anti-CTLA-4 (wo diese Vorteile kaum zu beobachten sind).
Für eine Kombi, bei der beide Kombipartner niedriger dosiert werden müssen, ist m.E. das Gesamtüberleben der richtigere Endpunkt.
Und klar, die Nebenwirkungen sind DER limitierende Faktor! Das ist das Thema um das es bei CTMX geht. Falls die CTMX probodies funktionieren, sollten diese kombiniert sowohl PFS als auch gigantische OS Vorteile bedingen.
Spannend wird es in den nächsten 12 Monaten allemal. Nichts oder Alles. Und wenn Alles, dann ist das sicherlich ein großes Vielfaches von Jetzt. Zudem könnte es eine Achterbahnfahrt werden (CX-2009 scheitert, CX-072 trotzdem Erfolg), also anschnallen.
Meine Paranoia werde ich bis dahin nicht ablegen und weiter nach allen Haaren in der Suppe suchen.
Zu meinen Medarex-Investor-Zeiten (mir kommt immer noch die Galle hoch, dass ich damals so billig von Pien und BMS enteignet wurde, denn sonst könnte ich schon finanziell unabhängig sein) war bereits klar ersichtlich, dass ipilimumab keine statistisch signifikanten PFS Vorteile erzeugen konnte, aber das Gesamtüberleben sehr sehr positiv beeinflusst wurde. Etwas, was die Zulassungsbehörden damals noch nicht wirklich verstanden haben...
Ich könnte mir vorstellen, dass ähnliche Effekte bei einer Kombi wirken. anti-PD(L1) scheint ja mehr PFS Vorteile zu bedingen als anti-CTLA-4 (wo diese Vorteile kaum zu beobachten sind).
Für eine Kombi, bei der beide Kombipartner niedriger dosiert werden müssen, ist m.E. das Gesamtüberleben der richtigere Endpunkt.
Und klar, die Nebenwirkungen sind DER limitierende Faktor! Das ist das Thema um das es bei CTMX geht. Falls die CTMX probodies funktionieren, sollten diese kombiniert sowohl PFS als auch gigantische OS Vorteile bedingen.
Spannend wird es in den nächsten 12 Monaten allemal. Nichts oder Alles. Und wenn Alles, dann ist das sicherlich ein großes Vielfaches von Jetzt. Zudem könnte es eine Achterbahnfahrt werden (CX-2009 scheitert, CX-072 trotzdem Erfolg), also anschnallen.
Meine Paranoia werde ich bis dahin nicht ablegen und weiter nach allen Haaren in der Suppe suchen.
Das Scheitern von BMS in 1st line RCC sehe ich persönlich mit einem lachenden Auge, da es meine EXEL (Cabozantinib) begünstigt. Die haben dann auch gleich gestern ihr 1st line filing auf Basis der CaboSun Daten Richtung FDA auf den Weg gebracht. So weit off topic... zurück zu der BMS Studie: ich denke, dass BMS trotz des Misserfolgs und trotz der erhöhten Nebenwirkungen in PFS auf Basis von OS Daten einen Zulassungsantrag in 1st line RCC stellen wird.
Perfekt wäre es, sollte die CTMX Technologie funktionieren, wenn man nicht nur Biologics maskieren könnte, sondern auch small molecules. Und noch perfekter, wenn dies sogar bei oraler Verabreichung gehen würde, sodass sogar z.B. orale TKIs maskiert werden könnten. Aber ich denke der Verdauungsapparat würde da sofort die Maskierung "verdauen" bzw. zerstören....
Perfekt wäre es, sollte die CTMX Technologie funktionieren, wenn man nicht nur Biologics maskieren könnte, sondern auch small molecules. Und noch perfekter, wenn dies sogar bei oraler Verabreichung gehen würde, sodass sogar z.B. orale TKIs maskiert werden könnten. Aber ich denke der Verdauungsapparat würde da sofort die Maskierung "verdauen" bzw. zerstören....
Antwort auf Beitrag Nr.: 55.541.493 von Ville7 am 17.08.17 09:36:51Korrektur: "trotz des Misserfolgs in PFS und trotz der erhöhten Nebenwirkungen" !
Auf der Unternehmenshomepage wurden der Audio Webcast sowie die Unternehmenspräsentation vom 16.08.2017 online gestellt.
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-irhome
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-irhome
Antwort auf Beitrag Nr.: 55.542.453 von biopadawan am 17.08.17 11:36:57
Yep, zum ersten Mal von Debanjan Ray präsentiert. Es war nichts unterschwellig Neues zu erfahren...
Zitat von biopadawan: Auf der Unternehmenshomepage wurden der Audio Webcast sowie die Unternehmenspräsentation vom 16.08.2017 online gestellt.
http://ir.cytomx.com/phoenix.zhtml?c=254195&p=irol-irhome
Yep, zum ersten Mal von Debanjan Ray präsentiert. Es war nichts unterschwellig Neues zu erfahren...
Eine Führungskraft hat CytomX verlassen: https://globenewswire.com/news-release/2017/08/17/1088296/0/…
Da kann man sich fragen, warum in dieser doch eigentlich spannenden Phase. Oder ist aus Forschungssicht der spannendste Teil bereits durch?
Da kann man sich fragen, warum in dieser doch eigentlich spannenden Phase. Oder ist aus Forschungssicht der spannendste Teil bereits durch?
Antwort auf Beitrag Nr.: 55.483.191 von Ville7 am 08.08.17 20:13:45Cytomx geht bei Proclaim-CX-072 übrigens nach dem klassischen 3 plus 3 Schema vor:
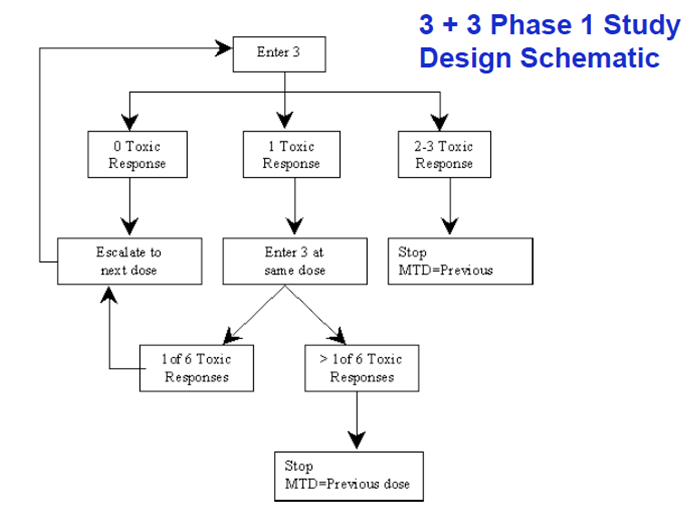
Ich persönlich stelle mir die Frage, was sie machen, wenn 30mg/kg noch keine Dosisbegrenzung darstellt. Noch höher dosieren oder bei 30mg/kg aufhören? Schließlich sollte bereits bei 10mg/kg die Vielfache Menge im Körper zirkulieren...

Ich persönlich stelle mir die Frage, was sie machen, wenn 30mg/kg noch keine Dosisbegrenzung darstellt. Noch höher dosieren oder bei 30mg/kg aufhören? Schließlich sollte bereits bei 10mg/kg die Vielfache Menge im Körper zirkulieren...
Zitat von Ville7: Wir sollten nun an der orangenen Linie sein:
@Joschka, es ist doch üblich die Anzahl der Patienten in den höheren Dosis-Gruppen zu erhöhen, oder? Wenn ich linear hochrechne wären wir mit multipler Dosierung frühestens sogar im Januar 2018 fertig bis zur höchsten Dosis in allen Gruppen - ohne expansion cohort Part D. Erste Daten zu ASCO 2018 sollten somit m.E. drin sein.
Antwort auf Beitrag Nr.: 55.556.016 von Ville7 am 18.08.17 20:42:01"die Vielfache Menge im Körper zirkulieren.." -> natürlich die vielfache Menge im Vgl. zu einem herkömmlichen PD-L1 AK.
Antwort auf Beitrag Nr.: 55.554.792 von fme_wo am 18.08.17 18:10:21Das dürfte auch der Grund für den heutigen abverkauf sein. Der gute Herr ist nun bei FPRX .
Es ist unklar, wie der Personalwechsel zu bewerten ist.
1) Irving bekommt bei FPT eine hierarchisch besser gestellte Position als er bei CytomX hatte. Bei FPT wird er Forschungschef.
2) Kavanaugh, Irvings (Research-)Chef bei CytomX, kam umgekehrt vor zwei Jahren von FPT zu CytomX.
3) Als Sandra Pool im Januar 2017 IMGN verließ (aus der Entfernung betrachtet eine schlechte Nachricht), notierte die IMGN-Aktie bei 2,85 USD. Einige Monate später lag der Kurs bei 8 USD.
Ich möchte nichts schönreden, aber ohne das passende Insiderwissen lassen sich vieldeutige Jobwechsel einfach nicht valide interpretieren (manchmal sind für einen Wechsel auch schlichtweg zwischenmenschliche Gründe oder ein besonderes finanzielles Angebot ausschlaggebend).
Insgesamt wäre es natürlich deutlich komfortabler, wenn der CTMX-Kurs stetig bergauf liefe. So bleibt das Ganze ein Nervenspiel, bei dem man letztlich dem eigenen Fachwissen vertrauen muss. Wie die Sache ausgehen wird, dürfte sich vermutlich Mitte 2018 zeigen.
PS: Roche ist über ihre VC-Tochter an CytomX beteiligt, wartet aber offensichtlich zunächst einmal die weiteren Entwicklungen ab, bevor möglicherweise eigene Kooperationsprojekte gestartet werden. Andere Unternehmen wie AbbVie führen gemeinsame Entwicklungsprojekte mit CytomX durch, haben sich jedoch nicht an CytomX beteiligt. Jeder setzt andere Schwerpunkte und betrachtet die Dinge aus einem anderen Blickwinkel. Bis zu einem gewissen Punkt ist dies durchaus wünschenswert, am Ende sollte das Investment aber schon eine deutliche Überrendite erzielen. Alles andere wäre eine einzige Enttäuschung.
1) Irving bekommt bei FPT eine hierarchisch besser gestellte Position als er bei CytomX hatte. Bei FPT wird er Forschungschef.
2) Kavanaugh, Irvings (Research-)Chef bei CytomX, kam umgekehrt vor zwei Jahren von FPT zu CytomX.
3) Als Sandra Pool im Januar 2017 IMGN verließ (aus der Entfernung betrachtet eine schlechte Nachricht), notierte die IMGN-Aktie bei 2,85 USD. Einige Monate später lag der Kurs bei 8 USD.
Ich möchte nichts schönreden, aber ohne das passende Insiderwissen lassen sich vieldeutige Jobwechsel einfach nicht valide interpretieren (manchmal sind für einen Wechsel auch schlichtweg zwischenmenschliche Gründe oder ein besonderes finanzielles Angebot ausschlaggebend).
Insgesamt wäre es natürlich deutlich komfortabler, wenn der CTMX-Kurs stetig bergauf liefe. So bleibt das Ganze ein Nervenspiel, bei dem man letztlich dem eigenen Fachwissen vertrauen muss. Wie die Sache ausgehen wird, dürfte sich vermutlich Mitte 2018 zeigen.
PS: Roche ist über ihre VC-Tochter an CytomX beteiligt, wartet aber offensichtlich zunächst einmal die weiteren Entwicklungen ab, bevor möglicherweise eigene Kooperationsprojekte gestartet werden. Andere Unternehmen wie AbbVie führen gemeinsame Entwicklungsprojekte mit CytomX durch, haben sich jedoch nicht an CytomX beteiligt. Jeder setzt andere Schwerpunkte und betrachtet die Dinge aus einem anderen Blickwinkel. Bis zu einem gewissen Punkt ist dies durchaus wünschenswert, am Ende sollte das Investment aber schon eine deutliche Überrendite erzielen. Alles andere wäre eine einzige Enttäuschung.
Ich brauch etwas mehr Informationen um das zu bewerten. Irving scheint ein reiner cancer immunology Mensch zu sein. Er war involviert in den discovery von atezolizumab.
Jetzt muss mir jemand weiterhelfen: hatte CTMX nicht mal verlauten lasen, dass CX072 sehr ähnlich zu atezolizumab sei? Oder bilde ich mir das ein?
In diesem Falle hätte Irving seine Aufgabe das discovery eines atezolizumab like Antikörpers für CTMX zu machen. Diese Aufgabe ist vollendet. Die weiteren Aktivitäten bei der CTMX scheinen weniger Richtung Immunoonkologie zu gehen. Wogegen FTP speziell an Immunotherapeuthika forscht und er sogar der Forschingschef wird.
Unter dieser Annahme würde mich dieser Wechsel nicht beunruhigen.
Jetzt muss mir jemand weiterhelfen: hatte CTMX nicht mal verlauten lasen, dass CX072 sehr ähnlich zu atezolizumab sei? Oder bilde ich mir das ein?
In diesem Falle hätte Irving seine Aufgabe das discovery eines atezolizumab like Antikörpers für CTMX zu machen. Diese Aufgabe ist vollendet. Die weiteren Aktivitäten bei der CTMX scheinen weniger Richtung Immunoonkologie zu gehen. Wogegen FTP speziell an Immunotherapeuthika forscht und er sogar der Forschingschef wird.
Unter dieser Annahme würde mich dieser Wechsel nicht beunruhigen.
Antwort auf Beitrag Nr.: 55.557.858 von Ville7 am 19.08.17 10:12:57Klar, das ist richtig: CX-072 steht in unmittelbarer Konkurrenz zu atezolizumab. CytomX hat mittlerweile einen anti-PD-L1-Probody (CX-072), einen anti-PD1-Probody (CX-188) und über BMY einen anti-CTLA-4-Probody im Programm. Mithin werden die drei (derzeit) wesentlichen I-O-Targets bereits durch Probodys adressiert. Weitere Immunokologika sind bereits selektiert, die dazugehörigen Targets wurden BMY im Vorfeld der Ausweitung des Kooperationsvertrags benannt (weil BMY gegen diese Targets keine eigenen Präparate entwickeln darf).
In seiner neuen Position bei FTP hätte Irving sicherlich mehr Gestaltungsmöglichkeiten.
Aber, wie bereits geschrieben, die konkreten Hintergründe für die berufliche Veränderung kennen wird nicht. Nach derzeitigem Kenntnisstand messe ich dem Wechsel keine große Bedeutung bei.
In seiner neuen Position bei FTP hätte Irving sicherlich mehr Gestaltungsmöglichkeiten.
Aber, wie bereits geschrieben, die konkreten Hintergründe für die berufliche Veränderung kennen wird nicht. Nach derzeitigem Kenntnisstand messe ich dem Wechsel keine große Bedeutung bei.
August 17, 2017
Five Prime Therapeutics Announces Addition of Bryan Irving, PhD, as Senior Vice President, Research
SOUTH SAN FRANCISCO, Calif., Aug. 17, 2017 (GLOBE NEWSWIRE) -- Five Prime Therapeutics, Inc. (Nasdaq:FPRX), a clinical-stage biotechnology company focused on discovering and developing innovative immuno-oncology protein therapeutics, today announced that Bryan Irving, Ph.D., will join Five Prime as Senior Vice President, Research, on Sept. 1, 2017.
"We are delighted to welcome Bryan as our Senior Vice President of Research, as he brings extensive immuno-oncology experience and a passion for innovative science that will be instrumental as he leads our Five Prime research group," said Lewis T. "Rusty" Williams, M.D., Ph.D., President and Chief Executive Officer of Five Prime. "Our unique Five Prime platform is producing exciting new targets and Bryan is an ideal scientist and executive to lead our research efforts to target key immune cells important in cancer and inflammation. In addition, among his most notable contributions was his principal inventorship and research leadership of atezolizumab (Tecentriq®), now approved for the treatment of several cancers. We look forward to his leadership as we continue to discover and develop innovative therapeutics."
"I'm thrilled to join Five Prime at this exciting time in the company's history," said Dr. Irving. "Five Prime has built an unparalleled proprietary library of more than 5,700 human extracellular proteins containing the majority of medically relevant protein drug targets. I look forward to applying my experience in immuno-oncology to this platform in an effort to identify new targets, which could translate into multiple therapeutic proteins."
Prior to joining Five Prime, Dr. Irving was at CytomX Therapeutics, where he most recently served as Vice President of Cancer Immunology, leading efforts to generate protease-activatable immunotherapies designed to mobilize anti-tumor immunity locally in the tumor microenvironment. His research has focused primarily on exploring ways to modulate T cell activity for therapeutic benefit in both autoimmune and oncology settings. Dr. Irving's doctoral work, performed in the laboratory of Dr. Art Weiss at University of California, San Francisco, pioneered the single-chain chimeric antigen receptor (CAR) technology now being used in patient's T cells to treat hematologic malignancies.
Following post-doctoral work at Harvard and UCSF on early T cell development, Dr. Irving joined Genentech in 2001 in the Department of Immunology to study mechanisms of immunological tolerance and strategies to restore regulation of autoreactive T cells in lupus and type 1 diabetes. In 2005, his interest shifted to the cancer/immune interface to understand why tumor-specific T cells were often unable to effectively respond to and eradicate tumor cells. These studies led to a program targeting PD-L1 that culminated in the development of the antibody MPDL3280A (atezolizumab). Dr. Irving left Genentech in 2013 to join CytomX Therapeutics.
Dr. Irving received a Ph.D. in Immunology from the University of California, San Francisco and a B.A. in Physiology from the University of California, Berkeley. In addition, Dr. Irving studied clarinet at the Eastman School of Music at the University of Rochester.
Five Prime Therapeutics Announces Addition of Bryan Irving, PhD, as Senior Vice President, Research
SOUTH SAN FRANCISCO, Calif., Aug. 17, 2017 (GLOBE NEWSWIRE) -- Five Prime Therapeutics, Inc. (Nasdaq:FPRX), a clinical-stage biotechnology company focused on discovering and developing innovative immuno-oncology protein therapeutics, today announced that Bryan Irving, Ph.D., will join Five Prime as Senior Vice President, Research, on Sept. 1, 2017.
"We are delighted to welcome Bryan as our Senior Vice President of Research, as he brings extensive immuno-oncology experience and a passion for innovative science that will be instrumental as he leads our Five Prime research group," said Lewis T. "Rusty" Williams, M.D., Ph.D., President and Chief Executive Officer of Five Prime. "Our unique Five Prime platform is producing exciting new targets and Bryan is an ideal scientist and executive to lead our research efforts to target key immune cells important in cancer and inflammation. In addition, among his most notable contributions was his principal inventorship and research leadership of atezolizumab (Tecentriq®), now approved for the treatment of several cancers. We look forward to his leadership as we continue to discover and develop innovative therapeutics."
"I'm thrilled to join Five Prime at this exciting time in the company's history," said Dr. Irving. "Five Prime has built an unparalleled proprietary library of more than 5,700 human extracellular proteins containing the majority of medically relevant protein drug targets. I look forward to applying my experience in immuno-oncology to this platform in an effort to identify new targets, which could translate into multiple therapeutic proteins."
Prior to joining Five Prime, Dr. Irving was at CytomX Therapeutics, where he most recently served as Vice President of Cancer Immunology, leading efforts to generate protease-activatable immunotherapies designed to mobilize anti-tumor immunity locally in the tumor microenvironment. His research has focused primarily on exploring ways to modulate T cell activity for therapeutic benefit in both autoimmune and oncology settings. Dr. Irving's doctoral work, performed in the laboratory of Dr. Art Weiss at University of California, San Francisco, pioneered the single-chain chimeric antigen receptor (CAR) technology now being used in patient's T cells to treat hematologic malignancies.
Following post-doctoral work at Harvard and UCSF on early T cell development, Dr. Irving joined Genentech in 2001 in the Department of Immunology to study mechanisms of immunological tolerance and strategies to restore regulation of autoreactive T cells in lupus and type 1 diabetes. In 2005, his interest shifted to the cancer/immune interface to understand why tumor-specific T cells were often unable to effectively respond to and eradicate tumor cells. These studies led to a program targeting PD-L1 that culminated in the development of the antibody MPDL3280A (atezolizumab). Dr. Irving left Genentech in 2013 to join CytomX Therapeutics.
Dr. Irving received a Ph.D. in Immunology from the University of California, San Francisco and a B.A. in Physiology from the University of California, Berkeley. In addition, Dr. Irving studied clarinet at the Eastman School of Music at the University of Rochester.
Antwort auf Beitrag Nr.: 55.559.655 von Joschka Schröder am 19.08.17 17:30:07Wie gesagt, irgendwie ist mir in Erinnerung, dass bei einer Präsentation gesagt wurde, CX-072 sei sehr ähnlich zu atezolizumab und damit war meines Wissens nicht (nur) das gemeinsame Target gemeint, sondern der generelle Aufbau, die spezifische Bindungsregion etc.. Daher war meine Vermutung, dass Irving diesen Job (einen geeigneten CX072 und in Folge einen geeigneten CX188 selektieren) vorwiegend geprägt hat - dafür ist er wahrscheinlich von Roche/Genentech gekommen.
Meines Wissens hat CTMX außer die PD1/PDL1 keine anderen reinen Immunoonkologie Projekte im Köcher. Ich vermute zudem, dass BMS sich neben anti-CTLA-4 alle möglichen weiteren aussichtsreichen Targets im Immunoonkologie reservieren hat lassen oder reservieren wird, da das deren strategische Domäne sein soll. Da ist für einen internen Forscher nicht mehr viel Gestaltungsfreiraum übrig.
Zudem, so habe ich es aus deren Präsentationen herausgehört, findet man gerade den PDC Weg als den eigentlichen Königsweg und sieht durch Öffnung von therapeuthischen Fenstern für bisher undrugable targets den größten Benefit der Technologie (so sie den funktioniert). Also klar ein Bereich indem Irving nicht der absolute Spezialist zu sein scheint bzw. in dem nicht sein Interesse primär zu liegen scheint....
Daher ist der Schritt für mich spekulativ nachvollziehbar, wobei man keineswegs andere Gründe ausschließen kann. Nervös werde ich, wenn weitere hochrangige Personen abziehen....
Meines Wissens hat CTMX außer die PD1/PDL1 keine anderen reinen Immunoonkologie Projekte im Köcher. Ich vermute zudem, dass BMS sich neben anti-CTLA-4 alle möglichen weiteren aussichtsreichen Targets im Immunoonkologie reservieren hat lassen oder reservieren wird, da das deren strategische Domäne sein soll. Da ist für einen internen Forscher nicht mehr viel Gestaltungsfreiraum übrig.
Zudem, so habe ich es aus deren Präsentationen herausgehört, findet man gerade den PDC Weg als den eigentlichen Königsweg und sieht durch Öffnung von therapeuthischen Fenstern für bisher undrugable targets den größten Benefit der Technologie (so sie den funktioniert). Also klar ein Bereich indem Irving nicht der absolute Spezialist zu sein scheint bzw. in dem nicht sein Interesse primär zu liegen scheint....
Daher ist der Schritt für mich spekulativ nachvollziehbar, wobei man keineswegs andere Gründe ausschließen kann. Nervös werde ich, wenn weitere hochrangige Personen abziehen....
8th World ADC San Diego - 20.-22.9.2017
http://worldadc-usa.com/program/agenda/22.9. 12:00 CX-2009: A Probody™ Drug Conjugate
Targeting CD166
• Probody drug conjugate technology enables
the targeting of high expression tumor
antigens such as CD166 regardless of normal
tissue expression
• Preclinical data show high CD166 expression
across multiple tumor types, potent
anti-tumor activity and safety in non-human
primates at clinically relevant doses
• The Phase I clinical study design for CX-2009
will be presented
Jason Sagert, Senior Scientist, CymtomX

Trial Updates:
CX-072 (PD-L1) PH1/2 Update: recruiting sites from 30 of 30 now (8 over last month & in EU now)
CX-2009 (PDC in s. tumors) PH 1/2 Update: recruiting sites from 5 of 5 to 6 of 6
CX-072 (PD-L1) PH1/2 Update: recruiting sites from 30 of 30 now (8 over last month & in EU now)
CX-2009 (PDC in s. tumors) PH 1/2 Update: recruiting sites from 5 of 5 to 6 of 6
Outlook:
• HERCULES Phase III data anticipated to be available in late Q3 2017
• Results from Phase I with caplacizumab in Japanese healthy volunteers planned
in Q4 2017
• Preparations for commercialisation of caplacizumab ongoing
• In Q4 2017, we expect to file for regulatory approvals
– to start a trial with ALX-0171 in Japanese infants infected with RSV
– to study the use of ALX-0171 in adults who have undergone a stem cell transplant and
have become infected with RSV
• The STEADY trial with vobarilizumab in SLE will report data in H1 2018
• The RESPIRE trial with ALX-0171 in RSV infected infants should report data in H2 2018
• Cash burn for full year 2017 is now forecast to be €65-75 million
• HERCULES Phase III data anticipated to be available in late Q3 2017
• Results from Phase I with caplacizumab in Japanese healthy volunteers planned
in Q4 2017
• Preparations for commercialisation of caplacizumab ongoing
• In Q4 2017, we expect to file for regulatory approvals
– to start a trial with ALX-0171 in Japanese infants infected with RSV
– to study the use of ALX-0171 in adults who have undergone a stem cell transplant and
have become infected with RSV
• The STEADY trial with vobarilizumab in SLE will report data in H1 2018
• The RESPIRE trial with ALX-0171 in RSV infected infants should report data in H2 2018
• Cash burn for full year 2017 is now forecast to be €65-75 million
Antwort auf Beitrag Nr.: 55.595.731 von biopadawan am 25.08.17 09:44:02Dem Augenschein nach war Dein letzter Beitrag für den Ablynx-Thread bestimmt.
Zu CytomX: Positiv, dass nun alle vorgesehenen Kliniken Patienten für die CX-072- und die CX-2009-Studien rekrutieren. Das Studientempo ist bislang top.
Zu CytomX: Positiv, dass nun alle vorgesehenen Kliniken Patienten für die CX-072- und die CX-2009-Studien rekrutieren. Das Studientempo ist bislang top.
Auch wenn man nicht viel darauf geben darf, ist es immer wieder interessant zu lesen, was Analysten schreiben. Jefferies nennt in ihrer Studie vom 25.8.2017 ein Kursziel von 25 USD. Das Kursziel der Bank of America vom 8.8.2017 lautete 30 USD, das derzeitige Consensus-Zeil aller Analysten 29 USD.
Consensus Ratings for CytomX Therapeutics (NASDAQ:CTMX)
Ratings Breakdown: 1 Sell Rating, 2 Hold Ratings, 5 Buy Ratings
Consensus Rating: Buy (Score: 2.50)
Consensus Price Target: $27.75 (73.87% upside)
Analysts' Ratings History for CytomX Therapeutics (NASDAQ:CTMX)
Show:
Date Firm Action Rating Price Target Impact on Share Price Details
8/25/2017 Jefferies Group LLC Set Price Target Buy $25.00 N/A View Rating Details
8/9/2017 Bank of America Corporation Reiterated Rating Buy $28.00 -> $30.00 High View Rating Details
8/8/2017 Cann Reiterated Rating Hold High View Rating Details
8/8/2017 Cowen and Company Reiterated Rating Buy High View Rating Details
5/8/2017 HC Wainwright Reiterated Rating Buy Low View Rating Details
3/20/2017 Instinet Boost Price Target Sell $21.00 -> $32.00 Medium View Rating Details
3/4/2017 Oppenheimer Holdings, Inc. Reiterated Rating Hold N/A View Rating Details
3/1/2017 Nomura Initiated Coverage Buy N/A View Rating Details
Ratings Breakdown: 1 Sell Rating, 2 Hold Ratings, 5 Buy Ratings
Consensus Rating: Buy (Score: 2.50)
Consensus Price Target: $27.75 (73.87% upside)
Analysts' Ratings History for CytomX Therapeutics (NASDAQ:CTMX)
Show:
Date Firm Action Rating Price Target Impact on Share Price Details
8/25/2017 Jefferies Group LLC Set Price Target Buy $25.00 N/A View Rating Details
8/9/2017 Bank of America Corporation Reiterated Rating Buy $28.00 -> $30.00 High View Rating Details
8/8/2017 Cann Reiterated Rating Hold High View Rating Details
8/8/2017 Cowen and Company Reiterated Rating Buy High View Rating Details
5/8/2017 HC Wainwright Reiterated Rating Buy Low View Rating Details
3/20/2017 Instinet Boost Price Target Sell $21.00 -> $32.00 Medium View Rating Details
3/4/2017 Oppenheimer Holdings, Inc. Reiterated Rating Hold N/A View Rating Details
3/1/2017 Nomura Initiated Coverage Buy N/A View Rating Details
What are analysts saying about CytomX Therapeutics stock?
Here are some recent quotes from research analysts about CytomX Therapeutics stock:
1. Cann analysts commented, "Loss per share was $0.69, compared to our estimate of $0.56. This was the result of higher than expected R&D expense of $28.1 million compared to our estimate of $15.2 million, which resulted from a $10 million payment to UCSB for a sublicense payment. This was partially offset by higher than estimated revenue of $8.8 million compared to our estimated $1.0 million." (8/8/2017)
2. Cowen and Company analysts commented, "CTMX announced that the first patient in CX-2009’s (CD166 PDC) Phase I trial has." (6/28/2017)
3. According to Zacks Investment Research, "CytomX Therapeutics, Inc. is an oncology focused biopharmaceutical company. The Company is engaged in developing Probody(TM) therapeutics for the treatment of cancer. Its pipeline focuses areas consist of Precision cancer immunotherapy and Probody drug conjugates. CytomX Therapeutics, Inc. is headquartered in South San Francisco, California. " (5/29/2017)
4. HC Wainwright analysts commented, "Before the market opened on May 5, TG reported 1Q17 results. The company recently reported preliminary data from its ongoing Phase II study of TG-1101 in patients with relapsing forms of multiple sclerosis. Preliminary results indicated that TG-1101 was well tolerated with no Grade III/IV adverse events (AEs) observed and the most commonly reported AE being infusion-related reactions, with median time on study of five months. All patients achieved the primary endpoint of greater than 95% B-cell depletion by four weeks. The median B-cell depletion at week four was reported to be 99% after two infusions with a cumulative dose of 600 mg, which compares favorably to other anti-CD20 monoclonal antibodies (mAbs). Management indicated that additional data from the ongoing Phase II study will be reported later this year and that the company is on track to initiate a Phase III trial in MS in 2H17." (5/8/2017)
5. Instinet analysts commented, "We are initiating on CytomX Therapeutics (CTMX) with a Buy rating and $21 12-month target price. We recommend owning CTMX shares ahead of 2H17 and 2018 data readouts for CX-072 and CX-2009, which we anticipate will validate the platforms MOA and frame breadth of utility. We remain focused on CX-072 in combo with Zelboraf, on the belief that a strong signal here will provide clear proof-of-concept for the approach, thus limiting downside risk. We look to CX-2009 as an opportunity for potentially significant upside given the high unmet need of solid tumors that express CD166. The potential for value to be ascribed to CTMX pipeline candidates presents upside potential to our estimates." (3/1/2017)
Here are some recent quotes from research analysts about CytomX Therapeutics stock:
1. Cann analysts commented, "Loss per share was $0.69, compared to our estimate of $0.56. This was the result of higher than expected R&D expense of $28.1 million compared to our estimate of $15.2 million, which resulted from a $10 million payment to UCSB for a sublicense payment. This was partially offset by higher than estimated revenue of $8.8 million compared to our estimated $1.0 million." (8/8/2017)
2. Cowen and Company analysts commented, "CTMX announced that the first patient in CX-2009’s (CD166 PDC) Phase I trial has." (6/28/2017)
3. According to Zacks Investment Research, "CytomX Therapeutics, Inc. is an oncology focused biopharmaceutical company. The Company is engaged in developing Probody(TM) therapeutics for the treatment of cancer. Its pipeline focuses areas consist of Precision cancer immunotherapy and Probody drug conjugates. CytomX Therapeutics, Inc. is headquartered in South San Francisco, California. " (5/29/2017)
4. HC Wainwright analysts commented, "Before the market opened on May 5, TG reported 1Q17 results. The company recently reported preliminary data from its ongoing Phase II study of TG-1101 in patients with relapsing forms of multiple sclerosis. Preliminary results indicated that TG-1101 was well tolerated with no Grade III/IV adverse events (AEs) observed and the most commonly reported AE being infusion-related reactions, with median time on study of five months. All patients achieved the primary endpoint of greater than 95% B-cell depletion by four weeks. The median B-cell depletion at week four was reported to be 99% after two infusions with a cumulative dose of 600 mg, which compares favorably to other anti-CD20 monoclonal antibodies (mAbs). Management indicated that additional data from the ongoing Phase II study will be reported later this year and that the company is on track to initiate a Phase III trial in MS in 2H17." (5/8/2017)
5. Instinet analysts commented, "We are initiating on CytomX Therapeutics (CTMX) with a Buy rating and $21 12-month target price. We recommend owning CTMX shares ahead of 2H17 and 2018 data readouts for CX-072 and CX-2009, which we anticipate will validate the platforms MOA and frame breadth of utility. We remain focused on CX-072 in combo with Zelboraf, on the belief that a strong signal here will provide clear proof-of-concept for the approach, thus limiting downside risk. We look to CX-2009 as an opportunity for potentially significant upside given the high unmet need of solid tumors that express CD166. The potential for value to be ascribed to CTMX pipeline candidates presents upside potential to our estimates." (3/1/2017)
Antwort auf Beitrag Nr.: 55.607.645 von 007coolinvestor am 27.08.17 21:43:40CEO hat mal wieder 18 K Aktien aus Optionen verscherbelt.
Man stellt sich schon die Frage, weshalb diese Verkäufe erfolgen. Kann natürlich auch ganz profane Gründe haben...
Wünschenswert wäre es natürlich gewesen, wenn diese Verkäufe nach anlaufen der Studien zurückgegangen wären.
Man stellt sich schon die Frage, weshalb diese Verkäufe erfolgen. Kann natürlich auch ganz profane Gründe haben...
Wünschenswert wäre es natürlich gewesen, wenn diese Verkäufe nach anlaufen der Studien zurückgegangen wären.
Antwort auf Beitrag Nr.: 55.651.514 von biopadawan am 01.09.17 23:04:47Eine wesentliche Gehaltskomponente besteht nun mal aus Aktienoptionen, wie dies bei US-Biotechs üblich ist. Insoweit ist es ein normaler Vorgang, dass in regelmäßigen Abständen Optionen zu Geld gemacht werden. Wenn CEO und CFO bei Börsenkursen um 15 USD und 16 USD Optionen in Aktien gewandelt und diese anschließend verkauft haben, dann werden Sie es auch bei Kursen um 17,50 USD oder 19 USD tun. Optionen besitzen die Burschen (leider) genug.
Altaktionär Third Rock Ventures wird mit Sicherheit auch bald wieder verkaufen und Frederic Gluck (letzte Verkäufe bei 14,61 USD) ist eigentlich auch schon länger überreif.
Die Aktienverkäufe werden erst dann abnehmen, wenn der Hebel der Optionen geringer wird. Die derzeitige Möglichkeit, Aktien (via Optionen aus der Prä-IPO-Zeit) zu zweistelligen Centpreisen zu beziehen und anschließend zu meinetwegen 17,50 USD zu verkaufen, ist deutlich verlockender als dies z.B. bei Bezugspreisen von 12 USD oder 15 USD der Fall wäre.
Altaktionär Third Rock Ventures wird mit Sicherheit auch bald wieder verkaufen und Frederic Gluck (letzte Verkäufe bei 14,61 USD) ist eigentlich auch schon länger überreif.
Die Aktienverkäufe werden erst dann abnehmen, wenn der Hebel der Optionen geringer wird. Die derzeitige Möglichkeit, Aktien (via Optionen aus der Prä-IPO-Zeit) zu zweistelligen Centpreisen zu beziehen und anschließend zu meinetwegen 17,50 USD zu verkaufen, ist deutlich verlockender als dies z.B. bei Bezugspreisen von 12 USD oder 15 USD der Fall wäre.
Antwort auf Beitrag Nr.: 55.651.712 von Joschka Schröder am 02.09.17 00:09:03Was soch m.E. Führungskräfte Aktien verkaufen, objektiv die Entwicklung nachwievor seitern kann und das Ergebnis nicht klar absehbar ist.
Sorry, das ist ja überhaupt kein deutsch.
Ich wollte sagen, wenn Führungskräfte Aktien verkaufen, sagt das zumindest aus, dass aus Sicht der Insider die Entwicklung nach wie vor objektiv scheitern kann.
Ich wollte sagen, wenn Führungskräfte Aktien verkaufen, sagt das zumindest aus, dass aus Sicht der Insider die Entwicklung nach wie vor objektiv scheitern kann.
Antwort auf Beitrag Nr.: 55.655.237 von 007coolinvestor am 02.09.17 23:25:25CEO und CFO sind keine Hellseher. Natürlich kann eine derartige Technik scheitern! Andernfalls wäre ich zu 100 % investiert und hätte erstmals in meinem Leben zusätzlich einen Kredit aufgenommen, um mehr CTMX-Aktien kaufen zu können.
Antwort auf Beitrag Nr.: 55.651.712 von Joschka Schröder am 02.09.17 00:09:03
2 Anmerkungen
Die Aktienverkäufe werden erst dann abnehmen, wenn der Hebel der Optionen geringer wird. Die derzeitige Möglichkeit, Aktien (via Optionen aus der Prä-IPO-Zeit) zu zweistelligen Centpreisen zu beziehen und anschließend zu meinetwegen 17,50 USD zu verkaufen, ist deutlich verlockender als dies z.B. bei Bezugspreisen von 12 USD oder 15 USD der Fall wäre
_______________________________________________________________________
Das ist natürlich so.
Aber ich glaube dass da Viele auch nicht sooo die Vorstellung der Risiken solcher "Seed" Aktivitäten haben,
die teilweise drastisch falsch eingeschätzt/unterschätzt werden.
Auch wenn man nicht viel darauf geben darf, ist es immer wieder interessant zu lesen, was Analysten schreiben. Jefferies nennt in ihrer Studie vom 25.8.2017 ein Kursziel von 25 USD. Das Kursziel der Bank of America vom 8.8.2017 lautete 30 USD, das derzeitige Consensus-Zeil aller Analysten 29 USD.
____________________________________________________________________________
hmmmmm,
naja.
Ich denke solche "Kursziele" können sehr Viel zu sagen haben, müssen aber gar Nichts.
Die Sache und Frage ist eben Letztlich ob man Die Begründung/Recherchehintergründe/Aufgestelltes Szenario usw kennt.
Wenn ja, und entsprechende Mühe vorausgesetzt, kann man sicher auch mehr zur Berechtigung des Kursziels, oder auch nicht, sagen;
aber Ohne ist das einfach -Diesbezüglich-Letztlich mehr eine Art Kaffeesatzlesen.
Anders gesagt: wenn du das Paper nicht richtig, in full, kennst halte ich die Aussage(kraft) nur für sehr, sehr begrenzt
2 Anmerkungen
Die Aktienverkäufe werden erst dann abnehmen, wenn der Hebel der Optionen geringer wird. Die derzeitige Möglichkeit, Aktien (via Optionen aus der Prä-IPO-Zeit) zu zweistelligen Centpreisen zu beziehen und anschließend zu meinetwegen 17,50 USD zu verkaufen, ist deutlich verlockender als dies z.B. bei Bezugspreisen von 12 USD oder 15 USD der Fall wäre
_______________________________________________________________________
Das ist natürlich so.
Aber ich glaube dass da Viele auch nicht sooo die Vorstellung der Risiken solcher "Seed" Aktivitäten haben,
die teilweise drastisch falsch eingeschätzt/unterschätzt werden.
Auch wenn man nicht viel darauf geben darf, ist es immer wieder interessant zu lesen, was Analysten schreiben. Jefferies nennt in ihrer Studie vom 25.8.2017 ein Kursziel von 25 USD. Das Kursziel der Bank of America vom 8.8.2017 lautete 30 USD, das derzeitige Consensus-Zeil aller Analysten 29 USD.
____________________________________________________________________________
hmmmmm,
naja.
Ich denke solche "Kursziele" können sehr Viel zu sagen haben, müssen aber gar Nichts.
Die Sache und Frage ist eben Letztlich ob man Die Begründung/Recherchehintergründe/Aufgestelltes Szenario usw kennt.
Wenn ja, und entsprechende Mühe vorausgesetzt, kann man sicher auch mehr zur Berechtigung des Kursziels, oder auch nicht, sagen;
aber Ohne ist das einfach -Diesbezüglich-Letztlich mehr eine Art Kaffeesatzlesen.
Anders gesagt: wenn du das Paper nicht richtig, in full, kennst halte ich die Aussage(kraft) nur für sehr, sehr begrenzt
Antwort auf Beitrag Nr.: 55.484.463 von Joschka Schröder am 08.08.17 23:33:02Zu der Thematik Insidersales: Es ist letztlich so, dass man Insidersales erst ab einer gewissen Größenordnung (in negativer Hinsicht) bewerten kann und Schlussfolgerungen für sein eigenes Investment ziehen sollte.
Bisher sind diese bei CTMX nicht auffällig und relativ konstant, so dass dies an der grundsätzlichen Situation auch nichts ändert. Nervös werde ich erst, wenn diese sich häufen.
Sicherlich wäre es wünschenswert gewesen, wenn der CEO hiervon bereits absieht, weil eine klare Linie bei den Studien erkennbar ist. Dies ist wohl bislang nicht der Fall, was jedoch nicht zwingend negativ sein muss.
Im Übrigen würde mich interessieren, ob du Joschka, mittlerweile einen Blick auf Affimed geworfen und eine vorläufige Einschätzung hierzu hast. Wie schätzt du insbesondere die Aussichten des Assets AFM 13 ein? Sicherlich auch ein sehr interessanter Titel mit einem interessanten wissenschaftlichen Ansatz (Neben PIRS, was ich auch auf dem Radar habe). Beide vorstehende Unternehmen fallen wohl unter die Rubrik außergewöhnlicher wissenschaftlicher Ansatz mit damit ggf. einhergehender Überrendite.
Viele Grüße
Bisher sind diese bei CTMX nicht auffällig und relativ konstant, so dass dies an der grundsätzlichen Situation auch nichts ändert. Nervös werde ich erst, wenn diese sich häufen.
Sicherlich wäre es wünschenswert gewesen, wenn der CEO hiervon bereits absieht, weil eine klare Linie bei den Studien erkennbar ist. Dies ist wohl bislang nicht der Fall, was jedoch nicht zwingend negativ sein muss.
Im Übrigen würde mich interessieren, ob du Joschka, mittlerweile einen Blick auf Affimed geworfen und eine vorläufige Einschätzung hierzu hast. Wie schätzt du insbesondere die Aussichten des Assets AFM 13 ein? Sicherlich auch ein sehr interessanter Titel mit einem interessanten wissenschaftlichen Ansatz (Neben PIRS, was ich auch auf dem Radar habe). Beide vorstehende Unternehmen fallen wohl unter die Rubrik außergewöhnlicher wissenschaftlicher Ansatz mit damit ggf. einhergehender Überrendite.
Viele Grüße
Antwort auf Beitrag Nr.: 55.657.884 von biopadawan am 03.09.17 18:14:45Es fällt mir sehr schwer, mir ein Urteil zu Affimed zu bilden. Den therapeutischen Ansatz via angeborener Immunabwehr verfolgen nur sehr wenige Unternehmen, hinsichtlich klinischer Daten herrscht bislang nahezu Fehlanzeige. Sollte die Stimulation natürlicher Killerzellen zu den gewünschten Ergebnissen führen, hätte Affimed aufgrund der geringen Marktkapitalisierung natürlich einen enormen Hebel. Da Affimed andererseits auch bispezif. Antikörper im Programm hat, die an CD3 binden, Affimed also nicht ausschließlich auf die NK-Schiene setzt, besitzt der Aktienkurs ein gewisses Sicherheitsnetz für den Fall, dass die Rekrutierung natürlicher Killerzellen nicht zum gewünschten Erfolg führt (d.h. der Aktienkurs würde nicht auf Null fallen). Vermutlich fährt man am besten damit, Affimed als einen Optionsschein zu betrachten und entsprechend vorsichtig zu agieren.
Und, jemand überrascht?
CFO hat mal wieder 2.500 Aktien (zu 17,17 USD) verkauft, gleichzeitig hat der CEO 9.930 Billigoptionen in Aktien gewandelt und anschließend die fast kostenlos bezogenen Aktien verkauft.
Diese Prä-IPO-Optionsprogramme sind immer ein Übel.
Ich rechne für morgen mit weiteren Verkaufsmitteilungen. Überraschend ist einzig, dass ThirdRockVentures noch durchhalten.
CFO hat mal wieder 2.500 Aktien (zu 17,17 USD) verkauft, gleichzeitig hat der CEO 9.930 Billigoptionen in Aktien gewandelt und anschließend die fast kostenlos bezogenen Aktien verkauft.
Diese Prä-IPO-Optionsprogramme sind immer ein Übel.
Ich rechne für morgen mit weiteren Verkaufsmitteilungen. Überraschend ist einzig, dass ThirdRockVentures noch durchhalten.
Antwort auf Beitrag Nr.: 55.657.884 von biopadawan am 03.09.17 18:14:45Noch off topic zu Affimed (vielleicht werde ich zu Affimed Unternehmen, wenn mehr Zeit ist, einen eigenen Thread beginnen): Es ist interessant zu sehen, dass sich mehr und mehr onkologisch tätige Pharma-/Biotech-Unternehmen mit Mechanismen der angeborenen Immunabwehr beschäftigen. Bislang waren auf diesem Gebiet nur Exoten wie Affimed tätig. Jüngstes Beispiel: Merck (USA) übernimmt das deutsche Biotech-Start up Rigontec (Ausgliederung der Uni Bonn, gerade mal 3 Jahre alt, bearbeitet den RIG-I-pathway) für 150 Mio. USD Cash plus bis zu 453 Mio. USD Meilensteinzahlungen.
Antwort auf Beitrag Nr.: 55.675.764 von Joschka Schröder am 06.09.17 00:39:41
Ich habe mal nachgeschaut: Der CEO hält Aktien im Wert von USD 2,6 Mio. Dieser Wert wird sich innerhalb von kurzer Zeit vervielfachen, wenn die klinischen Daten positiv ausfallen. Also wird er sich sagen, im positiven Fall bin ich finanziell durch und deshalb macht es für ihn Sinn ansonsten Kasse zu machen.
Anders ist das beim CFO, der die äusserst saftigen Pharmadeals eingetütet hat, die eine Bewertung reflektieren, die deutlich höher ist als die aktuelle Börsenbewertung. Er hält lediglich Aktien im Werte von USD 0,3 Mio. an Aktien.
Am Ende spielen bei diesen Dingen persönliche Umstände eine Rolle, die man nicht beurteilen kann. Ich würde die Herren mal befragen wollen, warum sie stets verkaufen. Bei britischen UnTernehmen habe ich es schon gesehen, dass die Manager Begründungen abgeben (zB Finanzierung einer Scheidung).
Shares und Optionen des Vorstands
Es sieht immer schlecht aus, wenn der Vorstand regelmäßig Kasse macht. Echte Unternehmer würden das nicht tun, aber wir haben es hier mit intelligenten Wissenschaftlern und ihrem Umfeld zu tun, die denken da glaube ich einfach anders als ein Jeff Bezos oder Bill Gates. Ich habe mal nachgeschaut: Der CEO hält Aktien im Wert von USD 2,6 Mio. Dieser Wert wird sich innerhalb von kurzer Zeit vervielfachen, wenn die klinischen Daten positiv ausfallen. Also wird er sich sagen, im positiven Fall bin ich finanziell durch und deshalb macht es für ihn Sinn ansonsten Kasse zu machen.
Anders ist das beim CFO, der die äusserst saftigen Pharmadeals eingetütet hat, die eine Bewertung reflektieren, die deutlich höher ist als die aktuelle Börsenbewertung. Er hält lediglich Aktien im Werte von USD 0,3 Mio. an Aktien.
Am Ende spielen bei diesen Dingen persönliche Umstände eine Rolle, die man nicht beurteilen kann. Ich würde die Herren mal befragen wollen, warum sie stets verkaufen. Bei britischen UnTernehmen habe ich es schon gesehen, dass die Manager Begründungen abgeben (zB Finanzierung einer Scheidung).
Antwort auf Beitrag Nr.: 55.681.134 von Joschka Schröder am 06.09.17 16:41:00Hallo Joschka,
einen eigenen Thread zu Affimed wäre super. Einige WO-User hier halten AFMD schon lange und haben den schmerzlichen Absturz im Kurs mitgemacht. Schlechte Nachrichten gab es ja nicht wirklich, aber ein maßlos überteuertes IPO. Was mir fehlt sind die Partnerschaften für eines der Programme. Neben AFM11 und AFM13, gab bzw. gibt es ja noch AFM21,22,23 und jetzt AFM24 und AFM26 ohne klinische Entwicklung. Mit der 100%igen Tochter Abcheck besitzt man ja zahlreiche Kontakte und Partnerschaften jedoch werden hier keine Größenordnungen der Deals bekannt gegeben. Bilanziell wirken sich die Verluste/Gewinne der Tochter kaum aus. Dann gibt es noch die Beteiligung an Amphivena Therapeutics, wo AFMD beständig Geld im geringen Umfang nachschießt und Janssen beim Hoffnungsträger AMV564 Mitte des Jahres ausgestiegen ist.
Zu den Verkäufen der Insider bei CTMX würde ich das auch nicht überbewerten. Sicherlich wäre ein halten der Aktien oder Käufe des Managements positiv zu bewerten. Vor Rückschlägen in der klinischen Entwicklung sichert das aber auch nicht. Es ist jetzt auch nicht so selten, dass die CFOs wenig bis gar keine Aktien halten.
Gruß
McNay
einen eigenen Thread zu Affimed wäre super. Einige WO-User hier halten AFMD schon lange und haben den schmerzlichen Absturz im Kurs mitgemacht. Schlechte Nachrichten gab es ja nicht wirklich, aber ein maßlos überteuertes IPO. Was mir fehlt sind die Partnerschaften für eines der Programme. Neben AFM11 und AFM13, gab bzw. gibt es ja noch AFM21,22,23 und jetzt AFM24 und AFM26 ohne klinische Entwicklung. Mit der 100%igen Tochter Abcheck besitzt man ja zahlreiche Kontakte und Partnerschaften jedoch werden hier keine Größenordnungen der Deals bekannt gegeben. Bilanziell wirken sich die Verluste/Gewinne der Tochter kaum aus. Dann gibt es noch die Beteiligung an Amphivena Therapeutics, wo AFMD beständig Geld im geringen Umfang nachschießt und Janssen beim Hoffnungsträger AMV564 Mitte des Jahres ausgestiegen ist.
Zu den Verkäufen der Insider bei CTMX würde ich das auch nicht überbewerten. Sicherlich wäre ein halten der Aktien oder Käufe des Managements positiv zu bewerten. Vor Rückschlägen in der klinischen Entwicklung sichert das aber auch nicht. Es ist jetzt auch nicht so selten, dass die CFOs wenig bis gar keine Aktien halten.
Gruß
McNay
Antwort auf Beitrag Nr.: 55.681.773 von JOWCOL am 06.09.17 17:47:38Natürlich stören mich die Verkäufe auch. Zumindest kann man daraus ableiten, dass wohl kein neuer Deal unmittelbar bevorsteht. Ich habe mir allerdings während der vergangenen 20 Jahre abgewöhnt, aus derartigen Verkäufen weitergehende Schlussfolgerungen ziehen zu wollen.
Bei 17 USD dürfte der Kurs jetzt erst einmal konsolidieren. Ein Kursrücksetzer würde mich nicht überraschen.
Bei 17 USD dürfte der Kurs jetzt erst einmal konsolidieren. Ein Kursrücksetzer würde mich nicht überraschen.
Laut Chartbild wäre nun ein Abtaucher bis bzw. knapp unter 16 USD angesagt bevor es weiter steigt (vorausgesetzt alles geht gut und die Politik und die Märkte bleiben stabil).... schauen wir mal.
Heute Abend gibt es zwei CytomX-Präsentationen zu den beiden derzeit durchgeführten klinischen Studien bei der ESMO-Konferenz.
Antwort auf Beitrag Nr.: 55.710.900 von Joschka Schröder am 11.09.17 09:41:01
bi. Mal abgesehen auf die Präsentationen gespannt. Links gerne einstellen.
Zitat von Joschka Schröder: Heute Abend gibt es zwei CytomX-Präsentationen zu den beiden derzeit durchgeführten klinischen Studien bei der ESMO-Konferenz.
bi. Mal abgesehen auf die Präsentationen gespannt. Links gerne einstellen.
http://cytomx.com/probody-therapeutics/publications/
Und auf der cytomx-Seite sind nun die 2 Präsentationen der Phase-1-Studien veröffentlicht!
Und auf der cytomx-Seite sind nun die 2 Präsentationen der Phase-1-Studien veröffentlicht!
Hier der Link zu den beiden Phase-1-Präsentationen auf der ESMO 2017
http://cytomx.com/probody-therapeutics/publications/
http://cytomx.com/probody-therapeutics/publications/
Antwort auf Beitrag Nr.: 55.483.191 von Ville7 am 08.08.17 20:13:45
Die aktuelle Präsentation klärt die Zeitfrage: Bei der Monotherapie-Untersuchung handelt sich um keine klassische 3 + 3 Studie, vielmehr werden in jeder Dosisstufe ab 0,3 mg/kg jeweils nach Abschluß der drei regulären Patienten zusätzlich sechs Patienten hinsichtlich Biomarker/Therapieeffekt untersucht (PART A2). Erst dann kann jeweils PART B1 beginnen.
Dies sollte jedoch nichts daran ändern, dass zur ASCO 2018 mit der Präsentation von Studiendaten zu rechnen ist.
Zitat von Ville7: Wenn ich linear hochrechne wären wir mit multipler Dosierung frühestens sogar im Januar 2018 fertig bis zur höchsten Dosis in allen Gruppen - ohne expansion cohort Part D. Erste Daten zu ASCO 2018 sollten somit m.E. drin sein.
Die aktuelle Präsentation klärt die Zeitfrage: Bei der Monotherapie-Untersuchung handelt sich um keine klassische 3 + 3 Studie, vielmehr werden in jeder Dosisstufe ab 0,3 mg/kg jeweils nach Abschluß der drei regulären Patienten zusätzlich sechs Patienten hinsichtlich Biomarker/Therapieeffekt untersucht (PART A2). Erst dann kann jeweils PART B1 beginnen.
Dies sollte jedoch nichts daran ändern, dass zur ASCO 2018 mit der Präsentation von Studiendaten zu rechnen ist.
Antwort auf Beitrag Nr.: 55.531.719 von Joschka Schröder am 16.08.17 00:19:48
Selbe Studie ist mit überragendem OS Vorteil gegen über SOC Sunitinib knapp ein Monat später DER Star auf ESMO. Wie schon geschrieben ist der PFS Endpunkt bei Immuntherapien einfach falsch angesetzt...
Zitat von Joschka Schröder: Enttäuschende Daten aus der CheckMate-214-Studie! Eine weitere Dosiserhöhung des Checkpointinhibitors Opdivo oder des anti-CTLA-4-Antikörpers Yervoy wäre wegen der starken Nebenwirkungen der Präparate (s. Ende der Meldung) nicht möglich. Hier könnte und sollte CytomX´s Probody-Technologie Abhilfe schaffen. Als Alternative für die besagte Opdivo/Yervoy-Kombi böte sich eine Kombinationstherapie z.B. aus CX-072 (CytomX) und dem anti-CTLA-4-Probody (CytomX/BMY) an. Hier sollte man - zumindest in der Therorie - deutlich höher dosieren können, ohne dass unakzeptable Nebenwirkungen auftreten.
Selbe Studie ist mit überragendem OS Vorteil gegen über SOC Sunitinib knapp ein Monat später DER Star auf ESMO. Wie schon geschrieben ist der PFS Endpunkt bei Immuntherapien einfach falsch angesetzt...
Antwort auf Beitrag Nr.: 55.716.150 von Joschka Schröder am 11.09.17 18:32:58Okay das Poster hilft die Studie und die Dauer besser zu vestehen.
Die 0.03-, 0.1-, und 0.3-mg/kg Dosisgruppen hatten jeweils nur einen Patienten benötigt. Erklärt auch die schnelle Dosiserhöhung. Wo waren wir zu August nochmal? 10mg?
Part A2 hat's irgendwie auch in sich. Welche Patienten machen das mit für eine P1 Dosiseskalationsstudie für eine definitiv suboptimale Dosis eine Biopsie über sich ergehen zu lassen? Erstaunlich, dass CTMX dennoch so weit in der Dosis war. Fanden sich bisher wohl schon einige Patienten, die das mitgemacht haben.
Die 0.03-, 0.1-, und 0.3-mg/kg Dosisgruppen hatten jeweils nur einen Patienten benötigt. Erklärt auch die schnelle Dosiserhöhung. Wo waren wir zu August nochmal? 10mg?
Part A2 hat's irgendwie auch in sich. Welche Patienten machen das mit für eine P1 Dosiseskalationsstudie für eine definitiv suboptimale Dosis eine Biopsie über sich ergehen zu lassen? Erstaunlich, dass CTMX dennoch so weit in der Dosis war. Fanden sich bisher wohl schon einige Patienten, die das mitgemacht haben.
Antwort auf Beitrag Nr.: 55.716.150 von Joschka Schröder am 11.09.17 18:32:58Eines habe ich aber aus dem Poster nicht ablesen können:
Wartet die Studie darauf, dass die vorangegangene Dosistufe von Part A2 rekrutiert ist, bevor dienächste Dosisstufe von Part A eröffnet wird? D.h. z.b. 3mg kg 3 Patienten Part A + 6 Patienten Part A2, dann erst 3 Patienten 10mg Part A? Oder wartet sie nicht und es wird mit A weitergemacht und entkoppelt die verträglichen Dosen von Part A mittels je 6 Patienten von Part A2 überprüft, sequentiell entkoppelt? Letzteres würde das Schaubild dazu suggerieren, denn es geht nur ein Pfeil ab 0.3mg /kg nach unten zu Part A2 und nicht ab jeder Dosisstufe. Somit könnte Part A2 zeitlich hinterherhinken....
Wartet die Studie darauf, dass die vorangegangene Dosistufe von Part A2 rekrutiert ist, bevor dienächste Dosisstufe von Part A eröffnet wird? D.h. z.b. 3mg kg 3 Patienten Part A + 6 Patienten Part A2, dann erst 3 Patienten 10mg Part A? Oder wartet sie nicht und es wird mit A weitergemacht und entkoppelt die verträglichen Dosen von Part A mittels je 6 Patienten von Part A2 überprüft, sequentiell entkoppelt? Letzteres würde das Schaubild dazu suggerieren, denn es geht nur ein Pfeil ab 0.3mg /kg nach unten zu Part A2 und nicht ab jeder Dosisstufe. Somit könnte Part A2 zeitlich hinterherhinken....
Antwort auf Beitrag Nr.: 55.717.518 von Ville7 am 11.09.17 20:53:16In der Fußnote wird es doch eigentlich recht gut beschrieben: "After successful completion of the monotherapy dose level in Part A, Part A2 will enroll an additional 6 patients with PD-L1+ cancer at each indicated dose to refine the MTD/MAD and to evaluate the relationship between dose/exposure and safety, efficacy, and pharmacodynamic biomarkers."
D.h., der A1-Studienarm schreitet unabhängig voran und immer, wenn eine A1-Dosis beendet wird, beginnt die Untersuchung der sechs A2-Patienten mit derselben Dosis.
Die senkrechten Pfeile symbolisieren den jeweiligen Anfang eine jeden Studienarmes.
D.h., der A1-Studienarm schreitet unabhängig voran und immer, wenn eine A1-Dosis beendet wird, beginnt die Untersuchung der sechs A2-Patienten mit derselben Dosis.
Die senkrechten Pfeile symbolisieren den jeweiligen Anfang eine jeden Studienarmes.
Wenn man sich entschieden hat, bereits bei einer Dosis von 0,3 mg/kg die zusätzlichen sechs A2-Patienten zu rekrutieren/untersuchen, so könnte dies dafür sprechen, dass bereits in diesem unteren Dosisbereich eine therapeutische Wirkung zu sehen ist. Das wäre sehr positiv!
Antwort auf Beitrag Nr.: 55.717.854 von Joschka Schröder am 11.09.17 21:21:59Also könnte A bereits auf 30 mg sein und A2 erst auf 3mg? Ist das dann nicht unethisch den A2 Patienten die schlechtere Dosis zu verabreichen?
Antwort auf Beitrag Nr.: 55.717.926 von Joschka Schröder am 11.09.17 21:30:41
Willst du damit suggerieren dass sie auf Basis von Erkenntnissen aus der Studie das Protokoll erweitert haben? Oder meinst du sie waren sich vor Studienstart schon sicher hier Effekte beobachten zu können und es war schon zur initialen Studien Konzeption so geplant?
Zitat von Joschka Schröder: Wenn man sich entschieden hat, bereits bei einer Dosis von 0,3 mg/kg die zusätzlichen sechs A2-Patienten zu rekrutieren/untersuchen, so könnte dies dafür sprechen, dass bereits in diesem unteren Dosisbereich eine therapeutische Wirkung zu sehen ist. Das wäre sehr positiv!
Willst du damit suggerieren dass sie auf Basis von Erkenntnissen aus der Studie das Protokoll erweitert haben? Oder meinst du sie waren sich vor Studienstart schon sicher hier Effekte beobachten zu können und es war schon zur initialen Studien Konzeption so geplant?
Joschka, ne Frage: Die Konzentrationen des CX072 im Blut wird ja wegen der langen Halbwertszeit extrem höher sein als bei einem klassischen PDL1 AK. Ist hier nicht die Gefahr dann auch extrem höher dass der Körper anti- CX072 Antikörper bildet, die das CX072 neutralisieren? Könnte das zu einem potentiellen Problem des Ansatzes werden?

Hallo Ville,
wenn ich in Ergänzung zu Joschka das Thema Autoantikörper mal kurz skizzieren darf:
Die gegen den therapeutischen Antikörper (z.B. Remsima/Remicade/Infliximab) sich bildenden Antikörper, die ein Antikörperkonjugat im Blutkreislauf bilden, und die Wirkung des Arzneimittels reduzieren und im schlimmsten Fall neutralisieren können, sind vor allem ein Problem bei aus Mauszell-Zellkulturen (SP20) entwickelten Antikörpern.
Hier sind erhebliche murine Komponenten vorhanden, unter anderem murine Sialinsäuren, die unterschiedlich sind zu z.B. vollkommen humanisierten Antikörpern, wie Tecentriq/Atezolizumab und CX072.
Insofern dürfte das Autoimmun- Risiko, welches bei obigem Bild für Infliximab bei 37% liegt, erheblich geringer sein.
Du hast mal erwähnt, daß CX072 dem Atezolizumab nachempfunden sei (Tel.Konferenz Quelle)
Das kann gut sein, in der Präsentation und Posterbeschreibung des CX072 (vor ESMO-Präsentation), wurde die Bindungsfähigkeit des cx072 gegen einen anderen, nicht namentlich erwähnten PD-L1-Inhibitor präklinisch verglichen. Hierbei müßte es sich eigentlich um Atezolizumab gehandelt haben.
Interessant auch, daß der Klinische-Zentren-Arzt, Alex Spira, welcher den ersten cx072-Patienten behandelt hatte, auch in die klinische Prüfung des Atezolizumabs eingebunden war.
Generell ist mir aufgefallen, das bei der Erstplanung der Proclaim-Studie 150 Patienten vorgesehen waren, und in der ESMO-Präsentation von 175 Patienten die Rede ist.
LG
Stefan
Antwort auf Beitrag Nr.: 55.722.633 von StefanR am 12.09.17 13:36:44Hallo Stefan,
diese Zusammenhänge sind mir bekannt. Du hast das toll zusammengefasst und dargestellt.
Nach weiteren Überlegungen stelle ich mir die Frage, ob wir überhaupt mit Sicherheit wissen, ob CX072 ein (voll)humaner AK ist. Woher hat CTMX seine AKs? Aus einer phage library oder von transgenen Mäusen? Entweder habe ich das bereits wieder vergessen oder es wurde nie thematisiert.
Unter meiner Annahme, dass CX072 vollhuman ist (denn ich ging davon aus, dass in 2017 kaum einer mehr mit AKs in die Klinik geht, die nicht-humane Anteile besitzen), bestand die konkrete Frage, ob die >10+ fache Serumkonzentration auch bei vollhumanen AKs zu einer erhöhten Immunogenicity führt. Ich könnte mir vorstellen, dass das Immunsystem auch so arbeitet, dass es "viel" von "wenig" unterscheiden kann und "viel" für es eine Gefahr darstellt.
Bezüglich der Studie und den 25 mehr Teilnehmern könnte das der Part A2 Teil von 4*6 = 24 Patienten sein; dieser Part A2 war meines Wissens nach auf der Studienpräsentation zu ASCO noch nicht mir dabei. Wurde wohl nachträglich ergänzt.
diese Zusammenhänge sind mir bekannt. Du hast das toll zusammengefasst und dargestellt.
Nach weiteren Überlegungen stelle ich mir die Frage, ob wir überhaupt mit Sicherheit wissen, ob CX072 ein (voll)humaner AK ist. Woher hat CTMX seine AKs? Aus einer phage library oder von transgenen Mäusen? Entweder habe ich das bereits wieder vergessen oder es wurde nie thematisiert.
Unter meiner Annahme, dass CX072 vollhuman ist (denn ich ging davon aus, dass in 2017 kaum einer mehr mit AKs in die Klinik geht, die nicht-humane Anteile besitzen), bestand die konkrete Frage, ob die >10+ fache Serumkonzentration auch bei vollhumanen AKs zu einer erhöhten Immunogenicity führt. Ich könnte mir vorstellen, dass das Immunsystem auch so arbeitet, dass es "viel" von "wenig" unterscheiden kann und "viel" für es eine Gefahr darstellt.
Bezüglich der Studie und den 25 mehr Teilnehmern könnte das der Part A2 Teil von 4*6 = 24 Patienten sein; dieser Part A2 war meines Wissens nach auf der Studienpräsentation zu ASCO noch nicht mir dabei. Wurde wohl nachträglich ergänzt.
Antwort auf Beitrag Nr.: 55.722.633 von StefanR am 12.09.17 13:36:44Zustimmung! Vielleicht sollte man noch ergänzend hinzufügen, dass es gelegentlich auch voll humane therapeutische Antikörper gibt, gegen die Patienten gehäuft Antikörper bilden. Ein gutes Beispiel dafür ist Humira. Antikörperbildung wiederum muss nicht zwangsläufig bedeuten, dass auch die Wirkung des therapeutischen Mabs beeinträchtigt wird. Zum Probody: Solange die Maske auf dem Probody sitzt, dürfte eine Antikörperbildung gegen die FAB-Bindungsstellen des Probodys nicht möglich sein.
Die Ausweitung der Studie ist mir auch aufgefallen. Ich führe dies auf den A2-Therapiearm zurück, über den in dieser Form erstmals in der aktuellen Präsentation berichtet worden ist.
Die Ausweitung der Studie ist mir auch aufgefallen. Ich führe dies auf den A2-Therapiearm zurück, über den in dieser Form erstmals in der aktuellen Präsentation berichtet worden ist.
Antwort auf Beitrag Nr.: 55.723.251 von Ville7 am 12.09.17 14:47:03Ville, unsere Beiträge haben sich offensichtlich überschnitten.
Die Probodies sind vollständig human. Details zur Herstellungsmethode müßte man in den Patentschriften nachlesen können. Vielleicht schau ich mal in den nächsten Tagen mal nach.
Soweit ich weiß, findet man gewöhnlich im normalen (meist recht weiten) Dosisbereich keine Korrelation zwischen therapeutischer Dosis und Häufigkeit/Schwere einer Antikörperbildung (gegen den therapeutischen Antikörper).
Die Probodies sind vollständig human. Details zur Herstellungsmethode müßte man in den Patentschriften nachlesen können. Vielleicht schau ich mal in den nächsten Tagen mal nach.
Soweit ich weiß, findet man gewöhnlich im normalen (meist recht weiten) Dosisbereich keine Korrelation zwischen therapeutischer Dosis und Häufigkeit/Schwere einer Antikörperbildung (gegen den therapeutischen Antikörper).
Antwort auf Beitrag Nr.: 55.717.926 von Joschka Schröder am 11.09.17 21:30:41
Ich habe nochmal die Poster von ASCO und ESMO abgeglichen. Der Part A2 wurde wohl nach ASCO ergänzt. Denkbar für die Ergänzung sind positive (siehe deine Erklärung) als auch andere Aspekte als Grund. Ein anderer Aspekt könnte z.B. sein, dass die Daten der ersten Patienten zu widersprüchlich sind und man daher mehr Daten zu den einzelnen Dosierungen benötigt. Wie pharmakogenetische und pharmakodynamische Aspekte oder auch dieses Immunogenitätsthema.
Zitat von Joschka Schröder: Wenn man sich entschieden hat, bereits bei einer Dosis von 0,3 mg/kg die zusätzlichen sechs A2-Patienten zu rekrutieren/untersuchen, so könnte dies dafür sprechen, dass bereits in diesem unteren Dosisbereich eine therapeutische Wirkung zu sehen ist. Das wäre sehr positiv!
Ich habe nochmal die Poster von ASCO und ESMO abgeglichen. Der Part A2 wurde wohl nach ASCO ergänzt. Denkbar für die Ergänzung sind positive (siehe deine Erklärung) als auch andere Aspekte als Grund. Ein anderer Aspekt könnte z.B. sein, dass die Daten der ersten Patienten zu widersprüchlich sind und man daher mehr Daten zu den einzelnen Dosierungen benötigt. Wie pharmakogenetische und pharmakodynamische Aspekte oder auch dieses Immunogenitätsthema.
Antwort auf Beitrag Nr.: 55.723.383 von Joschka Schröder am 12.09.17 15:01:06
Wäre interessant. Danke schon mal vorab.
Gibt es eigentlich AK-Medikamente, die durch Dosierung ähnlich hohe AK-Mengen im Körper ansammeln wie bei den probody-AKs zu erwarten ist? Ich vermute hier gibt es einfach keine Vergleiche, die Mengen der probody AKs werden zigfach höher sein....
Zitat von Joschka Schröder: Ville, unsere Beiträge haben sich offensichtlich überschnitten.
Die Probodies sind vollständig human. Details zur Herstellungsmethode müßte man in den Patentschriften nachlesen können. Vielleicht schau ich mal in den nächsten Tagen mal nach.
Soweit ich weiß, findet man gewöhnlich im normalen (meist recht weiten) Dosisbereich keine Korrelation zwischen therapeutischer Dosis und Häufigkeit/Schwere einer Antikörperbildung (gegen den therapeutischen Antikörper).
Wäre interessant. Danke schon mal vorab.
Gibt es eigentlich AK-Medikamente, die durch Dosierung ähnlich hohe AK-Mengen im Körper ansammeln wie bei den probody-AKs zu erwarten ist? Ich vermute hier gibt es einfach keine Vergleiche, die Mengen der probody AKs werden zigfach höher sein....
Ich kopier mir mal die im Poster definierten Untersuchungen des Translational Programs raus. Vielleicht hat jemand Lust zu erläutern, was damit ganz genau ermittelt werden wird und welche Aussagen man ableiten möchte... ansonsten werde ich das bei Gelegenheit mal er-googlen. 
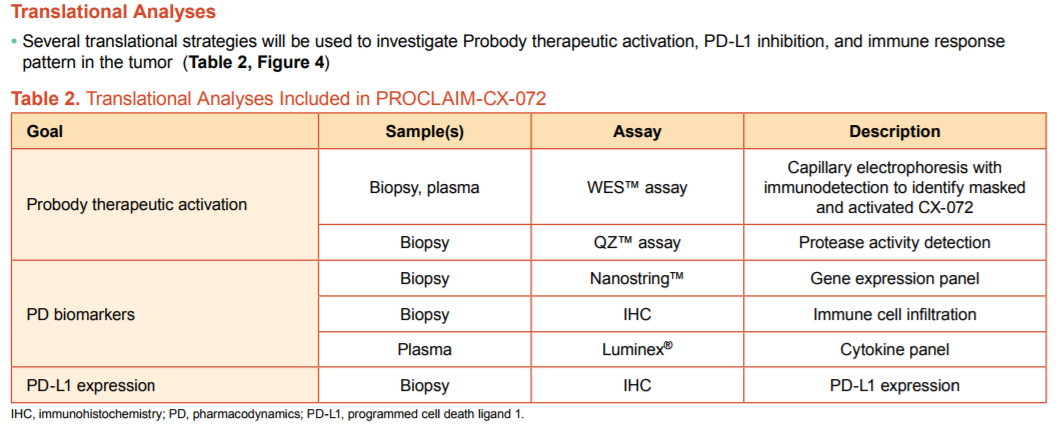


Antwort auf Beitrag Nr.: 55.723.404 von Ville7 am 12.09.17 15:02:51Über die genauen Gründe der Ausweitung kann man natürlich nur spekulieren.
Ich hatte übrigens geschrieben "Wenn man sich entschieden hat, bereits bei einer Dosis von 0,3 mg/kg die zusätzlichen sechs A2-Patienten zu rekrutieren/untersuchen, so könnte dies dafür sprechen, dass bereits in diesem unteren Dosisbereich eine therapeutische Wirkung zu sehen ist..
Diese Vermutung halte ich unverändert für richtig. Wenn kein therapeutischer Effekt zu beobachten wäre, hätte man wohl erst bei höheren Dosierungen angefangen, diesen erheblich Zusatzaufwand zu betreiben.
Ich hatte übrigens geschrieben "Wenn man sich entschieden hat, bereits bei einer Dosis von 0,3 mg/kg die zusätzlichen sechs A2-Patienten zu rekrutieren/untersuchen, so könnte dies dafür sprechen, dass bereits in diesem unteren Dosisbereich eine therapeutische Wirkung zu sehen ist..
Diese Vermutung halte ich unverändert für richtig. Wenn kein therapeutischer Effekt zu beobachten wäre, hätte man wohl erst bei höheren Dosierungen angefangen, diesen erheblich Zusatzaufwand zu betreiben.
Antwort auf Beitrag Nr.: 55.723.650 von Joschka Schröder am 12.09.17 15:32:40Nein, stop, das ist Quatsch. Bei dieser Grunderkrankung und diesem Studienkonzept lassen sich nach so kurzer Zeit wohl kaum Therapieeffekte validieren. Es muss sich um eine grundsätzliche Entscheidung handeln, möglichst viele Daten zu erfassen.
Antwort auf Beitrag Nr.: 55.723.743 von Joschka Schröder am 12.09.17 15:42:51Sehe ich auch so... v.a. bei Immuntherapien ist der therapeutische Effekt erst zeitverzögert wirk-
und feststellbar, siehe die Diskussion um den richtigen Endpoint bei der Checkmate-214 Studie.
und feststellbar, siehe die Diskussion um den richtigen Endpoint bei der Checkmate-214 Studie.
https://www.rheuma-online.de/rheuma-online/archiv/fua/antwor…
"Die Antwort gibt Priv. Doz. Dr. med. H.E. Langer, 1.11.2002:
Bei den meisten Patienten zeigt eine Therapie mit Remicade eine langanhaltende, konstant gute Wirkung. Bei einem kleinen Teil kommt es aber mit zunehmender Therapiedauer zu einem Wirkungsverlust. Oft ist diese nachlassende Wirkung von Remicade mit einer Antikörperbildung gegen den in Remicade enthaltenen Wirkstoff Infliximab zu erklären, genauer durch eine Antikörperbildung gegen den darin enthaltenen Mausanteil.
Infliximab ist ein sogenannter monoklonaler Antikörper gegen TNF-alpha, bei dem der eigentliche Antikörper aus produktionstechnischen Gründen einen Mausanteil aufweist. Durch diesen Mausanteil kann Infliximab im menschlichen Körper als Fremdstoff erkannt werden. In solchen Fällen produziert der Körper dann Antikörper gegen diesen Fremdstoff, im Fall von Infliximab sogenannte Humane Anti-Chimäre Antikörper (HACA´s). Die Bezeichnung Chimäre kommt dabei aus der griechischen Sagenwelt und bezeichnet Fabelwesen mit einer Mischung aus Mensch und Tier. Durch die HACA´s wird dann Infliximab unwirksam gemacht.
Die Bildung von HACA´s tritt nach den Erkenntnissen aus den klinischen Studien zu Infliximab (Remicade) häufiger auf, wenn die Infliximab-Dosierung niedriger ist (3 mg pro kg Körpergewicht gegenüber beispielsweise 10 mg pro kg Körpergewicht). Umgekehrt kommt es sehr viel seltener zum Auftreten von HACA´s und zu einem Wirkungsverlust von Remicade, wenn die Infliximab-Therapie mit Methotrexat (Mtx) kombiniert wird. Deshalb ist Remicade für die Therapie der rheumatoiden Arthritis (RA) bzw. chronischen Polyarthritis (cP) auch nur in Kombination mit Methotrexat zugelassen. In der Praxis wird Remicade bei der Therapie der rheumatoiden Arthritis zum Teil allerdings auch als Monotherapie ohne Mtx eingesetzt.
Kommt es unter einer Remicade-Therapie nach anfänglich guter Wirkung zu einem zunehmenden Wirkungsverlust, wird in der Regel zunächst das Dosisintervall verkürzt, d.h. der Abstand der Infusionen wird von beispielsweise alle 8 Wochen auf alle 6 Wochen oder alle 4 Wochen verringert. Falls bislang noch kein Mtx gegeben wurde, sollte in einem solchen Fall unbedingt mit der Mtx-Therapie (z.B. Lantarel) begonnen werden, wenn keine Gegenanzeigen („Kontraindikationen“) gegen eine solche Therapie bestehen. Reicht die Verkürzung der Dosisintervalle nicht aus, kann gleichzeitig die Dosis erhöht werden, beispielsweise von der üblicherweise verwendeten Dosis mit 3 mg pro kg Körpergewicht auf 5 mg pro kg Körpergewicht oder sogar 10 mg pro kg Körpergewicht. Damit ist allerdings eine erhebliche Steigerung der Behandlungskosten verbunden. Auch steigt mit der erhöhten Infliximab-Dosis das Risiko möglicher Nebenwirkungen. "
Der Beitrag ist zwar schon älter, bezieht sich aber auf eine Studie mit REMICADE/Johnson.
Daraus wird ersichtlich, daß die Immunantwort nicht unbedingt dosisabhängig ist.
Ergänzung:
Die Probody-Maskierung verhindert sicherlich eine Antikörperbildung gegen die Andockstellen. Ein Autoantikörper-Cx072-Konjugat hätte jedoch mögliche negative Pharmakokinetik-und HWZ-Daten zur Folge, so daß sie im Prinzip unerwünscht ist.
Für die Interpretation der Studie fehlt mir im Moment etwas die Zeit, und auch die Erfahrung. Danke für die erläuternden Kommentare von euch beiden!
"Die Antwort gibt Priv. Doz. Dr. med. H.E. Langer, 1.11.2002:
Bei den meisten Patienten zeigt eine Therapie mit Remicade eine langanhaltende, konstant gute Wirkung. Bei einem kleinen Teil kommt es aber mit zunehmender Therapiedauer zu einem Wirkungsverlust. Oft ist diese nachlassende Wirkung von Remicade mit einer Antikörperbildung gegen den in Remicade enthaltenen Wirkstoff Infliximab zu erklären, genauer durch eine Antikörperbildung gegen den darin enthaltenen Mausanteil.
Infliximab ist ein sogenannter monoklonaler Antikörper gegen TNF-alpha, bei dem der eigentliche Antikörper aus produktionstechnischen Gründen einen Mausanteil aufweist. Durch diesen Mausanteil kann Infliximab im menschlichen Körper als Fremdstoff erkannt werden. In solchen Fällen produziert der Körper dann Antikörper gegen diesen Fremdstoff, im Fall von Infliximab sogenannte Humane Anti-Chimäre Antikörper (HACA´s). Die Bezeichnung Chimäre kommt dabei aus der griechischen Sagenwelt und bezeichnet Fabelwesen mit einer Mischung aus Mensch und Tier. Durch die HACA´s wird dann Infliximab unwirksam gemacht.
Die Bildung von HACA´s tritt nach den Erkenntnissen aus den klinischen Studien zu Infliximab (Remicade) häufiger auf, wenn die Infliximab-Dosierung niedriger ist (3 mg pro kg Körpergewicht gegenüber beispielsweise 10 mg pro kg Körpergewicht). Umgekehrt kommt es sehr viel seltener zum Auftreten von HACA´s und zu einem Wirkungsverlust von Remicade, wenn die Infliximab-Therapie mit Methotrexat (Mtx) kombiniert wird. Deshalb ist Remicade für die Therapie der rheumatoiden Arthritis (RA) bzw. chronischen Polyarthritis (cP) auch nur in Kombination mit Methotrexat zugelassen. In der Praxis wird Remicade bei der Therapie der rheumatoiden Arthritis zum Teil allerdings auch als Monotherapie ohne Mtx eingesetzt.
Kommt es unter einer Remicade-Therapie nach anfänglich guter Wirkung zu einem zunehmenden Wirkungsverlust, wird in der Regel zunächst das Dosisintervall verkürzt, d.h. der Abstand der Infusionen wird von beispielsweise alle 8 Wochen auf alle 6 Wochen oder alle 4 Wochen verringert. Falls bislang noch kein Mtx gegeben wurde, sollte in einem solchen Fall unbedingt mit der Mtx-Therapie (z.B. Lantarel) begonnen werden, wenn keine Gegenanzeigen („Kontraindikationen“) gegen eine solche Therapie bestehen. Reicht die Verkürzung der Dosisintervalle nicht aus, kann gleichzeitig die Dosis erhöht werden, beispielsweise von der üblicherweise verwendeten Dosis mit 3 mg pro kg Körpergewicht auf 5 mg pro kg Körpergewicht oder sogar 10 mg pro kg Körpergewicht. Damit ist allerdings eine erhebliche Steigerung der Behandlungskosten verbunden. Auch steigt mit der erhöhten Infliximab-Dosis das Risiko möglicher Nebenwirkungen. "
Der Beitrag ist zwar schon älter, bezieht sich aber auf eine Studie mit REMICADE/Johnson.
Daraus wird ersichtlich, daß die Immunantwort nicht unbedingt dosisabhängig ist.
Ergänzung:
Die Probody-Maskierung verhindert sicherlich eine Antikörperbildung gegen die Andockstellen. Ein Autoantikörper-Cx072-Konjugat hätte jedoch mögliche negative Pharmakokinetik-und HWZ-Daten zur Folge, so daß sie im Prinzip unerwünscht ist.
Für die Interpretation der Studie fehlt mir im Moment etwas die Zeit, und auch die Erfahrung. Danke für die erläuternden Kommentare von euch beiden!
Antwort auf Beitrag Nr.: 55.723.530 von Ville7 am 12.09.17 15:18:17
Das kann man so eigentlich nicht sagen. Omalizumab wird z.B. bei Patienten mit hohem IgE-Titer in einer Dosierung bis 375 mg alle 2 Wochen gegeben, wobei die Halbwertszeit des Omalizumab mit 4 Wochen extrem lang ist. Obwohl zudem die komplementaritäts-bestimmende Region des Omalizumab muriner Herkunft ist, werden extremst selten (< 0,1 %) neutralisierende Antikörper gebildet.
Die 3 mg/kg-Dosis des CX-071 (Applikation in der laufenden Studie alle 2 bzw. 3 Wochen) entspräche in etwa 240 mg, läge also niedriger als besagte Omalizumabdosis. Die Höchststudiendosis des CX-071 (30 mg/kg) ist natürlich schon eine Hausnummer. StefanR dürfte spontan den besten Überblick haben, welche therapeutische Antikörper möglicherweise in ähnlichen Konzentrationen verabreicht werden.
In jedem Fall ist bei der Probody-Behandlung zu berücksichtigen, dass es sich um eine zeitlich begrenzte (Tumor-)Therapie handelt. Neutralisierende Antikörper werden gewöhnlich erst nach langer Therapiedauer gebildet (s. Adalimumab/Humira).
Zitat von Ville7: Gibt es eigentlich AK-Medikamente, die durch Dosierung ähnlich hohe AK-Mengen im Körper ansammeln wie bei den probody-AKs zu erwarten ist? Ich vermute hier gibt es einfach keine Vergleiche, die Mengen der probody AKs werden zigfach höher sein....
Das kann man so eigentlich nicht sagen. Omalizumab wird z.B. bei Patienten mit hohem IgE-Titer in einer Dosierung bis 375 mg alle 2 Wochen gegeben, wobei die Halbwertszeit des Omalizumab mit 4 Wochen extrem lang ist. Obwohl zudem die komplementaritäts-bestimmende Region des Omalizumab muriner Herkunft ist, werden extremst selten (< 0,1 %) neutralisierende Antikörper gebildet.
Die 3 mg/kg-Dosis des CX-071 (Applikation in der laufenden Studie alle 2 bzw. 3 Wochen) entspräche in etwa 240 mg, läge also niedriger als besagte Omalizumabdosis. Die Höchststudiendosis des CX-071 (30 mg/kg) ist natürlich schon eine Hausnummer. StefanR dürfte spontan den besten Überblick haben, welche therapeutische Antikörper möglicherweise in ähnlichen Konzentrationen verabreicht werden.
In jedem Fall ist bei der Probody-Behandlung zu berücksichtigen, dass es sich um eine zeitlich begrenzte (Tumor-)Therapie handelt. Neutralisierende Antikörper werden gewöhnlich erst nach langer Therapiedauer gebildet (s. Adalimumab/Humira).
Ich würde zu gern wissen bei welcher Dosis sie bei CX-2009 inzwischen sind.
Die Dosisgruppen sind
0,25 mg/kg
0,5 mg/kg
1 mg/kg
2 mg/kg
4 mg/kg
5 mg/kg
6 mg/kg
Die Zieldosis gemäß Präklinik wäre mind. 5mg/kg.
Die Dosis 0,25mg/kg startete mit nur einem Patienten, danach, wenn ich das ESMO Poster richtig verstanden habe, klassiches 3+3 design.
6 klinische Sites rekrutieren aktuell, einiges weniger als bei CX-072 (30 aktive Sites)....
Die Dosisgruppen sind
0,25 mg/kg
0,5 mg/kg
1 mg/kg
2 mg/kg
4 mg/kg
5 mg/kg
6 mg/kg
Die Zieldosis gemäß Präklinik wäre mind. 5mg/kg.
Die Dosis 0,25mg/kg startete mit nur einem Patienten, danach, wenn ich das ESMO Poster richtig verstanden habe, klassiches 3+3 design.
6 klinische Sites rekrutieren aktuell, einiges weniger als bei CX-072 (30 aktive Sites)....
Heute notiert CytomX erstmals wieder bei 18 USD. Ich hatte eigentlich mit einer Konsolidierungsphase gerechnet, zumal Großaktionär Third Rock Ventures vor einigen Monaten 2,47 Mio. Aktien zu Kursen zwischen 17 USD und 18 USD abgestoßen hatte. Es wäre schon überraschend, wenn TRV ihren Restbestandteil (4,32 Mio. USD) zu Kursen über 18 USD weiter halten würde. Man wird sehen.
Antwort auf Beitrag Nr.: 55.778.706 von Joschka Schröder am 19.09.17 18:52:19Perfekte Einschätzung. Siehe heutige Form 4, wenn auch nur eine Mini-Menge. VK Preis exakt 18USD.
etwas off topic:
Mersana therapeutics, ein Unterehmen, das in diesem Thread bereits öfters erwähnt worden ist, wurde am Wochenende der World ADC Award als "Best New Drug Developer" verliehen. Ein guter Anlass, um in den nächsten einen eigenen Thread für Mersana zu eröffnen. Bis dann.
Mersana therapeutics, ein Unterehmen, das in diesem Thread bereits öfters erwähnt worden ist, wurde am Wochenende der World ADC Award als "Best New Drug Developer" verliehen. Ein guter Anlass, um in den nächsten einen eigenen Thread für Mersana zu eröffnen. Bis dann.
@Joschka: Du scheinst in Mersana großes Potential zu sehen. Deren präklinische Daten zu ihrem HER2 Programm sehen auch wirklich gut aus. Bin mal gespannt auf deine Analyse. Und der Kurs kennt gerade nur eine Richtung: nach oben.
Antwort auf Beitrag Nr.: 55.830.012 von Ville7 am 27.09.17 07:25:32Bei 18 USD ist hier wohl (vorerst) der Deckel drauf. Bin gespannt, ob und wann Insiderverkäufe gemeldet werden.
Antwort auf Beitrag Nr.: 55.846.476 von biopadawan am 28.09.17 21:39:56Entscheidend wird nächstes Jahr.
In der letzten Präsentation wurde (was wir schon vermutet hatten) angekündigt, dass es erste Daten
* zu CX072 (in Mono und Kombinationen) auf ASCO 2018 (Anf. Juni) und
* zu CX2009 auf ESMO 2018 (übrigens dann in München)
geben wird.
In der letzten Präsentation wurde (was wir schon vermutet hatten) angekündigt, dass es erste Daten
* zu CX072 (in Mono und Kombinationen) auf ASCO 2018 (Anf. Juni) und
* zu CX2009 auf ESMO 2018 (übrigens dann in München)
geben wird.
Antwort auf Beitrag Nr.: 55.830.012 von Ville7 am 27.09.17 07:25:32Hinsichtlich Mersana habe ich mir noch kein abschließendes Urteil gebildet. Interessante Technik, aber einige Punkte sind durchaus störend, z.B.
1) Die Halbwertszeiten der ADC´s sind infolge der komplexen Molekülstruktur extrem kurz.
2) Gastrointestinale Toxizitäten (s. auch S. 10 der jüngsten Präsentation auf der Cantor Fitzgerald-Conference)
3) Überhebliche Selbstdarstellung ("World Class Investors" s. oben zitierte Präsentation; "World Class Management" s. letzter Quartalsbericht usw.)
1) Die Halbwertszeiten der ADC´s sind infolge der komplexen Molekülstruktur extrem kurz.
2) Gastrointestinale Toxizitäten (s. auch S. 10 der jüngsten Präsentation auf der Cantor Fitzgerald-Conference)
3) Überhebliche Selbstdarstellung ("World Class Investors" s. oben zitierte Präsentation; "World Class Management" s. letzter Quartalsbericht usw.)
Wo sieht man bitte ( falls überhaupt), wenn große aktienpakete ( z.b. Großaktionär Third Rock Ventures ) abgegeben werden und mit eelcher zeitverzögerung? Danke😊 ps: intraday über 19 usd
Antwort auf Beitrag Nr.: 55.867.708 von ciel34 am 02.10.17 21:18:19-> SEC-files auf der Unternehmenshomepage
Antwort auf Beitrag Nr.: 55.852.341 von Joschka Schröder am 29.09.17 16:42:48
Da ich mir bei Mersana hinsichtlich der Bewertung nicht ganz schlüssig bin, habe ich meine MRSN-Position nun erst einmal glatt gestellt, weil mir die Sache nach dem starken Kursanstieg der vergangenen Tage zu spekulativ wurde. Ich hoffe, dass es mir gelingen wird, den Stapel Mersana-Unterlagen auf meinem Schreibtisch bis Ende der Woche zuende zu lesen. Danach werde ich dann, wie bereits erwähnt, einen eigenen MRSN-Thread eröffnen. Interessant ist das Unternehmen auf jeden Fall, allerdings gibt es weitaus mehr Fragezeichen als bei CytomX, dessen Technik zudem universal einsetzbar und nicht auf ADCs beschränkt ist. CytomX bleibt mein Biotech-Kerninvestment, gefolgt von Ablynx.
Zitat von Joschka Schröder: Hinsichtlich Mersana habe ich mir noch kein abschließendes Urteil gebildet. Interessante Technik, aber einige Punkte sind durchaus störend, z.B.
1) Die Halbwertszeiten der ADC´s sind infolge der komplexen Molekülstruktur extrem kurz.
2) Gastrointestinale Toxizitäten (s. auch S. 10 der jüngsten Präsentation auf der Cantor Fitzgerald-Conference)
3) Überhebliche Selbstdarstellung ("World Class Investors" s. oben zitierte Präsentation; "World Class Management" s. letzter Quartalsbericht usw.)
Da ich mir bei Mersana hinsichtlich der Bewertung nicht ganz schlüssig bin, habe ich meine MRSN-Position nun erst einmal glatt gestellt, weil mir die Sache nach dem starken Kursanstieg der vergangenen Tage zu spekulativ wurde. Ich hoffe, dass es mir gelingen wird, den Stapel Mersana-Unterlagen auf meinem Schreibtisch bis Ende der Woche zuende zu lesen. Danach werde ich dann, wie bereits erwähnt, einen eigenen MRSN-Thread eröffnen. Interessant ist das Unternehmen auf jeden Fall, allerdings gibt es weitaus mehr Fragezeichen als bei CytomX, dessen Technik zudem universal einsetzbar und nicht auf ADCs beschränkt ist. CytomX bleibt mein Biotech-Kerninvestment, gefolgt von Ablynx.
Jetzt wird es spannend:
Nasdaq has suspended trading in CytomX Therapeutics (NASDAQ:CTMX) pending the release of news.
Nasdaq has suspended trading in CytomX Therapeutics (NASDAQ:CTMX) pending the release of news.
Amgen And Cytomx Therapeutics Announce Strategic Collaboration In Immuno-Oncology
Companies to Jointly Develop T-Cell Engaging Bispecific Probody
THOUSAND OAKS, Calif. and SOUTH SAN FRACISCO, Calif. (Oct. 3, 2017) – Amgen (NASDAQ:AMGN) and CytomX Therapeutics, Inc., (NASDAQ:CTMX) today announced that the companies have entered into a strategic collaboration in immuno-oncology. The companies will co-develop a CytomX Probody™ T-cell engaging bispecific against the Epidermal Growth Factor Receptor (EGFR), a highly validated oncology target expressed on multiple human cancer types. Probody T-cell engaging bispecifics are antibody constructs capable of directing cytotoxic T-cells in tumor microenvironments. In preclinical studies, CytomX’s Probody versions of EGFRxCD3 bispecific therapeutics induced tumor regressions and increased the therapeutic window for this high potential cancer target.
“Our collaboration with CytomX leverages Amgen’s development leadership in bispecifics and expands our immuno-oncology capabilities with an additional and complementary bispecific technology,” said Sean E. Harper, M.D., executive vice president of Research and Development at Amgen. “EGFR is a particularly compelling target on which to employ the CytomX Probody platform given its potential to localize activity within tumors while limiting potential toxicity.”
“Probody-based T-cell engaging bispecific antibodies offer significant potential in treating cancers by employing localized therapeutic activity within tumor tissue,” said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. “Through this collaboration, we are positioned to combine Amgen’s industry-leading expertise in leveraging bispecifics to activate a patient’s immune-system with CytomX’ ability to design potent new therapies that exploit unique conditions in the tumor microenvironment. Development of Probody-based T-cell engaging bispecifics further validates the broad applicability of the Probody platform in addressing unmet needs in oncology.”
Under the terms of the agreement, Amgen and CytomX will co-develop a Probody T-cell engaging bispecific against EGFRxCD3 with CytomX leading early development. Amgen will lead later development and commercialization with global late-stage development costs shared between the two companies. Amgen will make an upfront payment of $40 million and purchase $20 million of CytomX common stock. CytomX will be eligible to receive up to $455 million in development, regulatory and commercial milestones for the EGFR program. Amgen will lead global commercial activities with CytomX able to opt into a profit share in the U.S. and receive tiered, double-digit royalties on net product sales outside of the U.S.
Amgen will also receive exclusive worldwide rights to develop and commercialize up to three additional, undisclosed targets. Should Amgen ultimately pursue all of these targets, CytomX will be eligible to receive up to $950 million in additional upfront and milestone payments and high single-digit to mid-double digit royalty payments on any resulting products. CytomX will also receive the rights from Amgen to an undisclosed preclinical T-cell engaging bispecific program; Amgen is eligible to receive milestones and royalty payments on any resulting products from this CytomX program.
Conference Call / Webcast Information
CytomX will host a teleconference today at 5 p.m. ET to discuss the strategic collaboration. Sean McCarthy, D.Phil., president and chief executive officer at CytomX and Debanjan Ray, chief financial officer at CytomX, will lead the teleconference. Interested parties may access the live audio webcast of the teleconference through the Investor and News page of CytomX's website at http://ir.cytomx.com or by dialing (877) 809-6037 and using the passcode 94163867. A replay will be available on the CytomX website or by dialing (855) 859-2056 and using the passcode 94163867. The replay will be available from October 3, 2017, at 8:00 p.m. ET until October 10, 2017, at 8:00 p.m. ET.
About Amgen
Amgen is committed to unlocking the potential of biology for patients suffering from serious illnesses by discovering, developing, manufacturing and delivering innovative human therapeutics. This approach begins by using tools like advanced human genetics to unravel the complexities of disease and understand the fundamentals of human biology.
Amgen focuses on areas of high unmet medical need and leverages its expertise to strive for solutions that improve health outcomes and dramatically improve people's lives. A biotechnology pioneer since 1980, Amgen has grown to be one of the world's leading independent biotechnology companies, has reached millions of patients around the world and is developing a pipeline of medicines with breakaway potential.
For more information, visit www.amgen.com and follow us on www.twitter.com/amgen.
About CytomX Therapeutics
CytomX Therapeutics is a clinical-stage biopharmaceutical company with a deep and differentiated oncology pipeline of investigational Probody™ therapeutics. Probody therapeutics are designed to exploit unique conditions of the tumor microenvironment to more effectively localize antibody binding and activity while limiting activity in healthy tissues. The Company’s pipeline includes proprietary cancer immunotherapies against clinically-validated targets, such as PD-L1, and first-in-class Probody drug conjugates against highly attractive targets, such as CD166 and CD71, which are considered to be inaccessible to conventional antibody drug conjugates due to their presence on healthy tissue. In addition to its wholly owned programs, CytomX has strategic collaborations with AbbVie, Bristol-Myers Squibb Company, Pfizer Inc., MD Anderson Cancer Center and ImmunoGen, Inc. For more information, visit www.cytomx.com or follow us on Twitter.
CytomX Therapeutics Forward-Looking Statements
This press release includes forward-looking statements. Such forward-looking statements involve known and unknown risks, uncertainties and other important factors that are difficult to predict, may be beyond our control, and may cause the actual results, performance or achievements to be materially different from any future results, performance or achievements expressed or implied in such statements. Accordingly, you should not rely on any of these forward-looking statements, including those relating to the potential safety and efficacy of products and to CytomX’ ability and the ability of its collaborative partners to develop and advance product candidates into and successfully complete clinical trials. The process by which preclinical and clinical development could potentially lead to an approved product is long and subject to significant risks and uncertainties. Collaborations with partners may not result in products, and milestone payments and royalties may not be received. Applicable risks and uncertainties include those relating to our preclinical research and development, clinical development, collaborations, and other risks identified under the heading “Risk Factors” included in CytomX’ Quarterly Report on Form 10-Q filed with the SEC on August 7, 2017. The forward-looking statements contained in this press release are based on information currently available to CytomX and speak only as of the date on which they are made. CytomX does not undertake and specifically disclaims any obligation to update any forward-looking statements, whether as a result of any new information, future events, changed circumstances or otherwise.
Amgen Forward-Looking Statements
This news release contains forward-looking statements that are based on the current expectations and beliefs of Amgen. All statements, other than statements of historical fact, are statements that could be deemed forward-looking statements, including estimates of revenues, operating margins, capital expenditures, cash, other financial metrics, expected legal, arbitration, political, regulatory or clinical results or practices, customer and prescriber patterns or practices, reimbursement activities and outcomes and other such estimates and results. Forward-looking statements involve significant risks and uncertainties, including those discussed below and more fully described in the Securities and Exchange Commission reports filed by Amgen, including our most recent annual report on Form 10-K and any subsequent periodic reports on Form 10-Q and Form 8-K. Unless otherwise noted, Amgen is providing this information as of the date of this news release and does not undertake any obligation to update any forward-looking statements contained in this document as a result of new information, future events or otherwise.
No forward-looking statement can be guaranteed and actual results may differ materially from those we project. Discovery or identification of new product candidates or development of new indications for existing products cannot be guaranteed and movement from concept to product is uncertain; consequently, there can be no guarantee that any particular product candidate or development of a new indication for an existing product will be successful and become a commercial product. Further, preclinical results do not guarantee safe and effective performance of product candidates in humans. The complexity of the human body cannot be perfectly, or sometimes, even adequately modeled by computer or cell culture systems or animal models. The length of time that it takes for us to complete clinical trials and obtain regulatory approval for product marketing has in the past varied and we expect similar variability in the future. Even when clinical trials are successful, regulatory authorities may question the sufficiency for approval of the trial endpoints we have selected. We develop product candidates internally and through licensing collaborations, partnerships and joint ventures. Product candidates that are derived from relationships may be subject to disputes between the parties or may prove to be not as effective or as safe as we may have believed at the time of entering into such relationship. Also, we or others could identify safety, side effects or manufacturing problems with our products after they are on the market.
Our results may be affected by our ability to successfully market both new and existing products domestically and internationally, clinical and regulatory developments involving current and future products, sales growth of recently launched products, competition from other products including biosimilars, difficulties or delays in manufacturing our products and global economic conditions. In addition, sales of our products are affected by pricing pressure, political and public scrutiny and reimbursement policies imposed by third-party payers, including governments, private insurance plans and managed care providers and may be affected by regulatory, clinical and guideline developments and domestic and international trends toward managed care and healthcare cost containment. Furthermore, our research, testing, pricing, marketing and other operations are subject to extensive regulation by domestic and foreign government regulatory authorities. We or others could identify safety, side effects or manufacturing problems with our products after they are on the market. Our business may be impacted by government investigations, litigation and product liability claims. In addition, our business may be impacted by the adoption of new tax legislation or exposure to additional tax liabilities. If we fail to meet the compliance obligations in the corporate integrity agreement between us and the U.S. government, we could become subject to significant sanctions. Further, while we routinely obtain patents for our products and technology, the protection offered by our patents and patent applications may be challenged, invalidated or circumvented by our competitors, or we may fail to prevail in present and future intellectual property litigation. We perform a substantial amount of our commercial manufacturing activities at a few key facilities and also depend on third parties for a portion of our manufacturing activities, and limits on supply may constrain sales of certain of our current products and product candidate development. In addition, we compete with other companies with respect to many of our marketed products as well as for the discovery and development of new products. Further, some raw materials, medical devices and component parts for our products are supplied by sole third-party suppliers. The discovery of significant problems with a product similar to one of our products that implicate an entire class of products could have a material adverse effect on sales of the affected products and on our business and results of operations. Our efforts to acquire other companies or products and to integrate the operations of companies we have acquired may not be successful. We may not be able to access the capital and credit markets on terms that are favorable to us, or at all. We are increasingly dependent on information technology systems, infrastructure and data security. Our stock price is volatile and may be affected by a number of events. Our business performance could affect or limit the ability of our Board of Directors to declare a dividend or our ability to pay a dividend or repurchase our common stock.
The scientific information discussed in this news release related to our product candidates is preliminary and investigative. Such product candidates are not approved by the U.S. Food and Drug Administration, and no conclusions can or should be drawn regarding the safety or effectiveness of the product candidates.
CONTACT: Amgen, Thousand Oaks
Kristen Davis, 805-447-3008 (media)
Kristen Neese, 805-313-8267 (media)
Arvind Sood, 805-447-1060 (investors)
CONTACT: Cytomx Media Contact:
Spectrum
Amir Khan
akhan@spectrumscience.com
212-899-9730
CytomX Investor Contact:
Trout Group
Pete Rahmer
prahmer@troutgroup.com
646-378-2973
Companies to Jointly Develop T-Cell Engaging Bispecific Probody
THOUSAND OAKS, Calif. and SOUTH SAN FRACISCO, Calif. (Oct. 3, 2017) – Amgen (NASDAQ:AMGN) and CytomX Therapeutics, Inc., (NASDAQ:CTMX) today announced that the companies have entered into a strategic collaboration in immuno-oncology. The companies will co-develop a CytomX Probody™ T-cell engaging bispecific against the Epidermal Growth Factor Receptor (EGFR), a highly validated oncology target expressed on multiple human cancer types. Probody T-cell engaging bispecifics are antibody constructs capable of directing cytotoxic T-cells in tumor microenvironments. In preclinical studies, CytomX’s Probody versions of EGFRxCD3 bispecific therapeutics induced tumor regressions and increased the therapeutic window for this high potential cancer target.
“Our collaboration with CytomX leverages Amgen’s development leadership in bispecifics and expands our immuno-oncology capabilities with an additional and complementary bispecific technology,” said Sean E. Harper, M.D., executive vice president of Research and Development at Amgen. “EGFR is a particularly compelling target on which to employ the CytomX Probody platform given its potential to localize activity within tumors while limiting potential toxicity.”
“Probody-based T-cell engaging bispecific antibodies offer significant potential in treating cancers by employing localized therapeutic activity within tumor tissue,” said Sean McCarthy, D.Phil., president and chief executive officer of CytomX Therapeutics. “Through this collaboration, we are positioned to combine Amgen’s industry-leading expertise in leveraging bispecifics to activate a patient’s immune-system with CytomX’ ability to design potent new therapies that exploit unique conditions in the tumor microenvironment. Development of Probody-based T-cell engaging bispecifics further validates the broad applicability of the Probody platform in addressing unmet needs in oncology.”
Under the terms of the agreement, Amgen and CytomX will co-develop a Probody T-cell engaging bispecific against EGFRxCD3 with CytomX leading early development. Amgen will lead later development and commercialization with global late-stage development costs shared between the two companies. Amgen will make an upfront payment of $40 million and purchase $20 million of CytomX common stock. CytomX will be eligible to receive up to $455 million in development, regulatory and commercial milestones for the EGFR program. Amgen will lead global commercial activities with CytomX able to opt into a profit share in the U.S. and receive tiered, double-digit royalties on net product sales outside of the U.S.
Amgen will also receive exclusive worldwide rights to develop and commercialize up to three additional, undisclosed targets. Should Amgen ultimately pursue all of these targets, CytomX will be eligible to receive up to $950 million in additional upfront and milestone payments and high single-digit to mid-double digit royalty payments on any resulting products. CytomX will also receive the rights from Amgen to an undisclosed preclinical T-cell engaging bispecific program; Amgen is eligible to receive milestones and royalty payments on any resulting products from this CytomX program.
Conference Call / Webcast Information
CytomX will host a teleconference today at 5 p.m. ET to discuss the strategic collaboration. Sean McCarthy, D.Phil., president and chief executive officer at CytomX and Debanjan Ray, chief financial officer at CytomX, will lead the teleconference. Interested parties may access the live audio webcast of the teleconference through the Investor and News page of CytomX's website at http://ir.cytomx.com or by dialing (877) 809-6037 and using the passcode 94163867. A replay will be available on the CytomX website or by dialing (855) 859-2056 and using the passcode 94163867. The replay will be available from October 3, 2017, at 8:00 p.m. ET until October 10, 2017, at 8:00 p.m. ET.
About Amgen
Amgen is committed to unlocking the potential of biology for patients suffering from serious illnesses by discovering, developing, manufacturing and delivering innovative human therapeutics. This approach begins by using tools like advanced human genetics to unravel the complexities of disease and understand the fundamentals of human biology.
Amgen focuses on areas of high unmet medical need and leverages its expertise to strive for solutions that improve health outcomes and dramatically improve people's lives. A biotechnology pioneer since 1980, Amgen has grown to be one of the world's leading independent biotechnology companies, has reached millions of patients around the world and is developing a pipeline of medicines with breakaway potential.
For more information, visit www.amgen.com and follow us on www.twitter.com/amgen.
About CytomX Therapeutics
CytomX Therapeutics is a clinical-stage biopharmaceutical company with a deep and differentiated oncology pipeline of investigational Probody™ therapeutics. Probody therapeutics are designed to exploit unique conditions of the tumor microenvironment to more effectively localize antibody binding and activity while limiting activity in healthy tissues. The Company’s pipeline includes proprietary cancer immunotherapies against clinically-validated targets, such as PD-L1, and first-in-class Probody drug conjugates against highly attractive targets, such as CD166 and CD71, which are considered to be inaccessible to conventional antibody drug conjugates due to their presence on healthy tissue. In addition to its wholly owned programs, CytomX has strategic collaborations with AbbVie, Bristol-Myers Squibb Company, Pfizer Inc., MD Anderson Cancer Center and ImmunoGen, Inc. For more information, visit www.cytomx.com or follow us on Twitter.
CytomX Therapeutics Forward-Looking Statements
This press release includes forward-looking statements. Such forward-looking statements involve known and unknown risks, uncertainties and other important factors that are difficult to predict, may be beyond our control, and may cause the actual results, performance or achievements to be materially different from any future results, performance or achievements expressed or implied in such statements. Accordingly, you should not rely on any of these forward-looking statements, including those relating to the potential safety and efficacy of products and to CytomX’ ability and the ability of its collaborative partners to develop and advance product candidates into and successfully complete clinical trials. The process by which preclinical and clinical development could potentially lead to an approved product is long and subject to significant risks and uncertainties. Collaborations with partners may not result in products, and milestone payments and royalties may not be received. Applicable risks and uncertainties include those relating to our preclinical research and development, clinical development, collaborations, and other risks identified under the heading “Risk Factors” included in CytomX’ Quarterly Report on Form 10-Q filed with the SEC on August 7, 2017. The forward-looking statements contained in this press release are based on information currently available to CytomX and speak only as of the date on which they are made. CytomX does not undertake and specifically disclaims any obligation to update any forward-looking statements, whether as a result of any new information, future events, changed circumstances or otherwise.
Amgen Forward-Looking Statements
This news release contains forward-looking statements that are based on the current expectations and beliefs of Amgen. All statements, other than statements of historical fact, are statements that could be deemed forward-looking statements, including estimates of revenues, operating margins, capital expenditures, cash, other financial metrics, expected legal, arbitration, political, regulatory or clinical results or practices, customer and prescriber patterns or practices, reimbursement activities and outcomes and other such estimates and results. Forward-looking statements involve significant risks and uncertainties, including those discussed below and more fully described in the Securities and Exchange Commission reports filed by Amgen, including our most recent annual report on Form 10-K and any subsequent periodic reports on Form 10-Q and Form 8-K. Unless otherwise noted, Amgen is providing this information as of the date of this news release and does not undertake any obligation to update any forward-looking statements contained in this document as a result of new information, future events or otherwise.
No forward-looking statement can be guaranteed and actual results may differ materially from those we project. Discovery or identification of new product candidates or development of new indications for existing products cannot be guaranteed and movement from concept to product is uncertain; consequently, there can be no guarantee that any particular product candidate or development of a new indication for an existing product will be successful and become a commercial product. Further, preclinical results do not guarantee safe and effective performance of product candidates in humans. The complexity of the human body cannot be perfectly, or sometimes, even adequately modeled by computer or cell culture systems or animal models. The length of time that it takes for us to complete clinical trials and obtain regulatory approval for product marketing has in the past varied and we expect similar variability in the future. Even when clinical trials are successful, regulatory authorities may question the sufficiency for approval of the trial endpoints we have selected. We develop product candidates internally and through licensing collaborations, partnerships and joint ventures. Product candidates that are derived from relationships may be subject to disputes between the parties or may prove to be not as effective or as safe as we may have believed at the time of entering into such relationship. Also, we or others could identify safety, side effects or manufacturing problems with our products after they are on the market.
Our results may be affected by our ability to successfully market both new and existing products domestically and internationally, clinical and regulatory developments involving current and future products, sales growth of recently launched products, competition from other products including biosimilars, difficulties or delays in manufacturing our products and global economic conditions. In addition, sales of our products are affected by pricing pressure, political and public scrutiny and reimbursement policies imposed by third-party payers, including governments, private insurance plans and managed care providers and may be affected by regulatory, clinical and guideline developments and domestic and international trends toward managed care and healthcare cost containment. Furthermore, our research, testing, pricing, marketing and other operations are subject to extensive regulation by domestic and foreign government regulatory authorities. We or others could identify safety, side effects or manufacturing problems with our products after they are on the market. Our business may be impacted by government investigations, litigation and product liability claims. In addition, our business may be impacted by the adoption of new tax legislation or exposure to additional tax liabilities. If we fail to meet the compliance obligations in the corporate integrity agreement between us and the U.S. government, we could become subject to significant sanctions. Further, while we routinely obtain patents for our products and technology, the protection offered by our patents and patent applications may be challenged, invalidated or circumvented by our competitors, or we may fail to prevail in present and future intellectual property litigation. We perform a substantial amount of our commercial manufacturing activities at a few key facilities and also depend on third parties for a portion of our manufacturing activities, and limits on supply may constrain sales of certain of our current products and product candidate development. In addition, we compete with other companies with respect to many of our marketed products as well as for the discovery and development of new products. Further, some raw materials, medical devices and component parts for our products are supplied by sole third-party suppliers. The discovery of significant problems with a product similar to one of our products that implicate an entire class of products could have a material adverse effect on sales of the affected products and on our business and results of operations. Our efforts to acquire other companies or products and to integrate the operations of companies we have acquired may not be successful. We may not be able to access the capital and credit markets on terms that are favorable to us, or at all. We are increasingly dependent on information technology systems, infrastructure and data security. Our stock price is volatile and may be affected by a number of events. Our business performance could affect or limit the ability of our Board of Directors to declare a dividend or our ability to pay a dividend or repurchase our common stock.
The scientific information discussed in this news release related to our product candidates is preliminary and investigative. Such product candidates are not approved by the U.S. Food and Drug Administration, and no conclusions can or should be drawn regarding the safety or effectiveness of the product candidates.
CONTACT: Amgen, Thousand Oaks
Kristen Davis, 805-447-3008 (media)
Kristen Neese, 805-313-8267 (media)
Arvind Sood, 805-447-1060 (investors)
CONTACT: Cytomx Media Contact:
Spectrum
Amir Khan
akhan@spectrumscience.com
212-899-9730
CytomX Investor Contact:
Trout Group
Pete Rahmer
prahmer@troutgroup.com
646-378-2973
AMGEN hat wohl verstärkt Aktien für 20 Mio gekauft, was wohl zu dem Kursanstieg in den letzen Wochen mitursächlich gewesen sein könnte.
Wenn AMGEN sich bei dem Unternehmen verstärkt angagiert, ist das ein sehr positives Zeichen. Ich werde meine Beteiligung wohl aufstocken, wenn der Kurs nochmals zurückkommt.
Wenn AMGEN sich bei dem Unternehmen verstärkt angagiert, ist das ein sehr positives Zeichen. Ich werde meine Beteiligung wohl aufstocken, wenn der Kurs nochmals zurückkommt.
$26.74 war das nachbörsliche Hoch. Krass!
Antwort auf Beitrag Nr.: 55.873.969 von 007coolinvestor am 03.10.17 22:26:14Wie kommst du darauf amgen habe schon gekauft? Laut Pressemitteilung wird ( will ) Amgen die Aktien erst noch kaufen.
Antwort auf Beitrag Nr.: 55.379.498 von Joschka Schröder am 23.07.17 13:57:13
@Ville
Dies ist der bispezifische Probody, den CytomX jetzt verpartnert hat.
Zitat von Joschka Schröder: Aus den Angaben in den Geschäftsberichten für 2015 und 2016 und in den gängigen Patentdatenbanken ergibt sich:
1) Pfizer hat sich von CytomX drei Targets für PDC´s gesichert
2) Das erste Target war EGFR
3) Für das erste Target (EGFR) besitzt Pfizer Probody-Rechte ausschließlich für PDC´s (GB 2016, S. 29)
4) CytomX entwickelt schon seit langem einen eigenen bispezifischen anti-EGFR/CD3-Probody. Das entsprechende Patent ist am 13.7.2017 veröffentlicht worden, Prioritätsdatum war bereits der 27.4.2012. Präklinische Daten finden sich auf der Unternehmenshomepage.
5) Pfizer hat zu EGFR nichts patentiert.
6) Pfizer verfolgt derzeit nur noch zwei Probody-Projekte (GB 2016, S.10)
Schlussfolgerung: Pfizer hat das anti-EGFR-PDC-Projekt eingestellt, weil der von CytomX entwickelte bispezifische anti-EGFR/CD3-Probody zu besseren präklinischen Daten geführt hat. Wegen des eigenen Entwicklungsprojekts hat CytomX von Anfang an Lizenzrechte für EGFR an Pfizer nur im Hinblick auf PDC´s vergeben, während für die anderen Targets umfassende Probody-Rechte gewährt wurden.
So ist es stimmig und macht Sinn!
@Ville
Dies ist der bispezifische Probody, den CytomX jetzt verpartnert hat.
Antwort auf Beitrag Nr.: 55.874.263 von Joschka Schröder am 03.10.17 23:40:39@Joschka: ich weiß. Ich verstehe es aber so, dass beide Firmen auf der grünen Wiese neu anfangen und Amgen nun den bispezifischen AK ( auf Basis der Micromet Technologie) liefern wird. Oder versteht du das anders?
PS: immer wieder erstaunlich wie sich der Kreis schließt und die Mütter der alten Firmen, die einem geklaut ( übernommen) wurden, nun Geschäfte mit den neuen Investments machen. Wie Medarex (BMS) oder Micromet (Amgen). Das erhält in mir den Glauben aufrecht, dass man als Biotechinvestor den Dickfischen stets einen Schritt voraus sein kann.
PS: immer wieder erstaunlich wie sich der Kreis schließt und die Mütter der alten Firmen, die einem geklaut ( übernommen) wurden, nun Geschäfte mit den neuen Investments machen. Wie Medarex (BMS) oder Micromet (Amgen). Das erhält in mir den Glauben aufrecht, dass man als Biotechinvestor den Dickfischen stets einen Schritt voraus sein kann.
Antwort auf Beitrag Nr.: 55.874.296 von Ville7 am 03.10.17 23:54:37Wurde das so in der Telefonkonferenz kommuniziert? Ich hatte bislang leider keine Zeit, sie mir anzuhören.
Ganz eindeutig ist die Meldung nicht formuliert. Dafür, dass es sich tatsächlich um besagten anti-EGFRxCD3-Probody (also genau dieses Molekül) handelt, sprechen aber folgende Passagen:
"The companies will co-develop a CytomX Probody™ T-cell engaging bispecific against the Epidermal Growth Factor Receptor (EGFR)"
"Our collaboration with CytomX leverages Amgen’s development leadership in bispecifics and expands our immuno-oncology capabilities with an additional and complementary bispecific technology”
Die Zusammenarbeit umfasst ja noch andere Präparate, bei deren Entwicklung natürlich die BitE-Technologie zum Einsatz kommen kann.
Die Konditionen des Deals sind natürlich (mal wieder) top.
40 Mio. Upfront für einen Probody in der Präklinik, an dem CytomX eine Menge Rechte behält, bis zu 950 Millionen Upfront+Meilensteinzahlungen für jedes weitere Präparat ... so etwas sieht man sehr selten.
Da ich in der Hoffnung auf einen Zielkurs > 1.000 USD investiert habe, muss CytomX aber auch liefern, damit ich mich nicht lächerlich mache.
Ganz eindeutig ist die Meldung nicht formuliert. Dafür, dass es sich tatsächlich um besagten anti-EGFRxCD3-Probody (also genau dieses Molekül) handelt, sprechen aber folgende Passagen:
"The companies will co-develop a CytomX Probody™ T-cell engaging bispecific against the Epidermal Growth Factor Receptor (EGFR)"
"Our collaboration with CytomX leverages Amgen’s development leadership in bispecifics and expands our immuno-oncology capabilities with an additional and complementary bispecific technology”
Die Zusammenarbeit umfasst ja noch andere Präparate, bei deren Entwicklung natürlich die BitE-Technologie zum Einsatz kommen kann.
Die Konditionen des Deals sind natürlich (mal wieder) top.
40 Mio. Upfront für einen Probody in der Präklinik, an dem CytomX eine Menge Rechte behält, bis zu 950 Millionen Upfront+Meilensteinzahlungen für jedes weitere Präparat ... so etwas sieht man sehr selten.
Da ich in der Hoffnung auf einen Zielkurs > 1.000 USD investiert habe, muss CytomX aber auch liefern, damit ich mich nicht lächerlich mache.

Eine Zusammenfassung des CC via twitter:

Natürlich kauft Amgen die Aktien nicht an der Börse, auch wenn ich mir ein solches Vorgehen natürlich wünschen würde

https://twitter.com/MauriceOnTW/status/915334416909635585

Natürlich kauft Amgen die Aktien nicht an der Börse, auch wenn ich mir ein solches Vorgehen natürlich wünschen würde


https://twitter.com/MauriceOnTW/status/915334416909635585
PS: Gut gefällt mir an CytomX, dass sich derartige Deals nicht vorab augenscheinlich in der Kursentwicklung widerspiegeln, dass also diskret verhandelt wird und kein Insiderhandelt stattfindet (CEO und CFO hatten zuletzt ja noch Aktien verkauft, was in diesem Thread ausführlich diskutiert worden ist).
Eigentlich erwarte ich für das nächsten Jahr, wenn erste klinische Daten aus den laufenden Studien vorliegen, auch eine Zusammenarbeit mit Roche, das ja bereits über die VC-Tochter an CytomX beteiligt ist.
Eigentlich erwarte ich für das nächsten Jahr, wenn erste klinische Daten aus den laufenden Studien vorliegen, auch eine Zusammenarbeit mit Roche, das ja bereits über die VC-Tochter an CytomX beteiligt ist.
Antwort auf Beitrag Nr.: 55.874.377 von kmastra am 04.10.17 00:41:59Ville, in der Twitter-Zusammenfassung steht´s, es handelt sich wie vermutet um das betreffende anti-EGFRxCD3-Molekül aus der präklinischen CytomX-Pipeline (Patent vom 13.7.2017).
Die Formulierung im SEC-File zu Upfront- und Meilensteinzahlungen für die drei zusätzlichen Präparate ist mißverständlich:
"if Amgen exercises its option with respect to the Amgen Option Products, up to an additional $950 million in upfront, development, regulatory, and commercial milestone payments for all three potential Amgen Products"
In der beigefügten PR-Mitteilung wird präzisiert:
"Amgen will also receive exclusive worldwide rights to develop and commercialize up to three additional, undisclosed targets. Should Amgen ultimately pursue all of these targets, CytomX will be eligible to receive up to $950 million in additional upfront and milestone payments and high single-digit to mid-double digit royalty payments on any resulting products"
"if Amgen exercises its option with respect to the Amgen Option Products, up to an additional $950 million in upfront, development, regulatory, and commercial milestone payments for all three potential Amgen Products"
In der beigefügten PR-Mitteilung wird präzisiert:
"Amgen will also receive exclusive worldwide rights to develop and commercialize up to three additional, undisclosed targets. Should Amgen ultimately pursue all of these targets, CytomX will be eligible to receive up to $950 million in additional upfront and milestone payments and high single-digit to mid-double digit royalty payments on any resulting products"
Antwort auf Beitrag Nr.: 55.874.458 von Joschka Schröder am 04.10.17 01:59:12Ich sag es ungern Joschka, aber man könnte das "on any" auch nur auf die Royalities beziehen.
Zwei kurze Fragen noch zum Deal.
Was meint ihr, wo die Aktien herkommen, die Amgen kauft? Ist das eine kleine Kapitalerhöhung?
Wie habe ich die Einlizenzierung von Amgen an Cytomx zu verstehen? Was holt sich Cytomx da?
@Joschka: Kursziel > 1000 US-DOLLAR? Das ist grob überschlagen eine Marktkapitalisierung von über 35 Mrd. US-Dollar. Wieso sollten wir so hoch laufen?
Zwei kurze Fragen noch zum Deal.
Was meint ihr, wo die Aktien herkommen, die Amgen kauft? Ist das eine kleine Kapitalerhöhung?
Wie habe ich die Einlizenzierung von Amgen an Cytomx zu verstehen? Was holt sich Cytomx da?
@Joschka: Kursziel > 1000 US-DOLLAR? Das ist grob überschlagen eine Marktkapitalisierung von über 35 Mrd. US-Dollar. Wieso sollten wir so hoch laufen?
Der Deal war ja schon am 29. September. Wieso kommt die Meldung erst jetzt?
Antwort auf Beitrag Nr.: 55.874.485 von hinz12 am 04.10.17 03:11:07Dein semantischer Hinweis ist durchaus berechtigt. Es ist schrecklich, ich sollte endlich schlafen gehen.
Die Aktien, die an Amgen gehen, stammen aus einer kleinen KP-Erhöhung.
Warum Kursziel "DAUSEND"? Na ja, falls die Probody-Technik in der klinischen Anwendung so gut funktioniert wie in der Präklinik, wird man in der Onkologie (in jedem Fall bei soliden Tumoren, außerhalb der Onkologie aber aber auch in einigen entzündlichen Indikationen) nicht umhin kommen, nahezu jeden Antikörper/ADC/CAR-T mit einer Maskierung zu versehen, was für CytomX entsprechende Lizenzeinnahmen zur Folge hätte.
In meinem Morphosys-Thread habe ich vorhin eine kleine Übersicht über anti-BCMA-Biologics gepostet, der veranschaulicht, wie viele Unternehmen zeitgleich dasselbe Target bearbeiten. So verhält es sich bei den meisten Präparaten. Richtig viel Geld werden auf lange Sicht nur diejenigen Unternehmen verdienen, die eine besonders innovative Technik mit Alleinstellungsmerkmal auf den Markt bringen, die möglichst noch von der Konkurrenz einlizensiert werden muss. Aus diesem Grund ist CytomX meine größte Depotposition. Sollten die ersten klinischen Daten positiv ausfallen, mithin die Probody-Technik klinisch validiert, würde ich sogar weiter aufstocken.
Die Aktien, die an Amgen gehen, stammen aus einer kleinen KP-Erhöhung.
Warum Kursziel "DAUSEND"? Na ja, falls die Probody-Technik in der klinischen Anwendung so gut funktioniert wie in der Präklinik, wird man in der Onkologie (in jedem Fall bei soliden Tumoren, außerhalb der Onkologie aber aber auch in einigen entzündlichen Indikationen) nicht umhin kommen, nahezu jeden Antikörper/ADC/CAR-T mit einer Maskierung zu versehen, was für CytomX entsprechende Lizenzeinnahmen zur Folge hätte.
In meinem Morphosys-Thread habe ich vorhin eine kleine Übersicht über anti-BCMA-Biologics gepostet, der veranschaulicht, wie viele Unternehmen zeitgleich dasselbe Target bearbeiten. So verhält es sich bei den meisten Präparaten. Richtig viel Geld werden auf lange Sicht nur diejenigen Unternehmen verdienen, die eine besonders innovative Technik mit Alleinstellungsmerkmal auf den Markt bringen, die möglichst noch von der Konkurrenz einlizensiert werden muss. Aus diesem Grund ist CytomX meine größte Depotposition. Sollten die ersten klinischen Daten positiv ausfallen, mithin die Probody-Technik klinisch validiert, würde ich sogar weiter aufstocken.
Antwort auf Beitrag Nr.: 55.874.494 von Joschka Schröder am 04.10.17 03:58:23Ich frage mich, ob diese vielen Partner die Cytomx hat nicht schon eine Validierung der Technologie sind. Die investieren hier doch alle nicht zum Spaß. Können so viele Firmen irren?
Antwort auf Beitrag Nr.: 55.874.434 von Joschka Schröder am 04.10.17 01:25:35Ok , danke. Hatte ich wohl schlampig gelesen.
Perfekt, dann ist man schneller in der Klinik.
Perfekt, dann ist man schneller in der Klinik.
Zitat von Joschka Schröder: Ville, in der Twitter-Zusammenfassung steht´s, es handelt sich wie vermutet um das betreffende anti-EGFRxCD3-Molekül aus der präklinischen CytomX-Pipeline (Patent vom 13.7.2017).
mal ein Dankeschön an Joschka,ville & Co fürs detallierte posten..merci
Antwort auf Beitrag Nr.: 55.874.998 von HK12 am 04.10.17 08:31:09Schließe mich als Mediziner "Laie" an.
Auch von mir ein Danke Schön.
Auch von mir ein Danke Schön.
Antwort auf Beitrag Nr.: 55.874.998 von HK12 am 04.10.17 08:31:09
Dem möchte ich mich anschliessen.. Eure Recherche und Ausbreitung der Daten hatte hier enorm zur Entscheidung pro Depotbemischung vor ein paar Wochen beigetragen.
Aufrichtigen Dank!
Zitat von HK12: mal ein Dankeschön an Joschka,ville & Co fürs detallierte posten..merci
Dem möchte ich mich anschliessen.. Eure Recherche und Ausbreitung der Daten hatte hier enorm zur Entscheidung pro Depotbemischung vor ein paar Wochen beigetragen.
Aufrichtigen Dank!
Sehr schöner Deal !
Von mir auch ein Lob für die fachmännischen Beiträge.
Von mir auch ein Lob für die fachmännischen Beiträge.
Auch von meiner Seite an dieser Stelle einen großen Dank an Joschka! Ich habe im Juni nur aufgrund deiner Beiträge hier in die Aktie investiert. Für mich war das eher ein Zock; ich hätte mich auch über einen ordentlichen Verlust nicht beschwert. Umso schöner, was jetzt passiert.
Mein Investment ist auf jeden Fall mehr als gesichert und mal sehen, was die Zeit noch bringen wird. An die Dausend glaube ich nicht so ganz, ich bin ein gebranntes Kind diesbezüglich. Die Hundderd sehe ich aber als ein realistisches Ziel, dem man vor dem Hintergrund dieser Meldung relativ schnell nahekommen könnte.
Mein Investment ist auf jeden Fall mehr als gesichert und mal sehen, was die Zeit noch bringen wird. An die Dausend glaube ich nicht so ganz, ich bin ein gebranntes Kind diesbezüglich. Die Hundderd sehe ich aber als ein realistisches Ziel, dem man vor dem Hintergrund dieser Meldung relativ schnell nahekommen könnte.
Der Dank gebührt alleine Joschka, der diese (hoffentlich-) Perle ausgegraben hat.
Noch kann es allerdings komplett in die Hose gehen, darüber muss man sich immer klar sein. Es gibt noch keinen PoC. Wir wissen somit noch nicht, ob die Technologie funktioniert oder nicht. Das werden wir wohl erst zu ASCO 2018 im Mai 2018 erfahren, wenn die Abstracts veröffentlicht werden. Sofern wegen extrem guter Daten nicht sogar erst eine Veröffentlichung zum Kongress stattfindet (Anfang Juni 2018)....
Im Übrigen sind >USD 1000 durchaus drin, wenn die Technologie ihre Versprechungen voll erfüllt. CTMX würde dann auf der größten Goldmine sitzen, die je gefunden wurde. Bildlich gesprochen. $ 40 Mrd Markkapitalisierung (entspricht aktuell >1000 USD Kurs) wären dann fast noch zu billig in meinen Augen. Zudem besteht die Gefahr, dass ein big pharma die Firma vorher wegschnappt. Aber das dann sicher nicht ohne ein Bietergefecht, das sich gewaschen hat....
Noch kann es allerdings komplett in die Hose gehen, darüber muss man sich immer klar sein. Es gibt noch keinen PoC. Wir wissen somit noch nicht, ob die Technologie funktioniert oder nicht. Das werden wir wohl erst zu ASCO 2018 im Mai 2018 erfahren, wenn die Abstracts veröffentlicht werden. Sofern wegen extrem guter Daten nicht sogar erst eine Veröffentlichung zum Kongress stattfindet (Anfang Juni 2018)....
Im Übrigen sind >USD 1000 durchaus drin, wenn die Technologie ihre Versprechungen voll erfüllt. CTMX würde dann auf der größten Goldmine sitzen, die je gefunden wurde. Bildlich gesprochen. $ 40 Mrd Markkapitalisierung (entspricht aktuell >1000 USD Kurs) wären dann fast noch zu billig in meinen Augen. Zudem besteht die Gefahr, dass ein big pharma die Firma vorher wegschnappt. Aber das dann sicher nicht ohne ein Bietergefecht, das sich gewaschen hat....
Wedbush analyst Robert Driscoll raised his price target on CytomX Therapeutics (NASDAQ: CTMX) to $37.00 (from $26.00) while maintaining a Outperform
Quelle: http://www.stocknewswires.com
Quelle: http://www.stocknewswires.com
Ebenso großen danke an alle fundierte Schreiber hier, allen voran Joschka. Ich selbst bin ein medizinischer Laie.
Auch von mir ein Dankeschön an Joschka.
Deine Begeisterung und Deine Hoffnung in diesen Wert haben auch mich bewogen bei ca. 10 Euro mit einer kleinen Position einzusteigen.
einzusteigen.
Deine Begeisterung und Deine Hoffnung in diesen Wert haben auch mich bewogen bei ca. 10 Euro mit einer kleinen Position
 einzusteigen.
einzusteigen.
Wobei die Kursreaktion enttäuschend ist. Ich bin gerade zu 21,60 € nochmals mit einem Nachkauf bedient worden.
Von meiner Seite auch nochmals vielen Dank an Joschka und- auch wenn der den Dank nicht annehmen möchte- an Ville
Von meiner Seite auch nochmals vielen Dank an Joschka und- auch wenn der den Dank nicht annehmen möchte- an Ville
Antwort auf Beitrag Nr.: 55.878.697 von Bilanzgewinn am 04.10.17 15:50:16
Sorry 21,60$ an der Nasdaq
Zitat von Bilanzgewinn: Wobei die Kursreaktion enttäuschend ist. Ich bin gerade zu 21,60 € nochmals mit einem Nachkauf bedient worden.
Von meiner Seite auch nochmals vielen Dank an Joschka und- auch wenn der den Dank nicht annehmen möchte- an Ville
Sorry 21,60$ an der Nasdaq
Antwort auf Beitrag Nr.: 55.878.706 von Bilanzgewinn am 04.10.17 15:50:56

Zitat von Bilanzgewinn:Zitat von Bilanzgewinn: Wobei die Kursreaktion enttäuschend ist. Ich bin gerade zu 21,60 € nochmals mit einem Nachkauf bedient worden.
Von meiner Seite auch nochmals vielen Dank an Joschka und- auch wenn der den Dank nicht annehmen möchte- an Ville
Sorry 21,60$ an der Nasdaq

Antwort auf Beitrag Nr.: 55.875.895 von Ville7 am 04.10.17 10:10:55
Ville fasst die Situation gut zusammen. Es gibt viele Hinweise darauf, dass die Probody-Technik auch in vivo beim Menschen funktionieren sollte (die Studie mit CX-2009 läuft zum Glück auch noch), der eigentliche Nachweis ist aber noch nicht erbracht! Deshalb ist es auch so schwierig, einen vernünftigen Investitionsgrad/Depotanteil festzulegen. Einerseits möchte man schon die Chance auf außergewöhnliche Gewinne wahrnehmen, andererseits wäre es auch kein schöner Gedanke, im Fall eines Scheiterns, Haus und Hof zu verspielen. Die lukrativen Kooperationen mit großen Pharmakonzernen können da auch keine Sicherheit geben, sie belegen allenfalls, dass Unternehmen wie AbbVie, Amgen, Bristol Myers und Pfizer die Chancen der Probody-Technik ähnlich beurteilen, mehr aber auch nicht. Eine gangbare Lösung könnte sein, in einem gewissen Umfang CytomX-Aktien zu kaufen und im Fall positiver Meldungen, den Depotanteil ggf. prozyklisch weiter aufzustocken. Vom heutigen Kursanstieg auf aktuell 21,8 USD bin ich im Übrigen nicht enttäuscht, vor dem Hintergrund der bisherigen Kursentwicklung hatte mich eher das Ausmaß des vorbörslichen Kursanstiegs auf 26 USD oder mehr (positiv) überrascht.
Ich möchte die Gelegenheit nutzen, mich selbst bei Usern wie Ville, StefanR und anderen für die konstruktiven Diskussionen zu bedanken. Derartige Diskussionen bringen einen immer wieder auf neue Gedanken und bieten eine gute Möglichkeit, den eigenen Standpunkt zu reflektieren.
Zitat von Ville7: Noch kann es allerdings komplett in die Hose gehen, darüber muss man sich immer klar sein. Es gibt noch keinen PoC. Wir wissen somit noch nicht, ob die Technologie funktioniert oder nicht. Das werden wir wohl erst zu ASCO 2018 im Mai 2018 erfahren, wenn die Abstracts veröffentlicht werden. Sofern wegen extrem guter Daten nicht sogar erst eine Veröffentlichung zum Kongress stattfindet (Anfang Juni 2018)....
Im Übrigen sind >USD 1000 durchaus drin, wenn die Technologie ihre Versprechungen voll erfüllt. CTMX würde dann auf der größten Goldmine sitzen, die je gefunden wurde. Bildlich gesprochen. $ 40 Mrd Markkapitalisierung (entspricht aktuell >1000 USD Kurs) wären dann fast noch zu billig in meinen Augen. Zudem besteht die Gefahr, dass ein big pharma die Firma vorher wegschnappt. Aber das dann sicher nicht ohne ein Bietergefecht, das sich gewaschen hat....
Ville fasst die Situation gut zusammen. Es gibt viele Hinweise darauf, dass die Probody-Technik auch in vivo beim Menschen funktionieren sollte (die Studie mit CX-2009 läuft zum Glück auch noch), der eigentliche Nachweis ist aber noch nicht erbracht! Deshalb ist es auch so schwierig, einen vernünftigen Investitionsgrad/Depotanteil festzulegen. Einerseits möchte man schon die Chance auf außergewöhnliche Gewinne wahrnehmen, andererseits wäre es auch kein schöner Gedanke, im Fall eines Scheiterns, Haus und Hof zu verspielen. Die lukrativen Kooperationen mit großen Pharmakonzernen können da auch keine Sicherheit geben, sie belegen allenfalls, dass Unternehmen wie AbbVie, Amgen, Bristol Myers und Pfizer die Chancen der Probody-Technik ähnlich beurteilen, mehr aber auch nicht. Eine gangbare Lösung könnte sein, in einem gewissen Umfang CytomX-Aktien zu kaufen und im Fall positiver Meldungen, den Depotanteil ggf. prozyklisch weiter aufzustocken. Vom heutigen Kursanstieg auf aktuell 21,8 USD bin ich im Übrigen nicht enttäuscht, vor dem Hintergrund der bisherigen Kursentwicklung hatte mich eher das Ausmaß des vorbörslichen Kursanstiegs auf 26 USD oder mehr (positiv) überrascht.
Ich möchte die Gelegenheit nutzen, mich selbst bei Usern wie Ville, StefanR und anderen für die konstruktiven Diskussionen zu bedanken. Derartige Diskussionen bringen einen immer wieder auf neue Gedanken und bieten eine gute Möglichkeit, den eigenen Standpunkt zu reflektieren.
Antwort auf Beitrag Nr.: 55.879.144 von Joschka Schröder am 04.10.17 16:38:39Gibt es eigentlich nur die Möglichkeit, dass wir entweder zum Mond also Richtung 1000 fliegen oder auf null fallen? Was ist ein Szenario dazwischen und wie wahrscheinlich ist das?
Und dann wundert mich, dass keiner über die Einlizenzierung von Cytomx spricht. Was holen sie sich da? Was ist das Ziel und was das Potential? Ich dachte wir vergeben Lizenzen an große Pharmafirmen, weil,wir so eine gute Technologie haben und müssen uns selbst nichts kaufen.
Und dann wundert mich, dass keiner über die Einlizenzierung von Cytomx spricht. Was holen sie sich da? Was ist das Ziel und was das Potential? Ich dachte wir vergeben Lizenzen an große Pharmafirmen, weil,wir so eine gute Technologie haben und müssen uns selbst nichts kaufen.
Antwort auf Beitrag Nr.: 55.879.672 von hinz12 am 04.10.17 17:44:31Ein Dazwischen wäre prinzipiell auch denkbar, z.B. wenn die Abspaltung der Maskierung nur in xx% der Patienten stattfindet und in 100%-xx% = yy% nicht. D.h. in yy% wären die Medikamente unwirksam. Oder wenn der Reststummel der abgespalteten Masierung eine saubere Bindung verindert, aber doch genug Wirksamkeit verbleibt um das therapeutische Fenster mehr als bei der Konkurrenz zu öffnen. Oder oder oder....
Eigenentwicklungen bergen natürlich mehr finanzelles Potential als die max. high single digit (BMS) bis max. double digit (Amgen) Royalties.
Cytomx hat zwar die Maskentechnologie, aber Antikörpertechnologie, ADC-Technologie, bispezifische Technologie, CAT-NK müssen sie zukaufen. Zudem gibt es gute Targets auch nicht wie Sand am Meer.
Eigenentwicklungen bergen natürlich mehr finanzelles Potential als die max. high single digit (BMS) bis max. double digit (Amgen) Royalties.
Cytomx hat zwar die Maskentechnologie, aber Antikörpertechnologie, ADC-Technologie, bispezifische Technologie, CAT-NK müssen sie zukaufen. Zudem gibt es gute Targets auch nicht wie Sand am Meer.
Antwort auf Beitrag Nr.: 55.879.672 von hinz12 am 04.10.17 17:44:31Zu Frage 1:
Binär ist die ganze Angelegenheit natürlich nicht. Sollte die Technik noch nicht ausreichend funktionieren, ließe sich das Verfahren im Rahmen des Patentschutzes weiter optimieren. Auch könnte man im Fall eines Scheitern der laufenden klinischen Studien mit CX-072 und CX-2009 noch keine Rückschlüsse auf die Technik per se ziehen, weil unbefriedigende Studienergebnisse auch Folge einer schlechten Antikörper bzw. ADC-Selektion sein könnten. Insoweit ist das Absturzpotential zunächst einmal limitiert.
Wenn sich die Ergebnisse der Präklinik im Fall CX-072 und/oder CX-2009 auf die Klinik übertragen lassen, so ist umgekehrt jedoch der Nachweis erbracht, dass die Probody-Technik grundsätzlich funktioniert. Das wäre natürlich für die Aktionäre die komfortabelste Variante.
Zu Frage 2:
Wie oben erwähnt, kann die Probody-Technik nur dann erfolgreich sein, wenn die richtigen Moleküle (Antikörper, ADCs, CAR Ts usw.) maskiert werden. Im Hinblick auf die Konstruktion dieser zu maskierenden Moleküle ist z.B. Amgen viel erfahrener als CytomX, das sich ja im Grunde genommen auf die Maskierungstechnik spezialisiert hat. Insoweit macht es Sinn, dass CytomX bei der Entwicklung der benötigten Ausgangsmoleküle auch auf die Expertise seiner Partner zurückgreift. Dadurch läßt sich der Nachschub an Entwicklungsprojekten deutlich beschleunigen. Ein kleines Biotech-Unternehmen wäre allein schon personell völlig überfordert, wollte man alles in-house entwickeln. Dies ist der Grund dafür, dass CytomX geeignete (Ausgangs-)Moleküle von Amgen einlizensieren möchte, deren Bindungsstellen anschließend von CytomX mit der eigenen Probody-Technik maskiert werden. Gerade bei der Entwicklung bispezifischer Antikörper besitzt Amgen mit der von Mikromet übernommenen BitE-Technik nachweislich einige Expertise.
Trägt das zur Klärung bei?
Binär ist die ganze Angelegenheit natürlich nicht. Sollte die Technik noch nicht ausreichend funktionieren, ließe sich das Verfahren im Rahmen des Patentschutzes weiter optimieren. Auch könnte man im Fall eines Scheitern der laufenden klinischen Studien mit CX-072 und CX-2009 noch keine Rückschlüsse auf die Technik per se ziehen, weil unbefriedigende Studienergebnisse auch Folge einer schlechten Antikörper bzw. ADC-Selektion sein könnten. Insoweit ist das Absturzpotential zunächst einmal limitiert.
Wenn sich die Ergebnisse der Präklinik im Fall CX-072 und/oder CX-2009 auf die Klinik übertragen lassen, so ist umgekehrt jedoch der Nachweis erbracht, dass die Probody-Technik grundsätzlich funktioniert. Das wäre natürlich für die Aktionäre die komfortabelste Variante.
Zu Frage 2:
Wie oben erwähnt, kann die Probody-Technik nur dann erfolgreich sein, wenn die richtigen Moleküle (Antikörper, ADCs, CAR Ts usw.) maskiert werden. Im Hinblick auf die Konstruktion dieser zu maskierenden Moleküle ist z.B. Amgen viel erfahrener als CytomX, das sich ja im Grunde genommen auf die Maskierungstechnik spezialisiert hat. Insoweit macht es Sinn, dass CytomX bei der Entwicklung der benötigten Ausgangsmoleküle auch auf die Expertise seiner Partner zurückgreift. Dadurch läßt sich der Nachschub an Entwicklungsprojekten deutlich beschleunigen. Ein kleines Biotech-Unternehmen wäre allein schon personell völlig überfordert, wollte man alles in-house entwickeln. Dies ist der Grund dafür, dass CytomX geeignete (Ausgangs-)Moleküle von Amgen einlizensieren möchte, deren Bindungsstellen anschließend von CytomX mit der eigenen Probody-Technik maskiert werden. Gerade bei der Entwicklung bispezifischer Antikörper besitzt Amgen mit der von Mikromet übernommenen BitE-Technik nachweislich einige Expertise.
Trägt das zur Klärung bei?
Antwort auf Beitrag Nr.: 55.879.753 von Ville7 am 04.10.17 17:53:39Hinsichtlich der Bindungsaffinitäten muss man sich keine Sorgen machen, so etwas läßt sich im Tiermodell gleichwertig untersuchen, den Versuchstiere sind ja menschliche Tumoren implantiert worden.
Antwort auf Beitrag Nr.: 55.879.882 von Joschka Schröder am 04.10.17 18:11:30Das trägt zur Klärung bei. Danke ville, danke Joschka! Mein Gefühl sagt mir, dass die Aktie in zwei Jahren eigentlich nicht tiefer stehen kann als heute. Ich hoffe ich habe recht :-)
Wenn Amgen nun aber einen Antikörper auslizeniert, dann fragt man sich natürlich schon, wieso sie ihn nicht selber entwickeln. Das Geld dafür haben sie sicherlich. Das würde ja den Schluss nahe liegen, dass sie den Antikörper nicht für sehr aussichtsreich halten. Wieso sollten sie ihn sonst abgeben? Oder machen sie das mit Antikörpern, in denen sie nur geringes Marktpotential sehen? Auch das wäre nicht so gut.
Wenn Amgen nun aber einen Antikörper auslizeniert, dann fragt man sich natürlich schon, wieso sie ihn nicht selber entwickeln. Das Geld dafür haben sie sicherlich. Das würde ja den Schluss nahe liegen, dass sie den Antikörper nicht für sehr aussichtsreich halten. Wieso sollten sie ihn sonst abgeben? Oder machen sie das mit Antikörpern, in denen sie nur geringes Marktpotential sehen? Auch das wäre nicht so gut.
Antwort auf Beitrag Nr.: 55.880.221 von hinz12 am 04.10.17 19:02:29Das kann eine Gegenforderung von CytomX gewesen sein, die Amgen im Rahmen der Vertragsverhandlungen erfüllen mußte.
Eben ist eine Meldung über Insidertransaktionen über den Ticker gelaufen. Demnach hat CFO Ray am 2.10.17 zu einem Zeitpunkt, als der Amgen-Vertrag bereits in trockenen Tüchern war, abermals 2.500 Aktien - diesmal zu 18,1 USD je Aktie - verkauft. Nunmehr ist klar, dass die Verkäufe mehr oder weniger automatisiert über eine dazu beauftragte Stelle laufen. Sie besitzen also keinerlei Aussagekraft.
Eben ist eine Meldung über Insidertransaktionen über den Ticker gelaufen. Demnach hat CFO Ray am 2.10.17 zu einem Zeitpunkt, als der Amgen-Vertrag bereits in trockenen Tüchern war, abermals 2.500 Aktien - diesmal zu 18,1 USD je Aktie - verkauft. Nunmehr ist klar, dass die Verkäufe mehr oder weniger automatisiert über eine dazu beauftragte Stelle laufen. Sie besitzen also keinerlei Aussagekraft.
Antwort auf Beitrag Nr.: 55.880.314 von Joschka Schröder am 04.10.17 19:15:56Das mit der Gegenforderung könnte gut sein. Dann haben sie echt smart verhandelt.
Ich bin mir mittlerweile übrigens ziemlich sicher, dass die $950 million für Cytomx für alle drei Targets sind. Hab das noch ein paar mal gelesen und auch die meisten Nachrichten auf irgendwelchen werden so geschrieben. Ist aber immer noch gut.
Das die Verkäufe so vollkommen losgelöst von Deals sind, nötigt mir Respekt ab. Das scheinen solide Kaufleute und gute Wissenschaftler zu sein.
Was meint ihr, wann das erste Medikament mit der Technologie von Cytomx am Markt sein könnte? 2022 oder früher?
Ich bin mir mittlerweile übrigens ziemlich sicher, dass die $950 million für Cytomx für alle drei Targets sind. Hab das noch ein paar mal gelesen und auch die meisten Nachrichten auf irgendwelchen werden so geschrieben. Ist aber immer noch gut.
Das die Verkäufe so vollkommen losgelöst von Deals sind, nötigt mir Respekt ab. Das scheinen solide Kaufleute und gute Wissenschaftler zu sein.
Was meint ihr, wann das erste Medikament mit der Technologie von Cytomx am Markt sein könnte? 2022 oder früher?
Antwort auf Beitrag Nr.: 55.879.882 von Joschka Schröder am 04.10.17 18:11:30Ich bin ebenfalls dankbar, für die wertvollen Impulse, die ich hier bekomme. Ob es die Investitionsstrategie von ville ist, der gern sein Restrisiko durch Realisierung von Gewinnen minimiert, oder die Empfehlung von Joschka, bei positiven ASCO-Daten nächstes Jahr möglicherweise noch nach zulegen. Beides bietet Impulse zum Nachdenken.
Tatsächlich gibt es aus meiner Sicht hier bei der potentiell gamechanging technology nicht nur hopp oder top.
Vielleicht wirkt das Probody-Konjugat bei einem Tumor gut, beim anderen wegen geringerer proteolytischer microenvironment schlechter? Oder der Tumor "kapselt" sich ab, so das die Toxine der T-Zellen, oder die Toxinladungen der PDCs nicht den gesamten Tumor treffen.
Das Verhalten des individuell entwickelten Linkers in seiner spezifischen Zielumgebung, ist für mich das Kriterium an sich.
Diese Peptidverbindung kann für cx072 zu stabil entwickelt worden sein, für cx2009 möglicherweise zu instabil.
Gerade bei hochpotenten Konjugaten, wie den PDCs, oder dem bispezifischen EGFR- AB kann das durch die Präklinik definierte Projekt schnell durch unerwartete Instabilitäten gekillt werden. Bei einem anderen Linker und gleichem Target hätte das Konjugat jedoch mœglicherweise erwartungsgemäß funktionieren können.
Hier die gesamte Entwicklung noch mal neu zu starten nach Scheitern eines Konjugats in der Klinik, scheint jedoch zu zeitaufwändig und kostenintensiv.
Insofern ist die Vielzahl an Projekten, die durch die Eigenentwicklung, und liquiditätsneutral durch die Partnerprojekte begonnen werden, als Sicherheitsnetz äußerst wertvoll.
Darüber hinaus erscheint mir die ganze cytomx-Story wie ein von langer Hand geplantes Unterfangen, mit einer vielleicht gar nicht so aufwändigen Technik. Dafür wurde aber durch umfangreiche Patentabsicherungen für die Projekte ein Alleinstellungsmerkmal geschaffen, auf das die Topunternehmen der Branche im Erfolgsfall einfach nicht verzichten können.
Man kann nach der Verpartnerung mit BMS, AbbVie, und Amgen darauf gespannt sein, wen sich cytomx als nächsten vorknöpft.
Möglicherweise Novartis, mit seiner CAR-T-Technik, oder Roche, die spätestens nach Asco-Daten beginnen müssten, nervös zu werden. Vielleicht sichern sie sich ja Teil-Vertriebsrechte am CXO72?
Auch verschiedene PDCs in Kombination mit alkylierenden, neuen, Payloads von Sgen und imgn, bieten ausreichend Zusatzpotential.
Vielleicht erringen wir mit den ASCO2018-Daten einen klaren Sieg, vielleicht erreichen wir nur ein Etappenziel mit Nachbesserung- Bedarf?
Die vielfältigen Ansätze innerhalb kurzer Zeit machen einen wirtschaftlichen Erfolg trotz potentieller Anfangsniederlage (Asco) immer noch möglich.
Cytomx und seine Aktionäre sind somit in einer ziemlich komfortablen Situation.
Die Wahrscheinlichkeit, daß cytomx einen Sieg erringt, ist, kurz gesagt, wahrscheinlicher, als daß Kickers Offenbach den DFB-Pokal gewinnt.
Tatsächlich gibt es aus meiner Sicht hier bei der potentiell gamechanging technology nicht nur hopp oder top.
Vielleicht wirkt das Probody-Konjugat bei einem Tumor gut, beim anderen wegen geringerer proteolytischer microenvironment schlechter? Oder der Tumor "kapselt" sich ab, so das die Toxine der T-Zellen, oder die Toxinladungen der PDCs nicht den gesamten Tumor treffen.
Das Verhalten des individuell entwickelten Linkers in seiner spezifischen Zielumgebung, ist für mich das Kriterium an sich.
Diese Peptidverbindung kann für cx072 zu stabil entwickelt worden sein, für cx2009 möglicherweise zu instabil.
Gerade bei hochpotenten Konjugaten, wie den PDCs, oder dem bispezifischen EGFR- AB kann das durch die Präklinik definierte Projekt schnell durch unerwartete Instabilitäten gekillt werden. Bei einem anderen Linker und gleichem Target hätte das Konjugat jedoch mœglicherweise erwartungsgemäß funktionieren können.
Hier die gesamte Entwicklung noch mal neu zu starten nach Scheitern eines Konjugats in der Klinik, scheint jedoch zu zeitaufwändig und kostenintensiv.
Insofern ist die Vielzahl an Projekten, die durch die Eigenentwicklung, und liquiditätsneutral durch die Partnerprojekte begonnen werden, als Sicherheitsnetz äußerst wertvoll.
Darüber hinaus erscheint mir die ganze cytomx-Story wie ein von langer Hand geplantes Unterfangen, mit einer vielleicht gar nicht so aufwändigen Technik. Dafür wurde aber durch umfangreiche Patentabsicherungen für die Projekte ein Alleinstellungsmerkmal geschaffen, auf das die Topunternehmen der Branche im Erfolgsfall einfach nicht verzichten können.
Man kann nach der Verpartnerung mit BMS, AbbVie, und Amgen darauf gespannt sein, wen sich cytomx als nächsten vorknöpft.
Möglicherweise Novartis, mit seiner CAR-T-Technik, oder Roche, die spätestens nach Asco-Daten beginnen müssten, nervös zu werden. Vielleicht sichern sie sich ja Teil-Vertriebsrechte am CXO72?
Auch verschiedene PDCs in Kombination mit alkylierenden, neuen, Payloads von Sgen und imgn, bieten ausreichend Zusatzpotential.
Vielleicht erringen wir mit den ASCO2018-Daten einen klaren Sieg, vielleicht erreichen wir nur ein Etappenziel mit Nachbesserung- Bedarf?
Die vielfältigen Ansätze innerhalb kurzer Zeit machen einen wirtschaftlichen Erfolg trotz potentieller Anfangsniederlage (Asco) immer noch möglich.
Cytomx und seine Aktionäre sind somit in einer ziemlich komfortablen Situation.
Die Wahrscheinlichkeit, daß cytomx einen Sieg erringt, ist, kurz gesagt, wahrscheinlicher, als daß Kickers Offenbach den DFB-Pokal gewinnt.

Nun hat auch der CEO wieder durch automatische Verkäufe zugeschlagen.
Eine hier glaube ich noch offene indirekte Frage wurde im CC beantwortet: Amgen hatte keinen Einblick darüber erhalten wie die bisherigen Ergebnisse von CX072 oder CX2009 sind. Hatte zum Abschluss des deals also keine Hinweise, ob und wie gut die Technologie funktioniert....
Eine hier glaube ich noch offene indirekte Frage wurde im CC beantwortet: Amgen hatte keinen Einblick darüber erhalten wie die bisherigen Ergebnisse von CX072 oder CX2009 sind. Hatte zum Abschluss des deals also keine Hinweise, ob und wie gut die Technologie funktioniert....
Antwort auf Beitrag Nr.: 55.882.402 von Ville7 am 05.10.17 03:00:26Die Kooperation von cytomx und amgen, als Entwicklung gemeinsamer Wirkstoffkandidaten, mit der jeweils einzigartigen Technik, sowie
die Unternehmensbeteiligung von amgen an cytomx über 20 mio Dollar zeitgleich, wirft für mich folgende Frage auf:
Jedes Unternehmen möchte so viel wie möglich Informationen vor einer weitreichenden Kooperation erlangen, dazu gehört auch direkte oder indirekte Auskünfte über die 2 momentan laufenden klinischen Studien.
Erinnern wir uns, AbbVie hat den nächsten Schritt, der 15 mio milestoneZahlung hervorgerufen hat, auch erst nach der Veröffentlichung der cx072-proclaim-Daten getan.
Hier bei amgen liegen öffentlich keine direkten Daten zu den klinischen Studien vor, außer der Kenntnis, daß doch recht schnell die cx072-Kombostudien begonnen wurden, und die cx2009 Studie weiter läuft mit 6 Studienzentren.
Eine geplante aktienmäßige Beteiligung an einem anderen Unternehmen berechtigt jedoch zur Initiierung eines due diligence- Prozesses.
Hier erhält der Erwerber das Recht, das Unternehmen auf Herz und Nieren überprüfen zu können.
Dieser Kenntnisgewinn könnte es amgen erheblich erleichtert haben, mit cytomx die umfassende bispezifische Antikörper-Kooperation, mit wechselseitigen Nutzungsrechten, einzugehen.
Auch ohne explizit genaueres über den momentanen Zustand der Studien zu sagen, deren Datenlage ja noch gar nicht offiziell auslegbar ist, wird amgen durch den due diligence Prozeß in die Lage versetzt, die laufenden Studien, sowie andere, uns noch verborgene Fakten, rechtssicher einfordern und prüfen zu können, um dann die neulich veröffentlichte Kooperation zu vereinbaren.
Sean Mc Carthy wird schon die Wahrheit gesagt haben, aber zwischen den Zeilen können die amgen-Leute aufgrund der zur Verfügung gestellten, frischen Daten, ihre notwendigen Rückschlüsse ziehen.
LG
StefanR
die Unternehmensbeteiligung von amgen an cytomx über 20 mio Dollar zeitgleich, wirft für mich folgende Frage auf:
Jedes Unternehmen möchte so viel wie möglich Informationen vor einer weitreichenden Kooperation erlangen, dazu gehört auch direkte oder indirekte Auskünfte über die 2 momentan laufenden klinischen Studien.
Erinnern wir uns, AbbVie hat den nächsten Schritt, der 15 mio milestoneZahlung hervorgerufen hat, auch erst nach der Veröffentlichung der cx072-proclaim-Daten getan.
Hier bei amgen liegen öffentlich keine direkten Daten zu den klinischen Studien vor, außer der Kenntnis, daß doch recht schnell die cx072-Kombostudien begonnen wurden, und die cx2009 Studie weiter läuft mit 6 Studienzentren.
Eine geplante aktienmäßige Beteiligung an einem anderen Unternehmen berechtigt jedoch zur Initiierung eines due diligence- Prozesses.
Hier erhält der Erwerber das Recht, das Unternehmen auf Herz und Nieren überprüfen zu können.
Dieser Kenntnisgewinn könnte es amgen erheblich erleichtert haben, mit cytomx die umfassende bispezifische Antikörper-Kooperation, mit wechselseitigen Nutzungsrechten, einzugehen.
Auch ohne explizit genaueres über den momentanen Zustand der Studien zu sagen, deren Datenlage ja noch gar nicht offiziell auslegbar ist, wird amgen durch den due diligence Prozeß in die Lage versetzt, die laufenden Studien, sowie andere, uns noch verborgene Fakten, rechtssicher einfordern und prüfen zu können, um dann die neulich veröffentlichte Kooperation zu vereinbaren.
Sean Mc Carthy wird schon die Wahrheit gesagt haben, aber zwischen den Zeilen können die amgen-Leute aufgrund der zur Verfügung gestellten, frischen Daten, ihre notwendigen Rückschlüsse ziehen.
LG
StefanR
Antwort auf Beitrag Nr.: 55.884.373 von StefanR am 05.10.17 10:36:44Das ist m.E. eine rechtliche Frage, in welchem Umfang Amgen im Rahmen der abgeschlossenen Verträge Einblicke in die Datenlage bekommen hat. Im Rahmen einer due-diligence-Prüfung erhält der Käufer ja in der Regel den Zugang zu einem Datenpool. Was jedoch dort zum Zeitpunkt der Verhandlungen schon zugänglich und einsehbar war, wissen wir nicht.
Da es sich um laufende und (erst kürzlich) initiierte Studien handelt, gehe ich nicht davon aus, dass hierzu schon Daten bzw. Unterlagen an Amgen herausgegeben wurden, was der CEO von CTMX ja auch öffentlich versichert hat.
Insofern ist die Frage, aus welchen konkreten Unterlagen Amgen Rückschlüsse ziehen könnte oder ob Sie einfach generell (wie wir auch) aufgrund der Indizienlage (CX 2009 mit 6 Zentren, schnelles Hochfahren der CX-072 Studie) davon ausgehen, dass eine gewisse Wahrscheinlichkeit besteht, dass die Technologie funktioniert.
Wenn Du recht hast - und Experten von AMGN weitere Rückschlüsse ziehen konnten - wäre dies natürlich umso besser.
In jedem Fall ist der Zeitpunkt des Deals aber kein schlechtes Zeichen und in jedem Fall als positiv zu werten.
Da es sich um laufende und (erst kürzlich) initiierte Studien handelt, gehe ich nicht davon aus, dass hierzu schon Daten bzw. Unterlagen an Amgen herausgegeben wurden, was der CEO von CTMX ja auch öffentlich versichert hat.
Insofern ist die Frage, aus welchen konkreten Unterlagen Amgen Rückschlüsse ziehen könnte oder ob Sie einfach generell (wie wir auch) aufgrund der Indizienlage (CX 2009 mit 6 Zentren, schnelles Hochfahren der CX-072 Studie) davon ausgehen, dass eine gewisse Wahrscheinlichkeit besteht, dass die Technologie funktioniert.
Wenn Du recht hast - und Experten von AMGN weitere Rückschlüsse ziehen konnten - wäre dies natürlich umso besser.
In jedem Fall ist der Zeitpunkt des Deals aber kein schlechtes Zeichen und in jedem Fall als positiv zu werten.
Antwort auf Beitrag Nr.: 55.884.373 von StefanR am 05.10.17 10:36:44
Ich glaube nicht, dass es da einen kausalen Zusammenhang gibt. Das dürfte eher ein zufälliges zeitliches Zusammenfallen zweier voneinander unabhängiger Ereignisse gewesen sein.
Zitat von StefanR: Erinnern wir uns, AbbVie hat den nächsten Schritt, der 15 mio milestoneZahlung hervorgerufen hat, auch erst nach der Veröffentlichung der cx072-proclaim-Daten getan.
Ich glaube nicht, dass es da einen kausalen Zusammenhang gibt. Das dürfte eher ein zufälliges zeitliches Zusammenfallen zweier voneinander unabhängiger Ereignisse gewesen sein.
Insider Verkäufe
Die sich beschleunigenden Verkäufe des CEOs ( am 4.10.), wenn auch nach 10b5-1 trading plan bleiben für mich sehr irritierend. Rational betrachtet würde ich die doch stoppen, wenn ich wüsste, dass es Richtung Erfolg läuft. Aber im Gegenteil scheint der Plan nun von 1x pro Monat auf 2x pro Monat erhöht worden zu sein?!?
Antwort auf Beitrag Nr.: 55.900.384 von Ville7 am 07.10.17 02:24:10Noch befinden wir uns in einer sehr frühen Phase der klinischen Entwicklung, der CEO dürfte, was die endgültige, klinische Validierung der Probody-Technik betrifft, nicht viel schlauer sein als wir. Dass es reizvoll ist, für 0,945 USD Aktien zu beziehen und anschließend für über 24 USD zu verkaufen, kann ich nachvollziehen, zumal der CEO aus einem großen Fundus an Aktienoptionen schöpfen kann.
Viel überraschender ist für mich, dass Third Rock Ventures noch nicht Kasse gemacht hat. Ich habe eigentlich jeden Tag auf eine entsprechende Meldung gewartet.
Viel überraschender ist für mich, dass Third Rock Ventures noch nicht Kasse gemacht hat. Ich habe eigentlich jeden Tag auf eine entsprechende Meldung gewartet.
Antwort auf Beitrag Nr.: 55.902.889 von Joschka Schröder am 07.10.17 18:47:13Andere Vorstände (R.Humphrey), die etwa ein Drittel Optionen in Vgl zu McCarthy gewährt bekommen, verkaufen nicht, oder nur spärlich.
Ganz generell kann man in Kalifornien/San Francisco bei entsprechendem Lebensstil mehr Geld ausgeben, als man sich in Deutschland vorstellen kann. Gerade, wenn man die Immobilienpreise berücksichtigt.
Zum Amgen-Deal und dem Aktienerwerb noch kurz:
Vielleicht strebt amgen ja einen Direktorenposten bei cytomx an. Sofern sich die venture capital Firmen alle verabschieden, sind hier ein paar Stühle frei.
Zumindest ist eine Aktienbeteiligung ein zusätzliches Bindeglied zwischen den beiden Firmen.
Cytomx hätte im bispecific antibody markt eigenständig nicht annähernd das Kompetenzniveau erreichen können, wie amgen munich sich über Jahre erarbeitet hat.
Die komplett anderen pharmakokinetischen Eigenschaften der bispezifischen AB (HWZ 2,5h, 4wöchige Dauerinfusion mittels Pumpe) bedingen andere Stabilitäten der masking technology, wie bei klassischen checkpoints-probodies und pdc.
Daß cytomx darüber hinaus in Richtung neuer payloads denkt, sieht man an einer der neueren Stellenausschreibungen.
Hier könnte die DNA- crosslinking technology von sgen, die wirksam, aber relativ toxisch ist, eine zweite Chance bekommen.
@joschka, was wären für dich Meilensteine in Bezug auf proof of concept?
(Weniger zeitmäßig asco, esmo, sondern inhaltlich)
LG
StefanR
Ganz generell kann man in Kalifornien/San Francisco bei entsprechendem Lebensstil mehr Geld ausgeben, als man sich in Deutschland vorstellen kann. Gerade, wenn man die Immobilienpreise berücksichtigt.
Zum Amgen-Deal und dem Aktienerwerb noch kurz:
Vielleicht strebt amgen ja einen Direktorenposten bei cytomx an. Sofern sich die venture capital Firmen alle verabschieden, sind hier ein paar Stühle frei.
Zumindest ist eine Aktienbeteiligung ein zusätzliches Bindeglied zwischen den beiden Firmen.
Cytomx hätte im bispecific antibody markt eigenständig nicht annähernd das Kompetenzniveau erreichen können, wie amgen munich sich über Jahre erarbeitet hat.
Die komplett anderen pharmakokinetischen Eigenschaften der bispezifischen AB (HWZ 2,5h, 4wöchige Dauerinfusion mittels Pumpe) bedingen andere Stabilitäten der masking technology, wie bei klassischen checkpoints-probodies und pdc.
Daß cytomx darüber hinaus in Richtung neuer payloads denkt, sieht man an einer der neueren Stellenausschreibungen.
Hier könnte die DNA- crosslinking technology von sgen, die wirksam, aber relativ toxisch ist, eine zweite Chance bekommen.
@joschka, was wären für dich Meilensteine in Bezug auf proof of concept?
(Weniger zeitmäßig asco, esmo, sondern inhaltlich)
LG
StefanR
Antwort auf Beitrag Nr.: 55.902.889 von Joschka Schröder am 07.10.17 18:47:13
Der CEO dürfte bereits mit vielen Daten untermauerte Hinweise haben um die Erfolgswahrscheinlichkeit weit besser als wir einschätzen zu können. Inzwischen sollte bekannt sein, in wie vielen Fällen die Abspaltung der Maskierung funktioniert hat. Zudem sollten in einzelnen Fällen bereits frühe Daten über Sicherheit und Wirksamkeit vorliegen. All das wissen wir nicht. Daher hat der CEO einen erheblichen Vorteil gegenüber einem ausschließlich spekulierenden Investor.
Man muss aber fairerweise für diese Verkäufe ergänzen: Ein Trading Plan kann gar nicht gestoppt werden, wenn es erhebliche, nicht veröffentlichte News gibt, wie z.B. den Amgen deal.
Zitat von Joschka Schröder: ... der CEO dürfte, was die endgültige, klinische Validierung der Probody-Technik betrifft, nicht viel schlauer sein als wir.
Der CEO dürfte bereits mit vielen Daten untermauerte Hinweise haben um die Erfolgswahrscheinlichkeit weit besser als wir einschätzen zu können. Inzwischen sollte bekannt sein, in wie vielen Fällen die Abspaltung der Maskierung funktioniert hat. Zudem sollten in einzelnen Fällen bereits frühe Daten über Sicherheit und Wirksamkeit vorliegen. All das wissen wir nicht. Daher hat der CEO einen erheblichen Vorteil gegenüber einem ausschließlich spekulierenden Investor.
Man muss aber fairerweise für diese Verkäufe ergänzen: Ein Trading Plan kann gar nicht gestoppt werden, wenn es erhebliche, nicht veröffentlichte News gibt, wie z.B. den Amgen deal.
Antwort auf Beitrag Nr.: 55.904.806 von StefanR am 08.10.17 11:08:13Sollten die bispezifischen Probody-Antikörper nicht an den beiden verschiedenen Bindungsstellen maskiert sein und damit sich die Halbwertszeit drastisch erhöhen? Die veringerte Halbwertszeit unmaskierter BYTE-AKs kommt ja m.E. vor allem dadurch, dass die Bindungsmöglichkeiten drastisch erhöht sind, v.a. Richtung CD3.
Meiner Spekulation nach wäre das ein weiterer Vorteil, den bispezifische Antikörper aus einer Maskierung ziehen können.
Meiner Spekulation nach wäre das ein weiterer Vorteil, den bispezifische Antikörper aus einer Maskierung ziehen können.
Antwort auf Beitrag Nr.: 55.907.174 von Ville7 am 08.10.17 19:54:34„The short serum half-life and relatively high clearance suggest that blinatumomab is renally excreted.The metabolism of blinatumomab has not been identified“
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4589878/#!po=16…
Seite 2
wikipedia
Metabolism degradation into small peptides and amino acids
Es gibt zwar auch Metabolismen in Form von target metabolism, was aber hier nicht der Fall zu sein scheint.
Der Abbau scheint aufgrund der Größe (renale clearance nach Peptidspaltung), im Unterschied zu kompletten IGG_Antikörpern sehr viel schneller vonstatten zu gehen.
Ich weiß nicht, inwiefern die masking moiety die HWZ verändern würde. Das hängt möglicherweise von der Größe der Maskierung ab.
Wenn man die HWZ von Peptid-Arzneistoffen erhöhen möchte, wählt man eleganterweise jedoch eher den Pegylierungsweg.
Die kurze HWZ kann auch Vorteile haben, weil man bei überschießender Immunreaktion schneller reagieren kann, als bei AB mit 21 Tagen HWZ.
Die Bite-Technologie scheint so stark zu sein (vgl Dosierung microgramm-Bereich), daß eine besonders vorsichtige Dosierung i.v. 4 Wochen in der Klinik unter ständiger Beobachtung kein Nachteil sein muß.
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4589878/#!po=16…
Seite 2
wikipedia
Metabolism degradation into small peptides and amino acids
Es gibt zwar auch Metabolismen in Form von target metabolism, was aber hier nicht der Fall zu sein scheint.
Der Abbau scheint aufgrund der Größe (renale clearance nach Peptidspaltung), im Unterschied zu kompletten IGG_Antikörpern sehr viel schneller vonstatten zu gehen.
Ich weiß nicht, inwiefern die masking moiety die HWZ verändern würde. Das hängt möglicherweise von der Größe der Maskierung ab.
Wenn man die HWZ von Peptid-Arzneistoffen erhöhen möchte, wählt man eleganterweise jedoch eher den Pegylierungsweg.
Die kurze HWZ kann auch Vorteile haben, weil man bei überschießender Immunreaktion schneller reagieren kann, als bei AB mit 21 Tagen HWZ.
Die Bite-Technologie scheint so stark zu sein (vgl Dosierung microgramm-Bereich), daß eine besonders vorsichtige Dosierung i.v. 4 Wochen in der Klinik unter ständiger Beobachtung kein Nachteil sein muß.
Antwort auf Beitrag Nr.: 55.907.888 von StefanR am 08.10.17 22:34:30
Noch schnell dazu: Der Grund für die längere HWZ dürfte ganz einfach darin liegen, dass die maskierten Moleküle weniger an gesundes Gewebe binden, mithin länger zirkulieren.
Zitat von StefanR: Ich weiß nicht, inwiefern die masking moiety die HWZ verändern würde. Das hängt möglicherweise von der Größe der Maskierung ab.
Noch schnell dazu: Der Grund für die längere HWZ dürfte ganz einfach darin liegen, dass die maskierten Moleküle weniger an gesundes Gewebe binden, mithin länger zirkulieren.
Antwort auf Beitrag Nr.: 55.908.014 von Joschka Schröder am 08.10.17 23:19:23Hallo Joschka,
es gibt tatsächlich das Prinzip target metabolism, d.h. das außer Verkehr ziehen des Wirkstoffs durch Bindung an das auf gesundem oder „kranken“ Gewebe vorhandenen Rezeptoren.
Genauso gibt es jedoch den Abbau über Peptidspaltung und klassischer Nierenfiltration.
Laut der von mir gefundenen Quellen scheint bei Blinatumomab dieser zweite Weg der bestimmende zu sein.
es gibt tatsächlich das Prinzip target metabolism, d.h. das außer Verkehr ziehen des Wirkstoffs durch Bindung an das auf gesundem oder „kranken“ Gewebe vorhandenen Rezeptoren.
Genauso gibt es jedoch den Abbau über Peptidspaltung und klassischer Nierenfiltration.
Laut der von mir gefundenen Quellen scheint bei Blinatumomab dieser zweite Weg der bestimmende zu sein.
Antwort auf Beitrag Nr.: 55.908.053 von StefanR am 08.10.17 23:40:21Klar, mein Kommentar bezog sich auch ausschließlich auf den Einfluss der Probody-Maskierung auf die HWZ.
Cytomx hat bei der cx2009-Studie (pdc gegen cd 166) die Studienzentrenanzahl auf 10 Kliniken erhöht.
Antwort auf Beitrag Nr.: 55.914.539 von StefanR am 09.10.17 20:03:36Das ist eine sehr gute Nachricht. StefanR, Du fragtest in Beitrag 491 "was wären für dich Meilensteine in Bezug auf proof of concept? (Weniger zeitmäßig asco, esmo, sondern inhaltlich)"?
Es hört sich vielleicht überraschend an, aber derartige Meldungen sind für mich kleine Meilensteine. Die Maskierung scheint schon einmal stabil zu sein, andernfalls käme es bei einem Target wie CD166 sehr schnell zu üblen Komplikationen. Der nächste Schritt wäre ein therapeutischer Wirknachweis (-> proteolytische Abspaltung der Maskierung). Vermutlich läßt sich die Probody-Technik in der CX2009-Studie grundsätzlich schneller validieren als dies in der CX-072-Studie möglich ist, obwohl letztere schon länger läuft. Dass die in den jeweiligen Präparaten enthaltenen Antikörper eine ausreichende Bindungsaffinität zu den jeweiligen Targets besitzen, setze ich aufgrund der präklinischen Versuche mal voraus.
Es hört sich vielleicht überraschend an, aber derartige Meldungen sind für mich kleine Meilensteine. Die Maskierung scheint schon einmal stabil zu sein, andernfalls käme es bei einem Target wie CD166 sehr schnell zu üblen Komplikationen. Der nächste Schritt wäre ein therapeutischer Wirknachweis (-> proteolytische Abspaltung der Maskierung). Vermutlich läßt sich die Probody-Technik in der CX2009-Studie grundsätzlich schneller validieren als dies in der CX-072-Studie möglich ist, obwohl letztere schon länger läuft. Dass die in den jeweiligen Präparaten enthaltenen Antikörper eine ausreichende Bindungsaffinität zu den jeweiligen Targets besitzen, setze ich aufgrund der präklinischen Versuche mal voraus.
Off topic:
Wilde Kursbewegungen bei Mersana ohne greifbaren Grund. Nachdem die Aktie ohne News bis 20 USD durchgestartet war (was mir übertrieben schien), ist die Aktie während der vergangenen Tage nunmehr wieder auf 16,1 USD zurückgekommen und notiert nicht mehr weit über dem Emissionskurs (15 USD). Ein Grund für den aktuellen Kurseinbruch könnte sein, dass am Montag die Abstracts der EEORTC-NCI-AACR-Conference freigeschaltet werden, bei der Mersana über XMT-1522 berichten wird. Einige Anleger haben deshalb wohl heiße Füsse bekommen. Ich rechne nicht damit, dass sich im Abstract nennenswerte Neuigkeiten finden, sondernerwarte eher ältere Verträglichkeitsdaten (Abstract wurde schon vor Monaten eingereicht). Insoweit könnte der gegenwärtige Kurseinbruch für Trader evt. eine interessante Kaufgelegenheit darstellen. Meinen eigenen Meinungsbildungsprozess habe ich noch immer nicht abgeschlossen, die ADC-Technik ist zweifellos interessant, ob das ganze tatsächlich wie gewünscht funktionieren wird, ist nach aktuellem Kenntnisstand aber schwer abschätzbar.
Wilde Kursbewegungen bei Mersana ohne greifbaren Grund. Nachdem die Aktie ohne News bis 20 USD durchgestartet war (was mir übertrieben schien), ist die Aktie während der vergangenen Tage nunmehr wieder auf 16,1 USD zurückgekommen und notiert nicht mehr weit über dem Emissionskurs (15 USD). Ein Grund für den aktuellen Kurseinbruch könnte sein, dass am Montag die Abstracts der EEORTC-NCI-AACR-Conference freigeschaltet werden, bei der Mersana über XMT-1522 berichten wird. Einige Anleger haben deshalb wohl heiße Füsse bekommen. Ich rechne nicht damit, dass sich im Abstract nennenswerte Neuigkeiten finden, sondernerwarte eher ältere Verträglichkeitsdaten (Abstract wurde schon vor Monaten eingereicht). Insoweit könnte der gegenwärtige Kurseinbruch für Trader evt. eine interessante Kaufgelegenheit darstellen. Meinen eigenen Meinungsbildungsprozess habe ich noch immer nicht abgeschlossen, die ADC-Technik ist zweifellos interessant, ob das ganze tatsächlich wie gewünscht funktionieren wird, ist nach aktuellem Kenntnisstand aber schwer abschätzbar.
Beitrag zu dieser Diskussion schreiben
Investoren beobachten auch:
| Wertpapier | Perf. % |
|---|---|
| -1,38 | |
| +0,08 | |
| +5,49 | |
| +0,46 | |
| -1,35 | |
| +2,02 | |
| +2,16 | |
| +0,78 | |
| -2,92 | |
| -2,80 |
Meistdiskutiert
| Wertpapier | Beiträge | |
|---|---|---|
| 176 | ||
| 156 | ||
| 73 | ||
| 64 | ||
| 62 | ||
| 62 | ||
| 28 | ||
| 26 | ||
| 26 | ||
| 25 |
CytomX - ein bahnbrechender Ansatz in der Tumortherapie





















